JP2005524379A - 抗体依存性細胞傷害性の増強を伴う抗体グリコシル化改変体 - Google Patents
抗体依存性細胞傷害性の増強を伴う抗体グリコシル化改変体 Download PDFInfo
- Publication number
- JP2005524379A JP2005524379A JP2003517069A JP2003517069A JP2005524379A JP 2005524379 A JP2005524379 A JP 2005524379A JP 2003517069 A JP2003517069 A JP 2003517069A JP 2003517069 A JP2003517069 A JP 2003517069A JP 2005524379 A JP2005524379 A JP 2005524379A
- Authority
- JP
- Japan
- Prior art keywords
- antibody
- human
- host cell
- gntiii
- cells
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/10—Cells modified by introduction of foreign genetic material
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2887—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against CD20
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K49/00—Preparations for testing in vivo
- A61K49/06—Nuclear magnetic resonance [NMR] contrast preparations; Magnetic resonance imaging [MRI] contrast preparations
- A61K49/08—Nuclear magnetic resonance [NMR] contrast preparations; Magnetic resonance imaging [MRI] contrast preparations characterised by the carrier
- A61K49/10—Organic compounds
- A61K49/14—Peptides, e.g. proteins
- A61K49/16—Antibodies; Immunoglobulins; Fragments thereof
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2896—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against molecules with a "CD"-designation, not provided for elsewhere
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/30—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants from tumour cells
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/30—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants from tumour cells
- C07K16/3038—Kidney, bladder
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N9/00—Enzymes; Proenzymes; Compositions thereof; Processes for preparing, activating, inhibiting, separating or purifying enzymes
- C12N9/10—Transferases (2.)
- C12N9/1048—Glycosyltransferases (2.4)
- C12N9/1051—Hexosyltransferases (2.4.1)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P21/00—Preparation of peptides or proteins
- C12P21/005—Glycopeptides, glycoproteins
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/10—Immunoglobulins specific features characterized by their source of isolation or production
- C07K2317/14—Specific host cells or culture conditions, e.g. components, pH or temperature
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/24—Immunoglobulins specific features characterized by taxonomic origin containing regions, domains or residues from different species, e.g. chimeric, humanized or veneered
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/40—Immunoglobulins specific features characterized by post-translational modification
- C07K2317/41—Glycosylation, sialylation, or fucosylation
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/73—Inducing cell death, e.g. apoptosis, necrosis or inhibition of cell proliferation
- C07K2317/732—Antibody-dependent cellular cytotoxicity [ADCC]
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02P—CLIMATE CHANGE MITIGATION TECHNOLOGIES IN THE PRODUCTION OR PROCESSING OF GOODS
- Y02P20/00—Technologies relating to chemical industry
- Y02P20/50—Improvements relating to the production of bulk chemicals
- Y02P20/52—Improvements relating to the production of bulk chemicals using catalysts, e.g. selective catalysts
Abstract
Description
(発明の分野)
本発明は、タンパク質のグリコシル化操作の分野に関する。より詳細には、本発明は、改良された処置的特性を有するタンパク質(抗体依存性細胞傷害性の増強を伴う抗体)を生成するためのグリコシル化操作に関する。
糖タンパク質は、ヒト、その他の真核生物およびいくつかの原核生物における多数の不可欠な機能(触媒作用、シグナル伝達、細胞間コミュニケーション、ならびに分子認識および会合)を媒介する。それらは、真核生物において非細胞質ゾルタンパク質の大部分を構成する(Lisら、Eur.J.Biochem.218:1−27(1993))。多数の糖タンパク質が処置目的のために開発されてきており、過去20年の間、天然に存在する分泌糖タンパク質の組換えバージョンが生物工学産業の主要な産物であった。例としては、エリスロポエチン(EPO)、処置用モノクローナル抗体(処置用mAb)、組織プラスミノーゲンアクチベータ(tPA)、インターフェロン−β(IFN−β)、顆粒球−マクロファージコロニー刺激因子(GM−CSF)およびヒト絨毛性ゴナドトロピン(hCG)が挙げられる(Cummingら、Glycobiology 1:115−130(1991))。
テトラサイクリン調節様式で、N−アセチルグルコサミニルトランスフェラーゼIII(GnTIII;EC2.1.4.144)を過剰発現する遺伝子操作されたmAb産生細胞株を用いて、抗−CD20モノクローナル抗体(mAb)IDEC−C2B8(Rituximab)および抗癌mAb chG250の新規のグリコシル化改変体を、本発明者等はここに生成した。GnTIIIは、天然に存在するヒト抗体中に低から中レベルで見出されるが、標準工業細胞株中に産生されるmAbを欠いているバイセクトオリゴ糖の合成に必要とされる。新規のグリコシル化バージョンは、MabtheraTM(欧州で販売されているRixtuximabのバージョン)およびマウスミエローマ由来chG250より生物学的(ADCC)活性が優れていた。例えば、MabtheraTMのような最大ADCC活性に達するために必要とされる量は、最高レベルのバイセクトオリゴ糖を保有する改変体では10分の1であった。chG250に関しては、最高レベルのバイセクトオリゴ糖を保有する改変体は、非修飾コントロールchG250にさらに低いADCC活性を検出するために必要とされるものの125分の1の濃度で有意のADCC活性を媒介した。GnTIII発現およびADCC活性のレベル間に明らかな相関が見出された。
用語は、別に定義しない限り、以下のように当該技術分野で一般的に用いられるように本明細書中で用いられる。
「ヒト免疫エフェクター細胞」は、抗体またはFc融合タンパク質のFc領域と結合し、エフェクター機能を実施する、それらの表面上にFc受容体を提示する白血球の集団である。このような集団としては、末梢血単核球(PBMC)および/またはナチュラルキラー(NK)細胞が挙げられ得るが、これらに限定されない。
1)本アッセイは、抗体の抗原結合領域により認識される標的抗原を発現することが既知である標的細胞を用いる。
i)PBMCを、標準密度遠心分離法を用いて単離し、5×106細胞/mlでRPMI細胞培地中に懸濁する。
本発明は、グリコフォームの抗体または抗体フラグメント、あるいは抗体依存性細胞傷害性の増強を伴う抗体フラグメントを含む融合タンパク質の産生のための宿主細胞系の生成および使用の方法を提供する。標的エピトープの同定、ならびにグリコシル化パターンの変更が望ましい潜在的処置値を有する抗体の生成、ならびにそれらのそれぞれのコード核酸配列の単離は、本発明の範囲内である。
本発明は、変更されたグリコシル化パターンを有するタンパク質の生成のための宿主細胞発現系を提供する。特に本発明は、改良された処置値を有するグリコフォームのタンパク質の生成のための宿主細胞系を提供する。したがって、本発明は、糖タンパク質修飾グリコシルトランスフェラーゼ、すなわちβ(1,4)−N−アセチルグルコサミニルトランスフェラーゼIII(GnTIII)の発現を増強するよう選択または操作された宿主細胞発現系を提供する。特に、このような宿主細胞発現系は、任意に構成的プロモーター系または調節プロモーター系に作動可能に連結されるGnTIIIをコードする組換え核酸分子を含むように操作され得る。あるいは、GnTIIIを天然に産生し、産生するよう誘導され、かつ/または産生するよう選択される宿主細胞発現系が用いられ得る。
当業者に既知である方法を用いて、目的のタンパク質のコード配列、ならびにGnTIIIおよび適切な転写/翻訳制御シグナルのコード配列を含有する発現ベクターを構築し得る。これらの方法としては、組換えDNA法、合成法およびインビボ組換え/遺伝子組換えが挙げられる(例えば、Maniatisら、Molecular Cloning A Laboratory Manual,Cold Spring Harbor Laboratory,N.Y.(1989)およびAusubelら、Current Protocols in Molecular Biology,Greene Pubulishing AssociatesおよびWiley Interscience,N.Y.(1989)に記載された技法を参照)。
コード配列を含有し、生物学的に活性な遺伝子産物を発現する宿主細胞は、少なくとも4つの一般的アプローチにより同定され得る;(a)DNA−DNAハイブリダイゼーションまたはDNA−RNAハイブリダイゼーション;(b)「マーカー」遺伝子機能の存在または非存在;(c)宿主細胞中のそれぞれのmRNA転写体の発現により測定した場合の転写のレベルの評価;および(d)イムノアッセイにより、またはその生物学的活性により測定した場合の遺伝子産物の検出。
(i.抗体依存性細胞傷害性の増強を伴う抗体の生成および使用)
好ましい実施形態において、本発明は、抗体依存性細胞傷害性の増強を伴うグリコフォームの抗体および抗体フラグメントを提供する。
上記のように、本発明は、処置用抗体のADCC活性を増強するための方法に関する。これは、このような抗体のFc領域のグリコシル化パターンを操作することにより、特にそれらのFc領域の保存グリコシル化部位にN結合されるバイセクト複合オリゴ糖およびバイセクトハイブリッドオリゴ糖を保有する抗体分子の割合を最大にすることにより、達成される。この戦略は、処置用抗体によってだけでなく、免疫グロブリンのFc領域と等価である領域を保有する任意の分子により媒介される望ましくない細胞に対するFc媒介性細胞傷害性を増強するために適用され得るが、これは、グリコシル化の操作により導入される変化が、Fc領域のみに、したがってADCCメカニズムに関与するエフェクター細胞の表面のFc受容体とのその相互作用に、影響を及ぼすためである。本明細書に開示された方法が適用され得るFc含有分子としては、(a)Fc領域のN末端に融合されたターゲッティングタンパク質ドメインから作製される可溶性融合タンパク質(ChamovおよびAshkenazi,Trends Biotech.14:52(1996))、および(b)Fc領域のN末端に融合された原形質膜に局在化されるII型膜貫通ドメインから作製される原形質膜固定融合タンパク質(Stabila,P.F.,Nature Biotech.16:1357(1998))が挙げられるが、これらに限定されない。
(IDEC−CEB8産生細胞株のグリコシル化操作により得られる、増強された抗体依存性細胞傷害性を有する、キメラ抗CD20抗体IDEC−C2B8の新規バージョン)
IDEC−C2B8のVHおよびVLのコード領域の合成ならびに哺乳動物発現ベクターの構築。IDEC−C2B8抗体のVHおよびVL領域をコードするcDNAを、PCRを用いて、一段階法で、一組の重複一本鎖オリゴヌクレオチドから構築した(Kobayashi,N.ら、Biotechniques 23:500−503(1997))。国際公開特許出願(国際公開番号WO94/11026)から、IDEC−C2B8 VLおよびVHをコードするオリジナル配列データを得た。構築されたVLおよびVHcDNAフラグメントをpBluescriptIIKS(+)にサブクローニングし、配列決定して、オリジナルアミノ酸残基配列を変更せずに、可変領域および定常領域接合部に導入された独特の制限部位を用いて、それぞれヒト定常軽鎖(Igκ)および重鎖(IgG1)cDNAへの連結により直接結合した(Umana,P.ら、Nat Biotechnol.17:176−180(1999);Reff,M.E.ら、Blood 83:435−445(1994))。各完全長cDNAをpcDNA3.1(+)(Invitrogen,Leek,The Netherlands)に個別にサブクローニングし、キメラC2B8軽鎖(pC2B8L)および重鎖(pC2B8H)に関する哺乳動物発現ベクターを得た。
IDEC−C2B8の産生および特異的抗原結合の立証。GnTIIIの安定テトラサイクリン調節発現およびIDEC−C2B8の安定構成性発現を示すCHO−tet−GnTIII細胞を確立し、一組の抗体サンプルの産生のためにスケールアップした。スケールアップ中、同一クローンからの並行培養を、3つの異なるテトラサイクリン濃度、25ng/ml、50ng/mlおよび2000ng/ml下で増殖させた。これらのレベルのテトラサイクリンは、異なるレベルのGnTIIIおよびバイセクトオリゴ糖を生じることが以前に示されている(Umana,P.ら、Nat Biotechnol.17:176−180(1999);Umana,P.ら、Biotechnol.Bioeng.65:542−549(1999))。GnTIIIを発現しないC2B8産生コントロール細胞株も確立し、CHO−tet−GnTIIIの3つの並行培養に関するのと同一条件下で培養した。プロテインAアフィニティークロマトグラフィー後、SDS−PAGEおよびクーマシーブルー染色により、mAb純度を95%より高いと概算した。それらの産生のために培養培地に添加されたテトラサイクリン濃度に従い、サンプルを以下のように命名した:C2B8−25t、C2B8−50t、C2B8−2000tおよびC2B8−nt(すなわち非バイセクトコントロールに関しては無テトラサイクリン)。サンプルC2B8−25tは、CD20陽性細胞およびCD20陰性細胞を用いた間接的免疫蛍光法により、特異的抗原結合を示したが(図1)、これは、合成VLおよびVHの遺伝子フラグメントが機能的に誤りがなかったことを示す。
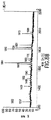
異なるC2B8mAbグリコシル化改変体を、CD20陽性SB細胞のインビトロ溶解として測定したADCC活性について比較した。GnTIIIを欠いている親細胞株由来の、さらに別のmAbサンプルであるC2B8−ntも試験した。基底GnTIII発現レベルで産生され、低レベルのバイセクトオリゴ糖を保有するサンプルC2B8−2000tは、C2B8−tよりわずかに活性であった(図4A)。GnTIII発現の次に高いレベルでは、サンプルC2B8−50tはほぼ等レベルのバイセクトオリゴ糖および非バイセクトオリゴ糖を保有したが、有意により高い標的細胞溶解を媒介しなかった。しかしながら、最低テトラサイクリン濃度では、80%までのバイセクトオリゴ糖構造を含有するサンプルC2B8−25tは、全抗体濃度範囲で、残りのサンプルより有意に活性であった。C2B8−25tは10分の1の抗体濃度で、サンプルC2B8−ntの最大レベルのADCC活性に達した(図4A)。サンプルC2B8−25tは、コントロールに関しての最大ADCC活性の有意の増強も示した(50%対30%溶解)。
(chG250産生細胞株のグリコシル化操作により得られる抗体依存性細胞傷害性の増強を伴う、抗腎細胞癌抗体chG250の新規バージョン)
(1.細胞培養)
chG250キメラmAbを産生するSP2/0マウスミエローマ細胞(wt−chG250−SP2/0細胞)を、1:100(容量/容量)のペニシリン/ストレプトマイシン/抗真菌性溶液(SIGMA,Buchs,Switzerland)を補充した標準細胞培地中で増殖させた。細胞を、組織培養フラスコ中で5%CO2湿潤大気中、37℃で培養した。培地を、3〜4日ごとに取り替えた。細胞を、10%DMSOを含有する培地中で凍結させた。
IRESを介してプロマイシン耐性遺伝子に作動可能に連結されるGnTIIIの構成性発現のためのベクターを用いて、電気穿孔により、wt−chG250−SP2/0ミエローマ細胞をトランスフェクトした。電気穿孔の24時間前に、培地を取り替えて、細胞を5×105細胞/mlで接種した。700万個の細胞を、4℃にて1300rmpで4分間、遠心分離した。細胞を3mLの新しい培地で洗浄し、再び遠心分離した。培地中の1.25%(容量/容量)DMSOおよび20〜30μgのDNAを含有する反応混合物0.3〜0.5mlの容量中に細胞を再懸濁した。次に電気穿孔混合物を0.4cmキュベットに移して、遺伝子パルサー(Bio Rad製)を用いて、低電圧(250〜300V)および高キャパシタンス(960μF)でパルスをかけた。電気穿孔後、細胞を迅速にT25培養フラスコ中の6mLの1.25%(容量/容量)DMSO培地に移して、37℃でインキュベートした。電気穿孔後2日目に培地に2μg/mLのプロマイシンを適用することにより、安定構成部分を選択した。2〜3週間後、安定したプロマイシン耐性混合集団を得た。単一細胞由来クローンをFACSにより得て、その後、展開し、プロマイシン選択下で保持した。
ウエスタンブロッティングにより、GnTIII発現に関してプロマイシン耐性クローンをスクリーニングした。ウエスタンブロットは、クローン5H12、4E6および4E8が最高レベルのGnTIIIを発現していることを明らかに示した。5G2も中強度のGnTIII帯域を示したが、2F1、3D3および4G3は最低帯域強度を有し、したがって低量のGnTIIIを発現した(図5)。
クローン2F1、3D3、4E6、4E8、4G3、5G2、5H12および野生型(wt−chG250−SP2/0細胞)を、130ml培地の総容量中に3×105細胞/mLで接種し、単一三重フラスコ中で培養した。接種のために用いた細胞は、すべて完全対数増殖期であり、したがって細胞は、生産バッチ開始時に同一の増殖状態であったと考えられた。細胞を4日間培養した。抗体を含有する上清を後期対数増殖期に収集して、再現性を保証した。chG250モノクローナル抗体を、2クロマトグラフィー工程で精製した。各バッチから得られたchG250モノクローナル抗体を含有する培養上清をまず、HiTrapプロテインAアフィニティークロマトグラフィーを用いて精製した。プロテインAは、ヒトIgGFc領域に高度に特異的である。プロテイン溶離物からのプールサンプルを、ResourceS 1mlカラム(Amersham Pharmacia Biotech)上での陽イオン交換クロマトグラフィーによりPBSに緩衝液交換した。SDS染色およびクーマシーブルー染色から、最終純度を95%より高いと判定した(図6)。既知の濃度を有する野生型抗体を用いた標準較正曲線で、各サンプルの濃度を確定した。
異なるオリゴ糖構造の分子量を正確に提供するマトリクス支援レーザ脱離/イオン化飛行時間型質量分析法(MALDI/TOF−MS)によって、オリゴ糖プロフィールを得た。この技法は、混合物内の異なるオリゴ糖構造間の割合の定量的分析を可能にする。中性オリゴ糖は、主に[M+Na+]イオンとして出現したが、時としてそれらはより小さい[M+K+]イオンを伴い、m/z16の質量増大をもたらした。カリウムイオン付加物として出現する構造のパーセンテージはマトリクスの含量に依存し、したがってサンプル間で変化し得る。各抗体調製物由来の中性N結合型オリゴ糖の混合物を、マトリクスとして2,5−デヒドロ安息香酸(2,5−DHB)を用いて分析した。既知の単糖組成および独特の質量のために、スペクトル中のピークのいくつかは、特定のオリゴ糖構造に明確に割り当てられた。しかしながら、多重構造はしばしば、特定の質量に割り当てられ得る。MALDIによって質量を確定することはできるが、異性体間の区別はできない。生合成経路についての知識および過去の構造データは、ほとんどの場合に、スペクトル中のピークへのオリゴ糖構造の割り当てを可能にする。
細胞傷害性を測定するカルセイン−AM保持法は、抗体を用いたインキュベーション後に細胞中に残留する染料蛍光を測定する。400万個のG250抗原陽性細胞(標的)を、10%ウシ胎仔血清を補充した1.8mLのRPMI−1640細胞培地(GIBCO BRL,Basel,Switzerland)中の10μMのカルセイン−AM(Molecular Probes,Eugene,OR)を用いて、5%CO2湿潤大気中で37℃にて30分間標識した。細胞を培地中で2回洗浄し、12mLのAIMV無血清培地(GIBCO BRL, Basel, Switzerland)中に再懸濁した。次に、標識細胞をU底96ウェルに移し(30,000細胞/ウェル)、異なる濃度の抗体を用いて、4℃で1時間、三連でインキュベートした。フィコール−パック(Pharmacia Biotech,Dubendorf,Switzerland)勾配上での遠心分離により、ヘパリン処理新鮮ヒト血液(全実験において、同一健常ドナーから得た)から末梢血単核球(PBMC)を分離した。PBMCを50μL容量で三連ウェルに添加し、25:1のエフェクター対標的比(E:T比)および200μLの最終容量を生じた。次に96ウエルプレートを、5%CO2大気中で37℃にて4時間インキュベートした。その後、96ウエルプレートを700×gで5分間遠心分離し、上清を捨てた。細胞ペレットをハンクス平衡塩溶液(HBSS)で2回洗浄し、200μLの0.05M ホウ酸ナトリウム、pH9、0.1%トリトンX−100中で溶解した。標的細胞中の蛍光染料の保持を、FLUOstar微小プレート読取器(BMG LabTechnologies,Offenburg,Germany)で測定した。抗体に曝露する代わりに、サポニン(AIMV中200μg/mL;SIGMA,Buchs,Switzerland)に標的細胞を曝露することにより、特異的溶解を総溶解コントロールに関して算定した。以下の式を用いて、特異的溶解(%)を算定した:
細胞傷害性%=(Fmed−Fexp)/(Fmed−Fdet)
(式中、Fmedは培地単独で処理した標的細胞の蛍光を表し、PMBCによる非特異的溶解を考察し、Fexpは抗体で処理した細胞の蛍光を表し、Fdetは抗体の代わりにサポニンで処理した細胞の蛍光を表す)。
(慢性対宿主性移植片病を有する患者における免疫媒介性血小板減少症の処置)
慢性対宿主性移植片病における自己免疫血小板減少症は、臨床疾患を引き起こすB細胞調節不全の一例を示す。慢性対宿主性移植片病を有する被験者における免疫媒介性血小板減少症を処置するために、本発明の方法により調製され、ADCCの増強を伴う抗CD20キメラモノクローナル抗体を、Ratanatharathorn,V.ら、Ann.Intern.Med.133(4):275−79(2000)(この記載内容全体が、参照により本明細書中に援用される)に記載されたように被験者に投与する。特に、抗体375mg/m2の毎週注入を被験者に4週間施した。抗体療法は、末梢血中のB細胞の顕著な枯渇ならびに血小板関連抗体レベルの低減を生じた。
(重症免疫媒介性赤芽球ろうおよび溶血性貧血の処置)
免疫媒介性後天性赤芽球ろう(PRCA)は、しばしばその他の自己免疫現象に関連するまれな障害である。被験者における免疫媒介性後天性赤芽球ろうを処置するために、本発明の方法により調製され、ADCCの増殖を伴う抗CD20キメラモノクローナル抗体を、Zecca,M.ら、Blood 12:3995−97(1997)(この記載内容全体が、参照により本明細書中に援用される)に記載されたように、被験者に投与する。特に、PRCAおよび自己免疫性溶血性貧血を有する被験者には、抗体375mg/m2/週を2用量投与する。抗体療法後、静脈内免疫グロブリンを用いた変換処置を開始する。この処置は、B細胞の顕著な枯渇およびヘモグロビンレベル増大を伴う網状赤血球数の有意の増大を生じる。
Claims (38)
- β(1,4)−N−アセチルグルコサミニルトランスフェラーゼIII(GnTIII)をコードする少なくとも1つの核酸の発現によりFc媒介性細胞傷害性の増強を伴うポリペプチドを産生するよう操作された宿主細胞であって、該宿主細胞により産生される該ポリペプチドは、全抗体分子、抗体フラグメント、および免疫グロブリンのFc領域と等価の領域を含む融合タンパク質から成る群から選択され、ここで、該GnTIIIは、Fc領域中にバイセクト複合オリゴ糖を保有するポリペプチドと比較して、Fc領域中にバイセクトハイブリッドオリゴ糖またはガラクトシル化複合オリゴ糖、あるいはそれらの混合物を保有する該ポリペプチドの割合を増大するのに十分な量で発現される、宿主細胞。
- 前記ポリペプチドがIgGまたはそのフラグメントである、請求項1に記載の宿主細胞。
- 前記ポリペプチドがIgG1またはそのフラグメントである、請求項1に記載の宿主細胞。
- 前記ポリペプチドがヒトIgGのFc領域と等価の領域を含む融合タンパク質である、請求項1に記載の宿主細胞。
- GnTIIIをコードする少なくとも1つの遺伝子を含む核酸分子が前記宿主細胞中に導入されている、請求項1に記載の宿主細胞。
- 内因性GnTIII遺伝子が活性化されるよう操作されている、請求項1に記載の宿主細胞。
- 前記内因性GnTIIIが宿主染色体中への遺伝子発現を増強するDNA要素の挿入により活性化されている、請求項6に記載の宿主細胞。
- 内因性GnTIIIの発現を誘発する突然変異を保有するよう選択されている、請求項6に記載の宿主細胞。
- CHO細胞変異体lec10である、請求項8に記載の宿主細胞。
- CHO細胞、BHK細胞、NS0細胞、SP2/0細胞、Y0ミエローマ細胞、P3X63マウスミエローマ細胞、PER細胞、PER.C6細胞またはハイブリドーマ細胞である、請求項1に記載の宿主細胞。
- 前記ポリペプチドが抗CD20抗体である、請求項10に記載の宿主細胞。
- 前記抗CD20抗体がIDEC−C2B8である、請求項11に記載の宿主細胞。
- SP2/0細胞である、請求項10に記載の宿主細胞。
- 前記抗体がキメラ抗ヒト腎細胞癌モノクローナル抗体chG250である、請求項13に記載の宿主細胞。
- GnTIIIをコードする前記少なくとも1つの遺伝子が前記宿主細胞染色体中に導入されている、請求項5に記載の宿主細胞。
- 前記内因性GnTIIIは、前記宿主細胞染色体中へのプロモーター要素、トランスポゾンまたはレトロウイルス要素の挿入により活性化されている、請求項6に記載の宿主細胞。
- 抗体分子、抗体フラグメントまたは免疫グロブリンのFc領域と等価の領域を含む融合タンパク質をコードする少なくとも1つのトランスフェクトされた核酸をさらに含む、請求項1に記載の宿主細胞。
- GnTIIIをコードする前記少なくとも1つの核酸が、構成プロモーター要素に作動可能に連結される、請求項1に記載の宿主細胞。
- 請求項17に記載の宿主細胞であって、該宿主細胞は、以下:抗CD20抗体、キメラ抗ヒト神経芽細胞腫モノクローナル抗体chCE7、キメラ抗ヒト腎細胞癌モノクローナル抗体chG250、キメラ抗ヒト結腸、肺および乳癌モノクローナル抗体ING−1、ヒト化抗ヒト17−1A抗原モノクローナル抗体3622W94、ヒト化抗ヒト結腸直腸腫瘍抗体A33、GD3ガングリオシドR24に対して向けられる抗ヒト黒色腫抗体、キメラ抗ヒト扁平上皮細胞癌モノクローナル抗体SF−25、抗ヒトEGFR抗体、抗ヒトEGFRvIII抗体、抗ヒトPSMA抗体、抗ヒトPSCA抗体、抗ヒトCD22抗体、抗ヒトCD30抗体、抗ヒトCD33抗体、抗ヒトCD38抗体、抗ヒトCD40抗体、抗ヒトCD45抗体、抗ヒトCD52抗体、抗ヒトCD138抗体、抗ヒトHLA−DR改変体抗体、抗ヒトEpCAM抗体、抗ヒトCEA抗体、抗ヒトMUC1抗体、抗ヒトMUC1コアタンパク質抗体、抗ヒト異常グリコシル化MUC1抗体、ED−Bドメインを含有するヒトフィブロネクチン改変体に対する抗体または抗ヒトHER2/neu抗体、
をコードする少なくとも1つのトランスフェクトされた核酸を含む、宿主細胞。 - 宿主細胞中でのポリペプチドの産生方法であって、該方法は、Fc媒介性細胞傷害性の増強を伴う前記ポリペプチドの産生を可能にする条件下で、請求項1〜19のいずれか一項記載の宿主細胞を培養する工程を包含する、方法。
- Fc媒介性細胞傷害性の増強を伴う前記ポリペプチドを単離する工程をさらに包含する、請求項20に記載の方法。
- 前記宿主細胞が、免疫グロブリンのFc領域と等価の領域を含む融合タンパク質をコードする少なくとも1つの核酸を含む、請求項20に記載の方法。
- 前記ポリペプチドのFc領域中の50%より多いオリゴ糖がバイセクトされる、請求項20に記載の方法。
- 前記ポリペプチドのFc領域中の70%より多いオリゴ糖がバイセクトされる、請求項20に記載の方法。
- Fc領域中のバイセクトハイブリッドオリゴ糖またはガラクトシル化複合オリゴ糖あるいはそれらの混合物の割合が、前記ポリペプチドのFc領域中のバイセクト複合オリゴ糖の割合より大きい、請求項20に記載の方法。
- 前記ポリペプチドは、抗CD20抗体IDEC−C2B8であり、前記宿主細胞により産生されるIDEC−C2B8抗体は、MALDI/TOF−MSにより分析した場合に、図2Eに示されるものと実質的に等価であるグリコシル化プロフィールを有する、請求項20に記載の方法。
- 前記ポリペプチドは、chG250モノクローナル抗体であり、前記宿主細胞により産生される前記chG250抗体は、MALDI/TOF−MSにより分析した場合に、図7Dに示されるものと実質的に等価であるグリコシル化プロフィールを有する、請求項20に記載の方法。
- 請求項21に記載の方法により産生される抗体依存性細胞傷害性(ADCC)の増強を伴う、抗体。
- IDEC−C2B8、chCE7、ch−G250、ヒト化抗HER2モノクローナル抗体、ING−1、3622W94、SF−25、A33およびR24から成る群から選択される、請求項28に記載の抗体。
- 免疫グロブリンのFc領域と等価の領域を含み、請求項21に記載の方法により産生されるFc媒介性細胞傷害性の増強を伴う、抗体フラグメント。
- 免疫グロブリンのFc領域と等価の領域を含み、かつ請求項21に記載の方法により産生されるFc媒介性細胞傷害性の増強を伴う、融合タンパク質。
- 請求項28に記載の抗体および薬学的に受容可能なキャリアを含む、薬学的組成物。
- 請求項30に記載の抗体フラグメントおよび薬学的に受容可能なキャリアを含む、薬学的組成物。
- 請求項31に記載の融合タンパク質および薬学的に受容可能なキャリアを含む、薬学的組成物。
- 請求項32〜34のいずれか一項に記載の処置上有効な量の薬学的組成物を、該薬学的組成物を必要とする患者に投与する工程を包含する、癌の処置方法。
- 処置上有効な量の抗体を、該抗体を必要とするヒト被験者に投与するこ工程を包含する、B細胞欠乏を基礎にした疾患処置の改良型方法であって、該改良が、請求項28に記載の方法により産生される処置上有効な量の抗体を投与する工程を包含する、改良型方法。
- 前記抗体が抗CD20モノクローナル抗体である、請求項36に記載の改良型方法。
- 前記抗CD20抗体がIDEC−C2B8である、請求項37に記載の改良型方法。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US30951601P | 2001-08-03 | 2001-08-03 | |
| PCT/US2002/024739 WO2003011878A2 (en) | 2001-08-03 | 2002-08-05 | Antibody glycosylation variants having increased antibody-dependent cellular cytotoxicity |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2008331038A Division JP2009114201A (ja) | 2001-08-03 | 2008-12-25 | 抗体依存性細胞傷害性の増強を伴う抗体グリコシル化改変体 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2005524379A true JP2005524379A (ja) | 2005-08-18 |
Family
ID=23198536
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2003517069A Pending JP2005524379A (ja) | 2001-08-03 | 2002-08-05 | 抗体依存性細胞傷害性の増強を伴う抗体グリコシル化改変体 |
| JP2008331038A Pending JP2009114201A (ja) | 2001-08-03 | 2008-12-25 | 抗体依存性細胞傷害性の増強を伴う抗体グリコシル化改変体 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2008331038A Pending JP2009114201A (ja) | 2001-08-03 | 2008-12-25 | 抗体依存性細胞傷害性の増強を伴う抗体グリコシル化改変体 |
Country Status (15)
| Country | Link |
|---|---|
| US (5) | US20030175884A1 (ja) |
| EP (2) | EP2180044A1 (ja) |
| JP (2) | JP2005524379A (ja) |
| KR (2) | KR20100018071A (ja) |
| CN (1) | CN1555411A (ja) |
| AU (1) | AU2002339845B2 (ja) |
| CA (2) | CA2838062C (ja) |
| HU (1) | HUP0700103A3 (ja) |
| IL (2) | IL160170A0 (ja) |
| MX (1) | MXPA04001072A (ja) |
| NO (1) | NO332457B1 (ja) |
| NZ (5) | NZ531219A (ja) |
| PL (1) | PL217751B1 (ja) |
| RU (1) | RU2321630C2 (ja) |
| WO (1) | WO2003011878A2 (ja) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2009526746A (ja) * | 2005-08-19 | 2009-07-23 | セントカー・インコーポレーテツド | タンパク質分解抵抗性の抗体調製物 |
| US8021856B2 (en) | 1998-04-20 | 2011-09-20 | Roche Glycart Ag | Antibody glycosylation variants having increased antibody-dependent cellular cytotoxicity |
Families Citing this family (918)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6136311A (en) | 1996-05-06 | 2000-10-24 | Cornell Research Foundation, Inc. | Treatment and diagnosis of cancer |
| ES2340112T3 (es) * | 1998-04-20 | 2010-05-28 | Glycart Biotechnology Ag | Ingenieria de glicosilacion de anticuerpos para la mejora de la citotoxicidad celular dependiente de anticuerpos. |
| DK1137789T3 (da) | 1998-12-09 | 2010-11-08 | Phyton Holdings Llc | Fremgangsmåde til fremstilling af et glycoprotein med glycosylering af human type |
| EP2204186B1 (en) | 1999-02-17 | 2016-04-06 | CSL Limited | Immunogenic complexes and methods relating thereto |
| NZ518532A (en) | 1999-10-26 | 2004-02-27 | Plant Res Internat B | Transgenic plant expressing mammalian beta-1,4- galactosyltransferase |
| AU5345901A (en) * | 2000-04-13 | 2001-10-30 | Univ Rockefeller | Enhancement of antibody-mediated immune responses |
| US7598055B2 (en) * | 2000-06-28 | 2009-10-06 | Glycofi, Inc. | N-acetylglucosaminyltransferase III expression in lower eukaryotes |
| EP2322644A1 (en) * | 2000-06-28 | 2011-05-18 | GlycoFi, Inc. | Methods for producing modified glycoproteins |
| US8697394B2 (en) * | 2000-06-28 | 2014-04-15 | Glycofi, Inc. | Production of modified glycoproteins having multiple antennary structures |
| US7449308B2 (en) | 2000-06-28 | 2008-11-11 | Glycofi, Inc. | Combinatorial DNA library for producing modified N-glycans in lower eukaryotes |
| CN100385006C (zh) | 2001-01-19 | 2008-04-30 | 陶氏化学公司 | 利用植物细胞分泌性生产具有人型糖链的糖蛋白的方法 |
| CA2442801A1 (en) * | 2001-04-02 | 2002-10-10 | Idec Pharmaceutical Corporation | Recombinant antibodies coexpressed with gntiii |
| CA2471092A1 (en) * | 2001-12-21 | 2003-07-10 | Antigenics Inc. | Compositions comprising immunoreactive reagents and saponins, and methods of use thereof |
| US8188231B2 (en) | 2002-09-27 | 2012-05-29 | Xencor, Inc. | Optimized FC variants |
| US20040132101A1 (en) | 2002-09-27 | 2004-07-08 | Xencor | Optimized Fc variants and methods for their generation |
| US7662925B2 (en) * | 2002-03-01 | 2010-02-16 | Xencor, Inc. | Optimized Fc variants and methods for their generation |
| US20080254027A1 (en) * | 2002-03-01 | 2008-10-16 | Bernett Matthew J | Optimized CD5 antibodies and methods of using the same |
| US7317091B2 (en) * | 2002-03-01 | 2008-01-08 | Xencor, Inc. | Optimized Fc variants |
| US20080260731A1 (en) * | 2002-03-01 | 2008-10-23 | Bernett Matthew J | Optimized antibodies that target cd19 |
| US20070148171A1 (en) * | 2002-09-27 | 2007-06-28 | Xencor, Inc. | Optimized anti-CD30 antibodies |
| AU2003219418B2 (en) | 2002-03-19 | 2008-02-28 | Stichting Dienst Landbouwkundig Onderzoek | Optimizing glycan processing in plants |
| NZ546945A (en) | 2002-03-19 | 2008-04-30 | Plant Res Int Bv | A plant host cell system for the expression of human GnTIII |
| US20060235208A1 (en) * | 2002-09-27 | 2006-10-19 | Xencor, Inc. | Fc variants with optimized properties |
| AR042145A1 (es) | 2002-11-27 | 2005-06-08 | Dow Agrociences Llc | Produccion de inmunoglobulinas en plantas con una fucocilacion reducida |
| EP1590437A4 (en) * | 2003-01-24 | 2008-06-18 | Agensys Inc | NUCLEIC ACIDS SUITABLE FOR THE TREATMENT AND DETECTION OF CANCER AND CORRESPONDING PROTEINS NAMED 254P1D6B |
| US7332299B2 (en) | 2003-02-20 | 2008-02-19 | Glycofi, Inc. | Endomannosidases in the modification of glycoproteins in eukaryotes |
| US8084582B2 (en) | 2003-03-03 | 2011-12-27 | Xencor, Inc. | Optimized anti-CD20 monoclonal antibodies having Fc variants |
| US20090010920A1 (en) * | 2003-03-03 | 2009-01-08 | Xencor, Inc. | Fc Variants Having Decreased Affinity for FcyRIIb |
| US20070275460A1 (en) * | 2003-03-03 | 2007-11-29 | Xencor.Inc. | Fc Variants With Optimized Fc Receptor Binding Properties |
| US8388955B2 (en) * | 2003-03-03 | 2013-03-05 | Xencor, Inc. | Fc variants |
| US9051373B2 (en) | 2003-05-02 | 2015-06-09 | Xencor, Inc. | Optimized Fc variants |
| AR044388A1 (es) | 2003-05-20 | 2005-09-07 | Applied Molecular Evolution | Moleculas de union a cd20 |
| US9714282B2 (en) | 2003-09-26 | 2017-07-25 | Xencor, Inc. | Optimized Fc variants and methods for their generation |
| US8101720B2 (en) | 2004-10-21 | 2012-01-24 | Xencor, Inc. | Immunoglobulin insertions, deletions and substitutions |
| EA036531B1 (ru) * | 2003-11-05 | 2020-11-19 | Роше Гликарт Аг | Гуманизированное антитело типа ii к cd20 (варианты), фармацевтическая композиция, содержащая эти варианты антитела, и их применение |
| WO2005077981A2 (en) * | 2003-12-22 | 2005-08-25 | Xencor, Inc. | Fc POLYPEPTIDES WITH NOVEL Fc LIGAND BINDING SITES |
| DE602005018325D1 (de) | 2004-02-19 | 2010-01-28 | Genentech Inc | Antikörper mit korrigierten cdr |
| TW200539855A (en) * | 2004-03-15 | 2005-12-16 | Wyeth Corp | Calicheamicin conjugates |
| AU2005227326B2 (en) * | 2004-03-24 | 2009-12-03 | Xencor, Inc. | Immunoglobulin variants outside the Fc region |
| JP2007532680A (ja) * | 2004-04-16 | 2007-11-15 | ジェネンテック・インコーポレーテッド | 疾患の治療方法 |
| BRPI0510915A (pt) | 2004-06-04 | 2007-11-13 | Genentech Inc | método para o tratamento da esclerose múltipla e artigo manufaturado |
| RU2427588C2 (ru) * | 2004-07-09 | 2011-08-27 | Чугаи Сейяку Кабусики Кайся | Антитело против глипикана 3 |
| US7759464B2 (en) | 2004-07-14 | 2010-07-20 | Greenovation Biotech Gmbh | N-glycosylated antibody |
| US20150010550A1 (en) | 2004-07-15 | 2015-01-08 | Xencor, Inc. | OPTIMIZED Fc VARIANTS |
| US20060074225A1 (en) * | 2004-09-14 | 2006-04-06 | Xencor, Inc. | Monomeric immunoglobulin Fc domains |
| CA2580271A1 (en) | 2004-10-05 | 2006-04-20 | Genentech, Inc. | Method for treating vasculitis |
| JO3000B1 (ar) | 2004-10-20 | 2016-09-05 | Genentech Inc | مركبات أجسام مضادة . |
| RU2451030C2 (ru) * | 2004-10-26 | 2012-05-20 | Чугаи Сейяку Кабусики Кайся | Анти-глипикан 3-антитело, имеющее модифицированную сахарную цепь |
| US8367805B2 (en) | 2004-11-12 | 2013-02-05 | Xencor, Inc. | Fc variants with altered binding to FcRn |
| US8546543B2 (en) | 2004-11-12 | 2013-10-01 | Xencor, Inc. | Fc variants that extend antibody half-life |
| DK2325207T3 (en) | 2004-11-12 | 2017-06-06 | Xencor Inc | Fc variants with altered binding to FcRn |
| US8802820B2 (en) | 2004-11-12 | 2014-08-12 | Xencor, Inc. | Fc variants with altered binding to FcRn |
| EP1858925A2 (en) * | 2005-01-12 | 2007-11-28 | Xencor, Inc. | Antibodies and fc fusion proteins with altered immunogenicity |
| CN102580084B (zh) | 2005-01-21 | 2016-11-23 | 健泰科生物技术公司 | Her抗体的固定剂量给药 |
| WO2006082515A2 (en) | 2005-02-07 | 2006-08-10 | Glycart Biotechnology Ag | Antigen binding molecules that bind egfr, vectors encoding same, and uses thereof |
| EP1848745B1 (en) * | 2005-02-18 | 2014-07-09 | Medarex, L.L.C. | Monoclonal antibodies against cd30 lacking in fucosyl residues |
| CN103251946A (zh) | 2005-02-23 | 2013-08-21 | 健泰科生物技术公司 | 使用her二聚化抑制剂在癌症患者中延长病情进展前时间或存活 |
| EP1871882A1 (en) * | 2005-03-25 | 2008-01-02 | GlycArt Biotechnology AG | Antigen binding molecules directed to mcsp and having increased fc receptor binding affinity and effector function |
| PA8672101A1 (es) | 2005-04-29 | 2006-12-07 | Centocor Inc | Anticuerpos anti-il-6, composiciones, métodos y usos |
| CN101228189A (zh) * | 2005-05-09 | 2008-07-23 | 格黎卡特生物技术股份公司 | 具有修饰的fc区域和改变的与fc受体的结合的抗原结合分子 |
| ZA200710496B (en) * | 2005-06-02 | 2009-04-29 | Astrazeneca Ab | Antibodies directed to CD20 and used thereof |
| AU2006255085A1 (en) * | 2005-06-03 | 2006-12-14 | Genentech, Inc. | Method of producing antibodies with modified fucosylation level |
| CN101252951B (zh) | 2005-06-30 | 2011-12-21 | 森托科尔公司 | 抗il-23抗体、组合物、方法和用途 |
| SG164379A1 (en) | 2005-07-21 | 2010-09-29 | Genmab As | Potency assays for antibody drug substance binding to an fc receptor |
| BRPI0615397B1 (pt) * | 2005-08-26 | 2023-10-03 | Roche Glycart Ag | Anticorpo anti-cd20, composição farmacêutica que o contém e uso do mesmo |
| CA2624189A1 (en) * | 2005-10-03 | 2007-04-12 | Xencor, Inc. | Fc variants with optimized fc receptor binding properties |
| JP4860703B2 (ja) * | 2005-10-06 | 2012-01-25 | ゼンコー・インコーポレイテッド | 最適化された抗cd30抗体 |
| US20070087005A1 (en) | 2005-10-14 | 2007-04-19 | Lazar Gregory A | Anti-glypican-3 antibody |
| MY149159A (en) | 2005-11-15 | 2013-07-31 | Hoffmann La Roche | Method for treating joint damage |
| CN105859886A (zh) | 2005-12-02 | 2016-08-17 | 健泰科生物技术公司 | 牵涉与il-22和il-22r结合的抗体的组合物和方法 |
| HUE034269T2 (en) | 2005-12-29 | 2018-02-28 | Janssen Biotech Inc | Human anti-IL-23 antibodies, preparations, methods and applications |
| DK1973950T3 (en) | 2006-01-05 | 2014-12-15 | Genentech Inc | ANTI-EphB4 ANTIBODIES AND METHODS FOR USING SAME |
| US20070166306A1 (en) * | 2006-01-17 | 2007-07-19 | Fey Georg H M | Anti-CD19 antibody composition and method |
| US7884264B2 (en) | 2006-01-17 | 2011-02-08 | Biolex Therapeutics, Inc. | Compositions and methods for inhibition of fucosyltransferase and xylosyltransferase expression in duckweed plants |
| EP2623986B1 (en) | 2006-02-10 | 2017-06-14 | Life Technologies Corporation | Labeling and detection of post translationally modified proteins |
| AR059851A1 (es) | 2006-03-16 | 2008-04-30 | Genentech Inc | Anticuerpos de la egfl7 y metodos de uso |
| US8940871B2 (en) | 2006-03-20 | 2015-01-27 | The Regents Of The University Of California | Engineered anti-prostate stem cell antigen (PSCA) antibodies for cancer targeting |
| RS53168B (en) | 2006-05-30 | 2014-06-30 | Genentech Inc. | Antibodies and Immunoconjugates and Their Use |
| CL2007001623A1 (es) | 2006-06-06 | 2008-01-18 | Genentech Inc | Anticuerpo anti-dll4; polinucleotido que lo codifica; vector y celula huesped que comprenden dicho polinucleotido; metodo para elaborar el anticuerpo e inmunojugado; metodo de deteccion de dll4 y metodo diagnostico de un trastorno asociado a dll4; composicion que comprende al anticuerpo. |
| CA2657681C (en) | 2006-07-14 | 2019-03-19 | Ac Immune S.A. | Humanized antibodies against beta amyloid protein |
| RS56986B1 (sr) | 2006-07-14 | 2018-05-31 | Ac Immune Sa | Humanizovana antitela na beta amiloid |
| AU2007275654A1 (en) | 2006-07-19 | 2008-01-24 | The Trustees Of The University Of Pennsylvania | WSX-1/p28 as a target for anti-inflammatory responses |
| AR062223A1 (es) | 2006-08-09 | 2008-10-22 | Glycart Biotechnology Ag | Moleculas de adhesion al antigeno que se adhieren a egfr, vectores que los codifican, y sus usos de estas |
| ES2457072T3 (es) | 2006-08-14 | 2014-04-24 | Xencor, Inc. | Anticuerpos optimizados que seleccionan como diana CD19 |
| MX346523B (es) | 2006-09-13 | 2017-03-23 | Abbvie Inc | Mejoras de cultivos celulares. |
| US8911964B2 (en) | 2006-09-13 | 2014-12-16 | Abbvie Inc. | Fed-batch method of making human anti-TNF-alpha antibody |
| CA2660795C (en) * | 2006-09-18 | 2014-11-18 | Xencor, Inc. | Optimized antibodies that target hm1.24 |
| CA2665644A1 (en) * | 2006-10-12 | 2008-05-29 | Genentech, Inc. | Antibodies to lymphotoxin-alpha |
| RS53942B1 (en) | 2006-10-27 | 2015-08-31 | Genentech Inc. | Antibodies and Immunoconjugates and Their Use |
| TWI447124B (zh) | 2006-12-01 | 2014-08-01 | Medarex Llc | 結合cd22的人類抗體與其應用 |
| BRPI0806403A2 (pt) | 2007-02-09 | 2011-09-06 | Genentech Inc | anticorpo anti-robo4, usode um anticorpo e método de obtenção de imagem |
| WO2008109440A2 (en) | 2007-03-02 | 2008-09-12 | Genentech, Inc. | Predicting response to a her dimerisation inhibitor based on low her3 expression |
| CN101679934B (zh) * | 2007-03-07 | 2014-04-02 | 格利科菲公司 | 具有经修饰的岩藻糖基化的糖蛋白的生产 |
| US7960139B2 (en) | 2007-03-23 | 2011-06-14 | Academia Sinica | Alkynyl sugar analogs for the labeling and visualization of glycoconjugates in cells |
| NZ580510A (en) | 2007-04-17 | 2011-06-30 | Stichting Dienst Landbouwkundi | Mammalian-type glycosylation in plants by expression of non-mammalian glycosyltransferases |
| WO2008143878A1 (en) | 2007-05-14 | 2008-11-27 | Medimmune, Llc | Methods of reducing eosinophil levels |
| ES2583377T3 (es) | 2007-06-08 | 2016-09-20 | Genentech, Inc. | Marcadores de expresión génica de la resistencia tumoral al tratamiento con inhibidor de HER2 |
| TWI557136B (zh) | 2007-06-12 | 2016-11-11 | Ac免疫公司 | 特異性結合β-類澱粉蛋白之抗體及相關核酸分子、表現載體、細胞、組合物、套組、方法及用途 |
| US7580304B2 (en) * | 2007-06-15 | 2009-08-25 | United Memories, Inc. | Multiple bus charge sharing |
| WO2008151440A1 (en) * | 2007-06-15 | 2008-12-18 | Medicago Inc. | Modifying glycoprotein production in plants |
| ES2751022T3 (es) | 2007-07-09 | 2020-03-30 | Genentech Inc | Prevención de la reducción de enlaces disulfuro durante la producción recombinante de polipéptidos |
| US8940298B2 (en) | 2007-09-04 | 2015-01-27 | The Regents Of The University Of California | High affinity anti-prostate stem cell antigen (PSCA) antibodies for cancer targeting and detection |
| MX342551B (es) | 2007-09-26 | 2016-10-04 | Chugai Pharmaceutical Co Ltd | Region constante de anticuerpo modificada. |
| ES2609918T3 (es) | 2007-10-05 | 2017-04-25 | Genentech, Inc. | Uso de anticuerpo anti-amiloide beta en enfermedades oculares |
| CN104888193A (zh) | 2007-11-07 | 2015-09-09 | 健泰科生物技术公司 | 用于治疗微生物病症的组合物和方法 |
| TWI468417B (zh) | 2007-11-30 | 2015-01-11 | Genentech Inc | 抗-vegf抗體 |
| AU2008342956A1 (en) * | 2007-12-21 | 2009-07-09 | Genentech, Inc. | Therapy of rituximab-refractory rheumatoid arthritis patients |
| WO2009080831A1 (en) * | 2007-12-26 | 2009-07-02 | Biotest Ag | Method of decreasing cytotoxic side-effects and improving efficacy of immunoconjugates |
| EP4098661A1 (en) | 2007-12-26 | 2022-12-07 | Xencor, Inc. | Fc variants with altered binding to fcrn |
| RU2547939C2 (ru) | 2007-12-26 | 2015-04-10 | Биотест Аг | Иммуноконъюгаты, направленные на cd138, и их применение |
| JP2011508738A (ja) * | 2007-12-26 | 2011-03-17 | バイオテスト・アクチエンゲゼルシヤフト | Cd138発現腫瘍細胞のターゲティングを向上させる方法及び剤 |
| MX341344B (es) * | 2007-12-26 | 2016-08-16 | Biotest Ag | Agentes dirigidos a cd138 y sus usos. |
| TWI472339B (zh) | 2008-01-30 | 2015-02-11 | Genentech Inc | 包含結合至her2結構域ii之抗體及其酸性變異體的組合物 |
| US20090269339A1 (en) * | 2008-04-29 | 2009-10-29 | Genentech, Inc. | Responses to immunizations in rheumatoid arthritis patients treated with a cd20 antibody |
| KR101054362B1 (ko) * | 2008-07-03 | 2011-08-05 | 재단법인 목암생명공학연구소 | 재조합 단백질의 푸코스 함량을 감소시키는 방법 |
| DK2318832T3 (da) | 2008-07-15 | 2014-01-20 | Academia Sinica | Glycan-arrays på PTFE-lignende aluminiumcoatede objektglas og relaterede fremgangsmåder |
| AR073295A1 (es) | 2008-09-16 | 2010-10-28 | Genentech Inc | Metodos para tratar la esclerosis multiple progresiva. articulo de fabricacion. |
| JP2012503656A (ja) * | 2008-09-26 | 2012-02-09 | エウレカ セラピューティクス,インコーポレイテッド | 変異体グリコシル化パターンを有する細胞株およびタンパク質 |
| CN110317272A (zh) | 2008-10-14 | 2019-10-11 | 霍夫曼-拉罗奇有限公司 | 免疫球蛋白变体及其用途 |
| SG195577A1 (en) | 2008-10-20 | 2013-12-30 | Abbott Lab | Viral inactivation during purification of antibodies |
| CN105111309A (zh) * | 2008-10-20 | 2015-12-02 | Abbvie公司 | 使用a蛋白亲和层析分离和纯化抗体 |
| HUE032693T2 (en) | 2008-11-22 | 2017-10-30 | Hoffmann La Roche | Use of anti-vegf antibody in combination with chemotherapy to treat breast cancer |
| AR074777A1 (es) | 2008-12-19 | 2011-02-09 | Glaxo Group Ltd | Proteinas de union a antigeno |
| WO2010075249A2 (en) | 2008-12-22 | 2010-07-01 | Genentech, Inc. | A method for treating rheumatoid arthritis with b-cell antagonists |
| KR20170143025A (ko) | 2008-12-23 | 2017-12-28 | 제넨테크, 인크. | 단백질 a에 대해 변경된 결합을 갖는 이뮤노글로불린 변이체 |
| EP3495000A1 (en) | 2009-02-17 | 2019-06-12 | Cornell Research Foundation, Inc. | Methods and kits for diagnosis of cancer and prediction of therapeutic value |
| EP2401696B1 (en) * | 2009-02-26 | 2017-06-21 | Intrexon CEU, Inc. | Mammalian cell line models and related methods |
| MA33198B1 (fr) | 2009-03-20 | 2012-04-02 | Genentech Inc | Anticorps anti-her di-spécifiques |
| US8124740B2 (en) | 2009-03-25 | 2012-02-28 | Genentech, Inc. | Anti- α5 β1 antibodies and uses thereof |
| CN102378767B (zh) | 2009-03-25 | 2015-01-14 | 健泰科生物技术公司 | 抗-fgfr3抗体及其使用方法 |
| MX345953B (es) * | 2009-05-06 | 2017-01-27 | Biotest Ag | Usos de inmunoconjugados dirigidos a cd138. |
| WO2010138184A2 (en) | 2009-05-27 | 2010-12-02 | Synageva Biopharma Corp. | Avian derived antibodies |
| US9676845B2 (en) | 2009-06-16 | 2017-06-13 | Hoffmann-La Roche, Inc. | Bispecific antigen binding proteins |
| US20100316639A1 (en) | 2009-06-16 | 2010-12-16 | Genentech, Inc. | Biomarkers for igf-1r inhibitor therapy |
| TW201106972A (en) | 2009-07-27 | 2011-03-01 | Genentech Inc | Combination treatments |
| SG178177A1 (en) | 2009-07-31 | 2012-03-29 | Genentech Inc | Inhibition of tumor metastasis using bv8- or g-csf-antagonists |
| LT2464725T (lt) | 2009-08-11 | 2020-06-10 | F. Hoffmann-La Roche Ag | Baltymų gamyba ląstelių mitybinėje terpėje, kurioje nėra glutamino |
| TW201431558A (zh) | 2009-08-15 | 2014-08-16 | 建南德克公司 | 用於治療先前治療過之乳癌之抗-血管新生療法 |
| TWI412375B (zh) * | 2009-08-28 | 2013-10-21 | Roche Glycart Ag | 人類化抗cdcp1抗體 |
| RU2570554C2 (ru) | 2009-08-31 | 2015-12-10 | Роше Гликарт Аг | Гуманизированные моноклональные антитела к сеа с созревшей аффинностью |
| WO2011028952A1 (en) | 2009-09-02 | 2011-03-10 | Xencor, Inc. | Compositions and methods for simultaneous bivalent and monovalent co-engagement of antigens |
| DK2473522T3 (en) | 2009-09-02 | 2016-11-28 | Genentech Inc | Smoothened MUTANT AND METHODS OF USING THE SAME |
| KR20120105447A (ko) | 2009-10-22 | 2012-09-25 | 제넨테크, 인크. | 항-헵신 항체 및 그의 사용 방법 |
| WO2011056497A1 (en) | 2009-10-26 | 2011-05-12 | Genentech, Inc. | Activin receptor type iib compositions and methods of use |
| WO2011056494A1 (en) | 2009-10-26 | 2011-05-12 | Genentech, Inc. | Activin receptor-like kinase-1 antagonist and vegfr3 antagonist combinations |
| WO2011056502A1 (en) | 2009-10-26 | 2011-05-12 | Genentech, Inc. | Bone morphogenetic protein receptor type ii compositions and methods of use |
| JP6007420B2 (ja) | 2009-11-04 | 2016-10-12 | ファブラス エルエルシー | 親和性成熟に基づく抗体最適化方法 |
| ES2636971T3 (es) | 2009-11-05 | 2017-10-10 | F. Hoffmann-La Roche Ag | Procedimientos y composición para la secreción de polipéptidos heterógenos |
| US10087236B2 (en) | 2009-12-02 | 2018-10-02 | Academia Sinica | Methods for modifying human antibodies by glycan engineering |
| US11377485B2 (en) | 2009-12-02 | 2022-07-05 | Academia Sinica | Methods for modifying human antibodies by glycan engineering |
| CA2782333C (en) | 2009-12-02 | 2019-06-04 | Imaginab, Inc. | J591 minibodies and cys-diabodies for targeting human prostate specific membrane antigen (psma) and methods for their use |
| TWI505836B (zh) | 2009-12-11 | 2015-11-01 | Genentech Inc | 抗-vegf-c抗體及其使用方法 |
| PL2516465T3 (pl) | 2009-12-23 | 2016-11-30 | Przeciwciała anty-bv8 i ich zastosowania | |
| US8362210B2 (en) | 2010-01-19 | 2013-01-29 | Xencor, Inc. | Antibody variants with enhanced complement activity |
| PE20170687A1 (es) | 2010-01-28 | 2017-06-13 | Glaxo Group Ltd | Proteinas de enlace a cd127 |
| CA2788758A1 (en) | 2010-02-09 | 2011-08-18 | Andrew Ian Bayliffe | Treatment of a metabolic disorder |
| RU2573994C2 (ru) | 2010-02-10 | 2016-01-27 | Иммьюноджен, Инк | Антитела против cd20 и их применение |
| WO2011101328A2 (en) | 2010-02-18 | 2011-08-25 | Roche Glycart Ag | Treatment with a humanized igg class anti egfr antibody and an antibody against insulin like growth factor 1 receptor |
| MX2012008958A (es) | 2010-02-18 | 2012-08-23 | Genentech Inc | Antagonista de neurogulina y usos de los mismos para el tratamiento contra el cancer. |
| KR20180028561A (ko) | 2010-02-23 | 2018-03-16 | 제넨테크, 인크. | 난소암의 치료를 위한 항혈관신생 요법 |
| UA108227C2 (xx) | 2010-03-03 | 2015-04-10 | Антигензв'язуючий білок | |
| BR112012022044A2 (pt) | 2010-03-24 | 2020-08-25 | Genentech Inc | ''anticorpo,imunoconjugado,formulação farmacêutica,uso do anticorpo,método de tratamento,anticorpo biespecifico isolado e célula hospedeira''. |
| US9441032B2 (en) | 2010-04-07 | 2016-09-13 | Agency For Science, Technology And Research | Binding molecules against Chikungunya virus and uses thereof |
| EP2374816B1 (en) | 2010-04-07 | 2016-09-28 | Agency For Science, Technology And Research | Binding molecules against Chikungunya virus and uses thereof |
| WO2011130332A1 (en) | 2010-04-12 | 2011-10-20 | Academia Sinica | Glycan arrays for high throughput screening of viruses |
| EP2568976B1 (en) | 2010-05-10 | 2015-09-30 | Academia Sinica | Zanamivir phosphonate congeners with anti-influenza activity and determining oseltamivir susceptibility of influenza viruses |
| WO2011146568A1 (en) | 2010-05-19 | 2011-11-24 | Genentech, Inc. | Predicting response to a her inhibitor |
| WO2011147834A1 (en) | 2010-05-26 | 2011-12-01 | Roche Glycart Ag | Antibodies against cd19 and uses thereof |
| WO2011153243A2 (en) | 2010-06-02 | 2011-12-08 | Genentech, Inc. | Anti-angiogenesis therapy for treating gastric cancer |
| AR081556A1 (es) | 2010-06-03 | 2012-10-03 | Glaxo Group Ltd | Proteinas de union al antigeno humanizadas |
| AU2011261362B2 (en) | 2010-06-03 | 2016-06-09 | Genentech, Inc. | Immuno-pet imaging of antibodies and immunoconjugates and uses therefor |
| CN103080136B (zh) | 2010-06-18 | 2015-08-12 | 霍夫曼-拉罗奇有限公司 | 抗Axl抗体及使用方法 |
| WO2011161119A1 (en) | 2010-06-22 | 2011-12-29 | F. Hoffmann-La Roche Ag | Antibodies against insulin-like growth factor i receptor and uses thereof |
| WO2011161189A1 (en) | 2010-06-24 | 2011-12-29 | F. Hoffmann-La Roche Ag | Anti-hepsin antibodies and methods of use |
| NZ605449A (en) | 2010-07-09 | 2015-03-27 | Genentech Inc | Anti-neuropilin antibodies and methods of use |
| EP2409993A1 (en) | 2010-07-19 | 2012-01-25 | International-Drug-Development-Biotech | Anti-CD19 antibody having ADCC function with improved glycosylation profile |
| EP2409989A1 (en) | 2010-07-19 | 2012-01-25 | International-Drug-Development-Biotech | Method to improve glycosylation profile for antibody |
| EP2409712A1 (en) | 2010-07-19 | 2012-01-25 | International-Drug-Development-Biotech | Anti-CD19 antibody having ADCC and CDC functions and improved glycosylation profile |
| WO2012010582A1 (en) | 2010-07-21 | 2012-01-26 | Roche Glycart Ag | Anti-cxcr5 antibodies and methods of use |
| JP2013538191A (ja) | 2010-07-23 | 2013-10-10 | トラスティーズ オブ ボストン ユニバーシティ | 病的血管新生および腫瘍細胞侵襲性の阻害のための治療法としてならびに分子イメージングおよび標的化送達のための抗DEsupR阻害剤 |
| BR112013002535A2 (pt) | 2010-08-03 | 2019-09-24 | Hoffmann La Roche | biomarcadores de leucemia linfocítica crônica (cll) |
| RU2013106217A (ru) | 2010-08-05 | 2014-09-10 | Ф. Хоффманн-Ля Рош Аг | Гибридный белок из антитела против мнс и противовирусного цитокина |
| MX2013001336A (es) | 2010-08-13 | 2013-03-08 | Roche Glycart Ag | Anticuerpos ani-tenascina c a2 y metodos de utilizacion. |
| AU2011288487B2 (en) | 2010-08-13 | 2015-10-01 | Roche Glycart Ag | Anti-FAP antibodies and methods of use |
| EP2609117B1 (en) | 2010-08-25 | 2015-09-16 | F.Hoffmann-La Roche Ag | Antibodies against il-18r1 and uses thereof |
| DK2612151T3 (en) | 2010-08-31 | 2017-10-02 | Genentech Inc | BIOMARKETS AND METHODS OF TREATMENT |
| AU2011312205B2 (en) | 2010-10-05 | 2015-08-13 | Curis, Inc. | Mutant smoothened and methods of using the same |
| CN104998254A (zh) | 2010-11-08 | 2015-10-28 | 基因技术公司 | 皮下施用的抗-il-6受体抗体 |
| JP6163429B2 (ja) | 2010-11-10 | 2017-07-12 | ジェネンテック, インコーポレイテッド | 神経疾患免疫治療のための方法及び組成物 |
| LT2643352T (lt) | 2010-11-23 | 2018-08-10 | Glaxo Group Limited | Antigeną onkostatiną m (osm) surišantys baltymai |
| KR20130121886A (ko) | 2010-11-24 | 2013-11-06 | 글락소 그룹 리미티드 | Hgf를 표적으로 하는 다중특이적 항원 결합 단백질 |
| ES2631356T3 (es) | 2010-11-30 | 2017-08-30 | F. Hoffmann-La Roche Ag | Anticuerpos anti-receptor de transferrina de baja afinidad y su uso para transferir scFv terapéuticos a través de la barrera hematoencefálica |
| NZ609493A (en) | 2010-12-16 | 2015-11-27 | Genentech Inc | Diagnosis and treatments relating to th2 inhibition |
| EA028744B1 (ru) | 2010-12-20 | 2017-12-29 | Дженентек, Инк. | Антитела против мезотелина и иммуноконъюгаты |
| KR20130118925A (ko) | 2010-12-22 | 2013-10-30 | 제넨테크, 인크. | 항-pcsk9 항체 및 사용 방법 |
| WO2012092539A2 (en) | 2010-12-31 | 2012-07-05 | Takeda Pharmaceutical Company Limited | Antibodies to dll4 and uses thereof |
| EP2482074A1 (en) * | 2011-01-27 | 2012-08-01 | Medizinische Hochschule Hannover | Methods and means for diagnosing vasculitis |
| EP2672999A2 (en) | 2011-02-10 | 2013-12-18 | Roche Glycart AG | Improved immunotherapy |
| LT3489255T (lt) | 2011-02-10 | 2021-08-25 | Roche Glycart Ag | Mutantiniai interleukino-2 polipeptidai |
| CA2824824A1 (en) | 2011-02-28 | 2012-09-07 | F. Hoffmann-La Roche Ag | Monovalent antigen binding proteins |
| CA2825081A1 (en) | 2011-02-28 | 2012-09-07 | Birgit Bossenmaier | Antigen binding proteins |
| PL2681244T3 (pl) | 2011-03-02 | 2018-04-30 | Roche Glycart Ag | Przeciwciała przeciwko antygenowi rakowo-płodowemu |
| RU2013143358A (ru) | 2011-04-07 | 2015-05-20 | Дженентек, Инк. | Анти-fgfr4 антитела и способы их применения |
| EP2702077A2 (en) | 2011-04-27 | 2014-03-05 | AbbVie Inc. | Methods for controlling the galactosylation profile of recombinantly-expressed proteins |
| EA201892619A1 (ru) | 2011-04-29 | 2019-04-30 | Роше Гликарт Аг | Иммуноконъюгаты, содержащие мутантные полипептиды интерлейкина-2 |
| WO2012146630A1 (en) | 2011-04-29 | 2012-11-01 | F. Hoffmann-La Roche Ag | N-terminal acylated polypeptides, methods for their production and uses thereof |
| MX2013013054A (es) | 2011-05-12 | 2014-02-20 | Genentech Inc | Metodo de monitoreo de lc-ms/ms de reaccion multiple para detectar anticuerpos terapeuticos en muestras de animales utilizando peptidos de firma de estructura. |
| PE20140995A1 (es) | 2011-05-16 | 2014-08-23 | Genentech Inc | Agonistas de fgfr1 y sus metodos de uso |
| MX351069B (es) | 2011-05-27 | 2017-09-29 | Glaxo Group Ltd | Proteinas de union abcma (cd269/tnfrsf17). |
| BR112013032235A2 (pt) | 2011-06-15 | 2016-11-22 | Hoffmann La Roche | anticorpos do receptor de epo anti-humano e métodos de uso |
| MX354663B (es) | 2011-06-22 | 2018-03-14 | Hoffmann La Roche | Eliminación de células diana por parte de células t citotóxicas específicas de virus utilizando complejos que comprenden mhc de clase i. |
| AR086823A1 (es) | 2011-06-30 | 2014-01-22 | Genentech Inc | Formulaciones de anticuerpo anti-c-met, metodos |
| US20130022551A1 (en) | 2011-07-22 | 2013-01-24 | Trustees Of Boston University | DEspR ANTAGONISTS AND AGONISTS AS THERAPEUTICS |
| CN103842380A (zh) | 2011-07-27 | 2014-06-04 | 葛兰素集团有限公司 | 融合至Fc结构域的抗VEGF单可变结构域 |
| RU2014109985A (ru) | 2011-08-17 | 2015-09-27 | Дженентек, Инк. | Ингибирование ангиогенеза в рефрактерных опухолях |
| CA2842375A1 (en) | 2011-08-17 | 2013-02-21 | Erica Jackson | Neuregulin antibodies and uses thereof |
| BR112014003999A2 (pt) | 2011-08-23 | 2017-06-13 | Roche Glycart Ag | anticorpo isolado que se liga a um epítopo próximo da membrana de mcsp humano, ácido nucleico isolado, célula hospedeira, método de produção de um anticorpo, imunoconjugado, formulação farmacêutica, uso do anticorpo, método de tratamento de indivíduos portadores de câncer, método de undução da lise celular em indivíduos e teste imuno-histoquímico de mcsp |
| LT2748202T (lt) | 2011-08-23 | 2018-09-25 | Roche Glycart Ag | Bispecifinės antigeną surišančios molekulės |
| MX2014003094A (es) | 2011-09-15 | 2014-04-25 | Genentech Inc | Metodos para promover diferenciacion. |
| CN103930111A (zh) | 2011-09-19 | 2014-07-16 | 霍夫曼-拉罗奇有限公司 | 包含c-met拮抗剂和b-raf拮抗剂的组合治疗 |
| US9663573B2 (en) | 2011-10-05 | 2017-05-30 | Genentech, Inc. | Methods of treating liver conditions using Notch2 antagonists |
| US9738727B2 (en) | 2011-10-14 | 2017-08-22 | Genentech, Inc. | Anti-HtrA1 antibodies and methods of use |
| CA2851053A1 (en) | 2011-10-19 | 2013-04-25 | Roche Glycart Ag | Separation method for fucosylated antibodies |
| WO2013059531A1 (en) | 2011-10-20 | 2013-04-25 | Genentech, Inc. | Anti-gcgr antibodies and uses thereof |
| SG11201401815XA (en) | 2011-10-28 | 2014-05-29 | Genentech Inc | Therapeutic combinations and methods of treating melanoma |
| RU2014124842A (ru) | 2011-11-21 | 2015-12-27 | Дженентек, Инк. | Очистка анти-с-мет антител |
| EP2788024A1 (en) | 2011-12-06 | 2014-10-15 | F.Hoffmann-La Roche Ag | Antibody formulation |
| ES2684950T3 (es) | 2011-12-08 | 2018-10-05 | Biotest Ag | Usos de inmunoconjugados dirigidos a CD138 |
| WO2013092743A2 (en) | 2011-12-22 | 2013-06-27 | F. Hoffmann-La Roche Ag | Expression vector element combinations, novel production cell generation methods and their use for the recombinant production of polypeptides |
| CA2853955C (en) | 2011-12-22 | 2021-09-28 | F. Hoffmann-La Roche Ag | Expression vector organization, novel production cell generation methods and their use for the recombinant production of polypeptides |
| BR112014013035A2 (pt) | 2011-12-22 | 2018-10-09 | Hoffmann La Roche | métodos de seleção de células, conjuntos de expressão bicistrônica, células eucarióticas, vetores lentivirais, uso de vetor lentiviral, bibliotecas de ventores lentivirais e de células eucarióticas, métodos de seleção de células, fluxos de trabalho e uso de célula |
| AR089434A1 (es) | 2011-12-23 | 2014-08-20 | Genentech Inc | Procedimiento para preparar formulaciones con alta concentracion de proteinas |
| WO2013101771A2 (en) | 2011-12-30 | 2013-07-04 | Genentech, Inc. | Compositions and method for treating autoimmune diseases |
| CN104411717A (zh) | 2012-01-09 | 2015-03-11 | 斯克利普斯研究所 | 具有超长cdr3s的人源化抗体 |
| AU2013208003B2 (en) | 2012-01-09 | 2017-12-14 | The Scripps Research Institute | Ultralong complementarity determining regions and uses thereof |
| WO2013109856A2 (en) | 2012-01-18 | 2013-07-25 | Genentech, Inc. | Methods of using fgf19 modulators |
| JP6242813B2 (ja) | 2012-01-18 | 2017-12-06 | ジェネンテック, インコーポレイテッド | 抗lrp5抗体及び使用方法 |
| WO2013113641A1 (en) | 2012-01-31 | 2013-08-08 | Roche Glycart Ag | Use of nkp46 as a predictive biomarker for cancer treatment with adcc- enhanced antibodies |
| CN113398268A (zh) | 2012-02-11 | 2021-09-17 | 霍夫曼-拉罗奇有限公司 | R-spondin易位及其使用方法 |
| WO2013120929A1 (en) | 2012-02-15 | 2013-08-22 | F. Hoffmann-La Roche Ag | Fc-receptor based affinity chromatography |
| KR20140130455A (ko) | 2012-03-02 | 2014-11-10 | 로슈 글리카트 아게 | Adcc-강화 항체를 사용한 암 치료용 예측 바이오마커 |
| AU2013240261A1 (en) | 2012-03-27 | 2014-09-18 | Genentech, Inc. | Diagnosis and treatments relating to HER3 inhibitors |
| AR090549A1 (es) | 2012-03-30 | 2014-11-19 | Genentech Inc | Anticuerpos anti-lgr5 e inmunoconjugados |
| US10130714B2 (en) | 2012-04-14 | 2018-11-20 | Academia Sinica | Enhanced anti-influenza agents conjugated with anti-inflammatory activity |
| US9181572B2 (en) | 2012-04-20 | 2015-11-10 | Abbvie, Inc. | Methods to modulate lysine variant distribution |
| WO2013158279A1 (en) | 2012-04-20 | 2013-10-24 | Abbvie Inc. | Protein purification methods to reduce acidic species |
| US9067990B2 (en) | 2013-03-14 | 2015-06-30 | Abbvie, Inc. | Protein purification using displacement chromatography |
| WO2013165940A1 (en) | 2012-05-01 | 2013-11-07 | Genentech, Inc. | Anti-pmel17 antibodies and immunoconjugates |
| WO2013170191A1 (en) | 2012-05-11 | 2013-11-14 | Genentech, Inc. | Methods of using antagonists of nad biosynthesis from nicotinamide |
| SG11201407512VA (en) | 2012-05-18 | 2014-12-30 | Genentech Inc | High-concentration monoclonal antibody formulations |
| MX2014014166A (es) | 2012-05-21 | 2015-03-03 | Genentech Inc | Metodos para mejorar la seguridad del transporte de la barrera hematoencefalica. |
| EP2852610B1 (en) | 2012-05-23 | 2018-07-11 | Glykos Finland Oy | Production of fucosylated glycoproteins |
| EP2852840B1 (en) | 2012-05-23 | 2019-10-09 | F.Hoffmann-La Roche Ag | Selection method for therapeutic agents |
| US9249182B2 (en) | 2012-05-24 | 2016-02-02 | Abbvie, Inc. | Purification of antibodies using hydrophobic interaction chromatography |
| CN103463633B (zh) * | 2012-06-07 | 2016-03-30 | 复旦大学 | 一种靶向的嵌合乙肝核心抗原治疗性疫苗及其用途 |
| WO2013188855A1 (en) | 2012-06-15 | 2013-12-19 | Genentech, Inc. | Anti-pcsk9 antibodies, formulations, dosing, and methods of use |
| WO2014004549A2 (en) | 2012-06-27 | 2014-01-03 | Amgen Inc. | Anti-mesothelin binding proteins |
| RU2630664C2 (ru) | 2012-07-04 | 2017-09-11 | Ф. Хоффманн-Ля Рош Аг | Антитела к теофиллину и способы их применения |
| RU2630296C2 (ru) | 2012-07-04 | 2017-09-06 | Ф. Хоффманн-Ля Рош Аг | Антитела к биотину и способы их применения |
| SG11201407420RA (en) | 2012-07-04 | 2015-02-27 | Hoffmann La Roche | Covalently linked antigen-antibody conjugates |
| CA3188124A1 (en) | 2012-07-05 | 2014-01-09 | Genentech, Inc. | Expression and secretion system |
| EA201590172A1 (ru) | 2012-07-09 | 2015-09-30 | Дженентек, Инк. | ИММУНОКОНЪЮГАТЫ, СОДЕРЖАЩИЕ АНТИТЕЛА К CD79b |
| IN2014DN10652A (ja) | 2012-07-09 | 2015-09-11 | Genentech Inc | |
| PE20150325A1 (es) | 2012-07-09 | 2015-03-05 | Genentech Inc | Inmunoconjugados que comprenden anticuerpos anti-cd22 y derivados de nemorrubicina. |
| AU2013288929A1 (en) | 2012-07-09 | 2014-12-04 | Genentech, Inc. | Immunoconjugates comprising anti-CD22 antibodies |
| WO2014009465A1 (en) | 2012-07-13 | 2014-01-16 | Roche Glycart Ag | Bispecific anti-vegf/anti-ang-2 antibodies and their use in the treatment of ocular vascular diseases |
| BR112015001459B1 (pt) | 2012-07-25 | 2023-02-14 | Celldex Therapeutics, Inc | Anticorpo isolado ou fragmento do mesmo, conjugado, usos dos mesmos, composição farmacêutica, polinucleotídeo, vetor, célula hospedeira, célula isolada, kit, método in vitro para inibir atividade da kit, método para produzir um anticorpo |
| MY175687A (en) | 2012-08-07 | 2020-07-06 | Roche Glycart Ag | Composition comprising two antibodies engineered to have reduced and increased effector function |
| AU2013306098A1 (en) | 2012-08-18 | 2015-02-12 | Academia Sinica | Cell-permeable probes for identification and imaging of sialidases |
| EP2888238A4 (en) | 2012-08-21 | 2016-01-27 | Academia Sinica | BENZOCYCLO-OCTYNE COMPOUNDS AND USES THEREOF |
| WO2014029752A1 (en) | 2012-08-22 | 2014-02-27 | Glaxo Group Limited | Anti lrp6 antibodies |
| EP3315514A1 (en) | 2012-08-29 | 2018-05-02 | F. Hoffmann-La Roche AG | Blood brain barrier shuttle |
| US9512214B2 (en) | 2012-09-02 | 2016-12-06 | Abbvie, Inc. | Methods to control protein heterogeneity |
| AU2013309506A1 (en) | 2012-09-02 | 2015-03-12 | Abbvie Inc. | Methods to control protein heterogeneity |
| NZ630166A (en) | 2012-09-07 | 2017-01-27 | Genentech Inc | Combination therapy of a type ii anti-cd20 antibody with a selective bcl-2 inhibitor |
| LT2839860T (lt) | 2012-10-12 | 2019-07-10 | Medimmune Limited | Pirolobenzodiazepinai ir jų konjugatai |
| WO2014070786A1 (en) | 2012-10-29 | 2014-05-08 | The University Of North Carolina At Chapel Hill | Compositions and methods for inhibiting pathogen infection |
| EP2914621B1 (en) | 2012-11-05 | 2023-06-07 | Foundation Medicine, Inc. | Novel ntrk1 fusion molecules and uses thereof |
| AR093378A1 (es) | 2012-11-08 | 2015-06-03 | Hoffmann La Roche | PROTEINAS LIGANTES DE ANTIGENO HER3 DE UNION A LA HORQUILLA b DE HER3 |
| EA201892509A1 (ru) | 2012-11-13 | 2019-04-30 | Дженентек, Инк. | Антитела к гемагглютинину и способы применения |
| WO2014096015A1 (en) | 2012-12-21 | 2014-06-26 | F. Hoffmann-La Roche Ag | Disulfide-linked multivalent mhc class i comprising multi-function proteins |
| CA2898326C (en) | 2013-01-18 | 2022-05-17 | Foundation Medicine, Inc. | Methods of treating cholangiocarcinoma |
| WO2014116749A1 (en) | 2013-01-23 | 2014-07-31 | Genentech, Inc. | Anti-hcv antibodies and methods of using thereof |
| WO2014114595A1 (en) | 2013-01-23 | 2014-07-31 | Roche Glycart Ag | Predictive biomarker for cancer treatment with adcc-enhanced antibodies |
| ES2755181T3 (es) | 2013-02-13 | 2020-04-21 | Lab Francais Du Fractionnement | Anticuerpos anti-TNF-alfa altamente galactosilados y usos de los mismos |
| WO2014140927A2 (en) | 2013-02-13 | 2014-09-18 | Laboratoire Francais Du Fractionnement Et Des Biotechnologies | Proteins with modified glycosylation and methods of production thereof |
| CA2900097A1 (en) | 2013-02-22 | 2014-08-28 | F. Hoffmann-La Roche Ag | Methods of treating cancer and preventing drug resistance |
| US20140242083A1 (en) | 2013-02-26 | 2014-08-28 | Roche Glycart Ag | Anti-mcsp antibodies |
| EP2964260A2 (en) | 2013-03-06 | 2016-01-13 | F. Hoffmann-La Roche AG | Methods of treating and preventing cancer drug resistance |
| WO2014143205A1 (en) | 2013-03-12 | 2014-09-18 | Abbvie Inc. | Human antibodies that bind human tnf-alpha and methods of preparing the same |
| CA2905181C (en) | 2013-03-13 | 2020-06-02 | Medimmune Limited | Pyrrolobenzodiazepines and conjugates thereof for providing targeted therapy |
| JP6436965B2 (ja) | 2013-03-14 | 2018-12-12 | ジェネンテック, インコーポレイテッド | 抗b7−h4抗体及びイムノコンジュゲート |
| US9562099B2 (en) | 2013-03-14 | 2017-02-07 | Genentech, Inc. | Anti-B7-H4 antibodies and immunoconjugates |
| US9499614B2 (en) | 2013-03-14 | 2016-11-22 | Abbvie Inc. | Methods for modulating protein glycosylation profiles of recombinant protein therapeutics using monosaccharides and oligosaccharides |
| BR112015022576A2 (pt) | 2013-03-14 | 2017-10-24 | Genentech Inc | produto farmacêutico e seu uso, kit e método para tratar uma disfunção hiperproliferativa |
| WO2014159579A1 (en) | 2013-03-14 | 2014-10-02 | Abbvie Inc. | MUTATED ANTI-TNFα ANTIBODIES AND METHODS OF THEIR USE |
| CN105307683A (zh) | 2013-03-14 | 2016-02-03 | 基因泰克公司 | 治疗癌症和预防癌症药物抗性的方法 |
| US9017687B1 (en) | 2013-10-18 | 2015-04-28 | Abbvie, Inc. | Low acidic species compositions and methods for producing and using the same using displacement chromatography |
| BR112015023203A8 (pt) | 2013-03-15 | 2018-01-23 | Constellation Pharmaceuticals Inc | métodos para tratamento de câncer, método para aumentar a eficiência de um tratamento de câncer, método para retardar e/ou prevenir o desenvolvimento de câncer, método para tratar um indivíduo com câncer, método para aumentar a sensibilidade para um agente de terapia para câncer, método para estender um período de sensibilidade e método para estender a duração da resposta para uma terapia para câncer. |
| KR20150128707A (ko) | 2013-03-15 | 2015-11-18 | 제넨테크, 인크. | 간암의 진단 및 치료를 위한 조성물 및 방법 |
| PL2970464T3 (pl) | 2013-03-15 | 2020-10-05 | Glaxosmithkline Intellectual Property Development Limited | Wiążące białka anty-lag-3 |
| BR112015023120A2 (pt) | 2013-03-15 | 2017-11-21 | Genentech Inc | método para identificar um indivíduo com uma doença ou disfunção, método para prever a responsividade de um indivíduo com uma doença ou disfunção, método para determinar a probabilidade de que um indivíduo com uma doença ou disfunção exibirá benefício do tratamento, método para selecionar uma terapia, usos de um antagonista de ligação do eixo pd-l1, ensaio para identificar um indivíduo com uma doença, kit de diagnóstico, método para avaliar uma resposta ao tratamento e método para monitorar a resposta de um indivíduo tratado |
| CN105143265A (zh) | 2013-03-15 | 2015-12-09 | 豪夫迈·罗氏有限公司 | 抗CRTh2抗体及其用途 |
| US9598485B2 (en) | 2013-03-15 | 2017-03-21 | Ac Immune S.A. | Anti-tau antibodies and methods of use |
| PE20151673A1 (es) | 2013-03-15 | 2015-11-27 | Genentech Inc | POLIPEPTIDOS DE IL-22 Y PROTEINAS DE FUSION DE IL-22 Fc Y METODOS DE USO |
| UA118028C2 (uk) | 2013-04-03 | 2018-11-12 | Рош Глікарт Аг | Біспецифічне антитіло, специфічне щодо fap і dr5, антитіло, специфічне щодо dr5, і спосіб їх застосування |
| AU2014261630B2 (en) | 2013-04-29 | 2019-05-09 | F. Hoffmann-La Roche Ag | Human FcRn-binding modified antibodies and methods of use |
| CN105164158A (zh) | 2013-04-29 | 2015-12-16 | 豪夫迈·罗氏有限公司 | 消除对FcRn-结合的抗-IGF-1R抗体及其在血管性眼病治疗中的用途 |
| RU2019108429A (ru) | 2013-04-29 | 2019-05-06 | Ф. Хоффманн-Ля Рош Аг | Модифицированные асимметричные антитела, связывающие fc-рецептор, и способы их применения |
| JP6612214B2 (ja) | 2013-05-20 | 2019-11-27 | ジェネンテック, インコーポレイテッド | 抗トランスフェリン受容体抗体及び使用方法 |
| EP3013365B1 (en) | 2013-06-26 | 2019-06-05 | Academia Sinica | Rm2 antigens and use thereof |
| WO2014210564A1 (en) | 2013-06-27 | 2014-12-31 | Academia Sinica | Glycan conjugates and use thereof |
| AU2014290361B2 (en) | 2013-07-18 | 2019-04-18 | Taurus Biosciences, Llc | Humanized antibodies with ultralong complementarity determining regions |
| EP3022224A2 (en) | 2013-07-18 | 2016-05-25 | Fabrus, Inc. | Antibodies with ultralong complementarity determining regions |
| LT3708583T (lt) | 2013-08-01 | 2022-04-11 | Five Prime Therapeutics, Inc. | Afukozilinti anti-fgfr2iiib antikūnai |
| EA201690213A1 (ru) | 2013-08-12 | 2016-07-29 | Дженентек, Инк. | Композиции и способ лечения связанных с комплементом состояний |
| CN105682666B (zh) | 2013-09-06 | 2021-06-01 | 中央研究院 | 使用醣脂激活人类iNKT细胞 |
| MX2016003248A (es) | 2013-09-17 | 2016-06-07 | Genentech Inc | Metodos de uso de anticuerpos anti-lgr5. |
| WO2015051293A2 (en) | 2013-10-04 | 2015-04-09 | Abbvie, Inc. | Use of metal ions for modulation of protein glycosylation profiles of recombinant proteins |
| MX2016003593A (es) | 2013-10-11 | 2016-06-02 | Hoffmann La Roche | Anticuerpos de cadena ligera variable comun intercambiada de dominio multiespecifico. |
| JP6502931B2 (ja) | 2013-10-11 | 2019-04-17 | アメリカ合衆国 | Tem8抗体およびその使用 |
| BR112016007635A2 (pt) | 2013-10-11 | 2017-09-12 | Genentech Inc | inibidores de nsp4 e métodos de uso |
| US8946395B1 (en) | 2013-10-18 | 2015-02-03 | Abbvie Inc. | Purification of proteins using hydrophobic interaction chromatography |
| CA2925598A1 (en) | 2013-10-18 | 2015-04-23 | Genentech, Inc. | Anti-rspo antibodies and methods of use |
| US9181337B2 (en) | 2013-10-18 | 2015-11-10 | Abbvie, Inc. | Modulated lysine variant species compositions and methods for producing and using the same |
| US9085618B2 (en) | 2013-10-18 | 2015-07-21 | Abbvie, Inc. | Low acidic species compositions and methods for producing and using the same |
| MX2016005159A (es) | 2013-10-23 | 2016-07-05 | Genentech Inc | Metodos de diagnostico y tratamiento de trastornos eosinofilicos. |
| WO2015073884A2 (en) | 2013-11-15 | 2015-05-21 | Abbvie, Inc. | Glycoengineered binding protein compositions |
| SI3071597T1 (sl) | 2013-11-21 | 2020-11-30 | F. Hoffmann-La Roche Ag | Anti alfa-sinukleinska protitelesa in postopki uporabe |
| CN114044825A (zh) | 2013-12-09 | 2022-02-15 | 爱乐科斯公司 | 抗Siglec-8抗体及其使用方法 |
| CA2931340A1 (en) | 2013-12-13 | 2015-06-18 | Genentech, Inc. | Anti-cd33 antibodies and immunoconjugates |
| US20160333063A1 (en) | 2013-12-13 | 2016-11-17 | The General Hospital Corporation | Soluble high molecular weight (hmw) tau species and applications thereof |
| PE20210107A1 (es) | 2013-12-17 | 2021-01-19 | Genentech Inc | Anticuerpos anti-cd3 y metodos de uso |
| US20150190506A1 (en) | 2013-12-17 | 2015-07-09 | Genentech, Inc. | Combination therapy comprising ox40 binding agonists and pd-1 axis binding antagonists |
| US20150210772A1 (en) | 2013-12-17 | 2015-07-30 | Genentech, Inc. | Methods of treating cancer using pd-1 axis binding antagonists and an anti-cd20 antibody |
| AU2014364601A1 (en) | 2013-12-17 | 2016-07-07 | Genentech, Inc. | Methods of treating HER2-positive cancers using PD-1 axis binding antagonists and anti-HER2 antibodies |
| TWI728373B (zh) | 2013-12-23 | 2021-05-21 | 美商建南德克公司 | 抗體及使用方法 |
| CN112142843A (zh) | 2013-12-24 | 2020-12-29 | 阿尔金克斯有限公司 | FcRn拮抗剂及使用方法 |
| KR102278429B1 (ko) | 2014-01-03 | 2021-07-16 | 에프. 호프만-라 로슈 아게 | 공유 연결된 폴리펩티드 독소-항체 콘쥬게이트 |
| KR20160104628A (ko) | 2014-01-03 | 2016-09-05 | 에프. 호프만-라 로슈 아게 | 이중특이성 항-합텐/항-혈액뇌장벽 수용체 항체, 그의 복합체 및 혈액뇌장벽 셔틀로서 그의 용도 |
| WO2015103549A1 (en) | 2014-01-03 | 2015-07-09 | The United States Of America, As Represented By The Secretary Department Of Health And Human Services | Neutralizing antibodies to hiv-1 env and their use |
| CN105873615B (zh) | 2014-01-03 | 2020-12-25 | 豪夫迈·罗氏有限公司 | 共价连接的helicar-抗helicar抗体缀合物及其用途 |
| CA2932547C (en) | 2014-01-06 | 2023-05-23 | F. Hoffmann-La Roche Ag | Monovalent blood brain barrier shuttle modules |
| KR20160107190A (ko) | 2014-01-15 | 2016-09-13 | 에프. 호프만-라 로슈 아게 | 변형된 FcRn-결합 및 유지된 단백질 A-결합 성질을 갖는 Fc-영역 변이체 |
| EP3094352B1 (en) | 2014-01-16 | 2020-09-23 | Academia Sinica | Compositions and methods for treatment and detection of cancers |
| US10150818B2 (en) | 2014-01-16 | 2018-12-11 | Academia Sinica | Compositions and methods for treatment and detection of cancers |
| KR20160111469A (ko) | 2014-01-24 | 2016-09-26 | 제넨테크, 인크. | 항-steap1 항체 및 면역접합체를 사용하는 방법 |
| CA2937539A1 (en) | 2014-02-04 | 2015-08-13 | Genentech, Inc. | Mutant smoothened and methods of using the same |
| TWI705824B (zh) | 2014-02-08 | 2020-10-01 | 美商建南德克公司 | 治療阿茲海默症之方法 |
| ES2873248T3 (es) | 2014-02-08 | 2021-11-03 | Hoffmann La Roche | Métodos para tratar la enfermedad de Alzheimer |
| SG10201808259TA (en) | 2014-02-12 | 2018-10-30 | Genentech Inc | Anti-jagged1 antibodies and methods of use |
| EP3107574A2 (en) | 2014-02-21 | 2016-12-28 | F. Hoffmann-La Roche AG | Anti-il-13/il-17 bispecific antibodies and uses thereof |
| DK3110446T3 (da) | 2014-02-28 | 2022-02-28 | Allakos Inc | Fremgangsmåder og sammensætninger til behandling af Siglec-8-associerede sygdomme |
| CN106103730B (zh) | 2014-03-14 | 2021-06-08 | 豪夫迈·罗氏有限公司 | 用于分泌异源多肽的方法和组合物 |
| WO2015140591A1 (en) | 2014-03-21 | 2015-09-24 | Nordlandssykehuset Hf | Anti-cd14 antibodies and uses thereof |
| JP2017516458A (ja) | 2014-03-24 | 2017-06-22 | ジェネンテック, インコーポレイテッド | c−met拮抗剤による癌治療及びc−met拮抗剤のHGF発現との相関 |
| TWI687428B (zh) | 2014-03-27 | 2020-03-11 | 中央研究院 | 反應性標記化合物及其用途 |
| KR20160145624A (ko) | 2014-03-31 | 2016-12-20 | 제넨테크, 인크. | 항-ox40 항체 및 사용 방법 |
| EP3126386A1 (en) | 2014-03-31 | 2017-02-08 | F. Hoffmann-La Roche AG | Combination therapy comprising anti-angiogenesis agents and ox40 binding agonists |
| WO2015164615A1 (en) | 2014-04-24 | 2015-10-29 | University Of Oslo | Anti-gluten antibodies and uses thereof |
| RU2016150370A (ru) | 2014-05-22 | 2018-06-26 | Дженентек, Инк. | Антитела и иммуноконъюгаты против GPC3 |
| WO2015179835A2 (en) | 2014-05-23 | 2015-11-26 | Genentech, Inc. | Mit biomarkers and methods using the same |
| KR20220151036A (ko) | 2014-05-27 | 2022-11-11 | 아카데미아 시니카 | 항-cd20 글리코항체 및 이의 용도 |
| AU2015267045B2 (en) | 2014-05-27 | 2021-02-25 | Academia Sinica | Anti-HER2 glycoantibodies and uses thereof |
| US10118969B2 (en) | 2014-05-27 | 2018-11-06 | Academia Sinica | Compositions and methods relating to universal glycoforms for enhanced antibody efficacy |
| AU2015267052A1 (en) | 2014-05-27 | 2016-12-15 | Academia Sinica | Compositions and methods relating to universal glycoforms for enhanced antibody efficacy |
| US11332523B2 (en) | 2014-05-28 | 2022-05-17 | Academia Sinica | Anti-TNF-alpha glycoantibodies and uses thereof |
| EP3155015A1 (en) | 2014-06-11 | 2017-04-19 | F. Hoffmann-La Roche AG | Anti-lgr5 antibodies and uses thereof |
| US20230190750A1 (en) | 2014-06-13 | 2023-06-22 | Genentech, Inc. | Methods of treating and preventing cancer drug resistance |
| EP3164419A1 (en) | 2014-06-26 | 2017-05-10 | F. Hoffmann-La Roche AG | Anti-brdu antibodies and methods of use |
| RU2017103289A (ru) | 2014-07-11 | 2018-08-14 | Дженентек, Инк. | Ингибирование пути notch |
| EP3166974A1 (en) | 2014-07-11 | 2017-05-17 | Genentech, Inc. | Anti-pd-l1 antibodies and diagnostic uses thereof |
| US10513724B2 (en) | 2014-07-21 | 2019-12-24 | Glykos Finland Oy | Production of glycoproteins with mammalian-like N-glycans in filamentous fungi |
| UA122395C2 (uk) | 2014-08-19 | 2020-11-10 | Мерк Шарп Енд Доум Корп. | Антитіло проти tigit |
| RU2764074C2 (ru) | 2014-08-28 | 2022-01-13 | Байоатла, Ллк | Условно активные химерные антигенные рецепторы для модифицированных т-клеток |
| TWI751102B (zh) | 2014-08-28 | 2022-01-01 | 美商奇諾治療有限公司 | 對cd19具專一性之抗體及嵌合抗原受體 |
| CN107001404B (zh) | 2014-09-08 | 2021-06-29 | 中央研究院 | 使用醣脂激活人类iNKT细胞 |
| CN106687141A (zh) | 2014-09-10 | 2017-05-17 | 麦迪穆有限责任公司 | 吡咯并苯并二氮杂卓及其缀合物 |
| CN113698488A (zh) | 2014-09-12 | 2021-11-26 | 基因泰克公司 | 抗-b7-h4抗体及免疫缀合物 |
| MA40576B1 (fr) | 2014-09-12 | 2020-11-30 | Genentech Inc | Anticorps et immunoconjugués anti-her2 |
| AU2015314744A1 (en) | 2014-09-12 | 2017-03-02 | Genentech, Inc. | Anti-CLL-1 antibodies and immunoconjugates |
| EP3197500A1 (en) | 2014-09-17 | 2017-08-02 | Genentech, Inc. | Immunoconjugates comprising anti-her2 antibodies and pyrrolobenzodiazepines |
| PL3262071T3 (pl) | 2014-09-23 | 2020-08-10 | F. Hoffmann-La Roche Ag | Sposób stosowania immunokoniugatów anty-CD79b |
| MA40764A (fr) | 2014-09-26 | 2017-08-01 | Chugai Pharmaceutical Co Ltd | Agent thérapeutique induisant une cytotoxicité |
| US9732148B2 (en) | 2014-10-16 | 2017-08-15 | Genentech, Inc. | Anti-α-synuclein antibodies and methods of use |
| WO2016059602A2 (en) | 2014-10-16 | 2016-04-21 | Glaxo Group Limited | Methods of treating cancer and related compositions |
| WO2016070001A1 (en) | 2014-10-31 | 2016-05-06 | Jounce Therapeutics, Inc. | Methods of treating conditions with antibodies that bind b7-h4 |
| US20160160290A1 (en) | 2014-11-03 | 2016-06-09 | Genentech, Inc. | Methods and biomarkers for predicting efficacy and evaluation of an ox40 agonist treatment |
| CA2966523A1 (en) | 2014-11-03 | 2016-05-12 | Genentech, Inc. | Assays for detecting t cell immune subsets and methods of use thereof |
| BR112017008666A2 (pt) | 2014-11-05 | 2018-01-30 | Genentech, Inc. | anticorpos anti-fgfr2/3 e métodos de uso dos mesmos |
| EP3215528B1 (en) | 2014-11-06 | 2019-08-07 | F.Hoffmann-La Roche Ag | Fc-region variants with modified fcrn-binding and methods of use |
| SG11201703376QA (en) | 2014-11-06 | 2017-05-30 | Genentech Inc | Combination therapy comprising ox40 binding agonists and tigit inhibitors |
| CN107074966A (zh) | 2014-11-06 | 2017-08-18 | 豪夫迈·罗氏有限公司 | 具有改变的FCRN‑和蛋白A‑结合性质的Fc区变体 |
| CN107172879B (zh) | 2014-11-10 | 2021-11-05 | 豪夫迈·罗氏有限公司 | 抗白细胞介素-33抗体及其用途 |
| CN107105632A (zh) | 2014-11-10 | 2017-08-29 | 豪夫迈·罗氏有限公司 | 肾病动物模型及其治疗剂 |
| EP3218397B8 (en) | 2014-11-14 | 2021-04-07 | The United States Of America, As Represented By The Secretary, Department Of Health And Human Services | Neutralizing antibodies to ebola virus glycoprotein and their use |
| MY191428A (en) | 2014-11-14 | 2022-06-27 | Hoffmann La Roche | Antigen binding molecules comprising a tnf family ligand trimer |
| CN106999583A (zh) | 2014-11-17 | 2017-08-01 | 豪夫迈·罗氏有限公司 | 包含ox40结合激动剂和pd‑1轴结合拮抗剂的组合疗法 |
| EP3845565A3 (en) | 2014-11-19 | 2021-09-08 | Genentech, Inc. | Antibodies against bace1 and use thereof for neural disease immunotherapy |
| JP6779876B2 (ja) | 2014-11-19 | 2020-11-04 | ジェネンテック, インコーポレイテッド | 抗トランスフェリン受容体抗体及びその使用方法 |
| EP3221361B1 (en) | 2014-11-19 | 2021-04-21 | Genentech, Inc. | Anti-transferrin receptor / anti-bace1 multispecific antibodies and methods of use |
| HUE053239T2 (hu) | 2014-11-19 | 2021-06-28 | Axon Neuroscience Se | Humanizált tau-ellenanyagok Alzheimer-kór kezelésére |
| SI3789402T1 (sl) | 2014-11-20 | 2022-10-28 | F. Hoffmann-La Roche Ag | Kombinirano zdravljenje z bispecifičnimi molekulami, ki vežejo antigen in aktivirajo celice T, ter antagonisti za vezavo osi PD-1 |
| WO2016087416A1 (en) | 2014-12-03 | 2016-06-09 | F. Hoffmann-La Roche Ag | Multispecific antibodies |
| LT3227336T (lt) | 2014-12-05 | 2019-09-25 | F. Hoffmann-La Roche Ag | Anti-cd79b antikūnai ir jų naudojimo būdai |
| KR20170085595A (ko) | 2014-12-10 | 2017-07-24 | 제넨테크, 인크. | 혈뇌 장벽 수용체 항체 및 사용 방법 |
| AU2015365167B2 (en) | 2014-12-19 | 2021-07-29 | Chugai Seiyaku Kabushiki Kaisha | Anti-C5 antibodies and methods of use |
| WO2016111947A2 (en) | 2015-01-05 | 2016-07-14 | Jounce Therapeutics, Inc. | Antibodies that inhibit tim-3:lilrb2 interactions and uses thereof |
| US9975965B2 (en) | 2015-01-16 | 2018-05-22 | Academia Sinica | Compositions and methods for treatment and detection of cancers |
| US10495645B2 (en) | 2015-01-16 | 2019-12-03 | Academia Sinica | Cancer markers and methods of use thereof |
| US20160208018A1 (en) | 2015-01-16 | 2016-07-21 | Juno Therapeutics, Inc. | Antibodies and chimeric antigen receptors specific for ror1 |
| JP2018511557A (ja) | 2015-01-22 | 2018-04-26 | 中外製薬株式会社 | 2種以上の抗c5抗体の組み合わせおよび使用方法 |
| KR20170104617A (ko) | 2015-01-24 | 2017-09-15 | 아카데미아 시니카 | 신규한 글리칸 콘주게이트 및 이를 사용하는 방법 |
| JP2018506275A (ja) | 2015-01-28 | 2018-03-08 | ジェネンテック, インコーポレイテッド | 多発性硬化症の遺伝子発現マーカー及び治療 |
| JP2018512597A (ja) | 2015-02-04 | 2018-05-17 | ジェネンテック, インコーポレイテッド | 突然変異体スムースンド及びその使用方法 |
| CN114773469A (zh) | 2015-02-05 | 2022-07-22 | 中外制药株式会社 | 包含离子浓度依赖性的抗原结合结构域的抗体,fc区变体,il-8-结合抗体及其应用 |
| US10301377B2 (en) | 2015-02-24 | 2019-05-28 | The United States Of America, As Represented By The Secretary, Department Of Health And Human Services | Middle east respiratory syndrome coronavirus immunogens, antibodies, and their use |
| MY188761A (en) | 2015-03-09 | 2021-12-29 | Argenx Bvba | Method of reducing serum levels of fc-containing agents using fcrn antagonists |
| AU2016233398A1 (en) | 2015-03-16 | 2017-09-07 | F. Hoffmann-La Roche Ag | Methods of detecting and quantifying IL-13 and uses in diagnosing and treating Th2-associated diseases |
| WO2016146833A1 (en) | 2015-03-19 | 2016-09-22 | F. Hoffmann-La Roche Ag | Biomarkers for nad(+)-diphthamide adp ribosyltransferase resistance |
| LT3271389T (lt) | 2015-03-20 | 2020-05-25 | The United States Of America, As Represented By The Secretary, Department Of Health And Human Services | Neutralizuojantys antikūnai prieš gp120 ir jų panaudojimas |
| DK3274370T3 (da) | 2015-03-23 | 2020-02-17 | Bayer Pharma AG | Anti-ceacam6-antistoffer og anvendelser deraf |
| PL3273992T3 (pl) | 2015-03-23 | 2020-11-16 | Jounce Therapeutics, Inc. | Przeciwciała przeciwko icos |
| CN114456272A (zh) | 2015-04-03 | 2022-05-10 | 优瑞科生物技术公司 | 靶向afp肽/mhc复合体的构建体及其用途 |
| JP7044553B2 (ja) | 2015-04-24 | 2022-03-30 | ジェネンテック, インコーポレイテッド | 結合ポリペプチドを含む細菌を特定する方法 |
| JP2018520642A (ja) | 2015-05-01 | 2018-08-02 | ジェネンテック, インコーポレイテッド | マスク抗cd3抗体及びその使用方法 |
| WO2016179194A1 (en) | 2015-05-04 | 2016-11-10 | Jounce Therapeutics, Inc. | Lilra3 and method of using the same |
| TWI820377B (zh) | 2015-05-07 | 2023-11-01 | 美商艾吉納斯公司 | 抗ox40抗體及其使用方法 |
| CN116196414A (zh) | 2015-05-11 | 2023-06-02 | 豪夫迈·罗氏有限公司 | 治疗狼疮性肾炎的组合物和方法 |
| IL295002A (en) | 2015-05-12 | 2022-09-01 | Genentech Inc | Therapeutic and diagnostic methods for cancer containing a pd–l1 binding antagonist |
| EP3303619B1 (en) | 2015-05-29 | 2020-06-10 | H. Hoffnabb-La Roche Ag | Pd-l1 promoter methylation in cancer |
| KR20180012753A (ko) | 2015-05-29 | 2018-02-06 | 제넨테크, 인크. | 암에 대한 치료 및 진단 방법 |
| WO2016196343A1 (en) | 2015-05-29 | 2016-12-08 | Genentech, Inc. | Humanized anti-ebola virus glycoprotein antibodies and methods of use |
| JP2018516933A (ja) | 2015-06-02 | 2018-06-28 | ジェネンテック, インコーポレイテッド | 抗il−34抗体を使用して神経学的疾患を治療するための組成物及び方法 |
| WO2016196975A1 (en) | 2015-06-03 | 2016-12-08 | The United States Of America, As Represented By The Secretary Department Of Health & Human Services | Neutralizing antibodies to hiv-1 env and their use |
| US10682391B2 (en) | 2015-06-04 | 2020-06-16 | Ospedale San Raffaele Srl | Inhibitors of IGFBP3 binding to TMEM219 for treatment of intestinal diseases |
| KR101978765B1 (ko) | 2015-06-04 | 2019-05-15 | 오스페달레 산 라파엘 에스.알.엘. | Igfbp3/tmem219 축 및 당뇨병의 저해제 |
| SG10201911349YA (en) | 2015-06-05 | 2020-01-30 | Genentech Inc | Anti-tau antibodies and methods of use |
| AU2016274585A1 (en) | 2015-06-08 | 2017-12-14 | Genentech, Inc. | Methods of treating cancer using anti-OX40 antibodies |
| KR20180025888A (ko) | 2015-06-08 | 2018-03-09 | 제넨테크, 인크. | 항-ox40 항체 및 pd-1 축 결합 길항제를 사용하여 암을 치료하는 방법 |
| US10017577B2 (en) | 2015-06-15 | 2018-07-10 | Genentech, Inc. | Antibodies and immunoconjugates |
| CN107847568B (zh) | 2015-06-16 | 2022-12-20 | 豪夫迈·罗氏有限公司 | 抗cll-1抗体和使用方法 |
| PE20180330A1 (es) | 2015-06-16 | 2018-02-13 | Genentech Inc | Anticuerpos madurados por afinidad y humanizados para fcrh5 y metodos para su uso |
| WO2016204966A1 (en) | 2015-06-16 | 2016-12-22 | Genentech, Inc. | Anti-cd3 antibodies and methods of use |
| WO2016205567A1 (en) | 2015-06-17 | 2016-12-22 | Allakos Inc. | Methods and compositions for treating fibrotic diseases |
| JP2018524312A (ja) | 2015-06-17 | 2018-08-30 | ジェネンテック, インコーポレイテッド | 抗her2抗体及び使用方法 |
| KR20180018538A (ko) | 2015-06-17 | 2018-02-21 | 제넨테크, 인크. | Pd-1 축 결합 길항제 및 탁산을 사용하여 국소적 진행성 또는 전이성 유방암을 치료하는 방법 |
| CN113999312A (zh) | 2015-06-24 | 2022-02-01 | 豪夫迈·罗氏有限公司 | 具有定制亲和力的抗转铁蛋白受体抗体 |
| CN108473573A (zh) | 2015-06-29 | 2018-08-31 | 豪夫迈·罗氏有限公司 | Ii型抗cd20抗体用于器官移植中 |
| EP3514174B1 (en) | 2015-06-29 | 2021-03-31 | Ventana Medical Systems, Inc. | Materials and methods for performing histochemical assays for human pro-epiregulin and amphiregulin |
| RU2611685C2 (ru) * | 2015-07-20 | 2017-02-28 | Илья Владимирович Духовлинов | Гуманизированное моноклональное антитело, специфичное к синдекану-1 |
| EP4137158A1 (en) | 2015-08-07 | 2023-02-22 | Imaginab, Inc. | Antigen binding constructs to target molecules |
| CN105384825B (zh) | 2015-08-11 | 2018-06-01 | 南京传奇生物科技有限公司 | 一种基于单域抗体的双特异性嵌合抗原受体及其应用 |
| CN108026180B (zh) | 2015-08-28 | 2022-06-07 | 豪夫迈·罗氏有限公司 | 抗羟腐胺赖氨酸抗体及其用途 |
| KR20180042412A (ko) | 2015-09-02 | 2018-04-25 | 이뮤텝 에스.에이.에스. | 항-lag-3 항체 |
| CA2999369C (en) | 2015-09-22 | 2023-11-07 | Spring Bioscience Corporation | Anti-ox40 antibodies and diagnostic uses thereof |
| AU2016326666B2 (en) | 2015-09-23 | 2023-06-15 | Genentech, Inc. | Optimized variants of anti-VEGF antibodies |
| CN108289954B (zh) | 2015-09-24 | 2022-05-31 | 阿布维特罗有限责任公司 | Hiv抗体组合物和使用方法 |
| WO2017058944A1 (en) | 2015-09-29 | 2017-04-06 | Amgen Inc. | Asgr inhibitors |
| AR106188A1 (es) | 2015-10-01 | 2017-12-20 | Hoffmann La Roche | Anticuerpos anti-cd19 humano humanizados y métodos de utilización |
| BR112018002570A2 (pt) | 2015-10-02 | 2018-10-16 | Hoffmann La Roche | molécula de ligação ao antígeno biespecífica, anticorpo biespecífico, polinucleotídeos, anticorpo que se liga especificamente ao ox40, composição farmacêutica e método para inibir o crescimento de células tumorais em um indivíduo |
| AR106189A1 (es) | 2015-10-02 | 2017-12-20 | Hoffmann La Roche | ANTICUERPOS BIESPECÍFICOS CONTRA EL A-b HUMANO Y EL RECEPTOR DE TRANSFERRINA HUMANO Y MÉTODOS DE USO |
| AU2016333512B2 (en) | 2015-10-02 | 2022-11-17 | F. Hoffmann-La Roche Ag | Bispecific anti-human CD20/human transferrin receptor antibodies and methods of use |
| EP3150636A1 (en) | 2015-10-02 | 2017-04-05 | F. Hoffmann-La Roche AG | Tetravalent multispecific antibodies |
| MA43345A (fr) | 2015-10-02 | 2018-08-08 | Hoffmann La Roche | Conjugués anticorps-médicaments de pyrrolobenzodiazépine et méthodes d'utilisation |
| KR102146319B1 (ko) | 2015-10-02 | 2020-08-25 | 에프. 호프만-라 로슈 아게 | Pd1 및 tim3에 특이적인 이중특이성 항체 |
| JP2018529747A (ja) | 2015-10-06 | 2018-10-11 | ジェネンテック, インコーポレイテッド | 多発性硬化症を治療するための方法 |
| US10392441B2 (en) | 2015-10-07 | 2019-08-27 | United States Of America, As Represented By The Secretary, Department Of Health And Human Services | IL-7R-alpha specific antibodies for treating acute lymphoblastic leukemia |
| WO2017060144A1 (en) | 2015-10-07 | 2017-04-13 | F. Hoffmann-La Roche Ag | Bispecific antibodies with tetravalency for a costimulatory tnf receptor |
| TW201723190A (zh) | 2015-10-22 | 2017-07-01 | 永斯醫療股份有限公司 | 用於測定icos表現之基因印記 |
| US10604577B2 (en) | 2015-10-22 | 2020-03-31 | Allakos Inc. | Methods and compositions for treating systemic mastocytosis |
| EP3184547A1 (en) | 2015-10-29 | 2017-06-28 | F. Hoffmann-La Roche AG | Anti-tpbg antibodies and methods of use |
| WO2017072210A1 (en) | 2015-10-29 | 2017-05-04 | F. Hoffmann-La Roche Ag | Anti-variant fc-region antibodies and methods of use |
| JO3555B1 (ar) | 2015-10-29 | 2020-07-05 | Merck Sharp & Dohme | جسم مضاد يبطل فعالية فيروس الالتهاب الرئوي البشري |
| KR102440160B1 (ko) | 2015-10-30 | 2022-09-02 | 제넨테크, 인크. | 항-HtrA1 항체 및 이의 사용 방법 |
| TW201730211A (zh) | 2015-10-30 | 2017-09-01 | 建南德克公司 | 抗因子d抗體及結合物 |
| CA3003878A1 (en) | 2015-11-03 | 2017-05-11 | The United States Of America, As Represented By The Secretary, Department Of Health And Human Services | Neutralizing antibodies to hiv-1 gp41 and their use |
| WO2017079768A1 (en) | 2015-11-08 | 2017-05-11 | Genentech, Inc. | Methods of screening for multispecific antibodies |
| RU2021107536A (ru) | 2015-11-23 | 2021-07-02 | Файв Прайм Терапьютикс, Инк. | Ингибиторы fgfr2 отдельно или в комбинации с иммуностимулирующими агентами в лечении рака |
| AU2016368469B2 (en) | 2015-12-09 | 2023-11-02 | F. Hoffmann-La Roche Ag | Type II anti-CD20 antibody for reducing formation of anti-drug antibodies |
| KR102467124B1 (ko) | 2015-12-18 | 2022-11-15 | 추가이 세이야쿠 가부시키가이샤 | 항-c5 항체 및 사용 방법 |
| AU2016380988B2 (en) | 2015-12-30 | 2022-07-21 | Genentech, Inc. | Formulations with reduced degradation of polysorbate |
| EP3862365A1 (en) | 2016-01-08 | 2021-08-11 | F. Hoffmann-La Roche AG | Methods of treating cea-positive cancers using pd-1 axis binding antagonists and anti-cea/anti-cd3 bispecific antibodies |
| CN108602883A (zh) | 2016-01-20 | 2018-09-28 | 基因泰克公司 | 用于阿尔茨海默氏病的高剂量治疗 |
| US11414477B2 (en) | 2016-01-27 | 2022-08-16 | Medimmune, Llc | Methods for preparing antibodies with a defined glycosylation pattern |
| CN109071625A (zh) | 2016-02-04 | 2018-12-21 | 柯瑞斯公司 | 平滑化突变体和其使用方法 |
| WO2017145166A1 (en) * | 2016-02-25 | 2017-08-31 | B. G. Negev Technologies And Applications Ltd., At Ben-Gurion University | Composition and method for treating amyotrophic lateral sclerosis |
| AU2017225854B2 (en) | 2016-02-29 | 2020-11-19 | Foundation Medicine, Inc. | Therapeutic and diagnostic methods for cancer |
| AU2017231749A1 (en) | 2016-03-08 | 2018-09-20 | Academia Sinica | Methods for modular synthesis of N-glycans and arrays thereof |
| JP6430025B2 (ja) | 2016-03-15 | 2018-11-28 | 中外製薬株式会社 | Pd−1系結合アンタゴニストおよび抗gpc3抗体を使用して癌を治療する方法 |
| EP4273551A3 (en) | 2016-03-25 | 2024-01-17 | F. Hoffmann-La Roche AG | Multiplexed total antibody and antibody-conjugated drug quantification assay |
| CN109071653A (zh) | 2016-03-29 | 2018-12-21 | 詹森生物科技公司 | 用增加的抗-il12和/或-23抗体给药间隔治疗牛皮癣 |
| AU2017247796A1 (en) | 2016-04-05 | 2018-09-27 | Glaxosmithkline Intellectual Property Development Limited | Inhibition of TGFBeta in immunotherapy |
| EP3865511A1 (en) | 2016-04-14 | 2021-08-18 | F. Hoffmann-La Roche AG | Anti-rspo3 antibodies and methods of use |
| MX2018012492A (es) | 2016-04-15 | 2019-06-06 | Genentech Inc | Métodos para monitorear y tratar el cáncer. |
| AU2017248766A1 (en) | 2016-04-15 | 2018-11-01 | Genentech, Inc. | Methods for monitoring and treating cancer |
| EP3443012A4 (en) | 2016-04-15 | 2019-09-11 | Bioatla, LLC | ANTI-AXL ANTIBODIES, ANTIBODY FRAGMENTS AND ITS IMMUNOCONJUGATES AND USES THEREOF |
| AU2017259869A1 (en) | 2016-05-02 | 2018-09-27 | F. Hoffmann-La Roche Ag | The contorsbody - a single chain target binder |
| WO2017192589A1 (en) | 2016-05-02 | 2017-11-09 | The United States Of America, As Represented By The Secretary, Department Of Health And Human Services | Neutralizing antibodies to influenza ha and their use and identification |
| JP7089483B2 (ja) | 2016-05-11 | 2022-06-22 | エフ・ホフマン-ラ・ロシュ・アクチェンゲゼルシャフト | 修飾された抗テネイシン抗体及び使用方法 |
| EP3243836A1 (en) | 2016-05-11 | 2017-11-15 | F. Hoffmann-La Roche AG | C-terminally fused tnf family ligand trimer-containing antigen binding molecules |
| JP7285076B2 (ja) | 2016-05-11 | 2023-06-01 | エフ・ホフマン-ラ・ロシュ・アクチェンゲゼルシャフト | Tnfファミリーリガンドトリマーとテネイシン結合部分とを含む抗原結合分子 |
| EP3243832A1 (en) | 2016-05-13 | 2017-11-15 | F. Hoffmann-La Roche AG | Antigen binding molecules comprising a tnf family ligand trimer and pd1 binding moiety |
| RS63698B1 (sr) | 2016-05-13 | 2022-11-30 | Bioatla Inc | Anti-ror2 antitela, fragmenti antitela, njihovi imunokonjugati i njihove upotrebe |
| ES2858151T3 (es) | 2016-05-20 | 2021-09-29 | Hoffmann La Roche | Conjugados de PROTAC-anticuerpo y procedimientos de uso |
| EP3465221B1 (en) | 2016-05-27 | 2020-07-22 | H. Hoffnabb-La Roche Ag | Bioanalytical method for the characterization of site-specific antibody-drug conjugates |
| CN110603266A (zh) | 2016-06-02 | 2019-12-20 | 豪夫迈·罗氏有限公司 | 用于治疗癌症的ii型抗cd20抗体和抗cd20/cd3双特异性抗体 |
| EP3252078A1 (en) | 2016-06-02 | 2017-12-06 | F. Hoffmann-La Roche AG | Type ii anti-cd20 antibody and anti-cd20/cd3 bispecific antibody for treatment of cancer |
| EP3475298A1 (en) | 2016-06-24 | 2019-05-01 | H. Hoffnabb-La Roche Ag | Anti-polyubiquitin multispecific antibodies |
| JP6983824B2 (ja) | 2016-07-04 | 2021-12-17 | エフ.ホフマン−ラ ロシュ アーゲーF. Hoffmann−La Roche Aktiengesellschaft | 新規抗体フォーマット |
| WO2018014260A1 (en) | 2016-07-20 | 2018-01-25 | Nanjing Legend Biotech Co., Ltd. | Multispecific antigen binding proteins and methods of use thereof |
| CA3031734A1 (en) | 2016-07-29 | 2018-02-01 | Juno Therapeutics, Inc. | Anti-idiotypic antibodies against anti-cd19 antibodies |
| MX2018015721A (es) | 2016-07-29 | 2019-05-27 | Chugai Pharmaceutical Co Ltd | Anticuerpos biespecificos que exhiben actividad de funcion de cofactor fviii alternativa mejorada. |
| NL2017270B1 (en) | 2016-08-02 | 2018-02-09 | Aduro Biotech Holdings Europe B V | New anti-hCTLA-4 antibodies |
| SG11201801024XA (en) | 2016-08-05 | 2018-05-30 | Chugai Pharmaceutical Co Ltd | Therapeutic or preventive compositions for il-8-related diseases |
| WO2018029124A1 (en) | 2016-08-08 | 2018-02-15 | F. Hoffmann-La Roche Ag | Therapeutic and diagnostic methods for cancer |
| CN109963868B (zh) | 2016-08-22 | 2023-11-14 | 醣基生医股份有限公司 | 抗体、结合片段及使用方法 |
| WO2018045379A1 (en) | 2016-09-02 | 2018-03-08 | Dana-Farber Cancer Institute, Inc. | Composition and methods of treating b cell disorders |
| EP3510046A4 (en) | 2016-09-07 | 2020-05-06 | The Regents of the University of California | ANTIBODIES AGAINST OXIDATION-SPECIFIC EPITOPES |
| SG10201607778XA (en) | 2016-09-16 | 2018-04-27 | Chugai Pharmaceutical Co Ltd | Anti-Dengue Virus Antibodies, Polypeptides Containing Variant Fc Regions, And Methods Of Use |
| WO2018050878A1 (en) | 2016-09-19 | 2018-03-22 | F. Hoffmann-La Roche Ag | Complement factor based affinity chromatography |
| UA124269C2 (uk) | 2016-09-23 | 2021-08-18 | Дженентек, Інк. | Застосування антагоністу il-13 для лікування атопічного дерматиту |
| JOP20190055A1 (ar) | 2016-09-26 | 2019-03-24 | Merck Sharp & Dohme | أجسام مضادة ضد cd27 |
| KR20190059305A (ko) | 2016-09-30 | 2019-05-30 | 얀센 바이오테크 인코포레이티드 | 항-il23 특이적 항체로 건선을 치료하는 안전하고 효과적인 방법 |
| MA46354A (fr) | 2016-10-03 | 2019-08-07 | Juno Therapeutics Inc | Molécules se liant spécifiquement au vph |
| EP3522933B1 (en) | 2016-10-05 | 2021-12-15 | F. Hoffmann-La Roche AG | Methods for preparing antibody drug conjugates |
| KR20190072528A (ko) | 2016-10-06 | 2019-06-25 | 제넨테크, 인크. | 암에 대한 치료 및 진단 방법 |
| WO2018068201A1 (en) | 2016-10-11 | 2018-04-19 | Nanjing Legend Biotech Co., Ltd. | Single-domain antibodies and variants thereof against ctla-4 |
| JP2019534882A (ja) | 2016-10-11 | 2019-12-05 | メドイミューン・リミテッドMedImmune Limited | 免疫介在性療法薬を有する抗体−薬物コンジュゲート |
| EP3532091A2 (en) | 2016-10-29 | 2019-09-04 | H. Hoffnabb-La Roche Ag | Anti-mic antibidies and methods of use |
| MD3535298T2 (ro) | 2016-11-02 | 2022-01-31 | Jounce Therapeutics Inc | Anticorpi ai PD-1 și utilizări ale acestora |
| CA3042435A1 (en) | 2016-11-15 | 2018-05-24 | Genentech, Inc. | Dosing for treatment with anti-cd20/anti-cd3 bispecific antibodies |
| WO2018093841A1 (en) | 2016-11-16 | 2018-05-24 | Janssen Biotech, Inc. | Method of treating psoriasis with anti-il-23 specific antibody |
| JOP20190100A1 (ar) | 2016-11-19 | 2019-05-01 | Potenza Therapeutics Inc | بروتينات ربط مولد ضد مضاد لـ gitr وطرق استخدامها |
| AU2017361887B2 (en) | 2016-11-21 | 2019-08-15 | Cureab Gmbh | Anti-GP73 antibodies and immunoconjugates |
| US10759855B2 (en) | 2016-12-02 | 2020-09-01 | Rigel Pharmaceuticals, Inc. | Antigen binding molecules to TIGIT |
| CN110300599A (zh) | 2016-12-07 | 2019-10-01 | 艾吉纳斯公司 | 抗体和其使用方法 |
| WO2018106781A1 (en) | 2016-12-07 | 2018-06-14 | Genentech, Inc | Anti-tau antibodies and methods of use |
| WO2018106776A2 (en) | 2016-12-07 | 2018-06-14 | Genentech, Inc. | Anti-tau antibodies and methods of use |
| KR20190095921A (ko) | 2016-12-12 | 2019-08-16 | 제넨테크, 인크. | 항-pd-l1 항체 및 안티안드로겐을 사용하여 암을 치료하는 방법 |
| TWI829628B (zh) | 2016-12-19 | 2024-01-21 | 瑞士商赫孚孟拉羅股份公司 | 與靶向4-1bb (cd137)促效劑併用之組合療法 |
| CA3039446A1 (en) | 2016-12-20 | 2018-06-28 | F. Hoffmann-La Roche Ag | Combination therapy of anti-cd20/anti-cd3 bispecific antibodies and 4-1bb (cd137) agonists |
| JOP20190134A1 (ar) | 2016-12-23 | 2019-06-02 | Potenza Therapeutics Inc | بروتينات رابطة لمولد ضد مضادة لنيوروبيلين وطرق استخدامها |
| RU2019123613A (ru) | 2017-01-03 | 2021-02-05 | Ф. Хоффманн-Ля Рош Аг | Биспецифические антигенсвязывающие молекулы, содержащие антитело к4-1вв, клон 20н4.9 |
| US20180230218A1 (en) | 2017-01-04 | 2018-08-16 | Immunogen, Inc. | Met antibodies and immunoconjugates and uses thereof |
| WO2018132597A1 (en) | 2017-01-12 | 2018-07-19 | Eureka Therapeutics, Inc. | Constructs targeting histone h3 peptide/mhc complexes and uses thereof |
| US11266745B2 (en) | 2017-02-08 | 2022-03-08 | Imaginab, Inc. | Extension sequences for diabodies |
| EP3580235B1 (en) | 2017-02-10 | 2024-05-01 | The United States of America, as represented by the Secretary, Department of Health and Human Services | Neutralizing antibodies to plasmodium falciparum circumsporozoite protein and their use |
| JP6995127B2 (ja) | 2017-02-10 | 2022-02-04 | ジェネンテック, インコーポレイテッド | 抗トリプターゼ抗体、その組成物、及びその使用 |
| CA3052670A1 (en) | 2017-03-01 | 2018-09-07 | Genentech, Inc. | Diagnostic and therapeutic methods for cancer |
| JP7227151B2 (ja) | 2017-03-22 | 2023-02-21 | ジェネンテック, インコーポレイテッド | 眼障害の治療のために最適化された抗体組成物 |
| AU2018244224A1 (en) | 2017-03-28 | 2019-09-19 | Genentech, Inc. | Methods of treating neurodegenerative diseases |
| CN110573528B (zh) | 2017-03-29 | 2023-06-09 | 豪夫迈·罗氏有限公司 | 针对共刺激性tnf受体的双特异性抗原结合分子 |
| EP3601346A1 (en) | 2017-03-29 | 2020-02-05 | H. Hoffnabb-La Roche Ag | Bispecific antigen binding molecule for a costimulatory tnf receptor |
| JOP20190203A1 (ar) | 2017-03-30 | 2019-09-03 | Potenza Therapeutics Inc | بروتينات رابطة لمولد ضد مضادة لـ tigit وطرق استخدامها |
| JP7247101B2 (ja) | 2017-04-03 | 2023-03-28 | エフ・ホフマン-ラ・ロシュ・アクチェンゲゼルシャフト | Steap-1に結合する抗体 |
| MX2019011907A (es) | 2017-04-04 | 2020-01-09 | Hoffmann La Roche | Nuevas moleculas de union a antigeno biespecificas capaces de unirse especificamente a cd40 y a fap. |
| KR102408873B1 (ko) | 2017-04-05 | 2022-06-15 | 에프. 호프만-라 로슈 아게 | Pd1 및 lag3에 특이적으로 결합하는 이중특이적 항체 |
| PL3606954T3 (pl) | 2017-04-05 | 2022-10-17 | F. Hoffmann-La Roche Ag | Przeciwciała anty-LAG3 |
| CN110621787A (zh) | 2017-04-14 | 2019-12-27 | 豪夫迈·罗氏有限公司 | 用于癌症的诊断和治疗方法 |
| PE20200150A1 (es) | 2017-04-21 | 2020-01-17 | Genentech Inc | Uso de antagonistas de klk5 para el tratamiento de una enfermedad |
| SG11201909728XA (en) | 2017-04-26 | 2019-11-28 | Eureka Therapeutics Inc | Constructs specifically recognizing glypican 3 and uses thereof |
| JP2020517695A (ja) | 2017-04-27 | 2020-06-18 | テサロ, インコーポレイテッド | リンパ球活性化遺伝子−3(lag−3)に対する抗体薬およびそれらの使用 |
| MX2019013137A (es) | 2017-05-05 | 2020-07-14 | Allakos Inc | Metodos y composiciones para tratar enfermedades oculares alergicas. |
| CN110621336A (zh) | 2017-05-16 | 2019-12-27 | 戊瑞治疗有限公司 | 癌症治疗中抗fgfr2抗体与化学治疗剂的组合 |
| EP3652206A1 (en) | 2017-07-10 | 2020-05-20 | International-Drug-Development-Biotech | Treatment of b cell malignancies using afucosylated pro-apoptotic anti-cd19 antibodies in combination with anti cd20 antibodies or chemotherapeutics |
| TWI823859B (zh) | 2017-07-21 | 2023-12-01 | 美商建南德克公司 | 癌症之治療及診斷方法 |
| AU2018308364C1 (en) | 2017-07-26 | 2023-02-16 | Forty Seven, Inc. | Anti-SIRP-alpha antibodies and related methods |
| MA49950A (fr) | 2017-08-25 | 2020-07-01 | Five Prime Therapeutics Inc | Anticorps anti-b7-h4 et leurs procédés d'utilisation |
| WO2019059411A1 (en) | 2017-09-20 | 2019-03-28 | Chugai Seiyaku Kabushiki Kaisha | DOSAGE FOR POLYTHERAPY USING PD-1 AXIS BINDING ANTAGONISTS AND GPC3 TARGETING AGENT |
| TW201922780A (zh) | 2017-09-25 | 2019-06-16 | 美商健生生物科技公司 | 以抗il12/il23抗體治療狼瘡之安全且有效之方法 |
| MA50613A (fr) | 2017-10-03 | 2020-08-12 | Editas Medicine Inc | Molécules de liaison spécifique à l'hpv |
| WO2019075090A1 (en) | 2017-10-10 | 2019-04-18 | Tilos Therapeutics, Inc. | ANTI-LAP ANTIBODIES AND USES THEREOF |
| WO2019075270A1 (en) | 2017-10-12 | 2019-04-18 | Amesino Llc | VEGFR ANTIBODY LIGHT CHAIN FUSION PROTEIN |
| EP3704155A2 (en) | 2017-11-01 | 2020-09-09 | F. Hoffmann-La Roche AG | Combination therapy with targeted ox40 agonists |
| KR20200079492A (ko) | 2017-11-01 | 2020-07-03 | 에프. 호프만-라 로슈 아게 | 이중특이성 2+1 컨터체 |
| WO2019086499A1 (en) | 2017-11-01 | 2019-05-09 | F. Hoffmann-La Roche Ag | Novel tnf family ligand trimer-containing antigen binding molecules |
| MA49911A (fr) | 2017-11-01 | 2020-06-24 | Juno Therapeutics Inc | Anticorps et récepteurs antigéniques chimériques spécifiques de l'antigene de maturation des lymphocytes b |
| AU2018359967A1 (en) | 2017-11-06 | 2020-04-23 | Genentech, Inc. | Diagnostic and therapeutic methods for cancer |
| SG11202003930YA (en) | 2017-12-01 | 2020-05-28 | Pfizer | Anti-cxcr5 antibodies and compositions and uses thereof |
| EP3720877A1 (en) | 2017-12-08 | 2020-10-14 | Argenx BVBA | Use of fcrn antagonists for treatment of generalized myasthenia gravis |
| US20210070845A1 (en) | 2017-12-15 | 2021-03-11 | Juno Therapeutics, Inc. | Anti-cct5 binding molecules and methods of use thereof |
| CN111527107A (zh) | 2017-12-21 | 2020-08-11 | 豪夫迈·罗氏有限公司 | 结合hla-a2/wt1的抗体 |
| EP3502140A1 (en) | 2017-12-21 | 2019-06-26 | F. Hoffmann-La Roche AG | Combination therapy of tumor targeted icos agonists with t-cell bispecific molecules |
| WO2019126472A1 (en) | 2017-12-22 | 2019-06-27 | Genentech, Inc. | Use of pilra binding agents for treatment of a disease |
| JP7391868B2 (ja) | 2017-12-22 | 2023-12-05 | ジョウンセ セラピューティクス, インク. | Lilrb2に対する抗体 |
| KR20200104886A (ko) | 2017-12-28 | 2020-09-04 | 난징 레전드 바이오테크 씨오., 엘티디. | Pd-l1에 대한 항체 및 변이체 |
| US11905327B2 (en) | 2017-12-28 | 2024-02-20 | Nanjing Legend Biotech Co., Ltd. | Single-domain antibodies and variants thereof against TIGIT |
| EP3731864A1 (en) | 2017-12-29 | 2020-11-04 | F. Hoffmann-La Roche SA | Anti-vegf antibodies and methods of use |
| WO2019136029A1 (en) | 2018-01-02 | 2019-07-11 | The United States Of America, As Represented By The Secretary, Department Of Health And Human Services | Neutralizing antibodies to ebola virus glycoprotein and their use |
| KR20200106525A (ko) | 2018-01-05 | 2020-09-14 | 에이씨 이뮨 에스.에이. | 미스폴딩된 tdp-43 결합 분자 |
| EP3508499A1 (en) | 2018-01-08 | 2019-07-10 | iOmx Therapeutics AG | Antibodies targeting, and other modulators of, an immunoglobulin gene associated with resistance against anti-tumour immune responses, and uses thereof |
| SG11202004233UA (en) | 2018-01-15 | 2020-06-29 | Nanjing Legend Biotech Co Ltd | Single-domain antibodies and variants thereof against pd-1 |
| US20200339686A1 (en) | 2018-01-16 | 2020-10-29 | Lakepharma, Inc. | Bispecific antibody that binds cd3 and another target |
| LT3743088T (lt) | 2018-01-26 | 2022-12-27 | F. Hoffmann-La Roche Ag | Il-22 fc kompozicijos ir jų naudojimo būdai |
| RU2020127792A (ru) | 2018-01-26 | 2022-02-28 | Дженентек, Инк. | СЛИТЫЕ БЕЛКИ IL-22- Fc И СПОСОБЫ ПРИМЕНЕНИЯ |
| JP7438953B2 (ja) | 2018-02-01 | 2024-02-27 | イノベント バイオロジックス (スウツォウ) カンパニー,リミテッド | 完全ヒト化抗b細胞成熟抗原(bcma)の単鎖抗体およびその応用 |
| MA51793A (fr) | 2018-02-08 | 2020-12-16 | Hoffmann La Roche | Molécules bispécifiques de liaison à l'antigène et procédés d'utilisation |
| JP7418337B2 (ja) | 2018-02-09 | 2024-01-19 | ジェネンテック, インコーポレイテッド | マスト細胞媒介性炎症性疾患の治療法及び診断法 |
| TWI829667B (zh) | 2018-02-09 | 2024-01-21 | 瑞士商赫孚孟拉羅股份公司 | 結合gprc5d之抗體 |
| JP7350756B2 (ja) | 2018-02-14 | 2023-09-26 | アバ セラピューティクス アーゲー | 抗ヒトpd-l2抗体 |
| SG11202007694UA (en) | 2018-02-21 | 2020-09-29 | Genentech Inc | DOSING FOR TREATMENT WITH IL-22 Fc FUSION PROTEINS |
| CA3091174A1 (en) | 2018-02-21 | 2019-08-29 | Five Prime Therapeutics, Inc. | B7-h4 antibody formulations |
| AU2019226034A1 (en) | 2018-02-21 | 2020-10-15 | The United States Of America, As Represented By The Secretary, Department Of Health And Human Services | Neutralizing antibodies to HIV-1 Env and their use |
| SG11202007820QA (en) | 2018-02-21 | 2020-09-29 | Five Prime Therapeutics Inc | B7-h4 antibody dosing regimens |
| TW202000702A (zh) | 2018-02-26 | 2020-01-01 | 美商建南德克公司 | 用於抗tigit拮抗劑抗體及抗pd-l1拮抗劑抗體治療之投藥 |
| WO2019169212A1 (en) | 2018-03-02 | 2019-09-06 | Five Prime Therapeutics, Inc. | B7-h4 antibodies and methods of use thereof |
| JP2021515770A (ja) | 2018-03-05 | 2021-06-24 | ヤンセン バイオテツク,インコーポレーテツド | 抗il−23特異的抗体を用いたクローン病の治療方法 |
| TW202003561A (zh) | 2018-03-13 | 2020-01-16 | 瑞士商赫孚孟拉羅股份公司 | 使用靶向4-1bb (cd137)之促效劑的組合療法 |
| EP3765489A1 (en) | 2018-03-13 | 2021-01-20 | F. Hoffmann-La Roche AG | Therapeutic combination of 4-1 bb agonists with anti-cd20 antibodies |
| US20200040103A1 (en) | 2018-03-14 | 2020-02-06 | Genentech, Inc. | Anti-klk5 antibodies and methods of use |
| RU2020128013A (ru) | 2018-03-14 | 2022-04-15 | Бейцзин Сюаньи Фармасайенсиз Ко., Лтд. | Антитела против клаудина 18.2 |
| CN112119090B (zh) | 2018-03-15 | 2023-01-13 | 中外制药株式会社 | 对寨卡病毒具有交叉反应性的抗登革热病毒抗体及使用方法 |
| SG11202008593PA (en) | 2018-03-21 | 2020-10-29 | Five Prime Therapeutics Inc | ANTIBODIES BINDING TO VISTA AT ACIDIC pH |
| CN111936625A (zh) | 2018-03-29 | 2020-11-13 | 豪夫迈·罗氏有限公司 | 调节哺乳动物细胞中的生乳活性 |
| SG11202006674QA (en) | 2018-03-30 | 2020-08-28 | Nanjing Legend Biotech Co Ltd | Single-domain antibodies against lag-3 and uses thereof |
| TW202011029A (zh) | 2018-04-04 | 2020-03-16 | 美商建南德克公司 | 偵測及定量fgf21之方法 |
| PE20201345A1 (es) | 2018-04-05 | 2020-11-25 | Juno Therapeutics Inc | Receptores de celulas t, y celulas disenadas que expresan los mismos |
| TW202012440A (zh) | 2018-04-13 | 2020-04-01 | 瑞士商赫孚孟拉羅股份公司 | 包含4-1bbl之靶向her2的抗原結合分子 |
| US20190345245A1 (en) | 2018-05-11 | 2019-11-14 | Janssen Biotech, Inc. | Methods of Treating Crohn's Disease with Anti-IL23 Specific Antibody |
| AU2019271149B2 (en) | 2018-05-14 | 2023-07-13 | Werewolf Therapeutics, Inc. | Activatable interleukin 12 polypeptides and methods of use thereof |
| ES2955511T3 (es) | 2018-05-14 | 2023-12-04 | Werewolf Therapeutics Inc | Polipéptidos de interleucina 2 activables y métodos de uso de los mismos |
| WO2019224275A1 (en) | 2018-05-23 | 2019-11-28 | Adc Therapeutics Sa | Molecular adjuvant |
| WO2019234576A1 (en) | 2018-06-03 | 2019-12-12 | Lamkap Bio Beta Ltd. | Bispecific antibodies against ceacam5 and cd47 |
| WO2019235426A1 (ja) | 2018-06-04 | 2019-12-12 | 中外製薬株式会社 | 細胞質内での半減期が変化した抗原結合分子 |
| US20200030443A1 (en) | 2018-06-23 | 2020-01-30 | Genentech, Inc. | Methods of treating lung cancer with a pd-1 axis binding antagonist, a platinum agent, and a topoisomerase ii inhibitor |
| JP2021528988A (ja) | 2018-07-04 | 2021-10-28 | エフ・ホフマン−ラ・ロシュ・アクチェンゲゼルシャフト | 新規の二重特異性アゴニスト4−1bb抗原結合分子 |
| BR112020027095A2 (pt) | 2018-07-09 | 2021-03-30 | Five Prime Therapeutics, Inc. | Anticorpos de ligação a ilt4 |
| WO2020014306A1 (en) | 2018-07-10 | 2020-01-16 | Immunogen, Inc. | Met antibodies and immunoconjugates and uses thereof |
| KR20210031722A (ko) | 2018-07-11 | 2021-03-22 | 파이브 프라임 테라퓨틱스, 인크. | 산성 pH에서 VISTA에 결합하는 항체 |
| US20200025776A1 (en) | 2018-07-18 | 2020-01-23 | Janssen Biotech, Inc. | Sustained Response Predictors After Treatment With Anti-IL23 Specific Antibody |
| KR20210034622A (ko) | 2018-07-18 | 2021-03-30 | 제넨테크, 인크. | Pd-1 축 결합 길항제, 항 대사제, 및 백금 제제를 이용한 폐암 치료 방법 |
| JP7072715B2 (ja) | 2018-07-20 | 2022-05-20 | サーフィス オンコロジー インコーポレイテッド | 抗cd112r組成物及び方法 |
| KR20210040989A (ko) | 2018-08-03 | 2021-04-14 | 추가이 세이야쿠 가부시키가이샤 | 서로 연결된 2개의 항원 결합 도메인을 포함하는 항원 결합 분자 |
| MA50586A (fr) | 2018-08-09 | 2020-09-16 | Regeneron Pharma | Procédés d'évaluation de l'affinité de liaison d'une variante d'anticorps au récepteur fc néonatal |
| EA202190451A1 (ru) | 2018-08-10 | 2021-07-13 | Чугаи Сейяку Кабусики Кайся | Анти-cd137 антигенсвязывающие молекулы и их применение |
| JP2021534196A (ja) | 2018-08-23 | 2021-12-09 | シージェン インコーポレイテッド | 抗tigit抗体 |
| GB201814281D0 (en) | 2018-09-03 | 2018-10-17 | Femtogenix Ltd | Cytotoxic agents |
| JP2022501332A (ja) | 2018-09-19 | 2022-01-06 | ジェネンテック, インコーポレイテッド | 膀胱がんの治療方法および診断方法 |
| ES2955032T3 (es) | 2018-09-21 | 2023-11-28 | Hoffmann La Roche | Métodos de diagnóstico para el cáncer de mama triple negativo |
| WO2020061560A1 (en) | 2018-09-21 | 2020-03-26 | The University Of North Carolina At Chapel Hill | Synthetic binding agents for limiting permeation through mucus |
| JP7359845B2 (ja) | 2018-09-24 | 2023-10-11 | ヤンセン バイオテツク,インコーポレーテツド | 抗il12/il23抗体で潰瘍性大腸炎を治療する安全かつ有効な方法 |
| WO2020069398A1 (en) | 2018-09-27 | 2020-04-02 | Akrevia Therapeutics Inc. | Masked cytokine polypeptides |
| CN112654641A (zh) | 2018-10-01 | 2021-04-13 | 豪夫迈·罗氏有限公司 | 具有与cd40的三价结合的双特异性抗原结合分子 |
| WO2020070041A1 (en) | 2018-10-01 | 2020-04-09 | F. Hoffmann-La Roche Ag | Bispecific antigen binding molecules comprising anti-fap clone 212 |
| EP3632929A1 (en) | 2018-10-02 | 2020-04-08 | Ospedale San Raffaele S.r.l. | Antibodies and uses thereof |
| AU2019355995A1 (en) | 2018-10-05 | 2021-04-08 | Five Prime Therapeutics, Inc. | Anti-FGFR2 antibody formulations |
| WO2020076969A2 (en) | 2018-10-10 | 2020-04-16 | Tilos Therapeutics, Inc. | Anti-lap antibody variants and uses thereof |
| WO2020081497A1 (en) | 2018-10-15 | 2020-04-23 | Five Prime Therapeutics, Inc. | Combination therapy for cancer |
| WO2020081493A1 (en) | 2018-10-16 | 2020-04-23 | Molecular Templates, Inc. | Pd-l1 binding proteins |
| WO2020081767A1 (en) | 2018-10-18 | 2020-04-23 | Genentech, Inc. | Diagnostic and therapeutic methods for sarcomatoid kidney cancer |
| US20210395390A1 (en) | 2018-10-31 | 2021-12-23 | Bayer Aktiengesellschaft | Reversal agents for neutralizing the therapeutic activity of anti-fxia antibodies |
| MX2021005751A (es) | 2018-11-16 | 2021-10-01 | Memorial Sloan Kettering Cancer Center | Anticuerpos contra mucina 16 y métodos de uso de los mismos. |
| CA3120237A1 (en) | 2018-11-20 | 2020-05-28 | Janssen Biotech, Inc. | Safe and effective method of treating psoriasis with anti-il-23 specific antibody |
| CA3121265A1 (en) | 2018-12-05 | 2020-06-11 | Genentech, Inc. | Diagnostic methods and compositions for cancer immunotherapy |
| EP3892299A4 (en) | 2018-12-07 | 2022-11-30 | ONO Pharmaceutical Co., Ltd. | IMMUNOSUPPRESSANT |
| EP3894427A1 (en) | 2018-12-10 | 2021-10-20 | Genentech, Inc. | Photocrosslinking peptides for site specific conjugation to fc-containing proteins |
| US20200197517A1 (en) | 2018-12-18 | 2020-06-25 | Janssen Biotech, Inc. | Safe and Effective Method of Treating Lupus with Anti-IL12/IL23 Antibody |
| EP3883609A2 (en) | 2018-12-20 | 2021-09-29 | The United States of America, as represented by the Secretary, Department of Health and Human Services | Ebola virus glycoprotein-specific monoclonal antibodies and uses thereof |
| JP2022514290A (ja) | 2018-12-20 | 2022-02-10 | ジェネンテック, インコーポレイテッド | 改変抗体fcおよび使用方法 |
| PE20211603A1 (es) | 2018-12-21 | 2021-08-18 | Hoffmann La Roche | Anticuerpos que se unen a cd3 |
| US11130804B2 (en) | 2018-12-21 | 2021-09-28 | Hoffmann-La Roche Inc. | Antibody that binds to VEGF and IL-1beta and methods of use |
| WO2020127628A1 (en) | 2018-12-21 | 2020-06-25 | F. Hoffmann-La Roche Ag | Tumor-targeted superagonistic cd28 antigen binding molecules |
| CA3123493A1 (en) | 2018-12-21 | 2020-06-25 | F. Hoffmann-La Roche Ag | Tumor-targeted agonistic cd28 antigen binding molecules |
| KR20210141447A (ko) | 2018-12-26 | 2021-11-23 | 실리오 디벨럽먼트, 인크. | 항-ctla4 항체 및 이의 사용 방법 |
| WO2020141145A1 (en) | 2018-12-30 | 2020-07-09 | F. Hoffmann-La Roche Ag | Anti-rabbit cd19 antibodies and methods of use |
| MX2021008434A (es) | 2019-01-14 | 2021-09-23 | Genentech Inc | Metodos para tratar el cancer con un antagonista de union al eje de pd-1 y una vacuna de arn. |
| WO2020148379A1 (en) | 2019-01-17 | 2020-07-23 | Bayer Aktiengesellschaft | Methods to determine whether a subject is suitable of being treated with an agonist of soluble guanylyl cyclase (sgc) |
| EP3915581A4 (en) | 2019-01-24 | 2023-03-22 | Chugai Seiyaku Kabushiki Kaisha | NOVEL CANCER ANTIGENS AND ANTIBODIES OF THESE ANTIGENS |
| GB201901197D0 (en) | 2019-01-29 | 2019-03-20 | Femtogenix Ltd | G-A Crosslinking cytotoxic agents |
| US20220096651A1 (en) | 2019-01-29 | 2022-03-31 | Juno Therapeutics, Inc. | Antibodies and chimeric antigen receptors specific for receptor tyrosine kinase like orphan receptor 1 (ror1) |
| MX2021010313A (es) | 2019-02-27 | 2021-09-23 | Genentech Inc | Dosificacion para el tratamiento con anticuerpos anti-tigit y anti-cd20 o anti-cd38. |
| AU2020238811A1 (en) | 2019-03-08 | 2021-07-22 | Genentech, Inc. | Methods for detecting and quantifying membrane-associated proteins on extracellular vesicles |
| CA3130446A1 (en) | 2019-03-14 | 2020-09-17 | Genentech, Inc. | Treatment of cancer with her2xcd3 bispecific antibodies in combination with anti-her2 mab |
| KR20210141990A (ko) | 2019-03-14 | 2021-11-23 | 얀센 바이오테크 인코포레이티드 | 항-il12/il23 항체 조성물을 생성하기 위한 제조 방법 |
| WO2020188466A1 (en) | 2019-03-18 | 2020-09-24 | Janssen Biotech, Inc. | Method of treating psoriasis in pediatric subjects with anti-il12/il23 antibody |
| GB2589049C (en) | 2019-04-11 | 2024-02-21 | argenx BV | Anti-IgE antibodies |
| WO2020208049A1 (en) | 2019-04-12 | 2020-10-15 | F. Hoffmann-La Roche Ag | Bispecific antigen binding molecules comprising lipocalin muteins |
| AU2020258480A1 (en) | 2019-04-19 | 2021-10-21 | Genentech, Inc. | Anti-mertk antibodies and their methods of use |
| KR20220004087A (ko) | 2019-04-19 | 2022-01-11 | 추가이 세이야쿠 가부시키가이샤 | 항체 개변 부위 인식 키메라 수용체 |
| WO2020227228A2 (en) | 2019-05-03 | 2020-11-12 | The United States Of America, As Represented By The Secretary, Department Of Health And Human Services | Neutralizing antibodies to plasmodium falciparum circumsporozoite protein and their use |
| WO2020226986A2 (en) | 2019-05-03 | 2020-11-12 | Genentech, Inc. | Methods of treating cancer with an anti-pd-l1 antibody |
| JP2022532217A (ja) | 2019-05-14 | 2022-07-13 | ウェアウルフ セラピューティクス, インコーポレイテッド | 分離部分及びその使用方法 |
| AU2020275415A1 (en) | 2019-05-14 | 2021-11-25 | Genentech, Inc. | Methods of using anti-CD79B immunoconjugates to treat follicular lymphoma |
| US20230085439A1 (en) | 2019-05-21 | 2023-03-16 | University Of Georgia Research Foundation, Inc. | Antibodies that bind human metapneumovirus fusion protein and their use |
| AU2020278907A1 (en) | 2019-05-23 | 2022-01-20 | Ac Immune Sa | Anti-TDP-43 binding molecules and uses thereof |
| CN113874073A (zh) | 2019-05-23 | 2021-12-31 | 詹森生物科技公司 | 用针对IL-23和TNFα的抗体的联合疗法治疗炎性肠病的方法 |
| MX2021014756A (es) | 2019-06-07 | 2022-01-18 | Argenx Bvba | Formulaciones farmaceuticas de inhibidores de fcrn adecuadas para administracion subcutanea. |
| CA3141378A1 (en) | 2019-06-26 | 2020-12-30 | F. Hoffmann-La Roche Ag | Fusion of an antibody binding cea and 4-1bbl |
| CN114531878A (zh) | 2019-06-27 | 2022-05-24 | 豪夫迈·罗氏有限公司 | 新颖icos抗体及包含它们的肿瘤靶向抗原结合分子 |
| EP3994173A1 (en) | 2019-07-02 | 2022-05-11 | The United States of America, as represented by the Secretary, Department of Health and Human Services | Monoclonal antibodies that bind egfrviii and their use |
| CN114401992A (zh) | 2019-07-05 | 2022-04-26 | 艾欧麦克斯治疗股份公司 | 结合igsf11(vsig3)的igc2的抗体及其用途 |
| CN114341187A (zh) | 2019-07-12 | 2022-04-12 | 中外制药株式会社 | 抗突变型fgfr3抗体及其用途 |
| AR119382A1 (es) | 2019-07-12 | 2021-12-15 | Hoffmann La Roche | Anticuerpos de pre-direccionamiento y métodos de uso |
| AR119393A1 (es) | 2019-07-15 | 2021-12-15 | Hoffmann La Roche | Anticuerpos que se unen a nkg2d |
| WO2021021605A1 (en) | 2019-07-26 | 2021-02-04 | Vanderbilt University | Human monoclonal antibodies to enterovirus d68 |
| JP2022543551A (ja) | 2019-07-31 | 2022-10-13 | エフ・ホフマン-ラ・ロシュ・アクチェンゲゼルシャフト | Gprc5dに結合する抗体 |
| CR20220019A (es) | 2019-07-31 | 2022-02-11 | Hoffmann La Roche | Anticuerpos que se fijan a gprc5d |
| KR102509648B1 (ko) | 2019-08-06 | 2023-03-15 | 아프리노이아 테라퓨틱스 리미티드 | 병리학적 타우 종에 결합하는 항체 및 이의 용도 |
| CN114340675A (zh) | 2019-09-12 | 2022-04-12 | 豪夫迈·罗氏有限公司 | 治疗狼疮性肾炎的组合物和方法 |
| PE20221906A1 (es) | 2019-09-18 | 2022-12-23 | Genentech Inc | Anticuerpos anti-klk7, anticuerpos anti-klk5, anticuerpos multiespecificos anti-klk5/klk7 y metodos de uso |
| MX2022003204A (es) | 2019-09-19 | 2022-04-18 | Bristol Myers Squibb Co | Anticuerpos de union al supresor de activacion de linfocitos t que contiene inmunoglobulina con dominio v (vista) a ph acido. |
| CR20220149A (es) | 2019-09-20 | 2022-05-23 | Genentech Inc | Dosis para anticuerpos anti-triptasa |
| JP2022548978A (ja) | 2019-09-27 | 2022-11-22 | ジェネンテック, インコーポレイテッド | 薬抗tigit及び抗pd-l1アンタゴニスト抗体を用いた処置のための投薬 |
| JP7413519B2 (ja) | 2019-10-18 | 2024-01-15 | ジェネンテック, インコーポレイテッド | びまん性大細胞型b細胞リンパ腫を処置するための抗cd79b免疫抱合体の使用方法 |
| IL292458A (en) | 2019-11-06 | 2022-06-01 | Genentech Inc | Diagnostic and treatment methods for the treatment of hematological cancer |
| CN114651006A (zh) | 2019-11-15 | 2022-06-21 | 恩瑟拉有限责任公司 | Tmem219抗体及其治疗性用途 |
| EP3822288A1 (en) | 2019-11-18 | 2021-05-19 | Deutsches Krebsforschungszentrum, Stiftung des öffentlichen Rechts | Antibodies targeting, and other modulators of, the cd276 antigen, and uses thereof |
| JP2023503105A (ja) | 2019-11-21 | 2023-01-26 | エンテラ・エッセ・エッレ・エッレ | Igfbp3抗体及びその治療的使用 |
| EP3831849A1 (en) | 2019-12-02 | 2021-06-09 | LamKap Bio beta AG | Bispecific antibodies against ceacam5 and cd47 |
| KR20220122656A (ko) | 2019-12-06 | 2022-09-02 | 주노 쎄러퓨티크스 인코퍼레이티드 | Gprc5d-표적화 결합 도메인에 대한 항-이디오타입 항체 및 관련 조성물 및 방법 |
| CA3163897A1 (en) | 2019-12-06 | 2021-06-10 | Juno Therapeutics, Inc. | Anti-idiotypic antibodies to bcma-targeted binding domains and related compositions and methods |
| AU2020403145A1 (en) | 2019-12-13 | 2022-07-07 | Genentech, Inc. | Anti-Ly6G6D antibodies and methods of use |
| US20210230278A1 (en) | 2019-12-18 | 2021-07-29 | Hoffmann-La Roche Inc. | Antibodies binding to HLA-A2/MAGE-A4 |
| CN113045655A (zh) | 2019-12-27 | 2021-06-29 | 高诚生物医药(香港)有限公司 | 抗ox40抗体及其用途 |
| AU2019479791A1 (en) | 2019-12-27 | 2022-07-14 | Chugai Seiyaku Kabushiki Kaisha | Anti-CTLA-4 antibody and use thereof |
| US20210236596A1 (en) | 2020-01-08 | 2021-08-05 | argenx BV | Methods for treating pemphigus disorders |
| KR20220107251A (ko) | 2020-01-09 | 2022-08-02 | 에프. 호프만-라 로슈 아게 | 새로운 4-1bbl 삼량체-함유 항원 결합 분자 |
| CN110818795B (zh) | 2020-01-10 | 2020-04-24 | 上海复宏汉霖生物技术股份有限公司 | 抗tigit抗体和使用方法 |
| WO2021194481A1 (en) | 2020-03-24 | 2021-09-30 | Genentech, Inc. | Dosing for treatment with anti-tigit and anti-pd-l1 antagonist antibodies |
| WO2022050954A1 (en) | 2020-09-04 | 2022-03-10 | Genentech, Inc. | Dosing for treatment with anti-tigit and anti-pd-l1 antagonist antibodies |
| EP4096708A1 (en) | 2020-01-31 | 2022-12-07 | Genentech, Inc. | Methods of inducing neoepitope-specific t cells with a pd-1 axis binding antagonist and an rna vaccine |
| WO2021155295A1 (en) | 2020-01-31 | 2021-08-05 | The Cleveland Clinic Foundation | Anti-müllerian hormone receptor 2 antibodies and methods of use |
| KR20220140568A (ko) | 2020-02-11 | 2022-10-18 | 벤더르빌트 유니버시티 | 중증 급성 호흡기 증후군 코로나바이러스 2(SARS-CoV-2)에 대한 인간 단일클론 항체 |
| TW202144395A (zh) | 2020-02-12 | 2021-12-01 | 日商中外製藥股份有限公司 | 用於癌症之治療的抗cd137抗原結合分子 |
| WO2021163064A2 (en) | 2020-02-14 | 2021-08-19 | Jounce Therapeutics, Inc. | Antibodies and fusion proteins that bind to ccr8 and uses thereof |
| US20230348568A1 (en) | 2020-02-20 | 2023-11-02 | The U.S.A., As Represented By The Secretary, Department Of Health And Human Services | Epstein-barr virus monoclonal antibodies and uses thereof |
| EP3868396A1 (en) | 2020-02-20 | 2021-08-25 | Enthera S.R.L. | Inhibitors and uses thereof |
| CA3169910A1 (en) | 2020-02-28 | 2021-09-02 | Shanghai Henlius Biotech, Inc. | Anti-cd137 constructs, multispecific antibody and uses thereof |
| CN115066440A (zh) | 2020-02-28 | 2022-09-16 | 上海复宏汉霖生物技术股份有限公司 | 抗cd137构建体及其用途 |
| AU2021231890A1 (en) | 2020-03-06 | 2022-09-29 | Go Therapeutics, Inc. | Anti-glyco-CD44 antibodies and their uses |
| IL296256A (en) | 2020-03-13 | 2022-11-01 | Genentech Inc | Antibodies against interleukin-33 and uses thereof |
| CN117510630A (zh) | 2020-03-19 | 2024-02-06 | 基因泰克公司 | 同种型选择性抗TGF-β抗体及使用方法 |
| JP2023518815A (ja) | 2020-03-23 | 2023-05-08 | ジェネンテック, インコーポレイテッド | Il6アンタゴニストによるcovid-19肺炎を含む肺炎の治療方法 |
| JP2023518814A (ja) | 2020-03-23 | 2023-05-08 | ジェネンテック, インコーポレイテッド | Covid-19肺炎における、il-6アンタゴニストに対する応答を予測するためのバイオマーカー |
| EP4107186A1 (en) | 2020-03-23 | 2022-12-28 | Genentech, Inc. | Tocilizumab and remdesivir combination therapy for covid-19 pneumonia |
| WO2021194913A1 (en) | 2020-03-24 | 2021-09-30 | Genentech, Inc. | Tie2-binding agents and methods of use |
| EP4127153A2 (en) | 2020-03-26 | 2023-02-08 | Genentech, Inc. | Modified mammalian cells having reduced host cell proteins |
| WO2021195385A1 (en) | 2020-03-26 | 2021-09-30 | Vanderbilt University | HUMAN MONOCLONAL ANTIBODIES TO SEVERE ACUTE RESPIRATORY SYNDROME CORONAVIRUS 2 (SARS-GoV-2) |
| CN115768790A (zh) | 2020-03-26 | 2023-03-07 | 范德比尔特大学 | 针对严重急性呼吸综合征冠状病毒2(SARS-CoV-2)的人单克隆抗体 |
| AR121706A1 (es) | 2020-04-01 | 2022-06-29 | Hoffmann La Roche | Moléculas de unión a antígeno biespecíficas dirigidas a ox40 y fap |
| WO2021202959A1 (en) | 2020-04-03 | 2021-10-07 | Genentech, Inc. | Therapeutic and diagnostic methods for cancer |
| WO2021207449A1 (en) | 2020-04-09 | 2021-10-14 | Merck Sharp & Dohme Corp. | Affinity matured anti-lap antibodies and uses thereof |
| WO2021207662A1 (en) | 2020-04-10 | 2021-10-14 | Genentech, Inc. | Use of il-22fc for the treatment or prevention of pneumonia, acute respiratory distress syndrome, or cytokine release syndrome |
| IL297541A (en) | 2020-04-24 | 2022-12-01 | Genentech Inc | Methods for using anti-cd79b immunoconjugates |
| WO2021222181A2 (en) | 2020-04-27 | 2021-11-04 | The Regents Of The University Of California | Isoform-independent antibodies to lipoprotein(a) |
| WO2021222167A1 (en) | 2020-04-28 | 2021-11-04 | Genentech, Inc. | Methods and compositions for non-small cell lung cancer immunotherapy |
| EP4146283A1 (en) | 2020-05-03 | 2023-03-15 | Levena (Suzhou) Biopharma Co., Ltd. | Antibody-drug conjugates (adcs) comprising an anti-trop-2 antibody, compositions comprising such adcs, as well as methods of making and using the same |
| WO2021233834A1 (en) | 2020-05-17 | 2021-11-25 | Astrazeneca Uk Limited | Sars-cov-2 antibodies and methods of selecting and using the same |
| EP4157881A1 (en) | 2020-05-27 | 2023-04-05 | Staidson (Beijing) Biopharmaceuticals Co., Ltd. | Antibodies specifically recognizing nerve growth factor and uses thereof |
| IL298735A (en) | 2020-06-02 | 2023-02-01 | Dynamicure Biotechnology Llc | Anti-CD93 constructs and their uses |
| CN116529260A (zh) | 2020-06-02 | 2023-08-01 | 当康生物技术有限责任公司 | 抗cd93构建体及其用途 |
| AR122569A1 (es) | 2020-06-08 | 2022-09-21 | Hoffmann La Roche | Anticuerpos anti-vhb y métodos de uso |
| WO2021252977A1 (en) | 2020-06-12 | 2021-12-16 | Genentech, Inc. | Methods and compositions for cancer immunotherapy |
| KR20230025691A (ko) | 2020-06-16 | 2023-02-22 | 제넨테크, 인크. | 삼중 음성 유방암을 치료하기 위한 방법과 조성물 |
| KR20230024368A (ko) | 2020-06-18 | 2023-02-20 | 제넨테크, 인크. | 항-tigit 항체 및 pd-1 축 결합 길항제를 사용한 치료 |
| TW202216766A (zh) | 2020-06-19 | 2022-05-01 | 瑞士商赫孚孟拉羅股份公司 | 與cd3結合之抗體 |
| WO2021255143A1 (en) | 2020-06-19 | 2021-12-23 | F. Hoffmann-La Roche Ag | Antibodies binding to cd3 and folr1 |
| AU2021291011A1 (en) | 2020-06-19 | 2023-01-05 | F. Hoffmann-La Roche Ag | Antibodies binding to CD3 and CD19 |
| WO2021255146A1 (en) | 2020-06-19 | 2021-12-23 | F. Hoffmann-La Roche Ag | Antibodies binding to cd3 and cea |
| EP4168448A1 (en) | 2020-06-23 | 2023-04-26 | F. Hoffmann-La Roche AG | Agonistic cd28 antigen binding molecules targeting her2 |
| JP2023533217A (ja) | 2020-06-24 | 2023-08-02 | ジェネンテック, インコーポレイテッド | アポトーシス耐性細胞株 |
| EP4172203A1 (en) | 2020-06-25 | 2023-05-03 | F. Hoffmann-La Roche AG | Anti-cd3/anti-cd28 bispecific antigen binding molecules |
| US20240010720A1 (en) | 2020-07-06 | 2024-01-11 | Iomx Therapeutics Ag | Antibodies binding igv of igsf11 (vsig3) and uses thereof |
| MX2023000339A (es) | 2020-07-10 | 2023-02-09 | Hoffmann La Roche | Anticuerpos que se unen a celulas cancerosas y dirigen radionucleotidos a dichas celulas. |
| PE20231300A1 (es) | 2020-07-17 | 2023-08-24 | Genentech Inc | Anticuerpos anti-notch2 y metodos de uso |
| GB2597532A (en) | 2020-07-28 | 2022-02-02 | Femtogenix Ltd | Cytotoxic compounds |
| CA3190328A1 (en) | 2020-07-29 | 2022-02-03 | Dynamicure Biotechnology Llc | Anti-cd93 constructs and uses thereof |
| JP2023536602A (ja) | 2020-08-03 | 2023-08-28 | ジェネンテック, インコーポレイテッド | リンパ腫のための診断及び治療方法 |
| JP2023536326A (ja) | 2020-08-05 | 2023-08-24 | ジュノー セラピューティクス インコーポレイテッド | Ror1標的結合ドメインに対する抗イディオタイプ抗体ならびに関連する組成物および方法 |
| MX2023001440A (es) | 2020-08-07 | 2023-03-06 | Genentech Inc | Proteinas de fusion del ligando para flt3 y metodos de uso. |
| WO2022034044A1 (en) | 2020-08-10 | 2022-02-17 | Astrazeneca Uk Limited | Sars-cov-2 antibodies for treatment and prevention of covid-19 |
| AR123254A1 (es) | 2020-08-14 | 2022-11-16 | Ac Immune Sa | Moléculas de unión anti-tdp-43 humanizadas y usos de las mismas |
| EP4204448A2 (en) | 2020-08-27 | 2023-07-05 | cureab GmbH | Anti-golph2 antibodies for macrophage and dendritic cell differentiation |
| CA3192344A1 (en) | 2020-08-28 | 2022-03-03 | Genentech, Inc. | Crispr/cas9 multiplex knockout of host cell proteins |
| KR20230061458A (ko) | 2020-09-04 | 2023-05-08 | 에프. 호프만-라 로슈 아게 | Vegf-a 및 ang2에 결합하는 항체 및 사용 방법 |
| TW202227505A (zh) | 2020-09-15 | 2022-07-16 | 德商拜耳廠股份有限公司 | 新穎抗a2ap抗體及其用途 |
| EP4213877A1 (en) | 2020-09-17 | 2023-07-26 | Genentech, Inc. | Results of empacta: a randomized, double-blind, placebo-controlled, multicenter study to evaluate the efficacy and safety of tocilizumab in hospitalized patients with covid-19 pneumonia |
| CN116406291A (zh) | 2020-10-05 | 2023-07-07 | 基因泰克公司 | 用抗fcrh5/抗cd3双特异性抗体进行治疗的给药 |
| WO2022079211A1 (en) | 2020-10-16 | 2022-04-21 | Adc Therapeutics Sa | Glycoconjugates |
| EP4232040A1 (en) | 2020-10-20 | 2023-08-30 | F. Hoffmann-La Roche AG | Combination therapy of pd-1 axis binding antagonists and lrrk2 inhitibors |
| AU2021366287A1 (en) | 2020-10-20 | 2023-04-13 | Kantonsspital St. Gallen | Antibodies or antigen-binding fragments specifically binding to Gremlin-1 and uses thereof |
| AR123855A1 (es) | 2020-10-20 | 2023-01-18 | Genentech Inc | Anticuerpos anti-mertk conjugados con peg y métodos de uso |
| WO2022093981A1 (en) | 2020-10-28 | 2022-05-05 | Genentech, Inc. | Combination therapy comprising ptpn22 inhibitors and pd-l1 binding antagonists |
| AU2021374803A1 (en) | 2020-11-03 | 2023-06-22 | Deutsches Krebsforschungszentrum Stiftung des öffentlichen Rechts | Target-cell restricted, costimulatory, bispecific and bivalent anti-cd28 antibodies |
| CA3196076A1 (en) | 2020-11-04 | 2022-05-12 | Chi-Chung Li | Subcutaneous dosing of anti-cd20/anti-cd3 bispecific antibodies |
| CA3196539A1 (en) | 2020-11-04 | 2022-05-12 | Chi-Chung Li | Dosing for treatment with anti-cd20/anti-cd3 bispecific antibodies |
| AU2021374594A1 (en) | 2020-11-04 | 2023-06-01 | Genentech, Inc. | Dosing for treatment with anti-cd20/anti-cd3 bispecific antibodies and anti-cd79b antibody drug conjugates |
| CN117916261A (zh) | 2020-11-16 | 2024-04-19 | 豪夫迈·罗氏有限公司 | 与靶向fap的cd40激动剂的组合疗法 |
| CA3199648A1 (en) | 2020-12-02 | 2022-06-09 | Gerben BOUMA | Il-7 binding proteins and their use in medical therapy |
| TW202237638A (zh) | 2020-12-09 | 2022-10-01 | 日商武田藥品工業股份有限公司 | 烏苷酸環化酶c(gcc)抗原結合劑之組成物及其使用方法 |
| TW202237639A (zh) | 2020-12-09 | 2022-10-01 | 日商武田藥品工業股份有限公司 | 鳥苷酸環化酶c(gcc)抗原結合劑之組成物及其使用方法 |
| WO2022132904A1 (en) | 2020-12-17 | 2022-06-23 | The United States Of America, As Represented By The Secretary, Department Of Health And Human Services | Human monoclonal antibodies targeting sars-cov-2 |
| CN116829598A (zh) | 2021-01-06 | 2023-09-29 | 豪夫迈·罗氏有限公司 | 采用pd1-lag3双特异性抗体和cd20 t细胞双特异性抗体的组合疗法 |
| EP4277705A1 (en) | 2021-01-12 | 2023-11-22 | F. Hoffmann-La Roche AG | Split antibodies which bind to cancer cells and target radionuclides to said cells |
| CA3204291A1 (en) | 2021-01-13 | 2022-07-21 | F. Hoffmann-La Roche Ag | Combination therapy |
| WO2022162587A1 (en) | 2021-01-27 | 2022-08-04 | Centre Hospitalier Universitaire Vaudois (C.H.U.V.) | Anti-sars-cov-2 antibodies and use thereof in the treatment of sars-cov-2 infection |
| WO2022162203A1 (en) | 2021-01-28 | 2022-08-04 | Vaccinvent Gmbh | Method and means for modulating b-cell mediated immune responses |
| EP4284422A1 (en) | 2021-01-28 | 2023-12-06 | Vaccinvent GmbH | Method and means for modulating b-cell mediated immune responses |
| CN117120084A (zh) | 2021-01-28 | 2023-11-24 | 维肯芬特有限责任公司 | 用于调节b细胞介导的免疫应答的方法和手段 |
| WO2022169872A1 (en) | 2021-02-03 | 2022-08-11 | Genentech, Inc. | Multispecific binding protein degrader platform and methods of use |
| CA3210753A1 (en) | 2021-02-09 | 2022-08-18 | University Of Georgia Research Foundation, Inc. | Human monoclonal antibodies against pneumococcal antigens |
| IL304955A (en) | 2021-02-09 | 2023-10-01 | Us Health | Antibodies targeting the spike protein of a coronavirus |
| CA3208365A1 (en) | 2021-02-15 | 2022-08-18 | Chantal KUHN | Cell therapy compositions and methods for modulating tgf-b signaling |
| GB202102396D0 (en) | 2021-02-19 | 2021-04-07 | Adc Therapeutics Sa | Molecular adjuvant |
| US20240124572A1 (en) | 2021-02-26 | 2024-04-18 | Bayer Aktiengesellschaft | INHIBITORS OF IL-11 OR IL-11Ra FOR USE IN THE TREATMENT OF ABNORMAL UTERINE BLEEDING |
| CA3209364A1 (en) | 2021-03-01 | 2022-09-09 | Jennifer O'neil | Combination of masked ctla4 and pd1/pdl1 antibodies for treating cancer |
| WO2022187270A1 (en) | 2021-03-01 | 2022-09-09 | Xilio Development, Inc. | Combination of ctla4 and pd1/pdl1 antibodies for treating cancer |
| WO2022184082A1 (en) | 2021-03-03 | 2022-09-09 | Sorrento Therapeutics, Inc. | Antibody-drug conjugates comprising an anti-bcma antibody |
| JP2024509191A (ja) | 2021-03-05 | 2024-02-29 | ダイナミキュア バイオテクノロジー エルエルシー | 抗vista構築物およびその使用 |
| WO2022187591A1 (en) | 2021-03-05 | 2022-09-09 | Go Therapeutics, Inc. | Anti-glyco-cd44 antibodies and their uses |
| WO2022192647A1 (en) | 2021-03-12 | 2022-09-15 | Genentech, Inc. | Anti-klk7 antibodies, anti-klk5 antibodies, multispecific anti-klk5/klk7 antibodies, and methods of use |
| WO2022190034A1 (en) | 2021-03-12 | 2022-09-15 | Janssen Biotech, Inc. | Method of treating psoriatic arthritis patients with inadequate response to tnf therapy with anti-il23 specific antibody |
| WO2022190033A1 (en) | 2021-03-12 | 2022-09-15 | Janssen Biotech, Inc. | Safe and effective method of treating psoriatic arthritis with anti-il23 specific antibody |
| WO2022198192A1 (en) | 2021-03-15 | 2022-09-22 | Genentech, Inc. | Compositions and methods of treating lupus nephritis |
| WO2022197877A1 (en) | 2021-03-19 | 2022-09-22 | Genentech, Inc. | Methods and compositions for time delayed bio-orthogonal release of cytotoxic agents |
| EP4314049A1 (en) | 2021-03-25 | 2024-02-07 | Dynamicure Biotechnology LLC | Anti-igfbp7 constructs and uses thereof |
| EP4314047A1 (en) | 2021-03-30 | 2024-02-07 | Bayer Aktiengesellschaft | Anti-sema3a antibodies and uses thereof |
| AR125344A1 (es) | 2021-04-15 | 2023-07-05 | Chugai Pharmaceutical Co Ltd | Anticuerpo anti-c1s |
| JP2024514222A (ja) | 2021-04-19 | 2024-03-28 | ジェネンテック, インコーポレイテッド | 改変された哺乳動物細胞 |
| JP2024514281A (ja) | 2021-04-23 | 2024-04-01 | エフ・ホフマン-ラ・ロシュ・アクチェンゲゼルシャフト | Nk細胞係合剤関連の有害作用の防止または軽減 |
| KR20240005691A (ko) | 2021-04-30 | 2024-01-12 | 에프. 호프만-라 로슈 아게 | 항-cd20/항-cd3 이중특이적 항체 및 항-cd79b 항체 약물 접합체를 이용한 병용 치료를 위한 투약 |
| CA3218170A1 (en) | 2021-05-12 | 2022-11-17 | Jamie Harue HIRATA | Methods of using anti-cd79b immunoconjugates to treat diffuse large b-cell lymphoma |
| WO2022241082A1 (en) | 2021-05-14 | 2022-11-17 | Genentech, Inc. | Agonists of trem2 |
| WO2022243261A1 (en) | 2021-05-19 | 2022-11-24 | F. Hoffmann-La Roche Ag | Agonistic cd40 antigen binding molecules targeting cea |
| WO2022246259A1 (en) | 2021-05-21 | 2022-11-24 | Genentech, Inc. | Modified cells for the production of a recombinant product of interest |
| BR112023024804A2 (pt) | 2021-05-28 | 2024-02-15 | Glaxosmithkline Ip Dev Ltd | Terapias de combinação para tratar câncer |
| AR126009A1 (es) | 2021-06-02 | 2023-08-30 | Hoffmann La Roche | Moléculas agonistas de unión al antígeno cd28 que se dirigen a epcam |
| TW202306994A (zh) | 2021-06-04 | 2023-02-16 | 日商中外製藥股份有限公司 | 抗ddr2抗體及其用途 |
| IL308015A (en) | 2021-06-09 | 2023-12-01 | Hoffmann La Roche | A combination of a specific BRAF inhibitor (paradox breaker) and a PD-1 spindle-binding antagonist for use in cancer treatment |
| WO2022261417A1 (en) | 2021-06-11 | 2022-12-15 | Genentech, Inc. | Method for treating chronic obstructive pulmonary disease with an st2 antagonist |
| WO2022263638A1 (en) | 2021-06-17 | 2022-12-22 | Centre Hospitalier Universitaire Vaudois (C.H.U.V.) | Anti-sars-cov-2 antibodies and use thereof in the treatment of sars-cov-2 infection |
| EP4355785A1 (en) | 2021-06-17 | 2024-04-24 | Amberstone Biosciences, Inc. | Anti-cd3 constructs and uses thereof |
| EP4361176A1 (en) | 2021-06-25 | 2024-05-01 | Chugai Seiyaku Kabushiki Kaisha | Use of anti-ctla-4 antibody |
| EP4361273A1 (en) | 2021-06-25 | 2024-05-01 | Chugai Seiyaku Kabushiki Kaisha | Anti-ctla-4 antibody |
| TW202317633A (zh) | 2021-07-08 | 2023-05-01 | 美商舒泰神(加州)生物科技有限公司 | 特異性識別tnfr2的抗體及其用途 |
| AU2022306973A1 (en) | 2021-07-09 | 2024-02-22 | Janssen Biotech, Inc. | Manufacturing methods for producing anti-il12/il23 antibody compositions |
| WO2023288182A1 (en) | 2021-07-12 | 2023-01-19 | Genentech, Inc. | Structures for reducing antibody-lipase binding |
| WO2023284714A1 (zh) | 2021-07-14 | 2023-01-19 | 舒泰神(北京)生物制药股份有限公司 | 特异性识别cd40的抗体及其应用 |
| IL309856A (en) | 2021-07-14 | 2024-02-01 | Genentech Inc | Antibodies anti-C-C motif receptor 8 (CCR8) and methods of use |
| WO2023004386A1 (en) | 2021-07-22 | 2023-01-26 | Genentech, Inc. | Brain targeting compositions and methods of use thereof |
| WO2023001884A1 (en) | 2021-07-22 | 2023-01-26 | F. Hoffmann-La Roche Ag | Heterodimeric fc domain antibodies |
| CN117794953A (zh) | 2021-08-03 | 2024-03-29 | 豪夫迈·罗氏有限公司 | 双特异性抗体及使用方法 |
| WO2023014863A1 (en) | 2021-08-05 | 2023-02-09 | Go Therapeutics, Inc. | Anti-glyco-muc4 antibodies and their uses |
| WO2023019092A1 (en) | 2021-08-07 | 2023-02-16 | Genentech, Inc. | Methods of using anti-cd79b immunoconjugates to treat diffuse large b-cell lymphoma |
| CA3228243A1 (en) | 2021-08-13 | 2023-02-16 | Peiling CHEN | Cytotoxicity targeting chimeras for ccr2-expressing cells |
| WO2023019239A1 (en) | 2021-08-13 | 2023-02-16 | Genentech, Inc. | Dosing for anti-tryptase antibodies |
| AU2022327859A1 (en) | 2021-08-13 | 2024-02-22 | Glaxosmithkline Intellectual Property Development Limited | Cytotoxicity targeting chimeras |
| WO2023021055A1 (en) | 2021-08-19 | 2023-02-23 | F. Hoffmann-La Roche Ag | Multivalent anti-variant fc-region antibodies and methods of use |
| CA3229448A1 (en) | 2021-08-23 | 2023-03-02 | Immunitas Therapeutics, Inc. | Anti-cd161 antibodies and uses thereof |
| AU2022332303A1 (en) | 2021-08-27 | 2024-02-01 | Genentech, Inc. | Methods of treating tau pathologies |
| TW202325727A (zh) | 2021-08-30 | 2023-07-01 | 美商建南德克公司 | 抗聚泛素多特異性抗體 |
| WO2023034571A1 (en) | 2021-09-03 | 2023-03-09 | Go Therapeutics, Inc. | Anti-glyco-lamp1 antibodies and their uses |
| AU2022339667A1 (en) | 2021-09-03 | 2024-04-11 | Go Therapeutics, Inc. | Anti-glyco-cmet antibodies and their uses |
| AU2022345251A1 (en) | 2021-09-17 | 2024-03-28 | The United States Of America, As Represented By The Secretary, Department Of Health And Human Services | Synthetic humanized llama nanobody library and use thereof to identify sars-cov-2 neutralizing antibodies |
| WO2023056403A1 (en) | 2021-09-30 | 2023-04-06 | Genentech, Inc. | Methods for treatment of hematologic cancers using anti-tigit antibodies, anti-cd38 antibodies, and pd-1 axis binding antagonists |
| WO2023057893A1 (en) | 2021-10-05 | 2023-04-13 | Glaxosmithkline Intellectual Property Development Limited | Combination therapies for treating cancer |
| WO2023073615A1 (en) | 2021-10-29 | 2023-05-04 | Janssen Biotech, Inc. | Methods of treating crohn's disease with anti-il23 specific antibody |
| WO2023081818A1 (en) | 2021-11-05 | 2023-05-11 | American Diagnostics & Therapy, Llc (Adxrx) | Monoclonal antibodies against carcinoembryonic antigens, and their uses |
| TW202342095A (zh) | 2021-11-05 | 2023-11-01 | 英商阿斯特捷利康英國股份有限公司 | 用於治療和預防covid—19之組成物 |
| WO2023086807A1 (en) | 2021-11-10 | 2023-05-19 | Genentech, Inc. | Anti-interleukin-33 antibodies and uses thereof |
| WO2023084488A1 (en) | 2021-11-15 | 2023-05-19 | Janssen Biotech, Inc. | Methods of treating crohn's disease with anti-il23 specific antibody |
| CA3235206A1 (en) | 2021-11-16 | 2023-05-25 | Davide BASCO | Novel molecules for therapy and diagnosis |
| TW202337494A (zh) | 2021-11-16 | 2023-10-01 | 美商建南德克公司 | 用莫蘇妥珠單抗治療全身性紅斑狼瘡(sle)之方法及組成物 |
| US20230159633A1 (en) | 2021-11-23 | 2023-05-25 | Janssen Biotech, Inc. | Method of Treating Ulcerative Colitis with Anti-IL23 Specific Antibody |
| WO2023094569A1 (en) | 2021-11-26 | 2023-06-01 | F. Hoffmann-La Roche Ag | Combination therapy of anti-tyrp1/anti-cd3 bispecific antibodies and tyrp1-specific antibodies |
| AR127887A1 (es) | 2021-12-10 | 2024-03-06 | Hoffmann La Roche | Anticuerpos que se unen a cd3 y plap |
| TW202340248A (zh) | 2021-12-20 | 2023-10-16 | 瑞士商赫孚孟拉羅股份公司 | 促效性ltbr抗體及包含其之雙特異性抗體 |
| WO2023131901A1 (en) | 2022-01-07 | 2023-07-13 | Johnson & Johnson Enterprise Innovation Inc. | Materials and methods of il-1beta binding proteins |
| TW202340251A (zh) | 2022-01-19 | 2023-10-16 | 美商建南德克公司 | 抗notch2抗體及結合物及其使用方法 |
| WO2023154824A1 (en) | 2022-02-10 | 2023-08-17 | The United States Of America, As Represented By The Secretary, Department Of Health And Human Services | Human monoclonal antibodies that broadly target coronaviruses |
| TW202342519A (zh) | 2022-02-16 | 2023-11-01 | 瑞士商Ac 免疫有限公司 | 人源化抗tdp-43結合分子及其用途 |
| TW202342520A (zh) | 2022-02-18 | 2023-11-01 | 美商樂天醫藥生技股份有限公司 | 抗計畫性死亡配體1(pd—l1)抗體分子、編碼多核苷酸及使用方法 |
| WO2023161876A1 (en) | 2022-02-25 | 2023-08-31 | Glaxosmithkline Intellectual Property Development Limited | Cytotoxicity targeting chimeras for cxcr3-expressing cells |
| WO2023161881A1 (en) | 2022-02-25 | 2023-08-31 | Glaxosmithkline Intellectual Property Development Limited | Cytotoxicity targeting chimeras for ccr2-expressing cells |
| WO2023161874A1 (en) | 2022-02-25 | 2023-08-31 | Glaxosmithkline Intellectual Property Development Limited | Cytotoxicity targeting chimeras for c-c chemokine receptor 2-expressing cells |
| WO2023161879A1 (en) | 2022-02-25 | 2023-08-31 | Glaxosmithkline Intellectual Property Development Limited | Cytotoxicity targeting chimeras for fibroblast activation protein-expressing cells |
| WO2023161875A1 (en) | 2022-02-25 | 2023-08-31 | Glaxosmithkline Intellectual Property Development Limited | Cytotoxicity targeting chimeras for prostate specific membrane antigen-expressing cells |
| WO2023161877A1 (en) | 2022-02-25 | 2023-08-31 | Glaxosmithkline Intellectual Property Development Limited | Cytotoxicity targeting chimeras for integrin avb6-expressing cells |
| WO2023161878A1 (en) | 2022-02-25 | 2023-08-31 | Glaxosmithkline Intellectual Property Development Limited | Cytotoxicity targeting chimeras for folate receptor-expressing cells |
| WO2023173026A1 (en) | 2022-03-10 | 2023-09-14 | Sorrento Therapeutics, Inc. | Antibody-drug conjugates and uses thereof |
| TW202346365A (zh) | 2022-03-23 | 2023-12-01 | 瑞士商赫孚孟拉羅股份公司 | 抗cd20/抗cd3雙特異性抗體及化學療法之組合治療 |
| WO2023192827A1 (en) | 2022-03-26 | 2023-10-05 | The United States Of America, As Represented By The Secretary, Department Of Health And Human Services | Bispecific antibodies to hiv-1 env and their use |
| WO2023192881A1 (en) | 2022-03-28 | 2023-10-05 | The United States Of America, As Represented By The Secretary, Department Of Health And Human Services | Neutralizing antibodies to hiv-1 env and their use |
| WO2023186756A1 (en) | 2022-03-28 | 2023-10-05 | F. Hoffmann-La Roche Ag | Interferon gamma variants and antigen binding molecules comprising these |
| WO2023187707A1 (en) | 2022-03-30 | 2023-10-05 | Janssen Biotech, Inc. | Method of treating mild to moderate psoriasis with il-23 specific antibody |
| WO2023191816A1 (en) | 2022-04-01 | 2023-10-05 | Genentech, Inc. | Dosing for treatment with anti-fcrh5/anti-cd3 bispecific antibodies |
| GB202204813D0 (en) | 2022-04-01 | 2022-05-18 | Bradcode Ltd | Human monoclonal antibodies and methods of use thereof |
| WO2023194565A1 (en) | 2022-04-08 | 2023-10-12 | Ac Immune Sa | Anti-tdp-43 binding molecules |
| WO2023198727A1 (en) | 2022-04-13 | 2023-10-19 | F. Hoffmann-La Roche Ag | Pharmaceutical compositions of anti-cd20/anti-cd3 bispecific antibodies and methods of use |
| WO2023201299A1 (en) | 2022-04-13 | 2023-10-19 | Genentech, Inc. | Pharmaceutical compositions of therapeutic proteins and methods of use |
| WO2023203177A1 (en) | 2022-04-20 | 2023-10-26 | Kantonsspital St. Gallen | Antibodies or antigen-binding fragments pan-specifically binding to gremlin-1 and gremlin-2 and uses thereof |
| WO2023209177A1 (en) | 2022-04-29 | 2023-11-02 | Astrazeneca Uk Limited | Sars-cov-2 antibodies and methods of using the same |
| US20230348604A1 (en) | 2022-04-29 | 2023-11-02 | 23Andme, Inc. | Antigen binding proteins |
| WO2023215737A1 (en) | 2022-05-03 | 2023-11-09 | Genentech, Inc. | Anti-ly6e antibodies, immunoconjugates, and uses thereof |
| WO2023217933A1 (en) | 2022-05-11 | 2023-11-16 | F. Hoffmann-La Roche Ag | Antibody that binds to vegf-a and il6 and methods of use |
| WO2023219613A1 (en) | 2022-05-11 | 2023-11-16 | Genentech, Inc. | Dosing for treatment with anti-fcrh5/anti-cd3 bispecific antibodies |
| US20230374122A1 (en) | 2022-05-18 | 2023-11-23 | Janssen Biotech, Inc. | Method for Evaluating and Treating Psoriatic Arthritis with IL23 Antibody |
| WO2023227641A1 (en) | 2022-05-27 | 2023-11-30 | Glaxosmithkline Intellectual Property Development Limited | Use of tnf-alpha binding proteins and il-7 binding proteins in medical treatment |
| WO2023235699A1 (en) | 2022-05-31 | 2023-12-07 | Jounce Therapeutics, Inc. | Antibodies to lilrb4 and uses thereof |
| WO2023240058A2 (en) | 2022-06-07 | 2023-12-14 | Genentech, Inc. | Prognostic and therapeutic methods for cancer |
| WO2023237706A2 (en) | 2022-06-08 | 2023-12-14 | Institute For Research In Biomedicine (Irb) | Cross-specific antibodies, uses and methods for discovery thereof |
| WO2024015897A1 (en) | 2022-07-13 | 2024-01-18 | Genentech, Inc. | Dosing for treatment with anti-fcrh5/anti-cd3 bispecific antibodies |
| WO2024020432A1 (en) | 2022-07-19 | 2024-01-25 | Genentech, Inc. | Dosing for treatment with anti-fcrh5/anti-cd3 bispecific antibodies |
| WO2024020407A1 (en) | 2022-07-19 | 2024-01-25 | Staidson Biopharma Inc. | Antibodies specifically recognizing b- and t-lymphocyte attenuator (btla) and uses thereof |
| WO2024020564A1 (en) | 2022-07-22 | 2024-01-25 | Genentech, Inc. | Anti-steap1 antigen-binding molecules and uses thereof |
| WO2024020579A1 (en) | 2022-07-22 | 2024-01-25 | Bristol-Myers Squibb Company | Antibodies binding to human pad4 and uses thereof |
| WO2024030829A1 (en) | 2022-08-01 | 2024-02-08 | The United States Of America, As Represented By The Secretary, Department Of Health And Human Services | Monoclonal antibodies that bind to the underside of influenza viral neuraminidase |
| WO2024028731A1 (en) | 2022-08-05 | 2024-02-08 | Janssen Biotech, Inc. | Transferrin receptor binding proteins for treating brain tumors |
| WO2024028732A1 (en) | 2022-08-05 | 2024-02-08 | Janssen Biotech, Inc. | Cd98 binding constructs for treating brain tumors |
| WO2024042112A1 (en) | 2022-08-25 | 2024-02-29 | Glaxosmithkline Intellectual Property Development Limited | Antigen binding proteins and uses thereof |
| WO2024044779A2 (en) | 2022-08-26 | 2024-02-29 | Juno Therapeutics, Inc. | Antibodies and chimeric antigen receptors specific for delta-like ligand 3 (dll3) |
| WO2024049949A1 (en) | 2022-09-01 | 2024-03-07 | Genentech, Inc. | Therapeutic and diagnostic methods for bladder cancer |
| WO2024054822A1 (en) | 2022-09-07 | 2024-03-14 | The United States Of America, As Represented By The Secretary, Department Of Health And Human Services | Engineered sars-cov-2 antibodies with increased neutralization breadth |
| WO2024054929A1 (en) | 2022-09-07 | 2024-03-14 | Dynamicure Biotechnology Llc | Anti-vista constructs and uses thereof |
| WO2024064826A1 (en) | 2022-09-22 | 2024-03-28 | The United States Of America, As Represented By The Secretary, Department Of Health And Human Services | Neutralizing antibodies to plasmodium falciparum circumsporozoite protein and their use |
| WO2024068996A1 (en) | 2022-09-30 | 2024-04-04 | Centre Hospitalier Universitaire Vaudois (C.H.U.V.) | Anti-sars-cov-2 antibodies and use thereof in the treatment of sars-cov-2 infection |
| WO2024077239A1 (en) | 2022-10-07 | 2024-04-11 | Genentech, Inc. | Methods of treating cancer with anti-c-c motif chemokine receptor 8 (ccr8) antibodies |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1997030087A1 (en) * | 1996-02-16 | 1997-08-21 | Glaxo Group Limited | Preparation of glycosylated antibodies |
| WO1999054342A1 (en) * | 1998-04-20 | 1999-10-28 | Pablo Umana | Glycosylation engineering of antibodies for improving antibody-dependent cellular cytotoxicity |
Family Cites Families (29)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4215051A (en) * | 1979-08-29 | 1980-07-29 | Standard Oil Company (Indiana) | Formation, purification and recovery of phthalic anhydride |
| KR850004274A (ko) * | 1983-12-13 | 1985-07-11 | 원본미기재 | 에리트로포이에틴의 제조방법 |
| US4946778A (en) | 1987-09-21 | 1990-08-07 | Genex Corporation | Single polypeptide chain binding molecules |
| US4978745A (en) * | 1987-11-23 | 1990-12-18 | Centocor, Inc. | Immunoreactive heterochain antibodies |
| US5047335A (en) * | 1988-12-21 | 1991-09-10 | The Regents Of The University Of Calif. | Process for controlling intracellular glycosylation of proteins |
| DE473721T1 (de) * | 1989-05-25 | 1993-04-29 | Sloan-Kettering Institute For Cancer Research, New York, N.Y., Us | Antiidiotypischer antikoerper, der eine immunantwort gegen ein glykosphingolipid induziert und seine verwendung. |
| DE4028800A1 (de) | 1990-09-11 | 1992-03-12 | Behringwerke Ag | Gentechnische sialylierung von glykoproteinen |
| WO1994004574A1 (en) | 1991-08-22 | 1994-03-03 | Nissin Shokuhin Kabushiki Kaisha | Hiv immunotherapeutics |
| US5753229A (en) * | 1991-09-25 | 1998-05-19 | Mordoh; Jose | Monoclonal antibodies reactive with tumor proliferating cells |
| US5958403A (en) * | 1992-02-28 | 1999-09-28 | Beth Israel Hospital Association | Methods and compounds for prevention of graft rejection |
| WO1994011026A2 (en) | 1992-11-13 | 1994-05-26 | Idec Pharmaceuticals Corporation | Therapeutic application of chimeric and radiolabeled antibodies to human b lymphocyte restricted differentiation antigen for treatment of b cell lymphoma |
| US5736137A (en) * | 1992-11-13 | 1998-04-07 | Idec Pharmaceuticals Corporation | Therapeutic application of chimeric and radiolabeled antibodies to human B lymphocyte restricted differentiation antigen for treatment of B cell lymphoma |
| JPH08507680A (ja) | 1993-01-12 | 1996-08-20 | バイオジェン インコーポレイテッド | 組換え抗vla4抗体分子 |
| JPH09509847A (ja) | 1994-03-09 | 1997-10-07 | アボツト・ラボラトリーズ | 人乳化乳 |
| US5811524A (en) * | 1995-06-07 | 1998-09-22 | Idec Pharmaceuticals Corporation | Neutralizing high affinity human monoclonal antibodies specific to RSV F-protein and methods for their manufacture and therapeutic use thereof |
| JP3606536B2 (ja) * | 1995-11-17 | 2005-01-05 | タカラバイオ株式会社 | ウイルス複製抑制剤 |
| AU4231897A (en) | 1996-08-16 | 1998-03-06 | Southwest Foundation For Biomedical Research | Compositions and methods for delivery of nucleic acids to hepatocytes |
| US6183744B1 (en) * | 1997-03-24 | 2001-02-06 | Immunomedics, Inc. | Immunotherapy of B-cell malignancies using anti-CD22 antibodies |
| US6306393B1 (en) | 1997-03-24 | 2001-10-23 | Immunomedics, Inc. | Immunotherapy of B-cell malignancies using anti-CD22 antibodies |
| US5952203A (en) * | 1997-04-11 | 1999-09-14 | The University Of British Columbia | Oligosaccharide synthesis using activated glycoside derivative, glycosyl transferase and catalytic amount of nucleotide phosphate |
| US6946292B2 (en) | 2000-10-06 | 2005-09-20 | Kyowa Hakko Kogyo Co., Ltd. | Cells producing antibody compositions with increased antibody dependent cytotoxic activity |
| CA2442801A1 (en) * | 2001-04-02 | 2002-10-10 | Idec Pharmaceutical Corporation | Recombinant antibodies coexpressed with gntiii |
| EP2180044A1 (en) * | 2001-08-03 | 2010-04-28 | GlycArt Biotechnology AG | Antibody glycosylation variants having increased anti-body-dependent cellular cytotoxicity |
| PL222219B1 (pl) | 2003-01-22 | 2016-07-29 | Glycart Biotechnology Ag | Komórka gospodarza i sposób wytwarzania polipeptydu w komórce gospodarza |
| EA036531B1 (ru) | 2003-11-05 | 2020-11-19 | Роше Гликарт Аг | Гуманизированное антитело типа ii к cd20 (варианты), фармацевтическая композиция, содержащая эти варианты антитела, и их применение |
| WO2006082515A2 (en) | 2005-02-07 | 2006-08-10 | Glycart Biotechnology Ag | Antigen binding molecules that bind egfr, vectors encoding same, and uses thereof |
| BRPI0615397B1 (pt) | 2005-08-26 | 2023-10-03 | Roche Glycart Ag | Anticorpo anti-cd20, composição farmacêutica que o contém e uso do mesmo |
| AR062223A1 (es) | 2006-08-09 | 2008-10-22 | Glycart Biotechnology Ag | Moleculas de adhesion al antigeno que se adhieren a egfr, vectores que los codifican, y sus usos de estas |
| RU2570554C2 (ru) | 2009-08-31 | 2015-12-10 | Роше Гликарт Аг | Гуманизированные моноклональные антитела к сеа с созревшей аффинностью |
-
2002
- 2002-08-05 EP EP20100000043 patent/EP2180044A1/en not_active Ceased
- 2002-08-05 KR KR1020107000746A patent/KR20100018071A/ko active Search and Examination
- 2002-08-05 CA CA2838062A patent/CA2838062C/en not_active Expired - Lifetime
- 2002-08-05 NZ NZ531219A patent/NZ531219A/en not_active IP Right Cessation
- 2002-08-05 JP JP2003517069A patent/JP2005524379A/ja active Pending
- 2002-08-05 IL IL16017002A patent/IL160170A0/xx unknown
- 2002-08-05 NZ NZ571596A patent/NZ571596A/en not_active IP Right Cessation
- 2002-08-05 AU AU2002339845A patent/AU2002339845B2/en not_active Expired
- 2002-08-05 KR KR10-2004-7001617A patent/KR20040054669A/ko not_active Application Discontinuation
- 2002-08-05 EP EP02778191A patent/EP1423510A4/en not_active Withdrawn
- 2002-08-05 NZ NZ592087A patent/NZ592087A/xx not_active IP Right Cessation
- 2002-08-05 PL PL374178A patent/PL217751B1/pl unknown
- 2002-08-05 RU RU2004106559/13A patent/RU2321630C2/ru active
- 2002-08-05 US US10/211,554 patent/US20030175884A1/en not_active Abandoned
- 2002-08-05 CA CA2455365A patent/CA2455365C/en not_active Expired - Lifetime
- 2002-08-05 CN CNA028181735A patent/CN1555411A/zh active Pending
- 2002-08-05 MX MXPA04001072A patent/MXPA04001072A/es active IP Right Grant
- 2002-08-05 WO PCT/US2002/024739 patent/WO2003011878A2/en active Application Filing
- 2002-08-05 NZ NZ581474A patent/NZ581474A/en not_active IP Right Cessation
- 2002-08-05 NZ NZ603111A patent/NZ603111A/en not_active IP Right Cessation
- 2002-08-05 HU HU0700103A patent/HUP0700103A3/hu not_active Application Discontinuation
-
2004
- 2004-02-02 IL IL160170A patent/IL160170A/en unknown
- 2004-02-02 NO NO20040453A patent/NO332457B1/no not_active IP Right Cessation
-
2005
- 2005-08-09 US US11/199,232 patent/US8021856B2/en not_active Expired - Fee Related
-
2008
- 2008-12-25 JP JP2008331038A patent/JP2009114201A/ja active Pending
-
2011
- 2011-08-02 US US13/196,724 patent/US8999324B2/en not_active Expired - Fee Related
-
2015
- 2015-03-23 US US14/665,191 patent/US9321843B2/en not_active Expired - Fee Related
-
2016
- 2016-03-24 US US15/080,020 patent/US9631023B2/en not_active Expired - Fee Related
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1997030087A1 (en) * | 1996-02-16 | 1997-08-21 | Glaxo Group Limited | Preparation of glycosylated antibodies |
| WO1999054342A1 (en) * | 1998-04-20 | 1999-10-28 | Pablo Umana | Glycosylation engineering of antibodies for improving antibody-dependent cellular cytotoxicity |
Non-Patent Citations (9)
| Title |
|---|
| BIOTECHNOL. PROG., vol. 14, JPN6008031711, 1998, pages 189 - 192, ISSN: 0001074740 * |
| EUR. J. CANCER, vol. 35, no. 4, JPN6008031694, 1999, pages 549 - 557, ISSN: 0001074735 * |
| GLYCOBIOLOGY, vol. 5, no. 8, JPN6008031707, 1995, pages 813 - 822, ISSN: 0001074738 * |
| J. BIOL. CHEM., vol. 261, no. 21, JPN6008031715, 1984, pages 13370 - 13378, ISSN: 0001074742 * |
| J. BIOL. CHEM., vol. 275, no. 31, JPN6008031709, 2000, pages 23456 - 23461, ISSN: 0001074739 * |
| J. IMMUNOTHERAPY, vol. 19, no. 3, JPN7008005164, 1996, pages 184 - 191, ISSN: 0001074736 * |
| NATURE BIOTECHNOLOGY, vol. 17, JPN6008031692, 1999, pages 176 - 180, ISSN: 0001074734 * |
| TIBTECH, vol. 15, JPN6008031705, 1997, pages 26 - 32, ISSN: 0001074737 * |
| TRANSPLANTATION PROCEEDINGS, vol. 29, JPN6008031712, 1997, pages 891 - 892, ISSN: 0001074741 * |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8021856B2 (en) | 1998-04-20 | 2011-09-20 | Roche Glycart Ag | Antibody glycosylation variants having increased antibody-dependent cellular cytotoxicity |
| US8999324B2 (en) | 1998-04-20 | 2015-04-07 | Roche Glycart Ag | Antibody glycosylation variants having increased antibody-dependent cellular cytotoxicity |
| US9321843B2 (en) | 1998-04-20 | 2016-04-26 | Roche Glycart Ag | Antibody glycosylation variants having increased antibody-dependent cellular cytotoxicity |
| US9631023B2 (en) | 1998-04-20 | 2017-04-25 | Roche Glycart Ag | Antibody glycosylation variants having increased antibody-dependent cellular cytotoxicity |
| JP2009526746A (ja) * | 2005-08-19 | 2009-07-23 | セントカー・インコーポレーテツド | タンパク質分解抵抗性の抗体調製物 |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US9631023B2 (en) | Antibody glycosylation variants having increased antibody-dependent cellular cytotoxicity | |
| AU2002339845A1 (en) | Antibody glycosylation variants having increased antibody-dependent cellular cytotoxicity | |
| AU2004205802B2 (en) | Fusion constructs and use of same to produce antibodies with increased Fc receptor binding affinity and effector function |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20050727 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20080625 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20080924 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20081001 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20081024 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20081031 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20081111 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20081118 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20081225 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20090129 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20090430 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20090512 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20090512 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20090611 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20090828 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20090904 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20091009 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20091019 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20091110 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20091117 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20100303 |