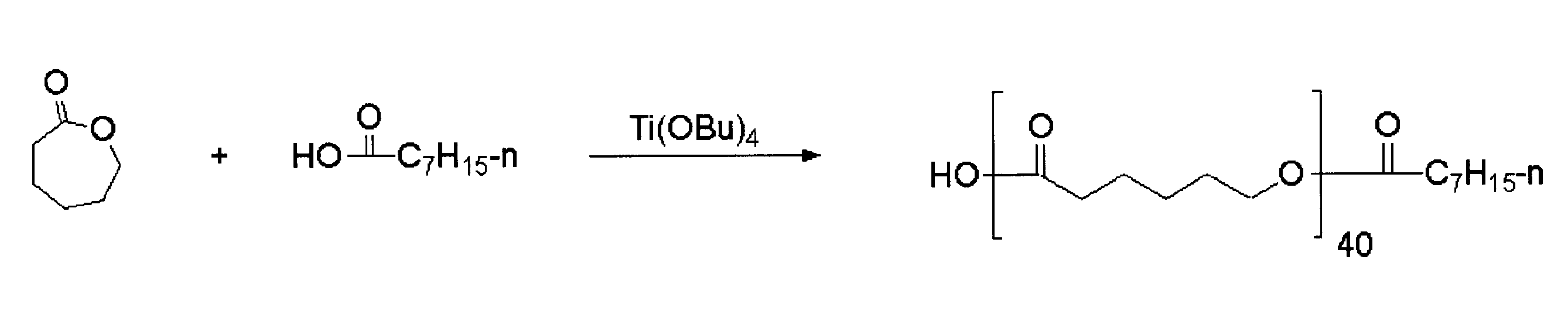WO2009096452A1 - 樹脂、顔料分散液、着色硬化性組成物、これを用いて製造されたカラーフィルタ及びその製造方法 - Google Patents
樹脂、顔料分散液、着色硬化性組成物、これを用いて製造されたカラーフィルタ及びその製造方法 Download PDFInfo
- Publication number
- WO2009096452A1 WO2009096452A1 PCT/JP2009/051430 JP2009051430W WO2009096452A1 WO 2009096452 A1 WO2009096452 A1 WO 2009096452A1 JP 2009051430 W JP2009051430 W JP 2009051430W WO 2009096452 A1 WO2009096452 A1 WO 2009096452A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- group
- resin
- pigment
- acid
- chain
- Prior art date
Links
- PUBNJSZGANKUGX-UHFFFAOYSA-N CCC(Cc1ccc(C)cc1)(C(c(cc1)ccc1N1CCOCC1)=O)N(C)C Chemical compound CCC(Cc1ccc(C)cc1)(C(c(cc1)ccc1N1CCOCC1)=O)N(C)C PUBNJSZGANKUGX-UHFFFAOYSA-N 0.000 description 1
- WZVJKOGIOIMIJA-WPWMEQJKSA-N CCN1c(ccc(/C(/C)=N/OC(C)=O)c2)c2C2=CC(C(c3c(C)cccc3)=O)=CCC12 Chemical compound CCN1c(ccc(/C(/C)=N/OC(C)=O)c2)c2C2=CC(C(c3c(C)cccc3)=O)=CCC12 WZVJKOGIOIMIJA-WPWMEQJKSA-N 0.000 description 1
- KQBNGKURCWDTNV-FMIFUCRQSA-N CC[n](c(ccc(C(/C(/CCSC1C=CC(Cl)=CC1)=N/OC(C)=O)=O)c1)c1c1c2)c1ccc2C(c1c(C)cccc1)=O Chemical compound CC[n](c(ccc(C(/C(/CCSC1C=CC(Cl)=CC1)=N/OC(C)=O)=O)c1)c1c1c2)c1ccc2C(c1c(C)cccc1)=O KQBNGKURCWDTNV-FMIFUCRQSA-N 0.000 description 1
- YHMYGUUIMTVXNW-UHFFFAOYSA-N Sc1nc2ccccc2[nH]1 Chemical compound Sc1nc2ccccc2[nH]1 YHMYGUUIMTVXNW-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- G—PHYSICS
- G02—OPTICS
- G02B—OPTICAL ELEMENTS, SYSTEMS OR APPARATUS
- G02B1/00—Optical elements characterised by the material of which they are made; Optical coatings for optical elements
- G02B1/04—Optical elements characterised by the material of which they are made; Optical coatings for optical elements made of organic materials, e.g. plastics
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F26/00—Homopolymers and copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and at least one being terminated by a single or double bond to nitrogen or by a heterocyclic ring containing nitrogen
- C08F26/02—Homopolymers and copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and at least one being terminated by a single or double bond to nitrogen or by a heterocyclic ring containing nitrogen by a single or double bond to nitrogen
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G73/00—Macromolecular compounds obtained by reactions forming a linkage containing nitrogen with or without oxygen or carbon in the main chain of the macromolecule, not provided for in groups C08G12/00 - C08G71/00
- C08G73/02—Polyamines
- C08G73/0206—Polyalkylene(poly)amines
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08L—COMPOSITIONS OF MACROMOLECULAR COMPOUNDS
- C08L79/00—Compositions of macromolecular compounds obtained by reactions forming in the main chain of the macromolecule a linkage containing nitrogen with or without oxygen or carbon only, not provided for in groups C08L61/00 - C08L77/00
- C08L79/02—Polyamines
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09B—ORGANIC DYES OR CLOSELY-RELATED COMPOUNDS FOR PRODUCING DYES, e.g. PIGMENTS; MORDANTS; LAKES
- C09B67/00—Influencing the physical, e.g. the dyeing or printing properties of dyestuffs without chemical reactions, e.g. by treating with solvents grinding or grinding assistants, coating of pigments or dyes; Process features in the making of dyestuff preparations; Dyestuff preparations of a special physical nature, e.g. tablets, films
- C09B67/006—Preparation of organic pigments
- C09B67/0063—Preparation of organic pigments of organic pigments with only macromolecular substances
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09B—ORGANIC DYES OR CLOSELY-RELATED COMPOUNDS FOR PRODUCING DYES, e.g. PIGMENTS; MORDANTS; LAKES
- C09B67/00—Influencing the physical, e.g. the dyeing or printing properties of dyestuffs without chemical reactions, e.g. by treating with solvents grinding or grinding assistants, coating of pigments or dyes; Process features in the making of dyestuff preparations; Dyestuff preparations of a special physical nature, e.g. tablets, films
- C09B67/0071—Process features in the making of dyestuff preparations; Dehydrating agents; Dispersing agents; Dustfree compositions
- C09B67/0084—Dispersions of dyes
- C09B67/0085—Non common dispersing agents
- C09B67/009—Non common dispersing agents polymeric dispersing agent
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09D—COATING COMPOSITIONS, e.g. PAINTS, VARNISHES OR LACQUERS; FILLING PASTES; CHEMICAL PAINT OR INK REMOVERS; INKS; CORRECTING FLUIDS; WOODSTAINS; PASTES OR SOLIDS FOR COLOURING OR PRINTING; USE OF MATERIALS THEREFOR
- C09D7/00—Features of coating compositions, not provided for in group C09D5/00; Processes for incorporating ingredients in coating compositions
- C09D7/40—Additives
- C09D7/45—Anti-settling agents
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/004—Photosensitive materials
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/004—Photosensitive materials
- G03F7/0045—Photosensitive materials with organic non-macromolecular light-sensitive compounds not otherwise provided for, e.g. dissolution inhibitors
-
- G—PHYSICS
- G02—OPTICS
- G02B—OPTICAL ELEMENTS, SYSTEMS OR APPARATUS
- G02B5/00—Optical elements other than lenses
- G02B5/20—Filters
- G02B5/201—Filters in the form of arrays
-
- G—PHYSICS
- G02—OPTICS
- G02B—OPTICAL ELEMENTS, SYSTEMS OR APPARATUS
- G02B5/00—Optical elements other than lenses
- G02B5/20—Filters
- G02B5/22—Absorbing filters
- G02B5/223—Absorbing filters containing organic substances, e.g. dyes, inks or pigments
Definitions
- the present invention produces a novel resin useful for pigment dispersants, a production method thereof, a pigment dispersion containing the same, a color filter used for liquid crystal display elements (LCD), solid-state imaging elements (CCD, CMOS, etc.), etc.
- the present invention relates to a colored curable composition suitable for the production, a color filter having a colored region formed by the colored curable composition, and a method for producing the same.
- the color filter is an essential component for liquid crystal displays and solid-state image sensors.
- the color filter is prepared using a curable composition containing a colorant (pigment or dye).
- a colorant pigment or dye
- polymer dispersants have been developed as dispersants having excellent dispersibility and dispersion stability (see, for example, JP-B-63-30057 and JP-A-9-169821). These polymer dispersants are used for color filter applications such as liquid crystal displays (see, for example, JP-A-9-176511 and JP-A-2001-272524).
- liquid crystal displays have been required to have higher image quality and improved contrast and color purity compared to conventional TV and monitor applications.
- curable compositions for use in color filter production attempts have been made to improve contrast by using finer pigment particle sizes (see, for example, JP-A-2006-30541).
- the particle size of the pigment is reduced, the surface area of the pigment increases, which causes a problem that the dispersibility and storage stability deteriorate. If the amount of the dispersant added is increased in order to ensure dispersibility and storage stability, there arises a problem that developability is lowered and it is difficult to form a good pattern.
- a further object of the present invention is to provide a color filter having a color pattern having a high resolution and good color characteristics formed from a colored curable composition having good dispersion stability and developability of the pigment, and a production method excellent in productivity thereof. Is to provide.
- the present inventors conducted extensive research and found that the dispersibility and dispersion stability of the resin having the specific structure of the present invention and the pigment dispersion containing the same are unexpectedly improved.
- the present invention has been completed. That is, the object of the present invention is achieved by the following means.
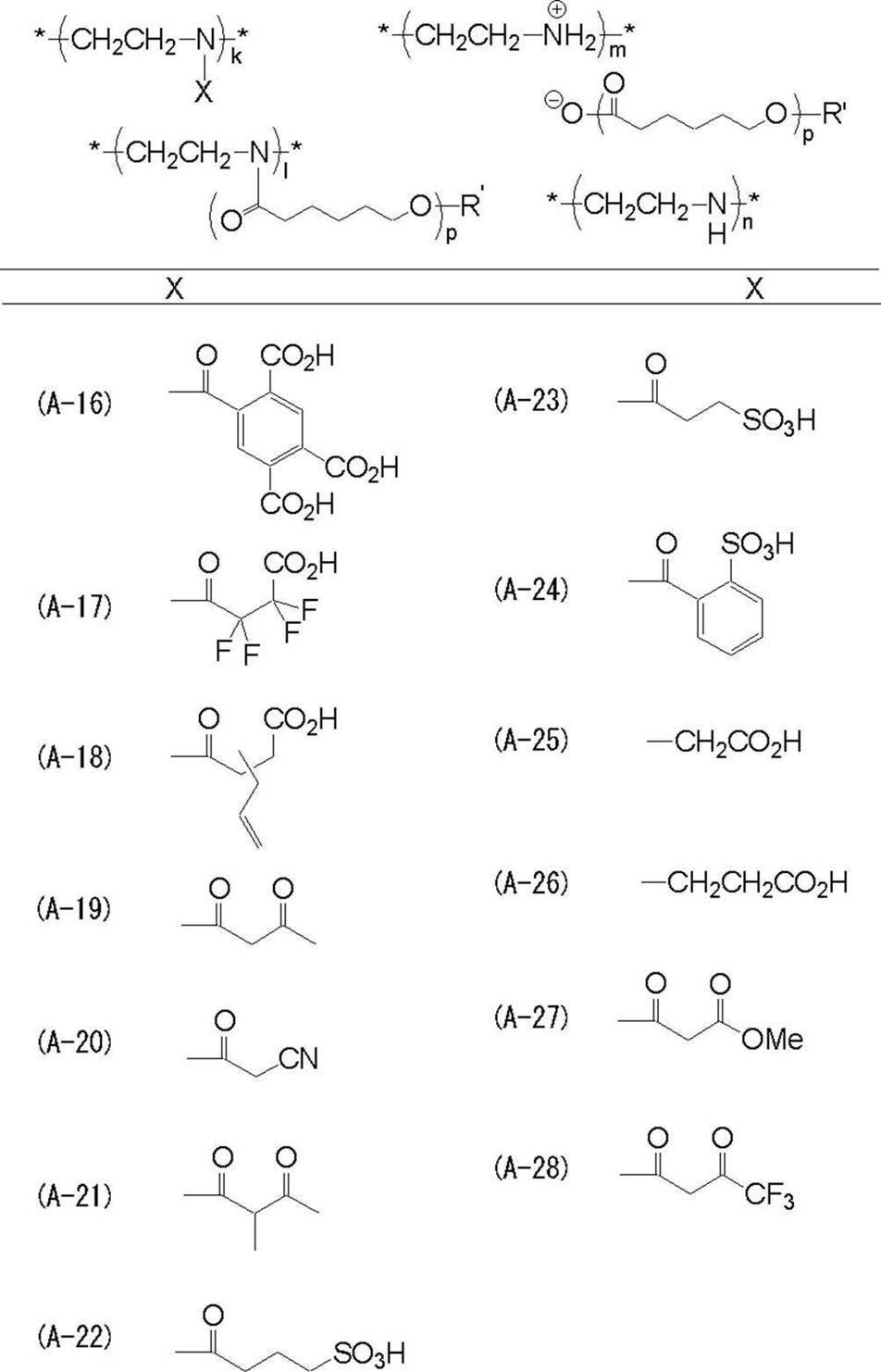
- ⁇ 1> (i) a main chain portion having a nitrogen atom; and (ii) a group “X” having a functional group having a pKa of 14 or less and bonded to the nitrogen atom present in the main chain portion.
- the main chain part (i) having a nitrogen atom of the resin is poly (lower alkyleneimine), polyallylamine, polydiallylamine, metaxylenediamine-epichlorohydrin polycondensate, polyvinylamine, 3-dialkylaminopropyl (meta).
- the functional group (ii) having a pKa of 14 or less of the resin is a functional group selected from carboxylic acid, sulfonic acid, and —COCH 2 CO—.
- ⁇ 1> to ⁇ 3> The resin according to any one of the above.
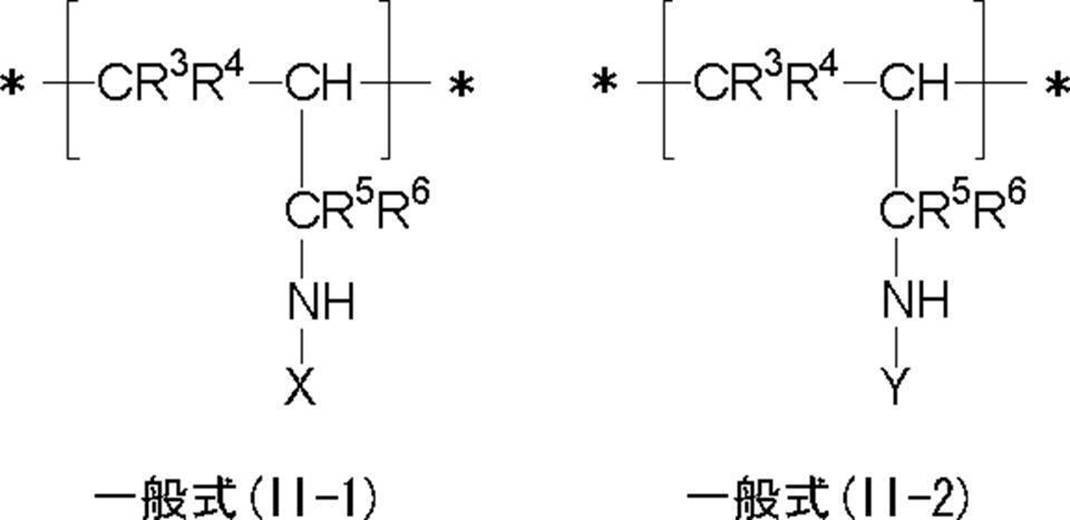
- ⁇ 5> Any one of ⁇ 1> to ⁇ 4>, including a repeating unit represented by the general formula (I-1) and a repeating unit represented by the general formula (I-2) The resin described.
- R 1 and R 2 each independently represents a hydrogen atom, a halogen atom or an alkyl group.
- a represents an integer of 1 to 5 independently.
- * represents a connecting part between repeating units.
- X represents a group containing a functional group having a pKa of 14 or less.
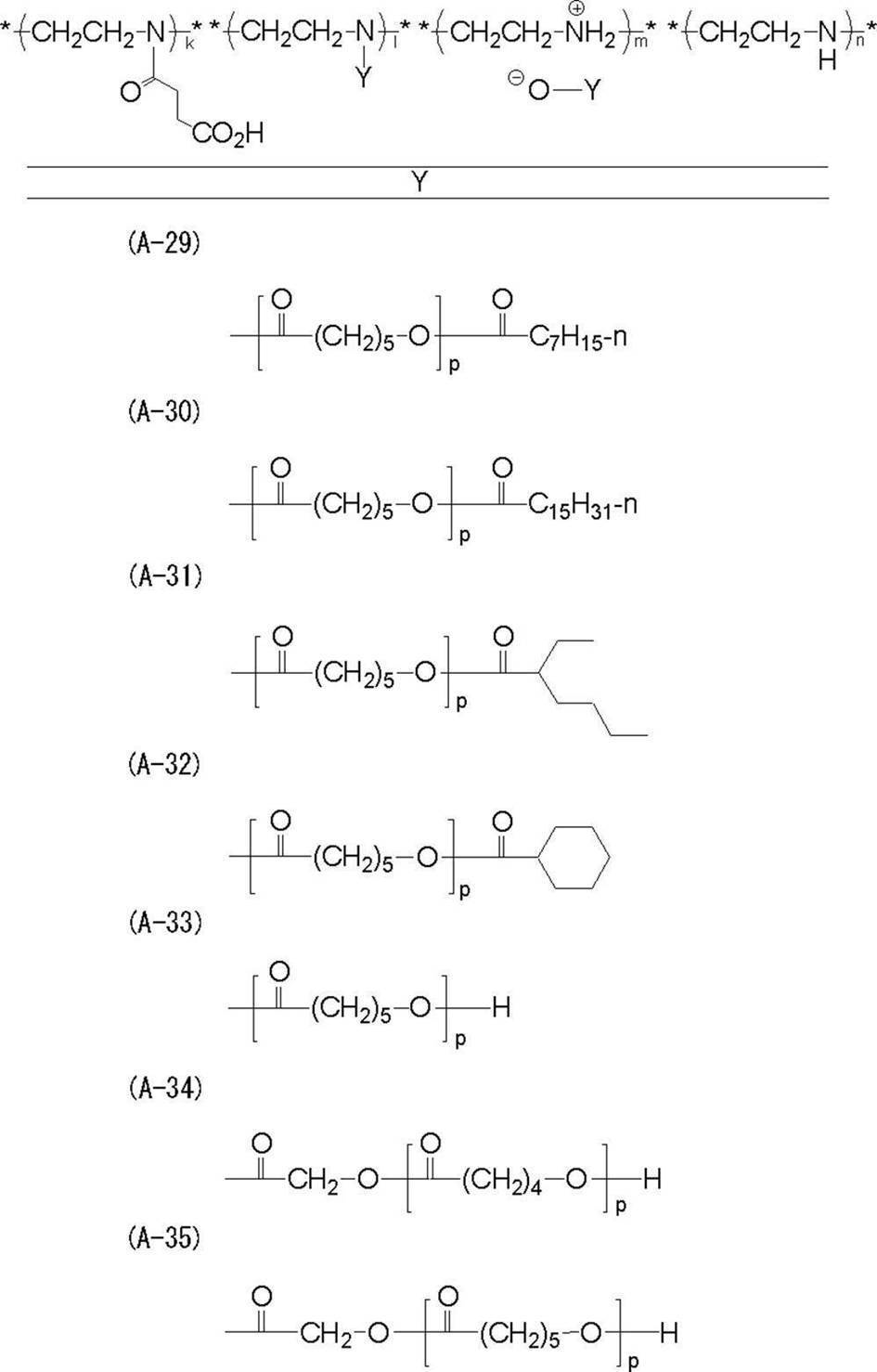
- Y represents an oligomer chain or a polymer chain having a number average molecular weight of 500 to 1,000,000.
- the repeating unit represented by the general formula (II-1) and the repeating unit represented by (II-2) are described in any one of ⁇ 1> to ⁇ 4> Resin.
- R 3 , R 4 , R 5 and R 6 each independently represent a hydrogen atom, a halogen atom or an alkyl group.
- *, X and Y have the same meanings as *, X and Y in formulas (I-1) and (I-2).
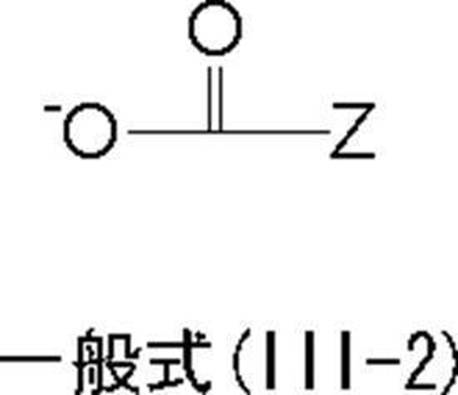
- the oligomer chain or polymer chain “Y” in which the resin has a (iii) number average molecular weight of 500 to 1,000,000 is represented by the following general formula (III-1) ⁇ 1
- Z is a polymer or oligomer having a polyester chain as a partial structure, and a residue obtained by removing the carboxyl group from a polyester having a free carboxyl group represented by the following general formula (IV) Represents.
- Z has the same meaning as Z in general formula (III-1).
- a resin having a primary or secondary amino group in a main chain portion, a precursor x of a group “X” having a functional group having a pKa of 14 or less, and a number average molecular weight of 500 to 500 The resin according to any one of ⁇ 1> to ⁇ 7>, which is a resin obtained by reacting with a precursor y of an oligomer chain or a polymer chain “Y” of 1,000,000.
- a resin having a primary or secondary amino group in the main chain is synthesized, and then the precursor “x” of the group “X” having a functional group having a pKa of 14 or less in the resin, and the number average molecular weight is The method for producing a resin according to any one of ⁇ 1> to ⁇ 8>, comprising reacting with a precursor y of an oligomer chain or polymer chain “Y” that is 500 to 1,000,000.
- ⁇ 10> A pigment dispersion containing the resin according to any one of ⁇ 1> to ⁇ 8>, (B) a pigment, and (C) a solvent.
- ⁇ 11> A) The resin according to any one of ⁇ 1> to ⁇ 8>, (B) a pigment, (C) a solvent, (D) a photopolymerization initiator, and (E) ethylenically unsaturated A colored curable composition comprising a compound containing a double bond.
- the colored curable composition according to ⁇ 11> further comprising (F) an alkali-soluble resin.
- a method for producing a color filter comprising:
- the colored region formed by the colored curable composition of the present invention has high resolution and high color purity. Therefore, by using such a colored curable composition, it is possible to obtain a color filter with high resolution and high contrast, a solid-state imaging device including the color filter, a liquid crystal display with a high contrast ratio, and the like.
- the colored region in the present invention includes a colored pixel (colored pattern) region and a light shielding film forming region in the color filter.
- a novel resin having a specific structure, useful as a dispersion resin for fine pigments, and a method for producing the same, and using the resin as a dispersant the dispersion can be achieved even when fine pigments are used.
- Pigment dispersion having excellent properties and dispersion stability can be provided.
- a colored curable composition excellent in pigment dispersion uniformity in a cured film and removability of an uncured region, pigment dispersion stability can provide a color filter having a color pattern with high resolution and good color characteristics formed from a colored curable composition having good properties and developability, and a novel resin that provides a production method with excellent productivity. .
- a pigment dispersion having extremely excellent dispersibility / dispersion stability and a colored curable composition exhibiting high developability are provided. I can do it.
- alkyl group includes not only an alkyl group having no substituent (unsubstituted alkyl group) but also an alkyl group having a substituent (substituted alkyl group).
- the resin of the present invention (hereinafter appropriately referred to as “specific resin”) has (i) a main chain portion having a nitrogen atom and (ii) a functional group having a pKa of 14 or less. A group "X" bonded to an existing nitrogen atom, and (iii) having an oligomer chain or a polymer chain "Y” having a number average molecular weight of 500 to 1,000,000 in a side chain To do.
- specific resin according to the present invention will be described in detail.
- the specific resin of the present invention has (i) a main chain portion having a nitrogen atom.
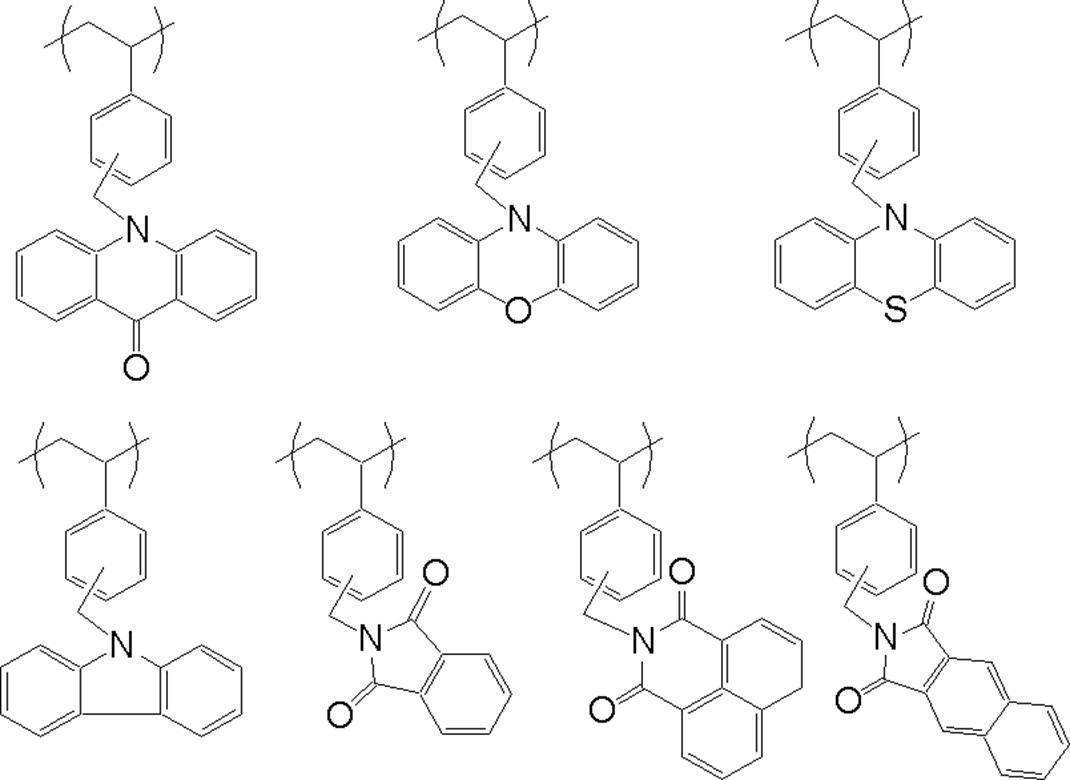
- the specific resin preferably has a main chain portion composed of an oligomer or polymer containing a known amino group, more preferably a primary or secondary amino group. More specifically, oligomers or polymers containing amino groups include poly (lower alkyleneimine), polyallylamine, polydiallylamine, metaxylenediamine-epichlorohydrin polycondensate, polyvinylamine, 3-dialkylaminopropyl (meth).
- the main chain structure is selected from an acrylic amide copolymer, a (meth) acrylic acid 2-dialkylaminoethyl copolymer, and the like.
- Most preferred is a main chain structure selected from dialkylaminoethyl copolymers.
- the poly (lower alkyleneimine) may be chain-like or network-like, but the dispersion stability and the material supply ability are particularly improved by being network-like.
- the number average molecular weight of the main chain in the specific resin of the present invention is preferably from 100 to 10,000, more preferably from 200 to 5,000, more preferably from 300 to 2,000, in particular, the number average molecular weight is from 500 to 1500. It is most preferable from the viewpoint of both dispersion stability and developability.
- the molecular weight of the main chain is determined from the ratio of the terminal group and the hydrogen atom integral value of the main chain measured by nuclear magnetic resonance spectroscopy, or by measuring the molecular weight of the oligomer or polymer containing the amino group as the raw material. Can do.
- the main chain portion of the specific resin is particularly preferably composed of a poly (lower alkyleneimine) or a polyallylamine skeleton.
- the term “lower” in the poly (lower alkylene imine) indicates that the number of carbon atoms is 1 to 5, and the term “lower alkylene imine” refers to an alkylene imine having 1 to 5 carbon atoms.
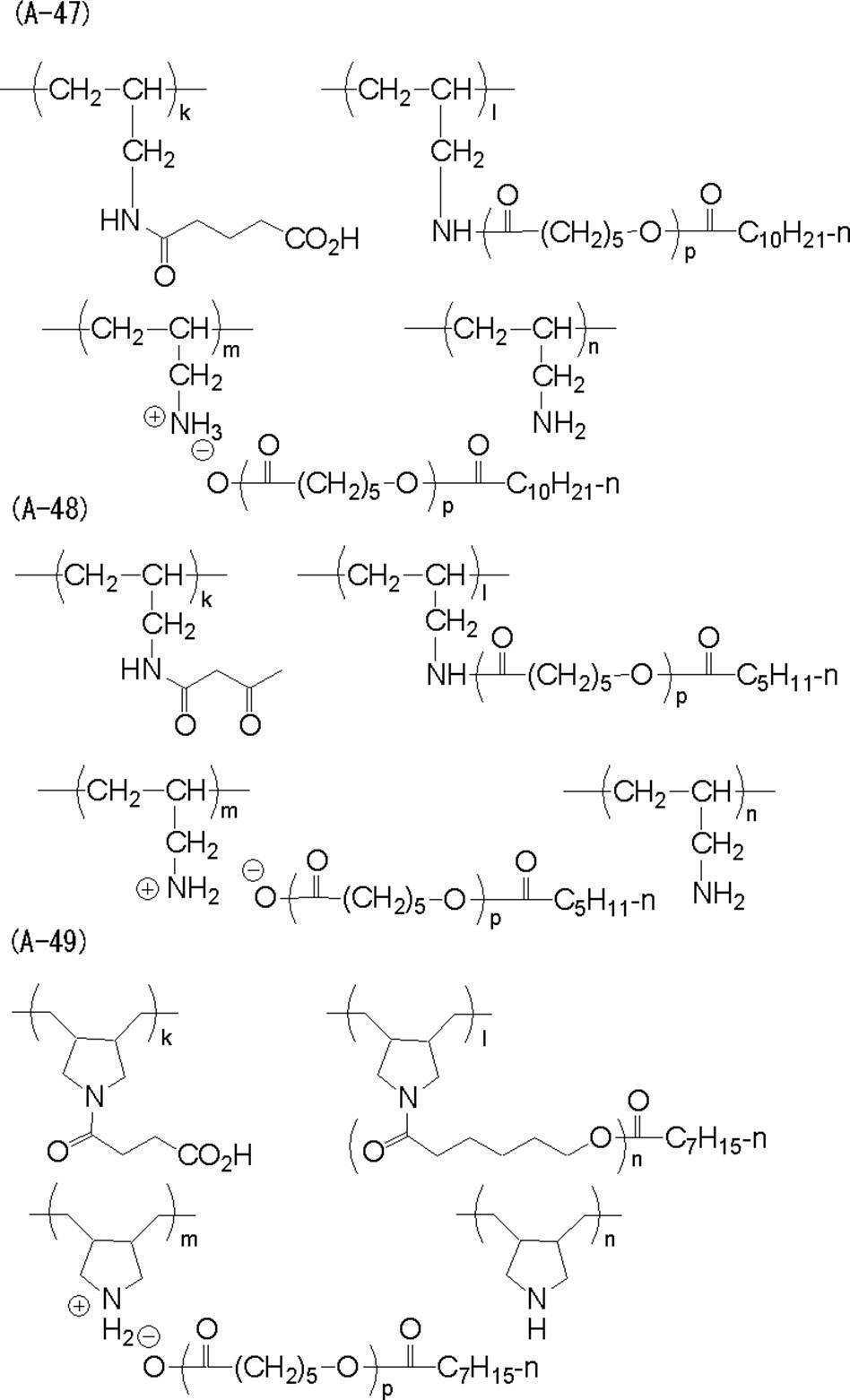
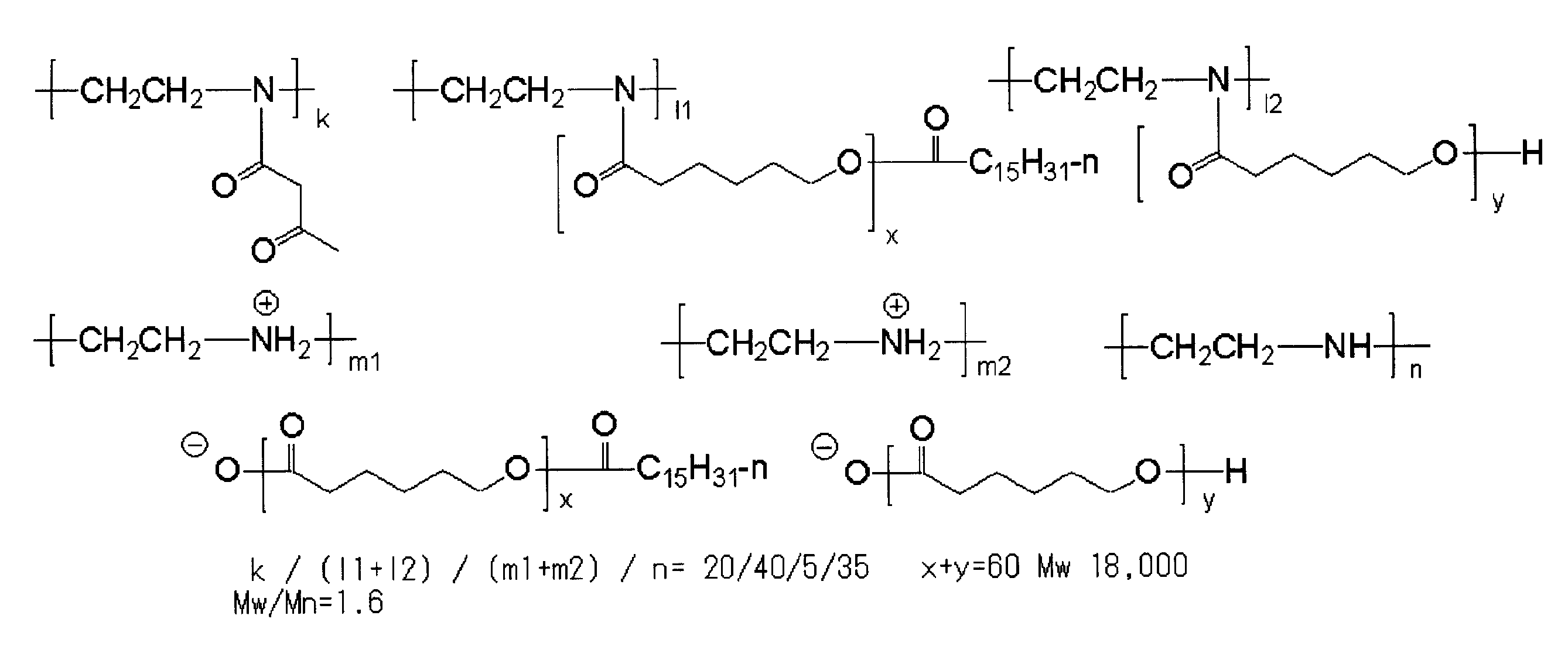
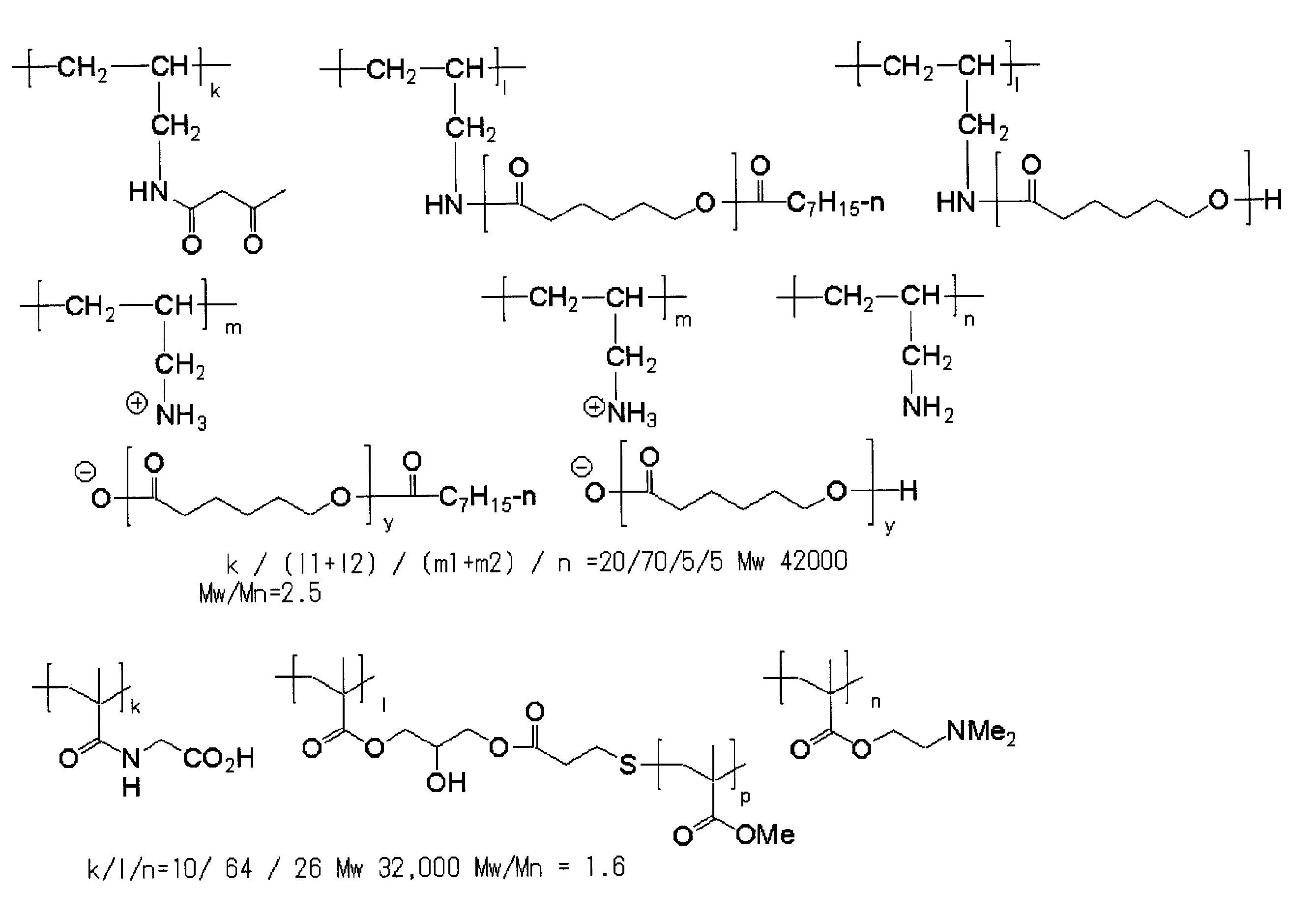
- the specific resin of the present invention has a structure having a repeating unit represented by the general formula (I-1) and a repeating unit represented by the general formula (I-2), or a general formula ( It preferably includes a structure containing a repeating unit represented by II-1) and a repeating unit represented by formula (II-2).
- R 1 and R 2 represent a hydrogen atom, a halogen atom, or an alkyl group.
- a represents an integer of 1 to 5 independently.
- * represents a connecting part between repeating units.
- X represents a group containing a functional group having a pKa of 14 or less.
- Y represents an oligomer chain or a polymer chain having a number average molecular weight of 500 to 1,000,000.
- the resin of the present invention further contains a repeating unit represented by the general formula (I-3) as a copolymerization component. It is preferable to have. By using such a repeating unit in combination, the dispersion performance is further improved when this resin is used as a fine particle dispersant such as a pigment.
- R 1 , R 2 and a are as defined in general formula (I-1).
- (Y ′) ⁇ represents an oligomer chain or a polymer chain having an anionic group and a number average molecular weight of 500 to 1,000,000.
- the repeating unit represented by the general formula (I-3) is obtained by adding an oligomer or polymer having a group that reacts with an amine to form a salt to a resin having a primary or secondary amino group in the main chain. It can be formed by reacting.
- the anionic group CO 2 — or SO 3 — is preferable, and CO 2 — is most preferable.
- the anionic group is preferably at the terminal position of the oligomer chain or polymer chain of (Y ′) ⁇ .
- R 1 and R 2 are particularly preferably hydrogen atoms.
- a is preferably 2 from the viewpoint of raw material availability.
- the resin of the present invention includes a lower alkylene containing a primary or tertiary amino group in addition to the repeating units represented by the general formula (I-1), general formula (I-2) and general formula (I-3). It may contain imine as a repeating unit.
- the nitrogen atom in such a lower alkyleneimine repeating unit may be further bonded to the group represented by the above X, Y or (Y ′) 2 — .
- Resins containing both a repeating unit having a group represented by X and a repeating unit having Y bonded to the main chain structure are also included in the specific resin of the present invention.
- the repeating unit represented by the general formula (I-1) is a repeating unit having a group X containing a functional group having a pKa of 14 or less. Such a repeating unit is a viewpoint of storage stability and developability. Therefore, the content is preferably 1 to 80 mol%, and most preferably 3 to 50 mol% in all repeating units contained in the resin of the present invention.
- the repeating unit represented by the general formula (I-2) is a repeating unit having an oligomer chain or a polymer chain Y having a number average molecular weight of 500 to 1,000,000, and such a repeating unit has a storage stability.
- the repeating unit (I-1) :( I-2) has a molar ratio in the range of 10: 1 to 1: 100.
- the range is from 1: 1 to 1:10.
- the repeating unit represented by the general formula (I-3) used in combination optionally has a partial structure including an oligomer chain or a polymer chain having a number average molecular weight of 500 to 1,000,000 in the main chain nitrogen atom. From the viewpoint of the effect, it is preferably contained in an amount of 0.5 to 20 mol%, preferably 1 to 10 mol% in all the repeating units of the resin of the present invention. Most preferred. It can be confirmed that the polymer chain “Y” is ionically bonded by infrared spectroscopy, acid value titration or base titration.
- R 3 , R 4 , R 5 and R 6 each independently represent a hydrogen atom, a halogen atom or an alkyl group.
- *, X and Y have the same meanings as *, X and Y in formulas (I-1) and (I-2).
- the resin of the present invention further includes a repeating unit represented by the general formula (II-3). It is preferable to contain a unit as a copolymerization component. By using such a repeating unit in combination, the dispersion performance is further improved when this resin is used as a fine particle dispersant such as a pigment.
- R 3 , R 4 , R 5 and R 6 have the same meaning as in general formula (II-1).
- (Y ') - is general formula (I-3) in the (Y') - synonymous.
- R 3 , R 4 , R 5 and R 6 are preferably hydrogen atoms from the viewpoint of availability of raw materials.
- the general formula (II-1) is a repeating unit having a group containing a functional group X having a pKa of 14 or less. Such a repeating unit is added to the resin of the present invention from the viewpoint of storage stability and developability. The content is preferably 1 to 80 mol%, and most preferably 3 to 50 mol%, in all the repeating units contained.
- the general formula (II-2) is a repeating unit having an oligomer chain or a polymer chain Y having a number average molecular weight of 500 to 1,000,000. Such a repeating unit is selected from the viewpoint of storage stability in the present invention. It is preferably contained in an amount of 10 to 90 mol%, and most preferably 30 to 70 mol%, in all the repeating units of the resin.
- the repeating unit (II-1) :( II-2) has a molar ratio in the range of 10: 1 to 1: 100. Preferably, the range is from 1: 1 to 1:10.
- the repeating unit represented by the general formula (II-3) used in combination is preferably contained in an amount of 0.5 to 20 mol%, preferably 1 to 10 mol%, based on all the repeating units of the resin of the present invention. Is most preferred.
- the specific resin of the present invention most preferably contains both the repeating unit represented by the general formula (I-1) and the repeating unit represented by the general formula (I-2) from the viewpoint of dispersibility. .
- a group “X” containing a functional group with a pKa of 14 or less X represents a group containing a functional group having a pKa of 14 or less at a water temperature of 25 ° C.
- pKa has the definition described in Chemical Handbook (II) (4th revised edition, 1993, edited by The Chemical Society of Japan, Maruzen Co., Ltd.).
- the “functional group having a pKa of 14 or less” is not particularly limited as long as the physical properties satisfy this condition, and examples thereof include a known functional group having a pKa that satisfies the above range.
- carboxylic acid about pKa 3 to 5
- sulfonic acid about pKa -3 to -2
- phosphoric acid about pKa 2
- -COCH 2 CO- about pKa 8 to 10
- -COCH 2 CN about pKa 8 to 11
- —CONHCO— phenolic hydroxyl group, —R F CH 2 OH or — (R F ) 2 CHOH
- R F represents a perfluoroalkyl group, pKa about 9 to 11
- sulfonamide group about pKa 9 ⁇ 11
- a carboxylic acid pKa 3 ⁇ about 5
- sulfonic acid pKa -3 ⁇ about -2
- - COCH 2 CO- pKa 8 ⁇ 10 It is preferred.
- the group “X” containing a functional group having a pKa of 14 or less is usually bonded directly to a nitrogen atom contained in the main chain structure. In addition to the covalent bond, they may be linked in a form that forms a salt by ionic bond. Moreover, the resin of this invention may have 2 or more types of mutually different X in a molecule
- the molecular weight of the group “X” containing a functional group having a pKa of 14 or less is preferably 50 to 1000, and most preferably 50 to 500. When the molecular weight is within this range, developability and dispersibility are improved.
- the group “X” containing a functional group having a pKa of 14 or less is particularly a structure represented by the general formula (V-1), the general formula (V-2) or the general formula (V-3). Those having the following are preferred.
- U represents a single bond or a divalent linking group.
- d and e each independently represents 0 or 1;
- W represents an acyl group or an alkoxycarbonyl group.
- Examples of the divalent linking group represented by U include alkylene (more specifically, for example, —CH 2 —, —CH 2 CH 2 —, —CH 2 CHMe—, — (CH 2 ) 5 —. , —CH 2 CH (n—C 10 H 21 ) —, etc.), oxygen-containing alkylene (more specifically, for example, —CH 2 OCH 2 —, —CH 2 CH 2 OCH 2 CH 2 —, etc.) , A cycloalkylene group (eg, cyclobutylene, cyclopentylene, cyclohexylene, cyclooctylene, etc.), an arylene group (eg, phenylene, tolylene, biphenylene, naphthylene, furylene, pyrrolylene, etc.), alkyleneoxy (eg, ethyleneoxy, Propyleneoxy, phenyleneoxy, etc.), and in particular, an alkylene group having 1 to 30 carbon atoms and
- Arylene radicals are preferred alkylene group or a C 6-20, alkylene group having 1 to 20 carbon atoms, an arylene group of a cycloalkylene group or a C 6 to 15 5 to 10 carbon atoms most preferred. Further, from the viewpoint of productivity, d is preferably 1, and e is preferably 0.
- W represents an acyl group or an alkoxycarbonyl group.
- the acyl group for W is preferably an acyl group having 1 to 30 carbon atoms (eg, formyl, acetyl, n-propanoyl, benzoyl, etc.), and particularly preferably acetyl.
- W is particularly preferably an acyl group, and an acetyl group is preferable from the viewpoint of ease of production and availability of raw materials (precursor X 'of X).
- “X” of the present invention is characterized by being bonded to a nitrogen atom in the main chain. Thereby, the dispersibility and dispersion stability of the pigment are dramatically improved. The reason for this is unknown, but it is thought as follows. That is, the nitrogen atom in the main chain part exists in the structure of an amino group, an ammonium group or an amide group, and these are adsorbed by interacting with the acidic part on the pigment surface, such as a hydrogen bond or an ionic bond. Conceivable. Furthermore, since “X” of the present invention functions as an acid group, it can interact with a basic part (such as a nitrogen atom) or a metal atom (such as copper of copper phthalocyanine) of the pigment.
- a basic part such as a nitrogen atom
- a metal atom such as copper of copper phthalocyanine
- the resin of the present invention can adsorb both the basic part and the acidic part of the pigment with nitrogen atoms and “X”, the adsorbing ability is improved, and the dispersibility and storage stability are dramatically improved. It is thought to have improved.
- “X” includes a functional group having a pKa of 14 or less as a partial structure
- “X” also functions as an alkali-soluble group.
- a dispersion resin containing a polycaprolactone chain is precipitated from a solvent at a low temperature because of high crystallinity as described in JP-A-2007-63472.
- the dispersion resin containing the polycaprolactone chain of the present invention unexpectedly has high solvent solubility and does not precipitate from the solvent even at low temperatures. Although the cause of this is unknown, it is considered that the solvent solubility is improved by the affinity of the partial structure represented by “X” in the resin with the solvent.
- the content of the functional group having a pKa of 14 or less in X is not particularly limited, but is preferably 0.01 to 5 mmol, most preferably 0.05 to 1 mmol with respect to 1 g of the specific resin of the present invention. . Within this range, the dispersibility and dispersion stability of the pigment are improved, and when the resin is used in the curable composition, the developability of the uncured portion is excellent. Further, from the viewpoint of the acid value, it is included that the acid value of the specific resin is contained in an amount of about 5 to 50 mgKOH / g. From the viewpoint of sex. The acid value titration can be performed by a known method.
- an indicator method (a method for determining a neutralization point with an indicator), a potentiometric method, or the like can be used.
- titrant used in acid value titration can be used a commercially available aqueous sodium hydroxide, a functional group having a relatively high pKa (e.g., -COCH 2 CO-, phenolic hydroxyl group) an acid value titration of If the acid value is difficult to measure with this aqueous sodium hydroxide solution, as in is there.
- Oligomer chain or polymer chain “Y” having a number average molecular weight of 500 to 1,000,000 “Y” represents an oligomer chain or a polymer chain having a number average molecular weight of 500 to 1,000,000.
- Y include known polymer chains such as polyester, polyamide, polyimide, and poly (meth) acrylic acid ester that can be connected to the main chain portion of the specific resin.
- the binding site of Y with the specific resin is preferably a terminal.
- the resin of the present invention may have two or more “Y” s (oligomer chain, polymer chain) having different structures in the molecule.
- Y is preferably bonded to a nitrogen atom in the main chain.
- the bonding mode between Y and the main chain is covalent bond, ionic bond, or a mixture of covalent bond and ionic bond.
- Y is preferably ionically bonded as a amide bond or carboxylate with a nitrogen atom in the main chain.
- the number average molecular weight of Y can be measured by the polystyrene conversion value by GPC method.
- the number average molecular weight of Y is particularly preferably 1,000 to 50,000, and most preferably 1,000 to 30,000 from the viewpoints of dispersibility, dispersion stability, and developability. It is preferable that two or more side chain structures represented by Y are connected to the main chain in one molecule of the resin, and most preferably five or more are connected.
- Y preferably has a structure represented by the general formula (III-1).
- Z is a polymer or oligomer having a polyester chain as a partial structure, and a residue obtained by removing the carboxyl group from a polyester having a free carboxyl group represented by the following general formula (IV) Represents.
- Z has the same meaning as Z in general formula (III-1).
- Z has the same meaning as Z in general formula (III-1).
- a polyester having a carboxyl group at one end includes (IV-1) polycondensation of carboxylic acid and lactone, (IV-2) polycondensation of hydroxy group-containing carboxylic acid, (IV -3) It can be obtained by polycondensation of a dihydric alcohol and a divalent carboxylic acid (or a cyclic acid anhydride).
- the carboxylic acid used in the polycondensation reaction of carboxylic acid and lactone is preferably an aliphatic carboxylic acid (a linear or branched carboxylic acid having 1 to 30 carbon atoms, such as formic acid, acetic acid, propionic acid, butyric acid, Valeric acid, n-hexanoic acid, n-octanoic acid, n-decanoic acid, n-dodecanoic acid, palmitic acid, 2-ethylhexanoic acid, cyclohexane acid, etc.), hydroxy group-containing carboxylic acid (directly having 1 to 30 carbon atoms) A chain or branched hydroxy group-containing carboxylic acid is preferable.
- aliphatic carboxylic acid a linear or branched carboxylic acid having 1 to 30 carbon atoms, such as formic acid, acetic acid, propionic acid, butyric acid, Valeric acid, n-hexanoic acid,
- glycolic acid for example, glycolic acid, lactic acid, 3-hydroxypropionic acid, 4-hydroxydodecanoic acid, 5-hydroxydodecanoic acid, ricinoleic acid, 12-hydroxydodecanoic acid, 12-hydroxystearic acid Acid, 2,2-bis (hydroxymethyl) butyric acid, etc.), in particular, straight-chain aliphatic having 6 to 20 carbon atoms
- Carboxylic acids or hydroxy group-containing carboxylic acids having 1 to 20 carbon atoms are preferred. These carboxylic acids may be used as a mixture.
- lactone a known lactone can be used, for example, ⁇ -propiolactone, ⁇ -butyrolactone, ⁇ -butyrolactone, ⁇ -hexanolactone, ⁇ -octanolactone, ⁇ -valerolactone, ⁇ -hexalanolactone. , ⁇ -octanolactone, ⁇ -caprolactone, ⁇ -dodecanolactone, ⁇ -methyl- ⁇ -butyrolactone, etc., and ⁇ -caprolactone is particularly preferred from the viewpoint of reactivity and availability.
- lactones may be used as a mixture of plural kinds.
- the hydroxy group-containing carboxylic acid in the polycondensation of the hydroxy group-containing carboxylic acid is the same as the hydroxy group-containing carboxylic acid in (IV-1), and the preferred range is also the same.
- a linear or branched aliphatic diol (a diol having 2 to 30 carbon atoms is preferable, For example, ethylene glycol, diethylene glycol, triethylene glycol, dipropylene glycol, 1,2-propanediol, 1,3-propanediol, 1,5-pentanediol, 1,6-hexanediol, 1,8-octanediol, etc.
- aliphatic diols having 2 to 20 carbon atoms are preferred.
- the divalent carboxylic acid a linear or branched divalent aliphatic carboxylic acid (a divalent aliphatic carboxylic acid having 1 to 30 carbon atoms is preferable.
- a divalent carboxylic acid having 3 to 20 carbon atoms is preferred.
- acid anhydrides equivalent to these divalent carboxylic acids for example, succinic anhydride, glutaric anhydride, etc.
- the divalent carboxylic acid and the dihydric alcohol are preferably charged at a molar ratio of 1: 1. This makes it possible to introduce a carboxylic acid at the terminal.
- the polycondensation during the production of the polyester is preferably performed by adding a catalyst.
- a catalyst that functions as a Lewis acid is preferable.
- a Ti compound eg, Ti (OBu) 4 , Ti (O—Pr) 4, etc.
- a Sn compound eg, tin octylate, dibutyltin oxide, dibutyltin laurate
- protonic acids for example, sulfuric acid, paratoluenesulfonic acid, etc.
- the catalyst amount is preferably from 0.01 to 10 mol%, most preferably from 0.1 to 5 mol%, based on the number of moles of all monomers.
- the reaction temperature is preferably 80 to 250 ° C, and most preferably 100 to 180 ° C.
- the reaction time varies depending on the reaction conditions, but is generally 1 to 24 hours.
- the number average molecular weight of the polyester can be measured as a polystyrene converted value by the GPC method.
- the number average molecular weight of the polyester is 500 to 1,000,000, preferably 2,000 to 100,000, and most preferably 3,000 to 50,000. When the molecular weight is in this range, both dispersibility and developability can be achieved.
- the polyester partial structure forming the polymer chain in Y is in particular a polyester obtained by (IV-1) polycondensation of carboxylic acid and lactone and (IV-2) polycondensation of hydroxy group-containing carboxylic acid. Is preferable from the viewpoint of ease of manufacture.
- p and q represent the number of linked polyester chains, and each independently represents 5 to 100,000.
- R ' represents a hydrogen atom or an alkoxycarbonyl group.
- a method of reacting a resin having a primary or secondary amino group with a precursor x of X and a precursor y of Y, (2) containing a nitrogen atom It is possible to manufacture by a method by polymerization of a monomer, a monomer containing X and a macromonomer containing Y.
- a resin having a primary or secondary amino group in the main chain is synthesized, and then The resin is preferably produced by reacting a precursor x of x and a precursor y of y with a resin and introducing them into a nitrogen atom present in the main chain by a polymer reaction.
- a method of reacting a resin having a primary or secondary amino group with an X precursor x and a Y precursor y will be described.
- the resin having a primary or secondary amino group include an oligomer or a polymer containing a primary or secondary amino group constituting the main chain portion having the nitrogen atom.
- poly (lower alkylene imine), poly (polymer) Examples include allylamine, polydiallylamine, metaxylenediamine-epichlorohydrin polycondensate, and polyvinylamine. Of these, oligomers or polymers composed of poly (lower alkyleneimine) or polyallylamine are preferred.
- the precursor x of the group “X” having a functional group having a pKa of 14 or less represents a compound capable of reacting with the resin having the primary or secondary amino group and introducing X into the main chain.
- Examples of x are cyclic carboxylic acid anhydrides (cyclic carboxylic acid anhydrides having 4 to 30 carbon atoms are preferred, such as succinic acid anhydride, glutaric acid anhydride, itaconic acid anhydride, maleic acid anhydride, allyl succinic acid.
- y is preferably a number average molecular weight of 500 to 1,000,000 oligomer or polymer having a group capable of covalently or ionically bonding with a nitrogen atom of a specific resin, and particularly a number average molecular weight having a free carboxyl group at one end. Most preferred are 500 to 1,000,000 oligomers or polymers.
- Examples of y include a polyester represented by the general formula (IV) having a free carboxyl group at one end, a polyamide having a free carboxyl group at one end, and a poly (meth) having a free carboxyl group at one end.
- Examples include acrylic acid resins, and polyesters containing a free carboxyl group at one end represented by the general formula (IV) are most preferable.
- y can be synthesized by a known method.
- a polyester containing a free carboxyl group at one end represented by the general formula (IV) is, as described above, composed of (IV-1) carboxylic acid and lactone. Examples thereof include polycondensation, (IV-2) polycondensation of a hydroxy group-containing carboxylic acid, and (IV-3) polycondensation of a dihydric alcohol and a divalent carboxylic acid (or a cyclic acid anhydride).
- a polyamide containing a free carboxyl group at one end can be produced by self-condensation of an amino group-containing carboxylic acid (for example, glycine, alanine, ⁇ -alanine, 2-aminobutyric acid, etc.).
- Poly (meth) acrylic acid ester having a free carboxyl group at one end is obtained by radical polymerization of a (meth) acrylic acid monomer in the presence of a carboxyl group-containing chain transfer agent (for example, 3-mercaptopropionic acid).
- a carboxyl group-containing chain transfer agent for example, 3-mercaptopropionic acid
- the specific resin of the present invention includes (a) a method in which a resin having a primary or secondary amino group and x and y are simultaneously reacted, and (b) a reaction between a resin having a primary or secondary amino group and x, and then y And (c) a method in which a resin having a primary or secondary amino group is reacted with y and then reacted with x.
- (c) a method in which a resin having a primary or secondary amino group is reacted with y and then reacted with x is preferable.
- the reaction temperature can be appropriately selected depending on the conditions, but is preferably 20 to 200 ° C, and most preferably 40 to 150 ° C.
- the reaction time is preferably 1 to 48 hours, and more preferably 1 to 24 hours from the viewpoint of productivity.
- the reaction may be performed in the presence of a solvent.
- a solvent examples include water, sulfoxide compounds (eg, dimethyl sulfoxide), ketone compounds (eg, acetone, methyl ethyl ketone, cyclohexanone, etc.), ester compounds (eg, ethyl acetate, butyl acetate, ethyl propionate, propylene glycol 1-monomethyl ether).
- ether compounds eg, diethyl ether, dibutyl ether, tetrahydrofuran, etc.
- aliphatic hydrocarbon compounds eg, pentane, hexane, etc.
- aromatic hydrocarbon compounds eg, toluene, xylene, mesitylene, etc.
- Nitrile compounds eg, acetonitrile, propiononitrile, etc.
- amide compounds eg, N, N-dimethylformamide, N, N-dimethylacetamide, N-methylpyrrolidone, etc.
- carboxylated compounds eg, acetic acid, propionic acid, etc.
- alcohol compounds eg, methanol, ethanol, isopropanol, n-butanol, 3-methylbutanol, 1-methoxy-2-propanol, etc.
- halogenated solvents eg, chloroform, 1, 2-dichloroethane.
- the specific resin of the present invention may be purified by a reprecipitation method. By removing the low molecular weight component by the reprecipitation method, the dispersion performance when the obtained specific resin is used as a pigment dispersant is improved.
- a hydrocarbon solvent such as hexane and an alcohol solvent such as methanol.
- a method by polymerization of a monomer containing a nitrogen atom, a monomer containing X, and a macromonomer containing Y will be described.
- a known monomer can be selected.
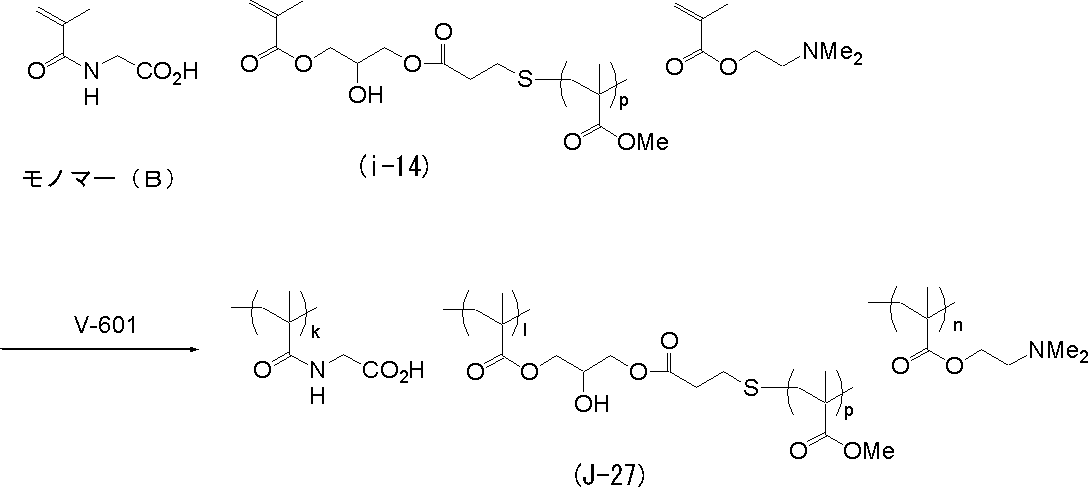
- 2-dialkylaminoethyl (meth) acrylate, 3-dialkylaminopropyl (meth) acrylamide, vinylpyridine, N -Vinylimidazole and the like can be mentioned, and monomers containing a tertiary amino group are particularly preferred, and 2-dialkylaminoethyl (meth) acrylate and 3-dialkylaminopropyl (meth) acrylamide are most preferred.
- (meth) acrylic acid amide containing X is preferable.
- amino acids containing a (meth) acryloyl group such as N- (meth) acryloylglycine and N- (meth) acryloylalanine are used.
- the macromonomer containing Y include known macromonomers, and a macromonomer having a polymerizable group at one end of poly (meth) acrylate, polystyrene, or polyester is preferable.
- Examples include macromonomer AA-6 (polymethyl methacrylate whose terminal group is methacryloyl group), AS-6 (polystyrene whose terminal group is methacryloyl group), AN-6S (terminal group is methacryloyl group).
- the polymerization is preferably performed using a radical polymerization initiator in a nitrogen atmosphere.
- a radical polymerization initiator a known radical polymerization initiator can be used, but azobisisobutyronitrile and methyl 2,2′-azobisisobutyrate are preferable from the viewpoint of molecular weight adjustment and handling.
- the radical polymerization initiator is preferably used in an amount of 0.01 mol% to 10 mol%, and most preferably 0.1 mol% to 5 mol%, based on the number of moles of all monomers.
- a chain transfer agent may be added to adjust the molecular weight.
- a thiol compound is particularly preferable, and alkanethiol having 5 to 20 carbon atoms, 2-mercaptoethanol and 2-mercaptopropionic acid are preferable.
- the chain transfer agent is preferably used in an amount of 0.01 mol% to 10 mol%, most preferably 0.1 mol% to 5 mol%, based on the total number of moles of monomers.
- the reaction temperature is preferably 60 to 100 ° C, and most preferably 70 to 90 ° C.
- the reaction solvent include the solvents mentioned in (1) The method of reacting the resin having a primary or secondary amino group with the X precursor x and the Y precursor y.
- the thus obtained novel resin of the present invention preferably has a weight average molecular weight measured by GPC method of 3,000 to 100,000, more preferably 5,000 to 50,000. .
- a weight average molecular weight measured by GPC method of 3,000 to 100,000, more preferably 5,000 to 50,000.
- the molecular weight is in the above range, there is an advantage that high developability and high storage stability can be achieved.
- the presence of a nitrogen atom in the main chain portion in the specific resin of the present invention can be confirmed by a method such as acid titration,
- the presence of a functional group having a pKa of 14 or less and The fact that the functional group is bonded to the nitrogen atom present in the main chain can be confirmed by methods such as base titration, nuclear magnetic resonance spectroscopy, and infrared spectroscopy.
- the point having an oligomer chain or polymer chain “Y” having a number average molecular weight of 500 to 1,000,000 in the side chain should be confirmed by a method such
- the specific resin of the present invention exhibits an excellent function particularly as a pigment dispersant.
- the pigment dispersion containing (A) the specific resin of the present invention, (B) pigment, and (C) solvent will be described in detail.
- the pigment dispersion of the present invention may contain only one type of (A) the specific resin of the present invention, or may contain two or more types.
- (A) the specific resin may be contained in the range of 1 part by mass to 200 parts by mass, preferably 5 parts by mass to 100 parts by mass with respect to 100 parts by mass of the pigment (B) described later. Parts, more preferably in the range of 5 to 60 parts by weight.
- ⁇ (B) Pigment> As the pigment that the pigment dispersion of the present invention has, conventionally known various inorganic pigments or organic pigments can be used. Further, considering that it is preferable to have a high transmittance, whether it is an inorganic pigment or an organic pigment, it is preferable to use a finer one as much as possible, and considering the handling properties, the average particle size of the pigment is 0.005 ⁇ m to 0.1 ⁇ m is preferable, and 0.005 ⁇ m to 0.05 ⁇ m is more preferable.
- the inorganic pigment examples include metal compounds such as metal oxides and metal complex salts. Specifically, iron, cobalt, aluminum, cadmium, lead, copper, titanium, magnesium, chromium, zinc, antimony And the like, and metal complex oxides such as the above.
- organic pigments examples include: C. I. Pigment Yellow 1, 1: 1, 2, 3, 4, 5, 6, 9, 10, 12, 13, 14, 16, 17, 24, 31, 32, 34, 35, 35: 1, 36, 36: 1, 37, 37: 1, 40, 41, 42, 43, 48, 53, 55, 61, 62, 62: 1, 63, 65, 73, 74, 75, 81, 83, 87, 93, 94, 95, 97, 100, 101, 104, 105, 108, 109, 110, 111, 116, 117, 119, 120, 126, 127, 127: 1, 128, 129, 133, 134, 136, 138, 139, 142, 147, 148, 150, 151, 153, 154, 155, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 172, 17 174, 175,
- those having a basic N atom in the structural formula of the pigment can be preferably used. These pigments having a basic N atom exhibit good dispersibility in the composition of the present invention. Although the cause is not fully elucidated, it is presumed that the good affinity between the photosensitive polymerization component and the pigment has an influence.
- organic pigments can be used alone or in various combinations in order to increase color purity. Specific examples of the above combinations are shown below.
- a red pigment an anthraquinone pigment, a perylene pigment, a diketopyrrolopyrrole pigment alone or at least one of them, a disazo yellow pigment, an isoindoline yellow pigment, a quinophthalone yellow pigment or a perylene red pigment , Etc.
- an anthraquinone pigment C.I. I. Pigment red 177
- perylene pigments include C.I. I. Pigment red 155, C.I. I.
- Pigment Red 224, and diketopyrrolopyrrole pigments include C.I. I. Pigment Red 254, and C.I. I. Mixing with Pigment Yellow 139 is preferred.
- the mass ratio of the red pigment to the yellow pigment is preferably 100: 5 to 100: 50. If the ratio is 100: 4 or less, it is difficult to suppress the light transmittance from 400 nm to 500 nm. If the ratio is 100: 51 or more, the main wavelength tends to be closer to the short wavelength, and the color resolution may not be improved. In particular, the mass ratio is optimally in the range of 100: 10 to 100: 30. In the case of a combination of red pigments, it can be adjusted in accordance with the required spectrum.
- a halogenated phthalocyanine pigment can be used alone, or a mixture thereof with a disazo yellow pigment, a quinophthalone yellow pigment, an azomethine yellow pigment, or an isoindoline yellow pigment can be used.
- a disazo yellow pigment e.g., a quinophthalone yellow pigment, an azomethine yellow pigment, or an isoindoline yellow pigment
- C.I. I. Pigment Green 7, 36, 37 and C.I. I. Pigment yellow 83 e. I. Pigment yellow 138, C.I. I. Pigment yellow 139, C.I. I. Pigment yellow 150, C.I. I. Pigment yellow 180 or C.I. I. Mixing with Pigment Yellow 185 is preferred.
- the mass ratio of green pigment to yellow pigment is preferably 100: 5 to 100: 150.
- the mass ratio is particularly preferably in the range of 100: 30 to 100: 120.
- a phthalocyanine pigment can be used alone, or a mixture of this with a dioxazine purple pigment can be used.
- C.I. I. Pigment blue 15: 6 and C.I. I. Mixing with pigment violet 23 is preferred.
- the mass ratio of the blue pigment to the violet pigment is preferably 100: 0 to 100: 100, more preferably 100: 10 or less.
- the pigment for the black matrix carbon, titanium black, iron oxide, titanium oxide alone or a mixture thereof is used, and a combination of carbon and titanium black is preferable.
- the mass ratio of carbon to titanium black is preferably in the range of 100: 0 to 100: 60.
- the pigment used in the present invention is preferably a pigment that has been subjected to a refinement treatment in advance.
- the finer primary particles of the pigment are well known by mechanically kneading with i) a pigment, ii) a water-soluble inorganic salt, and iii) a water-soluble organic solvent that does not substantially dissolve the inorganic salt with a kneader. (Salt milling method).
- a polymer compound for coating a soot pigment may be used at the same time.
- Pigment Examples of the pigment include the same pigments as described above.
- ii) Water-soluble inorganic salt The inorganic salt is not particularly limited as long as it is soluble in water, and sodium chloride, barium chloride, potassium chloride, sodium sulfate and the like can be used. Sodium sulfate is preferably used.
- the amount of the inorganic salt used for salt milling is preferably 1 to 30 times by weight, particularly 5 to 25 times by weight of the organic pigment, from the viewpoints of processing efficiency and production efficiency. This is because the finer efficiency is higher as the amount ratio of the inorganic salt to the organic pigment is larger, but the amount of treatment of one pigment is reduced.
- Water-soluble organic solvent functions to wet organic pigments and inorganic salts, and dissolves (mixes) in water and uses inorganic salts. If it does not melt
- a high boiling point solvent having a boiling point of 120 ° C. or higher is preferable from the viewpoint of safety because the temperature rises during salt milling and the solvent easily evaporates.
- water-soluble organic solvent examples include 2-methoxyethanol, 2-butoxyethanol, 2- (isopentyloxy) ethanol, 2- (hexyloxy) ethanol, ethylene glycol, diethylene glycol, diethylene glycol monoethyl ether, diethylene glycol monoethyl ether.
- the addition amount of the water-soluble organic solvent is preferably 5 to 50% by weight with respect to the inorganic salt. More preferably, it is 10% to 40% by weight based on the inorganic salt, and most preferably 15% to 35% by weight based on the inorganic salt. If the addition amount is less than 5% by weight, uniform kneading becomes difficult and the particle sizes may become uneven. When the addition amount is 50% by weight or more, the kneaded composition becomes too soft, and it becomes difficult to apply shear to the kneaded composition, so that a sufficient refinement effect cannot be obtained.
- the water-soluble organic solvent may be added all at the beginning of salt milling, or may be added in divided portions. A water-soluble organic solvent may be used independently and can also use 2 or more types together.
- Pigment-coating polymer compound The pigment-coating polymer compound that may be added is preferably solid at room temperature, insoluble in water, and at least partly in a water-soluble organic solvent used as a wetting agent during salt milling. It is necessary to be soluble, and natural resins, modified natural resins, synthetic resins, and synthetic resins modified with natural resins are used. When using a dried treated pigment, the compound used is preferably solid at room temperature.
- the natural resin is typically rosin
- the modified natural resin includes rosin derivatives, fiber derivatives, rubber derivatives, protein derivatives and oligomers thereof.
- Examples of the synthetic resin include epoxy resin, acrylic resin, maleic acid resin, butyral resin, polyester resin, melamine resin, phenol resin, polyurethane resin, and the like.
- Examples of synthetic resins modified with natural resins include rosin-modified maleic acid resins and rosin-modified phenolic resins.
- Synthetic resins include polyamidoamine and its salt, polycarboxylic acid and its salt, high molecular weight unsaturated acid ester, polyurethane, polyester, poly (meth) acrylate, (meth) acrylic copolymer, naphthalenesulfonic acid formalin condensate Is mentioned.
- the timing of adding these resins may be added all at the beginning of salt milling, or may be added in divided portions.
- the primary particle diameter of the pigment is preferably 5 to 100 nm, more preferably 5 to 70 nm, still more preferably 5 to 50 nm, from the viewpoint of color unevenness and contrast. Most preferred is 5-40 nm.
- the specific resin of the present invention is particularly effective in the range of 5 to 40 nm.
- the primary particle diameter of the pigment can be measured by a known method such as an electron microscope.
- the pigment is preferably a pigment selected from anthraquinone, azomethine, benzylidene, cyanine, diketopyrrolopyrrole, and phthalocyanine.
- the pigment content in the pigment dispersion of the present invention is preferably 30% by mass or more, more preferably 35% by mass or more and 80% by mass or less, based on the total solid content of the pigment dispersion. Most preferably, it is at least 70% by mass.
- the specific resin of the present invention is used as a pigment dispersant, it can be said that the effect is particularly remarkable under a high content condition in which the pigment is 40% by mass or more, in which stable uniform dispersion is difficult with a known dispersant.
- the pigment dispersion of the present invention has at least one (C) solvent.
- C) solvent the liquid selected from the organic solvent shown below is mentioned, The solubility of each component contained in a pigment dispersion liquid, the applicability
- the solvent include esters such as ethyl acetate, n-butyl acetate, isobutyl acetate, amyl formate, isoamyl acetate, butyl propionate, isopropyl butyrate, ethyl butyrate, butyl butyrate, methyl oxyacetate, and ethyl oxyacetate.
- esters such as ethyl acetate, n-butyl acetate, isobutyl acetate, amyl formate, isoamyl acetate, butyl propionate, isopropyl butyrate, ethyl butyrate, butyl butyrate, methyl oxyacetate, and ethyl oxyacetate.
- Ethers such as diethylene glycol dimethyl ether, tetrahydrofuran, ethylene glycol monomethyl ether, ethylene glycol monoethyl ether, methyl cellosolve acetate (ethylene glycol monomethyl ether acetate), ethyl cellosolve acetate (ethylene glycol monoethyl ether acetate), diethylene glycol monomethyl ether, diethylene glycol mono Ethyl ether, diethylene glycol monobutyl ether, diethylene glycol monoethyl ether acetate, diethylene glycol monobutyl ether acetate, propylene glycol methyl ether, propylene glycol monomethyl ether acetate, propylene glycol ethyl ether acetate, Propylene glycol propyl ether acetate; ketones such as methyl ethyl ketone, cyclohexanone, 2-heptanone, 3-heptanone; and aromatic hydrocarbons, e.g., to
- methyl 3-ethoxypropionate, ethyl 3-ethoxypropionate, ethyl cellosolve acetate, ethyl lactate, diethylene glycol dimethyl ether, butyl acetate, methyl 3-methoxypropionate, 2-heptanone, cyclohexanone, diethylene glycol monoethyl ether acetate, Diethylene glycol monobutyl ether acetate, propylene glycol methyl ether, propylene glycol monomethyl ether acetate (PGMEA) and the like are more preferable.
- the content of the solvent (C) in the pigment dispersion of the present invention is preferably 50 to 90% by mass, more preferably 60 to 95% by mass, and most preferably 70 to 90% by mass.
- the content of the solvent is within the above range, it is advantageous in terms of suppressing the generation of foreign matter.
- the pigment dispersion of the present invention contains other components depending on the purpose, such as the use of the pigment dispersion, as long as the effects of the present invention are not impaired. be able to.
- the pigment dispersion of the present invention preferably further contains a pigment derivative.
- a pigment derivative having an acidic group dispersibility and dispersion stability are dramatically improved.
- the pigment derivative preferably has a structure in which a part of an organic pigment, anthraquinones or acridones is substituted with an acidic group, a basic group or a phthalimidomethyl group.
- organic pigment constituting the pigment derivative examples include diketopyrrolopyrrole pigments, azo pigments such as azo, disazo, polyazo, phthalocyanine pigments such as copper phthalocyanine, halogenated copper phthalocyanine, and metal-free phthalocyanine, aminoanthraquinone, diaminodi Anthraquinone pigments such as anthraquinone, anthrapyrimidine, flavantron, anthanthrone, indanthrone, pyranthrone, violanthrone, quinacridone pigment, dioxazine pigment, perinone pigment, perylene pigment, thioindigo pigment, isoindoline pigment, isoindoline Examples thereof include linone pigments, quinophthalone pigments, selenium pigments, and metal complex pigments.
- the acidic group possessed by the pigment derivative sulfonic acid, carboxylic acid and quaternary ammonium salt thereof are preferable.
- an amino group is preferable.
- the amount of the pigment derivative used is not particularly limited, but it is preferably 5 to 50% by mass, more preferably 10 to 30% by mass, based on the pigment.
- the pigment dispersion of the present invention further comprises (G) a graft copolymer containing a monomer containing a heterocyclic ring and a polymerizable oligomer having an ethylenically unsaturated bond as a copolymer unit (hereinafter simply referred to as (G) graft copolymer). It is preferable to contain a combination). Thereby, dispersibility further improves.
- a graft copolymer containing a heterocyclic ring and a polymerizable oligomer having an ethylenically unsaturated bond as a copolymer unit
- a combination thereby, dispersibility further improves.
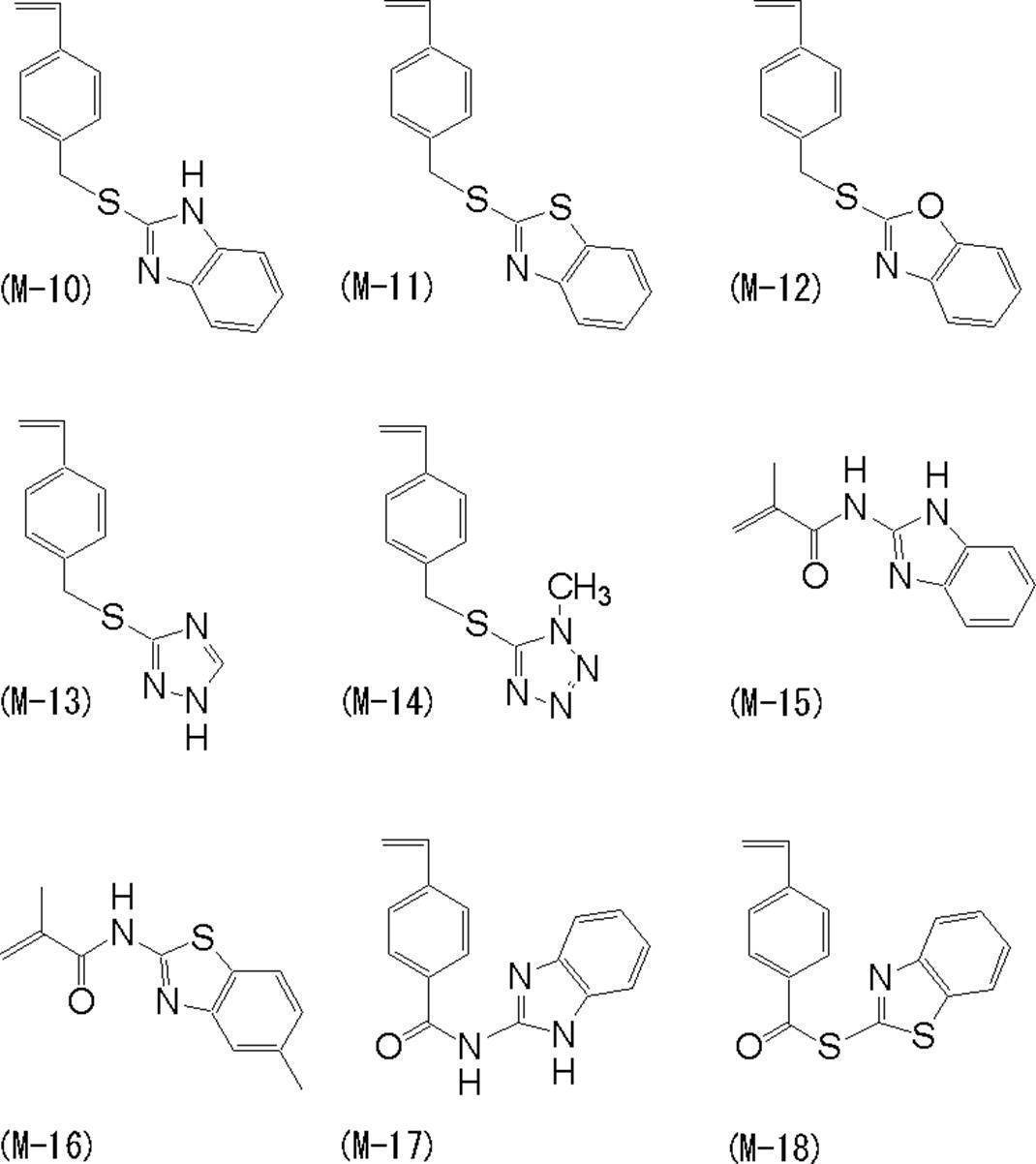
- the monomer containing a heterocyclic ring monomers represented by general formula (VI-1) and general formula (VI-2) are preferable.
- R 1 represents a hydrogen atom or a substituted or unsubstituted alkyl group.
- R 2 represents an alkylene group.
- W represents —CO—, —C ( ⁇ O) O—, —CONH—, —OC ( ⁇ O) —, or a phenylene group.
- X is —O—, —S—, —C ( ⁇ O) O—, —CONH—, —C ( ⁇ O) S—, —NHCONH—, —NHC ( ⁇ O) O—, —NHC ( ⁇ O ) S—, —OC ( ⁇ O) —, —OCONH—, —NHCO—.
- Y represents any one selected from NR 3 , O, and S, and R 3 represents a hydrogen atom, an alkyl group, or an aryl group.
- R 3 represents a hydrogen atom, an alkyl group, or an aryl group.
- N and Y are connected to each other to form a cyclic structure.
- m and n are each independently 0 or 1.
- R 1 represents a hydrogen atom or a substituted or unsubstituted alkyl group.
- the alkyl group is preferably an alkyl group having 1 to 12 carbon atoms, more preferably 1 to 8 carbon atoms, and particularly preferably 1 to 4 carbon atoms.
- Preferred alkyl groups are methyl, ethyl, propyl, n-butyl, i-butyl, t-butyl, n-hexyl, cyclohexyl, 2-hydroxyethyl, 3-hydroxypropyl, 2 -Hydroxypropyl group, 2-methoxyethyl group and the like can be mentioned.
- R 2 represents an alkylene group, preferably an alkylene group having 1 to 12 carbon atoms, more preferably 1 to 8 carbon atoms, and particularly preferably 1 to 4 carbon atoms.
- Preferred alkylene groups include a methylene group, an ethylene group, a propylene group, a trimethylene group, and a tetramethylene group.
- Y represents any one selected from NR 3 , O, and S, and R 3 represents a hydrogen atom, an alkyl group, or an aryl group. As Y, S and NH are particularly preferable.
- X is —O—, —S—, —C ( ⁇ O) O—, —CONH—, —C ( ⁇ O) S—, —NHCONH—, —NHC ( ⁇ O) O—, —NHC ( ⁇ O ) Represents S—, —OC ( ⁇ O) —, —OCONH—, —NHCO—, —O—, —S—, —CONH—, —NHCONH—, —NHC ( ⁇ O) S -Is particularly preferred.
- N and Y are connected to each other to form a cyclic structure.
- the cyclic structure formed include imidazole ring, pyrimidine ring, triazole ring, tetrazole ring, thiazole ring, monocyclic structure of oxazole ring, and benzimidazole ring, benzthiazole ring, benzoxazole ring, purine ring, quinazoline ring, perimidine
- condensed ring structures such as a ring, and in the present invention, a condensed ring structure is preferable. Of these, a benzimidazole ring, a benzthiazole ring, and a benzoxazole ring are particularly preferable.
- R 1 represents hydrogen or a methyl group
- R 2 represents an alkylene group
- Z represents a nitrogen-containing heterocyclic structure.
- alkylene group represented by R 2 include a methylene group, an ethylene group, a trimethylene group, a tetramethylene group, a hexamethylene group, a 2-hydroxypropylene group, a methyleneoxy group, an ethyleneoxy group, a methyleneoxycarbonyl group, a methylenethio group, And a methylene group, a methyleneoxy group, a methyleneoxycarbonyl group, and a methylenethio group are preferable.
- Z represents a nitrogen-containing heterocyclic structure.
- the heterocyclic structure represented by Z is preferably a structure represented by the following general formula (2) or (3).
- X represents a single bond, an alkylene group (for example, a methylene group, an ethylene group, a propylene group, a trimethylene group, a tetramethylene group, etc.), —O—, —S—, —NR—, and One selected from the group consisting of —C ( ⁇ O) —.
- R represents a hydrogen atom or an alkyl group.
- R represents an alkyl group
- examples of the alkyl group include a methyl group, an ethyl group, an n-propyl group, an i-propyl group, an n-butyl group, Examples thereof include t-butyl group, n-hexyl group, n-octyl group, 2-ethylhexyl group, n-octadecyl group and the like.
- X is preferably a single bond, a methylene group, —O— or —C ( ⁇ O) —, and particularly preferably —C ( ⁇ O) —.
- ring A, ring B, and ring C each independently represent an aromatic ring.
- the aromatic ring include a benzene ring, naphthalene ring, indene ring, azulene ring, fluorene ring, anthracene ring, pyridine ring, pyrazine ring, pyrimidine ring, pyrrole ring, imidazole ring, indole ring, quinoline ring, acridine ring, Examples include phenothiazine ring, phenoxazine ring, acridone ring, anthraquinone ring, among others, benzene ring, naphthalene ring, anthracene ring, pyridine ring, phenoxazine ring, acridine ring, phenothiazine ring, phenoxazine ring, acridone
- (G) Preferred examples of the polymerizable oligomer (macromonomer) that can be used for the synthesis of the graft copolymer include polymethyl (meth) acrylate, poly-n-butyl (meth) acrylate, and poly-i-butyl (meth).
- a polymer in which a (meth) acryloyl group is bonded to one molecular end of acrylate or polystyrene can be exemplified.
- the graft copolymer further contains a monomer having an acid group (structural unit) as a copolymerization component.
- the monomer having an acid group include (meth) acrylic acid, p-vinylbenzoic acid, maleic acid, fumaric acid, itaconic acid, succinic anhydride adduct of 2-hydroxyethyl (meth) acrylate, (meth) And phthalic anhydride adduct of 2-hydroxyethyl acrylate.
- the graft copolymer contains 2 to 50% by mass of the monomer represented by the general formula (IV-1) or (IV-2), and further has an ethylenic group at the end.
- a copolymer containing 10 to 90% by mass of a polymerizable oligomer having a saturated double bond and 1 to 30% by mass of a structural unit having an acid group is preferred.
- the pigment dispersion of the present invention is prepared from other polymer materials (for example, polyamidoamine and its salt, polycarboxylic acid and its salt, high molecular weight unsaturated acid ester, Modified polyurethane, modified polyester, modified poly (meth) acrylate, (meth) acrylic copolymer, naphthalenesulfonic acid formalin condensate], and polyoxyethylene alkyl phosphate ester, polyoxyethylene alkylamine, alkanolamine, etc.
- a dispersant can be further added.
- Such other polymer materials can be further classified into linear polymers, terminal-modified polymers, graft polymers, and block polymers based on their structures.
- polymer materials that can be used together are adsorbed on the surface of the pigment and act to prevent re-aggregation. Therefore, a terminal-modified polymer, a graft polymer and a block polymer having an anchor site to the pigment surface can be mentioned as preferred structures.
- Specific examples of other polymer materials that can be used in the present invention include “Disperbyk-101 (polyamidoamine phosphate), 107 (carboxylic acid ester), 110 (copolymer containing an acid group)”, 130, manufactured by BYK Chemie.
- the content of the polymer material in the present invention is preferably 1% by mass to 100% by mass with respect to the specific resin of the present invention, and 3% by mass to 80% by mass. More preferably, 5% by mass to 50% by mass is even more preferable. Since the pigment dispersion of the present invention uses the specific resin of the present invention as a pigment dispersant, the pigment dispersion is excellent in pigment dispersibility and dispersion stability even when a fine pigment is contained at a high concentration.
- the curable composition of the present invention contains (D) a photopolymerization initiator for improving sensitivity and pattern formation.
- the photopolymerization initiator in the present invention is a compound that decomposes by light and initiates and accelerates the polymerization of the polymerizable component in the present invention, and preferably has an absorption in the wavelength region of 300 to 500 nm.
- a photoinitiator can be used individually or in combination of 2 or more types.
- Examples of the photopolymerization initiator include organic halogenated compounds, oxydiazole compounds, carbonyl compounds, ketal compounds, benzoin compounds, acridine compounds, organic peroxide compounds, azo compounds, coumarin compounds, azide compounds, metallocene compounds, hexaaryls.
- Examples thereof include a rubiimidazole compound, an organic boric acid compound, a disulfonic acid compound, an oxime ester compound, an onium salt compound, an acylphosphine (oxide) compound, and an alkylamino compound.
- a rubiimidazole compound an organic boric acid compound, a disulfonic acid compound, an oxime ester compound, an onium salt compound, an acylphosphine (oxide) compound, and an alkylamino compound.
- organic halogenated compounds include Wakabayashi et al., “Bull Chem. Soc Japan” 42, 2924 (1969), US Pat. No. 3,905,815, Japanese Patent Publication No. 46-4605, JP 48-36281, JP 55-32070, JP 60-239736, JP 61-169835, JP 61-169837, JP 62-58241, JP 62 -212401, JP-A-63-70243, JP-A-63-298339, M.S. P. Hut “Journal of Heterocyclic Chemistry” 1 (No 3), (1970) ”and the like, and particularly, an oxazole compound substituted with a trihalomethyl group, and an s-triazine compound.
- an s-triazine derivative in which at least one mono-, di-, or trihalogen-substituted methyl group is bonded to the s-triazine ring specifically, for example, 2,4,6- Tris (monochloromethyl) -s-triazine, 2,4,6-tris (dichloromethyl) -s-triazine, 2,4,6-tris (trichloromethyl) -s-triazine, 2-methyl-4,6- Bis (trichloromethyl) -s-triazine, 2-n-propyl-4,6-bis (trichloromethyl) -s-triazine, 2- ( ⁇ , ⁇ , ⁇ -trichloroethyl) -4,6-bis (trichloro Methyl) -s-triazine, 2-phenyl-4,6-bis (trichloromethyl) -s-triazine, 2- (
- Examples of the oxodiazole compound include 2-trichloromethyl-5-styryl-1,3,4-oxodiazole, 2-trichloromethyl-5- (cyanostyryl) -1,3,4-oxodiazole, 2- And trichloromethyl-5- (naphth-1-yl) -1,3,4-oxodiazole, 2-trichloromethyl-5- (4-styryl) styryl-1,3,4-oxodiazole, and the like. .
- carbonyl compound examples include benzophenone, Michler ketone, 2-methylbenzophenone, 3-methylbenzophenone, 4-methylbenzophenone, 2-chlorobenzophenone, 4-bromobenzophenone, 2-carboxybenzophenone and other benzophenone derivatives, 2,2-dimethoxy-2 -Phenylacetophenone, 2,2-diethoxyacetophenone, 1-hydroxycyclohexyl phenyl ketone, ⁇ -hydroxy-2-methylphenylpropanone, 1-hydroxy-1-methylethyl- (p-isopropylphenyl) ketone, 1-hydroxy -1- (p-dodecylphenyl) ketone, 2-methyl- (4 ′-(methylthio) phenyl) -2-morpholino-1-propanone, 1,1,1-trichloromethyl- (p-butylphenyl) Acetophenone derivatives such as ketones, 2-benzyl-2-dimethylamino-4-morph
- Examples of the ketal compound include benzyl methyl ketal and benzyl- ⁇ -methoxyethyl ethyl acetal.
- Examples of the benzoin compound include m-benzoin isopropyl ether, benzoin isobutyl ether, benzoin methyl ether, and methyl-o-benzoylbenzoate.
- acridine compound examples include 9-phenylacridine, 1,7-bis (9-acridinyl) heptane and the like.
- organic peroxide compound examples include trimethylcyclohexanone peroxide, acetylacetone peroxide, 1,1-bis (tert-butylperoxy) -3,3,5-trimethylcyclohexane, 1,1-bis (tert-butylperoxide).
- Examples of the azo compound include azo compounds described in JP-A-8-108621.
- Examples of coumarin compounds include 3-methyl-5-amino-((s-triazin-2-yl) amino) -3-phenylcoumarin, 3-chloro-5-diethylamino-((s-triazin-2-yl). ) Amino) -3-phenylcoumarin, 3-butyl-5-dimethylamino-((s-triazin-2-yl) amino) -3-phenylcoumarin, and the like.
- azide compound examples include organic azide compounds described in US Pat. No. 2,848,328, US Pat. No. 2,852,379 and US Pat. No. 2,940,553, 2,6-bis (4-azidobenzylidene) -4-ethyl. And cyclohexanone (BAC-E).
- metallocene compound examples include JP-A-59-152396, JP-A-61-151197, JP-A-63-41484, JP-A-2-249, JP-A-2-4705, Various titanocene compounds described in JP-A-5-83588, such as di-cyclopentadienyl-Ti-bis-phenyl, di-cyclopentadienyl-Ti-bis-2,6-difluorophen-1-yl, di- -Cyclopentadienyl-Ti-bis-2,4-di-fluorophen-1-yl, di-cyclopentadienyl-Ti-bis-2,4,6-trifluorophen-1-yl, di- Cyclopentadienyl-Ti-bis-2,3,5,6-tetrafluorophen-1-yl, di-cyclopentadienyl-Ti-bis-2,3,4,5,6-pentaph Orofen-1-y
- hexaarylbiimidazole compounds include, for example, each specification such as JP-B-6-29285, US Pat. Nos. 3,479,185, 4,311,783, and 4,622,286. And, specifically, 2,2′-bis (o-chlorophenyl) -4,4 ′, 5,5′-tetraphenylbiimidazole, 2,2′-bis (o-bromophenyl) )) 4,4 ′, 5,5′-tetraphenylbiimidazole, 2,2′-bis (o, p-dichlorophenyl) -4,4 ′, 5,5′-tetraphenylbiimidazole, 2,2 ′ -Bis (o-chlorophenyl) -4,4 ', 5,5'-tetra (m-methoxyphenyl) biimidazole, 2,2'-bis (o, o'-dichlorophenyl) -4,4
- organic borate compound examples include JP-A-62-143044, JP-A-62-1050242, JP-A-9-188865, JP-A-9-188686, JP-A-9-188710, JP-A-2000. -131837, Japanese Patent Application Laid-Open No. 2002-107916, Japanese Patent No. 2764769, Japanese Patent Application No. 2000-310808, etc., and Kunz, Martin “Rad Tech'98. Proceeding April 19-22, 1998, Chicago”, etc.
- Organic borate salts organic boron sulfonium complexes or organic boron oxosulfonium complexes described in JP-A-6-157623, JP-A-6-175564, JP-A-6-175561, JP-A-6-175554 Gazette, JP-A-6-175553
- Organoboron iodonium complexes described in JP-A-9-188710, organoboron phosphonium complexes described in JP-A-9-188710, JP-A-6-34811, JP-A-7-128785, JP-A-7-140589, JP-A-7 Specific examples include organoboron transition metal coordination complexes described in JP-A-306527 and JP-A-7-292014.
- Examples of the disulfone compound include compounds described in JP-A No. 61-166544 and Japanese Patent Application No. 2001-132318.
- Oxime ester compounds include J. C. S. Perkin II (1979) 1653-1660, J. MoI. C. S. Perkin II (1979) 156-162, Journal of Photopolymer Science and Technology (1995) 202-232, Japanese Unexamined Patent Publication No. 2000-66385, Japanese Unexamined Patent Publication No. 2000-80068, Special Table No. 2004-534797 Compounds and the like.
- oxime initiators typified by the oxime ester compound
- a compound represented by the following general formula (3) is more preferable from the viewpoint of sensitivity, time stability, and coloring during post-heating.
- R and X each independently represent a monovalent substituent
- A represents a divalent organic group
- Ar represents an aryl group.
- n is an integer of 0 to 5.
- R is preferably an acyl group from the viewpoint of high sensitivity, and specifically, an acetyl group, a propionyl group, a benzoyl group, and a toluyl group are preferable.
- A is an unsubstituted alkylene group, an alkylene group substituted with an alkyl group (for example, a methyl group, an ethyl group, a tert-butyl group, or a dodecyl group) from the viewpoint of increasing sensitivity and suppressing coloration due to heating,
- An alkylene group substituted with an alkenyl group for example, vinyl group, allyl group
- aryl group for example, phenyl group, p-tolyl group, xylyl group, cumenyl group, naphthyl group, anthryl group, phenanthryl group, styryl group
- a substituted alkylene group is preferred.
- Ar is preferably a substituted or unsubstituted phenyl group from the viewpoint of increasing sensitivity and suppressing coloring due to heating.
- the substituent is preferably a halogen group such as a fluorine atom, a chlorine atom, a bromine atom or an iodine atom.
- X is an alkyl group that may have a substituent, an aryl group that may have a substituent, or an alkenyl that may have a substituent from the viewpoint of improving solvent solubility and absorption efficiency in the long wavelength region.
- An arylthioxy group which may have an amino group and an amino group which may have a substituent are preferable.
- n is preferably an integer of 1 to 2.
- the compound represented by the general formula (3) is a compound represented by the general formula ( ⁇ ) in paragraphs [0089] to [0108] of Japanese Patent Application No. 2008-251321 previously proposed by the present applicant. It is described in detail, and the compounds described herein can be suitably used in the present invention.
- onium salt compounds examples include S.I. I. Schlesinger, Photogr. Sci. Eng. , 18, 387 (1974), T.A. S. Bal et al, Polymer, 21, 423 (1980), diazonium salts, US Pat. No. 4,069,055, ammonium salts described in JP-A-4-365049, US Pat. No. 4,069, No. 055, No. 4,069,056, phosphonium salts described in European Patent Nos. 104 and 143, U.S. Pat. Nos. 339,049 and 410,201, JP -150848 and iodonium salts described in JP-A-2-296514.
- the iodonium salt that can be suitably used in the present invention is a diaryl iodonium salt, and is preferably substituted with two or more electron donating groups such as an alkyl group, an alkoxy group, and an aryloxy group from the viewpoint of stability.
- an iodonium salt in which one substituent of the triarylsulfonium salt has a coumarin or an anthraquinone structure and absorption at 300 nm or more is preferable.
- Examples of the sulfonium salt that can be suitably used in the present invention include European Patent Nos. 370,693, 390,214, 233,567, 297,443, 297,442, and U.S. Pat. 933,377, 161,811, 410,201, 339,049, 4,760,013, 4,734,444, 2,833,827, Germany
- Examples thereof include sulfonium salts described in the specifications of Patent Nos. 2,904,626, 3,604,580, and 3,604,581, and are preferably electron withdrawing groups from the viewpoint of stability and sensitivity. It is preferably substituted with.
- the electron withdrawing group preferably has a Hammett value greater than zero.
- Preferred electron-withdrawing groups include halogen atoms and carboxylic acids.
- Other preferable sulfonium salts include sulfonium salts in which one substituent of the triarylsulfonium salt has a coumarin or anthraquinone structure and absorbs at 300 nm or more.
- a sulfonium salt in which the triarylsulfonium salt has an allyloxy group or an arylthio group as a substituent and has absorption at 300 nm or more can be mentioned.
- onium salt compounds J. V. Crivello et al, Macromolecules, 10 (6), 1307 (1977), J. MoI. V. Crivello et al, J.A. Polymer Sci. , Polymer Chem. Ed. , 17, 1047 (1979), a selenonium salt described in C.I. S. Wen et al, Teh, Proc. Conf. Rad. Curing ASIA, p478 Tokyo, Oct (1988) and onium salts such as arsonium salts.
- acylphosphine (oxide) compound examples include Irgacure 819, Darocur 4265, and Darocur TPO manufactured by Ciba Specialty Chemicals.
- Examples of the alkylamino compound include compounds having a dialkylaminophenyl group described in paragraph No. [0047] of JP-A-9-281698, JP-A-6-19240, JP-A-6-19249, and the like.
- An amine compound is mentioned.
- examples of the compound having a dialkylaminophenyl group include compounds such as ethyl p-dimethylaminobenzoate, and dialkylaminophenyl carbaldehyde such as p-diethylaminobenzcarbaldehyde and 9-julolidylcarbaldehyde.
- Examples of the amine compound include triethanolamine, diethanolamine, and triethylamine.
- a compound selected from the group consisting of a methyloxadiazole compound and a 3-aryl-substituted coumarin compound is preferred.
- triazine compounds More preferred are triazine compounds, alkylamino compounds, ⁇ -aminoketone compounds, acylphosphine compounds, phosphine oxide compounds, oxime compounds, biimidazole compounds, onium compounds, benzophenone compounds, and acetophenone compounds.
- At least one compound selected from the group consisting of triazine compounds, alkylamino compounds, oxime compounds and biimidazole compounds is more preferred, and oxime compounds and biimidazole compounds are most preferred.
- the curable composition of the present invention when used for the formation of colored pixels in a color filter of a solid-state image sensor, the pigment concentration of the curable composition is high due to the formulation, so the amount of initiator added is reduced and the sensitivity is increased. Will fall.
- an initiator that generates a halogen-containing compound at the time of exposure such as a triazine compound, it causes corrosion of the equipment and is difficult to use.
- an oxime compound is preferable, and an oxime compound having absorption at 365 nm is most preferable.
- the content of the photopolymerization initiator is preferably 0.1% by mass to 50% by mass, more preferably 0.5% by mass to 30% by mass with respect to the total solid content of the curable composition of the present invention. % By mass, particularly preferably 1% by mass to 20% by mass. Within this range, good sensitivity and pattern formability can be obtained.
- the curable composition of the present invention contains a compound containing an ethylenically unsaturated double bond other than the resin (hereinafter, sometimes simply referred to as “compound containing an ethylenically unsaturated double bond”). can do.
- the compound containing an ethylenically unsaturated double bond that can be used in the present invention is an addition-polymerizable compound having at least one ethylenically unsaturated double bond other than the above-mentioned resin, and has terminal ethylene. Selected from compounds having at least one, preferably two or more, unsaturated unsaturated bonds. Such a compound group is widely known in the industrial field, and can be used without any particular limitation in the present invention. These have chemical forms such as monomers, prepolymers, i.e. dimers, trimers and oligomers, or mixtures thereof and copolymers thereof.
- Examples of monomers and copolymers thereof include unsaturated carboxylic acids (for example, acrylic acid, methacrylic acid, itaconic acid, crotonic acid, isocrotonic acid, maleic acid, etc.), and esters and amides thereof.
- unsaturated carboxylic acids for example, acrylic acid, methacrylic acid, itaconic acid, crotonic acid, isocrotonic acid, maleic acid, etc.
- esters and amides thereof examples include unsaturated carboxylic acids (for example, acrylic acid, methacrylic acid, itaconic acid, crotonic acid, isocrotonic acid, maleic acid, etc.), and esters and amides thereof.
- an ester of an unsaturated carboxylic acid and an aliphatic polyhydric alcohol compound, or an amide of an unsaturated carboxylic acid and an aliphatic polyvalent amine compound is used.
- an addition reaction product of an unsaturated carboxylic acid ester or amide having a nucleophilic substituent such as a hydroxy group, an amino group or a mercapto group with a monofunctional or polyfunctional isocyanate or epoxy, and a monofunctional or polyfunctional compound is also preferably used.
- a substitution reaction product of an unsaturated carboxylic acid ester or amide having a leaving substituent such as a tosyloxy group and a monofunctional or polyfunctional alcohol, amine or thiol is also suitable.
- ester monomer of an aliphatic polyhydric alcohol compound and an unsaturated carboxylic acid include acrylic acid esters such as ethylene glycol diacrylate, triethylene glycol diacrylate, 1,3-butanediol diacrylate, and tetramethylene glycol.
- Methacrylic acid esters include tetramethylene glycol dimethacrylate, triethylene glycol dimethacrylate, neopentyl glycol dimethacrylate, trimethylolpropane trimethacrylate, trimethylolethane trimethacrylate, ethylene glycol dimethacrylate, 1,3-butanediol dimethacrylate, Hexanediol dimethacrylate, pentaerythritol dimethacrylate, pentaerythritol trimethacrylate, pentaerythritol tetramethacrylate, dipentaerythritol dimethacrylate, dipentaerythritol hexamethacrylate, sorbitol trimethacrylate, sorbitol tetramethacrylate, bis [p- (3-methacryloxy- 2-hydroxyp Epoxy) phenyl] dimethyl methane, bis - [p- (me
- Itaconic acid esters include ethylene glycol diitaconate, propylene glycol diitaconate, 1,3-butanediol diitaconate, 1,4-butanediol diitaconate, tetramethylene glycol diitaconate, pentaerythritol diitaconate And sorbitol tetritaconate.
- crotonic acid esters include ethylene glycol dicrotonate, tetramethylene glycol dicrotonate, pentaerythritol dicrotonate, and sorbitol tetradicrotonate.
- isocrotonic acid esters include ethylene glycol diisocrotonate, pentaerythritol diisocrotonate, and sorbitol tetraisocrotonate.
- maleic acid esters include ethylene glycol dimaleate, triethylene glycol dimaleate, pentaerythritol dimaleate, and sorbitol tetramaleate.
- esters examples include, for example, aliphatic alcohol esters described in JP-B-51-47334 and JP-A-57-196231, JP-A-59-5240, and JP-A-59-5241. Those having an aromatic skeleton described in JP-A-2-226149 and those containing an amino group described in JP-A-1-165613 are also preferably used. Furthermore, the ester monomers described above can also be used as a mixture.
- monomers containing acid groups can also be used, for example, (meth) acrylic acid, pentaerythritol triacrylate succinic acid monoester, dipentaerythritol pentaacrylate succinic acid monoester, pentaerythritol triacrylate maleic acid monoester, dipenta Erythritol pentaacrylate maleic acid monoester, pentaerythritol triacrylate phthalic acid monoester, dipentaerythritol pentaacrylate phthalic acid monoester, pentaerythritol triacrylate tetrahydrophthalic acid monoester, dipentaerythritol pentaacrylate tetrahydrophthalic acid monoester It is done. In these, pentaerythritol triacrylate succinic acid monoester etc. are mentioned.
- amide monomers of aliphatic polyvalent amine compounds and unsaturated carboxylic acids include methylene bis-acrylamide, methylene bis-methacrylamide, 1,6-hexamethylene bis-acrylamide, 1,6-hexamethylene bis. -Methacrylamide, diethylenetriamine trisacrylamide, xylylene bisacrylamide, xylylene bismethacrylamide and the like.
- amide monomers include those having a cyclohexylene structure described in JP-B-54-21726.
- urethane-based addition-polymerizable compounds produced by using an addition reaction of isocyanate and hydroxyl group are also suitable. Specific examples thereof include, for example, one molecule described in JP-B-48-41708.
- a vinyl urethane compound containing two or more polymerizable vinyl groups in one molecule obtained by adding a vinyl monomer containing a hydroxyl group represented by the following general formula to a polyisocyanate compound having two or more isocyanate groups. Can be mentioned.
- urethane acrylates such as those described in JP-A-51-37193, JP-B-2-32293, JP-B-2-16765, JP-B-58-49860, JP-B-56-17654 Urethane compounds having an ethylene oxide skeleton described in JP-B-62-39417 and JP-B-62-39418 are also suitable. Furthermore, by using addition polymerizable compounds having an amino structure or a sulfide structure in the molecule described in JP-A-63-277653, JP-A-63-260909, JP-A-1-105238 Can obtain a photopolymerizable composition having an excellent photosensitive speed.
- the details of usage methods such as the structure, single use or combined use, addition amount and the like can be arbitrarily set according to the performance design of the curable composition. For example, it is selected from the following viewpoints. From the viewpoint of sensitivity, a structure having a large unsaturated group content per molecule is preferable, and in many cases, a bifunctional or higher functionality is preferable. Further, in order to increase the strength of the image portion, that is, the cured film, those having three or more functionalities are preferable, and further, different functional numbers and different polymerizable groups (for example, acrylic acid ester, methacrylic acid ester, styrene compound, vinyl ether type).
- a method of adjusting both sensitivity and strength by using a compound) is also effective.
- a compound containing two or more (meth) acrylic acid ester structures more preferably a compound containing three or more, and most preferably a compound containing four or more.
- the selection and use method of the addition polymerization compound is an important factor for the compatibility and dispersibility with other components (for example, resin, photopolymerization initiator, pigment) in the curable composition,
- the compatibility may be improved by using a low-purity compound or using two or more kinds in combination.
- a specific structure may be selected for the purpose of improving the adhesion with a substrate or the like.
- bisphenol A diacrylate EO modified pentaerythritol triacrylate, pentaerythritol tetraacrylate, dipentaerythritol pentaacrylate, dipentaerythritol hexaacrylate, tri (acryloyloxyethyl) isocyanurate, pentaerythritol tetraacrylate EO modified, di
- modified products such as pentaerythritol hexaacrylate EO include DPHA-40H (manufactured by Nippon Kayaku Co., Ltd.), UA-306H, UA-306T, UA-306I, AH-600, T-600, AI-600 ( Kyoeisha) is more preferable.
- the content of the compound (E) containing an ethylenically unsaturated double bond in the present invention is preferably 1% by mass to 90% by mass in the solid content of the curable composition of the present invention. % To 80% by mass is more preferable, and 10% to 70% by mass is even more preferable.
- the content of the compound (E) containing an ethylenically unsaturated double bond is 5% by mass to 50% by mass within the above range. %, More preferably 7% by mass to 40% by mass, and still more preferably 10% by mass to 35% by mass.
- the colored curable composition of the present invention preferably further contains (F) an alkali-soluble resin.
- an alkali-soluble resin By containing an alkali-soluble resin, developability and pattern formation are improved.
- the alkali-soluble resin that can be used in the present invention is a linear organic polymer, and at least 1 in a molecule (preferably a molecule having an acrylic copolymer or a styrene copolymer as a main chain). It can be appropriately selected from alkali-soluble resins having two groups that promote alkali solubility (for example, carboxyl group, phosphoric acid group, sulfonic acid group, hydroxyl group, etc.).
- the alkali-soluble resin is a polymer having a carboxylic acid in the side chain, such as JP-A-59-44615, JP-B-54-34327, JP-B-58-12577, JP-B-54-25957, A methacrylic acid copolymer, an acrylic acid copolymer, an itaconic acid copolymer, a crotonic acid copolymer, a maleic acid, as described in Japanese Unexamined Patent Publication Nos. 59-53836 and 59-71048.
- a carboxylic acid in the side chain such as JP-A-59-44615, JP-B-54-34327, JP-B-58-12577, JP-B-54-25957, A methacrylic acid copolymer, an acrylic acid copolymer, an itaconic acid copolymer, a crotonic acid copolymer, a maleic acid, as described in Japanese Unexamined Patent Publication No
- Acrylic copolymers such as acid copolymers, partially esterified maleic acid copolymers, etc., acidic cellulose derivatives having a carboxylic acid in the side chain, and acid anhydrides added to polymers having a hydroxyl group Can be mentioned.
- the acid value is preferably in the range of 20 to 200 mgKOH / g, preferably 30 to 150 mgKOH / g, more preferably 35 to 120 mgKOH / g.
- a copolymer of (meth) acrylic acid and another monomer copolymerizable therewith is particularly suitable.
- examples of other monomers copolymerizable with the (meth) acrylic acid include alkyl (meth) acrylates, aryl (meth) acrylates, and vinyl compounds.
- the hydrogen atom of the alkyl group and the aryl group may be substituted with a substituent.
- alkyl (meth) acrylate and aryl (meth) acrylate examples include CH 2 ⁇ C (R 1 ) (COOR 3 ) [wherein R 1 represents a hydrogen atom or an alkyl group having 1 to 5 carbon atoms, and R 2 Represents an aromatic hydrocarbon ring having 6 to 10 carbon atoms, and R 3 represents an alkyl group having 1 to 8 carbon atoms or an aralkyl group having 6 to 12 carbon atoms.
- a resin having a polyalkylene oxide chain in the molecular side chain is also preferred.
- the polyalkylene oxide chain may be a polyethylene oxide chain, a polypropylene oxide chain, a polytetramethylene glycol chain, or a combination thereof, and the terminal is a hydrogen atom or a linear or branched alkyl group.
- the repeating unit of the polyethylene oxide chain and the polypropylene oxide chain is preferably 1 to 20, and more preferably 2 to 12.
- Acrylic copolymers having a polyalkylene oxide chain in these side chains are, for example, 2-hydroxyethyl (meth) acrylate, hydroxypropyl (meth) acrylate, polyethylene glycol mono (meth) acrylate, polypropylene glycol mono (meth) acrylate , Poly (ethylene glycol-propylene glycol) mono (meth) acrylate and the like and compounds in which these terminal OH groups are blocked with an alkyl group, such as methoxypolyethylene glycol mono (meth) acrylate, ethoxypolypropylene glycol mono (meth) acrylate, methoxypoly (ethylene glycol) -An acrylic copolymer having propylene glycol) mono (meth) acrylate or the like as a copolymerization component.
- Examples of the vinyl compound include CH 2 ⁇ CR 1 R 2 [wherein R 1 represents a hydrogen atom or an alkyl group having 1 to 5 carbon atoms, and R 2 represents an aromatic hydrocarbon ring having 6 to 10 carbon atoms.
- R 3 represents an alkyl group having 1 to 8 carbon atoms or an aralkyl group having 6 to 12 carbon atoms.
- Specific examples include styrene, ⁇ -methylstyrene, vinyl toluene, acrylonitrile, vinyl acetate, N-vinyl pyrrolidone, polystyrene macromonomer, polymethyl methacrylate macromonomer, and the like. These other copolymerizable monomers can be used singly or in combination of two or more.
- alkyl (meth) acrylate alkyl is an alkyl group having 2 to 4 carbon atoms
- phenyl (meth) acrylate benzyl (meth) acrylate
- styrene benzyl (meth) acrylate / (meth) acrylic acid copolymers
- multi-component copolymers composed of benzyl (meth) acrylate / (meth) acrylic acid / other monomers are particularly suitable.
- the acrylic resin has an acid value in the range of 20 to 200 mgKOH / g.
- the acid value exceeds 200, the acrylic resin becomes too soluble in alkali and the appropriate development range (development latitude) becomes narrow.
- the solubility in alkali is so small that it takes too much time for development, which is not preferable.
- the mass average molecular weight Mw of the acrylic resin (polystyrene conversion value measured by the GPC method) is used to realize a viscosity range that is easy to use in the process of applying a color resist, etc., and to secure film strength. , Preferably from 2,000 to 100,000, more preferably from 3,000 to 50,000.
- the acid value of acrylic resin In order to make the acid value of acrylic resin into the range specified above, it can be easily performed by appropriately adjusting the copolymerization ratio of each monomer. Further, the range of the mass average molecular weight can be easily set by using an appropriate amount of a chain transfer agent according to the polymerization method when the monomers are copolymerized.
- the acrylic resin can be produced, for example, by a known radical polymerization method. Polymerization conditions such as temperature, pressure, type and amount of radical initiator, type of solvent, etc. when producing an acrylic resin by radical polymerization can be easily set by those skilled in the art. Is possible.
- the amount of the alkali-soluble resin added to the curable composition of the present invention is preferably 5 to 90% by mass, more preferably 10 to 60% by mass, based on the total solid content of the composition.
- the amount of the alkali-soluble resin is less than 5% by mass, the film strength is lowered.
- the amount is more than 90% by mass, the acid content increases, so that it becomes difficult to control the solubility and the pigment is relatively reduced. Therefore, sufficient image density cannot be obtained.
- a good coating can be obtained with a high yield for slit coating suitable for coating on a wide substrate having a large area.
- a resin having a polymerizable group in an alkali-soluble resin may be used alone or in combination with an alkali-soluble resin having no polymerizable group, Polymers containing an aryl group, a (meth) acryl group, an aryloxyalkyl group or the like in the side chain are useful.
- the alkali-soluble resin having a polymerizable double bond can be developed with an alkali developer, and is further provided with photocurability and thermosetting.
- Examples of the polymer containing these polymerizable groups are shown below, but are not limited to the following as long as alkali-soluble groups such as COOH groups and OH groups and carbon-carbon unsaturated bonds are included.
- Urethane modification obtained by reacting an isocyanate group and an OH group in advance, leaving one unreacted isocyanate group and reacting at least one (meth) acryloyl group with an acrylic resin containing a carboxyl group
- a polymerizable double bond-containing acrylic resin (2) an unsaturated group-containing acrylic resin obtained by a reaction between an acrylic resin containing a carboxyl group and a compound having both an epoxy group and a polymerizable double bond in the molecule; (3) Acid pendant type epoxy acrylate resin, (4) A polymerizable double bond-containing acrylic resin obtained by reacting an acrylic resin containing an OH group with a dibasic acid anhydride having a polymerizable double bond.
- the resins (1) and (2) are particularly preferable.
- the acid value of the alkali-soluble resin having a polymerizable double bond in the present invention is preferably 30 to 150 mgKOH / g, more preferably 35 to 120 mgKOH / g, and the mass average molecular weight Mw is preferably 2,000 to It is 50,000, more preferably 3,000 to 30,000.
- a copolymer of an OH group such as 2-hydroxyethyl acrylate, a COOH group such as methacrylic acid, and a monomer such as an acrylic or vinyl compound copolymerizable with these, an OH group A compound obtained by reacting an epoxy ring having reactivity with a compound having a carbon-carbon unsaturated bond group (for example, a compound such as glycidyl acrylate) can be used.
- a compound having an acid anhydride, an isocyanate group, or an acryloyl group in addition to the epoxy ring can be used.
- a compound obtained by reacting an unsaturated carboxylic acid such as acrylic acid with a compound having an epoxy ring described in JP-A-6-102669 and JP-A-6-1938 is saturated or unsaturated polybasic.
- a reaction product obtained by reacting an acid anhydride can also be used.
- Examples of compounds having both an alkali solubilizing group such as a COOH group and an intercarbon unsaturated group include, for example, Dynar NR series (manufactured by Mitsubishi Rayon Co., Ltd.); Ltd.); Biscote R-264, KS resist 106 (both manufactured by Osaka Organic Chemical Industry Co., Ltd.); Cyclomer P series, Plaxel CF200 series (both manufactured by Daicel Chemical Industries, Ltd.); Ebecryl 3800 (Daicel) And UCB Co., Ltd.).
- the curable composition of this invention may further contain the component explained in full detail below as needed.
- ⁇ Sensitizer> The curable composition of the present invention may contain a sensitizer for the purpose of improving the radical generation efficiency of the polymerization initiator and increasing the photosensitive wavelength.
- the sensitizer that can be used in the present invention those that sensitize the above-mentioned photopolymerization initiator by an electron transfer mechanism or an energy transfer mechanism are preferable.
- Examples of the sensitizer that can be used in the present invention include those belonging to the compounds listed below and having an absorption wavelength in a wavelength region of 300 nm to 450 nm.
- Examples of preferred sensitizers include those belonging to the following compounds and having an absorption wavelength in the range of 330 nm to 450 nm.
- polynuclear aromatics for example, phenanthrene, anthracene, pyrene, perylene, triphenylene, 9,10-dialkoxyanthracene
- xanthenes for example, fluorescein, eosin, erythrosine, rhodamine B, rose bengal
- thioxanthones Isopropylthioxanthone, diethylthioxanthone, chlorothioxanthone
- cyanines eg thiacarbocyanine, oxacarbocyanine
- merocyanines eg merocyanine, carbomerocyanine
- phthalocyanines thiazines
- thionine methylene blue, toluidine blue
- Acridines eg,
- a small amount of a thermal polymerization inhibitor may be added to prevent unnecessary thermal polymerization of a compound having an ethylenically unsaturated double bond that can be polymerized during the production or storage of the curable composition.
- the thermal polymerization inhibitor that can be used in the present invention include hydroquinone, p-methoxyphenol, di-t-butyl-p-cresol, pyrogallol, t-butylcatechol, benzoquinone, 4,4′-thiobis (3-methyl-6). -T-butylphenol), 2,2'-methylenebis (4-methyl-6-t-butylphenol), N-nitrosophenylhydroxyamine primary cerium salt and the like.
- the addition amount of the polymerization inhibitor is preferably about 0.01% by mass to about 5% by mass with respect to the mass of the entire composition. If necessary, a higher fatty acid derivative such as behenic acid or behenic acid amide may be added to prevent polymerization inhibition due to oxygen, and it may be unevenly distributed on the surface of the photosensitive layer in the course of drying after coating. .
- the amount of the higher fatty acid derivative added is preferably from about 0.5% to about 10% by weight of the total composition.
- plasticizers include dioctyl phthalate, didodecyl phthalate, triethylene glycol dicaprylate, dimethyl glycol phthalate, tricresyl phosphate, dioctyl adipate, dibutyl sebacate, and triacetyl glycerin. 10 mass% or less can be added with respect to the total mass of the compound which has an ionic unsaturated double bond, and binder.
- substrate adhesion agent an additive for improving the adhesion to the surface of the hard material.
- substrate adhesion agent known materials can be used, but it is particularly preferable to use a silane coupling agent, a titanate coupling agent, or an aluminum coupling agent.
- silane coupling agents include ⁇ - (2-aminoethyl) aminopropyltrimethoxysilane, ⁇ - (2-aminoethyl) aminopropyldimethoxysilane, and ⁇ - (3,4-epoxycyclohexyl) ethyltrimethoxy.
- Silane ⁇ -aminopropyltrimethoxysilane, ⁇ -aminopropyltriethoxysilane, ⁇ -methacryloxypropyltrimethoxysilane, ⁇ -methacryloxypropyltriethoxysilane, ⁇ -acryloxypropyltrimethoxysilane, ⁇ -acryloxypropyl Triethoxysilane, ⁇ -isocyanatopropyltrimethoxysilane, ⁇ -isocyanatopropyltriethoxysilane, N- ⁇ - (N-vinylbenzylaminoethyl) - ⁇ -aminopropyltrimethoxysilane hydrochloride, ⁇ -glycidoxypro Pyrtrimethoxysilane, ⁇ -glycidoxypropyltriethoxysilane, aminosilane, ⁇ -mercaptopropyltrimethoxysilane, ⁇ -mercaptopropyltrieth
- ⁇ -methacryloxypropyltrimethoxysilane, ⁇ -methacryloxypropyltriethoxysilane, ⁇ -acryloxypropyltrimethoxysilane, ⁇ -acryloxypropyltriethoxysilane, ⁇ -mercaptopropyltrimethoxysilane, ⁇ -aminopropyltri Ethoxysilane and phenyltrimethoxysilane are preferred, and ⁇ -methacryloxypropyltrimethoxysilane is most preferred.
- titanate coupling agents include isopropyl triisostearoyl titanate, isopropyl tridecylbenzenesulfonyl titanate, isopropyl tris (dioctyl pyrophosphate) titanate, tetraisopropyl bis (dioctyl phosphite) titanate, tetraoctyl bis (ditridecyl phosphite).
- Examples of the aluminum coupling agent include acetoalkoxyaluminum diisopropylate.
- the content of the substrate adhesion agent is 0.1% by mass or more and 30% by mass with respect to the total solid content of the curable composition of the present invention from the viewpoint of leaving no residue in the unexposed part of the curable composition. % Or less, more preferably 0.5% by mass or more and 20% by mass or less, and particularly preferably 1% by mass or more and 10% by mass or less.
- the colored curable composition of the present invention is cured with high sensitivity and has good storage stability. Moreover, the high adhesiveness to hard material surfaces, such as a board
- the pigment-containing colored curing of the present invention is particularly preferred. It can be said that the effect is remarkable by using a sex composition.
- the color filter of the present invention is characterized by having a colored pattern formed using the curable composition of the present invention on a support.
- the color filter of the present invention will be described in detail through its manufacturing method (color filter manufacturing method of the present invention).
- the method for producing a color filter of the present invention includes a colored layer forming step of forming a colored layer comprising the curable composition by applying the curable composition of the present invention on a support, and the colored layer as a mask. And a developing step of developing a colored layer after exposure to form a colored pattern.
- the curable composition of the present invention is applied on the support to form a colored layer comprising the curable composition.
- the support for example, soda glass, Pyrex (registered trademark) glass, quartz glass, and the like obtained by attaching a transparent conductive film to these, an image sensor, etc.
- the photoelectric conversion element substrate include a silicon substrate and a complementary metal oxide semiconductor (CMOS). These substrates may have black stripes that separate pixels.
- CMOS complementary metal oxide semiconductor
- an undercoat layer may be provided on these supports, if necessary, in order to improve adhesion to the upper layer, prevent diffusion of substances, or flatten the substrate surface.
- the film thickness immediately after application of the curable composition is preferably 0.1 to 10 ⁇ m, more preferably 0.2 to 5 ⁇ m, from the viewpoint of film thickness uniformity of the coating film and ease of drying of the coating solvent. 0.2 to 3 ⁇ m is more preferable.
- the drying (pre-baking) of the colored layer (curable composition layer) applied on the substrate can be performed at a temperature of 50 ° C. to 140 ° C. for 10 to 300 seconds using a hot plate, oven, or the like.
- the coating film thickness after drying of the curable composition (hereinafter referred to as “dry film thickness” as appropriate) can be used for LCD color filters and can be used for LCD thinning, from the viewpoint of securing color density.
- 0.1 ⁇ m or more and less than 2.0 ⁇ m is preferable, 0.2 ⁇ m or more and 1.8 ⁇ m or less is more preferable, and 0.3 ⁇ m or more and 1.75 ⁇ m or less is particularly preferable.
- the light in the oblique direction does not reach the light receiving unit from the viewpoint of securing the color density, and the difference in the light collection rate between the end and the center of the device becomes remarkable.
- it is preferably 0.05 ⁇ m or more and less than 1.0 ⁇ m, more preferably 0.1 ⁇ m or more and 0.8 ⁇ m or less, and particularly preferably 0.2 ⁇ m or more and 0.7 ⁇ m or less.
- the colored layer (curable composition layer) formed in the colored layer forming step is exposed through a mask having a predetermined mask pattern.
- the pattern exposure of the coating film can be performed by exposing through a predetermined mask pattern and curing only the part of the coating film irradiated with light.
- radiation that can be used for exposure ultraviolet rays such as g-line and i-line are particularly preferably used. Irradiation amount is more preferably 5 ⁇ 1500mJ / cm 2 is preferably 10 ⁇ 1000mJ / cm 2, and most preferably 10 ⁇ 500mJ / cm 2.
- the color filter of the present invention is a liquid crystal display element is more preferably 5 ⁇ 200mJ / cm 2 is preferably 10 ⁇ 150mJ / cm 2 within the above range, and most preferably 10 ⁇ 100mJ / cm 2. Further, when the color filter of the present invention is for a solid-state imaging device, more preferably 30 ⁇ 1500mJ / cm 2 is preferably 50 ⁇ 1000mJ / cm 2 within the above range, and most preferably 80 ⁇ 500mJ / cm 2.
- ⁇ Development process> by carrying out an alkali development treatment (development process), the light non-irradiated part in the exposure is eluted in an alkaline aqueous solution, and only the photocured part remains.
- Development with a developing solution can form a patterned film composed of pixels of each color (3 colors or 4 colors).
- the developer an organic alkali developer that does not damage the underlying circuit or the like is desirable.
- the development temperature is usually 20 ° C. to 30 ° C., and the development time is 20 to 90 seconds.
- alkaline agent used in the developer examples include ammonia water, ethylamine, diethylamine, dimethylethanolamine, tetramethylammonium hydroxide, tetraethylammonium hydroxide, choline, pyrrole, piperidine, 1,8-diazabicyclo- [5, 4, Organic alkaline compounds such as 0] -7-undecene, inorganic compounds such as sodium hydroxide, potassium hydroxide, sodium hydrogen carbonate, potassium hydrogen carbonate and the like, and concentrations of these alkaline agents in the range of 0.001% by mass to 10%.
- a developer composed of such an alkaline aqueous solution it is generally washed (rinsed) with pure water after development. Next, excess developer is washed away and dried.
- the specific resin of the present invention used as a pigment dispersant is excellent in pigment dispersibility and dispersion stability, and has a functional group having a pKa of 14 or less in the molecule. Since it has excellent developability, even when a fine pattern is formed, a residual film of an uncured portion is hardly generated. Therefore, a color pattern formation of a color filter for a CCD that requires fine pattern formation is required. It is suitable for.
- the colored pattern formed is cured by heating (post-baking) and / or exposure as necessary after performing the above-described colored layer forming step, exposure step, and development step.
- a curing step may be included.
- Post-baking is a heat treatment after development to complete the curing, and usually a heat curing treatment at 100 ° C. to 240 ° C. is performed.
- the substrate is a glass substrate or a silicon substrate, 200 ° C. to 240 ° C. is preferable in the above temperature range.
- This post-bake treatment is performed continuously or batchwise using a heating means such as a hot plate, a convection oven (hot air circulation dryer), a high-frequency heater, or the like so that the coating film after development is in the above-described condition. be able to.
- the use of the curable composition of the present invention has been mainly described for use in color filter pixels, but it goes without saying that it can also be applied to a black matrix provided between color filter pixels.
- the black matrix is subjected to pattern exposure and alkali development in the same manner as in the above pixel production method except that a black pigment such as carbon black or titanium black is added to the curable composition of the present invention as a colorant. Further, after that, post-baking can be performed to promote the curing of the film.
- the color filter of the present invention is produced using the curable composition of the present invention having excellent exposure sensitivity, the cured composition in the exposed area is excellent in adhesion to the substrate and development resistance, and formed coloration The adhesion between the pattern and the support substrate is high, and the pattern giving a desired cross-sectional shape has high resolution.
- the solid-state image sensor of this invention is equipped with the color filter of this invention manufactured by the manufacturing method of the color filter of the said invention. Therefore, specifically, the color filter of the present invention can be suitably used for a solid-state imaging device such as a liquid crystal display device or a CCD, and is particularly suitable for a high-resolution CCD device or CMOS that exceeds 1 million pixels. is there.
- the color filter of the present invention can be used as, for example, a color filter disposed between a light receiving portion of each pixel constituting a CCD element and a microlens for condensing light.
- Polyester (i-1) 6.4 g of n-octanoic acid, 200 g of ⁇ -caprolactone and 5 g of titanium (IV) tetrabutoxide were mixed, heated at 160 ° C. for 8 hours, and then cooled to room temperature. Polyester (i-1) was obtained. The scheme is shown below.
- Polyesters (i-2) to (i-10) were obtained in the same manner as in Synthesis Example 1 except that the charging amounts shown in Table 1 were used.
- the number average molecular weight and weight average molecular weight of the resins obtained in these synthesis examples were measured by the GPC method described above. The results are shown in Table 1 below.
- the number of lactone repeating units calculated from the raw material charging ratio is shown in Table 1 below.
- Resin (J-1) has a side chain derived from polyester (i-1) and a group having a functional group (carboxy group) having a pKa derived from succinic anhydride of 14 or less.
- a synthesis scheme is shown below.
- Y is a resin containing 50 mol% of poly ( ⁇ -caprolactone). Moreover, the weight average molecular weight by GPC method was 24,000.
- SP-003 polyethyleneimine (made by Nippon Shokubai) number average molecular weight 300
- SP-006 polyethyleneimine (made by Nippon Shokubai) number average molecular weight 600)
- SP-012 polyethyleneimine (made by Nippon Shokubai) number average molecular weight 1,200)
- SP-018 polyethyleneimine (manufactured by Nippon Shokubai) number average molecular weight 1,800)
- SP-020 polyethyleneimine (made by Nippon Shokubai) number average molecular weight 10,000)
- PAA-01 polyallylamine (manufactured by Nittobo) weight average molecular weight 1,000
- PAA-03 polyallylamine (Nittobo) weight average molecular weight 3,000)
- PAA-05 polyallylamine (Nittobo) weight average molecular weight 5,000)
- PAA-08 polyallylamine (manufactured by Nittobo) weight average molecular weight 8,000)
- PAA-15 (polyallylamine (manufactured by Nittobo) weight average molecular weight 15,000)
- A1-1 Preparation of pigment dispersion
- pigment dispersion C.I. I. Pigment Green 36 (PG36) 40 parts by mass (average particle size 60 nm) and a resin (J-1) solution 200 parts by mass (solid content 20 parts by mass) were mixed with a bead mill (zirconia beads 0.3 mm).
- a pigment dispersion was prepared by mixing and dispersing for 3 hours. With respect to the pigment dispersion, the average particle diameter of the pigment was measured by a dynamic light scattering method (measured without further dilution of P1 using Microtrac Nanotrac UPA-EX150 (manufactured by Nikkiso Co., Ltd.)), and was 25 nm. .
- Pigment Dispersibility and Dispersion Stability of Pigment Dispersion Preparation of Pigment Dispersion PGMEA 10 containing 40 parts by mass (average particle diameter 60 nm) of the pigments listed in Table 5 and the resins (J-1) to (J-31).
- a mixed liquid in which PGMEA was added to 180 parts by weight of a weight percent solution (18 parts by weight in terms of solid content) to 230 parts by weight was mixed and dispersed by a bead mill (zirconia beads 0.3 mm) for 3 hours to obtain a pigment dispersion.
- a bead mill zirconia beads 0.3 mm
- the average particle diameter of the pigment was measured by a dynamic light scattering method (measured using Microtrac Nanotrac UPA-EX150 (manufactured by Nikkiso Co., Ltd. without further dilution) P1). Indicated.
- the resin of the present invention is excellent in dispersibility and dispersion stability when used as a dispersant for very fine pigments.
- curable composition (coating liquid)
- a curable composition solution was prepared by stirring and mixing the pigment dispersion liquid that had been subjected to the dispersion treatment so that the composition ratio was as follows. -600 parts by mass of the pigment dispersion-Photopolymerization initiator (2,2'-bis (2-chlorophenyl) -4,4 ', 5,5' -Tetraphenyl-1,2'-biimidazole) 30 parts by mass, pentaerythritol tetraacrylate 50 parts by mass, alkali-soluble resin (benzyl methacrylate / methacrylic acid / hydroxyethyl methacrylate copolymer, molar ratio: 80/10/10, Mw: 10,000) 5 parts by mass / solvent: propylene glycol 1-monomethyl ether-2-acetate 900 parts by mass / substrate adhesion agent (3-methacryloxypropyltrimethoxysilane) 1 part by mass / (F
- A2-1 Formation of the curable composition layer
- the curable composition containing the pigment as a resist solution was slit-coated on a 550 mm ⁇ 650 mm glass substrate under the following conditions, and then allowed to stand for 10 minutes, followed by vacuum drying and pre-baking ( prebake) (100 ° C., 80 seconds) to form a curable composition coating film (curable composition layer).
- the coating film of the curable composition is exposed in a pattern using a test photomask having a line width of 20 ⁇ m using a 2.5 kW ultra-high pressure mercury lamp. After the exposure, the entire surface of the coating film is organic-based.
- the sample was covered with a 10% aqueous solution of a developer (trade name: CD, manufactured by FUJIFILM Electronics Materials Co., Ltd.) and allowed to stand for 60 seconds.
- A3-1 Storage Stability of Curable Composition After the curable composition (coating liquid) prepared above was stored at room temperature for 1 month, the viscosity of the liquid was measured and evaluated according to the following criteria. -Evaluation criteria- ⁇ : No increase in viscosity was observed. ⁇ : An increase in viscosity of 5% or more and less than 10% was observed. X: An increase in viscosity of 10% or more was observed.
- A3-2 Contrast of curable composition coating film (colored layer) Color filter is sandwiched between two polarizing films, and the luminance of transmitted light when the polarizing axis of the polarizing film is parallel and perpendicular is measured using a color luminance meter. And the contrast ratio was determined. The higher the contrast ratio, the better the performance as a color filter for a liquid crystal display.
- the cross-sectional shape of the formed pattern was observed.
- the pattern cross-sectional shape is most preferably a forward taper, and a rectangular shape is next preferred. Reverse taper is not preferred.
- the evaluation results are shown in Table 6 below.
- the colored curable compositions of Examples 28 to 54 containing the specific resin of the present invention are excellent in storage stability in the solution state.
- the contrast is high and developability is excellent for each comparative example not using the resin in the present invention. It can be seen that a color filter having an excellent cross-sectional shape is obtained.
- pigment dispersion As a pigment, C.I. I. Pigment green 36 (PG36) and C.I. I. Pigment Yellow 139 (PY139) mixture (mass ratio 70:30) 40 parts by mass (average particle size 65 nm) and resin (J-1) solution 160 parts by mass (solid content conversion 16 parts by mass) (Zirconia beads, diameter 0.3 mm) was mixed and dispersed for 3 hours to prepare a pigment dispersion. With respect to the pigment dispersion, the average particle diameter of the pigment was measured by the dynamic light scattering method in the same manner as in Example 1, and was 30 nm.
- curable composition solution was prepared by stirring and mixing the resulting pigment dispersion so as to have the following composition ratio.
- -Colorant 600 parts by mass-Photopolymerization initiator (oxime photopolymerization initiator) (CGI-124, manufactured by Ciba Specialty Chemicals Co., Ltd.) 30 parts by mass, TO-1382 (manufactured by Toagosei Co., Ltd.) 25 parts by mass, 30 parts by mass of dipentaerythritol hexaacrylate, 900 parts by mass of solvent (PGMEA), substrate Adhesive (3-methacryloxypropyltrimethoxysilane) 1 part by mass
- the silicon wafer substrate on which the irradiated coating film is formed is placed on a horizontal rotary table of a spin shower developing machine (DW-30 type, manufactured by Chemitronics), and CD-2000 (Fuji Film). Paddle development was performed at 23 ° C. for 60 seconds using Electronics Materials Co., Ltd. to form a colored pattern on the silicon wafer substrate.
- DW-30 type manufactured by Chemitronics
- CD-2000 Fluji Film
- the silicon wafer on which the colored pattern is formed is fixed to the horizontal rotary table by a vacuum chuck method, and the silicon wafer substrate is rotated at a rotational speed of 50 r. p. m. While being rotated, pure water was supplied from the upper part of the rotation center in the form of a shower through a spray nozzle, followed by rinsing treatment, and then spray drying. Thereafter, the size of the colored pattern was measured using a length measuring SEM “S-9260A” (manufactured by Hitachi High-Technologies Corporation). The exposure dose at which the pattern line width was 2 ⁇ m was evaluated as the exposure sensitivity.
- the cross-sectional shape of the formed pattern was observed.
- the pattern cross-sectional shape is preferably rectangular, and reverse taper is not preferable.
- ⁇ Storage stability of curable composition B4. After the curable composition (coating solution) prepared in 1 was stored at room temperature for 1 month, the viscosity of the solution was measured and evaluated according to the following criteria. -Evaluation criteria- ⁇ : No increase in viscosity was observed. ⁇ : An increase in viscosity of 5% or more and less than 10% was observed. X: An increase in viscosity of 10% or more was observed. ⁇ Color unevenness> The color unevenness was evaluated by analyzing the luminance distribution by the following method and based on the ratio of the pixels whose deviation from the average is within ⁇ 5% to the total number of pixels. The evaluation criteria are as follows. A method for measuring the luminance distribution will be described.
- the curable composition is mixed with the B2. It applied on the undercoat layer of the glass plate with an undercoat layer obtained by the same method, and the colored layer (coating film) was formed. Heat treatment (pre-baking) was performed for 120 seconds using a hot plate at 100 ° C. so that the dry film thickness of the coating film became 0.7 ⁇ m. The luminance distribution of the coated glass plate was analyzed for images taken with a microscope MX-50 (Olympus).
- the curable compositions (pigment systems) of Examples 55 to 81 containing the specific resin of the present invention are in the solution state even when used for forming a color filter for solid-state imaging devices. It can be seen that it has excellent storage stability. In addition, when a colored pattern is formed on a support using this curable composition, it has excellent developability as compared to the comparative example not using the resin in the present invention, and the pattern cross-sectional shape and color unevenness. It can be seen that an excellent color filter is obtained in any of the above. From these results, the curable compositions of the examples achieved excellent pattern formability even when producing color filters for solid-state imaging devices, as in the case of producing color filters for liquid crystal display devices. I found out that
- the resin of the present invention was excellent in dispersion stability even when the pigment concentration was high.
- (J-1), (J-2), (J-3), (J-4), (J-5), (J-10), ( J-11) and (J-12) are preferred, and (J-1), (J-2), (J-3), (J-4), (J-10), (J-11) and (J J-12) is more preferred, and (J-2), (J-3), (J-4), (J-11) and (J-12) are most preferred.
- the main chain portion having a nitrogen atom is preferably polyethyleneimine
- the main chain portion having a nitrogen atom is more preferably a polyethyleneimine having a number average molecular weight of 300 to 1,800, and the main chain having a nitrogen atom.
- the part is a polyethyleneimine having a number average molecular weight of 600 to 1,200.
- the structures of the photopolymerization initiators (Z-1) to (Z-7) shown in Table 9 used here are as follows.
- the colored curable composition coating film was exposed to 100 mJ / cm 2 in a pattern with LE4000A manufactured by Hitachi High-Technology Corporation using a photomask having a line width of 20 ⁇ m. . After the exposure, the entire surface of the coating film was covered with a 1% aqueous solution of an inorganic developer (trade name: CDK-1, manufactured by FUJIFILM Electronics Materials Co., Ltd.) and allowed to stand for 60 seconds.
- an inorganic developer trade name: CDK-1, manufactured by FUJIFILM Electronics Materials Co., Ltd.
- Contrast of color filter The color filter obtained as described above is sandwiched between two polarizing plates, and the luminance of transmitted light when the polarizing axis of the polarizing plate is parallel and perpendicular is measured by a color luminance meter (manufactured by Topcon Corporation). Using a color luminance meter BM-7), the contrast was obtained by dividing the luminance in the parallel case by the luminance in the vertical case. The higher the contrast, the better the performance as a color filter for a liquid crystal display device.
- Pattern formability The cross-sectional shape of the formed pattern was observed.
- the pattern cross-sectional shape is preferably rectangular, and reverse taper is not preferable. 6).
- Exposure Sensitivity In the exposure step, exposure was performed by changing to various exposure doses in the range of 10 mJ / cm 2 to 500 mJ / cm 2 , and the exposure dose at which the pattern line width after post-baking was 20 ⁇ m was evaluated as exposure sensitivity. . A smaller exposure sensitivity value indicates higher sensitivity.
- the colored curable compositions of Examples 98 to 120 containing the specific resin of the present invention are excellent in storage stability and developability. Moreover, when a colored pattern is formed on a support using a colored curable composition, it can be seen that the contrast is high, and the substrate adhesion and pattern forming properties are also good. On the other hand, in Comparative Examples 12 to 13 which did not use the colored curable composition of the present invention, the viscosity increased upon storage, the temporal stability was poor, a residue was generated during development, and the contrast was low. Moreover, it turns out that the color filter which was excellent also in the Example also in the pattern cross-sectional shape was obtained.
- i-line stepper exposure apparatus FPA-3000i5 + manufactured by Canon Inc.
- exposure was performed at various exposure doses of 50 to 1200 mJ / cm 2 through an Island pattern mask having a pattern of 1.2 ⁇ m square at a wavelength of 365 nm.
- the silicon wafer substrate on which the irradiated coating film is formed is placed on a horizontal rotary table of a spin shower developing machine (DW-30 type, manufactured by Chemitronics Co., Ltd.), and CD-2000 (Fuji Film).
- Paddle development was performed at 23 ° C. for 60 seconds using Electronics Materials Co., Ltd. to form a colored pattern on the silicon wafer substrate.
- the silicon wafer on which the colored pattern is formed is fixed to the horizontal rotary table by a vacuum chuck method, and the silicon wafer substrate is rotated at a rotational speed of 50 r. p. m. While being rotated, pure water was supplied from the upper part of the rotation center in the form of a shower through a spray nozzle, followed by rinsing treatment, and then spray drying. Thereafter, the size of the colored pattern was measured using a length measuring SEM “S-9260A” (manufactured by Hitachi High-Technologies Corporation). The exposure amount at which the pattern size was 1.2 ⁇ m was evaluated as the exposure sensitivity.
- Color filter color unevenness The color filter color unevenness obtained above is evaluated by analyzing the luminance distribution by the following method, and based on the ratio of pixels whose deviation from the average is within ⁇ 5% to the total number of pixels. Went to.
- the evaluation criteria are as follows. A method for measuring the luminance distribution will be described. First, the obtained colored curable composition was apply
- the luminance distribution of the coated glass plate was analyzed for an image taken with a microscope MX-50 (manufactured by Olympus), and the ratio (percentage) of pixels within ⁇ 5% from the average was calculated. The higher this value, the smaller the color unevenness and the better.
- Substrate adhesion As an evaluation of substrate adhesion, it was observed whether pattern defects occurred. These evaluation items were evaluated based on the following criteria: -Evaluation criteria- ⁇ : No pattern defect was observed. (Triangle
- Pattern formability The cross-sectional shape of the formed pattern was observed.
- the pattern cross-sectional shape is preferably rectangular, and reverse taper is not preferable. 6).
- Exposure Sensitivity Exposure was performed by changing the exposure dose to various exposure doses of 10 to 500 mJ / cm 2 , and the exposure dose at which the pattern line width after post-baking was 1.2 ⁇ m was evaluated as exposure sensitivity. A smaller exposure sensitivity value indicates higher sensitivity.
Abstract
Description
カラーフィルタ製造用途の硬化性組成物に関しては、使用する顔料の粒子サイズがより微小なものを用いることで、コントラストを向上させる試みがなされている(例えば、特開2006-30541号公報参照)。
しかしながら、顔料の粒子サイズを微小化すると、顔料の表面積が大きくなるため、分散性・保存安定性が悪化する問題があった。分散性・保存安定性を確保するために、分散剤の添加量を多くすると、現像性が低下し、良好なパターンが形成され難いという問題が生じた。一方、現像性を向上させるために、アルカリ可溶性樹脂の添加量を増やすと、分散性・保存安定性が悪化するという問題が発生した。つまり、現行の分散剤では分散性・保存安定性・現像性を同時に満たすことが非常に困難であった。
本発明の他の目的は、微細な顔料を多量含有する場合であっても、硬化膜中の顔料分散均一性、及び未硬化領域の除去性に優れた着色硬化性組成物を提供することにある。
本発明のさらなる目的は、顔料の分散安定性と現像性が良好な着色硬化性組成物により形成された高解像度で色特性の良好な着色パターンを有するカラーフィルタ及びその生産性に優れた製造方法を提供することにある。
即ち、本発明の目的は下記の手段により達成されるものである。
<2> 前記樹脂の(i)窒素原子を有する主鎖部が、アミノ基を有するオリゴマー又はポリマーを含むことを特徴とする<1>に記載の樹脂。
<3> 前記樹脂の(i)窒素原子を有する主鎖部が、ポリ(低級アルキレンイミン)、ポリアリルアミン、ポリジアリルアミン、メタキシレンジアミン-エピクロルヒドリン重縮合物、ポリビニルアミン、3-ジアルキルアミノプロピル(メタ)アクリル酸アミド共重合体、及び、(メタ)アクリル酸2-ジアルキルアミノエチル共重合体から選択される1種以上を含むことを特徴とする<1>又は<2>に記載の樹脂。
<4> 前記樹脂の(ii)pKaが14以下である官能基が、カルボン酸、スルホン酸及び-COCH2CO-から選択される官能基であることを特徴とする<1>~<3>のいずれか1項に記載の樹脂。
<5> 一般式(I-1)で表される繰り返し単位及び一般式(I-2)で表される繰り返し単位を含むことを特徴とする<1>~<4>のいずれか1項に記載の樹脂。
<6> 一般式(II-1)で表される繰り返し単位及び(II-2)で表される繰り返し単位を含有することを特徴とする<1>~<4>のいずれか1項に記載の樹脂。
<7> 前記樹脂の(iii)数平均分子量が500~1,000,000であるオリゴマー鎖又はポリマー鎖「Y」が下記一般式(III-1)で表されることを特徴とする<1>~<6>のいずれか1項に記載の樹脂。
<8> 前記樹脂が、主鎖部に一級又は二級アミノ基を有する樹脂に、前記pKaが14以下である官能基を有する基「X」の前駆体xと、前記数平均分子量が500~1,000,000であるオリゴマー鎖又はポリマー鎖「Y」の前駆体yとを反応させてなる樹脂であることを特徴とする<1>~<7>のいずれか1項に記載の樹脂。
<9> 主鎖部に一級又は二級アミノ基を有する樹脂を合成し、その後、該樹脂にpKaが14以下である官能基を有する基「X」の前駆体xと、前記数平均分子量が500~1,000,000であるオリゴマー鎖又はポリマー鎖「Y」の前駆体yとを反応させることを含む<1>~<8>のいずれか1項に記載の樹脂の製造方法。
<11> (A)<1>~<8>のいずれか1項に記載の樹脂、(B)顔料、(C)溶剤、(D)光重合開始剤、及び、(E)エチレン性不飽和二重結合を含有する化合物、を含有することを特徴とする着色硬化性組成物。
<12> さらに(F)アルカリ可溶性樹脂を含有することを特徴とする<11>に記載の着色硬化性組成物。
<13> 支持体上に、<11>又は<12>に記載の着色硬化性組成物により形成された着色パターンを有するカラーフィルタ。
<14> 支持体上に、<11>又は<12>に記載の着色硬化性組成物を塗布して該硬化性組成物からなる着色層を形成することと、該着色層を、マスクを介してパターン露光することと、露光後の着色層を現像して着色パターンを形成することと、を含むことを特徴とするカラーフィルタの製造方法。
なお、本発明における着色領域とは、カラーフィルタにおける着色画素(着色パターン)領域、及び、遮光膜形成領域を包含するものである。
また、本発明によれば、微細な顔料を多量含有する場合であっても、硬化膜中の顔料分散均一性、及び未硬化領域の除去性に優れた着色硬化性組成物、顔料の分散安定性と現像性が良好な着色硬化性組成物により形成された高解像度で色特性の良好な着色パターンを有するカラーフィルタ及びその生産性に優れた製造方法を提供する新規樹脂を提供することができる。
特に、本発明の樹脂を顔料分散・フォトレジストに用いることにより、分散性・分散安定性が非常に優れている顔料分散液、及び、高い現像性を発揮する着色硬化性組成物を提供することが出来る。
また、本発明によれば、高解像度で色特性の良好な着色パターンを有するカラーフィルタ及びその生産性に優れた製造方法、さらには、該カラーフィルタを備えた液晶ディスプレイや固体撮像素子を提供することができる。
本発明の特定樹脂は、(i)窒素原子を有する主鎖部を有する。これにより、顔料表面への吸着力が向上し、且つ顔料間の相互作用が低減できる。
特定樹脂は、公知のアミノ基、より好ましくは、1級又は2級アミノ基を含有するオリゴマー又はポリマーから構成される主鎖部を有することが好ましい。アミノ基を含有するオリゴマー又はポリマーとしては、より具体的には、ポリ(低級アルキレンイミン)、ポリアリルアミン、ポリジアリルアミン、メタキシレンジアミン-エピクロルヒドリン重縮合物、ポリビニルアミン、3-ジアルキルアミノプロピル(メタ)アクリル酸アミド共重合体、(メタ)アクリル酸2-ジアルキルアミノエチル共重合体等から選択される主鎖構造であることが好ましく、ポリ(低級アルキレンイミン)、ポリアリルアミン及び(メタ)アクリル酸2-ジアルキルアミノエチル共重合体から選択される主鎖構造であることが最も好ましい。
ポリ(低級アルキレンイミン)は鎖状であっても網目状であってもよいが、特に網目状であることにより、分散安定性及び素材供給性が高くなる。
本発明の特定樹脂における主鎖部の数平均分子量は、100~10,000が好ましく、200~5,000がさらに好ましく、300~2,000がより好ましく、特に、数平均分子量が500~1500の範囲であることが、分散安定性、現像性両立の観点から最も好ましい。主鎖部の分子量は、核磁気共鳴分光法で測定した末端基と主鎖部の水素原子積分値の比率から求めるか、原料であるアミノ基を含有するオリゴマー又はポリマーの分子量の測定により求めることができる。
この構造を明示すれば、本発明の特定樹脂は、一般式(I-1)で表される繰り返し単位及び一般式(I-2)で表される繰り返し単位を有する構造、或いは、一般式(II-1)で表される繰り返し単位及び一般式(II-2)で表される繰り返し単位を含有する構造を含むことが好ましい。
本発明の特定樹脂の好ましい構成成分である一般式(I-1)で表される繰り返し単位及び一般式(I-2)で表される繰り返し単位について詳細に説明する。
一般式(I-2)で表される繰り返し単位は、数平均分子量が500~1,000,000であるオリゴマー鎖又はポリマー鎖Yを有する繰り返し単位であり、このような繰り返し単位は、保存安定性の観点から、本発明の樹脂の全繰り返し単位中、10~90モル%含有することが好ましく、30~70モル%含有することが最も好ましい。
両者の含有比について検討するに、分散安定性、及び、親疎水性のバランスの観点からは、繰り返し単位(I-1):(I-2)はモル比で10:1~1:100の範囲であることが好ましく、1:1~1:10の範囲であることがより好ましい。
なお、ポリマー鎖「Y」がイオン的に結合していることは、赤外分光法、酸価滴定や塩基滴定により確認できる。
本発明の特定樹脂の他の好ましい構成成分である一般式(II-1)で表される繰り返し単位及び一般式(II-2)で表される繰り返し単位について詳細に説明する。
一般式(II-2)は数平均分子量が500~1,000,000であるオリゴマー鎖又はポリマー鎖Yを有する繰り返し単位であり、このような繰り返し単位は、保存安定性の観点から、本発明の樹脂の全繰り返し単位中、10~90モル%含有することが好ましく、30~70モル%含有することが最も好ましい。
所望により併用される一般式(II-3)で表される繰り返し単位は本発明の樹脂の全繰り返し単位中、0.5~20モル%含有することが好ましく、1~10モル%含有することが最も好ましい。
本発明の特定樹脂においては、分散性の観点から、特に一般式(I-1)で表される繰り返し単位と一般式(I-2)で表される繰り返し単位の双方を含むことが最も好ましい。
Xは水温25℃でのpKaが14以下である官能基を含有する基を表す。ここでいう「pKa」とは、化学便覧(II)(改訂4版、1993年、日本化学会編、丸善株式会社)に記載されている定義のものである。
「pKaが14以下である官能基」は、物性がこの条件を満たすものであれば、その構造などは特に限定されず、公知の官能基でpKaが上記範囲を満たすものが挙げられ、具体的には、例えば、カルボン酸(pKa 3~5程度)、スルホン酸(pKa -3~-2程度)、りん酸(pKa 2程度)、-COCH2CO-(pKa 8~10程度)、-COCH2CN(pKa 8~11程度)、-CONHCO-、フェノール性水酸基、-RFCH2OH又は-(RF)2CHOH(RFはペルフルオロアルキル基を表す pKa 9~11程度)、スルホンアミド基(pKa 9~11程度)等が挙げられ、特にカルボン酸(pKa 3~5程度)、スルホン酸(pKa -3~-2程度)、-COCH2CO-(pKa 8~10程度)が好ましい。
このpKaが14以下である官能基を含有する基「X」は、通常、主鎖構造に含まれる窒素原子に直接結合するものであるが、特定樹脂の主鎖部の窒素原子とXとは、共有結合のみならず、イオン結合して塩を形成する態様で連結していてもよい。また、本発明の樹脂は、分子内に2種以上の互いに異なるXを有していてもよい。
pKaが14以下である官能基を含有する基「X」の分子量は、50~1000であることが好ましく、50~500であることが最も好ましい。この分子量の範囲であることにより、現像性・分散性が良好となる。
また、一般的にポリカプロラクトン鎖を含有する分散樹脂は、特開2007-63472号公報に記載のように、結晶性が高いため、低温で溶剤から析出する。しかし、本発明のポリカプロラクトン鎖を含有する分散樹脂は、予想外にも、溶剤溶解性が高く、低温でも溶剤から析出しない。この原因は不明であるが、樹脂中の「X」で示される部分構造が溶剤と親和することにより、溶剤溶解性が向上しているものと考えている。
酸価滴定は、公知の方法により行うことができ、例えば指示薬法(中和点を指示薬により見極める方法)、又は電位差測定法等を用いることができる。また、酸価滴定に用いる滴定液は市販の水酸化ナトリウム水溶液を用いることができるが、比較的高いpKaを有する官能基(例えば、-COCH2CO-、フェノール性水酸基等)の酸価滴定を行う場合のように、この水酸化ナトリウム水溶液によって酸価が測定しにくい場合は、ナトリウムメトキシド-ジオキサン溶液等の非水系滴定液を調製し、非水系溶媒系で酸価測定することが可能である。
「Y」は数平均分子量500~1,000,000のオリゴマー鎖又はポリマー鎖を表す。Yは、特定樹脂の主鎖部と連結できるポリエステル、ポリアミド、ポリイミド、ポリ(メタ)アクリル酸エステル等の公知のポリマー鎖が挙げられる。Yの特定樹脂との結合部位は、末端であることが好ましい。なお、本発明の樹脂は、分子内に互いに構造の異なる2種以上の「Y」(オリゴマー鎖、ポリマー鎖)を有していてもよい。
Yで示される側鎖構造は、主鎖連鎖に対し、樹脂1分子中に、2つ以上連結していることが好ましく、5つ以上連結していることが最も好ましい。
これらラクトンは複数種を混合して用いても良い。
カルボン酸とラクトンの反応時の仕込み比率は、目的のポリエステル鎖の分子量によるため一義的に決定できないが、カルボン酸:ラクトン=1:1~1:1,000が好ましく、1:3~1:500が最も好ましい。
(IV-3)二価アルコールと二価カルボン酸(もしくは環状酸無水物)の重縮合反応における二価アルコールとしては、直鎖又は分岐の脂肪族ジオール(炭素数2~30のジオールが好ましく、例えば、エチレングリコール、ジエチレングリコール、トリエチレングリコール、ジプロピレングリコール、1,2-プロパンジオール、1,3-プロパンジオール、1,5-ペンタンジオール、1,6-ヘキサンジオール、1,8-オクタンジオール等)が挙げられ、特に炭素数2~20の脂肪族ジオールが好ましい。
二価カルボン酸としては、直鎖又は分岐の二価の脂肪族カルボン酸(炭素数1~30の二価の脂肪族カルボン酸が好ましく、例えば、コハク酸、マレイン酸、アジピン酸、セバシン酸、ドデカン二酸、グルタル酸、スベリン酸、酒石酸、シュウ酸、マロン酸等)が挙げられ、特に炭素数3~20の二価カルボン酸が好ましい。また、これら二価カルボン酸と等価な酸無水物(例えば、無水コハク酸、無水グルタル酸等)を用いてもよい。
二価カルボン酸と二価アルコールは、モル比1:1で仕込むことが好ましい。これにより、末端にカルボン酸を導入することが可能となる。
以下、(1)一級又は二級アミノ基を有する樹脂と、Xの前駆体x及びYの前駆体yとを反応させる方法について説明する。
一級又は二級アミノ基を有する樹脂としては、前記窒素原子を有する主鎖部を構成する1級又は2級アミノ基を含有するオリゴマー又はポリマーが挙げられ、例えば、ポリ(低級アルキレンイミン)、ポリアリルアミン、ポリジアリルアミン、メタキシレンジアミン-エピクロルヒドリン重縮合物、ポリビニルアミン等が挙げられる。これらのうち、ポリ(低級アルキレンイミン)、又は、ポリアリルアミンから構成されるオリゴマー又はポリマーが好ましい。
xの例としては、環状カルボン酸無水物(炭素数4~30の環状カルボン酸無水物が好ましく、例えば、コハク酸無水物、グルタル酸無水物、イタコン酸無水物、マレイン酸無水物、アリルコハク酸無水物、ブチルコハク酸無水物、n-オクチルコハク酸無水物、n-デシルコハク酸無水物、n-ドデシルコハク酸無水物、n-テトラデシルコハク酸無水物、n-ドコセニルコハク酸無水物、(2-ヘキセン-1-イル)コハク酸無水物、(2-メチルプロペン-1-イル)コハク酸無水物、(2-ドデセン-1-イル)コハク酸無水物、n-オクテニルコハク酸無水物、(2,7-オクタンジエン-1-イル)コハク酸無水物、アセチルリンゴ酸無水物、ジアセチル酒石酸無水物、ヘット酸無水物、シクロヘキサン-1,2-ジカルボン酸無水物、3又は4-メチルシクロヘキサン-1,2-ジカルボン酸無水物、テトラフルオロコハク酸無水物、3又は4-シクロヘキセン-1,2-ジカルボン酸無水物、4-メチル-4-シクロヘキセン-1,2-ジカルボン酸無水物、フタル酸無水物、テトラクロロフタル酸無水物、ナフタル酸無水物、ナフタル酸無水物、ビシクロ[2.2.2]オクト-7-エン-2,3,5,6-テトラカルボン酸二無水物、ピロメリット酸二無水物、meso-ブタン-1,2,3,4-テトラカルボン酸二無水物、1,2,3,4-シクロペンタンカルボン酸二無水物等)、ハロゲン原子含有カルボン酸(例えば、クロロ酢酸、ブロモ酢酸、ヨード酢酸、4-クロロ-n-酪酸等)、スルトン(例えば、プロパンスルトン、1,4-ブタンスルトン等)、ジケテン、環状スルホカルボン酸無水物(例えば、2-スルホ安息香酸無水物等)、-COCH2COClを含有する化合物(例えば、エチルマロニルクロリド等)、又はシアノ酢酸クロリド等が挙げられ、特に環状カルボン酸無水物、スルトン、ジケテンが、生産性の観点から好ましい。
yは、特定樹脂の窒素原子と共有結合又はイオン結合できる基を末端に有する数平均分子量500~1,000,000オリゴマー又はポリマーが好ましく、特に、片末端に遊離のカルボキシル基を有する数平均分子量500~1,000,000オリゴマー又はポリマーが最も好ましい。
yの例としては、一般式(IV)で表される片末端に遊離のカルボキシル基を有するポリエステル、片末端に遊離のカルボキシル基を有するポリアミド、片末端に遊離のカルボキシル基を有するポリ(メタ)アクリル酸系樹脂等が挙げられるが、特に、一般式(IV)で表される片末端に遊離のカルボキシル基を含有するポリエステルが最も好ましい。
溶媒を用いる場合、基質に対し、0.1~100重量倍用いることが好ましく、0.5~10重量倍用いることが最も好ましい。
本発明の特定樹脂は、再沈法で精製してもよい。再沈法で、低分子量成分を除去することにより、得られた特定樹脂を顔料分散剤として使用した場合の分散性能が向上する。
再沈には、ヘキサン等の炭化水素系溶媒、メタノールなどのアルコール系溶媒を用いることが好ましい。
この方法において用いる、窒素原子を含有するモノマーとしては、公知のモノマーを選ぶことができ、例えば、(メタ)アクリル酸2-ジアルキルアミノエチル、3-ジアルキルアミノプロピル(メタ)アクリルアミド、ビニルピリジン、N-ビニルイミダゾール等が挙げられるが、特に三級アミノ基を含有するモノマーが好ましく、(メタ)アクリル酸2-ジアルキルアミノエチル、3-ジアルキルアミノプロピル(メタ)アクリルアミドが最も好ましい。
Xを含有するモノマーとしては、Xを含有する(メタ)アクリル酸アミドが好ましく、例えば、N-(メタ)アクリロイルグリシン、N-(メタ)アクリロイルアラニン等の(メタ)アクリロイル基を含有するアミノ酸が好ましい。
Yを含有するマクロモノマーとしては、公知のマクロモノマーが挙げられるが、ポリ(メタ)アクリル酸エステル、ポリスチレン又はポリエステルの片末端に重合性基を有しているマクロモノマーが好ましい。例としては、東亜合成製マクロモノマーAA-6(末端基がメタクリロイル基であるポリメタクリル酸メチル)、AS-6(末端基がメタクリロイル基であるポリスチレン)、AN-6S(末端基がメタクリロイル基であるスチレンとアクリロニトリルの共重合体)、AB-6(末端基がメタクリロイル基であるポリアクリル酸ブチル)、ダイセル化学製プラクセルFM5(メタクリル酸2-ヒドロキシエチルのε-カプロラクトン5モル当量付加品)、FA10L(アクリル酸2-ヒドロキシエチルのε-カプロラクトン10モル当量付加品)及び特開平2-272009号公報に記載のポリエステル系マクロマーが好ましい。
ラジカル重合開始剤は、全モノマーのモル数に対し、0.01モル%~10モル%用いることが好ましく、0.1モル%~5モル%用いることが最も好ましい。
分子量を調整するのに、連鎖移動剤を添加しても良い。連鎖移動剤としては、特にチオール化合物が好ましく、炭素数5~20のアルカンチオール、2-メルカプトエタノール及び2-メルカプトプロピオン酸が好ましい。
連鎖移動剤は、全モノマーのモル数に対し、0.01モル%~10モル%用いることが好ましく、0.1モル%~5モル%用いることが最も好ましい。反応温度は60~100℃が好ましく、70~90℃が最も好ましい。
反応溶媒としては、前記(1)一級又は二級アミノ基を有する樹脂と、Xの前駆体x及びYの前駆体yとを反応させる方法で挙げた溶媒が挙げられる。
本発明の特定樹脂は、特に顔料分散剤として優れた機能を発揮する。以下、(A)本発明の特定樹脂、(B)顔料、(C)溶剤、を含有する顔料分散液について詳細に述べる。
本発明の顔料分散液には、(A)本発明の特定樹脂を1種のみ含んでいてもよく、2種以上を含んでいてもよい。
顔料分散液においては、(A)特定樹脂は、後述する(B)顔料100質量部に対して1質量部から200質量部の範囲で含有してもよく、好ましくは、5質量部から100質量部の範囲であり、より好ましくは、5質量部から60質量部の範囲である。
本発明の顔料分散液が有する顔料は、従来公知の種々の無機顔料または有機顔料を用いることができる。また、無機顔料であれ有機顔料であれ、高透過率であることが好ましいことを考慮すると、なるべく細かいものの使用が好ましく、ハンドリング性をも考慮すると、上記顔料の平均粒子径は、0.005μm~0.1μmが好ましく、0.005μm~0.05μmがより好ましい。
C.I.ピグメントイエロー1、1:1、2、3、4、5、6、9、10、12、13、14、16、17、24、31、32、34、35、35:1、36、36:1、37、37:1、40、41、42、43、48、53、55、61、62、62:1、63、65、73、74、75,81、83、87、93、94、95、97、100、101、104、105、108、109、110、111、116、117、119、120、126、127、127:1、128、129、133、134、136、138、139、142、147、148、150、151、153、154、155、157、158、159、160、161、162、163、164、165、166、167、168、169、170、172、173、174、175、176、180、181、182、183、184、185、188、189、190、191、191:1、192、193、194、195、196、197、198、199、200、202、203、204、205、206、207、208;
C.I.ピグメントレッド1、2、3、4、5、6、7、8、9、12、14、15、16、17、21、22、23、31、32、37、38、41、47、48、48:1、48:2、48:3、48:4、49、49:1、49:2、50:1、52:1、52:2、53、53:1、53:2、53:3、57、57:1、57:2、58:4、60、63、63:1、63:2、64、64:1、68、69、81、81:1、81:2、81:3、81:4、83、88、90:1、101、101:1、104、108、108:1、109、112、113、114、122、123、144、146、147、149、151、166、168、169、170、172、173、174、175、176、177、178、179、181、184、185、187、188、190、193、194、200、202、206、207、208、209、210、214、216、220、221、224、230、231、232、233、235、236、237、238、239、242、243、245、247、249、250、251、253、254、255、256、257、258、259、260、262、263、264、265、266、267、268、269、270、271、272、273、274、275、276;
C.I.ピグメントブルー1、1:2、9、14、15、15:1、15:2、15:3、15:4、15:6、16、17、19、25、27、28、29、33、35、36、56、56:1、60、61、61:1、62、63、66、67、68、71、72、73、74、75、76、78、79;
C.I.ピグメントグリーン1、2、4、7、8、10、13、14、15、17、18、19、26、36、45、48、50、51、54、55、58;
C.I.ピグメントブラウン23、25、26;
C.I.ピグメントブラック1,7;
カーボンブラック、アセチレンブラック、ランプブラック、ボーンブラック、黒鉛、鉄黒、アニリンブラック、シアニンブラック、チタンブラック等を挙げることができる。
C.I.ピグメントオレンジ36、71、
C.I.ピグメントレッド122、150、171、175、177、209、224、242、254、255、264、
C.I.ピグメントバイオレット19、23、32、
C.I.ピグメントブルー15:1、15:3、15:6、16、22、60、66、
C.I.ピグメントグリーン7、36、37、58;
C.I.ピグメントブラック1
顔料としては、既述の顔料と同様のものが挙げられる。
ii)水溶性の無機塩
無機塩は、水に溶解するものであれば特に限定されず、塩化ナトリウム、塩化バリウム、塩化カリウム、硫酸ナトリウム等を用いることができるが、価格の点から塩化ナトリウムまたは硫酸ナトリウムを用いるのが好ましい。ソルトミリングする際に用いる無機塩の量は、処理効率と生産効率の両面から、有機顔料の1~30重量倍、特に5~25重量倍であることが好ましい。有機顔料に対する無機塩の量比が大きいほど微細化効率が高いが、1回の顔料の処理量が少なくなるためである。
水溶性有機溶剤は、有機顔料、無機塩を湿潤する働きをするものであり、水に溶解(混和)し、かつ用いる無機塩を実質的に溶解しないものであれば特に限定されない。但し、ソルトミリング時に温度が上昇し、溶剤が蒸発し易い状態になるため、安全性の点から、沸点120℃以上の高沸点溶剤が好ましい。水溶性有機溶剤としては、例えば、2-メトキシエタノール、2-ブトキシエタノール、2-(イソペンチルオキシ)エタノール、2-(ヘキシルオキシ)エタノール、エチレングリコール、ジエチレングリコール、ジエチレングリコールモノエチルエーテル、ジエチレングリコールモノエチルエーテルアセテート、ジエチレングリコールモノブチルエーテル、トリエチレングリコール、トリエチレングリコールモノメチルエーテル、液状のポリエチレングリコール、1-メトキシ-2-プロパノール、1-エトキシ-2-プロパノール、ジプロピレングリコール、ジプロピレングリコールモノメチルエーテル、ジプロピレングリコールモノエチルエーテル、液状のポリプロピレングリコール等が用いられる。
水溶性有機溶剤はソルトミリング初期に全てを添加しても良いし、分割して添加しても良い。水溶性有機溶剤は単独で使用しても良いし、2種以上を併用することも出来る。
添加してもよい顔料被覆用高分子化合物は、好ましくは室温で固体であり、水不溶性で,かつソルトミリング時の湿潤剤に用いる水溶性有機溶剤に少なくとも一部可溶である必要があり,天然樹脂,変性天然樹脂,合成樹脂,天然樹脂で変性された合成樹脂が用いられる。乾燥した処理顔料を用いる場合には,用いる化合物は室温で固体であることが好ましい。天然樹脂としてはロジンが代表的であり,変性天然樹脂としては,ロジン誘導体,繊維素誘導体,ゴム誘導体,タンパク誘導体およびそれらのオリゴマーが挙げられる。合成樹脂としては,エポキシ樹脂,アクリル樹脂,マレイン酸樹脂,ブチラール樹脂,ポリエステル樹脂,メラミン樹脂,フェノール樹脂,ポリウレタン樹脂等が挙げられる。天然樹脂で変性された合成樹脂としては,ロジン変性マレイン酸樹脂,ロジン変性フェノール樹脂等が挙げられる。
これらの樹脂を加えるタイミングは、ソルトミリング初期にすべてを添加してもよく、分割して添加してもよい。
顔料の一次粒子径は、電子顕微鏡等の公知の方法で測定することができる。
本発明の顔料分散液は、少なくとも一種の(C)溶剤を有する。(C)溶剤としては、以下に示される有機溶剤から選択される液体が挙げられ、顔料分散液中に含まれる各成分の溶解性や、硬化性組成物に応用した場合の塗布性などを考慮して選択されるものであり、これら所望の物性を満足すれば基本的に特には限定されないが、安全性を考慮して選ばれることが好ましい。
溶剤の具体例としては、エステル類、例えば、酢酸エチル、酢酸-n-ブチル、酢酸イソブチル、ギ酸アミル、酢酸イソアミル、プロピオン酸ブチル、酪酸イソプロピル、酪酸エチル、酪酸ブチル、オキシ酢酸メチル、オキシ酢酸エチル、オキシ酢酸ブチル、メトキシ酢酸メチル、メトキシ酢酸エチル、メトキシ酢酸ブチル、エトキシ酢酸メチル、エトキシ酢酸エチル、3-オキシプロピオン酸メチル、3-オキシプロピオン酸エチル、3-メトキシプロピオン酸メチル、3-メトキシプロピオン酸エチル、3-エトキシプロピオン酸メチル、3-エトキシプロピオン酸エチル、2-オキシプロピオン酸メチル、2-オキシプロピオン酸エチル、2-オキシプロピオン酸プロピル、2-メトキシプロピオン酸メチル、2-メトキシプロピオン酸エチル、2-メトキシプロピオン酸プロピル、2-エトキシプロピオン酸メチル、2-エトキシプロピオン酸エチル、2-オキシ-2-メチルプロピオン酸メチル、2-オキシ-2-メチルプロピオン酸エチル、2-メトキシ-2-メチルプロピオン酸メチル、2-エトキシ-2-メチルプロピオン酸エチル、ピルビン酸メチル、ピルビン酸エチル、ピルビン酸プロピル、アセト酢酸メチル、アセト酢酸エチル、2-オキソブタン酸メチル、2-オキソブタン酸エチル等;
本発明の顔料分散液には、前記(A)~(C)の必須成分に加え、顔料分散液の用途など、目的に応じて、本発明の効果を損なわない限りにおいて他の成分を含有することができる。
本発明の顔料分散液は、さらに顔料誘導体を含有することが好ましい。特に、酸性基を有する顔料誘導体を含有することで、分散性・分散安定性が飛躍的に向上する。
顔料誘導体は、有機顔料、アントラキノン類又はアクリドン類の一部分を酸性基、塩基性基又はフタルイミドメチル基で置換した構造が好ましい。顔料誘導体を構成する有機顔料としては、ジケトピロロピロール系顔料、アゾ、ジスアゾ、ポリアゾ等のアゾ系顔料、銅フタロシアニン、ハロゲン化銅フタロシアニン、無金属フタロシアニン等のフタロシアニン系顔料、アミノアントラキノン、ジアミノジアントラキノン、アントラピリミジン、フラバントロン、アントアントロン、インダントロン、ピラントロン、ビオラントロン等のアントラキノン系顔料、キナクリドン系顔料、ジオキサジン系顔料、ペリノン系顔料、ペリレン系顔料、チオインジゴ系顔料、イソインドリン系顔料、イソインドリノン系顔料、キノフタロン系顔料、スレン系顔料、金属錯体系顔料等が挙げられる。
R2で表されるアルキレン基としては、メチレン基、エチレン基、トリメチレン基、テトラメチレン基、ヘキサメチレン基、2-ヒドロキシプロピレン基、メチレンオキシ基、エチレンオキシ基、メチレンオキシカルボニル基、メチレンチオ基、等が挙げられ、メチレン基、メチレンオキシ基、メチレンオキシカルボニル基、メチレンチオ基が好ましい。
これらのうち、Zで示される複素環構造としては、下記一般式(2)または(3)であらわされる構造であることが好ましい。
これらのうち、Xは単結合、メチレン基、-O-、-C(=O)-が好ましく、-C(=O)-が特に好ましい。
酸基を有する単量体としては、(メタ)アクリル酸、p-ビニル安息香酸、マレイン酸、フマル酸、イタコン酸、(メタ)アクリル酸2-ヒドロキシエチルの無水コハク酸付加体、(メタ)アクリル酸2-ヒドロキシエチルの無水フタル酸付加体、等が挙げられる。
このような他の高分子材料は、その構造からさらに直鎖状高分子、末端変性型高分子、グラフト型高分子、ブロック型高分子に分類することができる。
本発明の顔料分散液は、前記本発明の特定樹脂を顔料分散剤として用いるため、微細な顔料を高濃度で含む場合においても、顔料の分散性と分散安定性に優れる。
本発明の前記顔料分散液に、さらに(D)光重合開始剤、(E)エチレン性不飽和二重結合を含有する化合物を添加することで、解像性・色特性・塗布性・現像性に優れた着色硬化性組成物を提供することができる。
本発明の硬化性組成物は、感度及びパターン形成性向上のため(D)光重合開始剤を含有する。本発明における光重合開始剤は、光により分解し、本発明における重合可能な成分の重合を開始、促進する化合物であり、波長300~500nmの領域に吸収を有するものであることが好ましい。また、光重合開始剤は、単独で、又は2種以上を併用して用いることができる。
以下、これらの各化合物について詳細に述べる。
ベンゾイン化合物としてはm-ベンゾインイソプロピルエーテル、ベンゾインイソブチルエーテル、ベンゾインメチルエーテル、メチル-o-ベンゾイルベンゾエートなどを挙げることができる。
クマリン化合物としては、例えば、3-メチル-5-アミノ-((s-トリアジン-2-イル)アミノ)-3-フェニルクマリン、3-クロロ-5-ジエチルアミノ-((s-トリアジン-2-イル)アミノ)-3-フェニルクマリン、3-ブチル-5-ジメチルアミノ-((s-トリアジン-2-イル)アミノ)-3-フェニルクマリン等を挙げることができる。
また、一般式(3)におけるnは1~2の整数が好ましい。
一般式(3)で表される化合物については、本願出願人が先に提案した特願2008-251321号明細書段落番号〔0089〕~〔0108〕に一般式(α)で表される化合物として詳細に記載されており、ここに記載の化合物は本発明にも好適に使用しうる。
また、その他の好ましいスルホニウム塩としては、トリアリールスルホニウム塩の1つの置換基がクマリン、アントラキノン構造を有し、300nm以上に吸収を有するスルホニウム塩が挙げられる。別の好ましいスルホニウム塩としては、トリアリールスルホニウム塩が、アリロキシ基、アリールチオ基を置換基に有する300nm以上に吸収を有するスルホニウム塩が挙げられる。
本発明の硬化性組成物は、前記樹脂以外のエチレン性不飽和二重結合を含有する化合物(以下、単に「エチレン性不飽和二重結合を含有する化合物」と称する場合がある。)を含有することができる。
(ただし、R10及びR11は、H又はCH3を示す。)
感度の点では1分子あたりの不飽和基含量が多い構造が好ましく、多くの場合、2官能以上が好ましい。また、画像部すなわち硬化膜の強度を高くするためには、3官能以上のものがよく、更に、異なる官能数・異なる重合性基(例えばアクリル酸エステル、メタクリル酸エステル、スチレン系化合物、ビニルエーテル系化合物)のものを併用することで、感度と強度の両方を調節する方法も有効である。硬化感度の観点から、(メタ)アクリル酸エステル構造を2個以上含有する化合物を用いることが好ましく、3個以上含有する化合物を用いることがより好ましく、4個以上含有する化合物を用いることが最も好ましい。また、硬化感度、および、未露光部の現像性の観点では、EO変性体を含有することが好ましい。また、硬化感度、および、露光部強度の観点ではウレタン結合を含有することが好ましい。
本発明において使用しうるアルカリ可溶性樹脂としては、線状有機高分子重合体であって、分子(好ましくは、アクリル系共重合体、スチレン系共重合体を主鎖とする分子)中に少なくとも1つのアルカリ可溶性を促進する基(例えばカルボキシル基、リン酸基、スルホン酸基、ヒドロキシル基など)を有するアルカリ可溶性樹脂の中から適宜選択することができる。
上記アルカリ可溶性樹脂としてより好ましいものは、側鎖にカルボン酸を有するポリマー、例えば特開昭59-44615号、特公昭54-34327号、特公昭58-12577号、特公昭54-25957号、特開昭59-53836号、特開昭59-71048号の各公報に記載されているような、メタクリル酸共重合体、アクリル酸共重合体、イタコン酸共重合体、クロトン酸共重合体、マレイン酸共重合体、部分エステル化マレイン酸共重合体等、並びに側鎖にカルボン酸を有する酸性セルロース誘導体、水酸基を有するポリマーに酸無水物を付加させたもの等のアクリル系共重合体のものが挙げられる。
酸価としては、20~200mgKOH/g、好ましくは30~150mgKOH/g、更に好ましくは35~120mgKOH/gの範囲のものが好ましい。
前記アルキル(メタ)アクリレート及びアリール(メタ)アクリレートとしては、CH2=C(R1)(COOR3) 〔ここで、R1は水素原子又は炭素数1~5のアルキル基を表し、R2は炭素数6~10の芳香族炭化水素環を表し、R3は炭素数1~8のアルキル基又は炭素数6~12のアラルキル基を表す。〕具体的にはメチル(メタ)アクリレート、エチル(メタ)アクリレート、プロピル(メタ)アクリレート、ブチル(メタ)アクリレート、イソブチル(メタ)アクリレート、ペンチル(メタ)アクリレート、ヘキシル(メタ)アクリレート、オクチル(メタ)アクリレート、フェニル(メタ)アクリレート、ベンジル(メタ)アクリレート、トリル(メタ)アクリレート、ナフチル(メタ)アクリレート、シクロヘキシル(メタ)アクリレート、ヒドロキシアルキル(メタ)アクリレート(アルキルは炭素数1~8のアルキル基)、ヒドロキシグリシジルメタクリレート、テトラヒドロフルフリルメタクリレート等を挙げることができる。
ポリエチレンオキシド鎖、ポリプロピレンオキシド鎖の繰り返し単位は1~20が好ましく、2~12がより好ましい。これらの側鎖にポリアルキレンオキサイド鎖を有するアクリル系共重合体は、例えば2-ヒドロキシエチル(メタ)アクリレート、ヒドロキシプロピル(メタ)アクリレート、ポリエチレングリコールモノ(メタ)アクリレート、ポリプロピレングリコールモノ(メタ)アクリレート、ポリ(エチレングリコール-プロピレングリコール)モノ(メタ)アクリレートなどおよびこれらの末端OH基をアルキル封鎖した化合物、例えばメトキシポリエチレングリコールモノ(メタ)アクリレート、エトキシポリプロピレングリコールモノ(メタ)アクリレート、メトキシポリ(エチレングリコール-プロピレングリコール)モノ(メタ)アクリレートなどを共重合成分とするアクリル系共重合体である。
これら共重合可能な他の単量体は、1種単独であるいは2種以上を組み合わせて用いることができる。好ましい共重合可能な他の単量体は、アルキル(メタ)アクリレート(アルキルは炭素数2から4のアルキル基)、フェニル(メタ)アクリレート、ベンジル(メタ)アクリレート及びスチレンである。
これらの中では特に、ベンジル(メタ)アクリレート/(メタ)アクリル酸共重合体やベンジル(メタ)アクリレート/(メタ)アクリル酸/他のモノマーからなる多元共重合体が好適である。
また、アクリル系樹脂の質量平均分子量Mw(GPC法で測定されたポリスチレン換算値)は、カラーレジストを塗布等の工程上使用しやすい粘度範囲を実現するために、また膜強度を確保するために、2,000~100,000であることが好ましく、より好ましくは3,000~50,000である。
アクリル系樹脂の酸価を上記で特定した範囲とするには、各単量体の共重合割合を適切に調整することに容易に行うことができる。また、質量平均分子量の範囲を上記範囲とするには、単量体の共重合の際に、重合方法に応じた連鎖移動剤を適切な量使用することにより容易に行うことができる。
アクリル系樹脂は、例えばそれ自体公知のラジカル重合法により製造することができる。ラジカル重合法でアクリル系樹脂を製造する際の温度、圧力、ラジカル開始剤の種類及びその量、溶媒の種類等々の重合条件は、当業者であれば容易に設定することができるし、条件設定が可能である。
重合性二重結合を有するアルカリ可溶性樹脂は、アルカリ現像液での現像が可能であって、さらに光硬化性と熱硬化性を備えたものである。
これら重合性基を含有するポリマーの例を以下に示すが、COOH基、OH基等のアルカリ可溶性基と炭素-炭素間不飽和結合が含まれていれば下記に限定されない。
(1)予めイソシアネート基とOH基を反応させ、未反応のイソシアネート基を1つ残し、かつ(メタ)アクリロイル基を少なくとも1つ含む化合物とカルボキシル基を含むアクリル樹脂との反応によって得られるウレタン変性した重合性二重結合含有アクリル樹脂、
(2)カルボキシル基を含むアクリル樹脂と分子内にエポキシ基及び重合性二重結合を共に有する化合物との反応によって得られる不飽和基含有アクリル樹脂、
(3)酸ペンダント型エポキシアクリレート樹脂、
(4)OH基を含むアクリル樹脂と重合性二重結合を有する2塩基酸無水物を反応させた重合性二重結合含有アクリル樹脂。
上記のうち、特に(1)及び(2)の樹脂が好ましい。
具体例として、OH基を有する例えば2-ヒドロキシエチルアクリレートと、COOH基を含有する例えばメタクリル酸と、これらと共重合可能なアクリル系若しくはビニル系化合物等のモノマーとの共重合体に、OH基に対し反応性を有するエポキシ環と炭素間不飽和結合基を有する化合物(例えばグリシジルアクリレートなどの化合物)を反応させて得られる化合物、等を使用できる。OH基との反応ではエポキシ環のほかに酸無水物、イソシアネート基、アクリロイル基を有する化合物も使用できる。また、特開平6-102669号公報、特開平6-1938号公報に記載のエポキシ環を有する化合物にアクリル酸のような不飽和カルボン酸を反応させて得られる化合物に、飽和もしくは不飽和多塩基酸無水物を反応させて得られる反応物も使用できる。COOH基のようなアルカリ可溶化基と炭素間不飽和基とを併せ持つ化合物として、例えば、ダイヤナールNRシリーズ(三菱レイヨン(株)製);Photomer 6173(COOH基含有Polyurethane acrylic oligomer、Diamond Shamrock Co.Ltd.,製);ビスコートR-264、KSレジスト106(いずれも大阪有機化学工業(株)製);サイクロマーPシリーズ、プラクセルCF200シリーズ(いずれもダイセル化学工業(株)製);Ebecryl3800(ダイセルユーシービー(株)製)、などが挙げられる。
<増感剤>
本発明の硬化性組成物は、重合開始剤のラジカル発生効率の向上、感光波長の長波長化の目的で、増感剤を含有してもよい。本発明に用いることができる増感剤としては、前記した光重合開始剤に対し、電子移動機構又はエネルギー移動機構で増感させるものが好ましい。本発明に用いることができる増感剤としては、以下に列挙する化合物類に属しており、且つ300nm~450nmの波長領域に吸収波長を有するものが挙げられる。
例えば、多核芳香族類(例えば、フェナントレン、アントラセン、ピレン、ペリレン、トリフェニレン、9,10-ジアルコキシアントラセン)、キサンテン類(例えば、フルオレッセイン、エオシン、エリスロシン、ローダミンB、ローズベンガル)、チオキサントン類(イソプロピルチオキサントン、ジエチルチオキサントン、クロロチオキサントン)、シアニン類(例えばチアカルボシアニン、オキサカルボシアニン)、メロシアニン類(例えば、メロシアニン、カルボメロシアニン)、フタロシアニン類、チアジン類(例えば、チオニン、メチレンブルー、トルイジンブルー)、アクリジン類(例えば、アクリジンオレンジ、クロロフラビン、アクリフラビン)、アントラキノン類(例えば、アントラキノン)、スクアリウム類(例えば、スクアリウム)、アクリジンオレンジ、クマリン類(例えば、7-ジエチルアミノ-4-メチルクマリン)、ケトクマリン、フェノチアジン類、フェナジン類、スチリルベンゼン類、アゾ化合物、ジフェニルメタン、トリフェニルメタン、ジスチリルベンゼン類、カルバゾール類、ポルフィリン、スピロ化合物、キナクリドン、インジゴ、スチリル、ピリリウム化合物、ピロメテン化合物、ピラゾロトリアゾール化合物、ベンゾチアゾール化合物、バルビツール酸誘導体、チオバルビツール酸誘導体、アセトフェノン、ベンゾフェノン、チオキサントン、ミヒラーズケトンなどの芳香族ケトン化合物、N-アリールオキサゾリジノンなどのヘテロ環化合物などが挙げられる。
更に欧州特許第568,993号明細書、米国特許第4,508,811号明細書、同5,227,227号明細書、特開2001-125255号公報、特開平11-271969号公報等に記載の化合物等などが挙げられる。
本発明においては、硬化性組成物の製造中あるいは保存中において重合可能なエチレン性不飽和二重結合を有する化合物の不要な熱重合を阻止するために少量の熱重合防止剤を添加することが望ましい。
本発明に用いうる熱重合防止剤としては、ハイドロキノン、p-メトキシフェノール、ジ-t-ブチル-p-クレゾール、ピロガロール、t-ブチルカテコール、ベンゾキノン、4,4’-チオビス(3-メチル-6-t-ブチルフェノール)、2,2’-メチレンビス(4-メチル-6-t-ブチルフェノール)、N-ニトロソフェニルヒドロキシアミン第一セリウム塩等が挙げられる。
さらに、本発明においては、硬化皮膜の物性を改良するために無機充填剤や、可塑剤、感光層表面のインク着肉性を向上させうる感脂化剤等の公知の添加剤、基板密着性を向上させうる基板密着剤を加えてもよい。
可塑剤としては例えばジオクチルフタレート、ジドデシルフタレート、トリエチレングリコールジカプリレート、ジメチルグリコールフタレート、トリクレジルホスフェート、ジオクチルアジペート、ジブチルセバケート、トリアセチルグリセリン等があり、結合剤を使用した場合、エチレン性不飽和二重結合を有する化合物と結合剤との合計質量に対し10質量%以下添加することができる。
基板密着剤としては、公知の材料を用いることができるが、特にシラン系カップリング剤、チタネート系カップリング剤、アルミニウム系カップリング剤を用いることが好ましい。
中でもγ-メタクリロキシプロピルトリメトキシシラン、γ-メタクリロキシプロピルトリエトキシシラン、γ-アクリロキシプロピルトリメトキシシラン、γ-アクリロキシプロピルトリエトキシシラン、γ-メルカプトプロピルトリメトキシシラン、γ-アミノプロピルトリエトキシシラン、フェニルトリメトキシシラン、が好ましく、γ-メタクリロキシプロピルトリメトキシシランが最も好ましい。
また、本発明の着色硬化性組成物は、微細な顔料を高濃度で含有しても、顔料分散安定性と現像性に優れ、高精細で色特性の良好な着色領域を形成しうることから、固体撮像素子用のカラーフィルタの製造、特に、膜厚が0.8μm以下、好ましくは、0.1~0.5μmの範囲の画素を形成するような場合、特に本発明の顔料含有着色硬化性組成物を用いることでその効果が著しいといえる。
次に、本発明のカラーフィルタ及びその製造方法について説明する。
本発明のカラーフィルタは、支持体上に、本発明の硬化性組成物を用いてなる着色パターンを有することを特徴とする。
以下、本発明のカラーフィルタについて、その製造方法(本発明のカラーフィルタの製造方法)を通じて詳述する。
以下、本発明の製造方法における各工程について説明する。
着色層形成工程では、支持体上に、本発明の硬化性組成物を塗布して該硬化性組成物からなる着色層を形成する。
また、これらの支持体上には、必要により、上部の層との密着改良、物質の拡散防止或いは基板表面の平坦化のために下塗り層を設けてもよい。
硬化性組成物の塗布直後の膜厚としては、塗布膜の膜厚均一性、塗布溶剤の乾燥のしやすさの観点から、0.1~10μmが好ましく、0.2~5μmがより好ましく、0.2~3μmがさらに好ましい。
また、IS用カラーフィルタとして用いるためには、色濃度確保の観点、斜め方向の光が受光部に到達せず、又、デバイスの端と中央とで集光率の差が顕著になる等の不具合を低減する観点から、0.05μm以上1.0μm未満が好ましく、0.1μm以上0.8μm以下がより好ましく、0.2μm以上0.7μm以下が特に好ましい。
露光工程では、前記着色層形成工程において形成された着色層(硬化性組成物層)を、所定のマスクパターンを有するマスクを介して露光する。
本工程における露光においては、塗布膜のパターン露光は、所定のマスクパターンを介して露光し、光照射された塗布膜部分だけを硬化させることによりことにより行うことができる。露光に際して用いることができる放射線としては、特に、g線、i線等の紫外線が好ましく用いられる。照射量は5~1500mJ/cm2が好ましく10~1000mJ/cm2がより好ましく、10~500mJ/cm2が最も好ましい。
本発明のカラーフィルタが液晶表示素子用である場合は、上記範囲の中で5~200mJ/cm2が好ましく10~150mJ/cm2がより好ましく、10~100mJ/cm2が最も好ましい。また、本発明のカラーフィルタが固体撮像素子用である場合は、上記範囲の中で30~1500mJ/cm2が好ましく50~1000mJ/cm2がより好ましく、80~500mJ/cm2が最も好ましい。
次いでアルカリ現像処理(現像工程)を行うことにより、上記露光における光未照射部分をアルカリ水溶液に溶出させ、光硬化した部分だけが残る。現像液で現像して、各色(3色あるいは4色)の画素からなるパターン状皮膜を形成することができる。現像液としては、下地の回路などにダメージを起さない、有機アルカリ現像液が望ましい。現像温度としては通常20℃~30℃であり、現像時間は20~90秒である。
次いで、余剰の現像液を洗浄除去し、乾燥を施す。
本発明の硬化性組成物を用いた場合、顔料分散剤として用いられる本発明の特定樹脂は、顔料の分散性、分散安定性に優れ、且つ、分子内にpKaが14以下である官能基を有することから、現像性に優れるため、微細なパターンを形成する場合においても、未硬化部の残膜が生じがたく、このため、微細なパターン形成を必要とするCCD用カラーフィルターの着色パターン形成に好適である。
このポストベーク処理は、現像後の塗布膜を、上記条件になるようにホットプレートやコンベクションオーブン(熱風循環式乾燥機)、高周波加熱機等の加熱手段を用いて、連続式あるいはバッチ式で行うことができる。
また、本発明の固体撮像素子は、前記本発明のカラーフィルタの製造方法によって製造された本発明のカラーフィルタを備えることを特徴とする。
従って、具体的には、本発明のカラーフィルタを液晶表示素子やCCD等の固体撮像素子に好適に用いることができ、特に100万画素を超えるような高解像度のCCD素子やCMOS等に好適である。本発明のカラーフィルタは、例えば、CCD素子を構成する各画素の受光部と集光するためのマイクロレンズとの間に配置されるカラーフィルタとして用いることができる。
なお、実施例中、酸価及びアミン価は電位差法(溶媒テトラヒドロフラン/水=100/10(体積比)、滴定液 0.01N水酸化ナトリウム水溶液(酸価) 0.01N塩酸(アミン価))により決定した。但し、実施例18、及び実施例29では、0.01N水酸化ナトリウム水溶液に代えて、0.01Nナトリウムメトキシドジオキサン溶液系にて滴定した。
n-オクタン酸6.4g、ε-カプロラクトン200g、チタン(IV)テトラブトキシド5gを混合し、160℃で8時間加熱した後、室温まで冷却しポリエステル(i-1)を得た。
スキームを以下に示す。
表1に記載の仕込み量にした以外は合成例1と同様にしてポリエステル(i-2)~(i-10)を得た。これらの合成例で得た樹脂の数平均分子量、重量平均分子量を既述のGPC法により測定した。結果を下記表1に示す。また、原料仕込み比より算出したラクトン繰り返し単位の単位数をともに下記表1に示す。
窒素気流下、12-ヒドロキシステアリン酸100g、チタン(IV)テトラブトキシド0.1g及びキシレン300gを混合し、外温160℃で生成する水をディーンスターク管で留去しながら反応した。GPC測定における数平均分子量が8,000、重量平均分子量が12,000となったところで加熱を停止し、ポリエステル(i-11)を得た。
合成例11と同様の実験を行い、GPC測定における数平均分子量が6,000、重量平均分子量が11,000となったところで加熱を停止し、ポリエステル(i-12)を得た。
窒素気流下、アジピン酸307g、ネオペンチルグリコール110g、1,4-ブタンジオール57g及びエチレングリコール26gを外温160℃で生成する水をディーンスターク管で留去しながら反応した。GPC測定における数平均分子量が8,000、重量平均分子量が13,000となったところで反応を停止し、ポリエステル(i-13)を得た。
窒素気流下、メタクリル酸メチル50g(500mmol)、プロピレングリコールモノメチルエーテル100g、2-メルカプトプロピオン酸2.5g(23.6mmol)を80℃に加熱した。次に、V-601(和光純薬製)0.1gを添加し、3時間後、さらにV-601を0.1g添加し、4時間加熱した。その後、メタクリル酸グリシジル3.35g(23.6mmol)及びテトラブチルアンモニウムブロミド0.5gを添加し、80℃で5時間加熱した。放冷後、水200mLとメタノール800mLの混合溶媒を用いて再沈し、乾燥後、マクロモノマー(i-14)を55g得た。
[樹脂(J-1)の合成]
ポリエチレンイミン(SP-018、数平均分子量1,800、日本触媒製)10g及びポリエステル(i-1)(Y前駆体y)100gを混合し、120℃で3時間加熱して、中間体(J-1B)を得た。その後、65℃まで放冷し、無水コハク酸(X前駆体x)3.8gを含有するプロピレングリコール1-モノメチルエーテル2-アセテート(以下、PGMEAとよぶ)200gをゆっくり添加し2時間攪拌した。その後、PGMEAを添加し、樹脂(J-1)のPGMEA10重量%溶液を得た。樹脂(J-1)は、ポリエステル(i-1)由来の側鎖と無水コハク酸由来のpKaが14以下である官能基(カルボキシ基)を有する基を有するものである。
合成スキームを以下に示す。
即ち、一般式(I-1)で表される繰り返し単位において、Xが-COCH2CH2CO2Hである繰り返し単位を10モル%、一般式(I-2)で表される繰り返し単位において、Yがポリ(ε-カプロラクトン)であるものを50モル%含む樹脂であることがわかる。また、GPC法による重量平均分子量は24,000であった。
[樹脂(J-2)~(J-17)の合成]
表2及び表3に記載の如き、アミノ基含有樹脂と、X前駆体xと、前記合成例1~13で得たポリエステルと、を用いた他は、合成例15と同様に合成を行い、樹脂(J-2)~(J-17)のPGMEA10重量%溶液を得た。また、樹脂(J-13)は、反応液を水で再沈し、乾燥後、PEGMAで10質量%溶液としたものを用いた。
合成に用いたアミノ基含有樹脂は、以下に示すとおりである。
SP-003(ポリエチレンイミン(日本触媒製) 数平均分子量300)
SP-006(ポリエチレンイミン(日本触媒製) 数平均分子量600)
SP-012(ポリエチレンイミン(日本触媒製) 数平均分子量1,200)
SP-018(ポリエチレンイミン(日本触媒製) 数平均分子量1,800)
SP-020(ポリエチレンイミン(日本触媒製) 数平均分子量10,000)
[樹脂(J-18)の合成]
ディーンスターク管を備えた反応器中、ポリアリルアミン(PAA-03、重量平均分子量3,000、日本触媒製)水溶液100g、トルエン500gを外温130℃で水分の留去が停止するまで還流し、その後、濃縮してトルエンを除いた。次に、ポリエステル(i-1)100gを混合し、120℃で3時間加熱した。その後、65℃まで放冷し、無水コハク酸(X前駆体x)3.8gを含有するプロピレングリコール1-モノメチルエーテル2-アセテート(以下、PGMEAとよぶ)200gをゆっくり添加し2時間攪拌した。その後、PGMEAを添加し、樹脂(J-18)のPGMEA10重量%溶液を得た。
[樹脂(J-19)~(J-26)の合成]
表2及び表3に記載の如き、アミノ基含有樹脂と、X前駆体xと、前記合成例1~13で得たポリエステルと、を用いた他は、合成例32同様に合成を行い、樹脂(J-19)~(J-26)のPGMEA10重量%溶液を得た。
合成に用いたアミノ基含有樹脂は、以下に示すとおりである。
PAA-01(ポリアリルアミン(日東紡製)重量平均分子量1,000)
PAA-03(ポリアリルアミン(日東紡製)重量平均分子量3,000)
PAA-05(ポリアリルアミン(日東紡製)重量平均分子量5,000)
PAA-08(ポリアリルアミン(日東紡製)重量平均分子量8,000)
PAA-15(ポリアリルアミン(日東紡製)重量平均分子量15,000)
[樹脂(J-27)の合成]
モノマー(B)0.50g(3.5mmol)、マクロモノマー(i-14)55g(23mmol)、メタクリル酸2-(N,N-ジメチルアミノエチル)(9.6mmol)1.50g、ドデカンチオール0.2g(1.0mmol)をジメチルスルホキシド200gとN-メチルピロリドン100gの混合溶媒に溶解させた。80℃に加熱後、V-601を0.1g添加し3時間撹拌した。その後、V-601を0.1g添加し、3時間撹拌後、放冷した。得られた溶液を水4000Lに1時間かけて滴下し、析出した樹脂を濾過で採取した。乾燥後、1-メトキシ-2-プロパノールに溶解させ、10質量%溶液を得た。
合成スキームを以下に示す。
[比較用樹脂(J-28)の合成]
メタクリル酸0.50g(5.8mmol)、マクロモノマー(i-14)55g(23mmol)、メタクリル酸2-(N,N-ジメチルアミノエチル)(9.6mmol)1.50g、ドデカンチオール0.2g(1.0mmol)を1-メトキシ-2-プロパノール132gの混合溶媒に溶解させた。80℃に加熱後、V-601を0.1g添加し3時間撹拌した。その後、V-601を0.1g添加し、3時間撹拌後、放冷した。得られた溶液に1-メトキシ-2-プロパノールを添加し、10質量%溶液を得た。
合成スキームを以下に記す。
[比較用樹脂(J-29)~(J-31)の合成]
合成例15、34および39において、X前駆体xを添加しなかった以外は同様の操作を行い、比較用樹脂(J-29)~(J-31)を得た。
得られた樹脂(J-1)~(J-27)、比較例樹脂(J-28)~(J-31)の酸価及びアミン価を既述の方法により測定した。結果を表2及び表3に併記する。
これらの測定結果より、中間体酸価と目的樹脂酸価の側鎖にpKaが14以下である官能基が存在することが確認できる。
樹脂(J-1)~(J-6)、(J-14)~(J-19)、(J-29)及び(J-30)(すべて10wt%プロピレングリコールモノメチルエーテルアセテート溶液)を5℃で2日放置し、溶液から固体が析出しているかどうかを目視で確認した。その結果を下記表4に示す。
下記表4に明らかなように、本発明の樹脂は、ポリカプロラクトン鎖を有しているにもかかわらず、低温での溶剤溶解性に優れていることが分かった。
〔A1.硬化性組成物の調製〕
ここでは、液晶表示素子用途のカラーフィルタ形成用として顔料を含有する硬化性組成物を調整した例を挙げて説明する。
顔料分散液の調製
顔料としてC.I.ピグメントグリーン36(PG36)を40質量部(平均粒子径60nm)、樹脂(J-1)溶液200質量部(固形分換算20質量部)からなる混合液を、ビーズミル(ジルコニアビーズ0.3mm)により3時間混合・分散して、顔料分散液を調製した。顔料分散液について、顔料の平均粒径を動的光散乱法(Microtrac Nanotrac UPA-EX150(日機装社製)を用いて、P1を更に希釈することなく測定した)により測定したところ、25nmであった。
顔料分散液の調製
表5に記載の顔料を40質量部(平均粒子径60nm)、前記樹脂(J-1)~(J-31)のPGMEA10重量%溶液180質量部(固形分換算18質量部)にPGMEAを添加して230質量部にした混合液を、ビーズミル(ジルコニアビーズ0.3mm)により3時間混合・分散して、顔料分散液を調製した。顔料分散液について、顔料の平均粒径を動的光散乱法(Microtrac Nanotrac UPA-EX150(日機装社製)を用いて、P1を更に希釈することなく測定した)により測定し、表5に結果を示した。
前記分散処理した顔料分散液を用いて下記組成比となるよう撹拌混合して硬化性組成物溶液を調製した。
・前記顔料分散液 600質量部
・光重合開始剤(2,2’-ビス(2-クロロフェニル)-4,4’,5,5’
-テトラフェニル-1,2’-ビイミダゾール) 30質量部
・ペンタエリスリトールテトラアクリレート 50質量部
・アルカリ可溶性樹脂(ベンジルメタクリレート/メタクリル酸/ヒドロキシエチルメタクリレート共重合体、mol比:80/10/10、Mw:10000) 5質量部
・溶媒:プロピレングリコール1-モノメチルエーテル-2-アセテート 900質量部
・基板密着剤(3-メタクリロキシプロピルトリメトキシシラン) 1質量部
・(F)増感剤(下記化合物α) 15質量部
・(G)共増感剤(2-メルカプトベンゾイミダゾール) 15質量部
A2-1.硬化性組成物層の形成
上記顔料を含有する硬化性組成物をレジスト溶液として、550mm×650mmのガラス基板に下記条件でスリット塗布した後、10分間そのままの状態で待機させ、真空乾燥とプレベーク(prebake)(100℃80秒)を施して硬化性組成物塗布膜(硬化性組成物層)を形成した。
・塗布ヘッド先端の開口部の間隙: 50μm
・塗布速度: 100mm/秒
・基板と塗布ヘッドとのクリヤランス: 150μm
・乾燥膜厚 1.75μm
・塗布温度: 23℃
その後、2.5kWの超高圧水銀灯を用いて硬化性組成物塗布膜を、線幅20μmのテスト用フォトマスクを用いてパターン状に露光し、露光後、塗布膜の全面を有機系現像液(商品名:CD、富士フイルムエレクトロニクスマテリアルズ(株)製)の10%水溶液で被い、60秒間静止した。
静止後、純水をシャワー状に噴射して現像液を洗い流し、かかる露光(光硬化)処理及び現像処理を施した塗布膜を220℃のオーブンにて1時間加熱した(ポストベーク)。これにより、ガラス基板上に硬化性組成物塗布膜(着色層)を形成してなるカラーフィルタを得た。
〔A3.性能評価〕
上記で調製された硬化性組成物からなる塗布液の保存安定性、及び硬化性組成物を用いてガラス基板上に形成された硬化性組成物塗布膜(着色層)のコントラスト、現像性、さらに、パターン断面形状を下記のようにして評価した。結果を表6に示す。
前記にて調製された硬化性組成物(塗布液)を室温で1ケ月保存した後、液の粘度を測定し下記の基準に従って評価した。
-評価基準-
○:粘度上昇は認められなかった。
△:5%以上10%未満の粘度上昇が認められた。
×:10%以上の粘度上昇が認められた。
カラーフィルタを2枚の偏光フィルムの間に挟み、偏光フィルムの偏光軸が平行な場合と垂直な場合の透過光の輝度を、色彩輝度計を使用して測定し、コントラスト比を求めた。コントラスト比が高いほど、液晶ディスプレイ用カラーフィルタとして良好な性能を示す。
ポストベーク後の基板表面及び断面形状を、光学顕微鏡及びSEM写真観察により確認することにより、現像性、パターン断面形状、基板密着性を評価した。評価方法・評価基準の詳細は以下の通りである。
露光工程において、光が照射されなかった領域(未露光部)の残渣の有無を観察し、現像性を評価した。
-評価基準-
○:未露光部には、残渣がまったく確認されなかった。
△:未露光部に、残渣がわずかに確認されたが、実用上問題のない程度であった。
×:未露光部に、残渣が著しく確認された。
基板密着性の評価として、パターン欠損が発生しているか否かを観察した。これらの評価項目については、下記基準に基づいて評価を行った
-評価基準-
○:パターン欠損がまったく観察されなかった。
△:パターン欠損がほとんど観察されなかったが、一部分欠損が観察された。
×:パターン欠損が著しく観察された。
形成されたパターンの断面形状を観察した。パターン断面形状は順テーパーが最も好ましく、矩形が次に好ましい。逆テーパーは好ましくない。
これらの評価結果を下記表6に示す。
〔B1.レジスト液の調製〕
下記組成の成分を混合して溶解し、レジスト液を調製した。
<レジスト液の組成>
・プロピレングリコールモノメチルエーテルアセテート 19.20質量部
(PGMEA:溶剤)
・乳酸エチル 36.67質量部
・樹脂(メタクリル酸ベンジル/メタクリル酸/メタクリル酸-2-ヒドロキシ
エチル共重合体(モル比=60/22/18、重量平均分子量:15,000
数平均分子量:8,000)の40%PGMEA溶液) 30.51質量部
・エチレン性不飽和二重結合含有化合物
(ジペンタエリスリトールヘキサアクリレート) 12.20質量部
・重合禁止剤(p-メトキシフェノール) 0.0061質量部
・フッ素系界面活性剤(F-475、大日本インキ化学工業(株)製) 0.83質量部
・光重合開始剤(トリハロメチルトリアジン系の光重合開始剤) 0.586質量部
(TAZ-107、みどり化学社製)
6inch シリコンウエハをオーブン中で200℃のもと30分加熱処理した。次いで、このシリコンウエハ上に前記レジスト液を乾燥膜厚が1.5μmになるように塗布し、更に220℃のオーブン中で1時間加熱乾燥させて下塗り層を形成し、下塗り層付シリコンウエハ基板を得た。
顔料としてC.I.ピグメントグリーン36(PG36)及びC.I.ピグメントイエロー139(PY139)の混合物(質量比 70:30)40質量部(平均粒子径65nm)、樹脂(J-1)溶液160質量部(固形分換算16質量部)からなる混合液を、ビーズミル(ジルコニアビーズ、直径0.3mm)により3時間混合・分散して、顔料分散液を調製した。
顔料分散液について、顔料の平均粒径を動的光散乱法により実施例1と同様に測定したところ、30nmであった。
前記分散処理した顔料分散液を用いて下記組成比となるよう撹拌混合して硬化性組成物溶液を調製した。
・着色剤(前記顔料分散液) 600質量部
・光重合開始剤(オキシム系光重合開始剤)
(CGI-124、チバ・スペシャルティ・ケミカルズ社製) 30質量部
・TO-1382(東亞合成(株)製) 25質量部
・ジペンタエリスリトールヘキサアクリレート 30質量部
・溶媒(PGMEA) 900質量部
・基板密着剤(3-メタクリロキシプロピルトリメトキシシラン) 1質量部
<パターン形成>
上記のように調製した硬化性組成物を、前記B2.で得られた下塗り層付シリコンウエハの下塗り層上に塗布し、着色層(塗布膜)を形成した。そして、この塗布膜の乾燥膜厚が0.5μmになるように、100℃のホットプレートを用いて120秒間加熱処理(プリベーク)を行なった。
次いで、i線ステッパー露光装置FPA-3000i5+(Canon(株)製)を使用して365nmの波長でパターンが2μm四方のIslandパターンマスクを通して50~1200mJ/cm2の種々の露光量で露光した。
その後、照射された塗布膜が形成されているシリコンウエハー基板をスピン・シャワー現像機(DW-30型、(株)ケミトロニクス製)の水平回転テーブル上に載置し、CD-2000(富士フイルムエレクトロニクスマテリアルズ(株)製)を用いて23℃で60秒間パドル現像を行ない、シリコンウエハー基板に着色パターンを形成した。
その後、測長SEM「S-9260A」(日立ハイテクノロジーズ(株)製)を用いて、着色パターンのサイズを測定した。パターン線幅が2μmとなる露光量を露光感度として評価した。
露光工程において、光が照射されなかった領域(未露光部)の残渣の有無を観察し、現像性を評価した。
-評価基準-
○:未露光部には、残渣がまったく確認されなかった。
△:未露光部に、残渣がわずかに確認されたが、実用上問題のない程度であった。
×:未露光部に、残渣が著しく確認された。
基板密着性の評価として、パターン欠損が発生しているか否かを観察した。これらの評価項目については、下記基準に基づいて評価を行った
-評価基準-
○:パターン欠損がまったく観察されなかった。
△:パターン欠損がほとんど観察されなかったが、一部分欠損が観察された。
×:パターン欠損が著しく観察された。
形成されたパターンの断面形状を観察した。パターン断面形状は矩形が好ましく、逆テーパーは好ましくない。
前記B4.にて調製された硬化性組成物(塗布液)を室温で1ケ月保存した後、液の粘度を測定し下記判定基準に従って評価した。
-評価基準-
○:粘度上昇は認められなかった。
△:5%以上10%未満の粘度上昇が認められた。
×:10%以上の粘度上昇が認められた。
<色ムラ>
色ムラの評価は、輝度分布を下記方法で解析し、平均からのずれが±5%以内である画素が全画素数に占める割合をもとに行った。評価基準は以下の通りである。
輝度分布の測定方法について説明する。まず、硬化性組成物を、前記B2.と同様の方法で得られた下塗り層付ガラス板の下塗り層上に塗布し、着色層(塗布膜)を形成した。この塗布膜の乾燥膜厚が0.7μmになるように、100℃のホットプレートを用いて120秒間加熱処理(プリベーク)を行なった。この塗布済みガラス板の輝度分布を顕微鏡MX-50(オリンパス社製)にて撮影した画像を解析した。
-評価基準-
○:平均からのずれが±5%以内である画素が全画素数中の99%以上
△:平均からのずれが±5%以内である画素が全画素数中の95%以上99%未満
×:平均からのずれが±5%以内である画素が全画素数中の95%未満
これらの結果を下記表7に示す。
これらの結果より、実施例の硬化性組成物は、固体撮像素子用途のカラーフィルタを作製する場合においても、液晶表示素子用途のカラーフィルタを作製する場合と同様に、優れたパターン形成性が実現されることがわかった。
<高顔料濃度での顔料分散実験>
(顔料分散液の調製)
下記表8に記載の顔料を40質量部(平均粒子径60nm)、樹脂(PGMEA10重量%溶液150質量部(固形分換算15質量部)にPGMEAを添加して230質量部にした混合液を、ビーズミル(ジルコニアビーズ0.3mm)により3時間混合・分散して、顔料分散液を調製した。顔料分散液について、顔料の平均粒径を動的光散乱法(Microtrac Nanotrac UPA-EX150(日機装社製)を用いて、P1を更に希釈することなく測定した)により測定し、表8に結果を示した。
特に、粘度・粘度上昇抑制の観点から、特に、(J-1)、(J-2)、(J-3)、(J-4)、(J-5)、(J-10)、(J-11)及び(J-12)が好ましく、(J-1)、(J-2)、(J-3)、(J-4)、(J-10)、(J-11)及び(J-12)がさらに好ましく、(J-2)、(J-3)、(J-4)、(J-11)及び(J-12)が最も好ましい。つまり、窒素原子を有する主鎖部がポリエチレンイミンであることが好ましく、窒素原子を有する主鎖部が数平均分子量300~1,800のポリエチレンイミンであることがさらに好ましく、窒素原子を有する主鎖部が数平均分子量600~1,200のポリエチレンイミンであることがさらに好ましい。
<液晶表示素子用途のカラーフィルタ>
ここでは、液晶表示素子用途のカラーフィルタ形成用として顔料を含有する硬化性組成物を調整した例を挙げて説明する。
(着色硬化性組成物の調製)
・前記顔料分散液 600質量部
・光重合開始剤(表9に記載) 20質量部
・ペンタエリスリトールテトラアクリレート 25質量部
・アルカリ可溶性樹脂(表9に記載) 20質量部
・溶媒:プロピレングリコール1-モノメチルエーテル-2-アセテート 900質量部
・基板密着剤(3-メタクリロキシプロピルトリメトキシシラン) 1質量部
上記着色硬化性組成物をレジスト溶液として、550mm×650mmのガラス基板に下記条件でスリット塗布した後、真空乾燥とプリベーク(prebake)(100℃80秒)を施して、着色硬化性組成物の塗布膜(硬化性組成物層)を形成した。
・塗布ヘッド先端の開口部の間隙: 50μm
・塗布速度: 100mm/秒
・基板と塗布ヘッドとのクリヤランス: 150μm
・乾燥膜厚 1.75μm
・塗布温度: 23℃
その後、2.5kWの超高圧水銀灯を用いて、着色硬化性組成物の塗布膜を、線幅20μmのフォトマスクを用いて、日立ハイテクノロジー社製のLE4000Aでパターン状に 100mJ/cm2露光した。露光後、塗布膜の全面を無機系現像液(商品名:CDK-1、富士フイルムエレクトロニクスマテリアルズ(株)製)の1%水溶液で被い、60秒間静止した。
静止後、純水をシャワー状に噴射して現像液を洗い流し、かかる露光(光硬化)処理及び現像処理を施した塗布膜を220℃のオーブンにて1時間加熱した(ポストベーク)。これにより、ガラス基板上に着色硬化性組成物のパターン(着色層)を形成したカラーフィルタを得た。
上記で調製された着色硬化性組成物の保存安定性、現像性、露光感度及び着色硬化性組成物を用いてガラス基板上に形成された硬化性組成物塗布膜(着色層)のコントラスト、さらに、パターン断面形状を下記のようにして評価した。結果を表9に示す。
前記にようにして得られた着色硬化性組成物の、調製後1日経過したものと、1ヶ月経過したものの粘度をそれぞれ測定した。粘度の測定にはTV-22型粘度計コーンプレートタイプ(東機産業株式会社)を用いた。表9には、1日後の粘度と、1ヶ月後の粘度と、の差を示す。
粘度の値が小さいことで、顔料の分散性に優れることが分かり、また、粘度が小さく、かつ、経時による増粘度が小さいほど、顔料の分散安定性が良好であることを表す。
前記のようにして得られたカラーフィルタを2枚の偏光板の間に挟み、偏光板の偏光軸が平行な場合と垂直な場合の透過光の輝度を、色彩輝度計(トプコン社製色彩輝度計BM-7)を使用して測定し、平行な場合の輝度を垂直な場合の輝度で除してコントラストを求めた。コントラストが高いほど、液晶表示装置用カラーフィルタとして良好な性能を示す。
前記のようにして現像を行った後、20個の現像部(未露光部)をSEMで観察し、残渣の個数を数えた。
残渣が少ないほど現像性が良好であることを示す。
4.基板密着性
基板密着性の評価として、パターン欠損が発生しているか否かを観察した。これらの評価項目については、下記基準に基づいて評価を行った
-評価基準-
○:パターン欠損がまったく観察されなかった。
△:パターン欠損がほとんど観察されなかったが、一部分欠損が観察された。
×:パターン欠損が著しく観察された。
形成されたパターンの断面形状を観察した。パターン断面形状は矩形が好ましく、逆テーパーは好ましくない。
6.露光感度
前記露光工程において、10mJ/cm2~500mJ/cm2の範囲で種々の露光量に変更して露光を行い、ポストベーク後のパターン線幅が20μmとなる露光量を露光感度として評価した。露光感度の値が小さいほど感度が高いことを示す。
また、実施例はいずれも、パターン断面形状においても優れたカラーフィルタが得られたことが判る。
<固体撮像素子用途のカラーフィルタ形成>
以下、固体撮像素子用途のカラーフィルタ形成用として、着色硬化性組成物を調製した例を挙げて説明する。
下記組成の成分を混合して溶解し、レジスト液を調製した。
<レジスト液の組成>
・溶剤:プロピレングリコールモノメチルエーテルアセテート 19.20部
・溶剤:乳酸エチル 36.67部
・アルカリ可溶性樹脂:メタクリル酸ベンジル/メタクリル酸/メタクリル酸
-2-ヒドロキシエチル共重合体(モル比=60/22/18、重量平均
分子量15,000 数平均分子量)の40%PGMEA溶液 30.51部
・エチレン性不飽和二重結合含有化合物:ジペンタエリスリトールヘキサア
クリレート 12.20部
・重合禁止剤:p-メトキシフェノール 0.0061部
・フッ素系界面活性剤:F-475、DIC(株)製 0.83部
・光重合開始剤:トリハロメチルトリアジン系の光重合開始剤 0.586部
(TAZ-107、みどり化学社製)
6inchシリコンウエハをオーブン中で200℃のもと30分加熱処理した。次いで、このシリコンウエハ上に前記レジスト液を乾燥膜厚が1.5μmになるように塗布し、更に220℃のオーブン中で1時間加熱乾燥させて下塗り層を形成し、下塗り層付シリコンウエハ基板を得た。
前記顔料分散液(D-1)~(D-18)を用いて、下記組成比となるよう撹拌混合して着色硬化性組成物を調製した。
・前記顔料分散液 600部
・光重合開始剤 (表9に記載) 20部
・重合性化合物:ジペンタエリスリトールヘキサアクリレート 25部
・アルカリ可溶性樹脂(表9に記載) 20部
・溶剤:PGMEA 900部
<パターン形成>
上記のように調製した着色硬化性組成物を、前記のようにして得られた下塗り層付シリコンウエハの下塗り層上に塗布し、着色層(塗布膜)を形成した。そして、この塗布膜の乾燥膜厚が0.5μmになるように、100℃のホットプレートを用いて120秒間加熱処理(プリベーク)を行なった。
その後、照射された塗布膜が形成されているシリコンウエハ基板をスピン・シャワー現像機(DW-30型、(株)ケミトロニクス製)の水平回転テーブル上に載置し、CD-2000(富士フイルムエレクトロニクスマテリアルズ(株)製)を用いて23℃で60秒間パドル現像を行ない、シリコンウエハ基板に着色パターンを形成した。
その後、測長SEM「S-9260A」(日立ハイテクノロジーズ(株)製)を用いて、着色パターンのサイズを測定した。パターンサイズが1.2μmとなる露光量を露光感度として評価した。
前述のようにして調製された着色硬化性組成物の分散性、分散安定性、露光感度、塗布性、及び現像性を前記と同様にして評価し、表10に結果を示した。
また、上記のようにして得られたカラーフィルタの色ムラについて下記のように評価し、表10に結果を示した。
得られた着色硬化性組成物の調製後1日経過したものと1ヶ月経過したものの粘度をそれぞれ測定した。粘度の測定にはTV-22型粘度計コーンプレートタイプ(東機産業株式会社)を用いた。表10には、1日後の粘度と、1ヶ月後の粘度と、の差を示す。
粘度の値が小さいことで、顔料の分散性に優れることが分かり、また、粘度が小さく、かつ、経時による増粘度が小さいほど、顔料の分散安定性が良好であることを表す。
前記で得られたカラーフィルタの色ムラの評価は、輝度分布を下記方法で解析し、平均からのずれが±5%以内である画素が全画素数に占める割合をもとに行った。評価基準は以下の通りである。
輝度分布の測定方法について説明する。まず、得られた着色硬化性組成物を、前記の方法で作製した下塗り層付ガラス板の下塗り層上に塗布し、着色層(塗膜)を形成した。
この塗膜の乾燥膜厚が0.7μmになるように、100℃のホットプレートを用いて120秒間加熱処理(プリベーク)を行なった。
この塗布済みガラス板の輝度分布を、顕微鏡MX-50(オリンパス社製)にて撮影した画像を解析し、平均からのずれが±5%以内である画素の割合(百分率)を算出した。この値が高いほど色ムラが小さく良好であることを示す。
前記のように現像を行った後、現像部(未露光部)をSEMで20個観察し、残渣の個数を数えた。
基板密着性の評価として、パターン欠損が発生しているか否かを観察した。これらの評価項目については、下記基準に基づいて評価を行った
-評価基準-
○:パターン欠損がまったく観察されなかった。
△:パターン欠損がほとんど観察されなかったが、一部分欠損が観察された。
×:パターン欠損が著しく観察された。
形成されたパターンの断面形状を観察した。パターン断面形状は矩形が好ましく、逆テーパーは好ましくない。
6.露光感度
露光量を10~500mJ/cm2の種々の露光量に変更して露光し、ポストベイク後のパターン線幅が1.2μmとなる露光量を露光感度として評価した。露光感度の値が小さいほど感度が高いことを示す。
Claims (14)
- (i)窒素原子を有する主鎖部と、(ii)pKaが14以下である官能基を有し、該主鎖部に存在する窒素原子と結合する基「X」と、を有し、(iii)数平均分子量が500~1,000,000であるオリゴマー鎖又はポリマー鎖「Y」を側鎖に有する樹脂。
- 前記樹脂の(i)窒素原子を有する主鎖部が、アミノ基を有するオリゴマー又はポリマーを含むことを特徴とする請求項1に記載の樹脂。
- 前記樹脂の(i)窒素原子を有する主鎖部が、ポリ(低級アルキレンイミン)、ポリアリルアミン、ポリジアリルアミン、メタキシレンジアミン-エピクロルヒドリン重縮合物、ポリビニルアミン、3-ジアルキルアミノプロピル(メタ)アクリル酸アミド共重合体、及び、(メタ)アクリル酸2-ジアルキルアミノエチル共重合体から選択される1種以上を含むことを特徴とする請求項1に記載の樹脂。
- 前記樹脂の(ii)pKaが14以下である官能基が、カルボン酸、スルホン酸及び-COCH2CO-から選択される官能基であることを特徴とする請求項1に記載の樹脂。
- 前記樹脂が、主鎖部に一級又は二級アミノ基を有する樹脂に、前記pKaが14以下である官能基を有する基「X」の前駆体xと、前記数平均分子量が500~1,000,000であるオリゴマー鎖又はポリマー鎖「Y」の前駆体yとを反応させてなる樹脂であることを特徴とする請求項1に記載の樹脂。
- 主鎖部に一級又は二級アミノ基を有する樹脂を合成し、その後、該樹脂にpKaが14以下である官能基を有する基「X」の前駆体xと、前記数平均分子量が500~1,000,000であるオリゴマー鎖又はポリマー鎖「Y」の前駆体yとを反応させることを含む請求項1に記載の樹脂の製造方法。
- (A)請求項1に記載の樹脂、(B)顔料、及び、(C)溶剤、を含有する顔料分散液。
- (A)請求項1に記載の樹脂、(B)顔料、(C)溶剤、(D)光重合開始剤、及び、(E)エチレン性不飽和二重結合を含有する化合物、を含有することを特徴とする着色硬化性組成物。
- さらに(F)アルカリ可溶性樹脂を含有することを特徴とする請求項11に記載の着色硬化性組成物。
- 支持体上に、請求項11に記載の着色硬化性組成物により形成された着色パターンを有するカラーフィルタ。
- 支持体上に、請求項11に記載の着色硬化性組成物を塗布して該硬化性組成物からなる着色層を形成することと、該着色層を、マスクを介してパターン露光することと、露光後の着色層を現像して着色パターンを形成することと、を含むことを特徴とするカラーフィルタの製造方法。
Priority Applications (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN2009801032878A CN101925636B (zh) | 2008-01-31 | 2009-01-29 | 树脂、颜料分散液、着色固化性组合物、使用其制造的滤色片及其制造方法 |
| EP09706745.8A EP2246385B1 (en) | 2008-01-31 | 2009-01-29 | Resin, pigment dispersion liquid, coloring curable composition, color filter produced by using the composition, and method for producing the color filter |
| US12/865,683 US8728687B2 (en) | 2008-01-31 | 2009-01-29 | Resin, pigment dispersion, colored curable composition, color filter produced using the same, and method for producing the same |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008021457 | 2008-01-31 | ||
| JP2008-021457 | 2008-01-31 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2009096452A1 true WO2009096452A1 (ja) | 2009-08-06 |
Family
ID=40912803
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2009/051430 WO2009096452A1 (ja) | 2008-01-31 | 2009-01-29 | 樹脂、顔料分散液、着色硬化性組成物、これを用いて製造されたカラーフィルタ及びその製造方法 |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US8728687B2 (ja) |
| EP (1) | EP2246385B1 (ja) |
| JP (1) | JP5371449B2 (ja) |
| KR (1) | KR101559828B1 (ja) |
| CN (1) | CN101925636B (ja) |
| TW (1) | TWI460208B (ja) |
| WO (1) | WO2009096452A1 (ja) |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2009258668A (ja) * | 2008-03-17 | 2009-11-05 | Fujifilm Corp | 着色硬化性組成物、カラーフィルタ、及びカラーフィルタの製造方法 |
| US20100248095A1 (en) * | 2009-03-31 | 2010-09-30 | Fujifilm Corporation | Colored curable composition for color filter, color filter and method for producing the same, and solid state imaging device |
| WO2011037195A1 (ja) * | 2009-09-25 | 2011-03-31 | 東洋インキ製造株式会社 | 着色組成物及びカラーフィルタ |
| CN110531583A (zh) * | 2019-09-14 | 2019-12-03 | 浙江福斯特新材料研究院有限公司 | 感光性树脂组合物、干膜抗蚀层 |
Families Citing this family (142)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP5270205B2 (ja) * | 2008-03-24 | 2013-08-21 | 株式会社Dnpファインケミカル | インクジェット記録用油性緑色インク組成物およびインクジェット記録用油性インクセット |
| JP4835718B2 (ja) * | 2008-03-31 | 2011-12-14 | 大日本印刷株式会社 | カラーフィルタ用ネガ型レジスト組成物、カラーフィルタ及び液晶表示装置 |
| JP4826614B2 (ja) * | 2008-09-30 | 2011-11-30 | 大日本印刷株式会社 | カラーフィルタ用顔料分散液、カラーフィルタ用ネガ型レジスト組成物、カラーフィルタ及び液晶表示装置 |
| JP5668282B2 (ja) * | 2009-09-29 | 2015-02-12 | 大日本印刷株式会社 | カラーフィルタ用顔料分散液、カラーフィルタ用ネガ型レジスト組成物、カラーフィルタ及び液晶表示装置 |
| ES2666164T3 (es) * | 2009-11-20 | 2018-05-03 | Mitsui Chemicals, Inc. | Composición para la reparación de tejidos duros |
| JP2012003225A (ja) | 2010-01-27 | 2012-01-05 | Fujifilm Corp | ソルダーレジスト用重合性組成物及びソルダーレジストパターンの形成方法 |
| TWI543993B (zh) | 2010-03-25 | 2016-08-01 | 富士軟片股份有限公司 | 黑色硬化型組成物、用於固態攝像元件的遮光彩色濾光片及其製造方法、固態攝像元件、晶圓級透鏡及攝影模組 |
| TWI412795B (zh) * | 2010-05-11 | 2013-10-21 | Hon Hai Prec Ind Co Ltd | 彩色濾光片的製造方法 |
| EP2392621A3 (en) | 2010-06-01 | 2013-01-09 | FUJIFILM Corporation | Pigment dispersion composition, red colored composition, colored curable composition, color filter for a solid state imaging device and method for producing the same, and solid state imaging device |
| WO2012029481A1 (ja) * | 2010-08-31 | 2012-03-08 | 富士フイルム株式会社 | 感光性組成物、感光性フィルム、感光性積層体、永久パターン形成方法、及びプリント基板 |
| JP2012073600A (ja) * | 2010-08-31 | 2012-04-12 | Fujifilm Corp | 感光性組成物、並びに、感光性フィルム、永久パターン、永久パターン形成方法、及びプリント基板 |
| US8655093B2 (en) | 2010-09-02 | 2014-02-18 | Edge 3 Technologies, Inc. | Method and apparatus for performing segmentation of an image |
| JP5417364B2 (ja) | 2011-03-08 | 2014-02-12 | 富士フイルム株式会社 | 固体撮像素子用硬化性組成物、並びに、これを用いた感光層、永久パターン、ウエハレベルレンズ、固体撮像素子、及び、パターン形成方法 |
| JP5745458B2 (ja) * | 2011-05-18 | 2015-07-08 | 富士フイルム株式会社 | 分散組成物、これを用いた硬化性組成物、透明膜、マイクロレンズ、及び固体撮像素子、並びに透明膜の製造方法、マイクロレンズの製造方法、及び固体撮像素子の製造方法 |
| JP2013064993A (ja) * | 2011-08-31 | 2013-04-11 | Fujifilm Corp | カラーフィルタの製造方法、カラーフィルタ、及び固体撮像素子 |
| JP5734913B2 (ja) * | 2011-08-31 | 2015-06-17 | 富士フイルム株式会社 | 感放射線性組成物、パターン形成方法、カラーフィルタ及びその製造方法、並びに、固体撮像素子 |
| EP2715416B1 (en) | 2011-09-14 | 2019-10-30 | FUJIFILM Corporation | Colored radiation-sensitive composition for color filter, pattern forming method, color filter and method of producing the same, and solid-state image sensor |
| JP5976523B2 (ja) | 2011-12-28 | 2016-08-23 | 富士フイルム株式会社 | 光学部材セット及びこれを用いた固体撮像素子 |
| JP5922013B2 (ja) | 2011-12-28 | 2016-05-24 | 富士フイルム株式会社 | 光学部材セット及びこれを用いた固体撮像素子 |
| JP5934664B2 (ja) | 2012-03-19 | 2016-06-15 | 富士フイルム株式会社 | 着色感放射線性組成物、着色硬化膜、カラーフィルタ、着色パターン形成方法、カラーフィルタの製造方法、固体撮像素子、及び画像表示装置 |
| JP5775479B2 (ja) | 2012-03-21 | 2015-09-09 | 富士フイルム株式会社 | 着色感放射線性組成物、着色硬化膜、カラーフィルタ、パターン形成方法、カラーフィルタの製造方法、固体撮像素子、及び画像表示装置 |
| WO2014054539A1 (ja) * | 2012-10-03 | 2014-04-10 | 大日本印刷株式会社 | 金属粒子分散体、並びに、当該金属粒子分散体を用いた物品、焼結膜及び焼結膜の製造方法 |
| KR20150072428A (ko) | 2012-11-30 | 2015-06-29 | 후지필름 가부시키가이샤 | 경화성 수지 조성물, 이것을 사용한 이미지 센서칩의 제조 방법 및 이미지 센서칩 |
| JP6140593B2 (ja) | 2012-11-30 | 2017-05-31 | 富士フイルム株式会社 | 硬化性樹脂組成物、これを用いたイメージセンサチップの製造方法及びイメージセンサチップ |
| JP6170673B2 (ja) | 2012-12-27 | 2017-07-26 | 富士フイルム株式会社 | カラーフィルタ用組成物、赤外線透過フィルタ及びその製造方法、並びに赤外線センサー |
| US20140374645A1 (en) * | 2013-06-24 | 2014-12-25 | Fujifilm Corporation | Magnetic recording medium and coating composition for magnetic recording medium |
| JP6162084B2 (ja) | 2013-09-06 | 2017-07-12 | 富士フイルム株式会社 | 着色組成物、硬化膜、カラーフィルタ、カラーフィルタの製造方法、固体撮像素子、画像表示装置、ポリマー、キサンテン色素 |
| TWI507511B (zh) | 2013-11-05 | 2015-11-11 | Ind Tech Res Inst | 負介電異方性液晶化合物、液晶顯示器、與光電裝置 |
| DE102014205680A1 (de) * | 2014-03-26 | 2015-10-01 | Evonik Degussa Gmbh | Dispergierharze |
| JP5916824B2 (ja) * | 2014-03-31 | 2016-05-11 | 富士フイルム株式会社 | 磁気記録媒体および磁気記録媒体用磁性塗料組成物 |
| JP2017519249A (ja) * | 2014-04-04 | 2017-07-13 | コーニング インコーポレイテッド | 接着性を改善するためのガラス表面の処理 |
| WO2015198422A1 (ja) * | 2014-06-25 | 2015-12-30 | 大日精化工業株式会社 | A-bブロックコポリマー、a-bブロックコポリマーの製造方法、樹脂処理顔料組成物、樹脂処理顔料組成物の製造方法、顔料分散体及び顔料分散液 |
| JP6175418B2 (ja) * | 2014-08-29 | 2017-08-02 | 富士フイルム株式会社 | 磁気テープ |
| US9984711B2 (en) * | 2014-09-30 | 2018-05-29 | Fujifilm Corporation | Magnetic recording medium and coating composition for magnetic recording medium |
| CN104530313B (zh) * | 2014-12-15 | 2018-12-25 | 京东方科技集团股份有限公司 | 染料化合物及其制备方法、着色剂、感光树脂组合物、滤光片 |
| JP6260581B2 (ja) * | 2014-12-23 | 2018-01-17 | ベーイプシロンカー−シェミー ゲーエムベーハーBYK−Chemie GmbH | 水溶性顔料親和性基と一緒に分散剤を含む着色料組成物 |
| JP6368643B2 (ja) * | 2014-12-26 | 2018-08-01 | 花王株式会社 | カラーフィルター用顔料分散体 |
| JP6608148B2 (ja) * | 2015-02-24 | 2019-11-20 | キヤノン株式会社 | 距離情報生成装置、撮像装置、距離情報生成方法および距離情報生成プログラム |
| EP3294813A1 (en) * | 2015-05-15 | 2018-03-21 | Cabot Corporation | Amphoteric polymers and use in inkjet ink compositions |
| JP6316248B2 (ja) | 2015-08-21 | 2018-04-25 | 富士フイルム株式会社 | 磁気テープおよびその製造方法 |
| JP6433394B2 (ja) * | 2015-09-08 | 2018-12-05 | 富士フイルム株式会社 | 磁気記録媒体 |
| JP6411981B2 (ja) * | 2015-09-30 | 2018-10-24 | 富士フイルム株式会社 | 塗布型磁気記録媒体製造用金属酸化物粒子分散物、塗布型磁気記録媒体の磁性層形成用組成物の製造方法、および塗布型磁気記録媒体の製造方法 |
| US10540996B2 (en) | 2015-09-30 | 2020-01-21 | Fujifilm Corporation | Magnetic tape having characterized magnetic layer and magnetic tape device |
| JP6552402B2 (ja) | 2015-12-16 | 2019-07-31 | 富士フイルム株式会社 | 磁気テープ、磁気テープカートリッジ、磁気記録再生装置および磁気テープの製造方法 |
| US10403319B2 (en) | 2015-12-16 | 2019-09-03 | Fujifilm Corporation | Magnetic tape having characterized magnetic layer, tape cartridge, and recording and reproducing device |
| JP6430927B2 (ja) | 2015-12-25 | 2018-11-28 | 富士フイルム株式会社 | 磁気テープおよびその製造方法 |
| KR102158230B1 (ko) * | 2016-01-15 | 2020-09-21 | 토요잉크Sc홀딩스주식회사 | 고체 촬상 소자용 근적외선 흡수성 조성물 및 필터 |
| JP6427127B2 (ja) | 2016-02-03 | 2018-11-21 | 富士フイルム株式会社 | 磁気テープおよびその製造方法 |
| JP6465823B2 (ja) * | 2016-02-03 | 2019-02-06 | 富士フイルム株式会社 | 磁気テープおよびその製造方法 |
| JP7019607B2 (ja) * | 2016-02-16 | 2022-02-15 | ビーエーエスエフ ソシエタス・ヨーロピア | ポリエステル基を有するポリアルキレンイミン系ポリマー |
| JP6474748B2 (ja) | 2016-02-29 | 2019-02-27 | 富士フイルム株式会社 | 磁気テープ |
| JP6472764B2 (ja) | 2016-02-29 | 2019-02-20 | 富士フイルム株式会社 | 磁気テープ |
| JP6467366B2 (ja) | 2016-02-29 | 2019-02-13 | 富士フイルム株式会社 | 磁気テープ |
| JP6700915B2 (ja) * | 2016-03-31 | 2020-05-27 | 富士フイルム株式会社 | 磁気記録媒体および磁気記録媒体用組成物 |
| EP3452554A1 (en) * | 2016-05-05 | 2019-03-13 | 3M Innovative Properties Company | Compositions, method of making an article, and articles |
| JP6808969B2 (ja) * | 2016-05-13 | 2021-01-06 | 味の素株式会社 | ポリアリルアミン誘導体 |
| JP6556096B2 (ja) * | 2016-06-10 | 2019-08-07 | 富士フイルム株式会社 | 磁気テープおよび磁気テープ装置 |
| JP6534637B2 (ja) | 2016-06-13 | 2019-06-26 | 富士フイルム株式会社 | 磁気テープおよび磁気テープ装置 |
| JP6534969B2 (ja) * | 2016-06-22 | 2019-06-26 | 富士フイルム株式会社 | 磁気テープ |
| JP6556100B2 (ja) * | 2016-06-22 | 2019-08-07 | 富士フイルム株式会社 | 磁気テープ |
| JP6507126B2 (ja) | 2016-06-23 | 2019-04-24 | 富士フイルム株式会社 | 磁気テープおよび磁気テープ装置 |
| JP6496277B2 (ja) | 2016-06-23 | 2019-04-03 | 富士フイルム株式会社 | 磁気テープ |
| JP6556102B2 (ja) * | 2016-06-23 | 2019-08-07 | 富士フイルム株式会社 | 磁気テープおよび磁気テープ装置 |
| JP6549529B2 (ja) * | 2016-06-23 | 2019-07-24 | 富士フイルム株式会社 | 磁気テープおよび磁気テープ装置 |
| JP6717684B2 (ja) * | 2016-06-23 | 2020-07-01 | 富士フイルム株式会社 | 磁気テープおよび磁気テープ装置 |
| JP6549528B2 (ja) * | 2016-06-23 | 2019-07-24 | 富士フイルム株式会社 | 磁気テープおよび磁気テープ装置 |
| JP6498154B2 (ja) | 2016-06-23 | 2019-04-10 | 富士フイルム株式会社 | 磁気テープおよび磁気テープ装置 |
| JP6556101B2 (ja) * | 2016-06-23 | 2019-08-07 | 富士フイルム株式会社 | 磁気テープおよび磁気テープ装置 |
| JP6529933B2 (ja) | 2016-06-24 | 2019-06-12 | 富士フイルム株式会社 | 磁気テープ |
| JP2018025612A (ja) * | 2016-08-08 | 2018-02-15 | 株式会社Dnpファインケミカル | カラーフィルタ用着色組成物、カラーフィルタ及び表示装置 |
| JP6552467B2 (ja) * | 2016-08-31 | 2019-07-31 | 富士フイルム株式会社 | 磁気テープ |
| JP6556107B2 (ja) * | 2016-08-31 | 2019-08-07 | 富士フイルム株式会社 | 磁気テープ |
| JP6585570B2 (ja) | 2016-09-16 | 2019-10-02 | 富士フイルム株式会社 | 磁気記録媒体およびその製造方法 |
| JP6684203B2 (ja) | 2016-12-27 | 2020-04-22 | 富士フイルム株式会社 | 磁気テープ装置および磁気再生方法 |
| JP6588002B2 (ja) | 2016-12-27 | 2019-10-09 | 富士フイルム株式会社 | 磁気テープ装置および磁気再生方法 |
| JP2018106778A (ja) | 2016-12-27 | 2018-07-05 | 富士フイルム株式会社 | 磁気テープ装置および磁気再生方法 |
| JP6701072B2 (ja) | 2016-12-27 | 2020-05-27 | 富士フイルム株式会社 | 磁気テープ装置およびヘッドトラッキングサーボ方法 |
| JP6689223B2 (ja) * | 2017-02-20 | 2020-04-28 | 富士フイルム株式会社 | 磁気テープ |
| JP6689222B2 (ja) * | 2017-02-20 | 2020-04-28 | 富士フイルム株式会社 | 磁気テープ |
| JP6684235B2 (ja) | 2017-02-20 | 2020-04-22 | 富士フイルム株式会社 | 磁気テープ装置およびヘッドトラッキングサーボ方法 |
| JP6685248B2 (ja) | 2017-02-20 | 2020-04-22 | 富士フイルム株式会社 | 磁気テープ |
| JP6684236B2 (ja) | 2017-02-20 | 2020-04-22 | 富士フイルム株式会社 | 磁気テープ装置および磁気再生方法 |
| JP6684239B2 (ja) | 2017-02-20 | 2020-04-22 | 富士フイルム株式会社 | 磁気テープ |
| JP6602806B2 (ja) * | 2017-02-20 | 2019-11-06 | 富士フイルム株式会社 | 磁気テープ |
| JP6649297B2 (ja) | 2017-02-20 | 2020-02-19 | 富士フイルム株式会社 | 磁気テープ装置および磁気再生方法 |
| JP6684234B2 (ja) | 2017-02-20 | 2020-04-22 | 富士フイルム株式会社 | 磁気テープ装置および磁気再生方法 |
| JP6684238B2 (ja) | 2017-02-20 | 2020-04-22 | 富士フイルム株式会社 | 磁気テープ |
| JP6602805B2 (ja) | 2017-02-20 | 2019-11-06 | 富士フイルム株式会社 | 磁気テープ |
| JP6684237B2 (ja) | 2017-02-20 | 2020-04-22 | 富士フイルム株式会社 | 磁気テープ装置およびヘッドトラッキングサーボ方法 |
| JP6649298B2 (ja) | 2017-02-20 | 2020-02-19 | 富士フイルム株式会社 | 磁気テープ装置およびヘッドトラッキングサーボ方法 |
| JP6637456B2 (ja) | 2017-02-20 | 2020-01-29 | 富士フイルム株式会社 | 磁気テープ |
| CN106905688A (zh) * | 2017-03-17 | 2017-06-30 | 新疆广巨诚信防腐保温工程有限公司 | 一种聚氨酯用工业硅灰阻燃剂 |
| KR102241229B1 (ko) * | 2017-03-24 | 2021-04-16 | 후지필름 가부시키가이샤 | 감광성 착색 조성물, 경화막, 컬러 필터, 고체 촬상 소자 및 화상 표시 장치 |
| JP6649312B2 (ja) | 2017-03-29 | 2020-02-19 | 富士フイルム株式会社 | 磁気テープ装置および磁気再生方法 |
| JP6632561B2 (ja) | 2017-03-29 | 2020-01-22 | 富士フイルム株式会社 | 磁気テープ装置および磁気再生方法 |
| JP6632562B2 (ja) | 2017-03-29 | 2020-01-22 | 富士フイルム株式会社 | 磁気テープ |
| JP6649314B2 (ja) | 2017-03-29 | 2020-02-19 | 富士フイルム株式会社 | 磁気テープ装置およびヘッドトラッキングサーボ方法 |
| JP6649313B2 (ja) | 2017-03-29 | 2020-02-19 | 富士フイルム株式会社 | 磁気テープ装置および磁気再生方法 |
| JP6626031B2 (ja) | 2017-03-29 | 2019-12-25 | 富士フイルム株式会社 | 磁気テープ装置および磁気再生方法 |
| JP6626032B2 (ja) | 2017-03-29 | 2019-12-25 | 富士フイルム株式会社 | 磁気テープ装置および磁気再生方法 |
| JP6694844B2 (ja) | 2017-03-29 | 2020-05-20 | 富士フイルム株式会社 | 磁気テープ装置、磁気再生方法およびヘッドトラッキングサーボ方法 |
| JP6615814B2 (ja) | 2017-03-29 | 2019-12-04 | 富士フイルム株式会社 | 磁気テープ装置およびヘッドトラッキングサーボ方法 |
| JP6615815B2 (ja) | 2017-03-29 | 2019-12-04 | 富士フイルム株式会社 | 磁気テープ装置およびヘッドトラッキングサーボ方法 |
| JP6660336B2 (ja) | 2017-03-29 | 2020-03-11 | 富士フイルム株式会社 | 磁気テープ装置およびヘッドトラッキングサーボ方法 |
| JP6723198B2 (ja) | 2017-06-23 | 2020-07-15 | 富士フイルム株式会社 | 磁気テープおよび磁気テープ装置 |
| JP6691512B2 (ja) | 2017-06-23 | 2020-04-28 | 富士フイルム株式会社 | 磁気記録媒体 |
| JP6707061B2 (ja) | 2017-07-19 | 2020-06-10 | 富士フイルム株式会社 | 磁気記録媒体 |
| JP6723202B2 (ja) | 2017-07-19 | 2020-07-15 | 富士フイルム株式会社 | 磁気テープ |
| JP6717787B2 (ja) | 2017-07-19 | 2020-07-08 | 富士フイルム株式会社 | 磁気テープおよび磁気テープ装置 |
| JP6714548B2 (ja) | 2017-07-19 | 2020-06-24 | 富士フイルム株式会社 | 磁気テープおよび磁気テープ装置 |
| JP6717785B2 (ja) | 2017-07-19 | 2020-07-08 | 富士フイルム株式会社 | 磁気記録媒体 |
| US10839849B2 (en) | 2017-07-19 | 2020-11-17 | Fujifilm Corporation | Magnetic recording medium having characterized magnetic layer |
| JP6707060B2 (ja) | 2017-07-19 | 2020-06-10 | 富士フイルム株式会社 | 磁気テープ |
| JP6723203B2 (ja) * | 2017-07-19 | 2020-07-15 | 富士フイルム株式会社 | 磁気テープ |
| JP6678135B2 (ja) | 2017-07-19 | 2020-04-08 | 富士フイルム株式会社 | 磁気記録媒体 |
| JP6717786B2 (ja) | 2017-07-19 | 2020-07-08 | 富士フイルム株式会社 | 磁気テープおよび磁気テープ装置 |
| US10854227B2 (en) | 2017-07-19 | 2020-12-01 | Fujifilm Corporation | Magnetic recording medium having characterized magnetic layer |
| US10854230B2 (en) | 2017-07-19 | 2020-12-01 | Fujifilm Corporation | Magnetic tape having characterized magnetic layer |
| WO2019065200A1 (ja) | 2017-09-29 | 2019-04-04 | 富士フイルム株式会社 | 磁気テープおよび磁気記録再生装置 |
| JP6884874B2 (ja) | 2017-09-29 | 2021-06-09 | 富士フイルム株式会社 | 磁気テープおよび磁気記録再生装置 |
| US10515657B2 (en) | 2017-09-29 | 2019-12-24 | Fujifilm Corporation | Magnetic tape having characterized magnetic layer and magnetic recording and reproducing device |
| US10854233B2 (en) | 2017-09-29 | 2020-12-01 | Fujifilm Corporation | Magnetic recording medium having characterized magnetic layer and magnetic recording and reproducing device |
| US10854234B2 (en) | 2017-09-29 | 2020-12-01 | Fujifilm Corporation | Magnetic recording medium having characterized magnetic layer and magnetic recording and reproducing device |
| US10854231B2 (en) | 2017-09-29 | 2020-12-01 | Fujifilm Corporation | Magnetic recording medium having characterized magnetic layer and magnetic recording and reproducing device |
| US10978105B2 (en) * | 2017-09-29 | 2021-04-13 | Fujifilm Corporation | Magnetic recording medium having characterized magnetic layer and magnetic recording and reproducing device |
| US11138998B2 (en) | 2018-03-22 | 2021-10-05 | Fujifilm Corporation | Magnetic recording medium, magnetic recording and reproducing device and composition for magnetic recording medium including polyalkyleneimine compound |
| US11514944B2 (en) | 2018-03-23 | 2022-11-29 | Fujifilm Corporation | Magnetic tape and magnetic tape device |
| US11361792B2 (en) | 2018-03-23 | 2022-06-14 | Fujifilm Corporation | Magnetic tape having characterized magnetic layer and magnetic recording and reproducing device |
| US11514943B2 (en) | 2018-03-23 | 2022-11-29 | Fujifilm Corporation | Magnetic tape and magnetic tape device |
| US11361793B2 (en) | 2018-03-23 | 2022-06-14 | Fujifilm Corporation | Magnetic tape having characterized magnetic layer and magnetic recording and reproducing device |
| JP6830931B2 (ja) | 2018-07-27 | 2021-02-17 | 富士フイルム株式会社 | 磁気テープ、磁気テープカートリッジおよび磁気テープ装置 |
| JP6960383B2 (ja) * | 2018-08-31 | 2021-11-05 | 富士フイルム株式会社 | 磁気記録媒体、磁気記録再生装置および磁気記録媒体用組成物 |
| JP6784738B2 (ja) | 2018-10-22 | 2020-11-11 | 富士フイルム株式会社 | 磁気テープ、磁気テープカートリッジおよび磁気テープ装置 |
| JP6830945B2 (ja) | 2018-12-28 | 2021-02-17 | 富士フイルム株式会社 | 磁気テープ、磁気テープカートリッジおよび磁気テープ装置 |
| JP7042737B2 (ja) | 2018-12-28 | 2022-03-28 | 富士フイルム株式会社 | 磁気テープ、磁気テープカートリッジおよび磁気テープ装置 |
| JP7003073B2 (ja) | 2019-01-31 | 2022-01-20 | 富士フイルム株式会社 | 磁気テープ、磁気テープカートリッジおよび磁気テープ装置 |
| CN113683905A (zh) * | 2019-05-20 | 2021-11-23 | 浙江纳美新材料股份有限公司 | 一种纳米颜料晶型控制方法 |
| JP6778804B1 (ja) | 2019-09-17 | 2020-11-04 | 富士フイルム株式会社 | 磁気記録媒体および磁気記録再生装置 |
| CN115516039B (zh) * | 2020-05-22 | 2023-09-15 | 富士胶片株式会社 | 树脂组合物、膜、滤光器、固体摄像元件及图像显示装置 |
| JPWO2022168743A1 (ja) * | 2021-02-02 | 2022-08-11 | ||
| JPWO2022176787A1 (ja) * | 2021-02-18 | 2022-08-25 | ||
| WO2022176788A1 (ja) * | 2021-02-18 | 2022-08-25 | 富士フイルム株式会社 | 樹脂組成物、膜、光学フィルタ、固体撮像素子、画像表示装置、樹脂および樹脂の製造方法 |
Citations (120)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2833827A (en) | 1955-01-17 | 1958-05-06 | Bayer Ag | Tri (3, 5-di lower alkyl-4-hydroxy phenyl)-sulfonium chlorides and method of preparing same |
| US2848328A (en) | 1954-06-16 | 1958-08-19 | Eastman Kodak Co | Light sensitive diazo compound and binder composition |
| US2852379A (en) | 1955-05-04 | 1958-09-16 | Eastman Kodak Co | Azide resin photolithographic composition |
| US2940853A (en) | 1958-08-21 | 1960-06-14 | Eastman Kodak Co | Azide sensitized resin photographic resist |
| US3479185A (en) | 1965-06-03 | 1969-11-18 | Du Pont | Photopolymerizable compositions and layers containing 2,4,5-triphenylimidazoyl dimers |
| JPS4643946B1 (ja) | 1967-11-09 | 1971-12-27 | ||
| JPS4836281A (ja) | 1971-09-03 | 1973-05-28 | ||
| JPS4864183A (ja) | 1971-12-09 | 1973-09-05 | ||
| JPS4841708B1 (ja) | 1970-01-13 | 1973-12-07 | ||
| JPS4943191A (ja) | 1972-09-02 | 1974-04-23 | ||
| US3905815A (en) | 1971-12-17 | 1975-09-16 | Minnesota Mining & Mfg | Photopolymerizable sheet material with diazo resin layer |
| JPS5137193A (ja) | 1974-09-25 | 1976-03-29 | Toyo Boseki | |
| JPS5147334A (ja) | 1974-10-21 | 1976-04-22 | Hitachi Ltd | Batsufuamemoriseigyohoshiki |
| JPS5230490A (en) | 1975-09-03 | 1977-03-08 | Denki Kagaku Keiki Co Ltd | Gas concentration measuring electrode stable in air |
| US4069055A (en) | 1974-05-02 | 1978-01-17 | General Electric Company | Photocurable epoxy compositions containing group Va onium salts |
| US4069056A (en) | 1974-05-02 | 1978-01-17 | General Electric Company | Photopolymerizable composition containing group Va aromatic onium salts |
| JPS5421726A (en) | 1977-07-19 | 1979-02-19 | Canon Inc | Electrostatic printing method and device therefor |
| JPS5425957A (en) | 1977-07-29 | 1979-02-27 | Nippon Zeon Co Ltd | Curable rubber composition having excellent resistance to rancid gasoline |
| JPS5434327A (en) | 1977-08-12 | 1979-03-13 | Ciba Geigy Ag | Bispyridone dyes and use thereof in silver halide materials for photograph |
| DE2904626A1 (de) | 1978-02-08 | 1979-08-09 | Minnesota Mining & Mfg | Triarylsulfoniumkomplexsalze, verfahren zu ihrer herstellung und diese salze enthaltende photopolymerisierbare gemische |
| JPS5532070A (en) | 1978-08-29 | 1980-03-06 | Fuji Photo Film Co Ltd | Photosensitive resin composition |
| JPS5617654A (en) | 1979-07-25 | 1981-02-19 | Mitsubishi Electric Corp | Preventing apparatus for freezing of fountain nozzle |
| US4311783A (en) | 1979-08-14 | 1982-01-19 | E. I. Du Pont De Nemours And Company | Dimers derived from unsymmetrical 2,4,5,-triphenylimidazole compounds as photoinitiators |
| JPS57196231A (en) | 1981-05-20 | 1982-12-02 | Hoechst Ag | Mixture able to be polymerized by radiation and copying material mainly composed thereof |
| JPS5812577A (ja) | 1981-07-10 | 1983-01-24 | Mitsubishi Electric Corp | 変換器の制御装置 |
| JPS5849860A (ja) | 1981-09-18 | 1983-03-24 | Sanyo Electric Co Ltd | 太陽光エネルギ−変換器 |
| JPS595241A (ja) | 1982-06-21 | 1984-01-12 | ヘキスト・アクチエンゲゼルシヤフト | 放射線重合可能な混合物 |
| JPS595240A (ja) | 1982-06-21 | 1984-01-12 | ヘキスト・アクチエンゲゼルシヤフト | 放射線重合可能な混合物 |
| JPS5944615A (ja) | 1982-09-07 | 1984-03-13 | Furuno Electric Co Ltd | ジヤイロ装置 |
| JPS5953836A (ja) | 1982-09-21 | 1984-03-28 | Fuji Photo Film Co Ltd | 感光性平版印刷版 |
| EP0104143A1 (de) | 1982-09-18 | 1984-03-28 | Ciba-Geigy Ag | Diaryljodosylsalze enthaltende photopolymerisierbare Zusammensetzungen |
| JPS5971048A (ja) | 1982-10-18 | 1984-04-21 | Mitsubishi Chem Ind Ltd | 光重合系感光性組成物 |
| JPS59152396A (ja) | 1983-02-11 | 1984-08-31 | チバ−ガイギ− アクチエンゲゼルシヤフト | メタロセン,その製造方法およびメタロセンを含む光重合性組成物 |
| US4508811A (en) | 1983-01-17 | 1985-04-02 | U.S. Philips Corporation | Recording element having a pyrylium or thiopyrylium-squarylium dye layer and new pyrylium or thiopyrylium-squarylium compounds |
| JPS60239736A (ja) | 1984-05-14 | 1985-11-28 | Fuji Photo Film Co Ltd | 感光性組成物 |
| JPS6122048A (ja) | 1984-06-08 | 1986-01-30 | ヘキスト・アクチエンゲゼルシヤフト | 重合可能な化合物、その製法、およびこれを含有する放射線感性複写層 |
| JPS61151197A (ja) | 1984-12-20 | 1986-07-09 | チバ‐ガイギー アーゲー | チタノセン類およびこれらのチタノセン類を含有する照射重合開始剤 |
| JPS61166544A (ja) | 1985-01-18 | 1986-07-28 | Fuji Photo Film Co Ltd | 光可溶化組成物 |
| JPS61169837A (ja) | 1985-01-22 | 1986-07-31 | Fuji Photo Film Co Ltd | 光可溶化組成物 |
| JPS61169835A (ja) | 1985-01-22 | 1986-07-31 | Fuji Photo Film Co Ltd | 光可溶化組成物 |
| US4622286A (en) | 1985-09-16 | 1986-11-11 | E. I. Du Pont De Nemours And Company | Photoimaging composition containing admixture of leuco dye and 2,4,5-triphenylimidazolyl dimer |
| JPS6239417A (ja) | 1985-08-10 | 1987-02-20 | 川島 藤夫 | 折畳海苔束結束装置 |
| JPS6239418A (ja) | 1985-08-08 | 1987-02-20 | 川島 藤夫 | 海苔結束用紙テ−プ供給法及びその装置 |
| JPS6258241A (ja) | 1985-09-09 | 1987-03-13 | Fuji Photo Film Co Ltd | 感光性組成物 |
| JPS62143044A (ja) | 1985-11-20 | 1987-06-26 | サイカラー・インコーポレーテッド | 染料−ほう素化合物錯体を含有する光硬化性組成物およびその組成物を使用する感光性材料 |
| JPS62150242A (ja) | 1985-11-20 | 1987-07-04 | サイカラー・インコーポレーテッド | イオン性染料化合物を開始剤として含む感光性材料 |
| DE3604581A1 (de) | 1986-02-14 | 1987-08-20 | Basf Ag | 4-acylbenzylsulfoniumsalze, ihre herstellung sowie sie enthaltende photohaertbare gemische und aufzeichnungsmaterialien |
| DE3604580A1 (de) | 1986-02-14 | 1987-08-20 | Basf Ag | Haertbare mischungen, enthaltend n-sulfonylaminosulfoniumsalze als kationisch wirksame katalysatoren |
| JPS62212401A (ja) | 1986-03-14 | 1987-09-18 | Fuji Photo Film Co Ltd | 光重合性組成物 |
| JPS6341484A (ja) | 1986-08-01 | 1988-02-22 | チバ−ガイギ− ア−ゲ− | チタノセン、それらの製造法およびそれらを含有する組成物 |
| JPS6370243A (ja) | 1986-09-11 | 1988-03-30 | Fuji Photo Film Co Ltd | 感光性組成物 |
| JPS6330057B2 (ja) | 1977-07-15 | 1988-06-16 | Ici Plc | |
| US4760013A (en) | 1987-02-17 | 1988-07-26 | International Business Machines Corporation | Sulfonium salt photoinitiators |
| JPS63260909A (ja) | 1987-03-28 | 1988-10-27 | ヘキスト・アクチエンゲゼルシヤフト | 光重合性混合物及びこの混合物から製造される記録材料 |
| JPS63277653A (ja) | 1987-03-28 | 1988-11-15 | ヘキスト・アクチエンゲゼルシヤフト | 重合可能な化合物、これを含有する放射線重合可能な混合物及び放射線重合可能な記録材料 |
| JPS63298339A (ja) | 1987-05-29 | 1988-12-06 | Fuji Photo Film Co Ltd | 感光性組成物 |
| EP0297442A1 (de) | 1987-07-01 | 1989-01-04 | BASF Aktiengesellschaft | Sulfoniumsalze mit säurelabilen Gruppierungen |
| EP0297443A2 (de) | 1987-07-01 | 1989-01-04 | BASF Aktiengesellschaft | Strahlungsempfindliches Gemisch für lichtempfindliche Beschichtungsmaterialien |
| JPS6440337A (en) | 1987-08-06 | 1989-02-10 | Toyo Machinery & Metal | Molding number printing device |
| JPS6440336A (en) | 1987-08-05 | 1989-02-10 | Toppan Printing Co Ltd | Drying/deodorizing device of printer |
| JPH01105238A (ja) | 1987-03-28 | 1989-04-21 | Hoechst Ag | 光重合可能な混合物および光重合可能な記録材料 |
| JPH01152109A (ja) | 1987-12-09 | 1989-06-14 | Toray Ind Inc | 光重合性組成物 |
| JPH01165613A (ja) | 1987-11-16 | 1989-06-29 | Hoechst Ag | 重合可能な化合物、その放射線重合性混合物および放射線重合記録材料 |
| JPH01304453A (ja) | 1988-06-02 | 1989-12-08 | Toyobo Co Ltd | 光重合性組成物 |
| JPH02249A (ja) | 1987-12-01 | 1990-01-05 | Ciba Geigy Ag | チタノセンおよびそれを含有する光重合性組成物 |
| JPH024705A (ja) | 1988-03-24 | 1990-01-09 | Dentsply Internatl Inc | 光硬化性組成物用チタナート開始剤 |
| JPH0216765A (ja) | 1988-07-05 | 1990-01-19 | Fujitsu Ltd | 半導体装置 |
| JPH0225493A (ja) | 1988-05-21 | 1990-01-26 | Hoechst Ag | アルケニルホスホン酸エステルおよびアルケニルホスフイン酸エルテル、その製法並びに当該化合物を含有する放射線重合性混合物および記録材料 |
| JPH0232293A (ja) | 1988-07-22 | 1990-02-02 | Nippon Atom Ind Group Co Ltd | 沸騰水型原子炉 |
| EP0370693A2 (en) | 1988-11-21 | 1990-05-30 | Eastman Kodak Company | Novel onium salts and the use thereof as photoinitiators |
| JPH02150848A (ja) | 1988-12-02 | 1990-06-11 | Hitachi Ltd | 光退色性放射線感応性組成物およびそれを用いたパターン形成法 |
| US4933377A (en) | 1988-02-29 | 1990-06-12 | Saeva Franklin D | Novel sulfonium salts and the use thereof as photoinitiators |
| JPH02226149A (ja) | 1988-12-22 | 1990-09-07 | Hoechst Ag | 光重合性化合物、それを含む光重合性混合物及びそれから製造された光重合性複写材料 |
| EP0390214A2 (en) | 1989-03-31 | 1990-10-03 | E.F. Johnson Company | Method and apparatus for a distributive wide area network for a land mobile transmission trunked communication system |
| JPH02272009A (ja) | 1989-04-13 | 1990-11-06 | Mitsubishi Kasei Corp | ポリエステルマクロモノマー |
| JPH02296514A (ja) | 1989-05-12 | 1990-12-07 | Matsushita Electric Ind Co Ltd | 車両用サスペンション制御装置 |
| JPH04365049A (ja) | 1991-06-12 | 1992-12-17 | Fuji Photo Film Co Ltd | 感光性組成物 |
| JPH0583588A (ja) | 1991-09-24 | 1993-04-02 | Omron Corp | 画像処理装置 |
| US5227227A (en) | 1990-03-05 | 1993-07-13 | Johnson & Johnson Inc. | Non-woven fabric with a thermally activated adhesive surface, resulting product and applications thereof |
| EP0568993A2 (en) | 1992-05-06 | 1993-11-10 | Kyowa Hakko Kogyo Co., Ltd. | Chemical amplification resist composition |
| JPH061938A (ja) | 1992-06-19 | 1994-01-11 | Nippon Steel Corp | アルカリ現像型感光性カラーフィルター用インク及びそれを用いたカラーフィルター |
| JPH0619240A (ja) | 1992-06-30 | 1994-01-28 | Canon Inc | 画像形成装置 |
| JPH0619249A (ja) | 1992-06-30 | 1994-01-28 | Ricoh Co Ltd | 原稿給送装置 |
| JPH0629285A (ja) | 1992-07-08 | 1994-02-04 | Nec Corp | 半導体装置 |
| JPH06102669A (ja) | 1992-09-21 | 1994-04-15 | Goou Kagaku Kogyo Kk | 感光性樹脂組成物及びそれを用いたカラーフィルタ |
| JPH06157623A (ja) | 1992-08-14 | 1994-06-07 | Toyo Ink Mfg Co Ltd | 重合性組成物および重合方法 |
| JPH06175561A (ja) | 1992-12-04 | 1994-06-24 | Toyo Ink Mfg Co Ltd | ホログラム記録媒体及びそれを用いた体積位相型ホログラムの製造方法 |
| JPH06175554A (ja) | 1992-12-03 | 1994-06-24 | Toyo Ink Mfg Co Ltd | 体積位相型ホログラムの製造方法 |
| JPH06175553A (ja) | 1992-12-03 | 1994-06-24 | Toyo Ink Mfg Co Ltd | ホログラム記録媒体及びそれを用いた体積位相型ホログラムの製造方法 |
| JPH06175564A (ja) | 1992-12-04 | 1994-06-24 | Toyo Ink Mfg Co Ltd | ホログラム記録材料及びそれを用いた体積位相型ホログラムの製造方法 |
| JPH06348011A (ja) | 1993-06-04 | 1994-12-22 | Toyo Ink Mfg Co Ltd | 光重合性組成物 |
| JPH07128785A (ja) | 1993-11-02 | 1995-05-19 | Konica Corp | 画像形成材料及び画像形成方法 |
| JPH07140589A (ja) | 1993-11-19 | 1995-06-02 | Konica Corp | 画像形成材料および画像形成方法 |
| JPH07207012A (ja) * | 1994-01-10 | 1995-08-08 | Daicel Chem Ind Ltd | 顔料分散剤の製造方法 |
| JPH07292014A (ja) | 1994-04-25 | 1995-11-07 | Nippon Paint Co Ltd | 近赤外光重合性組成物 |
| JPH07306527A (ja) | 1994-05-11 | 1995-11-21 | Konica Corp | 画像形成材料及び画像形成方法 |
| JPH08108621A (ja) | 1994-10-06 | 1996-04-30 | Konica Corp | 画像記録媒体及びそれを用いる画像形成方法 |
| JPH09157374A (ja) * | 1995-12-08 | 1997-06-17 | Daicel Chem Ind Ltd | 顔料分散剤およびこれを含む塗料用または印刷インキ用組成物 |
| JPH09169821A (ja) | 1995-10-16 | 1997-06-30 | Ajinomoto Co Inc | 顔料分散剤 |
| JPH09176511A (ja) | 1995-12-21 | 1997-07-08 | Nippon Steel Chem Co Ltd | 顔料分散体組成物およびカラーレジストインキ |
| JPH09188686A (ja) | 1995-11-24 | 1997-07-22 | Ciba Geigy Ag | 光重合のための酸安定性硼酸塩 |
| JPH09188710A (ja) | 1995-11-24 | 1997-07-22 | Ciba Geigy Ag | モノボランからのボレート光開始剤 |
| JPH09188685A (ja) | 1995-11-24 | 1997-07-22 | Ciba Geigy Ag | 光重合のためのボレート補助開始剤 |
| JPH09281698A (ja) | 1996-04-11 | 1997-10-31 | Mitsubishi Chem Corp | カラーフィルター用光重合性組成物 |
| JP2764769B2 (ja) | 1991-06-24 | 1998-06-11 | 富士写真フイルム株式会社 | 光重合性組成物 |
| JPH11271969A (ja) | 1998-01-21 | 1999-10-08 | Mitsubishi Chemical Corp | 光重合性組成物及び感光性平版印刷版 |
| JP2000066385A (ja) | 1998-08-18 | 2000-03-03 | Ciba Specialty Chem Holding Inc | 高感度で高レジスト厚さのi線ホトレジスト用スルホニルオキシム類 |
| JP2000080068A (ja) | 1998-06-26 | 2000-03-21 | Ciba Specialty Chem Holding Inc | 新規o―アシルオキシム光開始剤 |
| JP2000131837A (ja) | 1998-08-17 | 2000-05-12 | Mitsubishi Chemicals Corp | 光重合性組成物、光重合性平版印刷版及び画像形成方法 |
| JP2000310808A (ja) | 1999-04-26 | 2000-11-07 | Canon Inc | 照明装置及びそれを用いた撮影装置 |
| JP2001125255A (ja) | 1999-10-27 | 2001-05-11 | Fuji Photo Film Co Ltd | 感光性平版印刷版 |
| JP2001132318A (ja) | 1999-10-29 | 2001-05-15 | Oi Seisakusho Co Ltd | 車両用開閉体の開閉装置 |
| JP2001272524A (ja) | 2000-03-24 | 2001-10-05 | Jsr Corp | カラーフィルタ用感放射線性組成物、カラーフィルタおよびカラー液晶表示装置 |
| JP2002107916A (ja) | 2000-09-27 | 2002-04-10 | Fuji Photo Film Co Ltd | 平版印刷版原版 |
| JP2002226587A (ja) * | 2001-01-29 | 2002-08-14 | Fuji Photo Film Co Ltd | 重合体、顔料分散組成物及び着色感光性組成物 |
| JP2004534797A (ja) | 2001-06-11 | 2004-11-18 | チバ スペシャルティ ケミカルズ ホールディング インコーポレーテッド | 組み合わされた構造を有するオキシムエステルの光開始剤 |
| JP2006030541A (ja) | 2004-07-15 | 2006-02-02 | Jsr Corp | カラーフィルタ用感放射線性組成物およびその調製法 |
| JP2006206902A (ja) * | 2005-01-28 | 2006-08-10 | Goldschmidt Gmbh | ポリエーテル/ポリエステルを含む分散用樹脂 |
| JP2007063472A (ja) | 2005-09-01 | 2007-03-15 | Dainichiseika Color & Chem Mfg Co Ltd | 顔料の高分子分散剤およびカラーフィルター用着色組成物 |
| JP2008251321A (ja) | 2007-03-30 | 2008-10-16 | Kuraray Luminas Co Ltd | 無機エレクトロルミネッセンス素子およびこれを備える照明装置 |
Family Cites Families (18)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2957028B2 (ja) | 1991-06-28 | 1999-10-04 | 積水フアインケミカル株式会社 | 光硬化性の着色組成物 |
| JP3413319B2 (ja) | 1995-12-08 | 2003-06-03 | ダイセル化学工業株式会社 | 顔料分散剤及びその製造方法 |
| EP0930540B1 (en) | 1996-10-02 | 2004-06-16 | Sanyo Chemical Industries, Ltd. | Photosensitive composition and use thereof |
| JP4481439B2 (ja) | 1999-06-16 | 2010-06-16 | サカタインクス株式会社 | カラーフィルター用緑色顔料分散物 |
| US6524757B2 (en) | 2000-07-13 | 2003-02-25 | Dainippon Ink And Chemicals, Inc. | Color filter and method for producing the same |
| US6878799B2 (en) * | 2001-03-12 | 2005-04-12 | King Industries, Inc. | Acid functional polymer dispersants |
| JP4428911B2 (ja) | 2002-07-05 | 2010-03-10 | Jsr株式会社 | カラーフィルタ用感放射線性組成物、カラーフィルタおよびカラー液晶表示素子 |
| DE602004011673T2 (de) * | 2003-07-18 | 2009-01-22 | The Lubrizol Corp., Wickliffe | Zusammensetzungen |
| JP4556479B2 (ja) | 2004-04-27 | 2010-10-06 | Jsr株式会社 | 着色層形成用感放射線性組成物、カラーフィルタおよび液晶表示パネル |
| JP2006045262A (ja) | 2004-07-30 | 2006-02-16 | Mitsubishi Chemicals Corp | 着色樹脂組成物、カラーフィルタ、及び液晶表示装置 |
| KR101334798B1 (ko) * | 2005-04-13 | 2013-11-29 | 루브리졸 어드밴스드 머티어리얼스, 인코포레이티드 | 분산제 |
| CN101410436B (zh) * | 2006-03-29 | 2013-10-16 | 西巴控股有限公司 | 聚乙烯亚胺基颜料分散剂 |
| JP4752648B2 (ja) * | 2006-07-10 | 2011-08-17 | Jsr株式会社 | 着色層形成用感放射線性組成物、カラーフィルタおよびカラー液晶表示素子 |
| KR100796517B1 (ko) * | 2006-07-18 | 2008-01-21 | 제일모직주식회사 | 컬러필터용 감광성 수지 조성물 및 이를 이용한 이미지센서컬러필터 |
| ES2342189T3 (es) * | 2006-12-21 | 2010-07-02 | Agfa Graphics N.V. | Metodo de impresion por chorro de tinta y cartuchos de tinta. |
| WO2009025297A1 (ja) | 2007-08-22 | 2009-02-26 | Mitsubishi Chemical Corporation | 樹脂ブラックマトリックス、遮光性感光性樹脂組成物、tft素子基板及び液晶表示装置 |
| JP5171514B2 (ja) * | 2008-09-29 | 2013-03-27 | 富士フイルム株式会社 | 着色硬化性組成物、カラーフィルタ、及びカラーフィルタの製造方法 |
| JP5479163B2 (ja) * | 2009-03-31 | 2014-04-23 | 富士フイルム株式会社 | カラーフィルタ用着色硬化性組成物、カラーフィルタ及びその製造方法、並びに固体撮像素子 |
-
2009
- 2009-01-06 JP JP2009000964A patent/JP5371449B2/ja active Active
- 2009-01-23 TW TW098102826A patent/TWI460208B/zh active
- 2009-01-29 US US12/865,683 patent/US8728687B2/en active Active
- 2009-01-29 WO PCT/JP2009/051430 patent/WO2009096452A1/ja active Application Filing
- 2009-01-29 KR KR1020107018545A patent/KR101559828B1/ko active IP Right Grant
- 2009-01-29 EP EP09706745.8A patent/EP2246385B1/en not_active Not-in-force
- 2009-01-29 CN CN2009801032878A patent/CN101925636B/zh active Active
Patent Citations (122)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2848328A (en) | 1954-06-16 | 1958-08-19 | Eastman Kodak Co | Light sensitive diazo compound and binder composition |
| US2833827A (en) | 1955-01-17 | 1958-05-06 | Bayer Ag | Tri (3, 5-di lower alkyl-4-hydroxy phenyl)-sulfonium chlorides and method of preparing same |
| US2852379A (en) | 1955-05-04 | 1958-09-16 | Eastman Kodak Co | Azide resin photolithographic composition |
| US2940853A (en) | 1958-08-21 | 1960-06-14 | Eastman Kodak Co | Azide sensitized resin photographic resist |
| US3479185A (en) | 1965-06-03 | 1969-11-18 | Du Pont | Photopolymerizable compositions and layers containing 2,4,5-triphenylimidazoyl dimers |
| JPS4643946B1 (ja) | 1967-11-09 | 1971-12-27 | ||
| JPS4841708B1 (ja) | 1970-01-13 | 1973-12-07 | ||
| JPS4836281A (ja) | 1971-09-03 | 1973-05-28 | ||
| JPS4864183A (ja) | 1971-12-09 | 1973-09-05 | ||
| US3905815A (en) | 1971-12-17 | 1975-09-16 | Minnesota Mining & Mfg | Photopolymerizable sheet material with diazo resin layer |
| JPS4943191A (ja) | 1972-09-02 | 1974-04-23 | ||
| US4069055A (en) | 1974-05-02 | 1978-01-17 | General Electric Company | Photocurable epoxy compositions containing group Va onium salts |
| US4069056A (en) | 1974-05-02 | 1978-01-17 | General Electric Company | Photopolymerizable composition containing group Va aromatic onium salts |
| JPS5137193A (ja) | 1974-09-25 | 1976-03-29 | Toyo Boseki | |
| JPS5147334A (ja) | 1974-10-21 | 1976-04-22 | Hitachi Ltd | Batsufuamemoriseigyohoshiki |
| JPS5230490A (en) | 1975-09-03 | 1977-03-08 | Denki Kagaku Keiki Co Ltd | Gas concentration measuring electrode stable in air |
| JPS6330057B2 (ja) | 1977-07-15 | 1988-06-16 | Ici Plc | |
| JPS5421726A (en) | 1977-07-19 | 1979-02-19 | Canon Inc | Electrostatic printing method and device therefor |
| JPS5425957A (en) | 1977-07-29 | 1979-02-27 | Nippon Zeon Co Ltd | Curable rubber composition having excellent resistance to rancid gasoline |
| JPS5434327A (en) | 1977-08-12 | 1979-03-13 | Ciba Geigy Ag | Bispyridone dyes and use thereof in silver halide materials for photograph |
| DE2904626A1 (de) | 1978-02-08 | 1979-08-09 | Minnesota Mining & Mfg | Triarylsulfoniumkomplexsalze, verfahren zu ihrer herstellung und diese salze enthaltende photopolymerisierbare gemische |
| JPS5532070A (en) | 1978-08-29 | 1980-03-06 | Fuji Photo Film Co Ltd | Photosensitive resin composition |
| JPS5617654A (en) | 1979-07-25 | 1981-02-19 | Mitsubishi Electric Corp | Preventing apparatus for freezing of fountain nozzle |
| US4311783A (en) | 1979-08-14 | 1982-01-19 | E. I. Du Pont De Nemours And Company | Dimers derived from unsymmetrical 2,4,5,-triphenylimidazole compounds as photoinitiators |
| JPS57196231A (en) | 1981-05-20 | 1982-12-02 | Hoechst Ag | Mixture able to be polymerized by radiation and copying material mainly composed thereof |
| JPS5812577A (ja) | 1981-07-10 | 1983-01-24 | Mitsubishi Electric Corp | 変換器の制御装置 |
| JPS5849860A (ja) | 1981-09-18 | 1983-03-24 | Sanyo Electric Co Ltd | 太陽光エネルギ−変換器 |
| JPS595241A (ja) | 1982-06-21 | 1984-01-12 | ヘキスト・アクチエンゲゼルシヤフト | 放射線重合可能な混合物 |
| JPS595240A (ja) | 1982-06-21 | 1984-01-12 | ヘキスト・アクチエンゲゼルシヤフト | 放射線重合可能な混合物 |
| JPS5944615A (ja) | 1982-09-07 | 1984-03-13 | Furuno Electric Co Ltd | ジヤイロ装置 |
| EP0104143A1 (de) | 1982-09-18 | 1984-03-28 | Ciba-Geigy Ag | Diaryljodosylsalze enthaltende photopolymerisierbare Zusammensetzungen |
| JPS5953836A (ja) | 1982-09-21 | 1984-03-28 | Fuji Photo Film Co Ltd | 感光性平版印刷版 |
| JPS5971048A (ja) | 1982-10-18 | 1984-04-21 | Mitsubishi Chem Ind Ltd | 光重合系感光性組成物 |
| US4508811A (en) | 1983-01-17 | 1985-04-02 | U.S. Philips Corporation | Recording element having a pyrylium or thiopyrylium-squarylium dye layer and new pyrylium or thiopyrylium-squarylium compounds |
| JPS59152396A (ja) | 1983-02-11 | 1984-08-31 | チバ−ガイギ− アクチエンゲゼルシヤフト | メタロセン,その製造方法およびメタロセンを含む光重合性組成物 |
| JPS60239736A (ja) | 1984-05-14 | 1985-11-28 | Fuji Photo Film Co Ltd | 感光性組成物 |
| JPS6122048A (ja) | 1984-06-08 | 1986-01-30 | ヘキスト・アクチエンゲゼルシヤフト | 重合可能な化合物、その製法、およびこれを含有する放射線感性複写層 |
| JPS61151197A (ja) | 1984-12-20 | 1986-07-09 | チバ‐ガイギー アーゲー | チタノセン類およびこれらのチタノセン類を含有する照射重合開始剤 |
| JPS61166544A (ja) | 1985-01-18 | 1986-07-28 | Fuji Photo Film Co Ltd | 光可溶化組成物 |
| JPS61169835A (ja) | 1985-01-22 | 1986-07-31 | Fuji Photo Film Co Ltd | 光可溶化組成物 |
| JPS61169837A (ja) | 1985-01-22 | 1986-07-31 | Fuji Photo Film Co Ltd | 光可溶化組成物 |
| JPS6239418A (ja) | 1985-08-08 | 1987-02-20 | 川島 藤夫 | 海苔結束用紙テ−プ供給法及びその装置 |
| JPS6239417A (ja) | 1985-08-10 | 1987-02-20 | 川島 藤夫 | 折畳海苔束結束装置 |
| JPS6258241A (ja) | 1985-09-09 | 1987-03-13 | Fuji Photo Film Co Ltd | 感光性組成物 |
| US4622286A (en) | 1985-09-16 | 1986-11-11 | E. I. Du Pont De Nemours And Company | Photoimaging composition containing admixture of leuco dye and 2,4,5-triphenylimidazolyl dimer |
| JPS62143044A (ja) | 1985-11-20 | 1987-06-26 | サイカラー・インコーポレーテッド | 染料−ほう素化合物錯体を含有する光硬化性組成物およびその組成物を使用する感光性材料 |
| JPS62150242A (ja) | 1985-11-20 | 1987-07-04 | サイカラー・インコーポレーテッド | イオン性染料化合物を開始剤として含む感光性材料 |
| DE3604581A1 (de) | 1986-02-14 | 1987-08-20 | Basf Ag | 4-acylbenzylsulfoniumsalze, ihre herstellung sowie sie enthaltende photohaertbare gemische und aufzeichnungsmaterialien |
| DE3604580A1 (de) | 1986-02-14 | 1987-08-20 | Basf Ag | Haertbare mischungen, enthaltend n-sulfonylaminosulfoniumsalze als kationisch wirksame katalysatoren |
| EP0233567A2 (de) | 1986-02-14 | 1987-08-26 | BASF Aktiengesellschaft | Härtbare Mischungen, enthaltend N-Sulfonylaminosulfoniumsalze als kationisch wirksame Katalysatoren |
| US4734444A (en) | 1986-02-14 | 1988-03-29 | Basf Aktiengesellschaft | Curable mixtures containing N-sulfonylaminosulfonium salts as cationically active catalysts |
| JPS62212401A (ja) | 1986-03-14 | 1987-09-18 | Fuji Photo Film Co Ltd | 光重合性組成物 |
| JPS6341484A (ja) | 1986-08-01 | 1988-02-22 | チバ−ガイギ− ア−ゲ− | チタノセン、それらの製造法およびそれらを含有する組成物 |
| JPS6370243A (ja) | 1986-09-11 | 1988-03-30 | Fuji Photo Film Co Ltd | 感光性組成物 |
| US4760013A (en) | 1987-02-17 | 1988-07-26 | International Business Machines Corporation | Sulfonium salt photoinitiators |
| JPS63260909A (ja) | 1987-03-28 | 1988-10-27 | ヘキスト・アクチエンゲゼルシヤフト | 光重合性混合物及びこの混合物から製造される記録材料 |
| JPS63277653A (ja) | 1987-03-28 | 1988-11-15 | ヘキスト・アクチエンゲゼルシヤフト | 重合可能な化合物、これを含有する放射線重合可能な混合物及び放射線重合可能な記録材料 |
| JPH01105238A (ja) | 1987-03-28 | 1989-04-21 | Hoechst Ag | 光重合可能な混合物および光重合可能な記録材料 |
| JPS63298339A (ja) | 1987-05-29 | 1988-12-06 | Fuji Photo Film Co Ltd | 感光性組成物 |
| EP0297442A1 (de) | 1987-07-01 | 1989-01-04 | BASF Aktiengesellschaft | Sulfoniumsalze mit säurelabilen Gruppierungen |
| EP0297443A2 (de) | 1987-07-01 | 1989-01-04 | BASF Aktiengesellschaft | Strahlungsempfindliches Gemisch für lichtempfindliche Beschichtungsmaterialien |
| JPS6440336A (en) | 1987-08-05 | 1989-02-10 | Toppan Printing Co Ltd | Drying/deodorizing device of printer |
| JPS6440337A (en) | 1987-08-06 | 1989-02-10 | Toyo Machinery & Metal | Molding number printing device |
| JPH01165613A (ja) | 1987-11-16 | 1989-06-29 | Hoechst Ag | 重合可能な化合物、その放射線重合性混合物および放射線重合記録材料 |
| JPH02249A (ja) | 1987-12-01 | 1990-01-05 | Ciba Geigy Ag | チタノセンおよびそれを含有する光重合性組成物 |
| JPH01152109A (ja) | 1987-12-09 | 1989-06-14 | Toray Ind Inc | 光重合性組成物 |
| US4933377A (en) | 1988-02-29 | 1990-06-12 | Saeva Franklin D | Novel sulfonium salts and the use thereof as photoinitiators |
| JPH024705A (ja) | 1988-03-24 | 1990-01-09 | Dentsply Internatl Inc | 光硬化性組成物用チタナート開始剤 |
| JPH0225493A (ja) | 1988-05-21 | 1990-01-26 | Hoechst Ag | アルケニルホスホン酸エステルおよびアルケニルホスフイン酸エルテル、その製法並びに当該化合物を含有する放射線重合性混合物および記録材料 |
| JPH01304453A (ja) | 1988-06-02 | 1989-12-08 | Toyobo Co Ltd | 光重合性組成物 |
| JPH0216765A (ja) | 1988-07-05 | 1990-01-19 | Fujitsu Ltd | 半導体装置 |
| JPH0232293A (ja) | 1988-07-22 | 1990-02-02 | Nippon Atom Ind Group Co Ltd | 沸騰水型原子炉 |
| EP0370693A2 (en) | 1988-11-21 | 1990-05-30 | Eastman Kodak Company | Novel onium salts and the use thereof as photoinitiators |
| JPH02150848A (ja) | 1988-12-02 | 1990-06-11 | Hitachi Ltd | 光退色性放射線感応性組成物およびそれを用いたパターン形成法 |
| JPH02226149A (ja) | 1988-12-22 | 1990-09-07 | Hoechst Ag | 光重合性化合物、それを含む光重合性混合物及びそれから製造された光重合性複写材料 |
| EP0390214A2 (en) | 1989-03-31 | 1990-10-03 | E.F. Johnson Company | Method and apparatus for a distributive wide area network for a land mobile transmission trunked communication system |
| JPH02272009A (ja) | 1989-04-13 | 1990-11-06 | Mitsubishi Kasei Corp | ポリエステルマクロモノマー |
| JPH02296514A (ja) | 1989-05-12 | 1990-12-07 | Matsushita Electric Ind Co Ltd | 車両用サスペンション制御装置 |
| US5227227A (en) | 1990-03-05 | 1993-07-13 | Johnson & Johnson Inc. | Non-woven fabric with a thermally activated adhesive surface, resulting product and applications thereof |
| JPH04365049A (ja) | 1991-06-12 | 1992-12-17 | Fuji Photo Film Co Ltd | 感光性組成物 |
| JP2764769B2 (ja) | 1991-06-24 | 1998-06-11 | 富士写真フイルム株式会社 | 光重合性組成物 |
| JPH0583588A (ja) | 1991-09-24 | 1993-04-02 | Omron Corp | 画像処理装置 |
| EP0568993A2 (en) | 1992-05-06 | 1993-11-10 | Kyowa Hakko Kogyo Co., Ltd. | Chemical amplification resist composition |
| JPH061938A (ja) | 1992-06-19 | 1994-01-11 | Nippon Steel Corp | アルカリ現像型感光性カラーフィルター用インク及びそれを用いたカラーフィルター |
| JPH0619240A (ja) | 1992-06-30 | 1994-01-28 | Canon Inc | 画像形成装置 |
| JPH0619249A (ja) | 1992-06-30 | 1994-01-28 | Ricoh Co Ltd | 原稿給送装置 |
| JPH0629285A (ja) | 1992-07-08 | 1994-02-04 | Nec Corp | 半導体装置 |
| JPH06157623A (ja) | 1992-08-14 | 1994-06-07 | Toyo Ink Mfg Co Ltd | 重合性組成物および重合方法 |
| JPH06102669A (ja) | 1992-09-21 | 1994-04-15 | Goou Kagaku Kogyo Kk | 感光性樹脂組成物及びそれを用いたカラーフィルタ |
| JPH06175554A (ja) | 1992-12-03 | 1994-06-24 | Toyo Ink Mfg Co Ltd | 体積位相型ホログラムの製造方法 |
| JPH06175553A (ja) | 1992-12-03 | 1994-06-24 | Toyo Ink Mfg Co Ltd | ホログラム記録媒体及びそれを用いた体積位相型ホログラムの製造方法 |
| JPH06175561A (ja) | 1992-12-04 | 1994-06-24 | Toyo Ink Mfg Co Ltd | ホログラム記録媒体及びそれを用いた体積位相型ホログラムの製造方法 |
| JPH06175564A (ja) | 1992-12-04 | 1994-06-24 | Toyo Ink Mfg Co Ltd | ホログラム記録材料及びそれを用いた体積位相型ホログラムの製造方法 |
| JPH06348011A (ja) | 1993-06-04 | 1994-12-22 | Toyo Ink Mfg Co Ltd | 光重合性組成物 |
| JPH07128785A (ja) | 1993-11-02 | 1995-05-19 | Konica Corp | 画像形成材料及び画像形成方法 |
| JPH07140589A (ja) | 1993-11-19 | 1995-06-02 | Konica Corp | 画像形成材料および画像形成方法 |
| JPH07207012A (ja) * | 1994-01-10 | 1995-08-08 | Daicel Chem Ind Ltd | 顔料分散剤の製造方法 |
| JPH07292014A (ja) | 1994-04-25 | 1995-11-07 | Nippon Paint Co Ltd | 近赤外光重合性組成物 |
| JPH07306527A (ja) | 1994-05-11 | 1995-11-21 | Konica Corp | 画像形成材料及び画像形成方法 |
| JPH08108621A (ja) | 1994-10-06 | 1996-04-30 | Konica Corp | 画像記録媒体及びそれを用いる画像形成方法 |
| JPH09169821A (ja) | 1995-10-16 | 1997-06-30 | Ajinomoto Co Inc | 顔料分散剤 |
| JPH09188686A (ja) | 1995-11-24 | 1997-07-22 | Ciba Geigy Ag | 光重合のための酸安定性硼酸塩 |
| JPH09188710A (ja) | 1995-11-24 | 1997-07-22 | Ciba Geigy Ag | モノボランからのボレート光開始剤 |
| JPH09188685A (ja) | 1995-11-24 | 1997-07-22 | Ciba Geigy Ag | 光重合のためのボレート補助開始剤 |
| JPH09157374A (ja) * | 1995-12-08 | 1997-06-17 | Daicel Chem Ind Ltd | 顔料分散剤およびこれを含む塗料用または印刷インキ用組成物 |
| JPH09176511A (ja) | 1995-12-21 | 1997-07-08 | Nippon Steel Chem Co Ltd | 顔料分散体組成物およびカラーレジストインキ |
| JPH09281698A (ja) | 1996-04-11 | 1997-10-31 | Mitsubishi Chem Corp | カラーフィルター用光重合性組成物 |
| JPH11271969A (ja) | 1998-01-21 | 1999-10-08 | Mitsubishi Chemical Corp | 光重合性組成物及び感光性平版印刷版 |
| JP2000080068A (ja) | 1998-06-26 | 2000-03-21 | Ciba Specialty Chem Holding Inc | 新規o―アシルオキシム光開始剤 |
| JP2000131837A (ja) | 1998-08-17 | 2000-05-12 | Mitsubishi Chemicals Corp | 光重合性組成物、光重合性平版印刷版及び画像形成方法 |
| JP2000066385A (ja) | 1998-08-18 | 2000-03-03 | Ciba Specialty Chem Holding Inc | 高感度で高レジスト厚さのi線ホトレジスト用スルホニルオキシム類 |
| JP2000310808A (ja) | 1999-04-26 | 2000-11-07 | Canon Inc | 照明装置及びそれを用いた撮影装置 |
| JP2001125255A (ja) | 1999-10-27 | 2001-05-11 | Fuji Photo Film Co Ltd | 感光性平版印刷版 |
| JP2001132318A (ja) | 1999-10-29 | 2001-05-15 | Oi Seisakusho Co Ltd | 車両用開閉体の開閉装置 |
| JP2001272524A (ja) | 2000-03-24 | 2001-10-05 | Jsr Corp | カラーフィルタ用感放射線性組成物、カラーフィルタおよびカラー液晶表示装置 |
| JP2002107916A (ja) | 2000-09-27 | 2002-04-10 | Fuji Photo Film Co Ltd | 平版印刷版原版 |
| JP2002226587A (ja) * | 2001-01-29 | 2002-08-14 | Fuji Photo Film Co Ltd | 重合体、顔料分散組成物及び着色感光性組成物 |
| JP2004534797A (ja) | 2001-06-11 | 2004-11-18 | チバ スペシャルティ ケミカルズ ホールディング インコーポレーテッド | 組み合わされた構造を有するオキシムエステルの光開始剤 |
| JP2006030541A (ja) | 2004-07-15 | 2006-02-02 | Jsr Corp | カラーフィルタ用感放射線性組成物およびその調製法 |
| JP2006206902A (ja) * | 2005-01-28 | 2006-08-10 | Goldschmidt Gmbh | ポリエーテル/ポリエステルを含む分散用樹脂 |
| JP2007063472A (ja) | 2005-09-01 | 2007-03-15 | Dainichiseika Color & Chem Mfg Co Ltd | 顔料の高分子分散剤およびカラーフィルター用着色組成物 |
| JP2008251321A (ja) | 2007-03-30 | 2008-10-16 | Kuraray Luminas Co Ltd | 無機エレクトロルミネッセンス素子およびこれを備える照明装置 |
Non-Patent Citations (10)
| Title |
|---|
| C. S. WEN ET AL., TEH. PROC. CONF. RAD. CURING ASIA, October 1988 (1988-10-01), pages 478 |
| J. C. S. PERKIN II, 1979, pages 156 - 162 |
| J. C. S. PERKIN, vol. 11, 1979, pages 1653 - 1660 |
| J. V. CRIVELLO ET AL., J. POLYMER SCI., POLYMER CHEM. ED., vol. 17, 1979, pages 1047 |
| J. V. CRIVELLO ET AL., MACROMOLECULES, vol. 10, no. 6, 1977, pages 1307 |
| JOURNAL OF ADHESION SOCIETY OF JAPAN, vol. 20, no. 7, 1984, pages 300 - 308 |
| JOURNAL OF PHOTOPOLYMER SCIENCE AND TECHNOLOGY, 1995, pages 202 - 232 |
| M. P. HUTT, JOURNAL OF HETEROCYCLIC CHEMISTRY, vol. I, no. 3, 1970 |
| See also references of EP2246385A4 * |
| WAKABAYASHI ET AL., BULL CHEM. SOC. JAPAN, vol. 42, 1969, pages 2924 |
Cited By (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2009258668A (ja) * | 2008-03-17 | 2009-11-05 | Fujifilm Corp | 着色硬化性組成物、カラーフィルタ、及びカラーフィルタの製造方法 |
| US20100248095A1 (en) * | 2009-03-31 | 2010-09-30 | Fujifilm Corporation | Colored curable composition for color filter, color filter and method for producing the same, and solid state imaging device |
| US8530116B2 (en) * | 2009-03-31 | 2013-09-10 | Fujifilm Corporation | Colored curable composition for color filter, color filter and method for producing the same, and solid state imaging device |
| WO2011037195A1 (ja) * | 2009-09-25 | 2011-03-31 | 東洋インキ製造株式会社 | 着色組成物及びカラーフィルタ |
| CN102549460A (zh) * | 2009-09-25 | 2012-07-04 | 东洋油墨Sc控股株式会社 | 着色组合物以及滤色器 |
| CN102549460B (zh) * | 2009-09-25 | 2014-09-24 | 东洋油墨Sc控股株式会社 | 着色组合物以及滤色器 |
| JP5836126B2 (ja) * | 2009-09-25 | 2015-12-24 | 東洋インキScホールディングス株式会社 | 着色組成物及びカラーフィルタ |
| CN110531583A (zh) * | 2019-09-14 | 2019-12-03 | 浙江福斯特新材料研究院有限公司 | 感光性树脂组合物、干膜抗蚀层 |
| CN110531583B (zh) * | 2019-09-14 | 2023-09-29 | 浙江福斯特新材料研究院有限公司 | 感光性树脂组合物、干膜抗蚀层 |
Also Published As
| Publication number | Publication date |
|---|---|
| KR20100119874A (ko) | 2010-11-11 |
| US20110003241A1 (en) | 2011-01-06 |
| KR101559828B1 (ko) | 2015-10-13 |
| CN101925636A (zh) | 2010-12-22 |
| EP2246385B1 (en) | 2017-11-29 |
| EP2246385A1 (en) | 2010-11-03 |
| US8728687B2 (en) | 2014-05-20 |
| CN101925636B (zh) | 2012-11-07 |
| JP5371449B2 (ja) | 2013-12-18 |
| JP2009203462A (ja) | 2009-09-10 |
| TWI460208B (zh) | 2014-11-11 |
| TW200940598A (en) | 2009-10-01 |
| EP2246385A4 (en) | 2013-12-25 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5371449B2 (ja) | 樹脂、顔料分散液、着色硬化性組成物、これを用いたカラーフィルタ及びその製造方法 | |
| JP5334624B2 (ja) | 着色硬化性組成物、カラーフィルタ、及びカラーフィルタの製造方法 | |
| JP5213375B2 (ja) | 顔料分散液、硬化性組成物、それを用いるカラーフィルタ及び固体撮像素子 | |
| KR101414099B1 (ko) | 안료 분산 조성물, 경화성 조성물, 컬러 필터 및 그 제조방법 | |
| JP5344790B2 (ja) | 硬化性組成物、カラーフィルタ及びその製造方法 | |
| JP5878492B2 (ja) | 固体撮像素子用着色光硬化性組成物、カラーフィルタ及びその製造方法、並びに固体撮像素子 | |
| JP5224936B2 (ja) | 分散液、黒色硬化性組成物、製造方法、固体撮像素子用の遮光膜または反射防止膜の製造方法、および固体撮像素子 | |
| JP4969189B2 (ja) | 固体撮像素子用途のカラーフィルタ形成用の硬化性組成物、固体撮像素子用途のカラーフィルタ及びその製造方法 | |
| JP5178081B2 (ja) | カラーフィルタ形成用硬化性組成物、これを用いたカラーフィルタ及びその製造方法、並びに固体撮像素子 | |
| JP5079653B2 (ja) | 着色硬化性組成物、カラーフィルタ及びその製造方法、並びに固体撮像素子 | |
| JP2007316445A (ja) | 硬化性組成物、カラーフィルタ、及びその製造方法 | |
| JP2009216913A (ja) | 着色硬化性組成物、カラーフィルタ、及び、固体撮像素子 | |
| JP5586828B2 (ja) | 顔料分散組成物、硬化性組成物、並びにカラーフィルタ及びその製造方法 | |
| JP2008032860A (ja) | 硬化性組成物、カラーフィルタ、及びその製造方法 | |
| JP5523655B2 (ja) | 顔料分散組成物、硬化性組成物、並びにカラーフィルタ及びその製造方法 | |
| JP5171514B2 (ja) | 着色硬化性組成物、カラーフィルタ、及びカラーフィルタの製造方法 | |
| JP2010113034A (ja) | 硬化性組成物、カラーフィルタ、その製造方法及び固体撮像素子 | |
| JP5184993B2 (ja) | 黒色硬化性組成物、固体撮像素子用遮光性カラーフィルタ、その製造方法、および固体撮像素子 | |
| JP2010018643A (ja) | ポリエステルの製造方法、樹脂、顔料分散液、光硬化性組成物、これを用いたカラーフィルタ、およびその製造方法 | |
| JP5105867B2 (ja) | 硬化性組成物、カラーフィルタ及びその製造方法 | |
| JP2011118060A (ja) | 顔料分散液、着色硬化性組成物、カラーフィルタ、カラーフィルタの製造方法、及び固体撮像素子 | |
| JP2010084021A (ja) | 樹脂、該樹脂の製造方法、顔料分散液、着色硬化性組成物、該着色硬化性組成物の調製方法、カラーフィルタ、及びカラーフィルタの製造方法 | |
| JP5456184B2 (ja) | 黒色硬化性組成物、固体撮像素子用遮光性カラーフィルタ、固体撮像素子用反射防止膜、固体撮像素子用遮光性カラーフィルタの製造方法、および固体撮像素子 | |
| JP2009075482A (ja) | 硬化性組成物、カラーフィルタ、カラーフィルタの製造方法、及び、固体撮像素子 | |
| JP4837500B2 (ja) | 硬化性組成物、カラーフィルタ、及びその製造方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| WWE | Wipo information: entry into national phase |
Ref document number: 200980103287.8 Country of ref document: CN |
|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 09706745 Country of ref document: EP Kind code of ref document: A1 |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 12865683 Country of ref document: US |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| REEP | Request for entry into the european phase |
Ref document number: 2009706745 Country of ref document: EP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2009706745 Country of ref document: EP |
|
| ENP | Entry into the national phase |
Ref document number: 20107018545 Country of ref document: KR Kind code of ref document: A |