JP7148401B2 - 免疫調節剤としての複素環化合物 - Google Patents
免疫調節剤としての複素環化合物 Download PDFInfo
- Publication number
- JP7148401B2 JP7148401B2 JP2018526213A JP2018526213A JP7148401B2 JP 7148401 B2 JP7148401 B2 JP 7148401B2 JP 2018526213 A JP2018526213 A JP 2018526213A JP 2018526213 A JP2018526213 A JP 2018526213A JP 7148401 B2 JP7148401 B2 JP 7148401B2
- Authority
- JP
- Japan
- Prior art keywords
- alkyl
- methyl
- cycloalkyl
- cancer
- membered heterocycloalkyl
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 150000002391 heterocyclic compounds Chemical class 0.000 title 1
- 239000002955 immunomodulating agent Substances 0.000 title 1
- 229940121354 immunomodulator Drugs 0.000 title 1
- 125000000217 alkyl group Chemical group 0.000 claims description 588
- 150000001875 compounds Chemical class 0.000 claims description 350
- 125000000592 heterocycloalkyl group Chemical group 0.000 claims description 316
- 125000001424 substituent group Chemical group 0.000 claims description 195
- -1 cyclohex-1-en-1-yl Chemical group 0.000 claims description 172
- 125000003118 aryl group Chemical group 0.000 claims description 157
- 125000001313 C5-C10 heteroaryl group Chemical group 0.000 claims description 146
- 125000006376 (C3-C10) cycloalkyl group Chemical group 0.000 claims description 120
- 229910052757 nitrogen Inorganic materials 0.000 claims description 96
- 150000003839 salts Chemical class 0.000 claims description 96
- 125000000882 C2-C6 alkenyl group Chemical group 0.000 claims description 84
- 125000005843 halogen group Chemical group 0.000 claims description 81
- 125000003601 C2-C6 alkynyl group Chemical group 0.000 claims description 80
- 229910052799 carbon Inorganic materials 0.000 claims description 75
- 125000004765 (C1-C4) haloalkyl group Chemical group 0.000 claims description 72
- 206010028980 Neoplasm Diseases 0.000 claims description 68
- 125000006570 (C5-C6) heteroaryl group Chemical group 0.000 claims description 65
- 229910052739 hydrogen Inorganic materials 0.000 claims description 47
- 125000000304 alkynyl group Chemical group 0.000 claims description 45
- 125000005913 (C3-C6) cycloalkyl group Chemical group 0.000 claims description 40
- 108010074708 B7-H1 Antigen Proteins 0.000 claims description 39
- 102000008096 B7-H1 Antigen Human genes 0.000 claims description 39
- 125000001072 heteroaryl group Chemical group 0.000 claims description 39
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims description 38
- 125000004433 nitrogen atom Chemical group N* 0.000 claims description 38
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims description 38
- 125000003342 alkenyl group Chemical group 0.000 claims description 37
- 201000011510 cancer Diseases 0.000 claims description 37
- 125000003545 alkoxy group Chemical group 0.000 claims description 33
- 125000000171 (C1-C6) haloalkyl group Chemical group 0.000 claims description 32
- 125000006708 (C5-C14) heteroaryl group Chemical group 0.000 claims description 32
- 229910052760 oxygen Inorganic materials 0.000 claims description 30
- 229910052717 sulfur Inorganic materials 0.000 claims description 29
- 125000004767 (C1-C4) haloalkoxy group Chemical group 0.000 claims description 27
- 201000010099 disease Diseases 0.000 claims description 26
- 125000004432 carbon atom Chemical group C* 0.000 claims description 24
- 239000003814 drug Substances 0.000 claims description 22
- 125000005842 heteroatom Chemical group 0.000 claims description 21
- 229910052794 bromium Inorganic materials 0.000 claims description 19
- 101150073096 NRAS gene Proteins 0.000 claims description 18
- 229910052801 chlorine Inorganic materials 0.000 claims description 17
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 claims description 16
- 125000004737 (C1-C6) haloalkoxy group Chemical group 0.000 claims description 15
- 239000000546 pharmaceutical excipient Substances 0.000 claims description 15
- 208000035475 disorder Diseases 0.000 claims description 12
- 239000008194 pharmaceutical composition Substances 0.000 claims description 12
- 230000002401 inhibitory effect Effects 0.000 claims description 11
- 208000015914 Non-Hodgkin lymphomas Diseases 0.000 claims description 8
- 239000003937 drug carrier Substances 0.000 claims description 7
- 229910052702 rhenium Inorganic materials 0.000 claims description 7
- 208000008839 Kidney Neoplasms Diseases 0.000 claims description 6
- 208000036142 Viral infection Diseases 0.000 claims description 6
- 210000003169 central nervous system Anatomy 0.000 claims description 6
- 125000006568 (C4-C7) heterocycloalkyl group Chemical group 0.000 claims description 5
- 206010014733 Endometrial cancer Diseases 0.000 claims description 5
- 206010014759 Endometrial neoplasm Diseases 0.000 claims description 5
- 206010058467 Lung neoplasm malignant Diseases 0.000 claims description 5
- 229910017711 NHRa Inorganic materials 0.000 claims description 5
- 206010038389 Renal cancer Diseases 0.000 claims description 5
- 206010039491 Sarcoma Diseases 0.000 claims description 5
- 230000028993 immune response Effects 0.000 claims description 5
- 230000003993 interaction Effects 0.000 claims description 5
- 201000010982 kidney cancer Diseases 0.000 claims description 5
- 201000005202 lung cancer Diseases 0.000 claims description 5
- 208000020816 lung neoplasm Diseases 0.000 claims description 5
- 201000001441 melanoma Diseases 0.000 claims description 5
- 208000031261 Acute myeloid leukaemia Diseases 0.000 claims description 4
- 206010005003 Bladder cancer Diseases 0.000 claims description 4
- 208000005718 Stomach Neoplasms Diseases 0.000 claims description 4
- 206010046458 Urethral neoplasms Diseases 0.000 claims description 4
- 208000007097 Urinary Bladder Neoplasms Diseases 0.000 claims description 4
- 208000002495 Uterine Neoplasms Diseases 0.000 claims description 4
- 230000002708 enhancing effect Effects 0.000 claims description 4
- 206010017758 gastric cancer Diseases 0.000 claims description 4
- 230000000306 recurrent effect Effects 0.000 claims description 4
- 201000011549 stomach cancer Diseases 0.000 claims description 4
- 201000005112 urinary bladder cancer Diseases 0.000 claims description 4
- 206010046766 uterine cancer Diseases 0.000 claims description 4
- ASLOXZSRPQODHA-VWLOTQADSA-N (2S)-1-[[2-(2-cyano-3-phenylphenyl)-7-methyl-1,3-benzoxazol-5-yl]methyl]piperidine-2-carboxylic acid Chemical compound C(#N)C1=C(C=CC=C1C=1OC2=C(N=1)C=C(C=C2C)CN1[C@@H](CCCC1)C(=O)O)C1=CC=CC=C1 ASLOXZSRPQODHA-VWLOTQADSA-N 0.000 claims description 3
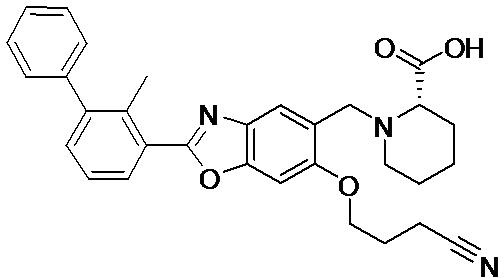
- NKKKZVPYXOVVKY-DEOSSOPVSA-N (2S)-1-[[2-(2-methyl-3-phenylphenyl)-1,3-benzoxazol-5-yl]methyl]piperidine-2-carboxylic acid Chemical compound CC1=C(C=CC=C1C=1OC2=C(N=1)C=C(C=C2)CN1[C@@H](CCCC1)C(=O)O)C1=CC=CC=C1 NKKKZVPYXOVVKY-DEOSSOPVSA-N 0.000 claims description 3
- FQXPNAAFCSYOKR-DEOSSOPVSA-N (2S)-1-[[2-(2-methyl-3-phenylphenyl)-1,3-benzoxazol-6-yl]methyl]piperidine-2-carboxylic acid Chemical compound CC1=C(C=CC=C1C=1OC2=C(N=1)C=CC(=C2)CN1[C@@H](CCCC1)C(=O)O)C1=CC=CC=C1 FQXPNAAFCSYOKR-DEOSSOPVSA-N 0.000 claims description 3
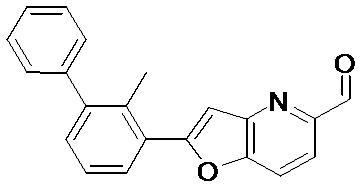
- YKTLZRGADYCTCL-DEOSSOPVSA-N (2S)-1-[[2-(2-methyl-3-phenylphenyl)furo[2,3-b]pyridin-5-yl]methyl]piperidine-2-carboxylic acid Chemical compound CC1=C(C=CC=C1C1=CC=2C(=NC=C(C=2)CN2[C@@H](CCCC2)C(=O)O)O1)C1=CC=CC=C1 YKTLZRGADYCTCL-DEOSSOPVSA-N 0.000 claims description 3
- NDXDZLYPPBLIIU-DEOSSOPVSA-N (2S)-1-[[2-(2-methyl-3-phenylphenyl)furo[3,2-b]pyridin-5-yl]methyl]piperidine-2-carboxylic acid Chemical compound CC1=C(C=CC=C1C1=CC2=NC(=CC=C2O1)CN1[C@@H](CCCC1)C(=O)O)C1=CC=CC=C1 NDXDZLYPPBLIIU-DEOSSOPVSA-N 0.000 claims description 3
- WXOGJKHSKFQFGH-VWLOTQADSA-N (2S)-1-[[2-[2-cyano-3-(2,3-dihydro-1,4-benzodioxin-6-yl)phenyl]-6-(cyanomethoxy)-1,3-benzoxazol-5-yl]methyl]piperidine-2-carboxylic acid Chemical compound C(#N)C1=C(C=CC=C1C1=CC2=C(OCCO2)C=C1)C=1OC2=C(N=1)C=C(C(=C2)OCC#N)CN1[C@@H](CCCC1)C(=O)O WXOGJKHSKFQFGH-VWLOTQADSA-N 0.000 claims description 3
- IRAOBULKNPMMHM-VWLOTQADSA-N (2S)-1-[[2-[2-cyano-3-(2,3-dihydro-1,4-benzodioxin-6-yl)phenyl]-7-methyl-1,3-benzoxazol-5-yl]methyl]piperidine-2-carboxylic acid Chemical compound C(#N)C1=C(C=CC=C1C1=CC2=C(OCCO2)C=C1)C=1OC2=C(N=1)C=C(C=C2C)CN1[C@@H](CCCC1)C(=O)O IRAOBULKNPMMHM-VWLOTQADSA-N 0.000 claims description 3
- GKMVSXNEUYMCFC-VWLOTQADSA-N (2S)-1-[[2-[3-(2,3-dihydro-1,4-benzodioxin-6-yl)-2-methylphenyl]-7-methyl-1,3-benzoxazol-5-yl]methyl]piperidine-2-carboxylic acid Chemical compound O1CCOC2=C1C=CC(=C2)C=1C(=C(C=CC=1)C=1OC2=C(N=1)C=C(C=C2C)CN1[C@@H](CCCC1)C(=O)O)C GKMVSXNEUYMCFC-VWLOTQADSA-N 0.000 claims description 3
- NWSIOQXWKIOUSR-DEOSSOPVSA-N (2S)-1-[[4-methyl-2-(2-methyl-3-phenylphenyl)-1,3-benzothiazol-6-yl]methyl]piperidine-2-carboxylic acid Chemical compound CC1=CC(=CC2=C1N=C(S2)C=1C(=C(C=CC=1)C1=CC=CC=C1)C)CN1[C@@H](CCCC1)C(=O)O NWSIOQXWKIOUSR-DEOSSOPVSA-N 0.000 claims description 3
- SIBPLBOHNSYTCP-VWLOTQADSA-N (2S)-1-[[6-(cyanomethoxy)-2-(2-methyl-3-phenylphenyl)-1,3-benzoxazol-5-yl]methyl]piperidine-2-carboxylic acid Chemical compound C(#N)COC1=CC2=C(N=C(O2)C=2C(=C(C=CC=2)C2=CC=CC=C2)C)C=C1CN1[C@@H](CCCC1)C(=O)O SIBPLBOHNSYTCP-VWLOTQADSA-N 0.000 claims description 3
- GHQBAIJMISZATI-QHCPKHFHSA-N (2S)-1-[[6-(cyanomethoxy)-2-[4-(2,3-dihydro-1,4-benzodioxin-6-yl)-3-methylpyridin-2-yl]-1,3-benzoxazol-5-yl]methyl]piperidine-2-carboxylic acid Chemical compound C(#N)COC1=CC2=C(N=C(O2)C2=NC=CC(=C2C)C2=CC3=C(OCCO3)C=C2)C=C1CN1[C@@H](CCCC1)C(=O)O GHQBAIJMISZATI-QHCPKHFHSA-N 0.000 claims description 3
- UWWIGOJLOPXCJZ-VWLOTQADSA-N (2S)-1-[[7-methyl-2-(2-methyl-3-phenylphenyl)-1,3-benzoxazol-5-yl]methyl]piperidine-2-carboxylic acid Chemical compound CC1=CC(=CC=2N=C(OC=21)C=1C(=C(C=CC=1)C1=CC=CC=C1)C)CN1[C@@H](CCCC1)C(=O)O UWWIGOJLOPXCJZ-VWLOTQADSA-N 0.000 claims description 3
- RJHBIIAMVGEWET-UHFFFAOYSA-N 2-[[6-(2-methyl-3-phenylphenyl)furo[2,3-b]pyrazin-2-yl]methylamino]ethanol Chemical compound CC1=C(C=CC=C1C1=CC=2C(=NC=C(N=2)CNCCO)O1)C1=CC=CC=C1 RJHBIIAMVGEWET-UHFFFAOYSA-N 0.000 claims description 3
- XXNFAMPXQMQCBZ-UHFFFAOYSA-N 2-[[7-methyl-2-(2-methyl-3-phenylphenyl)furo[2,3-c]pyridin-5-yl]methylamino]ethanol Chemical compound CC=1N=C(C=C2C=1OC(=C2)C=1C(=C(C=CC=1)C1=CC=CC=C1)C)CNCCO XXNFAMPXQMQCBZ-UHFFFAOYSA-N 0.000 claims description 3
- FOEMFYJOKXNLEX-UHFFFAOYSA-N 2-[[7-methyl-2-(2-methyl-3-phenylphenyl)furo[3,2-b]pyridin-5-yl]methylamino]ethanol Chemical compound CC1=C2C(=NC(=C1)CNCCO)C=C(O2)C=1C(=C(C=CC=1)C1=CC=CC=C1)C FOEMFYJOKXNLEX-UHFFFAOYSA-N 0.000 claims description 3
- COAGTFLTFZWZRK-UHFFFAOYSA-N 4-[[5-[(2-hydroxyethylamino)methyl]-7-methyl-2-(2-methyl-3-phenylphenyl)-1,3-benzoxazol-6-yl]oxy]butanenitrile Chemical compound OCCNCC=1C(=C(C2=C(N=C(O2)C=2C(=C(C=CC=2)C2=CC=CC=C2)C)C=1)C)OCCCC#N COAGTFLTFZWZRK-UHFFFAOYSA-N 0.000 claims description 3
- 208000024893 Acute lymphoblastic leukemia Diseases 0.000 claims description 3
- 208000032791 BCR-ABL1 positive chronic myelogenous leukemia Diseases 0.000 claims description 3
- 206010006187 Breast cancer Diseases 0.000 claims description 3
- 208000026310 Breast neoplasm Diseases 0.000 claims description 3
- 201000009030 Carcinoma Diseases 0.000 claims description 3
- 206010009944 Colon cancer Diseases 0.000 claims description 3
- 208000000461 Esophageal Neoplasms Diseases 0.000 claims description 3
- 208000017604 Hodgkin disease Diseases 0.000 claims description 3
- 208000010747 Hodgkins lymphoma Diseases 0.000 claims description 3
- 208000031422 Lymphocytic Chronic B-Cell Leukemia Diseases 0.000 claims description 3
- 206010025323 Lymphomas Diseases 0.000 claims description 3
- 208000033776 Myeloid Acute Leukemia Diseases 0.000 claims description 3
- 206010030155 Oesophageal carcinoma Diseases 0.000 claims description 3
- 206010033128 Ovarian cancer Diseases 0.000 claims description 3
- 206010061535 Ovarian neoplasm Diseases 0.000 claims description 3
- 206010061902 Pancreatic neoplasm Diseases 0.000 claims description 3
- 206010060862 Prostate cancer Diseases 0.000 claims description 3
- 208000000236 Prostatic Neoplasms Diseases 0.000 claims description 3
- 125000004414 alkyl thio group Chemical group 0.000 claims description 3
- 208000029742 colonic neoplasm Diseases 0.000 claims description 3
- 201000004101 esophageal cancer Diseases 0.000 claims description 3
- 230000001965 increasing effect Effects 0.000 claims description 3
- 201000007270 liver cancer Diseases 0.000 claims description 3
- 208000014018 liver neoplasm Diseases 0.000 claims description 3
- 208000015486 malignant pancreatic neoplasm Diseases 0.000 claims description 3
- 208000037819 metastatic cancer Diseases 0.000 claims description 3
- 208000011575 metastatic malignant neoplasm Diseases 0.000 claims description 3
- 208000002154 non-small cell lung carcinoma Diseases 0.000 claims description 3
- 201000002528 pancreatic cancer Diseases 0.000 claims description 3
- 208000008443 pancreatic carcinoma Diseases 0.000 claims description 3
- 206010041823 squamous cell carcinoma Diseases 0.000 claims description 3
- 208000029729 tumor suppressor gene on chromosome 11 Diseases 0.000 claims description 3
- 230000009385 viral infection Effects 0.000 claims description 3
- ASWOMJSTQYVKBX-DEOSSOPVSA-N (2S)-1-[[2-(2-methyl-3-phenylphenyl)-1,3-benzothiazol-5-yl]methyl]piperidine-2-carboxylic acid Chemical compound CC1=C(C=CC=C1C=1SC2=C(N=1)C=C(C=C2)CN1[C@@H](CCCC1)C(=O)O)C1=CC=CC=C1 ASWOMJSTQYVKBX-DEOSSOPVSA-N 0.000 claims description 2
- LYAMYGQYOOTPPZ-DEOSSOPVSA-N (2S)-1-[[2-(2-methyl-3-phenylphenyl)furo[2,3-b]pyridin-6-yl]methyl]piperidine-2-carboxylic acid Chemical compound CC1=C(C=CC=C1C1=CC=2C(=NC(=CC=2)CN2[C@@H](CCCC2)C(=O)O)O1)C1=CC=CC=C1 LYAMYGQYOOTPPZ-DEOSSOPVSA-N 0.000 claims description 2
- AODHRRFQPQTWJR-QHCPKHFHSA-N (2S)-1-[[6-(2-methyl-3-phenylphenyl)furo[2,3-b]pyrazin-2-yl]methyl]piperidine-2-carboxylic acid Chemical compound CC1=C(C=CC=C1C1=CC=2C(=NC=C(N=2)CN2[C@@H](CCCC2)C(=O)O)O1)C1=CC=CC=C1 AODHRRFQPQTWJR-QHCPKHFHSA-N 0.000 claims description 2
- DCSUWIPRZKZFBT-MHZLTWQESA-N (2S)-1-[[6-(3-cyanopropoxy)-2-(2-methyl-3-phenylphenyl)-1,3-benzoxazol-5-yl]methyl]piperidine-2-carboxylic acid Chemical compound C(#N)CCCOC1=CC2=C(N=C(O2)C=2C(=C(C=CC=2)C2=CC=CC=C2)C)C=C1CN1[C@@H](CCCC1)C(=O)O DCSUWIPRZKZFBT-MHZLTWQESA-N 0.000 claims description 2
- ZXGOOJXOOLGUEA-VWLOTQADSA-N (2S)-1-[[6-(cyanomethoxy)-2-[3-(2,3-dihydro-1,4-benzodioxin-6-yl)-2-methylphenyl]-1,3-benzoxazol-5-yl]methyl]piperidine-2-carboxylic acid Chemical compound C(#N)COC1=CC2=C(N=C(O2)C2=C(C(=CC=C2)C2=CC3=C(OCCO3)C=C2)C)C=C1CN1[C@@H](CCCC1)C(=O)O ZXGOOJXOOLGUEA-VWLOTQADSA-N 0.000 claims description 2
- SWDCNFAIGPONBQ-VWLOTQADSA-N (2S)-1-[[7-methyl-2-(2-methyl-3-phenylphenyl)furo[2,3-c]pyridin-5-yl]methyl]piperidine-2-carboxylic acid Chemical compound CC=1N=C(C=C2C=1OC(=C2)C=1C(=C(C=CC=1)C1=CC=CC=C1)C)CN1[C@@H](CCCC1)C(=O)O SWDCNFAIGPONBQ-VWLOTQADSA-N 0.000 claims description 2
- HPNPNFOZCWVOOS-VWLOTQADSA-N (2S)-1-[[7-methyl-2-(2-methyl-3-phenylphenyl)furo[3,2-b]pyridin-5-yl]methyl]piperidine-2-carboxylic acid Chemical compound CC1=C2C(=NC(=C1)CN1[C@@H](CCCC1)C(=O)O)C=C(O2)C=1C(=C(C=CC=1)C1=CC=CC=C1)C HPNPNFOZCWVOOS-VWLOTQADSA-N 0.000 claims description 2
- SZFLERAWEJDTCX-UHFFFAOYSA-N 2-(2,3-dihydro-1,4-benzodioxin-6-yl)-6-[5-[(2-hydroxyethylamino)methyl]-7-methyl-1,3-benzoxazol-2-yl]benzonitrile Chemical compound O1CCOC2=C1C=CC(=C2)C1=C(C#N)C(=CC=C1)C=1OC2=C(N=1)C=C(C=C2C)CNCCO SZFLERAWEJDTCX-UHFFFAOYSA-N 0.000 claims description 2
- HRHMBEUMFKXGIT-UHFFFAOYSA-N 2-[5-[(2-hydroxyethylamino)methyl]-7-methyl-1,3-benzoxazol-2-yl]-6-phenylbenzonitrile Chemical compound OCCNCC=1C=C(C2=C(N=C(O2)C2=C(C(=CC=C2)C2=CC=CC=C2)C#N)C=1)C HRHMBEUMFKXGIT-UHFFFAOYSA-N 0.000 claims description 2
- ZNOWLLPAHTWELC-UHFFFAOYSA-N 2-[[2-(2-methyl-3-phenylphenyl)-1,3-benzoxazol-5-yl]methylamino]ethanol Chemical compound CC1=C(C=CC=C1C=1OC2=C(N=1)C=C(C=C2)CNCCO)C1=CC=CC=C1 ZNOWLLPAHTWELC-UHFFFAOYSA-N 0.000 claims description 2
- VSLGIPZHVMRWRE-UHFFFAOYSA-N 2-[[2-(2-methyl-3-phenylphenyl)-6-(2-morpholin-4-ylethoxy)-1,3-benzoxazol-5-yl]methylamino]ethanol Chemical compound CC1=C(C=CC=C1C=1OC2=C(N=1)C=C(C(=C2)OCCN1CCOCC1)CNCCO)C1=CC=CC=C1 VSLGIPZHVMRWRE-UHFFFAOYSA-N 0.000 claims description 2
- GEHNLXIJMMXQRC-UHFFFAOYSA-N 2-[[2-(2-methyl-3-phenylphenyl)-6-(pyridin-2-ylmethoxy)-1,3-benzoxazol-5-yl]methylamino]ethanol Chemical compound CC1=C(C=CC=C1C=1OC2=C(N=1)C=C(C(=C2)OCC1=NC=CC=C1)CNCCO)C1=CC=CC=C1 GEHNLXIJMMXQRC-UHFFFAOYSA-N 0.000 claims description 2
- QIQCGXKKPNNLIA-UHFFFAOYSA-N 2-[[2-(2-methyl-3-phenylphenyl)-[1,3]oxazolo[5,4-c]pyridin-6-yl]methylamino]ethanol Chemical compound CC1=C(C=CC=C1C=1OC=2C=NC(=CC=2N=1)CNCCO)C1=CC=CC=C1 QIQCGXKKPNNLIA-UHFFFAOYSA-N 0.000 claims description 2
- UNWZQACEBMIMOT-UHFFFAOYSA-N 2-[[2-(2-methyl-3-phenylphenyl)furo[2,3-b]pyridin-5-yl]methylamino]ethanol Chemical compound CC1=C(C=CC=C1C1=CC=2C(=NC=C(C=2)CNCCO)O1)C1=CC=CC=C1 UNWZQACEBMIMOT-UHFFFAOYSA-N 0.000 claims description 2
- MTJPMMVLXHXMAH-UHFFFAOYSA-N 2-[[2-(2-methyl-3-phenylphenyl)furo[2,3-b]pyridin-6-yl]methylamino]ethanol Chemical compound CC1=C(C=CC=C1C1=CC=2C(=NC(=CC=2)CNCCO)O1)C1=CC=CC=C1 MTJPMMVLXHXMAH-UHFFFAOYSA-N 0.000 claims description 2
- MQVSHGQKTJHYIR-UHFFFAOYSA-N 2-[[2-(2-methyl-3-phenylphenyl)furo[3,2-b]pyridin-5-yl]methylamino]ethanol Chemical compound CC1=C(C=CC=C1C1=CC2=NC(=CC=C2O1)CNCCO)C1=CC=CC=C1 MQVSHGQKTJHYIR-UHFFFAOYSA-N 0.000 claims description 2
- MHIGPOAVCFTBOP-UHFFFAOYSA-N 2-[[2-[3-(2,3-dihydro-1,4-benzodioxin-6-yl)-2-methylphenyl]-7-methyl-1,3-benzoxazol-5-yl]methylamino]ethanol Chemical compound O1CCOC2=C1C=CC(=C2)C=1C(=C(C=CC=1)C=1OC2=C(N=1)C=C(C=C2C)CNCCO)C MHIGPOAVCFTBOP-UHFFFAOYSA-N 0.000 claims description 2
- DXVDOQLHOJBECW-UHFFFAOYSA-N 2-[[2-[3-(2-fluorophenyl)-2-methylphenyl]-5-[(2-hydroxyethylamino)methyl]-1,3-benzoxazol-6-yl]oxy]acetonitrile Chemical compound FC1=C(C=CC=C1)C1=C(C(=CC=C1)C=1OC2=C(N=1)C=C(C(=C2)OCC#N)CNCCO)C DXVDOQLHOJBECW-UHFFFAOYSA-N 0.000 claims description 2
- NKDFRHRYBVIZMD-UHFFFAOYSA-N 2-[[2-[3-(cyclohexen-1-yl)-2-methylphenyl]-5-[(2-hydroxyethylamino)methyl]-1,3-benzoxazol-6-yl]oxy]acetonitrile Chemical compound C1(=CCCCC1)C=1C(=C(C=CC=1)C=1OC2=C(N=1)C=C(C(=C2)OCC#N)CNCCO)C NKDFRHRYBVIZMD-UHFFFAOYSA-N 0.000 claims description 2
- VFOMDPPPRGYNHX-UHFFFAOYSA-N 2-[[4-methyl-2-(2-methyl-3-phenylphenyl)-1,3-benzothiazol-6-yl]methylamino]ethanol Chemical compound CC1=CC(=CC2=C1N=C(S2)C=1C(=C(C=CC=1)C1=CC=CC=C1)C)CNCCO VFOMDPPPRGYNHX-UHFFFAOYSA-N 0.000 claims description 2
- UXKBYCBXVYYRLV-UHFFFAOYSA-N 2-[[5-[(2-hydroxyethylamino)methyl]-2-(2-methyl-3-phenylphenyl)-1,3-benzoxazol-6-yl]oxy]acetonitrile Chemical compound OCCNCC=1C(=CC2=C(N=C(O2)C=2C(=C(C=CC=2)C2=CC=CC=C2)C)C=1)OCC#N UXKBYCBXVYYRLV-UHFFFAOYSA-N 0.000 claims description 2
- VHHDHDGZDVIVEH-UHFFFAOYSA-N 2-[[6-methoxy-2-(2-methyl-3-phenylphenyl)-1,3-benzoxazol-5-yl]methylamino]ethanol Chemical compound COC1=CC2=C(N=C(O2)C=2C(=C(C=CC=2)C2=CC=CC=C2)C)C=C1CNCCO VHHDHDGZDVIVEH-UHFFFAOYSA-N 0.000 claims description 2
- SSMMLRVAQHQCMT-UHFFFAOYSA-N 2-[[7-methyl-2-(2-methyl-3-phenylphenyl)-1,3-benzoxazol-5-yl]methylamino]ethanol Chemical compound CC1=CC(=CC=2N=C(OC=21)C=1C(=C(C=CC=1)C1=CC=CC=C1)C)CNCCO SSMMLRVAQHQCMT-UHFFFAOYSA-N 0.000 claims description 2
- FWIXRKUGYYFFQG-UHFFFAOYSA-N 3-[[5-[(2-hydroxyethylamino)methyl]-2-(2-methyl-3-phenylphenyl)-1,3-benzoxazol-6-yl]oxymethyl]benzonitrile Chemical compound OCCNCC=1C(=CC2=C(N=C(O2)C=2C(=C(C=CC=2)C2=CC=CC=C2)C)C=1)OCC=1C=C(C#N)C=CC=1 FWIXRKUGYYFFQG-UHFFFAOYSA-N 0.000 claims description 2
- 206010000830 Acute leukaemia Diseases 0.000 claims description 2
- 206010061424 Anal cancer Diseases 0.000 claims description 2
- 208000007860 Anus Neoplasms Diseases 0.000 claims description 2
- 208000010839 B-cell chronic lymphocytic leukemia Diseases 0.000 claims description 2
- 206010005949 Bone cancer Diseases 0.000 claims description 2
- 208000018084 Bone neoplasm Diseases 0.000 claims description 2
- 206010008342 Cervix carcinoma Diseases 0.000 claims description 2
- 208000001976 Endocrine Gland Neoplasms Diseases 0.000 claims description 2
- 201000001342 Fallopian tube cancer Diseases 0.000 claims description 2
- 208000013452 Fallopian tube neoplasm Diseases 0.000 claims description 2
- 208000021519 Hodgkin lymphoma Diseases 0.000 claims description 2
- 208000007766 Kaposi sarcoma Diseases 0.000 claims description 2
- 206010052178 Lymphocytic lymphoma Diseases 0.000 claims description 2
- 208000032271 Malignant tumor of penis Diseases 0.000 claims description 2
- 208000025205 Mantle-Cell Lymphoma Diseases 0.000 claims description 2
- 206010027480 Metastatic malignant melanoma Diseases 0.000 claims description 2
- 208000034578 Multiple myelomas Diseases 0.000 claims description 2
- 208000000821 Parathyroid Neoplasms Diseases 0.000 claims description 2
- 208000002471 Penile Neoplasms Diseases 0.000 claims description 2
- 206010034299 Penile cancer Diseases 0.000 claims description 2
- 208000007913 Pituitary Neoplasms Diseases 0.000 claims description 2
- 201000005746 Pituitary adenoma Diseases 0.000 claims description 2
- 206010061538 Pituitary tumour benign Diseases 0.000 claims description 2
- 206010035226 Plasma cell myeloma Diseases 0.000 claims description 2
- 208000015634 Rectal Neoplasms Diseases 0.000 claims description 2
- 208000000453 Skin Neoplasms Diseases 0.000 claims description 2
- 208000021712 Soft tissue sarcoma Diseases 0.000 claims description 2
- 206010042971 T-cell lymphoma Diseases 0.000 claims description 2
- 208000027585 T-cell non-Hodgkin lymphoma Diseases 0.000 claims description 2
- 208000024313 Testicular Neoplasms Diseases 0.000 claims description 2
- 206010057644 Testis cancer Diseases 0.000 claims description 2
- 208000024770 Thyroid neoplasm Diseases 0.000 claims description 2
- 206010046431 Urethral cancer Diseases 0.000 claims description 2
- 208000006105 Uterine Cervical Neoplasms Diseases 0.000 claims description 2
- 206010047741 Vulval cancer Diseases 0.000 claims description 2
- 208000004354 Vulvar Neoplasms Diseases 0.000 claims description 2
- 201000005188 adrenal gland cancer Diseases 0.000 claims description 2
- 208000024447 adrenal gland neoplasm Diseases 0.000 claims description 2
- 201000011165 anus cancer Diseases 0.000 claims description 2
- 239000010425 asbestos Substances 0.000 claims description 2
- 201000010881 cervical cancer Diseases 0.000 claims description 2
- 230000001684 chronic effect Effects 0.000 claims description 2
- 208000024207 chronic leukemia Diseases 0.000 claims description 2
- 208000009060 clear cell adenocarcinoma Diseases 0.000 claims description 2
- 208000035250 cutaneous malignant susceptibility to 1 melanoma Diseases 0.000 claims description 2
- 206010012818 diffuse large B-cell lymphoma Diseases 0.000 claims description 2
- 208000005017 glioblastoma Diseases 0.000 claims description 2
- 201000005787 hematologic cancer Diseases 0.000 claims description 2
- 208000024200 hematopoietic and lymphoid system neoplasm Diseases 0.000 claims description 2
- 208000032839 leukemia Diseases 0.000 claims description 2
- 208000029559 malignant endocrine neoplasm Diseases 0.000 claims description 2
- 208000020984 malignant renal pelvis neoplasm Diseases 0.000 claims description 2
- 208000026045 malignant tumor of parathyroid gland Diseases 0.000 claims description 2
- 208000021039 metastatic melanoma Diseases 0.000 claims description 2
- 230000036961 partial effect Effects 0.000 claims description 2
- 208000021310 pituitary gland adenoma Diseases 0.000 claims description 2
- 206010038038 rectal cancer Diseases 0.000 claims description 2
- 201000001275 rectum cancer Diseases 0.000 claims description 2
- 201000007444 renal pelvis carcinoma Diseases 0.000 claims description 2
- 229910052895 riebeckite Inorganic materials 0.000 claims description 2
- 201000000849 skin cancer Diseases 0.000 claims description 2
- 230000004936 stimulating effect Effects 0.000 claims description 2
- 201000003120 testicular cancer Diseases 0.000 claims description 2
- 201000002510 thyroid cancer Diseases 0.000 claims description 2
- 208000013077 thyroid gland carcinoma Diseases 0.000 claims description 2
- 230000005747 tumor angiogenesis Effects 0.000 claims description 2
- 206010046885 vaginal cancer Diseases 0.000 claims description 2
- 208000013139 vaginal neoplasm Diseases 0.000 claims description 2
- 201000005102 vulva cancer Diseases 0.000 claims description 2
- 125000004198 2-fluorophenyl group Chemical group [H]C1=C([H])C(F)=C(*)C([H])=C1[H] 0.000 claims 1
- 206010006143 Brain stem glioma Diseases 0.000 claims 1
- 201000003741 Gastrointestinal carcinoma Diseases 0.000 claims 1
- 208000031671 Large B-Cell Diffuse Lymphoma Diseases 0.000 claims 1
- 208000006265 Renal cell carcinoma Diseases 0.000 claims 1
- 201000003444 follicular lymphoma Diseases 0.000 claims 1
- 230000005764 inhibitory process Effects 0.000 claims 1
- 201000002313 intestinal cancer Diseases 0.000 claims 1
- 201000002575 ocular melanoma Diseases 0.000 claims 1
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 144
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 143
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 126
- 238000000034 method Methods 0.000 description 112
- 238000004895 liquid chromatography mass spectrometry Methods 0.000 description 106
- 239000000203 mixture Substances 0.000 description 106
- 239000000047 product Substances 0.000 description 100
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 77
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical class CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 76
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 72
- 235000019439 ethyl acetate Nutrition 0.000 description 67
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 56
- 239000011541 reaction mixture Substances 0.000 description 56
- 102100040678 Programmed cell death protein 1 Human genes 0.000 description 41
- 238000002953 preparative HPLC Methods 0.000 description 40
- 101710089372 Programmed cell death protein 1 Proteins 0.000 description 39
- 239000000243 solution Substances 0.000 description 39
- HZAXFHJVJLSVMW-UHFFFAOYSA-N 2-Aminoethan-1-ol Chemical compound NCCO HZAXFHJVJLSVMW-UHFFFAOYSA-N 0.000 description 38
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 31
- 239000003112 inhibitor Substances 0.000 description 30
- 238000010790 dilution Methods 0.000 description 29
- 239000012895 dilution Substances 0.000 description 29
- 125000000753 cycloalkyl group Chemical group 0.000 description 28
- 229910052943 magnesium sulfate Inorganic materials 0.000 description 28
- 235000019341 magnesium sulphate Nutrition 0.000 description 28
- KDLHZDBZIXYQEI-UHFFFAOYSA-N Palladium Chemical compound [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 26
- 239000012074 organic phase Substances 0.000 description 25
- 239000000741 silica gel Substances 0.000 description 24
- 229910002027 silica gel Inorganic materials 0.000 description 24
- 125000004429 atom Chemical group 0.000 description 23
- 239000013058 crude material Substances 0.000 description 23
- 238000011282 treatment Methods 0.000 description 22
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 21
- 238000004440 column chromatography Methods 0.000 description 21
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 20
- 238000003818 flash chromatography Methods 0.000 description 20
- 238000000746 purification Methods 0.000 description 20
- VHUUQVKOLVNVRT-UHFFFAOYSA-N Ammonium hydroxide Chemical compound [NH4+].[OH-] VHUUQVKOLVNVRT-UHFFFAOYSA-N 0.000 description 19
- 235000011114 ammonium hydroxide Nutrition 0.000 description 19
- 238000006243 chemical reaction Methods 0.000 description 19
- HXEACLLIILLPRG-YFKPBYRVSA-N L-pipecolic acid Chemical group [O-]C(=O)[C@@H]1CCCC[NH2+]1 HXEACLLIILLPRG-YFKPBYRVSA-N 0.000 description 18
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 17
- LWIHDJKSTIGBAC-UHFFFAOYSA-K tripotassium phosphate Chemical compound [K+].[K+].[K+].[O-]P([O-])([O-])=O LWIHDJKSTIGBAC-UHFFFAOYSA-K 0.000 description 16
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 15
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 13
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 12
- 208000015181 infectious disease Diseases 0.000 description 12
- 229910052740 iodine Inorganic materials 0.000 description 12
- MUJIDPITZJWBSW-UHFFFAOYSA-N palladium(2+) Chemical compound [Pd+2] MUJIDPITZJWBSW-UHFFFAOYSA-N 0.000 description 12
- 241000700605 Viruses Species 0.000 description 11
- 239000004480 active ingredient Substances 0.000 description 11
- 150000001721 carbon Chemical group 0.000 description 11
- 239000003054 catalyst Substances 0.000 description 11
- 125000003963 dichloro group Chemical group Cl* 0.000 description 11
- KTWOOEGAPBSYNW-UHFFFAOYSA-N ferrocene Chemical compound [Fe+2].C=1C=C[CH-]C=1.C=1C=C[CH-]C=1 KTWOOEGAPBSYNW-UHFFFAOYSA-N 0.000 description 11
- 229910052763 palladium Inorganic materials 0.000 description 11
- 101001043818 Mus musculus Interleukin-31 receptor subunit alpha Proteins 0.000 description 10
- 239000002585 base Substances 0.000 description 10
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 10
- NKLCNNUWBJBICK-UHFFFAOYSA-N dess–martin periodinane Chemical compound C1=CC=C2I(OC(=O)C)(OC(C)=O)(OC(C)=O)OC(=O)C2=C1 NKLCNNUWBJBICK-UHFFFAOYSA-N 0.000 description 10
- 125000002950 monocyclic group Chemical group 0.000 description 10
- 238000012360 testing method Methods 0.000 description 10
- 208000035473 Communicable disease Diseases 0.000 description 9
- 102000037982 Immune checkpoint proteins Human genes 0.000 description 9
- 108091008036 Immune checkpoint proteins Proteins 0.000 description 9
- 210000004027 cell Anatomy 0.000 description 9
- 238000009472 formulation Methods 0.000 description 9
- 230000006916 protein interaction Effects 0.000 description 9
- 239000011734 sodium Substances 0.000 description 9
- 239000002904 solvent Substances 0.000 description 9
- IFMFMTSKMLYKOB-UHFFFAOYSA-N 2-methyl-3-phenylbenzaldehyde Chemical compound CC1=C(C=O)C=CC=C1C1=CC=CC=C1 IFMFMTSKMLYKOB-UHFFFAOYSA-N 0.000 description 8
- PCLIMKBDDGJMGD-UHFFFAOYSA-N N-bromosuccinimide Chemical compound BrN1C(=O)CCC1=O PCLIMKBDDGJMGD-UHFFFAOYSA-N 0.000 description 8
- 150000001299 aldehydes Chemical class 0.000 description 8
- 230000037396 body weight Effects 0.000 description 8
- 239000003795 chemical substances by application Substances 0.000 description 8
- 125000004438 haloalkoxy group Chemical group 0.000 description 8
- 229910000160 potassium phosphate Inorganic materials 0.000 description 8
- 235000011009 potassium phosphates Nutrition 0.000 description 8
- 108090000623 proteins and genes Proteins 0.000 description 8
- 239000007787 solid Substances 0.000 description 8
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 8
- 230000001225 therapeutic effect Effects 0.000 description 8
- 229940045513 CTLA4 antagonist Drugs 0.000 description 7
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 7
- 239000002253 acid Substances 0.000 description 7
- 125000002947 alkylene group Chemical group 0.000 description 7
- 238000003556 assay Methods 0.000 description 7
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 7
- 238000001816 cooling Methods 0.000 description 7
- 239000002552 dosage form Substances 0.000 description 7
- 125000001188 haloalkyl group Chemical group 0.000 description 7
- 229940126546 immune checkpoint molecule Drugs 0.000 description 7
- 239000001301 oxygen Substances 0.000 description 7
- 102000004169 proteins and genes Human genes 0.000 description 7
- 238000006467 substitution reaction Methods 0.000 description 7
- 239000011593 sulfur Substances 0.000 description 7
- 239000000725 suspension Substances 0.000 description 7
- REXUYBKPWIPONM-UHFFFAOYSA-N 2-bromoacetonitrile Chemical compound BrCC#N REXUYBKPWIPONM-UHFFFAOYSA-N 0.000 description 6
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 6
- WSFSSNUMVMOOMR-UHFFFAOYSA-N Formaldehyde Chemical compound O=C WSFSSNUMVMOOMR-UHFFFAOYSA-N 0.000 description 6
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 6
- 229920000168 Microcrystalline cellulose Polymers 0.000 description 6
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 6
- 238000006069 Suzuki reaction reaction Methods 0.000 description 6
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 6
- JFDZBHWFFUWGJE-UHFFFAOYSA-N benzonitrile Chemical compound N#CC1=CC=CC=C1 JFDZBHWFFUWGJE-UHFFFAOYSA-N 0.000 description 6
- 125000002619 bicyclic group Chemical group 0.000 description 6
- 230000015572 biosynthetic process Effects 0.000 description 6
- 239000012043 crude product Substances 0.000 description 6
- 238000007865 diluting Methods 0.000 description 6
- 230000000694 effects Effects 0.000 description 6
- 239000004615 ingredient Substances 0.000 description 6
- 239000007788 liquid Substances 0.000 description 6
- 235000019813 microcrystalline cellulose Nutrition 0.000 description 6
- 239000008108 microcrystalline cellulose Substances 0.000 description 6
- 229940016286 microcrystalline cellulose Drugs 0.000 description 6
- 125000005476 oxopyrrolidinyl group Chemical group 0.000 description 6
- 244000052769 pathogen Species 0.000 description 6
- 239000000843 powder Substances 0.000 description 6
- 125000006239 protecting group Chemical group 0.000 description 6
- 239000000126 substance Substances 0.000 description 6
- 208000024891 symptom Diseases 0.000 description 6
- 238000003786 synthesis reaction Methods 0.000 description 6
- 125000000335 thiazolyl group Chemical group 0.000 description 6
- 125000001544 thienyl group Chemical group 0.000 description 6
- 125000001401 1,2,4-triazol-4-yl group Chemical group N=1N=C([H])N([*])C=1[H] 0.000 description 5
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 5
- YVVISLCKIQNUDL-UHFFFAOYSA-N 5-bromo-6-oxo-1h-pyridine-2-carboxylic acid Chemical compound OC(=O)C1=CC=C(Br)C(=O)N1 YVVISLCKIQNUDL-UHFFFAOYSA-N 0.000 description 5
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 5
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 5
- 229920003171 Poly (ethylene oxide) Polymers 0.000 description 5
- 210000001744 T-lymphocyte Anatomy 0.000 description 5
- 230000004913 activation Effects 0.000 description 5
- 239000000427 antigen Substances 0.000 description 5
- 239000012267 brine Substances 0.000 description 5
- 230000008878 coupling Effects 0.000 description 5
- 238000010168 coupling process Methods 0.000 description 5
- 238000005859 coupling reaction Methods 0.000 description 5
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 5
- CGJKMRXBVATMDG-UHFFFAOYSA-N furo[2,3-b]pyridine-6-carbaldehyde Chemical compound O=CC1=CC=C2C=COC2=N1 CGJKMRXBVATMDG-UHFFFAOYSA-N 0.000 description 5
- 238000002868 homogeneous time resolved fluorescence Methods 0.000 description 5
- 239000000543 intermediate Substances 0.000 description 5
- 230000003902 lesion Effects 0.000 description 5
- 125000005647 linker group Chemical group 0.000 description 5
- 230000003647 oxidation Effects 0.000 description 5
- 238000007254 oxidation reaction Methods 0.000 description 5
- 125000004043 oxo group Chemical group O=* 0.000 description 5
- 229960002621 pembrolizumab Drugs 0.000 description 5
- 238000002360 preparation method Methods 0.000 description 5
- 102000004196 processed proteins & peptides Human genes 0.000 description 5
- 108090000765 processed proteins & peptides Proteins 0.000 description 5
- 125000003226 pyrazolyl group Chemical group 0.000 description 5
- 125000006413 ring segment Chemical group 0.000 description 5
- 230000011664 signaling Effects 0.000 description 5
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 5
- 239000003826 tablet Substances 0.000 description 5
- 238000002560 therapeutic procedure Methods 0.000 description 5
- 210000001519 tissue Anatomy 0.000 description 5
- 210000004881 tumor cell Anatomy 0.000 description 5
- ARACVYIZGUFEFH-UHFFFAOYSA-N 2-(2-methyl-3-phenylphenyl)furo[2,3-b]pyridine-6-carbaldehyde Chemical compound CC1=C(C=CC=C1C1=CC=2C(=NC(=CC=2)C=O)O1)C1=CC=CC=C1 ARACVYIZGUFEFH-UHFFFAOYSA-N 0.000 description 4
- WSVLPVUVIUVCRA-KPKNDVKVSA-N Alpha-lactose monohydrate Chemical compound O.O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O WSVLPVUVIUVCRA-KPKNDVKVSA-N 0.000 description 4
- 208000035143 Bacterial infection Diseases 0.000 description 4
- 108010021064 CTLA-4 Antigen Proteins 0.000 description 4
- 102000008203 CTLA-4 Antigen Human genes 0.000 description 4
- 206010017533 Fungal infection Diseases 0.000 description 4
- 108010017213 Granulocyte-Macrophage Colony-Stimulating Factor Proteins 0.000 description 4
- 102000004457 Granulocyte-Macrophage Colony-Stimulating Factor Human genes 0.000 description 4
- 101000851370 Homo sapiens Tumor necrosis factor receptor superfamily member 9 Proteins 0.000 description 4
- 241000701806 Human papillomavirus Species 0.000 description 4
- 241000712079 Measles morbillivirus Species 0.000 description 4
- 241001465754 Metazoa Species 0.000 description 4
- 101100407308 Mus musculus Pdcd1lg2 gene Proteins 0.000 description 4
- 208000031888 Mycoses Diseases 0.000 description 4
- 239000007832 Na2SO4 Substances 0.000 description 4
- 208000030852 Parasitic disease Diseases 0.000 description 4
- 108700030875 Programmed Cell Death 1 Ligand 2 Proteins 0.000 description 4
- 102100024213 Programmed cell death 1 ligand 2 Human genes 0.000 description 4
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 4
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 4
- 108091008874 T cell receptors Proteins 0.000 description 4
- 102100036856 Tumor necrosis factor receptor superfamily member 9 Human genes 0.000 description 4
- 150000001345 alkine derivatives Chemical class 0.000 description 4
- 108091007433 antigens Proteins 0.000 description 4
- 102000036639 antigens Human genes 0.000 description 4
- 125000002393 azetidinyl group Chemical group 0.000 description 4
- 208000022362 bacterial infectious disease Diseases 0.000 description 4
- 125000001995 cyclobutyl group Chemical group [H]C1([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 4
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 4
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 4
- ZUOUZKKEUPVFJK-UHFFFAOYSA-N diphenyl Chemical compound C1=CC=CC=C1C1=CC=CC=C1 ZUOUZKKEUPVFJK-UHFFFAOYSA-N 0.000 description 4
- 150000002148 esters Chemical class 0.000 description 4
- 125000002541 furyl group Chemical group 0.000 description 4
- 229910052736 halogen Inorganic materials 0.000 description 4
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 4
- 125000002883 imidazolyl group Chemical group 0.000 description 4
- 238000009169 immunotherapy Methods 0.000 description 4
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 4
- 229960001021 lactose monohydrate Drugs 0.000 description 4
- 239000003446 ligand Substances 0.000 description 4
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 4
- 239000012044 organic layer Substances 0.000 description 4
- 125000002971 oxazolyl group Chemical group 0.000 description 4
- 238000007911 parenteral administration Methods 0.000 description 4
- 239000002245 particle Substances 0.000 description 4
- 230000037361 pathway Effects 0.000 description 4
- 239000006187 pill Substances 0.000 description 4
- 125000003367 polycyclic group Chemical group 0.000 description 4
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 4
- 125000004076 pyridyl group Chemical group 0.000 description 4
- 125000000168 pyrrolyl group Chemical group 0.000 description 4
- 230000004044 response Effects 0.000 description 4
- 230000019491 signal transduction Effects 0.000 description 4
- 229910052938 sodium sulfate Inorganic materials 0.000 description 4
- 235000011152 sodium sulphate Nutrition 0.000 description 4
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 4
- 229960005486 vaccine Drugs 0.000 description 4
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 4
- BGTLHJPGBIVQLJ-UHFFFAOYSA-N (2-methyl-3-phenylphenyl)methanol Chemical compound CC1=C(CO)C=CC=C1C1=CC=CC=C1 BGTLHJPGBIVQLJ-UHFFFAOYSA-N 0.000 description 3
- 125000006645 (C3-C4) cycloalkyl group Chemical group 0.000 description 3
- 125000006704 (C5-C6) cycloalkyl group Chemical group 0.000 description 3
- HZNVUJQVZSTENZ-UHFFFAOYSA-N 2,3-dichloro-5,6-dicyano-1,4-benzoquinone Chemical compound ClC1=C(Cl)C(=O)C(C#N)=C(C#N)C1=O HZNVUJQVZSTENZ-UHFFFAOYSA-N 0.000 description 3
- GUBGYTABKSRVRQ-UHFFFAOYSA-N 2-(hydroxymethyl)-6-[4,5,6-trihydroxy-2-(hydroxymethyl)oxan-3-yl]oxyoxane-3,4,5-triol Chemical compound OCC1OC(OC2C(O)C(O)C(O)OC2CO)C(O)C(O)C1O GUBGYTABKSRVRQ-UHFFFAOYSA-N 0.000 description 3
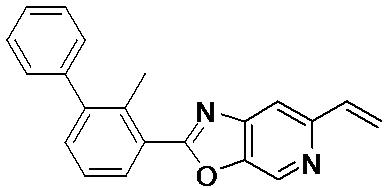
- XXPCCZNABRYMQG-UHFFFAOYSA-N 5-ethenyl-7-methyl-2-(2-methyl-3-phenylphenyl)furo[3,2-b]pyridine Chemical compound CC1=C2C(=NC(=C1)C=C)C=C(O2)C=1C(=C(C=CC=1)C1=CC=CC=C1)C XXPCCZNABRYMQG-UHFFFAOYSA-N 0.000 description 3
- 125000006163 5-membered heteroaryl group Chemical group 0.000 description 3
- ZWNXZAAWGKNBDN-UHFFFAOYSA-N 6-(2-methyl-3-phenylphenyl)furo[2,3-b]pyrazine-2-carbaldehyde Chemical compound CC1=C(C=CC=C1C1=CC=2C(=NC=C(N=2)C=O)O1)C1=CC=CC=C1 ZWNXZAAWGKNBDN-UHFFFAOYSA-N 0.000 description 3
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 3
- WFDIJRYMOXRFFG-UHFFFAOYSA-N Acetic anhydride Chemical compound CC(=O)OC(C)=O WFDIJRYMOXRFFG-UHFFFAOYSA-N 0.000 description 3
- WVDDGKGOMKODPV-UHFFFAOYSA-N Benzyl alcohol Chemical compound OCC1=CC=CC=C1 WVDDGKGOMKODPV-UHFFFAOYSA-N 0.000 description 3
- 102000004127 Cytokines Human genes 0.000 description 3
- 108090000695 Cytokines Proteins 0.000 description 3
- 238000006646 Dess-Martin oxidation reaction Methods 0.000 description 3
- 241000224466 Giardia Species 0.000 description 3
- 241000282412 Homo Species 0.000 description 3
- 101001137987 Homo sapiens Lymphocyte activation gene 3 protein Proteins 0.000 description 3
- 101000611936 Homo sapiens Programmed cell death protein 1 Proteins 0.000 description 3
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 3
- 102100037850 Interferon gamma Human genes 0.000 description 3
- 108010074328 Interferon-gamma Proteins 0.000 description 3
- 108010002350 Interleukin-2 Proteins 0.000 description 3
- 102000000588 Interleukin-2 Human genes 0.000 description 3
- 102000017578 LAG3 Human genes 0.000 description 3
- 241000124008 Mammalia Species 0.000 description 3
- 150000001204 N-oxides Chemical class 0.000 description 3
- 102000038030 PI3Ks Human genes 0.000 description 3
- 108091007960 PI3Ks Proteins 0.000 description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 3
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical group C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 3
- 102000016266 T-Cell Antigen Receptors Human genes 0.000 description 3
- DKGAVHZHDRPRBM-UHFFFAOYSA-N Tert-Butanol Chemical compound CC(C)(C)O DKGAVHZHDRPRBM-UHFFFAOYSA-N 0.000 description 3
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 3
- 102100033177 Vascular endothelial growth factor receptor 2 Human genes 0.000 description 3
- 230000002378 acidificating effect Effects 0.000 description 3
- 150000007513 acids Chemical class 0.000 description 3
- 150000001336 alkenes Chemical class 0.000 description 3
- 150000001412 amines Chemical class 0.000 description 3
- 239000002246 antineoplastic agent Substances 0.000 description 3
- 239000007864 aqueous solution Substances 0.000 description 3
- 150000001502 aryl halides Chemical class 0.000 description 3
- 230000001580 bacterial effect Effects 0.000 description 3
- 125000005605 benzo group Chemical group 0.000 description 3
- 239000004305 biphenyl Substances 0.000 description 3
- 235000010290 biphenyl Nutrition 0.000 description 3
- 229940125904 compound 1 Drugs 0.000 description 3
- 125000004093 cyano group Chemical group *C#N 0.000 description 3
- 210000004443 dendritic cell Anatomy 0.000 description 3
- 229910052805 deuterium Inorganic materials 0.000 description 3
- 229940079593 drug Drugs 0.000 description 3
- 229950009791 durvalumab Drugs 0.000 description 3
- 239000000284 extract Substances 0.000 description 3
- 239000000706 filtrate Substances 0.000 description 3
- 230000002538 fungal effect Effects 0.000 description 3
- 230000012010 growth Effects 0.000 description 3
- 150000002367 halogens Chemical class 0.000 description 3
- 208000006454 hepatitis Diseases 0.000 description 3
- 231100000283 hepatitis Toxicity 0.000 description 3
- 125000000623 heterocyclic group Chemical group 0.000 description 3
- 239000001257 hydrogen Substances 0.000 description 3
- 239000001866 hydroxypropyl methyl cellulose Substances 0.000 description 3
- 235000010979 hydroxypropyl methyl cellulose Nutrition 0.000 description 3
- 229920003088 hydroxypropyl methyl cellulose Polymers 0.000 description 3
- UFVKGYZPFZQRLF-UHFFFAOYSA-N hydroxypropyl methyl cellulose Chemical compound OC1C(O)C(OC)OC(CO)C1OC1C(O)C(O)C(OC2C(C(O)C(OC3C(C(O)C(O)C(CO)O3)O)C(CO)O2)O)C(CO)O1 UFVKGYZPFZQRLF-UHFFFAOYSA-N 0.000 description 3
- 238000000338 in vitro Methods 0.000 description 3
- 206010022000 influenza Diseases 0.000 description 3
- 239000011630 iodine Substances 0.000 description 3
- 125000000842 isoxazolyl group Chemical group 0.000 description 3
- 238000002372 labelling Methods 0.000 description 3
- 238000004519 manufacturing process Methods 0.000 description 3
- 230000007246 mechanism Effects 0.000 description 3
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 description 3
- PDBVQSFKFOUWSL-UHFFFAOYSA-N methyl 2-(2-methyl-3-phenylphenyl)furo[2,3-b]pyridine-6-carboxylate Chemical compound CC1=C(C=CC=C1C1=CC=2C(=NC(=CC=2)C(=O)OC)O1)C1=CC=CC=C1 PDBVQSFKFOUWSL-UHFFFAOYSA-N 0.000 description 3
- OZKJEDPAZXWTSM-UHFFFAOYSA-N methyl 5-amino-2,4-dihydroxybenzoate Chemical compound COC(=O)C1=CC(N)=C(O)C=C1O OZKJEDPAZXWTSM-UHFFFAOYSA-N 0.000 description 3
- TWOWZVIHHITOCV-UHFFFAOYSA-N methyl 6-hydroxy-2-(2-methyl-3-phenylphenyl)-1,3-benzoxazole-5-carboxylate Chemical compound OC1=CC2=C(N=C(O2)C=2C(=C(C=CC=2)C2=CC=CC=C2)C)C=C1C(=O)OC TWOWZVIHHITOCV-UHFFFAOYSA-N 0.000 description 3
- 125000001624 naphthyl group Chemical group 0.000 description 3
- 229960003301 nivolumab Drugs 0.000 description 3
- 239000002674 ointment Substances 0.000 description 3
- 230000026731 phosphorylation Effects 0.000 description 3
- 238000006366 phosphorylation reaction Methods 0.000 description 3
- 125000003386 piperidinyl group Chemical group 0.000 description 3
- 238000000159 protein binding assay Methods 0.000 description 3
- 238000010926 purge Methods 0.000 description 3
- 125000003373 pyrazinyl group Chemical group 0.000 description 3
- 125000002098 pyridazinyl group Chemical group 0.000 description 3
- 238000007363 ring formation reaction Methods 0.000 description 3
- 239000012321 sodium triacetoxyborohydride Substances 0.000 description 3
- 239000012453 solvate Substances 0.000 description 3
- 238000004809 thin layer chromatography Methods 0.000 description 3
- 239000012049 topical pharmaceutical composition Substances 0.000 description 3
- 241000701161 unidentified adenovirus Species 0.000 description 3
- 241001529453 unidentified herpesvirus Species 0.000 description 3
- 230000003612 virological effect Effects 0.000 description 3
- KWGRBVOPPLSCSI-WPRPVWTQSA-N (-)-ephedrine Chemical compound CN[C@@H](C)[C@H](O)C1=CC=CC=C1 KWGRBVOPPLSCSI-WPRPVWTQSA-N 0.000 description 2
- QCSLIRFWJPOENV-UHFFFAOYSA-N (2-fluorophenyl)boronic acid Chemical compound OB(O)C1=CC=CC=C1F QCSLIRFWJPOENV-UHFFFAOYSA-N 0.000 description 2
- 125000006700 (C1-C6) alkylthio group Chemical group 0.000 description 2
- 125000004607 1,2,3,4-tetrahydroquinolinyl group Chemical group N1(CCCC2=CC=CC=C12)* 0.000 description 2
- 125000004502 1,2,3-oxadiazolyl group Chemical group 0.000 description 2
- 125000004511 1,2,3-thiadiazolyl group Chemical group 0.000 description 2
- 125000001399 1,2,3-triazolyl group Chemical group N1N=NC(=C1)* 0.000 description 2
- 125000004504 1,2,4-oxadiazolyl group Chemical group 0.000 description 2
- 125000004514 1,2,4-thiadiazolyl group Chemical group 0.000 description 2
- 125000001376 1,2,4-triazolyl group Chemical group N1N=C(N=C1)* 0.000 description 2
- 125000004520 1,3,4-thiadiazolyl group Chemical group 0.000 description 2
- NOZVUPWWWWWFEV-UHFFFAOYSA-N 1,3-benzoxazole-5-carbaldehyde Chemical compound O=CC1=CC=C2OC=NC2=C1 NOZVUPWWWWWFEV-UHFFFAOYSA-N 0.000 description 2
- GPWNWKWQOLEVEQ-UHFFFAOYSA-N 2,4-diaminopyrimidine-5-carbaldehyde Chemical compound NC1=NC=C(C=O)C(N)=N1 GPWNWKWQOLEVEQ-UHFFFAOYSA-N 0.000 description 2
- UEJJHQNACJXSKW-UHFFFAOYSA-N 2-(2,6-dioxopiperidin-3-yl)-1H-isoindole-1,3(2H)-dione Chemical compound O=C1C2=CC=CC=C2C(=O)N1C1CCC(=O)NC1=O UEJJHQNACJXSKW-UHFFFAOYSA-N 0.000 description 2
- QTZSGIMSDOAZNT-UHFFFAOYSA-N 2-[[2-(3-bromo-2-methylphenyl)-5-[(2-hydroxyethylamino)methyl]-1,3-benzoxazol-6-yl]oxy]acetonitrile Chemical compound BrC=1C(=C(C=CC=1)C=1OC2=C(N=1)C=C(C(=C2)OCC#N)CNCCO)C QTZSGIMSDOAZNT-UHFFFAOYSA-N 0.000 description 2
- LAWLVHAMJJLRDP-UHFFFAOYSA-N 2-[[5-formyl-2-(2-methyl-3-phenylphenyl)-1,3-benzoxazol-6-yl]oxy]acetonitrile Chemical compound C(=O)C=1C(=CC2=C(N=C(O2)C=2C(=C(C=CC=2)C2=CC=CC=C2)C)C=1)OCC#N LAWLVHAMJJLRDP-UHFFFAOYSA-N 0.000 description 2
- DPGSPRJLAZGUBQ-UHFFFAOYSA-N 2-ethenyl-4,4,5,5-tetramethyl-1,3,2-dioxaborolane Chemical compound CC1(C)OB(C=C)OC1(C)C DPGSPRJLAZGUBQ-UHFFFAOYSA-N 0.000 description 2
- LPTADTJTTGBOIL-UHFFFAOYSA-N 2-formyl-6-phenylbenzonitrile Chemical compound O=CC1=CC=CC(C=2C=CC=CC=2)=C1C#N LPTADTJTTGBOIL-UHFFFAOYSA-N 0.000 description 2
- 239000001431 2-methylbenzaldehyde Substances 0.000 description 2
- MRNDJPJTSPDBHE-UHFFFAOYSA-N 3-(2,3-dihydro-1,4-benzodioxin-6-yl)-2-methylbenzaldehyde Chemical compound O1CCOC2=C1C=CC(=C2)C=1C(=C(C=O)C=CC=1)C MRNDJPJTSPDBHE-UHFFFAOYSA-N 0.000 description 2
- HHVUFPUWPWOWOA-UHFFFAOYSA-N 3-bromo-2-methylbenzaldehyde Chemical compound CC1=C(Br)C=CC=C1C=O HHVUFPUWPWOWOA-UHFFFAOYSA-N 0.000 description 2
- SMAGPNFNGTWVHI-UHFFFAOYSA-N 4-(2,3-dihydro-1,4-benzodioxin-6-yl)-3-methylpyridine-2-carbaldehyde Chemical compound O1CCOC2=C1C=CC(=C2)C1=C(C(=NC=C1)C=O)C SMAGPNFNGTWVHI-UHFFFAOYSA-N 0.000 description 2
- JPPGGOHDJOHSAG-UHFFFAOYSA-N 4-amino-6-chlorobenzene-1,3-diol Chemical compound NC1=CC(Cl)=C(O)C=C1O JPPGGOHDJOHSAG-UHFFFAOYSA-N 0.000 description 2
- NSPMIYGKQJPBQR-UHFFFAOYSA-N 4H-1,2,4-triazole Chemical compound C=1N=CNN=1 NSPMIYGKQJPBQR-UHFFFAOYSA-N 0.000 description 2
- QWSUEWOTLKIPNP-UHFFFAOYSA-N 5-chloro-7-methyl-2-(2-methyl-3-phenylphenyl)furo[3,2-b]pyridine Chemical compound ClC1=CC(=C2C(=N1)C=C(O2)C=1C(=C(C=CC=1)C1=CC=CC=C1)C)C QWSUEWOTLKIPNP-UHFFFAOYSA-N 0.000 description 2
- XVMSFILGAMDHEY-UHFFFAOYSA-N 6-(4-aminophenyl)sulfonylpyridin-3-amine Chemical compound C1=CC(N)=CC=C1S(=O)(=O)C1=CC=C(N)C=N1 XVMSFILGAMDHEY-UHFFFAOYSA-N 0.000 description 2
- MKBLVMGHGLNFIA-UHFFFAOYSA-N 6-bromo-2-iodo-4-methyl-1,3-benzothiazole Chemical compound BrC1=CC2=C(N=C(S2)I)C(=C1)C MKBLVMGHGLNFIA-UHFFFAOYSA-N 0.000 description 2
- RHWQEAGMEKKLTQ-UHFFFAOYSA-N 6-chloro-2-(2-methyl-3-phenylphenyl)-[1,3]oxazolo[5,4-c]pyridine Chemical compound ClC1=CC2=C(C=N1)OC(=N2)C=1C(=C(C=CC=1)C1=CC=CC=C1)C RHWQEAGMEKKLTQ-UHFFFAOYSA-N 0.000 description 2
- 125000004939 6-pyridyl group Chemical group N1=CC=CC=C1* 0.000 description 2
- 241000235389 Absidia Species 0.000 description 2
- 241000224424 Acanthamoeba sp. Species 0.000 description 2
- 208000006400 Arbovirus Encephalitis Diseases 0.000 description 2
- 241000228212 Aspergillus Species 0.000 description 2
- 102100029822 B- and T-lymphocyte attenuator Human genes 0.000 description 2
- 241000223848 Babesia microti Species 0.000 description 2
- 241000304886 Bacilli Species 0.000 description 2
- 241000193738 Bacillus anthracis Species 0.000 description 2
- 241001235572 Balantioides coli Species 0.000 description 2
- 241000228405 Blastomyces dermatitidis Species 0.000 description 2
- BTBUEUYNUDRHOZ-UHFFFAOYSA-N Borate Chemical compound [O-]B([O-])[O-] BTBUEUYNUDRHOZ-UHFFFAOYSA-N 0.000 description 2
- COVZYZSDYWQREU-UHFFFAOYSA-N Busulfan Chemical compound CS(=O)(=O)OCCCCOS(C)(=O)=O COVZYZSDYWQREU-UHFFFAOYSA-N 0.000 description 2
- 102100027207 CD27 antigen Human genes 0.000 description 2
- 102100038078 CD276 antigen Human genes 0.000 description 2
- 101710185679 CD276 antigen Proteins 0.000 description 2
- 101150013553 CD40 gene Proteins 0.000 description 2
- 241000222120 Candida <Saccharomycetales> Species 0.000 description 2
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 2
- ZEOWTGPWHLSLOG-UHFFFAOYSA-N Cc1ccc(cc1-c1ccc2c(n[nH]c2c1)-c1cnn(c1)C1CC1)C(=O)Nc1cccc(c1)C(F)(F)F Chemical compound Cc1ccc(cc1-c1ccc2c(n[nH]c2c1)-c1cnn(c1)C1CC1)C(=O)Nc1cccc(c1)C(F)(F)F ZEOWTGPWHLSLOG-UHFFFAOYSA-N 0.000 description 2
- 241000606161 Chlamydia Species 0.000 description 2
- 241000193155 Clostridium botulinum Species 0.000 description 2
- 241000223205 Coccidioides immitis Species 0.000 description 2
- 241000711573 Coronaviridae Species 0.000 description 2
- 241000709687 Coxsackievirus Species 0.000 description 2
- 201000007336 Cryptococcosis Diseases 0.000 description 2
- 241000221204 Cryptococcus neoformans Species 0.000 description 2
- 241000295636 Cryptosporidium sp. Species 0.000 description 2
- RGSFGYAAUTVSQA-UHFFFAOYSA-N Cyclopentane Chemical compound C1CCCC1 RGSFGYAAUTVSQA-UHFFFAOYSA-N 0.000 description 2
- 241000725619 Dengue virus Species 0.000 description 2
- YZCKVEUIGOORGS-OUBTZVSYSA-N Deuterium Chemical compound [2H] YZCKVEUIGOORGS-OUBTZVSYSA-N 0.000 description 2
- AOJJSUZBOXZQNB-TZSSRYMLSA-N Doxorubicin Chemical compound O([C@H]1C[C@@](O)(CC=2C(O)=C3C(=O)C=4C=CC=C(C=4C(=O)C3=C(O)C=21)OC)C(=O)CO)[C@H]1C[C@H](N)[C@H](O)[C@H](C)O1 AOJJSUZBOXZQNB-TZSSRYMLSA-N 0.000 description 2
- 241001115402 Ebolavirus Species 0.000 description 2
- 241001466953 Echovirus Species 0.000 description 2
- 241000224432 Entamoeba histolytica Species 0.000 description 2
- 241000709661 Enterovirus Species 0.000 description 2
- 241000991587 Enterovirus C Species 0.000 description 2
- 102000004190 Enzymes Human genes 0.000 description 2
- 108090000790 Enzymes Proteins 0.000 description 2
- 102100031968 Ephrin type-B receptor 2 Human genes 0.000 description 2
- 102100023593 Fibroblast growth factor receptor 1 Human genes 0.000 description 2
- 101710182386 Fibroblast growth factor receptor 1 Proteins 0.000 description 2
- 102100023600 Fibroblast growth factor receptor 2 Human genes 0.000 description 2
- 101710182389 Fibroblast growth factor receptor 2 Proteins 0.000 description 2
- 102100027842 Fibroblast growth factor receptor 3 Human genes 0.000 description 2
- 101710182396 Fibroblast growth factor receptor 3 Proteins 0.000 description 2
- 102100027844 Fibroblast growth factor receptor 4 Human genes 0.000 description 2
- 241000710831 Flavivirus Species 0.000 description 2
- 102100039619 Granulocyte colony-stimulating factor Human genes 0.000 description 2
- 102100034458 Hepatitis A virus cellular receptor 2 Human genes 0.000 description 2
- 208000005176 Hepatitis C Diseases 0.000 description 2
- 208000037262 Hepatitis delta Diseases 0.000 description 2
- 241000228404 Histoplasma capsulatum Species 0.000 description 2
- 101000864344 Homo sapiens B- and T-lymphocyte attenuator Proteins 0.000 description 2
- 101000914511 Homo sapiens CD27 antigen Proteins 0.000 description 2
- 101000917134 Homo sapiens Fibroblast growth factor receptor 4 Proteins 0.000 description 2
- 101001068133 Homo sapiens Hepatitis A virus cellular receptor 2 Proteins 0.000 description 2
- 101000916644 Homo sapiens Macrophage colony-stimulating factor 1 receptor Proteins 0.000 description 2
- 101000914514 Homo sapiens T-cell-specific surface glycoprotein CD28 Proteins 0.000 description 2
- 101000914484 Homo sapiens T-lymphocyte activation antigen CD80 Proteins 0.000 description 2
- 101000801234 Homo sapiens Tumor necrosis factor receptor superfamily member 18 Proteins 0.000 description 2
- 101000997835 Homo sapiens Tyrosine-protein kinase JAK1 Proteins 0.000 description 2
- 101000666896 Homo sapiens V-type immunoglobulin domain-containing suppressor of T-cell activation Proteins 0.000 description 2
- 241000598436 Human T-cell lymphotropic virus Species 0.000 description 2
- 241000700588 Human alphaherpesvirus 1 Species 0.000 description 2
- 241000701024 Human betaherpesvirus 5 Species 0.000 description 2
- 241000701044 Human gammaherpesvirus 4 Species 0.000 description 2
- 241000725303 Human immunodeficiency virus Species 0.000 description 2
- XQFRJNBWHJMXHO-RRKCRQDMSA-N IDUR Chemical compound C1[C@H](O)[C@@H](CO)O[C@H]1N1C(=O)NC(=O)C(I)=C1 XQFRJNBWHJMXHO-RRKCRQDMSA-N 0.000 description 2
- 229940076838 Immune checkpoint inhibitor Drugs 0.000 description 2
- 102100040061 Indoleamine 2,3-dioxygenase 1 Human genes 0.000 description 2
- 102000037984 Inhibitory immune checkpoint proteins Human genes 0.000 description 2
- 108091008026 Inhibitory immune checkpoint proteins Proteins 0.000 description 2
- 102000042838 JAK family Human genes 0.000 description 2
- 108091082332 JAK family Proteins 0.000 description 2
- 241000701460 JC polyomavirus Species 0.000 description 2
- 241000588748 Klebsiella Species 0.000 description 2
- OUYCCCASQSFEME-QMMMGPOBSA-N L-tyrosine Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-QMMMGPOBSA-N 0.000 description 2
- 239000002144 L01XE18 - Ruxolitinib Substances 0.000 description 2
- 241001245510 Lambia <signal fly> Species 0.000 description 2
- 241000589248 Legionella Species 0.000 description 2
- 208000007764 Legionnaires' Disease Diseases 0.000 description 2
- 241000222727 Leishmania donovani Species 0.000 description 2
- 241000589902 Leptospira Species 0.000 description 2
- 102100028198 Macrophage colony-stimulating factor 1 receptor Human genes 0.000 description 2
- YNAVUWVOSKDBBP-UHFFFAOYSA-N Morpholine Chemical compound C1COCCN1 YNAVUWVOSKDBBP-UHFFFAOYSA-N 0.000 description 2
- 241000235395 Mucor Species 0.000 description 2
- 241000711386 Mumps virus Species 0.000 description 2
- 241000699670 Mus sp. Species 0.000 description 2
- 241000872931 Myoporum sandwicense Species 0.000 description 2
- NWIBSHFKIJFRCO-WUDYKRTCSA-N Mytomycin Chemical compound C1N2C(C(C(C)=C(N)C3=O)=O)=C3[C@@H](COC(N)=O)[C@@]2(OC)[C@@H]2[C@H]1N2 NWIBSHFKIJFRCO-WUDYKRTCSA-N 0.000 description 2
- JGFZNNIVVJXRND-UHFFFAOYSA-N N,N-Diisopropylethylamine (DIPEA) Chemical compound CCN(C(C)C)C(C)C JGFZNNIVVJXRND-UHFFFAOYSA-N 0.000 description 2
- LRHPLDYGYMQRHN-UHFFFAOYSA-N N-Butanol Chemical compound CCCCO LRHPLDYGYMQRHN-UHFFFAOYSA-N 0.000 description 2
- LQZMLBORDGWNPD-UHFFFAOYSA-N N-iodosuccinimide Chemical compound IN1C(=O)CCC1=O LQZMLBORDGWNPD-UHFFFAOYSA-N 0.000 description 2
- 241000224438 Naegleria fowleri Species 0.000 description 2
- 241001126260 Nippostrongylus Species 0.000 description 2
- 241001631646 Papillomaviridae Species 0.000 description 2
- 241000526686 Paracoccidioides brasiliensis Species 0.000 description 2
- 208000037581 Persistent Infection Diseases 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- NQRYJNQNLNOLGT-UHFFFAOYSA-N Piperidine Chemical compound C1CCNCC1 NQRYJNQNLNOLGT-UHFFFAOYSA-N 0.000 description 2
- 206010035148 Plague Diseases 0.000 description 2
- 241000223810 Plasmodium vivax Species 0.000 description 2
- 241000233872 Pneumocystis carinii Species 0.000 description 2
- 241000588769 Proteus <enterobacteria> Species 0.000 description 2
- 241000125945 Protoparvovirus Species 0.000 description 2
- 241000589516 Pseudomonas Species 0.000 description 2
- 241000711798 Rabies lyssavirus Species 0.000 description 2
- 241000725643 Respiratory syncytial virus Species 0.000 description 2
- 241000606701 Rickettsia Species 0.000 description 2
- 241000702670 Rotavirus Species 0.000 description 2
- 241000710799 Rubella virus Species 0.000 description 2
- 241000315672 SARS coronavirus Species 0.000 description 2
- 241000607142 Salmonella Species 0.000 description 2
- 241000607720 Serratia Species 0.000 description 2
- WQDUMFSSJAZKTM-UHFFFAOYSA-N Sodium methoxide Chemical compound [Na+].[O-]C WQDUMFSSJAZKTM-UHFFFAOYSA-N 0.000 description 2
- 241001149962 Sporothrix Species 0.000 description 2
- 241000295644 Staphylococcaceae Species 0.000 description 2
- 101100215487 Sus scrofa ADRA2A gene Proteins 0.000 description 2
- 230000005867 T cell response Effects 0.000 description 2
- 102100027213 T-cell-specific surface glycoprotein CD28 Human genes 0.000 description 2
- 102100027222 T-lymphocyte activation antigen CD80 Human genes 0.000 description 2
- NKANXQFJJICGDU-QPLCGJKRSA-N Tamoxifen Chemical compound C=1C=CC=CC=1C(/CC)=C(C=1C=CC(OCCN(C)C)=CC=1)/C1=CC=CC=C1 NKANXQFJJICGDU-QPLCGJKRSA-N 0.000 description 2
- 206010043376 Tetanus Diseases 0.000 description 2
- 241000223996 Toxoplasma Species 0.000 description 2
- YZCKVEUIGOORGS-NJFSPNSNSA-N Tritium Chemical compound [3H] YZCKVEUIGOORGS-NJFSPNSNSA-N 0.000 description 2
- 241000223105 Trypanosoma brucei Species 0.000 description 2
- 241000223109 Trypanosoma cruzi Species 0.000 description 2
- 102100033728 Tumor necrosis factor receptor superfamily member 18 Human genes 0.000 description 2
- 102100022153 Tumor necrosis factor receptor superfamily member 4 Human genes 0.000 description 2
- 101710165473 Tumor necrosis factor receptor superfamily member 4 Proteins 0.000 description 2
- 102100040245 Tumor necrosis factor receptor superfamily member 5 Human genes 0.000 description 2
- 102100033438 Tyrosine-protein kinase JAK1 Human genes 0.000 description 2
- 108010079206 V-Set Domain-Containing T-Cell Activation Inhibitor 1 Proteins 0.000 description 2
- 102100038929 V-set domain-containing T-cell activation inhibitor 1 Human genes 0.000 description 2
- 102100038282 V-type immunoglobulin domain-containing suppressor of T-cell activation Human genes 0.000 description 2
- 241000700618 Vaccinia virus Species 0.000 description 2
- 108010053099 Vascular Endothelial Growth Factor Receptor-2 Proteins 0.000 description 2
- 241000607626 Vibrio cholerae Species 0.000 description 2
- 208000000260 Warts Diseases 0.000 description 2
- 241000607479 Yersinia pestis Species 0.000 description 2
- VXIPETUJOOUGEW-UHFFFAOYSA-N [2-(2-methyl-3-phenylphenyl)furo[3,2-b]pyridin-5-yl]methanol Chemical compound CC1=C(C=CC=C1C1=CC2=NC(=CC=C2O1)CO)C1=CC=CC=C1 VXIPETUJOOUGEW-UHFFFAOYSA-N 0.000 description 2
- RJURFGZVJUQBHK-UHFFFAOYSA-N actinomycin D Natural products CC1OC(=O)C(C(C)C)N(C)C(=O)CN(C)C(=O)C2CCCN2C(=O)C(C(C)C)NC(=O)C1NC(=O)C1=C(N)C(=O)C(C)=C2OC(C(C)=CC=C3C(=O)NC4C(=O)NC(C(N5CCCC5C(=O)N(C)CC(=O)N(C)C(C(C)C)C(=O)OC4C)=O)C(C)C)=C3N=C21 RJURFGZVJUQBHK-UHFFFAOYSA-N 0.000 description 2
- 239000000443 aerosol Substances 0.000 description 2
- 150000001335 aliphatic alkanes Chemical class 0.000 description 2
- 238000010171 animal model Methods 0.000 description 2
- 239000008346 aqueous phase Substances 0.000 description 2
- 125000002029 aromatic hydrocarbon group Chemical group 0.000 description 2
- XRWSZZJLZRKHHD-WVWIJVSJSA-N asunaprevir Chemical compound O=C([C@@H]1C[C@H](CN1C(=O)[C@@H](NC(=O)OC(C)(C)C)C(C)(C)C)OC1=NC=C(C2=CC=C(Cl)C=C21)OC)N[C@]1(C(=O)NS(=O)(=O)C2CC2)C[C@H]1C=C XRWSZZJLZRKHHD-WVWIJVSJSA-N 0.000 description 2
- 125000003725 azepanyl group Chemical group 0.000 description 2
- 125000003943 azolyl group Chemical group 0.000 description 2
- 210000003719 b-lymphocyte Anatomy 0.000 description 2
- 208000007456 balantidiasis Diseases 0.000 description 2
- XUZMWHLSFXCVMG-UHFFFAOYSA-N baricitinib Chemical compound C1N(S(=O)(=O)CC)CC1(CC#N)N1N=CC(C=2C=3C=CNC=3N=CN=2)=C1 XUZMWHLSFXCVMG-UHFFFAOYSA-N 0.000 description 2
- 229950000971 baricitinib Drugs 0.000 description 2
- 230000008901 benefit Effects 0.000 description 2
- 125000000499 benzofuranyl group Chemical group O1C(=CC2=C1C=CC=C2)* 0.000 description 2
- 125000004196 benzothienyl group Chemical group S1C(=CC2=C1C=CC=C2)* 0.000 description 2
- 125000004541 benzoxazolyl group Chemical group O1C(=NC2=C1C=CC=C2)* 0.000 description 2
- 150000005347 biaryls Chemical group 0.000 description 2
- 230000031018 biological processes and functions Effects 0.000 description 2
- 230000033228 biological regulation Effects 0.000 description 2
- 230000000903 blocking effect Effects 0.000 description 2
- 239000000872 buffer Substances 0.000 description 2
- 239000007853 buffer solution Substances 0.000 description 2
- 229960002092 busulfan Drugs 0.000 description 2
- 239000002775 capsule Substances 0.000 description 2
- 239000011203 carbon fibre reinforced carbon Substances 0.000 description 2
- 125000002915 carbonyl group Chemical group [*:2]C([*:1])=O 0.000 description 2
- 230000003197 catalytic effect Effects 0.000 description 2
- 125000003636 chemical group Chemical group 0.000 description 2
- 239000003153 chemical reaction reagent Substances 0.000 description 2
- 229940125758 compound 15 Drugs 0.000 description 2
- 229940125833 compound 23 Drugs 0.000 description 2
- 229940125961 compound 24 Drugs 0.000 description 2
- 229940126214 compound 3 Drugs 0.000 description 2
- 239000006071 cream Substances 0.000 description 2
- 125000004122 cyclic group Chemical group 0.000 description 2
- 125000000582 cycloheptyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 2
- 125000000596 cyclohexenyl group Chemical group C1(=CCCCC1)* 0.000 description 2
- 229940127089 cytotoxic agent Drugs 0.000 description 2
- 230000001419 dependent effect Effects 0.000 description 2
- 238000010511 deprotection reaction Methods 0.000 description 2
- 125000004431 deuterium atom Chemical group 0.000 description 2
- 125000000723 dihydrobenzofuranyl group Chemical group O1C(CC2=C1C=CC=C2)* 0.000 description 2
- 125000004852 dihydrofuranyl group Chemical group O1C(CC=C1)* 0.000 description 2
- 125000005043 dihydropyranyl group Chemical group O1C(CCC=C1)* 0.000 description 2
- 206010013023 diphtheria Diseases 0.000 description 2
- 208000037765 diseases and disorders Diseases 0.000 description 2
- 231100000673 dose–response relationship Toxicity 0.000 description 2
- 239000012636 effector Substances 0.000 description 2
- 229940007078 entamoeba histolytica Drugs 0.000 description 2
- 239000012055 enteric layer Substances 0.000 description 2
- 229940088598 enzyme Drugs 0.000 description 2
- 229910052731 fluorine Inorganic materials 0.000 description 2
- 125000001153 fluoro group Chemical group F* 0.000 description 2
- IJJVMEJXYNJXOJ-UHFFFAOYSA-N fluquinconazole Chemical compound C=1C=C(Cl)C=C(Cl)C=1N1C(=O)C2=CC(F)=CC=C2N=C1N1C=NC=N1 IJJVMEJXYNJXOJ-UHFFFAOYSA-N 0.000 description 2
- 229960004279 formaldehyde Drugs 0.000 description 2
- 235000019256 formaldehyde Nutrition 0.000 description 2
- 238000010575 fractional recrystallization Methods 0.000 description 2
- 230000006870 function Effects 0.000 description 2
- 244000053095 fungal pathogen Species 0.000 description 2
- 239000000499 gel Substances 0.000 description 2
- 235000011187 glycerol Nutrition 0.000 description 2
- 238000011194 good manufacturing practice Methods 0.000 description 2
- 230000036541 health Effects 0.000 description 2
- 230000003862 health status Effects 0.000 description 2
- 208000005252 hepatitis A Diseases 0.000 description 2
- 208000002672 hepatitis B Diseases 0.000 description 2
- BXWNKGSJHAJOGX-UHFFFAOYSA-N hexadecan-1-ol Chemical compound CCCCCCCCCCCCCCCCO BXWNKGSJHAJOGX-UHFFFAOYSA-N 0.000 description 2
- 238000004128 high performance liquid chromatography Methods 0.000 description 2
- 150000004677 hydrates Chemical class 0.000 description 2
- 150000002430 hydrocarbons Chemical group 0.000 description 2
- 229940031702 hydroxypropyl methylcellulose 2208 Drugs 0.000 description 2
- 210000000987 immune system Anatomy 0.000 description 2
- 239000012274 immune-checkpoint protein inhibitor Substances 0.000 description 2
- 230000036039 immunity Effects 0.000 description 2
- 238000010874 in vitro model Methods 0.000 description 2
- 238000011065 in-situ storage Methods 0.000 description 2
- 125000001041 indolyl group Chemical group 0.000 description 2
- 230000003834 intracellular effect Effects 0.000 description 2
- 229960005386 ipilimumab Drugs 0.000 description 2
- 125000002183 isoquinolinyl group Chemical group C1(=NC=CC2=CC=CC=C12)* 0.000 description 2
- 125000001786 isothiazolyl group Chemical group 0.000 description 2
- JVTAAEKCZFNVCJ-UHFFFAOYSA-N lactic acid Chemical compound CC(O)C(O)=O JVTAAEKCZFNVCJ-UHFFFAOYSA-N 0.000 description 2
- GLXDVVHUTZTUQK-UHFFFAOYSA-M lithium;hydroxide;hydrate Chemical compound [Li+].O.[OH-] GLXDVVHUTZTUQK-UHFFFAOYSA-M 0.000 description 2
- 210000002540 macrophage Anatomy 0.000 description 2
- 235000019359 magnesium stearate Nutrition 0.000 description 2
- IUYHWZFSGMZEOG-UHFFFAOYSA-M magnesium;propane;chloride Chemical compound [Mg+2].[Cl-].C[CH-]C IUYHWZFSGMZEOG-UHFFFAOYSA-M 0.000 description 2
- 239000000463 material Substances 0.000 description 2
- 230000001404 mediated effect Effects 0.000 description 2
- JJDQEISQLXVSPY-VWLOTQADSA-N methyl (2S)-1-[[2-(2-methyl-3-phenylphenyl)-1,3-benzothiazol-5-yl]methyl]piperidine-2-carboxylate Chemical compound CC1=C(C=CC=C1C=1SC2=C(N=1)C=C(C=C2)CN1[C@@H](CCCC1)C(=O)OC)C1=CC=CC=C1 JJDQEISQLXVSPY-VWLOTQADSA-N 0.000 description 2
- VHLBJWCXFIGALN-UHFFFAOYSA-N methyl 1,3-benzoxazole-5-carboxylate Chemical compound COC(=O)C1=CC=C2OC=NC2=C1 VHLBJWCXFIGALN-UHFFFAOYSA-N 0.000 description 2
- IIFCLXHRIYTHPV-UHFFFAOYSA-N methyl 2,4-dihydroxybenzoate Chemical compound COC(=O)C1=CC=C(O)C=C1O IIFCLXHRIYTHPV-UHFFFAOYSA-N 0.000 description 2
- JPFGNOBFMVOBHJ-UHFFFAOYSA-N methyl 4-bromo-5-hydroxy-6-methylpyridine-2-carboxylate Chemical compound BrC1=CC(=NC(=C1O)C)C(=O)OC JPFGNOBFMVOBHJ-UHFFFAOYSA-N 0.000 description 2
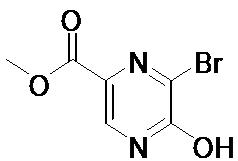
- IHBJNSCXVJDJST-UHFFFAOYSA-N methyl 5-bromo-6-oxo-1h-pyrazine-3-carboxylate Chemical compound COC(=O)C1=CN=C(O)C(Br)=N1 IHBJNSCXVJDJST-UHFFFAOYSA-N 0.000 description 2
- QPJVMBTYPHYUOC-UHFFFAOYSA-N methyl benzoate Chemical compound COC(=O)C1=CC=CC=C1 QPJVMBTYPHYUOC-UHFFFAOYSA-N 0.000 description 2
- 238000003801 milling Methods 0.000 description 2
- 239000002480 mineral oil Substances 0.000 description 2
- 235000010446 mineral oil Nutrition 0.000 description 2
- 150000007522 mineralic acids Chemical class 0.000 description 2
- UHOVQNZJYSORNB-UHFFFAOYSA-N monobenzene Natural products C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 2
- 125000004593 naphthyridinyl group Chemical group N1=C(C=CC2=CC=CN=C12)* 0.000 description 2
- 125000006574 non-aromatic ring group Chemical group 0.000 description 2
- 231100000252 nontoxic Toxicity 0.000 description 2
- 230000003000 nontoxic effect Effects 0.000 description 2
- 150000007524 organic acids Chemical class 0.000 description 2
- 150000002894 organic compounds Chemical class 0.000 description 2
- 239000003960 organic solvent Substances 0.000 description 2
- 239000012285 osmium tetroxide Substances 0.000 description 2
- 229910000489 osmium tetroxide Inorganic materials 0.000 description 2
- 239000007800 oxidant agent Substances 0.000 description 2
- NFHFRUOZVGFOOS-UHFFFAOYSA-N palladium;triphenylphosphane Chemical compound [Pd].C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 NFHFRUOZVGFOOS-UHFFFAOYSA-N 0.000 description 2
- 244000045947 parasite Species 0.000 description 2
- 230000001717 pathogenic effect Effects 0.000 description 2
- 229940124531 pharmaceutical excipient Drugs 0.000 description 2
- HXITXNWTGFUOAU-UHFFFAOYSA-N phenylboronic acid Chemical compound OB(O)C1=CC=CC=C1 HXITXNWTGFUOAU-UHFFFAOYSA-N 0.000 description 2
- 125000004193 piperazinyl group Chemical group 0.000 description 2
- 229910000027 potassium carbonate Inorganic materials 0.000 description 2
- 238000011321 prophylaxis Methods 0.000 description 2
- 125000000561 purinyl group Chemical group N1=C(N=C2N=CNC2=C1)* 0.000 description 2
- 125000004309 pyranyl group Chemical group O1C(C=CC=C1)* 0.000 description 2
- 125000000714 pyrimidinyl group Chemical group 0.000 description 2
- 125000000719 pyrrolidinyl group Chemical group 0.000 description 2
- 125000002943 quinolinyl group Chemical group N1=C(C=CC2=CC=CC=C12)* 0.000 description 2
- 125000004621 quinuclidinyl group Chemical group N12C(CC(CC1)CC2)* 0.000 description 2
- 108091006082 receptor inhibitors Proteins 0.000 description 2
- 230000002829 reductive effect Effects 0.000 description 2
- HFNKQEVNSGCOJV-OAHLLOKOSA-N ruxolitinib Chemical compound C1([C@@H](CC#N)N2N=CC(=C2)C=2C=3C=CNC=3N=CN=2)CCCC1 HFNKQEVNSGCOJV-OAHLLOKOSA-N 0.000 description 2
- 229960000215 ruxolitinib Drugs 0.000 description 2
- 229920006395 saturated elastomer Polymers 0.000 description 2
- 238000007423 screening assay Methods 0.000 description 2
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 2
- 239000000377 silicon dioxide Substances 0.000 description 2
- 235000012239 silicon dioxide Nutrition 0.000 description 2
- 201000010153 skin papilloma Diseases 0.000 description 2
- 229910000029 sodium carbonate Inorganic materials 0.000 description 2
- JQWHASGSAFIOCM-UHFFFAOYSA-M sodium periodate Chemical compound [Na+].[O-]I(=O)(=O)=O JQWHASGSAFIOCM-UHFFFAOYSA-M 0.000 description 2
- 239000008247 solid mixture Substances 0.000 description 2
- 239000007858 starting material Substances 0.000 description 2
- 239000000829 suppository Substances 0.000 description 2
- 238000010189 synthetic method Methods 0.000 description 2
- 239000006188 syrup Substances 0.000 description 2
- 235000020357 syrup Nutrition 0.000 description 2
- 230000009885 systemic effect Effects 0.000 description 2
- 125000003718 tetrahydrofuranyl group Chemical group 0.000 description 2
- 125000001412 tetrahydropyranyl group Chemical group 0.000 description 2
- CXWXQJXEFPUFDZ-UHFFFAOYSA-N tetralin Chemical compound C1=CC=C2CCCCC2=C1 CXWXQJXEFPUFDZ-UHFFFAOYSA-N 0.000 description 2
- 125000003831 tetrazolyl group Chemical group 0.000 description 2
- 229960003433 thalidomide Drugs 0.000 description 2
- 125000000101 thioether group Chemical group 0.000 description 2
- 125000005505 thiomorpholino group Chemical group 0.000 description 2
- 238000011200 topical administration Methods 0.000 description 2
- 231100000419 toxicity Toxicity 0.000 description 2
- 230000001988 toxicity Effects 0.000 description 2
- 229960000575 trastuzumab Drugs 0.000 description 2
- 125000004306 triazinyl group Chemical group 0.000 description 2
- AQRLNPVMDITEJU-UHFFFAOYSA-N triethylsilane Chemical compound CC[SiH](CC)CC AQRLNPVMDITEJU-UHFFFAOYSA-N 0.000 description 2
- MPMSZXWCZKCHLQ-UHFFFAOYSA-N trihydridoiodine Chemical compound [H]I([H])[H] MPMSZXWCZKCHLQ-UHFFFAOYSA-N 0.000 description 2
- 229910052722 tritium Inorganic materials 0.000 description 2
- 230000004565 tumor cell growth Effects 0.000 description 2
- 230000004614 tumor growth Effects 0.000 description 2
- OUYCCCASQSFEME-UHFFFAOYSA-N tyrosine Natural products OC(=O)C(N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-UHFFFAOYSA-N 0.000 description 2
- 238000002255 vaccination Methods 0.000 description 2
- 239000003981 vehicle Substances 0.000 description 2
- 229940118696 vibrio cholerae Drugs 0.000 description 2
- BMKDZUISNHGIBY-ZETCQYMHSA-N (+)-dexrazoxane Chemical compound C([C@H](C)N1CC(=O)NC(=O)C1)N1CC(=O)NC(=O)C1 BMKDZUISNHGIBY-ZETCQYMHSA-N 0.000 description 1
- FMCGSUUBYTWNDP-ONGXEEELSA-N (1R,2S)-2-(dimethylamino)-1-phenyl-1-propanol Chemical compound CN(C)[C@@H](C)[C@H](O)C1=CC=CC=C1 FMCGSUUBYTWNDP-ONGXEEELSA-N 0.000 description 1
- QBYIENPQHBMVBV-HFEGYEGKSA-N (2R)-2-hydroxy-2-phenylacetic acid Chemical compound O[C@@H](C(O)=O)c1ccccc1.O[C@@H](C(O)=O)c1ccccc1 QBYIENPQHBMVBV-HFEGYEGKSA-N 0.000 description 1
- DNISEZBAYYIQFB-PHDIDXHHSA-N (2r,3r)-2,3-diacetyloxybutanedioic acid Chemical compound CC(=O)O[C@@H](C(O)=O)[C@H](C(O)=O)OC(C)=O DNISEZBAYYIQFB-PHDIDXHHSA-N 0.000 description 1
- XYDXDWXAAQXHLK-UHFFFAOYSA-N (3-bromo-2-methylphenyl)methanol Chemical compound CC1=C(Br)C=CC=C1CO XYDXDWXAAQXHLK-UHFFFAOYSA-N 0.000 description 1
- IWZSHWBGHQBIML-ZGGLMWTQSA-N (3S,8S,10R,13S,14S,17S)-17-isoquinolin-7-yl-N,N,10,13-tetramethyl-2,3,4,7,8,9,11,12,14,15,16,17-dodecahydro-1H-cyclopenta[a]phenanthren-3-amine Chemical compound CN(C)[C@H]1CC[C@]2(C)C3CC[C@@]4(C)[C@@H](CC[C@@H]4c4ccc5ccncc5c4)[C@@H]3CC=C2C1 IWZSHWBGHQBIML-ZGGLMWTQSA-N 0.000 description 1
- YPBKTZBXSBLTDK-PKNBQFBNSA-N (3e)-3-[(3-bromo-4-fluoroanilino)-nitrosomethylidene]-4-[2-(sulfamoylamino)ethylamino]-1,2,5-oxadiazole Chemical compound NS(=O)(=O)NCCNC1=NON\C1=C(N=O)/NC1=CC=C(F)C(Br)=C1 YPBKTZBXSBLTDK-PKNBQFBNSA-N 0.000 description 1
- LRYNOAHPGHSFEV-UHFFFAOYSA-N (4-diazo-2-methyl-3-oxobutan-2-yl)phosphonic acid Chemical compound CC(C)(C(=O)C=[N+]=[N-])P(O)(O)=O LRYNOAHPGHSFEV-UHFFFAOYSA-N 0.000 description 1
- FPVKHBSQESCIEP-UHFFFAOYSA-N (8S)-3-(2-deoxy-beta-D-erythro-pentofuranosyl)-3,6,7,8-tetrahydroimidazo[4,5-d][1,3]diazepin-8-ol Natural products C1C(O)C(CO)OC1N1C(NC=NCC2O)=C2N=C1 FPVKHBSQESCIEP-UHFFFAOYSA-N 0.000 description 1
- 125000006582 (C5-C6) heterocycloalkyl group Chemical group 0.000 description 1
- FDKXTQMXEQVLRF-ZHACJKMWSA-N (E)-dacarbazine Chemical compound CN(C)\N=N\c1[nH]cnc1C(N)=O FDKXTQMXEQVLRF-ZHACJKMWSA-N 0.000 description 1
- MIOPJNTWMNEORI-GMSGAONNSA-N (S)-camphorsulfonic acid Chemical compound C1C[C@@]2(CS(O)(=O)=O)C(=O)C[C@@H]1C2(C)C MIOPJNTWMNEORI-GMSGAONNSA-N 0.000 description 1
- BJEPYKJPYRNKOW-REOHCLBHSA-N (S)-malic acid Chemical compound OC(=O)[C@@H](O)CC(O)=O BJEPYKJPYRNKOW-REOHCLBHSA-N 0.000 description 1
- SQHSJJGGWYIFCD-UHFFFAOYSA-N (e)-1-diazonio-1-dimethoxyphosphorylprop-1-en-2-olate Chemical compound COP(=O)(OC)C(\[N+]#N)=C(\C)[O-] SQHSJJGGWYIFCD-UHFFFAOYSA-N 0.000 description 1
- XGQXULJHBWKUJY-LYIKAWCPSA-N (z)-but-2-enedioic acid;n-[2-(diethylamino)ethyl]-5-[(z)-(5-fluoro-2-oxo-1h-indol-3-ylidene)methyl]-2,4-dimethyl-1h-pyrrole-3-carboxamide Chemical compound OC(=O)\C=C/C(O)=O.CCN(CC)CCNC(=O)C1=C(C)NC(\C=C/2C3=CC(F)=CC=C3NC\2=O)=C1C XGQXULJHBWKUJY-LYIKAWCPSA-N 0.000 description 1
- 125000005919 1,2,2-trimethylpropyl group Chemical group 0.000 description 1
- 125000001781 1,3,4-oxadiazolyl group Chemical group 0.000 description 1
- AVSFPLJXSHRMHM-UHFFFAOYSA-N 1,3-benzothiazole-6-carbaldehyde Chemical compound O=CC1=CC=C2N=CSC2=C1 AVSFPLJXSHRMHM-UHFFFAOYSA-N 0.000 description 1
- HJTAZXHBEBIQQX-UHFFFAOYSA-N 1,5-bis(chloromethyl)naphthalene Chemical compound C1=CC=C2C(CCl)=CC=CC2=C1CCl HJTAZXHBEBIQQX-UHFFFAOYSA-N 0.000 description 1
- MRPPDKMVELHEDA-UHFFFAOYSA-N 1-[3-(6-chloro-1,3-benzoxazol-2-yl)-5-(3,5-dimethylphenyl)pyridin-4-yl]piperidin-4-amine Chemical compound ClC1=CC2=C(N=C(O2)C=2C=NC=C(C2N2CCC(CC2)N)C2=CC(=CC(=C2)C)C)C=C1 MRPPDKMVELHEDA-UHFFFAOYSA-N 0.000 description 1
- RFUOKCSSXNEZBW-UHFFFAOYSA-N 1-bromo-2-chloro-4-nitro-5-phenylmethoxybenzene Chemical compound [O-][N+](=O)C1=CC(Cl)=C(Br)C=C1OCC1=CC=CC=C1 RFUOKCSSXNEZBW-UHFFFAOYSA-N 0.000 description 1
- ULYNHWCYWYOFHF-UHFFFAOYSA-N 1-chloro-5-nitro-2,4-bis(phenylmethoxy)benzene Chemical compound C(C1=CC=CC=C1)OC1=C(C=C(C(=C1)OCC1=CC=CC=C1)[N+](=O)[O-])Cl ULYNHWCYWYOFHF-UHFFFAOYSA-N 0.000 description 1
- VBICKXHEKHSIBG-UHFFFAOYSA-N 1-monostearoylglycerol Chemical compound CCCCCCCCCCCCCCCCCC(=O)OCC(O)CO VBICKXHEKHSIBG-UHFFFAOYSA-N 0.000 description 1
- KKVYYGGCHJGEFJ-UHFFFAOYSA-N 1-n-(4-chlorophenyl)-6-methyl-5-n-[3-(7h-purin-6-yl)pyridin-2-yl]isoquinoline-1,5-diamine Chemical compound N=1C=CC2=C(NC=3C(=CC=CN=3)C=3C=4N=CNC=4N=CN=3)C(C)=CC=C2C=1NC1=CC=C(Cl)C=C1 KKVYYGGCHJGEFJ-UHFFFAOYSA-N 0.000 description 1
- RQEUFEKYXDPUSK-UHFFFAOYSA-N 1-phenylethylamine Chemical compound CC(N)C1=CC=CC=C1 RQEUFEKYXDPUSK-UHFFFAOYSA-N 0.000 description 1
- QWENRTYMTSOGBR-UHFFFAOYSA-N 1H-1,2,3-Triazole Chemical compound C=1C=NNN=1 QWENRTYMTSOGBR-UHFFFAOYSA-N 0.000 description 1
- RAXXELZNTBOGNW-UHFFFAOYSA-N 1H-imidazole Chemical compound C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 description 1
- YBYIRNPNPLQARY-UHFFFAOYSA-N 1H-indene Natural products C1=CC=C2CC=CC2=C1 YBYIRNPNPLQARY-UHFFFAOYSA-N 0.000 description 1
- LFHLEABTNIQIQO-UHFFFAOYSA-N 1H-isoindole Chemical compound C1=CC=C2CN=CC2=C1 LFHLEABTNIQIQO-UHFFFAOYSA-N 0.000 description 1
- GBBSAMQTQCPOBF-UHFFFAOYSA-N 2,4,6-trimethyl-1,3,5,2,4,6-trioxatriborinane Chemical compound CB1OB(C)OB(C)O1 GBBSAMQTQCPOBF-UHFFFAOYSA-N 0.000 description 1
- 150000005059 2,6-naphthyridines Chemical class 0.000 description 1
- HVHIMQJQBIFFID-UHFFFAOYSA-N 2-(2,3-dihydro-1,4-benzodioxin-6-yl)-6-formylbenzonitrile Chemical group O1CCOC2=C1C=CC(=C2)C1=C(C#N)C(=CC=C1)C=O HVHIMQJQBIFFID-UHFFFAOYSA-N 0.000 description 1
- FTYYEJNZLXVVSG-UHFFFAOYSA-N 2-(2-methyl-3-phenylphenyl)-1,3-benzoxazole-5-carbaldehyde Chemical compound CC1=C(C=CC=C1C=1OC2=C(N=1)C=C(C=C2)C=O)C1=CC=CC=C1 FTYYEJNZLXVVSG-UHFFFAOYSA-N 0.000 description 1
- DWGYVQKVNXXHDB-UHFFFAOYSA-N 2-(2-methyl-3-phenylphenyl)-1,3-benzoxazole-6-carbaldehyde Chemical compound CC1=C(C=CC=C1C=1OC2=C(N=1)C=CC(=C2)C=O)C1=CC=CC=C1 DWGYVQKVNXXHDB-UHFFFAOYSA-N 0.000 description 1
- WKAZFTJUAHNTBA-UHFFFAOYSA-N 2-(2-methyl-3-phenylphenyl)-[1,3]oxazolo[5,4-c]pyridine-6-carbaldehyde Chemical compound CC1=C(C=CC=C1C=1OC=2C=NC(=CC=2N=1)C=O)C1=CC=CC=C1 WKAZFTJUAHNTBA-UHFFFAOYSA-N 0.000 description 1
- SPMYRIJCGVCNAC-UHFFFAOYSA-N 2-(2-methyl-3-phenylphenyl)furo[2,3-b]pyridine-5-carbaldehyde Chemical compound CC1=C(C=CC=C1C1=CC=2C(=NC=C(C=2)C=O)O1)C1=CC=CC=C1 SPMYRIJCGVCNAC-UHFFFAOYSA-N 0.000 description 1
- JRWPRNNADHBGIL-UHFFFAOYSA-N 2-(2-methyl-3-phenylphenyl)furo[3,2-b]pyridine-5-carbaldehyde Chemical compound CC1=C(C=CC=C1C1=CC2=NC(=CC=C2O1)C=O)C1=CC=CC=C1 JRWPRNNADHBGIL-UHFFFAOYSA-N 0.000 description 1
- UMTPKUDMLGJXFT-UHFFFAOYSA-N 2-(5-chloro-6-hydroxy-1,3-benzoxazol-2-yl)-6-(2,3-dihydro-1,4-benzodioxin-6-yl)benzonitrile Chemical compound ClC=1C(=CC2=C(N=C(O2)C2=C(C#N)C(=CC=C2)C2=CC3=C(OCCO3)C=C2)C=1)O UMTPKUDMLGJXFT-UHFFFAOYSA-N 0.000 description 1
- OFPWMRMIFDHXFE-UHFFFAOYSA-N 2-(bromomethyl)pyridine Chemical compound BrCC1=CC=CC=N1 OFPWMRMIFDHXFE-UHFFFAOYSA-N 0.000 description 1
- QNZFUMVTUFOLRT-UHFFFAOYSA-N 2-(cyclohexen-1-yl)-4,4,5,5-tetramethyl-1,3,2-dioxaborolane Chemical compound O1C(C)(C)C(C)(C)OB1C1=CCCCC1 QNZFUMVTUFOLRT-UHFFFAOYSA-N 0.000 description 1
- UZYQSNQJLWTICD-UHFFFAOYSA-N 2-(n-benzoylanilino)-2,2-dinitroacetic acid Chemical compound C=1C=CC=CC=1N(C(C(=O)O)([N+]([O-])=O)[N+]([O-])=O)C(=O)C1=CC=CC=C1 UZYQSNQJLWTICD-UHFFFAOYSA-N 0.000 description 1
- QXLQZLBNPTZMRK-UHFFFAOYSA-N 2-[(dimethylamino)methyl]-1-(2,4-dimethylphenyl)prop-2-en-1-one Chemical compound CN(C)CC(=C)C(=O)C1=CC=C(C)C=C1C QXLQZLBNPTZMRK-UHFFFAOYSA-N 0.000 description 1
- KTBSXLIQKWEBRB-UHFFFAOYSA-N 2-[1-[1-[3-fluoro-2-(trifluoromethyl)pyridine-4-carbonyl]piperidin-4-yl]-3-[4-(7h-pyrrolo[2,3-d]pyrimidin-4-yl)pyrazol-1-yl]azetidin-3-yl]acetonitrile Chemical compound C1=CN=C(C(F)(F)F)C(F)=C1C(=O)N1CCC(N2CC(CC#N)(C2)N2N=CC(=C2)C=2C=3C=CNC=3N=CN=2)CC1 KTBSXLIQKWEBRB-UHFFFAOYSA-N 0.000 description 1
- JLPMBEMXXQELAE-UHFFFAOYSA-N 2-[5-chloro-6-(cyanomethoxy)-1,3-benzoxazol-2-yl]-6-(2,3-dihydro-1,4-benzodioxin-6-yl)benzonitrile Chemical compound ClC=1C(=CC2=C(N=C(O2)C2=C(C#N)C(=CC=C2)C2=CC3=C(OCCO3)C=C2)C=1)OCC#N JLPMBEMXXQELAE-UHFFFAOYSA-N 0.000 description 1
- ZSUMEXJWKCANBT-UHFFFAOYSA-N 2-[6-(cyanomethoxy)-5-formyl-1,3-benzoxazol-2-yl]-6-(2,3-dihydro-1,4-benzodioxin-6-yl)benzonitrile Chemical compound C(#N)COC1=CC2=C(N=C(O2)C2=C(C#N)C(=CC=C2)C2=CC3=C(OCCO3)C=C2)C=C1C=O ZSUMEXJWKCANBT-UHFFFAOYSA-N 0.000 description 1
- RTQWWZBSTRGEAV-PKHIMPSTSA-N 2-[[(2s)-2-[bis(carboxymethyl)amino]-3-[4-(methylcarbamoylamino)phenyl]propyl]-[2-[bis(carboxymethyl)amino]propyl]amino]acetic acid Chemical compound CNC(=O)NC1=CC=C(C[C@@H](CN(CC(C)N(CC(O)=O)CC(O)=O)CC(O)=O)N(CC(O)=O)CC(O)=O)C=C1 RTQWWZBSTRGEAV-PKHIMPSTSA-N 0.000 description 1
- YAVMANYRYAJWQA-UHFFFAOYSA-N 2-[[2-(3-bromo-2-methylphenyl)-5-formyl-1,3-benzoxazol-6-yl]oxy]acetonitrile Chemical compound BrC=1C(=C(C=CC=1)C=1OC2=C(N=1)C=C(C(=C2)OCC#N)C=O)C YAVMANYRYAJWQA-UHFFFAOYSA-N 0.000 description 1
- IJXJGQCXFSSHNL-UHFFFAOYSA-N 2-amino-2-phenylethanol Chemical compound OCC(N)C1=CC=CC=C1 IJXJGQCXFSSHNL-UHFFFAOYSA-N 0.000 description 1
- GDFDRJARZUTLES-UHFFFAOYSA-N 2-amino-4-bromo-6-methylphenol Chemical compound CC1=CC(Br)=CC(N)=C1O GDFDRJARZUTLES-UHFFFAOYSA-N 0.000 description 1
- DRQWUAAWZFIVTF-UHFFFAOYSA-N 2-amino-5-bromophenol Chemical compound NC1=CC=C(Br)C=C1O DRQWUAAWZFIVTF-UHFFFAOYSA-N 0.000 description 1
- TVTJUIAKQFIXCE-HUKYDQBMSA-N 2-amino-9-[(2R,3S,4S,5R)-4-fluoro-3-hydroxy-5-(hydroxymethyl)oxolan-2-yl]-7-prop-2-ynyl-1H-purine-6,8-dione Chemical compound NC=1NC(C=2N(C(N(C=2N=1)[C@@H]1O[C@@H]([C@H]([C@H]1O)F)CO)=O)CC#C)=O TVTJUIAKQFIXCE-HUKYDQBMSA-N 0.000 description 1
- KMGUEILFFWDGFV-UHFFFAOYSA-N 2-benzoyl-2-benzoyloxy-3-hydroxybutanedioic acid Chemical compound C=1C=CC=CC=1C(=O)C(C(C(O)=O)O)(C(O)=O)OC(=O)C1=CC=CC=C1 KMGUEILFFWDGFV-UHFFFAOYSA-N 0.000 description 1
- XJEJNHNJWBNPEN-UHFFFAOYSA-N 2-bromo-6-(2,3-dihydro-1,4-benzodioxin-6-yl)benzonitrile Chemical compound BrC1=C(C#N)C(=CC=C1)C1=CC2=C(OCCO2)C=C1 XJEJNHNJWBNPEN-UHFFFAOYSA-N 0.000 description 1
- IHHFLQMZNYDGFS-UHFFFAOYSA-N 2-bromo-6-(hydroxymethyl)pyridin-3-ol Chemical compound OCC1=CC=C(O)C(Br)=N1 IHHFLQMZNYDGFS-UHFFFAOYSA-N 0.000 description 1
- LXIBANSYVFWOAR-UHFFFAOYSA-N 2-bromo-6-iodobenzonitrile Chemical compound BrC1=CC=CC(I)=C1C#N LXIBANSYVFWOAR-UHFFFAOYSA-N 0.000 description 1
- HCYZWISVIGZVOT-UHFFFAOYSA-N 2-bromo-6-phenylbenzonitrile Chemical compound BrC1=C(C(=CC=C1)C1=CC=CC=C1)C#N HCYZWISVIGZVOT-UHFFFAOYSA-N 0.000 description 1
- WHCRABJNJRAJIP-UHFFFAOYSA-N 2-chloro-4-iodo-3-methylpyridine Chemical compound CC1=C(I)C=CN=C1Cl WHCRABJNJRAJIP-UHFFFAOYSA-N 0.000 description 1
- 125000004493 2-methylbut-1-yl group Chemical group CC(C*)CC 0.000 description 1
- 125000004105 2-pyridyl group Chemical group N1=C([*])C([H])=C([H])C([H])=C1[H] 0.000 description 1
- VHMICKWLTGFITH-UHFFFAOYSA-N 2H-isoindole Chemical compound C1=CC=CC2=CNC=C21 VHMICKWLTGFITH-UHFFFAOYSA-N 0.000 description 1
- CVKOOKPNCVYHNY-UHFFFAOYSA-N 3-(bromomethyl)benzonitrile Chemical compound BrCC1=CC=CC(C#N)=C1 CVKOOKPNCVYHNY-UHFFFAOYSA-N 0.000 description 1
- LKKMLIBUAXYLOY-UHFFFAOYSA-N 3-Amino-1-methyl-5H-pyrido[4,3-b]indole Chemical compound N1C2=CC=CC=C2C2=C1C=C(N)N=C2C LKKMLIBUAXYLOY-UHFFFAOYSA-N 0.000 description 1
- 125000003349 3-pyridyl group Chemical group N1=C([H])C([*])=C([H])C([H])=C1[H] 0.000 description 1
- AOJJSUZBOXZQNB-VTZDEGQISA-N 4'-epidoxorubicin Chemical compound O([C@H]1C[C@@](O)(CC=2C(O)=C3C(=O)C=4C=CC=C(C=4C(=O)C3=C(O)C=21)OC)C(=O)CO)[C@H]1C[C@H](N)[C@@H](O)[C@H](C)O1 AOJJSUZBOXZQNB-VTZDEGQISA-N 0.000 description 1
- JLCGPSNHSULUGI-UHFFFAOYSA-N 4-(2-bromoethyl)morpholine;hydrochloride Chemical compound Cl.BrCCN1CCOCC1 JLCGPSNHSULUGI-UHFFFAOYSA-N 0.000 description 1
- QCQCHGYLTSGIGX-GHXANHINSA-N 4-[[(3ar,5ar,5br,7ar,9s,11ar,11br,13as)-5a,5b,8,8,11a-pentamethyl-3a-[(5-methylpyridine-3-carbonyl)amino]-2-oxo-1-propan-2-yl-4,5,6,7,7a,9,10,11,11b,12,13,13a-dodecahydro-3h-cyclopenta[a]chrysen-9-yl]oxy]-2,2-dimethyl-4-oxobutanoic acid Chemical compound N([C@@]12CC[C@@]3(C)[C@]4(C)CC[C@H]5C(C)(C)[C@@H](OC(=O)CC(C)(C)C(O)=O)CC[C@]5(C)[C@H]4CC[C@@H]3C1=C(C(C2)=O)C(C)C)C(=O)C1=CN=CC(C)=C1 QCQCHGYLTSGIGX-GHXANHINSA-N 0.000 description 1
- ZUYLSPMIGQJBGC-UHFFFAOYSA-N 4-amino-6-chloropyridin-3-ol Chemical compound NC1=CC(Cl)=NC=C1O ZUYLSPMIGQJBGC-UHFFFAOYSA-N 0.000 description 1
- CQPGDDAKTTWVDD-UHFFFAOYSA-N 4-bromobutanenitrile Chemical group BrCCCC#N CQPGDDAKTTWVDD-UHFFFAOYSA-N 0.000 description 1
- IXPKGTUILPMSQY-UHFFFAOYSA-N 4-methyl-2-(2-methyl-3-phenylphenyl)-1,3-benzothiazole-6-carbaldehyde Chemical compound CC1=CC(=CC2=C1N=C(S2)C=1C(=C(C=CC=1)C1=CC=CC=C1)C)C=O IXPKGTUILPMSQY-UHFFFAOYSA-N 0.000 description 1
- 125000000339 4-pyridyl group Chemical group N1=C([H])C([H])=C([*])C([H])=C1[H] 0.000 description 1
- 102100022464 5'-nucleotidase Human genes 0.000 description 1
- TYZVVWDJPPAYJY-UHFFFAOYSA-N 5-(hydroxymethyl)-2-(2-methyl-3-phenylphenyl)-1,3-benzoxazol-6-ol Chemical compound OCC=1C(=CC2=C(N=C(O2)C=2C(=C(C=CC=2)C2=CC=CC=C2)C)C=1)O TYZVVWDJPPAYJY-UHFFFAOYSA-N 0.000 description 1
- XAUDJQYHKZQPEU-KVQBGUIXSA-N 5-aza-2'-deoxycytidine Chemical compound O=C1N=C(N)N=CN1[C@@H]1O[C@H](CO)[C@@H](O)C1 XAUDJQYHKZQPEU-KVQBGUIXSA-N 0.000 description 1
- NMUSYJAQQFHJEW-KVTDHHQDSA-N 5-azacytidine Chemical compound O=C1N=C(N)N=CN1[C@H]1[C@H](O)[C@H](O)[C@@H](CO)O1 NMUSYJAQQFHJEW-KVTDHHQDSA-N 0.000 description 1
- AVVBQIWUGVFBGR-UHFFFAOYSA-N 5-bromo-4-chloro-2-nitrophenol Chemical compound OC1=CC(Br)=C(Cl)C=C1[N+]([O-])=O AVVBQIWUGVFBGR-UHFFFAOYSA-N 0.000 description 1
- CNAUCIIJJMPIIQ-UHFFFAOYSA-N 5-bromo-7-methyl-2-(2-methyl-3-phenylphenyl)-1,3-benzoxazole Chemical compound BrC=1C=C(C2=C(N=C(O2)C=2C(=C(C=CC=2)C2=CC=CC=C2)C)C=1)C CNAUCIIJJMPIIQ-UHFFFAOYSA-N 0.000 description 1
- NWXOACKDGAWBIA-UHFFFAOYSA-N 5-ethenyl-7-methyl-2-(2-methyl-3-phenylphenyl)-1,3-benzoxazole Chemical compound CC1=CC(=CC=2N=C(OC=21)C=1C(=C(C=CC=1)C1=CC=CC=C1)C)C=C NWXOACKDGAWBIA-UHFFFAOYSA-N 0.000 description 1
- WYWHKKSPHMUBEB-UHFFFAOYSA-N 6-Mercaptoguanine Natural products N1C(N)=NC(=S)C2=C1N=CN2 WYWHKKSPHMUBEB-UHFFFAOYSA-N 0.000 description 1
- GEEYJBBOQFJGGT-UHFFFAOYSA-N 6-bromo-2-(2-methyl-3-phenylphenyl)-1,3-benzoxazole Chemical compound BrC1=CC2=C(N=C(O2)C=2C(=C(C=CC=2)C2=CC=CC=C2)C)C=C1 GEEYJBBOQFJGGT-UHFFFAOYSA-N 0.000 description 1
- CQNDRYGENLEDAA-UHFFFAOYSA-N 6-bromo-4-methyl-1,3-benzothiazol-2-amine Chemical compound CC1=CC(Br)=CC2=C1N=C(N)S2 CQNDRYGENLEDAA-UHFFFAOYSA-N 0.000 description 1
- XXARZIJMPRNALX-UHFFFAOYSA-N 6-chloro-2-iodo-4-methylpyridin-3-ol Chemical compound ClC1=CC(=C(C(=N1)I)O)C XXARZIJMPRNALX-UHFFFAOYSA-N 0.000 description 1
- LGIWBJAKRNDPOO-UHFFFAOYSA-N 6-ethenyl-2-(2-methyl-3-phenylphenyl)-[1,3]oxazolo[5,4-c]pyridine Chemical compound CC1=C(C=CC=C1C=1OC=2C=NC(=CC=2N=1)C=C)C1=CC=CC=C1 LGIWBJAKRNDPOO-UHFFFAOYSA-N 0.000 description 1
- FHVDTGUDJYJELY-UHFFFAOYSA-N 6-{[2-carboxy-4,5-dihydroxy-6-(phosphanyloxy)oxan-3-yl]oxy}-4,5-dihydroxy-3-phosphanyloxane-2-carboxylic acid Chemical compound O1C(C(O)=O)C(P)C(O)C(O)C1OC1C(C(O)=O)OC(OP)C(O)C1O FHVDTGUDJYJELY-UHFFFAOYSA-N 0.000 description 1
- VVIAGPKUTFNRDU-UHFFFAOYSA-N 6S-folinic acid Natural products C1NC=2NC(N)=NC(=O)C=2N(C=O)C1CNC1=CC=C(C(=O)NC(CCC(O)=O)C(O)=O)C=C1 VVIAGPKUTFNRDU-UHFFFAOYSA-N 0.000 description 1
- STQGQHZAVUOBTE-UHFFFAOYSA-N 7-Cyan-hept-2t-en-4,6-diinsaeure Natural products C1=2C(O)=C3C(=O)C=4C(OC)=CC=CC=4C(=O)C3=C(O)C=2CC(O)(C(C)=O)CC1OC1CC(N)C(O)C(C)O1 STQGQHZAVUOBTE-UHFFFAOYSA-N 0.000 description 1
- OOZNFXSESDYGDQ-UHFFFAOYSA-N 7-methyl-2-(2-methyl-3-phenylphenyl)-1,3-benzoxazole-5-carbaldehyde Chemical compound CC1=CC(=CC=2N=C(OC=21)C=1C(=C(C=CC=1)C1=CC=CC=C1)C)C=O OOZNFXSESDYGDQ-UHFFFAOYSA-N 0.000 description 1
- ALHPWEIDDBNLGT-UHFFFAOYSA-N 7-methyl-2-(2-methyl-3-phenylphenyl)furo[2,3-c]pyridine-5-carbaldehyde Chemical compound CC=1N=C(C=C2C=1OC(=C2)C=1C(=C(C=CC=1)C1=CC=CC=C1)C)C=O ALHPWEIDDBNLGT-UHFFFAOYSA-N 0.000 description 1
- HBAQYPYDRFILMT-UHFFFAOYSA-N 8-[3-(1-cyclopropylpyrazol-4-yl)-1H-pyrazolo[4,3-d]pyrimidin-5-yl]-3-methyl-3,8-diazabicyclo[3.2.1]octan-2-one Chemical class C1(CC1)N1N=CC(=C1)C1=NNC2=C1N=C(N=C2)N1C2C(N(CC1CC2)C)=O HBAQYPYDRFILMT-UHFFFAOYSA-N 0.000 description 1
- SHGAZHPCJJPHSC-ZVCIMWCZSA-N 9-cis-retinoic acid Chemical compound OC(=O)/C=C(\C)/C=C/C=C(/C)\C=C\C1=C(C)CCCC1(C)C SHGAZHPCJJPHSC-ZVCIMWCZSA-N 0.000 description 1
- 101150107888 AKT2 gene Proteins 0.000 description 1
- 244000215068 Acacia senegal Species 0.000 description 1
- 208000014697 Acute lymphocytic leukaemia Diseases 0.000 description 1
- 101150051155 Akt3 gene Proteins 0.000 description 1
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 1
- 102000004452 Arginase Human genes 0.000 description 1
- 108700024123 Arginases Proteins 0.000 description 1
- BFYIZQONLCFLEV-DAELLWKTSA-N Aromasine Chemical compound O=C1C=C[C@]2(C)[C@H]3CC[C@](C)(C(CC4)=O)[C@@H]4[C@@H]3CC(=C)C2=C1 BFYIZQONLCFLEV-DAELLWKTSA-N 0.000 description 1
- 108010024976 Asparaginase Proteins 0.000 description 1
- 102000015790 Asparaginase Human genes 0.000 description 1
- 241000416162 Astragalus gummifer Species 0.000 description 1
- 108091008875 B cell receptors Proteins 0.000 description 1
- MLDQJTXFUGDVEO-UHFFFAOYSA-N BAY-43-9006 Chemical compound C1=NC(C(=O)NC)=CC(OC=2C=CC(NC(=O)NC=3C=C(C(Cl)=CC=3)C(F)(F)F)=CC=2)=C1 MLDQJTXFUGDVEO-UHFFFAOYSA-N 0.000 description 1
- 102100035080 BDNF/NT-3 growth factors receptor Human genes 0.000 description 1
- 229940125565 BMS-986016 Drugs 0.000 description 1
- 101000840545 Bacillus thuringiensis L-isoleucine-4-hydroxylase Proteins 0.000 description 1
- 108010006654 Bleomycin Proteins 0.000 description 1
- 241000283690 Bos taurus Species 0.000 description 1
- 238000006443 Buchwald-Hartwig cross coupling reaction Methods 0.000 description 1
- FIPWRIJSWJWJAI-UHFFFAOYSA-N Butyl carbitol 6-propylpiperonyl ether Chemical compound C1=C(CCC)C(COCCOCCOCCCC)=CC2=C1OCO2 FIPWRIJSWJWJAI-UHFFFAOYSA-N 0.000 description 1
- IMIXESFKWRUZKW-UHFFFAOYSA-N CC1=C(C=CC=C1C2=CC3=C(O2)N=CC=C3)C4=CC=CC=C4 Chemical compound CC1=C(C=CC=C1C2=CC3=C(O2)N=CC=C3)C4=CC=CC=C4 IMIXESFKWRUZKW-UHFFFAOYSA-N 0.000 description 1
- IUEZOLCMLANKFT-UHFFFAOYSA-N CC1=C(C=CC=C1C2=NC3=C(O2)C=CC(=C3C)C(=O)O)C4=CC=CC=C4 Chemical compound CC1=C(C=CC=C1C2=NC3=C(O2)C=CC(=C3C)C(=O)O)C4=CC=CC=C4 IUEZOLCMLANKFT-UHFFFAOYSA-N 0.000 description 1
- LPNJEASOPGNUKF-UHFFFAOYSA-N COC(=O)c1ccc(O)c(C)n1 Chemical compound COC(=O)c1ccc(O)c(C)n1 LPNJEASOPGNUKF-UHFFFAOYSA-N 0.000 description 1
- 101100381481 Caenorhabditis elegans baz-2 gene Proteins 0.000 description 1
- 241000282472 Canis lupus familiaris Species 0.000 description 1
- GAGWJHPBXLXJQN-UORFTKCHSA-N Capecitabine Chemical compound C1=C(F)C(NC(=O)OCCCCC)=NC(=O)N1[C@H]1[C@H](O)[C@H](O)[C@@H](C)O1 GAGWJHPBXLXJQN-UORFTKCHSA-N 0.000 description 1
- GAGWJHPBXLXJQN-UHFFFAOYSA-N Capecitabine Natural products C1=C(F)C(NC(=O)OCCCCC)=NC(=O)N1C1C(O)C(O)C(C)O1 GAGWJHPBXLXJQN-UHFFFAOYSA-N 0.000 description 1
- 239000004215 Carbon black (E152) Substances 0.000 description 1
- DLGOEMSEDOSKAD-UHFFFAOYSA-N Carmustine Chemical compound ClCCNC(=O)N(N=O)CCCl DLGOEMSEDOSKAD-UHFFFAOYSA-N 0.000 description 1
- ABMPKFGOKPZWFW-UHFFFAOYSA-N Cc1c(CO)cccc1-c1ccc2OCCOc2c1 Chemical compound Cc1c(CO)cccc1-c1ccc2OCCOc2c1 ABMPKFGOKPZWFW-UHFFFAOYSA-N 0.000 description 1
- 102000000844 Cell Surface Receptors Human genes 0.000 description 1
- 108010001857 Cell Surface Receptors Proteins 0.000 description 1
- 206010007953 Central nervous system lymphoma Diseases 0.000 description 1
- JWBOIMRXGHLCPP-UHFFFAOYSA-N Chloditan Chemical compound C=1C=CC=C(Cl)C=1C(C(Cl)Cl)C1=CC=C(Cl)C=C1 JWBOIMRXGHLCPP-UHFFFAOYSA-N 0.000 description 1
- 208000010833 Chronic myeloid leukaemia Diseases 0.000 description 1
- PTOAARAWEBMLNO-KVQBGUIXSA-N Cladribine Chemical compound C1=NC=2C(N)=NC(Cl)=NC=2N1[C@H]1C[C@H](O)[C@@H](CO)O1 PTOAARAWEBMLNO-KVQBGUIXSA-N 0.000 description 1
- 206010056370 Congestive cardiomyopathy Diseases 0.000 description 1
- 229910021595 Copper(I) iodide Inorganic materials 0.000 description 1
- VMQMZMRVKUZKQL-UHFFFAOYSA-N Cu+ Chemical class [Cu+] VMQMZMRVKUZKQL-UHFFFAOYSA-N 0.000 description 1
- XDTMQSROBMDMFD-UHFFFAOYSA-N Cyclohexane Chemical compound C1CCCCC1 XDTMQSROBMDMFD-UHFFFAOYSA-N 0.000 description 1
- CMSMOCZEIVJLDB-UHFFFAOYSA-N Cyclophosphamide Chemical compound ClCCN(CCCl)P1(=O)NCCCO1 CMSMOCZEIVJLDB-UHFFFAOYSA-N 0.000 description 1
- UHDGCWIWMRVCDJ-CCXZUQQUSA-N Cytarabine Chemical compound O=C1N=C(N)C=CN1[C@H]1[C@@H](O)[C@H](O)[C@@H](CO)O1 UHDGCWIWMRVCDJ-CCXZUQQUSA-N 0.000 description 1
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 1
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 1
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 1
- 108010092160 Dactinomycin Proteins 0.000 description 1
- 101100481408 Danio rerio tie2 gene Proteins 0.000 description 1
- ZBNZXTGUTAYRHI-UHFFFAOYSA-N Dasatinib Chemical compound C=1C(N2CCN(CCO)CC2)=NC(C)=NC=1NC(S1)=NC=C1C(=O)NC1=C(C)C=CC=C1Cl ZBNZXTGUTAYRHI-UHFFFAOYSA-N 0.000 description 1
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 1
- 201000010046 Dilated cardiomyopathy Diseases 0.000 description 1
- 206010059866 Drug resistance Diseases 0.000 description 1
- 108010055196 EphA2 Receptor Proteins 0.000 description 1
- 108010055191 EphA3 Receptor Proteins 0.000 description 1
- 108010055334 EphB2 Receptor Proteins 0.000 description 1
- 102100030322 Ephrin type-A receptor 1 Human genes 0.000 description 1
- 102100030340 Ephrin type-A receptor 2 Human genes 0.000 description 1
- 102100030324 Ephrin type-A receptor 3 Human genes 0.000 description 1
- 102100031983 Ephrin type-B receptor 4 Human genes 0.000 description 1
- HTIJFSOGRVMCQR-UHFFFAOYSA-N Epirubicin Natural products COc1cccc2C(=O)c3c(O)c4CC(O)(CC(OC5CC(N)C(=O)C(C)O5)c4c(O)c3C(=O)c12)C(=O)CO HTIJFSOGRVMCQR-UHFFFAOYSA-N 0.000 description 1
- 241000283086 Equidae Species 0.000 description 1
- 229910052693 Europium Inorganic materials 0.000 description 1
- 108010007457 Extracellular Signal-Regulated MAP Kinases Proteins 0.000 description 1
- 108091008794 FGF receptors Proteins 0.000 description 1
- 101150009958 FLT4 gene Proteins 0.000 description 1
- JNCMHMUGTWEVOZ-UHFFFAOYSA-N F[CH]F Chemical compound F[CH]F JNCMHMUGTWEVOZ-UHFFFAOYSA-N 0.000 description 1
- 241000282326 Felis catus Species 0.000 description 1
- 108010029961 Filgrastim Proteins 0.000 description 1
- KRHYYFGTRYWZRS-UHFFFAOYSA-M Fluoride anion Chemical compound [F-] KRHYYFGTRYWZRS-UHFFFAOYSA-M 0.000 description 1
- GHASVSINZRGABV-UHFFFAOYSA-N Fluorouracil Chemical compound FC1=CNC(=O)NC1=O GHASVSINZRGABV-UHFFFAOYSA-N 0.000 description 1
- VWUXBMIQPBEWFH-WCCTWKNTSA-N Fulvestrant Chemical compound OC1=CC=C2[C@H]3CC[C@](C)([C@H](CC4)O)[C@@H]4[C@@H]3[C@H](CCCCCCCCCS(=O)CCCC(F)(F)C(F)(F)F)CC2=C1 VWUXBMIQPBEWFH-WCCTWKNTSA-N 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- 208000032612 Glial tumor Diseases 0.000 description 1
- 206010018338 Glioma Diseases 0.000 description 1
- 206010018364 Glomerulonephritis Diseases 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- 108010069236 Goserelin Proteins 0.000 description 1
- 108010017080 Granulocyte Colony-Stimulating Factor Proteins 0.000 description 1
- 229920000084 Gum arabic Polymers 0.000 description 1
- 108010081348 HRT1 protein Hairy Proteins 0.000 description 1
- 102100021881 Hairy/enhancer-of-split related with YRPW motif protein 1 Human genes 0.000 description 1
- 102000002812 Heat-Shock Proteins Human genes 0.000 description 1
- 108010004889 Heat-Shock Proteins Proteins 0.000 description 1
- 102100035108 High affinity nerve growth factor receptor Human genes 0.000 description 1
- 101000678236 Homo sapiens 5'-nucleotidase Proteins 0.000 description 1
- 101000596896 Homo sapiens BDNF/NT-3 growth factors receptor Proteins 0.000 description 1
- 101000938354 Homo sapiens Ephrin type-A receptor 1 Proteins 0.000 description 1
- 101000596894 Homo sapiens High affinity nerve growth factor receptor Proteins 0.000 description 1
- 101001037256 Homo sapiens Indoleamine 2,3-dioxygenase 1 Proteins 0.000 description 1
- 101001055145 Homo sapiens Interleukin-2 receptor subunit beta Proteins 0.000 description 1
- 101000868279 Homo sapiens Leukocyte surface antigen CD47 Proteins 0.000 description 1
- 101001138062 Homo sapiens Leukocyte-associated immunoglobulin-like receptor 1 Proteins 0.000 description 1
- 101001117317 Homo sapiens Programmed cell death 1 ligand 1 Proteins 0.000 description 1
- 101001012157 Homo sapiens Receptor tyrosine-protein kinase erbB-2 Proteins 0.000 description 1
- 101000932478 Homo sapiens Receptor-type tyrosine-protein kinase FLT3 Proteins 0.000 description 1
- 101000831007 Homo sapiens T-cell immunoreceptor with Ig and ITIM domains Proteins 0.000 description 1
- 101000596234 Homo sapiens T-cell surface protein tactile Proteins 0.000 description 1
- 101000611183 Homo sapiens Tumor necrosis factor Proteins 0.000 description 1
- 101000997832 Homo sapiens Tyrosine-protein kinase JAK2 Proteins 0.000 description 1
- 239000004354 Hydroxyethyl cellulose Substances 0.000 description 1
- 229920000663 Hydroxyethyl cellulose Polymers 0.000 description 1
- 206010020751 Hypersensitivity Diseases 0.000 description 1
- 238000004566 IR spectroscopy Methods 0.000 description 1
- XDXDZDZNSLXDNA-TZNDIEGXSA-N Idarubicin Chemical compound C1[C@H](N)[C@H](O)[C@H](C)O[C@H]1O[C@@H]1C2=C(O)C(C(=O)C3=CC=CC=C3C3=O)=C3C(O)=C2C[C@@](O)(C(C)=O)C1 XDXDZDZNSLXDNA-TZNDIEGXSA-N 0.000 description 1
- XDXDZDZNSLXDNA-UHFFFAOYSA-N Idarubicin Natural products C1C(N)C(O)C(C)OC1OC1C2=C(O)C(C(=O)C3=CC=CC=C3C3=O)=C3C(O)=C2CC(O)(C(C)=O)C1 XDXDZDZNSLXDNA-UHFFFAOYSA-N 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- 108060003951 Immunoglobulin Proteins 0.000 description 1
- 108010078049 Interferon alpha-2 Proteins 0.000 description 1
- 108010050904 Interferons Proteins 0.000 description 1
- 102000014150 Interferons Human genes 0.000 description 1
- 102100026879 Interleukin-2 receptor subunit beta Human genes 0.000 description 1
- 229940122245 Janus kinase inhibitor Drugs 0.000 description 1
- 102000002698 KIR Receptors Human genes 0.000 description 1
- 108010043610 KIR Receptors Proteins 0.000 description 1
- FBOZXECLQNJBKD-ZDUSSCGKSA-N L-methotrexate Chemical compound C=1N=C2N=C(N)N=C(N)C2=NC=1CN(C)C1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)C=C1 FBOZXECLQNJBKD-ZDUSSCGKSA-N 0.000 description 1
- 239000005411 L01XE02 - Gefitinib Substances 0.000 description 1
- 239000005551 L01XE03 - Erlotinib Substances 0.000 description 1
- 239000002147 L01XE04 - Sunitinib Substances 0.000 description 1
- 239000005511 L01XE05 - Sorafenib Substances 0.000 description 1
- 239000002067 L01XE06 - Dasatinib Substances 0.000 description 1
- 239000002136 L01XE07 - Lapatinib Substances 0.000 description 1
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 1
- XNRVGTHNYCNCFF-UHFFFAOYSA-N Lapatinib ditosylate monohydrate Chemical compound O.CC1=CC=C(S(O)(=O)=O)C=C1.CC1=CC=C(S(O)(=O)=O)C=C1.O1C(CNCCS(=O)(=O)C)=CC=C1C1=CC=C(N=CN=C2NC=3C=C(Cl)C(OCC=4C=C(F)C=CC=4)=CC=3)C2=C1 XNRVGTHNYCNCFF-UHFFFAOYSA-N 0.000 description 1
- 241000222722 Leishmania <genus> Species 0.000 description 1
- 102100032913 Leukocyte surface antigen CD47 Human genes 0.000 description 1
- 102100020943 Leukocyte-associated immunoglobulin-like receptor 1 Human genes 0.000 description 1
- 108010000817 Leuprolide Proteins 0.000 description 1
- HLFSDGLLUJUHTE-SNVBAGLBSA-N Levamisole Chemical compound C1([C@H]2CN3CCSC3=N2)=CC=CC=C1 HLFSDGLLUJUHTE-SNVBAGLBSA-N 0.000 description 1
- 239000002841 Lewis acid Substances 0.000 description 1
- 229910010082 LiAlH Inorganic materials 0.000 description 1
- GQYIWUVLTXOXAJ-UHFFFAOYSA-N Lomustine Chemical compound ClCCN(N=O)C(=O)NC1CCCCC1 GQYIWUVLTXOXAJ-UHFFFAOYSA-N 0.000 description 1
- 241000712899 Lymphocytic choriomeningitis mammarenavirus Species 0.000 description 1
- 102000001291 MAP Kinase Kinase Kinase Human genes 0.000 description 1
- 102000043136 MAP kinase family Human genes 0.000 description 1
- 108091054455 MAP kinase family Proteins 0.000 description 1
- 108060006687 MAP kinase kinase kinase Proteins 0.000 description 1
- 229930195725 Mannitol Natural products 0.000 description 1
- 102000007557 Melanoma-Specific Antigens Human genes 0.000 description 1
- 108010071463 Melanoma-Specific Antigens Proteins 0.000 description 1
- 102000000440 Melanoma-associated antigen Human genes 0.000 description 1
- 108050008953 Melanoma-associated antigen Proteins 0.000 description 1
- 229920003091 Methocel™ Polymers 0.000 description 1
- 229920003094 Methocel™ K4M Polymers 0.000 description 1
- QXKHYNVANLEOEG-UHFFFAOYSA-N Methoxsalen Chemical compound C1=CC(=O)OC2=C1C=C1C=COC1=C2OC QXKHYNVANLEOEG-UHFFFAOYSA-N 0.000 description 1
- 241000235388 Mucorales Species 0.000 description 1
- 101100381978 Mus musculus Braf gene Proteins 0.000 description 1
- 101100481410 Mus musculus Tek gene Proteins 0.000 description 1
- 208000033761 Myelogenous Chronic BCR-ABL Positive Leukemia Diseases 0.000 description 1
- FMCGSUUBYTWNDP-UHFFFAOYSA-N N-Methylephedrine Natural products CN(C)C(C)C(O)C1=CC=CC=C1 FMCGSUUBYTWNDP-UHFFFAOYSA-N 0.000 description 1
- ZDZOTLJHXYCWBA-VCVYQWHSSA-N N-debenzoyl-N-(tert-butoxycarbonyl)-10-deacetyltaxol Chemical compound O([C@H]1[C@H]2[C@@](C([C@H](O)C3=C(C)[C@@H](OC(=O)[C@H](O)[C@@H](NC(=O)OC(C)(C)C)C=4C=CC=CC=4)C[C@]1(O)C3(C)C)=O)(C)[C@@H](O)C[C@H]1OC[C@]12OC(=O)C)C(=O)C1=CC=CC=C1 ZDZOTLJHXYCWBA-VCVYQWHSSA-N 0.000 description 1
- 125000000815 N-oxide group Chemical group 0.000 description 1
- 102000003945 NF-kappa B Human genes 0.000 description 1
- 108010057466 NF-kappa B Proteins 0.000 description 1
- 238000005481 NMR spectroscopy Methods 0.000 description 1
- 102100029166 NT-3 growth factor receptor Human genes 0.000 description 1
- 101150117329 NTRK3 gene Proteins 0.000 description 1
- 238000006411 Negishi coupling reaction Methods 0.000 description 1
- GRYLNZFGIOXLOG-UHFFFAOYSA-N Nitric acid Chemical compound O[N+]([O-])=O GRYLNZFGIOXLOG-UHFFFAOYSA-N 0.000 description 1
- 102000007607 Non-Receptor Type 11 Protein Tyrosine Phosphatase Human genes 0.000 description 1
- 108010032107 Non-Receptor Type 11 Protein Tyrosine Phosphatase Proteins 0.000 description 1
- 102000002001 Non-Receptor Type 6 Protein Tyrosine Phosphatase Human genes 0.000 description 1
- 108010015793 Non-Receptor Type 6 Protein Tyrosine Phosphatase Proteins 0.000 description 1
- YGACXVRLDHEXKY-WXRXAMBDSA-N O[C@H](C[C@H]1c2c(cccc2F)-c2cncn12)[C@H]1CC[C@H](O)CC1 Chemical compound O[C@H](C[C@H]1c2c(cccc2F)-c2cncn12)[C@H]1CC[C@H](O)CC1 YGACXVRLDHEXKY-WXRXAMBDSA-N 0.000 description 1
- VNQABZCSYCTZMS-UHFFFAOYSA-N Orthoform Chemical compound COC(=O)C1=CC=C(O)C(N)=C1 VNQABZCSYCTZMS-UHFFFAOYSA-N 0.000 description 1
- 241000283973 Oryctolagus cuniculus Species 0.000 description 1
- 229940124780 PI3K delta inhibitor Drugs 0.000 description 1
- 229930012538 Paclitaxel Natural products 0.000 description 1
- 235000019483 Peanut oil Nutrition 0.000 description 1
- 241001494479 Pecora Species 0.000 description 1
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 description 1
- 102000014750 Phosphorylase Kinase Human genes 0.000 description 1
- 108010064071 Phosphorylase Kinase Proteins 0.000 description 1
- 108091000080 Phosphotransferase Proteins 0.000 description 1
- 239000004793 Polystyrene Substances 0.000 description 1
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 1
- 208000006664 Precursor Cell Lymphoblastic Leukemia-Lymphoma Diseases 0.000 description 1
- 241000288906 Primates Species 0.000 description 1
- 102000003923 Protein Kinase C Human genes 0.000 description 1
- 108090000315 Protein Kinase C Proteins 0.000 description 1
- 102000001892 Protein Kinase C-theta Human genes 0.000 description 1
- 108010015499 Protein Kinase C-theta Proteins 0.000 description 1
- 102000004022 Protein-Tyrosine Kinases Human genes 0.000 description 1
- 108090000412 Protein-Tyrosine Kinases Proteins 0.000 description 1
- 241000589517 Pseudomonas aeruginosa Species 0.000 description 1
- 201000004681 Psoriasis Diseases 0.000 description 1
- WTKZEGDFNFYCGP-UHFFFAOYSA-N Pyrazole Chemical compound C=1C=NNC=1 WTKZEGDFNFYCGP-UHFFFAOYSA-N 0.000 description 1
- IWYDHOAUDWTVEP-UHFFFAOYSA-N R-2-phenyl-2-hydroxyacetic acid Natural products OC(=O)C(O)C1=CC=CC=C1 IWYDHOAUDWTVEP-UHFFFAOYSA-N 0.000 description 1
- 241000700159 Rattus Species 0.000 description 1
- 101100372762 Rattus norvegicus Flt1 gene Proteins 0.000 description 1
- 102100030086 Receptor tyrosine-protein kinase erbB-2 Human genes 0.000 description 1
- 102100029986 Receptor tyrosine-protein kinase erbB-3 Human genes 0.000 description 1
- 101710100969 Receptor tyrosine-protein kinase erbB-3 Proteins 0.000 description 1
- 102100029981 Receptor tyrosine-protein kinase erbB-4 Human genes 0.000 description 1
- 101710100963 Receptor tyrosine-protein kinase erbB-4 Proteins 0.000 description 1
- 102100020718 Receptor-type tyrosine-protein kinase FLT3 Human genes 0.000 description 1
- 102000007056 Recombinant Fusion Proteins Human genes 0.000 description 1
- 108010008281 Recombinant Fusion Proteins Proteins 0.000 description 1
- 206010070308 Refractory cancer Diseases 0.000 description 1
- 241000283984 Rodentia Species 0.000 description 1
- 101001037255 Saccharomyces cerevisiae (strain ATCC 204508 / S288c) Indoleamine 2,3-dioxygenase Proteins 0.000 description 1
- 238000006223 Seyferth-Gilbert homologation reaction Methods 0.000 description 1
- 229920001800 Shellac Polymers 0.000 description 1
- 241000700584 Simplexvirus Species 0.000 description 1
- KEAYESYHFKHZAL-UHFFFAOYSA-N Sodium Chemical compound [Na] KEAYESYHFKHZAL-UHFFFAOYSA-N 0.000 description 1
- 238000003477 Sonogashira cross-coupling reaction Methods 0.000 description 1
- 241000191967 Staphylococcus aureus Species 0.000 description 1
- 229920002472 Starch Polymers 0.000 description 1
- 238000006619 Stille reaction Methods 0.000 description 1
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 1
- 229930006000 Sucrose Natural products 0.000 description 1
- 241000282887 Suidae Species 0.000 description 1
- UCKMPCXJQFINFW-UHFFFAOYSA-N Sulphide Chemical compound [S-2] UCKMPCXJQFINFW-UHFFFAOYSA-N 0.000 description 1
- 230000006044 T cell activation Effects 0.000 description 1
- 102100024834 T-cell immunoreceptor with Ig and ITIM domains Human genes 0.000 description 1
- 102100035268 T-cell surface protein tactile Human genes 0.000 description 1
- 108091005729 TAM receptors Proteins 0.000 description 1
- 102000013530 TOR Serine-Threonine Kinases Human genes 0.000 description 1
- 108010065917 TOR Serine-Threonine Kinases Proteins 0.000 description 1
- NAVMQTYZDKMPEU-UHFFFAOYSA-N Targretin Chemical compound CC1=CC(C(CCC2(C)C)(C)C)=C2C=C1C(=C)C1=CC=C(C(O)=O)C=C1 NAVMQTYZDKMPEU-UHFFFAOYSA-N 0.000 description 1
- BPEGJWRSRHCHSN-UHFFFAOYSA-N Temozolomide Chemical compound O=C1N(C)N=NC2=C(C(N)=O)N=CN21 BPEGJWRSRHCHSN-UHFFFAOYSA-N 0.000 description 1
- FOCVUCIESVLUNU-UHFFFAOYSA-N Thiotepa Chemical compound C1CN1P(N1CC1)(=S)N1CC1 FOCVUCIESVLUNU-UHFFFAOYSA-N 0.000 description 1
- 229920001615 Tragacanth Polymers 0.000 description 1
- 102000004887 Transforming Growth Factor beta Human genes 0.000 description 1
- 108090001012 Transforming Growth Factor beta Proteins 0.000 description 1
- 102100039094 Tyrosinase Human genes 0.000 description 1
- 108060008724 Tyrosinase Proteins 0.000 description 1
- 102100033444 Tyrosine-protein kinase JAK2 Human genes 0.000 description 1
- 108091008605 VEGF receptors Proteins 0.000 description 1
- 102000016663 Vascular Endothelial Growth Factor Receptor-3 Human genes 0.000 description 1
- JXLYSJRDGCGARV-WWYNWVTFSA-N Vinblastine Natural products O=C(O[C@H]1[C@](O)(C(=O)OC)[C@@H]2N(C)c3c(cc(c(OC)c3)[C@]3(C(=O)OC)c4[nH]c5c(c4CCN4C[C@](O)(CC)C[C@H](C3)C4)cccc5)[C@@]32[C@H]2[C@@]1(CC)C=CCN2CC3)C JXLYSJRDGCGARV-WWYNWVTFSA-N 0.000 description 1
- 208000027418 Wounds and injury Diseases 0.000 description 1
- PCWZKQSKUXXDDJ-UHFFFAOYSA-N Xanthotoxin Natural products COCc1c2OC(=O)C=Cc2cc3ccoc13 PCWZKQSKUXXDDJ-UHFFFAOYSA-N 0.000 description 1
- XRVDKIQEFCJTBZ-UHFFFAOYSA-N [1,3]oxazolo[5,4-c]pyridine Chemical compound C1=NC=C2OC=NC2=C1 XRVDKIQEFCJTBZ-UHFFFAOYSA-N 0.000 description 1
- AIWRTTMUVOZGPW-HSPKUQOVSA-N abarelix Chemical compound C([C@@H](C(=O)N[C@H](CC(N)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCCNC(C)C)C(=O)N1[C@@H](CCC1)C(=O)N[C@H](C)C(N)=O)N(C)C(=O)[C@H](CO)NC(=O)[C@@H](CC=1C=NC=CC=1)NC(=O)[C@@H](CC=1C=CC(Cl)=CC=1)NC(=O)[C@@H](CC=1C=C2C=CC=CC2=CC=1)NC(C)=O)C1=CC=C(O)C=C1 AIWRTTMUVOZGPW-HSPKUQOVSA-N 0.000 description 1
- 229960002184 abarelix Drugs 0.000 description 1
- 108010023617 abarelix Proteins 0.000 description 1
- 230000002159 abnormal effect Effects 0.000 description 1
- 235000010489 acacia gum Nutrition 0.000 description 1
- 239000000205 acacia gum Substances 0.000 description 1
- 229940081735 acetylcellulose Drugs 0.000 description 1
- RJURFGZVJUQBHK-IIXSONLDSA-N actinomycin D Chemical compound C[C@H]1OC(=O)[C@H](C(C)C)N(C)C(=O)CN(C)C(=O)[C@@H]2CCCN2C(=O)[C@@H](C(C)C)NC(=O)[C@H]1NC(=O)C1=C(N)C(=O)C(C)=C2OC(C(C)=CC=C3C(=O)N[C@@H]4C(=O)N[C@@H](C(N5CCC[C@H]5C(=O)N(C)CC(=O)N(C)[C@@H](C(C)C)C(=O)O[C@@H]4C)=O)C(C)C)=C3N=C21 RJURFGZVJUQBHK-IIXSONLDSA-N 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 239000013543 active substance Substances 0.000 description 1
- 229940121359 adenosine receptor antagonist Drugs 0.000 description 1
- 239000002671 adjuvant Substances 0.000 description 1
- 238000009098 adjuvant therapy Methods 0.000 description 1
- 101150045355 akt1 gene Proteins 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- 125000003172 aldehyde group Chemical group 0.000 description 1
- 108700025316 aldesleukin Proteins 0.000 description 1
- 229960005310 aldesleukin Drugs 0.000 description 1
- 229960000548 alemtuzumab Drugs 0.000 description 1
- 229940072056 alginate Drugs 0.000 description 1
- 235000010443 alginic acid Nutrition 0.000 description 1
- 229920000615 alginic acid Polymers 0.000 description 1
- 229960001445 alitretinoin Drugs 0.000 description 1
- 239000003513 alkali Substances 0.000 description 1
- 125000004450 alkenylene group Chemical group 0.000 description 1
- 150000005215 alkyl ethers Chemical class 0.000 description 1
- SHGAZHPCJJPHSC-YCNIQYBTSA-N all-trans-retinoic acid Chemical compound OC(=O)\C=C(/C)\C=C\C=C(/C)\C=C\C1=C(C)CCCC1(C)C SHGAZHPCJJPHSC-YCNIQYBTSA-N 0.000 description 1
- OFCNXPDARWKPPY-UHFFFAOYSA-N allopurinol Chemical compound OC1=NC=NC2=C1C=NN2 OFCNXPDARWKPPY-UHFFFAOYSA-N 0.000 description 1
- 229960003459 allopurinol Drugs 0.000 description 1
- HSFWRNGVRCDJHI-UHFFFAOYSA-N alpha-acetylene Natural products C#C HSFWRNGVRCDJHI-UHFFFAOYSA-N 0.000 description 1
- BJEPYKJPYRNKOW-UHFFFAOYSA-N alpha-hydroxysuccinic acid Natural products OC(=O)C(O)CC(O)=O BJEPYKJPYRNKOW-UHFFFAOYSA-N 0.000 description 1
- 229960000473 altretamine Drugs 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- 239000000908 ammonium hydroxide Substances 0.000 description 1
- 229960002932 anastrozole Drugs 0.000 description 1
- YBBLVLTVTVSKRW-UHFFFAOYSA-N anastrozole Chemical compound N#CC(C)(C)C1=CC(C(C)(C#N)C)=CC(CN2N=CN=C2)=C1 YBBLVLTVTVSKRW-UHFFFAOYSA-N 0.000 description 1
- 239000004037 angiogenesis inhibitor Substances 0.000 description 1
- 229940121369 angiogenesis inhibitor Drugs 0.000 description 1
- 239000002260 anti-inflammatory agent Substances 0.000 description 1
- 229940121363 anti-inflammatory agent Drugs 0.000 description 1
- 230000006023 anti-tumor response Effects 0.000 description 1
- 229940124691 antibody therapeutics Drugs 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- 239000008365 aqueous carrier Substances 0.000 description 1
- 239000003125 aqueous solvent Substances 0.000 description 1
- GOLCXWYRSKYTSP-UHFFFAOYSA-N arsenic trioxide Inorganic materials O1[As]2O[As]1O2 GOLCXWYRSKYTSP-UHFFFAOYSA-N 0.000 description 1
- 229960002594 arsenic trioxide Drugs 0.000 description 1
- 125000000732 arylene group Chemical group 0.000 description 1
- 229960003272 asparaginase Drugs 0.000 description 1
- DCXYFEDJOCDNAF-UHFFFAOYSA-M asparaginate Chemical compound [O-]C(=O)C(N)CC(N)=O DCXYFEDJOCDNAF-UHFFFAOYSA-M 0.000 description 1
- 239000012131 assay buffer Substances 0.000 description 1
- 230000005784 autoimmunity Effects 0.000 description 1
- 229960002756 azacitidine Drugs 0.000 description 1
- VSRXQHXAPYXROS-UHFFFAOYSA-N azanide;cyclobutane-1,1-dicarboxylic acid;platinum(2+) Chemical compound [NH2-].[NH2-].[Pt+2].OC(=O)C1(C(O)=O)CCC1 VSRXQHXAPYXROS-UHFFFAOYSA-N 0.000 description 1
- XYOVOXDWRFGKEX-UHFFFAOYSA-N azepine Chemical compound N1C=CC=CC=C1 XYOVOXDWRFGKEX-UHFFFAOYSA-N 0.000 description 1
- 125000004567 azetidin-3-yl group Chemical group N1CC(C1)* 0.000 description 1
- 150000001555 benzenes Chemical class 0.000 description 1
- 125000004603 benzisoxazolyl group Chemical group O1N=C(C2=C1C=CC=C2)* 0.000 description 1
- 235000019445 benzyl alcohol Nutrition 0.000 description 1
- AGEZXYOZHKGVCM-UHFFFAOYSA-N benzyl bromide Chemical compound BrCC1=CC=CC=C1 AGEZXYOZHKGVCM-UHFFFAOYSA-N 0.000 description 1
- KGNDCEVUMONOKF-UGPLYTSKSA-N benzyl n-[(2r)-1-[(2s,4r)-2-[[(2s)-6-amino-1-(1,3-benzoxazol-2-yl)-1,1-dihydroxyhexan-2-yl]carbamoyl]-4-[(4-methylphenyl)methoxy]pyrrolidin-1-yl]-1-oxo-4-phenylbutan-2-yl]carbamate Chemical compound C1=CC(C)=CC=C1CO[C@H]1CN(C(=O)[C@@H](CCC=2C=CC=CC=2)NC(=O)OCC=2C=CC=CC=2)[C@H](C(=O)N[C@@H](CCCCN)C(O)(O)C=2OC3=CC=CC=C3N=2)C1 KGNDCEVUMONOKF-UGPLYTSKSA-N 0.000 description 1
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 1
- 229960000397 bevacizumab Drugs 0.000 description 1
- 229960002938 bexarotene Drugs 0.000 description 1
- 125000002618 bicyclic heterocycle group Chemical group 0.000 description 1
- SIPUZPBQZHNSDW-UHFFFAOYSA-N bis(2-methylpropyl)aluminum Chemical compound CC(C)C[Al]CC(C)C SIPUZPBQZHNSDW-UHFFFAOYSA-N 0.000 description 1
- IPWKHHSGDUIRAH-UHFFFAOYSA-N bis(pinacolato)diboron Chemical compound O1C(C)(C)C(C)(C)OB1B1OC(C)(C)C(C)(C)O1 IPWKHHSGDUIRAH-UHFFFAOYSA-N 0.000 description 1
- 229960001561 bleomycin Drugs 0.000 description 1
- OYVAGSVQBOHSSS-UAPAGMARSA-O bleomycin A2 Chemical compound N([C@H](C(=O)N[C@H](C)[C@@H](O)[C@H](C)C(=O)N[C@@H]([C@H](O)C)C(=O)NCCC=1SC=C(N=1)C=1SC=C(N=1)C(=O)NCCC[S+](C)C)[C@@H](O[C@H]1[C@H]([C@@H](O)[C@H](O)[C@H](CO)O1)O[C@@H]1[C@H]([C@@H](OC(N)=O)[C@H](O)[C@@H](CO)O1)O)C=1N=CNC=1)C(=O)C1=NC([C@H](CC(N)=O)NC[C@H](N)C(N)=O)=NC(N)=C1C OYVAGSVQBOHSSS-UAPAGMARSA-O 0.000 description 1
- 238000009835 boiling Methods 0.000 description 1
- 238000010322 bone marrow transplantation Methods 0.000 description 1
- ZADPBFCGQRWHPN-UHFFFAOYSA-N boronic acid Chemical compound OBO ZADPBFCGQRWHPN-UHFFFAOYSA-N 0.000 description 1
- GXJABQQUPOEUTA-RDJZCZTQSA-N bortezomib Chemical compound C([C@@H](C(=O)N[C@@H](CC(C)C)B(O)O)NC(=O)C=1N=CC=NC=1)C1=CC=CC=C1 GXJABQQUPOEUTA-RDJZCZTQSA-N 0.000 description 1
- 229960001467 bortezomib Drugs 0.000 description 1
- 210000000133 brain stem Anatomy 0.000 description 1
- 125000001246 bromo group Chemical group Br* 0.000 description 1
- KVNRLNFWIYMESJ-UHFFFAOYSA-N butyronitrile Chemical compound CCCC#N KVNRLNFWIYMESJ-UHFFFAOYSA-N 0.000 description 1
- 210000004899 c-terminal region Anatomy 0.000 description 1
- 239000001506 calcium phosphate Substances 0.000 description 1
- 229910000389 calcium phosphate Inorganic materials 0.000 description 1
- 229960001714 calcium phosphate Drugs 0.000 description 1
- 235000011010 calcium phosphates Nutrition 0.000 description 1
- 239000000378 calcium silicate Substances 0.000 description 1
- 229910052918 calcium silicate Inorganic materials 0.000 description 1
- 229960003340 calcium silicate Drugs 0.000 description 1
- 235000012241 calcium silicate Nutrition 0.000 description 1
- OYACROKNLOSFPA-UHFFFAOYSA-N calcium;dioxido(oxo)silane Chemical compound [Ca+2].[O-][Si]([O-])=O OYACROKNLOSFPA-UHFFFAOYSA-N 0.000 description 1
- 238000009566 cancer vaccine Methods 0.000 description 1
- 229940022399 cancer vaccine Drugs 0.000 description 1
- 229960004117 capecitabine Drugs 0.000 description 1
- 125000003917 carbamoyl group Chemical group [H]N([H])C(*)=O 0.000 description 1
- 150000001720 carbohydrates Chemical class 0.000 description 1
- 235000014633 carbohydrates Nutrition 0.000 description 1
- 229910021386 carbon form Inorganic materials 0.000 description 1
- 229960004562 carboplatin Drugs 0.000 description 1
- 150000001735 carboxylic acids Chemical class 0.000 description 1
- 229960005243 carmustine Drugs 0.000 description 1
- 239000000969 carrier Substances 0.000 description 1
- 230000010261 cell growth Effects 0.000 description 1
- 230000004663 cell proliferation Effects 0.000 description 1
- 235000010980 cellulose Nutrition 0.000 description 1
- 229920002678 cellulose Polymers 0.000 description 1
- 239000001913 cellulose Substances 0.000 description 1
- 229920002301 cellulose acetate Polymers 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- 229960005395 cetuximab Drugs 0.000 description 1
- 229960000541 cetyl alcohol Drugs 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 239000003610 charcoal Substances 0.000 description 1
- 238000002512 chemotherapy Methods 0.000 description 1
- 229960004630 chlorambucil Drugs 0.000 description 1
- JCKYGMPEJWAADB-UHFFFAOYSA-N chlorambucil Chemical compound OC(=O)CCCC1=CC=C(N(CCCl)CCCl)C=C1 JCKYGMPEJWAADB-UHFFFAOYSA-N 0.000 description 1
- 125000001309 chloro group Chemical group Cl* 0.000 description 1
- 238000004587 chromatography analysis Methods 0.000 description 1
- 229960004316 cisplatin Drugs 0.000 description 1
- DQLATGHUWYMOKM-UHFFFAOYSA-L cisplatin Chemical compound N[Pt](N)(Cl)Cl DQLATGHUWYMOKM-UHFFFAOYSA-L 0.000 description 1
- 229960002436 cladribine Drugs 0.000 description 1
- 238000003776 cleavage reaction Methods 0.000 description 1
- WDDPHFBMKLOVOX-AYQXTPAHSA-N clofarabine Chemical compound C1=NC=2C(N)=NC(Cl)=NC=2N1[C@@H]1O[C@H](CO)[C@@H](O)[C@@H]1F WDDPHFBMKLOVOX-AYQXTPAHSA-N 0.000 description 1
- 229960000928 clofarabine Drugs 0.000 description 1
- 238000000576 coating method Methods 0.000 description 1
- 239000003240 coconut oil Substances 0.000 description 1
- 235000019864 coconut oil Nutrition 0.000 description 1
- 238000002648 combination therapy Methods 0.000 description 1
- 229940125810 compound 20 Drugs 0.000 description 1
- 229940125851 compound 27 Drugs 0.000 description 1
- 229940125898 compound 5 Drugs 0.000 description 1
- 239000000470 constituent Substances 0.000 description 1
- 239000000356 contaminant Substances 0.000 description 1
- 239000012050 conventional carrier Substances 0.000 description 1
- 239000012059 conventional drug carrier Substances 0.000 description 1
- 229940028617 conventional vaccine Drugs 0.000 description 1
- LSXDOTMGLUJQCM-UHFFFAOYSA-M copper(i) iodide Chemical compound I[Cu] LSXDOTMGLUJQCM-UHFFFAOYSA-M 0.000 description 1
- 235000012343 cottonseed oil Nutrition 0.000 description 1
- 239000002385 cottonseed oil Substances 0.000 description 1
- 125000006165 cyclic alkyl group Chemical group 0.000 description 1
- 150000001923 cyclic compounds Chemical class 0.000 description 1
- 125000002188 cycloheptatrienyl group Chemical group C1(=CC=CC=CC1)* 0.000 description 1
- 125000003678 cyclohexadienyl group Chemical group C1(=CC=CCC1)* 0.000 description 1
- SSJXIUAHEKJCMH-UHFFFAOYSA-N cyclohexane-1,2-diamine Chemical compound NC1CCCCC1N SSJXIUAHEKJCMH-UHFFFAOYSA-N 0.000 description 1
- 125000000640 cyclooctyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C([H])([H])C1([H])[H] 0.000 description 1
- 125000002433 cyclopentenyl group Chemical group C1(=CCCC1)* 0.000 description 1
- 229960004397 cyclophosphamide Drugs 0.000 description 1
- 229960000684 cytarabine Drugs 0.000 description 1
- 230000016396 cytokine production Effects 0.000 description 1
- KWGRBVOPPLSCSI-UHFFFAOYSA-N d-ephedrine Natural products CNC(C)C(O)C1=CC=CC=C1 KWGRBVOPPLSCSI-UHFFFAOYSA-N 0.000 description 1
- 229960003901 dacarbazine Drugs 0.000 description 1
- 229960000640 dactinomycin Drugs 0.000 description 1
- 229940018872 dalteparin sodium Drugs 0.000 description 1
- 230000006378 damage Effects 0.000 description 1
- 229960002448 dasatinib Drugs 0.000 description 1
- STQGQHZAVUOBTE-VGBVRHCVSA-N daunorubicin Chemical compound O([C@H]1C[C@@](O)(CC=2C(O)=C3C(=O)C=4C=CC=C(C=4C(=O)C3=C(O)C=21)OC)C(C)=O)[C@H]1C[C@H](N)[C@H](O)[C@H](C)O1 STQGQHZAVUOBTE-VGBVRHCVSA-N 0.000 description 1
- 229960000975 daunorubicin Drugs 0.000 description 1
- 229960003603 decitabine Drugs 0.000 description 1
- 230000002950 deficient Effects 0.000 description 1
- 230000003111 delayed effect Effects 0.000 description 1
- 108010017271 denileukin diftitox Proteins 0.000 description 1
- 229960002923 denileukin diftitox Drugs 0.000 description 1
- 238000001514 detection method Methods 0.000 description 1
- 150000001975 deuterium Chemical group 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 229960000605 dexrazoxane Drugs 0.000 description 1
- 239000008121 dextrose Substances 0.000 description 1
- ZJULYDCRWUEPTK-UHFFFAOYSA-N dichloromethyl Chemical compound Cl[CH]Cl ZJULYDCRWUEPTK-UHFFFAOYSA-N 0.000 description 1
- YNHIGQDRGKUECZ-UHFFFAOYSA-N dichloropalladium;triphenylphosphanium Chemical compound Cl[Pd]Cl.C1=CC=CC=C1[PH+](C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1[PH+](C=1C=CC=CC=1)C1=CC=CC=C1 YNHIGQDRGKUECZ-UHFFFAOYSA-N 0.000 description 1
- 238000005906 dihydroxylation reaction Methods 0.000 description 1
- 239000003085 diluting agent Substances 0.000 description 1
- NYDXNILOWQXUOF-UHFFFAOYSA-L disodium;2-[[4-[2-(2-amino-4-oxo-1,7-dihydropyrrolo[2,3-d]pyrimidin-5-yl)ethyl]benzoyl]amino]pentanedioate Chemical compound [Na+].[Na+].C=1NC=2NC(N)=NC(=O)C=2C=1CCC1=CC=C(C(=O)NC(CCC([O-])=O)C([O-])=O)C=C1 NYDXNILOWQXUOF-UHFFFAOYSA-L 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- DLNKOYKMWOXYQA-UHFFFAOYSA-N dl-pseudophenylpropanolamine Natural products CC(N)C(O)C1=CC=CC=C1 DLNKOYKMWOXYQA-UHFFFAOYSA-N 0.000 description 1
- 229960003668 docetaxel Drugs 0.000 description 1
- 229960004679 doxorubicin Drugs 0.000 description 1
- NOTIQUSPUUHHEH-UXOVVSIBSA-N dromostanolone propionate Chemical compound C([C@@H]1CC2)C(=O)[C@H](C)C[C@]1(C)[C@@H]1[C@@H]2[C@@H]2CC[C@H](OC(=O)CC)[C@@]2(C)CC1 NOTIQUSPUUHHEH-UXOVVSIBSA-N 0.000 description 1
- 239000006196 drop Substances 0.000 description 1
- 229950004683 drostanolone propionate Drugs 0.000 description 1
- 238000007908 dry granulation Methods 0.000 description 1
- 210000001198 duodenum Anatomy 0.000 description 1
- 229960002224 eculizumab Drugs 0.000 description 1
- 239000008157 edible vegetable oil Substances 0.000 description 1
- 239000012039 electrophile Substances 0.000 description 1
- 238000010828 elution Methods 0.000 description 1
- 239000012156 elution solvent Substances 0.000 description 1
- 239000003995 emulsifying agent Substances 0.000 description 1
- 230000001804 emulsifying effect Effects 0.000 description 1
- 239000000839 emulsion Substances 0.000 description 1
- 239000002158 endotoxin Substances 0.000 description 1
- 239000002702 enteric coating Substances 0.000 description 1
- 230000002255 enzymatic effect Effects 0.000 description 1
- 229950006370 epacadostat Drugs 0.000 description 1
- 229960002179 ephedrine Drugs 0.000 description 1
- 102000052116 epidermal growth factor receptor activity proteins Human genes 0.000 description 1
- 108700015053 epidermal growth factor receptor activity proteins Proteins 0.000 description 1
- 229960001904 epirubicin Drugs 0.000 description 1
- AAKJLRGGTJKAMG-UHFFFAOYSA-N erlotinib Chemical compound C=12C=C(OCCOC)C(OCCOC)=CC2=NC=NC=1NC1=CC=CC(C#C)=C1 AAKJLRGGTJKAMG-UHFFFAOYSA-N 0.000 description 1
- 229960001433 erlotinib Drugs 0.000 description 1
- 229960001842 estramustine Drugs 0.000 description 1
- FRPJXPJMRWBBIH-RBRWEJTLSA-N estramustine Chemical compound ClCCN(CCCl)C(=O)OC1=CC=C2[C@H]3CC[C@](C)([C@H](CC4)O)[C@@H]4[C@@H]3CCC2=C1 FRPJXPJMRWBBIH-RBRWEJTLSA-N 0.000 description 1
- YFXCNIVBAVFOBX-UHFFFAOYSA-N ethenylboronic acid Chemical compound OB(O)C=C YFXCNIVBAVFOBX-UHFFFAOYSA-N 0.000 description 1
- 125000000816 ethylene group Chemical group [H]C([H])([*:1])C([H])([H])[*:2] 0.000 description 1
- 125000002534 ethynyl group Chemical group [H]C#C* 0.000 description 1
- VJJPUSNTGOMMGY-MRVIYFEKSA-N etoposide Chemical compound COC1=C(O)C(OC)=CC([C@@H]2C3=CC=4OCOC=4C=C3[C@@H](O[C@H]3[C@@H]([C@@H](O)[C@@H]4O[C@H](C)OC[C@H]4O3)O)[C@@H]3[C@@H]2C(OC3)=O)=C1 VJJPUSNTGOMMGY-MRVIYFEKSA-N 0.000 description 1
- 229960005420 etoposide Drugs 0.000 description 1
- LIQODXNTTZAGID-OCBXBXKTSA-N etoposide phosphate Chemical compound COC1=C(OP(O)(O)=O)C(OC)=CC([C@@H]2C3=CC=4OCOC=4C=C3[C@@H](O[C@H]3[C@@H]([C@@H](O)[C@@H]4O[C@H](C)OC[C@H]4O3)O)[C@@H]3[C@@H]2C(OC3)=O)=C1 LIQODXNTTZAGID-OCBXBXKTSA-N 0.000 description 1
- 229960000752 etoposide phosphate Drugs 0.000 description 1
- OGPBJKLSAFTDLK-UHFFFAOYSA-N europium atom Chemical compound [Eu] OGPBJKLSAFTDLK-UHFFFAOYSA-N 0.000 description 1
- GWQVMPWSEVRGPY-UHFFFAOYSA-N europium cryptate Chemical compound [Eu+3].N=1C2=CC=CC=1CN(CC=1N=C(C=CC=1)C=1N=C(C3)C=CC=1)CC(N=1)=CC(C(=O)NCCN)=CC=1C(N=1)=CC(C(=O)NCCN)=CC=1CN3CC1=CC=CC2=N1 GWQVMPWSEVRGPY-UHFFFAOYSA-N 0.000 description 1
- 229960000255 exemestane Drugs 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 238000000605 extraction Methods 0.000 description 1
- IVLVTNPOHDFFCJ-UHFFFAOYSA-N fentanyl citrate Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O.C=1C=CC=CC=1N(C(=O)CC)C(CC1)CCN1CCC1=CC=CC=C1 IVLVTNPOHDFFCJ-UHFFFAOYSA-N 0.000 description 1
- 229960004207 fentanyl citrate Drugs 0.000 description 1
- 102000052178 fibroblast growth factor receptor activity proteins Human genes 0.000 description 1
- 229960004177 filgrastim Drugs 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 235000020375 flavoured syrup Nutrition 0.000 description 1
- 229960000961 floxuridine Drugs 0.000 description 1
- ODKNJVUHOIMIIZ-RRKCRQDMSA-N floxuridine Chemical compound C1[C@H](O)[C@@H](CO)O[C@H]1N1C(=O)NC(=O)C(F)=C1 ODKNJVUHOIMIIZ-RRKCRQDMSA-N 0.000 description 1
- 229960000390 fludarabine Drugs 0.000 description 1
- GIUYCYHIANZCFB-FJFJXFQQSA-N fludarabine phosphate Chemical compound C1=NC=2C(N)=NC(F)=NC=2N1[C@@H]1O[C@H](COP(O)(O)=O)[C@@H](O)[C@@H]1O GIUYCYHIANZCFB-FJFJXFQQSA-N 0.000 description 1
- 125000003709 fluoroalkyl group Chemical group 0.000 description 1
- 229960002949 fluorouracil Drugs 0.000 description 1
- VVIAGPKUTFNRDU-ABLWVSNPSA-N folinic acid Chemical compound C1NC=2NC(N)=NC(=O)C=2N(C=O)C1CNC1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)C=C1 VVIAGPKUTFNRDU-ABLWVSNPSA-N 0.000 description 1
- 235000008191 folinic acid Nutrition 0.000 description 1
- 239000011672 folinic acid Substances 0.000 description 1
- 230000003325 follicular Effects 0.000 description 1
- 235000013305 food Nutrition 0.000 description 1
- 235000003599 food sweetener Nutrition 0.000 description 1
- 238000001640 fractional crystallisation Methods 0.000 description 1
- 239000012458 free base Substances 0.000 description 1
- 238000007710 freezing Methods 0.000 description 1
- 230000008014 freezing Effects 0.000 description 1
- YRTCKZIKGWZNCU-UHFFFAOYSA-N furo[3,2-b]pyridine Chemical compound C1=CC=C2OC=CC2=N1 YRTCKZIKGWZNCU-UHFFFAOYSA-N 0.000 description 1
- 229960002584 gefitinib Drugs 0.000 description 1
- XGALLCVXEZPNRQ-UHFFFAOYSA-N gefitinib Chemical compound C=12C=C(OCCCN3CCOCC3)C(OC)=CC2=NC=NC=1NC1=CC=C(F)C(Cl)=C1 XGALLCVXEZPNRQ-UHFFFAOYSA-N 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 229940014259 gelatin Drugs 0.000 description 1
- 239000007903 gelatin capsule Substances 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- 229960005277 gemcitabine Drugs 0.000 description 1
- SDUQYLNIPVEERB-QPPQHZFASA-N gemcitabine Chemical compound O=C1N=C(N)C=CN1[C@H]1C(F)(F)[C@H](O)[C@@H](CO)O1 SDUQYLNIPVEERB-QPPQHZFASA-N 0.000 description 1
- 229960003297 gemtuzumab ozogamicin Drugs 0.000 description 1
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 1
- 229960003690 goserelin acetate Drugs 0.000 description 1
- JAXFJECJQZDFJS-XHEPKHHKSA-N gtpl8555 Chemical compound OC(=O)C[C@H](N)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](C(C)C)C(=O)N1CCC[C@@H]1C(=O)N[C@H](B1O[C@@]2(C)[C@H]3C[C@H](C3(C)C)C[C@H]2O1)CCC1=CC=C(F)C=C1 JAXFJECJQZDFJS-XHEPKHHKSA-N 0.000 description 1
- 230000003394 haemopoietic effect Effects 0.000 description 1
- 150000004820 halides Chemical class 0.000 description 1
- 201000010536 head and neck cancer Diseases 0.000 description 1
- 208000014829 head and neck neoplasm Diseases 0.000 description 1
- 230000002489 hematologic effect Effects 0.000 description 1
- DMEGYFMYUHOHGS-UHFFFAOYSA-N heptamethylene Natural products C1CCCCCC1 DMEGYFMYUHOHGS-UHFFFAOYSA-N 0.000 description 1
- 229940022353 herceptin Drugs 0.000 description 1
- UUVWYPNAQBNQJQ-UHFFFAOYSA-N hexamethylmelamine Chemical compound CN(C)C1=NC(N(C)C)=NC(N(C)C)=N1 UUVWYPNAQBNQJQ-UHFFFAOYSA-N 0.000 description 1
- BKEMVGVBBDMHKL-VYFXDUNUSA-N histrelin acetate Chemical compound CC(O)=O.CC(O)=O.CCNC(=O)[C@@H]1CCCN1C(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC=1N=CNC=1)NC(=O)[C@H]1NC(=O)CC1)CC(N=C1)=CN1CC1=CC=CC=C1 BKEMVGVBBDMHKL-VYFXDUNUSA-N 0.000 description 1
- 229960003911 histrelin acetate Drugs 0.000 description 1
- 239000008240 homogeneous mixture Substances 0.000 description 1
- 229940088597 hormone Drugs 0.000 description 1
- 239000005556 hormone Substances 0.000 description 1
- 102000048776 human CD274 Human genes 0.000 description 1
- 102000048362 human PDCD1 Human genes 0.000 description 1
- 229930195733 hydrocarbon Natural products 0.000 description 1
- 239000012051 hydrophobic carrier Substances 0.000 description 1
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 1
- 235000019447 hydroxyethyl cellulose Nutrition 0.000 description 1
- 229960001001 ibritumomab tiuxetan Drugs 0.000 description 1
- 229960000908 idarubicin Drugs 0.000 description 1
- 229940121569 ieramilimab Drugs 0.000 description 1
- 229960001101 ifosfamide Drugs 0.000 description 1
- HOMGKSMUEGBAAB-UHFFFAOYSA-N ifosfamide Chemical compound ClCCNP1(=O)OCCCN1CCCl HOMGKSMUEGBAAB-UHFFFAOYSA-N 0.000 description 1
- 238000003384 imaging method Methods 0.000 description 1
- 229960003685 imatinib mesylate Drugs 0.000 description 1
- YLMAHDNUQAMNNX-UHFFFAOYSA-N imatinib methanesulfonate Chemical compound CS(O)(=O)=O.C1CN(C)CCN1CC1=CC=C(C(=O)NC=2C=C(NC=3N=C(C=CN=3)C=3C=NC=CC=3)C(C)=CC=2)C=C1 YLMAHDNUQAMNNX-UHFFFAOYSA-N 0.000 description 1
- 230000002519 immonomodulatory effect Effects 0.000 description 1
- 210000002865 immune cell Anatomy 0.000 description 1
- 238000002649 immunization Methods 0.000 description 1
- 230000003053 immunization Effects 0.000 description 1
- 230000002163 immunogen Effects 0.000 description 1
- 102000018358 immunoglobulin Human genes 0.000 description 1
- 230000003308 immunostimulating effect Effects 0.000 description 1
- 239000003018 immunosuppressive agent Substances 0.000 description 1
- 229940125721 immunosuppressive agent Drugs 0.000 description 1
- 238000000099 in vitro assay Methods 0.000 description 1
- 238000001727 in vivo Methods 0.000 description 1
- 238000005462 in vivo assay Methods 0.000 description 1
- 238000011534 incubation Methods 0.000 description 1
- 125000003392 indanyl group Chemical group C1(CCC2=CC=CC=C12)* 0.000 description 1
- 125000003454 indenyl group Chemical group C1(C=CC2=CC=CC=C12)* 0.000 description 1
- 239000011261 inert gas Substances 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 208000014674 injury Diseases 0.000 description 1
- 229910052500 inorganic mineral Inorganic materials 0.000 description 1
- 229940079322 interferon Drugs 0.000 description 1
- 229960003521 interferon alfa-2a Drugs 0.000 description 1
- 108010093036 interleukin receptors Proteins 0.000 description 1
- 102000002467 interleukin receptors Human genes 0.000 description 1
- 238000001361 intraarterial administration Methods 0.000 description 1
- 238000000185 intracerebroventricular administration Methods 0.000 description 1
- 238000007917 intracranial administration Methods 0.000 description 1
- 238000003402 intramolecular cyclocondensation reaction Methods 0.000 description 1
- 238000010255 intramuscular injection Methods 0.000 description 1
- 239000007927 intramuscular injection Substances 0.000 description 1
- 238000007912 intraperitoneal administration Methods 0.000 description 1
- 239000007928 intraperitoneal injection Substances 0.000 description 1
- 238000007913 intrathecal administration Methods 0.000 description 1
- 238000001990 intravenous administration Methods 0.000 description 1
- 125000002346 iodo group Chemical group I* 0.000 description 1
- INQOMBQAUSQDDS-UHFFFAOYSA-N iodomethane Chemical group IC INQOMBQAUSQDDS-UHFFFAOYSA-N 0.000 description 1
- UWKQSNNFCGGAFS-XIFFEERXSA-N irinotecan Chemical compound C1=C2C(CC)=C3CN(C(C4=C([C@@](C(=O)OC4)(O)CC)C=4)=O)C=4C3=NC2=CC=C1OC(=O)N(CC1)CCC1N1CCCCC1 UWKQSNNFCGGAFS-XIFFEERXSA-N 0.000 description 1
- 229960004768 irinotecan Drugs 0.000 description 1
- 230000007794 irritation Effects 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- 125000000555 isopropenyl group Chemical group [H]\C([H])=C(\*)C([H])([H])[H] 0.000 description 1
- 125000003253 isopropoxy group Chemical group [H]C([H])([H])C([H])(O*)C([H])([H])[H] 0.000 description 1
- 239000004310 lactic acid Substances 0.000 description 1
- 235000014655 lactic acid Nutrition 0.000 description 1
- 229960001375 lactose Drugs 0.000 description 1
- 239000008101 lactose Substances 0.000 description 1
- 229960004891 lapatinib Drugs 0.000 description 1
- 229960004942 lenalidomide Drugs 0.000 description 1
- GOTYRUGSSMKFNF-UHFFFAOYSA-N lenalidomide Chemical compound C1C=2C(N)=CC=CC=2C(=O)N1C1CCC(=O)NC1=O GOTYRUGSSMKFNF-UHFFFAOYSA-N 0.000 description 1
- HPJKCIUCZWXJDR-UHFFFAOYSA-N letrozole Chemical compound C1=CC(C#N)=CC=C1C(N1N=CN=C1)C1=CC=C(C#N)C=C1 HPJKCIUCZWXJDR-UHFFFAOYSA-N 0.000 description 1
- 229960003881 letrozole Drugs 0.000 description 1
- 229960001691 leucovorin Drugs 0.000 description 1
- GFIJNRVAKGFPGQ-LIJARHBVSA-N leuprolide Chemical compound CCNC(=O)[C@@H]1CCCN1C(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](CC(C)C)NC(=O)[C@@H](NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC=1N=CNC=1)NC(=O)[C@H]1NC(=O)CC1)CC1=CC=C(O)C=C1 GFIJNRVAKGFPGQ-LIJARHBVSA-N 0.000 description 1
- 229960004338 leuprorelin Drugs 0.000 description 1
- 229960001614 levamisole Drugs 0.000 description 1
- 150000007517 lewis acids Chemical class 0.000 description 1
- 229920006008 lipopolysaccharide Polymers 0.000 description 1
- 229940057995 liquid paraffin Drugs 0.000 description 1
- YQNQTEBHHUSESQ-UHFFFAOYSA-N lithium aluminate Chemical compound [Li+].[O-][Al]=O YQNQTEBHHUSESQ-UHFFFAOYSA-N 0.000 description 1
- 229960002247 lomustine Drugs 0.000 description 1
- 239000006210 lotion Substances 0.000 description 1
- 239000007937 lozenge Substances 0.000 description 1
- 239000000314 lubricant Substances 0.000 description 1
- 206010025135 lupus erythematosus Diseases 0.000 description 1
- 239000012931 lyophilized formulation Substances 0.000 description 1
- 201000004792 malaria Diseases 0.000 description 1
- 239000001630 malic acid Substances 0.000 description 1
- 235000011090 malic acid Nutrition 0.000 description 1
- 230000036210 malignancy Effects 0.000 description 1
- 229960002510 mandelic acid Drugs 0.000 description 1
- 239000000594 mannitol Substances 0.000 description 1
- 235000010355 mannitol Nutrition 0.000 description 1
- 238000004949 mass spectrometry Methods 0.000 description 1
- HAWPXGHAZFHHAD-UHFFFAOYSA-N mechlorethamine Chemical compound ClCCN(C)CCCl HAWPXGHAZFHHAD-UHFFFAOYSA-N 0.000 description 1
- 229960004961 mechlorethamine Drugs 0.000 description 1
- 239000002609 medium Substances 0.000 description 1
- 229960004296 megestrol acetate Drugs 0.000 description 1
- RQZAXGRLVPAYTJ-GQFGMJRRSA-N megestrol acetate Chemical compound C1=C(C)C2=CC(=O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@@](C(C)=O)(OC(=O)C)[C@@]1(C)CC2 RQZAXGRLVPAYTJ-GQFGMJRRSA-N 0.000 description 1
- SGDBTWWWUNNDEQ-LBPRGKRZSA-N melphalan Chemical compound OC(=O)[C@@H](N)CC1=CC=C(N(CCCl)CCCl)C=C1 SGDBTWWWUNNDEQ-LBPRGKRZSA-N 0.000 description 1
- 229960001924 melphalan Drugs 0.000 description 1
- 229960000901 mepacrine Drugs 0.000 description 1
- GLVAUDGFNGKCSF-UHFFFAOYSA-N mercaptopurine Chemical compound S=C1NC=NC2=C1NC=N2 GLVAUDGFNGKCSF-UHFFFAOYSA-N 0.000 description 1
- 229960001428 mercaptopurine Drugs 0.000 description 1
- 230000004060 metabolic process Effects 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- 229960000485 methotrexate Drugs 0.000 description 1
- 229960004469 methoxsalen Drugs 0.000 description 1
- YIFVTNKWHMPOLC-LBPRGKRZSA-N methyl (2S)-1-[(2-chloro-1,3-benzothiazol-5-yl)methyl]piperidine-2-carboxylate Chemical compound ClC=1SC2=C(N=1)C=C(C=C2)CN1[C@@H](CCCC1)C(=O)OC YIFVTNKWHMPOLC-LBPRGKRZSA-N 0.000 description 1
- APCHKWZTSCBBJX-RGMNGODLSA-N methyl (2s)-piperidine-2-carboxylate;hydrochloride Chemical compound [Cl-].COC(=O)[C@@H]1CCCC[NH2+]1 APCHKWZTSCBBJX-RGMNGODLSA-N 0.000 description 1
- JGJDORZNOSWWDS-UHFFFAOYSA-N methyl 1,3-oxazole-5-carboxylate Chemical compound COC(=O)C1=CN=CO1 JGJDORZNOSWWDS-UHFFFAOYSA-N 0.000 description 1
- RTNOQYZDKMGQGE-UHFFFAOYSA-N methyl 2,4-dihydroxy-5-nitrobenzoate Chemical compound COC(=O)C1=CC([N+]([O-])=O)=C(O)C=C1O RTNOQYZDKMGQGE-UHFFFAOYSA-N 0.000 description 1
- LSLBCILBADRAGX-UHFFFAOYSA-N methyl 2-(2-methyl-3-phenylphenyl)furo[2,3-b]pyridine-5-carboxylate Chemical compound CC1=C(C=CC=C1C1=CC=2C(=NC=C(C=2)C(=O)OC)O1)C1=CC=CC=C1 LSLBCILBADRAGX-UHFFFAOYSA-N 0.000 description 1
- KKMVACLRBBJYIJ-UHFFFAOYSA-N methyl 5-bromo-6-oxo-1h-pyridine-3-carboxylate Chemical compound COC(=O)C1=CNC(=O)C(Br)=C1 KKMVACLRBBJYIJ-UHFFFAOYSA-N 0.000 description 1
- BRLAPVHKRHAGFJ-UHFFFAOYSA-N methyl 6-(2-methyl-3-phenylphenyl)furo[2,3-b]pyrazine-2-carboxylate Chemical compound CC1=C(C=CC=C1C1=CC=2C(=NC=C(N=2)C(=O)OC)O1)C1=CC=CC=C1 BRLAPVHKRHAGFJ-UHFFFAOYSA-N 0.000 description 1
- GAVHSGPZDJCNDR-UHFFFAOYSA-N methyl 6-bromo-5-hydroxypyridine-2-carboxylate Chemical compound COC(=O)C1=CC=C(O)C(Br)=N1 GAVHSGPZDJCNDR-UHFFFAOYSA-N 0.000 description 1
- ALZAWRNDQCCYPC-UHFFFAOYSA-N methyl 6-hydroxy-7-methyl-2-(2-methyl-3-phenylphenyl)-1,3-benzoxazole-5-carboxylate Chemical compound OC1=C(C2=C(N=C(O2)C=2C(=C(C=CC=2)C2=CC=CC=C2)C)C=C1C(=O)OC)C ALZAWRNDQCCYPC-UHFFFAOYSA-N 0.000 description 1
- VNFXNPFSTYYFCZ-UHFFFAOYSA-N methyl 6-oxo-1h-pyrazine-3-carboxylate Chemical compound COC(=O)C1=CN=C(O)C=N1 VNFXNPFSTYYFCZ-UHFFFAOYSA-N 0.000 description 1
- VEQPFRRUDYTHJR-UHFFFAOYSA-N methyl 7-methyl-2-(2-methyl-3-phenylphenyl)furo[2,3-c]pyridine-5-carboxylate Chemical compound CC=1N=C(C=C2C=1OC(=C2)C=1C(=C(C=CC=1)C1=CC=CC=C1)C)C(=O)OC VEQPFRRUDYTHJR-UHFFFAOYSA-N 0.000 description 1
- 229940095102 methyl benzoate Drugs 0.000 description 1
- 229920000609 methyl cellulose Polymers 0.000 description 1
- XORMSHHWDYAUEF-UHFFFAOYSA-N methyl furo[2,3-c]pyridine-5-carboxylate Chemical compound C1=NC(C(=O)OC)=CC2=C1OC=C2 XORMSHHWDYAUEF-UHFFFAOYSA-N 0.000 description 1
- 239000001923 methylcellulose Substances 0.000 description 1
- 125000001570 methylene group Chemical group [H]C([H])([*:1])[*:2] 0.000 description 1
- 238000012737 microarray-based gene expression Methods 0.000 description 1
- 235000010755 mineral Nutrition 0.000 description 1
- 239000011707 mineral Substances 0.000 description 1
- CFCUWKMKBJTWLW-BKHRDMLASA-N mithramycin Chemical compound O([C@@H]1C[C@@H](O[C@H](C)[C@H]1O)OC=1C=C2C=C3C[C@H]([C@@H](C(=O)C3=C(O)C2=C(O)C=1C)O[C@@H]1O[C@H](C)[C@@H](O)[C@H](O[C@@H]2O[C@H](C)[C@H](O)[C@H](O[C@@H]3O[C@H](C)[C@@H](O)[C@@](C)(O)C3)C2)C1)[C@H](OC)C(=O)[C@@H](O)[C@@H](C)O)[C@H]1C[C@@H](O)[C@H](O)[C@@H](C)O1 CFCUWKMKBJTWLW-BKHRDMLASA-N 0.000 description 1
- 229960004857 mitomycin Drugs 0.000 description 1
- 229960000350 mitotane Drugs 0.000 description 1
- KKZJGLLVHKMTCM-UHFFFAOYSA-N mitoxantrone Chemical compound O=C1C2=C(O)C=CC(O)=C2C(=O)C2=C1C(NCCNCCO)=CC=C2NCCNCCO KKZJGLLVHKMTCM-UHFFFAOYSA-N 0.000 description 1
- 229960001156 mitoxantrone Drugs 0.000 description 1
- 239000011259 mixed solution Substances 0.000 description 1
- 239000012046 mixed solvent Substances 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 238000012544 monitoring process Methods 0.000 description 1
- 229910000403 monosodium phosphate Inorganic materials 0.000 description 1
- 235000019799 monosodium phosphate Nutrition 0.000 description 1
- 238000012243 multiplex automated genomic engineering Methods 0.000 description 1
- NALMPLUMOWIVJC-UHFFFAOYSA-N n,n,4-trimethylbenzeneamine oxide Chemical compound CC1=CC=C([N+](C)(C)[O-])C=C1 NALMPLUMOWIVJC-UHFFFAOYSA-N 0.000 description 1
- BLCLNMBMMGCOAS-UHFFFAOYSA-N n-[1-[[1-[[1-[[1-[[1-[[1-[[1-[2-[(carbamoylamino)carbamoyl]pyrrolidin-1-yl]-5-(diaminomethylideneamino)-1-oxopentan-2-yl]amino]-4-methyl-1-oxopentan-2-yl]amino]-3-[(2-methylpropan-2-yl)oxy]-1-oxopropan-2-yl]amino]-3-(4-hydroxyphenyl)-1-oxopropan-2-yl]amin Chemical compound C1CCC(C(=O)NNC(N)=O)N1C(=O)C(CCCN=C(N)N)NC(=O)C(CC(C)C)NC(=O)C(COC(C)(C)C)NC(=O)C(NC(=O)C(CO)NC(=O)C(CC=1C2=CC=CC=C2NC=1)NC(=O)C(CC=1NC=NC=1)NC(=O)C1NC(=O)CC1)CC1=CC=C(O)C=C1 BLCLNMBMMGCOAS-UHFFFAOYSA-N 0.000 description 1
- YOHYSYJDKVYCJI-UHFFFAOYSA-N n-[3-[[6-[3-(trifluoromethyl)anilino]pyrimidin-4-yl]amino]phenyl]cyclopropanecarboxamide Chemical compound FC(F)(F)C1=CC=CC(NC=2N=CN=C(NC=3C=C(NC(=O)C4CC4)C=CC=3)C=2)=C1 YOHYSYJDKVYCJI-UHFFFAOYSA-N 0.000 description 1
- SYSQUGFVNFXIIT-UHFFFAOYSA-N n-[4-(1,3-benzoxazol-2-yl)phenyl]-4-nitrobenzenesulfonamide Chemical class C1=CC([N+](=O)[O-])=CC=C1S(=O)(=O)NC1=CC=C(C=2OC3=CC=CC=C3N=2)C=C1 SYSQUGFVNFXIIT-UHFFFAOYSA-N 0.000 description 1
- 125000004370 n-butenyl group Chemical group [H]\C([H])=C(/[H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- AGVKXDPPPSLISR-UHFFFAOYSA-N n-ethylcyclohexanamine Chemical compound CCNC1CCCCC1 AGVKXDPPPSLISR-UHFFFAOYSA-N 0.000 description 1
- 125000001280 n-hexyl group Chemical group C(CCCCC)* 0.000 description 1
- 229940073569 n-methylephedrine Drugs 0.000 description 1
- 125000000740 n-pentyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000003506 n-propoxy group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])O* 0.000 description 1
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- UBWXUGDQUBIEIZ-QNTYDACNSA-N nandrolone phenpropionate Chemical compound O([C@H]1CC[C@H]2[C@H]3[C@@H]([C@H]4CCC(=O)C=C4CC3)CC[C@@]21C)C(=O)CCC1=CC=CC=C1 UBWXUGDQUBIEIZ-QNTYDACNSA-N 0.000 description 1
- 229960001133 nandrolone phenpropionate Drugs 0.000 description 1
- 210000000581 natural killer T-cell Anatomy 0.000 description 1
- 239000013642 negative control Substances 0.000 description 1
- 210000005036 nerve Anatomy 0.000 description 1
- 229910017604 nitric acid Inorganic materials 0.000 description 1
- 150000002825 nitriles Chemical class 0.000 description 1
- QJGQUHMNIGDVPM-UHFFFAOYSA-N nitrogen group Chemical group [N] QJGQUHMNIGDVPM-UHFFFAOYSA-N 0.000 description 1
- 239000012457 nonaqueous media Substances 0.000 description 1
- 125000002868 norbornyl group Chemical group C12(CCC(CC1)C2)* 0.000 description 1
- 125000005482 norpinyl group Chemical group 0.000 description 1
- JRZJOMJEPLMPRA-UHFFFAOYSA-N olefin Natural products CCCCCCCC=C JRZJOMJEPLMPRA-UHFFFAOYSA-N 0.000 description 1
- 238000011275 oncology therapy Methods 0.000 description 1
- 244000309459 oncolytic virus Species 0.000 description 1
- 238000005457 optimization Methods 0.000 description 1
- 235000005985 organic acids Nutrition 0.000 description 1
- 125000002524 organometallic group Chemical group 0.000 description 1
- 229950006098 orthocaine Drugs 0.000 description 1
- 229940127084 other anti-cancer agent Drugs 0.000 description 1
- DWAFYCQODLXJNR-BNTLRKBRSA-L oxaliplatin Chemical compound O1C(=O)C(=O)O[Pt]11N[C@@H]2CCCC[C@H]2N1 DWAFYCQODLXJNR-BNTLRKBRSA-L 0.000 description 1
- 229960001756 oxaliplatin Drugs 0.000 description 1
- 125000004430 oxygen atom Chemical group O* 0.000 description 1
- 229960001592 paclitaxel Drugs 0.000 description 1
- YJVFFLUZDVXJQI-UHFFFAOYSA-L palladium(ii) acetate Chemical compound [Pd+2].CC([O-])=O.CC([O-])=O YJVFFLUZDVXJQI-UHFFFAOYSA-L 0.000 description 1
- 229940046231 pamidronate Drugs 0.000 description 1
- WRUUGTRCQOWXEG-UHFFFAOYSA-N pamidronate Chemical compound NCCC(O)(P(O)(O)=O)P(O)(O)=O WRUUGTRCQOWXEG-UHFFFAOYSA-N 0.000 description 1
- 229960001972 panitumumab Drugs 0.000 description 1
- 239000000312 peanut oil Substances 0.000 description 1
- HQQSBEDKMRHYME-UHFFFAOYSA-N pefloxacin mesylate Chemical compound [H+].CS([O-])(=O)=O.C1=C2N(CC)C=C(C(O)=O)C(=O)C2=CC(F)=C1N1CCN(C)CC1 HQQSBEDKMRHYME-UHFFFAOYSA-N 0.000 description 1
- 229960001744 pegaspargase Drugs 0.000 description 1
- 108010001564 pegaspargase Proteins 0.000 description 1
- 229960001373 pegfilgrastim Drugs 0.000 description 1
- 108010044644 pegfilgrastim Proteins 0.000 description 1
- 229960003349 pemetrexed disodium Drugs 0.000 description 1
- 125000003538 pentan-3-yl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])C([H])([H])[H] 0.000 description 1
- 229960002340 pentostatin Drugs 0.000 description 1
- FPVKHBSQESCIEP-JQCXWYLXSA-N pentostatin Chemical compound C1[C@H](O)[C@@H](CO)O[C@H]1N1C(N=CNC[C@H]2O)=C2N=C1 FPVKHBSQESCIEP-JQCXWYLXSA-N 0.000 description 1
- 125000005004 perfluoroethyl group Chemical group FC(F)(F)C(F)(F)* 0.000 description 1
- 230000010412 perfusion Effects 0.000 description 1
- 235000019271 petrolatum Nutrition 0.000 description 1
- 239000008177 pharmaceutical agent Substances 0.000 description 1
- 230000000144 pharmacologic effect Effects 0.000 description 1
- DLNKOYKMWOXYQA-APPZFPTMSA-N phenylpropanolamine Chemical compound C[C@@H](N)[C@H](O)C1=CC=CC=C1 DLNKOYKMWOXYQA-APPZFPTMSA-N 0.000 description 1
- 229960000395 phenylpropanolamine Drugs 0.000 description 1
- 229910052698 phosphorus Inorganic materials 0.000 description 1
- 239000011574 phosphorus Substances 0.000 description 1
- 102000020233 phosphotransferase Human genes 0.000 description 1
- 229950010773 pidilizumab Drugs 0.000 description 1
- 229960005235 piperonyl butoxide Drugs 0.000 description 1
- 229960000952 pipobroman Drugs 0.000 description 1
- NJBFOOCLYDNZJN-UHFFFAOYSA-N pipobroman Chemical compound BrCCC(=O)N1CCN(C(=O)CCBr)CC1 NJBFOOCLYDNZJN-UHFFFAOYSA-N 0.000 description 1
- 229960003171 plicamycin Drugs 0.000 description 1
- 229920000136 polysorbate Polymers 0.000 description 1
- 229920002223 polystyrene Polymers 0.000 description 1
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 1
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 1
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 1
- 239000011591 potassium Substances 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- LJCNRYVRMXRIQR-OLXYHTOASA-L potassium sodium L-tartrate Chemical compound [Na+].[K+].[O-]C(=O)[C@H](O)[C@@H](O)C([O-])=O LJCNRYVRMXRIQR-OLXYHTOASA-L 0.000 description 1
- 230000003389 potentiating effect Effects 0.000 description 1
- 239000002244 precipitate Substances 0.000 description 1
- 239000003755 preservative agent Substances 0.000 description 1
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 1
- 208000016800 primary central nervous system lymphoma Diseases 0.000 description 1
- 229960000624 procarbazine Drugs 0.000 description 1
- CPTBDICYNRMXFX-UHFFFAOYSA-N procarbazine Chemical compound CNNCC1=CC=C(C(=O)NC(C)C)C=C1 CPTBDICYNRMXFX-UHFFFAOYSA-N 0.000 description 1
- 230000001737 promoting effect Effects 0.000 description 1
- QELSKZZBTMNZEB-UHFFFAOYSA-N propylparaben Chemical compound CCCOC(=O)C1=CC=C(O)C=C1 QELSKZZBTMNZEB-UHFFFAOYSA-N 0.000 description 1
- 229960003415 propylparaben Drugs 0.000 description 1
- 201000005825 prostate adenocarcinoma Diseases 0.000 description 1
- 230000002685 pulmonary effect Effects 0.000 description 1
- 239000000296 purinergic P1 receptor antagonist Substances 0.000 description 1
- NIPZZXUFJPQHNH-UHFFFAOYSA-M pyrazine-2-carboxylate Chemical compound [O-]C(=O)C1=CN=CC=N1 NIPZZXUFJPQHNH-UHFFFAOYSA-M 0.000 description 1
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 1
- QJZUKDFHGGYHMC-UHFFFAOYSA-N pyridine-3-carbaldehyde Chemical compound O=CC1=CC=CN=C1 QJZUKDFHGGYHMC-UHFFFAOYSA-N 0.000 description 1
- 238000010791 quenching Methods 0.000 description 1
- 230000000171 quenching effect Effects 0.000 description 1
- GPKJTRJOBQGKQK-UHFFFAOYSA-N quinacrine Chemical compound C1=C(OC)C=C2C(NC(C)CCCN(CC)CC)=C(C=CC(Cl)=C3)C3=NC2=C1 GPKJTRJOBQGKQK-UHFFFAOYSA-N 0.000 description 1
- 230000002285 radioactive effect Effects 0.000 description 1
- 238000001959 radiotherapy Methods 0.000 description 1
- 229960000424 rasburicase Drugs 0.000 description 1
- 108010084837 rasburicase Proteins 0.000 description 1
- 239000000376 reactant Substances 0.000 description 1
- 102000005962 receptors Human genes 0.000 description 1
- 108020003175 receptors Proteins 0.000 description 1
- 230000007115 recruitment Effects 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 238000006722 reduction reaction Methods 0.000 description 1
- 238000006268 reductive amination reaction Methods 0.000 description 1
- 208000016691 refractory malignant neoplasm Diseases 0.000 description 1
- 230000000241 respiratory effect Effects 0.000 description 1
- 230000029058 respiratory gaseous exchange Effects 0.000 description 1
- 230000004043 responsiveness Effects 0.000 description 1
- 230000002441 reversible effect Effects 0.000 description 1
- 229960004641 rituximab Drugs 0.000 description 1
- 239000012266 salt solution Substances 0.000 description 1
- 229930195734 saturated hydrocarbon Natural products 0.000 description 1
- 230000007017 scission Effects 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 239000008159 sesame oil Substances 0.000 description 1
- 235000011803 sesame oil Nutrition 0.000 description 1
- 239000004208 shellac Substances 0.000 description 1
- ZLGIYFNHBLSMPS-ATJNOEHPSA-N shellac Chemical compound OCCCCCC(O)C(O)CCCCCCCC(O)=O.C1C23[C@H](C(O)=O)CCC2[C@](C)(CO)[C@@H]1C(C(O)=O)=C[C@@H]3O ZLGIYFNHBLSMPS-ATJNOEHPSA-N 0.000 description 1
- 229940113147 shellac Drugs 0.000 description 1
- 235000013874 shellac Nutrition 0.000 description 1
- 201000002314 small intestine cancer Diseases 0.000 description 1
- 150000003384 small molecules Chemical class 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- BEOOHQFXGBMRKU-UHFFFAOYSA-N sodium cyanoborohydride Chemical compound [Na+].[B-]C#N BEOOHQFXGBMRKU-UHFFFAOYSA-N 0.000 description 1
- AJPJDKMHJJGVTQ-UHFFFAOYSA-M sodium dihydrogen phosphate Chemical compound [Na+].OP(O)([O-])=O AJPJDKMHJJGVTQ-UHFFFAOYSA-M 0.000 description 1
- 239000012312 sodium hydride Substances 0.000 description 1
- 229910000104 sodium hydride Inorganic materials 0.000 description 1
- 239000011697 sodium iodate Substances 0.000 description 1
- 235000015281 sodium iodate Nutrition 0.000 description 1
- 229940032753 sodium iodate Drugs 0.000 description 1
- 235000011006 sodium potassium tartrate Nutrition 0.000 description 1
- 229960003787 sorafenib Drugs 0.000 description 1
- 239000000600 sorbitol Substances 0.000 description 1
- 235000010356 sorbitol Nutrition 0.000 description 1
- 229950007213 spartalizumab Drugs 0.000 description 1
- 238000002798 spectrophotometry method Methods 0.000 description 1
- 238000004611 spectroscopical analysis Methods 0.000 description 1
- VNFWTIYUKDMAOP-UHFFFAOYSA-N sphos Chemical group COC1=CC=CC(OC)=C1C1=CC=CC=C1P(C1CCCCC1)C1CCCCC1 VNFWTIYUKDMAOP-UHFFFAOYSA-N 0.000 description 1
- 239000007921 spray Substances 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 239000008107 starch Substances 0.000 description 1
- 235000019698 starch Nutrition 0.000 description 1
- 230000000707 stereoselective effect Effects 0.000 description 1
- 239000012058 sterile packaged powder Substances 0.000 description 1
- 230000001954 sterilising effect Effects 0.000 description 1
- 238000004659 sterilization and disinfection Methods 0.000 description 1
- 150000003431 steroids Chemical class 0.000 description 1
- 238000003756 stirring Methods 0.000 description 1
- 210000002784 stomach Anatomy 0.000 description 1
- ZSJLQEPLLKMAKR-GKHCUFPYSA-N streptozocin Chemical compound O=NN(C)C(=O)N[C@H]1[C@@H](O)O[C@H](CO)[C@@H](O)[C@@H]1O ZSJLQEPLLKMAKR-GKHCUFPYSA-N 0.000 description 1
- 229960001052 streptozocin Drugs 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- 239000007929 subcutaneous injection Substances 0.000 description 1
- 239000005720 sucrose Substances 0.000 description 1
- 125000001174 sulfone group Chemical group 0.000 description 1
- 150000003462 sulfoxides Chemical class 0.000 description 1
- 229960001796 sunitinib Drugs 0.000 description 1
- WINHZLLDWRZWRT-ATVHPVEESA-N sunitinib Chemical compound CCN(CC)CCNC(=O)C1=C(C)NC(\C=C/2C3=CC(F)=CC=C3NC\2=O)=C1C WINHZLLDWRZWRT-ATVHPVEESA-N 0.000 description 1
- 238000001356 surgical procedure Methods 0.000 description 1
- 230000004083 survival effect Effects 0.000 description 1
- 239000000375 suspending agent Substances 0.000 description 1
- 230000002459 sustained effect Effects 0.000 description 1
- 238000013268 sustained release Methods 0.000 description 1
- 239000012730 sustained-release form Substances 0.000 description 1
- 239000003765 sweetening agent Substances 0.000 description 1
- 239000007916 tablet composition Substances 0.000 description 1
- 239000000454 talc Substances 0.000 description 1
- 229910052623 talc Inorganic materials 0.000 description 1
- 235000012222 talc Nutrition 0.000 description 1
- 229960001603 tamoxifen Drugs 0.000 description 1
- 238000002626 targeted therapy Methods 0.000 description 1
- 230000008685 targeting Effects 0.000 description 1
- RCINICONZNJXQF-MZXODVADSA-N taxol Chemical compound O([C@@H]1[C@@]2(C[C@@H](C(C)=C(C2(C)C)[C@H](C([C@]2(C)[C@@H](O)C[C@H]3OC[C@]3([C@H]21)OC(C)=O)=O)OC(=O)C)OC(=O)[C@H](O)[C@@H](NC(=O)C=1C=CC=CC=1)C=1C=CC=CC=1)O)C(=O)C1=CC=CC=C1 RCINICONZNJXQF-MZXODVADSA-N 0.000 description 1
- 229960004964 temozolomide Drugs 0.000 description 1
- 229960001278 teniposide Drugs 0.000 description 1
- NRUKOCRGYNPUPR-QBPJDGROSA-N teniposide Chemical compound COC1=C(O)C(OC)=CC([C@@H]2C3=CC=4OCOC=4C=C3[C@@H](O[C@H]3[C@@H]([C@@H](O)[C@@H]4O[C@@H](OC[C@H]4O3)C=3SC=CC=3)O)[C@@H]3[C@@H]2C(OC3)=O)=C1 NRUKOCRGYNPUPR-QBPJDGROSA-N 0.000 description 1
- IOGXOCVLYRDXLW-UHFFFAOYSA-N tert-butyl nitrite Chemical compound CC(C)(C)ON=O IOGXOCVLYRDXLW-UHFFFAOYSA-N 0.000 description 1
- 239000012414 tert-butyl nitrite Substances 0.000 description 1
- 229960005353 testolactone Drugs 0.000 description 1
- BPEWUONYVDABNZ-DZBHQSCQSA-N testolactone Chemical compound O=C1C=C[C@]2(C)[C@H]3CC[C@](C)(OC(=O)CC4)[C@@H]4[C@@H]3CCC2=C1 BPEWUONYVDABNZ-DZBHQSCQSA-N 0.000 description 1
- 125000000383 tetramethylene group Chemical group [H]C([H])([*:1])C([H])([H])C([H])([H])C([H])([H])[*:2] 0.000 description 1
- OULAJFUGPPVRBK-UHFFFAOYSA-N tetratriacontan-1-ol Chemical compound CCCCCCCCCCCCCCCCCCCCCCCCCCCCCCCCCCO OULAJFUGPPVRBK-UHFFFAOYSA-N 0.000 description 1
- ZRKFYGHZFMAOKI-QMGMOQQFSA-N tgfbeta Chemical compound C([C@H](NC(=O)[C@H](C(C)C)NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](CC(C)C)NC(=O)CNC(=O)[C@H](C)NC(=O)[C@H](CO)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@@H](NC(=O)[C@H](C)NC(=O)[C@H](C)NC(=O)[C@@H](NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](N)CCSC)C(C)C)[C@@H](C)CC)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](C)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](C)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](C)C(=O)N[C@@H](CC(C)C)C(=O)N1[C@@H](CCC1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(C)C)C(O)=O)C1=CC=C(O)C=C1 ZRKFYGHZFMAOKI-QMGMOQQFSA-N 0.000 description 1
- 239000002562 thickening agent Substances 0.000 description 1
- 125000002813 thiocarbonyl group Chemical group *C(*)=S 0.000 description 1
- 229960001196 thiotepa Drugs 0.000 description 1
- 229960003087 tioguanine Drugs 0.000 description 1
- MNRILEROXIRVNJ-UHFFFAOYSA-N tioguanine Chemical compound N1C(N)=NC(=S)C2=NC=N[C]21 MNRILEROXIRVNJ-UHFFFAOYSA-N 0.000 description 1
- 230000000699 topical effect Effects 0.000 description 1
- UCFGDBYHRUNTLO-QHCPKHFHSA-N topotecan Chemical compound C1=C(O)C(CN(C)C)=C2C=C(CN3C4=CC5=C(C3=O)COC(=O)[C@]5(O)CC)C4=NC2=C1 UCFGDBYHRUNTLO-QHCPKHFHSA-N 0.000 description 1
- 229960000303 topotecan Drugs 0.000 description 1
- 229960005026 toremifene Drugs 0.000 description 1
- XFCLJVABOIYOMF-QPLCGJKRSA-N toremifene Chemical compound C1=CC(OCCN(C)C)=CC=C1C(\C=1C=CC=CC=1)=C(\CCCl)C1=CC=CC=C1 XFCLJVABOIYOMF-QPLCGJKRSA-N 0.000 description 1
- 229960005267 tositumomab Drugs 0.000 description 1
- 239000003053 toxin Substances 0.000 description 1
- 231100000765 toxin Toxicity 0.000 description 1
- 108700012359 toxins Proteins 0.000 description 1
- 235000010487 tragacanth Nutrition 0.000 description 1
- 239000000196 tragacanth Substances 0.000 description 1
- 229940116362 tragacanth Drugs 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- 229960001727 tretinoin Drugs 0.000 description 1
- QORWJWZARLRLPR-UHFFFAOYSA-H tricalcium bis(phosphate) Chemical compound [Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O QORWJWZARLRLPR-UHFFFAOYSA-H 0.000 description 1
- ZBZJXHCVGLJWFG-UHFFFAOYSA-N trichloromethyl(.) Chemical compound Cl[C](Cl)Cl ZBZJXHCVGLJWFG-UHFFFAOYSA-N 0.000 description 1
- 125000000876 trifluoromethoxy group Chemical group FC(F)(F)O* 0.000 description 1
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 description 1
- 125000003258 trimethylene group Chemical group [H]C([H])([*:2])C([H])([H])C([H])([H])[*:1] 0.000 description 1
- HJOAXCLZLHDZDX-UHFFFAOYSA-N tris(1,2,2-trifluoroethenyl) borate Chemical compound FC(F)=C(F)OB(OC(F)=C(F)F)OC(F)=C(F)F HJOAXCLZLHDZDX-UHFFFAOYSA-N 0.000 description 1
- 241000712461 unidentified influenza virus Species 0.000 description 1
- 210000003708 urethra Anatomy 0.000 description 1
- 229960000653 valrubicin Drugs 0.000 description 1
- ZOCKGBMQLCSHFP-KQRAQHLDSA-N valrubicin Chemical compound O([C@H]1C[C@](CC2=C(O)C=3C(=O)C4=CC=CC(OC)=C4C(=O)C=3C(O)=C21)(O)C(=O)COC(=O)CCCC)[C@H]1C[C@H](NC(=O)C(F)(F)F)[C@H](O)[C@H](C)O1 ZOCKGBMQLCSHFP-KQRAQHLDSA-N 0.000 description 1
- 229960003048 vinblastine Drugs 0.000 description 1
- JXLYSJRDGCGARV-XQKSVPLYSA-N vincaleukoblastine Chemical compound C([C@@H](C[C@]1(C(=O)OC)C=2C(=CC3=C([C@]45[C@H]([C@@]([C@H](OC(C)=O)[C@]6(CC)C=CCN([C@H]56)CC4)(O)C(=O)OC)N3C)C=2)OC)C[C@@](C2)(O)CC)N2CCC2=C1NC1=CC=CC=C21 JXLYSJRDGCGARV-XQKSVPLYSA-N 0.000 description 1
- GBABOYUKABKIAF-GHYRFKGUSA-N vinorelbine Chemical compound C1N(CC=2C3=CC=CC=C3NC=22)CC(CC)=C[C@H]1C[C@]2(C(=O)OC)C1=CC([C@]23[C@H]([C@]([C@H](OC(C)=O)[C@]4(CC)C=CCN([C@H]34)CC2)(O)C(=O)OC)N2C)=C2C=C1OC GBABOYUKABKIAF-GHYRFKGUSA-N 0.000 description 1
- 229960002066 vinorelbine Drugs 0.000 description 1
- 229920002554 vinyl polymer Polymers 0.000 description 1
- WAEXFXRVDQXREF-UHFFFAOYSA-N vorinostat Chemical compound ONC(=O)CCCCCCC(=O)NC1=CC=CC=C1 WAEXFXRVDQXREF-UHFFFAOYSA-N 0.000 description 1
- 229960000237 vorinostat Drugs 0.000 description 1
- 239000003643 water by type Substances 0.000 description 1
- 238000005550 wet granulation Methods 0.000 description 1
- 238000001238 wet grinding Methods 0.000 description 1
- 239000000080 wetting agent Substances 0.000 description 1
- 239000003871 white petrolatum Substances 0.000 description 1
- 239000011701 zinc Substances 0.000 description 1
- CITILBVTAYEWKR-UHFFFAOYSA-L zinc trifluoromethanesulfonate Chemical compound [Zn+2].[O-]S(=O)(=O)C(F)(F)F.[O-]S(=O)(=O)C(F)(F)F CITILBVTAYEWKR-UHFFFAOYSA-L 0.000 description 1
- XRASPMIURGNCCH-UHFFFAOYSA-N zoledronic acid Chemical compound OP(=O)(O)C(P(O)(O)=O)(O)CN1C=CN=C1 XRASPMIURGNCCH-UHFFFAOYSA-N 0.000 description 1
- 229960004276 zoledronic acid Drugs 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D491/00—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00
- C07D491/02—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00 in which the condensed system contains two hetero rings
- C07D491/04—Ortho-condensed systems
- C07D491/044—Ortho-condensed systems with only one oxygen atom as ring hetero atom in the oxygen-containing ring
- C07D491/048—Ortho-condensed systems with only one oxygen atom as ring hetero atom in the oxygen-containing ring the oxygen-containing ring being five-membered
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/42—Oxazoles
- A61K31/423—Oxazoles condensed with carbocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/425—Thiazoles
- A61K31/428—Thiazoles condensed with carbocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/4353—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems
- A61K31/4355—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems the heterocyclic ring system containing a five-membered ring having oxygen as a ring hetero atom
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/04—Immunostimulants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D263/00—Heterocyclic compounds containing 1,3-oxazole or hydrogenated 1,3-oxazole rings
- C07D263/52—Heterocyclic compounds containing 1,3-oxazole or hydrogenated 1,3-oxazole rings condensed with carbocyclic rings or ring systems
- C07D263/54—Benzoxazoles; Hydrogenated benzoxazoles
- C07D263/56—Benzoxazoles; Hydrogenated benzoxazoles with only hydrogen atoms, hydrocarbon or substituted hydrocarbon radicals, directly attached in position 2
- C07D263/57—Aryl or substituted aryl radicals
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D277/00—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings
- C07D277/60—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings condensed with carbocyclic rings or ring systems
- C07D277/62—Benzothiazoles
- C07D277/64—Benzothiazoles with only hydrocarbon or substituted hydrocarbon radicals attached in position 2
- C07D277/66—Benzothiazoles with only hydrocarbon or substituted hydrocarbon radicals attached in position 2 with aromatic rings or ring systems directly attached in position 2
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/06—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings linked by a carbon chain containing only aliphatic carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/10—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/06—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings linked by a carbon chain containing only aliphatic carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/10—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D491/00—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00
- C07D491/02—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00 in which the condensed system contains two hetero rings
- C07D491/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D498/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D498/02—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and oxygen atoms as the only ring hetero atoms in which the condensed system contains two hetero rings
- C07D498/04—Ortho-condensed systems
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Medicinal Chemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Immunology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Epidemiology (AREA)
- Communicable Diseases (AREA)
- Oncology (AREA)
- Virology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Heterocyclic Carbon Compounds Containing A Hetero Ring Having Nitrogen And Oxygen As The Only Ring Hetero Atoms (AREA)
- Plural Heterocyclic Compounds (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
- Agricultural Chemicals And Associated Chemicals (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
Description
本開示は、とりわけ、式(I’):
X1及びX2の一方はOまたはSであり、X1及びX2の他方はN、CR1、またはCR2であり;
X3はNまたはCR3であり;
X4はNまたはCR4であり;
X5はNまたはCR5であり;
X6はNまたはCR6であり;
X1、X2、X3、X4、X5、及びX6の少なくとも1つはNであり;
Y1はNまたはCR8aであり;
Y2はNまたはCR8bであり;
Y3はNまたはCR8cであり;
Cyは、C6-10アリール、C3-10シクロアルキル、5~14員ヘテロアリール、または4~10員ヘテロシクロアルキルであり、それぞれが場合により1、2、3、4、または5個の独立して選択されるR7置換基で置換され;
R1、R2、R8a、R8b、及びR8cはそれぞれ独立して、H、C1-4アルキル、C3-6シクロアルキル、C3-6シクロアルキル-C1-4アルキル-、C6-10アリール、C6-10アリール-C1-4アルキル-、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、(5~10員ヘテロアリール)-C1-4アルキル-、(4~10員ヘテロシクロアルキル)-C1-4アルキル-、C2-4アルケニル、C2-4アルキニル、ハロ、CN、OR10、C1-4ハロアルキル、C1-4ハロアルコキシ、NH2、-NHR10、-NR10R10、NHOR10、C(O)R10、C(O)NR10R10、C(O)OR10、OC(O)R10、OC(O)NR10R10、NR10C(O)R10、NR10C(O)OR10、NR10C(O)NR10R10、C(=NR10)R10、C(=NR10)NR10R10、NR10C(=NR10)NR10R10、NR10S(O)R10、NR10S(O)2R10、NR10S(O)2NR10R10、S(O)R10、S(O)NR10R10、S(O)2R10、及びS(O)2NR10R10から選択され、ここで、各R10は独立して、H、C1-4アルキル、C2-4アルケニル、C2-4アルキニル、C1-4アルコキシ、C3-6シクロアルキル、C3-6シクロアルキル-C1-4アルキル-、C6-10アリール、C6-10アリール-C1-4アルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、(5~10員ヘテロアリール)-C1-4アルキル-、及び(4~10員ヘテロシクロアルキル)-C1-4アルキル-から選択され、R1、R2、R8a、R8b、R10、及びR8cのC1-4アルキル、C2-4アルケニル、C2-4アルキニル、C1-4アルコキシ、C3-6シクロアルキル、C3-6シクロアルキル-C1-4アルキル-、C6-10アリール、C6-10アリール-C1-4アルキル-、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、(5~10員ヘテロアリール)-C1-4アルキル-、及び(4~10員ヘテロシクロアルキル)-C1-4アルキル-は、それぞれ場合により1、2、または3個の独立して選択されるRd置換基で置換され;
R9は、Cl、Br、I、C1-6アルキル、C2-6アルケニル、C2-6アルキニル、C1-6ハロアルキル、C1-6ハロアルコキシ、C6-10アリール、C3-10シクロアルキル、5~14員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~14員ヘテロアリール)-C1-4アルキル-、(4~10員ヘテロシクロアルキル)-C1-4アルキル-、CN、NO2、OR11a、SR11、NH2、-NHR11、-NR11R11、NHOR11、C(O)R11、C(O)NR11R11、C(O)OR11、OC(O)R11、OC(O)NR11R11、NR11C(O)R11、NR11C(O)OR11、NR11C(O)NR11R11、C(=NR11)R11、C(=NR11)NR11R11、NR11C(=NR11)NR11R11、NR11S(O)R11、NR11S(O)2R11、NR11S(O)2NR11R11、S(O)R11、S(O)NR11R11、S(O)2R11、及びS(O)2NR11R11であり、ここで、R9のC1-6アルキル、C2-6アルケニル、C2-6アルキニル、C1-6ハロアルキル、C1-6ハロアルコキシ、C6-10アリール、C3-10シクロアルキル、5~14員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~14員ヘテロアリール)-C1-4アルキル-、及び(4~10員ヘテロシクロアルキル)-C1-4アルキル-は、それぞれ場合により1、2、または3個のRb置換基で置換され;
各R11は独立して、H、C1-6アルキル、C1-6ハロアルキル、C2-6アルケニル、C2-6アルキニル、C6-10アリール、C3-10シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~10員ヘテロアリール)-C1-4アルキル-、及び(4~10員ヘテロシクロアルキル)-C1-4アルキル-から選択され、ここで、R11のC1-6アルキル、C2-6アルケニル、C2-6アルキニル、C6-10アリール、C3-10シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~10員ヘテロアリール)-C1-4アルキル-、及び(4~10員ヘテロシクロアルキル)-C1-4アルキル-は、それぞれ場合により1、2、または3個の独立して選択されるRb置換基で置換され;
R11aは、C1-6アルキル、C1-6ハロアルキル、C2-6アルケニル、C2-6アルキニル、C6-10アリール、C3-10シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~10員ヘテロアリール)-C1-4アルキル-、及び(4~10員ヘテロシクロアルキル)-C1-4アルキル-から選択され、それぞれが場合により1、2、または3個の独立して選択されるRb置換基で置換され;
R3、R4、R5、R6、及びR7はそれぞれ独立して、H、ハロ、C1-6アルキル、C2-6アルケニル、C2-6アルキニル、C1-6ハロアルキル、C1-6ハロアルコキシ、C6-10アリール、C3-10シクロアルキル、5~14員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~14員ヘテロアリール)-C1-4アルキル-、(4~10員ヘテロシクロアルキル)-C1-4アルキル-、CN、NO2、ORa、SRa、NHORa、C(O)Ra、C(O)NRaRa、C(O)ORa、OC(O)Ra、OC(O)NRaRa、NHRa、NRaRa、NRaC(O)Ra、NRaC(O)ORa、NRaC(O)NRaRa、C(=NRa)Ra、C(=NRa)NRaRa、NRaC(=NRa)NRaRa、NRaS(O)Ra、NRaS(O)2Ra、NRaS(O)2NRaRa、S(O)Ra、S(O)NRaRa、S(O)2Ra、及びS(O)2NRaRaから選択され、ここで、R3、R4、R5、R6、及びR7のC1-6アルキル、C2-6アルケニル、C2-6アルキニル、C6-10アリール、C3-10シクロアルキル、5~14員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~14員ヘテロアリール)-C1-4アルキル-、及び(4~10員ヘテロシクロアルキル)-C1-4アルキル-は、それぞれ場合により1、2、3、または4個のRb置換基で置換され、ただしその場合、R3、R4、R5、及びR6の少なくとも1つはH以外であるか;
または、Cy環上の2つの隣接するR7置換基は、それらが結合する原子とともに縮合フェニル環、縮合5~7員ヘテロシクロアルキル環、縮合5員もしくは6員ヘテロアリール環、または縮合C5-6シクロアルキル環を形成し、その場合、縮合5~7員ヘテロシクロアルキル環及び縮合5員または6員ヘテロアリール環はそれぞれ、環員としてN、O、及びSから選択される1~4個のヘテロ原子を有し、縮合フェニル環、縮合5~7員ヘテロシクロアルキル環、縮合5員または6員ヘテロアリール環、及び縮合C5-6シクロアルキル環は、それぞれ場合により1、2、または3個の独立して選択されるRb置換基で置換され;
各Raは独立して、H、CN、C1-6アルキル、C1-4ハロアルキル、C2-6アルケニル、C2-6アルキニル、C6-10アリール、C3-10シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~10員ヘテロアリール)-C1-4アルキル-、及び(4~10員ヘテロシクロアルキル)-C1-4アルキル-から選択され、ここで、RaのC1-6アルキル、C2-6アルケニル、C2-6アルキニル、C6-10アリール、C3-10シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~10員ヘテロアリール)-C1-4アルキル-、及び(4~10員ヘテロシクロアルキル)-C1-4アルキル-は、それぞれ場合により1、2、3、4、または5個のRd置換基で置換され;
各Rdは独立して、C1-6アルキル、C1-6ハロアルキル、ハロ、C6-10アリール、5~10員ヘテロアリール、C3-10シクロアルキル、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~10員ヘテロアリール)-C1-4アルキル-、(4~10員ヘテロシクロアルキル)-C1-4アルキル-、CN、NH2、NHORe、ORe、SRe、C(O)Re、C(O)NReRe、C(O)ORe、OC(O)Re、OC(O)NReRe、NHRe、NReRe、NReC(O)Re、NReC(O)NReRe、NReC(O)ORe、C(=NRe)NReRe、NReC(=NRe)NReRe、NReC(=NOH)NReRe、NReC(=NCN)NReRe、S(O)Re、S(O)NReRe、S(O)2Re、NReS(O)2Re、NReS(O)2NReRe、及びS(O)2NReReから選択され、ここで、RdのC1-6アルキル、C1-6ハロアルキル、C6-10アリール、5~10員ヘテロアリール、C3-10シクロアルキル、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~10員ヘテロアリール)-C1-4アルキル-、及び(4~10員ヘテロシクロアルキル)-C1-4アルキル-は、それぞれ場合により1~3個の独立して選択されるRh置換基で置換され;
各Rb置換基は独立して、ハロ、C1-4アルキル、C1-4ハロアルキル、C1-4ハロアルコキシ、C6-10アリール、C3-10シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~10員ヘテロアリール)-C1-4アルキル-、(4~10員ヘテロシクロアルキル)-C1-4アルキル-、CN、OH、NH2、NO2、NHORc、ORc、SRc、C(O)Rc、C(O)NRcRc、C(O)ORc、OC(O)Rc、OC(O)NRcRc、C(=NRc)NRcRc、NRcC(=NRc)NRcRc、NHRc、NRcRc、NRcC(O)Rc、NRcC(O)ORc、NRcC(O)NRcRc、NRcS(O)Rc、NRcS(O)2Rc、NRcS(O)2NRcRc、S(O)Rc、S(O)NRcRc、S(O)2Rc、及びS(O)2NRcRcから選択され;ここで、RbのC1-4アルキル、C1-4ハロアルキル、C1-4ハロアルコキシ、C6-10アリール、C3-10シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~10員ヘテロアリール)-C1-4アルキル-、及び(4~10員ヘテロシクロアルキル)-C1-4アルキル-は、それぞれさらに場合により1~3個の独立して選択されるRd置換基で置換され;
各RCは独立して、H、C1-6アルキル、C1-4ハロアルキル、C2-6アルケニル、C2-6アルキニル、C6-10アリール、C3-10シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~10員ヘテロアリール)-C1-4アルキル-、及び(4~10員ヘテロシクロアルキル)-C1-4アルキル-から選択され、ここで、RCのC1-6アルキル、C2-6アルケニル、C2-6アルキニル、C6-10アリール、C3-10シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~10員ヘテロアリール)-C1-4アルキル-、及び(4~10員ヘテロシクロアルキル)-C1-4アルキル-は、それぞれ場合により、C1-4アルキル、C1-4ハロアルキル、C2-6アルケニル、C2-6アルキニル、C6-10アリール、C3-10シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~10員ヘテロアリール)-C1-4アルキル-、(4-10員ヘテロシクロアルキル)-C1-4アルキル-、ハロ、CN、NHORg、ORg、SRg、C(O)Rg、C(O)NRgRg、C(O)ORg、OC(O)Rg、OC(O)NRgRg、NHRg、NRgRg、NRgC(O)Rg、NRgC(O)NRgRg、NRgC(O)ORg、C(=NRg)NRgRg、NRgC(=NRg)NRgRg、S(O)Rg、S(O)NRgRg、S(O)2Rg、NRgS(O)2Rg、NRgS(O)2NRgRg、及びS(O)2NRgRgから独立して選択される1、2、3、4、または5個のRf置換基で置換され;その場合、RfのC1-4アルキル、C1-4ハロアルキル、C2-6アルケニル、C2-6アルキニル、C6-10アリール、C3-10シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~10員ヘテロアリール)-C1-4アルキル-、及び(4~10員ヘテロシクロアルキル)-C1-4アルキル-は、それぞれ場合により、C1-4アルキル、C1-4ハロアルキル、ハロ、CN、Ro、NHORo、ORo、SRo、C(O)Ro、C(O)NRoRo、C(O)ORo、OC(O)Ro、OC(O)NRoRo、NHRo、NRoRo、NRoC(O)Ro、NRoC(O)NRoRo、NRoC(O)ORo、C(=NRo)NRoRo、NRoC(=NRo)NRoRo、S(O)Ro、S(O)NRoRo、S(O)2Ro、NRoS(O)2Ro、NRoS(O)2NRoRo、及びS(O)2NRoRoから独立して選択される1、2、3、4、または5個のRn置換基で置換され;
各Rgは独立して、H、C1-6アルキル、C1-4ハロアルキル、C2-6アルケニル、C2-6アルキニル、C6-10アリール、C3-10シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~10員ヘテロアリール)-C1-4アルキル-、及び(4~10員ヘテロシクロアルキル)-C1-4アルキル-から選択され、ここで、RgのC1-6アルキル、C2-6アルケニル、C2-6アルキニル、C6-10アリール、C3-10シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~10員ヘテロアリール)-C1-4アルキル-、及び(4~10員ヘテロシクロアルキル)-C1-4アルキル-は、それぞれ場合により、C1-6アルキル、C1-6ハロアルキル、C2-6アルケニル、C2-6アルキニル、C6-10アリール、C3-10シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~10員ヘテロアリール)-C1-4アルキル-、(4-10員ヘテロシクロアルキル)-C1-4アルキル-、ハロ、CN、NHORr、ORr、SRr、C(O)Rr、C(O)NRrRr、C(O)ORr、OC(O)Rr、OC(O)NRrRr、NHRr、NRrRr、NRrC(O)Rr、NRrC(O)NRrRr、NRrC(O)ORr、C(=NRr)NRrRr、NRrC(=NRr)NRrRr、NRrC(=NOH)NRrRr、NRrC(=NCN)NRrRr、S(O)Rr、S(O)NRrRr、S(O)2Rr、NRrS(O)2Rr、NRrS(O)2NRrRr、及びS(O)2NRrRrから独立して選択される1~3個のRp置換基で置換され、RpのC1-6アルキル、C1-6ハロアルキル、C2-6アルケニル、C2-6アルキニル、C6-10アリール、C3-10シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~10員ヘテロアリール)-C1-4アルキル-、及び(4~10員ヘテロシクロアルキル)-C1-4アルキル-は、場合により1、2、または3個のRq置換基で置換されるか;
あるいは、任意の2つのRa置換基はそれらが結合する窒素原子とともに、4員、5員、6員、7員、8員、9員、または10員ヘテロシクロアルキル基を形成し、それらの基は場合により、C1-6アルキル、C3-10シクロアルキル、4~7員ヘテロシクロアルキル、C6-10アリール、5~6員ヘテロアリール、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~6員ヘテロアリール)-C1-4アルキル-、(4~7員ヘテロシクロアルキル)-C1-4アルキル-、C1-6ハロアルキル、C1-6ハロアルコキシ、C2-6アルケニル、C2-6アルキニル、ハロ、CN、ORi、SRi、NHORi、C(O)Ri、C(O)NRiRi、C(O)ORi、OC(O)Ri、OC(O)NRiRi、NHRi、NRiRi、NRiC(O)Ri、NRiC(O)NRiRi、NRiC(O)ORi、C(=NRi)NRiRi、NRiC(=NRi)NRiRi、S(O)Ri、S(O)NRiRi、S(O)2Ri、NRiS(O)2Ri、NRiS(O)2NRiRi、及びS(O)2NRiRiから独立して選択される1、2、または3個のRh置換基で置換されており、ここで、RhのC1-6アルキル、C2-6アルケニル、C2-6アルキニル、C3-10シクロアルキル、4~7員ヘテロシクロアルキル、C6-10アリール、5~6員ヘテロアリール、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~6員ヘテロアリール)-C1-4アルキル-、及び(4~7員ヘテロシクロアルキル)-C1-4アルキル-は、それぞれさらに場合により、C3-6シクロアルキル、C6-10アリール、5または6員ヘテロアリール、4~7員ヘテロシクロアルキル、C2-4アルケニル、C2-4アルキニル、ハロ、C1-4アルキル、C1-4ハロアルキル、CN、NHORk、ORk、SRk、C(O)Rk、C(O)NRkRk、C(O)ORk、OC(O)Rk、OC(O)NRkRk、NHRk、NRkRk、NRkC(O)Rk、NRkC(O)NRkRk、NRkC(O)ORk、C(=NRk)NRkRk、NRkC(=NRk)NRkRk、S(O)Rk、S(O)NRkRk、S(O)2Rk、NRkS(O)2Rk、NRkS(O)2NRkRk、及びS(O)2NRkRkから独立して選択される1、2、または3個のRj置換基で置換され、RjのC1-4アルキル、C3-6シクロアルキル、C6-10アリール、5員または6員ヘテロアリール、4~6員ヘテロシクロアルキル、C2-4アルケニル、C2-4アルキニル、C1-4ハロアルキル、及びC1-4ハロアルコキシは、それぞれ場合により1、2、または3個の独立して選択されるRq置換基で置換されるか;または、4~10員ヘテロシクロアルキルの同じ炭素原子に結合する2つのRh基は、それらが結合する炭素原子とともに、O、N、及びSから選択される1~2個のヘテロ原子を環員として有するC3-6シクロアルキルもしくは4~6員ヘテロシクロアルキルを形成するか;
あるいは、任意の2つのRc置換基はそれらが結合する窒素原子とともに、4員、5員、6員、または7員ヘテロシクロアルキル基を形成し、それらの基は場合により1、2、または3個の独立して選択されるRh置換基で置換されるか;
あるいは、任意の2つのRe置換基はそれらが結合する窒素原子とともに、4員、5員、6員、または7員ヘテロシクロアルキル基を形成し、それらの基は場合により1、2、または3個の独立して選択されるRh置換基で置換されるか;
あるいは、任意の2つのRg置換基はそれらが結合する窒素原子とともに、4員、5員、6員、または7員ヘテロシクロアルキル基を形成し、それらの基は場合により1、2、または3個の独立して選択されるRh置換基で置換されるか;
あるいは、任意の2つのRi置換基はそれらが結合する窒素原子とともに、4員、5員、6員、または7員ヘテロシクロアルキル基を形成し、それらの基は場合により1、2、または3個の独立して選択されるRh置換基で置換されるか;
あるいは、任意の2つのRk置換基はそれらが結合する窒素原子とともに、4員、5員、6員、または7員ヘテロシクロアルキル基を形成し、それらの基は場合により1、2、または3個の独立して選択されるRh置換基で置換されるか;
あるいは、任意の2つのRo置換基はそれらが結合する窒素原子とともに、4員、5員、6員、または7員ヘテロシクロアルキル基を形成し、それらの基は場合により1、2、または3個の独立して選択されるRh置換基で置換されており;
各Re、Ri、Rk、Ro、またはRpは独立して、H、C1-4アルキル、C3-6シクロアルキル、C6-10アリール、5員または6員ヘテロアリール、4~7員ヘテロシクロアルキル、C1-4ハロアルキル、C2-4アルケニル、及びC2-4アルキニルから選択され、ここで、Re、Ri、Rk、Ro、またはRpのC1-4アルキル、C3-6シクロアルキル、C6-10アリール、5員または6員ヘテロアリール、4~7員ヘテロシクロアルキル、C2-4アルケニル、及びC2-4アルキニルは、それぞれ場合により1、2、または3個のRq置換基で置換され;
各Rqは独立して、OH、CN、-COOH、NH2、ハロ、C1-6ハロアルキル、C1-6アルキル、C1-6アルコキシ、C1-6アルキルチオ、フェニル、5~6員ヘテロアリール、4~6員ヘテロシクロアルキル、C3-6シクロアルキル、NHR12、NR12R12、及びC1-4ハロアルコキシから選択され、ここで、RqのC1-6アルキル、フェニル、C3-6シクロアルキル、4~6員ヘテロシクロアルキル、及び5~6員ヘテロアリールは、それぞれ場合により、ハロ、OH、CN、-COOH、NH2、C1-4アルキル、C1-4アルコキシ、C1-4ハロアルキル、C1-4ハロアルコキシ、フェニル、C3-10シクロアルキル、5~6員ヘテロアリール、及び4~6員ヘテロシクロアルキルで置換され、各R12は独立してC1-6アルキルであり;
式(I’)の部分
化合物は1-[3-(6-クロロ-2-ベンゾオキサゾリル)-5-(3,5-ジメチルフェニル)-4-ピリジニル]-4-ピペリジンアミンではない。
X1及びX2の一方はOまたはSであり、X1及びX2の他方はN、CR1、またはCR2であり;
X3はNまたはCR3であり;
X4はNまたはCR4であり;
X5はNまたはCR5であり;
X6はNまたはCR6であり;
X1、X2、X3、X4、X5、及びX6の少なくとも1つはNであり;
Y1はNまたはCR8aであり;
Y2はNまたはCR8bであり;
Y3はNまたはCR8cであり;
Cyは、C6-10アリール、C3-10シクロアルキル、5~14員ヘテロアリール、または4~10員ヘテロシクロアルキルであり、それぞれが場合により1、2、3、4、または5個の独立して選択されるR7置換基で置換され;
R1、R2、R8a、R8b、及びR8cはそれぞれ独立して、H、C1-4アルキル、C3-6シクロアルキル、C2-4アルケニル、C2-4アルキニル、ハロ、CN、OH、C1-4アルコキシ、C1-4ハロアルキル、C1-4ハロアルコキシ、NH2、-NH-C1-4アルキル、-N(C1-4アルキル)2、NHOR10、C(O)R10、C(O)NR10R10、C(O)OR10、OC(O)R10、OC(O)NR10R10、NR10C(O)R10、NR10C(O)OR10、NR10C(O)NR10R10、C(=NR10)R10、C(=NR10)NR10R10、NR10C(=NR10)NR10R10、NR10S(O)R10、NR10S(O)2R10、NR10S(O)2NR10R10、S(O)R10、S(O)NR10R10、S(O)2R10、及びS(O)2NR10R10から選択され、ここで、各R10は独立して、H、またはハロ、OH、CN、及びC1-4アルコキシから独立して選択される1個もしくは2個の基で場合により置換されるC1-4アルキルであり、かつ、R1、R2、R8a、R8b、またはR8cのC1-4アルキル、C3-4シクロアルキル、C2-4アルケニル、及びC2-4アルキニルは、それぞれ場合により、ハロ、OH、CN、C1-4アルキル、及びC1-4アルコキシから独立して選択される1個または2個の置換基で置換され;
R9は、C1-4アルキル、Cl、Br、CN、シクロプロピル、C2-4アルキニル、C1-4ハロアルキル、C1-4ハロアルコキシ、NH2、-NH-C1-4アルキル、-N(C1-4アルキル)2、NHOR11、C(O)R11、C(O)NR11R11、C(O)OR11、OC(O)R11、OC(O)NR11R11、NR11C(O)R11、NR11C(O)OR11、NR11C(O)NR11R11、C(=NR11)R11、C(=NR11)NR11R11、NR11C(=NR11)NR11R11、NR11S(O)R11、NR11S(O)2R11、NR11S(O)2NR11R11、S(O)R11、S(O)NR11R11、S(O)2R11、及びS(O)2NR11R11であり、ここで、R9のC1-4アルキル、シクロプロピル、C2-4アルキニル、及びC1-4アルコキシは、それぞれ場合により、1個または2個のハロ、OH、CN、またはOCH3置換基で置換され、各R11は独立して、H、または1個もしくは2個のハロ、OH、CN、もしくはOCH3で場合により置換されるC1-4アルキルであり;
R3、R4、R5、R6、及びR7はそれぞれ独立して、H、ハロ、C1-6アルキル、C2-6アルケニル、C2-6アルキニル、C1-6ハロアルキル、C1-6ハロアルコキシ、C6-10アリール、C3-10シクロアルキル、5~14員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~14員ヘテロアリール)-C1-4アルキル-、(4~10員ヘテロシクロアルキル)-C1-4アルキル-、CN、NO2、ORa、SRa、NHORa、C(O)Ra、C(O)NRaRa、C(O)ORa、OC(O)Ra、OC(O)NRaRa、NHRa、NRaRa、NRaC(O)Ra、NRaC(O)ORa、NRaC(O)NRaRa、C(=NRa)Ra、C(=NRa)NRaRa、NRaC(=NRa)NRaRa、NRaS(O)Ra、NRaS(O)2Ra、NRaS(O)2NRaRa、S(O)Ra、S(O)NRaRa、S(O)2Ra、及びS(O)2NRaRaから選択され、ここで、R3、R4、R5、R6、及びR7のC1-6アルキル、C2-6アルケニル、C2-6アルキニル、C6-10アリール、C3-10シクロアルキル、5~14員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~14員ヘテロアリール)-C1-4アルキル-、及び(4~10員ヘテロシクロアルキル)-C1-4アルキル-は、それぞれ場合により1、2、3、または4個のRb置換基で置換され、ただしその場合、R3、R4、R5、及びR6の少なくとも1つはH以外であるか;
または、Cy環上の2つの隣接するR7置換基は、それらが結合する原子とともに縮合フェニル環、縮合5~7員ヘテロシクロアルキル環、縮合5員もしくは6員ヘテロアリール環、または縮合C5-6シクロアルキル環を形成し、その場合、縮合5~7員ヘテロシクロアルキル環及び縮合5員または6員ヘテロアリール環はそれぞれ、環員としてN、O、及びSから選択される1~4個のヘテロ原子を有し、縮合フェニル環、縮合5~7員ヘテロシクロアルキル環、縮合5員または6員ヘテロアリール環、及び縮合C5-6シクロアルキル環は、それぞれ場合により1もしくは2個の独立して選択されるRb置換基、または1個もしくは2個の独立して選択されるRq置換基で置換され;
各Raは独立して、H、CN、C1-6アルキル、C1-4ハロアルキル、C2-6アルケニル、C2-6アルキニル、C6-10アリール、C3-10シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~10員ヘテロアリール)-C1-4アルキル-、及び(4~10員ヘテロシクロアルキル)-C1-4アルキル-から選択され、ここで、RaのC1-6アルキル、C2-6アルケニル、C2-6アルキニル、C6-10アリール、C3-10シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~10員ヘテロアリール)-C1-4アルキル-、及び(4~10員ヘテロシクロアルキル)-C1-4アルキル-は、それぞれ場合により1、2、3、4、または5個のRd置換基で置換され;
各Rdは独立して、C1-4アルキル、C1-4ハロアルキル、ハロ、C3-10シクロアルキル、4-10員ヘテロシクロアルキル、CN、NH2、NHORe、ORe、SRe、C(O)Re、C(O)NReRe、C(O)ORe、OC(O)Re、OC(O)NReRe、NHRe、NReRe、NReC(O)Re、NReC(O)NReRe、NReC(O)ORe、C(=NRe)NReRe、NReC(=NRe)NReRe、S(O)Re、S(O)NReRe、S(O)2Re、NReS(O)2Re、NReS(O)2NReRe、及びS(O)2NReReから選択され、ここで、RdのC1-4アルキル、C3-10シクロアルキル、及び4~10員ヘテロシクロアルキルは、それぞれさらに場合により1~3個の独立して選択されるRq置換基で置換され;
各Rb置換基は独立して、ハロ、C1-4アルキル、C1-4ハロアルキル、C1-4ハロアルコキシ、C6-10アリール、C3-10シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~10員ヘテロアリール)-C1-4アルキル-、(4~10員ヘテロシクロアルキル)-C1-4アルキル-、CN、OH、NH2、NO2、NHORc、ORc、SRc、C(O)Rc、C(O)NRcRc、C(O)ORc、OC(O)Rc、OC(O)NRcRc、C(=NRc)NRcRc、NRcC(=NRc)NRcRc、NHRc、NRcRc、NRcC(O)Rc、NRcC(O)ORc、NRcC(O)NRcRc、NRcS(O)Rc、NRcS(O)2Rc、NRcS(O)2NRcRc、S(O)Rc、S(O)NRcRc、S(O)2Rc、及びS(O)2NRcRcから選択され;ここで、RbのC1-4アルキル、C1-4ハロアルキル、C1-4ハロアルコキシ、C6-10アリール、C3-10シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~10員ヘテロアリール)-C1-4アルキル-、及び(4~10員ヘテロシクロアルキル)-C1-4アルキル-は、それぞれさらに場合により1~3個の独立して選択されるRd置換基で置換され;
各RCは独立して、H、C1-6アルキル、C1-4ハロアルキル、C2-6アルケニル、C2-6アルキニル、C6-10アリール、C3-10シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~10員ヘテロアリール)-C1-4アルキル-、及び(4~10員ヘテロシクロアルキル)-C1-4アルキル-から選択され、ここで、RCのC1-6アルキル、C2-6アルケニル、C2-6アルキニル、C6-10アリール、C3-10シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~10員ヘテロアリール)-C1-4アルキル-、及び(4~10員ヘテロシクロアルキル)-C1-4アルキル-は、それぞれ場合により、C1-4アルキル、C1-4ハロアルキル、C2-6アルケニル、C2-6アルキニル、C6-10アリール、C3-10シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~10員ヘテロアリール)-C1-4アルキル-、(4~10員ヘテロシクロアルキル)-C1-4アルキル-、ハロ、CN、NHORg、ORg、SRg、C(O)Rg、C(O)NRgRg、C(O)ORg、OC(O)Rg、OC(O)NRgRg、NHRg、NRgRg、NRgC(O)Rg、NRgC(O)NRgRg、NRgC(O)ORg、C(=NRg)NRgRg、NRgC(=NRg)NRgRg、S(O)Rg、S(O)NRgRg、S(O)2Rg、NRgS(O)2Rg、NRgS(O)2NRgRg、及びS(O)2NRgRgから独立して選択される1、2、3、4、または5個のRf置換基で置換され;その場合、RfのC1-4アルキル、C1-4ハロアルキル、C2-6アルケニル、C2-6アルキニル、C6-10アリール、C3-10シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~10員ヘテロアリール)-C1-4アルキル-、及び(4~10員ヘテロシクロアルキル)-C1-4アルキル-は、それぞれ場合により、C1-4アルキル、C1-4ハロアルキル、ハロ、CN、Ro、NHORo、ORo、SRo、C(O)Ro、C(O)NRoRo、C(O)ORo、OC(O)Ro、OC(O)NRoRo、NHRo、NRoRo、NRoC(O)Ro、NRoC(O)NRoRo、NRoC(O)ORo、C(=NRo)NRoRo、NRoC(=NRo)NRoRo、S(O)Ro、S(O)NRoRo、S(O)2Ro、NRoS(O)2Ro、NRoS(O)2NRoRo、及びS(O)2NRoRoから独立して選択される1、2、3、4、または5個のRn置換基で置換され;
各Rgは独立して、H、C1-6アルキル、C1-4ハロアルキル、C2-6アルケニル、C2-6アルキニル、C6-10アリール、C3-10シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~10員ヘテロアリール)-C1-4アルキル-、及び(4~10員ヘテロシクロアルキル)-C1-4アルキル-から選択され、ここで、RgのC1-6アルキル、C2-6アルケニル、C2-6アルキニル、C6-10アリール、C3-10シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~10員ヘテロアリール)-C1-4アルキル-、及び(4~10員ヘテロシクロアルキル)-C1-4アルキル-は、それぞれ場合により1~3個の独立して選択されるRp置換基で置換されるか;
あるいは、任意の2つのRa置換基はそれらが結合する窒素原子とともに、4員、5員、6員、7員、8員、9員、または10員ヘテロシクロアルキル基を形成し、それらの基は場合により、C1-6アルキル、C3-10シクロアルキル、4~7員ヘテロシクロアルキル、C6-10アリール、5~6員ヘテロアリール、C3-10シクロアルキル-C1-4アルキル-、(5~6員ヘテロアリール)-C1-4アルキル-、(4~7員ヘテロシクロアルキル)-C1-4アルキル-、C1-6ハロアルキル、C2-6アルケニル、C2-6アルキニル、ハロ、CN、ORi、SRi、NHORi、C(O)Ri、C(O)NRiRi、C(O)ORi、OC(O)Ri、OC(O)NRiRi、NHRi、NRiRi、NRiC(O)Ri、NRiC(O)NRiRi、NRiC(O)ORi、C(=NRi)NRiRi、NRiC(=NRi)NRiRi、S(O)Ri、S(O)NRiRi、S(O)2Ri、NRiS(O)2Ri、NRiS(O)2NRiRi、及びS(O)2NRiRiから独立して選択される1、2、または3個のRh置換基で置換されており、ここで、RhのC1-6アルキル、C3-10シクロアルキル、4~7員ヘテロシクロアルキル、C6-10アリール、5~6員ヘテロアリール、C3-10シクロアルキル-C1-4アルキル-、(5~6員ヘテロアリール)-C1-4アルキル-、(4~7員ヘテロシクロアルキル)-C1-4アルキル-は、それぞれさらに場合により、C3-6シクロアルキル、C6-10アリール、5員または6員ヘテロアリール、C2-4アルケニル、C2-4アルキニル、ハロ、C1-4アルキル、C1-4ハロアルキル、CN、NHORk、ORk、SRk、C(O)Rk、C(O)NRkRk、C(O)ORk、OC(O)Rk、OC(O)NRkRk、NHRk、NRkRk、NRkC(O)Rk、NRkC(O)NRkRk、NRkC(O)ORk、C(=NRk)NRkRk、NRkC(=NRk)NRkRk、S(O)Rk、S(O)NRkRk、S(O)2Rk、NRkS(O)2Rk、NRkS(O)2NRkRk、及びS(O)2NRkRkから独立して選択される1、2、または3個のRj置換基で置換されるか;または、4~10員ヘテロシクロアルキルの同じ炭素原子に結合する2つのRh基は、それらが結合する炭素原子とともに、O、N、もしくはSから選択される1~2個のヘテロ原子を環員として有するC3-6シクロアルキルもしくは4~6員ヘテロシクロアルキルを形成するか;
あるいは、任意の2つのRc置換基はそれらが結合する窒素原子とともに、4員、5員、6員、または7員ヘテロシクロアルキル基を形成し、それらの基は場合により1、2、または3個の独立して選択されるRh置換基で置換されるか;
あるいは、任意の2つのRe置換基はそれらが結合する窒素原子とともに、4員、5員、6員、または7員ヘテロシクロアルキル基を形成し、それらの基は場合により1、2、または3個の独立して選択されるRh置換基で置換されるか;
あるいは、任意の2つのRg置換基はそれらが結合する窒素原子とともに、4員、5員、6員、または7員ヘテロシクロアルキル基を形成し、それらの基は場合により1、2、または3個の独立して選択されるRh置換基で置換されるか;
あるいは、任意の2つのRi置換基はそれらが結合する窒素原子とともに、4員、5員、6員、または7員ヘテロシクロアルキル基を形成し、それらの基は場合により1、2、または3個の独立して選択されるRh置換基で置換されるか;
あるいは、任意の2つのRk置換基はそれらが結合する窒素原子とともに、4員、5員、6員、または7員ヘテロシクロアルキル基を形成し、それらの基は場合により1、2、または3個の独立して選択されるRh置換基で置換されるか;
あるいは、任意の2つのRo置換基はそれらが結合する窒素原子とともに、4員、5員、6員、または7員ヘテロシクロアルキル基を形成し、それらの基は場合により1、2、または3個の独立して選択されるRh置換基で置換されており;
各Re、Ri、Rk、Ro、またはRpは独立して、H、C1-4アルキル、C3-6シクロアルキル、C6-10アリール、5員または6員ヘテロアリール、C1-4ハロアルキル、C2-4アルケニル、及びC2-4アルキニルから選択され、ここで、Re、Ri、Rk、Ro、またはRpのC1-4アルキル、C3-6シクロアルキル、C6-10アリール、5員または6員ヘテロアリール、C2-4アルケニル、及びC2-4アルキニルは、それぞれ場合により1、2、または3個のRq置換基で置換され;
各Rqは独立して、OH、CN、-COOH、NH2、ハロ、C1-4アルキル、C1-4アルコキシ、C1-4アルキルチオ、フェニル、5~6員ヘテロアリール、C3-6シクロアルキル、NHR12、NR12R12、及びC1-4ハロアルコキシから選択され、ここで、RqのC1-4アルキル、フェニル、及び5~6員ヘテロアリールは、それぞれ場合により、OH、CN、-COOH、NH2、C1-4アルコキシ、C3-10シクロアルキル、及び4~6員ヘテロシクロアルキルで置換され、各R12は独立してC1-6アルキルであり;
式(I’)の部分
X1及びX2の一方はOまたはSであり、X1及びX2の他方はN、CR1、またはCR2であり;
X3はNまたはCR3であり;
X4はNまたはCR4であり;
X5はNまたはCR5であり;
X6はNまたはCR6であり;
X1、X2、X3、X4、X5、及びX6の少なくとも1つはNであり;
R1、R2、及びR8はそれぞれ独立して、H、C1-4アルキル、C3-6シクロアルキル、C2-4アルケニル、C2-4アルキニル、ハロ、CN、OH、C1-4アルコキシ、C1-4ハロアルキル、C1-4ハロアルコキシ、NH2、-NH-C1-4アルキル、-N(C1-4アルキル)2、NHOR10、C(O)R10、C(O)NR10R10、C(O)OR10、OC(O)R10、OC(O)NR10R10、NR10C(O)R10、NR10C(O)OR10、NR10C(O)NR10R10、C(=NR10)R10、C(=NR10)NR10R10、NR10C(=NR10)NR10R10、NR10S(O)R10、NR10S(O)2R10、NR10S(O)2NR10R10、S(O)R10、S(O)NR10R10、S(O)2R10、及びS(O)2NR10R10から選択され、ここで、各R10は独立して、H、またはハロ、OH、CN、及びC1-4アルコキシから独立して選択される1個もしくは2個の基で場合により置換されるC1-4アルキルであり、かつ、R1、R2、またはR8のC1-4アルキル、C3-4シクロアルキル、C2-4アルケニル、及びC2-4アルキニルは、それぞれ場合により、ハロ、OH、CN、C1-4アルキル、及びC1-4アルコキシから独立して選択される1個または2個の置換基で置換され;
R9は、C1-4アルキル、Cl、Br、CN、シクロプロピル、C2-4アルキニル、C1-4ハロアルキル、C1-4ハロアルコキシ、NH2、-NH-C1-4アルキル、-N(C1-4アルキル)2、NHOR11、C(O)R11、C(O)NR11R11、C(O)OR11、OC(O)R11、OC(O)NR11R11、NR11C(O)R11、NR11C(O)OR11、NR11C(O)NR11R11、C(=NR11)R11、C(=NR11)NR11R11、NR11C(=NR11)NR11R11、NR11S(O)R11、NR11S(O)2R11、NR11S(O)2NR11R11、S(O)R11、S(O)NR11R11、S(O)2R11、及びS(O)2NR11R11であり、ここで、各R11は独立して、H、または1個もしくは2個のハロ、OH、CN、もしくはOCH3で場合により置換されるC1-4アルキルであり;
R3、R4、R5、R6、及びR7はそれぞれ独立して、H、ハロ、C1-6アルキル、C2-6アルケニル、C2-6アルキニル、C1-6ハロアルキル、C1-6ハロアルコキシ、C6-10アリール、C3-10シクロアルキル、5~14員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~14員ヘテロアリール)-C1-4アルキル-、(4~10員ヘテロシクロアルキル)-C1-4アルキル-、CN、NO2、ORa、SRa、NHORa、C(O)Ra、C(O)NRaRa、C(O)ORa、OC(O)Ra、OC(O)NRaRa、NHRa、NRaRa、NRaC(O)Ra、NRaC(O)ORa、NRaC(O)NRaRa、C(=NRa)Ra、C(=NRa)NRaRa、NRaC(=NRa)NRaRa、NRaS(O)Ra、NRaS(O)2Ra、NRaS(O)2NRaRa、S(O)Ra、S(O)NRaRa、S(O)2Ra、及びS(O)2NRaRaから選択され、ここで、R3、R4、R5、R6、及びR7のC1-6アルキル、C2-6アルケニル、C2-6アルキニル、C6-10アリール、C3-10シクロアルキル、5~14員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~14員ヘテロアリール)-C1-4アルキル-、及び(4~10員ヘテロシクロアルキル)-C1-4アルキル-は、それぞれ場合により1、2、3、または4個のRb置換基で置換され、ただしその場合、R3、R4、R5、及びR6の少なくとも1つはH以外であるか;
または、フェニル環上の2つの隣接するR7置換基は、それらが結合する炭素原子とともに縮合フェニル環、縮合5~7員ヘテロシクロアルキル環、縮合5員もしくは6員ヘテロアリール環、または縮合C5-6シクロアルキル環を形成し、その場合、縮合5~7員ヘテロシクロアルキル環及び縮合5員または6員ヘテロアリール環はそれぞれ、環員としてN、O、及びSから選択される1~4個のヘテロ原子を有し、縮合フェニル環、縮合5~7員ヘテロシクロアルキル環、縮合5員または6員ヘテロアリール環、及び縮合C5-6シクロアルキル環は、それぞれ場合により1個または2個の独立して選択されるRq置換基で置換され;
各Raは独立して、H、CN、C1-6アルキル、C1-4ハロアルキル、C2-6アルケニル、C2-6アルキニル、C6-10アリール、C3-10シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~10員ヘテロアリール)-C1-4アルキル-、及び(4~10員ヘテロシクロアルキル)-C1-4アルキル-から選択され、ここで、RaのC1-6アルキル、C2-6アルケニル、C2-6アルキニル、C6-10アリール、C3-10シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~10員ヘテロアリール)-C1-4アルキル-、及び(4~10員ヘテロシクロアルキル)-C1-4アルキル-は、それぞれ場合により1、2、3、4、または5個のRd置換基で置換され;
各Rdは独立して、C1-4アルキル、C1-4ハロアルキル、ハロ、C3-10シクロアルキル、4-10員ヘテロシクロアルキル、CN、NH2、NHORe、ORe、SRe、C(O)Re、C(O)NReRe、C(O)ORe、OC(O)Re、OC(O)NReRe、NHRe、NReRe、NReC(O)Re、NReC(O)NReRe、NReC(O)ORe、C(=NRe)NReRe、NReC(=NRe)NReRe、S(O)Re、S(O)NReRe、S(O)2Re、NReS(O)2Re、NReS(O)2NReRe、及びS(O)2NReReから選択され、ここで、RdのC1-4アルキル、C3-10シクロアルキル、及び4~10員ヘテロシクロアルキルは、それぞれさらに場合により1~3個の独立して選択されるRq置換基で置換され;
各Rb置換基は独立して、ハロ、C1-4アルキル、C1-4ハロアルキル、C1-4ハロアルコキシ、C6-10アリール、C3-10シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~10員ヘテロアリール)-C1-4アルキル-、(4~10員ヘテロシクロアルキル)-C1-4アルキル-、CN、OH、NH2、NO2、NHORc、ORc、SRc、C(O)Rc、C(O)NRcRc、C(O)ORc、OC(O)Rc、OC(O)NRcRc、C(=NRc)NRcRc、NRcC(=NRc)NRcRc、NHRc、NRcRc、NRcC(O)Rc、NRcC(O)ORc、NRcC(O)NRcRc、NRcS(O)Rc、NRcS(O)2Rc、NRcS(O)2NRcRc、S(O)Rc、S(O)NRcRc、S(O)2Rc、及びS(O)2NRcRcから選択され;ここで、RbのC1-4アルキル、C1-4ハロアルキル、C1-4ハロアルコキシ、C6-10アリール、C3-10シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~10員ヘテロアリール)-C1-4アルキル-、及び(4~10員ヘテロシクロアルキル)-C1-4アルキル-は、それぞれさらに場合により1~3個の独立して選択されるRd置換基で置換され;
各Rcは独立して、H、C1-6アルキル、C1-4ハロアルキル、C2-6アルケニル、C2-6アルキニル、C6-10アリール、C3-10シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~10員ヘテロアリール)-C1-4アルキル-、及び(4~10員ヘテロシクロアルキル)-C1-4アルキル-から選択され、ここで、RcのC1-6アルキル、C2-6アルケニル、C2-6アルキニル、C6-10アリール、C3-10シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~10員ヘテロアリール)-C1-4アルキル-、及び(4~10員ヘテロシクロアルキル)-C1-4アルキル-は、それぞれ場合により、C1-4アルキル、C1-4ハロアルキル、C2-6アルケニル、C2-6アルキニル、C6-10アリール、C3-10シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~10員ヘテロアリール)-C1-4アルキル-、(4-10員ヘテロシクロアルキル)-C1-4アルキル-、ハロ、CN、NHORg、ORg、SRg、C(O)Rg、C(O)NRgRg、C(O)ORg、OC(O)Rg、OC(O)NRgRg、NHRg、NRgRg、NRgC(O)Rg、NRgC(O)NRgRg、NRgC(O)ORg、C(=NRg)NRgRg、NRgC(=NRg)NRgRg、S(O)Rg、S(O)NRgRg、S(O)2Rg、NRgS(O)2Rg、NRgS(O)2NRgRg、及びS(O)2NRgRgから独立して選択される1、2、3、4、または5個のRf置換基で置換され;その場合、RfのC1-4アルキル、C1-4ハロアルキル、C2-6アルケニル、C2-6アルキニル、C6-10アリール、C3-10シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~10員ヘテロアリール)-C1-4アルキル-、及び(4~10員ヘテロシクロアルキル)-C1-4アルキル-は、それぞれ場合により、C1-4アルキル、C1-4ハロアルキル、ハロ、CN、Ro、NHORo、ORo、SRo、C(O)Ro、C(O)NRoRo、C(O)ORo、OC(O)Ro、OC(O)NRoRo、NHRo、NRoRo、NRoC(O)Ro、NRoC(O)NRoRo、NRoC(O)ORo、C(=NRo)NRoRo、NRoC(=NRo)NRoRo、S(O)Ro、S(O)NRoRo、S(O)2Ro、NRoS(O)2Ro、NRoS(O)2NRoRo、及びS(O)2NRoRoから独立して選択される1、2、3、4、または5個のRn置換基で置換され;
各Rgは独立して、H、C1-6アルキル、C1-4ハロアルキル、C2-6アルケニル、C2-6アルキニル、C6-10アリール、C3-10シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~10員ヘテロアリール)-C1-4アルキル-、及び(4~10員ヘテロシクロアルキル)-C1-4アルキル-から選択され、ここで、RgのC1-6アルキル、C2-6アルケニル、C2-6アルキニル、C6-10アリール、C3-10シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~10員ヘテロアリール)-C1-4アルキル-、及び(4~10員ヘテロシクロアルキル)-C1-4アルキル-は、それぞれ場合により1~3個の独立して選択されるRp置換基で置換さるか;
あるいは、任意の2つのRa置換基はそれらが結合する窒素原子とともに、4員、5員、6員、7員、8員、9員、または10員ヘテロシクロアルキル基を形成し、それらの基は場合により、C1-6アルキル、C3-10シクロアルキル、4~7員ヘテロシクロアルキル、C6-10アリール、5~6員ヘテロアリール、C3-10シクロアルキル-C1-4アルキル-、(5~6員ヘテロアリール)-C1-4アルキル-、(4~7員ヘテロシクロアルキル)-C1-4アルキル-、C1-6ハロアルキル、C2-6アルケニル、C2-6アルキニル、ハロ、CN、ORi、SRi、NHORi、C(O)Ri、C(O)NRiRi、C(O)ORi、OC(O)Ri、OC(O)NRiRi、NHRi、NRiRi、NRiC(O)Ri、NRiC(O)NRiRi、NRiC(O)ORi、C(=NRi)NRiRi、NRiC(=NRi)NRiRi、S(O)Ri、S(O)NRiRi、S(O)2Ri、NRiS(O)2Ri、NRiS(O)2NRiRi、及びS(O)2NRiRiから独立して選択される1、2、または3個のRh置換基で置換されており、ここで、RhのC1-6アルキル、C3-10シクロアルキル、4~7員ヘテロシクロアルキル、C6-10アリール、5~6員ヘテロアリール、C3-10シクロアルキル-C1-4アルキル-、(5~6員ヘテロアリール)-C1-4アルキル-、(4~7員ヘテロシクロアルキル)-C1-4アルキル-は、それぞれさらに場合により、C3-6シクロアルキル、C6-10アリール、5または6員ヘテロアリール、C2-4アルケニル、C2-4アルキニル、ハロ、C1-4アルキル、C1-4ハロアルキル、CN、NHORk、ORk、SRk、C(O)Rk、C(O)NRkRk、C(O)ORk、OC(O)Rk、OC(O)NRkRk、NHRk、NRkRk、NRkC(O)Rk、NRkC(O)NRkRk、NRkC(O)ORk、C(=NRk)NRkRk、NRkC(=NRk)NRkRk、S(O)Rk、S(O)NRkRk、S(O)2Rk、NRkS(O)2Rk、NRkS(O)2NRkRk、及びS(O)2NRkRkから独立して選択される1、2、または3個のRj置換基で置換されるか;または、4~10員ヘテロシクロアルキルの同じ炭素原子に結合する2つのRh基は、それらが結合する炭素原子とともに、O、N、もしくはSから選択される1~2個のヘテロ原子を環員として有するC3-6シクロアルキルもしくは4~6員ヘテロシクロアルキルを形成するか;
あるいは、任意の2つのRc置換基はそれらが結合する窒素原子とともに、4員、5員、6員、または7員ヘテロシクロアルキル基を形成し、それらの基は場合により1、2、または3個の独立して選択されるRh置換基で置換されるか;
あるいは、任意の2つのRe置換基はそれらが結合する窒素原子とともに、4員、5員、6員、または7員ヘテロシクロアルキル基を形成し、それらの基は場合により1、2、または3個の独立して選択されるRh置換基で置換されるか;
あるいは、任意の2つのRg置換基はそれらが結合する窒素原子とともに、4員、5員、6員、または7員ヘテロシクロアルキル基を形成し、それらの基は場合により1、2、または3個の独立して選択されるRh置換基で置換されるか;
あるいは、任意の2つのRi置換基はそれらが結合する窒素原子とともに、4員、5員、6員、または7員ヘテロシクロアルキル基を形成し、それらの基は場合により1、2、または3個の独立して選択されるRh置換基で置換されるか;
あるいは、任意の2つのRk置換基はそれらが結合する窒素原子とともに、4員、5員、6員、または7員ヘテロシクロアルキル基を形成し、それらの基は場合により1、2、または3個の独立して選択されるRh置換基で置換されるか;
あるいは、任意の2つのRo置換基はそれらが結合する窒素原子とともに、4員、5員、6員、または7員ヘテロシクロアルキル基を形成し、それらの基は場合により1、2、または3個の独立して選択されるRh置換基で置換されており;
各Re、Ri、Rk、Ro、またはRpは独立して、H、C1-4アルキル、C3-6シクロアルキル、C6-10アリール、5員または6員ヘテロアリール、C1-4ハロアルキル、C2-4アルケニル、及びC2-4アルキニルから選択され、ここで、Re、Ri、Rk、Ro、またはRpのC1-4アルキル、C3-6シクロアルキル、C6-10アリール、5員または6員ヘテロアリール、C2-4アルケニル、及びC2-4アルキニルは、それぞれ場合により1、2、または3個のRq置換基で置換され;
各Rqは独立して、OH、CN、-COOH、NH2、ハロ、C1-4アルキル、C1-4アルコキシ、C1-4アルキルチオ、フェニル、5~6員ヘテロアリール、C3-6シクロアルキル、NHR12、NR12R12、及びC1-4ハロアルコキシから選択され、ここで、RqのC1-4アルキル、フェニル、及び5~6員ヘテロアリールは、それぞれ場合により、OH、CN、-COOH、NH2、C1-4アルコキシ、C3-10シクロアルキル、及び4~6員ヘテロシクロアルキルで置換され、各R12は独立してC1-6アルキルであり;
下付き文字nは、整数1、2、3、4または5であり;下付き文字mは、整数1、2、3または4である。式(I)の化合物のいくつかの実施形態では、下付き文字mは、整数1、2、または3である。本明細書に記載の化合物、またはその薬学的に許容される塩もしくは立体異性体は、PD-1/PD-L1のタンパク質/タンパク質相互作用の阻害剤として有用である。例えば、本明細書に記載の化合物またはその薬学的に許容される塩もしくは立体異性体は、PD-1経路におけるPD-1/PD-L1のタンパク質/タンパク質相互作用を妨害することができる。
本発明の化合物(その塩を含む)は、既知の有機合成技術を使用して調製することができ、以下のスキームに示すような多数の可能な合成経路のいずれかに従って合成することができる。
本開示の化合物はPD-1/PD-L1のタンパク質/タンパク質相互作用の活性を阻害することができるため、PD-1の活性に関連する疾患及び障害、ならびにPD-1及びB7-1(CD80)などの他のタンパク質との相互作用を含めた、PD-L1に関連する疾患及び障害の治療に有用である。ある特定の実施形態では、本開示の化合物、またはその薬学的に許容される塩もしくは立体異性体は、ワクチン接種に対する応答の増強を含め、がんまたは慢性感染において免疫を増強、刺激、及び/または増加させるための治療投与に有用である。いくつかの実施形態では、本開示は、PD-1/PD-L1のタンパク質/タンパク質相互作用を阻害する方法を提供する。この方法は、式(I’)、式(I)、もしくは本明細書に記載のいずれかの式の化合物、もしくは請求項のいずれかに列挙される及び本明細書に記載される化合物、またはそれらの薬学的に許容される塩もしくは立体異性体を個体または患者に投与することを含む。本開示の化合物は、がんまたは感染性疾患を含む疾患または障害の治療のために、単独で、他の薬剤もしくは療法と組み合わせて、またはアジュバントもしくはネオアジュバントとして使用することができる。その実施形態のいずれを含め、本開示の化合物はいずれも本明細書に記載される用途に使用することができる。
がん細胞の成長及び生存は、複数のシグナル伝達経路によって影響される可能性がある。したがって、活性を調節する標的について異なった選択性を示す、異なる酵素/タンパク質/受容体阻害剤を組み合わせることは、そのような病態の治療に有用である。複数のシグナル伝達経路(または所与のシグナル伝達経路に関与する複数の生物学的分子)を標的とすることで、細胞集団に生じる薬物耐性の可能性を低減する、及び/または治療の毒性を低下させることができる。
医薬として使用する場合、本開示の化合物は、医薬組成物の形態で投与することができる。したがって、本開示は、式(I’)、式(I)、もしくは本明細書に記載のいずれかの式の化合物、請求項のいずれかに列挙される及び本明細書に記載される化合物、もしくはそれらの薬学的に許容される塩、またはそれらのいずれかの実施形態と、少なくとも1種の薬学的に許容される担体または賦形剤とを含む組成物を提供する。これらの組成物は、製薬分野で周知の方法で調製することができ、局所処置または全身処置いずれに適応であるか、及び処置されるべき領域に応じて、様々な経路で投与することができる。投与は、局所(経皮、上皮、眼内、ならびに鼻腔内送達、膣送達、及び直腸送達を含む経粘膜)、肺(例えば、ネブライザーを含む、粉末またはエアロゾルの吸引または吸入による;気管内または鼻腔内)、経口、または非経口であり得る。非経口投与には、静脈内、動脈内、皮下、腹腔内、もしくは筋肉内への注射もしくは注入;または頭蓋内、例えば、くも膜下腔内または脳室内投与が含まれる。非経口投与は、単回ボーラス投与の形態であってもよく、または例えば、連続灌流ポンプによるものであってもよい。局所投与用の医薬組成物及び製剤には、経皮パッチ剤、軟膏剤、ローション剤、クリーム剤、ゲル剤、滴剤、坐剤、スプレー剤、液状剤、及び散剤が含まれ得る。従来の医薬担体、水性、粉末、または油性の基剤、粘稠剤などが必要とされる、または望ましい場合がある。
本開示の化合物はさらに、正常組織及び異常組織における生物過程の調査に有用であり得る。したがって、本発明の別の態様は、イメージング技術のみならず、in vitro及びin vivo両方のアッセイにおいて、ヒトを含む組織サンプル中のPD-1またはPD-L1タンパク質を局在確認及び定量する、ならびに標識化合物の結合阻害によりPD-L1リガンドを同定するために有用である本発明の標識化合物(放射性標識、蛍光標識など)に関する。したがって、本発明には、そのような標識化合物を含むPD-1/PD-L1結合アッセイを含む。
本開示はまた、例えばPD-1及びB7-1(CD80)などの他のタンパク質とのその相互作用を含むPD-L1の活性に関連する疾患または障害、例えばがんまたは感染症の治療または予防に有用な医薬キットを含み、これには、治療有効量の式(I’)、式(I)の化合物、またはその実施形態のいずれかを含む医薬組成物が収容されている1つ以上の容器が含まれる。そのようなキットはさらに、例えば、当業者にとっては容易に明らかであるような、1種以上の薬学的に許容される担体を有する容器、追加の容器などのように1つ以上の様々な従来の医薬キット構成品を含み得る。投与すべき成分の量、投与のためのガイドライン、及び/または成分を混合するためのガイドラインを示す、添付文書またはラベルいずれかの形態の説明書もまたキットに含めることができる。
2-(2-メチルビフェニル-3-イル)フロ[2,3-b]ピリジン-6-カルバルデヒド(10mg、0.03mmol)及びエタノールアミン(5.5μL、0.092mmol)の塩化メチレン(0.4mL)溶液を室温で2時間撹拌した。次いで、トリアセトキシ水素化ホウ素ナトリウム(19mg、0.092mmol)及び酢酸(3.5μL、0.061mmol)を添加し、その混合物を一晩撹拌した。反応混合物をMeOHで希釈した後、分取HPLC(pH=2、アセトニトリル/水+TFA)により精製し、目的生成物をTFA塩として得た。C23H23N2O2に対するLC-MS計算値(M+H)+:m/z=359.2;実測値359.2。
(2S)-1-{[2-(2-メチルビフェニル-3-イル)フロ[2,3-b]ピリジン-6-イル]メチル}ピペリジン-2-カルボン酸
この化合物は、2-(2-メチルビフェニル-3-イル)フロ[2,3-b]ピリジン-6-カルバルデヒドの代わりに7-メチル-2-(2-メチルビフェニル-3-イル)フロ[3,2-b]ピリジン-5-カルバルデヒド(ステップ4の生成物)を用いて、実施例1ステップ5の記載と同様の手順を使用して調製した。反応混合物をMeOHで希釈した後、分取HPLC(pH=2、アセトニトリル/水+TFA)により精製し、目的生成物をTFA塩として得た。C24H25N2O2に対するLC-MS計算値(M+H)+:m/z=373.2;実測値373.2。
(2S)-1-{[7-メチル-2-(2-メチルビフェニル-3-イル)フロ[3,2-b]ピリジン-5-イル]メチル}ピペリジン-2-カルボン酸
この化合物は、2-(2-メチルビフェニル-3-イル)フロ[2,3-b]ピリジン-6-カルバルデヒドの代わりに7-メチル-2-(2-メチルビフェニル-3-イル)フロ[2,3-c]ピリジン-5-カルバルデヒド(ステップ4の生成物)を用いて、実施例1ステップ5の記載と同様の手順を使用して調製した。粗物質をメタノールで希釈し、分取HPLC(pH=10、アセトニトリル/水+NH4OH)により精製し、目的生成物を得た。C24H25N2O2に対するLC-MS計算値(M+H)+:m/z=373.2;実測値373.2。
(2S)-1-{[7-メチル-2-(2-メチルビフェニル-3-イル)フロ[2,3-c]ピリジン-5-イル]メチル}ピペリジン-2-カルボン酸
この化合物は、2-(2-メチルビフェニル-3-イル)フロ[2,3-b]ピリジン-6-カルバルデヒドの代わりに2-(2-メチルビフェニル-3-イル)-1,3-ベンゾオキサゾール-5-カルバルデヒド(ステップ2の生成物)、エタノールアミンの代わりに(S)-ピペリジン-2-カルボン酸を用いて、実施例1ステップ5の記載と同様の手順を使用して調製した。反応混合物をメタノールで希釈した後、分取HPLC(pH=2、アセトニトリル/水+TFA)により精製し、目的生成物をTFA塩として得た。C27H27N2O3に対するLC-MS計算値(M+H)+:m/z=427.2;実測値427.2。
2-({[2-(2-メチルビフェニル-3-イル)-1,3-ベンゾオキサゾール-5-イル]メチル}アミノ)エタノール
この化合物は、2-(2-メチルビフェニル-3-イル)フロ[2,3-b]ピリジン-6-カルバルデヒドの代わりに2-(2-メチルビフェニル-3-イル)フロ[2,3-b]ピリジン-5-カルバルデヒド(ステップ2の生成物)、エタノールアミンの代わりに(S)-ピペリジン-2-カルボン酸を用いて、実施例1ステップ5の記載と同様の手順を使用して調製した。反応混合物をメタノールで希釈した後、分取HPLC(pH=2、アセトニトリル/水+TFA)により精製し、目的生成物をTFA塩として得た。C27H27N2O3に対するLC-MS計算値(M+H)+:m/z=427.2;実測値427.2。
2-({[2-(2-メチルビフェニル-3-イル)フロ[2,3-b]ピリジン-5-イル]メチル}アミノ)エタノール
この化合物は、2-(2-メチルビフェニル-3-イル)フロ[2,3-b]ピリジン-6-カルバルデヒドの代わりに7-メチル-2-(2-メチルビフェニル-3-イル)-1,3-ベンゾオキサゾール-5-カルバルデヒド(ステップ3の生成物)、エタノールアミンの代わりに(S)-ピペリジン-2-カルボン酸を用いて、実施例1ステップ5の記載と同様の手順を使用して調製した。粗物質を分取HPLC(pH=10、アセトニトリル/水+NH4OH)により精製し、目的生成物を得た。C28H29N2O3に対するLC-MS計算値(M+H)+:m/z=441.2;実測値441.2。
2-({[7-メチル-2-(2-メチルビフェニル-3-イル)-1,3-ベンゾオキサゾール-5-イル]メチル}アミノ)エタノール
この化合物は、ステップ1で2-メチルビフェニル-3-カルバルデヒドの代わりに3-ホルミルビフェニル-2-カルボニトリル(ステップ2の生成物)を用いて、実施例11の記載と同様の手順を使用して調製した。反応混合物を分取HPLC(pH=10、アセトニトリル/水+NH4OH)により精製し、目的生成物を得た。C28H26N3O3に対するLC-MS計算値(M+H)+:m/z=452.2;実測値452.2。
3-(5-{[(2-ヒドロキシエチル)アミノ]メチル}-7-メチル-1,3-ベンゾオキサゾール-2-イル)ビフェニル-2-カルボニトリル
(2S)-1-({2-[3-(2,3-ジヒドロ-1,4-ベンゾジオキシン-6-イル)-2-メチルフェニル]-7-メチル-1,3-ベンゾオキサゾール-5-イル}メチル)ピペリジン-2-カルボン酸
この化合物は、ステップ1で2-メチルビフェニル-3-カルバルデヒドの代わりに3-(2,3-ジヒドロ-1,4-ベンゾジオキシン-6-イル)-2-メチルベンズアルデヒド(ステップ2の生成物)を用いて、実施例11の記載と同様の手順を使用して調製した。得られた混合物を分取HPLC(pH=10、アセトニトリル/水+NH4OH)により精製し、目的生成物を得た。C30H31N2O5に対するLC-MS計算値(M+H)+:m/z=499.2;実測値499.2。
2-[({2-[3-(2,3-ジヒドロ-1,4-ベンゾジオキシン-6-イル)-2-メチルフェニル]-7-メチル-1,3-ベンゾオキサゾール-5-イル}メチル)アミノ]エタノール
(2S)-1-({2-[2-シアノ-3-(2,3-ジヒドロ-1,4-ベンゾジオキシン-6-イル)フェニル]-7-メチル-1,3-ベンゾオキサゾール-5-イル}メチル)ピペリジン-2-カルボン酸
この化合物は、ステップ1で2-メチルビフェニル-3-カルバルデヒドの代わりに3-(2,3-ジヒドロ-1,4-ベンゾジオキシン-6-イル)-2-メチルベンズアルデヒド(ステップ3の生成物)を用いて、実施例11の記載と同様の手順を使用して調製した。反応混合物を分取HPLC(pH=10、アセトニトリル/水+NH4OH)により精製し、目的生成物を得た。C30H28N3O5に対するLC-MS計算値(M+H)+:m/z=510.2;実測値510.2。
2-(2,3-ジヒドロ-1,4-ベンゾジオキシン-6-イル)-6-(5-{[(2-ヒドロキシエチル)アミノ]メチル}-7-メチル-1,3-ベンゾオキサゾール-2-イル)ベンゾニトリル
テトラヒドロフラン(0.1mL)及びメタノール(0.1mL)中の、(2S)-1-{[2-(2-メチルビフェニル-3-イル)-1,3-ベンゾチアゾール-5-イル]メチル}ピペリジン-2-カルボン酸メチル(7.0mg、0.015mmol)の混合物に、水酸化リチウム水和物(8mg、0.2mmol)及び水(0.1mL)を添加した。得られた混合物を室温で一晩撹拌した。反応混合物をメタノールで希釈した後、分取HPLC(pH=2、アセトニトリル/水+TFA)により精製し、目的生成物をTFA塩として得た。C27H27N2O2Sに対するLC-MS計算値(M+H)+:m/z=443.2;実測値443.2。
この化合物は、2-(2-メチルビフェニル-3-イル)フロ[2,3-b]ピリジン-6-カルバルデヒドの代わりに2-(2-メチルビフェニル-3-イル)フロ[3,2-b]ピリジン-5-カルバルデヒド(ステップ2の生成物)、エタノールアミンの代わりに(S)-ピペリジン-2-カルボン酸を用いて、実施例1ステップ5の記載と同様の手順を使用して調製した。反応混合物をMeOHで希釈した後、分取HPLC(pH=2、アセトニトリル/水+TFA)により精製し、目的生成物をTFA塩として得た。C27H27N2O3に対するLC-MS計算値(M+H)+:m/z=427.2;実測値427.2。
2-({[2-(2-メチルビフェニル-3-イル)フロ[3,2-b]ピリジン-5-イル]メチル}アミノ)エタノール
この化合物は、2-(2-メチルビフェニル-3-イル)フロ[2,3-b]ピリジン-6-カルバルデヒドの代わりに4-メチル-2-(2-メチルビフェニル-3-イル)-1,3-ベンゾチアゾール-6-カルバルデヒド(ステップ3の生成物)、エタノールアミンの代わりに(S)-ピペリジン-2-カルボン酸を用いて、実施例1ステップ5の記載と同様の手順を使用して調製した。反応混合物をメタノールで希釈した後、分取HPLC(pH=10、アセトニトリル/水+NH4OH)により精製し、目的生成物を得た。C28H29N2O2Sに対するLC-MS計算値(M+H)+:m/z=457.2;実測値457.2。
2-({[4-メチル-2-(2-メチルビフェニル-3-イル)-1,3-ベンゾチアゾール-6-イル]メチル}アミノ)エタノール
この化合物は、2-(2-メチルビフェニル-3-イル)フロ[2,3-b]ピリジン-6-カルバルデヒドの代わりに6-(2-メチルビフェニル-3-イル)フロ[2,3-b]ピラジン-2-カルバルデヒド(ステップ3の生成物)を用いて、実施例1ステップ5の記載と同様の手順を使用して調製した。反応混合物をメタノールで希釈した後、分取HPLC(pH=10、アセトニトリル/水+NH4OH)により精製し、目的生成物を得た。C22H22N3O2に対するLC-MS計算値(M+H)+:m/z=360.2;実測値360.2。
(2S)-1-{[6-(2-メチルビフェニル-3-イル)フロ[2,3-b]ピラジン-2-イル]メチル}ピペリジン-2-カルボン酸
この化合物は、2-(2-メチルビフェニル-3-イル)フロ[2,3-b]ピリジン-6-カルバルデヒドの代わりに{[5-ホルミル-2-(2-メチルビフェニル-3-イル)-1,3-ベンゾオキサゾール-6-イル]オキシ}アセトニトリル(ステップ6の生成物)を、ステップ5でエタノールアミンの代わりに(S)-ピペリジン-2-カルボン酸を用いて、実施例1の記載と同様の手順を使用して調製した。反応混合物をメタノールで希釈した後、分取HPLC(pH=10、アセトニトリル/水+NH4OH)により精製し、目的生成物を得た。C29H28N3O4に対するLC-MS計算値(M+H)+:m/z=482.2;実測値482.2。
{[5-{[(2-ヒドロキシエチル)アミノ]メチル}-2-(2-メチルビフェニル-3-イル)-1,3-ベンゾオキサゾール-6-イル]オキシ}アセトニトリル
(2S)-1-{[6-(3-シアノプロポキシ)-2-(2-メチルビフェニル-3-イル)-1,3-ベンゾオキサゾール-5-イル]メチル}ピペリジン-2-カルボン酸
3-({[5-{[(2-ヒドロキシエチル)アミノ]メチル}-2-(2-メチルビフェニル-3-イル)-1,3-ベンゾオキサゾール-6-イル]オキシ}メチル)ベンゾニトリル
2-({[2-(2-メチルビフェニル-3-イル)-6-(ピリジン-2-イルメトキシ)-1,3-ベンゾオキサゾール-5-イル]メチル}アミノ)エタノール
2-({[6-メトキシ-2-(2-メチルビフェニル-3-イル)-1,3-ベンゾオキサゾール-5-イル]メチル}アミノ)エタノール
2-({[2-(2-メチルビフェニル-3-イル)-6-(2-モルホリン-4-イルエトキシ)-1,3-ベンゾオキサゾール-5-イル]メチル}アミノ)エタノール
この化合物は、ステップ5で2-(2-メチルビフェニル-3-イル)フロ[2,3-b]ピリジン-6-カルバルデヒドの代わりに2-(2-メチルビフェニル-3-イル)[1,3]オキサゾロ[5,4-c]ピリジン-6-カルバルデヒド(ステップ3の生成物)を用いて、実施例1の記載と同様の手順を使用して調製した。反応混合物をMeOHで希釈した後、分取HPLC(pH=2、アセトニトリル/水+TFA)により精製し、目的生成物をTFA塩として得た。C22H22N3O2に対するLC-MS計算値(M+H)+:m/z=360.2;実測値360.1。
この化合物は、ステップ5で2-(2-メチルビフェニル-3-イル)フロ[2,3-b]ピリジン-6-カルバルデヒドの代わりに4-{[5-ホルミル-7-メチル-2-(2-メチルビフェニル-3-イル)-1,3-ベンゾオキサゾール-6-イル]オキシ}ブタンニトリル(ステップ3の生成物)を用いて、実施例1の記載と同様の手順を使用して調製した。反応混合物をMeOHで希釈した後、分取HPLC(pH=10、アセトニトリル/水+NH4OH)により精製し、目的生成物を得た。C28H30N3O3に対するLC-MS計算値(M+H)+:m/z=456.2;実測値456.2。
(2S)-1-({6-(シアノメトキシ)-2-[4-(2,3-ジヒドロ-1,4-ベンゾジオキシン-6-イル)-3-メチルピリジン-2-イル]-1,3-ベンゾオキサゾール-5-イル}メチル)ピペリジン-2-カルボン酸
この化合物は、最後のステップで2-(2-メチルビフェニル-3-イル)フロ[2,3-b]ピリジン-6-カルバルデヒドの代わりに({2-[4-(2,3-ジヒドロ-1,4-ベンゾジオキシン-6-イル)-3-メチルピリジン-2-イル]-5-ホルミル-1,3-ベンゾオキサゾール-6-イル}オキシ)アセトニトリル(ステップ2の生成物)を用いて、実施例2の記載と同様の手順を使用して調製した。反応混合物をMeOHで希釈した後、分取HPLC(pH=2、アセトニトリル/水+TFA)により精製し、目的生成物をTFA塩として得た。C30H29N4O6に対するLC-MS計算値(M+H)+:m/z=541.2;実測値541.3。
(2S)-1-({6-(シアノメトキシ)-2-[3-(2,3-ジヒドロ-1,4-ベンゾジオキシン-6-イル)-2-メチルフェニル]-1,3-ベンゾオキサゾール-5-イル}メチル)ピペリジン-2-カルボン酸
(2S)-1-{[2-[2-シアノ-3-(2,3-ジヒドロ-1,4-ベンゾジオキシン-6-イル)フェニル]-6-(シアノメトキシ)-1,3-ベンゾオキサゾール-5-イル]メチル}ピペリジン-2-カルボン酸
この化合物は、最後のステップで{[5-ホルミル-2-(2-メチルビフェニル-3-イル)-1,3-ベンゾオキサゾール-6-イル]オキシ}アセトニトリルの代わりに2-[6-(シアノメトキシ)-5-ホルミル-1,3-ベンゾオキサゾール-2-イル]-6-(2,3-ジヒドロ-1,4-ベンゾジオキシン-6-イル)ベンゾニトリル(ステップ5の生成物)を用いて、実施例26の記載と同様の手順を使用して調製した。反応混合物をMeOHで希釈した後、分取HPLC(pH=10、アセトニトリル/水+NH4OH)により精製し、目的生成物を得た。C31H27N4O6に対するLC-MS計算値(M+H)+:m/z=551.2;実測値551.2。
この化合物は、ステップ5で2-(2-メチルビフェニル-3-イル)フロ[2,3-b]ピリジン-6-カルバルデヒドの代わりに2-(2-メチルビフェニル-3-イル)-1,3-ベンゾオキサゾール-6-カルバルデヒド(ステップ2の生成物)を用いて、実施例2の記載と同様の手順を使用して調製した。反応混合物をMeOHで希釈した後、分取HPLC(pH=10、アセトニトリル/水+NH4OH)により精製し、目的生成物を得た。C27H27N2O3に対するLC-MS計算値(M+H)+:m/z=427.2;実測値427.1。
tert-ブチルアルコール(0.1mL)と水(0.05mL)との混合溶媒中の、[(2-(3-ブロモ-2-メチルフェニル)-5-{[(2-ヒドロキシエチル)アミノ]メチル}-1,3-ベンゾオキサゾール-6-イル)オキシ]アセトニトリル(10.7mg、0.0257mmol)、(2-フルオロフェニル)ボロン酸(4.32mg、0.0308mmol)、ジクロロ[1,1’-ビス(ジシクロヘキシルホスフィノ)フェロセン]パラジウム(II)(0.97mg、0.0013mmol)、及び炭酸ナトリウム(6.81mg、0.0643mmol)のN2脱気溶液を3時間かけて100℃に加熱した。反応物を室温に冷却した。反応混合物をMeOHで希釈した後、分取HPLC(pH=2、アセトニトリル/水+TFA)により精製し、目的生成物をTFA塩として得た。C25H23FN3O3に対するLC-MS計算値(M+H)+:m/z=432.2;実測値432.2。
[(2-(3-シクロヘキサ-1-エン-1-イル-2-メチルフェニル)-5-{[(2-ヒドロキシエチル)アミノ]メチル}-1,3-ベンゾオキサゾール-6-イル)オキシ]アセトニトリル
本アッセイは、最終容積20μLの標準的な黒色384ウェルポリスチレンプレート中で実施した。最初に阻害剤をDMSOで連続希釈してからプレートのウェルに添加し、その後、他の反応成分を添加した。アッセイ時のDMSOの最終濃度は1%であった。0.05%Tween(登録商標)-20及び0.1%BSAを加えたPBS緩衝液(pH7.4)中、25℃でアッセイを実施した。組換えヒトPD-L1タンパク質(19-238)のC末端にHisタグを付加したもの(PD1-H5229)をAcroBiosystemsから購入した。組換えヒトPD-1タンパク質(25-167)のC末端にFcタグを付加したもの(PD1-H5257)もAcroBiosystemsから購入した。PD-L1タンパク質及びPD-1タンパク質をアッセイ緩衝液で希釈し、10μLをプレートのウェルに添加した。プレートを遠心分離し、タンパク質を阻害剤と40分間プレインキュベートした。インキュベーションに続いて、Fcに特異的なユーロピウムクリプテート標識抗ヒトIgG(PerkinElmer-AD0212)、及びSureLight(登録商標)-アロフィコシアニン(APC、PerkinElmer-AD0059H)にコンジュゲートした抗His抗体を補充したHTRF検出緩衝液10μLを添加した。遠心分離後、プレートを25℃で60分間インキュベートした後、PHERAstar FSプレートリーダー(665nm/620nm比)で読み取った。アッセイ時の最終濃度は、PD1が3nM、PD-L1が10nM、ユーロピウム抗ヒトIgGが1nM、及び抗His-アロフィコシアニンが20nMであった。GraphPad Prism 5.0ソフトウェアを使用して、阻害剤濃度の対数に対する対照の活性比の曲線をフィッティングすることによりIC50の測定を実施した。
[態様1]
式(I’):
[式中:
X 1 及びX 2 の一方はOまたはSであり、X 1 及びX 2 の他方はN、CR 1 、またはCR 2 であり;
X 3 はNまたはCR 3 であり;
X 4 はNまたはCR 4 であり;
X 5 はNまたはCR 5 であり;
X 6 はNまたはCR 6 であり;
X 1 、X 2 、X 3 、X 4 、X 5 、及びX 6 の少なくとも1つはNであり;
Y 1 はNまたはCR 8a であり;
Y 2 はNまたはCR 8b であり;
Y 3 はNまたはCR 8c であり;
Cyは、C 6-10 アリール、C 3-10 シクロアルキル、5~14員ヘテロアリール、または4~10員ヘテロシクロアルキルであり、それぞれが場合により1、2、3、4、または5個の独立して選択されるR 7 置換基で置換され;
R 1 、R 2 、R 8a 、R 8b 、及びR 8c はそれぞれ独立して、H、C 1-4 アルキル、C 3-6 シクロアルキル、C 3-6 シクロアルキル-C 1-4 アルキル-、C 6-10 アリール、C 6-10 アリール-C 1-4 アルキル-、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、(5~10員ヘテロアリール)-C 1-4 アルキル-、(4~10員ヘテロシクロアルキル)-C 1-4 アルキル-、C 2-4 アルケニル、C 2-4 アルキニル、ハロ、CN、OR 10 、C 1-4 ハロアルキル、C 1-4 ハロアルコキシ、NH 2 、-NHR 10 、-NR 10 R 10 、NHOR 10 、C(O)R 10 、C(O)NR 10 R 10 、C(O)OR 10 、OC(O)R 10 、OC(O)NR 10 R 10 、NR 10 C(O)R 10 、NR 10 C(O)OR 10 、NR 10 C(O)NR 10 R 10 、C(=NR 10 )R 10 、C(=NR 10 )NR 10 R 10 、NR 10 C(=NR 10 )NR 10 R 10 、NR 10 S(O)R 10 、NR 10 S(O) 2 R 10 、NR 10 S(O) 2 NR 10 R 10 、S(O)R 10 、S(O)NR 10 R 10 、S(O) 2 R 10 、及びS(O) 2 NR 10 R 10 から選択され、ここで、各R 10 は独立して、H、C 1-4 アルキル、C 2-4 アルケニル、C 2-4 アルキニル、C 1-4 アルコキシ、C 3-6 シクロアルキル、C 3-6 シクロアルキル-C 1-4 アルキル-、C 6-10 アリール、C 6-10 アリール-C 1-4 アルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、(5~10員ヘテロアリール)-C 1-4 アルキル-、及び(4~10員ヘテロシクロアルキル)-C 1-4 アルキル-から選択され、R 1 、R 2 、R 8a 、R 8b 、R 10 、及びR 8c のC 1-4 アルキル、C 2-4 アルケニル、C 2-4 アルキニル、C 1-4 アルコキシ、C 3-6 シクロアルキル、C 3-6 シクロアルキル-C 1-4 アルキル-、C 6-10 アリール、C 6-10 アリール-C 1-4 アルキル-、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、(5~10員ヘテロアリール)-C 1-4 アルキル-、及び(4~10員ヘテロシクロアルキル)-C 1-4 アルキル-は、それぞれ場合により1、2、または3個の独立して選択されるR d 置換基で置換され;
R 9 は、Cl、Br、I、C 1-6 アルキル、C 2-6 アルケニル、C 2-6 アルキニル、C 1-6 ハロアルキル、C 1-6 ハロアルコキシ、C 6-10 アリール、C 3-10 シクロアルキル、5~14員ヘテロアリール、4~10員ヘテロシクロアルキル、C 6-10 アリール-C 1-4 アルキル-、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~14員ヘテロアリール)-C 1-4 アルキル-、(4~10員ヘテロシクロアルキル)-C 1-4 アルキル-、CN、NO 2 、OR 11a 、SR 11 、NH 2 、-NHR 11 、-NR 11 R 11 、NHOR 11 、C(O)R 11 、C(O)NR 11 R 11 、C(O)OR 11 、OC(O)R 11 、OC(O)NR 11 R 11 、NR 11 C(O)R 11 、NR 11 C(O)OR 11 、NR 11 C(O)NR 11 R 11 、C(=NR 11 )R 11 、C(=NR 11 )NR 11 R 11 、NR 11 C(=NR 11 )NR 11 R 11 、NR 11 S(O)R 11 、NR 11 S(O) 2 R 11 、NR 11 S(O) 2 NR 11 R 11 、S(O)R 11 、S(O)NR 11 R 11 、S(O) 2 R 11 、及びS(O) 2 NR 11 R 11 であり、ここで、R 9 のC 1-6 アルキル、C 2-6 アルケニル、C 2-6 アルキニル、C 1-6 ハロアルキル、C 1-6 ハロアルコキシ、C 6-10 アリール、C 3-10 シクロアルキル、5~14員ヘテロアリール、4~10員ヘテロシクロアルキル、C 6-10 アリール-C 1-4 アルキル-、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~14員ヘテロアリール)-C 1-4 アルキル-、及び(4~10員ヘテロシクロアルキル)-C 1-4 アルキル-は、それぞれ場合により1、2、または3個のR b 置換基で置換され;
各R 11 は独立して、H、C 1-6 アルキル、C 1-6 ハロアルキル、C 2-6 アルケニル、C 2-6 アルキニル、C 6-10 アリール、C 3-10 シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C 6-10 アリール-C 1-4 アルキル-、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~10員ヘテロアリール)-C 1-4 アルキル-、及び(4~10員ヘテロシクロアルキル)-C 1-4 アルキル-から選択され、ここで、R 11 のC 1-6 アルキル、C 2-6 アルケニル、C 2-6 アルキニル、C 6-10 アリール、C 3-10 シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C 6-10 アリール-C 1-4 アルキル-、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~10員ヘテロアリール)-C 1-4 アルキル-、及び(4~10員ヘテロシクロアルキル)-C 1-4 アルキル-は、それぞれ場合により1、2、または3個の独立して選択されるR b 置換基で置換され;
R 11a は、C 1-6 アルキル、C 1-6 ハロアルキル、C 2-6 アルケニル、C 2-6 アルキニル、C 6-10 アリール、C 3-10 シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C 6-10 アリール-C 1-4 アルキル-、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~10員ヘテロアリール)-C 1-4 アルキル-、及び(4~10員ヘテロシクロアルキル)-C 1-4 アルキル-から選択され、それぞれが場合により1、2、または3個の独立して選択されるR b 置換基で置換され;
R 3 、R 4 、R 5 、R 6 、及びR 7 はそれぞれ独立して、H、ハロ、C 1-6 アルキル、C 2-6 アルケニル、C 2-6 アルキニル、C 1-6 ハロアルキル、C 1-6 ハロアルコキシ、C 6-10 アリール、C 3-10 シクロアルキル、5~14員ヘテロアリール、4~10員ヘテロシクロアルキル、C 6-10 アリール-C 1-4 アルキル-、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~14員ヘテロアリール)-C 1-4 アルキル-、(4~10員ヘテロシクロアルキル)-C 1-4 アルキル-、CN、NO 2 、OR a 、SR a 、NHOR a 、C(O)R a 、C(O)NR a R a 、C(O)OR a 、OC(O)R a 、OC(O)NR a R a 、NHR a 、NR a R a 、NR a C(O)R a 、NR a C(O)OR a 、NR a C(O)NR a R a 、C(=NR a )R a 、C(=NR a )NR a R a 、NR a C(=NR a )NR a R a 、NR a S(O)R a 、NR a S(O) 2 R a 、NR a S(O) 2 NR a R a 、S(O)R a 、S(O)NR a R a 、S(O) 2 R a 、及びS(O) 2 NR a R a から選択され、ここで、R 3 、R 4 、R 5 、R 6 、及びR 7 のC 1-6 アルキル、C 2-6 アルケニル、C 2-6 アルキニル、C 6-10 アリール、C 3-10 シクロアルキル、5~14員ヘテロアリール、4~10員ヘテロシクロアルキル、C 6-10 アリール-C 1-4 アルキル-、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~14員ヘテロアリール)-C 1-4 アルキル-、及び(4~10員ヘテロシクロアルキル)-C 1-4 アルキル-は、それぞれ場合により1、2、3、または4個のR b 置換基で置換され、ただしその場合、R 3 、R 4 、R 5 、及びR 6 の少なくとも1つはH以外であるか;
または、Cy環上の2つの隣接するR 7 置換基は、それらが結合する原子とともに縮合フェニル環、縮合5~7員ヘテロシクロアルキル環、縮合5員もしくは6員ヘテロアリール環、または縮合C 5-6 シクロアルキル環を形成し、その場合、縮合5~7員ヘテロシクロアルキル環及び縮合5員または6員ヘテロアリール環はそれぞれ、環員としてN、O、及びSから選択される1~4個のヘテロ原子を有し、縮合フェニル環、縮合5~7員ヘテロシクロアルキル環、縮合5員または6員ヘテロアリール環、及び縮合C 5-6 シクロアルキル環は、それぞれ場合により1、2、または3個の独立して選択されるR b 置換基で置換され;
各R a は独立して、H、CN、C 1-6 アルキル、C 1-4 ハロアルキル、C 2-6 アルケニル、C 2-6 アルキニル、C 6-10 アリール、C 3-10 シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C 6-10 アリール-C 1-4 アルキル-、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~10員ヘテロアリール)-C 1-4 アルキル-、及び(4~10員ヘテロシクロアルキル)-C 1-4 アルキル-から選択され、ここで、R a のC 1-6 アルキル、C 2-6 アルケニル、C 2-6 アルキニル、C 6-10 アリール、C 3-10 シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C 6-10 アリール-C 1-4 アルキル-、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~10員ヘテロアリール)-C 1-4 アルキル-、及び(4~10員ヘテロシクロアルキル)-C 1-4 アルキル-は、それぞれ場合により1、2、3、4、または5個のR d 置換基で置換され;
各R d は独立して、C 1-6 アルキル、C 1-6 ハロアルキル、ハロ、C 6-10 アリール、5~10員ヘテロアリール、C 3-10 シクロアルキル、4~10員ヘテロシクロアルキル、C 6-10 アリール-C 1-4 アルキル-、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~10員ヘテロアリール)-C 1-4 アルキル-、(4~10員ヘテロシクロアルキル)-C 1-4 アルキル-、CN、NH 2 、NHOR e 、OR e 、SR e 、C(O)R e 、C(O)NR e R e 、C(O)OR e 、OC(O)R e 、OC(O)NR e R e 、NHR e 、NR e R e 、NR e C(O)R e 、NR e C(O)NR e R e 、NR e C(O)OR e 、C(=NR e )NR e R e 、NR e C(=NR e )NR e R e 、NR e C(=NOH)NR e R e 、NR e C(=NCN)NR e R e 、S(O)R e 、S(O)NR e R e 、S(O) 2 R e 、NR e S(O) 2 R e 、NR e S(O) 2 NR e R e 、及びS(O) 2 NR e R e から選択され、ここで、R d のC 1-6 アルキル、C 1-6 ハロアルキル、C 6-10 アリール、5~10員ヘテロアリール、C 3-10 シクロアルキル、4~10員ヘテロシクロアルキル、C 6-10 アリール-C 1-4 アルキル-、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~10員ヘテロアリール)-C 1-4 アルキル-、及び(4~10員ヘテロシクロアルキル)-C 1-4 アルキル-は、それぞれ場合により1~3個の独立して選択されるR h 置換基で置換され;
各R b 置換基は独立して、ハロ、C 1-4 アルキル、C 1-4 ハロアルキル、C 1-4 ハロアルコキシ、C 6-10 アリール、C 3-10 シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C 6-10 アリール-C 1-4 アルキル-、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~10員ヘテロアリール)-C 1-4 アルキル-、(4~10員ヘテロシクロアルキル)-C 1-4 アルキル-、CN、OH、NH 2 、NO 2 、NHOR c 、OR c 、SR c 、C(O)R c 、C(O)NR c R c 、C(O)OR c 、OC(O)R c 、OC(O)NR c R c 、C(=NR c )NR c R c 、NR c C(=NR c )NR c R c 、NHR c 、NR c R c 、NR c C(O)R c 、NR c C(O)OR c 、NR c C(O)NR c R c 、NR c S(O)R c 、NR c S(O) 2 R c 、NR c S(O) 2 NR c R c 、S(O)R c 、S(O)NR c R c 、S(O) 2 R c 、及びS(O) 2 NR c R c から選択され;ここで、R b のC 1-4 アルキル、C 1-4 ハロアルキル、C 1-4 ハロアルコキシ、C 6-10 アリール、C 3-10 シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C 6-10 アリール-C 1-4 アルキル-、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~10員ヘテロアリール)-C 1-4 アルキル-、及び(4~10員ヘテロシクロアルキル)-C 1-4 アルキル-は、それぞれさらに場合により1~3個の独立して選択されるR d 置換基で置換され;
各R c は独立して、H、C 1-6 アルキル、C 1-4 ハロアルキル、C 2-6 アルケニル、C 2-6 アルキニル、C 6-10 アリール、C 3-10 シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C 6-10 アリール-C 1-4 アルキル-、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~10員ヘテロアリール)-C 1-4 アルキル-、及び(4~10員ヘテロシクロアルキル)-C 1-4 アルキル-から選択され、ここで、R c のC 1-6 アルキル、C 2-6 アルケニル、C 2-6 アルキニル、C 6-10 アリール、C 3-10 シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C 6-10 アリール-C 1-4 アルキル-、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~10員ヘテロアリール)-C 1-4 アルキル-、及び(4~10員ヘテロシクロアルキル)-C 1-4 アルキル-は、それぞれ場合により、C 1-4 アルキル、C 1-4 ハロアルキル、C 2-6 アルケニル、C 2-6 アルキニル、C 6-10 アリール、C 3-10 シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C 6-10 アリール-C 1-4 アルキル-、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~10員ヘテロアリール)-C 1-4 アルキル-、(4-10員ヘテロシクロアルキル)-C 1-4 アルキル-、ハロ、CN、NHOR g 、OR g 、SR g 、C(O)R g 、C(O)NR g R g 、C(O)OR g 、OC(O)R g 、OC(O)NR g R g 、NHR g 、NR g R g 、NR g C(O)R g 、NR g C(O)NR g R g 、NR g C(O)OR g 、C(=NR g )NR g R g 、NR g C(=NR g )NR g R g 、S(O)R g 、S(O)NR g R g 、S(O) 2 R g 、NR g S(O) 2 R g 、NR g S(O) 2 NR g R g 、及びS(O) 2 NR g R g から独立して選択される1、2、3、4、または5個のR f 置換基で置換され;その場合、R f のC 1-4 アルキル、C 1-4 ハロアルキル、C 2-6 アルケニル、C 2-6 アルキニル、C 6-10 アリール、C 3-10 シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C 6-10 アリール-C 1-4 アルキル-、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~10員ヘテロアリール)-C 1-4 アルキル-、及び(4~10員ヘテロシクロアルキル)-C 1-4 アルキル-は、それぞれ場合により、C 1-4 アルキル、C 1-4 ハロアルキル、ハロ、CN、R o 、NHOR o 、OR o 、SR o 、C(O)R o 、C(O)NR o R o 、C(O)OR o 、OC(O)R o 、OC(O)NR o R o 、NHR o 、NR o R o 、NR o C(O)R o 、NR o C(O)NR o R o 、NR o C(O)OR o 、C(=NR o )NR o R o 、NR o C(=NR o )NR o R o 、S(O)R o 、S(O)NR o R o 、S(O) 2 R o 、NR o S(O) 2 R o 、NR o S(O) 2 NR o R o 、及びS(O) 2 NR o R o から独立して選択される1、2、3、4、または5個のR n 置換基で置換され;
各R g は独立して、H、C 1-6 アルキル、C 1-4 ハロアルキル、C 2-6 アルケニル、C 2-6 アルキニル、C 6-10 アリール、C 3-10 シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C 6-10 アリール-C 1-4 アルキル-、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~10員ヘテロアリール)-C 1-4 アルキル-、及び(4~10員ヘテロシクロアルキル)-C 1-4 アルキル-から選択され、ここで、R g のC 1-6 アルキル、C 2-6 アルケニル、C 2-6 アルキニル、C 6-10 アリール、C 3-10 シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C 6-10 アリール-C 1-4 アルキル-、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~10員ヘテロアリール)-C 1-4 アルキル-、及び(4~10員ヘテロシクロアルキル)-C 1-4 アルキル-は、それぞれ場合により、C 1-6 アルキル、C 1-6 ハロアルキル、C 2-6 アルケニル、C 2-6 アルキニル、C 6-10 アリール、C 3-10 シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C 6-10 アリール-C 1-4 アルキル-、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~10員ヘテロアリール)-C 1-4 アルキル-、(4-10員ヘテロシクロアルキル)-C 1-4 アルキル-、ハロ、CN、NHOR r 、OR r 、SR r 、C(O)R r 、C(O)NR r R r 、C(O)OR r 、OC(O)R r 、OC(O)NR r R r 、NHR r 、NR r R r 、NR r C(O)R r 、NR r C(O)NR r R r 、NR r C(O)OR r 、C(=NR r )NR r R r 、NR r C(=NR r )NR r R r 、NR r C(=NOH)NR r R r 、NR r C(=NCN)NR r R r 、S(O)R r 、S(O)NR r R r 、S(O) 2 R r 、NR r S(O) 2 R r 、NR r S(O) 2 NR r R r 、及びS(O) 2 NR r R r から独立して選択される1~3個のR p 置換基で置換され、R p のC 1-6 アルキル、C 1-6 ハロアルキル、C 2-6 アルケニル、C 2-6 アルキニル、C 6-10 アリール、C 3-10 シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C 6-10 アリール-C 1-4 アルキル-、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~10員ヘテロアリール)-C 1-4 アルキル-、及び(4~10員ヘテロシクロアルキル)-C 1-4 アルキル-は、場合により1、2、または3個のR q 置換基で置換されるか;
あるいは、任意の2つのR a 置換基はそれらが結合する窒素原子とともに、4員、5員、6員、7員、8員、9員、または10員ヘテロシクロアルキル基を形成し、それらの基は場合により、C 1-6 アルキル、C 3-10 シクロアルキル、4~7員ヘテロシクロアルキル、C 6-10 アリール、5~6員ヘテロアリール、C 6-10 アリール-C 1-4 アルキル-、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~6員ヘテロアリール)-C 1-4 アルキル-、(4~7員ヘテロシクロアルキル)-C 1-4 アルキル-、C 1-6 ハロアルキル、C 1-6 ハロアルコキシ、C 2-6 アルケニル、C 2-6 アルキニル、ハロ、CN、OR i 、SR i 、NHOR i 、C(O)R i 、C(O)NR i R i 、C(O)OR i 、OC(O)R i 、OC(O)NR i R i 、NHR i 、NR i R i 、NR i C(O)R i 、NR i C(O)NR i R i 、NR i C(O)OR i 、C(=NR i )NR i R i 、NR i C(=NR i )NR i R i 、S(O)R i 、S(O)NR i R i 、S(O) 2 R i 、NR i S(O) 2 R i 、NR i S(O) 2 NR i R i 、及びS(O) 2 NR i R i から独立して選択される1、2、または3個のR h 置換基で置換されており、ここで、R h のC 1-6 アルキル、C 2-6 アルケニル、C 2-6 アルキニル、C 3-10 シクロアルキル、4~7員ヘテロシクロアルキル、C 6-10 アリール、5~6員ヘテロアリール、C 6-10 アリール-C 1-4 アルキル-、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~6員ヘテロアリール)-C 1-4 アルキル-、及び(4~7員ヘテロシクロアルキル)-C 1-4 アルキル-は、それぞれさらに場合により、C 3-6 シクロアルキル、C 6-10 アリール、5員または6員ヘテロアリール、4~7員ヘテロシクロアルキル、C 2-4 アルケニル、C 2-4 アルキニル、ハロ、C 1-4 アルキル、C 1-4 ハロアルキル、CN、NHOR k 、OR k 、SR k 、C(O)R k 、C(O)NR k R k 、C(O)OR k 、OC(O)R k 、OC(O)NR k R k 、NHR k 、NR k R k 、NR k C(O)R k 、NR k C(O)NR k R k 、NR k C(O)OR k 、C(=NR k )NR k R k 、NR k C(=NR k )NR k R k 、S(O)R k 、S(O)NR k R k 、S(O) 2 R k 、NR k S(O) 2 R k 、NR k S(O) 2 NR k R k 、及びS(O) 2 NR k R k から独立して選択される1、2、または3個のR j 置換基で置換され、R j のC 1-4 アルキル、C 3-6 シクロアルキル、C 6-10 アリール、5員または6員ヘテロアリール、4~6員ヘテロシクロアルキル、C 2-4 アルケニル、C 2-4 アルキニル、C 1-4 ハロアルキル、及びC 1-4 ハロアルコキシは、それぞれ場合により1、2、または3個の独立して選択されるR q 置換基で置換されるか;または、4~10員ヘテロシクロアルキルの同じ炭素原子に結合する2つのR h 基は、それらが結合する炭素原子とともに、O、N、及びSから選択される1~2個のヘテロ原子を環員として有するC 3-6 シクロアルキルもしくは4~6員ヘテロシクロアルキルを形成するか;
あるいは、任意の2つのR c 置換基はそれらが結合する窒素原子とともに、4員、5員、6員、または7員ヘテロシクロアルキル基を形成し、それらの基は場合により1、2、または3個の独立して選択されるR h 置換基で置換されるか;
あるいは、任意の2つのR e 置換基はそれらが結合する窒素原子とともに、4員、5員、6員、または7員ヘテロシクロアルキル基を形成し、それらの基は場合により1、2、または3個の独立して選択されるR h 置換基で置換されるか;
あるいは、任意の2つのR g 置換基はそれらが結合する窒素原子とともに、4員、5員、6員、または7員ヘテロシクロアルキル基を形成し、それらの基は場合により1、2、または3個の独立して選択されるR h 置換基で置換されるか;
あるいは、任意の2つのR i 置換基はそれらが結合する窒素原子とともに、4員、5員、6員、または7員ヘテロシクロアルキル基を形成し、それらの基は場合により1、2、または3個の独立して選択されるR h 置換基で置換されるか;
あるいは、任意の2つのR k 置換基はそれらが結合する窒素原子とともに、4員、5員、6員、または7員ヘテロシクロアルキル基を形成し、それらの基は場合により1、2、または3個の独立して選択されるR h 置換基で置換されるか;
あるいは、任意の2つのR o 置換基はそれらが結合する窒素原子とともに、4員、5員、6員、または7員ヘテロシクロアルキル基を形成し、それらの基は場合により1、2、または3個の独立して選択されるR h 置換基で置換されており;
各R e 、R i 、R k 、R o 、またはR p は独立して、H、C 1-4 アルキル、C 3-6 シクロアルキル、C 6-10 アリール、5員または6員ヘテロアリール、4~7員ヘテロシクロアルキル、C 1-4 ハロアルキル、C 2-4 アルケニル、及びC 2-4 アルキニルから選択され、ここで、R e 、R i 、R k 、R o 、またはR p のC 1-4 アルキル、C 3-6 シクロアルキル、C 6-10 アリール、5員または6員ヘテロアリール、4~7員ヘテロシクロアルキル、C 2-4 アルケニル、及びC 2-4 アルキニルは、それぞれ場合により1、2、または3個のR q 置換基で置換され;
各R q は独立して、OH、CN、-COOH、NH 2 、ハロ、C 1-6 ハロアルキル、C 1-6 アルキル、C 1-6 アルコキシ、C 1-6 アルキルチオ、フェニル、5~6員ヘテロアリール、4~6員ヘテロシクロアルキル、C 3-6 シクロアルキル、NHR 12 、NR 12 R 12 、及びC 1-4 ハロアルコキシから選択され、ここで、R q のC 1-6 アルキル、フェニル、C 3-6 シクロアルキル、4~6員ヘテロシクロアルキル、及び5~6員ヘテロアリールは、それぞれ場合により、ハロ、OH、CN、-COOH、NH 2 、C 1-4 アルキル、C 1-4 アルコキシ、C 1-4 ハロアルキル、C 1-4 ハロアルコキシ、フェニル、C 3-10 シクロアルキル、5~6員ヘテロアリール、及び4~6員ヘテロシクロアルキルで置換され、各R 12 は独立してC 1-6 アルキルであり;
式(I’)の部分
前記化合物は1-[3-(6-クロロ-2-ベンゾオキサゾリル)-5-(3,5-ジメチルフェニル)-4-ピリジニル]-4-ピペリジンアミンではない]。
[態様2]
態様1に記載の化合物、またはその薬学的に許容される塩もしくは立体異性体
[式中:
X 1 及びX 2 の一方はOまたはSであり、X 1 及びX 2 の他方はN、CR 1 、またはCR 2 であり;
X 3 はNまたはCR 3 であり;
X 4 はNまたはCR 4 であり;
X 5 はNまたはCR 5 であり;
X 6 はNまたはCR 6 であり;
X 1 、X 2 、X 3 、X 4 、X 5 、及びX 6 の少なくとも1つはNであり;
Y 1 はNまたはCR 8a であり;
Y 2 はNまたはCR 8b であり;
Y 3 はNまたはCR 8c であり;
Cyは、C 6-10 アリール、C 3-10 シクロアルキル、5~14員ヘテロアリール、または4~10員ヘテロシクロアルキルであり、それぞれが場合により1、2、3、4、または5個の独立して選択されるR 7 置換基で置換され;
R 1 、R 2 、R 8a 、R 8b 、及びR 8c はそれぞれ独立して、H、C 1-4 アルキル、C 3-6 シクロアルキル、C 2-4 アルケニル、C 2-4 アルキニル、ハロ、CN、OH、C 1-4 アルコキシ、C 1-4 ハロアルキル、C 1-4 ハロアルコキシ、NH 2 、-NH-C 1-4 アルキル、-N(C 1-4 アルキル) 2 、NHOR 10 、C(O)R 10 、C(O)NR 10 R 10 、C(O)OR 10 、OC(O)R 10 、OC(O)NR 10 R 10 、NR 10 C(O)R 10 、NR 10 C(O)OR 10 、NR 10 C(O)NR 10 R 10 、C(=NR 10 )R 10 、C(=NR 10 )NR 10 R 10 、NR 10 C(=NR 10 )NR 10 R 10 、NR 10 S(O)R 10 、NR 10 S(O) 2 R 10 、NR 10 S(O) 2 NR 10 R 10 、S(O)R 10 、S(O)NR 10 R 10 、S(O) 2 R 10 、及びS(O) 2 NR 10 R 10 から選択され、ここで、各R 10 は独立して、H、またはハロ、OH、CN、及びC 1-4 アルコキシから独立して選択される1個もしくは2個の基で場合により置換されるC 1-4 アルキルであり、かつ、R 1 、R 2 、R 8a 、R 8b 、またはR 8c のC 1-4 アルキル、C 3-4 シクロアルキル、C 2-4 アルケニル、及びC 2-4 アルキニルは、それぞれ場合により、ハロ、OH、CN、C 1-4 アルキル、及びC 1-4 アルコキシから独立して選択される1個または2個の置換基で置換され;
R 9 は、C 1-4 アルキル、Cl、Br、CN、シクロプロピル、C 2-4 アルキニル、C 1-4 ハロアルキル、C 1-4 ハロアルコキシ、NH 2 、-NH-C 1-4 アルキル、-N(C 1-4 アルキル) 2 、NHOR 11 、C(O)R 11 、C(O)NR 11 R 11 、C(O)OR 11 、OC(O)R 11 、OC(O)NR 11 R 11 、NR 11 C(O)R 11 、NR 11 C(O)OR 11 、NR 11 C(O)NR 11 R 11 、C(=NR 11 )R 11 、C(=NR 11 )NR 11 R 11 、NR 11 C(=NR 11 )NR 11 R 11 、NR 11 S(O)R 11 、NR 11 S(O) 2 R 11 、NR 11 S(O) 2 NR 11 R 11 、S(O)R 11 、S(O)NR 11 R 11 、S(O) 2 R 11 、及びS(O) 2 NR 11 R 11 であり、ここで、R 9 のC 1-4 アルキル、シクロプロピル、C 2-4 アルキニル、及びC 1-4 アルコキシは、それぞれ場合により、1個または2個のハロ、OH、CN、またはOCH 3 置換基で置換され、かつ、各R 11 は独立して、H、または1個もしくは2個のハロ、OH、CN、もしくはOCH 3 で場合により置換されるC 1-4 アルキルであり;
R 3 、R 4 、R 5 、R 6 、及びR 7 はそれぞれ独立して、H、ハロ、C 1-6 アルキル、C 2-6 アルケニル、C 2-6 アルキニル、C 1-6 ハロアルキル、C 1-6 ハロアルコキシ、C 6-10 アリール、C 3-10 シクロアルキル、5~14員ヘテロアリール、4~10員ヘテロシクロアルキル、C 6-10 アリール-C 1-4 アルキル-、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~14員ヘテロアリール)-C 1-4 アルキル-、(4~10員ヘテロシクロアルキル)-C 1-4 アルキル-、CN、NO 2 、OR a 、SR a 、NHOR a 、C(O)R a 、C(O)NR a R a 、C(O)OR a 、OC(O)R a 、OC(O)NR a R a 、NHR a 、NR a R a 、NR a C(O)R a 、NR a C(O)OR a 、NR a C(O)NR a R a 、C(=NR a )R a 、C(=NR a )NR a R a 、NR a C(=NR a )NR a R a 、NR a S(O)R a 、NR a S(O) 2 R a 、NR a S(O) 2 NR a R a 、S(O)R a 、S(O)NR a R a 、S(O) 2 R a 、及びS(O) 2 NR a R a から選択され、ここで、R 3 、R 4 、R 5 、R 6 、及びR 7 のC 1-6 アルキル、C 2-6 アルケニル、C 2-6 アルキニル、C 6-10 アリール、C 3-10 シクロアルキル、5~14員ヘテロアリール、4~10員ヘテロシクロアルキル、C 6-10 アリール-C 1-4 アルキル-、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~14員ヘテロアリール)-C 1-4 アルキル-、及び(4~10員ヘテロシクロアルキル)-C 1-4 アルキル-は、それぞれ場合により1、2、3、または4個のR b 置換基で置換され、ただしその場合、R 3 、R 4 、R 5 、及びR 6 の少なくとも1つはH以外であるか;
または、Cy環上の2つの隣接するR 7 置換基は、それらが結合する原子とともに縮合フェニル環、縮合5~7員ヘテロシクロアルキル環、縮合5員もしくは6員ヘテロアリール環、または縮合C 5-6 シクロアルキル環を形成し、その場合、縮合5~7員ヘテロシクロアルキル環及び縮合5員または6員ヘテロアリール環はそれぞれ、環員としてN、O、及びSから選択される1~4個のヘテロ原子を有し、縮合フェニル環、縮合5~7員ヘテロシクロアルキル環、縮合5員または6員ヘテロアリール環、及び縮合C 5-6 シクロアルキル環は、それぞれ場合により1個または2個の独立して選択されるR b 置換基で置換され;
各R a は独立して、H、CN、C 1-6 アルキル、C 1-4 ハロアルキル、C 2-6 アルケニル、C 2-6 アルキニル、C 6-10 アリール、C 3-10 シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C 6-10 アリール-C 1-4 アルキル-、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~10員ヘテロアリール)-C 1-4 アルキル-、及び(4~10員ヘテロシクロアルキル)-C 1-4 アルキル-から選択され、ここで、R a のC 1-6 アルキル、C 2-6 アルケニル、C 2-6 アルキニル、C 6-10 アリール、C 3-10 シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C 6-10 アリール-C 1-4 アルキル-、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~10員ヘテロアリール)-C 1-4 アルキル-、及び(4~10員ヘテロシクロアルキル)-C 1-4 アルキル-は、それぞれ場合により1、2、3、4、または5個のR d 置換基で置換され;
各R d は独立して、C 1-4 アルキル、C 1-4 ハロアルキル、ハロ、C 3-10 シクロアルキル、4-10員ヘテロシクロアルキル、CN、NH 2 、NHOR e 、OR e 、SR e 、C(O)R e 、C(O)NR e R e 、C(O)OR e 、OC(O)R e 、OC(O)NR e R e 、NHR e 、NR e R e 、NR e C(O)R e 、NR e C(O)NR e R e 、NR e C(O)OR e 、C(=NR e )NR e R e 、NR e C(=NR e )NR e R e 、S(O)R e 、S(O)NR e R e 、S(O) 2 R e 、NR e S(O) 2 R e 、NR e S(O) 2 NR e R e 、及びS(O) 2 NR e R e から選択され、ここで、R d のC 1-4 アルキル、C 3-10 シクロアルキル、及び4~10員ヘテロシクロアルキルは、それぞれさらに場合により1~3個の独立して選択されるR q 置換基で置換され;
各R b 置換基は独立して、ハロ、C 1-4 アルキル、C 1-4 ハロアルキル、C 1-4 ハロアルコキシ、C 6-10 アリール、C 3-10 シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C 6-10 アリール-C 1-4 アルキル-、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~10員ヘテロアリール)-C 1-4 アルキル-、(4~10員ヘテロシクロアルキル)-C 1-4 アルキル-、CN、OH、NH 2 、NO 2 、NHOR c 、OR c 、SR c 、C(O)R c 、C(O)NR c R c 、C(O)OR c 、OC(O)R c 、OC(O)NR c R c 、C(=NR c )NR c R c 、NR c C(=NR c )NR c R c 、NHR c 、NR c R c 、NR c C(O)R c 、NR c C(O)OR c 、NR c C(O)NR c R c 、NR c S(O)R c 、NR c S(O) 2 R c 、NR c S(O) 2 NR c R c 、S(O)R c 、S(O)NR c R c 、S(O) 2 R c 、及びS(O) 2 NR c R c から選択され;ここで、R b のC 1-4 アルキル、C 1-4 ハロアルキル、C 1-4 ハロアルコキシ、C 6-10 アリール、C 3-10 シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C 6-10 アリール-C 1-4 アルキル-、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~10員ヘテロアリール)-C 1-4 アルキル-、及び(4~10員ヘテロシクロアルキル)-C 1-4 アルキル-は、それぞれさらに場合により1~3個の独立して選択されるR d 置換基で置換され;
各R c は独立して、H、C 1-6 アルキル、C 1-4 ハロアルキル、C 2-6 アルケニル、C 2-6 アルキニル、C 6-10 アリール、C 3-10 シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C 6-10 アリール-C 1-4 アルキル-、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~10員ヘテロアリール)-C 1-4 アルキル-、及び(4~10員ヘテロシクロアルキル)-C 1-4 アルキル-から選択され、ここで、R c のC 1-6 アルキル、C 2-6 アルケニル、C 2-6 アルキニル、C 6-10 アリール、C 3-10 シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C 6-10 アリール-C 1-4 アルキル-、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~10員ヘテロアリール)-C 1-4 アルキル-、及び(4~10員ヘテロシクロアルキル)-C 1-4 アルキル-は、それぞれ場合により、C 1-4 アルキル、C 1-4 ハロアルキル、C 2-6 アルケニル、C 2-6 アルキニル、C 6-10 アリール、C 3-10 シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C 6-10 アリール-C 1-4 アルキル-、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~10員ヘテロアリール)-C 1-4 アルキル-、(4-10員ヘテロシクロアルキル)-C 1-4 アルキル-、ハロ、CN、NHOR g 、OR g 、SR g 、C(O)R g 、C(O)NR g R g 、C(O)OR g 、OC(O)R g 、OC(O)NR g R g 、NHR g 、NR g R g 、NR g C(O)R g 、NR g C(O)NR g R g 、NR g C(O)OR g 、C(=NR g )NR g R g 、NR g C(=NR g )NR g R g 、S(O)R g 、S(O)NR g R g 、S(O) 2 R g 、NR g S(O) 2 R g 、NR g S(O) 2 NR g R g 、及びS(O) 2 NR g R g から独立して選択される1、2、3、4、または5個のR f 置換基で置換され;その場合、R f のC 1-4 アルキル、C 1-4 ハロアルキル、C 2-6 アルケニル、C 2-6 アルキニル、C 6-10 アリール、C 3-10 シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C 6-10 アリール-C 1-4 アルキル-、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~10員ヘテロアリール)-C 1-4 アルキル-、及び(4~10員ヘテロシクロアルキル)-C 1-4 アルキル-は、それぞれ場合により、C 1-4 アルキル、C 1-4 ハロアルキル、ハロ、CN、R o 、NHOR o 、OR o 、SR o 、C(O)R o 、C(O)NR o R o 、C(O)OR o 、OC(O)R o 、OC(O)NR o R o 、NHR o 、NR o R o 、NR o C(O)R o 、NR o C(O)NR o R o 、NR o C(O)OR o 、C(=NR o )NR o R o 、NR o C(=NR o )NR o R o 、S(O)R o 、S(O)NR o R o 、S(O) 2 R o 、NR o S(O) 2 R o 、NR o S(O) 2 NR o R o 、及びS(O) 2 NR o R o から独立して選択される1、2、3、4、または5個のR n 置換基で置換され;
各R g は独立して、H、C 1-6 アルキル、C 1-4 ハロアルキル、C 2-6 アルケニル、C 2-6 アルキニル、C 6-10 アリール、C 3-10 シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C 6-10 アリール-C 1-4 アルキル-、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~10員ヘテロアリール)-C 1-4 アルキル-、及び(4~10員ヘテロシクロアルキル)-C 1-4 アルキル-から選択され、ここで、R g のC 1-6 アルキル、C 2-6 アルケニル、C 2-6 アルキニル、C 6-10 アリール、C 3-10 シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C 6-10 アリール-C 1-4 アルキル-、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~10員ヘテロアリール)-C 1-4 アルキル-、及び(4~10員ヘテロシクロアルキル)-C 1-4 アルキル-は、それぞれ場合により1~3個の独立して選択されるR p 置換基で置換されるか;
あるいは、任意の2つのR a 置換基はそれらが結合する窒素原子とともに、4員、5員、6員、7員、8員、9員、または10員ヘテロシクロアルキル基を形成し、それらの基は場合により、C 1-6 アルキル、C 3-10 シクロアルキル、4~7員ヘテロシクロアルキル、C 6-10 アリール、5~6員ヘテロアリール、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~6員ヘテロアリール)-C 1-4 アルキル-、(4~7員ヘテロシクロアルキル)-C 1-4 アルキル-、C 1-6 ハロアルキル、C 2-6 アルケニル、C 2-6 アルキニル、ハロ、CN、OR i 、SR i 、NHOR i 、C(O)R i 、C(O)NR i R i 、C(O)OR i 、OC(O)R i 、OC(O)NR i R i 、NHR i 、NR i R i 、NR i C(O)R i 、NR i C(O)NR i R i 、NR i C(O)OR i 、C(=NR i )NR i R i 、NR i C(=NR i )NR i R i 、S(O)R i 、S(O)NR i R i 、S(O) 2 R i 、NR i S(O) 2 R i 、NR i S(O) 2 NR i R i 、及びS(O) 2 NR i R i から独立して選択される1、2、または3個のR h 置換基で置換されており、ここで、R h のC 1-6 アルキル、C 3-10 シクロアルキル、4~7員ヘテロシクロアルキル、C 6-10 アリール、5~6員ヘテロアリール、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~6員ヘテロアリール)-C 1-4 アルキル-、及び(4~7員ヘテロシクロアルキル)-C 1-4 アルキル-は、それぞれさらに場合により、C 3-6 シクロアルキル、C 6-10 アリール、5員または6員ヘテロアリール、C 2-4 アルケニル、C 2-4 アルキニル、ハロ、C 1-4 アルキル、C 1-4 ハロアルキル、CN、NHOR k 、OR k 、SR k 、C(O)R k 、C(O)NR k R k 、C(O)OR k 、OC(O)R k 、OC(O)NR k R k 、NHR k 、NR k R k 、NR k C(O)R k 、NR k C(O)NR k R k 、NR k C(O)OR k 、C(=NR k )NR k R k 、NR k C(=NR k )NR k R k 、S(O)R k 、S(O)NR k R k 、S(O) 2 R k 、NR k S(O) 2 R k 、NR k S(O) 2 NR k R k 、及びS(O) 2 NR k R k から独立して選択される1、2、または3個のR j 置換基で置換されるか;または、4~10員ヘテロシクロアルキルの同じ炭素原子に結合する2つのR h 基は、それらが結合する炭素原子とともに、O、N、及びSから選択される1~2個のヘテロ原子を環員として有するC 3-6 シクロアルキルもしくは4~6員ヘテロシクロアルキルを形成するか;
あるいは、任意の2つのR c 置換基はそれらが結合する窒素原子とともに、4員、5員、6員、または7員ヘテロシクロアルキル基を形成し、それらの基は場合により1、2、または3個の独立して選択されるR h 置換基で置換されるか;
あるいは、任意の2つのR e 置換基はそれらが結合する窒素原子とともに、4員、5員、6員、または7員ヘテロシクロアルキル基を形成し、それらの基は場合により1、2、または3個の独立して選択されるR h 置換基で置換されるか;
あるいは、任意の2つのR g 置換基はそれらが結合する窒素原子とともに、4員、5員、6員、または7員ヘテロシクロアルキル基を形成し、それらの基は場合により1、2、または3個の独立して選択されるR h 置換基で置換されるか;
あるいは、任意の2つのR i 置換基はそれらが結合する窒素原子とともに、4員、5員、6員、または7員ヘテロシクロアルキル基を形成し、それらの基は場合により1、2、または3個の独立して選択されるR h 置換基で置換されるか;
あるいは、任意の2つのR k 置換基はそれらが結合する窒素原子とともに、4員、5員、6員、または7員ヘテロシクロアルキル基を形成し、それらの基は場合により1、2、または3個の独立して選択されるR h 置換基で置換されるか;
あるいは、任意の2つのR o 置換基はそれらが結合する窒素原子とともに、4員、5員、6員、または7員ヘテロシクロアルキル基を形成し、それらの基は場合により1、2、または3個の独立して選択されるR h 置換基で置換されており;
各R e 、R i 、R k 、R o 、またはR p は独立して、H、C 1-4 アルキル、C 3-6 シクロアルキル、C 6-10 アリール、5員または6員ヘテロアリール、C 1-4 ハロアルキル、C 2-4 アルケニル、及びC 2-4 アルキニルから選択され、ここで、R e 、R i 、R k 、R o 、またはR p のC 1-4 アルキル、C 3-6 シクロアルキル、C 6-10 アリール、5員または6員ヘテロアリール、C 2-4 アルケニル、及びC 2-4 アルキニルは、それぞれ場合により1、2、または3個のR q 置換基で置換され;
各R q は独立して、OH、CN、-COOH、NH 2 、ハロ、C 1-4 アルキル、C 1-4 アルコキシ、C 1-4 アルキルチオ、フェニル、5~6員ヘテロアリール、C 3-6 シクロアルキル、NHR 12 、NR 12 R 12 、及びC 1-4 ハロアルコキシから選択され、ここで、R q のC 1-4 アルキル、フェニル、及び5~6員ヘテロアリールは、それぞれ場合により、OH、CN、-COOH、NH 2 、C 1-4 アルコキシ、C 3-10 シクロアルキル、及び4~6員ヘテロシクロアルキルで置換され、各R 12 は独立してC 1-6 アルキルであり;
式(I’)の部分
[態様3]
Cyが、1、2、3、4、または5個のR 7 置換基で場合により置換されるフェニルである、態様1に記載の化合物、またはその薬学的に許容される塩もしくは立体異性体。
[態様4]
式(I):
[式中:
X 1 及びX 2 の一方はOまたはSであり、X 1 及びX 2 の他方はN、CR 1 、またはCR 2 であり;
X 3 はNまたはCR 3 であり;
X 4 はNまたはCR 4 であり;
X 5 はNまたはCR 5 であり;
X 6 はNまたはCR 6 であり;
X 1 、X 2 、X 3 、X 4 、X 5 、及びX 6 の少なくとも1つはNであり;
R 1 、R 2 、及びR 8 はそれぞれ独立して、H、C 1-4 アルキル、C 3-6 シクロアルキル、C 2-4 アルケニル、C 2-4 アルキニル、ハロ、CN、OH、C 1-4 アルコキシ、C 1-4 ハロアルキル、C 1-4 ハロアルコキシ、NH 2 、-NH-C 1-4 アルキル、-N(C 1-4 アルキル) 2 、NHOR 10 、C(O)R 10 、C(O)NR 10 R 10 、C(O)OR 10 、OC(O)R 10 、OC(O)NR 10 R 10 、NR 10 C(O)R 10 、NR 10 C(O)OR 10 、NR 10 C(O)NR 10 R 10 、C(=NR 10 )R 10 、C(=NR 10 )NR 10 R 10 、NR 10 C(=NR 10 )NR 10 R 10 、NR 10 S(O)R 10 、NR 10 S(O) 2 R 10 、NR 10 S(O) 2 NR 10 R 10 、S(O)R 10 、S(O)NR 10 R 10 、S(O) 2 R 10 、及びS(O) 2 NR 10 R 10 から選択され、ここで、各R 10 は独立して、H、またはハロ、OH、CN、及びC 1-4 アルコキシから独立して選択される1個もしくは2個の基で場合により置換されるC 1-4 アルキルであり、かつ、R 1 、R 2 、またはR 8 のC 1-4 アルキル、C 3-4 シクロアルキル、C 2-4 アルケニル、及びC 2-4 アルキニルは、それぞれ場合により、ハロ、OH、CN、C 1-4 アルキル、及びC 1-4 アルコキシから独立して選択される1個または2個の置換基で置換され;
R 9 は、C 1-4 アルキル、Cl、Br、CN、シクロプロピル、C 2-4 アルキニル、C 1-4 ハロアルキル、C 1-4 ハロアルコキシ、NH 2 、-NH-C 1-4 アルキル、-N(C 1-4 アルキル) 2 、NHOR 11 、C(O)R 11 、C(O)NR 11 R 11 、C(O)OR 11 、OC(O)R 11 、OC(O)NR 11 R 11 、NR 11 C(O)R 11 、NR 11 C(O)OR 11 、NR 11 C(O)NR 11 R 11 、C(=NR 11 )R 11 、C(=NR 11 )NR 11 R 11 、NR 11 C(=NR 11 )NR 11 R 11 、NR 11 S(O)R 11 、NR 11 S(O) 2 R 11 、NR 11 S(O) 2 NR 11 R 11 、S(O)R 11 、S(O)NR 11 R 11 、S(O) 2 R 11 、及びS(O) 2 NR 11 R 11 であり、ここで、各R 11 は独立して、H、または1個もしくは2個のハロ、OH、CN、もしくはOCH 3 で場合により置換されるC 1-4 アルキルであり;
R 3 、R 4 、R 5 、R 6 、及びR 7 はそれぞれ独立して、H、ハロ、C 1-6 アルキル、C 2-6 アルケニル、C 2-6 アルキニル、C 1-6 ハロアルキル、C 1-6 ハロアルコキシ、C 6-10 アリール、C 3-10 シクロアルキル、5~14員ヘテロアリール、4~10員ヘテロシクロアルキル、C 6-10 アリール-C 1-4 アルキル-、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~14員ヘテロアリール)-C 1-4 アルキル-、(4~10員ヘテロシクロアルキル)-C 1-4 アルキル-、CN、NO 2 、OR a 、SR a 、NHOR a 、C(O)R a 、C(O)NR a R a 、C(O)OR a 、OC(O)R a 、OC(O)NR a R a 、NHR a 、NR a R a 、NR a C(O)R a 、NR a C(O)OR a 、NR a C(O)NR a R a 、C(=NR a )R a 、C(=NR a )NR a R a 、NR a C(=NR a )NR a R a 、NR a S(O)R a 、NR a S(O) 2 R a 、NR a S(O) 2 NR a R a 、S(O)R a 、S(O)NR a R a 、S(O) 2 R a 、及びS(O) 2 NR a R a から選択され、ここで、R 3 、R 4 、R 5 、R 6 、及びR 7 のC 1-6 アルキル、C 2-6 アルケニル、C 2-6 アルキニル、C 6-10 アリール、C 3-10 シクロアルキル、5~14員ヘテロアリール、4~10員ヘテロシクロアルキル、C 6-10 アリール-C 1-4 アルキル-、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~14員ヘテロアリール)-C 1-4 アルキル-、及び(4~10員ヘテロシクロアルキル)-C 1-4 アルキル-は、それぞれ場合により1、2、3、または4個のR b 置換基で置換され、ただしその場合、R 3 、R 4 、R 5 、及びR 6 の少なくとも1つはH以外であるか;
または、フェニル環上の2つの隣接するR 7 置換基は、それらが結合する炭素原子とともに縮合フェニル環、縮合5~7員ヘテロシクロアルキル環、縮合5員もしくは6員ヘテロアリール環、または縮合C 5-6 シクロアルキル環を形成し、その場合、縮合5~7員ヘテロシクロアルキル環及び縮合5員または6員ヘテロアリール環はそれぞれ、環員としてN、O、及びSから選択される1~4個のヘテロ原子を有し、縮合フェニル環、縮合5~7員ヘテロシクロアルキル環、縮合5員または6員ヘテロアリール環、及び縮合C 5-6 シクロアルキル環は、それぞれ場合により1個または2個の独立して選択されるR q 置換基で置換され;
各R a は独立して、H、CN、C 1-6 アルキル、C 1-4 ハロアルキル、C 2-6 アルケニル、C 2-6 アルキニル、C 6-10 アリール、C 3-10 シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C 6-10 アリール-C 1-4 アルキル-、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~10員ヘテロアリール)-C 1-4 アルキル-、及び(4~10員ヘテロシクロアルキル)-C 1-4 アルキル-から選択され、ここで、R a のC 1-6 アルキル、C 2-6 アルケニル、C 2-6 アルキニル、C 6-10 アリール、C 3-10 シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C 6-10 アリール-C 1-4 アルキル-、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~10員ヘテロアリール)-C 1-4 アルキル-、及び(4~10員ヘテロシクロアルキル)-C 1-4 アルキル-は、それぞれ場合により1、2、3、4、または5個のR d 置換基で置換され;
各R d は独立して、C 1-4 アルキル、C 1-4 ハロアルキル、ハロ、C 3-10 シクロアルキル、4-10員ヘテロシクロアルキル、CN、NH 2 、NHOR e 、OR e 、SR e 、C(O)R e 、C(O)NR e R e 、C(O)OR e 、OC(O)R e 、OC(O)NR e R e 、NHR e 、NR e R e 、NR e C(O)R e 、NR e C(O)NR e R e 、NR e C(O)OR e 、C(=NR e )NR e R e 、NR e C(=NR e )NR e R e 、S(O)R e 、S(O)NR e R e 、S(O) 2 R e 、NR e S(O) 2 R e 、NR e S(O) 2 NR e R e 、及びS(O) 2 NR e R e から選択され、ここで、R d のC 1-4 アルキル、C 3-10 シクロアルキル、及び4~10員ヘテロシクロアルキルは、それぞれさらに場合により1~3個の独立して選択されるR q 置換基で置換され;
各R b 置換基は独立して、ハロ、C 1-4 アルキル、C 1-4 ハロアルキル、C 1-4 ハロアルコキシ、C 6-10 アリール、C 3-10 シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C 6-10 アリール-C 1-4 アルキル-、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~10員ヘテロアリール)-C 1-4 アルキル-、(4~10員ヘテロシクロアルキル)-C 1-4 アルキル-、CN、OH、NH 2 、NO 2 、NHOR c 、OR c 、SR c 、C(O)R c 、C(O)NR c R c 、C(O)OR c 、OC(O)R c 、OC(O)NR c R c 、C(=NR c )NR c R c 、NR c C(=NR c )NR c R c 、NHR c 、NR c R c 、NR c C(O)R c 、NR c C(O)OR c 、NR c C(O)NR c R c 、NR c S(O)R c 、NR c S(O) 2 R c 、NR c S(O) 2 NR c R c 、S(O)R c 、S(O)NR c R c 、S(O) 2 R c 、及びS(O) 2 NR c R c から選択され;ここで、R b のC 1-4 アルキル、C 1-4 ハロアルキル、C 1-4 ハロアルコキシ、C 6-10 アリール、C 3-10 シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C 6-10 アリール-C 1-4 アルキル-、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~10員ヘテロアリール)-C 1-4 アルキル-、及び(4~10員ヘテロシクロアルキル)-C 1-4 アルキル-は、それぞれさらに場合により1~3個の独立して選択されるR d 置換基で置換され;
各R c は独立して、H、C 1-6 アルキル、C 1-4 ハロアルキル、C 2-6 アルケニル、C 2-6 アルキニル、C 6-10 アリール、C 3-10 シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C 6-10 アリール-C 1-4 アルキル-、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~10員ヘテロアリール)-C 1-4 アルキル-、及び(4~10員ヘテロシクロアルキル)-C 1-4 アルキル-から選択され、ここで、R c のC 1-6 アルキル、C 2-6 アルケニル、C 2-6 アルキニル、C 6-10 アリール、C 3-10 シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C 6-10 アリール-C 1-4 アルキル-、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~10員ヘテロアリール)-C 1-4 アルキル-、及び(4~10員ヘテロシクロアルキル)-C 1-4 アルキル-は、それぞれ場合により、C 1-4 アルキル、C 1-4 ハロアルキル、C 2-6 アルケニル、C 2-6 アルキニル、C 6-10 アリール、C 3-10 シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C 6-10 アリール-C 1-4 アルキル-、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~10員ヘテロアリール)-C 1-4 アルキル-、(4-10員ヘテロシクロアルキル)-C 1-4 アルキル-、ハロ、CN、NHOR g 、OR g 、SR g 、C(O)R g 、C(O)NR g R g 、C(O)OR g 、OC(O)R g 、OC(O)NR g R g 、NHR g 、NR g R g 、NR g C(O)R g 、NR g C(O)NR g R g 、NR g C(O)OR g 、C(=NR g )NR g R g 、NR g C(=NR g )NR g R g 、S(O)R g 、S(O)NR g R g 、S(O) 2 R g 、NR g S(O) 2 R g 、NR g S(O) 2 NR g R g 、及びS(O) 2 NR g R g から独立して選択される1、2、3、4、または5個のR f 置換基で置換され;その場合、R f のC 1-4 アルキル、C 1-4 ハロアルキル、C 2-6 アルケニル、C 2-6 アルキニル、C 6-10 アリール、C 3-10 シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C 6-10 アリール-C 1-4 アルキル-、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~10員ヘテロアリール)-C 1-4 アルキル-、及び(4~10員ヘテロシクロアルキル)-C 1-4 アルキル-は、それぞれ場合により、C 1-4 アルキル、C 1-4 ハロアルキル、ハロ、CN、R o 、NHOR o 、OR o 、SR o 、C(O)R o 、C(O)NR o R o 、C(O)OR o 、OC(O)R o 、OC(O)NR o R o 、NHR o 、NR o R o 、NR o C(O)R o 、NR o C(O)NR o R o 、NR o C(O)OR o 、C(=NR o )NR o R o 、NR o C(=NR o )NR o R o 、S(O)R o 、S(O)NR o R o 、S(O) 2 R o 、NR o S(O) 2 R o 、NR o S(O) 2 NR o R o 、及びS(O) 2 NR o R o から独立して選択される1、2、3、4、または5個のR n 置換基で置換され;
各R g は独立して、H、C 1-6 アルキル、C 1-4 ハロアルキル、C 2-6 アルケニル、C 2-6 アルキニル、C 6-10 アリール、C 3-10 シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C 6-10 アリール-C 1-4 アルキル-、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~10員ヘテロアリール)-C 1-4 アルキル-、及び(4~10員ヘテロシクロアルキル)-C 1-4 アルキル-から選択され、ここで、R g のC 1-6 アルキル、C 2-6 アルケニル、C 2-6 アルキニル、C 6-10 アリール、C 3-10 シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C 6-10 アリール-C 1-4 アルキル-、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~10員ヘテロアリール)-C 1-4 アルキル-、及び(4~10員ヘテロシクロアルキル)-C 1-4 アルキル-は、それぞれ場合により1~3個の独立して選択されるR p 置換基で置換されるか;
あるいは、任意の2つのR a 置換基はそれらが結合する窒素原子とともに、4員、5員、6員、7員、8員、9員、または10員ヘテロシクロアルキル基を形成し、それらの基は場合により、C 1-6 アルキル、C 3-10 シクロアルキル、4~7員ヘテロシクロアルキル、C 6-10 アリール、5~6員ヘテロアリール、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~6員ヘテロアリール)-C 1-4 アルキル-、(4~7員ヘテロシクロアルキル)-C 1-4 アルキル-、C 1-6 ハロアルキル、C 2-6 アルケニル、C 2-6 アルキニル、ハロ、CN、OR i 、SR i 、NHOR i 、C(O)R i 、C(O)NR i R i 、C(O)OR i 、OC(O)R i 、OC(O)NR i R i 、NHR i 、NR i R i 、NR i C(O)R i 、NR i C(O)NR i R i 、NR i C(O)OR i 、C(=NR i )NR i R i 、NR i C(=NR i )NR i R i 、S(O)R i 、S(O)NR i R i 、S(O) 2 R i 、NR i S(O) 2 R i 、NR i S(O) 2 NR i R i 、及びS(O) 2 NR i R i から独立して選択される1、2、または3個のR h 置換基で置換されており、ここで、R h のC 1-6 アルキル、C 3-10 シクロアルキル、4~7員ヘテロシクロアルキル、C 6-10 アリール、5~6員ヘテロアリール、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~6員ヘテロアリール)-C 1-4 アルキル-、及び(4~7員ヘテロシクロアルキル)-C 1-4 アルキル-は、それぞれさらに場合により、C 3-6 シクロアルキル、C 6-10 アリール、5員または6員ヘテロアリール、C 2-4 アルケニル、C 2-4 アルキニル、ハロ、C 1-4 アルキル、C 1-4 ハロアルキル、CN、NHOR k 、OR k 、SR k 、C(O)R k 、C(O)NR k R k 、C(O)OR k 、OC(O)R k 、OC(O)NR k R k 、NHR k 、NR k R k 、NR k C(O)R k 、NR k C(O)NR k R k 、NR k C(O)OR k 、C(=NR k )NR k R k 、NR k C(=NR k )NR k R k 、S(O)R k 、S(O)NR k R k 、S(O) 2 R k 、NR k S(O) 2 R k 、NR k S(O) 2 NR k R k 、及びS(O) 2 NR k R k から独立して選択される1、2、または3個のR j 置換基で置換されるか;または、4~10員ヘテロシクロアルキルの同じ炭素原子に結合する2つのR h 基は、それらが結合する炭素原子とともに、O、N、及びSから選択される1~2個のヘテロ原子を環員として有するC 3-6 シクロアルキルもしくは4~6員ヘテロシクロアルキルを形成するか;
あるいは、任意の2つのR c 置換基はそれらが結合する窒素原子とともに、4員、5員、6員、または7員ヘテロシクロアルキル基を形成し、それらの基は場合により1、2、または3個の独立して選択されるR h 置換基で置換されるか;
あるいは、任意の2つのR e 置換基はそれらが結合する窒素原子とともに、4員、5員、6員、または7員ヘテロシクロアルキル基を形成し、それらの基は場合により1、2、または3個の独立して選択されるR h 置換基で置換されるか;
あるいは、任意の2つのR g 置換基はそれらが結合する窒素原子とともに、4員、5員、6員、または7員ヘテロシクロアルキル基を形成し、それらの基は場合により1、2、または3個の独立して選択されるR h 置換基で置換されるか;
あるいは、任意の2つのR i 置換基はそれらが結合する窒素原子とともに、4員、5員、6員、または7員ヘテロシクロアルキル基を形成し、それらの基は場合により1、2、または3個の独立して選択されるR h 置換基で置換されるか;
あるいは、任意の2つのR k 置換基はそれらが結合する窒素原子とともに、4員、5員、6員、または7員ヘテロシクロアルキル基を形成し、それらの基は場合により1、2、または3個の独立して選択されるR h 置換基で置換されるか;
あるいは、任意の2つのR o 置換基はそれらが結合する窒素原子とともに、4員、5員、6員、または7員ヘテロシクロアルキル基を形成し、それらの基は場合により1、2、または3個の独立して選択されるR h 置換基で置換されており;
各R e 、R i 、R k 、R o 、またはR p は独立して、H、C 1-4 アルキル、C 3-6 シクロアルキル、C 6-10 アリール、5員または6員ヘテロアリール、C 1-4 ハロアルキル、C 2-4 アルケニル、及びC 2-4 アルキニルから選択され、ここで、R e 、R i 、R k 、R o 、またはR p のC 1-4 アルキル、C 3-6 シクロアルキル、C 6-10 アリール、5または6員ヘテロアリール、C 2-4 アルケニル、及びC 2-4 アルキニルは、それぞれ場合により1、2、または3個のR q 置換基で置換され;
各R q は独立して、OH、CN、-COOH、NH 2 、ハロ、C 1-4 アルキル、C 1-4 アルコキシ、C 1-4 アルキルチオ、フェニル、5~6員ヘテロアリール、C 3-6 シクロアルキル、NHR 12 、NR 12 R 12 、及びC 1-4 ハロアルコキシから選択され、ここで、R q のC 1-4 アルキル、フェニル、及び5~6員ヘテロアリールは、それぞれ場合により、OH、CN、-COOH、NH 2 、C 1-4 アルコキシ、C 3-10 シクロアルキル、及び4~6員ヘテロシクロアルキルで置換され、各R 12 は独立してC 1-6 アルキルであり;
下付き文字nは、整数1、2、3、4または5であり;下付き文字mは、整数1、2、または3である]。
[態様5]
式(II):
[態様6]
式(III):
[態様7]
式(IV):
[態様8]
式(V):
[態様9]
式(VI):
[態様10]
式(VII):
[態様11]
式(VIII):
[態様12]
式(IX):
[態様13]
前記部分
[態様14]
R 1 、R 2 、R 3 、及びR 5 が存在する場合、それぞれHである、態様1~13のいずれか1つに記載の化合物、またはその薬学的に許容される塩もしくは立体異性体。
[態様15]
R 3 及びR 5 がそれぞれHである、態様1~14のいずれか1つに記載の化合物、またはその薬学的に許容される塩もしくは立体異性体。
[態様16]
R 4 及びR 6 がそれぞれHである、態様1~15のいずれか1つに記載の化合物、またはその薬学的に許容される塩もしくは立体異性体。
[態様17]
X 1 がCHであり、X 2 がOであり、X 3 がNであり、X 5 及びX 6 がそれぞれCHである、態様1~9のいずれか1つに記載の化合物、またはその薬学的に許容される塩もしくは立体異性体。
[態様18]
X 1 がOであり、X 2 がCHであり、X 3 がNであり、X 5 がCHであり、X 6 がCR 6 である、態様1~9のいずれか1つに記載の化合物、またはその薬学的に許容される塩もしくは立体異性体。
[態様19]
X 1 がOであり、X 2 がCHであり、X 3 がCHであり、X 5 がNであり、X 6 がCR 6 である、態様1~9のいずれか1つに記載の化合物、またはその薬学的に許容される塩もしくは立体異性体。
[態様20]
X 1 がOであり、X 2 がNであり、X 3 がCHであり、X 5 がCHであり、X 6 がCR 6 である、態様1~9のいずれか1つに記載の化合物、またはその薬学的に許容される塩もしくは立体異性体。
[態様21]
X 1 がOであり、X 2 がCHであり、X 3 がCHであり、X 5 がCHであり、X 6 がNである、態様1~9のいずれか1つに記載の化合物、またはその薬学的に許容される塩もしくは立体異性体。
[態様22]
X 1 がSであり、X 2 がNであり、X 3 がCHであり、X 5 がCHであり、X 6 がCR 6 である、態様1~9のいずれか1つに記載の化合物、またはその薬学的に許容される塩もしくは立体異性体。
[態様23]
X 1 がNであり、X 2 がSであり、X 3 がCHであり、X 5 がCHであり、X 6 がCR 6 である、態様1~9のいずれか1つに記載の化合物、またはその薬学的に許容される塩もしくは立体異性体。
[態様24]
X 1 がOであり、X 2 がCHであり、X 3 がCHであり、X 5 がCHであり、X 6 がNである、態様1~9のいずれか1つに記載の化合物、またはその薬学的に許容される塩もしくは立体異性体。
[態様25]
X 1 がOであり、X 2 がNであり、X 3 がCHであり、X 6 がCR 6 である、態様1~9のいずれか1つに記載の化合物、またはその薬学的に許容される塩もしくは立体異性体。
[態様26]
X 2 がOであり、X 1 がNであり、X 3 がCHであり、X 6 がCR 6 である、態様1~9のいずれか1つに記載の化合物、またはその薬学的に許容される塩もしくは立体異性体。
[態様27]
X 1 がOであり、X 2 がNであり、X 3 がCHであり、X 5 がNであり、X 6 がCR 6 である、態様1~9のいずれか1つに記載の化合物、またはその薬学的に許容される塩もしくは立体異性体。
[態様28]
X 1 がOまたはSであり、X 2 がNまたはCR 2 である、態様1~9のいずれか1つに記載の化合物、またはその薬学的に許容される塩もしくは立体異性体。
[態様29]
X 2 がOまたはSであり、X 1 がNまたはCR 1 である、態様1~9のいずれか1つに記載の化合物、またはその薬学的に許容される塩もしくは立体異性体。
[態様30]
R 4 が-CH 2 -R b である、態様1~15及び17~29のいずれか1つに記載の化合物、またはその薬学的に許容される塩もしくは立体異性体。
[態様31]
R 5 が-CH 2 -R b である、態様1~13、16、及び25~29のいずれか1つに記載の化合物、またはその薬学的に許容される塩もしくは立体異性体。
[態様32]
R b が-NHR c である、態様30または31に記載の化合物、またはその薬学的に許容される塩もしくは立体異性体。
[態様33]
R c が場合によりR d 置換基で置換されるC 1-4 アルキルである、態様32に記載の化合物、またはその薬学的に許容される塩もしくは立体異性体。
[態様34]
R 4 が2-ヒドロキシエチルアミノメチルである、態様1~15及び17~33のいずれか1つに記載の化合物、またはその薬学的に許容される塩もしくは立体異性体。
[態様35]
R b が-NR c R c である、態様30または31に記載の化合物、またはその薬学的に許容される塩もしくは立体異性体。
[態様36]
2つのR c 置換基が、それらが結合する窒素原子とともに、4員、5員、6員、または7員ヘテロシクロアルキル基を形成し、それらの基が場合により1、2、または3個の独立して選択されるR h 置換基で置換される、態様35に記載の化合物、またはその薬学的に許容される塩もしくは立体異性体。
[態様37]
2つのR c 置換基が、それらが結合する窒素原子とともに、1個のR h 置換基で置換された6員ヘテロシクロアルキルを形成する、態様36に記載の化合物、またはその薬学的に許容される塩もしくは立体異性体。
[態様38]
R 4 が、2-ヒドロキシエチルアミノメチル、2-カルボキシピペリジン-1-イルメチル、(S)-2-カルボキシピペリジン-1-イルメチル、または(R)-2-カルボキシピペリジン-1-イルメチルである、態様1~15及び17~31のいずれか1つに記載の化合物、またはその薬学的に許容される塩もしくは立体異性体。
[態様39]
R 4 及びR 5 がそれぞれ独立して、2-ヒドロキシエチルアミノメチル、2-カルボキシピペリジン-1-イルメチル、(S)-2-カルボキシピペリジン-1-イルメチル、(R)-2-カルボキシピペリジン-1-イルメチル、(3-シアノフェニル)メトキシ、シアノメトキシ、2-シアノエトキシ、3-シアノプロポキシ、2-モルホリノ-4-イルエトキシ、及びピリジン-2-イルメトキシから選択される、態様1~13及び25~29のいずれか1つに記載の化合物、またはその薬学的に許容される塩もしくは立体異性体。
[態様40]
態様1~4のいずれか1つに記載の化合物であって、
2-({[2-(2-メチルビフェニル-3-イル)フロ[2,3-b]ピリジン-6-イル]メチル}アミノ)エタノール;
(2S)-1-{[2-(2-メチルビフェニル-3-イル)フロ[2,3-b]ピリジン-6-イル]メチル}ピペリジン-2-カルボン酸;
2-({[7-メチル-2-(2-メチルビフェニル-3ーイル)フロ[3,2-b]ピリジン-5-イル]メチル}アミノ)エタノール;
(2S)-1-{[7-メチル-2-(2-メチルビフェニル-3-イル)フロ[3,2-b]ピリジン-5-イル]メチル}ピペリジン-2-カルボン酸;
2-({[7-メチル-2-(2-メチルビフェニル-3-イル)フロ[2,3-c]ピリジン-5-イル]メチル}アミノ)エタノール;
(2S)-1-{[7-メチル-2-(2-メチルビフェニル-3-イル)フロ[2,3-c]ピリジン-5-イル]メチル}ピペリジン-2-カルボン酸;
(2S)-1-{[2-(2-メチルビフェニル-3-イル)-1,3-ベンゾオキサゾール-5-イル]メチル}ピペリジン-2-カルボン酸;
2-({[2-(2-メチルビフェニル-3-イル)-1,3-ベンゾオキサゾール-5-イル]メチル}アミノ)エタノール;
(2S)-1-{[2-(2-メチルビフェニル-3-イル)フロ[2,3-b]ピリジン-5-イル]メチル}ピペリジン-2-カルボン酸;
2-({[2-(2-メチルビフェニル-3-イル)フロ[2,3-b]ピリジン-5-イル]メチル}アミノ)エタノール;
(2S)-1-{[7-メチル-2-(2-メチルビフェニル-3-イル)-1,3-ベンゾオキサゾール-5-イル]メチル}ピペリジン-2-カルボン酸;
2-({[7-メチル-2-(2-メチルビフェニル-3-イル)-1,3-ベンゾオキサゾール-5-イル]メチル}アミノ)エタノール;
(2S)-1-{[2-(2-シアノビフェニル-3-イル)-7-メチル-1,3-ベンゾオキサゾール-5-イル]メチル}ピペリジン-2-カルボン酸;
3-(5-{[(2-ヒドロキシエチル)アミノ]メチル}-7-メチル-1,3-ベンゾオキサゾール-2-イル)ビフェニル-2-カルボニトリル;
(2S)-1-({2-[3-(2,3-ジヒドロ-1,4-ベンゾジオキシン-6-イル)-2-メチルフェニル]-7-メチル-1,3-ベンゾオキサゾール-5-イル}メチル)ピペリジン-2-カルボン酸;
2-[({2-[3-(2,3-ジヒドロ-1,4-ベンゾジオキシン-6-イル)-2-メチルフェニル]-7-メチル-1,3-ベンゾオキサゾール-5-イル}メチル)アミノ]エタノール;
(2S)-1-({2-[2-シアノ-3-(2,3-ジヒドロ-1,4-ベンゾジオキシン-6-イル)フェニル]-7-メチル-1,3-ベンゾオキサゾール-5-イル}メチル)ピペリジン-2-カルボン酸;
2-(2,3-ジヒドロ-1,4-ベンゾジオキシン-6-イル)-6-(5-{[(2-ヒドロキシエチル)アミノ]メチル}-7-メチル-1,3-ベンゾオキサゾール-2-イル)ベンゾニトリル;
(2S)-1-{[2-(2-メチルビフェニル-3-イル)-1,3-ベンゾチアゾール-5-イル]メチル}ピペリジン-2-カルボン酸;
(2S)-1-{[2-(2-メチルビフェニル-3-イル)フロ[3,2-b]ピリジン-5-イル]メチル}ピペリジン-2-カルボン酸;
2-({[2-(2-メチルビフェニル-3-イル)フロ[3,2-b]ピリジン-5-イル]メチル}アミノ)エタノール;
(2S)-1-{[4-メチル-2-(2-メチルビフェニル-3-イル)-1,3-ベンゾチアゾール-6-イル]メチル}ピペリジン-2-カルボン酸;
2-({[4-メチル-2-(2-メチルビフェニル-3-イル)-1,3-ベンゾチアゾール-6-イル]メチル}アミノ)エタノール;
2-({[6-(2-メチルビフェニル-3-イル)フロ[2,3-b]ピラジン-2-イル]メチル}アミノ)エタノール;及び
(2S)-1-{[6-(2-メチルビフェニル-3-イル)フロ[2,3-b]ピラジン-2-イル]メチル}ピペリジン-2-カルボン酸から選択される前記化合物、またはその薬学的に許容される塩もしくは立体異性体。
[態様41]
態様1~4のいずれか1つに記載の化合物であって、
(2S)-1-{[6-(シアノメトキシ)-2-(2-メチルビフェニル-3-イル)-1,3-ベンゾオキサゾール-5-イル]メチル}ピペリジン-2-カルボン酸;
{[5-{[(2-ヒドロキシエチル)アミノ]メチル}-2-(2-メチルビフェニル-3-イル)-1,3-ベンゾオキサゾール-6-イル]オキシ}アセトニトリル;
(2S)-1-{[6-(3-シアノプロポキシ)-2-(2-メチルビフェニル-3-イル)-1,3-ベンゾオキサゾール-5-イル]メチル}ピペリジン-2-カルボン酸;
3-({[5-{[(2-ヒドロキシエチル)アミノ]メチル}-2-(2-メチルビフェニル-3-イル)-1,3-ベンゾオキサゾール-6-イル]オキシ}メチル)ベンゾニトリル;
2-({[2-(2-メチルビフェニル-3-イル)-6-(ピリジン-2-イルメトキシ)-1,3-ベンゾオキサゾール-5-イル]メチル}アミノ)エタノール;
2-({[6-メトキシ-2-(2-メチルビフェニル-3-イル)-1,3-ベンゾオキサゾール-5-イル]メチル}アミノ)エタノール;
2-({[2-(2-メチルビフェニル-3-イル)-6-(2-モルホリン-4-イルエトキシ)-1,3-ベンゾオキサゾール-5-イル]メチル}アミノ)エタノール;
2-({[2-(2-メチルビフェニル-3-イル)[1,3]オキサゾロ[5,4-c]ピリジン-6-イル]メチル}アミノ)エタノール;
4-{[5-{[(2-ヒドロキシエチル)アミノ]メチル}-7-メチル-2-(2-メチルビフェニル-3-イル)-1,3-ベンゾオキサゾール-6-イル]オキシ}ブタンニトリル;
(2S)-1-({6-(シアノメトキシ)-2-[4-(2,3-ジヒドロ-1,4-ベンゾジオキシン-6-イル)-3-メチルピリジン-2-イル]-1,3-ベンゾオキサゾール-5-イル}メチル)ピペリジン-2-カルボン酸;
(2S)-1-({6-(シアノメトキシ)-2-[3-(2,3-ジヒドロ-1,4-ベンゾジオキシン-6-イル)-2-メチルフェニル]-1,3-ベンゾオキサゾール-5-イル}メチル)ピペリジン-2-カルボン酸;
(2S)-1-{[2-[2-シアノ-3-(2,3-ジヒドロ-1,4-ベンゾジオキシン-6-イル)フェニル]-6-(シアノメトキシ)-1,3-ベンゾオキサゾール-5-イル]メチル}ピペリジン-2-カルボン酸;
(2S)-1-{[2-(2-メチルビフェニル-3-イル)-1,3-ベンゾオキサゾール-6-イル]メチル}ピペリジン-2-カルボン酸;
[(2-(2’-フルオロ-2-メチルビフェニル-3-イル)-5-{[(2-ヒドロキシエチル)アミノ]メチル}-1,3-ベンゾオキサゾール-6-イル)オキシ]アセトニトリル;及び
[(2-(3-シクロヘキサ-1-エン-1-イル-2-メチルフェニル)-5-{[(2-ヒドロキシエチル)アミノ]メチル}-1,3-ベンゾオキサゾール-6-イル)オキシ]アセトニトリルから選択される前記化合物、またはその薬学的に許容される塩もしくは立体異性体。
[態様42]
態様1~41のいずれかに記載の化合物、またはその薬学的に許容される塩もしくは立体異性体、及び少なくとも1種の薬学的に許容される担体または賦形剤を含む医薬組成物。
[態様43]
個体におけるPD-1/PD-L1相互作用を阻害する方法であって、態様1~41のいずれかに記載の化合物、またはその薬学的に許容される塩もしくは立体異性体を前記個体に投与することを含む、前記方法。
[態様44]
PD-1/PD-L1相互作用の阻害と関連する疾患または障害の治療方法であって、治療有効量の、態様1~41のいずれかに記載の化合物、またはその薬学的に許容される塩もしくは立体異性体、または態様42に記載の組成物を、それを必要とする患者に投与することを含む、前記方法。
[態様45]
前記疾患または障害がウイルス感染症またはがんである、態様44に記載の方法。
[態様46]
患者の免疫応答を増強、刺激、及び/または増加させる方法であって、治療有効量の、態様1~41のいずれかに記載の化合物、またはその薬学的に許容される塩もしくは立体異性体、または態様42に記載の組成物を、それを必要とする前記患者に投与することを含む、前記方法。
上記の説明から、本明細書に記載されたものに加えて本発明の様々な変形例が当業者に明らかであろう。そのような変形例も、添付の特許請求の範囲の範囲内に包含されることを意図する。すべての特許、特許出願、及び刊行物を含むがこれらに限定されない、本出願に引用される各参照文献は、その全体が参照により本明細書に組み込まれる。
Claims (41)
- 式(I’):
[式中:
X1及びX2の一方はOまたはSであり、X1及びX2の他方はN、CR1、またはCR2であり;
X3はNまたはCR3であり;
X4はNまたはCR4であり;
X5はNまたはCR5であり;
X6はNまたはCR6であり;
X1、X2、X3、X4、X5、及びX6の少なくとも1つはNであり;
Y1はNまたはCHであり;
Y2はNまたはCHであり;
Y3はNまたはCHであり;
X4がCR4である場合、部分
Cyは、フェニル、2-フルオロフェニル、シクロヘキサ-1-エン-1-イルまたは2,3-ジヒドロ-1,4-ベンゾジオキシン-6-イルであり;
R1、及びR2はそれぞれ、Hであり;
R9は、C1-4アルキル、Cl、Br、またはCNであり;
R3は、Hであり;
R4、及びR5はそれぞれ独立して、H、ハロ、C1-6アルキル、C2-6アルケニル、C2-6アルキニル、C1-6ハロアルキル、C1-6ハロアルコキシ、C6-10アリール、C3-10シクロアルキル、5~14員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~14員ヘテロアリール)-C1-4アルキル-、(4~10員ヘテロシクロアルキル)-C1-4アルキル-、CN、NO2、ORa、SRa、NHORa、C(O)Ra、C(O)NRaRa、C(O)ORa、OC(O)Ra、OC(O)NRaRa、NHRa、NRaRa、NRaC(O)Ra、NRaC(O)ORa、NRaC(O)NRaRa、C(=NRa)Ra、C(=NRa)NRaRa、NRaC(=NRa)NRaRa、NRaS(O)Ra、NRaS(O)2Ra、NRaS(O)2NRaRa、S(O)Ra、S(O)NRaRa、S(O)2Ra、及びS(O)2NRaRaから選択され、ここで、R4、及びR5のC1-6アルキル、C2-6アルケニル、C2-6アルキニル、C6-10アリール、C3-10シクロアルキル、5~14員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~14員ヘテロアリール)-C1-4アルキル-、及び(4~10員ヘテロシクロアルキル)-C1-4アルキル-は、それぞれ場合により1、2、3、または4個のRb置換基で置換され;
R6は、HまたはCH3であり;
ただし、R4、R5、及びR6の少なくとも1つはH以外であり;
各Raは独立して、H、CN、C1-6アルキル、C1-4ハロアルキル、C2-6アルケニル、C2-6アルキニル、C6-10アリール、C3-10シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~10員ヘテロアリール)-C1-4アルキル-、及び(4~10員ヘテロシクロアルキル)-C1-4アルキル-から選択され、ここで、RaのC1-6アルキル、C2-6アルケニル、C2-6アルキニル、C6-10アリール、C3-10シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~10員ヘテロアリール)-C1-4アルキル-、及び(4~10員ヘテロシクロアルキル)-C1-4アルキル-は、それぞれ場合により1、2、3、4、または5個のRd置換基で置換され;
各Rdは独立して、C1-4アルキル、C1-4ハロアルキル、ハロ、C3-10シクロアルキル、4~10員ヘテロシクロアルキル、CN、NH2、NHORe、ORe、SRe、C(O)Re、C(O)NReRe、C(O)ORe、OC(O)Re、OC(O)NReRe、NHRe、NReRe、NReC(O)Re、NReC(O)NReRe、NReC(O)ORe、C(=NRe)NReRe、NReC(=NRe)NReRe、S(O)Re、S(O)NReRe、S(O)2Re、NReS(O)2Re、NReS(O)2NReRe、及びS(O)2NReReから選択され、ここで、RdのC1-4アルキル、C3-10シクロアルキル、及び4~10員ヘテロシクロアルキルは、それぞれ場合により1~3個の独立して選択されるRq置換基でさらに置換され;
各Rb置換基は独立して、ハロ、C1-4アルキル、C1-4ハロアルキル、C1-4ハロアルコキシ、C6-10アリール、C3-10シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~10員ヘテロアリール)-C1-4アルキル-、(4~10員ヘテロシクロアルキル)-C1-4アルキル-、CN、OH、NH2、NO2、NHORc、ORc、SRc、C(O)Rc、C(O)NRcRc、C(O)ORc、OC(O)Rc、OC(O)NRcRc、C(=NRc)NRcRc、NRcC(=NRc)NRcRc、NHRc、NRcRc、NRcC(O)Rc、NRcC(O)ORc、NRcC(O)NRcRc、NRcS(O)Rc、NRcS(O)2Rc、NRcS(O)2NRcRc、S(O)Rc、S(O)NRcRc、S(O)2Rc、及びS(O)2NRcRcから選択され;ここで、RbのC1-4アルキル、C1-4ハロアルキル、C1-4ハロアルコキシ、C6-10アリール、C3-10シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~10員ヘテロアリール)-C1-4アルキル-、及び(4~10員ヘテロシクロアルキル)-C1-4アルキル-は、それぞれさらに場合により1~3個の独立して選択されるRd置換基で置換され;
各Rcは独立して、H、C1-6アルキル、C1-4ハロアルキル、C2-6アルケニル、C2-6アルキニル、C6-10アリール、C3-10シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~10員ヘテロアリール)-C1-4アルキル-、及び(4~10員ヘテロシクロアルキル)-C1-4アルキル-から選択され、ここで、RcのC1-6アルキル、C2-6アルケニル、C2-6アルキニル、C6-10アリール、C3-10シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~10員ヘテロアリール)-C1-4アルキル-、及び(4~10員ヘテロシクロアルキル)-C1-4アルキル-は、それぞれ場合により、1、2、3、4、または5個のRf置換基で置換され;
各R f は、C 1-4 アルキル、C 1-4 ハロアルキル、C 2-6 アルケニル、C 2-6 アルキニル、C 6-10 アリール、C 3-10 シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C 6-10 アリール-C 1-4 アルキル-、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~10員ヘテロアリール)-C 1-4 アルキル-、(4-10員ヘテロシクロアルキル)-C 1-4 アルキル-、ハロ、CN、NHOR g 、OR g 、SR g 、C(O)R g 、C(O)NR g R g 、C(O)OR g 、OC(O)R g 、OC(O)NR g R g 、NHR g 、NR g R g 、NR g C(O)R g 、NR g C(O)NR g R g 、NR g C(O)OR g 、C(=NR g )NR g R g 、NR g C(=NR g )NR g R g 、S(O)R g 、S(O)NR g R g 、S(O) 2 R g 、NR g S(O) 2 R g 、NR g S(O) 2 NR g R g 、及びS(O) 2 NR g R g から独立して選択され、ここで、RfのC1-4アルキル、C1-4ハロアルキル、C2-6アルケニル、C2-6アルキニル、C6-10アリール、C3-10シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~10員ヘテロアリール)-C1-4アルキル-、及び(4~10員ヘテロシクロアルキル)-C1-4アルキル-は、それぞれ場合により、1、2、3、4、または5個のRn置換基で置換され;
各R n は、C 1-4 アルキル、C 1-4 ハロアルキル、ハロ、CN、R o 、NHOR o 、OR o 、SR o 、C(O)R o 、C(O)NR o R o 、C(O)OR o 、OC(O)R o 、OC(O)NR o R o 、NHR o 、NR o R o 、NR o C(O)R o 、NR o C(O)NR o R o 、NR o C(O)OR o 、C(=NR o )NR o R o 、NR o C(=NR o )NR o R o 、S(O)R o 、S(O)NR o R o 、S(O) 2 R o 、NR o S(O) 2 R o 、NR o S(O) 2 NR o R o 、及びS(O) 2 NR o R o から独立して選択され;
各Rgは独立して、H、C1-6アルキル、C1-4ハロアルキル、C2-6アルケニル、C2-6アルキニル、C6-10アリール、C3-10シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~10員ヘテロアリール)-C1-4アルキル-、及び(4~10員ヘテロシクロアルキル)-C1-4アルキル-から選択され、ここで、RgのC1-6アルキル、C2-6アルケニル、C2-6アルキニル、C6-10アリール、C3-10シクロアルキル、5~10員ヘテロアリール、4~10員ヘテロシクロアルキル、C6-10アリール-C1-4アルキル-、C3-10シクロアルキル-C1-4アルキル-、(5~10員ヘテロアリール)-C1-4アルキル-、及び(4~10員ヘテロシクロアルキル)-C1-4アルキル-は、それぞれ場合により、独立して選択される1~3個のRp置換基で置換されるか;
あるいは、任意の2つのRa置換基はそれらが結合する窒素原子とともに、4員、5員、6員、7員、8員、9員、または10員ヘテロシクロアルキル基を形成し、それらの基は場合により、1、2、または3個のRh置換基で置換されており、
各R h は、C 1-6 アルキル、C 3-10 シクロアルキル、4~7員ヘテロシクロアルキル、C 6-10 アリール、5~6員ヘテロアリール、C 3-10 シクロアルキル-C 1-4 アルキル-、(5~6員ヘテロアリール)-C 1-4 アルキル-、(4~7員ヘテロシクロアルキル)-C 1-4 アルキル-、C 1-6 ハロアルキル、C 2-6 アルケニル、C 2-6 アルキニル、ハロ、CN、OR i 、SR i 、NHOR i 、C(O)R i 、C(O)NR i R i 、C(O)OR i 、OC(O)R i 、OC(O)NR i R i 、NHR i 、NR i R i 、NR i C(O)R i 、NR i C(O)NR i R i 、NR i C(O)OR i 、C(=NR i )NR i R i 、NR i C(=NR i )NR i R i 、S(O)R i 、S(O)NR i R i 、S(O) 2 R i 、NR i S(O) 2 R i 、NR i S(O) 2 NR i R i 、及びS(O) 2 NR i R i から独立して選択され、ここで、RhのC1-6アルキル、C3-10シクロアルキル、4~7員ヘテロシクロアルキル、C6-10アリール、5~6員ヘテロアリール、C3-10シクロアルキル-C1-4アルキル-、(5~6員ヘテロアリール)-C1-4アルキル-、及び(4~7員ヘテロシクロアルキル)-C1-4アルキル-は、それぞれさらに場合により、1、2、または3個のRj置換基で置換され;
各R j は、C 3-6 シクロアルキル、C 6-10 アリール、5員または6員ヘテロアリール、C 2-4 アルケニル、C 2-4 アルキニル、ハロ、C 1-4 アルキル、C 1-4 ハロアルキル、CN、NHOR k 、OR k 、SR k 、C(O)R k 、C(O)NR k R k 、C(O)OR k 、OC(O)R k 、OC(O)NR k R k 、NHR k 、NR k R k 、NR k C(O)R k 、NR k C(O)NR k R k 、NR k C(O)OR k 、C(=NR k )NR k R k 、NR k C(=NR k )NR k R k 、S(O)R k 、S(O)NR k R k 、S(O) 2 R k 、NR k S(O) 2 R k 、NR k S(O) 2 NR k R k 、及びS(O) 2 NR k R k から独立して選択されるか;
または、4~10員ヘテロシクロアルキルの同じ炭素原子に結合する2つのRh基は、それらが結合する炭素原子とともに、C3-6シクロアルキル、または、O、N、及びSから選択される1~2個のヘテロ原子を環員として有する4~6員ヘテロシクロアルキルを形成するか;
あるいは、任意の2つのRc置換基はそれらが結合する窒素原子とともに、4員、5員、6員、または7員ヘテロシクロアルキル基を形成し、それらの基は場合により1、2、または3個の独立して選択されるRh置換基で置換されるか;
あるいは、任意の2つのRe置換基はそれらが結合する窒素原子とともに、4員、5員、6員、または7員ヘテロシクロアルキル基を形成し、それらの基は場合により1、2、または3個の独立して選択されるRh置換基で置換されるか;
あるいは、任意の2つのRg置換基はそれらが結合する窒素原子とともに、4員、5員、6員、または7員ヘテロシクロアルキル基を形成し、それらの基は場合により1、2、または3個の独立して選択されるRh置換基で置換されるか;
あるいは、任意の2つのRo置換基はそれらが結合する窒素原子とともに、4員、5員、6員、または7員ヘテロシクロアルキル基を形成し、それらの基は場合により1、2、または3個の独立して選択されるRh置換基で置換されており;
各Re、Ri、Rk、Ro、またはRpは独立して、H、C1-4アルキル、C3-6シクロアルキル、C6-10アリール、5員または6員ヘテロアリール、C1-4ハロアルキル、C2-4アルケニル、及びC2-4アルキニルから選択され、ここで、Re、Ri、Rk、Ro、またはRpのC1-4アルキル、C3-6シクロアルキル、C6-10アリール、5員または6員ヘテロアリール、C2-4アルケニル、及びC2-4アルキニルは、それぞれ場合により1、2、または3個のRq置換基で置換され;
各Rqは独立して、OH、CN、-COOH、NH2、ハロ、C1-4アルキル、C1-4アルコキシ、C1-4アルキルチオ、フェニル、5~6員ヘテロアリール、C3-6シクロアルキル、NHR12、NR12R12、及びC1-4ハロアルコキシから選択され、ここで、RqのC1-4アルキル、フェニル、及び5~6員ヘテロアリールは、それぞれ場合により、OH、CN、-COOH、NH2、C1-4アルコキシ、C3-10シクロアルキル、及び4~6員ヘテロシクロアルキルで置換され、各R12は独立してC1-6アルキルであり;
- Cyが、フェニルである、請求項1に記載の化合物、またはその薬学的に許容される塩もしくは立体異性体。
- 式:
- R5がHである、請求項1~9のいずれか1項に記載の化合物、またはその薬学的に許容される塩もしくは立体異性体。
- R4及びR6がそれぞれHである、請求項1~3および5~9のいずれか1項に記載の化合物、またはその薬学的に許容される塩もしくは立体異性体。
- R4が-CH2-Rbである、請求項1~10のいずれか1項に記載の化合物、またはその薬学的に許容される塩もしくは立体異性体。
- R5が-CH2-Rbである、請求項1~9、11および12のいずれか1項に記載の化合物、またはその薬学的に許容される塩もしくは立体異性体。
- Rbが-NHRcである、請求項12または13に記載の化合物、またはその薬学的に許容される塩もしくは立体異性体。
- Rcが場合によりRd置換基で置換されるC1-4アルキルである、請求項14に記載の化合物、またはその薬学的に許容される塩もしくは立体異性体。
- R4が2-ヒドロキシエチルアミノメチルである、請求項1~10のいずれか1項に記載の化合物、またはその薬学的に許容される塩もしくは立体異性体。
- Rbが-NRcRcである、請求項12または13に記載の化合物、またはその薬学的に許容される塩もしくは立体異性体。
- 2つのRc置換基が、それらが結合する窒素原子とともに、4員、5員、6員、または7員ヘテロシクロアルキル基を形成し、それらの基が場合により1、2、または3個の独立して選択されるRh置換基で置換される、請求項17に記載の化合物、またはその薬学的に許容される塩もしくは立体異性体。
- 2つのRc置換基が、それらが結合する窒素原子とともに、1個のRh置換基で置換された6員ヘテロシクロアルキルを形成する、請求項18に記載の化合物、またはその薬学的に許容される塩もしくは立体異性体。
- R4が、2-ヒドロキシエチルアミノメチル、2-カルボキシピペリジン-1-イルメチル、(S)-2-カルボキシピペリジン-1-イルメチル、または(R)-2-カルボキシピペリジン-1-イルメチルである、請求項1~10のいずれか1項に記載の化合物、またはその薬学的に許容される塩もしくは立体異性体。
- R4及びR5がそれぞれ独立して、2-ヒドロキシエチルアミノメチル、2-カルボキシピペリジン-1-イルメチル、(S)-2-カルボキシピペリジン-1-イルメチル、(R)-2-カルボキシピペリジン-1-イルメチル、(3-シアノフェニル)メトキシ、シアノメトキシ、2-シアノエトキシ、3-シアノプロポキシ、2-モルホリノ-4-イルエトキシ、及びピリジン-2-イルメトキシから選択される、請求項1~9のいずれか1項に記載の化合物、またはその薬学的に許容される塩もしくは立体異性体。
- 請求項1に記載の化合物であって、
2-({[2-(2-メチルビフェニル-3-イル)フロ[2,3-b]ピリジン-6-イル]メチル}アミノ)エタノール;
(2S)-1-{[2-(2-メチルビフェニル-3-イル)フロ[2,3-b]ピリジン-6-イル]メチル}ピペリジン-2-カルボン酸;
2-({[7-メチル-2-(2-メチルビフェニル-3ーイル)フロ[3,2-b]ピリジン-5-イル]メチル}アミノ)エタノール;
(2S)-1-{[7-メチル-2-(2-メチルビフェニル-3-イル)フロ[3,2-b]ピリジン-5-イル]メチル}ピペリジン-2-カルボン酸;
2-({[7-メチル-2-(2-メチルビフェニル-3-イル)フロ[2,3-c]ピリジン-5-イル]メチル}アミノ)エタノール;
(2S)-1-{[7-メチル-2-(2-メチルビフェニル-3-イル)フロ[2,3-c]ピリジン-5-イル]メチル}ピペリジン-2-カルボン酸;
(2S)-1-{[2-(2-メチルビフェニル-3-イル)-1,3-ベンゾオキサゾール-5-イル]メチル}ピペリジン-2-カルボン酸;
2-({[2-(2-メチルビフェニル-3-イル)-1,3-ベンゾオキサゾール-5-イル]メチル}アミノ)エタノール;
(2S)-1-{[2-(2-メチルビフェニル-3-イル)フロ[2,3-b]ピリジン-5-イル]メチル}ピペリジン-2-カルボン酸;
2-({[2-(2-メチルビフェニル-3-イル)フロ[2,3-b]ピリジン-5-イル]メチル}アミノ)エタノール;
(2S)-1-{[7-メチル-2-(2-メチルビフェニル-3-イル)-1,3-ベンゾオキサゾール-5-イル]メチル}ピペリジン-2-カルボン酸;
2-({[7-メチル-2-(2-メチルビフェニル-3-イル)-1,3-ベンゾオキサゾール-5-イル]メチル}アミノ)エタノール;
(2S)-1-{[2-(2-シアノビフェニル-3-イル)-7-メチル-1,3-ベンゾオキサゾール-5-イル]メチル}ピペリジン-2-カルボン酸;
3-(5-{[(2-ヒドロキシエチル)アミノ]メチル}-7-メチル-1,3-ベンゾオキサゾール-2-イル)ビフェニル-2-カルボニトリル;
(2S)-1-({2-[3-(2,3-ジヒドロ-1,4-ベンゾジオキシン-6-イル)-2-メチルフェニル]-7-メチル-1,3-ベンゾオキサゾール-5-イル}メチル)ピペリジン-2-カルボン酸;
2-[({2-[3-(2,3-ジヒドロ-1,4-ベンゾジオキシン-6-イル)-2-メチルフェニル]-7-メチル-1,3-ベンゾオキサゾール-5-イル}メチル)アミノ]エタノール;
(2S)-1-({2-[2-シアノ-3-(2,3-ジヒドロ-1,4-ベンゾジオキシン-6-イル)フェニル]-7-メチル-1,3-ベンゾオキサゾール-5-イル}メチル)ピペリジン-2-カルボン酸;
2-(2,3-ジヒドロ-1,4-ベンゾジオキシン-6-イル)-6-(5-{[(2-ヒドロキシエチル)アミノ]メチル}-7-メチル-1,3-ベンゾオキサゾール-2-イル)ベンゾニトリル;
(2S)-1-{[2-(2-メチルビフェニル-3-イル)-1,3-ベンゾチアゾール-5-イル]メチル}ピペリジン-2-カルボン酸;
(2S)-1-{[2-(2-メチルビフェニル-3-イル)フロ[3,2-b]ピリジン-5-イル]メチル}ピペリジン-2-カルボン酸;
2-({[2-(2-メチルビフェニル-3-イル)フロ[3,2-b]ピリジン-5-イル]メチル}アミノ)エタノール;
(2S)-1-{[4-メチル-2-(2-メチルビフェニル-3-イル)-1,3-ベンゾチアゾール-6-イル]メチル}ピペリジン-2-カルボン酸;
2-({[4-メチル-2-(2-メチルビフェニル-3-イル)-1,3-ベンゾチアゾール-6-イル]メチル}アミノ)エタノール;
2-({[6-(2-メチルビフェニル-3-イル)フロ[2,3-b]ピラジン-2-イル]メチル}アミノ)エタノール;及び
(2S)-1-{[6-(2-メチルビフェニル-3-イル)フロ[2,3-b]ピラジン-2-イル]メチル}ピペリジン-2-カルボン酸
から選択される前記化合物、またはその薬学的に許容される塩。 - 請求項1に記載の化合物であって、
(2S)-1-{[6-(シアノメトキシ)-2-(2-メチルビフェニル-3-イル)-1,3-ベンゾオキサゾール-5-イル]メチル}ピペリジン-2-カルボン酸;
{[5-{[(2-ヒドロキシエチル)アミノ]メチル}-2-(2-メチルビフェニル-3-イル)-1,3-ベンゾオキサゾール-6-イル]オキシ}アセトニトリル;
(2S)-1-{[6-(3-シアノプロポキシ)-2-(2-メチルビフェニル-3-イル)-1,3-ベンゾオキサゾール-5-イル]メチル}ピペリジン-2-カルボン酸;
3-({[5-{[(2-ヒドロキシエチル)アミノ]メチル}-2-(2-メチルビフェニル-3-イル)-1,3-ベンゾオキサゾール-6-イル]オキシ}メチル)ベンゾニトリル;
2-({[2-(2-メチルビフェニル-3-イル)-6-(ピリジン-2-イルメトキシ)-1,3-ベンゾオキサゾール-5-イル]メチル}アミノ)エタノール;
2-({[6-メトキシ-2-(2-メチルビフェニル-3-イル)-1,3-ベンゾオキサゾール-5-イル]メチル}アミノ)エタノール;
2-({[2-(2-メチルビフェニル-3-イル)-6-(2-モルホリン-4-イルエトキシ)-1,3-ベンゾオキサゾール-5-イル]メチル}アミノ)エタノール;
4-{[5-{[(2-ヒドロキシエチル)アミノ]メチル}-7-メチル-2-(2-メチルビフェニル-3-イル)-1,3-ベンゾオキサゾール-6-イル]オキシ}ブタンニトリル;
(2S)-1-({6-(シアノメトキシ)-2-[4-(2,3-ジヒドロ-1,4-ベンゾジオキシン-6-イル)-3-メチルピリジン-2-イル]-1,3-ベンゾオキサゾール-5-イル}メチル)ピペリジン-2-カルボン酸;
(2S)-1-({6-(シアノメトキシ)-2-[3-(2,3-ジヒドロ-1,4-ベンゾジオキシン-6-イル)-2-メチルフェニル]-1,3-ベンゾオキサゾール-5-イル}メチル)ピペリジン-2-カルボン酸;
(2S)-1-{[2-[2-シアノ-3-(2,3-ジヒドロ-1,4-ベンゾジオキシン-6-イル)フェニル]-6-(シアノメトキシ)-1,3-ベンゾオキサゾール-5-イル]メチル}ピペリジン-2-カルボン酸;
(2S)-1-{[2-(2-メチルビフェニル-3-イル)-1,3-ベンゾオキサゾール-6-イル]メチル}ピペリジン-2-カルボン酸;
[(2-(2’-フルオロ-2-メチルビフェニル-3-イル)-5-{[(2-ヒドロキシエチル)アミノ]メチル}-1,3-ベンゾオキサゾール-6-イル)オキシ]アセトニトリル;及び
[(2-(3-シクロヘキサ-1-エン-1-イル-2-メチルフェニル)-5-{[(2-ヒドロキシエチル)アミノ]メチル}-1,3-ベンゾオキサゾール-6-イル)オキシ]アセトニトリル
から選択される前記化合物、またはその薬学的に許容される塩。 - 2-({[2-(2-メチルビフェニル-3-イル)[1,3]オキサゾロ[5,4-c]ピリジン-6-イル]メチル}アミノ)エタノールである化合物またはその薬学的に許容される塩。
- 請求項1~21のいずれか1項に記載の化合物またはその薬学的に許容される塩もしくは立体異性体、または請求項22~24のいずれか1項記載の化合物またはその薬学的に許容される塩、及び少なくとも1種の薬学的に許容される担体または賦形剤を含む医薬組成物。
- PD-1/PD-L1相互作用を阻害するための医薬であって、請求項1~21のいずれか1項に記載の化合物またはその薬学的に許容される塩もしくは立体異性体、または請求項22~24のいずれか1項記載の化合物またはその薬学的に許容される塩を含む、前記医薬。
- PD-1/PD-L1相互作用の阻害と関連する疾患または障害を治療するための医薬であって、請求項1~21のいずれか1項に記載の化合物またはその薬学的に許容される塩もしくは立体異性体、または請求項22~24のいずれか1項記載の化合物またはその薬学的に許容される塩を含む、前記医薬。
- 前記疾患または障害がウイルス感染症である、請求項27に記載の医薬。
- 前記疾患または障害ががんである、請求項27に記載の医薬。
- がんが、骨癌、膵臓癌、皮膚癌、皮膚または眼内の悪性黒色腫、子宮癌、卵巣癌、直腸癌、肛門部癌、胃癌、精巣癌、卵管癌、子宮内膜癌、子宮体癌、子宮頸部癌、膣癌、外陰部癌、小腸癌、内分泌系癌、甲状腺癌、副甲状腺癌、副腎癌、軟部肉腫、尿道癌、陰茎癌、慢性または急性白血病、小児の固形腫瘍、リンパ球性リンパ腫、膀胱癌、腎盂癌、中枢神経系(CNS)の腫瘍、原発性中枢神経系(CNS)リンパ腫、腫瘍血管形成、脊髄軸腫瘍、脳幹神経膠腫、下垂体腺腫、カポジ肉腫、表皮癌、扁平上皮癌、T細胞リンパ腫、環境誘発癌(アスベストによって誘発される癌を含む)、黒色腫、転移性悪性黒色腫、腎臓癌、明細胞癌、前立腺癌、乳癌、結腸癌、肺癌、非小細胞肺癌、固形腫瘍、食道癌、肝臓癌、胃癌、頭頸部癌、甲状腺癌、膠芽腫、肉腫、血液癌、リンパ腫、白血病、急性リンパ芽球性白血病(ALL)、急性骨髄性白血病(AML)、慢性リンパ性白血病(CLL)、慢性骨髄性白血病(CML)、びまん性大細胞型リンパ腫(DLBCL)、マントル細胞リンパ腫、非ホジキンリンパ腫(NHL)、再発性または難治性非ホジキンリンパ腫(NHL)、再発性濾胞非ホジキンリンパ腫(NHL)、ホジキンリンパ腫、及び多発性骨髄腫から選択される、請求項29に記載の医薬。
- がんがPD-L1を発現する転移性がんである、請求項29に記載の医薬。
- がんが肺癌である、請求項29に記載の医薬。
- 肺癌が非小細胞肺癌である、請求項32に記載の医薬。
- がんが肝臓癌である、請求項29に記載の医薬。
- がんが黒色腫である、請求項29に記載の医薬。
- がんが膀胱の癌である、請求項29に記載の医薬。
- がんが尿道の癌である、請求項29に記載の医薬。
- がんが腎臓癌(renal cancer)である、請求項29に記載の医薬。
- 腎臓癌が腎細胞癌である、請求項38に記載の医薬。
- がんが扁平上皮癌である、請求項29に記載の医薬。
- 患者の免疫応答を増強、刺激、及び/または増加させるための医薬であって、請求項1~21のいずれか1項に記載の化合物またはその薬学的に許容される塩もしくは立体異性体、または請求項22~24のいずれか1項記載の化合物またはその薬学的に許容される塩を含む、前記医薬。
Applications Claiming Priority (7)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201562257342P | 2015-11-19 | 2015-11-19 | |
| US62/257,342 | 2015-11-19 | ||
| US201662332632P | 2016-05-06 | 2016-05-06 | |
| US62/332,632 | 2016-05-06 | ||
| US201662385099P | 2016-09-08 | 2016-09-08 | |
| US62/385,099 | 2016-09-08 | ||
| PCT/US2016/062730 WO2017087777A1 (en) | 2015-11-19 | 2016-11-18 | Heterocyclic compounds as immunomodulators |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2018538269A JP2018538269A (ja) | 2018-12-27 |
| JP7148401B2 true JP7148401B2 (ja) | 2022-10-05 |
Family
ID=57472102
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2018526213A Active JP7148401B2 (ja) | 2015-11-19 | 2016-11-18 | 免疫調節剤としての複素環化合物 |
Country Status (25)
| Country | Link |
|---|---|
| US (2) | US20170145025A1 (ja) |
| EP (2) | EP3377488B1 (ja) |
| JP (1) | JP7148401B2 (ja) |
| KR (1) | KR20180095824A (ja) |
| CN (1) | CN109641885B (ja) |
| AU (2) | AU2016358100B2 (ja) |
| CA (1) | CA3005727A1 (ja) |
| DK (1) | DK3377488T3 (ja) |
| EA (1) | EA201891203A1 (ja) |
| ES (1) | ES2928856T3 (ja) |
| HR (1) | HRP20221035T1 (ja) |
| HU (1) | HUE060680T2 (ja) |
| IL (2) | IL259406B (ja) |
| LT (1) | LT3377488T (ja) |
| MD (1) | MD3377488T2 (ja) |
| MX (1) | MX2018006207A (ja) |
| PH (1) | PH12018501084A1 (ja) |
| PL (1) | PL3377488T3 (ja) |
| PT (1) | PT3377488T (ja) |
| RS (1) | RS63762B1 (ja) |
| SG (2) | SG11201804152RA (ja) |
| SI (1) | SI3377488T1 (ja) |
| TW (1) | TWI763641B (ja) |
| WO (1) | WO2017087777A1 (ja) |
| ZA (1) | ZA201803958B (ja) |
Families Citing this family (163)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2012088266A2 (en) | 2010-12-22 | 2012-06-28 | Incyte Corporation | Substituted imidazopyridazines and benzimidazoles as inhibitors of fgfr3 |
| CN107652289B (zh) | 2012-06-13 | 2020-07-21 | 因塞特控股公司 | 作为fgfr抑制剂的取代的三环化合物 |
| JP6449244B2 (ja) | 2013-04-19 | 2019-01-09 | インサイト・ホールディングス・コーポレイションIncyte Holdings Corporation | Fgfr抑制剤としての二環式複素環 |
| US10851105B2 (en) | 2014-10-22 | 2020-12-01 | Incyte Corporation | Bicyclic heterocycles as FGFR4 inhibitors |
| WO2016134320A1 (en) | 2015-02-20 | 2016-08-25 | Incyte Corporation | Bicyclic heterocycles as fgfr inhibitors |
| MA41551A (fr) | 2015-02-20 | 2017-12-26 | Incyte Corp | Hétérocycles bicycliques utilisés en tant qu'inhibiteurs de fgfr4 |
| EP3365340B1 (en) | 2015-10-19 | 2022-08-10 | Incyte Corporation | Heterocyclic compounds as immunomodulators |
| HRP20221035T1 (hr) | 2015-11-19 | 2022-11-11 | Incyte Corporation | Heterociklički spojevi kao imunomodulatori |
| PE20230731A1 (es) | 2015-12-22 | 2023-05-03 | Incyte Corp | Compuestos heterociclicos como inmunomoduladores |
| AR108396A1 (es) | 2016-05-06 | 2018-08-15 | Incyte Corp | Compuestos heterocíclicos como inmunomoduladores |
| EP3464279B1 (en) | 2016-05-26 | 2021-11-24 | Incyte Corporation | Heterocyclic compounds as immunomodulators |
| TWI771305B (zh) | 2016-06-20 | 2022-07-21 | 美商英塞特公司 | 作為免疫調節劑之雜環化合物 |
| EP3474845B1 (en) | 2016-06-27 | 2024-03-20 | ChemoCentryx, Inc. | Immunomodulator compounds |
| WO2018013789A1 (en) | 2016-07-14 | 2018-01-18 | Incyte Corporation | Heterocyclic compounds as immunomodulators |
| US20180057486A1 (en) | 2016-08-29 | 2018-03-01 | Incyte Corporation | Heterocyclic compounds as immunomodulators |
| CR20190181A (es) | 2016-10-14 | 2019-08-21 | Prec Biosciences Inc | Meganucleasas diseñadas específicamente para el reconocimiento de secuencias en el genoma del virus de la hepatitis b. |
| WO2018119266A1 (en) | 2016-12-22 | 2018-06-28 | Incyte Corporation | Benzooxazole derivatives as immunomodulators |
| PE20200005A1 (es) | 2016-12-22 | 2020-01-06 | Incyte Corp | Derivados de tetrahidro imidazo[4,5-c]piridina como inductores de internalizacion pd-l1 |
| WO2018119221A1 (en) | 2016-12-22 | 2018-06-28 | Incyte Corporation | Pyridine derivatives as immunomodulators |
| ES2874756T3 (es) | 2016-12-22 | 2021-11-05 | Incyte Corp | Derivados de triazolo[1,5-A]piridina como inmunomoduladores |
| JOP20180040A1 (ar) | 2017-04-20 | 2019-01-30 | Gilead Sciences Inc | مثبطات pd-1/pd-l1 |
| WO2018200571A1 (en) | 2017-04-25 | 2018-11-01 | Arbutus Biopharma Corporation | Substituted 2,3-dihydro-1h-indene analogs and methods using same |
| AR111960A1 (es) | 2017-05-26 | 2019-09-04 | Incyte Corp | Formas cristalinas de un inhibidor de fgfr y procesos para su preparación |
| IL272258B (en) | 2017-07-28 | 2022-08-01 | Chemocentryx Inc | Immunomodulator compounds |
| US10392405B2 (en) | 2017-08-08 | 2019-08-27 | Chemocentryx, Inc. | Macrocyclic immunomodulators |
| CN111511754B (zh) | 2017-12-20 | 2023-09-12 | 捷克共和国有机化学与生物化学研究所 | 活化sting转接蛋白的具有膦酸酯键的2’3’环状二核苷酸 |
| AU2018392213B2 (en) | 2017-12-20 | 2021-03-04 | Institute Of Organic Chemistry And Biochemistry Ascr, V.V.I. | 3'3' cyclic dinucleotides with phosphonate bond activating the STING adaptor protein |
| CN110092799B (zh) * | 2018-01-29 | 2021-11-12 | 广州丹康医药生物有限公司 | 一种环状化合物、其制备方法和应用 |
| AU2019222644B2 (en) | 2018-02-13 | 2021-04-01 | Gilead Sciences, Inc. | PD-1/PD-L1 inhibitors |
| US10568874B2 (en) | 2018-02-22 | 2020-02-25 | Chemocentryx, Inc. | Indane-amines as PD-L1 antagonists |
| KR102526964B1 (ko) | 2018-02-26 | 2023-04-28 | 길리애드 사이언시즈, 인코포레이티드 | Hbv 복제 억제제로서의 치환된 피롤리진 화합물 |
| IL303087B1 (en) | 2018-02-27 | 2024-08-01 | Incyte Corp | Midazopyrimidines and triazolopyrimidines as A2A /A2B inhibitors |
| US12083118B2 (en) | 2018-03-29 | 2024-09-10 | Arbutus Biopharma Corporation | Substituted 1,1′-biphenyl compounds, analogues thereof, and methods using same |
| CN112423759A (zh) | 2018-03-30 | 2021-02-26 | 因赛特公司 | 使用jak抑制剂治疗化脓性汗腺炎 |
| FI3774791T3 (fi) * | 2018-03-30 | 2023-03-21 | Incyte Corp | Heterosyklisiä yhdisteitä immunomodulaattoreina |
| EP3774883A1 (en) | 2018-04-05 | 2021-02-17 | Gilead Sciences, Inc. | Antibodies and fragments thereof that bind hepatitis b virus protein x |
| TWI818007B (zh) | 2018-04-06 | 2023-10-11 | 捷克科學院有機化學與生物化學研究所 | 2'3'-環二核苷酸 |
| TW202005654A (zh) | 2018-04-06 | 2020-02-01 | 捷克科學院有機化學與生物化學研究所 | 2,2,─環二核苷酸 |
| TWI833744B (zh) | 2018-04-06 | 2024-03-01 | 捷克科學院有機化學與生物化學研究所 | 3'3'-環二核苷酸 |
| CN108409686A (zh) * | 2018-04-08 | 2018-08-17 | 青岛康庆和医药科技有限责任公司 | 一种可用于制备治疗呼吸道合胞体病毒感染的药物及其制备方法 |
| US11142750B2 (en) | 2018-04-12 | 2021-10-12 | Precision Biosciences, Inc. | Optimized engineered meganucleases having specificity for a recognition sequence in the Hepatitis B virus genome |
| CN112041311B (zh) | 2018-04-19 | 2023-10-03 | 吉利德科学公司 | Pd-1/pd-l1抑制剂 |
| WO2019211799A1 (en) | 2018-05-03 | 2019-11-07 | Institute Of Organic Chemistry And Biochemistry Ascr, V.V.I. | 2'3'-cyclic dinucleotide analogue comprising a cyclopentanyl modified nucleotide |
| SG11202010882XA (en) | 2018-05-04 | 2020-11-27 | Incyte Corp | Salts of an fgfr inhibitor |
| DK3788047T3 (da) | 2018-05-04 | 2024-09-16 | Incyte Corp | Faste former af en FGFR-inhibitor og fremgangsmåder til fremstilling deraf |
| BR112020022936A2 (pt) | 2018-05-11 | 2021-02-02 | Incyte Corporation | derivados de tetra-hidro-imidazo[4,5-c]piridina como imunomoduladores de pd-l1 |
| US11168089B2 (en) | 2018-05-18 | 2021-11-09 | Incyte Corporation | Fused pyrimidine derivatives as A2A / A2B inhibitors |
| MX2020012939A (es) | 2018-05-31 | 2021-02-15 | Ono Pharmaceutical Co | Biomarcadores para determinar la eficacia de los inhibidores de puntos de control inmunitarios. |
| CN113166153A (zh) | 2018-07-05 | 2021-07-23 | 因赛特公司 | 作为a2a/a2b抑制剂的稠合吡嗪衍生物 |
| EP4234030A3 (en) | 2018-07-13 | 2023-10-18 | Gilead Sciences, Inc. | Pd-1/pd-l1 inhibitors |
| CN112424194B (zh) * | 2018-07-19 | 2024-02-06 | 贝达药业股份有限公司 | 免疫调节剂及其组合物和制备方法 |
| WO2020028097A1 (en) | 2018-08-01 | 2020-02-06 | Gilead Sciences, Inc. | Solid forms of (r)-11-(methoxymethyl)-12-(3-methoxypropoxy)-3,3-dimethyl-8-0x0-2,3,8,13b-tetrahydro-1h-pyrido[2,1-a]pyrrolo[1,2-c] phthalazine-7-c arboxylic acid |
| CA3112286A1 (en) * | 2018-09-13 | 2020-03-19 | Betta Pharmaceuticals Co., Ltd | Immunomodulators, compositions and methods there of |
| ES2973117T3 (es) | 2018-09-25 | 2024-06-18 | Incyte Corp | Compuestos de pirazolo[4,3-d]pirimidina como moduladores de ALK2 y/o FGFR |
| US11066404B2 (en) | 2018-10-11 | 2021-07-20 | Incyte Corporation | Dihydropyrido[2,3-d]pyrimidinone compounds as CDK2 inhibitors |
| SG11202103573YA (en) | 2018-10-11 | 2021-05-28 | Ono Pharmaceutical Co | STING Agonistic Compound |
| WO2020086556A1 (en) | 2018-10-24 | 2020-04-30 | Gilead Sciences, Inc. | Pd-1/pd-l1 inhibitors |
| EP3873903B1 (en) | 2018-10-31 | 2024-01-24 | Gilead Sciences, Inc. | Substituted 6-azabenzimidazole compounds as hpk1 inhibitors |
| US11071730B2 (en) | 2018-10-31 | 2021-07-27 | Gilead Sciences, Inc. | Substituted 6-azabenzimidazole compounds |
| KR20210089195A (ko) | 2018-11-02 | 2021-07-15 | 상하이 맥시노벨 파마수티컬스 씨오., 엘티디. | 비페닐계 화합물, 이의 중간체, 제조 방법, 약학 조성물 및 용도 |
| US11459329B2 (en) | 2018-12-20 | 2022-10-04 | Incyte Corporation | Imidazopyridazine and imidazopyridine compounds and uses thereof |
| TWI829857B (zh) | 2019-01-29 | 2024-01-21 | 美商英塞特公司 | 作為a2a / a2b抑制劑之吡唑并吡啶及三唑并吡啶 |
| WO2020156323A1 (en) * | 2019-01-31 | 2020-08-06 | Betta Pharmaceuticals Co., Ltd | Immunomodulators, compositions and methods thereof |
| EP3923949A1 (en) | 2019-02-15 | 2021-12-22 | Incyte Corporation | Cyclin-dependent kinase 2 biomarkers and uses thereof |
| WO2020168197A1 (en) | 2019-02-15 | 2020-08-20 | Incyte Corporation | Pyrrolo[2,3-d]pyrimidinone compounds as cdk2 inhibitors |
| US11472791B2 (en) | 2019-03-05 | 2022-10-18 | Incyte Corporation | Pyrazolyl pyrimidinylamine compounds as CDK2 inhibitors |
| KR20210137518A (ko) | 2019-03-07 | 2021-11-17 | 인스티튜트 오브 오가닉 케미스트리 앤드 바이오케미스트리 에이에스 씨알 브이.브이.아이. | 3'3'-사이클릭 다이뉴클레오티드 및 이의 프로드럭 |
| US11766447B2 (en) | 2019-03-07 | 2023-09-26 | Institute Of Organic Chemistry And Biochemistry Ascr, V.V.I. | 3′3′-cyclic dinucleotide analogue comprising a cyclopentanyl modified nucleotide as sting modulator |
| CN113543851A (zh) | 2019-03-07 | 2021-10-22 | 捷克共和国有机化学与生物化学研究所 | 2’3’-环二核苷酸及其前药 |
| US11628162B2 (en) | 2019-03-08 | 2023-04-18 | Incyte Corporation | Methods of treating cancer with an FGFR inhibitor |
| CA3134171A1 (en) | 2019-03-22 | 2020-10-01 | Guangzhou Maxinovel Pharmaceuticals Co., Ltd. | Small-molecule inhibitor of pd-1/pd-l1, pharmaceutical composition thereof with pd-l1 antibody, and application of same |
| WO2020205560A1 (en) | 2019-03-29 | 2020-10-08 | Incyte Corporation | Sulfonylamide compounds as cdk2 inhibitors |
| CN111793077B (zh) * | 2019-04-01 | 2023-08-04 | 东莞市东阳光新药研发有限公司 | Pd-1/pd-l1小分子抑制剂及其在药物中的应用 |
| TW202212339A (zh) | 2019-04-17 | 2022-04-01 | 美商基利科學股份有限公司 | 類鐸受體調節劑之固體形式 |
| TW202210480A (zh) | 2019-04-17 | 2022-03-16 | 美商基利科學股份有限公司 | 類鐸受體調節劑之固體形式 |
| US11447494B2 (en) | 2019-05-01 | 2022-09-20 | Incyte Corporation | Tricyclic amine compounds as CDK2 inhibitors |
| WO2020223469A1 (en) | 2019-05-01 | 2020-11-05 | Incyte Corporation | N-(1-(methylsulfonyl)piperidin-4-yl)-4,5-di hydro-1h-imidazo[4,5-h]quinazolin-8-amine derivatives and related compounds as cyclin-dependent kinase 2 (cdk2) inhibitors for treating cancer |
| AU2020276277A1 (en) | 2019-05-15 | 2021-12-09 | Chemocentryx, Inc. | Triaryl compounds for treatment of PD-L1 diseases |
| WO2020237025A1 (en) | 2019-05-23 | 2020-11-26 | Gilead Sciences, Inc. | Substituted exo-methylene-oxindoles which are hpk1/map4k1 inhibitors |
| KR20220024701A (ko) | 2019-06-20 | 2022-03-03 | 케모센트릭스, 인크. | Pd-l1 질환의 치료를 위한 화합물 |
| WO2021007269A1 (en) | 2019-07-09 | 2021-01-14 | Incyte Corporation | Bicyclic heterocycles as fgfr inhibitors |
| BR112021025888A2 (pt) | 2019-07-10 | 2022-04-26 | Chemocentryx Inc | Indanos como inibidores de pd-l1 |
| US20220257619A1 (en) | 2019-07-18 | 2022-08-18 | Gilead Sciences, Inc. | Long-acting formulations of tenofovir alafenamide |
| CN114206386A (zh) | 2019-08-05 | 2022-03-18 | 小野药品工业株式会社 | 免疫检查点抑制剂的有效性判定生物标记 |
| WO2021030162A1 (en) | 2019-08-09 | 2021-02-18 | Incyte Corporation | Salts of a pd-1/pd-l1 inhibitor |
| WO2021030537A1 (en) | 2019-08-14 | 2021-02-18 | Incyte Corporation | Imidazolyl pyrimidinylamine compounds as cdk2 inhibitors |
| WO2021034804A1 (en) | 2019-08-19 | 2021-02-25 | Gilead Sciences, Inc. | Pharmaceutical formulations of tenofovir alafenamide |
| JP7559059B2 (ja) | 2019-09-30 | 2024-10-01 | インサイト・コーポレイション | 免疫調節剤としてのピリド[3,2-d]ピリミジン化合物 |
| JP2022550427A (ja) * | 2019-09-30 | 2022-12-01 | メッドシャイン ディスカバリー インコーポレイテッド | Pd-1/pd-l1小分子阻害剤としての化合物及びその使用 |
| MX2022003658A (es) | 2019-09-30 | 2022-04-25 | Gilead Sciences Inc | Vacunas contra el virus de la hepatitis b (vhb) y metodos para tratar el vhb. |
| WO2021067374A1 (en) | 2019-10-01 | 2021-04-08 | Incyte Corporation | Bicyclic heterocycles as fgfr inhibitors |
| PE20221905A1 (es) | 2019-10-11 | 2022-12-23 | Incyte Corp | Aminas biciclicas como inhibidoras de la cdk2 |
| MX2022004513A (es) | 2019-10-14 | 2022-07-19 | Incyte Corp | Heterociclos biciclicos como inhibidores de los receptores del factor de crecimiento de fibroblastos (fgfr). |
| WO2021076728A1 (en) | 2019-10-16 | 2021-04-22 | Incyte Corporation | Bicyclic heterocycles as fgfr inhibitors |
| MX2022004450A (es) | 2019-10-16 | 2022-05-03 | Chemocentryx Inc | Aminas de heteroaril-bifenilo para el tratamiento de enfermedades pd-l1. |
| US11713307B2 (en) | 2019-10-16 | 2023-08-01 | Chemocentryx, Inc. | Heteroaryl-biphenyl amides for the treatment of PD-L1 diseases |
| MX2022005651A (es) | 2019-11-11 | 2022-07-27 | Incyte Corp | Sales y formas cristalinas de un inhibidor de la proteina de muerte celular programada 1 (pd-1)/ligando de muerte celular programada 1 (pd-l1). |
| BR112022010664A2 (pt) | 2019-12-04 | 2022-08-16 | Incyte Corp | Derivados de um inibidor de fgfr |
| JP2023505258A (ja) | 2019-12-04 | 2023-02-08 | インサイト・コーポレイション | Fgfr阻害剤としての三環式複素環 |
| WO2021113765A1 (en) | 2019-12-06 | 2021-06-10 | Precision Biosciences, Inc. | Optimized engineered meganucleases having specificity for a recognition sequence in the hepatitis b virus genome |
| CN115279766A (zh) | 2020-01-03 | 2022-11-01 | 因赛特公司 | 包含a2a/a2b和pd-1/pd-l1抑制剂的组合疗法 |
| CA3163216A1 (en) | 2020-01-10 | 2021-07-15 | Incyte Corporation | Tricyclic compounds as inhibitors of kras |
| US12012409B2 (en) | 2020-01-15 | 2024-06-18 | Incyte Corporation | Bicyclic heterocycles as FGFR inhibitors |
| WO2021150613A1 (en) | 2020-01-20 | 2021-07-29 | Incyte Corporation | Spiro compounds as inhibitors of kras |
| US20230111910A1 (en) * | 2020-01-21 | 2023-04-13 | Shanghai Synergy Pharmaceutical Sciences Co., Ltd. | Pd-1/pd-l1 inhibitor, preparation method therefor, and use thereof |
| WO2021158891A1 (en) | 2020-02-06 | 2021-08-12 | Incyte Corporation | Salts and solid forms and processes of preparing a pi3k inhibitor |
| EP4114401A1 (en) | 2020-03-06 | 2023-01-11 | Incyte Corporation | Combination therapy comprising axl/mer and pd-1/pd-l1 inhibitors |
| JP2023518433A (ja) | 2020-03-20 | 2023-05-01 | ギリアード サイエンシーズ, インコーポレイテッド | 4’-c-置換-2-ハロ-2’-デオキシアデノシンヌクレオシドのプロドラッグ並びにその製造法及び使用法 |
| US20230141284A1 (en) | 2020-04-10 | 2023-05-11 | Ono Pharmaceutical Co., Ltd. | Cancer therapeutic method |
| WO2021205631A1 (ja) | 2020-04-10 | 2021-10-14 | 小野薬品工業株式会社 | Sting作動化合物 |
| EP4135844A1 (en) | 2020-04-16 | 2023-02-22 | Incyte Corporation | Fused tricyclic kras inhibitors |
| MX2022013864A (es) | 2020-05-05 | 2023-03-09 | Teon Therapeutics Inc | Moduladores del receptor cannabinoide tipo 2 (cb2) y usos de los mismos. |
| WO2021231526A1 (en) | 2020-05-13 | 2021-11-18 | Incyte Corporation | Fused pyrimidine compounds as kras inhibitors |
| CN113717165A (zh) * | 2020-05-22 | 2021-11-30 | 上海长森药业有限公司 | 新型三环芳香杂环化合物,及其制备方法、药物组合物和应用 |
| CN115956081A (zh) | 2020-06-12 | 2023-04-11 | 因赛特公司 | 具有作为alk2抑制剂的活性的咪唑并哒嗪化合物 |
| WO2021257863A1 (en) | 2020-06-19 | 2021-12-23 | Incyte Corporation | Pyrrolotriazine compounds as jak2 v617f inhibitors |
| US11691971B2 (en) | 2020-06-19 | 2023-07-04 | Incyte Corporation | Naphthyridinone compounds as JAK2 V617F inhibitors |
| WO2022006456A1 (en) | 2020-07-02 | 2022-01-06 | Incyte Corporation | Tricyclic pyridone compounds as jak2 v617f inhibitors |
| WO2022006457A1 (en) | 2020-07-02 | 2022-01-06 | Incyte Corporation | Tricyclic urea compounds as jak2 v617f inhibitors |
| WO2022046989A1 (en) | 2020-08-27 | 2022-03-03 | Incyte Corporation | Tricyclic urea compounds as jak2 v617f inhibitors |
| US11999752B2 (en) | 2020-08-28 | 2024-06-04 | Incyte Corporation | Vinyl imidazole compounds as inhibitors of KRAS |
| EP4212511A1 (en) | 2020-09-09 | 2023-07-19 | Guangzhou Maxinovel Pharmaceuticals Co., Ltd. | Aromatic ethylene compound and preparation method therefor, and intermediate, pharmaceutical composition, and application thereof |
| WO2022072783A1 (en) | 2020-10-02 | 2022-04-07 | Incyte Corporation | Bicyclic dione compounds as inhibitors of kras |
| EP4225742A1 (en) | 2020-10-05 | 2023-08-16 | Enliven Therapeutics, Inc. | 5- and 6-azaindole compounds for inhibition of bcr-abl tyrosine kinases |
| TW202233615A (zh) | 2020-11-06 | 2022-09-01 | 美商英塞特公司 | Pd—1/pd—l1抑制劑之結晶形式 |
| KR20230117573A (ko) * | 2020-11-06 | 2023-08-08 | 인사이트 코포레이션 | Pd-1 및 pd-l1 억제제, 및 이의 염 및 결정형의 제조 방법 |
| US11780836B2 (en) | 2020-11-06 | 2023-10-10 | Incyte Corporation | Process of preparing a PD-1/PD-L1 inhibitor |
| WO2022140231A1 (en) | 2020-12-21 | 2022-06-30 | Incyte Corporation | Deazaguaine compounds as jak2 v617f inhibitors |
| JP2024502005A (ja) | 2020-12-29 | 2024-01-17 | インサイト・コーポレイション | A2a/a2b阻害剤、pd-1/pd-l1阻害剤、及び抗cd73抗体を含む併用療法 |
| AR125273A1 (es) | 2021-02-25 | 2023-07-05 | Incyte Corp | Lactamas espirocíclicas como inhibidores de jak2 v617f |
| US12077539B2 (en) | 2021-03-22 | 2024-09-03 | Incyte Corporation | Imidazole and triazole KRAS inhibitors |
| EP4323405A1 (en) | 2021-04-12 | 2024-02-21 | Incyte Corporation | Combination therapy comprising an fgfr inhibitor and a nectin-4 targeting agent |
| TW202310852A (zh) | 2021-05-13 | 2023-03-16 | 美商基利科學股份有限公司 | TLR8調節化合物及抗HBV siRNA療法之組合 |
| WO2022261159A1 (en) | 2021-06-09 | 2022-12-15 | Incyte Corporation | Tricyclic heterocycles as fgfr inhibitors |
| CA3220274A1 (en) | 2021-06-09 | 2022-12-15 | Incyte Corporation | Tricyclic heterocycles as fgfr inhibitors |
| TW202317200A (zh) | 2021-06-11 | 2023-05-01 | 美商基利科學股份有限公司 | Mcl-1抑制劑與抗體藥物接合物之組合 |
| TW202315637A (zh) | 2021-06-11 | 2023-04-16 | 美商基利科學股份有限公司 | Mcl-1抑制劑與抗癌劑之組合 |
| US11981671B2 (en) | 2021-06-21 | 2024-05-14 | Incyte Corporation | Bicyclic pyrazolyl amines as CDK2 inhibitors |
| EP4359411A1 (en) | 2021-06-23 | 2024-05-01 | Gilead Sciences, Inc. | Diacylglyercol kinase modulating compounds |
| US11932634B2 (en) | 2021-06-23 | 2024-03-19 | Gilead Sciences, Inc. | Diacylglycerol kinase modulating compounds |
| CN117396478A (zh) | 2021-06-23 | 2024-01-12 | 吉利德科学公司 | 二酰基甘油激酶调节化合物 |
| EP4359415A1 (en) | 2021-06-23 | 2024-05-01 | Gilead Sciences, Inc. | Diacylglyercol kinase modulating compounds |
| TW202317565A (zh) | 2021-07-07 | 2023-05-01 | 美商英塞特公司 | 作為kras抑制劑的三環化合物 |
| JP2024529347A (ja) | 2021-07-14 | 2024-08-06 | インサイト・コーポレイション | Krasの阻害剤としての三環式化合物 |
| EP4396187A1 (en) | 2021-08-31 | 2024-07-10 | Incyte Corporation | Naphthyridine compounds as inhibitors of kras |
| WO2023034530A1 (en) | 2021-09-02 | 2023-03-09 | Teon Therapeutics, Inc. | Methods of improving growth and function of immune cells |
| US12030883B2 (en) | 2021-09-21 | 2024-07-09 | Incyte Corporation | Hetero-tricyclic compounds as inhibitors of KRAS |
| JP2024537824A (ja) | 2021-10-01 | 2024-10-16 | インサイト・コーポレイション | ピラゾロキノリンkras阻害剤 |
| IL312114A (en) | 2021-10-14 | 2024-06-01 | Incyte Corp | Quinoline compounds as Kras inhibitors |
| WO2023081730A1 (en) | 2021-11-03 | 2023-05-11 | Teon Therapeutics, Inc. | 4-hydroxy-2-oxo-1,2-dihydro-1,8-naphthyridine-3-carboxamide derivatives as cannabinoid cb2 receptor modulators for the treatment of cancer |
| TW202320792A (zh) | 2021-11-22 | 2023-06-01 | 美商英塞特公司 | 包含fgfr抑制劑及kras抑制劑之組合療法 |
| WO2023097211A1 (en) | 2021-11-24 | 2023-06-01 | The University Of Southern California | Methods for enhancing immune checkpoint inhibitor therapy |
| US11976073B2 (en) | 2021-12-10 | 2024-05-07 | Incyte Corporation | Bicyclic amines as CDK2 inhibitors |
| AR128043A1 (es) | 2021-12-22 | 2024-03-20 | Incyte Corp | Sales y formas sólidas de un inhibidor de fgfr y procesos para su preparación |
| US12084430B2 (en) | 2022-03-17 | 2024-09-10 | Incyte Corporation | Tricyclic urea compounds as JAK2 V617F inhibitors |
| US20230399342A1 (en) | 2022-06-08 | 2023-12-14 | Incyte Corporation | Tricyclic triazolo compounds as dgk inhibitors |
| US20240101557A1 (en) | 2022-07-11 | 2024-03-28 | Incyte Corporation | Fused tricyclic compounds as inhibitors of kras g12v mutants |
| WO2024015372A1 (en) | 2022-07-14 | 2024-01-18 | Teon Therapeutics, Inc. | Adenosine receptor antagonists and uses thereof |
| WO2024086717A2 (en) * | 2022-10-19 | 2024-04-25 | University Of Florida Research Foundation, Incorporated | Heteroaryl enhancers of the particulate guanylyl cyclase receptor a |
| US20240190876A1 (en) | 2022-10-21 | 2024-06-13 | Incyte Corporation | Tricyclic Urea Compounds As JAK2 V617F Inhibitors |
| TW202428272A (zh) | 2022-11-18 | 2024-07-16 | 美商英塞特公司 | 作為dgk抑制劑之雜芳基氟烯烴 |
| TW202428575A (zh) | 2023-01-12 | 2024-07-16 | 美商英塞特公司 | 作為dgk抑制劑之雜芳基氟代烯烴 |
| US20240317744A1 (en) | 2023-03-13 | 2024-09-26 | Incyte Corporation | Bicyclic Ureas As Kinase Inhibitors |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2013033901A1 (en) | 2011-09-08 | 2013-03-14 | Merck Sharp & Dohme Corp. | Heterocyclic-substituted benzofuran derivatives and methods of use thereof for the treatment of viral diseases |
| JP2013084945A (ja) | 2011-09-29 | 2013-05-09 | Toyo Ink Sc Holdings Co Ltd | 太陽電池封止材用樹脂組成物 |
| WO2015034820A1 (en) | 2013-09-04 | 2015-03-12 | Bristol-Myers Squibb Company | Compounds useful as immunomodulators |
| WO2015197028A1 (en) | 2014-06-28 | 2015-12-30 | Sunshine Lake Pharma Co., Ltd. | Compounds as hepatitis c virus (hcv) inhibitors and uses thereof in medicine |
| JP2019530732A (ja) | 2016-08-03 | 2019-10-24 | アライジング・インターナショナル・インコーポレイテッドArising International, Inc. | 免疫モジュレータとして有用な対称または半対称化合物 |
Family Cites Families (335)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3272781A (en) | 1963-08-07 | 1966-09-13 | American Potash & Chem Corp | Boroureas of phosphinoborine polymers |
| FR1425700A (fr) | 1965-02-22 | 1966-01-24 | Basf Ag | Composés formant des complexes métalliques et procédé pour les préparer et les utiliser |
| US4208328A (en) | 1978-04-27 | 1980-06-17 | General Electric Company | Alkyl 3,5-dihydroxy-4-(2-benzothiazolyl)benzoates |
| US4789711A (en) | 1986-12-02 | 1988-12-06 | Ciba-Geigy Corporation | Multifunctional epoxide resins |
| DE3828535A1 (de) | 1988-08-23 | 1990-03-08 | Basf Ag | Benzimidazol-2-carbonsaeureanilide, ihre verwendung als lichtschutzmittel fuer organisches material und mit diesen aniliden stabilisiertes organisches material |
| US5077164A (en) | 1989-06-21 | 1991-12-31 | Minolta Camera Kabushiki Kaisha | Photosensitive member containing an azo dye |
| DE69421982T2 (de) | 1993-09-20 | 2000-03-30 | Fuji Photo Film Co., Ltd. | Positiv arbeitende Photoresistzusammensetzung |
| JP3461397B2 (ja) | 1995-01-11 | 2003-10-27 | 富士写真フイルム株式会社 | ポジ型フオトレジスト組成物 |
| JP2001505585A (ja) | 1996-12-16 | 2001-04-24 | 藤沢薬品工業株式会社 | 新規アミド化合物およびそれらの一酸化窒素シンターゼ阻害剤としての用途 |
| JPH10316853A (ja) | 1997-05-15 | 1998-12-02 | Sumitomo Bakelite Co Ltd | 半導体多層配線用層間絶縁膜樹脂組成物及び該絶縁膜の製造方法 |
| EP1019391A1 (en) | 1997-10-02 | 2000-07-19 | Merck & Co. Inc. | Inhibitors of prenyl-protein transferase |
| WO1999044992A1 (fr) | 1998-03-05 | 1999-09-10 | Nissan Chemical Industries, Ltd. | Composes d'anilide et herbicide |
| JP2000128986A (ja) | 1998-10-28 | 2000-05-09 | Sumitomo Bakelite Co Ltd | ポリベンゾオキサゾール前駆体及びポリベンゾオキサゾール |
| JP2000128987A (ja) | 1998-10-28 | 2000-05-09 | Sumitomo Bakelite Co Ltd | ポリベンゾオキサゾール前駆体及びポリベンゾオキサゾール |
| JP2000128984A (ja) | 1998-10-28 | 2000-05-09 | Sumitomo Bakelite Co Ltd | ポリベンゾオキサゾール前駆体及び樹脂 |
| US6297351B1 (en) | 1998-12-17 | 2001-10-02 | Sumitomo Bakelite Company Limited | Polybenzoxazole resin and precursor thereof |
| EA200100675A1 (ru) | 1998-12-18 | 2001-12-24 | Аксис Фармасьютикалз, Инк. | Ингибиторы протеазы |
| JP2000212281A (ja) | 1999-01-27 | 2000-08-02 | Sumitomo Bakelite Co Ltd | ポリベンゾオキサゾ―ル前駆体及びポリベンゾオキサゾ―ル樹脂 |
| WO2001007409A1 (en) | 1999-07-23 | 2001-02-01 | Astrazeneca Uk Limited | Carbazole derivatives and their use as neuropeptide y5 receptor ligands |
| JP2001114893A (ja) | 1999-10-15 | 2001-04-24 | Sumitomo Bakelite Co Ltd | ポリベンゾオキサゾール樹脂およびその前駆体 |
| US6372907B1 (en) | 1999-11-03 | 2002-04-16 | Apptera Corporation | Water-soluble rhodamine dye peptide conjugates |
| JP2001163975A (ja) | 1999-12-03 | 2001-06-19 | Sumitomo Bakelite Co Ltd | ポリベンゾオキサゾール樹脂及びその前駆体 |
| CN1623984A (zh) | 1999-12-27 | 2005-06-08 | 日本烟草产业株式会社 | 稠环化合物及其药物用途 |
| DE50112961D1 (de) | 2000-02-01 | 2007-10-18 | Abbott Gmbh & Co Kg | Heterozyklische verbindungen und deren anwendung als parp-inhibitoren |
| US6521618B2 (en) | 2000-03-28 | 2003-02-18 | Wyeth | 3-cyanoquinolines, 3-cyano-1,6-naphthyridines, and 3-cyano-1,7-naphthyridines as protein kinase inhibitors |
| ATE361297T1 (de) | 2000-03-31 | 2007-05-15 | Ortho Mcneil Pharm Inc | Phenyl-substituierte imidazopyridine |
| EP1278734A2 (en) | 2000-04-24 | 2003-01-29 | Merck Frosst Canada & Co. | Method of treatment using phenyl and biaryl derivatives as prostaglandin e inhibitors and compounds useful therefore |
| CZ303572B6 (cs) | 2000-06-28 | 2012-12-12 | Smithkline Beecham P. L. C. | Jemne rozmelnený prostredek a zpusob jeho prípravy |
| WO2002014321A1 (en) | 2000-08-11 | 2002-02-21 | The Regents Of The University Of California | Use of stat-6 inhibitors as therapeutic agents |
| AU2002224927A1 (en) | 2000-12-13 | 2002-06-24 | Basf Aktiengesellschaft | Use of substituted imidazoazines, novel imidazoazines, methods for the production thereof, and agents containing these compounds |
| US6919352B2 (en) | 2000-12-15 | 2005-07-19 | Smithkline Beecham Corporation | Pyrazolopyridinyl pyridine and pyrimidine therapeutic compounds |
| SE0100567D0 (sv) | 2001-02-20 | 2001-02-20 | Astrazeneca Ab | Compounds |
| AU2002258550B2 (en) | 2001-03-14 | 2006-04-27 | Eli Lilly And Company | Retinoid X receptor modulators |
| WO2002078700A1 (en) | 2001-03-30 | 2002-10-10 | Smithkline Beecham Corporation | Pyralopyridines, process for their preparation and use as therapteutic compounds |
| WO2002083672A1 (en) | 2001-04-10 | 2002-10-24 | Smithkline Beecham Corporation | Antiviral pyrazolopyridine compounds |
| JP2002316966A (ja) | 2001-04-19 | 2002-10-31 | Ueno Seiyaku Oyo Kenkyusho:Kk | ビナフトール誘導体およびその製法 |
| WO2002088124A2 (en) | 2001-04-27 | 2002-11-07 | Smithkline Beecham Corporation | Pyrazolo'1,5-a!pyridine derivatives |
| AR035543A1 (es) | 2001-06-26 | 2004-06-16 | Japan Tobacco Inc | Agente terapeutico para la hepatitis c que comprende un compuesto de anillo condensado, compuesto de anillo condensado, composicion farmaceutica que lo comprende, compuestos de benzimidazol, tiazol y bifenilo utiles como intermediarios para producir dichos compuestos, uso del compuesto de anillo con |
| EP1423389B1 (en) | 2001-09-07 | 2007-06-06 | SmithKline Beecham Corporation | Pyrazolo-pyridines for the treatment of herpes infections |
| TWI331526B (en) | 2001-09-21 | 2010-10-11 | Bristol Myers Squibb Pharma Co | Lactam-containing compounds and derivatives thereof as factor xa inhibitors |
| MXPA04003419A (es) | 2001-10-09 | 2004-07-08 | Upjohn Co | Tetrahidro y hexahidro-carbazoles sustituidos con arilsulfonilo como ligandos del receptor 5-ht-6. |
| WO2003031587A2 (en) | 2001-10-09 | 2003-04-17 | The Regents Of The University Of California | Use of stat-6 inhibitors as therapeutic agents |
| JP4024579B2 (ja) | 2002-01-22 | 2007-12-19 | 住友ベークライト株式会社 | プラスチック光導波路用材料及び光導波路 |
| PL373399A1 (en) | 2002-04-11 | 2005-08-22 | Vertex Pharmaceuticals Incorporated | Inhibitors of serine proteases, particularly hcv ns3-ns4a protease |
| WO2003091256A1 (fr) | 2002-04-23 | 2003-11-06 | Shionogi & Co., Ltd. | Derive de pyrazolo[1,5-a]pyrimidine et inhibiteur de la nad(p)h oxydase contenant ledit derive |
| US20060004010A1 (en) | 2002-07-10 | 2006-01-05 | Hiromu Habashita | Ccr4 antagonist and medical use thereof |
| WO2004006906A2 (en) | 2002-07-15 | 2004-01-22 | Combinatorx, Incorporated | Methods for the treatment of neoplasms |
| JP2004059761A (ja) | 2002-07-30 | 2004-02-26 | Sumitomo Bakelite Co Ltd | ポリベンゾオキサゾール樹脂、その前駆体及びこれらを用いた光導波路材料並びに光導波路 |
| US20050260126A1 (en) | 2002-08-30 | 2005-11-24 | Yukitsuka Kudo | Diagnostic probes and remedies for diseases with accumulation of prion protein, and stains for prion protein |
| JP2004091369A (ja) | 2002-08-30 | 2004-03-25 | Sumitomo Pharmaceut Co Ltd | 新規ビフェニル化合物 |
| AU2003275266A1 (en) | 2002-10-03 | 2004-05-04 | Smithkline Beecham Corporation | Therapeutic compounds based on pyrazolopyridine derivatives |
| JP2006504755A (ja) | 2002-10-15 | 2006-02-09 | スミスクライン ビーチャム コーポレーション | Gsk−3阻害薬としてのピリダジン化合物 |
| KR100624406B1 (ko) | 2002-12-30 | 2006-09-18 | 삼성에스디아이 주식회사 | 비페닐 유도체 및 이를 채용한 유기 전계 발광 소자 |
| US7320989B2 (en) | 2003-02-28 | 2008-01-22 | Encysive Pharmaceuticals, Inc. | Pyridine, pyrimidine, quinoline, quinazoline, and naphthalene urotensin-II receptor antagonists |
| US7078419B2 (en) | 2003-03-10 | 2006-07-18 | Boehringer Ingelheim Pharmaceuticals, Inc. | Cytokine inhibitors |
| AR043633A1 (es) | 2003-03-20 | 2005-08-03 | Schering Corp | Ligandos de receptores de canabinoides |
| JP4595288B2 (ja) | 2003-03-25 | 2010-12-08 | 住友ベークライト株式会社 | ポリベンゾオキサゾール樹脂、その前駆体及びこれらを用いた光導波路材料並びに光導波路 |
| BRPI0409747A (pt) | 2003-04-11 | 2006-05-09 | Glenmark Pharmaceuticals Sa | novos compostos heterocìclicos úteis para tratamento de distúrbios inflamatórios e alérgicos, processo para sua preparação e composições farmacêuticas contendo estes |
| PE20050158A1 (es) | 2003-05-19 | 2005-05-12 | Irm Llc | Compuestos inmunosupresores y composiciones |
| JP2005002330A (ja) | 2003-05-19 | 2005-01-06 | Sumitomo Electric Ind Ltd | 光学樹脂材料、光学素子、光モジュール、フッ素化ポリマー前駆体及びフッ素化ポリマー |
| US7405295B2 (en) | 2003-06-04 | 2008-07-29 | Cgi Pharmaceuticals, Inc. | Certain imidazo[1,2-a]pyrazin-8-ylamines and method of inhibition of Bruton's tyrosine kinase by such compounds |
| US20060183746A1 (en) | 2003-06-04 | 2006-08-17 | Currie Kevin S | Certain imidazo[1,2-a]pyrazin-8-ylamines and method of inhibition of Bruton's tyrosine kinase by such compounds |
| US7393848B2 (en) | 2003-06-30 | 2008-07-01 | Cgi Pharmaceuticals, Inc. | Certain heterocyclic substituted imidazo[1,2-A]pyrazin-8-ylamines and methods of inhibition of Bruton's tyrosine kinase by such compounds |
| EP1644335A4 (en) | 2003-07-11 | 2008-06-04 | Bristol Myers Squibb Co | TETRAHYDROQUINOLINE DERIVATIVES COMPRISING MODULATORS OF CANNABINOID RECEPTORS |
| US7691870B2 (en) | 2003-07-11 | 2010-04-06 | Merck Patent Gmbh | Benzimidazole carboxamides as raf kinase inhibitors |
| EP1661879A4 (en) | 2003-08-04 | 2006-11-29 | Ono Pharmaceutical Co | A DIPHENYL ETHER COMPOUND, PROCESS FOR THE PRODUCTION AND USE THEREOF |
| WO2005014543A1 (ja) | 2003-08-06 | 2005-02-17 | Japan Tobacco Inc. | 縮合環化合物及びそのhcvポリメラーゼ阻害剤としての利用 |
| US7504401B2 (en) | 2003-08-29 | 2009-03-17 | Locus Pharmaceuticals, Inc. | Anti-cancer agents and uses thereof |
| SG146624A1 (en) | 2003-09-11 | 2008-10-30 | Kemia Inc | Cytokine inhibitors |
| JP4758349B2 (ja) | 2003-10-08 | 2011-08-24 | アイアールエム・リミテッド・ライアビリティ・カンパニー | タンパク質キナーゼ阻害剤としての化合物および組成物 |
| EP1679309A4 (en) | 2003-10-24 | 2007-03-28 | Ono Pharmaceutical Co | ANTISTRESS MEDICAMENT AND ITS MEDICAL USE |
| WO2005047290A2 (en) | 2003-11-11 | 2005-05-26 | Cellular Genomics Inc. | Imidazo[1,2-a] pyrazin-8-ylamines as kinase inhibitors |
| EP1699763A1 (de) | 2003-12-23 | 2006-09-13 | Basf Aktiengesellschaft | 3-trifluormethylpicolins ureanilide und ihre verwendung als fungizide |
| EP1715867A4 (en) | 2004-02-12 | 2009-04-15 | Merck & Co Inc | BIPYRIDYL AMIDES AS MODULATORS OF GLUTAMATE METABOTROPIC REPEATER-5 |
| JPWO2005077948A1 (ja) | 2004-02-16 | 2008-01-10 | 第一製薬株式会社 | 抗真菌作用複素環化合物 |
| GB0403864D0 (en) | 2004-02-20 | 2004-03-24 | Ucl Ventures | Modulator |
| JP2005248082A (ja) | 2004-03-05 | 2005-09-15 | Sumitomo Electric Ind Ltd | ポリベンゾオキサゾール樹脂前駆体の製造方法およびポリベンゾオキサゾール樹脂の製造方法 |
| AU2005220882A1 (en) | 2004-03-08 | 2005-09-22 | Georgia State University Research Foundation, Inc | Novel dicationic imidazo(1,2-a)pyridines and 5,6,7,8-tetrahydro-imidazo(1,2a)pyridines as antiprotozoal agents |
| WO2005086904A2 (en) | 2004-03-08 | 2005-09-22 | Amgen Inc. | Therapeutic modulation of ppar (gamma) activity |
| US7423147B2 (en) | 2004-03-31 | 2008-09-09 | Janssen Pharmaceutical, N.V. | Pyridine compounds as histamine H3 modulators |
| JP2005290301A (ja) | 2004-04-02 | 2005-10-20 | Sumitomo Electric Ind Ltd | ポリベンゾオキサゾール樹脂前駆体の製造方法およびポリベンゾオキサゾール樹脂の製造方法 |
| WO2005099656A2 (en) | 2004-04-06 | 2005-10-27 | The Procter & Gamble Company | Keratin dyeing compounds, keratin dyeing compositions containing them, and use thereof |
| CN1946703A (zh) | 2004-04-20 | 2007-04-11 | 特兰斯泰克制药公司 | 取代的噻唑和嘧啶衍生物作为黑素细胞皮质激素受体调节剂 |
| DE102004021716A1 (de) | 2004-04-30 | 2005-12-01 | Grünenthal GmbH | Substituierte Imidazo[1,2-a]pyridin-Verbindungen und Arzneimittel enthaltend substituierte Imidazo[1,2-a]pyridin-Verbindungen |
| EP1745036A2 (en) | 2004-05-03 | 2007-01-24 | Boehringer Ingelheim Pharmaceuticals Inc. | Cytokine inhibitors |
| PE20060748A1 (es) | 2004-09-21 | 2006-10-01 | Smithkline Beecham Corp | Derivados de indolcarboxamida como inhibidores de quinasa ikk2 |
| JP2008514611A (ja) | 2004-09-23 | 2008-05-08 | ワイス | C型肝炎ウイルスによる感染を処置するためのカルバゾールおよびシクロペンタインドールの誘導体 |
| US7713973B2 (en) | 2004-10-15 | 2010-05-11 | Takeda Pharmaceutical Company Limited | Kinase inhibitors |
| WO2006053121A2 (en) | 2004-11-10 | 2006-05-18 | Cgi Pharmaceuticals, Inc. | Imidazo[1 , 2-a] pyrazin-8-ylamines useful as modulators of kinase activity |
| DE102004054665A1 (de) | 2004-11-12 | 2006-05-18 | Bayer Cropscience Gmbh | Substituierte bi- und tricyclische Pyrazol-Derivate Verfahren zur Herstellung und Verwendung als Herbizide und Pflanzenwachstumsregulatoren |
| WO2006094235A1 (en) | 2005-03-03 | 2006-09-08 | Sirtris Pharmaceuticals, Inc. | Fused heterocyclic compounds and their use as sirtuin modulators |
| TW200716551A (en) | 2005-03-10 | 2007-05-01 | Cgi Pharmaceuticals Inc | Certain substituted amides, method of making, and method of use thereof |
| JP2006290883A (ja) | 2005-03-17 | 2006-10-26 | Nippon Nohyaku Co Ltd | 置換ヘテロ環カルボン酸アニリド誘導体、その中間体及び農園芸用薬剤並びにその使用方法 |
| EP1902056A2 (en) | 2005-05-20 | 2008-03-26 | Array Biopharma, Inc. | Raf inhibitor compounds and methods of use thereof |
| US20080220968A1 (en) | 2005-07-05 | 2008-09-11 | Ge Healthcare Bio-Sciences Ab | [1, 2, 4] Triazolo [1, 5-A] Pyrimidine Derivatives as Chromatographic Adsorbent for the Selective Adsorption of Igg |
| WO2007034282A2 (en) | 2005-09-19 | 2007-03-29 | Pfizer Products Inc. | Diaryl-imidazole compounds condensed with a heterocycle as c3a receptor antagonists |
| US7723336B2 (en) | 2005-09-22 | 2010-05-25 | Bristol-Myers Squibb Company | Fused heterocyclic compounds useful as kinase modulators |
| US20070078136A1 (en) | 2005-09-22 | 2007-04-05 | Bristol-Myers Squibb Company | Fused heterocyclic compounds useful as kinase modulators |
| ES2572263T3 (es) | 2005-10-25 | 2016-05-31 | Shionogi & Co | Derivados de dihidrooxazina y tetrahidropirimidina como inhibidores de BACE 1 |
| AU2006316322B2 (en) | 2005-11-22 | 2011-08-25 | Merck Canada Inc. | Tricyclic compounds useful as inhibitors of kinases |
| WO2007067711A2 (en) | 2005-12-08 | 2007-06-14 | Amphora Discovery Corporation | Certain chemical entities, compositions, and methods for modulating trpv1 |
| US20090281120A1 (en) | 2005-12-12 | 2009-11-12 | Ono Pharmaceutical Co., Ltd | Bicyclic heterocyclic compound |
| US20090281075A1 (en) | 2006-02-17 | 2009-11-12 | Pharmacopeia, Inc. | Isomeric purinones and 1h-imidazopyridinones as pkc-theta inhibitors |
| WO2007096764A2 (en) | 2006-02-27 | 2007-08-30 | Glenmark Pharmaceuticals S.A. | Bicyclic heteroaryl derivatives as cannabinoid receptor modulators |
| US20090304821A1 (en) | 2006-03-08 | 2009-12-10 | Takeda Pharmaceutical Company Limited | Pharmaceutical Combination |
| MX2008012617A (es) | 2006-03-31 | 2008-10-10 | Novartis Ag | Compuestos organicos. |
| EP2023919A4 (en) | 2006-05-08 | 2010-12-22 | Molecular Neuroimaging Llc | COMPOUNDS AND AMYLOID PROBES FOR THERAPY AND IMAGING USES |
| AU2007257959A1 (en) | 2006-06-09 | 2007-12-21 | Kemia, Inc. | Therapy using cytokine inhibitors |
| US20080280891A1 (en) | 2006-06-27 | 2008-11-13 | Locus Pharmaceuticals, Inc. | Anti-cancer agents and uses thereof |
| EP2044061A2 (en) | 2006-07-20 | 2009-04-08 | Mehmet Kahraman | Benzothiophene inhibitors of rho kinase |
| DE102006035018B4 (de) | 2006-07-28 | 2009-07-23 | Novaled Ag | Oxazol-Triplett-Emitter für OLED-Anwendungen |
| WO2008021745A2 (en) | 2006-08-16 | 2008-02-21 | Itherx Pharmaceuticals, Inc. | Hepatitis c virus entry inhibitors |
| TWI389895B (zh) | 2006-08-21 | 2013-03-21 | Infinity Discovery Inc | 抑制bcl蛋白質與結合夥伴間之交互作用的化合物及方法 |
| WO2008027812A2 (en) | 2006-08-28 | 2008-03-06 | Forest Laboratories Holdings Limited | Imidazopyridine and imidazopyrimidine derivatives |
| PE20081370A1 (es) | 2006-09-11 | 2008-11-28 | Cgi Pharmaceuticals Inc | Determinadas amidas sustituidas, metodo de elaboracion y metodo de uso de las mismas |
| AR063706A1 (es) | 2006-09-11 | 2009-02-11 | Cgi Pharmaceuticals Inc | Determinadas amidas sustituidas, el uso de las mismas para el tratamiento de enfermedades mediadas por la inhibicion de la actividad de btk y composiciones farmaceuticas que las comprenden. |
| US7838523B2 (en) | 2006-09-11 | 2010-11-23 | Cgi Pharmaceuticals, Inc. | Certain substituted amides, method of making, and method of use thereof |
| JP2010502751A (ja) | 2006-09-11 | 2010-01-28 | シージーアイ ファーマシューティカルズ,インコーポレイティド | キナーゼ阻害物質、およびキナーゼ阻害物質の使用および同定方法 |
| CA2663178C (en) | 2006-09-11 | 2016-01-12 | Matrix Laboratories Ltd. | Dibenzofuran derivatives as inhibitors of pde-4 and pde-10 |
| FR2906250B1 (fr) | 2006-09-22 | 2008-10-31 | Sanofi Aventis Sa | Derives de 2-aryl-6phenyl-imidazo(1,2-a) pyridines, leur preparation et leur application en therapeutique |
| MX2009004289A (es) | 2006-10-27 | 2009-05-05 | Wyeth Corp | Compuestos triciclicos como inhibidores de metaloproteinasas matriciales. |
| EP2089364B1 (en) | 2006-11-08 | 2013-06-12 | Bristol-Myers Squibb Company | Pyridinone compounds |
| GB0623209D0 (en) | 2006-11-21 | 2007-01-03 | F2G Ltd | Antifungal agents |
| WO2008064317A1 (en) | 2006-11-22 | 2008-05-29 | University Of Medicine And Dentistry Of New Jersey | Lipophilic opioid receptor active compounds |
| WO2008064318A2 (en) | 2006-11-22 | 2008-05-29 | University Of Medicine And Dentistry Of New Jersey | Peripheral opioid receptor active compounds |
| WO2008071944A1 (en) * | 2006-12-14 | 2008-06-19 | Boehringer Ingelheim International Gmbh | Benzoxazoles useful in the treatment of inflammation |
| US8513270B2 (en) | 2006-12-22 | 2013-08-20 | Incyte Corporation | Substituted heterocycles as Janus kinase inhibitors |
| US8338437B2 (en) | 2007-02-28 | 2012-12-25 | Methylgene Inc. | Amines as small molecule inhibitors |
| EP1964840A1 (en) | 2007-02-28 | 2008-09-03 | sanofi-aventis | Imidazo[1,2-a]pyridines and their use as pharmaceuticals |
| EP1964841A1 (en) | 2007-02-28 | 2008-09-03 | sanofi-aventis | Imidazo[1,2-a]azine and their use as pharmaceuticals |
| JP2008218327A (ja) | 2007-03-07 | 2008-09-18 | Hitachi Ltd | 電解質、電解質膜、それを用いた膜電極接合体、燃料電池電源及び燃料電池電源システム |
| JP2010120852A (ja) | 2007-03-09 | 2010-06-03 | Daiichi Sankyo Co Ltd | 新規なジアミド誘導体 |
| ES2388454T3 (es) | 2007-03-22 | 2012-10-15 | Astrazeneca Ab | Derivados de quinolina para el tratamiento de enfermedades inflamatorias |
| EP2151435A4 (en) | 2007-04-24 | 2011-09-14 | Shionogi & Co | PHARMACEUTICAL COMPOSITION FOR THE TREATMENT OF ALZHEIMER'S DISEASE |
| EP2147914B1 (en) | 2007-04-24 | 2014-06-04 | Shionogi&Co., Ltd. | Aminodihydrothiazine derivatives substituted with cyclic groups |
| WO2008134553A1 (en) | 2007-04-26 | 2008-11-06 | Xenon Pharmaceuticals Inc. | Methods of using bicyclic compounds in treating sodium channel-mediated diseases |
| ES2395583T3 (es) | 2007-05-10 | 2013-02-13 | Ge Healthcare Limited | IMIDAZOL (1,2-A)PIRIDINAS y compuestos relacionados con actividad frente a los receptores cannabinoides CB2 |
| WO2009027733A1 (en) | 2007-08-24 | 2009-03-05 | Astrazeneca Ab | (2-pyridin-3-ylimidazo[1,2-b]pyridazin-6-yl) urea derivatives as antibacterial agents |
| CL2008002793A1 (es) | 2007-09-20 | 2009-09-04 | Cgi Pharmaceuticals Inc | Compuestos derivados de amidas sustituidas, inhibidores de la actividad de btk; composicion farmaceutica que los comprende; utiles en el tratamiento del cancer, trastornos oseos, enfermedades autoinmunes, entre otras |
| ATE505454T1 (de) | 2007-09-20 | 2011-04-15 | Amgen Inc | 1-(4-(4-benzylbenzamid)-benzyl)-azetidin-3- carboxylsäurederivate und entsprechende verbindungen als s1p-rezeptor-modulatoren zur behandlung von immunerkrankungen |
| DE102007048716A1 (de) | 2007-10-11 | 2009-04-23 | Merck Patent Gmbh | Imidazo[1,2-a]pyrimidinderivate |
| TW200932219A (en) | 2007-10-24 | 2009-08-01 | Astellas Pharma Inc | Oxadiazolidinedione compound |
| AU2008315746A1 (en) * | 2007-10-25 | 2009-04-30 | Astrazeneca Ab | Pyridine and pyrazine derivatives useful in the treatment of cell proliferative disorders |
| US7868001B2 (en) | 2007-11-02 | 2011-01-11 | Hutchison Medipharma Enterprises Limited | Cytokine inhibitors |
| WO2009062059A2 (en) | 2007-11-08 | 2009-05-14 | Pharmacopeia, Inc. | Isomeric purinones and 1h-imidazopyridinones as pkc-theta inhibitors |
| CA2707491A1 (en) | 2007-12-13 | 2009-06-18 | Merck Sharp & Dohme Corp. | Inhibitors of janus kinases |
| RU2364597C1 (ru) | 2007-12-14 | 2009-08-20 | Андрей Александрович Иващенко | ГЕТЕРОЦИКЛИЧЕСКИЕ ИНГИБИТОРЫ Hh-СИГНАЛЬНОГО КАСКАДА, ЛЕКАРСТВЕННЫЕ КОМПОЗИЦИИ НА ИХ ОСНОВЕ И СПОСОБ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ, СВЯЗАННЫХ С АББЕРАНТНОЙ АКТИВНОСТЬЮ Hh СИГНАЛЬНОЙ СИСТЕМЫ |
| AU2008337876A1 (en) | 2007-12-19 | 2009-06-25 | Syngenta Participations Ag | Insecticidal compounds |
| WO2009079683A1 (en) | 2007-12-21 | 2009-07-02 | The University Of Sydney | Translocator protein ligands |
| WO2009086303A2 (en) | 2007-12-21 | 2009-07-09 | University Of Rochester | Method for altering the lifespan of eukaryotic organisms |
| ES2548774T3 (es) | 2008-01-18 | 2015-10-20 | Eisai R&D Management Co., Ltd. | Derivado de aminodihidrotiazina condensado |
| JP5381718B2 (ja) | 2008-01-31 | 2014-01-08 | コニカミノルタ株式会社 | ハロ多環芳香族化合物及びその製造方法 |
| AU2009218515A1 (en) | 2008-02-26 | 2009-09-03 | Novartis Ag | Heterocyclic compounds as inhibitors of CXCR2 |
| EP2095818A1 (en) | 2008-02-29 | 2009-09-02 | AEterna Zentaris GmbH | Use of LHRH antagonists at non-castrating doses |
| FR2928922B1 (fr) | 2008-03-21 | 2010-04-23 | Sanofi Aventis | Derives de 2-aryl-6-phenyl-imidazo°1,2-a!pyridines polysubstitues, leur preparation et leur application en therapeutique |
| FR2928921B1 (fr) | 2008-03-21 | 2010-04-23 | Sanofi Aventis | Derives polysubstitues de 2-aryl-6-phenyl-imidazo°1,2-a!pyridines, leur preparation et leur application en therapeutique |
| FR2928924B1 (fr) | 2008-03-21 | 2010-04-23 | Sanofi Aventis | Derives polysubstitues de 6-heteroaryle-imidazo°1,2-a! pyridines, leur preparation et leur application en therapeutique |
| JP5432982B2 (ja) | 2008-03-31 | 2014-03-05 | 武田薬品工業株式会社 | アポトーシスシグナル調節キナーゼ1阻害剤 |
| KR101034351B1 (ko) * | 2008-05-14 | 2011-05-16 | 한국화학연구원 | 신규 벤즈옥사졸로 치환된 피리딘 유도체 또는 이의약학적으로 허용가능한 염, 이의 제조방법 및 이를유효성분으로 함유하는 이상세포 성장 질환의 예방 및치료용 약학적 조성물 |
| JP5774982B2 (ja) | 2008-05-19 | 2015-09-09 | サノビオン ファーマシューティカルズ インクSunovion Pharmaceuticals Inc. | イミダゾ[1,2−a]ピリジン化合物 |
| US20110077248A1 (en) | 2008-05-29 | 2011-03-31 | Sirtris Pharmaceuticals, Inc. | Imidazopyridine and related analogs as sirtuin modulators |
| EP2280946B1 (en) | 2008-06-05 | 2016-02-10 | Glaxo Group Limited | 4-carboxamide indazole derivatives useful as inhibitors of p13-kinases |
| EP2323665B1 (en) | 2008-07-24 | 2013-06-19 | Bristol-Myers Squibb Company | Fused heterocyclic compounds useful as kinase modulators |
| US9643922B2 (en) | 2008-08-18 | 2017-05-09 | Yale University | MIF modulators |
| US9540322B2 (en) | 2008-08-18 | 2017-01-10 | Yale University | MIF modulators |
| JP2011231017A (ja) | 2008-09-09 | 2011-11-17 | Nissan Chem Ind Ltd | 光学活性エポキシ化合物及び光学活性スルホキシド化合物の製造方法、並びに該方法に用いる配位子、錯体及び該錯体の製造方法 |
| EP2365970B1 (en) | 2008-11-12 | 2018-03-21 | Gilead Connecticut, Inc. | Pyridazinones and their use as btk inhibitors |
| EP2376490B1 (en) | 2008-12-04 | 2013-01-23 | Proximagen Limited | Imidazopyridine compounds |
| CN102325753B (zh) | 2008-12-19 | 2014-09-10 | 百时美施贵宝公司 | 用作激酶抑制剂的咔唑甲酰胺化合物 |
| JP5557849B2 (ja) | 2008-12-19 | 2014-07-23 | ブリストル−マイヤーズ スクイブ カンパニー | カルバゾールおよびカルボリンキナーゼ阻害剤 |
| AR074830A1 (es) | 2008-12-19 | 2011-02-16 | Cephalon Inc | Pirrolotriazinas como inhibidores de alk y jak2 |
| JP5624275B2 (ja) | 2008-12-22 | 2014-11-12 | ユー・ディー・シー アイルランド リミテッド | 有機電界発光素子 |
| WO2010075376A2 (en) | 2008-12-23 | 2010-07-01 | Abbott Laboratories | Anti-viral compounds |
| WO2010074284A1 (ja) | 2008-12-26 | 2010-07-01 | 味の素株式会社 | ピラゾロピリミジン化合物 |
| JP2010202530A (ja) | 2009-02-27 | 2010-09-16 | Tokyo Institute Of Technology | 含ヘテロ芳香族化合物および光学材料 |
| KR20100101054A (ko) | 2009-03-07 | 2010-09-16 | 주식회사 메디젠텍 | 세포핵에서 세포질로의 gsk3의 이동을 억제하는 화합물을 함유하는 세포핵에서 세포질로의 gsk3 이동에 의해 발생되는 질환의 치료 또는 예방용 약학적 조성물 |
| SG10201401169QA (en) | 2009-04-02 | 2014-05-29 | Merck Serono Sa | Dihydroorotate dehydrogenase inhibitors |
| ES2475091T3 (es) | 2009-04-16 | 2014-07-10 | Centro Nacional De Investigaciones Oncol�Gicas (Cnio) | Imidazopirazinas como inhibidores de proteína cinasas |
| US8338441B2 (en) | 2009-05-15 | 2012-12-25 | Gilead Sciences, Inc. | Inhibitors of human immunodeficiency virus replication |
| US8993604B2 (en) | 2009-06-30 | 2015-03-31 | Siga Technologies, Inc. | Treatment and prevention of dengue virus infections |
| KR20120049852A (ko) | 2009-06-30 | 2012-05-17 | 시가 테크놀로지스, 인크. | 뎅기 바이러스 감염의 치료 및 예방 |
| TWI598347B (zh) | 2009-07-13 | 2017-09-11 | 基利科學股份有限公司 | 調節細胞凋亡信號之激酶的抑制劑 |
| JP2011057661A (ja) | 2009-08-14 | 2011-03-24 | Bayer Cropscience Ag | 殺虫性カルボキサミド類 |
| UA108363C2 (uk) | 2009-10-08 | 2015-04-27 | Похідні імінотіадіазиндіоксиду як інгібітори bace, композиція на їх основі і їх застосування | |
| US9095596B2 (en) | 2009-10-15 | 2015-08-04 | Southern Research Institute | Treatment of neurodegenerative diseases, causation of memory enhancement, and assay for screening compounds for such |
| MX2012004340A (es) | 2009-10-16 | 2012-11-23 | Rib X Pharmaceuticals Inc | Compuestos antimicrobianos y metodos para fabricar y utilizar los mismos. |
| WO2011050245A1 (en) | 2009-10-23 | 2011-04-28 | Yangbo Feng | Bicyclic heteroaryls as kinase inhibitors |
| EP2518072A4 (en) | 2009-12-24 | 2014-06-04 | Ajinomoto Kk | IMIDAZOPYRIDAZINE COMPOUNDS |
| WO2011082400A2 (en) | 2010-01-04 | 2011-07-07 | President And Fellows Of Harvard College | Modulators of immunoinhibitory receptor pd-1, and methods of use thereof |
| US20130085133A1 (en) | 2010-02-08 | 2013-04-04 | Sourthern Research Institute Office of Commercialization and Intellectual Prop. | Anti-viral treatment and assay to screenfor anti-viral agent |
| AR080433A1 (es) | 2010-03-02 | 2012-04-11 | Merck Sharp & Dohme | Derivados de benzofurancarboxamidas utiles para tratar o prevenir infecciones por vhc y composiciones farmaceuticas que los contienen. |
| KR101720824B1 (ko) | 2010-03-04 | 2017-03-28 | 머크 샤프 앤드 돔 코포레이션 | 카테콜 o-메틸 트랜스퍼라제의 억제제 및 정신병적 장애의 치료에서의 그의 용도 |
| EP2547678B1 (en) | 2010-03-18 | 2016-03-16 | Institut Pasteur Korea | Anti-infective compounds |
| US8410117B2 (en) | 2010-03-26 | 2013-04-02 | Hoffmann-La Roche Inc. | Imidazopyrimidine derivatives |
| WO2011159857A1 (en) | 2010-06-16 | 2011-12-22 | Bristol-Myers Squibb Company | Carboline carboxamide compounds useful as kinase inhibitors |
| CN102295642B (zh) | 2010-06-25 | 2016-04-06 | 中国人民解放军军事医学科学院毒物药物研究所 | 2-芳基咪唑并[1,2-a]吡啶-3-乙酰胺衍生物、其制备方法及用途 |
| EP2402345A1 (en) | 2010-06-29 | 2012-01-04 | Basf Se | Pyrazole fused bicyclic compounds |
| CN101891895B (zh) | 2010-07-28 | 2011-11-30 | 南京航空航天大学 | 基于桥联双水杨醛结构的苯并噻唑类金属配位聚合物及其制法及应用 |
| WO2012016133A2 (en) | 2010-07-29 | 2012-02-02 | President And Fellows Of Harvard College | Ros1 kinase inhibitors for the treatment of glioblastoma and other p53-deficient cancers |
| US8633200B2 (en) | 2010-09-08 | 2014-01-21 | Bristol-Myers Squibb Company | Inhibitors of human immunodeficiency virus replication |
| CN101993415B (zh) | 2010-09-15 | 2013-08-14 | 北京韩美药品有限公司 | 作为Hedgehog通路抑制剂的化合物以及包含该化合物的药物组合物及其应用 |
| WO2012047856A2 (en) | 2010-10-04 | 2012-04-12 | Institute For Hepatitis And Virus Research | Novel inhibitors of secretion of hepatitis b virus antigens |
| EP2444084A1 (en) | 2010-10-21 | 2012-04-25 | Centro Nacional de Investigaciones Oncológicas (CNIO) | Use of PI3K inibitors for the treatment of obesity |
| WO2012052745A1 (en) | 2010-10-21 | 2012-04-26 | Centro Nacional De Investigaciones Oncológicas (Cnio) | Combinations of pi3k inhibitors with a second anti -tumor agent |
| CN103282034A (zh) | 2010-11-18 | 2013-09-04 | 利亘制药公司 | 造血生长因子模拟物的用途 |
| WO2012080376A1 (en) | 2010-12-17 | 2012-06-21 | Syngenta Participations Ag | Insecticidal compounds |
| TWI617559B (zh) | 2010-12-22 | 2018-03-11 | 江蘇恆瑞醫藥股份有限公司 | 2-芳基咪唑并[1,2-b]嗒.2-苯基咪唑并[1,2-a]吡啶,和2-苯基咪唑并[1,2-a]吡衍生物 |
| KR20140027090A (ko) | 2011-01-04 | 2014-03-06 | 노파르티스 아게 | 연령-관련 황반 변성 (amd)의 치료에 유용한 인돌 화합물 또는 그의 유사체 |
| CA2825098C (en) | 2011-01-27 | 2020-03-10 | Universite De Montreal | Pyrazolopyridine and pyrazolopyrimidine derivatives as melanocortin-4 receptor modulators |
| US8921368B2 (en) | 2011-03-17 | 2014-12-30 | Bristol-Myers Squibb Company | Pyrrolopyridazine JAK3 inhibitors and their use for the treatment of inflammatory and autoimmune diseases |
| US9464065B2 (en) | 2011-03-24 | 2016-10-11 | The Scripps Research Institute | Compounds and methods for inducing chondrogenesis |
| WO2012139425A1 (en) | 2011-04-13 | 2012-10-18 | Schering Corporation | 5-substituted iminothiazines and their mono-and dioxides as bace inhibitors,compositions,and their use |
| CN102796103A (zh) | 2011-05-23 | 2012-11-28 | 南京英派药业有限公司 | 6-(芳基甲酰)咪唑并[1,2-a]嘧啶和6-(芳基甲酰)[1,2,4]三唑并[4,3-a]嘧啶作为Hedgehog抑制剂及其应用 |
| US9278910B2 (en) | 2011-05-31 | 2016-03-08 | Receptos, Inc. | GLP-1 receptor stabilizers and modulators |
| GB201109763D0 (en) | 2011-06-10 | 2011-07-27 | Ucl Business Plc | Compounds |
| WO2012175991A1 (en) | 2011-06-24 | 2012-12-27 | Pharminox Limited | Fused pentacyclic anti - proliferative compounds |
| AU2012282229B2 (en) | 2011-07-08 | 2015-05-07 | Novartis Ag | Novel pyrrolo pyrimidine derivatives |
| EP2548877A1 (en) | 2011-07-19 | 2013-01-23 | MSD Oss B.V. | 4-(5-Membered fused pyridinyl)benzamides as BTK-inhibitors |
| WO2013040528A1 (en) | 2011-09-16 | 2013-03-21 | Microbiotix, Inc. | Antimicrobial compounds |
| EP2757884B1 (en) | 2011-09-22 | 2022-07-27 | Merck Sharp & Dohme LLC | Pyrazolopyridyl compounds as aldosterone synthase inhibitors |
| CA2851445A1 (en) | 2011-10-13 | 2013-04-18 | Novartis Ag | Novel oxazine derivatives and their use in the treatment of disease |
| RU2014120180A (ru) | 2011-10-20 | 2015-11-27 | ГЛЭКСОСМИТКЛАЙН ЭлЭлСи | Замещенные бициклические аза-гетероциклы и аналоги в качестве модуляторов сиртуина |
| CA2852615A1 (en) | 2011-10-21 | 2013-04-25 | Torrent Pharmaceuticals Limited | Novel substituted imidazopyrimidines as gpbar1 receptor modulators |
| WO2013120040A1 (en) | 2012-02-10 | 2013-08-15 | Children's Medical Center Corporation | Targeted pathway inhibition to improve muscle structure, function and activity in muscular dystrophy |
| US9034882B2 (en) | 2012-03-05 | 2015-05-19 | Bristol-Myers Squibb Company | Inhibitors of human immunodeficiency virus replication |
| US20150011751A1 (en) | 2012-03-09 | 2015-01-08 | Carna Biosciences, Inc. | Novel triazine derivative |
| ES2571479T3 (es) | 2012-04-20 | 2016-05-25 | Gilead Sciences Inc | Derivados del ácido benzotiazol-6-il acético y su uso para tratar una infección por VIH |
| WO2013157021A1 (en) | 2012-04-20 | 2013-10-24 | Advinus Therapeutics Limited | Bicyclic compounds, compositions and medicinal applications thereof |
| US20150105433A1 (en) | 2012-04-27 | 2015-04-16 | The Uab Research Foundation | TREATING VIRAL INFECTIONS HAVING VIRAL RNAs TRANSLATED BY A NON-IRES MEDIATED MECHANISM |
| WO2013191113A1 (ja) | 2012-06-18 | 2013-12-27 | 住友化学株式会社 | 縮合複素環化合物 |
| EP2871179A4 (en) | 2012-07-03 | 2016-03-16 | Ono Pharmaceutical Co | CONNECTION WITH AGONISTIC EFFECT ON THE SOMATOSTATIN RECEPTOR AND ITS USE FOR MEDICAL PURPOSES |
| EA028722B1 (ru) | 2012-07-13 | 2017-12-29 | Юсб Байофарма Спрл | Производные имидазопиридина в качестве модуляторов активности tnf |
| GB201212513D0 (en) | 2012-07-13 | 2012-08-29 | Ucb Pharma Sa | Therapeutic agents |
| JP2015178457A (ja) | 2012-07-25 | 2015-10-08 | 杏林製薬株式会社 | ピラゾロピリジン誘導体、またはその薬理学的に許容される塩 |
| US9428511B2 (en) | 2012-09-06 | 2016-08-30 | Bristol-Myers Squibb Company | Imidazopyridazine JAK3 inhibitors and their use for the treatment of inflammatory and autoimmune diseases |
| WO2014048939A1 (en) | 2012-09-26 | 2014-04-03 | F. Hoffmann-La Roche Ag | Cyclic ether pyrazol-4-yl-heterocyclyl-carboxamide compounds and methods of use |
| WO2014061693A1 (ja) | 2012-10-17 | 2014-04-24 | 塩野義製薬株式会社 | 新規非芳香族炭素環又は非芳香族複素環誘導体 |
| US9163027B2 (en) | 2012-11-21 | 2015-10-20 | Stategics, Inc. | Substituted triazolo-pyrimidine compounds for modulating cell proliferation differentiation and survival |
| JP6037804B2 (ja) | 2012-12-03 | 2016-12-07 | 富士フイルム株式会社 | ガス分離膜 |
| ME03780B (me) | 2013-01-15 | 2021-04-20 | Incyte Holdings Corp | Jedinjenja tiazolkarboksamida i piridinkarboksamida korisna kao inhibitori pim kinaze |
| JP2016505055A (ja) | 2013-01-22 | 2016-02-18 | エフ.ホフマン−ラ ロシュ アーゲーF. Hoffmann−La Roche Aktiengesellschaft | Bace1阻害剤としてのフルオロ−[1,3]オキサジン |
| CN103933036B (zh) | 2013-01-23 | 2017-10-13 | 中国人民解放军军事医学科学院毒物药物研究所 | 2‑芳基咪唑并[1,2‑α]吡啶‑3‑乙酰胺衍生物在制备防治PTSD的药物中的用途 |
| EP2950814A4 (en) | 2013-01-31 | 2016-06-08 | Univ Jefferson | PD-L1 AND PD-L2 BASED FUSION PROTEINS AND USES THEREOF |
| EP2963037B1 (en) | 2013-02-27 | 2019-03-27 | Mochida Pharmaceutical Co., Ltd. | Novel pyrazole derivative |
| SG11201507196WA (en) | 2013-03-08 | 2015-10-29 | Amgen Inc | Perfluorinated cyclopropyl fused 1,3-oxazin-2-amine compounds as beta-secretase inhibitors and methods of use |
| JP2016516399A (ja) | 2013-03-13 | 2016-06-09 | オーストラリアン ニュークリア サイエンス アンド テクノロジー オーガニゼーション | 非機能性tspo遺伝子を有するトランスジェニック非ヒト生物 |
| CN104045552B (zh) | 2013-03-13 | 2019-06-11 | 江苏先声药业有限公司 | 作为神经保护剂的药用化合物 |
| DK2968304T3 (en) | 2013-03-14 | 2019-01-28 | Univ Columbia | 4-PHENYLPIPERIDINES, THEIR PREPARATION AND USE. |
| EP2968265A4 (en) | 2013-03-14 | 2016-12-28 | Celtaxsys Inc | INHIBITORS OF THE LEUKOTRIEN A4 HYDROLASE |
| US9527842B2 (en) | 2013-03-14 | 2016-12-27 | VIIV Healthcare UK (No.5) Limited | Inhibitors of human immunodeficiency virus replication |
| CA2902594C (en) | 2013-03-14 | 2023-01-10 | Curadev Pharma Private Ltd. | Inhibitors of the kynurenine pathway |
| US9308236B2 (en) | 2013-03-15 | 2016-04-12 | Bristol-Myers Squibb Company | Macrocyclic inhibitors of the PD-1/PD-L1 and CD80(B7-1)/PD-L1 protein/protein interactions |
| WO2014181287A1 (en) | 2013-05-09 | 2014-11-13 | Piramal Enterprises Limited | Heterocyclyl compounds and uses thereof |
| NZ754039A (en) | 2013-06-26 | 2021-06-25 | Abbvie Inc | Primary carboxamides as btk inhibitors |
| MX2015017821A (es) | 2013-07-02 | 2016-04-15 | Syngenta Participations Ag | Heterociclos bi-o triciclicos activos como plaguicidas con sustituyentes que contienen azufre. |
| TWI641595B (zh) | 2013-07-17 | 2018-11-21 | 日商大塚製藥股份有限公司 | 氰基三唑化合物類 |
| BR112016001457A2 (pt) | 2013-07-25 | 2017-08-29 | Dana Farber Cancer Inst Inc | Inibidores de fatores de transcrição e usos dos mesmos |
| EP2835375A1 (en) | 2013-08-09 | 2015-02-11 | Fundació Institut Català d'Investigació Química | Bis-salphen compounds and carbonaceous material composites comprising them |
| KR101715090B1 (ko) | 2013-08-28 | 2017-03-13 | 한국화학연구원 | 신규한 화합물 또는 이의 약학적으로 허용가능한 염, 및 이를 유효성분으로 함유하는 인플루엔자 바이러스 감염으로 인한 질환의 예방 또는 치료용 약학적 조성물 |
| HUE038169T2 (hu) | 2013-09-06 | 2018-09-28 | Aurigene Discovery Tech Ltd | 1,2,4-Oxadiazol származékok mint immunomodulátorok |
| KR20160081898A (ko) | 2013-09-06 | 2016-07-08 | 오리진 디스커버리 테크놀로지스 리미티드 | 면역조절제로서 1,3,4-옥사디아졸 및 1,3,4-티아디아졸 유도체 |
| WO2015036927A1 (en) | 2013-09-10 | 2015-03-19 | Aurigene Discovery Technologies Limited | Immunomodulating peptidomimetic derivatives |
| JP6336870B2 (ja) | 2013-09-30 | 2018-06-06 | 日本ポリプロ株式会社 | ビフェノール化合物及びそれを用いるオレフィン重合用触媒並びにオレフィン重合体の製造方法 |
| FR3012140B1 (fr) | 2013-10-18 | 2016-08-26 | Arkema France | Unite et procede pour la purification de methacrylate de methyle brut |
| GB201321736D0 (en) | 2013-12-09 | 2014-01-22 | Ucb Pharma Sa | Therapeutic agents |
| GB201321746D0 (en) | 2013-12-09 | 2014-01-22 | Ucb Pharma Sa | Therapeutic agents |
| GB201321733D0 (en) | 2013-12-09 | 2014-01-22 | Ucb Pharma Sa | Therapeutic agents |
| GB201321743D0 (en) | 2013-12-09 | 2014-01-22 | Ucb Pharma Sa | Therapeutic agents |
| WO2015095337A2 (en) | 2013-12-18 | 2015-06-25 | The Rockefeller University | PYRAZOLO[1,5-a]PYRIMIDINECARBOXAMIDE DERIVATIVES FOR TREATING COGNITIVE IMPAIRMENT |
| RU2016131792A (ru) | 2014-01-03 | 2018-02-06 | Байер Энимэл Хельс ГмбХ | Новые пиразолил-гетероариламиды в качестве средств для борьбы с вредителями |
| CA2938152A1 (en) | 2014-02-10 | 2015-08-13 | Merck Sharp & Dohme Corp. | Antibodies that bind to human tau and assay for quantifying human tau using the antibodies |
| PT3110418T (pt) | 2014-02-25 | 2020-01-22 | Achillion Pharmaceuticals Inc | Compostos de arilo, heteroarilo e heterocíclicos para tratamento de distúrbios mediados por complemento |
| US9394365B1 (en) | 2014-03-12 | 2016-07-19 | Yeda Research And Development Co., Ltd | Reducing systemic regulatory T cell levels or activity for treatment of alzheimer's disease |
| JP6490464B2 (ja) | 2014-03-26 | 2019-03-27 | 三井化学株式会社 | 遷移金属化合物、オレフィン重合用触媒およびオレフィン系重合体の製造方法 |
| WO2015150097A1 (en) | 2014-04-04 | 2015-10-08 | Iomet Pharma Ltd | Indole derivatives for use in medicine |
| US9850225B2 (en) | 2014-04-14 | 2017-12-26 | Bristol-Myers Squibb Company | Compounds useful as immunomodulators |
| CN104211726B (zh) | 2014-08-11 | 2017-06-16 | 中南民族大学 | 非茂类三齿双核钛配合物、制备方法及用途 |
| US20170305922A1 (en) | 2014-09-17 | 2017-10-26 | Epizyme, Inc. | Carm1 inhibitors and uses thereof |
| EP3194368B1 (en) | 2014-09-19 | 2020-12-23 | MacKay Medical Foundation the Presbyterian Church in Taiwan MacKay Memorial Hospital | Benzo-heterocyclic compounds and their applications |
| AU2015328285B2 (en) | 2014-10-06 | 2019-07-18 | Merck Patent Gmbh | Heteroaryl compounds as BTK inhibitors and uses thereof |
| AU2015360416A1 (en) | 2014-12-10 | 2017-06-08 | Massachusetts Institute Of Technology | Fused 1,3-azole derivatives useful for the treatment of proliferative diseases |
| JP6853619B2 (ja) | 2015-01-16 | 2021-03-31 | 大塚製薬株式会社 | シアノトリアゾール化合物の医薬用途 |
| DE112016000383A5 (de) | 2015-01-20 | 2017-10-05 | Cynora Gmbh | Organische Moleküle, insbesondere zur Verwendung in optoelektronischen Bauelementen |
| WO2016118404A1 (en) | 2015-01-20 | 2016-07-28 | Merck Sharp & Dohme Corp. | Iminothiadiazine dioxides bearing an amine-linked substituent as bace inhibitors, compositions, and their use |
| WO2016156282A1 (en) | 2015-04-02 | 2016-10-06 | Bayer Cropscience Aktiengesellschaft | Novel triazole compounds for controlling phytopathogenic harmful fungi |
| WO2017035405A1 (en) | 2015-08-26 | 2017-03-02 | Achillion Pharmaceuticals, Inc. | Amino compounds for treatment of immune and inflammatory disorders |
| US10745382B2 (en) | 2015-10-15 | 2020-08-18 | Bristol-Myers Squibb Company | Compounds useful as immunomodulators |
| EP3365340B1 (en) | 2015-10-19 | 2022-08-10 | Incyte Corporation | Heterocyclic compounds as immunomodulators |
| WO2017070320A1 (en) | 2015-10-21 | 2017-04-27 | University Of Pittsburgh - Of The Commonwealth System Of Higher Education | Phenyl indole allosteric inhibitors of p97 atpase |
| KR101717601B1 (ko) | 2015-11-10 | 2017-03-20 | 한국화학연구원 | 신규한 화합물 또는 이의 약학적으로 허용가능한 염, 및 이를 유효성분으로 함유하는 인플루엔자 바이러스 감염으로 인한 질환의 예방 또는 치료용 약학적 조성물 |
| HRP20221035T1 (hr) | 2015-11-19 | 2022-11-11 | Incyte Corporation | Heterociklički spojevi kao imunomodulatori |
| US20170174671A1 (en) | 2015-12-17 | 2017-06-22 | Incyte Corporation | Heterocyclic compounds as immunomodulators |
| WO2017107052A1 (en) | 2015-12-22 | 2017-06-29 | Merck Sharp & Dohme Corp. | Soluble guanylate cyclase stimulators |
| AU2016378482A1 (en) | 2015-12-22 | 2018-07-12 | Synthon B.V. | Pharmaceutical composition comprising amorphous lenalidomide and an antioxidant |
| SG10202111399YA (en) | 2015-12-22 | 2021-11-29 | Immatics Biotechnologies Gmbh | Peptides and combination of peptides for use in immunotherapy against breast cancer and other cancers |
| CN108463109B (zh) | 2015-12-22 | 2022-04-29 | 先正达参股股份有限公司 | 杀有害生物活性吡唑衍生物 |
| PE20230731A1 (es) | 2015-12-22 | 2023-05-03 | Incyte Corp | Compuestos heterociclicos como inmunomoduladores |
| KR101653560B1 (ko) | 2016-02-02 | 2016-09-12 | 한국화학연구원 | 신규한 화합물 또는 이의 약학적으로 허용가능한 염, 및 이를 유효성분으로 함유하는 인플루엔자 바이러스 감염으로 인한 질환의 예방 또는 치료용 약학적 조성물 |
| BR112018071585B1 (pt) | 2016-04-22 | 2024-01-02 | Incyte Corporation | Formulações de um inibidor de lsd1, seus usos e método de preparação das mesmas |
| AR108396A1 (es) | 2016-05-06 | 2018-08-15 | Incyte Corp | Compuestos heterocíclicos como inmunomoduladores |
| EP3464279B1 (en) | 2016-05-26 | 2021-11-24 | Incyte Corporation | Heterocyclic compounds as immunomodulators |
| TWI771305B (zh) | 2016-06-20 | 2022-07-21 | 美商英塞特公司 | 作為免疫調節劑之雜環化合物 |
| MX2018016331A (es) | 2016-06-20 | 2019-05-20 | Novartis Ag | Formas cristalinas de compuesto de triazolopirimidina. |
| MX2018016295A (es) | 2016-06-20 | 2019-09-16 | Elanco Us Inc | Interferon porcino pegilado y metodos de utilizacion del mismo. |
| ES2870920T3 (es) | 2016-06-21 | 2021-10-28 | X4 Pharmaceuticals Inc | Inhibidores de CXCR4 y usos de los mismos |
| WO2018013789A1 (en) | 2016-07-14 | 2018-01-18 | Incyte Corporation | Heterocyclic compounds as immunomodulators |
| US20180057486A1 (en) | 2016-08-29 | 2018-03-01 | Incyte Corporation | Heterocyclic compounds as immunomodulators |
| CN110167560B (zh) | 2016-08-30 | 2023-08-18 | 四相制药公司 | 四环素化合物和治疗方法 |
| KR102559851B1 (ko) | 2016-12-21 | 2023-07-25 | 아세르타 파마. 비.브이. | 브루톤 티로신 키나제의 이미다조피라진 저해제 |
| TWI795381B (zh) | 2016-12-21 | 2023-03-11 | 比利時商健生藥品公司 | 作為malt1抑制劑之吡唑衍生物 |
| WO2018119286A1 (en) | 2016-12-22 | 2018-06-28 | Incyte Corporation | Bicyclic heteroaromatic compounds as immunomodulators |
| WO2018119221A1 (en) | 2016-12-22 | 2018-06-28 | Incyte Corporation | Pyridine derivatives as immunomodulators |
| WO2018119263A1 (en) | 2016-12-22 | 2018-06-28 | Incyte Corporation | Heterocyclic compounds derivatives as pd-l1 internalization inducers |
| ES2874756T3 (es) | 2016-12-22 | 2021-11-05 | Incyte Corp | Derivados de triazolo[1,5-A]piridina como inmunomoduladores |
| PE20200005A1 (es) | 2016-12-22 | 2020-01-06 | Incyte Corp | Derivados de tetrahidro imidazo[4,5-c]piridina como inductores de internalizacion pd-l1 |
| WO2018119266A1 (en) | 2016-12-22 | 2018-06-28 | Incyte Corporation | Benzooxazole derivatives as immunomodulators |
| SI3559009T1 (sl) | 2016-12-22 | 2021-08-31 | Calithera Biosciences, Inc. | Sestavki in postopki za zaviranje arginazne dejavnosti |
| JOP20180040A1 (ar) | 2017-04-20 | 2019-01-30 | Gilead Sciences Inc | مثبطات pd-1/pd-l1 |
| IL272258B (en) | 2017-07-28 | 2022-08-01 | Chemocentryx Inc | Immunomodulator compounds |
| US10392405B2 (en) | 2017-08-08 | 2019-08-27 | Chemocentryx, Inc. | Macrocyclic immunomodulators |
| CN109400522B (zh) | 2017-08-18 | 2023-04-28 | 上海轶诺药业有限公司 | 一种具有pd-l1抑制活性的化合物、其制备方法及用途 |
| FI3774791T3 (fi) | 2018-03-30 | 2023-03-21 | Incyte Corp | Heterosyklisiä yhdisteitä immunomodulaattoreina |
| WO2019192506A1 (en) | 2018-04-03 | 2019-10-10 | Betta Pharmaceuticals Co., Ltd | Immunomodulators, compositions and methods thereof |
| CN112041311B (zh) | 2018-04-19 | 2023-10-03 | 吉利德科学公司 | Pd-1/pd-l1抑制剂 |
| BR112020022936A2 (pt) | 2018-05-11 | 2021-02-02 | Incyte Corporation | derivados de tetra-hidro-imidazo[4,5-c]piridina como imunomoduladores de pd-l1 |
| WO2020086556A1 (en) | 2018-10-24 | 2020-04-30 | Gilead Sciences, Inc. | Pd-1/pd-l1 inhibitors |
| KR20210089195A (ko) | 2018-11-02 | 2021-07-15 | 상하이 맥시노벨 파마수티컬스 씨오., 엘티디. | 비페닐계 화합물, 이의 중간체, 제조 방법, 약학 조성물 및 용도 |
| WO2020156323A1 (en) | 2019-01-31 | 2020-08-06 | Betta Pharmaceuticals Co., Ltd | Immunomodulators, compositions and methods thereof |
| WO2021030162A1 (en) | 2019-08-09 | 2021-02-18 | Incyte Corporation | Salts of a pd-1/pd-l1 inhibitor |
| JP7559059B2 (ja) | 2019-09-30 | 2024-10-01 | インサイト・コーポレイション | 免疫調節剤としてのピリド[3,2-d]ピリミジン化合物 |
| MX2022005651A (es) | 2019-11-11 | 2022-07-27 | Incyte Corp | Sales y formas cristalinas de un inhibidor de la proteina de muerte celular programada 1 (pd-1)/ligando de muerte celular programada 1 (pd-l1). |
| KR20230117573A (ko) | 2020-11-06 | 2023-08-08 | 인사이트 코포레이션 | Pd-1 및 pd-l1 억제제, 및 이의 염 및 결정형의 제조 방법 |
| US11780836B2 (en) | 2020-11-06 | 2023-10-10 | Incyte Corporation | Process of preparing a PD-1/PD-L1 inhibitor |
| TW202233615A (zh) | 2020-11-06 | 2022-09-01 | 美商英塞特公司 | Pd—1/pd—l1抑制劑之結晶形式 |
| TW202241420A (zh) | 2020-12-18 | 2022-11-01 | 美商英塞特公司 | Pd-l1抑制劑之口服調配物 |
-
2016
- 2016-11-18 HR HRP20221035TT patent/HRP20221035T1/hr unknown
- 2016-11-18 WO PCT/US2016/062730 patent/WO2017087777A1/en active Application Filing
- 2016-11-18 TW TW105137807A patent/TWI763641B/zh active
- 2016-11-18 PL PL16805690.1T patent/PL3377488T3/pl unknown
- 2016-11-18 CA CA3005727A patent/CA3005727A1/en active Pending
- 2016-11-18 CN CN201680077700.8A patent/CN109641885B/zh active Active
- 2016-11-18 EP EP16805690.1A patent/EP3377488B1/en active Active
- 2016-11-18 ES ES16805690T patent/ES2928856T3/es active Active
- 2016-11-18 HU HUE16805690A patent/HUE060680T2/hu unknown
- 2016-11-18 MD MDE20180924T patent/MD3377488T2/ro unknown
- 2016-11-18 US US15/355,494 patent/US20170145025A1/en not_active Abandoned
- 2016-11-18 AU AU2016358100A patent/AU2016358100B2/en active Active
- 2016-11-18 SG SG11201804152RA patent/SG11201804152RA/en unknown
- 2016-11-18 SG SG10202004618TA patent/SG10202004618TA/en unknown
- 2016-11-18 DK DK16805690.1T patent/DK3377488T3/da active
- 2016-11-18 KR KR1020187017417A patent/KR20180095824A/ko not_active Application Discontinuation
- 2016-11-18 EP EP22188807.6A patent/EP4141002A1/en active Pending
- 2016-11-18 EA EA201891203A patent/EA201891203A1/ru unknown
- 2016-11-18 JP JP2018526213A patent/JP7148401B2/ja active Active
- 2016-11-18 LT LTEPPCT/US2016/062730T patent/LT3377488T/lt unknown
- 2016-11-18 PT PT168056901T patent/PT3377488T/pt unknown
- 2016-11-18 RS RS20221010A patent/RS63762B1/sr unknown
- 2016-11-18 MX MX2018006207A patent/MX2018006207A/es unknown
- 2016-11-18 SI SI201631607T patent/SI3377488T1/sl unknown
-
2018
- 2018-05-16 IL IL259406A patent/IL259406B/en unknown
- 2018-05-18 PH PH12018501084A patent/PH12018501084A1/en unknown
- 2018-06-13 ZA ZA2018/03958A patent/ZA201803958B/en unknown
-
2020
- 2020-08-24 US US17/001,129 patent/US11572366B2/en active Active
-
2021
- 2021-08-26 AU AU2021221887A patent/AU2021221887A1/en not_active Abandoned
- 2021-10-14 IL IL287267A patent/IL287267A/en unknown
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2013033901A1 (en) | 2011-09-08 | 2013-03-14 | Merck Sharp & Dohme Corp. | Heterocyclic-substituted benzofuran derivatives and methods of use thereof for the treatment of viral diseases |
| JP2013084945A (ja) | 2011-09-29 | 2013-05-09 | Toyo Ink Sc Holdings Co Ltd | 太陽電池封止材用樹脂組成物 |
| WO2015034820A1 (en) | 2013-09-04 | 2015-03-12 | Bristol-Myers Squibb Company | Compounds useful as immunomodulators |
| WO2015197028A1 (en) | 2014-06-28 | 2015-12-30 | Sunshine Lake Pharma Co., Ltd. | Compounds as hepatitis c virus (hcv) inhibitors and uses thereof in medicine |
| JP2019530732A (ja) | 2016-08-03 | 2019-10-24 | アライジング・インターナショナル・インコーポレイテッドArising International, Inc. | 免疫モジュレータとして有用な対称または半対称化合物 |
Non-Patent Citations (1)
| Title |
|---|
| NISHINO; ET AL,COPPER-MEDIATED C-H/C-H BIARYL COUPLING OF BENZOIC ACID DERIVATIVES AND 1,3-AZOLES,ANGEW. CHEM. INT. ED.,2013年03月19日,VOL. 52, NO. 16,PAGES: 4457 - 4461,http://dx.doi.org/10.1002/anie.201300587 |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7148401B2 (ja) | 免疫調節剤としての複素環化合物 | |
| US11866435B2 (en) | Heterocyclic compounds as immunomodulators | |
| US11407749B2 (en) | Heterocyclic compounds as immunomodulators | |
| JP7394824B2 (ja) | 免疫調節剤としての複素環化合物 | |
| US11608337B2 (en) | Heterocyclic compounds as immunomodulators | |
| US11566026B2 (en) | Heterocyclic compounds as immunomodulators | |
| EA040988B1 (ru) | Гетероциклические соединения в качестве иммуномодуляторов |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20191114 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20201008 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20201013 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20210112 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20210311 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20210413 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20210518 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20210817 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20211015 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20211112 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20220412 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20220711 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20220801 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20220830 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20220922 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7148401 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |