JP5048866B2 - 複数分子の抗原に繰り返し結合する抗原結合分子 - Google Patents
複数分子の抗原に繰り返し結合する抗原結合分子 Download PDFInfo
- Publication number
- JP5048866B2 JP5048866B2 JP2011268497A JP2011268497A JP5048866B2 JP 5048866 B2 JP5048866 B2 JP 5048866B2 JP 2011268497 A JP2011268497 A JP 2011268497A JP 2011268497 A JP2011268497 A JP 2011268497A JP 5048866 B2 JP5048866 B2 JP 5048866B2
- Authority
- JP
- Japan
- Prior art keywords
- antigen
- antibody
- binding
- binding molecule
- bound
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/10—Processes for the isolation, preparation or purification of DNA or RNA
- C12N15/1034—Isolating an individual clone by screening libraries
- C12N15/1037—Screening libraries presented on the surface of microorganisms, e.g. phage display, E. coli display
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/12—Viral antigens
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/12—Viral antigens
- A61K39/145—Orthomyxoviridae, e.g. influenza virus
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/24—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against cytokines, lymphokines or interferons
- C07K16/244—Interleukins [IL]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/24—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against cytokines, lymphokines or interferons
- C07K16/244—Interleukins [IL]
- C07K16/248—IL-6
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2866—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against receptors for cytokines, lymphokines, interferons
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/68—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids
- G01N33/6854—Immunoglobulins
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/54—Medicinal preparations containing antigens or antibodies characterised by the route of administration
- A61K2039/541—Mucosal route
- A61K2039/544—Mucosal route to the airways
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/545—Medicinal preparations containing antigens or antibodies characterised by the dose, timing or administration schedule
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/55—Medicinal preparations containing antigens or antibodies characterised by the host/recipient, e.g. newborn with maternal antibodies
- A61K2039/552—Veterinary vaccine
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/24—Immunoglobulins specific features characterized by taxonomic origin containing regions, domains or residues from different species, e.g. chimeric, humanized or veneered
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
- C07K2317/565—Complementarity determining region [CDR]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/60—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments
- C07K2317/62—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments comprising only variable region components
- C07K2317/622—Single chain antibody (scFv)
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/76—Antagonist effect on antigen, e.g. neutralization or inhibition of binding
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/77—Internalization into the cell
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/92—Affinity (KD), association rate (Ka), dissociation rate (Kd) or EC50 value
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2760/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA ssRNA viruses negative-sense
- C12N2760/00011—Details
- C12N2760/16011—Orthomyxoviridae
- C12N2760/16111—Influenzavirus A, i.e. influenza A virus
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2760/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA ssRNA viruses negative-sense
- C12N2760/00011—Details
- C12N2760/16011—Orthomyxoviridae
- C12N2760/16111—Influenzavirus A, i.e. influenza A virus
- C12N2760/16134—Use of virus or viral component as vaccine, e.g. live-attenuated or inactivated virus, VLP, viral protein
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2770/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA ssRNA viruses positive-sense
- C12N2770/00011—Details
- C12N2770/20011—Coronaviridae
- C12N2770/20071—Demonstrated in vivo effect
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2500/00—Screening for compounds of potential therapeutic value
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Immunology (AREA)
- Organic Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Molecular Biology (AREA)
- Engineering & Computer Science (AREA)
- Genetics & Genomics (AREA)
- Biochemistry (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Biophysics (AREA)
- Biomedical Technology (AREA)
- Microbiology (AREA)
- Virology (AREA)
- Biotechnology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Pharmacology & Pharmacy (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Animal Behavior & Ethology (AREA)
- Hematology (AREA)
- Urology & Nephrology (AREA)
- Physics & Mathematics (AREA)
- General Engineering & Computer Science (AREA)
- Wood Science & Technology (AREA)
- Zoology (AREA)
- Epidemiology (AREA)
- Mycology (AREA)
- Pathology (AREA)
- General Physics & Mathematics (AREA)
- Analytical Chemistry (AREA)
- Food Science & Technology (AREA)
- Cell Biology (AREA)
- Crystallography & Structural Chemistry (AREA)
- Plant Pathology (AREA)
- Pulmonology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
Description
〔1〕抗原に対するpH5.8でのKDとpH7.4でのKDの比であるKD(pH5.8)/KD(pH7.4)の値が2以上である抗原結合分子、
〔2〕KD(pH5.8)/KD(pH7.4)の値が10以上である〔1〕に記載の抗原結合分子、
〔3〕KD(pH5.8)/KD(pH7.4)の値が40以上である〔1〕に記載の抗原結合分子、
〔4〕少なくとも1つのアミノ酸がヒスチジンで置換され又は少なくとも1つのヒスチジンが挿入されていることを特徴とする〔1〕〜〔3〕いずれかに記載の抗原結合分子、
〔5〕アンタゴニスト活性を有することを特徴とする〔1〕〜〔4〕いずれかに記載の抗原結合分子、
〔6〕膜抗原又は可溶型抗原に結合することを特徴とする〔1〕〜〔5〕いずれかに記載の抗原結合分子、
〔7〕抗原結合分子が抗体であることを特徴とする〔1〕〜〔6〕いずれかに記載の抗原結合分子、
〔8〕〔1〕〜〔7〕いずれかに記載の抗原結合分子を含む医薬組成物、
〔9〕抗原結合分子のpH5.8における抗原結合活性をpH7.4における抗原結合活性より弱くすることにより抗原結合分子の薬物動態を向上させる方法、
〔10〕抗原結合分子のpH5.8における抗原結合活性をpH7.4における抗原結合活性より弱くすることにより、抗原結合分子の抗原への結合回数を増やす方法、
〔11〕抗原結合分子のpH5.8における抗原結合活性をpH7.4における抗原結合活性より弱くすることにより、抗原結合分子が結合可能な抗原の数を増やす方法、
〔12〕抗原結合分子のpH5.8における抗原結合活性をpH7.4における抗原結合活性より弱くすることにより、細胞外で抗原結合分子に結合した抗原を細胞内で抗原結合分子から解離させる方法、
〔13〕抗原結合分子のpH5.8における抗原結合活性をpH7.4における抗原結合活性より弱くすることにより、抗原と結合した状態で細胞内に取り込まれた抗原結合分子を、抗原と結合していない状態で細胞外に放出させる方法、
〔14〕抗原結合分子のpH5.8における抗原結合活性をpH7.4における抗原結合活性より弱くすることにより、抗原結合分子の血漿中抗原消失能を増加させる方法、
〔15〕抗原に対するpH5.8でのKDとpH7.4でのKDの比であるKD(pH5.8)/KD(pH7.4)の値を2以上とすることを特徴とする〔9〕〜〔14〕いずれかに記載の方法、
〔16〕KD(pH5.8)/KD(pH7.4)の値を10以上とすることを特徴とする〔9〕〜〔14〕いずれかに記載の方法、
〔17〕KD(pH5.8)/KD(pH7.4)の値を40以上とすることを特徴とする〔9〕〜〔14〕いずれかに記載の方法、
〔18〕抗原結合分子の少なくとも1つのアミノ酸をヒスチジンで置換する又は少なくとも1つのヒスチジンを挿入することにより薬物動態を向上させる方法、
〔19〕抗原結合分子の少なくとも1つのアミノ酸をヒスチジンで置換する又は少なくとも1つのヒスチジンを挿入することにより、抗原結合分子の抗原への結合回数を増やす方法、
〔20〕抗原結合分子の少なくとも1つのアミノ酸をヒスチジンで置換する又は少なくとも1つのヒスチジンを挿入することにより、抗原結合分子が結合可能な抗原の数を増やす方法、
〔21〕抗原結合分子の少なくとも1つのアミノ酸をヒスチジンで置換する又は少なくとも1つのヒスチジンを挿入することにより、細胞外で抗原結合分子に結合した抗原を細胞内で抗原結合分子から解離させる方法、
〔22〕抗原結合分子の少なくとも1つのアミノ酸をヒスチジンで置換する又は少なくとも1つのヒスチジンを挿入することにより、抗原と結合した状態で細胞内に取り込まれた抗原結合分子を、抗原と結合していない状態で細胞外に放出させる方法、
〔23〕抗原結合分子の少なくとも1つのアミノ酸をヒスチジンで置換する又は少なくとも1つのヒスチジンを挿入することにより、抗原結合分子の血漿中抗原消失能を増加させる方法、
〔24〕ヒスチジンへの置換又はヒスチジンの挿入により、pH5.8での抗原結合活性とpH7.4での抗原結合活性の比であるKD(pH5.8)/KD(pH7.4)の値がヒスチジン置換又は挿入前と比較して大きくなることを特徴とする〔18〕〜〔23〕いずれかに記載の方法、
〔25〕抗原結合分子がアンタゴニスト活性を有することを特徴とする〔9〕〜〔24〕いずれかに記載の方法、
〔26〕抗原結合分子が膜抗原又は可溶型抗原に結合することを特徴とする〔9〕〜〔25〕いずれかに記載の方法、
〔27〕抗原結合分子が抗体であることを特徴とする〔9〕〜〔26〕いずれかに記載の方法、
〔28〕以下の工程を含む抗原結合分子のスクリーニング方法、
(a)pH6.7〜pH10.0における抗原結合分子の抗原結合活性を得る工程、
(b)pH4.0〜pH6.5における抗原結合分子の抗原結合活性を得る工程、
(c)pH6.7〜pH10.0での抗原結合活性がpH4.0〜pH6.5での抗原結合活性より高い抗原結合分子を選択する工程、
〔29〕pH6.7〜pH10.0における抗原結合活性がpH4.0〜pH6.5での抗原結合活性の2倍以上である抗体を選択することを特徴とする〔28〕に記載のスクリーニング方法、
〔30〕以下の工程を含む抗原結合分子のスクリーニング方法、
(a) pH6.7〜pH10.0の条件下で抗原結合分子を抗原に結合させる工程、
(b) (a)の抗原に結合した抗原結合分子をpH4.0〜pH6.5の条件下に置く工程、
(c) pH4.0〜pH6.5の条件下で解離した抗原結合分子を取得する工程、
〔31〕以下の工程を含む第一のpHでの結合活性が第二のpHでの結合活性よりも高い抗原結合分子のスクリーニング方法、
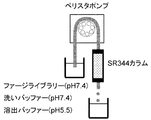
(a) 抗原を固定したカラムに第一のpH条件下で抗原結合分子を結合させる工程、
(b) 第一のpH条件下でカラムに結合した抗原結合分子を、第二のpH条件下でカラムから溶出する工程、
(c) 溶出された抗原結合分子を取得する工程、
〔32〕以下の工程を含む第一のpHでの結合活性が第二のpHでの結合活性よりも高い抗原結合分子のスクリーニング方法、
(a) 抗原結合分子ライブラリーを、抗原を固定したカラムに第一のpH条件下で結合させる工程、
(b) カラムから第二のpH条件下で抗原結合分子を溶出する工程、
(c) 溶出された抗原結合分子をコードする遺伝子を増幅する工程、
(d) 溶出された抗原結合分子を取得する工程、
〔33〕第一のpHがpH6.7.〜pH10.0、第二のpHが4.0〜pH6.5であることを特徴とする〔31〕または〔32〕に記載のスクリーニング方法、
〔34〕抗原結合分子が、抗原結合分子中の少なくとも1つ以上のアミノ酸がヒスチジンで置換された又は少なくとも1つのヒスチジンが挿入された抗原結合分子である〔28〕〜〔33〕いずれかに記載のスクリーニング方法、
〔35〕血漿中滞留性が優れた抗原結合分子を得ることを目的とする〔28〕〜〔33〕いずれかに記載のスクリーニング方法、
〔36〕抗原に2回以上結合することができる抗原結合分子を得ることを目的とする〔28〕〜〔33〕いずれかに記載のスクリーニング方法、
〔37〕結合可能な抗原の数が抗原結合部位より多い抗原結合分子を得ることを目的とする〔28〕〜〔33〕いずれかに記載のスクリーニング方法、
〔38〕細胞外で結合した抗原を細胞内で解離する抗原結合分子を得ることを目的とする〔28〕〜〔33〕いずれかに記載のスクリーニング方法、
〔39〕抗原と結合した状態で細胞内に取り込まれ、抗原と結合していない状態で細胞外に放出される抗原結合分子を得ることを目的とする〔28〕〜〔33〕いずれかに記載のスクリーニング方法、
〔40〕血漿中抗原消失能が増加した抗原結合分子を得ることを目的とする〔28〕〜〔33〕いずれかに記載のスクリーニング方法、
〔41〕抗原結合分子が医薬組成物として用いられる抗原結合分子である〔28〕〜〔40〕いずれかに記載のスクリーニング方法、
〔42〕抗原結合分子が抗体であることを特徴とする〔28〕〜〔41〕いずれかに記載のスクリーニング方法、
〔43〕以下の工程を含む抗原結合分子の製造方法、
(a) pH6.7〜pH10.0における抗原結合分子の抗原結合活性を得る工程、
(b) pH4.0〜pH6.5における抗原結合分子の抗原結合活性を得る工程、
(c) pH6.7〜pH10.0での抗原結合活性がpH4.0〜pH6.5での抗原結合活性より高い抗原結合分子を選択する工程、
(d) (c)で選択された抗原結合分子をコードする遺伝子を得る工程、
(e) (d)で得られた遺伝子を用いて抗原結合分子を製造する工程、
〔44〕以下の工程を含む抗原結合分子の製造方法、
(a) pH6.7〜pH10.0の条件下で抗原結合分子を抗原に結合させる工程、
(b) (a)の抗原に結合した抗原結合分子をpH4.0〜pH6.5の条件下に置く工程、
(c) pH4.0〜pH6.5の条件下で解離した抗原結合分子を取得する工程、
(d) (c)で取得された抗原結合分子をコードする遺伝子を得る工程、
(e) (d)で得られた遺伝子を用いて抗原結合分子を製造する工程、
〔45〕以下の工程を含む第一のpHでの結合活性が第二のpHでの結合活性よりも高い抗原結合分子の製造方法、
(a) 抗原を固定したカラムに第一のpH条件下で抗原結合分子を結合させる工程、
(b) 第一のpH条件下でカラムに結合した抗原結合分子を、第二のpH条件下でカラムから溶出する工程、
(c) 溶出された抗原結合分子を取得する工程、
(d) (c)で取得された抗原結合分子をコードする遺伝子を得る工程、
(e) (d)で得られた遺伝子を用いて抗原結合分子を製造する工程、
〔46〕以下の工程を含む第一のpHでの結合活性が第二のpHでの結合活性よりも高い抗原結合分子の製造方法、
(a) 抗原結合分子ライブラリーを、抗原を固定したカラムに第一のpH条件下で結合させる工程、
(b) カラムから第二のpH条件下で抗原結合分子を溶出する工程、
(c) 溶出された抗原結合分子をコードする遺伝子を増幅する工程、
(d) 溶出された抗原結合分子を取得する工程、
(e) (d)で取得された抗原結合分子をコードする遺伝子を得る工程、
(f) (e)で得られた遺伝子を用いて抗原結合分子を製造する工程、
〔47〕第一のpHがpH6.7.〜pH10.0、第二のpHが4.0〜pH6.5であることを特徴とする〔45〕または〔46〕に記載の製造方法、
〔48〕抗原結合分子中の少なくとも1つ以上のアミノ酸をヒスチジンで置換する又は少なくとも1つのヒスチジンを挿入する工程をさらに含む〔43〕〜〔47〕いずれかに記載の製造方法、
〔49〕抗原結合分子が抗体であることを特徴とする〔43〕〜〔48〕いずれかに記載の製造方法、
〔50〕〔43〕〜〔49〕いずれかに記載の製造方法により製造された抗原結合分子を含む医薬組成物、
を提供するものである。
本発明は、抗原結合分子の抗原への結合回数を増やす方法を提供する。より具体的には抗原結合分子の酸性pHにおける抗原結合能を中性pHにおける抗原結合能よりも弱くすることにより、抗原結合分子の抗原への結合回数を増やす方法を提供する。さらに、本発明は抗原結合分子の少なくとも1つのアミノ酸をヒスチジンに置換する又は少なくとも1つのヒスチジンを挿入することを特徴とする抗原結合分子の抗原への結合回数を増やす方法を提供する。さらに本発明は、抗原結合分子に含まれる抗体定常領域中のアミノ酸を置換、欠失、付加及び/又は挿入することを特徴とする抗原結合分子の抗原への結合回数を増やす方法を提供する。
(1)抗原結合分子が投与されてから、抗原結合分子が血漿中から消失するまでの時間の延長。
(2)抗原結合分子が投与されてから、抗原結合分子が抗原に結合可能な状態で血漿中に存在する時間の延長。
(3)抗原結合分子が投与されてから、生体内の抗原が抗原結合分子と結合していない時間の減少(生体内の抗原に抗原結合分子が結合している時間の延長)。
(4)生体内に存在する抗原に対する抗原結合分子に結合した抗原の割合の上昇。
軽鎖:L24、L27、L28、L32、L53、L54、L56、L90、L92、L94
軽鎖:L24、L27、L28、L32、L53、L56、L90、L92、L94
軽鎖:L53、L54、L90、L94
さらに、本発明はpH4.0〜pH6.5での抗原結合活性がpH6.7〜pH10.0での抗原結合活性よりも低い抗原結合分子、好ましくはpH5.0〜pH6.0での抗原結合活性がpH7.0〜8.0での抗原結合活性よりも低い抗原結合分子を提供する。pH4.0〜pH6.5での抗原結合活性がpH6.7〜10.0での抗原結合活性よりも低い抗原結合分子の具体的な例としては、pH5.8での抗原結合活性がpH7.4での抗原結合活性よりも低い抗原結合分子を挙げることができる。又、pH5.8での抗原結合活性がpH7.4での抗原結合活性よりも低い抗原結合分子は、pH7.4での抗原結合活性がpH5.8での抗原結合活性よりも高い抗原結合分子ということもできる。
軽鎖:L24、L27、L28、L32、L53、L54、L56、L90、L92、L94
軽鎖:L24、L27、L28、L32、L53、L56、L90、L92、L94
軽鎖:L53、L54、L90、L94
(1)疎水性:アラニン、イソロイシン、バリン、メチオニン及びロイシン;
(2)中性親水性:アスパラギン、グルタミン、システイン、スレオニン及びセリン;
(3)酸性:アスパラギン酸及びグルタミン酸;
(4)塩基性:アルギニン、ヒスチジン及びリジン;
(5)鎖の配向に影響する残基:グリシンおよびプロリン;ならびに
(6)芳香族性:チロシン、トリプトファン及びフェニルアラニン
のグループに分類される。
本発明は抗原結合分子の酸性pHにおける抗原結合活性が中性pHにおける抗原結合活性よりも低い抗原結合分子をスクリーニングする方法を提供する。又、本発明は1分子で複数の抗原に結合することが可能な抗原結合分子のスクリーニング方法を提供する。又、本発明は血漿中滞留性に優れた抗原結合分子のスクリーニング方法を提供する。又、本発明は細胞外で抗原結合分子に結合した抗原を細胞内で解離する抗原結合分子のスクリーニング方法を提供する。又、本発明は抗原と結合した状態で細胞内に取り込まれ、抗原と結合していない状態で細胞外に放出される抗原結合分子のスクリーニング方法を提供する。又、本発明は血漿中抗原消失能が増加した抗原結合分子のスクリーニング方法を提供する。さらに、本発明は医薬組成物として用いる際に特に有用である抗原結合分子のスクリーニング方法を提供する。
(a) pH6.7〜pH10.0における抗原結合分子の抗原結合活性を得る工程、
(b) pH4.0〜pH6.5における抗原結合分子の抗原結合活性を得る工程、
(c) pH6.7〜pH10.0での抗原結合活性がpH4.0〜pH6.5での抗原結合活性より高い抗原結合分子を選択する工程。
(a) pH6.7〜pH10.0の条件下で抗原結合分子を抗原に結合させる工程、
(b) (a)の抗原に結合した抗原結合分子をpH4.0〜pH6.5の条件下に置く工程、
(c) pH4.0〜pH6.5の条件下で解離した抗原結合分子を取得する工程。
(a) pH4.0〜pH6.5の条件下で抗原に結合しない抗原結合分子を選択する工程、
(b) (a)で選択された抗原結合分子をpH6.7〜pH10.0の条件下で抗原に結合させる工程、
(c) pH6.7〜pH10.0の条件下で抗原に結合した抗原結合分子を取得する工程。
(a) pH6.7〜pH10.0の条件下で抗原結合分子を抗原に結合させる工程、
(b) (a)の抗原に結合した抗原結合分子をpH4.0〜pH6.5の条件下に置く工程、
(c) pH4.0〜pH6.5の条件下で解離した抗原結合分子を取得する工程、
(d) 解離した抗原結合分子をコードする遺伝子を増幅する工程、
(e) 溶出された抗原結合分子を取得する工程。
(a) pH4.0〜pH6.5の条件下で抗原に結合しない抗原結合分子を選択する工程、
(b) (a)で選択された抗原結合分子をpH6.7〜pH10.0の条件下で抗原に結合させる工程、
(c) pH6.7〜pH10.0の条件下で抗原に結合した抗原結合分子を取得する工程、
(d) 解離した抗原結合分子をコードする遺伝子を増幅する工程、
(e) 溶出された抗原結合分子を取得する工程。
(a) 抗原を固定したカラムに第一のpH条件下で抗原結合分子を結合させる工程、
(b) 第一のpH条件下でカラムに結合した抗原結合分子を、第二のpH条件下でカラムから溶出する工程、
(c) 溶出された抗原結合分子を取得する工程。
(a) 抗原を固定したカラムに第一のpH条件下で抗原結合分子を通過させる工程、
(b) (a)の工程でカラムに結合せずに溶出した抗原結合分子を回収する工程、
(c) (b)で回収された抗原結合分子を第二のpH条件下でカラムに結合させる工程、
(d) (c)の工程においてカラムに結合した抗原結合分子を取得する工程。
(a) 抗原結合分子ライブラリーを、抗原を固定したカラムに第一のpH条件下で結合させる工程、
(b) カラムから第二のpH条件下で抗原結合分子を溶出する工程、
(c) 溶出された抗原結合分子をコードする遺伝子を増幅する工程、
(d) 溶出された抗原結合分子を取得する工程。
本発明は抗原結合分子のエンドソーム内でのpHにおける抗原結合活性が血漿中でのpHにおける抗原結合活性よりも低い抗原結合分子の製造方法を提供する。又、本発明は血漿中滞留性に優れた抗原結合分子の製造方法を提供する。さらに、本発明は医薬組成物として用いる際に特に有用である抗原結合分子の製造方法を提供する。
(a) pH6.7〜pH10.0における抗原結合分子の抗原結合活性を得る工程、
(b) pH4.0〜pH6.5における抗原結合分子の抗原結合活性を得る工程、
(c) pH6.7〜pH10.0での抗原結合活性がpH4.0〜pH6.5での抗原結合活性より高い抗原結合分子を選択する工程、
(d) (c)で選択された抗原結合分子をコードする遺伝子を得る工程、
(e) (d)で得られた遺伝子を用いて抗原結合分子を製造する工程。
(a) pH6.7〜pH10.0の条件下で抗原結合分子を抗原に結合させる工程、
(b) (a)の抗原に結合した抗原結合分子をpH4.0〜pH6.5の条件下に置く工程、
(c) pH4.0〜pH6.5の条件下で解離した抗原結合分子を取得する工程、
(d) (c)で取得された抗原結合分子をコードする遺伝子を得る工程、
(e) (d)で得られた遺伝子を用いて抗原結合分子を製造する工程。
(a) pH4.0〜pH6.5の条件下で抗原に結合しない抗原結合分子を選択する工程、
(b) (a)で選択された抗原結合分子をpH6.7〜pH10.0の条件下で抗原に結合させる工程、
(c) pH6.7〜pH10.0の条件下で抗原に結合した抗原結合分子を取得する工程、
(d) (c)で取得された抗原結合分子をコードする遺伝子を得る工程、
(e) (d)で得られた遺伝子を用いて抗原結合分子を製造する工程。
(a) pH6.7〜10.0の条件下で抗原結合分子を抗原に結合させる工程、
(b) (a)の抗原に結合した抗原結合分子をpH4.0〜pH6.5の条件下に置く工程、
(c) pH4.0〜pH6.5の条件下で解離した抗原結合分子を取得する工程、
(d) 解離した抗原結合分子をコードする遺伝子を増幅する工程、
(e) 溶出された抗原結合分子を取得する工程、
(f) (e)で取得された抗原結合分子をコードする遺伝子を得る工程、
(g) (f)で得られた遺伝子を用いて抗原結合分子を製造する工程。
(a) pH4.0〜pH6.5の条件下で抗原に結合しない抗原結合分子を選択する工程、
(b) (a)で選択された抗原結合分子をpH6.7〜pH10.0の条件下で抗原に結合させる工程、
(c) pH6.7〜pH10.0の条件下で抗原に結合した抗原結合分子を取得する工程、
(d) 解離した抗原結合分子をコードする遺伝子を増幅する工程、
(e) 溶出された抗原結合分子を取得する工程、
(f) (e)で取得された抗原結合分子をコードする遺伝子を得る工程、
(g) (f)で得られた遺伝子を用いて抗原結合分子を製造する工程。
(a) 抗原を固定したカラムに第一のpH条件下で抗原結合分子を結合させる工程、
(b) 第一のpH条件下でカラムに結合した抗原結合分子を、第二のpH条件下でカラムから溶出する工程、
(c) 溶出された抗原結合分子を取得する工程、
(d) (c)で取得された抗原結合分子をコードする遺伝子を得る工程、
(e) (d)で得られた遺伝子を用いて抗原結合分子を製造する工程。
(a) 抗原結合分子ライブラリーを、抗原を固定したカラムに第一のpH条件下で結合させる工程、
(b) カラムから第二のpH条件下で抗原結合分子を溶出する工程、
(c) 溶出された抗原結合分子をコードする遺伝子を増幅する工程、
(d) 溶出された抗原結合分子を取得する工程、
(e) (d)で取得された抗原結合分子をコードする遺伝子を得る工程、
(f) (e)で得られた遺伝子を用いて抗原結合分子を製造する工程。
さらに、本発明は以下の(a)〜(m)のいずれかに記載の抗IL-6受容体抗体を提供する。
(a) 配列番号:1(H53可変領域)のアミノ酸配列において27番目のTyr、31番目のAsp、32番目のAsp、35番目のTrp、51番目のTyr、59番目のAsn、63番目のSer、106番目のMet、108番目のTyrの少なくとも1つがHisに置換されたアミノ酸配列を有する重鎖可変領域を含む抗体、
(b) 配列番号:1(H53可変領域)のアミノ酸配列において27番目のTyr、31番目のAspおよび35番目のTrpがHisに置換されたアミノ酸配列を有する重鎖可変領域を含む抗体(H3pI)、
(c) 配列番号:1(H53可変領域)のアミノ酸配列において27番目のTyr、31番目のAsp、32番目のAsp、35番目のTrp、59番目のAsn、63番目およびSer、108番目のTyrがHisに置換されたアミノ酸配列を有する重鎖可変領域を含む抗体、
(d) 配列番号:1(H53可変領域)のアミノ酸配列において27番目のTyr、31番目のAsp、32番目のAsp、35番目のTrp、59番目のAsn、63番目およびSer、108番目のTyrがHisに置換され、かつ99番目のSerがValに、103番目のThrがIleに置換されたアミノ酸配列を有する重鎖可変領域を含む抗体(H170)、
(e) 配列番号:1(H53可変領域)のアミノ酸配列において31番目のAsp、51番目のTyr、63番目のSer、106番目のMetおよび108番目のTyrがHisに置換されたアミノ酸配列を有する重鎖可変領域を含む抗体、
(f) 配列番号:1(H53可変領域)のアミノ酸配列において31番目のAsp、51番目のTyr、63番目のSer、106番目のMetおよび108番目のTyrがHisに置換され、かつ99番目のSerがPheに、103番目のThrがIleに置換されたアミノ酸配列を有する重鎖可変領域を含む抗体(CLH5)、
(g) 配列番号:2(PF1L可変領域)のアミノ酸配列において、28番目のAsp、32番目のTyr、53番目のGlu、56番目のSer、92番目のAsnの少なくとも1つがHisに置換されたアミノ酸配列を有する軽鎖可変領域を含む抗体、
(h) 配列番号:2(PF1L可変領域)のアミノ酸配列において、28番目のAsp、32番目のTyrおよび53番目のGluがHisに置換されたアミノ酸配列を有する軽鎖可変領域を含む抗体(L73)、
(i) 配列番号:1(H53可変領域)のアミノ酸配列において、32番目のTyrおよび53番目のGluがHisに置換されたアミノ酸配列を有する軽鎖可変領域を含む抗体(L82)、
(j) 配列番号:2(PF1L可変領域)のアミノ酸配列において、32番目のTyr、53番目のGlu、56番目のSerおよび92番目のAsnがHisに置換されたアミノ酸配列を有する軽鎖可変領域を含む抗体(CLL5)、
(k) (b)の重鎖可変領域および(h)の軽鎖可変領域を含む抗体、
(l) (d)の重鎖可変領域および(i)の軽鎖可変領域を含む抗体、
(m) (f)の重鎖可変領域および(h)の軽鎖可変領域を含む抗体。
配列番号:3(H3pI)のアミノ酸配列を有する重鎖可変領域
配列番号:4(H170)のアミノ酸配列を有する重鎖可変領域
配列番号:5(CLH5)のアミノ酸配列を有する重鎖可変領域
配列番号:6(L73)のアミノ酸配列を有する軽鎖可変領域
配列番号:7(L82)のアミノ酸配列を有する軽鎖可変領域
配列番号:8(CLL5)のアミノ酸配列を有する軽鎖可変領域
(1) 配列番号:21(VH1-IgG1)の1番目から119番目までのアミノ酸配列を有する重鎖可変領域(VH1-IgG1可変領域)を含む抗体、
(2) 配列番号:22(VH2-IgG1)の1番目から119番目までのアミノ酸配列を有する重鎖可変領域(VH2-IgG1可変領域)を含む抗体、
(3) 配列番号:23(VH3-IgG1)の1番目から119番目までのアミノ酸配列を有する重鎖可変領域(VH3-IgG1可変領域)を含む抗体、
(4) 配列番号:24(VH4-IgG1)の1番目から119番目までのアミノ酸配列を有する重鎖可変領域(VH4-IgG1可変領域)を含む抗体、
(5) 配列番号:25(VL1-CK)の1番目から107番目までのアミノ酸配列を有する軽鎖可変領域(VL1-CK可変領域)を含む抗体、
(6) 配列番号:26(VL2-CK)の1番目から107番目までのアミノ酸配列を有する軽鎖可変領域(VL2-CK可変領域)を含む抗体、
(7) 配列番号:27(VL3-CK)の1番目から107番目までのアミノ酸配列を有する軽鎖可変領域(VL3-CK可変領域)を含む抗体、
(8) (2)の重鎖可変領域と(6)の軽鎖可変領域を含む抗体(Fv1-IgG1)、
(9) (1)の重鎖可変領域と配列番号:7(L82)に記載のアミノ酸配列を有する軽鎖可変領域を含む抗体(Fv2-IgG1)、
(10) (4)の重鎖可変領域と(5)の軽鎖可変領域を含む抗体(Fv3-IgG1)、
(11) (3)の重鎖可変領域と(7)の軽鎖可変領域を含む抗体(Fv4-IgG1)、
(12) 配列番号:33に記載のアミノ酸配列を有する重鎖を含む抗体(VH3-IgG2ΔGK)、
(13) 配列番号:34に記載のアミノ酸配列を有する重鎖を含む抗体(VH3-M58)、
(14) 配列番号:35に記載のアミノ酸配列を有する重鎖を含む抗体(VH3-M73)、
(15) (12)の重鎖と配列番号:27(VL3-CK)のアミノ酸配列を有する軽鎖を含む抗体(Fv4-IgG2ΔGK)、
(16) (13)の重鎖と配列番号:27(VL3-CK)のアミノ酸配列を有する軽鎖を含む抗体(Fv4-M58)、
(17) (14)の重鎖と配列番号:27(VL3-CK)のアミノ酸配列を有する軽鎖を含む抗体(Fv4-M73)、
(18) 配列番号:36(VH2-M71)のアミノ酸配列を有する重鎖を含む抗体(VH2-M71)、
(19) 配列番号:37(VH2-M73)のアミノ酸配列を有する重鎖を含む抗体(VH2-M73)、
(20) 配列番号:38(VH4-M71)のアミノ酸配列を有する重鎖を含む抗体(VH4-M71)、
(21) 配列番号:39(VH4-M73)のアミノ酸配列を有する重鎖を含む抗体(VH4-M73)、
(22) (18)の重鎖と配列番号:26(VL2-CK)のアミノ酸配列を有する軽鎖を含む抗体(Fv1-M71)、
(23) (19)の重鎖と配列番号:26(VL2-CK)のアミノ酸配列を有する軽鎖を含む抗体(Fv1-M73)、
(24) (20)の重鎖と配列番号:25(VL1-CK)のアミノ酸配列を有する軽鎖を含む抗体(Fv3-M71)、
(25) (21)の重鎖と配列番号:25(VL1-CK)のアミノ酸配列を有する軽鎖を含む抗体(Fv3-M73)、
(26) 配列番号:25(VL1-CK)のアミノ酸配列を有する軽鎖を含む抗体、
(27) 配列番号:26(VL2-CK)のアミノ酸配列を有する軽鎖を含む抗体、
(28) 配列番号:27(VL3-CK)のアミノ酸配列を有する軽鎖を含む抗体。
(a) 配列番号:40に記載の重鎖CDR1(VH1,2,3,4)、
(b) 配列番号:41に記載の重鎖CDR2(VH1,2)、
(c) 配列番号:42に記載の重鎖CDR2(VH3)、
(d) 配列番号:43に記載の重鎖CDR2(VH4)、
(e) 配列番号:44に記載の重鎖CDR3(VH1,2)、
(f) 配列番号:45に記載の重鎖CDR3(VH3,4)、
(g) 配列番号:46に記載の重鎖FR1(VH1,2)、
(h) 配列番号:47に記載の重鎖FR1(VH3,4)、
(i) 配列番号:48に記載の重鎖FR2(VH1,2,3,4)
(j) 配列番号:49に記載の重鎖FR3(VH1)、
(k) 配列番号:50に記載の重鎖FR3(VH2)、
(l) 配列番号:51に記載の重鎖FR3(VH3,4)、
(m) 配列番号:52に記載の重鎖FR4(VH1,2,3,4)
(n) 配列番号:53に記載の軽鎖CDR1(VL1,2)、
(o) 配列番号:54に記載の軽鎖CDR1(VL3)、
(p) 配列番号:55に記載の軽鎖CDR2(VL1,VL3)、
(q) 配列番号:56に記載の軽鎖CDR2(VL2)、
(r) 配列番号:57に記載の軽鎖CDR3(VL1,2,3)、
(s) 配列番号:58に記載の軽鎖FR1(VL1,2,3)、
(t) 配列番号:59に記載の軽鎖FR2(VL1,2,3)、
(u) 配列番号:60に記載の軽鎖FR3(VL1,2,3)、
(v) 配列番号:61に記載の軽鎖FR4(VL1,2,3)。
(a)本発明のポリペプチドをコードする遺伝子が導入されたベクターを含む宿主細胞を培養する工程、
(b)当該遺伝子によりコードされるポリペプチドを取得する工程。
また本発明は、本発明の抗原結合分子、本発明のスクリーニング方法により単離された抗原結合分子、または本発明の製造方法により製造された抗原結合分子を含む医薬組成物に関する。本発明の抗原結合分子または本発明の製造方法により製造された抗原結合分子は血漿中滞留性に優れており、抗原結合分子の投与頻度を減らせることが期待されるので医薬組成物として有用である。本発明の医薬組成物は医薬的に許容される担体を含むことができる。
組み換え可溶型ヒトIL-6レセプター(SR344)の調製
抗原であるヒトIL-6レセプターの組み換えヒトIL-6レセプターは以下のように調製した。J.Biochem. 108, 673-676 (1990)で報告されているN末端側1番目から344番目のアミノ酸配列からなる可溶型ヒトIL-6レセプター(以下、SR344)(Yamasakiら、Science 1988;241:825-828 (GenBank # X12830))のCHO細胞定常発現株を作製した。
公開されているアカゲザルIL-6レセプター遺伝子配列(Birney et al, Ensembl 2006, Nucleic Acids Res. 2006 Jan 1;34(Database issue):D556-61.)を元にオリゴDNAプライマー Rhe6Rf1(配列番号:16)、Rhe6Rr2(配列番号:17)を作製した。カニクイザル膵臓から調製されたcDNAを鋳型とし、プライマーRhe6Rf1およびRhe6Rr2を用いて、PCR法によりカニクイザルIL-6レセプター遺伝子全長をコードするDNA断片を調製した。得られたDNA断片を鋳型に、オリゴDNAプライマーCynoIL6R N-EcoRI(配列番号:18)およびCynoIL6R C-NotI-His(配列番号:19)を用いて、PCR法によりカニクイザルIL-6レセプター遺伝子のシグナル領域を含む可溶型領域(Met1-Pro363)のC末端に6xHisが付加されたタンパク質をコードする1131 bpのDNA断片(配列番号:20)を増幅した。得られたDNA断片をEcoRI-NotIで消化し、動物細胞発現ベクターへ挿入し、これを用いてCHO定常発現株(cyno.sIL-6R産生CHO細胞)を作製した。
カニクイザルIL-6は以下のように調製した。SWISSPROT Accession No.P79341に登録されている212アミノ酸をコードする塩基配列を作成し、動物細胞発現ベクターにクローニングし、CHO細胞に導入することで定常発現細胞株を作製した(cyno.IL-6産生CHO細胞)。cyno.IL-6産生CHO細胞の培養液をSP-Sepharose/FFカラム(GEヘルスケアバイオサイエンス)で精製後、Amicon Ultra-15 Ultracel-5k(Millipore)を用いて濃縮し、Superdex75pg26/60ゲルろ過カラム(GEヘルスケアバイオサイエンス)でさらに精製を行い、Amicon Ultra-15 Ultracel-5k(Millipore)を用いて濃縮し、カニクイザルIL-6(以下、cIL-6)の最終精製品とした。
IL-6依存増殖性を示す細胞株を得るために、以下に示すとおり、ヒトgp130を発現したBaF3細胞株の樹立を行った。
Cancer Res. 1993 Feb 15;53(4):851-6においてヒト化されたマウスPM1抗体(以降Wild type、WTと略、H鎖WTをH(WT)(アミノ酸配列 配列番号:9)とし、L鎖WTをL(WT)(アミノ酸配列 配列番号:10)とする)のフレームワーク配列とCDR配列に変異を導入し、改変H鎖としてH53(アミノ酸配列 配列番号:1)、PF1H(アミノ酸配列 配列番号:11)、改変L鎖としてL28(アミノ酸配列 配列番号:12)、PF1L(アミノ酸配列 配列番号:2)を作製した。具体的には、QuikChange Site-Directed Mutagenesis Kit(Stratagene)を用いて、添付説明書記載の方法で変異体を作製し、得られたプラスミド断片を動物細胞発現ベクターに挿入し、目的のH鎖発現ベクターおよびL鎖発現ベクターを作製した。得られた発現ベクターの塩基配列は当業者公知の方法で決定した。
抗体の発現は以下の方法を用いて行った。ヒト胎児腎癌細胞由来HEK293H株(Invitrogen)を10 % Fetal Bovine Serum(Invitrogen)を含むDMEM培地(Invitrogen)へ懸濁し、5〜6 × 105個 /mLの細胞密度で接着細胞用ディッシュ(直径10 cm, CORNING)の各ディッシュへ10 mLずつ蒔きこみCO2インキュベーター(37℃、5 % CO2)内で一昼夜培養した後に、培地を吸引除去し、CHO-S-SFM-II(Invitrogen)培地6.9 mLを添加した。調製したプラスミドをlipofection法により細胞へ導入した。得られた培養上清を回収した後、遠心分離(約2000 g、5分間、室温)して細胞を除去し、さらに0.22μmフィルターMILLEX(R)-GV(Millipore)を通して滅菌して培養上清を得た。得られた培養上清にrProtein A SepharoseTM Fast Flow(Amersham Biosciences)を用いて当業者公知の方法で精製した。精製抗体濃度は、分光光度計を用いて280 nmでの吸光度を測定した。得られた値からPACE法により算出された吸光係数を用いて抗体濃度を算出した(Protein Science 1995 ; 4 : 2411-2423)。
複数回抗原を中和できる抗体の創製方法
IgG分子は2価であるため2ヶ所で抗原に結合した場合、1分子のIgG分子で最大2分子の抗原を中和することが可能であるが、3分子以上の抗原を中和することは出来ない。そのため中和抗体の場合、その中和効果を一定期間持続させるためには、その一定期間に産生される抗原量以上の抗体量が投与される必要があり、抗体の薬物動態向上やアフィニティー向上技術だけでは、必要抗体投与量の低減には限界が存在する。そこで1分子のIgG分子で2分子以上の抗原を中和することができれば、同じ投与量であれば中和効果の持続性が向上し、また、同じ持続性を達成するために必要な投与量を低減することが可能である。
pH依存的な結合を抗原抗体反応に導入する方法として、CDRにヒスチジンを導入する方法が報告されている(FEBS Letter (vol.309, No.1, 85-88, 1992))。実施例1で作製したH53/PF1Lの可変領域表面に露出するアミノ酸残基および抗原と相互作用していると考えられる残基を確認するために、MOEソフトウェア(Chemical Computing Group Inc.)を用いて、ホモロジーモデリングによりH53/PF1LのFv領域モデルを作製した。H53/PF1Lの配列情報を元に作成した立体構造モデルより、ヒスチジン導入により抗原とのpH依存的結合を導入できると考えられる変異箇所をH27、H31、H35、L28、L32、L53(Kabatナンバリング、Kabat EA et al. 1991. Sequences of Proteins of Immunological Interest.NIH)に選定した。H27、H31、H35の残基をヒスチジンに置換する変異を実施例1で作成したH53に対して導入したものをH3pI(アミノ酸配列 配列番号:3)とし、L28、L32、L53の残基をヒスチジンに置換する変異を実施例1で作成したPF1Lに対して導入したものをL73(アミノ酸配列 配列番号:6)とした。
選定された箇所について改変抗体を作製するためのアミノ酸改変を行った。実施例1において作製したH53(塩基配列 配列番号:13)およびPF1L(塩基配列 配列番号:14)に変異を導入して、H3pI(アミノ酸配列 配列番号:3)とL73(アミノ酸配列 配列番号:6)を作製した。具体的には、QuikChange Site-Directed Mutagenesis Kit(Stratagene)を用いて、添付説明書記載の方法で作製し、得られたプラスミド断片を動物細胞発現ベクターに挿入し、目的のH鎖発現ベクターおよびL鎖発現ベクターを作製した。得られた発現ベクターの塩基配列は当業者公知の方法で決定した。H鎖としてH3pI、L鎖としてL73を用いたH3pI/L73の発現・精製は実施例1に記載した方法で行った。
ヒト化PM1抗体のscFv分子の作製
ヒト化抗IL-6R抗体であるヒト化PM1抗体(Cancer Res. 1993 Feb 15;53(4):851-6)のscFv化を行った。VH、VL領域をPCRによって増幅し、リンカー配列GGGGSGGGGSGGGGS(配列番号:15)をVH、VLの間に持つヒト化PM1 HL scFvを作製した。
作製したヒト化PM1 HL scFv DNAを鋳型にしたPCRにより、各CDRアミノ酸のうちの一つのアミノ酸がヒスチジンとなるヒスチジンライブラリーを作製した。ライブラリー化したいアミノ酸のコドンをヒスチジンに相当するコドンであるCATとしたプライマーを用いたPCR反応によってライブラリー部分を構築、それ以外の部分を通常のPCRによって作製し、assemble PCR法により連結して構築した。構築したライブラリーをSfi Iで消化し、同様にSfi Iで消化したphagemideベクターpELBG lacIベクターに挿入し、XL1-Blue(stratagene)にtransformした。得られたコロニーを用い、phage ELISAによる抗原結合性評価とHL scFv配列解析を行った。J.Mol.Biol 1992 ; 227 : 381-388に習い、SR344を1μg/mLでcoatingしたプレートを用いたphage-ELISAを行った。SR344への結合性が認められたクローンについて、特異的プライマーを用い、配列解析を行った。
H31, H50, H54, H56, H57, H58, H59, H60, H61, H62, H63, H64, H65, H100a, H100b, H102
L24, L26, L27, L28, L30, L31, L32, L52, L53, L54, L56, L90, L92, L93, L94
表2に示した、ヒスチジンに置換しても結合能に大きな変化がないCDR残基(ヒスチジン導入可能箇所)のアミノ酸を、元の配列(天然型配列)もしくはヒスチジンとなるライブラリーの設計を行った。実施例1で作製したH鎖PF1H、L鎖PF1Lの配列を元にし、ライブラリー箇所において、元の配列あるいはヒスチジン(元の配列かヒスチジンのどちらか一方)、となるようにライブラリーを構築した。
SR344への結合能をもつscFvのみを濃縮させるため、Nature Biotechnology 2000 Dec ; 18 : 1287-1292 に習い、ribosome display法によるパンニングを2回行った。調製されたSR344を、NHS-PEO4-Biotin(Pierce)を用いてビオチン化し抗原とした。ビオチン化抗原量を40 nM使用し、パンニングを行った。
上記のシングルコロニーを100μL 2YT/100μg/mLアンピシリン/2% glucose/12.5μg/mLテトラサイクリンに植菌し、30℃で一晩培養した。この2μLを300μL 2YT/100μg/mLアンピシリン/2% glucoseに植菌、37℃、4時間培養後、ヘルパーファージ(M13KO7)9 x 108pfuを加え、37℃で30分間静置培養、37℃30分間攪拌培養をおこない感染させた。この後2YT/100μg/mLアンピシリン/25μg/mLカナマイシン/0.5 mM IPTG 300μLに培地交換を行った。続いて30℃にて一晩培養し、遠心上清を回収した。遠心上清40μLに50 mM PBS(pH7.4)360μL加え、ELISAに供した。StreptaWell 96マイクロタイタープレート(Roche)を62.5 ng/mLビオチン標識SR344を含むPBS 100μLにて一晩コートした。PBSTにて洗浄し抗原を除いた後、2% BSA-PBS 250μLにて1時間以上ブロッキングした。2% BSA-PBSを除き、ここに調製した培養上清を加え37℃で1時間静置し抗体を結合させた。洗浄後、50 mM PBS(pH7.4)もしくは50 mM PBS(pH5.5)を加え37℃で30分間静置しインキュベートした。洗浄後、2% BSA-PBSにて希釈したHRP結合抗M13抗体(Amersham Parmacia Biotech)とTMB single solution(ZYMED)で検出し、硫酸の添加により反応を停止した後、450 nmの吸光度を測定した。
H50, H58, H61, H62, H63, H64, H65, H102
L24, L27, L28, L32, L53, L56, L90, L92, L94
一般的な磁気ビーズに固定化した抗原を用いたパンニングでは強いpH依存的結合能を有するクローンは得られなかった。磁気ビーズに固定化した抗原を用いたパンニングやプレートに固定化した抗原を用いたパンニングの場合は、磁気ビーズあるいはプレートから酸性条件下で解離したファージを全て回収するため、pH依存性が弱いクローンのファージであっても回収されてしまい、最終的に濃縮されるクローンに強いpH依存性を有するクローンが含まれる可能性が低いことが原因と考えられる。
ファージELISAにより、得られたphageの評価をおこなった。pH依存性が強く認められたクローンについて、特異的プライマーを用い、配列解析を行った。その結果、WTと比較してpH依存的な結合が強く見られたクローンが複数得られた。図6に示すとおり、WTと比較してクローンCL5(H鎖CLH5、L鎖CLL5)(CLH5:アミノ酸配列 配列番号:5、CLL5:アミノ酸配列 配列番号:8)は特に強いpH依存的な結合が確認された。一般的な磁気ビーズに固定化した抗原を用いたパンニングでは取れなかった強いpH依存的結合を示す抗体が、抗原を固定化したカラムを用いたパンニングにより取得できることが分かり、pH依存的結合抗体をライブラリーから取得する方法としては抗原を固定化したカラムを用いたパンニングが非常に有効であることが分かった。pH依存的な結合が見られた複数のクローンのアミノ酸配列解析の結果、濃縮されたクローンにおいて高い確率でヒスチジンとなっていた箇所を表4に示した。
H31, H50, H58, H62, H63, H65, H100b, H102
L24, L27, L28, L32, L53, L56, L90, L92, L94
ヒト化IL-6レセプター抗体のヒスチジン改変抗体の発現ベクターの作製・発現・精製
ファージELISAにてpH依存性が強く認められたクローンについて、IgG化するために、VH、および、VLをそれぞれPCRによって増幅し、XhoI/NheI消化およびEcoRI消化により動物細胞発現用ベクターに挿入した。各DNA断片の塩基配列は、当業者公知の方法で決定した。H鎖としてCLH5、L鎖として実施例2で得られたL73を用いたCLH5/L73をIgGとして発現・精製した。発現・精製は実施例1に記載した方法で行った。
IgG化したクローンのヒトIL-6レセプター中和活性評価
ヒト化PM1抗体(野生型:WT)、および、実施例2、4で作製したH3pI/L73、CLH5/L73、H170/L82の4種類についてIL-6レセプター中和活性を評価した。
pH依存的結合クローンの可溶型IL-6レセプターへの結合解析
ヒト化PM1抗体(野生型:WT)、および、実施例2、4で作製したH3pI/L73、CLH5/L73、H170/L82の4種類について、Biacore T100(GE Healthcare)を用いてpH5.8とpH7.4における抗原抗体反応の速度論的解析を実施した(バッファーは10 mM MES pH7.4あるいはpH5.8, 150 mM NaCl, 0.05% Tween20)。アミンカップリング法によりrecomb-proteinA/G(Pierce)を固定化したセンサーチップ上に種々の抗体を結合させ、そこにアナライトとして9.8-400 nMの濃度に調製したSR344を注入した。pH依存的結合クローンのSR344への結合および解離をリアルタイムに観測した(図8および図9)。測定は全て37℃で実施した。Biacore T100 Evaluation Software(GE Healthcare)を用い、結合速度定数 ka(1/Ms)、および解離速度定数 kd(1/s)を算出し、その値をもとに解離定数 KD (M) を算出した(表5)。さらにそれぞれについてpH5.8とpH7.4のaffinity比を算出し、pH依存性結合を評価した。測定は全て37℃で実施した。
作製した上記pH依存的結合クローンについて、Biacore T100(GE Healthcare)を用いてpH5.8, pH7.4における膜型IL-6レセプターへの抗原抗体反応を観測した。センサーチップ上に固定化したIL-6レセプターへの結合を評価することで、膜型IL-6レセプターへの結合を評価した。SR344を当業者公知の方法に従ってビオチン化し、ストレプトアビジンとビオチンの親和性を利用し、ストレプトアビジンを介してビオチン化SR344をセンサーチップ上に固定化した。測定は全て37℃で実施し、移動相のバッファーは10 mM MES pH5.8, 150 mM NaCl, 0.05% Tween20とし、そこにpH依存的結合クローンをpH7.4の条件下で注入してSR344と結合させたのち(注入サンプルのバッファーは10 mM MES pH7.4, 150 mM NaCl, 0.05% Tween20)、移動相のpHである5.8で各クローンのpH依存的な解離を観測した(図10)。
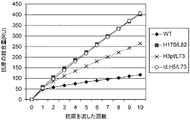
実施例2で記したように、pH依存的結合抗体は抗原に複数回結合することが可能になると考えられる。すなわち、抗原が結合したpH依存的結合抗体は非特異的にエンドソーム内に取り込まれるが、エンドソーム内の酸性条件下において可溶型抗原から解離する。抗体はFcRnに結合することによって再び血漿中に戻り、血漿中に戻った抗体には抗原が結合していないことから、再び新たな抗原に結合することが可能である。これを繰り返すことによって、pH依存的結合抗体は抗原に複数回結合することが可能である。しかしながらpH依存的結合を有さないIgG抗体は、エンドソームの酸性条件下で全ての抗原が抗体から解離することは無いため、FcRnにより血漿中に戻った抗体は抗原を結合したままであり、再び新たな抗原に結合することは出来ない。そのため、ほとんどの場合1分子のIgG抗体は2つの抗原しか中和することが出来ない(2価で結合した場合)。
IL-6レセプターは生体内に可溶型IL-6レセプターおよび膜型IL-6レセプターの両方の形で存在する(Nat Clin Pract Rheumatol. 2006 Nov;2(11):619-26)。抗IL-6レセプター抗体は可溶型IL-6レセプターおよび膜型IL-6レセプター両方に結合してそれらの生物学的な作用を中和する。抗IL-6レセプター抗体は膜型IL-6レセプターに結合後、膜型IL-6レセプターに結合したままインターナライゼーションによって細胞内のエンドソームに取り込まれ、その後、抗IL-6レセプター抗体は膜型IL-6レセプターに結合したままライソソームへ移行し一緒にライソソームにより分解されると考えられている。実施例6で評価したpH依存的結合抗IL-6レセプター抗体であるH3pI/L73、CLH5/L73、H170/L82が、エンドソーム内の酸性条件下で解離することでFcRnを介して血漿中へ戻ることが出来れば、血漿中に戻った抗体は再度抗原に結合することが可能になり、抗体1分子で複数の膜型IL-6レセプターを中和することが可能となる。エンドソーム内の酸性条件下で解離することでFcRnを介して血漿中へ戻ることが作製したpH依存的結合抗IL-6レセプター抗体で達成できているかどうかは、これらの抗体の薬物動態がWTと比較して改善しているかどうかを評価することで可能である。
実施例8において、pH依存的結合抗IL-6レセプター抗体において薬物動態が大幅に改善したことから、pH依存的結合抗IL-6レセプター抗体はエンドソーム内の酸性条件下において抗原である膜型IL-6レセプターから解離することでFcRnを介して再び血漿中に戻っていると考えられた。再び血漿中に戻った抗体が再度膜型IL-6レセプターに結合することができれば、天然型抗IL-6レセプター抗体と比較して、pH依存的結合抗IL-6レセプター抗体は同じ投与量でより長く抗原である膜型IL-6レセプターの中和が持続すると考えられる。また、IL-6レセプターには可溶型IL-6レセプターも存在することから、可溶型IL-6レセプターの中和に関しても、同じ投与量でより長く中和が持続することが考えられる。
可変領域H3pI/L73およびCLH5/L82の最適化
実施例9において、pH依存的結合能を有する抗体が優れた効果を発揮することが示されたことから、さらにpH依存的結合能を向上させるため、実施例3で得られたCLH5のCDR配列に変異を導入し、VH1-IgG1(配列番号:21)、VH2-IgG1(配列番号:22)を作製した。また、H3pIのフレームワーク配列とCDR配列に変異を導入し、改変H鎖としてVH3-IgG1(配列番号:23)、VH4-IgG1(配列番号:24)を作製した。L73、L82のCDR配列に変異を導入し、改変L鎖としてVL1-CK(配列番号:25)、VL2-CK(配列番号:26)、VL3-CK(配列番号:27)を作製した。具体的には、QuikChange Site-Directed Mutagenesis Kit(Stratagene)を用いて、添付説明書記載の方法で変異体を作製し、得られたプラスミド断片を哺乳動物細胞発現ベクターに挿入し、目的のH鎖発現ベクターおよびL鎖発現ベクターを作製した。得られた発現ベクターの塩基配列は当業者公知の方法で決定した。
ヒト化PM1抗体(野生型:WT)、および、実施例2および10で作製したWT、H3pI/L73-IgG1、Fv2-IgG1、Fv4-IgG1の4種類について、Biacore T100(GE Healthcare)を用いてpH7.4における抗原抗体反応の速度論的解析を実施した(バッファーは10 mM MES pH7.4, 150 mM NaCl, 0.05% Tween20)。アミンカップリング法によりanti-IgG γchain specific F(ab)2(Pierce)を固定化したセンサーチップ上に種々の抗体を結合させ、そこにアナライトとして9.8-40 nMの濃度に調製したSR344を注入した。pH依存的結合クローンのSR344への結合および解離をリアルタイムに観測した。測定は全て37℃で実施した。Biacore T100 Evaluation Software(GE Healthcare)を用い、結合速度定数 ka (1/Ms)、および解離速度定数 kd (1/s) を算出し、その値をもとに 解離定数 KD (M) を算出した(表7)。
作製したWT、H3pI/L73-IgG1、Fv2-IgG1、Fv4-IgG1の4種類について、Biacore T100(GE Healthcare)を用いてpH5.8, pH7.4における膜型IL-6レセプターへの抗原抗体反応を観測した。センサーチップ上に固定化したIL-6レセプターへの結合を評価することで、膜型IL-6レセプターへの結合を評価した。SR344を当業者公知の方法に従ってビオチン化し、ストレプトアビジンとビオチンの親和性を利用し、ストレプトアビジンを介してビオチン化SR344をセンサーチップ上に固定化した。測定は全て37℃で実施し、移動相のバッファーは10 mM MES pH5.8, 150 mM NaCl, 0.05% Tween20とし、そこにpH依存的結合クローンをpH7.4の条件下で注入してSR344と結合させたのち(注入サンプルのバッファーは10 mM MES pH7.4, 150 mM NaCl, 0.05% Tween20)、移動相のpHである5.8で各クローンのpH依存的な解離を観測した(図17)。
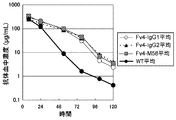
実施例8で使用したヒトIL-6レセプタートランスジェニックマウスを用いて、実施例10で作製・評価したFv2-IgG1とFv4-IgG1およびWTとH3pI/L73-IgG1の薬物動態を評価した。WTおよびH3pI/L73-IgG1、Fv2-IgG1、Fv4-IgG1をhIL-6R tgマウスに25 mg/kgで静脈内に単回投与し、実施例8と同様に各抗体の血漿中濃度の測定を行った。WTおよびH3pI/L73-IgG1、Fv2-IgG1、Fv4-IgG1の血漿中濃度推移を図18に示した。
Fv4-IgG1の定常領域の最適化
一般的に膜型抗原に対する結合は抗体の定常領域によって変化することが報告されている(J Immunol Methods. 1997 Jun 23;205(1):67-72.)。これまで作製したpH依存的結合抗体の定常領域はIgG1アイソタイプであった。そこで膜型IL-6レセプターへのpH依存的結合を向上させるために定常領域の最適化を検討した。
作製したFv4-IgG1、Fv4-IgG2、Fv4-M58、Fv4-M73およびWTに関して、実施例10と同様の方法でSR344への結合および解離をリアルタイムに観測した。同様に解析を行い、結合速度定数 ka (1/Ms)、および解離速度定数 kd (1/s) を算出し、その値をもとに解離定数 KD (M) を算出した(表9)。
作製したFv4-IgG1、Fv4-IgG2、Fv4-M58、Fv4-M73およびWTに関して、実施例10と同様の方法でBiacore T100(GE Healthcare)を用いてpH5.8, pH7.4における膜型IL-6レセプターへの抗原抗体反応を観測した。pH依存的結合クローンをpH7.4の条件下で注入してSR344と結合させたのちに、pH5.8の移動相で各クローンのpH依存的な解離を観測した結果を図19に示す。さらに実施例10と同様の方法で解析を行い、各クローンのpH依存的な解離速度を表10に示した。
実施例8で使用したヒトIL-6レセプタートランスジェニックマウス(hIL-6R tgマウス)を用いて、実施例13で作成したFv4-IgG1、Fv4-IgG2、Fv4-M58の薬物動態を評価し、定常領域の及ぼす薬物動態への影響を検討した。WTおよびFv4-IgG1、Fv4-IgG2、Fv4-M58をhIL-6R tgマウスに25 mg/kgで静脈内に単回投与し、実施例8と同様に各抗体の血漿中濃度の測定を行った。WTおよびFv4-IgG1、Fv4-IgG2、Fv4-M58の血漿中濃度推移を図20に示した。
これまでと同様の方法を用い、VH2-IgG1の定常領域をM71, M73としたVH2-M71(配列番号:36)、VH2-M73(配列番号:37)、VH4-IgG1の定常領域をM71, M73としたVH4-M71(配列番号:38)、VH4-M73(配列番号:39)を作製した。
ヒト化PM1抗体(野生型:WT)、および、これまでに作製したH3pI/L73-IgG1、Fv1-M71、Fv1-M73、Fv2-IgG1、Fv3-M71、Fv3-M73、Fv4-IgG1、Fv4-IgG2、Fv4-M58、Fv4-M73の11種類について、実施例10と同様の方法でSR344への結合および解離をリアルタイムに観測した。同様に解析を行い、結合速度定数 ka (1/Ms) 、および解離速度定数 kd (1/s) を算出し、その値をもとに解離定数 KD (M) を算出した(表11)。
ヒト化PM1抗体(野生型:WT)、および、これまでに作製したH3pI/L73-IgG1、Fv1-M71、Fv1-M73、Fv2-IgG1、Fv3-M71、Fv3-M73、Fv4-IgG1、Fv4-IgG2、Fv4-M58、Fv4-M73の11種類について、実施例10と同様の方法でBiacore T100(GE Healthcare)を用いてpH5.8, pH7.4における膜型IL-6レセプターへの抗原抗体反応を観測した。pH依存的結合クローンをpH7.4の条件下で注入してSR344と結合させたのちに、移動相のpHである5.8で各クローンのpH依存的な解離を観測した結果を図21に示した(Fv1-M71、Fv1-M73、Fv3-M71、Fv3-M73については図21、他は図17および19に示した)。さらに実施例10と同様の方法で解析を行い、全11種類のクローンについて、解離速度定数のpH依存性を表12に示した。
公知の高親和性抗IL-6レセプター抗体の作製
公知の高親和性抗IL-6レセプター抗体として、US 2007/0280945 A1に記載されている高親和性抗IL-6レセプター抗体であるVQ8F11-21 hIgG1(US 2007/0280945 A1, アミノ酸配列19および27)を発現させるため、動物細胞発現用ベクターを構築した。抗体可変領域については、合成オリゴDNAを組み合わせたPCR法(assembly PCR)により作製した。定常領域については、実施例1で使用した発現ベクターからPCR法により増幅した。Assembly PCR法により抗体可変領域と定常領域を結合させ、哺乳動物発現用ベクターへ挿入した。得られたH鎖およびL鎖DNA断片を哺乳動物細胞発現ベクターに挿入し、目的のH鎖発現ベクターおよびL鎖発現ベクターを作製した。得られた発現ベクターの塩基配列は当業者公知の方法で決定した。作製した発現ベクターを用い、発現・精製を行った。発現・精製は実施例1に記載した方法で行い、高親和性高IL-6レセプター抗体(high affinity Ab)を得た。
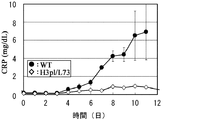
pH依存的結合抗体であるH3pI/L73-IgG1およびFv1-M71、Fv1-M73、Fv2-IgG1、Fv3-M73、Fv4-M73および公知の高親和性抗IL-6レセプター抗体(high affinity Ab)のカニクイザルにおける薬物動態および薬効を評価した。H3pI/L73-IgG1およびFv1-M71、Fv1-M73、Fv2-IgG1、Fv3-M73、Fv4-M73をカニクイザルに0.5 mg/kgで静脈内に単回投与し、またhigh affinity Abは1.0 mg/kgで静脈内に単回投与し、投与前および経時的に採血した。実施例9と同様に各抗体の血漿中濃度の測定を行った。H3pI/L73-IgG1およびFv1-M71、Fv1-M73、Fv2-IgG1、Fv3-M73、Fv4-M73、high affinity Abの血漿中濃度推移を図21に示した。カニクイザル膜型IL-6レセプターがどの程度中和されているかの薬効を評価するために、実施例9と同様に、抗体投与後3日目から10日目(high affinity Abに関しては6日目から10日目)までカニクイザルIL-6 5μg/kgを腰背部に連日皮下投与し、24時間後の各個体のCRP濃度を測定した。各抗体投与時のCRP濃度推移を図22に示した。カニクイザル可溶型IL-6レセプターがどの程度中和されているかの薬効を評価するために、実施例9と同様に、カニクイザル血漿中の非結合型のカニクイザル可溶型IL-6レセプター濃度を測定した。各抗体投与時の非結合型のカニクイザル可溶型IL-6レセプター濃度推移を図23に示した。
抗IL-6抗体の発現と精製
実施例1〜15におけるヒト化抗IL-6レセプター抗体において、ヒト化抗IL-6レセプター抗体の可変領域に対して、そのCDR配列を中心にヒスチジン等への置換を導入することによって、ヒト化抗IL-6レセプター抗体とIL-6レセプターとの結合にpH依存性を付与した抗体を複数創製することに成功し、それらは全てIL-6レセプターへ繰り返し結合し、PK/PDが大きく改善することが見出された。
H鎖(WT)(アミノ酸配列 配列番号:62)とL鎖(WT)(アミノ酸配列 配列番号:63)からなる抗IL-6抗体(anti-IL6 wild type)に対して、CDRのアミノ酸に対してヒスチジンへの置換を導入することで、抗体とIL-6の結合にpH依存性を付与する検討を行った。CDRのアミノ酸に対してヒスチジンへの置換を検討し、スクリーニングを行った結果、pH7.4における結合と比較して、pH5.5における結合が大幅に低下し、pH依存的な結合を示すクローンがいくつか得られた。pH依存的クローンにおけるヒスチジン置換箇所を表13に示した。そのうち、H鎖(c1)(アミノ酸配列 配列番号:64)とL鎖(c1)(アミノ酸配列 配列番号:65)からなるanti-IL6 clone1、および、H鎖(c1)(アミノ酸配列 配列番号:64)とL鎖(c2)(アミノ酸配列 配列番号:66)からなるanti-IL6 clone2、が挙げられた。Anti-IL6 clone1とanti-IL6 clone2の発現と精製は実施例1に記載した方法で行った。
H32、H59、H61、H99
L53、L54、L90、L94
上記で作製したanti-IL6 wild type、anti-IL6 clone1、および、anti-IL6 clone2の3種類について、Biacore T100 (GE Healthcare) を用いてpH5.5とpH7.4における抗原抗体反応の速度論的解析を実施した(バッファーはDPBS(-) pH7.4あるいはpH5.5, 150 mM NaCl)。アミンカップリング法によりrecomb-proteinA/G (Pierce) を固定化したセンサーチップ上に種々の抗体を結合させ、そこにアナライトとして適切な濃度に調製したヒトIL-6(TORAY)を注入した。測定は全て37℃で実施した。Biacore T100 Evaluation Software (GE Healthcare)を用い、結合速度定数 ka (1/Ms) 、および解離速度定数 kd (1/s) を算出し、その値をもとに解離定数 KD (M) を算出した(表14)。さらにそれぞれについてpH5.5とpH7.4のaffinity比を算出し、pH依存性結合を評価した。
抗IL-31レセプター抗体の発現と精製
実施例1〜15において、ヒト化抗IL-6レセプター抗体において、ヒト化抗IL-6レセプター抗体の可変領域に対して、そのCDR配列を中心にヒスチジン等への置換を導入することによって、ヒト化抗IL-6レセプター抗体とIL-6レセプターとの結合にpH依存性を付与した抗体を複数創製することに成功し、それらは全てIL-6レセプターへ繰り返し結合し、PK/PDが大きく改善することが見出された。
H鎖(WT)(アミノ酸配列 配列番号:67)とL鎖(WT)(アミノ酸配列 配列番号:68)からなる抗IL-31レセプター抗体(anti-IL31R wild type)に対して、CDRのアミノ酸に対してヒスチジンへの置換を導入することで、抗体とIL-31レセプターの結合にpH依存性を付与する検討を行った。CDRのアミノ酸に対してヒスチジンへの置換を検討し、スクリーニングを行った結果、pH7.4における結合と比較して、pH5.5における結合が大幅に低下し、pH依存的な結合を示すクローンがいくつか得られた。pH依存的クローンにおけるヒスチジン置換箇所を表15に示した。そのうちの一つとして、H鎖(c1)(アミノ酸配列 配列番号:69)とL鎖(WT)からなるanti-IL31R clone1が挙げられた。Anti-IL31R clone1の発現と精製は実施例1に記載した方法で行った。
H33
上記で作製したanti-IL31R wild type、anti-IL31R clone1の2種類について、Biacore T100 (GE Healthcare) を用いてpH5.5とpH7.4における抗原抗体反応の速度論的解析を実施した(バッファーはDPBS(-) pH7.4あるいはpH5.5, 150 mM NaCl, 0.01% Tween20, 0.02% NaN3)。アミンカップリング法によりrecomb-proteinA/G (Pierce) を固定化したセンサーチップ上に種々の抗体を結合させ、そこにアナライトとして適切な濃度に調製した可溶型マウスIL-31レセプター(WO2007/142325に記載の方法で調製)を注入した。測定は全て25℃で実施した。Biacore T100 Evaluation Software (GE Healthcare)を用い、結合速度定数 ka (1/Ms) 、および解離速度定数 kd (1/s) を算出し、その値をもとに解離定数 KD (M) を算出した(表16)。さらにそれぞれについてpH5.5とpH7.4のaffinity比を算出し、pH依存性結合を評価した。
マウス投与抗体の発現と精製
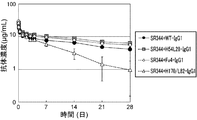
ヒト化IL-6レセプター抗体として、以下の4種類を作製した。IL-6レセプターに対してpH依存的な結合を示さない通常の抗体としてH(WT)(アミノ酸配列 配列番号:9)とL(WT)(アミノ酸配列 配列番号:10)からなるWT-IgG1、H54(アミノ酸配列 配列番号:70)とL28(アミノ酸配列 配列番号:12)からなるH54/L28-IgG1を、IL-6レセプターに対してpH依存的な結合を示す抗体として実施例3で作製したH170(アミノ酸配列 配列番号:4)とL82(アミノ酸配列 配列番号:7)からなるH170/L82-IgG1、および、実施例10で作製したVH3-IgG1(配列番号:23)とVL3-CK(配列番号:27)からなるFv4-IgG1を実施例1に示した方法で発現と精製を行った。
調製したWT-IgG1、H54/L28-IgG1、H170/L82-IgG1、および、Fv4-IgG1の4種類について、Biacore T100 (GE Healthcare) を用いてpH7.4およびpH5.8における抗原抗体反応の速度論的解析を実施した(バッファーは10 mM MES pH7.4、またはpH5.8, 150 mM NaCl, 0.05% Surfactant-P20)。アミンカップリング法によりrecomb-proteinA/G (Pierce) を固定化したセンサーチップ上に種々の抗体を結合させ、そこにアナライトとして適切な濃度に調製したSR344を注入した。各種抗体のSR344への結合および解離をリアルタイムに観測した。測定は全て37℃で実施した。Biacore T100 Evaluation Software (GE Healthcare)を用い、結合速度定数 ka (1/Ms) 、および解離速度定数 kd (1/s) を算出し、その値をもとに 解離定数 KD (M) を算出した(表17)。
ヒトIl-6レセプターを発現していないマウス(C57BL/6J;これらの抗ヒトIL-6レセプター抗体はマウスのIL-6レセプターに結合しない)にSR344(ヒトIL-6レセプター:実施例1で作製)を単独投与、もしくはSR344および抗ヒトIL-6レセプター抗体を同時投与した後のSR344および抗ヒトIL-6レセプター抗体の体内動態を評価した。SR344溶液(5μg/mL)もしくはSR344および抗ヒトIL-6レセプター抗体の混合溶液(それぞれ5μg/mL、0.1 mg/mL)を尾静脈に10 mL/kgで単回投与した。このとき、SR344に対して抗ヒトIL-6レセプター抗体は十分量過剰に存在することから、SR344はほぼ全て抗体に結合していると考えられる。投与後15分間、2時間、8時間、1日間、2日間、3日間、4日間、7日間、14日間、21日間、28日間で採血を行った。採取した血液は直ちに4℃、15,000 rpmで15分間遠心分離し、血漿を得た。分離した血漿は、測定を実施するまで-20℃以下に設定された冷凍庫に保存した。抗ヒトIL-6レセプター抗体としては、上述のWT-IgG1、H54/L28-IgG1、H170/L82-IgG1、および、Fv4-IgG1を使用した。
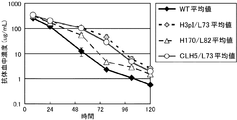
マウス血漿中の抗ヒトIL-6レセプター抗体濃度はELISA法にて測定した。まずAnti-Human IgG(γ-chain specific) F(ab')2 Fragment of Antibody (SIGMA) をNunc-Immuno Plate, MaxiSoup (Nalge nunc International)に分注し、4℃で1晩静置しAnti-Human IgG固相化プレートを作成した。血漿中濃度として0.8、0.4、0.2、0.1、0.05、0.025、0.0125μg/mLの検量線試料と100倍以上希釈したマウス血漿測定試料を調製し、これら検量線試料および血漿測定試料100μLに20 ng/mLのSR344を200μL加え、室温で1時間静置した。その後Anti-Human IgG固相化プレートに分注しさらに室温で1時間静置した。その後Biotinylated Anti-human IL-6 R Antibody(R&D)を室温で1時間反応させ、さらにStreptavidin-PolyHRP80 (Stereospecific Detection Technologies)を室温で1時間反応させ、TMB One Component HRP Microwell Substrate (BioFX Laboratories)を基質として用い発色反応を行い、1N-Sulfuric acid(Showa Chemical)で反応停止後、マイクロプレートリーダーにて450 nmの吸光度を測定した。マウス血漿中濃度は検量線の吸光度から解析ソフトウェアSOFTmax PRO(Molecular Devices)を用いて算出した。この方法で測定した静脈内投与後の血漿中抗体濃度推移を図28に示した。
マウスの血漿中SR344濃度は電気化学発光法にて測定した。2000、1000、500、250、125、62.5、31.25 pg/mLに調整したSR344検量線試料および50倍以上希釈したマウス血漿測定試料を調製し、SULFO-TAG NHS Ester(Meso Scale Discovery)でルテニウム化したMonoclonal Anti-human IL-6R Antibody(R&D)およびBiotinylated Anti-human IL-6 R Antibody (R&D)およびWT-IgG1溶液を混合し37℃で1晩反応させた。その際のWT-IgG1の終濃度はサンプルに含まれる抗ヒトIL-6レセプター抗体濃度より過剰の333μg/mLであり、サンプル中のほぼ全てのSR344をWT-IgG1と結合した状態にすることを目的とした。その後、MA400 PR Streptavidin Plate(Meso Scale Discovery)に分注した。さらに室温で1時間反応させ洗浄後、Read Buffer T(×4)(Meso Scale Discovery)を分注し、ただちにSECTOR PR 400 reader(Meso Scale Discovery)で測定を行った。SR344濃度は検量線のレスポンスから解析ソフトウェアSOFTmax PRO(Molecular Devices)を用いて算出した。この方法で測定した静脈内投与後の血漿中SR344濃度推移を図29に示した。
pH依存的な結合を示さない抗体であるWT-IgG1とH54/L28-IgG1、および、pH依存的な結合を示す抗体であるH170/L82-IgG1とFv4-IgG1の抗体濃度推移に関しては、WT-IgG1、H54/L28-IgG1、および、Fv4-IgG1はほぼ同等であり、H170/L82-IgG1は若干早い消失を示した。血漿中濃度推移のデータを薬物動態解析ソフトWinNonlin(Pharsight)で解析した結果、WT-IgG1、H54/L28-IgG1、Fv4-IgG1、H170/L82-IgG1の血漿中半減期はそれぞれ21.0、28.8、26.2、7.5 dayであった。
Claims (5)
- 以下の工程;
(a) pH6.7〜pH10.0における抗体の抗原結合活性を得る工程、
(b) pH4.0〜pH6.5における抗体の抗原結合活性を得る工程、
(c) pH6.7〜pH10.0での抗原結合活性がpH4.0〜pH6.5での抗原結合活性より高い抗体を選択する工程、
(d) (c)で選択された抗体をコードする遺伝子を得る工程、
(e) (d)で得られた遺伝子を用いて抗体を製造する工程、
を含む、以下のいずれか;
(i) 血漿中滞留性が優れた抗体、
(ii) FcRnを発現する細胞を含む動物での測定で抗原に2回以上結合することができる抗体、
(iii) FcRnを発現する細胞を含む動物での測定で結合可能な抗原の数が抗原結合部位より多い抗体、
(iv) 細胞外で結合した抗原を細胞内で解離する抗体、
(v) 抗原と結合した状態で細胞内に取り込まれ、抗原と結合していない状態で細胞外に放出される抗体、または、
(vi) 血漿中抗原消失能が増加した抗体、
を含む医薬品の製造方法。 - 以下の工程;
(a) pH6.7〜pH10.0の条件下で抗体を抗原に結合させる工程、
(b) (a)の抗原に結合した抗体をpH4.0〜pH6.5の条件下に置く工程、
(c) pH4.0〜pH6.5の条件下で解離した抗体を取得する工程、
(d) (c)で取得された抗体をコードする遺伝子を得る工程、
(e) (d)で得られた遺伝子を用いて抗体を製造する工程、
を含む、以下のいずれか;
(i) 血漿中滞留性が優れた抗体、
(ii) FcRnを発現する細胞を含む動物での測定で抗原に2回以上結合することができる抗体、
(iii) FcRnを発現する細胞を含む動物での測定で結合可能な抗原の数が抗原結合部位より多い抗体、
(iv) 細胞外で結合した抗原を細胞内で解離する抗体、
(v) 抗原と結合した状態で細胞内に取り込まれ、抗原と結合していない状態で細胞外に放出される抗体、または、
(vi) 血漿中抗原消失能が増加した抗体、
を含む医薬品の製造方法。 - 以下の工程;
(a) 抗原を固定したカラムに第一のpH条件下で抗体を結合させる工程、
(b) 第一のpH条件下でカラムに結合した抗体を、第二のpH条件下でカラムから溶出する工程、
(c) 溶出された抗体を取得する工程、
(d) (c)で取得された抗体をコードする遺伝子を得る工程、
(e) (d)で得られた遺伝子を用いて抗体を製造する工程、
を含む製造方法であって、以下のいずれか;
(i) 血漿中滞留性が優れた抗体、
(ii) FcRnを発現する細胞を含む動物での測定で抗原に2回以上結合することができる抗体、
(iii) FcRnを発現する細胞を含む動物での測定で結合可能な抗原の数が抗原結合部位より多い抗体、
(iv) 細胞外で結合した抗原を細胞内で解離する抗体、
(v) 抗原と結合した状態で細胞内に取り込まれ、抗原と結合していない状態で細胞外に放出される抗体、または、
(vi) 血漿中抗原消失能が増加した抗体、
であって、第一のpHがpH6.7.〜pH10.0、第二のpHが4.0〜pH6.5である、第一のpHでの抗原への結合活性が第二のpHでの抗原への結合活性よりも高い抗体を含む医薬品の製造方法。 - 以下の工程;
(a) 抗体ライブラリーを、抗原を固定したカラムに第一のpH条件下で結合させる工程、
(b) カラムから第二のpH条件下で抗体を溶出する工程、
(c) 溶出された抗体をコードする遺伝子を増幅する工程、
(d) 溶出された抗体を取得する工程、
(e) (d)で取得された抗体をコードする遺伝子を得る工程、
(f) (e)で得られた遺伝子を用いて抗体を製造する工程。
を含む製造方法であって、以下のいずれか;
(i) 血漿中滞留性が優れた抗体、
(ii) FcRnを発現する細胞を含む動物での測定で抗原に2回以上結合することができる抗体、
(iii) FcRnを発現する細胞を含む動物での測定で結合可能な抗原の数が抗原結合部位より多い抗体、
(iv) 細胞外で結合した抗原を細胞内で解離する抗体、
(v) 抗原と結合した状態で細胞内に取り込まれ、抗原と結合していない状態で細胞外に放出される抗体、または、
(vi) 血漿中抗原消失能が増加した抗体、
であって、第一のpHがpH6.7.〜pH10.0、第二のpHが4.0〜pH6.5である、第一のpHでの結合活性が第二のpHでの結合活性よりも高い抗体を含む医薬品の製造方法。 - 抗体中の少なくとも1つ以上のアミノ酸をヒスチジンで置換する又は少なくとも1つのヒスチジンを挿入する工程をさらに含む請求項1〜4いずれかに記載の製造方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2011268497A JP5048866B2 (ja) | 2008-04-11 | 2011-12-08 | 複数分子の抗原に繰り返し結合する抗原結合分子 |
Applications Claiming Priority (7)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008104147 | 2008-04-11 | ||
| JP2008104147 | 2008-04-11 | ||
| JP2008247713 | 2008-09-26 | ||
| JP2008247713 | 2008-09-26 | ||
| JP2009068744 | 2009-03-19 | ||
| JP2009068744 | 2009-03-19 | ||
| JP2011268497A JP5048866B2 (ja) | 2008-04-11 | 2011-12-08 | 複数分子の抗原に繰り返し結合する抗原結合分子 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011171225A Division JP4961501B2 (ja) | 2008-04-11 | 2011-08-04 | 複数分子の抗原に繰り返し結合する抗原結合分子 |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2012160692A Division JP5503698B2 (ja) | 2008-04-11 | 2012-07-19 | 複数分子の抗原に繰り返し結合する抗原結合分子 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2012116837A JP2012116837A (ja) | 2012-06-21 |
| JP2012116837A5 JP2012116837A5 (ja) | 2012-08-02 |
| JP5048866B2 true JP5048866B2 (ja) | 2012-10-17 |
Family
ID=41161956
Family Applications (15)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2010507273A Active JP4954326B2 (ja) | 2008-04-11 | 2009-04-10 | 複数分子の抗原に繰り返し結合する抗原結合分子 |
| JP2011171225A Active JP4961501B2 (ja) | 2008-04-11 | 2011-08-04 | 複数分子の抗原に繰り返し結合する抗原結合分子 |
| JP2011268497A Active JP5048866B2 (ja) | 2008-04-11 | 2011-12-08 | 複数分子の抗原に繰り返し結合する抗原結合分子 |
| JP2012160692A Active JP5503698B2 (ja) | 2008-04-11 | 2012-07-19 | 複数分子の抗原に繰り返し結合する抗原結合分子 |
| JP2014051047A Active JP5824095B2 (ja) | 2008-04-11 | 2014-03-14 | 複数分子の抗原に繰り返し結合する抗原結合分子 |
| JP2015199906A Active JP6082447B2 (ja) | 2008-04-11 | 2015-10-08 | 複数分子の抗原に繰り返し結合する抗原結合分子 |
| JP2017008075A Active JP6417431B2 (ja) | 2008-04-11 | 2017-01-20 | 複数分子の抗原に繰り返し結合する抗原結合分子 |
| JP2018189946A Withdrawn JP2019048810A (ja) | 2008-04-11 | 2018-10-05 | 複数分子の抗原に繰り返し結合する抗原結合分子 |
| JP2020169016A Active JP7033176B2 (ja) | 2008-04-11 | 2020-10-06 | 複数分子の抗原に繰り返し結合する抗原結合分子 |
| JP2020169015A Withdrawn JP2021011490A (ja) | 2008-04-11 | 2020-10-06 | 複数分子の抗原に繰り返し結合する抗原結合分子 |
| JP2020169014A Active JP7177808B2 (ja) | 2008-04-11 | 2020-10-06 | 複数分子の抗原に繰り返し結合する抗原結合分子 |
| JP2021094209A Active JP7397823B2 (ja) | 2008-04-11 | 2021-06-04 | 複数分子の抗原に繰り返し結合する抗原結合分子 |
| JP2022027962A Pending JP2022081533A (ja) | 2008-04-11 | 2022-02-25 | 複数分子の抗原に繰り返し結合する抗原結合分子 |
| JP2023105711A Active JP7366312B2 (ja) | 2008-04-11 | 2023-06-28 | 複数分子の抗原に繰り返し結合する抗原結合分子 |
| JP2024084653A Pending JP2024105708A (ja) | 2008-04-11 | 2024-05-24 | 複数分子の抗原に繰り返し結合する抗原結合分子 |
Family Applications Before (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2010507273A Active JP4954326B2 (ja) | 2008-04-11 | 2009-04-10 | 複数分子の抗原に繰り返し結合する抗原結合分子 |
| JP2011171225A Active JP4961501B2 (ja) | 2008-04-11 | 2011-08-04 | 複数分子の抗原に繰り返し結合する抗原結合分子 |
Family Applications After (12)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2012160692A Active JP5503698B2 (ja) | 2008-04-11 | 2012-07-19 | 複数分子の抗原に繰り返し結合する抗原結合分子 |
| JP2014051047A Active JP5824095B2 (ja) | 2008-04-11 | 2014-03-14 | 複数分子の抗原に繰り返し結合する抗原結合分子 |
| JP2015199906A Active JP6082447B2 (ja) | 2008-04-11 | 2015-10-08 | 複数分子の抗原に繰り返し結合する抗原結合分子 |
| JP2017008075A Active JP6417431B2 (ja) | 2008-04-11 | 2017-01-20 | 複数分子の抗原に繰り返し結合する抗原結合分子 |
| JP2018189946A Withdrawn JP2019048810A (ja) | 2008-04-11 | 2018-10-05 | 複数分子の抗原に繰り返し結合する抗原結合分子 |
| JP2020169016A Active JP7033176B2 (ja) | 2008-04-11 | 2020-10-06 | 複数分子の抗原に繰り返し結合する抗原結合分子 |
| JP2020169015A Withdrawn JP2021011490A (ja) | 2008-04-11 | 2020-10-06 | 複数分子の抗原に繰り返し結合する抗原結合分子 |
| JP2020169014A Active JP7177808B2 (ja) | 2008-04-11 | 2020-10-06 | 複数分子の抗原に繰り返し結合する抗原結合分子 |
| JP2021094209A Active JP7397823B2 (ja) | 2008-04-11 | 2021-06-04 | 複数分子の抗原に繰り返し結合する抗原結合分子 |
| JP2022027962A Pending JP2022081533A (ja) | 2008-04-11 | 2022-02-25 | 複数分子の抗原に繰り返し結合する抗原結合分子 |
| JP2023105711A Active JP7366312B2 (ja) | 2008-04-11 | 2023-06-28 | 複数分子の抗原に繰り返し結合する抗原結合分子 |
| JP2024084653A Pending JP2024105708A (ja) | 2008-04-11 | 2024-05-24 | 複数分子の抗原に繰り返し結合する抗原結合分子 |
Country Status (33)
| Country | Link |
|---|---|
| US (10) | US20110111406A1 (ja) |
| EP (7) | EP3521311A1 (ja) |
| JP (15) | JP4954326B2 (ja) |
| KR (7) | KR20240113501A (ja) |
| CN (6) | CN102056946A (ja) |
| AR (2) | AR071656A1 (ja) |
| BR (2) | BR122020017346B1 (ja) |
| CA (1) | CA2721052C (ja) |
| CO (1) | CO6311005A2 (ja) |
| CR (3) | CR11783A (ja) |
| DK (3) | DK2708559T3 (ja) |
| EC (1) | ECSP10010600A (ja) |
| ES (4) | ES2671010T3 (ja) |
| HK (3) | HK1246157A1 (ja) |
| HR (3) | HRP20160209T1 (ja) |
| HU (3) | HUE028718T2 (ja) |
| IL (3) | IL208516A (ja) |
| LT (1) | LT2708559T (ja) |
| MA (1) | MA32754B1 (ja) |
| MX (2) | MX2010011184A (ja) |
| MY (1) | MY195714A (ja) |
| NO (1) | NO2708559T3 (ja) |
| NZ (4) | NZ602884A (ja) |
| PH (2) | PH12014502054B1 (ja) |
| PL (4) | PL2275443T3 (ja) |
| PT (2) | PT2275443E (ja) |
| RU (2) | RU2571225C2 (ja) |
| SG (3) | SG10201608379YA (ja) |
| SI (2) | SI2275443T1 (ja) |
| TR (2) | TR201808046T4 (ja) |
| TW (7) | TW201920257A (ja) |
| UA (1) | UA121453C2 (ja) |
| WO (1) | WO2009125825A1 (ja) |
Cited By (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US11053308B2 (en) | 2016-08-05 | 2021-07-06 | Chugai Seiyaku Kabushiki Kaisha | Method for treating IL-8-related diseases |
| US11180548B2 (en) | 2015-02-05 | 2021-11-23 | Chugai Seiyaku Kabushiki Kaisha | Methods of neutralizing IL-8 biological activity |
| US11236168B2 (en) | 2012-08-24 | 2022-02-01 | Chugai Seiyaku Kabushiki Kaisha | Mouse FcγammaRII-specific Fc antibody |
| US11248053B2 (en) | 2007-09-26 | 2022-02-15 | Chugai Seiyaku Kabushiki Kaisha | Method of modifying isoelectric point of antibody via amino acid substitution in CDR |
| US11267868B2 (en) | 2013-04-02 | 2022-03-08 | Chugai Seiyaku Kabushiki Kaisha | Fc region variant |
| US11359194B2 (en) | 2008-04-11 | 2022-06-14 | Chugai Seiyaku Kabushiki Kaisha | Antigen-binding molecule capable of binding two or more antigen molecules repeatedly |
| US11454633B2 (en) | 2014-12-19 | 2022-09-27 | Chugai Seiyaku Kabushiki Kaisha | Anti-myostatin antibodies, polypeptides containing variant Fc regions, and methods of use |
| US11891434B2 (en) | 2010-11-30 | 2024-02-06 | Chugai Seiyaku Kabushiki Kaisha | Antigen-binding molecule capable of binding to plurality of antigen molecules repeatedly |
| US12473375B2 (en) | 2006-03-31 | 2025-11-18 | Chugai Seiyaku Kabushiki Kaisha | Methods for controlling blood pharmacokinetics of antibodies |
| US12595299B2 (en) | 2015-02-05 | 2026-04-07 | Chugai Seiyaku Kabushiki Kaisha | FC variants |
Families Citing this family (225)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2005035753A1 (ja) | 2003-10-10 | 2005-04-21 | Chugai Seiyaku Kabushiki Kaisha | 機能蛋白質を代替する二重特異性抗体 |
| TWI544076B (zh) | 2005-03-31 | 2016-08-01 | 中外製藥股份有限公司 | A method of manufacturing a polypeptide that controls assembly |
| US8470316B2 (en) * | 2005-10-14 | 2013-06-25 | Chugai Seiyaku Kabushiki Kaisha | Agents for suppressing damage to transplanted islets after islet transplantation |
| US8945558B2 (en) * | 2005-10-21 | 2015-02-03 | Chugai Seiyaku Kabushiki Kaisha | Methods for treating myocardial infarction comprising administering an IL-6 inhibitor |
| AR057582A1 (es) * | 2005-11-15 | 2007-12-05 | Nat Hospital Organization | Agentes para suprimir la induccion de linfocitos t citotoxicos |
| US8771686B2 (en) * | 2006-01-27 | 2014-07-08 | Chugai Seiyaku Kabushiki Kaisha | Methods for treating a disease involving choroidal neovascularization by administering an IL-6 receptor antibody |
| JP5144499B2 (ja) | 2006-03-31 | 2013-02-13 | 中外製薬株式会社 | 二重特異性抗体を精製するための抗体改変方法 |
| EP2025346B1 (en) * | 2006-04-07 | 2016-08-10 | Osaka University | Muscle regeneration promoter |
| US9725514B2 (en) | 2007-01-23 | 2017-08-08 | Shinshu University | Chronic rejection inhibitor |
| JOP20080381B1 (ar) | 2007-08-23 | 2023-03-28 | Amgen Inc | بروتينات مرتبطة بمولدات مضادات تتفاعل مع بروبروتين كونفيرتاز سيتيليزين ككسين من النوع 9 (pcsk9) |
| SG193868A1 (en) * | 2007-09-26 | 2013-10-30 | Chugai Pharmaceutical Co Ltd | Modified antibody constant region |
| TWI548418B (zh) * | 2007-12-05 | 2016-09-11 | 中外製藥股份有限公司 | Anti-NR10 / IL-31RA antibody and its use |
| TWI528973B (zh) | 2008-06-05 | 2016-04-11 | Chugai Pharmaceutical Co Ltd | Nerve infiltration inhibitor |
| TWI440469B (zh) | 2008-09-26 | 2014-06-11 | Chugai Pharmaceutical Co Ltd | Improved antibody molecules |
| AR073770A1 (es) * | 2008-10-20 | 2010-12-01 | Imclone Llc | Anticuerpo aislado que se enlaza especificamente con, e induce la degradacion del receptor-3 del factor de crecimiento del fibroblasto humano (fgfr-3), fragmento de enlace fgfr-3 humano del mismo, composicion farmaceutica y producto que lo comprenden |
| JO3672B1 (ar) | 2008-12-15 | 2020-08-27 | Regeneron Pharma | أجسام مضادة بشرية عالية التفاعل الكيماوي بالنسبة لإنزيم سبتيليسين كنفرتيز بروبروتين / كيكسين نوع 9 (pcsk9). |
| US20130064834A1 (en) | 2008-12-15 | 2013-03-14 | Regeneron Pharmaceuticals, Inc. | Methods for treating hypercholesterolemia using antibodies to pcsk9 |
| AU2023203304B9 (en) * | 2009-03-09 | 2026-02-05 | Bioatla, Llc | Mirac Proteins |
| AU2015204268B2 (en) * | 2009-03-09 | 2017-03-02 | Bioatla, Llc | Mirac Proteins |
| PT2406399T (pt) | 2009-03-09 | 2018-03-05 | Bioatla Llc | Proteínas mirac |
| JP5717624B2 (ja) | 2009-03-19 | 2015-05-13 | 中外製薬株式会社 | 抗体定常領域改変体 |
| TWI457134B (zh) * | 2009-03-19 | 2014-10-21 | Chugai Pharmaceutical Co Ltd | Rheumatoid arthritis treatment |
| SG174428A1 (en) * | 2009-03-19 | 2011-10-28 | Chugai Pharmaceutical Co Ltd | Pharmaceutical formulation containing improved antibody molecules |
| WO2010107109A1 (ja) | 2009-03-19 | 2010-09-23 | 中外製薬株式会社 | 抗体定常領域改変体 |
| US9506919B2 (en) | 2009-04-13 | 2016-11-29 | The Board Of Trustees Of The Leland Stanford Junior University | Methods and devices for detecting the presence of an analyte in a sample |
| TW201041595A (en) | 2009-05-15 | 2010-12-01 | Chugai Pharmaceutical Co Ltd | Anti-axl antibody |
| WO2011037158A1 (ja) | 2009-09-24 | 2011-03-31 | 中外製薬株式会社 | 抗体定常領域改変体 |
| JO3417B1 (ar) | 2010-01-08 | 2019-10-20 | Regeneron Pharma | الصيغ المستقرة التي تحتوي على الأجسام المضادة لمضاد مستقبل( interleukin-6 (il-6r |
| TWI505838B (zh) | 2010-01-20 | 2015-11-01 | 中外製藥股份有限公司 | Stabilized antibody solution containing |
| EP2543730B1 (en) | 2010-03-04 | 2018-10-31 | Chugai Seiyaku Kabushiki Kaisha | Antibody constant region variant |
| CN105218674A (zh) * | 2010-03-11 | 2016-01-06 | 瑞纳神经科学公司 | 呈pH依赖性抗原结合的抗体 |
| CN102652259B (zh) | 2010-03-12 | 2016-07-27 | 小利兰·斯坦福大学托管委员会 | 基于磁性传感器的定量结合动力学分析 |
| TWI667346B (zh) * | 2010-03-30 | 2019-08-01 | 中外製藥股份有限公司 | 促進抗原消失之具有經修飾的FcRn親和力之抗體 |
| HRP20221490T1 (hr) | 2010-05-28 | 2023-02-03 | Chugai Seiyaku Kabushiki Kaisha | Poboljšanje antitumorskog odgovora t stanice |
| JP6121904B2 (ja) * | 2010-09-08 | 2017-04-26 | ハロザイム インコーポレイテッド | 条件的活性治療用タンパク質を評価および同定する、または発展させる方法 |
| EP2622074B1 (en) | 2010-09-30 | 2014-11-12 | Board Of Trustees Of Northern Illinois University | Library-based methods and compositions for introducing molecular switch functionality into protein affinity reagents |
| KR101398290B1 (ko) | 2010-11-17 | 2014-05-22 | 추가이 세이야쿠 가부시키가이샤 | 혈액응고 제viii 인자의 기능을 대체하는 기능을 갖는 다중특이성 항원 결합 분자 |
| KR20220136466A (ko) | 2011-01-28 | 2022-10-07 | 사노피 바이오테크놀로지 | 특정 대상자 그룹의 치료 방법에 이용하기 위한 pcsk9에 대한 인간 항체 |
| WO2012133782A1 (ja) | 2011-03-30 | 2012-10-04 | 中外製薬株式会社 | 抗原結合分子の血漿中滞留性と免疫原性を改変する方法 |
| WO2012132067A1 (ja) | 2011-03-30 | 2012-10-04 | 中外製薬株式会社 | 抗原結合分子の血漿中滞留性と免疫原性を改変する方法 |
| SG10201609665PA (en) | 2011-02-25 | 2017-01-27 | Chugai Pharmaceutical Co Ltd | FcɣRIIb-SPECIFIC Fc ANTIBODY |
| CN113980952A (zh) * | 2011-03-30 | 2022-01-28 | 中外制药株式会社 | 改变抗原结合分子的血浆中滞留性和免疫原性的方法 |
| JOP20200043A1 (ar) | 2011-05-10 | 2017-06-16 | Amgen Inc | طرق معالجة أو منع الاضطرابات المختصة بالكوليسترول |
| RU2641256C2 (ru) | 2011-06-30 | 2018-01-16 | Чугаи Сейяку Кабусики Кайся | Гетеродимеризованный полипептид |
| AR087305A1 (es) | 2011-07-28 | 2014-03-12 | Regeneron Pharma | Formulaciones estabilizadas que contienen anticuerpos anti-pcsk9, metodo de preparacion y kit |
| CN103930444B (zh) | 2011-09-16 | 2020-08-04 | 瑞泽恩制药公司 | 用前蛋白转化酶枯草溶菌素-9(PCSK9)抑制剂降低脂蛋白(a)水平的方法 |
| AU2012313594C1 (en) * | 2011-09-30 | 2018-05-10 | Chugai Seiyaku Kabushiki Kaisha | Ion concentration-dependent binding molecule library |
| SG11201401100UA (en) * | 2011-09-30 | 2014-07-30 | Chugai Pharmaceutical Co Ltd | Antigen-binding molecule inducing immune response to target antigen |
| JP6322411B2 (ja) * | 2011-09-30 | 2018-05-09 | 中外製薬株式会社 | 複数の生理活性を有する抗原の消失を促進する抗原結合分子 |
| US20140335089A1 (en) * | 2011-09-30 | 2014-11-13 | Chugai Seiyaku Kabushiki Kaisha | Antigen-binding molecule for promoting elimination of antigens |
| TW201817745A (zh) | 2011-09-30 | 2018-05-16 | 日商中外製藥股份有限公司 | 具有促進抗原清除之FcRn結合域的治療性抗原結合分子 |
| US20150299313A1 (en) * | 2011-10-05 | 2015-10-22 | Chugai Seiyaku Kabushiki Kaisha | Antigen-binding molecule for promoting clearance from plasma of antigen comprising suger chain receptor-binding domain |
| TWI589299B (zh) | 2011-10-11 | 2017-07-01 | 再生元醫藥公司 | 用於治療類風濕性關節炎之組成物及其使用方法 |
| PT3216871T (pt) | 2011-10-17 | 2022-03-15 | Regeneron Pharma | Ratos com cadeia pesada de imunoglobulina restrita |
| MX359775B (es) | 2011-10-31 | 2018-10-10 | Chugai Pharmaceutical Co Ltd | Molecula enlazada al antigeno que tiene conjugacion regulada entre cadena ligera y cadena pesada. |
| CN113416257A (zh) | 2011-11-30 | 2021-09-21 | 中外制药株式会社 | 包含进入细胞内以形成免疫复合体的搬运体(载体)的药物 |
| CN104204204A (zh) | 2012-02-09 | 2014-12-10 | 中外制药株式会社 | 抗体的Fc区变异体 |
| ES2676031T3 (es) | 2012-02-15 | 2018-07-16 | F. Hoffmann-La Roche Ag | Cromatografía de afinidad basada en el receptor Fc |
| KR102219987B1 (ko) * | 2012-02-24 | 2021-02-25 | 추가이 세이야쿠 가부시키가이샤 | FcγRIIB를 매개로 항원의 소실을 촉진하는 항원 결합 분자 |
| RU2014141536A (ru) * | 2012-03-16 | 2016-05-10 | Регенерон Фармасьютикалз, Инк. | Мыши, которые продуцируют антигенсвязывающие белки с зависимыми от величины ph характеристиками связывания |
| KR102213535B1 (ko) * | 2012-03-16 | 2021-02-08 | 리제너론 파마슈티칼스 인코포레이티드 | pH-민감성 면역글로불린 서열을 발현하는 비-사람 동물 |
| US20140013456A1 (en) | 2012-03-16 | 2014-01-09 | Regeneron Pharmaceuticals, Inc. | Histidine Engineered Light Chain Antibodies and Genetically Modified Non-Human Animals for Generating the Same |
| ES2849349T3 (es) | 2012-03-16 | 2021-08-17 | Regeneron Pharma | Anticuerpos de cadena ligera modificados mediante ingeniería con histidina y roedores modificados genéticamente para la generación de los mismos |
| CA2870876C (en) | 2012-05-23 | 2019-10-01 | Genentech, Inc. | Selection method for therapeutic agents |
| EP2857419B1 (en) * | 2012-05-30 | 2021-01-13 | Chugai Seiyaku Kabushiki Kaisha | Antigen-binding molecule for eliminating aggregated antigens |
| CN104487457B (zh) * | 2012-05-30 | 2018-01-26 | 中外制药株式会社 | 靶组织特异性抗原结合分子 |
| JP2013253842A (ja) | 2012-06-06 | 2013-12-19 | Univ Of Tokyo | pH依存的に標的分子に結合するペプチドのスクリーニング方法 |
| DK2858487T3 (da) | 2012-06-12 | 2020-01-20 | Regeneron Pharma | Humaniserede ikke-humane dyr med begrænsede immunoglobulin-tungkæde-loci |
| EP2862875B1 (en) | 2012-06-14 | 2023-09-06 | Chugai Seiyaku Kabushiki Kaisha | ANTIGEN-BINDING MOLECULE CONTAINING MODIFIED Fc REGION |
| TWI596115B (zh) | 2012-08-13 | 2017-08-21 | 再生元醫藥公司 | 具有pH-依賴性結合特性之抗-PCSK9抗體 |
| TWI717591B (zh) | 2012-08-24 | 2021-02-01 | 日商中外製藥股份有限公司 | FcγRIIb特異性Fc區域變異體 |
| JP6433297B2 (ja) | 2012-12-27 | 2018-12-05 | 中外製薬株式会社 | ヘテロ二量化ポリペプチド |
| CN109769752A (zh) | 2013-02-20 | 2019-05-21 | 瑞泽恩制药公司 | 具有修饰的免疫球蛋白重链序列的非人类动物 |
| SI2958938T1 (sl) * | 2013-02-20 | 2019-08-30 | Regeneron Pharmaceuticals, Inc. | Miši, ki izražajo humanizirane koreceptorje za celice T |
| RS57963B1 (sr) * | 2013-02-22 | 2019-01-31 | Regeneron Pharma | Miševi koji eksprimiraju humanizovani glavni kompleks histokompatibilnosti |
| WO2014164638A1 (en) * | 2013-03-11 | 2014-10-09 | Regeneron Pharmaceuticals, Inc. | Transgenic mice expressing chimeric major histocompatibility comples (mhc) class ii molecules |
| CN105452298B (zh) * | 2013-03-15 | 2021-08-31 | 拜尔健康护理有限责任公司 | 改善药代动力学的具有跨pH范围差异结合的抗TFPI抗体变体 |
| JP6574754B2 (ja) | 2013-03-19 | 2019-09-11 | ベイジン シェノゲン ファーマ グループ リミテッド | エストロゲン受容体関連疾患を処置するための抗体及び方法 |
| WO2014160958A1 (en) | 2013-03-29 | 2014-10-02 | Alexion Pharmaceuticals, Inc. | Compositions and methods for increasing the serum half-life of a therapeutic agent targeting complement c5 |
| US10111953B2 (en) | 2013-05-30 | 2018-10-30 | Regeneron Pharmaceuticals, Inc. | Methods for reducing remnant cholesterol and other lipoprotein fractions by administering an inhibitor of proprotein convertase subtilisin kexin-9 (PCSK9) |
| CN105705521A (zh) | 2013-06-07 | 2016-06-22 | 再生元制药公司 | 通过施用pcsk9抑制剂抑制动脉粥样硬化的方法 |
| WO2014200018A1 (ja) | 2013-06-11 | 2014-12-18 | 独立行政法人 国立精神・神経医療研究センター | 再発寛解型多発性硬化症(rrms)患者の治療予後予測方法、及び新規治療適応判断方法 |
| ES2962489T3 (es) | 2013-09-18 | 2024-03-19 | Regeneron Pharma | Anticuerpos de cadena ligera diseñados genéticamente con histidina y animales no humanos modificados genéticamente para generar los mismos |
| AU2014325063B2 (en) | 2013-09-27 | 2019-10-31 | Chugai Seiyaku Kabushiki Kaisha | Method for producing polypeptide heteromultimer |
| US20160280787A1 (en) | 2013-11-11 | 2016-09-29 | Chugai Seiyaku Kabushiki Kaisha | Antigen-binding molecule containing modified antibody variable region |
| KR20160081978A (ko) | 2013-11-12 | 2016-07-08 | 사노피 바이오테크놀로지 | Pcsk9 억제제의 사용을 위한 투약 요법 |
| EP3078744B1 (en) | 2013-12-04 | 2020-08-26 | Chugai Seiyaku Kabushiki Kaisha | Antigen-binding molecules, the antigen-binding activity of which varies according to the concentration of compounds, and libraries of said molecules |
| NZ631007A (en) | 2014-03-07 | 2015-10-30 | Alexion Pharma Inc | Anti-c5 antibodies having improved pharmacokinetics |
| US10329556B2 (en) | 2014-05-13 | 2019-06-25 | Bioatla, Llc | Conditionally active biological proteins |
| CN106459192B (zh) * | 2014-06-30 | 2021-08-03 | 默克专利股份公司 | 具有pH依赖性抗原结合的抗TNFa抗体 |
| KR20230074283A (ko) | 2014-07-16 | 2023-05-26 | 사노피 바이오테크놀로지 | 이형접합성 가족성 고콜레스테롤혈증(heFH) 환자의 치료방법 |
| MA40764A (fr) | 2014-09-26 | 2017-08-01 | Chugai Pharmaceutical Co Ltd | Agent thérapeutique induisant une cytotoxicité |
| DK3215528T3 (da) | 2014-11-06 | 2019-10-07 | Hoffmann La Roche | Fc-regionvarianter med modificeret FcRn-binding og anvendelsesfremgangsmåder |
| JP7125248B2 (ja) | 2014-11-11 | 2022-08-24 | 中外製薬株式会社 | 改変された抗体可変領域を含む抗原結合分子のライブラリ |
| WO2016098356A1 (en) | 2014-12-19 | 2016-06-23 | Chugai Seiyaku Kabushiki Kaisha | Anti-c5 antibodies and methods of use |
| JP2018511557A (ja) | 2015-01-22 | 2018-04-26 | 中外製薬株式会社 | 2種以上の抗c5抗体の組み合わせおよび使用方法 |
| EP3253788A4 (en) | 2015-02-06 | 2018-08-08 | Cell IDX, Inc. | Antigen-coupled immunoreagents |
| TWI805046B (zh) | 2015-02-27 | 2023-06-11 | 日商中外製藥股份有限公司 | Il-6受體抗體用於製備醫藥組成物的用途 |
| HK1250040A1 (zh) | 2015-03-31 | 2018-11-23 | Sorriso Pharmaceuticals, Inc. | 多肽 |
| KR102789821B1 (ko) | 2015-03-31 | 2025-04-02 | 소리소 파마슈티컬스 인크. | 프로테아제-절단가능 링커를 갖는 펩티드 구조물 |
| JP7082484B2 (ja) | 2015-04-01 | 2022-06-08 | 中外製薬株式会社 | ポリペプチド異種多量体の製造方法 |
| US10676723B2 (en) | 2015-05-11 | 2020-06-09 | David Gordon Bermudes | Chimeric protein toxins for expression by therapeutic bacteria |
| WO2016186154A1 (ja) | 2015-05-19 | 2016-11-24 | 国立研究開発法人国立精神・神経医療研究センター | 多発性硬化症(ms)患者の新規治療適用判断方法 |
| US10294306B2 (en) * | 2015-05-28 | 2019-05-21 | Bio-Rad Laboratories, Inc. | Affinity ligands and methods relating thereto |
| WO2017031151A1 (en) | 2015-08-18 | 2017-02-23 | Regeneron Pharmaceuticals, Inc. | Anti-pcsk9 inhibitory antibodies for treating patients with hyperlipidemia undergoing lipoprotein apheresis |
| AU2016323088B2 (en) * | 2015-09-18 | 2020-12-10 | Chugai Seiyaku Kabushiki Kaisha | IL-8-binding antibodies and uses thereof |
| CA3002422C (en) * | 2015-12-18 | 2024-04-16 | Chugai Seiyaku Kabushiki Kaisha | Anti-myostatin antibodies, polypeptides containing variant fc regions, and methods of use |
| RU2742606C2 (ru) | 2015-12-18 | 2021-02-09 | Чугаи Сейяку Кабусики Кайся | Антитела к с5 и способы их применения |
| US11359009B2 (en) | 2015-12-25 | 2022-06-14 | Chugai Seiyaku Kabushiki Kaisha | Anti-myostatin antibodies and methods of use |
| AU2016381992B2 (en) | 2015-12-28 | 2024-01-04 | Chugai Seiyaku Kabushiki Kaisha | Method for promoting efficiency of purification of Fc region-containing polypeptide |
| KR20180116215A (ko) | 2016-03-14 | 2018-10-24 | 추가이 세이야쿠 가부시키가이샤 | 암의 치료에 이용하기 위한 세포상해 유도 치료제 |
| AU2017238172B2 (en) | 2016-03-21 | 2024-06-27 | Marengo Therapeutics, Inc. | Multispecific and multifunctional molecules and uses thereof |
| CR20180554A (es) | 2016-04-28 | 2019-01-10 | Chugai Pharmaceutical Co Ltd | Preparaciones que contienen anticuerpos |
| BR112018073945A2 (pt) | 2016-05-27 | 2019-02-26 | Alexion Pharmaceuticals, Inc. | métodos para tratamento de miastenia grave generalizada refratária |
| AU2017283470B2 (en) | 2016-06-14 | 2024-03-21 | Regeneron Pharmaceuticals, Inc. | Anti-C5 antibodies and uses thereof |
| KR102680483B1 (ko) * | 2016-06-17 | 2024-07-01 | 추가이 세이야쿠 가부시키가이샤 | 항-마이오스타틴 항체 및 사용 방법 |
| PE20240825A1 (es) * | 2016-06-17 | 2024-04-18 | Chugai Pharmaceutical Co Ltd | Anticuerpos anti-c5 y metodos de uso |
| CN116515950A (zh) * | 2016-07-18 | 2023-08-01 | 赛尔伊迪克斯公司 | 抗原偶联的杂交试剂 |
| US20190256853A1 (en) * | 2016-07-28 | 2019-08-22 | Laboratoire Francais Du Fractionnement Et Des Biot Echnologies | Method for Obtaining Aptamers |
| MX2019002199A (es) | 2016-08-31 | 2019-05-16 | Bioatla Llc | Polipeptidos condicionalmente activos y métodos para generarlos. |
| SG10201607778XA (en) | 2016-09-16 | 2018-04-27 | Chugai Pharmaceutical Co Ltd | Anti-Dengue Virus Antibodies, Polypeptides Containing Variant Fc Regions, And Methods Of Use |
| AU2017364817B2 (en) | 2016-11-28 | 2023-11-09 | Chugai Seiyaku Kabushiki Kaisha | Antigen-binding domain, and polypeptide including conveying section |
| US11129906B1 (en) | 2016-12-07 | 2021-09-28 | David Gordon Bermudes | Chimeric protein toxins for expression by therapeutic bacteria |
| JP2020504105A (ja) * | 2016-12-19 | 2020-02-06 | グレンマーク・ファーマシューティカルズ・エスエー | 新規なtnfrアゴニストおよびその使用 |
| JP7191833B2 (ja) | 2017-01-30 | 2022-12-19 | 中外製薬株式会社 | 抗スクレロスチン抗体およびその使用 |
| UA129282C2 (uk) | 2017-01-31 | 2025-03-12 | Чугаі Сейяку Кабусікі Кайся | Спосіб лікування або профілактики пов'язаних з c5 хвороб |
| WO2018151820A1 (en) | 2017-02-16 | 2018-08-23 | Elstar Therapeutics, Inc. | Multifunctional molecules comprising a trimeric ligand and uses thereof |
| WO2018156180A1 (en) | 2017-02-24 | 2018-08-30 | Kindred Biosciences, Inc. | Anti-il31 antibodies for veterinary use |
| JP7556687B2 (ja) | 2017-02-24 | 2024-09-26 | 中外製薬株式会社 | 薬学的組成物、抗原結合分子、治療方法、およびスクリーニング方法 |
| UA125757C2 (uk) | 2017-03-16 | 2022-06-01 | Медімм'Юн Лімітед | Антитіло до par2 і його застосування |
| CA3059133A1 (en) | 2017-04-21 | 2018-10-25 | Staten Biotechnology B.V. | Anti-apoc3 antibodies and methods of use thereof |
| EP3620531A4 (en) | 2017-05-02 | 2021-03-17 | National Center of Neurology and Psychiatry | METHOD OF PREDICTION AND EVALUATION OF THERAPEUTIC EFFECT IN DISEASES RELATING TO IL-6 AND NEUTROPHILS |
| GB201707484D0 (en) * | 2017-05-10 | 2017-06-21 | Argenx Bvba | Method of preparing ph-dependent antibodies |
| US20210246227A1 (en) | 2017-05-31 | 2021-08-12 | Elstar Therapeutics, Inc. | Multispecific molecules that bind to myeloproliferative leukemia (mpl) protein and uses thereof |
| US11912775B2 (en) | 2017-07-18 | 2024-02-27 | Kyowa Kirin Co., Ltd. | Anti-human CCR1 monoclonal antibody |
| SI3658184T1 (sl) | 2017-07-27 | 2024-01-31 | Alexion Pharmaceuticals, Inc., | Formulacije z visoko koncentracijo protiteles proti-C5 |
| WO2019035938A1 (en) | 2017-08-16 | 2019-02-21 | Elstar Therapeutics, Inc. | MULTISPECIFIC MOLECULES BINDING TO BCMA AND USES THEREOF |
| KR102771895B1 (ko) | 2017-10-20 | 2025-02-21 | 가꼬우호우징 효고 이카다이가쿠 | 항il-6 수용체 항체를 함유하는 수술 후의 유착을 억제하기 위한 의약 조성물 |
| WO2019084438A1 (en) | 2017-10-26 | 2019-05-02 | Alexion Pharmaceuticals, Inc. | ASSAY AND ADMINISTRATION OF ANTI-C5 ANTIBODIES FOR THE TREATMENT OF NOCTURNAL PAROXYSTIC HEMOGLOBINURIA (PNH) AND ATYPICAL HEMOLYTIC AND UREMIC SYNDROME (AHUS) |
| KR20200074975A (ko) | 2017-10-31 | 2020-06-25 | 스태튼 바이오테크놀로지 비.브이. | 항-ApoC3 항체 및 이의 사용 방법 |
| US10538583B2 (en) | 2017-10-31 | 2020-01-21 | Staten Biotechnology B.V. | Anti-APOC3 antibodies and compositions thereof |
| CN119161488A (zh) | 2017-11-01 | 2024-12-20 | 中外制药株式会社 | 具有降低的生物活性的抗体变体和同种型 |
| EP3710589A4 (en) * | 2017-11-14 | 2021-11-10 | Chugai Seiyaku Kabushiki Kaisha | ANTI-C1S ANTIBODIES AND METHOD OF USING |
| EP3719035A4 (en) | 2017-11-28 | 2021-09-01 | Chugai Seiyaku Kabushiki Kaisha | POLYPEPTIDE WITH ANTIGEN-BINDING AREA AND CARRYING SECTION |
| TW201938194A (zh) | 2017-12-05 | 2019-10-01 | 日商中外製藥股份有限公司 | 包含結合cd3及cd137的改變的抗體可變區之抗原結合分子 |
| WO2019118556A1 (en) | 2017-12-13 | 2019-06-20 | Regeneron Pharmaceuticals, Inc. | Anti-c5 antibody combinations and uses thereof |
| US12247060B2 (en) | 2018-01-09 | 2025-03-11 | Marengo Therapeutics, Inc. | Calreticulin binding constructs and engineered T cells for the treatment of diseases |
| GB201802487D0 (en) | 2018-02-15 | 2018-04-04 | Argenx Bvba | Cytokine combination therapy |
| JP7049569B2 (ja) * | 2018-03-06 | 2022-04-07 | 国立大学法人 東京大学 | pH依存的に標的分子に結合するペプチドのスクリーニング方法 |
| WO2019178362A1 (en) | 2018-03-14 | 2019-09-19 | Elstar Therapeutics, Inc. | Multifunctional molecules that bind to calreticulin and uses thereof |
| US20210009711A1 (en) | 2018-03-14 | 2021-01-14 | Elstar Therapeutics, Inc. | Multifunctional molecules and uses thereof |
| CN116327926A (zh) | 2018-03-15 | 2023-06-27 | 中外制药株式会社 | 对寨卡病毒具有交叉反应性的抗登革热病毒抗体及使用方法 |
| MA52248A (fr) | 2018-04-13 | 2021-02-17 | Chugai Pharmaceutical Co Ltd | Anticorps dirigés contre un composant du complément et procédés d'utilisation |
| JPWO2019230868A1 (ja) | 2018-05-30 | 2021-06-24 | 中外製薬株式会社 | 単ドメイン抗体含有リガンド結合分子 |
| WO2019231983A1 (en) | 2018-05-31 | 2019-12-05 | Alexion Pharmaceuticals, Inc. | Dosage and administration of anti-c5 antibodies for treatment of paroxysmal nocturnal hemoglobinuria (pnh) in pediatric patients |
| EP3802603A1 (en) | 2018-06-04 | 2021-04-14 | Alexion Pharmaceuticals, Inc. | Dosage and administration of anti-c5 antibodies for treatment of atypical hemolytic uremic syndrome (ahus) in pediatric patients |
| AU2019295279B2 (en) | 2018-06-26 | 2025-06-19 | Kagoshima University | Antibody binding to cell adhesion molecule 3 |
| US11965035B2 (en) | 2018-06-26 | 2024-04-23 | Kyowa Kirin Co., Ltd. | Antibody binding to chondroitin sulfate proteoglycan 5 |
| US12312394B2 (en) | 2018-06-28 | 2025-05-27 | Alexion Pharmaceuticals, Inc. | Methods of producing anti-C5 antibodies |
| JP7554742B2 (ja) | 2018-07-03 | 2024-09-20 | マレンゴ・セラピューティクス,インコーポレーテッド | 抗tcr抗体分子およびその使用 |
| WO2020022262A1 (en) * | 2018-07-23 | 2020-01-30 | Chugai Seiyaku Kabushiki Kaisha | Target cell specific cytosol-penetrating antigen-binding molecules |
| CR20210103A (es) | 2018-08-01 | 2021-03-22 | Chugai Pharmaceutical Co Ltd | Composición farmacéutica para usarse en el tratamiento o prevención de una enfermedad relacionada con c5 y método para tratar o prevenir una enfermedad relacionada con c5 |
| PE20210343A1 (es) | 2018-08-10 | 2021-02-23 | Chugai Pharmaceutical Co Ltd | Molecula de union al antigeno anti grupo de diferenciacion 137 (cd137) y su uso |
| JP7523349B2 (ja) | 2018-08-29 | 2024-07-26 | 中外製薬株式会社 | 抗体半分子、および抗体半分子のホモ二量体形成を抑制する方法 |
| JP2022512632A (ja) | 2018-10-30 | 2022-02-07 | アレクシオン ファーマシューティカルズ, インコーポレイテッド | 発作性夜間ヘモグロビン尿症(pnh)の処置のための抗c5抗体の皮下投薬及び投与 |
| CN113227789B (zh) * | 2018-12-30 | 2024-12-24 | 豪夫迈·罗氏有限公司 | 基于pH梯度SPR的结合测定 |
| KR20210122810A (ko) | 2019-01-31 | 2021-10-12 | 사노피 바이오테크놀로지 | 청소년 특발성 관절염을 치료하기 위한 항 il-6 수용체 항체 |
| WO2020172601A1 (en) | 2019-02-21 | 2020-08-27 | Elstar Therapeutics, Inc. | Multifunctional molecules that bind to calreticulin and uses thereof |
| EP3927745A1 (en) | 2019-02-21 | 2021-12-29 | Marengo Therapeutics, Inc. | Multifunctional molecules that bind to t cells and uses thereof to treat autoimmune disorders |
| GB2597851B (en) | 2019-02-21 | 2024-05-29 | Marengo Therapeutics Inc | Antibody molecules that bind to NKP30 and uses thereof |
| AU2020226893B2 (en) | 2019-02-21 | 2025-02-27 | Marengo Therapeutics, Inc. | Multifunctional molecules that bind to T cell related cancer cells and uses thereof |
| SG11202109122SA (en) | 2019-02-21 | 2021-09-29 | Marengo Therapeutics Inc | Anti-tcr antibody molecules and uses thereof |
| CN113613676A (zh) | 2019-03-19 | 2021-11-05 | 中外制药株式会社 | 包含对抗原的结合活性因mta而变化的抗原结合结构域的抗原结合分子及用于获得该抗原结合结构域的文库 |
| KR20210149779A (ko) | 2019-04-10 | 2021-12-09 | 추가이 세이야쿠 가부시키가이샤 | Fc 영역 개변 항체의 정제 방법 |
| GB2589049C (en) | 2019-04-11 | 2024-02-21 | argenx BV | Anti-IgE antibodies |
| JP7501876B2 (ja) | 2019-04-17 | 2024-06-18 | 国立大学法人広島大学 | Il-6阻害剤及びccr2阻害剤を組み合わせて投与することを特徴とする泌尿器がんの治療剤 |
| TW202106712A (zh) | 2019-04-24 | 2021-02-16 | 美商再生元醫藥公司 | 類風溼性關節炎之診斷及治療方法 |
| AU2020275348A1 (en) | 2019-05-15 | 2021-12-09 | Chugai Seiyaku Kabushiki Kaisha | An antigen-binding molecule, a pharmaceutical composition, and a method |
| WO2020233695A1 (zh) | 2019-05-23 | 2020-11-26 | 厦门大学 | 抗乙肝病毒新型抗体及其用途 |
| CA3142710A1 (en) | 2019-06-04 | 2020-12-10 | Sanofi Biotechnology | Compositions and methods for treating pain in subjects with rheumatoid arthritis |
| WO2020246563A1 (ja) | 2019-06-05 | 2020-12-10 | 中外製薬株式会社 | 抗体切断部位結合分子 |
| WO2020246567A1 (ja) | 2019-06-05 | 2020-12-10 | 中外製薬株式会社 | プロテアーゼ基質、及びプロテアーゼ切断配列を含むポリペプチド |
| AU2020287378A1 (en) * | 2019-06-06 | 2022-02-03 | Mythic Therapeutics, Inc. | Antigen-binding protein constructs and uses thereof |
| WO2020247929A1 (en) | 2019-06-07 | 2020-12-10 | Adimab, Llc | High affinity anti-cd3 antibodies, and methods for their generation and use |
| KR20220035368A (ko) * | 2019-06-07 | 2022-03-22 | 아디맵 엘엘씨 | 조작된 ph-의존성 항-cd3 항체, 및 이의 생성 및 사용 방법 |
| EP3980129A1 (en) * | 2019-06-07 | 2022-04-13 | Mythic Therapeutics, Inc. | Antigen-binding protein constructs and uses thereof |
| JP7692844B2 (ja) | 2019-06-21 | 2025-06-16 | ソリッソ ファーマシューティカルズ,インク. | ポリペプチド |
| CA3144200A1 (en) | 2019-06-21 | 2020-12-24 | Sorriso Pharmaceuticals, Inc. | Compositions |
| EP3986931A1 (en) | 2019-06-21 | 2022-04-27 | Sorriso Pharmaceuticals, Inc. | Polypeptides |
| BR112022001693A2 (pt) * | 2019-07-30 | 2022-06-07 | Mythic Therapeutics Inc | Construtos de proteína de ligação ao antígeno e usos dos mesmos |
| US12012451B2 (en) * | 2019-08-19 | 2024-06-18 | The Rockefeller University | Engineering pH-dependent antigen binding activity into anti-HIV antibodies with improved pharmacokinetics |
| US20240092889A1 (en) | 2019-10-16 | 2024-03-21 | Chugai Seiyaku Kabushiki Kaisha | An antibody, a pharmaceutical composition, and a method |
| MX2022007479A (es) | 2019-12-18 | 2022-06-29 | Hoffmann La Roche | Anticuerpos anti-ccl2 biespecificos. |
| CR20220357A (es) | 2019-12-27 | 2022-08-24 | Chugai Pharmaceutical Co Ltd | Anticuerpo anti antígeno-4 asociado al linfocito t citotóxico (ctla-4) y uso del mismo |
| WO2021138407A2 (en) | 2020-01-03 | 2021-07-08 | Marengo Therapeutics, Inc. | Multifunctional molecules that bind to cd33 and uses thereof |
| GB2609554B (en) | 2020-01-03 | 2025-08-20 | Marengo Therapeutics Inc | Anti-TCR antibody molecules and uses thereof |
| TWI895351B (zh) | 2020-02-12 | 2025-09-01 | 日商中外製藥股份有限公司 | 用於癌症之治療的抗cd137抗原結合分子 |
| MX2022013147A (es) * | 2020-04-22 | 2023-02-09 | Kindred Biosciences Inc | Anticuerpos anti-interleucina 31 de acción prolongada para uso veterinario. |
| JP2023523011A (ja) | 2020-04-24 | 2023-06-01 | マレンゴ・セラピューティクス,インコーポレーテッド | T細胞関連のがん細胞に結合する多機能性分子およびその使用 |
| EP4159236A4 (en) | 2020-05-29 | 2024-08-21 | Chugai Seiyaku Kabushiki Kaisha | Antibody-containing formulation |
| BR112023000216A2 (pt) | 2020-07-28 | 2023-02-07 | Chugai Pharmaceutical Co Ltd | Preparação de seringa pré-carregada com agulha, com proteção de agulha e incluindo anticorpo modificado |
| JPWO2022025220A1 (ja) | 2020-07-31 | 2022-02-03 | ||
| GB2616354A (en) | 2020-08-26 | 2023-09-06 | Marengo Therapeutics Inc | Methods of detecting TRBC1 or TRBC2 |
| EP4204096A4 (en) | 2020-08-26 | 2024-10-02 | Marengo Therapeutics, Inc. | ANTIBODY MOLECULES BINDING TO NKP30 AND USES THEREOF |
| JP2023542080A (ja) | 2020-08-26 | 2023-10-05 | マレンゴ・セラピューティクス,インコーポレーテッド | カルレティキュリンに結合する多機能性分子およびその使用 |
| US20230416371A1 (en) | 2020-08-28 | 2023-12-28 | Chugai Seiyaku Kabushiki Kaisha | Heterodimer fc polypeptide |
| EP4494660A3 (en) * | 2021-02-03 | 2025-04-16 | Mythic Therapeutics, Inc. | Anti-met antibodies and uses thereof |
| US12376573B2 (en) | 2021-03-31 | 2025-08-05 | Regeneron Pharmaceuticals, Inc. | Genetically modified mice comprising humanized cellular immune system components with improved diversity of TCRB repertoire |
| AU2022255506A1 (en) | 2021-04-08 | 2023-11-09 | Marengo Therapeutics, Inc. | Multifunctional molecules binding to tcr and uses thereof |
| AR125344A1 (es) | 2021-04-15 | 2023-07-05 | Chugai Pharmaceutical Co Ltd | Anticuerpo anti-c1s |
| EP4342984A4 (en) | 2021-05-19 | 2025-04-23 | Chugai Seiyaku Kabushiki Kaisha | Method for predicting in vivo pharmacokinetics of molecule |
| EP4355785A1 (en) | 2021-06-17 | 2024-04-24 | Amberstone Biosciences, Inc. | Anti-cd3 constructs and uses thereof |
| KR20240021859A (ko) | 2021-06-18 | 2024-02-19 | 에프. 호프만-라 로슈 아게 | 이중특이적 항-ccl2 항체 |
| IL309115A (en) | 2021-06-25 | 2024-02-01 | Chugai Pharmaceutical Co Ltd | Anti-CTLA-4 antibodies |
| TWI879694B (zh) | 2021-06-25 | 2025-04-01 | 日商中外製藥股份有限公司 | 抗ctla-4抗體的用途 |
| CA3236108A1 (en) | 2022-01-18 | 2023-07-27 | Paul Sebastian VAN DER WONING | Galectin-10 antibodies |
| JPWO2023153471A1 (ja) | 2022-02-09 | 2023-08-17 | ||
| GB202211100D0 (en) | 2022-07-29 | 2022-09-14 | Stam Jord Cornelis | Lysosomal degradation |
| KR20240054896A (ko) | 2022-10-18 | 2024-04-26 | 추가이 세이야쿠 가부시키가이샤 | 항C1s 항체의 사용 |
| KR20240080281A (ko) | 2022-11-29 | 2024-06-07 | 엘지디스플레이 주식회사 | 표시 장치 및 표시 장치의 제조 방법 |
| AU2024324215A1 (en) * | 2023-08-11 | 2026-02-26 | Abalytics Oncology, Inc. | Anti-ctla-4 antibodies and related binding molecules and methods and uses thereof |
| GB202319605D0 (en) | 2023-12-20 | 2024-01-31 | argenx BV | Monovalent binding molecules and methods of use |
| WO2026011013A1 (en) | 2024-07-02 | 2026-01-08 | Epibiologics, Inc. | Binding agents and uses thereof |
| WO2026037841A1 (en) | 2024-08-12 | 2026-02-19 | ONA Therapeutics S.L. | Anti-fgfr4 molecules and uses thereof |
| WO2026050572A2 (en) | 2024-08-29 | 2026-03-05 | Marengo Therapeutics, Inc. | Multifunctional molecules binding to tcr and uses thereof |
Family Cites Families (498)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS5229888B2 (ja) | 1972-02-01 | 1977-08-04 | ||
| US4769320A (en) | 1982-07-27 | 1988-09-06 | New England Medical Center Hospitals, Inc. | Immunoassay means and methods useful in human native prothrombin and human abnormal prothorombin determinations |
| ES521371A0 (es) * | 1982-04-12 | 1984-05-16 | Hybritech Inc | Un procedimiento para la purificacion de un anticuerpo. |
| JPS58201994A (ja) | 1982-05-21 | 1983-11-25 | Hideaki Hagiwara | 抗原特異的ヒト免疫グロブリンの生産方法 |
| US4689299A (en) * | 1982-09-30 | 1987-08-25 | University Of Rochester | Human monoclonal antibodies against bacterial toxins |
| US4816567A (en) | 1983-04-08 | 1989-03-28 | Genentech, Inc. | Recombinant immunoglobin preparations |
| JPS6088703A (ja) | 1983-10-18 | 1985-05-18 | 新日本製鐵株式会社 | 耐重荷重性舗装体 |
| GB8607679D0 (en) | 1986-03-27 | 1986-04-30 | Winter G P | Recombinant dna product |
| JPH06104071B2 (ja) | 1986-08-24 | 1994-12-21 | 財団法人化学及血清療法研究所 | 第▲ix▼因子コンホメ−シヨン特異性モノクロ−ナル抗体 |
| US4801687A (en) * | 1986-10-27 | 1989-01-31 | Bioprobe International, Inc. | Monoclonal antibody purification process using protein A |
| JPS63149900A (ja) | 1986-12-15 | 1988-06-22 | Toshiba Corp | 半導体メモリ |
| US4851341A (en) | 1986-12-19 | 1989-07-25 | Immunex Corporation | Immunoaffinity purification system |
| JPH01144991A (ja) | 1987-12-02 | 1989-06-07 | Kagaku Oyobi Ketsusei Riyouhou Kenkyusho | 血液凝固第8因子の精製方法 |
| US5670373A (en) * | 1988-01-22 | 1997-09-23 | Kishimoto; Tadamitsu | Antibody to human interleukin-6 receptor |
| US5322678A (en) * | 1988-02-17 | 1994-06-21 | Neorx Corporation | Alteration of pharmacokinetics of proteins by charge modification |
| AR242986A1 (es) | 1988-09-28 | 1993-06-30 | Lilly Co Eli | Un metodo de reduccion de la heterogeneidad de anticuerpos secretados por celulas productoras de anticuerpo. |
| US5126250A (en) * | 1988-09-28 | 1992-06-30 | Eli Lilly And Company | Method for the reduction of heterogeneity of monoclonal antibodies |
| US5530101A (en) | 1988-12-28 | 1996-06-25 | Protein Design Labs, Inc. | Humanized immunoglobulins |
| US5202253A (en) | 1988-12-30 | 1993-04-13 | Oklahoma Medical Research Foundation | Monoclonal antibody specific for protein C and antibody purification method |
| CA2006684C (en) | 1988-12-30 | 1996-12-17 | Charles T. Esmon | Monoclonal antibody against protein c |
| JPH0636741B2 (ja) | 1989-11-08 | 1994-05-18 | 帝人株式会社 | ヒト・プロテインcの分離方法 |
| CA2075927A1 (en) | 1990-02-16 | 1991-08-17 | Victor A. Raso | Hybrid reagents capable of selectively releasing molecules into cells |
| US5130129A (en) | 1990-03-06 | 1992-07-14 | The Regents Of The University Of California | Method for enhancing antibody transport through capillary barriers |
| EP0585287B1 (en) | 1990-07-10 | 1999-10-13 | Cambridge Antibody Technology Limited | Methods for producing members of specific binding pairs |
| GB9015198D0 (en) | 1990-07-10 | 1990-08-29 | Brien Caroline J O | Binding substance |
| DE69133476T2 (de) | 1990-08-29 | 2006-01-05 | GenPharm International, Inc., Palo Alto | Transgene Mäuse fähig zur Produktion heterologer Antikörper |
| GB9022547D0 (en) | 1990-10-17 | 1990-11-28 | Wellcome Found | Purified immunoglobulin |
| KR100249937B1 (ko) | 1991-04-25 | 2000-04-01 | 나가야마 오사무 | 인간 인터루킨-6 수용체에 대한 재구성 인간 항체 |
| US5468634A (en) * | 1991-06-24 | 1995-11-21 | The University Of North Carolina At Chapel Hill | Axl oncogene |
| JP3087857B2 (ja) | 1991-07-04 | 2000-09-11 | 東洋紡績株式会社 | 交編編地の染色処理方法 |
| WO1993006213A1 (en) | 1991-09-23 | 1993-04-01 | Medical Research Council | Production of chimeric antibodies - a combinatorial approach |
| ES2341666T3 (es) | 1991-12-02 | 2010-06-24 | Medimmune Limited | Produccion de autoanticuerpos de repertorios de segmentos de anticue rpos expresados en la superficie de fagos. |
| AU3328493A (en) | 1991-12-17 | 1993-07-19 | Genpharm International, Inc. | Transgenic non-human animals capable of producing heterologous antibodies |
| US5667988A (en) | 1992-01-27 | 1997-09-16 | The Scripps Research Institute | Methods for producing antibody libraries using universal or randomized immunoglobulin light chains |
| GB9203459D0 (en) | 1992-02-19 | 1992-04-08 | Scotgen Ltd | Antibodies with germ-line variable regions |
| JP3507073B2 (ja) | 1992-03-24 | 2004-03-15 | ケンブリッジ アンティボディー テクノロジー リミティド | 特異的結合対の成員の製造方法 |
| EP0640094A1 (en) | 1992-04-24 | 1995-03-01 | The Board Of Regents, The University Of Texas System | Recombinant production of immunoglobulin-like domains in prokaryotic cells |
| NZ255101A (en) | 1992-07-24 | 1997-08-22 | Cell Genesys Inc | A yeast artificial chromosome (yac) vector containing an hprt minigene expressible in murine stem cells and genetically modified rodent therefor |
| BR9204244A (pt) | 1992-10-26 | 1994-05-03 | Cofap | Ferro fundido cinzento |
| JPH08503617A (ja) | 1992-12-01 | 1996-04-23 | プロテイン デザイン ラブズ、インコーポレーテッド | L−セレクチンに反応性のヒト化抗体 |
| US7393682B1 (en) | 1993-03-19 | 2008-07-01 | The Johns Hopkins University School Of Medicine | Polynucleotides encoding promyostatin polypeptides |
| EP1333035A3 (en) | 1993-03-19 | 2004-07-07 | The Johns Hopkins University School Of Medicine | Growth differentiation factor-8 |
| DE69434689D1 (de) * | 1993-06-10 | 2006-05-18 | Genetic Therapy Inc | Adenovirale vektoren für die behandlung der hämophilie |
| GB9313509D0 (en) | 1993-06-30 | 1993-08-11 | Medical Res Council | Chemisynthetic libraries |
| GB9314271D0 (en) | 1993-07-09 | 1993-08-18 | Inst Of Cancer The Research | Cell growth factor receptors |
| FR2707189B1 (fr) | 1993-07-09 | 1995-10-13 | Gradient Ass | Procédé de traitement de résidus de combustion et installation de mise en Óoeuvre dudit procédé. |
| IL107742A0 (en) | 1993-11-24 | 1994-02-27 | Yeda Res & Dev | Chemically-modified binding proteins |
| US6214613B1 (en) | 1993-12-03 | 2001-04-10 | Ashai Kasei Kogyo Kabushiki Kaisha | Expression screening vector |
| CA2177367A1 (en) | 1993-12-03 | 1995-06-08 | Andrew David Griffiths | Recombinant binding proteins and peptides |
| JPH07177572A (ja) | 1993-12-20 | 1995-07-14 | Matsushita Electric Ind Co Ltd | コードレス電話の留守番方法 |
| US6074642A (en) | 1994-05-02 | 2000-06-13 | Alexion Pharmaceuticals, Inc. | Use of antibodies specific to human complement component C5 for the treatment of glomerulonephritis |
| US5945311A (en) * | 1994-06-03 | 1999-08-31 | GSF--Forschungszentrumfur Umweltund Gesundheit | Method for producing heterologous bi-specific antibodies |
| DE122009000068I2 (de) | 1994-06-03 | 2011-06-16 | Ascenion Gmbh | Verfahren zur Herstellung von heterologen bispezifischen Antikörpern |
| US8017121B2 (en) * | 1994-06-30 | 2011-09-13 | Chugai Seiyaku Kabushika Kaisha | Chronic rheumatoid arthritis therapy containing IL-6 antagonist as effective component |
| JP4361133B2 (ja) | 1994-07-11 | 2009-11-11 | ボード オブ リージェンツ, ザ ユニバーシティ オブ テキサス システム | 血管系の特異的凝固のための方法および組成物 |
| JP3865418B2 (ja) | 1994-07-13 | 2007-01-10 | 中外製薬株式会社 | ヒトインターロイキン−8に対する再構成ヒト抗体 |
| US6048972A (en) | 1994-07-13 | 2000-04-11 | Chugai Pharmaceutical Co., Ltd. | Recombinant materials for producing humanized anti-IL-8 antibodies |
| TW416960B (en) | 1994-07-13 | 2001-01-01 | Chugai Pharmaceutical Co Ltd | Reshaped human antibody to human interleukin-8 |
| CN1156460A (zh) | 1994-07-13 | 1997-08-06 | 中外制药株式会社 | 抗人白细胞介素-8的重构人抗体 |
| AU701342B2 (en) | 1994-07-13 | 1999-01-28 | Chugai Seiyaku Kabushiki Kaisha | Reconstituted human antibody against human interleukin-8 |
| US6309636B1 (en) | 1995-09-14 | 2001-10-30 | Cancer Research Institute Of Contra Costa | Recombinant peptides derived from the Mc3 anti-BA46 antibody, methods of use thereof, and methods of humanizing antibody peptides |
| PT783893E (pt) | 1994-10-07 | 2012-05-24 | Chugai Pharmaceutical Co Ltd | Inibição do crescimento anormal das células sinoviais usando antagonistas de il-6 como componente ativo |
| CN1306963C (zh) | 1994-10-21 | 2007-03-28 | 岸本忠三 | 用于治疗il-6产生所致疾病的药物组合物 |
| US5876950A (en) | 1995-01-26 | 1999-03-02 | Bristol-Myers Squibb Company | Monoclonal antibodies specific for different epitopes of human GP39 and methods for their use in diagnosis and therapy |
| US5731168A (en) | 1995-03-01 | 1998-03-24 | Genentech, Inc. | Method for making heteromultimeric polypeptides |
| DE69637481T2 (de) | 1995-04-27 | 2009-04-09 | Amgen Fremont Inc. | Aus immunisierten Xenomäusen stammende menschliche Antikörper gegen IL-8 |
| AU2466895A (en) | 1995-04-28 | 1996-11-18 | Abgenix, Inc. | Human antibodies derived from immunized xenomice |
| US5830478A (en) | 1995-06-07 | 1998-11-03 | Boston Biomedical Research Institute | Method for delivering functional domains of diphtheria toxin to a cellular target |
| US6018032A (en) * | 1995-09-11 | 2000-01-25 | Kyowa Hakko Kogyo Co., Ltd. | Antibody against human interleukin-5-receptor α chain |
| US5783186A (en) | 1995-12-05 | 1998-07-21 | Amgen Inc. | Antibody-induced apoptosis |
| JP4046354B2 (ja) | 1996-03-18 | 2008-02-13 | ボード オブ リージェンツ,ザ ユニバーシティ オブ テキサス システム | 増大した半減期を有する免疫グロブリン様ドメイン |
| WO1998003546A1 (en) | 1996-07-19 | 1998-01-29 | Amgen Inc. | Analogs of cationic proteins |
| ES2300113T3 (es) | 1996-08-02 | 2008-06-01 | Bristol-Myers Squibb Company | Un procedimiento para inhibir toxicidad inducida por inmunoglobulinas que resulta del uso de inmunoglobulinas en terapia y diagnostico in vivo. |
| US7247302B1 (en) | 1996-08-02 | 2007-07-24 | Bristol-Myers Squibb Company | Method for inhibiting immunoglobulin-induced toxicity resulting from the use of immunoglobulins in therapy and in vivo diagnosis |
| KR100847441B1 (ko) | 1996-09-26 | 2008-07-21 | 츄가이 세이야꾸 가부시키가이샤 | 인간의 부갑상선 호르몬 관련 펩티드에 대한 항체 |
| US6025158A (en) | 1997-02-21 | 2000-02-15 | Genentech, Inc. | Nucleic acids encoding humanized anti-IL-8 monoclonal antibodies |
| US6277375B1 (en) | 1997-03-03 | 2001-08-21 | Board Of Regents, The University Of Texas System | Immunoglobulin-like domains with increased half-lives |
| EP2011514B1 (en) | 1997-03-21 | 2012-02-29 | Chugai Seiyaku Kabushiki Kaisha | A preventive or therapeutic agent for sensitized T cell-mediated diseases comprising IL-6 antagonist as an active ingredient |
| US6884879B1 (en) | 1997-04-07 | 2005-04-26 | Genentech, Inc. | Anti-VEGF antibodies |
| FR2761994B1 (fr) | 1997-04-11 | 1999-06-18 | Centre Nat Rech Scient | Preparation de recepteurs membranaires a partir de baculovirus extracellulaires |
| AU7132798A (en) | 1997-04-17 | 1998-11-11 | Amgen, Inc. | Compositions comprising conjugates of stable, active, human ob protein with antibody fc chain and methods |
| ES2246069T3 (es) | 1997-05-02 | 2006-02-01 | Genentech, Inc. | Procedimiento de preparacion de anticuerpos multiespecificos que tienen componentes comunes y multimericos. |
| US5980893A (en) | 1997-07-17 | 1999-11-09 | Beth Israel Deaconess Medical Center, Inc. | Agonist murine monoclonal antibody as a stimulant for megakaryocytopoiesis |
| US20020187150A1 (en) * | 1997-08-15 | 2002-12-12 | Chugai Seiyaku Kabushiki Kaisha | Preventive and/or therapeutic agent for systemic lupus erythematosus comprising anti-IL-6 receptor antibody as an active ingredient |
| AU747883B2 (en) | 1997-08-15 | 2002-05-30 | Chugai Seiyaku Kabushiki Kaisha | Preventives and/or remedies for systemic lupus erythematosus containing anti-IL-6 receptor antibody as the active ingredient |
| AU750453B2 (en) | 1997-10-03 | 2002-07-18 | Chugai Seiyaku Kabushiki Kaisha | Natural human antibody |
| US6458355B1 (en) | 1998-01-22 | 2002-10-01 | Genentech, Inc. | Methods of treating inflammatory disease with anti-IL-8 antibody fragment-polymer conjugates |
| US6723319B1 (en) * | 1998-03-17 | 2004-04-20 | Chugai Seiyaku Kabushiki Kaisha | Method of treating inflammatory intestinal diseases containing as the ingredient IL-6 receptors antibodies |
| CA2323757C (en) | 1998-04-02 | 2011-08-02 | Genentech, Inc. | Antibody variants and fragments thereof |
| EP1071700B1 (en) | 1998-04-20 | 2010-02-17 | GlycArt Biotechnology AG | Glycosylation engineering of antibodies for improving antibody-dependent cellular cytotoxicity |
| GB9809951D0 (en) | 1998-05-08 | 1998-07-08 | Univ Cambridge Tech | Binding molecules |
| EP1105427A2 (en) * | 1998-08-17 | 2001-06-13 | Abgenix, Inc. | Generation of modified molecules with increased serum half-lives |
| US6475718B2 (en) | 1998-09-08 | 2002-11-05 | Schering Aktiengesellschaft | Methods and compositions for modulating the interaction between the APJ receptor and the HIV virus |
| AU764211C (en) * | 1998-12-01 | 2006-03-30 | Abbvie Biotherapeutics Inc. | Humanized antibodies to gamma-interferon |
| JP2002534959A (ja) | 1998-12-08 | 2002-10-22 | バイオベーション リミテッド | 免疫原性タンパク質の改変方法 |
| HUP0104865A3 (en) | 1999-01-15 | 2004-07-28 | Genentech Inc | Polypeptide variants with altered effector function |
| US6737056B1 (en) | 1999-01-15 | 2004-05-18 | Genentech, Inc. | Polypeptide variants with altered effector function |
| US7183387B1 (en) | 1999-01-15 | 2007-02-27 | Genentech, Inc. | Polypeptide variants with altered effector function |
| AU2006225302B2 (en) | 1999-03-25 | 2010-08-12 | AbbVie Deutschland GmbH & Co. KG | Human antibodies that bind human IL-12 and methods for producing |
| EP2264166B1 (en) | 1999-04-09 | 2016-03-23 | Kyowa Hakko Kirin Co., Ltd. | Method for controlling the activity of immunologically functional molecule |
| AU4952400A (en) * | 1999-06-02 | 2000-12-28 | Chugai Research Institute For Molecular Medicine, Inc. | Novel hemopoietin receptor protein nr10 |
| US6331642B1 (en) | 1999-07-12 | 2001-12-18 | Hoffmann-La Roche Inc. | Vitamin D3 analogs |
| SK782002A3 (en) * | 1999-07-21 | 2003-08-05 | Lexigen Pharm Corp | FC fusion proteins for enhancing the immunogenicity of protein and peptide antigens |
| US20040058393A1 (en) | 2000-04-17 | 2004-03-25 | Naoshi Fukishima | Agonist antibodies |
| CZ20023913A3 (cs) | 2000-05-03 | 2003-09-17 | Munich Biotech Ag | Kationtová diagnostická, zobrazovací a terapeutická činidla spojená s aktivovanými cévními místy |
| KR20120053525A (ko) * | 2000-06-16 | 2012-05-25 | 캠브리지 안티바디 테크놀로지 리미티드 | 면역특이적으로 BLyS에 결합하는 항체 |
| AU2011244851A1 (en) | 2000-07-27 | 2011-11-24 | The John Hopkins University School Of Medicine | Promyostatin peptides and methods of using same |
| AU2002218166A1 (en) | 2000-09-08 | 2002-03-22 | Universitat Zurich | Collections of repeat proteins comprising repeat modules |
| HU231090B1 (hu) | 2000-10-06 | 2020-07-28 | Kyowa Kirin Co., Ltd. | Antitest-kompozíciót termelő sejt |
| ES2333775T3 (es) | 2000-10-10 | 2010-03-01 | Genentech, Inc. | Inhibicion de la activacion del complemento c5 para el tratamiento y la prevencion de rechazo de xenoinjerto retrasado o rechazo vascular agudo. |
| WO2002032925A2 (en) | 2000-10-16 | 2002-04-25 | Phylos, Inc. | Protein scaffolds for antibody mimics and other binding proteins |
| CA2426679C (en) | 2000-10-25 | 2012-11-20 | Chugai Seiyaku Kabushiki Kaisha | Preventive or therapeutic agent for psoriasis comprising il-6 antagonist as active ingredient |
| AU2000279625A1 (en) * | 2000-10-27 | 2002-05-15 | Chugai Seiyaku Kabushiki Kaisha | Blood mmp-3 level-lowering agent containing il-6 antgonist as the active ingredient |
| AU2002248184C1 (en) | 2000-12-12 | 2018-01-04 | Board Of Regents, The University Of Texas System | Molecules with extended half-lives, compositions and uses thereof |
| US7754208B2 (en) | 2001-01-17 | 2010-07-13 | Trubion Pharmaceuticals, Inc. | Binding domain-immunoglobulin fusion proteins |
| CA2442801A1 (en) | 2001-04-02 | 2002-10-10 | Idec Pharmaceutical Corporation | Recombinant antibodies coexpressed with gntiii |
| UA80091C2 (en) | 2001-04-02 | 2007-08-27 | Chugai Pharmaceutical Co Ltd | Remedies for infant chronic arthritis-relating diseases and still's disease which contain an interleukin-6 (il-6) antagonist |
| ES2347532T3 (es) * | 2001-04-13 | 2010-11-02 | Biogen Idec Ma Inc. | Anticuerpos contra vla-1. |
| US7667004B2 (en) | 2001-04-17 | 2010-02-23 | Abmaxis, Inc. | Humanized antibodies against vascular endothelial growth factor |
| US20030157561A1 (en) | 2001-11-19 | 2003-08-21 | Kolkman Joost A. | Combinatorial libraries of monomer domains |
| ES2353335T3 (es) | 2001-06-22 | 2011-03-01 | Chugai Seiyaku Kabushiki Kaisha | Inhibidores del crecimiento celular que contienen anticuerpo anti-glipicano 3. |
| WO2003002609A2 (en) | 2001-06-28 | 2003-01-09 | Domantis Limited | Dual-specific ligand and its use |
| US20040161741A1 (en) | 2001-06-30 | 2004-08-19 | Elazar Rabani | Novel compositions and processes for analyte detection, quantification and amplification |
| WO2003015819A1 (en) | 2001-08-17 | 2003-02-27 | Tanox, Inc. | Complement pathway inhibitors binding to c5 and c5a without preventing formation of c5b |
| US7320789B2 (en) | 2001-09-26 | 2008-01-22 | Wyeth | Antibody inhibitors of GDF-8 and uses thereof |
| US20030190705A1 (en) | 2001-10-29 | 2003-10-09 | Sunol Molecular Corporation | Method of humanizing immune system molecules |
| CA2467719C (en) | 2001-11-14 | 2015-03-17 | Jill Giles-Komar | Anti-il-6 antibodies, compositions, methods and uses |
| US7771951B2 (en) | 2001-12-03 | 2010-08-10 | Amgen Fremont Inc. | Antibody categorization based on binding characteristics |
| AU2002362197A1 (en) | 2001-12-28 | 2003-07-24 | Chugai Seiyaku Kabushiki Kaisha | Method of stabilizing protein |
| CN100575482C (zh) | 2002-01-18 | 2009-12-30 | 津莫吉尼蒂克斯公司 | 新的细胞因子zcytor17配体 |
| WO2004003140A2 (en) * | 2002-01-18 | 2004-01-08 | Zymogenetics, Inc. | Cytokine receptor zcytor17 multimers |
| BR0307548A (pt) | 2002-02-11 | 2006-01-17 | Genentech Inc | Método de produção de uma variante de anticorpo, variante de anticorpo, composição, ácido nucléico isolado, vetor, célula hospedeira, processo para a produção de uma variante de anticorpo e método de determinação do coeficiente de associação de antìgeno de um anticorpo |
| AR038568A1 (es) | 2002-02-20 | 2005-01-19 | Hoffmann La Roche | Anticuerpos anti-a beta y su uso |
| US20040110226A1 (en) | 2002-03-01 | 2004-06-10 | Xencor | Antibody optimization |
| US8188231B2 (en) | 2002-09-27 | 2012-05-29 | Xencor, Inc. | Optimized FC variants |
| US20040132101A1 (en) | 2002-09-27 | 2004-07-08 | Xencor | Optimized Fc variants and methods for their generation |
| US8093357B2 (en) | 2002-03-01 | 2012-01-10 | Xencor, Inc. | Optimized Fc variants and methods for their generation |
| US7317091B2 (en) | 2002-03-01 | 2008-01-08 | Xencor, Inc. | Optimized Fc variants |
| EP1509770B1 (en) | 2002-05-31 | 2014-07-09 | GE Healthcare Bio-Sciences AB | Method of coupling binding agents to a substrate surface |
| US20050130224A1 (en) * | 2002-05-31 | 2005-06-16 | Celestar Lexico- Sciences, Inc. | Interaction predicting device |
| EP1511861A4 (en) * | 2002-06-12 | 2007-12-05 | Genencor Int | METHODS AND BINDING COMPOSITIONS DEPENDENT FROM THE MEDIUM OF A TARGET AGENT TO A TARGET |
| EP2107116A3 (en) * | 2002-06-12 | 2009-12-09 | Genencor International, Inc. | Methods for improving a binding characteristic of a molecule |
| ITMI20021527A1 (it) | 2002-07-11 | 2004-01-12 | Consiglio Nazionale Ricerche | Anticorpi anti componente c5 del complemento e loro uso |
| EP1382969A1 (en) | 2002-07-17 | 2004-01-21 | Max-Planck-Gesellschaft zur Förderung der Wissenschaften e.V. | Diagnosis and prevention of cancer cell invasion |
| DE60331778D1 (de) | 2002-09-16 | 2010-04-29 | Univ Johns Hopkins | Metalloproteaseaktivierung von myostatin und verfahren zur modulation der myostatinaktivität |
| SI2345671T1 (sl) | 2002-09-27 | 2016-03-31 | Xencor Inc. | Optimizirane Fc-variante in postopki za njihovo izdelavo |
| WO2004035752A2 (en) | 2002-10-15 | 2004-04-29 | Protein Design Labs, Inc. | ALTERATION OF FcRn BINDING AFFINITIES OR SERUM HALF-LIVES OF ANTIBODIES BY MUTAGENESIS |
| US7217797B2 (en) | 2002-10-15 | 2007-05-15 | Pdl Biopharma, Inc. | Alteration of FcRn binding affinities or serum half-lives of antibodies by mutagenesis |
| US7361740B2 (en) | 2002-10-15 | 2008-04-22 | Pdl Biopharma, Inc. | Alteration of FcRn binding affinities or serum half-lives of antibodies by mutagenesis |
| US7335743B2 (en) * | 2002-10-16 | 2008-02-26 | Amgen Inc. | Human anti-IFN-γ neutralizing antibodies as selective IFN-γ pathway inhibitors |
| US7261893B2 (en) | 2002-10-22 | 2007-08-28 | Wyeth | Neutralizing antibodies against GDF-8 and uses therefor |
| EP1590364B1 (en) | 2002-12-16 | 2011-10-05 | Genmab A/S | Human monoclonal antibodies against interleukin 8 (il-8) |
| CA2511910A1 (en) | 2002-12-27 | 2004-07-15 | Domantis Limited | Dual specific single domain antibodies specific for a ligand and for the receptor of the ligand |
| US20040223970A1 (en) * | 2003-02-28 | 2004-11-11 | Daniel Afar | Antibodies against SLC15A2 and uses thereof |
| KR20060026004A (ko) | 2003-02-28 | 2006-03-22 | 안티제닉스 아이엔씨 | 당단백질 및 항원성 분자의 올리고머화를 조장하는 렉틴의용도 |
| PT1601697E (pt) | 2003-02-28 | 2007-09-04 | Lonza Biologics Plc | Purificação de anticorpos através de proteína a e cromatografia de troca iónica. |
| US8388955B2 (en) | 2003-03-03 | 2013-03-05 | Xencor, Inc. | Fc variants |
| ES2527414T3 (es) | 2003-03-04 | 2015-01-23 | Alexion Pharmaceuticals, Inc. | Método para el tratamiento de una enfermedad autoinmune mediante la inducción de la presentación de antígeno mediante células presentadoras de antígeno que inducen tolerancia |
| DE602004028347D1 (de) | 2003-03-24 | 2010-09-09 | Zymogenetics Inc | Anti-il-22ra antikörper und bindungspartner und verwendungsmethoden bei entzündung |
| GB2401040A (en) | 2003-04-28 | 2004-11-03 | Chugai Pharmaceutical Co Ltd | Method for treating interleukin-6 related diseases |
| US9051373B2 (en) | 2003-05-02 | 2015-06-09 | Xencor, Inc. | Optimized Fc variants |
| JP5110877B2 (ja) | 2003-06-02 | 2012-12-26 | ワイス・エルエルシー | 神経筋障害を処置するための、コルチコステロイドと組み合わせたミオスタチン(gdf8)インヒビターの使用 |
| JP2005004970A (ja) | 2003-06-09 | 2005-01-06 | Hitachi Cable Ltd | 複合ケーブルおよびこれを用いた先行配線システム |
| EP1636264A2 (en) | 2003-06-24 | 2006-03-22 | MERCK PATENT GmbH | Tumour necrosis factor receptor molecules with reduced immunogenicity |
| US7011924B2 (en) * | 2003-07-30 | 2006-03-14 | Hynix Semiconductor Inc. | Photoresist polymers and photoresist compositions comprising the same |
| WO2005023193A2 (en) | 2003-09-04 | 2005-03-17 | Interleukin Genetics, Inc. | Methods of treating endometriosis |
| AU2004273791A1 (en) * | 2003-09-05 | 2005-03-31 | Genentech, Inc. | Antibodies with altered effector functions |
| US8101720B2 (en) | 2004-10-21 | 2012-01-24 | Xencor, Inc. | Immunoglobulin insertions, deletions and substitutions |
| WO2005035753A1 (ja) | 2003-10-10 | 2005-04-21 | Chugai Seiyaku Kabushiki Kaisha | 機能蛋白質を代替する二重特異性抗体 |
| US20080075712A1 (en) * | 2003-10-14 | 2008-03-27 | Kunihiro Hattori | Double Specific Antibodies Substituting For Functional Proteins |
| JP2007531707A (ja) | 2003-10-15 | 2007-11-08 | ピーディーエル バイオファーマ, インコーポレイテッド | IGの重鎖定常領域の位置250、314および/または428の変異誘発によるFc融合タンパク質血清半減期の改変 |
| MY149856A (en) | 2003-10-17 | 2013-10-31 | Chugai Pharmaceutical Co Ltd | Therapeutic agent for mesothelioma |
| AU2004284090A1 (en) | 2003-10-24 | 2005-05-06 | Avidia, Inc. | LDL receptor class A and EGF domain monomers and multimers |
| HRP20070196T3 (hr) * | 2003-11-05 | 2007-06-30 | Ares Trading S.A. | Postupak za pročišćavanje il-18 vezivnog proteina |
| US20050100965A1 (en) | 2003-11-12 | 2005-05-12 | Tariq Ghayur | IL-18 binding proteins |
| JP2008504002A (ja) | 2003-11-12 | 2008-02-14 | バイオジェン・アイデック・エムエイ・インコーポレイテッド | 新生児Fcレセプター(FcRn)結合ポリペプチド改変体、ダイマーFc結合タンパク質、およびそれらに関連する方法 |
| EP1701979A2 (en) | 2003-12-03 | 2006-09-20 | Xencor, Inc. | Optimized antibodies that target the epidermal growth factor receptor |
| CA2548817A1 (en) | 2003-12-04 | 2005-06-23 | Xencor, Inc. | Methods of generating variant proteins with increased host string content and compositions thereof |
| ES2388435T3 (es) * | 2003-12-10 | 2012-10-15 | Medarex, Inc. | Anticuerpos de IP-10 y sus usos |
| AR048210A1 (es) | 2003-12-19 | 2006-04-12 | Chugai Pharmaceutical Co Ltd | Un agente preventivo para la vasculitis. |
| US20050249723A1 (en) | 2003-12-22 | 2005-11-10 | Xencor, Inc. | Fc polypeptides with novel Fc ligand binding sites |
| US7371726B2 (en) | 2003-12-31 | 2008-05-13 | Schering-Plough Animal Health Corporation | Neutralizing GDF8 epitope-based growth enhancing vaccine |
| PT1706424E (pt) | 2004-01-12 | 2009-10-01 | Applied Molecular Evolution | Variantes da região fc |
| US20070116710A1 (en) | 2004-02-03 | 2007-05-24 | Leonard Bell | Methods of treating hemolytic anemia |
| US20050169921A1 (en) | 2004-02-03 | 2005-08-04 | Leonard Bell | Method of treating hemolytic disease |
| EP1715891B2 (en) | 2004-02-11 | 2014-08-13 | Warner-Lambert Company LLC | Methods of treating osteoarthritis with anti-il-6 antibodies |
| BRPI0508716A (pt) | 2004-03-23 | 2007-08-07 | Lilly Co Eli | anticorpo monoclonal, processo para produzir o mesmo, composição farmacêutica, e, uso de um anticorpo monoclonal |
| EP1728801A4 (en) | 2004-03-24 | 2009-10-21 | Chugai Pharmaceutical Co Ltd | SUBTYP OF A HUMANIZED ANTIBODY AGAINST THE INTERLEUKIN-6 RECEPTOR |
| AR048335A1 (es) | 2004-03-24 | 2006-04-19 | Chugai Pharmaceutical Co Ltd | Agentes terapeuticos para trastornos del oido interno que contienen un antagonista de il- 6 como un ingrediente activo |
| KR20070035482A (ko) | 2004-03-24 | 2007-03-30 | 추가이 세이야쿠 가부시키가이샤 | 인터로킨-6 안타고니스트를 활성성분으로 함유하는내이장해 치료제 |
| EP1737890A2 (en) * | 2004-03-24 | 2007-01-03 | Xencor, Inc. | Immunoglobulin variants outside the fc region |
| US20050260711A1 (en) * | 2004-03-30 | 2005-11-24 | Deepshikha Datta | Modulating pH-sensitive binding using non-natural amino acids |
| WO2005123780A2 (en) | 2004-04-09 | 2005-12-29 | Protein Design Labs, Inc. | Alteration of fcrn binding affinities or serum half-lives of antibodies by mutagenesis |
| SG173322A1 (en) | 2004-04-16 | 2011-08-29 | Macrogenics Inc Dw Us | Fc gammad riib - specific antibodies and methods of use thereof |
| US7632924B2 (en) * | 2004-06-18 | 2009-12-15 | Ambrx, Inc. | Antigen-binding polypeptides and their uses |
| CA2572133A1 (en) * | 2004-06-25 | 2006-01-12 | Medimmune, Inc. | Increasing the production of recombinant antibodies in mammalian cells by site-directed mutagenesis |
| DE102004032634A1 (de) | 2004-07-06 | 2006-02-16 | Sms Demag Ag | Verfahren und Einrichtung zum Messen und Regeln der Planheit und/oder der Bandspannungen eines Edelstahlbandes oder einer Edelstahlfolie beim Kaltwalzen in einem Vielwalzengerüst, insbesondere in einem 20-Walzen-Sendizimir-Walzwerk |
| WO2006023144A2 (en) | 2004-07-06 | 2006-03-02 | Bioren Inc. | Look-through mutagenesis for developing altered polypeptides with enhanced properties |
| WO2006085967A2 (en) | 2004-07-09 | 2006-08-17 | Xencor, Inc. | OPTIMIZED ANTI-CD20 MONOCONAL ANTIBODIES HAVING Fc VARIANTS |
| AU2005272993B2 (en) | 2004-07-15 | 2010-02-11 | Xencor, Inc. | Optimized Fc variants |
| BRPI0513706A (pt) * | 2004-07-20 | 2008-05-13 | Symphogen As | anticorpo policlonal recombinante anti-rhesus d e métodos de produção |
| PL2213683T3 (pl) | 2004-08-04 | 2013-10-31 | Mentrik Biotech Llc | WARIANTY REGIONÓW Fc |
| EP1778726A4 (en) | 2004-08-16 | 2009-03-18 | Medimmune Inc | INTEGRIN ANTAGONISTS WITH IMPROVED ANTIBODY-DEPENDENT CELL-ASSAYED CYTOTOXICITY ACTIVITY |
| EP1778728A2 (en) | 2004-08-19 | 2007-05-02 | Genentech, Inc. | Polypeptide variants with altered effector function |
| WO2006047350A2 (en) | 2004-10-21 | 2006-05-04 | Xencor, Inc. | IgG IMMUNOGLOBULIN VARIANTS WITH OPTIMIZED EFFECTOR FUNCTION |
| CN102731654A (zh) | 2004-10-22 | 2012-10-17 | 米迪缪尼有限公司 | 抗hmgb1的高亲和力抗体及其用法 |
| AU2005299716B2 (en) * | 2004-10-22 | 2012-09-06 | Amgen Inc. | Methods for refolding of recombinant antibodies |
| US20060115485A1 (en) | 2004-10-29 | 2006-06-01 | Medimmune, Inc. | Methods of preventing and treating RSV infections and related conditions |
| US7632497B2 (en) | 2004-11-10 | 2009-12-15 | Macrogenics, Inc. | Engineering Fc Antibody regions to confer effector function |
| US20070135620A1 (en) | 2004-11-12 | 2007-06-14 | Xencor, Inc. | Fc variants with altered binding to FcRn |
| RU2412200C2 (ru) | 2004-11-12 | 2011-02-20 | Ксенкор, Инк. | Fc-ВАРИАНТЫ С ИЗМЕНЕННЫМ СВЯЗЫВАНИЕМ С FcRn |
| EP2332985A3 (en) | 2004-11-12 | 2012-01-25 | Xencor, Inc. | Fc variants with altered binding to FcRn |
| US8802820B2 (en) | 2004-11-12 | 2014-08-12 | Xencor, Inc. | Fc variants with altered binding to FcRn |
| US8367805B2 (en) | 2004-11-12 | 2013-02-05 | Xencor, Inc. | Fc variants with altered binding to FcRn |
| US8329186B2 (en) | 2004-12-20 | 2012-12-11 | Isu Abxis Co., Ltd | Treatment of inflammation using BST2 inhibitor |
| EP1829961A4 (en) * | 2004-12-22 | 2008-06-04 | Chugai Pharmaceutical Co Ltd | METHOD FOR THE PRODUCTION OF AN ANTIBODY USING A CELL WITH HARDENED FUCOSET TRANSPORT FUNCTION |
| BRPI0519399A2 (pt) | 2004-12-23 | 2009-01-20 | Novo Nordisk As | material de suporte sàlido e mÉtodo para isolamento de anticorpos ou derivados destes |
| US20090087478A1 (en) | 2004-12-27 | 2009-04-02 | Progenics Pharmaceuticals (Nevada), Inc. | Orally Deliverable and Anti-Toxin Antibodies and Methods for Making and Using Them |
| KR101564713B1 (ko) | 2004-12-28 | 2015-11-06 | 이나뜨 파르마 | Nkg2a에 대한 단클론 항체 |
| WO2006076594A2 (en) | 2005-01-12 | 2006-07-20 | Xencor, Inc. | Antibodies and fc fusion proteins with altered immunogenicity |
| GB0502358D0 (en) | 2005-02-04 | 2005-03-16 | Novartis Ag | Organic compounds |
| NZ538097A (en) | 2005-02-07 | 2006-07-28 | Ovita Ltd | Method and compositions for improving wound healing |
| CA2594490A1 (en) * | 2005-02-14 | 2006-08-24 | Zymogenetics Inc. | Methods of treating skin disorders using an il-31ra antagonist |
| EP1869192B1 (en) | 2005-03-18 | 2016-01-20 | MedImmune, LLC | Framework-shuffling of antibodies |
| CA2602663A1 (en) | 2005-03-31 | 2006-10-05 | Xencor, Inc. | Fc variants with optimized properties |
| EP1870458B1 (en) | 2005-03-31 | 2018-05-09 | Chugai Seiyaku Kabushiki Kaisha | sc(Fv)2 STRUCTURAL ISOMERS |
| TWI544076B (zh) | 2005-03-31 | 2016-08-01 | 中外製藥股份有限公司 | A method of manufacturing a polypeptide that controls assembly |
| ES2494921T3 (es) | 2005-04-08 | 2014-09-16 | Chugai Seiyaku Kabushiki Kaisha | Anticuerpo que sustituye la función del factor VIII de coagulación sanguínea |
| EA017420B9 (ru) * | 2005-04-18 | 2013-03-29 | Микромет Аг | Антитела-нейтрализаторы гранулоцитарно-макрофагального колониестимулирующего фактора человека |
| WO2006113643A2 (en) | 2005-04-20 | 2006-10-26 | Amgen Fremont Inc. | High affinity fully human monoclonal antibodies to interleukin-8 and epitopes for such antibodies |
| BRPI0610248A2 (pt) | 2005-04-25 | 2010-06-08 | Pfizer | anticorpos contra miostatina, composição farmacêutica compreendendo os mesmos, linhas celulares que os produzem , moléculas de ácido nucleico codificantes dos mesmos bem como seus usos |
| WO2006116260A2 (en) | 2005-04-26 | 2006-11-02 | Medimmune, Inc. | Modulation of antibody effector function by hinge domain engineering |
| PE20061323A1 (es) | 2005-04-29 | 2007-02-09 | Rinat Neuroscience Corp | Anticuerpos dirigidos contra el peptido amiloide beta y metodos que utilizan los mismos |
| PA8672101A1 (es) | 2005-04-29 | 2006-12-07 | Centocor Inc | Anticuerpos anti-il-6, composiciones, métodos y usos |
| US8003108B2 (en) | 2005-05-03 | 2011-08-23 | Amgen Inc. | Sclerostin epitopes |
| US7592429B2 (en) | 2005-05-03 | 2009-09-22 | Ucb Sa | Sclerostin-binding antibody |
| EP1896503B1 (en) | 2005-05-31 | 2014-10-29 | Board of Regents, The University of Texas System | IgG1 ANTIBODIES WITH MUTATED Fc PORTION FOR INCREASED BINDING TO FcRn RECEPTOR AND USES TEHEREOF |
| CA2610987C (en) * | 2005-06-10 | 2013-09-10 | Chugai Seiyaku Kabushiki Kaisha | Stabilizer for protein preparation comprising meglumine and use thereof |
| US7557190B2 (en) | 2005-07-08 | 2009-07-07 | Xencor, Inc. | Optimized proteins that target Ep-CAM |
| SG155912A1 (en) | 2005-07-25 | 2009-10-29 | Trubion Pharmaceuticals Inc | B-cell reduction using cd37-specific and cd20-specific binding molecules |
| SI2573114T1 (sl) | 2005-08-10 | 2016-08-31 | Macrogenics, Inc. | Identifikacija in inženiring protiteles z variantnimi fc regijami in postopki za njih uporabo |
| EP3327033A1 (en) | 2005-08-19 | 2018-05-30 | Wyeth LLC | Antagonist antibodies against gdf-8 and uses in treatment of als and other gdf-8-associated disorders |
| CA2624189A1 (en) | 2005-10-03 | 2007-04-12 | Xencor, Inc. | Fc variants with optimized fc receptor binding properties |
| AU2006302254B2 (en) | 2005-10-06 | 2011-05-26 | Xencor, Inc. | Optimized anti-CD30 antibodies |
| JP5052517B2 (ja) | 2005-10-06 | 2012-10-17 | イーライ リリー アンド カンパニー | 抗ミオスタチン抗体 |
| UA92504C2 (en) | 2005-10-12 | 2010-11-10 | Эли Лилли Энд Компани | Anti-myostatin monoclonal antibody |
| US8470316B2 (en) | 2005-10-14 | 2013-06-25 | Chugai Seiyaku Kabushiki Kaisha | Agents for suppressing damage to transplanted islets after islet transplantation |
| US8945558B2 (en) | 2005-10-21 | 2015-02-03 | Chugai Seiyaku Kabushiki Kaisha | Methods for treating myocardial infarction comprising administering an IL-6 inhibitor |
| EP2465870A1 (en) * | 2005-11-07 | 2012-06-20 | Genentech, Inc. | Binding polypeptides with diversified and consensus VH/VL hypervariable sequences |
| AR057582A1 (es) | 2005-11-15 | 2007-12-05 | Nat Hospital Organization | Agentes para suprimir la induccion de linfocitos t citotoxicos |
| AR057579A1 (es) | 2005-11-23 | 2007-12-05 | Merck & Co Inc | Compuestos espirociclicos como inhibidores de histona de acetilasa (hdac) |
| WO2007060411A1 (en) | 2005-11-24 | 2007-05-31 | Ucb Pharma S.A. | Anti-tnf alpha antibodies which selectively inhibit tnf alpha signalling through the p55r |
| TW200803894A (en) | 2005-11-25 | 2008-01-16 | Univ Keio | Prostate cancer therapeutic agents |
| US20080311122A1 (en) | 2005-11-28 | 2008-12-18 | Medimmune, Llc | Antagonists of Hmgb1 and/or Rage and Methods of Use Thereof |
| WO2007059782A1 (en) | 2005-11-28 | 2007-05-31 | Genmab A/S | Recombinant monovalent antibodies and methods for production thereof |
| ES2407429T3 (es) | 2005-12-12 | 2013-06-12 | Ac Immune S.A. | Vacuna terapéurica |
| US9084777B2 (en) * | 2005-12-28 | 2015-07-21 | Chugai Seiyaku Kabushiki Kaisha | Stabilized antibody-containing formulations |
| EP2548577B1 (en) | 2005-12-29 | 2017-02-15 | Janssen Biotech, Inc. | Human anti-il-23 antibodies, compositions, methods and uses |
| EP2001906A2 (en) | 2006-01-10 | 2008-12-17 | Zymogenetics, Inc. | Methods of treating pain and inflammation in neuronal tissue using il-31ra and osmrb antagonists |
| US8771686B2 (en) | 2006-01-27 | 2014-07-08 | Chugai Seiyaku Kabushiki Kaisha | Methods for treating a disease involving choroidal neovascularization by administering an IL-6 receptor antibody |
| CA2638811A1 (en) | 2006-02-03 | 2007-08-16 | Medimmune, Llc | Protein formulations |
| US20070190056A1 (en) | 2006-02-07 | 2007-08-16 | Ravi Kambadur | Muscle regeneration compositions and uses therefor |
| JP4179517B2 (ja) | 2006-02-21 | 2008-11-12 | プロテノバ株式会社 | イムノグロブリン親和性リガンド |
| WO2007097361A1 (ja) | 2006-02-21 | 2007-08-30 | Protenova Co., Ltd. | イムノグロブリン親和性リガンド |
| BRPI0708424A2 (pt) | 2006-03-02 | 2011-05-31 | Alexion Pharma Inc | prolongamento da sobreviência de uma aloenxerto por inibição da atividade do complemento |
| RU2477137C2 (ru) | 2006-03-08 | 2013-03-10 | АРКЕМИКС Эл Эл Си | Связывающие комплемент аптамеры и средства против с5, пригодные для лечения глазных нарушений |
| PL3167888T3 (pl) | 2006-03-15 | 2024-08-26 | Alexion Pharmaceuticals, Inc. | Leczenie pacjentów z napadową nocną hemoglobinurią za pomocą inhibitora dopełniacza |
| CA2646508A1 (en) | 2006-03-17 | 2007-09-27 | Biogen Idec Ma Inc. | Stabilized polypeptide compositions |
| JP4294082B2 (ja) | 2006-03-23 | 2009-07-08 | 協和発酵キリン株式会社 | ヒトトロンボポエチン受容体に対するアゴニスト抗体 |
| AU2007245164A1 (en) | 2006-03-28 | 2007-11-08 | Biogen Idec Ma Inc. | Anti-IGF-IR antibodies and uses thereof |
| CA2647846C (en) | 2006-03-31 | 2016-06-21 | Chugai Seiyaku Kabushiki Kaisha | Methods for controlling blood pharmacokinetics of antibodies |
| JP5144499B2 (ja) | 2006-03-31 | 2013-02-13 | 中外製薬株式会社 | 二重特異性抗体を精製するための抗体改変方法 |
| EP2004689A4 (en) | 2006-04-05 | 2010-06-02 | Abbott Biotech Ltd | PURIFICATION OF ANTIBODIES |
| EP2025346B1 (en) * | 2006-04-07 | 2016-08-10 | Osaka University | Muscle regeneration promoter |
| TWI395754B (zh) | 2006-04-24 | 2013-05-11 | Amgen Inc | 人類化之c-kit抗體 |
| KR101416078B1 (ko) | 2006-05-25 | 2014-07-07 | 글락소 그룹 리미티드 | 변형된 인간화 항인터루킨18 항체 |
| US8080248B2 (en) | 2006-06-02 | 2011-12-20 | Regeneron Pharmaceuticals, Inc. | Method of treating rheumatoid arthritis with an IL-6R antibody |
| DK2374818T3 (da) | 2006-06-02 | 2013-01-21 | Regeneron Pharma | Højaffinitetsantistoffer mod human IL-6-receptor |
| CN103272232B (zh) | 2006-06-08 | 2018-07-24 | 中外制药株式会社 | 炎性疾病的预防或治疗药 |
| ES2415655T3 (es) * | 2006-06-15 | 2013-07-26 | The Board Of Trustees Of The University Of Arkansas | Anticuerpos monoclonales que reconocen selectivamente Metanfetamina y compuestos similares a Metanfetamina |
| CL2007001829A1 (es) | 2006-06-23 | 2008-01-25 | Smithkline Beecham Corp | P-toluensulfonato de n-[4-cloro-2-hidroxi-3-(piperazina-1-sulfonil)fenil]-n-(2-cloro-3-fluorofenil)urea;procedimiento de preparacion;composicion farmaceutica;combinacion farmaceutica;y uso en el tratamiento de una enfermedad mediada por la quiimioquina il-8, tales como asma y epoc. |
| AR062223A1 (es) | 2006-08-09 | 2008-10-22 | Glycart Biotechnology Ag | Moleculas de adhesion al antigeno que se adhieren a egfr, vectores que los codifican, y sus usos de estas |
| SI2383297T1 (sl) | 2006-08-14 | 2013-06-28 | Xencor Inc. | Optimizirana antitelesa, ki ciljajo cd19 |
| DE102006038844B4 (de) | 2006-08-18 | 2018-03-22 | Robert Bosch Gmbh | Vorrichtung und Verfahren zur Ansteuerung von Personenschutzmittel |
| PT2066695E (pt) | 2006-09-05 | 2013-05-23 | Lilly Co Eli | Anticorpos anti-miostatina |
| CN103694349A (zh) | 2006-09-08 | 2014-04-02 | 米迪缪尼有限公司 | 人源化抗cd19抗体及其在治疗癌症、移植病和自身免疫病中的应用 |
| WO2008036688A2 (en) | 2006-09-18 | 2008-03-27 | Xencor, Inc. | Optimized antibodies that target hm1.24 |
| JP2008104147A (ja) | 2006-09-19 | 2008-05-01 | Ricoh Co Ltd | 撮像装置、撮像システム、画像データ処理方法およびプログラム |
| AU2007319576B2 (en) | 2006-10-06 | 2014-01-16 | The Government Of The United States Of America As Represented By The Secretary Of The Department Of Health And Human Services | Prevention of tissue ischemia, related methods and compositions |
| US20100034194A1 (en) | 2006-10-11 | 2010-02-11 | Siemens Communications Inc. | Eliminating unreachable subscribers in voice-over-ip networks |
| WO2008121160A2 (en) | 2006-11-21 | 2008-10-09 | Xencor, Inc. | Optimized antibodies that target cd5 |
| CN100455598C (zh) | 2006-11-29 | 2009-01-28 | 中国抗体制药有限公司 | 功能人源化抗人cd20抗体及其应用 |
| WO2008091798A2 (en) | 2007-01-22 | 2008-07-31 | Xencor, Inc. | Optimized ca9 antibodies and methods of using the same |
| US9725514B2 (en) | 2007-01-23 | 2017-08-08 | Shinshu University | Chronic rejection inhibitor |
| WO2008091954A2 (en) | 2007-01-23 | 2008-07-31 | Xencor, Inc. | Optimized cd40 antibodies and methods of using the same |
| WO2008090960A1 (ja) | 2007-01-24 | 2008-07-31 | Kyowa Hakko Kirin Co., Ltd. | ガングリオシドgm2に特異的に結合する遺伝子組換え抗体組成物 |
| WO2008092117A2 (en) | 2007-01-25 | 2008-07-31 | Xencor, Inc. | Immunoglobulins with modifications in the fcr binding region |
| WO2008098115A2 (en) | 2007-02-07 | 2008-08-14 | Xencor, Inc. | Optimized igf-1r antibodies and methods of using the same |
| WO2008100995A1 (en) * | 2007-02-14 | 2008-08-21 | Vaccinex, Inc. | Humanized anti-cd100 antibodies |
| AR065420A1 (es) | 2007-02-23 | 2009-06-03 | Schering Corp | Anticuerpos anti-il-23 p19 de ingenieria |
| NZ578870A (en) | 2007-03-20 | 2012-01-12 | Lilly Co Eli | Anti-sclerostin antibodies |
| CN101679486A (zh) | 2007-03-22 | 2010-03-24 | 诺瓦提斯公司 | C5抗原及其用途 |
| CL2008001071A1 (es) | 2007-04-17 | 2009-05-22 | Smithkline Beecham Corp | Metodo para obtener anticuerpo penta-especifico contra il-8/cxcl8, gro-alfa/cxcl1, gro-beta/cxcl2), gro-gama/cxcl3 y ena-78/cxcl5 humanas; anticuerpo penta-especifico; proceso de produccion del mismo; vector, hbridoma o celela que lo comprende; composicion farmceutica; uso para tratar copd, otras enfermedades. |
| GB0708002D0 (en) | 2007-04-25 | 2007-06-06 | Univ Sheffield | Antibodies |
| US20090252729A1 (en) | 2007-05-14 | 2009-10-08 | Farrington Graham K | Single-chain Fc (scFc) regions, binding polypeptides comprising same, and methods related thereto |
| LT2176298T (lt) | 2007-05-30 | 2018-04-10 | Xencor, Inc. | Būdai ir kompozicijos, skirti cd32b ekspresuojančių ląstelių slopinimui |
| EP2155790A1 (en) | 2007-05-31 | 2010-02-24 | Genmab A/S | Method for extending the half-life of exogenous or endogenous soluble molecules |
| CN111253484A (zh) | 2007-06-25 | 2020-06-09 | 艾斯巴技术-诺华有限责任公司 | 修饰抗体的方法和具有改善的功能性质的修饰抗体 |
| KR101530723B1 (ko) | 2007-06-25 | 2015-06-22 | 에스바테크 - 어 노바티스 컴파니 엘엘씨 | 단일 쇄 항체의 서열에 기초한 공학처리 및 최적화 |
| CN101796408B (zh) | 2007-06-29 | 2014-05-07 | 奎斯特诊断投资公司 | 用液相层析-质谱法分析体液内的氨基酸 |
| EP2174667B1 (en) | 2007-07-26 | 2017-01-04 | Osaka University | Agent for treatment of ophthalmia containing interleukin-6 receptor inhibitor as active ingredient |
| WO2009026117A2 (en) | 2007-08-16 | 2009-02-26 | Glaxo Group Limited | Novel compounds |
| US20090130105A1 (en) | 2007-08-28 | 2009-05-21 | Biogen Idec Ma Inc. | Compositions that bind multiple epitopes of igf-1r |
| US20090092614A1 (en) | 2007-08-28 | 2009-04-09 | Biogen Idec Ma Inc. | Anti-IGF-1R Antibodies and Uses Thereof |
| EP2031064A1 (de) | 2007-08-29 | 2009-03-04 | Boehringer Ingelheim Pharma GmbH & Co. KG | Verfahren zur Steigerung von Proteintitern |
| CL2008002775A1 (es) | 2007-09-17 | 2008-11-07 | Amgen Inc | Uso de un agente de unión a esclerostina para inhibir la resorción ósea. |
| PE20091205A1 (es) | 2007-09-26 | 2009-09-09 | Chugai Pharmaceutical Co Ltd | Anticuerpo anti-receptor de il-6 |
| SG193868A1 (en) | 2007-09-26 | 2013-10-30 | Chugai Pharmaceutical Co Ltd | Modified antibody constant region |
| RU2510400C9 (ru) | 2007-09-26 | 2014-07-20 | Чугаи Сейяку Кабусики Кайся | Способ модификации изоэлектрической точки антитела с помощью аминокислотных замен в cdr |
| WO2009041734A1 (ja) | 2007-09-26 | 2009-04-02 | Kyowa Hakko Kirin Co., Ltd. | ヒトトロンボポエチン受容体に対するアゴニスト抗体 |
| EP2617736A1 (en) | 2007-09-28 | 2013-07-24 | Chugai Seiyaku Kabushiki Kaisha | Anti-glypican 3 antibody having improved kinetics in plasma |
| KR101601986B1 (ko) | 2007-10-02 | 2016-03-17 | 추가이 세이야쿠 가부시키가이샤 | 인터류킨 6 수용체 저해제를 유효 성분으로 하는 이식편대숙주병 치료제 |
| KR100888133B1 (ko) | 2007-10-02 | 2009-03-13 | 에스케이에너지 주식회사 | 4종의 금속성분으로 구성된 다성분계 비스무스몰리브데이트 촉매 제조방법 및 상기촉매를 이용하여1,3-부타디엔을 제조하는 방법 |
| AR068767A1 (es) | 2007-10-12 | 2009-12-02 | Novartis Ag | Anticuerpos contra esclerostina, composiciones y metodos de uso de estos anticuerpos para tratar un trastorno patologico mediado por esclerostina |
| AU2008314687A1 (en) | 2007-10-22 | 2009-04-30 | Merck Serono S.A. | Method for purifying Fc-fusion proteins |
| PE20091163A1 (es) | 2007-11-01 | 2009-08-09 | Wyeth Corp | Anticuerpos para gdf8 |
| BRPI0820543A2 (pt) | 2007-11-15 | 2015-06-16 | Chugai Pharmaceutical Co Ltd | Anticorpo monoclonal capaz de ligar a anexelekto, e uso do mesmo |
| CN101939025B (zh) | 2007-12-05 | 2015-03-25 | 中外制药株式会社 | 搔痒症治疗药 |
| TWI548418B (zh) | 2007-12-05 | 2016-09-11 | 中外製藥股份有限公司 | Anti-NR10 / IL-31RA antibody and its use |
| CA2709354C (en) | 2007-12-21 | 2014-06-17 | Amgen Inc. | Anti-amyloid antibodies and uses thereof |
| DK2235059T3 (en) | 2007-12-26 | 2015-03-30 | Xencor Inc | FC-VERSIONS OF MODIFIED BINDING TO FcRn |
| WO2009089846A1 (en) | 2008-01-18 | 2009-07-23 | Stichting Sanquin Bloedvoorziening | Methods for increasing the therapeutic efficacy of immunoglobulin g class 3 (igg3) antibodies |
| WO2009095235A1 (en) | 2008-01-29 | 2009-08-06 | Ablynx N.V. | Methods to stabilize proteins and polypeptides |
| AU2015227424A1 (en) | 2008-04-11 | 2015-10-01 | Chugai Seiyaku Kabushiki Kaisha | Antigen-binding molecule capable of binding to two or more antigen molecules repeatedly |
| TW201920257A (zh) | 2008-04-11 | 2019-06-01 | 日商中外製藥股份有限公司 | 重複結合複數個抗原的抗原結合分子 |
| US9315577B2 (en) * | 2008-05-01 | 2016-04-19 | Amgen Inc. | Anti-hepcidin antibodies and methods of use |
| CA2723987C (en) | 2008-05-14 | 2019-06-11 | Agriculture Victoria Services Pty Ltd | Use of angiogenin or angiogenin agonists for treating diseases and disorders |
| TWI528973B (zh) | 2008-06-05 | 2016-04-11 | Chugai Pharmaceutical Co Ltd | Nerve infiltration inhibitor |
| PY09026846A (es) | 2008-08-05 | 2015-09-01 | Novartis Ag | Composiciones y métodos para anticuerpos que se dirigen a la proteína de complemento c5 |
| EP3190128B1 (en) | 2008-09-17 | 2018-11-14 | Xencor, Inc. | Compositions and methods for treating ige-mediated disorders |
| TWI440469B (zh) | 2008-09-26 | 2014-06-11 | Chugai Pharmaceutical Co Ltd | Improved antibody molecules |
| JP5229888B2 (ja) | 2008-09-30 | 2013-07-03 | 独立行政法人産業技術総合研究所 | 弱酸性域での易解離性を向上したプロテインa変異型タンパク質及び抗体捕捉剤 |
| KR101834999B1 (ko) | 2008-10-14 | 2018-03-06 | 제넨테크, 인크. | 이뮤노글로불린 변이체 및 그의 용도 |
| HUE061548T2 (hu) | 2008-11-10 | 2023-07-28 | Alexion Pharma Inc | Komplementtel összefüggõ rendellenességek kezelésére szolgáló eljárások és készítmények |
| WO2010058860A1 (ja) | 2008-11-18 | 2010-05-27 | 株式会社シノテスト | 試料中のc反応性蛋白質の測定方法及び測定試薬 |
| BRPI0921569A2 (pt) | 2008-11-25 | 2019-09-24 | Alder Biopharmaceuticals Inc | anticorpos para il-6 e uso dos mesmos |
| AR074777A1 (es) | 2008-12-19 | 2011-02-09 | Glaxo Group Ltd | Proteinas de union a antigeno |
| JP5851842B2 (ja) | 2009-01-12 | 2016-02-03 | サイトムエックス セラピューティクス, インク.CytomX Therapeutics, Inc. | 改変した抗体組成物、それを作製および使用する方法 |
| WO2010085682A2 (en) | 2009-01-23 | 2010-07-29 | Biogen Idec Ma Inc. | Stabilized fc polypeptides with reduced effector function and methods of use |
| US20100292443A1 (en) * | 2009-02-26 | 2010-11-18 | Sabbadini Roger A | Humanized platelet activating factor antibody design using anti-lipid antibody templates |
| WO2010107109A1 (ja) * | 2009-03-19 | 2010-09-23 | 中外製薬株式会社 | 抗体定常領域改変体 |
| SG174428A1 (en) | 2009-03-19 | 2011-10-28 | Chugai Pharmaceutical Co Ltd | Pharmaceutical formulation containing improved antibody molecules |
| JP5717624B2 (ja) * | 2009-03-19 | 2015-05-13 | 中外製薬株式会社 | 抗体定常領域改変体 |
| EP2233500A1 (en) | 2009-03-20 | 2010-09-29 | LFB Biotechnologies | Optimized Fc variants |
| TW201041595A (en) | 2009-05-15 | 2010-12-01 | Chugai Pharmaceutical Co Ltd | Anti-axl antibody |
| WO2010138610A2 (en) | 2009-05-26 | 2010-12-02 | The Johns Hopkins University | Novel desmin phosphorylation sites useful in diagnosis and intervention of cardiac disease |
| US8609097B2 (en) | 2009-06-10 | 2013-12-17 | Hoffmann-La Roche Inc. | Use of an anti-Tau pS422 antibody for the treatment of brain diseases |
| BRPI1012759A2 (pt) | 2009-06-23 | 2019-07-02 | Alexion Pharma Inc | anticorpos biespecíficos que se ligam as proteínas do complemento. |
| US8945511B2 (en) | 2009-06-25 | 2015-02-03 | Paul Weinberger | Sensitive methods for detecting the presence of cancer associated with the over-expression of galectin-3 using biomarkers derived from galectin-3 |
| RU2522002C2 (ru) | 2009-06-26 | 2014-07-10 | Ридженерон Фармасьютикалз, Инк. | Легковыделяемые биспецифические антитела с природным иммуноглобулиновым форматом |
| GB0914691D0 (en) | 2009-08-21 | 2009-09-30 | Lonza Biologics Plc | Immunoglobulin variants |
| US8709424B2 (en) | 2009-09-03 | 2014-04-29 | Merck Sharp & Dohme Corp. | Anti-GITR antibodies |
| WO2011037158A1 (ja) * | 2009-09-24 | 2011-03-31 | 中外製薬株式会社 | 抗体定常領域改変体 |
| MX338063B (es) | 2009-10-06 | 2016-04-01 | Medimmune Ltd | Molecula de union especifica al rsv. |
| US8568726B2 (en) | 2009-10-06 | 2013-10-29 | Medimmune Limited | RSV specific binding molecule |
| CA2776385C (en) | 2009-10-07 | 2019-04-09 | Macrogenics, Inc. | Fc region-containing polypeptides that exhibit improved effector function due to alterations of the extent of fucosylation, and methods for their use |
| CA2778673A1 (en) | 2009-10-27 | 2011-05-05 | Karen Margrete Miller | Function modifying nav 1.7 antibodies |
| CN101875696B (zh) | 2009-11-11 | 2012-02-08 | 中国人民解放军军事医学科学院生物工程研究所 | 一种抗体及其制备方法与应用 |
| EP2327725A1 (en) | 2009-11-26 | 2011-06-01 | InflaRx GmbH | Anti-C5a binding moieties with high blocking activity |
| AU329016S (en) | 2009-12-03 | 2009-12-22 | Non Entity 49398 | Induction system with integral air filter |
| PL2522724T3 (pl) | 2009-12-25 | 2020-07-13 | Chugai Seiyaku Kabushiki Kaisha | Sposób modyfikowania polipetydów do oczyszczania multimerów polipeptydowych |
| JP6101489B2 (ja) | 2010-01-28 | 2017-03-22 | アブ バイオサイエンシズ インコーポレイテッド | 親和性が低下した抗体およびそれを作製する方法 |
| CA2789416A1 (en) | 2010-02-09 | 2011-08-18 | Glaxosmithkline Llc | Novel uses |
| TW201127310A (en) * | 2010-02-11 | 2011-08-16 | jin-zhu Chen | Step-less finetuning buckle |
| SI2536745T1 (sl) | 2010-02-19 | 2016-10-28 | Xencor Inc. | Novi imunoadhezini CTLA4-Ig |
| ES2615732T3 (es) | 2010-03-01 | 2017-06-08 | Alexion Pharmaceuticals, Inc. | Composiciones para tratar la enfermedad de Degos |
| EP2543730B1 (en) | 2010-03-04 | 2018-10-31 | Chugai Seiyaku Kabushiki Kaisha | Antibody constant region variant |
| CN105218674A (zh) | 2010-03-11 | 2016-01-06 | 瑞纳神经科学公司 | 呈pH依赖性抗原结合的抗体 |
| JP2011184418A (ja) | 2010-03-11 | 2011-09-22 | Tokyo Institute Of Technology | 親和性可変抗体 |
| TW201206466A (en) | 2010-03-11 | 2012-02-16 | Rinat Neuroscience Corp | Antibodies with pH dependent antigen binding |
| TWI667346B (zh) | 2010-03-30 | 2019-08-01 | 中外製藥股份有限公司 | 促進抗原消失之具有經修飾的FcRn親和力之抗體 |
| WO2011137362A1 (en) | 2010-04-30 | 2011-11-03 | Rother Russell P | Antibodies having reduced immunogenicity in a human |
| JO3340B1 (ar) | 2010-05-26 | 2019-03-13 | Regeneron Pharma | مضادات حيوية لـعامل تمايز النمو 8 البشري |
| WO2011149046A1 (ja) | 2010-05-28 | 2011-12-01 | 独立行政法人国立がん研究センター | 膵癌治療剤 |
| UY33421A (es) | 2010-06-03 | 2011-12-30 | Glaxo Wellcome House | Proteinas de union al antígeno humanizados |
| US8637641B2 (en) | 2010-07-29 | 2014-01-28 | Xencor, Inc. | Antibodies with modified isoelectric points |
| SG10201506405YA (en) | 2010-08-16 | 2015-10-29 | Amgen Inc | Polypeptides That Bind Myostatin, Compositions And Methods |
| JP6121904B2 (ja) | 2010-09-08 | 2017-04-26 | ハロザイム インコーポレイテッド | 条件的活性治療用タンパク質を評価および同定する、または発展させる方法 |
| EP2640745B1 (en) | 2010-09-10 | 2018-11-07 | MedImmune Limited | Bivalent and bispecific anti-il6/anti-il23 antibodies |
| KR102116202B1 (ko) | 2010-11-08 | 2020-05-28 | 제넨테크, 인크. | 피하 투여용 항―il―6 수용체 항체 |
| SG10201509790YA (en) | 2010-11-30 | 2015-12-30 | Chugai Pharmaceutical Co Ltd | Antigen-Binding Molecule Capable Of Binding To Plurality Of Antigen Molecules Repeatedly |
| WO2012088247A2 (en) | 2010-12-22 | 2012-06-28 | Medimmune, Llc | Anti-c5/c5a/c5adesr antibodies and fragments |
| US20140080153A1 (en) | 2011-01-07 | 2014-03-20 | Chugai Seiyaku Kabushiki Kaisha | Method for improving physical properties of antibody |
| SG10201609665PA (en) | 2011-02-25 | 2017-01-27 | Chugai Pharmaceutical Co Ltd | FcɣRIIb-SPECIFIC Fc ANTIBODY |
| WO2012132067A1 (ja) | 2011-03-30 | 2012-10-04 | 中外製薬株式会社 | 抗原結合分子の血漿中滞留性と免疫原性を改変する方法 |
| WO2012133782A1 (ja) | 2011-03-30 | 2012-10-04 | 中外製薬株式会社 | 抗原結合分子の血漿中滞留性と免疫原性を改変する方法 |
| MX2013010011A (es) | 2011-03-01 | 2014-10-24 | Amgen Inc | Agentes de unión biespecífica. |
| EP2686345B1 (en) | 2011-03-16 | 2018-04-25 | Amgen Inc. | Fc variants |
| ES2685479T3 (es) | 2011-04-19 | 2018-10-09 | Amgen Inc. | Método para el tratamiento de la osteoporosis |
| CN106928362B (zh) | 2011-04-29 | 2021-10-26 | 埃派斯进有限公司 | 抗-cd40抗体及其使用方法 |
| MX347691B (es) | 2011-05-04 | 2017-05-09 | Omeros Corp | Composiciones para inhibir la activacion del complemento dependiente de la masp-2. |
| RS58765B1 (sr) | 2011-05-21 | 2019-06-28 | Macrogenics Inc | Cd3-vezujući molekuli sposobni za vezivanje za humani i nehumani cd3 |
| AU2012258907A1 (en) | 2011-05-25 | 2013-11-07 | Merck Sharp & Dohme Corp. | Method for preparing Fc-containing polypeptides having improved properties |
| WO2012177653A2 (en) | 2011-06-20 | 2012-12-27 | St. Louis University | Targeting the neuromuscular junction for treatment |
| UA117901C2 (uk) | 2011-07-06 | 2018-10-25 | Ґенмаб Б.В. | Спосіб посилення ефекторної функції вихідного поліпептиду, його варіанти та їх застосування |
| WO2013012733A1 (en) | 2011-07-15 | 2013-01-24 | Biogen Idec Ma Inc. | Heterodimeric fc regions, binding molecules comprising same, and methods relating thereto |
| SG11201401100UA (en) | 2011-09-30 | 2014-07-30 | Chugai Pharmaceutical Co Ltd | Antigen-binding molecule inducing immune response to target antigen |
| JP6322411B2 (ja) | 2011-09-30 | 2018-05-09 | 中外製薬株式会社 | 複数の生理活性を有する抗原の消失を促進する抗原結合分子 |
| US20140335089A1 (en) | 2011-09-30 | 2014-11-13 | Chugai Seiyaku Kabushiki Kaisha | Antigen-binding molecule for promoting elimination of antigens |
| TW201817745A (zh) | 2011-09-30 | 2018-05-16 | 日商中外製藥股份有限公司 | 具有促進抗原清除之FcRn結合域的治療性抗原結合分子 |
| AU2012313594C1 (en) | 2011-09-30 | 2018-05-10 | Chugai Seiyaku Kabushiki Kaisha | Ion concentration-dependent binding molecule library |
| US20150299313A1 (en) | 2011-10-05 | 2015-10-22 | Chugai Seiyaku Kabushiki Kaisha | Antigen-binding molecule for promoting clearance from plasma of antigen comprising suger chain receptor-binding domain |
| CN113416257A (zh) | 2011-11-30 | 2021-09-21 | 中外制药株式会社 | 包含进入细胞内以形成免疫复合体的搬运体(载体)的药物 |
| KR102219987B1 (ko) | 2012-02-24 | 2021-02-25 | 추가이 세이야쿠 가부시키가이샤 | FcγRIIB를 매개로 항원의 소실을 촉진하는 항원 결합 분자 |
| MY171761A (en) | 2012-03-14 | 2019-10-28 | Regeneron Pharma | Multispecific antigen-binding molecules and uses thereof |
| KR102213535B1 (ko) | 2012-03-16 | 2021-02-08 | 리제너론 파마슈티칼스 인코포레이티드 | pH-민감성 면역글로불린 서열을 발현하는 비-사람 동물 |
| ES2849349T3 (es) | 2012-03-16 | 2021-08-17 | Regeneron Pharma | Anticuerpos de cadena ligera modificados mediante ingeniería con histidina y roedores modificados genéticamente para la generación de los mismos |
| PL2831117T3 (pl) | 2012-03-29 | 2018-03-30 | Novimmune Sa | Przeciwciała anty-TLR4 i ich zastosowania |
| TWI619729B (zh) | 2012-04-02 | 2018-04-01 | 再生元醫藥公司 | 抗-hla-b*27抗體及其用途 |
| JP5988659B2 (ja) | 2012-04-09 | 2016-09-07 | シャープ株式会社 | 送風機 |
| US9605058B2 (en) | 2012-05-01 | 2017-03-28 | Glaxosmithkline Llc | Antibodies against the CXC-ELR family of chemokines |
| US9255154B2 (en) | 2012-05-08 | 2016-02-09 | Alderbio Holdings, Llc | Anti-PCSK9 antibodies and use thereof |
| EP2857419B1 (en) | 2012-05-30 | 2021-01-13 | Chugai Seiyaku Kabushiki Kaisha | Antigen-binding molecule for eliminating aggregated antigens |
| CN104487457B (zh) | 2012-05-30 | 2018-01-26 | 中外制药株式会社 | 靶组织特异性抗原结合分子 |
| MX364738B (es) | 2012-06-15 | 2019-05-03 | Pfizer | Anticuerpos antagonistas mejorados contra factor-8 de crecimiento y diferenciacion y usos de los mismos. |
| SG10201605703TA (en) | 2012-07-06 | 2016-09-29 | Genmab Bv | Dimeric protein with triple mutations |
| TWI596115B (zh) | 2012-08-13 | 2017-08-21 | 再生元醫藥公司 | 具有pH-依賴性結合特性之抗-PCSK9抗體 |
| US11236168B2 (en) | 2012-08-24 | 2022-02-01 | Chugai Seiyaku Kabushiki Kaisha | Mouse FcγammaRII-specific Fc antibody |
| US9133269B2 (en) | 2012-08-24 | 2015-09-15 | Anaptysbio, Inc. | Humanized antibodies directed against complement protein C5 |
| TWI717591B (zh) | 2012-08-24 | 2021-02-01 | 日商中外製藥股份有限公司 | FcγRIIb特異性Fc區域變異體 |
| TWI660972B (zh) | 2012-09-10 | 2019-06-01 | 愛爾蘭商尼歐托普生物科學公司 | 抗mcam抗體及相關使用方法 |
| HRP20240676T1 (hr) | 2012-09-13 | 2024-10-11 | Bristol-Myers Squibb Company | Proteini domena skele na bazi fibronektina koji vezuju miostatin |
| TW201418707A (zh) | 2012-09-21 | 2014-05-16 | Alexion Pharma Inc | 補體組分c5拮抗劑之篩選分析 |
| JP2016500704A (ja) | 2012-11-06 | 2016-01-14 | スカラー ロック インコーポレイテッドScholar Rock,Inc. | 細胞シグナル伝達を変調するための組成物及び方法 |
| AU2013364133B2 (en) | 2012-12-21 | 2018-10-11 | Aveo Pharmaceuticals, Inc. | Anti-GDF15 antibodies |
| US9701759B2 (en) | 2013-01-14 | 2017-07-11 | Xencor, Inc. | Heterodimeric proteins |
| KR20150110659A (ko) | 2013-01-24 | 2015-10-02 | 글락소스미스클라인 인털렉츄얼 프로퍼티 디벨로프먼트 리미티드 | Tnf-알파 항원-결합 단백질 |
| JP6608702B2 (ja) | 2013-01-31 | 2019-11-20 | ソウル大学校産学協力団 | 補体関連疾患の予防及び治療のためのc5抗体及び方法 |
| US9481725B2 (en) | 2013-03-14 | 2016-11-01 | Alderbio Holdings, Llc | Antibodies to HGF and compositions containing |
| US9321686B2 (en) | 2013-03-15 | 2016-04-26 | Forta Corporation | Reinforcement fiber coating compositions, methods of making and treating, and uses for improved adhesion to asphalt and portland cement concrete |
| WO2014145159A2 (en) | 2013-03-15 | 2014-09-18 | Permeon Biologics, Inc. | Charge-engineered antibodies or compositions of penetration-enhanced targeting proteins and methods of use |
| JP2016516064A (ja) | 2013-03-15 | 2016-06-02 | アムジェン インコーポレイテッド | ヒト対象におけるミオスタチンの拮抗 |
| US10858417B2 (en) | 2013-03-15 | 2020-12-08 | Xencor, Inc. | Heterodimeric proteins |
| US20160032014A1 (en) | 2013-03-15 | 2016-02-04 | Amgen Inc. | Human antigen binding proteins that bind to proprotein convertase subtilisin kexin type 9 |
| EP3936521B1 (en) | 2013-03-15 | 2026-02-11 | Xencor, Inc. | Heterodimeric proteins |
| WO2014160958A1 (en) | 2013-03-29 | 2014-10-02 | Alexion Pharmaceuticals, Inc. | Compositions and methods for increasing the serum half-life of a therapeutic agent targeting complement c5 |
| TWI636062B (zh) | 2013-04-02 | 2018-09-21 | 中外製藥股份有限公司 | Fc region variant |
| PL3816625T3 (pl) | 2013-05-06 | 2026-01-26 | Scholar Rock, Inc. | Kompozycje i sposoby modulacji czynnika wzrostu |
| CN105392800B (zh) | 2013-05-17 | 2020-07-31 | 国家科学研究中心 | 抗cxcl1、cxcl7和cxcl8抗体及其应用 |
| AU2014273817B2 (en) | 2013-05-31 | 2019-03-14 | Zymeworks Bc Inc. | Heteromultimers with reduced or silenced effector function |
| CN113150164A (zh) | 2013-07-25 | 2021-07-23 | 西托姆克斯治疗公司 | 多特异性抗体、多特异性可活化抗体及其使用方法 |
| WO2015022658A2 (en) | 2013-08-14 | 2015-02-19 | Novartis Ag | Methods of treating sporadic inclusion body myositis |
| EP3033093A1 (en) | 2013-08-16 | 2016-06-22 | Alexion Pharmaceuticals, Inc. | Treatment of graft rejection by administering a complement inhibitor to an organ prior to transplant |
| JP6456831B2 (ja) | 2013-09-04 | 2019-01-23 | プロテノバ株式会社 | イムノグロブリン結合ドメイン多量体 |
| EP2853898B1 (en) | 2013-09-27 | 2017-01-04 | Medizinische Hochschule Hannover | Analysis of myostatin in serum |
| EP3327038B1 (en) | 2013-12-20 | 2020-09-23 | F. Hoffmann-La Roche AG | Bispecific her2 antibodies and methods of use |
| JP2017510622A (ja) | 2014-01-27 | 2017-04-13 | ノバルティス アーゲー | 筋萎縮を予測するバイオマーカー、方法および使用 |
| EP3107935B1 (en) | 2014-02-20 | 2020-06-24 | Allergan, Inc. | Complement component c5 antibodies |
| NZ631007A (en) | 2014-03-07 | 2015-10-30 | Alexion Pharma Inc | Anti-c5 antibodies having improved pharmacokinetics |
| TW201622746A (zh) | 2014-04-24 | 2016-07-01 | 諾華公司 | 改善或加速髖部骨折術後身體復原之方法 |
| CN106459192B (zh) | 2014-06-30 | 2021-08-03 | 默克专利股份公司 | 具有pH依赖性抗原结合的抗TNFa抗体 |
| WO2016073906A2 (en) | 2014-11-06 | 2016-05-12 | Scholar Rock, Inc. | Transforming growth factor-related immunoassays |
| WO2016073853A1 (en) | 2014-11-06 | 2016-05-12 | Scholar Rock, Inc. | Anti-pro/latent-myostatin antibodies and uses thereof |
| TN2017000217A1 (en) | 2014-12-08 | 2018-10-19 | Novartis Ag | Myostatin or activin antagonists for the treatment of sarcopenia |
| WO2016098356A1 (en) | 2014-12-19 | 2016-06-23 | Chugai Seiyaku Kabushiki Kaisha | Anti-c5 antibodies and methods of use |
| KR102650420B1 (ko) | 2014-12-19 | 2024-03-21 | 추가이 세이야쿠 가부시키가이샤 | 항-마이오스타틴 항체, 변이체 Fc 영역을 함유하는 폴리펩타이드, 및 사용 방법 |
| JP2018511557A (ja) | 2015-01-22 | 2018-04-26 | 中外製薬株式会社 | 2種以上の抗c5抗体の組み合わせおよび使用方法 |
| CN112142844B (zh) | 2015-02-05 | 2025-07-25 | 中外制药株式会社 | 包含离子浓度依赖性的抗原结合结构域的抗体,fc区变体,il-8-结合抗体及其应用 |
| TWI805046B (zh) | 2015-02-27 | 2023-06-11 | 日商中外製藥股份有限公司 | Il-6受體抗體用於製備醫藥組成物的用途 |
| JP6944375B2 (ja) | 2015-03-31 | 2021-10-06 | アレクシオン ファーマシューティカルズ, インコーポレイテッド | 発作性夜間血色素尿症(pnh)患者の亜集団の同定および処置 |
| CN107771081A (zh) | 2015-04-15 | 2018-03-06 | 瑞泽恩制药公司 | 用gdf8抑制剂增加力量和功能的方法 |
| EP3288586A1 (en) | 2015-05-01 | 2018-03-07 | Alexion Pharmaceuticals, Inc. | Efficacy of an anti-c5 antibody in the prevention of antibody mediated rejection in sensitized recipients of kindney thansplant |
| US20180142010A1 (en) | 2015-06-26 | 2018-05-24 | Alexion Pharmaceuticals, Inc. | Method for treating a patient in compliance with vaccination with eculizumab or an eculizumab variant |
| US10940126B2 (en) | 2015-07-03 | 2021-03-09 | Camilla Svensson | Inhibition of IL-8 in the treatment of pain and/or bone loss |
| WO2017049011A1 (en) | 2015-09-15 | 2017-03-23 | Scholar Rock, Inc. | Anti-pro/latent-myostatin antibodies and uses thereof |
| AU2016323088B2 (en) | 2015-09-18 | 2020-12-10 | Chugai Seiyaku Kabushiki Kaisha | IL-8-binding antibodies and uses thereof |
| TW201718014A (zh) | 2015-10-12 | 2017-06-01 | 諾華公司 | C5抑制劑於移植相關微血管病之用途 |
| RU2742606C2 (ru) | 2015-12-18 | 2021-02-09 | Чугаи Сейяку Кабусики Кайся | Антитела к с5 и способы их применения |
| CA3002422C (en) | 2015-12-18 | 2024-04-16 | Chugai Seiyaku Kabushiki Kaisha | Anti-myostatin antibodies, polypeptides containing variant fc regions, and methods of use |
| US10233252B2 (en) | 2015-12-21 | 2019-03-19 | Wisconsin Alumni Research Foundation | pH-dependent antibodies targeting the transferrin receptor and methods of use thereof to deliver a therapeutic agent |
| US11359009B2 (en) | 2015-12-25 | 2022-06-14 | Chugai Seiyaku Kabushiki Kaisha | Anti-myostatin antibodies and methods of use |
| MX2018008369A (es) | 2016-01-08 | 2019-05-15 | Scholar Rock Inc | Anticuerpos de anti-miostatina pro/latente y metodo de uso de los mismos. |
| US20190023775A1 (en) | 2016-01-11 | 2019-01-24 | Alexion Pharmaceuticals, Inc. | Dosage and administration of anti-c5 antibodies for treatment |
| WO2017132259A1 (en) | 2016-01-25 | 2017-08-03 | Shire Human Genetic Therapies, Inc. | Anti-c5 antibodies with enhanced ph switch |
| SMT202000598T1 (it) | 2016-06-13 | 2021-01-05 | Scholar Rock Inc | Utilizzo di inibitori di miostatina e terapie combinate |
| AU2017283470B2 (en) | 2016-06-14 | 2024-03-21 | Regeneron Pharmaceuticals, Inc. | Anti-C5 antibodies and uses thereof |
| KR102680483B1 (ko) | 2016-06-17 | 2024-07-01 | 추가이 세이야쿠 가부시키가이샤 | 항-마이오스타틴 항체 및 사용 방법 |
| PE20240825A1 (es) | 2016-06-17 | 2024-04-18 | Chugai Pharmaceutical Co Ltd | Anticuerpos anti-c5 y metodos de uso |
| MX2019001448A (es) | 2016-08-05 | 2019-09-13 | Chugai Pharmaceutical Co Ltd | Composicion para profilaxis o tratamiento de enfermedades relacionadas con interleucina 8 (il-8). |
| JP7191833B2 (ja) | 2017-01-30 | 2022-12-19 | 中外製薬株式会社 | 抗スクレロスチン抗体およびその使用 |
| UA129282C2 (uk) | 2017-01-31 | 2025-03-12 | Чугаі Сейяку Кабусікі Кайся | Спосіб лікування або профілактики пов'язаних з c5 хвороб |
| CN110740749B (zh) | 2017-03-14 | 2024-12-10 | 戊瑞治疗有限公司 | 在酸性pH下与VISTA结合的抗体 |
| UA125757C2 (uk) | 2017-03-16 | 2022-06-01 | Медімм'Юн Лімітед | Антитіло до par2 і його застосування |
| EP3411400B1 (en) | 2017-04-03 | 2021-09-22 | InflaRx GmbH | Treatment of inflammatory diseases with inhibitors of c5a activity |
| WO2019084438A1 (en) | 2017-10-26 | 2019-05-02 | Alexion Pharmaceuticals, Inc. | ASSAY AND ADMINISTRATION OF ANTI-C5 ANTIBODIES FOR THE TREATMENT OF NOCTURNAL PAROXYSTIC HEMOGLOBINURIA (PNH) AND ATYPICAL HEMOLYTIC AND UREMIC SYNDROME (AHUS) |
| RU2020117578A (ru) | 2017-12-04 | 2022-01-14 | Ра Фармасьютикалз, Инк. | Модуляторы активности комплемента |
| CR20210103A (es) | 2018-08-01 | 2021-03-22 | Chugai Pharmaceutical Co Ltd | Composición farmacéutica para usarse en el tratamiento o prevención de una enfermedad relacionada con c5 y método para tratar o prevenir una enfermedad relacionada con c5 |
| KR20210149779A (ko) | 2019-04-10 | 2021-12-09 | 추가이 세이야쿠 가부시키가이샤 | Fc 영역 개변 항체의 정제 방법 |
-
2009
- 2009-04-10 TW TW108102915A patent/TW201920257A/zh unknown
- 2009-04-10 EP EP19154335.4A patent/EP3521311A1/en not_active Ceased
- 2009-04-10 CA CA2721052A patent/CA2721052C/en active Active
- 2009-04-10 KR KR1020247019249A patent/KR20240113501A/ko active Pending
- 2009-04-10 BR BR122020017346-7A patent/BR122020017346B1/pt active IP Right Grant
- 2009-04-10 TW TW105123386A patent/TWI700293B/zh active
- 2009-04-10 HR HRP20160209T patent/HRP20160209T1/hr unknown
- 2009-04-10 CN CN2009801224666A patent/CN102056946A/zh active Pending
- 2009-04-10 BR BRPI0911431A patent/BRPI0911431B8/pt active IP Right Grant
- 2009-04-10 LT LTEP13195718.5T patent/LT2708559T/lt unknown
- 2009-04-10 MX MX2010011184A patent/MX2010011184A/es active IP Right Grant
- 2009-04-10 HU HUE09729337A patent/HUE028718T2/en unknown
- 2009-04-10 CN CN201710902296.XA patent/CN107551270A/zh active Pending
- 2009-04-10 HU HUE19154342A patent/HUE067049T2/hu unknown
- 2009-04-10 EP EP19154342.0A patent/EP3514180B1/en active Active
- 2009-04-10 SG SG10201608379YA patent/SG10201608379YA/en unknown
- 2009-04-10 CN CN201710902297.4A patent/CN107469077A/zh active Pending
- 2009-04-10 PL PL09729337T patent/PL2275443T3/pl unknown
- 2009-04-10 RU RU2010145939/10A patent/RU2571225C2/ru active
- 2009-04-10 EP EP13195713.6A patent/EP2708558B1/en not_active Revoked
- 2009-04-10 TW TW109128061A patent/TWI787643B/zh active
- 2009-04-10 HU HUE13195718A patent/HUE037386T2/hu unknown
- 2009-04-10 NZ NZ602884A patent/NZ602884A/en unknown
- 2009-04-10 TW TW103130346A patent/TW201447062A/zh unknown
- 2009-04-10 SG SG2013027180A patent/SG189775A1/en unknown
- 2009-04-10 KR KR1020207005619A patent/KR102269708B1/ko active Active
- 2009-04-10 KR KR1020177021142A patent/KR102057826B1/ko active Active
- 2009-04-10 KR KR1020217019078A patent/KR102469853B1/ko active Active
- 2009-04-10 DK DK13195718.5T patent/DK2708559T3/en active
- 2009-04-10 CN CN2013101606315A patent/CN103251948A/zh active Pending
- 2009-04-10 KR KR1020227040226A patent/KR20220162801A/ko not_active Ceased
- 2009-04-10 TW TW112134224A patent/TW202423982A/zh unknown
- 2009-04-10 TR TR2018/08046T patent/TR201808046T4/tr unknown
- 2009-04-10 UA UAA201411972A patent/UA121453C2/uk unknown
- 2009-04-10 CN CN201710902064.4A patent/CN107488228A/zh active Pending
- 2009-04-10 NZ NZ717429A patent/NZ717429A/en unknown
- 2009-04-10 MY MYPI2010004751A patent/MY195714A/en unknown
- 2009-04-10 PT PT97293377T patent/PT2275443E/pt unknown
- 2009-04-10 NZ NZ588507A patent/NZ588507A/xx unknown
- 2009-04-10 NO NO13195718A patent/NO2708559T3/no unknown
- 2009-04-10 PL PL13195718T patent/PL2708559T3/pl unknown
- 2009-04-10 ES ES13195713.6T patent/ES2671010T3/es active Active
- 2009-04-10 ES ES13195718.5T patent/ES2671403T3/es active Active
- 2009-04-10 JP JP2010507273A patent/JP4954326B2/ja active Active
- 2009-04-10 PL PL13195713T patent/PL2708558T3/pl unknown
- 2009-04-10 DK DK13195713.6T patent/DK2708558T3/en active
- 2009-04-10 KR KR1020197036522A patent/KR102084925B1/ko active Active
- 2009-04-10 WO PCT/JP2009/057309 patent/WO2009125825A1/ja not_active Ceased
- 2009-04-10 TW TW111124130A patent/TWI818604B/zh active
- 2009-04-10 EP EP22212441.4A patent/EP4238993A3/en active Pending
- 2009-04-10 TR TR2018/08535T patent/TR201808535T4/tr unknown
- 2009-04-10 EP EP13195718.5A patent/EP2708559B1/en active Active
- 2009-04-10 SI SI200931376T patent/SI2275443T1/sl unknown
- 2009-04-10 ES ES19154342T patent/ES2978400T3/es active Active
- 2009-04-10 TW TW098111949A patent/TWI564021B/zh active
- 2009-04-10 NZ NZ623716A patent/NZ623716A/en unknown
- 2009-04-10 US US12/936,587 patent/US20110111406A1/en not_active Abandoned
- 2009-04-10 HR HRP20240722TT patent/HRP20240722T1/hr unknown
- 2009-04-10 EP EP09729337.7A patent/EP2275443B1/en not_active Revoked
- 2009-04-10 SG SG2013027206A patent/SG2013027206A/en unknown
- 2009-04-10 KR KR1020107025124A patent/KR102051275B1/ko active Active
- 2009-04-10 SI SI200931852T patent/SI2708559T1/en unknown
- 2009-04-10 ES ES09729337.7T patent/ES2563483T3/es active Active
- 2009-04-10 CN CN201210295963XA patent/CN102993304A/zh active Pending
- 2009-04-10 DK DK09729337.7T patent/DK2275443T3/en active
- 2009-04-10 PT PT131957185T patent/PT2708559T/pt unknown
- 2009-04-10 PL PL19154342.0T patent/PL3514180T3/pl unknown
- 2009-04-10 EP EP15188815.3A patent/EP3056513A1/en not_active Withdrawn
- 2009-04-13 AR ARP090101284A patent/AR071656A1/es not_active Application Discontinuation
-
2010
- 2010-10-06 CO CO10123949A patent/CO6311005A2/es not_active Application Discontinuation
- 2010-10-06 IL IL208516A patent/IL208516A/en active IP Right Grant
- 2010-10-11 MX MX2014000923A patent/MX354670B/es unknown
- 2010-11-02 MA MA33312A patent/MA32754B1/fr unknown
- 2010-11-08 CR CR11783A patent/CR11783A/es unknown
- 2010-11-10 EC EC2010010600A patent/ECSP10010600A/es unknown
-
2011
- 2011-08-04 JP JP2011171225A patent/JP4961501B2/ja active Active
- 2011-12-08 JP JP2011268497A patent/JP5048866B2/ja active Active
-
2012
- 2012-07-19 JP JP2012160692A patent/JP5503698B2/ja active Active
- 2012-08-27 US US13/595,139 patent/US20130011866A1/en active Granted
-
2013
- 2013-05-08 US US13/889,484 patent/US9868948B2/en active Active
- 2013-05-08 US US13/889,512 patent/US9890377B2/en active Active
-
2014
- 2014-03-14 JP JP2014051047A patent/JP5824095B2/ja active Active
- 2014-07-10 RU RU2014128324A patent/RU2756029C2/ru active
- 2014-09-15 PH PH12014502054A patent/PH12014502054B1/en unknown
-
2015
- 2015-03-08 IL IL237599A patent/IL237599B/en active IP Right Grant
- 2015-10-08 JP JP2015199906A patent/JP6082447B2/ja active Active
- 2015-12-10 CR CR20150656A patent/CR20150656A/es unknown
- 2015-12-10 CR CR20150655A patent/CR20150655A/es unknown
-
2017
- 2017-01-20 JP JP2017008075A patent/JP6417431B2/ja active Active
-
2018
- 2018-04-13 US US15/952,951 patent/US20180282719A1/en not_active Abandoned
- 2018-04-13 US US15/952,945 patent/US10472623B2/en active Active
- 2018-04-30 HK HK18105598.5A patent/HK1246157A1/zh unknown
- 2018-04-30 HK HK18105594.9A patent/HK1246311A1/zh unknown
- 2018-04-30 HK HK18105600.1A patent/HK1246158A1/zh unknown
- 2018-05-07 HR HRP20180708TT patent/HRP20180708T1/hr unknown
- 2018-06-12 IL IL259956A patent/IL259956B/en active IP Right Grant
- 2018-08-30 PH PH12018501850A patent/PH12018501850A1/en unknown
- 2018-10-05 JP JP2018189946A patent/JP2019048810A/ja not_active Withdrawn
-
2019
- 2019-03-22 US US16/361,498 patent/US20200048627A1/en not_active Abandoned
-
2020
- 2020-09-14 US US17/020,497 patent/US11359194B2/en active Active
- 2020-09-14 US US17/020,543 patent/US11371039B2/en active Active
- 2020-10-06 JP JP2020169016A patent/JP7033176B2/ja active Active
- 2020-10-06 JP JP2020169015A patent/JP2021011490A/ja not_active Withdrawn
- 2020-10-06 JP JP2020169014A patent/JP7177808B2/ja active Active
-
2021
- 2021-06-04 JP JP2021094209A patent/JP7397823B2/ja active Active
-
2022
- 2022-02-25 JP JP2022027962A patent/JP2022081533A/ja active Pending
-
2023
- 2023-01-18 US US18/156,138 patent/US20240002836A1/en active Pending
- 2023-03-03 AR ARP230100542A patent/AR128700A2/es unknown
- 2023-06-28 JP JP2023105711A patent/JP7366312B2/ja active Active
-
2024
- 2024-05-24 JP JP2024084653A patent/JP2024105708A/ja active Pending
Cited By (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US12473375B2 (en) | 2006-03-31 | 2025-11-18 | Chugai Seiyaku Kabushiki Kaisha | Methods for controlling blood pharmacokinetics of antibodies |
| US11248053B2 (en) | 2007-09-26 | 2022-02-15 | Chugai Seiyaku Kabushiki Kaisha | Method of modifying isoelectric point of antibody via amino acid substitution in CDR |
| US12122840B2 (en) | 2007-09-26 | 2024-10-22 | Chugai Seiyaku Kabushiki Kaisha | Method of modifying isoelectric point of antibody via amino acid substitution in CDR |
| US12116414B2 (en) | 2007-09-26 | 2024-10-15 | Chugai Seiyaku Kabushiki Kaisha | Method of modifying isoelectric point of antibody via amino acid substitution in CDR |
| US11359194B2 (en) | 2008-04-11 | 2022-06-14 | Chugai Seiyaku Kabushiki Kaisha | Antigen-binding molecule capable of binding two or more antigen molecules repeatedly |
| US11371039B2 (en) | 2008-04-11 | 2022-06-28 | Chugai Seiyaku Kabushiki Kaisha | Antigen-binding molecule capable of binding to two or more antigen molecules repeatedly |
| US11891434B2 (en) | 2010-11-30 | 2024-02-06 | Chugai Seiyaku Kabushiki Kaisha | Antigen-binding molecule capable of binding to plurality of antigen molecules repeatedly |
| US11236168B2 (en) | 2012-08-24 | 2022-02-01 | Chugai Seiyaku Kabushiki Kaisha | Mouse FcγammaRII-specific Fc antibody |
| US11267868B2 (en) | 2013-04-02 | 2022-03-08 | Chugai Seiyaku Kabushiki Kaisha | Fc region variant |
| US12169205B2 (en) | 2014-12-19 | 2024-12-17 | Chugai Seiyaku Kabushiki Kaisha | Anti-myostatin antibodies, polypeptides containing variant fc regions, and methods of use |
| US11454633B2 (en) | 2014-12-19 | 2022-09-27 | Chugai Seiyaku Kabushiki Kaisha | Anti-myostatin antibodies, polypeptides containing variant Fc regions, and methods of use |
| US11180548B2 (en) | 2015-02-05 | 2021-11-23 | Chugai Seiyaku Kabushiki Kaisha | Methods of neutralizing IL-8 biological activity |
| US12595299B2 (en) | 2015-02-05 | 2026-04-07 | Chugai Seiyaku Kabushiki Kaisha | FC variants |
| US11780912B2 (en) | 2016-08-05 | 2023-10-10 | Chugai Seiyaku Kabushiki Kaisha | Composition for prophylaxis or treatment of IL-8 related diseases |
| US11053308B2 (en) | 2016-08-05 | 2021-07-06 | Chugai Seiyaku Kabushiki Kaisha | Method for treating IL-8-related diseases |
| US12516115B2 (en) | 2016-08-05 | 2026-01-06 | Chugai Seiyaku Kabushiki Kaisha | Composition for prophylaxis or treatment of IL-8 related diseases |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7366312B2 (ja) | 複数分子の抗原に繰り返し結合する抗原結合分子 | |
| HK1154029A (en) | Antigen-binding molecule capable of binding to two or more antigen molecules repeatedly |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20120409 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20120529 |
|
| A871 | Explanation of circumstances concerning accelerated examination |
Free format text: JAPANESE INTERMEDIATE CODE: A871 Effective date: 20120529 |
|
| A975 | Report on accelerated examination |
Free format text: JAPANESE INTERMEDIATE CODE: A971005 Effective date: 20120619 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20120625 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20120719 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20150727 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5048866 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20150727 Year of fee payment: 3 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |