ES2941716T3 - Compuestos heterocíclicos como inmunomoduladores - Google Patents
Compuestos heterocíclicos como inmunomoduladores Download PDFInfo
- Publication number
- ES2941716T3 ES2941716T3 ES17761781T ES17761781T ES2941716T3 ES 2941716 T3 ES2941716 T3 ES 2941716T3 ES 17761781 T ES17761781 T ES 17761781T ES 17761781 T ES17761781 T ES 17761781T ES 2941716 T3 ES2941716 T3 ES 2941716T3
- Authority
- ES
- Spain
- Prior art keywords
- alkyl
- cycloalkyl
- membered
- independently selected
- membered heteroaryl
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D231/00—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings
- C07D231/02—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings not condensed with other rings
- C07D231/10—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members
- C07D231/14—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D233/00—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, not condensed with other rings
- C07D233/54—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, not condensed with other rings having two double bonds between ring members or between ring members and non-ring members
- C07D233/66—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, not condensed with other rings having two double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D233/90—Carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D263/00—Heterocyclic compounds containing 1,3-oxazole or hydrogenated 1,3-oxazole rings
- C07D263/02—Heterocyclic compounds containing 1,3-oxazole or hydrogenated 1,3-oxazole rings not condensed with other rings
- C07D263/30—Heterocyclic compounds containing 1,3-oxazole or hydrogenated 1,3-oxazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members
- C07D263/34—Heterocyclic compounds containing 1,3-oxazole or hydrogenated 1,3-oxazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D277/00—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings
- C07D277/02—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings
- C07D277/20—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members
- C07D277/32—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D277/56—Carbon atoms having three bonds to hetero atoms with at the most one bond to halogen
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/06—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings linked by a carbon chain containing only aliphatic carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/06—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a carbon chain containing only aliphatic carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/12—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/06—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings linked by a carbon chain containing only aliphatic carbon atoms
Abstract
Se describen compuestos de Fórmula (I), métodos para usar los compuestos como inmunomoduladores y composiciones farmacéuticas que comprenden tales compuestos. Los compuestos son útiles para tratar, prevenir o mejorar enfermedades o trastornos tales como cáncer o infecciones. (Traducción automática con Google Translate, sin valor legal)
Description
DESCRIPCIÓN
Compuestos heterocíclicos como inmunomoduladores
CAMPO DE LA INVENCIÓN
La presente solicitud se refiere a compuestos farmacéuticamente activos. La divulgación proporciona compuestos así como sus composiciones y sus usos. Los compuestos modulan la interacción proteína/proteína de PD-1/PD-L1 y son útiles en el tratamiento de varias enfermedades, incluyendo enfermedades infecciosas y cáncer. Debe interpretarse que cualquier referencia a métodos de tratamiento en los párrafos siguientes de esta descripción son referencias a los compuestos, composiciones farmacéuticas y medicamentos de la presente invención para su uso en un método de tratamiento del cuerpo humano (o animal) mediante terapia (o para diagnóstico).
ANTECEDENTES DE LA INVENCIÓN
El sistema inmunitario desempeña un papel importante en el control y la erradicación de enfermedades como el cáncer. Sin embargo, las células cancerosas a menudo desarrollan estrategias para evadir o inhibir el sistema inmunitario para favorecer su crecimiento. Uno de tales mecanismos es alterar la expresión de moléculas coestimuladoras y coinhibidoras expresadas en células inmunes (Postow et al, J. Clinical Oncology 2015, 1-9). El bloqueo de la señalización de un punto de control inmunitario inhibidor, como PD-1, ha demostrado ser una modalidad de tratamiento prometedora y eficaz.
La muerte celular programada-1 (PD-1), también conocida como CD279, es un receptor de superficie celular expresado en células T activadas, células T asesinas naturales, células B y macrófagos (Greenwald et al, Annu. Rev. Immunol 2005, 23:515-548; Okazaki y Honjo, Trends Immunol 2006, (4):195-201). Funciona como un sistema de retroalimentación negativa intrínseca para prevenir la activación de las células T, que a su vez reduce la autoinmunidad y promueve la autotolerancia. Además, también se sabe que PD-1 desempeña un papel crítico en la supresión de la respuesta de células T específicas de antígeno en enfermedades como el cáncer y la infección viral (Sharpe et al, Nat Immunol 20078, 239-245; Postow et al, J. Clinical Oncol 2015, 1-9).
La estructura de PD-1 consiste en un dominio de tipo variable de inmunoglobulina extracelular seguido de una región transmembrana y un dominio intracelular (Parry et al, Mol Cell Biol 2005, 9543-9553). El dominio intracelular contiene dos sitios de fosforilación localizados en un motivo inhibidor basado en tirosina inmunorreceptor y un motivo conmutador basado en tirosina inmunorreceptor, lo que sugiere que PD-1 regula negativamente las señales mediadas por el receptor de células T. PD-1 tiene dos ligandos, PD-L1 y PD-L2 (Parry et al, Mol Cell Biol 2005, 9543-9553; Latchman et al, Nat Immunol 2001, 2, 261-268), y difieren en sus patrones de expresión. La proteína de PD-L1 se regula por incremento en macrófagos y células dendríticas en respuesta al tratamiento con lipopolisacáridos y GM-CSF, y en células T y células B tras la señalización del receptor de células T y del receptor de células B. PD-L1 también se expresa en gran medida en casi todas las células tumorales, y la expresión aumenta adicionalmente después del tratamiento con IFN-y (Iwai et al, PNAS2002, 99(19):12293-7; Blank et al, Cancer Res 2004, 64(3):1140-5). De hecho, se ha demostrado que el estado de expresión de PD-L1 en el tumor es un pronóstico en múltiples tipos de tumores (Wang et al, Eur J Surg Oncol 2015; Huang et al, Oncol Rep 2015; Sabatier et al, Oncotarget 2015, 6(7): 5449-5464). La expresión de PD-L2, por el contrario, está más restringida y es expresada principalmente por células dendríticas (Nakae et al, J Immunol 2006, 177:566-73). La ligación de PD-1 con sus ligandos PD-L1 y PD-L2 en células T suministra una señal que inhibe la producción de IL-2 e IFN-y, así como la proliferación celular inducida por la activación del receptor de células T (Carter et al, Eur J Immunol 2002, 32(3):634-43; Freeman et al., J Exp Med 2000, 192(7): 1027-34). El mecanismo implica el reclutamiento de SHP-2 o SHP-1 fosfatasas para inhibir la señalización del receptor de células T como la fosforilación de Syk y Lck (Sharpe et al, Nat Immunol 2007, 8, 239-245). La activación del eje de señalización de PD-1 también atenúa la fosforilación del bucle de activación de PKC-0, que es necesaria para la activación de las vías NF-kB y AP1, y para la producción de citoquinas como IL-2, IFN-y y TNF (Sharpe et al., Nat Immunol 2007, 8, 239-245; Carter et al., Eur J Immunol 2002, 32(3):634-43; Freeman et al., J Exp Med 2000, 192(7):1027-34).
La WO2011/082400 divulga un ensayo para identificar moduladores de la vía PD-1 :PD-L y moduladores de la vía PD-1 :PD-L, por ejemplo compuestos y composiciones farmacéuticas de los mismos, y métodos para tratar enfermedades influenciadas por la modulación de la vía PD-1 : PD-L. Varias líneas de evidencia de estudios preclínicos en animales indican que PD-1 y sus ligandos regulan negativamente las respuestas inmunes. Se ha demostrado que los ratones deficientes en PD-1 desarrollan glomerulonefritis de tipo lupus y miocardiopatía dilatada (Nishimura et al, Immunity 1999, 11: 141-151; Nishimura et al, Science 2001, 291:319-222). Usando un modelo de LCMV de infección crónica, se ha demostrado que la interacción de PD-1/PD-L1 inhibe la activación, expansión y adquisición de funciones efectoras de las células T CD8 específicas de virus (Barber et al, Nature 2006, 439, 682-7). Juntos, estos datos apoyan el desarrollo de un enfoque terapéutico para bloquear la cascada de señalización inhibidora mediada por PD-1 para aumentar o "rescatar" la respuesta de las células T. Por consiguiente, hay una necesidad de nuevos compuestos que bloqueen la interacción proteína/proteína de PD-1/PD-L1.
SUMARIO
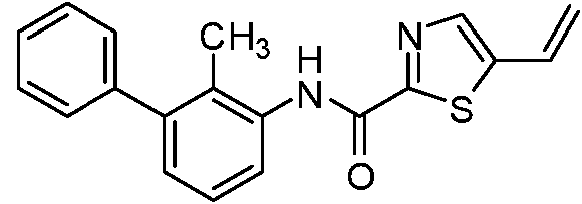
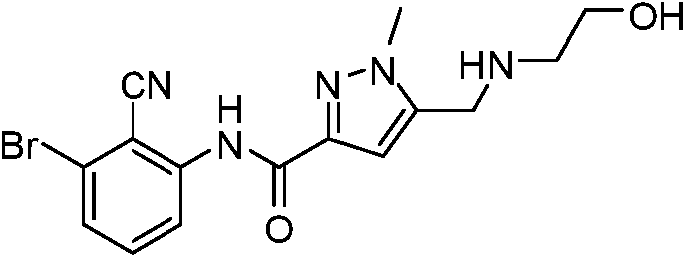
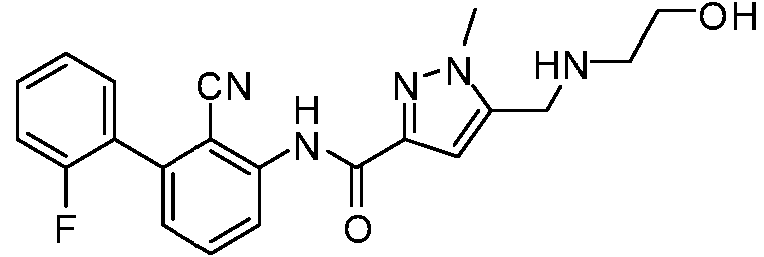
La presente invención proporciona, entre otras cosas, un compuesto de Fórmula (II):
o una sal farmacéuticamente aceptable o un estereoisómero del mismo, en donde las variables constituyentes se definen en la presente.
La presente invención proporciona además una composición farmacéutica que comprende un compuesto de la invención, o una sal farmacéuticamente aceptable o un estereoisómero del mismo, y por lo menos un portador o excipiente farmacéuticamente aceptable.
La presente invención proporciona además compuestos y composiciones para su uso en métodos para modular o inhibir la interacción proteína/proteína de PD-1/PD-L1, que comprenden administrar a un individuo un compuesto de la invención, o una sal farmacéuticamente aceptable o un estereoisómero del mismo.
La presente invención proporciona además métodos para tratar una enfermedad o trastorno en un paciente que comprenden administrar al paciente una cantidad terapéuticamente eficaz de un compuesto de la invención, o una sal farmacéuticamente aceptable o un estereoisómero del mismo.
DESCRIPCIÓN DETALLADA
I. Compuestos
La presente divulgación proporciona un compuesto de Fórmula (II):
o una sal farmacéuticamente aceptable o un estereoisómero del mismo, en donde:
(i) X4 es S y X5 es CR5; (ii) X4 es O y X5 es CR5; X4 es NR4 y X5 es CR5 ; o (iv) X4 es CR4 y X5 es CR5;
Cy es fenilo, que está opcionalmente sustituido con de 1 a 5 sustituyentes R6 independientemente seleccionados;
R1, R2 y R3 se seleccionan cada uno independientemente de H, alquilo C1 -4 , cicloalquilo C3-10, cicloalquilo C3 -10-alquilo C1-4-, arilo C6 -10, arilo C6-10-alquilo C1-4-, heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, (heteroarilo de 5-10 miembros)-alquilo C1-4-, (heterocicloalquilo de 4-10 miembros)-alquilo C1-4-, alquenilo C2-4, alquinilo C2-4, halo, CN, OR10, haloalquilo C1.4 , haloalcoxi C1.4 , NH2 , -NHR10, -NR10R10, NHOR10, C(O)R10, C(O)NR10R10, C(O)OR10, OC(O)R10, OC(O)NR10R10, NR10C(O)R10, NR10C(O)OR10, NR10C(O)NR10R10, C(=NR10)R10, C(=NR10)NR10R10, NR10C(=NR10)NR10R10, NR10S(O)R10, NR10S(O)2R10, NR10S(O)2NR10R10, S(O)R10, S(O)NR10R10, S(O)2 R10, y S(O)2Nr10R10, en donde cada R10 se selecciona independientemente de H, alquilo C1 -4 , alquenilo C2-4, alquinilo C2-4, alcoxi C1 -4 , cicloalquilo C3 -10 , cicloalquilo C3-10-alquilo arilo C6-10-alquilo C1 -4 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, (heteroarilo de 5-10 miembros)-alquilo C1-4-y (heterocicloalquilo de 4-10 miembros)-alquilo C1.4-, en donde el alquilo C1 -4 , alcoxi C1.4 , cicloalquilo C3 -10 , cicloalquilo C3 -10-alquilo C1-4-, arilo C6 -10 , arilo C6-10-alquilo C1.4-, heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, (heteroarilo de 5-10 miembros)-alquilo C1-4- y (heterocicloalquilo de 4-10 miembros)-alquilo C1.4-, de R1, R2 , R3 y R10 están cada uno opcionalmente sustituidos con 1 o 2 sustituyentes Rd
independientemente seleccionados;
R4, R5 y R6 se seleccionan cada uno independientemente de H, halo, alquilo C1 -6, alquenilo C2-6, alquinilo C2-6, haloalquilo C1 -6, haloalcoxi C1 -6, arilo C6-10 , cicloalquilo C3-10 , heteroarilo de 5-14 miembros, heterocicloalquilo de 4-10 miembros, arilo C6-10-alquilo C1 -4-, cicloalquilo C3-10-alquilo C1 -4-, (heteroarilo de 5-14 miembros)-alquilo C1 -4-, (heterocicloalquilo de 4-10 miembros)-alquilo C1.4-, CN, NO2 , ORa, SRa, NHORa, C(O)Ra, C(O)NRaRa, C(O)ORa, OC(O)Ra, OC(O)NRaRa, NHRa, NRaRa, NRaC(O)Ra, NRaC(O)ORa, NRaC(O)NRaRa, C(=NRa)Ra, C(=NRa)NRaRa, NRaC(=NRa)NRaRa, NRaC(=NOH)NRaRa, NRaC(=NCN)NRaRa, NRaS(O)Ra, NRaS(O)2Ra, NRaS(O)2NRaRa, S(O)Ra, S(O)NRaRa, S(O)2 Ra, y S(O)2 NRaRa, en donde el alquilo C1 -6, alquenilo C2-6, alquinilo C2-6, arilo C6-10 , cicloalquilo C3-10 , heteroarilo de 5-14 miembros, heterocicloalquilo de 4-10 miembros, arilo C6-10-alquilo C1.4-, cicloalquilo C3-10-alquilo C1.4-, (heteroarilo de 5-14 miembros)-alquilo C1.4-, y (heterocicloalquilo de 4-10 miembros)-alquilo C1.4- de R4, R5 y R6 están cada uno cada uno opcionalmente sustituidos con 1, 2, 3, 4 o 5 sustituyentes Rb independientemente seleccionados;
o dos sustituyentes R6 adyacentes en el anillo Cy, tomados junto con los átomos a los que están unidos, forman un anillo de fenilo fusionado, un anillo de heterocicloalquilo fusionado de 5, 6 o 7 miembros, un anillo de heteroarilo fusionado de 5 o 6 miembros o un anillo de cicloalquilo C3-6 fusionado, en donde el anillo de heterocicloalquilo de 5, 6 o 7 miembros fusionado y el anillo de heteroarilo de 5 o 6 miembros fusionado tienen cada uno 1-4 heteroátomos como miembros del anillo seleccionados de N, O y S y en donde el anillo de fenilo fusionado, el anillo de heterocicloalquilo de 5, 6 o 7 miembros fusionado, el anillo de heteroarilo de 5 o 6 miembros fusionado y el anillo de cicloalquilo C3-6 fusionado están cada uno opcionalmente sustituidos con 1,2 o 3 sustituyentes Rb independientemente seleccionados;
R7 es halo, alquilo C1 -6, alquenilo C2-6, alquinilo C2-6, haloalquilo C1 -6, haloalcoxi C1 -6, arilo C6-10 , cicloalquilo C3-10 , heteroarilo de 5-14 miembros, heterocicloalquilo de 4-10 miembros, arilo C6-10-alquilo C1 -4-, cicloalquilo C3-10-alquilo C1 -4-, (heteroarilo de 5-14 miembros)-alquilo C1 -4-, (heterocicloalquilo de 4-10 miembros)-alquilo C1 -4-, CN, NO2 , OR11, SR11, NH2 , -NHR11, -NR11R11, NHOR11, C(O)R11, C(O)NR11R11, C(O)OR11, OC(O)R11, OC(O)NR11R11, NR11C(O)R11, NR11C(O)OR11, NR11C(O)NR11R11, C(=NR11)R11, C(=NR11)NR11R11, NR11C(=NR11)NR11R11, NR11C(=NOH)NR11R11, NR11C(=NCN)NR11R11, NR11S(O)R11, NR11S(O)2R11, NR11S(O)2NR11R11, S(O)R11, S(O)NR11R11, S(O)2 R11, o S(O)2 NR11R11, en donde el alquilo C1.6, alquenilo C2-6, alquinilo C2-6, haloalquilo C1.6, haloalcoxi C1.6, arilo C6-10 , cicloalquilo C3-10 , heteroarilo de 5-14 miembros, heterocicloalquilo de 4-10 miembros, arilo C6-10-alquilo C1 -4-, cicloalquilo C3-10-alquilo C1.4-, (heteroarilo de 5-14 miembros)-alquilo C1 -4- y (heterocicloalquilo de 4-10 miembros)-alquilo C1.4- de R7 están cada uno opcionalmente sustituidos con 1, 2 o 3 sustituyentes Rb independientemente seleccionados;
R8 es alquilo C1.6 sustituido con 1-3 sustituyentes Rb2 independientemente seleccionados o (heterociclo de 4-10 miembros)-alquilo C1 -4- opcionalmente sustituido con 1, 2 o 3 sustituyentes Rb independientemente seleccionados;
cada R11 se selecciona independientemente de H, alquilo C1-6, haloalquilo C1.6, alquenilo C2-6, alquinilo C2-6, arilo C6-10 , cicloalquilo C3-10 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, arilo C6-10-alquilo C1 -4-, cicloalquilo C3-10-alquilo C1.4-, (heteroarilo de 5-10 miembros)-alquilo C1.4-, y (heterocicloalquilo de 4-10 miembros)-alquilo C1 -4-, en donde el alquilo C1 -6, alquenilo C2-6, alquinilo C2-6, arilo C6-10 , cicloalquilo C3-10 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, arilo C6-10-alquilo C1 -4-, cicloalquilo C3-10-alquilo C1 -4-, (heteroarilo de 5-10 miembros)-alquilo C1.4- y (heterocicloalquilo de 4-10 miembros)-alquilo C1.4- de R11 están cada uno opcionalmente sustituidos con 1,2 o 3 sustituyentes Rb independientemente seleccionados; cada Ra se selecciona independientemente de H, alquilo C1 -6, haloalquilo C1 -6, alquenilo C2-6, alquinilo C2-6, arilo C6-10 , cicloalquilo C3-10 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, aril C6-10 -alquilo C1.4-, cicloalquilo C3-10-alquilo C1.4-, (heteroarilo de 5-10 miembros)-alquilo C1 -4-, y (heterocicloalquilo de 4-10 miembros)-alquilo C1 -4-, en donde el alquilo C1 -6, haloalquilo C1 -6, alquenilo C2-6, alquinilo C2-6, arilo C6-10 , C3-10 cicloalquilo, 5-10 miembros heteroarilo, heterocicloalquilo de 4-10 miembros, C6-10 arilo-C1-4 alquilo-, cicloalquilo C3-10-alquilo C1.4-, (heteroarilo de 5-10 miembros)-alquilo C1.4- y (heterocicloalquilo de 4-10 miembros)-alquilo C1.4 - de Ra están cada uno opcionalmente sustituidos con 1, 2 o 3 sustituyentes Rd independientemente seleccionados;
cada sustituyente Rb se selecciona independientemente de halo, alquilo C1 -6, haloalquilo C1 -6, haloalcoxi C1 -6, arilo C6-10 , cicloalquilo C3-10 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, arilo C6-10 -alquilo C1.4-, cicloalquilo C3-10-alquilo C1.4-, (heteroarilo de 5-10 miembros)-alquilo C1.4-, (heterocicloalquilo de 4-10 miembros)-alquilo C1.4-, CN, OH, NH2 , NO2 , NHORc, ORc, SRc, C(O)Rc, C(O)NRcRc, C(O)ORc, OC(O)Rc, OC(O)NRcRc, C(=NRc)NRcRc, NRcC(=NRc)NRcRc, NRcC(=NOH)NRcRc, NRcC(=NCN)NRcRc, NHRc, NRcRc, NRcC(O)Rc, NRcC(O)ORc, NRcC(O)NRcRc, NRcS(O)Rc, NRcS(O)2Rc, NRcS(O)2NRcRc, S(O)Rc, S(O)NRcRc, S(O)2 Rc y S(O)2 NRcRc; en donde el alquilo C1 -6, haloalquilo C1 -6, haloalcoxi C1 -6, arilo C6-10 , cicloalquilo C3-10 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, arilo C6-10-alquilo C1 -4-, cicloalquilo C3-10-alquilo C1.4-, (heteroarilo de 5-10 miembros)-alquilo C1.4- y (heterocicloalquilo de 4-10 miembros)-alquilo C1 -4- de Rb están cada uno opcionalmente sustituidos con 1 -3 sustituyentes Rd independientemente seleccionados; cada Rb2 se selecciona independientemente de halo, haloalquilo C1 -6, haloalcoxi C1.6, arilo C6-10 , cicloalquilo C3-10 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, arilo C6-10-alquilo C1 -4-, cicloalquilo C3-10-alquilo C1.4-, (heteroarilo de 5-10 miembros)-alquilo C1.4-, (heterocicloalquilo de 4-10 miembros)-alquilo C1.4-, CN, OH, NH2, NO2, NHORc, ORc, SRc, C(O)Rc, C(O)NRcRc, C(O)ORc, OC(O)Rc, OC(O)NRcRc, C(=NRc)NRcRc, NRcC(=NRc)NRcRc, NRcC(=NOH)NRcRc, NRcC(=NCN)NRcRc, NHRc, NRcRc, NRcC(O)Rc, NRcC(O)ORc, NRcC(O)NRcRc, NRcS(O)Rc, NRcS(O)2 Rc, NRcS(O)2 NRcRc, S(O)Rc, S(O)NRcRc, S(O)2 Rc, y S(O)2 NRcRc; en
donde el haloalquilo C1 -6 , haloalcoxi C1-6 , arilo C6 -10, cicloalquilo C3 -10 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, arilo C6-10-alquilo C1-4-, cicloalquilo C3-10-alquilo C1-4-, (heteroarilo de 5-10 miembros)-alquilo C1.4- y (heterocicloalquilo de 4-10 miembros)-alquilo C1.4- de Rb2 están cada uno opcionalmente sustituidos con 1-3 sustituyentes Rd independientemente seleccionados.
cada Rc se selecciona independientemente de H, alquilo C1 -6 , haloalquilo C1.6 , alquenilo C2-6, alquinilo C2-6, arilo C6 -10 , cicloalquilo C3 -10 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, arilo C6-10-alquilo C1-4-, cicloalquilo C3-10-alquilo C1.4-, (heteroarilo de 5-10 miembros)-alquilo C1.4-, y (heterocicloalquilo de 4-10 miembros) -alquilo C 1-4 -, en donde el alquilo C1.6 , haloalquilo C1 -6 , alquenilo C2-6, alquinilo C2-6, arilo C6 -10 , cicloalquilo C3 -10 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, arilo C6-10-alquilo C1-4-, cicloalquilo C3-10-alquilo C1.4-, (heteroarilo de 5-10 miembros)-alquilo C1.4- y (heterocicloalquilo de 4-10 miembros)-alquilo C1.4- de Rc están cada uno opcionalmente sustituidos con 1, 2 o 3 sustituyentes Rf independientemente seleccionados de alquilo C1 -6 , haloalquilo C1.6 , alquenilo C2-6, alquinilo C2-6, arilo C6 -10 , cicloalquilo C3 -10 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, arilo C6-10-alquilo C1-4-, cicloalquilo C3-10-alquilo C1.4-, (heteroarilo de 5-10 miembros)-alquilo C1.4-, (heterocicloalquilo de 4-10 miembros)-alquilo C1.4-, halo, CN, NHORg, ORg, SRg, C(O)Rg, C(O)NRgRg, C(O)ORg, OC(O)Rg, OC(O)NRgRg, NHRg, NRgRg, NRgC(O)Rg, NRgC(O)NRgRg, NRgC(O)ORg, C(=NRg)NRgRg, NRgC(=NRg)NRgRg, NRgC(=NOH)NRgRg, NRgC(=NCN)NRgRg, S(O)Rg, S(O)NRgRg, S(O)2 Rg, NRgS(O)2 Rg, NRgS(O)2 NRgRg, y S(O)2 NRgRg; en donde el alquilo C1 -6 , haloalquilo C1.6 , alquenilo C2-6, alquinilo C2-6, arilo C6-10, cicloalquilo C3 -10 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, arilo C6-10-alquilo C1.4-, cicloalquilo C3-10-alquilo C1.4-, (heteroarilo de 5-10 miembros)-alquilo C1.4-, y (heterocicloalquilo de 4-10 miembros)-alquilo C1-4- de Rf están cada uno opcionalmente sustituidos con 1, 2 o 3 sustituyentes Rn independientemente seleccionados de alquilo C1 -6 , haloalquilo C1.6 , halo, CN, fenilo, cicloalquilo C3-6, heteroarilo de 5-6 miembros, heterocicloalquilo de 4-6 miembros, NHORo, ORo, SRo, C(O)Ro, C(O)NR° R° , C(O)ORo, OC(O)Ro, OC(O)NR° R° , NHRo, NR° R° , NR° C(O)R° , NR° C(O)NR° R° , NR° C(O)OR° , C(=NR° )NR° R° , NR° C(=NR° )NR° R° , S(O)R° , S(O)NR° R° , S(O)2R° , NR°S(o)2R°, NR° S(O)2 NR° R° , y S(O)2 NR° R° , en donde el alquilo C1 -6 , haloalquilo C1.6 , fenilo, cicloalquilo C3-6, heteroarilo de 5-6 miembros y heterocicloalquilo de 4-6 miembros de Rn está opcionalmente sustituido con 1,2 o 3 sustituyentes Rq;
cada Rd se selecciona independientemente de alquilo C1 -6 , haloalquilo C1 -6 , halo, arilo C6-10, heteroarilo de 5-10 miembros, cicloalquilo C3 -10 , heterocicloalquilo de 4-10 miembros, arilo C6-10-alquilo C1.4-, cicloalquilo C3-10-alquilo C1.4-, (heteroarilo de 5-10 miembros)-alquilo C1.4-, (heterocicloalquilo de 4-10 miembros)-alquilo C1.4-, CN, NH2 , NHORe , ORe , SRe , C(O)Re, C(O)NReRe, C(O)ORe , OC(O)Re, OC(O)NReRe, NHRe, NReRe, NReC(O)Re, NReC(O)NReRe , NReC(O)ORe, C(=NRe)NReRe, NReC(=NRe)NReRe , NReC(=NOH)NReRe, NReC(=NCN)NReRe, S(O)Re, S(O)NReRe , S(O)2 Re, NReS(O)2 Re , NReS(O)2 NReRe, y S(O)2 NReRe, en donde el alquilo C1 -6 , haloalquilo C1.6 , arilo C6 -10, heteroarilo de 5-10 miembros, cicloalquilo C3 -10 , heterocicloalquilo de 4-10 miembros, arilo C6-10-alquilo C1.4-, cicloalquilo C3-10-alquilo C1-4-, (heteroarilo de 5-10 miembros)-alquilo C1.4-, y (heterocicloalquilo de 4 10 miembros)-alquilo C1.4- de Rd están cada uno opcionalmente sustituidos con 1-3 sustituyentes Rf independientemente seleccionados;
cada Re se selecciona independientemente de H, alquilo C1 -6 , haloalquilo C1 -6 , alquenilo C2-6, alquinilo C2-6, arilo C6 -10 , cicloalquilo C3 -10 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, arilo C6-10-alquilo C1-4-, cicloalquilo C3-10-alquilo C1.4-, (heteroarilo de 5-10 miembros)-alquilo C1.4-, y (heterocicloalquilo de 4-10 miembros)-alquilo C1-4-, en donde el alquilo C1 -6 , haloalquilo C1 -6 , alquenilo C2-6, alquinilo C2-6, arilo C6 -10 , cicloalquilo C3 -10 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, arilo C6-10-alquilo C1.4-, cicloalquilo C3-10-alquilo C1.4-, (heteroarilo de 5-10 miembros)-alquilo C1.4- y (heterocicloalquilo de 4-10 miembros)-alquilo C1-4- de Re están cada uno opcionalmente sustituidos con 1, 2 o 3 sustituyentes Rf independientemente seleccionados;
cada Rg se selecciona independientemente de H, alquilo C1 -6 , haloalquilo C1 -6 , alquenilo C2-6, alquinilo C2-6, arilo C6 -10 , cicloalquilo C3 -10 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, arilo C6-10-alquilo C1-4-, cicloalquilo C3-10-alquilo C1.4-, (heteroarilo de 5-10 miembros)-alquilo C1.4-, y (heterocicloalquilo de 4-10 miembros)-alquilo C1-4-, en donde el alquilo C1 -6 , alquenilo C2-6, alquinilo C2-6, arilo C6 -10 , cicloalquilo C3 -10 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, arilo C6-10-alquilo C1-4-, cicloalquilo C3-10-alquilo C1-4-, (heteroarilo de 5-10 miembros)-alquilo C1.4 - y (heterocicloalquilo de 4-10 miembros)-alquilo C1.4 - de Rg están cada uno opcionalmente sustituidos con 1-3 sustituyentes Rp independientemente seleccionados de alquilo C1 -6 , haloalquilo C1 -6 , alquenilo C2-6, alquinilo C2-6, arilo C6 -10 , cicloalquilo C3 -10 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, arilo C6-10-alquilo C1-4-, cicloalquilo C3-10-alquilo C1.4-, (heteroarilo de 5-10 miembros)-alquilo C1.4-, (heterocicloalquilo de 4-10 miembros)-alquilo C1.4 -, halo, Cn, NHORr, ORr, SRr, C(O)Rr, C(O)NRrRr, C(O)ORr, OC(O)Rr, OC(O)NRrRr, NHRr, NRrRr, NRrC(O)Rr, NRrC(O)NRrRr, NRrC(O)ORr, C(=NRr)NRrRr, NRrC(=NRr)NRrRr, NRrC(=NOH)NRrRr, NRrC(=NCN)NRrRr, S(O)Rr, S(O)NRrRr, S(O)2Rr, NRrS(O)2 Rr, NRrS(O)2 NRrRr, y S(O)2 NRrRr, en donde el alquilo C1 -6 , haloalquilo C1.6 , C2-6 alquenilo, C2-6 alquinilo, C6-10 arilo, C3-10 cicloalquilo, heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, arilo C6-10-alquilo C1-4-, cicloalquilo C3-10-alquilo C1.4-, (heteroarilo de 5-10 miembros)-alquilo C1.4- y (heterocicloalquilo de 4-10 miembros)-alquilo C1.4- de Rp está opcionalmente sustituido con 1,2 o 3 sustituyentes Rq;
o dos sustituyentes Ra cualquiera junto con el átomo de nitrógeno, fósforo o boro al que están unidos forman un grupo heterocicloalquilo de 4, 5, 6, 7, 8, 9 o 10 miembros opcionalmente sustituido con 1, 2 o 3 sustituyentes Rh independientemente seleccionados de alquilo C1 -6 , haloalquilo C1 -6 , haloalcoxi C1 -6 , cicloalquilo C3 -10 , heterocicloalquilo de 4-7 miembros, arilo C6 -10, heteroarilo de 5-6 miembros, cicloalquilo C3-10-alquilo C1.4-,
(heteroarilo de 5-6 miembros)-alquilo C1-4-, (heterocicloalquilo de 4-7 miembros)-alquilo C1.4-, arilo C6 -io-alquilo C1.4-, alquenilo C2-6, alquinilo C2-6, halo, CN, ORi, SRi, NHORi, C(O)Ri, C(O)NRiRi, C(O)ORi, OC(O)Ri, OC(O)NRiRi, NHRi, NRiRi, NRiC(O)Ri, NRiC(O)NRiRi, NRiC(O)ORi, C(=NRi)NRiRi, NRiC(=NRi)NRiRi, NRiC(=NOH)NRiRi, NRiC(=NCN)NRiRi, S(O)Ri, S(O)NRiRi, S(O)2 Ri, NRiS(O)2 Ri, NRiS(O)2 NRiRi, y S(O)2 NRiRi, en donde el alquilo C1 -6 , haloalquilo C1.6 , haloalcoxi C1.6 , cicloalquilo C3.10 , heterocicloalquilo de 4-7 miembros, arilo C6 -10 , heteroarilo de 5-6 miembros, arilo C6-10-alquilo C1.4-, cicloalquilo C3-10 -alquilo C1-4-, (heteroarilo de 5-6 miembros)-alquilo C1.4-, y (heterocicloalquilo de 4-7 miembros)-alquilo C1.4- de Rh están cada unoo opcionalmente sustituidos con 1, 2 o 3 sustituyentes Rj independientemente seleccionados de alquilo C1 -4 , cicloalquilo C3-6, arilo C6 -10 , heteroarilo de 5 o 6 miembros, heterocicloalquilo de 4-6 miembros, alquenilo C2-4, alquinilo C2-4, halo, haloalquilo C1.4 , haloalcoxi C1.4 , CN, NHORk, ORk, SRk, C(O)Rk, C(O)NRkRk, OC(O)Rk, OC(O)NRkRk, NHRk, NRkRk, NRkC(O)Rk, NRkC(O)NRkRk, NRkC(O)ORk, C(=NRk)NRkRk, NRkC(=NRk)NRkRk, S(O)Rk, S(O)NRkRk, S(O)2 Rk, NRkS(O)2 Rk, NRkS(O)2 NRkRk, y S(O)2 NRkRk, en donde el alquilo C1.4 , cicloalquilo C3-6, arilo C6 -10, heteroarilo de 5 o 6 miembros, heterocicloalquilo de 4-6 miembros, alquenilo C2-4, haloalquilo C1.4 y haloalcoxi C1.4 de Rj están cada uno opcionalmente sustituidos con 1, 2 o 3 sustituyentes Rq independientemente seleccionados;
o dos grupos Rh unidos al mismo átomo de carbono del heterocicloalquilo de 4 a 10 miembros, tomados junto con el átomo de carbono al que están unidos, forman un cicloalquilo C3-6 o un heterocicloalquilo de 4 a 6 miembros que tiene 1 -2 heteroátomos como miembros del anillo seleccionados de O, N o S;
o dos sustituyentes Rc cualquiera junto con el átomo de nitrógeno al que están unidos forman un grupo heterocicloalquilo de 4, 5, 6 o 7 miembros opcionalmente sustituido con 1, 2 o 3 sustituyentes Rh independientemente seleccionados;
o dos sustituyentes Re cualquiera junto con el átomo de nitrógeno al que están unidos forman un grupo heterocicloalquilo de 4, 5, 6 o 7 miembros opcionalmente sustituido con 1, 2 o 3 sustituyentes Rh independientemente seleccionados;
o dos sustituyentes Rh cualquiera junto con el átomo de nitrógeno al que están unidos forman un grupo heterocicloalquilo de 4, 5, 6 o 7 miembros opcionalmente sustituido con 1, 2 o 3 sustituyentes Rh independientemente seleccionados;
o dos sustituyentes Ro cualquiera junto con el átomo de nitrógeno al que están unidos forman un grupo heterocicloalquilo de 4, 5, 6 o 7 miembros opcionalmente sustituido con 1, 2 o 3 sustituyentes Rh independientemente seleccionados;
o dos sustituyentes Rr cualquiera junto con el átomo de nitrógeno al que están unidos forman un grupo heterocicloalquilo de 4, 5, 6 o 7 miembros opcionalmente sustituido con 1, 2 o 3 sustituyentes Rh independientemente seleccionados;
cada Ri, Rk, R° o Rr se selecciona independientemente de H, alquilo C1 -6 , haloalquilo C1 -6 , cicloalquilo C3-6, arilo C6 -10 , heterocicloalquilo de 4-6 miembros, heteroarilo de 5 o 6 miembros, haloalquilo C1 -4 , alquenilo C2-4 y alquinilo C2-4, en donde el alquilo C1 -4 , haloalquilo C1-6 , cicloalquilo C3-6, arilo C6 -10 , heterocicloalquilo de 4-6 miembros, heteroarilo de 5 o 6 miembros, alquenilo C2-4 y alquinilo C2-4 de Ri, Rk, Ro o Rr están cada uno opcionalmente sustituidos con 1, 2 o 3 sustituyentes Rq;
cada Rq se selecciona independientemente de OH, CN, -COOH, NH2 , halo, haloalquilo C1 -6 , alquilo C1-6 , alcoxi C1 -6 , haloalcoxi C1 -6 , alquiltio C1.6 , fenilo, heteroarilo de 5-6 miembros, heterocicloalquilo de 4-6 miembros, cicloalquilo C3-6, NHR12 y NR12 R12 , en donde el alquilo C1-6 , fenilo, cicloalquilo C3-6, heterocicloalquilo de 4-6 miembros y heteroarilo de 5-6 miembros de Rq están cada uno opcionalmente sustituidos con halo, OH, CN, -COOH, NH2 , alquilo C1 -4 , alcoxi C1.4 , haloalquilo C1 -4 , haloalcoxi C1.4 , fenilo, cicloalquilo C3-10 y heterocicloalquilo de 4-6 miembros y cada R12 ess independientemente alquilo C1 -6 ; y
!_____es un enlace simple o un enlace doble para que el anillo A siga siendo aromático.
En algunas realizaciones, el compuesto proporcionado en la presente es un compuesto que tiene la Fórmula (III):
o una sal farmacéuticamente aceptable o un estereoisómero del mismo, en donde:
L es un enlace, -C(O)NR13-, -NR13 C(O)-, O, -(CR14 R15 )q-, -(CR14 R15 )q-O-, -O(CR14 R15 )q-, -NR13-, -(CR14 R15 )q-NR13-, -NR13-(CR14 R15 )q-, -CH=CH-, -C=C-, -SO2 NR13-, -NR13 SO2-, -NR13 SO2 NR13-, -NR13 C(O)O-, -OC(O)NR13 or
-NR13 C(O)NR13-;
cada R13 es independientemente H, haloalquilo C1-6 o alquilo C1-6 opcionalmente sustituido con un sustituyente seleccionado de alquilo C1 -4 , alcoxi C1.4 , haloalquilo C1.4 , haloalcoxi C1.4 , CN, halo, OH, -COOH, NH2 , -NHalquilo C1.4 y -N(alquilo C1 -4)2 ;
R14 y R15 se seleccionan cada uno independientemente de H, halo, CN, OH, -COOH, alquilo C 1.4 , alcoxi C 1.4 , -NHalquilo C 1.4 , -N(alquilo C1 -4)2 , haloalquilo C1.4 , haloalcoxi C1.4 , cicloalquilo C3-6, fenilo, heteroarilo de 5-6 miembros y heterocicloalquilo de 4-6 miembros, en donde el alquilo C1 -4 , alcoxi C1 -4 , haloalquilo C1 -4 , haloalcoxi C1 -4 , cicloalquilo C3-6, fenilo, heteroarilo de 5-6 miembros y heterocicloalquilo de 4-6 miembros de R14 o R15 están cada uno opcionalmente sustituidos con 1,2 o 3 sustituyentes Rq independientemente seleccionados;
o R14 y R15 tomados junto con el átomo de carbono al que están unidos forman cicloalquilo de 3, 4, 5 o 6 miembros o heterocicloalquilo de 3, 4, 5 o 6 miembros, cada uno de los cuales es opcionalmente sustituido con 1 o 2 sustituyentes Rq independientemente seleccionados;
el anillo B es arilo C6 -10, cicloalquilo C3 -10 , heteroarilo de 5-10 miembros o heterocicloalquilo de 4-10 miembros, cada uno de los cuales está opcionalmente sustituido con 1, 2 o 3 sustituyentes Rd independientemente seleccionados; y
el subíndice n es un número entero de 1, 2, 3 o 4.
En algunas realizaciones, el compuesto proporcionado en la presente es un compuesto que tiene la Fórmula (Mía):
o una sal farmacéuticamente aceptable o un estereoisómero del mismo, en donde el anillo B, L, R6, n, R1, R2, R3, R7, X4, X5 y R8 son como se describen en la presente.
En algunas realizaciones, el compuesto proporcionado en la presente es un compuesto que tiene la Fórmula (MIa-1):
o una sal farmacéuticamente aceptable o un estereoisómero del mismo, en donde el anillo B, L, R6, R1, R2, R3, R7, X4, X5 y R8 son como se describen en la presente
En algunas realizaciones, el compuesto proporcionado en la presente es un compuesto que tiene la Fórmula (Mía-2):
o una sal farmacéuticamente aceptable o un estereoisómero del mismo, en donde el anillo B, L, R6, n, R1 , R2 , R3 , R7 , R5 y R8 son como se describen en la presente.
En algunas realizaciones, Rd es alquilo C1 -6 , fenilo, heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, (heteroarilo de 5-10 miembros)-alquilo C1-4-, (heterocicloalquilo de 4-10 miembros)-alquilo C1-4-, ORe, C(O)Re , halo o CN, en donde el alquilo C1 -6 , fenilo, heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, (heteroarilo de 5-10 miembros)-alquilo C1-4- y (heterocicloalquilo de 4-10 miembros)-alquilo C1.4- de Rd están cada uno opcionalmente sustituidos con 1,2 o 3 sustituyentes Rf independientemente seleccionados.
En algunas realizaciones, Rd es (3-carboxipirrolidin-1-il)metilo, (R)-(3-carboxipirrolidin-1-il)metilo, (S)-(3-carboxipirrolidin-1-il)metilo, (3-hidroxipirrolidin-1-il)metilo, (3-hidroxipirrolidin-1-il)metilo)metilo, (R)-(3-hidroxipirrolidin-1-il)metilo, (S)-(3-hidroxipirrolidin-1-il)metilo, (2-hidroxietilamino)metilo, (2-hidroxi-2-metilpropilamino)metilo, 2-(dimetilamino)etanoilo, 2-(3-carboxiazetidin-1-il)etanoilo, (R)-2-(3-carboxiazetidin-1-il)etanoilo, (S)-2-(3-carboxiazetidin-1-il)etanoilo, 2-(2-carboxipiperidin-1-il)etanoilo, (R)-2-(2-carboxipiperidin-1-il)etanoilo, (S)-2-(2-carboxipiperidin-1-il)etanoilo, 2-(3-carboxipirrolidin-1-il)etanoilo, (S)-2-(3-carboxipirrolidin-1-il)etanoilo, (R)-2-(3-carboxipirrolidin-1-il)etanoilo, (5-cianopiridin-3-il)metoxi, (2-hidroxietilamino)metilo, 2-carboxi-1-piperidinilmetilo, (S)-2-carboxi-1-piperidinilmetilo, (R)-2-carboxi-1-piperidinilmetilo, halo o CN.
En algunas realizaciones, la fracción
se selecciona de:
En algunas realizaciones, la fracción
En algunas realizaciones, la fracción
En algunas realizaciones, la fracción
En algunas realizaciones, la fracción
En algunas realizaciones, (i) X4 es S y X5 es CR5; (ii) X4 es O y X5 es CR5; (iii) X4 es NR4 y X5 es CR5 ; o (iv)
X4 es CR4 y X5 es NR5. En algunas realizaciones, X4 es S y X5 es CR5. En algunas realizaciones, X4 es O y X5 es
CR5. En algunas realizaciones, X4 es NR4 y X5 es CR5. En algunas realizaciones, X4 es CR4 y X5 es NR5.
En algunas realizaciones, Cy es fenilo, que está opcionalmente sustituido con de 1 a 5 sustituyentes R6 independientemente seleccionados; o dos sustituyentes R6 adyacentes en el anillo Cy, tomados junto con los átomos
a los que están unidos, forman un anillo de fenilo fusionado, un anillo de heterocicloalquilo de 5, 6 o 7 miembros fusionado, un anillo de heteroarilo de 5 o 6 miembros fusionado o un anillo de cicloalquilo C3-6 fusionado, en donde el anillo de heterocicloalquilo de 5, 6 o 7 miembros fusionado y el anillo de heteroarilo de 5 o 6 miembros fusionado
tienen cada uno de 1 a 4 heteroátomos como miembros del anillo seleccionados de N, O y S y en donde el anillo de
fenilo fusionado, anillo de heterocicloalquilo de 5, 6 o 7 miembros fusionado, anillo de heteroarilo de 5 o 6 miembros fusionado y anillo de cicloalquilo C3-6 fusionado están opcionalmente sustituidos con 1, 2 o 3 sustituyentes Rb independientemente seleccionados.
En algunas realizaciones, Cy es fenilo, que está opcionalmente sustituido con de 1 a 5 sustituyentes R6 independientemente seleccionados.
En algunas realizaciones, Cy es fenilo. Por ejemplo, Cy es fenilo no sustituido. En algunas realizaciones, Cy
es fenilo opcionalmente sustituido con de 1 a 5 sustituyentes R6 independientemente seleccionados. En ciertas realizaciones, Cy es fenilo y está sustituido con de 1 a 5 sustituyentes seleccionados de halo u ORa . En ciertas realizaciones, Cy es fenilo sustituido con 1 a 2 sustituyentes seleccionados de halo u O-alquilo C1 -6.
En algunas realizaciones, R1, R2 y R3 se seleccionan cada uno independientemente de H, alquilo C1 -4 , cicloalquilo C3 -10 , cicloalquilo C3-10-alquilo C1-4-, arilo C6 -10 , arilo C6-10-alquilo C1 -4 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, (heteroarilo de 5-10 miembros)-alquilo C1-4-, (heterocicloalquilo de 4-10 miembros)-alquilo C1-4-, alquenilo C2-4, alquinilo C2-4, halo, CN, OR10, haloalquilo C1 -4 , haloalcoxi C1 -4 , NH2 , NR10R10, NHOR10, C(O)R10, C(O)NR10R10, C(O)OR10, OC(O)R10, OC(O)NR10R10, NR10C(O)R10, NR10C(O)OR10, NR10C(O)NR10R10, C(=NR10)R10, C(=NR10)NR10R10, NR10C(=NR10)NR10R10, NR10S(O)R10, NR10S(O)2R10, NR10S(O)2 NR10R10, S(O)R10, S(O)NR10R10, S(O)2 R10, y S(O)2 NR10R10, en donde cada R10 se selecciona independientemente de H, alquenilo C2-4, alquinilo C2-4, alquilo C1 -4 , alcoxi C1 -4 , cicloalquilo C3 -10 , cicloalquilo C3-10-alquilo C1-4-, arilo C6 -10, arilo C6-10-alquilo C1 -4 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, (heteroarilo de 5-10 miembros)-alquilo C1-4-, y (heterocicloalquilo de 4-10 miembros)-alquilo C1-4-, en donde el alquilo
C1 -4 , alcoxi C1 -4 , cicloalquilo C3 -10 , cicloalquilo C3-10-alquilo C1-4-, arilo C6 -10 , arilo C6 -10 -alquilo C1.4-, heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, (heteroarilo de 5-10 miembros)-alquilo C1-4-, y (heterocicloalquilo de
4-10 miembros)-alquilo C1-4- de R1, R2 , R3 y R10 están opcionalmente sustituidos con 1 o 2 grupos independientemente seleccionados de halo, OH, CN y alcoxi C1 -4.
En algunas realizaciones, R1, R2 y R3 se seleccionan cada uno independientemente de H, alquilo C1 -4 , alquenilo C2-4, alquinilo C2-4, halo, CN, OH, alcoxi C1 -4 , haloalquilo C1 -4 , haloalcoxi C1 -4 , NH2 , -NH-alquilo C1-4 y -N(alquilo C1 -4 )2.
En algunas realizaciones, R1, R2 y R3 se seleccionan cada uno independientemente de H, alquilo C1 -4 , alquenilo C2-4, alquinilo C2-4, halo, CN y OH. Por ejemplo, R1, R2 y R3 se seleccionan cada uno independientemente
de H, alquilo C1 -4 , alquenilo C2-4 y alquinilo C2-4. En ciertas realizaciones, R1, R2 y R3 son H.
En algunas realizaciones, R4 es H, halo, alquilo C1 -6 , alquenilo C2-6, alquinilo C2-6, haloalquilo C1-6 o haloalcoxi C1 -6. En algunas realizaciones, R4 es H.
En algunas realizaciones, R5 es H, halo, alquilo C1 -6 , alquenilo C2-6, alquinilo C2-6, haloalquilo C1-6 o haloalcoxi C1 -6. En algunas realizaciones, R5 es H.
En algunas realizaciones, R6 es H, halo, alquilo C1-6 , alquenilo C2-6, alquinilo C2-6, CN, ORa, C(O)NRaRa o NRaC(O)Ra , en donde el alquilo C1 -6 , el alquenilo C2-6 y el alquinilo C2-6 de R6 están cada uno opcionalmente sustituidos con 1, 2, 3, 4 o 5 sustituyentes Rb independientemente seleccionados; o dos sustituyentes R6 adyacentes en el anillo Cy, tomados junto con los átomos a los que están unidos, forman un anillo de fenilo fusionado, un anillo de heterocicloalquilo de 5, 6 o 7 miembros fusionado, un anillo de heteroarilo de 5 o 6 miembros fusionado o un anillo de cicloalquilo C3-6 fusionado, en donde el anillo de heterocicloalquilo de 5, 6 o 7 miembros fusionado y el anillo de heteroarilo de 5 o 6 miembros fusionado tienen cada uno de 1 a 4 heteroátomos como miembros del anillo seleccionados entre N, O y S y en donde el anillo de fenilo fusionado, el anillo de heterocicloalquilo de 5, 6 o 7 miembros fusionado, el anillo de heteroarilo de 5 o 6 miembros fusionado y el anillo de cicloalquilo C3-6 fusionado están opcionalmente sustituidos con 1, 2 o 3 sustituyentes Rb independientemente seleccionados.
En algunas realizaciones, R6 es H, halo, alquilo C1 -6 , alquenilo C2-6, alquinilo C2-6, CN u ORa, en donde el alquilo C1 -6 , alquenilo C2-6 y alquinilo C2-6 de R6 están cada uno opcionalmente sustituidos con 1, 2, 3, 4 o 5 sustituyentes Rb independientemente seleccionados; o dos sustituyentes R6 adyacentes en el anillo Cy, tomados junto con los átomos a los que están unidos, forman un anillo de fenilo fusionado, un anillo de heterocicloalquilo de 5, 6 o 7 miembros fusionado, un anillo de heteroarilo de 5 o 6 miembros fusionado o un anillo de cicloalquilo C3-6 fusionado de, en donde el anillo de heterocicloalquilo de 5, 6 o 7 miembros fusionado y el anillo de heteroarilo de 5 o 6 miembros fusionado tienen cada uno de 1 a 4 heteroátomos como miembros del anillo seleccionados de N, O y S y en donde el anillo de fenilo fusionado, el anillo de heterocicloalquilo de 5, 6 o 7 miembros fusionado, el anillo de heteroarilo de 5 o 6 miembros fusionado y el anillo de cicloalquilo C3-6 fusionado están opcionalmente sustituidos con 1, 2 o 3 sustituyentes Rb independientemente seleccionados.
En algunas realizaciones, R7 es halo, alquilo C1-6 , alquenilo C2-6, alquinilo C2-6, haloalquilo C1-6 , haloalcoxi C1 -6 , CN, NH2 , NH(alquilo C1 -6 ), N(alquilo C1 -6 )2 , cicloalquilo C3-6, heterocicloalquilo de 4-6 miembros, heteroarilo de 5-6 miembros o fenilo, en donde el alquilo C1 -6 , alquenilo C2-6, alquinilo C2-6, cicloalquilo C3-6, heterocicloalquilo de 4-6 miembros, heteroarilo de 5-6 miembros y fenilo están opcionalmente sustituidos con 1, 2 o 3 sustituyentes Rq independientemente seleccionados.
En algunas realizaciones, R8 es alquilo C1-6 sustituido con 1-3 sustituyentes Rb2 independientemente seleccionados o (heterocicloalquilo de 4-10 miembros)-alquilo C1-4- opcionalmente sustituido con 1, 2 o 3 sustituyentes Rb independientemente seleccionados. En algunas realizaciones, R8 es alquilo C1-6 sustituido con 1-3 sustituyentes Rb2 independientemente seleccionados.
En algunas realizaciones, R8 es alquilo C1-6 o (heterocicloalquilo de 4-10 miembros)-alquilo C1-4-, en donde el alquilo C1-6 y el (heterocicloalquilo de 4-10 miembros)-alquilo C1-4- están cada uno opcionalmente sustituidos con 1,2 o 3 sustituyentes Rb independientemente seleccionados.
En algunas realizaciones, R8 es alquilo C1-6 sustituido con Rb.
En algunas realizaciones, R8 es -CH2 NHRc o -CH2 NRcRc.
En algunas realizaciones, R8 es (2-hidroxietilamino)metilo, 2-carboxi-1 -piperidinilmetilo, (S)-2-carboxi-1-piperidinilmetilo, (R)-2-carboxi-1-piperidinilmetilo o 3-hidroxipirrolidina -1-ilmetilo.
En algunas realizaciones, R8 es (2-hidroxietilamino)metilo, 2-carboxi-1 -piperidinilmetilo, (S)-2-carboxi-1-piperidinilmetilo o (R)-2-carboxi-1-piperidinilmetilo.
En algunas realizaciones:
Cy es fenilo, que está opcionalmente sustituido con de 1 a 5 sustituyentes R6 independientemente seleccionados; o dos sustituyentes R6 adyacentes en el anillo Cy, tomados junto con los átomos a los que están unidos, forman un anillo heterocicloalquilo de 5, 6 o 7 miembros fusionado, o un anillo heteroarilo de 5 o 6 miembros fusionado, en donde el anillo de heterocicloalquilo de 5, 6 o 7 miembros fusionado y el anillo de heteroarilo de 5 o 6 miembros fusionado tienen cada uno 1-4 heteroátomos como miembros del anillo seleccionados de N, O y S y en donde el anillo de heterocicloalquilo de 5, 6 o 7 miembros fusionado y el anillo de heteroarilo de 5 o 6 miembros fusionado están cada uno opcionalmente sustituidos con 1, 2 o 3 sustituyentes Rb independientemente seleccionados;
R1 , R2 y R3 se seleccionan cada uno independientemente de H, alquilo C1 -4 , alquenilo C2-4, alquinilo C2-4, halo, CN, OH, COOH, alcoxi C1 -4 , haloalquilo C1 -4 , haloalcoxi C1 -4 , ciclopropilo, ciclopropilmetilo, fenilo, fenil-alquilo C1 -4-, heteroarilo de 5-6 miembros, (heteroarilo de 5-6 miembros)-alquilo C1-4-, heterocicloalquilo de 4-6 miembros, (heterocicloalquilo de 4-6 miembros) -alquilo C1-4-, NH2 , -NHalquilo C1 -4 , -N(alquilo C1 -4 )2 , -C(O)R10 , -O(CO)R10 ,
C(O)OR10, -O(CO)NHR10, -NHC(O)OR10, -NHC(O)NHR10, -C(O)NHR10, -NHC(O)R10, -SO2 R10, -NHSO2 R10 y -SO2 NHR10, en donde el alquilo C1 -4, alquenilo C2-4, alquinilo C2-4, alcoxi C1.4, ciclopropilo, ciclopropilmetilo, fenilo, fenil-alquilo C1.4-, heteroarilo de 5-6 miembros, (heteroarilo de 5-6 miembros)-alquilo C1 -4-, heterocicloalquilo de
4-6 miembros y (heterocicloalquilo de 4-6 miembros)-alquilo C1 -4- de R1, R2 o R3 están cada uno opcionalmente sustituidos con halo, OH, CN o alcoxi C1 -4;
R4, R5 y R6 se seleccionan cada uno independientemente de H, halo, alquilo C1 -6, alcoxi C1.6, alquenilo C2-6, alquinilo C2-6, haloalquilo C1.6, haloalcoxi C1.6, fenilo, cicloalquilo C3-6, heterocicloalquilo de 4-6 miembros, heteroarilo de 5-6 miembros, fenil-alquilo C1 -4-, cicloalquilo C3-6-alquilo C1.4-, (heteroarilo de 5-6 miembros)-alquilo
C1.4- o (heterocicloalquilo de 4-6 miembros)-alquilo C1.4-, CN, o H, COOH, NO2 , ORa, C(O)ORa, NH2 , -NHRa, -N(Ra)2, -C(O)Ra, -O(CO)Ra, -C(O)ORa, -O(CO)NRaRa, -NHC(O)ORa, -NHC(O)NRaRa, -C(O)NRaRa, -SO2 Ra, -NHSo2 Ra y -SO2 NRaRa, en donde el alquilo C1 -6, alquenilo C2-6, alquinilo C2-6, fenilo, cicloalquilo C3-6, heterocicloalquilo de 4-6 miembros, heteroarilo de 5-6 miembros, fenil-alquilo C1 -4-, cicloalquilo C3-6-alquilo C1.4-, (heteroarilo de 5-6 miembros)-alquilo C1.4- y (heterocicloalquilo de 4-6 miembros)-alquilo C1.4-- de R4, R5 y R6 están cada uno opcionalmente sustituidos con 1 o 2 sustituyentes Rb;
R7 es halo, alquilo C1 -6, CN, cicloalquilo C3-6, heterocicloalquilo de 4-6 miembros, heteroarilo de 5-6 miembros, cicloalquilo C3-6-alquilo C1 -4-, (heterocicloalquilo de 4-6 miembros)-alquilo C1.4-, (heteroarilo de 5-6 miembros)-alquilo C1.4, en donde el alquilo C1 -6, cicloalquilo C3-6, heterocicloalquilo de 4-6 miembros, heteroarilo de 5-6 miembros, cicloalquilo C3-6-alquilo C1 -4-, (heterocicloalquilo de 4-6 miembros)-alquilo C1.4- y (heteroarilo de 5-6 miembros)-alquilo C1.4 de R7 están cada uno opcionalmente sustituidos con 1 o 2 sustituyentes independientemente seleccionados de halo, alquilo C1 -6, haloalquilo C1 -6, haloalcoxi C1 -6, CN, OH, NH2 , -NH(alquilo C1 -6), -N(alquilo C1 -6)2 , COOH, -Oalquilo C1 -6, -Salquilo C1 -6, C(O)NH2 , -C(O)NH(alquilo C1 -6), -C(O)NH(alquilo C1 -6)2 , -C(O)OCalquilo 1 -6, -OC(O)NHalquilo C1 -6, -OC(O)NH2 , -OC(O)NH(alquilo C1 -6)2 , -NHC(O)alquilo C1 -6, -NHC(O)H, -N(alquilo C1 -6)C(O)alquilo C1 -6, -NHC(O)Oalquilo C1 -6, -N(alquilo C1 -6)C(O)Oalquilo C1 -6, -NHC(O)NH(alquilo C1 -6), -NHC(O)N(alquilo C1 -6)2 , -NHC(O)NH2 , -N(alquilo C1 -6)C(O)NH
alquilo (C1 -6), -N(alquilo C1 -6)C(O)N(alquilo C1 -6)2 , -N(alquilo C1 -6)C(O)NH2 , -NHS(O)2(alquilo C1 -6), -N(alquilo C1 -6)S(O)2(alquilo C1 -6), -NHS(O)2 NH2 , -NHS(O)2 NH(alquilo C1 -6), -NHS(O)2 N(alquilo C1 -6)2 , -N(alquilo C1 -6)2 , -N(alquilo C1 -6))S(O)2 NH2 , -N(alquilo C1 -6)S(O)2 NH(alquilo C1 -6), -N(alquilo C1 -6)S(O)2 N(alquilo C1 -6)2 , -S(O)2(alquilo
C1.6), -S(O)2 NH2 , -S(O)2 NH(alquilo C1.6) y -S(O)2 N(alquilo C ^ ;
R8 es alquilo C1-6 sustituido con 1-3 sustituyentes Rb2 independientemente seleccionados o (heterocicloalquilo de
4- 10 miembros)-alquilo-C1 -4- opcionalmente sustituido con 1, 2 o 3 sustituyentes Rb independientemente seleccionados;
cada R11 se selecciona independientemente de H, alquilo C1 -6, haloalquilo C1 -6, alquenilo C2-6, alquinilo C2-6, fenilo, cicloalquilo C3-6, heteroarilo de 5-6 miembros, heterocicloalquilo de 4-6miembros, fenilo-alquilo C1 -4-, cicloalquilo C3-6 -alquilo C1.4-, (heteroarilo de 5-6 miembros)-alquilo C1 -4- y (heterocicloalquilo de 4-6 miembros)-alquilo C1.4-, en donde el alquilo C1 -6, haloalquilo C1.6, alquenilo C2-6, alquinilo C2-6, fenilo, cicloalquilo C3-6, heteroarilo de 5-6 miembros, heterocicloalquilo de 4-6 miembros, fenilo-alquilo C1 -4-, cicloalquilo C3-6-alquilo C1.4-, (heteroarilo de 5-6 miembros)-alquilo C1.4- y (heterocicloalquilo de 4-6 miembros)-alquilo C1 -4- de R11 están cada uno opcionalmente sustituidos con 1 o 2 sustituyentes Rb;
cada Ra se selecciona independientemente de H, alquilo C1 -6, haloalquilo C1.6, alquenilo C2-6, alquinilo C2-6, fenilo, cicloalquilo C3-6, heterocicloalquilo de 4-6 miembros, heteroarilo de 5-6 miembros, fenilo-alquilo C1 -4-, cicloalquilo
C3-6-alquilo C1.4-, (heteroarilo de 5-6 miembros)-alquilo C1.4- y (heterocicloalquilo de 4-6 miembros)-alquilo C1 -4-;
cada Rb se selecciona independientemente de halo, alquilo C1 -6, alcoxi C1.6, haloalquilo C1.6, haloalcoxi C1 -6, alquenilo C2-6, alquinilo C2-6, fenilo, cicloalquilo C3-6, heteroarilo de 5-6 miembros, heterocicloalquilo de 4-6 miembros, fenil-alquilo C1 -4-, cicloalquilo C3-6-alquilo C1 -4-, (heteroarilo de 5-6 miembros)-alquilo C1.4-, y (heterocicloalquilo de 4-6 miembros)-alquilo C1.4-, CN, OH, NH2 , NHRc, N(Rc)2 , ORc, C(O)NRcRc, C(O)ORc, COOH, NRcC(O)Rc, OC(O)NRcRc, NRcC(O)ORc, NRcC(O)NRcRc, NRcS(O)2Rc, NRcS(O)2NRcRc, S(O)2Rcy
S(O)2 NRcRc, en donde el alquilo C1 -6, alcoxi C1.6, alquenilo C2-6, alquinilo C2-6, fenilo, cicloalquilo C3-6, heteroarilo de 5-6 miembros, heterocicloalquilo de 4-6 miembros, fenil-alquilo C1 -4-, cicloalquilo C3-6-alquilo C1.4-, (heteroarilo de 5-6 miembros)-alquilo C1 -4- y (heterocicloalquilo de 4-6 miembros)-alquilo C1.4- de Rb están cada uno opcionalmente sustituidos con 1 o 2 sustituyentes Rd independientemente seleccionados de halo, C1-6 alquilo, alcoxi C1 -6, alquenilo C2-6, alquinilo C2-6, haloalquilo C1.6, haloalcoxi C1 -6, fenilo, cicloalquilo C3-6, cicloalquil alquilo C1.4-, heterocicloalquilo de 4-6 miembros, (heterocicloalquilo de 4-6 miembros)-alquilo C1 -4-, heteroarilo de
5- 6 miembros, (heteroarilo de 4-6 miembros)-alquilo C1 -4-, CN, OH, COOH, ORe, C(O)ORe, NH2 , -NHRe, -N(Re)2 , -C(O)NReRe, -NReC(O)Re, OC(O)NReRe, NReC(O)ORe, NReC(O)NReRe, NReS(O)2Re, NReS(O)2NReRe, S(O)2Rey
S(O)2 NReRe, en donde Re es H o alquilo C1 -6;
cada Rc se selecciona independientemente de H, alquilo C1 -6, haloalquilo C1.6, alquenilo C2-6, alquinilo C2-6, fenilo, cicloalquilo C3-6, heteroarilo de 5-6 miembros, heterocicloalquilo de 4-6 miembros, fenil-alquilo C1 -4-, cicloalquilo
C3-6-alquilo C1.4-, (heteroarilo de 5-6 miembros)-alquilo C1.4- y (heterocicloalquilo de 4-6 miembros)-alquilo C1.4-, en donde el alquilo C1 -6, alquenilo C2-6, alquinilo C2-6, fenilo, cicloalquilo C3-6, heteroarilo de 5-6 miembros, heterocicloalquilo de 4-6 miembros, fenil-alquilo C1 -4-, cicloalquilo C3-6-alquilo C1.4-, (heteroarilo de 5-6 miembros)-alquilo C1.4- y (heterocicloalquilo de 4-6 miembros)-alquilo C1 -4- de Rc están cada uno opcionalmente sustituidos con 1 o 2 sustituyentes Rf;
o dos sustituyentes Rc junto con el átomo de nitrógeno al que están unidos forman un grupo heterocicloalquilo de
4, 5, 6 o 7 miembros opcionalmente sustituido con 1 o 2 sustituyentes Rh independientemente seleccionados;
cada Rf se selecciona independientemente de halo, alquilo C1 -6, alcoxi C1 -6, alquenilo C2-6, alquinilo C2-6,
haloalquilo C1 -6 , haloalcoxi C1-6 , fenilo, cicloalquilo C3-6, heterocicloalquilo de 4-6 miembros, heteroarilo de 5-6 miembros, CN, OH, COOH, ORg, C(O)ORg, NH2 , -NHRg, -N(Rg)2 , -C(O)NRgRg, -NRgC(O)Rg, OC(O)NRgRg, NRgC(O)ORg, NRgC(O)NRgRg, NRgS(O)2 Rg, NRgS(O)2 NRgRg, S(O)2 Rg y S(O)2 NRgRg, en donde cada Rg es independientemente H, alquilo C1 -6 , haloalquilo C1-6 , alquenilo C2-6 o alquinilo C2 -6 ;y
cada Rh se selecciona independientemente de halo, alquilo C1 -6 , haloalquilo C1 -6 , haloalcoxi C1 -6 , CN, OH, NH2 , NHRi, N(Ri)2 , ORi, C(O)NRiRi, NRiC(O)Ri y C(O)ORi, en donde R1 es H o alquilo C1 -6.
En algunas realizaciones:
Cy es fenilo que está opcionalmente sustituido con 1 a 5 sustituyentes R6 independientemente seleccionados;
R1, R2 y R3 se seleccionan cada uno independientemente de H, alquilo C1 -4 , cicloalquilo C3 -10 , arilo C6 -10 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, alquenilo C2-4, alquinilo C2-4, halo, CN, OH, alcoxi C1.4 , haloalquilo C1.4 , haloalcoxi C1.4 , NH2 , -NHR10, -NR10R10, NHOR10, C(O)R10, C(O)NR10 OC(O)R10, OC(O)NR10R10, NR10C(O)R10, y NR10C(O)OR10, en donde cada R10 se selecciona independientemente de H, alquilo C1 -4 , alcoxi C1.4 , cicloalquilo C3 -10 , arilo C6 -10 , heteroarilo de 5-10 miembros y heterocicloalquilo de 4-10 miembros, en donde el alquilo C1 -4 , alcoxi C1 -4 , cicloalquilo C3 -10 , arilo C6-10, heteroarilo
de 5-10 miembros y heterocicloalquilo de 4-10 miembros de R1, R2 , R3 y R10 están cada uno opcionalmente sustituidos con 1 o 2 sustituyentes Rd independientemente seleccionados;
R4, R5 y R6 se seleccionan cada uno independientemente de H, halo, alquilo C1 -6 , alquenilo C2-6, alquinilo C2-6, haloalquilo C1.6 , haloalcoxi C1.6 , arilo C6 -10 , cicloalquilo C3 -10 , heteroarilo de 5-14 miembros, heterocicloalquilo de
4-10 miembros, CN, NO2 , ORa, SRa, NHORa, C(O)Ra, C(O)NRaRa, C(O)ORa, OC(O)Ra , OC(O)NRaRa, NHRa, NRaRa , NRaC(O)Ra , y NRaC(O)ORa, en donde el alquilo C1.6 , alquenilo C2-6, alquinilo C2-6, arilo C6 -10 , cicloalquilo
C3 -10 , heteroarilo de 5-14 miembros y heterocicloalquilo de 4-10 miembros de R4, R5 y R6 están cada uno opcionalmente sustituidos con 1, 2, 3, 4 o 5 sustituyentes Rb independientemente seleccionados;
o dos sustituyentes R6 adyacentes en el anillo Cy, tomados junto con los átomos a los que están unidos, forman
un anillo de fenilo fusionado, un anillo de heterocicloalquilo de 5, 6 o 7 miembros fusionado, un anillo de heteroarilo de 5 o 6 miembros fusionado o un anillo de cicloalquilo C3-6 fusionado, en donde el anillo de heterocicloalquilo de 5, 6 o 7 miembros fusionado y el anillo de heteroarilo de 5 o 6 miembros fusionado tienen
cada uno 1-4 heteroátomos como miembros del anillo seleccionados de N, O y S y en donde el anillo de fenilo fusionado, el anillo de heterocicloalquilo de 5, 6 o 7 miembros fusionado, el anillo de heteroarilo de 5 o 6 miembros fusionado y el anillo de cicloalquilo C3-6 fusionado están cada uno opcionalmente sustituidos con 1,2 o
3 sustituyentes Rb independientemente seleccionados;
R7 es halo, alquilo C1 -6 , alquenilo C2-6, alquinilo C2-6, haloalquilo C1 -6 , haloalcoxi C1-6 , arilo C6-10, cicloalquilo C3 -10 , heteroarilo de 5-14 miembros, heterocicloalquilo de 4 a 10 miembros, CN, NO2 , OR11, SR11, NH2 , -NHR11, -NR11R11, NHOR11, C(O)R11, C(O)NR11R11, C(O)OR11, OC(O)R11, OC(O)NR11R11, NR11C(O)R11, y NR11C(O)OR11, en donde el alquilo C1 -6 , alquenilo C2-6, alquinilo C2-6, haloalquilo C1.6 , haloalcoxi C1.6 , arilo C6 -10 , cicloalquilo C3 -10 , heteroarilo de 5-14 miembros y heterocicloalquilo de 4-10 miembros de R7 están cada uno opcionalmente sustituido con 1,2 o 3 sustituyentes Rb independientemente seleccionados;
R8 es alquilo C1-6 sustituido con 1-3 sustituyentes Rb2 independientemente seleccionados o (heterocicloalquilo de
4-10 miembros)-alquilo C1.4- opcionalmente sustituido con 1, 2 o 3 sustituyentes Rb independientemente seleccionados;
cada R11 se selecciona independientemente de H, alquilo C1-6 , haloalquilo C1.6 , alquenilo C2-6, alquinilo C2-6, arilo
C6 -10 , cicloalquilo C3 -10 , heteroarilo de 5-10 miembros, y heterocicloalquilo de 4-10 miembros, en donde el alquilo
C1 -6 , alquenilo C2-6, alquinilo C2-6, arilo C6-10, cicloalquilo C3 -10 , heteroarilo de 5-10 miembros y heterocicloalquilo
de 4-10 miembros de R11 están cada uno opcionalmente sustituidos con 1, 2 o 3 sustituyentes Rb independientemente seleccionados;
cada Ra se selecciona independientemente de H, alquilo C1 -6 , haloalquilo C1 -6 , alquenilo C2-6, alquinilo C2-6, arilo
C6 -10 , cicloalquilo C3 -10 , heteroarilo de 5-10 miembros, y heterocicloalquilo de 4-10 miembros, en donde el alquilo
C1 -6 , haloalquilo C1 -6 , alquenilo C2-6, alquinilo C2-6, arilo C6 -10 , cicloalquilo C3 -10 , heteroarilo de 5-10 miembros y heterocicloalquilo de 4-10 miembros de Ra están cada uno opcionalmente sustituidos con 1,2 o 3 sustituyentes
Rd independientemente seleccionados;
cada sustituyente Rb se selecciona independientemente de halo, alquilo C1 -6 , haloalquilo C1 -6 , haloalcoxi C1.6 , arilo C6 -10 , cicloalquilo C3 -10 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, CN, OH, NH2 ,
NO2 , NHORc, ORc, SRc , C(O)Rc, C(O)NRcRc, C(O)ORc , OC(O)Rc, y OC(O)NRcRc; en donde el alquilo C1.6 , haloalquilo C1.6 , haloalcoxi C1.6 , arilo C6 -10 , cicloalquilo C3 -10 , heteroarilo de 5-10 miembros y heterocicloalquilo de
4-10 miembros de Rb están cada uno opcionalmente sustituidos con 1-3 sustituyentes Rd independientemente seleccionados;
cada Rb2 se selecciona independientemente de halo, haloalquilo C1 -6 , haloalcoxi C1-6 , arilo C6 -10 , cicloalquilo C3 -10 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, CN, OH, NH2 , NO2 , NHORc, Orc, SRc , C(O)Rc, C(O)NRcRc , C(O)ORc, OC(O)Rc, OC(O)NRcRc , NHRc , NRcRc, NRcC(O)Rc, y NRcC(O)ORc; en donde el haloalquilo C1.6 , haloalcoxi C1.6 , arilo C6 -10 , cicloalquilo C3 -10 , heteroarilo de 5-10 miembros y heterocicloalquilo de
4-10 miembros de Rb2 están cada uno opcionalmente sustituidos con 1-3 sustituyentes Rd independientemente seleccionados;
cada Rc se selecciona independientemente de H, alquilo C1 -6 , haloalquilo C1 -6 , alquenilo C2-6, alquinilo C2-6, arilo
C6 -10 , cicloalquilo C3 -10 , heteroarilo de 5-10 miembros, y heterocicloalquilo de 4-10 miembros, en donde el alquilo
C1 -6 , haloalquilo C1 -6 , alquenilo C2-6, alquinilo C2-6, arilo C6 -10 , cicloalquilo C3 -10 , heteroarilo de 5-10 miembros y heterocicloalquilo de 4-10 miembros de Rc están cada uno opcionalmente sustituidos con 1, 2 o 3 sustituyentes Rf independientemente seleccionados de alquilo C1-6 , haloalquilo C1 -6 , alquenilo C2-6, alquinilo C2-6, arilo C6 -10 , cicloalquilo C3 -10 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, halo, CN, CN, NHORg, ORg, SRg, C(O)Rg, C(O)NRgRg, C(O)ORg, OC(O)Rg, OC(O)NRgRg, NHRg, NRgRg, NRgC(O)Rg, NRgC(O)NRgRg, y NRgC(O)ORg; en donde el alquilo C1 -6 , haloalquilo C1.6 , alquenilo C2-6, alquinilo C2-6, arilo C6-10, cicloalquilo C3 -10 , heteroarilo de 5-10 miembros y heterocicloalquilo de 4-10 miembros de Rf están cada uno opcionalmente sustituidos con 1, 2 o 3 sustituyentes Rn independientemente seleccionados de alquilo C1 -6 , haloalquilo C1.6 , halo, CN, fenilo, cicloalquilo C3-6, heteroarilo de 5-6 miembros, heterocicloalquilo de 4-6 miembros, NHORo, ORo, SRo, C(O)Ro, C(O)NR° R° , C(O)ORo, OC(O)Ro, OC(O)NR° R° , NHRo, NR° R° , NR° C(O)R° , NR° C(O)NR° R° , y NR° C(O)OR° , en donde el alquilo C1-6 , haloalquilo C1.6 , fenilo, cicloalquilo C3-6, heteroarilo de 5-6 miembros, y heterocicloalquilo de 4-6 miembros de Rn están cada uno opcionalmente sustituidos con 1, 2 o 3 sustituyentes Rq;
cada Rd se selecciona independientemente de alquilo C1 -6 , haloalquilo C1.6 , halo, arilo C6 -10 , heteroarilo de 5-10 miembros, cicloalquilo C3 -10 , heterocicloalquilo de 4-10 miembros, CN, NH2 , NHORe, ORe , SRe, C(O)Re, C(O)NRe Re, C(O)ORe, OC(O)Re, OC(O)NReRe, NHRe , NRe Re , NReC(O)Re, NReC(O)NReRe, y NReC(O)ORe, en donde el alquilo C1 -6 , haloalquilo C1.6 , arilo C6 -10 , heteroarilo de 5-10 miembros, cicloalquilo C3-10 y heterocicloalquilo de 4 10 miembros de Rd están cada uno opcionalmente sustituidos con 1-3 sustituyentes Rf independientemente seleccionados;
cada Re se selecciona independientemente de H, alquilo C1-6 , haloalquilo C1.6 , alquenilo C2-6 y alquinilo C2-6; cada Rg se selecciona independientemente de H, alquilo C1-6 , haloalquilo C1.6 , alquenilo C2-6 y alquinilo C2-6; cada R° se selecciona independientemente de H, alquilo C1 -6 , haloalquilo C1.6 , cicloalquilo C3-6, arilo C6 -10 , heterocicloalquilo de 4-6 miembros, heteroarilo de 5 o 6 miembros, haloalquilo C1.4 , alquenilo C2-4 y alquinilo C2-4; cada Rq se selecciona independientemente de OH, CN, -COOH, NH2 , halo, haloalquilo C1 -6 , alquilo C1.6 , alcoxi C1.6 , haloalcoxi C1.6 , alquiltio C1-6 , fenilo, heteroarilo de 5-6 miembros, heterocicloalquilo de 4-6 miembros, cicloalquilo C3-6, NHR12 y NR12R12 y cada R12 es independientemente alquilo C1 -6 ; y
-------es un enlace simple o un enlace doble para que el anillo A siga siendo aromático.
En algunas realizaciones:
Cy es fenilo que está opcionalmente sustituido con de 1 a 5 sustituyentes R6 independientemente seleccionados; R1, R2 y R3 se seleccionan cada uno independientemente de H, alquilo C1 -4 , alquenilo C2-4, alquinilo C2-4, halo, CN, OH, alcoxi C1.4 , haloalquilo C1.4 , haloalcoxi C1 -4 , NH2 , -NH-alquilo C1.4 , -N(alquilo C1 -4 )2 , en donde el alquilo C1-4 y el alcoxi C1.4 de R1, R2 y R3 están cada uno opcionalmente sustituidos con 1 o 2 sustituyentes Rd independientemente seleccionados;
R4, R5 y R6 se seleccionan cada uno independientemente de H, halo, alquilo C1 -6 , alquenilo C2-6, alquinilo C2-6, haloalquilo C1.6 , haloalcoxi C1.6 , CN, NO2 , ORa , SRa, NHORa, C(O)Ra, C(O)NRaRa , C(O)ORa , NHRa y NRaRa, en donde el alquilo C1.6 , alquenilo C2-6 y alquinilo C2-6 de R4, R5 y R6 están cada uno opcionalmente sustituidos con 1, 2, 3, 4 o 5 sustituyentes Rb independientemente seleccionados;
o dos sustituyentes R6 adyacentes en el anillo Cy, tomados junto con los átomos a los que están unidos, forman un anillo de fenilo fusionado, un anillo de heterocicloalquilo de 5, 6 o 7 miembros fusionado, un anillo de heteroarilo de 5 o 6 miembros fusionado o un anillo de cicloalquilo C3-6 fusionado, en donde el anillo de heterocicloalquilo de 5, 6 o 7 miembros fusionado y el anillo de heteroarilo de 5 o 6 miembros fusionado tienen cada uno 1-4 heteroátomos como miembros del anillo seleccionados de N, O y S y en donde el anillo de fenilo fusionado, el anillo de heterocicloalquilo de 5, 6 o 7 miembros fusionado, el anillo de heteroarilo de 5 o 6 miembros fusionado y el anillo de cicloalquilo C3-6 fusionado están opcionalmente sustituidos con 1, 2 o 3 sustituyentes Rb independientemente seleccionados;
R7 es halo, alquilo C1-6 , alquenilo C2-6, alquinilo C2-6, haloalquilo C1 -6 , haloalcoxi C1 -6 , CN, NO2 , OR11, SR11, NH2 , -NHR11, -NR11R11, C(O)R11, C(O)NR11R11, C(O)OR11, NR11C(O)R11, y NR11C(O)OR11, en donde el alquilo C1.6 , alquenilo C2-6, alquinilo C2-6, haloalquilo C1.6 y haloalcoxi C1.6 de R7 están cada uno opcionalmente sustituidos con 1,2 o 3 sustituyentes Rb independientemente seleccionados;
R8 es alquilo C1-6 sustituido con 1-3 sustituyentes Rb2 independientemente seleccionados o (heterocicloalquilo de 4-10 miembros)-alquilo C1.4- opcionalmente sustituido con 1, 2 o 3 sustituyentes Rb independientemente seleccionados;
cada R11 se selecciona independientemente de H, alquilo C1-6 , haloalquilo C1.6 , alquenilo C2-6 y alquinilo C2-6, en donde el alquilo C1.6 , alquenilo C2 -6 y alquinilo C2-6 de R11 están cada uno opcionalmente sustituidos con 1,2 o 3 sustituyentes Rb independientemente seleccionados;
cada Ra se selecciona independientemente de H, alquilo C1 -6 , haloalquilo C1.6 , alquenilo C2-6 y alquinilo C2-6, en donde el alquilo C1.6 , haloalquilo C1.6 , alquenilo C2-6 y alquinilo C2-6 de Ra están cada uno opcionalmente sustituidos con 1,2 o 3 sustituyentes Rd independientemente seleccionados;
cada sustituyente Rb se selecciona independientemente de halo, alquilo C1 -6 , haloalquilo C1 -6 , haloalcoxi C1.6 , CN, OH, NH2 , n Ho Rc, ORc, C(O)Rc, C(O)NRcRc y C(O)ORc ; en donde el alquilo C1-6 , el haloalquilo C1.6 y el haloalcoxi C1-6 de Rb están cada uno opcionalmente sustituidos con 1-3 sustituyentes Rd independientemente seleccionados;
cada Rb2 se selecciona independientemente de halo, haloalquilo C1 -6 , haloalcoxi C1-6 , arilo C6 -10, cicloalquilo C3 -10 ,
heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, CN, OH, NH2 , NO2 , NHORc, ORc , SRc , C(O)Rc, C(O)NRcRc , C(O)ORc, OC(O)Rc, OC(O)NRcRc, NHRc , NRcRc, NRcC(O)Rc, y NRcC(O)ORc ; en donde el haloalquilo C1.6 , el haloalcoxi C1.6 , el arilo C6 -10 , el cicloalquilo C3.10 , el heteroarilo de 5-10 miembros y el heterocicloalquilo de 4-10 miembros de Rb2 están cada uno además opcionalmente sustituidos con 1-3 sustituyentes Rd independientemente seleccionados;
cada Rc se selecciona independientemente de H, alquilo C1-6 , haloalquilo C1 -6 , alquenilo C2-6 y alquinilo C2-6, en
donde el alquilo C1 -6 , haloalquilo C1.6 , alquenilo C2-6 y alquinilo C2-6 de Rc están cada uno opcionalmente sustituidos con 1, 2 o 3 sustituyentes Rf independientemente seleccionados de alquilo C1 -6 , haloalquilo C1.6 , alquenilo C2-6, alquinilo C2-6, halo, CN, ORg, C(O)Rg, C(O)NRgRg, C(O)ORg, NHRg, NRgRg, y se selecciona independientemente de alquilo C1-6 , haloalquilo C1.6 , halo, CN, NH2 , NHORe , ORe, C(O)Re , C(O)NReRe, C(O)ORe , NHRe , NReRe , NReC(O)Re , NReC(O)NReRe , y NReC(O)ORe ;
cada Re se selecciona independientemente de H, alquilo C1-6 , haloalquilo C1.6 , alquenilo C2-6 y alquinilo C2-6;
cada Rg se selecciona independientemente de H, alquilo C1-6 , haloalquilo C1.6 , alquenilo C2-6 y alquinilo C2-6;
-------- es un enlace simple o un enlace doble para que el anillo A siga siendo aromático.
En algunas realizaciones:
Cy es fenilo que está opcionalmente sustituido con de 1 a 5 sustituyentes R6 independientemente seleccionados;
R1, R2 y R3 se seleccionan cada uno independientemente de H, alquilo C1 -4 , alquenilo C2-4, alquinilo C2-4, halo,
CN, OH, NH2 , -NH- alquilo C1-4 y -N(alquilo C1 -4 )2 ;
R4, R5 y R6 se seleccionan cada uno independientemente de H, halo, alquilo C1-6 , alquenilo C2-6, alquinilo C2-6 y
ORa , en donde el alquilo C1 -6 , alquenilo C2-6 y alquinilo C2-6 de R4, R5 y R6 están cada uno opcionalmente sustituido con 1, 2, 3, 4 o 5 sustituyentes Rb independientemente seleccionados;
o dos sustituyentes R6 adyacentes en el anillo Cy, tomados junto con los átomos a los que están unidos, forman
un anillo de fenilo fusionado, un anillo de heterocicloalquilo de 5, 6 o 7 miembros fusionado, un anillo de heteroarilo de 5 o 6 miembros fusionadoo o un anillo de cicloalquilo C3-6 fusionado, en donde el anillo de heterocicloalquilo de 5, 6 o 7 miembros fusionado y el anillo de heteroarilo de 5 o 6 miembros fusionado tienen
cada uno 1-4 heteroátomos como miembros del anillo seleccionados de N, O y S y en donde el anillo de fenilo fusionado, el anillo de heterocicloalquilo de 5, 6 o 7 miembros fusionado, el anillo de heteroarilo de 5 o 6 miembros fusionado y el anillo de cicloalquilo C3-6 fusionado están cada uno opcionalmente sustituidos con 1,2 o
3 sustituyentes Rb independientemente seleccionados;
R7 es halo, alquilo C1 -6 , alquenilo C2-6, alquinilo C2-6 o CN, en donde el alquilo C1-6 , el alquenilo C2-6 y el alquinilo
C2-6 de R7 están cada uno opcionalmente sustituidos con 1, 2 o 3 sustituyentes Rb independientemente seleccionados;
R8 es alquilo C1-6 sustituido con 1-3 sustituyentes Rb2 independientemente seleccionados o (heterocicloalquilo de
4-10 miembros)-alquilo C1-4- opcionalmente sustituido con 1, 2 o 3 sustituyentes Rb independientemente seleccionados;
cada Ra se selecciona independientemente de H, alquilo C1-6 , alquenilo C2-6 y alquinilo C2-6;
cada sustituyente Rb se selecciona independientemente de halo y alquilo C1 -6 ;
cada Rb2 se selecciona independientemente de halo, haloalquilo C1 -6 , haloalcoxi C1 -6 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, NHRc , NRcRc y NRcC(O)Rc; en donde el haloalquilo C1 -6 , el haloalcoxi C1 -6 , el heteroarilo de 5-10 miembros y el heterocicloalquilo de 4-10 miembros de Rb2 están cada uno opcionalmente sustituidos con 1-3 sustituyentes Rd independientemente seleccionados;
cada Rc se selecciona independientemente de H, alquilo C1-6 , haloalquilo C1 -6 , alquenilo C2-6 y alquinilo C2-6, en
donde el alquilo C1 -6 , haloalquilo C1 -6 , alquenilo C2-6 y alquinilo C2-6 de Rc están cada uno opcionalmente sustituidos con 1, 2 o 3 sustituyentes Rf independientemente seleccionados de alquilo C1 -6 , haloalquilo C1.6 , alquenilo C2-6, alquinilo C2-6, halo, ORg, C(O)Rg, C(O)NRgRg, NHRg y NRgRg;
cada Rd se selecciona independientemente de alquilo C1-6 , haloalquilo C1 -6 , halo, CN, NH2 , ORe, C(O)Re, C(O)NReRe, C(O)ORe , NHRe , NReRe , y NReC(O)Re;
cada Re se selecciona independientemente de H, alquilo C1-6 , alquenilo C2-6 y alquinilo C2-6;
cada Rg se selecciona independientemente de H, alquilo C1-6 , alquenilo C2-6 y alquinilo C2-6;
-------- es un enlace simple o un enlace doble para que el anillo A siga siendo aromático.
En algunas realizaciones:
Cy es fenilo que está opcionalmente sustituido con 1 a 5 sustituyentes R6 independientemente seleccionados;
R1, R2 y R3 se seleccionan cada uno independientemente de H, alquilo C1 -4 , cicloalquilo C3 -10 , arilo C6 -10 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, alquenilo C2-4, alquinilo C2-4, halo, CN, OH, alcoxi C1 -4 , haloalquilo C1 -4 , haloalcoxi C1 -4 , NH2 , -NHR10, -NR10R10, NHOR10, C(O)R10, C(O)NR10 OC(O)R10 , OC(O)NR10 R10 , NR10C(O)R10 , y NR10C(O)OR10 , en donde cada R10 se selecciona independientemente de H, alquilo C1.4 , alcoxi C1 -4 , cicloalquilo C3.10 , arilo C6 -10 , heteroarilo de 5-10 miembros y heterocicloalquilo de 4-10 miembros, en donde el alquilo C1 -4 , alcoxi C1 -4 , cicloalquilo C3 -10 , arilo C6-10, heteroarilo
de 5-10 miembros y heterocicloalquilo de 4-10 miembros de R1, R2 , R3 y R10 están cada uno opcionalmente sustituidos con 1 o 2 sustituyentes Rd independientemente seleccionados;
R4, R5 y R6 se seleccionan cada uno independientemente de H, halo, alquilo C1 -6 , alquenilo C2-6, alquinilo C2-6,
haloalquilo C1 -6 , haloalcoxi C1 -6 , arilo C6 -10 , cicloalquilo C3 -10 , heteroarilo de 5-14 miembros, heterocicloalquilo de 4-10 miembros, CN, NO2 , ORa, SRa, NHORa, C(O)Ra, C(O)NRaRa, C(O)ORa, OC(O)Ra , OC(O)NRaRa, NHRa, NRaRa , NRaC(O)Ra , y NRaC(O)ORa, en donde el alquilo C1-6 , alquenilo C2-6, alquinilo C2-6, arilo C6 -10 , cicloalquilo C3 -10 , heteroarilo de 5-14 miembros y heterocicloalquilo de 4-10 miembros de R4, R5 y R6 están cada uno opcionalmente sustituidos con 1, 2, 3, 4 o 5 sustituyentes Rb independientemente seleccionados;
o dos sustituyentes R6 adyacentes en el anillo Cy, tomados junto con los átomos a los que están unidos, forman un anillo de fenilo fusionado, un anillo de heterocicloalquilo de 5, 6 o 7 miembros fusionado, un anillo de heteroarilo de 5 o 6 miembros fusionado o un anillo de cicloalquilo C3-6 fusionado, en donde el anillo de heterocicloalquilo de 5, 6 o 7 miembros fusionado y el anillo de heteroarilo de 5 o 6 miembros fusionado tienen cada uno 1-4 heteroátomos como miembros del anillo seleccionados de N, O y S y en donde el anillo de fenilo fusionado, el anillo de heterocicloalquilo de 5, 6 o 7 miembros fusionado, el anillo de heteroarilo de 5 o 6 miembros fusionado y el anillo de cicloalquilo C3-6 fusionado están cada uno opcionalmente sustituidos con 1,2 o 3 sustituyentes Rb independientemente seleccionados;
R7 es halo, alquilo C1 -6 , alquenilo C2-6, alquinilo C2-6, haloalquilo C1 -6 , haloalcoxi C1-6 , arilo C6-10, cicloalquilo C3 -10 , heteroarilo de 5-14 miembros, heterocicloalquilo de 4 a 10 miembros, CN, NO2 , OR11, SR11, NH2 , -NHR11, -NR11R11, NHOR11, C(O)R11, C(O)NR11R11, C(O)OR11, OC(O)R11, OC(O)NR11R11, NR11C(O)R11, y NR11C(O)OR11, en donde el alquilo C1 -6 , alquenilo C2-6, alquinilo C2-6, haloalquilo C1.6 , haloalcoxi C1 -6 , arilo C6 -10 , cicloalquilo C3 -10 , heteroarilo de 5-14 miembros y heterocicloalquilo de 4-10 miembros de R7 están cada uno opcionalmente sustituido con 1,2 o 3 sustituyentes Rb independientemente seleccionados;
R8 es alquilo C1-6 sustituido con 1-3 sustituyentes Rb2 independientemente seleccionados o (heterocicloalquilo de 4-10 miembros)-alquilo C1.4- opcionalmente sustituido con 1, 2 o 3 sustituyentes Rb independientemente seleccionados;
cada R11 se selecciona independientemente de H, alquilo C1-6 , haloalquilo C1.6 , alquenilo C2-6, alquinilo C2-6, arilo C6 -10 , cicloalquilo C3 -10 , heteroarilo de 5-10 miembros, y heterocicloalquilo de 4-10 miembros, en donde el alquilo C1 -6 , alquenilo C2-6, alquinilo C2-6, arilo C6-10, cicloalquilo C3 -10 , heteroarilo de 5-10 miembros y heterocicloalquilo de 4-10 miembros de R11 están cada uno opcionalmente sustituidos con 1, 2 o 3 sustituyentes Rb independientemente seleccionados;
cada Ra se selecciona independientemente de H, alquilo C1 -6 , haloalquilo C1 -6 , alquenilo C2-6, alquinilo C2-6, arilo C6 -10 , cicloalquilo C3 -10 , heteroarilo de 5-10 miembros, y heterocicloalquilo de 4-10 miembros, en donde el alquilo C1 -6 , haloalquilo C1 -6 , alquenilo C2-6, alquinilo C2-6, arilo C6 -10 , cicloalquilo C3 -10 , heteroarilo de 5-10 miembros y heterocicloalquilo de 4-10 miembros de Ra están cada uno opcionalmente sustituidos con 1,2 o 3 sustituyentes Rd independientemente seleccionados;
cada sustituyente Rb se selecciona independientemente de halo, alquilo C1 -6 , haloalquilo C1 -6 , haloalcoxi C1.6 , arilo C6 -10 , cicloalquilo C3 -10 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, CN, OH, NH2 , NO2 , NHORc, ORc, SRc , C(O)Rc, C(O)NRcRc, C(O)ORc , OC(O)Rc, y OC(O)NRcRc; en donde el alquilo C1.6 , haloalquilo C1.6 , haloalcoxi C1.6 , arilo C6 -10 , cicloalquilo C3 -10 , heteroarilo de 5-10 miembros y heterocicloalquilo de 4-10 miembros de Rb están cada uno opcionalmente sustituidos con 1-3 sustituyentes Rd independientemente seleccionados;
cada Rb2 se selecciona independientemente de halo, haloalquilo C1 -6 , haloalcoxi C1-6 , arilo C6 -10 , cicloalquilo C3 -10 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, CN, OH, NH2 , NO2 , NHORc, Orc, SRc , C(O)Rc, C(O)NRcRc , C(O)ORc, OC(O)Rc, OC(O)NRcRc , NHRc , NRcRc, NRcC(O)Rc, y NRcC(O)ORc; en donde el haloalquilo C1.6 , haloalcoxi C1 -6 , arilo C6 -10 , cicloalquilo C3 -10 , heteroarilo de 5-10 miembros y heterocicloalquilo de 4- 10 miembros de Rb2 están cada uno opcionalmente sustituidos con 1-3 sustituyentes Rd independientemente seleccionados;
cada Rc se selecciona independientemente de H, alquilo C1 -6 , haloalquilo C1 -6 , alquenilo C2-6, alquinilo C2-6, arilo C6 -10 , cicloalquilo C3 -10 , heteroarilo de 5-10 miembros, y heterocicloalquilo de 4-10 miembros, en donde el alquilo C1 -6 , haloalquilo C1.6 , alquenilo C2-6, alquinilo C2-6, arilo C6 -10 , cicloalquilo C3 -10 , heteroarilo de 5-10 miembros y heterocicloalquilo de 4-10 miembros de Rc están cada uno opcionalmente sustituidos con 1, 2 o 3 sustituyentes Rf independientemente seleccionados de alquilo C1-6 , haloalquilo C1 -6 , alquenilo C2-6, alquinilo C2-6, arilo C6 -10 , cicloalquilo C3 -10 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, halo, CN, CN, NHORg, ORg, SRg, C(O)Rg, C(O)NRgRg, C(O)ORg, OC(O)Rg, OC(O)NRgRg, NHRg, NRgRg, NRgC(O)Rg, NRgC(O)NRgRg, y NRgC(O)ORg; en donde el alquilo C1 -6 , haloalquilo C1.6 , alquenilo C2-6, alquinilo C2-6, arilo C6-10, cicloalquilo C3 -10 , heteroarilo de 5-10 miembros y heterocicloalquilo de 4-10 miembros de Rf están cada uno opcionalmente sustituidos con 1, 2 o 3 sustituyentes Rn independientemente seleccionados de alquilo C1 -6 , haloalquilo C1.6 , halo, CN, fenilo, cicloalquilo C3-6, heteroarilo de 5-6 miembros, heterocicloalquilo de 4-6 miembros, NHORo, ORo, SRo, C(O)Ro, C(O)NR° R° , C(O)ORo, OC(O)Ro, OC(O)NR° R° , NHRo, NR° R° , NR° C(O)R° , NR° C(O)NR° R° , y NR° C(O)OR° , en donde el alquilo C1-6 , haloalquilo C1.6 , fenilo, cicloalquilo C3-6, heteroarilo de 5-6 miembros, y heterocicloalquilo de 4-6 miembros de Rn están cada uno opcionalmente sustituidos con 1, 2 o 3 sustituyentes Rq;
cada Rd se selecciona independientemente de alquilo C1 -6 , haloalquilo C1.6 , halo, arilo C6 -10 , heteroarilo de 5-10 miembros, cicloalquilo C3 -10 , heterocicloalquilo de 4-10 miembros, (heterocicloalquilo de 4-10 miembros)-alquilo C1.4-, CN, NH2 , NHORe, ORe, SRe , C(O)Re , C(O)NRe Re, C(O)ORe , OC(O)Re, OC(O)NReRe, NHRe, NRe Re, NReC(O)Re, NReC(O)NReRe , y NReC(O)ORe , en donde el alquilo C1 -6 , haloalquilo C1.6 , arilo C6 -10, heteroarilo de 5- 10 miembros, cicloalquilo C3 -10 , heterocicloalquilo de 4-10 miembros y (heterocicloalquilo de 4-10 miembros)-alquilo C1.4- de Rd están cada uno opcionalmente sustituidos con 1-3 sustituyentes Rf independientemente
seleccionados;
cada Re se selecciona independientemente de H, alquilo C1-6 , haloalquilo C1 -6 , alquenilo C2-6 y alquinilo C2-6; cada Rg se selecciona independientemente de H, alquilo C1 -6 , haloalquilo C1 -6 , alquenilo C2-6 y alquinilo C2-6 y (heteroarilo de 5-10 miembros)-alquilo C1-4-; en donde el alquilo C1-6 y (heteroarilo de 5-10 miembros)-alquilo C1 -4- de Rg están cada uno opcionalmente sustituidos con 1-3 sustituyentes RP independientemente seleccionados de alquilo C1 -6 , haloalquilo C1.6 , alquenilo C2-6, alquinilo C2-6, halo, CN, ORr, C(O)Rr, C(O)NRrRr, C(O)ORr, OC(O)Rr, OC(O)NRrRr, NHRr, NRrRr, and NRrC(O)Rr;
cada Ro se selecciona independientemente de H, alquilo C1 -6 , haloalquilo C1.6 , cicloalquilo C3.6, arilo C6 -10 , heterocicloalquilo de 4-6 miembros, heteroarilo de 5 o 6 miembros, haloalquilo C1 -4 , alquenilo C2-4 y alquinilo C2-4; cada Rq se selecciona independientemente de OH, CN, -COOH, NH2 , halo, haloalquilo C1 -6 , alquilo C1.6 , alcoxi C1.6 , haloalcoxi C1.6 , alquiltio C1.6 , fenilo, heteroarilo de 5-6 miembros, heterocicloalquilo de 4-6 miembros, cicloalquilo C3-6, NHR12 y NR12R12 y cada R12 es independientemente alquilo C1 -6 ; y
-------es un enlace simple o un enlace doble para que el anillo A siga siendo aromático.
En algunas realizaciones
Cy es fenilo que está opcionalmente sustituido con de 1 a 5 sustituyentes R6 independientemente seleccionados; R1, R2 y R3 se seleccionan cada uno independientemente de H, alquilo C1 -4 , alquenilo C2-4, alquinilo C2-4, halo, CN, OH, alcoxi C1.4 , haloalquilo C1.4 , haloalcoxi C1 -4 , NH2 , -NH-alquilo C1.4 , -N(alquilo C1 -4 )2 , en donde el alquilo C1-4 y el alcoxi C1.4 de R1, R2 y R3 están cada uno opcionalmente sustituidos con 1 o 2 sustituyentes Rd independientemente seleccionados;
R4, R5 y R6 se seleccionan cada uno independientemente de H, halo, alquilo C1 -6 , alquenilo C2-6, alquinilo C2-6, haloalquilo C1.6 , haloalcoxi C1.6 , CN, NO2 , ORa , SRa, NHORa, C(O)Ra, C(O)NRaRa , C(O)ORa , NHRa y NRaRa, en donde el alquilo C1-6 , alquenilo C2-6 y alquinilo C2-6 de R4, R5 y R6 están cada uno opcionalmente sustituidos con 1, 2, 3, 4 o 5 sustituyentes Rb independientemente seleccionados;
o dos sustituyentes R6 adyacentes en el anillo Cy, tomados junto con los átomos a los que están unidos, forman un anillo de fenilo fusionado, un anillo de heterocicloalquilo de 5, 6 o 7 miembros fusionado, un anillo de heteroarilo de 5 o 6 miembros fusionado o un anillo de cicloalquilo C3-6 fusionado, en donde el anillo de heterocicloalquilo de 5, 6 o 7 miembros fusionado y el anillo de heteroarilo de 5 o 6 miembros fusionado tienen cada uno 1-4 heteroátomos como miembros del anillo seleccionados de N, O y S y en donde el anillo de fenilo fusionado, el anillo de heterocicloalquilo de 5, 6 o 7 miembros fusionado, el anillo de heteroarilo de 5 o 6 miembros fusionado y el anillo de cicloalquilo C3-6 fusionado están opcionalmente sustituidos con 1, 2 o 3 sustituyentes Rb independientemente seleccionados;
R7 es halo, alquilo C1-6 , alquenilo C2-6, alquinilo C2-6, haloalquilo C1 -6 , haloalcoxi C1 -6 , CN, NO2 , OR11, SR11, NH2 , -NHR11, -NR11R11, C(O)R11, C(O)NR11R11, C(O)OR11, NR11C(O)R11, y NR11C(O)OR11, en donde el alquilo C1.6 , alquenilo C2-6, alquinilo C2-6, haloalquilo C1-6 y haloalcoxi C1-6 de R7 están cada uno opcionalmente sustituidos con 1,2 o 3 sustituyentes Rb independientemente seleccionados;
R8 es alquilo C1-6 sustituido con 1-3 sustituyentes Rb2 independientemente seleccionados o (heterocicloalquilo de 4-10 miembros)-alquilo C1-4- opcionalmente sustituido con 1, 2 o 3 sustituyentes Rb independientemente seleccionados;
cada R11 se selecciona independientemente de H, alquilo C1-6 , haloalquilo C1.6 , alquenilo C2-6 y alquinilo C2-6, en donde el alquilo C1.6 , alquenilo C2 -6 y alquinilo C2-6 de R11 están cada uno opcionalmente sustituidos con 1,2 o 3 sustituyentes Rb independientemente seleccionados;
cada Ra se selecciona independientemente de H, alquilo C1 -6 , haloalquilo C1.6 , alquenilo C2-6, alquinilo C2-6, y heteroarilo de 5-10 miembros en donde el alquilo C1 -6 , haloalquilo C1 -6 , alquenilo C2-6, alquinilo C2-6 y heteroarilo de 5-10 miembros de Ra están cada uno opcionalmente sustituidos con 1, 2 o 3 sustituyentes Rd independientemente seleccionados;
cada sustituyente Rb se selecciona independientemente de halo, alquilo C1 -6 , haloalquilo C1 -6 , haloalcoxi C1 -6 , CN, OH, NH2 , nHoRc, ORc, C(O)Rc, C(O)NRcRc y C(O)ORc ; en donde el alquilo C1-6 , el haloalquilo C1.6 y el haloalcoxi C1-6 de Rb están cada uno además opcionalmente sustituidos con 1-3 sustituyentes Rd independientemente seleccionados;
cada Rb2 se selecciona independientemente de halo, haloalquilo C1 -6 , haloalcoxi C1.6 , arilo C6 -10, cicloalquilo C3.10 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, CN, OH, NH2 , NO2 , NHORc, Orc, SRc , C(O)Rc, C(O)NRcRc , C(O)ORc, OC(O)Rc, OC(O)NRcRc, NHRc , NRcRc, NRcC(O)Rc, y NRcC(O)ORc ; en donde el haloalquilo C1 -6 , el haloalcoxi C1.6 , el arilo C6 -10 , el cicloalquilo C3 -10 , el heteroarilo de 5-10 miembros y el heterocicloalquilo de 4-10 miembros de Rb2 están cada uno además opcionalmente sustituidos con 1-3 sustituyentes Rd independientemente seleccionados;
cada Rc se selecciona independientemente de H, alquilo C1-6 , haloalquilo C1 -6 , alquenilo C2-6, alquinilo C2-6 y arilo C6-10 en donde el alquilo C1 -6 , haloalquilo C1 -6 , alquenilo C2-6, alquinilo C2-6 y arilo C6-10 de Rc están cada uno opcionalmente sustituidos con 1, 2 o 3 sustituyentes Rf independientemente seleccionados de alquilo C1 -6 , haloalquilo C1 -6 , alquenilo C2-6, alquinilo C2-6 (heterocicloalquilo de 4-10 miembros)-alquilo C1.4-, halo, CN, ORg, C(O)Rg, C(O)NRgRg, C(O)ORg, NHRg, NRgRg, y NRgC(O)Rg; en donde el alquilo C1 -6 , alquenilo C2-6, alquinilo C2-6 , y (heterocicloalquilo de 4-10 miembros)-alquilo C1.4- de Rf están cada uno opcionalmente sustituidos con 1,2 o 3 sustituyentes Rn independientemente seleccionados de alquilo C1 -6 , haloalquilo C1 -6 , halo, CN, fenilo, ORo, C(O)Ro, C(O)NR° R° , C(O)ORo, NHRo, NR° R° y NR° C(O)R° ;
cada Rd se selecciona independientemente de alquilo C1-6 , haloalquilo C1 -6 , halo, (heterocicloalquilo de 4-10 miembros)-alquilo C1.4-CN, NH2 , NHORe , ORe, C(O)Re, C(O)NReRe , C(O)ORe, NHRe, NReRe, NReC(O)Re , NReC(O)NReRe , y NReC(O)ORe , en donde el alquilo C1-6 y el (heterocicloalquilo de 4-10 miembros)-alquilo C1-4-de Rd están cada uno opcionalmente sustituidos con 1-3 sustituyentes Rf independientemente seleccionados;
cada Re se selecciona independientemente de H, alquilo C1-6 , haloalquilo C1.6 , alquenilo C2-6 y alquinilo C2-6;
cada Rg se selecciona independientemente de H, alquilo C1 -6 , haloalquilo C1.6 , alquenilo C2-6, alquinilo C2-6 y (heteroarilo de 5-10 miembros)-alquilo C1.4-; en done el alquilo C1 -6 , haloalquilo C1.6 , alquenilo C2-6, alquinilo C2-6 y (heteroarilo de 5-10 miembros)-alquilo C1.4- de Rg están cada uno opcionalmente sustituidos con 1-3 sustituyentes Rp independientemente seleccionados de alquilo C1 -6 , haloalquilo C1.6 , alquenilo C2-6, alquinilo C2-6, halo, CN, ORr, C(O)Rr, C(O)NRr Rr, y C(O)rNRrRr, y C(O)ORr;
cada Ro se selecciona independientemente de H y alquilo C1-6 ; y
es un enlace simple o un enlace doble para que el anillo A siga siendo aromático.
En algunas realizaciones:
Cy es fenilo que está opcionalmente sustituido con de 1 a 5 sustituyentes R6 independientemente seleccionados;
R1, R2 y R3 se seleccionan cada uno independientemente de H, alquilo C1 -4 , alquenilo C2-4, alquinilo C2-4, halo,
CN, OH, NH2 , -NH-alquilo C1.4 y -N(alquilo ^ -4)2 ;
R4, R5 y R6 se seleccionan cada uno independientemente de H, halo, alquilo C1-6 , alquenilo C2-6, alquinilo C2-6, ORa , C(O)NRaRa y NRaC(O)Ra, en donde el alquilo C1 -6 , el alquenilo C2-6 y el alquinilo C2-6 de R4 , R5 y R6 están cada uno opcionalmente sustituidos con 1, 2, 3, 4 o 5 sustituyentes Rb independientemente seleccionados;
o dos sustituyentes R6 adyacentes en el anillo Cy, tomados junto con los átomos a los que están unidos, forman un anillo de fenilo fusionado, un anillo de heterocicloalquilo de 5, 6 o 7 miembros fusionado, un anillo de heteroarilo de 5 o 6 miembros fusionado o un anillo de cicloalquilo C3-6 fusionado, en donde el anillo de heterocicloalquilo de 5, 6 o 7 miembros fusionado y el anillo de heteroarilo de 5 o 6 miembros fusionado tienen cada uno 1-4 heteroátomos como miembros del anillo seleccionados de N, O y S y en donde el anillo de fenilo fusionado, el anillo de heterocicloalquilo de 5, 6 o 7 miembros fusionado, el anillo de heteroarilo de 5 o 6 miembros fusionado y el anillo de cicloalquilo C3-6 fusionado están cada uno opcionalmente sustituidos con 1,2 o
3 sustituyentes Rb independientemente seleccionados;
R7 es halo, alquilo C1 -6 , alquenilo C2-6, alquinilo C2-6 o CN, en donde el alquilo C1-6 , el alquenilo C2-6 y el alquinilo
C2-6 de R7 están cada uno opcionalmente sustituidos con 1, 2 o 3 sustituyentes Rb independientemente seleccionados;
R8 es alquilo C1-6 sustituido con 1-3 sustituyentes Rb2 independientemente seleccionados o (heterocicloalquilo de
4-10 miembros)-alquilo C1-4- opcionalmente sustituido con 1, 2 o 3 sustituyentes Rb independientemente seleccionados;
cada Ra se selecciona independientemente de H, alquilo C1-6 , alquenilo C2-6, alquinilo C2-6 y heteroarilo de 5-10 miembros, en donde el alquilo C1 -6 , alquenilo C2-6, alquinilo C2-66 y heteroarilo de 5 a 10 miembros de Ra están cada uno opcionalmente sustituidos con 1,2 o 3 sustituyentes Rd independientemente seleccionados;
cada sustituyente Rb se selecciona independientemente de halo, alquilo C1-6 y ORc ;
cada Rb2 se selecciona independientemente de halo, haloalquilo C1 -6 , haloalcoxi C1 -6 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, NHRc , NRcRc y NRcC(O)Rc; en donde el haloalquilo C1 -6 , el haloalcoxi C1 -6 , el heteroarilo de 5-10 miembros y el heterocicloalquilo de 4-10 miembros de Rb2 están cada uno opcionalmente sustituidos con 1-3 sustituyentes Rd independientemente seleccionados;
cada Rc se selecciona independientemente de H, alquilo C1-6 , haloalquilo C1 -6 , alquenilo C2-6, alquinilo C2-6 y arilo
C6 -10 , en donde el alquilo C1 -6 , haloalquilo C1.66, alquenilo C2-6, alquinilo C2-6 y arilo C6-10 de Rc están cada uno opcionalmente sustituidos con 1, 2 o 3 sustituyentes Rf independientemente seleccionados de alquilo C1 -6 , haloalquilo C1.6 , alquenilo C2-6, alquinilo C2-6, (heterocicloalquilo de 4-10 miembros)-alquilo C1 -4 l-, halo, ORg, C(O)Rg, C(O)NRgRg, NHRg, y NRgRg; en donde el alquilo C1 -6 , alquenilo C2-6, alquinilo C2-6 y (heterocicloalquilo de 4-10 miembros)-alquilo C1.4- de Rf están cada uno opcionalmente sustituidos con 1, 2 o 3 sustituyentes Rn independientemente seleccionados de alquilo C1 -6 , halo, Cn, OR° y o (O)OR° ;
cada Rd se selecciona independientemente de alquilo C1-6 , haloalquilo C1.6 , halo, (heterocicloalquilo de 4-10 miembros)-alquilo C1.4-, CN, NH2 , ORe, C(O)Re, C(O)NReRe , C(O)ORe , NHRe, NReRe, y NReC(O) alquilo C1-6 y (heterocicloalquilo de 4-10 miembros)-alquilo C1.4- de Rd están cada uno opcionalmente sustituidos con 1-3 sustituyentes Rf independientemente seleccionados;
cada Re se selecciona independientemente de H, alquilo C1-6 , alquenilo C2-6 y alquinilo C2-6;
cada Rg se selecciona independientemente de H, alquilo C1-6 , alquenilo C2-6, alquinilo C2-6 y (heteroarilo de 5-10 miembros)-alquilo C1-4-; en donde el alquilo C1.6 , el alquenilo C2-6, el alquinilo C2-6 y el (heteroarilo de 5-10 miembros)-alquilo C1.4- de Rg están cada uno opcionalmente sustituidos con 1-3 sustituyentes Rp independientemente seleccionados de alquilo C1 -6 , alquenilo C2-6, alquinilo C2-6, halo y CN;
cada Ro se selecciona independientemente de H y alquilo C1-6 ; y
-------- es un enlace simple o un enlace doble para que el anillo A siga siendo aromático.
Se aprecia además que ciertas características de la invención que, por claridad, se describen en el contexto de realizaciones separadas, también pueden proporcionarse en combinación en una única realización (mientras que se pretende que las realizaciones se combinen como si estuvieran escritas en forma dependiente múltiple). A la
inversa, varias características de la invención que, por brevedad, se describen en el contexto de una única realización, también pueden proporcionarse por separado o en cualquier subcombinación adecuada. Por tanto, se contempla que las características descritas como realizaciones de los compuestos de Fórmula (I) puedan combinarse en cualquier combinación adecuada.
En varios lugares de la presente memoria descriptiva, ciertas características de los compuestos se divulgan en grupos o en intervalos. Se pretende específicamente que dicha divulgación incluya todas y cada una de las subcombinaciones individuales de los miembros de tales grupos e intervalos. Por ejemplo, se pretende específicamente que el término "alquilo C1-6" divulgue individualmente (sin limitación) metilo, etilo, alquilo C3, alquilo C4, alquilo C5 y alquilo C6.
El término "de n miembros", donde n es un número entero, describe típicamente el número de átomos que forman el anillo en una fracción donde el número de átomos que forman el anillo es n. Por ejemplo, piperidinilo es un ejemplo de un anillo heterocicloalquilo de 6 miembros, pirazolilo es un ejemplo de un anillo heteroarilo de 5 miembros, piridilo es un ejemplo de un anillo heteroarilo de 6 miembros y 1,2,3,4-tetrahidro-naftaleno es un ejemplo de un grupo cicloalquilo de 10 miembros.
En varios lugares de la presente memoria descriptiva, pueden describirse variables que definen grupos de enlace divalentes. Se pretende específicamente que cada sustituyente de enlace incluya tanto la forma directa como la inversa del sustituyente de enlace. Por ejemplo, -NR(CR'R'')n- incluye tanto -NR(CR'R'')n- como -(CR'R'')nNR- y se pretende que divulgue cada una de las formas individualmente. Donde la estructura requiere un grupo de enlace, se entiende que las variables de Markush enumeradas para ese grupo son grupos de enlace. Por ejemplo, si la estructura requiere un grupo de enlace y la definición de grupo de Markush para esa variable enumera "alquilo" o "arilo", se entiende entonces que el "alquilo" o "arilo" representa un grupo alquileno o grupo arileno de enlace, respectivamente.
El término "sustituido" significa que un átomo o grupo de átomos reemplaza formalmente al hidrógeno como un "sustituyente" unido a otro grupo. El término "sustituido", a menos que se indique lo contrario, se refiere a cualquier nivel de sustitución, por ejemplo, mono-, di-, tri-, tetra- o penta-sustitución, donde se permita tal sustitución. Los sustituyentes se seleccionan independientemente y la sustitución puede estar en cualquier posición químicamente accesible. Debe entenderse que la sustitución en un átomo dado está limitada por la valencia. Debe entenderse que la sustitución en un átomo dado da como resultado una molécula químicamente estable. La frase "opcionalmente sustituido" significa sustituido o no sustituido. El término "sustituido" significa que se elimina un átomo de hidrógeno y se reemplaza por un sustituyente. Un único sustituyente divalente, por ejemplo, oxo, puede reemplazar dos átomos de hidrógeno.
El término "Cn-m" indica un intervalo que incluye los puntos finales, donde n y m son números enteros e indican el número de carbonos. Los ejemplos incluyen C1-4 y C1 -6.
El término "alquilo" empleado solo o en combinación con otros términos, se refiere a un grupo hidrocarbonado saturado que puede ser de cadena lineal o ramificada. El término " alquilo Cn-m" se refiere a un grupo alquilo que tiene de n a m átomos de carbono. Un grupo alquilo corresponde formalmente a un alcano con un enlace C-H reemplazado por el punto de unión del grupo alquilo al resto del compuesto. En algunas realizaciones, el grupo alquilo contiene de 1 a 6 átomos de carbono, de 1 a 4 átomos de carbono, de 1 a 3 átomos de carbono o de 1 a 2 átomos de carbono. Los ejemplos de fracciones alquilo incluyen, pero no se limitan a, grupos químicos como metilo, etilo, n-propilo, isopropilo, n-butilo, tere-butilo, isobutilo, sec-butilo; homólogos superiores como 2-metil-1 -butilo, npentilo, 3-pentilo, n-hexilo, 1,2,2-trimetilpropilo y similares.
El término "alquenilo" empleado solo o en combinación con otros términos, se refiere a un grupo hidrocarbonado de cadena lineal o ramificada correspondiente a un grupo alquilo que tiene uno o más enlaces dobles carbono-carbono. Un grupo alquenilo corresponde formalmente a un alqueno con un enlace C-H reemplazado por el punto de unión del grupo alquenilo al resto del compuesto. El término "alquenilo Cn-m" se refiere a un grupo alquenilo que tiene de n a m carbonos. En algunas realizaciones, la fracción alquenilo contiene de 2 a 6, d e 2 a 4 o d e 2 a 3 átomos de carbono. Los ejemplos de grupos alquenilo incluyen, pero no se limitan a, etenilo, n-propenilo, isopropenilo, n-butenilo, see-butenilo y similares.
El término "alquinilo" empleado solo o en combinación con otros términos, se refiere a un grupo hidrocarbonado de cadena lineal o ramificada correspondiente a un grupo alquilo que tiene uno o más enlaces triples carbono-carbono. Un grupo alquinilo corresponde formalmente a un alquino con un enlace C-H reemplazado por el punto de unión del grupo alquilo al resto del compuesto. El término "alquinilo Cn-m" se refiere a un grupo alquinilo que tiene de n a m carbonos. Los grupos alquinilo ejemplares incluyen, pero no se limitan a, etinilo, propin-1-ilo, propin-2-ilo y similares. En algunas realizaciones, la fracción alquinilo contiene de 2 a 6, de 2 a 4 o de 2 a 3 átomos de carbono.
El término "alquileno", empleado solo o en combinación con otros términos, se refiere a un grupo de enlace
alquilo divalente. Un grupo alquileno corresponde formalmente a un alcano con dos enlaces C-H reemplazados por puntos de unión del grupo alquileno al resto del compuesto. El término "alquileno Cn-m" se refiere a un grupo alquileno que tiene de n a m átomos de carbono. Los ejemplos de grupos alquileno incluyen, pero no se limitan a, etan-1,2-diilo, propan-1,3-diilo, propan-1,2-diilo, butan-1,4-diilo, butan-1,3-diilo, butan-1,2-diilo, 2-metil-propan-1,3-diilo y similares.
El término "alcoxi", empleado solo o en combinación con otros términos, se refiere a un grupo de fórmula -O-alquilo, en donde el grupo alquilo es como se ha definido anteriormente. El término "alcoxi Cn-m" se refiere a un grupo alcoxi, cuyo grupo alquilo tiene de n a m carbonos. Los ejemplos de grupos alcoxi incluyen metoxi, etoxi, propoxi (por ejemplo, n-propoxi e isopropoxi), f-butoxi y similares. En algunas realizaciones, el grupo alquilo tiene de 1 a 6, de 1 a 4 o de 1 a 3 átomos de carbono.
El término "amino" se refiere a un grupo de fórmula -NH2.
El término "carbonilo", empleado solo o en combinación con otros términos, se refiere a un grupo -C(=O)-, que también puede escribirse como C(O).
El término "ciano" o "nitrilo" se refiere a un grupo de fórmula -C=N, que también puede escribirse como -CN. Los términos "halo" o "halógeno", usados solos o en combinación con otros términos, se refieren a flúor, cloro, bromo y yodo. En algunas realizaciones, "halo" se refiere a un átomo de halógeno seleccionado de F, Cl o Br. En algunas realizaciones, los grupos halo son F.
El término "haloalquilo", como se usa en la presente, se refiere a un grupo alquilo en el que uno o más de los átomos de hidrógeno han sido reemplazados por un átomo de halógeno. El término "haloalquilo Cn-m" se refiere a un grupo alquilo Cn-m que tiene de n a m átomos de carbono y de por lo menos uno hasta {2(n a m)+1} átomos de halógeno, que pueden ser iguales o diferentes. En algunas realizaciones, los átomos de halógeno son átomos de flúor. En algunas realizaciones, el grupo haloalquilo tiene de 1 a 6 o de 1 a 4 átomos de carbono. Los ejemplos de grupos haloalquilo incluyen CF3 , C2F5 , CHF2 , CCl3 , CHCh, C2Cl5 y similares. En algunas realizaciones, el grupo haloalquilo es un grupo fluoroalquilo.
El término "haloalcoxi", empleado solo o en combinación con otros términos, se refiere a un grupo de fórmula -O-haloalquilo, en donde el grupo haloalquilo es como se ha definido anteriormente. El término "haloalcoxi Cn-m" se refiere a un grupo haloalcoxi, cuyo grupo haloalquilo tiene de n a m carbonos. Los ejemplos de grupos haloalcoxi incluyen trifluorometoxi y similares. En algunas realizaciones, el grupo haloalcoxi tiene de 1 a 6, de 1 a 4 o de 1 a 3 átomos de carbono.
El término "oxo" se refiere a un átomo de oxígeno como un sustituyente divalente, que forma un grupo carbonilo cuando está unido al carbono, o unido a un heteroátomo que forma un grupo sulfóxido o sulfona, o un grupo N-óxido. En algunas realizaciones, los grupos heterocíclicos pueden estar opcionalmente sustituidos con 1 o 2 sustituyentes oxo (=O).
El término "sulfido" se refiere a un átomo de azufre como sustituyente divalente, que forma un grupo tiocarbonilo (C=S) cuando se une al carbono.
El término "aromático" se refiere a un carbociclo o heterociclo que tiene uno o más anillos poliinsaturados que tienen carácter aromático (es decir, que tienen (4n 2) electrones n (pi) deslocalizados donde n es un número entero).
El término "arilo", empleado solo o en combinación con otros términos, se refiere a un grupo hidrocarbonado aromático, que puede ser monocíclico o policíclico (por ejemplo, que tiene 2 anillos fusionados). El término "arilo Cn-m" se refiere a un grupo arilo que tiene de n a m átomos de carbono en el anillo. Los grupos arilo incluyen, por ejemplo, fenilo, naftilo, indanilo e indenilo. En algunas realizaciones, los grupos arilo tienen de 6 a aproximadamente 1o átomos de carbono. En algunas realizaciones, los grupos arilo tienen 6 átomos de carbono. En algunas realizaciones, los grupos arilo tienen 10 átomos de carbono. En algunas realizaciones, el grupo arilo es fenilo. En algunas realizaciones, el grupo arilo es naftilo.
El término "heteroátomo" usado en la presente se pretende que incluya boro, fósforo, azufre, oxígeno y nitrógeno.
El término "heteroarilo" o "heteroaromático", empleado solo o en combinación con otros términos, se refiere a un heterociclo aromático monocíclico o policíclico que tiene por lo menos un miembro del anillo de heteroátomos seleccionado de boro, azufre, sulfuro, oxígeno y nitrógeno. En algunas realizaciones, el anillo heteroarilo tiene 1, 2, 3 o 4 miembros del anillo de heteroátomos independientemente seleccionados de nitrógeno, azufre y oxígeno. En algunas realizaciones, cualquier N que forma el anillo en una fracción heteroarilo puede ser un N-óxido. En algunas
realizaciones, el heteroarilo tiene 5-14 átomos en el anillo que incluyen átomos de carbono y 1, 2, 3 o 4 miembros del anillo de heteroátomos seleccionados independientemente de nitrógeno, azufre y oxígeno. En algunas realizaciones, el heteroarilo tiene 5-10 átomos de anillo que incluyen átomos de carbono y 1, 2, 3 o 4 miembros del anillo de heteroátomos seleccionados independientemente de nitrógeno, azufre y oxígeno. En algunas realizaciones, el heteroarilo tiene 5-6 átomos en el anillo y 1 o 2 miembros del anillo de heteroátomos seleccionados independientemente de nitrógeno, azufre y oxígeno. En algunas realizaciones, el heteroarilo es un anillo heteroarilo de cinco o seis miembros. En otras realizaciones, el heteroarilo es un anillo heteroarilo bicíclico fusionado de ocho miembros, nueve miembros o diez miembros. Ejemplos de grupos heteroarilo incluyen, pero no se limitan a, piridinilo (piridilo), pirimidinilo, pirazinilo, piridazinilo, pirrolilo, pirazolilo, azolilo, oxazolilo, tiazolilo, imidazolilo, furanilo, tiofenilo, quinolinilo, isoquinolinilo, naftiridinilo (incluyendo 1,2-, 1,3-, 1,4-, 1,5-, 1,6-, 1,7-, 1,8-, 2 ,3-y 2,6-naftiridina), indolilo, benzotiofenilo, benzofuranilo, benzoisoxazolilo, imidazo[1,2-£i] tiazolilo, purinilo y similares.
Un anillo heteroarilo de cinco miembros es un grupo heteroarilo que tiene cinco átomos del anillo en donde uno o más (por ejemplo, 1, 2 o 3) átomos del anillo se seleccionan independientemente de N, O y S. Los heteroarilos del anillo de cinco miembros ejemplares incluyen tienilo, furilo, pirrolilo, imidazolilo, tiazolilo, oxazolilo, pirazolilo, isotiazolilo, isoxazolilo, 1,2,3-triazolilo, tetrazolilo, 1,2,3-tiadiazolilo, 1,2,3-oxadiazolilo, 1,2,4-triazolilo, 1,2,4-tiadiazolilo, 1,2,4-oxadiazolilo, 1,3,4-triazolilo, 1,3,4-tiadiazolilo y 1,3,4-oxadiazolilo.
Un anillo heteroarilo de seis miembros es un grupo heteroarilo que tiene seis átomos en el anillo en donde uno o más (por ejemplo, 1, 2 o 3) átomos del anillo se seleccionan independientemente de N, O y S. Los heteroarilos del anillo de seis miembros ejemplares son piridilo, pirazinilo, pirimidinilo, triazinilo y piridazinilo.
El término "cicloalquilo", empleado solo o en combinación con otros términos, se refiere a un sistema de anillo hidrocarbonado no aromático (monocíclico, bicíclico o policíclico), que incluye grupos alquilo y alquenilo ciclados. El término "cicloalquilo Cn-m" se refiere a un cicloalquilo que tiene de n a m átomos de carbono en el anillo. Los grupos cicloalquilo pueden incluir grupos mono- o policíclicos (por ejemplo, que tienen 2, 3 o 4 anillos fusionados) y espirociclos. Los grupos cicloalquilo pueden tener 3, 4, 5, 6 o 7 carbonos que forman el anillo (C3 -7). En algunas realizaciones, el grupo cicloalquilo tiene de 3 a 6 miembros del anillo, de 3 a 5 miembros del anillo o de 3 a 4 miembros del anillo. En algunas realizaciones, el grupo cicloalquilo es monocíclico. En algunas realizaciones, el grupo cicloalquilo es monocíclico o bicíclico. En algunas realizaciones, el grupo cicloalquilo es un grupo cicloalquilo C3-6 monocíclico. Los átomos de carbono que forman el anillo de un grupo cicloalquilo pueden oxidarse opcionalmente para formar un grupo oxo o sulfido. Los grupos cicloalquilo también incluyen cicloalquilidenos. En algunas realizaciones, el cicloalquilo es ciclopropilo, ciclobutilo, ciclopentilo o ciclohexilo. También se incluyen en la definición de cicloalquilo fracciones que tienen uno o más anillos aromáticos fusionados (es decir, que tienen un enlace en común con) al anillo cicloalquilo, por ejemplo, derivados benzo o tienilo de ciclopentano y ciclohexano. Un grupo cicloalquilo que contiene un anillo aromático fusionado puede unirse a través de cualquier átomo que forma el anillo, incluyendo un átomo que forma el anillo del anillo aromático fusionado. Los ejemplos de grupos cicloalquilo incluyen ciclopropilo, ciclobutilo, ciclopentilo, ciclohexilo, cicloheptilo, ciclopentenilo, ciclohexenilo, ciclohexadienilo, cicloheptatrienilo, norbornilo, norpinilo, norcarnilo, biciclo[1.1.1]pentanilo, biciclo[2.1.1]hexanilo y similares. En algunas realizaciones, el grupo cicloalquilo es ciclopropilo, ciclobutilo, ciclopentilo o ciclohexilo.
El término "heterocicloalquilo", empleado solo o en combinación con otros términos, se refiere a un anillo o sistema de anillos no aromático, que puede contener opcionalmente uno o más grupos alquenileno como parte de la estructura del anillo, que tiene por lo menos un miembro del anillo de heteroátomos seleccionado independientemente de nitrógeno, boro, azufre, oxígeno y fósforo, y que tiene 4-10 miembros del anillo, 4-7 miembros del anillo o 4-6 miembros del anillo. Dentro del término "heterocicloalquilo" se incluyen los grupos heterocicloalquilo monocíclicos de 4, 5, 6 y 7 miembros. Los grupos heterocicloalquilo pueden incluir sistemas de anillos mono- o bicíclicos (por ejemplo, que tienen dos anillos fusionados o que forman puente). En algunas realizaciones, el grupo heterocicloalquilo es un grupo monocíclico que tiene 1, 2 o 3 heteroátomos seleccionados independientemente de nitrógeno, azufre y oxígeno. Los átomos de carbono que forman el anillo y los heteroátomos de un grupo heterocicloalquilo pueden oxidarse opcionalmente para formar un grupo oxo o sulfido u otro enlace oxidado (por ejemplo, C(O), S(O), C(S) o S(O)2 , N-óxido, etc.) o un átomo de nitrógeno puede cuaternizarse. El grupo heterocicloalquilo puede estar unido a través de un átomo de carbono que forma el anillo o un heteroátomo que forma el anillo. En algunas realizaciones, el grupo heterocicloalquilo contiene de 0 a 3 enlaces dobles. En algunas realizaciones, el grupo heterocicloalquilo contiene de 0 a 2 enlaces dobles. También se incluyen en la definición de heterocicloalquilo las fracciones que tienen uno o más anillos aromáticos fusionados (es decir, que tienen un enlace en común con) al anillo heterocicloalquilo, por ejemplo, derivados benzo o tienilo de piperidina, morfolina, azepina, etc. Un grupo heterocicloalquilo que contiene un anillo aromático fusionado puede unirse a través de cualquier átomo que forma el anillo, incluyendo un átomo que forma el anillo del anillo aromático fusionado. Los ejemplos de grupos heterocicloalquilo incluyen azetidinilo, azepanilo, dihidrobenzofuranilo, dihidrofuranilo, dihidropiranilo, morfolino, 3-oxa-9-azaespiro[5.5]undecanilo, 1-oxa-8-azaespiro[4.5]decanilo, piperidinilo, piperazinilo, oxopiperazinilo, piranilo, pirrolidinilo, quinuclidinilo, tetrahidrofuranilo, tetrahidropiranilo, 1,2,3,4-tetrahidroquinolinilo, tropanilo y tiomorfolino
En ciertos lugares, las definiciones o realizaciones se refieren a anillos específicos (por ejemplo, un anillo
de azetidina, un anillo de piridina, etc.). A menos que se indique lo contrario, estos anillos pueden unirse a cualquier miembro del anillo siempre que no se exceda la valencia del átomo. Por ejemplo, un anillo de azetidina puede unirse en cualquier posición del anillo, mientras que un anillo de azetidin-3-ilo se une en la posición 3.
Los compuestos descritos en la presente pueden ser asimétricos (por ejemplo, tener uno o más estereocentros). Se incluyen todos los estereoisómeros, como enantiómeros y diastereómeros, a menos que se indique lo contrario. Los compuestos de la presente invención que contienen átomos de carbono asimétricamente sustituidos pueden aislarse en formas ópticamente activas o racémicas. En la técnica se conocen métodos sobre cómo preparar formas ópticamente activas a partir de materiales de partida ópticamente inactivos, como mediante resolución de mezclas racémicas o mediante síntesis estereoselectiva. También pueden estar presentes en los compuestos descritos en la presente muchos isómeros geométricos de olefinas y enlaces dobles C=N y similares, y en la presente invención se contemplan todos estos isómeros estables. Se describen los isómeros geométricos cis y trans de los compuestos de la presente invención y pueden aislarse como una mezcla de isómeros o como formas isoméricas separadas.
La resolución de mezclas racémicas de compuestos puede llevarse a cabo mediante cualquiera de los numerosos métodos conocidos en la técnica. Un método incluye la recristalización fraccionada usando un ácido de resolución quiral que es un ácido orgánico formador de sales ópticamente activo. Los agentes de resolución adecuados para métodos de recristalización fraccionada son, por ejemplo, ácidos ópticamente activos, como las formas D y L de ácido tartárico, ácido diacetiltartárico, ácido dibenzoiltartárico, ácido mandélico, ácido málico, ácido láctico o los varios ácidos canforsulfónicos ópticamente activos como ácido p-canforsulfónico. Otros agentes de resolución adecuados para métodos de cristalización fraccionada incluyen formas estereoisoméricamente puras de a-metilbencilamina (por ejemplo, formas S y R, o formas diastereoméricamente puras), 2-fenilglicinol, norefedrina, efedrina, W-metilefedrina, ciclohexiletilamina y 1,2-diaminociclohexano y similares.
La resolución de mezclas racémicas también puede llevarse a cabo mediante elución en una columna empaquetada con un agente de resolución ópticamente activo (por ejemplo, dinitrobenzoilfenilglicina). Un experto en la técnica puede determinar la composición de solvente de elución adecuada.
En algunas realizaciones, los compuestos de la invención tienen la configuración (R). En otras realizaciones, los compuestos tienen la configuración (S). En compuestos con más de un centro quiral, cada uno de los centros quirales en el compuesto puede ser independientemente (R) o (S), a menos que se indique lo contrario.
Los compuestos de la invención también incluyen formas tautoméricas. Las formas tautoméricas resultan del intercambio de un enlace simple con un enlace doble adyacente junto con la migración concomitante de un protón. Las formas tautoméricas incluyen tautómeros prototrópicos que son estados de protonación isoméricos que tienen la misma fórmula empírica y carga total. Los ejemplos de tautómeros prototrópicos incluyen pares cetonaenol, pares amida-ácido imídico, pares lactama-lactima, pares enamina-imina y formas anulares donde un protón puede ocupar dos o más posiciones de un sistema heterocíclico, por ejemplo, 1H- y 3H -imidazol, 1H- 2H- y 4H-1,2,4-triazol, 1H- y 2H-isoindol y 1H- y 2H-pirazol. Las formas tautoméricas pueden estar en equilibrio o bloqueadas estéricamente en una forma mediante una sustitución apropiada.
Los compuestos de la invención también pueden incluir todos los isótopos de átomos que se producen en los compuestos intermedios o finales. Los isótopos incluyen aquellos átomos que tienen el mismo número atómico pero diferentes números de masa. Por ejemplo, los isótopos de hidrógeno incluyen tritio y deuterio. Uno o más átomos constituyentes de los compuestos de la invención pueden reemplazarse o sustituirse con isótopos de los átomos en abundancia natural o no natural. En algunas realizaciones, el compuesto incluye por lo menos un átomo de deuterio. Por ejemplo, uno o más átomos de hidrógeno en un compuesto de la presente divulgación pueden reemplazarse o sustituirse por deuterio. En algunas realizaciones, el compuesto incluye dos o más átomos de deuterio. En algunas realizaciones, el compuesto incluye 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 o 12 átomos de deuterio. En la técnica se conocen los métodos sintéticos para incluir isótopos en compuestos orgánicos.
Como se usa en la presente, se pretende que el término "compuesto" incluya todos los estereoisómeros, isómeros geométricos, tautómeros e isótopos de las estructuras representadas. También se pretende que el término se refiera a los compuestos de la invención, independientemente de cómo se preparen, por ejemplo, sintéticamente, a través de un proceso biológico (por ejemplo, metabolismo o conversión enzimática), o una combinación de los mismos.
Todos los compuestos, y sales farmacéuticamente aceptables de los mismos, pueden encontrarse junto con otras sustancias como agua y solventes (por ejemplo, hidratos y solvatos) o pueden aislarse. Cuando están en estado sólido, los compuestos descritos en la presente y las sales de los mismos pueden presentarse de varias maneras y pueden, por ejemplo, tomar la forma de solvatos, incluyendo hidratos. Los compuestos pueden estar en cualquier forma en estado sólido, como un polimorfo o solvato, por lo que, a menos que se indique claramente lo contrario, debe entenderse que la referencia en la memoria descriptiva a compuestos y sales de los mismos abarca cualquier forma en estado sólido del compuesto.
En algunas realizaciones, los compuestos de la invención, o sales de los mismos, están sustancialmente aislados. Por "sustancialmente aislado" se entiende que el compuesto está por lo menos parcial o sustancialmente separado del entorno en el que se formó o detectó. La separación parcial puede incluir, por ejemplo, una composición enriquecida en los compuestos de la invención. La separación sustancial puede incluir composiciones que contienen por lo menos aproximadamente un 50%, por lo menos aproximadamente un 60%, por lo menos aproximadamente un 70%, por lo menos aproximadamente un 80%, por lo menos aproximadamente un 90%, por lo menos aproximadamente un 95%, por lo menos aproximadamente un 97% o por lo menos aproximadamente un 99% en peso de los compuestos de la invención, o una sal de los mismos.
La frase "farmacéuticamente aceptable" se emplea en la presente para referirse a aquellos compuestos, materiales, composiciones y/o formas de dosificación que, dentro del alcance del buen juicio médico, son adecuados para su uso en contacto con los tejidos de seres humanos y animales sin una toxicidad, irritación, respuesta alérgica u otro problema o complicación excesivos, acorde con una relación beneficio/riesgo razonable.
La expresión "temperatura ambiente", como se usa en la presente, se entiende en la técnica y se refiere de manera general a una temperatura, por ejemplo, una temperatura de reacción, que es aproximadamente la temperatura de la habitación en la que se lleva a cabo la reacción, por ejemplo, una temperatura de aproximadamente 20° C a aproximadamente 30° C.
La presente invención también incluye sales farmacéuticamente aceptables de los compuestos descritos en la presente. El término "sales farmacéuticamente aceptables" se refiere a derivados de los compuestos divulgados en donde el compuesto original se modifica convirtiendo una fracción de ácido o base existente en su forma de sal. Los ejemplos de sales farmacéuticamente aceptables incluyen, pero no se limitan a, sales de ácidos minerales u orgánicos de residuos básicos como aminas; sales alcalinas u orgánicas de residuos ácidos como ácidos carboxílicos, y similares. Las sales farmacéuticamente aceptables de la presente invención incluyen las sales no tóxicas del compuesto original formado, por ejemplo, a partir de ácidos orgánicos o inorgánicos no tóxicos. Las sales farmacéuticamente aceptables de la presente invención pueden sintetizarse a partir del compuesto original que contiene una fracción básica o ácida mediante métodos químicos convencionales. Generalmente, tales sales pueden prepararse haciendo reaccionar las formas de ácido o base libre de estos compuestos con una cantidad estequiométrica de la base o ácido apropiado en agua o en un solvente orgánico, o en una mezcla de los dos; generalmente se prefieren medios no acuosos como éter, acetato de etilo, alcoholes (por ejemplo, metanol, etanol, isopropanol o butanol) o acetonitrilo (MeCN). Las listas de sales adecuadas se encuentran en Remington's Pharmaceutical Sciences, 17a edición, (Mack Publishing Company, Easton, 1985), p. 1418, Berge et al., J. Pharm. Sci., 1977, 66(1), 1-19 y en Stahl et al., Handbook of Pharmaceutical Salts: Properties, Selection, and Use, (Wiley, 2002). En algunas realizaciones, los compuestos descritos en la presente incluyen las formas de N-óxido.
II. Síntesis
Los compuestos de la invención, incluyendo las sales de los mismos, pueden prepararse usando técnicas de síntesis orgánica conocidas y pueden sintetizarse de acuerdo con cualquiera de las numerosas vías sintéticas posibles, como las de los Esquemas siguientes.
Las reacciones para preparar compuestos de la invención pueden llevarse a cabo en solventes adecuados que pueden ser seleccionados fácilmente por un experto en la técnica de síntesis orgánica. Los solventes adecuados pueden ser sustancialmente no reactivos con los materiales de partida (reactivos), los productos intermedios o productos a las temperaturas a las que se llevan a cabo las reacciones, por ejemplo, temperaturas que pueden variar entre la temperatura de congelación del solvente y la temperatura de ebullición del solvente. Una reacción dada puede llevarse a cabo en un solvente o en una mezcla de más de un solvente. Dependiendo del paso de reacción particular, el experto en la técnica puede seleccionar los solventes adecuados para un paso de reacción particular.
La preparación de compuestos de la invención puede implicar la protección y desprotección de varios grupos químicos. Un experto en la técnica puede determinar fácilmente la necesidad de protección y desprotección, y la selección de grupos protectores apropiados. La química de los grupos protectores se describe, por ejemplo, en Kocienski, Protecting Groups, (Thieme, 2007); Robertson, Protecting Group Chemistry, (Oxford University Press, 2000); Smith et al., March's Advanced Organic Chemistry: Reactions, Mechanisms, and Structure, 6a Ed. (Wiley, 2007); Peturssion et al., "Protecting Groups in Carbohydrate Chemistry," J. Chem. Educ., 1997, 74(11), 1297; y Wuts et al., Protective Groups in Organic Synthesis, 4 a Ed., (Wiley, 2006).
Las reacciones pueden monitorizarse de acuerdo con cualquier método adecuado conocido en la técnica. Por ejemplo, la formación del producto puede monitorizarse mediante medios espectroscópicos, como la espectroscopia por resonancia magnética nuclear (por ejemplo, 1H o 13C), espectroscopia infrarroja, espectrofotometría (por ejemplo, UV-visible), espectrometría de masas o mediante métodos cromatográficos como cromatografía líquida de alto rendimiento (HPLC) o cromatografía en capa fina (TLC).
Los Esquemas siguientes proporcionan una guía general en relación con la preparación de los compuestos de la invención. Un experto en la técnica comprenderá que las preparaciones mostradas en los Esquemas pueden modificarse u optimizarse usando el conocimiento general de la química orgánica para preparar varios compuestos de la invención.
Los compuestos de Fórmula (I) pueden prepararse, por ejemplo, usando un proceso como se ilustra en los Esquemas 1-3.
Los compuestos de fórmula 1-5 pueden prepararse usando los procedimientos descritos en el Esquema 1. Los ácidos de fórmula 1-2 pueden reaccionar con aminas aromáticas de fórmula 1-1 en condiciones de acoplamiento de amida [por ejemplo, en presencia de 3-óxido hexafluorofosfato de 1-[bis(dimetilamino)metileno]-1H-1,2,3-triazolo[4,5-b]piridinio (HATU) y una base adecuada como N,N-diisopropiletilamina (DIPEA)] para dar derivados de amida de fórmula 1-3. El haluro (por ejemplo, Hal1 = Cl, Br, I) en los compuestos 1-3 puede acoplarse con los compuestos de fórmula 1-4, en los que M es un ácido borónico, un éster borónico o un metal adecuadamente sustituido [por ejemplo, M es B(O)2 , Sn(Alquilo 4, o Zn-Hal], en condiciones de acoplamiento de Suzuki (por ejemplo, en presencia de un catalizador de paladio y una base adecuada) o condiciones de acoplamiento de Stille (por ejemplo, en presencia de un catalizador de paladio), o condiciones de acoplamiento de Negishi (por ejemplo, en la presencia de un catalizador de paladio) para dar derivados de fórmula 1-5. Alternativamente, el compuesto 1-4 puede ser una amina cíclica (donde M es H y está unida a un nitrógeno de amina en el anillo Cy) y el acoplamiento del haluro de arilo 1-3 con la amina cíclica 1-4 puede realizarse en condiciones de aminación de Buchwald (por ejemplo, en presencia de un catalizador de paladio y una base como terc-butóxido de sodio).
Alternativamente, los compuestos de fórmula 2-5 también pueden prepararse usando la secuencia de reacción como se describe en el Esquema 2. El acoplamiento de haluros aromáticos de fórmula 2-1 con compuestos de fórmula 2-2 puede lograrse usando condiciones similares a las descritas en el Esquema 1 para dar compuestos de fórmula 2-3. Los ácidos de fórmula 2-4 pueden reaccionar con aminas aromáticas de fórmula 2-3 en condiciones
de acoplamiento de amida para dar compuestos de fórmula 2-5.
Los compuestos de fórmula 3-6 pueden prepararse como se describe en el Esquema 3, comenzando con los compuestos de fórmula 3-1 que pueden prepararse usando rutas sintéticas como se describe en el Esquema 2 o el Esquema 1. El acoplamiento del haluro de heteroarilo 3-1 con el ácido/éster vinilborónico 3-2 en condiciones de acoplamiento de Suzuki puede dar derivados vinílicos de fórmula 3-3. La escisión oxidativa del grupo vinilo en 3-3 (es decir, en presencia de NaIO4 y OsO4) puede proporcionar el aldehído 3-4. La aminación reductora del aldehído 3-4 con la amina 3-5 puede dar los compuestos finales de fórmula 3-6.
III. Usos de los compuestos
Los compuestos de la presente divulgación pueden inhibir la actividad de la interacción proteína/proteína de PD-1/PD-L1 y, por tanto, son útiles en el tratamiento de enfermedades y trastornos asociados con la actividad de PD-1 y las enfermedades y trastornos asociados con PD-L1 incluyendo su interacción con otras proteínas como PD-1 y B7-1 (CD80). Ventajosamente, los compuestos de la presente divulgación, demuestran mejor eficacia y perfiles de seguridad y de toxicidad favorables en estudios animales. En ciertas realizaciones, los compuestos de la presente divulgación, o las sales farmacéuticamente aceptables o estereoisómeros de los mismos, son útiles para la administración terapéutica para potenciar, estimular y/o incrementar la inmunidad en el cáncer, la sepsis o la infección crónica, incluyendo la potenciación de la respuesta a la vacunación. En algunas realizaciones, la presente divulgación proporciona compuestos y composiciones para su uso en un método para inhibir o bloquear la interacción proteína/proteína de PD-1/PD-L1. El método incluye administrar a un individuo o un paciente un compuesto de Fórmula (I) o cualquiera de las fórmulas como se describe en la presente o de un compuesto como se enumera en cualquiera de las reivindicaciones y se describe en la presente, o una sal farmacéuticamente aceptable o estereoisómero del mismo. Los compuestos de la presente divulgación pueden usarse solos, en combinación con otros agentes o terapias o como un adyuvante o neoadyuvante para el tratamiento de enfermedades o trastornos, incluyendo el cáncer o enfermedades infecciosas. Para los usos descritos en la presente, puede usarse cualquiera de los compuestos de la divulgación, incluyendo cualquier realización de los mismos.
Los compuestos de la presente divulgación inhiben la interacción proteína/proteína de PD-1/PD-L1, dando como resultado un bloqueo de la vía PD-1. El bloqueo de PD-1 puede potenciar la respuesta inmunitaria a células cancerosas y enfermedades infecciosas en mamíferos, incluyendo humanos. En algunas realizaciones, la presente divulgación proporciona el tratamiento de un individuo o un paciente in vivo usando un compuesto de Fórmula (I) o una sal o estereoisómero del mismo de tal manera que se inhibe el crecimiento de tumores cancerosos. Para inhibir el crecimiento de tumores cancerosos puede usarse un compuesto de Fórmula (I) o cualquiera de las fórmulas como se describe en la presente, o un compuesto como se enumera en cualquiera de las reivindicaciones y se describe en la presente, o una sal o estereoisómero del mismo. Alternativamente, puede usarse un compuesto de Fórmula (I) o cualquiera de las fórmulas como se describe en la presente, o un compuesto como se enumera en cualquiera de las reivindicaciones y se describe en la presente, o una sal o estereoisómero del mismo, junto con otros agentes o tratamientos contra el cáncer estándar, como se describe a continuación. En una realización, la presente divulgación proporciona un método para inhibir el crecimiento de células tumorales in vitro. El método incluye poner en contacto las células tumorales in vitro con un compuesto de Fórmula (I) o de cualquiera de las fórmulas como se describe en la presente, o de un compuesto como se enumera en cualquiera de las reivindicaciones y se describe en la presente, o de una sal o estereoisómero del mismo. En otra realización, la presente divulgación proporciona compuestos y composiciones para su uso en un método para inhibir el crecimiento de células tumorales en un individuo o un paciente. El método incluye administrar al individuo o paciente con necesidad de ello una cantidad terapéuticamente
eficaz de un compuesto de Fórmula (I) o de cualquiera de las fórmulas como se describe en la presente, o de un compuesto como se enumera en cualquiera de las reivindicaciones y se describe en la presente, o una sal o un estereoisómero del mismo.
En algunas realizaciones, en la presente se proporcionan compuestos y composiciones para su uso en un método para tratar el cáncer. El método incluye administrar a un paciente con necesidad de ello una cantidad terapéuticamente eficaz de un compuesto de Fórmula (I) o cualquiera de las fórmulas como se describe en la presente, un compuesto como se enumera en cualquiera de las reivindicaciones y se describe en la presente, o una sal del mismo. Los ejemplos de cánceres incluyen aquellos cuyo crecimiento puede inhibirse usando compuestos de la divulgación y cánceres que responden típicamente a la inmunoterapia.
En algunas realizaciones, la presente divulgación proporciona compuestos y composiciones para su uso en un método para potenciar, estimular y/o aumentar la respuesta inmunitaria en un paciente. El método incluye administrar al paciente con necesidad de ello una cantidad terapéuticamente eficaz de un compuesto de Fórmula (I) o cualquiera de las fórmulas como se describe en la presente, un compuesto como se enumera en cualquiera de las reivindicaciones y se describe en la presente, o una sal del mismo.
Los ejemplos de cánceres que pueden tratarse usando los compuestos de la presente divulgación incluyen, pero no se limitan a, cáncer de hueso, cáncer de páncreas, cáncer de piel, cáncer de cabeza o cuello, melanoma maligno cutáneo o intraocular, cáncer de útero, cáncer de ovario, cáncer de recto, cáncer de la región anal, cáncer de estómago, cáncer de testículo, cáncer de útero, carcinoma de las trompas de Falopio, carcinoma de endometrio, cáncer de endometrio, carcinoma de cuello uterino, carcinoma de vagina, carcinoma de vulva, enfermedad de Hodgkin, linfoma no Hodgkin, cáncer de esófago, cáncer de intestino delgado, cáncer del sistema endocrino, cáncer de la glándula tiroides, cáncer de la glándula paratiroidea, cáncer de la glándula suprarrenal, sarcoma de tejidos blandos, cáncer de uretra, cáncer de pene, leucemias crónicas o agudas incluyendo leucemia mieloide aguda, leucemia mieloide crónica, leucemia linfoblástica aguda, leucemia linfocítica crónica, tumores sólidos de la niñez, linfoma linfocítico, cáncer de vejiga, cáncer de riñón o uretra, carcinoma de pelvis renal, neoplasia de la sistema nervioso central (SNC), linfoma primario del SNC, angiogénesis tumoral, tumor del eje espinal, glioma de tronco encefálico, adenoma pituitario, sarcoma de Kaposi, cáncer epidermoide, cáncer de células escamosas, linfoma de células T, cánceres inducidos por el medio ambiente incluyendo aquellos inducidos por asbesto, y combinaciones de dichos cánceres. Los compuestos de la presente divulgación también son útiles para el tratamiento de cánceres metastásicos, especialmente cánceres metastásicos que expresan PD-LI.
En algunas realizaciones, los cánceres que pueden tratarse con los compuestos de la presente divulgación incluyen melanoma (por ejemplo, melanoma maligno metastásico), cáncer renal (por ejemplo, carcinoma de células claras), cáncer de próstata (por ejemplo, adenocarcinoma de próstata resistente a hormonas), cáncer de mama, cáncer de mama triple negativo, cáncer de colon y cáncer de pulmón (por ejemplo, cáncer de pulmón de células no pequeñas y cáncer de pulmón de células pequeñas), cáncer de cabeza y cuello de células escamosas, cáncer urotelial (por ejemplo, vejiga) y cánceres con alta inestabilidad de microsatélites (MSIalta). Además, la divulgación incluye enfermedades malignas refractarias o recurrentes cuyo crecimiento puede inhibirse usando los compuestos de la divulgación.
En algunas realizaciones, los cánceres que pueden tratarse usando los compuestos de la presente divulgación incluyen, pero no se limitan a, tumores sólidos (por ejemplo, cáncer de próstata, cáncer de colon, cáncer de esófago, cáncer de endometrio, cáncer de ovario, cáncer de útero, cáncer de riñón, cáncer hepático, cáncer de páncreas, cáncer gástrico, cáncer de mama, cáncer de pulmón, cánceres de cabeza y cuello, cáncer de tiroides, glioblastoma, sarcoma, cáncer de vejiga, etc.), cánceres hematológicos (por ejemplo, linfoma, leucemia como leucemia linfoblástica aguda (ALL), leucemia mielógena aguda (AML), leucemia linfocítica crónica (CLL), leucemia mielógena crónica (CML), DLBCL, linfoma de células del manto, linfoma no Hodgkin (incluyendo NHL recidivante o refractario y folicular recurrente), linfoma de Hodgkin o mieloma múltiple) y combinaciones de dichos cánceres.
En algunas realizaciones, las enfermedades e indicaciones que pueden tratarse usando los compuestos de la presente divulgación incluyen, pero no se limitan a, cánceres hematológicos, sarcomas, cánceres de pulmón, cánceres gastrointestinales, cánceres del tracto genitourinario, cánceres de hígado, cánceres de huesos, cánceres del sistema nervioso, cánceres ginecológicos y cánceres de piel.
Los cánceres hematológicos ejemplares incluyen linfomas y leucemias como leucemia linfoblástica aguda (ALL), leucemia mielógena aguda (AML), leucemia promielocítica aguda (APL), leucemia linfocítica crónica (CLL), leucemia mielógena crónica (CML), linfoma difuso de células B grandes (DLBCL), linfoma de células del manto, linfoma no Hodgkin (incluyendo NHL recidivante o refractario y folicular recurrente), linfoma de Hodgkin, enfermedades mieloproliferativas (por ejemplo, mielofibrosis primaria (PMF), policitemia vera (PV), trombocitosis esencial (ET)), síndrome de mielodisplasia (MDS), linfoma linfoblástico agudo de células T (T-ALL) y mieloma múltiple (MM).
Los sarcomas ejemplares incluyen condrosarcoma, sarcoma de Ewing, osteosarcoma, rabdomiosarcoma,
angiosarcoma, fibrosarcoma, liposarcoma, mixoma, rabdomioma, rabdosarcoma, fibroma, lipoma, harmatoma y teratoma.
Los cánceres de pulmón ejemplares incluyen cáncer de pulmón de células no pequeñas (NSCLC), cáncer de pulmón de células pequeñas, carcinoma broncogénico (células escamosas, células pequeñas no diferenciadas, células grandes no diferenciadas, adenocarcinoma), carcinoma alveolar (bronquiolar), adenoma bronquial, hamartoma condromatoso y mesotelioma.
Los cánceres gastrointestinales ejemplares incluyen cánceres de esófago (carcinoma de células escamosas, adenocarcinoma, leiomiosarcoma, linfoma), estómago (carcinoma, linfoma, leiomiosarcoma), páncreas (adenocarcinoma ductal, insulinoma, glucagonoma, gastrinoma, tumores carcinoides, vipoma), intestino delgado (adenocarcinoma, linfoma, tumores carcinoides, sarcoma de Kaposi, leiomioma, hemangioma, lipoma, neurofibroma, fibroma), intestino grueso (adenocarcinoma, adenoma tubular, adenoma velloso, hamartoma, leiomioma) y cáncer colorrectal.
Los cánceres del tracto genitourinario ejemplares incluyen cánceres de riñón (adenocarcinoma, tumor de Wilm [nefroblastoma]), vejiga y uretra (carcinoma de células escamosas, carcinoma de células de transición, adenocarcinoma), próstata (adenocarcinoma, sarcoma) y testículos (seminoma, teratoma, carcinoma embrionario, teratocarcinoma, coriocarcinoma, sarcoma, carcinoma de células intersticiales, fibroma, fibroadenoma, tumores adenomatoides, lipoma).
Los cánceres de hígado ejemplares incluyen hepatoma (carcinoma hepatocelular), colangiocarcinoma, hepatoblastoma, angiosarcoma, adenoma hepatocelular y hemangioma.
Los cánceres de hueso ejemplares incluyen, por ejemplo, sarcoma osteogénico (osteosarcoma), fibrosarcoma, histiocitoma fibroso maligno, condrosarcoma, sarcoma de Ewing, linfoma maligno (sarcoma de células reticulares), mieloma múltiple, cordoma de tumor maligno de células gigantes, osteocronoma (exostosis osteocartilaginosa), condroma benigno, condroblastoma, condromixofibroma, osteoma osteoide y tumores de células gigantes
Los cánceres del sistema nervioso ejemplares incluyen cánceres de cráneo (osteoma, hemangioma, granuloma, xantoma, osteítis deformante), meninges (meningioma, meningiosarcoma, gliomatosis), cerebro (astrocitoma, meduoblastoma, glioma, ependimoma, germinoma (pinealoma), glioblastoma, glioblastoma multiforme, oligodendroglioma, schwannoma, retinoblastoma, tumores congénitos) y de la médula espinal (neurofibroma, meningioma, glioma, sarcoma), así como neuroblastoma y enfermedad de Lhermitte-Duclos.
Los cánceres ginecológicos ejemplares incluyen cánceres de útero (carcinoma endometrial), cuello uterino (carcinoma cervical, displasia cervical pretumoral), ovarios (carcinoma de ovario (cistadenocarcinoma seroso, cistoadenocarcinoma mucinoso, carcinoma no clasificado), tumores de células de la granulosa-tecal, tumores de células de Sertoli-Leydig, disgerminoma, teratoma maligno), vulva (carcinoma de células escamosas, carcinoma intraepitelial, adenocarcinoma, fibrosarcoma, melanoma), vagina (carcinoma de células claras, carcinoma de células escamosas, sarcoma botrioide (rabdomiosarcoma embrionario) y trompas de Falopio (carcinoma).
Los cánceres de piel ejemplares incluyen melanoma, carcinoma de células basales, carcinoma de células escamosas, sarcoma de Kaposi, lunares nevus displásicos, lipoma, angioma, dermatofibroma y queloides. En algunas realizaciones, las enfermedades e indicaciones que pueden tratarse usando los compuestos de la presente divulgación incluyen, pero no se limitan a, enfermedad de células falciformes (por ejemplo, anemia de células falciformes), cáncer de mama triple negativo (TNBC), síndromes mielodisplásicos, cáncer testicular, cáncer de las vías biliares, cáncer de esófago y carcinoma urotelial.
También puede usarse el bloqueo de la vía de PD-1 con compuestos de la presente divulgación para tratar infecciones como infecciones víricas, bacterianas, fúngicas y parasitarias. La presente divulgación proporciona compuestos y composiciones para su uso en un método para tratar infecciones como infecciones víricas. El método incluye administrar a un paciente con necesidad de ello una cantidad terapéuticamente eficaz de un compuesto de Fórmula (I) o cualquiera de las fórmulas como se describe en la presente, un compuesto como se enumera en cualquiera de las reivindicaciones y descrito en la presente, o una sal del mismo. Los ejemplos de virus que provocan infecciones que pueden tratarse mediante los métodos de la presente divulgación incluyen, pero no se limitan a, virus de inmunodeficiencia humana, virus del papiloma humano, gripe, virus de la hepatitis A, B, C o D, adenovirus, virus de la viruela, virus del herpes simple, citomegalovirus humano, virus del síndrome respiratorio agudo severo, virus del ébola y virus del sarampión. En algunas realizaciones, los virus que provocan infecciones que pueden tratarse mediante los métodos de la presente divulgación incluyen, pero no se limitan a, hepatitis (A, B o C), virus del herpes (por ejemplo, VZV, HSV-1, HAV-6, HSV-II, y CMV, virus de Epstein Barr), adenovirus, virus de la gripe, flavivirus, echovirus, rinovirus, virus coxsackie, coronavirus, virus sincitial respiratorio, virus de las paperas, rotavirus, virus del sarampión, virus de la rubéola, parvovirus, virus vaccinia, virus hTlV, virus del dengue, virus del papiloma, virus del molusco, virus de la polio, virus de la rabia, virus JC y virus de la encefalitis arboviral.
La presente divulgación proporciona compuestos y composiciones para su uso en un método para tratar infecciones bacterianas. El método incluye administrar a un paciente con necesidad de ello, una cantidad terapéuticamente eficaz de un compuesto de Fórmula (I) o cualquiera de las fórmulas como se describe en la presente, un compuesto como se enumera en cualquiera de las reivindicaciones y se describe en la presente o una sal del mismo. Los ejemplos no limitativos de bacterias patógenas que provocan infecciones que pueden tratarse mediante los métodos de la divulgación incluyen clamidia, bacterias rickettsial, micobacterias, estafilococos, estreptococos, neumococos, meningococos y conococos, klebsiella, proteus, serratia, pseudomonas, legionella, difteria, salmonella, bacilos, cólera, tétanos, botulismo, ántrax, peste, leptospirosis y bacterias de la enfermedad de Lyme.
La presente divulgación proporciona compuestos y composiciones para su uso en un método para tratar infecciones fúngicas. El método incluye administrar a un paciente con necesidad de ello, una cantidad terapéuticamente eficaz de un compuesto de Fórmula (I) o cualquiera de las fórmulas como se describe en la presente, un compuesto como se enumera en cualquiera de las reivindicaciones y se describe en la presente o una sal del mismo. Los ejemplos no limitativos de hongos patógenos que provocan infecciones que pueden tratarse mediante los métodos de la divulgación incluyen Candida (albicans, krusei, glabrata, tropicalis, etc.), Cryptococcus neoformans, Aspergillus (fumigatus, niger, etc.), género Mucorales (mucor, absidia, rhizophus), Sporothrix schenkii, Blastomyces dermatitidis, Paracoccidioides brasiliensis, Coccidioides immitis e Histoplasma capsulatum.
La presente divulgación proporciona compuestos y composiciones para su uso en un método para tratar infecciones parasitarias. El método incluye administrar a un paciente con necesidad de ello, una cantidad terapéuticamente eficaz de un compuesto de Fórmula (I) o cualquiera de las fórmulas como se describe en la presente, un compuesto como se enumera en cualquiera de las reivindicaciones y se describe en la presente, o una sal del mismo. Los ejemplos no limitativos de parásitos patógenos que provocan infecciones que pueden tratarse por los métodos de la divulgación incluyen Entamoeba histolytica, Balantidium coli, Naegleriafowleri, Acanthamoeba sp., Giardia lambia, Cryptosporidium sp., Pneumocystis carinii, Plasmodium vivax, Babesia microti, Trypanosoma brucei, Trypanosoma cruzi, Leishmania donovani, Toxoplasma gondi, y Nippostrongylus brasiliensis.
Los términos "individuo" o "paciente", usados indistintamente, se refieren a cualquier animal, incluyendo mamíferos, preferiblemente ratones, ratas, otros roedores, conejos, perros, gatos, cerdos, vacas, ovejas, caballos o primates, y lo más preferible humanos.
La frase "cantidad terapéuticamente eficaz" se refiere a la cantidad de compuesto activo o agente farmacéutico que provoca la respuesta biológica o medicinal en un tejido, sistema, animal, individuo o humano que está siendo buscada por un investigador, veterinario, médico u otro practicante clínico.
Como se usa en la presente, el término "tratar" o "tratamiento" se refiere a uno o más de (1) inhibir la enfermedad; por ejemplo, inhibir una enfermedad, afección o trastorno en un individuo que está experimentando o mostrando la patología o sintomatología de la enfermedad, afección o trastorno (es decir, detener el desarrollo adicional de la patología y/o sintomatología); y (2) mejorar la enfermedad; por ejemplo, mejorar una enfermedad, afección o trastorno en un individuo que está experimentando o mostrando la patología o sintomatología de la enfermedad, afección o trastorno (es decir, revertir la patología y/o sintomatología), como disminuir la gravedad de la enfermedad.
En algunas realizaciones, los compuestos de la invención son útiles para prevenir o reducir el riesgo de desarrollar cualquiera de las enfermedades a las que se hace referencia en la presente; por ejemplo, prevenir o reducir el riesgo de desarrollar una enfermedad, afección o trastorno en un individuo que puede estar predispuesto a la enfermedad, afección o trastorno pero que todavía no experimenta ni muestra la patología o sintomatología de la enfermedad.
Terapias de combinación
El crecimiento y la supervivencia de las células cancerosas pueden verse afectados por múltiples vías de señalización. Por tanto, es útil combinar diferentes inhibidores de enzimas/proteínas/receptores, que muestren diferentes preferencias en los objetivos cuyas actividades modulan para tratar tales afecciones. Dirigirse a más de una vía de señalización (o más de una molécula biológica implicada en una vía de señalización dada) puede reducir la probabilidad de que surja resistencia a los fármacos en una población celular y/o reducir la toxicidad del tratamiento.
Los compuestos de la presente divulgación pueden usarse en combinación con uno o más de otros inhibidores de enzimas/proteínas/receptores o una o más terapias para el tratamiento de enfermedades, como cáncer o infecciones. Los ejemplos de cánceres incluyen tumores sólidos y tumores líquidos, como los cánceres de la sangre. Los ejemplos de infecciones incluyen infecciones víricas, infecciones bacterianas, infecciones fúngicas o infecciones parasitarías. Por ejemplo, los compuestos de la presente divulgación pueden combinarse con uno o más
inhibidores de las siguientes quinasas para el tratamiento del cáncer: Akt1, Akt2, Akt3, TGF-PR, PKA, PKG, PKC, CaM-quinasa, fosforilasa quinasa, MEKK, ERK, MAPK, mTOR, EGFR, HER2, HER3, HER4, INS-R, IGF-1R, IR-R, PDGFaR, PDGFpR, PI3K (alfa, beta, gamma, delta), CSFIR, KIT, FLK-II, KDR/FLK-1, FLK-4, flt-1, FGFR1, FGFR2, FGFR3, FGFR4, c-Met, Ron, Sea, TRKA, TRKB, TRKC, TAM quinasas (Axl, Mer, Tyro3), FLT3, VEGFR/Flt2, Flt4, EphAI, EphA2, EphA3, EphB2, EphB4, Tie2, Src, Fyn, Lck, Fgr, Btk, Fak, SYK, FRK, JAK, ABL, ALK y B-Raf. En algunas realizaciones, los compuestos de la presente divulgación pueden combinarse con uno o más de los siguientes inhibidores para el tratamiento de cáncer o infecciones. Los ejemplos no limitativos de inhibidores que pueden combinarse con los compuestos de la presente divulgación para el tratamiento del cáncer e infecciones incluyen un inhibidor de FGFR (FGFR1, FGFR2, FGFR3 o FGFR4, por ejemplo, INCB54828, INCB62079 e INCB63904), un inhibidor de JAK (JAK1 y/o JAK2, por ejemplo, ruxolitinib, baricitinib o INCB39110), un inhibidor de IDO (por ejemplo, epacadostat, NLG919, un inhibidor de LsDl (por ejemplo, INCB59872 e INCB60003), un inhibidor de tDo, un inhibidor de PI3K-delta (por ejemplo, INCB50797 e INCB50465), un inhibidor de PI3K-gamma como un inhibidor selectivo de PI3K-gamma, un inhibidor de Pim (INCB53914), un inhibidor de CSFIR, tirosina quinasas del receptor TAM (Tyro-3, Axl y Mer), un inhibidor de la angiogénesis, un inhibidor del receptor de interleucinas, inhibidores de miembros de la familia de bromo y extraterminal (por ejemplo, inhibidores de bromodominio o inhibidores de BET como INCB54329 e INCB57643), un inhibidor de la arginasa (INCB01158), y un antagonista del receptor de adenosina o combinaciones de los mismos.
Los compuestos de la presente divulgación pueden usarse en combinación con uno o más inhibidores de puntos de control inmunitarios. Los inhibidores de puntos de control inmunitarios ejemplares incluyen inhibidores contra moléculas de puntos de control inmunitarios como CD27, CD28, CD40, CD122, Cd96, CD73, CD47, OX40, GITR, CSF1R, JAK, PI3K delta, PI3K gama, TAM, arginasa, CD137 (también conocido como 4-1BB), ICOS, A2AR, B7-H3, B7-H4, BTLA, CTLA-4, LAG3, TIM3, VISTA, PD-1, PD-L1 y PD-L2. En algunas realizaciones, la molécula de punto de control inmunitario es una molécula de punto de control estimuladora seleccionada de CD27, CD28, CD40, ICOS, OX40, GITR y CD137. En algunas realizaciones, la molécula del punto de control inmunitario es una molécula del punto de control inhibidora seleccionada de A2AR, B7-H3, B7-H4, BTLA, CTLA-4, IDO, KIR, LAG3, PD-1, TIM3 y VISTA. En algunas realizaciones, los compuestos proporcionados en la presente pueden usarse en combinación con uno o más agentes seleccionados de inhibidores de KIR, inhibidores de TIGIT, inhibidores de LAIR1, inhibidores de CD160, inhibidores de 2B4 e inhibidores de TGFR beta.
En algunas realizaciones, el inhibidor de una molécula de punto de control inmunitario es un anticuerpo anti-PD1, un anticuerpo anti-PD-LI o un anticuerpo anti-CTLA-4.
En algunas realizaciones, el inhibidor de una molécula de punto de control inmunitario es un inhibidor de PD-1, por ejemplo, un anticuerpo monoclonal anti-PD-1. En algunas realizaciones, el anticuerpo monoclonal anti-PD-1 es nivolumab, pembrolizumab (también conocido como MK-3475), pidilizumab, SHR-1210, PDR001 o AMP-224. En algunas realizaciones, el anticuerpo monoclonal anti-PD-1 es nivolumab o pembrolizumab. En algunas realizaciones, el anticuerpo anti-PD1 es pembrolizumab. En algunas realizaciones, el anticuerpo anti PD-1 es SHR-1210.
En algunas realizaciones, el inhibidor de una molécula de punto de control inmunitario es un inhibidor de PD-L1, por ejemplo, un anticuerpo monoclonal anti-PD-L1. En algunas realizaciones, el anticuerpo monoclonal anti-PD-Ll es BMS-935559, MEDI4736, MPDL3280A (también conocido como RG7446) o MSB0010718C. En algunas realizaciones, el anticuerpo monoclonal anti-PD-L1 es MPDL3280A o MEDI4736.
En algunas realizaciones, el inhibidor de una molécula de punto de control inmunitario es un inhibidor de CTLA-4, por ejemplo, un anticuerpo anti-CTLA-4. En algunas realizaciones, el anticuerpo anti-CTLA-4 es ipilimumab o tremelimumab.
En algunas realizaciones, el inhibidor de una molécula de punto de control inmunitario es un inhibidor de LAG3, por ejemplo, un anticuerpo anti-LAG3. En algunas realizaciones, el anticuerpo anti-LAG3 es BMS-986016, INCAGN2385 o LAG525.
En algunas realizaciones, el inhibidor de una molécula de punto de control inmunitario es un inhibidor de GITR, por ejemplo, un anticuerpo anti-GITR. En algunas realizaciones, el anticuerpo anti-GITR es TRX518, INCAGN1876, MK-1248, AMG228, BMS-986156, GWN323, MEDI1873 o MK-4166.
En algunas realizaciones, el inhibidor de una molécula de punto de control inmunitario es un inhibidor de OX40, por ejemplo, un anticuerpo anti-OX40 o una proteína de fusión de OX40L. En algunas realizaciones, el anticuerpo anti-OX40 es MEDI0562, MOXR-0916, PF-04518600, GSK3174998, o BMS-986178. En algunas realizaciones, la proteína de fusión de OX40L es MEDI6383.
Los compuestos de la presente divulgación pueden usarse en combinación con uno o más agentes para el tratamiento de enfermedades como el cáncer. En algunas realizaciones, el agente es un agente alquilante, un inhibidor del proteasoma, un corticosteroide o un agente inmunomodulador. Los ejemplos de un agente alquilante
incluyen ciclofosfamida (CY), melfalán (MEL) y bendamustina. En algunas realizaciones, el inhibidor del proteasoma es carfilzomib. En algunas realizaciones, el corticosteroide es dexametasona (DEX). En algunas realizaciones, el agente inmunomodulador es lenalidomida (LEN) o pomalidomida (POM).
Los compuestos de la presente divulgación pueden usarse además en combinación con otros métodos para tratar cánceres, por ejemplo, mediante quimioterapia, radioterapia, terapia dirigida a tumores, terapia adyuvante, inmunoterapia o cirugía. Los ejemplos de inmunoterapia incluyen tratamiento con citoquinas (por ejemplo, interferones, GM-CSF, G-CSF, IL-2), inmunoterapia CRS-207, vacuna contra el cáncer, anticuerpo monoclonal, transferencia de células T adoptivas, agonistas de los receptores Toll, agonistas de STING, viroterapia oncolítica y moléculas pequeñas inmunomoduladoras, incluyendo la talidomida o el inhibidor de JAK1/2 y similares. Los compuestos pueden administrarse en combinación con uno o más fármacos contra el cáncer, como un agente quimioterapéutico. Los ejemplos de agentes quimioterapéuticos incluyen cualquiera de: abarelix, aldesleucina, alemtuzumab, alitretinoína, alopurinol, altretamina, anastrozol, trióxido de arsénico, asparaginasa, azacitidina, bevacizumab, bexaroteno, baricitinib, bleomicina, bortezombi, bortezomib, busulfano intravenoso, busulfano oral, calusterona, capecitabina, carboplatino, carmustina, cetuximab, clorambucilo, cisplatino, cladribina, clofarabina, ciclofosfamida, citarabina, dacarbazina, dactinomicina, dalteparina sódica, dasatinib, daunorrubicina, decitabina, denileucina, denileucina diftitox, dexrazoxano, docetaxel, doxorrubicina, propionato de dromostanolona, eculizumab, epirrubicina, erlotinib, estramustina, etopósido fosfato, etopósido, exemestano, citrato de fentanil, filgrastim, floxuridina, fludarabina, fluorouracilo, fulvestrant, gefitinib, gemcitabina, gemtuzumab ozogamicina, acetato de goserelina, acetato de histrelina, ibritumomab tiuxetan, idarrubicina, ifosfamida, mesilato de imatinib, interferón alfa 2a, irinotecán, ditosilato de lapatinib, lenalidomida, letrozol, leucovorina, acetato de leuprolida, levamisol, lomustina, mecloretamina, acetato de megestrol, melfalán, mercaptopurina, metotrexato, metoxsaleno, mitomicina C, mitotano, mitoxantrona, fenpropionato de nandrolona, nelarabina, nofetumomab, oxaliplatino, paclitaxel, pamidronato, panitumumab, pegaspargasa, pegfilgrastim, pemetrexed disódico, pentostatina, pipobroman, plicamicina, procarbazina, quinacrina, rasburicasa, rituximab, ruxolitinib, sorafenib, estreptozocina, sunitinib, maleato de sunitinib, tamoxifeno, temozolomida, tenipósido, testolactona, talidomida, tioguanina, tiotepa, topotecán, toremifeno, tositumomab, trastuzumab, tretinoína, mostaza de uracilo, valrubicina, vinblastina, vincristina, vinorelbina, vorinostat y zoledronato.
Otros agentes anticancerígenos incluyen agentes terapéuticos de anticuerpos como trastuzumab (Herceptin), anticuerpos contra moléculas coestimuladoras como CTLA-4 (por ejemplo, ipilimumab), 4-1BB, anticuerpos contra PD-1 y PD-L1, o anticuerpos contra citoquinas (IL-10, TGF-p, etc.). Los ejemplos de anticuerpos contra PD-1 y/o PD-L1 que pueden combinarse con los compuestos de la presente divulgación para el tratamiento del cáncer o de infecciones como infecciones víricas, bacterianas, fúngicas y parasitarias incluyen, pero no se limitan a, nivolumab, pembrolizumab, MPDL3280A, MEDI-4736 y SHR-1210.
Los compuestos de la presente divulgación pueden usarse además en combinación con uno o más agentes antiinflamatorios, esteroides, inmunosupresores o anticuerpos terapéuticos.
Los compuestos de Fórmula (I) o cualquiera de las fórmulas como se describe en la presente, un compuesto como se enumera en cualquiera de las reivindicaciones y se describe en la presente, o sales de los mismos pueden combinarse con otro agente inmunogénico, como células cancerosas, antígenos tumorales purificados (incluyendo proteínas recombinantes, péptidos y moléculas de carbohidratos), células y células transfectadas con genes que codifican citoquinas inmunoestimuladoras. Los ejemplos no limitativos de vacunas tumorales que pueden usarse incluyen péptidos de antígenos de melanoma, como péptidos de gp100, antígenos MAGE, Trp-2, MARTI y/o tirosinasa, o células tumorales transfectadas para expresar la citoquina GM-CSF.
Los compuestos de Fórmula (I) o cualquiera de las fórmulas como se describe en la presente, un compuesto como se enumera en cualquiera de las reivindicaciones y se describe en la presente, o sales de los mismos pueden usarse en combinación con un protocolo de vacunación para el tratamiento del cáncer. En algunas realizaciones, las células tumorales se transducen para expresar GM-CSF. En algunas realizaciones, las vacunas contra tumores incluyen las proteínas de virus implicados en cánceres humanos como virus del papiloma humano (VPH), virus de la hepatitis (VHB y VHC) y virus del sarcoma del herpes de Kaposi (KHSV). En algunas realizaciones, los compuestos de la presente divulgación pueden usarse en combinación con antígenos específicos de tumores como proteínas de choque térmico aisladas del propio tejido tumoral. En algunas realizaciones, los compuestos de Fórmula (I) o cualquiera de las fórmulas como se describe en la presente, un compuesto como se enumera en cualquiera de las reivindicaciones y se describe en la presente, o sales de los mismos pueden combinarse con la inmunización de células dendríticas para activar respuestas antitumorales potentes.
Los compuestos de la presente divulgación pueden usarse en combinación con péptidos macrocíclicos biespecíficos que se dirigen a células efectoras que expresan el receptor Fe alfa o Fe gamma para células tumorales. Los compuestos de la presente divulgación también pueden combinarse con péptidos macrocíclicos que activan la capacidad de respuesta inmunitaria del huésped.
Los compuestos de la presente divulgación pueden usarse en combinación con trasplante de médula ósea
para el tratamiento de una variedad de tumores de origen hematopoyético.
Los compuestos de Fórmula (I) o cualquiera de las fórmulas como se describe en la presente, un compuesto como se enumera en cualquiera de las reivindicaciones y se describe en la presente, o sales de los mismos pueden usarse en combinación con vacunas para estimular la respuesta inmunitaria contra patógenos, toxinas y autoantígenos. Los ejemplos de patógenos para los que puede ser particularmente útil este enfoque terapéutico incluyen patógenos para los que actualmente no hay una vacuna eficaz, o patógenos para los que las vacunas convencionales no son completamente eficaces. Estos incluyen, pero no se limitan a, VIH, Hepatitis (A, B y C), Gripe, Herpes, Giardia, Malaria, Leishmania, Staphylococcus aureus, Pseudomonas Aeruginosa.
Los virus que provocan infecciones que pueden tratarse mediante los métodos de la presente divulgación incluyen, pero no se limitan a, virus del papiloma humano, gripe, virus de la hepatitis A, B, C o D, adenovirus, virus de la viruela, virus del herpes simple, citomegalovirus humano, virus del síndrome respiratorio agudo severo, virus del ébola, virus del sarampión, virus del herpes (por ejemplo, VZV, HSV-1, HAV-6, HSV-II y CMV, virus de Epstein Barr), flavivirus, echovirus, rhinovirus, virus coxsackie, cornovirus, virus respiratorio sincitial, virus de las paperas, rotavirus, virus del sarampión, virus de la rubéola, parvovirus, virus vaccinia, virus HTLV, virus del dengue, virus del papiloma, virus del molusco, virus de la polio, virus de la rabia, virus JC y virus de la encefalitis arboviral.
Las bacterias patógenas que provocan infecciones que pueden tratarse mediante los métodos de la divulgación incluyen, pero no se limitan a, clamidia, bacterias rickettsiales, micobacterias, estafilococos, estreptococos, neumococos, meningococos y conococos, klebsiella, proteus, serratia, pseudomonas, legionela, difteria, salmonela, bacilos, cólera, tétanos, botulismo, ántrax, peste, leptospirosis y bacterias de la enfermedad de Lyme.
Los hongos patógenos que provocan infecciones que pueden tratarse mediante los métodos de la divulgación incluyen, pero no se limitan a, Candida (albicans, krusei, glabrata, tropicalis, etc.), Cryptococcus neoformans, Aspergillus (fumigatus, niger, etc.), género Mucorales (mucor, absidia, rhizophus), Sporothrix schenkii, Blastomyces dermatitidis, Paracoccidioides brasiliensis, Coccidioides immitis e Histoplasma capsulatum.
Los parásitos patógenos que provocan infecciones que pueden tratarse mediante los métodos de la divulgación incluyen, pero no se limitan a, Entamoeba histolytica, Balantidium coli, Naegleriafowleri, Acanthamoeba sp., Giardia lambia, Cryptosporidium sp., Pneumocystis carinii, Plasmodium vivax, Babesia microti, Trypanosoma brucei, Trypanosoma cruzi, Leishmania donovani, Toxoplasma gondi y Nippostrongylus brasiliensis.
Cuando se administra más de un agente farmacéutico a un paciente, pueden administrarse simultáneamente, por separado, secuencialmente o en combinación (por ejemplo, para más de dos agentes).
IV. Formulación, formas de dosificación y administración
Cuando se emplean como productos farmacéuticos, los compuestos de la presente divulgación pueden administrarse en forma de composiciones farmacéuticas. Por tanto, la presente divulgación proporciona una composición que comprende un compuesto de Fórmula (I) o cualquiera de las fórmulas como se describe en la presente, un compuesto como se enumera en cualquiera de las reivindicaciones y se describe en la presente, o una sal farmacéuticamente aceptable del mismo, o cualquier realización de los mismos y por lo menos un portador o excipiente farmacéuticamente aceptable. Estas composiciones pueden prepararse de una manera bien conocida en la técnica farmacéutica y pueden administrarse mediante una variedad de vías, dependiendo de si está indicado un tratamiento local o sistémico y del área a tratar. La administración puede ser tópica (incluyendo transdérmica, epidérmica, oftálmica y a las membranas mucosas incluyendo administración intranasal, vaginal y rectal), pulmonar (por ejemplo, por inhalación o insuflación de polvos o aerosoles, incluyendo por nebulizador; intratraqueal o intranasal), oral o parenteral. La administración parenteral incluye administración intravenosa, intraarterial, subcutánea, intraperitoneal, intramuscular o por inyección o por infusión; o administración intracraneal, por ejemplo, intratecal o intraventricular. La administración parenteral puede ser en forma de una sola dosis en bolo o puede ser, por ejemplo, mediante una bomba de perfusión continua. Las composiciones y formulaciones farmacéuticas para administración tópica pueden incluir parches transdérmicos, pomadas, lociones, cremas, geles, gotas, supositorios, espráis, líquidos y polvos. Pueden ser necesarios o deseables portadores farmacéuticos convencionales, bases acuosas, en polvo u oleosas, espesantes y similares.
Esta invención también incluye composiciones farmacéuticas que contienen, como ingrediente activo, el compuesto de la presente divulgación o una sal farmacéuticamente aceptable del mismo, en combinación con uno o más portadores o excipientes farmacéuticamente aceptables. En algunas realizaciones, la composición es adecuada para administración tópica. Al elaborar las composiciones de la invención, el ingrediente activo típicamente se mezcla con un excipiente, se diluye con un excipiente o se encierra dentro de dicho portador en forma de, por ejemplo, una cápsula, bolsita, papel u otro recipiente. Cuando el excipiente sirve como diluyente, puede ser un material sólido, semisólido o líquido, que actúa como vehículo, portador o medio para el ingrediente activo. Por tanto, las composiciones pueden estar en forma de comprimidos, píldoras, polvos, pastillas para chupar, bolsitas, obleas,
elixires, suspensiones, emulsiones, soluciones, jarabes, aerosoles (como un medio sólido o líquido), pomadas que contienen, por ejemplo, hasta un 10% en peso del compuesto activo, cápsulas de gelatina blanda y dura, supositorios, soluciones inyectables estériles y polvos envasados estériles.
Al preparar una formulación, puede molerse el compuesto activo para proporcionar el tamaño de partícula apropiado antes de combinarlo con los otros ingredientes. Si el compuesto activo es sustancialmente insoluble, puede molerse hasta un tamaño de partícula de menos de 200 mesh. Si el compuesto activo es sustancialmente soluble en agua, el tamaño de partícula puede ajustarse mediante molienda para proporcionar una distribución sustancialmente uniforme en la formulación, por ejemplo, aproximadamente 40 mesh.
Los compuestos de la invención pueden molerse usando procedimientos de molienda conocidos, como molienda en húmedo, para obtener un tamaño de partícula apropiado para la formación de comprimidos y para otros tipos de formulaciones. Las preparaciones finamente divididas (nanopartículas) de los compuestos de la invención pueden prepararse mediante procesos conocidos en la técnica, ver, por ejemplo, la WO 2002/000196.
Algunos ejemplos de excipientes adecuados incluyen lactosa, dextrosa, sacarosa, sorbitol, manitol, almidones, goma acacia, fosfato de calcio, alginatos, tragacanto, gelatina, silicato de calcio, celulosa microcristalina, polivinilpirrolidona, celulosa, agua, jarabe y metilcelulosa. Las formulaciones pueden incluir adicionalmente: agentes lubricantes como talco, estearato de magnesio y aceite mineral; agentes humectantes; agentes emulsionantes y de suspensión; agentes conservantes como metil- y propilhidroxibenzoatos; agentes edulcorantes; y agentes aromatizantes. Las composiciones de la invención pueden formularse para proporcionar una liberación rápida, sostenida o retardada del ingrediente activo después de la administración al paciente empleando procedimientos conocidos en la técnica.
En algunas realizaciones, la composición farmacéutica comprende celulosa microcristalina silicificada (SMCC) y por lo menos un compuesto descrito en la presente, o una sal farmacéuticamente aceptable del mismo. En algunas realizaciones, la celulosa microcristalina silicificada comprende aproximadamente un 98% de celulosa microcristalina y aproximadamente un 2% de dióxido de silicio p/p.
En algunas realizaciones, la composición es una composición de liberación sostenida que comprende por lo menos un compuesto descrito en la presente, o una sal farmacéuticamente aceptable del mismo, y por lo menos un portador o excipiente farmacéuticamente aceptable. En algunas realizaciones, la composición comprende por lo menos un compuesto descrito en la presente, o una sal farmacéuticamente aceptable del mismo, y por lo menos un componente seleccionado de celulosa microcristalina, lactosa monohidrato, hidroxipropilmetilcelulosa y óxido de polietileno. En algunas realizaciones, la composición comprende por lo menos un compuesto descrito en la presente, o una sal farmacéuticamente aceptable del mismo, y celulosa microcristalina, lactosa monohidrato e hidroxipropilmetilcelulosa. En algunas realizaciones, la composición comprende por lo menos un compuesto descrito en la presente, o una sal farmacéuticamente aceptable del mismo, y celulosa microcristalina, lactosa monohidrato y óxido de polietileno. En algunas realizaciones, la composición comprende además estearato de magnesio o dióxido de silicio. En algunas realizaciones, la celulosa microcristalina es Avicel PH102™. En algunas realizaciones, la lactosa monohidrato es Fast-flo 316™. En algunas realizaciones, la hidroxipropilmetilcelulosa es hidroxipropilmetilcelulosa 2208 K4M (por ejemplo, Methocel K4 M Premier™) y/o hidroxipropilmetilcelulosa 2208 K100LV (por ejemplo, Methocel K00LV™). En algunas realizaciones, el óxido de polietileno es óxido de polietileno WSR 1105 (por ejemplo, PolyoxWSR 1105™).
En algunas realizaciones, se usa un proceso de granulación en húmedo para producir la composición. En algunas realizaciones, se usa un proceso de granulación en seco para producir la composición.
Las composiciones pueden formularse en una forma de dosificación unitaria, cada dosificación conteniendo de aproximadamente 5 a aproximadamente 1000 mg (1g), más habitualmente de aproximadamente 100 mg a aproximadamente 500 mg, del ingrediente activo. En algunas realizaciones, cada dosificación contiene aproximadamente 10 mg del ingrediente activo. En algunas realizaciones, cada dosificación contiene aproximadamente 50 mg del ingrediente activo. En algunas realizaciones, cada dosificación contiene aproximadamente 25 mg del ingrediente activo. El término "formas de dosificación unitarias" se refiere a unidades físicamente discretas adecuadas como dosificaciones unitarias para sujetos humanos y otros mamíferos, cada unidad conteniendo una cantidad predeterminada de material activo calculada para producir el efecto terapéutico deseado, en asociación con un excipiente farmacéutico adecuado.
Los componentes usados para formular las composiciones farmacéuticas son de alta pureza y están sustancialmente libres de contaminantes potencialmente dañinos (por ejemplo, por lo menos de calidad alimentaria nacional, generalmente por lo menos de calidad analítica y más típicamente por lo menos de calidad farmacéutica). Particularmente para el consumo humano, la composición se fabrica o formula preferiblemente bajo los estándares de Buenas Prácticas de Fabricación como se define en las regulaciones aplicables de la Administración de Fármacos y Alimentos de los Estados Unidos. Por ejemplo, las formulaciones adecuadas pueden ser estériles y/o sustancialmente isotónicas y/o en total conformidad con todas las regulaciones de Buenas Prácticas de Fabricación
de la Administración de Fármacos y Alimentos de los Estados Unidos.
El compuesto activo puede ser eficaz en un amplio intervalo de dosificación y generalmente se administra en una cantidad terapéuticamente eficaz. Sin embargo, se entenderá que la cantidad del compuesto administrado realmente será determinada habitualmente por un médico, de acuerdo con las circunstancias relevantes, incluyendo la afección a tratar, la vía de administración elegida, el compuesto real administrado, la edad, peso y respuesta del paciente individual, la gravedad de los síntomas del paciente.
La dosificación terapéutica de un compuesto de la presente invención puede variar de acuerdo con, por ejemplo, el uso particular para el que se realiza el tratamiento, la forma de administración del compuesto, la salud y el estado del paciente y el criterio del médico que prescribe. La proporción o concentración de un compuesto de la invención en una composición farmacéutica puede variar dependiendo de una serie de factores que incluyen la dosificación, las características químicas (por ejemplo, hidrofobicidad) y la vía de administración. Por ejemplo, los compuestos de la invención pueden proporcionarse en una solución de tampón fisiológica acuosa que contiene de aproximadamente el 0,1 a aproximadamente el 10% p/v del compuesto para administración parenteral. Algunos intervalos de dosis típicos son de aproximadamente 1 pg/kg a aproximadamente 1 g/kg de peso corporal al día. En algunas realizaciones, el intervalo de dosis es de aproximadamente 0,01 mg/kg a aproximadamente 100 mg/kg de peso corporal al día. Es probable que la dosificación dependa de variables como el tipo y grado de progresión de la enfermedad o trastorno, el estado de salud general del paciente particular, la eficacia biológica relativa del compuesto seleccionado, la formulación del excipiente y su vía de administración. Las dosis eficaces pueden extrapolarse a partir de curvas de respuesta a la dosis derivadas de sistemas de ensayo de modelos animales o in vitro.
Para preparar composiciones sólidas como comprimidos, el ingrediente activo principal se mezcla con un excipiente farmacéutico para formar una composición de preformulación sólida que contiene una mezcla homogénea de un compuesto de la presente invención. Cuando se hace referencia a estas composiciones de preformulación como homogéneas, el ingrediente activo típicamente se dispersa uniformemente por toda la composición para que la composición pueda subdividirse fácilmente en formas de dosificación unitarias igualmente eficaces, como comprimidos, píldoras y cápsulas. Esta preformulación sólida se subdivide luego en formas de dosificación unitaria del tipo descrito anteriormente que contienen, por ejemplo, de aproximadamente 0,1 a aproximadamente 1000 mg del ingrediente activo de la presente invención.
Los comprimidos o píldoras de la presente invención pueden recubrirse o combinarse de otro modo para proporcionar una forma de dosificación que proporcione la ventaja de una acción prolongada. Por ejemplo, el comprimido o píldora puede comprender un componente de dosificación interno y uno de dosificación exteno, estando este último en forma de envoltura sobre el primero. Los dos componentes pueden estar separados por una capa entérica que sirve para resistir la disgregación en el estómago y permitir que el componente interno pase intacto al duodeno o que se retrase su liberación. Pueden usarse una variedad de materiales para tales capas o recubrimientos entéricos, tales materiales incluyendo una serie de ácidos poliméricos y mezclas de ácidos poliméricos con materiales como goma laca, alcohol cetílico y acetato de celulosa.
Las formas líquidas en las que los compuestos y las composiciones de la presente invención pueden incorporarse para su administración por vía oral o por inyección incluyen soluciones acuosas, jarabes adecuadamente aromatizados, suspensiones acuosas u oleosas y emulsiones aromatizadas con aceites comestibles como aceite de semilla de algodón, aceite de sésamo, aceite de coco, o aceite de cacahuete, así como elixires y vehículos farmacéuticos similares.
Las composiciones para inhalación o insuflación incluyen soluciones y suspensiones en solventes acuosos u orgánicos farmacéuticamente aceptables, o mezclas de los mismos, y polvos. Las composiciones líquidas o sólidas pueden contener excipientes farmacéuticamente aceptables adecuados como se ha descrito anteriormente. En algunas realizaciones, las composiciones se administran por vía respiratoria oral o nasal para un efecto local o sistémico. Las composiciones pueden nebulizarse mediante el uso de gases inertes. Las soluciones nebulizadas pueden respirarse directamente desde el dispositivo nebulizador o el dispositivo nebulizador puede conectarse a una máscara facial, máscara tipo tienda o máquina de respiración de presión positiva intermitente. Las composiciones en solución, suspensión o polvo pueden administrarse por vía oral o nasal desde dispositivos que administran la formulación de manera apropiada.
Las formulaciones tópicas pueden contener uno o más portadores convencionales. En algunas realizaciones, las pomadas pueden contener agua y uno o más portadores hidrófobos seleccionados de, por ejemplo, parafina líquida, polioxietilen alquil éter, propilenglicol y vaselina blanca. Las composiciones portadoras de cremas pueden estar basadas en agua en combinación con glicerol y uno o más de otros componentes, por ejemplo, monoestearato de glicerina, monoestearato de glicerina-PEG y alcohol cetilestearílico. Los geles pueden formularse usando alcohol isopropílico y agua, adecuadamente en combinación con otros componentes como, por ejemplo, glicerol, hidroxietilcelulosa y similares. En algunas realizaciones, las formulaciones tópicas contienen por lo menos aproximadamente el 0,1, por lo menos aproximadamente el 0,25, por lo menos aproximadamente el 0,5, por lo
menos aproximadamente el 1, por lo menos aproximadamente el 2 o por lo menos aproximadamente el 5% en peso del compuesto de la invención. Las formulaciones tópicas pueden envasarse adecuadamente en tubos de, por ejemplo, 100 g que están asociados opcionalmente con instrucciones para el tratamiento de la indicación seleccionada, por ejemplo, psoriasis u otra afección de la piel.
La cantidad de compuesto o composición administrada a un paciente variará dependiendo de lo que se esté administrando, el propósito de la administración, como profilaxis o terapia, el estado del paciente, la forma de administración y similares. En aplicaciones terapéuticas, las composiciones pueden administrarse a un paciente que ya padece una enfermedad en una cantidad suficiente para curar o por lo menos detener parcialmente los síntomas de la enfermedad y sus complicaciones. Las dosis eficaces dependerán del estado patológico que se esté tratando, así como del criterio del practicante clínico, dependiendo de factores como la gravedad de la enfermedad, la edad, el peso y el estado general del paciente.
Las composiciones administradas a un paciente pueden estar en forma de las composiciones farmacéuticas descritas anteriormente. Estas composiciones pueden esterilizarse mediante técnicas de esterilización convencionales, o pueden esterilizarse por filtración. Las soluciones acuosas pueden envasarse para su uso tal cual, o liofilizarse, la preparación liofilizada combinándose con un portador acuoso estéril antes de la administración. El pH de las preparaciones de compuestos típicamente estará entre 3 y 11, más preferiblemente entre 5 y 9 y lo más preferible entre 7 y 8. Se entenderá que el uso de algunos de los excipientes, portadores o estabilizadores anteriores dará como resultado la formación de sales farmacéuticas.
La dosificación terapéutica de un compuesto de la presente invención puede variar de acuerdo con, por ejemplo, el uso particular para el cual se hace el tratamiento, la forma de administración del compuesto, la salud y el estado del paciente, y el criterio del médico que prescribe. La proporción o concentración de un compuesto de la invención en una composición farmacéutica puede variar dependiendo de una serie de factores que incluyen la dosificación, las características químicas (por ejemplo, hidrofobicidad) y la vía de administración. Por ejemplo, los compuestos de la invención pueden proporcionarse en una solución tampón fisiológica acuosa que contiene de aproximadamente el 0,1 a aproximadamente el 10% p/v del compuesto para administración parenteral. Algunos intervalos de dosis típicos son de aproximadamente 1 pg/kg a aproximadamente 1 g/kg, de peso corporal al día. En algunas realizaciones, el intervalo de dosis es de aproximadamente 0,01 mg/kg a aproximadamente 100 mg/kg de peso corporal al día. Es probable que la dosificación dependa de variables como el tipo y grado de progresión de la enfermedad o trastorno, el estado de salud general del paciente particular, la eficacia biológica relativa del compuesto seleccionado, la formulación del excipiente y su vía de administración. Las dosis eficaces pueden extrapolarse a partir de curvas de respuesta a dosis derivadas de sistemas de prueba in vitro o en modelos animales.
V. Compuestos marcados y métodos de ensayo
Los compuestos de la presente divulgación pueden ser útiles además en investigaciones de procesos biológicos en tejidos normales y anormales. Por tanto, otro aspecto de la presente invención se refiere a compuestos marcados de la invención (radiomarcados, marcados fluorescentes, etc.) que serían útiles no solo en técnicas de imagenología sino también en ensayos, tanto in vitro como in vivo, para localizar y cuantificar la proteína de PD-1 o PD-L1 en muestras de tejido, incluyendo el humano, y para identificar ligandos de PD-L1 mediante la unión por inhibición de un compuesto marcado. Por consiguiente, la presente invención incluye ensayos de unión de PD-1/PD-L1 que contienen tales compuestos marcados.
La presente invención incluye además compuestos de la divulgación sustituidos isotópicamente. Un compuesto "sustituido isotópicamente" es un compuesto de la invención en el que uno o más átomos se reemplazan o sustituyen por un átomo que tiene el mismo número atómico pero diferente masa atómica o número de masa, por ejemplo una masa atómico o número de masa diferentes de la masa atómica o número de masa que se encuentra típicamente en la naturaleza (es decir, de origen natural). Debe entenderse que un compuesto "radiomarcado" es un compuesto que ha incorporado por lo menos un isótopo que es radioactivo (por ejemplo, radionúclido). Los radionúclidos adecuados que pueden incorporarse en los compuestos de la presente invención incluyen, pero no se limitan a 3H (también escrito como T para tritio), 11C, 13C, 14C, 13N, 15N, 15O, 17O, 18O, 18F, 35S, 36Cl, 82Br, 75Br, 76Br, 77Br, 123I, 124I, 125I y 131I. El radionúclido que se incorpora en los presentes compuestos radiomarcados dependerá de la aplicación específica de ese compuesto radiomarcado. Por ejemplo, para ensayos de competencia y marcado de proteínas de PD-L1 in vitro, serán generalmente más útiles compuestos que incorporan 3H, 14C, 82Br, 125I, 131I, 35S. Para aplicaciones de radio-imagenología serán generalmente más útiles 11C, 18F, 125I, 123I, 124I, 131I, 75Br, 76Bro 77Br.
Debe entenderse que un "compuesto radiomarcado" o "marcado" es un compuesto que ha incorporado por lo menos un radionúclido. En algunas realizaciones, el radionúclido se selecciona del grupo que consiste en 3H, 14C, 125I, 35S y 82Br. En la técnica se conocen los métodos sintéticos para incorporar radioisótopos en compuestos orgánicos.
Un compuesto radiomarcado de la invención puede usarse en un ensayo de selección para identificar y/o
evaluar compuestos. Por ejemplo, un compuesto recién sintetizado o identificado (es decir, compuesto de prueba) que está marcado puede evaluarse para determinar su capacidad para unirse a una proteína de PD-L1 monitorizando su variación de la concentración cuando entra en contacto con la proteína de PD-L1, haciendo un seguimiento del marcado. Por ejemplo, puede evaluarse un compuesto de prueba (radiomarcado) para determinar su capacidad para reducir la unión de otro compuesto que se sabe que se une a una proteína de PD-L1 (es decir, compuesto estándar). Por consiguiente, la capacidad de un compuesto de prueba para competir con el compuesto estándar para unirse a la proteína de PD-L1 se correlaciona directamente con su afinidad de unión. Por el contrario, en algunos otros ensayos de selección, el compuesto estándar está marcado y los compuestos de prueba no están marcados. Por consiguiente, se monitoriza la concentración del compuesto estándar marcado para evaluar la competencia entre el compuesto estándar y el compuesto de prueba, y por tanto se determina la afinidad de unión relativa del compuesto de prueba.
VI. Kits
La presente divulgación también incluye kits farmacéuticos útiles, por ejemplo, en el tratamiento o prevención de enfermedades o trastornos asociados con la actividad de PD-L1, incluyendo su interacción con otras proteínas como PD-1 y B7-1 (CD80), como el cáncer o infecciones, que incluyen uno o más recipientes que contienen una composición farmacéutica que comprende una cantidad terapéuticamente eficaz de un compuesto de Fórmula (I), o cualquier realización del mismo. Tales kits pueden incluir además uno o más de varios componentes de kits farmacéuticos convencionales como, por ejemplo, recipientes con uno o más portadores farmacéuticamente aceptables, recipientes adicionales, etc. como será fácilmente evidente para los expertos en la técnica. También pueden incluirse en el kit instrucciones, ya sea como prospectos o etiquetas, que indiquen las cantidades de los componentes que se administrarán, las pautas para la administración y/o las pautas para mezclar los componentes.
La invención se describirá con mayor detalle a modo de ejemplos específicos. Los siguientes ejemplos se ofrecen con propósitos ilustrativos y no se pretende que limiten la invención de ninguna manera. Los expertos en la técnica reconocerán fácilmente una variedad de parámetros no críticos que pueden cambiarse o modificarse para proporcionar esencialmente los mismos resultados. Se ha descubierto que los compuestos de los Ejemplos inhiben la actividad de la interacción proteína/proteína de PD-1/PD-L1 de acuerdo con por lo menos un ensayo descrito en la presente.
EJEMPLOS
A continuación se proporcionan los procedimientos experimentales para los compuestos de la invención. La purificación por LCMS preparativa de acceso abierto de algunos de los compuestos preparados se realizó en sistemas de fraccionamiento dirigido por masas de Waters. La configuración básica del equipo, los protocolos y el software de control para el funcionamiento de estos sistemas se han descrito en detalle en la bibliografía. Consultar, por ejemplo, Blom, "Two-Pump At Column Dilution Configuration for Preparative LC-MS", K. Blom, J. Combi. Chem., 2002, 4, 295-301; Blom et al., "Optimizing Preparative LC-MS Configurations and Methods for Parallel Synthesis Purification", J. Combi. Chem., 2003, 5, 670-83; y Blom et al., "Preparative LC-MS Purification: Improved Compound Specific Method Optimization", J. Combi. Chem., 2004, 6, 874-883.
Ejemplo 1
Ácido (2S)-1-[(2-{[(2-metilbifenil-3-il)amino]carbonil}-1,3-tiazol-5-il)metil]piperidina-2-carboxílico
Paso 1: 2-metilbifenil-3-amina
A una solución de 3-bromo-2-metilanilina (1,0 g, 5,4 mmol) en agua (2,9 ml) y 1,4-dioxano (10 ml) se le añadió ácido fenilborónico (0,79 g, 6,4 mmol), complejo de [1,1'-bis(difenilfosfino)ferroceno]dicloropaladio(II) con diclorometano (1:1) (0,3 g, 0,3 mmol) y carbonato de sodio (1,2 g, 11 mmol). La mezcla resultante se purgó con
nitrógeno y luego se agitó a 100° C durante 3 h. La mezcla de la reacción se enfrió a temperatura ambiente, luego se filtró y se concentró hasta la sequedad. El residuo se purificó por cromatografía sobre gel de sílice eluyendo con acetato de etilo al 20% en hexanos para dar el producto deseado. LC-MS calculada para C13 H14N (M+H)+: m/z=184.1; encontrado 184.1.
Paso 2: 5-bromo-N-(2-metilbifenil-3-il)-1,3-tiazol-2-carboxamida
A una solución de acido 5-bromo-1,3-tiazol-2-carboxmco (AstaTech, N° de cat. 450324: 90 mg, 0,43 mmol) y 2-metilbifenil-3-amina (87 mg, 0,48 mmol) en N,N-dimetilformamida (5 ml) se le añadió hexafluorofosfato de N,N,N',N'-tetrametil-O-(7-azabenzotriazol-1-il)uronio (250 mg, 0,65 mmol), seguido de N,N-diisopropiletilamina (230 |jl, 1,3 mmol). La mezcla resultante se agitó a temperatura ambiente durante 3 h, luego se diluyó con EtOAc y se lavó con agua y salmuera. La capa orgánica se secó sobre Na2SO4, se filtró y se concentró. El residuo se usó en el paso siguiente sin purificación adicional. LC-MS calculada para C-^H-mB ^ O S (M+H)+: m/z=373.0; encontrado 373.0.
Paso 3: N-(2-metilbifenil-3-il)-5-vinil-1,3-tiazol-2-carboxamida
Se purgó con nitrógeno una mezcla de 5-bromo-N-(2-metilbifenil-3-il)-1,3-tiazol-2-carboxamida (producto bruto del Paso 2: 160 mg, 0,43 mmol), 4,4,5,5-tetrametil-2-vinil-1,3,2-dioxaborolano (110 jl, 0,64 mmol), complejo de [1 ,1 '-bis(difenilfosfino)ferroceno]dicloropaladio(N) con diclorometano (1 :1 ) ( 20 mg, 0 , 0 2 mmol) y carbonato de sodio (95 mg, 0,90 mmol) en 1,4-dioxano (4,7 ml) y agua (800 jl) y luego se agitó a 100° C durante 2 horas. La mezcla de la reacción se enfrió a temperatura ambiente, luego se filtró y se concentró. El residuo se purificó mediante cromatografía ultrarrápida en una columna de gel de sílice eluyendo con AcOEt al 15% en hexanos para dar el producto deseado (115 mg, 84%). LC-MS calculada para C19H17 N2OS (M+H)+: m/z=321.1; encontrado 321.1.
Paso 4: 5-formil-N-(2-metilbifenil-3-il)-1,3-tiazol-2-carboxamida
A una solución de N-(2-metilbifenil-3-il)-5-vinil-1,3-tiazol-2-carboxamida (115 mg, 0,359 mmol) en 1,4-dioxano (3,6 ml) se le añadió 2,6-lutidina (170 jl, 1,4 mmol), seguido de tetraóxido de osmio (4% en peso en agua, 340 jl, 0,054 mmol) a temperatura ambiente. La mezcla se agitó durante 10 min y luego se añadió peryodato de sodio (230 mg, 1,1 mmol) en agua (1,5 ml). La mezcla de la reacción se agitó a temperatura ambiente durante la noche. La mezcla de la reacción se diluyó con agua y luego se extrajo con DCM. Los extractos combinados se lavaron con agua y salmuera y luego se secaron sobre Na2SO4, se filtraron y se concentraron a presión reducida. El residuo se purificó mediante cromatografía ultrarrápida en una columna de gel de sílice eluyendo con AcOEt al 20% en hexanos para dar el producto deseado. LC-Ms calculada para C18H15 N2O2S (M+H)+: m/z=323.1; encontrado 323.1.
Paso 5: ácido (2S)-1-[(2-{[(2-metilbifenil-3-il)amino]carbonil}-1,3-tiazol-5-il)metil]piperidina-2-carboxílico
A una solución de 5-formil-N-(2-metilbifenil-3-il)-1,3-tiazol-2-carboxamida (20 mg, 0,062 mmol) en 1,2-dicloroetano (1 ml) se le añadió ácido (2S)-piperidina-2-carboxílico (TCI, N° de cat. P1404: 16 mg, 0,12 mmol). La mezcla se agitó a temperatura ambiente durante 20 min y luego se añadió triacetoxiborohidruro de sodio (39 mg, 0,19 mmol). La mezcla de la reacción se agitó a temperatura ambiente durante la noche y luego se concentró. El residuo se disolvió en MeOH y se purificó por HPLC preparativa (pH=10, acetonitrilo/agua+NH4OH) para dar el producto deseado. LC-MS calculada para C24H26N3O3S (M+H)+: m/z=436.2; encontrado 436.2.
Ejemplo 2
5-{[(2-hidroxietil)amino]metil}-N-(2-metilbifenil-3-il-3-il)-1,3-tiazol-2-carboxamida
A una solución de 5-formil-N-(2-metilbifenil-3-il)-1,3-tiazol-2-carboxamida (Ejemplo 1, Paso 4: 12,0 mg, 0,0372 mmol) en 1,2-dicloroetano (0,8 ml) se añadió etanolamina (4,5 pl, 0,074 mmol). La mezcla resultante se agitó a temperatura ambiente durante 20 min y luego se añadió triacetoxiborohidruro de sodio (24 mg, 0,11 mmol). La mezcla se agitó a temperatura ambiente durante la noche y luego se concentró. El residuo se disolvió en MeOH y luego se purificó por HPLC preparativa (pH = 10, acetonitrilo/agua NH4OH) para dar el producto deseado. LC-MS calculada para C20H22N3O2S (M+H)+: m/z=368.1; encontrado 368.1.
Ejemplo 3
5-{[(2-hidroxietil)amino]metil}-N-(2-metilbifenil-3-il)-1,3-oxazol-2-carboxamida
Paso 1: 5-({[terc-butil(dimetil)silil]oxi}metil)-1,3-oxazol
A una solución de 1,3-oxazol-5-ilmetanol (Ark Pharm, N° de cat. AK-25343: 1,0 g, 10, mmol) en cloruro de metileno (10 ml) se le añadieron trietilamina (1,68 ml, 12,0 mmol) y 4-dimetilaminopiridina (65,2 mg, 0,534 mmol), seguido de cloruro de terc-butildimetilsililo (1,59 g, 10,6 mmol) a temperatura ambiente. La mezcla se agitó a temperatura ambiente durante la noche, luego se diluyó con agua y se extrajo con DCM. Los extractos combinados se lavaron con agua y salmuera, se secaron sobre Na2SO4, se filtraron y se concentraron a presión reducida. El residuo se purificó mediante cromatografía ultrarrápida en una columna de gel de sílice eluyendo con AcOEt al 18% en hexanos para dar el producto deseado. LC-Ms calculada para C1üH20NO2Si (M+H)+: m/z=214.1; encontrado 214.1.
Paso 2: ácido 5-({[terc-butil(dimetil)silil]oxi}metil)-1,3-oxazol-2-carboxílico
A una solución de 5-({[terc-butil(dimetil)silil]oxi}metil)-1,3-oxazol (0,75 g, 3,5 mmol) en tetrahidrofurano (30 ml) se le añadió n-butillitio 2,5 M en hexano (2,25 ml, 5,62 mmol) a -78° C gota a gota. La mezcla resultante se agitó a -78° C durante 1 hora y luego se añadió hielo seco. La mezcla de la reacción se calentó lentamente a temperatura ambiente y se agitó a temperatura ambiente durante la noche y luego se inactivó con agua. La mezcla se extrajo con DCM/iPrOH. Los extractos combinados se lavaron con salmuera, se secaron sobre Na2SO4, se filtraron y se concentraron a presión reducida. El residuo se purificó mediante cromatografía ultrarrápida en una columna de gel de sílice eluyendo con del 10 al 20% de MeOH en DCM para dar el producto deseado. LC-MS calculada para CnH20NO4Si (M+H)+: m/z=258.1; encontrado 258.1.
Paso 3: 5-({[terc-butil(dimetil)silil]oxi}metil)-N-(2-metilbifenil-3-il)-1,3-oxazol-2-carboxamida
A una solución de ácido 5-({[terc-butil(dimetil)silil]oxi}metil)-1,3-oxazol-2-carboxílico (42 mg, 0,16 mmol) y 2-metilbifenil-3-amina (Ejemplo 1, Paso 1: 35 mg, 0,19 mmol) en N,N-dimetilformamida (2 ml) se le añadió hexafluorofosfato de N,N,N',N'-tetrametil-O-(7-azabenzotriazol-1-il)uronio (93 mg, 0,24 mmol), seguido de N,N-dMsopropiletilamina (85 pl, 0,49 mmol). La mezcla resultante se agitó a temperatura ambiente durante 3 h. La reacción se diluyó con EtOAc y se lavó con agua y salmuera. La capa orgánica se secó sobre Na2SO4, se filtró y se concentró. El residuo se usó en el paso siguiente sin purificación adicional. LC-MS calculada para C24H31N2OaSi (M+H)+: m/z=423.2; encontrado 423.1.
Paso 4: 5-(hidroximetil)-N-(2-metilbifenil-3-il)-1,3-oxazol-2-carboxamida
A una solución de 5-({[terc-butil(dimetil)silil]oxi}metil)-N-(2-metilbifenil-3-il)-1,3-oxazol-2-carboxamida (180 mg, 0,42 mmol) en tetrahidrofurano (2 ml) se le añadió fluoruro de tetra-n-butilamonio (1 M en THF, 0,85 ml, 0,85 mmol). La mezcla se agitó a temperatura ambiente durante 3 h y luego se diluyó con EtOAc, se lavó con agua y salmuera. La capa orgánica se secó sobre Na2SO4, se filtró y se concentró. El residuo se purificó mediante cromatografía ultrarrápida en una columna de gel de sílice eluyendo con AcOEt al 50% en hexanos para dar el producto deseado. lC-MS calculada para C1 sH17 N2O3 (M+H)+: m/z=309.1; encontrado 309.2. 1H NMR (600 MHz, DMSO) 6 10.37 (s, 1H), 7.49-7.44 (m, 2H), 7.42-7.37 (m, 2H), 7.35-7.28 (m, 4H), 7.17-7.14 (m, 1H), 5.61 (s, 1H), 4.58 (s, 2H), 2.10 (s, 3H).
Paso 5: 5-formil-N-(2-metilbifenil-3-il)-1,3-oxazol-2-carboxamida
Se añadió sulfóxido de dimetilo (40 pl, 0,56 mmol) a una solución de cloruro de oxalilo (2 M en DCM, 0,14 ml, 0,28 mmol) en cloruro de metileno (0,6 ml) a -78° C, luego se añadió lentamente una solución de 5-(hidroximetil)-N-(2-metilbifenil-3-il)-1,3-oxazol-2-carboxamida (43 mg, 0,14 mmol) en cloruro de metileno (0,2 ml). La mezcla se agitó a -78° C durante 30 min y luego se añadió N,N-diisopropiletilamina (0,19 ml, 1,1 mmol). La mezcla de la reacción se calentó lentamente a 0°C, luego se inactivó con una solución acuosa saturada de NaHCO3 y se extrajo con DCM. Los extractos combinados se lavaron con agua y salmuera, se secaron sobre Na2SO4, se filtraron y se concentraron. El residuo se usó en el paso siguiente sin purificación adicional. LC-MS calculada para C1 sH15 N2O3 (M+H)+: m/z=307.1; encontrado 307.1.
Paso 6: 5-{[(2-hidroxietil)amino]metil}-N-(2-metilbifenil-3-il)-1,3-oxazol-2-carboxamida
A una solución de 5-formil-N-(2-metilbifenil-3-il)-1,3-oxazol-2-carboxamida (11,4 mg, 0,0372 mmol) en cloruro de metileno (1 ml) se le añadió etanolamina (4,5 pl, 0,074 milimoles). La mezcla se agitó a temperatura ambiente durante 20 min y luego se añadió triacetoxiborohidruro de sodio (24 mg, 0,11 mmol). La mezcla de la reacción se agitó a temperatura ambiente durante la noche y luego se añadieron NaBH4 (10 mg) y MeOH (0,2 ml). La mezcla se agitó durante otras 2 h a temperatura ambiente, que luego se concentró. El residuo se disolvió en MeOH y luego se purificó por HPLC preparativa (pH = 10, acetonitrilo/agua NH4OH) para dar el producto deseado. LC-MS calculada para C20H-i2 N3O3 (M+H)+: m/z=352.2; encontrado 352.2.
Ejemplo 4
Ácido (2S)-1-[(1-metil-2-{[(2-metilbifenil-3-il)amino]carbonil}-1H-imidazol-5-il)metil]piperidina-2-carboxílico
Paso 1: ácido 5-bromo-1-metil-1H-imidazol-2-carboxílico
A una mezcla de 5-bromo-1-metil-1H-imidazol-2-carboxilato de etilo (Anichem, N° de cat. K20110: 250 mg, 1,1 mmol) en tetrahidrofurano (20 ml) se le añadieron hidróxido de litio monohidrato (230 mg, 5,6 mmol) y agua (0,4 ml). La mezcla resultante se agitó a temperatura ambiente durante 2 h y luego se concentró. El residuo se usó en el paso siguiente sin purificación adicional. LC-MS calculada para CsH6BrN2O2 (M+H)+: m/z=205.0; encontrado 205.0. Paso 2: ácido (2S)-1-[(1-metil-2-{[(2-metilbifenil-3-il)amino]carbonil}-1H-imidazol-5-il)metil]piperídina-2-carboxílico Este compuesto se preparó usando procedimientos similares a los descritos en el Ejemplo 1 con ácido 5-bromo-1-metil-1H-imidazol-2-carboxílico (Paso 1) reemplazando al ácido 5-bromo-1,3-tiazol-2-carboxílico en el Paso 2. La mezcla de la reacción se purificó mediante HPLC preparativa (pH = 10, acetonitrilo/agua NH4OH) para dar el producto deseado. LC-MS calculada para C25H2gN4O3 (M+H)+: m/z=433.2; encontrado 433.2.
Ejemplo 5
5-{[(2-hidroxietil)amino]metil}-1-metil-N-(2-metilbifenil-3-il)-1H-imidazol-2-carboxamida
Este compuesto se preparó usando procedimientos similares a los descritos para el Ejemplo 4 con etanolamina reemplazando al ácido (2S)-piperidina-2-carboxílico. La mezcla de la reacción se purificó por HPLC preparativa (pH=10, acetonitrilo/agua NH4OH) para dar el producto deseado. LC-MS calculada para C21 H25N4O2 (M+H)+: m/z=365.2; encontrado 365.2.
Ejemplo 6
Ácido (2S)-1-[(1-metil-3-{[(2-metilbifenil-3-il)amino]carbonil}-1H-pirazol-5-il)metil]piperidina-2-carboxílico
Este compuesto se preparó usando procedimientos similares a los descritos en el Ejemplo 1 con ácido 5-bromo-1-metil-1H-pirazol-3-carboxílico (AstaTech, N° de cat. 80200) reemplazando al ácido 5-bromo-1,3-tiazol-2-carboxílico en el Paso 2. La mezcla de la reacción se purificó mediante HPLC preparativa (pH = 2, acetonitrilo/agua TFA) para dar el producto deseado como la sal de TFA. LC-MS calculada para C25H2gN4O3 (M+H)+: m/z=433.2; encontrado 433.2.
Ejemplo 7
5-{[(2-hidroxietil)amino]metil}-1-metil-N-(2-metilbifenil-3-il)-1H-pirazol-3-carboxamida
Este compuesto se preparó usando procedimientos similares a los descritos para el Ejemplo 6 con etanolamina reemplazando al ácido (2S)-piperidina-2-carboxílico. La mezcla de la reacción se purificó mediante HPLC preparativa (pH=2, acetonitrilo/agua TFA) para dar el producto deseado como la sal de TFA. LC-MS calculada para C2-iH25N4O2 (M+H)+: m/z=365.2; encontrado 365.2.
Ejemplo 8
4-cloro-5-{[(2-hidroxietil)amino]metil}-N-(2-metilbifenil-3-il)-1,3-tiazol-2-carboxamida
Paso 1: 2,4-didoro-5-(1,3-dioxolan-2-il)-1,3-tiazol
Se disolvieron 2,4-dicloro-1,3-tiazol-5-carbaldehído (Combi-Blocks, N° de cat. HI-1210: 3,5 g, 19 mmol) y monohidrato de ácido p-toluenosulfónico (180 mg, 0,96 mmol) en tolueno (40 ml) y luego se añadió 1,2-etanodiol (3,2 ml, 58 mmol). La mezcla se calentó a reflujo durante la noche con eliminación azotrópica de agua a través de una trampa Dean Stark. La solución se enfrió a temperatura ambiente y se lavó con solución saturada de NaHCO3 y salmuera. La capa orgánica se secó sobre Na2SO4, se filtró y se concentró. El residuo se purificó mediante cromatografía ultrarrápida eluyendo con 15% de EtOA/Hexanos para dar el producto deseado (3,9 g, 90%). LC-MS calculada para C6^ChNO 2S (M+H)+: m/z=225.9; encontrado 226.0.
Paso 2: ácido 4-doro-5-(1,3-dioxolan-2-il)-1,3-tiazol-2-carboxWco
A una solución de 2,4-dicloro-5-(1,3-dioxolan-2-il)-1,3-tiazol (3,9 g, 17 mmol) en tetrahidrofurano (60 ml) se le añadió n-butillitio 2,5 M en hexanos (7,24 ml, 18,1 mmol) gota a gota a -78° C. La mezcla resultante se agitó a -78° C durante 30 min y luego se burbujeó gas CO2 (generado a partir de hielo seco) a través de la mezcla durante 10 min. La mezcla de la reacción se calentó lentamente a temperatura ambiente y se agitó durante la noche, luego se concentró hasta la sequedad. El residuo se tituló con EtOAc frío, luego se filtró y se secó para dar el producto deseado (4,0 g, 98%), que se usó en el paso siguiente sin purificación adicional. LC-MS calculada para C7 H7CNO4S (M+H)+: m/z=236.0; encontrado 235.9.
Paso 3: 4-doro-5-(1,3-dioxolan-2-il)-N-(2-metilbifenil-3-il)-1,3-tiazol-2-carboxamida
A una solución de ácido 4-cloro-5-(1,3-dioxolan-2-il)-1,3-tiazol-2-carboxílico (400,0 mg, 1,697 mmol) y 2-metilbifenil-3-amina (Ejemplo 1, Paso 1: 360 mg, 2,0 mmol) en N,N-dimetilformamida (20 ml) se le añadió hexafluorofosfato de N,N,N',N'-tetrametil-O-(7-azabenzotriazol-1-il)uronio (970 mg, 2,5 mmol), seguido de N,N-diisopropiletilamina (890 pl, 5,1 mmol). La mezcla se agitó a temperatura ambiente durante 3 h y luego se diluyó con EtOAc, se lavó con agua y salmuera. La capa orgánica se secó sobre Na2SO4, se filtró y se concentró. El residuo se purificó mediante cromatografía ultrarrápida en una columna de gel de sílice eluyendo con AcOEt al 25% en hexanos
para dar el producto deseado (0,65 g, 96%). LC-MS calculada para C20H18CIN2O3S (M+H)+: m/z=401.1; encontrado 401.1.
Paso 4: 4-doro-5-formil-N-(2-metilbifenil-3-il)-1,3-tiazol-2-carboxamida
A una solución de 4-doro-5-(1,3-dioxolan-2-il)-N-(2-metilbifenil-3-il)-1,3-tiazol-2-carboxamida (650 mg, 1,6 mmol) en tetrahidrofurano (3 ml) se le añadió cloruro de hidrógeno 2,0 M en agua (8,1 ml, 16 mmol). La mezcla resultante se agitó a 50° C durante la noche, luego se enfrió a temperatura ambiente y se concentró. El residuo se disolvió en EtOAc y luego se lavó con una solución acuosa saturada de NaHCO3 y salmuera. La capa orgánica se secó sobre Na2 SO4, se filtró y se concentró. El residuo se usó en el paso siguiente sin purificación adicional. LC-MS calculada para C18H14CIN2O2S (M+H)+: m/z=357.0; encontrado 357.0.
Paso 5: 4-doro-5-{[(2-hidroxietil)amino]metil}-N-(2-metilbifenil-3-il)-1,3-tiazol-2-carboxamida
A una solución de 4-cloro-5-formil-N-(2-metilbifenil-3-il)-1,3-tiazol-2-carboxamida (200 mg, 0,560 mmol) en cloruro de metileno (20 ml) se le añadió etanolamina ( 68 pl, 1,1 mmol). La mezcla se agitó a temperatura ambiente durante 20 min y luego se añadió triacetoxiborohidruro de sodio (360 mg, 1,7 mmol). La mezcla de la reacción se agitó a temperatura ambiente durante la noche. La LC-MS indicó que parte del producto intermedio de imina no se había reducido, por lo que se añadió una pequeña cantidad de NaBH4 (30 mg) y MeOH (1 ml). La mezcla se agitó durante otras 2 h a temperatura ambiente y luego se concentró. El residuo se disolvió en DCM, luego se lavó con una solución de NaHCO3 y salmuera. La capa orgánica se secó sobre Na2SO4, se filtró y se concentró. El residuo se purificó mediante cromatografía ultrarrápida en una columna de gel de sílice eluyendo con MeOH al 5% en DCM para dar el producto deseado (105 mg, 47%). LC-MS calculada para C20H21CIN3O2S (M+H)+: m/z=402.1; encontrado 402.1.
Ejemplo 9
5-{[(2-hidroxietil)amino]metil}-4-metil-N-(2-metilbifenil-3-il)-1,3-tiazol-2-carboxamida
A una solución de 4-cloro-5-{[(2-hidroxietil)amino]metil}-N-(2-metilbifenil-3-il)-1,3-tiazol-2-carboxamida (Ejemplo 8 : 20,0 mg, 0,0498 mmol) en tetrahidrofurano (1 ml) se le añadió dimetilzinc 2,0 M en tolueno (50 pl, 0,10 mmol). La mezcla se purgó con nitrógeno y luego se agitó en un vial sellado a 110° C durante 2 h. La mezcla se enfrió a temperatura ambiente, se concentró y luego se disolvió en MeOH y se purificó por HPLC preparativa (acetonitrilo/agua NH4OH) para dar el producto deseado. LC-MS calculada para C21 H24N3O2S (M+H)+: m/z=382.2; encontrado 382.1.
Ejemplo 10
N-[2-ciano-3-(2,3-dihidro-1,4-benzodioxin-6-il)fenil]-5-{[(2-hidroxietil)amino]metil}-1-metil-1H-pirazol-3-carboxamida
Paso 1: 1-metil-5-vinil-1H-pirazol-3-carboxilato de etilo
A la mezcla de 5-bromo-1-metil-1H-pirazol-3-carboxilato de etilo (AstaTech, N° de cat. 80198: 500 mg, 2 mmol) en 1,4-dioxano (20 ml) se le añadió 4,4,5,5-tetrametil-2-vinil-1,3,2-dioxaborolano (730 pl, 4,3 mmol) seguido de complejo de [1,1'-bis(difenilfosfino)ferroceno]dicloropaladio(N) con diclorometano (1:1) (100 mg, 0,1 mmol), carbonato de sodio (0,45 g, 4,3 mmol) y agua (4 ml). La mezcla resultante se purgó con nitrógeno y se agitó a 95° C durante 3 h. La mezcla de la reacción se enfrió a temperatura ambiente, se filtró y se concentró. El residuo se purificó mediante cromatografía ultrarrápida en una columna de gel de sílice eluyendo con AcOEt al 20% en DCM para dar el producto deseado. LC-MS calculada para CgH-i3N2O2 (M+H)+: m/z=181.1; encontrado 181.1.
Paso 2: N-(3-bromo-2-danofenil)-1-metil-5-vinil-1H-pirazol-3-carboxamida
A una mezcla de 2-amino-6-bromobenzonitrilo (AstaTech, N° de cat. CL8148: 407 mg, 2,06 mmol) y 1-metil-5-vinil-1H-pirazol-3-carboxilato de etilo (310,0 mg, 1,720 mmol) en tetrahidrofurano (20 ml) se le añadió gota a gota hexametildisilazano sódico 1,0 M en THF (2,06 ml, 2,06 mmol) a temperatura ambiente. La mezcla se agitó a temperatura ambiente durante 1 h, luego se inactivó con agua y se extrajo con DCM. Los extractos combinados se lavaron con salmuera, luego se secaron sobre Na2SO4, se filtraron y se concentraron. El residuo se purificó mediante cromatografía ultrarrápida en una columna de gel de sílice eluyendo con DCM para dar el producto deseado. LC-MS calculada para C-nH-^Br^O (M+H)+: m/z=331.0; encontrado 331.0.
Paso 3: N-(3-bromo-2-cianofenil)-5-formil-1-metil-1H-pirazol-3-carboxamida
A una solución de N-(3-bromo-2-cianofenil)-1-metil-5-vinil-1H-pirazol-3-carboxamida (0,41 g, 1,2 mmol) en 1,4-dioxano (8 ml) y agua (2 ml) se le añadió tetraóxido de osmio (4% en peso en agua, 0,79 ml, 0,12 mmol). La mezcla resultante se agitó durante 5 min y luego se añadió peryodato de sodio (794 mg, 3,71 mmol). La mezcla se agitó durante otras 2 h a temperatura ambiente y luego se diluyó con DCM, se lavó con agua y salmuera. La capa orgánica se secó sobre Na2SO4, se filtró y se concentró. El residuo se purificó mediante cromatografía ultrarrápida en una columna de gel de sílice eluyendo con AcOEt al 10% en DCM para dar el producto deseado. . LC-MS calculada para C-i3H1 QBrN4O2(M+H)+: m/z=333.0; encontrado 333.0.
Paso 4: N-(3-bromo-2-cianofenil)-5-{[(2-hidroxietil)amino]metil}-1-metil-1H-pirazol-3-carboxamida
A una solución de N-(3-bromo-2-cianofenil)-5-formil-1-metil-1H-pirazol-3-carboxamida (0,20 g, 0,60 mmol) en cloruro de metileno (5 ml) se le añadió etanolamina (140 pl, 2,4 mmol). La mezcla se agitó a temperatura ambiente durante 20 min y luego se añadió triacetoxiborohidruro de sodio (300 mg, 1,4 mmol). La mezcla de la reacción se agitó a temperatura ambiente durante la noche. La LC-MS indicó que todavía existía algo del producto intermedio de imina, por lo que se añadieron NaBH4 (45 mg, 1,2 mmol) y MeOH (2 ml). La mezcla se agitó a temperatura ambiente durante otras 2 h y luego se concentró. El residuo se purificó mediante cromatografía ultrarrápida en una columna de gel de sílice eluyendo con MeOH al 15% en DCM para dar el producto deseado. LC-MS calculada para C15 H-i7 BrN5O2 (M+H)+: m/z=378.1; encontrado 378.0.
Paso 5: N-[2-dano-3-(2,3-dihidro-1,4-benzodioxin-6-il)fenil]-5-{[(2-hidroxietil)amino]metil}-1-metil-1H-pirazol-3-carboxamida
Se purgó con N2 una mezcla de N-(3-bromo-2-cianofenil)-5-([(2-hidroxietil)amino]metil}-1-metiMH-pirazol-3-carboxamida (10 mg, 0,03 mmol), 6-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-2,3-dihidro-1,4-benzodioxina (14 mg, 0,053 mmol), complejo de [1,1-bis(difenilfosfino)ferroceno]dicloropaladio(N) con diclorometano (1:1) (0,9 mg, 0,001 mmol) y carbonato de sodio (3,8 mg, 0,036 mmol) en 1,4-dioxano (1 ml) y agua (0,2 ml) y luego se agitó a 95°C durante la noche. La mezcla de la reacción se enfrió a temperatura ambiente, se diluyó con MeOH, se filtró y se purificó por HPLC preparativa (pH=2, acetonitrilo/agua TFA) para dar el producto deseado como la sal de TFA. LC-MS calculada para C23H-mN504(M+H)+: m/z=434.2; encontrado 434.2.
Ejemplo 11
N-(2-ciano-2'-fluorobifenil-3-il)-5-{[(2-hidroxietil)amino]metil}-1-metil-1H-pirazol-3-carboxamida
Este compuesto se preparó usando procedimientos similares a los descritos para el Ejemplo 10, Paso 5 con ácido 2-fluorofenilborónico (Aldrich, N° de cat. 445223) reemplazando a la 6-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-2,3-dihidro-1,4-benzodioxina. La mezcla de la reacción se purificó por HPLC preparativa (pH=2, acetonitrilo/agua TFA) para dar el producto deseado como la sal de TFA. Lc -MS calculada para C2-iH2-iFn5 0 2 (M+H)+: m/z=394.2; encontrado 394.1.
Ejemplo 12
N-(2-ciano-2'-fluoro-3'-metoxibifenil-3-il)-5-{[(2-hidroxietil)amino]metil}-1-metil-1H-pirazol-3-carboxamida
Este compuesto se preparó usando procedimientos similares a los descritos para el Ejemplo 10, Paso 5 con ácido 2-fluoro-3-metoxifenilborónico (Aldrich, N° de cat. 594253) reemplazando a la 6-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-2,3-dihidro-1,4-benzodioxina. La mezcla de la reacción se purificó por HPLC preparativa (pH=2, acetonitrilo/agua TFA) para dar el producto deseado como la sal de TFA. LC-MS calculada para C22H23FN50s(M+H)+: m/z=424.2; encontrado 424.2.
Ejemplo 13
N-[2-ciano-3-(1-metil-1H-indazol-4-il)fenil]-5-{[(2-hidroxietil)amino]metil}-1-metil-1H-pirazol-3-carboxamida
Este compuesto se preparó usando procedimientos similares a los descritos para el Ejemplo 10, Paso 5 con ácido 1-metilindazol-4-borónico (AstaTech, N° de cat. 64580) reemplazando a la 6-(4,4,5,5-tetrametil-1,3,2 -dioxaborolan-2-il)-2,3-dihidro-1,4-benzodioxina. La mezcla de la reacción se purificó por HPLC preparativa (pH=2, acetonitrilo/agua+TFA) para dar el producto deseado como la sal de TFA. LC-Ms calculada para C23^ 4N7O2 (M+H)+: m/z=430.2; encontrado 430.2.
Ejemplo 14
N-[2-ciano-3-(2,3-dihidro-1,4-benzodioxin-6-il)fenil]-5-{[(2-hidroxietil)amino]metil}-1-metil-1H-imidazol -2-carboxamida
Paso 1: N-(3-bromo-2-danofenil)-5-{[(2-hidroxietil)amino]metil}-1-metil-1H-imidazol-2-carboxamida
Este compuesto se preparó usando procedimientos similares a los descritos para el Ejemplo 10, Paso 1-4 con 5-bromo-1-metil-1H-imidazol-2-carboxilato de etilo (Anichem, N° de cat. K20110) reemplazando al 5-bromo-1-metil-1H-pirazol-3-carboxilato de etilo en el Paso 1. El producto bruto se purificó mediante cromatografía ultrarrápida en una columna de gel de sílice eluyendo con MeOH al 15% en DCM para dar el producto deseado. LC-MS calculada para C-i5H-i7 BrN5O2 (M+H)+: m/z=378.1; encontrado 378.0.
Paso 2: N-[2-ciano-3-(2,3-dihidro-1,4-benzodioxin-6-il)fenil]-5-{[(2-hidroxietil)amino]metil}-1-metil- 1H-imidazol-2-carboxamida
Se purgó con nitrógeno una mezcla de N-(3-bromo-2-cianofenil)-5-{[(2-hidroxietil)amino]metil}-1-metil-1H-imidazol-2-carboxamida (10 mg, 0,03 mmol), 6-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-2,3-dihidro-1,4-benzodioxina (14 mg, 0,053 mmol), complejo de [1,1-bis(difenilfosfino)ferroceno]dicloropaladio(N) con diclorometano (1:1) (0,9 mg, 0,001 mmol) y carbonato de sodio (3,8 mg, 0,036 mmol) en 1,4-dioxano (1 ml) y agua (0,2 ml) y luego se agitó a 95°C durante la noche. La mezcla de la reacción se enfrió a temperatura ambiente, se diluyó con metanol, se filtró y luego se purificó por HPLC preparativa (pH = 2, acetonitrilo/agua TFA) para dar el producto deseado como la sal de TFA. LC-MS calculada para C23H-mN504(M+H)+: m/z=434.2; encontrado 434.2.
Ejemplo 15
N-(2-ciano-2'-fluoro-3'-metoxibifenil-3-il)-5-{[(2-hidroxietil)amino]metil}-1-metil-1H-imidazol-2-carboxamida
Este compuesto se preparó usando procedimientos similares a los descritos para el Ejemplo 14, Paso 2 con ácido 2-fluoro-3-metoxifenilborónico (Aldrich, N° de cat. 594253) reemplazando a la 6-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-2,3-dihidro-1,4-benzodioxina. La mezcla de la reacción se purificó por HPLC preparativa (pH=2, acetonitrilo/agua TFA) para dar el producto deseado como la sal de TFA. LC-MS calculada para C22H2aFN5Oa(M+H)+: m/z=424.2; encontrado 424.1.
Ejemplo 16
N-[2-ciano-3-(1-metil-1H-indazol-4-il)fenil]-5-{[(2-hidroxietil)amino]metil}-1-metil-1H-imidazol-2-carboxamida
Este compuesto se preparó usando procedimientos similares a los descritos para el Ejemplo 15, Paso 2 con ácido 1-metilindazol-4-borónico (AstaTech, N° de cat. 64580) reemplazando a la 6-(4,4,5,5-tetrametil-1,3,2 -dioxaborolan-2-il)-2,3-dihidro-1,4-benzodioxina. La mezcla de la reacción se purificó por HPLC preparativa (pH=2, acetonitrilo/agua TFA) para dar el producto deseado como la sal de TFA. LC-MS calculada para C23H24NyO2 (M+H)+: m/z=430.2; encontrado 430.1.
Ejemplo 17
Ácido (S)-1-(5-cloro-2-((5-cianopiridin-3-il)metoxi)-4-((3'-(5-(((2-hidroxietil)amino)metil)tiazol-2-carboxamido)-2,2,-dimetil-[1,1,-bifenil]-3-il)metoxi)bencil)piperidina-2-carboxílico
Paso 1: 4-((3-bromo-2-metilbendl)oxi)-5-doro-2-hidroxibenzaldehído
A una mezcla de (3-bromo-2-metilfenil)metanol (2,33 g, 11,59 mmol), 5-cloro-2,4-dihidroxibenzaldehído (2,0 g, 11,59 mmol) y trifenilfosfina (3,65 g, 13,91 mmol) en THF (10 ml) a 0° C se le añadió DIAD (2,93 ml, 15,07 mmol). La mezcla se agitó a temperatura ambiente durante la noche. La mezcla se concentró y se diluyó con EtOAc. El sólido se recogió por filtración para dar 4-((3-bromo-2-metilbencil)oxi)-5-cloro-2-hidroxibenzaldehído (2,0 g, 5,62 mmol, 48,5% de rendimiento). lCm S calculada para C15 H-i3BrClO3 (M+H)+: m/z=355.0; encontrado 355.2.
Paso 2: 5-((5-((3-bromo-2-metilbendl)oxi)-4-doro-2-formilfenoxi)metil)nicotinonitrílo
Se agitó a 70° C durante 3 horas una mezcla de 4-((3-bromo-2-metilbencil)oxi)-5-cloro-2-hidroxibenzaldehído (2,0 g, 5,62 mmol), 5-(clorometil)nicotinonitrilo (0,927 g, 6,07 mmol) y carbonato de cesio (2,75 g, 8,44 mmol) en DMF (12 ml). La mezcla se enfrió a temperatura ambiente y luego se vertió en agua. El sólido se recogió por filtración y se secó al aire para dar 5-((5-((3-bromo-2-metilbencil)oxi)-4-cloro-2-formilfenoxi)metil)nicotinonitrilo (2,2 g, 4,66 mmol, 83% de rendimiento). LCMS calculada para C22H-i7 BrClN2O3(M+H)+: m/z=471.0; encontrado 471.2.
Paso 3: ácido (S)-1-(4-((3-bromo-2-metilbendl)oxi)-5-dom-2-((5-danopiridin-3-il)metoxi)bendl)piperidina-2- carboxílico
Se añadió triacetoxiborohidruro de sodio (158 mg, 0,746 mmol) a una mezcla de 5-((5-((3-bromo-2-metilbencil)oxi)-4-doro-2-formilfenoxi)metil)nicotinonitrilo (176 mg, 0,373 mmol), ácido (S)-piperidina-2-carboxílico (72,3 mg, 0,560 mmol) y trietilamina (0,156 ml, 1,119 mmol) en DCM (1,0 ml). Después de agitar a temperatura ambiente durante la noche, la mezcla se purificó en HPLC preparativa (pH = 2, acetonitrilo/agua TFA) para dar el producto deseado como la sal de TfA (150 mg). Lc Ms calculada para C28H2sBrClN3O4(M+H)+: m/z=584.1; encontrado 584.1.
Paso 4: 5-viniltiazol-2-carboxilato de metilo
Se pesaron en un vial de microondas 5-bromotiazol-2-carboxilato de metilo (0,72 g, 3,24 mmol), 4,4,5,5-tetrametil-2-vinil-1,3,2-dioxaborolano (0,55 ml, 3,24 mmol), tetrakis(trifenilfosfina)paladio(0) (0,375 g, 0,324 mmol) y carbonato de potasio (0,896 g, 6,48 mmol). Se añadieron 1,4-dioxano (3 ml) y agua (0,6 ml) y la mezcla se purgó con N2 durante 5 min. La mezcla se calentó a 100° C durante 2 h y luego se enfrió a temperatura ambiente y se concentró. El residuo se purificó en columna de gel de sílice (0-100% de EtOAc/Hexanos) para dar 5-viniltiazol-2-carboxilato de metilo (0,3 g, 1,773 mmol, 54,7% de rendimiento). LCMS calculada para C7 H8NO2S (M+H)+: m/z=170.0; encontrado 170.0.
Paso 5: N-(3-bromo-2-metilfenil)-5-viniltiazol-2-carboxamida
Se añadió una solución de terc-butóxido de potasio en THF 1,0 M (5,32 ml, 5,32 mmol) a una solución de 5-viniltiazol-2-carboxilato de metilo (0,3 g, 1,773 mmol) y 3-bromo-2-metilanilina (0,24 ml, 1,950 mmol) en THF (5 ml) a 0° C. Después de agitarla a temperatura ambiente durante 2 h, la mezcla de la reacción se inactivó con agua, se extrajo con acetato de etilo, se concentró y se purificó en una columna de gel de sílice (0-100% de EtOAc/Hexanos) para dar N-(3-bromo-2-metilfenil)-5-viniltiazol-2-carboxamida (0,4 g, 1,238 mmol, 69,8% de rendimiento). LCMS calculada para C13 H12 BrN2OS (M+H)+: m/z=323.0; encontrado 323.0.
Paso 6: N-(3-bromo-2-metilfenil)-5-formiltiazol-2-carboxamida
A una mezcla de N-(3-bromo-2-metilfenil)-5-viniltiazol-2-carboxamida (0,22 g, 0,681 mmol) en THF (4 ml)/agua (1 ml) enfriada en un baño de hielo se le añadió solución acuosa al 4% de tetróxido de osmio (0,83 ml, 0,136 mmol). La reacción se agitó durante 5 min y luego se añadió peryodato de sodio (0,437 g, 2,042 mmol). Después de agitarla a temperatura ambiente durante la noche, la reacción se inactivó con una solución acuosa saturada de tiosulfato de sodio. A continuación, la mezcla se extrajo con DCM, se concentró al vacío y se purificó en
una columna de gel de sílice (0-100% de EtOAc en hexanos) para dar N-(3-bromo-2-metilfenil)-5-formiltiazol-2-carboxamida (0,19 g, 0,584 mmol, 86 % de rendimiento). LCMS calculada para C12 H1 üBrN2O2S (M+H)+: m/z=325.0; encontrado 325.0.
Paso 7: 5-formil-N-(2-metil-3-(4, 4,5,5-tetrametil-1,3,2-dioxaborlan-2-il)fenil)tiazol-2-carboxamida
Se purgó con nitrógeno una mezcla de N-(3-bromo-2-metilfenil)-5-formiltiazol-2-carboxamida (0,17 g, 0,523 mmol), bis(pinacolato)diboro (0,199 g, 0,784 mmol), acetato de potasio (0,103 g, 1,046 mmol) y dicloruro de [1,1'-bis(difenilfosfino)ferroceno]paladio(II) (0,043 g, 0,052 mmol) y luego se añadió 1,4-dioxano (4 ml). La mezcla resultante se agitó a 100° C durante 2 h y luego se enfrió a temperatura ambiente y se concentró. El residuo se purificó en columna de gel de sílice (0-100% de EtOAc/Hexanos) para dar 5-formil-N-(2-metil-3-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)fenil)tiazol-2-carboxamida (0,17 g, 0,457 mmol, 87% de rendimiento). LCMS calculada para C18H22BN2O4S (M+H)+: m/z=373.1; encontrado 373.1.
Paso 8: ácido (S)-1-(5-doro-2-((5-cianopirídin-3-il)metoxi)-4-((3'-(5-formiltiazol-2-carboxamido)-2,2'-dimetil-[1,1 bifenil]-3-il)metoxi)bencil)piperidin-2-carboxílico
Se purgó con nitrógeno una mezcla de ácido (S)-1-(4-((3-bromo-2-metilbencil)oxi)-5-cloro-2-((5-cianopiridin-3-il)metoxi)bencil)piperidina-2-carboxílico (24 mg, 0,04 mmol), 5-formil-N-(2-metil-3-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)fenil)tiazol-2-carboxamida (15 mg, 0,040 mmol), carbonato de potasio (11 mg, 0,08 mmol) y tetrakis(trifenilfosfina)paladio(0) (4,7 mg, 4,0 pmol) en 1,4-dioxano (2 ml) y agua (1 ml) y luego se calentó a 100° C durante 2 h. Después de enfriarla a temperatura ambiente, la mezcla se concentró y el residuo se purificó en una columna de gel de sílice (0-15% de MeOH/DCM) para dar ácido (S)-1-(5-cloro-2-((5-cianopiridin-3 -il)metoxi)-4-((3'-(5-formiltiazol-2-carboxamido)-2,2-dimetil-[1,1'-bifenil]-3-il)metoxi)bencil)piperidina-2-carboxílico (20 mg, 0,027 mmol, 66,2% de rendimiento). LCm S calculada para C40H3/ClN5O6S (M+H)+: m/z=750.2; encontrado 750.2.
Paso 9: ácido (S)-1-(5-cloro-2-((5-cianopiridin-3-il)metoxi)-4-((3'-(5-(((2-hidroxietil)amino)metil)tiazol-2-carboxamido)-2,2'-dimetil-[1,1 '-bifenil]-3-il)metoxi)bencil)piperídina-2-carboxílico
Se agitó una mezcla de ácido (S)-1-(5-cloro-2-((5-cianopiridin-3-il)metoxi)-4-((3-(5-formiltiazol-2-carboxamido)-2,2-dimetil-[1,1-bifenil]-3-il)metoxi)bencil)piperidina-2-carboxílico (6 mg, 8,00 pmol) y 2-aminometan-1-ol (0,5 mg, 8,00 pmol) en DCM (1,0 ml) durante 30 min a temperatura ambiente y luego se añadió triacetoxiborohidruro de sodio (2,5 mg, 0,012 mmol). Después de agitar a temperatura ambiente durante 2 h, la mezcla se purificó en HPLC preparativa (pH = 2, acetonitrilo/agua TFA) para dar el producto deseado como la sal de TFA. LCMS calculada para C42H44ClN6O6S (M+H)+: m/z=795.3; encontrado 795.3.
Ejemplo 18
Ácido (S)-1-(5-cloro-2-((5-cianopiridin-3-il)metoxi)-4-((3'-(5-(((R)-3-hidroxipirrolidin-1-il)metil)tiazol-2-carboxamido)-2,2,-dimetil-[1,1,-bifenil]-3-il)metoxi)bencil)piperidina-2-carboxílico
Este compuesto se preparó usando procedimientos similares a los descritos para el Ejemplo 17, Paso 9 con (R)-pirrolidin-3-ol reemplazando 2-aminometan-1-ol. La mezcla de la reacción se purificó por HPLC preparativa (pH=2, acetonitrilo/agua TFA) para dar el producto deseado como la sal de TFA. LC-MS calculada para C44H46ClN6O6S (M+H)+: m/z=821.3; encontrado 821.3.
Ejemplo 19
5-(((R)-3-hidroxipirrolidin-1-il)metil)-N-(3'-(5-(((R)-3-hidroxipirrolidin-1-il)metil)-1-metil-1H-pirazol-3-carboxamido)-2,2,-dimetil-[1,1,-bifenil]-3-il)tiazol-2-carboxamida
Paso 1: N-(3-bromo-2-metilfenil)-1-metil-5-vinil-1H-pirazol-3-carboxamida
Se añadió una solución de terc-butóxido de potasio en THF 1 M (4,16 ml, 4,16 mmol) a una solución de 1-metil-5-vinil-H-pirazol-3-carboxilato de etilo (Ejemplo 10, Paso 1: 0,25 g, 1,387 mmol) y 3-bromo-2-metilanilina (0,188 ml, 1,526 mmol) en THF (5 ml) a 0° C. Después de agitarla a temperatura ambiente durante 2 h, la mezcla de la reacción se inactivó con agua, se extrajo con acetato de etilo, se concentró y se purificó en columna de gel de sílice (0-100% de EtOAc/Hexanos) para dar N-(3-bromo-2-metilfenil)-1-metil-5-vinil-1H-pirazol-3-carboxamida (0,4 g, 1,249 mmol, 90% de rendimiento). LCMS calculada para C14 H15 BrN3O (M+H)+: m/z=320.0; encontrado 320.0.
Paso 2: N-(3-bromo-2-metilfenil)-5-formil-1-metil-1H-pirazol-3-carboxamida
A una mezcla de N-(3-bromo-2-metilfenil)-1-metil-5-vinil-1H-pirazol-3-carboxamida (0,4 g, 1,25 mmol) en THF (10 ml) y agua (2,5 ml) enfriada en un baño de hielo se le añadió tetróxido de osmio ac. al 4% (1,53 ml, 0,25 mmol). La mezcla de la reacción se agitó durante 5 min y luego se añadió peryodato de sodio (0,802 g, 3,75 mmol). Después de agitarla a temperatura ambiente durante 1 h, la reacción se inactivó con solución sat. ac. de tiosulfato de sodio. Luego, la mezcla se extrajo con DCM, se concentró al vacío y se purificó en una columna de gel de sílice (0-100% de EtOAc/Hexanos) para dar N-(3-bromo-2-metilfenil)-5-formil-1-metil-1H- pirazol-3-carboxamida (0,29 g, 0,900 mmol, 72,1% de rendimiento). . LCm S calculada para C-i3H-i3BrN3O2(M+H)+: m/z=322.0; encontrado 322.0.
Paso 3: 5-formil-N-(3'-(5-formil-1-metil-1H-pirazol-3-carboxamido)-2,2'-dimetil-[1,1 '-bifenil]-3-ilo) tiazol-2-carboxamida
Se purgó con nitrógeno una mezcla de N-(3-bromo-2-metilfenil)-5-formil-1-metil-1H-pirazol-3-carboxamida (17,31 mg, 0,054 mmol), 5-formil-N-(2-metil-3-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)fenil)tiazol-2-carboxamida (Ejemplo 17, Paso 7: 20 mg, 0,054 mmol), carbonato de potasio (15 mg, 0,11 mmol) y tetrakis(trifenilfosfina)paladio(0) (6,2 mg, 5,4 pmol) en 1,4-dioxano (3 ml) y agua (0,6 ml) y se calentó a 100° C durante 2 H. La mezcla se purificó en columna de gel de sílice (0-100% de EtOAc/Hexanos) para dar 5-formil-N-(3-(5-formil-1-metil-1H-pirazol-3-carboxamido)-2,2'-dimetil-[1,1'-bifenil]-3-il)tiazol-2-carboxamida (20 mg, 0,041 mmol, 76% de rendimiento). LCMS calculada para C25H12 N5O4S (M+H)+: m/z=488.1; encontrado 488.1.
Paso 4: 5-(((R)-3-hidroxipirrolidin-1-il)metil)-N-(3'-(5-(((R)-3-hidroxipirrolidin-1-il)metil)-1- metil-1H-pirazol-3-carboxamido)-2, 2'-dimetil-[1,1 ’-bifenil]-3-il) tiazol-2-carboxamida
Se agitó durante 30 min a temperatura ambiente una mezcla de 5-formil-N-(3'-(5-formil-1-metil-1H-pirazol-3-carboxamido)-2,2'-dimetil-[1,1'-bifenil]-3-il)tiazol-2-carboxamida (20 mg, 0,041 mmol) y (R)-pirrolidin-3-ol (7,9 mg, 0,09 mmol) en DCM (1,0 ml) y luego se añadió triacetoxiborohidruro de sodio (26,1 mg, 0,123 mmol). Después de agitarla a temperatura ambiente durante 2 h, la mezcla se purificó en HPLC preparativa (pH = 2, acetonitrilo/agua TFA) para dar el producto deseado como la sal de TFA. LCMS calculada para C33H40N7O4S (M+H)+: m/z=630.3; encontrado 630.3.
Ejemplo A. Ensayo de unión de fluorescencia homogénea resuelta en el tiempo (HTRF) de PD-1/PD-L1 Los ensayos se realizaron en una placa de poliestireno de 384 pocillos negra estándar con un volumen final de 20 |jl. Primero se diluyeron en serie en DMSO los inhibidores y luego se añadieron a los pocillos de la placa antes de la adición de los otros componentes de la reacción. La concentración final de DMSO en el ensayo fue del 1%. Los ensayos se llevaron a cabo a 25° C en tampón PBS (pH 7,4) con Tween-20 al 0,05% y BSA al 0,1%. La proteína PD-L1 humana recombinante (19-238) con una etiqueta His en el extremo C-terminal se adquirió de AcroBiosystems (PD1-H5229). La proteína de PD-1 humana recombinante (25-167) con etiqueta Fc en el extremo C terminal también se adquirió de AcroBiosystems (PD1-H5257). Las proteínas PD-L1 y PD-1 se diluyeron en el tampón de ensayo y se añadieron 10 j l al pocillo de la placa. Las placas se centrifugaron y las proteínas se preincubaron con inhibidores durante 40 minutos. A la incubación le siguió la adición de 10 pl de tampón de detección de HTRF suplementado con IgG anti-humana marcada con criptato de europio (PerkinElmer-AD0212) específica para el anticuerpo de Fc y anti-His conjugado con SureLight®-Aloficocianina (APC, PerkinElmer-AD0059H). Después de la centrifugación, la placa se incubó a 25° C durante 60 min antes de leerla en un lector de placas PHERAstar FS (relación 665nm/620nm). Las concentraciones finales en el ensayo fueron: PD1 3 nM, PD-L1 10 nM, IgG antihumana de europio 1 nM y aloficocianina anti-His- 20 nM. La determinación de la IC50 se realizó ajustado la curva del porcentaje de actividad de control frente al logaritmo de la concentración de inhibidor usando el software GraphPad Prism 5.0.
Los compuestos de la presente divulgación, como se ejemplifica en los Ejemplos, mostraron valores de IC50 en los siguientes intervalos: = IC50 ^ 100 nM; + = 100 nM < 1C50 ^ 500 nM; ++ = 500 nM < IC50 ^ 10000 nM Los datos obtenidos para los compuestos del Ejemplo usando el ensayo de unión de fluorescencia homogénea resuelta en el tiempo (HTRF) de PD-1/PD-L1 descrito en el Ejemplo A se proporcionan en la Tabla 1.
Tabla 1
continuación
Claims (24)
1. Un compuesto de Fórmula (II):
o una sal farmacéuticamente aceptable o un estereoisómero del mismo, en donde:
(i) X4 es S y X5 es CR5; (ii) X4 es O y X5 es CR5; X4 es NR4 y X5 es CR5; o (iv) X4 es CR4 y X5 es CR5; Cy es fenilo, que está opcionalmente sustituido con de 1 a 5 sustituyentes R6 independientemente seleccionados;
R1, R2 y R3 se seleccionan cada uno independientemente de H, alquilo C1 -4 , cicloalquilo C3 -10 , cicloalquilo C3 -10-alquilo C1-4-, arilo C6 -10 , arilo C6-10-alquilo C1-4-, heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, (heteroarilo de 5-10 miembros)-alquilo C1-4-, (heterocicloalquilo de 4-10 miembros)-alquilo C1.4-, alquenilo C2-4 , alquinilo C2-4, halo, CN, OR10, haloalquilo C1 -4 , haloalcoxi C1 -4 , NH2 , -NHR10, -NR10R10, NHOR10, C(O)R10, C(O)NR10R10, C(O)OR10, OC(O)R10, OC(O)NR10R10, NR10C(O)R10, NR10C(O)OR10, NR10C(O)NR10R10, C(=NR10)R10, C(=NR10)NR10R10, NR10C(=NR10)NR10R10, NR10S(O)R10, NR10S(O)2R10, NR10S(O)2NR10R10, S(O)R10, S(O)NR10R10, S(O)2 R10, y S(O)2 NR10R10, en donde cada R10 se selecciona independientemente de H, alquilo C1 -4 , alquenilo C2-4 , alquinilo C2-4 , alcoxi C1 -4 , cicloalquilo C3 -10 , cicloalquilo C3 -10-alquilo C1-4-, arilo C6 -10 , arilo C6-10-alquilo C1 -4 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, (heteroarilo de 5-10 miembros)-alquilo C1.4- y (heterocicloalquilo de 4-10 miembros)-alquilo C1.4-, en donde el alquilo C1-4 , alcoxi C1 -4 , cicloalquilo C3 -10 , cicloalquilo C3 -10-alquilo C1.4-, arilo C6 -10, arilo C6-10-alquilo C1.4-, heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, (heteroarilo de 5-10 miembros)-alquilo C1-4- y (heterocicloalquilo de 4-10 miembros)-alquilo C1-4-, de R1, R2, R3 y R10 están cada uno opcionalmente sustituidos con 1 o 2 sustituyentes Rd independientemente seleccionados;
R4, R5 y R6 se seleccionan cada uno independientemente de H, halo, alquilo C1 -6 , alquenilo C2-6, alquinilo C2-6, haloalquilo C1.6 , haloalcoxi C1.6 , arilo C6 -10 , cicloalquilo C3 -10 , heteroarilo de 5-14 miembros, heterocicloalquilo de
4-10 miembros, arilo C6-10-alquilo C1.4-, cicloalquilo C3-10-alquilo C1.4-, (heteroarilo de 5-14 miembros)-alquilo C1.4-, (heterocicloalquilo de 4-10 miembros)-alquilo C1.4-, CN, NO2 , ORa, SRa, NHORa, C(O)Ra, C(O)NRaRa, C(O)ORa, OC(O)Ra, OC(O)NRaRa, NHRa, NRaRa, NRaC(O)Ra, NRaC(O)ORa, NRaC(O)NRaRa, C(=NRa)Ra, C(=NRa)NRaRa, NRaC(=NRa)NRaRa, NRaC(=NOH)NRaRa, NRaC(=NCN)NRaRa, NRaS(O)Ra, NRaS(O)2Ra, NRaS(O)2NRaRa, S(O)Ra, S(O)NRaRa, S(O)2 Ra, y S(O)2 NRaRa, en donde el alquilo C1 -6 , alquenilo C2-6, alquinilo C2-6, arilo C6 -10 , cicloalquilo C3 -10 , heteroarilo de 5-14 miembros, heterocicloalquilo de 4-10 miembros, arilo C6-10-alquilo C1-4-, cicloalquilo C3 -10-alquilo C1-4-, (heteroarilo de 5-14 miembros)-alquilo C1-4-, y (heterocicloalquilo de 4-10 miembros)-alquilo C1-4- de R4, R5 y R6 están cada uno cada uno opcionalmente sustituidos con 1, 2, 3, 4 o 5 sustituyentes Rb independientemente seleccionados;
o dos sustituyentes R6 adyacentes en el anillo Cy, tomados junto con los átomos a los que están unidos, forman un anillo de fenilo fusionado, un anillo de heterocicloalquilo de 5, 6 o 7 miembros fusionado, un anillo de heteroarilo de 5 o 6 miembros fusionado o un anillo de cicloalquilo C3-6 fusionado, en donde el anillo de heterocicloalquilo de 5, 6 o 7 miembros fusionado y el anillo de heteroarilo de 5 o 6 miembros fusionado tienen cada uno 1-4 heteroátomos como miembros del anillo seleccionados de N, O y S y en donde el anillo de fenilo fusionado, el anillo de heterocicloalquilo de 5, 6 o 7 miembros fusionado, el anillo de heteroarilo de 5 o 6 miembros fusionado y el anillo de cicloalquilo C3-6 fusionado están cada uno opcionalmente sustituidos con 1,2 o
3 sustituyentes Rb independientemente seleccionados;
R7 es halo, alquilo C1 -6 , alquenilo C2-6, alquinilo C2-6, haloalquilo C1 -6 , haloalcoxi C1 -6 , arilo C6 -10, cicloalquilo C3 -10 , heteroarilo de 5-14 miembros, heterocicloalquilo de 4-10 miembros, arilo C6-10-alquilo C1-4-, cicloalquilo C3 -10-alquilo C1-4-, (heteroarilo de 5-14 miembros)-alquilo C1-4-, (heterocicloalquilo de 4-10 miembros)-alquilo C1-4-, CN, NO2 , OR11, SR11, NH2 , -NHR11, -NR11R11, NHOR11, C(O)R11, C(O)NR11R11, C(O)OR11, OC(O)R11, OC(O)NR11R11, NR11C(O)R11, NR11C(O)OR11, NR11C(O)NR11R11, C(=NR11)R11, C(=NR11)NR11R11, NR11C(=NR11)NR11R11, NR11C(=NOH)NR11R11, NR11C(=NCN)NR11R11, NR11S(O)R11, NR11S(O)2R11, NR11S(O)2NR11R11, S(O)R11, S(O)NR11R11, S(O)2 R11, o S(O)2 NR11R11, en donde el alquilo C1 -6 , alquenilo C2-6, alquinilo C2-6, haloalquilo C1 -6 , haloalcoxi C1 -6 , arilo C6 -10 , cicloalquilo C3 -10 , heteroarilo de 5-14 miembros, heterocicloalquilo de 4-10 miembros, arilo C6-10-alquilo C1-4-, cicloalquilo C3 -10-alquilo C1-4-, (heteroarilo de 5-14 miembros)-alquilo C1-4- y (heterocicloalquilo de 4-10 miembros)-alquilo C1-4- de R7 están cada uno opcionalmente sustituidos con 1, 2 o 3 sustituyentes Rb independientemente seleccionados;
R8 es alquilo C1-6 sustituido con 1-3 sustituyentes Rb2 independientemente seleccionados o (heterociclo de 4-10 miembros)-alquilo C1-4- opcionalmente sustituido con 1, 2 o 3 sustituyentes Rb independientemente seleccionados;
cada R11 se selecciona independientemente de H, alquilo C1-6 , haloalquilo C1.6 , alquenilo C2-6, alquinilo C2-6, arilo C6 -10 , cicloalquilo C3.10 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, arilo C6-10-alquilo C1-4-, cicloalquilo C3-10-alquilo C1.4-, (heteroarilo de 5-10 miembros)-alquilo C1.4-, y (heterocicloalquilo de 4-10 miembros)-alquilo C1.4-, en donde el alquilo C1 -6 , alquenilo C2-6, alquinilo C2-6, arilo C6 -10 , cicloalquilo C3 -10 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, arilo C6-10-alquilo C1.4-, cicloalquilo C3-10-alquilo C1.4-, (heteroarilo de 5-10 miembros)-alquilo C1.4- y (heterocicloalquilo de 4-10 miembros)-alquilo C1.4- de R11 están cada uno opcionalmente sustituidos con 1,2 o 3 sustituyentes Rb independientemente seleccionados; cada Ra se selecciona independientemente de H, alquilo C1 -6 , haloalquilo C1.6 , alquenilo C2-6, alquinilo C2-6, arilo C6 -10 , cicloalquilo C3 -10 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, arilo C6 -10 -alquilo C1 -4-, cicloalquilo C3-10-alquilo C1.4-, (heteroarilo de 5-10 miembros)-alquilo C1.4-, y (heterocicloalquilo de 4-10 miembros)-alquilo C1.4-, en donde el alquilo C1 -6 , haloalquilo C1.6 , alquenilo C2-6, alquinilo C2-6, arilo C6 -10 , C3-10 cicloalquilo, 5-10 miembros heteroarilo, heterocicloalquilo de 4-10 miembros, C6-10 arilo-C1-4 alquilo-, cicloalquilo C3-10-alquilo C1.4-, (heteroarilo de 5-10 miembros)-alquilo C1-4- y (heterocicloalquilo de 4-10 miembros)-alquilo C1.4 - de Ra están cada uno opcionalmente sustituidos con 1, 2 o 3 sustituyentes Rd independientemente seleccionados;
cada sustituyente Rb se selecciona independientemente de halo, alquilo C1 -6 , haloalquilo C1 -6 , haloalcoxi C1.6 , arilo C6 -10 , cicloalquilo C3 -10 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, arilo C6-10 -alquilo C1.4-, cicloalquilo C3-10-alquilo C1.4-, (heteroarilo de 5-10 miembros)-alquilo C1.4-, (heterocicloalquilo de 4-10 miembros)-alquilo C1.4-, CN, OH, NH2 , NO2 , NHORc, ORc, SRc, C(O)Rc, C(O)NRcRc, C(O)ORc, OC(O)Rc, OC(O)NRcRc, C(=NRc)NRcRc, NRcC(=NRc)NRcRc, NRcC(=NOH)NRcRc, NRcC(=NCN)NRcRc, NHRc, NRcRc, NRcC(O)Rc, NRcC(O)ORc, NRcC(O)NRcRc, NRcS(O)Rc, NRcS(O)2Rc, NRcS(O)2NRcRc, S(O)Rc, S(O)NRcRc, S(O)2 Rc y S(O)2 NRcRc; en donde el alquilo C1 -6 , haloalquilo C1.6 , haloalcoxi C1.6 , arilo C6 -10, cicloalquilo C3 -10 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, arilo C6-10-alquilo C1.4-, cicloalquilo C3-10-alquilo C1-4-, (heteroarilo de 5-10 miembros)-alquilo C1.4- y (heterocicloalquilo de 4-10 miembros)-alquilo C1.4- de Rb están cada uno opcionalmente sustituidos con 1 -3 sustituyentes Rd independientemente seleccionados; cada Rb2 se selecciona independientemente de halo, haloalquilo C1 -6 , haloalcoxi C1 -6 , arilo C6 -10, cicloalquilo C3.10 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, arilo C6-10-alquilo C1-4-, cicloalquilo C3-10-alquilo C1.4-, (heteroarilo de 5-10 miembros)-alquilo C1.4-, (heterocicloalquilo de 4-10 miembros)-alquilo C1.4-, CN, OH, NH2, NO2, NHORc, ORc, SRc, C(O)Rc, C(O)NRcRc, C(O)ORc, OC(O)Rc, OC(O)NRcRc, C(=NRc)NRcRc, NRcC(=NRc)NRcRc, NRcC(=NOH)NRcRc, NRcC(=NCN)NRcRc, NHRc, NRcRc, NRcC(O)Rc, NRcC(O)ORc, NRcC(O)NRcRc, NRcS(O)Rc, NRcS(O)2 Rc, NRcS(O)2 NRcRc, S(O)Rc, S(O)NRcRc, S(O)2 Rc, y S(O)2 NRcRc; en donde el haloalquilo C1 -6 , haloalcoxi C1.6 , arilo C6 -10, cicloalquilo C3 -10 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, arilo C6-10-alquilo C1-4-, cicloalquilo C3-10-alquilo C1.4-, (heteroarilo de 5-10 miembros)-alquilo C1.4- y (heterocicloalquilo de 4-10 miembros)-alquilo C1.4- de Rb2 están cada uno opcionalmente sustituidos con 1-3 sustituyentes Rd independientemente seleccionados.
cada Rc se selecciona independientemente de H, alquilo C1 -6 , haloalquilo C1 -6 , alquenilo C2-6, alquinilo C2-6, arilo C6 -10 , cicloalquilo C3 -10 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, arilo C6-10-alquilo C1-4-, cicloalquilo C3-10-alquilo C1.4-, (heteroarilo de 5-10 miembros)-alquilo C1.4-, y (heterocicloalquilo de 4-10 miembros) -alquilo C1-4-, en donde el alquilo C1 -6 , haloalquilo C1.6 , alquenilo C2-6, alquinilo C2-6, arilo C6 -10 , cicloalquilo C3 -10 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, arilo C6-10-alquilo C1.4-, cicloalquilo C3-10-alquilo C1-4-, (heteroarilo de 5-10 miembros)-alquilo C1.4- y (heterocicloalquilo de 4-10 miembros)-alquilo C1.4- de Rc están cada uno opcionalmente sustituidos con 1, 2 o 3 sustituyentes Rf independientemente seleccionados de alquilo C1 -6 , haloalquilo C1.6 , alquenilo C2-6, alquinilo C2-6, arilo C6 -10 , cicloalquilo C3 -10 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, arilo C6-10-alquilo C1-4-, cicloalquilo C3-10-alquilo C1.4-, (heteroarilo de 5-10 miembros)-alquilo C1.4-, (heterocicloalquilo de 4-10 miembros)-alquilo C1.4-, halo, CN, NHORg, ORg, SRg, C(O)Rg, C(O)NRgRg, C(O)ORg, OC(O)Rg, OC(O)NRgRg, NHRg, NRgRg, NRgC(O)Rg, NRgC(O)NRgRg, NRgC(O)ORg, C(=NRg)NRgRg, NRgC(=NRg)NRgRg, NRgC(=NOH)NRgRg, NRgC(=NCN)NRgRg, S(O)Rg, S(O)NRgRg, S(O)2 Rg, NRgS(O)2 Rg, NRgS(O)2 NRgRg, y S(O)2 NRgRg; en donde el alquilo C1.6 , haloalquilo C1.6 , alquenilo C2-6, alquinilo C2-6, arilo C6-10, cicloalquilo C3 -10 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, arilo C6-10-alquilo C1-4-, cicloalquilo C3-10-alquilo C1.4-, (heteroarilo de 5-10 miembros)-alquilo C1.4-, y (heterocicloalquilo de 4-10 miembros)-alquilo C1.4- de Rf están cada uno opcionalmente sustituidos con 1, 2 o 3 sustituyentes Rn independientemente seleccionados de alquilo C1 -6 , haloalquilo C1 -6 , halo, CN, fenilo, cicloalquilo C3-6, heteroarilo de 5-6 miembros, heterocicloalquilo de 4-6 miembros, NHORo, ORo, SRo, C(O)Ro, C(O)NR°R°, C(O)ORo, OC(O)Ro, OC(O)NR°R°, NHRo, NR°R°, NR°C(O)R°, NR°C(O)NR°R°, NR°C(O)OR°, C(=NR°)NR°R°, NR°C(=NR°)NR°R°, S(O)R°, S(O)NR°R°, S(O)2R°, NR°S(o )2 R°, NR°S(O)2 NR°R°, y S(O)2 NR°R°, en donde el alquilo C1 -6 , haloalquilo C1.6 , fenilo, cicloalquilo C3-6, heteroarilo de 5-6 miembros y heterocicloalquilo de 4-6 miembros de Rn está opcionalmente sustituido con 1,2 o 3 sustituyentes Rq;
cada Rd se selecciona independientemente de alquilo C1 -6 , haloalquilo C1.6 , halo, arilo C6-10, heteroarilo de 5-10 miembros, cicloalquilo C3 -10 , heterocicloalquilo de 4-10 miembros, arilo C6-10-alquilo C1-4-, cicloalquilo C3-10-alquilo C1.4-, (heteroarilo de 5-10 miembros)-alquilo C1.4-, (heterocicloalquilo de 4-10 miembros)-alquilo C1.4-, CN, NH2 , NHORe, ORe, SRe, C(O)Re, C(O)NReRe, C(O)ORe, OC(O)Re, OC(O)NReRe, NHRe, NReRe, NReC(O)Re,
NReC(O)NReRe, NReC(O)ORe, C(=NRe)NReRe, NReC(=NRe)NReRe, NReC(=NOH)NReRe, NReC(=NCN)NReRe, S(O)Re, S(O)NReRe, S(O)2 Re, NReS(O)2 Re, NReS(O)2 NReRe, y S(O)2 NReRe, en donde el alquilo C1 -6 , haloalquilo C1 -6 , arilo C6 -10, heteroarilo de 5-10 miembros, cicloalquilo C3 -10 , heterocicloalquilo de 4-10 miembros, arilo C6-10-alquilo C1-4-, cicloalquilo C3-10-alquilo C1-4-, (heteroarilo de 5-10 miembros)-alquilo C1-4-, y (heterocicloalquilo de 4 10 miembros)-alquilo C1-4- de Rd están cada uno opcionalmente sustituidos con 1-3 sustituyentes Rf independientemente seleccionados;
cada Re se selecciona independientemente de H, alquilo C1 -6 , haloalquilo C1.6 , alquenilo C2-6, alquinilo C2-6, arilo C6 -10 , cicloalquilo C3 -10 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, arilo C6-10-alquilo C1-4-, cicloalquilo C3-10-alquilo C1.4-, (heteroarilo de 5-10 miembros)-alquilo C1.4-, y (heterocicloalquilo de 4-10 miembros)-alquilo C1.4-, en donde el alquilo C1 -6 , haloalquilo C1.6 , alquenilo C2-6, alquinilo C2-6, arilo C6 -10 , cicloalquilo C3 -10 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, arilo C6-10-alquilo C1.4-, cicloalquilo C3-10-alquilo C1.4-, (heteroarilo de 5-10 miembros)-alquilo C1.4- y (heterocicloalquilo de 4-10 miembros)-alquilo C1.4- de Re están cada uno opcionalmente sustituidos con 1, 2 o 3 sustituyentes Rf independientemente seleccionados;
cada Rg se selecciona independientemente de H, alquilo C1 -6 , haloalquilo C1.6 , alquenilo C2-6, alquinilo C2-6, arilo C6 -10 , cicloalquilo C3 -10 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, arilo C6-10-alquilo C1-4-, cicloalquilo C3-10-alquilo C1.4-, (heteroarilo de 5-10 miembros)-alquilo C1.4-, y (heterocicloalquilo de 4-10 miembros)-alquilo C1.4-, en donde el alquilo C1 -6 , alquenilo C2-6, alquinilo C2-6, arilo C6 -10 , cicloalquilo C3 -10 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, arilo C6-10-alquilo C1.4-, cicloalquilo C3-10-alquilo C1-4-, (heteroarilo de 5-10 miembros)-alquilo C1.4- y (heterocicloalquilo de 4-10 miembros)-alquilo C1.4- de Rg están cada uno opcionalmente sustituidos con 1-3 sustituyentes Rp independientemente seleccionados de alquilo C1 -6 , haloalquilo C1 -6 , alquenilo C2-6, alquinilo C2-6, arilo C6 -10 , cicloalquilo C3 -10 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, arilo C6-10-alquilo C1-4-, cicloalquilo C3-10-alquilo C1.4-, (heteroarilo de 5-10 miembros)-alquilo C1.4-, (heterocicloalquilo de 4-10 miembros)-alquilo C1.4 -, halo, Cn , NHORr, ORr, SRr, C(O)Rr, C(O)NRrRr, C(O)ORr, OC(O)Rr, OC(O)NRrRr, NHRr, NRrRr, NRrC(O)Rr, NRrC(O)NRrRr, NRrC(O)ORr, C(=NRr)NRrRr, NRrC(=NRr)NRrRr, NRrC(=NOH)NRrRr, NRrC(=NCN)NRrRr, S(O)Rr, S(O)NRrRr, S(O)2Rr, NRrS(O)2 Rr, NRrS(O)2 NRrRr, y S(O)2 NRrRr, en donde el alquilo C1 -6 , haloalquilo C1.6 , C2-6 alquenilo, C2-6 alquinilo, C6-10 arilo, C3-10 cicloalquilo, heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, arilo C6-10-alquilo C1-4-, cicloalquilo C3-10-alquilo C1.4-, (heteroarilo de 5-10 miembros)-alquilo C1.4- y (heterocicloalquilo de 4-10 miembros)-alquilo C1.4- de Rp está opcionalmente sustituido con 1,2 o 3 sustituyentes Rq;
o dos sustituyentes Ra cualquiera junto con el átomo de nitrógeno, fósforo o boro al que están unidos forman un grupo heterocicloalquilo de 4, 5, 6, 7, 8, 9 o 10 miembros opcionalmente sustituido con 1, 2 o 3 sustituyentes Rh independientemente seleccionados de alquilo C1 -6 , haloalquilo C1 -6 , haloalcoxi C1 -6 , cicloalquilo C3 -10 , heterocicloalquilo de 4-7 miembros, arilo C6 -10, heteroarilo de 5-6 miembros, cicloalquilo C3-10-alquilo C1.4-, (heteroarilo de 5-6 miembros)-alquilo C1.4-, (heterocicloalquilo de 4-7 miembros)-alquilo C1.4-, arilo C6-10-alquilo C1.4-, alquenilo C2-6, alquinilo C2-6, halo, CN, ORi, SRi, NHORi, C(O)Ri, C(O)NRiRi, C(O)ORi, OC(O)Ri, OC(O)NRiRi, NHRi, NRiRi, NRiC(O)Ri, NRiC(O)NRiRi, NRiC(O)ORi, C(=NRi)NRiRi, NRiC(=NRi)NRiRi, NRiC(=NOH)NRiRi, NRiC(=NCN)NRiRi, S(O)Ri, S(O)NRiRi, S(O)2 Ri, NRiS(O)2 Ri, NRiS(O)2 NRiRi, y S(O)2 NRiRi, en donde el alquilo C1 -6 , haloalquilo C1.6 , haloalcoxi C1.6 , cicloalquilo C3 -10 , heterocicloalquilo de 4-7 miembros, arilo C6 -10 , heteroarilo de 5-6 miembros, arilo C6-10-alquilo C1-4-, cicloalquilo C3-10 -alquilo C1.4-, (heteroarilo de 5-6 miembros)-alquilo C1-4-, y (heterocicloalquilo de 4-7 miembros)-alquilo C1.4- de Rh están cada unoo opcionalmente sustituidos con 1, 2 o 3 sustituyentes Rj independientemente seleccionados de alquilo C1 -4 , cicloalquilo C3-6, arilo C6 -10 , heteroarilo de 5 o 6 miembros, heterocicloalquilo de 4-6 miembros, alquenilo C2-4, alquinilo C2-4, halo, haloalquilo C1.4 , haloalcoxi C1.4 , CN, NHORk, ORk, SRk, C(O)Rk, C(O)NRkRk, C(O)ORk, OC(O)Rk, OC(O)NRkRk, NHRk, NRkRk, NRkC(O)Rk, NRkC(O)NRkRk, NRkC(O)ORk, C(=NRk)NRkRk, NRkC(=NRk)NRkRk, S(O)Rk, S(O)NRkRk, S(O)2 Rk, NRkS(O)2 Rk, NRkS(O)2 NRkRk, y S(O)2 NRkRk, en donde el alquilo C1.4 , cicloalquilo C3-6, arilo C6 -10, heteroarilo de 5 o 6 miembros, heterocicloalquilo de 4-6 miembros, alquenilo C2-4, haloalquilo C1.4 y haloalcoxi C1.4 de Rj están cada uno opcionalmente sustituidos con 1, 2 o 3 sustituyentes Rq independientemente seleccionados;
o dos grupos Rh unidos al mismo átomo de carbono del heterocicloalquilo de 4 a 10 miembros, tomados junto con el átomo de carbono al que están unidos, forman un cicloalquilo C3-6 o un heterocicloalquilo de 4 a 6 miembros que tiene 1-2 heteroátomos como miembros del anillo seleccionados de O, N o S;
o dos sustituyentes Rc cualquiera junto con el átomo de nitrógeno al que están unidos forman un grupo heterocicloalquilo de 4, 5, 6 o 7 miembros opcionalmente sustituido con 1, 2 o 3 sustituyentes Rh independientemente seleccionados;
o dos sustituyentes Re cualquiera junto con el átomo de nitrógeno al que están unidos forman un grupo heterocicloalquilo de 4, 5, 6 o 7 miembros opcionalmente sustituido con 1, 2 o 3 sustituyentes Rh independientemente seleccionados;
o dos sustituyentes Rh cualquiera junto con el átomo de nitrógeno al que están unidos forman un grupo heterocicloalquilo de 4, 5, 6 o 7 miembros opcionalmente sustituido con 1, 2 o 3 sustituyentes Rh independientemente seleccionados;
o dos sustituyentes Ro cualquiera junto con el átomo de nitrógeno al que están unidos forman un grupo heterocicloalquilo de 4, 5, 6 o 7 miembros opcionalmente sustituido con 1, 2 o 3 sustituyentes Rh independientemente seleccionados;
o dos sustituyentes Rr cualquiera junto con el átomo de nitrógeno al que están unidos forman un grupo
heterocicloalquilo de 4, 5, 6 o 7 miembros opcionalmente sustituido con 1, 2 o 3 sustituyentes Rh independientemente seleccionados;
cada Ri, Rk, R°o Rr se selecciona independientemente de H, alquilo C1 -6, haloalquilo C1 -6, cicloalquilo C3-6, arilo C6-10 , heterocicloalquilo de 4-6 miembros, heteroarilo de 5 o 6 miembros, haloalquilo C1 -4, alquenilo C2-4 y alquinilo C2-4, en donde el alquilo C1 -4, haloalquilo C1 -6, cicloalquilo C3-6, arilo C6-10 , heterocicloalquilo de 4-6 miembros, heteroarilo de 5 o 6 miembros, alquenilo C2-4 y alquinilo C2-4 de Ri, Rk, Ro o Rr están cada uno opcionalmente sustituidos con 1, 2 o 3 sustituyentes Rq;
cada Rq se selecciona independientemente de OH, CN, -COOH, NH2 , halo, haloalquilo C1 -6, alquilo C1 -6, alcoxi C1 -6, haloalcoxi C1 -6, alquiltio C1 -6, fenilo, heteroarilo de 5-6 miembros, heterocicloalquilo de 4-6 miembros, cicloalquilo C3-6, NHR12 y NR12R12, en donde el alquilo C1 -6, fenilo, cicloalquilo C3-6, heterocicloalquilo de 4-6 miembros y heteroarilo de 5-6 miembros de Rq están cada uno opcionalmente sustituidos con halo, OH, CN, -COOH, NH2 , alquilo C1 -4, alcoxi C1 -4, haloalquilo C1.4, haloalcoxi C1.4, fenilo, cicloalquilo C3-10 y heterocicloalquilo de 4-6 miembros y cada R12 ess independientemente alquilo C1.6; y
!_____es un enlace simple o un enlace doble para que el anillo A siga siendo aromático.
2. El compuesto de la reivindicación 1, o una sal farmacéuticamente aceptable o estereoisómero del mismo en donde Cy es fenilo, 2,3-dihidro-1,4-benzodioxin-6-ilo, 2-fluorofenilo, 2-fluoro-3-metoxifenilo o 1-metil-1H-indazol-4-ilo.
3. El compuesto de la reivindicación 1 o 2, o una sal farmacéuticamente aceptable o estereoisómero del mismo en donde R1, R2 y R3 se seleccionan cada uno independientemente de H, alquilo C1 -4, cicloalquilo C3-6, cicloalquilo C3-6-alquilo C1 -4-, arilo C6-10 , arilo C6-10-alquilo C1 -4, heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, (heteroarilo de 5-10 miembros)-alquilo C1.4-, (heterocicloalquilo de 4-10 miembros)-alquilo C1.4-, alquenilo C2-4, alquinilo C2-4, halo, CN, OH, alcoxi C1.4, haloalquilo C1.4, haloalcoxi C1 -4, NH2 , -NH-alquilo C1.4, -N(alquilo C1 -4)2 , NHOR10, C(O)R10, C(O)NR10R10, C(O)OR10, OC(O)R10, OC(O)NR10R10, NR10C(O)R10, NR10C(O)OR10, NR10C(O)NR10R10, C(=NR10)R10, C(=NR10)NR10R10, NR10C(=NR10)NR10R10, NR10S(O)R10, NR10S(O)2R10, NR10S(O)2 NR10R10, S(O)R10, S(O)NR10R10, S(O)2 R10, y S(O)2 NR10R10, en donde cada R10 se selecciona independientemente de H, alquilo C1 -4, alcoxi C1.4, cicloalquilo C3-6, cicloalquilo C3-6-alquilo C1.4-, arilo C6-10 , arilo C6-10-alquilo C1.4, heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, (heteroarilo de 5-10 miembros)-alquilo C1 -4-, y (heterocicloalquilo de 4-10 miembros)-alquilo C1 -4-, en donde el alquilo C1.4, alcoxi C1.4, cicloalquilo C3-6, cicloalquilo C3-6-alquilo C1.4-, arilo C6-10 , arilo C6-10-alquilo C1.4-, heteroarilo de 5-10 miembros, heterocicloalquilo de 4- 10 miembros, (heteroarilo de 5-10 miembros)-alquilo C1 -4-, y (heterocicloalquilo de 4-10 miembros)-alquilo C1.4- de R1, R2, R3 y R10 están cada uno opcionalmente sustituidos con 1 o 2 grupos independientemente seleccionados de halo, OH, CN y alcoxi C1 -4.
4. El compuesto de cualquiera de las reivindicaciones 1-3, o una sal farmacéuticamente aceptable o un estereoisómero del mismo, en donde R4 es H, halo, alquilo C1 -6, alquenilo C2-6, alquinilo C2-6, haloalquilo C1-6 o haloalcoxi C1 -6.
5. El compuesto de cualquiera de las reivindicaciones 1-4, o una sal farmacéuticamente aceptable o un estereoisómero del mismo, en donde R5 es H, halo, alquilo C1 -6, alquenilo C2-6, alquinilo C2-6, haloalquilo C1-6 o haloalcoxi C1 -6.
6. El compuesto de cualquiera de las reivindicaciones 1 y 3-5, o una sal farmacéuticamente aceptable o un estereoisómero del mismo, en donde R6 es H, halo, alquilo C1 -6, alquenilo C2-6, alquinilo C2-6, CN u ORa, en donde el alquilo C1 -6, alquenilo C2-6 y alquinilo C2-6 de R6 están cada uno opcionalmente sustituidos con 1, 2, 3, 4 o 5 sustituyentes Rb independientemente seleccionados; o dos sustituyentes R6 adyacentes en el anillo Cy, tomados junto con los átomos a los que están unidos, forman un anillo de fenilo fusionado, un anillo de heterocicloalquilo de 5, 6 o 7 miembros fusionado, un anillo de heteroarilo de 5 o 6 miembros fusionado o un anillo de cicloalquilo C3-6 fusionado de, en donde el anillo de heterocicloalquilo de 5, 6 o 7 miembros fusionado y el anillo de heteroarilo de 5 o 6 miembros fusionado tienen cada uno de 1-4 heteroátomos como miembros del anillo seleccionados de N, O y S y en donde el anillo de fenilo fusionado, el anillo de heterocicloalquilo de 5, 6 o 7 miembros fusionado, el anillo de heteroarilo de 5 o 6 miembros fusionado y el anillo de cicloalquilo C3-6 fusionado están opcionalmente sustituidos con 1, 2 o 3 sustituyentes Rb independientemente seleccionados.
7. El compuesto de cualquiera de las reivindicaciones 1-6, o una sal farmacéuticamente aceptable o un estereoisómero del mismo, en donde R7 es halo, alquilo C1 -6, alquenilo C2-6, alquinilo C2-6, haloalquilo C1 -6, haloalcoxi C1 -6, CN, NH2 , NH(alquilo C1 -6), N(alquilo C1 -6)2 , cicloalquilo C3-6, heterocicloalquilo de 4-6 miembros, heteroarilo de 5- 6 miembros o fenilo, en donde el alquilo C1 -6, alquenilo C2-6, alquinilo C2-6, cicloalquilo C3-6, heterocicloalquilo de 4-6 miembros, heteroarilo de 5-6 miembros y fenilo están opcionalmente sustituidos con 1, 2 o 3 sustituyentes Rq independientemente seleccionados.
8. El compuesto de cualquiera de las reivindicaciones 1-7, o una sal farmacéuticamente aceptable o estereoisómero del mismo en donde:
(a) R8 es -CH2 NHRc o -CH2 NRcRc;
(b) R8 es (2-hidroxietilamino)metilo, 2-carboxi-1-piperidinilmetilo, (S)-2-carboxi-1-piperidinilmetilo o (R)-2-carboxi-1-piperidinilmetilo.
9. El compuesto de la reivindicación 1, o una sal farmacéuticamente aceptable o estereoisómero del mismo en donde:
Cy es fenilo, que está opcionalmente sustituido con de 1 a 5 sustituyentes R6 independientemente seleccionados; o dos sustituyentes R6 adyacentes en el anillo Cy, tomados junto con los átomos a los que están unidos, forman un anillo heterocicloalquilo de 5, 6 o 7 miembros fusionado, o un anillo heteroarilo de 5 o 6 miembros fusionado, en donde el anillo de heterocicloalquilo de 5, 6 o 7 miembros fusionado y el anillo de heteroarilo de 5 o 6 miembros fusionado tienen cada uno 1-4 heteroátomos como miembros del anillo seleccionados de N, O y S y en donde el anillo de heterocicloalquilo de 5, 6 o 7 miembros fusionado y el anillo de heteroarilo de 5 o 6 miembros fusionado están cada uno opcionalmente sustituidos con 1, 2 o 3 sustituyentes Rb independientemente seleccionados;
R1, R2 y R3 se seleccionan cada uno independientemente de H, alquilo C1 -4 , alquenilo C2-4, alquinilo C2-4, halo, CN, OH, COOH, alcoxi C1 -4 , haloalquilo C1 -4 , haloalcoxi C1 -4 , ciclopropilo, ciclopropilmetilo, fenilo, fenil-alquilo C1 -4-, heteroarilo de 5-6 miembros, (heteroarilo de 5-6 miembros)-alquilo C1-4-, heterocicloalquilo de 4-6 miembros, (heterocicloalquilo de 4-6 miembros) -alquilo C1-4-, NH2 , -NHalquilo C1 -4 , -N(alquilo C1 -4 )2 , -C(O)R10, -O(CO)R10, -C(O)OR10, -O(CO)NHR10, -NHC(O)OR10, -NHC(O)NHR10, -C(O)NHR10, -NHC(O)R10, -SO2 R10 , -NHSO2 R10 y -SO2 NHR10 , en donde el alquilo C1 -4 , alquenilo C2-4, alquinilo C2-4, alcoxi C1.4 , ciclopropilo, ciclopropilmetilo, fenilo, fenil-alquilo C1-4-, heteroarilo de 5-6 miembros, (heteroarilo de 5-6 miembros)-alquilo C1.4-, heterocicloalquilo de 4-6 miembros y (heterocicloalquilo de 4-6 miembros)-alquilo C1-4- de R1, R2 o R3 están cada uno opcionalmente sustituidos con halo, OH, CN o alcoxi C1 -4 ;
R4, R5 y R6 se seleccionan cada uno independientemente de H, halo, alquilo C1 -6 , alcoxi C1.6 , alquenilo C2-6, alquinilo C2-6, haloalquilo C1.6 , haloalcoxi C1.6 , fenilo, cicloalquilo C3-6, heterocicloalquilo de 4-6 miembros, heteroarilo de 5-6 miembros, fenil-alquilo C1-4-, cicloalquilo C3-6-alquilo C1.4-, (heteroarilo de 5-6 miembros)-alquilo C1.4- o (heterocicloalquilo de 4-6 miembros)-alquilo C1.4-, CN, o H, COOH, NO2 , ORa, C(O)ORa, NH2 , -NHRa, -N(Ra)2, -C(O)Ra, -O(CO)Ra, -C(O)ORa, -O(CO)NRaRa, -NHC(O)ORa, -NHC(O)NRaRa, -C(O)NRaRa, -NHC(O)Ra, -SO2 Ra, -NHSo2 Ra y -SO2 NRaRa, en donde el alquilo C1 -6 , alquenilo C2-6, alquinilo C2-6, fenilo, cicloalquilo C3-6, heterocicloalquilo de 4-6 miembros, heteroarilo de 5-6 miembros, fenil-alquilo C1-4-, cicloalquilo C3-6-alquilo C1.4-, (heteroarilo de 5-6 miembros)-alquilo C1.4- y (heterocicloalquilo de 4-6 miembros)-alquilo C1.4-- de R4, R5 y R6 están cada uno opcionalmente sustituidos con 1 o 2 sustituyentes Rb;
R7 es halo, alquilo C1 -6 , CN, cicloalquilo C3-6, heterocicloalquilo de 4-6 miembros, heteroarilo de 5-6 miembros, cicloalquilo C3-6-alquilo C1-4-, (heterocicloalquilo de 4-6 miembros)-alquilo C1.4-, (heteroarilo de 5-6 miembros)-alquilo C1.4 , en donde el alquilo C1-6 , cicloalquilo C3-6, heterocicloalquilo de 4-6 miembros, heteroarilo de 5-6 miembros, cicloalquilo C3-6-alquilo C1-4-, (heterocicloalquilo de 4-6 miembros)-alquilo C1.4- y (heteroarilo de 5-6 miembros)-alquilo C1.4 de R7 están cada uno opcionalmente sustituidos con 1 o 2 sustituyentes independientemente seleccionados de halo, alquilo C1 -6 , haloalquilo C1 -6 , haloalcoxi C1 -6 , CN, OH, NH2 , -NH(alquilo C1 -6 ), -N(alquilo C1 -6 )2 , COOH, -Oalquilo C1 -6 , -Salquilo C1 -6 , C(O)NH2 , -C(O)NH(alquilo C1-6), -C(O)NH(alquilo C1 -6 )2 , -C(O)OCalquilo 1 -6 , -OC(O)NHalquilo C1 -6 , -OC(O)NH2 , -OC(O)NH(alquilo C1-6)2 , -NHC(O)alquilo C1 -6 , -NHC(O)H, -N(alquilo C1 -6 )C(O)alquilo C1 -6 , -NHC(O)Oalquilo C1-6 , -N(alquilo C1 -6)C(O)Oalquilo C1 -6 , -NHC(O)NH(alquilo C1 -6 ), -NHC(O)N(alquilo C1 -6 )2 , -NHC(O)NH2 , -N(alquilo C1-6)C(O)NH alquilo (C1 -6 ), -N(alquilo C1 -6 )C(O)N(alquilo C1 -6 )2 , -N(alquilo C1 -6 )C(O)NH2 , -NHS(O)2(alquilo C1 -6 ), -N(alquilo C1 -6)S(O)2(alquilo C1 -6 ), -NHS(O)2 NH2 , -NHS(O)2 NH(alquilo C1 -6 ), -NHS(O)2 N(alquilo C1 -6 )2 , -N(alquilo C1 -6 )2 , -N(alquilo C1 -6 ))S(O)2 NH2 , -N(alquilo C1 -6 )S(O)2 NH(alquilo C1-6), -N(alquilo C1 -6 )S(O)2 N(alquilo C1 -6 )2 , -S(O)2(alquilo C1.6 ), -S(O)2 NH2 , -S(O)2 NH(alquilo C1.6 ) y -S(O)2 N(alquilo C ^ ;
cada R11 se selecciona independientemente de H, alquilo C1 -6 , haloalquilo C1.6 , alquenilo C2-6, alquinilo C2-6, fenilo, cicloalquilo C3-6, heteroarilo de 5-6 miembros, heterocicloalquilo de 4-6 miembros, fenilo-alquilo C1-4-, cicloalquilo C3-6-alquilo C1.4-, (heteroarilo de 5-6 miembros)-alquilo C1.4- y (heterocicloalquilo de 4-6 miembros)-alquilo C1-4-, en donde el alquilo C1.6 , haloalquilo C1.6 , alquenilo C2-6, alquinilo C2-6, fenilo, cicloalquilo C3-6, heteroarilo de 5-6 miembros, heterocicloalquilo de 4-6 miembros, fenilo-alquilo C1-4-, cicloalquilo C3-6-alquilo C1.4-, (heteroarilo de 5-6 miembros)-alquilo C1.4- y (heterocicloalquilo de 4-6 miembros)-alquilo C1.4- de R11 están cada uno opcionalmente sustituidos con 1 o 2 sustituyentes Rb;
cada Ra se selecciona independientemente de H, alquilo C1-6 , haloalquilo C1.6 , alquenilo C2-6, alquinilo C2-6, fenilo, cicloalquilo C3-6, heterocicloalquilo de 4-6 miembros, heteroarilo de 5-6 miembros, fenilo-alquilo C1-4-, cicloalquilo C3-6-alquilo C1.4-, (heteroarilo de 5-6 miembros)-alquilo C1.4- y (heterocicloalquilo de 4-6 miembros)-alquilo C1.4-; cada Rb se selecciona independientemente de halo, alquilo C1 -6 , alcoxi C1.6 , haloalquilo C1.6 , haloalcoxi C1.6 , alquenilo C2-6, alquinilo C2-6, fenilo, cicloalquilo C3-6, heteroarilo de 5-6 miembros, heterocicloalquilo de 4-6 miembros, fenil-alquilo C1-4-, cicloalquilo C3-6-alquilo C1.4-, (heteroarilo de 5-6 miembros)-alquilo C1.4-, y (heterocicloalquilo de 4-6 miembros)-alquilo C1.4-, CN, OH, NH2 , NHRc, N(Rc)2 , ORc, C(O)NRcRc, C(O)ORc, COOH, NRcC(O)Rc, OC(O)NRcRc, NRcC(O)ORc, NRcC(O)NRcRc, NRcS(O)2Rc, NRcS(O)2NRcRc, S(O)2Rcy S(O)2 NRcRc, en donde el alquilo C1-6 , alcoxi C1.6 , alquenilo C2-6, alquinilo C2-6, fenilo, cicloalquilo C3-6, heteroarilo de 5-6 miembros, heterocicloalquilo de 4-6 miembros, fenil-alquilo C1-4-, cicloalquilo C3-6-alquilo C1.4-, (heteroarilo de 5-6 miembros)-alquilo C1.4- y (heterocicloalquilo de 4-6 miembros)-alquilo C1.4- de Rb están cada uno opcionalmente sustituidos con 1 o 2 sustituyentes Rd independientemente seleccionados de halo, alquilo C1 -6 ,
alcoxi C1 -6 , alquenilo C2-6, alquinilo C2-6, haloalquilo C1-6 , haloalcoxi C1 -6 , fenilo, cicloalquilo C3-6, cicloalquilo C3-6-alquilo C1-4-, heterocicloalquilo de 4-6 miembros, (heterocicloalquilo de 4-6 miembros)-alquilo C1-4-, heteroarilo de 5-6 miembros, (heteroarilo de 4-6 miembros)-alquilo C1.4-, CN, OH, COOH, ORe, C(O)ORe, NH2 , -NHRe, -N(Re)2 , -C(O)NReRe, -NReC(O)Re, OC(O)NReRe, NReC(O)ORe, NReC(O)NReRe, NReS(O)2Re, NReS(O)2NReRe, S(O)2Rey S(O)2 NReRe, en donde Re es H o alquilo C1-6 ;
cada Rc se selecciona independientemente de H, alquilo C1-6 , haloalquilo C1.6 , alquenilo C2-6, alquinilo C2-6, fenilo, cicloalquilo C3-6, heteroarilo de 5-6 miembros, heterocicloalquilo de 4-6 miembros, fenil-alquilo C1-4-, cicloalquilo C3-6-alquilo C1.4-, (heteroarilo de 5-6 miembros)-alquilo C1.4- y (heterocicloalquilo de 4-6 miembros)-alquilo C1.4-, en donde el alquilo C1 -6 , alquenilo C2-6, alquinilo C2-6, fenilo, cicloalquilo C3-6, heteroarilo de 5-6 miembros, heterocicloalquilo de 4-6 miembros, fenil-alquilo C1-4-, cicloalquilo C3-6-alquilo C1.4-, (heteroarilo de 5-6 miembros)-alquilo C1.4- y (heterocicloalquilo de 4-6 miembros)-alquilo C1.4- de Rc están cada uno opcionalmente sustituidos con 1 o 2 sustituyentes Rf;
o dos sustituyentes Rc junto con el átomo de nitrógeno al que están unidos forman un grupo heterocicloalquilo de 4, 5, 6 o 7 miembros opcionalmente sustituido con 1 o 2 sustituyentes Rh independientemente seleccionados; cada Rf se selecciona independientemente de halo, alquilo C1 -6 , alcoxi C1 -6 , alquenilo C2-6, alquinilo C2-6, haloalquilo C1.6 , haloalcoxi C1-6 , fenilo, cicloalquilo C3-6, heterocicloalquilo de 4-6 miembros, heteroarilo de 5-6 miembros, CN, OH, COOH, ORg, C(O)ORg, NH2 , -NHRg, -N(Rg)2 , -C(O)NRgRg, -NRgC(O)Rg, OC(O)NRgRg, NRgC(O)ORg, NRgC(O)NRgRg, NRgS(O)2 Rg, NRgS(O)2 NRgRg, S(O)2 Rgy S(O)2 NRgRg, en donde cada Rg es independientemente H, alquilo C1 -6 , haloalquilo C1.6 , alquenilo C2-6 o alquinilo C2-6;y
cada Rh se selecciona independientemente de halo, alquilo C1 -6 , haloalquilo C1 -6 , haloalcoxi C1 -6 , CN, OH, NH2 , NHRi, N(Ri)2 , ORi, C(O)NRiRi, NRiC(O)Riy C(O)ORi, en donde R1 es H o alquilo Cm
10. El compuesto de la reivindicación 1, o una sal farmacéuticamente aceptable o estereoisómero del mismo en donde:
R1, R2 y R3 se seleccionan cada uno independientemente de H, alquilo C1 -4 , alquenilo C2-4, alquinilo C2-4, halo, CN, OH, alcoxi C1 -4 , haloalquilo C1.4 , haloalcoxi C1.4 , NH2 , -NH-alquilo C1.4 , -N(alquilo C1 -4 )2 , en donde el alquilo C1-4 y el alcoxi C1.4 de R1, R2 y R3 están cada uno opcionalmente sustituidos con 1 o 2 sustituyentes Rd independientemente seleccionados;
R4, R5 y R6 se seleccionan cada uno independientemente de H, halo, alquilo C1 -6 , alquenilo C2-6, alquinilo C2-6, haloalquilo C1.6 , haloalcoxi C1.6 , CN, NO2 , ORa, SRa, NHORa, C(O)Ra, C(O)NRaRa, C(O)ORa, NHRa y NRaRa, en donde el alquilo C1-6 , alquenilo C2-6 y alquinilo C2-6 de R4, R5 y R6 están cada uno opcionalmente sustituidos con 1, 2, 3, 4 o 5 sustituyentes Rb independientemente seleccionados;
o dos sustituyentes R6 adyacentes en el anillo Cy, tomados junto con los átomos a los que están unidos, forman un anillo de fenilo fusionado, un anillo de heterocicloalquilo de 5, 6 o 7 miembros fusionado, un anillo de heteroarilo de 5 o 6 miembros fusionado o un anillo de cicloalquilo C3-6 fusionado, en donde el anillo de heterocicloalquilo de 5, 6 o 7 miembros fusionado y el anillo de heteroarilo de 5 o 6 miembros fusionado tienen cada uno 1-4 heteroátomos como miembros del anillo seleccionados de N, O y S y en donde el anillo de fenilo fusionado, el anillo de heterocicloalquilo de 5, 6 o 7 miembros fusionado, el anillo de heteroarilo de 5 o 6 miembros fusionado y el anillo de cicloalquilo C3-6 fusionado están opcionalmente sustituidos con 1, 2 o 3 sustituyentes Rb independientemente seleccionados;
R7 es halo, alquilo C1-6 , alquenilo C2-6, alquinilo C2-6, haloalquilo C1 -6 , haloalcoxi C1 -6 , CN, NO2 , OR11, SR11, NH2 , -NHR11, -NR11R11, C(O)R11, C(O)NR11R11, C(O)OR11, NR11C(O)R11, y NR11C(O)OR11, en donde el alquilo C1.6 , alquenilo C2-6, alquinilo C2-6, haloalquilo C1-6 y haloalcoxi C1-6 de R7 están cada uno opcionalmente sustituidos con 1,2 o 3 sustituyentes Rb independientemente seleccionados;
cada R11 se selecciona independientemente de H, alquilo C1-6 , haloalquilo C1.6 , alquenilo C2-6 y alquinilo C2-6, en donde el alquilo C1.6 , alquenilo C2 -6 y alquinilo C2-6 de R11 están cada uno opcionalmente sustituidos con 1,2 o 3 sustituyentes Rb independientemente seleccionados;
cada Ra se selecciona independientemente de H, alquilo C1 -6 , haloalquilo C1.6 , alquenilo C2-6 y alquinilo C2-6, en donde el alquilo C1.6 , haloalquilo C1.6 , alquenilo C2-6 y alquinilo C2-6 de Ra están cada uno opcionalmente sustituidos con 1,2 o 3 sustituyentes Rd independientemente seleccionados;
cada sustituyente Rb se selecciona independientemente de halo, alquilo C1 -6 , haloalquilo C1.6 , haloalcoxi C1 -6 , CN, OH, NH2 , n Ho Rc, ORc, C(O)Rc, C(O)NRcRc y C(O)ORc; en donde el alquilo C1-6 , el haloalquilo C1.6 y el haloalcoxi C1-6 de Rb están cada uno opcionalmente sustituidos con 1-3 sustituyentes Rd independientemente seleccionados;
cada Rb2 se selecciona independientemente de halo, haloalquilo C1 -6 , haloalcoxi C1.6 , arilo C6 -10, cicloalquilo C3 -10 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, CN, OH, NH2 , NO2 , NHORc, Orc, SRc, C(O)Rc, C(O)NRcRc, C(O)ORc, OC(O)Rc, OC(O)NRcRc, NHRc, NRcRc, NRcC(O)Rc, y NRcC(O)ORc; en donde el haloalquilo C1 -6 , el haloalcoxi C1.6 , el arilo C6 -10 , el cicloalquilo C3 -10 , el heteroarilo de 5-10 miembros y el heterocicloalquilo de 4-10 miembros de Rb2 están cada uno además opcionalmente sustituidos con 1-3 sustituyentes Rd independientemente seleccionados;
cada Rc se selecciona independientemente de H, alquilo C1-6 , haloalquilo C1 -6 , alquenilo C2-6 y alquinilo C2-6, en donde el alquilo C1 -6 , haloalquilo C1 -6 , alquenilo C2-6 y alquinilo C2-6 de Rc están cada uno opcionalmente sustituidos con 1, 2 o 3 sustituyentes Rf independientemente seleccionados de alquilo C1 -6 , haloalquilo C1-6 , alquenilo C2-6, alquinilo C2-6, halo, CN, ORg, C(O)Rg, C(O)NRgRg, C(O)ORg, NHRg, NRgRg, y NRgC(O)Rg; cada Rd
se selecciona independientemente de alquilo C1 -6, haloalquilo C1 -6, halo, CN, NH2 , NHORe, ORe, C(O)Re, C(O)NReRe, C(O)ORe, NHRe, NReRe, NReC(O)Re, NReC(O)NReRe, y NReC(O)ORe;
cada Re se selecciona independientemente de H, alquilo C1 -6, haloalquilo C1 -6, alquenilo C2-6 y alquinilo C2-6; cada Rg se selecciona independientemente de H, alquilo C1 -6, haloalquilo C1 -6, alquenilo C2-6 y alquinilo C2-6; -------- es un enlace simple o un enlace doble para que el anillo A siga siendo aromático.
11. El compuesto de la reivindicación 1, o una sal farmacéuticamente aceptable o un estereoisómero del mismo en donde:
R1, R2 y R3 se seleccionan cada uno independientemente de H, alquilo C1 -4, alquenilo C2-4, alquinilo C2-4, halo, CN, OH, NH2 , -NH- alquilo C1-4 y -N(alquilo C1 -4)2 ;
R4, R5 y R6 se seleccionan cada uno independientemente de H, halo, alquilo C1 -6, alquenilo C2-6, alquinilo C2-6 y ORa, en donde el alquilo C1 -6, alquenilo C2-6 y alquinilo C2-6 de R4, R5 y R6 están cada uno opcionalmente sustituido con 1, 2, 3, 4 o 5 sustituyentes Rb independientemente seleccionados;
o dos sustituyentes R6 adyacentes en el anillo Cy, tomados junto con los átomos a los que están unidos, forman un anillo de fenilo fusionado, un anillo de heterocicloalquilo de 5, 6 o 7 miembros fusionado, un anillo de heteroarilo de 5 o 6 miembros fusionadoo o un anillo de cicloalquilo C3-6 fusionado, en donde el anillo de heterocicloalquilo de 5, 6 o 7 miembros fusionado y el anillo de heteroarilo de 5 o 6 miembros fusionado tienen cada uno 1-4 heteroátomos como miembros del anillo seleccionados de N, O y S y en donde el anillo de fenilo fusionado, el anillo de heterocicloalquilo de 5, 6 o 7 miembros fusionado, el anillo de heteroarilo de 5 o 6 miembros fusionado y el anillo de cicloalquilo C3-6 fusionado están cada uno opcionalmente sustituidos con 1,2 o 3 sustituyentes Rb independientemente seleccionados;
R7 es halo, alquilo C1 -6, alquenilo C2-6, alquinilo C2-6 o CN, en donde el alquilo C1 -6, el alquenilo C2-6 y el alquinilo C2-6 de R7 están cada uno opcionalmente sustituidos con 1, 2 o 3 sustituyentes Rb independientemente seleccionados;
cada Ra se selecciona independientemente de H, alquilo C1 -6, alquenilo C2-6 y alquinilo C2-6;
cada sustituyente Rb se selecciona independientemente de halo y alquilo C1 -6;
cada Rb2 se selecciona independientemente de halo, haloalquilo C1 -6, haloalcoxi C1 -6, heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, NHRc, NRcRc y NRcC(O)Rc; en donde el haloalquilo C1 -6, el haloalcoxi C1 -6, el heteroarilo de 5-10 miembros y el heterocicloalquilo de 4-10 miembros de Rb2 están cada uno opcionalmente sustituidos con 1-3 sustituyentes Rd independientemente seleccionados;
cada Rc se selecciona independientemente de H, alquilo C1 -6, haloalquilo C1 -6, alquenilo C2-6 y alquinilo C2-6, en donde el alquilo C1 -6, haloalquilo C1 -6, alquenilo C2-6 y alquinilo C2-6 de Rc están cada uno opcionalmente sustituidos con 1, 2 o 3 sustituyentes Rf independientemente seleccionados de alquilo C1 -6, haloalquilo C1 -6, alquenilo C2-6, alquinilo C2-6, halo, ORg, C(O)Rg, C(O)NRgRg, NHRg y NRgRg;
cada Rd se selecciona independientemente de alquilo C1-6, haloalquilo C1.6, halo, CN, NH2 , ORe, C(O)Re, C(O)NReRe, C(O)ORe, NHRe, NReRe, y NReC(O)Re;
cada Re se selecciona independientemente de H, alquilo C1 -6, alquenilo C2-6 y alquinilo C2-6;
cada Rg se selecciona independientemente de H, alquilo C1 -6, alquenilo C2-6 y alquinilo C2-6;
-------- es un enlace simple o un enlace doble para que el anillo A siga siendo aromático.
12. El compuesto de la reivindicación 1, seleccionado de:
ácido (2S)-1-[(2-{[(2-metilbifenil-3-il)amino]carbonil}-1,3-tiazol-5-il)metil]piperidina-2-carboxílico,
5-{[(2-hidroxietil)amino]metil}-N-(2-metilbifenil-3-il)-1,3-tiazol-2-carboxamida,
5- { [(2-hidroxietil)amino]metil} -N-(2-metilbifenil-3-il)-1,3 -oxazol-2-carboxamida,
ácido (2S)-1-[(1-metil-2-{[(2-metilbifenil-3-il)amino]carbonil}-1H-imidazol-5-il)metil]piperidina-2-carboxílico, 5-{[(2-hidroxietil)amino]metil}-1-metil-N-(2-metilbifenil-3-il)-1H-imidazol-2-carboxamida,
ácido (2S)-1-[(1-metil-3-{[(2-metilbifenil-3-il)amino]carbonil}-1H-pirazol-5-il)metil]piperidina-2-carboxílico, 5-{[(2-hidroxietil)amino]metil}-1-metil-N-(2-metilbifenil-3-il)-1H-pirazol-3-carboxamida,
4- cloro-5-{[(2-hidroxietil)amino]metil}-N-(2-metilbifenil-3-il)-1,3-tiazol-2-carboxamida,
5- {[(2-hidroxietil)amino]metil}-4-metil-N-(2-metilbifenil-3-il)-1,3-tiazol-2-carboxamida,
N-[2-ciano-3-(2,3-dihidro-1,4-benzodioxin-6-il)fenil]-5-{[(2-hidroxietil)amino]metil}-1-metil-1H-pirazol-3-carboxamida,
N-(2-ciano-2'-fluorobifenil-3-il)-5-{[(2-hidroxietil)amino]metil}-1-metil-1H-pirazol-3-carboxamida
N-(2-ciano-2'-fluoro-3'-metoxibifenil-3-il)-5-{[(2-hidroxietil)amino]metil}-1-metil-1H-pirazol-3-carboxamida, N-[2-ciano-3-(1-metil-1H-indazol-4-il)fenil]-5-{[(2-hidroxietil)amino]metil}-1-metil-1H-pirazol-3-carboxamida, N-[2-ciano-3-(2,3-dihidro-1,4-benzodioxin-6-il)fenil]-5-{[(2-hidroxietil)amino]metil}-1-metil-1H-imidazol-2-carboxamida,
N-(2-ciano-2'-fluoro-3'-metoxibifenil-3-il)-5-{[(2-hidroxietil)amino]metil}-1-metil-1H-imidazol-2-carboxamida, y N-[2-ciano-3-(1-metil-1H-indazol-4-il)fenil]-5-{[(2-hidroxietil)amino]metil}-1-metil-1H-imidazol-2-carboxamida, o una sal farmacéuticamente aceptable del mismo.
13. El compuesto de la reivindicación 1, seleccionado de:
(S)-1-(5-doro-2-((5-cianopiridin-3-il)metoxi)-4-((3'-(5-(((2-hidroxietil)amino)metil)tiazol-2-carboxamido)-2,2'-dimetil-[1,1'-bifenil]-3-il)metoxi)benzil)piperidina-2-carboxílico ácido;
(S)-1-(5-cloro-2-((5-cianopiridin-3-il)metoxi)-4-((3'-(5-(((R)-3-hidroxipirrolidin-1-il)metil)tiazol-2-carboxamido)-2,2'-dimetil-[1,1'-bifenil]-3-il)metoxi)benzil)piperidina-2-carboxílico ácido; y
5-(((R)-3-hidroxipirrolidin-1-il)metil)-N-(3'-(5-(((R)-3-hidroxipirrolidin-1-il)metil)-1-metil-1H-pirazol-3-carboxamido)-2,2'-dimetil-[1,1'-bifenil]-3-il)tiazol-2-carboxamida;
o una sal farmacéuticamente aceptable del mismo.
14. Una composición farmacéutica que comprende un compuesto de cualquiera de las reivindicaciones 1-11, o una sal farmacéuticamente aceptable o un estereoisómero del mismo, o un compuesto de la reivindicación 12, o una sal farmacéuticamente aceptable del mismo, y por lo menos un portador o excipiente farmacéuticamente aceptable.
15. Una composición farmacéutica que comprende un compuesto de la reivindicación 13, o una sal farmacéuticamente aceptable del mismo, y por lo menos un portador o excipiente farmacéuticamente aceptable.
16. Un compuesto de cualquiera de las reivindicaciones 1-11, o una sal farmacéuticamente aceptable o un estereoisómero del mismo; un compuesto de la reivindicación 12, o una sal farmacéuticamente aceptable del mismo; o una composición de la reivindicación 14 para uso en un método de tratamiento de una enfermedad o trastorno, en donde la enfermedad o trastorno es cáncer o una infección.
17. El compuesto, sal, estereoisómero o composición para el uso de acuerdo con la reivindicación 16, en donde la enfermedad o trastorno es una infección y la infección es una infección vírica.
18. El compuesto, sal, estereoisómero o composición para el uso de acuerdo con la reivindicación 16, en donde la enfermedad o trastorno es cáncer.
19. El compuesto, sal, estereoisómero o composición para el uso de acuerdo con la reivindicación 18, en donde:
(a) el cáncer se selecciona de cáncer de hueso, cáncer de páncreas, cáncer de piel, cáncer de cabeza o cuello, melanoma maligno cutáneo o intraocular, cáncer de útero, cáncer de ovario, cáncer de recto, cáncer de la región anal, cáncer testicular, carcinoma de las trompas de Falopio, carcinoma de endometrio, cáncer de endometrio, carcinoma de cuello uterino, carcinoma de vagina, carcinoma de vulva, cáncer de esófago, cáncer de intestino delgado, cáncer del sistema endocrino, cáncer de la glándula tiroides, cáncer de la glándula paratiroides, cáncer de la glándula suprarrenal, sarcoma de tejidos blandos, cáncer de uretra, cáncer de pene, leucemias crónicas o agudas, tumores sólidos de la infancia, linfoma linfocítico, cáncer de vejiga, carcinoma de pelvis renal, neoplasia del sistema nervioso central (SNC), linfoma primario del sistema nervioso central (SNC), angiogénesis tumoral, tumor del eje espinal, glioma del tronco encefálico, adenoma pituitario, cáncer epidermoide, cáncer de células escamosas, linfoma de células T, cánceres inducidos por el medio ambiente, incluyendo los inducidos por asbesto, melanoma, melanoma maligno metastásico, cáncer renal, carcinoma de células claras, cáncer de próstata, adenocarcinoma de próstata refractario a hormonas, cáncer de mama, cáncer de colon, cáncer de pulmón, cáncer de pulmón de células no pequeñas (NSCLC), cáncer de pulmón de células pequeñas, tumores sólidos, cáncer hepático, cáncer gástrico, cánceres de cabeza y cuello, glioblastoma, sarcoma, cánceres hematológicos, linfoma, leucemia, leucemia linfoblástica aguda (ALL), leucemia mielógena aguda (AML), leucemia promielocítica aguda (APL), leucemia linfocítica crónica (CLL), leucemia mielógena crónica (CML), leucemia difusa de células B grandes (DLBCL), linfoma de células del manto, linfoma no Hodgkin, linfoma no Hodgkin (NHL) en recaída o refractario, linfoma folicular recurrente, linfoma de Hodgkin, mielofibrosis primaria (PMF), policitemia vera (PV), trombocitosis esencial (ET), síndrome de mielodisplasia (MDS), linfoma linfoblástico agudo de células T (T-ALL), mieloma múltiple (MM), osteosarcoma, rabdomiosarcoma, angiosarcoma, fibrosarcoma, liposarcoma, mixoma, rabdomioma, rabdosarcoma, fibroma, lipoma, teratoma, carcinoma broncogénico, sarcoma de células escamosas, sarcoma de células grandes indiferenciadas, adenocarcinoma, carcinoma alveolar (bronquiolar), adenoma bronquial, hamartoma condromatoso, mesotelioma, cánceres gastrointestinales, carcinoma de células escamosas, carcinoma, leiomiosarcoma, adenocarcinoma ductal, insulinoma, glucagonoma, gastrinoma, vipoma, cánceres del intestino delgado, tumores carcinoides, leiomioma, neurofibroma, cánceres del intestino grueso, adenoma tubular, adenoma velloso, hamartoma, cáncer colorrectal, cánceres del tracto genitourinario, tumor de Wilm [nefroblastoma], carcinoma de células de transición, seminoma, carcinoma embrionario, teratocarcinoma, coriocarcinoma, carcinoma de células intersticiales, fibroadenoma, tumores adenomatoides, hepatoma, carcinoma hepatocelular, colangiocarcinoma, hepatoblastoma, adenoma hepatocelular, histiocitoma fibroso maligno, condrosarcoma, sarcoma de Ewing, linfoma maligno, sarcoma de células reticulares, cordoma de tumor de células gigantes maligno, osteocronoma, exostosis osteocartilaginosa, condroma benigno, condroblastoma, condromixofibroma, osteoma osteoide, tumores de células gigantes, cánceres del sistema nervioso, cánceres de cráneo, osteoma, hemangioma, granuloma, xantoma, osteítis deformante, meninges, meningioma, meningiosarcoma, gliomatosis, cánceres de cerebro, astrocitoma, meduloblastoma, glioma, ependimoma, germinoma (pinealoma), glioblastoma multiforme, oligodendroglioma, schwannoma, retinoblastoma, tumores congénitos, cánceres de la médula espinal, neuroblastoma, enfermedad de Lhermitte-Duclos, cánceres ginecológicos, carcinoma de endometrio, cánceres de cuello uterino, displasia
cervical pretumoral, carcinoma de ovario, cistoadenocarcinoma seroso, cistoadenocarcinoma mucinoso, carcinoma no clasificado, tumores de células de la granulosa-tecal, tumores de células de Sertoli-Leydig, disgerminoma, teratoma maligno, cánceres de vulva, carcinoma intraepitelial, cánceres de vagina, sarcoma botrioide, rabdomiosarcoma embrionario, cánceres de las trompas de Falopio, carcinoma de células basales, sarcoma de Kaposi, nevos displásicos de lunares, angioma, dermatofibroma, queloides, cáncer de mama triple negativo (TNBC), cáncer de las vías biliares o carcinoma urotelial; o
(b) el cáncer es un cáncer metastásico que expresa PD-L1.
20. El compuesto, sal, estereoisómero o composición para el uso de acuerdo con la reivindicación 18, en donde el cáncer es cáncer de pulmón, cáncer de pulmón de células pequeñas, cáncer de pulmón de células no pequeñas, cáncer hepático, carcinoma hepatocelular, melanoma, cáncer de vejiga, cáncer de uretra, cáncer renal o carcinoma de células renales de células claras.
21. Un compuesto de cualquiera de las reivindicaciones 1-11, o una sal farmacéuticamente aceptable o estereoisómero del mismo; un compuesto de la reivindicación 12, o una sal farmacéuticamente aceptable del mismo; o una composición de la reivindicación 14 para su uso en un método para potenciar, estimular y/o aumentar la respuesta inmunitaria en un paciente, en donde el paciente tiene cáncer o una infección.
22. Un compuesto de la reivindicación 13, o una sal farmacéuticamente aceptable del mismo, o una composición de la reivindicación 15 para su uso en un método para tratar una enfermedad o trastorno, en donde la enfermedad o trastorno es cáncer o una infección.
23. El compuesto, sal o composición para el uso de acuerdo con la reivindicación 22, en donde la enfermedad o trastorno es cáncer.
24. El compuesto, sal o composición para el uso de acuerdo con la reivindicación 23, en donde el cáncer se selecciona de cáncer de cabeza y cuello de células escamosas, cáncer urotelial y cánceres con alta inestabilidad de microsatélites (MSIalto).
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201662380599P | 2016-08-29 | 2016-08-29 | |
| PCT/US2017/048880 WO2018044783A1 (en) | 2016-08-29 | 2017-08-28 | Heterocyclic compounds as immunomodulators |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2941716T3 true ES2941716T3 (es) | 2023-05-25 |
Family
ID=59772844
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES17761781T Active ES2941716T3 (es) | 2016-08-29 | 2017-08-28 | Compuestos heterocíclicos como inmunomoduladores |
Country Status (5)
| Country | Link |
|---|---|
| US (3) | US20180057486A1 (es) |
| EP (1) | EP3504198B1 (es) |
| ES (1) | ES2941716T3 (es) |
| MA (1) | MA46045A (es) |
| WO (1) | WO2018044783A1 (es) |
Families Citing this family (133)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| IL289834B1 (en) | 2012-06-13 | 2024-03-01 | Incyte Holdings Corp | Conversion of tricyclic compounds as FGFR inhibitors |
| SI2986610T1 (en) | 2013-04-19 | 2018-04-30 | Incyte Holdings Corporation | Bicyclic heterocycles as inhibitors of FGFR |
| ES2751669T3 (es) | 2015-02-20 | 2020-04-01 | Incyte Corp | Heterociclos bicíclicos como inhibidores FGFR |
| MA41551A (fr) | 2015-02-20 | 2017-12-26 | Incyte Corp | Hétérocycles bicycliques utilisés en tant qu'inhibiteurs de fgfr4 |
| ES2928164T3 (es) | 2015-10-19 | 2022-11-15 | Incyte Corp | Compuestos heterocíclicos como inmunomoduladores |
| TWI763641B (zh) | 2015-11-19 | 2022-05-11 | 美商英塞特公司 | 作為免疫調節劑之雜環化合物 |
| MA55194A (fr) | 2015-12-22 | 2022-05-04 | Incyte Corp | Composés hétérocycliques en tant qu'immunomodulateurs |
| WO2017192961A1 (en) | 2016-05-06 | 2017-11-09 | Incyte Corporation | Heterocyclic compounds as immunomodulators |
| MA45116A (fr) | 2016-05-26 | 2021-06-02 | Incyte Corp | Composés hétérocycliques comme immunomodulateurs |
| UA125391C2 (uk) | 2016-06-20 | 2022-03-02 | Інсайт Корпорейшн | Гетероциклічні сполуки як імуномодулятори |
| CN109803651B (zh) | 2016-06-27 | 2022-05-31 | 凯莫森特里克斯股份有限公司 | 免疫调节剂化合物 |
| US20180016260A1 (en) | 2016-07-14 | 2018-01-18 | Incyte Corporation | Heterocyclic compounds as immunomodulators |
| MA46045A (fr) | 2016-08-29 | 2021-04-28 | Incyte Corp | Composés hétérocycliques utilisés comme immunomodulateurs |
| SG11201903042VA (en) | 2016-10-14 | 2019-05-30 | Precision Biosciences Inc | Engineered meganucleases specific for recognition sequences in the hepatitis b virus genome |
| ES2934230T3 (es) | 2016-12-22 | 2023-02-20 | Incyte Corp | Derivados de benzooxazol como inmunomoduladores |
| WO2018119236A1 (en) | 2016-12-22 | 2018-06-28 | Incyte Corporation | Triazolo[1,5-a]pyridine derivatives as immunomodulators |
| HRP20221216T1 (hr) | 2016-12-22 | 2022-12-23 | Incyte Corporation | Derivati tetrahidro imidazo[4,5-c]piridina kao induktori internalizacije pd-l1 |
| US20180179179A1 (en) | 2016-12-22 | 2018-06-28 | Incyte Corporation | Heterocyclic compounds as immunomodulators |
| JOP20180040A1 (ar) | 2017-04-20 | 2019-01-30 | Gilead Sciences Inc | مثبطات pd-1/pd-l1 |
| WO2018200571A1 (en) | 2017-04-25 | 2018-11-01 | Arbutus Biopharma Corporation | Substituted 2,3-dihydro-1h-indene analogs and methods using same |
| AR111960A1 (es) | 2017-05-26 | 2019-09-04 | Incyte Corp | Formas cristalinas de un inhibidor de fgfr y procesos para su preparación |
| US10919852B2 (en) | 2017-07-28 | 2021-02-16 | Chemocentryx, Inc. | Immunomodulator compounds |
| MA49859A (fr) | 2017-08-08 | 2021-04-07 | Chemocentryx Inc | Immunomodulateurs macrocycliques |
| AU2018392212B9 (en) | 2017-12-20 | 2021-03-18 | Institute Of Organic Chemistry And Biochemistry Ascr, V.V.I. | 2'3' cyclic dinucleotides with phosphonate bond activating the STING adaptor protein |
| AU2018392213B2 (en) | 2017-12-20 | 2021-03-04 | Institute Of Organic Chemistry And Biochemistry Ascr, V.V.I. | 3'3' cyclic dinucleotides with phosphonate bond activating the STING adaptor protein |
| CN111448189A (zh) * | 2018-02-05 | 2020-07-24 | 上海和誉生物医药科技有限公司 | 一种联芳基衍生物、其制备方法和在药学上的应用 |
| CR20200347A (es) | 2018-02-13 | 2020-09-23 | Gilead Sciences Inc | Inhibidores pd-1/pd-l1 |
| EP3755311A4 (en) | 2018-02-22 | 2021-11-10 | ChemoCentryx, Inc. | USEFUL INDANE-AMINES AS AN AGONISTS OF PD-L1 |
| US10836769B2 (en) | 2018-02-26 | 2020-11-17 | Gilead Sciences, Inc. | Substituted pyrrolizine compounds and uses thereof |
| CA3092470A1 (en) | 2018-02-27 | 2019-09-06 | Incyte Corporation | Imidazopyrimidines and triazolopyrimidines as a2a / a2b inhibitors |
| PE20211911A1 (es) | 2018-03-30 | 2021-09-28 | Incyte Corp | Compuestos heterociclicos como inmunomoduladores |
| WO2019192506A1 (en) * | 2018-04-03 | 2019-10-10 | Betta Pharmaceuticals Co., Ltd | Immunomodulators, compositions and methods thereof |
| EP3774883A1 (en) | 2018-04-05 | 2021-02-17 | Gilead Sciences, Inc. | Antibodies and fragments thereof that bind hepatitis b virus protein x |
| JP7296398B2 (ja) | 2018-04-06 | 2023-06-22 | インスティチュート オブ オーガニック ケミストリー アンド バイオケミストリー エーエスシーアール,ヴイ.ヴイ.アイ. | 3’3’-環状ジヌクレオチド |
| TW202005654A (zh) | 2018-04-06 | 2020-02-01 | 捷克科學院有機化學與生物化學研究所 | 2,2,─環二核苷酸 |
| TWI818007B (zh) | 2018-04-06 | 2023-10-11 | 捷克科學院有機化學與生物化學研究所 | 2'3'-環二核苷酸 |
| US11142750B2 (en) | 2018-04-12 | 2021-10-12 | Precision Biosciences, Inc. | Optimized engineered meganucleases having specificity for a recognition sequence in the Hepatitis B virus genome |
| CA3093130C (en) | 2018-04-19 | 2023-10-17 | Gilead Sciences, Inc. | Pd-1/pd-l1 inhibitors |
| WO2019211799A1 (en) | 2018-05-03 | 2019-11-07 | Institute Of Organic Chemistry And Biochemistry Ascr, V.V.I. | 2'3'-cyclic dinucleotide analogue comprising a cyclopentanyl modified nucleotide |
| MX2020011639A (es) | 2018-05-04 | 2021-02-15 | Incyte Corp | Sales de un inhibidor de receptores de factor de crecimiento de fibroblastos (fgfr). |
| EP3788047A2 (en) | 2018-05-04 | 2021-03-10 | Incyte Corporation | Solid forms of an fgfr inhibitor and processes for preparing the same |
| MD3790877T2 (ro) | 2018-05-11 | 2023-08-31 | Incyte Corp | Derivați de tetrahidro-imidazo[4,5-c]piridină în calitate de imunomodulatori PD-L1 |
| JP7391046B2 (ja) | 2018-05-18 | 2023-12-04 | インサイト・コーポレイション | A2a/a2b阻害剤としての縮合ピリミジン誘導体 |
| WO2019232319A1 (en) | 2018-05-31 | 2019-12-05 | Peloton Therapeutics, Inc. | Compositions and methods for inhibiting cd73 |
| AU2019301811B2 (en) | 2018-07-13 | 2022-05-26 | Gilead Sciences, Inc. | PD-1/PD-L1 inhibitors |
| WO2020028097A1 (en) | 2018-08-01 | 2020-02-06 | Gilead Sciences, Inc. | Solid forms of (r)-11-(methoxymethyl)-12-(3-methoxypropoxy)-3,3-dimethyl-8-0x0-2,3,8,13b-tetrahydro-1h-pyrido[2,1-a]pyrrolo[1,2-c] phthalazine-7-c arboxylic acid |
| MA53726A (fr) | 2018-09-25 | 2022-05-11 | Incyte Corp | Composés pyrazolo[4,3-d]pyrimidine en tant que modulateurs des alk2 et/ou fgfr |
| US11066404B2 (en) | 2018-10-11 | 2021-07-20 | Incyte Corporation | Dihydropyrido[2,3-d]pyrimidinone compounds as CDK2 inhibitors |
| WO2020086556A1 (en) | 2018-10-24 | 2020-04-30 | Gilead Sciences, Inc. | Pd-1/pd-l1 inhibitors |
| CN112969505B (zh) | 2018-10-31 | 2023-11-14 | 吉利德科学公司 | 具有hpk1抑制活性的取代的6-氮杂苯并咪唑化合物 |
| PE20211655A1 (es) | 2018-10-31 | 2021-08-24 | Gilead Sciences Inc | Compuestos de 6-azabencimidazol sustituidos como inhibidores de hpk1 |
| JP2022513592A (ja) | 2018-11-02 | 2022-02-09 | シャンハイ マキシノベル ファーマシューティカルズ カンパニー リミテッド | ビフェニル系化合物、その中間体、製造方法、医薬組成物及び使用 |
| TWI827760B (zh) | 2018-12-12 | 2024-01-01 | 加拿大商愛彼特生物製藥公司 | 經取代之芳基甲基脲類及雜芳基甲基脲類、其類似物及其使用方法 |
| SG11202106582YA (en) | 2018-12-20 | 2021-07-29 | Incyte Corp | Imidazopyridazine and imidazopyridine compounds as inhibitors of activin receptor-like kinase-2 |
| JP7268921B2 (ja) * | 2019-01-25 | 2023-05-08 | 北京賽特明強医薬科技有限公司 | アミド基架橋複素環式化合物、その組成物および応用 |
| TWI829857B (zh) | 2019-01-29 | 2024-01-21 | 美商英塞特公司 | 作為a2a / a2b抑制劑之吡唑并吡啶及三唑并吡啶 |
| MX2021009682A (es) | 2019-02-15 | 2021-11-12 | Incyte Corp | Biomarcadores de cinasa 2 dependientes de ciclinas y sus usos. |
| WO2020168197A1 (en) | 2019-02-15 | 2020-08-20 | Incyte Corporation | Pyrrolo[2,3-d]pyrimidinone compounds as cdk2 inhibitors |
| WO2020180959A1 (en) | 2019-03-05 | 2020-09-10 | Incyte Corporation | Pyrazolyl pyrimidinylamine compounds as cdk2 inhibitors |
| DK3934757T3 (da) | 2019-03-07 | 2023-04-17 | Inst Of Organic Chemistry And Biochemistry Ascr V V I | 2'3'-cykliske dinukleotider og prodrugs deraf |
| US20220143061A1 (en) | 2019-03-07 | 2022-05-12 | Institute Of Organic Chemistry And Biochemistry Ascr, V.V.I. | 3'3'-cyclic dinucleotides and prodrugs thereof |
| WO2020178768A1 (en) | 2019-03-07 | 2020-09-10 | Institute Of Organic Chemistry And Biochemistry Ascr, V.V.I. | 3'3'-cyclic dinucleotide analogue comprising a cyclopentanyl modified nucleotide as sting modulator |
| US11628162B2 (en) | 2019-03-08 | 2023-04-18 | Incyte Corporation | Methods of treating cancer with an FGFR inhibitor |
| WO2020192570A1 (zh) | 2019-03-22 | 2020-10-01 | 上海再极医药科技有限公司 | 小分子pd-1/pd-l1抑制剂、其与pd-l1抗体的药物组合物及其应用 |
| US11919904B2 (en) | 2019-03-29 | 2024-03-05 | Incyte Corporation | Sulfonylamide compounds as CDK2 inhibitors |
| TW202210480A (zh) | 2019-04-17 | 2022-03-16 | 美商基利科學股份有限公司 | 類鐸受體調節劑之固體形式 |
| TW202212339A (zh) | 2019-04-17 | 2022-04-01 | 美商基利科學股份有限公司 | 類鐸受體調節劑之固體形式 |
| US11440914B2 (en) | 2019-05-01 | 2022-09-13 | Incyte Corporation | Tricyclic amine compounds as CDK2 inhibitors |
| WO2020223558A1 (en) | 2019-05-01 | 2020-11-05 | Incyte Corporation | Tricyclic amine compounds as cdk2 inhibitors |
| KR20220009420A (ko) | 2019-05-15 | 2022-01-24 | 케모센트릭스, 인크. | Pd-l1 질환의 치료를 위한 트리아릴 화합물 |
| TWI826690B (zh) | 2019-05-23 | 2023-12-21 | 美商基利科學股份有限公司 | 經取代之烯吲哚酮化物及其用途 |
| CN110128415B (zh) * | 2019-05-31 | 2022-03-25 | 沈阳药科大学 | 用作免疫调节剂的吲哚啉类化合物及其制备方法 |
| BR112021023750A2 (pt) | 2019-06-20 | 2022-01-11 | Chemocentryx Inc | Compostos para tratamento de doenças pd-l1 |
| US11591329B2 (en) | 2019-07-09 | 2023-02-28 | Incyte Corporation | Bicyclic heterocycles as FGFR inhibitors |
| US11872217B2 (en) | 2019-07-10 | 2024-01-16 | Chemocentryx, Inc. | Indanes as PD-L1 inhibitors |
| US20220380342A1 (en) * | 2019-07-18 | 2022-12-01 | Abbisko Therapeutics Co., Ltd. | Biphenyl derivatives for blocking pd-1/pd-l1 interaction, preparation method therefor and use thereof |
| WO2021011891A1 (en) | 2019-07-18 | 2021-01-21 | Gilead Sciences, Inc. | Long-acting formulations of tenofovir alafenamide |
| WO2021030162A1 (en) | 2019-08-09 | 2021-02-18 | Incyte Corporation | Salts of a pd-1/pd-l1 inhibitor |
| PE20221010A1 (es) | 2019-08-14 | 2022-06-15 | Incyte Corp | Compuestos de imidazolil pirimidinilamina como inhibidores de cdk2 |
| EP4017476A1 (en) | 2019-08-19 | 2022-06-29 | Gilead Sciences, Inc. | Pharmaceutical formulations of tenofovir alafenamide |
| KR20220075382A (ko) | 2019-09-30 | 2022-06-08 | 인사이트 코포레이션 | 면역조절제로서의 피리도[3,2-d]피리미딘 화합물 |
| US11497808B2 (en) | 2019-09-30 | 2022-11-15 | Gilead Sciences, Inc. | HBV vaccines and methods treating HBV |
| JP2022551668A (ja) | 2019-10-11 | 2022-12-12 | インサイト・コーポレイション | Cdk2阻害剤としての二環式アミン |
| BR112022007163A2 (pt) | 2019-10-14 | 2022-08-23 | Incyte Corp | Heterociclos bicíclicos como inibidores de fgfr |
| CN114555080A (zh) | 2019-10-16 | 2022-05-27 | 凯莫森特里克斯股份有限公司 | 用于治疗pd-l1疾病的杂芳基联苯胺 |
| JP2022551973A (ja) | 2019-10-16 | 2022-12-14 | ケモセントリックス,インコーポレイティド | Pd-l1疾患の処置のためのヘテロアリール-ビフェニルアミド |
| WO2021076728A1 (en) | 2019-10-16 | 2021-04-22 | Incyte Corporation | Bicyclic heterocycles as fgfr inhibitors |
| AU2020385113A1 (en) | 2019-11-11 | 2022-05-19 | Incyte Corporation | Salts and crystalline forms of a PD-1/PD-L1 inhibitor |
| US11897891B2 (en) | 2019-12-04 | 2024-02-13 | Incyte Corporation | Tricyclic heterocycles as FGFR inhibitors |
| KR20220131900A (ko) | 2019-12-04 | 2022-09-29 | 인사이트 코포레이션 | Fgfr 억제제의 유도체 |
| US20230031465A1 (en) | 2019-12-06 | 2023-02-02 | Precision Biosciences, Inc. | Optimized engineered meganucleases having specificity for a recognition sequence in the hepatitis b virus genome |
| CA3163389A1 (en) | 2020-01-03 | 2021-07-08 | Mi ZENG | Biphenyl derivative inhibitor, preparation method therefor and use thereof |
| US20210275666A1 (en) | 2020-03-06 | 2021-09-09 | Incyte Corporation | Combination therapy comprising axl/mer and pd-1/pd-l1 inhibitors |
| JP2023518433A (ja) | 2020-03-20 | 2023-05-01 | ギリアード サイエンシーズ, インコーポレイテッド | 4’-c-置換-2-ハロ-2’-デオキシアデノシンヌクレオシドのプロドラッグ並びにその製造法及び使用法 |
| US20210355121A1 (en) | 2020-04-16 | 2021-11-18 | Incyte Corporation | Fused tricyclic kras inhibitors |
| KR20230041654A (ko) | 2020-05-05 | 2023-03-24 | 테온 테라퓨틱스, 인크. | 칸나비노이드 수용체 유형 2 (cb2) 조정제 및 그의 용도 |
| US11739102B2 (en) | 2020-05-13 | 2023-08-29 | Incyte Corporation | Fused pyrimidine compounds as KRAS inhibitors |
| US11840546B2 (en) | 2020-06-12 | 2023-12-12 | Incyte Corporation | Imidazopyridazine compounds and uses thereof |
| WO2022047093A1 (en) | 2020-08-28 | 2022-03-03 | Incyte Corporation | Vinyl imidazole compounds as inhibitors of kras |
| US20230331675A1 (en) | 2020-09-09 | 2023-10-19 | Guangzhou Maxinovel Pharmaceuticals Co., Ltd. | Aromatic ethylene compound and preparation method therefor, and intermediate, pharmaceutical composition, and application thereof |
| US11767320B2 (en) | 2020-10-02 | 2023-09-26 | Incyte Corporation | Bicyclic dione compounds as inhibitors of KRAS |
| US11760756B2 (en) | 2020-11-06 | 2023-09-19 | Incyte Corporation | Crystalline form of a PD-1/PD-L1 inhibitor |
| US11780836B2 (en) | 2020-11-06 | 2023-10-10 | Incyte Corporation | Process of preparing a PD-1/PD-L1 inhibitor |
| CA3200844A1 (en) | 2020-11-06 | 2022-05-12 | Incyte Corporation | Process for making a pd-1/pd-l1 inhibitor and salts and crystalline forms thereof |
| CA3215903A1 (en) | 2021-04-12 | 2022-10-20 | Incyte Corporation | Combination therapy comprising an fgfr inhibitor and a nectin-4 targeting agent |
| CN113135895A (zh) * | 2021-04-30 | 2021-07-20 | 中国药科大学 | 一种新型联苯类衍生物及其制备方法与医药用途 |
| TW202348237A (zh) | 2021-05-13 | 2023-12-16 | 美商基利科學股份有限公司 | TLR8調節化合物及抗HBV siRNA療法之組合 |
| EP4352059A1 (en) | 2021-06-09 | 2024-04-17 | Incyte Corporation | Tricyclic heterocycles as fgfr inhibitors |
| CA3220155A1 (en) | 2021-06-09 | 2022-12-15 | Incyte Corporation | Tricyclic heterocycles as fgfr inhibitors |
| TW202317200A (zh) | 2021-06-11 | 2023-05-01 | 美商基利科學股份有限公司 | Mcl-1抑制劑與抗體藥物接合物之組合 |
| CA3222269A1 (en) | 2021-06-11 | 2022-12-15 | Gilead Sciences, Inc. | Combination mcl-1 inhibitors with anti-cancer agents |
| AU2022297367A1 (en) | 2021-06-23 | 2023-12-07 | Gilead Sciences, Inc. | Diacylglyercol kinase modulating compounds |
| KR20240025616A (ko) | 2021-06-23 | 2024-02-27 | 길리애드 사이언시즈, 인코포레이티드 | 다이아실글리세롤 키나제 조절 화합물 |
| AU2022298639A1 (en) | 2021-06-23 | 2023-12-07 | Gilead Sciences, Inc. | Diacylglyercol kinase modulating compounds |
| US20230060354A1 (en) | 2021-06-23 | 2023-03-02 | Gilead Sciences, Inc. | Diacylglyercol kinase modulating compounds |
| US20230056631A1 (en) | 2021-07-07 | 2023-02-23 | Incyte Corporation | Tricyclic compounds as inhibitors of kras |
| WO2023287896A1 (en) | 2021-07-14 | 2023-01-19 | Incyte Corporation | Tricyclic compounds as inhibitors of kras |
| WO2023034290A1 (en) | 2021-08-31 | 2023-03-09 | Incyte Corporation | Naphthyridine compounds as inhibitors of kras |
| WO2023034530A1 (en) | 2021-09-02 | 2023-03-09 | Teon Therapeutics, Inc. | Methods of improving growth and function of immune cells |
| US20230151005A1 (en) | 2021-09-21 | 2023-05-18 | Incyte Corporation | Hetero-tricyclic compounds as inhibitors of kras |
| WO2023050104A1 (zh) * | 2021-09-28 | 2023-04-06 | 中国医学科学院药物研究所 | 二氢吲哚衍生物、及其制法和药物组合物与用途 |
| WO2023056421A1 (en) | 2021-10-01 | 2023-04-06 | Incyte Corporation | Pyrazoloquinoline kras inhibitors |
| US11939328B2 (en) | 2021-10-14 | 2024-03-26 | Incyte Corporation | Quinoline compounds as inhibitors of KRAS |
| WO2023081730A1 (en) | 2021-11-03 | 2023-05-11 | Teon Therapeutics, Inc. | 4-hydroxy-2-oxo-1,2-dihydro-1,8-naphthyridine-3-carboxamide derivatives as cannabinoid cb2 receptor modulators for the treatment of cancer |
| WO2023091746A1 (en) | 2021-11-22 | 2023-05-25 | Incyte Corporation | Combination therapy comprising an fgfr inhibitor and a kras inhibitor |
| WO2023097211A1 (en) | 2021-11-24 | 2023-06-01 | The University Of Southern California | Methods for enhancing immune checkpoint inhibitor therapy |
| WO2023110473A1 (en) | 2021-12-14 | 2023-06-22 | Basf Se | Heterocyclic compounds for the control of invertebrate pests |
| EP4198033A1 (en) * | 2021-12-14 | 2023-06-21 | Basf Se | Heterocyclic compounds for the control of invertebrate pests |
| US20230192722A1 (en) | 2021-12-22 | 2023-06-22 | Incyte Corporation | Salts and solid forms of an fgfr inhibitor and processes of preparing thereof |
| WO2023239768A1 (en) | 2022-06-08 | 2023-12-14 | Incyte Corporation | Tricyclic triazolo compounds as dgk inhibitors |
| CN115385865B (zh) * | 2022-06-29 | 2023-06-16 | 深圳大学 | 一种具有cxcr2抑制活性的小分子抑制剂及其制备方法与应用 |
| US20240101557A1 (en) | 2022-07-11 | 2024-03-28 | Incyte Corporation | Fused tricyclic compounds as inhibitors of kras g12v mutants |
| WO2024015372A1 (en) | 2022-07-14 | 2024-01-18 | Teon Therapeutics, Inc. | Adenosine receptor antagonists and uses thereof |
Family Cites Families (338)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3272781A (en) | 1963-08-07 | 1966-09-13 | American Potash & Chem Corp | Boroureas of phosphinoborine polymers |
| FR1425700A (fr) | 1965-02-22 | 1966-01-24 | Basf Ag | Composés formant des complexes métalliques et procédé pour les préparer et les utiliser |
| US4208328A (en) | 1978-04-27 | 1980-06-17 | General Electric Company | Alkyl 3,5-dihydroxy-4-(2-benzothiazolyl)benzoates |
| US4789711A (en) | 1986-12-02 | 1988-12-06 | Ciba-Geigy Corporation | Multifunctional epoxide resins |
| DE3828535A1 (de) | 1988-08-23 | 1990-03-08 | Basf Ag | Benzimidazol-2-carbonsaeureanilide, ihre verwendung als lichtschutzmittel fuer organisches material und mit diesen aniliden stabilisiertes organisches material |
| US5077164A (en) | 1989-06-21 | 1991-12-31 | Minolta Camera Kabushiki Kaisha | Photosensitive member containing an azo dye |
| DE69421982T2 (de) | 1993-09-20 | 2000-03-30 | Fuji Photo Film Co Ltd | Positiv arbeitende Photoresistzusammensetzung |
| JP3461397B2 (ja) | 1995-01-11 | 2003-10-27 | 富士写真フイルム株式会社 | ポジ型フオトレジスト組成物 |
| WO1998027108A2 (en) | 1996-12-16 | 1998-06-25 | Fujisawa Pharmaceutical Co., Ltd. | New amide compounds and their use as nitric oxide synthase inhibitors |
| JPH10316853A (ja) | 1997-05-15 | 1998-12-02 | Sumitomo Bakelite Co Ltd | 半導体多層配線用層間絶縁膜樹脂組成物及び該絶縁膜の製造方法 |
| JP2001519345A (ja) | 1997-10-02 | 2001-10-23 | メルク エンド カムパニー インコーポレーテッド | プレニルタンパク質トランスフェラーゼの阻害剤 |
| WO1999044992A1 (fr) | 1998-03-05 | 1999-09-10 | Nissan Chemical Industries, Ltd. | Composes d'anilide et herbicide |
| JP2000128986A (ja) | 1998-10-28 | 2000-05-09 | Sumitomo Bakelite Co Ltd | ポリベンゾオキサゾール前駆体及びポリベンゾオキサゾール |
| JP2000128984A (ja) | 1998-10-28 | 2000-05-09 | Sumitomo Bakelite Co Ltd | ポリベンゾオキサゾール前駆体及び樹脂 |
| JP2000128987A (ja) | 1998-10-28 | 2000-05-09 | Sumitomo Bakelite Co Ltd | ポリベンゾオキサゾール前駆体及びポリベンゾオキサゾール |
| US6297351B1 (en) | 1998-12-17 | 2001-10-02 | Sumitomo Bakelite Company Limited | Polybenzoxazole resin and precursor thereof |
| BR9916363A (pt) | 1998-12-18 | 2001-12-11 | Axys Pharm Inc | Composto, composição farmacêutica e método paratratar ou prevenir um distúrbio tromboembólico |
| JP2000212281A (ja) | 1999-01-27 | 2000-08-02 | Sumitomo Bakelite Co Ltd | ポリベンゾオキサゾ―ル前駆体及びポリベンゾオキサゾ―ル樹脂 |
| WO2001007409A1 (en) | 1999-07-23 | 2001-02-01 | Astrazeneca Uk Limited | Carbazole derivatives and their use as neuropeptide y5 receptor ligands |
| JP2001114893A (ja) | 1999-10-15 | 2001-04-24 | Sumitomo Bakelite Co Ltd | ポリベンゾオキサゾール樹脂およびその前駆体 |
| US6372907B1 (en) | 1999-11-03 | 2002-04-16 | Apptera Corporation | Water-soluble rhodamine dye peptide conjugates |
| JP2001163975A (ja) | 1999-12-03 | 2001-06-19 | Sumitomo Bakelite Co Ltd | ポリベンゾオキサゾール樹脂及びその前駆体 |
| ID30204A (id) | 1999-12-27 | 2001-11-15 | Japan Tobacco Inc | Senyawa-senyawa cincin terfusi dan penggunaannya sebagai obat |
| EP1257551B1 (de) | 2000-02-01 | 2007-09-05 | Abbott GmbH & Co. KG | Heterozyklische verbindungen und deren anwendung als parp-inhibitoren |
| US6521618B2 (en) | 2000-03-28 | 2003-02-18 | Wyeth | 3-cyanoquinolines, 3-cyano-1,6-naphthyridines, and 3-cyano-1,7-naphthyridines as protein kinase inhibitors |
| WO2001074815A2 (en) | 2000-03-31 | 2001-10-11 | Ortho Mcneil Pharmaceutical, Inc. | Phenyl-substituted imidazopyridines |
| EP1278734A2 (en) | 2000-04-24 | 2003-01-29 | Merck Frosst Canada & Co. | Method of treatment using phenyl and biaryl derivatives as prostaglandin e inhibitors and compounds useful therefore |
| SI1294358T1 (en) | 2000-06-28 | 2004-12-31 | Smithkline Beecham Plc | Wet milling process |
| WO2002014321A1 (en) | 2000-08-11 | 2002-02-21 | The Regents Of The University Of California | Use of stat-6 inhibitors as therapeutic agents |
| AU2002224927A1 (en) | 2000-12-13 | 2002-06-24 | Basf Aktiengesellschaft | Use of substituted imidazoazines, novel imidazoazines, methods for the production thereof, and agents containing these compounds |
| EP1341788B1 (en) | 2000-12-15 | 2005-08-10 | Glaxo Group Limited | Pyrazolopyridines |
| SE0100567D0 (sv) | 2001-02-20 | 2001-02-20 | Astrazeneca Ab | Compounds |
| WO2002071827A2 (en) | 2001-03-14 | 2002-09-19 | Eli Lilly And Company | Retinoid x receptor modulators |
| JP4237497B2 (ja) | 2001-03-30 | 2009-03-11 | スミスクライン ビーチャム コーポレーション | ピラゾロピリジン類、その調製方法及びその治療用化合物としての使用 |
| DE60212949T2 (de) | 2001-04-10 | 2007-01-04 | Smithkline Beecham Corp. | Antivirale pyrazolopyridin verbindungen |
| JP2002316966A (ja) | 2001-04-19 | 2002-10-31 | Ueno Seiyaku Oyo Kenkyusho:Kk | ビナフトール誘導体およびその製法 |
| WO2002088124A2 (en) | 2001-04-27 | 2002-11-07 | Smithkline Beecham Corporation | Pyrazolo'1,5-a!pyridine derivatives |
| AR035543A1 (es) | 2001-06-26 | 2004-06-16 | Japan Tobacco Inc | Agente terapeutico para la hepatitis c que comprende un compuesto de anillo condensado, compuesto de anillo condensado, composicion farmaceutica que lo comprende, compuestos de benzimidazol, tiazol y bifenilo utiles como intermediarios para producir dichos compuestos, uso del compuesto de anillo con |
| US20040214834A1 (en) | 2001-09-07 | 2004-10-28 | Kristjan Gudmunsson | Pyrazolo-pyridines for the treatment of herpes infections |
| TWI331526B (en) | 2001-09-21 | 2010-10-11 | Bristol Myers Squibb Pharma Co | Lactam-containing compounds and derivatives thereof as factor xa inhibitors |
| BR0213208A (pt) | 2001-10-09 | 2004-08-31 | Upjohn Co | Compostos de tetraidro- e hexaidro-carbazóis de arilsulfonila substituìda, suas composições e usos |
| WO2003031587A2 (en) | 2001-10-09 | 2003-04-17 | The Regents Of The University Of California | Use of stat-6 inhibitors as therapeutic agents |
| JP4024579B2 (ja) | 2002-01-22 | 2007-12-19 | 住友ベークライト株式会社 | プラスチック光導波路用材料及び光導波路 |
| JP2005535574A (ja) | 2002-04-11 | 2005-11-24 | バーテックス ファーマシューティカルズ インコーポレイテッド | セリンプロテアーゼ、特にhcvns3−ns4aプロテアーゼのインヒビター |
| MXPA04010441A (es) | 2002-04-23 | 2005-02-14 | Shionogi & Co | Derivado de pirazolo[1,5-a]pirimidina e inhibidor de nad(p)h oxidasa que contiene el mismo. |
| WO2004007472A1 (ja) | 2002-07-10 | 2004-01-22 | Ono Pharmaceutical Co., Ltd. | Ccr4アンタゴニストおよびその医薬用途 |
| WO2004006906A2 (en) | 2002-07-15 | 2004-01-22 | Combinatorx, Incorporated | Methods for the treatment of neoplasms |
| JP2004059761A (ja) | 2002-07-30 | 2004-02-26 | Sumitomo Bakelite Co Ltd | ポリベンゾオキサゾール樹脂、その前駆体及びこれらを用いた光導波路材料並びに光導波路 |
| JP2004091369A (ja) | 2002-08-30 | 2004-03-25 | Sumitomo Pharmaceut Co Ltd | 新規ビフェニル化合物 |
| CA2496633A1 (en) | 2002-08-30 | 2004-04-29 | Bf Research Institute, Inc. | Diagnostic probes and remedies for diseases with accumulation of prion protein, and stains for prion protein |
| US7153863B2 (en) | 2002-10-03 | 2006-12-26 | Smithkline Beecham Corporation | Therapeutic compounds based on pyrazolopyridline derivatives |
| EP1551842A1 (en) | 2002-10-15 | 2005-07-13 | Smithkline Beecham Corporation | Pyradazine compounds as gsk-3 inhibitors |
| KR100624406B1 (ko) | 2002-12-30 | 2006-09-18 | 삼성에스디아이 주식회사 | 비페닐 유도체 및 이를 채용한 유기 전계 발광 소자 |
| US7320989B2 (en) | 2003-02-28 | 2008-01-22 | Encysive Pharmaceuticals, Inc. | Pyridine, pyrimidine, quinoline, quinazoline, and naphthalene urotensin-II receptor antagonists |
| US7078419B2 (en) | 2003-03-10 | 2006-07-18 | Boehringer Ingelheim Pharmaceuticals, Inc. | Cytokine inhibitors |
| AR043633A1 (es) | 2003-03-20 | 2005-08-03 | Schering Corp | Ligandos de receptores de canabinoides |
| JP4595288B2 (ja) | 2003-03-25 | 2010-12-08 | 住友ベークライト株式会社 | ポリベンゾオキサゾール樹脂、その前駆体及びこれらを用いた光導波路材料並びに光導波路 |
| JP2006522789A (ja) | 2003-04-11 | 2006-10-05 | グレンマーク・ファーマシューティカルズ・エス・エー | 炎症性およびアレルギー性障害の治療に有用な新規な複素環式化合物;それらの調製方法および医薬組成物 |
| CL2004001120A1 (es) | 2003-05-19 | 2005-04-15 | Irm Llc | Compuestos derivados de amina sustituidas con heterociclos, inmunosupresores; composicion farmaceutica; y uso para tratar enfermedades mediadas por interacciones de linfocito, tales como enfermedades autoinmunes, inflamatorias, infecciosas, cancer. |
| JP2005002330A (ja) | 2003-05-19 | 2005-01-06 | Sumitomo Electric Ind Ltd | 光学樹脂材料、光学素子、光モジュール、フッ素化ポリマー前駆体及びフッ素化ポリマー |
| WO2005014599A1 (en) | 2003-06-04 | 2005-02-17 | Cellular Genomics, Inc. | Imidazo[1,2-a]pyrazin-8-ylamines and method of inhibition of bruton’s tyrosine kinase by such compounds |
| US20060183746A1 (en) | 2003-06-04 | 2006-08-17 | Currie Kevin S | Certain imidazo[1,2-a]pyrazin-8-ylamines and method of inhibition of Bruton's tyrosine kinase by such compounds |
| US7393848B2 (en) | 2003-06-30 | 2008-07-01 | Cgi Pharmaceuticals, Inc. | Certain heterocyclic substituted imidazo[1,2-A]pyrazin-8-ylamines and methods of inhibition of Bruton's tyrosine kinase by such compounds |
| EP1644335A4 (en) | 2003-07-11 | 2008-06-04 | Bristol Myers Squibb Co | TETRAHYDROQUINOLINE DERIVATIVES COMPRISING MODULATORS OF CANNABINOID RECEPTORS |
| EP1643991B1 (en) | 2003-07-11 | 2014-03-12 | Merck Patent GmbH | Benzimidazole carboxamides as raf kinase inhibitors |
| JPWO2005012221A1 (ja) | 2003-08-04 | 2006-09-14 | 小野薬品工業株式会社 | ジフェニルエーテル化合物、その製造方法および用途 |
| WO2005014543A1 (ja) | 2003-08-06 | 2005-02-17 | Japan Tobacco Inc. | 縮合環化合物及びそのhcvポリメラーゼ阻害剤としての利用 |
| US7504401B2 (en) | 2003-08-29 | 2009-03-17 | Locus Pharmaceuticals, Inc. | Anti-cancer agents and uses thereof |
| EP1670787B1 (en) | 2003-09-11 | 2012-05-30 | iTherX Pharma, Inc. | Cytokine inhibitors |
| US7449582B2 (en) | 2003-10-08 | 2008-11-11 | Irm Llc | Compounds and compositions as protein kinase inhibitors |
| EP1679309A4 (en) | 2003-10-24 | 2007-03-28 | Ono Pharmaceutical Co | ANTISTRESS MEDICAMENT AND ITS MEDICAL USE |
| WO2005047290A2 (en) | 2003-11-11 | 2005-05-26 | Cellular Genomics Inc. | Imidazo[1,2-a] pyrazin-8-ylamines as kinase inhibitors |
| JP2007534652A (ja) | 2003-12-23 | 2007-11-29 | ビーエーエスエフ アクチェンゲゼルシャフト | 3−トリフルオロメチルピコリン酸アニリドおよび殺菌剤としてのその使用 |
| US20070149547A1 (en) | 2004-02-12 | 2007-06-28 | Celine Bonnefous | Bipyridyl amides as modulators of metabotropic glutamate receptor-5 |
| US20070191395A1 (en) | 2004-02-16 | 2007-08-16 | Katsuhiro Kawakami | Heterocyclic compounds having antifungal activity |
| GB0403864D0 (en) | 2004-02-20 | 2004-03-24 | Ucl Ventures | Modulator |
| JP2005248082A (ja) | 2004-03-05 | 2005-09-15 | Sumitomo Electric Ind Ltd | ポリベンゾオキサゾール樹脂前駆体の製造方法およびポリベンゾオキサゾール樹脂の製造方法 |
| CN1930159A (zh) | 2004-03-08 | 2007-03-14 | 北卡罗来纳大学查珀尔希尔分校 | 作为抗原生动物药的新的双阳离子咪唑并[1,2-a]吡啶和5,6,7,8-四氢-咪唑并[1,2-a]吡啶化合物 |
| EP1722789A2 (en) | 2004-03-08 | 2006-11-22 | Amgen Inc. | Therapeutic modulation of ppar (gamma) activity |
| US7423147B2 (en) | 2004-03-31 | 2008-09-09 | Janssen Pharmaceutical, N.V. | Pyridine compounds as histamine H3 modulators |
| JP2005290301A (ja) | 2004-04-02 | 2005-10-20 | Sumitomo Electric Ind Ltd | ポリベンゾオキサゾール樹脂前駆体の製造方法およびポリベンゾオキサゾール樹脂の製造方法 |
| EP1735059A2 (en) | 2004-04-06 | 2006-12-27 | The Procter and Gamble Company | Keratin dyeing compounds, keratin dyeing compositions containing them, and use thereof |
| CN1946703A (zh) | 2004-04-20 | 2007-04-11 | 特兰斯泰克制药公司 | 取代的噻唑和嘧啶衍生物作为黑素细胞皮质激素受体调节剂 |
| DE102004021716A1 (de) | 2004-04-30 | 2005-12-01 | Grünenthal GmbH | Substituierte Imidazo[1,2-a]pyridin-Verbindungen und Arzneimittel enthaltend substituierte Imidazo[1,2-a]pyridin-Verbindungen |
| EP1745036A2 (en) | 2004-05-03 | 2007-01-24 | Boehringer Ingelheim Pharmaceuticals Inc. | Cytokine inhibitors |
| TW200626142A (en) | 2004-09-21 | 2006-08-01 | Glaxo Group Ltd | Chemical compounds |
| EP1793819A2 (en) | 2004-09-23 | 2007-06-13 | Wyeth a Corporation of the State of Delaware | Carbazole and cyclopentaindole derivatives to treat infection with hepatitis c virus |
| WO2006044687A2 (en) | 2004-10-15 | 2006-04-27 | Takeda San Diego, Inc. | Kinase inhibitors |
| BRPI0517619A (pt) * | 2004-11-10 | 2008-10-14 | Cgi Pharmaceuticals Inc | entidades quìmicas de imidazo[1,2-a] pirazin-8-ilaminas, suas composições farmacêuticas, uso dos referidos compostos na preparação de medicamento, processo de preparação de medicamento e métodos de utilização dos referidos compostos |
| DE102004054665A1 (de) | 2004-11-12 | 2006-05-18 | Bayer Cropscience Gmbh | Substituierte bi- und tricyclische Pyrazol-Derivate Verfahren zur Herstellung und Verwendung als Herbizide und Pflanzenwachstumsregulatoren |
| WO2006094235A1 (en) | 2005-03-03 | 2006-09-08 | Sirtris Pharmaceuticals, Inc. | Fused heterocyclic compounds and their use as sirtuin modulators |
| TW200716551A (en) | 2005-03-10 | 2007-05-01 | Cgi Pharmaceuticals Inc | Certain substituted amides, method of making, and method of use thereof |
| JP2006290883A (ja) | 2005-03-17 | 2006-10-26 | Nippon Nohyaku Co Ltd | 置換ヘテロ環カルボン酸アニリド誘導体、その中間体及び農園芸用薬剤並びにその使用方法 |
| EP1902056A2 (en) | 2005-05-20 | 2008-03-26 | Array Biopharma, Inc. | Raf inhibitor compounds and methods of use thereof |
| US20080220968A1 (en) | 2005-07-05 | 2008-09-11 | Ge Healthcare Bio-Sciences Ab | [1, 2, 4] Triazolo [1, 5-A] Pyrimidine Derivatives as Chromatographic Adsorbent for the Selective Adsorption of Igg |
| WO2007034282A2 (en) | 2005-09-19 | 2007-03-29 | Pfizer Products Inc. | Diaryl-imidazole compounds condensed with a heterocycle as c3a receptor antagonists |
| US7723336B2 (en) | 2005-09-22 | 2010-05-25 | Bristol-Myers Squibb Company | Fused heterocyclic compounds useful as kinase modulators |
| US20070078136A1 (en) | 2005-09-22 | 2007-04-05 | Bristol-Myers Squibb Company | Fused heterocyclic compounds useful as kinase modulators |
| EP2597087B1 (en) | 2005-10-25 | 2016-03-30 | Shionogi&Co., Ltd. | Dihydrooxazine and tetrahydropyrimidine derivatives as BACE 1 inhibitors |
| ES2390135T3 (es) | 2005-11-22 | 2012-11-06 | Merck Sharp & Dohme Corp. | Compuestos tricíclicos útiles como inhibidores de quinasas |
| WO2007067711A2 (en) | 2005-12-08 | 2007-06-14 | Amphora Discovery Corporation | Certain chemical entities, compositions, and methods for modulating trpv1 |
| US20090281120A1 (en) | 2005-12-12 | 2009-11-12 | Ono Pharmaceutical Co., Ltd | Bicyclic heterocyclic compound |
| US20090281075A1 (en) | 2006-02-17 | 2009-11-12 | Pharmacopeia, Inc. | Isomeric purinones and 1h-imidazopyridinones as pkc-theta inhibitors |
| WO2007096764A2 (en) | 2006-02-27 | 2007-08-30 | Glenmark Pharmaceuticals S.A. | Bicyclic heteroaryl derivatives as cannabinoid receptor modulators |
| WO2007102531A1 (ja) | 2006-03-08 | 2007-09-13 | Takeda Pharmaceutical Company Limited | 併用薬 |
| JP2009531390A (ja) | 2006-03-31 | 2009-09-03 | ノバルティス アクチエンゲゼルシャフト | 有機化合物 |
| WO2008118122A2 (en) | 2006-05-08 | 2008-10-02 | Molecular Neuroimaging, Llc | Compounds and amyloid probes thereof for therapeutic and imaging uses |
| EP2035005A4 (en) | 2006-06-09 | 2011-07-06 | Kemia Inc | THERAPY BASED ON CYTOKINE INHIBITORS |
| US20080280891A1 (en) | 2006-06-27 | 2008-11-13 | Locus Pharmaceuticals, Inc. | Anti-cancer agents and uses thereof |
| JP2009544625A (ja) | 2006-07-20 | 2009-12-17 | メーメット・カーラマン | Rhoキナーゼのベンゾチオフェン阻害剤 |
| DE102006035018B4 (de) | 2006-07-28 | 2009-07-23 | Novaled Ag | Oxazol-Triplett-Emitter für OLED-Anwendungen |
| WO2008021745A2 (en) | 2006-08-16 | 2008-02-21 | Itherx Pharmaceuticals, Inc. | Hepatitis c virus entry inhibitors |
| TWI389895B (zh) | 2006-08-21 | 2013-03-21 | Infinity Discovery Inc | 抑制bcl蛋白質與結合夥伴間之交互作用的化合物及方法 |
| US7563797B2 (en) | 2006-08-28 | 2009-07-21 | Forest Laboratories Holding Limited | Substituted imidazo(1,2-A)pyrimidines and imidazo(1,2-A) pyridines as cannabinoid receptor ligands |
| EP2074106B1 (en) | 2006-09-11 | 2013-04-17 | Mylan Laboratories Limited | Dibenzofuran derivatives as inhibitors of pde-4 and pde-10 |
| AR063707A1 (es) | 2006-09-11 | 2009-02-11 | Cgi Pharmaceuticals Inc | Determinadas amidas sustituidas, el uso de las mismas para el tratamiento de enfermedades mediadas por la inhibicion de la actividad de btk y composiciones farmacéuticas que las comprenden. |
| US20100160292A1 (en) | 2006-09-11 | 2010-06-24 | Cgi Pharmaceuticals, Inc | Kinase Inhibitors, and Methods of Using and Identifying Kinase Inhibitors |
| PE20080839A1 (es) | 2006-09-11 | 2008-08-23 | Cgi Pharmaceuticals Inc | Determinadas amidas sustituidas, metodo de elaboracion y metodo de uso de las mismas |
| US7838523B2 (en) | 2006-09-11 | 2010-11-23 | Cgi Pharmaceuticals, Inc. | Certain substituted amides, method of making, and method of use thereof |
| FR2906250B1 (fr) | 2006-09-22 | 2008-10-31 | Sanofi Aventis Sa | Derives de 2-aryl-6phenyl-imidazo(1,2-a) pyridines, leur preparation et leur application en therapeutique |
| EP2074107A2 (en) | 2006-10-27 | 2009-07-01 | Wyeth a Corporation of the State of Delaware | Tricyclic compounds as matrix metalloproteinase inhibitors |
| CA2669266C (en) | 2006-11-08 | 2014-04-29 | Bristol-Myers Squibb Company | Pyridinone compounds |
| GB0623209D0 (en) | 2006-11-21 | 2007-01-03 | F2G Ltd | Antifungal agents |
| WO2008064318A2 (en) | 2006-11-22 | 2008-05-29 | University Of Medicine And Dentistry Of New Jersey | Peripheral opioid receptor active compounds |
| WO2008064317A1 (en) | 2006-11-22 | 2008-05-29 | University Of Medicine And Dentistry Of New Jersey | Lipophilic opioid receptor active compounds |
| WO2008071944A1 (en) | 2006-12-14 | 2008-06-19 | Boehringer Ingelheim International Gmbh | Benzoxazoles useful in the treatment of inflammation |
| ES2415863T3 (es) | 2006-12-22 | 2013-07-29 | Incyte Corporation | Heterociclos sustituidos como inhibidores de Janus Quinasas |
| EP1964841A1 (en) | 2007-02-28 | 2008-09-03 | sanofi-aventis | Imidazo[1,2-a]azine and their use as pharmaceuticals |
| WO2008104077A1 (en) | 2007-02-28 | 2008-09-04 | Methylgene Inc. | Small molecule inhibitors of protein arginine methyltransferases (prmts) |
| EP1964840A1 (en) | 2007-02-28 | 2008-09-03 | sanofi-aventis | Imidazo[1,2-a]pyridines and their use as pharmaceuticals |
| JP2008218327A (ja) | 2007-03-07 | 2008-09-18 | Hitachi Ltd | 電解質、電解質膜、それを用いた膜電極接合体、燃料電池電源及び燃料電池電源システム |
| JP2010120852A (ja) | 2007-03-09 | 2010-06-03 | Daiichi Sankyo Co Ltd | 新規なジアミド誘導体 |
| AR065806A1 (es) | 2007-03-22 | 2009-07-01 | Astrazeneca Ab | Derivados de quinolina, procesos para su preparacion, composiciones farmaceuticas que los contienen y usos para el tratamiento de la artritis reumatoidea. |
| WO2008133274A1 (ja) | 2007-04-24 | 2008-11-06 | Shionogi & Co., Ltd. | 環式基で置換されたアミノジヒドロチアジン誘導体 |
| JP5383483B2 (ja) | 2007-04-24 | 2014-01-08 | 塩野義製薬株式会社 | アルツハイマー症治療用医薬組成物 |
| WO2008134553A1 (en) | 2007-04-26 | 2008-11-06 | Xenon Pharmaceuticals Inc. | Methods of using bicyclic compounds in treating sodium channel-mediated diseases |
| PT2155747E (pt) | 2007-05-10 | 2012-12-19 | Ge Healthcare Ltd | Imidazol(1,2-a)piridinas e compostos relacionados com actividade nos receptores de canabinóides cb2 |
| WO2009027733A1 (en) | 2007-08-24 | 2009-03-05 | Astrazeneca Ab | (2-pyridin-3-ylimidazo[1,2-b]pyridazin-6-yl) urea derivatives as antibacterial agents |
| CL2008002793A1 (es) | 2007-09-20 | 2009-09-04 | Cgi Pharmaceuticals Inc | Compuestos derivados de amidas sustituidas, inhibidores de la actividad de btk; composicion farmaceutica que los comprende; utiles en el tratamiento del cancer, trastornos oseos, enfermedades autoinmunes, entre otras |
| MX2010002885A (es) | 2007-09-20 | 2010-04-01 | Amgen Inc | Derivados de acido 1-(4-(bencilbenzamido)-bencil)-azetidin-3-carbo xilico y compuestos relacionados como moduladores de receptores de s1p para el tratamiento de trastornos inmunitarios. |
| DE102007048716A1 (de) | 2007-10-11 | 2009-04-23 | Merck Patent Gmbh | Imidazo[1,2-a]pyrimidinderivate |
| TW200932219A (en) | 2007-10-24 | 2009-08-01 | Astellas Pharma Inc | Oxadiazolidinedione compound |
| CA2703653A1 (en) | 2007-10-25 | 2009-04-30 | Astrazeneca Ab | Pyridine and pyrazine derivatives -083 |
| US7868001B2 (en) | 2007-11-02 | 2011-01-11 | Hutchison Medipharma Enterprises Limited | Cytokine inhibitors |
| WO2009062059A2 (en) | 2007-11-08 | 2009-05-14 | Pharmacopeia, Inc. | Isomeric purinones and 1h-imidazopyridinones as pkc-theta inhibitors |
| US8431569B2 (en) | 2007-12-13 | 2013-04-30 | Merck Sharp & Dohme Corp. | Inhibitors of janus kinases |
| RU2364597C1 (ru) | 2007-12-14 | 2009-08-20 | Андрей Александрович Иващенко | ГЕТЕРОЦИКЛИЧЕСКИЕ ИНГИБИТОРЫ Hh-СИГНАЛЬНОГО КАСКАДА, ЛЕКАРСТВЕННЫЕ КОМПОЗИЦИИ НА ИХ ОСНОВЕ И СПОСОБ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ, СВЯЗАННЫХ С АББЕРАНТНОЙ АКТИВНОСТЬЮ Hh СИГНАЛЬНОЙ СИСТЕМЫ |
| WO2009077197A1 (en) | 2007-12-19 | 2009-06-25 | Syngenta Participations Ag | Insecticidal compounds |
| US8492379B2 (en) | 2007-12-21 | 2013-07-23 | The University Of Sydney | Translocator protein ligands |
| JP2011507910A (ja) | 2007-12-21 | 2011-03-10 | ユニバーシティー オブ ロチェスター | 真核生物の寿命を変更するための方法 |
| CN101910143B (zh) | 2008-01-18 | 2013-08-21 | 卫材R&D管理有限公司 | 稠合的氨基二氢噻嗪衍生物 |
| JP5381718B2 (ja) | 2008-01-31 | 2014-01-08 | コニカミノルタ株式会社 | ハロ多環芳香族化合物及びその製造方法 |
| US20110009429A1 (en) | 2008-02-26 | 2011-01-13 | Paul Oakley | Heterocyclic compounds as inhibitors of cxcr2 |
| EP2095818A1 (en) | 2008-02-29 | 2009-09-02 | AEterna Zentaris GmbH | Use of LHRH antagonists at non-castrating doses |
| FR2928921B1 (fr) | 2008-03-21 | 2010-04-23 | Sanofi Aventis | Derives polysubstitues de 2-aryl-6-phenyl-imidazo°1,2-a!pyridines, leur preparation et leur application en therapeutique |
| FR2928922B1 (fr) | 2008-03-21 | 2010-04-23 | Sanofi Aventis | Derives de 2-aryl-6-phenyl-imidazo°1,2-a!pyridines polysubstitues, leur preparation et leur application en therapeutique |
| FR2928924B1 (fr) | 2008-03-21 | 2010-04-23 | Sanofi Aventis | Derives polysubstitues de 6-heteroaryle-imidazo°1,2-a! pyridines, leur preparation et leur application en therapeutique |
| JP5432982B2 (ja) | 2008-03-31 | 2014-03-05 | 武田薬品工業株式会社 | アポトーシスシグナル調節キナーゼ1阻害剤 |
| KR101034351B1 (ko) | 2008-05-14 | 2011-05-16 | 한국화학연구원 | 신규 벤즈옥사졸로 치환된 피리딘 유도체 또는 이의약학적으로 허용가능한 염, 이의 제조방법 및 이를유효성분으로 함유하는 이상세포 성장 질환의 예방 및치료용 약학적 조성물 |
| CA2724842A1 (en) | 2008-05-19 | 2009-11-26 | Sunovion Pharmaceuticals Inc. | Imidazo[1,2-a]pyridine compounds |
| MX2010012961A (es) | 2008-05-29 | 2011-03-03 | Sirtris Pharmaceuticals Inc Star | Imidazopiridina y analogos relacionados como moduladores de sirtuina. |
| US8163743B2 (en) | 2008-06-05 | 2012-04-24 | GlaxoGroupLimited | 4-carboxamide indazole derivatives useful as inhibitors of PI3-kinases |
| US8476430B2 (en) | 2008-07-24 | 2013-07-02 | Bristol-Myers Squibb Company | Fused heterocyclic compounds useful as kinase modulators |
| US9540322B2 (en) | 2008-08-18 | 2017-01-10 | Yale University | MIF modulators |
| US9643922B2 (en) | 2008-08-18 | 2017-05-09 | Yale University | MIF modulators |
| JP2011231017A (ja) | 2008-09-09 | 2011-11-17 | Nissan Chem Ind Ltd | 光学活性エポキシ化合物及び光学活性スルホキシド化合物の製造方法、並びに該方法に用いる配位子、錯体及び該錯体の製造方法 |
| US8598174B2 (en) | 2008-11-12 | 2013-12-03 | Genetech, Inc. | Pyridazinones, method of making, and method of use thereof |
| WO2010064020A1 (en) | 2008-12-04 | 2010-06-10 | Proximagen Ltd. | Imidazopyridine compounds |
| WO2010071885A1 (en) | 2008-12-19 | 2010-06-24 | Cephalon, Inc. | Pyrrolotriazines as alk and jak2 inhibitors |
| WO2010080474A1 (en) | 2008-12-19 | 2010-07-15 | Bristol-Myers Squibb Company | Carbazole and carboline kinase inhibitors |
| EA019041B1 (ru) | 2008-12-19 | 2013-12-30 | Бристол-Маерс Сквибб Компани | Карбазолкарбоксамидные соединения, применимые в качестве ингибиторов киназы |
| JP5624275B2 (ja) | 2008-12-22 | 2014-11-12 | ユー・ディー・シー アイルランド リミテッド | 有機電界発光素子 |
| ES2567047T3 (es) | 2008-12-23 | 2016-04-19 | Abbvie Inc. | Derivados de pirimidina anti-virales |
| WO2010074284A1 (ja) | 2008-12-26 | 2010-07-01 | 味の素株式会社 | ピラゾロピリミジン化合物 |
| JP2010202530A (ja) | 2009-02-27 | 2010-09-16 | Tokyo Institute Of Technology | 含ヘテロ芳香族化合物および光学材料 |
| KR20100101054A (ko) | 2009-03-07 | 2010-09-16 | 주식회사 메디젠텍 | 세포핵에서 세포질로의 gsk3의 이동을 억제하는 화합물을 함유하는 세포핵에서 세포질로의 gsk3 이동에 의해 발생되는 질환의 치료 또는 예방용 약학적 조성물 |
| AU2010233917B2 (en) | 2009-04-02 | 2015-07-02 | Merck Serono S.A. | Dihydroorotate dehydrogenase inhibitors |
| NZ596185A (en) | 2009-04-16 | 2013-01-25 | Ct Nac Investigaciones Oncologicas Cnio | Imidazopyrazines for use as kinase inhibitors |
| US8338441B2 (en) | 2009-05-15 | 2012-12-25 | Gilead Sciences, Inc. | Inhibitors of human immunodeficiency virus replication |
| US8993604B2 (en) | 2009-06-30 | 2015-03-31 | Siga Technologies, Inc. | Treatment and prevention of dengue virus infections |
| KR20120049852A (ko) | 2009-06-30 | 2012-05-17 | 시가 테크놀로지스, 인크. | 뎅기 바이러스 감염의 치료 및 예방 |
| TWI491606B (zh) | 2009-07-13 | 2015-07-11 | Gilead Sciences Inc | 調節細胞凋亡信號之激酶的抑制劑 |
| JP2011057661A (ja) | 2009-08-14 | 2011-03-24 | Bayer Cropscience Ag | 殺虫性カルボキサミド類 |
| UA108363C2 (uk) | 2009-10-08 | 2015-04-27 | Похідні імінотіадіазиндіоксиду як інгібітори bace, композиція на їх основі і їх застосування | |
| US9095596B2 (en) | 2009-10-15 | 2015-08-04 | Southern Research Institute | Treatment of neurodegenerative diseases, causation of memory enhancement, and assay for screening compounds for such |
| WO2011047319A2 (en) | 2009-10-16 | 2011-04-21 | Rib-X Pharmaceuticals, Inc. | Antimicrobial compounds and methods of making and using the same |
| WO2011050245A1 (en) | 2009-10-23 | 2011-04-28 | Yangbo Feng | Bicyclic heteroaryls as kinase inhibitors |
| JPWO2011078221A1 (ja) | 2009-12-24 | 2013-05-09 | 味の素株式会社 | イミダゾピリダジン化合物 |
| WO2011082400A2 (en) * | 2010-01-04 | 2011-07-07 | President And Fellows Of Harvard College | Modulators of immunoinhibitory receptor pd-1, and methods of use thereof |
| US20130085133A1 (en) | 2010-02-08 | 2013-04-04 | Sourthern Research Institute Office of Commercialization and Intellectual Prop. | Anti-viral treatment and assay to screenfor anti-viral agent |
| TW201136919A (en) | 2010-03-02 | 2011-11-01 | Merck Sharp & Amp Dohme Corp | Inhibitors of hepatitis C virus NS5B polymerase |
| KR101720824B1 (ko) | 2010-03-04 | 2017-03-28 | 머크 샤프 앤드 돔 코포레이션 | 카테콜 o-메틸 트랜스퍼라제의 억제제 및 정신병적 장애의 치료에서의 그의 용도 |
| CN102869661B (zh) | 2010-03-18 | 2015-08-05 | 韩国巴斯德研究所 | 抗感染化合物 |
| US8410117B2 (en) | 2010-03-26 | 2013-04-02 | Hoffmann-La Roche Inc. | Imidazopyrimidine derivatives |
| US8685969B2 (en) | 2010-06-16 | 2014-04-01 | Bristol-Myers Squibb Company | Carboline carboxamide compounds useful as kinase inhibitors |
| CN102295642B (zh) | 2010-06-25 | 2016-04-06 | 中国人民解放军军事医学科学院毒物药物研究所 | 2-芳基咪唑并[1,2-a]吡啶-3-乙酰胺衍生物、其制备方法及用途 |
| EP2402345A1 (en) | 2010-06-29 | 2012-01-04 | Basf Se | Pyrazole fused bicyclic compounds |
| CN101891895B (zh) | 2010-07-28 | 2011-11-30 | 南京航空航天大学 | 基于桥联双水杨醛结构的苯并噻唑类金属配位聚合物及其制法及应用 |
| WO2012016133A2 (en) | 2010-07-29 | 2012-02-02 | President And Fellows Of Harvard College | Ros1 kinase inhibitors for the treatment of glioblastoma and other p53-deficient cancers |
| US8633200B2 (en) | 2010-09-08 | 2014-01-21 | Bristol-Myers Squibb Company | Inhibitors of human immunodeficiency virus replication |
| CN101993415B (zh) | 2010-09-15 | 2013-08-14 | 北京韩美药品有限公司 | 作为Hedgehog通路抑制剂的化合物以及包含该化合物的药物组合物及其应用 |
| CN103889428A (zh) | 2010-10-04 | 2014-06-25 | 肝炎与病毒研究所 | 乙型肝炎病毒抗原分泌的新型抑制剂 |
| EP2444084A1 (en) | 2010-10-21 | 2012-04-25 | Centro Nacional de Investigaciones Oncológicas (CNIO) | Use of PI3K inibitors for the treatment of obesity |
| WO2012052745A1 (en) | 2010-10-21 | 2012-04-26 | Centro Nacional De Investigaciones Oncológicas (Cnio) | Combinations of pi3k inhibitors with a second anti -tumor agent |
| JP6261340B2 (ja) | 2010-11-18 | 2018-01-17 | リガンド ファーマシューティカルズ インコーポレイテッド | 造血成長因子模倣体の使用 |
| CN103261188A (zh) | 2010-12-17 | 2013-08-21 | 先正达参股股份有限公司 | 杀虫化合物 |
| TWI617559B (zh) | 2010-12-22 | 2018-03-11 | 江蘇恆瑞醫藥股份有限公司 | 2-芳基咪唑并[1,2-b]嗒.2-苯基咪唑并[1,2-a]吡啶,和2-苯基咪唑并[1,2-a]吡衍生物 |
| ES2647664T3 (es) | 2011-01-04 | 2017-12-26 | Novartis Ag | Compuestos de indol o análogos de los mismos útiles para el tratamiento de la degeneración macular relacionada con la edad (AMD) |
| CA2825098C (en) | 2011-01-27 | 2020-03-10 | Universite De Montreal | Pyrazolopyridine and pyrazolopyrimidine derivatives as melanocortin-4 receptor modulators |
| EP2685981B1 (en) | 2011-03-17 | 2016-08-24 | Bristol-Myers Squibb Company | Pyrrolopyridazine jak3 inhibitors and their use for the treatment of inflammatory and autoimmune diseases |
| WO2012129562A2 (en) | 2011-03-24 | 2012-09-27 | The Scripps Research Institute | Compounds and methods for inducing chondrogenesis |
| WO2012139425A1 (en) | 2011-04-13 | 2012-10-18 | Schering Corporation | 5-substituted iminothiazines and their mono-and dioxides as bace inhibitors,compositions,and their use |
| CN102796103A (zh) | 2011-05-23 | 2012-11-28 | 南京英派药业有限公司 | 6-(芳基甲酰)咪唑并[1,2-a]嘧啶和6-(芳基甲酰)[1,2,4]三唑并[4,3-a]嘧啶作为Hedgehog抑制剂及其应用 |
| PT2713722T (pt) | 2011-05-31 | 2017-06-27 | Receptos Llc | Novos estabilizadores e moduladores do receptor glp-1 |
| GB201109763D0 (en) | 2011-06-10 | 2011-07-27 | Ucl Business Plc | Compounds |
| WO2012175991A1 (en) | 2011-06-24 | 2012-12-27 | Pharminox Limited | Fused pentacyclic anti - proliferative compounds |
| AU2012282229B2 (en) | 2011-07-08 | 2015-05-07 | Novartis Ag | Novel pyrrolo pyrimidine derivatives |
| EP2548877A1 (en) | 2011-07-19 | 2013-01-23 | MSD Oss B.V. | 4-(5-Membered fused pyridinyl)benzamides as BTK-inhibitors |
| WO2013033901A1 (en) | 2011-09-08 | 2013-03-14 | Merck Sharp & Dohme Corp. | Heterocyclic-substituted benzofuran derivatives and methods of use thereof for the treatment of viral diseases |
| WO2013040528A1 (en) | 2011-09-16 | 2013-03-21 | Microbiotix, Inc. | Antimicrobial compounds |
| EP2757884B1 (en) | 2011-09-22 | 2022-07-27 | Merck Sharp & Dohme LLC | Pyrazolopyridyl compounds as aldosterone synthase inhibitors |
| JP6040677B2 (ja) | 2011-09-29 | 2016-12-07 | 東洋インキScホールディングス株式会社 | 太陽電池封止材用樹脂組成物 |
| IN2014DN03206A (es) | 2011-10-13 | 2015-05-22 | Novartis Ag | |
| US20140288052A1 (en) | 2011-10-20 | 2014-09-25 | GlaxoSmithKline, LLC | Substituted bicyclic aza-heterocycles and analogues as sirtuin modulators |
| SG11201401359SA (en) | 2011-10-21 | 2014-05-29 | Torrent Pharmaceuticals Ltd | Novel substituted imidazopyrimidines as gpbar1 receptor modulators |
| WO2013120040A1 (en) | 2012-02-10 | 2013-08-15 | Children's Medical Center Corporation | Targeted pathway inhibition to improve muscle structure, function and activity in muscular dystrophy |
| US9034882B2 (en) | 2012-03-05 | 2015-05-19 | Bristol-Myers Squibb Company | Inhibitors of human immunodeficiency virus replication |
| EP2824099A4 (en) * | 2012-03-09 | 2015-11-11 | Carna Biosciences Inc | NOVEL TRIAZINE DERIVATIVE |
| WO2013157021A1 (en) | 2012-04-20 | 2013-10-24 | Advinus Therapeutics Limited | Bicyclic compounds, compositions and medicinal applications thereof |
| MX2014005002A (es) | 2012-04-20 | 2014-07-09 | Gilead Sciences Inc | Derivados de acido benzotiazol-6-il acetico y su uso para tratar una infeccion por vih. |
| WO2013163404A1 (en) | 2012-04-27 | 2013-10-31 | The Uab Research Foundation | TREATING VIRAL INFECTIONS HAVING VIRAL RNAs TRANSLATED BY A NON-IRES MEDIATED MECHANISM |
| BR112014029578B1 (pt) | 2012-06-18 | 2019-10-22 | Sumitomo Chemical Co | composto heterocíclico fundido, composição e método de controle de peste |
| WO2014007228A1 (ja) | 2012-07-03 | 2014-01-09 | 小野薬品工業株式会社 | ソマトスタチン受容体作動活性を有する化合物およびその医薬用途 |
| GB201212513D0 (en) | 2012-07-13 | 2012-08-29 | Ucb Pharma Sa | Therapeutic agents |
| EA028722B1 (ru) | 2012-07-13 | 2017-12-29 | Юсб Байофарма Спрл | Производные имидазопиридина в качестве модуляторов активности tnf |
| JP2015178457A (ja) | 2012-07-25 | 2015-10-08 | 杏林製薬株式会社 | ピラゾロピリジン誘導体、またはその薬理学的に許容される塩 |
| EP2892899B1 (en) | 2012-09-06 | 2018-03-21 | Bristol-Myers Squibb Company | Imidazopyridazine jak3 inhibitors and their use for the treatment of inflammatory and autoimmune diseases |
| CN104640858B (zh) | 2012-09-26 | 2018-11-06 | 霍夫曼-拉罗奇有限公司 | 环醚吡唑-4-基-杂环基-甲酰胺化合物及使用方法 |
| WO2014061693A1 (ja) | 2012-10-17 | 2014-04-24 | 塩野義製薬株式会社 | 新規非芳香族炭素環又は非芳香族複素環誘導体 |
| US9657024B2 (en) | 2012-11-21 | 2017-05-23 | Stategics, Inc. | Substituted triazolo-pyrimidine compounds for modulating cell proliferation, differentiation and survival |
| JP6037804B2 (ja) | 2012-12-03 | 2016-12-07 | 富士フイルム株式会社 | ガス分離膜 |
| EA035929B1 (ru) | 2013-01-15 | 2020-09-02 | Инсайт Холдингс Корпорейшн | ТИАЗОЛКАРБОКСАМИДЫ И ПИРИДИНКАРБОКСАМИДЫ, ИСПОЛЬЗУЕМЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ Pim-КИНАЗЫ |
| KR20150109429A (ko) | 2013-01-22 | 2015-10-01 | 시에나 바이오테크 에스.피.에이. | Bace1 억제제로서의 플루오로-[1,3]옥사진 |
| CN103933036B (zh) | 2013-01-23 | 2017-10-13 | 中国人民解放军军事医学科学院毒物药物研究所 | 2‑芳基咪唑并[1,2‑α]吡啶‑3‑乙酰胺衍生物在制备防治PTSD的药物中的用途 |
| US9657082B2 (en) | 2013-01-31 | 2017-05-23 | Thomas Jefferson University | PD-L1 and PD-L2-based fusion proteins and uses thereof |
| PT2963037T (pt) | 2013-02-27 | 2019-04-23 | Mochida Pharm Co Ltd | Novo derivado de pirazole |
| AP2015008716A0 (en) | 2013-03-08 | 2015-09-30 | Amgen Inc | Perfluorinated cyclopropyl fused 1,3-oxazin-2-amine compounds as beta-secretase inhibitors and methods of use |
| EP2971007A4 (en) | 2013-03-13 | 2017-03-22 | Australian Nuclear Science And Technology Organisation | Transgenic non-human organisms with non-functional tspo genes |
| CN104045552B (zh) | 2013-03-13 | 2019-06-11 | 江苏先声药业有限公司 | 作为神经保护剂的药用化合物 |
| JP6562898B2 (ja) | 2013-03-14 | 2019-08-21 | セルタクシス,インコーポレイテッド | ロイコトリエンa4加水分解酵素の阻害剤 |
| WO2014159959A1 (en) | 2013-03-14 | 2014-10-02 | Bristol-Myers Squibb Company | Inhibitors of human immunodeficiency virus replication |
| DK2968304T3 (en) | 2013-03-14 | 2019-01-28 | Univ Columbia | 4-PHENYLPIPERIDINES, THEIR PREPARATION AND USE. |
| WO2014186035A1 (en) | 2013-03-14 | 2014-11-20 | Curadev Pharma Private Ltd. | Inhibitors of the kynurenine pathway |
| US9308236B2 (en) | 2013-03-15 | 2016-04-12 | Bristol-Myers Squibb Company | Macrocyclic inhibitors of the PD-1/PD-L1 and CD80(B7-1)/PD-L1 protein/protein interactions |
| WO2014181287A1 (en) | 2013-05-09 | 2014-11-13 | Piramal Enterprises Limited | Heterocyclyl compounds and uses thereof |
| RS58273B1 (sr) | 2013-06-26 | 2019-03-29 | Abbvie Inc | Primarni karboksamidi kao btk inhibitori |
| EP3016949B1 (en) | 2013-07-02 | 2020-05-13 | Syngenta Participations AG | Pesticidally active bi- or tricyclic heterocycles with sulfur containing substituents |
| US10626095B2 (en) | 2013-07-17 | 2020-04-21 | Otsuka Pharmaceutical Co., Ltd. | Cyanotriazole compounds |
| EP3024327B1 (en) | 2013-07-25 | 2019-09-04 | Dana-Farber Cancer Institute, Inc. | Inhibitors of transcription factors and uses thereof |
| EP2835375A1 (en) | 2013-08-09 | 2015-02-11 | Fundació Institut Català d'Investigació Química | Bis-salphen compounds and carbonaceous material composites comprising them |
| KR101715090B1 (ko) | 2013-08-28 | 2017-03-13 | 한국화학연구원 | 신규한 화합물 또는 이의 약학적으로 허용가능한 염, 및 이를 유효성분으로 함유하는 인플루엔자 바이러스 감염으로 인한 질환의 예방 또는 치료용 약학적 조성물 |
| US9872852B2 (en) | 2013-09-04 | 2018-01-23 | Bristol-Myers Squibb Company | Compounds useful as immunomodulators |
| AU2014316682B2 (en) | 2013-09-06 | 2018-11-22 | Aurigene Discovery Technologies Limited | 1,2,4-oxadiazole derivatives as immunomodulators |
| ES2682040T3 (es) | 2013-09-06 | 2018-09-18 | Aurigene Discovery Technologies Limited | Derivados de 1,3,4-oxadiazol y 1,3,4-tiadiazol como inmunomoduladores |
| WO2015036927A1 (en) | 2013-09-10 | 2015-03-19 | Aurigene Discovery Technologies Limited | Immunomodulating peptidomimetic derivatives |
| JP6336870B2 (ja) | 2013-09-30 | 2018-06-06 | 日本ポリプロ株式会社 | ビフェノール化合物及びそれを用いるオレフィン重合用触媒並びにオレフィン重合体の製造方法 |
| GB201321733D0 (en) | 2013-12-09 | 2014-01-22 | Ucb Pharma Sa | Therapeutic agents |
| GB201321746D0 (en) | 2013-12-09 | 2014-01-22 | Ucb Pharma Sa | Therapeutic agents |
| GB201321743D0 (en) | 2013-12-09 | 2014-01-22 | Ucb Pharma Sa | Therapeutic agents |
| GB201321736D0 (en) | 2013-12-09 | 2014-01-22 | Ucb Pharma Sa | Therapeutic agents |
| WO2015095337A2 (en) | 2013-12-18 | 2015-06-25 | The Rockefeller University | PYRAZOLO[1,5-a]PYRIMIDINECARBOXAMIDE DERIVATIVES FOR TREATING COGNITIVE IMPAIRMENT |
| RU2016131792A (ru) | 2014-01-03 | 2018-02-06 | Байер Энимэл Хельс ГмбХ | Новые пиразолил-гетероариламиды в качестве средств для борьбы с вредителями |
| WO2015120364A1 (en) | 2014-02-10 | 2015-08-13 | Merck Sharp & Dohme Corp. | Antibodies that bind to human tau and assay for quantifying human tau using the antibodies |
| JP2017508788A (ja) | 2014-02-25 | 2017-03-30 | アキリオン ファーマシューティカルズ,インコーポレーテッド | 補体媒介障害の治療のためのエーテル化合物 |
| JP6490464B2 (ja) | 2014-03-26 | 2019-03-27 | 三井化学株式会社 | 遷移金属化合物、オレフィン重合用触媒およびオレフィン系重合体の製造方法 |
| DK3125883T3 (da) | 2014-04-04 | 2020-10-19 | Iomet Pharma Ltd | Indolderivater til anvendelse i medicin |
| US9850225B2 (en) | 2014-04-14 | 2017-12-26 | Bristol-Myers Squibb Company | Compounds useful as immunomodulators |
| WO2015197028A1 (en) | 2014-06-28 | 2015-12-30 | Sunshine Lake Pharma Co., Ltd. | Compounds as hepatitis c virus (hcv) inhibitors and uses thereof in medicine |
| CN104211726B (zh) | 2014-08-11 | 2017-06-16 | 中南民族大学 | 非茂类三齿双核钛配合物、制备方法及用途 |
| WO2016044604A1 (en) | 2014-09-17 | 2016-03-24 | Epizyme, Inc. | Carm1 inhibitors and uses thereof |
| AU2015317566B2 (en) | 2014-09-19 | 2019-10-10 | Mackay Medical Foundation The Presbyterian Church In Taiwan Mackay Memorial Hospital | Benzo-heterocyclic compounds and their applications |
| EP3204382B1 (en) * | 2014-10-06 | 2021-12-01 | Merck Patent GmbH | Heteroaryl compounds as btk inhibitors and uses thereof |
| AU2015360416A1 (en) | 2014-12-10 | 2017-06-08 | Massachusetts Institute Of Technology | Fused 1,3-azole derivatives useful for the treatment of proliferative diseases |
| JP6853619B2 (ja) | 2015-01-16 | 2021-03-31 | 大塚製薬株式会社 | シアノトリアゾール化合物の医薬用途 |
| EP3261442B1 (en) | 2015-01-20 | 2020-04-01 | Merck Sharp & Dohme Corp. | Iminothiadiazine dioxides bearing an amine-linked substituent as bace inhibitors, compositions, and their use |
| WO2016116525A1 (de) | 2015-01-20 | 2016-07-28 | Cynora Gmbh | Organische moleküle, insbesondere zur verwendung in optoelektronischen bauelementen |
| WO2016156282A1 (en) | 2015-04-02 | 2016-10-06 | Bayer Cropscience Aktiengesellschaft | Novel triazole compounds for controlling phytopathogenic harmful fungi |
| WO2017035405A1 (en) | 2015-08-26 | 2017-03-02 | Achillion Pharmaceuticals, Inc. | Amino compounds for treatment of immune and inflammatory disorders |
| US10745382B2 (en) | 2015-10-15 | 2020-08-18 | Bristol-Myers Squibb Company | Compounds useful as immunomodulators |
| ES2928164T3 (es) * | 2015-10-19 | 2022-11-15 | Incyte Corp | Compuestos heterocíclicos como inmunomoduladores |
| WO2017070320A1 (en) | 2015-10-21 | 2017-04-27 | University Of Pittsburgh - Of The Commonwealth System Of Higher Education | Phenyl indole allosteric inhibitors of p97 atpase |
| KR101717601B1 (ko) | 2015-11-10 | 2017-03-20 | 한국화학연구원 | 신규한 화합물 또는 이의 약학적으로 허용가능한 염, 및 이를 유효성분으로 함유하는 인플루엔자 바이러스 감염으로 인한 질환의 예방 또는 치료용 약학적 조성물 |
| TWI763641B (zh) | 2015-11-19 | 2022-05-11 | 美商英塞特公司 | 作為免疫調節劑之雜環化合物 |
| TW201726623A (zh) | 2015-12-17 | 2017-08-01 | 英塞特公司 | 作為免疫調節劑之雜環化合物 |
| WO2017107052A1 (en) | 2015-12-22 | 2017-06-29 | Merck Sharp & Dohme Corp. | Soluble guanylate cyclase stimulators |
| WO2017108569A1 (en) | 2015-12-22 | 2017-06-29 | Syngenta Participations Ag | Pesticidally active pyrazole derivatives |
| MA55194A (fr) | 2015-12-22 | 2022-05-04 | Incyte Corp | Composés hétérocycliques en tant qu'immunomodulateurs |
| MX2018007704A (es) | 2015-12-22 | 2018-11-09 | Synthon Bv | Composicion farmaceutica que comprende lenalidomida amorfa y un antioxidante. |
| SG10202111399YA (en) | 2015-12-22 | 2021-11-29 | Immatics Biotechnologies Gmbh | Peptides and combination of peptides for use in immunotherapy against breast cancer and other cancers |
| KR101653560B1 (ko) | 2016-02-02 | 2016-09-12 | 한국화학연구원 | 신규한 화합물 또는 이의 약학적으로 허용가능한 염, 및 이를 유효성분으로 함유하는 인플루엔자 바이러스 감염으로 인한 질환의 예방 또는 치료용 약학적 조성물 |
| WO2017184934A1 (en) | 2016-04-22 | 2017-10-26 | Incyte Corporation | Formulations of an lsd1 inhibitor |
| WO2017192961A1 (en) | 2016-05-06 | 2017-11-09 | Incyte Corporation | Heterocyclic compounds as immunomodulators |
| MA45116A (fr) | 2016-05-26 | 2021-06-02 | Incyte Corp | Composés hétérocycliques comme immunomodulateurs |
| UA125391C2 (uk) | 2016-06-20 | 2022-03-02 | Інсайт Корпорейшн | Гетероциклічні сполуки як імуномодулятори |
| NZ749962A (en) | 2016-06-20 | 2020-06-26 | Elanco Us Inc | Pegylated porcine interferon and methods of use thereof |
| US11091489B2 (en) | 2016-06-20 | 2021-08-17 | Novartis Ag | Crystalline forms of a triazolopyrimidine compound |
| EP3808748A1 (en) | 2016-06-21 | 2021-04-21 | X4 Pharmaceuticals, Inc. | Substituted piperidines as cxcr4-inhibitors |
| US20180016260A1 (en) | 2016-07-14 | 2018-01-18 | Incyte Corporation | Heterocyclic compounds as immunomodulators |
| JP2019530732A (ja) | 2016-08-03 | 2019-10-24 | アライジング・インターナショナル・インコーポレイテッドArising International, Inc. | 免疫モジュレータとして有用な対称または半対称化合物 |
| MA46045A (fr) | 2016-08-29 | 2021-04-28 | Incyte Corp | Composés hétérocycliques utilisés comme immunomodulateurs |
| AU2017319513B2 (en) | 2016-08-30 | 2022-05-19 | Tetraphase Pharmaceuticals, Inc. | Tetracycline compounds and methods of treatment |
| TWI795381B (zh) | 2016-12-21 | 2023-03-11 | 比利時商健生藥品公司 | 作為malt1抑制劑之吡唑衍生物 |
| ES2856248T3 (es) | 2016-12-21 | 2021-09-27 | Acerta Pharma Bv | Inhibidores de imidazopirazina de la tirosina quinasa de Bruton |
| WO2018119236A1 (en) | 2016-12-22 | 2018-06-28 | Incyte Corporation | Triazolo[1,5-a]pyridine derivatives as immunomodulators |
| AU2017382405B2 (en) | 2016-12-22 | 2021-12-16 | Calithera Biosciences, Inc. | Compositions and methods for inhibiting arginase activity |
| US20180179179A1 (en) | 2016-12-22 | 2018-06-28 | Incyte Corporation | Heterocyclic compounds as immunomodulators |
| EP3558963B1 (en) | 2016-12-22 | 2022-03-23 | Incyte Corporation | Bicyclic heteroaromatic compounds as immunomodulators |
| ES2934230T3 (es) | 2016-12-22 | 2023-02-20 | Incyte Corp | Derivados de benzooxazol como inmunomoduladores |
| US20180177784A1 (en) | 2016-12-22 | 2018-06-28 | Incyte Corporation | Heterocyclic compounds as immunomodulators |
| HRP20221216T1 (hr) | 2016-12-22 | 2022-12-23 | Incyte Corporation | Derivati tetrahidro imidazo[4,5-c]piridina kao induktori internalizacije pd-l1 |
| JOP20180040A1 (ar) | 2017-04-20 | 2019-01-30 | Gilead Sciences Inc | مثبطات pd-1/pd-l1 |
| US10919852B2 (en) | 2017-07-28 | 2021-02-16 | Chemocentryx, Inc. | Immunomodulator compounds |
| MA49859A (fr) | 2017-08-08 | 2021-04-07 | Chemocentryx Inc | Immunomodulateurs macrocycliques |
| WO2019034172A1 (zh) | 2017-08-18 | 2019-02-21 | 上海轶诺药业有限公司 | 一种具有pd-l1抑制活性的化合物、其制备方法及用途 |
| PE20211911A1 (es) | 2018-03-30 | 2021-09-28 | Incyte Corp | Compuestos heterociclicos como inmunomoduladores |
| WO2019192506A1 (en) | 2018-04-03 | 2019-10-10 | Betta Pharmaceuticals Co., Ltd | Immunomodulators, compositions and methods thereof |
| CA3093130C (en) | 2018-04-19 | 2023-10-17 | Gilead Sciences, Inc. | Pd-1/pd-l1 inhibitors |
| MD3790877T2 (ro) | 2018-05-11 | 2023-08-31 | Incyte Corp | Derivați de tetrahidro-imidazo[4,5-c]piridină în calitate de imunomodulatori PD-L1 |
| WO2020086556A1 (en) | 2018-10-24 | 2020-04-30 | Gilead Sciences, Inc. | Pd-1/pd-l1 inhibitors |
| JP2022513592A (ja) | 2018-11-02 | 2022-02-09 | シャンハイ マキシノベル ファーマシューティカルズ カンパニー リミテッド | ビフェニル系化合物、その中間体、製造方法、医薬組成物及び使用 |
| MX2021009246A (es) | 2019-01-31 | 2021-09-08 | Betta Pharmaceuticals Co Ltd | Inmunomoduladores, composiciones y metodos de los mismos. |
| WO2021030162A1 (en) | 2019-08-09 | 2021-02-18 | Incyte Corporation | Salts of a pd-1/pd-l1 inhibitor |
| KR20220075382A (ko) | 2019-09-30 | 2022-06-08 | 인사이트 코포레이션 | 면역조절제로서의 피리도[3,2-d]피리미딘 화합물 |
| AU2020385113A1 (en) | 2019-11-11 | 2022-05-19 | Incyte Corporation | Salts and crystalline forms of a PD-1/PD-L1 inhibitor |
| CA3200844A1 (en) | 2020-11-06 | 2022-05-12 | Incyte Corporation | Process for making a pd-1/pd-l1 inhibitor and salts and crystalline forms thereof |
| US11780836B2 (en) | 2020-11-06 | 2023-10-10 | Incyte Corporation | Process of preparing a PD-1/PD-L1 inhibitor |
| US11760756B2 (en) | 2020-11-06 | 2023-09-19 | Incyte Corporation | Crystalline form of a PD-1/PD-L1 inhibitor |
| TW202241420A (zh) | 2020-12-18 | 2022-11-01 | 美商英塞特公司 | Pd-l1抑制劑之口服調配物 |
-
2017
- 2017-08-28 MA MA046045A patent/MA46045A/fr unknown
- 2017-08-28 WO PCT/US2017/048880 patent/WO2018044783A1/en unknown
- 2017-08-28 ES ES17761781T patent/ES2941716T3/es active Active
- 2017-08-28 EP EP17761781.8A patent/EP3504198B1/en active Active
- 2017-08-28 US US15/687,697 patent/US20180057486A1/en not_active Abandoned
-
2020
- 2020-02-04 US US16/781,920 patent/US20200172533A1/en not_active Abandoned
-
2021
- 2021-05-04 US US17/307,547 patent/US11613536B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| US20200172533A1 (en) | 2020-06-04 |
| EP3504198B1 (en) | 2023-01-25 |
| US11613536B2 (en) | 2023-03-28 |
| EP3504198A1 (en) | 2019-07-03 |
| WO2018044783A1 (en) | 2018-03-08 |
| US20220089588A1 (en) | 2022-03-24 |
| MA46045A (fr) | 2021-04-28 |
| US20180057486A1 (en) | 2018-03-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2941716T3 (es) | Compuestos heterocíclicos como inmunomoduladores | |
| ES2930092T3 (es) | Compuestos heterocíclicos como inmunomoduladores | |
| ES2874756T3 (es) | Derivados de triazolo[1,5-A]piridina como inmunomoduladores | |
| ES2899402T3 (es) | Derivados de piridina como inmunomoduladores | |
| ES2905980T3 (es) | Compuestos heterocíclicos como inmunomoduladores | |
| ES2916874T3 (es) | Derivados de N-fenil-piridina-2-carboxamida y su uso como moduladores de la interacción proteína/proteína PD-1/PD-L1 | |
| ES2943028T3 (es) | Derivados de tetrahidro-imidazo[4,5-c]piridina como inmunomoduladores de PD-L1 | |
| ES2906460T3 (es) | Compuestos heterocíclicos como inmunomoduladores | |
| ES2918974T3 (es) | Compuestos heteroaromaticos biciclicos como inmunomoduladores | |
| ES2928856T3 (es) | Compuestos heterocíclicos como inmunomoduladores | |
| ES2844374T3 (es) | Compuestos heterocíclicos como inmunomoduladores | |
| ES2928164T3 (es) | Compuestos heterocíclicos como inmunomoduladores | |
| AU2021250978B2 (en) | Heterocyclic compounds as immunomodulators | |
| ES2940750T3 (es) | Compuestos heterocíclicos como inmunomoduladores | |
| ES2929193T3 (es) | Derivados de tetrahidro imidazo[4,5-c]piridina como inductores de la internalización de PD-L1 | |
| WO2018119263A1 (en) | Heterocyclic compounds derivatives as pd-l1 internalization inducers |