DE10304819A1 - Carbazol-enthaltende konjugierte Polymere und Blends, deren Darstellung und Verwendung - Google Patents
Carbazol-enthaltende konjugierte Polymere und Blends, deren Darstellung und Verwendung Download PDFInfo
- Publication number
- DE10304819A1 DE10304819A1 DE10304819A DE10304819A DE10304819A1 DE 10304819 A1 DE10304819 A1 DE 10304819A1 DE 10304819 A DE10304819 A DE 10304819A DE 10304819 A DE10304819 A DE 10304819A DE 10304819 A1 DE10304819 A1 DE 10304819A1
- Authority
- DE
- Germany
- Prior art keywords
- atoms
- replaced
- substituted
- different
- chain
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
- UJOBWOGCFQCDNV-UHFFFAOYSA-N 9H-carbazole Chemical compound C1=CC=C2C3=CC=CC=C3NC2=C1 UJOBWOGCFQCDNV-UHFFFAOYSA-N 0.000 title claims abstract description 40
- 229920000547 conjugated polymer Polymers 0.000 title claims abstract description 18
- 239000000203 mixture Substances 0.000 title claims description 82
- 229920000642 polymer Polymers 0.000 claims abstract description 169
- 239000000463 material Substances 0.000 claims abstract description 13
- 125000004432 carbon atom Chemical group C* 0.000 claims description 100
- 125000003118 aryl group Chemical group 0.000 claims description 76
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 claims description 51
- 229910052760 oxygen Inorganic materials 0.000 claims description 36
- 229910052717 sulfur Inorganic materials 0.000 claims description 34
- -1 aromatic radicals Chemical class 0.000 claims description 32
- 125000001424 substituent group Chemical group 0.000 claims description 32
- 239000000243 solution Substances 0.000 claims description 31
- 229910052731 fluorine Inorganic materials 0.000 claims description 29
- 238000000034 method Methods 0.000 claims description 28
- 229910052757 nitrogen Inorganic materials 0.000 claims description 28
- 239000002904 solvent Substances 0.000 claims description 28
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 claims description 24
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 claims description 17
- 239000011737 fluorine Substances 0.000 claims description 17
- UFWIBTONFRDIAS-UHFFFAOYSA-N Naphthalene Chemical compound C1=CC=CC2=CC=CC=C21 UFWIBTONFRDIAS-UHFFFAOYSA-N 0.000 claims description 16
- YTPLMLYBLZKORZ-UHFFFAOYSA-N Thiophene Chemical compound C=1C=CSC=1 YTPLMLYBLZKORZ-UHFFFAOYSA-N 0.000 claims description 16
- MWPLVEDNUUSJAV-UHFFFAOYSA-N anthracene Chemical compound C1=CC=CC2=CC3=CC=CC=C3C=C21 MWPLVEDNUUSJAV-UHFFFAOYSA-N 0.000 claims description 16
- YNPNZTXNASCQKK-UHFFFAOYSA-N phenanthrene Chemical compound C1=CC=C2C3=CC=CC=C3C=CC2=C1 YNPNZTXNASCQKK-UHFFFAOYSA-N 0.000 claims description 16
- 125000003545 alkoxy group Chemical group 0.000 claims description 15
- RDOXTESZEPMUJZ-UHFFFAOYSA-N anisole Chemical compound COC1=CC=CC=C1 RDOXTESZEPMUJZ-UHFFFAOYSA-N 0.000 claims description 15
- 125000001072 heteroaryl group Chemical group 0.000 claims description 15
- 230000008569 process Effects 0.000 claims description 15
- FCEHBMOGCRZNNI-UHFFFAOYSA-N 1-benzothiophene Chemical compound C1=CC=C2SC=CC2=C1 FCEHBMOGCRZNNI-UHFFFAOYSA-N 0.000 claims description 14
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims description 14
- 229910052801 chlorine Inorganic materials 0.000 claims description 13
- 238000002347 injection Methods 0.000 claims description 13
- 239000007924 injection Substances 0.000 claims description 13
- 125000004104 aryloxy group Chemical group 0.000 claims description 12
- 239000000412 dendrimer Substances 0.000 claims description 12
- 229920000736 dendritic polymer Polymers 0.000 claims description 12
- NIHNNTQXNPWCJQ-UHFFFAOYSA-N fluorene Chemical compound C1=CC=C2CC3=CC=CC=C3C2=C1 NIHNNTQXNPWCJQ-UHFFFAOYSA-N 0.000 claims description 11
- 229910052751 metal Inorganic materials 0.000 claims description 11
- 239000002184 metal Substances 0.000 claims description 11
- CTQNGGLPUBDAKN-UHFFFAOYSA-N O-Xylene Chemical compound CC1=CC=CC=C1C CTQNGGLPUBDAKN-UHFFFAOYSA-N 0.000 claims description 10
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 claims description 10
- BBEAQIROQSPTKN-UHFFFAOYSA-N pyrene Chemical compound C1=CC=C2C=CC3=CC=CC4=CC=C1C2=C43 BBEAQIROQSPTKN-UHFFFAOYSA-N 0.000 claims description 10
- 238000006467 substitution reaction Methods 0.000 claims description 10
- 150000003254 radicals Chemical class 0.000 claims description 9
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 claims description 8
- 125000000217 alkyl group Chemical group 0.000 claims description 8
- 125000004122 cyclic group Chemical group 0.000 claims description 8
- 229930192474 thiophene Natural products 0.000 claims description 8
- 229910052723 transition metal Inorganic materials 0.000 claims description 8
- 239000008096 xylene Substances 0.000 claims description 8
- 239000002243 precursor Substances 0.000 claims description 7
- 238000012546 transfer Methods 0.000 claims description 7
- 125000005275 alkylenearyl group Chemical group 0.000 claims description 6
- UZKWTJUDCOPSNM-UHFFFAOYSA-N methoxybenzene Substances CCCCOC=C UZKWTJUDCOPSNM-UHFFFAOYSA-N 0.000 claims description 6
- 238000006619 Stille reaction Methods 0.000 claims description 5
- 230000021615 conjugation Effects 0.000 claims description 5
- GVEPBJHOBDJJJI-UHFFFAOYSA-N fluoranthrene Natural products C1=CC(C2=CC=CC=C22)=C3C2=CC=CC3=C1 GVEPBJHOBDJJJI-UHFFFAOYSA-N 0.000 claims description 5
- 125000002524 organometallic group Chemical group 0.000 claims description 5
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 claims description 5
- ICPSWZFVWAPUKF-UHFFFAOYSA-N 1,1'-spirobi[fluorene] Chemical compound C1=CC=C2C=C3C4(C=5C(C6=CC=CC=C6C=5)=CC=C4)C=CC=C3C2=C1 ICPSWZFVWAPUKF-UHFFFAOYSA-N 0.000 claims description 4
- DTFKRVXLBCAIOZ-UHFFFAOYSA-N 2-methylanisole Chemical compound COC1=CC=CC=C1C DTFKRVXLBCAIOZ-UHFFFAOYSA-N 0.000 claims description 4
- 125000005218 alkyleneheteroaryl group Chemical group 0.000 claims description 4
- 230000008859 change Effects 0.000 claims description 4
- 125000006165 cyclic alkyl group Chemical group 0.000 claims description 4
- 125000000753 cycloalkyl group Chemical group 0.000 claims description 4
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims description 4
- 125000004958 1,4-naphthylene group Chemical group 0.000 claims description 3
- SNFCXVRWFNAHQX-UHFFFAOYSA-N 9,9'-spirobi[fluorene] Chemical compound C12=CC=CC=C2C2=CC=CC=C2C21C1=CC=CC=C1C1=CC=CC=C21 SNFCXVRWFNAHQX-UHFFFAOYSA-N 0.000 claims description 3
- 238000006546 Horner-Wadsworth-Emmons reaction Methods 0.000 claims description 3
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 claims description 3
- 230000005669 field effect Effects 0.000 claims description 3
- 239000010408 film Substances 0.000 claims description 3
- PJULCNAVAGQLAT-UHFFFAOYSA-N indeno[2,1-a]fluorene Chemical compound C1=CC=C2C=C3C4=CC5=CC=CC=C5C4=CC=C3C2=C1 PJULCNAVAGQLAT-UHFFFAOYSA-N 0.000 claims description 3
- 125000005731 2,5-thiophenylene group Chemical group [H]C1=C([*:1])SC([*:2])=C1[H] 0.000 claims description 2
- 125000000732 arylene group Chemical group 0.000 claims description 2
- 150000001846 chrysenes Chemical class 0.000 claims description 2
- 150000001882 coronenes Chemical class 0.000 claims description 2
- 150000002739 metals Chemical class 0.000 claims description 2
- 150000002964 pentacenes Chemical class 0.000 claims description 2
- 150000002979 perylenes Chemical class 0.000 claims description 2
- 150000003518 tetracenes Chemical class 0.000 claims description 2
- 239000010409 thin film Substances 0.000 claims description 2
- 125000005259 triarylamine group Chemical group 0.000 claims description 2
- SMWDFEZZVXVKRB-UHFFFAOYSA-N Quinoline Chemical compound N1=CC=CC2=CC=CC=C21 SMWDFEZZVXVKRB-UHFFFAOYSA-N 0.000 claims 2
- 125000005565 oxadiazolylene group Chemical group 0.000 claims 2
- 150000003624 transition metals Chemical class 0.000 claims 2
- 238000006069 Suzuki reaction reaction Methods 0.000 claims 1
- 230000008878 coupling Effects 0.000 claims 1
- 238000010168 coupling process Methods 0.000 claims 1
- 238000005859 coupling reaction Methods 0.000 claims 1
- 150000002220 fluorenes Chemical class 0.000 claims 1
- 239000000178 monomer Substances 0.000 description 35
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 20
- 238000006243 chemical reaction Methods 0.000 description 14
- 238000003786 synthesis reaction Methods 0.000 description 14
- KDLHZDBZIXYQEI-UHFFFAOYSA-N palladium Substances [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 13
- QPTWWBLGJZWRAV-UHFFFAOYSA-N 2,7-dibromo-9h-carbazole Chemical compound BrC1=CC=C2C3=CC=C(Br)C=C3NC2=C1 QPTWWBLGJZWRAV-UHFFFAOYSA-N 0.000 description 12
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 12
- 230000008901 benefit Effects 0.000 description 12
- 150000001875 compounds Chemical class 0.000 description 12
- 238000006116 polymerization reaction Methods 0.000 description 12
- 230000015572 biosynthetic process Effects 0.000 description 11
- 239000000460 chlorine Substances 0.000 description 11
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 11
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 10
- 150000003384 small molecules Chemical class 0.000 description 10
- 230000006872 improvement Effects 0.000 description 9
- 239000000047 product Substances 0.000 description 9
- 238000005160 1H NMR spectroscopy Methods 0.000 description 8
- FIHILUSWISKVSR-UHFFFAOYSA-N 3,6-Br2Car Natural products C1=C(Br)C=C2C3=CC(Br)=CC=C3NC2=C1 FIHILUSWISKVSR-UHFFFAOYSA-N 0.000 description 8
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 8
- 229920001577 copolymer Polymers 0.000 description 8
- MVPPADPHJFYWMZ-UHFFFAOYSA-N chlorobenzene Chemical compound ClC1=CC=CC=C1 MVPPADPHJFYWMZ-UHFFFAOYSA-N 0.000 description 7
- 238000004128 high performance liquid chromatography Methods 0.000 description 7
- 229910052741 iridium Inorganic materials 0.000 description 7
- 239000012074 organic phase Substances 0.000 description 7
- 229910052763 palladium Inorganic materials 0.000 description 7
- QPUYECUOLPXSFR-UHFFFAOYSA-N 1-methylnaphthalene Chemical compound C1=CC=C2C(C)=CC=CC2=C1 QPUYECUOLPXSFR-UHFFFAOYSA-N 0.000 description 6
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 6
- 239000002253 acid Substances 0.000 description 6
- 239000003086 colorant Substances 0.000 description 6
- 229920002521 macromolecule Polymers 0.000 description 6
- 229920002098 polyfluorene Polymers 0.000 description 6
- 238000010992 reflux Methods 0.000 description 6
- 210000002023 somite Anatomy 0.000 description 6
- 238000003756 stirring Methods 0.000 description 6
- RICKKZXCGCSLIU-UHFFFAOYSA-N 2-[2-[carboxymethyl-[[3-hydroxy-5-(hydroxymethyl)-2-methylpyridin-4-yl]methyl]amino]ethyl-[[3-hydroxy-5-(hydroxymethyl)-2-methylpyridin-4-yl]methyl]amino]acetic acid Chemical compound CC1=NC=C(CO)C(CN(CCN(CC(O)=O)CC=2C(=C(C)N=CC=2CO)O)CC(O)=O)=C1O RICKKZXCGCSLIU-UHFFFAOYSA-N 0.000 description 5
- 229910052786 argon Inorganic materials 0.000 description 5
- 125000004429 atom Chemical group 0.000 description 5
- 125000000609 carbazolyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3NC12)* 0.000 description 5
- 238000001816 cooling Methods 0.000 description 5
- 239000011521 glass Substances 0.000 description 5
- 229910052736 halogen Inorganic materials 0.000 description 5
- 150000002367 halogens Chemical class 0.000 description 5
- 229910052749 magnesium Inorganic materials 0.000 description 5
- 239000011777 magnesium Substances 0.000 description 5
- 238000004519 manufacturing process Methods 0.000 description 5
- 125000004433 nitrogen atom Chemical group N* 0.000 description 5
- 239000000758 substrate Substances 0.000 description 5
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 4
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 4
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 4
- 229920000265 Polyparaphenylene Polymers 0.000 description 4
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 4
- 229910052794 bromium Inorganic materials 0.000 description 4
- QARVLSVVCXYDNA-UHFFFAOYSA-N bromobenzene Chemical compound BrC1=CC=CC=C1 QARVLSVVCXYDNA-UHFFFAOYSA-N 0.000 description 4
- 238000005265 energy consumption Methods 0.000 description 4
- 125000003983 fluorenyl group Chemical class C1(=CC=CC=2C3=CC=CC=C3CC12)* 0.000 description 4
- 239000007789 gas Substances 0.000 description 4
- 150000004820 halides Chemical class 0.000 description 4
- 125000000623 heterocyclic group Chemical group 0.000 description 4
- 229910052744 lithium Inorganic materials 0.000 description 4
- HXITXNWTGFUOAU-UHFFFAOYSA-N phenylboronic acid Chemical compound OB(O)C1=CC=CC=C1 HXITXNWTGFUOAU-UHFFFAOYSA-N 0.000 description 4
- 230000001681 protective effect Effects 0.000 description 4
- XSCHRSMBECNVNS-UHFFFAOYSA-N quinoxaline Chemical compound N1=CC=NC2=CC=CC=C21 XSCHRSMBECNVNS-UHFFFAOYSA-N 0.000 description 4
- 239000011541 reaction mixture Substances 0.000 description 4
- 229910052703 rhodium Inorganic materials 0.000 description 4
- 239000011877 solvent mixture Substances 0.000 description 4
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 4
- 241001136792 Alle Species 0.000 description 3
- 238000003089 Pariser Parr Pople method Methods 0.000 description 3
- 229920001609 Poly(3,4-ethylenedioxythiophene) Polymers 0.000 description 3
- 150000001408 amides Chemical class 0.000 description 3
- 239000003054 catalyst Substances 0.000 description 3
- 230000000052 comparative effect Effects 0.000 description 3
- 150000004696 coordination complex Chemical class 0.000 description 3
- 210000001035 gastrointestinal tract Anatomy 0.000 description 3
- 238000010348 incorporation Methods 0.000 description 3
- 239000000543 intermediate Substances 0.000 description 3
- 150000002500 ions Chemical class 0.000 description 3
- GKOZUEZYRPOHIO-UHFFFAOYSA-N iridium atom Chemical compound [Ir] GKOZUEZYRPOHIO-UHFFFAOYSA-N 0.000 description 3
- 229910052762 osmium Inorganic materials 0.000 description 3
- 229910052697 platinum Inorganic materials 0.000 description 3
- 238000001953 recrystallisation Methods 0.000 description 3
- 229910052707 ruthenium Inorganic materials 0.000 description 3
- 229920006395 saturated elastomer Polymers 0.000 description 3
- 239000000126 substance Substances 0.000 description 3
- DWLZULQNIPIABE-UHFFFAOYSA-N 1-ethyl-3-methoxybenzene Chemical compound CCC1=CC=CC(OC)=C1 DWLZULQNIPIABE-UHFFFAOYSA-N 0.000 description 2
- HDCPQTBWYINLEL-UHFFFAOYSA-N 2,3,5,6-tetraphenylbenzene-1,4-diamine Chemical compound C=1C=CC=CC=1C1=C(N)C(C=2C=CC=CC=2)=C(C=2C=CC=CC=2)C(N)=C1C1=CC=CC=C1 HDCPQTBWYINLEL-UHFFFAOYSA-N 0.000 description 2
- VAEJRLCFEWHJDX-UHFFFAOYSA-N 2,7-dibromo-9-(4-tert-butylphenyl)-1-methylcarbazole Chemical compound Cc1c(Br)ccc2c3ccc(Br)cc3n(-c3ccc(cc3)C(C)(C)C)c12 VAEJRLCFEWHJDX-UHFFFAOYSA-N 0.000 description 2
- IRTCJFCIQKNFPP-UHFFFAOYSA-N 2-methyl-1,4-dioxane Chemical compound CC1COCCO1 IRTCJFCIQKNFPP-UHFFFAOYSA-N 0.000 description 2
- DSNQPNGWFBNTQE-UHFFFAOYSA-N 4-(4-aminophenyl)-2,3,5,6-tetraphenylaniline Chemical group C1=CC(N)=CC=C1C(C(=C(C=1C=CC=CC=1)C(N)=C1C=2C=CC=CC=2)C=2C=CC=CC=2)=C1C1=CC=CC=C1 DSNQPNGWFBNTQE-UHFFFAOYSA-N 0.000 description 2
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 2
- 229940122361 Bisphosphonate Drugs 0.000 description 2
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 2
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 2
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 2
- 241001295925 Gegenes Species 0.000 description 2
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 2
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 2
- 125000002947 alkylene group Chemical group 0.000 description 2
- UNKKIEMUNUHYPD-UHFFFAOYSA-K aluminum 2-carboxy-5-hydroxy-4-oxo-1H-quinolin-3-olate Chemical compound [Al+3].[O-]C(=O)C1=C(O)C(O)=C2C(O)=CC=CC2=N1.[O-]C(=O)C1=C(O)C(O)=C2C(O)=CC=CC2=N1.[O-]C(=O)C1=C(O)C(O)=C2C(O)=CC=CC2=N1 UNKKIEMUNUHYPD-UHFFFAOYSA-K 0.000 description 2
- 150000004663 bisphosphonates Chemical class 0.000 description 2
- 230000031709 bromination Effects 0.000 description 2
- 238000005893 bromination reaction Methods 0.000 description 2
- 229910052791 calcium Inorganic materials 0.000 description 2
- 238000006555 catalytic reaction Methods 0.000 description 2
- 238000000576 coating method Methods 0.000 description 2
- 229920001940 conductive polymer Polymers 0.000 description 2
- 239000004020 conductor Substances 0.000 description 2
- JHIVVAPYMSGYDF-UHFFFAOYSA-N cyclohexanone Chemical compound O=C1CCCCC1 JHIVVAPYMSGYDF-UHFFFAOYSA-N 0.000 description 2
- 238000011161 development Methods 0.000 description 2
- 230000018109 developmental process Effects 0.000 description 2
- 239000006185 dispersion Substances 0.000 description 2
- 230000000694 effects Effects 0.000 description 2
- 238000001914 filtration Methods 0.000 description 2
- 238000010438 heat treatment Methods 0.000 description 2
- 125000005842 heteroatom Chemical group 0.000 description 2
- 229920006158 high molecular weight polymer Polymers 0.000 description 2
- 229920001519 homopolymer Polymers 0.000 description 2
- 239000012535 impurity Substances 0.000 description 2
- AMGQUBHHOARCQH-UHFFFAOYSA-N indium;oxotin Chemical compound [In].[Sn]=O AMGQUBHHOARCQH-UHFFFAOYSA-N 0.000 description 2
- 238000009434 installation Methods 0.000 description 2
- PNDPGZBMCMUPRI-UHFFFAOYSA-N iodine Chemical compound II PNDPGZBMCMUPRI-UHFFFAOYSA-N 0.000 description 2
- 229910052740 iodine Inorganic materials 0.000 description 2
- 239000011630 iodine Substances 0.000 description 2
- 229920000267 ladder-type polyparaphenylene Polymers 0.000 description 2
- 239000003446 ligand Substances 0.000 description 2
- 239000007788 liquid Substances 0.000 description 2
- 125000003261 o-tolyl group Chemical group [H]C1=C([H])C(*)=C(C([H])=C1[H])C([H])([H])[H] 0.000 description 2
- 239000003960 organic solvent Substances 0.000 description 2
- 230000003647 oxidation Effects 0.000 description 2
- 238000007254 oxidation reaction Methods 0.000 description 2
- 239000001301 oxygen Substances 0.000 description 2
- 230000000737 periodic effect Effects 0.000 description 2
- 239000012071 phase Substances 0.000 description 2
- 125000000843 phenylene group Chemical group C1(=C(C=CC=C1)*)* 0.000 description 2
- 229920003227 poly(N-vinyl carbazole) Polymers 0.000 description 2
- 229920000767 polyaniline Polymers 0.000 description 2
- 229920000139 polyethylene terephthalate Polymers 0.000 description 2
- 229920000123 polythiophene Polymers 0.000 description 2
- 238000000746 purification Methods 0.000 description 2
- MNWBNISUBARLIT-UHFFFAOYSA-N sodium cyanide Chemical compound [Na+].N#[C-] MNWBNISUBARLIT-UHFFFAOYSA-N 0.000 description 2
- ODHXBMXNKOYIBV-UHFFFAOYSA-N triphenylamine Chemical compound C1=CC=CC=C1N(C=1C=CC=CC=1)C1=CC=CC=C1 ODHXBMXNKOYIBV-UHFFFAOYSA-N 0.000 description 2
- RMNIZOOYFMNEJJ-UHFFFAOYSA-K tripotassium;phosphate;hydrate Chemical compound O.[K+].[K+].[K+].[O-]P([O-])([O-])=O RMNIZOOYFMNEJJ-UHFFFAOYSA-K 0.000 description 2
- QZNQSIHCDAGZIA-UHFFFAOYSA-N 1-(bromomethyl)-4-tert-butylbenzene Chemical compound CC(C)(C)C1=CC=C(CBr)C=C1 QZNQSIHCDAGZIA-UHFFFAOYSA-N 0.000 description 1
- XHCAGOVGSDHHNP-UHFFFAOYSA-N 1-bromo-4-tert-butylbenzene Chemical compound CC(C)(C)C1=CC=C(Br)C=C1 XHCAGOVGSDHHNP-UHFFFAOYSA-N 0.000 description 1
- WQVIVQDHNKQWTM-UHFFFAOYSA-N 1-tert-butyl-4-iodobenzene Chemical compound CC(C)(C)C1=CC=C(I)C=C1 WQVIVQDHNKQWTM-UHFFFAOYSA-N 0.000 description 1
- NPNOAVKACBFSEB-UHFFFAOYSA-N 2,7-dibromo-9-(4-tert-butylphenyl)carbazole Chemical compound C1=CC(C(C)(C)C)=CC=C1N1C2=CC(Br)=CC=C2C2=CC=C(Br)C=C21 NPNOAVKACBFSEB-UHFFFAOYSA-N 0.000 description 1
- JIWBCHGVZITSFJ-UHFFFAOYSA-N 3,6-dibromo-9-(4-tert-butylphenyl)carbazole Chemical compound C1=CC(C(C)(C)C)=CC=C1N1C2=CC=C(Br)C=C2C2=CC(Br)=CC=C21 JIWBCHGVZITSFJ-UHFFFAOYSA-N 0.000 description 1
- UUOSGUHCBIZSGB-UHFFFAOYSA-N 3,6-dibromo-9-[(4-tert-butylphenyl)methyl]carbazole Chemical compound C1=CC(C(C)(C)C)=CC=C1CN1C2=CC=C(Br)C=C2C2=CC(Br)=CC=C21 UUOSGUHCBIZSGB-UHFFFAOYSA-N 0.000 description 1
- 125000004800 4-bromophenyl group Chemical group [H]C1=C([H])C(*)=C([H])C([H])=C1Br 0.000 description 1
- WCKADLRYWIXOEW-UHFFFAOYSA-N 9-(4-tert-butylphenyl)carbazole Chemical compound C1=CC(C(C)(C)C)=CC=C1N1C2=CC=CC=C2C2=CC=CC=C21 WCKADLRYWIXOEW-UHFFFAOYSA-N 0.000 description 1
- AAJBJZJJLKVJBA-UHFFFAOYSA-N 9-(4-tert-butylphenyl)carbazole-3,6-dicarbaldehyde Chemical compound C1=CC(C(C)(C)C)=CC=C1N1C2=CC=C(C=O)C=C2C2=CC(C=O)=CC=C21 AAJBJZJJLKVJBA-UHFFFAOYSA-N 0.000 description 1
- GZSUIHUAFPHZSU-UHFFFAOYSA-N 9-ethyl-2,3-dihydro-1h-carbazol-4-one Chemical compound C12=CC=CC=C2N(CC)C2=C1C(=O)CCC2 GZSUIHUAFPHZSU-UHFFFAOYSA-N 0.000 description 1
- 229920002799 BoPET Polymers 0.000 description 1
- 229910021591 Copper(I) chloride Inorganic materials 0.000 description 1
- MYMOFIZGZYHOMD-UHFFFAOYSA-N Dioxygen Chemical compound O=O MYMOFIZGZYHOMD-UHFFFAOYSA-N 0.000 description 1
- MZRVEZGGRBJDDB-UHFFFAOYSA-N N-Butyllithium Chemical compound [Li]CCCC MZRVEZGGRBJDDB-UHFFFAOYSA-N 0.000 description 1
- 238000007126 N-alkylation reaction Methods 0.000 description 1
- CBENFWSGALASAD-UHFFFAOYSA-N Ozone Chemical compound [O-][O+]=O CBENFWSGALASAD-UHFFFAOYSA-N 0.000 description 1
- ABLZXFCXXLZCGV-UHFFFAOYSA-N Phosphorous acid Chemical class OP(O)=O ABLZXFCXXLZCGV-UHFFFAOYSA-N 0.000 description 1
- 229910052772 Samarium Inorganic materials 0.000 description 1
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 1
- DGEZNRSVGBDHLK-UHFFFAOYSA-N [1,10]phenanthroline Chemical compound C1=CN=C2C3=NC=CC=C3C=CC2=C1 DGEZNRSVGBDHLK-UHFFFAOYSA-N 0.000 description 1
- NPRDEIDCAUHOJU-UHFFFAOYSA-N [Pt].N1C(C=C2N=C(C=C3NC(=C4)C=C3)C=C2)=CC=C1C=C1C=CC4=N1 Chemical compound [Pt].N1C(C=C2N=C(C=C3NC(=C4)C=C3)C=C2)=CC=C1C=C1C=CC4=N1 NPRDEIDCAUHOJU-UHFFFAOYSA-N 0.000 description 1
- 150000007513 acids Chemical class 0.000 description 1
- 239000003513 alkali Substances 0.000 description 1
- 150000001336 alkenes Chemical group 0.000 description 1
- 239000002168 alkylating agent Substances 0.000 description 1
- 229940100198 alkylating agent Drugs 0.000 description 1
- 229910052782 aluminium Inorganic materials 0.000 description 1
- 239000004411 aluminium Substances 0.000 description 1
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 1
- 239000010405 anode material Substances 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 239000012300 argon atmosphere Substances 0.000 description 1
- 125000005264 aryl amine group Chemical group 0.000 description 1
- 125000001769 aryl amino group Chemical group 0.000 description 1
- 238000006254 arylation reaction Methods 0.000 description 1
- 239000012298 atmosphere Substances 0.000 description 1
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 1
- 239000002585 base Substances 0.000 description 1
- 229920005601 base polymer Polymers 0.000 description 1
- 238000005574 benzylation reaction Methods 0.000 description 1
- 230000000903 blocking effect Effects 0.000 description 1
- 150000001642 boronic acid derivatives Chemical class 0.000 description 1
- 150000001716 carbazoles Chemical class 0.000 description 1
- 239000000969 carrier Substances 0.000 description 1
- 230000003197 catalytic effect Effects 0.000 description 1
- 238000012512 characterization method Methods 0.000 description 1
- 238000006757 chemical reactions by type Methods 0.000 description 1
- 239000003638 chemical reducing agent Substances 0.000 description 1
- 125000004218 chloromethyl group Chemical group [H]C([H])(Cl)* 0.000 description 1
- 238000004140 cleaning Methods 0.000 description 1
- 239000011248 coating agent Substances 0.000 description 1
- 239000000356 contaminant Substances 0.000 description 1
- OXBLHERUFWYNTN-UHFFFAOYSA-M copper(I) chloride Chemical compound [Cu]Cl OXBLHERUFWYNTN-UHFFFAOYSA-M 0.000 description 1
- 150000004292 cyclic ethers Chemical class 0.000 description 1
- 230000007547 defect Effects 0.000 description 1
- 125000004986 diarylamino group Chemical group 0.000 description 1
- 238000009792 diffusion process Methods 0.000 description 1
- 238000001035 drying Methods 0.000 description 1
- 239000000428 dust Substances 0.000 description 1
- 230000005684 electric field Effects 0.000 description 1
- 238000005401 electroluminescence Methods 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 150000002148 esters Chemical class 0.000 description 1
- 238000001704 evaporation Methods 0.000 description 1
- 230000008020 evaporation Effects 0.000 description 1
- 230000007717 exclusion Effects 0.000 description 1
- 238000000605 extraction Methods 0.000 description 1
- 150000004675 formic acid derivatives Chemical class 0.000 description 1
- 238000007306 functionalization reaction Methods 0.000 description 1
- 239000007863 gel particle Substances 0.000 description 1
- 238000007646 gravure printing Methods 0.000 description 1
- 150000002366 halogen compounds Chemical class 0.000 description 1
- 150000002391 heterocyclic compounds Chemical class 0.000 description 1
- 238000004770 highest occupied molecular orbital Methods 0.000 description 1
- 239000005457 ice water Substances 0.000 description 1
- 150000003949 imides Chemical class 0.000 description 1
- 238000007641 inkjet printing Methods 0.000 description 1
- 150000002503 iridium Chemical class 0.000 description 1
- RTRAMYYYHJZWQK-UHFFFAOYSA-N iridium;2-phenylpyridine Chemical compound [Ir].C1=CC=CC=C1C1=CC=CC=N1 RTRAMYYYHJZWQK-UHFFFAOYSA-N 0.000 description 1
- 239000004973 liquid crystal related substance Substances 0.000 description 1
- 230000005923 long-lasting effect Effects 0.000 description 1
- 239000011159 matrix material Substances 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 1
- 239000013580 millipore water Substances 0.000 description 1
- 150000002816 nickel compounds Chemical class 0.000 description 1
- 238000007645 offset printing Methods 0.000 description 1
- 230000005693 optoelectronics Effects 0.000 description 1
- 229920000620 organic polymer Polymers 0.000 description 1
- 150000002902 organometallic compounds Chemical class 0.000 description 1
- WCPAKWJPBJAGKN-UHFFFAOYSA-N oxadiazole Chemical group C1=CON=N1 WCPAKWJPBJAGKN-UHFFFAOYSA-N 0.000 description 1
- 125000004430 oxygen atom Chemical group O* 0.000 description 1
- NRNFFDZCBYOZJY-UHFFFAOYSA-N p-quinodimethane Chemical compound C=C1C=CC(=C)C=C1 NRNFFDZCBYOZJY-UHFFFAOYSA-N 0.000 description 1
- LXNAVEXFUKBNMK-UHFFFAOYSA-N palladium(II) acetate Substances [Pd].CC(O)=O.CC(O)=O LXNAVEXFUKBNMK-UHFFFAOYSA-N 0.000 description 1
- YJVFFLUZDVXJQI-UHFFFAOYSA-L palladium(ii) acetate Chemical compound [Pd+2].CC([O-])=O.CC([O-])=O YJVFFLUZDVXJQI-UHFFFAOYSA-L 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- NFBAXHOPROOJAW-UHFFFAOYSA-N phenindione Chemical compound O=C1C2=CC=CC=C2C(=O)C1C1=CC=CC=C1 NFBAXHOPROOJAW-UHFFFAOYSA-N 0.000 description 1
- 238000007750 plasma spraying Methods 0.000 description 1
- 229920003023 plastic Polymers 0.000 description 1
- 239000004033 plastic Substances 0.000 description 1
- 238000006068 polycondensation reaction Methods 0.000 description 1
- 229920001690 polydopamine Polymers 0.000 description 1
- 229920006254 polymer film Polymers 0.000 description 1
- 230000000379 polymerizing effect Effects 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 239000002244 precipitate Substances 0.000 description 1
- 238000001556 precipitation Methods 0.000 description 1
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 1
- 238000007639 printing Methods 0.000 description 1
- 238000004886 process control Methods 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 150000003222 pyridines Chemical class 0.000 description 1
- 239000012429 reaction media Substances 0.000 description 1
- 230000009257 reactivity Effects 0.000 description 1
- 238000001226 reprecipitation Methods 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 230000000717 retained effect Effects 0.000 description 1
- 238000007650 screen-printing Methods 0.000 description 1
- 239000000741 silica gel Substances 0.000 description 1
- 229910002027 silica gel Inorganic materials 0.000 description 1
- 239000008149 soap solution Substances 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 239000007790 solid phase Substances 0.000 description 1
- 238000004544 sputter deposition Methods 0.000 description 1
- KXCAEQNNTZANTK-UHFFFAOYSA-N stannane Chemical class [SnH4] KXCAEQNNTZANTK-UHFFFAOYSA-N 0.000 description 1
- 229910052712 strontium Inorganic materials 0.000 description 1
- 150000003462 sulfoxides Chemical class 0.000 description 1
- 239000011593 sulfur Substances 0.000 description 1
- 125000004434 sulfur atom Chemical group 0.000 description 1
- ISIJQEHRDSCQIU-UHFFFAOYSA-N tert-butyl 2,7-diazaspiro[4.5]decane-7-carboxylate Chemical compound C1N(C(=O)OC(C)(C)C)CCCC11CNCC1 ISIJQEHRDSCQIU-UHFFFAOYSA-N 0.000 description 1
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 238000002207 thermal evaporation Methods 0.000 description 1
- TVIVIEFSHFOWTE-UHFFFAOYSA-K tri(quinolin-8-yloxy)alumane Chemical compound [Al+3].C1=CN=C2C([O-])=CC=CC2=C1.C1=CN=C2C([O-])=CC=CC2=C1.C1=CN=C2C([O-])=CC=CC2=C1 TVIVIEFSHFOWTE-UHFFFAOYSA-K 0.000 description 1
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 description 1
- 230000001960 triggered effect Effects 0.000 description 1
- 238000007740 vapor deposition Methods 0.000 description 1
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 1
- 150000003738 xylenes Chemical class 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G61/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
- C08G61/12—Macromolecular compounds containing atoms other than carbon in the main chain of the macromolecule
-
- H—ELECTRICITY
- H05—ELECTRIC TECHNIQUES NOT OTHERWISE PROVIDED FOR
- H05B—ELECTRIC HEATING; ELECTRIC LIGHT SOURCES NOT OTHERWISE PROVIDED FOR; CIRCUIT ARRANGEMENTS FOR ELECTRIC LIGHT SOURCES, IN GENERAL
- H05B33/00—Electroluminescent light sources
- H05B33/12—Light sources with substantially two-dimensional radiating surfaces
- H05B33/14—Light sources with substantially two-dimensional radiating surfaces characterised by the chemical or physical composition or the arrangement of the electroluminescent material, or by the simultaneous addition of the electroluminescent material in or onto the light source
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G61/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
- C08G61/12—Macromolecular compounds containing atoms other than carbon in the main chain of the macromolecule
- C08G61/122—Macromolecular compounds containing atoms other than carbon in the main chain of the macromolecule derived from five- or six-membered heterocyclic compounds, other than imides
- C08G61/123—Macromolecular compounds containing atoms other than carbon in the main chain of the macromolecule derived from five- or six-membered heterocyclic compounds, other than imides derived from five-membered heterocyclic compounds
- C08G61/124—Macromolecular compounds containing atoms other than carbon in the main chain of the macromolecule derived from five- or six-membered heterocyclic compounds, other than imides derived from five-membered heterocyclic compounds with a five-membered ring containing one nitrogen atom in the ring
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G83/00—Macromolecular compounds not provided for in groups C08G2/00 - C08G81/00
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08L—COMPOSITIONS OF MACROMOLECULAR COMPOUNDS
- C08L65/00—Compositions of macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain; Compositions of derivatives of such polymers
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09B—ORGANIC DYES OR CLOSELY-RELATED COMPOUNDS FOR PRODUCING DYES, e.g. PIGMENTS; MORDANTS; LAKES
- C09B69/00—Dyes not provided for by a single group of this subclass
- C09B69/10—Polymeric dyes; Reaction products of dyes with monomers or with macromolecular compounds
- C09B69/101—Polymeric dyes; Reaction products of dyes with monomers or with macromolecular compounds containing an anthracene dye
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09B—ORGANIC DYES OR CLOSELY-RELATED COMPOUNDS FOR PRODUCING DYES, e.g. PIGMENTS; MORDANTS; LAKES
- C09B69/00—Dyes not provided for by a single group of this subclass
- C09B69/10—Polymeric dyes; Reaction products of dyes with monomers or with macromolecular compounds
- C09B69/101—Polymeric dyes; Reaction products of dyes with monomers or with macromolecular compounds containing an anthracene dye
- C09B69/102—Polymeric dyes; Reaction products of dyes with monomers or with macromolecular compounds containing an anthracene dye containing a perylene dye
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09B—ORGANIC DYES OR CLOSELY-RELATED COMPOUNDS FOR PRODUCING DYES, e.g. PIGMENTS; MORDANTS; LAKES
- C09B69/00—Dyes not provided for by a single group of this subclass
- C09B69/10—Polymeric dyes; Reaction products of dyes with monomers or with macromolecular compounds
- C09B69/105—Polymeric dyes; Reaction products of dyes with monomers or with macromolecular compounds containing a methine or polymethine dye
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent, e.g. electroluminescent, chemiluminescent materials
- C09K11/06—Luminescent, e.g. electroluminescent, chemiluminescent materials containing organic luminescent materials
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/10—Organic polymers or oligomers
- H10K85/111—Organic polymers or oligomers comprising aromatic, heteroaromatic, or aryl chains, e.g. polyaniline, polyphenylene or polyphenylene vinylene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/10—Organic polymers or oligomers
- H10K85/151—Copolymers
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08L—COMPOSITIONS OF MACROMOLECULAR COMPOUNDS
- C08L101/00—Compositions of unspecified macromolecular compounds
- C08L101/005—Dendritic macromolecules
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/14—Macromolecular compounds
- C09K2211/1408—Carbocyclic compounds
- C09K2211/1416—Condensed systems
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/14—Macromolecular compounds
- C09K2211/1441—Heterocyclic
- C09K2211/1458—Heterocyclic containing sulfur as the only heteroatom
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/14—Macromolecular compounds
- C09K2211/1441—Heterocyclic
- C09K2211/1466—Heterocyclic containing nitrogen as the only heteroatom
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/14—Macromolecular compounds
- C09K2211/1441—Heterocyclic
- C09K2211/1475—Heterocyclic containing nitrogen and oxygen as heteroatoms
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/14—Macromolecular compounds
- C09K2211/1441—Heterocyclic
- C09K2211/1483—Heterocyclic containing nitrogen and sulfur as heteroatoms
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K2101/00—Properties of the organic materials covered by group H10K85/00
- H10K2101/10—Triplet emission
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/11—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/10—Organic polymers or oligomers
- H10K85/111—Organic polymers or oligomers comprising aromatic, heteroaromatic, or aryl chains, e.g. polyaniline, polyphenylene or polyphenylene vinylene
- H10K85/115—Polyfluorene; Derivatives thereof
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E10/00—Energy generation through renewable energy sources
- Y02E10/50—Photovoltaic [PV] energy
- Y02E10/549—Organic PV cells
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10S—TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10S428/00—Stock material or miscellaneous articles
- Y10S428/917—Electroluminescent
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Health & Medical Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Polyoxymethylene Polymers And Polymers With Carbon-To-Carbon Bonds (AREA)
- Electroluminescent Light Sources (AREA)
- Indole Compounds (AREA)
- Compositions Of Macromolecular Compounds (AREA)
Abstract
Die vorliegende Erfindung betrifft konjugierte Polymere, die spezielle Carbazol-Struktureinheiten enthalten. Die erfindungsgemäßen Materialien zeigen steilere Strom-Spannungs-Kurven und sind daher besser für den Einsatz in organischen Leuchtdioden geeignet als Vergleichspolymere, die diese Einheiten nicht enthalten.
Description
- Seit ca. 12 Jahren läuft eine breit angelegte Forschung zur Kommerzialisierung von Anzeige- und Beleuchtungselementen auf Basis polymerer (organischer) Leuchtdioden (PLEDs). Ausgelöst wurde diese Entwicklung durch die Grundlagenentwicklungen, welche in
EP 423 283 - Als Polymere für vollfarbige Anzeigeelemente (sog. Full-Colour-Displays) wurden bereits verschiedene Materialklassen vorgeschlagen bzw. entwickelt. So kommen Polyfluoren-Derivate, wie diese beispielsweise in
EP-A-0 842 208 , WO 99/54385, WO 00/22027, WO 00/22026 und WO 00/46321 offenbart werden, in Betracht. Des weiteren sind auch Poly-Spirobifluoren-Derivate, wie inEP-A-0 707 020 ,EP-A-0 894 107 und der nicht-offengelegten AnmeldeschriftDE 10143353 .0 offenbart, eine Möglichkeit. Auch Polymere, die eine Kombination der beiden erstgenannten Strukturelemente enthalten, wie in WO 02/077060 offenbart, wurden bereits vorgeschlagen. Im allgemeinen sind für derartigen Einsatz Polymere, welche Polypara-Phenylen (PPP) als Strukturelement enthalten, möglich. Neben den oben bereits genannten Klassen kommen hier beispielsweise auch die sogenannten Leiter-PPPs ("Ladder-PPPs" = LPPP) (z. B. gemäß WO 92/18552), die Poly- Tetrahydropyrene (z. B. gemäßEP-A-699699 EP-A-690086 - Wie in einigen der o. g. Anmeldeschriften bereits heraus gearbeitet wurde, ist es für die Erzeugung aller drei Emissionsfarben notwendig, bestimmte Comonomere in die entsprechenden Polymere einzupolymerisieren (vgl. z. B. WO 00/46321,
DE 10143353.0 und WO 02/077060). So ist dann i. d. R. – ausgehend von einem blau emittierenden Grundpolymer ("backbone") – die Erzeugung der beiden anderen Primärfarben Rot und Grün möglich. - Des weiteren wurde berichtet, dass das Einfügen bestimmter Aryl-amino-Gruppierungen eine Verbesserung der Eigenschaften ergibt:
- – WO 99/54385 beschreibt Polyfluorene, deren Effizienz und Einsatzspannung verbessert werden kann, indem Derivate von Triphenylamin, Tetraphenyl-p-diamino-benzol oder Tetraphenyl-4,4'-diamino-biphenyl in die Hauptkette der entsprechenden Polymere mit einpolymerisiert werden.
- –
DE-A-19846767 beschreibt Polyfluorene, bei denen ebenfalls die Effizienz und Einsatzspannung verbessert wird, indem substituierte Diarylamino-Einheiten in die Hauptkette eingebaut werden. - – WO 01/49769 beschreibt allgemein Polymere, welche Triarylamino-Gruppen enthalten, bei welchen mindestens eine der Arylgruppen eine Heteroarylgruppe darstellt. Besondere Vorteile dieser Polymere werden nicht beschrieben.
- – WO 01/66618 beschreibt Copolymere, welche neben Aryleinheiten auch spezielle Triarylamino- bzw. Tetraaryl-p-diamino-arylen-einheiten in der Hauptkette enthalten. Die entsprechenden Aminobausteine enthalten dabei jeweils mit Trifluormethylgruppen substituierte Phenyle, die direkt an die Stickstoffatome gebunden sind, allerdings nicht in die Hauptkette eingebaut werden. Als Vorteil wird erwähnt, dass diese Materialien – v. a. im Gegensatz zu den Derivaten, welche in der o. g. WO 99/54385 genannt werden – eine besser einstellbare HOMO-Lage besitzen und dies deshalb in der Anwendung Vorteile erbringt.
- Trotz der in den o. g. Anmeldeschriften zitierten Fortschritte gibt es immer noch einen erheblichen Bedarf an Verbesserung für entsprechende Materialien. U. a. auf folgenden Feldern ist noch ein deutlicher Verbesserungsbedarf zu sehen:
- (1) Die Strom-Spannungskennlinien müssen noch deutlich steiler werden, damit für Anwendungen große Helligkeit bei ausreichend niedrigen Spannungen erzielt wird und somit eine höhere Leistungseffizienz erzielt wird. Dies ist von enormer Bedeutung, da somit einerseits gleiche Helligkeit bei geringerem Energieverbrauch erzielt werden kann, was vor allem bei mobilen Applikationen (Displays für Handys, Pager, PDA etc.) sehr wichtig ist. Andererseits erhält man bei gleichem Energieverbrauch höhere Helligkeiten, was beispielsweise für Beleuchtungsanwendungen interessant sein kann.
- (2) Viele der beschriebenen BLAU emittierenden Polymere zeigen keine gesättigte tiefblaue Emission, sondern eine hellblaue Emission, deren Farbsättigung nicht für alle Anwendungen ausreichend ist.
- Wie aus dieser Beschreibung des Stands der Technik ersichtlich ist, besteht daher weiterhin ein großer Bedarf an Verbesserungen auf dem Gebiet der lichtemittierenden Polymere.
- Wir haben überraschend gefunden, dass – bisher unbekannte – Polymere, die bestimmte Carbazol-Einheiten enthalten, deutliche Verbesserungen, gerade auf den beiden o. g. Gebieten, d. h. der Steilheit der Strom-Spannungs-Kennlinien (und damit der Betriebsspannung) und der Farbe, ergeben. Diese sind daher Gegenstand der vorliegenden Anmeldung.
- Gegenstand der Erfindung sind daher konjugierte Polymere, die 1 – 100 mol%, bevorzugt 5 – 100 mol%, besonders bevorzugt 10 – 100 mol% Einheiten gemäß Formel (I) enthalten, FORMEL (I) wobei die Symbole und Indizes folgende Bedeutung besitzen:
R ist bei jedem Auftreten gleich oder verschieden einem Cycloalkylsystem mit 3 bis 40 C-Atomen, welches substituiert oder unsubstituiert sein kann, einem aromatischen oder heteroaromatischen Ringsystem mit 2 bis 40 C-Atomen, welches substituiert oder unsubstituiert sein kann, oder einem Alkylen-aryl-, Alkylen-cycloalkyl- oder Alkylen-heteroaryl-System mit linearer oder verzweigter Alkylkette mit 1 bis 16 C-Atomen, welches substituiert oder auch unsubstituiert sein kann; die Aryl- und Heteroaryl-Systeme können dabei auch Teil eines größeren kondensierten aromatischen Ringsystems sein; die möglichen Substituenten R1 können potentiell an jeder freien Position sitzen;
Aryl sind bei jedem Auftreten gleich oder verschieden einem aromatischen oder heteroaromatischen Ringsystem mit 2 bis 40 C-Atomen, welches substituiert oder auch unsubstituiert sein kann, oder eine substituierte oder unsubstituierte Stilbenylen- bzw. Tolanyleneinheit; die möglichen Substituenten R1 können dabei potentiell an jeder freien Position sitzen;
R1 ist bei jedem Auftreten gleich oder verschieden eine geradkettige, verzweigte oder cyclische Alkyl- oder Alkoxykette mit 1 bis 22 C-Atomen, in der auch ein oder mehrere nicht benachbarte C-Atome durch N-R2, O, S, -CO-O-, O-CO-O ersetzt sein können, wobei auch ein oder mehrere H-Atome durch Fluor ersetzt sein können, eine Aryl- oder Aryloxygruppe mit 5 bis 40 C-Atomen, bei der auch ein oder mehrere C-Atome durch O, S oder N ersetzt sein können, welche auch durch ein oder mehrere nicht-aromatische Reste R1 substituiert sein können, oder Cl, F, CN, N(R2)2, B(R2)2, wobei auch zwei oder mehrere Reste R1 miteinander ein Ringsystem bilden können;
Ra ist bei jedem Auftreten gleich oder verschieden eine geradkettige, verzweigte oder cyclische Alkyl- oder Alkoxykette mit 1 bis 22 C-Atomen, in der auch ein oder mehrere nicht benachbarte C-Atome durch N-R2, O, S, -CO-O-, O-CO-O ersetzt sein können, wobei auch ein oder mehrere H-Atome durch Fluor ersetzt sein können, eine Aryl- oder Aryloxygruppe mit 5 bis 40 C-Atomen, bei der auch ein oder mehrere C-Atome durch O, S oder N ersetzt sein können, welche auch durch ein oder mehrere nicht-aromatische Reste R1 substituiert sein können, oder Cl, F, CN, N(R2)2, B(R2)2,;
Rb ist bei jedem Auftreten gleich oder verschieden eine geradkettige, verzweigte oder cyclische Alkyl- oder Alkoxykette mit 1 bis 22 C-Atomen, in der auch ein oder mehrere nicht benachbarte C-Atome durch N-R2, O, S, -CO-O-, O-CO-O ersetzt sein können, wobei auch ein oder mehrere H-Atome durch Fluor ersetzt sein können, eine Aryl- oder Aryloxygruppe mit 5 bis 40 C-Atomen, bei der auch ein oder mehrere C-Atome durch O, S oder N ersetzt sein können, welche auch durch ein oder mehrere nicht-aromatische Reste R1 substituiert sein können, oder Cl, F, CN, N(R2)2, B(R2)2, wobei auch zwei oder mehrere Reste Rb miteinander ein Ringsystem bilden können;
R2 ist bei jedem Auftreten gleich oder verschieden H, eine geradkettige, verzweigte oder cyclische Alkylkette mit 1 bis 22 C-Atomen, in der auch ein oder mehrere nicht benachbarte C-Atome durch O, S, -CO-O-, O-CO-O ersetzt sein können, wobei auch ein oder mehrere H-Atome durch Fluor ersetzt sein können, eine Arylgruppe mit 5 bis 40 C-Atomen, bei der auch ein oder mehrere C-Atome durch O, S oder N ersetzt sein können, welche auch durch ein oder mehrere nicht-aromatische Reste R1 substituiert sein können;
m ist bei jedem Auftreten gleich oder verschieden 0, 1 oder 2;
o ist bei jedem Auftreten gleich oder verschieden 0, 1 oder 2, unter der Bedingung, dass o nicht 0 sein darf, wenn m = 2 ist;
r ist bei jedem Auftreten gleich oder verschieden 0 oder 1,
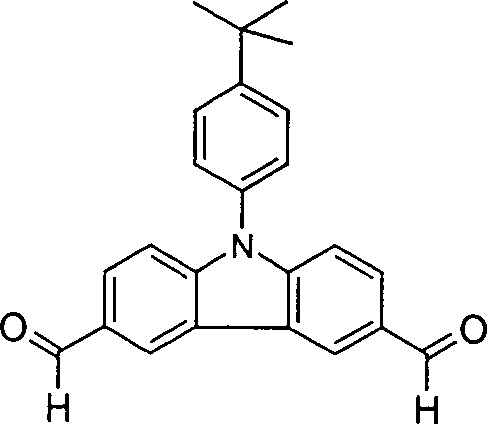
z ist bei jedem Auftreten gleich oder verschieden 0, 1, 2 oder 3. - Dabei sind verschiedene Verknüpfungen für die Carbazoleinheit in der Polymerkette möglich: Verknüpfung an nur einer der Stellen führt zu einer Endgruppe oder zum Einbau der Struktureinheit gemäß Formel (I) in die Seitenkette, Verknüpfung an zwei Stellen führt zur Inkorporation des Monomers in die Hauptkette des Polymers; der Einbau der Struktureinheit gemäß Formel (I) in die Hauptkette soll entweder über die 3,6- oder die 2,7-Position des Carbazols erfolgen oder aber auch über die 2,9- oder 3,9-Position, sofern in den letzten beiden Fällen R ein aromatisches oder heteroaromatisches Ringsystem beschreibt, damit die Konjugation des Polymers gewahrt bleibt. Besonders bevorzugt erfolgt der Einbau über die 3,6- oder die 2,7-Position oder über die 3,9-Position, sofern R ein aromatisches oder heteroaromatisches Ringsystem beschreibt. Ganz besonders bevorzugt erfolgt der Einbau über die 3,6- oder die 2,7-Position. Zur Klarheit wird die Nummerierung des Carbazols in folgender Struktur aufgezeigt:
- Konjugierte Polymere im Sinne dieser Erfindung sollen Polymere sein, die in der Hauptkette hauptsächlich sp2-hybridisierte (bzw. teilweise auch sp-hybridisierte) Kohlenstoffatome enthalten, die auch durch entsprechende Heteroatome ersetzt sein können. Dies bedeutet im einfachsten Fall abwechselndes Vorliegen von Doppel- und Einfachbindungen in der Hauptkette. Hauptsächlich meint, dass natürlich auftretende Defekte, die zu Konjugationsunterbrechungen führen, den Begriff "konjugierte Polymere" nicht entwerten. Es sind jedoch keine Polymere gemeint, welche absichtlich eingefügte größere Mengen an nicht-konjugierten Segmenten enthalten. Des weiteren wird in diesem Anmeldetext ebenfalls als konjugiert bezeichnet, wenn sich in der Hauptkette beispielsweise Arylamineinheiten wie das Carbazol gemäß Formel (I) oder andere derartige Einheiten und/oder bestimmte Heterocyclen (d. h. Konjugation über N-, O-, oder S-Atome) und/oder metallorganische Komplexe (d. h. Konjugation über das Metallatom) befinden. Hingegen würden Einheiten wie beispielsweise einfache (Thio)Etherbrücken, Esterverknüpfungen, Amid- oder Imidverknüpfungen eindeutig als nicht-konjugierte Segmente definiert.
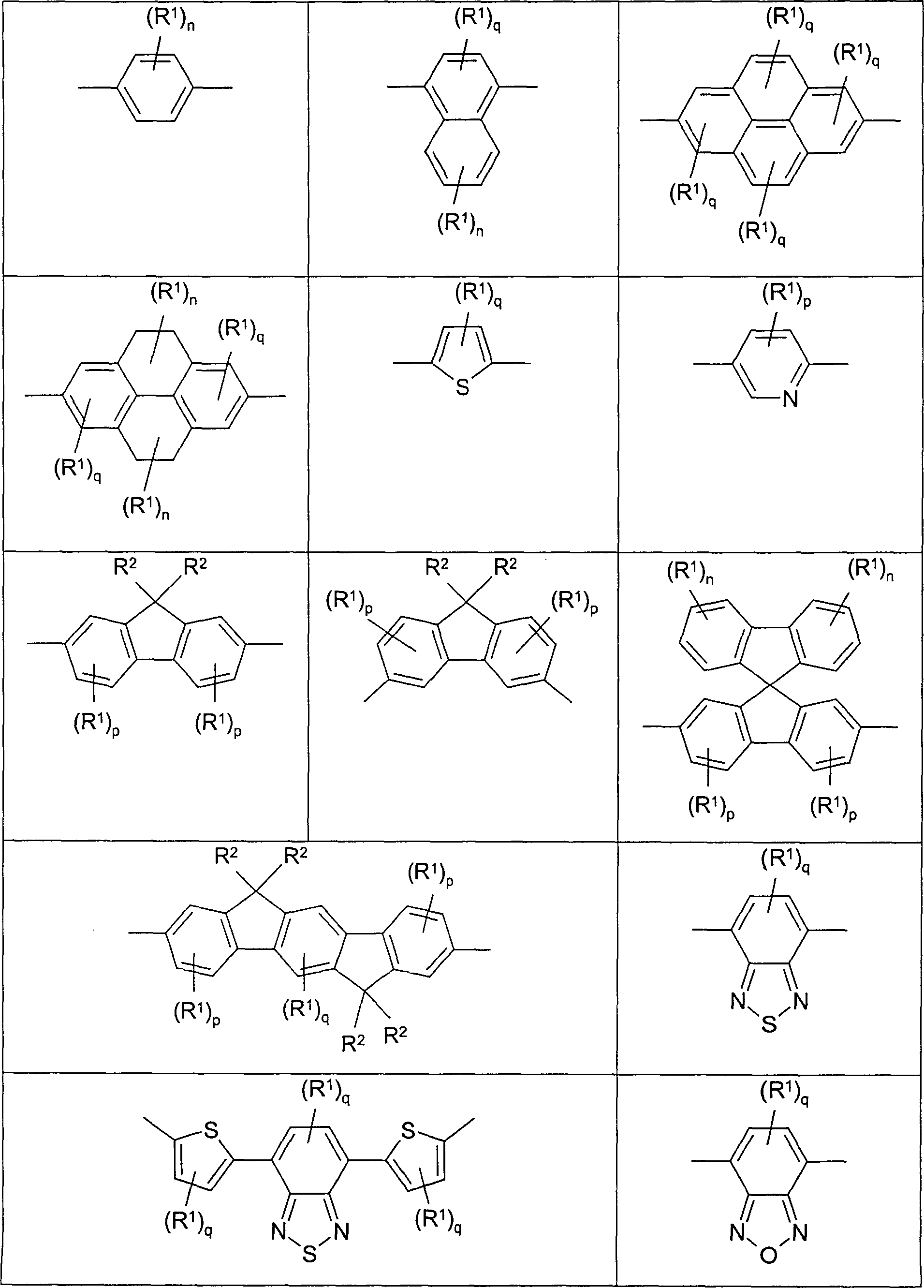
- Die erfindungsgemäßen Polymere können neben den Einheiten gemäß Formel (I) noch weitere Strukturelemente enthalten. Dies sind u. a. solche, wie sie in den o. g. Patentanmeldungen bereits offenbart sind. Hier sei vor allem auch auf die relativ umfangreiche Auflistung in der oben schon erwähnten Anmeldeschrift WO 02/077060 verwiesen; diese wird via Zitat als Bestandteil der vorliegenden Erfindung betrachtet. Diese weiteren Struktureinheiten können beispielsweise aus den im Folgenden beschriebenen Klassen stammen:
- 1. Struktureinheiten, die das Polymergrundgerüst bilden können, bzw. BLAU emittierende Einheiten: – Hier sind zunächst Poly-Phenylene und davon abgeleitete Strukturen bildende Einheiten zu nennen. Dies sind beispielsweise (jeweils substituierte oder unsubstituierte) ortho-, meta- oder para-Phenylene, 1,4-Naphthylene, 9,10-Anthracenylene, 2,7-Phenanthrenylene, 1,6- bzw. 2,7- bzw. 4,9-Pyrene oder 2,7-Tetrahydropyrene. Auch entsprechende heterocyclische "Poly-Phenylen"-bildende Strukturen, wie beispielsweise 2,5-Thiophenylen, 2,5-Pyrrolylen, 2,5-Furanylen, 2,5-Pyridylen, 2,5-Pyrimidinylen oder 5,8-Chinolinylen kommen in Frage. – Des weiteren sind komplexere Einheiten, wie die o. g. Fluorene, Spiro-9,9'-bifluorene, mehrfach überbrückte Einheiten (z. B. kurze Teilsegmente der o. g. LPPP-Polymere), aber auch "doppelte Fluoren"-Einheiten (Indenofluorene) möglich. Auch diese können substituiert bzw. unsubstituiert sein. Auch entsprechende heterocyclische Strukturen, in denen beispielsweise einzelne Ringkohlenstoffatome durch Heteroatome wie beispielsweise Schwefel ersetzt sind, kommen hier in Frage.
- 2. Struktureinheiten, die die Ladungsinjektions- bzw. Ladungstransporteigenschaften
erhöhen.
Dies kann sich sowohl auf die Elektroneninjektions- oder -transporteigenschaften
(wie beispielsweise Oxadiazol-Einheiten) wie auch auf die Lochinjektions-
oder -transporteigenschaften (wie beispielsweise Triarylamin-Einheiten)
beziehen. Hier sei nochmals auf umfangreiche Auflistung derartiger
Struktureinheiten in der oben zitierter Anmeldeschrift WOO2/077060
verwiesen; diese wird via Zitat als Bestandteil der vorliegenden
Erfindung betrachtet. Ebenso kommen für diesen Zweck Naphthyl-aryl-amine
in Frage, wie sie in der nicht offengelegten Anmeldeschrift
DE 10249723.0 beschrieben werden. - 3. Struktureinheiten, die beispielsweise die Farbe der Emission verschieben, damit auch die Bandlücke des Polymers verändern und somit i. d. R. auch die Ladungsinjektions- bzw. -transporteigenschaften verändern: – Hier sind beispielsweise weitere heterocyclische Verbindungen, wie die in der o. g. Anmeldung WO 02/077060 unter den Formeln (XX) bis (XXXXV) genannten Strukturen zu nennen. – Des weiteren sind hier auch Arylen-vinylen- oder Arylen-acetylen-Strukturen, wie substituierte oder unsubstituierte Stilbenylene, Tolanylene, Bisstyrylarylene, Bis(arylacetylen)-arylene zu nennen. – Schließlich kann auch der Einbau von größeren aromatischen Einheiten, wie zum Beispiel Chrysenen, Naphthacenen, Pentacenen, Perylenen oder Coronenen, den o. g, farbverschiebenden Effekt erzeugen.
- 4. Struktureinheiten, welche einen Transfer von sogenannten
Singulett-Excitonen zu Triplett-Excitonen ermöglichen, und welche auch bei
Raumtemperatur mit hoher Effizienz aus dem Triplettzustand Licht
emittieren können:
– Hier sind
zunächst
vor allem Verbindungen, welche Schweratome, d. h. Atome aus dem
Periodensystem der Elemente mit einer Ordnungszahl von mehr als
36, enthalten, zu verstehen.
– Besonders geeignet hierfür sind Verbindungen,
welche d- und f-Übergangsmetalle,
die die o. g. Bedingung erfüllen.
Ganz besonders bevorzugt sind hier entsprechende Struktureinheiten,
welche Elemente der Gruppe 8 bis 10 (d. h. Ru, Os, Rh, Ir, Pd, Pt)
enthalten.
– Als
Struktureinheiten für
die erfindungsgemäßen Polymere
kommen hier verschiedene Komplexe in Frage, welche beispielsweise
in den Anmeldeschriften WO 02/068435, WO 02/081488,
EP 1239526 und der nicht offengelegten AnmeldeschriftDE 10238903.9 beschrieben sind. -
- Die dabei verwendeten Symbole Aryl, R1 und R2 sind analog dem oben bereits beschriebenen zu verstehen.
n ist bei jedem Auftreten gleich oder verschieden 0, 1, 2, 3 oder 4;
p ist bei jedem Auftreten gleich oder verschieden 0, 1, 2 oder 3;
q ist bei jedem Auftreten gleich oder verschieden 0, 1 oder 2;
M ist bei jedem Auftreten gleich oder verschieden Rh oder Ir; - Mit den abgebildeten Einfachbindung ist jeweils die Verknüpfung zum nächsten Monomer symbolisiert; diese sollen hier keine Methylgruppen darstellen.
- Die erfindungsgemäßen Polymere sind entweder Homopolymere, d. h. sie enthalten dann nur eine Struktur der Formel (I), oder es sind Copolymere. Hierbei kann es bevorzugt sein, dass diese entweder mehrere verschiedene Struktureinheiten gemäß Formel (I) enthalten, oder neben einer oder mehrerer Struktureinheiten) gemäß Formel (I), eine oder mehrere der oben beschriebenen bzw. aufgezählten Struktureinheiten enthalten.
- Die erfindungsgemäßen Copolymere können sowohl statistische als auch alternierende oder auch blockartige Strukturen aufweisen oder auch mehrere dieser Strukturen abwechselnd besitzen. Durch das Verwenden mehrerer verschiedener Strukturelemente können Eigenschaften wie Löslichkeit, Festphasenmorphologie, Farbe etc. eingestellt werden.
- Wie oben beschrieben, enthalten besonders bevorzugte erfindungsgemäße Polymere mindestens 10 mol% Struktureinheiten gemäß Formel (I). Gerade für die Anwendung in den genannten PLEDs als emittierendes Material hat sich ein Anteil in dieser Größenordnung als günstig erwiesen. Für andere Anwendungen, z. B. als Ladungstransportschicht in organischen Feld-Effekt-Transistoren (OFETs), kann sich auch ein deutlich höherer Anteil (bis zu 100 mol%) als günstig erweisen.
- Für bevorzugte Strukturen gemäß Formel (I) gilt folgendes:
R ist bei jedem Auftreten gleich oder verschieden einem aromatischen oder heteroaromatischen Ringsystem, ausgewählt aus Thiophen, Benzothiophen, Benzol, Pyridin, Chinoxalin, Fluoren, Spirobifluoren, Naphthalin, Anthracen, Pyren oder Phenanthren, welches an den freien Positionen 0 bis 3 Substituenten R1 trägt, oder einem Alkylen-aryl- oder Alkylen-heteroaryl-Ringsystem, dessen Alkylen-Kette linear oder verzweigt sein kann und aus 1 bis 16 C-Atomen besteht, und dessen Aryl- und Heteroaryl-System aus den oben im einzelnen aufgeführten Systemen besteht, welche an den freien Positionen 0 bis 3 Substituenten R1 tragen;
Aryl ist bei jedem Auftreten gleich oder verschieden einem aromatischen oder heteroaromatischen Ringsystem mit 2 bis 40 C-Atomen, welches substituiert oder auch unsubstituiert sein kann; die Aryl- und Heteroaryl-Systeme können dabei auch Teil eines größeren kondensierten aromatischen Ringsystems sein; die möglichen Substituenten R1 können, wenn vorhanden, an jeder freien Position sitzen;
R1, R2, Ra, Rb, r, z sind analog den oben gemachten Angaben;
m ist bei jedem Auftreten gleich oder verschieden 0 oder 1;
o ist bei jedem Auftreten gleich oder verschieden 0, 1 oder 2;
die Verknüpfung der Struktureinheit gemäß Formel (I) in die Hauptkette des Polymers erfolgt über die 3,6- oder 2,7-Position oder über die 2,9- oder 3,9-Position, sofern R eine aromatische oder heteroaromatische Einheit ist. - Für besonders bevorzugte Strukturen gemäß Formel (I) gilt folgendes:
R ist bei jedem Auftreten gleich oder verschieden einem aromatischen oder heteroaromatischen Ringsystem, ausgewählt aus Thiophen, Benzothiophen, Benzol, Pyridin, Naphthalin, Anthracen, Pyren oder Phenanthren, welche unsubstituiert oder mit einem Substituenten R1 substituiert sind, oder einem 9,9'-substituierten Fluoren oder einem Methylen-aryl- oder Methylen-heteroaryl-Ringsystem, dessen Aryl- bzw. Heteroaryl-System aus den oben im einzelnen aufgeführten Systemen besteht, welche dasselbe Substitutionsmuster tragen können wie die oben genannten Systeme;
Aryl ist bei jedem Auftreten gleich oder verschieden einem aromatischen oder heteroaromatischen Ringsystem mit 2 bis 20 C-Atomen, welches substituiert oder auch unsubstituiert sein kann; die Aryl- und Heteroaryl-Systeme können dabei auch Teil eines größeren kondensierten aromatischen Ringsystems sein; die möglichen Substituenten R1 können dabei potentiell an jeder freien Position sitzen;
R1, R2, Ra, Rb, r sind analog den oben gemachten Angaben;
m ist bei jedem Auftreten gleich oder verschieden 0 oder 1;
o ist bei jedem Auftreten gleich oder verschieden 0 oder 1;
z ist bei jedem Auftreten gleich oder verschieden 0 oder 1
die Verknüpfung der Struktureinheit gemäß Formel (I) in die Hauptkette des Polymers ist über die 3,6-Position, die 2,7-Position oder die 3,9-Position, sofern R ein Aryl- oder Heteroarylsystem ist. - Besonders bevorzugte Strukturen gemäß Formel (I) sind substituierte oder unsubstituierte Strukturen gemäß den abgebildeten Formeln (II) bis (XXXI), wobei die Einzelbindungen die Verknüpfung im Polymer definieren und potentielle Substituenten wegen der besseren Übersichtlichkeit i. d. R. nicht abgebildet sind:
- Für ganz besonders bevorzugte Strukturen gemäß Formel (I) gilt folgendes:
R ist bei jedem Auftreten gleich oder verschieden einem aromatischen oder heteroaromatischen Ringsystem, ausgewählt aus Thiophen, Benzothiophen, Benzol, Naphthalin, Anthracen, oder Phenanthren, welche unsubstituiert oder mit einem Substituenten R1 substituiert sind, oder einem Benzyl-Ringsystem, dessen Phenylgruppe dasselbe Substitutionsmuster tragen kann wie die oben genannten Systeme;
Aryl ist bei jedem Auftreten gleich oder verschieden einem aromatischen oder heteroaromatischen Ringsystem mit 2 bis 20 C-Atomen, welches substituiert oder auch unsubstituiert sein kann; die Aryl- und Heteroaryl-Systeme können dabei auch Teil eines größeren kondensierten aromatischen Ringsystems sein; die möglichen Substituenten R1 können dabei potentiell an jeder freien Position sitzen;
R1, R2, r sind analog den oben gemachten Angaben;
m ist bei jedem Auftreten gleich oder verschieden 0 oder 1;
o ist bei jedem Auftreten gleich 1. - Dabei erfolgt die Verknüpfung in die Polymerkette über die 3,6- oder die 2,7-Position des Carbazols.
- Auch wenn dies aus der Beschreibung hervorgeht, sei hier nochmals explizit darauf verwiesen, dass sowohl die Struktureinheiten gemäß Formel (I), als auch jene gemäß den Formeln (II) bis (XXXI) unsymmetrisch substituiert sein können, d. h. an einer Einheit unterschiedliche Substituenten R1 vorhanden sein können, bzw. diese auch an unterschiedlichen Positionen gebunden sein können.
- Die erfindungsgemäßen Polymere weisen in der Regel 10 bis 10000, bevorzugt 50 bis 5000, besonders bevorzugt 50 bis 2000 Wiederholeinheiten auf. Dabei beträgt die Polydispersität PD bevorzugt weniger als 10, besonders bevorzugt weniger als 5.
- Die nötige Löslichkeit wird v. a. durch die Substituenten R1, sowohl an Strukturen gemäß Formel (I), als auch an solchen, die wie oben geschildert, in entsprechenden Copolymeren noch zusätzlich vorhanden sind, erreicht.
- In der Regel ist es deshalb nötig, dass im Durchschnitt pro Wiederholeinheit mindestens 2 nicht-aromatische C-Atome in den Substituenten vorhanden sind. Bevorzugt sind dabei mindestens 4, besonders bevorzugt mindestens 8 C-Atome. Einzelne dieser C-Atome können auch noch durch O oder S ersetzt sein. Dies schließt nicht aus, dass ein gewisser Anteil von Wiederholeinheiten, sowohl solche gemäß Formel (I) als auch anderer Strukturtypen, keine weiteren nicht-aromatischen Substituenten tragen.
- Es ist bevorzugt, keine langkettigen Substituenten mit mehr als 12 C-Atomen, bevorzugt keine mit mehr als 8 C-Atomen, besonders bevorzugt keine mit mehr als 6 C-Atomen in einer linearen Kette zu haben, um die Morphologie des Filmes nicht zu verschlechtern.
- Nicht-aromatische C-Atome sind, wie in der Beschreibung für R1, in entsprechenden geradkettigen, verzweigten oder cyclischen Alkyl- oder Alkoxyketten enthalten.
- Bevorzugt sind deshalb weiterhin erfindungsgemäße Polymere, bei denen gilt:
R1 ist bei jedem Auftreten gleich oder verschieden eine geradkettige, verzweigte oder cyclische Alkyl- oder Alkoxykette mit 1 bis 10 C-Atomen, wobei auch ein oder mehrere H-Atome durch Fluor ersetzt sein können, oder eine Arylgruppe mit 6 bis 14 C-Atomen, welche auch durch ein oder mehrere nicht-aromatische Reste R1 substituiert ist. - Weiterhin besonders bevorzugt sind deshalb erfindungsgemäße Polymere, bei denen gilt:
R1 ist bei jedem Auftreten gleich oder verschieden eine geradkettige oder verzweigte Alkyl- oder Alkoxykette mit 1 bis 8 C-Atomen, oder eine Arylgruppe mit 6 bis 10 C-Atomen, welche auch durch ein oder mehrere nicht-aromatische Reste R1 substituiert ist. - Die erfindungsgemäßen Polymere weisen gegenüber dem o. g. Stand der Technik u. a. folgende überraschenden Vorteile auf:
- – Der
Strom bei gegebener Spannung ist bei vergleichbaren Polymeren bei
der Verwendung in PLEDs deutlich höher (vgl. Angaben in Tabelle
2 und in
1 ), d.h. die Strom-Spannungskennlinie ist steiler, wenn das Polymer Struktureinheiten der Formel (I) enthält. Dies bringt für die Anwendung – wie oben bereits ausgeführt – deutliche Vorteile, da somit das Ziel, effiziente Vollfarbdisplays mit geringerem Energieverbrauch zu erzeugen, ermöglicht wird. Überraschend hat die Verwendung von erfindungsgemäßen Polymeren für die Erzeugung blauer Emission noch weitere Vorteile: die Emissionsfarbe wird noch tiefer (d. h. tiefblau), als diejenige bei analogen Polymeren ohne Struktureinheiten gemäß Formel (I). (vgl. beispielsweise Polymere P1 und P2 mit Polymer V1 und V2). - – Entsprechende Copolymere können so aufgebaut werden, dass diese alle Grundfarben (Rot, Grün, Blau) emittieren können.
- – Die Löslichkeit in organischen Lösemitteln ist i. d. R. gut, d. h. in Lösemitteln, wie beispielsweise Toluol, Xylol, Anisol, Methylanisol oder Methylnaphthalin, sind die Polymere in Konzentrationen von 1 bis mindestens 30 g/L (je nach Molekulargewicht) löslich.
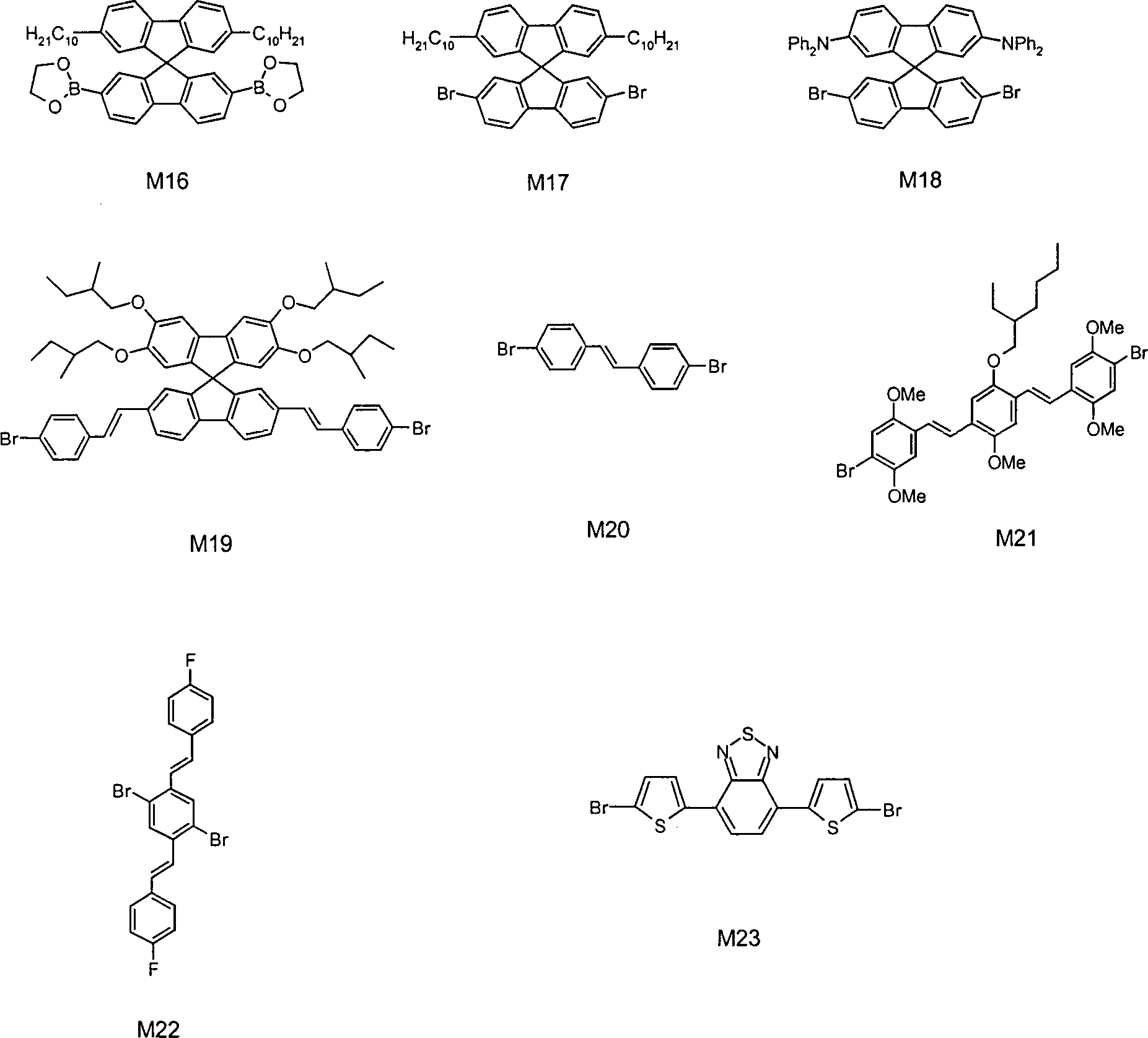
- Die erfindungsgemäßen Polymere werden in der Regel durch Polymerisation von einem oder mehreren Monomeren, von denen mindestens eines Strukturen der Formel (I) enthält, hergestellt.
- Entsprechende Polymerisationsreaktionen gibt es prinzipiell relativ viele verschiedene; es haben sich jedoch die im folgenden aufgeführten Typen, die alle zu C-C-Verknüpfungen führen, besonders bewährt:
- (A) Polymerisation gemäß SUZUKI: Hierbei werden als
Monomere zum einen Bishalogenide, zum anderen Bisboronsäuren und
entsprechende -derivate oder entsprechende Monohalogenid-monoboronsäurederivate
eingesetzt und unter Palladiumkatalyse, in Anwesenheit von Lösemitteln
und unter basischen Bedingungen gekuppelt. Derartige Reaktionen,
welche zu konjugierten Polymeren führen, sind bereits vielfach beschrieben.
Es gibt eine ganze Reihe von Vorschlägen, wie derartige Reaktionen
effizient ablaufen und zu hochmolekularen Polymeren führen; diese
sind u. a. in den folgenden Stellen aufgeführt: (i)
EP 707.020 EP 842.208 EP 1.025.142 , (iv) WO 00/53656, (v) der nicht oftengelegten AnmeldeschriftDE 10159946.3 und (vi) in den darin zitierten Literaturstellen. Die entsprechenden Beschreibungen werden hiermit via Zitat als Bestandteil der Anmeldung erachtet. - (B) Polymerisationen gemäß YAMAMOTO:
Hierbei werden als Monomere ausschließlich Bishalogenide verwendet.
Diese werden in Anwesenheit von Lösemitteln, einer Nickel-Verbindung
und gegebenenfalls eines Reduktionsmittels sowie weiterer Liganden
durchgeführt.
Derartige Reaktionen, welche zu konjugierten Polymeren führen, sind
bereits mehrfach beschrieben. Es gibt einige Vorschläge, wie
derartige Reaktionen effizient ablaufen und zu hochmolekularen Polymeren
führen;
diese sind u. a. in den folgenden Stellen aufgeführt: (i) M. Ueda et al., Macromolecules,
1991, 24, 2694; (ii) T. Yamamoto et al., Macromolecules 1992, 25,
1214; (iii) T. Yamamoto et al., Synth. Met. 1995, 69, 529–31; (iv)
T. Yamamoto et al., J. Organometallic Chem. 1992, 428, 223; (v)
I. Colon et al., J. Poly. Sci.: Part A: Poly. Chem. 1990, 28, 367;
(vi) T. Yamamoto et al., Macromol. Chem. Phys. 1997, 198, 341. (vii)
Ein gut funktionierendes Verfahren ist auch noch in der noch nicht
offengelegten Anmeldeschrift
DE 10241814.4 beschrieben. Die entsprechenden Beschreibungen werden hiermit via Zitat als Bestandteil der Anmeldung erachtet. (C) Polymerisationen gemäß STILLE: Hierbei werden als Monomere zum einen Bishalogenide, zum anderen Bisstannane oder entsprechende Monohalogenidmonostannane eingesetzt und unter Palladiumkatalyse in Anwesenheit von Lösemitteln gekuppelt. Derartige Reaktionen, welche zu konjugierten Polymeren führen, sind bereits beschrieben. Sie sind allerdings noch nicht so weit ausgearbeitet, wie dies bei der SUZUKI- oder YAMAMOTO-Kupplung der Fall ist. Ein konjugiertes Polymer, welches durch STILLE-Kupplung erhalten wurde, wird z. B. in W. Schorf et al., J. Opt. Soc. Am. 8 1998, 15, 889 beschrieben. Eine Übersicht über die Möglichkeiten und die Schwierigkeiten der STILLE-Reaktion gibt u. a. V. Farina, V. Krishnamurthy, W. J. Scott (Hers.) "The Stille Reaction" 1998, Verlag: Wiley, New York, N. Y. Die entsprechenden Beschreibungen werden hiermit via Zitat als Bestandteil der Anmeldung erachtet. - Für Polymere, die Doppelbindungen (Alken-Einheiten) enthalten, kommen auch folgende Methoden zur Polymerisation in Frage:
- (D) Polymerisation gemäß WITTIG-HORNER: Hierbei werden als Monomere zum einen Bisaldehyde, zum anderen Bisphosphonate oder entsprechende Monoaldehyd-monophosphonate eingesetzt und unter basischen Bedingungen in Anwesenheit von Lösemitteln zu den entsprechenden Alkenverbindungen umgesetzt. Derartige Reaktionen, welche zu konjugierten Polymeren führen, sind bereits beschrieben: (i) A. P. Davey, A. Drury, S. Maier, H. J. Byrne, W. J. Blau, Synth. Met. 1999, 103, 2478–2479, (ii) S.-H. Jin, J.-E. Jung, I.-S. Yeom, S.-B. Moon, K. Koh, S.-H. Kim, Y.-S. Gal, Eur. Polym. J. 2002, 38, 895–901. Die entsprechenden Beschreibungen werden hiermit via Zitat als Bestandteil der Anmeldung erachtet.
- (E) Polymerisation nach Precursor-Methoden (beispielsweise Sulfoxy Precursor Methode): Ausgehend von Bis(chlormethyl)-Verbindungen, die in der Lage sind ein Chinodimethan zu bilden, werden zunächst durch einseitige Substitution Alkylthiomethyl-Chlormethyl-Intermediate erhalten. Daraus wird durch Oxidation das Sulfoxid gewonnen. Dieses Vorläufer-Monomer wird unter Bedingungen der Gilch-Polymerisation umgesetzt, wobei das effektive Monomer ein Alkylsulfoxychinodimethan ist. Das somit erhaltene relativ temperaturstabile Vorläufer-Polymer stellt ein Poly(arylen alkylsulfoxyethylen) dar, das durch reine Temperaturbehandlung unterhalb 200°C Alkylsulfinsäure eliminiert, unter Bildung des vollständig konjugierten Polymers. Diese Reaktionen sind u. a. in den folgenden Stellen aufgeführt: (i) WO 00/35987 (ii) A. Issaris, D. Vanderzande, Macromolecules 1998, 31, 4426–4431. Die entsprechenden Beschreibungen werden hiermit via Zitat als Bestandteil der Anmeldung erachtet.
- Die eigentliche Polymerisation (Polykondensation) (vgl. auch die Angaben bei den Beispielen) läuft allgemein dadurch ab, dass das/die Monomer(e) in einem geeigneten Konzentrationsbereich in Lösung mit den entsprechenden Katalysatoren und/oder Hilfssystemen zur Reaktion gebracht werden. Dabei kann es vorteilhaft sein, durch geringe Abweichungen von der idealen Stöchiometrie, bzw. durch das Vorhandensein geringer Mengen mono-funktioneller Verbindungen, eine Molekulargewichtsbegrenzung durchzuführen. Die Reaktion wird i. d. R. bis zum gewünschten Molekulargewicht durchgeführt (dabei kann beispielsweise Prozesskontrolle über Viskositätsmessung, etc. erfolgen). Danach wird die Reaktion abgebrochen. Dies kann auf verschiedene Weise erfolgen. Um reaktive Endgruppen zu vermeiden, hat es sich bewährt, ein sogenanntes "Endcapping" durchzuführen, d. h. nach Erreichen des gewünschten Molekulargewichts werden monofunktionelle Verbindungen zuzugeben. Bei den Reaktionstypen A, C und D kann dies auch doppelt erfolgen, d. h. man gibt zuerst eine/mehrere monofunktionelle Verbindungen) des einen Typs (z. B. Monohalogenid) und anschließend des anderen Typs (z. B. Monoboronsäurederivat) zu.
- Danach müssen die synthetisierten Polymere zunächst vom Reaktionsmedium abgetrennt werden. Dies geschieht in der Regel durch Ausfällen in einem Nicht-Lösemittel. Anschließend müssen die erhaltenen Polymere aufgereinigt werden, da gerade der Gehalt an organischen niedermolekularen Verunreinigungen und auch der Ionengehalt bzw. Gehalt an sonstigen anorganischen Verunreinigungen teilweise sehr starke Auswirkungen auf die Anwendungseigenschaften der Polymere in PLEDs oder auch anderen Applikationen haben. So können niedermolekulare Bestandteile zum einen die Effizienz erheblich absenken, aber auch die operative Lebensdauer dramatisch verschlechtern (z. B. durch Diffusion etc. während des Betriebs). Analoges gilt für die Anwesenheit von anorganischen Verunreinigungen. Geeignete Reinigungsverfahren sind einerseits Umfällvorgänge, bei denen das Polymer wiederholt gelöst und in einem Nicht-Lösemittel gefällt wird. Es ist dabei sinnvoll, die Polymerlösung über einen Filter zu geben, um von ungelösten Bestandteilen (chemisch oder physikalisch vernetzten Gelpartikel) und auch Staubpartikeln abzutrennen. Eine weitere Möglichkeit ist das Verwenden von Ionenaustauschern, um den Gehalt an Ionen zu verringern. Hierbei kann auch das Ausrühren einer Polymerlösung mit einer wässrigen Lösung, welche z. B. chelatisierende Liganden enthält, helfen. Auch weitere organische oder anorganische Extraktionsverfahren, z. B. mit Lösemittel / Nicht-Lösemittelgemischen oder mit überkritischem CO2, können hier deutliche Verbesserungen bringen.
- Um die entsprechenden erfindungsgemäßen Polymere beispielsweise durch die o.g. Verfahren herstellen zu können, benötigt man – wie beschrieben – die entsprechenden Monomere.
- Für Strukturen gemäß Formel (I) können diese beispielsweise wie im folgenden beschrieben, erhalten werden:
- – Die Synthese von 3,6-Dibromcarbazol erfolgt durch Bromierung des Carbazols, wie in der Literatur beschrieben: Smith et al., Tetrahedron 1992, 48(36), 7479-7488.
- – Die Synthese von 2,7-Dibromcarbazol erfolgt durch Aufbau des Carbazols, wie in der Literatur beschrieben: Tidwell et al., Eur. J. Med. Chem. 1997, 32(10), 781-793.
- – Eine entsprechende Funktionalisierung, die eine Verwendung als Monomere ermöglicht (also z. B. Einführung von Halogen-Endgruppen), kann entweder an den Vorstufen erfolgen oder als letzter Schritt an dem bereits vollständig aufgebauten monomeren Grundgerüst. Beide Varianten haben, je nach angestrebter Zielstruktur, sowohl Vor- als auch Nachteile.
- – Vorab können die Funktionalitäten bereits vorhanden sein, wenn diese bei der Reaktion zum entsprechenden Monomer gemäß Formel (I) entweder nicht oder sehr erschwert reagieren. Dies kann z. B. der Fall sein bei einfacher Substitutionsreaktion oder, wenn man unterschiedliche Reaktivitäten (z. B. Iod gegenüber Brom, bzw. Brom gegenüber Chlor) ausnutzen kann. So kann beispielsweise ein Monomer gemäß Strukturformeln (III) unter Ausnutzung der Selektivität von Iod gegenüber Brom hergestellt werden, wie dies unten in Beispiel 2 beschrieben ist.
- – Andererseits kann es auch vorteilhaft sein (bei z. B. vorliegender Substitution bzw. dirigierenden Resten), zunächst den N-substituierten Carbazolgrundkörper aufzubauen und in einem letzten Schritt das Halogenid einzuführen. So ist es beispielsweise für Strukturen gemäß Formel (II) möglich, in die 3 und 6 Positionen des Carbazols Brom einzuführen (beispielsweise durch milde NBS-Bromierung, vgl. z. B. Creason et al., J. org. Chem, 1972, 37, 4440), wenn an dem N-Arylsubstituenten in para-Stellung ein Substituent vorhanden ist. Wie oben geschildert, kann dieses Verfahren bei Vorhandensein (i) entsprechender blockierender Substituenten, (ii) entsprechend dirigierender Reste oder (iii) aktivierter bzw. deaktivierter Heterocyclen auch für weitere Strukturen gemäß Formel (I) im allgemeinen angewendet werden.
- – Die N-Alkylierung oder N-Benzylierung von Carbazolen ist in der Literatur bekannt. Ebenso können N-Alkyl-aryl- und N-Cycloalkyl-Carbazole gewonnen werden. Die Synthese erfolgt durch Reaktion des Carbazols mit einem Alkylierungsmittel unter basischen Bedinungen, wie beispielsweise beschrieben in: M. E. Wright, M.-J. Jin, J. Org. Chem. 1989, 54, 965–968.
- – Die N-Arylierung des Carbazols kann gemäß Hartwig-Buchwald erfolgen und wird für Carbazol beispielsweise beschrieben in: M. Watanabe, M. Nishiyama, T. Yamamoto, Y. Koie, Tetrahedron Lett. 2000, 41, 481–483.
- – Ausgehend von den so erzeugten Halogenidderivaten können über Standardverfahren entsprechende Bisboronsäurederivate bzw. Bisstannanderivate (die für die o. g. Polymerisationsverfahren der Typen A und C benötigt werden) hergestellt werden. Diese Verfahren sind dem Fachmann hinlänglich bekannt und bestehen i. d. R. darin, das vorhandene Halogen gegen ein Metall auszutauschen (z. B. Magnesium, Lithium) und dieses dann mit einer Boresterverbindung bzw. einer Trialkylzinnhalogenverbindung umzusetzen. Für die Herstellung von Boronsäurederivaten sind auch katalytische Verfahren zur direkten Umsetzung der Halogenide mit beispielsweise Diboranen unter Anwesenheit von Palladium bekannt. Entsprechende Monohalogenid-monoboronsäure-Derivate bzw. Monohalogenid-monostannan-Verbindungen sind bei geeigneter Stöchiometrie auch erhältlich.
- – Ausgehend von den Halogenidderivaten können ebenfalls die entprechenden Bisaldehydderivate, die für das o. g. Polymerisationsverfahren des Typs D benötigt wird, hergestellt werden. Dieses Verfahren ist dem Fachmann hinlänglich bekannt und besteht i. d. R. darin, das vorhandene Halogen gegen ein Metall auszutauschen (z. B. Magnesium, Lithium) und dieses dann mit Ameisensäurederivat (z. B. Dimethylformamid) umzusetzen.
- – Die entsprechenden Phosphonatderivate, die für das o. g. Polymerisationsverfahren des Typs D benötigt werden, können ausgehend von den entsprechenden Methylenhalogenidverbindungen erzeugt werden, die dann mit phosphoriger Säure Trialkylester umgesetzt werden. Derartige Verfahren sind dem Fachmann hinlänglich bekannt.
- Die Synthese der weiteren Monomere, welche zu Strukturen führen, die nicht denen der Formel (I) entsprechen, die aber oben beschrieben wurden, ist in den bereits oben genannten Anmeldeschriften und Patenten ausführlich beschrieben.
- Einen guten Überblick hierzu gibt dabei die Anmeldeschrift WO 021077060, die dort gemachten entsprechenden Ausführungen werden via Zitat als Bestandteil dieser Anmeldung betrachtet.
- Die so erhaltenen Polymere können als Einzelkomponente in unten näher beschriebenen Anwendungen verwendet werden. Sie können auch als Blends (Mischungen des Polymers mit weiteren polymeren oder niedermolekularen Komponenten) verwendet werden. Gegenstand der Erfindung ist also auch ein Blend des erfindungsgemäßen Polymers mit anderen konjugierten oder nichtkonjugierten Polymeren.
- Bekannt und Stand der Technik ist weiterhin, dass Blends (Mischungen) von nichtkonjugierten Polymeren wie zum Beispiel PVK (Poly-vinylcarbazol) mit niedermolekularen Metallkomplexen, welche einen Transfer sogenannter Singulett-Excitonen zu Triplett-Excitonen ermöglichen und welche aus dem Triplett-Zustand Licht emittieren können, in effizienter Elektrolumineszenz des Metallkomplexes resultieren. Solche Mischungen werden beispielsweise beschrieben von Chen et al. (F.-C. Chen, Y. Yang, M. E. Thompson, J. Kido, Appl. Phys. Lett. 2002, 80, 2308-2310). Während reine Metallkomplexe für eine Anwendung in einem aufwändigen und teuren Prozess aufgedampft werden müssen, bieten diese Blends den Vorteil, dass sie aus Lösung einfacher und kostengünstiger verarbeitbar sind. Jedoch sind die Betriebsspannungen für solche Systeme mit nicht-konjugierten Polymeren sehr hoch, was in einer sehr niedrigen Leistungseffizienz resultiert.
- Blends aus niedermolekularen Metallkomplexen, die aus dem Triplett-Zustand Licht emittieren, mit konjugierten Polymeren sind in der Literatur ebenfalls beschrieben. Guo et al. (T. F. Guo, S. C. Chang, Y. Yang, R. C. Kwong, M. E. Thompson, Organic Electronics 2000, 1, 15) und O'Brien et al. (D. F. O'Brien, C. Giebler, R. B. Fletcher, J. Cadlby, L. C. Palilis, D. G. Lidzey, P. A. Lane, D. D. C. Bradley, W. Blau, Synth. Met. 2001, 116, 379) beschreiben gute Quanteneffizienzen mit Blends aus einem Platin-Porphyrin-Komplex mit Polyfluorenen, wobei in beiden Fällen die Effizienzen niedriger sind als bei vergleichbaren Devices aufgebaut aus kleinen Molekülen. Zhu et al. (W. Zhu, Y. Mo, M. Yuan, W. Yang, Y. Cao, Appl. Phys. Lett. 2002, 80, 2045-2047) beschreibt einen Blend aus einem löslichen Iridium-Phenylpyridin-Komplex mit einem Poly-para-phenylen. Hier wurden bessere, aber weiterhin relativ niedrige, Quanteneffizienzen gemessen. Insbesondere wurden für dieses System sehr hohe Spannungen für gute Effizienzen benötigt, die einer technischen Anwendung im Wege stehen würden.
- Für eine technische Anwendung besteht hier also noch weiterhin großer Verbesserungsbedarf.
- Überraschend wurde gefunden, dass – bisher unbekannte – Blends (also Mischungen) aus den im folgenden beschriebenen Polymeren mit Dendrimeren und/oder niedermolekularen Verbindungen und eventuell, aber nicht notwendigerweise, einem weiteren konjugierten oder auch nicht-konjugierten Polymer für die Anwendung hier unerwartete Vorteile bringen. Wie schon die erfindungsgemäßen Polymere enthaltend Struktureinheiten gemäß Formel (I) resultieren auch diese neuen Blends in steileren Strom-Spannungs-Kennlinien und damit in niedrigeren Betriebsspannungen.
- Ein weiterer Gegenstand der Erfindung sind also Blends (Mischungen) enthaltend
(A) 5 – 99,5 Gew.-% konjugierte Polymer (POLY2), das 1 – 100 mol%, bevorzugt 5 – 100 mol%, besonders bevorzugt 10 – 100 mol% Einheiten gemäß Formel (XXXII) Formel (XXXII) enthält, wobei die Symbole und Indizes folgende Bedeutung besitzen:
R3 ist bei jedem Auftreten gleich oder verschieden einer linearen oder verzweigten Alkylkette mit 1 bis 40 C-Atomen, die substituiert oder auch unsubstituiert sein kann, einem Cycloalkylsystem mit 3 bis 40 C-Atomen, das substituiert oder auch unsubstituiert sein kann, einem aromatischen oder heteroaromatischen Ringsystem mit 2 bis 40 C-Atomen, welches jeweils substituiert oder unsubstituiert sein kann, oder einem Alkylen-aryl-, Alkylen-cycloalkyl- oder Alkylen-heteroaryl-System, welches substituiert oder auch unsubstituiert sein kann; die möglichen Substituenten R1 können dabei potentiell an jeder freien Position sitzen; die Aryl- und Heteroaryl-Systeme können auch Teil eines größeren kondensierten aromatischen Ringsystems sein;
Aryl sind bei jedem Auftreten gleich oder verschieden einem aromatischen oder heteroaromatischen Ringsystem mit 2 bis 40 C-Atomen, welches substituiert oder auch unsubstituiert sein kann, oder eine substituierte oder unsubstituierte Stilbenylen- bzw. Tolanyleneinheit; die möglichen Substituenten R1 können dabei potentiell an jeder freien Position sitzen;
R1 ist bei jedem Auftreten gleich oder verschieden eine geradkettige, verzweigte oder cyclische Alkyl- oder Alkoxykette mit 1 bis 22 C-Atomen, in der auch ein oder mehrere nicht benachbarte C-Atome durch N-R2, O, S, -CO-O-, O-CO-O ersetzt sein können, wobei auch ein oder mehrere N-Atome durch Fluor ersetzt sein können, eine Aryl- oder Aryloxygruppe mit 5 bis 40 C-Atomen, bei der auch ein oder mehrere C-Atome durch O, S oder N ersetzt sein können, welche auch durch ein oder mehrere nicht-aromatische Reste R1 substituiert sein können, oder Cl, F, CN, N(R2)2, B(R2)2, wobei auch zwei oder mehrere Reste R1 miteinander ein Ringsystem bilden können;
Ra ist bei jedem Auftreten gleich oder verschieden eine geradkettige, verzweigte oder cyclische Alkyl- oder Alkoxykette mit 1 bis 22 C-Atomen, in der auch ein oder mehrere nicht benachbarte C-Atome durch N-R2, O, S, -CO-O-, O-CO-O ersetzt sein können, wobei auch ein oder mehrere N-Atome durch Fluor ersetzt sein können, eine Aryl- oder Aryloxygruppe mit 5 bis 40 C-Atomen, bei der auch ein oder mehrere C-Atome durch O, S oder N ersetzt sein können, welche auch durch ein oder mehrere nicht-aromatische Reste R1 substituiert sein können, oder Cl, F, CN, N(R2)2, B(R2)2,;
Rb ist bei jedem Auftreten gleich oder verschieden eine geradkettige, verzweigte oder cyclische Alkyl- oder Alkoxykette mit 1 bis 22 C-Atomen, in der auch ein oder mehrere nicht benachbarte C-Atome durch N-R2, O, S, -CO-O-, O-CO-O ersetzt sein können, wobei auch ein oder mehrere N-Atome durch Fluor ersetzt sein können, eine Aryl- oder Aryloxygruppe mit 5 bis 40 C-Atomen, bei der auch ein oder mehrere C-Atome durch O, S oder N ersetzt sein können, welche auch durch ein oder mehrere nicht-aromatische Reste R1 substituiert sein können, oder Cl, F, CN, N(R2)2, B(R2)2, wobei auch zwei oder mehrere Reste Rb miteinander ein Ringsystem bilden können;
R2 ist bei jedem Auftreten gleich oder verschieden H, eine geradkettige, verzweigte oder cyclische Alkylkette mit 1 bis 22 C-Atomen, in der auch ein oder mehrere nicht benachbarte C-Atome durch O, S, -CO-O-, O-CO-O ersetzt sein können, wobei auch ein oder mehrere H-Atome durch Fluor ersetzt sein können, eine Arylgruppe mit 5 bis 40 C-Atomen, bei der auch ein oder mehrere C-Atome durch O, S oder N ersetzt sein können, welche auch durch ein oder mehrere nicht-aromatische Reste R1 substituiert sein können;
m ist bei jedem Auftreten gleich oder verschieden 0, 1 oder 2;
o ist bei jedem Auftreten gleich oder verschieden 0, 1 oder 2, unter der Bedingung, dass o nicht 0 sein darf, wenn m = 2 ist;
r ist bei jedem Auftreten gleich oder verschieden 0 oder 1,
z ist bei jedem Auftreten gleich oder verschieden 0, 1, 2 oder 3.
(B) 0,5 – 95 Gew.-% mindestens eines organischen oder metallorganischen Dendrimeren oder mindestens eines niedermolekularen Moleküls im Molekulargewichtsbereich < 10.000 bedeutet (VERB1), welches im reinen oder verdünnten Film zu Fluoreszenz oder Phosphoreszenz befähigt ist, und welches eine ausreichende Löslichkeit in geeigneten Lösungsmitteln, bevorzugt Toluol, Xylol, Anisol, THF, Methylanisol oder Methylnaphathalin, aufweist, um im Blend gemeinsam mit dem Polymer aus Lösung in diesem Lösungsmittel verarbeitet zu werden. - Bevorzugt beträgt der Anteil des Dendrimers oder der niedermolekularen Verbindung im Blend 0,5 bis 80 Gew.-%, besonders bevorzugt 1 bis 50 Gew.-%, insbesondere 2 bis 25 Gew.-%.
- Bevorzugt beträgt der Anteil des Polymeren (POLY2) im Blend 20 bis 99,5 Gew.-%, besonders bevorzugt 50 bis 99 Gew.-%, insbesondere 75 bis 98 Gew.-%.
- Unter Dendrimer soll hier eine hochverzweigte Verbindung verstanden werden, die aus einem multifunktionellen Zentrum (core) aufgebaut ist, an das in einem regelmäßigen Aufbau verzweigte Monomere gebunden werden, so dass eine baumartige Struktur erhalten wird. Dabei können sowohl das Zentrum, als auch die Monomere beliebige verzweigte Strukturen annehmen, die sowohl aus rein organischen Einheiten, als auch Organometallverbindungen oder Koordinationsverbindungen bestehen. Dendrimer soll hier allgemein so verstanden werden, wie dies beispielsweise in M. Fischer, F. Vögtle, Angewandte Chemie, Int. Ed. 1999, 38, 885–905 beschrieben ist.
- Die Struktureinheit gemäß Formel (XXXII) ist Bestandteil von Homopolymeren und Copolymeren, wie bereits für die Struktureinheit gemäß Formel (I) beschrieben. Dabei kommen auch hier dieselben Comonomere wie beispielsweise die oben gezeigten Monomere M1 bis M23 in Frage. Die Synthese dieser Polymere kann nach den oben beschriebenen Methoden durchgeführt werden. Dabei hat sich gezeigt, dass für Blends, die aus dem Singulett-Zustand Licht emittieren, ein Anteil im Bereich von 10% Struktureinheiten gemäß Formel (XXXII) im Polymeren gute Ergebnisse erzielt. Für andere Anwendungen, insbesondere für Blends, die aus dem Triplett-Zustand Licht emittieren, kann es bevorzugt sein, einen höheren Anteil als 10% Struktureinheiten gemäß Formel (XXXII) im Polymeren vorliegen zu haben. Bevorzugt ist also für Blends, die aus dem Triplettzustand Licht emittieren, ein Anteil von 20 – 100 % Struktureinheiten gemäß Formel (XXXII). Besonders bevorzugt ist für diese Blends ein Anteil von 30 – 100 % Struktureinheiten gemäß Formel (XXXII).
- Für bevorzugte Polymere POLY2 gilt folgendes:
R3 ist bei jedem Auftreten gleich oder verschieden einer linearen oder verzweigten Alkylkette mit 1 bis 40 C-Atomen, die substituiert oder auch unsubstituiert sein kann, einem aromatischen oder heteroaromatischen Ringsystem, ausgewählt aus Thiophen, Benzothiophen, Benzol, Pyridin, Chinoxalin, Fluoren, Spirobifluoren, Naphthalin, Anthracen, Pyren oder Phenanthren, welches an den freien Positionen 0 bis 3 Substituenten R1 trägt, oder einem Alkylen-aryl- oder Alkylenheteroaryl-Ringsystem, dessen Alkylen-Kette linear oder verzweigt sein kann und aus 1 bis 16 C-Atomen besteht und dessen Aryl- und Heteroaryl-System aus den oben im einzelnen aufgeführten Systemen besteht, welche an den freien Positionen 0 bis 3 Substituenten R1 tragen;
die weiteren Symbole und Indizes haben dieselbe Bedeutung wie bereits oben für bevorzugte Strukturen gemäß Formel (I) beschrieben. - Für besonders bevorzugte Polymere POLY2 gilt folgendes:
R3 ist bei jedem Auftreten gleich oder verschieden einer linearen oder verzweigten Alkylkette mit 2 bis 30 C-Atomen, die substituiert oder auch unsubstituiert sein kann, einem aromatischen oder heteroaromatischen Ringsystem, ausgewählt aus Thiophen, Benzothiophen, Benzol, Pyridin, Naphthalin, Anthracen, Pyren oder Phenanthren, welche unsubstituiert oder mit einem Substituenten R1 substituiert sind, oder einem 9,9'-substituierten Fluoren oder einem Methylen-aryl- oder Methylen heteroaryl-Ringsystem, dessen Aryl- bzw. Heteroaryl-System aus den oben im einzelnen aufgeführten Systemen besteht, welche dasselbe Substitutionsmuster tragen können wie die oben genannten Systeme;
die weiteren Symbole und Indizes haben dieselbe Bedeutung wie bereits oben für besonders bevorzugte Strukturen gemäß Formel (I) beschrieben. - Für ganz besonders bevorzugte Polymere POLY2 gilt folgendes:
R3 ist bei jedem Auftreten gleich oder verschieden einer linearen oder verzweigten Alkylkette mit 3 bis 20 C-Atomen, die substituiert oder auch unsubstituiert sein kann, einem aromatischen oder heteroaromatischen Ringsystem, ausgewählt aus Thiophen, Benzothiophen, Benzol, Naphthalin, Anthracen, oder Phenanthren, welche unsubstituiert oder mit einem Substituenten R1 substituiert sind, oder einem Benzyl-Ringsystem, dessen Phenylgruppe dasselbe Substitutionsmuster tragen kann wie die oben genannten Systeme;
die weiteren Symbole und Indizes haben dieselbe Bedeutung wie bereits oben für ganz besonders bevorzugte Strukturen gemäß Formel (I) beschrieben. - Die im Blend verwendeten Dendrimere oder niedermolekularen Verbindungen VERB1 können aus den unterschiedlichsten Substanzklassen ausgewählt werden. Bevorzugt sind hier Dendrimere oder niedermolekulare Verbindungen, deren elektronische Eigenschaften die Anwendung des Polymers verbessern, indem sie beispielsweise die Ladungsinjektions-, Ladungstransport- oder Emissionseigenschaften des Blends günstig beeinflussen. Besonders bevorzugt sind hier Blends aus Polymeren POLY2 mit einem oder mehreren Dendrimeren oder einer oder mehreren niedermolekularen Verbindungen, welche einen Transfer von sogenannten Singulett-Excitonen zu Triplett-Excitonen ermöglichen und welche auch bei Raumtemperatur mit hoher Effizienz aus dem Triplettzustand Licht emittieren können: Dies sind zunächst vor allem Verbindungen, welche Schweratome, d. h. Atome aus dem Periodensystem der Elemente mit einer Ordnungszahl von mehr als 36, enthalten. Besonders geeignet sind hierfür Verbindungen, welche d- und f-Übergangsmetalle enthalten, die die o. g. Bedingung erfüllen. Ganz besonders bevorzugt sind hier entsprechende Struktureinheiten, welche Elemente der Gruppe 8 bis 10 (d. h. Ru, Os, Rh, Ir, Pd, Pt) enthalten. Als solche niedermolekularen Struktureinheiten kommen hier z. B. verschiedene Komplexe, welche beispielsweise in den Anmeldeschriften WO 02/068435, WO 02/081488,
EP 1239526 und der nicht offengelegten AnmeldeschriftDE 10238903.9 beschrieben sind, in Frage. Als Dendrimer-Strukturen kommen hierfür Komplexe, wie beispielsweise in den Anmeldeschriften WO 99/21935, WO 01/059030 und WO 02/066552 beschrieben sind, in Frage. Die entsprechenden Beschreibungen werden hiermit via Zitat als Bestandteil der Anmeldung erachtet. - Die erfindungsgemäßen Blends weisen gegenüber dem o. g. Stand der Technik u. a. folgende überraschenden Vorteile auf:
- – Der Strom bei gegebener Spannung ist bei vergleichbaren Blends bei der Verwendung in PLEDs deutlich höher (vgl. Angaben in Tabelle 3), d.h. die Strom-Spannungskennlinie ist steiler, wenn die Polymerkomponente des Blends Struktureinheiten der Formel (XXXII) enthält. Dies bringt für die Anwendung – wie oben bereits ausgeführt – deutliche Vorteile, da somit das Ziel, effiziente Vollfarbdisplays mit geringerem Energieverbrauch zu erzeugen, ermöglicht wird.
- – Überraschend hat die Verwendung von erfindungsgemäßen Blends mit Komponenten, die aus dem Triplett-Zustand emittieren, noch folgenden Vorteil: Der Energietransfer vom Polymer auf den Metallkomplex läuft in einem erfindungsgemäßen Blend effizienter ab als in vergleichbaren Blends, was zu einer effizienteren Emission des Metallkomplexes führt (vgl. Angaben in Tabelle 3).
- – Entsprechende Blends können so zusammengesetzt werden, dass diese alle Grundfarben (Rot, Grün, Blau) emittieren können. Dies ist zwar keine Verbesserung gegenüber dem Stand der Technik an sich, jedoch ist es wichtig, dass diese Eigenschaft bei Einführung von neuen Strukturen erhalten bleibt.
- – Die Löslichkeit in organischen Lösemitteln ist i. d. R. gut, d. h. in Lösemitteln, wie beispielsweise Toluol, Xylol, Anisol, Methylanisol oder Methylnaphthalin, sind die Polymere in Konzentrationen im Bereich von 1 bis mindestens 30 g/L (je nach Molekulargewicht) löslich. Als Lösemittel und Lösemittelgemische kommen beispielsweise diejenigen, wie sie in der Anmeldeschrift WO 02/072714 beschrieben bzw. zitiert sind, in Frage.
- Die erfindungsgemäßen Polymere oder die erfindungsgemäßen Blends können in PLEDs verwendet werden. Dazu wird in der Regel folgendes allgemeine Verfahren verwendet, das entsprechend für den Einzelfall anzupassen ist:
- – Ein Substrat (z. B. Glas oder auch ein Kunststoff, wie speziell behandeltes PET) wird mit einem transparenten Anodenmaterial beschichtet (beispielsweise Indium-Zinn-Oxid, ITO); anschließend wird die Anode (z. B. photolithografisch) der gewünschten Anwendung gemäß strukturiert und verschaltet. Es kann hier auch sein, dass das ganze Substrat und die entsprechende Verschaltung zunächst über einen recht aufwändigen Prozess erzeugt wird, um dadurch eine sogenannte Aktiv-Matrix-Steuerung zu ermöglichen.
- – Anschließend wird entweder vollflächig oder nur auf die aktiven (= anodischen) Stellen i. d. R. zunächst ein leitfähiges Polymer, z. B. ein dotiertes Polythiophen- oder Polyanilinderivat, aufgebracht. Dies erfolgt in aller Regel durch Beschichtungsverfahren, welche eine Dispersion des entsprechenden Polymers aufbringen. Hierzu eignen sich prinzipiell die weiter unten für das lichtemittierende Polymer beschriebenen Verfahren. Die Schichtdicke dieser Polymerlage kann in weiten Bereichen variieren, wird aber für die praktische Anwendung im Bereich zwischen 10 und 1000 nm, bevorzugt zwischen 20 und 500 nm liegen.
- – Darauf bringt man dann, je nach Anwendung, eine Lösung eines erfindungsgemäßen Polymers oder Blends auf. Für mehr- oder vollfarbige Anzeigeelemente (Displays) werden dann mehrere verschiedene Lösungen in verschiedenen Regionen aufgebracht, um entsprechende Farben zu erzeugen. Die erfindungsgemäßen Polymeren oder Blends werden dazu zunächst einzeln in einem Lösemittel oder Lösemittelgemisch gelöst und schließlich filtriert. Da die organischen Polymere und v. a. die Zwischenschichten (Interface) in der PLED teilweise extrem durch Sauerstoff oder andere Luftbestandteile beeinflusst werden, empfiehlt es sich, diese Operation unter Schutzgas durchzuführen. Als Lösemittel eignen sich aromatische Flüssigkeiten wie beispielsweise Toluol, Xylole, Anisol, Chlorbenzol, aber auch andere, wie beispielsweise cyclische Ether (z. B. Dioxan, Methyldioxan) oder auch Amide, wie beispielsweise NMP oder DMF, aber auch Lösemittelgemische, wie diese in der Anmeldeschrift WO 02/072714 beschrieben werden. Mit diesen Lösungen können die vorher beschriebenen Träger beschichtet werden, und zwar entweder ganzflächig z. B. durch Spin-Coat-Verfahren oder Rackel-Techniken, oder auch ortsaufgelöst durch Druckverfahren im weitesten Sinne, wie Tintenstrahldrucken, Off-Set-Drucken, Screen-Printing-Verfahren, Tiefdruckverfahren und ähnlichen.
- – Auf diese Polymerschichten können optional weitere Elektroneninjektionsmaterialien aufgebracht werden, z. B. durch Aufdampfen, oder auch aus Lösung, durch Methoden, wie diese für die emittierenden Polymere beschrieben wurden. Als Elektroneninjektionsmaterialien können beispielsweise niedermolekulare Verbindungen, wie Triarylboranverbindungen oder auch Aluminium-trishydroxychinolinat (Alq3), aber auch entsprechende Polymere, wie beispielsweise Poly-pyridinderivate und ähnliche, verwendet werden. Es ist auch möglich, dünne Schichten des emittierenden Polymers durch entsprechendes Dotieren in Elektroneninjektionsschichten umzuwandeln.
- – Daran anschließend wird eine Kathode aufgedampft. Dies erfolgt i. d. R. durch einen Vakuumprozess und kann beispielsweise sowohl durch thermisches Bedampfen als auch durch Plasmaspritzen (Sputtern) geschehen. Die Kathode kann dabei vollflächig oder auch durch eine Maske strukturiert aufgebracht werden. Als Kathode werden i. d. R. Metalle mit geringer Austrittsarbeit, z. B. Alkali-, Erdalkali- und f-Übergangsmetalle, wie z. B. Li, Ca, Mg, Sr, Ba, Yb, Sm oder Aluminium oder auch Legierungen von Metallen oder mehrlagige Strukturen mit verschiedenen Metallen verwendet. Bei letzterem können auch Metalle mitverwendet werden, die eine relativ hohe Austrittsarbeit aufweisen, wie z. B. Ag. Es kann auch bevorzugt sein, zwischen das Metall und das emittierende Polymer bzw. die Elektroneninjektionsschicht, eine sehr dünne dielektrische Schicht (z. B. LiF oder ähnliches) einzubringen. Die Kathoden sind i. d. R. zwischen 10 und 10000 nm, bevorzugt zwischen 20 und 1000 nm, dick.
- – Anschließend werden die so erzeugten PLEDs bzw. Displays entsprechend angeschlossen und verkapselt, um dann getestet oder verwendet zu werden.
- Wie oben beschrieben, eignen sich die erfindungsgemäßen Polymere und Blends ganz besonders als Elektroluminszenzmaterialien in den derart hergestellten PLEDs oder Displays.
- Als Elektrolumineszenzmaterialien im Sinne der Erfindung gelten Materialien, die als aktive Schicht in einer PLED Verwendung finden können. Aktive Schicht bedeutet, dass die Schicht befähigt ist, bei Anlegen eines elektrischen Feldes Licht abzustrahlen (lichtemittierende Schicht), und/oder dass sie die Injektion und/oder den Transport der positiven und/oder negativen Ladungen verbessert (Ladungsinjektions- oder Ladungstransportschicht).
- Gegenstand der Erfindung ist daher auch die Verwendung eines erfindungsgemäßen Polymers oder Blends in einer PLED, insbesondere als Elektrolumineszenzmaterial.
- Gegenstand der Erfindung ist somit ebenfalls eine PLED mit einer oder mehreren aktiven Schichten, wobei mindestens eine dieser aktiven Schichten ein oder mehrere erfindungsgemäße Polymere und/oder Blends enthält. Die aktive Schicht kann beispielsweise eine lichtemittierende Schicht und/oder eine Transportschicht und/oder eine Ladungsinjektionsschicht sein.
- PLEDs finden z.B. Anwendung als selbstleuchtende Anzeigeelemente, wie Kontrollampen, alphanumerische Displays, mehr- oder vollfarbigen Displays, Hinweisschilder und in optoelektronischen Kopplern.
- Im vorliegenden Anmeldetext und auch in den im weiteren folgenden Beispielen wird auf die Verwendung erfindungsgemäßer Polymere oder Blends aus erfindungsgemäßen Polymeren in Bezug auf PLEDs und den entsprechenden Displays abgezielt. Trotz dieser Beschränkung der Beschreibung ist es für den Fachmann ohne weiteres erfinderisches Zutun möglich, die erfindungsgemäßen Polymere auch für weitere Verwendungen in anderen elektronischen Devices (Vorrichtungen) zu benutzen, z. B. für organische Integrierte Schaltungen (O-ICs), in organischen Feld-Effekt-Transistoren (OFETs), in organischen Dünnfilmtransistoren (OTFTs), für organische Solarzellen (O-SCs), nicht-lineare Optik oder auch organische Laserdioden (O-Laser), um nur einige Anwendungen zu nennen. Gerade für O-ICs und OFETs können entsprechende erfindungsgemäße Polymere, welche einen relativ hohen Anteil an Strukturelementen gemäß Formel (I) besitzen (bevorzugt einen Anteil von mehr als 20%), Verwendung finden.
- Die Erfindung wird durch die nachfolgenden Beispiele näher erläutert, ohne sie dadurch einschränken zu wollen.
- Teil A: Synthese der Monomere und Blendbestandteile:
- A1: Monomere für Einheiten gemäß Formel (I)
- 3,6-Dibromcarbazol und 2,7-Dibromcarbazol wurden gemäß Smith et al., Tetrahedron 1992, 48(36), 7479–7488, und Tidwell et al., Eur. J. Med. Chem. 1997, 32(10), 781–793 synthetisiert.
- Die strukturelle Integrität aller Produkte wurde mittels 1H-NMR-Spektroskopie bewiesen, die Reinheit der Produkte wurde mittels HPLC bestimmt.
- Eine entgaste Lösung von 17g (80 mmol) 1-Brom-4-tert-butylbenzol (50 mmol) in 1500 mL Xylol wurde 1 h lang mit N2 gesättigt. Anschließend wurde die Lösung mit 500 g Glaskugeln (6mm) und 15.37 g (160 mmol) K3PO4 versetzt und 15 min. nachgerührt. Nach 5 min Rühren wurde die Reaktionsmischung mit 90 mg (0.4 mmol) Palladium(II)acetat, 400 mg (2 mmol) P(t-Bu)3 und 10 g (60 mmol) Carbazol versetzt. Die Reaktionsmischung wurde 4 h unter Rückfluss erhitzt. Nach Abkühlen wurde das Lösungsmittel im Vakuum entfernt und das Produkt aus n-Hexan umkristallisiert. Reinheit gem. HPLC: 99,6 %.
Ausbeute: 13 g (68%).
1H-NMR (CDCl3, 500 MHz): 1.42 (s, 9 H), 7.26 (t, J3 = 7.7 Hz, J4 = 1.3, 2H), 7.40 (m, 4H), 7.48 (d,J = 8.7 Hz, 2 H), 7.59 (d, J = 8.7 Hz, 2H), 8.14 (d, J = 8 Hz, 2 H). - 12 g (40 mmol) N-(4-tert-Butylphenyl)carbazol und 70 g Kieselgel wurden mit 700 mL CH2Cl2 vorgelegt. Anschließend wurde die Lösung unter Lichtausschluss bei 0°C portionsweise mit 13 g (80 mmol) NBS versetzt und 2 h bei dieser Temperatur gerührt. Anschließend wurde die Mischung mit 100 mL Wasser versetzt und mit CH2Cl2 extrahiert. Die organische Phase wurde mit MgSO4 getrocknet und die Lösungsmittel in Vakuum entfernt. Das Produkt wurde mit Hexan heiß ausgerührt und abgesaugt. Ausbeute: 11g (66 %) farbloses Pulver, welches eine HPLC-Reinheit von 99,2 % aufwies.
1H-NMR (CDCl3, 500 MHz): 1.42 (s, 9 H), 7.25 (d, J = 8.7 Hz, 2 H), 7.39 (d, J = 8.3 Hz, 2 H), 7.48 (dd, J3 = B. 7 Hz, J4 = 2 Hz, 2 H), 7.61 (d, J = 8.7 Hz, 2 H), 8.18 (d, J4 = 8 Hz, 2 H). - Eine entgaste Lösung von 489.5 mg (0.156%) Kupfer(I)chlorid und 906 mg (1 %) mmol) 1,10-Phenanthrolin in 100 mL Toluol wurde 1 h lang unter N2 gesättigt und auf 130°C erhitzt. Anschließend wurde die Lösung mit 16.2 g (50 mmol) 2,7-Dibromcarbazol und 13.2 g (50 mmol) 1-lod-4-tert-butylbenzol versetzt und 2 h auf 180°C erhitzt. Nach Abkühlen wurde die Mischung mit 180 ml Wasser versetzt, die organische Phase getrennt und das Lösungsmittel im Vakuum entfernt. Das Produkt wurde aus n-Hexan umkristallisiert.
Ausbeute: 13 g (59%). Reinheit gem. HPLC: 99.5 %
1H-NMR (CDCl3, 500 MHz): 1.43 (s, 9 H), 7.21 (t, J = 7.7 , 2 H), 7.23 (t, J = 7.7 , 2 H), 7.32 (dd, J3 = B. 7 Hz, J4 = 1.6 Hz, 2 H), 7.50 (d, J4 = 1.6 Hz, 2 H), 7.89 (d, J = 8.7 Hz, 2 H). - In einem 250 mL Einhalskolben mit Rückflusskühler wurde unter Schutzgas 990 mg (41.2 mmol) NaH in 80 mL trockenem DMF suspendiert. Zu dieser Reaktionsmischung wurden 10 g (30.8 mmol) 3,6-Dibromcarbazol in 80 mL DMF innerhalb 20 min bei RT zugetropft. Anschließend wurde eine Lösung 4-(Tert-butyl)benzylbromid in 50 mL DMF zugetropft und 8 h bei 60°C erhitzt. Nach Abkühlen auf Raumtemperatur wurden vorsichtig 300 mL Wasser und 200 mL Ethylacetat zugesetzt. Die organische Phase wurde mit 4 × 50 mL H2O gewaschen, dann mit MgSO4 getrocknet und die Lösungsmittel in Vakuum entfernt. Das reine Produkt erhielt man durch Umkristallisation aus n-Hexan. Ausbeute: 11 g (78%); HPLC-Reinheit 99.4%.
1H-NMR (CDCl3, 500 MHz): 1.22 (s, 9 H), 5.42 (s, 2 H), 6.98 (d, J = 8.7 Hz, 2H), 7.22 (d, J = 8.7 Hz, 2 H), 7.26 (d, J = 8.4 Hz, 2 H), 7.50 (dd, J3 = 8.4 Hz, J4 = 2 Hz, 2 H), 8.14 (d, J4 = 2 Hz, 2 H). - Beispiel 4: N-(4-tert-Butylphenyl)methyl-2,7-dibromcarbazol (EM4)
- Die Synthese erfolgte in Analogie zu Beispiel 3, ausgehend von 2,7-Dibromcarbazol. Die Ausbeute betrug 94 %.
1H-NMR (CDCl3, 500 MHz): 1.21 (s, 9 H), 5.41 (s, 2 H), 6.97 (d, J = 8.7 Hz, 2H), 7.23 (d, J = 8.7 Hz, 2 H), 7.33 (dd, J3 = 8.7 Hz, J4 = 1.6 Hz, 2 H), 7.51 (d, J4 = 1.6 Hz, 2 H), 7.88 (d, J = 8.7 Hz, 2 H). - In einem 250 mL Dreihalskolben wurden unter Schutzgas (32 mmol) EM1 in 100 mL trockenem THF gelöst. Nach Abkühlung auf –78°C injiziert man über ein Septum vorgekühltes BuLi (80 mmol, 15 %-ig) unter Rühren in die Lösung. Unter weiterer Kühlung werden nach 2 h bei –60°C 5.2 mL DMF zugetropft. Man ließ auf RT erwärmen und rührte über Nacht weiter. Anschließend wurden vorsichtig 200 mL Eiswasser zugesetzt und mit Chloroform extrahiert. Die organische Phase wurde mit MgSO4 getrocknet und die Lösungsmittel in Vakuum entfernt. Das reine Produkt erhielt man durch Umkristallisation aus n-Hexan. Ausbeute: 8 g (68%). Reinheit gem. HPLC: 99.1 %
1H-NMR (CDCl3, 500 MHz): 1.34 (s, 9 H), 6.38 (d, J = 8.1 Hz, 2 H), 6.82 (d, J = 8.7 Hz, 2 H), 7.04 (d, J = 8.1 Hz, 2 H), 7.18 (d, J = 8. 7 Hz, 2 H), 7. 31 (d, J = 8. 7 Hz, 2 H), 9. 2 (s, 2 H). - 32 mmol 4-Bromobenzyldiethylphosphonat wurden unter Schutzgas in 90 mL trockenem DMF gelöst und auf 5°C abgekühlt. Anschließend wurde 60 mmol NaOtBu in kleinen Portionen zugegeben, wobei die Temperatur 5°C nicht überstieg. Nach 30 min wurden 14.7 mmol EM5 in 25 mL DMF bei 5°C zugetropft und noch weitere 30 min bei dieser Temperatur gerührt. Das Reaktionsgemisch wurde abgekühlt, 25 mL 4 M HCl zugetropft und der Niederschlag abgesaugt. Anschließend wurden vorsichtig 100 mL Wasser zugesetzt und mit CH2Cl2 extrahiert. Die organische Phase wurde über MgSO4 getrocknet und die Lösungsmittel in Vakuum entfernt. Das reine Produkt erhielt man durch Umkristallisation aus Essigsäureethylester/CH2Cl2-Mischung (1:1). Ausbeute: 79 g (90%). Reinheit gemäß HPLC: 99.6
1H-NMR (CDCl3, 500 MHz): 1.33 (s, 9 H), 6.34 (d, J = 8.1 Hz, 2 H), 7.02 (d, J = 8.1 Hz, 2 H), 7.08 (d, J = 16.4 Hz, 2 H), 7.30 (d, J = 16.4 Hz, 2 H), 7.37 (d, J = 8.3 Hz, 2 H), 7.41 (d, J = 8.3 Hz, 4 H), 7.48 (d, J = 8.3 Hz, 4 H), 7.64 (dd, J3 = 8.3 Hz, J4 = 1.6 Hz, 2 H), 8.23 (d, J4 = 1.6 Hz, 2 H). - Weitere Monomere gemäß Formel (I) bzw. Formeln (II) bis (XXXI) wurden in Analogie zu den oben genannten Beispielen synthetisiert.
- A2: Monomere für weitere Einheiten
-
- A3: Niedermolekulare Verbindungen zur Verwendung in Blends
- Bei den hier in erfindungsgemäßen Blends beispielhaft verwendeten niedermolekularen Verbindungen handelt es sich beispielsweise um lösliche Derivate von triε-(Phenyl-pyridyl)-Iridium(III). Die Synthese dieser Verbindungen ist bereits beschrieben in der Anmeldeschrift WO 02/081488 und in der noch nicht offengelegten Patentanmeldung
DE 10238903.9 . Es sei jedoch an dieser Stelle nochmals eindeutig darauf hingewiesen, dass sich die erfindungsgemäßen Elends nicht auf diese hier verwendeten niedermolekularen Verbindungen beschränken, sondern dass die nicht-polymere Komponente die oben genauer spezifizierten Verbindungen VERB1 sein können. Zur Übersicht sind die beiden beispielhaft hier verwendeten Iridium-Komplexe im Folgenden nochmals aufgeführt: - Teil B: Herstellung der Polymere und Blends
- Synthese von Polymer P1:
- 3,2026 g (4 mmol) Monomer M2, 1,6237 g (2,4 mmol) Monomer M7, 0,6069 g (0,8 mmol) Monomer M9, 0,3770 g (0,8 mmol) EM1 und 3,91 g (2.125 Äquivalente) Kaliumphosphat Hydrat wurden gelöst in 37,5 ml Dioxan, 12,5 ml Toluol und 6,8 ml H2O (alle Lösungsmittel sauerstofffrei). Die Reaktionslösung wurde 30 Minuten bei 40°C mit Argon entgast. Dann wurden 0,45 mg (0,025 %) Pd(OAc)2 und 3,65 mg (0,15 %) P(o-tolyl)3 als Katalysator zugegeben, und die Lösung wurde 1,5 h unter Rückfluss unter einer Argon-Atmosphäre erhitzt. Die hochviskose Polymerlösung wurde mit 20 ml Toluol verdünnt. Dann wurde das Endcapping durchgeführt, indem 100 mg Benzolboronsäure zugegeben wurden, 45 Minuten unter Rückfluss erhitzt, dann Zugabe von 0,2 ml Brombenzol und weitere 45 Minuten unter Rückfluss erhitzt. Die Polymerlösung wurde bei 60°C mit 100 ml 0,01 %-iger wässriger NaCN-Lösung 3 h gerührt. Dann wurden die Phasen getrennt und die organische Phase mit 4 × 100 ml H2O gewaschen. Das Polymer wurde durch Zugabe des doppelten Volumens an Methanol ausgefällt und filtriert. Weitere Reinigung erfolgte durch Lösen in 200 ml Toluol bei 60°C unter Argon, Filtration durch eine Glasfritte und erneute Ausfällung durch Zugabe des doppelten Volumens Methanol. Das Polymer wurde filtriert und unter Vakuum getrocknet. Es wurden 4,85 g (96 % d. Th.) Polymer isoliert, Mw = 578.000, Mn = 156.000, Polydispersität = 3,7.
- Synthese von Polymer P2:
- 3,2026 g (4 mmol) Monomer M2, 1,0825 g (1,6 mmol) Monomer M7, 0,6069 g (0,8 mmol) Monomer M9, 0,8185 g (0,8 mmol) Monomer M19, 0,3658 g (0,8 mmol) EM4 und 3,91 g (2.125 Äquivalente) Kaliumphosphat Hydrat wurden gelöst in 25 ml Dioxan, 25 ml Toluol und 6,8 ml H2O (alle Lösungsmittel sauerstofffrei). Die Reaktionslösung wurde 30 Minuten bei 40°C mit Argon entgast. Dann wurden 0,45 mg (0,025 %) Pd(OAc)2 und 3,65 mg (0,15 %) P(o-tolyl)3 als Katalysator zugegeben, und die Lösung wurde 4 h unter Rückfluss unter einer Argon-Atmosphäre erhitzt. Die hochviskose Polymerlösung wurde mit 60 ml Toluol verdünnt. Dann wurde das Endcapping durchgeführt, indem 100 mg Benzolboronsäure zugegeben wurden, 45 Minuten unter Rückfluss erhitzt, dann Zugabe von 0,2 ml Brombenzol und 30 ml Toluol und weitere 45 Minuten unter Rückfluss erhitzt. Die Polymerlösung wurde bei 60°C mit 100 ml 0,01 %-iger wässriger NaCN-Lösung 3 h gerührt. Dann wurden die Phasen getrennt und die organische Phase mit 4 × 100 ml H2O gewaschen. Das Polymer wurde durch Zugabe des doppelten Volumens an Methanol ausgefällt und filtriert. Weitere Reinigung erfolgte durch Lösen in 300 ml Toluol bei 60°C unter Argon, Filtration durch eine Glasfritte und erneute Ausfällung durch Zugabe des doppelten Volumens Methanol. Das Polymer wurde filtriert und unter Vakuum getrocknet. Es wurden 4,57 g (92 % d. Th.) Polymer isoliert, Mw = 791.000, Mn = 239.000, Polydispersität = 3,3.
- Weitere Polymere wurden analog den Beschreibungen für P1 und P2 dargestellt. Die chemischen Eigenschaften sind in Tabelle 1 zusammengefasst. Es wurden auch einige Vergleichspolymere (die keine Einheiten gemäß Formel (I) enthalten) dargestellt. Auch diese sind in der Tabelle mit aufgeführt.
- Herstellung der Blends:
- Die Synthese der Blends erfolgt durch Lösen des Polymers zusammen mit dem Dendrimer oder der niedermolekularen Verbindung im gewünschen Verhältnis zueinander in einem geeigneten Lösungsmittel wie beispielsweise Toluol, Xylol, THF, Chlorbenzol oder Anisol und direktes Verarbeiten der Lösung ohne Isolierung des Blends in fester Substanz.
- All diese Polymere und Blends wurden auch für einen Einsatz in PLEDs untersucht. Wie PLEDs dargestellt werden können, ist zum einen oben schon ausgeführt und wird detaillierter noch in Teil C beschrieben.
- Auch einige Device-Eigenschaften (Farbe, Effizienz und Betriebsspannung) sind in der Tabelle 1 mit aufgeführt.
- In Tabelle 2 und
1 sind die Strom-Spannungs-Charakteristika einiger Polymere dokumentiert. Hier kann man sehr gut erkennen, dass die Kurven bei den erfindungsgemäßen Polymeren deutlich steiler ansteigen und der Strom bei gegebener Spannung bei den erfindungsgemäßen Polymeren und Blends deutlich höher ist als bei den Vergleichspolymeren bzw. Blends aus unkonjugierten Polymeren mit niedermolekularen Verbindungen gemäß Stand der Technik. - In Tabelle 3 sind einige Device-Eigenschaften (Farbe, Effizienz und Betriebsspannung) von erfindungsgemäßen Blends aufgeführt und verglichen mit Blends, die dem Stand der Technik entsprechen.
- Vergleich des Stroms bei unterschiedlichen Spannungen (am Beispiel eines erfindungsgemäßen Polymeren und zwei Polymeren ähnlicher Zusammensetzung, die jedoch keine Struktureinheiten gemäß Formel (I) enthalten).
- Vergleich der Strom-Spannungs-Kennlinien für das erfindungsgemäße Polymer P5 (enthaltend 10% Carbazol) mit dem Vergleichspolymer V2 (enthaltend 10% des Lochleiters M9, aber kein Carbazol) und mit dem Vergleichspolymer V4 (enthaltend keinen anderen Lochleiter und auch kein Carbazol).
- Teil C: Herstellung und Charakterisierung von LEDs:
- Die Herstellung von LEDs erfolgte nach dem im Folgenden skizzierten allgemeinen Verfahren. Dieses musste im Einzelfall auf die jeweiligen Gegebenheiten (z. B. Polymerviskosität und optimale Schichtdicke des Polymers im Device) angepasst werden. Die im nachfolgenden beschriebenen LEDs waren jeweils Zweischichtsysteme, d. h. Substrat//ITO//PEDOT//Polymer//Kathode.
- PEDOT ist ein Polythiophen-Derivat.
- Allgemeines Verfahren zur Herstellung von hocheffizienten, langlebigen LEDs:
- Nachdem man die ITO-beschichteten Substrate (z. B. Glasträger, PET-Folie) auf die richtige Größe zugeschnitten hat, werden sie in mehreren Reinigungsschritten im Ultraschallbad gereinigt (z.B. Seifenlösung, Millipore-Wasser, Isopropanol).
- Zur Trocknung werden sie mit einer N2-Pistole abgepustet und in einem Exsikkator gelagert. Vor der Beschichtung mit dem Polymer werden sie mit einem Ozon-Plasma-Gerät für ca. 20 Minuten behandelt. Von dem jeweiligen Polymer oder Blend wird eine Lösung (in der Regel mit einer Konzentration von 4–25 mg/ml in beispielsweise Toluol, Chlorbenzol, Xylol:Cyclohexanon (4:1)) angesetzt und durch Rühren bei Raumtemperatur gelöst. Je nach Polymer kann es auch vorteilhaft sein, für einige Zeit bei 50 – 70°C zu rühren. Hat sich das Polymer vollständig gelöst, wird es durch einen 5μm Filter filtriert und bei variablen Geschwindigkeiten (400–6000) mit einem Spin-coater aufgeschleudert. Die Schichtdicken können dadurch im Bereich von ca. 50 und 300nm variiert werden. Vorab wird meist auf das (strukturierte) ITO ein leitfähiges Polymer, bevorzugt gedoptes PEDOT oder PANI, aufgebracht.
- Auf die Polymerfilme werden noch Elektroden aufgebracht. Dies geschieht in der Regel durch thermisches Verdampfen (Balzer BA360 bzw. Pfeiffer PL S 500). Anschließend wird die durchsichtige ITO-Elektrode als Anode und die Metallelektrode (z. B. Ba, Yb, Ca) als Kathode kontaktiert und die Device-Parameter bestimmt.
- Die mit den beschriebenen Polymeren erhaltenen Resultate sind in den Tabellen in Teil B zusammengefasst.
Claims (26)
- Polymere die 1 – 100 mol% Einheiten gemäß Formel (I) enthalten, FORMEL (I) wobei die Symbole und Indizes folgende Bedeutung besitzen: R ist bei jedem Auftreten gleich oder verschieden einem Cycloalkylsystem mit 3 bis 40 C-Atomen, welches substituiert oder unsubstituiert sein kann, einem aromatischen oder heteroaromatischen Ringsystem mit 2 bis 40 C-Atomen, welches substituiert oder unsubstituiert sein kann, oder einem Alkylen-aryl-, Alkylen-cycloalkyl- oder Alkylen-heteroaryl-System mit linearer oder verzweigter Alkylkette mit 1 bis 16 C-Atomen, welches substituiert oder auch unsubstituiert sein kann; die Aryl- und Heteroaryl-Systeme können dabei auch Teil eines größeren kondensierten aromatischen Ringsystems sein; die möglichen Substituenten R1 können potentiell an jeder freien Position sitzen; Aryl sind bei jedem Auftreten gleich oder verschieden einem aromatischen oder heteroaromatischen Ringsystem mit 2 bis 40 C-Atomen, welches substituiert oder auch unsubstituiert sein kann, oder eine substituierte oder unsubstituierte Stilbenylen- bzw. Tolanyleneinheit; die möglichen Substituenten R1 können dabei potentiell an jeder freien Position sitzen; R1 ist bei jedem Auftreten gleich oder verschieden eine geradkettige, verzweigte oder cyclische Alkyl- oder Alkoxykette mit 1 bis 22 C-Atomen, in der auch ein oder mehrere nicht benachbarte C-Atome durch N-R2, O, S, -CO-O-, O-CO-O ersetzt sein können, wobei auch ein oder mehrere H-Atome durch Fluor ersetzt sein können, eine Aryl- oder Aryloxygruppe mit 5 bis 40 C-Atomen, bei der auch ein oder mehrere C-Atome durch O, S oder N ersetzt sein können, welche auch durch ein oder mehrere nicht-aromatische Reste R1 substituiert sein können, oder Cl, F, CN, N(R2)2, B(R2)2, wobei auch zwei oder mehrere Reste R' miteinander ein Ringsystem bilden können; Ra ist bei jedem Auftreten gleich oder verschieden eine geradkettige, verzweigte oder cyclische Alkyl- oder Alkoxykette mit 1 bis 22 C-Atomen, in der auch ein oder mehrere nicht benachbarte C-Atome durch N-R2, O, S, -CO-O-, O-CO-O ersetzt sein können, wobei auch ein oder mehrere H-Atome durch Fluor ersetzt sein können, eine Aryl- oder Aryloxygruppe mit 5 bis 40 C-Atomen, bei der auch ein oder mehrere C-Atome durch O, S oder N ersetzt sein können, welche auch durch ein oder mehrere nicht-aromatische Reste R1 substituiert sein können, oder Cl, F, CN, N(R2)2, B(R2)2,; Rb ist bei jedem Auftreten gleich oder verschieden eine geradkettige, verzweigte oder cyclische Alkyl- oder Alkoxykette mit 1 bis 22 C-Atomen, in der auch ein oder mehrere nicht benachbarte C-Atome durch N-R2, O, S, -CO-O-, O-CO-O ersetzt sein können, wobei auch ein oder mehrere H-Atome durch Fluor ersetzt sein können, eine Aryl- oder Aryloxygruppe mit 5 bis 40 C-Atomen, bei der auch ein oder mehrere C-Atome durch O, S oder N ersetzt sein können, welche auch durch ein oder mehrere nicht-aromatische Reste R1 substituiert sein können, oder Cl, F, CN, N(R2)2, B(R2)2, wobei auch zwei oder mehrere Reste Rb miteinander ein Ringsystem bilden können; R2 ist bei jedem Auftreten gleich oder verschieden H, eine geradkettige, verzweigte oder cyclische Alkylkette mit 1 bis 22 C-Atomen, in der auch ein oder mehrere nicht benachbarte C-Atome durch O, S, -CO-O-, O-CO-O ersetzt sein können, wobei auch ein oder mehrere H-Atome durch Fluor ersetzt sein können, eine Arylgruppe mit 5 bis 40 C-Atomen, bei der auch ein oder mehrere C-Atome durch O, S oder N ersetzt sein können, welche auch durch ein oder mehrere nicht-aromatische Reste R1 substituiert sein können; m ist bei jedem Auftreten gleich oder verschieden 0, 1 oder 2; o ist bei jedem Auftreten gleich oder verschieden 0, 1 oder 2, unter der Bedingung, dass o nicht 0 sein darf, wenn m = 2 ist; r ist bei jedem Auftreten gleich oder verschieden 0 oder 1, z ist bei jedem Auftreten gleich oder verschieden 0, 1, 2 oder 3.
- Polymere gemäß Anspruch 1, dadurch gekennzeichnet, dass die Einheiten gemäß Formel (I) über die Position 2 oder die Position 3 des Carbazols mit der Hauptkette des Polymers verknüpft sind.
- Polymere gemäß Anspruch 1 dadurch gekennzeichnet, dass die Struktureinheiten gemäß Formel (I) über die Positionen 3 und 6 des Carbazols oder über die Positionen 2 und 7 des Carbazols in die Polymerkette eingebaut sind.
- Polymere gemäß Anspruch 1 dadurch gekennzeichnet, dass die Struktureinheiten gemäß Formel (I) über die Positionen 3 und 9 des Carbazols oder über die Positionen 2 und 9 des Carbazols in die Polymerkette eingebaut sind, sofern R ein Aryl- oder Heteroarylsystem ist, so dass die Konjugation der Kette erhalten bleibt.
- Polymere gemäß Anspruch 4 dadurch gekennzeichnet, dass die weiteren Strukturelemente aus den Gruppen ortho-, meta- oder para-Phenylene, 1,4-Naphthylene, 9,10-Anthracenylene, 2,7-Phenanthrenylene, 1,6- bzw. 2,7- bzw. 4,9-Pyrene oder 2,7-Tetrahydropyrene, Oxadiazolylene, 2,5-Thiophenylene, 2,5-Pyrrolylene; 2,5-Furanylene, 2,5-Pyridylene, 2,5-Pyrimidinylene, 5,8-Chinolinylene, Fluorene, Spiro-9,9'-bifluorene, Indenofluorene oder Heteroindenofluorene ausgewählt sind.
- Polymere gemäß Anspruch 4 und/oder 5 dadurch gekennzeichnet, dass weitere Strukturelemente anwesend sind, die Ladungstransport und/oder -injektion verbessern.
- Polymere gemäß einem oder mehreren der Ansprüche 4 bis 6 dadurch gekennzeichnet, dass die weiteren Strukturelemente aus den Gruppen der Triarylamine bzw. der Oxadiazolylene ausgewählt sind.
- Polymere gemäß einem oder mehreren der Ansprüche 4 bis 7 dadurch gekennzeichnet, dass die weiteren Strukturelemente aus Gruppen, die die Farbe der Emission verschieben, damit auch die Bandlücke des Polymers verändern und somit i. d. R. auch die Ladungsinjektions- bzw. -transporteigenschaften verändern, ausgewählt sind.
- Polymere gemäß einem oder mehreren der Ansprüche 4 bis 8 dadurch gekennzeichnet, dass die weiteren Strukturelemente aus den Gruppen Arylen-vinylen- oder Arylen-acetylen-strukturen, wie substituierten oder unsubstituierten Stilbenyle, Tolanyle, Bisstyrylarylene, Bis(arylacetylen)-arylene und/oder größeren aromatischen Einheiten, wie Chrysenen, Naphthacenen, Pentacenen, Perylenen oder Coronenen, ausgewählt sind.
- Polymere gemäß einem oder mehreren der Ansprüche 4 bis 9 dadurch gekennzeichnet, dass sie Metallkomplexe enthalten, welche einen Transfer von Singulett-Excitonen zu Triplett-Excitonen ermöglichen und die aus dem Triplettzustand Licht emittieren.
- Polymere gemäß Anspruch 10 dadurch gekennzeichnet, dass die weiteren Strukturelemente d- und f-Übergangsmetalle, enthalten.
- Polymere gemäß Anspruch 10 und/oder 11 dadurch gekennzeichnet, dass die weiteren Strukturelemente Metalle der Gruppe 8 bis 10 enthalten.
- Polymere gemäß einem oder mehreren der Ansprüche 1 bis 12 dadurch gekennzeichnet, dass für die Symbole und Indizes folgendes gilt: R ist bei jedem Auftreten gleich oder verschieden einem aromatischen oder heteroaromatischen Ringsystem, ausgewählt aus Thiophen, Benzothiophen, Benzol, Naphthalin, Anthracen, oder Phenanthren, welche unsubstituiert oder mit einem Substituenten R1 substituiert sind, oder einem Benzyl-Ringsystem, dessen Phenylgruppe dasselbe Substitutionsmuster trägt wie die oben genannten Systeme; Aryl ist bei jedem Auftreten gleich oder verschieden einem aromatischen oder heteroaromatischen Ringsystem, ausgewählt aus Thiophen, Benzol, Pyridin, Fluoren, Spirobifluoren, Anthracen, Phenanthren, Pyren, Chinolin oder Naphthalin, welches an den freien Positionen 0 bis 2 Substituenten R1 trägt; R1, R2, o, r, z sind wie in Anspruch 1 beschrieben; m ist bei jedem Auftreten gleich oder verschieden 0 oder 1.
- Polymere gemäß einem oder mehreren der Ansprüche 1 bis 13 dadurch gekennzeichnet, dass die Strukturelemente gemäß Formel (I) aus den Formeln (II) bis (XXXI) ausgewählt werden, die substituiert oder unsubstituiert sein können.
- Polymere gemäß einem oder mehreren der Ansprüche 1 bis 14 dadurch gekennzeichnet, dass im Durchschnitt pro Wiederholeinheit mindestens 2 nichtaromatische C-Atome in den Substituenten vorhanden sind.
- Polymere gemäß einem oder mehreren der Ansprüche 1 bis 15 dadurch gekennzeichnet, dass keine Substituenten mit mehr als 12 C-Atomen in einer linearen Kette enthalten sind.
- Polymere gemäß einem oder mehreren der Ansprüche 1 bis 16 dadurch gekennzeichnet, dass diese durch SUZUKI-Kopplung, YAMAMOTO-Kopplung, STILLE-Kopplung, WITTIG-HORNER-Reaktion oder einem Precursor-Verfahren hergestellt werden.
- Mischungen, von einem Polymeren gemäß einem oder mehreren der Ansprüche 1 bis 17 mit konjugierten oder nicht-konjugierten Polymeren.
- Mischungen enthaltend (A) 5 – 99,5 Gew.-% konjugierte Polymer (POLY2), das 1 – 100 mol%, bevorzugt 5 – 100 mol%, besonders bevorzugt 10 – 100 mol% Einheiten gemäß Formel (XXXII) Formel (XXXII) enthält, wobei die Symbole und Indizes folgende Bedeutung besitzen: R3 ist bei jedem Auftreten gleich oder verschieden einer linearen oder verzweigten Alkylkette mit 1 bis 40 C-Atomen, die substituiert oder auch unsubstituiert sein kann, einem Cycloalkylsystem mit 3 bis 40 C-Atomen, das substituiert oder auch unsubstituiert sein kann, einem aromatischen oder heteroaromatischen Ringsystem mit 2 bis 40 C-Atomen, welches jeweils substituiert oder unsubstituiert sein kann, oder einem Alkylen-aryl-, Alkylen-cycloalkyl- oder Alkylen-heteroaryl-System, welches substituiert oder auch unsubstituiert sein kann; die möglichen Substituenten R1 können dabei potentiell an jeder freien Position sitzen; die Aryl- und Heteroaryl-Systeme können auch Teil eines größeren kondensierten aromatischen Ringsystems sein; Aryl sind bei jedem Auftreten gleich oder verschieden einem aromatischen oder heteroaromatischen Ringsystem mit 2 bis 40 C-Atomen, welches substituiert oder auch unsubstituiert sein kann, oder eine substituierte oder unsubstituierte Stilbenylen- bzw. Tolanyleneinheit; die möglichen Substituenten R1 können dabei potentiell an jeder freien Position sitzen; R1 ist bei jedem Auftreten gleich oder verschieden eine geradkettige, verzweigte oder cyclische Alkyl- oder Alkoxykette mit 1 bis 22 C-Atomen, in der auch ein oder mehrere nicht benachbarte C-Atome durch N-R2, O, S, -CO-O-, O-CO-O ersetzt sein können, wobei auch ein oder mehrere H-Atome durch Fluor ersetzt sein können, eine Aryl- oder Aryloxygruppe mit 5 bis 40 C-Atomen, bei der auch ein oder mehrere C-Atome durch O, S oder N ersetzt sein können, welche auch durch ein oder mehrere nicht-aromatische Reste R' substituiert sein können, oder Cl, F, CN, N(R2)2, B(R2)2, wobei auch zwei oder mehrere Reste R' miteinander ein Ringsystem bilden können; Ra ist bei jedem Auftreten gleich oder verschieden eine geradkettige, verzweigte oder cyclische Alkyl- oder Alkoxykette mit 1 bis 22 C-Atomen, in der auch ein oder mehrere nicht benachbarte C-Atome durch N-R2, O, S, -CO-O-, O-CO-O ersetzt sein können, wobei auch ein oder mehrere H-Atome durch Fluor ersetzt sein können, eine Aryl- oder Aryloxygruppe mit 5 bis 40 C-Atomen, bei der auch ein oder mehrere C-Atome durch O, S oder N ersetzt sein können, welche auch durch ein oder mehrere nicht-aromatische Reste R1 substituiert sein können, oder Cl, F, CN, N(R2)2, B(R2)2,; Rb ist bei jedem Auftreten gleich oder verschieden eine geradkettige, verzweigte oder cyclische Alkyl- oder Alkoxykette mit 1 bis 22 C-Atomen, in der auch ein oder mehrere nicht benachbarte C-Atome durch N-R2, O, S, -CO-O-, O-CO-O ersetzt sein können, wobei auch ein oder mehrere H-Atome durch Fluor ersetzt sein können, eine Aryl- oder Aryloxygruppe mit 5 bis 40 C-Atomen, bei der auch ein oder mehrere C-Atome durch O, S oder N ersetzt sein können, welche auch durch ein oder mehrere nicht-aromatische Reste R1 substituiert sein können, oder Cl, F, CN, N(R2)2, B(R2)2, wobei auch zwei oder mehrere Reste Rb miteinander ein Ringsystem bilden können; R2 ist bei jedem Auftreten gleich oder verschieden H, eine geradkettige, verzweigte oder cyclische Alkylkette mit 1 bis 22 C-Atomen, in der auch ein oder mehrere nicht benachbarte C-Atome durch O, S, -CO-O-, O-CO-O ersetzt sein können, wobei auch ein oder mehrere H-Atome durch Fluor ersetzt sein können, eine Arylgruppe mit 5 bis 40 C-Atomen, bei der auch ein oder mehrere C-Atome durch O, S oder N ersetzt sein können, welche auch durch ein oder mehrere nicht-aromatische Reste R1 substituiert sein können; m ist bei jedem Auftreten gleich oder verschieden 0, 1 oder 2; o ist bei jedem Auftreten gleich oder verschieden 0, 1 oder 2, unter der Bedingung, dass o nicht 0 sein darf, wenn m = 2 ist; r ist bei jedem Auftreten gleich oder verschieden 0 oder 1, z ist bei jedem Auftreten gleich oder verschieden 0, 1, 2 oder 3. (B) 0,5 – 95 Gew.-% mindestens eines organischen oder metallorganischen Dendrimeren oder mindestens eines niedermolekularen Moleküls im Molekulargewichtsbereich < 10.000 bedeutet (VERB1), welches im reinen oder verdünnten Film zu Fluoreszenz oder Phosphoreszenz befähigt ist, und welches eine ausreichende Löslichkeit in geeigneten Lösungsmitteln, bevorzugt Toluol, Xylol, Anisol, THF, Methylanisol oder Methylnaphathalin, aufweist, um im Blend gemeinsam mit dem Polymer aus Lösung in diesem Lösungsmittel verarbeitet zu werden.
- Blends gemäß Anspruch 19, dadurch gekennzeichnet, dass die elektronischen Eigenschaften der niedermolekularen Komponente bzw. des Dendrimers VERB1 die Ladungstransport-, Ladungsinjektions- oder Emissionseigenschaften des Blends in der Anwendung verbessern.
- Blends gemäß Anspruch 19 bis 21 dadurch gekennzeichnet, dass die Komponente VERB1 des Blends aus einem oder mehreren Metallkomplexen besteht, welche einen Transfer von sogenannten Singulett-Excitonen zu Triplett-Excitonen ermöglichen und aus dem Triplettzustand Licht emittieren.
- Blends gemäß Anspruch 19 bis 21 dadurch gekennzeichnet, dass die VERB1 aus Strukturelementen, enthaltend d- und f-Übergangsmetalle, besteht.
- Blends gemäß Anspruch 19 bis 23 dadurch gekennzeichnet, dass die VERB1 aus Strukturelementen, enthaltend Übergangsmetalle der Gruppen 8 bis 10, besteht.
- Blends gemäß Anspruch 19 bis 24 dadurch gekennzeichnet, dass POLY2 30 – 100 % Struktureinheiten gemäß Formel (XXXII) enthält.
- Verwendung eines Polymers oder eines Blends gemäß einem oder mehreren der Ansprüche 1 bis 24 in organischen Integrierten Schaltungen (O-ICs), in organischen Feld-Effekt-Transistoren (OFETs), in organischen Dünnfilmtransistoren (OTFTs), in organischen Solarzellen (O-SCs), organischen Leuchtdioden (OLED), organischen Laserdioden (O-Laser) oder in der nichtlinearen Optik, aber insbesondere als Elektrolumineszenzmaterial.
- Elektronisches Bauteil, insbesondere eine organische Leuchtdiode, welches eine oder mehrere aktiven Schichten umfasst, wobei mindestens eine dieser aktiven Schichten ein oder mehrere Polymere oder Blends gemäß einem oder mehreren der Ansprüche 1 bis 24 enthält.
Priority Applications (11)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE10304819A DE10304819A1 (de) | 2003-02-06 | 2003-02-06 | Carbazol-enthaltende konjugierte Polymere und Blends, deren Darstellung und Verwendung |
| KR1020057014550A KR101041766B1 (ko) | 2003-02-06 | 2004-02-04 | 카르바졸을 함유하는 공액 중합체 및 배합물, 그의제조방법 및 용도 |
| EP08003260A EP1932866B1 (de) | 2003-02-06 | 2004-02-04 | Blends enthaltend konjugierte Carbazol-Polymere, deren Darstellung und Verwendung |
| JP2006501725A JP4566185B2 (ja) | 2003-02-06 | 2004-02-04 | カルバゾールを含有する共役系ポリマー及びブレンド、その製造及びその使用 |
| EP04707888A EP1592729B1 (de) | 2003-02-06 | 2004-02-04 | Carbazol-enthaltende konjugierte polymere und blends, deren darstellung und verwendung |
| CNB2004800037941A CN100360579C (zh) | 2003-02-06 | 2004-02-04 | 含有咔唑的共轭聚合物和掺和物及其制备和用途 |
| CN2007101863516A CN101333328B (zh) | 2003-02-06 | 2004-02-04 | 含有咔唑的共轭聚合物和掺和物及其制备和用途 |
| US10/544,437 US7834136B2 (en) | 2003-02-06 | 2004-02-04 | Conjugated polymers and blends containing carbazole, representation and use thereof |
| PCT/EP2004/000994 WO2004070772A2 (de) | 2003-02-06 | 2004-02-04 | Carbazol-enthaltende konjugierte polymere und blends, deren darstellung und verwendung |
| DE502004006904T DE502004006904D1 (de) | 2003-02-06 | 2004-02-04 | Carbazol-enthaltende konjugierte polymere und blends, deren darstellung und verwendung |
| US12/911,119 US8053547B2 (en) | 2003-02-06 | 2010-10-25 | Conjugated polymers and blends containing carbazole, representation and use thereof |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE10304819A DE10304819A1 (de) | 2003-02-06 | 2003-02-06 | Carbazol-enthaltende konjugierte Polymere und Blends, deren Darstellung und Verwendung |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| DE10304819A1 true DE10304819A1 (de) | 2004-08-19 |
Family
ID=32730814
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| DE10304819A Withdrawn DE10304819A1 (de) | 2003-02-06 | 2003-02-06 | Carbazol-enthaltende konjugierte Polymere und Blends, deren Darstellung und Verwendung |
| DE502004006904T Expired - Lifetime DE502004006904D1 (de) | 2003-02-06 | 2004-02-04 | Carbazol-enthaltende konjugierte polymere und blends, deren darstellung und verwendung |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| DE502004006904T Expired - Lifetime DE502004006904D1 (de) | 2003-02-06 | 2004-02-04 | Carbazol-enthaltende konjugierte polymere und blends, deren darstellung und verwendung |
Country Status (7)
| Country | Link |
|---|---|
| US (2) | US7834136B2 (de) |
| EP (2) | EP1592729B1 (de) |
| JP (1) | JP4566185B2 (de) |
| KR (1) | KR101041766B1 (de) |
| CN (2) | CN100360579C (de) |
| DE (2) | DE10304819A1 (de) |
| WO (1) | WO2004070772A2 (de) |
Cited By (52)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2005014689A2 (de) | 2003-08-12 | 2005-02-17 | Covion Organic Semiconductors Gmbh | Konjugierte polymere enthaltend dihydrophenanthren-einheiten und deren verwendung |
| EP1927610A2 (de) | 2003-08-12 | 2008-06-04 | Merck Patent GmbH | Prozeß zur Herstellung von Aryl- oder Heteroarylamin-Boronsäurederivaten |
| DE102008049037A1 (de) | 2008-09-25 | 2010-04-22 | Merck Patent Gmbh | Neue Polymere mit niedriger Polydispersität |
| US7728137B2 (en) | 2003-03-11 | 2010-06-01 | Merck Patent Gmbh | Metal complexes |
| US7790057B2 (en) | 2006-07-11 | 2010-09-07 | Merck Patent Gmbh | Electroluminescent polymers and use thereof |
| WO2011015265A2 (en) | 2009-08-04 | 2011-02-10 | Merck Patent Gmbh | Electronic devices comprising multi cyclic hydrocarbons |
| WO2011076323A1 (en) | 2009-12-22 | 2011-06-30 | Merck Patent Gmbh | Formulations comprising phase-separated functional materials |
| WO2011076326A1 (en) | 2009-12-22 | 2011-06-30 | Merck Patent Gmbh | Electroluminescent functional surfactants |
| WO2011076314A1 (en) | 2009-12-22 | 2011-06-30 | Merck Patent Gmbh | Electroluminescent formulations |
| WO2011110275A2 (en) | 2010-03-11 | 2011-09-15 | Merck Patent Gmbh | Radiative fibers |
| WO2011110277A1 (en) | 2010-03-11 | 2011-09-15 | Merck Patent Gmbh | Fibers in therapy and cosmetics |
| WO2011147522A1 (en) | 2010-05-27 | 2011-12-01 | Merck Patent Gmbh | Compositions comprising quantum dots |
| WO2011147521A1 (en) | 2010-05-27 | 2011-12-01 | Merck Patent Gmbh | Down conversion |
| US8580395B2 (en) | 2008-08-29 | 2013-11-12 | Merck Patent Gmbh | Electroluminescent polymers, method for the production thereof, and use thereof |
| US9029539B2 (en) | 2003-10-30 | 2015-05-12 | Merck Patent Gmbh | Metal complexes with bipodal ligands |
| WO2016034262A1 (de) | 2014-09-05 | 2016-03-10 | Merck Patent Gmbh | Formulierungen und elektronische vorrichtungen |
| WO2016107663A1 (de) | 2014-12-30 | 2016-07-07 | Merck Patent Gmbh | Formulierungen und elektronische vorrichtungen |
| WO2016155866A1 (en) | 2015-03-30 | 2016-10-06 | Merck Patent Gmbh | Formulation of an organic functional material comprising a siloxane solvent |
| WO2016198141A1 (en) | 2015-06-12 | 2016-12-15 | Merck Patent Gmbh | Esters containing non-aromatic cycles as solvents for oled formulations |
| WO2017036572A1 (en) | 2015-08-28 | 2017-03-09 | Merck Patent Gmbh | Formulation of an organic functional material comprising an epoxy group containing solvent |
| WO2017097391A1 (en) | 2015-12-10 | 2017-06-15 | Merck Patent Gmbh | Formulations containing ketones comprising non-aromatic cycles |
| WO2017102048A1 (en) | 2015-12-15 | 2017-06-22 | Merck Patent Gmbh | Esters containing aromatic groups as solvents for organic electronic formulations |
| WO2017102052A1 (en) | 2015-12-16 | 2017-06-22 | Merck Patent Gmbh | Formulations containing a solid solvent |
| WO2017102049A1 (en) | 2015-12-16 | 2017-06-22 | Merck Patent Gmbh | Formulations containing a mixture of at least two different solvents |
| WO2017140404A1 (en) | 2016-02-17 | 2017-08-24 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2017157783A1 (de) | 2016-03-15 | 2017-09-21 | Merck Patent Gmbh | Behälter umfassend eine formulierung enthaltend mindestens einen organischen halbleiter |
| WO2017216128A1 (en) | 2016-06-17 | 2017-12-21 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2017216129A1 (en) | 2016-06-16 | 2017-12-21 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2018001928A1 (en) | 2016-06-28 | 2018-01-04 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2018024719A1 (en) | 2016-08-04 | 2018-02-08 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2018077660A1 (en) | 2016-10-31 | 2018-05-03 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2018077662A1 (en) | 2016-10-31 | 2018-05-03 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2018104202A1 (en) | 2016-12-06 | 2018-06-14 | Merck Patent Gmbh | Preparation process for an electronic device |
| WO2018108760A1 (en) | 2016-12-13 | 2018-06-21 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2018138319A1 (en) | 2017-01-30 | 2018-08-02 | Merck Patent Gmbh | Method for forming an organic electroluminescence (el) element |
| WO2018138318A1 (en) | 2017-01-30 | 2018-08-02 | Merck Patent Gmbh | Method for forming an organic element of an electronic device |
| WO2018178136A1 (en) | 2017-03-31 | 2018-10-04 | Merck Patent Gmbh | Printing method for an organic light emitting diode (oled) |
| WO2018189050A1 (en) | 2017-04-10 | 2018-10-18 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2018202603A1 (en) | 2017-05-03 | 2018-11-08 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2019016184A1 (en) | 2017-07-18 | 2019-01-24 | Merck Patent Gmbh | FORMULATION OF AN ORGANIC FUNCTIONAL MATERIAL |
| WO2019115573A1 (en) | 2017-12-15 | 2019-06-20 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2019162483A1 (en) | 2018-02-26 | 2019-08-29 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2019238782A1 (en) | 2018-06-15 | 2019-12-19 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2020094538A1 (en) | 2018-11-06 | 2020-05-14 | Merck Patent Gmbh | Method for forming an organic element of an electronic device |
| WO2021213918A1 (en) | 2020-04-21 | 2021-10-28 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2021213917A1 (en) | 2020-04-21 | 2021-10-28 | Merck Patent Gmbh | Emulsions comprising organic functional materials |
| WO2022122607A1 (en) | 2020-12-08 | 2022-06-16 | Merck Patent Gmbh | An ink system and a method for inkjet printing |
| WO2022223675A1 (en) | 2021-04-23 | 2022-10-27 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2023012084A1 (en) | 2021-08-02 | 2023-02-09 | Merck Patent Gmbh | A printing method by combining inks |
| WO2023057327A1 (en) | 2021-10-05 | 2023-04-13 | Merck Patent Gmbh | Method for forming an organic element of an electronic device |
| WO2023237458A1 (en) | 2022-06-07 | 2023-12-14 | Merck Patent Gmbh | Method of printing a functional layer of an electronic device by combining inks |
| WO2024126635A1 (en) | 2022-12-16 | 2024-06-20 | Merck Patent Gmbh | Formulation of an organic functional material |
Families Citing this family (255)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE10304819A1 (de) * | 2003-02-06 | 2004-08-19 | Covion Organic Semiconductors Gmbh | Carbazol-enthaltende konjugierte Polymere und Blends, deren Darstellung und Verwendung |
| EP1491568A1 (de) * | 2003-06-23 | 2004-12-29 | Covion Organic Semiconductors GmbH | Halbleitende Polymere |
| JP2007502251A (ja) * | 2003-08-15 | 2007-02-08 | ユニヴェルシテ・ラヴァル | 2位官能化及び2,7位二官能化カルバゾール類のモノマー類、オリゴマー類、及びポリマー類 |
| WO2005031891A1 (en) * | 2003-10-02 | 2005-04-07 | National Research Council Of Canada | 2,7-carbazolenevinylene derivatives as novel materials in producing organic based electronic devices |
| JP2007517079A (ja) | 2003-10-22 | 2007-06-28 | メルク パテント ゲーエムベーハー | エレクトロルミネセンスのための新規材料、およびそれらの使用 |
| DE102004020299A1 (de) * | 2004-04-26 | 2005-12-01 | Covion Organic Semiconductors Gmbh | Konjugierte Polymere, deren Darstellung und Verwendung |
| DE102004020298A1 (de) | 2004-04-26 | 2005-11-10 | Covion Organic Semiconductors Gmbh | Elektrolumineszierende Polymere und deren Verwendung |
| US7825249B2 (en) * | 2004-05-19 | 2010-11-02 | Merck Patent Gmbh | Metal complexes |
| DE102004032527A1 (de) | 2004-07-06 | 2006-02-02 | Covion Organic Semiconductors Gmbh | Elektrolumineszierende Polymere |
| DE102004034517A1 (de) | 2004-07-16 | 2006-02-16 | Covion Organic Semiconductors Gmbh | Metallkomplexe |
| GB0428445D0 (en) * | 2004-12-29 | 2005-02-02 | Cambridge Display Tech Ltd | Blue-shifted triarylamine polymer |
| GB2460358B (en) | 2004-12-29 | 2010-01-13 | Cambridge Display Tech Ltd | Rigid amines |
| JP2006228935A (ja) * | 2005-02-17 | 2006-08-31 | Ricoh Co Ltd | 有機薄膜トランジスタ |
| JP4806208B2 (ja) * | 2005-04-28 | 2011-11-02 | 関東化学株式会社 | ポリカルバゾール誘導体 |
| DE102005022903A1 (de) | 2005-05-18 | 2006-11-23 | Merck Patent Gmbh | Lösungen organischer Halbleiter |
| DE102005040411A1 (de) | 2005-08-26 | 2007-03-01 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102005043163A1 (de) * | 2005-09-12 | 2007-03-15 | Merck Patent Gmbh | Verbindungen für organische elektronische Vorrichtungen |
| DE102005060473A1 (de) | 2005-12-17 | 2007-06-28 | Merck Patent Gmbh | Konjugierte Polymere, deren Darstellung und Verwendung |
| DE102006003710A1 (de) * | 2006-01-26 | 2007-08-02 | Merck Patent Gmbh | Elektrolumineszierende Materialien und deren Verwendung |
| JP5003002B2 (ja) * | 2006-04-03 | 2012-08-15 | Jsr株式会社 | 有機エレクトロルミネッセンス素子用材料およびその製造方法、並びに有機エレクトロルミネッセンス素子 |
| US8277955B2 (en) * | 2006-10-17 | 2012-10-02 | Seiko Epson Corporation | Compound for organic EL device and organic EL device |
| KR100781921B1 (ko) | 2006-12-22 | 2007-12-04 | (재)대구경북과학기술연구원 | 카바졸 유도체 및 이를 이용한 유기 전계발광소자 |
| JP4811314B2 (ja) * | 2007-03-27 | 2011-11-09 | セイコーエプソン株式会社 | 有機elデバイス |
| DE102007024850A1 (de) | 2007-05-29 | 2008-12-04 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| US20080319155A1 (en) * | 2007-06-21 | 2008-12-25 | General Electric Company | Optoelectronic polymer compositions, and devices therefrom |
| JP2009073808A (ja) * | 2007-08-30 | 2009-04-09 | Sumitomo Chemical Co Ltd | 高分子化合物およびそれを用いた有機光電変換素子 |
| WO2009053088A1 (de) | 2007-10-24 | 2009-04-30 | Merck Patent Gmbh | Optoelektronische vorrichtung |
| DE102008045664A1 (de) | 2008-09-03 | 2010-03-04 | Merck Patent Gmbh | Optoelektronische Vorrichtung |
| DE102008045662A1 (de) | 2008-09-03 | 2010-03-04 | Merck Patent Gmbh | Optoelektronische Vorrichtung |
| DE102008015526B4 (de) | 2008-03-25 | 2021-11-11 | Merck Patent Gmbh | Metallkomplexe |
| DE102008017591A1 (de) | 2008-04-07 | 2009-10-08 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102008018670A1 (de) | 2008-04-14 | 2009-10-15 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102008027005A1 (de) | 2008-06-05 | 2009-12-10 | Merck Patent Gmbh | Organische elektronische Vorrichtung enthaltend Metallkomplexe |
| WO2009155595A2 (en) * | 2008-06-20 | 2009-12-23 | Tempur-Pedic Management, Inc. | Inflatable mattress and method of operating same |
| DE102008033943A1 (de) | 2008-07-18 | 2010-01-21 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| GB0814971D0 (en) | 2008-08-15 | 2008-09-24 | Cambridge Display Tech Ltd | Opto-electrical devices and methods of manufacturing the same |
| DE102008045663A1 (de) | 2008-09-03 | 2010-03-04 | Merck Patent Gmbh | Fluorverbrückte Assoziate für optoelektronische Anwendungen |
| KR101356953B1 (ko) * | 2008-09-19 | 2014-01-28 | 주식회사 엘지화학 | 카바졸 유도체 및 이를 이용한 유기 발광 소자 |
| DE102008050841B4 (de) | 2008-10-08 | 2019-08-01 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102008054141A1 (de) | 2008-10-31 | 2010-05-06 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102009022858A1 (de) | 2009-05-27 | 2011-12-15 | Merck Patent Gmbh | Organische Elektrolumineszenzvorrichtungen |
| DE102008056688A1 (de) | 2008-11-11 | 2010-05-12 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| CN102076813B (zh) | 2008-11-11 | 2016-05-18 | 默克专利有限公司 | 有机电致发光器件 |
| DE102008057050B4 (de) | 2008-11-13 | 2021-06-02 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102008057051B4 (de) | 2008-11-13 | 2021-06-17 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102009005288A1 (de) | 2009-01-20 | 2010-07-22 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102009005289B4 (de) | 2009-01-20 | 2023-06-22 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen, Verfahren zu deren Herstellung und elektronische Vorrichtungen, enthaltend diese |
| DE102009005746A1 (de) | 2009-01-23 | 2010-07-29 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102009007038A1 (de) | 2009-02-02 | 2010-08-05 | Merck Patent Gmbh | Metallkomplexe |
| DE102009009277B4 (de) | 2009-02-17 | 2023-12-07 | Merck Patent Gmbh | Organische elektronische Vorrichtung, Verfahren zu deren Herstellung und Verwendung von Verbindungen |
| DE102009010713A1 (de) | 2009-02-27 | 2010-09-02 | Merck Patent Gmbh | Polymer mit Aldehydgruppen, Umsetzung sowie Vernetzung dieses Polymers, vernetztes Polymer sowie Elektrolumineszenzvorrichtung enthaltend dieses Polymer |
| DE102009059985A1 (de) | 2009-12-22 | 2011-07-07 | Merck Patent GmbH, 64293 | Polymer mit Aldehydgruppen, Umsetzung sowie Vernetzung dieses Polymers, vernetztes Polymer sowie Elektrolumineszenzvorrichtung enthaltend dieses Polymer |
| DE102009010714A1 (de) | 2009-02-27 | 2010-09-02 | Merck Patent Gmbh | Vernetzbare und vernetzte Polymere, Verfahren zu deren Herstellung sowie deren Verwendung |
| WO2010097155A1 (de) | 2009-02-27 | 2010-09-02 | Merck Patent Gmbh | Polymer mit aldehydgruppen, umsetzung sowie vernetzung dieses polymers, vernetztes polymer sowie elektrolumineszenzvorrichtung enthaltend dieses polymer |
| DE102009011223A1 (de) | 2009-03-02 | 2010-09-23 | Merck Patent Gmbh | Metallkomplexe |
| DE102009013041A1 (de) | 2009-03-13 | 2010-09-16 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| KR101102079B1 (ko) * | 2009-04-08 | 2012-01-04 | 한국화학연구원 | 카바졸이 함유된 전도성 고분자 및 그를 이용한 유기 광기전력 장치 |
| DE102009023156A1 (de) | 2009-05-29 | 2010-12-02 | Merck Patent Gmbh | Polymere, die substituierte Indenofluorenderivate als Struktureinheit enthalten, Verfahren zu deren Herstellung sowie deren Verwendung |
| DE102009023155A1 (de) * | 2009-05-29 | 2010-12-02 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102009023154A1 (de) | 2009-05-29 | 2011-06-16 | Merck Patent Gmbh | Zusammensetzung, enthaltend mindestens eine Emitterverbindung und mindestens ein Polymer mit konjugationsunterbrechenden Einheiten |
| DE102009030848A1 (de) | 2009-06-26 | 2011-02-03 | Merck Patent Gmbh | Polymere enthaltend Struktureinheiten, die Alkylalkoxygruppen aufweisen, Blends enthaltend diese Polymere sowie optoelektronische Vorrichtungen enthaltend diese Polymere und Blends |
| DE102009030847A1 (de) | 2009-06-26 | 2010-12-30 | Merck Patent Gmbh | Polymere enthaltend substituierte Anthracenyleinheiten, Blends enthaltend diese Polymere sowie Vorrichtungen enthaltend diese Polymere oder Blends |
| DE102009031021A1 (de) | 2009-06-30 | 2011-01-05 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102009033371A1 (de) | 2009-07-16 | 2011-05-12 | Merck Patent Gmbh | Materialien für elektronische Vorrichtungen |
| DE102009034194A1 (de) | 2009-07-22 | 2011-01-27 | Merck Patent Gmbh | Materialien für elektronische Vorrichtungen |
| DE102009034625A1 (de) | 2009-07-27 | 2011-02-03 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| KR101931922B1 (ko) | 2009-09-16 | 2018-12-21 | 메르크 파텐트 게엠베하 | 전자 소자 제조를 위한 제형 |
| DE102009053644B4 (de) | 2009-11-17 | 2019-07-04 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102009042693A1 (de) | 2009-09-23 | 2011-03-24 | Merck Patent Gmbh | Materialien für elektronische Vorrichtungen |
| DE102009048791A1 (de) | 2009-10-08 | 2011-04-14 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102009049587A1 (de) | 2009-10-16 | 2011-04-21 | Merck Patent Gmbh | Metallkomplexe |
| DE102009053191A1 (de) | 2009-11-06 | 2011-05-12 | Merck Patent Gmbh | Materialien für elektronische Vorrichtungen |
| DE102009052428A1 (de) | 2009-11-10 | 2011-05-12 | Merck Patent Gmbh | Verbindung für elektronische Vorrichtungen |
| DE102009053382A1 (de) | 2009-11-14 | 2011-05-19 | Merck Patent Gmbh | Materialien für elektronische Vorrichtungen |
| DE102009053836A1 (de) | 2009-11-18 | 2011-05-26 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102010004803A1 (de) | 2010-01-16 | 2011-07-21 | Merck Patent GmbH, 64293 | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102010005697A1 (de) | 2010-01-25 | 2011-07-28 | Merck Patent GmbH, 64293 | Verbindungen für elektronische Vorrichtungen |
| DE102010006377A1 (de) | 2010-01-29 | 2011-08-04 | Merck Patent GmbH, 64293 | Styrolbasierte Copolymere, insbesondere für die Anwendung in optoelektronischen Bauteilen |
| DE102010007938A1 (de) | 2010-02-12 | 2011-10-06 | Merck Patent Gmbh | Elektrolumineszierende Polymere, Verfahren zu ihrer Herstellung sowie ihre Verwendung |
| DE102010009903A1 (de) | 2010-03-02 | 2011-09-08 | Merck Patent Gmbh | Verbindungen für elektronische Vorrichtungen |
| KR20130031827A (ko) | 2010-03-23 | 2013-03-29 | 메르크 파텐트 게엠베하 | 유기 전계발광 소자용 재료 |
| DE102010012738A1 (de) | 2010-03-25 | 2011-09-29 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102010014933A1 (de) | 2010-04-14 | 2011-10-20 | Merck Patent Gmbh | Materialien für elektronische Vorrichtungen |
| CN105949177B (zh) | 2010-05-03 | 2019-02-01 | 默克专利有限公司 | 制剂和电子器件 |
| DE102010019306B4 (de) | 2010-05-04 | 2021-05-20 | Merck Patent Gmbh | Organische Elektrolumineszenzvorrichtungen |
| DE102010024335A1 (de) | 2010-06-18 | 2011-12-22 | Merck Patent Gmbh | Verbindungen für elektronische Vorrichtungen |
| DE102010024542A1 (de) | 2010-06-22 | 2011-12-22 | Merck Patent Gmbh | Materialien für elektronische Vorrichtungen |
| DE102010024897A1 (de) | 2010-06-24 | 2011-12-29 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102010027316A1 (de) | 2010-07-16 | 2012-01-19 | Merck Patent Gmbh | Metallkomplexe |
| DE102010027320A1 (de) | 2010-07-16 | 2012-01-19 | Merck Patent Gmbh | Polymere Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102010032737A1 (de) | 2010-07-29 | 2012-02-02 | Merck Patent Gmbh | Polymere enthaltend substituierte Benzodithiopheneinheiten, Blends enthaltend diese Polymere sowie Vorrichtungen enthaltend diese Polymere oder Blends |
| DE102010033080A1 (de) | 2010-08-02 | 2012-02-02 | Merck Patent Gmbh | Polymere mit Struktureinheiten, die Elektronen-Transport-Eigenschaften aufweisen |
| DE102010033548A1 (de) | 2010-08-05 | 2012-02-09 | Merck Patent Gmbh | Materialien für elektronische Vorrichtungen |
| DE102010033777A1 (de) * | 2010-08-09 | 2012-02-09 | Merck Patent Gmbh | Polymere mit Carbazol-Struktureinheiten |
| DE102010045369A1 (de) | 2010-09-14 | 2012-03-15 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102010048498A1 (de) | 2010-10-14 | 2012-04-19 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102010048607A1 (de) | 2010-10-15 | 2012-04-19 | Merck Patent Gmbh | Verbindungen für elektronische Vorrichtungen |
| DE102010048608A1 (de) | 2010-10-15 | 2012-04-19 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102010055901A1 (de) | 2010-12-23 | 2012-06-28 | Merck Patent Gmbh | Organische Elektrolumineszenzvorrichtung |
| DE102010056151A1 (de) | 2010-12-28 | 2012-06-28 | Merck Patent Gmbh | Materiallen für organische Elektrolumineszenzvorrichtungen |
| DE112011104715A5 (de) | 2011-01-13 | 2014-02-06 | Merck Patent Gmbh | Verbindungen für organische Elektrolumineszenzvorrichtungen |
| DE102012000064A1 (de) | 2011-01-21 | 2012-07-26 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| US8751777B2 (en) | 2011-01-28 | 2014-06-10 | Honeywell International Inc. | Methods and reconfigurable systems to optimize the performance of a condition based health maintenance system |
| DE102011010841A1 (de) | 2011-02-10 | 2012-08-16 | Merck Patent Gmbh | (1,3)-Dioxan-5-on-Verbindungen |
| DE102011011539A1 (de) | 2011-02-17 | 2012-08-23 | Merck Patent Gmbh | Verbindungen für elektronische Vorrichtungen |
| KR101947206B1 (ko) | 2011-04-13 | 2019-02-12 | 메르크 파텐트 게엠베하 | 전자 소자용 재료 |
| EP2697226B1 (de) | 2011-04-13 | 2017-01-18 | Merck Patent GmbH | Verbindungen für elektronische vorrichtungen |
| WO2012143079A1 (de) | 2011-04-18 | 2012-10-26 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| WO2012149992A1 (de) | 2011-05-04 | 2012-11-08 | Merck Patent Gmbh | Vorrichtung zur aufbewahrung von frischwaren |
| WO2012149999A1 (de) | 2011-05-05 | 2012-11-08 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| EP2705552B1 (de) | 2011-05-05 | 2015-03-04 | Merck Patent GmbH | Verbindungen für elektronische vorrichtungen |
| DE102011104745A1 (de) | 2011-06-17 | 2012-12-20 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| US10193069B2 (en) * | 2011-06-27 | 2019-01-29 | Nippon Steel & Sumikin Chemical Co., Ltd. | Polymer for use in organic electroluminescent element and organic electroluminescent element employing same |
| KR102088637B1 (ko) | 2011-07-29 | 2020-03-13 | 메르크 파텐트 게엠베하 | 전자 소자용 화합물 |
| KR101983019B1 (ko) | 2011-08-03 | 2019-05-28 | 메르크 파텐트 게엠베하 | 전자 소자용 물질 |
| DE102011116165A1 (de) | 2011-10-14 | 2013-04-18 | Merck Patent Gmbh | Benzodioxepin-3-on-Verbindungen |
| EP2782975B1 (de) | 2011-10-27 | 2018-01-10 | Merck Patent GmbH | Materialien für elektronische vorrichtungen |
| DE102011117422A1 (de) | 2011-10-28 | 2013-05-02 | Merck Patent Gmbh | Hyperverzweigte Polymere, Verfahren zu deren Herstellung sowie deren Verwendung in elektronischen Vorrichtungen |
| WO2013083216A1 (de) | 2011-11-17 | 2013-06-13 | Merck Patent Gmbh | Spiro -dihydroacridinderivate und ihre verwendung als materialien für organische elektrolumineszenzvorrichtungen |
| KR101961613B1 (ko) | 2011-12-12 | 2019-03-25 | 메르크 파텐트 게엠베하 | 전자 소자용 화합물 |
| CN103159934B (zh) * | 2011-12-13 | 2016-01-13 | 海洋王照明科技股份有限公司 | 含并噻唑单元的聚合物及其制备方法和太阳能电池器件 |
| DE102012022880A1 (de) | 2011-12-22 | 2013-06-27 | Merck Patent Gmbh | Elektronische Vorrichtungen enthaltend organische Schichten |
| CN104114672B (zh) | 2012-02-14 | 2017-03-15 | 默克专利有限公司 | 用于有机电致发光器件的螺二芴化合物 |
| EP2817350A2 (de) | 2012-02-22 | 2014-12-31 | Merck Patent GmbH | Polymere enthaltend dibenzocycloheptan-struktureinheiten |
| EP2828266B1 (de) | 2012-03-23 | 2017-10-18 | Merck Patent GmbH | 9,9'-spirobixanthenderivate für elektrolumineszenzvorrichtungen |
| KR102040350B1 (ko) | 2012-04-17 | 2019-11-04 | 메르크 파텐트 게엠베하 | 가교성 및 가교된 중합체, 그의 제조 방법 및 그의 용도 |
| DE102012011335A1 (de) | 2012-06-06 | 2013-12-12 | Merck Patent Gmbh | Verbindungen für Organische Elekronische Vorrichtungen |
| WO2014000860A1 (de) | 2012-06-29 | 2014-01-03 | Merck Patent Gmbh | Polymere enthaltend 2,7-pyren-struktureinheiten |
| KR102076481B1 (ko) | 2012-07-13 | 2020-02-12 | 메르크 파텐트 게엠베하 | 금속 착물 |
| KR102696532B1 (ko) | 2012-07-23 | 2024-08-19 | 메르크 파텐트 게엠베하 | 플루오렌 및 이를 함유하는 전자 소자 |
| CN104487541B (zh) | 2012-07-23 | 2019-07-26 | 默克专利有限公司 | 化合物以及有机电致发光器件 |
| EP2875699B1 (de) | 2012-07-23 | 2017-02-15 | Merck Patent GmbH | Derivate von 2-diarylaminofluoren und diese enthaltnde organische elektronische verbindungen |
| KR102192286B1 (ko) | 2012-08-07 | 2020-12-17 | 메르크 파텐트 게엠베하 | 금속 착물 |
| WO2014044347A1 (de) | 2012-09-20 | 2014-03-27 | Merck Patent Gmbh | Metallkomplexe |
| KR101716069B1 (ko) | 2012-11-12 | 2017-03-13 | 메르크 파텐트 게엠베하 | 전자 소자용 재료 |
| JP6363090B2 (ja) | 2012-11-30 | 2018-07-25 | メルク パテント ゲーエムベーハー | 電子素子 |
| KR20150100913A (ko) | 2012-12-28 | 2015-09-02 | 메르크 파텐트 게엠베하 | 중합체성 유기 반도성 화합물을 포함하는 조성물 |
| WO2014106522A1 (de) | 2013-01-03 | 2014-07-10 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| JP2016506414A (ja) | 2013-01-03 | 2016-03-03 | メルク パテント ゲーエムベーハー | 電子素子のための材料 |
| FR3001730B1 (fr) * | 2013-02-07 | 2016-01-08 | Commissariat Energie Atomique | Nouveaux metallopolymeres et leur utilisation |
| CN111909187A (zh) | 2013-10-02 | 2020-11-10 | 默克专利有限公司 | 用于oled中的含硼化合物 |
| EP3069392B1 (de) | 2013-11-15 | 2019-08-07 | Merck Patent GmbH | Verbindung mit neuartiger sechsgliedriger ringstruktur zur verwendung bei organischen elektronischen vorrichtungen |
| KR101772371B1 (ko) | 2013-12-06 | 2017-08-29 | 메르크 파텐트 게엠베하 | 화합물 및 유기 전자 소자 |
| KR101993129B1 (ko) | 2013-12-12 | 2019-06-26 | 메르크 파텐트 게엠베하 | 전자 소자용 물질 |
| EP3708634B1 (de) | 2013-12-19 | 2024-08-14 | Merck Patent GmbH | Heterocyclische spiroverbindungen |
| JP6642428B2 (ja) * | 2014-07-03 | 2020-02-05 | 住友化学株式会社 | 高分子化合物およびそれを用いた発光素子 |
| KR102496045B1 (ko) | 2014-11-11 | 2023-02-03 | 메르크 파텐트 게엠베하 | 유기 전계발광 소자용 재료 |
| JP6837975B2 (ja) | 2014-12-30 | 2021-03-03 | メルク、パテント、ゲゼルシャフト、ミット、ベシュレンクテル、ハフツングMerck Patent GmbH | 少なくとも1つのポリマーおよび少なくとも1つの塩を含んでなる組成物、ならびにその組成物を含むエレクトロルミネッセンス素子 |
| WO2016120007A1 (en) | 2015-01-30 | 2016-08-04 | Merck Patent Gmbh | Formulations with a low particle content |
| CN107108578A (zh) | 2015-01-30 | 2017-08-29 | 默克专利有限公司 | 电子器件的材料 |
| CN107207550B (zh) | 2015-02-03 | 2020-06-05 | 默克专利有限公司 | 金属络合物 |
| KR102543777B1 (ko) | 2015-06-10 | 2023-06-14 | 메르크 파텐트 게엠베하 | 유기 전계발광 소자용 재료 |
| KR102643183B1 (ko) | 2015-07-15 | 2024-03-04 | 메르크 파텐트 게엠베하 | 유기 반도전성 화합물들을 포함하는 조성물 |
| US20180219156A1 (en) | 2015-07-22 | 2018-08-02 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| GB201513037D0 (en) | 2015-07-23 | 2015-09-09 | Merck Patent Gmbh | Phenyl-derived compound for use in organic electronic devices |
| JP6983754B2 (ja) | 2015-07-29 | 2021-12-17 | メルク パテント ゲーエムベーハー | 有機エレクトロルミネッセンス素子のための材料 |
| KR20180031766A (ko) | 2015-07-30 | 2018-03-28 | 메르크 파텐트 게엠베하 | 유기 전계발광 소자용 재료 |
| CN107949561B (zh) | 2015-08-14 | 2021-11-02 | 默克专利有限公司 | 用于有机电致发光器件的吩噁嗪衍生物 |
| US20180327339A1 (en) | 2015-08-28 | 2018-11-15 | Merck Patent Gmbh | Compounds for electronic devices |
| US20190040034A1 (en) | 2016-02-05 | 2019-02-07 | Merck Patent Gmbh | Materials for electronic devices |
| US10273329B2 (en) | 2016-03-11 | 2019-04-30 | Lei Fang | Organic semiconductor polymer |
| TWI821807B (zh) | 2016-03-17 | 2023-11-11 | 德商麥克專利有限公司 | 具有螺聯茀結構之化合物 |
| CN108884087A (zh) | 2016-04-11 | 2018-11-23 | 默克专利有限公司 | 包含二苯并呋喃和/或二苯并噻吩结构的杂环化合物 |
| KR102487147B1 (ko) | 2016-06-03 | 2023-01-11 | 메르크 파텐트 게엠베하 | 유기 전계발광 소자용 재료 |
| WO2018001990A1 (de) | 2016-06-30 | 2018-01-04 | Merck Patent Gmbh | Verfahren zur auftrennung von enantiomerenmischungen von metallkomplexen |
| WO2018007421A1 (en) | 2016-07-08 | 2018-01-11 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| CN109415344B (zh) | 2016-07-14 | 2022-06-03 | 默克专利有限公司 | 金属络合物 |
| KR102468446B1 (ko) | 2016-09-14 | 2022-11-18 | 메르크 파텐트 게엠베하 | 스피로바이플루오렌-구조를 갖는 화합물 |
| CN109689655A (zh) | 2016-09-14 | 2019-04-26 | 默克专利有限公司 | 具有咔唑结构的化合物 |
| TWI766884B (zh) | 2016-09-30 | 2022-06-11 | 德商麥克專利有限公司 | 具有二氮雜二苯并呋喃或二氮雜二苯并噻吩結構的化合物、其製法及其用途 |
| TWI814711B (zh) | 2016-09-30 | 2023-09-11 | 德商麥克專利有限公司 | 具有二氮雜二苯並呋喃或二氮雜二苯並噻吩結構之咔唑、製備彼之方法及其用途 |
| KR102654996B1 (ko) | 2016-10-06 | 2024-04-05 | 메르크 파텐트 게엠베하 | 유기 전계발광 소자용 재료 |
| TWI764942B (zh) | 2016-10-10 | 2022-05-21 | 德商麥克專利有限公司 | 電子裝置 |
| WO2018083053A1 (de) | 2016-11-02 | 2018-05-11 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| KR20230121632A (ko) | 2016-11-08 | 2023-08-18 | 메르크 파텐트 게엠베하 | 전자 소자용 화합물 |
| TWI756292B (zh) | 2016-11-14 | 2022-03-01 | 德商麥克專利有限公司 | 具有受體基團與供體基團之化合物 |
| TW201833118A (zh) | 2016-11-22 | 2018-09-16 | 德商麥克專利有限公司 | 用於電子裝置之材料 |
| CN109963856A (zh) | 2016-11-25 | 2019-07-02 | 默克专利有限公司 | 作为用于有机电致发光器件(oled)的材料的双苯并呋喃稠合的茚并[1,2-b]芴衍生物和相关化合物 |
| KR102540425B1 (ko) | 2016-11-25 | 2023-06-07 | 메르크 파텐트 게엠베하 | 유기 전계발광 소자 (oled) 용 재료로서 비스벤조푸란-융합된 2,8-디아미노인데노[1,2-b]플루오렌 유도체 및 관련 화합물 |
| JP7023957B2 (ja) | 2016-11-30 | 2022-02-22 | メルク パテント ゲゼルシャフト ミット ベシュレンクテル ハフツング | 非対称性の繰り返し単位を有するポリマー |
| KR102539246B1 (ko) | 2016-11-30 | 2023-06-01 | 메르크 파텐트 게엠베하 | 발레로락탐 구조를 갖는 화합물 |
| TW201831468A (zh) | 2016-12-05 | 2018-09-01 | 德商麥克專利有限公司 | 含氮的雜環化合物 |
| TWI761406B (zh) | 2016-12-22 | 2022-04-21 | 德商麥克專利有限公司 | 電子裝置用材料 |
| WO2018114883A1 (de) | 2016-12-22 | 2018-06-28 | Merck Patent Gmbh | Mischungen umfassend mindestens zwei organisch funktionelle verbindungen |
| US11974494B2 (en) * | 2016-12-27 | 2024-04-30 | Samsung Electronics Co., Ltd. | Polymer compound, composition including the polymer compound, light-emitting device including the polymer compound |
| KR102594781B1 (ko) | 2017-01-23 | 2023-10-26 | 메르크 파텐트 게엠베하 | 유기 전계발광 디바이스용 재료 |
| KR102625926B1 (ko) | 2017-01-25 | 2024-01-17 | 메르크 파텐트 게엠베하 | 카르바졸 유도체 |
| JP7069184B2 (ja) | 2017-02-02 | 2022-05-17 | メルク パテント ゲーエムベーハー | 電子デバイス用材料 |
| WO2018157981A1 (de) | 2017-03-02 | 2018-09-07 | Merck Patent Gmbh | Materialien für organische elektronische vorrichtungen |
| TW201843143A (zh) | 2017-03-13 | 2018-12-16 | 德商麥克專利有限公司 | 含有芳基胺結構之化合物 |
| KR102585423B1 (ko) | 2017-04-25 | 2023-10-05 | 메르크 파텐트 게엠베하 | 전자 디바이스용 화합물 |
| JP2020520970A (ja) | 2017-05-22 | 2020-07-16 | メルク パテント ゲーエムベーハー | 電子デバイス用六環性ヘテロ芳香族化合物 |
| TW201920343A (zh) | 2017-06-21 | 2019-06-01 | 德商麥克專利有限公司 | 電子裝置用材料 |
| KR20200020841A (ko) | 2017-06-23 | 2020-02-26 | 메르크 파텐트 게엠베하 | 유기 전계발광 디바이스용 재료 |
| KR20240059634A (ko) | 2017-06-28 | 2024-05-07 | 메르크 파텐트 게엠베하 | 전자 디바이스용 재료 |
| TWI813576B (zh) | 2017-07-03 | 2023-09-01 | 德商麥克專利有限公司 | 具有低含量苯酚類雜質的調配物 |
| JP7413252B2 (ja) | 2017-07-28 | 2024-01-15 | メルク パテント ゲーエムベーハー | 電子デバイスに使用するためのスピロビフルオレン誘導体 |
| CN118405982A (zh) | 2017-09-08 | 2024-07-30 | 默克专利有限公司 | 用于电子器件的材料 |
| KR102371109B1 (ko) * | 2017-10-30 | 2022-03-04 | 주식회사 엘지화학 | 공중합체, 및 이를 포함하는 유기발광소자 |
| TWI815831B (zh) | 2017-11-23 | 2023-09-21 | 德商麥克專利有限公司 | 用於電子裝置之材料 |
| JP2021506822A (ja) | 2017-12-15 | 2021-02-22 | メルク パテント ゲーエムベーハー | 有機エレクトロルミネッセントデバイスに使用するための置換芳香族アミン |
| TW201938562A (zh) | 2017-12-19 | 2019-10-01 | 德商麥克專利有限公司 | 雜環化合物 |
| EP3728275B1 (de) | 2017-12-20 | 2024-09-04 | Merck Patent GmbH | Heteroaromatische verbindungen |
| CN111819167A (zh) | 2018-03-16 | 2020-10-23 | 默克专利有限公司 | 用于有机电致发光器件的材料 |
| CN108929392B (zh) * | 2018-04-17 | 2019-09-03 | 江南大学 | 一种硅基双光子引发剂及其制备方法 |
| CN108912329B (zh) * | 2018-06-15 | 2021-02-02 | 南京工业大学 | 一种图案化二维共轭微孔聚合物的制备方法和应用 |
| CN108808449B (zh) * | 2018-06-22 | 2020-05-08 | 南京邮电大学 | 一种基于三线态激子放大器的有机激光薄膜器件及应用 |
| WO2020011701A1 (de) | 2018-07-11 | 2020-01-16 | Merck Patent Gmbh | Formulierung enthaltend ein hochverzweigtes polymer, hochverzweigtes polymer sowie elektrooptische vorrichtung enthaltend dieses hochverzweigte polymer |
| JP2022502829A (ja) | 2018-09-24 | 2022-01-11 | メルク パテント ゲーエムベーハー | 粒状材料を製造するための方法 |
| EP3856868B1 (de) | 2018-09-27 | 2023-01-25 | Merck Patent GmbH | Verbindungen, die in einer organischen elektronischen vorrichtung als aktive verbindungen einsetzbar sind |
| EP3856717A2 (de) | 2018-09-27 | 2021-08-04 | Merck Patent GmbH | Verfahren zur herstellung von sterisch gehinderten stickstoffhaltigen heteroaromatischen verbindungen |
| WO2020094539A1 (de) | 2018-11-05 | 2020-05-14 | Merck Patent Gmbh | In einer organischen elektronischen vorrichtung einsetzbare verbindungen |
| US12065536B2 (en) | 2018-11-07 | 2024-08-20 | Merck Patent Gmbh | Polymers with amine-group-containing repeating units |
| WO2020099349A1 (de) | 2018-11-14 | 2020-05-22 | Merck Patent Gmbh | Zur herstellung einer organischen elektronischen vorrichtung einsetzbare verbindungen |
| TW202110935A (zh) | 2019-04-16 | 2021-03-16 | 德商麥克專利有限公司 | 含有可交聯聚合物之調配物 |
| CN114514628A (zh) | 2019-10-22 | 2022-05-17 | 默克专利有限公司 | 用于有机电致发光器件的材料 |
| EP4048675A1 (de) | 2019-10-25 | 2022-08-31 | Merck Patent GmbH | In einer organischen elektronischen vorrichtung einsetzbare verbindungen |
| US20230069061A1 (en) | 2019-12-18 | 2023-03-02 | Merck Patent Gmbh | Aromatic compounds for organic electroluminescent devices |
| CN114867729A (zh) | 2019-12-19 | 2022-08-05 | 默克专利有限公司 | 用于有机电致发光器件的多环化合物 |
| US20230139809A1 (en) | 2020-01-29 | 2023-05-04 | Merck Patent Gmbh | Benzimidazole derivatives |
| CN115135741A (zh) | 2020-02-25 | 2022-09-30 | 默克专利有限公司 | 杂环化合物在有机电子器件中的用途 |
| WO2021175706A1 (de) | 2020-03-02 | 2021-09-10 | Merck Patent Gmbh | Verwendung von sulfonverbindungen in einer organischen elektronischen vorrichtung |
| CN115298847A (zh) | 2020-03-17 | 2022-11-04 | 默克专利有限公司 | 用于有机电致发光器件的杂环化合物 |
| US20230157170A1 (en) | 2020-03-17 | 2023-05-18 | Merck Patent Gmbh | Heteroaromatic compounds for organic electroluminescent devices |
| KR20220158771A (ko) | 2020-03-26 | 2022-12-01 | 메르크 파텐트 게엠베하 | 유기 전계 발광 디바이스용 환형 화합물 |
| CN115362159A (zh) | 2020-04-06 | 2022-11-18 | 默克专利有限公司 | 用于有机电致发光器件的多环化合物 |
| CN115916767A (zh) | 2020-06-18 | 2023-04-04 | 默克专利有限公司 | 茚并氮杂萘 |
| EP4169082A1 (de) | 2020-06-23 | 2023-04-26 | Merck Patent GmbH | Verfahren zur herstellung einer mischung |
| JP2023530915A (ja) | 2020-06-29 | 2023-07-20 | メルク パテント ゲゼルシャフト ミット ベシュレンクテル ハフツング | 有機エレクトロルミネッセンス素子のためのヘテロ環式化合物 |
| JP2023531470A (ja) | 2020-06-29 | 2023-07-24 | メルク パテント ゲゼルシャフト ミット ベシュレンクテル ハフツング | 有機エレクトロルミネッセンス素子のためのヘテロ芳香族化合物 |
| TW202222748A (zh) | 2020-09-30 | 2022-06-16 | 德商麥克專利有限公司 | 用於結構化有機電致發光裝置的功能層之化合物 |
| TW202229215A (zh) | 2020-09-30 | 2022-08-01 | 德商麥克專利有限公司 | 用於有機電致發光裝置功能層之結構化的化合物 |
| EP4229064A1 (de) | 2020-10-16 | 2023-08-23 | Merck Patent GmbH | Heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| CN116406414A (zh) | 2020-10-16 | 2023-07-07 | 默克专利有限公司 | 用于有机电致发光器件的包含杂原子的化合物 |
| CN116724040A (zh) | 2020-12-18 | 2023-09-08 | 默克专利有限公司 | 用于有机电致发光器件的含氮化合物 |
| WO2022129116A1 (de) | 2020-12-18 | 2022-06-23 | Merck Patent Gmbh | Indolo[3.2.1-jk]carbazole-6-carbonitril-derivate als blau fluoreszierende emitter zur verwendung in oleds |
| WO2022129113A1 (de) | 2020-12-18 | 2022-06-23 | Merck Patent Gmbh | Stickstoffhaltige heteroaromaten für organische elektrolumineszenzvorrichtungen |
| CN117425655A (zh) | 2021-04-30 | 2024-01-19 | 默克专利有限公司 | 用于有机电致发光器件的含氮杂环化合物 |
| WO2022243403A1 (de) | 2021-05-21 | 2022-11-24 | Merck Patent Gmbh | Verfahren zur kontinuierlichen aufreinigung von mindestens einem funktionalen material und vorrichtung zur kontinuierlichen aufreinigung von mindestens einem funktionalen material |
| WO2023041454A1 (de) | 2021-09-14 | 2023-03-23 | Merck Patent Gmbh | Borhaltige, heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2023072799A1 (de) | 2021-10-27 | 2023-05-04 | Merck Patent Gmbh | Bor- und stickstoffhaltige, heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2023099543A1 (en) | 2021-11-30 | 2023-06-08 | Merck Patent Gmbh | Compounds having fluorene structures |
| WO2023161167A1 (de) | 2022-02-23 | 2023-08-31 | Merck Patent Gmbh | Stickstoffhaltige heterocyclen für organische elektrolumineszenzvorrichtungen |
| CN118647622A (zh) | 2022-02-23 | 2024-09-13 | 默克专利有限公司 | 用于有机电致发光器件的芳族杂环 |
| WO2023213759A1 (de) | 2022-05-04 | 2023-11-09 | Merck Patent Gmbh | Polymere enthaltend speziell substituierte triarylamin-einheiten sowie elektrolumineszenzvorrichtungen enthaltend diese polymere |
| WO2023213837A1 (de) | 2022-05-06 | 2023-11-09 | Merck Patent Gmbh | Cyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2023247338A1 (de) | 2022-06-20 | 2023-12-28 | Merck Patent Gmbh | Organische heterocyclen für photoelektrische vorrichtungen |
| WO2023247345A1 (de) | 2022-06-20 | 2023-12-28 | Merck Patent Gmbh | Heterocyclen für photoelektrische vorrichtungen |
| WO2024061948A1 (de) | 2022-09-22 | 2024-03-28 | Merck Patent Gmbh | Stickstoffenthaltende heterocyclen für organische elektrolumineszenzvorrichtungen |
| WO2024061942A1 (de) | 2022-09-22 | 2024-03-28 | Merck Patent Gmbh | Stickstoffenthaltende verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2024094592A2 (de) | 2022-11-01 | 2024-05-10 | Merck Patent Gmbh | Stickstoffhaltige heterocyclen für organische elektrolumineszenzvorrichtungen |
| WO2024115426A1 (de) | 2022-12-01 | 2024-06-06 | Merck Patent Gmbh | Polymere enthaltend spirotruxenderivate als wiederholungseinheit sowie elektrolumineszenzvorrichtungen enthaltend diese polymere |
| WO2024149694A1 (de) | 2023-01-10 | 2024-07-18 | Merck Patent Gmbh | Stickstoffhaltige heterocyclen für organische elektrolumineszenzvorrichtungen |
| WO2024153568A1 (de) | 2023-01-17 | 2024-07-25 | Merck Patent Gmbh | Heterocyclen für organische elektrolumineszenzvorrichtungen |
| WO2024184050A1 (de) | 2023-03-07 | 2024-09-12 | Merck Patent Gmbh | Cyclische stickstoffverbindungen für organische elektrolumineszenzvorrichtungen |
Family Cites Families (32)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS646305A (en) * | 1987-06-29 | 1989-01-10 | Nippon Oil Co Ltd | Manufacture of p-type electrically active conducting material |
| JPS646305U (de) | 1987-07-02 | 1989-01-13 | ||
| GB8909011D0 (en) | 1989-04-20 | 1989-06-07 | Friend Richard H | Electroluminescent devices |
| DE4111878A1 (de) | 1991-04-11 | 1992-10-15 | Wacker Chemie Gmbh | Leiterpolymere mit konjugierten doppelbindungen |
| JPH06345854A (ja) * | 1993-06-08 | 1994-12-20 | Toray Ind Inc | カルバゾール系重合体の製造方法 |
| DE4422670A1 (de) | 1994-06-30 | 1996-01-04 | Hoechst Ag | Konjugierte Polymere mit Ansateilstrukturen und ihre Verwendung als Elektrolumineszenzmaterialien |
| DE4431039A1 (de) | 1994-09-01 | 1996-03-07 | Hoechst Ag | Poly(4,5,9,10-tetrahydropyren-2,7-diyl)-Derivate und ihre Verwendung als Elektrolumineszenzmaterialien |
| DE4436773A1 (de) | 1994-10-14 | 1996-04-18 | Hoechst Ag | Konjugierte Polymere mit Spirozentren und ihre Verwendung als Elektrolumineszenzmaterialien |
| DE69608446T3 (de) | 1995-07-28 | 2010-03-11 | Sumitomo Chemical Company, Ltd. | 2,7-aryl-9-substituierte fluorene und 9-substituierte fluorenoligomere und polymere |
| DE19614971A1 (de) | 1996-04-17 | 1997-10-23 | Hoechst Ag | Polymere mit Spiroatomen und ihre Verwendung als Elektrolumineszenzmaterialien |
| EP0863931A2 (de) * | 1995-12-01 | 1998-09-16 | Ciba SC Holding AG | Poly(9,9'-spirobisfluorene), deren herstellung und deren verwendung |
| US6309763B1 (en) | 1997-05-21 | 2001-10-30 | The Dow Chemical Company | Fluorene-containing polymers and electroluminescent devices therefrom |
| GB2328212B (en) * | 1997-08-12 | 2000-11-29 | Samsung Display Devices Co Ltd | Organic electroluminescent polymer for light emitting diode |
| DE19846766A1 (de) | 1998-10-10 | 2000-04-20 | Aventis Res & Tech Gmbh & Co | Konjugierte Polymere, enthaltend spezielle Fluorenbausteine mit verbesserten Eigenschaften |
| DE19846768A1 (de) | 1998-10-10 | 2000-04-20 | Aventis Res & Tech Gmbh & Co | Konjugierte Polymere enthaltend 2,7-Fluorenyleinheiten mit verbesserten Eigenschaften |
| DE19857661A1 (de) | 1998-12-15 | 2000-06-21 | Aventis Res & Tech Gmbh & Co | Verfahren zur Herstellung von Derivaten des Polyarylenvinylenen |
| US6353083B1 (en) | 1999-02-04 | 2002-03-05 | The Dow Chemical Company | Fluorene copolymers and devices made therefrom |
| GB0005842D0 (en) | 2000-03-10 | 2000-05-03 | Cambridge Display Tech Ltd | Copoymer |
| US6512082B2 (en) * | 2000-01-05 | 2003-01-28 | Cambridge Display Technology Ltd. | Polymers, their preparation and uses |
| AU2001269790A1 (en) * | 2000-06-12 | 2001-12-24 | Maxdem Incorporated | Polymer matrix electroluminescent materials and devices |
| DE10109027A1 (de) | 2001-02-24 | 2002-09-05 | Covion Organic Semiconductors | Rhodium- und Iridium-Komplexe |
| JP4438042B2 (ja) | 2001-03-08 | 2010-03-24 | キヤノン株式会社 | 金属配位化合物、電界発光素子及び表示装置 |
| EP1370619B1 (de) | 2001-03-10 | 2006-06-21 | MERCK PATENT GmbH | Lösung und dispersionen organischer halbleiter |
| JP4259875B2 (ja) | 2001-03-24 | 2009-04-30 | メルク パテント ゲーエムベーハー | スピロビフルオレン単位およびフルオレン単位を含む共役ポリマーおよびその使用 |
| DE10116962A1 (de) | 2001-04-05 | 2002-10-10 | Covion Organic Semiconductors | Rhodium- und Iridium-Komplexe |
| KR100480769B1 (ko) * | 2001-06-13 | 2005-04-06 | 삼성에스디아이 주식회사 | 백색 전계발광 고분자 및 이를 이용한 유기 전계발광 소자 |
| DE10143353A1 (de) | 2001-09-04 | 2003-03-20 | Covion Organic Semiconductors | Konjugierte Polymere enthaltend Spirobifluoren-Einheiten und deren Verwendung |
| JP2003217862A (ja) * | 2002-01-18 | 2003-07-31 | Honda Motor Co Ltd | 有機エレクトロルミネッセンス素子 |
| GB0204989D0 (en) | 2002-03-04 | 2002-04-17 | Opsys Ltd | Phosphorescent compositions and organic light emitting devices containing them |
| DE10238903A1 (de) | 2002-08-24 | 2004-03-04 | Covion Organic Semiconductors Gmbh | Rhodium- und Iridium-Komplexe |
| DE10249723A1 (de) | 2002-10-25 | 2004-05-06 | Covion Organic Semiconductors Gmbh | Arylamin-Einheiten enthaltende konjugierte Polymere, deren Darstellung und Verwendung |
| DE10304819A1 (de) * | 2003-02-06 | 2004-08-19 | Covion Organic Semiconductors Gmbh | Carbazol-enthaltende konjugierte Polymere und Blends, deren Darstellung und Verwendung |
-
2003
- 2003-02-06 DE DE10304819A patent/DE10304819A1/de not_active Withdrawn
-
2004
- 2004-02-04 EP EP04707888A patent/EP1592729B1/de not_active Expired - Lifetime
- 2004-02-04 KR KR1020057014550A patent/KR101041766B1/ko active IP Right Grant
- 2004-02-04 JP JP2006501725A patent/JP4566185B2/ja not_active Expired - Lifetime
- 2004-02-04 CN CNB2004800037941A patent/CN100360579C/zh not_active Expired - Lifetime
- 2004-02-04 DE DE502004006904T patent/DE502004006904D1/de not_active Expired - Lifetime
- 2004-02-04 CN CN2007101863516A patent/CN101333328B/zh not_active Expired - Lifetime
- 2004-02-04 WO PCT/EP2004/000994 patent/WO2004070772A2/de active IP Right Grant
- 2004-02-04 EP EP08003260A patent/EP1932866B1/de not_active Expired - Lifetime
- 2004-02-04 US US10/544,437 patent/US7834136B2/en not_active Expired - Fee Related
-
2010
- 2010-10-25 US US12/911,119 patent/US8053547B2/en not_active Expired - Lifetime
Cited By (56)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7728137B2 (en) | 2003-03-11 | 2010-06-01 | Merck Patent Gmbh | Metal complexes |
| EP1927610A2 (de) | 2003-08-12 | 2008-06-04 | Merck Patent GmbH | Prozeß zur Herstellung von Aryl- oder Heteroarylamin-Boronsäurederivaten |
| WO2005014689A2 (de) | 2003-08-12 | 2005-02-17 | Covion Organic Semiconductors Gmbh | Konjugierte polymere enthaltend dihydrophenanthren-einheiten und deren verwendung |
| US9029539B2 (en) | 2003-10-30 | 2015-05-12 | Merck Patent Gmbh | Metal complexes with bipodal ligands |
| US7790057B2 (en) | 2006-07-11 | 2010-09-07 | Merck Patent Gmbh | Electroluminescent polymers and use thereof |
| US8580395B2 (en) | 2008-08-29 | 2013-11-12 | Merck Patent Gmbh | Electroluminescent polymers, method for the production thereof, and use thereof |
| DE102008049037A1 (de) | 2008-09-25 | 2010-04-22 | Merck Patent Gmbh | Neue Polymere mit niedriger Polydispersität |
| WO2011015265A2 (en) | 2009-08-04 | 2011-02-10 | Merck Patent Gmbh | Electronic devices comprising multi cyclic hydrocarbons |
| WO2011076326A1 (en) | 2009-12-22 | 2011-06-30 | Merck Patent Gmbh | Electroluminescent functional surfactants |
| WO2011076323A1 (en) | 2009-12-22 | 2011-06-30 | Merck Patent Gmbh | Formulations comprising phase-separated functional materials |
| WO2011076314A1 (en) | 2009-12-22 | 2011-06-30 | Merck Patent Gmbh | Electroluminescent formulations |
| WO2011110277A1 (en) | 2010-03-11 | 2011-09-15 | Merck Patent Gmbh | Fibers in therapy and cosmetics |
| WO2011110275A2 (en) | 2010-03-11 | 2011-09-15 | Merck Patent Gmbh | Radiative fibers |
| WO2011147522A1 (en) | 2010-05-27 | 2011-12-01 | Merck Patent Gmbh | Compositions comprising quantum dots |
| WO2011147521A1 (en) | 2010-05-27 | 2011-12-01 | Merck Patent Gmbh | Down conversion |
| EP3309236A1 (de) | 2010-05-27 | 2018-04-18 | Merck Patent GmbH | Zusammensetzungen mit quantenpunkten |
| WO2016034262A1 (de) | 2014-09-05 | 2016-03-10 | Merck Patent Gmbh | Formulierungen und elektronische vorrichtungen |
| WO2016107663A1 (de) | 2014-12-30 | 2016-07-07 | Merck Patent Gmbh | Formulierungen und elektronische vorrichtungen |
| WO2016155866A1 (en) | 2015-03-30 | 2016-10-06 | Merck Patent Gmbh | Formulation of an organic functional material comprising a siloxane solvent |
| WO2016198141A1 (en) | 2015-06-12 | 2016-12-15 | Merck Patent Gmbh | Esters containing non-aromatic cycles as solvents for oled formulations |
| EP3581633A1 (de) | 2015-06-12 | 2019-12-18 | Merck Patent GmbH | Ester mit nichtaromatischen zyklen als lösungsmittel für oled-formulierungen |
| WO2017036572A1 (en) | 2015-08-28 | 2017-03-09 | Merck Patent Gmbh | Formulation of an organic functional material comprising an epoxy group containing solvent |
| WO2017097391A1 (en) | 2015-12-10 | 2017-06-15 | Merck Patent Gmbh | Formulations containing ketones comprising non-aromatic cycles |
| WO2017102048A1 (en) | 2015-12-15 | 2017-06-22 | Merck Patent Gmbh | Esters containing aromatic groups as solvents for organic electronic formulations |
| EP4084109A1 (de) | 2015-12-15 | 2022-11-02 | Merck Patent GmbH | Ester mit aromatischen gruppen als lösungsmittel für organische elektronische formulierungen |
| WO2017102052A1 (en) | 2015-12-16 | 2017-06-22 | Merck Patent Gmbh | Formulations containing a solid solvent |
| WO2017102049A1 (en) | 2015-12-16 | 2017-06-22 | Merck Patent Gmbh | Formulations containing a mixture of at least two different solvents |
| WO2017140404A1 (en) | 2016-02-17 | 2017-08-24 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2017157783A1 (de) | 2016-03-15 | 2017-09-21 | Merck Patent Gmbh | Behälter umfassend eine formulierung enthaltend mindestens einen organischen halbleiter |
| DE102016003104A1 (de) | 2016-03-15 | 2017-09-21 | Merck Patent Gmbh | Behälter umfassend eine Formulierung enthaltend mindestens einen organischen Halbleiter |
| WO2017216129A1 (en) | 2016-06-16 | 2017-12-21 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2017216128A1 (en) | 2016-06-17 | 2017-12-21 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2018001928A1 (en) | 2016-06-28 | 2018-01-04 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2018024719A1 (en) | 2016-08-04 | 2018-02-08 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2018077662A1 (en) | 2016-10-31 | 2018-05-03 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2018077660A1 (en) | 2016-10-31 | 2018-05-03 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2018104202A1 (en) | 2016-12-06 | 2018-06-14 | Merck Patent Gmbh | Preparation process for an electronic device |
| WO2018108760A1 (en) | 2016-12-13 | 2018-06-21 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2018138319A1 (en) | 2017-01-30 | 2018-08-02 | Merck Patent Gmbh | Method for forming an organic electroluminescence (el) element |
| WO2018138318A1 (en) | 2017-01-30 | 2018-08-02 | Merck Patent Gmbh | Method for forming an organic element of an electronic device |
| WO2018178136A1 (en) | 2017-03-31 | 2018-10-04 | Merck Patent Gmbh | Printing method for an organic light emitting diode (oled) |
| WO2018189050A1 (en) | 2017-04-10 | 2018-10-18 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2018202603A1 (en) | 2017-05-03 | 2018-11-08 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2019016184A1 (en) | 2017-07-18 | 2019-01-24 | Merck Patent Gmbh | FORMULATION OF AN ORGANIC FUNCTIONAL MATERIAL |
| WO2019115573A1 (en) | 2017-12-15 | 2019-06-20 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2019162483A1 (en) | 2018-02-26 | 2019-08-29 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2019238782A1 (en) | 2018-06-15 | 2019-12-19 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2020094538A1 (en) | 2018-11-06 | 2020-05-14 | Merck Patent Gmbh | Method for forming an organic element of an electronic device |
| WO2021213918A1 (en) | 2020-04-21 | 2021-10-28 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2021213917A1 (en) | 2020-04-21 | 2021-10-28 | Merck Patent Gmbh | Emulsions comprising organic functional materials |
| WO2022122607A1 (en) | 2020-12-08 | 2022-06-16 | Merck Patent Gmbh | An ink system and a method for inkjet printing |
| WO2022223675A1 (en) | 2021-04-23 | 2022-10-27 | Merck Patent Gmbh | Formulation of an organic functional material |
| WO2023012084A1 (en) | 2021-08-02 | 2023-02-09 | Merck Patent Gmbh | A printing method by combining inks |
| WO2023057327A1 (en) | 2021-10-05 | 2023-04-13 | Merck Patent Gmbh | Method for forming an organic element of an electronic device |
| WO2023237458A1 (en) | 2022-06-07 | 2023-12-14 | Merck Patent Gmbh | Method of printing a functional layer of an electronic device by combining inks |
| WO2024126635A1 (en) | 2022-12-16 | 2024-06-20 | Merck Patent Gmbh | Formulation of an organic functional material |
Also Published As
| Publication number | Publication date |
|---|---|
| EP1932866A1 (de) | 2008-06-18 |
| KR20050102101A (ko) | 2005-10-25 |
| WO2004070772A3 (de) | 2004-12-02 |
| JP2006516666A (ja) | 2006-07-06 |
| WO2004070772A2 (de) | 2004-08-19 |
| EP1592729A2 (de) | 2005-11-09 |
| KR101041766B1 (ko) | 2011-06-17 |
| US7834136B2 (en) | 2010-11-16 |
| US8053547B2 (en) | 2011-11-08 |
| CN100360579C (zh) | 2008-01-09 |
| CN1747981A (zh) | 2006-03-15 |
| EP1592729B1 (de) | 2008-04-23 |
| DE502004006904D1 (de) | 2008-06-05 |
| CN101333328B (zh) | 2013-11-06 |
| EP1932866B1 (de) | 2011-07-13 |
| JP4566185B2 (ja) | 2010-10-20 |
| US20060149022A1 (en) | 2006-07-06 |
| CN101333328A (zh) | 2008-12-31 |
| US20110068304A1 (en) | 2011-03-24 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP1932866B1 (de) | Blends enthaltend konjugierte Carbazol-Polymere, deren Darstellung und Verwendung | |
| EP1641894B1 (de) | Neue materialien für die elektrolumineszenz | |
| EP1558662B1 (de) | Arylamin-einheiten enthaltende konjugierte polymere, deren darstellung und verwendung | |
| DE102005037734B4 (de) | Elektrolumineszierende Polymere, ihre Verwendung und bifunktionelle monomere Verbindungen | |
| EP1656407B1 (de) | Konjugierte copolymere, deren darstellung und verwendung | |
| EP0793698B1 (de) | Konjugierte polymere mit hetero-spiroatomen und ihre verwendung als elektrolumineszenzmaterialien | |
| EP1656408B1 (de) | Konjugierte polymere enthaltend dihydrophenanthren-einheiten und deren verwendung | |
| EP1668058B1 (de) | Konjugierte polymere, deren darstellung und verwendung | |
| EP1427768B1 (de) | Konjugierte polymere enthaltend spirobifluoren-einheiten und deren verwendung | |
| DE60103442T2 (de) | Polymerisches fluoreszentes Material, Verfahren zu ihrer Herstellung, und lumineszentes Polymergerät worin es eingesetzt wird | |
| EP1381639B1 (de) | Konjugierte polymere enthaltend spirobifluoren-einheiten und fluoren-einheiten und deren verwendung | |
| EP2038241B1 (de) | Elektrolumineszierende polymere und ihre verwendung | |
| EP1709699B1 (de) | Konjugierte polymere, deren darstellung und verwendung | |
| DE102004020298A1 (de) | Elektrolumineszierende Polymere und deren Verwendung | |
| DE102004020299A1 (de) | Konjugierte Polymere, deren Darstellung und Verwendung | |
| DE10349033A1 (de) | Neue Materialien für die Elektrolumineszenz und deren Verwendung | |
| DE10357317A1 (de) | Konjugierte Polymere, deren Darstellung und Verwendung |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 8181 | Inventor (new situation) |
Inventor name: BREUNING, ESTHER, DR., 65527 NIEDERNHAUSEN, DE Inventor name: PARHAM, AMIR, DIPL.-CHEM. DR., 65929 FRANKFURT, DE Inventor name: BECKER, HEINRICH, DIPL.-CHEM. DR., 65719 HOFHEIM, Inventor name: HEUN, SUSANNE, DR., 65812 BAD SODEN, DE Inventor name: FALCOU, AURELIE, DIPL.-CHEM. DR., 60322 FRANKFURT, |
|
| 8127 | New person/name/address of the applicant |
Owner name: MERCK PATENT GMBH, 64293 DARMSTADT, DE |
|
| 8139 | Disposal/non-payment of the annual fee |