KR20170028268A - 유기 전계발광 재료 및 소자 - Google Patents
유기 전계발광 재료 및 소자 Download PDFInfo
- Publication number
- KR20170028268A KR20170028268A KR1020160112495A KR20160112495A KR20170028268A KR 20170028268 A KR20170028268 A KR 20170028268A KR 1020160112495 A KR1020160112495 A KR 1020160112495A KR 20160112495 A KR20160112495 A KR 20160112495A KR 20170028268 A KR20170028268 A KR 20170028268A
- Authority
- KR
- South Korea
- Prior art keywords
- group
- alkyl
- unsubstituted
- compound
- cycloalkyl
- Prior art date
Links
- 239000000463 material Substances 0.000 title description 84
- 150000001875 compounds Chemical class 0.000 claims abstract description 94
- 239000010410 layer Substances 0.000 claims description 96
- 125000000217 alkyl group Chemical group 0.000 claims description 47
- 239000003446 ligand Substances 0.000 claims description 42
- 125000000753 cycloalkyl group Chemical group 0.000 claims description 37
- 125000004432 carbon atom Chemical group C* 0.000 claims description 31
- 125000003118 aryl group Chemical group 0.000 claims description 30
- 125000001072 heteroaryl group Chemical group 0.000 claims description 30
- 229910052751 metal Inorganic materials 0.000 claims description 30
- 239000002184 metal Substances 0.000 claims description 30
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 claims description 28
- 229910052739 hydrogen Inorganic materials 0.000 claims description 28
- 239000001257 hydrogen Substances 0.000 claims description 28
- YZCKVEUIGOORGS-OUBTZVSYSA-N Deuterium Chemical compound [2H] YZCKVEUIGOORGS-OUBTZVSYSA-N 0.000 claims description 27
- 229910052805 deuterium Inorganic materials 0.000 claims description 27
- 239000012044 organic layer Substances 0.000 claims description 26
- 150000002431 hydrogen Chemical class 0.000 claims description 25
- 238000000034 method Methods 0.000 claims description 25
- 125000001424 substituent group Chemical group 0.000 claims description 25
- 229910052760 oxygen Inorganic materials 0.000 claims description 24
- 239000002019 doping agent Substances 0.000 claims description 23
- 229910052757 nitrogen Inorganic materials 0.000 claims description 22
- UJOBWOGCFQCDNV-UHFFFAOYSA-N 9H-carbazole Chemical compound C1=CC=C2C3=CC=CC=C3NC2=C1 UJOBWOGCFQCDNV-UHFFFAOYSA-N 0.000 claims description 18
- 125000003342 alkenyl group Chemical group 0.000 claims description 18
- 125000003710 aryl alkyl group Chemical group 0.000 claims description 18
- 125000000304 alkynyl group Chemical group 0.000 claims description 17
- 125000002252 acyl group Chemical group 0.000 claims description 16
- 125000002915 carbonyl group Chemical group [*:2]C([*:1])=O 0.000 claims description 16
- 229910052799 carbon Inorganic materials 0.000 claims description 15
- 125000003545 alkoxy group Chemical group 0.000 claims description 14
- 125000004104 aryloxy group Chemical group 0.000 claims description 14
- TXCDCPKCNAJMEE-UHFFFAOYSA-N dibenzofuran Chemical compound C1=CC=C2C3=CC=CC=C3OC2=C1 TXCDCPKCNAJMEE-UHFFFAOYSA-N 0.000 claims description 14
- IYYZUPMFVPLQIF-UHFFFAOYSA-N dibenzothiophene Chemical compound C1=CC=C2C3=CC=CC=C3SC2=C1 IYYZUPMFVPLQIF-UHFFFAOYSA-N 0.000 claims description 14
- 150000002148 esters Chemical class 0.000 claims description 14
- 125000004404 heteroalkyl group Chemical group 0.000 claims description 14
- 150000002527 isonitriles Chemical class 0.000 claims description 14
- 150000002825 nitriles Chemical class 0.000 claims description 14
- 125000000475 sulfinyl group Chemical group [*:2]S([*:1])=O 0.000 claims description 14
- 125000003396 thiol group Chemical group [H]S* 0.000 claims description 14
- 150000001732 carboxylic acid derivatives Chemical class 0.000 claims description 13
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 claims description 12
- 150000004820 halides Chemical class 0.000 claims description 12
- 229910052741 iridium Inorganic materials 0.000 claims description 12
- 229910052717 sulfur Inorganic materials 0.000 claims description 12
- SLGBZMMZGDRARJ-UHFFFAOYSA-N Triphenylene Natural products C1=CC=C2C3=CC=CC=C3C3=CC=CC=C3C2=C1 SLGBZMMZGDRARJ-UHFFFAOYSA-N 0.000 claims description 11
- 125000005580 triphenylene group Chemical group 0.000 claims description 11
- 230000003647 oxidation Effects 0.000 claims description 9
- 238000007254 oxidation reaction Methods 0.000 claims description 9
- 125000002950 monocyclic group Chemical group 0.000 claims description 6
- 239000000126 substance Substances 0.000 claims description 6
- 125000005119 alkyl cycloalkyl group Chemical group 0.000 claims description 5
- DHFABSXGNHDNCO-UHFFFAOYSA-N dibenzoselenophene Chemical compound C1=CC=C2C3=CC=CC=C3[se]C2=C1 DHFABSXGNHDNCO-UHFFFAOYSA-N 0.000 claims description 5
- 238000005286 illumination Methods 0.000 claims description 5
- 229910052697 platinum Inorganic materials 0.000 claims description 5
- BPMFPOGUJAAYHL-UHFFFAOYSA-N 9H-Pyrido[2,3-b]indole Chemical compound C1=CC=C2C3=CC=CC=C3NC2=N1 BPMFPOGUJAAYHL-UHFFFAOYSA-N 0.000 claims description 3
- 229910052762 osmium Inorganic materials 0.000 claims description 3
- 229910052737 gold Inorganic materials 0.000 claims description 2
- 229910052702 rhenium Inorganic materials 0.000 claims description 2
- 229910052703 rhodium Inorganic materials 0.000 claims description 2
- 229910052707 ruthenium Inorganic materials 0.000 claims description 2
- KRHYYFGTRYWZRS-UHFFFAOYSA-M Fluoride anion Chemical compound [F-] KRHYYFGTRYWZRS-UHFFFAOYSA-M 0.000 claims 1
- 229910052802 copper Inorganic materials 0.000 claims 1
- 125000002524 organometallic group Chemical group 0.000 abstract 2
- 0 C*=C([*@](*(C)=*)C(C(C1=I)=*)=I(*=[*-])=C)C1=C(C)*=* Chemical compound C*=C([*@](*(C)=*)C(C(C1=I)=*)=I(*=[*-])=C)C1=C(C)*=* 0.000 description 38
- -1 for example Chemical group 0.000 description 28
- 239000011541 reaction mixture Substances 0.000 description 27
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 24
- 239000000047 product Substances 0.000 description 24
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 21
- IOJUPLGTWVMSFF-UHFFFAOYSA-N benzothiazole Chemical compound C1=CC=C2SC=NC2=C1 IOJUPLGTWVMSFF-UHFFFAOYSA-N 0.000 description 20
- 239000000758 substrate Substances 0.000 description 19
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N silicon dioxide Inorganic materials O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 17
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 16
- 238000004440 column chromatography Methods 0.000 description 16
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 15
- FCEHBMOGCRZNNI-UHFFFAOYSA-N 1-benzothiophene Chemical compound C1=CC=C2SC=CC2=C1 FCEHBMOGCRZNNI-UHFFFAOYSA-N 0.000 description 14
- 238000005259 measurement Methods 0.000 description 14
- 230000004888 barrier function Effects 0.000 description 13
- 150000004696 coordination complex Chemical class 0.000 description 13
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 12
- UFWIBTONFRDIAS-UHFFFAOYSA-N Naphthalene Chemical compound C1=CC=CC2=CC=CC=C21 UFWIBTONFRDIAS-UHFFFAOYSA-N 0.000 description 12
- 150000003384 small molecules Chemical class 0.000 description 12
- 239000000203 mixture Substances 0.000 description 11
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 10
- 230000000903 blocking effect Effects 0.000 description 10
- 238000006243 chemical reaction Methods 0.000 description 10
- ZUOUZKKEUPVFJK-UHFFFAOYSA-N diphenyl Chemical compound C1=CC=CC=C1C1=CC=CC=C1 ZUOUZKKEUPVFJK-UHFFFAOYSA-N 0.000 description 10
- 238000004770 highest occupied molecular orbital Methods 0.000 description 10
- 238000004768 lowest unoccupied molecular orbital Methods 0.000 description 10
- 230000032258 transport Effects 0.000 description 10
- 230000015572 biosynthetic process Effects 0.000 description 9
- 238000001228 spectrum Methods 0.000 description 9
- YLQBMQCUIZJEEH-UHFFFAOYSA-N Furan Chemical compound C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 8
- YTPLMLYBLZKORZ-UHFFFAOYSA-N Thiophene Chemical compound C=1C=CSC=1 YTPLMLYBLZKORZ-UHFFFAOYSA-N 0.000 description 8
- 235000019439 ethyl acetate Nutrition 0.000 description 8
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 8
- XSCHRSMBECNVNS-UHFFFAOYSA-N quinoxaline Chemical compound N1=CC=NC2=CC=CC=C21 XSCHRSMBECNVNS-UHFFFAOYSA-N 0.000 description 8
- 239000000377 silicon dioxide Substances 0.000 description 8
- 239000000243 solution Substances 0.000 description 8
- 238000003786 synthesis reaction Methods 0.000 description 8
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 8
- 125000000392 cycloalkenyl group Chemical group 0.000 description 7
- GKOZUEZYRPOHIO-UHFFFAOYSA-N iridium atom Chemical compound [Ir] GKOZUEZYRPOHIO-UHFFFAOYSA-N 0.000 description 7
- 230000003287 optical effect Effects 0.000 description 7
- WCPAKWJPBJAGKN-UHFFFAOYSA-N oxadiazole Chemical compound C1=CON=N1 WCPAKWJPBJAGKN-UHFFFAOYSA-N 0.000 description 7
- 229920000642 polymer Polymers 0.000 description 7
- 239000002243 precursor Substances 0.000 description 7
- 239000007787 solid Substances 0.000 description 7
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 6
- KYQCOXFCLRTKLS-UHFFFAOYSA-N Pyrazine Chemical compound C1=CN=CC=N1 KYQCOXFCLRTKLS-UHFFFAOYSA-N 0.000 description 6
- SMWDFEZZVXVKRB-UHFFFAOYSA-N Quinoline Chemical compound N1=CC=CC2=CC=CC=C21 SMWDFEZZVXVKRB-UHFFFAOYSA-N 0.000 description 6
- MWPLVEDNUUSJAV-UHFFFAOYSA-N anthracene Chemical compound C1=CC=CC2=CC3=CC=CC=C3C=C21 MWPLVEDNUUSJAV-UHFFFAOYSA-N 0.000 description 6
- 238000000151 deposition Methods 0.000 description 6
- RAXXELZNTBOGNW-UHFFFAOYSA-N imidazole Natural products C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 description 6
- AWJUIBRHMBBTKR-UHFFFAOYSA-N isoquinoline Chemical compound C1=NC=CC2=CC=CC=C21 AWJUIBRHMBBTKR-UHFFFAOYSA-N 0.000 description 6
- 239000011368 organic material Substances 0.000 description 6
- YNPNZTXNASCQKK-UHFFFAOYSA-N phenanthrene Chemical compound C1=CC=C2C3=CC=CC=C3C=CC2=C1 YNPNZTXNASCQKK-UHFFFAOYSA-N 0.000 description 6
- FVZVCSNXTFCBQU-UHFFFAOYSA-N phosphanyl Chemical group [PH2] FVZVCSNXTFCBQU-UHFFFAOYSA-N 0.000 description 6
- BBEAQIROQSPTKN-UHFFFAOYSA-N pyrene Chemical compound C1=CC=C2C=CC3=CC=CC4=CC=C1C2=C43 BBEAQIROQSPTKN-UHFFFAOYSA-N 0.000 description 6
- 125000000472 sulfonyl group Chemical group *S(*)(=O)=O 0.000 description 6
- MPTVNPMFAZVTJG-UHFFFAOYSA-N 2-(benzenesulfonyl)pyridine Chemical class C=1C=CC=NC=1S(=O)(=O)C1=CC=CC=C1 MPTVNPMFAZVTJG-UHFFFAOYSA-N 0.000 description 5
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical group CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 5
- 239000004305 biphenyl Substances 0.000 description 5
- 235000010290 biphenyl Nutrition 0.000 description 5
- 230000000875 corresponding effect Effects 0.000 description 5
- 125000004122 cyclic group Chemical group 0.000 description 5
- 239000000412 dendrimer Substances 0.000 description 5
- 229920000736 dendritic polymer Polymers 0.000 description 5
- 230000000694 effects Effects 0.000 description 5
- 125000000623 heterocyclic group Chemical group 0.000 description 5
- 230000005525 hole transport Effects 0.000 description 5
- 230000005693 optoelectronics Effects 0.000 description 5
- 150000002894 organic compounds Chemical class 0.000 description 5
- JYEUMXHLPRZUAT-UHFFFAOYSA-N 1,2,3-triazine Chemical compound C1=CN=NN=C1 JYEUMXHLPRZUAT-UHFFFAOYSA-N 0.000 description 4
- YJTKZCDBKVTVBY-UHFFFAOYSA-N 1,3-Diphenylbenzene Chemical group C1=CC=CC=C1C1=CC=CC(C=2C=CC=CC=2)=C1 YJTKZCDBKVTVBY-UHFFFAOYSA-N 0.000 description 4
- SIKJAQJRHWYJAI-UHFFFAOYSA-N Indole Chemical compound C1=CC=C2NC=CC2=C1 SIKJAQJRHWYJAI-UHFFFAOYSA-N 0.000 description 4
- IMNFDUFMRHMDMM-UHFFFAOYSA-N N-Heptane Chemical compound CCCCCCC IMNFDUFMRHMDMM-UHFFFAOYSA-N 0.000 description 4
- PCNDJXKNXGMECE-UHFFFAOYSA-N Phenazine Natural products C1=CC=CC2=NC3=CC=CC=C3N=C21 PCNDJXKNXGMECE-UHFFFAOYSA-N 0.000 description 4
- WTKZEGDFNFYCGP-UHFFFAOYSA-N Pyrazole Chemical compound C=1C=NNC=1 WTKZEGDFNFYCGP-UHFFFAOYSA-N 0.000 description 4
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical compound [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 description 4
- WIUZHVZUGQDRHZ-UHFFFAOYSA-N [1]benzothiolo[3,2-b]pyridine Chemical compound C1=CN=C2C3=CC=CC=C3SC2=C1 WIUZHVZUGQDRHZ-UHFFFAOYSA-N 0.000 description 4
- 125000006615 aromatic heterocyclic group Chemical group 0.000 description 4
- 230000008859 change Effects 0.000 description 4
- 230000003111 delayed effect Effects 0.000 description 4
- RMBPEFMHABBEKP-UHFFFAOYSA-N fluorene Chemical compound C1=CC=C2C3=C[CH]C=CC3=CC2=C1 RMBPEFMHABBEKP-UHFFFAOYSA-N 0.000 description 4
- 238000009472 formulation Methods 0.000 description 4
- 229910052736 halogen Inorganic materials 0.000 description 4
- 150000002367 halogens Chemical class 0.000 description 4
- VVVPGLRKXQSQSZ-UHFFFAOYSA-N indolo[3,2-c]carbazole Chemical compound C1=CC=CC2=NC3=C4C5=CC=CC=C5N=C4C=CC3=C21 VVVPGLRKXQSQSZ-UHFFFAOYSA-N 0.000 description 4
- 238000002347 injection Methods 0.000 description 4
- 239000007924 injection Substances 0.000 description 4
- 238000004020 luminiscence type Methods 0.000 description 4
- 239000011159 matrix material Substances 0.000 description 4
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 4
- NIHNNTQXNPWCJQ-UHFFFAOYSA-N o-biphenylenemethane Natural products C1=CC=C2CC3=CC=CC=C3C2=C1 NIHNNTQXNPWCJQ-UHFFFAOYSA-N 0.000 description 4
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 4
- 229910052698 phosphorus Inorganic materials 0.000 description 4
- 230000008569 process Effects 0.000 description 4
- PBMFSQRYOILNGV-UHFFFAOYSA-N pyridazine Chemical compound C1=CC=NN=C1 PBMFSQRYOILNGV-UHFFFAOYSA-N 0.000 description 4
- 238000010992 reflux Methods 0.000 description 4
- 230000003595 spectral effect Effects 0.000 description 4
- 238000006467 substitution reaction Methods 0.000 description 4
- VLLMWSRANPNYQX-UHFFFAOYSA-N thiadiazole Chemical compound C1=CSN=N1.C1=CSN=N1 VLLMWSRANPNYQX-UHFFFAOYSA-N 0.000 description 4
- 229930192474 thiophene Natural products 0.000 description 4
- 230000007704 transition Effects 0.000 description 4
- 238000010626 work up procedure Methods 0.000 description 4
- FLBAYUMRQUHISI-UHFFFAOYSA-N 1,8-naphthyridine Chemical compound N1=CC=CC2=CC=CN=C21 FLBAYUMRQUHISI-UHFFFAOYSA-N 0.000 description 3
- HYZJCKYKOHLVJF-UHFFFAOYSA-N 1H-benzimidazole Chemical compound C1=CC=C2NC=NC2=C1 HYZJCKYKOHLVJF-UHFFFAOYSA-N 0.000 description 3
- OLGGLCIDAMICTA-UHFFFAOYSA-N 2-pyridin-2-yl-1h-indole Chemical compound N1C2=CC=CC=C2C=C1C1=CC=CC=N1 OLGGLCIDAMICTA-UHFFFAOYSA-N 0.000 description 3
- BCHZICNRHXRCHY-UHFFFAOYSA-N 2h-oxazine Chemical compound N1OC=CC=C1 BCHZICNRHXRCHY-UHFFFAOYSA-N 0.000 description 3
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 3
- KWYUFKZDYYNOTN-UHFFFAOYSA-M Potassium hydroxide Chemical compound [OH-].[K+] KWYUFKZDYYNOTN-UHFFFAOYSA-M 0.000 description 3
- CZPWVGJYEJSRLH-UHFFFAOYSA-N Pyrimidine Chemical compound C1=CN=CN=C1 CZPWVGJYEJSRLH-UHFFFAOYSA-N 0.000 description 3
- RWRDLPDLKQPQOW-UHFFFAOYSA-N Pyrrolidine Chemical compound C1CCNC1 RWRDLPDLKQPQOW-UHFFFAOYSA-N 0.000 description 3
- QZLAKPGRUFFNRD-UHFFFAOYSA-N [1]benzoselenolo[3,2-b]pyridine Chemical compound C1=CN=C2C3=CC=CC=C3[se]C2=C1 QZLAKPGRUFFNRD-UHFFFAOYSA-N 0.000 description 3
- 125000004429 atom Chemical group 0.000 description 3
- 230000008021 deposition Effects 0.000 description 3
- 238000010586 diagram Methods 0.000 description 3
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 3
- GVEPBJHOBDJJJI-UHFFFAOYSA-N fluoranthrene Natural products C1=CC(C2=CC=CC=C22)=C3C2=CC=CC3=C1 GVEPBJHOBDJJJI-UHFFFAOYSA-N 0.000 description 3
- 229960005544 indolocarbazole Drugs 0.000 description 3
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 3
- 238000004895 liquid chromatography mass spectrometry Methods 0.000 description 3
- 230000007246 mechanism Effects 0.000 description 3
- 125000004433 nitrogen atom Chemical group N* 0.000 description 3
- 239000003921 oil Substances 0.000 description 3
- NQFOGDIWKQWFMN-UHFFFAOYSA-N phenalene Chemical compound C1=CC([CH]C=C2)=C3C2=CC=CC3=C1 NQFOGDIWKQWFMN-UHFFFAOYSA-N 0.000 description 3
- 239000002244 precipitate Substances 0.000 description 3
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 3
- JWVCLYRUEFBMGU-UHFFFAOYSA-N quinazoline Chemical compound N1=CN=CC2=CC=CC=C21 JWVCLYRUEFBMGU-UHFFFAOYSA-N 0.000 description 3
- 230000005855 radiation Effects 0.000 description 3
- 230000035945 sensitivity Effects 0.000 description 3
- 229910052710 silicon Inorganic materials 0.000 description 3
- 238000002207 thermal evaporation Methods 0.000 description 3
- BCMCBBGGLRIHSE-UHFFFAOYSA-N 1,3-benzoxazole Chemical compound C1=CC=C2OC=NC2=C1 BCMCBBGGLRIHSE-UHFFFAOYSA-N 0.000 description 2
- BNRDGHFESOHOBF-UHFFFAOYSA-N 1-benzoselenophene Chemical compound C1=CC=C2[se]C=CC2=C1 BNRDGHFESOHOBF-UHFFFAOYSA-N 0.000 description 2
- NHDODQWIKUYWMW-UHFFFAOYSA-N 1-bromo-4-chlorobenzene Chemical compound ClC1=CC=C(Br)C=C1 NHDODQWIKUYWMW-UHFFFAOYSA-N 0.000 description 2
- BAXOFTOLAUCFNW-UHFFFAOYSA-N 1H-indazole Chemical compound C1=CC=C2C=NNC2=C1 BAXOFTOLAUCFNW-UHFFFAOYSA-N 0.000 description 2
- BWCDLEQTELFBAW-UHFFFAOYSA-N 3h-dioxazole Chemical compound N1OOC=C1 BWCDLEQTELFBAW-UHFFFAOYSA-N 0.000 description 2
- HOUOKNVRFVDYLA-UHFFFAOYSA-N 4-(4-chlorophenyl)-2-phenylpyridine Chemical compound C1=CC(Cl)=CC=C1C1=CC=NC(C=2C=CC=CC=2)=C1 HOUOKNVRFVDYLA-UHFFFAOYSA-N 0.000 description 2
- ZOXJGFHDIHLPTG-UHFFFAOYSA-N Boron Chemical group [B] ZOXJGFHDIHLPTG-UHFFFAOYSA-N 0.000 description 2
- 101100118680 Caenorhabditis elegans sec-61.G gene Proteins 0.000 description 2
- ZCQWOFVYLHDMMC-UHFFFAOYSA-N Oxazole Chemical compound C1=COC=N1 ZCQWOFVYLHDMMC-UHFFFAOYSA-N 0.000 description 2
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 2
- DZBUGLKDJFMEHC-UHFFFAOYSA-N acridine Chemical compound C1=CC=CC2=CC3=CC=CC=C3N=C21 DZBUGLKDJFMEHC-UHFFFAOYSA-N 0.000 description 2
- 125000001931 aliphatic group Chemical group 0.000 description 2
- VQGHOUODWALEFC-UHFFFAOYSA-N alpha-Phenylpyridine Natural products C1=CC=CC=C1C1=CC=CC=N1 VQGHOUODWALEFC-UHFFFAOYSA-N 0.000 description 2
- 150000004982 aromatic amines Chemical class 0.000 description 2
- CUFNKYGDVFVPHO-UHFFFAOYSA-N azulene Chemical compound C1=CC=CC2=CC=CC2=C1 CUFNKYGDVFVPHO-UHFFFAOYSA-N 0.000 description 2
- 230000008901 benefit Effects 0.000 description 2
- RFRXIWQYSOIBDI-UHFFFAOYSA-N benzarone Chemical compound CCC=1OC2=CC=CC=C2C=1C(=O)C1=CC=C(O)C=C1 RFRXIWQYSOIBDI-UHFFFAOYSA-N 0.000 description 2
- 230000008033 biological extinction Effects 0.000 description 2
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 2
- 238000004364 calculation method Methods 0.000 description 2
- 239000002800 charge carrier Substances 0.000 description 2
- WDECIBYCCFPHNR-UHFFFAOYSA-N chrysene Chemical compound C1=CC=CC2=CC=C3C4=CC=CC=C4C=CC3=C21 WDECIBYCCFPHNR-UHFFFAOYSA-N 0.000 description 2
- WCZVZNOTHYJIEI-UHFFFAOYSA-N cinnoline Chemical compound N1=NC=CC2=CC=CC=C21 WCZVZNOTHYJIEI-UHFFFAOYSA-N 0.000 description 2
- 230000002596 correlated effect Effects 0.000 description 2
- 230000007423 decrease Effects 0.000 description 2
- 238000005401 electroluminescence Methods 0.000 description 2
- 238000001194 electroluminescence spectrum Methods 0.000 description 2
- 238000002474 experimental method Methods 0.000 description 2
- 125000000524 functional group Chemical group 0.000 description 2
- JVZRCNQLWOELDU-UHFFFAOYSA-N gamma-Phenylpyridine Natural products C1=CC=CC=C1C1=CC=NC=C1 JVZRCNQLWOELDU-UHFFFAOYSA-N 0.000 description 2
- 239000011521 glass Substances 0.000 description 2
- 125000005842 heteroatom Chemical group 0.000 description 2
- PZOUSPYUWWUPPK-UHFFFAOYSA-N indole Natural products CC1=CC=CC2=C1C=CN2 PZOUSPYUWWUPPK-UHFFFAOYSA-N 0.000 description 2
- RKJUIXBNRJVNHR-UHFFFAOYSA-N indolenine Natural products C1=CC=C2CC=NC2=C1 RKJUIXBNRJVNHR-UHFFFAOYSA-N 0.000 description 2
- 150000002484 inorganic compounds Chemical class 0.000 description 2
- 229910010272 inorganic material Inorganic materials 0.000 description 2
- UEEXRMUCXBPYOV-UHFFFAOYSA-N iridium;2-phenylpyridine Chemical group [Ir].C1=CC=CC=C1C1=CC=CC=N1.C1=CC=CC=C1C1=CC=CC=N1.C1=CC=CC=C1C1=CC=CC=N1 UEEXRMUCXBPYOV-UHFFFAOYSA-N 0.000 description 2
- 239000007788 liquid Substances 0.000 description 2
- KWGKDLIKAYFUFQ-UHFFFAOYSA-M lithium chloride Chemical compound [Li+].[Cl-] KWGKDLIKAYFUFQ-UHFFFAOYSA-M 0.000 description 2
- SKEDXQSRJSUMRP-UHFFFAOYSA-N lithium;quinolin-8-ol Chemical compound [Li].C1=CN=C2C(O)=CC=CC2=C1 SKEDXQSRJSUMRP-UHFFFAOYSA-N 0.000 description 2
- 125000001971 neopentyl group Chemical group [H]C([*])([H])C(C([H])([H])[H])(C([H])([H])[H])C([H])([H])[H] 0.000 description 2
- AZHVQJLDOFKHPZ-UHFFFAOYSA-N oxathiazine Chemical compound O1SN=CC=C1 AZHVQJLDOFKHPZ-UHFFFAOYSA-N 0.000 description 2
- 125000004430 oxygen atom Chemical group O* 0.000 description 2
- YJVFFLUZDVXJQI-UHFFFAOYSA-L palladium(ii) acetate Chemical compound [Pd+2].CC([O-])=O.CC([O-])=O YJVFFLUZDVXJQI-UHFFFAOYSA-L 0.000 description 2
- 150000005359 phenylpyridines Chemical class 0.000 description 2
- 125000004437 phosphorous atom Chemical group 0.000 description 2
- LFSXCDWNBUNEEM-UHFFFAOYSA-N phthalazine Chemical compound C1=NN=CC2=CC=CC=C21 LFSXCDWNBUNEEM-UHFFFAOYSA-N 0.000 description 2
- 229920003229 poly(methyl methacrylate) Polymers 0.000 description 2
- 239000004926 polymethyl methacrylate Substances 0.000 description 2
- 239000011241 protective layer Substances 0.000 description 2
- 238000010791 quenching Methods 0.000 description 2
- 238000011160 research Methods 0.000 description 2
- 239000004065 semiconductor Substances 0.000 description 2
- 239000010703 silicon Substances 0.000 description 2
- 239000002356 single layer Substances 0.000 description 2
- 238000010129 solution processing Methods 0.000 description 2
- 125000004434 sulfur atom Chemical group 0.000 description 2
- 239000003826 tablet Substances 0.000 description 2
- 238000007725 thermal activation Methods 0.000 description 2
- 239000010409 thin film Substances 0.000 description 2
- RIOQSEWOXXDEQQ-UHFFFAOYSA-N triphenylphosphine Chemical compound C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 RIOQSEWOXXDEQQ-UHFFFAOYSA-N 0.000 description 2
- LWIHDJKSTIGBAC-UHFFFAOYSA-K tripotassium phosphate Chemical compound [K+].[K+].[K+].[O-]P([O-])([O-])=O LWIHDJKSTIGBAC-UHFFFAOYSA-K 0.000 description 2
- 239000011701 zinc Substances 0.000 description 2
- VNDYJBBGRKZCSX-UHFFFAOYSA-L zinc bromide Chemical compound Br[Zn]Br VNDYJBBGRKZCSX-UHFFFAOYSA-L 0.000 description 2
- QXYOAWHKJRWNID-RRKCRQDMSA-N (1s,3r,4r)-3-bromobicyclo[2.2.1]heptane Chemical compound C1C[C@H]2[C@H](Br)C[C@@H]1C2 QXYOAWHKJRWNID-RRKCRQDMSA-N 0.000 description 1
- CAYQIZIAYYNFCS-UHFFFAOYSA-N (4-chlorophenyl)boronic acid Chemical compound OB(O)C1=CC=C(Cl)C=C1 CAYQIZIAYYNFCS-UHFFFAOYSA-N 0.000 description 1
- KTZQTRPPVKQPFO-UHFFFAOYSA-N 1,2-benzoxazole Chemical compound C1=CC=C2C=NOC2=C1 KTZQTRPPVKQPFO-UHFFFAOYSA-N 0.000 description 1
- KCZDTZZRNNRKQE-UHFFFAOYSA-N 1-(4-bromophenyl)adamantane Chemical compound C1=CC(Br)=CC=C1C1(C2)CC(C3)CC2CC3C1 KCZDTZZRNNRKQE-UHFFFAOYSA-N 0.000 description 1
- XACJBFHSZJWBBP-UHFFFAOYSA-N 1-phenyladamantane Chemical compound C1C(C2)CC(C3)CC1CC23C1=CC=CC=C1 XACJBFHSZJWBBP-UHFFFAOYSA-N 0.000 description 1
- WJFKNYWRSNBZNX-UHFFFAOYSA-N 10H-phenothiazine Chemical compound C1=CC=C2NC3=CC=CC=C3SC2=C1 WJFKNYWRSNBZNX-UHFFFAOYSA-N 0.000 description 1
- VEPOHXYIFQMVHW-XOZOLZJESA-N 2,3-dihydroxybutanedioic acid (2S,3S)-3,4-dimethyl-2-phenylmorpholine Chemical compound OC(C(O)C(O)=O)C(O)=O.C[C@H]1[C@@H](OCCN1C)c1ccccc1 VEPOHXYIFQMVHW-XOZOLZJESA-N 0.000 description 1
- PCMMSLVJMKQWMQ-UHFFFAOYSA-N 2,4-dibromopyridine Chemical compound BrC1=CC=NC(Br)=C1 PCMMSLVJMKQWMQ-UHFFFAOYSA-N 0.000 description 1
- YASXBDJBCBUIHT-UHFFFAOYSA-N 2,4-diphenylpyridine Chemical compound C1=CC=CC=C1C1=CC=NC(C=2C=CC=CC=2)=C1 YASXBDJBCBUIHT-UHFFFAOYSA-N 0.000 description 1
- AZCNDGAXOZWQPV-UHFFFAOYSA-N 2-(4-bromophenyl)-4,4,5,5-tetramethyl-1,3,2-dioxaborolane Chemical compound O1C(C)(C)C(C)(C)OB1C1=CC=C(Br)C=C1 AZCNDGAXOZWQPV-UHFFFAOYSA-N 0.000 description 1
- RICKKZXCGCSLIU-UHFFFAOYSA-N 2-[2-[carboxymethyl-[[3-hydroxy-5-(hydroxymethyl)-2-methylpyridin-4-yl]methyl]amino]ethyl-[[3-hydroxy-5-(hydroxymethyl)-2-methylpyridin-4-yl]methyl]amino]acetic acid Chemical compound CC1=NC=C(CO)C(CN(CCN(CC(O)=O)CC=2C(=C(C)N=CC=2CO)O)CC(O)=O)=C1O RICKKZXCGCSLIU-UHFFFAOYSA-N 0.000 description 1
- JWUJQDFVADABEY-UHFFFAOYSA-N 2-methyltetrahydrofuran Chemical compound CC1CCCO1 JWUJQDFVADABEY-UHFFFAOYSA-N 0.000 description 1
- UJRVBGVVJVIAEX-FIBGUPNXSA-N 2-phenyl-4-[4-(trideuteriomethyl)phenyl]pyridine Chemical compound [2H]C([2H])([2H])c1ccc(cc1)-c1ccnc(c1)-c1ccccc1 UJRVBGVVJVIAEX-FIBGUPNXSA-N 0.000 description 1
- 150000005360 2-phenylpyridines Chemical class 0.000 description 1
- QMEQBOSUJUOXMX-UHFFFAOYSA-N 2h-oxadiazine Chemical compound N1OC=CC=N1 QMEQBOSUJUOXMX-UHFFFAOYSA-N 0.000 description 1
- 125000003542 3-methylbutan-2-yl group Chemical group [H]C([H])([H])C([H])(*)C([H])(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- KWIVRAVCZJXOQC-UHFFFAOYSA-N 3h-oxathiazole Chemical compound N1SOC=C1 KWIVRAVCZJXOQC-UHFFFAOYSA-N 0.000 description 1
- KKLCYBZPQDOFQK-UHFFFAOYSA-N 4,4,5,5-tetramethyl-2-phenyl-1,3,2-dioxaborolane Chemical compound O1C(C)(C)C(C)(C)OB1C1=CC=CC=C1 KKLCYBZPQDOFQK-UHFFFAOYSA-N 0.000 description 1
- DHDHJYNTEFLIHY-UHFFFAOYSA-N 4,7-diphenyl-1,10-phenanthroline Chemical group C1=CC=CC=C1C1=CC=NC2=C1C=CC1=C(C=3C=CC=CC=3)C=CN=C21 DHDHJYNTEFLIHY-UHFFFAOYSA-N 0.000 description 1
- UCWOUEGBUIDPSL-UHFFFAOYSA-N 4-[4-(1-adamantyl)phenyl]-2-phenylpyridine Chemical compound C12(CC3CC(CC(C1)C3)C2)C1=CC=C(C=C1)C1=CC(=NC=C1)C1=CC=CC=C1 UCWOUEGBUIDPSL-UHFFFAOYSA-N 0.000 description 1
- JJPALPPJXMRPLY-BPPAMHLBSA-N 4-[4-[cyclopentyl(dideuterio)methyl]phenyl]-2-phenylpyridine Chemical compound C1(CCCC1)C(C1=CC=C(C=C1)C1=CC(=NC=C1)C1=CC=CC=C1)([2H])[2H] JJPALPPJXMRPLY-BPPAMHLBSA-N 0.000 description 1
- HCQHVQSQHXZRGA-UHFFFAOYSA-N 4-bromo-2-phenylpyridine Chemical compound BrC1=CC=NC(C=2C=CC=CC=2)=C1 HCQHVQSQHXZRGA-UHFFFAOYSA-N 0.000 description 1
- BFRWDRFLYBYSFX-UHFFFAOYSA-N 4-chloro-2-phenylpyridine Chemical compound ClC1=CC=NC(C=2C=CC=CC=2)=C1 BFRWDRFLYBYSFX-UHFFFAOYSA-N 0.000 description 1
- DIVZFUBWFAOMCW-UHFFFAOYSA-N 4-n-(3-methylphenyl)-1-n,1-n-bis[4-(n-(3-methylphenyl)anilino)phenyl]-4-n-phenylbenzene-1,4-diamine Chemical group CC1=CC=CC(N(C=2C=CC=CC=2)C=2C=CC(=CC=2)N(C=2C=CC(=CC=2)N(C=2C=CC=CC=2)C=2C=C(C)C=CC=2)C=2C=CC(=CC=2)N(C=2C=CC=CC=2)C=2C=C(C)C=CC=2)=C1 DIVZFUBWFAOMCW-UHFFFAOYSA-N 0.000 description 1
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 1
- GJCOSYZMQJWQCA-UHFFFAOYSA-N 9H-xanthene Chemical compound C1=CC=C2CC3=CC=CC=C3OC2=C1 GJCOSYZMQJWQCA-UHFFFAOYSA-N 0.000 description 1
- NLXLAEXVIDQMFP-UHFFFAOYSA-N Ammonia chloride Chemical class [NH4+].[Cl-] NLXLAEXVIDQMFP-UHFFFAOYSA-N 0.000 description 1
- PAYRUJLWNCNPSJ-UHFFFAOYSA-N Aniline Chemical compound NC1=CC=CC=C1 PAYRUJLWNCNPSJ-UHFFFAOYSA-N 0.000 description 1
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 1
- OMQJPNCDWANGKD-UHFFFAOYSA-N CC(C1)N=C1c1ccccc1 Chemical compound CC(C1)N=C1c1ccccc1 OMQJPNCDWANGKD-UHFFFAOYSA-N 0.000 description 1
- OTCZTHIOAWHECF-UHFFFAOYSA-N CC1(C)OB(c2cc(-c3ccccc3)ncc2)OC1(C)C Chemical compound CC1(C)OB(c2cc(-c3ccccc3)ncc2)OC1(C)C OTCZTHIOAWHECF-UHFFFAOYSA-N 0.000 description 1
- CJMTVLGFGYQFDJ-UHFFFAOYSA-N CC1(C)c2cc3c(-c4cc(cccc5)c5cc4)c(cccc4)c4c(-c(cc4)ccc4-c4nc(cccc5)c5[n]4-c4ccccc4)c3cc2-c2c1cccc2 Chemical compound CC1(C)c2cc3c(-c4cc(cccc5)c5cc4)c(cccc4)c4c(-c(cc4)ccc4-c4nc(cccc5)c5[n]4-c4ccccc4)c3cc2-c2c1cccc2 CJMTVLGFGYQFDJ-UHFFFAOYSA-N 0.000 description 1
- ADRAXRKPXLMCMY-UHFFFAOYSA-N C[OH]COS(C(F)(F)F)(=O)=O Chemical compound C[OH]COS(C(F)(F)F)(=O)=O ADRAXRKPXLMCMY-UHFFFAOYSA-N 0.000 description 1
- MORMGEIDEHOPMA-UHFFFAOYSA-N Cc1nc2ccccc2[n]1-c(cc1)ccc1-c1c(cccc2)c2c(-c2cc(cccc3)c3cc2)c2c1cccc2 Chemical compound Cc1nc2ccccc2[n]1-c(cc1)ccc1-c1c(cccc2)c2c(-c2cc(cccc3)c3cc2)c2c1cccc2 MORMGEIDEHOPMA-UHFFFAOYSA-N 0.000 description 1
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 1
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 description 1
- JMWWRIVQMZWNIJ-UHFFFAOYSA-N Nc(cc1nc2-c3cccc(-c4c(cccc5)c5c(-c5cc(cccc6)c6cc5)c5c4cccc5)c3)ccc1[n]2-c1ccccc1 Chemical compound Nc(cc1nc2-c3cccc(-c4c(cccc5)c5c(-c5cc(cccc6)c6cc5)c5c4cccc5)c3)ccc1[n]2-c1ccccc1 JMWWRIVQMZWNIJ-UHFFFAOYSA-N 0.000 description 1
- 101100030361 Neurospora crassa (strain ATCC 24698 / 74-OR23-1A / CBS 708.71 / DSM 1257 / FGSC 987) pph-3 gene Proteins 0.000 description 1
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 description 1
- 229920001609 Poly(3,4-ethylenedioxythiophene) Polymers 0.000 description 1
- DHXVGJBLRPWPCS-UHFFFAOYSA-N Tetrahydropyran Chemical compound C1CCOCC1 DHXVGJBLRPWPCS-UHFFFAOYSA-N 0.000 description 1
- FZWLAAWBMGSTSO-UHFFFAOYSA-N Thiazole Chemical compound C1=CSC=N1 FZWLAAWBMGSTSO-UHFFFAOYSA-N 0.000 description 1
- YHFUYFQTIVPPAE-UHFFFAOYSA-M [Cl-].C1(CCCC1)C[Zn+] Chemical compound [Cl-].C1(CCCC1)C[Zn+] YHFUYFQTIVPPAE-UHFFFAOYSA-M 0.000 description 1
- CCGGTOGOFBBGSC-UHFFFAOYSA-M [Cl-].[Mg+]CC1=CC=C(Cl)C=C1 Chemical compound [Cl-].[Mg+]CC1=CC=C(Cl)C=C1 CCGGTOGOFBBGSC-UHFFFAOYSA-M 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- 125000005073 adamantyl group Chemical group C12(CC3CC(CC(C1)C3)C2)* 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- 150000004945 aromatic hydrocarbons Chemical group 0.000 description 1
- 229910052796 boron Inorganic materials 0.000 description 1
- 229910052794 bromium Inorganic materials 0.000 description 1
- 230000005587 bubbling Effects 0.000 description 1
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- ZJHJKKPAWSYUQM-UHFFFAOYSA-N c(cc1)ccc1-[n]1c(-c(cc2)ccc2-c(cc2)ccc2-c2c(ccc3ccccc33)c3nc3c(cccc4)c4ccc23)nc2c1cccc2 Chemical compound c(cc1)ccc1-[n]1c(-c(cc2)ccc2-c(cc2)ccc2-c2c(ccc3ccccc33)c3nc3c(cccc4)c4ccc23)nc2c1cccc2 ZJHJKKPAWSYUQM-UHFFFAOYSA-N 0.000 description 1
- FXCLOFHTDRAVFH-UHFFFAOYSA-N c(cc1)ccc1-c(cc1)ccc1-c1nc(-c(cc2)ccc2-c2cccc(-c3cc(-c4nc5c(cccn6)c6c6ncccc6c5cc4)ccc3)c2)nc(-c(cc2)cc3c2-c2ccccc2C32c3ccccc3-c3ccccc23)n1 Chemical compound c(cc1)ccc1-c(cc1)ccc1-c1nc(-c(cc2)ccc2-c2cccc(-c3cc(-c4nc5c(cccn6)c6c6ncccc6c5cc4)ccc3)c2)nc(-c(cc2)cc3c2-c2ccccc2C32c3ccccc3-c3ccccc23)n1 FXCLOFHTDRAVFH-UHFFFAOYSA-N 0.000 description 1
- JOVZLVGOUNBOFN-UHFFFAOYSA-N c(cc1)ccc1-c1c(-c2c(c-3ccc4-c5cc(-c6nc(cccc7)c7[n]6-c6ccccc6)ccc5)c4ccc2)c-3c(-c2ccccc2)c2c1cccc2 Chemical compound c(cc1)ccc1-c1c(-c2c(c-3ccc4-c5cc(-c6nc(cccc7)c7[n]6-c6ccccc6)ccc5)c4ccc2)c-3c(-c2ccccc2)c2c1cccc2 JOVZLVGOUNBOFN-UHFFFAOYSA-N 0.000 description 1
- HZUJQNWHEKLRRN-UHFFFAOYSA-N c(cc1)ccc1-c1c(cccc2)c2c(-c(cc2)ccc2-c2c(-c3ccccc3)c3ncncc3c3c2cccc3)c2c1cccc2 Chemical compound c(cc1)ccc1-c1c(cccc2)c2c(-c(cc2)ccc2-c2c(-c3ccccc3)c3ncncc3c3c2cccc3)c2c1cccc2 HZUJQNWHEKLRRN-UHFFFAOYSA-N 0.000 description 1
- XCYYEEPNWJJNAU-UHFFFAOYSA-N c(cc1)ccc1-c1cc(-c2cc(-c3nc(-c4ccccc4)nc(-c4ccccc4)c3)cc(-c3nc(-c4ccccc4)nc(-c4ccccc4)c3)c2)cc(-c2ccccc2)n1 Chemical compound c(cc1)ccc1-c1cc(-c2cc(-c3nc(-c4ccccc4)nc(-c4ccccc4)c3)cc(-c3nc(-c4ccccc4)nc(-c4ccccc4)c3)c2)cc(-c2ccccc2)n1 XCYYEEPNWJJNAU-UHFFFAOYSA-N 0.000 description 1
- YFRHCRCGWJBZQK-UHFFFAOYSA-N c(cc1)ccc1-c1nc(c(-c2cc(cccc3)c3cc2)c(cccc2)c2c2-c3cc(cccc4)c4cc3)c2[n]1-c1ccccc1 Chemical compound c(cc1)ccc1-c1nc(c(-c2cc(cccc3)c3cc2)c(cccc2)c2c2-c3cc(cccc4)c4cc3)c2[n]1-c1ccccc1 YFRHCRCGWJBZQK-UHFFFAOYSA-N 0.000 description 1
- UTNBVZZNYFUEKK-UHFFFAOYSA-N c1cc(-c(cc2)ncc2-c2cc(-c(cc3)cnc3-c3cccc(-c4ccccn4)n3)cc(-c3cccnc3)c2)ncc1 Chemical compound c1cc(-c(cc2)ncc2-c2cc(-c(cc3)cnc3-c3cccc(-c4ccccn4)n3)cc(-c3cccnc3)c2)ncc1 UTNBVZZNYFUEKK-UHFFFAOYSA-N 0.000 description 1
- QUKBOURVNURZPV-UHFFFAOYSA-N c1ccc(cc(cc2)-c3c(cccc4)c4c(-c(cc4)ccc4-c4nc5c6ncccc6ccc5cc4)c4c3cccc4)c2c1 Chemical compound c1ccc(cc(cc2)-c3c(cccc4)c4c(-c(cc4)ccc4-c4nc5c6ncccc6ccc5cc4)c4c3cccc4)c2c1 QUKBOURVNURZPV-UHFFFAOYSA-N 0.000 description 1
- UHFBRTROMDDJEP-UHFFFAOYSA-N c1ccc(cc(cc2)-c3c(cccc4)c4c(-c4cc5ccccc5cc4)c4c3ccc(-c3nc(c(cccc5)c5cc5)c5cc3)c4)c2c1 Chemical compound c1ccc(cc(cc2)-c3c(cccc4)c4c(-c4cc5ccccc5cc4)c4c3ccc(-c3nc(c(cccc5)c5cc5)c5cc3)c4)c2c1 UHFBRTROMDDJEP-UHFFFAOYSA-N 0.000 description 1
- 238000005229 chemical vapour deposition Methods 0.000 description 1
- 239000000460 chlorine Substances 0.000 description 1
- 229910052801 chlorine Inorganic materials 0.000 description 1
- 230000000052 comparative effect Effects 0.000 description 1
- 239000002131 composite material Substances 0.000 description 1
- 229920001940 conductive polymer Polymers 0.000 description 1
- 238000012937 correction Methods 0.000 description 1
- 238000010168 coupling process Methods 0.000 description 1
- 238000005859 coupling reaction Methods 0.000 description 1
- 238000004132 cross linking Methods 0.000 description 1
- 150000004292 cyclic ethers Chemical class 0.000 description 1
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- 125000004987 dibenzofuryl group Chemical group C1(=CC=CC=2OC3=C(C21)C=CC=C3)* 0.000 description 1
- IYYZUPMFVPLQIF-ALWQSETLSA-N dibenzothiophene Chemical group C1=CC=CC=2[34S]C3=C(C=21)C=CC=C3 IYYZUPMFVPLQIF-ALWQSETLSA-N 0.000 description 1
- QPJFIVIVOOQUKD-UHFFFAOYSA-N dipyrazino[2,3-f:2,3-h]quinoxaline Chemical group C1=CN=C2C3=NC=CN=C3C3=NC=CN=C3C2=N1 QPJFIVIVOOQUKD-UHFFFAOYSA-N 0.000 description 1
- 238000009826 distribution Methods 0.000 description 1
- 238000000295 emission spectrum Methods 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 239000003822 epoxy resin Substances 0.000 description 1
- 239000010408 film Substances 0.000 description 1
- 229910052731 fluorine Inorganic materials 0.000 description 1
- 239000011737 fluorine Substances 0.000 description 1
- 239000012634 fragment Substances 0.000 description 1
- WHGLQYBALPTZNJ-UHFFFAOYSA-N furan;oxolane Chemical compound C1CCOC1.C=1C=COC=1 WHGLQYBALPTZNJ-UHFFFAOYSA-N 0.000 description 1
- 239000007789 gas Substances 0.000 description 1
- 125000005843 halogen group Chemical group 0.000 description 1
- 125000004051 hexyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 1
- 239000005457 ice water Substances 0.000 description 1
- 239000007943 implant Substances 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- AMGQUBHHOARCQH-UHFFFAOYSA-N indium;oxotin Chemical compound [In].[Sn]=O AMGQUBHHOARCQH-UHFFFAOYSA-N 0.000 description 1
- 239000011147 inorganic material Substances 0.000 description 1
- 239000011630 iodine Substances 0.000 description 1
- 229910052740 iodine Inorganic materials 0.000 description 1
- 150000002503 iridium Chemical class 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- 238000010030 laminating Methods 0.000 description 1
- 239000002346 layers by function Substances 0.000 description 1
- QDLAGTHXVHQKRE-UHFFFAOYSA-N lichenxanthone Natural products COC1=CC(O)=C2C(=O)C3=C(C)C=C(OC)C=C3OC2=C1 QDLAGTHXVHQKRE-UHFFFAOYSA-N 0.000 description 1
- 239000004973 liquid crystal related substance Substances 0.000 description 1
- 239000011777 magnesium Substances 0.000 description 1
- 238000004519 manufacturing process Methods 0.000 description 1
- 238000000691 measurement method Methods 0.000 description 1
- 229910044991 metal oxide Inorganic materials 0.000 description 1
- 150000004706 metal oxides Chemical class 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 239000000178 monomer Substances 0.000 description 1
- 125000001624 naphthyl group Chemical group 0.000 description 1
- 150000002829 nitrogen Chemical class 0.000 description 1
- 238000013041 optical simulation Methods 0.000 description 1
- 238000013086 organic photovoltaic Methods 0.000 description 1
- CQDAMYNQINDRQC-UHFFFAOYSA-N oxatriazole Chemical compound C1=NN=NO1 CQDAMYNQINDRQC-UHFFFAOYSA-N 0.000 description 1
- 238000000059 patterning Methods 0.000 description 1
- 125000001147 pentyl group Chemical group C(CCCC)* 0.000 description 1
- 125000002080 perylenyl group Chemical group C1(=CC=C2C=CC=C3C4=CC=CC5=CC=CC(C1=C23)=C45)* 0.000 description 1
- CSHWQDPOILHKBI-UHFFFAOYSA-N peryrene Natural products C1=CC(C2=CC=CC=3C2=C2C=CC=3)=C3C2=CC=CC3=C1 CSHWQDPOILHKBI-UHFFFAOYSA-N 0.000 description 1
- KBBSSGXNXGXONI-UHFFFAOYSA-N phenanthro[9,10-b]pyrazine Chemical compound C1=CN=C2C3=CC=CC=C3C3=CC=CC=C3C2=N1 KBBSSGXNXGXONI-UHFFFAOYSA-N 0.000 description 1
- RIYPENPUNLHEBK-UHFFFAOYSA-N phenanthro[9,10-b]pyridine Chemical compound C1=CC=C2C3=CC=CC=C3C3=CC=CC=C3C2=N1 RIYPENPUNLHEBK-UHFFFAOYSA-N 0.000 description 1
- 229950000688 phenothiazine Drugs 0.000 description 1
- 125000000843 phenylene group Chemical group C1(=C(C=CC=C1)*)* 0.000 description 1
- 150000003009 phosphonic acids Chemical class 0.000 description 1
- 239000011574 phosphorus Substances 0.000 description 1
- 238000000103 photoluminescence spectrum Methods 0.000 description 1
- IEQIEDJGQAUEQZ-UHFFFAOYSA-N phthalocyanine Chemical class N1C(N=C2C3=CC=CC=C3C(N=C3C4=CC=CC=C4C(=N4)N3)=N2)=C(C=CC=C2)C2=C1N=C1C2=CC=CC=C2C4=N1 IEQIEDJGQAUEQZ-UHFFFAOYSA-N 0.000 description 1
- 230000010287 polarization Effects 0.000 description 1
- 125000003367 polycyclic group Chemical group 0.000 description 1
- 229920000647 polyepoxide Polymers 0.000 description 1
- 239000002861 polymer material Substances 0.000 description 1
- 150000004033 porphyrin derivatives Chemical class 0.000 description 1
- 229910000160 potassium phosphate Inorganic materials 0.000 description 1
- 235000011009 potassium phosphates Nutrition 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 238000007639 printing Methods 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- CPNGPNLZQNNVQM-UHFFFAOYSA-N pteridine Chemical compound N1=CN=CC2=NC=CN=C21 CPNGPNLZQNNVQM-UHFFFAOYSA-N 0.000 description 1
- 125000004076 pyridyl group Chemical group 0.000 description 1
- 238000006862 quantum yield reaction Methods 0.000 description 1
- 239000010453 quartz Substances 0.000 description 1
- 230000006798 recombination Effects 0.000 description 1
- 238000005215 recombination Methods 0.000 description 1
- 238000001953 recrystallisation Methods 0.000 description 1
- 230000007261 regionalization Effects 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 125000006413 ring segment Chemical group 0.000 description 1
- 229920006395 saturated elastomer Polymers 0.000 description 1
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 125000003548 sec-pentyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- MABNMNVCOAICNO-UHFFFAOYSA-N selenophene Chemical compound C=1C=C[se]C=1 MABNMNVCOAICNO-UHFFFAOYSA-N 0.000 description 1
- 230000011664 signaling Effects 0.000 description 1
- 150000004756 silanes Chemical class 0.000 description 1
- 238000004088 simulation Methods 0.000 description 1
- 229910000029 sodium carbonate Inorganic materials 0.000 description 1
- AKHNMLFCWUSKQB-UHFFFAOYSA-L sodium thiosulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=S AKHNMLFCWUSKQB-UHFFFAOYSA-L 0.000 description 1
- 235000019345 sodium thiosulphate Nutrition 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- VNFWTIYUKDMAOP-UHFFFAOYSA-N sphos Chemical compound COC1=CC=CC(OC)=C1C1=CC=CC=C1P(C1CCCCC1)C1CCCCC1 VNFWTIYUKDMAOP-UHFFFAOYSA-N 0.000 description 1
- 238000004528 spin coating Methods 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 125000001973 tert-pentyl group Chemical group [H]C([H])([H])C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 238000012360 testing method Methods 0.000 description 1
- KTQYWNARBMKMCX-UHFFFAOYSA-N tetraphenylene Chemical group C1=CC=C2C3=CC=CC=C3C3=CC=CC=C3C3=CC=CC=C3C2=C1 KTQYWNARBMKMCX-UHFFFAOYSA-N 0.000 description 1
- 150000003852 triazoles Chemical class 0.000 description 1
- 238000007740 vapor deposition Methods 0.000 description 1
- 238000003466 welding Methods 0.000 description 1
- 229910052724 xenon Inorganic materials 0.000 description 1
- FHNFHKCVQCLJFQ-UHFFFAOYSA-N xenon atom Chemical compound [Xe] FHNFHKCVQCLJFQ-UHFFFAOYSA-N 0.000 description 1
- 229910052725 zinc Inorganic materials 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/14—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D409/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms
- C07D409/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains two hetero rings
- C07D487/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D491/00—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00
- C07D491/02—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00 in which the condensed system contains two hetero rings
- C07D491/04—Ortho-condensed systems
- C07D491/044—Ortho-condensed systems with only one oxygen atom as ring hetero atom in the oxygen-containing ring
- C07D491/048—Ortho-condensed systems with only one oxygen atom as ring hetero atom in the oxygen-containing ring the oxygen-containing ring being five-membered
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F15/00—Compounds containing elements of Groups 8, 9, 10 or 18 of the Periodic Table
- C07F15/0006—Compounds containing elements of Groups 8, 9, 10 or 18 of the Periodic Table compounds of the platinum group
- C07F15/0033—Iridium compounds
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent, e.g. electroluminescent, chemiluminescent materials
- C09K11/02—Use of particular materials as binders, particle coatings or suspension media therefor
- C09K11/025—Use of particular materials as binders, particle coatings or suspension media therefor non-luminescent particle coatings or suspension media
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent, e.g. electroluminescent, chemiluminescent materials
- C09K11/06—Luminescent, e.g. electroluminescent, chemiluminescent materials containing organic luminescent materials
-
- H01L51/0085—
-
- H01L51/5012—
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/11—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/30—Coordination compounds
- H10K85/341—Transition metal complexes, e.g. Ru(II)polypyridine complexes
- H10K85/342—Transition metal complexes, e.g. Ru(II)polypyridine complexes comprising iridium
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/40—Organosilicon compounds, e.g. TIPS pentacene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
- H10K85/622—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene containing four rings, e.g. pyrene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
- H10K85/626—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene containing more than one polycyclic condensed aromatic rings, e.g. bis-anthracene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/654—Aromatic compounds comprising a hetero atom comprising only nitrogen as heteroatom
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6572—Polycyclic condensed heteroaromatic hydrocarbons comprising only nitrogen in the heteroaromatic polycondensed ring system, e.g. phenanthroline or carbazole
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6576—Polycyclic condensed heteroaromatic hydrocarbons comprising only sulfur in the heteroaromatic polycondensed ring system, e.g. benzothiophene
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1029—Heterocyclic compounds characterised by ligands containing one nitrogen atom as the heteroatom
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/18—Metal complexes
- C09K2211/185—Metal complexes of the platinum group, i.e. Os, Ir, Pt, Ru, Rh or Pd
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K2101/00—Properties of the organic materials covered by group H10K85/00
- H10K2101/10—Triplet emission
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E10/00—Energy generation through renewable energy sources
- Y02E10/50—Photovoltaic [PV] energy
- Y02E10/549—Organic PV cells
Landscapes
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Organic Chemistry (AREA)
- Physics & Mathematics (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Crystallography & Structural Chemistry (AREA)
- Inorganic Chemistry (AREA)
- Optics & Photonics (AREA)
- Electroluminescent Light Sources (AREA)
- Detergent Compositions (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
- Nitrogen And Oxygen Or Sulfur-Condensed Heterocyclic Ring Systems (AREA)
- Plural Heterocyclic Compounds (AREA)
- Luminescent Compositions (AREA)
- Pyridine Compounds (AREA)
- Transition And Organic Metals Composition Catalysts For Addition Polymerization (AREA)
- Peptides Or Proteins (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
Abstract
본 발명은, 화합물의 분자가 0.67 초과의 배향 인자를 갖는, 이미터로서 사용하기 위한 유기금속 착물, 및 이것을 포함하는 유기 발광 다이오드와 같은 소자에 관한 것이다.
Description
관련 출원의 상호 참조
본 출원은 35 U.S.C.§119(e)(1)하에 2016년 5월 2일에 출원된 미국 가출원 제62/330,412호, 2016년 4월 14일에 출원된 미국 가출원 제62/332,510호, 2016년 2월 5일에 출원된 미국 가출원 제62/291,960호, 2015년 9월 24일에 출원된 미국 가출원 제62/232,194호, 2015년 9월 3일에 출원된 미국 가출원 제62/213,757호에 대해 우선권을 주장하며, 이들 문헌의 내용은 그 전문이 본원에 참고로 포함된다.
합동 연구 협약 당사자
당해 발명은 산학 합동 연구 협약에 따라 더 리전츠 오브 더 유니버시티 오브 미시간, 프린스턴 유니버시티, 유니버시티 오브 서던 캘리포니아 및 더 유니버셜 디스플레이 코포레이션 당사자 중 하나 이상에 의하여, 이를 대신하여 및/또는 이와 관련하여 완성되었다. 본 협약은 당해 발명이 완성된 일자에 그리고 그 일자 이전에 발효되었으며, 당해 발명은 협약서의 범주내에서 수행된 활동의 결과로서 완성되었다.
본 발명의 분야
본 발명은 이미터로서 사용하기 위한 화합물 및 이것을 포함하는 유기 발광 다이오드와 같은 소자에 관한 것이다.
유기 물질을 사용하는 광전자 소자는 여러 이유로 인하여 점차로 중요해지고 있다. 이와 같은 소자를 제조하는데 사용되는 다수의 물질은 비교적 저렴하여 유기 광전자 소자는 무기 소자에 비하여 경제적 잇점면에서 잠재성을 갖는다. 또한, 유기 물질의 고유한 성질, 예컨대 이의 가요성은 가요성 기판상에서의 제조와 같은 특정 적용예에 매우 적합하게 될 수 있다. 유기 광전자 소자의 예로는 유기 발광 소자(OLED), 유기 광트랜지스터, 유기 광전지 및 유기 광검출기를 들 수 있다. OLED의 경우, 유기 물질은 통상의 물질에 비하여 성능면에서의 잇점을 가질 수 있다. 예를 들면, 유기 발광층이 광을 방출하는 파장은 일반적으로 적절한 도펀트로 용이하게 조절될 수 있다.
OLED는 소자에 전압을 인가시 광을 방출하는 유기 박막을 사용하게 한다. OLED는 평판 패널 디스플레이, 조명 및 역광 조명과 같은 적용예에 사용하기 위한 점차로 중요해지는 기술이다. 여러가지의 OLED 물질 및 구조는 미국 특허 제5,844,363호, 제6,303,238호 및 제5,707,745호에 기재되어 있으며, 이들 특허 문헌은 그 전문이 본원에 참고로 포함된다.
인광 방출 분자에 대한 하나의 적용예는 풀 컬러 디스플레이이다. 이러한 디스플레이에 대한 산업적 기준은 "포화" 색상으로서 지칭하는 특정 색상을 방출하도록 조정된 픽셀을 필요로 한다. 특히, 이러한 기준은 포화 적색, 녹색 및 청색 픽셀을 필요로 한다. 대안으로, OLED는 백색 광을 방출하도록 설계될 수 있다. 통상적인 액정 디스플레이에서, 백색 백라이트에서 나온 발광이 흡수 필터를 사용하여 여과되어 적색, 녹색 및 청색 발광을 생성한다. 동일한 기법이 OLED에도 사용될 수 있다. 백색 OLED는 단일 EML 소자 또는 스택 구조일 수 있다. 색상은 당업계에 공지된 CIE 좌표를 사용하여 측정될 수 있다.
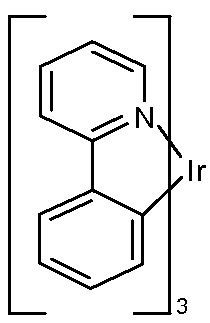
녹색 발광 분자의 일례로는 하기 화학식을 갖는 Ir(ppy)3으로 나타낸 트리스(2-페닐피리딘) 이리듐이다:
본원에서의 이와 같은 화학식 및 하기의 화학식에서, 본 출원인은 질소로부터 금속(여기에서는 Ir)으로의 배위 결합을 직선으로 도시한다.
본원에서, 용어 "유기"라는 것은 유기 광전자 소자를 제조하는데 사용될 수 있는 중합체 물질뿐 아니라, 소분자 유기 물질을 포함한다. "소분자"는 중합체가 아닌 임의의 유기 물질을 지칭하며, "소분자"는 실제로 꽤 클 수도 있다. 소분자는 일부의 상황에서는 반복 단위를 포함할 수 있다. 예를 들면, 치환기로서 장쇄 알킬 기를 사용하는 것은 "소분자" 부류로부터 분자를 제거하지 않는다. 소분자는 또한 예를 들면 중합체 주쇄상에서의 측쇄기로서 또는 주쇄의 일부로서 중합체에 혼입될 수 있다. 소분자는 또한 코어 부분상에 생성된 일련의 화학적 셸로 이루어진 덴드리머의 코어 부분으로서 작용할 수 있다. 덴드리머의 코어 부분은 형광 또는 인광 소분자 이미터일 수 있다. 덴드리머는 "소분자"일 수 있으며, OLED 분야에서 통상적으로 사용되는 모든 덴드리머는 소분자인 것으로 밝혀졌다.
본원에서 사용한 바와 같이, "상부"는 기판으로부터 가장 멀리 떨어졌다는 것을 의미하며, "하부"는 기판에 가장 근접하다는 것을 의미한다. 제1층이 제2층"의 상부에 배치되는" 것으로 기재될 경우, 제1층은 기판으로부터 멀리 떨어져 배치된다. 제1층이 제2층과 "접촉되어 있는" 것으로 명시되지 않는다면 제1층과 제2층 사이에는 다른 층이 존재할 수 있다. 예를 들면, 캐소드와 애노드의 사이에 다양한 유기층이 존재할 수 있을지라도, 캐소드는 애노드"의 상부에 배치되는" 것으로 기재될 수 있다.
본원에서 사용한 바와 같이, "용액 가공성"은 용액 또는 현탁액 형태로 액체 매체에 용해, 분산 또는 수송될 수 있거나 및/또는 액체 매체로부터 증착될 수 있다는 것을 의미한다.
리간드가 발광 물질의 광활성 성질에 직접적으로 기여하는 것으로 밝혀질 경우, 리간드는 "광활성"으로서 지칭될 수 있다. 보조적 리간드가 광활성 리간드의 성질을 변경시킬 수 있을지라도, 리간드가 발광 물질의 광활성 성질에 기여하지 않는 것으로 밝혀질 경우, 리간드는 "보조적"인 것으로 지칭될 수 있다.
본원에서 사용한 바와 같이 그리고 일반적으로 당업자가 이해하고 있는 바와 같이, 제1의 "최고 점유 분자 궤도"(HOMO) 또는 "최저 비점유 분자 궤도"(LUMO) 에너지 준위가 진공 에너지 준위에 근접할 경우, 제1의 에너지 준위는 제2의 HOMO 또는 LUMO보다 "더 크거나" 또는 "더 높다". 이온화 전위(IP)가 진공 준위에 대하여 음의 에너지로서 측정되므로, 더 높은 HOMO 에너지 준위는 더 작은 절대값을 갖는 IP에 해당한다(IP는 음의 값이 더 작다). 유사하게, 더 높은 LUMO 에너지 준위는 절대값이 더 작은 전자 친화도(EA)에 해당한다(EA의 음의 값이 더 작다). 상부에서의 진공 준위를 갖는 통상의 에너지 준위 다이아그램에서, 물질의 LUMO 에너지 준위는 동일한 물질의 HOMO 에너지 준위보다 더 높다. "더 높은" HOMO 또는 LUMO 에너지 준위는 "더 낮은" HOMO 또는 LUMO 에너지 준위보다 상기 다이아그램의 상부에 더 근접한다는 것을 나타낸다.
본원에서 사용한 바와 같이 그리고 일반적으로 당업자가 이해하는 바와 같이, 제1의 일 함수의 절대값이 더 클 경우, 제1의 일 함수는 제2의 일 함수보다 "더 크거나" 또는 "더 높다". 일 함수는 일반적으로 진공 준위에 대하여 음의 수로서 측정되므로, 이는 "더 높은" 일 함수의 음의 값이 더 크다는 것을 의미한다. 상부에서 진공 준위를 갖는 통상의 에너지 준위 다이아그램에서, "더 높은" 일 함수는 진공 준위로부터 아래 방향으로 더 먼 것으로서 도시된다. 그래서, HOMO 및 LUMO 에너지 준위의 정의는 일 함수와는 상이한 조약을 따른다.
OLED에 대한 세부사항 및 전술한 정의는 미국 특허 제7,279,704호에서 찾아볼 수 있으며, 이 특허 문헌의 개시내용은 그 전문이 본원에 참고로 포함된다.
한 실시양태에 따르면, 하기 화학식을 갖고 그 분자가 0.67을 초과하는 배향 인자 값을 갖는 화합물이 제공된다:
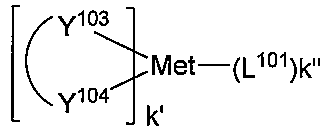
M(LA)h(LB)y(LC)z
상기 화학식에서,
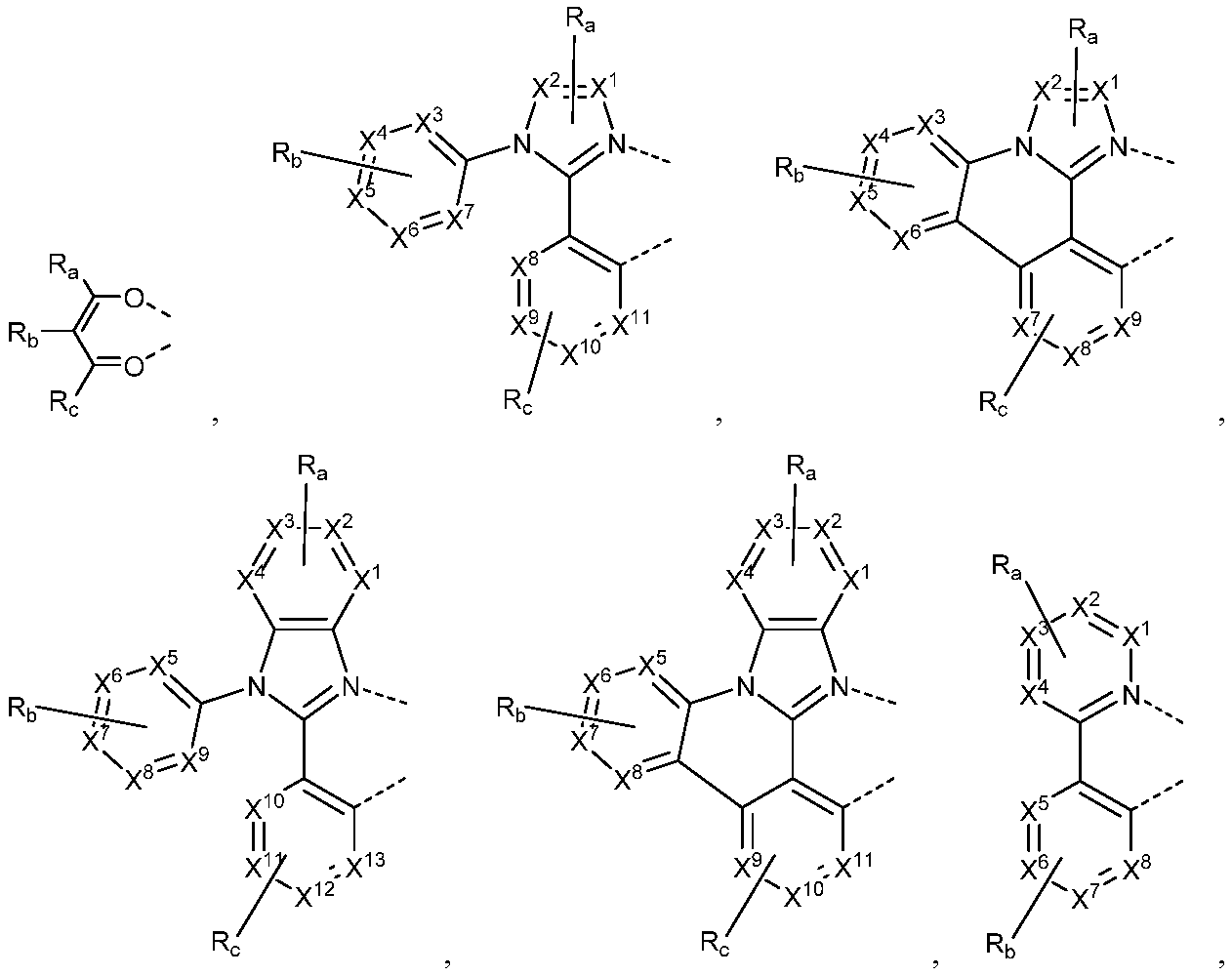
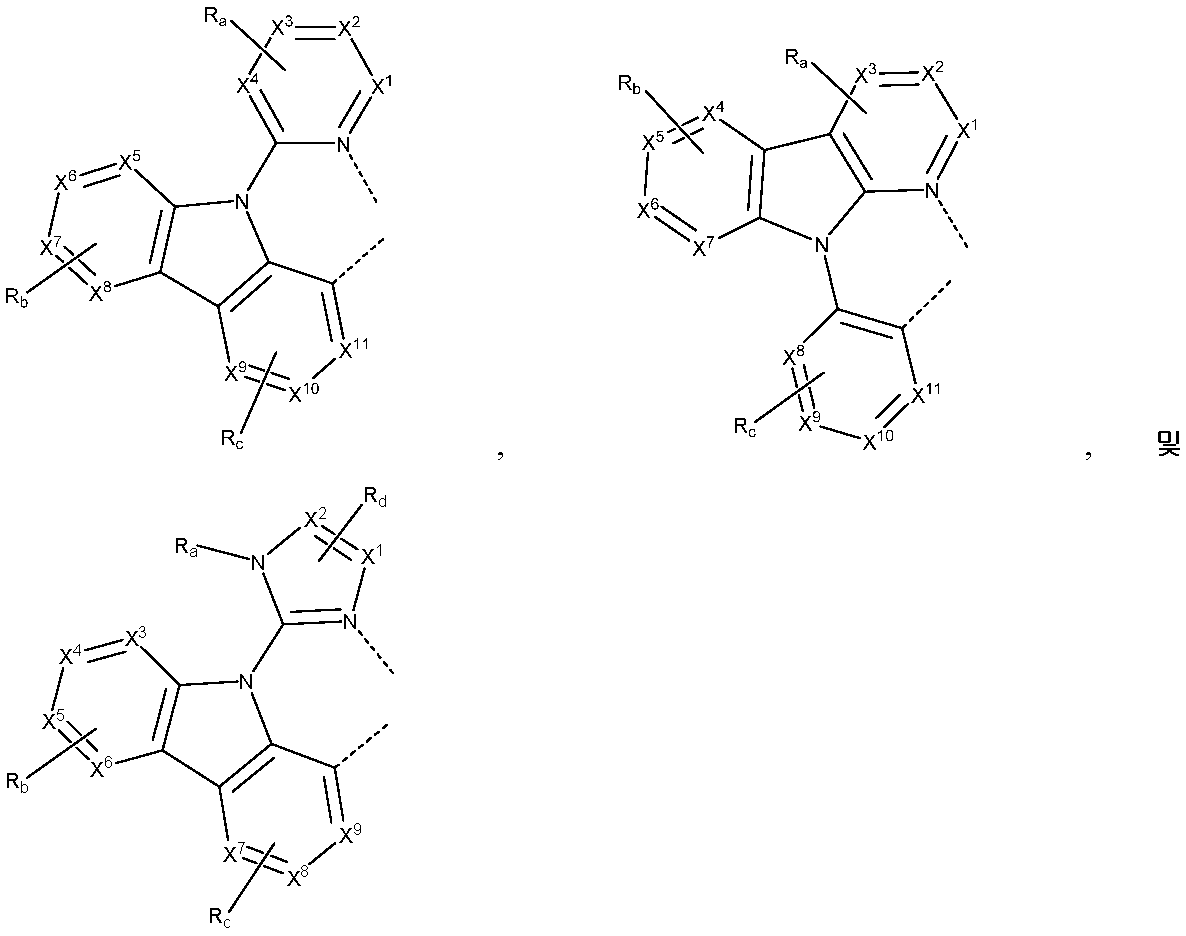
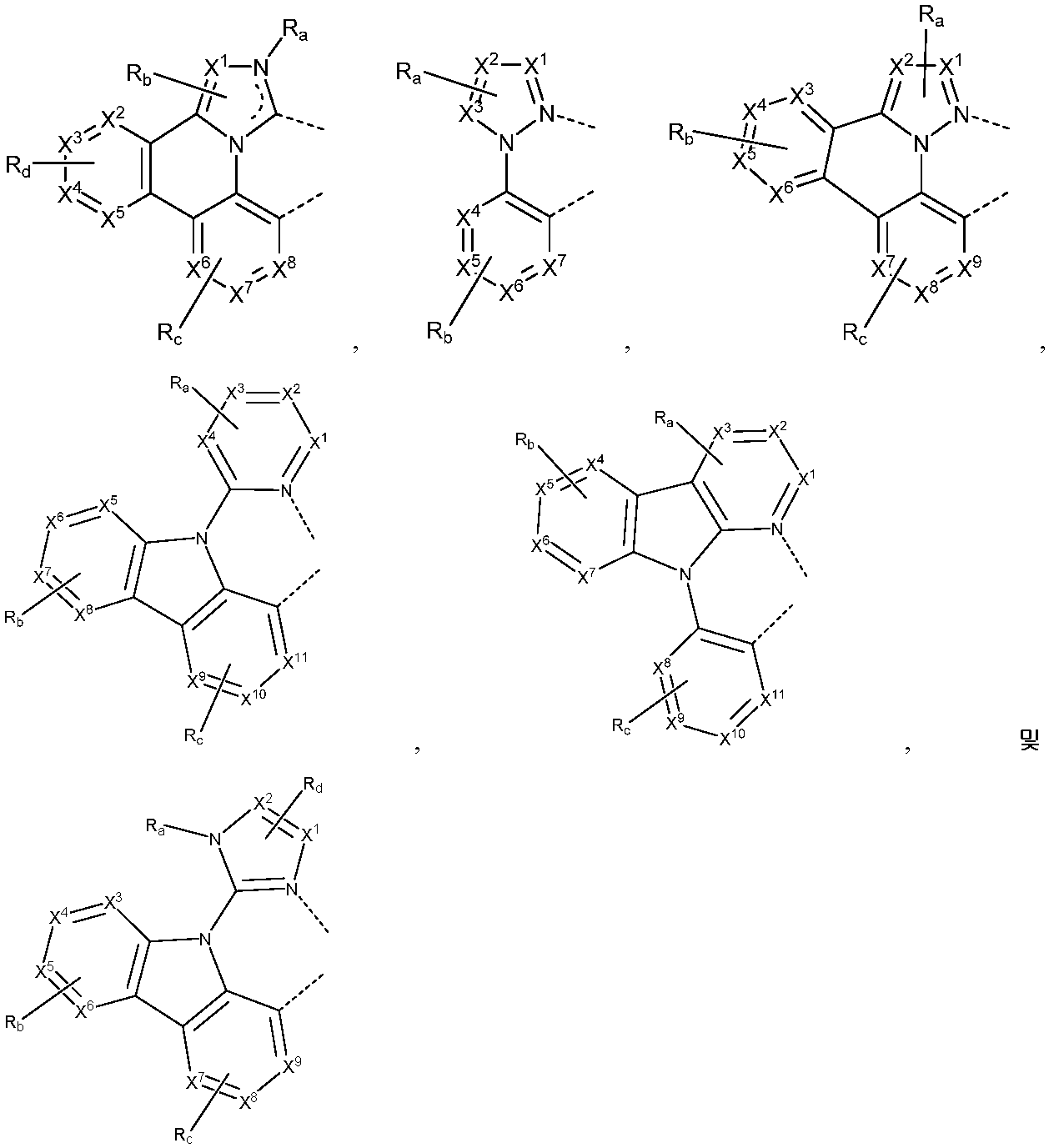
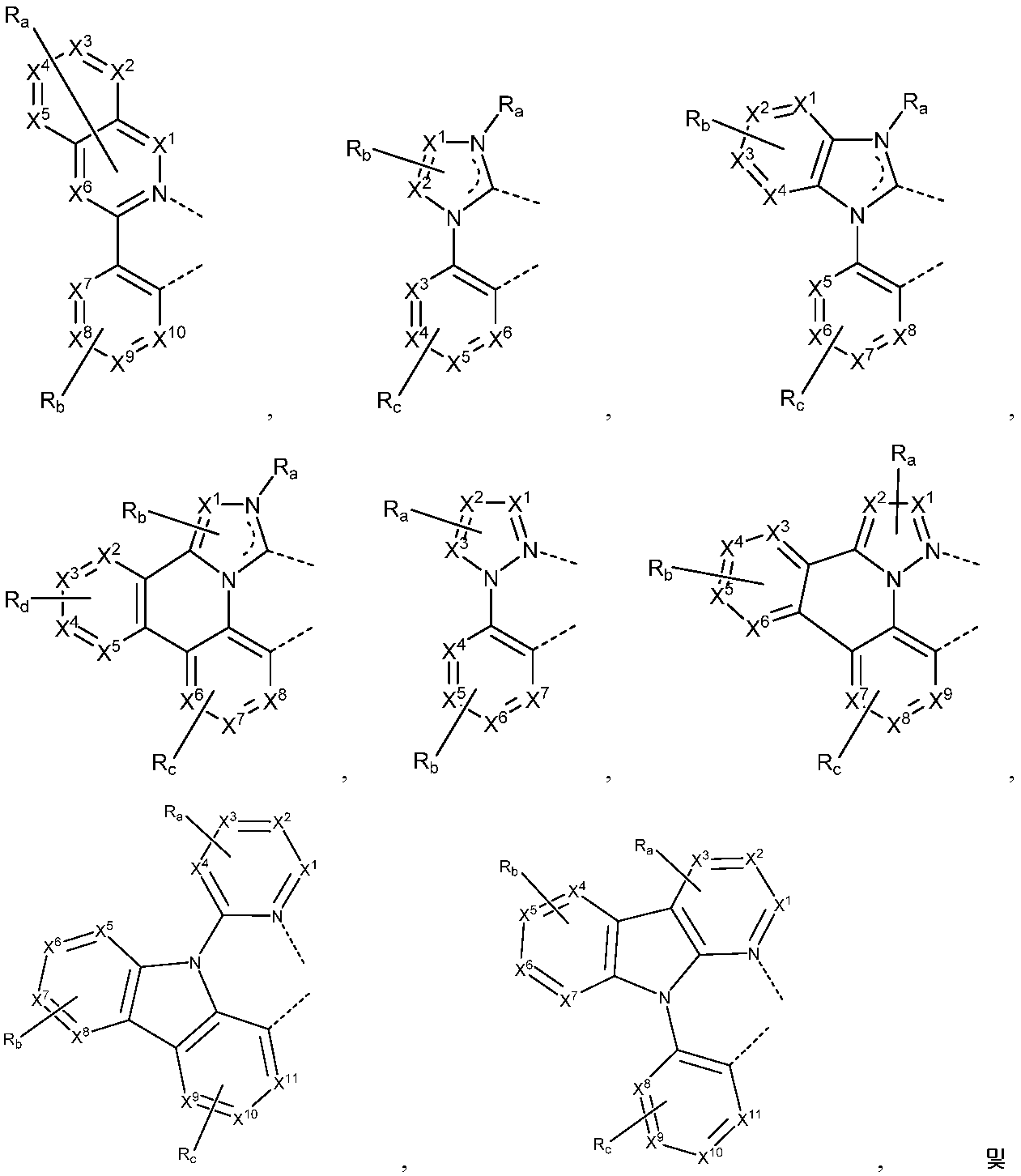
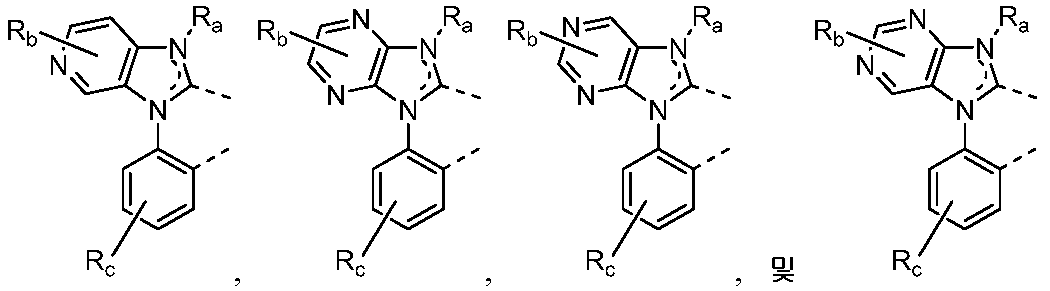
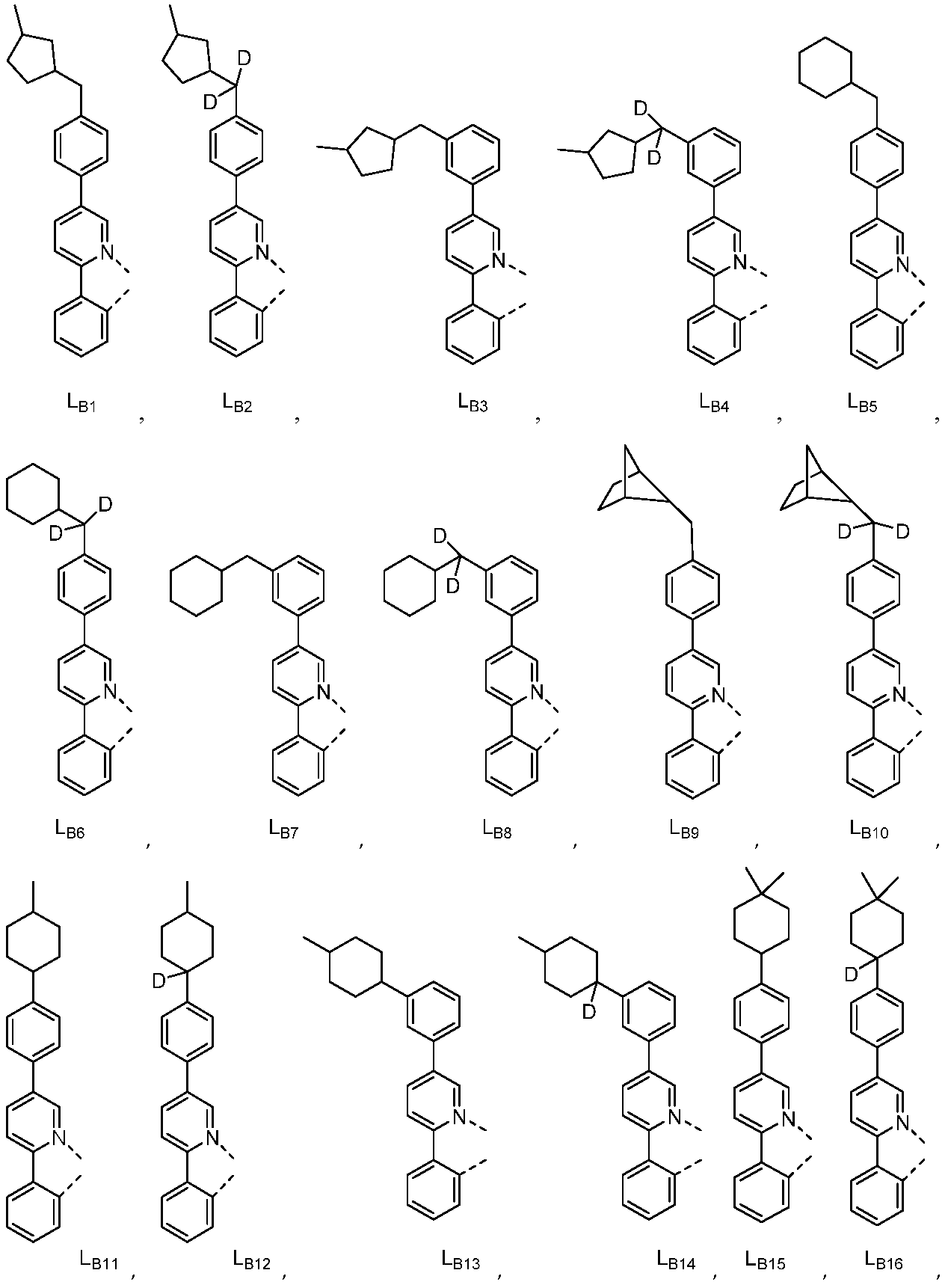
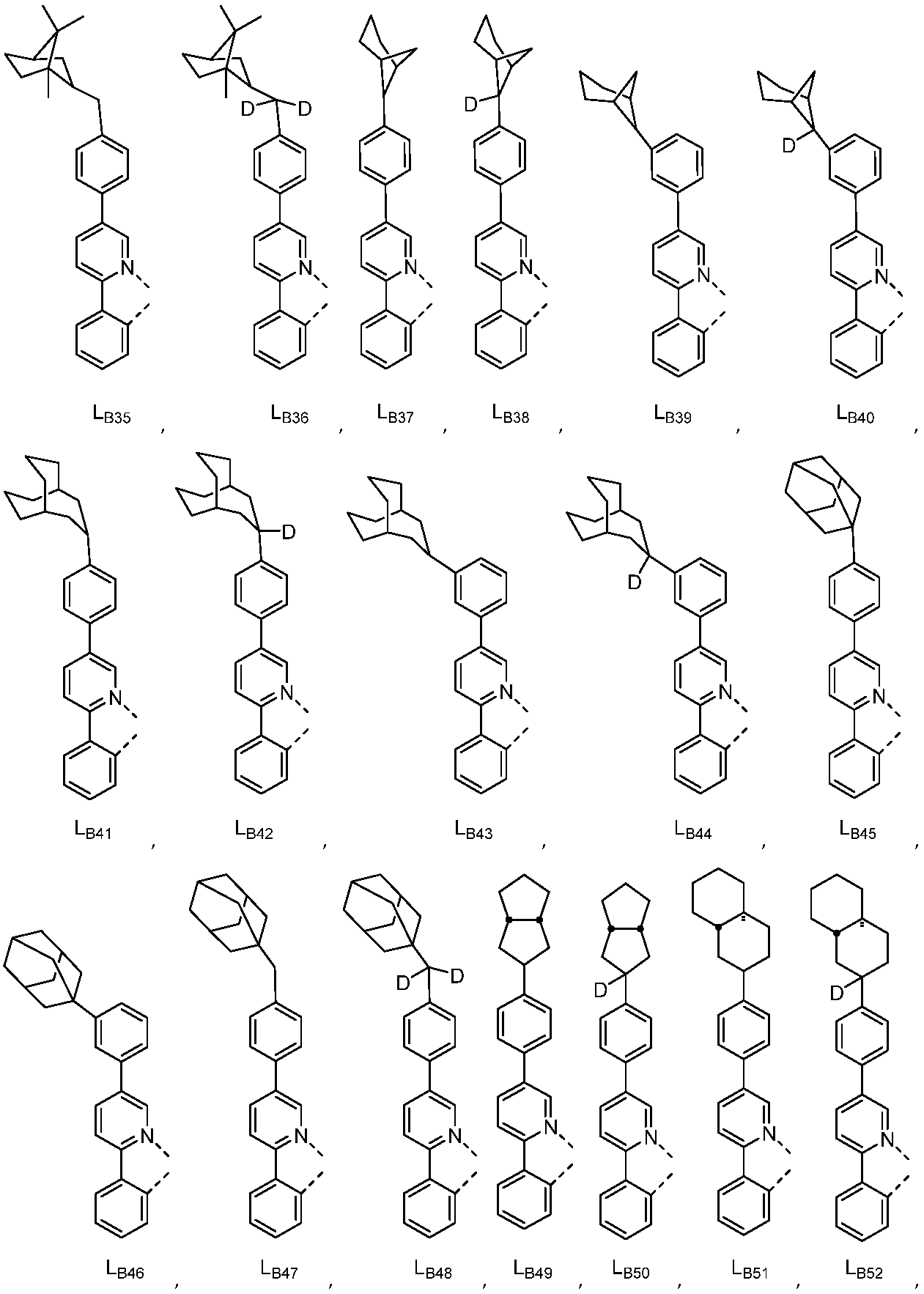
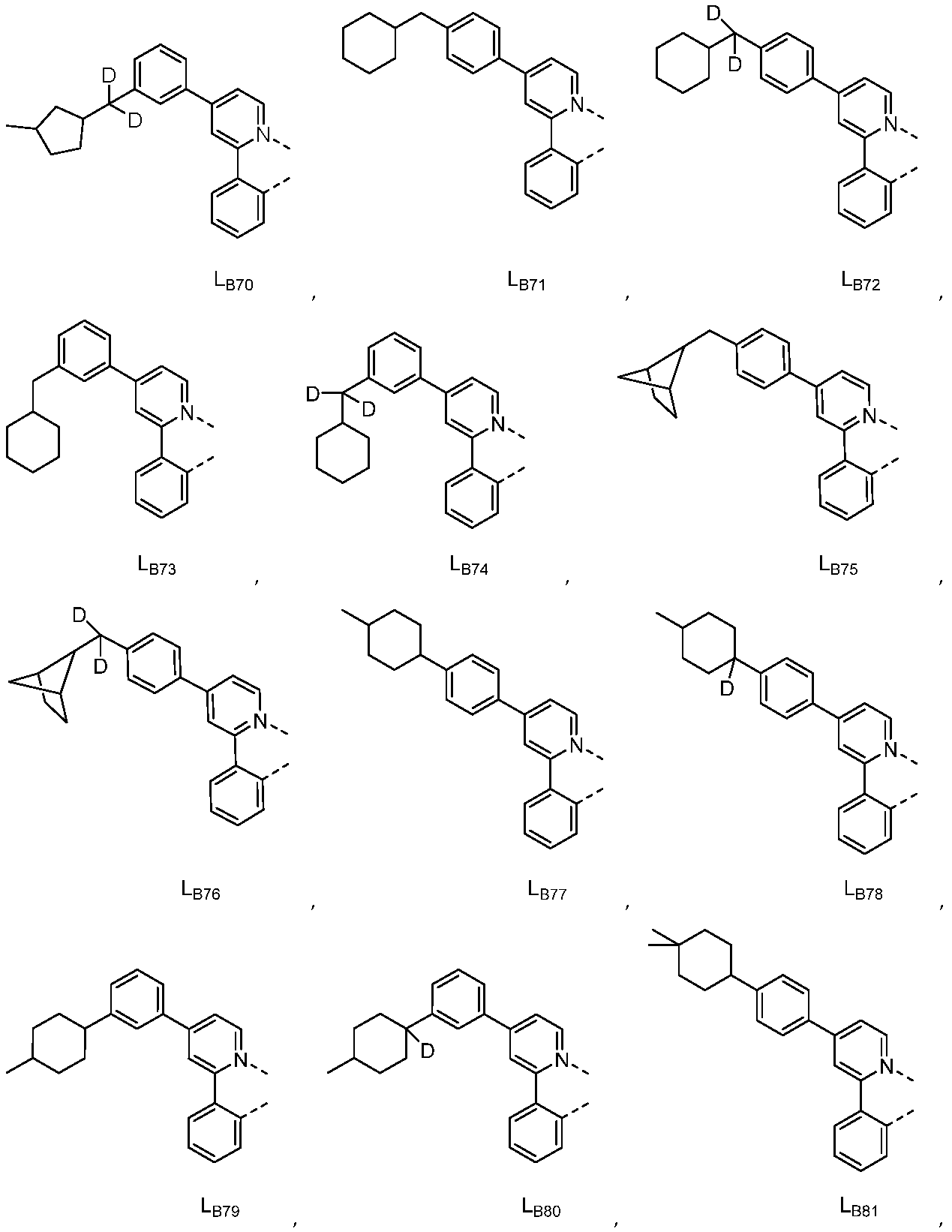
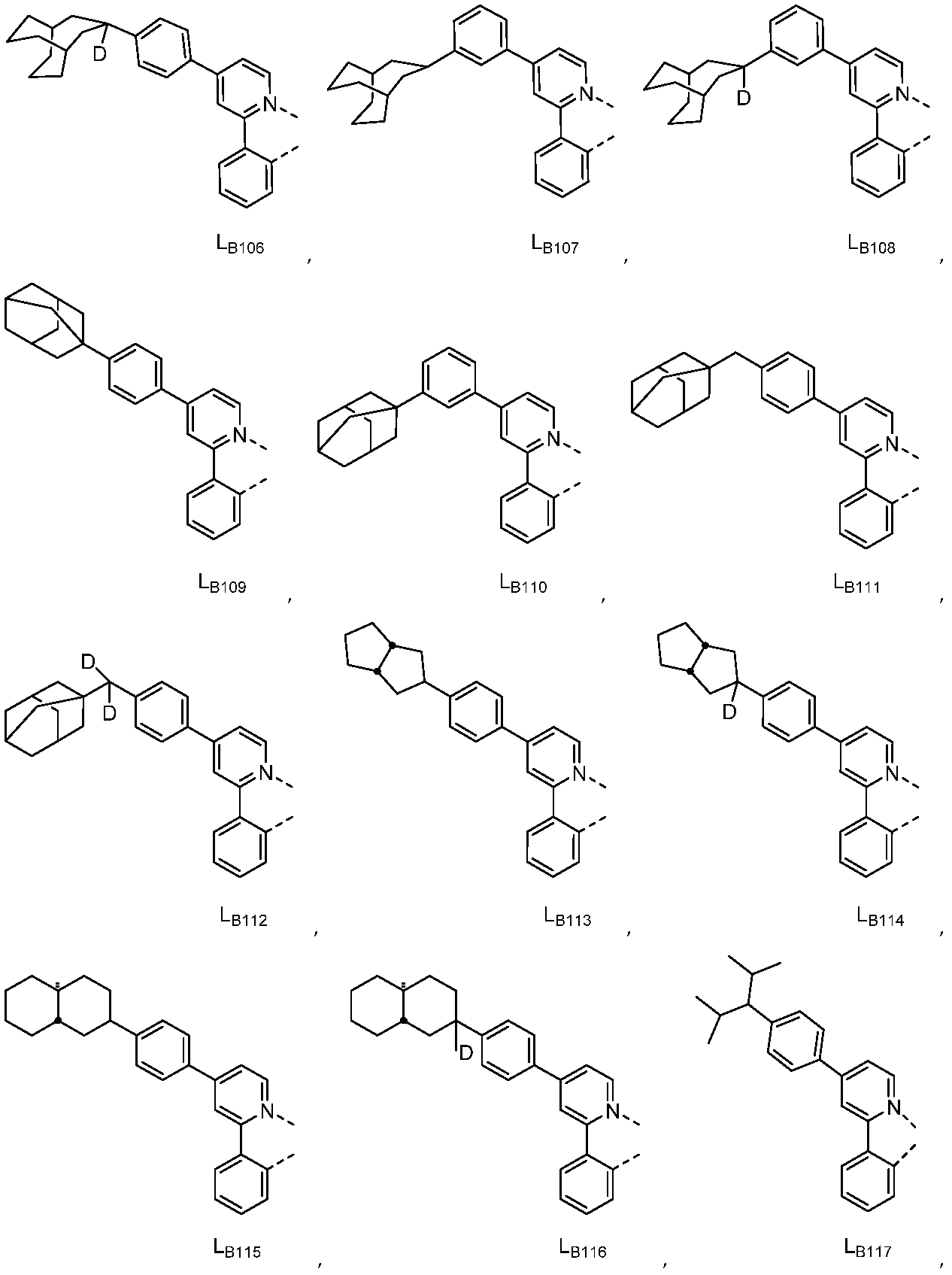
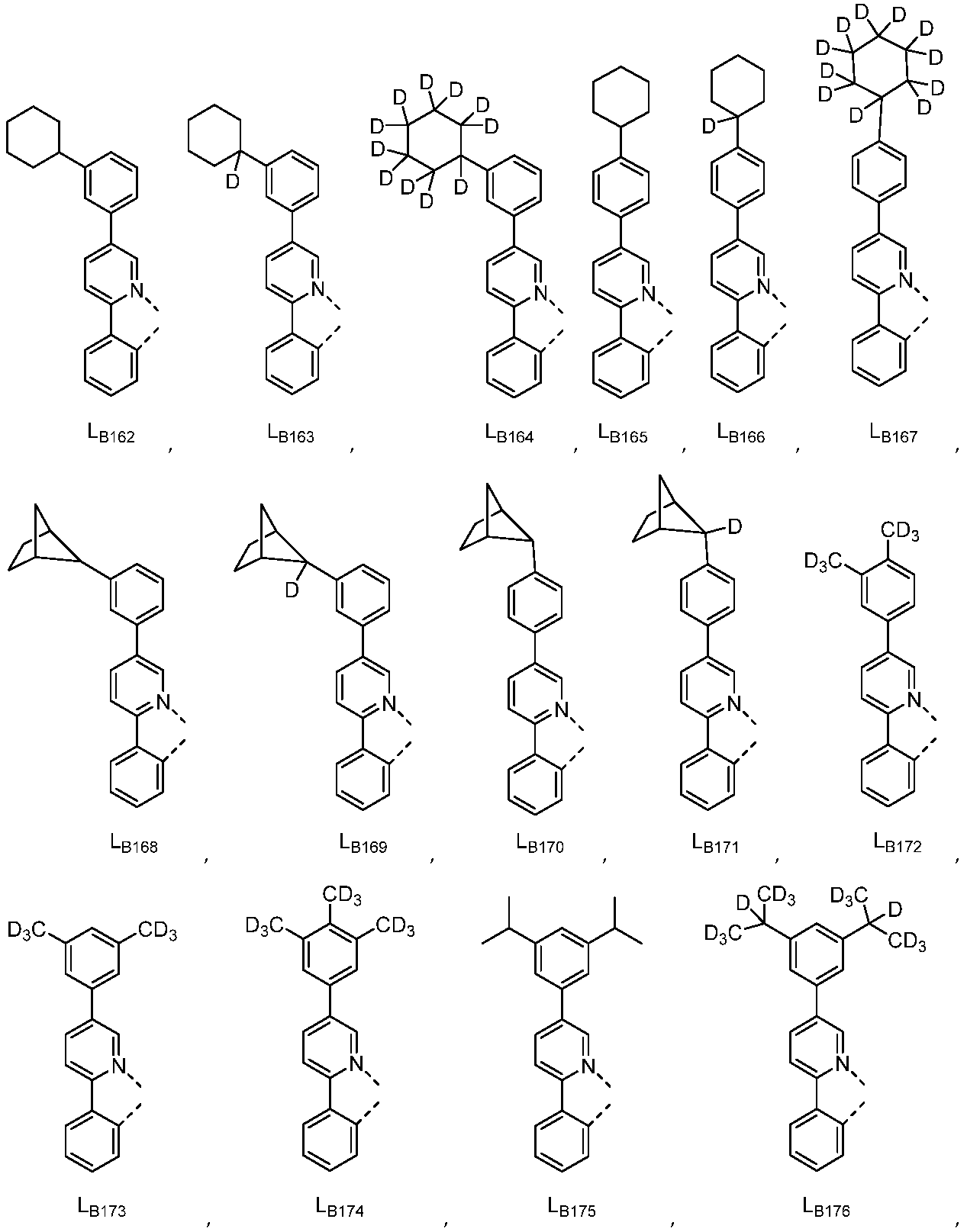
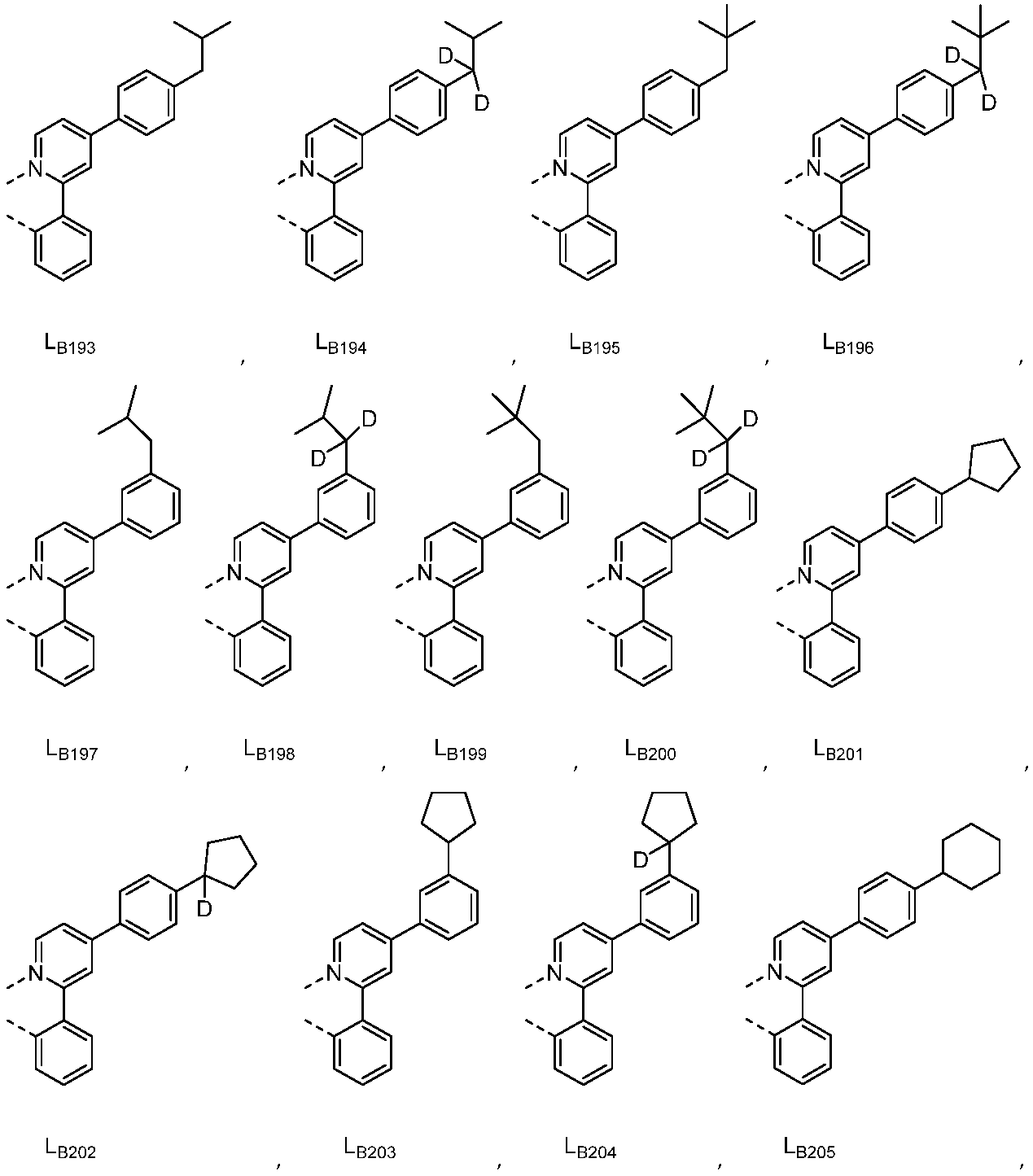
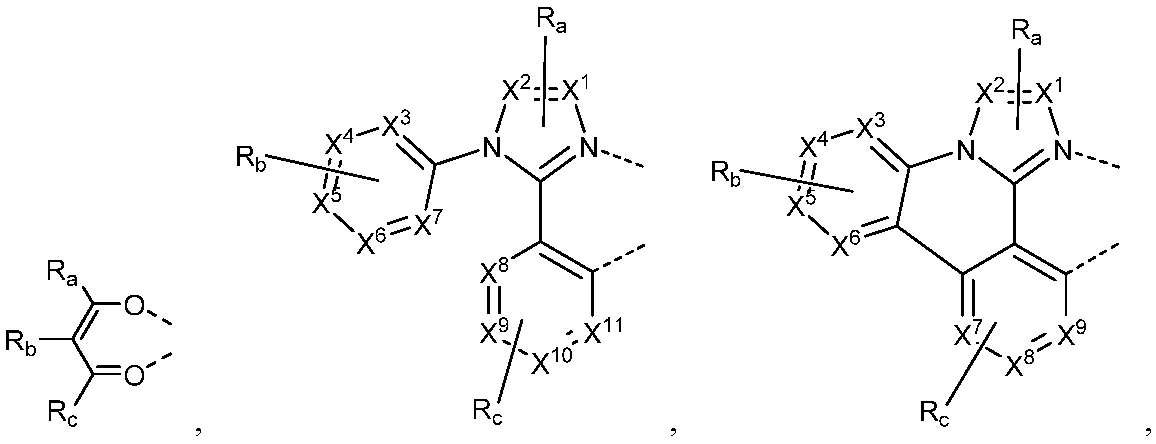
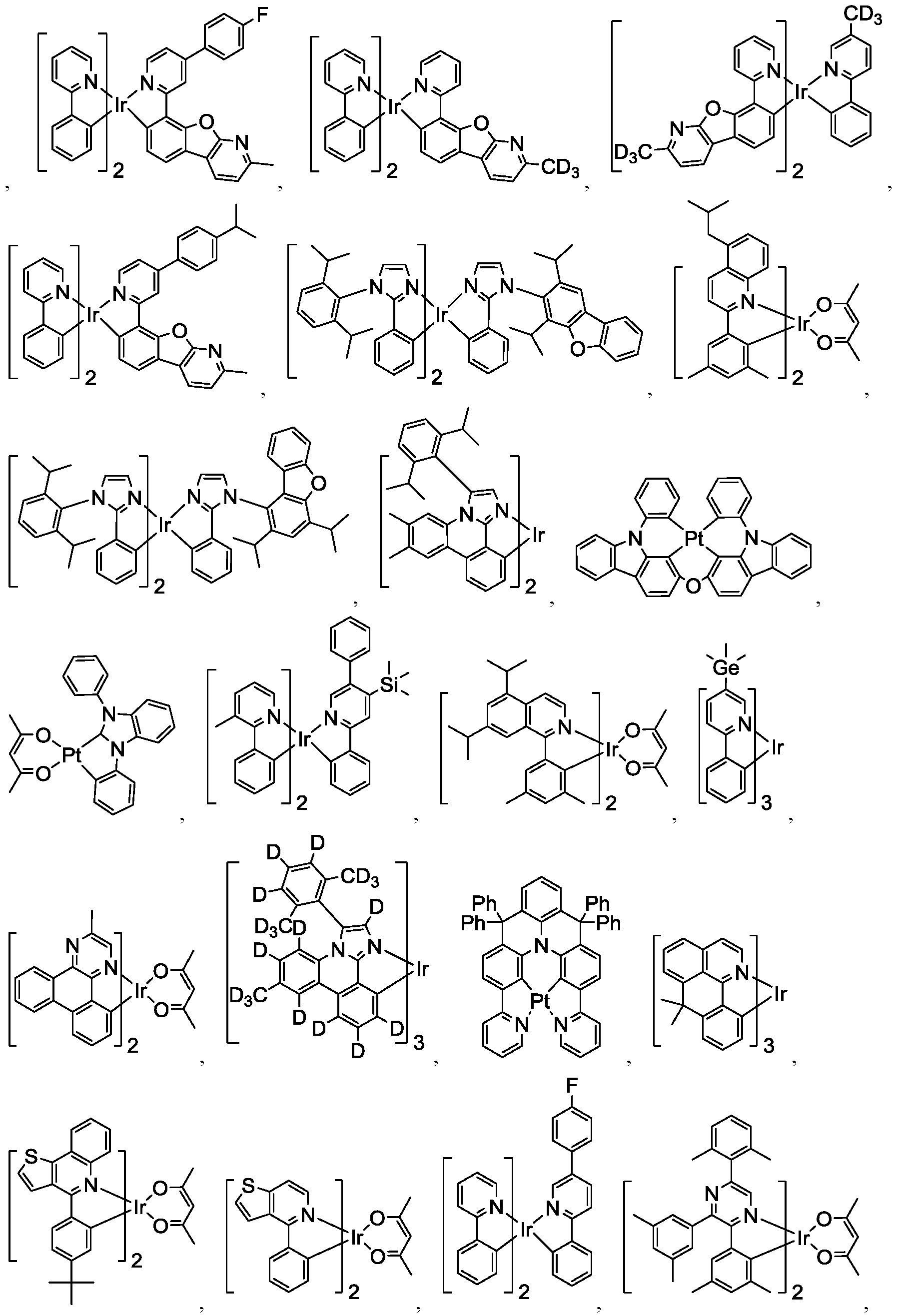
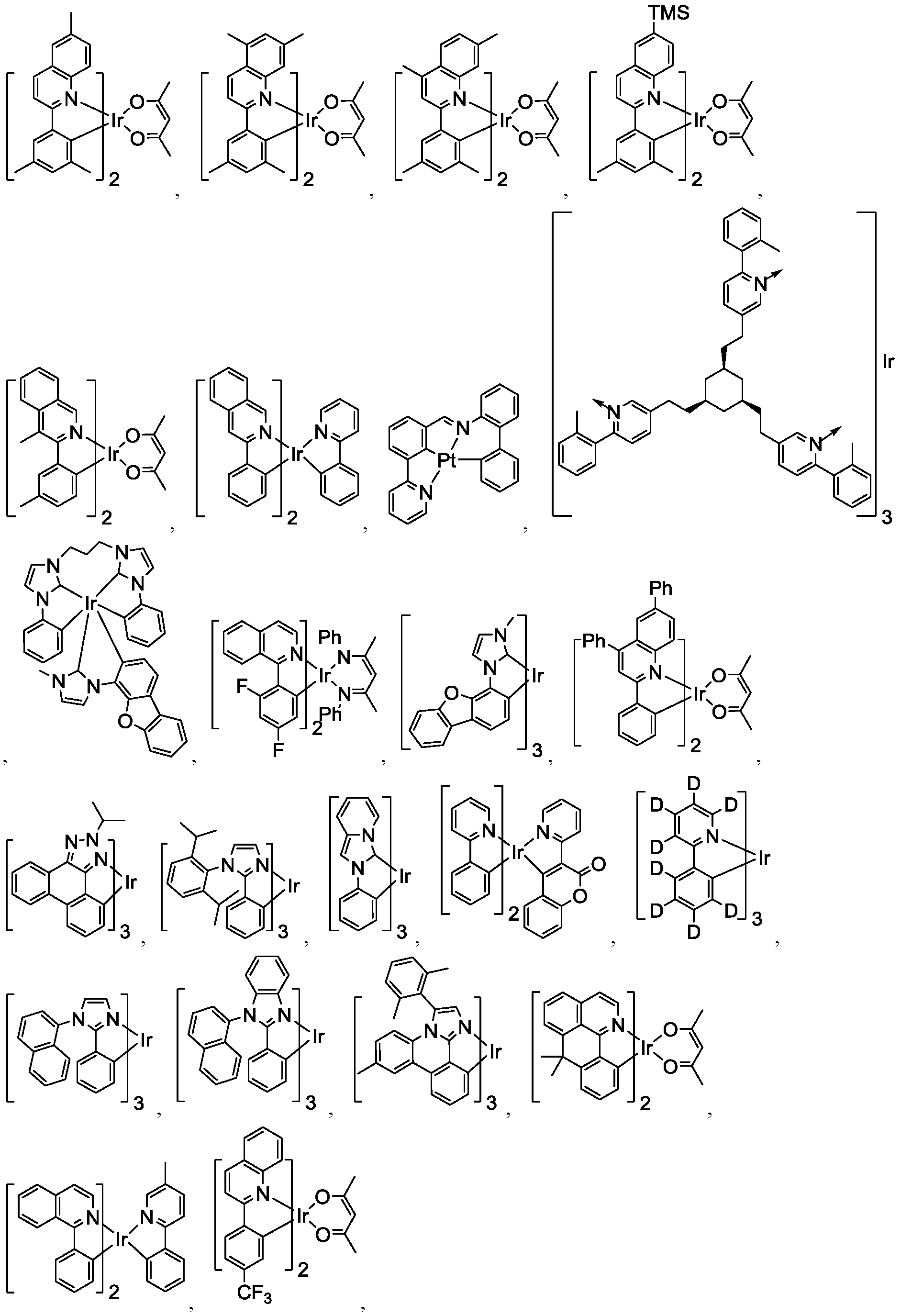
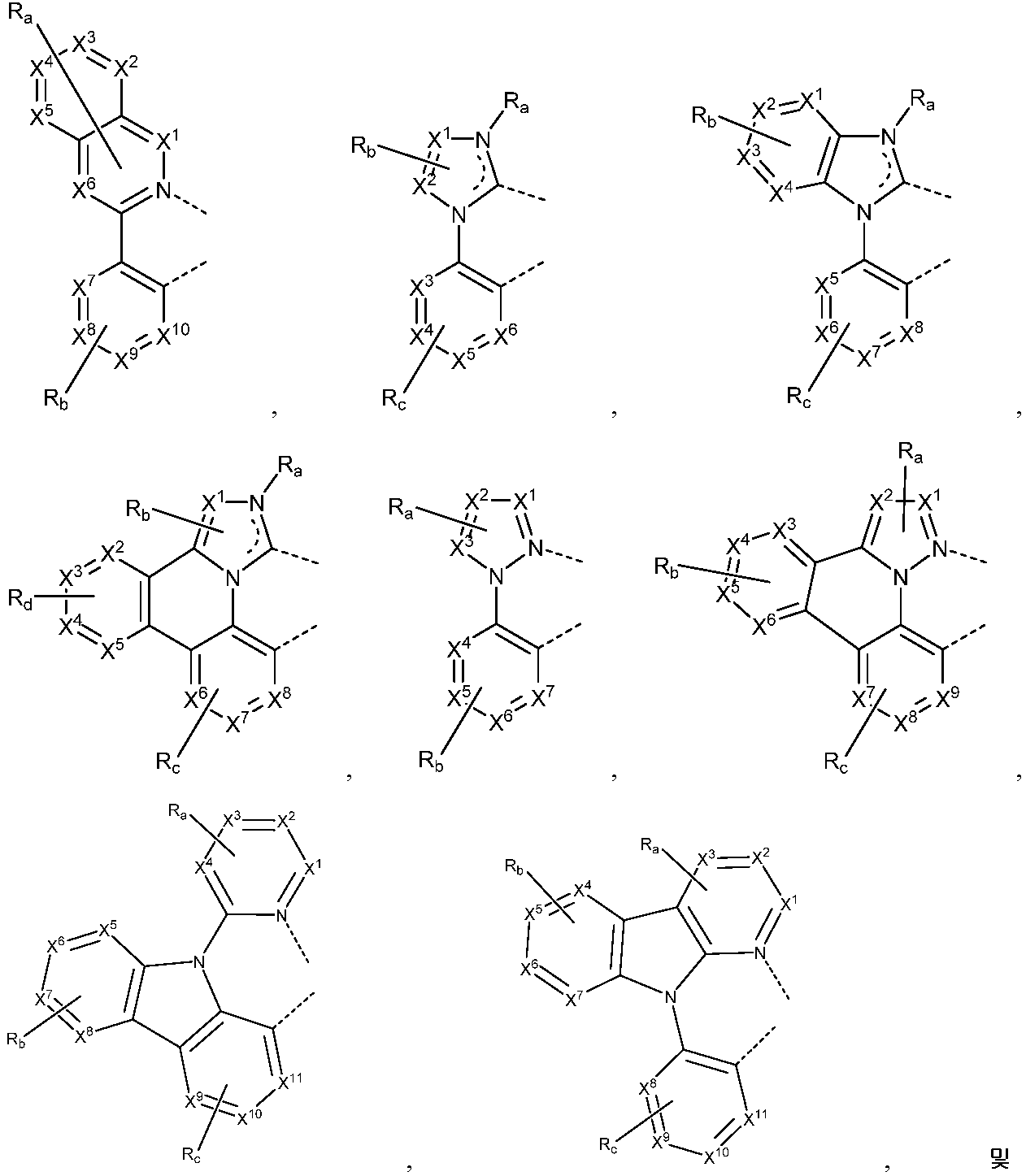
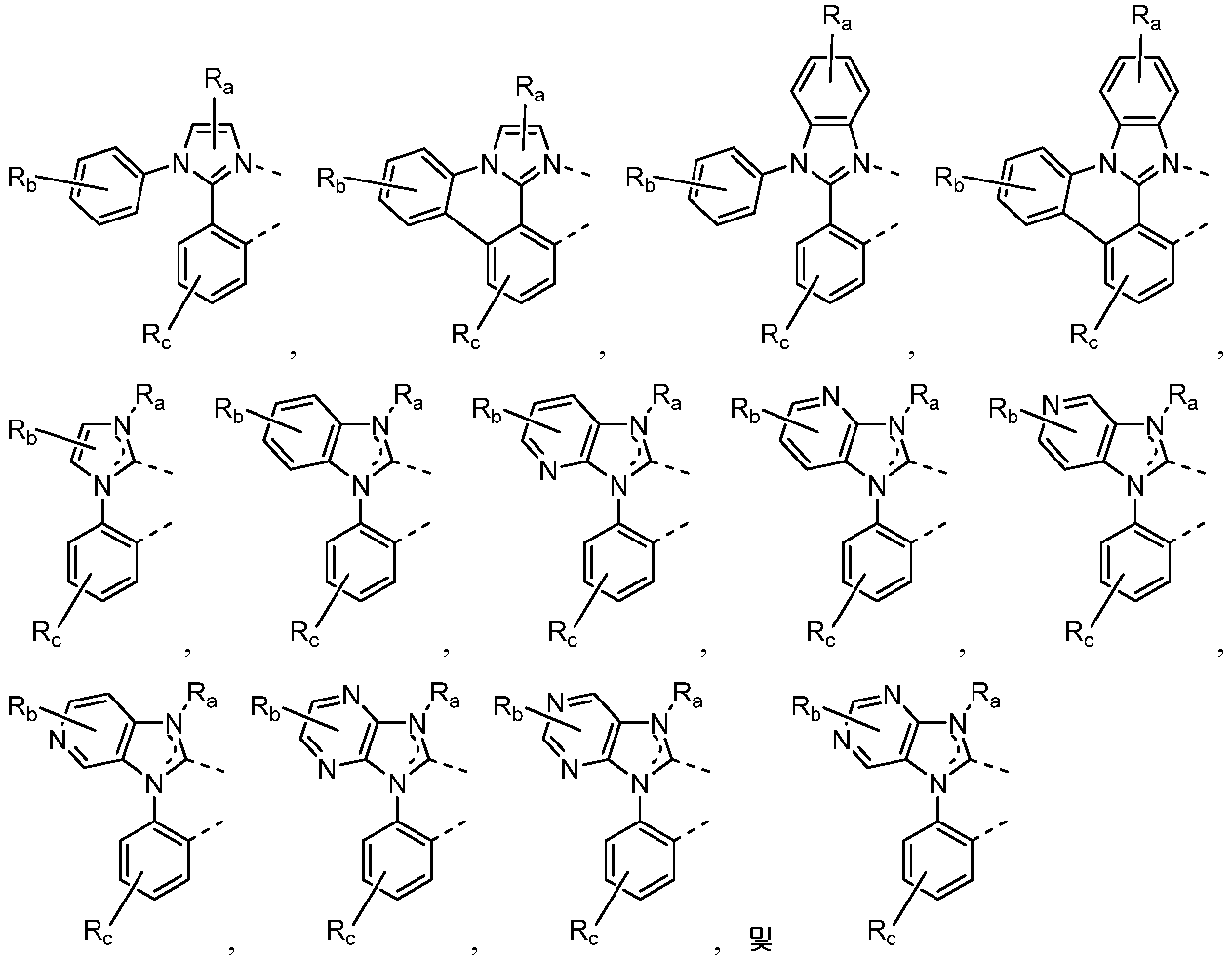
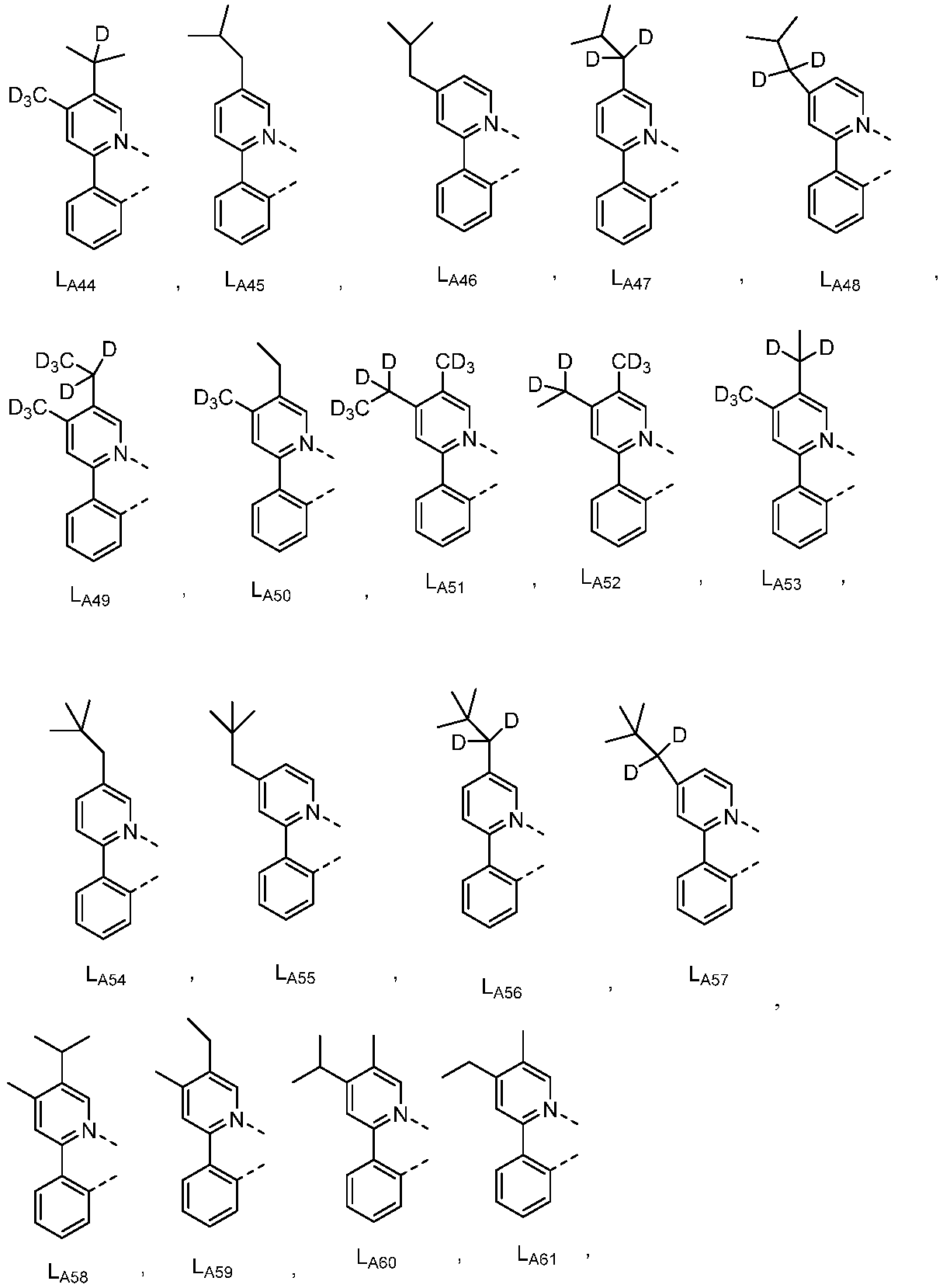
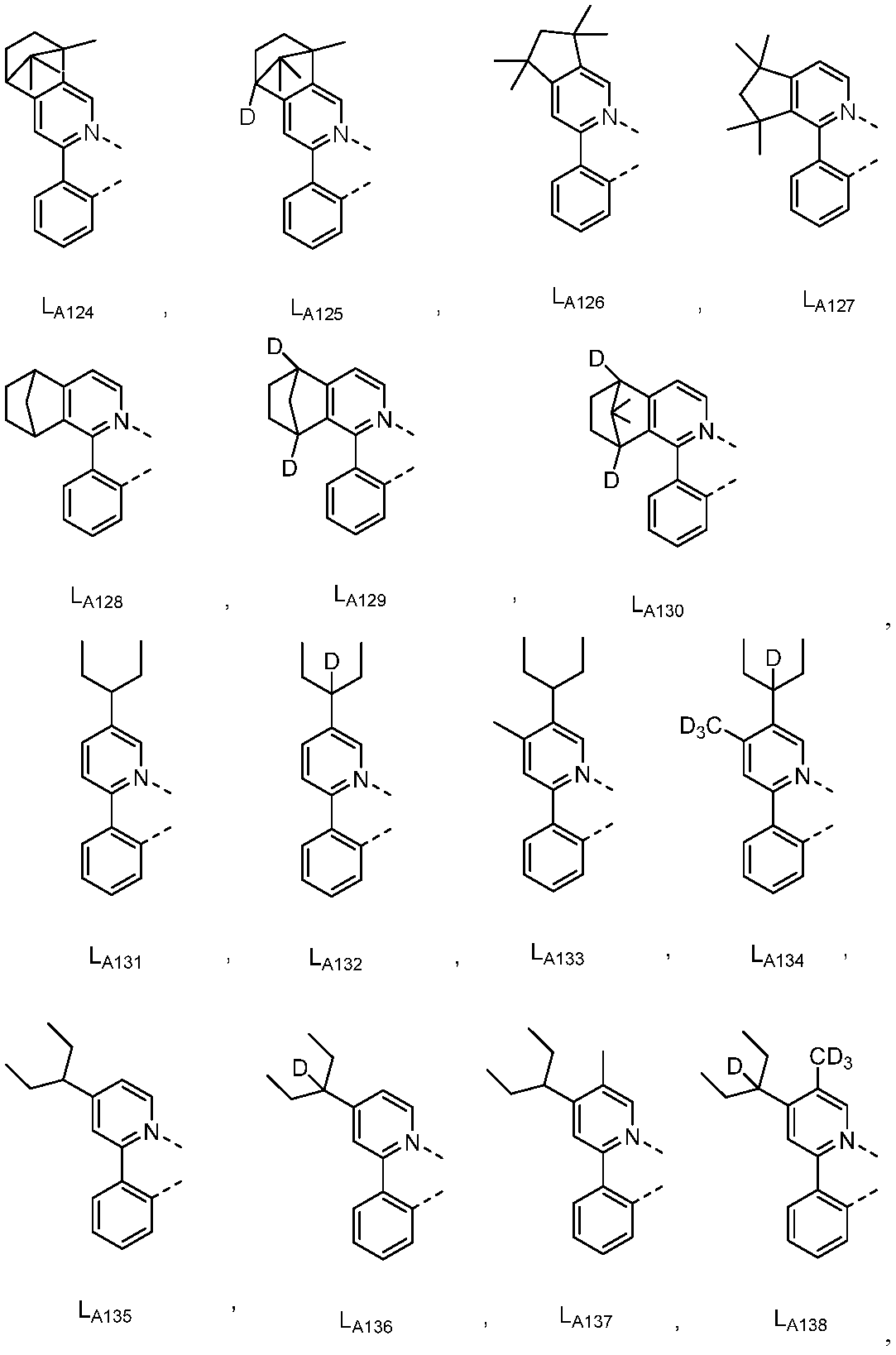
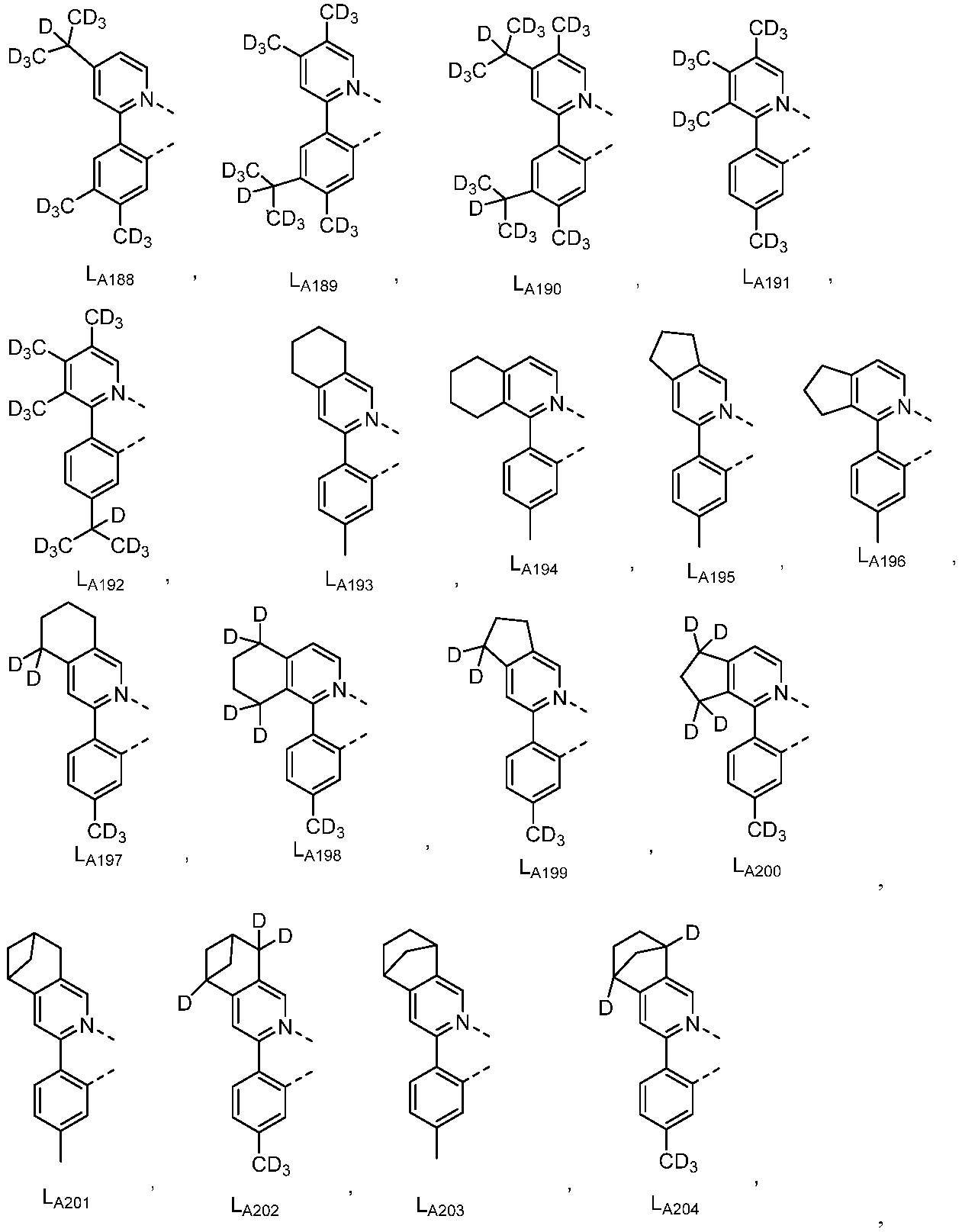
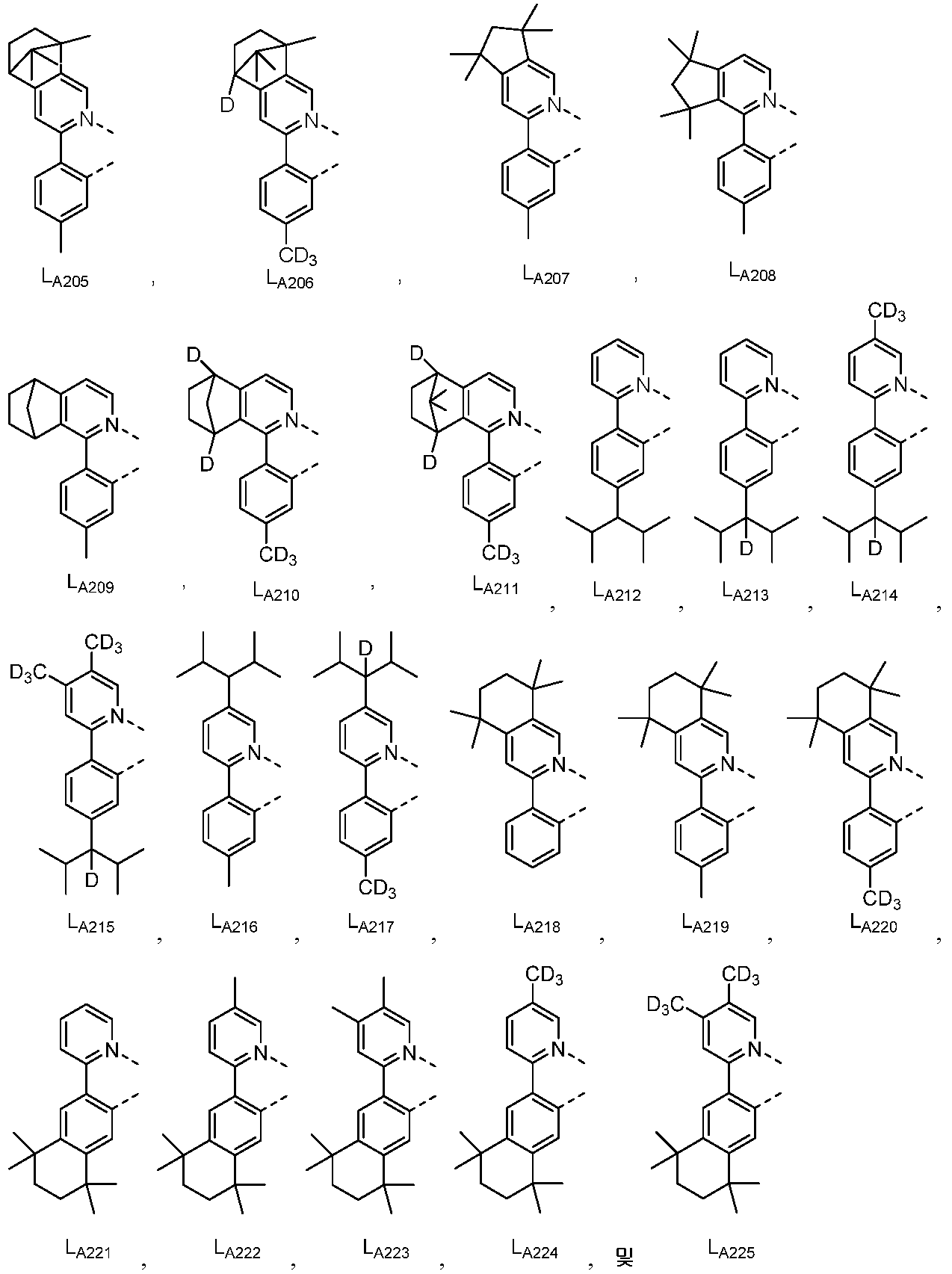
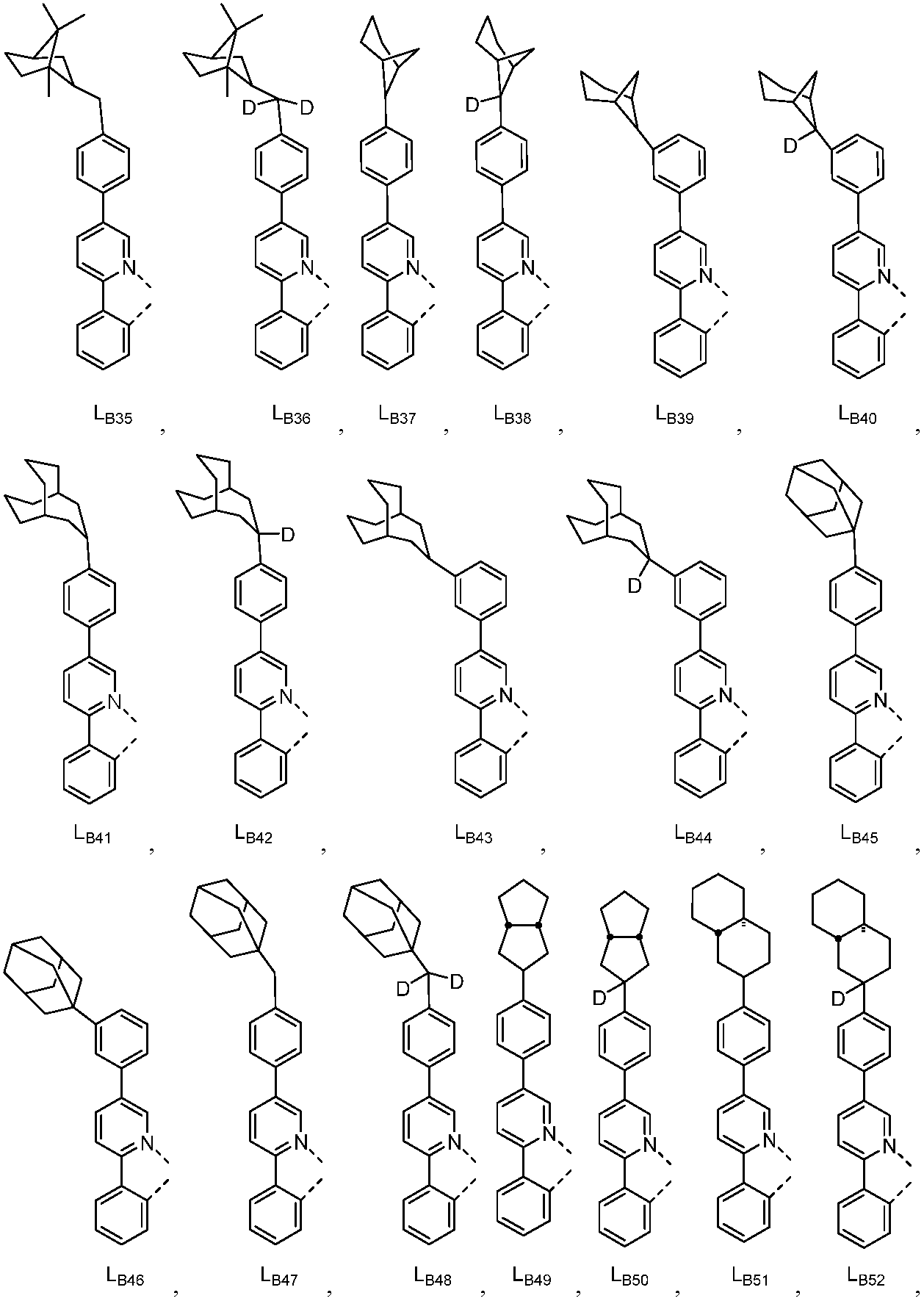
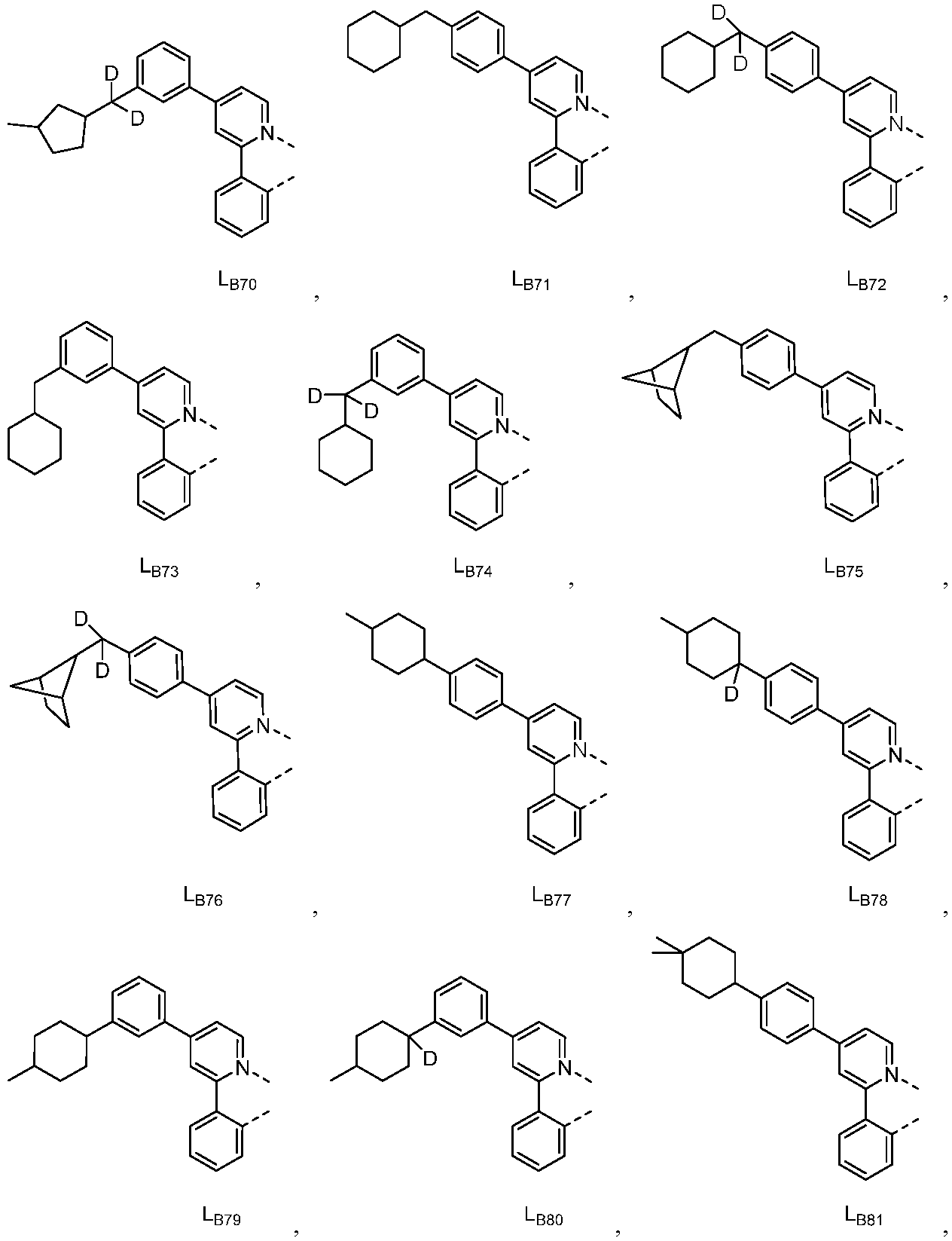
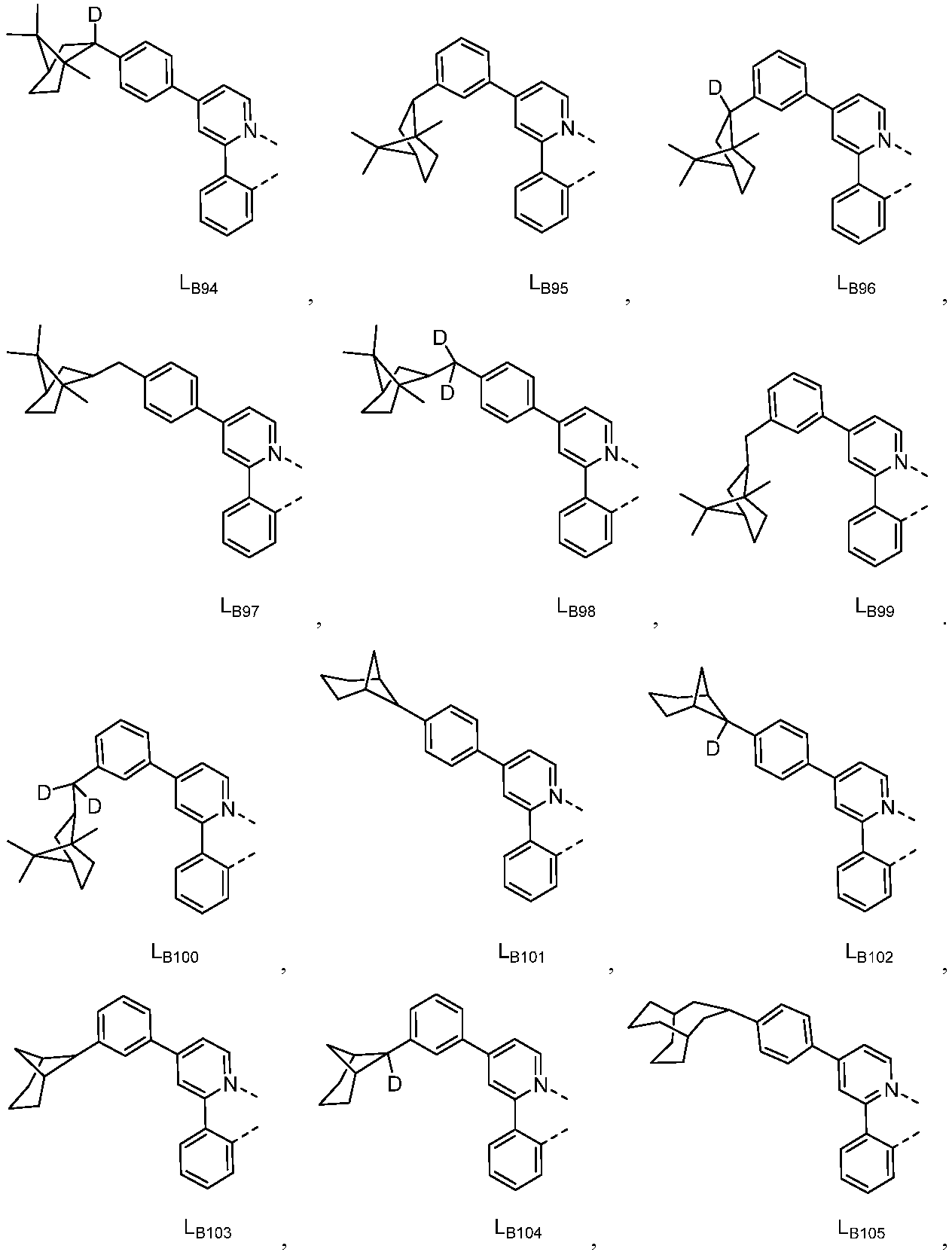
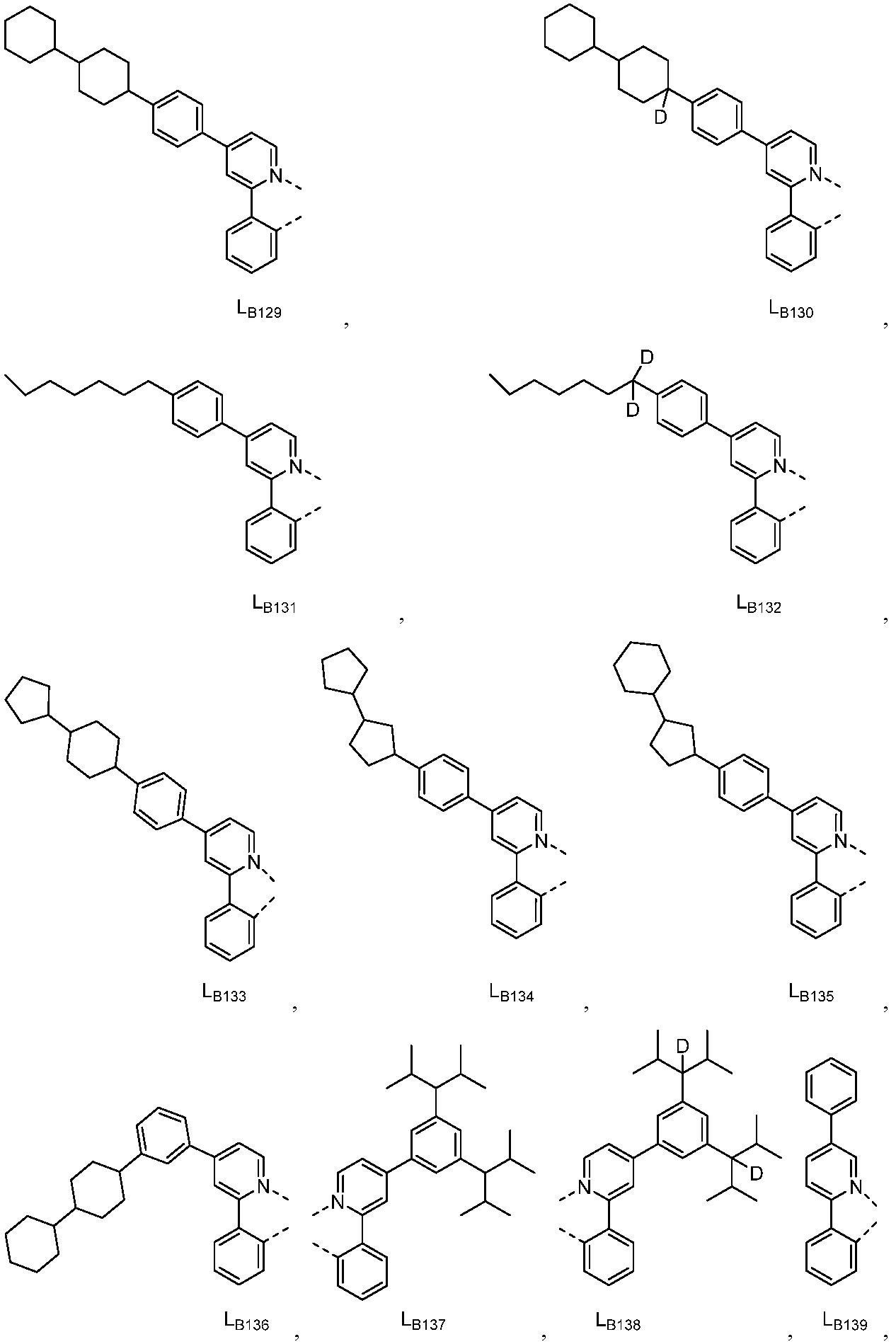
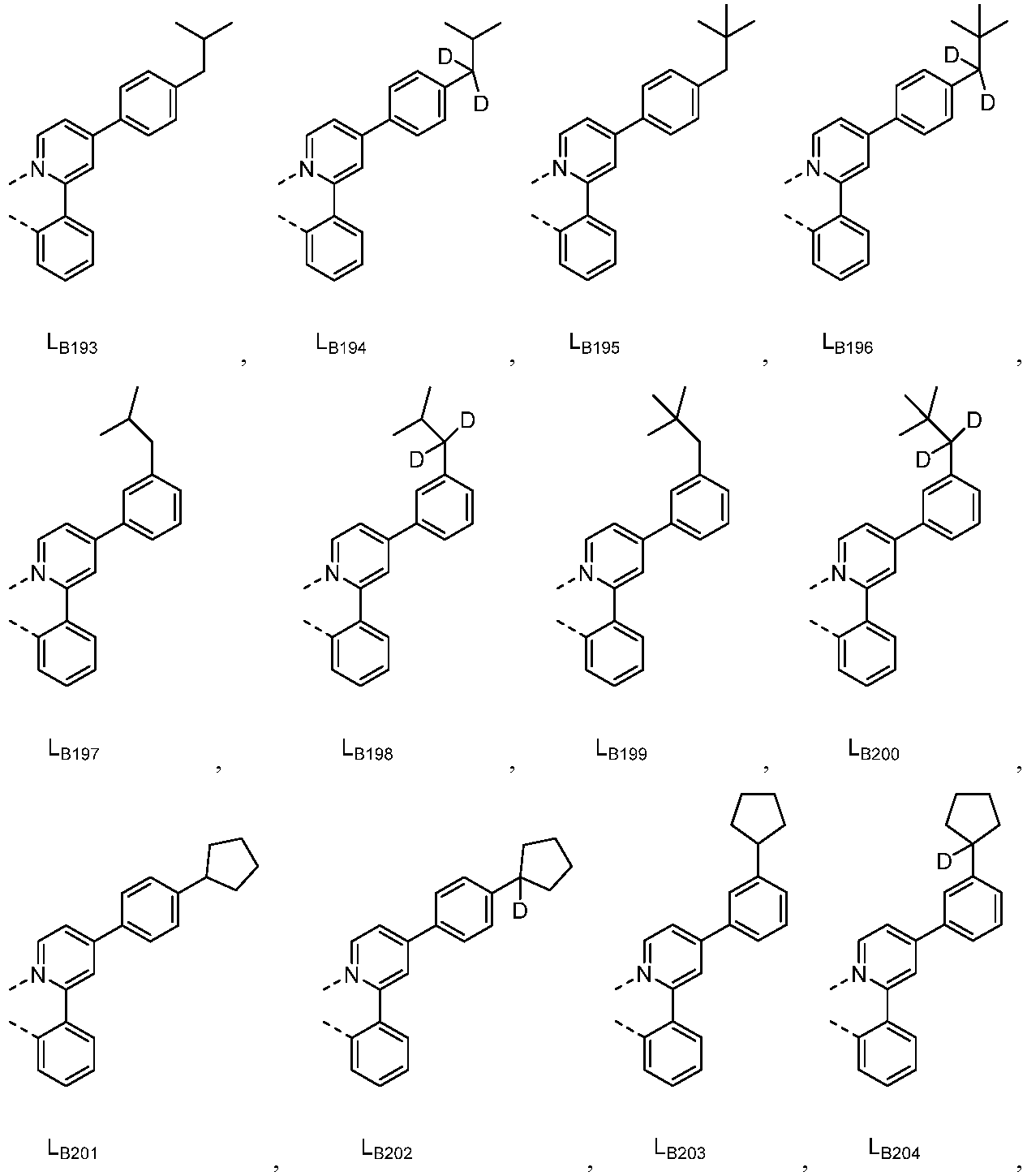
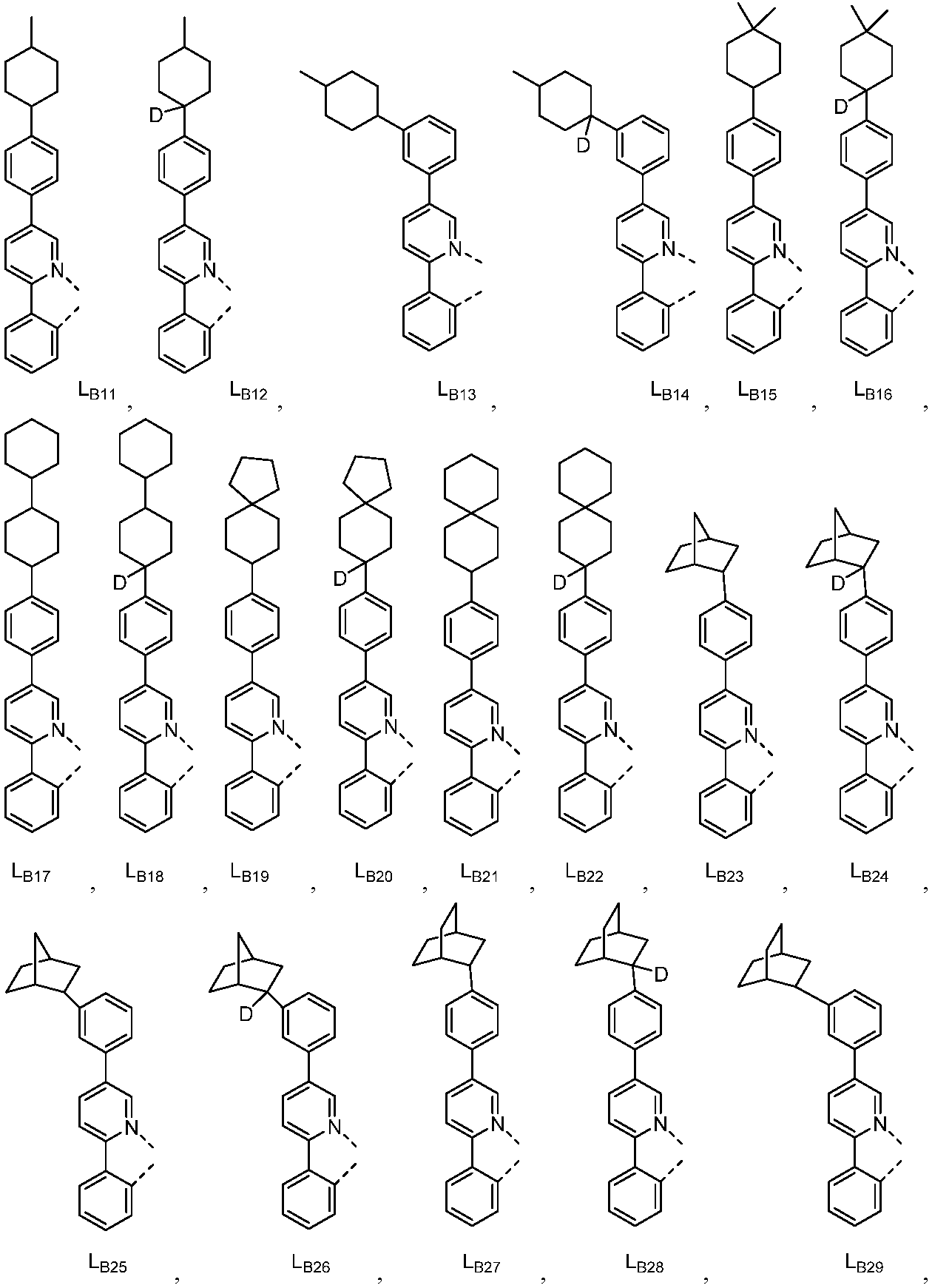
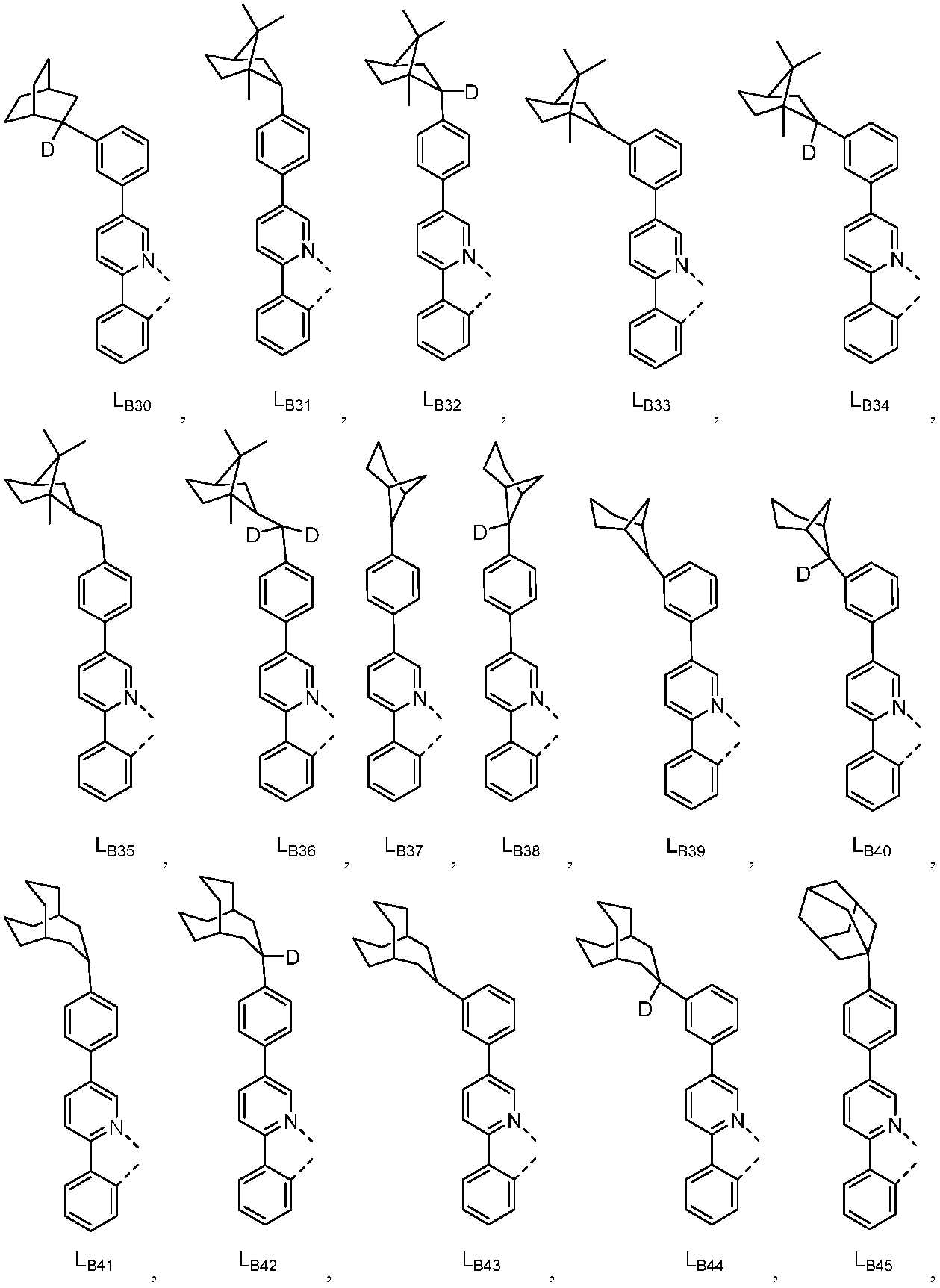
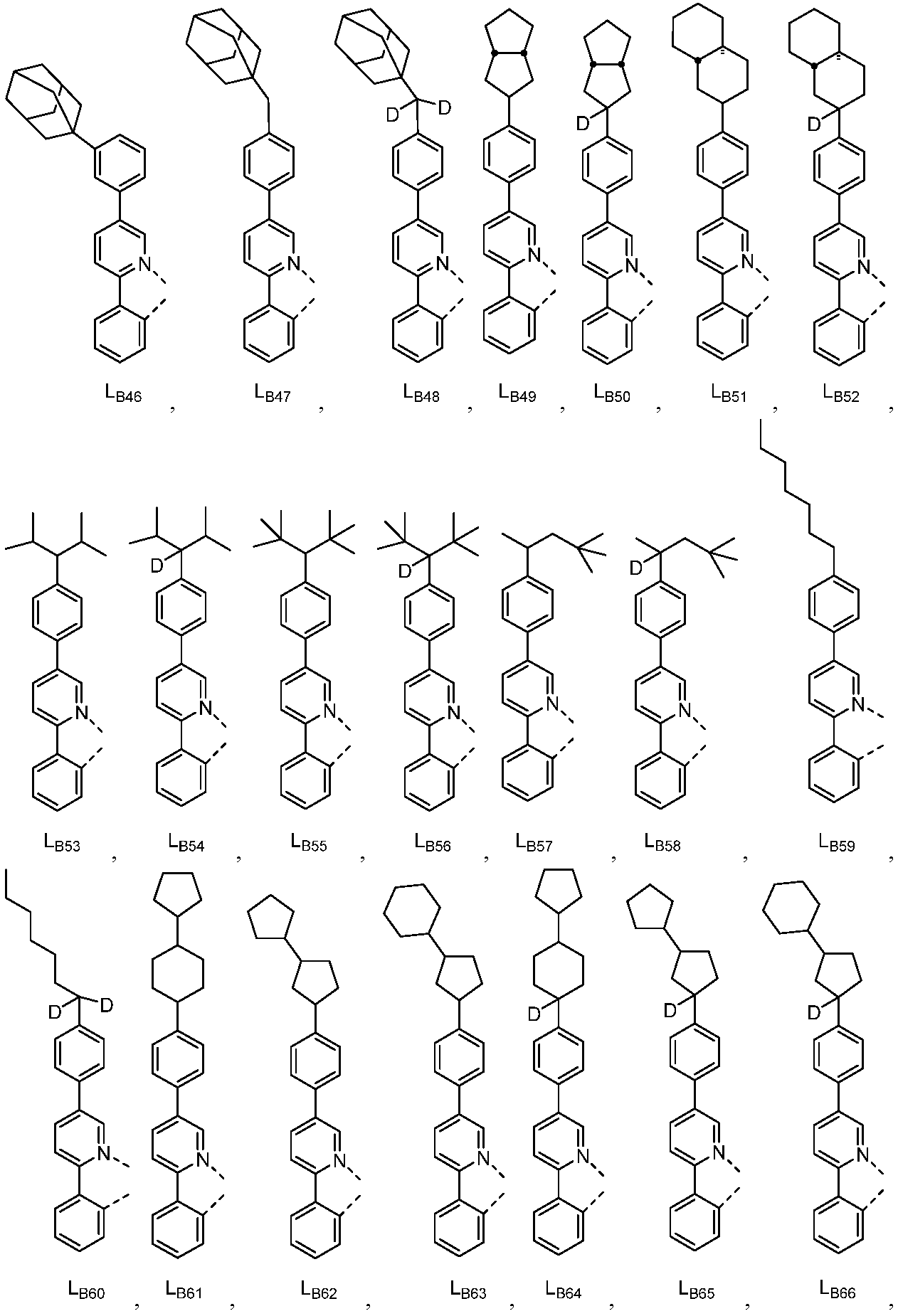
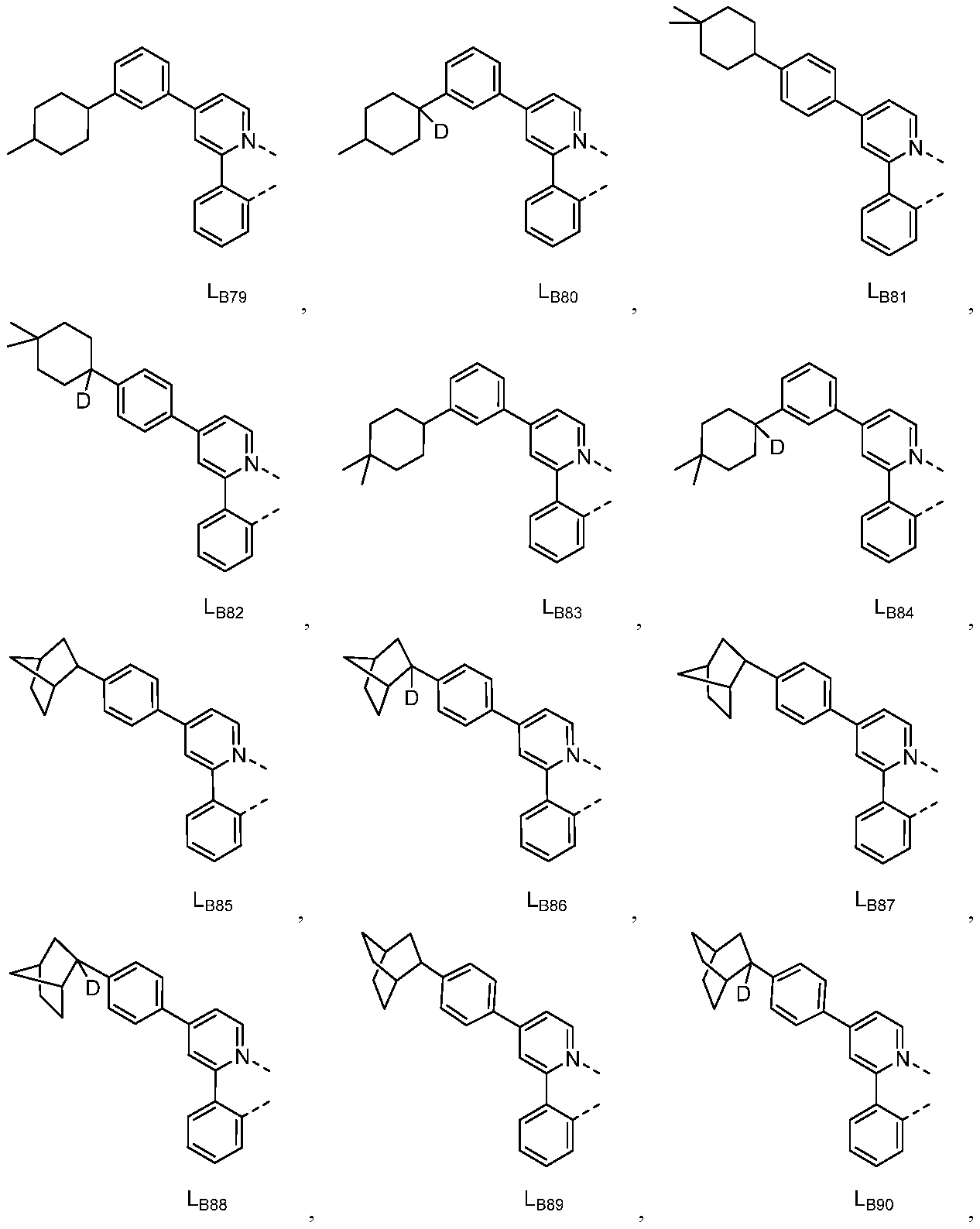
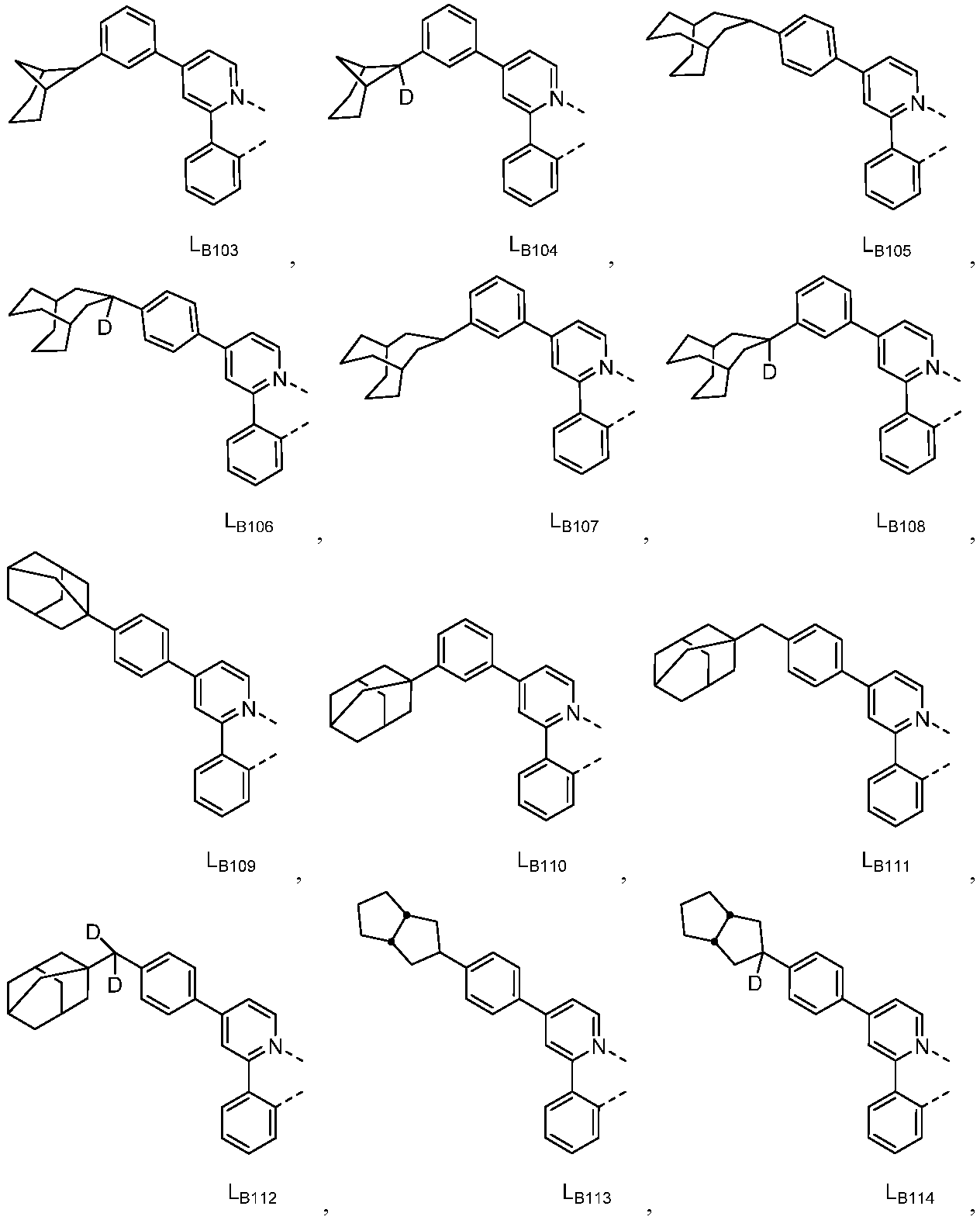
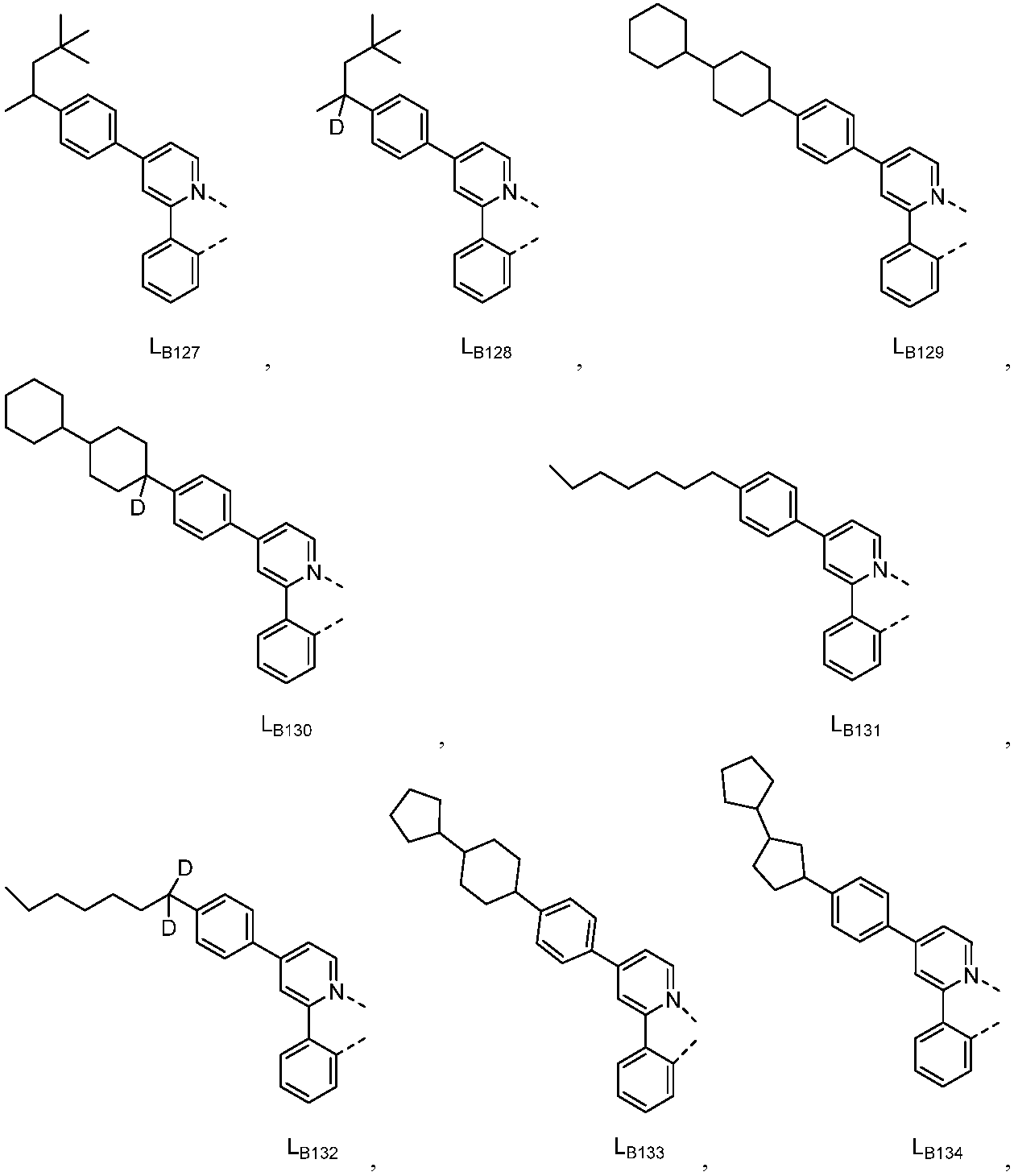
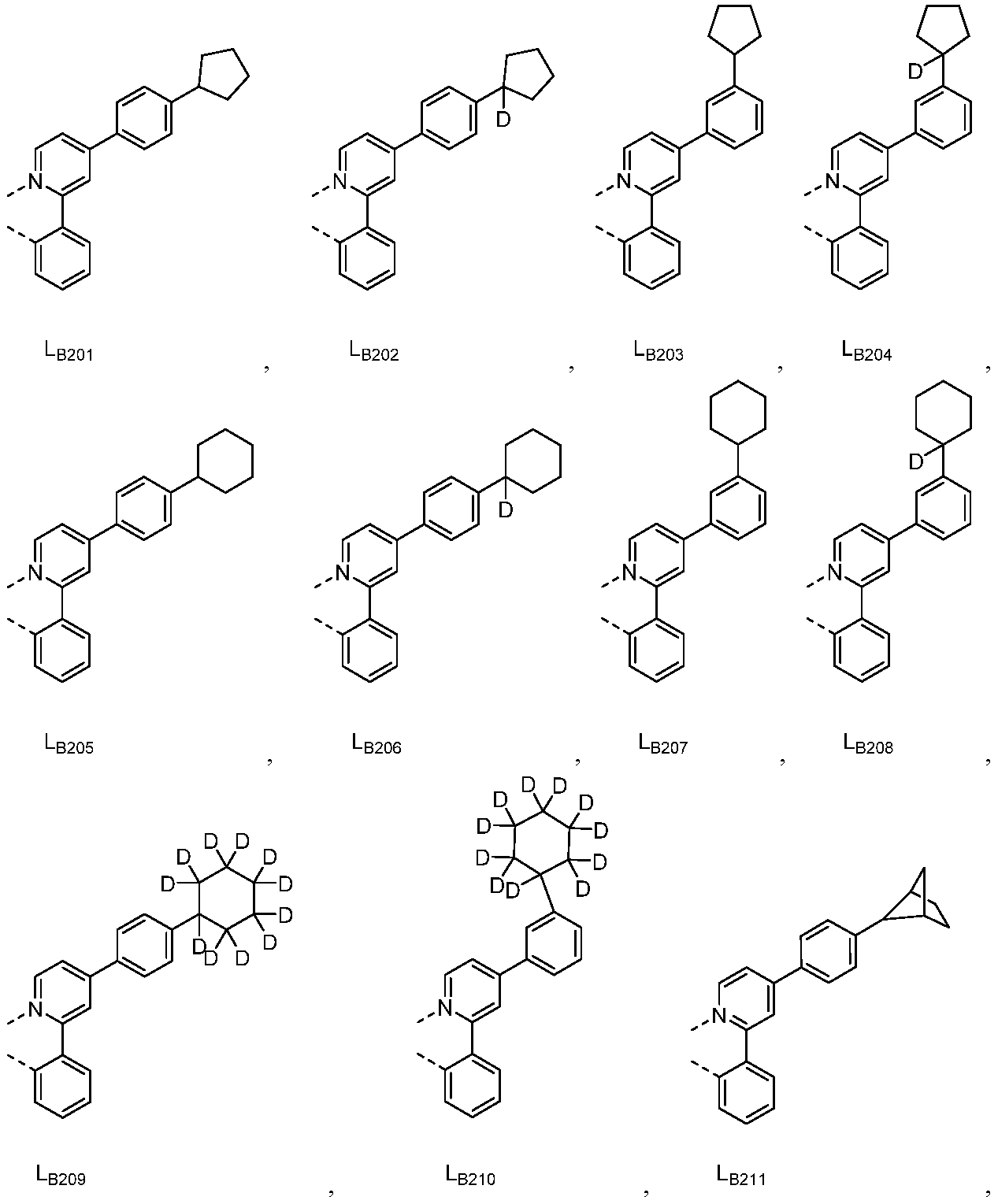
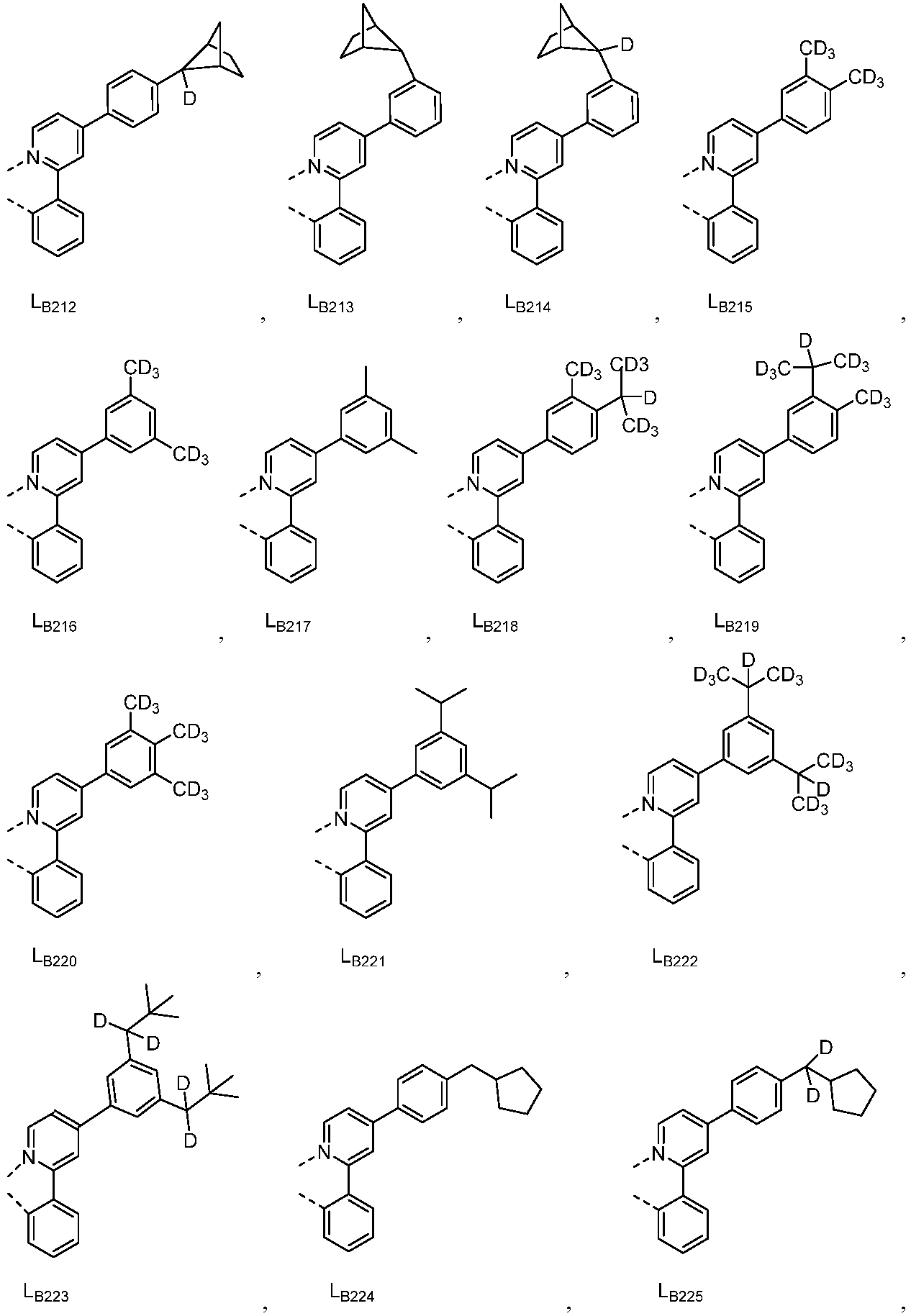
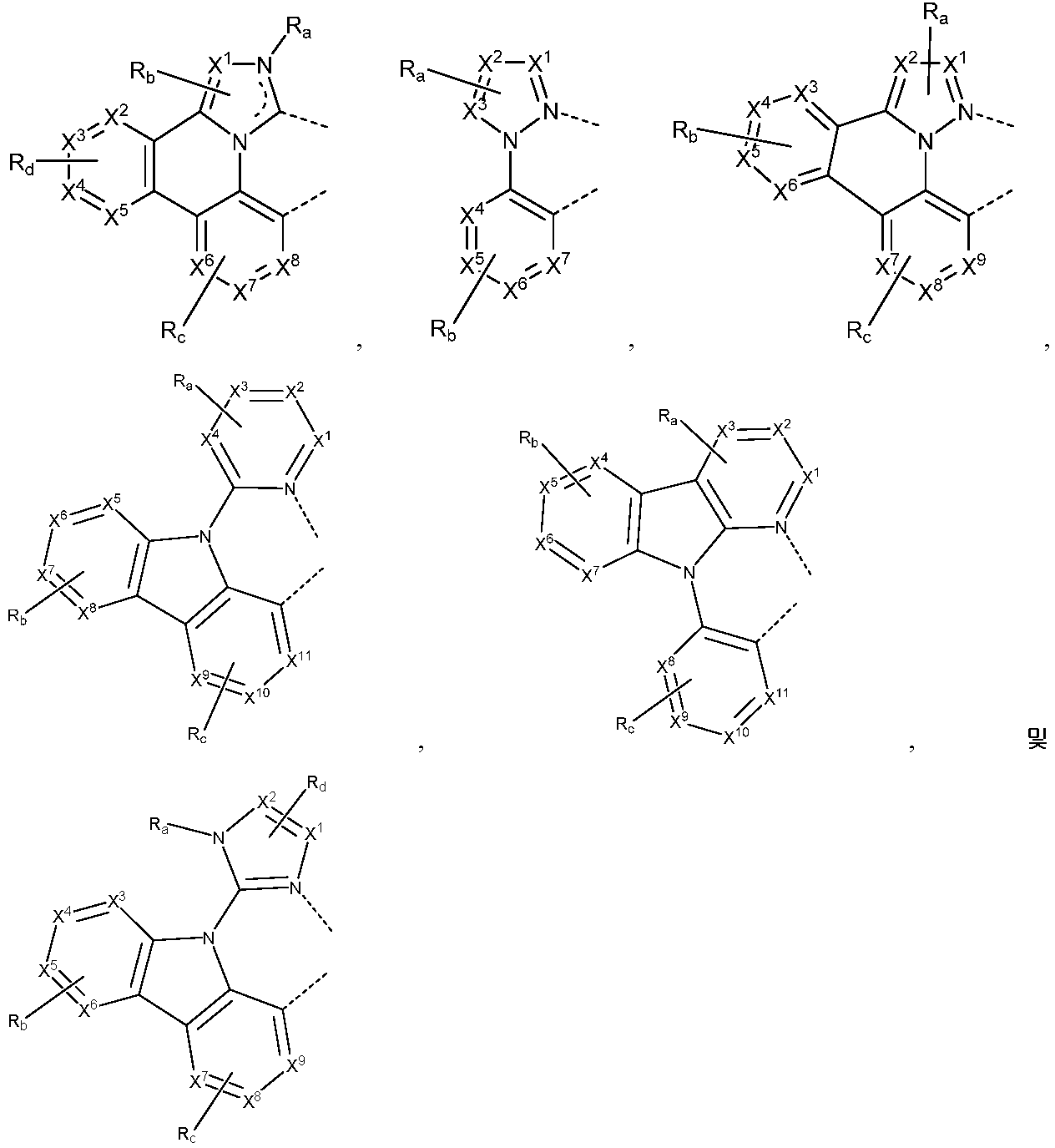
리간드 LA, LB, 및 LC는 각각 독립적으로 하기로 이루어지는 군에서 선택되고:
각각의 X1 내지 X13은 독립적으로 탄소 및 질소로 이루어지는 군에서 선택되며;
X는 BR', NR', PR', O, S, Se, C=O, S=O, SO2, CR'R", SiR'R", 및 GeR'R"로 이루어지는 군에서 선택되고;
R' 및 R"은 임의로 융합 또는 결합되어 고리를 형성하며;
각각의 Ra, Rb, Rc, 및 Rd는 일치환 내지 가능한 최대수의 치환 또는 비치환을 나타낼 수 있고;
R', R", Ra, Rb, Rc, 및 Rd는 각각 독립적으로 수소, 중수소, 할라이드, 알킬, 시클로알킬, 헤테로알킬, 아릴알킬, 알콕시, 아릴옥시, 아미노, 실릴, 알케닐, 시클로알케닐, 헤테로알케닐, 알키닐, 아릴, 헤테로아릴, 아실, 카르보닐, 카르복실산, 에스테르, 니트릴, 이소니트릴, 설파닐, 설피닐, 설포닐, 포스피노, 및 이의 조합으로 이루어지는 군에서 선택되며;
Ra, Rb, Rc, 및 Rd 중 임의의 2개의 인접한 치환기는 임의로 융합 또는 결합되어 고리를 형성하거나 또는 다좌(multidentate) 리간드를 형성하고;
M은 40 초과의 원자 질량을 갖는 금속이며;
h는 1 또는 2이고;
y는 0, 1, 또는 2이며;
z는 0, 1, 또는 2이고;
h+y+z는 금속 M의 산화 상태이다.
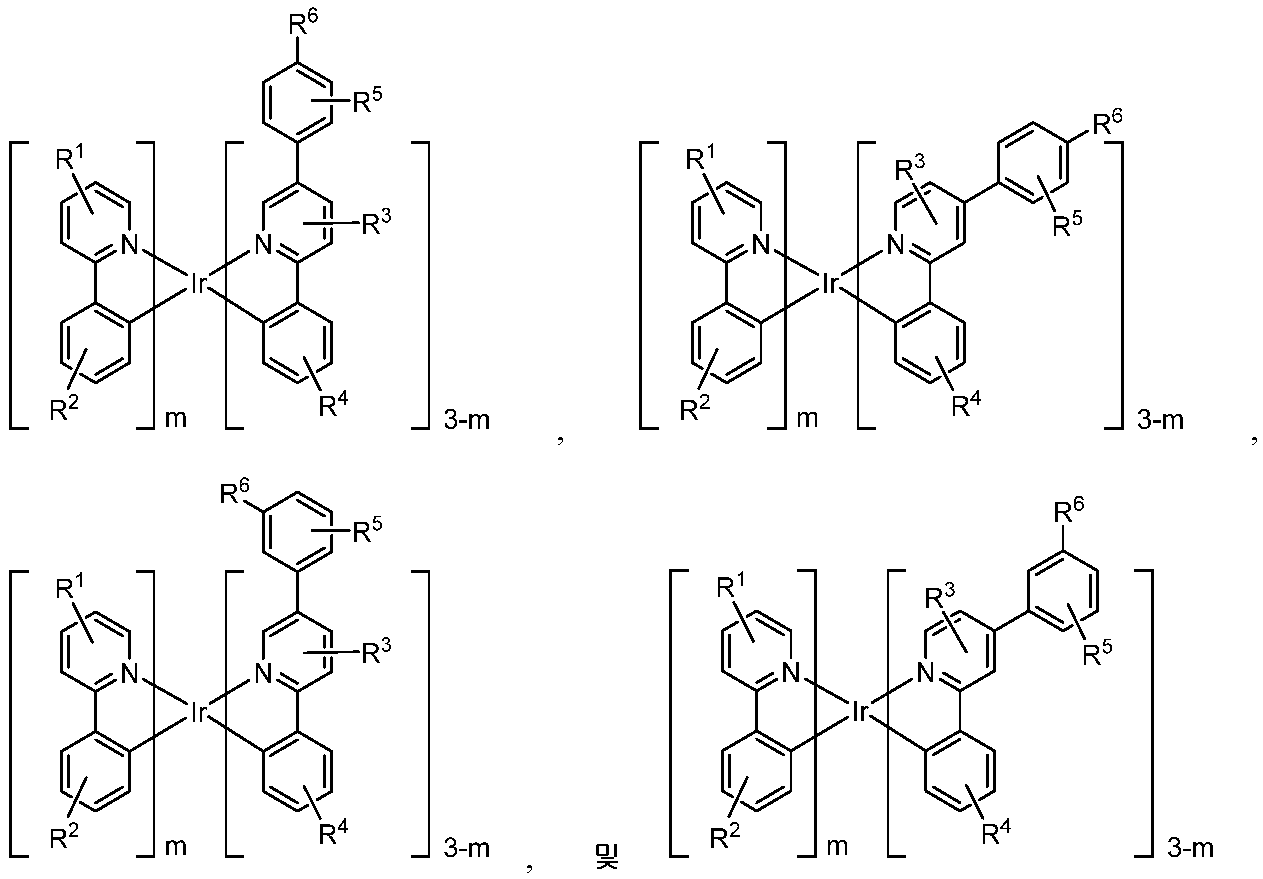
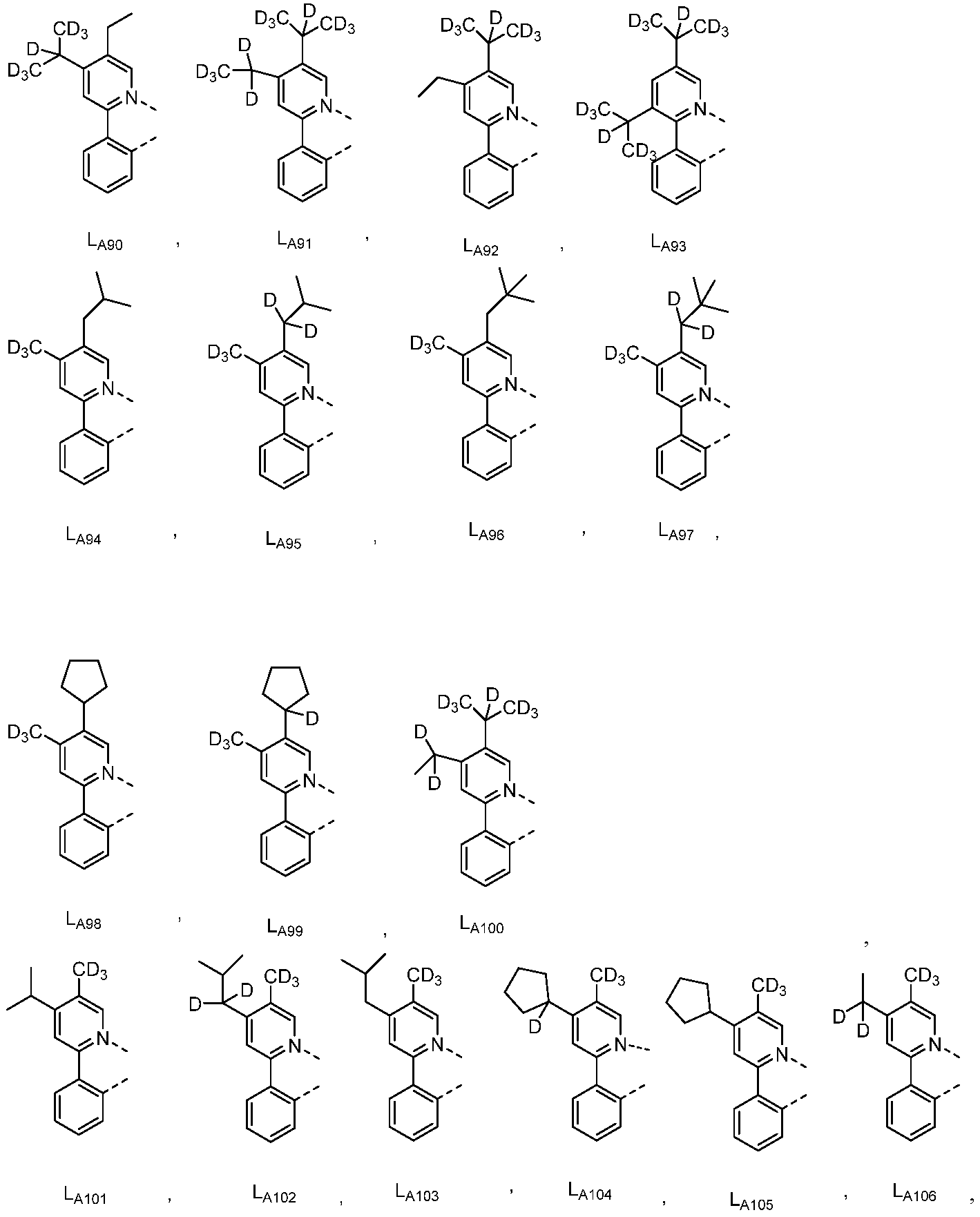
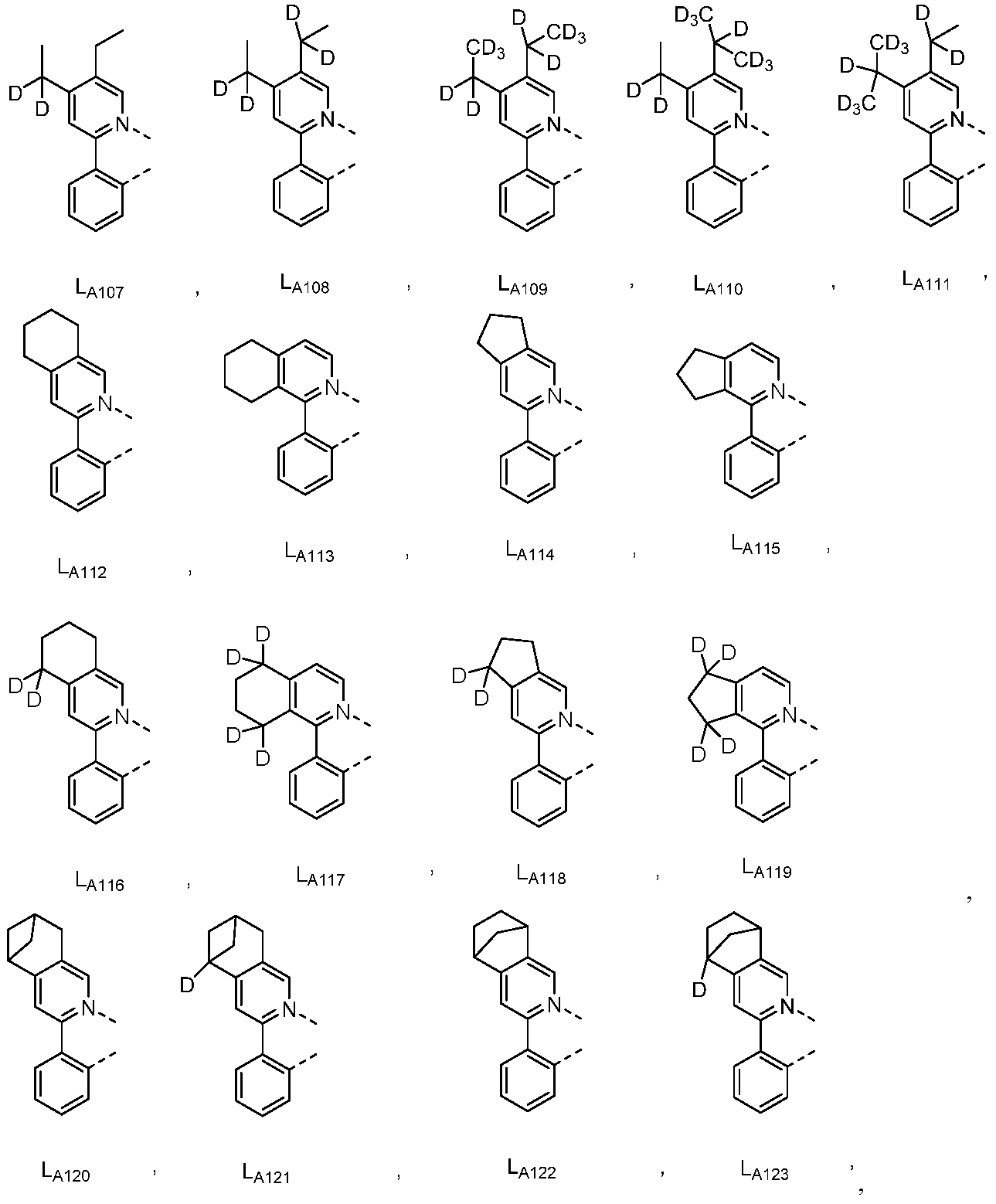
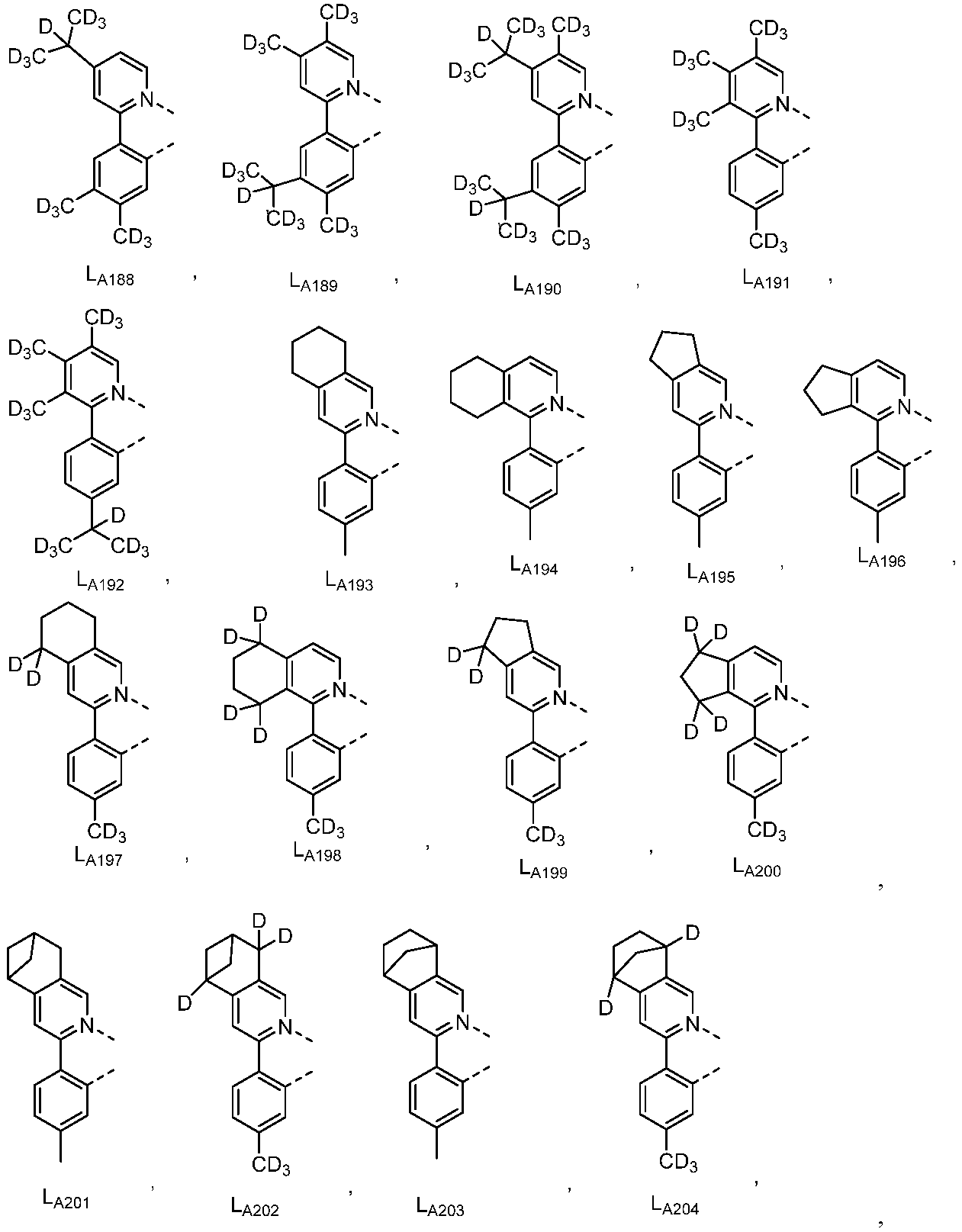
다른 실시양태에 따르면, 하기로 이루어지는 군에서 선택되는 구조를 갖는 화학식 (LA)mIr(LB)3-m을 갖는 화합물이 개시된다:
상기 화학식들에서,
m은 1 또는 2이고;
R1, R2, R4, 및 R5는 각각 독립적으로 일치환, 이치환, 삼치환 또는 사치환, 또는 비치환을 나타내며;
R3은 일치환, 이치환 또는 삼치환, 또는 비치환을 나타내고;
R6은 일치환 또는 비치환을 나타내며;
R1, R2, R3, R4, R5 및 R6는 각각 독립적으로 수소, 중수소, 알킬, 시클로알킬, 이의 부분 또는 완전 중수소화된 또는 불화된 변이체로 이루어지는 군에서 선택된다.
다른 실시양태에 따르면, 유기 발광 다이오드/소자(OLED)도 또한 개시된다. OLED는 애노드, 캐소드, 및 애노드와 캐소드 사이에 배치된 유기층을 포함할 수 있다. 유기층은 하기 화학식으로 이루어지는 군에서 선택되는 화학식을 갖는 화합물을 포함할 수 있다:
M(LA)h(LB)y(LC)z,
상기 화학식에서,
m은 1 또는 2이고;
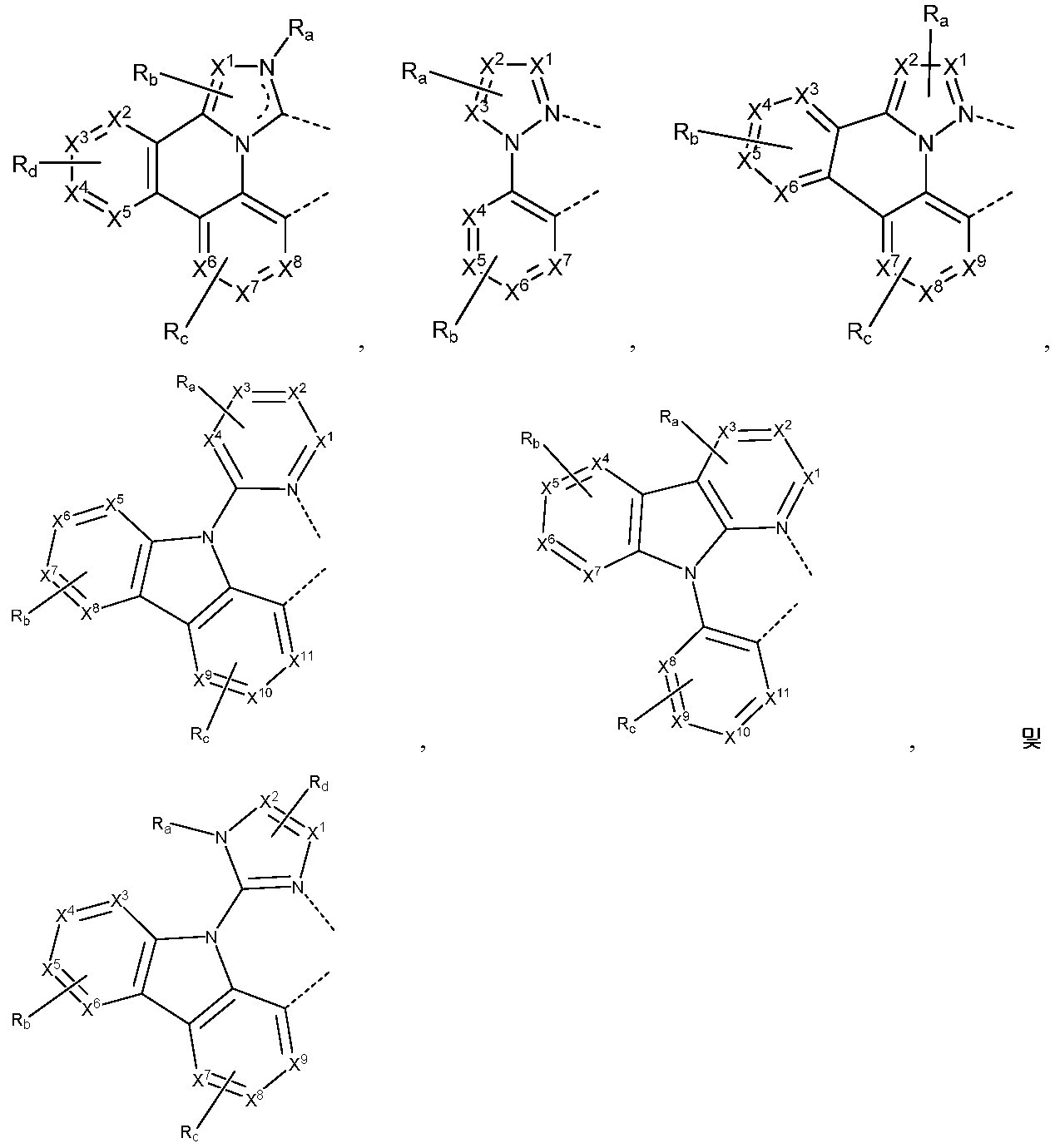
리간드 LA, LB, 및 LC는 각각 독립적으로 하기로 이루어지는 군에서 선택되고:
각각의 X1 내지 X13은 독립적으로 탄소 및 질소로 이루어지는 군에서 선택되며;
X는 BR', NR', PR', O, S, Se, C=O, S=O, SO2, CR'R", SiR'R", 및 GeR'R"로 이루어지는 군에서 선택되고;
R' 및 R"은 임의로 융합 또는 결합되어 고리를 형성하며;
각각의 Ra, Rb, Rc, 및 Rd는 일치환 내지 가능한 최대수의 치환 또는 비치환을 나타낼 수 있고;
R', R", Ra, Rb, Rc, 및 Rd는 각각 독립적으로 수소, 중수소, 할라이드, 알킬, 시클로알킬, 헤테로알킬, 아릴알킬, 알콕시, 아릴옥시, 아미노, 실릴, 알케닐, 시클로알케닐, 헤테로알케닐, 알키닐, 아릴, 헤테로아릴, 아실, 카르보닐, 카르복실산, 에스테르, 니트릴, 이소니트릴, 설파닐, 설피닐, 설포닐, 포스피노, 및 이의 조합으로 이루어지는 군에서 선택되며;
Ra, Rb, Rc, 및 Rd 중 임의의 2개의 인접한 치환기는 임의로 융합 또는 결합되어 고리를 형성하거나 또는 다좌 리간드를 형성하고;
M은 40 초과의 원자 질량을 갖는 금속이며;
h는 1 또는 2이고;
y는 0, 1, 또는 2이며;
z는 0, 1, 또는 2이고;
x+y+z는 금속 M의 산화 상태이며;
상기 화합물의 분자는 0.67을 초과하는 배향 인자 값을 갖고;
R1, R2, R4, 및 R5는 각각 독립적으로 일치환, 이치환, 삼치환 또는 사치환, 또는 비치환을 나타내며;
R3은 일치환, 이치환 또는 삼치환, 또는 비치환을 나타내고;
R6은 일치환 또는 비치환을 나타내며;
R1, R2, R3, R4, R5 및 R6은 각각 독립적으로 수소, 중수소, 알킬, 시클로알킬, 이의 부분 또는 완전 중수소화된 또는 불화된 변이체, 및 이의 조합으로 이루어지는 군에서 선택된다.
또 다른 실시양태에 따르면, 하기 화학식으로 이루어지는 군에서 선택되는 화학식을 갖는 화합물을 함유하는 제제가 개시된다:
상기 화학식에서,
m은 1 또는 2이고;
리간드 LA, LB, 및 LC는 각각 독립적으로 하기로 이루어지는 군에서 선택되고:
각각의 X1 내지 X13은 독립적으로 탄소 및 질소로 이루어지는 군에서 선택되며;
X는 BR', NR', PR', O, S, Se, C=O, S=O, SO2, CR'R", SiR'R", 및 GeR'R"로 이루어지는 군에서 선택되고;
R' 및 R"은 임의로 융합 또는 결합되어 고리를 형성하며;
각각의 Ra, Rb, Rc, 및 Rd는 일치환 내지 가능한 최대수의 치환 또는 비치환을 나타낼 수 있고;
R', R", Ra, Rb, Rc, 및 Rd는 각각 독립적으로 수소, 중수소, 할라이드, 알킬, 시클로알킬, 헤테로알킬, 아릴알킬, 알콕시, 아릴옥시, 아미노, 실릴, 알케닐, 시클로알케닐, 헤테로알케닐, 알키닐, 아릴, 헤테로아릴, 아실, 카르보닐, 카르복실산, 에스테르, 니트릴, 이소니트릴, 설파닐, 설피닐, 설포닐, 포스피노, 및 이의 조합으로 이루어지는 군에서 선택되며;
Ra, Rb, Rc, 및 Rd 중 임의의 2개의 인접한 치환기는 임의로 융합 또는 결합되어 고리를 형성하거나 또는 다좌 리간드를 형성하고;
M은 40 초과의 원자 질량을 갖는 금속이며;
h는 1 또는 2이고;
y는 0, 1, 또는 2이며;
z는 0, 1, 또는 2이고;
x+y+z는 금속 M의 산화 상태이며;
M(LA)h(LB)y(LC)z의 분자는 0.67을 초과하는 배향 인자 값을 갖고;
R1, R2, R4, 및 R5는 각각 독립적으로 일치환, 이치환, 삼치환 또는 사치환, 또는 비치환을 나타내며;
R3은 일치환, 이치환 또는 삼치환, 또는 비치환을 나타내고;
R6은 일치환 또는 비치환을 나타내며;
R1, R2, R3, R4, R5 및 R6은 각각 독립적으로 수소, 중수소, 알킬, 시클로알킬, 이의 부분 또는 완전 중수소화된 또는 불화된 변이체, 및 이의 조합으로 이루어지는 군에서 선택된다.
도 1은 유기 발광 소자를 도시한 것이다.
도 2는 별도의 전자 수송층을 갖지 않는 역전된 유기 발광 소자를 도시한 것이다.
도 3은 표 1에 정의된 소자 구조를 갖는 소자 실시예 2의 에미터에 대하여 0∼60°의 각도에서 편광자를 통해 측정한 스펙트럼을 도시한 것이다.
도 4는 SETFOS-4.1에 의해 생성된 상응하는 스펙트럼을 도시한 것이다.
도 5는 0°수치로 정규화된 적분 방사휘도의 실험적 각도 의존성을 나타낸 것이다. 40°각도에서의 적분 p/s 방사휘도 비는 1.67이다.
도 6은 쌍극자 배향 보정(calibration) 대 SETFOS-4.1 프로그램에 의해 시뮬레이션된 p/s 방출 비를 나타낸 것이다. 이 특정 실시예에 대하여, 40°각도에서의 적분 p/s 방사휘도비는 0.15의 쌍극자 배향(DO)에 상응하는 1.67이다.
도 7은 상이한 DO에 대한 방사휘도-p 프로파일 때 관찰 각도를 나타낸 것이다.
도 8은 상이한 DO에 대한 방사휘도-s 프로파일 때 관찰 각도를 나타낸 것이다.
도 9는 이미터 배향 인자와 소자에서의 최대 추산 EQE의 상관관계를 나타낸 것이다.
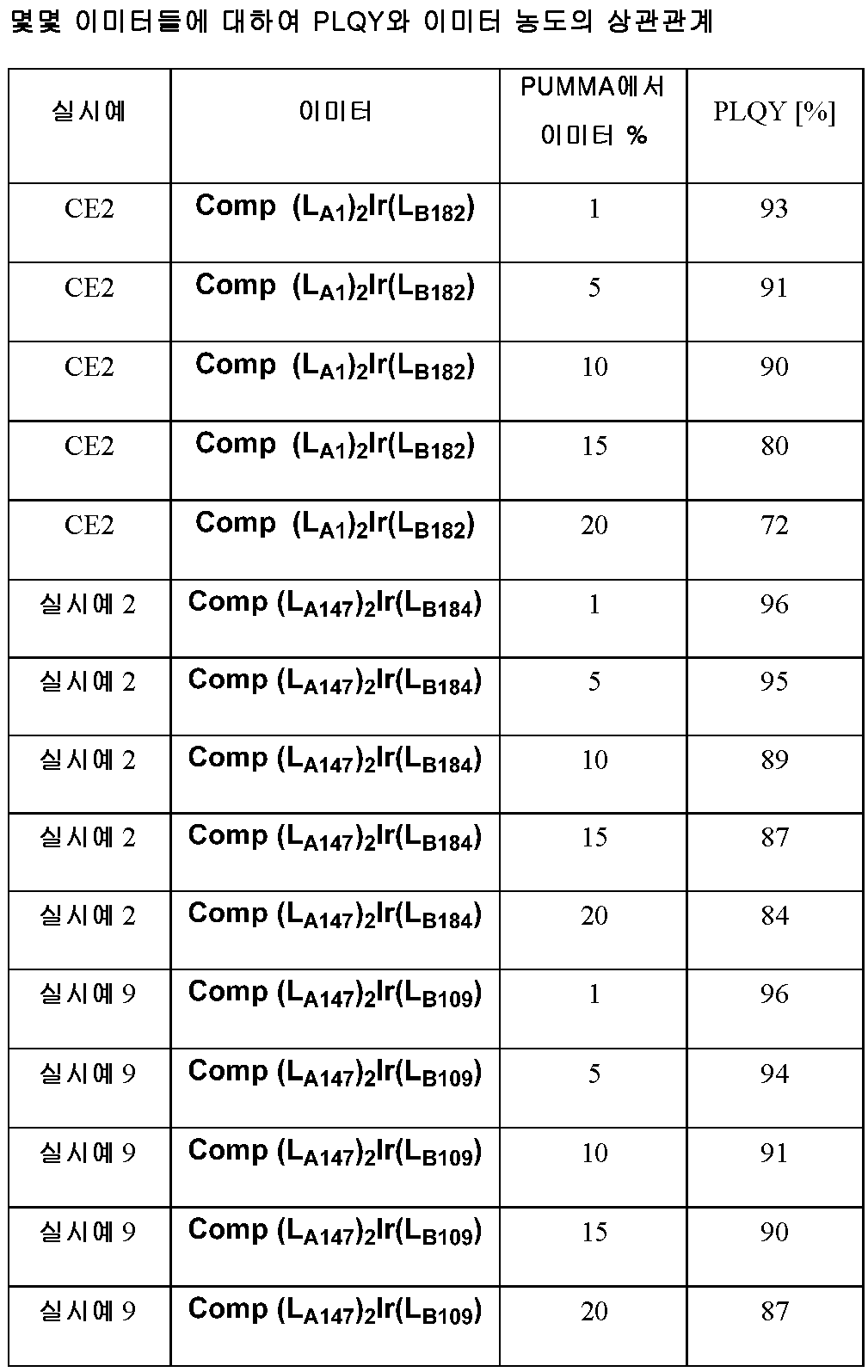
도 10은 일부 이미터들에 대하여 PLQY와 이미터 농도의 상관관계를 나타낸 것이다. 이미터의 입체 부피(steric bulk)는 높은 도핑 %에서의 자가 켄칭을 방지한다.
도 2는 별도의 전자 수송층을 갖지 않는 역전된 유기 발광 소자를 도시한 것이다.
도 3은 표 1에 정의된 소자 구조를 갖는 소자 실시예 2의 에미터에 대하여 0∼60°의 각도에서 편광자를 통해 측정한 스펙트럼을 도시한 것이다.
도 4는 SETFOS-4.1에 의해 생성된 상응하는 스펙트럼을 도시한 것이다.
도 5는 0°수치로 정규화된 적분 방사휘도의 실험적 각도 의존성을 나타낸 것이다. 40°각도에서의 적분 p/s 방사휘도 비는 1.67이다.
도 6은 쌍극자 배향 보정(calibration) 대 SETFOS-4.1 프로그램에 의해 시뮬레이션된 p/s 방출 비를 나타낸 것이다. 이 특정 실시예에 대하여, 40°각도에서의 적분 p/s 방사휘도비는 0.15의 쌍극자 배향(DO)에 상응하는 1.67이다.
도 7은 상이한 DO에 대한 방사휘도-p 프로파일 때 관찰 각도를 나타낸 것이다.
도 8은 상이한 DO에 대한 방사휘도-s 프로파일 때 관찰 각도를 나타낸 것이다.
도 9는 이미터 배향 인자와 소자에서의 최대 추산 EQE의 상관관계를 나타낸 것이다.
도 10은 일부 이미터들에 대하여 PLQY와 이미터 농도의 상관관계를 나타낸 것이다. 이미터의 입체 부피(steric bulk)는 높은 도핑 %에서의 자가 켄칭을 방지한다.
일반적으로, OLED는 애노드 및 캐소드 사이에 배치되어 이에 전기 접속되는 1종 이상의 유기층을 포함한다. 전류가 인가되면, 애노드는 정공을 유기층(들)에 주입하고, 캐소드는 전자를 주입한다. 주입된 정공 및 전자는 각각 반대로 하전된 전극을 향하여 이동한다. 전자 및 정공이 동일한 분자상에 편재화될 경우, 여기된 에너지 상태를 갖는 편재화된 전자-정공쌍인 "엑시톤"이 형성된다. 엑시톤이 광발광 메카니즘에 의하여 이완될 경우 광이 방출된다. 일부의 경우에서, 엑시톤은 엑시머 또는 엑시플렉스상에 편재화될 수 있다. 비-방사 메카니즘, 예컨대 열 이완도 또한 발생할 수 있으나, 일반적으로 바람직하지 않은 것으로 간주된다.
초기 OLED는 예를 들면 미국 특허 제 4,769,292호에 개시된 바와 같은 단일항 상태로부터 광("형광")을 방출하는 발광 분자를 사용하였으며, 상기 특허 문헌은 그 전문이 본원에 참고로 포함된다. 형광 방출은 일반적으로 10 나노초 미만의 시간 기간으로 발생한다.
보다 최근에는, 삼중항 상태로부터의 광("인광")을 방출하는 발광 물질을 갖는 OLED가 예시되어 있다. 문헌[Baldo et al., "Highly Efficient Phosphorescent Emission from Organic Electroluminescent Devices," Nature, vol. 395, 151-154, 1998 ("Baldo-I")] 및 [Baldo et al., "Very high-efficiency green organic light-emitting devices based on electrophosphorescence," Appl. Phys. Lett., vol. 75, No. 3, 4-6 (1999) ("Baldo-II")]을 참조하며, 이들 문헌은 그 전문이 본원에 참고로 포함된다. 인광은 참고로 포함되는 미국 특허 제7,279,704호의 컬럼 5-6에 보다 구체적으로 기재되어 있다.
도 1은 유기 발광 소자(100)를 도시한다. 도면은 반드시 축척에 의하여 도시하지는 않았다. 소자(100)는 기판(110), 애노드(115), 정공 주입층(120), 정공 수송층(125), 전자 차단층(130), 발광층(135), 정공 차단층(140), 전자 수송층(145), 전자 주입층(150), 보호층(155), 캐소드(160) 및 차단층(170)을 포함할 수 있다. 캐소드(160)는 제1의 전도층(162) 및 제2의 전도층(164)을 갖는 화합물 캐소드이다. 소자(100)는 기재된 순서로 층을 증착시켜 제조될 수 있다. 이들 다양한 층뿐 아니라, 예시의 물질의 성질 및 기능은 참고로 포함되는 미국 특허 제7,279,704호의 컬럼 6-10에 보다 구체적으로 기재되어 있다.
이들 각각의 층에 대한 더 많은 예도 이용 가능하다. 예를 들면 가요성 및 투명한 기판-애노드 조합은 미국 특허 제 5,844,363호에 개시되어 있으며, 이 특허 문헌은 그 전문이 본원에 참고로 포함된다. p-도핑된 정공 수송층의 예는 미국 특허 출원 공개 공보 제2003/0230980호에 개시된 바와 같이, 50:1의 몰비로 F4-TCNQ로 도핑된 m-MTDATA이며, 이 특허 문헌은 그 전문이 본원에 참고로 포함된다. 발광 및 호스트 물질의 예는 미국 특허 제6,303,238호(Thompson et al.)에 개시되어 있으며, 이 특허 문헌은 그 전문이 본원에 참고로 포함된다. n-도핑된 전자 수송층의 예는 미국 특허 출원 공개 공보 제2003/0230980호에 개시된 바와 같이, 1:1의 몰비로 Li로 도핑된 BPhen이고, 이 특허 문헌은 그 전문이 본원에 참고로 포함된다. 그 전문이 본원에 참고로 포함되는 미국 특허 제5,703,436호 및 제5,707,745호에는 적층된 투명, 전기전도성 스퍼터-증착된 ITO 층을 갖는 Mg:Ag와 같은 금속의 박층을 갖는 화합물 캐소드를 비롯한 캐소드의 예가 개시되어 있다. 차단층의 이론 및 용도는 미국 특허 제 6,097,147호 및 미국 특허 출원 공개 공보 제2003/0230980호에 보다 구체적으로 기재되어 있으며, 이들 특허 문헌은 그 전문이 본원에 참고로 포함된다. 주입층의 예는 미국 특허 출원 공개 공보 제2004/0174116호에 제공되어 있으며, 이 특허 문헌은 그 전문이 본원에 참고로 포함된다. 보호층의 설명은 미국 특허 출원 공개 공보 제2004/0174116호에서 찾아볼 수 있으며, 이들 특허 문헌은 그 전문이 본원에 참고로 포함된다.
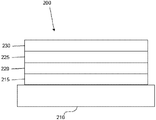
도 2는 역전된 OLED(200)를 도시한다. 소자는 기판(210), 캐소드(215), 발광층(220), 정공 수송층(225) 및 애노드(230)를 포함한다. 소자(200)는 기재된 순서로 층을 적층시켜 제조될 수 있다. 가장 흔한 OLED 구조는 애노드의 위에 캐소드가 배치되어 있고 소자(200)가 애노드(230)의 아래에 캐소드(215)가 배치되어 있으므로, 소자(200)는 "역전된" OLED로 지칭될 수 있다. 소자(100)에 관하여 기재된 것과 유사한 물질이 소자(200)의 해당 층에 사용될 수 있다. 도 2는 소자(100)의 구조로부터 일부 층이 얼마나 생략될 수 있는지의 일례를 제공한다.
도 1 및 도 2에 도시된 단순 적층된 구조는 비제한적인 예로서 제공하며, 본 발명의 실시양태는 다양한 기타의 구조와 관련하여 사용될 수 있는 것으로 이해하여야 한다. 기재된 특정한 물질 및 구조는 사실상 예시를 위한 것이며, 기타의 물질 및 구조도 사용될 수 있다. 작용성 OLED는 기재된 다양한 층을 상이한 방식으로 조합하여 달성될 수 있거나 또는 층은 디자인, 성능 및 비용 요인에 기초하여 전적으로 생략할 수 있다. 구체적으로 기재되지 않은 기타의 층도 또한 포함될 수 있다. 이들 구체적으로 기재된 층을 제외한 물질을 사용할 수 있다. 본원에 제공된 다수의 예가 단일 물질을 포함하는 것으로서 다양한 층을 기재하기는 하나, 물질, 예컨대 호스트 및 도펀트의 혼합물 또는 보다 일반적으로 혼합물을 사용할 수 있다. 또한, 층은 다수의 하부층을 가질 수 있다. 본원에서 다양한 층에 제시된 명칭은 엄격하게 제한하고자 하는 것은 아니다. 예를 들면, 소자(200)에서 정공 수송층(225)은 정공을 수송하며, 정공을 발광층(220)에 주입하며, 정공 수송층 또는 정공 주입층으로서 기재될 수 있다. 하나의 실시양태에서, OLED는 캐소드와 애노드 사이에 배치된 "유기층"을 갖는 것으로 기재될 수 있다. 이러한 유기층은 단일층을 포함할 수 있거나 또는 예를 들면 도 1 및 도 2와 관련하여 기재된 바와 같은 상이한 유기 물질의 복수의 층을 더 포함할 수 있다.
구체적으로 기재하지 않은 구조 및 물질, 예컨대 미국 특허 제 5,247,190호(Friend et al.)에 기재된 바와 같은 중합체 물질(PLED)을 포함하는 OLED를 사용할 수 있으며, 이 특허 문헌은 그 전문이 본원에 참고로 포함된다. 추가의 예로서, 단일 유기층을 갖는 OLED를 사용할 수 있다. OLED는 예를 들면 미국 특허 제 5,707,745호(Forrest et al.)에 기재된 바와 같이 적층될 수 있으며, 이 특허 문헌은 그 전문이 본원에 참고로 포함된다. OLED 구조는 도 1 및 도 2에 도시된 단순 적층된 구조로부터 벗어날 수 있다. 예를 들면, 기판은 미국 특허 제 6,091,195호(Forrest et al.)에 기재된 바와 같은 메사형(mesa) 구조 및/또는 미국 특허 제 5,834,893호(Bulovic et al.)에 기재된 피트형(pit) 구조와 같은 아웃-커플링(out-coupling)을 개선시키기 위한 각진 반사면을 포함할 수 있으며, 이들 특허 문헌은 그 전문이 본원에 참고로 포함된다.
반대의 의미로 명시하지 않는 한, 다양한 실시양태의 임의의 층은 임의의 적절한 방법에 의하여 적층될 수 있다. 유기층의 경우, 바람직한 방법으로는 미국 특허 제6,013,982호 및 제6,087,196호(이 특허 문헌은 그 전문이 본원에 참고로 포함됨)에 기재된 바와 같은 열 증발, 잉크-제트, 미국 특허 제 6,337,102호(Forrest et al.)(이 특허 문헌은 그 전문이 본원에 참고로 포함됨)에 기재된 바와 같은 유기 증기상 증착(OVPD), 미국 특허 출원 제7,431,968호(이 특허 문헌은 그 전문이 본원에 참고로 포함됨)에 기재된 바와 같은 유기 증기 제트 프린팅(OVJP)에 의한 증착을 들 수 있다. 기타의 적절한 증착 방법은 스핀 코팅 및 기타의 용액계 공정을 포함한다. 용액계 공정은 질소 또는 불활성 분위기 중에서 실시되는 것이 바람직하다. 기타의 층의 경우, 바람직한 방법은 열 증발을 포함한다. 바람직한 패턴 형성 방법은 마스크를 통한 증착, 미국 특허 제6,294,398호 및 제6,468,819호(이 특허 문헌은 그 전문이 본원에 참고로 포함됨)에 기재된 바와 같은 냉간 용접 및, 잉크-제트 및 OVJD와 같은 일부 증착 방법과 관련된 패턴 형성을 포함한다. 증착시키고자 하는 물질은 특정한 증착 방법과 상용성을 갖도록 변형될 수 있다. 예를 들면, 분지형 또는 비분지형, 바람직하게는 3개 이상의 탄소를 포함하는 알킬 및 아릴 기와 같은 치환기는 이의 용액 가공의 처리 능력을 향상시키기 위하여 소분자에 사용될 수 있다. 20개 이상의 탄소를 갖는 치환기를 사용할 수 있으며, 3 내지 20개의 탄소가 바람직한 범위이다. 비대칭 구조를 갖는 물질은 대칭 구조를 갖는 것보다 더 우수한 용액 가공성을 가질 수 있는데, 비대칭 물질은 재결정화되는 경향이 낮을 수 있기 때문이다. 덴드리머 치환기는 용액 가공을 처리하는 소분자의 능력을 향상시키기 위하여 사용될 수 있다.
본 발명의 실시양태에 의하여 제조된 소자는 차단층을 추가로 임의로 포함할 수 있다. 차단층의 하나의 목적은 전극 및 유기층이 수분, 증기 및/또는 기체 등을 포함하는 환경에서 유해한 종에 대한 노출로 인하여 손상되지 않도록 한다. 차단층은 기판의 위에서, 기판의 아래에서 또는 기판의 옆에서, 전극 또는, 엣지를 포함하는 소자의 임의의 기타 부분의 위에서 증착될 수 있다. 차단층은 단일층 또는 다중층을 포함할 수 있다. 차단층은 각종 공지의 화학적 증착 기법에 의하여 형성될 수 있으며 복수의 상을 갖는 조성물뿐 아니라 단일 상을 갖는 조성물을 포함할 수 있다. 임의의 적절한 물질 또는 물질의 조합을 차단층에 사용할 수 있다. 차단층은 무기 또는 유기 화합물 또는 둘다를 혼입할 수 있다. 바람직한 차단층은 미국 특허 제7,968,146호, PCT 특허 출원 번호 PCT/US2007/023098 및 PCT/US2009/042829에 기재된 바와 같은 중합체 물질 및 비-중합체 물질의 혼합물을 포함하며, 이들 문헌의 개시내용은 본원에 그 전문이 참고로 포함된다. "혼합물"을 고려하면, 차단층을 포함하는 전술한 중합체 및 비-중합체 물질은 동일한 반응 조건하에서 및/또는 동일한 시간에서 증착되어야만 한다. 중합체 대 비-중합체 물질의 중량비는 95:5 내지 5:95 범위내일 수 있다. 중합체 및 비-중합체 물질은 동일한 전구체 물질로부터 생성될 수 있다. 한 예에서, 중합체 및 비-중합체 물질의 혼합물은 본질적으로 중합체 규소 및 무기 규소로 이루어진다.
본 발명의 실시양태에 따라 제조되는 소자는 다양한 전자 제품 또는 중간 부품에 도입될 수 있는 광범위한 다양한 전자 부품 모듈 (또는 유닛)에 도입될 수 있다. 이러한 전자 제품 또는 중간 부품의 예는 최종 사용자 제품 제조자에 의해 이용될 수 있는 디스플레이 스크린, 조명 소자 예컨대 개개 광원 소자 또는 조명 패널, 등을 포함한다. 이러한 전자 부품 모듈은 경우에 따라 구동 전자장치 및/또는 전원(들)을 포함할 수 있다. 본 발명의 실시양태에 따라 제조되는 소자는 전자 부품 모듈 (또는 유닛) 중 하나 이상이 도입되는 광범위의 다양한 소비재(consumer product)에 도입될 수 있다. 이러한 소비재는 하나 이상의 광원(들) 및/또는 몇몇 타입의 영상 디스플레이 중 하나 이상을 포함하는 임의 종류의 제품을 포함한다. 이러한 소비재의 일부 예는 평판 패널 디스플레이, 컴퓨터 모니터, 의료용 모니터, 텔레비젼, 광고판, 실내 또는 옥외 조명 및/또는 시그널링을 위한 라이트, 헤드업 디스플레이, 완전 또는 부분 투명 디스플레이, 플렉시블 디스플레이, 레이저 프린터, 전화기, 휴대폰, 태블릿, 파블릿, 개인용 정보 단말기(PDA), 웨어러블 소자, 랩탑 컴퓨터, 디지털 카메라, 캠코더, 뷰파인더, 마이크로-디스플레이, 3-D 디스플레이, 비히클, 대형벽, 극장 또는 스타디움 스크린, 또는 간판을 포함한다. 패시브 매트릭스 및 액티브 매트릭스를 비롯한 다양한 제어 메카니즘을 사용하여 본 발명에 따라 제조되는 소자를 제어할 수 있다. 다수의 소자는 사람에게 안락감을 주는 온도 범위, 예컨대 18℃ 내지 30℃, 더욱 바람직하게는 실온(20℃ 내지 25℃)에서 사용하도록 의도되지만, 이러한 온도 범위를 벗어나서, 예를 들면 -40℃ 내지 +80℃에서 사용될 수 있다.
본원에 기재된 재료 및 구조는 OLED 이외의 소자에서의 적용예를 가질 수 있다. 예를 들면, 기타의 광전자 소자, 예컨대 유기 태양 전지 및 유기 광검출기가 이러한 재료 및 구조를 사용할 수 있다. 보다 일반적으로, 유기 소자, 예컨대 유기 트랜지스터가 이러한 재료 및 구조를 사용할 수 있다.
본원에서 사용되는 용어 "할로" 또는 "할로겐"은 불소, 염소, 브롬 및 요오드를 포함한다.
본원에서 사용되는 용어 "알킬"은 직쇄 또는 분지쇄 알킬 라디칼을 모두 의미한다. 바람직한 알킬기는 1∼15 개의 탄소 원자를 함유하는 것으로서, 메틸, 에틸, 프로필, 1-메틸에틸, 부틸, 1-메틸프로필, 2-메틸프로필, 펜틸, 1-메틸부틸, 2-메틸부틸, 3-메틸부틸, 1,1-디메틸프로필, 1,2-디메틸프로필, 2,2-디메틸프로필 등을 포함한다. 추가로, 알킬기는 임의 치환될 수 있다.
본원에서 사용되는 용어 "시클로알킬"은 환형 알킬 라디칼을 의미한다. 바람직한 시클로알킬기는 3∼10 개의 탄소 원자를 함유하는 것으로서, 시클로프로필, 시클로펜틸, 시클로헥실, 아다만틸 등을 포함한다. 추가로, 시클로알킬기는 임의 치환될 수 있다.
본원에서 사용되는 용어 "알케닐"은 직쇄 및 분지쇄 알켄 라디칼을 모두 의미한다. 바람직한 알케닐기는 2∼15 개의 탄소 원자를 함유하는 것이다. 추가로, 알케닐기는 임의 치환될 수 있다.
본원에서 사용되는 용어 "알키닐"은 직쇄 및 분지쇄 알킨 라디칼을 모두 의미한다. 바람직한 알키닐기는 2∼15 개의 탄소 원자를 함유하는 것이다. 추가로, 알키닐기는 임의 치환될 수 있다.
본원에서 사용되는 용어 "아랄킬" 또는 "아릴알킬"은 치환기로서 방향족 기를 갖는 알킬기를 고려한다. 또한, 아랄킬기는 임의로 치환될 수 있다.
본원에서 사용되는 용어 "헤테로시클릭 기"는 방향족 및 비방향족 환형 라디칼이 고려된다. 헤테로-방향족 환형 라디칼은 또한 헤테로아릴을 의미한다. 바람직한 헤테로-비방향족 환형 기는 하나 이상의 헤테로 원자를 포함하는 3∼7개의 고리 원자를 함유하는 기이며, 환형 아민, 예컨대 모르폴리노, 피페리디노, 피롤리디노 등, 및 환형 에테르, 예컨대 테트라히드로푸란, 테트라히드로피란 등을 포함한다. 부가적으로, 헤테로시클릭 기는 경우에 따라 치환될 수 있다.
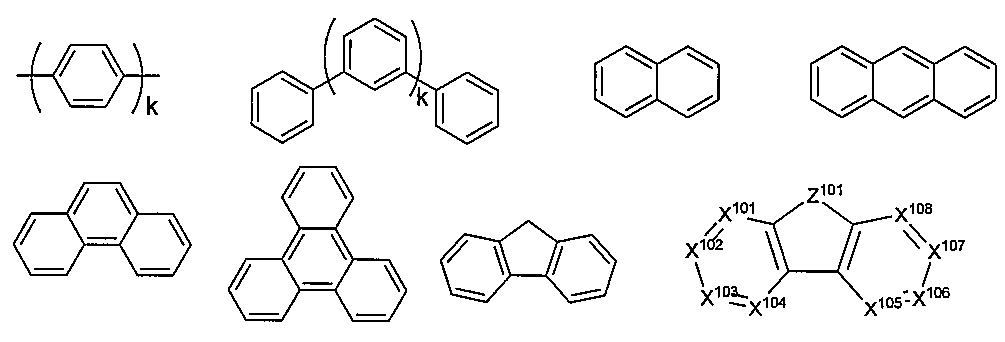
본원에서 사용될 때 "아릴" 또는 "방향족 기"는 단일 고리 기 및 다환 고리계가 고려된다. 다환 고리는 2개의 탄소가 두 인접 고리에 공통인 2개 이상의 고리("축합" 고리)를 가질 수 있으며, 고리들 중 하나 이상은 예컨대 방향족이고, 다른 고리들은 시클로알킬, 시클로알케닐, 아릴, 헤테로사이클 및/또는 헤테로아릴일 수 있다. 바람직한 아릴 기는 6∼30 개의 탄소 원자, 바람직하게는 6∼20 개의 탄소 원자, 더 바람직하게는 6∼12 개의 탄소 원자를 함유하는 것들이다. 6 개의 탄소, 10 개의 탄소 또는 12 개의 탄소를 갖는 아릴 기가 특히 바람직하다. 적합한 아릴 기는 페닐, 비페닐, 트리페닐, 트리페닐렌, 테트라페닐렌, 나프탈렌, 안트라센, 페날렌, 페난트렌, 플루오렌, 피렌, 크리센, 페릴렌 및 아줄렌, 바람직하게는 페닐, 비페닐, 트리페닐, 트리페닐렌, 플루오렌 및 나프탈렌을 포함한다. 추가로, 아릴 기는 임의 치환될 수 있다.
본원에서 사용된 용어 "헤테로아릴"은 1 내지 5개의 헤테로원자를 포함할 수있는 단일-고리 헤테로-방향족 기를 포함한다. 용어 헤테로아릴은 또한 2개 이상의 고리를 가진 폴리시클릭 헤테로-방향족 시스템을 포함하며, 여기서 2개의 원자가 인접한 2개의 고리에 공통이고 (고리들이 "융합됨") 고리들 중 하나 이상이 헤테로아릴이며, 예를 들면, 나머지 고리들은 시클로알킬, 시클로알케닐, 아릴, 헤테로환, 및/또는 헤테로아릴일 수 있다. 바람직한 헤테로아릴기는 3 내지 30개의 탄소 원자, 바람직하게는 3 내지 20개의 탄소 원자, 더 바람직하게는 3 내지 12개의 탄소 원자를 함유하는 것들이다. 적합한 헤테로아릴기는 디벤조티오펜, 디벤조푸란, 디벤조셀레노펜, 푸란, 티오펜, 벤조푸란, 벤조티오펜, 벤조셀레노펜, 카바졸, 인돌로카바졸, 피리딜인돌, 피롤로디피리딘, 피라졸, 이미다졸, 트리아졸, 옥사졸, 티아졸, 옥사디아졸, 옥사트리아졸, 디옥사졸, 티아디아졸, 피리딘, 피리다진, 피리미딘, 피라진, 트리아진, 옥사진, 옥사티아진, 옥사디아진, 인돌, 벤즈이미다졸, 인다졸, 인독사진, 벤족사졸, 벤즈이속사졸, 벤조티아졸, 퀴놀린, 이소퀴놀린, 시놀린, 퀴나졸린, 퀴녹살린, 나프티리딘, 프탈라진, 프테리딘, 크산텐, 아크리딘, 페나진, 페노티아진, 페녹사진, 벤조푸로피리딘, 푸로디피리딘, 벤조티에노피리딘, 티에노디피리딘, 벤조셀레노페노피리딘, 및 셀레노페노디피리딘, 바람직하게는 디벤조티오펜, 디벤조푸란, 디벤조셀레노펜, 카바졸, 인돌로카바졸, 이미다졸, 피리딘, 트리아진, 벤즈이미다졸, 및 이의 아자-유사체를 포함한다. 부가적으로, 헤테로아릴기는 경우에 따라 치환될 수 있다.
알킬, 시클로알킬, 알케닐, 알키닐, 아르알킬, 헤테로시클릭 기, 아릴, 및 헤테로아릴은 수소, 듀테륨, 할로겐, 알킬, 시클로알킬, 헤테로알킬, 아릴알킬, 알콕시, 아릴옥시, 아미노, 시클릭 아미노, 실릴, 알케닐, 시클로알케닐, 헤테로알케닐, 알키닐, 아릴, 헤테로아릴, 아실, 카르보닐, 카르복실산, 에테르, 에스테르, 니트릴, 이소니트릴, 설파닐, 술피닐, 술포닐, 포스피노 및 이의 조합으로 이루어진 군으로부터 선택된 하나 이상의 치환기로 임의 치환될 수 있다.
본원에서 사용된 "치환된"은 H 이외의 치환기가 관련 위치, 예컨대 탄소에 결합됨을 나타낸다. 따라서, 예를 들어, R1이 단일 치환되는 경우, 하나의 R1은 H 외외의 것이어야 한다. 유사하게, R1이 이치환된 경우, R1 중 2개는 H 이외의 것이어야 한다. 유사하게, R1이 비치환된 경우, R1은 모든 가능한 위치에 대하여 수소이다.
본원에 기술된 분절, 즉 아자-디벤조푸란, 아자-디벤조티오펜 등에서 "아자" 표기는 각각의 분절에서의 C-H 기 중 하나 이상이 질소 원자로 치환될 수 있다는 것을 의미하며, 예를 들면(이에 한정되지 않음) 아자트리페닐렌은 디벤조[f,h]퀴녹살린 및 디벤조[f,h]퀴놀린 모두를 포함한다. 당업자는 상기 기술된 아자-유도체의 기타 질소 유사체를 용이하게 고려할 수 있으며, 상기 모든 유사체는 본원에 기술된 용어를 포괄하는 것으로 간주된다.
당업자라면 분자 분절이 치환기인 것으로 기술되거나 그렇지 않은 경우 또다른 모이어티에 결합될 때 이의 명칭은 분절(예, 페닐, 페닐렌, 나프틸, 디벤조푸릴)인 것처럼 또는 전체 분자(예, 벤젠, 나프탈렌, 디벤조푸란)인 것처럼 기재될 수 있다는 것을 이해할 것이다. 본원에 사용된 바와 같이, 이러한 치환기 또는 결합된 분절의 상이한 표기 방식은 동일한 것으로 간주된다.
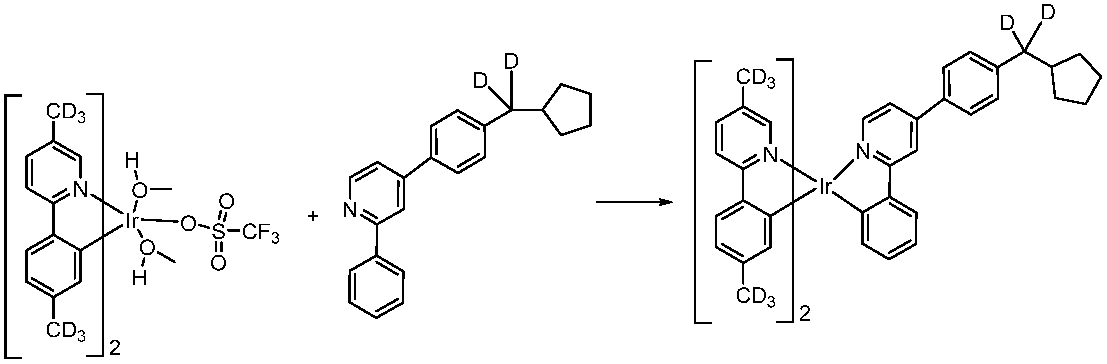
단순 알킬 치환된 페닐피리딘 리간드를 갖는 이리듐 착물은 인광 OLED에서 이미터로서 널리 사용되어 왔다. 일부 실시양태에서, 본 개시는 Ir 착물 상에 벌키 기를 형성하는 특정 치환 패턴 또는 특정의 새로운 치환을 갖는 치환된 페닐피리딘 리간드를 포함하는 이리듐 착물을 개시한다. Pt 착물 리간드 상의 벌키 기는 또한 더 높은 EQE 및 더 적은 엑시머 형성을 보였다. 이들 치환은 소자 효율 및 수명을 예상밖으로 개선한다. 이들 치환은 또한 금속 착물의 전이 쌍극자 모멘트가 OLED 기판에 평행하여 이미터의 외부 양자 효율을 증대시키도록 금속 착물을 배향시킨다. 광 방출이 이미터 화합물의 전이 쌍극자에 대하여 수직이기 때문에 이미터 금속 착물의 전이 쌍극자 모멘트의 평행한 배향은 OLED로부터 추출되는 광량을 증가시킨다.
이미터 전이 쌍극자 모멘트 배향의 측정 - OLED에서 이미터의 전이 쌍극자 모멘트의 배향은 외부 양자 효율을 제한하는 중요한 인자들 중 하나로서 많은 주목을 받아왔다. 최근의 문헌에서 다수의 상이한 배향 측정 방법이 이용되고 보고되어 왔다. 보고된 방법은 광학 시뮬레이션이 후속되는 각도 광루미네센스 프로파일 측정; 일련의 ETL 두께를 갖는 소자를 이용하는 아웃커필링 렌즈를 구비/비구비한 EL 소자의 적분구 EGE 측정; 및 단색 일렉트로루미네센스 원거리장 각도 패턴 측정을 포함한다. 이들 방법 모두는 데이터 계산 및 해석을 위해 시판 광학 시뮬레이션 소프트웨어를 사용한다.
이하 개시되는 방법은 표준 재료 세트를 갖는 소자에서 사용되는 다수의 OLED의 배향 인자를 평가하기 위해 고안되었다. 통상적으로, 해당 재료는 최대 효율을 위해 최적화된 구조를 갖는 소자에 사용된다. 상기 방법은 이미터의 쌍극자 배향에 대해 측정된 방출의 감도를 증대시키기 위하여 층 두께가 변화된 변형 구조를 필요로 한다.
소자 구조 선택 - OLED 이미터의 쌍극자 배향 연구에서 중요한 요소는 상극자 배향에 대하여 가장 민감한 광학적 방출 특성을 증대시키기 위하여 샘플 소자의 구조를 맞추는 것이다. 바텀-방출 소자에서, 이것이 캐비티 효과를 생성하기 위하여 방출 스펙트럼의 최대 파장으로 조정되는 경우, 반사 캐소드로부터 이미터 위치의 거리가 지배적인 파라미터가 된다. 이러한 식으로 활성화되는 캐비티 효과는 편광 방출의 각도 측정에서 가장 잘 보일 수 있다.
상기 구조는 이미터의 전계발광을 활성화하기 위하여 잘 정해진 위치 및 경로에 이미터를 유지하는 매트릭스를 제공하여야 한다. 상기 구조는 다수의 계면을 갖는 복합 광학계를 구성하고 상이한 광학 특성을 갖는 재료를 포함할지라도, 이것은 공기 중에서 원거리장 패턴을 규정하는 주요 요소인 반사 캐소드와 방출 부위 사이의 거리를 만들도록 설계될 수 있다.
* 얇은 EML에 방출원을 가두기 위한 캐리어 차단층.
** HBL 및 EML 부분과 함께 황색 또는 녹색 방출과 공명하는 두꺼운 ETL.
*** 재조합 구역(RZ)을 좁은 영역에 한정하기 위한 얇은 100Å EML.
황색 이미터 화합물의 배향 인자를 측정하기 위해 사용될 수 있는 소자 구조의 예를 표 1에 나타낸다. 표 1에 제공된 층 두께는 황색 이미터 배향 인자 측정을 위해 설계된다. 녹색 이미터 화합물의 배향 인자를 측정하기 위해 사용될 수 있는 소자 구조의 예를 표 2에 나타낸다. 층 두께는 그 방출 파장에 따라 적색, 녹색, 또는 청색 이미터를 위해 조절될 수 있다. 일반적인 규칙은 적절한 층들의 두께를 조절함으로써 EML의 RZ, 반사 전극 및 투명 전극 사이의 거리를 조정하여 반사 전극으로부터 반사되는 빛과 RZ로부터 방출되는 빛의 보강 간섭에 의해 광 출력을 최대화하는 것이다. 거리는 소자 층 두께에 의해 조정되고, 방출 파장에 비례한다. 유기 이미터는 100Å-두께 EML에 놓인다. 유기 이미터의 방출은 보통 엄격히 단색이 아니다. 스펙트럼의 상이한 부분들이 캐소드에 의해 반사되는 빛과 상이하게 상호작용하여, 원래 스펙트럼을 변형시킨다. 그 때문에 원거리장 도구에 의해 관찰되는 스펙트럼은 이미터의 원래 PL 스펙트럼과 상이할 수 있다.
황색 및 녹색 이미터 배향 인자 측정을 위한 실시예 소자 구조에서 상이한 부품들에 대한 재료의 예는 다음과 같다:
ㆍ
애노드: ITO;
ㆍ
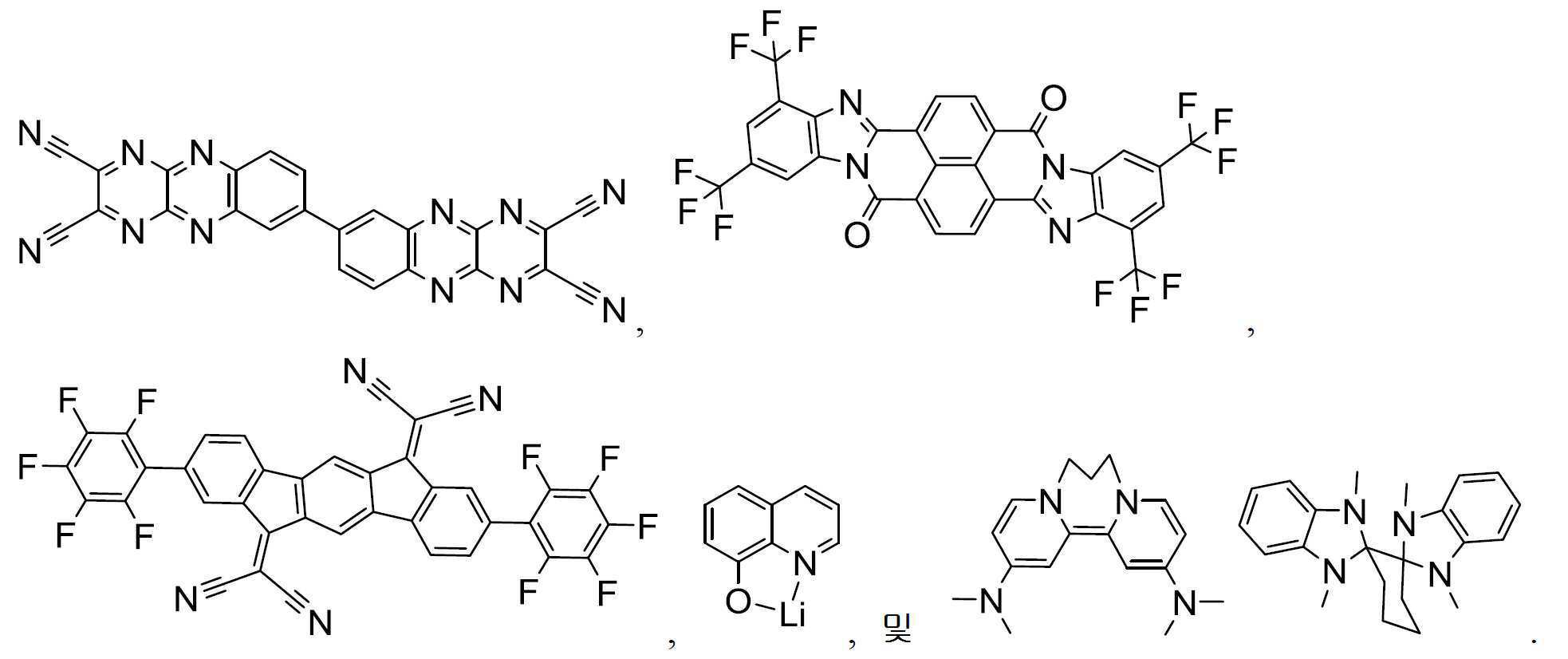
HIL: HATCN;
ㆍ
EML은 이하의 두 호스트로 이루어진다:
ㆍ
EIL: LiF 또는 Liq; 및
ㆍ
캐소드: Al.
이 재료 세트는 적색, 녹색, 또는 청색 이미터에 따라 조절되어야 한다. 당업자는 적색, 녹색, 또는 청색 이미터에 대해 재료 세트를 조절하는 방법을 알 것이다. 각도 스펙트럼 측정의 편의를 위해 5 mm2의 비교적 큰 소자 픽셀이 선택되었다.
시험: 표 3의 이미터 실시예 2, Comp (LA147)2Ir(LB184)에 대한 배향 인자 측정 절차를 이제 설명한다. 표 1의 소자 구조의 스펙트럼 측정은 보정된 분광광도계 모델 PR740을 이용하여 행한다. 상기 기구는 작은 천공을 갖는 셔터 상에 투영되는 도트 이미지를 이용하므로, 한 각도에서 객체를 관찰할 때 작은 시차가 예상된다. 이것은 간단한 기하학을 이용하여 보정될 필요가 있다. 50°를 넘는 각도에서는 소자의 이면 유리 커버로부터의 빛의 반사를 관찰하는 기구의 추가의 효과가 있다. 그러한 이유에서, 50°보다 넓은 각도에서 취한 데이터는 단지 경향을 나타내기 위하여 이용되며, 계산은 오직 30∼50°각도에서 취한 데이터에 기초한다. 대부분의 샘플에 있어서 40°각도에서 분석된 효과는 신뢰가능한 데이터를 제공하기에 충분히 강하므로, 더 넓은 각도에서 얻어진 데이터를 정량할 필요가 없다.
측정된 스펙트럼 데이터와 시뮬레이션된 스펙트럼 데이터를 비교하는 것은 시뮬레이션된 데이터와 실제 방출 사이의 매칭 품질에 대한 가장 감도 높은 측정이다. 시뮬레이션 소프트웨어 방법은 광원의 광학적 특성에 기초하므로, 관찰 데이터와 시뮬레이션된 데이터 사이의 일치는, 시뮬레이션을 이용하여 계산된 쌍극자 배향 면에서의 이미터의 성능을 보정하는 것의 타당성을 확인해 준다. 30∼50°범위에서 측정된 p- 대 s-방출의 비는 배향 인자와 강한 상관관계가 있다. p 대 s 방사휘도 비를 이용하는 것은 광학계의 불완전에서 유래하는 방사휘도 측정의 절대 보정으로 인한 잠재적인 문제를 제거한다.
스펙트럼: 도 3은 s-편광자를 통해 0∼60°의 다양한 각도에서 취한 표 1에 나타낸 구조의 이미터 실시예 2에 대한 소자의 EL 스펙트럼을 나타낸 것이다. 표 4는 Fluxim에 의한 프로그램 SETFOS-4.1을 이용한 동일한 소자 구조의 시뮬레이션된 각도 의존적 s-EL 스펙트럼이다.
결과 및 해석: 주어진 스펙트럼 및 소자 구조의 각도 데이터에 대한 추산된 쌍극자 배향 수치의 의존성의 상세를 이하에 설명한다. 도 5의 그래프는 표 1에 나타낸 구조 및 도 3∼4에 나타낸 바와 같이 매칭된 스펙트럼을 갖는 샘플의 시뮬레이션 소프트웨어에 의해 생성된 데이터에 기초한 것이다. 이 특정 실시예에서, 40°각도에서의 적분 p/s 방사휘도 비는 1.67이고 상응하는 쌍극자 배향(DO)은 0.15(도 6)이다. 시뮬레이션 소프트웨어에 의해 생성된 DO 수치는 수직 대 수평 배향의 통계적 분포를 나타낸다. 수직 및 수평 배향은 기판에 대한 것이며 수직은 기판면에 직교하는 방향을 의미하고 수평은 기판면에 평행한 방향을 의미한다. 한 수직 방향 및 두 수평 방향을 갖는 경우, DO 수치 스케일은 0(평행 또는 수평) 내지 0.33(등방성)이다. 1∼0.67의 상응하는 스케일은 쌍극자 배향으로 인한 손실 후 원래의 EQE의 퍼센트를 나타낸다. Θ=1-DO로서 정의되는 이 값은 이미터 배향 인자(우리의 실시예에서 Θ=1-0.15=0.85, 또는 최대 EQE의 85%)라고 불리며 실험 데이터에서 더 이용된다. 이것은 기판에 대하여 평행하게 정렬된 이미터 쌍극자의 %를 나타낸다. 도 7 및 8의 그래프는 30∼50°각도에서의 쌍극자 배향에 대한 각도 응답이 s-방출보다 p-방출에서 더 강함을 나타낸다. 또한, 쌍극자 배향 수치가 증가함에 따라 p-방사휘도 값은 상승하는 반면에 s-방사휘도는 작아진다. 얻어지는 p/s 비는 30°관찰 각도로부터 출발하여 쌍극자 배향에 대하여 매우 높은 감도를 나타낸다. 현재의 측정에서는 40°가 s 방출과 p 방출 사이의 최대 차이 및 최고 감도를 나타내므로 40°각도가 선택된다.
재료가 바람직한 배향('배향 인자')을 갖는다는 것은 고체 상태 박막에서 이것이 비등방성 수평 대 수직 쌍극자 비를 가짐을 의미한다. 즉, 수평 대 수직 쌍극자 비가 0.67:0.33(등방성의 경우)을 초과, 예컨대 0.77:0.23이다. 이것을 다른 식으로 설명하면, 배향 인자(Θ), 수평 쌍극자 대 총 쌍극자의 비는 0.67을 초과한다.
도 9는 추산된 최대 EQE 대 배향 인자 사이에 얻어진 상관관계를 나타낸 것이다. 배향 인자가 증가함에 따라 명백한 EQE 증가가 관찰된다. 배향 인자가 1에 가까울수록 더 많은 이미터 분자가 기판에 대하여 평행하게 정렬되는데, 이것은 소자 효율 개선에 바람직하다.
PMMA에서 이미터 광루미네센스 양자 수율(PLQY) 측정 절차를 여기에 개시한다. 고체 상태 샘플에 대한 일반적인 준비 및 실험: PMMA 및 이미터(여러가지 중량%)를 계측하여 톨루엔에 용해시킨다. 용액을 2 미크론 필터를 통해 여과하고 미리 세정한 석영 기판 상에 드롭 캐스팅한다. 크세논 램프, 적분구 및 모델 C10027 광자 다채널 분석기가 장착된 Hamamatsu C9920 시스템에서 PL 양자 효율 측정을 행하였다.
이미터 배향 인자에 의해 알 수 있는 바와 같이, 이미터 배향은 2,4-디페닐피리딘 리간드의 4-페닐 고리 상의 기의 벌크성이 증가할수록 더 평행하다. 추산된 EQE는 이미터 배향과 직접적인 상관관계가 있는 것으로 보고되었다.
도 10은 이미터 농도의 함수로서 박막 중의 이미터 PLQY의 상관관계를 나타낸 것이다. 소자 CE2에서 사용되는 Comp (LA1)2Ir(LB182)와 같은 벌키하지 않은 이미터에 대하여, PLQY는 10%를 넘는 이미터 농도 증가와 더불어 현저히 떨어진다. 그러나, 더 벌키한 이미터(예컨대, 소자 실시예 2 및 실시예 9에 사용되는 이미터)의 경우, PLQY는 이미터 농도가 증가함에 따라 빠르게 감소하지 않는다. 따라서, 이미터 분자의 입체적 부피가 높은 이미터 %에서의 자가 켄칭을 방지한다.
상기 이미터 배향 및 PLQY 측정으로부터, 분자 상의 특정 방향으로 더 큰 입체 부피를 갖는 이미터는 (OLED의 기판에 대하여) 더 평행한 배향을 제공하므로 소자에서 더 높은 EQE를 나타낸다는 결론이 나온다. 이들 이미터 실시예들을 이하에 도시하고 표 3 및 4에 열거한다.
본 개시의 일부 실시양태에 따르면, 하기 화학식을 갖는 화합물이 개시된다:
M(LA)h(LB)y(LC)z
상기 화학식에서, 리간드 LA, LB, 및 LC는 각각 독립적으로 하기로 이루어지는 군에서 선택되고:
각각의 X1 내지 X13은 독립적으로 탄소 및 질소로 이루어지는 군에서 선택되며;
X는 BR', NR', PR', O, S, Se, C=O, S=O, SO2, CR'R", SiR'R", 및 GeR'R"로 이루어지는 군에서 선택되고;
R' 및 R"은 임의로 융합 또는 결합되어 고리를 형성하며;
각각의 Ra, Rb, Rc, 및 Rd는 일치환 내지 가능한 최대수의 치환 또는 비치환을 나타낼 수 있고;
R', R", Ra, Rb, Rc, 및 Rd는 각각 독립적으로 수소, 중수소, 할라이드, 알킬, 시클로알킬, 헤테로알킬, 아릴알킬, 알콕시, 아릴옥시, 아미노, 실릴, 알케닐, 시클로알케닐, 헤테로알케닐, 알키닐, 아릴, 헤테로아릴, 아실, 카르보닐, 카르복실산, 에스테르, 니트릴, 이소니트릴, 설파닐, 설피닐, 설포닐, 포스피노, 및 이의 조합으로 이루어지는 군에서 선택되며;
Ra, Rb, Rc, 및 Rd 중 임의의 2개의 인접한 치환기는 임의로 융합 또는 결합되어 고리를 형성하거나 또는 다좌 리간드를 형성하고;
M은 40 초과의 원자 질량을 갖는 금속이며;
h는 1 또는 2이고;
y는 0, 1, 또는 2이며;
z는 0, 1, 또는 2이고;
x+y+z는 금속 M의 산화 상태이며;
M(LA)h(LB)y(LC)z의 분자는 0.67을 초과하는 배향 인자 값을 가진다.
화학식 M(LA)h(LB)y(LC)z을 갖는 화합물의 일부 실시양태에서, M은 Ir, Rh, Re, Ru, Os, Pt, Au, 및 Cu로 이루어지는 군에서 선택된다. 다른 실시양태에서, M은 Ir 또는 Pt이다.
일부 실시양태에서, 상기 화합물의 분자는 0.75 이상의 배향 인자 값(Θ)을 가진다. 다른 실시양태들에서, 상기 분자는 0.80 이상의 배향 인자 값을 가진다. 다른 실시양태들에서, 상기 분자는 0.85 이상의 배향 인자 값을 가진다. 다른 실시양태들에서, 상기 분자는 0.91 이상의 배향 인자 값을 가진다. 다른 실시양태들에서, 상기 분자는 0.92 이상의 배향 인자 값을 가진다. 다른 실시양태들에서, 상기 분자는 0.93 이상의 배향 인자 값을 가진다. 일부 실시양태에서, 상기 분자는 0.94 이상의 배향 인자 값을 가진다.
화학식 M(LA)h(LB)y(LC)z을 갖는 화합물의 일부 실시양태에서, Ra, Rb, Rc, 및 Rd 중 하나는 13개 이상의 탄소 원자를 갖는 일치환이고, Ra, Rb, Rc, 및 Rd의 나머지 모두는 6의 최대 탄소수를 가진다.
화학식 M(LA)h(LB)y(LC)z을 갖는 화합물의 일부 실시양태에서, 각각의 X1 내지 X13은 탄소이다.
화학식 M(LA)h(LB)y(LC)z을 갖는 화합물의 일부 실시양태에서, 화합물은 화학식 Ir(LA)2(LB)을 가진다.
화학식 Ir(LA)2(LB)을 갖는 화합물의 실시양태에서, LA는 하기로 이루어지는 군에서 선택되는 화학식을 갖고:
LB는 하기 화학식을 가진다:
. 일부 다른 실시양태들에서, LB는 화학식 을 가지며; 여기서, Re, Rf, Rh, 및 Ri는 독립적으로 알킬, 시클로알킬, 아릴, 및 헤테로아릴로 이루어지는 군에서 선택되고; Re, Rf, Rh, 및 Ri 중 적어도 하나는 2개 이상의 탄소 원자를 가지며; Rg는 수소, 중수소, 할라이드, 알킬, 시클로알킬, 헤테로알킬, 아릴알킬, 알콕시, 아릴옥시, 아미노, 실릴, 알케닐, 시클로알케닐, 헤테로알케닐, 알키닐, 아릴, 헤테로아릴, 아실, 카르보닐, 카르복실산, 에스테르, 니트릴, 이소니트릴, 설파닐, 설피닐, 설포닐, 포스피노, 및 이의 조합으로 이루어지는 군에서 선택된다.
화학식 Ir(LA)2(LB)을 갖는 화합물의 일부 실시양태에서, LA 및 LB는 상이하고 각각 독립적으로 하기로 이루어지는 군에서 선택된다:
화학식 Ir(LA)2(LB)을 갖는 화합물의 일부 실시양태에서, LA 및 LB는 각각 독립적으로 하기로 이루어지는 군에서 선택된다:
화학식 M(LA)h(LB)y(LC)z을 갖는 화합물의 일부 실시양태에서, 화합물은 화학식 Pt(LA)(LB)을 갖고, 상기 화학식에서 LA 및 LB는 상이하다. 상기 화합물의 일부 실시양태에서, LA는 LB에 결합하여 4좌 리간드를 형성한다.
화학식 M(LA)h(LB)y(LC)z을 갖는 화합물의 일부 실시양태에서, 상기 화합물은 하기로 이루어지는 군(군 1)에서 선택되는 구조를 갖는 화학식 (LA)mIr(LB)3-m을 가진다:
상기 화학식들에서, m은 1 또는 2이고; R1, R2, R4, 및 R5는 각각 독립적으로 일치환, 이치환, 삼치환 또는 사치환, 또는 비치환을 나타내며; R3은 일치환, 이치환 또는 삼치환, 또는 비치환을 나타내고; R1, R2, R3, R4, 및 R5는 각각 독립적으로 수소, 중수소, C1 내지 C6 알킬, C1 내지 C6 시클로알킬, 및 이의 부분 또는 완전 중수소화된 또는 불화된 변이체로 이루어지는 군에서 선택되며; R6은 7개 이상의 탄소 원자를 갖는 알킬, 7개 이상의 탄소 원자를 갖는 시클로알킬, 7개 이상의 탄소 원자를 갖는 알킬-시클로알킬, 및 이의 부분 또는 완전 중수소화된 또는 불화된 변이체로 이루어지는 군에서 선택된다. 상기 화합물의 일부 실시양태에서 m은 2이다.
화학식 M(LA)h(LB)y(LC)z을 갖는 화합물의 일부 실시양태에서, 상기 화합물은 하기로 이루어지는 군에서 선택되는 구조를 갖는 화학식 (LA)mIr(LB)3-m을 가진다:
상기 화학식들에서, m은 1 또는 2이다.
화학식 M(LA)h(LB)y(LC)z을 갖는 화합물의 일부 실시양태에서, 상기 화합물은 군 1에서 선택되는 구조를 갖는 화학식 (LA)mIr(LB)3-m을 가지며, 상기 화학식에서 m은 1 또는 2이고; R2, R3, R4, 및 R5는 각각 독립적으로 수소, 중수소, 메틸, 에틸, 프로필, 이소프로필, 및 이의 조합으로 이루어지는 군에서 선택된다.
화학식 M(LA)h(LB)y(LC)z을 갖는 화합물의 일부 실시양태에서, 상기 화합물은 군 1에서 선택되는 구조를 갖는 화학식 (LA)mIr(LB)3-m을 가지며, 상기 화학식에서 m은 1 또는 2이고; R6은 8개 이상의 탄소 원자를 갖는 알킬, 8개 이상의 탄소 원자를 갖는 시클로알킬, 8개 이상의 탄소 원자를 갖는 알킬-시클로알킬, 및 이의 부분 또는 완전 중수소화된 또는 불화된 변이체로 이루어지는 군에서 선택된다.
화학식 M(LA)h(LB)y(LC)z을 갖는 화합물의 일부 실시양태에서, 상기 화합물은 군 1에서 선택되는 구조를 갖는 화학식 (LA)mIr(LB)3-m을 가지며, 상기 화학식에서 m은 1 또는 2이고; R3, R4, 및 R5는 각각 수소이다.
화학식 M(LA)h(LB)y(LC)z을 갖는 화합물의 일부 실시양태에서, 상기 화합물은 화학식 (LA)mIr(LB)3-m을 가지며, 상기 화학식에서 m은 1 또는 2이고; LA는 하기로 이루어지는 군에서 선택된다:
화학식 M(LA)h(LB)y(LC)z을 갖는 화합물의 일부 실시양태에서, 상기 화합물은 화학식 (LA)mIr(LB)3-m을 가지며, 상기 화학식에서 m은 1 또는 2이고; LB는 이하 도시되는 LB1 내지 LB227로 이루어지는 군에서 선택된다:
군 1에서 선택되는 구조를 갖는 화학식 (LA)mIr(LB)3-m(여기서, LA는 LA1 내지 LA225 중 하나임)의 화합물의 일부 실시양태에서, 상기 화합물은 화학식 Ir(L Aj )2(LBk)(여기서, x = 227j + k - 227이고, j는 1∼225의 정수이며, k는 1∼227의 정수임)을 갖는 화합물 x이다.
군 1에서 선택되는 구조를 갖는 화학식 (LA)Pt(LB)(여기서, LA는 LA1 내지 LA225 중 하나임)의 화합물의 일부 실시양태에서, 상기 화합물은 화학식 Pt(LA j )(LB k )(여기서, y = 227j + k - 227이고, j는 1∼225의 정수이며, k는 1∼227의 정수임)을 갖는 화합물 y이다. LB1 내지 LB227은 상기 정의된 바와 같은 구조를 가진다.
본 개시의 다른 양태에 따르면, 화학식 (LA)mIr(LB)3-m을 갖는 화합물이 개시되며, 상기 화합물은 하기로 이루어지는 군(군 2)에서 선택되는 구조를 가진다:
상기 화학식들에서,
m은 1 또는 2이고;
R1, R2, R4, 및 R5는 각각 독립적으로 일치환, 이치환, 삼치환 또는 사치환, 또는 비치환을 나타내며;
R3은 일치환, 이치환 또는 삼치환, 또는 비치환을 나타내고;
R6은 일치환 또는 비치환을 나타내며;
R1, R2, R3, R4, R5 및 R6는 각각 독립적으로 수소, 중수소, 알킬, 시클로알킬, 이의 부분 또는 완전 중수소화된 또는 불화된 변이체, 및 이의 조합으로 이루어지는 군에서 선택된다.
군 2에서 선택되는 구조를 갖는 화합물의 일부 실시양태에서, R1, R2, R3, R4, 및 R5는 각각 독립적으로 수소, 중수소, C1 내지 C6 알킬, C1 내지 C6 시클로알킬, 및 이의 부분 또는 완전 중수소화된 또는 불화된 변이체로 이루어지는 군에서 선택되며; R6은 7개 이상의 탄소 원자를 갖는 알킬, 7개 이상의 탄소 원자를 갖는 시클로알킬, 7개 이상의 탄소 원자를 갖는 알킬-시클로알킬, 및 이의 부분 또는 완전 중수소화된 또는 불화된 변이체로 이루어지는 군에서 선택된다.
군 2에서 선택되는 구조를 갖는 화합물의 일부 실시양태에서, m은 2이다.
군 2에서 선택되는 구조를 갖는 화합물의 일부 실시양태에서, R1, R2, R3, R4, 및 R5는 각각 독립적으로 수소, 중수소, 메틸, 에틸, 프로필, 이소프로필, 및 이의 조합으로 이루어지는 군에서 선택된다.
군 2에서 선택되는 구조를 갖는 화합물의 일부 실시양태에서, R6은 8개 이상의 탄소 원자를 갖는 알킬, 8개 이상의 탄소 원자를 갖는 시클로알킬, 8개 이상의 탄소 원자를 갖는 알킬-시클로알킬, 및 이의 부분 또는 완전 중수소화된 또는 불화된 변이체로 이루어지는 군에서 선택된다.
군 2에서 선택되는 구조를 갖는 화합물의 일부 실시양태에서, R3, R4, 및 R5는 각각 수소이다.
군 2에서 선택되는 구조를 갖는 화합물의 일부 실시양태에서, LA는 상기 열거한 LA1 내지 LA225로 이루어지는 군에서 선택된다.
군 2에서 선택되는 구조를 갖는 화합물의 일부 실시양태에서, LB는 LB1 내지 LB227로 이루어지는 군에서 선택된다. LB1 내지 LB227의 구조는 상기 도시되어 있다.
본 개시의 다른 양태에 따르면, 애노드; 캐소드; 및 애노드와 캐소드 사이에 배치된 유기층을 포함하는 OLED가 개시되며, 상기 유기층은 하기 화학식으로 이루어지는 군에서 선택되는 화학식을 갖는 화합물을 포함한다:
상기 화학식들에서, m은 1 또는 2이고;
리간드 LA, LB, 및 LC는 각각 독립적으로 하기로 이루어지는 군에서 선택되고:
각각의 X1 내지 X13은 독립적으로 탄소 및 질소로 이루어지는 군에서 선택되며;
X는 BR', NR', PR', O, S, Se, C=O, S=O, SO2, CR'R", SiR'R", 및 GeR'R"로 이루어지는 군에서 선택되고;
R' 및 R"은 임의로 융합 또는 결합되어 고리를 형성하며;
각각의 Ra, Rb, Rc, 및 Rd는 일치환 내지 가능한 최대수의 치환 또는 비치환을 나타낼 수 있고;
R', R", Ra, Rb, Rc, 및 Rd는 각각 독립적으로 수소, 중수소, 할라이드, 알킬, 시클로알킬, 헤테로알킬, 아릴알킬, 알콕시, 아릴옥시, 아미노, 실릴, 알케닐, 시클로알케닐, 헤테로알케닐, 알키닐, 아릴, 헤테로아릴, 아실, 카르보닐, 카르복실산, 에스테르, 니트릴, 이소니트릴, 설파닐, 설피닐, 설포닐, 포스피노, 및 이의 조합으로 이루어지는 군에서 선택되며;
Ra, Rb, Rc, 및 Rd 중 임의의 2개의 인접한 치환기는 임의로 융합 또는 결합되어 고리를 형성하거나 또는 다좌 리간드를 형성하고;
M은 40 초과의 원자 질량을 갖는 금속이며;
h는 1 또는 2이고;
y는 0, 1, 또는 2이며;
z는 0, 1, 또는 2이고;
x+y+z는 금속 M의 산화 상태이며;
M(LA)h(LB)y(LC)z의 분자는 0.67을 초과하는 배향 인자 값을 갖고;
R1, R2, R4, 및 R5는 각각 독립적으로 일치환, 이치환, 삼치환 또는 사치환, 또는 비치환을 나타내며;
R3은 일치환, 이치환 또는 삼치환, 또는 비치환을 나타내고;
R6은 일치환 또는 비치환을 나타내며;
R1, R2, R3, R4, R5 및 R6은 각각 독립적으로 수소, 중수소, 알킬, 시클로알킬, 이의 부분 또는 완전 중수소화된 또는 불화된 변이체, 및 이의 조합으로 이루어지는 군에서 선택된다.
일부 실시양태에서, OLED는 소비재, 전자 부품 모듈, 및 조명 패널로 이루어진 군에서 선택되는 소자 내에 도입된다.
OLED의 일부 실시양태에서, 유기층은 발광층이고 화합물은 발광 도펀트 또는 비발광 도펀트일 수 있다.
도 1에 도시된 소자 구조와 관련하여 논할 때, 유기층과 애노드 사이 및/또는 유기층과 캐소드 사이에 OLED의 다른 기능층들이 제공될 수 있다. 따라서, 구체적인 실시양태에 따라, 본 개시의 신규 화합물을 함유하는 유기층은 개재층 위에 또는 전극 기판 위에 직접 놓일 수 있다.
OLED의 일부 실시양태에서, 유기층은 호스트를 추가로 포함하고, 상기 호스트는 트리페닐렌을 함유하는 벤조융합 티오펜 또는 벤조융합 푸란을 포함하고; 호스트 중의 임의의 치환기는 독립적으로 CnH2n+1, OCnH2n+1, OAr1, N(CnH2n+1)2, N(Ar1)(Ar2), CH=CH-CnH2n+1, C≡CCnH2n+1, Ar1, Ar1-Ar2, CnH2n-Ar1으로 이루어지는 군에서 선택되는 비융합 치환기이거나 비치환이며; 여기서 n은 1∼10이고; Ar1 및 Ar2는 독립적으로 벤젠, 비페닐, 나프탈렌, 트리페닐렌, 카르바졸, 및 이의 헤테로방향족 유사체로 이루어지는 군에서 선택된다.
OLED의 일부 실시양태에서, 유기층은 호스트를 추가로 포함하고, 상기 호스트는 트리페닐렌, 카르바졸, 디벤조티오펜, 디벤조푸란, 디벤조셀레노펜, 아자트리페닐렌, 아자카르바졸, 아자-디벤조티오펜, 아자-디벤조푸란 및 아자-디벤조셀레노펜으로 이루어지는 군에서 선택된 하나 이상의 화학 기를 포함한다.
OLED의 일부 실시양태에서, 유기층은 호스트를 추가로 포함하고, 상기 호스트는 하기로 이루어지는 군에서 선택된다:
OLED의 일부 실시양태에서, 유기층은 호스트를 추가로 포함하고, 상기 호스트는 금속 착물을 포함한다.
일부 실시양태에서, 상기 화합물은 발광성 도펀트일 수 있다. 일부 실시양태에서, 상기 화합물은 인광, 형광, 열 활성화 지연 형광, 즉 TADF(E형 지연 형광으로도 지칭됨), 삼중항-삼중항 소멸, 또는 이들 과정의 조합을 통해 발광을 생성할 수 있다.
다른 양태에 따르면, 하기 화학식으로 이루어지는 군에서 선택되는 화학식을 갖는 화합물을 포함하는 제제가 개시된다:
상기 화학식에서,
m은 1 또는 2이고;
리간드 LA, LB, 및 LC는 각각 독립적으로 하기로 이루어지는 군에서 선택되고:
각각의 X1 내지 X13은 독립적으로 탄소 및 질소로 이루어지는 군에서 선택되며;
X는 BR', NR', PR', O, S, Se, C=O, S=O, SO2, CR'R", SiR'R", 및 GeR'R"로 이루어지는 군에서 선택되고;
R' 및 R"은 임의로 융합 또는 결합되어 고리를 형성하며;
각각의 Ra, Rb, Rc, 및 Rd는 일치환 내지 가능한 최대수의 치환 또는 비치환을 나타낼 수 있고;
R', R", Ra, Rb, Rc, 및 Rd는 각각 독립적으로 수소, 중수소, 할라이드, 알킬, 시클로알킬, 헤테로알킬, 아릴알킬, 알콕시, 아릴옥시, 아미노, 실릴, 알케닐, 시클로알케닐, 헤테로알케닐, 알키닐, 아릴, 헤테로아릴, 아실, 카르보닐, 카르복실산, 에스테르, 니트릴, 이소니트릴, 설파닐, 설피닐, 설포닐, 포스피노, 및 이의 조합으로 이루어지는 군에서 선택되며;
Ra, Rb, Rc, 및 Rd 중 임의의 2개의 인접한 치환기는 임의로 융합 또는 결합되어 고리를 형성하거나 또는 다좌 리간드를 형성하고;
M은 40 초과의 원자 질량을 갖는 금속이며;
h는 1 또는 2이고;
y는 0, 1, 또는 2이며;
z는 0, 1, 또는 2이고;
x+y+z는 금속 M의 산화 상태이며;
M(LA)h(LB)y(LC)z의 분자는 0.67을 초과하는 배향 인자 값을 갖고;
R1, R2, R4, 및 R5는 각각 독립적으로 일치환, 이치환, 삼치환 또는 사치환, 또는 비치환을 나타내며;
R3은 일치환, 이치환 또는 삼치환, 또는 비치환을 나타내고;
R6은 일치환 또는 비치환을 나타내며;
R1, R2, R3, R4, R5 및 R6은 각각 독립적으로 수소, 중수소, 알킬, 시클로알킬, 이의 부분 또는 완전 중수소화된 또는 불화된 변이체, 및 이의 조합으로 이루어지는 군에서 선택된다.
본원에 개시된 OLED는 소비재, 전자 부품 모듈, 및 조명 패널 중 1 이상에 도입될 수 있다. 일부 실시양태에서 상기 유기층은 발광층일 수 있고, 상기 화합물은 발광성 도펀트일 수 있으며, 다른 실시양태에서 상기 화합물은 비발광성 도펀트일 수 있다.
유기층은 또한 호스트를 포함할 수 있다. 일부 실시양태에서는, 2 이상의 호스트가 바람직하다. 일부 실시양태에서, 호스트는 a) 바이폴라, b) 전자 수송, c) 정공 수송 또는 전하 수송에서의 역할이 거의 없는 d) 와이드 밴드 갭 물질일 수 있다. 일부 실시양태에서, 호스트는 금속 착물을 포함할 수 있다. 상기 호스트는 트리페닐렌 함유 벤조 융합된 티오펜 또는 벤조 융합된 푸란일 수 있다. 호스트 내 임의의 치환기는 독립적으로 CnH2n+1, OCnH2n+1, OAr1, N(CnH2n+1)2, N(Ar1)(Ar2), CH=CH-CnH2n+1, C≡CCnH2n+1, Ar1, Ar1-Ar2 및 CnH2n-Ar1로 이루어진 군에서 선택되는 비융합 치환기일 수 있거나, 또는 비치환일 수 있다. 상기 치환기에서, n은 1∼10 범위일 수 있고; Ar1 및 Ar2는 독립적으로 벤젠, 비페닐, 나프탈렌, 트리페닐렌, 카르바졸 및 이의 헤테로방향족 유사체로 이루어진 군에서 선택될 수 있다. 호스트는 무기 화합물일 수 있다. 예를 들어 Zn 함유 무기 물질, 예컨대 ZnS일 수 있다.
상기 호스트는 트리페닐렌, 카르바졸, 디벤조티오펜, 디벤조푸란, 디벤조셀레노펜, 아자트리페닐렌, 아자카르바졸, 아자-디벤조티오펜, 아자-디벤조푸란 및 아자-디벤조셀레노펜으로 이루어진 군에서 선택되는 1 이상의 화학적 기를 포함하는 화합물일 수 있다. 상기 호스트는 금속 착물을 포함할 수 있다. 상기 호스트는 하기로 이루어진 군에서 선택되는 특정 화합물일 수 있으나 이에 한정되지 않는다:
및 이의 조합.
가능한 호스트에 대한 추가의 정보를 이하에 제공한다.
본 개시의 또 다른 양태에서는, 화학식 I에 따른 화합물을 포함하는 제제가 개시된다. 상기 제제는 본 명세서에 개시된 용매, 호스트, 정공 주입 물질, 정공 수송 물질, 및 전자 수송층 물질로 이루어진 군에서 선택되는 1 이상의 성분을 포함할 수 있다.
다른 물질과의 조합
유기 발광 소자에서 특정 층에 대하여 유용한 것으로 본원에 기재된 물질은 소자에 존재하는 다양한 기타의 물질과의 조합에 사용될 수 있다. 예를 들면, 본원에 개시된 발광 도펀트는 호스트, 수송층, 차단층, 주입층, 전극 및 존재할 수 있는 기타의 층과 결합되어 사용될 수 있다. 하기에 기재되거나 또는 지칭된 물질은 본원에 개시된 화합물과 조합하여 유용할 수 있는 비제한적인 물질이며, 당업자는 조합에 유용할 수 있는 기타의 물질을 확인하는 문헌을 용이하게 참조할 수 있다.
전도성(Conductivity) 도펀트:
전하 수송층은 전도성 도펀트로 도핑되어 전하 캐리어의 밀도를 실질적으로 변경시킬 수 있고, 이는 이의 전도성을 변경할 것이다. 전도성은 매트릭스 재료에서 전하 캐리어를 생성함으로써 증가되고, 도펀트의 종류에 따라, 반도체의 페르미 준위에 있어 변화가 또한 달성될 수 있다. 정공 수송층은 p형 전도성 도펀트에 의해 도핑될 수 있고 n형 전도성 도펀트는 전자 수송층에 사용된다.
본원에 개시된 재료와 함께 OLED에 사용될 수 있는 전도성 도펀트의 비제한적인 예는 이들 재료를 개시하는 참고문헌들과 함께 이하에서 예시된다: EP01617493, EP01968131, EP2020694, EP2684932, US20050139810, US20070160905, US20090167167, US2010288362, WO06081780, WO2009003455, WO2009008277, WO2009011327, WO2014009310, US2007252140, US2015060804 및 US2012146012.
HIL/HTL:
본 발명에서 사용하고자 하는 정공 주입/수송 물질은 특정하게 한정되지 않으며, 화합물이 정공 주입/수송 물질로서 사용되는 한 임의의 화합물을 사용할 수 있다. 물질의 비제한적인 예로는 프탈로시아닌 또는 포르피린 유도체; 방향족 아민 유도체; 인돌로카르바졸 유도체; 플루오로탄화수소를 포함하는 중합체; 전도성 도펀트를 갖는 중합체; 전도성 중합체, 예컨대 PEDOT/PSS; 포스폰산 및 실란 유도체와 같은 화합물로부터 유도된 자체조립 단량체; 금속 산화물 유도체, 예컨대 MoOx; p-형 반도체 유기 화합물, 예컨대 1,4,5,8,9,12-헥사아자트리페닐렌헥사카르보니트릴; 금속 착물 및 가교성 화합물을 들 수 있다.
HIL 또는 HTL에 사용된 방향족 아민 유도체의 비제한적인 예로는 하기 화학식을 들 수 있다:
각각의 Ar1 내지 Ar9는 벤젠, 비페닐, 트리페닐, 트리페닐렌, 나프탈렌, 안트라센, 페날렌, 페난트렌, 플루오렌, 피렌, 크리센, 페릴렌, 아줄렌과 같은 방향족 탄화수소 고리형 화합물로 이루어진 군; 디벤조티오펜, 디벤조푸란, 디벤조셀레노펜, 푸란, 티오펜, 벤조푸란, 벤조티오펜, 벤조셀레노펜, 카르바졸, 인돌로카르바졸, 피리딜인돌, 피롤로디피리딘, 피라졸, 이미다졸, 트리아졸, 옥사졸, 티아졸, 옥사디아졸, 옥사트리아졸, 디옥사졸, 티아디아졸, 피리딘, 피리다진, 피리미딘, 피라진, 트리아진, 옥사진, 옥사티아진, 옥사디아진, 인돌, 벤즈이미다졸, 인다졸, 인독사진, 벤족사졸, 벤즈이속사졸, 벤조티아졸, 퀴놀린, 이소퀴놀린, 시놀린, 퀴나졸린, 퀴녹살린, 나프티리딘, 프탈라진, 프테리딘, 크산텐, 아크리딘, 페나진, 페노티아진, 펜옥사진, 벤조푸로피리딘, 푸로디피리딘, 벤조티에노피리딘, 티에노디피리딘, 벤조셀레노페노피리딘 및 셀레노페노디피리딘과 같은 방향족 헤테로시클릭 화합물로 이루어진 군; 및 방향족 탄화수소 고리형 기 및 방향족 헤테로시클릭 기로부터 선택된 동일한 유형 또는 상이한 유형의 군이며 산소 원자, 질소 원자, 황 원자, 규소 원자, 인 원자, 붕소 원자, 쇄 구조 단위 및 지방족 고리형 기에 서로 직접 또는 이들 중 1종 이상을 통하여 결합되는 2 내지 10개의 고리형 구조 단위로 이루어진 군으로부터 선택된다. 각각의 Ar은 중수소, 할라이드, 알킬, 시클로알킬, 헤테로알킬, 아릴알킬, 알콕시, 아릴옥시, 아미노, 실릴, 알케닐, 시클로알케닐, 헤테로알케닐, 알키닐, 아릴, 헤테로아릴, 아실, 카르보닐, 카르복실산, 에스테르, 니트릴, 이소니트릴, 설파닐, 술피닐, 술포닐, 포스피노 및 이의 조합으로 이루어진 군으로부터 선택된 치환기로 치환되거나 또는 비치환될 수 있다.
하나의 실시양태에서, Ar1 내지 Ar9는 독립적으로 하기로 이루어진 군으로부터 선택되며:
k는 1 내지 20의 정수이며; X101 내지 X108은 C(CH 포함) 또는 N이고; Z101은 NAr1, O 또는 S이고; Ar1은 상기 정의된 바와 동일한 기를 갖는다.
HIL 또는 HTL에 사용된 금속 착물의 비제한적인 예는 하기를 들 수 있다:
Met는 40 초과의 원자량을 가질 수 있는 금속이며; (Y101-Y102)는 2좌 리간드이고, Y101 및 Y102는 독립적으로 C, N, O, P 및 S로부터 선택되며; L101은 보조 리간드이며; k'는 1 내지 금속에 결합될 수 있는 리간드 최대수의 정수값이고; k'+k"는 금속에 결합될 수 있는 리간드 최대수이다.
일 양태에서, (Y101-Y102)는 2-페닐피리딘 유도체이다. 다른 양태에서, (Y101-Y102)는 카르벤 리간드이다. 다른 양태에서, Met은 Ir, Pt, Os 및 Zn으로부터 선택된다. 추가의 양태에서, 금속 착물은 약 0.6 V 미만의 용액중의 최소 산화 전위 대 Fc+/Fc 커플을 갖는다.
본원에 개시된 재료와 함께 OLED에 사용될 수 있는 HIL 및 HTL 재료의 비제한적인 예는 이들 재료를 개시하는 참고문헌과 함께 이하에 예시된다: CN102702075, DE102012005215, EP01624500, EP01698613, EP01806334, EP01930964, EP01972613, EP01997799, EP02011790, EP02055700, EP02055701, EP1725079, EP2085382, EP2660300, EP650955, JP07-073529, JP2005112765, JP2007091719, JP2008021687, JP2014-009196, KR20110088898, KR20130077473, TW201139402, US06517957, US20020158242, US20030162053, US20050123751, US20060182993, US20060240279, US20070145888, US20070181874, US20070278938, US20080014464, US20080091025, US20080106190, US20080124572, US20080145707, US20080220265, US20080233434, US20080303417, US2008107919, US20090115320, US20090167161, US2009066235, US2011007385, US20110163302, US2011240968, US2011278551, US2012205642, US2013241401, US20140117329, US2014183517, US5061569, US5639914, WO05075451, WO07125714, WO08023550, WO08023759, WO2009145016, WO2010061824, WO2011075644, WO2012177006, WO2013018530, WO2013039073, WO2013087142, WO2013118812, WO2013120577, WO2013157367, WO2013175747, WO2014002873, WO2014015935, WO2014015937, WO2014030872, WO2014030921, WO2014034791, WO2014104514, WO2014157018,
EBL:
전자 차단층(EBL)은 발광층을 떠나는 전자 및/또는 엑시톤의 수를 감소시키기 위해 사용될 수 있다. 소자 내의 이러한 차단층의 존재는 차단층이 없는 유사한 소자와 비교했을 때 실질적으로 더 높은 효율 및/또는 더 긴 수명을 유도할 수 있다. 또한, 차단층은 OLED의 원하는 영역에 발광을 국한시키기 위해 사용될 수 있다. 일부 실시양태들에서, EBL 재료는 EBL 계면에 가장 가까운 이미터보다 더 높은 LUMO(진공 수준에 보다 가까움) 및/또는 보다 높은 삼중항 에너지를 갖는다. 일부 실시양태들에서, EBL 재료는 EBL 계면에 가장 가까운 호스트들 중 하나 이상보다 더 높은 LUMO(진공 수준에 보다 가까움) 및/또는 보다 높은 삼중항 에너지를 갖는다. 일 양태에서, EBL에 사용되는 화합물은 이하에 기재된 호스트들 중 하나로서 사용되는 동일한 분자 또는 동일한 작용기를 함유한다.
호스트:
본 발명의 유기 EL 소자의 발광층은 바람직하게는 발광 물질로서 적어도 금속 착물을 포함하며, 도펀트 물질로서 금속 착물을 사용하는 호스트 물질을 포함할 수 있다. 호스트 물질의 예로는 특정하여 한정되지는 않았으나, 임의의 금속 착물 또는 유기 화합물은 호스트의 삼중항 에너지가 도펀트의 것보다 더 크기만 하다면 사용할 수 있다. 삼중항 기준을 충족하는 한, 임의의 호스트 물질은 임의의 도펀트와 함께 사용될 수 있다.
호스트로서 사용된 금속 착물의 예는 하기 화학식을 갖는 것이 바람직하다:
Met는 금속이고; (Y103-Y104)는 2좌 리간드이고, Y103 및 Y104는 독립적으로 C, N, O, P 및 S로부터 선택되며; L101은 또 다른 리간드이며; k'는 1 내지 금속이 결합될 수 있는 리간드 최대수의 정수값이고; k'+k"는 금속에 결합될 수 있는 리간드 최대수이다.
(O-N)은 원자 O 및 N에 배위결합된 금속을 갖는 2좌 리간드이다.
또 다른 양태에서, Met는 Ir 및 Pt로부터 선택된다. 추가의 양태에서, (Y103-Y104)는 카르벤 리간드이다.
호스트로서 사용된 유기 화합물의 예는 방향족 탄화수소 고리형 화합물, 예컨대 벤젠, 비페닐, 트리페닐, 트리페닐렌, 나프탈렌, 안트라센, 페날렌, 페난트렌, 플루오렌, 피렌, 크리센, 페릴렌, 아줄렌으로 이루어진 군; 방향족 헤테로시클릭 화합물, 예컨대 디벤조티오펜, 디벤조푸란, 디벤조셀레노펜, 푸란, 티오펜, 벤조푸란, 벤조티오펜, 벤조셀레노펜, 카르바졸, 인돌로카르바졸, 피리딜인돌, 피롤로디피리딘, 피라졸, 이미다졸, 트리아졸, 옥사졸, 티아졸, 옥사디아졸, 옥사트리아졸, 디옥사졸, 티아디아졸, 피리딘, 피리다진, 피리미딘, 피라진, 트리아진, 옥사진, 옥사티아진, 옥사디아진, 인돌, 벤즈이미다졸, 인다졸, 인독사진, 벤족사졸, 벤즈이속사졸, 벤조티아졸, 퀴놀린, 이소퀴놀린, 신놀린, 퀴나졸린, 퀴녹살린, 나프티리딘, 프탈라진, 프테리딘, 크산텐, 아크리딘, 페나진, 페노티아진, 펜옥사진, 벤조푸로피리딘, 푸로디피리딘, 벤조티에노피리딘, 티에노디피리딘, 벤조셀레노페노피리딘 및 셀레노페노디피리딘으로 이루어진 군; 및 방향족 탄화수소 고리형 기 및 방향족 헤테로시클릭 기로부터 선택된 동일한 유형 또는 상이한 유형의 기이며 그리고 서로 직접 결합되거나 또는 산소 원자, 질소 원자, 황 원자, 규소 원자, 인 원자, 붕소 원자, 쇄 구조 단위 및 지방족 고리형 기 중 1종 이상에 의하여 결합되는 2 내지 10개의 고리형 구조 단위로 이루어진 군으로부터 선택된다. 여기서 각각의 기에서의 옵션은 중수소, 할라이드, 알킬, 시클로알킬, 헤테로알킬, 아릴알킬, 알콕시, 아릴옥시, 아미노, 실릴, 알케닐, 시클로알케닐, 헤테로알케닐, 알키닐, 아릴, 헤테로아릴, 아실, 카르보닐, 카르복실산, 에스테르, 니트릴, 이소니트릴, 설파닐, 술피닐, 술포닐, 포스피노 및 이의 조합으로 이루어진 군으로부터 선택된 치환기로 치환되거나 또는 비치환될 수 있다.
일 양태에서, 호스트 화합물은 분자에서 하기 기 중 1종 이상을 포함한다:
R101 내지 R107 각각은 수소, 중수소, 할로겐, 알킬, 시클로알킬, 헤테로알킬, 아릴알킬, 알콕시, 아릴옥시, 아미노, 실릴, 알케닐, 시클로알케닐, 헤테로알케닐, 알키닐, 아릴, 헤테로아릴, 아실, 카르보닐, 카르복실산, 에스테르, 니트릴, 이소니트릴, 설파닐, 술피닐, 술포닐, 포스피노 및 이의 조합으로 이루어진 군으로부터 독립적으로 선택되며, 아릴 또는 헤테로아릴인 경우, 전술한 Ar과 유사한 정의를 갖는다. k는 0 내지 20 또는 1 내지 20의 정수이며; k"'는 0 내지 20의 정수이다. X101 내지 X108는 C(CH 포함) 또는 N으로부터 선택된다.
Z101 및 Z102는 NR101, O 또는 S로부터 선택된다.
본원에 개시된 재료와 함께 OLED에 사용될 수 있는 호스트 재료의 비제한적인 예는 이들 재료를 개시하는 참고문헌과 함께 이하에 예시된다: EP2034538, EP2034538A, EP2757608, JP2007254297, KR20100079458, KR20120088644, KR20120129733, KR20130115564, TW201329200, US20030175553, US20050238919, US20060280965, US20090017330, US20090030202, US20090167162, US20090302743, US20090309488, US20100012931, US20100084966, US20100187984, US2010187984, US2012075273, US2012126221, US2013009543, US2013105787, US2013175519, US2014001446, US20140183503, US20140225088, US2014034914, US7154114, WO2001039234, WO2004093207, WO2005014551, WO2005089025, WO2006072002, WO2006114966, WO2007063754, WO2008056746, WO2009003898, WO2009021126, WO2009063833, WO2009066778, WO2009066779, WO2009086028, WO2010056066, WO2010107244, WO2011081423, WO2011081431, WO2011086863, WO2012128298, WO2012133644, WO2012133649, WO2013024872, WO2013035275, WO2013081315, WO2013191404, WO2014142472,
추가의 이미터:
하나 이상의 추가의 이미터 도펀트는 본 개시의 화합물과 함께 사용될 수 있다. 추가의 이미터 도펀트의 예는 특별히 한정되지 않으며, 이미터 재료로서 전형적으로 사용되는 한 임의의 화합물이 사용될 수 있다. 적합한 이미터 재료의 예는 인광, 형광, 열 활성화 지연 형광, 즉, TADF(E형 지연 형광이라고도 함), 삼중항-삼중항 소멸, 또는 이들 프로세스의 조합에 의해 발광을 일으킬 수 있는 화합물을 포함하지만 이에 한정되지 않는다.
본원에 개시된 재료와 함께 OLED에 사용될 수 있는 이미터 재료의 비제한적인 예는 이들 재료를 개시하는 참고문헌과 함께 이하에 예시된다: CN103694277, CN1696137, EB01238981, EP01239526, EP01961743, EP1239526, EP1244155, EP1642951, EP1647554, EP1841834, EP1841834B, EP2062907, EP2730583, JP2012074444, JP2013110263, JP4478555, KR1020090133652, KR20120032054, KR20130043460, TW201332980, US06699599, US06916554, US20010019782, US20020034656, US20030068526, US20030072964, US20030138657, US20050123788, US20050244673, US2005123791, US2005260449, US20060008670, US20060065890, US20060127696, US20060134459, US20060134462, US20060202194, US20060251923, US20070034863, US20070087321, US20070103060, US20070111026, US20070190359, US20070231600, US2007034863, US2007104979, US2007104980, US2007138437, US2007224450, US2007278936, US20080020237, US20080233410, US20080261076, US20080297033, US200805851, US2008161567, US2008210930, US20090039776, US20090108737, US20090115322, US20090179555, US2009085476, US2009104472, US20100090591, US20100148663, US20100244004, US20100295032, US2010102716, US2010105902, US2010244004, US2010270916, US20110057559, US20110108822, US20110204333, US2011215710, US2011227049, US2011285275, US2012292601, US20130146848, US2013033172, US2013165653, US2013181190, US2013334521, US20140246656, US2014103305, US6303238, US6413656, US6653654, US6670645, US6687266, US6835469, US6921915, US7279704, US7332232, US7378162, US7534505, US7675228, US7728137, US7740957, US7759489, US7951947, US8067099, US8592586, US8871361, WO06081973, WO06121811, WO07018067, WO07108362, WO07115970, WO07115981, WO08035571, WO2002015645, WO2003040257, WO2005019373, WO2006056418, WO2008054584, WO2008078800, WO2008096609, WO2008101842, WO2009000673, WO2009050281, WO2009100991, WO2010028151, WO2010054731, WO2010086089, WO2010118029, WO2011044988, WO2011051404, WO2011107491, WO2012020327, WO2012163471, WO2013094620, WO2013107487, WO2013174471, WO2014007565, WO2014008982, WO2014023377, WO2014024131, WO2014031977, WO2014038456, WO2014112450.
HBL:
정공 차단층(HBL)은 발광층을 떠나는 정공 및/또는 엑시톤의 수를 감소시키는데 사용될 수 있다. 소자 내 이러한 차단층의 존재는 차단층이 결여된 유사한 소자에 비하여 실질적으로 더 높은 효율 및/또는 더 긴 수명을 나타낼 수 있다. 또한, 차단층은 OLED의 원하는 부위로 방출을 국한시키는데 사용될 수 있다. 일부 실시양태들에서, HBL 재료는 HBL 계면에 가장 가까운 이미터보다 더 낮은 HOMO(진공 수준으로부터 보다 먼) 및/또는 보다 높은 삼중항 에너지를 갖는다. 일부 실시양태들에서, HBL 재료는 HBL 계면에 가장 가까운 호스트들 중 하나 이상보다 더 낮은 HOMO(진공 수준으로부터 보다 먼) 및/또는 보다 높은 삼중항 에너지를 갖는다.
한 양태에서, HBL에 사용된 화합물은 전술한 호스트로서 사용된 동일한 작용기 또는 동일한 분자를 포함한다.
또 다른 양태에서, HBL에 사용된 화합물은 분자에서 하기의 기 중 1종 이상을 포함한다:
k는 1 내지 20의 정수이고; L101은 또 다른 리간드이고, k'은 1 내지 3의 정수이다.
ETL:
전자 수송층(ETL)은 전자를 수송할 수 있는 물질을 포함할 수 있다. 전자 수송층은 고유하거나(도핑되지 않음) 또는 도핑될 수 있다. 도핑은 전도율을 향상시키는데 사용될 수 있다. ETL 물질의 예는 특정하게 한정되지는 않았으며, 임의의 금속 착물 또는 유기 화합물은 통상적으로 전자를 수송하는데 사용되는 한 사용될 수 있다.
한 양태에서, ETL에 사용되는 화합물은 분자에서 하기 기 중 1종 이상을 포함한다:
R101은 수소, 중수소, 할라이드, 알킬, 시클로알킬, 헤테로알킬, 아릴알킬, 알콕시, 아릴옥시, 아미노, 실릴, 알케닐, 시클로알케닐, 헤테로알케닐, 알키닐, 아릴, 헤테로아릴, 아실, 카르보닐, 카르복실산, 에스테르, 니트릴, 이소니트릴, 설파닐, 술피닐, 술포닐, 포스피노 및 이의 조합으로 이루어진 군으로부터 선택되며, 아릴 또는 헤테로아릴인 경우, 전술한 Ar과 유사한 정의를 갖는다. Ar1 내지 Ar3은 전술한 Ar과 유사한 정의를 갖는다. k는 1 내지 20의 정수이다. X101 내지 X108은 C(CH 포함) 또는 N으로부터 선택된다.
다른 양태에서, ETL에 사용된 금속 착물은 하기의 화학식을 포함하지만, 이에 한정되는 것은 아니다:
(O-N) 또는 (N-N)은 원자 O, N 또는 N,N에 배위결합된 금속을 갖는 2좌 리간드이며; L101은 또 다른 리간드이며; k'는 1 내지 금속에 결합될 수 있는 리간드 최대수의 정수값이다.
본원에 개시된 재료와 함께 OLED에 사용될 수 있는 ETL 재료의 비제한적인 예는 이들 재료를 개시하는 참고문헌과 함께 이하에 예시된다: CN103508940, EP01602648, EP01734038, EP01956007, JP2004-022334, JP2005149918, JP2005-268199, KR0117693, KR20130108183, US20040036077, US20070104977, US2007018155, US20090101870, US20090115316, US20090140637, US20090179554, US2009218940, US2010108990, US2011156017, US2011210320, US2012193612, US2012214993, US2014014925, US2014014927, US20140284580, US6656612, US8415031, WO2003060956, WO2007111263, WO2009148269, WO2010067894, WO2010072300, WO2011074770, WO2011105373, WO2013079217, WO2013145667, WO2013180376, WO2014104499, WO2014104535,
전하 생성층(CGL)
탠덤 또는 스택된 OLED에서, CGL은 성능에 있어 필수적인 역할을 수행하며, 이는 전자 및 정공 각각의 주입을 위한 n-도핑 층 및 p-도핑 층으로 구성된다. 전자 및 정공은 CGL 및 전극으로부터 공급된다. CGL에서 소비된 전자 및 정공은 캐소드 및 애노드 각각으로부터 주입되는 전자 및 정공에 의해 재충전되고, 이후에, 양극성 전류가 점진적으로 정류 상태에 도달한다. 전형적인 CGL 재료는 수송층들에 사용되는 n 및 p 전도성 도펀트를 포함한다.
OLED 소자의 각 층에 사용되는 임의의 상기 언급된 화합물에서, 수소 원자가 부분적으로 또는 완전히 중수소화될 수 있다. 이에, 메틸, 페닐, 피리딜 등(제한되지 않음)과 같은 임의의 구체적으로 나열된 치환기가 이의 중수소화되지 않은, 부분적으로 중수소화된, 및 완전히 중수소화된 버전일 수 있다. 마찬가지로, 알킬, 아릴, 시클로알킬, 헤테로아릴, 등(제한없이)과 같은 부류의 치환기가 또한 이의 중수소화되지 않은, 부분적으로 중수소화된, 및 완전히 중수소화된 버전일 수 있다.
실험
합성 실시예
1. Comp (LA1)2Ir(LB227)의 합성
500 mL의 둥근 바닥 플라스크에, 1-브로모-4-클로로벤젠(9.60 g, 50.1 mmol), 2-페닐-4-(4,4,5,5-테트라메틸-1,3,2-디옥사보롤란-2-일)피리딘(11.75 g, 41.8 mmol), Pd(PPh3)4(2.415 g, 2.090 mmol), 탄산나트륨(13.29 g, 125 mmol), DME(200 mL) 및 물(100 mL)을 첨가하고 밤새 환류시켰다. 반응 혼합물을 워크업 처리하고 정제하여 9.1 g의 원하는 생성물(수율 89%)을 얻었다. GC 및 NMR로 원하는 생성물을 확인하였다.
500 mL의 둥근 바닥 플라스크에, 네오펜틸보론산(5.0 g, 43.1 mmol), 디시클로헥실(2',6'-디메톡시-[1,1'-비페닐]-2-일)포스판(SPhos)(1.112 g, 2.71 mmol), Pd2(dba)3(0.620 g, 0.677 mmol), 인산칼륨(21.57 g, 102 mmol), 물(25 ml), 및 톨루엔(250 ml)을 첨가하였다. 15분 동안 질소 중에서 버블링함으로써 반응 혼합물을 탈기한 다음 오일조에서 가열하고 24 시간 동안 환류시켰다. 반응을 냉각시키고 실리카 칼럼 크로마토그래프로 정제하여 8.0 g의 원하는 생성물(78.3% 수율)을 얻었다.
이 중수소화 반응을 Tetrahedron 71(2015)1425-1430에 공개된 문헌상의 절차에 기초하여 행하였다.
100 mL의 둥근 바닥 플라스크에, 이리듐 전구체(1.7 g, 2.38 mmol), 4-(4-(2,2-디메틸프로필-11-d2)페닐)피리딘(1.8 g , 5.93 mmol), 에탄올(25 mL) 및 메탄올(25 mL)을 첨가하고 오일조에서 질소하에 가열하고 2일 동안 80℃에서 환류시켰다. 반응 혼합물을 실리카 칼럼 크로마토그래프로 정제하여 0.9 g(47% 수율)의 원하는 생성물을 얻었고 이것은 LC-MS 및 NMR로 확인되었다.
2. Comp (LA147)2Ir(LB184)의 합성
100 mL의 플라스크에, 이리듐 전구체(2.5 g, 3.20 mmol), 4-(4-(메틸-d3)페닐)-2-페닐피리딘(2.382 g, 9.59 mmol), 에탄올(25 mL), 및 메탄올(25 mL)을 첨가하였다. 반응 혼합물을 오일조 내에서 질소하에 가열하고 15 시간 동안 80℃에서 환류시켰다. 반응을 실온까지 냉각되게 두고 고체를 여과하고, 메탄올로 세정하고 건조시켰다. 황색 고체를 실리카 칼럼 크로마토그래프로 더 정제하여 1.25 g의 생성물(수율 48.9%)을 얻었고 이것은 LC-MS 및 NMR로 확인되었다.
3. Comp (LA147)2Ir(LB86)의 합성
500 mL의 둥근 바닥 플라스크에, 이리듐 전구체(2 g, 2.56 mmol), 4-(4-((1S,2S,4R)-비시클로[2.2.1]헵탄-2-일-2-d)페닐)-2-페닐피리딘(2.104 g, 6.45 mmol), 에탄올(40 mL) 및 메탄올(40 mL)을 첨가하고 23 시간 동안 80℃에서 환류시켰다. 반응 혼합물을 냉각시키고 여과하였다. 수거한 황색 고체에 실리카 칼럼 크로마토그래프를 행하여 원하는 생성물(0.61g, 26% 수율)을 얻었다.
4. Comp (LA147)2Ir(LB109)의 합성
100 mL의 플라스크에 1-페닐아다만탄(2 g, 9.42 mmol), CCl4(40 mL), 디브로민(19.40 mL, 377 mmol)을 넣고, 밤새 교반하고 빛으로부터 보호하였다. 반응 혼합물을 서서히 빙수에 붓고 티오황산나트륨으로 켄칭하였다. 반응 혼합물을 에틸 아세테이트로 추출하였다. 유기 부분을 증발시켜 원하는 생성물(2.74 g, 100%)을 얻었다.
250 mL의 플라스크에 1-(4-브로모페닐)아다만탄(2.76 g, 9.48 mmol), 2-페닐-4-(4,4,5,5-테트라메틸-1,3,2-디옥사보롤란-2-일)피리딘(4.00 g, 14.22 mmol), 디아세톡시팔라듐(0.064 g, 0.284 mmol), 디시클로헥실(2',6'-디메톡시-[1,1'-비페닐]-2-일)포스판(SPhos)(0.233 g, 0.569 mmol), K3PO4(4.02 g, 18.95 mmol), 톨루엔(30 mL) 및 물(3 mL)을 넣었다. 반응 혼합물을 밤새 100℃로 가열하고 EtOAc로 수성 워크업 처리하였다. 유기 부분을 합하고 칼럼 크로마토그래피를 행하여 원하는 생성물(2.46 g, 71%)을 얻었다.
500 mL의 플라스크에 이리듐 전구체(2.0 g, 2.56 mmol), 4-(4-(아다만탄-1-일)페닐)-2-페닐피리딘(2.10 g, 5.75 mmol), 에탄올(25 mL) 및 메탄올(25 mL)을 넣었다. 반응 혼합물을 5일 동안 80℃로 가열하였다. 반응 혼합물을 여과하고 수거한 침전물에 칼럼 크로마토그래피를 행하여 원하는 생성물(0.74 g, 31%)을 얻었다. NMR 및 LC-MS로 원하는 생성물을 확인하였다.
5. Comp (LA147)2Ir(LB88)의 합성
100 mL의 플라스크에 (니트로옥시)은(0.137 g, 0.805 mmol)을 넣고, 100 mL의 무수 에테르, (1R,2S,4S)-2-브로모비시클로[2.2.1]헵탄(3.45 mL, 26.8 mmol)을 첨가한 후, (4-클로로벤질)마그네슘 클로라이드(2-MeTHF 중 0.5 M 용액, 77 mL, 38.5 mmol)를 20분 동안 적하 방식으로 첨가 깔대기를 통해 첨가하였다. 반응 혼합물을 실온에서 밤새 교반하였다. 반응 혼합물을 물로 희석하고 에테르로 추출하였다. 유기 부분을 합하고 칼럼 크로마토그래피를 행하여 원하는 생성물(2.48 g, 41%)을 얻었다.
250 mL의 플라스크에 (1R,2R,4S)-2-(4-클로로벤질)비시클로[2.2.1]헵탄(2.48 g, 11.23 mmol), 2-페닐-4-(4,4,5,5-테트라메틸-1,3,2-디옥사보롤란-2-일)피리딘(4.11 g, 14.61 mmol), 디아세톡시팔라듐(0.076 g, 0.337 mmol), 디시클로헥실(2',6'-디메톡시-[1,1'-비페닐]-2-일)포스판(SPhos)(0.277 g, 0.674 mmol), K3PO4(4.77 g, 22.47 mmol), 톨루엔(30 mL) 및 물(3.00 mL)을 넣었다. 반응 혼합물을 밤새 105℃로 가열하였다. 반응 혼합물을 수성 워크업 처리하고 에틸 아세테이트로 추출하였다. 유기 부분을 합하고 실리카 칼럼 크로마토그래프를 행하여 순수한 생성물(3.69 g, 97%)을 얻었다.
Tetrahedron 71(2015)1425-1430에 공개된 문헌상의 절차에 기초하여 중수소화 반응을 행하였다.
500 mL의 둥근 바닥 플라스크에 이리듐 전구체(2.8 g, 3.58 mmol), 4-(4-(((1R,2S,4S)-비시클로[2.2.1]헵탄-2-일)메틸-d2)페닐)-2-페닐피리딘(2.446 g, 7.16 mmol), 에탄올(25 mL) 및 MeOH(25 mL)를 넣었다. 반응 혼합물을 4일 동안 80℃로 가열하였다. 반응 혼합물을 여과하고 침전물을 수거하고 실리카 칼럼 크로마토그래프로 정제하여 원하는 생성물(1 g, 30.7%)을 얻었다.
6. Comp (LA147)2Ir(LB225)의 합성
500 mL의 플라스크에 2-(4-브로모페닐)-4,4,5,5-테트라메틸-1,3,2-디옥사보롤란(10.5 g, 37.1 mmol), 디시클로헥실(2',6'-디메톡시-[1,1'-비페닐]-2-일)포스판(SPhos)(0.914 g, 2.226 mmol), 및 디아세톡시팔라듐(0.250 g, 1.113 mmol)을 넣었다. (시클로펜틸메틸)아연(II) 클로라이드(20.48 g, 111 mmol) 용액을 캐뉼러를 통해 반응 플라스크로 옮겼다. 반응 혼합물을 실온에서 밤새 교반하였다. 반응 혼합물을 포화 염화암모늄 용액으로 희석하고 에틸 아세테이트로 추출하였다. 유기 부분을 합하고 실리카 칼럼 크로마토그래프를 행하여 원하는 생성물(7.10 g, 67%)을 얻었다.
250 mL의 플라스크에 4-클로로-2-페닐피리딘(3.92 g, 20.67 mmol), 2-(4-(시클로펜틸메틸)페닐)-4,4,5,5-테트라메틸-1,3,2-디옥사보롤란(7.10 g, 24.80 mmol), Pd2(dba)3(0.379 g, 0.413 mmol), 디시클로헥실(2',6'-디메톡시-[1,1'-비페닐]-2-일)포스판(SPhos)(0.679 g, 1.654 mmol), K3PO4(13.16 g, 62.0 mmol), 톨루엔(70 mL) 및 물(7.0 mL)을 넣었다. 반응을 밤새 100℃로 가열하였다. 반응 혼합물을 수성 워크업 처리하고 EtOAc로 추출하였다. 유기 부분을 합하고 칼럼 크로마토그래프를 행하여 생성물(5.71 g, 88%)을 얻었다.
Tetrahedron 71(2015)1425-1430에 공개된 문헌상의 절차에 기초하여 중수소화 반응을 행하였다.
100 mL의 둥근 바닥 플라스크에 이리듐 전구체(2.22 g, 2.84 mmol), 4-(4-(시클로펜틸메틸-d2)페닐)-2-페닐피리딘(1.791 g, 5.68 mmol), 에탄올(25 mL) 및 MeOH(25.00 mL)를 넣었다. 반응 혼합물을 5일 동안 68℃로 가열하였다. 반응 혼합물을 여과하고 수거한 침전물에 칼럼 크로마토그래피를 행하여 원하는 생성물(0.9 g, 36%)을 얻었다.
7. Comp (LA153)2Ir(LB86)의 합성
1000 mL의 둥근 바닥 플라스크에 2,4-디브로모-피리딘(9.45 g, 40.4 mmol), 4,4,5,5-테트라메틸-2-페닐-1,3,2-디옥사보롤란(11.37 g, 55.7 mmol), 디아세톡시팔라듐(0.569 g, 2.53 mmol), 트리페닐포스판(2.66 g, 10.13 mmol), 수산화칼륨(5.68 g, 101 mmol) 및 아세토니트릴(600 mL)을 넣었다. 반응 혼합물을 50 시간 동안 60℃로 가열하였다. 반응 혼합물을 EtOAc로 수성 워크업 처리하였다. 유기 부분을 합하고 실리카 칼럼 크로마토그래프를 행하여 원하는 생성물(9.45 g, 80%)을 얻었다.
500 mL의 둥근 바닥 플라스크에 4-브로모-2-페닐피리딘(9.52 g, 35.8 mmol ), (4-클로로페닐)보론산(6.94 g, 44.4 mmol), 디아세톡시팔라듐(0.453 g, 2.018 mmol), 트리페닐포스판(1.059 g, 4.04 mmol), K2CO3(11.16 g, 81 mmol), 아세토니트릴(200 mL) 및 MeOH(100 mL)를 넣었다. 반응을 21 시간 동안 40℃로 가열하였다. 반응 혼합물을 물로 희석하고 에틸 아세테이트로 추출하였다. 유기 부분을 증발 건조하였다. 잔류물에 칼럼 크로마토그래피를 행하여 원하는 화합물(9.52 g, 89%)을 얻었다.
250 mL의 플라스크에 4-(4-클로로페닐)-2-페닐피리딘(3 g, 11.29 mmol), 염화리튬(6.52 g, 154 mmol), PEPPSI-Ipr(0.460 g, 0.677 mmol) 및 THF 중 ((1S,2R,4R)-비시클로[2.2.1]헵탄-2-일)아연(II) 브로마이드(79 ml, 39.5 mmol)를 넣었다. 반응 혼합물을 실온에서 밤새 교반하였다. 반응 혼합물을 물로 희석하고 에틸 아세테이트로 추출하였다. 유기 부분을 합하고 칼럼 크로마토그래프를 행하여 (3.67 g, 100%)를 얻었다.
Tetrahedron 71(2015)1425-1430에 공개된 문헌상의 절차에 기초하여 중수소화 반응을 행하였다.
500 mL의 플라스크에 이리듐 전구체(4.28 g, 5.24 mmol), 4-(4-((1S,2S,4R)-비시클로[2.2.1]헵탄-2-일-2-d)페닐)-2-페닐피리딘(4.36 g, 13.36 mmol), 에탄올(40 mL) 및 메탄올(40 mL)을 넣고, 50 시간 동안 70℃로 가열하였다. 반응 혼합물을 여과하고 황색 고체를 수거하고 칼럼 크로마토그래피를 행하여 원하는 생성물(1.18 g)을 얻었다.
소자 실시예
모든 실시예 소자는 고진공(<10-7 Torr) 열증발에 의해 제조되었다. 애노드 전극은 750Å의 인듐주석산화물(ITO)이었다. 캐소드는 10Å의 Liq (8-히드록시퀴놀린 리튬) 및 이어서 1,000Å의 Al로 이루어졌다. 소자를 제조 직후 질소 글로브 박스(<1 ppm의 H2O 및 O2) 안에 에폭시 수지로 밀봉된 유리 뚜껑으로 봉입하고 패키지 안에 흡습제(moisture getter)를 넣었다. 소자 실시예의 스택은 순차적으로, ITO 표면으로부터, 정공 주입층(HIL)으로서 100Å의 HATCN; 정공 운반층(HTL)으로서 450Å의 HTM; 전자 차단층으로서 50Å의 EBM, 2성분 호스트(H1:H2 1:1 비) 및 이미터 12%(본 발명 또는 비교 이미터 실시예)를 포함하는 400Å의 발광층(EML), 및 전자 운반층 ETL로서 40%의 ETM으로 도핑된 350Å의 Liq (8-히드록시퀴놀린 리튬)으로 이루어졌다. 소자 재료의 화학 구조를 이하에 나타낸다.
표 5는 소자의 층 두께 및 재료를 나타낸다.
이미터 실시예 1, 2, 5, 7, 8, 9, 10 및 CE2를 이용하여 소자 EQE 및 이미터 배향 인자 사이의 상관관계를 입증하였다. 1,000 nit에서 측정된 소자 EQE를 표 6에 나타낸다.
이미터 배향 인자가 증가함에 따라 관찰되는 소자 EQE의 증가는 EQE가 이미터 배향과 직접적인 상관관계가 있음을 보여준다.
본원에 기술된 다양한 실시양태는 단지 예시에 의한 것이며, 본 발명의 범위를 한정하려는 것이 아님을 이해하여야 한다. 예를 들면, 본원에 기술된 물질 및 구조의 대다수는 본 발명의 취지로부터 벗어나는 일 없이 다른 물질 및 구조로 대체될 수 있다. 특허 청구된 본 발명은 이에 따라 당업자에게 명백한 바와 같이 본원에 기술된 특정 예시 및 바람직한 실시양태로부터 변형예를 포함할 수 있다. 본 발명이 왜 효과가 있는지에 관한 다양한 이론은 한정적인 의도가 아님을 이해할 것이다.
Claims (20)
- 하기 화학식을 갖고 그 분자가 0.67을 초과하는 배향 인자 값을 갖는 화합물:
M(LA)h(LB)y(LC)z
상기 화학식에서,
리간드 LA, LB, 및 LC는 각각 독립적으로 하기로 이루어지는 군에서 선택되고:
;
각각의 X1 내지 X13은 독립적으로 탄소 및 질소로 이루어지는 군에서 선택되며;
X는 BR', NR', PR', O, S, Se, C=O, S=O, SO2, CR'R", SiR'R", 및 GeR'R"로 이루어지는 군에서 선택되고;
R' 및 R"은 임의로 융합 또는 결합되어 고리를 형성하며;
각각의 Ra, Rb, Rc, 및 Rd는 일치환 내지 가능한 최대수의 치환 또는 비치환을 나타낼 수 있고;
R', R", Ra, Rb, Rc, 및 Rd는 각각 독립적으로 수소, 중수소, 할라이드, 알킬, 시클로알킬, 헤테로알킬, 아릴알킬, 알콕시, 아릴옥시, 아미노, 실릴, 알케닐, 시클로알케닐, 헤테로알케닐, 알키닐, 아릴, 헤테로아릴, 아실, 카르보닐, 카르복실산, 에스테르, 니트릴, 이소니트릴, 설파닐, 설피닐, 설포닐, 포스피노, 및 이의 조합으로 이루어지는 군에서 선택되며;
Ra, Rb, Rc, 및 Rd 중 임의의 2개의 인접한 치환기는 임의로 융합 또는 결합되어 고리를 형성하거나 또는 다좌(multidentate) 리간드를 형성하고;
M은 40 초과의 원자 질량을 갖는 금속이며;
h는 1 또는 2이고;
y는 0, 1, 또는 2이며;
z는 0, 1, 또는 2이고;
x+y+z는 금속 M의 산화 상태이다. - 제1항에 있어서, M은 Ir, Rh, Re, Ru, Os, Pt, Au, 및 Cu로 이루어지는 군에서 선택되는 것인 화합물.
- 제1항에 있어서, Ra, Rb, Rc, 및 Rd 중 하나는 13개 이상의 탄소 원자를 갖는 일치환이고, Ra, Rb, Rc, 및 Rd의 나머지 모두는 6의 최대 탄소수를 갖는 것인 화합물.
- 제1항에 있어서, 각각의 X1 내지 X13은 탄소인 화합물.
- 제1항에 있어서, 화학식 Ir(LA)2(LB)을 갖는 화합물.
- 제1항에 있어서, Pt(LA)(LB)의 화학식을 갖고, 상기 화학식에서 LA 및 LB는 상이한 것인 화합물.
- 제1항에 있어서, 하기로 이루어지는 군에서 선택되는 구조를 갖는 화학식 (LA)mIr(LB)3-m을 갖는 화합물:
상기 화학식들에서,
m은 1 또는 2이고;
R1, R2, R4, 및 R5는 각각 독립적으로 일치환, 이치환, 삼치환 또는 사치환, 또는 비치환을 나타내며;
R3은 일치환, 이치환 또는 삼치환, 또는 비치환을 나타내고;
R1, R2, R3, R4, 및 R5는 각각 독립적으로 수소, 중수소, C1 내지 C6 알킬, C1 내지 C6 시클로알킬, 및 이의 부분 또는 완전 중수소화된 또는 불화된 변이체로 이루어지는 군에서 선택되며;
R6은 7개 이상의 탄소 원자를 갖는 알킬, 7개 이상의 탄소 원자를 갖는 시클로알킬, 7개 이상의 탄소 원자를 갖는 알킬-시클로알킬, 및 이의 부분 또는 완전 중수소화된 또는 불화된 변이체로 이루어지는 군에서 선택된다. - 제10항에 있어서, R6은 8개 이상의 탄소 원자를 갖는 알킬, 8개 이상의 탄소 원자를 갖는 시클로알킬, 8개 이상의 탄소 원자를 갖는 알킬-시클로알킬, 및 이의 부분 또는 완전 중수소화된 또는 불화된 변이체로 이루어지는 군에서 선택되는 것인 화합물.
- 하기로 이루어지는 군에서 선택되는 구조를 갖는 화학식 (LA)mIr(LB)3-m을 갖는 화합물:
상기 화학식들에서,
m은 1 또는 2이고;
R1, R2, R4, 및 R5는 각각 독립적으로 일치환, 이치환, 삼치환 또는 사치환, 또는 비치환을 나타내며;
R3은 일치환, 이치환 또는 삼치환, 또는 비치환을 나타내고;
R6은 일치환 또는 비치환을 나타내며;
R1, R2, R3, R4, R5 및 R6는 각각 독립적으로 수소, 중수소, 알킬, 시클로알킬, 이의 부분 또는 완전 중수소화된 또는 불화된 변이체, 및 이의 조합으로 이루어지는 군에서 선택된다. - 애노드;
캐소드; 및
애노드와 캐소드 사이에 배치된, 하기 화학식으로 이루어지는 군에서 선택되는 화학식을 갖는 화합물을 포함하는 유기층
을 포함하는 유기 발광 소자(OLED):
M(LA)h(LB)y(LC)z,
상기 화학식에서,
m은 1 또는 2이며;
리간드 LA, LB, 및 LC는 각각 독립적으로 하기로 이루어지는 군에서 선택되고:
;
각각의 X1 내지 X13은 독립적으로 탄소 및 질소로 이루어지는 군에서 선택되며;
X는 BR', NR', PR', O, S, Se, C=O, S=O, SO2, CR'R", SiR'R", 및 GeR'R"로 이루어지는 군에서 선택되고;
R' 및 R"은 임의로 융합 또는 결합되어 고리를 형성하며;
각각의 Ra, Rb, Rc, 및 Rd는 일치환 내지 가능한 최대수의 치환 또는 비치환을 나타낼 수 있고;
R', R", Ra, Rb, Rc, 및 Rd는 각각 독립적으로 수소, 중수소, 할라이드, 알킬, 시클로알킬, 헤테로알킬, 아릴알킬, 알콕시, 아릴옥시, 아미노, 실릴, 알케닐, 시클로알케닐, 헤테로알케닐, 알키닐, 아릴, 헤테로아릴, 아실, 카르보닐, 카르복실산, 에스테르, 니트릴, 이소니트릴, 설파닐, 설피닐, 설포닐, 포스피노, 및 이의 조합으로 이루어지는 군에서 선택되며;
Ra, Rb, Rc, 및 Rd 중 임의의 2개의 인접한 치환기는 임의로 융합 또는 결합되어 고리를 형성하거나 또는 다좌 리간드를 형성하고;
M은 40 초과의 원자 질량을 갖는 금속이며;
h는 1 또는 2이고;
y는 0, 1, 또는 2이며;
z는 0, 1, 또는 2이고;
x+y+z는 금속 M의 산화 상태이며;
M(LA)h(LB)y(LC)z의 분자는 0.67을 초과하는 배향 인자 값을 갖고;
R1, R2, R4, 및 R5는 각각 독립적으로 일치환, 이치환, 삼치환 또는 사치환, 또는 비치환을 나타내며;
R3은 일치환, 이치환 또는 삼치환, 또는 비치환을 나타내고;
R6은 일치환 또는 비치환을 나타내며;
R1, R2, R3, R4, R5 및 R6은 각각 독립적으로 수소, 중수소, 알킬, 시클로알킬, 이의 부분 또는 완전 중수소화된 또는 불화된 변이체, 및 이의 조합으로 이루어지는 군에서 선택된다. - 제16항에 있어서, 소비재, 전자 부품 모듈, 및 조명 패널로 이루어진 군에서 선택되는 소자 내에 포함되는 OLED.
- 제16항에 있어서, 유기층은 발광층이고 화합물은 발광 도펀트 또는 비발광 도펀트인 OLED.
- 제16항에 있어서, 유기층은 호스트를 추가로 포함하고, 상기 호스트는 트리페닐렌, 카르바졸, 디벤조티오펜, 디벤조푸란, 디벤조셀레노펜, 아자트리페닐렌, 아자카르바졸, 아자-디벤조티오펜, 아자-디벤조푸란 및 아자-디벤조셀레노펜으로 이루어지는 군에서 선택된 하나 이상의 화학 기를 포함하는 것인 OLED.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020240051434A KR20240058808A (ko) | 2015-09-03 | 2024-04-17 | 유기 전계발광 재료 및 소자 |
Applications Claiming Priority (12)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201562213757P | 2015-09-03 | 2015-09-03 | |
| US62/213,757 | 2015-09-03 | ||
| US201562232194P | 2015-09-24 | 2015-09-24 | |
| US62/232,194 | 2015-09-24 | ||
| US201662291960P | 2016-02-05 | 2016-02-05 | |
| US62/291,960 | 2016-02-05 | ||
| US201662322510P | 2016-04-14 | 2016-04-14 | |
| US62/322,510 | 2016-04-14 | ||
| US201662330412P | 2016-05-02 | 2016-05-02 | |
| US62/330,412 | 2016-05-02 | ||
| US15/239,961 US10672996B2 (en) | 2015-09-03 | 2016-08-18 | Organic electroluminescent materials and devices |
| US15/239,961 | 2016-08-18 |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020240051434A Division KR20240058808A (ko) | 2015-09-03 | 2024-04-17 | 유기 전계발광 재료 및 소자 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20170028268A true KR20170028268A (ko) | 2017-03-13 |
| KR102659792B1 KR102659792B1 (ko) | 2024-04-22 |
Family
ID=58237213
Family Applications (4)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020160112440A KR102693087B1 (ko) | 2015-09-03 | 2016-09-01 | 유기 전계발광 물질 및 디바이스 |
| KR1020160112495A KR102659792B1 (ko) | 2015-09-03 | 2016-09-01 | 유기 전계발광 재료 및 소자 |
| KR1020240051434A KR20240058808A (ko) | 2015-09-03 | 2024-04-17 | 유기 전계발광 재료 및 소자 |
| KR1020240102940A KR20240123292A (ko) | 2015-09-03 | 2024-08-02 | 유기 전계발광 물질 및 디바이스 |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020160112440A KR102693087B1 (ko) | 2015-09-03 | 2016-09-01 | 유기 전계발광 물질 및 디바이스 |
Family Applications After (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020240051434A KR20240058808A (ko) | 2015-09-03 | 2024-04-17 | 유기 전계발광 재료 및 소자 |
| KR1020240102940A KR20240123292A (ko) | 2015-09-03 | 2024-08-02 | 유기 전계발광 물질 및 디바이스 |
Country Status (6)
| Country | Link |
|---|---|
| US (6) | US10672996B2 (ko) |
| EP (2) | EP3159350B1 (ko) |
| JP (7) | JP6725369B2 (ko) |
| KR (4) | KR102693087B1 (ko) |
| CN (2) | CN106946940B (ko) |
| TW (2) | TWI721009B (ko) |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20200066575A (ko) * | 2018-11-30 | 2020-06-10 | 유니버셜 디스플레이 코포레이션 | 표면-플라즈몬-펌핑된 발광 디바이스 |
| US11145829B2 (en) | 2018-02-02 | 2021-10-12 | Samsung Display Co., Ltd. | Organic electroluminescent device, organic electroluminescent display device including the same, and organometallic compound for organic electroluminescent device |
| US11569461B2 (en) | 2017-12-08 | 2023-01-31 | Samsung Display Co., Ltd. | Organic electroluminescence device and organometallic compound for organic electroluminescence device |
| US11731994B2 (en) | 2018-12-05 | 2023-08-22 | Samsung Electronics Co., Ltd. | Organometallic compound, organic light-emitting device including the organometallic compound, and diagnostic composition including the organometallic compound |
Families Citing this family (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| TWI638807B (zh) * | 2009-04-28 | 2018-10-21 | 環球展覽公司 | 具有甲基-d3取代之銥錯合物 |
| US10158089B2 (en) * | 2011-05-27 | 2018-12-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US9634264B2 (en) * | 2012-11-09 | 2017-04-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10672996B2 (en) * | 2015-09-03 | 2020-06-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11932659B2 (en) * | 2016-07-25 | 2024-03-19 | Udc Ireland Limited | Metal complexes for use as emitters in organic electroluminescence devices |
| KR102129508B1 (ko) * | 2017-07-14 | 2020-07-02 | 삼성에스디아이 주식회사 | 유기 광전자 소자용 조성물, 유기 광전자 소자 및 표시 장치 |
| JP7206611B2 (ja) * | 2018-03-28 | 2023-01-18 | 三菱ケミカル株式会社 | 有機電界発光素子の発光層用組成物、有機電界発光素子、表示装置及び照明 |
| US11515482B2 (en) * | 2018-10-23 | 2022-11-29 | Universal Display Corporation | Deep HOMO (highest occupied molecular orbital) emitter device structures |
| KR20200076969A (ko) * | 2018-12-20 | 2020-06-30 | 엘지디스플레이 주식회사 | 유기 발광 소자를 이용한 조명 장치 |
| TWI738164B (zh) * | 2019-02-01 | 2021-09-01 | 日商住友重機械工業股份有限公司 | 防腐裝置及防腐方法 |
| US20200274080A1 (en) * | 2019-02-22 | 2020-08-27 | Matrix Sensors, Inc. | Crystalline film and lighting-emitting device having oriented luminescent emitters |
| US11569480B2 (en) * | 2019-03-12 | 2023-01-31 | Universal Display Corporation | Plasmonic OLEDs and vertical dipole emitters |
| KR20220097064A (ko) * | 2020-12-31 | 2022-07-07 | 엘지디스플레이 주식회사 | 발광 표시 장치 |
| WO2024170609A1 (en) | 2023-02-17 | 2024-08-22 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20110105800A (ko) * | 2008-12-12 | 2011-09-27 | 유니버셜 디스플레이 코포레이션 | 이미다조[1,2f] 펜안트리딘 이리듐 착체계 고효율 청색 이미터 |
| KR20140015306A (ko) * | 2011-03-10 | 2014-02-06 | 린텍 가부시키가이샤 | 인광 발광 재료, 인광 발광 재료의 제조 방법, 및 인광 발광 소자 |
| KR20140027389A (ko) * | 2011-05-27 | 2014-03-06 | 유니버셜 디스플레이 코포레이션 | Oled 디바이스용 고 효율 황색광 이미터 |
| KR20140104926A (ko) * | 2013-02-21 | 2014-08-29 | 유니버셜 디스플레이 코포레이션 | 인광성 화합물 |
| KR20140117401A (ko) * | 2012-01-13 | 2014-10-07 | 미쓰비시 가가꾸 가부시키가이샤 | 이리듐 착물 화합물 그리고 그 화합물을 함유하는 용액 조성물, 유기 전계 발광 소자, 표시 장치 및 조명 장치 |
| KR20150040912A (ko) * | 2012-08-08 | 2015-04-15 | 미쓰비시 가가꾸 가부시키가이샤 | 이리듐 착물 화합물, 그리고 그 화합물을 포함하는 조성물, 유기 전계 발광 소자, 표시 장치 및 조명 장치 |
| KR20150066202A (ko) * | 2013-12-06 | 2015-06-16 | 롬엔드하스전자재료코리아유한회사 | 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 |
Family Cites Families (408)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4769292A (en) | 1987-03-02 | 1988-09-06 | Eastman Kodak Company | Electroluminescent device with modified thin film luminescent zone |
| GB8909011D0 (en) | 1989-04-20 | 1989-06-07 | Friend Richard H | Electroluminescent devices |
| US5061569A (en) | 1990-07-26 | 1991-10-29 | Eastman Kodak Company | Electroluminescent device with organic electroluminescent medium |
| JPH0773529A (ja) | 1993-08-31 | 1995-03-17 | Hitachi Ltd | 光磁気記録方式および光磁気記録媒体 |
| DE69412567T2 (de) | 1993-11-01 | 1999-02-04 | Hodogaya Chemical Co., Ltd., Tokio/Tokyo | Aminverbindung und sie enthaltende Elektrolumineszenzvorrichtung |
| US5707745A (en) | 1994-12-13 | 1998-01-13 | The Trustees Of Princeton University | Multicolor organic light emitting devices |
| US5703436A (en) | 1994-12-13 | 1997-12-30 | The Trustees Of Princeton University | Transparent contacts for organic devices |
| KR0117693Y1 (ko) | 1995-03-16 | 1998-04-23 | 천일선 | 곡물볶음기의 도어개폐장치 |
| US6939625B2 (en) | 1996-06-25 | 2005-09-06 | Nôrthwestern University | Organic light-emitting diodes and methods for assembly and enhanced charge injection |
| US5844363A (en) | 1997-01-23 | 1998-12-01 | The Trustees Of Princeton Univ. | Vacuum deposited, non-polymeric flexible organic light emitting devices |
| US6013982A (en) | 1996-12-23 | 2000-01-11 | The Trustees Of Princeton University | Multicolor display devices |
| US5834893A (en) | 1996-12-23 | 1998-11-10 | The Trustees Of Princeton University | High efficiency organic light emitting devices with light directing structures |
| US6091195A (en) | 1997-02-03 | 2000-07-18 | The Trustees Of Princeton University | Displays having mesa pixel configuration |
| EP0879868B1 (en) | 1997-05-19 | 2002-04-03 | Canon Kabushiki Kaisha | Organic compound and electroluminescent device using the same |
| US6413656B1 (en) | 1998-09-14 | 2002-07-02 | The University Of Southern California | Reduced symmetry porphyrin molecules for producing enhanced luminosity from phosphorescent organic light emitting devices |
| US6303238B1 (en) | 1997-12-01 | 2001-10-16 | The Trustees Of Princeton University | OLEDs doped with phosphorescent compounds |
| US6337102B1 (en) | 1997-11-17 | 2002-01-08 | The Trustees Of Princeton University | Low pressure vapor phase deposition of organic thin films |
| US6087196A (en) | 1998-01-30 | 2000-07-11 | The Trustees Of Princeton University | Fabrication of organic semiconductor devices using ink jet printing |
| US20060024762A1 (en) * | 1998-07-28 | 2006-02-02 | Brooks Edwards | Heteroaryl substituted benzothiazole dioxetanes |
| US6528187B1 (en) | 1998-09-08 | 2003-03-04 | Fuji Photo Film Co., Ltd. | Material for luminescence element and luminescence element using the same |
| US6097147A (en) | 1998-09-14 | 2000-08-01 | The Trustees Of Princeton University | Structure for high efficiency electroluminescent device |
| US6830828B2 (en) | 1998-09-14 | 2004-12-14 | The Trustees Of Princeton University | Organometallic complexes as phosphorescent emitters in organic LEDs |
| US6461747B1 (en) | 1999-07-22 | 2002-10-08 | Fuji Photo Co., Ltd. | Heterocyclic compounds, materials for light emitting devices and light emitting devices using the same |
| US6294398B1 (en) | 1999-11-23 | 2001-09-25 | The Trustees Of Princeton University | Method for patterning devices |
| US6458475B1 (en) | 1999-11-24 | 2002-10-01 | The Trustee Of Princeton University | Organic light emitting diode having a blue phosphorescent molecule as an emitter |
| US6821645B2 (en) | 1999-12-27 | 2004-11-23 | Fuji Photo Film Co., Ltd. | Light-emitting material comprising orthometalated iridium complex, light-emitting device, high efficiency red light-emitting device, and novel iridium complex |
| KR100377321B1 (ko) | 1999-12-31 | 2003-03-26 | 주식회사 엘지화학 | 피-형 반도체 성질을 갖는 유기 화합물을 포함하는 전기소자 |
| US7953615B2 (en) * | 2000-04-03 | 2011-05-31 | Mitchell International, Inc. | System and method of administering, tracking and managing of claims processing |
| US6670645B2 (en) | 2000-06-30 | 2003-12-30 | E. I. Du Pont De Nemours And Company | Electroluminescent iridium compounds with fluorinated phenylpyridines, phenylpyrimidines, and phenylquinolines and devices made with such compounds |
| US20020121638A1 (en) | 2000-06-30 | 2002-09-05 | Vladimir Grushin | Electroluminescent iridium compounds with fluorinated phenylpyridines, phenylpyrimidines, and phenylquinolines and devices made with such compounds |
| JP2002050860A (ja) | 2000-08-04 | 2002-02-15 | Toray Eng Co Ltd | 実装方法および実装装置 |
| CN100505375C (zh) | 2000-08-11 | 2009-06-24 | 普林斯顿大学理事会 | 有机金属化合物和发射转换有机电致磷光 |
| KR100825183B1 (ko) | 2000-11-30 | 2008-04-24 | 캐논 가부시끼가이샤 | 발광 소자 및 표시 장치 |
| JP4154145B2 (ja) | 2000-12-01 | 2008-09-24 | キヤノン株式会社 | 金属配位化合物、発光素子及び表示装置 |
| US6579630B2 (en) | 2000-12-07 | 2003-06-17 | Canon Kabushiki Kaisha | Deuterated semiconducting organic compounds used for opto-electronic devices |
| JP3812730B2 (ja) | 2001-02-01 | 2006-08-23 | 富士写真フイルム株式会社 | 遷移金属錯体及び発光素子 |
| JP4438042B2 (ja) | 2001-03-08 | 2010-03-24 | キヤノン株式会社 | 金属配位化合物、電界発光素子及び表示装置 |
| JP4307000B2 (ja) | 2001-03-08 | 2009-08-05 | キヤノン株式会社 | 金属配位化合物、電界発光素子及び表示装置 |
| JP4307001B2 (ja) | 2001-03-14 | 2009-08-05 | キヤノン株式会社 | 金属配位化合物、電界発光素子及び表示装置 |
| DE10116962A1 (de) | 2001-04-05 | 2002-10-10 | Covion Organic Semiconductors | Rhodium- und Iridium-Komplexe |
| JP4310077B2 (ja) | 2001-06-19 | 2009-08-05 | キヤノン株式会社 | 金属配位化合物及び有機発光素子 |
| EP1407501B1 (en) | 2001-06-20 | 2009-05-20 | Showa Denko K.K. | Light emitting material and organic light-emitting device |
| US7071615B2 (en) | 2001-08-20 | 2006-07-04 | Universal Display Corporation | Transparent electrodes |
| US7250226B2 (en) | 2001-08-31 | 2007-07-31 | Nippon Hoso Kyokai | Phosphorescent compound, a phosphorescent composition and an organic light-emitting device |
| US7431968B1 (en) | 2001-09-04 | 2008-10-07 | The Trustees Of Princeton University | Process and apparatus for organic vapor jet deposition |
| US6835469B2 (en) | 2001-10-17 | 2004-12-28 | The University Of Southern California | Phosphorescent compounds and devices comprising the same |
| US7166368B2 (en) | 2001-11-07 | 2007-01-23 | E. I. Du Pont De Nemours And Company | Electroluminescent platinum compounds and devices made with such compounds |
| US6863997B2 (en) | 2001-12-28 | 2005-03-08 | The Trustees Of Princeton University | White light emitting OLEDs from combined monomer and aggregate emission |
| KR100691543B1 (ko) | 2002-01-18 | 2007-03-09 | 주식회사 엘지화학 | 새로운 전자 수송용 물질 및 이를 이용한 유기 발광 소자 |
| US6653654B1 (en) | 2002-05-01 | 2003-11-25 | The University Of Hong Kong | Electroluminescent materials |
| JP4106974B2 (ja) | 2002-06-17 | 2008-06-25 | コニカミノルタホールディングス株式会社 | 有機エレクトロルミネッセンス素子及び表示装置 |
| US20030230980A1 (en) | 2002-06-18 | 2003-12-18 | Forrest Stephen R | Very low voltage, high efficiency phosphorescent oled in a p-i-n structure |
| US6916554B2 (en) | 2002-11-06 | 2005-07-12 | The University Of Southern California | Organic light emitting materials and devices |
| US7189989B2 (en) | 2002-08-22 | 2007-03-13 | Fuji Photo Film Co., Ltd. | Light emitting element |
| DE10238903A1 (de) | 2002-08-24 | 2004-03-04 | Covion Organic Semiconductors Gmbh | Rhodium- und Iridium-Komplexe |
| EP1550707B1 (en) | 2002-08-27 | 2016-03-23 | UDC Ireland Limited | Organometallic complexes, organic el devices, and organic el displays |
| JP4261855B2 (ja) | 2002-09-19 | 2009-04-30 | キヤノン株式会社 | フェナントロリン化合物及びそれを用いた有機発光素子 |
| US6687266B1 (en) | 2002-11-08 | 2004-02-03 | Universal Display Corporation | Organic light emitting materials and devices |
| JP4365199B2 (ja) | 2002-12-27 | 2009-11-18 | 富士フイルム株式会社 | 有機電界発光素子 |
| JP4365196B2 (ja) | 2002-12-27 | 2009-11-18 | 富士フイルム株式会社 | 有機電界発光素子 |
| US7390670B2 (en) * | 2003-02-20 | 2008-06-24 | Lumigen, Inc. | Signalling compounds and methods for detecting hydrogen peroxide |
| US20060194073A1 (en) * | 2003-03-07 | 2006-08-31 | Masato Okada | Organic compound and organic electrolumiscent device |
| DE10310887A1 (de) | 2003-03-11 | 2004-09-30 | Covion Organic Semiconductors Gmbh | Matallkomplexe |
| EP1602648B1 (en) | 2003-03-13 | 2013-04-17 | Idemitsu Kosan Co., Ltd. | Nitrogen-containing heterocycle derivative and organic electroluminescent element using the same |
| ATE438654T1 (de) | 2003-03-24 | 2009-08-15 | Univ Southern California | Ir-phenylpyrazolkomplexe |
| US7090928B2 (en) | 2003-04-01 | 2006-08-15 | The University Of Southern California | Binuclear compounds |
| EP1618170A2 (de) | 2003-04-15 | 2006-01-25 | Covion Organic Semiconductors GmbH | Mischungen von organischen zur emission befähigten halbleitern und matrixmaterialien, deren verwendung und elektronikbauteile enthaltend diese mischungen |
| US7029765B2 (en) | 2003-04-22 | 2006-04-18 | Universal Display Corporation | Organic light emitting devices having reduced pixel shrinkage |
| US20060186791A1 (en) | 2003-05-29 | 2006-08-24 | Osamu Yoshitake | Organic electroluminescent element |
| JP2005011610A (ja) | 2003-06-18 | 2005-01-13 | Nippon Steel Chem Co Ltd | 有機電界発光素子 |
| JP4891615B2 (ja) | 2003-07-22 | 2012-03-07 | 出光興産株式会社 | 金属錯体化合物及びそれを用いた有機エレクトロルミネッセンス素子 |
| US20050025993A1 (en) | 2003-07-25 | 2005-02-03 | Thompson Mark E. | Materials and structures for enhancing the performance of organic light emitting devices |
| JP4561221B2 (ja) | 2003-07-31 | 2010-10-13 | 三菱化学株式会社 | 化合物、電荷輸送材料および有機電界発光素子 |
| TWI390006B (zh) | 2003-08-07 | 2013-03-21 | Nippon Steel Chemical Co | Organic EL materials with aluminum clamps |
| DE10338550A1 (de) | 2003-08-19 | 2005-03-31 | Basf Ag | Übergangsmetallkomplexe mit Carbenliganden als Emitter für organische Licht-emittierende Dioden (OLEDs) |
| US7504049B2 (en) | 2003-08-25 | 2009-03-17 | Semiconductor Energy Laboratory Co., Ltd. | Electrode device for organic device, electronic device having electrode device for organic device, and method of forming electrode device for organic device |
| HU0302888D0 (en) | 2003-09-09 | 2003-11-28 | Pribenszky Csaba Dr | In creasing of efficacity of stable storage by freezing of embryos in preimplantation stage with pretreatment by pressure |
| US20060269780A1 (en) | 2003-09-25 | 2006-11-30 | Takayuki Fukumatsu | Organic electroluminescent device |
| DE10345572A1 (de) | 2003-09-29 | 2005-05-19 | Covion Organic Semiconductors Gmbh | Metallkomplexe |
| JP5112601B2 (ja) | 2003-10-07 | 2013-01-09 | 三井化学株式会社 | 複素環化合物および該化合物を含有する有機電界発光素子 |
| KR101044087B1 (ko) | 2003-11-04 | 2011-06-27 | 다카사고 고료 고교 가부시키가이샤 | 백금 착체 및 발광소자 |
| JP4215621B2 (ja) | 2003-11-17 | 2009-01-28 | 富士電機アセッツマネジメント株式会社 | 回路遮断器の外部操作ハンドル装置 |
| JP4822687B2 (ja) | 2003-11-21 | 2011-11-24 | 富士フイルム株式会社 | 有機電界発光素子 |
| DE10357044A1 (de) | 2003-12-04 | 2005-07-14 | Novaled Gmbh | Verfahren zur Dotierung von organischen Halbleitern mit Chinondiiminderivaten |
| US20050123791A1 (en) | 2003-12-05 | 2005-06-09 | Deaton Joseph C. | Organic electroluminescent devices |
| US7029766B2 (en) | 2003-12-05 | 2006-04-18 | Eastman Kodak Company | Organic element for electroluminescent devices |
| TWI347311B (en) | 2003-12-26 | 2011-08-21 | Hodogaya Chemical Co Ltd | Tetramine compound and organic el device |
| US7332232B2 (en) | 2004-02-03 | 2008-02-19 | Universal Display Corporation | OLEDs utilizing multidentate ligand systems |
| TW200535134A (en) | 2004-02-09 | 2005-11-01 | Nippon Steel Chemical Co | Aminodibenzodioxin derivative and organic electroluminescent device using same |
| KR20080064201A (ko) | 2004-03-11 | 2008-07-08 | 미쓰비시 가가꾸 가부시키가이샤 | 전하 수송막용 조성물 및 이온 화합물, 이를 이용한 전하수송막 및 유기 전계 발광 장치, 및 유기 전계 발광 장치의제조 방법 및 전하 수송막의 제조 방법 |
| TW200531592A (en) | 2004-03-15 | 2005-09-16 | Nippon Steel Chemical Co | Organic electroluminescent device |
| ATE447558T1 (de) | 2004-04-07 | 2009-11-15 | Idemitsu Kosan Co | Stickstoffhaltiges heterocyclusderivat und organisches elektrolumineszentes element, bei dem dieses verwendung findet |
| JP4869565B2 (ja) | 2004-04-23 | 2012-02-08 | 富士フイルム株式会社 | 有機電界発光素子 |
| US7534505B2 (en) | 2004-05-18 | 2009-05-19 | The University Of Southern California | Organometallic compounds for use in electroluminescent devices |
| US7491823B2 (en) | 2004-05-18 | 2009-02-17 | The University Of Southern California | Luminescent compounds with carbene ligands |
| US7445855B2 (en) | 2004-05-18 | 2008-11-04 | The University Of Southern California | Cationic metal-carbene complexes |
| US7154114B2 (en) | 2004-05-18 | 2006-12-26 | Universal Display Corporation | Cyclometallated iridium carbene complexes for use as hosts |
| US7279704B2 (en) | 2004-05-18 | 2007-10-09 | The University Of Southern California | Complexes with tridentate ligands |
| US7393599B2 (en) | 2004-05-18 | 2008-07-01 | The University Of Southern California | Luminescent compounds with carbene ligands |
| WO2005124889A1 (en) | 2004-06-09 | 2005-12-29 | E.I. Dupont De Nemours And Company | Organometallic compounds and devices made with such compounds |
| WO2005123873A1 (ja) | 2004-06-17 | 2005-12-29 | Konica Minolta Holdings, Inc. | 有機エレクトロルミネッセンス素子材料、有機エレクトロルミネッセンス素子、表示装置及び照明装置 |
| JP5000496B2 (ja) | 2004-06-28 | 2012-08-15 | チバ ホールディング インコーポレーテッド | トリアゾールとベンゾトリアゾールのエレクトロルミネセンス金属錯体 |
| US20060008670A1 (en) | 2004-07-06 | 2006-01-12 | Chun Lin | Organic light emitting materials and devices |
| JP4925569B2 (ja) | 2004-07-08 | 2012-04-25 | ローム株式会社 | 有機エレクトロルミネッセント素子 |
| JP4858169B2 (ja) | 2004-07-23 | 2012-01-18 | コニカミノルタホールディングス株式会社 | 有機エレクトロルミネッセンス素子 |
| EP1624500B1 (de) | 2004-08-05 | 2016-03-16 | Novaled GmbH | Spiro-Bifluoren Verbindungen als organisches Halbleiter-Matrixmaterial |
| US20060182993A1 (en) | 2004-08-10 | 2006-08-17 | Mitsubishi Chemical Corporation | Compositions for organic electroluminescent device and organic electroluminescent device |
| KR100880220B1 (ko) | 2004-10-04 | 2009-01-28 | 엘지디스플레이 주식회사 | 유기 실리콘을 갖는 페닐 피리딘기를 포함하는 이리듐화합물계 발광 화합물 및 이를 발색 재료로서 사용하는유기전계발광소자 |
| JPWO2006046441A1 (ja) | 2004-10-29 | 2008-05-22 | 出光興産株式会社 | 芳香族アミン化合物及びそれを用いた有機エレクトロルミネッセンス素子 |
| DE102004057072A1 (de) | 2004-11-25 | 2006-06-01 | Basf Ag | Verwendung von Übergangsmetall-Carbenkomplexen in organischen Licht-emittierenden Dioden (OLEDs) |
| US8021765B2 (en) | 2004-11-29 | 2011-09-20 | Samsung Mobile Display Co., Ltd. | Phenylcarbazole-based compound and organic electroluminescent device employing the same |
| JP4478555B2 (ja) | 2004-11-30 | 2010-06-09 | キヤノン株式会社 | 金属錯体、発光素子及び画像表示装置 |
| US20060134459A1 (en) | 2004-12-17 | 2006-06-22 | Shouquan Huo | OLEDs with mixed-ligand cyclometallated complexes |
| TWI242596B (en) | 2004-12-22 | 2005-11-01 | Ind Tech Res Inst | Organometallic compound and organic electroluminescent device including the same |
| CN101087863B (zh) | 2004-12-23 | 2012-06-20 | 西巴特殊化学品控股有限公司 | 具有亲核卡宾配体的电致发光金属络合物 |
| US8121679B2 (en) | 2004-12-29 | 2012-02-21 | Fruitman Clinton O | Transcutaneous electrical nerve stimulator with hot or cold thermal application |
| JP2008526766A (ja) | 2004-12-30 | 2008-07-24 | イー・アイ・デュポン・ドウ・ヌムール・アンド・カンパニー | 有機金属錯体 |
| US20070181874A1 (en) | 2004-12-30 | 2007-08-09 | Shiva Prakash | Charge transport layers and organic electron devices comprising same |
| KR101169901B1 (ko) | 2005-01-05 | 2012-07-31 | 이데미쓰 고산 가부시키가이샤 | 방향족 아민 유도체 및 이를 이용한 유기 전기발광 소자 |
| DE502006008326D1 (de) | 2005-02-03 | 2010-12-30 | Merck Patent Gmbh | Metallkomplexe |
| WO2006081780A1 (de) | 2005-02-04 | 2006-08-10 | Novaled Ag | Dotanden für organische halbleiter |
| JPWO2006082742A1 (ja) | 2005-02-04 | 2008-06-26 | コニカミノルタホールディングス株式会社 | 有機エレクトロルミネッセンス素子材料、有機エレクトロルミネッセンス素子、表示装置及び照明装置 |
| KR100803125B1 (ko) | 2005-03-08 | 2008-02-14 | 엘지전자 주식회사 | 적색 인광 화합물 및 이를 사용한 유기전계발광소자 |
| KR100797469B1 (ko) | 2005-03-08 | 2008-01-24 | 엘지전자 주식회사 | 적색 인광 화합물 및 이를 사용한 유기전계발광소자 |
| WO2006098120A1 (ja) | 2005-03-16 | 2006-09-21 | Konica Minolta Holdings, Inc. | 有機エレクトロルミネッセンス素子材料、有機エレクトロルミネッセンス素子 |
| DE102005014284A1 (de) | 2005-03-24 | 2006-09-28 | Basf Ag | Verwendung von Verbindungen, welche aromatische oder heteroaromatische über Carbonyl-Gruppen enthaltende Gruppen verbundene Ringe enthalten, als Matrixmaterialien in organischen Leuchtdioden |
| WO2006103874A1 (ja) | 2005-03-29 | 2006-10-05 | Konica Minolta Holdings, Inc. | 有機エレクトロルミネッセンス素子材料、有機エレクトロルミネッセンス素子、表示装置及び照明装置 |
| JP2006278651A (ja) | 2005-03-29 | 2006-10-12 | Dainippon Printing Co Ltd | 有機エレクトロルミネッセンス素子 |
| JP5157442B2 (ja) | 2005-04-18 | 2013-03-06 | コニカミノルタホールディングス株式会社 | 有機エレクトロルミネッセンス素子、表示装置及び照明装置 |
| JP4934026B2 (ja) | 2005-04-18 | 2012-05-16 | 出光興産株式会社 | 芳香族トリアミン化合物及びそれを用いた有機エレクトロルミネッセンス素子 |
| US7807275B2 (en) | 2005-04-21 | 2010-10-05 | Universal Display Corporation | Non-blocked phosphorescent OLEDs |
| CN1321125C (zh) | 2005-04-30 | 2007-06-13 | 中国科学院长春应用化学研究所 | 喹啉类氮杂环为配体的红光铱配合物及其应用 |
| US9051344B2 (en) | 2005-05-06 | 2015-06-09 | Universal Display Corporation | Stability OLED materials and devices |
| US7902374B2 (en) | 2005-05-06 | 2011-03-08 | Universal Display Corporation | Stability OLED materials and devices |
| US8586204B2 (en) | 2007-12-28 | 2013-11-19 | Universal Display Corporation | Phosphorescent emitters and host materials with improved stability |
| JP4533796B2 (ja) | 2005-05-06 | 2010-09-01 | 富士フイルム株式会社 | 有機電界発光素子 |
| US8007927B2 (en) | 2007-12-28 | 2011-08-30 | Universal Display Corporation | Dibenzothiophene-containing materials in phosphorescent light emitting diodes |
| EP2277978B1 (en) | 2005-05-31 | 2016-03-30 | Universal Display Corporation | Triphenylene hosts in phosphorescent light emitting diodes |
| US8709614B2 (en) | 2005-06-07 | 2014-04-29 | Nippon Steel & Sumikin Chemical Co., Ltd. | Organic metal complex and its use in organic electroluminescent device |
| EP1899993B1 (en) | 2005-06-27 | 2012-06-27 | E.I. Du Pont De Nemours And Company | Electrically conductive polymer compositions |
| US20090039771A1 (en) | 2005-07-01 | 2009-02-12 | Konica Minolta Holdings, Inc. | Organic electroluminescent element material, organic electroluminescent element, display device and lighting device |
| US20090140637A1 (en) | 2005-07-11 | 2009-06-04 | Idemitsu Kosan Co., Ltd. | Nitrogen-containing heterocyclic derivative having electron-attracting substituent and organic electroluminescence element using the same |
| US8187727B2 (en) | 2005-07-22 | 2012-05-29 | Lg Chem, Ltd. | Imidazole derivatives, preparation method thereof and organic electronic device using the same |
| KR20080037006A (ko) | 2005-08-05 | 2008-04-29 | 이데미쓰 고산 가부시키가이샤 | 전이금속 착체화합물 및 그것을 이용한 유기 전기발광 소자 |
| JP5317386B2 (ja) | 2005-08-05 | 2013-10-16 | 出光興産株式会社 | 含窒素複素環誘導体及びそれを用いた有機エレクトロルミネッセンス素子 |
| JP4848152B2 (ja) | 2005-08-08 | 2011-12-28 | 出光興産株式会社 | 芳香族アミン誘導体及びそれを用いた有機エレクトロルミネッセンス素子 |
| JP5040216B2 (ja) | 2005-08-30 | 2012-10-03 | 三菱化学株式会社 | 有機化合物、電荷輸送材料、有機電界発光素子用材料、電荷輸送材料組成物及び有機電界発光素子 |
| WO2007028417A1 (en) | 2005-09-07 | 2007-03-15 | Technische Universität Braunschweig | Triplett emitter having condensed five-membered rings |
| KR20080063291A (ko) | 2005-09-30 | 2008-07-03 | 이데미쓰 고산 가부시키가이샤 | 유기 전계 발광 소자 |
| JP4887731B2 (ja) | 2005-10-26 | 2012-02-29 | コニカミノルタホールディングス株式会社 | 有機エレクトロルミネッセンス素子、表示装置及び照明装置 |
| US20070104977A1 (en) | 2005-11-07 | 2007-05-10 | Idemitsu Kosan Co., Ltd. | Organic electroluminescent device |
| US9023489B2 (en) | 2005-11-07 | 2015-05-05 | Lg Display Co., Ltd. | Red phosphorescent compounds and organic electroluminescent devices using the same |
| KR100662378B1 (ko) | 2005-11-07 | 2007-01-02 | 엘지전자 주식회사 | 적색 인광 화합물 및 이를 사용한 유기전계발광소자 |
| US7462406B2 (en) | 2005-11-15 | 2008-12-09 | Eastman Kodak Company | OLED devices with dinuclear copper compounds |
| US20070145888A1 (en) | 2005-11-16 | 2007-06-28 | Idemitsu Kosan Co., Ltd. | Aromatic amine derivatives and organic electroluminescence device using the same |
| US20080233410A1 (en) | 2005-11-17 | 2008-09-25 | Idemitsu Kosan Co., Ltd. | Transition metal complex compound |
| EP1956666A4 (en) | 2005-12-01 | 2010-06-16 | Nippon Steel Chemical Co | ORGANIC ELECTROLUMINESCENCE ELEMENT |
| CN102633820B (zh) | 2005-12-01 | 2015-01-21 | 新日铁住金化学株式会社 | 有机电致发光元件用化合物及有机电致发光元件 |
| JP2007153778A (ja) | 2005-12-02 | 2007-06-21 | Idemitsu Kosan Co Ltd | 含窒素複素環誘導体及びそれを用いた有機エレクトロルミネッセンス素子 |
| US7999103B2 (en) | 2005-12-15 | 2011-08-16 | Chuo University | Metal complex compound and organic electroluminescence device using the compound |
| KR20080081277A (ko) | 2005-12-15 | 2008-09-09 | 가코호진 쥬오 다이가쿠 | 금속 착체 화합물 및 그것을 이용한 유기 전기 발광 소자 |
| WO2007077766A1 (ja) | 2005-12-27 | 2007-07-12 | Idemitsu Kosan Co., Ltd. | 有機エレクトロルミネッセンス素子用材料及び有機エレクトロルミネッセンス素子 |
| JPWO2007080801A1 (ja) | 2006-01-11 | 2009-06-11 | 出光興産株式会社 | 新規イミド誘導体、有機エレクトロルミネッセンス素子用材料及びそれを用いた有機エレクトロルミネッセンス素子 |
| JP2007186461A (ja) | 2006-01-13 | 2007-07-26 | Idemitsu Kosan Co Ltd | 芳香族アミン誘導体及びそれを用いた有機エレクトロルミネッセンス素子 |
| US7759489B2 (en) | 2006-01-27 | 2010-07-20 | Idemitsu Kosan Co., Ltd. | Transition metal complex compound and organic electroluminescence device using the compound |
| KR102103062B1 (ko) | 2006-02-10 | 2020-04-22 | 유니버셜 디스플레이 코포레이션 | 시클로금속화 이미다조[1,2-f]페난트리딘 및 디이미다조[1,2-a:1',2'-c]퀴나졸린 리간드, 및 이의 등전자성 및 벤즈고리화된 유사체의 금속 착체 |
| US8142909B2 (en) | 2006-02-10 | 2012-03-27 | Universal Display Corporation | Blue phosphorescent imidazophenanthridine materials |
| JPWO2007102361A1 (ja) | 2006-03-07 | 2009-07-23 | 出光興産株式会社 | 芳香族アミン誘導体及びそれらを用いた有機エレクトロルミネッセンス素子 |
| WO2007108362A1 (ja) | 2006-03-17 | 2007-09-27 | Konica Minolta Holdings, Inc. | 有機エレクトロルミネッセンス素子、表示装置および照明装置 |
| JP4823730B2 (ja) | 2006-03-20 | 2011-11-24 | 新日鐵化学株式会社 | 発光層化合物及び有機電界発光素子 |
| ATE394800T1 (de) | 2006-03-21 | 2008-05-15 | Novaled Ag | Heterocyclisches radikal oder diradikal, deren dimere, oligomere, polymere, dispiroverbindungen und polycyclen, deren verwendung, organisches halbleitendes material sowie elektronisches bauelement |
| KR20070097139A (ko) | 2006-03-23 | 2007-10-04 | 엘지전자 주식회사 | 적색 인광 화합물 및 이를 사용한 유기전계발광소자 |
| KR20080105113A (ko) | 2006-03-27 | 2008-12-03 | 이데미쓰 고산 가부시키가이샤 | 함질소 복소환 유도체 및 그것을 이용한 유기 전기 발광 소자 |
| JP5273910B2 (ja) | 2006-03-31 | 2013-08-28 | キヤノン株式会社 | 発光素子用有機化合物、発光素子および画像表示装置 |
| EP2007781B1 (de) | 2006-04-04 | 2012-09-12 | Basf Se | Übergangsmetallkomplexe, enthaltend einen nicht-carben- und ein oder zwei carbenliganden und deren verwendung in oleds |
| WO2007115970A1 (de) | 2006-04-05 | 2007-10-18 | Basf Se | Heteroleptische übergangsmetall-carben-komplexe und deren verwendung in organischen leuchtdioden (oleds) |
| JP5103781B2 (ja) * | 2006-04-20 | 2012-12-19 | コニカミノルタホールディングス株式会社 | 化合物、該化合物を含む有機エレクトロルミネッセンス素子、照明装置 |
| EP2020694A4 (en) | 2006-04-20 | 2009-05-20 | Idemitsu Kosan Co | ORGANIC LIGHTING ELEMENT |
| WO2007125714A1 (ja) | 2006-04-26 | 2007-11-08 | Idemitsu Kosan Co., Ltd. | 芳香族アミン誘導体及びそれらを用いた有機エレクトロルミネッセンス素子 |
| US8076839B2 (en) | 2006-05-11 | 2011-12-13 | Idemitsu Kosan Co., Ltd. | Organic electroluminescence device |
| US8563145B2 (en) | 2006-06-02 | 2013-10-22 | Idemitsu Kosan Co., Ltd. | Material containing two or three dibenzofuran groups, dibenzothiophene groups, or a combination thereof, which is operable for organic electroluminescence elements, and organic electroluminescence elements using the material |
| US20070278936A1 (en) | 2006-06-02 | 2007-12-06 | Norman Herron | Red emitter complexes of IR(III) and devices made with such compounds |
| TW200815446A (en) | 2006-06-05 | 2008-04-01 | Idemitsu Kosan Co | Organic electroluminescent device and material for organic electroluminescent device |
| US7675228B2 (en) | 2006-06-14 | 2010-03-09 | E.I. Du Pont De Nemours And Company | Electroluminescent iridium compounds with silylated, germanylated, and stannylated ligands, and devices made with such compounds |
| US7629158B2 (en) | 2006-06-16 | 2009-12-08 | The Procter & Gamble Company | Cleaning and/or treatment compositions |
| JP5616582B2 (ja) | 2006-06-22 | 2014-10-29 | 出光興産株式会社 | 複素環含有アリールアミン誘導体を用いた有機エレクトロルミネッセンス素子 |
| JP2008021687A (ja) | 2006-07-10 | 2008-01-31 | Mitsubishi Chemicals Corp | 有機電界発光素子用材料、有機電界発光素子用組成物及び有機電界発光素子 |
| US7736756B2 (en) | 2006-07-18 | 2010-06-15 | Global Oled Technology Llc | Light emitting device containing phosphorescent complex |
| JP5203207B2 (ja) | 2006-08-23 | 2013-06-05 | 出光興産株式会社 | 芳香族アミン誘導体及びそれらを用いた有機エレクトロルミネッセンス素子 |
| JP2008069120A (ja) | 2006-09-15 | 2008-03-27 | Idemitsu Kosan Co Ltd | 芳香族アミン誘導体及びそれらを用いた有機エレクトロルミネッセンス素子 |
| WO2008035571A1 (fr) | 2006-09-20 | 2008-03-27 | Konica Minolta Holdings, Inc. | Élément électroluminescent organique |
| JP5589251B2 (ja) | 2006-09-21 | 2014-09-17 | コニカミノルタ株式会社 | 有機エレクトロルミネッセンス素子材料 |
| US7968146B2 (en) | 2006-11-01 | 2011-06-28 | The Trustees Of Princeton University | Hybrid layers for use in coatings on electronic devices or other articles |
| US8062769B2 (en) | 2006-11-09 | 2011-11-22 | Nippon Steel Chemical Co., Ltd. | Indolocarbazole compound for use in organic electroluminescent device and organic electroluminescent device |
| EP2518045A1 (en) | 2006-11-24 | 2012-10-31 | Idemitsu Kosan Co., Ltd. | Aromatic amine derivative and organic electroluminescent element using the same |
| US8778508B2 (en) | 2006-12-08 | 2014-07-15 | Universal Display Corporation | Light-emitting organometallic complexes |
| US8119255B2 (en) | 2006-12-08 | 2012-02-21 | Universal Display Corporation | Cross-linkable iridium complexes and organic light-emitting devices using the same |
| WO2008072596A1 (ja) | 2006-12-13 | 2008-06-19 | Konica Minolta Holdings, Inc. | 有機エレクトロルミネッセンス素子、表示装置及び照明装置 |
| JP2008150310A (ja) | 2006-12-15 | 2008-07-03 | Idemitsu Kosan Co Ltd | 芳香族アミン誘導体及びそれらを用いた有機エレクトロルミネッセンス素子 |
| JP5262104B2 (ja) | 2006-12-27 | 2013-08-14 | 住友化学株式会社 | 金属錯体、高分子化合物及びこれらを含む素子 |
| WO2008096609A1 (ja) | 2007-02-05 | 2008-08-14 | Idemitsu Kosan Co., Ltd. | 遷移金属錯体化合物及びそれを用いた有機エレクトロルミネッセンス素子 |
| JP5546255B2 (ja) | 2007-02-23 | 2014-07-09 | ビーエーエスエフ ソシエタス・ヨーロピア | 電界発光性のベンゾトリアゾールとの金属錯体 |
| TWI510598B (zh) | 2007-03-08 | 2015-12-01 | Universal Display Corp | 磷光材料 |
| US9130177B2 (en) | 2011-01-13 | 2015-09-08 | Universal Display Corporation | 5-substituted 2 phenylquinoline complexes materials for light emitting diode |
| CN101687893B (zh) | 2007-04-26 | 2014-01-22 | 巴斯夫欧洲公司 | 含有吩噻嗪s-氧化物或吩噻嗪s,s-二氧化物基团的硅烷及其在oled中的用途 |
| JP5053713B2 (ja) | 2007-05-30 | 2012-10-17 | キヤノン株式会社 | リン光発光材料、それを用いた有機電界発光素子及び画像表示装置 |
| CN101720330B (zh) | 2007-06-22 | 2017-06-09 | Udc爱尔兰有限责任公司 | 发光Cu(I)络合物 |
| DE102007031220B4 (de) | 2007-07-04 | 2022-04-28 | Novaled Gmbh | Chinoide Verbindungen und deren Verwendung in halbleitenden Matrixmaterialien, elektronischen und optoelektronischen Bauelementen |
| JP5675349B2 (ja) | 2007-07-05 | 2015-02-25 | ビーエーエスエフ ソシエタス・ヨーロピアBasf Se | カルベン遷移金属錯体発光体、ならびにジシリルカルバゾール、ジシリルジベンゾフラン、ジシリルジベンゾチオフェン、ジシリルジベンゾホスホール、ジシリルジベンゾチオフェンs−オキシドおよびジシリルジベンゾチオフェンs,s−ジオキシドから選択される少なくとも1つの化合物を含む有機発光ダイオード |
| US20090045731A1 (en) | 2007-07-07 | 2009-02-19 | Idemitsu Kosan Co., Ltd. | Organic electroluminescence device and material for organic electroluminescence device |
| WO2009008201A1 (ja) | 2007-07-07 | 2009-01-15 | Idemitsu Kosan Co., Ltd. | ナフタレン誘導体、有機el素子用材料及びそれを用いた有機el素子 |
| WO2009008205A1 (ja) | 2007-07-07 | 2009-01-15 | Idemitsu Kosan Co., Ltd. | 有機エレクトロルミネッセンス素子および有機エレクトロルミネッセンス素子用材料 |
| JP5473600B2 (ja) | 2007-07-07 | 2014-04-16 | 出光興産株式会社 | クリセン誘導体及びそれを用いた有機エレクトロルミネッセンス素子 |
| US8779655B2 (en) | 2007-07-07 | 2014-07-15 | Idemitsu Kosan Co., Ltd. | Organic electroluminescence device and material for organic electroluminescence device |
| US8080658B2 (en) | 2007-07-10 | 2011-12-20 | Idemitsu Kosan Co., Ltd. | Material for organic electroluminescent element and organic electroluminescent element employing the same |
| US8114530B2 (en) | 2007-07-10 | 2012-02-14 | Idemitsu Kosan Co., Ltd. | Material for organic electroluminescence device and organic electroluminescence device utilizing the same |
| KR20100031127A (ko) | 2007-07-11 | 2010-03-19 | 이데미쓰 고산 가부시키가이샤 | 유기 전계 발광 소자용 재료 및 유기 전계 발광 소자 |
| JP5289979B2 (ja) | 2007-07-18 | 2013-09-11 | 出光興産株式会社 | 有機エレクトロルミネッセンス素子用材料及び有機エレクトロルミネッセンス素子 |
| CN101688052A (zh) | 2007-07-27 | 2010-03-31 | E.I.内穆尔杜邦公司 | 包含无机纳米颗粒的导电聚合物的含水分散体 |
| KR20100038193A (ko) | 2007-08-06 | 2010-04-13 | 이데미쓰 고산 가부시키가이샤 | 방향족 아민 유도체 및 그것을 사용한 유기 전기 발광 소자 |
| TWI511964B (zh) | 2007-08-08 | 2015-12-11 | Universal Display Corp | 苯并稠合噻吩/聯伸三苯混合材料 |
| JP2009040728A (ja) | 2007-08-09 | 2009-02-26 | Canon Inc | 有機金属錯体及びこれを用いた有機発光素子 |
| US8956737B2 (en) | 2007-09-27 | 2015-02-17 | Lg Display Co., Ltd. | Red phosphorescent compound and organic electroluminescent device using the same |
| US8067100B2 (en) | 2007-10-04 | 2011-11-29 | Universal Display Corporation | Complexes with tridentate ligands |
| KR101642030B1 (ko) | 2007-10-17 | 2016-07-25 | 바스프 에스이 | 가교된 카르벤 리간드를 포함하는 전이 금속 착물 및 이의 용도 |
| WO2009050281A1 (de) | 2007-10-17 | 2009-04-23 | Basf Se | Übergangsmetallkomplexe mit verbrückten carbenliganden und deren verwendung in oleds |
| KR100950968B1 (ko) | 2007-10-18 | 2010-04-02 | 에스에프씨 주식회사 | 적색 인광 화합물 및 이를 이용한 유기전계발광소자 |
| US20090101870A1 (en) | 2007-10-22 | 2009-04-23 | E. I. Du Pont De Nemours And Company | Electron transport bi-layers and devices made with such bi-layers |
| US7914908B2 (en) | 2007-11-02 | 2011-03-29 | Global Oled Technology Llc | Organic electroluminescent device having an azatriphenylene derivative |
| DE102007053771A1 (de) | 2007-11-12 | 2009-05-14 | Merck Patent Gmbh | Organische Elektrolumineszenzvorrichtungen |
| KR101353635B1 (ko) | 2007-11-15 | 2014-01-20 | 이데미쓰 고산 가부시키가이샤 | 벤조크리센 유도체 및 이것을 사용한 유기 전계 발광 소자 |
| KR100933226B1 (ko) | 2007-11-20 | 2009-12-22 | 다우어드밴스드디스플레이머티리얼 유한회사 | 신규한 적색 인광 화합물 및 이를 발광재료로서 채용하고있는 유기발광소자 |
| US8759819B2 (en) | 2007-11-22 | 2014-06-24 | Idemitsu Kosan Co., Ltd. | Organic electroluminescence device |
| KR101583097B1 (ko) | 2007-11-22 | 2016-01-07 | 이데미쓰 고산 가부시키가이샤 | 유기 el 소자 및 유기 el 재료 함유 용액 |
| US8221905B2 (en) | 2007-12-28 | 2012-07-17 | Universal Display Corporation | Carbazole-containing materials in phosphorescent light emitting diodes |
| JPWO2009084268A1 (ja) | 2007-12-28 | 2011-05-12 | 出光興産株式会社 | 芳香族アミン誘導体及びそれらを用いた有機エレクトロルミネッセンス素子 |
| KR101691613B1 (ko) | 2008-02-12 | 2017-01-02 | 유디씨 아일랜드 리미티드 | 디벤조[f,h]퀴녹살린과의 전계발광 금속 착물 |
| JP2009221125A (ja) | 2008-03-14 | 2009-10-01 | Konica Minolta Business Technologies Inc | 銅錯体化合物及び電子写真用トナー |
| WO2009145016A1 (ja) | 2008-05-29 | 2009-12-03 | 出光興産株式会社 | 芳香族アミン誘導体及びそれらを用いた有機エレクトロルミネッセンス素子 |
| KR101011857B1 (ko) | 2008-06-04 | 2011-02-01 | 주식회사 두산 | 벤조플루오란센 유도체 및 이를 이용한 유기 발광 소자 |
| US8049411B2 (en) | 2008-06-05 | 2011-11-01 | Idemitsu Kosan Co., Ltd. | Material for organic electroluminescence device and organic electroluminescence device using the same |
| US8318323B2 (en) | 2008-06-05 | 2012-11-27 | Idemitsu Kosan Co., Ltd. | Polycyclic compounds and organic electroluminescence device employing the same |
| US8057919B2 (en) | 2008-06-05 | 2011-11-15 | Idemitsu Kosan Co., Ltd. | Material for organic electroluminescence device and organic electroluminescence device using the same |
| WO2009150151A1 (de) | 2008-06-10 | 2009-12-17 | Basf Se | Deuterierte übergangsmetall- komplexe und deren verwendung in organischen leuchtdioden - v |
| KR101913462B1 (ko) | 2008-06-30 | 2018-10-30 | 유니버셜 디스플레이 코포레이션 | 황 함유 그룹을 포함하는 정공 수송 물질 |
| KR101176261B1 (ko) | 2008-09-02 | 2012-08-22 | 주식회사 두산 | 안트라센 유도체 및 이를 이용한 유기 전계 발광 소자 |
| WO2010027583A1 (en) | 2008-09-03 | 2010-03-11 | Universal Display Corporation | Phosphorescent materials |
| TWI482756B (zh) | 2008-09-16 | 2015-05-01 | Universal Display Corp | 磷光物質 |
| EP2327679B1 (en) | 2008-09-24 | 2017-03-01 | LG Chem, Ltd. | Novel anthracene derivatives and organic electronic device using same |
| JP5530695B2 (ja) | 2008-10-23 | 2014-06-25 | 株式会社半導体エネルギー研究所 | 有機金属錯体、発光素子、及び電子機器 |
| KR101348699B1 (ko) | 2008-10-29 | 2014-01-08 | 엘지디스플레이 주식회사 | 적색 인광 물질 및 이를 이용한 유기전계발광소자 |
| KR100901888B1 (ko) | 2008-11-13 | 2009-06-09 | (주)그라쎌 | 신규한 전기발광용 유기금속 화합물 및 이를 발광재료로 채용하고 있는 전기발광소자 |
| DE102008057050B4 (de) | 2008-11-13 | 2021-06-02 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102008057051B4 (de) | 2008-11-13 | 2021-06-17 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| KR101571986B1 (ko) | 2008-11-25 | 2015-11-25 | 이데미쓰 고산 가부시키가이샤 | 방향족 아민 유도체 및 유기 전기발광 소자 |
| JP2010138121A (ja) | 2008-12-12 | 2010-06-24 | Canon Inc | トリアジン化合物及びこれを用いた有機発光素子 |
| DE102008064200A1 (de) | 2008-12-22 | 2010-07-01 | Merck Patent Gmbh | Organische Elektrolumineszenzvorrichtung |
| KR20100079458A (ko) | 2008-12-31 | 2010-07-08 | 덕산하이메탈(주) | 비스-카바졸 화합물 및 이를 이용한 유기전기소자, 그 단말 |
| US9067947B2 (en) | 2009-01-16 | 2015-06-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| DE102009007038A1 (de) | 2009-02-02 | 2010-08-05 | Merck Patent Gmbh | Metallkomplexe |
| WO2010101839A2 (en) * | 2009-03-02 | 2010-09-10 | Life Technologies Corporation | Chemiluminescent compositions, methods, assays and kits for oxidative enzymes |
| KR101511072B1 (ko) | 2009-03-20 | 2015-04-10 | 롬엔드하스전자재료코리아유한회사 | 신규한 유기 발광 화합물 및 이를 포함하는 유기 전계 발광소자 |
| US8709615B2 (en) * | 2011-07-28 | 2014-04-29 | Universal Display Corporation | Heteroleptic iridium complexes as dopants |
| US8722205B2 (en) | 2009-03-23 | 2014-05-13 | Universal Display Corporation | Heteroleptic iridium complex |
| WO2010118029A1 (en) | 2009-04-06 | 2010-10-14 | Universal Display Corporation | Metal complex comprising novel ligand structures |
| TWI638807B (zh) | 2009-04-28 | 2018-10-21 | 環球展覽公司 | 具有甲基-d3取代之銥錯合物 |
| US8603642B2 (en) | 2009-05-13 | 2013-12-10 | Global Oled Technology Llc | Internal connector for organic electronic devices |
| US8586203B2 (en) | 2009-05-20 | 2013-11-19 | Universal Display Corporation | Metal complexes with boron-nitrogen heterocycle containing ligands |
| JP2011018765A (ja) | 2009-07-08 | 2011-01-27 | Furukawa Electric Co Ltd:The | 光増幅用光ファイバおよび光ファイバ増幅器ならびに光ファイバレーザ |
| US8846965B2 (en) | 2009-07-22 | 2014-09-30 | Konica Minolta Business Technologies, Inc. | Toner for electrophotography and metal-containing compound |
| JP4590020B1 (ja) | 2009-07-31 | 2010-12-01 | 富士フイルム株式会社 | 電荷輸送材料及び有機電界発光素子 |
| KR101761431B1 (ko) | 2009-08-21 | 2017-07-25 | 토소가부시키가이샤 | 환상 아진 유도체와 그들의 제조방법 및 그들을 구성 성분으로 하는 유기 전계발광소자 |
| JP4551480B1 (ja) | 2009-08-31 | 2010-09-29 | 富士フイルム株式会社 | 有機電界発光素子 |
| DE102009042693A1 (de) * | 2009-09-23 | 2011-03-24 | Merck Patent Gmbh | Materialien für elektronische Vorrichtungen |
| DE102009049587A1 (de) | 2009-10-16 | 2011-04-21 | Merck Patent Gmbh | Metallkomplexe |
| EP2492986B1 (en) | 2009-10-23 | 2016-06-15 | Hodogaya Chemical Co., Ltd. | Organic electroluminescent element |
| US20120205645A1 (en) | 2009-10-28 | 2012-08-16 | Basf Se | Heteroleptic carbene complexes and the use thereof in organic electronics |
| JP2011121876A (ja) * | 2009-12-08 | 2011-06-23 | Canon Inc | 新規イリジウム錯体とそれを有する有機発光素子 |
| KR101288566B1 (ko) | 2009-12-16 | 2013-07-22 | 제일모직주식회사 | 유기광전소자용 화합물 및 이를 포함하는 유기광전소자 |
| WO2011075644A2 (en) | 2009-12-18 | 2011-06-23 | Plextronics, Inc. | Copolymers of 3,4-dialkoxythiophenes and methods for making and devices |
| KR101290011B1 (ko) | 2009-12-30 | 2013-07-30 | 주식회사 두산 | 유기발광 화합물 및 이를 포함한 유기 전계 발광 소자 |
| KR101183722B1 (ko) | 2009-12-30 | 2012-09-17 | 주식회사 두산 | 트리페닐렌계 화합물 및 이를 포함하는 유기 전계 발광 소자 |
| JP4617393B1 (ja) | 2010-01-15 | 2011-01-26 | 富士フイルム株式会社 | 有機電界発光素子 |
| EP2527334A4 (en) | 2010-01-21 | 2013-10-16 | Idemitsu Kosan Co | AROMATIC AMINE DERIVATIVE AND ORGANIC ELECTROLUMINESCENT ELEMENT THEREWITH |
| KR20110088898A (ko) | 2010-01-29 | 2011-08-04 | 주식회사 이엘엠 | 유기 전기 발광 조성물 및 이를 포함하는 유기 전기 발광 소자 |
| US9156870B2 (en) | 2010-02-25 | 2015-10-13 | Universal Display Corporation | Phosphorescent emitters |
| US20120319098A1 (en) | 2010-02-25 | 2012-12-20 | Shinshu University | Substituted pyridyl compound and organic electroluminescent element |
| DE102010002482B3 (de) | 2010-03-01 | 2012-01-05 | Technische Universität Braunschweig | Lumineszente Organometallverbindung |
| US9175211B2 (en) | 2010-03-03 | 2015-11-03 | Universal Display Corporation | Phosphorescent materials |
| KR101182444B1 (ko) | 2010-04-01 | 2012-09-12 | 삼성디스플레이 주식회사 | 유기 발광 소자 |
| EP2558476B1 (en) | 2010-04-16 | 2015-02-25 | Basf Se | Bridged benzimidazole-carbene complexes and use thereof in oleds |
| TWI395804B (zh) | 2010-05-18 | 2013-05-11 | Ind Tech Res Inst | 有機金屬化合物及包含其之有機電激發光裝置及組合物 |
| WO2011157339A1 (de) | 2010-06-15 | 2011-12-22 | Merck Patent Gmbh | Metallkomplexe |
| WO2012008281A1 (ja) | 2010-07-13 | 2012-01-19 | 東レ株式会社 | 発光素子 |
| KR20120032054A (ko) | 2010-07-28 | 2012-04-05 | 롬엔드하스전자재료코리아유한회사 | 신규한 유기 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 |
| TW201300501A (zh) | 2010-07-30 | 2013-01-01 | 羅門哈斯電子材料韓國公司 | 使用電場發光化合物作為發光材料之電場發光裝置 |
| JP5825846B2 (ja) | 2010-09-13 | 2015-12-02 | キヤノン株式会社 | 新規縮合多環化合物およびそれを有する有機発光素子 |
| JP5707818B2 (ja) | 2010-09-28 | 2015-04-30 | コニカミノルタ株式会社 | 有機エレクトロルミネッセンス素子用材料、有機エレクトロルミネッセンス素子、表示素子、照明装置及び金属錯体化合物 |
| JP5656534B2 (ja) | 2010-09-29 | 2015-01-21 | キヤノン株式会社 | インドロ[3,2,1−jk]カルバゾール化合物及びこれを有する有機発光素子 |
| DE102010054893A1 (de) * | 2010-12-17 | 2012-06-21 | Osram Opto Semiconductors Gmbh | Strahlungsemittierende organisch-elektronische Vorrichtung und Verfahren zu deren Herstellung |
| US9349964B2 (en) | 2010-12-24 | 2016-05-24 | Lg Chem, Ltd. | Organic light emitting diode and manufacturing method thereof |
| KR101350581B1 (ko) | 2010-12-29 | 2014-01-16 | 주식회사 엘지화학 | 새로운 화합물 및 이를 이용한 유기 발광 소자 |
| US8415031B2 (en) | 2011-01-24 | 2013-04-09 | Universal Display Corporation | Electron transporting compounds |
| CN115448957A (zh) | 2011-02-23 | 2022-12-09 | 通用显示公司 | 新型的四齿铂络合物 |
| EP2690093A4 (en) | 2011-03-24 | 2014-08-13 | Idemitsu Kosan Co | BISCARBAZOLE DERIVATIVE AND ORGANIC ELECTROLUMINESCENT ELEMENT THEREWITH |
| JP5984450B2 (ja) | 2011-03-31 | 2016-09-06 | ユー・ディー・シー アイルランド リミテッド | 有機電界発光素子、並びに、該素子を用いた発光装置、表示装置、照明装置及び該素子用の化合物 |
| JP5906114B2 (ja) | 2011-03-31 | 2016-04-20 | ユー・ディー・シー アイルランド リミテッド | 電荷輸送材料、有機電界発光素子、発光装置、表示装置および照明装置 |
| KR101298735B1 (ko) | 2011-04-06 | 2013-08-21 | 한국화학연구원 | 신규 유기금속 화합물 및 이를 이용한 유기 발광 소자 |
| KR101888658B1 (ko) | 2011-04-15 | 2018-08-14 | 에스에프씨 주식회사 | 신규한 화합물 및 이를 포함하는 유기전계발광소자 |
| US8795850B2 (en) | 2011-05-19 | 2014-08-05 | Universal Display Corporation | Phosphorescent heteroleptic phenylbenzimidazole dopants and new synthetic methodology |
| KR20120129733A (ko) | 2011-05-20 | 2012-11-28 | (주)씨에스엘쏠라 | 유기발광화합물 및 이를 이용한 유기 광소자 |
| US10158089B2 (en) * | 2011-05-27 | 2018-12-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| CN103619860B (zh) | 2011-06-03 | 2016-08-17 | 默克专利有限公司 | 金属络合物 |
| WO2012177006A2 (ko) | 2011-06-22 | 2012-12-27 | 덕산하이메탈(주) | 유기전기소자용 화합물, 이를 이용한 유기전기소자 및 그 전자 장치 |
| US9309223B2 (en) | 2011-07-08 | 2016-04-12 | Semiconductor Energy Laboratory Co., Ltd. | Heterocyclic compound, light-emitting element, light-emitting device, electronic device, and lighting device |
| JP5882621B2 (ja) | 2011-08-01 | 2016-03-09 | キヤノン株式会社 | アミノインドロ[3,2,1−jk]カルバゾール化合物及びそれを有する有機発光素子 |
| US9167260B2 (en) * | 2011-08-02 | 2015-10-20 | Advanced Micro Devices, Inc. | Apparatus and method for video processing |
| TWI429652B (zh) | 2011-08-05 | 2014-03-11 | Ind Tech Res Inst | 有機金屬化合物及包含其之有機電激發光裝置 |
| KR102138351B1 (ko) | 2011-08-18 | 2020-07-28 | 이데미쓰 고산 가부시키가이샤 | 비스카르바졸 유도체 및 이것을 사용한 유기 일렉트로루미네선스 소자 |
| CN103797605B (zh) | 2011-09-09 | 2016-12-21 | 株式会社Lg化学 | 用于有机发光器件的材料及使用该材料的有机发光器件 |
| KR102048688B1 (ko) | 2011-09-09 | 2019-11-26 | 이데미쓰 고산 가부시키가이샤 | 질소 함유 헤테로 방향족환 화합물 |
| KR101992874B1 (ko) | 2011-09-12 | 2019-06-26 | 닛테츠 케미컬 앤드 머티리얼 가부시키가이샤 | 유기 전계 발광 소자 |
| US9634255B2 (en) | 2011-09-15 | 2017-04-25 | Idemitsu Kosan Co., Ltd. | Aromatic amine derivative and organic electroluminescence element using same |
| KR101897044B1 (ko) | 2011-10-20 | 2018-10-23 | 에스에프씨 주식회사 | 유기금속 화합물 및 이를 포함하는 유기전계발광소자 |
| KR20130053846A (ko) | 2011-11-16 | 2013-05-24 | 롬엔드하스전자재료코리아유한회사 | 신규한 유기 발광 화합물 및 이를 채용하고 있는 유기 전계 발광 소자 |
| JP5783007B2 (ja) | 2011-11-21 | 2015-09-24 | コニカミノルタ株式会社 | 有機エレクトロルミネッセンス素子および照明装置 |
| WO2013081315A1 (ko) | 2011-11-28 | 2013-06-06 | 덕산하이메탈(주) | 유기전기소자용 화합물, 이를 포함하는 유기전기소자 및 그 전자 장치 |
| WO2013079217A1 (en) | 2011-11-30 | 2013-06-06 | Novaled Ag | Display |
| CN103959503B (zh) | 2011-12-05 | 2016-08-24 | 出光兴产株式会社 | 有机电致发光元件用材料以及有机电致发光元件 |
| US9512355B2 (en) | 2011-12-09 | 2016-12-06 | Universal Display Corporation | Organic light emitting materials |
| KR101961613B1 (ko) | 2011-12-12 | 2019-03-25 | 메르크 파텐트 게엠베하 | 전자 소자용 화합물 |
| TWI523845B (zh) | 2011-12-23 | 2016-03-01 | 半導體能源研究所股份有限公司 | 有機金屬錯合物,發光元件,發光裝置,電子裝置及照明裝置 |
| KR101497135B1 (ko) | 2011-12-29 | 2015-03-02 | 제일모직 주식회사 | 유기광전자소자용 화합물, 이를 포함하는 유기발광소자 및 상기 유기발광소자를 포함하는 표시장치 |
| CN107814821A (zh) | 2012-01-12 | 2018-03-20 | Udc 爱尔兰有限责任公司 | 具有二苯并[f,h]喹喔啉的金属配合物 |
| CN106986858B (zh) | 2012-01-16 | 2019-08-27 | 默克专利有限公司 | 有机金属络合物 |
| US10211413B2 (en) | 2012-01-17 | 2019-02-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| JP5857754B2 (ja) | 2012-01-23 | 2016-02-10 | コニカミノルタ株式会社 | 有機エレクトロルミネッセンス素子、有機エレクトロルミネッセンス素子の製造方法、表示装置及び照明装置 |
| JP5981770B2 (ja) | 2012-01-23 | 2016-08-31 | ユー・ディー・シー アイルランド リミテッド | 有機電界発光素子、有機電界発光素子用電荷輸送材料、並びに、該素子を用いた発光装置、表示装置及び照明装置 |
| WO2013118812A1 (ja) | 2012-02-10 | 2013-08-15 | 出光興産株式会社 | 有機エレクトロルミネッセンス素子 |
| CN104114672B (zh) | 2012-02-14 | 2017-03-15 | 默克专利有限公司 | 用于有机电致发光器件的螺二芴化合物 |
| DE102012005215B3 (de) | 2012-03-15 | 2013-04-11 | Novaled Ag | Aromatische Amin-Terphenyl-Verbindungen und Verwendung derselben in organischen halbleitenden Bauelementen |
| US9054323B2 (en) | 2012-03-15 | 2015-06-09 | Universal Display Corporation | Secondary hole transporting layer with diarylamino-phenyl-carbazole compounds |
| US20130248830A1 (en) | 2012-03-22 | 2013-09-26 | Rohm And Haas Electronic Materials Korea Ltd. | Charge transport layers and films containing the same |
| EP2828274A4 (en) | 2012-03-23 | 2015-10-21 | Du Pont | GREEN FLUORES |
| WO2013145667A1 (ja) | 2012-03-29 | 2013-10-03 | ソニー株式会社 | 有機エレクトロルミネッセンス素子 |
| DE102012205945A1 (de) | 2012-04-12 | 2013-10-17 | Siemens Aktiengesellschaft | Organische Superdonoren mit mindestens zwei gekoppelten Carben-Gruppen und deren Verwendung als n-Dotierstoffe |
| KR101565200B1 (ko) | 2012-04-12 | 2015-11-02 | 주식회사 엘지화학 | 신규한 화합물 및 이를 이용한 유기 발광 소자 |
| JP2015155378A (ja) | 2012-04-18 | 2015-08-27 | 保土谷化学工業株式会社 | トリフェニレン環構造を有する化合物および有機エレクトロルミネッセンス素子 |
| WO2013175747A1 (ja) | 2012-05-22 | 2013-11-28 | 出光興産株式会社 | 有機エレクトロルミネッセンス素子 |
| EP2856528B1 (en) | 2012-05-24 | 2019-07-03 | Merck Patent GmbH | Metal complexes comprising condensed heteroaromatic rings |
| WO2013180376A1 (en) | 2012-05-30 | 2013-12-05 | Alpha Chem Co., Ltd. | New electron transport material and organic electroluminescent device using the same |
| CN102702075A (zh) | 2012-06-13 | 2012-10-03 | 吉林奥来德光电材料股份有限公司 | 含有三芳胺结构的有机电致发光材料及制备方法和应用 |
| CN103508940B (zh) | 2012-06-21 | 2017-05-03 | 昆山维信诺显示技术有限公司 | 一种6,6‑双取代‑6‑H‑苯并[cd]芘衍生物、中间体及制备方法和应用 |
| KR101507423B1 (ko) | 2012-06-22 | 2015-04-08 | 덕산네오룩스 주식회사 | 화합물, 이를 이용한 유기전기소자 및 그 전자 장치 |
| JP6088161B2 (ja) | 2012-06-29 | 2017-03-01 | 出光興産株式会社 | 芳香族アミン誘導体及び有機エレクトロルミネッセンス素子 |
| EP2871222B1 (en) | 2012-07-04 | 2017-04-26 | Samsung SDI Co., Ltd. | Compound for organic optoelectric device, organic optoelectric device comprising same, and display apparatus comprising organic optoelectric device |
| EP2684932B8 (en) | 2012-07-09 | 2016-12-21 | Hodogaya Chemical Co., Ltd. | Diarylamino matrix material doped with a mesomeric radialene compound |
| KR20140008126A (ko) | 2012-07-10 | 2014-01-21 | 삼성디스플레이 주식회사 | 유기 발광 장치 |
| US9559310B2 (en) | 2012-07-11 | 2017-01-31 | Samsung Display Co., Ltd. | Compound with electron injection and/or electron transport capabilities and organic light-emitting device including the same |
| KR102076481B1 (ko) | 2012-07-13 | 2020-02-12 | 메르크 파텐트 게엠베하 | 금속 착물 |
| KR101452577B1 (ko) | 2012-07-20 | 2014-10-21 | 주식회사 두산 | 유기 발광 화합물 및 이를 이용한 유기 전계 발광 소자 |
| CN104487541B (zh) | 2012-07-23 | 2019-07-26 | 默克专利有限公司 | 化合物以及有机电致发光器件 |
| KR102696532B1 (ko) | 2012-07-23 | 2024-08-19 | 메르크 파텐트 게엠베하 | 플루오렌 및 이를 함유하는 전자 소자 |
| KR102192286B1 (ko) | 2012-08-07 | 2020-12-17 | 메르크 파텐트 게엠베하 | 금속 착물 |
| EP2882766B1 (en) | 2012-08-09 | 2019-11-27 | UDC Ireland Limited | Transition metal complexes with carbene ligands and use thereof in oleds |
| KR101497138B1 (ko) | 2012-08-21 | 2015-02-27 | 제일모직 주식회사 | 유기광전자소자 및 이를 포함하는 표시장치 |
| KR102128702B1 (ko) | 2012-08-21 | 2020-07-02 | 롬엔드하스전자재료코리아유한회사 | 신규한 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 |
| US9711741B2 (en) | 2012-08-24 | 2017-07-18 | Arizona Board Of Regents On Behalf Of Arizona State University | Metal compounds and methods and uses thereof |
| US20150228899A1 (en) | 2012-08-31 | 2015-08-13 | Idemitsu Kosan Co., Ltd. | Organic electroluminescent element |
| JP6119754B2 (ja) | 2012-09-04 | 2017-04-26 | コニカミノルタ株式会社 | 有機エレクトロルミネッセンス素子、照明装置及び表示装置 |
| JP2014082235A (ja) | 2012-10-12 | 2014-05-08 | Semiconductor Energy Lab Co Ltd | 発光素子 |
| KR101848885B1 (ko) | 2012-10-29 | 2018-04-16 | 삼성디스플레이 주식회사 | 아민계 화합물 및 이를 포함한 유기 발광 소자 |
| US9595682B2 (en) * | 2012-10-30 | 2017-03-14 | Massachusetts Institute Of Technology | Organic conductive materials and devices |
| US9634264B2 (en) * | 2012-11-09 | 2017-04-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US8946697B1 (en) | 2012-11-09 | 2015-02-03 | Universal Display Corporation | Iridium complexes with aza-benzo fused ligands |
| US9685617B2 (en) * | 2012-11-09 | 2017-06-20 | Universal Display Corporation | Organic electronuminescent materials and devices |
| JP6253971B2 (ja) | 2012-12-28 | 2017-12-27 | 株式会社半導体エネルギー研究所 | 発光素子、発光装置、電子機器、及び照明装置 |
| KR101684979B1 (ko) | 2012-12-31 | 2016-12-09 | 제일모직 주식회사 | 유기광전자소자 및 이를 포함하는 표시장치 |
| KR20140087647A (ko) | 2012-12-31 | 2014-07-09 | 제일모직주식회사 | 유기광전자소자용 화합물, 이를 포함하는 유기발광소자 및 상기 유기발광소자를 포함하는 표시장치 |
| WO2014104535A1 (ko) | 2012-12-31 | 2014-07-03 | 제일모직 주식회사 | 유기광전자소자용 화합물, 이를 포함하는 유기발광소자 및 상기 유기발광소자를 포함하는 표시장치 |
| JP6071569B2 (ja) | 2013-01-17 | 2017-02-01 | キヤノン株式会社 | 有機発光素子 |
| US9627629B2 (en) | 2013-02-12 | 2017-04-18 | Samsung Electronics Co., Ltd. | Compound for organic optoelectronic device, organic light emitting diode including the same, and display including the organic light emitting diode |
| EP3882254B1 (en) * | 2013-02-21 | 2023-10-04 | Universal Display Corporation | Phosphorescent homoleptic tris-[deuterated-2(2-pyridinyl)phenyl]-iridium complexes for use in light-emitting devices |
| TWI612051B (zh) | 2013-03-01 | 2018-01-21 | 半導體能源研究所股份有限公司 | 有機金屬錯合物、發光元件、發光裝置、電子裝置、照明設備 |
| KR102081689B1 (ko) | 2013-03-15 | 2020-02-26 | 덕산네오룩스 주식회사 | 유기전기 소자용 화합물, 이를 이용한 유기전기소자 및 그 전자 장치 |
| US20140284580A1 (en) | 2013-03-22 | 2014-09-25 | E-Ray Optoelectronics Techonology Co., Ltd. | Electron transporting compounds and organic electroluminescent devices using the same |
| KR102136040B1 (ko) | 2013-03-26 | 2020-07-20 | 가부시키가이샤 한도오따이 에네루기 켄큐쇼 | 유기 화합물, 발광 소자, 발광 장치, 표시 장치, 전자 기기 및 조명 장치 |
| CN103254243A (zh) | 2013-05-02 | 2013-08-21 | 太原理工大学 | 一种多取代苯基喹啉铱(iii)配合物及其制备方法和应用 |
| EP3023477B1 (en) | 2013-07-17 | 2019-02-06 | Sumitomo Chemical Company Limited | Composition, and light-emitting element using same |
| CN105555792B (zh) | 2013-09-17 | 2019-12-31 | 默克专利有限公司 | 用于oled的多环苯基吡啶铱络合物及其衍生物 |
| KR20150052913A (ko) | 2013-11-06 | 2015-05-15 | 주식회사 네패스 | 이리듐 발광 화합물 및 이를 채용한 유기발광 소자 |
| CN103694277A (zh) | 2013-12-12 | 2014-04-02 | 江西冠能光电材料有限公司 | 一种红色磷光有机发光二极管 |
| US9847496B2 (en) | 2013-12-23 | 2017-12-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2015104045A1 (de) | 2014-01-13 | 2015-07-16 | Merck Patent Gmbh | Metallkomplexe |
| WO2015112561A1 (en) | 2014-01-23 | 2015-07-30 | E. I. Du Pont De Nemours And Company | Electroactive metal complexes |
| CN105980519B (zh) | 2014-02-05 | 2019-06-14 | 默克专利有限公司 | 金属络合物 |
| JP2015173199A (ja) | 2014-03-12 | 2015-10-01 | キヤノン株式会社 | 有機発光素子 |
| JP5842989B2 (ja) * | 2014-04-18 | 2016-01-13 | 住友化学株式会社 | 組成物およびそれを用いた発光素子 |
| KR102384222B1 (ko) * | 2014-09-26 | 2022-04-07 | 삼성전자주식회사 | 유기금속 화합물 및 이를 포함한 유기 발광 소자 |
| US20160155962A1 (en) * | 2014-11-28 | 2016-06-02 | Samsung Electronics Co., Ltd. | Organometallic compound and organic light-emitting device including the same |
| KR102343146B1 (ko) * | 2014-12-16 | 2021-12-27 | 삼성디스플레이 주식회사 | 유기금속 화합물 및 이를 포함한 유기 발광 소자 |
| KR102395990B1 (ko) * | 2014-12-30 | 2022-05-10 | 삼성전자주식회사 | 유기금속 화합물 및 이를 포함한 유기 발광 소자 |
| US10672996B2 (en) * | 2015-09-03 | 2020-06-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10236456B2 (en) * | 2016-04-11 | 2019-03-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11081647B2 (en) * | 2016-04-22 | 2021-08-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11482683B2 (en) * | 2016-06-20 | 2022-10-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10862054B2 (en) * | 2016-06-20 | 2020-12-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10608186B2 (en) * | 2016-09-14 | 2020-03-31 | Universal Display Corporation | Organic electroluminescent materials and devices |
-
2016
- 2016-08-18 US US15/239,961 patent/US10672996B2/en active Active
- 2016-08-18 US US15/240,044 patent/US10361381B2/en active Active
- 2016-08-31 EP EP16186500.1A patent/EP3159350B1/en active Active
- 2016-08-31 EP EP20192873.6A patent/EP3760635A1/en active Pending
- 2016-09-01 KR KR1020160112440A patent/KR102693087B1/ko active IP Right Grant
- 2016-09-01 KR KR1020160112495A patent/KR102659792B1/ko active IP Right Grant
- 2016-09-02 CN CN201610843457.8A patent/CN106946940B/zh active Active
- 2016-09-02 JP JP2016171524A patent/JP6725369B2/ja active Active
- 2016-09-02 CN CN202310717040.7A patent/CN116731083A/zh active Pending
- 2016-09-02 TW TW105128541A patent/TWI721009B/zh active
- 2016-09-02 TW TW110108557A patent/TWI841827B/zh active
- 2016-09-02 JP JP2016171527A patent/JP6910770B2/ja active Active
-
2019
- 2019-06-12 US US16/438,819 patent/US11605789B2/en active Active
-
2020
- 2020-03-10 US US16/814,529 patent/US11626563B2/en active Active
- 2020-06-25 JP JP2020109327A patent/JP7042871B2/ja active Active
-
2021
- 2021-07-07 JP JP2021112802A patent/JP2021178826A/ja not_active Withdrawn
-
2022
- 2022-02-03 JP JP2022015318A patent/JP7370400B2/ja active Active
-
2023
- 2023-01-12 US US18/153,542 patent/US20230354690A1/en active Pending
- 2023-02-17 US US18/171,274 patent/US20230209990A1/en active Pending
- 2023-06-09 JP JP2023095236A patent/JP2023126777A/ja active Pending
- 2023-10-17 JP JP2023178539A patent/JP2024009984A/ja active Pending
-
2024
- 2024-04-17 KR KR1020240051434A patent/KR20240058808A/ko active Search and Examination
- 2024-08-02 KR KR1020240102940A patent/KR20240123292A/ko active Search and Examination
Patent Citations (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20110105800A (ko) * | 2008-12-12 | 2011-09-27 | 유니버셜 디스플레이 코포레이션 | 이미다조[1,2f] 펜안트리딘 이리듐 착체계 고효율 청색 이미터 |
| KR20140015306A (ko) * | 2011-03-10 | 2014-02-06 | 린텍 가부시키가이샤 | 인광 발광 재료, 인광 발광 재료의 제조 방법, 및 인광 발광 소자 |
| KR20140027389A (ko) * | 2011-05-27 | 2014-03-06 | 유니버셜 디스플레이 코포레이션 | Oled 디바이스용 고 효율 황색광 이미터 |
| JP2014532033A (ja) * | 2011-05-27 | 2014-12-04 | ユニバーサル ディスプレイ コーポレイション | Oledデバイス用高効率黄色光発光体 |
| KR20140117401A (ko) * | 2012-01-13 | 2014-10-07 | 미쓰비시 가가꾸 가부시키가이샤 | 이리듐 착물 화합물 그리고 그 화합물을 함유하는 용액 조성물, 유기 전계 발광 소자, 표시 장치 및 조명 장치 |
| KR20150040912A (ko) * | 2012-08-08 | 2015-04-15 | 미쓰비시 가가꾸 가부시키가이샤 | 이리듐 착물 화합물, 그리고 그 화합물을 포함하는 조성물, 유기 전계 발광 소자, 표시 장치 및 조명 장치 |
| KR20140104926A (ko) * | 2013-02-21 | 2014-08-29 | 유니버셜 디스플레이 코포레이션 | 인광성 화합물 |
| KR20150066202A (ko) * | 2013-12-06 | 2015-06-16 | 롬엔드하스전자재료코리아유한회사 | 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US11569461B2 (en) | 2017-12-08 | 2023-01-31 | Samsung Display Co., Ltd. | Organic electroluminescence device and organometallic compound for organic electroluminescence device |
| US11145829B2 (en) | 2018-02-02 | 2021-10-12 | Samsung Display Co., Ltd. | Organic electroluminescent device, organic electroluminescent display device including the same, and organometallic compound for organic electroluminescent device |
| KR20200066575A (ko) * | 2018-11-30 | 2020-06-10 | 유니버셜 디스플레이 코포레이션 | 표면-플라즈몬-펌핑된 발광 디바이스 |
| US11731994B2 (en) | 2018-12-05 | 2023-08-22 | Samsung Electronics Co., Ltd. | Organometallic compound, organic light-emitting device including the organometallic compound, and diagnostic composition including the organometallic compound |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7370400B2 (ja) | 有機エレクトロルミネセンス材料及びデバイス | |
| KR102635068B1 (ko) | 유기 전계발광 물질 및 디바이스 | |
| JP7373536B2 (ja) | 有機エレクトロルミネセンス材料及びデバイス | |
| KR102495218B1 (ko) | 유기 전계발광 물질 및 디바이스 | |
| JP7482939B2 (ja) | 有機エレクトロルミネセンス材料及びデバイス | |
| KR20230054647A (ko) | 유기 전계발광 물질 및 디바이스 | |
| EP3231809B1 (en) | Organic electroluminescent materials and devices | |
| KR20160041771A (ko) | 유기 전계발광 물질 및 소자 | |
| KR20160141661A (ko) | 유기 전계발광 재료 및 디바이스 | |
| EP3858844A1 (en) | Organic electroluminescent materials and devices | |
| KR20180057544A (ko) | 유기 전계발광 물질 및 디바이스 | |
| KR20220074833A (ko) | 유기 전계발광 물질 및 디바이스 | |
| US10177318B2 (en) | Organic electroluminescent materials and devices |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| E902 | Notification of reason for refusal | ||
| E701 | Decision to grant or registration of patent right | ||
| GRNT | Written decision to grant |