JP7003349B2 - ホメオトロピック配向を有する液晶媒体 - Google Patents
ホメオトロピック配向を有する液晶媒体 Download PDFInfo
- Publication number
- JP7003349B2 JP7003349B2 JP2015046649A JP2015046649A JP7003349B2 JP 7003349 B2 JP7003349 B2 JP 7003349B2 JP 2015046649 A JP2015046649 A JP 2015046649A JP 2015046649 A JP2015046649 A JP 2015046649A JP 7003349 B2 JP7003349 B2 JP 7003349B2
- Authority
- JP
- Japan
- Prior art keywords
- atoms
- group
- independently
- formula
- groups
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/06—Non-steroidal liquid crystal compounds
- C09K19/34—Non-steroidal liquid crystal compounds containing at least one heterocyclic ring
- C09K19/3402—Non-steroidal liquid crystal compounds containing at least one heterocyclic ring having oxygen as hetero atom
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/06—Non-steroidal liquid crystal compounds
- C09K19/08—Non-steroidal liquid crystal compounds containing at least two non-condensed rings
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/06—Non-steroidal liquid crystal compounds
- C09K19/08—Non-steroidal liquid crystal compounds containing at least two non-condensed rings
- C09K19/10—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing at least two benzene rings
- C09K19/14—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing at least two benzene rings linked by a carbon chain
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/06—Non-steroidal liquid crystal compounds
- C09K19/08—Non-steroidal liquid crystal compounds containing at least two non-condensed rings
- C09K19/30—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing saturated or unsaturated non-aromatic rings, e.g. cyclohexane rings
- C09K19/3001—Cyclohexane rings
- C09K19/3003—Compounds containing at least two rings in which the different rings are directly linked (covalent bond)
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/06—Non-steroidal liquid crystal compounds
- C09K19/08—Non-steroidal liquid crystal compounds containing at least two non-condensed rings
- C09K19/30—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing saturated or unsaturated non-aromatic rings, e.g. cyclohexane rings
- C09K19/3001—Cyclohexane rings
- C09K19/3066—Cyclohexane rings in which the rings are linked by a chain containing carbon and oxygen atoms, e.g. esters or ethers
- C09K19/3068—Cyclohexane rings in which the rings are linked by a chain containing carbon and oxygen atoms, e.g. esters or ethers chain containing -COO- or -OCO- groups
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/38—Polymers
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/38—Polymers
- C09K19/3833—Polymers with mesogenic groups in the side chain
- C09K19/3842—Polyvinyl derivatives
- C09K19/3852—Poly(meth)acrylate derivatives
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/42—Mixtures of liquid crystal compounds covered by two or more of the preceding groups C09K19/06 - C09K19/40
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/52—Liquid crystal materials characterised by components which are not liquid crystals, e.g. additives with special physical aspect: solvents, solid particles
- C09K19/54—Additives having no specific mesophase characterised by their chemical composition
- C09K19/56—Aligning agents
-
- G—PHYSICS
- G02—OPTICS
- G02F—OPTICAL DEVICES OR ARRANGEMENTS FOR THE CONTROL OF LIGHT BY MODIFICATION OF THE OPTICAL PROPERTIES OF THE MEDIA OF THE ELEMENTS INVOLVED THEREIN; NON-LINEAR OPTICS; FREQUENCY-CHANGING OF LIGHT; OPTICAL LOGIC ELEMENTS; OPTICAL ANALOGUE/DIGITAL CONVERTERS
- G02F1/00—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics
- G02F1/01—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics for the control of the intensity, phase, polarisation or colour
- G02F1/13—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics for the control of the intensity, phase, polarisation or colour based on liquid crystals, e.g. single liquid crystal display cells
- G02F1/133—Constructional arrangements; Operation of liquid crystal cells; Circuit arrangements
- G02F1/1333—Constructional arrangements; Manufacturing methods
- G02F1/1337—Surface-induced orientation of the liquid crystal molecules, e.g. by alignment layers
-
- G—PHYSICS
- G02—OPTICS
- G02F—OPTICAL DEVICES OR ARRANGEMENTS FOR THE CONTROL OF LIGHT BY MODIFICATION OF THE OPTICAL PROPERTIES OF THE MEDIA OF THE ELEMENTS INVOLVED THEREIN; NON-LINEAR OPTICS; FREQUENCY-CHANGING OF LIGHT; OPTICAL LOGIC ELEMENTS; OPTICAL ANALOGUE/DIGITAL CONVERTERS
- G02F1/00—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics
- G02F1/01—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics for the control of the intensity, phase, polarisation or colour
- G02F1/13—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics for the control of the intensity, phase, polarisation or colour based on liquid crystals, e.g. single liquid crystal display cells
- G02F1/133—Constructional arrangements; Operation of liquid crystal cells; Circuit arrangements
- G02F1/1333—Constructional arrangements; Manufacturing methods
- G02F1/1337—Surface-induced orientation of the liquid crystal molecules, e.g. by alignment layers
- G02F1/13378—Surface-induced orientation of the liquid crystal molecules, e.g. by alignment layers by treatment of the surface, e.g. embossing, rubbing or light irradiation
- G02F1/133788—Surface-induced orientation of the liquid crystal molecules, e.g. by alignment layers by treatment of the surface, e.g. embossing, rubbing or light irradiation by light irradiation, e.g. linearly polarised light photo-polymerisation
-
- G—PHYSICS
- G02—OPTICS
- G02F—OPTICAL DEVICES OR ARRANGEMENTS FOR THE CONTROL OF LIGHT BY MODIFICATION OF THE OPTICAL PROPERTIES OF THE MEDIA OF THE ELEMENTS INVOLVED THEREIN; NON-LINEAR OPTICS; FREQUENCY-CHANGING OF LIGHT; OPTICAL LOGIC ELEMENTS; OPTICAL ANALOGUE/DIGITAL CONVERTERS
- G02F1/00—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics
- G02F1/01—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics for the control of the intensity, phase, polarisation or colour
- G02F1/13—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics for the control of the intensity, phase, polarisation or colour based on liquid crystals, e.g. single liquid crystal display cells
- G02F1/133—Constructional arrangements; Operation of liquid crystal cells; Circuit arrangements
- G02F1/1333—Constructional arrangements; Manufacturing methods
- G02F1/1341—Filling or closing of cells
-
- G—PHYSICS
- G02—OPTICS
- G02F—OPTICAL DEVICES OR ARRANGEMENTS FOR THE CONTROL OF LIGHT BY MODIFICATION OF THE OPTICAL PROPERTIES OF THE MEDIA OF THE ELEMENTS INVOLVED THEREIN; NON-LINEAR OPTICS; FREQUENCY-CHANGING OF LIGHT; OPTICAL LOGIC ELEMENTS; OPTICAL ANALOGUE/DIGITAL CONVERTERS
- G02F1/00—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics
- G02F1/01—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics for the control of the intensity, phase, polarisation or colour
- G02F1/13—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics for the control of the intensity, phase, polarisation or colour based on liquid crystals, e.g. single liquid crystal display cells
- G02F1/133—Constructional arrangements; Operation of liquid crystal cells; Circuit arrangements
- G02F1/1333—Constructional arrangements; Manufacturing methods
- G02F1/1343—Electrodes
- G02F1/134309—Electrodes characterised by their geometrical arrangement
- G02F1/134363—Electrodes characterised by their geometrical arrangement for applying an electric field parallel to the substrate, i.e. in-plane switching [IPS]
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K2019/0425—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit characterized by a specific unit that results in a functional effect
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K2019/0444—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit characterized by a linking chain between rings or ring systems, a bridging chain between extensive mesogenic moieties or an end chain group
- C09K2019/0448—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit characterized by a linking chain between rings or ring systems, a bridging chain between extensive mesogenic moieties or an end chain group the end chain group being a polymerizable end group, e.g. -Sp-P or acrylate
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/06—Non-steroidal liquid crystal compounds
- C09K19/08—Non-steroidal liquid crystal compounds containing at least two non-condensed rings
- C09K19/10—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing at least two benzene rings
- C09K19/12—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing at least two benzene rings at least two benzene rings directly linked, e.g. biphenyls
- C09K2019/121—Compounds containing phenylene-1,4-diyl (-Ph-)
- C09K2019/122—Ph-Ph
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/06—Non-steroidal liquid crystal compounds
- C09K19/08—Non-steroidal liquid crystal compounds containing at least two non-condensed rings
- C09K19/10—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing at least two benzene rings
- C09K19/12—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing at least two benzene rings at least two benzene rings directly linked, e.g. biphenyls
- C09K2019/121—Compounds containing phenylene-1,4-diyl (-Ph-)
- C09K2019/123—Ph-Ph-Ph
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/06—Non-steroidal liquid crystal compounds
- C09K19/08—Non-steroidal liquid crystal compounds containing at least two non-condensed rings
- C09K19/30—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing saturated or unsaturated non-aromatic rings, e.g. cyclohexane rings
- C09K19/3001—Cyclohexane rings
- C09K19/3003—Compounds containing at least two rings in which the different rings are directly linked (covalent bond)
- C09K2019/3004—Cy-Cy
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/06—Non-steroidal liquid crystal compounds
- C09K19/08—Non-steroidal liquid crystal compounds containing at least two non-condensed rings
- C09K19/30—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing saturated or unsaturated non-aromatic rings, e.g. cyclohexane rings
- C09K19/3001—Cyclohexane rings
- C09K19/3003—Compounds containing at least two rings in which the different rings are directly linked (covalent bond)
- C09K2019/3009—Cy-Ph
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/06—Non-steroidal liquid crystal compounds
- C09K19/08—Non-steroidal liquid crystal compounds containing at least two non-condensed rings
- C09K19/30—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing saturated or unsaturated non-aromatic rings, e.g. cyclohexane rings
- C09K19/3001—Cyclohexane rings
- C09K19/3003—Compounds containing at least two rings in which the different rings are directly linked (covalent bond)
- C09K2019/301—Cy-Cy-Ph
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/06—Non-steroidal liquid crystal compounds
- C09K19/08—Non-steroidal liquid crystal compounds containing at least two non-condensed rings
- C09K19/30—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing saturated or unsaturated non-aromatic rings, e.g. cyclohexane rings
- C09K19/3001—Cyclohexane rings
- C09K19/3003—Compounds containing at least two rings in which the different rings are directly linked (covalent bond)
- C09K2019/3016—Cy-Ph-Ph
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/06—Non-steroidal liquid crystal compounds
- C09K19/08—Non-steroidal liquid crystal compounds containing at least two non-condensed rings
- C09K19/30—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing saturated or unsaturated non-aromatic rings, e.g. cyclohexane rings
- C09K19/3001—Cyclohexane rings
- C09K19/3003—Compounds containing at least two rings in which the different rings are directly linked (covalent bond)
- C09K2019/3027—Compounds comprising 1,4-cyclohexylene and 2,3-difluoro-1,4-phenylene
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/06—Non-steroidal liquid crystal compounds
- C09K19/08—Non-steroidal liquid crystal compounds containing at least two non-condensed rings
- C09K19/30—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing saturated or unsaturated non-aromatic rings, e.g. cyclohexane rings
- C09K19/3001—Cyclohexane rings
- C09K19/3028—Cyclohexane rings in which at least two rings are linked by a carbon chain containing carbon to carbon single bonds
- C09K2019/304—Cy-C2H4-Ph-Ph
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/06—Non-steroidal liquid crystal compounds
- C09K19/08—Non-steroidal liquid crystal compounds containing at least two non-condensed rings
- C09K19/30—Non-steroidal liquid crystal compounds containing at least two non-condensed rings containing saturated or unsaturated non-aromatic rings, e.g. cyclohexane rings
- C09K19/3001—Cyclohexane rings
- C09K19/3066—Cyclohexane rings in which the rings are linked by a chain containing carbon and oxygen atoms, e.g. esters or ethers
- C09K19/3068—Cyclohexane rings in which the rings are linked by a chain containing carbon and oxygen atoms, e.g. esters or ethers chain containing -COO- or -OCO- groups
- C09K2019/3078—Cy-Cy-COO-Ph-Cy
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/06—Non-steroidal liquid crystal compounds
- C09K19/34—Non-steroidal liquid crystal compounds containing at least one heterocyclic ring
- C09K19/3402—Non-steroidal liquid crystal compounds containing at least one heterocyclic ring having oxygen as hetero atom
- C09K2019/3422—Non-steroidal liquid crystal compounds containing at least one heterocyclic ring having oxygen as hetero atom the heterocyclic ring being a six-membered ring
-
- G—PHYSICS
- G02—OPTICS
- G02F—OPTICAL DEVICES OR ARRANGEMENTS FOR THE CONTROL OF LIGHT BY MODIFICATION OF THE OPTICAL PROPERTIES OF THE MEDIA OF THE ELEMENTS INVOLVED THEREIN; NON-LINEAR OPTICS; FREQUENCY-CHANGING OF LIGHT; OPTICAL LOGIC ELEMENTS; OPTICAL ANALOGUE/DIGITAL CONVERTERS
- G02F1/00—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics
- G02F1/01—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics for the control of the intensity, phase, polarisation or colour
- G02F1/13—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics for the control of the intensity, phase, polarisation or colour based on liquid crystals, e.g. single liquid crystal display cells
- G02F1/133—Constructional arrangements; Operation of liquid crystal cells; Circuit arrangements
- G02F1/1333—Constructional arrangements; Manufacturing methods
- G02F1/1337—Surface-induced orientation of the liquid crystal molecules, e.g. by alignment layers
- G02F1/133742—Surface-induced orientation of the liquid crystal molecules, e.g. by alignment layers for homeotropic alignment
Description
さらに、VA-IPSディスプレイはまた、正のVAおよびHT-VAの名称の下で知られている。
VAおよびVA-IPSディスプレイは、一般的に、極めて高い比抵抗を広汎な作業温度範囲、短い応答時間および低いしきい値電圧と同時に有するこ
とが意図され、その補助によって様々なグレーシェードを発生させることができる。
VAディスプレイは、著しくより良好な視野角依存性を有し、したがって主にテレビおよびモニターに使用される。
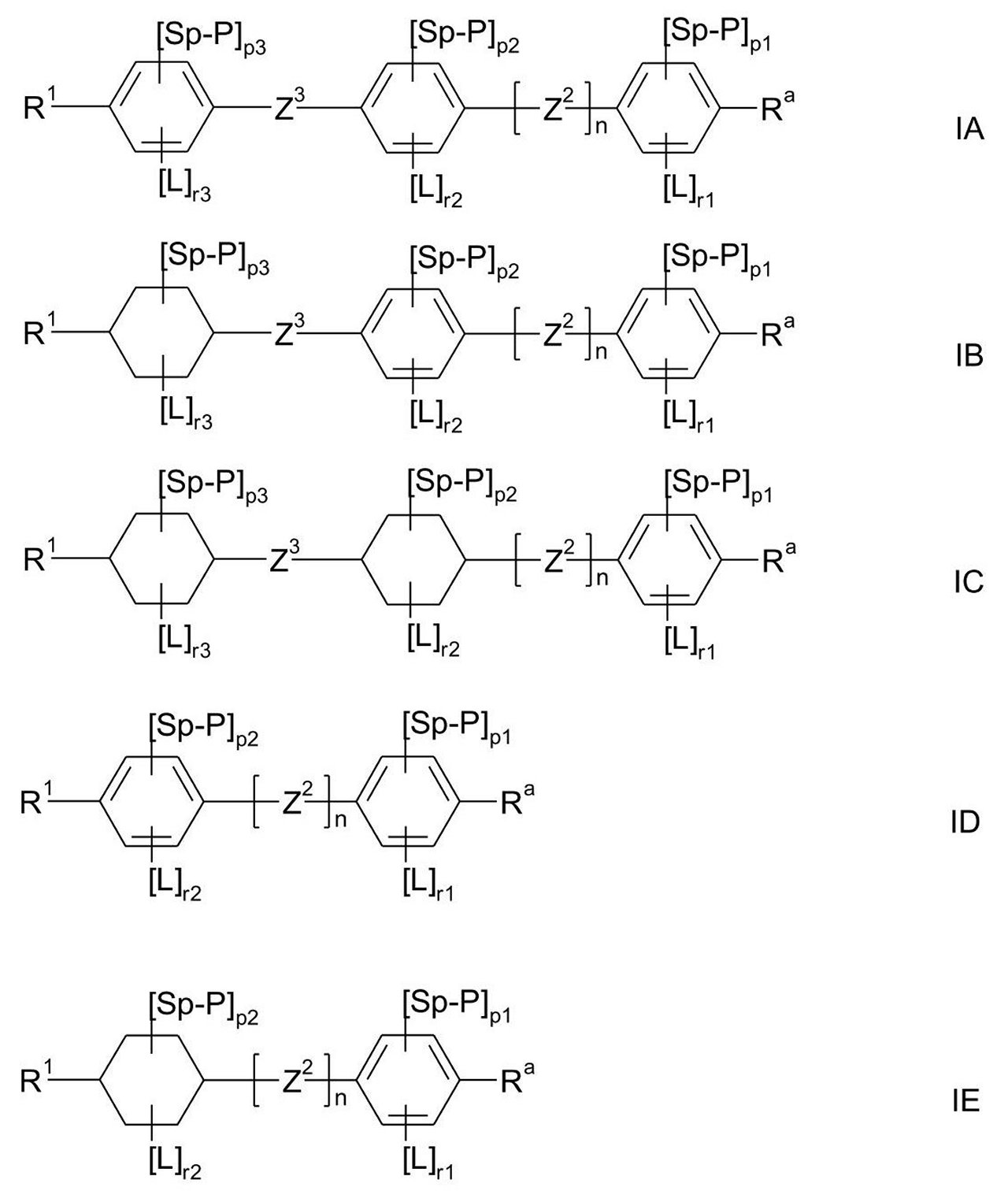
R1-[A3-Z3]m-[A2]k-[Z2]n-A1-Ra (I)
A1、A2、A3は、それぞれ、互いに独立して芳香族、複素芳香族、脂環式または複素環式基を示し、それはまた縮合される環を含有してもよく、それはまた基Lまたは-Sp-Pによって単置換または多置換されていてもよく、
Pは、重合性基を示し、
Spは、スペーサー基(スペーサーとも称する)または単結合を示し、
Z3は、それぞれの場合において互いに独立して、単結合、-O-、-S-、-CO-、-CO-O-、-OCO-、-O-CO-O-、-OCH2-、-CH2O-、-SCH2-、-CH2S-、-CF2O-、-OCF2-、-CF2S-、-SCF2-、-(CH2)n1-、-CF2CH2-、-CH2CF2-、-(CF2)n1-、-CH=CH-、-CF=CF-、-C≡C-、-CH=CH-COO-、-OCO-CH=CH-、-(CR0R00)n1-、-CH(-Sp-P)-、-CH2CH(-Sp-P)-、-CH(-Sp-P)CH(-Sp-P)-を示し、
nは、0または1を示し、
mは、0、1、2、3、4、5または6、好ましくは0、1、2または3を示し、
kは、0または1を示し、
R00は、それぞれの場合において互いに独立して、Hまたは1~12個のC原子を有するアルキルを示し、
qは、2または3を示し、
Bは、置換または非置換の環系または縮合環系、好ましくはベンゼン、ピリジン、シクロヘキサン、ジオキサンまたはテトラヒドロピランから選択された環系を示し、
Yは、互いに独立して、-O-、-S-、-C(O)-、-C(O)O-、-OC(O)-、-NR11-または単結合を示し、
oは、0または1を示し、
R11は、1~12個のC原子を有するアルキルを示し、
Spa、Spc、Spdは、それぞれ、互いに独立してスペーサー基または単結合を示し、
Spbは、3価または4価の基、好ましくはCH、NまたはCを示し、
ここで式Iで表される化合物は、基A1、A2、A3、Z2およびZ3内において、少なくとも1つの重合性基Pを、存在するものとして含有する、
の重合によって得られる、前記LC媒体に関する。
本発明はさらに、式Iで表される化合物の、LC媒体の境界を定める表面に関するホメオトロピック配向を達成するためのLC媒体のための添加剤としての使用に関する。
- セルを本発明のLC媒体で満たすこと、ここでLC媒体の基板表面に対するホメオトロピック(垂直)配向が確立されるようになる、および
- 重合性構成成分(単数または複数)を、1つまたは2つ以上のプロセスステップで、任意に電圧のセルへの印加でまたは電場の作用の下で、重合させること
を含む、前記方法に関する。
R1-[A3-Z3]m-[A2]k-[Z2]n-A1-Ra I’
式中、m、k、nおよび基Raは、上記の式Iについて定義した通りであり、ならびに
A1、A2、A3は、それぞれ、互いに独立して、芳香族、複素芳香族、脂環式または複素環式基を示し、それはまた縮合される環を含有してもよく、それはまた基Lによって単置換または多置換されていてもよく、
Z3は、それぞれの場合において互いに独立して、単結合、-O-、-S-、-CO-、-CO-O-、-OCO-、-O-CO-O-、-OCH2-、-CH2O-、-SCH2-、-CH2S-、-CF2O-、-OCF2-、-CF2S-、-SCF2-、-(CH2)n1-、-CF2CH2-、-CH2CF2-、-(CF2)n1-、-CH=CH-、-CF=CF-、-C≡C-、-CH=CH-COO-、-OCO-CH=CH-、-(CR0R00)n1-を示し、
Lは、それぞれの場合において互いに独立して、H、F、Cl、Br、I、-CN、-NO2、-NCO、-NCS、-OCN、-SCN、-C(=O)N(R0)2、-C(=O)R0、3~20個のC原子を有する任意に置換されたシリル、任意に置換されたアリールもしくはシクロアルキル、または1~25個のC原子を有する直鎖状もしくは分枝状アルキル、アルコキシ、アルキルカルボニル、アルコキシカルボニル、アルキルカルボニルオキシもしくはアルコキシカルボニルオキシを示し、ここでさらに1個または2個以上のH原子は、FまたはClによって置き換えられていてもよく、
R00は、それぞれの場合において互いに独立して、Hまたは1~12個のC原子を有するアルキルを示し、
ならびに
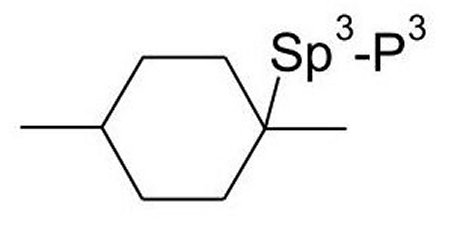
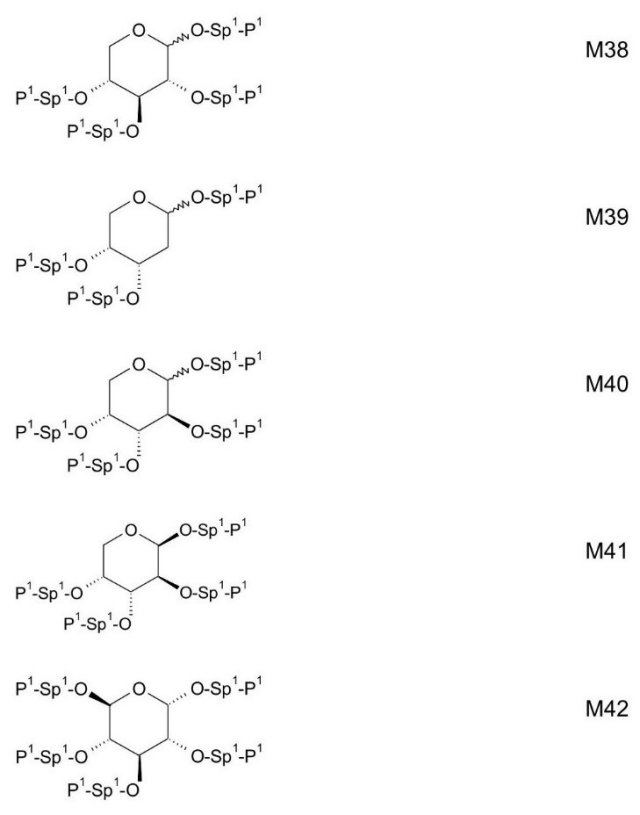
自己配向添加剤、特に重合性自己配向添加剤の好ましい例示的な構造を、以下に開示する:
好ましくは、以下の式:
-Spa-X1
式中、それぞれの場合において独立して、基は、本明細書中で定義した通りである、
から選択されたアンカー基、
CH、C(Me)、C(CH2CH3)またはNから選択された式で表される3価の基、または4価の基C(4価の炭素原子)
を示す。
基Spaは、好ましくは式-CH2-、-CH2CH2-、-OCH2CH2-、-CH2CH2CH2-、-OCH2CH2CH2-、-CH2CH2CH2CH2-、-OCH2CH2CH2CH2-、-CH2CH2OCH2CH2-、-OCH2CH2OCH2CH2-から選択された基を示す。
基SpcまたはSpdは、好ましくは式-CH2-、-CH2CH2-、-CH2CH2CH2-、-CH2CH2CH2CH2-、-CH2CH2OCH2CH2-から選択された基を示す。
a) 1,4-フェニレンおよび1,3-フェニレンからなる群、ここでさらに1個または2個以上のH原子は、Lまたは-Sp-Pによって置き換えられていてもよい、
b) トランス-1,4-シクロヘキシレン、1,4-シクロヘキセニレンおよび4,4’-ビシクロヘキシレンからなる群、ここでさらに1つまたは2つ以上の隣接していないCH2基は、-O-および/または-S-によって置き換えられていてもよく、かつここでさらに1個または2個以上のH原子は、F、L、-Sp-Pによって置き換えられていてもよい。基A1およびA2は、特に好ましくは上記の従属群a)からの基を示す。A1およびA2は、独立して非常に特に好ましくは1,4-フェニレンまたはシクロヘキサン-1,4-ジイルを示し、それは基Lまたは-Sp-Pによって単置換または多置換されていてもよい。
p1、p2、p3は、独立して0、1、2または3を示し、ならびに
r1、r2、r3は、独立して0、1、2または3を示し、
ここで式Iで表される化合物は、存在するものとして、全体的に(つまり合計で)少なくとも1つの重合性基Pを基A1、A2、A3、Z2およびZ3内に含む。
r1、r2、r3は、独立して0、1、2、3または4、好ましくは0、1または2を示す。
用語「アリール」は、芳香族炭素基またはそれから誘導される基を示す。用語「ヘテロアリール」は、1個または2個以上のヘテロ原子を含む上に定義した「アリール」を示す。
1)例えば以下のもの:
-
-
- フェノールを得るためのボロン酸酸化、それと共に
による官能化、
2) メタクリル酸を使用するエステル化:
定義:X=CH2、Oまたは単結合、Pg2=例えばベンジル、Sp=例えば:0~3個のC原子を有するスペーサー。
P1-Sp1-A2-(Z1-A1)n-Sp2-P2 M
式中、個々のラジカルは以下の意味を有する:
P1、P2は、それぞれ、互いに独立して重合性基を示し、
Sp1、Sp2は、それぞれの出現において同一であるかまたは異なって、スペーサー基または単結合を示し、
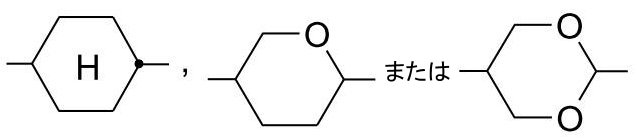
a) トランス-1,4-シクロヘキシレン、1,4-シクロヘキセニレンおよび4,4’-ビシクロヘキシレン、ここでさらに、1つまたは2つ以上の隣接していないCH2基は、-O-および/または-S-によって置き換えられていてもよく、ここでさらに、1個または2個以上のH原子は、基Lによって置き換えられていてもよく、あるいは式
c) テトラヒドロピラン-2,5-ジイル、1,3-ジオキサン-2,5-ジイル、テトラヒドロフラン-2,5-ジイル、シクロブタン-1,3-ジイル、ピペリジン-1,4-ジイル、チオフェン-2,5-ジイルおよびセレノフェン-2,5-ジイルからなる群、そのそれぞれはまた、基Lによって単置換または多置換されていてもよい、
Sp3は、スペーサー基を示し、
nは、0、1、2または3、好ましくは1または2を示し、
Z1は、それぞれの場合において互いに独立して-CO-O-、-O-CO-、-CH2O-、-OCH2-、-CF2O-、-OCF2-または-(CH2)n-、式中nは2、3または4である、-O-、-CO-、-C(RcRd)-、-CH2CF2-、-CF2CF2-または単結合を示し、
R0、R00は、それぞれ、互いに独立して、H、Fまたは1~12個のC原子を有する直鎖状もしくは分枝状アルキルを示し、ここでさらに、1個または2個以上のH原子は、Fによって置き換えられていてもよく、
Mは、-O-、-S-、-CH2-、-CHY1-または-CY1Y2-を示し、ならびに
W1、W2は、それぞれ、互いに独立して-CH2CH2-、-CH=CH-、-CH2-O-、-O-CH2-、-C(RcRd )-または-O-を示し、
RcおよびRdは、それぞれ、互いに独立して、Hまたは1~6個のC原子を有するアルキル、好ましくはH、メチルまたはエチルを示す。
Sp’’は、1~20個、好ましくは1~12個のC原子を有するアルキレンを示し、それは、任意にF、Cl、Br、IまたはCNによって単置換または多置換されており、およびここでさらに、1つまたは2つ以上の隣接していないCH2基は、それぞれ、互いに独立して、-O-、-S-、-Si(R00R000)-、-CO-、-CO-O-、-O-CO-、-O-CO-O-、-S-CO-、-CO-S-、-N(R00)-CO-O-、-O-CO-N(R00)-、-N(R00)-CO-N(R00)-、-CH=CH-または-C≡C-によって、Oおよび/またはS原子が互いに直接結合しないように置き換えられていてもよく、
R000は、それぞれの場合において独立してHまたは1~12個のC原子を有するアルキルを示し、ならびに
Y2およびY3は、それぞれ、互いに独立してH、F、ClまたはCNを示す。
典型的なスペーサー基Sp’’は、例えば単結合、-(CH2)p1-、-(CH2CH2O)q1-CH2CH2-、-CH2CH2-S-CH2CH2-または-(SiR00R000-O)p1-であり、ここでp1は1~12の整数であり、q1は1~3の整数であり、およびR00およびR000は上に示した意味を有する。
P1、P2およびP3は、それぞれ、互いに独立して、好ましくはPについて本明細書中に示した意味の1つを有する重合性基、好ましくはアクリレート、メタクリレート、フルオロアクリレート、オキセタン、ビニルオキシまたはエポキシド基を示し、
ここでさらに、ラジカルP1-Sp1-、P2-Sp2-およびP3-Sp3-の1つまたは2つ以上は、ラジカルRaaを示してもよく、ただし存在するラジカルP1-Sp1-、P2-Sp2-およびP3-Sp3-の少なくとも一方は、Raaを示さず、
ここで-OH、-NH2、-SH、-NHR、-C(O)OHおよび-CHOは、基Raa中に存在せず、
RyおよびRzは、それぞれ、互いに独立してH、F、CH3またはCF3を示し、
X1、X2およびX3は、それぞれ、互いに独立して-CO-O-、O-CO-または単結合を示し、
Z2およびZ3は、それぞれ、互いに独立して-CO-O-、-O-CO-、-CH2O-、-OCH2-、-CF2O-、-OCF2-または-(CH2)n-を示し、式中nは2、3または4であり、
rは、0、1、2、3または4を示し、
sは、0、1、2または3を示し、
tは、0、1または2を示し、
xは、0または1を示す。
LCDおよびとりわけIPSディスプレイに適している、正の誘電異方性を有する好適なLC混合物は、例えば、JP 07-181 439 (A)、EP 0 667 555、EP 0 673 986、DE 195 09 410、DE 195 28 106、DE 195 28 107、WO 96/23 851およびWO 96/28 521から知られている。
R2A、R2BおよびR2Cは、それぞれ、互いに独立してH、15個までのC原子を有し、非置換であるか、CNもしくはCF3によって単置換されているか、またはハロゲンによって少なくとも単置換されているアルキルラジカルを示し、ここでさらに、これらのラジカル中の1つまたは2つ以上のCH2基は、
によって、O原子が互いに直接結合しないように置き換えられていてもよく、
Z2およびZ2’は、それぞれ、互いに独立して単結合、-CH2CH2-、-CH=CH-、-CF2O-、-OCF2-、-CH2O-、-OCH2-、-COO-、-OCO-、-C2F4-、-CF=CF-、-CH=CHCH2O-を示し、
pは、1または2、好ましくは1を示し、
qは、0または1を示し、ならびに
vは、1~6を示す。
液晶混合物中における複屈折Δnの値は、一般的に0.07~0.16、好ましくは0.08~0.12である。重合前の20℃での回転粘度γ1は、好ましくは≦165mPa・s、特に≦140mPa・sである。
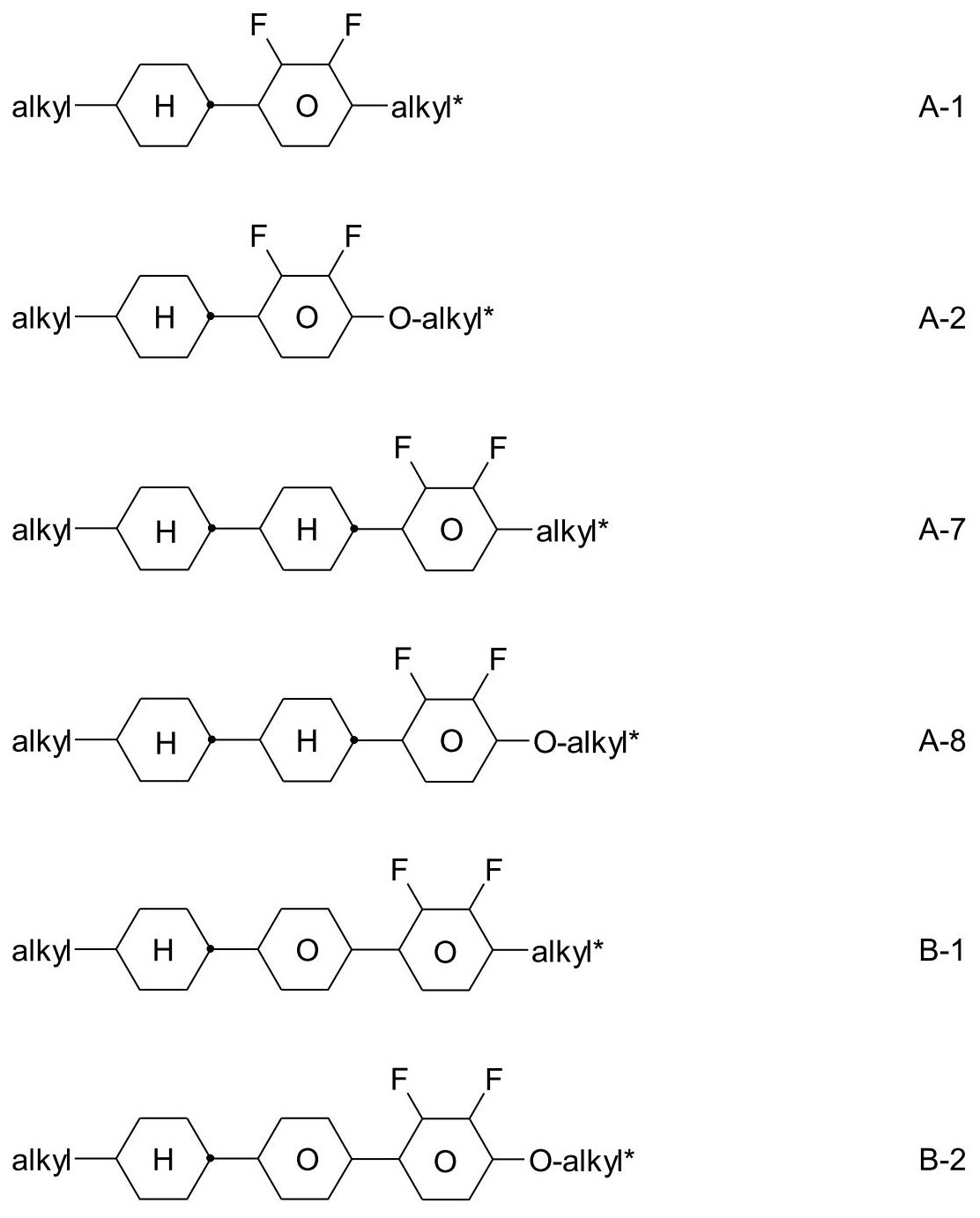
式IIおよび/またはIIIで表される1種または2種以上の化合物をさらに含むLC媒体:
環Aは、1,4-フェニレンまたはトランス-1,4-シクロヘキシレンを示し、
aは、0または1であり、
R4は、それぞれの場合において互いに独立して、1~12個のC原子を有する非置換であるかまたはハロゲン化されたアルキルラジカルを示し、ここでさらに、1つまたは2つの隣接していないCH2基は、-O-、-CH=CH-、-CH=CF-、-(CO)-、-O(CO)-または-(CO)O-によって、O原子が互いに直接結合しないように置き換えられていてもよく、および好ましくは1~12個のC原子を有するアルキルまたは2~9個のC原子を有するアルケニルを示す。
R0は、1~15個のC原子を有するアルキルまたはアルコキシラジカルを示し、ここでさらに、これらのラジカル中の1つまたは2つ以上のCH2基は、任意に、互いに独立して、
Y1~4は、それぞれ、互いに独立してHまたはFを示し、
Z0は、-CF2O-、-(CO)O-または単結合を示し、および
cは、0、1または2、好ましくは1または2を示し、
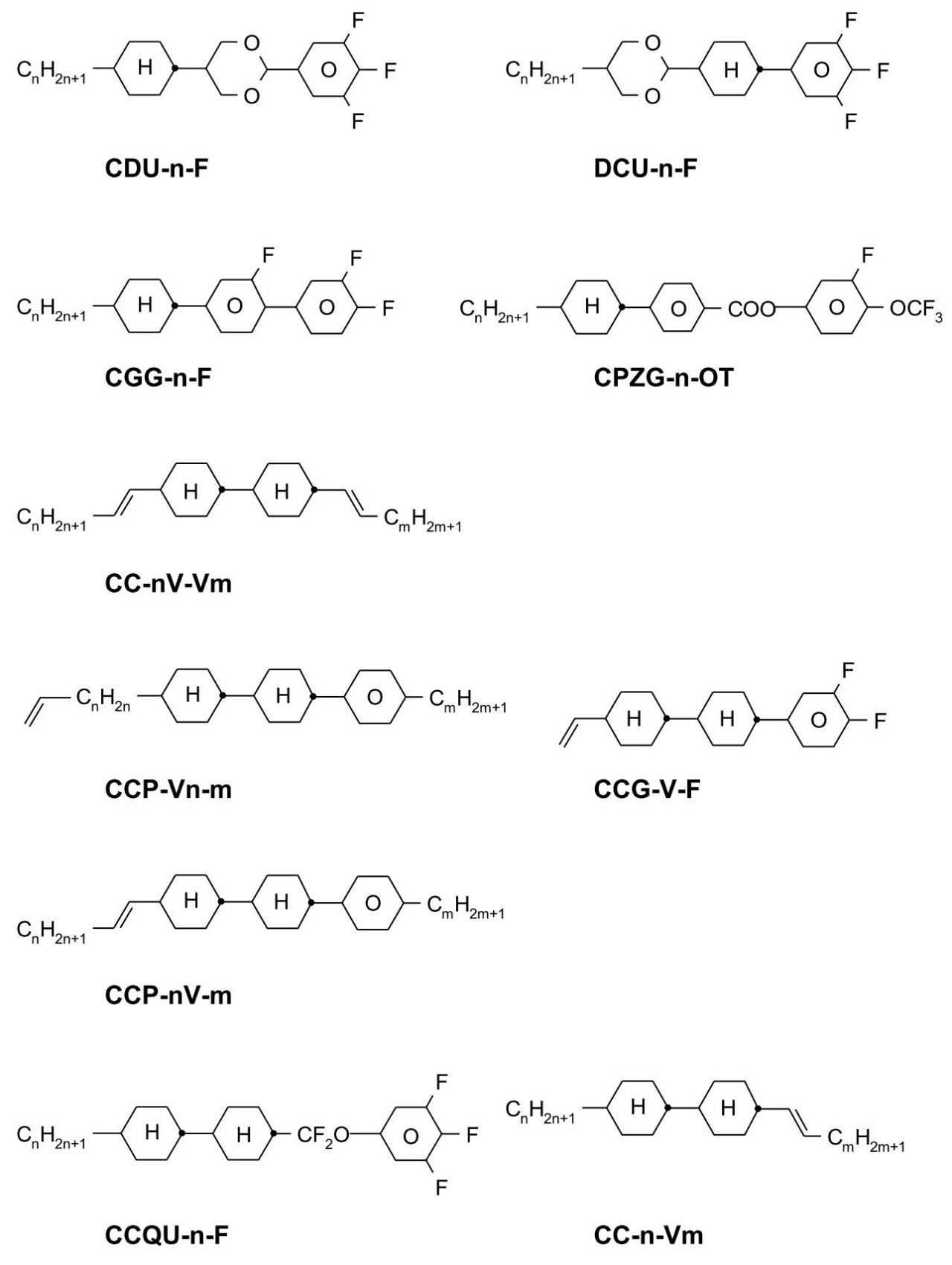
表Fは、本発明のLC媒体において、好ましくは非重合性自己配向添加剤として使用することができる例示的な化合物を示す。
ne 20℃および589nmでの異常光屈折率、
no 20℃および589nmでの常光屈折率、
Δn 20℃および589nmでの光学異方性、
ε⊥ 20℃および1kHzでのダイレクターに垂直な誘電体誘電率、
ε││ 20℃および1kHzでのダイレクターに平行な誘電体誘電率、
Δε 20℃および1kHzでの誘電異方性、
cl.p.、T(N,I) 透明点[℃]、
γ1 20℃での回転粘度[mPa・s]、
K1 20℃での弾性定数、「スプレー」変形[pN]、
K2 20℃での弾性定数、「ねじれ」変形[pN]、
K3 20℃での弾性定数、「ベント」変形[pN]。
V0 20℃での容量性しきい値(Freedericksしきい値)[V]。
本明細書による本発明の態様および変法のさらなる組み合わせはまた、特許請求の範囲から生じる。
使用した化合物は、商業的に入手できない場合には、標準的な実験室手順によって合成する。LC媒体は、Merck KGaA、ドイツ国が起源である。
例1
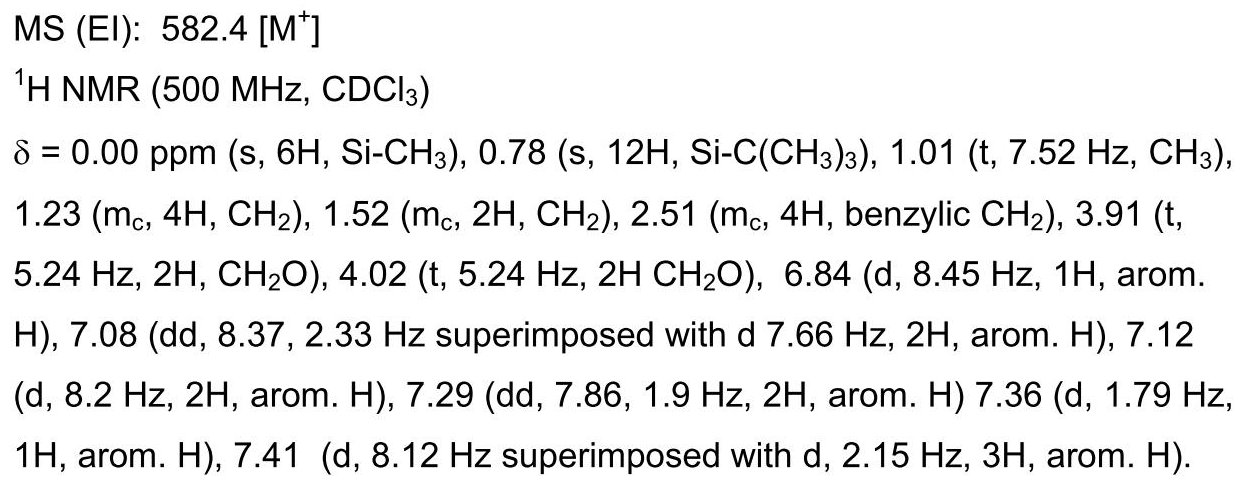
2-メチルアクリル酸 2-[2’-エチル-4-(2-ヒドロキシエトキシ)-4’’-ペンチル-[1,1’;4’,1’’]ターフェニル-3-イル]エチルエステル 1の合成
2-メチルアクリル酸 2’-エチル-4’’-(2-ヒドロキシエチル)-6’’-(2-メチル-アクリロイルオキシ)-4-ペンチル-[1,1’;4’,1’’]ターフェニル-3’’-イルエステル 2の合成
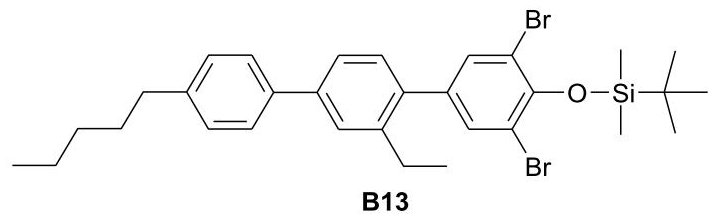
2-{5-[2-エチル-4-(4-ペンチルフェニル)フェニル]-2-[4-ヒドロキシ-3-(ヒドロキシメチル)ブトキシ]フェニル}エチル 2-メチルプロパ-2-エノアート 4の合成
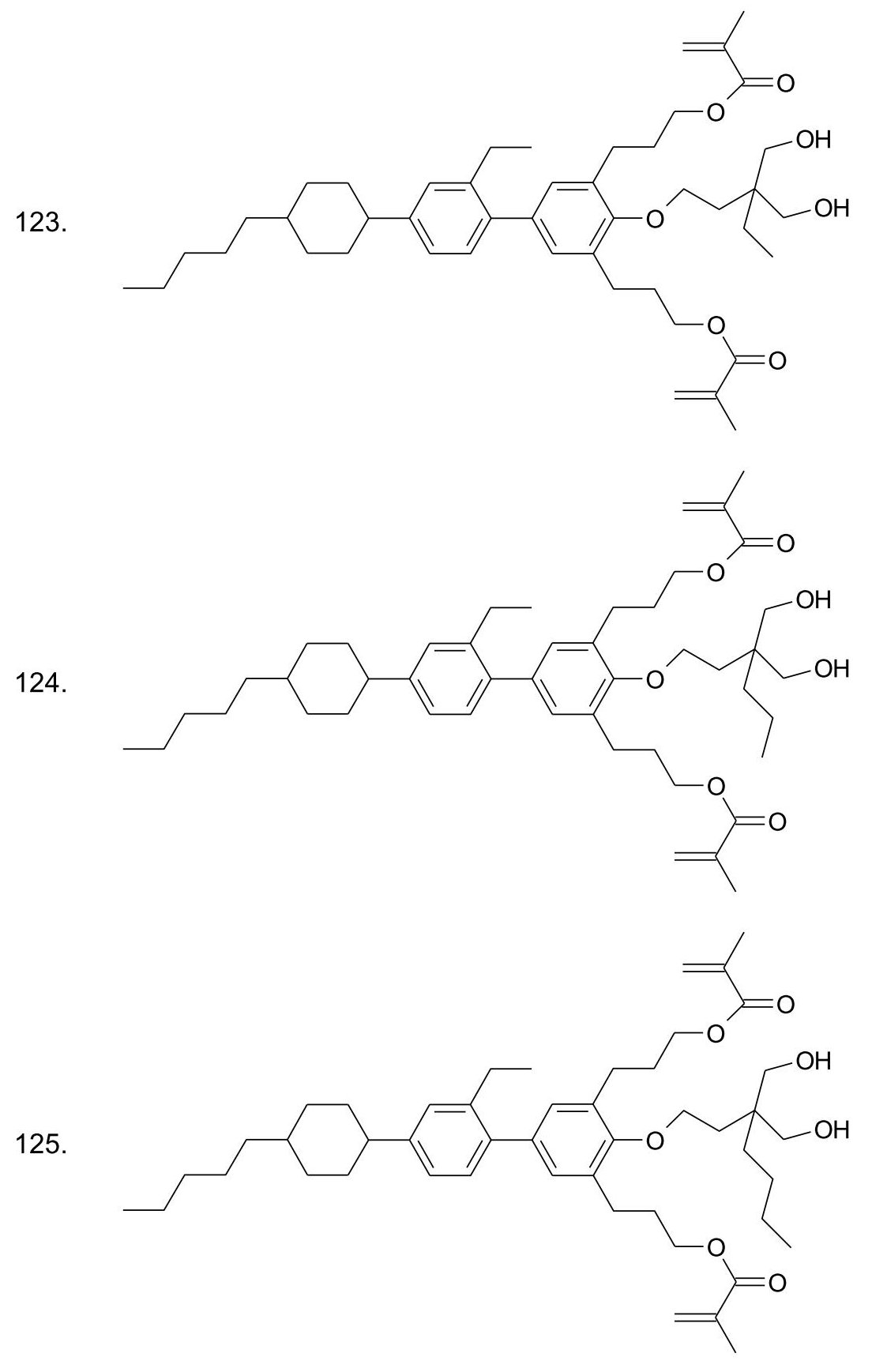
3-{5-[2-エチル-4-(4-ペンチルフェニル)フェニル]-2-(3-ヒドロキシプロポキシ)-3-{3-[(2-メチルプロパ-2-エノイル)オキシ]プロピル}フェニル}プロピル 2-メチルプロパ-2-エノエート 13の合成
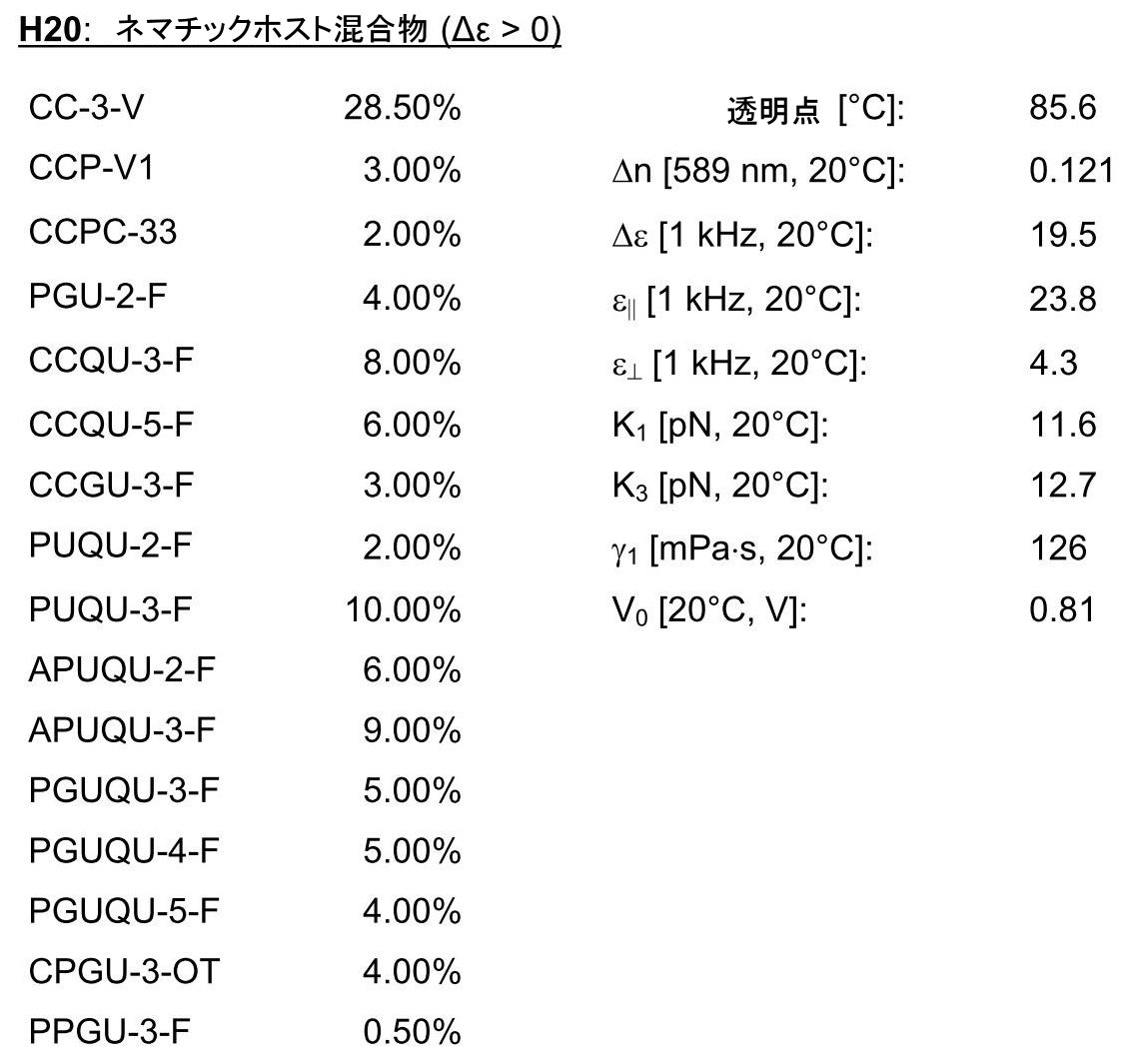
本発明のLC媒体を、示した重量パーセント比率での低分子量構成成分からなる以下の液晶混合物を使用して調製する。
重合性自己配向添加剤1(2.0重量%)を、VAタイプのネマチックLC媒体H1(Δε<0)に加え、混合物を均質化する。
形成した混合物を、試験セル(ポリイミド配向層なし、層厚さd≒4.0μm、両側にITOコーティング、マルチドメイン切換のための構築されたITO、保護層なし)中に導入する。LC媒体は、基板表面に関して自発的なホメオトロピック(垂直)配向を有する。この配向は透明点までずっと安定であり、形成したVAセルは電圧の印加により可逆的に切り換えることができる。
重合性自己配向添加剤1(2.0重量%)を、VA-IPSタイプのネマチックLC媒体H15(Δε>0)に加え、混合物を均質化する。
形成した混合物を、試験セル(ポリイミド配向層なし、層厚さd≒4μm、ITOインターデジタル電極が一方の基板表面上に配置されている、対向する基板表面上にガラス、保護層なし)中に導入する。LC媒体は、基板表面に関して自発的なホメオトロピック(垂直)配向を有する。この配向は透明点までずっと安定であり、形成したVA-IPSセルは電圧の印加により可逆的に切り換えることができる。
重合性自己配向添加剤2~19(表5による重量%)を、混合物例1と同様にしてネマチックLC媒体H1(Δε<0)に加え、混合物を均質化する。形成した混合物を、前配向層なしの試験セル中に導入する。LC媒体は、基板表面に関して自発的なホメオトロピック(垂直)配向を有する。この配向は透明点までずっと安定であり、形成したVAセルは電圧の印加により可逆的に切り換えることができる。
重合性自己配向添加剤2~4、7、10、12~19(表5による重量%)を、混合物例2と同様にしてネマチックLC媒体H15(Δε>0)に加え、混合物を均質化する。形成した混合物を、前配向層なしの試験セル中に導入する。LC媒体は、基板表面に関して自発的なホメオトロピック(垂直)配向を有する。この配向は透明点までずっと安定でり、形成したVA-IPSセルは電圧の印加により可逆的に切り換えることができる。
重合性自己配向添加剤1、4、13、18および19(表5による重量%)を、混合物例1と同様にしてネマチックLC媒体H2~H14(Δε<0)に加え、混合物を均質化する。形成した混合物を、前配向層なしの試験セル中に導入する(混合物例1を参照)。LC媒体は、基板表面に関して自発的なホメオトロピック(垂直)配向を有する。この配向は透明点までずっと安定であり、形成したVAセルを、電圧の印加によって可逆的に切り換えることができる。
重合性自己配向添加剤1、4、13、18および19(表5による重量%)を、混合物例2と同様にしてネマチックLC媒体H16~H20(Δε>0)に加え、混合物を均質化する。形成した混合物を、前配向層なしの試験セル中に導入する。LC媒体は、基板表面に関して自発的なホメオトロピック(垂直)配向を有する。この配向は透明点までずっと安定であり、形成したVA-IPSセルは電圧の印加により可逆的に切り換えることができる。
それぞれの場合において、重合性自己配向添加剤1、2~4、7、10、12~18(表5による重量%)を、ネマチックLC媒体H1(Δε<0)に加え、混合物を均質化する。
形成した混合物を、試験セル(ポリイミド配向層なし、層厚さd≒4.0μm、両側にITOコーティング(マルチドメイン切換のための構築されたITO)、保護層なし)中に導入する。LC媒体は、基板表面に関して自発的なホメオトロピック(垂直)配向を有する。この配向は透明点までずっと安定であり、形成したVAセルを、電圧の印加によって可逆的に切り換えることができる。
重合性化合物(RM-1、0.3重量%)および重合性自己配向添加剤1、2~4、7、10、12~18(表5による重量%)を、ネマチックLC媒体H1(Δε<0)に加え、混合物を均質化する。
形成した混合物を、試験セル(ポリイミド配向層なし、層厚さd≒4.0μm、両側にITOコーティング(マルチドメイン切換のための構造化ITO)、保護層なし)中に導入する。LC媒体は、基板表面に関して自発的なホメオトロピック(垂直)配向を有する。この配向は、透明点までずっと安定であり、形成したVAセルを、電圧印加により可逆的に切り換えることができる。
Claims (25)
- 低分子量、非重合性液晶構成成分と、式Iで表される1種または2種以上の化合物を、すべての固体または液晶構成成分を含み、溶媒を含まない、全体としての10重量%未満の濃度において含む重合性の、または重合した構成成分とを含むLC媒体であって、重合した構成成分が重合性構成成分
R1-[A3-Z3]m-[A2]k-[Z2]n-A1-Ra (I)
式中、
A1、A2、A3は、それぞれ、互いに独立して、1,4-フェニレン、ナフタレン-1,4-ジイルまたはナフタレン-2,6-ジイル、ここでさらに、これらの基における1つまたは2つ以上のCH基はNによって置き換えられていてもよい、シクロヘキサン-1,4-ジイル、ここでさらに、1つまたは2つ以上の隣接していないCH2基はOおよび/またはSによって置き換えられていてもよい、3,3’-ビシクロブチリデン、1,4-シクロヘキセニレン、ビシクロ[1.1.1]ペンタン-1,3-ジイル、ビシクロ[2.2.2]オクタン-1,4-ジイル、スピロ[3.3]ヘプタン-2,6-ジイル、ピペリジン-1,4-ジイル、デカヒドロナフタレン-2,6-ジイル、1,2,3,4-テトラヒドロナフタレン-2,6-ジイル、インダン-2,5-ジイルまたはオクタヒドロ-4,7-メタノインダン-2,5-ジイル、パーヒドロシクロペンタ[a]フェナントレン-3,17-ジイルを示し、
ここですべてのこれらの基が非置換であるかまたは基Lもしくは-Sp-Pによって単置換もしくは多置換されていてもよい、
Lは、それぞれの場合において互いに独立して、H、F、Cl、Br、I、-CN、-NO2、-NCO、-NCS、-OCN、-SCN、-C(=O)N(R0)2、-C(=O)R0、3~20個のC原子を有する任意に置換されたシリル、任意に置換されたアリールもしくはシクロアルキル、または1~25個のC原子を有し、ここでさらに1個もしくは2個以上のH原子がFもしくはClによって置き換えられていてもよい直鎖状もしくは分枝状アルキル、アルコキシ、アルキルカルボニル、アルコキシカルボニル、アルキルカルボニルオキシもしくはアルコキシカルボニルオキシを示し、
Pは、重合性基を示し、
Spは、スペーサー基または単結合を示し、
Z2は、それぞれの場合において互いに独立して、-O-、-S-、-CO-、-CO-O-、-OCO-、-O-CO-O-、-OCH2-、-CH2O-、-SCH2-、-CH2S-、-CF2O-、-OCF2-、-CF2S-、-SCF2-、-(CH2)n1-、-CF2CH2-、-CH2CF2-、-(CF2)n1-、-CH=CH-、-CF=CF-、-C≡C-、-CH=CH-COO-、-OCO-CH=CH-、-(CR0R00)n1-、-CH(-Sp-P)-、-CH2CH(-Sp-P)-、-CH(-Sp-P)CH(-Sp-P)-を示し、
Z3は、それぞれの場合において互いに独立して、単結合、-O-、-S-、-CO-、-CO-O-、-OCO-、-O-CO-O-、-OCH2-、-CH2O-、-SCH2-、-CH2S-、-CF2O-、-OCF2-、-CF2S-、-SCF2-、-(CH2)n1-、-CF2CH2-、-CH2CF2-、-(CF2)n1-、-CH=CH-、-CF=CF-、-C≡C-、-CH=CH-COO-、-OCO-CH=CH-、-(CR0R00)n1-、-CH(-Sp-P)-、-CH2CH(-Sp-P)-、-CH(-Sp-P)CH(-Sp-P)-を示し、
n1は、1、2、3または4を示し、
nは、0または1を示し、
mは、0、1、2、3、4、5または6を示し、
kは、0または1を示し、
ここでmおよびkの少なくとも1つは、1以上であり、
R0は、それぞれの場合において互いに独立して、1~12個のC原子を有するアルキルを示し、
R00は、それぞれの場合において互いに独立して、Hまたは1~12個のC原子を有するアルキルを示し、
R1は、ハロゲン、1~25個のC原子を有する直鎖状、分枝状または環状アルキルを示し、ここでさらに1つまたは2つ以上の隣接していないCH2基は、-O-、-S-、-CO-、-CO-O-、-O-CO-、-O-CO-O-によって、Oおよび/またはS原子が直接結合しないように置き換えられていてもよく、かつここでさらに1個または2個以上のH原子は、FまたはClによって置き換えられていてもよく、あるいは基-Sp-Pを示し、
Raは、式
qは、2または3を示し、
Bは、ベンゼン、ピリジン、シクロヘキサン、ジオキサンまたはテトラヒドロピランから選択された環系を示し、
Yは、互いに独立して、-O-、-S-、-C(O)-、-C(O)O-、-OC(O)-、-NR11-または単結合を示し、
oは、0または1を示し、
X1は、互いに独立して、H、アルキル、フルオロアルキル、OH、NH2、NHR11、NR11 2、OR11、C(O)OH、-CHOを示し、ここで少なくとも1つの基X1は、-OH、-NH2、NHR11、C(O)OHおよび-CHOから選択されたラジカルを示し、
R11は、1~12個のC原子を有するアルキルを示し、
Spa、Spc、Spdは、それぞれ、互いに独立してスペーサー基または単結合を示し、
Spbは、3価または4価の基を示し、
ここで式Iで表される化合物は、基A1、A2、A3、Z2およびZ3内において、少なくとも1つの重合性基Pを、存在するものとして含有し、ただしR1が-Sp-Pを示す場合、式Iで表される化合物は、かかる少なくとも1つの重合性基Pを、R1における-Sp-PのPに加えて、基A1、A2およびA3内において含有する、
の重合によって得られる、基板がホメオトロピック配向のための配向層がないLCディスプレイ用の、前記LC媒体。 - 式Iで表される化合物が式I1
A1、A2、A3は、それぞれ、互いに独立して、1,4-フェニレン、ここでさらに、これらの基における1つまたは2つ以上のCH基はNによって置き換えられていてもよい、シクロヘキサン-1,4-ジイル、ここでさらに、1つまたは2つ以上の隣接していないCH2基はOおよび/またはSによって置き換えられていてもよい、1,4-シクロヘキセニレン、ピペリジン-1,4-ジイル、を示し、
ここですべてのこれらの基が非置換であるかまたは基Lもしくは-Sp-Pによって単置換もしくは多置換されていてもよい、
R1、Ra、Z2、Z3、L、Sp、P、k、mおよびnは、独立して請求項1において定義した通りであり、ならびに
p1、p2、p3は、独立して0、1、2または3を示し、ならびに
r1、r2、r3は、独立して0、1、2または3を示し、
ここで式I1で表される化合物は、存在するものとして、少なくとも1つの重合性基Pを基A1、A2、A3、Z2およびZ3内に含有し、ただしR1が-Sp-Pを示す場合、式Iで表される化合物は、かかる少なくとも1つの重合性基Pを、R1における-Sp-PのPに加えて、基A1、A2およびA3内において含有する、
で表される化合物であることを特徴とする、請求項1または2に記載の媒体。 - 式Iで表される化合物が、合計で少なくとも1つの重合性基-Sp-Pを基A1、A2およびA3上に、存在するものとして含有することを特徴とする、請求項1または2に記載のLC媒体。
- 式Iで表される1種または2種以上の化合物に加えて、重合性の、または重合した構成成分が1種または2種以上のさらなる重合性の、または重合した化合物を含み、ここで重合した構成成分が重合性構成成分の重合によって得られることを特徴とする、請求項1~4のいずれか一項に記載のLC媒体。
- 式Iで表される1種または2種以上の化合物に加えて、さらに式I’
R1-[A3-Z3]m-[A2]k-[Z2]n-A1-Ra I’
式中、m、k、nおよび基Raは、請求項1に記載の式Iについて定義した通りであり、ならびに
A1、A2、A3は、それぞれ、互いに独立して、芳香族、複素芳香族、脂環式または複素環式基を示し、それはまた縮合される環を含有してもよく、それはまた基Lによって単置換または多置換されていてもよく、
Z2は、それぞれの場合において互いに独立して、-O-、-S-、-CO-、-CO-O-、-OCO-、-O-CO-O-、-OCH2-、-CH2O-、-SCH2-、-CH2S-、-CF2O-、-OCF2-、-CF2S-、-SCF2-、-(CH2)n1-、-CF2CH2-、-CH2CF2-、-(CF2)n1-、-CH=CH-、-CF=CF-、-C≡C-、-CH=CH-COO-、-OCO-CH=CH-、-(CR0R00)n1-を示し、
Z3は、それぞれの場合において互いに独立して、単結合、-O-、-S-、-CO-、-CO-O-、-OCO-、-O-CO-O-、-OCH2-、-CH2O-、-SCH2-、-CH2S-、-CF2O-、-OCF2-、-CF2S-、-SCF2-、-(CH2)n1-、-CF2CH2-、-CH2CF2-、-(CF2)n1-、-CH=CH-、-CF=CF-、-C≡C-、-CH=CH-COO-、-OCO-CH=CH-、-(CR0R00)n1-を示し、
n1は、1、2、3または4を示し、
Lは、それぞれの場合において互いに独立して、H、F、Cl、Br、I、-CN、-NO2、-NCO、-NCS、-OCN、-SCN、-C(=O)N(R0)2、-C(=O)R0、3~20個のC原子を有する任意に置換されたシリル、任意に置換されたアリールもしくはシクロアルキル、または1~25個のC原子を有する直鎖状もしくは分枝状アルキル、アルコキシ、アルキルカルボニル、アルコキシカルボニル、アルキルカルボニルオキシもしくはアルコキシカルボニルオキシを示し、ここでさらに1個または2個以上のH原子は、FまたはClによって置き換えられていてもよく、
R0は、それぞれの場合において互いに独立して、1~12個のC原子を有するアルキルを示し、
R00は、それぞれの場合において互いに独立して、Hまたは1~12個のC原子を有するアルキルを示し、
ならびに
R1は、H、ハロゲン、1~25個のC原子を有する直鎖状、分枝状または環状アルキルを示し、ここでさらに1つまたは2つ以上の隣接していないCH2基は、-O-、-S-、-CO-、-CO-O-、-O-CO-、-O-CO-O-によって、Oおよび/またはS原子が互いに直接結合しないように置き換えられていてもよく、かつここでさらに1個または2個以上のH原子は、FまたはClによって置き換えられていてもよい、
で表される1種または2種以上の非重合性化合物を含むことを特徴とする、請求項1~7のいずれか一項に記載のLC媒体。 - 式Iで表される化合物が以下の式:
ならびに
Z3は、単結合または-CH2CH2-を示し、
nは、0または1を示し、
p1、p2、p3は、独立して0、1、2または3を示し、
r1、r2、r3は、独立して0、1、2または3を示し、ならびに
R1は、H、ハロゲン、1~25個のC原子を有し、ここでさらに1つまたは2つ以上の隣接していないCH2基が-O-、-S-、-CO-、-CO-O-、-O-CO-、-O-CO-O-によって、Oおよび/またはS原子が互いに直接結合しないように置き換えられていてもよく、かつここでさらに、1個または2個以上のH原子がFまたはClによって置き換えられていてもよい、直鎖状、分枝状または環状アルキルを示す、
から選択された1種または2種以上の化合物を含むことを特徴とする、請求項1~9のいずれか一項に記載のLC媒体。 - 式I中の基Raが1つ、2つまたは3つのOH基を含むことを特徴とする、請求項1~10のいずれか一項に記載のLC媒体。
- 式Iで表される化合物について、
n=0であることを特徴とする、請求項1~13のいずれか一項に記載のLC媒体。 - 式Iで表される化合物について、基Pがビニルオキシ、アクリレート、メタクリレート、フルオロアクリレート、クロロアクリレート、オキセタンおよびエポキシドから選択されることを特徴とする、請求項1~14のいずれか一項に記載のLC媒体。
- 式Mで表される1種または2種以上の重合性化合物または式Mで表される化合物を含む(コ)ポリマーを含むことを特徴とする、請求項1~15のいずれか一項に記載のLC媒体:
P1-Sp1-A2-(Z1-A1)n-Sp2-P2 M
式中、個々のラジカルは以下の意味を有する:
P1、P2は、それぞれ独立して重合性基を示し、
Sp1、Sp2は、それぞれ独立してスペーサー基、または単結合を示し、
A1、A2は、それぞれ、互いに独立して以下の群から選択されたラジカルを示し:
a) トランス-1,4-シクロヘキシレン、1,4-シクロヘキセニレンおよび4,4’-ビシクロヘキシレンからなる群、ここでさらに、1つまたは2つ以上の隣接していないCH2基は、-O-および/または-S-によって置き換えられていてもよく、かつここでさらに、1個または2個以上のH原子は、基Lによって置き換えられていてもよい、あるいは
b) 1,4-フェニレンおよび1,3-フェニレンからなる群、ここでさらに、1つまたは2つのCH基は、Nによって置き換えられていてもよく、およびここでさらに、1個または2個以上のH原子は、基Lまたは-Sp3-Pによって置き換えられていてもよい、
c) テトラヒドロピラン-2,5-ジイル、1,3-ジオキサン-2,5-ジイル、テトラヒドロフラン-2,5-ジイル、シクロブタン-1,3-ジイル、ピペリジン-1,4-ジイル、チオフェン-2,5-ジイルおよびセレノフェン-2,5-ジイルからなる群、そのそれぞれはまた、基Lによって単置換または多置換されていてもよい、
d) 5~20個の環状C原子を有し、その1個または2個以上がさらにヘテロ原子によって置き換えられていてもよい、飽和の、部分的に不飽和の、または完全に不飽和の、および任意に置換された多環式ラジカルからなる群、
P3は、重合性基を示し、
Sp3は、スペーサー基を示し、
nは、0、1、2または3を示し、
Z1は、それぞれの場合において互いに独立して-CO-O-、-O-CO-、-CH2O-、-OCH2-、-CF2O-、-OCF2-または-(CH2)n-、式中nは2、3または4である、-O-、-CO-、-C(RcRd)-、-CH2CF2-、-CF2CF2-または単結合を示し、
Lは、それぞれの出現において同一であるか、または異なって、F、Cl、CN、SCN、SF5または直鎖状もしくは分枝状の、それぞれの場合において任意にフッ素化された、1~12個のC原子を有するアルキル、アルコキシ、アルキルカルボニル、アルコキシカルボニル、アルキルカルボニルオキシもしくはアルコキシカルボニルオキシを示し、
R0、R00は、それぞれ、互いに独立して、H、Fまたは1~12個のC原子を有する直鎖状もしくは分枝状アルキルを示し、ここでさらに、1個または2個以上のH原子は、Fによって置き換えられていてもよく、ならびに
RcおよびRdは、それぞれ、互いに独立して、Hまたは1~6個のC原子を有するアルキルを示し、
ここで基P1-Sp1-、-Sp2-P2および-Sp3-P3の1つまたは2つ以上は、ラジカルRaaを示してもよく、ただし存在する基P1-Sp1-、-Sp2-P2および-Sp3-P3の少なくとも1つはRaaを示さず、
Raaは、H、F、Cl、CNまたは1~25個のC原子を有する直鎖状もしくは分枝状アルキルを示し、ここでさらに1つまたは2つ以上の隣接していないCH2基は、それぞれ、互いに独立して、C(R0)=C(R00)-、-C≡C-、-O-、-S-、-CO-、-CO-O-、-O-CO-、-O-CO-O-によって、Oおよび/またはS原子が互いに直接結合しないように置き換えられていてもよく、かつここでさらに1個または2個以上のH原子は、F、Cl、またはCNによって置き換えられていてもよく、ここで基-OH、-NH2、-SH、-NHR11、-C(O)OHおよび-CHOは、式Mで表される化合物中に存在しない、ここでR11は、1~12個のC原子を有するアルキルを示す。 - 重合性の、または重合した構成成分が、0.01~5重量%の請求項16に記載の式M
P1-Sp1-A2-(Z1-A1)n-Sp2-P2 M
式中、個々のラジカルは以下の意味を有する:
P1、P2は、それぞれ独立して重合性基を示し、
Sp1、Sp2は、それぞれ独立してスペーサー基、または単結合を示し、
A1、A2は、それぞれ、互いに独立して以下の群から選択されたラジカルを示し:
a) トランス-1,4-シクロヘキシレン、1,4-シクロヘキセニレンおよび4,4’-ビシクロヘキシレンからなる群、ここでさらに、1つまたは2つ以上の隣接していないCH2基は、-O-および/または-S-によって置き換えられていてもよく、かつここでさらに、1個または2個以上のH原子は、基Lによって置き換えられていてもよい、あるいは
b) 1,4-フェニレンおよび1,3-フェニレンからなる群、ここでさらに、1つまたは2つのCH基は、Nによって置き換えられていてもよく、およびここでさらに、1個または2個以上のH原子は、基Lまたは-Sp3-Pによって置き換えられていてもよい、
c) テトラヒドロピラン-2,5-ジイル、1,3-ジオキサン-2,5-ジイル、テトラヒドロフラン-2,5-ジイル、シクロブタン-1,3-ジイル、ピペリジン-1,4-ジイル、チオフェン-2,5-ジイルおよびセレノフェン-2,5-ジイルからなる群、そのそれぞれはまた、基Lによって単置換または多置換されていてもよい、
d) 5~20個の環状C原子を有し、その1個または2個以上がさらにヘテロ原子によって置き換えられていてもよい、飽和の、部分的に不飽和の、または完全に不飽和の、および任意に置換された多環式ラジカルからなる群、
P3は、重合性基を示し、
Sp3は、スペーサー基を示し、
nは、0、1、2または3を示し、
Z1は、それぞれの場合において互いに独立して-CO-O-、-O-CO-、-CH2O-、-OCH2-、-CF2O-、-OCF2-または-(CH2)n-、式中nは2、3または4である、-O-、-CO-、-C(RcRd)-、-CH2CF2-、-CF2CF2-または単結合を示し、
Lは、それぞれの出現において同一であるか、または異なって、F、Cl、CN、SCN、SF5または直鎖状もしくは分枝状の、それぞれの場合において任意にフッ素化された、1~12個のC原子を有するアルキル、アルコキシ、アルキルカルボニル、アルコキシカルボニル、アルキルカルボニルオキシもしくはアルコキシカルボニルオキシを示し、
R0、R00は、それぞれ、互いに独立して、H、Fまたは1~12個のC原子を有する直鎖状もしくは分枝状アルキルを示し、ここでさらに、1個または2個以上のH原子は、Fによって置き換えられていてもよく、
RcおよびRdは、それぞれ、互いに独立して、Hまたは1~6個のC原子を有するアルキルを示し、
ここで基P1-Sp1-、-Sp2-P2および-Sp3-P3の1つまたは2つ以上は、ラジカルRaaを示してもよく、ただし存在する基P1-Sp1-、-Sp2-P2および-Sp3-P3の少なくとも1つはRaaを示さず、
Raaは、H、F、Cl、CNまたは1~25個のC原子を有する直鎖状もしくは分枝状アルキルを示し、ここでさらに1つまたは2つ以上の隣接していないCH2基は、それぞれ、互いに独立して、C(R0)=C(R00)-、-C≡C-、-O-、-S-、-CO-、-CO-O-、-O-CO-、-O-CO-O-によって、Oおよび/またはS原子が互いに直接結合しないように置き換えられていてもよく、かつここでさらに1個または2個以上のH原子は、F、Cl、またはCNによって置き換えられていてもよく、ここで基-OH、-NH2、-SH、-NHR11、-C(O)OHおよび-CHOは、式Mで表される化合物中に存在しない、ここでR11は、1~12個のC原子を有するアルキルを示し、
で表される1種もしくは2種以上の化合物、および/または0.01~10重量%の式I’
R1-[A3-Z3]m-[A2]k-[Z2]n-A1-Ra I’
式中、m、k、nおよび基Raは、請求項1に記載の式Iについて定義した通りであり、ならびに
A1、A2、A3は、それぞれ、互いに独立して、芳香族、複素芳香族、脂環式または複素環式基を示し、それはまた縮合される環を含有してもよく、それはまた基Lによって単置換または多置換されていてもよく、
Z2は、それぞれの場合において互いに独立して、-O-、-S-、-CO-、-CO-O-、-OCO-、-O-CO-O-、-OCH2-、-CH2O-、-SCH2-、-CH2S-、-CF2O-、-OCF2-、-CF2S-、-SCF2-、-(CH2)n1-、-CF2CH2-、-CH2CF2-、-(CF2)n1-、-CH=CH-、-CF=CF-、-C≡C-、-CH=CH-COO-、-OCO-CH=CH-、-(CR0R00)n1-を示し、
Z3は、それぞれの場合において互いに独立して、単結合、-O-、-S-、-CO-、-CO-O-、-OCO-、-O-CO-O-、-OCH2-、-CH2O-、-SCH2-、-CH2S-、-CF2O-、-OCF2-、-CF2S-、-SCF2-、-(CH2)n1-、-CF2CH2-、-CH2CF2-、-(CF2)n1-、-CH=CH-、-CF=CF-、-C≡C-、-CH=CH-COO-、-OCO-CH=CH-、-(CR0R00)n1-を示し、
n1は、1、2、3または4を示し、
Lは、それぞれの場合において互いに独立して、H、F、Cl、Br、I、-CN、-NO2、-NCO、-NCS、-OCN、-SCN、-C(=O)N(R0)2、-C(=O)R0、3~20個のC原子を有する任意に置換されたシリル、任意に置換されたアリールもしくはシクロアルキル、または1~25個のC原子を有する直鎖状もしくは分枝状アルキル、アルコキシ、アルキルカルボニル、アルコキシカルボニル、アルキルカルボニルオキシもしくはアルコキシカルボニルオキシを示し、ここでさらに1個または2個以上のH原子は、FまたはClによって置き換えられていてもよく、
R0は、それぞれの場合において互いに独立して、1~12個のC原子を有するアルキルを示し、
R00は、それぞれの場合において互いに独立して、Hまたは1~12個のC原子を有するアルキルを示し、
ならびに
R1は、互いに独立して、H、ハロゲン、1~25個のC原子を有する直鎖状、分枝状または環状アルキルを示し、ここでさらに1つまたは2つ以上の隣接していないCH2基は、-O-、-S-、-CO-、-CO-O-、-O-CO-、-O-CO-O-によって、Oおよび/またはS原子が互いに直接結合しないように置き換えられていてもよく、かつここでさらに1個または2個以上のH原子は、FまたはClによって置き換えられていてもよい、
で表される1種もしくは2種以上の非重合性化合物を含むことを特徴とする、請求項1~16のいずれか一項に記載のLC媒体。 - 重合性の、または重合した構成成分が以下の式:
P1、P2およびP3は、それぞれ、互いに独立して、重合性基を示し、
Sp1、Sp2およびSp3は、それぞれ、互いに独立して、単結合またはスペーサー基、ここでさらに、ラジカルP1-Sp1-、P2-Sp2-およびP3-Sp3-の1つまたは2つ以上は、ラジカルRaaを示してもよく、ただし存在するラジカルP1-Sp1-、P2-Sp2-およびP3-Sp3-の少なくとも一方は、Raaを示さず、
Raaは、H、F、Cl、CNまたは1~25個のC原子を有する直鎖状もしくは分枝状アルキルを示し、ここでさらに、1つまたは2つ以上の隣接していないCH2基は、それぞれ、互いに独立して、C(R0)=C(R00)-、-C≡C-、-N(R0)-、-O-、-S-、-CO-、-CO-O-、-O-CO-、-O-CO-O-によって、Oおよび/またはS原子が互いに直接結合しないように置き換えられていてもよく、およびここでさらに、1個または2個以上のH原子は、F、Cl、またはCNによって置き換えられていてもよく、ここで-OH、-NH2、-SH、-NHR11、-C(O)OHおよび-CHOは、式Mで表される化合物中に存在せず、
R11は、1~12個のC原子を有するアルキルを示し、
R0、R00は、それぞれ、互いに独立して、およびそれぞれの出現において同一であるかまたは異なってHまたは1~12個のC原子を有するアルキルを示し、
RyおよびRzは、それぞれ、互いに独立してH、F、CH3またはCF3を示し、
X1、X2およびX3は、それぞれ、互いに独立して-CO-O-、O-CO-または単結合を示し、
Z1は、-O-、-CO-、-C(RyRz)-または-CF2CF2-を示し、
Z2およびZ3は、それぞれ、互いに独立して-CO-O-、-O-CO-、-CH2O-、-OCH2-、-CF2O-、-OCF2-または-(CH2)n-を示し、式中nは2、3または4であり、
Lは、それぞれの出現において同一であるか、または異なって、F、Cl、CN、SCN、SF5または1~12個のC原子を有する直鎖状もしくは分枝状の、任意に一フッ素化もしくは多フッ素化されたアルキル、アルコキシ、アルケニル、アルキニル、アルキルカルボニル、アルコキシカルボニル、アルキルカルボニルオキシもしくはアルコキシカルボニルオキシを示し、
L’およびL’’は、それぞれ、互いに独立してH、FまたはClを示し、
rは、0、1、2、3または4を示し、
sは、0、1、2または3を示し、
tは、0、1または2を示し、ならびに
xは、0または1を示す、
で表される化合物から選択された1種または2種以上の化合物を含むことを特徴とする、請求項1~17のいずれか一項に記載のLC媒体。 - 式A、BおよびC
R2A、R2BおよびR2Cは、それぞれ、互いに独立してH、15個までのC原子を有し、非置換であるか、CNもしくはCF3によって単置換されているか、またはハロゲンによって少なくとも単置換されているアルキルラジカルを示し、ここでさらに、これらのラジカル中の1つまたは2つ以上のCH2基は、
によって、O原子が互いに直接結合しないように置き換えられていてもよく、
L1~4は、それぞれ、互いに独立してF、Cl、CF3またはCHF2を示し、
Z2およびZ2’は、それぞれ、互いに独立して単結合、-CH2CH2-、-CH=CH-、-CF2O-、-OCF2-、-CH2O-、-OCH2-、-COO-、-OCO-、-C2F4-、-CF=CF-、-CH=CHCH2O-を示し、
pは、1または2を示し、
qは、0または1を示し、ならびに
vは、1~6を示す、
で表される化合物の群から選択された1種または2種以上の化合物をさらに含む、請求項1に記載のLC媒体。 - 2つの基板および少なくとも2つの電極を有し、少なくとも1つの基板が光に対して透明であり、少なくとも1つの基板が1つまたは2つの電極を有し、かつ基板間に位置する請求項1~19のいずれか一項に記載のLC媒体の層を有するLCセルを含むLCディスプレイ。
- 基板がホメオトロピック配向のための配向層がないことを特徴とする、請求項20に記載のLCディスプレイ。
- 負の誘電異方性を有するLC媒体および相対する基板上に配置された電極を含むVAディスプレイであることを特徴とする、請求項20または21に記載のLCディスプレイ。
- 正の誘電異方性を有するLC媒体および少なくとも1つの基板上に配置されたインターデジタル電極を含むVA-IPSディスプレイであることを特徴とする、請求項20または21に記載のLCディスプレイ。
- 請求項1に記載のLC媒体の調製方法であって、式Iで表される1種または2種以上の化合物を、すべての固体または液晶構成成分を含み、溶媒を含まない、全体としての10重量%未満の濃度において、低分子量液晶構成成分と混合し、1種または2種以上の重合性化合物および/または任意の所望の添加剤を任意に加えることを特徴とする、前記方法。
- 2つの基板および少なくとも2つの電極を有するLCセルを含み、ここで少なくとも1つの基板が光に対して透明であり、少なくとも1つの基板が1つまたは2つの電極を有するLCディスプレイの製造方法であって、以下のプロセスステップ:
- セルを請求項1~19のいずれか一項に記載のLC媒体で満たし、ここでLC媒体の基板表面に関してのホメオトロピック配向が確立されること、および
- 重合性構成成分(単数または複数)を、任意に電圧のセルへの印加と共に、または電場の作用の下で、1または2以上のプロセスステップにおいて重合させること
を含む、前記方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2021071843A JP7331033B2 (ja) | 2014-03-10 | 2021-04-21 | ホメオトロピック配向を有する液晶媒体 |
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP14000831.9 | 2014-03-10 | ||
| EP14000831 | 2014-03-10 | ||
| EP14003943 | 2014-11-24 | ||
| EP14003943.9 | 2014-11-24 |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021071843A Division JP7331033B2 (ja) | 2014-03-10 | 2021-04-21 | ホメオトロピック配向を有する液晶媒体 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2015168826A JP2015168826A (ja) | 2015-09-28 |
| JP7003349B2 true JP7003349B2 (ja) | 2022-02-10 |
Family
ID=52472171
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2015046649A Active JP7003349B2 (ja) | 2014-03-10 | 2015-03-10 | ホメオトロピック配向を有する液晶媒体 |
| JP2021071843A Active JP7331033B2 (ja) | 2014-03-10 | 2021-04-21 | ホメオトロピック配向を有する液晶媒体 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021071843A Active JP7331033B2 (ja) | 2014-03-10 | 2021-04-21 | ホメオトロピック配向を有する液晶媒体 |
Country Status (6)
| Country | Link |
|---|---|
| US (2) | US9809748B2 (ja) |
| EP (2) | EP3730590A1 (ja) |
| JP (2) | JP7003349B2 (ja) |
| KR (1) | KR102417092B1 (ja) |
| CN (2) | CN105001879B (ja) |
| TW (3) | TWI760748B (ja) |
Families Citing this family (142)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN104837956B (zh) * | 2012-12-12 | 2018-01-30 | 默克专利股份有限公司 | 液晶介质 |
| EP3730590A1 (de) * | 2014-03-10 | 2020-10-28 | Merck Patent GmbH | Flüssigkristalline medien mit homöotroper ausrichtung |
| JP6896614B2 (ja) * | 2014-07-28 | 2021-06-30 | メルク パテント ゲゼルシャフト ミット ベシュレンクテル ハフツングMerck Patent Gesellschaft mit beschraenkter Haftung | ホメオトロピック配向を有する液晶媒体 |
| EP3656757A1 (en) * | 2015-01-14 | 2020-05-27 | JNC Corporation | Compound having polymerizable group, liquid crystal composition and liquid crystal display element |
| DE102016000361A1 (de) * | 2015-02-13 | 2016-08-18 | Merck Patent Gmbh | Verfahren zur Herstellung von Aryl- und Heteroarylalkoholen |
| US10647921B2 (en) | 2015-03-24 | 2020-05-12 | Jnc Corporation | Liquid crystal composition and liquid crystal display device |
| WO2017013981A1 (ja) * | 2015-07-23 | 2017-01-26 | Jnc株式会社 | 液晶組成物および液晶表示素子 |
| US11214736B2 (en) | 2015-09-09 | 2022-01-04 | Merck Patent Gmbh | Liquid-crystalline medium |
| TWI744235B (zh) * | 2015-09-15 | 2021-11-01 | 日商捷恩智股份有限公司 | 聚合性極性化合物、液晶組成物及液晶顯示元件 |
| KR20180054688A (ko) * | 2015-09-15 | 2018-05-24 | 메르크 파텐트 게엠베하 | 호메오트로픽 정렬을 갖는 액정 매질 |
| JP2018534630A (ja) * | 2015-09-23 | 2018-11-22 | メルク パテント ゲゼルシャフト ミット ベシュレンクテル ハフツングMerck Patent Gesellschaft mit beschraenkter Haftung | ポリマー安定化液晶ディスプレイにおいてプレチルト角を制御する方法 |
| TWI694068B (zh) * | 2015-10-13 | 2020-05-21 | 日商捷恩智股份有限公司 | 具有苯並噻吩的液晶性化合物、液晶組成物和液晶顯示元件 |
| EP3162875B1 (en) * | 2015-10-30 | 2018-05-23 | Merck Patent GmbH | Polymerisable compounds and the use thereof in liquid-crystal displays |
| KR20180090257A (ko) * | 2015-12-08 | 2018-08-10 | 제이엔씨 주식회사 | 액정 조성물 및 액정 표시 소자 |
| CN108368426B (zh) * | 2015-12-17 | 2022-03-11 | 默克专利股份有限公司 | 肉桂酸衍生物 |
| JP2017115122A (ja) * | 2015-12-21 | 2017-06-29 | Jnc株式会社 | 液晶組成物および液晶表示素子 |
| JPWO2017145611A1 (ja) * | 2016-02-25 | 2018-12-20 | Jnc株式会社 | 液晶組成物および液晶表示素子 |
| JP6860008B2 (ja) * | 2016-04-18 | 2021-04-14 | Jnc株式会社 | 液晶組成物および液晶表示素子 |
| CN105733608B (zh) * | 2016-04-22 | 2018-06-01 | 深圳市华星光电技术有限公司 | 液晶材料、液晶显示面板的制作方法、及液晶显示面板 |
| CN105936830A (zh) * | 2016-04-22 | 2016-09-14 | 深圳市华星光电技术有限公司 | 液晶材料、液晶显示面板的制作方法及液晶显示面板 |
| CN105733557B (zh) * | 2016-04-22 | 2017-12-29 | 深圳市华星光电技术有限公司 | 配体修饰量子点材料、液晶显示面板的制作方法及液晶显示面板 |
| US20190292457A1 (en) * | 2016-05-17 | 2019-09-26 | Merck Patent Gmbh | Light modulation element |
| JP6669255B2 (ja) * | 2016-06-03 | 2020-03-18 | Jnc株式会社 | 重合性極性化合物、液晶組成物、および液晶表示素子 |
| JP6766873B2 (ja) * | 2016-06-14 | 2020-10-14 | Jnc株式会社 | 液晶組成物および液晶表示素子 |
| JP6573091B2 (ja) | 2016-06-28 | 2019-09-11 | Jnc株式会社 | 液晶表示素子の製造方法および液晶表示素子 |
| US20180002604A1 (en) * | 2016-06-30 | 2018-01-04 | Merck Patent Gmbh | Liquid-crystalline medium |
| TWI612129B (zh) * | 2016-07-01 | 2018-01-21 | 友達光電股份有限公司 | 液晶配向化合物、液晶面板以及製造液晶面板的方法 |
| CN106281363B (zh) * | 2016-07-18 | 2019-01-22 | 深圳市华星光电技术有限公司 | 自取向液晶介质组合物、液晶显示面板及其制作方法 |
| JP2019527381A (ja) * | 2016-07-20 | 2019-09-26 | メルク パテント ゲゼルシャフト ミット ベシュレンクテル ハフツングMerck Patent Gesellschaft mit beschraenkter Haftung | 光学スイッチ素子において使用するためのスイッチ層 |
| CN106281364B (zh) * | 2016-07-21 | 2019-01-22 | 深圳市华星光电技术有限公司 | 自取向液晶介质组合物、液晶显示面板及其制作方法 |
| US10344213B2 (en) | 2016-07-22 | 2019-07-09 | Samsung Display Co., Ltd. | Reactive mesogen and liquid crystal composition including the same |
| WO2018025974A1 (ja) * | 2016-08-03 | 2018-02-08 | Jnc株式会社 | 液晶表示素子、表示装置 |
| KR102637055B1 (ko) * | 2016-08-09 | 2024-02-15 | 삼성디스플레이 주식회사 | 액정 표시 장치 및 그 제조 방법 |
| JPWO2018043144A1 (ja) * | 2016-09-01 | 2018-08-30 | Dic株式会社 | 液晶表示素子 |
| TWI710623B (zh) * | 2016-09-09 | 2020-11-21 | 日商捷恩智股份有限公司 | 液晶組成物及其用途、液晶顯示元件 |
| US20190359889A1 (en) * | 2016-09-14 | 2019-11-28 | Merck Patent Gmbh | Polymerisable liquid crystal material and polymerised liquid crystal film |
| TWI737834B (zh) | 2016-10-26 | 2021-09-01 | 日商迪愛生股份有限公司 | 液晶組成物用自發配向助劑 |
| JP6399261B1 (ja) * | 2016-11-01 | 2018-10-03 | Dic株式会社 | 液晶組成物用自発配向助剤 |
| DE102017010159A1 (de) * | 2016-11-21 | 2018-05-24 | Merck Patent Gmbh | Verbindungen zur homöotropen Ausrichtung von flüssigkristallinen Medien |
| TW201820009A (zh) * | 2016-11-28 | 2018-06-01 | 日商捷恩智股份有限公司 | 不具有配向膜的液晶顯示元件的製造方法以及顯示裝置 |
| CN106833677A (zh) * | 2016-12-29 | 2017-06-13 | 深圳市华星光电技术有限公司 | 一种垂直取向剂材料 |
| WO2018162454A1 (en) | 2017-03-09 | 2018-09-13 | Merck Patent Gmbh | Polymerisable compounds and the use thereof in liquid-crystal displays |
| CN107118781B (zh) * | 2017-03-09 | 2019-11-12 | 浙江工业大学 | 一种液晶介质的合成方法 |
| CN110199008A (zh) * | 2017-03-17 | 2019-09-03 | 捷恩智株式会社 | 液晶组合物及液晶显示元件 |
| CN110612476A (zh) | 2017-05-11 | 2019-12-24 | 默克专利股份有限公司 | 经聚合物稳定的液晶显示器的制造方法 |
| JP6624305B2 (ja) * | 2017-06-01 | 2019-12-25 | Dic株式会社 | 重合性モノマー、それを用いた液晶組成物及び液晶表示素子 |
| CN110651022A (zh) * | 2017-06-01 | 2020-01-03 | Dic株式会社 | 聚合性单体、使用其的液晶组合物及液晶显示元件 |
| US11174217B2 (en) * | 2017-06-12 | 2021-11-16 | Dic Corporation | Polymerizable compound and liquid crystal composition |
| JP6610833B2 (ja) * | 2017-06-26 | 2019-11-27 | Dic株式会社 | 液晶組成物用自発配向助剤 |
| CN110621761A (zh) * | 2017-06-29 | 2019-12-27 | Dic株式会社 | 液晶组合物及液晶显示元件 |
| KR20200062261A (ko) | 2017-09-29 | 2020-06-03 | 메르크 파텐트 게엠베하 | 중합성 화합물 및 이의 액정 디스플레이에서의 용도 |
| KR20190041918A (ko) * | 2017-10-13 | 2019-04-23 | 메르크 파텐트 게엠베하 | 액정 매질 |
| KR20190047160A (ko) | 2017-10-25 | 2019-05-08 | 삼성디스플레이 주식회사 | 액정 조성물 및 이를 포함하는 표시 장치 |
| JP6725893B2 (ja) | 2017-11-17 | 2020-07-22 | Dic株式会社 | 重合性化合物、並びにそれを使用した液晶組成物及び液晶表示素子 |
| TW201925437A (zh) | 2017-12-04 | 2019-07-01 | 德商馬克專利公司 | 液晶介質 |
| KR102349230B1 (ko) * | 2017-12-13 | 2022-01-10 | 주식회사 이엔에프테크놀로지 | 수직 배향 안정성이 높은 액정 조성물 |
| EP3502209B1 (en) | 2017-12-20 | 2020-10-14 | Merck Patent GmbH | Liquid-crystalline media having homeotropic alignment |
| EP3502210B1 (en) * | 2017-12-20 | 2020-09-09 | Merck Patent GmbH | Liquid-crystal medium |
| KR20200101325A (ko) * | 2017-12-21 | 2020-08-27 | 디아이씨 가부시끼가이샤 | 액정 조성물 |
| KR20200100034A (ko) * | 2017-12-21 | 2020-08-25 | 디아이씨 가부시끼가이샤 | 액정 조성물 |
| CN111344277B (zh) * | 2017-12-21 | 2023-03-28 | Dic株式会社 | 聚合性化合物以及使用其的液晶组合物及液晶显示元件 |
| TWI773854B (zh) | 2017-12-22 | 2022-08-11 | 日商迪愛生股份有限公司 | 液晶顯示元件 |
| TWI774891B (zh) * | 2017-12-22 | 2022-08-21 | 日商迪愛生股份有限公司 | 液晶組成物及液晶顯示元件 |
| KR20200100628A (ko) | 2017-12-22 | 2020-08-26 | 디아이씨 가부시끼가이샤 | 중합성 액정 조성물 및 액정 표시 소자 그리고 중합성 화합물 |
| CN108003897A (zh) * | 2017-12-25 | 2018-05-08 | 深圳市华星光电技术有限公司 | 垂直取向剂、自取向液晶混合物及其应用 |
| CN110093166B (zh) * | 2018-01-31 | 2021-03-16 | 北京八亿时空液晶科技股份有限公司 | 一种含有自配向化合物的液晶组合物及其应用 |
| DE102019000286A1 (de) | 2018-02-05 | 2019-08-08 | Merck Patent Gmbh | Verbindungen zur homöotropen Ausrichtung von flüssigkristallinen Medien |
| TW201936907A (zh) | 2018-02-06 | 2019-09-16 | 德商馬克專利公司 | 液晶介質 |
| CN108410475A (zh) | 2018-03-01 | 2018-08-17 | 深圳市华星光电半导体显示技术有限公司 | 一种液晶材料及液晶显示面板 |
| US11739270B2 (en) | 2018-03-01 | 2023-08-29 | Dic Corporation | Polymerizable compound as well as liquid crystal composition and liquid crystal display device each including polymerizable compound |
| CN110229678B (zh) * | 2018-03-06 | 2020-10-27 | 北京八亿时空液晶科技股份有限公司 | 一种自配向添加剂及其制备方法与应用 |
| CN110358550B (zh) * | 2018-03-26 | 2021-02-19 | 北京八亿时空液晶科技股份有限公司 | 一种新型液晶垂直自配向添加剂及其制备方法与应用 |
| CN110358551B (zh) * | 2018-03-26 | 2020-12-18 | 北京八亿时空液晶科技股份有限公司 | 一种新型液晶垂直配向剂及其制备方法与应用 |
| US20190322938A1 (en) * | 2018-04-20 | 2019-10-24 | Shenzhen China Star Optoelectronics Semiconductor Display Technology Co., Ltd. | Liquid crystal medium mixture, liquid crystal display panel and manufacturing method of liquid crystal display panel |
| KR20190124631A (ko) | 2018-04-26 | 2019-11-05 | 제이엔씨 주식회사 | 액정 조성물 및 액정 표시 소자 |
| EP3802734A1 (en) | 2018-06-07 | 2021-04-14 | Merck Patent GmbH | Additives for liquid-crystal mixtures |
| CN110803983A (zh) * | 2018-08-04 | 2020-02-18 | 石家庄诚志永华显示材料有限公司 | 化合物、液晶组合物、液晶显示元件及液晶显示器 |
| CN110804005A (zh) * | 2018-08-04 | 2020-02-18 | 石家庄诚志永华显示材料有限公司 | 化合物、液晶组合物、液晶显示元件及液晶显示器 |
| CN110872520B (zh) * | 2018-08-31 | 2022-12-09 | 石家庄诚志永华显示材料有限公司 | 液晶显示器件 |
| US11254872B2 (en) | 2018-09-06 | 2022-02-22 | Merck Patent Gmbh | Liquid crystal media comprising polymerisable compounds |
| EP3847224A1 (en) | 2018-09-06 | 2021-07-14 | Merck Patent GmbH | Polymerisable compounds and the use thereof in liquid-crystal displays |
| JP7271896B2 (ja) * | 2018-10-02 | 2023-05-12 | Dic株式会社 | 重合性化合物並びにそれを使用した液晶組成物及び液晶表示素子 |
| CN111040779B (zh) * | 2018-10-15 | 2022-06-10 | 北京八亿时空液晶科技股份有限公司 | 一种液晶垂直自配向添加剂及其制备方法与应用 |
| CN111073663A (zh) * | 2018-10-22 | 2020-04-28 | 北京八亿时空液晶科技股份有限公司 | 一种新型自配向添加剂及其制备方法与应用 |
| CN112912468B (zh) | 2018-10-25 | 2024-03-08 | 默克专利股份有限公司 | 液晶介质 |
| CN111116367A (zh) * | 2018-10-31 | 2020-05-08 | 默克专利股份有限公司 | 包含可聚合化合物的液晶介质 |
| US20230029961A1 (en) | 2018-11-07 | 2023-02-02 | Merck Patent Gmbh | Liquid crystal media comprising polymerisable compounds |
| CN109705881A (zh) * | 2018-11-30 | 2019-05-03 | 成都中电熊猫显示科技有限公司 | 液晶以及显示面板和显示装置 |
| US11739266B2 (en) | 2018-12-07 | 2023-08-29 | Merck Patent Gmbh | Polymerisable compounds and the use thereof in liquid-crystal displays |
| US20230007940A1 (en) * | 2018-12-07 | 2023-01-12 | Merckp Patent Gmbh | Liquid-crystal medium comprising polymerisable compounds and the use thereof in liquid-crystal displays |
| EP3666853B1 (en) | 2018-12-10 | 2021-06-16 | Merck Patent GmbH | Liquid-crystal medium |
| DE102019008296A1 (de) | 2018-12-20 | 2020-06-25 | Merck Patent Gmbh | Flüssigkristallines Medium |
| JP2020100600A (ja) * | 2018-12-25 | 2020-07-02 | Dic株式会社 | 重合性安定剤及びそれを用いた液晶組成物 |
| TWI719394B (zh) * | 2019-01-25 | 2021-02-21 | 達興材料股份有限公司 | 添加劑及其應用 |
| EP3924447B1 (en) | 2019-02-15 | 2024-01-24 | Merck Patent GmbH | Polymerisable compounds and the use thereof in liquid-crystal displays |
| CN113677657A (zh) * | 2019-05-15 | 2021-11-19 | Dic株式会社 | 聚合性液晶组合物及液晶显示元件、以及化合物 |
| CN112143507A (zh) | 2019-06-28 | 2020-12-29 | 默克专利股份有限公司 | Lc介质 |
| EP3789470A1 (en) | 2019-09-03 | 2021-03-10 | Merck Patent GmbH | Liquid crystal media comprising polymerisable compounds |
| EP3816264A1 (en) | 2019-10-29 | 2021-05-05 | Merck Patent GmbH | Liquid crystal media comprising polymerisable compounds |
| KR20210077615A (ko) | 2019-12-17 | 2021-06-25 | 메르크 파텐트 게엠베하 | 액정 매질 |
| WO2021148421A1 (en) | 2020-01-23 | 2021-07-29 | Merck Patent Gmbh | Liquid-crystal medium |
| WO2021151846A1 (en) | 2020-01-29 | 2021-08-05 | Merck Patent Gmbh | Method for adjustment of alignment of liquid crystals |
| TW202136871A (zh) | 2020-02-13 | 2021-10-01 | 德商馬克專利公司 | 液晶裝置 |
| TW202322824A (zh) | 2020-02-18 | 2023-06-16 | 美商基利科學股份有限公司 | 抗病毒化合物 |
| CN113444531A (zh) * | 2020-03-27 | 2021-09-28 | Dic株式会社 | 聚合性化合物、含有聚合性化合物的液晶组合物和使用其的液晶显示元件 |
| WO2021192439A1 (ja) * | 2020-03-27 | 2021-09-30 | Dic株式会社 | 液晶組成物、液晶表示素子及び化合物 |
| KR20210125922A (ko) | 2020-04-09 | 2021-10-19 | 메르크 파텐트 게엠베하 | 액정 매질 |
| CN113046096A (zh) | 2020-06-10 | 2021-06-29 | 默克专利股份有限公司 | 包含可聚合化合物的液晶介质 |
| WO2022003001A1 (en) | 2020-07-03 | 2022-01-06 | Merck Patent Gmbh | Liquid crystal medium |
| EP3933009B1 (en) | 2020-07-03 | 2023-08-16 | Merck Patent GmbH | Liquid crystal medium |
| WO2022002997A1 (en) | 2020-07-03 | 2022-01-06 | Merck Patent Gmbh | Liquid crystal medium |
| EP3944011A1 (en) | 2020-07-21 | 2022-01-26 | Merck Patent GmbH | Liquid-crystal display |
| CN114525139A (zh) | 2020-10-07 | 2022-05-24 | 默克专利股份有限公司 | 液晶介质 |
| WO2022084168A1 (en) | 2020-10-19 | 2022-04-28 | Merck Patent Gmbh | 4,6-difluorodibenzothiophene derivatives and liquid-crystal medium containing these |
| US20220119711A1 (en) | 2020-10-19 | 2022-04-21 | Merck Patent Gmbh | Liquid-crystal medium |
| US20230407180A1 (en) | 2020-11-06 | 2023-12-21 | Merck Patent Gmbh | Liquid-crystal medium comprising polymerizable compounds |
| WO2022101151A1 (en) * | 2020-11-12 | 2022-05-19 | Merck Patent Gmbh | Liquid-crystal medium comprising polymerizable compounds |
| JP2022080289A (ja) | 2020-11-17 | 2022-05-27 | メルク パテント ゲゼルシャフト ミット ベシュレンクテル ハフツング | 液晶媒体 |
| EP4267693A1 (en) | 2020-12-22 | 2023-11-01 | Merck Patent GmbH | Polymerisable compounds and the use thereof in liquid-crystal displays |
| CN113088297A (zh) | 2021-03-09 | 2021-07-09 | 默克专利股份有限公司 | 包含可聚合化合物的液晶介质 |
| CN113214083B (zh) * | 2021-04-06 | 2022-04-22 | 北京八亿时空液晶科技股份有限公司 | 一种自配向可聚合化合物及其应用 |
| CN113149839B (zh) * | 2021-04-06 | 2022-02-22 | 北京八亿时空液晶科技股份有限公司 | 一种自配向液晶介质化合物及其应用 |
| AU2022256476A1 (en) | 2021-04-16 | 2023-10-12 | Gilead Sciences, Inc. | Methods of preparing carbanucleosides using amides |
| CN115287081A (zh) | 2021-05-04 | 2022-11-04 | 默克专利股份有限公司 | 包含可聚合化合物的染料掺杂液晶介质 |
| DE102022001602A1 (de) | 2021-05-07 | 2022-11-10 | MERCK Patent Gesellschaft mit beschränkter Haftung | Flüssigkristallmedium enthaltend polymerisierbare Verbindungen |
| CN113583684A (zh) * | 2021-09-07 | 2021-11-02 | 石家庄诚志永华显示材料有限公司 | 液晶组合物及液晶显示元器件 |
| TW202330872A (zh) | 2021-09-28 | 2023-08-01 | 德商馬克專利公司 | 液晶介質 |
| WO2023066953A1 (en) | 2021-10-20 | 2023-04-27 | Merck Patent Gmbh | Liquid-crystal medium comprising polymerizable compounds |
| WO2023094404A1 (en) | 2021-11-24 | 2023-06-01 | Merck Patent Gmbh | Liquid crystal medium and liquid crystal display |
| KR20230088622A (ko) | 2021-12-10 | 2023-06-20 | 메르크 파텐트 게엠베하 | 중합성 화합물을 포함하는 액정 매질 |
| WO2023110962A1 (en) | 2021-12-17 | 2023-06-22 | Merck Patent Gmbh | Liquid-crystal display |
| CN116554891A (zh) | 2022-01-30 | 2023-08-08 | 默克专利股份有限公司 | 包含可聚合化合物的液晶介质 |
| EP4249570A1 (en) | 2022-03-21 | 2023-09-27 | Merck Patent GmbH | Liquid-crystalline medium |
| WO2023198669A1 (en) | 2022-04-12 | 2023-10-19 | Merck Patent Gmbh | Liquid-crystalline medium |
| WO2023198673A1 (en) | 2022-04-12 | 2023-10-19 | Merck Patent Gmbh | Liquid-crystalline medium |
| WO2023198671A1 (en) | 2022-04-12 | 2023-10-19 | Merck Patent Gmbh | Liquid-crystalline medium |
| WO2023203043A1 (en) | 2022-04-22 | 2023-10-26 | Merck Patent Gmbh | Liquid-crystal medium |
| KR20230151725A (ko) | 2022-04-26 | 2023-11-02 | 연세대학교 산학협력단 | 온도감응성 이온 열전 물질 및 이를 포함하는 온도감응성 형광 이온 열전 센서 |
| WO2023208801A1 (en) | 2022-04-27 | 2023-11-02 | Merck Patent Gmbh | Liquid-crystal medium comprising polymerizable compounds |
| WO2023209049A1 (en) | 2022-04-29 | 2023-11-02 | Merck Patent Gmbh | Liquid-crystal medium |
| EP4286493A1 (en) | 2022-06-02 | 2023-12-06 | Merck Patent GmbH | Liquid-crystal medium |
| EP4306614A1 (en) | 2022-07-15 | 2024-01-17 | Merck Patent GmbH | Liquid-crystalline medium |
Citations (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2000327924A (ja) | 1999-05-25 | 2000-11-28 | Nitto Denko Corp | 液晶ポリマー組成物、位相差板および楕円偏光板 |
| JP2002356515A (ja) | 2000-12-27 | 2002-12-13 | Canon Inc | 化合物、高分子化合物とその利用方法 |
| JP2004182949A (ja) | 2002-12-06 | 2004-07-02 | Dainippon Ink & Chem Inc | 重合性液晶組成物及び光学異方体 |
| JP2007182423A (ja) | 2005-12-08 | 2007-07-19 | Chisso Corp | 側方α−置換アクリレート化合物およびその重合体 |
| WO2008027210A2 (en) | 2006-08-29 | 2008-03-06 | Den-Mat Holdings Llc | Biocompatible stent |
| JP2008164925A (ja) | 2006-12-28 | 2008-07-17 | Hayashi Telempu Co Ltd | 位相差フィルムおよびその製造方法 |
| WO2009019656A1 (en) | 2007-08-07 | 2009-02-12 | Piramal Life Sciences Limited | Pyridyl derivatives, their preparation and use |
| WO2010019861A1 (en) | 2008-08-15 | 2010-02-18 | University Of Louisville Research Foundation, Inc. | Compounds, their syntheses, and their uses |
| JP2002542219A5 (ja) | 2000-04-11 | 2011-03-17 | ||
| WO2011139936A2 (en) | 2010-05-03 | 2011-11-10 | Levin, Leana | Dental compositions |
| WO2014090362A1 (en) | 2012-12-12 | 2014-06-19 | Merck Patent Gmbh | Liquid-crystalline medium |
| WO2014094959A1 (en) | 2012-12-17 | 2014-06-26 | Merck Patent Gmbh | Liquid-crystal displays and liquid-crystalline media having homeotropic alignment |
| JP2014196265A (ja) | 2013-03-29 | 2014-10-16 | Dic株式会社 | 重合性化合物及び光学素子 |
| WO2015114864A1 (ja) | 2014-01-30 | 2015-08-06 | 公立大学法人兵庫県立大学 | 光反応性液晶組成物、表示素子、光学素子、表示素子の製造方法、光学素子の製造方法 |
| WO2016114093A1 (ja) | 2015-01-14 | 2016-07-21 | Jnc株式会社 | 重合性基を有する化合物、液晶組成物および液晶表示素子 |
| JP2017523289A (ja) | 2014-07-28 | 2017-08-17 | メルク パテント ゲゼルシャフト ミット ベシュレンクテル ハフツングMerck Patent Gesellschaft mit beschraenkter Haftung | ホメオトロピック配向を有する液晶媒体 |
Family Cites Families (65)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3162676A (en) * | 1962-06-18 | 1964-12-22 | Nat Starch Chem Corp | Ethylenically unsaturated derivatives of 2, 4-dihydroxybenzophenone |
| US3972589A (en) | 1972-06-23 | 1976-08-03 | General Electric Company | Nematic liquid crystal mixtures with stable homeotropic boundary conditions and methods of making the same |
| FR2204002A1 (en) | 1972-10-20 | 1974-05-17 | Matsushita Electric Ind Co Ltd | Liquid crystal screen with room temp nematic props - contg substd phenyl alkoxy benzoate(s), for use in electro-optical equipment |
| JPS5035076A (ja) | 1973-08-01 | 1975-04-03 | ||
| EP0058981B1 (en) | 1981-02-25 | 1986-01-22 | Hitachi, Ltd. | Colorless liquid crystalline compounds |
| JPS57140737A (en) | 1981-02-25 | 1982-08-31 | Kanto Kagaku Kk | Colorless liquid crystal substance, colorless liquid crystal composition, and display element of liquid crystal |
| JPS5841827A (ja) | 1981-08-06 | 1983-03-11 | イギリス国 | 液晶組成物 |
| US4482472A (en) | 1981-08-06 | 1984-11-13 | The Secretary Of State For Defence In Her Britannic Majesty's Government Of The United Kingdom Of Great Britian And Northern Ireland | Liquid crystal materials |
| DE3211601A1 (de) | 1982-03-30 | 1983-10-06 | Merck Patent Gmbh | Hydroterphenyle |
| JPH02180909A (ja) * | 1988-12-30 | 1990-07-13 | Ipposha Oil Ind Co Ltd | ベンゾフェノン系化合物及びその単独重合物或いは共重合物 |
| DE4000451B4 (de) | 1990-01-09 | 2004-12-09 | Merck Patent Gmbh | Elektrooptisches Flüssigkristallschaltelement |
| DE69229621D1 (de) | 1991-09-13 | 1999-08-26 | Merck Patent Gmbh | Elektrooptisches System |
| US5427713A (en) | 1992-03-10 | 1995-06-27 | Raychem Corporation | Encapsulated liquid crystal structures, apparatus containing the same, and methods therefor |
| EP0588568B1 (en) | 1992-09-18 | 2002-12-18 | Hitachi, Ltd. | A liquid crystal display device |
| JPH07181439A (ja) | 1993-12-24 | 1995-07-21 | Hitachi Ltd | アクティブマトリクス型液晶表示装置 |
| JP3543351B2 (ja) | 1994-02-14 | 2004-07-14 | 株式会社日立製作所 | アクティブマトリクス型液晶表示装置 |
| TW262553B (ja) | 1994-03-17 | 1995-11-11 | Hitachi Seisakusyo Kk | |
| US5993691A (en) | 1995-02-03 | 1999-11-30 | Merck Patent Gesellschaft Mit | Electro-optical liquid crystal display |
| DE19528106A1 (de) | 1995-02-03 | 1996-08-08 | Merck Patent Gmbh | Elektrooptische Flüssigkristallanzeige |
| DE19528107B4 (de) | 1995-03-17 | 2010-01-21 | Merck Patent Gmbh | Flüssigkristallines Medium und seine Verwendung in einer elektrooptischen Flüssigkristallanzeige |
| DE19509410A1 (de) | 1995-03-15 | 1996-09-19 | Merck Patent Gmbh | Elektrooptische Flüssigkristallanzeige |
| DE19539141B4 (de) | 1995-10-20 | 2016-07-07 | Merck Patent Gmbh | 2,6-Di-tert.-butylphenole |
| JPH1036847A (ja) | 1996-07-25 | 1998-02-10 | Seiko Epson Corp | 液晶表示素子およびその製造方法 |
| JP3287288B2 (ja) | 1996-11-22 | 2002-06-04 | チッソ株式会社 | ポリハロアルキルエーテル誘導体とそれらを含む液晶組成物及び液晶表示素子 |
| JP3531713B2 (ja) | 1996-11-22 | 2004-05-31 | チッソ株式会社 | 液晶組成物および液晶表示素子 |
| JP4013090B2 (ja) * | 1997-11-18 | 2007-11-28 | 大日本インキ化学工業株式会社 | 液晶性(メタ)アクリレート化合物と該化合物を含有する組成物及びこれを用いた光学異方体 |
| TWI239997B (en) | 1998-02-04 | 2005-09-21 | Merck Patent Gmbh | Liquid-crystal composition, method of adjusting the resistance of a liquid-crystal composition, liquid-crystal display and substituted phenols |
| US6177972B1 (en) | 1999-02-04 | 2001-01-23 | International Business Machines Corporation | Polymer stabilized in-plane switched LCD |
| GB9908934D0 (en) * | 1999-04-19 | 1999-06-16 | Rolic Ag | Liquid crystalline compounds |
| DE10117224B4 (de) | 2000-04-19 | 2015-12-31 | Merck Patent Gmbh | Verfahren zur Stabilisierung von Halogenaromaten |
| JP2002023199A (ja) | 2000-07-07 | 2002-01-23 | Fujitsu Ltd | 液晶表示装置およびその製造方法 |
| JP2003253265A (ja) | 2002-02-27 | 2003-09-10 | Dainippon Ink & Chem Inc | 調光層形成材料及び液晶デバイス |
| JP4175826B2 (ja) | 2002-04-16 | 2008-11-05 | シャープ株式会社 | 液晶表示装置 |
| ATE354623T1 (de) | 2002-07-06 | 2007-03-15 | Merck Patent Gmbh | Flüssigkristallines medium |
| US6905633B2 (en) | 2002-12-13 | 2005-06-14 | Xerox Corporation | Compounds of formula (3) to stabilize liquid crystal domains |
| JP2004294605A (ja) | 2003-03-26 | 2004-10-21 | Fujitsu Display Technologies Corp | 液晶パネル |
| JP4505709B2 (ja) * | 2003-04-25 | 2010-07-21 | Dic株式会社 | 重合性液晶組成物及び光学異方体 |
| JP4506105B2 (ja) | 2003-06-10 | 2010-07-21 | Dic株式会社 | 液晶配向促進剤、液晶組成物及び光学異方体 |
| JP2005084271A (ja) | 2003-09-08 | 2005-03-31 | Dainippon Printing Co Ltd | 光学機能層、光学機能層の形成方法、および液晶表示素子 |
| JP4387276B2 (ja) | 2004-09-24 | 2009-12-16 | シャープ株式会社 | 液晶表示装置 |
| JP2008522958A (ja) * | 2004-10-07 | 2008-07-03 | メルク パテント ゲゼルシャフト ミット ベシュレンクテル ハフトング | クロマン誘導体類、それらの調製方法、およびそれらの使用 |
| JP2006139047A (ja) | 2004-11-12 | 2006-06-01 | Sharp Corp | 液晶表示装置およびその製造方法 |
| JP4876402B2 (ja) | 2005-02-16 | 2012-02-15 | Jnc株式会社 | 液晶組成物および液晶表示素子 |
| JP4876408B2 (ja) | 2005-03-01 | 2012-02-15 | Jnc株式会社 | 液晶組成物および液晶表示素子 |
| JP5315590B2 (ja) | 2006-02-14 | 2013-10-16 | Jnc株式会社 | 液晶化合物、液晶組成物および液晶表示素子 |
| JP5186116B2 (ja) * | 2006-06-12 | 2013-04-17 | 富士フイルム株式会社 | 化合物、それを含有する液晶組成物、異方性材料、偏光板保護フィルム、光学補償フィルムならびに液晶表示装置 |
| JP4720634B2 (ja) | 2006-06-13 | 2011-07-13 | ソニー株式会社 | 重合性液晶組成物、光学素子、光学素子の製造方法、および液晶表示装置 |
| CA2657639A1 (en) * | 2006-07-19 | 2008-01-24 | Astrazeneca Ab | Novel tricyclic spiropiperidine compounds, their synthesis and their uses as modulators of chemokine receptor activity |
| EP1911828B1 (de) | 2006-10-12 | 2010-09-01 | Merck Patent GmbH | Flüssigkristallanzeige |
| WO2008150231A1 (en) * | 2007-06-08 | 2008-12-11 | Astrazeneca Ab | New heterocyclic compounds for treatment of respiratory, airway or inflammatory disorders |
| US8114310B2 (en) | 2007-10-22 | 2012-02-14 | Merck Patent Gmbh | Liquid-crystal display |
| WO2009086911A1 (en) * | 2008-01-11 | 2009-07-16 | Merck Patent Gmbh | Reactive mesogenic compounds and mixtures |
| WO2009153168A1 (de) * | 2008-06-17 | 2009-12-23 | Basf Se | Polymerisierbare chirale verbindungen, enthaltend 2,6-naphthyl- und isomannit-einheiten, und deren verwendung als chirale dotierstoffe |
| JP5093820B2 (ja) | 2008-12-26 | 2012-12-12 | エルジー ディスプレイ カンパニー リミテッド | 液晶表示装置及び液晶組成物 |
| DE102010006691A1 (de) | 2009-02-06 | 2010-10-28 | Merck Patent Gmbh | Flüssigkristallines Medium und Flüssigkristallanzeige |
| JP6069197B2 (ja) * | 2010-07-15 | 2017-02-01 | メルク パテント ゲゼルシャフト ミット ベシュレンクテル ハフツングMerck Patent Gesellschaft mit beschraenkter Haftung | 液晶媒体およびポリマー安定化ホメオトロピック配向を有する液晶ディスプレイ |
| KR101869113B1 (ko) * | 2010-08-19 | 2018-06-19 | 메르크 파텐트 게엠베하 | 액정 매질 및 액정 디스플레이 |
| DE102011108708A1 (de) * | 2010-09-25 | 2012-03-29 | Merck Patent Gmbh | Flüssigkristallanzeigen und flüssigkristalline Medien mit homöotroper Ausrichtung |
| KR101926207B1 (ko) * | 2011-02-05 | 2018-12-06 | 메르크 파텐트 게엠베하 | 호메오트로픽 정렬을 갖는 액정 디스플레이 |
| CN107083243A (zh) | 2011-07-07 | 2017-08-22 | 默克专利股份有限公司 | 液晶介质 |
| JP6146577B2 (ja) * | 2011-12-28 | 2017-06-14 | 日産化学工業株式会社 | 液晶配向剤、液晶配向膜及び液晶表示素子 |
| US9157027B2 (en) * | 2012-04-24 | 2015-10-13 | Jnc Corporation | Compound having four polymerizable groups, liquid crystal composition and liquid crystal display device |
| CN102660299B (zh) * | 2012-04-28 | 2015-02-04 | 深圳市华星光电技术有限公司 | 液晶介质混合物及使用其的液晶显示器 |
| JP6212912B2 (ja) * | 2012-07-03 | 2017-10-18 | Jsr株式会社 | 液晶配向剤、液晶配向膜、液晶表示素子及び液晶表示素子の製造方法 |
| EP3730590A1 (de) * | 2014-03-10 | 2020-10-28 | Merck Patent GmbH | Flüssigkristalline medien mit homöotroper ausrichtung |
-
2015
- 2015-02-13 EP EP20174018.0A patent/EP3730590A1/de active Pending
- 2015-02-13 EP EP15000445.5A patent/EP2918658B1/de active Active
- 2015-03-09 KR KR1020150032438A patent/KR102417092B1/ko active IP Right Grant
- 2015-03-10 US US14/643,147 patent/US9809748B2/en active Active
- 2015-03-10 TW TW109116247A patent/TWI760748B/zh active
- 2015-03-10 CN CN201510328582.0A patent/CN105001879B/zh active Active
- 2015-03-10 TW TW108118580A patent/TWI695880B/zh active
- 2015-03-10 JP JP2015046649A patent/JP7003349B2/ja active Active
- 2015-03-10 CN CN201910154496.0A patent/CN109825312B/zh active Active
- 2015-03-10 TW TW104107659A patent/TWI663249B/zh active
-
2017
- 2017-11-03 US US15/803,156 patent/US10513657B2/en active Active
-
2021
- 2021-04-21 JP JP2021071843A patent/JP7331033B2/ja active Active
Patent Citations (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2000327924A (ja) | 1999-05-25 | 2000-11-28 | Nitto Denko Corp | 液晶ポリマー組成物、位相差板および楕円偏光板 |
| JP2002542219A5 (ja) | 2000-04-11 | 2011-03-17 | ||
| JP2002356515A (ja) | 2000-12-27 | 2002-12-13 | Canon Inc | 化合物、高分子化合物とその利用方法 |
| JP2004182949A (ja) | 2002-12-06 | 2004-07-02 | Dainippon Ink & Chem Inc | 重合性液晶組成物及び光学異方体 |
| JP2007182423A (ja) | 2005-12-08 | 2007-07-19 | Chisso Corp | 側方α−置換アクリレート化合物およびその重合体 |
| WO2008027210A2 (en) | 2006-08-29 | 2008-03-06 | Den-Mat Holdings Llc | Biocompatible stent |
| JP2008164925A (ja) | 2006-12-28 | 2008-07-17 | Hayashi Telempu Co Ltd | 位相差フィルムおよびその製造方法 |
| WO2009019656A1 (en) | 2007-08-07 | 2009-02-12 | Piramal Life Sciences Limited | Pyridyl derivatives, their preparation and use |
| WO2010019861A1 (en) | 2008-08-15 | 2010-02-18 | University Of Louisville Research Foundation, Inc. | Compounds, their syntheses, and their uses |
| WO2011139936A2 (en) | 2010-05-03 | 2011-11-10 | Levin, Leana | Dental compositions |
| WO2014090362A1 (en) | 2012-12-12 | 2014-06-19 | Merck Patent Gmbh | Liquid-crystalline medium |
| WO2014094959A1 (en) | 2012-12-17 | 2014-06-26 | Merck Patent Gmbh | Liquid-crystal displays and liquid-crystalline media having homeotropic alignment |
| JP2014196265A (ja) | 2013-03-29 | 2014-10-16 | Dic株式会社 | 重合性化合物及び光学素子 |
| WO2015114864A1 (ja) | 2014-01-30 | 2015-08-06 | 公立大学法人兵庫県立大学 | 光反応性液晶組成物、表示素子、光学素子、表示素子の製造方法、光学素子の製造方法 |
| JP2017523289A (ja) | 2014-07-28 | 2017-08-17 | メルク パテント ゲゼルシャフト ミット ベシュレンクテル ハフツングMerck Patent Gesellschaft mit beschraenkter Haftung | ホメオトロピック配向を有する液晶媒体 |
| WO2016114093A1 (ja) | 2015-01-14 | 2016-07-21 | Jnc株式会社 | 重合性基を有する化合物、液晶組成物および液晶表示素子 |
Non-Patent Citations (1)
| Title |
|---|
| Journal of the American Chemical Society,2005年,127(42),14922-14929 |
Also Published As
| Publication number | Publication date |
|---|---|
| EP2918658B1 (de) | 2020-05-13 |
| TW201536898A (zh) | 2015-10-01 |
| CN109825312A (zh) | 2019-05-31 |
| JP2021119159A (ja) | 2021-08-12 |
| TWI663249B (zh) | 2019-06-21 |
| JP2015168826A (ja) | 2015-09-28 |
| EP3730590A1 (de) | 2020-10-28 |
| US20150252265A1 (en) | 2015-09-10 |
| TWI695880B (zh) | 2020-06-11 |
| TW202106862A (zh) | 2021-02-16 |
| KR102417092B1 (ko) | 2022-07-05 |
| TW201942340A (zh) | 2019-11-01 |
| US20180057743A1 (en) | 2018-03-01 |
| TWI760748B (zh) | 2022-04-11 |
| CN105001879A (zh) | 2015-10-28 |
| CN109825312B (zh) | 2022-07-29 |
| KR20150105928A (ko) | 2015-09-18 |
| US9809748B2 (en) | 2017-11-07 |
| CN105001879B (zh) | 2019-04-09 |
| EP2918658A3 (de) | 2015-10-07 |
| US10513657B2 (en) | 2019-12-24 |
| EP2918658A2 (de) | 2015-09-16 |
| JP7331033B2 (ja) | 2023-08-22 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7331033B2 (ja) | ホメオトロピック配向を有する液晶媒体 | |
| JP6896614B2 (ja) | ホメオトロピック配向を有する液晶媒体 | |
| TWI557213B (zh) | 可聚合化合物及其於液晶顯示器內之用途 | |
| JP6510419B2 (ja) | 液晶ディスプレイ、およびホメオトロピック配列を有する液晶媒体 | |
| CN108026448B (zh) | 具有垂面配向的液晶介质 | |
| KR101939739B1 (ko) | 호메오트로픽 정렬을 갖는 액정 디스플레이 및 액정 매질 | |
| JP2019508511A (ja) | 液晶混合物および液晶ディスプレイ | |
| JP2018090569A (ja) | 液晶媒体のホメオトロピック配向のための化合物 | |
| JP5844357B2 (ja) | 重合性化合物および液晶ディスプレイにおけるそれらの使用 | |
| TWI532714B (zh) | 可聚合化合物及其於液晶顯示器之用途 | |
| JP2019112628A (ja) | ホメオトロピック配向を示す液晶媒体 | |
| JP2019505496A (ja) | ケイ皮酸誘導体 | |
| JP2019506630A (ja) | 液晶ディスプレイ装置および液晶混合物を作製する方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20180312 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20190515 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20190815 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20191009 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20200117 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20200409 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20200616 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20200716 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20201221 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20210421 |
|
| C60 | Trial request (containing other claim documents, opposition documents) |
Free format text: JAPANESE INTERMEDIATE CODE: C60 Effective date: 20210421 |
|
| C60 | Trial request (containing other claim documents, opposition documents) |
Free format text: JAPANESE INTERMEDIATE CODE: C60 Effective date: 20210421 |
|
| RD13 | Notification of appointment of power of sub attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7433 Effective date: 20210513 |
|
| C272 | Notice of ex officio correction |
Free format text: JAPANESE INTERMEDIATE CODE: C272 Effective date: 20210514 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20210521 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20210701 |
|
| C21 | Notice of transfer of a case for reconsideration by examiners before appeal proceedings |
Free format text: JAPANESE INTERMEDIATE CODE: C21 Effective date: 20210721 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20211012 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20211005 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20211109 |
|
| RD14 | Notification of resignation of power of sub attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7434 Effective date: 20211111 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7003349 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |