WO2003046020A1 - Polymere dienique conjugue, procede de fabrication et compositions elastomeres contenant ce polymere - Google Patents
Polymere dienique conjugue, procede de fabrication et compositions elastomeres contenant ce polymere Download PDFInfo
- Publication number
- WO2003046020A1 WO2003046020A1 PCT/JP2002/012390 JP0212390W WO03046020A1 WO 2003046020 A1 WO2003046020 A1 WO 2003046020A1 JP 0212390 W JP0212390 W JP 0212390W WO 03046020 A1 WO03046020 A1 WO 03046020A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- group
- compound
- carbon atoms
- conjugated
- based polymer
- Prior art date
Links
Classifications
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B60—VEHICLES IN GENERAL
- B60C—VEHICLE TYRES; TYRE INFLATION; TYRE CHANGING; CONNECTING VALVES TO INFLATABLE ELASTIC BODIES IN GENERAL; DEVICES OR ARRANGEMENTS RELATED TO TYRES
- B60C1/00—Tyres characterised by the chemical composition or the physical arrangement or mixture of the composition
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08C—TREATMENT OR CHEMICAL MODIFICATION OF RUBBERS
- C08C19/00—Chemical modification of rubber
- C08C19/30—Addition of a reagent which reacts with a hetero atom or a group containing hetero atoms of the macromolecule
- C08C19/34—Addition of a reagent which reacts with a hetero atom or a group containing hetero atoms of the macromolecule reacting with oxygen or oxygen-containing groups
- C08C19/38—Addition of a reagent which reacts with a hetero atom or a group containing hetero atoms of the macromolecule reacting with oxygen or oxygen-containing groups with hydroxy radicals
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08C—TREATMENT OR CHEMICAL MODIFICATION OF RUBBERS
- C08C19/00—Chemical modification of rubber
- C08C19/30—Addition of a reagent which reacts with a hetero atom or a group containing hetero atoms of the macromolecule
- C08C19/42—Addition of a reagent which reacts with a hetero atom or a group containing hetero atoms of the macromolecule reacting with metals or metal-containing groups
- C08C19/44—Addition of a reagent which reacts with a hetero atom or a group containing hetero atoms of the macromolecule reacting with metals or metal-containing groups of polymers containing metal atoms exclusively at one or both ends of the skeleton
Definitions
- the present invention relates to a conjugated gen-based polymer, a method for producing the conjugated polymer, and a rubber composition using the same. More specifically, a conjugated gen-based polymer having low hysteresis (low fuel consumption) and enhanced reinforcing properties with a filler, and suppressed gel formation, a method for producing the same, and a rubber composition using the same And pneumatic tires.
- the present invention suppresses the formation of a gel in the conventional method, and further enhances the low hysteresis loss property and reinforcing property when used in a rubber composition, and provides abrasion resistance and mechanical properties.
- the present inventors have conducted intensive studies in order to achieve the above object, and as a result, after reacting a polymer having an active terminal with a hydrocarbyloxysilane compound, and subsequently reacting a second compound with a specific compound It has been found that the reaction is useful. Undesirable gelation was also closely related to the change in catalyst residue due to the presence of water or oxygen during heat treatment such as desolvation, and it was also found that this modification technique can significantly improve the gelation.
- the present invention has been completed based on such findings.
- a method for producing a conjugated gen-based polymer characterized by performing a second modification (2) An active terminal which is obtained by polymerizing a gen-based monomer alone or together with another monomer and having a cis-1,4-bond content of at least 75 mol% in the conjugated gen part of the main chain.
- a method for producing a conjugated polymer which comprises reacting a hydrocarbyloxysilane compound with the active terminal of the conjugated polymer having the active terminal and then reacting with a carboxylic acid partial ester of a polyhydric alcohol.
- a rubber composition comprising a rubber component containing the modified conjugated gen-based polymer of (6) and a filler;
- a pneumatic tire wherein the rubber composition according to (7) is used as a constituent member of a tire.
- the terminal is further added to the terminal.
- the introduced hydrocarbyloxysilane compound residue is reacted with a specific compound.
- a method for producing a polymer having an active terminal having a cis-1,4 bond content of 75% or more is not particularly limited, and any of a solution polymerization method, a gas phase polymerization method, and a Balta polymerization method can be used, but the solution polymerization method is particularly preferable.
- the polymerization type may be either a batch type or a continuous type.
- conjugated diene compound as a polymerization monomer examples include 1,3-butadiene; isoprene; 1,3-pentadiene; 2,3-dimethylbutadiene; 2-phenyl-1,3-butadiene; 1,3-hexadiene; Is mentioned. These may be used alone or in combination of two or more. Among them, 1,3-butadiene is particularly preferred.
- the cis bond is 75. /.
- the method for producing the intermediate of the conjugated gen-based polymer is not particularly limited, and known methods can be used.
- Examples of the polymerization catalyst include the following (A), (B),
- ⁇ , ⁇ -diketonyl group those having a total of three ligands freely selected from the group consisting of or a Lewis base compound (in particular, free carboxylic acid, free alcohol, ⁇ -diketone, cyclic ether, Linear ether, trihydrocarbyl phosphine, trihydrocarbyl phosphite, etc.).
- neodymium tree 2-ethylhexanoate a complex compound thereof with acetyl aceton, neodymium trinedecanoate, a complex compound thereof with acetyl aceton, neodymium tri ⁇ -butoxide, and the like.
- ( ⁇ 2) A complex compound of a rare earth trihalide and a Lewis base.
- An example is the THF complex of neodymium trichloride.
- (A3) An organic rare earth compound having 3 oxidation atoms in which at least one (substituted) aryl group is directly bonded to a rare earth atom. For example, there is a salt of tetraaryl neodymium and lithium.
- A4 An organic rare earth compound having at least one (substituted) cyclopentagenenyl group bonded directly to a rare earth atom and having an oxidation number of 2 or 3, or this compound and a trialkylaluminum or a non-coordinating ayuon It is a reaction product with an ionizable compound composed of a cation.
- the rare earth element of the above rare earth compound is preferably lanthanum, neodymium, praseodymium, samarium, or potassium hydroxide, and more preferably lanthanum, neodymium, or samarium.
- a carboxylate of neodymium and a substituted cyclopentagenenyl compound of samarium are preferred.
- At least one kind of organoaluminum compound selected from one of the following can be used simultaneously.
- (B 1) a trihydrocarbyl aluminum compound represented by the formula R 12 3 A1 (where R 12 is a hydrocarbon group having 1 to 30 carbon atoms, which may be the same or different)
- (B 2) a hydrocarbyl aluminum hydride represented by the formula R 13 2 A 1 H or R 13 A 1 H 2 (where R 13 is a hydrocarbon group having 1 to 30 carbon atoms, and May also be different)
- (B3) A hydrocarbylaluminoxane compound having a hydrocarbon group having 1 to 30 carbon atoms.
- component (B) examples include trialkylaluminum, dialkylaluminum hydride, alkylaluminum dihydride, and alkylaluminoxane. These compounds may be used as a mixture. Among the components (B), a combination of an aluminoxane and another organic aluminum compound is preferred.
- (C1) A group II, III, or IV inorganic or organic compound having a hydrolyzable halogen or a complex compound thereof with a Lewis base.
- a Lewis base for example, alkyl aluminum dichloride, dialkyl aluminum chloride, silicon tetrachloride, tin tetrachloride, a complex of zinc chloride with a Lewis base such as alcohol, and a complex of magnesium chloride with a Lewis base such as alcohol.
- (C 2) An organic halide having a structure selected from at least one tertiary alkyl halide, benzyl halide, and aryl halide. Examples include benzyl chloride, t-butyl chloride, benzyl bromide, and t-butyl bromide.
- C 4 An ionizing compound comprising a non-coordinating anion and a counter cation.
- Trife-Norekanoreboemtetrakis (pentaf / leo-phenyl) borate is preferably used.
- Preparation of the above catalyst is carried out beforehand by using, in addition to the above components (A), (B) and (C), if necessary, the same conjugated and Z or non-conjugated gen monomers as the monomers for polymerization. You may.
- part or all of the component (A) or the component (C) may be supported on an inert solid, and in this case, it can be carried out by so-called gas phase polymerization.
- the amount of the catalyst to be used can be appropriately set, but the component (A) is usually 0.001 to 0.5 millimol per 100 grams of the monomer.
- the components (B) and (A) have a molar ratio of 5 to 1,000, and the components (C) / (A) have a molar ratio of 0.5 to: L0.
- Solvents used in the case of solution polymerization include organic solvents inert to the reaction, for example, hydrocarbon solvents such as aliphatic, alicyclic and aromatic hydrocarbon compounds. Specifically, those having 3 to 8 carbon atoms are preferable.
- Examples thereof include isobutene, trans-1-butene, cis-2-butene, 11-pentene, 21-pentene, 1-1hexene, 2-hexene, benzene, tonolen, xylene, and ethylbenzene. These can be used alone They may be used in combination of two or more.
- the temperature in this polymerization reaction is preferably selected in the range of 180 to 150 ° C, more preferably in the range of ⁇ 20 to 120 ° C.
- the polymerization reaction can be carried out under the pressure generated, but it is usually desirable to operate at a pressure sufficient to keep the monomer in a substantially liquid phase. That is, the pressure depends on the particular material to be polymerized, the polymerization medium used and the polymerization temperature, but higher pressures can be used if desired, and such pressures may be reacted with gases inert to the polymerization reaction. Obtained by an appropriate method such as pressurizing the vessel.
- all raw materials involved in the polymerization such as catalysts, solvents, and monomers, should be those from which reaction inhibitors such as water, oxygen, carbon dioxide, and protonic compounds have been substantially removed. desirable.
- the polymer used in the first modification reaction, is preferably one in which at least 10% of the polymer chains have a living property.
- the hydrocarbyloxysilane compound used for the reaction with the active terminal of the polymer is preferably a compound represented by the general formula (I)
- a 1 is (thio) epoxy, (thio) incinate, (theo) ketone, (thio) aldehyde, imine, amide, isocyanuric acid triester, (thio) carbonic acid hydrocarbyl ester, (Chio) metal salts of carboxylic acids, carboxylic acid anhydrides, the force carboxylic Sanhaguchi plasminogen halides and monovalent group having less without even one functional group selected from among carbonic acid dihydrazide de port force Rubiruesuteru, R 1 is A single bond or a divalent inert hydrocarbon group, R 2 and R 3 are each independently a monovalent aliphatic hydrocarbon group having 1 to 20 carbon atoms or a monovalent aromatic group having 6 to 18 carbon atoms.
- n is Ri integer der 0-2
- the plurality of oR 3 may be the same as or different from each other, also in the molecule active pro tons and Oniumu Salt is not included.
- imine ketimine, aldimine encompasses Amijin
- (Chio) carboxylic acid esters include unsaturated carboxylic acid esters such as Atari rate and methacrylates I do.
- examples of the metal of the metal salt of (thio) carboxylic acid include an alkali metal, an alkaline earth metal, A 1, Sn, and Zn.
- an alkylene group having 1 to 20 carbon atoms can be preferably exemplified.
- the alkylene group may be straight, branched, or cyclic, but is preferably a straight-chain alkylene group.
- Examples of the linear alkylene group include a methylene group, an ethylene group, a trimethylene group, a tetramethylene group, a pentamethylene group, a hexamethylene group, an otatamethylene group, a decamethylene group, and a dodecamethylene group.
- the alkyl group and the alkenyl group may be linear, branched or cyclic, and examples thereof include a methyl group, an ethyl group, an n-propyl group, an isopropyl group, and an n- Butyl group, isobutyl group, sec-butynol group, tert-butyl group, pentyl group, hexyl group, octyl group, decyl group, dodecyl group, cyclopentyl group, cyclohexyl group, butyl group, probenyl group, ⁇
- Examples include a linole group, a hexenyl group, an octenyl group, a cyclopentyl group and a cyclohexenyl group.
- the aryl group may have a substituent such as a lower alkyl group on the aromatic ring, and examples thereof include a phenyl group, a trinole group, a xylyl group, and a naphthyl group.
- the aralkyl group may have a substituent such as a lower alkyl group on the aromatic ring, and examples thereof include a benzyl group, a phenethyl group and a naphthylmethyl group.
- n is an integer of 0 to 2, preferably 0, and it is necessary that this molecule does not have an active proton or an ionic salt.
- hydrocarbyloxysilane compound represented by the general formula (I) examples include, for example, 2-thioepoxy group-containing hydrocarboxyloxysilane compound. Lisidoxyshethyltrimethoxysilane, 2-Dalicydoxyshethyltriethoxysilane, (2-glycidoxyshethyl) methyldimethoxysilane, 3-glycidoxypip-biltrimethoxysilane, 3-glycidoxypropyltriethoxysilane, (3— Glycidoxypropyl) methyldimethoxysilane, 2- (3,4-epoxycyclohexyl) ⁇ -ethyltrimethoxysilane, 2- (3,4-epoxycyclohexyl) ethyltriethoxysilane, 2- (3,4 _Epoxycyclohexyl) ethyl (methyl) dimethoxysilane and those in which the epoxy group in
- an imine group-containing hydrocarbyloxycyanide compound -(1,3-dimethylbutylidene) -13- (triethoxysilinole) -11-propanamine, ⁇ — (1-methylinoethylidene) 13- (Triethoxysilyl) 1-1-propanamine, diethylidene 3- (triethoxysilyl) 1-1-propanamine, ⁇ 1- (1-methylpropylidene) -3- (triethoxysilyl) -1-propanamine, ⁇ — (4—-, ⁇ -dimethylaminobenzylidene) 1-3- (triethoxysilyl) 1-1-propanamine, ⁇ — (cyclohexylidene) -13- (triethoxysilyl) -1-propanamine and their triethoxysilyl compounds Trimethoxysilyl compound, methyl ethoxysilyl compound, technolyl ethoxysilyl compound, Pre
- hydrocarbyloxy compounds there are 11- [3- (triethoxysilyl) propyl] -14,5-dihydroimidazole and 1- [3— (trimethoxysilinole) propyl] 14,5- Dihydromidazole, 3- [10- (triethoxysilyl) decyl] -14-oxazoline and the like can be mentioned.
- N- (3-triethoxysilylpropyl) -4,5-dihydroimidazole N- (3-isopropoxysilinolepropyl) -1,4,5-dihydromidazole, N- (3-methylethoxysilyl) Pentyl) -1,4,5-dihydroimidazole and the like, of which N- (3-triethoxysilylpropyl) _4,5-dihydroimidazole is preferred.
- carboxylic acid ester group-containing compounds examples include 3-methacryloyl mouth xip mouth pinoletriethoxysilane, 3-methacryloyloxypropyltrimethoxysilane, 3-methacryloyloxypropylmethyljetoxysilane, and 3-methacryloyloxypropyltrimethoxysilane.
- Isopropoxysilane and the like are preferable, and among them, preferred is 3-methacryloyl mouth xypropyltrimethoxysilane.
- isocyanate group-containing compounds 3-isocyanatopropyltrimethoxysilane, 3-isocyanatopropyltriethoxysilane, 3-isocyanatopropinolemethinoresethoxyethoxysilane, and 3-isocyanatopropyltriisopropoate Xysilane and the like are listed, and among them, 3-isocyanatopropyltriethoxysilane is preferable.
- the carboxylic acid anhydride-containing compound include 3-triethoxysilylpropyl succinic anhydride, 3-trimethoxysilylpropyl succinic anhydride, and 3-methylethoxysilylpropyl succinic anhydride. Among them, preferred is 3-triethoxysilylpropyl succinic anhydride.
- hydrocarbyloxysilane compounds may be used alone, or two or more thereof may be used in combination. Further, a partial condensate of the above hydrocarbyloxysilane compound can also be used.
- the terminal having a polymer having an active terminal and the hydrocarbyloxysilane compound react first, and the introduced residue is subsequently reacted with (1) a carboxylic acid partial ester of a polyhydric alcohol.
- Hydrocarbyl remaining or newly added in the presence of the condensation accelerator Any method of reacting with the compound is required. As the latter method (2), there are the following embodiments (2-1) to (2-3). That is,
- (2-2) a method comprising, after the first modification, adding a condensation accelerator to carry out a condensation reaction between the unreacted hydrocarbyloxysilane compound and the residue of the hydrocarbyloxysilane compound introduced at the terminal, as well as
- the carboxylic acid partial ester of a polyhydric alcohol is an ester of a polyhydric alcohol and carboxylic acid, and means a partial ester having at least one hydroxyl group.
- an ester of a saccharide having 4 or more carbon atoms or a modified saccharide and a fatty acid is preferably used.
- This ester is more preferably a partial ester of a fatty acid of a polyhydric alcohol, in particular, a partial ester of a saturated higher fatty acid or unsaturated higher fatty acid having 10 to 20 carbon atoms with a polyhydric alcohol (monoester, diester, Triesters may be used.), 2 Ester compounds in which one or three partial esters of a polyhydric carboxylic acid and a higher alcohol are bonded to one or more polyhydric alcohols.
- the polyhydric alcohol used as a raw material for the above partial ester is preferably a saccharide having at least three hydroxyl groups and having 5 or 6 carbon atoms (whether hydrogenated or non-hydrogenated), glycol And polyhydroxy compounds.
- the raw material fatty acid is preferably a saturated or unsaturated fatty acid having 10 to 20 carbon atoms, for example, stearic acid, lauric acid, and palmitic acid.
- sorbitan fatty acid esters are preferred, specifically, sorbitan monolaurate and sorbitan monono.
- examples include noremitic acid ester, sonolebitan monostearate, sonolebitan tristearate, sorbitan monooleate and sorbitan trioleate.
- SPAN 60 As a commercial product, SPAN 60 (Sorbitance SPAN 80 (sorbitan monooleate), SPAN 85 (sorbitan trioleate) and the like.
- the amount of the partial ester to be added is preferably from 0.2 to 10 mol, particularly preferably from 1 to 10 mol, per 1 mol of the hydrocarbyloxysilinole group added to the polymer.
- a 2 is annular tertiary Amin, acyclic tertiary Amin, pyridine, Surufui de, having at least one functional group selected from the Ma Ruchisurufi de and nitrile - valent group
- R 4 is a single A bond or a divalent inert hydrocarbon group
- R 5 and R 6 are each independently a monovalent aliphatic hydrocarbon group having 1 to 20 carbon atoms or a monovalent aromatic group having 6 to 18 carbon atoms.
- m is an integer of 0 to 2
- oR 6 there are multiple, oR 6 in multiple may be the same or different from each other, also in the molecule active pro tons and Oniumu salt Is not included.
- the hydrocarbyloxysilane compound represented by the general formula (I) and / or a partial condensate thereof are converted to the hydrocarbanoloxysilane compound represented by the general formula (I). It can be used in combination with a condensate.
- the partial condensate refers to a product in which a part (but not all) of SioR of a rubyroxysilane compound having a high oral strength is bonded by SioSi by condensation.
- hydrocarbyloxysilane compound represented by the general formula (II) and / or the partial condensate thereof does not substantially react directly with the active terminal and remains unreacted in the reaction system, It is consumed for condensation with the carboxyloxysilane compound residue introduced at the active end.
- the acyclic tertiary amine of A 2 contains N, N— (disubstituted) aromatic amine such as N, N— (disubstituted) aniline, Grade amines can include (thio) ethers as part of the ring.
- Divalent inactive hydrocarbon group among R 4, the R 5 and R 6 are put to each of the general formula (I) RR 2 and R 3 are explained. It is necessary that this molecule does not have active protons and osmite salts.
- hydrocarbyloxysilane compound represented by the general formula (II) examples include, for example, 3-dimethylaminopropyl (triethoxy) as an acyclic tertiary amine group-containing hydryloxysilane compound.
- Silane 3-dimethylaminopropyl (trimethoxy) silane, 3-dimethylaminopropyl (triethoxy) silane, 3-dimethylaminopropyl (trimethoxy) silane, 2-dimethylaminoethyl (triethoxy) silane ) Silane, 2-dimethylaminoethyl (trimethoxy) silane, 3-dimethylaminopropyl (ethoxy) methylsilane, 3-dibutylaminopropyl (triethoxy) silane, etc.
- Aminopropyl (triethoxy) silane and 3-dimethylaminobutyral pill (tri Butoxy) silane are preferred.
- cyclic tertiary amine group-containing hydrocarbyloxy silane compounds include 3_ (11-hexamethyleneimino) propyl (triethoxy) silane and 31- (11-hexamethyleneimino) propyl (trimethoxy) silane.
- Silane (1-hexamethyleneimino) methyl (trimethoxy) silane, (1 -hexamethyleneimino) methyl (triethoxy) silane, 2- (1 -hexamethyleneimino) ethyl (triethoxy) silane, 2 -(1 -hexamethyleneimino) ethyl (trimethoxy) silane, 3- (1-pyrrolidinyl) propyl (triethoxy) silane, 3- (1-pyrrolidinyl) propyl (trimethoxy) silane, 3- (1 -1 Heptamethyleneimino) Pup pill (triethoxy) silane, 3— (11-dodecamethyleneimino) propyl (triethoxy)
- Preferable examples include silane, 3- (1-hexamethyleneimino) propyl (jetoxy) methylsilane and 3- (1-hexamethyleneimino) propyl (jetoxy) ethylinolesilane.
- hydrocarbyloxysilane compounds 2- (trimethoxysilylethyl) pyridine, 2- (triethoxysilylethyl) pyridine, 4-ethylethylpyridine and the like can be mentioned.
- hydrocarbyloxysilane compounds may be used alone. Two or more kinds may be used in combination. Further, partial condensates of these hydrocarbyloxysilane compounds can also be used.
- the hydrocarbyloxysilane compound II to be condensed with the residue of the above-mentioned hydroforce rubyoxysilane compound I introduced at the active terminal of the polymer includes: A hydrocarbyloxysilane compound represented by the general formula (I) and a partial condensate thereof; a hydrocarbyloxysilane compound represented by the general formula (II) and a partial condensate thereof; and a general formula (III)
- a 3 is an alcohol, thiol, primary amine or its salt, a cyclic secondary amine or its salt, an acyclic secondary amine or its salt, or a cyclic tertiary amine salt
- R 8 and R 9 are each independently a monovalent aliphatic hydrocarbon group having 1 to 20 carbon atoms or a monovalent aromatic hydrocarbon having 6 to 18 carbon atoms.
- OR 9 represents a group
- q is an integer of 0 to 2
- the OR 9 there are a plurality the plurality of OR 9 may be the same with or different from each other.
- At least one compound selected from the group consisting of the hydrodynamic noreviroxysilane compound and partial condensates thereof can be used.
- the primary amine in A 3 includes an aromatic amine such as adiline
- the non-cyclic secondary amine is an N-(— substituted) such as N- (monosubstituted) aniline.
- aromatic amines include aromatic amines.
- the acyclic tertiary amine amine salt includes the N, N- (disubstituted) aromatic amine amine salt such as N, N- (disubstituted) aniline.
- (thio) ether can be included as a part of the ring.
- Divalent inactive hydrocarbon group out of R 7, the R s ⁇ beauty R 9 is as respectively described RR 2 and R 3 in formula (I).
- Examples of the hydrocarbyloxysilane compound represented by the general formula (III) include 3-aminopropyltrimethoxysilane, 3-aminopropyltriethoxysilane, hydroxymethyltrimethoxysilane, and hydroxymethyltrimethoxysilane.
- hydrocarbyloxysilane compound II one type may be used alone, or two or more types may be used in combination.
- a polymer having an active terminal is firstly reacted with a reaction system. Reacts with a substantially stoichiometric amount of the hydryloxysilane I added to the compound to introduce a hydrocarbyloxysilyl group into substantially all of its termini (primary modification).
- the condensation reaction between alkoxysilyl groups in the above method (2) is
- the free alkoxysilane residual or newly added
- the alkoxysilyl group at the polymer end and in some cases, preferably between the alkoxysilyl groups at the polymer end.
- This reaction is unnecessary. Therefore, when adding a new alkoxysilane compound, It is preferable from the viewpoint of efficiency that the hydrolyzability of the oxysilyl group does not exceed the hydrolyzability of the alkoxysilyl group at the terminal of the polymer.
- alkoxysilane I uses a highly hydrolyzable compound containing a trimethoxysilyl group
- newly added alkoxysilane II contains an alkoxysilyl group (for example, a triethoxysilyl group) that is less hydrolyzable. Combinations using compounds are preferred.
- the alkoxysilane I contains a triethoxysilyl group and the II contains a trimethoxysilyl group, but it is not preferable from the viewpoint of reaction efficiency.
- any of a solution reaction and a solid phase reaction can be used, but a solution reaction (a solution containing an unreacted monomer used at the time of polymerization may be used) is preferable.
- the type of the denaturation reaction is not particularly limited, and may be carried out using a batch type reactor or may be carried out continuously using an apparatus such as a multi-stage continuous reactor and a line mixer. In addition, it is important that the denaturation reaction is carried out after completion of the polymerization reaction and before performing desolvation treatment, water treatment, heat treatment, various operations necessary for polymer isolation, and the like.
- the polymerization temperature of the conjugated gen-based polymer can be used as it is. Specifically, the preferable range is 20 to 100 ° C. If the temperature is low, the viscosity of the polymer tends to increase, and if the temperature is high, the polymerization active terminal tends to be deactivated, which is not preferable.
- condensation accelerator a combination of a metal compound, which is generally known as a curing catalyst for alkoxy condensation-curable room temperature crosslinking (RTV) silicone, and water can be used.
- a combination of tin carboxylate and / or titanium alkoxide with water can be preferably mentioned.
- a solution of an organic solvent compatible with water, such as alcohol, may be used, or water may be directly injected, dispersed, and dissolved in a hydrocarbon solution using various chemical engineering techniques.
- Such a condensation accelerator may be at least one selected from the group consisting of metal compounds represented by the following (1) to (3) and water. preferable.
- R 11 is an aliphatic hydrocarbon group having 1 to 30 carbon atoms
- B 1 is a hydroxyl group or a halogen.
- a 4 is: (1) a carboxyl group having 2 to 30 carbon atoms; (2) an ⁇ , ⁇ -dionyl group having 5 to 30 carbon atoms; (3) a hydrocarbyloxy group having 3 to 30 carbon atoms; a human Dorokarubiru group and / or a group selected from human mud total trisubstituted by ribs Ruo alkoxy group (which may be the same or different) has been shea port alkoxy group of a carbon number of 1 to 20, Alpha 4 there are a plurality of In this case, they may be the same or different. ]
- Titanium compound with oxidation number 4 that satisfies the following general formula
- X is an integer of 2 or 4.
- a 5 represents, 1 alkoxy group having 3 to 30 carbon atoms, a 2 Total trisubstituted siloxy group by an alkoxy group the alkyl group and / or 1 to 20 carbon atoms having 1 to 30 carbon atoms, A 5 is more In this case, they may be the same or different.
- B 2 is an ⁇ , ⁇ -dionyl group having 5 to 30 carbon atoms.
- tin carboxylate examples include (1) a divalent tin dicarboxylate (particularly preferably a carboxylate having 8 to 20 carbon atoms), and (2) a tetravalent dihydroforce.
- Rubiltin dicarboxylate including bis (hydrodynamic norevir dicarponic acid) salt), bis (a, ⁇ -diketonate), alkoxy halide, monocarboxylate hydroxide, alkoxy (trihydrocarbyl) (Siloxide), alkoxy (dihydronorolevir alkoxysiloxide), bis (trihydrocanolevirsilsiloxide), bis (dihydrocarbylalkoxysiloxide) and the like can be preferably used.
- the hydrocarbyl group directly bonded to tin preferably has 4 or more carbon atoms. 8 are particularly preferred.
- titanium compound examples include tetraalkoxides of titanium having an oxidation number of 4, dialkoxybis (g, ⁇ -diketonate), tetrakis (trihydrocarboxysiloxide), and the like. Particularly, tetraalkoxides are suitably used.
- the water is preferably used in the form of a simple substance, a solution of alcohol or the like, or micelles dispersed in a hydrocarbon solvent, and, if necessary, in the reaction system such as water adsorbed on a solid surface or hydrated water of a hydrate. In some cases, water that can potentially release water can be effectively used.
- condensation accelerator may be charged separately to the reaction system or mixed immediately before use and charged as a mixture, but long-term storage of the mixture is not preferable because it causes decomposition of the metal compound. .
- the mole ratio of the metal of the metal compound and the water effective for the reaction and the mole ratio to the total amount of the hydrocarbyloxysilyl groups present in the reaction system are both 0.1 or more. Is preferred. The upper limit varies depending on the purpose and reaction conditions, but there is effective water with a molar ratio of about 0.5-3 to the total amount of hydrocarbyloxysilyl groups bonded to the polymer terminals before the condensation treatment. Is preferred. Although the molar ratio of the metal of the metal compound and the water effective for the reaction varies depending on the required reaction conditions, it is preferably about 0.5 to 1/20.
- a condensation accelerator is added and reacted, and then further reacted with the carboxylic acid ester compound of the polyhydric alcohol. You can also.
- a known antioxidant or a short stop agent is added, if desired, in a step after the introduction of the hydrocarbyloxysilane compound residue to the active terminal of the polymer. be able to.
- the modified polymer preferably has a Mooney viscosity (ML 1 +4 , 100 ° C.) of 10 to 150, more preferably 15 to 70. If the Mooney viscosity is low, rubber properties such as fracture characteristics tend to decrease, and if it is high, workability is poor and it is difficult to knead with the compounding agent.
- Mooney viscosity ML 1 +4 , 100 ° C.
- the present invention also provides the modified polymer thus obtained.
- the modified polymer of the present invention is used as a rubber component in a rubber composition containing an inorganic compound such as silica or carbon black as a filler, regardless of the type, the interaction with the filler is enhanced, and the destructive properties and Abrasion resistance and low heat generation can be simultaneously improved, and good workability can be exhibited.
- an inorganic compound such as silica or carbon black
- the rubber composition of the present invention preferably contains at least 30% by weight of the modified polymer as a rubber component. If the amount is less than 30% by weight, it is difficult to obtain a rubber composition having desired physical properties, and the object of the present invention may not be achieved.
- the more preferred content of the modified polymer in the rubber component is 35% by weight or more, and particularly preferably 40 to 100% by weight.
- This modified polymer may be used alone or in combination of two or more.
- rubber components used in combination with the modified polymer include natural rubber and gen-based synthetic rubber.
- gen-based synthetic rubber include styrene-butadiene copolymer (SBR), polybutadiene (BR), Examples include polyisoprene (IR), butyl rubber (IIR), ethylene-propylene copolymer, and mixtures thereof.
- SBR styrene-butadiene copolymer
- BR polybutadiene
- IR polyisoprene
- IIR butyl rubber
- ethylene-propylene copolymer and mixtures thereof.
- a part thereof may have a branched structure by using a polyfunctional type, for example, a modifier such as tin tetrachloride or silicon tetrachloride.
- the rubber composition of the present invention preferably contains a filler.
- a filler any filler that can be used for general rubber compositions can be used.
- Specific examples include carbon black and inorganic fillers. Among them, carbon black, silica, and alumina are preferred. There is no particular limitation on the carbon black.
- SRF, GPF, FEF, HAF, ISAF, SAF, etc. are used.
- the iodine adsorption (IA) is 60 mg / g or more
- the dibutyl phthalate oil absorption (DBP) is 80 m.
- l / l Force of 00 g or more Monobon black is preferred. Grip performance by using carbon black HAF, ISAF, and SAF, which are excellent in wear resistance, are particularly preferable, although the effect of improving the performance and fracture resistance is increased.
- the silica is not particularly limited, and examples thereof include wet silicic acid (hydrous silicate), dry silicic acid (silicic anhydride), calcium silicate, aluminum silicate and the like.
- wet silica which has the most remarkable effect of achieving both todalip properties and low rolling resistance, is preferred.
- aluminas those represented by the following general formula (IV) are preferable. .
- M is at least one selected from the group consisting of metals selected from the group consisting of aluminum, magnesium, titanium, and calcium, oxides or hydroxides of these metals, and hydrates thereof.
- X, y, and z are each an integer of 1 to 5, an integer of 0 to 10, an integer of 2 to 5, and an integer of 0 to: L0.
- it may contain metals such as potassium, sodium, iron and magnesium, and elements such as fluorine.
- inorganic filler silica, alumina monohydrate ( ⁇ 1 2 0 3 ⁇ ⁇ 2 0), Gibusai bets, aluminum hydroxide, etc.
- Baiyarai preparative [A 1 (OH) 3] water magnesium oxide [Mg (OH) 2], magnesium oxide (MgO), talc (3 Mg O ⁇ 4 S i 0 2 ⁇ H 2 ⁇ ), Ataparujai bets (5Mg O - 8 S I_ ⁇ 2 - 9 H 2 0) , Titanium White (T i 0 2 ), Titanium Black (T i 0 2n —, Calcium Oxide (C a 0), Calcium Hydroxide [C a (OH) 2 ], Aluminum Oxide Magnesium (Mg 0 A 1 2 ⁇ 3), click rate (A l 2 ⁇ 3 '23 1_Rei 2), Kaorin (eight 1 2 0 3 ⁇ 2 S i 0 2 ⁇ 2 H 2 ⁇ ), Nono
- the inorganic filler preferably has a particle size of 10 ⁇ m or less, more preferably 3 ⁇ m or less. By setting the particle size of the inorganic filler to 10 zm or less, it is possible to maintain good fracture resistance and wear resistance of the vulcanized rubber composition.
- one kind of the inorganic filler may be used alone, or two or more kinds thereof may be used in combination.
- the filler is added in an amount of 10 to 250 parts by weight with respect to 100 parts by weight of the rubber component. 0 parts by weight is preferred. If the amount is small, the effect of improving the resistance to crushing and the like is not sufficient, and if it is large, the processability of the rubber composition tends to be poor.
- the rubber composition of the present invention contains the modified polymer obtained by the above method, and usually contains a rubber component containing at least 30% by weight of the modified polymer, and silica per 100 parts by weight of silica. And a composition containing 100 parts by weight of Z or carbon black. .
- silane capprig agent when silica is used as a reinforcing filler, a silane capprig agent can be blended for the purpose of further improving the reinforcing property.
- silane coupling agent include bis (3-triethoxysilylpropyl) tetrasulfide, bis (3_triethoxysilylpropyl) trisulfide, and bis (3-triethoxysilylpropynole) disulfide.
- Bis (3-triethoxysilylpropyl) polysulfide and 3-trimethoxysilylpropyl benzothiazyl tetrasulfide are preferred from the viewpoint of the reinforcing effect.
- One of these silane coupling agents may be used alone, or two or more thereof may be used in combination.
- a modified polymer having a functional group having a high affinity for silica introduced at the molecular terminal is used as a rubber component. It can be further reduced.
- the preferred amount of the silane coupling agent varies depending on the type of the silane coupling agent and the like, but is usually selected in the range of 1 to 20% by weight based on the silylation force. If the amount is too small, the effect as a coupling agent is not sufficiently exerted, and if it is too large, gelation of rubber balls may be caused.
- the amount of the silane coupling agent is preferably in the range of 5 to 15% by weight from the viewpoint of the effect as a coupling agent and prevention of gelation.
- the rubber composition of the present invention may contain, if desired, various chemicals usually used in the rubber industry, such as vulcanizing agents, vulcanization accelerators, process oils, antioxidants, as long as the object of the present invention is not impaired.
- vulcanizing agents such as vulcanizing agents, vulcanization accelerators, process oils, antioxidants, as long as the object of the present invention is not impaired.
- Can contain scorch inhibitor, zinc white, stearic acid, etc.
- the rubber composition of the present invention can be obtained by kneading using a kneading machine such as an open kneading machine such as a roll or a closed kneading machine such as a Banbury mixer, and vulcanization after shaping. It is applicable to various rubber products. For example, it can be used for tire applications such as tire treads, undertreads, carcass, side walls, beads, etc., as well as applications for anti-vibration rubber, fenders, belts, hoses and other industrial products. It is suitably used as a tire tread rubber.
- the pneumatic tire of the present invention using the above rubber composition, it is possible to obtain a performance excellent in durability by improving the reinforcing property with the filler while ensuring low fuel consumption.
- the gas to be filled in the tire include air and an inert gas such as nitrogen.
- the physical properties of the polymer were measured according to the following methods.
- the microstructure of the butadiene portion of the polymer was determined by an infrared method (Morello method).
- the Mooney viscosity of the polymer was measured at 100 ° C using an RLM-01 tester manufactured by Toyo Seiki Seisaku-sho.
- a 0.2 w / v% solution of the polymer was prepared using tetrahydrofuran as a solvent, and after 24 hours without stirring at room temperature, the presence or absence of the polymer was visually determined.
- Mooney viscosity [ML 1 + 4 130 ° C] was measured at 130 ° C in accordance with JISK 6300-1994.
- ta ⁇ 50 ° C was measured at a temperature of 50 ° C, a strain of 5%, and a frequency of 15 Hz. The smaller the value of t a ⁇ ⁇ (50.C), the lower the heat generation.
- the wear resistance of the control was defined as 100, and the wear resistance index was indicated as an index. The higher the index, the better.
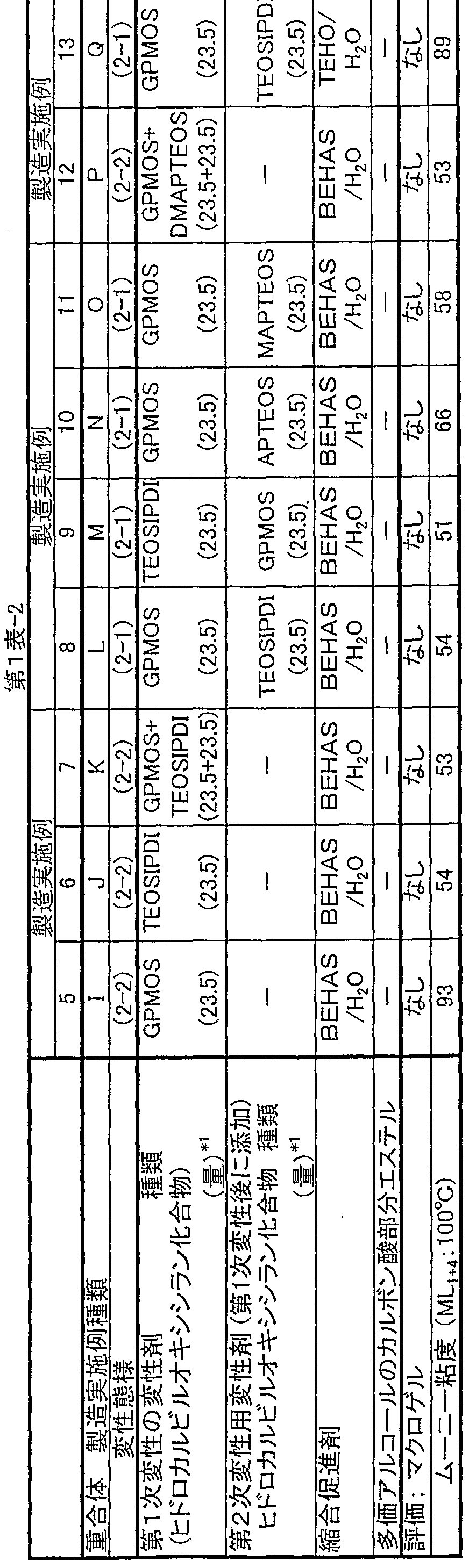
- a hexane compound of the type shown in Table 1 was added as a hexane solution (1.0 M) in an amount shown in the same table and treated at 50 ° C. for 60 minutes.
- a hexane solution (1.0 M) of a silane compound of the type shown in Table 1 was charged in the amount shown in the table, and treated at 50 ° C for 60 minutes to obtain a first-order modifier. The following denaturation reaction was performed.
- a hexane compound of the type shown in Table 1 as a hexane solution (1.0 M) is charged in the amount shown in the same table, and treated at 50 ° C for 30 minutes to form the first stage. The reaction was performed.
- a hexane compound (secondary modifier) of the type shown in Table 1 was added as a hexane solution (1.0 M), and the amount shown in the same table was added.
- a condensation promoter 1.76 ml (equivalent to 70.5 eq / Nd) of bis (2-ethylhexanoate) tin solution in cyclohexane (1.05 M / equivalent) and 32 ul (70 55eq / Nd) and treated in a 50 ° C warm water bath for 1.0 hour. Thereafter, O was obtained from the polymer L in the same manner as in Production Example 1.
- the resulting polymerization Table 1 shows the body analysis values.
- a polymer was produced in the same manner as in Production Example 8 except that titanium tetrakis (2-ethylhexyloxide) was used in place of bis (2-ethylhexanoate) tin as a condensation accelerator in Production Example 8. Got Q.
- the analytical values of the obtained polymer are shown in Table 1.
- the charge amount of the catalyst solution was set to 1.83 m 1, and after the polymerization of the polymer intermediate, the first and second modification treatments were not performed.
- Polymer A was obtained in the same manner as in Production Example 1 except that the reaction was stopped by adding 2 ml of a 5% solution of isopropanol in 5).
- the microstructure of the obtained polymer was as follows: cis-bond amount 95.5%, trans-bond amount 3.9%, and Bull-bond amount 0.6%. Table 1 shows other analysis values of the obtained polymer.
- Polymers B to D were obtained in the same manner as in Production Example 1, except that only the first modification treatment was performed, and the second modification treatment was not performed.
- the analytical values of the obtained polymer are shown in Table 1.
- Coupling agent Degussa silane coupling agent, trademark: Si69
- the Mooney viscosity (i 3 o ° c) ⁇ was measured and found to be 160. (: Vulcanized under the conditions of 15 minutes, and evaluated the low heat build-up and fracture properties (tensile strength) 'wear resistance of the vulcanized rubber. Table 3 shows the results.
- Example 5 Example 6 Example 7 Example 8 Example 9 Example 10 Example 11 Example 12 Example 13 Polymer IJK MN0PQ Formulation 1 (silica compound rubber composition)
- Viscosity (ML 1 + 4: 130 ° C) 104 77 86 88 81 94 91 88 97
- Tensile strength Tb (MPa) 19.5 19.6 18.4 19.6 18.6 20.1 19.6 19.7 19.0
- Low heat generation tan (10%, 50C) 0.079 0.092 0.073 0.071 0.082 0.070 0.072 0.085 0.088
- Formulation 2 Carbon black compounded rubber composition
- the problem of macrogel formation which arises in the polymer finishing process such as desolvation and drying is solved, the excessive increase in Mooney viscosity of the polymer is suppressed, and the unvulcanized rubber of the rubber compound is removed. Can be greatly improved.
- the rubber composition containing silica and the composition containing carbon black the silicic acid and the interaction with carbon black are enhanced, and the vulcanized rubber composition has a crushing property, abrasion resistance and low heat generation. Since the properties can be simultaneously improved, it can be applied particularly to a rubber composition for tires. Further, the cold flow resistance of the gen-based copolymer can be improved.
Description
Claims
Priority Applications (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP02783661A EP1449857B1 (en) | 2001-11-27 | 2002-11-27 | Conjugated diene polymer, process for its production and rubber compositions containing the same |
| DE60237986T DE60237986D1 (de) | 2001-11-27 | 2002-11-27 | Polymer auf basis von konjugierten dienen, herstellungsverfahren dafür und dieses enthaltende kautschukzusammensetzungen |
| US10/496,983 US7781533B2 (en) | 2001-11-27 | 2002-11-27 | Conjugated diene polymer, process for its production and rubber compositions containing the same |
| JP2003547468A JP4117250B2 (ja) | 2001-11-27 | 2002-11-27 | 共役ジエン系重合体、その製法及びそれを用いたゴム組成物 |
| US12/829,889 US8642705B2 (en) | 2001-11-27 | 2010-07-02 | Conjugated diene polymer, process for its production and rubber compositions containing the same |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2001-361354 | 2001-11-27 | ||
| JP2001361354 | 2001-11-27 |
Related Child Applications (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| US10496983 A-371-Of-International | 2002-11-27 | ||
| US12/829,889 Division US8642705B2 (en) | 2001-11-27 | 2010-07-02 | Conjugated diene polymer, process for its production and rubber compositions containing the same |
| US12/829,889 Continuation US8642705B2 (en) | 2001-11-27 | 2010-07-02 | Conjugated diene polymer, process for its production and rubber compositions containing the same |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2003046020A1 true WO2003046020A1 (fr) | 2003-06-05 |
Family
ID=19172032
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2002/012390 WO2003046020A1 (fr) | 2001-11-27 | 2002-11-27 | Polymere dienique conjugue, procede de fabrication et compositions elastomeres contenant ce polymere |
Country Status (7)
| Country | Link |
|---|---|
| US (2) | US7781533B2 (ja) |
| EP (1) | EP1449857B1 (ja) |
| JP (1) | JP4117250B2 (ja) |
| CN (1) | CN100334118C (ja) |
| DE (1) | DE60237986D1 (ja) |
| ES (1) | ES2351302T3 (ja) |
| WO (1) | WO2003046020A1 (ja) |
Cited By (59)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP1479698A1 (en) * | 2003-05-22 | 2004-11-24 | JSR Corporation | Method for producing modified conjugated diene polymer and rubber composition |
| WO2004111094A1 (en) * | 2003-06-09 | 2004-12-23 | Bridgestone Corporation | Improved hysteresis elastomeric compositions comprising sequentially terminated polymers |
| JP2005008870A (ja) * | 2003-05-22 | 2005-01-13 | Jsr Corp | 変性共役ジエン系重合体の製造方法およびゴム組成物 |
| JP2005232364A (ja) * | 2004-02-20 | 2005-09-02 | Bridgestone Corp | 変性共役ジエン系重合体、並びにそれを用いたゴム組成物及びタイヤ |
| JP2005232367A (ja) * | 2004-02-20 | 2005-09-02 | Bridgestone Corp | 変性共役ジエン系重合体、並びにそれを用いたゴム組成物及びタイヤ |
| JP2006249189A (ja) * | 2005-03-09 | 2006-09-21 | Bridgestone Corp | 変性重合体及びそれを用いたゴム組成物及びタイヤ |
| WO2006101025A1 (ja) * | 2005-03-18 | 2006-09-28 | Jsr Corporation | 変性重合体の製造方法、その方法によって得られた変性重合体とそのゴム組成物 |
| JP2007505208A (ja) * | 2003-06-09 | 2007-03-08 | 株式会社ブリヂストン | イソシアナートアルコキシシランを用いて停止させた重合体を含む改良されたヒステリシスのエラストマー組成物 |
| WO2007040252A1 (ja) | 2005-10-05 | 2007-04-12 | Jsr Corporation | 変性共役ジエン系重合体の製造方法、その方法によって得られた変性共役ジエン系重合体とそのゴム組成物 |
| WO2007083765A1 (ja) * | 2006-01-20 | 2007-07-26 | Bridgestone Corporation | 変性ポリブタジエンゴム配合ゴム組成物及びタイヤ |
| JP2007308653A (ja) * | 2006-05-22 | 2007-11-29 | Bridgestone Corp | タイヤトレッド用ゴム組成物及びそれを用いた空気入りタイヤ |
| JP2007326990A (ja) * | 2006-06-09 | 2007-12-20 | Bridgestone Corp | ゴム組成物及びそれを用いたタイヤ |
| JP2007326942A (ja) * | 2006-06-07 | 2007-12-20 | Bridgestone Corp | 空気入りタイヤ |
| WO2008004676A1 (fr) | 2006-07-06 | 2008-01-10 | Bridgestone Corporation | Composition de caoutchouc et bandage pneumatique fabriqué à partir de celle-ci |
| WO2008004675A1 (fr) | 2006-07-06 | 2008-01-10 | Bridgestone Corporation | Composition de caoutchouc et bandage pneumatique fabriqué à partir de celle-ci |
| WO2008050845A1 (fr) * | 2006-10-25 | 2008-05-02 | Bridgestone Corporation | Procédé de production de polymères diènes conjugués modifiés, polymères diènes conjugués modifiés produits par ce procédé, compositions de caoutchouc et pneus |
| WO2008050851A1 (fr) * | 2006-10-25 | 2008-05-02 | Jsr Corporation | Procédé de production d'un polymère modifié, polymère modifié obtenu par ce procédé et composition de caoutchouc contenant celui-ci |
| WO2008078813A1 (ja) | 2006-12-27 | 2008-07-03 | Jsr Corporation | 変性共役ジエン系重合体の製造方法、変性共役ジエン系重合体、及びゴム組成物 |
| WO2008084724A1 (ja) | 2006-12-27 | 2008-07-17 | Jsr Corporation | 変性共役ジエン系重合体の製造方法、変性共役ジエン系重合体、及びゴム組成物 |
| JP2008163338A (ja) * | 2006-12-28 | 2008-07-17 | Bridgestone Corp | 高シス−1,4−結合量と高い官能性とを有する変性シス−1,4−ポリジエンの製造方法 |
| JP2008195923A (ja) * | 2006-12-28 | 2008-08-28 | Bridgestone Corp | 含アミンアルコキシシリル官能化ポリマー |
| WO2009022665A1 (ja) * | 2007-08-10 | 2009-02-19 | Bridgestone Corporation | 空気入りタイヤ |
| JP2009120758A (ja) * | 2007-11-16 | 2009-06-04 | Jsr Corp | 変性共役ジエン系重合体の製造方法、変性共役ジエン系重合体、及びゴム組成物 |
| JP2009120757A (ja) * | 2007-11-16 | 2009-06-04 | Jsr Corp | 変性共役ジエン系重合体の製造方法、変性共役ジエン系重合体、及びゴム組成物 |
| JP2009173838A (ja) * | 2008-01-28 | 2009-08-06 | Bridgestone Corp | ゴム組成物及びそれを用いた空気入りタイヤ |
| DE102008007713A1 (de) | 2008-02-04 | 2009-08-06 | Byk-Chemie Gmbh | Netz- und Dispergiermittel |
| JP2009242788A (ja) * | 2008-03-10 | 2009-10-22 | Bridgestone Corp | ゴム組成物及びそれを用いたタイヤ |
| WO2009133936A1 (ja) * | 2008-04-30 | 2009-11-05 | 株式会社ブリヂストン | 変性重合体を含有するゴム組成物を使用したタイヤ |
| JP2009287018A (ja) * | 2008-04-28 | 2009-12-10 | Bridgestone Corp | 変性低分子量共役ジエン系重合体 |
| JP2010530464A (ja) * | 2007-06-18 | 2010-09-09 | 株式会社ブリヂストン | アミノ基を含有するハロシラン類で官能基化された重合体 |
| WO2010104149A1 (ja) | 2009-03-11 | 2010-09-16 | Jsr株式会社 | ゴム組成物及び空気入りタイヤ |
| JP2010536945A (ja) * | 2007-08-16 | 2010-12-02 | ランクセス・ドイチュランド・ゲーエムベーハー | 共役ジエンをベースとするナノ構造化ポリマー |
| WO2010150827A1 (ja) | 2009-06-24 | 2010-12-29 | 株式会社ブリヂストン | ポリマー組成物、ゴム組成物及びそれを用いたタイヤ |
| JP2011522928A (ja) * | 2008-06-06 | 2011-08-04 | スティロン ヨーロッパ ゲゼルシャフト ミット ベシュレンクテル ハフツング | 変性エラストマーポリマー |
| US8022159B2 (en) | 2008-11-24 | 2011-09-20 | The Goodyear Tire & Rubber Company | Terminating compounds, polymers, and their uses in rubber compositions and tires |
| JP2012031314A (ja) * | 2010-07-30 | 2012-02-16 | Bridgestone Corp | メタロセン系複合触媒、触媒組成物及び共重合体の製造方法 |
| WO2012073880A1 (ja) * | 2010-12-01 | 2012-06-07 | Jsr株式会社 | 変性共役ジエン系ゴムの製造方法、変性共役ジエン系ゴム、及びゴム組成物 |
| US8476374B2 (en) | 2006-04-05 | 2013-07-02 | Bridgestone Corporation | Activated silane compound, rubber composition using the same and tire |
| JP2014098162A (ja) * | 2008-03-10 | 2014-05-29 | Bridgestone Corp | 変性共役ジエン(共)重合体の製造方法、変性共役ジエン(共)重合体、並びにそれを用いたゴム組成物及びタイヤ |
| US8754159B2 (en) | 2009-07-22 | 2014-06-17 | Bridgestone Corporation | Tire |
| WO2017126629A1 (ja) | 2016-01-19 | 2017-07-27 | 株式会社ブリヂストン | ゴム組成物及びタイヤ |
| KR20170142492A (ko) * | 2016-06-17 | 2017-12-28 | 주식회사 엘지화학 | 변성 공액디엔계 중합체의 제조방법 및 이를 이용하여 제조된 변성 공액디엔계 중합체 |
| EP3301131A1 (en) | 2016-09-30 | 2018-04-04 | Sumitomo Rubber Industries, Ltd. | Cap tread rubber composition for cold weather tires |
| EP3392058A1 (en) | 2017-04-13 | 2018-10-24 | Sumitomo Rubber Industries, Ltd. | Cap tread rubber composition for cold weather tires |
| WO2019116804A1 (ja) | 2017-12-15 | 2019-06-20 | 株式会社ブリヂストン | ゴム組成物及び空気入りタイヤ |
| WO2019123749A1 (ja) | 2017-12-20 | 2019-06-27 | 株式会社ブリヂストン | ゴム組成物 |
| WO2021124637A1 (ja) | 2019-12-19 | 2021-06-24 | 株式会社ブリヂストン | タイヤ |
| WO2021124640A1 (ja) | 2019-12-19 | 2021-06-24 | 株式会社ブリヂストン | タイヤ |
| KR20210125427A (ko) | 2020-04-08 | 2021-10-18 | 아사히 가세이 가부시키가이샤 | 공액 디엔계 중합체 및 그의 제조 방법, 그리고 고무 조성물 |
| JP2022520984A (ja) * | 2019-09-30 | 2022-04-04 | エルジー・ケム・リミテッド | 変性共役ジエン系重合体、その製造方法、およびそれを含むゴム組成物 |
| WO2022124147A1 (ja) | 2020-12-09 | 2022-06-16 | 株式会社ブリヂストン | ゴム組成物、ゴム組成物の製造方法及びタイヤ |
| JP2022544242A (ja) * | 2019-09-19 | 2022-10-17 | エルジー・ケム・リミテッド | 変性共役ジエン系重合体の製造方法 |
| WO2022249637A1 (ja) | 2021-05-28 | 2022-12-01 | 株式会社ブリヂストン | タイヤ用ゴム組成物、トレッドゴム及びタイヤ |
| WO2022249764A1 (ja) | 2021-05-28 | 2022-12-01 | 株式会社ブリヂストン | タイヤ用ゴム組成物、トレッドゴム及びタイヤ |
| WO2022249765A1 (ja) | 2021-05-28 | 2022-12-01 | 株式会社ブリヂストン | タイヤ用ゴム組成物、トレッドゴム及びタイヤ |
| WO2022249763A1 (ja) | 2021-05-28 | 2022-12-01 | 株式会社ブリヂストン | タイヤ用ゴム組成物、トレッドゴム及びタイヤ |
| WO2022249636A1 (ja) | 2021-05-28 | 2022-12-01 | 株式会社ブリヂストン | タイヤ用ゴム組成物、トレッドゴム及びタイヤ |
| WO2022249767A1 (ja) | 2021-05-28 | 2022-12-01 | 株式会社ブリヂストン | タイヤ用ゴム組成物、トレッドゴム及びタイヤ |
| WO2022254751A1 (ja) | 2021-05-31 | 2022-12-08 | 株式会社ブリヂストン | ゴム組成物及びタイヤ |
Families Citing this family (34)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP4117250B2 (ja) * | 2001-11-27 | 2008-07-16 | 株式会社ブリヂストン | 共役ジエン系重合体、その製法及びそれを用いたゴム組成物 |
| EP1462459B1 (en) * | 2001-12-03 | 2012-12-26 | Bridgestone Corporation | Process for producing modified polymer, modified polymer obtained by the process, and rubber composition |
| WO2003087171A1 (fr) * | 2002-04-12 | 2003-10-23 | Bridgestone Corporation | Procede de production de polymere modifie, polymere ainsi obtenu et composition elastomere |
| JP5101291B2 (ja) * | 2004-10-26 | 2012-12-19 | 株式会社ブリヂストン | 連結基を有する官能化ポリマー |
| EP1841603B1 (en) * | 2005-01-14 | 2009-11-25 | Bridgestone Corporation | Method for preparing a tire having improved silica reinforcement |
| KR101271929B1 (ko) | 2005-04-15 | 2013-06-05 | 가부시키가이샤 브리지스톤 | 변성공역디엔계 공중합체, 고무 조성물 및 타이어 |
| CN101528839B (zh) * | 2006-09-04 | 2013-06-19 | 株式会社普利司通 | 橡胶组合物以及使用该橡胶组合物的充气轮胎 |
| EP2116396B1 (en) * | 2007-03-05 | 2014-04-23 | Bridgestone Corporation | Pneumatic tire |
| SG159473A1 (en) | 2008-08-27 | 2010-03-30 | Sumitomo Chemical Co | Conjugated diene polymer, conjugated diene polymer composition, and method for producing conjugated diene polymer |
| US8426512B2 (en) | 2009-08-31 | 2013-04-23 | The Goodyear Tire & Rubber Company | Rubber composition containing silica reinforcement and functionalized polybutadiene rubber and tires having a component thereof |
| US8809440B2 (en) * | 2009-10-21 | 2014-08-19 | Jsr Corporation | Method of producing modified conjugated diene rubber, modified conjugated diene rubber, and rubber composition |
| KR101702697B1 (ko) * | 2010-02-26 | 2017-02-06 | 제온 코포레이션 | 공액 디엔계 고무, 고무 조성물, 고무 가교물, 및 타이어, 그리고 공액 디엔계 고무의 제조 방법 |
| EP2368918A1 (en) | 2010-03-24 | 2011-09-28 | LANXESS Deutschland GmbH | Process for the production of water and solvent-free polymers |
| WO2011155326A1 (ja) * | 2010-06-08 | 2011-12-15 | Jsr株式会社 | 変性共役ジエン系ゴム、その製造方法、及びゴム組成物 |
| EP2471852A1 (de) * | 2010-12-29 | 2012-07-04 | Lanxess Deutschland GmbH | Vulkanisierbare Zusammensetzungen auf Basis Epoxygruppen-haltiger Nitrilkautschuke |
| TWI428357B (zh) * | 2010-12-31 | 2014-03-01 | Chi Mei Corp | 共軛二烯-乙烯基芳香烴共聚物及其製備方法 |
| TWI413648B (zh) * | 2010-12-31 | 2013-11-01 | Chi Mei Corp | 共軛二烯-乙烯基芳香烴共聚物及其製備方法 |
| US9527932B2 (en) | 2011-08-31 | 2016-12-27 | Jsr Corporation | Method for producing denatured conjugated diene polymer |
| EP2752433B1 (en) * | 2011-08-31 | 2015-12-16 | JSR Corporation | Method for producing denatured conjugated diene polymer |
| US9512263B2 (en) * | 2011-12-09 | 2016-12-06 | Bridgestone Corporation | Method for producing polydienes and polydiene copolymers with reduced cold flow |
| TWI432465B (zh) * | 2011-12-16 | 2014-04-01 | Chi Mei Corp | 改質的高順式共軛二烯聚合物及其製造方法 |
| KR101948024B1 (ko) | 2011-12-28 | 2019-02-14 | 제온 코포레이션 | 변성 공액 디엔계 고무의 제조 방법 |
| JP5961382B2 (ja) | 2012-01-10 | 2016-08-02 | 株式会社ブリヂストン | タイヤ用ゴム組成物、タイヤ用加硫ゴム組成物及びそれらを用いたタイヤ |
| CN105191448B (zh) * | 2013-04-19 | 2019-04-05 | Lg电子株式会社 | 在无线接入系统中的功率控制方法和设备 |
| TWI522378B (zh) | 2013-12-13 | 2016-02-21 | 奇美實業股份有限公司 | 改質的高順式丁二烯-異戊二烯系共聚物、其製造方法及含有前述聚合物的輪胎 |
| TWI508979B (zh) | 2013-12-18 | 2015-11-21 | Chi Mei Corp | 改質的高順式異戊二烯聚合物、其製造方法及含有前述聚合物的輪胎 |
| WO2016027401A1 (ja) | 2014-08-20 | 2016-02-25 | 株式会社ブリヂストン | 末端変性共役ジエン重合体の製造方法、末端変性共役ジエン重合体、ゴム組成物及びタイヤ |
| JP6723269B2 (ja) * | 2015-05-15 | 2020-07-15 | ケーエルエー コーポレイション | 焦点感応オーバーレイターゲットを使用する焦点決定のためのシステムおよび方法 |
| US10179479B2 (en) | 2015-05-19 | 2019-01-15 | Bridgestone Americas Tire Operations, Llc | Plant oil-containing rubber compositions, tread thereof and race tires containing the tread |
| US11021595B2 (en) * | 2015-10-16 | 2021-06-01 | Bridgestone Corporation | Multicomponent copolymer, rubber composition, cross-linked rubber composition, rubber product, and tire |
| US10899718B2 (en) | 2016-09-02 | 2021-01-26 | Bridgestone Corporation | Polymers functionalized with N-protected hydantoin compounds |
| JP7006425B2 (ja) * | 2018-03-22 | 2022-02-10 | 横浜ゴム株式会社 | タイヤ用ゴム組成物および空気入りタイヤ |
| US20220185931A1 (en) * | 2019-03-10 | 2022-06-16 | Bridgestone Corporation | Modified High Cis Polydiene Polymer, Related Methods And Rubber Compositions |
| US20220195074A1 (en) * | 2019-09-11 | 2022-06-23 | Lg Chem, Ltd. | Modified Conjugated Diene-Based Polymer and Rubber Composition Including the Same |
Citations (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2001131344A (ja) * | 1999-11-08 | 2001-05-15 | Bridgestone Corp | ゴム組成物及びそれを用いた空気入りタイヤ |
| JP2001131230A (ja) * | 1999-10-29 | 2001-05-15 | Bridgestone Corp | 重合体、その製造方法、及びそれを用いたゴム組成物 |
| JP2001131340A (ja) * | 1999-11-08 | 2001-05-15 | Bridgestone Corp | ゴム組成物及びそれを用いた空気入りタイヤ |
| JP2001131343A (ja) * | 1999-11-08 | 2001-05-15 | Bridgestone Corp | ゴム組成物及びそれを用いた空気入りタイヤ |
| JP2001131345A (ja) * | 1999-11-08 | 2001-05-15 | Bridgestone Corp | ゴム組成物,油展ゴム及び空気入りタイヤ |
| JP2001158835A (ja) * | 1999-12-02 | 2001-06-12 | Bridgestone Corp | ゴム組成物及びそれを用いた空気入りタイヤ |
| JP2001158834A (ja) * | 1999-12-02 | 2001-06-12 | Bridgestone Corp | ゴム組成物及びそれを用いた空気入りタイヤ |
| JP2001158836A (ja) * | 1999-12-02 | 2001-06-12 | Bridgestone Corp | ゴム組成物,油展ゴム及び空気入りタイヤ |
| US6294624B1 (en) * | 1999-01-22 | 2001-09-25 | Ube Industries, Ltd. | Modified diene elastomer and its preparation |
| JP2001302704A (ja) * | 2000-04-20 | 2001-10-31 | Ube Ind Ltd | 変性ポリブタジエンの製造方法、変性ポリブタジエン、およびゴム組成物 |
| JP2001302703A (ja) * | 2000-04-18 | 2001-10-31 | Ube Ind Ltd | 変性ポリブタジエンの製法、変性ポリブタジエン、及びゴム組成物 |
| JP2001335663A (ja) * | 2000-05-30 | 2001-12-04 | Bridgestone Corp | 油展ゴム、それを用いたゴム組成物及び空気入りタイヤ |
Family Cites Families (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5096942A (en) | 1990-05-29 | 1992-03-17 | Eastman Kodak Company | Organic/inorganic composites |
| JPH0987426A (ja) * | 1995-09-20 | 1997-03-31 | Bridgestone Corp | ゴム組成物の製造方法 |
| EP0767206B1 (fr) * | 1995-10-04 | 2002-07-10 | Compagnie Generale Des Etablissements Michelin-Michelin & Cie | Composition de caoutchouc à base d'un polymère diénique comprenant un dérivé organosilane, utilisable pour la fabrication de bandes de roulement de pneumatiques |
| US6228908B1 (en) * | 1997-07-11 | 2001-05-08 | Bridgestone Corporation | Diene polymers and copolymers incorporating partial coupling and terminals formed from hydrocarboxysilane compounds |
| US6525118B2 (en) * | 1997-07-11 | 2003-02-25 | Bridgestone Corporation | Processability of silica-filled rubber stocks with reduced hysteresis |
| US6403693B2 (en) * | 1999-06-18 | 2002-06-11 | The Goodyear Tire & Rubber Company | Silica reinforced rubber composition and use in tires |
| CN1295910A (zh) * | 1999-11-11 | 2001-05-23 | 固特异轮胎和橡胶公司 | 强化弹性体制造、弹性体复合材料及具有该成分的轮胎 |
| JP4898045B2 (ja) * | 1999-11-12 | 2012-03-14 | 株式会社ブリヂストン | ランタニドを基にした触媒を用いて製造した変性重合体 |
| JP4367590B2 (ja) | 1999-11-12 | 2009-11-18 | Jsr株式会社 | 共役ジエン系重合体の製造方法およびゴム組成物 |
| JP2001158832A (ja) | 1999-12-02 | 2001-06-12 | Asahi Kasei Corp | 複合ゴム系組成物 |
| US6433065B1 (en) * | 2000-10-13 | 2002-08-13 | Bridgestone Corporation | Silica-reinforced rubber compounded with mercaptosilanes and alkyl alkoxysilanes |
| JP4117250B2 (ja) * | 2001-11-27 | 2008-07-16 | 株式会社ブリヂストン | 共役ジエン系重合体、その製法及びそれを用いたゴム組成物 |
| KR101271929B1 (ko) * | 2005-04-15 | 2013-06-05 | 가부시키가이샤 브리지스톤 | 변성공역디엔계 공중합체, 고무 조성물 및 타이어 |
-
2002
- 2002-11-27 JP JP2003547468A patent/JP4117250B2/ja not_active Expired - Lifetime
- 2002-11-27 EP EP02783661A patent/EP1449857B1/en not_active Expired - Lifetime
- 2002-11-27 WO PCT/JP2002/012390 patent/WO2003046020A1/ja active Application Filing
- 2002-11-27 DE DE60237986T patent/DE60237986D1/de not_active Expired - Lifetime
- 2002-11-27 ES ES02783661T patent/ES2351302T3/es not_active Expired - Lifetime
- 2002-11-27 CN CNB028234561A patent/CN100334118C/zh not_active Expired - Lifetime
- 2002-11-27 US US10/496,983 patent/US7781533B2/en active Active
-
2010
- 2010-07-02 US US12/829,889 patent/US8642705B2/en not_active Expired - Lifetime
Patent Citations (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6294624B1 (en) * | 1999-01-22 | 2001-09-25 | Ube Industries, Ltd. | Modified diene elastomer and its preparation |
| JP2001131230A (ja) * | 1999-10-29 | 2001-05-15 | Bridgestone Corp | 重合体、その製造方法、及びそれを用いたゴム組成物 |
| JP2001131344A (ja) * | 1999-11-08 | 2001-05-15 | Bridgestone Corp | ゴム組成物及びそれを用いた空気入りタイヤ |
| JP2001131340A (ja) * | 1999-11-08 | 2001-05-15 | Bridgestone Corp | ゴム組成物及びそれを用いた空気入りタイヤ |
| JP2001131343A (ja) * | 1999-11-08 | 2001-05-15 | Bridgestone Corp | ゴム組成物及びそれを用いた空気入りタイヤ |
| JP2001131345A (ja) * | 1999-11-08 | 2001-05-15 | Bridgestone Corp | ゴム組成物,油展ゴム及び空気入りタイヤ |
| JP2001158835A (ja) * | 1999-12-02 | 2001-06-12 | Bridgestone Corp | ゴム組成物及びそれを用いた空気入りタイヤ |
| JP2001158834A (ja) * | 1999-12-02 | 2001-06-12 | Bridgestone Corp | ゴム組成物及びそれを用いた空気入りタイヤ |
| JP2001158836A (ja) * | 1999-12-02 | 2001-06-12 | Bridgestone Corp | ゴム組成物,油展ゴム及び空気入りタイヤ |
| JP2001302703A (ja) * | 2000-04-18 | 2001-10-31 | Ube Ind Ltd | 変性ポリブタジエンの製法、変性ポリブタジエン、及びゴム組成物 |
| JP2001302704A (ja) * | 2000-04-20 | 2001-10-31 | Ube Ind Ltd | 変性ポリブタジエンの製造方法、変性ポリブタジエン、およびゴム組成物 |
| JP2001335663A (ja) * | 2000-05-30 | 2001-12-04 | Bridgestone Corp | 油展ゴム、それを用いたゴム組成物及び空気入りタイヤ |
Non-Patent Citations (1)
| Title |
|---|
| See also references of EP1449857A4 * |
Cited By (92)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP1479698A1 (en) * | 2003-05-22 | 2004-11-24 | JSR Corporation | Method for producing modified conjugated diene polymer and rubber composition |
| JP2005008870A (ja) * | 2003-05-22 | 2005-01-13 | Jsr Corp | 変性共役ジエン系重合体の製造方法およびゴム組成物 |
| US7202306B2 (en) | 2003-05-22 | 2007-04-10 | Jsr Corporation | Method for producing modified conjugated diene polymer and rubber composition |
| JP4596126B2 (ja) * | 2003-05-22 | 2010-12-08 | Jsr株式会社 | 変性共役ジエン系重合体の製造方法およびゴム組成物 |
| WO2004111094A1 (en) * | 2003-06-09 | 2004-12-23 | Bridgestone Corporation | Improved hysteresis elastomeric compositions comprising sequentially terminated polymers |
| US7534839B2 (en) * | 2003-06-09 | 2009-05-19 | Bridgestone Corporation | Sequentially terminated elastomers |
| JP2007505208A (ja) * | 2003-06-09 | 2007-03-08 | 株式会社ブリヂストン | イソシアナートアルコキシシランを用いて停止させた重合体を含む改良されたヒステリシスのエラストマー組成物 |
| JP2005232364A (ja) * | 2004-02-20 | 2005-09-02 | Bridgestone Corp | 変性共役ジエン系重合体、並びにそれを用いたゴム組成物及びタイヤ |
| JP2005232367A (ja) * | 2004-02-20 | 2005-09-02 | Bridgestone Corp | 変性共役ジエン系重合体、並びにそれを用いたゴム組成物及びタイヤ |
| JP2006249189A (ja) * | 2005-03-09 | 2006-09-21 | Bridgestone Corp | 変性重合体及びそれを用いたゴム組成物及びタイヤ |
| JP5720082B2 (ja) * | 2005-03-18 | 2015-05-20 | Jsr株式会社 | 変性重合体の製造方法、その方法によって得られた変性重合体とそのゴム組成物 |
| KR101262406B1 (ko) * | 2005-03-18 | 2013-05-08 | 제이에스알 가부시끼가이샤 | 변성 중합체의 제조 방법 |
| WO2006101025A1 (ja) * | 2005-03-18 | 2006-09-28 | Jsr Corporation | 変性重合体の製造方法、その方法によって得られた変性重合体とそのゴム組成物 |
| US7700686B2 (en) | 2005-03-18 | 2010-04-20 | Jsr Corporation | Process for producing modified polymer, modified polymer obtained by the process, and rubber composition thereof |
| CN101180345B (zh) * | 2005-03-18 | 2012-05-23 | Jsr株式会社 | 制造改性聚合物的方法、由该方法获得的改性聚合物及其橡胶组合物 |
| JP5657855B2 (ja) * | 2005-10-05 | 2015-01-21 | Jsr株式会社 | 変性共役ジエン系重合体の製造方法、その方法によって得られた変性共役ジエン系重合体とそのゴム組成物 |
| US7893153B2 (en) | 2005-10-05 | 2011-02-22 | Jsr Corporation | Process for producing modified conjugated diene polymer, modified conjugated diene polymer obtained by the process, and rubber composition containing the same |
| KR101057224B1 (ko) * | 2005-10-05 | 2011-08-16 | 가부시키가이샤 브리지스톤 | 변성 공액 디엔계 중합체의 제조 방법, 그 방법에 의해서얻어진 변성 공액 디엔계 중합체, 및 이를 함유하는 고무조성물 |
| WO2007040252A1 (ja) | 2005-10-05 | 2007-04-12 | Jsr Corporation | 変性共役ジエン系重合体の製造方法、その方法によって得られた変性共役ジエン系重合体とそのゴム組成物 |
| JP2007191611A (ja) * | 2006-01-20 | 2007-08-02 | Bridgestone Corp | 変性ポリブタジエンゴム配合ゴム組成物及びタイヤ |
| WO2007083765A1 (ja) * | 2006-01-20 | 2007-07-26 | Bridgestone Corporation | 変性ポリブタジエンゴム配合ゴム組成物及びタイヤ |
| US8846820B2 (en) | 2006-04-05 | 2014-09-30 | Bridgestone Corporation | Activated silane compound, rubber composition using the same and tire |
| US8476374B2 (en) | 2006-04-05 | 2013-07-02 | Bridgestone Corporation | Activated silane compound, rubber composition using the same and tire |
| JP2007308653A (ja) * | 2006-05-22 | 2007-11-29 | Bridgestone Corp | タイヤトレッド用ゴム組成物及びそれを用いた空気入りタイヤ |
| JP2007326942A (ja) * | 2006-06-07 | 2007-12-20 | Bridgestone Corp | 空気入りタイヤ |
| JP2007326990A (ja) * | 2006-06-09 | 2007-12-20 | Bridgestone Corp | ゴム組成物及びそれを用いたタイヤ |
| WO2008004676A1 (fr) | 2006-07-06 | 2008-01-10 | Bridgestone Corporation | Composition de caoutchouc et bandage pneumatique fabriqué à partir de celle-ci |
| WO2008004675A1 (fr) | 2006-07-06 | 2008-01-10 | Bridgestone Corporation | Composition de caoutchouc et bandage pneumatique fabriqué à partir de celle-ci |
| KR101417165B1 (ko) * | 2006-10-25 | 2014-07-08 | 가부시키가이샤 브리지스톤 | 변성 공액 디엔계 중합체의 제조 방법, 그 방법에 의해 얻어진 변성 공액 디엔계 중합체, 고무 조성물 및 타이어 |
| CN101553522B (zh) * | 2006-10-25 | 2012-09-05 | Jsr株式会社 | 改性聚合物的制造方法、由该方法得到的改性聚合物及其橡胶组合物 |
| JP5683070B2 (ja) * | 2006-10-25 | 2015-03-11 | 株式会社ブリヂストン | 変性共役ジエン系重合体の製造方法、その方法により得られた変性共役ジエン系重合体、ゴム組成物及びタイヤ |
| WO2008050845A1 (fr) * | 2006-10-25 | 2008-05-02 | Bridgestone Corporation | Procédé de production de polymères diènes conjugués modifiés, polymères diènes conjugués modifiés produits par ce procédé, compositions de caoutchouc et pneus |
| US9056925B2 (en) | 2006-10-25 | 2015-06-16 | Bridgestone Corporation | Process for production of modified conjugated diene polymers, modified conjugated diene polymers produced by the process, rubber compositions, and tires |
| WO2008050851A1 (fr) * | 2006-10-25 | 2008-05-02 | Jsr Corporation | Procédé de production d'un polymère modifié, polymère modifié obtenu par ce procédé et composition de caoutchouc contenant celui-ci |
| JP2008106118A (ja) * | 2006-10-25 | 2008-05-08 | Jsr Corp | 変性重合体の製造方法、その方法により得られた変性重合体とそのゴム組成物 |
| US8404785B2 (en) | 2006-12-27 | 2013-03-26 | Jsr Corporation | Method for producing modified conjugated diene polymer, modified conjugated diene polymer, and rubber composition |
| KR101440169B1 (ko) * | 2006-12-27 | 2014-09-12 | 제이에스알 가부시끼가이샤 | 변성 공액 디엔계 중합체의 제조 방법, 변성 공액 디엔계 중합체, 및 고무 조성물 |
| WO2008084724A1 (ja) | 2006-12-27 | 2008-07-17 | Jsr Corporation | 変性共役ジエン系重合体の製造方法、変性共役ジエン系重合体、及びゴム組成物 |
| WO2008078813A1 (ja) | 2006-12-27 | 2008-07-03 | Jsr Corporation | 変性共役ジエン系重合体の製造方法、変性共役ジエン系重合体、及びゴム組成物 |
| JP5428340B2 (ja) * | 2006-12-27 | 2014-02-26 | Jsr株式会社 | 変性共役ジエン系重合体の製造方法 |
| JP2008163338A (ja) * | 2006-12-28 | 2008-07-17 | Bridgestone Corp | 高シス−1,4−結合量と高い官能性とを有する変性シス−1,4−ポリジエンの製造方法 |
| JP2008195923A (ja) * | 2006-12-28 | 2008-08-28 | Bridgestone Corp | 含アミンアルコキシシリル官能化ポリマー |
| JP2016222927A (ja) * | 2007-06-18 | 2016-12-28 | 株式会社ブリヂストン | アミノ基を含有するハロシラン類で官能基化された重合体 |
| JP2010530464A (ja) * | 2007-06-18 | 2010-09-09 | 株式会社ブリヂストン | アミノ基を含有するハロシラン類で官能基化された重合体 |
| JP2015071764A (ja) * | 2007-06-18 | 2015-04-16 | 株式会社ブリヂストン | アミノ基を含有するハロシラン類で官能基化された重合体 |
| WO2009022665A1 (ja) * | 2007-08-10 | 2009-02-19 | Bridgestone Corporation | 空気入りタイヤ |
| JP2010536945A (ja) * | 2007-08-16 | 2010-12-02 | ランクセス・ドイチュランド・ゲーエムベーハー | 共役ジエンをベースとするナノ構造化ポリマー |
| JP2009120757A (ja) * | 2007-11-16 | 2009-06-04 | Jsr Corp | 変性共役ジエン系重合体の製造方法、変性共役ジエン系重合体、及びゴム組成物 |
| JP2009120758A (ja) * | 2007-11-16 | 2009-06-04 | Jsr Corp | 変性共役ジエン系重合体の製造方法、変性共役ジエン系重合体、及びゴム組成物 |
| JP2009173838A (ja) * | 2008-01-28 | 2009-08-06 | Bridgestone Corp | ゴム組成物及びそれを用いた空気入りタイヤ |
| US8097076B2 (en) | 2008-02-04 | 2012-01-17 | Byk-Chemie Gmbh | Wetting and dispersing agent |
| DE102008007713A1 (de) | 2008-02-04 | 2009-08-06 | Byk-Chemie Gmbh | Netz- und Dispergiermittel |
| JP2009242788A (ja) * | 2008-03-10 | 2009-10-22 | Bridgestone Corp | ゴム組成物及びそれを用いたタイヤ |
| JP5547058B2 (ja) * | 2008-03-10 | 2014-07-09 | 株式会社ブリヂストン | 変性共役ジエン(共)重合体の製造方法、変性共役ジエン(共)重合体、並びにそれを用いたゴム組成物及びタイヤ |
| JP2014098162A (ja) * | 2008-03-10 | 2014-05-29 | Bridgestone Corp | 変性共役ジエン(共)重合体の製造方法、変性共役ジエン(共)重合体、並びにそれを用いたゴム組成物及びタイヤ |
| JP2009287018A (ja) * | 2008-04-28 | 2009-12-10 | Bridgestone Corp | 変性低分子量共役ジエン系重合体 |
| WO2009133936A1 (ja) * | 2008-04-30 | 2009-11-05 | 株式会社ブリヂストン | 変性重合体を含有するゴム組成物を使用したタイヤ |
| US9279045B2 (en) | 2008-04-30 | 2016-03-08 | Bridgestone Corporation | Tire prepared by using rubber composition containing modified polymer |
| JP2009287019A (ja) * | 2008-04-30 | 2009-12-10 | Bridgestone Corp | 変性重合体を含有するゴム組成物を使用したタイヤ |
| RU2475368C2 (ru) * | 2008-04-30 | 2013-02-20 | Бриджстоун Корпорейшн | Покрышка, изготовленная с использованием каучуковой композиции, содержащей модифицированный полимер |
| JP2011522928A (ja) * | 2008-06-06 | 2011-08-04 | スティロン ヨーロッパ ゲゼルシャフト ミット ベシュレンクテル ハフツング | 変性エラストマーポリマー |
| US8022159B2 (en) | 2008-11-24 | 2011-09-20 | The Goodyear Tire & Rubber Company | Terminating compounds, polymers, and their uses in rubber compositions and tires |
| WO2010104149A1 (ja) | 2009-03-11 | 2010-09-16 | Jsr株式会社 | ゴム組成物及び空気入りタイヤ |
| WO2010150827A1 (ja) | 2009-06-24 | 2010-12-29 | 株式会社ブリヂストン | ポリマー組成物、ゴム組成物及びそれを用いたタイヤ |
| US8754159B2 (en) | 2009-07-22 | 2014-06-17 | Bridgestone Corporation | Tire |
| JP2012031314A (ja) * | 2010-07-30 | 2012-02-16 | Bridgestone Corp | メタロセン系複合触媒、触媒組成物及び共重合体の製造方法 |
| KR101824466B1 (ko) | 2010-12-01 | 2018-02-01 | 제이에스알 가부시끼가이샤 | 변성 공액 디엔계 고무, 고무 조성물, 가교 고무 조성물 및 타이어의 제조 방법 |
| JP6003651B2 (ja) * | 2010-12-01 | 2016-10-05 | Jsr株式会社 | 変性共役ジエン系ゴムの製造方法、変性共役ジエン系ゴム、及びゴム組成物 |
| WO2012073880A1 (ja) * | 2010-12-01 | 2012-06-07 | Jsr株式会社 | 変性共役ジエン系ゴムの製造方法、変性共役ジエン系ゴム、及びゴム組成物 |
| JPWO2012073880A1 (ja) * | 2010-12-01 | 2014-05-19 | Jsr株式会社 | 変性共役ジエン系ゴムの製造方法、変性共役ジエン系ゴム、及びゴム組成物 |
| US8980987B2 (en) | 2010-12-01 | 2015-03-17 | Jsr Corporation | Method for producing modified conjugated diene rubber, modified conjugated diene rubber, and rubber composition |
| WO2017126629A1 (ja) | 2016-01-19 | 2017-07-27 | 株式会社ブリヂストン | ゴム組成物及びタイヤ |
| KR102150526B1 (ko) | 2016-06-17 | 2020-09-01 | 주식회사 엘지화학 | 변성 공액디엔계 중합체의 제조방법 및 이를 이용하여 제조된 변성 공액디엔계 중합체 |
| KR20170142492A (ko) * | 2016-06-17 | 2017-12-28 | 주식회사 엘지화학 | 변성 공액디엔계 중합체의 제조방법 및 이를 이용하여 제조된 변성 공액디엔계 중합체 |
| EP3301131A1 (en) | 2016-09-30 | 2018-04-04 | Sumitomo Rubber Industries, Ltd. | Cap tread rubber composition for cold weather tires |
| EP3392058A1 (en) | 2017-04-13 | 2018-10-24 | Sumitomo Rubber Industries, Ltd. | Cap tread rubber composition for cold weather tires |
| WO2019116804A1 (ja) | 2017-12-15 | 2019-06-20 | 株式会社ブリヂストン | ゴム組成物及び空気入りタイヤ |
| WO2019123749A1 (ja) | 2017-12-20 | 2019-06-27 | 株式会社ブリヂストン | ゴム組成物 |
| JP7462735B2 (ja) | 2019-09-19 | 2024-04-05 | エルジー・ケム・リミテッド | 変性共役ジエン系重合体の製造方法 |
| JP2022544242A (ja) * | 2019-09-19 | 2022-10-17 | エルジー・ケム・リミテッド | 変性共役ジエン系重合体の製造方法 |
| JP2022520984A (ja) * | 2019-09-30 | 2022-04-04 | エルジー・ケム・リミテッド | 変性共役ジエン系重合体、その製造方法、およびそれを含むゴム組成物 |
| WO2021124637A1 (ja) | 2019-12-19 | 2021-06-24 | 株式会社ブリヂストン | タイヤ |
| WO2021124640A1 (ja) | 2019-12-19 | 2021-06-24 | 株式会社ブリヂストン | タイヤ |
| KR20210125427A (ko) | 2020-04-08 | 2021-10-18 | 아사히 가세이 가부시키가이샤 | 공액 디엔계 중합체 및 그의 제조 방법, 그리고 고무 조성물 |
| WO2022124147A1 (ja) | 2020-12-09 | 2022-06-16 | 株式会社ブリヂストン | ゴム組成物、ゴム組成物の製造方法及びタイヤ |
| WO2022249637A1 (ja) | 2021-05-28 | 2022-12-01 | 株式会社ブリヂストン | タイヤ用ゴム組成物、トレッドゴム及びタイヤ |
| WO2022249764A1 (ja) | 2021-05-28 | 2022-12-01 | 株式会社ブリヂストン | タイヤ用ゴム組成物、トレッドゴム及びタイヤ |
| WO2022249765A1 (ja) | 2021-05-28 | 2022-12-01 | 株式会社ブリヂストン | タイヤ用ゴム組成物、トレッドゴム及びタイヤ |
| WO2022249763A1 (ja) | 2021-05-28 | 2022-12-01 | 株式会社ブリヂストン | タイヤ用ゴム組成物、トレッドゴム及びタイヤ |
| WO2022249636A1 (ja) | 2021-05-28 | 2022-12-01 | 株式会社ブリヂストン | タイヤ用ゴム組成物、トレッドゴム及びタイヤ |
| WO2022249767A1 (ja) | 2021-05-28 | 2022-12-01 | 株式会社ブリヂストン | タイヤ用ゴム組成物、トレッドゴム及びタイヤ |
| WO2022254751A1 (ja) | 2021-05-31 | 2022-12-08 | 株式会社ブリヂストン | ゴム組成物及びタイヤ |
Also Published As
| Publication number | Publication date |
|---|---|
| US20100280173A1 (en) | 2010-11-04 |
| EP1449857A4 (en) | 2008-12-31 |
| US7781533B2 (en) | 2010-08-24 |
| DE60237986D1 (de) | 2010-11-25 |
| JPWO2003046020A1 (ja) | 2005-04-07 |
| ES2351302T3 (es) | 2011-02-02 |
| JP4117250B2 (ja) | 2008-07-16 |
| EP1449857B1 (en) | 2010-10-13 |
| US20050070672A1 (en) | 2005-03-31 |
| US8642705B2 (en) | 2014-02-04 |
| EP1449857A1 (en) | 2004-08-25 |
| CN100334118C (zh) | 2007-08-29 |
| CN1592760A (zh) | 2005-03-09 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| WO2003046020A1 (fr) | Polymere dienique conjugue, procede de fabrication et compositions elastomeres contenant ce polymere | |
| JP4159993B2 (ja) | 変性重合体の製造方法、その方法で得られた変性重合体及びゴム組成物 | |
| JP5069593B2 (ja) | ゴム組成物及びそれを用いたタイヤ | |
| US7767774B2 (en) | Silyl-diamine initiators for anionic polymerization of 1,3-butadiene and styrene, and rubber compositions | |
| JP5189253B2 (ja) | 空気入りタイヤ | |
| EP2272909B1 (en) | Tire prepared by using rubber composition containing modified polymer | |
| JP2007308653A (ja) | タイヤトレッド用ゴム組成物及びそれを用いた空気入りタイヤ | |
| JP2007262206A (ja) | タイヤトレッド用ゴム組成物及びそれを用いた空気入りタイヤ | |
| JP4111590B2 (ja) | 重合体の製造方法、得られた重合体、及びそれを用いたゴム組成物 | |
| JP5965657B2 (ja) | タイヤトレッド用ゴム組成物及びそれを用いた空気入りタイヤ | |
| JP2006274049A (ja) | ゴム組成物及びそれを用いた空気入りタイヤ | |
| JP2013237724A (ja) | トレッド用ゴム組成物及びそれを用いた空気入りタイヤ | |
| JP4909520B2 (ja) | 変性重合体及びそれを用いたゴム組成物及びタイヤ | |
| JP2005336303A (ja) | 空気入りタイヤ | |
| JP2008001742A (ja) | 空気入りタイヤ | |
| JP4801827B2 (ja) | 重合体、その製造方法、及びそれを用いたゴム組成物 | |
| JP2005232364A (ja) | 変性共役ジエン系重合体、並びにそれを用いたゴム組成物及びタイヤ | |
| JP2006274046A (ja) | ゴム組成物及びそれを用いた空気入りタイヤ | |
| JP4610035B2 (ja) | ゴム組成物及びそれを用いた空気入りタイヤ |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| AK | Designated states |
Kind code of ref document: A1 Designated state(s): CN JP US |
|
| AL | Designated countries for regional patents |
Kind code of ref document: A1 Designated state(s): AT BE BG CH CY CZ DE DK EE ES FI FR GB GR IE IT LU MC NL PT SE SK TR |
|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application | ||
| WWE | Wipo information: entry into national phase |
Ref document number: 2003547468 Country of ref document: JP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 20028234561 Country of ref document: CN |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2002783661 Country of ref document: EP |
|
| WWP | Wipo information: published in national office |
Ref document number: 2002783661 Country of ref document: EP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 10496983 Country of ref document: US |