RU2531758C2 - Моноклональные антитела для лечения опухолей - Google Patents
Моноклональные антитела для лечения опухолей Download PDFInfo
- Publication number
- RU2531758C2 RU2531758C2 RU2010135585/10A RU2010135585A RU2531758C2 RU 2531758 C2 RU2531758 C2 RU 2531758C2 RU 2010135585/10 A RU2010135585/10 A RU 2010135585/10A RU 2010135585 A RU2010135585 A RU 2010135585A RU 2531758 C2 RU2531758 C2 RU 2531758C2
- Authority
- RU
- Russia
- Prior art keywords
- seq
- batrh
- antibody
- batrκ
- tumor
- Prior art date
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/28—Compounds containing heavy metals
- A61K31/282—Platinum compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/335—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin
- A61K31/337—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin having four-membered rings, e.g. taxol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/513—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim having oxo groups directly attached to the heterocyclic ring, e.g. cytosine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7042—Compounds having saccharide radicals and heterocyclic rings
- A61K31/7052—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides
- A61K31/706—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides containing six-membered rings with nitrogen as a ring hetero atom
- A61K31/7064—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides containing six-membered rings with nitrogen as a ring hetero atom containing condensed or non-condensed pyrimidines
- A61K31/7068—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides containing six-membered rings with nitrogen as a ring hetero atom containing condensed or non-condensed pyrimidines having oxo groups directly attached to the pyrimidine ring, e.g. cytidine, cytidylic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
- A61K39/39533—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals
- A61K39/39558—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals against tumor tissues, cells, antigens
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61N—ELECTROTHERAPY; MAGNETOTHERAPY; RADIATION THERAPY; ULTRASOUND THERAPY
- A61N5/00—Radiation therapy
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/02—Antineoplastic agents specific for leukemia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/30—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants from tumour cells
- C07K16/3061—Blood cells
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Immunology (AREA)
- Molecular Biology (AREA)
- Biomedical Technology (AREA)
- Cell Biology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Biochemistry (AREA)
- Biophysics (AREA)
- Genetics & Genomics (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Oncology (AREA)
- Hematology (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Microbiology (AREA)
- Mycology (AREA)
- Pathology (AREA)
- Radiology & Medical Imaging (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Peptides Or Proteins (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
Abstract
Настоящее изобретение относится к иммунологии и биотехнологии. Предложено применение гуманизированного моноклонального антитела или его фрагмента, включающего вариабельные области лёгкой и тяжелой цепи, полученные из моноклонального антитела мыши mBAT-1, в комбинации по меньшей мере с одним химиотерапевтическим агентом на основе платины, антиметаболитов или паклитаксела для лечения опухолевого заболевания. Описано применение гуманизированного моноклонального антитела или его фрагмента, включающего вариабельные области лёгкой и тяжелой цепи, полученные из моноклонального антитела мыши mBAT-1, в комбинации с по меньшей мере одним химиотерапевтическим агентом на основе платины, антиметаболитов или паклитаксела для повышения выживаемости субъекта с опухолью, которого лечат по меньшей мере одним химиотерапевтическим агентом. Изобретение обеспечивает синергетический эффект, выраженный в увеличении жизнеспособности лимфоцитов или уменьшении объёма опухоли по сравнению с использованием h-ВАТ, что может найти применение в медицине для лечения опухолей. 2 н. и 9 з.п. ф-лы, 20 ил., 2 табл., 8 пр.
Description
Область изобретения
Настоящее изобретение относится к способам ингибирования роста опухоли, повышения выживаемости пациента, страдающего опухолевым заболеванием, и индуцирования защиты от рецидива опухоли у млекопитающих. Данные способы включают введение гуманизированных моноклональных антител, включающих CDR-области (гипервариабельные участки, определяющие комплементарность), полученные из моноклонального антитела мыши, обозначенного mBAT-1, в сочетании по меньшей мере с одним химиотерапевтическим агентом.
Предпосылки создания изобретения
За последние годы быстрое развитие знаний о молекулярных и клеточных основах иммунной регуляции, в частности, относительно уровня Т-клеточного ответа обеспечивает новый арсенал иммунотерапевтических подходов, включая разработку противоопухолевых вакцин. Обнаружено, что отдельные моноклональные антитела обладают иммуномодулирующей активностью, включая способность связывать детерминанты на поверхности Т-клеток и индуцировать пролиферацию, активацию, созревание или дифференцировку этих клеток.
ВАТ (также называемое mBAT-1 или ВАТ-1) представляет собой моноклональное антитело мыши против мембранного препарата клеточной линии лимфомы Беркитта (линия Дауди), которое обладает противоопухолевым и иммуностимулирующим действием на различные виды опухолей (Hardy с сотр., 2001, Int. J. Oncol. 19:897). Данное моноклональное антитело первоначально было описано Hardy с сотр. в патенте США №5,897,862. ВАТ-1 секретируется клеточной линией гибридомы с номером I-1397 базы CNCM.
Полинуклеотидная и аминокислотная последовательности ВАТ мыши описаны Hardy с сотр. в WO 00/58363 и в публикации патента США №2003/0026800. Ряд гуманизированных моноклональных антител на основе ВАТ мыши описаны в публикации патента США №2008/0025980. В соответствии с данным описанием гуманизированное моноклональное антитело ВАТ индуцирует более выраженное противоопухолевое действие, чем исходное (материнское) антитело ВАТ мыши. Среди многих протестированных модельных систем противоопухолевую активность ВАТ изучали с использованием SCID-мышей (тяжелый комбинированный иммунодефицит - ТКИД), beige мышей, которые являются дефицитными по NK-клеткам, и nude мышей, которые являются дефицитными по Т-клеткам (Hardy В., 1997, Proc. Natl. Acad. Sci. USA 94:5756). Всем мышам вводили внутривенно клетки меланомы В16 мыши, из которых впоследствии развивались опухолевые образования в легких. ВАТ оказывал противоопухолевое действие только у SCID-мышей, которым прививали лимфоциты мыши или человека. У бестимусных nude мышей и beige мышей ВАТ проявлял противоопухолевую активность, хотя эта активность была менее эффективной по сравнению с противоопухолевой активностью ВАТ у мышей дикого типа.
Иммуномодулирующее действие ВАТ мыши также изучали in vitro. BAT мыши активирует CD4+ Т-клетки и индуцирует секрецию IFN-γ данными клетками (Hardy с сотр., 2000, bit. Immunol. 12:1623 и Quaglino E. с сотр, 2005, Vaccine 9:23(25):3280-7, соответственно). Кроме того, было показано, что ВАТ запускает пролиферацию Т-клеток и повышает их цитолитическую активность (Hardy В. с сотр., 1997, Hum. Antibodies, 8:95).
Berger с сотр. (2008) предложил введение гуманизированного моноклонального антитела СТ-011, которое основано на mBAT-1, пациентам, страдающим запущенными гемобластозами, и соответсвующую фармакокинетику (Berger с сотр. din. Cancer Res., 2008; 14(10) 15 мая 2008 года).
Следует принимать во внимание, что мишенью антител ВАТ являются не опухолевые клетки, а скорее иммунные клетки субъекта или пациента, чтобы модулировать иммунный ответ благоприятным образом.
Одним из самых распространенных способов терапевтического лечения рака является химиотерапия. Лекарственные препараты для химиотерапии разделяют на несколько групп в зависимости от оказываемого действия на специфические химические соединения внутри раковых клеток, активность клеток или вовлекаемые процессы, или на специфические фазы клеточного цикла. Группы препаратов для химиотерапии включают: алкилирующие агенты, производные нитрозомочевины, антиметаболиты, антрациклиновые соединения, ингибиторы топоизомеразы I и II, митотические ингибиторы и стероидные ингибиторы.
Химиотерапевтический лекарственный препарат может обеспечиваться в качестве отдельной терапии, (монотерапии), но чаще всего используют в комбинации с одним или более другими активными агентами. В некоторых случаях специфические комбинации препаратов были адаптированы для обеспечения значительно более высоких клинических результатов. Например, антиметаболит фторурацил (5-ФУ) и алкилирующий агент оксалиплатин используют в комбинации для лечения рака ободочной и прямой кишки (колоноректального). Комбинированная терапия фторурацилом, лейковорином (фолиниевая кислота) и оксалимлатином также предназначена для лечения рака ободочной и прямой кишки и имеет аббревиатуру FOLFOX. Комбинированную терапию циклофосфамидом, доксорубицином, винкристином и преднизолоном (имеет аббревиатуру CHOP) используют для лечения неходжкинской лимфомы, а комбинацию CHOP и химерного моноклонального антитела ритуксимаб (имеет аббревиатуру R-CHOP) используют для лечения диффузной крупноклеточной В-клеточной лимфомы и других злокачественных B-клеточных неходжкинских лимфом.
Комбинированная терапия урацилом, 5-ФУ или урамустином совместно с облучением (радиационной терапией) и терапией моноклональным антителом, которое специфически связывается с внеклеточным доменом рецептора фактора роста эндотелия сосудов (VEGF), описана в патенте США №6,811,779. Такая комбинированная терапия направлена на ингибирование ангиогенеза. В патенте США №6,217,866 описан способ подавления роста клеток опухоли человека, экспрессирующих рецепторы фактора роста эпидермиса человека (EGF), включающий введение пациенту с раковым заболеванием, имеющего указанные клетки опухоли, эффективного количества антинеопластического (противоопухолевого) агента и эффективного количества моноклонального антитела; (i) причем указанное антитело связывается с внеклеточным доменом рецептора EGF человека указанных клеток опухоли; (ii) причем антитело не конъюгировано с антинеопластическим агентом; и (iii) причем антитело подавляет связывание EGF с рецептором EGF.
В уровне техники полностью отсутствуют рекомендации или предположения относительно того, что использование гуманизированного моноклонального антитела mBAT-1 в комбинации с химиотерапией может быть полезным. Фактически, поскольку известно, что ВАТ и антитела на его основе обладают иммуностимулирующими свойствами, удивительно и неожиданно, что такие антитела в комбинации с цитотоксическими или другими химиотерапевтическими агентами, действие которых заключается в уничтожении пролиферирующих клеточных популяций, могут быть использованы для достижения более высокой клинической эффективности, чем любой из агентов в отдельности.
Краткое описание изобретения
Настоящее изобретение обеспечивает способы ингибирования роста опухоли, уменьшения объема опухоли, повышения выживаемости субъекта и индуцирования защиты от рецидива опухоли у субъектов, имеющих солидные и несолидные опухоли. Данные способы включают использование гуманизированного моноклонального антитела, содержащего по меньшей мере один гипервариабельный участок, определяющий комплементарность (CDR) моноклонального антитела BAT-1 (mBAT-1) мыши и каркасного участка (FR), полученного из акцепторного иммуноглобулина человека. Примером подобного антитела является hBAT-1 (также называемое здесь СТ-011). Некоторые из способов, описанных в данном документе, предпочтительно включают использование гуманизированного моноклонального антитела в комбинации по меньшей мере с одним химиотерапевтическим агентом, тогда как другие способы, описываемые в данном документе, относятся к использованию собственно гуманизированного моноклонального антитела, но которое может быть использовано в комбинации с одним или более химиотерапевтическими агентами.
Принципы настоящего изобретения изложены в данном документе с использованием как mBAT-1, так и СТ-011 в культурах лимфоцитов и на моделях опухоли животных и при действии СТ-011 на человека с различными типами гематологических опухолей.
Настоящее изобретение частично основано на неожиданно обнаруженном факте, что включение СТ-011 в схему лечения различными химиотерапевтическими агентами приводит к некоторым полезным противоопухолевым и противораковым эффектам, включая, например, снижение скорости роста опухоли, ингибирование роста опухоли и увеличение времени выживаемости по сравнению с монотерапией любым из способов лечения отдельно. Также было обнаружено, что включение гуманизированного антитела, такого как СТ-011, в схему химиотерапевтического лечения может обеспечить дополнительный полезный эффект, заключающийся в повышении переносимости уровней дозолимитирующей токсичности (ДЛТ) химиотерапевтического агента.
Настоящее изобретение также частично основано на наблюдении, что лечение индуцированных опухолей в животных моделях заявленными антителами, используемых отдельно или в комбинации с химиотерапевтическими агентами, приводит не только к "исцелению", но также к возникновению эффекта памяти (запоминания) для продолжительной защиты от рецидива опухоли при последующем поражении такими опухолевыми клетками. Животные, вылеченные с использованием гуманизированного антитела СТ-011, оказались, таким образом, устойчивыми к рецидиву или повторному проявлению данной опухоли. Более того, в настоящее время описано, что в определенных обстоятельствах у людей, которые принимали участие на ранних этапах клинических исследований с использованием СТ-011, также наблюдался длительный контроль опухоли и защитные эффекты после введения однократной дозы данного антитела и его элиминации из системы кровотока.
Не основываясь на какой-либо теории или механизме действия, активность гуманизированного моноклонального антитела ВАТ в отношении защиты от рецидива опухоли или ее развития может быть связана с активностью данного антитела по защите эффекторных Т-клеток / Т-клеток памяти от апоптоза, как описано в данном документе и пояснено на примере антитела СТ-011.
Таким образом, в различных аспектах настоящее изобретение обеспечивает комбинации противоопухолевых агентов, неизвестные до настоящего времени в качестве обладающих кумулятивным или даже аддитивным эффектом. В соответствии с определенными принципами настоящего изобретения указанные комбинации включают один вариант лечения, представляющий собой введение по меньшей мере одного химиотерапевтического агента, и другой вариант лечения, представляющий собой введение иммуностимулирующего гуманизированного моноклонального антитела, основанного на mBAT-1. Неожиданно проведение указанных двух вариантов лечения обеспечивает больший полезный противоопухолевый эффект при их использовании в комбинации, а не раздельно или при использовании каждого из них по отдельности. Комбинированная терапия, как показано в описании и формуле изобретения может относиться к любому числу различных комбинированных вариантов лечения, включая, например, по существу перекрывающиеся периоды применения двух или более вариантов лечения; одновременное, последовательное или поочередное применение двух или более вариантов лечения или регулярное применение двух или более вариантов лечения в течение переменных периодов времени.
В соответствии с первым аспектом настоящее изобретение обеспечивает способ лечения опухоли, включающий (i) введение субъекту, нуждающемуся в таком лечении, эффективного количества гуманизированного моноклонального антитела или его фрагмента, причем указанное антитело или его фрагмент имеет по меньшей мере один участок, определяющий комплементарность моноклонального антитела ВАТ (mBAT-1) мыши, и каркасный участок (FR) из акцепторного иммуноглобулина человека, или их модификации; и (ii) введение субъекту эффективного количества по меньшей мере одного химиотерапевтического агента; таким образом обеспечивая лечение опухоли.
В соответствии с другим аспектом настоящее изобретение также обеспечивает способ улучшения переносимости по меньшей мере одного химиотерапевтического агента, включающий введение субъекту, нуждающемуся в таком лечении, эффективного количества гуманизированного моноклонального антитела или его фрагмента, причем указанное антитело или его фрагмент имеет по меньшей мере один участок, определяющий комплементарность моноклонального антитела ВАТ (mBAT-1) мыши, и каркасный участок (FR) из акцепторного иммуноглобулина человека или их модификации; причем указанный субъект подвергается химиотерапии по меньшей мере с одним химиотерапевтическим агентом; таким образом обеспечивая улучшение переносимости указанного химиотерапевтического агента.
В соответствии с еще одним аспектом настоящего изобретения обеспечивается способ увеличения выживаемости или подавления (ингибирования) прогрессирования заболевания у субъекта, имеющего опухоль, причем указанный субъект подвергается лечению по меньшей мере одним химиотерапевтическим агентом, где указанный способ включает введение эффективного количества гуманизированного моноклонального антитела или его фрагмента, причем указанное антитело или его фрагмент имеет по меньшей мере один участок, определяющий комплементарность моноклонального антитела ВАТ (mBAT-1) мыши, и каркасный участок (FR) из акцепторного иммуноглобулина человека или их модификации; таким образом обеспечивая увеличение выживаемости указанного субъекта.
В соответствии с еще одним аспектом настоящее изобретение обеспечивает способ снижения или предотвращения рецидива опухоли, включающий введение субъекту, нуждающемуся в таком лечении, эффективного количества гуманизированного моноклонального антитела или его фрагмента, причем указанное антитело или его фрагмент имеет по меньшей мере один участок, определяющий комплементарность моноклонального антитела ВАТ (mBAT-1) мыши, и каркасный участок (FR) из акцепторного иммуноглобулина человека или их модификации; таким образом обеспечивая снижение или предотвращение рецидива опухоли.
В соответствии с одним вариантом осуществления изобретения указанный способ снижения или предотвращения рецидива опухоли дополнительно включает введение субъекту по меньшей мере одного химиотерапевтического агента.
В соответствии с другими вариантами осуществления изобретения субъект подвергается или закончил курс химиотерапии с применением по меньшей мере одного химиотерапевтического агента.
В соответствии с различными вариантами осуществления изобретения вариабельный участок легкой цепи гуманизированного моноклонального антитела описывается формулой:
FRL1-CDRL1-FRL2-CDRL2-FRL3-CDRL3-FRL4,
где каждый FR независимо представляет собой каркасный участок антитела человека и каждый CDR независимо представляет собой участок, определяющий комплементарность моноклонального антитела mBAT-1.
В соответствии с другими вариантами осуществления изобретения вариабельный участок тяжелой цепи гуманизированного моноклонального антитела описывается формулой:
FRH1-CDRH1-FRH2-CDRH2-FRH3-CDRH3-FRH4,
где каждый FR независимо представляет собой каркасный участок антитела человека и каждый CDRнезависимо представляет собой участок, определяющий комплементарность моноклонального антитела mBAT-1.
В соответствии с другими вариантами осуществления изобретения FR-участки получены из вариабельных участков легкой цепи антитела Т9 человека (SEQ ID NO:130) или его модификации.
В соответствии с другими вариантами осуществления изобретения аминокислотные последовательности FR, полученные или модифицированные из вариабельного участка легкой цепи антитела TEL9 человека, выбраны из группы, состоящей из: FRL1, [EIVLT QSPSS LSASV GDRVT ITC; SEQ ID NO:1]; FRL2, [W (F или Y) QQKPG KAPKL (W или L) IY; SEQ ID NO:2]; FRL3, [GVPSR FSGSG SGT (D или S) (Y или F) (С или Т) LTINS LQPED FATYY C; SEQ ID NO:3]; и FRL4, [FGGGT KLEIK; SEQ ID NO:4].
В соответствии с другими вариантами осуществления изобретения FR получены из вариабельных участков тяжелой цепи антитела hsighv1295 человека (SEQ ID NO:146) или их модификаций.
В соответствии с другими вариантами осуществления изобретения аминокислотные последовательности FR, полученные или модифицированные из вариабельного участка тяжелой цепи антитела hsighvl295 человека, выбраны из группы, состоящей из: FRH1, [Q (I или V) QLV QSGSE LKKPG ASVKI SCKAS GY (Т или S) F (Т или S); SEQ ID NO:5]; FRH2, [WV (R OR K) QAPGQ GL (Q или K) WMG; SEQ ID NO:6]; FRH3, [RF (V или A) FSLDT SV (N или S) TAYLQ ITSL (Т или N) AEDTG MYFC (V или A) (R или K); SEQ ID NO:7]; и FRH4, [WGQGT LVTVS S; SEQ ID NO:8].
В соответствии с другими вариантами осуществления изобретения вариабельный участок легкой цепи включает по меньшей мере одну аминокислотную последовательность, выбранную из группы, состоящей из: CDRL1 [SARSS VSYMH; SEQ ID NO:9]; CDRL2 [RTSNL AS; SEQ ID NO:10]; CDRL3 [QQRSS FPLT; и SEQ ID NO:11], причем CDR получены из антитела BAT-1, мыши и нижние индексы "L" и "Н" обозначают участки легких и тяжелых цепей соответственно.
В соответствии с другими вариантами осуществления изобретения вариабельный участок тяжелой цепи включает по меньшей мере одну аминокислотную последовательность, выбранную из группы, состоящей из: CDRH1 [NYGMN; SEQ ID NO:12]; CDRH2 [WINTD SGEST YAEEF KG; SEQ ID NO:13]; и CDRH3 [VGYDA LDY; SEQ ID NO:14].
В соответствии с другими вариантами осуществления изобретения гуманизированное антитело включает вариабельный участок легкой цепи, выбранный из группы, состоящей из: BATRκA (SEQ ID NO:15), BATRκB (SEQ ID NO:16), BATRκC (SEQ ID NO:17), и BATRκD (SEQ ID NO:18); и вариабельный участок тяжелой цепи, выбранный из группы, состоящей из: А (SEQ ID NO:20), BATRHB (SEQ ID NO:21), BATRHC (SEQ ID NO:22), BATRHD (SEQ ID NO:23) и BATRHE (SEQ ID NO:24).
В соответствии с другими вариантами осуществления изобретения гуманизированное антитело включает вариабельные участки, выбранные из группы, состоящей из: BATRHA/BATRκA (SEQ ID NO:20/SEQ ID NO:15), BATRHB/BATRκA (SEQ ID NO:21/SEQ ID NO:15), BATRHB/BATRκB (SEQ ID NO:21/SEQ ID NO:16), BATRHC/BATRκB (SEQ ID NO:22/SEQ ID NO:16), BATRHB/BATRκD (SEQ ID NO:21/SEQ ID NO:18) и BATRHC/BATRκD (SEQ ID NO:22/SEQ ID NO:18).
В соответствии с другими предпочтительными вариантами осуществления изобретения вариабельные участки гуманизированного моноклонального антитела соответствуют BATRHC/BATRκD (SEQ ID NO:22/SEQ ID NO:18).
В соответствии с другими вариантами осуществления изобретения противоопухолевая активность гуманизированного антитела или его фрагмента аналогична или превосходит активность mBAT-1.
В соответствии с другими вариантами осуществления изобретения фрагмент гуманизированного антитела выбирают из группы, состоящей из: Fv, F(ab'), F(ab')2 и одноцепочечного антитела.
Гуманизированное моноклональное антитело согласно настоящему изобретению, предпочтительно получают с использованием технологии рекомбинантной ДНК, применяя CDR-привитие (grafting). Соответственно, гуманизированное антитело получают путем экспрессии полинуклеотидов, причем полинуклеотиды могут кодировать гуманизированное антитело полностью или вариабельный участок легкой цепи, или вариабельный участок тяжелой цепи, или вариабельные участки обеих цепей гуманизированного антитела. Кроме того, гуманизированное антитело может экспрессироваться в клетках-хозяевах после ко-трансфекции различных векторов, каждый из которых включает полинуклеотиды, кодирующие легкую или тяжелую цепь, или после трансфекции одного вектора, включающего обе полинуклеотидные последовательности легкой и тяжелой цепи.
В соответствии с другими вариантами осуществления изобретения легкая цепь гуманизированного антитела кодируется полинуклеотидной последовательностью, выбранной из группы, состоящей из: SEQ ID NO:87, SEQ ID NO:88 и SEQ ID NO:89.
В соответствии с другими вариантами осуществления изобретения тяжелая цепь гуманизированного антитела кодируется полинуклеотидной последовательностью, выбранной из группы, состоящей из: SEQ ID NO:90, SEQ ID NO:91, и SEQ ID NO:92.
В соответствии с другими вариантами осуществления изобретения по меньшей мере один химиотерапевтический агент выбирают из следующей группы: антиметаболиты, лекарственные средства на основе платины, митотические ингибиторы, антрациклиновые антибиотики, ингибиторы топоизомеразы, антиангиогенные агенты и их комбинации.
В соответствии с предпочитаемым в настоящее время вариантом осуществления изобретения по меньшей мере один химиотерапевтический агент выбирают таким образом, что hBAT-1 повышает выживаемость лимфоцитов при использовании в комбинации с указанным химиотерапевтическим агентом. Обычно повышенная или улучшенная выживаемость может быть удобным образом проанализирована in vitro, как показано далее на примерах.
В соответствии с некоторыми вариантами осуществления изобретения по меньшей мере один химиотерапевтический агент представляет собой антиметаболит, включая антагонисты пуринов, антагонисты пиримидинов и антагонисты фолатов. В соответствии с некоторыми вариантами осуществления изобретения указанный антиметаболит представляет собой антагонист пиримидина. В соответствии с некоторыми вариантами осуществления изобретения антиметаболит выбирают из группы, включающей 5-фторурацил, урамустин, урацил, капецитабин, 6-меркаптопурин, метотрексат, гемцитабин, цитарабин, флударабин и пеметрексед.
В соответствии с некоторыми вариантами осуществления изобретения по меньшей мере один химиотерапевтический агент представляет собой 5-фторурацил.
В соответствии с некоторыми вариантами осуществления изобретения по меньшей мере один химиотерапевтический агент представляет собой цитарабин.
В соответствии с некоторыми вариантами осуществления изобретения по меньшей мере один химиотерапевтический агент представляет собой лекарственное средство на основе платины, выбранное из группы, включающей ципластин, карбоплатин и оксалиплатин.
В соответствии с другими дополнительными вариантами осуществления изобретения по меньшей мере один химиотерапевтический агент представляет собой митотический ингибитор, выбранный из группы, включающей паклитаксел, доцетаксел, этопозид, винбластин, винкристин и виноребин.
В соответствии с другими дополнительными вариантами осуществления изобретения по меньшей мере один химиотерапевтический агент представляет собой антрациклиновый антибиотик, выбранный из группы, включающей даунорубицин, респиномицин D и идарубицин.
В соответствии с некоторыми вариантами осуществления изобретения по меньшей мере один химиотерапевтический агент представляет собой антиангиогенный агент, выбранный из группы, включающей бевацизумаб, допамин, тетратиомолибдат и антиангиогенные варианты VEGF.
В соответствии с некоторыми вариантами осуществления изобретения по меньшей мере один химиотерапевтический агент не является ингибитором топоизомеразы I. В соответствии с некоторыми вариантами осуществления изобретения по меньшей мере один химиотерапевтический агент не является алкилирующим агентом.
В соответствии с другими вариантами осуществления изобретения введение гуманизированного антитела и по меньшей мере одного химиотерапевтического агента осуществляют по существу одновременно, параллельно, альтернативно, последовательно или поочередно. При некоторых вариантах осуществления изобретения гуманизированное антитело и по меньшей мере один химиотерапевтический агент вводят в соответствии с перекрывающимися режимами применения.
В соответствии с некоторыми вариантами осуществления изобретения введение гуманизированного антитела осуществляют до первоначального введения по меньшей мере одного химиотерапевтического агента.
В соответствии с другими вариантами осуществления изобретения введение одного из или обоих препаратов - гуманизированного антитела и по меньшей мере одного химиотерапевтического агента - осуществляют по одному из следующих способов, выбранных из следующей группы: внутривенно, перорально, внутрибрюшинно, подкожно, путем изолированной перфузии конечностей, путем инфузии внутрь органа или их комбинаций.
В соответствии с другими вариантами осуществления изобретения способы дополнительно включают лечение субъекта посредством радиационной терапии (облучение). В соответствии с различными вариантами осуществления изобретения указанные способы включают введение гуманизированного антитела, введение по меньшей мере одного химиотерапевтического агента и радиационной терапии.
В соответствии с некоторыми вариантами осуществления изобретения введение гуманизированного антитела, введение по меньшей мере одного химиотерапевтического агента и применение радиационной терапии осуществляют по существу одновременно, параллельно, альтернативно, поочередно или в соответствии с перекрывающимися режимами применения.
В некоторых вариантах осуществления изобретения способы согласно изобретению дополнительно включают оценку по меньшей мере одного параметра, выбранного из следующей группы, включающей: скорость роста опухоли, объем опухоли, число метастазов, рецидив опухоли и их комбинации.
При некоторых вариантах осуществления изобретения опухоль является солидной или несолидной. При некоторых вариантах осуществления изобретения несолидная опухоль представляет собой гематобластозы. В некоторых вариантах осуществления изобретения опухоль относится к одному из следующих заболеваний: колоректальная карцинома; немелкоклеточный рак легких (НМРЛ); мелкоклеточный рак легких (МРЛ); карцинома молочной железы; меланома; карцинома яичников; карцинома шейки матки; рак поджелудочной железы; карцинома головы и шеи; карцинома желудочно-кишечного тракта; рак пищевода; печеночноклеточная карцинома; множественная миелома; почечноклеточная карцинома; рак простаты; неходжкинская лимфома; болезнь Ходжкина (лимфогранулематоз); лимфома из клеток мантийной зоны; саркома Капоши; плоскоклеточная карцинома; базальноклеточная карцинома; острая миелоидная лейкемия (ОМЛ); хронический миелоидный лейкоз (ХМЛ); острый лимфоцитарный лейкоз (ОЛЛ) и хронический лимфоцитарный лейкоз (ХЛЛ).
В соответствии с различными вариантами осуществления изобретения субъект представляет собой человека или млекопитающее, отличное от человека. В соответствии с различными предпочитаемыми вариантами осуществления изобретения субъектом является человек.
В дополнительном аспекте настоящее изобретение обеспечивает использование (i) гуманизированного моноклонального антитела или его фрагмента, причем указанное антитело или его фрагмент имеет по меньшей мере один участок, определяющий комплементарность моноклонального антитела ВАТ (mBAT-1) мыши и каркасный участок (FR) из акцепторного иммуноглобулина человека, или их модификаций; и (ii) по меньшей мере один химиотерапевтический агент; для приготовления медикамента для лечения опухолей.
В другом аспекте настоящее изобретение обеспечивает гуманизированное моноклинальное антитело или его фрагмент, причем указанное антитело или его фрагмент имеет по меньшей мере один участок, определяющий комплементарность моноклонального антитела ВАТ (mBAT-1) мыши и каркасный участок (FR) из акцепторного иммуноглобулина человека, или их модификаций; для лечения опухоли у субъекта, подвергнутого химиотерапии с применением по меньшей мере одного химиотерапевтического агента.
В другом аспекте настоящее изобретение обеспечивает использование гуманизированного моноклонального антитела или его фрагмента, причем указанное антитело или его фрагмент имеет по меньшей мере один участок, определяющий комплементарность моноклонального антитела ВАТ (mBAT-1) мыши и каркасный участок (FR) из акцепторного иммуноглобулина человека, или их модификаций, для приготовления медикамента для улучшения переносимости по меньшей мере одного химиотерапевтического агента у субъекта, подвергнутого химиотерапии с применением указанного по меньшей мере одного химиотерапевтического агента.
В дополнительном аспекте настоящее изобретение обеспечивает гуманизированное моноклональное антитело или его фрагмент, причем указанное антитело или его фрагмент имеет по меньшей мере один участок, определяющий комплементарность моноклонального антитела ВАТ (mBAT-1) мыши и каркасный участок (FR) из акцепторного иммуноглобулина человека, или их модификаций, для улучшения переносимости по меньшей мере одного химиотерапевтического агента у субъекта, подвергнутого химиотерапии с применением указанного по меньшей мере одного химиотерапевтического агента.
Согласно другому аспекту настоящее изобретение обеспечивает использование гуманизированного моноклонального антитела или его фрагмента, причем указанное антитело или его фрагмент имеет по меньшей мере один участок, определяющий комплементарность моноклонального антитела ВАТ (mBAT-1) мыши и каркасный участок (FR) из акцепторного иммуноглобулина человека, или их модификаций, для приготовления медикамента для улучшения (увеличения) выживаемости или подавления прогрессирования заболевания у субъекта, имеющего опухоль, причем субъект подвергается воздействию по меньшей мере одного химиотерапевтического агента.
Согласно другому аспекту настоящее изобретение обеспечивает гуманизированное моноклональное антитело или его фрагмент, причем указанное антитело или его фрагмент имеет по меньшей мере один участок, определяющий комплементарность моноклонального антитела ВАТ (mBAT-1) мыши и каркасный участок (FR) из акцепторного иммуноглобулина человека, или их модификаций, для улучшения выживаемости или подавления развития заболевания у субъекта, имеющего опухоль, причем субъект подвергается воздействию по меньшей мере одного химиотерапевтического агента.
В соответствии с другим аспектом настоящее изобретение обеспечивает использование гуманизированного моноклонального антитела или его фрагмента, причем антитело или его фрагмент имеет по меньшей мере один участок, определяющий комплементарность моноклонального антитела ВАТ (mBAT-1) мыши и каркасный участок (FR) из акцепторного иммуноглобулина человека, или их модификаций; для приготовления медикамента для снижения или предотвращения рецидива опухоли.
В соответствии с другим аспектом настоящее изобретение обеспечивает гуманизированное моноклональное антитело или его фрагмента, причем указанное антитело или его фрагмент имеет по меньшей мере один участок, определяющий комплементарность, моноклонального антитела ВАТ (mBAT-1) мыши и каркасный участок (FR) из акцепторного иммуноглобулина человека, или их модификаций; для снижения или предотвращения рецидива опухоли.
При некоторых вариантах осуществления изобретения субъект был подвергнут, подвергается или будет подвергнут химиотерапии с применением по меньшей мере одного химиотерапевтического агента.
Краткое описание фигур
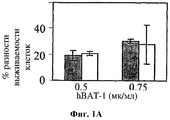
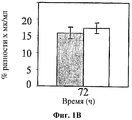
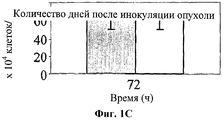
На фигуре 1 показано влияние hBAT-1 в анализе, основанном на жизнеспособности лимфоцитов при добавлении к культурам параллельно с контрольным опытом со средой (серые столбцы) или в комбинации с 5-ФУ (0,5 мг/мл, белые столбцы) и последующего инкубирования в течение 72 часов. Фиг.1А. Активность hBAT-1 (0,5 или 0,75 мкг/мл, как указано) в отсутствие и в присутствии 5-ФУ, представленная как % разность выживаемости клеток. Фиг.1В. Активность hBAT-1 (0,75 мкг/мл) в отсутствие и в присутствии 5-ФУ, выраженная площадью под кривой эффекта дозы (AUC, представленной как % разность × мкг/мл). Время инкубирования с hBAT-1 (72 часа) указано по оси X. Фиг.1C. Влияние 5-ФУ или контрольной среды при проведении функционального теста, представленное в числе жизнеспособных клеток/мл. Время инкубации с 5-ФУ или контрольной средой (72 часа) указано по оси X.
На фигуре 2 показано влияние hBAT-1 в анализе, основанном на жизнеспособности лимфоцитов при добавлении к культурам за 24 часа перед добавлением контрольной среды (серые столбцы) или 5-ФУ (0,5 мг/мл, белые столбцы) и последующего инкубирования в течение 72 часов. Фиг.2А. Активность hBAT-1 (0,5 или 0,75 мкг/мл как указано) в отсутствие и в присутствии 5-ФУ, представленная как % разность выживаемости клеток. Фиг.2В. Активность hBAT-1 (0,75 мкг/мл) в отсутствие и в присутствии 5-ФУ, представленная площадью под кривой эффекта дозы (AUC, представленная как % разность × мкг/мл). Время инкубирования с hBAT-1 (72 часа) указано по оси X.
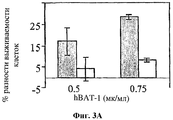
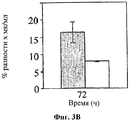
На фигуре 3 показано влияние hBAT-1 в анализе, основанном на жизнеспособности лимфоцитов при параллельном добавлении к культурам с контрольной средой (серые столбцы) или в комбинации с SN-38 (активная форма иринотекана в концентрации 0,1 мг/мл, белые столбцы) и последующего инкубирования в течение 72 часов. Фиг.3А. Активность hBAT-1 (0,5 или 0,75 мкг/мл как указано) в отсутствие и в присутствии SN-38, представленная как % разность выживаемости клеток. Фиг.3В. Активность hBAT-1 (0,75 мкг/мл), выраженная площадью под кривой эффекта дозы (AUC, представленная как % разность × мкг/мл). Время инкубирования с hBAT-1 (72 часа) указано по оси X.
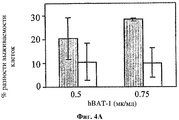
На фигуре 4 показано влияние hBAT-1 в анализе, основанном на жизнеспособности лимфоцитов при добавлении к культурам за 24 часа перед добавлением контрольной среды (серые столбцы) или SN-38 (активная форма иринотекана в концентрации 0,1 мг/мл, белые столбцы) и инкубировании в течение 72 часов. Фиг.4А. Активность hBAT-1 (0,5 или 0,75 мкг/мл как указано) в отсутствие и в присутствии SN-38, представленная как % разность выживаемости клеток. Фиг.4В. Активность hBAT-1 (0,75 мкг/мл), выраженная площадью под кривой эффекта дозы (AUC, представленная как % разность × мкг/мл). Время инкубирования с hBAT-1 (72 часа) указано по оси X.
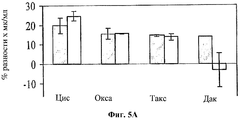
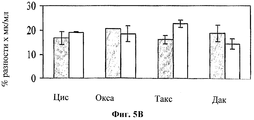
На фигуре 5 показано влияние hBAT-1 в анализе, основанном на жизнеспособности лимфоцитов при добавлении к культурам (в дозозависимых концентрациях от 0,25 до 1,25 мкг/мл) параллельно (Фиг.5А) или за 24 часа (Фиг.5В) перед добавлением контрольной среды (серые столбцы) или указанного химиотерапевтического агента (белые столбцы) и инкубировании в течение 72 часов. Цис, циспластин (10 мкг/мл); Окса, оксалиплатин (10 мкг/мл); Такс, паклитаксел (0,43 мкг/мл); Дак, дакарбазин (1 мкг/мл). Активность hBAT-1 представлена как площадь под кривой эффекта дозы (AUC, представленная как % разность × мкг/мл). Время инкубирования с hBAT-1 (72 часа) указано по оси X.
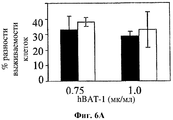
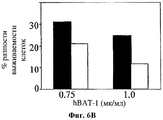
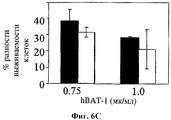
На фигуре 6 показано влияние hBAT-1 (0,75 или 1 мкг/мл, как указано) в анализе, основанном на жизнеспособности лимфоцитов при параллельном добавлении к культурам с контрольной средой (черные столбцы) или в комбинации с химиотерапевтическим агентом (белые столбцы) и инкубировании в течение 72 часов. Были использованы следующие химиотерапевтические агенты: цитарабин в концентрации 2 мг/мл (Фиг.6А), циклофосфамид в концентрации 1 мг/мл (Фиг.6В) и доксорубицин в концентрации 0,03 мг/мл (Фиг.6С). Активность hBAT-1 представлена как % разность клеточной выживаемости.
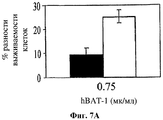
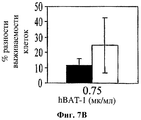
На фигуре 7 показано влияние hBAT-1 в анализе, основанном на жизнеспособности изолированных CD4+ лимфоцитов человека при добавлении (в концентрации 0,75 мкг/мл) за 24 часа до добавления контрольной среды (черные столбцы) или химиотерапевтического агента (белые столбцы) и инкубировании в течение 72 часов. Были использованы следующие химиотерапевтические агенты: 5-ФУ в концентрации 1 мкг/мл (Фиг.7А) и цисплатин в концентрации 10 мкг/мл (Фиг.7В). Активность hBAT-1 представлена как % разность клеточной выживаемости.
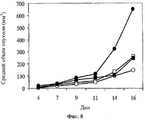
На фигуре 8 показано противоопухолевое действие среды у мышей с колоректальной аденокарциномой (CRC) (черные кружки); 5-ФУ (введение 20 мг/кг в дни 6-9 и 15-16; белые квадраты); hBAT-1 (введение 10 мкг/мышь на 10 день; черные квадраты); и комбинированной схемы применения (белые кружки) hBAT-1 (введение 10 мкг/мышь на 10 день) и 5-ФУ (введение 20 мг/кг в дни 6-9 и 15-16).
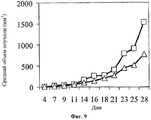
На фигуре 9 показано противоопухолевое действие 5-ФУ у CRC мышей (введение 20 мг/кг в дни 6-9, 15-17, 22-24 и 29-31; белые квадраты) и комбинированной схемы применения (белые треугольники) hBAT-1 (введение 10 мкг/мышь в дни 10, 18 и 25) и 5-ФУ (введение 20 мг/кг в дни 6-9, 15-17, 22-24 и 29-31).
На фигуре 10 показан процент выживаемости CRC мышей при использовании для лечения среды (белые кружки); 5-ФУ (введение 20 мг/кг в дни 6-9, 15-17, 22-24, 29-31, 36-38 и 43-45; черные треугольники); hBAT-1 (введение 10 мкг/мышь в дни 10, 18, 25, 32 и 39; черные квадраты); и комбинированной схемы применения (черные ромбы) hBAT-1 (введение 10 мкг/мышь в дни 10, 18, 25, 32 и 39) и 5-ФУ (введение 20 мг/кг в дни 6-9, 15-17, 22-24, 29-31, 36-38 и 43-45).
На фигуре 11 показан процент выживаемости мышей, которым сделана инъекция клеток меланомы В 16 и проведено лечение 5-ФУ (введение 50 мг/кг в дни 1-4 и 7-8; черные ромбы) или при лечении по комбинированной схеме применения (белые квадраты) hBAT-1 (введение 10 мкг/мышь на день 10) и 5-ФУ (введение 50 мг/кг в дни 1-4 и 7-8).
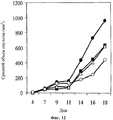
На фигуре 12 показано противоопухолевое действие, которое оценивали по среднему объему опухоли, при использовании для лечения среды (черные кружки); иринотекана (100 мг/кг в дни 7 и 15; черные квадраты); hBAT-1 (введение 10 мкг/мышь на 10 день; белые кружки); и при лечении по комбинированной схеме применения (белые треугольники) hBAT-1 (введение 10 мкг/мышь на 10 день) и иринотекана (введение 100 мг/кг в дни 7 и 15) у CRC мышей.
На фигуре 13 показан процент выживаемости CRC мышей при использовании для лечения среды (черные кружки); иринотекана (введение 100 мг/кг в дни 7 и 15, 22 и 29; черные треугольники); hBAT-1 (введение 10 мкг/мышь в дни 10, 18, 25 и 32; белые квадраты); и при лечении по комбинированной схеме применения (черные ромбы) hBAT-1 (введение 10 мкг/мышь в дни 10, 18, 25 и 32) и иринотекана (введение 100 мг/кг в дни 7 и 15, 22 и 29).
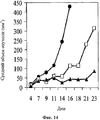
На фигуре 14 показано противоопухолевое действие, которое оценивали по среднему объему опухоли, при использовании для лечения среды (черные кружки); оксалиплатина (1 мг/кг в дни 4, 7-10, 14-17 и 22-23; белые квадраты); и при лечении по комбинированной схеме применения (черные треугольники) hBAT-1 (введение 10 мкг/мышь в дни 11 и 18) и оксалиплатина (1 мг/кг в дни 4, 7-10, 14-17 и 22-23) CRC мышей.
На фигуре 15 показан процент выживаемости CRC мышей при использовании для лечения среды (черные кружки); оксалиплатина (1 мг/кг в дни 4, 7-10, 14-17, 22-24, 29-31; белые квадраты); и при лечении по комбинированной схеме применения (черные треугольники) of hBAT-1 (10 мкг/мышь в дни 11, 18, 25 и 32) и оксалиплатина (1 мг/кг в дни 4, 7-10, 14-17, 22-24, 29-31).
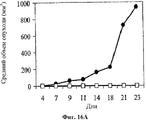
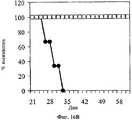
На фигуре 16 показано влияние совместного применения hBAT-1 и химиотерапевтического агента относительно защиты от рецидива опухоли, которое оценивали по среднему объему опухоли (Фиг.16А) и проценту выживаемости (Фиг.16В). Мыши (n=3), которые были излечены от CRC (колоректальной аденокарциномы) в течение 2 или 5 месяцев путем лечения по комбинированной схеме применения hBAT-1 и оксалиплатина, были повторно заражены той же клеточной линией CRC (белые квадраты). Кроме того, CRC вводили ранее не подвергнутым эксперименту (naive mice) мышам (n=6) (черные кружки).
На фигуре 17 показано влияние совместного применения hBAT-1 и химиотерапевтического агента относительно защиты от рецидива опухоли, которое оценивали по среднему объему опухоли (Фиг.17А) и проценту выживаемости (Фиг.17В). Мыши (n=2), которые были излечены от CRC путем лечения по комбинированной схеме применения hBAT-1 и оксалиплатина, что подтверждало отсутствие рецидива опухоли при повторном введении той же клеточной линии CRC, были повторно заражены карциномой молочной железы (белые квадраты). Поражение карциномой молочной железы проводили через 2 месяца после того, как у данных мышей проявилась устойчивость к рецидиву опухоли CRC. Кроме того, CRC вводили ранее не подвергнутым эксперименту мышам (naive mice) (n=6) (черные кружки).
На фигуре 18 показано влияние СТ-11 в анализе на выживаемость клеток с использованием CD4+CD45RO+ эффекторных Т-клеток / Т-памяти клеток человека (черные столбцы) и нативных (naive) CD4+CD45RO- Т-клеток (белые столбцы), подвергнутых действию hBAT (1 мкг/мл) и последующем инкубировании в течение 72 и 96 часов. Результаты выражали как % разность выживаемости клеток.
На фигуре 19 представлены аминокислотные последовательности различных вариантов осуществления изобретения относительно VK-участка гуманизированного ВАТ-1 (SEQ ID NOS. 15-18). Совпадающие остатки VK-участка ВАТ-1 и последовательности V□-участка TEL9 человека (SEQ ID NO. 130) отмечены точками [.]. Отсутствие аминокислоты на специфическом участке остатка отмечены тире [-]. Аминокислотная замена FR TEL9 в V□-участке гуманизированного ВАТ-1 выделена полужирным шрифтом. CDR-участки описаны с использованием номенклатуры [==L1==]. Нумерацию использовали согласно Kabat (Kabat с сотр., Sequences of proteins of immunological interest, Fifth Edition, U.S. Department of Health и Human Services, U.S. Government Printing Office, 1991).
На фигуре 20 представлены аминокислотные последовательности различных вариантов осуществления изобретения относительно VH-участка гуманизированного BAT-1 (SEQ ID NOS. 20-24). Совпадающие остатки V□-участка ВАТ-1 и последовательности VH-участка hsighv1295 человека (SEQ ID NO. 146) отмечены точками [.] Отсутствие аминокислоты на специфическом участке остатка отмечены тире [-]. Аминокислотная замена FR TEL9 в VH-участке гуманизированного ВАТ-1 выделена полужирным шрифтом. CDR-участки описаны с использованием номенклатуры [==Н1==], где [-----] обозначает часть структурной петли H1. Нумерацию использовали согласно Kabat (Kabat с сотр., ibid).
Подробное описание изобретения
Определения
Термин "антитело" (также обозначаемый "иммуноглобулин") используется в самом широком смысле и включает моноклональные антитела (включая полноразмерные моноклональные антитела) и фрагменты антител достаточной длины для сохранения их биологической активности. "Фрагменты антитела" включают часть полноразмерного антитела, обычно его антигенсвязывающий или вариабельный участок. Примеры фрагментов антитела включают: Fab, Fab', F(ab')2, и Fv-фрагменты; диатела; линейные антитела; одноцепочечные молекулы антител и мультиспецифичные антитела, полученные из фрагментов антител.
Базовой единицей природной молекулы антитела является гетеротетрамерный гликопротеиновый комплекс размером приблизительно 150000 Да, состоящий из двух идентичных легких (L) и двух идентичных тяжелых (Н) цепей, связанных вместе нековалентными и дисульфидными связями. Каждая тяжелая и легкая цепь также имеет внутрицепочечные регулярно расположенные дисульфидные мостики. Выделяют пять классов антител человека (IgG, IgA, IgM, IgD и IgE) и внутри данных классов выделяют несколько подклассов на основании структурных различий, таких как число единиц иммуноглобулина в отдельной молекуле антитела, структура дисульфидного мостика отдельных структурных единиц и различия в длине и последовательности цепей. Класс и подкласс антитела представляют его изотип.
N-концевые участки тяжелых и легких цепей характеризуются большим разнообразием последовательности, чем C-концевые участки, и поэтому называются вариабельными доменами. Данный участок структуры антитела отвечает за антигенсвязывающую специфичность антитела. Вариабельные домены тяжелой (VH) и легкой (VL) цепей вместе формируют единый антигенсвязывающий сайт, таким образом, базовая единица иммуноглобулина содержит два антигенсвязывающих сайта. Считается, что особенные аминокислотные остатки формируют поверхность между вариабельными доменами легкой и тяжелой цепей (Chothia с сотр., J. Mol. Biol. 186, 651-63 (1985); Novotny и Haber, (1985) Proc. Natl. Acad. Sci. USA 82 4592-4596).
C-концевые участки тяжелых и легких цепей формируют константные домены, т.е. СН1, СН2, СН3, CL. Такие домены в значительно меньшей степени варьируются, поэтому имеются видоспецифические различия между разными животными и, более того, у одного и того же субъекта имеются несколько изотипов одного антитела, каждый из которых имеет отдельную функцию.
Термин "каркасный участок", или "FR", относится к аминокислотным остаткам в вариабельном домене антитела, которые отличаются от аминокислотных остатков гипервариабельного участка, как указано в описании. Термин "гипервариабельный участок", используемый в описании, относится к аминокислотным остаткам в вариабельном домене антитела, которые отвечают за связывание антигена. Гипервариабельный участок состоит из аминокислотных остатков "участка, определяющего комплементарность", или "CDR". CDR отвечают в первую очередь за связывание эпитопа антигена. Размеры FR и CDR были точно определены (см. Kabat с сотр., ibid).
Термин "акцепторный иммуноглобулин человека" относится к иммуноглобулину человека, который обеспечивает каркас гуманизированного антитела.
Термин "гуманизированное антитело" в описании относится к антителу, состоящему из каркасного участка антитела человека и одного или более CDR нечеловеческого иммуноглобулина (обычно мыши или крысы). Участки гуманизированного иммуноглобулина, возможно, за исключением CDR, по существу идентичны соответствующим участкам последовательностей природного иммуноглобулина человека. Однако в некоторых случаях могут быть модифицированы специфические аминокислотные остатки, например, каркасных участков для оптимизации свойств гуманизированного антитела. Важное предположение состоит в том, что гуманизированное антитело связывает тот же самый антиген, что и донорное антитело, которое обеспечивает CDR. Подробная информация представлена, например, в патенте США №5,225,539, принадлежащем Совету по медицинским исследованиями (Соединенное Королевство).
Термины "каркасный участок из акцепторного иммуноглобулина человека" и "каркасный участок, полученный из акцепторного иммуноглобулина человека" и похожие выражения используют в описании взаимозаменяемо для обозначения каркасного участка или его части, который имеет аналогичную аминокислотную последовательность акцепторного иммуноглобулина человека.
Термин "каркасный участок модифицированный из акцепторного иммуноглобулина человека" и похожие выражения относятся к каркасному участку, в аминокислотную последовательность которого были внесены изменения, например замена, делеция или химическая модификация одного или более аминокислотных остатков,по сравнению с последовательностью исходного акцепторного иммуноглобулина человека. Модификации FR-участка могут проводиться для оптимизации свойств конструируемого гуманизированного антитела, например, для оптимизации связывания антигена и исключения стерических затруднений. Подробное объяснение основы и логическое обоснование модификации специфических остатков FR-участков акцепторного иммуноглобулина при создании гуманизированного антитела ВАТ обеспечивается в публикации заявки на патент США №2008/0025980.
Кроме того, FR может быть подвергнут химической модификации на одном или более аминокислотных остатках как с использованием естественных процессов, таких как процессинг или другие посттрансляционные модификации, так и с использованием технологий химической модификации. Химические модификации включают без ограничений: ацетилирование, ацилирование, аминирование, АДФ-рибозилирование, гликозилирование, формирование ГФИ-якорной последовательности, ковалентное присоединение жидкости или липидных производных, метилирование, миристилирование, пегилирование, пренилирование, фосфорилирование, убиквитинилирование или другие похожие процессы.
Термин "антитело человека" относится к антителу, кодируемому геном, фактически характерным для человека, или его аллелью, или вариантом, или мутантом человека.
Термин "противоопухолевое действие (эффект)", в настоящем описании относится к полезному биологическому эффекту, который может проявляться в виде одного или более из перечисленных: уменьшение или стабилизация объема опухоли, уменьшение или стабилизация числа клеток опухоли, уменьшение или стабилизация скорости роста опухоли, уменьшение или стабилизация числа метастазов, защита от рецидива опухоли, увеличение ожидаемого срока жизни или выживаемости субъекта с опухолью, увеличение ожидаемого срока жизни или выживаемости без прогрессирования заболевания у субъекта с опухолью, или улучшение различных физиологических симптомов, связанных с раком. "Противоопухолевое действие" также проявляется в в способности комбинации согласно изобретению предотвращать возникновение опухоли или рецидив опухоли. С учетом свойств способов согласно изобретению они могут применяться при лечении острых, латентных, контролируемых или стабилизированных форм рака, а также для профилактики его возникновения.
Термин "млекопитающее" означает любое млекопитающее, включая домашних животных, таких как собаки и кошки; сельскохозяйственные животные, такие как свиньи, крупный рогатый скот, овцы и козы; лабораторные животные, такие как мыши и крысы; приматы, такие как мартышки, человекообразные обезьяны и шимпанзе; и предпочтительно человек.
Термин "эффективное количество" в отношении гуманизированного антитела и химиотерапевтического агента (ов) согласно настоящему изобретению следует понимать как количество каждого из данных активных агентов, требуемое для достижения терапевтического эффекта без возникновения избыточных или неконтролируемых нежелательных побочных явлений. Эффективное количество, требуемое для достижения терапевтического конечного результата, может зависеть от ряда факторов, включая, например, специфический тип опухоли и тяжесть состояния пациента, а также совместного применения такой комбинации и облучения. Эффективное количество (доза) активных агентов в контексте настоящего изобретения должно быть достаточным для достижения полезного ответа у субъекта со временем, включая подавление (ингибирование) роста опухоли, снижение скорости роста опухоли, предотвращение роста опухоли и образования метастазов, а также улучшение выживаемости.
Термин "улучшение выживаемости", используемый в описании, относится к продленному периоду времени, в течение которого субъект или пациент жив после проведения лечения по способу согласно изобретению. Улучшение выживаемости означает повышение вероятности отсутствия прогрессирования болезни у субъекта, страдающего раковым заболеванием, после конкретного лечения. Данный термин также используют для описания повышенного процента субъектов в группе, болезнь которых, очевидно стабилизируется (не проявляет признаков прогрессирования) по прошествии определенного периода времени по сравнению с контрольной группой. Данный термин также используют для описания повышенного процента субъектов в группе, очевидно вылеченных (не проявляют симптомов болезни) по прошествии определенного периода времени по сравнению с контрольной группой. Данный параметр может быть определен с использованием одного из типичных клинических результатов, обозначенного как "выживаемость без прогрессирования заболевания", "общая выживаемость" и "выживаемость без признаков рецидива заболевания", используемых для определения эффективности режима лечения.
Термин "переносимость химиотерапевтических агентов" относится к физиологической, физико-химической и иммунологической способности субъекта переносить нежелательные побочные эффекты, связанные с лечением с применением одного или более химиотерапевтических агентов. Также термин "улучшение переносимости химиотерапевтических агентов" относится к улучшению физиологической и физико-химической устойчивости к данным нежелательным побочным эффектам, таким образом, что тяжесть данных нежелательных побочных эффектов снижается и/или число нежелательных побочных эффектов снижается. Также "улучшение переносимости химиотерапевтических агентов" может относиться к улучшению качества жизни раковых пациентов, подвергнутых лечению с использованием химиотерапевтических агентов.
Термин "рецидив опухоли" относится к возобновлению, повторному появлению, повторному росту или пролиферации опухоли такого же типа в том же или ином месте по прошествии периода времени, в течение которого рост исходной опухоли был реверсирован, приостановлен или подавлен.
Термин "улучшение или повышение выживаемости лимфоцитов", используемый в описании, относится к способности определенной комбинации лечения пролонгировать жизнеспособность лимфоцитов in vitro или in vivo по сравнению с жизнеспособностью идентичной популяции клеток при применении только одного варианта лечения. Например, использование определенных комбинаций hBAT-1 и химиотерапевтических агентов повышает выживаемость лимфоцитов, что показано при проведении тестов in vitro как продемонстрировано в Примере 1.
Способы согласно изобретению
Способы иммунотерапевтического лечения рака нацелены и основаны на модулировании ответа иммунной системы на индукцию или усиление уничтожения опухолевых клеток и контроле роста опухоли. При осуществлении данного подхода используют различные иммуномодуляторы, включая моноклональные антитела, которые избирательно связываются со специфическими детерминантами на поверхности Т-клеток и, таким образом, инициируют путь активации или индуцируют эффект подавления.
В соответствии с определенными аспектами настоящего изобретения введение гуманизированного антитела, обладающего иммуностимулирующим действием, в комбинации по меньшей мере с одним противоопухолевым химиотерапевтическим агентом усиливает противоопухолевое действие химиотерапевтических агентов и наоборот. В предпочтительных вариантах изобретения введение гуманизированного антитела, обладающего иммуностимулирующим действием, в комбинации по меньшей мере с одним химиотерапевтическим агентом приводит к значительному улучшению исхода болезни по сравнению с применением только одного из способов лечения. В предпочтительных вариантах изобретения отмечали синергетическое действие при лечении опухолей с использованием гуманизированного антитела согласно изобретению в комбинации по меньшей мере с одним химиотерапевтическим агентом и, возможно, дополнительно в сочетании с применением облучения.
Другими словами, в соответствии с одним из аспектов настоящего изобретения противоопухолевое действие гуманизированного антитела согласно изобретению превышает ожидаемый результат при комбинировании по меньшей мере с одним химиотерапевтическим агентом. Синергетический эффект состоит в превышающем ожидания противоопухолевом действии комбинированного способа лечения, чем это может прогнозироваться исходя из аддитивного эффекта лечения с использованием гуманизированного антитела и химиотерапевтического агента (ов) в отдельности. Например, синергетический эффект продемонстрирован в Примерах 2, 3 и 6, где показано, что комбинированная терапия в соответствии с настоящим изобретением оказывает повышенное противоопухолевое действие, на основании измерения объема опухоли и выживаемости мышей с опухолью по сравнению с действием только антитела или химиотерапии в отдельности. В частности, при оценке объема опухоли показано (Фиг.8), что введение комбинации hBAT-1 и 5-ФУ является более эффективным по сравнению с каждым из данных агентов в отдельности, и на Фиг.9 показано, что комбинация hBAT-1 и 5-ФУ приводит к синергетическому эффекту по сравнению с использованием только 5-ФУ. Аналогично, при проведении оценки на выживаемость показано, что введение комбинации hBAT-1 и 5-ФУ является более эффективным по сравнению с каждым из данных агентов в отдельности (Фиг.10) или по сравнению с использованием только 5-ФУ (Фиг.11). Использование другой комбинации, а именно hBAT-1 и оксалиплатина, не только обладает преимуществами по сравнению с использованием одного оксалиплатина для повышения выживаемости, но также индуцирует полную ремиссию у некоторых субъектов (Фиг.15). Синергетический эффект комбинированной терапии, описываемой в настоящем изобретении, по сравнению с соответствующей монотерапией также представлен полной ремиссией и созданием защитной опухоль-специфической памяти у мышей с опухолью (Фиг.10, 15, 16, 17).
Эффекты in vivo, проявляемые комбинациями согласно изобретению, подтверждаются при проведении функциональных тестов на выживаемость лимфоцитов in vitro, как показано в Примере 1. Как показано в данном примере, последовательная обработка лимфоцитов мыши hBAT-1 и затем 5-ФУ (вводили через 24 часа) неожиданным образом приводила к повышению выживаемости лимфоцитов приблизительно на 30% (Фиг.2А). При одновременной обработке лимфоцитов hBAT-1 и 5-ФУ выживаемость лимфоцитов повышалась незначительно (Фиг.1А) по сравнению с обработкой отдельно hBAT-1 и отдельно 5-ФУ, что не повышало выживаемости клеток (Фиг.1C), это свидетельствует о наличии механистического синергетического эффекта последовательного режима лечения. Синергетическую активность также наблюдали при проведении тестов in vitro с использованием комбинации химиотерапевтического агента цисплатина и гуманизированного антитела (Фиг.7В). Таким образом, сочетания определенных химиотерапевтических агентов и гуманизированного антитела согласно изобретению приводит к синергетическим эффектам in vitro и in vivo.
Синергетический эффект, обнаруженный и подтвержденный примерами в данном документе, является полностью неожиданным, учитывая, что известные механизмы действия и мишени антител ВАТ и химиотерапевтических агентов полностью различны и даже противоположны. Антитела ВАТ оказывают действие путем стимулирования иммунных клеток (как показано, например. Hardy с сотр., 1994; Hardy с сотр., 1997), тогда как действие химиотерапевтических агентов, таких как 5-ФУ и оксалиплатин, обусловлено уничтожением быстро делящихся клеток, включая иммунные клетки.
Как показано на примере, комбинации согласно данному изобретению, представляющие собой такие, которые используют химиотерапевтические агенты в комбинации с гуманизированным антителом согласно изобретению, демонстрируют повышение или улучшение выживаемости лимфоцитов. Как показано в Примере 1 и на Фиг.1-7, оценку выживаемости лимфоцитов можно проводить с использованием типичных in vitro тестов.
Таким образом, в разных вариантах изобретения химиотерапевтический агент может быть выбран из группы антиметаболитов, таких как аналог пиримидина 5-фторурацил, или цитарабин, или лекарственное вещество на основе платины, такое как оксалиплатин или цисплатин. Более того, в различных вариантах осуществления изобретения химиотерапевтический агент может отличаться от агента, выбранного из ингибиторов топоизомеразы I (таких, как SN-38) или алкилирующих агентов (таких, как циклофосфамид). Противоопухолевое действие, индуцированное комбинациями согласно изобретению, включает предотвращение, подавление прогрессирования опухоли, снижение роста опухоли и защиту от рецидива опухоли, включая злокачественные и доброкачественные опухоли. Прогрессирование опухоли включает инвазивность, формирование метастазов, возобновление роста и увеличение размеров опухоли. Снижение роста опухоли также включает разрушение или элиминацию опухоли, которое приводит к полному выздоровлению.
Кроме того, было показано, что настоящее изобретение также является эффективным для улучшения переносимости химиотерапевтических агентов. Как известно в данной области техники, главным препятствием использования противораковой химиотерапии является проявление острых и разрушительных нежелательных побочных эффектов по причине сильной токсичности большинства химиотерапевтических агентов. Как показано в Примере 3, использование гуманизированного антитела ВАТ (СТ-011) в комбинации с 5-ФУ при концентрациях дозолимитирующей токсичности (DLT) с использованием последовательного введения приводит к улучшению выживаемости у мышей. Данные наблюдения подтверждают использование гуманизированного антитела ВАТ для улучшения переносимости химиотерапевтических агентов у пациентов, подвергаемых химиотерапии.
Данное изобретение также обеспечивает способ повышения выживаемости субъектов с опухолью, включающий введение гуманизированного антитела согласно изобретению, или отдельно, или возможно в комбинации с дополнительным введением одного или более химиотерапевтических агентов. Например, эффект "исцеления", индуцированный введением СТ-011 людям с раковыми опухолями (Пример 8), подтверждает такую монотерапию с использованием антитела. Данный аспект изобретения обладает особенным преимуществом в случаях, где применение химиотерапии оказалось неэффективным или где пациент не способен переносить химиотерапевтические агенты.
Данное изобретение также обеспечивает способ снижения или предотвращения рецидива опухоли, включающий введение гуманизированного антитела согласно изобретению, или отдельно, или возможно в комбинации с дополнительным введением одного или более химиотерапевтических агентов. Как показано в Примере 6, комбинированное лечение экспериментальных животных с использованием гуманизированного антитела согласно изобретению и химиотерапевтических агентов явным образом индуцирует "эффект памяти", обеспечивающий подавление рецидива опухоли при повторном заражении исходным типом опухоли.
Можно проводить лечение всех типов опухолей с применением способов согласно изобретению. Опухоли могут быть солидными и несолидными.
Некоторые примеры солидных опухолей, лечение которых можно проводить с использованием комбинаций согласно настоящему изобретению, включают карциномы, саркомы, бластомы или глиомы. Некоторые примеры таких опухолей включают эпидермальные карциномы, ороговевающие карциномы, такие как карциномы головы и шеи, колоректальные карциномы, карциномы простаты, карциномы молочных желез, карцинома легких, включая немелкоклеточный рак легких (НМРЛ) и мелкоклеточный рак легких (МРЛ), рак поджелудочной железы, карциномы щитовидной железы, карциномы яичников, рак печени, рак пищевода и рак желудка. Другие примеры включают такие заболевания, как: саркома Капоши, новообразования в ЦНС, нейробластомы, капиллярные гемангиобластомы, менингиомы и церебральные метастазы, меланому, карциному желудочно-кишечного тракта и почечные карциномы и саркомы, рабдомиобластома, глиобластома, особенно мультиформная глиобастома, и лейомиосаркома. Примеры васкуляризированных раковых заболеваний кожи включают такие заболевания, как: плоскоклеточная карцинома, базальноклеточная карцинома и типы раковых заболеваний кожи, которые могут быть вылечены при подавлении роста злокачественных кератиноцитов, таких как злокачественный кератиноцитоз.
Некоторые примеры несолидных опухолей включают лейкемии, множественные миеломы и лимфомы. Некоторые примеры лейкемий включают острую миелоидную лейкемию (ОМЛ); хронический миелоидный лейкоз (ХМЛ); острый лимфоцитарный лейкоз (ОЛЛ) и хронический лимфоцитарный лейкоз (ХЛЛ), эритроцитарный лейкоз или моноцитарный лейкоз. Некоторые примеры лимфом включают такие заболевания, как: болезнь Ходжкина (лимфогранулематоз), неходжкинская лимфома или лимфома из клеток мантийной зоны.
В настоящее время предпочтительные типы опухолевых заболеваний выбирают из следующей группы: колоректальная карцинома; карцинома легких, включая немелкоклеточный рак легких (НМРЛ) и мелкоклеточный рак легких (МРЛ); карцинома молочной железы; меланома; карцинома яичников; карцинома шейки матки; рак поджелудочной железы; карцинома головы и шеи; карцинома желудочно-кишечного тракта; рак пищевода; печеночноклеточная карцинома; множественная миелома; почечноклеточная карцинома; рак простаты; неходжкинская лимфома; болезнь Ходжкина (лимфогранулематоз); лимфома из клеток мантийной зоны; саркома Капоши; плоскоклеточная карцинома; базальноклеточная карцинома; острая миелоидная лейкемия (ОМЛ); хронический миелоидный лейкоз (ХМЛ); острый лимфоцитарный лейкоз (ОЛЛ) и хронический лимфоцитарный лейкоз (ХЛЛ).
Следует отметить, что в соответствии с рекомендациями настоящего изобретения гуманизированное антитело согласно изобретению можно вводить до, во время или после начала химиотерапии и, возможно, лучевой терапии, как и любой их комбинации, т.е. до и во время, до и после, во время и после, или до, во время и после начала химиотерапии и, возможно, лучевой терапии. Например, введение антитела согласно изобретению, может быть осуществлено между 1 и 30 сутками до или после начала химиотерапии. В антитело можно дополнительно вводить между курсами химиотерапии.
При использовании способов комбинированной терапии согласно изобретению, антитела могут вводиться параллельно с химиотерапией, например по существу одновременно или согласованно. Также могут быть использованы другие схемы введения, например перекрывающиеся режимы или схемы, включающие альтернативное, последовательное или поочередное введение двух вариантов лечения.
Гуманизированное антитело согласно изобретению
В данном документе, термины "ВАТ" и "антитело ВАТ " используют в широком смысле для обозначения антител, идентичных или основанных на моноклональном антителе мыши, известном как mBAT-1, или его антиген-связывающем фрагменте. Моноклональное антитело mBAT-1 секретируется клеточной линией гибридомы, которые хранятся в Национальной коллекции культур микроорганизмов (Collection Nationale de Cultures de Microorganismes, CNCM), под номером доступа 1-1397, как указано в Патенте США №5,897,862. Также термины "ВАТ" и "антитело ВАТ" могут обозначать антитело, которое распознает такой же эпитоп антигена, как mBAT-1, например химерное антитело, описанное в Публикации заявки на патент США №2003/0026800. Термин антитело ВАТ также включает гуманизированные антитела, различные примеры которых описаны в WO03/099196 и Публикации заявки на патент США №2008/0025980. Термины "СТ-011", "hBAT" и "hBAT-1" используют в описании взаимозаменяемо для обозначения одного гуманизированного антитела согласно изобретению.
В общем виде вариабельный участок легкой цепи гуманизированного моноклонального антитела описывают формулой:
FRL1-CDRL1-FRL2-CDRL2-FRL3-CDRL3-FRL4,
где каждый FR независимо представляет собой каркасный участок антитела человека и каждый CDR независимо представляет собой участок, определяющий комплементарность, моноклонального антитела mBAT-1.
В общем виде вариабельный участок тяжелой цепи гуманизированного моноклонального антитела описывают формулой:
FRH1-CDRH1-FRH2-CDRH2-FRH3-CDRH3-FRH4,
где каждый FR независимо представляет собой каркасный участок антитела человека, и каждый CDR независимо представляет собой участок, определяющий комплементарность, моноклонального антитела mBAT-1.
В частных вариантах осуществления изобретения FR получены из вариабельного участка легкой цепи антитела TEL9 человека (SEQ ID NO:130) или их модификаций в определенных аминокислотных остатках.
Антитело TEL-9 человека было идентифицировано в различных библиотеках вариабельных (V) генов тяжелой (VH) и легкой (V каппа и V лямбда) цепей иммуноглобулинов, полученных из лимфоцитов периферической крови неиммунизированных доноров (Marks с сотр., J Mol Biol. 1991, 222:581-97). Было показано, что данное антитело специфически связывает антиген лизоцима яичного белка индейки (turkey egg-white, TEL).
Аминокислотные последовательности FR получены из вариабельных участков легкой цепи антитела TEL9 человека или их модификаций и могут быть выбраны из следующей группы: FRL1, [EIVLT QSPSS LSASV GDRVT ITC; SEQ ID NO:1]; FRL2, [W (F или Y) QQKPG KAPKL (W или L) IY; SEQ ID NO:2]; FRL3, [GVPSR FSGSG SGT (D или S) (Y или F) (С или Т) LTINS LQPED FATYY C; SEQ ID NO:3]; и FRL4, [FGGGT KLEIK; SEQ ID NO:4].
В частных вариантах осуществления изобретения FR получены из вариабельных участков тяжелой цепи антитела hsighv1295 человека (SEQ ID NO:146) или их модификаций в определенных аминокислотных остатках.
Антитело hsiggv1295 человека было выделено из стабильных гибридом и B-клеточных линий, трансформированных вирусом Эпштейна-Барра из синовиальной жидкости или периферической крови трех пациентов с диагнозом ревматоидный артрит и одного пациента с диагнозом системная красная волчанка (Fang с сотр., J Exp Med. 1994, 179:1445-56).
Аминокислотные последовательности FR получены из вариабельных участков тяжелой цепи антитела hsighvl295 человека или их модификаций и могут быть выбраны из следующей группы: FRH1, [Q (I или V) QLV QSGSE LKKPG ASVKI SCKAS GY (Т или S) F (Т или S); SEQ ID NO:5]; FRH2, [WV (R OR K) QAPGQ GL (Q или K) WMG; SEQ ID NO:6]; FRH3, [RF (V или A) FSLDT SV (N или S) TAYLQ ITSL (Т или N) AEDTG MYFC (V или А) (R или K); SEQ ID NO:7]; и FRH4, [WGQGT LVTVS S; SEQ ID NO:8].
В соответствии с различными вариантами осуществления изобретения вариабельный участок легкой цепи состоит по крайней мере из одной аминокислотной последовательности, выбранной из следующей группы: CDRL1 [SARSS VSYMH; SEQ ID NO:9]; CDRL2 [RTSNL AS; SEQ ID NO:10]; CDRL3 [QQRSS FPLT; SEQ ID NO:11], где CDR получены из антитела BAT-1 мыши, где нижние индексы "L" и "Н" относятся к участкам легкой и тяжелой цепи, соответственно.
В соответствии с различными вариантами осуществления изобретения вариабельный участок тяжелой цепи состоит по меньшей мере из одной аминокислотной последовательности, выбранной из следующей группы: CDRH1 [NYGMN; SEQ ID NO:12]; CDRH2 [WINTD SGEST YAEEF KG; SEQ ID NO:13]; CDRH3 [VGYDA LDY; SEQ ID NO:14].
В соответствии с различными вариантами осуществления изобретения данное гуманизированное антитело включает вариабельный участок легкой цепи, выбранный из группы: BATRκA (SEQ ID NO:15), BATRκB (SEQ ID NO:16), BATRκC (SEQ ID NO:17), и BATRκD (SEQ ID NO:18); и вариабельный участок тяжелой цепи, выбранный из группы: А (SEQ ID NO:20), BATRHB (SEQ ID NO:21), BATRHC (SEQ ID NO:22), BATRHD (SEQ ID NO:23) и BATRHE (SEQ ID NO:24).
В соответствии с другими вариантами осуществления изобретения гуманизированное антитело включает вариабельные участки, выбранные из группы: BATRHA/BATRκA (SEQ ID NO:20/SEQ ID NO:15), BATRHB/BATRκA (SEQ ID NO:21/SEQ ID NO:15), BATRHB/BATRκB (SEQ ID NO:21/SEQ ID NO:16), BATRHC/BATRκB (SEQ ГО NO:22/SEQ ID NO:16), BATRHB/BATRκD (SEQ ID NO:21/SEQ ID NO:18) и BATRHC/BATRκD (SEQ ID NO:22/SEQ ID NO:18).
В соответствии с другими предпочтительными вариантами осуществления изобретения вариабельные участки гуманизированного моноклонального антитела соответствуют BATRHC/BATRκD (SEQ ID NO:22/SEQ ID NO:18).
В одном варианте осуществления изобретения вариабельный участок тяжелой цепи гуманизированного антитела ВАТ соответствует SEQ ID NO:22, которая может кодироваться полинуклеотидной последовательностью SEQ ID NO:90.
В одном варианте осуществления изобретения вариабельный участок легкой цепи гуманизированного антитела соответствует SEQ ID NO:18, которая может кодироваться полинуклеотидной последовательностью SEQ ID NO:89. Аминокислотная и нуклеотидная последовательности гуманизированного антитела, пригодного для использования согласно изобретению, описаны в Публикации заявки на патент США №2008/0025980. Каркасные участки вариабельных участков тяжелой цепи и вариабельные участки легкой цепи антитела человека, пригодны для использования согласно изобретению включают, например, SEQ ID NOS: 111-128 и SEQ ID NOS: 130-144 соответственно.
Химиотерапия
Лекарственные препараты для химиотерапии разделяют на несколько групп в зависимости от оказываемого действия на раковые клетки, активность клетки или вовлекаемые процессы или специфические фазы клеточного цикла. Соответственно препараты для химиотерапии попадают в одну из следующих категорий: алкилирующие агенты, нитрозомочевины, антиметаболиты, антрациклины, ингибиторы топоизомеразы I и II, митотические ингибиторы, inter alia лекарственные препараты на основе платины, стероиды и антиангиогенные агенты.
Антиметаболиты, также называемые "аналоги нуклеозидов", замещают природные вещества в качестве структурных блоков молекул ДНК и, таким образом, изменяют функционирование ферментов, требуемых для метаболизма клетки и синтеза белка. В случае если они замещают нутриенты, требуемые для роста клеток, данные клетки в итоге подвергаются лизису. Если происходит замещение нуклеозида его нефункциональным аналогом, последний встраивается в ДНК и РНК, что в конечном итоге приводит к задержанию клеточного цикла и апоптозу путем подавления способности клетки синтезировать ДНК. Антиметаболиты являются специфичными в отношении стадий клеточного цикла и наиболее эффективно действуют в S-фазе клеточного деления, так как в первую очередь их действие направлено на клетки, осуществляющие синтез новой ДНК для формирования новых клеток. Токсичность, ассоциированная с данным типом лекарственных препаратов, наблюдается для быстро растущих и делящихся клеток. Примеры антиметаболитов включают антагонисты пуринов, антагонисты пиримидинов и антагонисты фолатов. Данные агенты повреждают клетки в S-фазе, и обычно их используют для лечения лейкемии, карциномы молочной железы, карциномы яичников и карциномы желудочно-кишечного тракта, а также при других типах рака. Специфические примеры антиметаболитов включают 5-фторурацил (также называемый 5-ФУ), капецитабин, 6-меркаптопурин, метотрексат, гемцитабин, флударабин и пеметрексед.
Химиотерапевтические агенты на основе платины перекрестно связывают ДНК разными способами, что подавляет клеточное деление путем митоза. Поврежденная ДНК запускает механизмы репарации ДНК, которые, в свою очередь, активируют апоптоз, в том случае если репарация невозможна. Наиболее заметными изменениями ДНК являются 1,2-внутринитевые поперечные сшивки пуриновых оснований, которые включают 1,2-внутринитевые d(GpG) аддукты, которые формируют приблизительно 90% аддуктов, и менее распространенные 1,2-внутринитевые d(ApG) аддукты. Формирование 1,3-внутринитевых d(GpXpG) аддуктов происходит, но быстро устраняется путем эксцизионной репарации нуклеотидов. Другие аддукты включают внутринитевые поперечные сшивки и нефункциональные аддукты, которые, как утверждают, вносят вклад в активность лекарственных препаратов на основе платины. Взаимодействие с клеточными белками, особенно с белками доменов HMG, также было предложено в качестве механизма, вовлекающегося в митоз, хотя это, вероятно, не является первичным способом действия. Химиотерапевтические препараты на основе платины включают цисплатин (также называемый цисплатинум или цис-диаминдихлоридоплатина II) (CDDP), карбоплатин и оксалиплатин. Цисплатин часто относят к алкилирующим агентам, хотя он не имеет алкильной группы и не может принимать участия в реакциях алкилирования. Корректно классифицировать данный агент как подобный алкилирующему агенту. Химиотерапевтические препараты на основе платины используют для лечения разных типов опухолевых заболеваний, включая саркомы, некоторые карциномы (например, мелкоклеточный рак легких и карциному яичников), лимфомы и эмбрионально-клеточные опухоли.
Митотические ингибиторы вовлекаются в деление клетки. Наиболее известным химиотерапевтическим агентом в данной категории является паклитаксел (также называемый Таксол®, "растительный алкалоид", "таксан" и "противомикротрубочковый агент"). При совместном применении с доцетакселем паклитаксел формирует категорию лекарственных препаратов - таксаны. Однако другие известные митотические ингибиторы, включают (но не ограничиваясь указанными) этопозид, винбластин и винкристин. Паклитаксел препятствует нормальному росту микротрубочек в процессе деления клеток, подавляя их функцию; это гиперстабилизирует структуру микротрубочек, что лишает клетку способности использовать гибкость цитоскелета. В частности, паклитаксел связывает β-субъединицу тубулина, «строительные блоки» микротрубочек, и связывание паклитаксела удерживает эти строительные блоки на месте. Полученный комплекс микротрубочка / паклитаксел не обладает способностью разбираться. Это оказывает нежелательное действие на функции клетки, поскольку укорачивание и удлинение микротрубочек (динамическая нестабильность) необходимы для их функционирования в качестве механизма для транспортировки других клеточных компонентов. Например, в процессе митоза микротрубочки позиционируют хромосомы в течение всего процесса репликации и последующего разделения в два дочерних ядра клетки. Более того, паклитаксел индуцирует механизм программируемой клеточной смерти (апоптоз) раковых клеток, связываясь с белком останавливающим апоптоз Вс1-2 (В-клеточная лейкемия 2) и таким образом останавливая его действие.
Другой группой лекарственных препаратов, взаимодействующих с ДНК, являются широко используемые при противораковой химиотерапии препараты из группы антрациклиновых антибиотиков, которая включает, inter alia, даунорубицин, доксорубицин (также называемый Адриамицин® и доксорубицина гидрохлорид), респиномицин D и идарубицин. Данные агенты взаимодействуют с ДНК путем интеркаляции и подавляют биосинтез макромолекул, таким образом, ингибируя передвижение фермента топоизомеразы II, которая раскручивает ДНК для транскрипции. Они стабилизируют комплекс топоизомеразы II после того, как произошел разрыв цепи ДНК для репликации, предотвращая восстановлению двойной спирали ДНК, и таким образом останавливают процесс репликации. Это широко применяют для лечения широкого спектра раковых заболеваний.
Алкилирующие антинеопластичекие агенты непосредственно атакуют ДНК. Они присоединяются алкильной группой к ДНК, образуя поперечные сшивки гуаниновых оснований в двойных цепях ДНК, что делает невозможным раскручивание и разделение цепей. Поскольку это необходимо при репликации ДНК, клетки не могут больше делиться. Данные лекарственные препараты действуют неспецифически. Циклофосфамид является алкилирующим агентом, однако также представляет собой высокоактивный иммуносупрессор.
Ингибиторы топоизомеразы I и II влияют на ферментативную активность топоизомеразы I и 2, соответственно, что со временем приводит к подавлению репликации и транскрипции ДНК. Примеры ингибиторов топоизомеразы I включают топотекан и иринотекан. Иринотекан представляет собой пролекарство, которое превращается в биологически активный метаболит 7-этил-10-гидрокси-кампотецин (SN-38) при действии карбоксилэстераза-превращающего фермента. Будучи в тысячу раз более активным, чем исходное вещество иринотекан, SN-38 подавляет активность топоизомеразы I, стабилизируя расщепляемый комплекс между топоизомеразой I и ДНК, что приводит к разрывам в молекуле ДНК, которые являются причиной подавления репликации ДНК и запускают апоптотическую гибель клетки. Поскольку продолжающийся синтез ДНК необходим для приведения в действие цитотоксического эффекта иринотекана, данный агент также классифицируют как агент, специфичный для S-фазы. Примеры ингибиторов топоизомеразы II включают этопозид и тенипозид.
Антиангиогенные агенты вовлекаются в образование новых кровеносных сосудов, что со временем приводит к "голоданию" опухоли. Примеры антиангиогенных агентов включают (не ограничиваясь указанными) моноклональное антитело бевацизумаб, допамин и тетратиомолибдат.
Фактор роста эндотелия сосудов (vascular endothelial growth factor, VEGF) представляет собой димерный гликопротеин размером 32-42 кДа, опосредующий вазодилятацию, повышенную проницаемость сосудов и митогенез клеток эндотелия. Дифференциальный сплайсинг экзонов гена VEGF приводит к образованию трех основных видов мРНК, кодирующих три секретируемые изоформы (нижний индекс обозначает число аминокислотных остатков): VEGF189, VEGP165, и VEGF121. Также описан ряд второстепенных вариантов сплайсинга (VEGF206, VEGF183, VEGF145 и VEGF148). Варианты полипептидов VEGF и их использование при лечении рака описаны, например, в WO/2003/012105.
Лучевая терапия
Источник радиационного излучения, который может быть использован в комбинации с гуманизированном антителом согласно изобретению, и химиотерапевтическим агентом (агентами) может быть как внешним, так и внутренним относительно пациента. При использовании внешнего относительно пациента источника радиационного излучения терапию называют наружной лучевой терапией (НЛТ). При использовании внутреннего относительно пациента источника радиационного излучения лечение называют брахитерапией (контактной лучевой терапией (КЛТ)).
Радиационное излучение применяют в соответствии с хорошо известными стандартными технологиями и с использованием стандартного оборудования, предназначенного для этих целей, например AECL Theratron и Varian Clinac.
Расстояние между внешним источником излучения и точкой входа в пациента может быть любым расстоянием, которое обеспечивает приемлемое соотношение между уничтожением клеток-мишеней и минимизированием нежелательных побочных эффектов. Обычно расстояние между внешним источником и точкой входа в пациента находится между 70 и 100 см.
Лечение способом КЛТ (брахитерапия) обычно проводят путем помещения источника радиационного излучения внутрь пациента. Обычно источник излучения помещают на расстоянии приблизительно 0-3 см от обрабатываемой ткани. Известные технологии включают внутритканевую, внутриполостную и поверхностную контактную лучевую терапию. Радиоактивные импланты ("семена") могут быть помещены внутрь пациента на временной или постоянной основе. Для перманентных имплантов используют несколько типов радиоактивных атомов, включая йод-125 и радон. Для временных имплантов используют несколько типов радиоактивных атомов, включая радий, цезий-137 и иридий-192. Дополнительно при брахитерапии используют америций-241 и золото-198.
Доза радиации зависит от ряда факторов, которые хорошо известны специалистам в данной области техники. Данные факторы включают такие, как орган, подвергаемый облучению, здоровые органы на пути радиационного излучения, которым может быть нанесен непреднамеренный вред, переносимость пациентом лучевой терапии и площадь тела, которую необходимо подвергнуть облучению. Обычно доза составляет от 1 Гр до 100 Гр, зачастую между 2 Гр и 80 Гр. Некоторые отдельные дозы составляют 35 Гр при лечении спинного мозга, 15 Гр - при лечении почек, 20 Гр - при лечении печени и 65-80 Гр при лечении простаты. Однако следует отметить, что настоящее изобретение не ограничено какой-либо определенной дозой. Дозу излучения определяет лечащий специалист в соответствии с конкретными факторами в данной ситуации, включая вышеперечисленные факторы.
Доза радиационного излучения для проведения брахитерапии может быть аналогичной указанной выше для проведения наружной лучевой терапии. Кроме вышеперечисленных факторов при определении дозы для проведения наружной лучевой терапии при определении дозы для КЛТ принимают во внимание природу используемого радиоактивного атома.
Композиции, введение и дозировки
Для применения способов согласно изобретению гуманизированное антитело может быть включено в состав общепринятым способом, используя один или более фармацевтически приемлемых носителей, стабилизаторов или вспомогательных веществ (сред) для формирования фармацевтической композиции, как известно в данной области техники, в частности, в отношении активных веществ белковой природы. Носитель (носители) являются "приемлемыми" с точки зрения совместимости с остальными компонентами композиции и не обладать вредными свойствами для реципиента. Пригодные носители обычно включают физиологический раствор или этанол, полиолы, такие как глицерин или пропиленгликоль.
Антитело может включаться в состав как в нейтральной форме, так и в форме соли. Фармацевтически приемлемые соли включают соли присоединения кислоты (сформированные свободными аминогруппами) и полученные из неорганических кислот, таких как соляная или фосфорная кислота, или органических кислот, таких как уксусная кислота, щавелевая кислота, винная кислота и малеиновая кислота. Соли, полученные за счет свободных карбоксильных групп, также могут быть получены из неорганических оснований, например гидроксидов натрия, калия, аммония, кальция или железа, и органических оснований, таких как изопропиламин, триметиламин, 2-этиламиноэтанол, гистидин и прокаин.
Композиция может быть составлена для внутривенного, внутримышечного, подкожного или внутрибрюшинного введения и традиционно включает стерильный водный раствор антитела, предпочтительно изотоничный крови реципиента. Такие составы обычно приготавливают путем растворения твердого активного ингридиента в воде, содержащей физиологически совместимые вещества, такие как хлорид натрия, глицин и подобные им, с добавлением буферных веществ для поддержания совместимого с физиологическими условиями значения рН с получением водного раствора и обеспечения указанного раствора стерильным. Они могут быть приготовлены в одно- или многодозовых контейнерах, например в запаянных ампулах или флаконах.
Такие композиции могут включать стабилизатор, например полиэтиленгликоль, белки, сахариды (например, трегалозу), аминокислоты, неорганические кислоты и их смеси. Стабилизаторы используют в водных растворах при подходящих концентрациях и значениях рН. Значение рН водного раствора должно быть доведено до интервала 5,0-9,0 единиц рН, предпочтительно интервала 6-8 единиц рН. При разработке состава антитела могут использовать антиадсорбционные агенты. Другие пригодные вспомогательные вещества обычно включают антиоксиданты, такие как аскорбиновая кислота.
Композиции могут быть составлены в виде препаратов с контролируемым высвобождением, что может быть достигнуто при использовании полимера, связывающего в комплекс или абсорбирующего белки. Подходящие полимеры для получения составов с контролируемым высвобождением включают, например, полиэфир, полиаминокислоты, поливинил, пирролидон, этиленвинилацетат и метилцеллюлозу. Другой возможный способ обеспечения контролируемого высвобождения представляет собой введение антитела внутрь частиц из полимерных материалов, таких как полиэфир, полиаминокислоты, гидрогели, сополимера молочной кислоты или этиленвинилацетата. Альтернативно вместо введения указанных агентов в полимерные частицы можно заключить такие материалы в микрокапсулы, полученные, например, с использованием технологий коацервации или межфазной полимеризации, например капсулы из гидроксиметилцеллюлозы, или желатиновые микрокапсулы, или капсулы из полиметилметакрилата соответственно, или использовать коллоидные системы для доставки лекарственных препаратов, такие как липосомы, альбуминовые микросферы, микроэмульсии, наночастицы, нанокапсулы или макроэмульсии.
Если необходимы пероральные препараты, то композиции могут быть составлены с такими носителями, как лактоза, сахароза, крахмал, тальк, стеарат магния, кристаллическая целлюлоза, метилцеллюлоза, карбоксиметилцеллюлоза, глицерин, альгинат натрия или гуммиарабик.
Предпочтительно парентеральное введение гуманизированного антитела согласно изобретению, обычно путем внутривенной инфузии. Введение также могут осуществлять внутрибрюшинно, перорально, подкожно или внутримышечно. Антитела обычно вводят в интервале концентраций от приблизительно 0,1 до приблизительно 20 мг/кг массы пациента, обычно от приблизительно 0,5 до приблизительно 10 мг/кг, и часто от приблизительно 1 до приблизительно 5 мг/кг. В связи с этим предпочтительно использовать антитела с периодом полураспада в кровотоке по меньшей мере 12 часов, предпочтительно по меньшей мере 4 дней, наиболее предпочтительно до 21 дня. Ожидаемые значения периода полураспада в кровотоке химерных и гуманизированных антител составляют до четырех и до 14-21 дня соответственно. В некоторых случаях может быть полезно ввести большую ударную дозу, после которой вводить периодические поддерживающие дозы (например, еженедельно) в течение периода лечения. Антитела также могут быть доставлены с использованием систем медленной доставки, системы насосов и других известных систем доставки для продолжительной инфузии. Режим дозирования может варьироваться для обеспечения желаемого уровня циркулирования конкретного антитела на основании его фармакокинетических свойств. Таким образом, дозы рассчитывают так, чтобы поддерживать желаемую концентрацию (уровень циркулирования) терапевтического агента.
Обычно эффективную дозу определяют исходя из активности терапевтической комбинации и состояния субъекта, а также на основании массы тела или площади поверхности субъекта, который подвергается лечению. Размер дозы и режим дозирования также определяют с учетом наличия, природы и степени любых нежелательных побочных эффектов, которые сопровождают применение каждого агента комбинации согласно изобретению у конкретного субъекта. При определении эффективного количества терапевтической композиции для введения специалист должен оценивать inter alia уровень активного вещества в плазме крови, токсичность и прогрессирования заболевания.
В различных вариантах осуществления комбинации способов согласно изобретению гуманизированное антитело и химиотерапевтический агент можно вводить в соответствии с любым числом схем лечения, также называемыми "схемами дозирования " и "режимами введения", относящимся к частоте введения и порядку введения каждого активного агента. Например, гуманизированное антитело и химиотерапевтический агент могут быть введены по существу одновременно, т.е. в одно время, например, с использованием комбинированных дозированных форм или отдельных дозированных форм. Данная форма введения также может быть названа "сопутствующим" введением. Сопутствующее введение относится к введению активных веществ в течение одного общего периода времени, например в тот же день (дни), но не обязательно в одно время. Например, одно из активных веществ требуется принимать во время еды, тогда как остальные нужно принимать натощак. Альтернативное применение включает введение одного агента в течение определенного периода времени, например в течение курса из нескольких дней или недели, после чего следует введение другого агента в течение последующего идентичного периода времени, и затем данная схема повторяется в течение одного или более циклов. Последовательное или поочередное применение включает введение одного агента в течение первого периода времени с использованием одной или более доз, после чего следует введение второго агента в течение второго периода времени с использованием одной или более доз. Также может быть использован режим перекрывания, который включает введение активных агентов в разные дни в течение одного периода лечения, необязательно в соответствии с регулярной последовательностью. Также могут быть использованы разные варианты данных общих схем в соответствии с используемыми агентами и состоянием субъекта.
В некоторых частных случаях может быть полезно использование специфической последовательности введения, например одного перед другим. Например, как показано в данном документе (Фиг.5), нежелательные побочные явления дакарбазина оказывают влияние на активность антитела при совместном применении, но не в случае введения через 24 часа после гуманизированного антитела.
После общего описания настоящего изобретения изложенные принципы будут более понятными при обращении к нижеследующим примерам, которые представлены для пояснения и не ограничивают настоящего изобретения.
Примеры
Пример 1. Функциональный тест in vitro
Функциональный тест основан на способности hBAT-1 повышать выживаемость лимфоцитов мыши и лимфоцитов человека в культуре. В данном Примере проводили оценку влияния hBAT-1 на повышение выживаемости лимфоцитов как отдельно, так и в комбинации с химиотерапевтическими лекарственными препаратами; полученные результаты выражали в % разности выживаемости клеток или по площади под кривой эффекта дозы (AUC, выраженная в % разности × мкг/мл). Химиотерапевтический агент применяли одновременно или через 24 часа после лечения hBAT-1 в указанных концентрациях. Влияние химиотерапевтических агентов оценивали в функциональном тесте, включающим 5-ФУ (Фиг.1, 2 и 7), SN - 38 (активное производное иринотекана) (Фиг.3 и 4), цисплатин, оксалиплатин, таксол (паклитаксел) и дакарбазин (Фиг.5 и 7), цитарабин, циклофосфамид и доксорубицин (Фиг.6).
Полученные результаты указывают на то, что специфические агенты (например, 5-ФУ, цисплатин, оксалиплатин, паклитаксел и цитарабин) не оказывают нежелательного побочного действия на активность hBAT-1 в лимфоцитах мышей. Более того, при одновременном (цисплатин) или последовательном применении (5-ФУ и паклитаксел) с hBAT-1, наблюдали синергетический эффект, который выражался в повышении значений активности от 20% до 30% (% разности выживаемости клеток и AUC). При использовании только химиотерапевтического агента не наблюдали активности в повышении выживаемости лимфоцитов при проведении данного теста (Фиг.1C). Синергические результаты были получены с использованием изолированных CD4+ лимфоцитов человека и показывали, что последовательное лечение 5-ФУ или цисплатином в комбинации с hBAT приводит к двукратному повышению активности (% разности выживаемости клеток) по сравнению с активностью антитела, используемого отдельно (Фиг.7). Полученные результаты также позволяют предположить, что определенные химиотерапевтические агенты (например, SN - 38; циклофосфамид) могут не быть пригодными для использования в комбинации с гуманизированными антителами ВАТ, поскольку они не приводят к повышению выживаемости клеток при использовании в комбинации с hBAT-1 в культуре лимфоцитов мыши. Кроме того, определенные химиотерапевтические агенты (например, дакарбазин) могут быть пригодными только при последовательном введении (Фиг.3-5).
Пример 2. Комбинированная терапия для лечения колоректальной карциномы
Колоректальные карциномы (опухоли СТ26) индуцировали путем подкожной инъекции суспензии клеток СТ26 в количестве 106 клеток/мышь (n=6). День введения инъекции обозначен как день 0. 5-ФУ в количестве 20 мг/кг вводили внутрибрюшинно (i.p.) в дни 6-9, 15-17, 22-24 и 29-31, 36-38 и 43-45. hBAT-1 в количестве 10 мг/мышь вводили внутривенно (i.v.) в дни 10, 18, 25, 32 и 39 (Фиг.8-10). В случае рецидива заболевания после полного выздоровления (наблюдали только в группе животных, подвергнутых комбинированной терапии) продолжали лечение 5-ФУ в количестве 20 мг/кг в дни 73-74, 77-80, 85-87, 92-93 и hBAT-1 в количестве 10 мг/мышь внутривенно в дни 81 и 88.
При проведении исследования размеров опухоли после проведения единичного курса лечения объемы опухоли измеряли через день в дни с 4 по 16 после инокуляции опухолевых клеток. Полученные результаты указывают на то, что комбинированная терапия с использованием 5-ФУ является более эффективной по сравнению с применением 5-ФУ или hBAT-1 по отдельности (Фиг.8).
При проведении исследования размеров опухоли после проведения трех альтернативных курсов лечения, объемы опухоли измеряли через день в дни с 4 по 28. Полученные результаты указывают на то, что комбинированная терапия с использованием антитела hBAT-1 и химиотерапевтического агента 5-ФУ не только является более эффективной по сравнению с монотерапией 5-ФУ, но также сопровождается синергетическим эффектом повышения активности (Фиг.9).
При проведении исследования общей выживаемости определяли процент выживаемости, полученные данные представлены на Фиг.10 начиная с дня 28 и далее. Полученные результаты четко показывают, что среди мышей, подвергнутых комбинированной терапии, процент выживаемости значительно выше, чем среди мышей, подвергнутых монотерапии с использованием hBAT-1 или 5-ФУ, что приводит к стойкому полному выздоровлению приблизительно 17% мышей.
Пример 3. Комбинированная терапия для лечения меланомы
Мышам (n=7) подкожно вводили клетки В 16 меланомы в количестве 5×105 клеток/мышь. День инокуляции обозначен как день 0. 5-ФУ вводили внутрибрюшинно в количестве 50 мг/кг в дни 1-4 и 7-8. Группе мышей, подвергнутых комбинированной терапии, вводили внутривенно единичную дозу hBAT-1 в количестве 10 мг/мышь в день 10.
Процент выживаемости определяли начиная с 8 дня. У мышей, подвергнутых комбинированной терапии, процент выживаемости был значительно выше, чем у мышей, подвергнутых лечению высокими дозами 5-ФУ (Фиг.11).
Напротив, применение комбинированного лечения с использованием схемы последовательного введения, где введение гуманизированного антитела проводили после окончания 9-дневных циклов введения 5-ФУ на уровне дозолимитирующей токсичности (DLT) (50 мг/кг/день), что привело к повышению выживаемости мышей с экспериментальной моделью меланомы. Полученные результаты очевидно позволяют предположить, что применение комбинированной терапии повышает переносимость уровней DLT 5-ФУ.
Пример 4. Комбинированная терапия с использованием иринотекана (1)
Мышам (n=6) подкожно вводили клетки колоректальной карциномы (СТ26 опухоли) в количестве 106 клеток/мышь. День инокуляции обозначен как день 0. Иринотекан вводили i.p. в количестве 100 мг/кг в дни 7 и 15. hBAT-1 вводили внутривенно i.v. в количестве 10 мг/мышь на 10 день (Фиг.12).
При проведении исследования размеров опухоли после проведения единичного курса лечения объемы опухоли измеряли через день в дни с 4 по 18. Полученные результаты указывают на то, что комбинированная терапия с использованием антитела hBAT-1 и иринотекана является такой же эффективной, как монотерапия с использованием иринотекана, но менее эффективной, чем монотерапия с использованием hBAT-1 (Фиг.12).
Пример 5. Комбинированная терапия с использованием иринотекана (2)
Мышам (n=6) подкожно вводили клетки колоректальной карциномы (СТ26 опухоли) в количестве 106 клеток/мышь. День инокуляции обозначен как день 0. Иринотекан вводили i.p. в количестве 100 мг/кг в дни 7 и 15. hBAT-1 вводили внутривенно в количестве 10 мг/мышь на 10 день (Фиг.13).
Процент выживаемости определяли начиная с 16 дня. Полученные результаты показывают, что у мышей, подвергнутых комбинированной терапии, процент выживаемости сравним с процентом выживаемости мышей, подвергнутых монотерапии с использованием иринотекана, но ниже, чем у мышей, подвергнутых монотерапии с использованием hBAT-1 (Фиг.13).
Пример 6. Комбинированная терапия с использованием оксалиплатина
Мышам (n=6) подкожно вводили клетки колоректальной карциномы (СТ26 опухоли) в количестве 106 клеток/мышь. День инокуляции обозначен как день 0. Оксалиплатин вводили i.p. в количестве 1 мг/кг в дни 4, 7-10, 14-17, 22-24 и 29-31. hBAT-1 вводили внутривенно в количестве 10 мг/мышь в дни 11, 18, 25 и 32 (Фиг.14-15).
При проведении исследования размеров опухоли объем опухолей измеряли через день в дни с 4 по 23 после инокуляции. Полученные результаты указывают на то, что применение комбинированной терапии с использованием оксалиплатина более эффективно по сравнению с применение только оксалиплатина (Фиг.14).
При проведении исследования общей выживаемости процент выживаемости определяли начиная с 15 дня. Полученные результаты четко показывают, что у мышей, подвергнутых комбинированной терапии, процент выживаемости значительно выше, чем у мышей, подвергнутых монотерапии с использованием оксалиплатина, и приводит к стойкому полному выздоровлению у приблизительно 20% мышей (Фиг.15).
Мышам (n=3), которые были вылечены с применением комбинированной терапии с использованием hBAT-1 и оксалиплатина в течение 2-5 месяцев, повторно подкожно вводили клетки колоректальной карциномы (СТ26 опухоли) в количестве 10 клеток/мышь. Клетки колоректальной карциномы также вводили мышам, не подвергавшимся такому лечению ранее (naive) такого же возраста, используемым в качестве контроля (n=6). День инокуляции обозначен как день 0 (Фиг.16). Перед повторной инъекцией клеток CRC (заражением) мышам, проводили оценку ранее подвергнутые лечению мышей для полного клиренса уровня hBAT-1 в сыворотке крови с использованием способа специфической ELISA.
При проведении исследования размеров опухоли, объем опухолей измеряли через день в дни с 4 по 23 после инокуляции. У мышей, ранее вылеченных с применением комбинированной терапии с использованием hBAT-1 и оксалиплатина, не наблюдали развития опухоли в течение 2 месяцев последующего наблюдения, тогда как у мышей из контрольной группы в течение нескольких дней развитие опухоли было обнаружено у всех животных (Фиг.16А).
При проведении исследования общей выживаемости процент выживаемости определяли начиная с 21 дня после повторной инокуляции. Мыши, которым впервые вводили опухолевые клетки (CRC) умерли в течение 35 дней, тогда как у мышей, ранее вылеченных с применением комбинированной терапии с использованием hBAT-1 и оксалиплатина, не наблюдали роста опухоли, рецидива опухоли, и смертности в течение более чем 72 дней (Фиг.16В).
Мышам (описанные на Фиг.16, n=2), которые были вылечены с применением hBAT-1 и оксалиплатина и оказались устойчивыми к повторному заражению CRC в течение примерно 3 месяцев, вводили подкожно клетки опухоли карциномы молочной железы (опухоли 4Т1) в количестве 106 клеток/мышь. Данным мышам клетки опухоли вводили подкожно в участок, отличающийся от 1-го и 2-го (повторное заражение CRC) участков инъекции клеток CRC. Клетки 4Т1 также вводили мышам, не подвергавшимся такому лечению ранее (naive), такого же возраста (n=6). День инокуляции обозначен как день 0 (Фиг.17).
При проведении исследования размеров опухоли объем опухолей измеряли через день в дни с 3 по 21 после инокуляции. Развитие карциномы молочной железы наблюдали у мышей из обеих групп (Фиг.17А). Полученные результаты четко показывают, что мыши, вылеченные с применением комбинированной терапии hBAT-1 и оксалиплатина и обладающие приобретенной полной защитой против развития колоректальной карциномы (Фиг.16А), не обладают защитой против развития карциномы молочных желез (Фиг.17А).
При проведении исследования общей выживаемости процент выживаемости определяли начиная с 21 дня после повторной инокуляции. Мыши из обеих групп умерли в течение периода времени от 28 до 35 дней по причине развития карциномы молочных желез, что указывает на то, что мыши, обладающие продолжительной устойчивостью против рецидива CRC не обладают полной защитой от развития опухоли другого типа, например, карциномы молочных желез. Поскольку все мыши, ранее подвергнутые лечению, были протестированы на полную элиминацию циркулирующего в сыворотке крови антитела согласно изобретению, вероятно, что приобретенная специфическая устойчивость к развитию колоректальной карциномы является результатом не активной терапии, а скорее, ответной реакции иммунной памяти, индуцированной ранее проведенным лечением с использованием антитела согласно изобретению, и оксалиплатина.
В целом, применение комбинированной терапии с использованием антитела согласно изобретению и специфических химиотерапевтических агентов, таких как 5-ФУ или оксалиплатин, при переменном режиме введения приводит к повышению противоопухолевой активности, что подтверждается снижением роста опухоли и повышением выживаемости мышей с опухолью. Неожиданным образом, у мышей, подвергнутых комбинированной терапии, наблюдали полное стойкое выздоровление и, в случае использования оксалиплатина, даже приобретение защитной памяти против рецидива опухоли, что было показано при повторном заражении специфической опухолью (CRC).
Пример 7. Влияние СТ-011 на Т - эффекторные / Т - клетки памяти человека
Активность hBAT-1 (СТ-011) оценивали при проведении теста, основанного на жизнеспособности лимфоцитов человека. Эффекторные клетки / клетки памяти CD4+CD45RO+ и нативные (naive) CD4+CD45RO - лимфоциты обрабатывали hBAT в концентрации 1 мкг/мл с последующей инкубацией в течение 72 часов и 96 часов. Полученные результаты выражали как % разности выживаемости клеток (Фиг.18).
Полученные результаты четко указывают на то, что СТ-011 значительно влияет на повышение выживаемости эффекторных клеток / клеток памяти CD4+CD45RO+ лимфоцитов человека, но не нативных (naive) CD4+CD45RO - лимфоцитов. Данные об активности СТ-011 по обеспечению жизнеспособности предшественников клеток памяти находятся в соответствии с результатами, полученными in vivo, которые указывают на то, что СТ-011 индуцирует формирование иммунной памяти против рецидива опухоли.
Пример 8. Клиническое испытание фазы I гуманизированного моноклонального антитела СТ-011
Введение
Целью данного исследования является проведение оценки значений дозолимитирующей токсичности (DLT, ДЛТ), определение максимальной переносимой дозы (MTD, МПД) и изучение фармакокинетических параметров СТ-011 при единичном введении пациентам с диагнозом запущенные гематобластозы (поздняя стадия). Полное описание проведенного исследования см. Berger с сотр. (Clin. Cancer Res. 2008; 14(10) May 15, 2008).
Пациенты и способы
В данное исследование включали пациентов с диагнозом, который соответствовал одному из нижеперечисленных гемобластозов: острый лимфоцитарный лейкоз (ОЛЛ), хронический лимфоцитарный лейкоз (ХЛЛ), неходжкинская лимфома (НХЛ), лимфома Ходжкина (ХЛ) или множественная миелома (ММ) в поздней стадии после проведения химиотерапии и/или трансплантации стволовых клеток (SCT, ТСК). Пациенты допускались до участия в данном исследовании при условии, что они соответствовали критериям, установленным Berger et al.
Важно заметить, что данные критерии включали: не менее 4 недель после трансплантации стволовых клеток (ТСК) или 1 недели после инфузии донорских лимфоцитов (DLI, ИДЛ); ожидаемая продолжительность жизни >3 месяцев. Исключали пациентов, которые или получали или еще не отвечали на действия иммуносупрессивной терапии, или с диагнозами аутоиммунных нарушений. Исключение было сделано для лечения с применением гидроксимочевины у пациентов с диагнозом ОЛЛ (AML), которым было разрешено принять участие в данном исследовании. Было запрещено применение сопутствующего противоракового лечения (химиотерапии и иммунотерапии), которое соответственно должно было быть закончено по меньшей мере за 4 недели до введения СТ-011.
В данном исследовании принимали участие 17 пациентов. Один из пациентов, получавший самую низкую дозу препарата (0,2 мг/кг), был повторно принят для участия в исследовании через 5 месяцев после первого введения самой высокой дозы (3,0 мг/кг) в качестве благотворительно-испытательного лечения в целом для 18 типов лечения. Общее количество СТ-011 определяли на основании планового дозирования (мг/кг) и массы тела. Инфузию проводили пошаговым способом с повышением скорости потока с 50 мл/час до 100 мл/час, и все пациенты получали предварительное лекарственное средство до начала инфузии, состоящее из болеутоляющего средства (парацетамол), кортикостероидного препарата (гидрокортизона 100 мг) и антигистаминный препарат (фенерган). Начальная доза составляла 0,2 мг/кг, которая была в несколько десятков раз более низкой, чем самая высокая доза, проверенная при проведении токсикологических исследований у низших приматов и мышей на основании дозы, эквивалентной для человека. В дальнейшем применяли дозы 0,6 мг/кг; 1,5 мг/кг; 3 мг/кг, и 6 мг/кг. Повышение дозы с одного уровня на другой осуществляли только после оценки параметров всех пациентов, получавшие предыдущую дозу, в течение по меньшей мере 7 дней после введения дозы.
Токсичность оценивали в соответствии с Общими критериями токсичности Национального института рака (CTCAE V2) и по интенсивности (т.е., слабо выраженная, умеренная, острая). ДЛТ определяли как дозу, которая индуцирует любое проявление токсичности уровня 3 или уровня 4 у одного или более пациентов, или любое проявление токсичности уровня 2 по меньшей мере у 2/3 или 3/6 пациентов. Развитие нежелательных явлений, которые не были отнесены к СТ-011, не считали связанными с токсичностью в отношении повышения дозы и правил МПД.
После введения лекарственного препарата проводили проверку пациентов на безопасность, включая развитие нежелательных явлений и оценку клинических и лабораторных ответных реакций через 24 часа, 48 часов, и в дни 7, 14, и 21.
Отбор образцов и показателей, используемых для оценки клинических реакций, анализа фармакокинетических параметров, активации иммунной системы и статистического анализа проводили согласно Berger с сотр. (2008).
Результаты
Основные характеристики пациентов, принимавших участие в данном исследовании (n=17), перечислены в Таблице 1. Пациенту 003, изначально получавшему дозу 0,2 мг/кг, потребовалось повторное благотворительно-испытательное лечение, в виде повторного лечения с использованием дозы 3 мг/кг. Интервал в 5 месяцев между первым и вторым этапом лечения, разные схемы лечения были проанализированы у отдельных пациентов. Таким образом, число введений СТ-011, используемых для проведения анализа, составило 18.
| Таблица 1 | ||||||||
| Характеристики пациентов | ||||||||
| Индентификацнонный номер | Доза (мг/кг) | Возраст | Пол | Заболевание | Классификация/ Тип | Стадия | Восточная объединенная группа онкологов, уровень заболевания ECOG | Лечение, предшествующее терапии СТ-011 |
| 001 | 0,2 | 64 | ОЛЛ | М4-миеломоно-цитарный | NR | 2 | Аллогенная ТСК | |
| 002 | 0,2 | 62 | НХЛ | ОЛЛ | III | 3 | Лучевая терапия | |
| 003 | 0,2 | 73 | ОЛЛ | М4-миеломоно-цитарный | NR | 0 | Гранулоцитарный колониестимулирующий фактор (G-CSF) Эритропоэтин Переливание крови | |
| 004 | 0,6 | 60 | Ж | НХЛ | ДККЛ | IV | 1 | Лучевая терапия |
| 005 | 0,6 | 52 | М | ХЛЛ | С | 2 | Лучевая терапия | |
| 006 | 0,6 | 26 | Ж | HD | IVB | 0 | Лучевая терапия | |
| 007 | 1,5 | 58 | Ж | ХЛЛ | С | 2 | Митоксантрон | |
| 008 | 1,5 | 68 | Ж | ХЛЛ | А | 1 | Хлорамбуцил | |
| 009 | 1,5 | 53 | М | ОЛЛ | М2-миелоцитарный | NR | 1 | Аллогеннаятек |
| 010 | 3,0 | 33 | Ж | ОЛЛ | М4 миеломоно-цитарный | NR | 1 | Аллогеннаятек |
| 011 | 3,0 | 20 | М | ОЛЛ | M1 миелоцитарный | NR | 0 | Митоксантрон + цитозар |
| 012 | 3,0 | 78 | М | MDS | ХМЛ | NR | 2 | Гидроксимочев ина, Талидомид |
| 013 | 6,0 | 65 | М | ОЛЛ | М4 миеломоно-цитарный | NR | 2 | Аллогеннаятек |
| 014 | 3,0 | 40 | НХЛ | ДККЛ | I | 4 | Аутологичнаятек | |
| 015 | 3,0 | 56 | НХЛ | Фолликулярный Лимфома | II | 1 | Отсутствует | |
| 016 | 3,0 | 73 | ОЛЛ | М4 миеломоно-цитарный | R | 1 | СТ-011 | |
| 017 | 6,0 | 78 | ММ | IgG; Каппа | А | 1 | Отсутствует | |
| 018 | 6,0 | 72 | ОЛЛ | М4 миеломоно-цитарный | R | 1 | Гидроксимочев ина | |
Сокращения: ОЛЛ - острый лимфоцитарный лейкоз, ХМЛ - хронический миеломоноцитарный лейкоз, ДККЛ - диффузная крупноклеточная В-клеточная лимфома; FAB классификация - French, American и British (французский, американский и британский); M1, M2, М4 в соответствии с FAB- классификацией; NR - незначимый; ТСК - трансплантация стволовых клеток.
При проведении данного исследования отсутствует ДЛТ. Показаны безопасность и хорошая переносимость СТ-011 без проявления токсичности, связанной с лечением. Отсутствует МПД единичной дозы.
При проведении данного исследования 61% (11 из 18) пациентов отмечали развитие нежелательных явлений (АЕ), наиболее частым из которых была диарея, но решено, что развитие данной нежелательной реакции не было связано с лечением СТ-011.
Наблюдали развитие четырех случаев нежелательных явлений, которые закончились смертью пациентов и проявившихся у пациентов с диагнозом ОЛЛ. При проведении клинического анализа показано, что причиной смерти указанных пациентов был приступ устойчивой лейкемии, что не связано с исследованием лекарственным препаратом.
Через 21 день после начала исследования не наблюдали изменений среднего процентного значения бластных клеток в периферической крови у пациентов с диагнозом ОЛЛ за исключением одного пациента с диагнозом ОЛЛ (снижение числа бластных клеток в периферической крови с 50% до 5%). Кроме того, не наблюдали изменений параметров заболевания в течение 21 для исследования у 2 пациентов с диагнозом ХЛЛ, у 4 пациентов с диагнозом НХЛ и у одного пациента с диагнозом Множественная Миелома.
Общая выживаемость всех пациентов (n=18) в течение 21 дня составила 76%, с 95% доверительным интервалом 48% - 90%. Не отмечено различий в средних значениях времени выживания в зависимости от применяемой дозы.
Проводили наблюдение выживаемости пациентов по прошествии 21 дня исследования. Среднее время выживания при проведении исследования составило 25±27 недель в интервале от 1,7 до более 77 недель. Результаты данного исследования позволяют предположить, что у 6 пациентов наблюдали заметную реакцию на лечение, которая сопровождалась продлением времени выживания в среднем но меньшей мере 60 недель. Данные 6 "ответивших на лечение" пациентов представлены в Таблице 2. У одного пациента, 015, получавшего дозу четвертого уровня 3,0 мг/кг наблюдали полную ремиссию. Данному пациенту был поставлен диагноз фолликулярная лимфома III стадии, включая узлы ниже и выше диафрагмы. Данный пациент ранее не получал никакого лечения указанного заболевания. При проведении компьютерной томографии при периодической проверке через 10 после лечения с использованием СТ-011 наблюдали полное исчезновение опухолевых образований. Интересно отметить, что данный пациент не получал никакого дальнейшего лечения между лечением с использованием СТ-011 и проверкой по истечении 10 месяцев. У данного пациентов наблюдали стойкое выздоровление через 68 недель после завершения лечения с использованием СТ-011. Одну минимальную ответную реакцию наблюдали у пациента с диагнозом ОЛЛ, получавшим СТ-011 в концентрациях 0,2 и 3 мг/кг). У данного пациента наблюдалась прогрессия 61 неделю после получения СТ-011. У четырех пациентов наблюдали стабильное течение заболевание: один пациент с диагнозом болезнь Ходжкина получал СТ-011 в количестве 0,6 мг/кг имел стабильное течение заболевания в течение 35 недель. Два пациента с диагнозом ХЛЛ получали антитело в количестве 0,6 мг/кг и в количестве 1,5 мг/кг и показывали стабильное течение заболевания в течение 36 недель и более 78 недель соответственно. Пациент с диагнозом ММ получавший СТ-011 в количестве 6,0 мг/кг, показывал стабильное течение заболевание в течение более 60 недель.
| Таблица 2 | ||||
| Клинические реакции, полученные при проведении исследования на период отслеживания. | ||||
| Заболевание (Номер пациента) | Доза (мг/кг) | Наблюдения | Общая выживаемость (недели) | Комментарии |
| НХЛ (015) | 3,0 | ПОР | >68 | Фолликулярная В-клеточная лимфома с формированием крупных опухолей в узлах выше и ниже диафрагмы и в средостении Предыдущее лечение данного заболевания отсутствует Исчезновение опухолевых образований на КТ замечено через 10 месяцев после использования СТ-011 |
| ХЛЛ (008) | 1,5 | СТЗ | >78 | Стадия А по Binet с проникновением в костный мозг и уровень заболевания 3 согласно классификации Восточной объединенной группы онкологов Лейкеран (хлорамбуцил) приблизительно за 2 года до использования СТ-011 Стабильное течение заболевания >17 месяцев |
| ХЛЛ (005) | 0,6 | СТЗ | 36 | Стадия С по Binet, крупные опухолевые образования, устойчивы к химиотерапии, лучевой терапии и аллогенной ТСК Стабильное течение заболевания в течение 8 месяцев до ухудшения |
| Болезнь Ходжкина (006) | 0,6 | СТЗ | 35 | Классификация IV В; устойчивое заболевание, неудачное аутологичная ТСК и лучевая терапия Стабильное течение заболевания в течение 8 месяцев до ухудшения |
| MM (017) | 6,0 | СТЗ | >60 | Обычного типа, IgG каппа на Стадии IA и уровень заболевания 1 согласно классификации Восточной объединенной группы онкологов Предыдущее лечение данного заболевания отсутствует Стабильное течение заболевания в течение >13 месяцев |
| ОЛЛ (003/016) | 0,2/3,0 | МР | 61 | Введение второй дозы через 5 месяцев после введения первой дозы· Трансфузия тромбоцитов - независимо в течение 9 месяцев Снижение числа периферических бластных клеток (с 50% до 5%) при получении первой дозы |
| ПОР = полная ответная реакция; СТЗ = стабильное течение заболевания; МР = минимальная реакция. | ||||
Обсуждение и выводы
Общая выживаемость всех пациентов в течение периода лечения составила 76% и при последующем наблюдении по прошествии 21 дней данного исследования средняя выживаемость составила 25 недель. При том обстоятельстве, что большинство пациентов находились на поздней стадии заболевания, удивительным и неожиданным оказалось то, что у шести пациентов наблюдали признаки клинического улучшения и пролонгированный период выживаемости, который в среднем составил 60 недель.
Среднее значение t½ CT - 011 находилось в интервале от 217 часов до 410 часов (от 9 до 17 дней) в соответствии с результатами наблюдений по другим моноклональным антителам у человека. Важно заметить, что средние значения t½ для шести пациентов с выраженными клиническими результатами (Таблица 2) были несколько выше, чем у остальных пациентов. Принимая во внимание продолжительность реакции, которая у данных шести пациентов в среднем составила 60 недель, и фармакокинетические параметры для данного антитела, по которым наивысшее значение времени полужизни составило 410 часов, вероятно, что у некоторых пациентов индуцируются механизмы опухоль-специфической иммунной памяти, что приводит к продолжительному противоопухолевой иммунной реакции, которая сохраняется в течение продолжительного периода времени после элиминации антитела из кровотока.
Последующее описание специфических вариантов осуществления изобретения содержит достаточно полное описание сущности настоящего изобретения и с использованием современных знаний специалист способен легко модифицировать и/или адаптировать данные специфические варианты осуществления изобретения для различного применения без проведения дополнительной экспериментальной работы и без отклонения от центральной концепции. Таким образом, данные адаптации и модификации включены в изобретение и находятся в числе эквивалентов описанных вариантов осуществления изобретения. Следует понимать, что стиль или терминология используются для описания изобретения, но не для его ограничения. Могут быть внесены изменения в средства, материалы и стадии процесса, необходимые для осуществления различных действий, описываемых в настоящем документе, без отклонения от сущности настоящего изобретения.
Claims (11)
1. Применение (i) гуманизированного моноклонального антитела или его фрагмента, содержащего вариабельную область легкой цепи, выбранную из группы, состоящей из: BATRκA (SEQ ID NO: 15), BATRκB (SEQ ID NO: 16), BATRκC (SEQ ID NO: 17)и BATRκD (SEQ ID NO: 18), и вариабельную область тяжелой цепи, выбранную из группы, состоящей из: BATRHА (SEQ ID NO: 20), BATRHB (SEQ ID NO: 21), BATRHC (SEQ ID NO: 22), BATRHD (SEQ ID NO: 23) и BATRHE (SEQ ID NO: 24) в комбинации с (ii) по меньшей мере одним химиотерапевтическим агентом, выбранным из лекарственных средств на основе платины, антиметаболитов или паклитаксела, для лечения опухолевого заболевания.
2. Применение (i) гуманизированного моноклонального антитела или его фрагмента, содержащего вариабельную область легкой цепи, выбранную из группы, состоящей из: BATRκA (SEQ ID NO: 15), BATRκB (SEQ ID NO: 16), BATRκC (SEQ ID NO: 17)и BATRκD (SEQ ID NO: 18), и вариабельную область тяжелой цепи, выбранную из группы, состоящей из: BATRHА (SEQ ID NO: 20), BATRHB (SEQ ID NO: 21), BATRHC (SEQ ID NO: 22), BATRHD (SEQ ID NO: 23) и BATRHE (SEQ ID NO: 24), в комбинации с (ii) по меньшей мере одним химиотерапевтическим агентом, выбранным из лекарственных средств на основе платины, антиметаболитов или паклитаксела, для повышения выживаемости субъекта с опухолью, причём указанного субъекта лечат с использованием по меньшей мере одного химиотерапевтического агента.
3. Применение гуманизированного моноклонального антитела по п.1, причём указанное гуманизированное антитело включает вариабельные участки, выбранные из группы, включающей: BATRHA/BATRκA (SEQ ID NO: 20/SEQ ID NO: 15), BATRHB/BATRκA (SEQ ID NO: 21/SEQ ID NO: 15), BATRHB/BATRκB (SEQ ID NO: 21/SEQ ID NO: 16), BATRHC/BATRκB (SEQ ID NO: 22/SEQ ID NO: 16), BATRHB/BATRκD (SEQ ID NO: 21/SEQ ID NO: 18), и BATRHC/BATRκD (SEQ ID NO: 22/SEQ ID NO: 18), предпочтительно где указанное гуманизированное моноклональное антитело включает вариабельные области, соответствующие BATRHC/BATRκD (SEQ ID NO: 22/SEQ ID NO: 18).
4. Применение гуманизированного моноклонального антитела по любому из пп.1-3, в котором фрагмент гуманизированного антитела выбран из группы, включающей: Fv, F(ab'), F(ab')2 и одноцепочечное антитело, или в котором гуманизированное антитело или его фрагмент сохраняет противоопухолевую активность mBAT-1.
5. Применение гуманизированного моноклонального антитела по любому из пп.1 или 2, в котором указанный по меньшей мере один химиотерапевтический агент выбран из группы, включающей антиметаболит, выбранный из группы, состоящей из следующего: 5-фторурацил, урамустин, урацил, капецитабин, 6-меркаптопурин, метотрексат, гемцитабин, цитарабин, флударабин и пеметрексед; и лекарственное средство на основе платины, выбранное из группы, включающей: цисплатин, карбоплатин и оксалиплатин.
6. Применение гуманизированного моноклонального антитела по любому из пп.1-3, в котором указанный по меньшей мере один химиотерапевтический агент выбран из группы, состоящей из 5-фторурацила, цитарабина, оксалиплатина, паклитаксела и их комбинаций.
7. Применение гуманизированного антитела по любому из пп.1-2, в котором введение гуманизированного антитела и по меньшей мере одного химиотерапевтического агента осуществляют по существу одновременно, параллельно, альтернативно, последовательно или поочередно или в котором введение гуманизированного антитела осуществляют до первичного введения по меньшей мере одного химиотерапевтического агента.
8. Применение по любому из пп.1-2, в котором гуманизированное антитело и по меньшей мере один химиотерапевтический агент вводят по перекрывающейся схеме; или дополнительно включающее лечение субъекта путём лучевой терапии.
9. Применение по п.1, дополнительно включающее оценку по меньшей мере одного параметра, выбранного из группы, состоящей из: скорости роста опухоли, объема опухоли, количества метастазов, рецидива опухоли и их комбинаций.
10. Применение по любому из пп.1-2, в котором введение гуманизированного антитела и по меньшей мере одного химиотерапевтического агента, либо каждого отдельно, либо обоих осуществляют способом, выбранным из группы, включающей внутривенное, пероральное, внутрибрюшинное, подкожное введение, изолированную перфузию конечностей, инфузию внутрь органа и их комбинаций.
11. Применение гуманизированного моноклонального антитела по любому из пп.1-2, в котором опухолевое заболевание выбрано из группы, включающей следующие: колоректальная карцинома; легочная карцинома; карцинома молочных желез; меланома; карцинома яичников; карцинома шейки матки, рак поджелудочной железы; множественная миелома; почечноклеточная карцинома; неходжкинская лимфома; Болезнь Ходжкина; лимфома из клеток мантийной зоны; саркома Капоши, плоскоклеточная карцинома, базальноклеточная карцинома, острый миелолейкоз; хронический миелоцитоз; острый лимфоцитарный лейкоз и хронический лимфоцитарный лейкоз.
Applications Claiming Priority (7)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US2750108P | 2008-02-11 | 2008-02-11 | |
| US61/027,501 | 2008-02-11 | ||
| US3734008P | 2008-03-18 | 2008-03-18 | |
| US61/037,340 | 2008-03-18 | ||
| US11631908P | 2008-11-20 | 2008-11-20 | |
| US61/116,319 | 2008-11-20 | ||
| PCT/IL2009/000153 WO2009101611A1 (en) | 2008-02-11 | 2009-02-11 | Monoclonal antibodies for tumor treatment |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2014134177A Division RU2014134177A (ru) | 2008-02-11 | 2014-08-20 | Моноклональные антитела для лечения опухолей |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2010135585A RU2010135585A (ru) | 2012-03-20 |
| RU2531758C2 true RU2531758C2 (ru) | 2014-10-27 |
Family
ID=40535624
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2010135585/10A RU2531758C2 (ru) | 2008-02-11 | 2009-02-11 | Моноклональные антитела для лечения опухолей |
| RU2014134177A RU2014134177A (ru) | 2008-02-11 | 2014-08-20 | Моноклональные антитела для лечения опухолей |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2014134177A RU2014134177A (ru) | 2008-02-11 | 2014-08-20 | Моноклональные антитела для лечения опухолей |
Country Status (16)
| Country | Link |
|---|---|
| US (2) | US8747847B2 (ru) |
| EP (1) | EP2242773B1 (ru) |
| JP (2) | JP2011512332A (ru) |
| CN (2) | CN101970499B (ru) |
| AU (1) | AU2009213738B2 (ru) |
| BR (1) | BRPI0907718A2 (ru) |
| CA (1) | CA2715166C (ru) |
| DK (1) | DK2242773T3 (ru) |
| ES (1) | ES2639857T3 (ru) |
| HK (1) | HK1209653A1 (ru) |
| HU (1) | HUE034465T2 (ru) |
| MX (1) | MX2010008786A (ru) |
| PL (1) | PL2242773T3 (ru) |
| PT (1) | PT2242773T (ru) |
| RU (2) | RU2531758C2 (ru) |
| WO (1) | WO2009101611A1 (ru) |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2625598C2 (ru) * | 2015-12-31 | 2017-07-17 | Федеральное государственное бюджетное учреждение "Ростовский научно-исследовательский онкологический институт" Министерства здравоохранения Российской Федерации | Способ лечения больных локальным раком простаты, относящихся к группе высокого риска прогрессирования заболевания |
| RU2725819C2 (ru) * | 2014-12-05 | 2020-07-06 | Мемориал Слоан-Кеттеринг Кэнсер Сентер | Антитела, нацеленные на рецептор, связанный с g-белками, и способы их применения |
| RU2797268C2 (ru) * | 2018-02-09 | 2023-06-01 | Ф. Хоффманн-Ля Рош Аг | Антитела, связывающиеся с gprc5d |
Families Citing this family (517)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP1355666B1 (en) | 2000-12-22 | 2012-06-13 | Max-Planck-Gesellschaft zur Förderung der Wissenschaften e.V. | Use of repulsive guidance molecule (RGM) and its modulators |
| US8906864B2 (en) | 2005-09-30 | 2014-12-09 | AbbVie Deutschland GmbH & Co. KG | Binding domains of proteins of the repulsive guidance molecule (RGM) protein family and functional fragments thereof, and their use |
| EP2033971A1 (de) * | 2007-09-06 | 2009-03-11 | Abbott GmbH & Co. KG | Bone Morphogenetic Protein (BMP)-bindende Domänen von Proteinen der Repulsive Guidance Molecule (RGM) Proteinfamilie und funktionale Fragmente davon sowie deren Verwendung |
| WO2009095478A1 (en) | 2008-01-31 | 2009-08-06 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Antibodies against human cd39 and use thereof for inhibiting t regulatory cells activity |
| US8962803B2 (en) | 2008-02-29 | 2015-02-24 | AbbVie Deutschland GmbH & Co. KG | Antibodies against the RGM A protein and uses thereof |
| RS54233B1 (sr) | 2008-08-25 | 2015-12-31 | Amplimmune Inc. | Kompozicije pd-1 antagonista i postupci za njihovu primenu |
| MX2012006560A (es) * | 2009-12-08 | 2012-10-05 | Abbott Gmbh & Co Kg | Anticuerpos monoclonales contra la proteina rgm a para utilizarse en el tratamiento de degeneracion de capa de fibra de nervio retinal. |
| CN102675460B (zh) * | 2011-02-28 | 2015-08-19 | 珠海市丽珠单抗生物技术有限公司 | 抗肿瘤坏死因子α的人源化抗体 |
| JP6072771B2 (ja) * | 2011-04-20 | 2017-02-01 | メディミューン,エルエルシー | B7−h1およびpd−1に結合する抗体およびその他の分子 |
| JP6240600B2 (ja) * | 2011-07-24 | 2017-11-29 | キュアテク リミテッド | ヒト化免疫モノクローナル抗体の変異体 |
| EA026924B1 (ru) | 2011-08-01 | 2017-05-31 | Дженентек, Инк. | Способы лечения рака с использованием антагонистов, связывающихся с осью pd-1, и ингибиторов mek |
| WO2013059740A1 (en) | 2011-10-21 | 2013-04-25 | Foundation Medicine, Inc. | Novel alk and ntrk1 fusion molecules and uses thereof |
| PE20190907A1 (es) | 2012-01-27 | 2019-06-26 | AbbVie Deutschland GmbH and Co KG | Composicion y metodo para el diagnostico y el tratamiento de las enfermedades asociadas a la degeneracion de las neuritas |
| RU2689760C2 (ru) | 2012-05-31 | 2019-05-30 | Дженентек, Инк. | Способы лечения рака с применением антагонистов аксиального связывания pd-1 и vegf антагонистов |
| US9758591B2 (en) | 2012-08-24 | 2017-09-12 | The Regents Of The University Of California | Antibodies and vaccines for use in treating ROR1 cancers and inhibiting metastasis |
| AU2013337277B2 (en) | 2012-11-05 | 2018-03-08 | Foundation Medicine, Inc. | Novel NTRK1 fusion molecules and uses thereof |
| HK1214831A1 (zh) | 2012-11-05 | 2016-08-05 | Foundation Medicine, Inc. | 新型融合分子及其应用 |
| WO2014089113A1 (en) | 2012-12-03 | 2014-06-12 | Bristol-Myers Squibb Company | Enhancing anti-cancer activity of immunomodulatory fc fusion proteins |
| US9221908B2 (en) | 2012-12-12 | 2015-12-29 | Vasculox, Inc. | Therapeutic CD47 antibodies |
| HK1216647A1 (zh) | 2012-12-12 | 2016-11-25 | Vasculox Inc. | 治疗性cd47抗体 |
| UA117466C2 (uk) | 2012-12-13 | 2018-08-10 | Мерк Шарп Енд Доме Корп. | СТАБІЛЬНИЙ СКЛАД У ВИГЛЯДІ РОЗЧИНУ АНТИТІЛА ДО IL-23p19 |
| US10980804B2 (en) | 2013-01-18 | 2021-04-20 | Foundation Medicine, Inc. | Methods of treating cholangiocarcinoma |
| ES2814962T3 (es) | 2013-02-20 | 2021-03-29 | Novartis Ag | Fijación eficaz como objetivo de la leucemia humana primaria utilizando células T modificadas con receptor de antígeno quimérico anti-CD123 |
| PL2958943T3 (pl) | 2013-02-20 | 2020-04-30 | The Trustees Of The University Of Pennsylvania | Leczenie nowotworu złośliwego za pomocą humanizowanego chimerycznego receptora antygenowego anty-egfrviii |
| DK2964638T3 (en) | 2013-03-06 | 2017-10-30 | Astrazeneca Ab | QUINAZOLIN INHIBITORS TO ACTIVATE MUTANEOUS FORMS OF EPIDERMAL GROWTH FACTOR RECEPTOR |
| TWI654206B (zh) | 2013-03-16 | 2019-03-21 | 諾華公司 | 使用人類化抗-cd19嵌合抗原受體治療癌症 |
| AU2014251087B2 (en) | 2013-04-09 | 2019-05-02 | Lixte Biotechnology, Inc. | Formulations of oxabicycloheptanes and oxabicycloheptenes |
| AU2014290069B2 (en) | 2013-07-16 | 2019-01-03 | Genentech, Inc. | Methods of treating cancer using PD-1 axis binding antagonists and TIGIT inhibitors |
| CN105612175B (zh) | 2013-08-08 | 2023-05-09 | 赛腾制药 | 基于IL-15和IL-15Rαsushi结构域的调节因子 |
| PT3030262T (pt) | 2013-08-08 | 2019-12-11 | Inst Gustave Roussy Igr | Composição farmacêutica de associação |
| US10570204B2 (en) | 2013-09-26 | 2020-02-25 | The Medical College Of Wisconsin, Inc. | Methods for treating hematologic cancers |
| WO2015066413A1 (en) | 2013-11-01 | 2015-05-07 | Novartis Ag | Oxazolidinone hydroxamic acid compounds for the treatment of bacterial infections |
| US9580504B1 (en) * | 2013-11-07 | 2017-02-28 | Curetech Ltd. | Pidilizumab monoclonal antibody therapy following stem cell transplantation |
| CA2929181A1 (en) | 2013-11-13 | 2015-05-21 | Novartis Ag | Mtor inhibitors for enhancing the immune response |
| US20150140125A1 (en) * | 2013-11-19 | 2015-05-21 | Life Plus, LLC | Synergistic cancer therapy drug combinations |
| CA2934028A1 (en) | 2013-12-17 | 2015-06-25 | Genentech, Inc. | Combination therapy comprising ox40 binding agonists and pd-1 axis binding antagonists |
| MX2016007885A (es) | 2013-12-17 | 2017-01-11 | Genentech Inc | Metodos de tratamiento de cancer usando antagonistas de union del eje de pd-1 y un anticuerpo anti-cd20. |
| NZ760065A (en) * | 2013-12-17 | 2022-12-23 | Genentech Inc | Methods of treating cancers using pd-1 axis binding antagonists and taxanes |
| CA2931684C (en) | 2013-12-19 | 2024-02-20 | Novartis Ag | Human mesothelin chimeric antigen receptors and uses thereof |
| JO3517B1 (ar) | 2014-01-17 | 2020-07-05 | Novartis Ag | ان-ازاسبيرو الكان حلقي كبديل مركبات اريل-ان مغايرة وتركيبات لتثبيط نشاط shp2 |
| TWI681969B (zh) | 2014-01-23 | 2020-01-11 | 美商再生元醫藥公司 | 針對pd-1的人類抗體 |
| TWI680138B (zh) | 2014-01-23 | 2019-12-21 | 美商再生元醫藥公司 | 抗pd-l1之人類抗體 |
| ES2716685T3 (es) | 2014-01-24 | 2019-06-14 | Dana Farber Cancer Inst Inc | Moléculas de anticuerpo para PD-1 y usos de las mismas |
| DK3099717T3 (da) | 2014-01-31 | 2019-07-01 | Novartis Ag | Antistofmolekyler med tim-3 og anvendelser deraf |
| TWI777174B (zh) | 2014-03-14 | 2022-09-11 | 瑞士商諾華公司 | 針對lag-3之抗體分子及其用途 |
| JP2017513818A (ja) | 2014-03-15 | 2017-06-01 | ノバルティス アーゲー | キメラ抗原受容体を使用する癌の処置 |
| KR20170003912A (ko) | 2014-03-19 | 2017-01-10 | 매카이 메디컬 파운데이션 더 프레즈비티리언 처치 인 타이완 매카이 메모리얼 호스피탈 | 면역원성 당펩타이드에 대한 항체, 이를 포함하는 조성물 및 이의 용도 |
| WO2015148379A1 (en) | 2014-03-24 | 2015-10-01 | Novartis Ag | Monobactam organic compounds for the treatment of bacterial infections |
| RU2016142476A (ru) | 2014-03-31 | 2018-05-07 | Дженентек, Инк. | Комбинированная терапия, включающая антиангиогенезные агенты и агонисты, связывающие ох40 |
| HRP20192285T1 (hr) | 2014-03-31 | 2020-03-06 | F. Hoffmann - La Roche Ag | Anti-ox40 protutijela i postupci uporabe |
| SI3888674T1 (sl) | 2014-04-07 | 2024-08-30 | Novartis Ag | Zdravljenje raka z uporabo antigenskega himernega receptorja proti-CD19 |
| EP3129509B1 (en) | 2014-04-10 | 2020-06-17 | Bio-Marcare Technologies Ltd. | Methods and kits for identifying pre-cancerous colorectal polyps and colorectal cancer |
| TWI693232B (zh) | 2014-06-26 | 2020-05-11 | 美商宏觀基因股份有限公司 | 與pd-1和lag-3具有免疫反應性的共價結合的雙抗體和其使用方法 |
| AU2015287227B2 (en) | 2014-07-10 | 2021-02-18 | Universitat Zurich | Immune-stimulating monoclonal antibodies against human interleukin-2 |
| BR112017000497B1 (pt) | 2014-07-11 | 2023-12-26 | Ventana Medical Systems, Inc | Anticorpo isolado, célula hospedeira procariótica, imunoconjugado e método de detecção da presença ou do nível de expressão de pd-l1 |
| EP3563870A1 (en) | 2014-07-15 | 2019-11-06 | F. Hoffmann-La Roche AG | Methods of treating cancer using pd-1 axis binding antagonists and mek inhibitors |
| EP3193915A1 (en) | 2014-07-21 | 2017-07-26 | Novartis AG | Combinations of low, immune enhancing. doses of mtor inhibitors and cars |
| WO2016014553A1 (en) | 2014-07-21 | 2016-01-28 | Novartis Ag | Sortase synthesized chimeric antigen receptors |
| SG10201913765YA (en) | 2014-07-21 | 2020-03-30 | Novartis Ag | Treatment of cancer using a cd33 chimeric antigen receptor |
| EP4205749A1 (en) | 2014-07-31 | 2023-07-05 | Novartis AG | Subset-optimized chimeric antigen receptor-containing cells |
| CN107001316A (zh) | 2014-08-06 | 2017-08-01 | 诺华股份有限公司 | 作为抗菌剂的喹诺酮衍生物 |
| AU2015301460B2 (en) | 2014-08-14 | 2021-04-08 | Novartis Ag | Treatment of cancer using GFR alpha-4 chimeric antigen receptor |
| RU2020117196A (ru) | 2014-08-19 | 2020-10-15 | Новартис Аг | Химерный антигенный рецептор (car) против cd123 для использования в лечении злокачественных опухолей |
| EP3191126B1 (en) | 2014-09-13 | 2020-05-13 | Novartis AG | Combination therapies of alk inhibitors |
| HRP20201656T1 (hr) | 2014-09-16 | 2021-03-05 | Innate Pharma | Neutralizacija inhibitornih putova u limfocitima |
| JP6839074B2 (ja) | 2014-09-17 | 2021-03-03 | ノバルティス アーゲー | 養子免疫療法のためのキメラ受容体での細胞毒性細胞のターゲティング |
| DK3262071T3 (da) | 2014-09-23 | 2020-06-15 | Hoffmann La Roche | Fremgangsmåde til anvendelse af anti-CD79b-immunkonjugater |
| EP3662903A3 (en) | 2014-10-03 | 2020-10-14 | Novartis AG | Combination therapies |
| CA2963935A1 (en) | 2014-10-08 | 2016-04-14 | Novartis Ag | Biomarkers predictive of therapeutic responsiveness to chimeric antigen receptor therapy and uses thereof |
| MA41044A (fr) | 2014-10-08 | 2017-08-15 | Novartis Ag | Compositions et procédés d'utilisation pour une réponse immunitaire accrue et traitement contre le cancer |
| KR102536786B1 (ko) | 2014-10-10 | 2023-05-26 | 이나뜨 파르마 에스.에이. | Cd73 차단 |
| UY36351A (es) | 2014-10-14 | 2016-06-01 | Novartis Ag | Moléculas de anticuerpo que se unen a pd-l1 y usos de las mismas |
| AU2015343337A1 (en) | 2014-11-03 | 2017-06-15 | Genentech, Inc. | Assays for detecting T cell immune subsets and methods of use thereof |
| CN107109484B (zh) | 2014-11-03 | 2021-12-14 | 豪夫迈·罗氏有限公司 | 用于ox40激动剂治疗的功效预测和评估的方法和生物标志物 |
| US20170313775A1 (en) | 2014-11-13 | 2017-11-02 | The Johns Hopkins University | Checkpoint Blockade and Microsatellite Instability |
| TW201625692A (zh) | 2014-11-14 | 2016-07-16 | 諾華公司 | 抗體藥物結合物 |
| MX2017006320A (es) | 2014-11-17 | 2017-08-10 | Genentech Inc | Terapia combinada que comprende agonistas de unión de ox40 y antagonistas de unión del eje de pd-1. |
| RU2753902C2 (ru) | 2014-11-20 | 2021-08-24 | Ф.Хоффманн-Ля Рош Аг | Комбинированная терапия на основе активирующих т-клетки биспецифических антигенсвязывающих молекул против cd3 и фолатного рецептора 1 (folr1) и антагонистов, связывающихся с осью pd-1 |
| CN107531690B (zh) | 2014-11-27 | 2020-11-06 | 基因泰克公司 | 用作CBP和/或EP300抑制剂的4,5,6,7-四氢-1H-吡唑并[4,3-c]吡啶-3-胺化合物 |
| US20180334490A1 (en) | 2014-12-03 | 2018-11-22 | Qilong H. Wu | Methods for b cell preconditioning in car therapy |
| PT3227339T (pt) | 2014-12-05 | 2022-01-14 | Eureka Therapeutics Inc | Recetores de antigénio quiméricos que têm como alvo o recetor 4 acoplado a proteína g e utilizações dos mesmos |
| CN107206088A (zh) | 2014-12-05 | 2017-09-26 | 豪夫迈·罗氏有限公司 | 使用pd‑1轴拮抗剂和hpk1拮抗剂用于治疗癌症的方法和组合物 |
| HRP20192009T1 (hr) | 2014-12-16 | 2020-02-07 | Novartis Ag | Spojevi izoksazol hidroksamske kiseline kao inhibitori lpxc-a |
| EP3233918A1 (en) | 2014-12-19 | 2017-10-25 | Novartis AG | Combination therapies |
| EP3250250A4 (en) | 2015-01-30 | 2019-05-22 | President and Fellows of Harvard College | PERITUMORAL AND INTRATUMORAL MATERIALS FOR CANCER THERAPY |
| US11161907B2 (en) | 2015-02-02 | 2021-11-02 | Novartis Ag | Car-expressing cells against multiple tumor antigens and uses thereof |
| EP3259288A1 (en) | 2015-02-20 | 2017-12-27 | Innate Pharma | Cd73 blockade |
| AR103726A1 (es) * | 2015-02-27 | 2017-05-31 | Merck Sharp & Dohme | Cristales de anticuerpos monoclonales anti-pd-1 humanos |
| CA2979215A1 (en) | 2015-03-10 | 2016-09-15 | Aduro Biotech, Inc. | Compositions and methods for activating "stimulator of interferon gene"-dependent signalling |
| EP3067062A1 (en) | 2015-03-13 | 2016-09-14 | Ipsen Pharma S.A.S. | Combination of tasquinimod or a pharmaceutically acceptable salt thereof and a pd1 and/or pdl1 inhibitor, for use as a medicament |
| EP3280795B1 (en) | 2015-04-07 | 2021-03-24 | Novartis AG | Combination of chimeric antigen receptor therapy and amino pyrimidine derivatives |
| MX2017012805A (es) | 2015-04-07 | 2018-04-11 | Genentech Inc | Complejo de unión a antígenos con actividad agonista y métodos de uso. |
| WO2016168595A1 (en) | 2015-04-17 | 2016-10-20 | Barrett David Maxwell | Methods for improving the efficacy and expansion of chimeric antigen receptor-expressing cells |
| EP3286211A1 (en) | 2015-04-23 | 2018-02-28 | Novartis AG | Treatment of cancer using chimeric antigen receptor and protein kinase a blocker |
| PL3291679T3 (pl) | 2015-05-06 | 2022-04-25 | Snipr Technologies Limited | Zmiana populacji drobnoustrojowych i modyfikowanie mikrobioty |
| EP3294770B2 (en) | 2015-05-12 | 2024-03-20 | F. Hoffmann-La Roche AG | Therapeutic and diagnostic methods for cancer |
| CN104987421A (zh) * | 2015-05-13 | 2015-10-21 | 北京比洋生物技术有限公司 | 抗ctla-4和pd-1的双重可变结构域免疫球蛋白 |
| ES2889906T3 (es) | 2015-05-21 | 2022-01-14 | Harpoon Therapeutics Inc | Proteínas de unión triespecíficas y usos médicos |
| SI3303394T1 (sl) | 2015-05-29 | 2020-10-30 | Agenus Inc. | Protitelesa proti-CTLA-4 in postopki njihove uporabe |
| KR20250151554A (ko) | 2015-05-29 | 2025-10-21 | 제넨테크, 인크. | 암에 대한 치료 및 진단 방법 |
| TWI773646B (zh) | 2015-06-08 | 2022-08-11 | 美商宏觀基因股份有限公司 | 結合lag-3的分子和其使用方法 |
| EP3303399A1 (en) | 2015-06-08 | 2018-04-11 | H. Hoffnabb-La Roche Ag | Methods of treating cancer using anti-ox40 antibodies |
| IL256080B2 (en) | 2015-06-17 | 2025-06-01 | Genentech Inc | Methods of treating locally advanced or metastatic breast cancers using pd-1 axis binding antagonists and taxanes |
| US20190194315A1 (en) | 2015-06-17 | 2019-06-27 | Novartis Ag | Antibody drug conjugates |
| CN114591433A (zh) | 2015-07-13 | 2022-06-07 | 西托姆克斯治疗公司 | 抗pd-1抗体、可活化抗pd-1抗体及其使用方法 |
| AU2016297014B2 (en) | 2015-07-21 | 2021-06-17 | Novartis Ag | Methods for improving the efficacy and expansion of immune cells |
| LT3317301T (lt) | 2015-07-29 | 2021-07-26 | Novartis Ag | Kombinuotos terapijos, apimančios antikūno molekules prieš lag-3 |
| KR20180034426A (ko) | 2015-07-29 | 2018-04-04 | 노파르티스 아게 | 암의 치료에서의 항 pd-1 및 항 m-csf 항체의 조합 용도 |
| EP3328407A1 (en) | 2015-07-29 | 2018-06-06 | Novartis AG | Combination of pd-1 antagonist with an egfr inhibitor |
| EP3316902A1 (en) | 2015-07-29 | 2018-05-09 | Novartis AG | Combination therapies comprising antibody molecules to tim-3 |
| CN108025051B (zh) | 2015-07-29 | 2021-12-24 | 诺华股份有限公司 | 包含抗pd-1抗体分子的联合疗法 |
| HUE055207T2 (hu) | 2015-07-30 | 2021-11-29 | Macrogenics Inc | PD-1 és LAG-3 kötõ molekulák és eljárások azok alkalmazására |
| US11747346B2 (en) | 2015-09-03 | 2023-09-05 | Novartis Ag | Biomarkers predictive of cytokine release syndrome |
| CN108349985A (zh) | 2015-09-14 | 2018-07-31 | 无限药品股份有限公司 | 异喹啉酮的固体形式、其制备方法、包含其的组合物及其使用方法 |
| EP3349787A4 (en) | 2015-09-18 | 2019-03-27 | Arch Oncology, Inc. | THERAPEUTIC CD47 ANTIBODIES |
| HK1251158A1 (zh) | 2015-09-29 | 2019-01-25 | 细胞基因公司 | Pd-1结合蛋白及其使用方法 |
| JP2018529719A (ja) | 2015-09-30 | 2018-10-11 | メルク パテント ゲゼルシャフト ミット ベシュレンクテル ハフツングMerck Patent Gesellschaft mit beschraenkter Haftung | Alk陰性がんを処置するためのpd−1系結合アンタゴニストおよびalk阻害剤の組合せ |
| SMT202100506T1 (it) | 2015-10-02 | 2021-11-12 | Hoffmann La Roche | Anticorpi bispecifici specifici per pd1 e tim3 |
| WO2017064043A1 (en) | 2015-10-12 | 2017-04-20 | Innate Pharma | Cd73 blocking agents |
| EP3362074B1 (en) | 2015-10-16 | 2023-08-09 | President and Fellows of Harvard College | Regulatory t cell pd-1 modulation for regulating t cell effector immune responses |
| CN108430515B (zh) | 2015-10-29 | 2021-11-12 | 诺华股份有限公司 | 包含toll-样受体激动剂的抗体缀合物 |
| LT3370733T (lt) | 2015-11-02 | 2021-10-25 | Board Of Regents, The University Of Texas System | Cd40 aktyvinimo ir imuninės kontrolės taškų blokados būdai |
| EP3371311B1 (en) | 2015-11-06 | 2021-07-21 | Orionis Biosciences BV | Bi-functional chimeric proteins and uses thereof |
| KR20180104597A (ko) | 2015-11-07 | 2018-09-21 | 멀티비르 인코포레이티드 | 암 치료를 위한 종양 억제 유전자 요법 및 면역관문 봉쇄를 포함하는 조성물 |
| CN121154828A (zh) | 2015-11-19 | 2025-12-19 | 豪夫迈·罗氏有限公司 | 使用b-raf抑制剂和免疫检查点抑制剂治疗癌症的方法 |
| EP3178848A1 (en) | 2015-12-09 | 2017-06-14 | F. Hoffmann-La Roche AG | Type ii anti-cd20 antibody for reducing formation of anti-drug antibodies |
| ES2901794T3 (es) | 2015-12-09 | 2022-03-23 | Hoffmann La Roche | Anticuerpo anti-CD20 de tipo II para reducir la formación de anticuerpos antifármaco |
| EA201891178A1 (ru) | 2015-12-14 | 2019-01-31 | Макродженикс, Инк. | Биспецифичные молекулы, обладающие иммунореактивностью в отношении pd-1 и ctla-4, и способы их применения |
| ES2986067T3 (es) | 2015-12-17 | 2024-11-08 | Novartis Ag | Moléculas de anticuerpos frente a PD-1 y usos de las mismas |
| UY37030A (es) | 2015-12-18 | 2017-07-31 | Novartis Ag | Anticuerpos dirigidos a cd32b y métodos de uso de los mismos |
| US11433136B2 (en) | 2015-12-18 | 2022-09-06 | The General Hospital Corporation | Polyacetal polymers, conjugates, particles and uses thereof |
| MA44146B1 (fr) | 2015-12-22 | 2023-10-31 | Regeneron Pharma | Combinaison d'anticorps anti-pd-1 et d'anticorps bispécifiques anti-cd20/anti-cd3 pour traiter le cancer |
| US11413340B2 (en) | 2015-12-22 | 2022-08-16 | Novartis Ag | Mesothelin chimeric antigen receptor (CAR) and antibody against PD-L1 inhibitor for combined use in anticancer therapy |
| AR107303A1 (es) | 2016-01-08 | 2018-04-18 | Hoffmann La Roche | Métodos de tratamiento de cánceres positivos para ace utilizando antagonistas de unión a eje pd-1 y anticuerpos biespecíficos anti-ace / anti-cd3, uso, composición, kit |
| BR112018014150A2 (en) | 2016-01-11 | 2018-12-11 | Novartis Ag | immunostimulating humanized monoclonal antibodies to human interleukin-2, and fusion proteins thereof |
| PL3405495T3 (pl) | 2016-01-21 | 2021-10-11 | Innate Pharma | Neutralizacja szlaków inhibitorowych w limfocytach |
| WO2017129763A1 (en) | 2016-01-28 | 2017-08-03 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Methods and pharmaceutical compositions for the treatment of signet ring cell gastric cancer |
| DK3411398T3 (da) | 2016-02-05 | 2024-06-24 | Orionis Biosciences BV | Målrettede terapeutiske midler og anvendelse heraf |
| AU2017219216B2 (en) | 2016-02-19 | 2019-12-19 | Novartis Ag | Tetracyclic pyridone compounds as antivirals |
| WO2017151517A1 (en) | 2016-02-29 | 2017-09-08 | Foundation Medicine, Inc. | Methods of treating cancer |
| KR102500659B1 (ko) | 2016-02-29 | 2023-02-16 | 제넨테크, 인크. | 암에 대한 치료 및 진단 방법 |
| WO2017149515A1 (en) | 2016-03-04 | 2017-09-08 | Novartis Ag | Cells expressing multiple chimeric antigen receptor (car) molecules and uses therefore |
| AU2017230850B2 (en) | 2016-03-08 | 2024-04-18 | Innate Pharma | Siglec neutralizing antibodies |
| MX2018010546A (es) | 2016-03-15 | 2019-02-20 | Chugai Pharmaceutical Co Ltd | Metodos de tratamiento de cancer que usan antagonistas de union al eje de muerte programada 1 (pd-1) y anticuerpos anti glipicano 3 (gpc3). |
| WO2017165412A2 (en) | 2016-03-21 | 2017-09-28 | Dana-Farber Cancer Institute, Inc. | T-cell exhaustion state-specific gene expression regulators and uses thereof |
| FI3433257T3 (fi) | 2016-03-24 | 2024-01-08 | Novartis Ag | Alkynyylinukleosidianalogeja ihmisen rinoviruksen estäjinä |
| JP7208010B2 (ja) | 2016-03-29 | 2023-01-18 | ユニバーシティ オブ サザン カリフォルニア | 癌を標的とするキメラ抗原受容体 |
| EP3436829A1 (en) | 2016-03-30 | 2019-02-06 | Centre Léon-Bérard | Lymphocytes expressing cd73 in cancerous patient dictates therapy |
| WO2017173091A1 (en) | 2016-03-30 | 2017-10-05 | Musc Foundation For Research Development | Methods for treatment and diagnosis of cancer by targeting glycoprotein a repetitions predominant (garp) and for providing effective immunotherapy alone or in combination |
| EP3225253A1 (en) | 2016-04-01 | 2017-10-04 | Deutsches Krebsforschungszentrum Stiftung des Öffentlichen Rechts | Cancer therapy with an oncolytic virus combined with a checkpoint inhibitor |
| AU2017250191A1 (en) | 2016-04-13 | 2018-11-08 | Orimabs Ltd. | Anti-PSMA antibodies and use thereof |
| US20190218515A1 (en) | 2016-04-13 | 2019-07-18 | Vivia Biotech, S.L. | Ex vivo bite-activated t cells |
| CA3019921A1 (en) | 2016-04-15 | 2017-10-19 | Genentech, Inc. | Methods for monitoring and treating cancer |
| CN114634569B (zh) * | 2016-04-15 | 2024-08-20 | 达特茅斯大学理事会 | 高亲和力b7-h6抗体和抗体片段 |
| EP3443120A2 (en) | 2016-04-15 | 2019-02-20 | H. Hoffnabb-La Roche Ag | Methods for monitoring and treating cancer |
| JP7131773B2 (ja) | 2016-04-29 | 2022-09-06 | ボード オブ リージェンツ,ザ ユニバーシティ オブ テキサス システム | ホルモン受容体に関連する転写活性の標的尺度 |
| TWI786044B (zh) | 2016-05-13 | 2022-12-11 | 美商再生元醫藥公司 | 藉由投予pd-1抑制劑治療皮膚癌之方法 |
| EP3243832A1 (en) | 2016-05-13 | 2017-11-15 | F. Hoffmann-La Roche AG | Antigen binding molecules comprising a tnf family ligand trimer and pd1 binding moiety |
| JP7105200B2 (ja) | 2016-05-13 | 2022-07-22 | オリオニス バイオサイエンシズ ビーブイ | 標的突然変異体インターフェロン-ベータおよびその使用 |
| EP3455245A2 (en) | 2016-05-13 | 2019-03-20 | Orionis Biosciences NV | Therapeutic targeting of non-cellular structures |
| US11623958B2 (en) | 2016-05-20 | 2023-04-11 | Harpoon Therapeutics, Inc. | Single chain variable fragment CD3 binding proteins |
| JP7160688B2 (ja) | 2016-05-24 | 2022-10-25 | ジェネンテック, インコーポレイテッド | Cbp/ep300の複素環式インヒビターおよびがんの処置におけるそれらの使用 |
| CN109476663B (zh) | 2016-05-24 | 2021-11-09 | 基因泰克公司 | 用于治疗癌症的吡唑并吡啶衍生物 |
| TWI781934B (zh) | 2016-05-27 | 2022-11-01 | 美商艾吉納斯公司 | 抗-tim-3抗體及其使用方法 |
| GB201609811D0 (en) | 2016-06-05 | 2016-07-20 | Snipr Technologies Ltd | Methods, cells, systems, arrays, RNA and kits |
| SG11201810656WA (en) | 2016-06-14 | 2018-12-28 | Novartis Ag | Crystalline form of (r)-4-(5-(cyclopropylethynyl)isoxazol-3-yl)-n-hydroxy-2-methyl-2-(methylsulfonyl)butanamide as an antibacterial agent |
| WO2017216686A1 (en) | 2016-06-16 | 2017-12-21 | Novartis Ag | 8,9-fused 2-oxo-6,7-dihydropyrido-isoquinoline compounds as antivirals |
| WO2017216685A1 (en) | 2016-06-16 | 2017-12-21 | Novartis Ag | Pentacyclic pyridone compounds as antivirals |
| CA3028718A1 (en) | 2016-06-24 | 2017-12-28 | Infinity Pharmaceuticals, Inc. | Combination therapies |
| MX2018016330A (es) | 2016-06-27 | 2020-02-17 | Univ California | Combinaciones para tratamiento del cáncer. |
| WO2018009466A1 (en) | 2016-07-05 | 2018-01-11 | Aduro Biotech, Inc. | Locked nucleic acid cyclic dinucleotide compounds and uses thereof |
| CN116769050A (zh) | 2016-07-20 | 2023-09-19 | 犹他大学研究基金会 | Cd229 car t细胞及其使用方法 |
| US20210369746A1 (en) | 2016-08-01 | 2021-12-02 | Molecular Templates, Inc. | Administration of hypoxia activated prodrugs in combination with immune modulatory agents for treating cancer |
| EP3494139B1 (en) | 2016-08-05 | 2022-01-12 | F. Hoffmann-La Roche AG | Multivalent and multiepitopic anitibodies having agonistic activity and methods of use |
| BR112019002036A2 (pt) | 2016-08-12 | 2019-05-14 | Genentech Inc | métodos de tratamento de um sujeito com câncer colorretal, kit para tratamento do câncer colorretal em um sujeito humano e combinação de fármacos para a terapia do câncer colorretal |
| MA45999A (fr) | 2016-08-22 | 2019-06-26 | Arbutus Biopharma Corp | Anticorps anti-pd-1, ou leurs fragments, pour le traitement de l'hépatite b |
| US11583516B2 (en) | 2016-09-07 | 2023-02-21 | Trustees Of Tufts College | Dash inhibitors, and uses related thereto |
| TW201811788A (zh) | 2016-09-09 | 2018-04-01 | 瑞士商諾華公司 | 作為抗病毒劑之多環吡啶酮化合物 |
| MX2019002728A (es) | 2016-09-09 | 2019-08-16 | Tg Therapeutics Inc | Combinacion de un anticuerpo anti-cd20, inhibidor de quinasa pi3-delta, y anticuerpo anti-pd-1 o anti-pd-l1 para el tratamiento hematologico de los canceres. |
| AU2017329024A1 (en) | 2016-09-19 | 2019-03-21 | Celgene Corporation | Methods of treating immune disorders using pd-1 binding proteins |
| WO2018053401A1 (en) | 2016-09-19 | 2018-03-22 | Celgene Corporation | Methods of treating vitiligo using pd-1 binding proteins |
| EP3515475B1 (en) | 2016-09-21 | 2024-05-01 | The U.S.A. as represented by the Secretary, Department of Health and Human Services | Chimeric antigen receptor (car) that targets chemokine receptor ccr4 and its use |
| US11673971B2 (en) | 2016-09-23 | 2023-06-13 | Marengo Therapeutics, Inc. | Multispecific antibody molecules comprising lambda and kappa light chains |
| BR112019006041A2 (pt) | 2016-09-27 | 2019-09-03 | Board Of Regents, The University Of Texas System | métodos para aprimorar a terapia de bloqueio do ponto de verificação imunológico por modulação do microbioma |
| JOP20190061A1 (ar) | 2016-09-28 | 2019-03-26 | Novartis Ag | مثبطات بيتا-لاكتاماز |
| CN109862917A (zh) | 2016-09-29 | 2019-06-07 | 基因泰克公司 | Mek抑制剂,pd-1轴抑制剂,和紫杉烷的组合疗法 |
| IL265759B2 (en) | 2016-10-06 | 2025-10-01 | Genentech Inc | Therapeutic and diagnostic methods for cancer |
| MY200337A (en) | 2016-10-07 | 2023-12-20 | Novartis Ag | Nucleic acid molecules encoding chimeric antigen receptors comprising a cd20 binding domain |
| TW202436356A (zh) | 2016-10-11 | 2024-09-16 | 美商艾吉納斯公司 | 抗lag-3抗體及其使用方法 |
| WO2018071668A1 (en) | 2016-10-12 | 2018-04-19 | Board Of Regents, The University Of Texas System | Methods and compositions for tusc2 immunotherapy |
| WO2018071576A1 (en) | 2016-10-14 | 2018-04-19 | The United States Of America, As Represented By The Secretary, Department Of Health And Human Services | Treatment of tumors by inhibition of cd300f |
| WO2018073753A1 (en) | 2016-10-18 | 2018-04-26 | Novartis Ag | Fused tetracyclic pyridone compounds as antivirals |
| WO2018075960A1 (en) | 2016-10-21 | 2018-04-26 | Tioma Therapeutics, Inc. | Therapeutic cd47 antibodies |
| ES2917000T3 (es) | 2016-10-24 | 2022-07-06 | Orionis Biosciences BV | Interferón-gamma mutante diana y usos del mismo |
| JP2019535250A (ja) | 2016-10-29 | 2019-12-12 | ジェネンテック, インコーポレイテッド | 抗mic抗体及び使用方法 |
| US11124577B2 (en) | 2016-11-02 | 2021-09-21 | Engmab Sàrl | Bispecific antibody against BCMA and CD3 and an immunological drug for combined use in treating multiple myeloma |
| WO2018083087A2 (en) | 2016-11-02 | 2018-05-11 | Glaxosmithkline Intellectual Property (No.2) Limited | Binding proteins |
| EP3538112B1 (en) | 2016-11-09 | 2026-02-25 | Musc Foundation for Research Development | Cd38-nad+ regulated metabolic axis in anti-tumor immunotherapy |
| US11466094B2 (en) | 2016-11-15 | 2022-10-11 | Genentech, Inc. | Dosing for treatment with anti-CD20/anti-CD3 bispecific antibodies |
| US11446302B2 (en) | 2016-11-17 | 2022-09-20 | Board Of Regents, The University Of Texas System | Compounds with anti-tumor activity against cancer cells bearing EGFR or HER2 exon 20 mutations |
| WO2018098352A2 (en) | 2016-11-22 | 2018-05-31 | Jun Oishi | Targeting kras induced immune checkpoint expression |
| WO2018102786A1 (en) | 2016-12-03 | 2018-06-07 | Juno Therapeutics, Inc. | Methods for modulation of car-t cells |
| WO2018106738A1 (en) | 2016-12-05 | 2018-06-14 | Massachusetts Institute Of Technology | Brush-arm star polymers, conjugates and particles, and uses thereof |
| CN118634323A (zh) | 2016-12-07 | 2024-09-13 | 艾吉纳斯公司 | 抗体和其使用方法 |
| US11013802B2 (en) | 2016-12-07 | 2021-05-25 | Agenus Inc. | Anti-CTLA-4 antibodies and methods of use thereof |
| NZ754522A (en) | 2016-12-08 | 2025-11-28 | Lixte Biotechnology Inc | Oxabicycloheptanes for modulation of immune response |
| CN110366562A (zh) | 2016-12-12 | 2019-10-22 | 豪夫迈·罗氏有限公司 | 使用抗pd-l1抗体和抗雄激素治疗癌症的方法 |
| JP2020510624A (ja) | 2016-12-12 | 2020-04-09 | マルチビア インコーポレイテッド | がんおよび感染性疾患の治療および予防のための、ウイルス遺伝子治療および免疫チェックポイント阻害剤を含む方法および組成物 |
| WO2018112364A1 (en) | 2016-12-16 | 2018-06-21 | Evelo Biosciences, Inc. | Combination therapies for treating melanoma |
| WO2018112360A1 (en) | 2016-12-16 | 2018-06-21 | Evelo Biosciences, Inc. | Combination therapies for treating cancer |
| US12162932B2 (en) | 2017-01-05 | 2024-12-10 | Netris Pharma | Combined treatment with Netrin-1 interfering drug and immune checkpoint inhibitors drugs |
| EP3568412A2 (en) | 2017-01-13 | 2019-11-20 | Agenus Inc. | T cell receptors that bind to ny-eso-1 and methods of use thereof |
| JOP20190187A1 (ar) | 2017-02-03 | 2019-08-01 | Novartis Ag | مترافقات عقار جسم مضاد لـ ccr7 |
| US10906985B2 (en) | 2017-02-06 | 2021-02-02 | Orionis Biosciences, Inc. | Targeted engineered interferon and uses thereof |
| CA3052523A1 (en) | 2017-02-06 | 2018-08-09 | Orionis Biosciences Nv | Targeted chimeric proteins and uses thereof |
| US20200023071A1 (en) | 2017-02-06 | 2020-01-23 | Innate Pharma | Immunomodulatory antibody drug conjugates binding to a human mica polypeptide |
| US20200291089A1 (en) | 2017-02-16 | 2020-09-17 | Elstar Therapeutics, Inc. | Multifunctional molecules comprising a trimeric ligand and uses thereof |
| US11693007B2 (en) | 2017-02-24 | 2023-07-04 | Board Of Regents, The University Of Texas System | Assay for detection of early stage pancreatic cancer |
| BR112019017696A2 (pt) | 2017-02-27 | 2020-04-07 | Bristol Myers Squibb | programa de dosagem para uma combinação de ceritinib e uma molécula de anticorpo anti-pd-1 |
| PL3589754T3 (pl) | 2017-03-01 | 2023-10-09 | F. Hoffmann-La Roche Ag | Sposoby diagnostyczne i terapeutyczne w chorobach nowotworowych |
| US11179413B2 (en) | 2017-03-06 | 2021-11-23 | Novartis Ag | Methods of treatment of cancer with reduced UBB expression |
| KR102584011B1 (ko) | 2017-03-16 | 2023-09-27 | 이나뜨 파르마 에스.에이. | 암 치료를 위한 조성물 및 방법 |
| WO2018175790A1 (en) * | 2017-03-22 | 2018-09-27 | Arch Oncology, Inc. | Combination therapy for the treatment of solid and hematological cancers |
| CN108623686A (zh) | 2017-03-25 | 2018-10-09 | 信达生物制药(苏州)有限公司 | 抗ox40抗体及其用途 |
| CN110475567A (zh) | 2017-03-31 | 2019-11-19 | 勃林格殷格翰国际有限公司 | 抗癌组合疗法 |
| WO2018185618A1 (en) | 2017-04-03 | 2018-10-11 | Novartis Ag | Anti-cdh6 antibody drug conjugates and anti-gitr antibody combinations and methods of treatment |
| KR20190121816A (ko) | 2017-04-03 | 2019-10-28 | 에프. 호프만-라 로슈 아게 | 항-pd-1 항체와 돌연변이 il-2 또는 il-15의 면역접합체 |
| BR112019021032A2 (pt) | 2017-04-05 | 2020-05-05 | Boehringer Ingelheim International Gmbh | terapia combinada anticâncer |
| PL3606955T3 (pl) | 2017-04-05 | 2025-02-24 | F. Hoffmann-La Roche Ag | Przeciwciała dwuswoiste swoiście wiążące się z PD1 i LAG3 |
| US11603407B2 (en) | 2017-04-06 | 2023-03-14 | Regeneron Pharmaceuticals, Inc. | Stable antibody formulation |
| JP2020516638A (ja) | 2017-04-13 | 2020-06-11 | エフ・ホフマン−ラ・ロシュ・アクチェンゲゼルシャフト | がんを処置する方法における使用のための、インターロイキン2イムノコンジュゲート、cd40アゴニスト、および任意選択のpd−1軸結合アンタゴニスト |
| KR102629972B1 (ko) | 2017-04-13 | 2024-01-29 | 아게누스 인코포레이티드 | 항-cd137 항체 및 이의 사용 방법 |
| EP3610042A1 (en) | 2017-04-14 | 2020-02-19 | H. Hoffnabb-La Roche Ag | Diagnostic and therapeutic methods for cancer |
| CA3058944A1 (en) | 2017-04-19 | 2018-10-25 | Elstar Therapeutics, Inc. | Multispecific molecules and uses thereof |
| AR111419A1 (es) | 2017-04-27 | 2019-07-10 | Novartis Ag | Compuestos fusionados de indazol piridona como antivirales |
| US20200179511A1 (en) | 2017-04-28 | 2020-06-11 | Novartis Ag | Bcma-targeting agent, and combination therapy with a gamma secretase inhibitor |
| WO2018201056A1 (en) | 2017-04-28 | 2018-11-01 | Novartis Ag | Cells expressing a bcma-targeting chimeric antigen receptor, and combination therapy with a gamma secretase inhibitor |
| UY37695A (es) | 2017-04-28 | 2018-11-30 | Novartis Ag | Compuesto dinucleótido cíclico bis 2’-5’-rr-(3’f-a)(3’f-a) y usos del mismo |
| WO2018201047A1 (en) | 2017-04-28 | 2018-11-01 | Elstar Therapeutics, Inc. | Multispecific molecules comprising a non-immunoglobulin heterodimerization domain and uses thereof |
| AR111651A1 (es) | 2017-04-28 | 2019-08-07 | Novartis Ag | Conjugados de anticuerpos que comprenden agonistas del receptor de tipo toll y terapias de combinación |
| US11021537B2 (en) | 2017-05-01 | 2021-06-01 | Agenus Inc. | Anti-TIGIT antibodies and methods of use thereof |
| JOP20190260A1 (ar) | 2017-05-02 | 2019-10-31 | Merck Sharp & Dohme | صيغ ثابتة لأجسام مضادة لمستقبل الموت المبرمج 1 (pd-1) وطرق استخدامها |
| AU2018263868A1 (en) | 2017-05-02 | 2019-12-12 | Merck Sharp & Dohme Llc | Formulations of anti-LAG3 antibodies and co-formulations of anti-LAG3 antibodies and anti-PD-1 antibodies |
| UY37718A (es) | 2017-05-05 | 2018-11-30 | Novartis Ag | 2-quinolinonas triciclicas como agentes antibacteriales |
| BR112019023855B1 (pt) | 2017-05-12 | 2021-11-30 | Harpoon Therapeutics, Inc | Proteínas de ligação à mesotelina |
| IL322309A (en) | 2017-05-24 | 2025-09-01 | Novartis Ag | IL2 antibody grafted proteins and methods of use in cancer treatment |
| WO2018215937A1 (en) | 2017-05-24 | 2018-11-29 | Novartis Ag | Interleukin-7 antibody cytokine engrafted proteins and methods of use in the treatment of cancer |
| CN111107868A (zh) | 2017-05-24 | 2020-05-05 | 诺华股份有限公司 | 抗体细胞因子移植蛋白及使用方法 |
| WO2018222901A1 (en) | 2017-05-31 | 2018-12-06 | Elstar Therapeutics, Inc. | Multispecific molecules that bind to myeloproliferative leukemia (mpl) protein and uses thereof |
| EP3630834A1 (en) | 2017-05-31 | 2020-04-08 | STCube & Co., Inc. | Methods of treating cancer using antibodies and molecules that immunospecifically bind to btn1a1 |
| KR20200041834A (ko) | 2017-06-01 | 2020-04-22 | 젠코어 인코포레이티드 | Cd123 및 cd3에 결합하는 이중특이성 항체 |
| WO2018223004A1 (en) | 2017-06-01 | 2018-12-06 | Xencor, Inc. | Bispecific antibodies that bind cd20 and cd3 |
| KR20200054160A (ko) | 2017-06-02 | 2020-05-19 | 주노 쎄러퓨티크스 인코퍼레이티드 | 입양 세포 요법을 사용한 치료를 위한 물품 제조 및 방법 |
| CA3061053A1 (en) | 2017-06-02 | 2018-12-06 | Boehringer Ingelheim International Gmbh | Anti-cancer combination therapy |
| CN121609797A (zh) | 2017-06-06 | 2026-03-06 | 斯特库伯株式会社 | 使用结合btn1a1或btn1a1-配体的抗体和分子治疗癌症的方法 |
| WO2019006427A1 (en) | 2017-06-29 | 2019-01-03 | Juno Therapeutics, Inc. | WALL MODEL FOR ASSESSING TOXICITIES ASSOCIATED WITH IMMUNOTHERAPIES |
| KR102677225B1 (ko) | 2017-07-10 | 2024-06-24 | 이나뜨 파르마 에스.에이. | Siglec-9 중화 항체 |
| CN111492245A (zh) | 2017-07-21 | 2020-08-04 | 基因泰克公司 | 癌症的治疗和诊断方法 |
| WO2019025545A1 (en) | 2017-08-04 | 2019-02-07 | Genmab A/S | BINDING AGENTS BINDING TO PD-L1 AND CD137 AND THEIR USE |
| KR20200052327A (ko) | 2017-09-04 | 2020-05-14 | 아게누스 인코포레이티드 | 혼합 계통 백혈병 (mll)-특이적 포스포펩타이드에 결합하는 t 세포 수용체 및 그것의 사용 방법 |
| US20200216542A1 (en) | 2017-09-20 | 2020-07-09 | Chugai Seiyaku Kabushiki Kaisha | Dosage regimen for combination therapy using pd-1 axis binding antagonists and gpc3 targeting agent |
| JP2020535180A (ja) | 2017-09-29 | 2020-12-03 | ベーリンガー インゲルハイム インターナショナル ゲゼルシャフト ミット ベシュレンクテル ハフツング | 抗igf、抗pf−1の抗がん組み合わせ治療 |
| BR112020006809A2 (pt) | 2017-10-06 | 2020-10-06 | Innate Pharma | anticorpos, agente, uso, composto, composição farmacêutica, kits e composição ou uso |
| KR102823603B1 (ko) | 2017-10-12 | 2025-06-23 | 더 보드 오브 리젠츠 오브 더 유니버시티 오브 텍사스 시스템 | 면역요법을 위한 t 세포 수용체 |
| JP7084990B2 (ja) | 2017-10-13 | 2022-06-15 | ハープーン セラピューティクス,インク. | 三重特異性タンパク質と使用方法 |
| IL315737A (en) | 2017-10-13 | 2024-11-01 | Harpoon Therapeutics Inc | B-cell maturation antigen-binding proteins |
| WO2019077062A1 (en) | 2017-10-18 | 2019-04-25 | Vivia Biotech, S.L. | C-CELLS ACTIVATED BY BIT |
| KR20200074997A (ko) | 2017-11-01 | 2020-06-25 | 주노 쎄러퓨티크스 인코퍼레이티드 | B-세포 성숙 항원에 특이적인 항체 및 키메릭 항원 수용체 |
| WO2019089858A2 (en) | 2017-11-01 | 2019-05-09 | Juno Therapeutics, Inc. | Methods of assessing or monitoring a response to a cell therapy |
| KR102845789B1 (ko) | 2017-11-01 | 2025-08-14 | 주노 쎄러퓨티크스 인코퍼레이티드 | B 세포 성숙 항원에 특이적인 키메라 항원 수용체 및 암호화 폴리뉴클레오타이드 |
| CN111601823B (zh) | 2017-11-07 | 2024-09-24 | 德克萨斯大学体系董事会 | 用car-t或car-nk细胞在癌症治疗中靶向lilrb4 |
| EP3710057A1 (en) | 2017-11-14 | 2020-09-23 | Pfizer Inc | Ezh2 inhibitor combination therapies |
| JP2021503458A (ja) | 2017-11-17 | 2021-02-12 | ノバルティス アーゲー | 新規のジヒドロイソキサゾール化合物及びb型肝炎治療のためのそれらの使用 |
| MA50900A (fr) | 2017-11-17 | 2020-09-23 | Merck Sharp & Dohme | Anticorps spécifiques du transcrit 3 de type immunoglobuline (ilt3) et leurs utilisations |
| US20200377571A1 (en) | 2017-12-08 | 2020-12-03 | Elstar Therapeutics, Inc. | Multispecific molecules and uses thereof |
| KR102923958B1 (ko) | 2017-12-15 | 2026-02-06 | 더 보드 오브 리젠츠 오브 더 유니버시티 오브 텍사스 시스템 | 엑소좀 관련 유전자 편집을 이용한 암 치료 방법 및 조성물 |
| WO2019118937A1 (en) | 2017-12-15 | 2019-06-20 | Juno Therapeutics, Inc. | Anti-cct5 binding molecules and methods of use thereof |
| WO2019123285A1 (en) | 2017-12-20 | 2019-06-27 | Novartis Ag | Fused tricyclic pyrazolo-dihydropyrazinyl-pyridone compounds as antivirals |
| WO2019129137A1 (zh) | 2017-12-27 | 2019-07-04 | 信达生物制药(苏州)有限公司 | 抗lag-3抗体及其用途 |
| CN109970856B (zh) | 2017-12-27 | 2022-08-23 | 信达生物制药(苏州)有限公司 | 抗lag-3抗体及其用途 |
| US12247060B2 (en) | 2018-01-09 | 2025-03-11 | Marengo Therapeutics, Inc. | Calreticulin binding constructs and engineered T cells for the treatment of diseases |
| US20200354424A1 (en) | 2018-01-26 | 2020-11-12 | Orionis Biosciences, Inc. | Xcr1 binding agents and uses thereof |
| KR20200128014A (ko) | 2018-01-31 | 2020-11-11 | 셀진 코포레이션 | 입양 세포 요법 및 체크포인트 억제제를 이용한 병용 요법 |
| JP2021511793A (ja) | 2018-01-31 | 2021-05-13 | エフ・ホフマン−ラ・ロシュ・アクチェンゲゼルシャフト | Lag3に結合する抗原結合部位を含む二重特異性抗体 |
| US20200407365A1 (en) | 2018-02-28 | 2020-12-31 | Novartis Ag | Indole-2-carbonyl compounds and their use for the treatment of hepatitis b |
| EP3765085A1 (en) | 2018-03-12 | 2021-01-20 | Université de Paris | Use of caloric restriction mimetics for potentiating chemo-immunotherapy for the treatment of cancers |
| WO2019178362A1 (en) | 2018-03-14 | 2019-09-19 | Elstar Therapeutics, Inc. | Multifunctional molecules that bind to calreticulin and uses thereof |
| WO2019178364A2 (en) | 2018-03-14 | 2019-09-19 | Elstar Therapeutics, Inc. | Multifunctional molecules and uses thereof |
| US12454561B2 (en) | 2018-03-19 | 2025-10-28 | Multivir Inc. | Methods and compositions comprising tumor suppressor gene therapy and CD122/CD132 agonists for the treatment of cancer |
| US10760075B2 (en) | 2018-04-30 | 2020-09-01 | Snipr Biome Aps | Treating and preventing microbial infections |
| WO2019185551A1 (en) | 2018-03-25 | 2019-10-03 | Snipr Biome Aps. | Treating & preventing microbial infections |
| WO2019191279A2 (en) | 2018-03-27 | 2019-10-03 | Board Of Regents, The University Of Texas System | Compounds with anti-tumor activity against cancer cells bearing her2 exon 19 mutations |
| AU2019254237B2 (en) | 2018-04-16 | 2025-01-30 | Onquality Pharmaceuticals China Ltd. | Method for preventing or treating side effects of cancer therapy |
| EP3781596A1 (en) | 2018-04-18 | 2021-02-24 | Xencor, Inc. | Il-15/il-15ra heterodimeric fc fusion proteins and uses thereof |
| MX2020010910A (es) | 2018-04-18 | 2021-02-09 | Xencor Inc | Proteinas de fusion heterodimericas dirigidas a pd-1 que contienen proteinas de fusion il-15 / il-15ra fc y dominios de union al antigeno pd-1 y usos de los mismos. |
| US11065317B2 (en) | 2018-04-26 | 2021-07-20 | Agenus Inc. | Heat shock protein-binding peptide compositions and methods of use thereof |
| WO2019210153A1 (en) | 2018-04-27 | 2019-10-31 | Novartis Ag | Car t cell therapies with enhanced efficacy |
| EP3788369A1 (en) | 2018-05-01 | 2021-03-10 | Novartis Ag | Biomarkers for evaluating car-t cells to predict clinical outcome |
| BR112020022294A2 (pt) | 2018-05-04 | 2021-02-23 | Tollys | composição e uso de uma composição |
| EP3569618A1 (en) | 2018-05-19 | 2019-11-20 | Boehringer Ingelheim International GmbH | Antagonizing cd73 antibody |
| CN112165974B (zh) | 2018-05-31 | 2024-11-08 | 诺华股份有限公司 | 乙型肝炎抗体 |
| TW202017569A (zh) | 2018-05-31 | 2020-05-16 | 美商佩樂敦治療公司 | 用於抑制cd73之組合物及方法 |
| CA3102256A1 (en) | 2018-06-01 | 2019-12-05 | Novartis Ag | Dosing of a bispecific antibody that bind cd123 and cd3 |
| JP7403479B2 (ja) | 2018-06-03 | 2023-12-22 | ランカプ バイオ ベータ リミテッド | Ceacam5およびcd47に対する二重特異性抗体 |
| CA3103610A1 (en) | 2018-06-12 | 2019-12-19 | The Regents Of The University Of California | Single-chain bispecific chimeric antigen receptors for the treatment of cancer |
| JP7438988B2 (ja) | 2018-06-13 | 2024-02-27 | ノバルティス アーゲー | Bcmaキメラ抗原受容体及びその使用 |
| PT3807316T (pt) | 2018-06-18 | 2024-07-29 | Innate Pharma | Composições e métodos para tratamento de cancro |
| AU2019288728A1 (en) | 2018-06-23 | 2021-01-14 | Genentech, Inc. | Methods of treating lung cancer with a pd-1 axis binding antagonist, a platinum agent, and a topoisomerase ii inhibitor |
| CA3105448A1 (en) | 2018-07-03 | 2020-01-09 | Elstar Therapeutics, Inc. | Anti-tcr antibody molecules and uses thereof |
| AR116109A1 (es) | 2018-07-10 | 2021-03-31 | Novartis Ag | Derivados de 3-(5-amino-1-oxoisoindolin-2-il)piperidina-2,6-diona y usos de los mismos |
| BR122022012697B1 (pt) | 2018-07-10 | 2023-04-04 | Novartis Ag | Usos de derivados de 3-(5-hidróxi-1-oxoisoindolin-2-il)piperidina-2,6- diona, e kit |
| BR112021000673A2 (pt) | 2018-07-18 | 2021-04-20 | Genentech, Inc. | métodos para tratar um indivíduo com câncer de pulmão, kits, anticorpo anti-pd-l1 e composições |
| WO2020048942A1 (en) | 2018-09-04 | 2020-03-12 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Methods and pharmaceutical compositions for enhancing cytotoxic t lymphocyte-dependent immune responses |
| AU2019336197A1 (en) | 2018-09-07 | 2021-02-18 | Pfizer Inc. | Anti-avb8 antibodies and compositions and uses thereof |
| WO2020053742A2 (en) | 2018-09-10 | 2020-03-19 | Novartis Ag | Anti-hla-hbv peptide antibodies |
| WO2020053654A1 (en) | 2018-09-12 | 2020-03-19 | Novartis Ag | Antiviral pyridopyrazinedione compounds |
| EP3853251A1 (en) | 2018-09-19 | 2021-07-28 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Methods and pharmaceutical composition for the treatment of cancers resistant to immune checkpoint therapy |
| US12195544B2 (en) | 2018-09-21 | 2025-01-14 | Harpoon Therapeutics, Inc. | EGFR binding proteins and methods of use |
| CN113286817B (zh) | 2018-09-25 | 2025-01-28 | 哈普恩治疗公司 | Dll3结合蛋白及使用方法 |
| WO2020069372A1 (en) | 2018-09-27 | 2020-04-02 | Elstar Therapeutics, Inc. | Csf1r/ccr2 multispecific antibodies |
| US20210347851A1 (en) | 2018-09-28 | 2021-11-11 | Novartis Ag | Cd19 chimeric antigen receptor (car) and cd22 car combination therapies |
| WO2020069405A1 (en) | 2018-09-28 | 2020-04-02 | Novartis Ag | Cd22 chimeric antigen receptor (car) therapies |
| IL305106B2 (en) | 2018-09-29 | 2025-08-01 | Novartis Ag | Process of manufacture of a compound for inhibiting the activity of shp2 |
| WO2020070053A1 (en) | 2018-10-01 | 2020-04-09 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Use of inhibitors of stress granule formation for targeting the regulation of immune responses |
| MX2021003765A (es) | 2018-10-03 | 2021-07-15 | Xencor Inc | Proteínas il-12 de fusión a fc heterodimérico. |
| US20210388101A1 (en) | 2018-10-15 | 2021-12-16 | Industry-Academic Cooperation Foundation, Yonsei University | Productivity-enhanced antibody and method for producing same |
| JP7467438B2 (ja) | 2018-10-18 | 2024-04-15 | メルク・シャープ・アンド・ドーム・エルエルシー | 抗rsv抗体の製剤及びその使用方法 |
| AU2019369299A1 (en) | 2018-10-29 | 2021-05-20 | Wisconsin Alumni Research Foundation | Dendritic polymers complexed with immune checkpoint inhibitors for enhanced cancer immunotherapy |
| US11564995B2 (en) | 2018-10-29 | 2023-01-31 | Wisconsin Alumni Research Foundation | Peptide-nanoparticle conjugates |
| CN113015748B (zh) | 2018-10-31 | 2025-12-12 | 默沙东有限责任公司 | 抗人pd-1抗体晶体及其使用方法 |
| US20230053449A1 (en) | 2018-10-31 | 2023-02-23 | Novartis Ag | Dc-sign antibody drug conjugates |
| CA3116413A1 (en) | 2018-11-01 | 2020-05-07 | Juno Therapeutics, Inc. | Chimeric antigen receptors specific for g protein-coupled receptor class c group 5 member d (gprc5d) |
| MX2021005024A (es) | 2018-11-01 | 2021-07-21 | Juno Therapeutics Inc | Metodos de tratamiento que utilizan receptores de antigenos quimericos especificos para antigeno de maduracion de celulas b. |
| CN113316458B (zh) | 2018-11-07 | 2024-08-02 | 默沙东有限责任公司 | 抗lag3抗体和抗pd-1抗体的共制剂 |
| CA3118892A1 (en) | 2018-11-08 | 2020-05-14 | Orionis Biosciences, Inc. | Modulation of dendritic cell lineages |
| SG11202105084VA (en) | 2018-11-16 | 2021-06-29 | Juno Therapeutics Inc | Methods of dosing engineered t cells for the treatment of b cell malignancies |
| JP7630832B2 (ja) | 2018-11-19 | 2025-02-18 | ボード オブ リージェンツ,ザ ユニバーシティ オブ テキサス システム | Carおよびtcr形質導入用のモジュール式ポリシストロニックベクター |
| EP3947715A4 (en) | 2018-11-21 | 2022-11-23 | Board of Regents, The University of Texas System | METHODS AND COMPOSITIONS FOR THE TREATMENT OF CANCER |
| BR112021010297A2 (pt) | 2018-11-28 | 2021-08-24 | Board Of Regents, The University Of Texas System | Edição de genomas multiplexadores de células imunes para aumentar a funcionalidade e resistência ao ambiente supressivo |
| US20220018828A1 (en) | 2018-11-28 | 2022-01-20 | Inserm (Institut National De La Santé Et La Recherche Médicale | Methods and kit for assaying lytic potential of immune effector cells |
| WO2020112493A1 (en) | 2018-11-29 | 2020-06-04 | Board Of Regents, The University Of Texas System | Methods for ex vivo expansion of natural killer cells and use thereof |
| FI3886875T3 (fi) | 2018-11-30 | 2024-07-23 | Juno Therapeutics Inc | Adoptiivista soluterapiaa käyttäviä hoitomenetelmiä |
| EP3891270A1 (en) | 2018-12-07 | 2021-10-13 | Institut National de la Santé et de la Recherche Médicale (INSERM) | Use of cd26 and cd39 as new phenotypic markers for assessing maturation of foxp3+ t cells and uses thereof for diagnostic purposes |
| CN113195467A (zh) | 2018-12-11 | 2021-07-30 | 施万生物制药研发Ip有限责任公司 | 适用作alk5抑制剂的萘啶和喹啉衍生物 |
| US20220047556A1 (en) | 2018-12-17 | 2022-02-17 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Use of sulconazole as a furin inhibitor |
| MX2021007392A (es) | 2018-12-20 | 2021-08-24 | Novartis Ag | Regimen de dosificacion y combinacion farmaceutica que comprende derivados de 3-(1-oxoisoindolin-2-il)piperidina-2,6-diona. |
| CN113438961A (zh) | 2018-12-20 | 2021-09-24 | Xencor股份有限公司 | 含有IL-15/IL-15Rα和NKG2D抗原结合结构域的靶向异二聚体Fc融合蛋白 |
| MX2021007271A (es) | 2018-12-21 | 2021-07-15 | Onxeo | Nuevas moleculas de acido nucleico conjugado y sus usos. |
| KR20240052881A (ko) | 2018-12-21 | 2024-04-23 | 노파르티스 아게 | Pmel17에 대한 항체 및 이의 접합체 |
| SG11202107606VA (en) | 2019-01-15 | 2021-08-30 | Inst Nat Sante Rech Med | Mutated interleukin-34 (il-34) polypeptides and uses thereof in therapy |
| TWI894135B (zh) | 2019-01-25 | 2025-08-21 | 德商百靈佳殷格翰國際股份有限公司 | 編碼ccl21之重組棒狀病毒 |
| CN113365660A (zh) | 2019-01-29 | 2021-09-07 | 朱诺治疗学股份有限公司 | 对受体酪氨酸激酶样孤儿受体1(ror1)具特异性的抗体及嵌合抗原受体 |
| KR20210126078A (ko) | 2019-02-13 | 2021-10-19 | 더 브리검 앤드 우먼즈 하스피털, 인크. | 항-말초 림프절 어드레신 항체 및 그의 용도 |
| WO2020165834A1 (en) | 2019-02-15 | 2020-08-20 | Novartis Ag | Substituted 3-(1-oxoisoindolin-2-yl)piperidine-2,6-dione derivatives and uses thereof |
| BR112021015783A2 (pt) | 2019-02-15 | 2021-10-05 | Novartis Ag | Derivados de 3-(1-oxo-5-(piperidin-4-il)isoindolin-2-il)piperidina-2,6-diona e usos dos mesmos |
| WO2020169472A2 (en) | 2019-02-18 | 2020-08-27 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Methods of inducing phenotypic changes in macrophages |
| GB2597851B (en) | 2019-02-21 | 2024-05-29 | Marengo Therapeutics Inc | Antibody molecules that bind to NKP30 and uses thereof |
| EP3927744A1 (en) | 2019-02-21 | 2021-12-29 | Marengo Therapeutics, Inc. | Multifunctional molecules that bind to t cell related cancer cells and uses thereof |
| US20220184121A1 (en) | 2019-03-18 | 2022-06-16 | The Regents Of The University Of California | Augmentation of t-cell activation by oscillatory forces and engineered antigen-presenting cells |
| WO2020201362A2 (en) | 2019-04-02 | 2020-10-08 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Methods of predicting and preventing cancer in patients having premalignant lesions |
| WO2020208060A1 (en) | 2019-04-09 | 2020-10-15 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Use of sk2 inhibitors in combination with immune checkpoint blockade therapy for the treatment of cancer |
| EP3956446A1 (en) | 2019-04-17 | 2022-02-23 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Methods and compositions for treatment of nlrp3 inflammasome mediated il-1beta dependent disorders |
| MX2021012692A (es) | 2019-04-19 | 2021-11-12 | Genentech Inc | Anticuerpos anti-mertk y sus metodos de uso. |
| MX2021012769A (es) | 2019-04-23 | 2021-11-18 | Innate Pharma | Anticuerpos bloqueadores cd73. |
| CA3138348A1 (en) | 2019-05-09 | 2020-11-12 | FUJIFILM Cellular Dynamics, Inc. | Methods for the production of hepatocytes |
| EP3969040A1 (en) | 2019-05-13 | 2022-03-23 | Regeneron Pharmaceuticals, Inc. | Combination of pd-1 inhibitors and lag-3 inhibitors for enhanced efficacy in treating cancer |
| EP3968971A1 (en) | 2019-05-17 | 2022-03-23 | Cancer Prevention Pharmaceuticals, Inc. | Methods for treating familial adenomatous polyposis |
| CA3144533A1 (en) | 2019-06-03 | 2020-12-10 | The University Of Chicago | Methods and compositions for treating cancer with cancer-targeted adjuvants |
| AU2020289485A1 (en) | 2019-06-03 | 2022-02-03 | The University Of Chicago | Methods and compositions for treating cancer with collagen binding drug carriers |
| EP3986454A1 (en) | 2019-06-18 | 2022-04-27 | Janssen Sciences Ireland Unlimited Company | Combination of hepatitis b virus (hbv) vaccines and anti-pd-1 or anti-pd-l1 antibody |
| US20220349890A1 (en) * | 2019-06-18 | 2022-11-03 | Arizona Board Of Regents On Behalf Of The University Of Arizona | A method for predicting risk of recurrence for early-stage colon cancer by measuring focal adhesion kinase |
| CA3143634A1 (en) | 2019-06-18 | 2020-12-24 | Janssen Sciences Ireland Unlimited Company | Combination of hepatitis b virus (hbv) vaccines and anti-pd-1 antibody |
| WO2021024020A1 (en) | 2019-08-06 | 2021-02-11 | Astellas Pharma Inc. | Combination therapy involving antibodies against claudin 18.2 and immune checkpoint inhibitors for treatment of cancer |
| US12098212B2 (en) | 2019-08-12 | 2024-09-24 | Purinomia Biotech, Inc. | Methods and compositions for promoting and potentiating T-cell mediated immune responses through ADCC targeting of CD39 expressing cells |
| WO2021042066A1 (en) | 2019-08-30 | 2021-03-04 | Foundation Medicine, Inc. | Kmt2a-maml2 fusion molecules and uses thereof |
| AU2020335928A1 (en) | 2019-08-30 | 2022-02-17 | Agenus Inc. | Anti-CD96 antibodies and methods of use thereof |
| BR112022004995A2 (pt) | 2019-09-18 | 2022-06-21 | Lamkap Bio Alpha AG | Anticorpos biespecíficos contra ceacam5 e cd3 |
| CR20220107A (es) | 2019-09-18 | 2022-04-25 | Novartis Ag | Proteínas de fusión nkg2d y sus usos |
| CN114667285B (zh) | 2019-09-26 | 2025-08-08 | 诺华股份有限公司 | 抗病毒吡唑并吡啶酮化合物 |
| EP3800201A1 (en) | 2019-10-01 | 2021-04-07 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Cd28h stimulation enhances nk cell killing activities |
| EP4037700A2 (en) | 2019-10-03 | 2022-08-10 | Xencor, Inc. | Targeted il-12 heterodimeric fc-fusion proteins |
| WO2021064184A1 (en) | 2019-10-04 | 2021-04-08 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Methods and pharmaceutical composition for the treatment of ovarian cancer, breast cancer or pancreatic cancer |
| TW202128757A (zh) | 2019-10-11 | 2021-08-01 | 美商建南德克公司 | 具有改善之特性的 PD-1 標靶 IL-15/IL-15Rα FC 融合蛋白 |
| US20220380765A1 (en) | 2019-11-02 | 2022-12-01 | Board Of Regents, The University Of Texas System | Targeting nonsense-mediated decay to activate p53 pathway for the treatment of cancer |
| TWI895295B (zh) | 2019-11-12 | 2025-09-01 | 美商方得生醫療公司 | 偵測編碼新生抗原之融合基因之方法 |
| EP4061809A1 (en) | 2019-11-22 | 2022-09-28 | Theravance Biopharma R&D IP, LLC | Substituted 1,5-naphthyridines or quinolines as alk5 inhibitors |
| IL292924A (en) | 2019-11-26 | 2022-07-01 | Novartis Ag | Chimeric antigen receptors cd19 and cd22 and their uses |
| EP3831849A1 (en) | 2019-12-02 | 2021-06-09 | LamKap Bio beta AG | Bispecific antibodies against ceacam5 and cd47 |
| JP2023504568A (ja) | 2019-12-04 | 2023-02-03 | オルナ セラピューティクス インコーポレイテッド | 環状rna組成物及び方法 |
| WO2021113644A1 (en) | 2019-12-05 | 2021-06-10 | Multivir Inc. | Combinations comprising a cd8+ t cell enhancer, an immune checkpoint inhibitor and radiotherapy for targeted and abscopal effects for the treatment of cancer |
| CN113045655A (zh) | 2019-12-27 | 2021-06-29 | 高诚生物医药(香港)有限公司 | 抗ox40抗体及其用途 |
| EP4084823A4 (en) | 2020-01-03 | 2024-05-15 | Marengo Therapeutics, Inc. | ANTI-TCR ANTIBODY MOLECULES AND THEIR USES |
| WO2021138407A2 (en) | 2020-01-03 | 2021-07-08 | Marengo Therapeutics, Inc. | Multifunctional molecules that bind to cd33 and uses thereof |
| US11396647B2 (en) | 2020-01-07 | 2022-07-26 | Board Of Regents, The University Of Texas System | Human methylthioadenosine/adenosine depleting enzyme variants for cancer therapy |
| JP2023511439A (ja) | 2020-01-28 | 2023-03-17 | ジェネンテック, インコーポレイテッド | がんの治療のためのil15/il15rアルファヘテロ二量体fc融合タンパク質 |
| EP4096789A4 (en) | 2020-01-29 | 2023-10-11 | Board of Regents, The University of Texas System | USE OF POZIOTINIB TO TREAT CANCER WITH NRG1 FUSIONS |
| CN115362270A (zh) | 2020-01-29 | 2022-11-18 | 得克萨斯州大学系统董事会 | Egfr/her2酪氨酸激酶抑制剂和/或her2/her3抗体在具有nrg1融合的癌症的治疗中的用途 |
| EP4107173A1 (en) | 2020-02-17 | 2022-12-28 | Board of Regents, The University of Texas System | Methods for expansion of tumor infiltrating lymphocytes and use thereof |
| IL295896A (en) | 2020-02-26 | 2022-10-01 | Biograph 55 Inc | c19 c38 bispecific antibodies |
| WO2021171264A1 (en) | 2020-02-28 | 2021-09-02 | Novartis Ag | Dosing of a bispecific antibody that binds cd123 and cd3 |
| WO2021176330A1 (en) | 2020-03-03 | 2021-09-10 | Array Biopharma Inc. | Methods to treat cancer using (r)-n-(3-fluoro-4-((3-((1-hydroxypropan-2-yl)amino)-1h-pyrazolo[3,4-b]pyridin-4-yl)oxy)phenyl)-3-(4-fluorophenyl)-1-isopropyl-2,4-dioxo-1,2,3,4-tetrahydropyrimidine-5-carboxamide |
| JP2023518295A (ja) | 2020-03-20 | 2023-04-28 | オルナ セラピューティクス インコーポレイテッド | 環状rna組成物及び方法 |
| WO2021191870A1 (en) | 2020-03-27 | 2021-09-30 | Dcprime B.V. | Ex vivo use of modified cells of leukemic origin for enhancing the efficacy of adoptive cell therapy |
| EP4126824A1 (en) | 2020-03-31 | 2023-02-08 | Theravance Biopharma R&D IP, LLC | Substituted pyrimidines and methods of use |
| BR112022020333A2 (pt) | 2020-04-10 | 2022-11-22 | Juno Therapeutics Inc | Métodos e usos relacionados à terapia celular projetada com um receptor de antígeno quimérico que alveja o antígeno de maturação de células b |
| US20230181756A1 (en) | 2020-04-30 | 2023-06-15 | Novartis Ag | Ccr7 antibody drug conjugates for treating cancer |
| EP4153316A1 (en) | 2020-05-19 | 2023-03-29 | Boehringer Ingelheim International GmbH | Binding molecules for the treatment of cancer |
| TW202208418A (zh) | 2020-05-21 | 2022-03-01 | 美國德州系統大學評議委員會 | 具有vgll1特異性之t細胞受體及其用途 |
| MX2022014943A (es) | 2020-05-26 | 2023-03-08 | Inst Nat Sante Rech Med | Polipéptidos de coronavirus 2 causante del síndrome respiratorio agudo severo (sars-cov-2) y usos de los mismos para propositos de vacuna. |
| JP7565384B2 (ja) | 2020-06-03 | 2024-10-10 | ベーリンガー インゲルハイム インターナショナル ゲゼルシャフト ミット ベシュレンクテル ハフツング | CD80細胞外ドメインFc融合タンパク質をコードするリコンビナントラブドウイルス |
| WO2021247836A1 (en) | 2020-06-03 | 2021-12-09 | Board Of Regents, The University Of Texas System | Methods for targeting shp-2 to overcome resistance |
| US20210387983A1 (en) | 2020-06-10 | 2021-12-16 | Theravance Biopharma R&D Ip, Llc | Crystalline alk5 inhibitors and uses thereof |
| KR20230024967A (ko) | 2020-06-11 | 2023-02-21 | 노파르티스 아게 | Zbtb32 억제제 및 이의 용도 |
| TW202214857A (zh) | 2020-06-19 | 2022-04-16 | 法商昂席歐公司 | 新型結合核酸分子及其用途 |
| WO2021260528A1 (en) | 2020-06-23 | 2021-12-30 | Novartis Ag | Dosing regimen comprising 3-(1-oxoisoindolin-2-yl)piperidine-2,6-dione derivatives |
| JP2023531537A (ja) | 2020-06-30 | 2023-07-24 | メンドゥス・ベスローテン・フェンノートシャップ | 卵巣癌ワクチンでの白血病由来細胞の使用 |
| US20250262293A1 (en) | 2020-07-07 | 2025-08-21 | BioNTech SE | Therapeutic rna for hpv-positive cancer |
| JP7819176B2 (ja) | 2020-08-03 | 2026-02-24 | ノバルティス アーゲー | ヘテロアリール置換3-(1-オキソイソインドリン-2-イル)ピペリジン-2,6-ジオン誘導体及びその使用 |
| IL300328A (en) | 2020-08-26 | 2023-04-01 | Regeneron Pharma | Methods for treating cancer by administering a PD-1 inhibitor |
| JP2023540248A (ja) | 2020-08-26 | 2023-09-22 | マレンゴ・セラピューティクス,インコーポレーテッド | Trbc1またはtrbc2を検出する方法 |
| CA3188236A1 (en) | 2020-09-14 | 2022-03-17 | Boehringer Ingelheim International Gmbh | Heterologous prime boost vaccine |
| WO2022084210A1 (en) | 2020-10-20 | 2022-04-28 | F. Hoffmann-La Roche Ag | Combination therapy of pd-1 axis binding antagonists and lrrk2 inhitibors |
| AR123855A1 (es) | 2020-10-20 | 2023-01-18 | Genentech Inc | Anticuerpos anti-mertk conjugados con peg y métodos de uso |
| MX2023005192A (es) | 2020-11-04 | 2023-05-15 | Heidelberg Pharma Res Gmbh | Composicion que comprende una combinacion de inhibidor de punto de control inmunitario y conjugado de anticuerpo-amatoxina para uso en la terapia del cancer. |
| EP4240377A4 (en) | 2020-11-05 | 2025-01-15 | Board of Regents, The University of Texas System | Engineered t cell receptors targeting egfr antigens and methods of use |
| CA3200878A1 (en) | 2020-11-12 | 2022-05-19 | Inserm (Institut National De La Sante Et De La Recherche Medicale) | Antibodies conjugated or fused to the receptor-binding domain of the sars-cov-2 spike protein and uses thereof for vaccine purposes |
| CA3201499A1 (en) | 2020-11-13 | 2022-05-19 | Catamaran Bio, Inc. | Genetically modified natural killer cells and methods of use thereof |
| WO2022101463A1 (en) | 2020-11-16 | 2022-05-19 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Use of the last c-terminal residues m31/41 of zikv m ectodomain for triggering apoptotic cell death |
| CA3204091A1 (en) | 2020-12-08 | 2022-06-16 | Infinity Pharmaceuticals, Inc. | Eganelisib for use in the treatment of pd-l1 negative cancer |
| RS65211B1 (sr) | 2020-12-18 | 2024-03-29 | Lamkap Bio Beta Ag | Bispecifična antitela protiv ceacam5 i cd47 |
| WO2022135666A1 (en) | 2020-12-21 | 2022-06-30 | BioNTech SE | Treatment schedule for cytokine proteins |
| WO2022135667A1 (en) | 2020-12-21 | 2022-06-30 | BioNTech SE | Therapeutic rna for treating cancer |
| TW202245808A (zh) | 2020-12-21 | 2022-12-01 | 德商拜恩迪克公司 | 用於治療癌症之治療性rna |
| WO2022159492A1 (en) | 2021-01-19 | 2022-07-28 | William Marsh Rice University | Bone-specific delivery of polypeptides |
| EP4281102A1 (en) | 2021-01-22 | 2023-11-29 | Mendus B.V. | Methods of tumor vaccination |
| CA3210196A1 (en) | 2021-01-29 | 2022-08-04 | Board Of Regents, The University Of Texas System | Methods of treating cancer with kinase inhibitors |
| CN117222413A (zh) | 2021-02-10 | 2023-12-12 | 同润生物医药(上海)有限公司 | 治疗肿瘤的方法和组合 |
| EP4301784A4 (en) * | 2021-03-02 | 2025-01-01 | NovaRock Biotherapeutics, Ltd. | Antibodies against claudin-6 and uses thereof |
| JP2024510947A (ja) | 2021-03-05 | 2024-03-12 | レアダルティス、ソシエダッド リミターダ | 三量体ポリペプチドおよびがん治療におけるその使用 |
| CA3212351A1 (en) | 2021-03-12 | 2022-09-15 | Mendus B.V. | Methods of vaccination and use of cd47 blockade |
| WO2022194988A2 (en) | 2021-03-19 | 2022-09-22 | Heidelberg Pharma Research Gmbh | B-lymphocyte specific amatoxin antibody conjugates |
| MX2023011007A (es) | 2021-03-23 | 2023-12-07 | Regeneron Pharma | Metodos para tratar el cancer en pacientes inmunosuprimidos o inmunocomprometidos mediante la administracion de un inhibidor de pd-1. |
| TW202304506A (zh) | 2021-03-25 | 2023-02-01 | 日商安斯泰來製藥公司 | 涉及抗claudin 18.2抗體的組合治療以治療癌症 |
| KR20240004462A (ko) | 2021-04-08 | 2024-01-11 | 마렝고 테라퓨틱스, 인크. | Tcr에 결합하는 다기능성 분자 및 이의 용도 |
| AU2022254104A1 (en) | 2021-04-08 | 2023-10-26 | Nurix Therapeutics, Inc. | Combination therapies with cbl-b inhibitor compounds |
| WO2022216979A1 (en) | 2021-04-08 | 2022-10-13 | Board Of Regents, The University Of Texas System | Compounds and methods for theranostic targeting of parp activity |
| US20240239895A1 (en) | 2021-04-09 | 2024-07-18 | Genentech, Inc. | Combination therapy with a raf inhibitor and a pd-1 axis inhibitor |
| US20240228659A1 (en) | 2021-04-14 | 2024-07-11 | INSERM (Institut National de la Santé et de la Recherche Médicale) | New method to improve nk cells cytotoxicity |
| CA3216880A1 (en) | 2021-04-16 | 2022-10-20 | Novartis Ag | Antibody drug conjugates and methods for making thereof |
| AR125874A1 (es) | 2021-05-18 | 2023-08-23 | Novartis Ag | Terapias de combinación |
| CN117396222A (zh) | 2021-05-21 | 2024-01-12 | 天津立博美华基因科技有限责任公司 | 药物组合及其用途 |
| WO2022251359A1 (en) | 2021-05-26 | 2022-12-01 | Theravance Biopharma R&D Ip, Llc | Bicyclic inhibitors of alk5 and methods of use |
| WO2022254337A1 (en) | 2021-06-01 | 2022-12-08 | Novartis Ag | Cd19 and cd22 chimeric antigen receptors and uses thereof |
| EP4367269A1 (en) | 2021-07-05 | 2024-05-15 | Inserm (Institut National De La Sante Et De La Recherche Medicale) | Gene signatures for predicting survival time in patients suffering from renal cell carcinoma |
| MX2024000674A (es) | 2021-07-13 | 2024-02-07 | BioNTech SE | Agentes de union multiespecificos contra cd40 y cd137 en terapia de combinacion. |
| WO2023015198A1 (en) | 2021-08-04 | 2023-02-09 | Genentech, Inc. | Il15/il15r alpha heterodimeric fc-fusion proteins for the expansion of nk cells in the treatment of solid tumours |
| IL310550A (en) | 2021-08-04 | 2024-03-01 | Univ Colorado Regents | LAT-activating chimeric antigen receptor T cells and methods of using them |
| CA3231180A1 (en) | 2021-09-08 | 2023-03-16 | Redona Therapeutics, Inc. | Papd5 and/or papd7 inhibiting 4-oxo-1,4-dihydroquinoline-3-carboxylic acid derivatives |
| WO2023056361A1 (en) | 2021-09-29 | 2023-04-06 | Board Of Regents, The University Of Texas System | Anti-hsp70 antibodies and therapeutic uses thereof |
| WO2023051926A1 (en) | 2021-09-30 | 2023-04-06 | BioNTech SE | Treatment involving non-immunogenic rna for antigen vaccination and pd-1 axis binding antagonists |
| IL311790A (en) | 2021-10-05 | 2024-05-01 | Chang Hao Ming | Natural killer cells and methods of use thereof |
| US20250002600A1 (en) | 2021-10-06 | 2025-01-02 | Genmab A/S | Multispecific binding agents against pd-l1 and cd137 in combination therapy |
| TW202333802A (zh) | 2021-10-11 | 2023-09-01 | 德商拜恩迪克公司 | 用於肺癌之治療性rna(二) |
| TW202330612A (zh) | 2021-10-20 | 2023-08-01 | 日商武田藥品工業股份有限公司 | 靶向bcma之組合物及其使用方法 |
| WO2023076880A1 (en) | 2021-10-25 | 2023-05-04 | Board Of Regents, The University Of Texas System | Foxo1-targeted therapy for the treatment of cancer |
| WO2023083439A1 (en) | 2021-11-09 | 2023-05-19 | BioNTech SE | Tlr7 agonist and combinations for cancer treatment |
| CN118765283A (zh) | 2021-11-17 | 2024-10-11 | 国家健康科学研究所 | 通用沙贝病毒疫苗 |
| US20240294926A1 (en) | 2021-12-16 | 2024-09-05 | Valerio Therapeutics | New conjugated nucleic acid molecules and their uses |
| WO2023129438A1 (en) | 2021-12-28 | 2023-07-06 | Wisconsin Alumni Research Foundation | Hydrogel compositions for use for depletion of tumor associated macrophages |
| WO2023142996A1 (zh) | 2022-01-28 | 2023-08-03 | 上海岸阔医药科技有限公司 | 预防或治疗与抗肿瘤剂相关的疾病或病症的方法 |
| WO2023154799A1 (en) | 2022-02-14 | 2023-08-17 | The United States Of America, As Represented By The Secretary, Department Of Health And Human Services | Combination immunotherapy for treating cancer |
| TWI864587B (zh) | 2022-02-14 | 2024-12-01 | 美商基利科學股份有限公司 | 抗病毒吡唑并吡啶酮化合物 |
| CA3243885A1 (en) | 2022-02-17 | 2023-08-24 | Vyriad, Inc. | COMBINATIONS OF CHECKPOINT INHIBITORS AND ONCOLYTIC VIRUS FOR CANCER TREATMENT |
| KR20240150493A (ko) | 2022-02-21 | 2024-10-15 | 온퀄리티 파마슈티컬스 차이나 리미티드 | 화합물 및 그 용도 |
| JP2025515324A (ja) | 2022-04-28 | 2025-05-14 | エムユーエスシー ファウンデーション フォー リサーチ ディベロップメント | がんを処置するためのキメラ抗原受容体改変調節性t細胞 |
| WO2023214325A1 (en) | 2022-05-05 | 2023-11-09 | Novartis Ag | Pyrazolopyrimidine derivatives and uses thereof as tet2 inhibitors |
| AU2023269545A1 (en) | 2022-05-12 | 2024-11-14 | BioNTech SE | Binding agents capable of binding to cd27 in combination therapy |
| KR20250025384A (ko) | 2022-06-16 | 2025-02-21 | 람카프 바이오 베타 엘티디. | Ceacam5 및 cd47에 대한 이중특이적 항체 및 ceacam5 및 cd3에 대한 이중특이적 항체의 조합 요법 |
| US20250381272A1 (en) | 2022-06-22 | 2025-12-18 | Juno Therapeutics, Inc. | Treatment methods for second line therapy of cd19-targeted car t cells |
| GB202209518D0 (en) | 2022-06-29 | 2022-08-10 | Snipr Biome Aps | Treating & preventing E coli infections |
| WO2024028794A1 (en) | 2022-08-02 | 2024-02-08 | Temple Therapeutics BV | Methods for treating endometrial and ovarian hyperproliferative disorders |
| KR20250047766A (ko) | 2022-08-05 | 2025-04-04 | 주노 쎄러퓨티크스 인코퍼레이티드 | Gprc5d 및 bcma에 특이적인 키메라 항원 수용체 |
| EP4583860A1 (en) | 2022-09-06 | 2025-07-16 | Institut National de la Santé et de la Recherche Médicale | Inhibitors of the ceramide metabolic pathway for overcoming immunotherapy resistance in cancer |
| KR20250099224A (ko) | 2022-11-01 | 2025-07-01 | 하이델베르크 파마 리서치 게엠베하 | 항-gucy2c 항체 및 이의 용도 |
| EP4626446A1 (en) | 2022-12-01 | 2025-10-08 | BioNTech SE | Multispecific antibody against cd40 and cd137 in combination therapy with anti-pd1 ab and chemotherapy |
| CN120712102A (zh) | 2022-12-13 | 2025-09-26 | 朱诺治疗学股份有限公司 | 对baff-r和cd19具特异性的嵌合抗原受体及其方法和用途 |
| IL321098A (en) | 2022-12-14 | 2025-07-01 | Astellas Pharma Europe Bv | Combination therapy including bispecific binding agents that bind to CLDN18.2- and CD3- and immune checkpoint inhibitors |
| CN121002071A (zh) | 2023-01-20 | 2025-11-21 | 勃林格殷格翰国际有限公司 | IL-12 Fc融合蛋白 |
| EP4658687A1 (en) | 2023-01-31 | 2025-12-10 | University of Rochester | Immune checkpoint blockade therapy for treating staphylococcus aureus infections |
| EP4680285A1 (en) | 2023-03-13 | 2026-01-21 | Heidelberg Pharma Research GmbH | Subcutaneously administered antibody-drug conjugates for use in cancer treatment |
| KR20250155054A (ko) | 2023-03-13 | 2025-10-29 | 리제너론 파마슈티칼스 인코포레이티드 | 흑색종 치료에서의 효능 강화를 위한 pd-1 억제제와 lag-3 억제제의 병용 |
| TW202440636A (zh) | 2023-03-21 | 2024-10-16 | 美商傳記55有限公司 | Cd19/cd38多特異性抗體 |
| WO2024209072A1 (en) | 2023-04-06 | 2024-10-10 | Genmab A/S | Multispecific binding agents against pd-l1 and cd137 for treating cancer |
| WO2024216028A1 (en) | 2023-04-12 | 2024-10-17 | Agenus Inc. | Methods of treating cancer using an anti-ctla4 antibody and an enpp1 inhibitor |
| WO2024213767A1 (en) | 2023-04-14 | 2024-10-17 | Institut National de la Santé et de la Recherche Médicale | Engraftment of mesenchymal stromal cells engineered to stimulate immune infiltration in tumors |
| TW202509071A (zh) | 2023-05-12 | 2025-03-01 | 丹麥商珍美寶股份有限公司 | 能夠與ox40結合之抗體、其變異體及其用途 |
| WO2024261302A1 (en) | 2023-06-22 | 2024-12-26 | Institut National de la Santé et de la Recherche Médicale | Nlrp3 inhibitors, pak1/2 inhibitors and/or caspase 1 inhibitors for use in the treatment of rac2 monogenic disorders |
| WO2025003193A1 (en) | 2023-06-26 | 2025-01-02 | Institut National de la Santé et de la Recherche Médicale | Sertraline and indatraline for disrupting intracellular cholesterol trafficking and subsequently inducing lysosomal damage and anti-tumor immunity |
| WO2025012417A1 (en) | 2023-07-13 | 2025-01-16 | Institut National de la Santé et de la Recherche Médicale | Anti-neurotensin long fragment and anti-neuromedin n long fragment antibodies and uses thereof |
| WO2025042742A1 (en) | 2023-08-18 | 2025-02-27 | Bristol-Myers Squibb Company | Compositions comprising antibodies that bind bcma and cd3 and methods of treatment |
| WO2025050009A2 (en) | 2023-09-01 | 2025-03-06 | Children's Hospital Medical Center | Identification of targets for immunotherapy in melanoma using splicing-derived neoantigens |
| WO2025056180A1 (en) | 2023-09-15 | 2025-03-20 | BioNTech SE | Methods of treatment using agents binding to epcam and cd137 in combination with pd-1 axis binding antagonists |
| US20250114468A1 (en) | 2023-10-09 | 2025-04-10 | Regeneron Pharmaceuticals, Inc. | Methods of treating cancer with a combination of a pd1 inhibitor and a targeted immunocytokine |
| WO2025106736A2 (en) | 2023-11-15 | 2025-05-22 | Regeneron Pharmaceuticals, Inc. | Combination of pd-1 inhibitors and lag-3 inhibitors for enhanced efficacy in treating lung cancer |
| TW202540189A (zh) | 2023-11-30 | 2025-10-16 | 德商生物新技術公司 | 在組合療法中能夠結合ox40之抗體 |
| WO2025120866A1 (en) | 2023-12-08 | 2025-06-12 | Astellas Pharma Inc. | Combination therapy involving bispecific binding agents binding to cldn18.2 and cd3 and agents stabilizing or increasing expression of cldn18.2 |
| WO2025120867A1 (en) | 2023-12-08 | 2025-06-12 | Astellas Pharma Inc. | Combination therapy involving bispecific binding agents binding to cldn18.2 and cd3 and anti-vegfr2 antibodies |
| TW202541837A (zh) | 2023-12-08 | 2025-11-01 | 日商安斯泰來製藥公司 | 含有結合至cldn18.2和cd3之雙特異性結合劑和穩定或增加cldn18.2表現之藥劑之組合療法 |
| WO2026033885A1 (en) | 2024-08-08 | 2026-02-12 | Astellas Pharma Inc. | Combination therapy involving bispecific binding agents binding to cldn18.2 and cd3 and agents stabilizing or increasing expression of cldn18.2 |
| WO2025132695A1 (en) | 2023-12-19 | 2025-06-26 | Boehringer Ingelheim International Gmbh | Recombinant rhabdovirus encoding for a gasdermin |
| WO2025210175A1 (en) | 2024-04-04 | 2025-10-09 | Centre National De La Recherche Scientifique | Mutant csf-1r extracellular domain fusion molecules and therapeutic uses thereof |
| WO2025248505A1 (en) | 2024-05-31 | 2025-12-04 | Wayne State University | Methods for treating endometrial and ovarian hyperproliferative disorders |
| WO2026003224A2 (en) | 2024-06-26 | 2026-01-02 | Iomx Therapeutics Ag | Bispecific antigen binding proteins (abp) targeting immune checkpoint molecules and both leukocyte immunoglobulin-like receptor subfamily b1 (lilrb1) and lilrb2; combinations and uses thereof |
| WO2026012976A1 (en) | 2024-07-08 | 2026-01-15 | Institut National de la Santé et de la Recherche Médicale | Use of inhibitor of gasdermind for treatment of rac2 monogenic disorders |
| WO2026037839A2 (en) | 2024-08-12 | 2026-02-19 | ONA Therapeutics S.L. | Anti-fgfr4 molecules and uses thereof |
| WO2026050572A2 (en) | 2024-08-29 | 2026-03-05 | Marengo Therapeutics, Inc. | Multifunctional molecules binding to tcr and uses thereof |
| WO2026052851A2 (en) | 2024-09-09 | 2026-03-12 | Institut National de la Santé et de la Recherche Médicale | Inhibitor of ciliogenesis for use in a method of preventing therapeutic resistance in cancer |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2235131C2 (ru) * | 1999-03-31 | 2004-08-27 | Мор-Рисёч Эппликейшенс Лтд. | Моноклональное антитело, нуклеиновая кислота и вектор, кодирующие антитело, и использование антитела для диагностики и лечения злокачественных заболеваний |
| WO2006021955A2 (en) * | 2004-08-23 | 2006-03-02 | Mor Research Applications Ltd. | Use of bat monoclonal antibody for immunotherapy |
Family Cites Families (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5225539A (en) * | 1986-03-27 | 1993-07-06 | Medical Research Council | Recombinant altered antibodies and methods of making altered antibodies |
| AU4128089A (en) * | 1988-09-15 | 1990-03-22 | Rorer International (Overseas) Inc. | Monoclonal antibodies specific to human epidermal growth factor receptor and therapeutic methods employing same |
| IL108501A (en) * | 1994-01-31 | 1998-10-30 | Mor Research Applic Ltd | Antibodies and pharmaceutical compositions containing them |
| US6811779B2 (en) * | 1994-02-10 | 2004-11-02 | Imclone Systems Incorporated | Methods for reducing tumor growth with VEGF receptor antibody combined with radiation and chemotherapy |
| WO2003012105A2 (en) | 2001-08-01 | 2003-02-13 | University Of Bristol | Vegf isoform |
| IL149820A0 (en) * | 2002-05-23 | 2002-11-10 | Curetech Ltd | Humanized immunomodulatory monoclonal antibodies for the treatment of neoplastic disease or immunodeficiency |
| EP2206517B1 (en) | 2002-07-03 | 2023-08-02 | Ono Pharmaceutical Co., Ltd. | Immunopotentiating compositions comprising anti-PD-L1 antibodies |
| US20060032289A1 (en) | 2004-08-11 | 2006-02-16 | Pinnaduwage Lal A | Non-optical explosive sensor based on two-track piezoresistive microcantilever |
| CA2647282A1 (en) * | 2006-04-05 | 2007-10-11 | Pfizer Products Inc. | Ctla4 antibody combination therapy |
-
2009
- 2009-02-11 EP EP09711038.1A patent/EP2242773B1/en not_active Not-in-force
- 2009-02-11 DK DK09711038.1T patent/DK2242773T3/en active
- 2009-02-11 ES ES09711038.1T patent/ES2639857T3/es active Active
- 2009-02-11 MX MX2010008786A patent/MX2010008786A/es active IP Right Grant
- 2009-02-11 AU AU2009213738A patent/AU2009213738B2/en not_active Ceased
- 2009-02-11 PL PL09711038T patent/PL2242773T3/pl unknown
- 2009-02-11 PT PT97110381T patent/PT2242773T/pt unknown
- 2009-02-11 HU HUE09711038A patent/HUE034465T2/en unknown
- 2009-02-11 BR BRPI0907718A patent/BRPI0907718A2/pt not_active IP Right Cessation
- 2009-02-11 CA CA2715166A patent/CA2715166C/en not_active Expired - Fee Related
- 2009-02-11 US US12/867,208 patent/US8747847B2/en active Active
- 2009-02-11 CN CN200980107451.2A patent/CN101970499B/zh not_active Expired - Fee Related
- 2009-02-11 RU RU2010135585/10A patent/RU2531758C2/ru not_active IP Right Cessation
- 2009-02-11 CN CN201410715096.XA patent/CN104548091A/zh active Pending
- 2009-02-11 WO PCT/IL2009/000153 patent/WO2009101611A1/en not_active Ceased
- 2009-02-11 JP JP2010545610A patent/JP2011512332A/ja active Pending
-
2014
- 2014-04-29 US US14/264,338 patent/US9309308B2/en active Active
- 2014-08-20 RU RU2014134177A patent/RU2014134177A/ru not_active Application Discontinuation
- 2014-09-04 JP JP2014179986A patent/JP5911539B2/ja not_active Expired - Fee Related
-
2015
- 2015-10-29 HK HK15110690.5A patent/HK1209653A1/xx unknown
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2235131C2 (ru) * | 1999-03-31 | 2004-08-27 | Мор-Рисёч Эппликейшенс Лтд. | Моноклональное антитело, нуклеиновая кислота и вектор, кодирующие антитело, и использование антитела для диагностики и лечения злокачественных заболеваний |
| WO2006021955A2 (en) * | 2004-08-23 | 2006-03-02 | Mor Research Applications Ltd. | Use of bat monoclonal antibody for immunotherapy |
Non-Patent Citations (2)
| Title |
|---|
| HARDY et al., "BAT monoclonal antibody immunotherapy of human metastatic. colorectal carcinoma in mice", Cancer Letters 229, 2005, pp. 217"222 http://dx.doi.org/10.1016/j.canlet.2005.06.046. * |
| При публикации сведений о выдаче патента будет использовано описание в первоначальной редакции заявителя. При публикации сведений о выдаче патента будут использованы первоначальные чертежи * |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2725819C2 (ru) * | 2014-12-05 | 2020-07-06 | Мемориал Слоан-Кеттеринг Кэнсер Сентер | Антитела, нацеленные на рецептор, связанный с g-белками, и способы их применения |
| RU2625598C2 (ru) * | 2015-12-31 | 2017-07-17 | Федеральное государственное бюджетное учреждение "Ростовский научно-исследовательский онкологический институт" Министерства здравоохранения Российской Федерации | Способ лечения больных локальным раком простаты, относящихся к группе высокого риска прогрессирования заболевания |
| RU2801208C2 (ru) * | 2017-07-20 | 2023-08-03 | Новартис Аг | Режимы дозирования антител анти-lag-3 и их применение |
| RU2797268C2 (ru) * | 2018-02-09 | 2023-06-01 | Ф. Хоффманн-Ля Рош Аг | Антитела, связывающиеся с gprc5d |
Also Published As
| Publication number | Publication date |
|---|---|
| PT2242773T (pt) | 2017-09-15 |
| US8747847B2 (en) | 2014-06-10 |
| BRPI0907718A2 (pt) | 2017-06-13 |
| CN104548091A (zh) | 2015-04-29 |
| CN101970499A (zh) | 2011-02-09 |
| JP2011512332A (ja) | 2011-04-21 |
| WO2009101611A1 (en) | 2009-08-20 |
| JP2015038080A (ja) | 2015-02-26 |
| HUE034465T2 (en) | 2018-02-28 |
| RU2010135585A (ru) | 2012-03-20 |
| RU2014134177A (ru) | 2016-03-20 |
| PL2242773T3 (pl) | 2017-11-30 |
| CA2715166C (en) | 2017-05-16 |
| MX2010008786A (es) | 2010-12-01 |
| JP5911539B2 (ja) | 2016-04-27 |
| US20140302032A1 (en) | 2014-10-09 |
| US9309308B2 (en) | 2016-04-12 |
| ES2639857T3 (es) | 2017-10-30 |
| AU2009213738A1 (en) | 2009-08-20 |
| US20110117085A1 (en) | 2011-05-19 |
| EP2242773B1 (en) | 2017-06-14 |
| DK2242773T3 (en) | 2017-09-25 |
| AU2009213738B2 (en) | 2015-01-22 |
| CN101970499B (zh) | 2014-12-31 |
| EP2242773A1 (en) | 2010-10-27 |
| HK1209653A1 (en) | 2016-04-08 |
| CA2715166A1 (en) | 2009-08-20 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2531758C2 (ru) | Моноклональные антитела для лечения опухолей | |
| RU2604814C2 (ru) | Варианты гуманизированных иммуномодулирующих моноклональных антител | |
| CN1200734C (zh) | 用表皮生长因子拮抗物治疗顽固性的人肿瘤 | |
| AU2012288413A1 (en) | Variants of humanized immunomodulatory monoclonal antibodies | |
| CN103687877B (zh) | 人源化免疫调节单克隆抗体的变体 | |
| AU2015201986A1 (en) | Monoclonal antibodies for tumor treatment |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20190212 |