JP2012505520A - 高い比放電容量を有するリチウムイオン電池用正極材料およびこれらの材料を合成するためのプロセス - Google Patents
高い比放電容量を有するリチウムイオン電池用正極材料およびこれらの材料を合成するためのプロセス Download PDFInfo
- Publication number
- JP2012505520A JP2012505520A JP2011531092A JP2011531092A JP2012505520A JP 2012505520 A JP2012505520 A JP 2012505520A JP 2011531092 A JP2011531092 A JP 2011531092A JP 2011531092 A JP2011531092 A JP 2011531092A JP 2012505520 A JP2012505520 A JP 2012505520A
- Authority
- JP
- Japan
- Prior art keywords
- positive electrode
- active material
- metal
- electrode active
- lithium
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/48—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides
- H01M4/52—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides of nickel, cobalt or iron
- H01M4/525—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides of nickel, cobalt or iron of mixed oxides or hydroxides containing iron, cobalt or nickel for inserting or intercalating light metals, e.g. LiNiO2, LiCoO2 or LiCoOxFy
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/13—Electrodes for accumulators with non-aqueous electrolyte, e.g. for lithium-accumulators; Processes of manufacture thereof
- H01M4/139—Processes of manufacture
- H01M4/1391—Processes of manufacture of electrodes based on mixed oxides or hydroxides, or on mixtures of oxides or hydroxides, e.g. LiCoOx
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01G—COMPOUNDS CONTAINING METALS NOT COVERED BY SUBCLASSES C01D OR C01F
- C01G45/00—Compounds of manganese
- C01G45/12—Manganates manganites or permanganates
- C01G45/1221—Manganates or manganites with a manganese oxidation state of Mn(III), Mn(IV) or mixtures thereof
- C01G45/1228—Manganates or manganites with a manganese oxidation state of Mn(III), Mn(IV) or mixtures thereof of the type [MnO2]n-, e.g. LiMnO2, Li[MxMn1-x]O2
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01G—COMPOUNDS CONTAINING METALS NOT COVERED BY SUBCLASSES C01D OR C01F
- C01G51/00—Compounds of cobalt
- C01G51/40—Cobaltates
- C01G51/42—Cobaltates containing alkali metals, e.g. LiCoO2
- C01G51/44—Cobaltates containing alkali metals, e.g. LiCoO2 containing manganese
- C01G51/50—Cobaltates containing alkali metals, e.g. LiCoO2 containing manganese of the type [MnO2]n-, e.g. Li(CoxMn1-x)O2, Li(MyCoxMn1-x-y)O2
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01G—COMPOUNDS CONTAINING METALS NOT COVERED BY SUBCLASSES C01D OR C01F
- C01G53/00—Compounds of nickel
- C01G53/40—Nickelates
- C01G53/42—Nickelates containing alkali metals, e.g. LiNiO2
- C01G53/44—Nickelates containing alkali metals, e.g. LiNiO2 containing manganese
- C01G53/50—Nickelates containing alkali metals, e.g. LiNiO2 containing manganese of the type [MnO2]n-, e.g. Li(NixMn1-x)O2, Li(MyNixMn1-x-y)O2
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/052—Li-accumulators
- H01M10/0525—Rocking-chair batteries, i.e. batteries with lithium insertion or intercalation in both electrodes; Lithium-ion batteries
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/04—Processes of manufacture in general
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/362—Composites
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/48—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides
- H01M4/50—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides of manganese
- H01M4/505—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides of manganese of mixed oxides or hydroxides containing manganese for inserting or intercalating light metals, e.g. LiMn2O4 or LiMn2OxFy
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2002/00—Crystal-structural characteristics
- C01P2002/50—Solid solutions
- C01P2002/52—Solid solutions containing elements as dopants
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2002/00—Crystal-structural characteristics
- C01P2002/70—Crystal-structural characteristics defined by measured X-ray, neutron or electron diffraction data
- C01P2002/72—Crystal-structural characteristics defined by measured X-ray, neutron or electron diffraction data by d-values or two theta-values, e.g. as X-ray diagram
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2004/00—Particle morphology
- C01P2004/80—Particles consisting of a mixture of two or more inorganic phases
- C01P2004/82—Particles consisting of a mixture of two or more inorganic phases two phases having the same anion, e.g. both oxidic phases
- C01P2004/84—Particles consisting of a mixture of two or more inorganic phases two phases having the same anion, e.g. both oxidic phases one phase coated with the other
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2006/00—Physical properties of inorganic compounds
- C01P2006/40—Electric properties
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/052—Li-accumulators
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/42—Methods or arrangements for servicing or maintenance of secondary cells or secondary half-cells
- H01M10/4235—Safety or regulating additives or arrangements in electrodes, separators or electrolyte
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M2004/021—Physical characteristics, e.g. porosity, surface area
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/58—Selection of substances as active materials, active masses, active liquids of inorganic compounds other than oxides or hydroxides, e.g. sulfides, selenides, tellurides, halogenides or LiCoFy; of polyanionic structures, e.g. phosphates, silicates or borates
- H01M4/582—Halogenides
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/62—Selection of inactive substances as ingredients for active masses, e.g. binders, fillers
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/10—Energy storage using batteries
Abstract
中程度の放電レートにおける室温でのサイクル後に非常に高い比放電容量を有する正極活物質について記載する。注目する材料のいくつかは、式Li1+xNiαMnβCoγO2を有し、式中、xは約0.05〜約0.25の範囲、αは約0.1〜約0.4の範囲、βは約0.4〜約0.65の範囲、γは約0.05〜約0.3の範囲である。材料を金属フッ化物で被覆することにより、とりわけサイクル後の材料の性能を改善することが可能である。また、被覆材料は、セルの第1の充電および放電後に不可逆的容量損失における非常に著しい減少を示すことが可能である。これらの材料を生産するための手法は、例えば、金属水酸化物を伴う共沈アプローチおよびゾル−ゲルアプローチを含む。
Description
本発明は、中程度のレートにおけるサイクル後に高い比放電容量を提供するリチウム二次電池用正極活物質に関する。さらにその上、本発明は、サイクル中の放電容量を著しく安定化および増加させる金属フッ化物被覆を有する高い比放電容量の組成物に関する。加えて、本発明は、層状構造を有する高い比容量の正極材料を合成するための方法に関する。
リチウム電池は、その比較的高いエネルギー密度のため、消費者用電子機器において広く用いられている。充電式電池は、また、二次電池とも呼ばれ、リチウムイオン二次電池は、一般に、リチウムをインターカレーションする負極材料を有する。いくつかの現在の商用電池については、負極材料は、グラファイトとすることが可能であり、正極材料は、コバルト酸リチウム(LiCoO2)を含むことが可能である。実際には、カソードの理論容量の概ね50%のみ(例えば、概ね140mAh/g)を用いることが可能である。また、現在、少なくとも2つの他のリチウムベースのカソード材料が商業的に用いられている。これらの2つの材料とは、スピネル構造を有するLiMn2O4と、オリビン構造を有するLiFePO4とである。これらの他の材料は、エネルギー密度においては何らの著しい改善も提供していない。
「Comments on the structural complexity of lithium−rich Li1+xM1−xO2 electrodes (M=Mn,Ni,Co) for lithium batteries」(Electrochemistry Communications 8 (2006) 1531−1538)
「Materials Chemistry & Physics」(Vol. 87, 2004, pp. 246−255)
「AlF3−Coating to Improve High Voltage Cycling Performance of Li[Ni1/3Co1/3Mn1/3]O2 Cathode Materials for Lithium Secondary Batteries」(J. of the Electrochemical Society, 154 (3), A168−A172 (2007))
「Significant Improvement of Electrochemical Performance of AlF3−Coated Li[Ni0.8Co0.1Mn0.1]O2 Cathode Materials」(J. of the Electrochemical Society, 154 (11) A1005−A1009 (2007))
「High Capacity, Surface−Modified Layered Li[Li(1−x)/3Mn(2−x)/3Nix/3Cox/3]O2 Cathodes with Low Irreversible Capacity Loss」(Electrochemical and Solid State Letters, 9 (5) A221−A224 (2006))
リチウムイオン電池は、一般に、それらのアプリケーションに基づいて2つのカテゴリーに分類される。第1のカテゴリーは、高パワー電池に関わるものであり、リチウムイオン電池セルは、動力工具およびハイブリッド電気自動車(HEV)などのアプリケーションのために大電流(アンペア)を供給するように設計されている。しかし、大電流を提供する設計は、一般に、セルから供給可能な総エネルギーを削減するため、これらの電池セルは、設計上、より低いエネルギーとなる。第2の設計カテゴリーは、高エネルギーセルに関するものであり、リチウムイオン電池セルは、携帯電話、ラップトップコンピュータ、電気自動車(EV)、およびプラグインハイブリッド電気自動車(PHEV)などのアプリケーションのためにより高い総容量で小〜中程度の電流(アンペア)を供給するように設計されている。
第1の態様では、本発明は、4.6ボルトから2.0ボルトへの放電時の放電レートC/3における室温での第10放電サイクル放電容量が、少なくとも240mAh/gである、リチウムイオンセル用正極活物質に関する。
さらなる態様では、本発明は、結晶格子内に+4金属カチオン、+3金属カチオン、および+2金属カチオンを含む層状リチウム金属酸化物を含むリチウムイオンセル用正極活物質に関する。材料は金属/半金属フッ化物被覆を有し、正極材料は、放電レートC/10における第1サイクル不可逆的容量損失が、無被覆材料の第1サイクル不可逆的容量損失の約2/3以下であり、放電レートC/3における室温での放電時の第20サイクル放電容量が、第5サイクル放電容量の少なくとも約98%である。
追加の態様では、本発明は、層状リチウム金属酸化物組成物を合成するための方法に関する。いくつかの実施形態では、方法は、+2カチオンを含む溶液から混合金属水酸化物組成物を沈殿させるステップを含み、水酸化物組成物は選択された組成物を有する。
別の態様では、本発明は、層状リチウム金属酸化物組成物を合成するための方法に関する。いくつかの実施形態では、方法は、リチウムイオンおよび+2金属カチオンを含むゾル−ゲル組成物を少なくとも約750℃の温度で焼成して結晶性層状リチウム金属酸化物組成物を形成するステップを含む。
本明細書に記載のリチウムイオンセル設計は、高い比容量を示しつつ改善されたサイクル性能を達成するものである。高い比容量の正極材料は、商業生産のためにスケール変更可能な手法に基づく改善された材料性能をもたらす手法を用いて生産される。好適な合成手法は、例えば、共沈アプローチおよびゾル−ゲルアプローチを含む。特に注目する材料の化学量論は、商業アプリケーションのために望ましい特性を有する。材料は、優れたサイクル特性を有する。金属フッ化物被覆または他の好適な被覆を用いることにより、さらなるサイクルの向上が提供される。また、正極材料は、放電サイクルにわたり高い平均電圧を示すため、セルは、高い比容量とともに高いパワー出力を有する。さらにその上、正極材料は、セルの第1の充電および放電後の不可逆的容量損失の割合の低下を示すため、所望される場合、それに応じて負極材料を削減することが可能である。優れたサイクル性能と高い比容量との組み合わせにより、これらの結果的に得られるリチウムイオン電池は、特に電気自動車、プラグインハイブリッド自動車などの高エネルギーアプリケーションのための改善されたパワーソースとなる。
本明細書に記載の電池は、非水電解質溶液がリチウムイオンを含むリチウムイオン電池である。二次リチウムイオン電池については、リチウムイオンが放電中に負極から解放されることにより、負極は放電中にアノードとして機能し、電極からの解放後にリチウムが酸化して電子が生成される。これに対応して、正極は、放電中にインターカレーションまたは類似のプロセスを通じてリチウムイオンを取り込むことにより、放電中に電子を消費するカソードとして機能する。二次セルの再充電後は、セルを通るリチウムイオンの流れが逆転し、負極がリチウムを取り込むとともに正極がリチウムをリチウムイオンとして解放する。
リチウムイオン電池は、基準の均質な電気活性リチウム金属酸化物組成物に対してリチウムリッチな正極活物質を用いることが可能である。理論による限定を望むものではないが、適切に形成されたリチウムリッチなリチウム金属酸化物は、複合結晶構造を有するものと思われる。例えば、リチウムリッチな材料のいくつかの実施形態では、Li2MnO3材料を、層状LiMnO2成分またはマンガンカチオンを同等の酸化状態を有する他の遷移金属カチオンで置換した類似の複合組成物のいずれかと構造的に一体化させてもよい。いくつかの実施形態では、正極材料を、xLi2MO3・(1−x)LiM’O2として2成分表記で表すことが可能であり、式中、M’は、平均原子価が+3である1つ以上の金属カチオンであって少なくとも1つのカチオンがMn+3またはNi+3であり、Mは、平均原子価が+4である1つ以上の金属カチオンである。これらの組成物は、例えば、「Lithium Metal Oxide Electrodes for Lithium Cells and Batteries」と題されたThackeray他による特許文献1においてさらに記載されており、当該明細書は、参照により本明細書に組み込まれる。特に注目する正極活物質は、式Li1+xNiαMnβCoγMδO2−zFzを有し、式中、xは約0.05〜約0.25の範囲、αは約0.1〜約0.4の範囲、βは約0.4〜約0.65の範囲、γは約0.05〜約0.3の範囲、δは約0〜約0.1の範囲、zは約0〜約0.1の範囲であり、MはMg、Zn、Al、Ga、B、Zr、Ti、Ca、Ce、Y、Nb、またはそれらの組み合わせである。特に、以下の実施例において提示するように、Li[Li0.2Ni0.175Co0.10Mn0.525]O2について驚くほど良好な結果が得られている。これらの組成物は、層状構造および削減した量のニッケルを有するそれらの固有の組成物により発火のリスクが低く、安全性特性が改善されている。これらの組成物は、環境の観点から望ましくない元素を少量のみ用い、商業スケール生産のために合理的なコストを有する出発物質から生産することが可能である。
「元素」との単語は、本明細書中では、組成物中であれば適切な酸化状態を有し、元素形態であることが記載されているときのみその元素形態M0である、周期表の要素に言及するという、その従来の用法で用いられる。このため、金属元素は、一般に、その元素形態における金属状態であるか、または金属の元素形態の対応する合金である。換言すれば、金属合金以外の金属酸化物または他の金属組成物は、一般に、金属性ではない。
Thackeray他は、特許文献1において、固相反応を用いる層状のリチウムリッチなリチウム金属酸化物の合成について記載している。本明細書に記載のように、共沈アプローチを用いて改善された性能が得られ、一般に、所望される金属化学量論を有する水酸化物が沈殿する溶液が形成される。水酸化リチウムを沈殿剤として用いることにより、他のカチオンからの望ましくない汚濁を低減し、より高い容量を達成することが可能である。また、ゾル−ゲル合成アプローチも、適切な前駆体を加水分解することにより形成される望ましい水酸化物組成物を産生する。ゾル−ゲルプロセスについては、結果的に得られるゲルは、プロセスに導入された金属イオンを含む水酸化物ネットワークを有する。続いて、共沈またはゾル−ゲルからの水酸化物組成物を熱処理することにより、適切な結晶性を有する対応する酸化物組成物を形成することが可能である。最初の共沈もしくはゾル−ゲルプロセスにリチウムカチオンを組み入れることが可能であり、または、水酸化物組成物から酸化物組成物を形成する熱処理中またはその後の固相反応においてリチウムを導入することが可能である。以下の実施例において実証するように、共沈プロセスで形成される結果的に得られるリチウムリッチな金属酸化物材料は、改善された性能特性を有する。
インターカレーションベースの正極活物質を有する対応する電池を用いるときは、格子からのリチウムイオンのインターカレーションおよび解放により、電気活性材料の結晶格子における変化が誘発される。これらの変化が本質的に可逆的である限り、材料の容量は変化しない。しかし、活物質の容量は、変動する度合いでサイクルとともに減少することが観測されている。従って、一定数のサイクル後、セルの性能は許容値を下回り、セルは交換される。また、セルの第1サイクルにおいて、一般に、後続のサイクルにおけるサイクル毎の容量損失よりも著しく大きい不可逆的容量損失が生じる。不可逆的容量損失とは、新しいセルの充電容量と最初の放電容量との差である。この第1サイクル不可逆的容量損失を補償するため、余剰な電気活性材料を負極に含めることによりセルを十分に充電することを可能にしているが、セルの寿命のほとんどの間はこの失われた容量にアクセスすることができないため、負極材料は本質的に無駄になる。第1サイクル不可逆的容量損失の大半は、一般に、正極材料に起因するものである。
適切な被覆材料により、材料の長期サイクル性能を改善するとともに、第1サイクル不可逆的容量損失を減少させることが可能である。理論による限定を望むものではないが、被覆は、リチウムイオンの取り込みおよび解放中に結晶格子を安定化させ得るため、結晶格子における不可逆的変化を著しく低減させる。特に、金属フッ化物組成物を有効な被覆として用いることが可能である。カソード活物質(具体的には、LiCoO2およびLiMn2O4)のための被覆として金属フッ化物組成物を一般に用いることは、「Cathode Active Material Coated with Fluorine Compound for Lithium Secondary Batteries and Method for Preparing the Same」と題されたSun他による公開PCT出願の特許文献2において記載されており、当該明細書は、参照により本明細書に組み込まれる。
金属フッ化物被覆は、本明細書に記載のリチウムリッチな層状正極活物質に著しい改善を提供することが可能であることが発見されている。これらの改善は、容量の劣化を著しく低減し、第1サイクル不可逆的容量損失を著しく減少させ、容量全般を改善させた長期サイクルに関する。被覆材料の量は、観測される性能の改善を際立たせるように選択することが可能である。
本明細書に記載のように、複合結晶構造を有するリチウムリッチな正極活物質は、4.6ボルトからの放電について良好なサイクル特性で、室温での250mAh/gを上回る高い比容量を示すことが可能である。一般に、放電中のセルの容量は、放電レートに依存する。特定のセルの最大容量は、非常に遅い放電レートにおいて測定される。実際の使用では、実際の容量は、放電が制限されたレートで行われるため最大値よりも小さい。使用中のレートにより近い合理的な放電レートを用いて、より現実的な容量を測定することが可能である。低〜中程度のレートのアプリケーションについては、合理的な試験レートは、3時間にわたるセルの放電に関わる。従来の表記では、これをC/3または0.33Cと書く。本明細書に記載の正極活物質は、4.6ボルトからの放電時の室温での第10放電/充電サイクルにおける放電レートC/3における比放電容量が、少なくとも約250mAh/gであることが可能である。最大の容量性能は、被覆材料で得られている。
充電式電池は、電話機などの移動通信装置、MP3プレーヤおよびテレビジョンなどの移動娯楽装置、携帯型コンピュータ、幅広い用途を見出すこれらの装置の組み合わせ、ならびに自動車およびフォークリフトなどの輸送装置など、様々な用途を有する。比容量およびサイクルについて改善された正極活物質を組み込んだ本明細書に記載の電池は、消費者、とりわけ中電流アプリケーションに対して改善された性能を提供することが可能である。
電池構造
図1を参照して、負極102と、正極104と、負極102と正極104との間のセパレータ106とを有する電池100が概略的に示されている。電池は、適切に配置されたセパレータとともに、積層体などの複数の正極と複数の負極とを備えることが可能である。電極に接する電解質により、反対の極性の電極間にセパレータを通じたイオン伝導性が提供される。電池は、一般に、それぞれ負極102および正極104に関連付けられた集電体108、110を備える。
図1を参照して、負極102と、正極104と、負極102と正極104との間のセパレータ106とを有する電池100が概略的に示されている。電池は、適切に配置されたセパレータとともに、積層体などの複数の正極と複数の負極とを備えることが可能である。電極に接する電解質により、反対の極性の電極間にセパレータを通じたイオン伝導性が提供される。電池は、一般に、それぞれ負極102および正極104に関連付けられた集電体108、110を備える。
リチウムは、一次電池と二次電池との両方において用いられている。リチウム金属の魅力的な特長は、その軽量であること、および最も陽性な金属であるという事実であり、これらの特長の側面は、また、リチウムイオン電池においても有益に取り込むことが可能である。インターカレーションまたは類似のメカニズムを通じてリチウムイオンをその構造に組み入れた特定の形態の金属、金属酸化物、および炭素材料が既知である。二次リチウムイオン電池における正極用の電気活性材料として機能する望ましい混合金属酸化物について本明細書中でさらに説明する。リチウムイオン電池とは、負極活物質もリチウムインターカレーション材料である電池を言う。リチウム金属そのものがアノードとして用いられる場合、結果的に得られる電池は、一般に、単にリチウム電池と呼ばれる。
電圧とはカソードおよびアノードにおける半電池電位間の差であるため、負極インターカレーション材料の性質は、電池の結果的に得られる電圧に影響を与える。好適な負極リチウムインターカレーション組成物は、例えば、グラファイト、合成グラファイト、コークス、フラーレン、五酸化ニオブ、錫合金、ケイ素、酸化チタン、酸化錫、およびLixTiO2(0.5<x≦1)またはLi1+xTi2−xO4(0≦x≦1/3)などのチタン酸リチウムを含む。さらなる負極材料は、同時係属の「Inter−metallic Compositions, Negative Electrodes With Inter−Metallic Compositions and Batteries」と題されたKumarによる特許文献3および「Lithium Ion Batteries With Particular Negative Electrode Compositions」と題されたKumar他による特許文献4において記載されており、両明細書は、参照により本明細書に組み込まれる。
正極活性組成物および負極活性組成物は、一般に、対応する電極において高分子結合剤で固められた粉末組成物である。結合剤は、電解質に接しているときに活性粒子にイオン伝導性を提供する。好適な高分子結合剤は、例えば、ポリフッ化ビニリデン、ポリエチレンオキシド、ポリエチレン、ポリプロピレン、ポリテトラフルオロエチレン、ポリアクリレート、エチレン−(プロピレン−ジエンモノマー)共重合体(EPDM)、ならびにそれらの混合物および共重合体を含む。
結合剤における粒子の充填量は、約80重量パーセント超など、大きくすることが可能である。電極を形成するには、重合体用の溶媒などの好適な液体中で、粉末を重合体と混合させることが可能である。結果的に得られるペーストを、プレス処理により電極構造にすることが可能である。
正極組成物は、および恐らくは負極組成物は、一般に、電気活性組成物とは異なる導電性粉末も含む。好適な補足的導電性粉末は、例えば、グラファイト、カーボンブラック、銀粉末などの金属粉末、ステンレス鋼繊維などの金属繊維など、およびそれらの混合物を含む。一般に、正極は、約1重量パーセント〜約25重量パーセントの、さらなる実施形態では約2重量パーセント〜約15重量パーセントの、異なる導電性粉末を含むことが可能である。上で明記した範囲内で導電性粉末の量のさらなる範囲が考えられ、それらの範囲も本開示内であることを、当業者は認識するであろう。
電極は、一般に、電極と外部回路との間の電子の流れを容易にするため、導電性集電体に関連付けられる。集電体は、金属箔または金属グリッドなどの金属を含むことが可能である。いくつかの実施形態では、集電体は、ニッケル、アルミニウム、ステンレス鋼、銅などから形成することが可能である。電極材料は、集電体に接した状態で流延成形することが可能である。例えば、いくつかの実施形態では、集電体箔または他の構造に接した状態の電極材料に、約2〜約10kg/cm2(キログラム毎平方センチメートル)の圧力を加えることが可能である。加圧された構造を例えばオーブン中で乾燥させることにより、電極から溶媒を除去することが可能である。
セパレータは、正極と負極との間に配置される。セパレータは、2つの電極間に少なくとも選択されたイオン伝導性を提供しながらも、電気的に絶縁性である。種々の材料をセパレータとして用いることが可能である。例えば、多孔性マット状に形成されたガラス繊維をセパレータとして用いることが可能である。商用セパレータ材料は、一般に、イオン伝導性を提供する多孔性シートであるポリエチレンおよび/またはポリプロピレンなどの重合体から形成される。商用重合体セパレータは、例えば、Hoechst Celanese(Charlotte,N.C)のCelgard(登録商標)ラインのセパレータ材料を含む。
リチウムイオン電池用の電解質は、1つ以上の選択されたリチウム塩を含むことが可能である。適切なリチウム塩は、一般に、不活性アニオンを有する。好適なリチウム塩は、例えば、ヘキサフルオロリン酸リチウム、ヘキサフルオロヒ酸リチウム、リチウムビス(トリフルオロメチルスルホニルイミド)、リチウムトリフルオロメタンスルホネート、リチウムトリス(トリフルオロメチルスルホニル)メチド、リチウムテトラフルオロボレート、リチウム過塩素酸塩、リチウムテトラクロロアルミナート、塩化リチウム、およびそれらの組み合わせを含む。伝統的には、電解質は、濃度1Mのリチウム塩を含む。
注目するリチウムイオン電池については、非水液体を一般に用いてリチウム塩を溶解させる。溶媒は、一般に、不活性であり、電気活性材料を溶解させない。適切な溶媒は、例えば、プロピレンカーボネート、ジメチルカーボネート、ジエチルカーボネート、2−メチルテトラヒドロフラン、ジオキソラン、テトラヒドロフラン、メチルエチルカーボネート、γ−ブチロラクトン、ジメチルスルホキシド、アセトニトリル、ホルムアミド、ジメチルホルムアミド、トリグリム(トリ(エチレングリコール)ジメチルエーテル)、ジグリム(ジエチレングリコールジメチルエーテル)、DME(グリムまたは1,2−ジメチルオキシエタンまたはエチレングリコールジメチルエーテル)、ニトロメタン、およびそれらの混合物を含む。
本明細書に記載の電極は、様々な商用セル設計に組み込むことが可能である。例えば、カソード組成物は、角柱形状のセル、巻回円筒状のセル、コイン型セル、または他の合理的なセル形状について用いることが可能である。実施例における試験は、コイン型セルを用いて行う。セルは、単一のカソード構造、または並列および/もしくは直列の電気接続で組み立てられた複数のカソード構造を備えることが可能である。正極活物質は、一次すなわち単一の充電で用いるための電池において用いることが可能であるが、結果的に得られる電池は、一般に、セルの複数のサイクルにわたり二次電池として用いるために望ましいサイクル特性を有する。
いくつかの実施形態では、正極および負極を、それらの間にセパレータを挟んで積層させることが可能であり、結果的に得られる積層構造を円筒状または角柱状に巻くことにより、電池構造を形成することが可能である。適切な導電性タブを、集電体に溶接などにより取り付けることが可能であり、結果的に得られるゼリーロール構造は、負極タブおよび正極タブが適切な外部接点に溶接された状態で金属キャニスタまたは重合体パッケージに配置することが可能である。電解質をキャニスタに追加し、キャニスタを封止して電池を完成させる。いくつかの現在用いられている充電式商用セルは、例えば、円筒状の18650型セル(直径18mmおよび長さ65mm)および26700型セル(直径26mmおよび長さ70mm)を含むが、他のセルサイズを用いることも可能である。
正極活物質
正極活物質は、リチウムインターカレーション金属酸化物組成物を含む。いくつかの実施形態では、リチウム金属酸化物組成物は、一般に層状組成物構造を形成すると思われるリチウムリッチな組成物を含むことが可能である。正極活物質は、現実的な放電条件下でリチウムイオンセルにおいて驚くほど高い比容量を示すことが可能である。所望される電極活物質は、本明細書に記載の具体的な合成アプローチを用いて合成することが可能である。
正極活物質は、リチウムインターカレーション金属酸化物組成物を含む。いくつかの実施形態では、リチウム金属酸化物組成物は、一般に層状組成物構造を形成すると思われるリチウムリッチな組成物を含むことが可能である。正極活物質は、現実的な放電条件下でリチウムイオンセルにおいて驚くほど高い比容量を示すことが可能である。所望される電極活物質は、本明細書に記載の具体的な合成アプローチを用いて合成することが可能である。
特に注目するいくつかの組成物において、組成物は、式Li1+xNiαMnβCoγMδO2−zFzにより記載することが可能であり、式中、xは約0.05〜約0.25の範囲、αは約0.1〜約0.4の範囲、βは約0.4〜約0.65の範囲、γは約0.05〜約0.3の範囲、δは約0〜約0.1の範囲、zは約0〜約0.1の範囲であり、MはMg、Zn、Al、Ga、B、Zr、Ti、Ca、Ce、Y、Nb、またはそれらの組み合わせである。フッ素は、材料の改善された安全性に加え、サイクル安定性に寄与することが可能なドーパントである。z=0である実施形態では、この式は、Li1+xNiαMnβCoγMδO2に縮小される。好適な被覆により、フッ素ドーパントを用いることなくサイクル特性における望ましい改善が提供されることが見出されているが、いくつかの実施形態では、フッ素ドーパントを有することが望ましいかもしれない。さらにその上、いくつかの実施形態では、改善された性能を提供しながら組成物がより単純になるように、δ=0であるのが望ましい。これらの実施形態については、zも0であれば、式は、Li1+xNiαMnβCoγO2に単純化され、パラメータは上で説明したとおりである。
本明細書に記載の材料のいくつかの実施形態に対して、Thackeryおよび共同研究者は、Li2M’O3組成物がLiMO2成分を有する層状構造に構造的に一体化されているいくつかのリチウムリッチな金属酸化物組成物についての複合結晶構造を提案している。電極材料は、aLi2M’O3・(1−a)LiMO2として2成分表記で表すことが可能であり、式中、Mは、平均原子価が+3である1つ以上の金属元素であって少なくとも1つの元素がMnまたはNiであり、M’は、平均原子価が+4である金属元素であり、0<a<1である。例えば、Mは、Ni+2、Co+3、およびMn+4の組み合わせであることが可能である。これらの組成物についての全体的な式は、Li1+xM’2xM1−3xO2と書くことが可能である。これらの材料から形成された電池は、対応するLiMO2組成物で形成された電池よりも高い電圧および高い容量でサイクルすることが観測されている。これらの材料は、「Lithium Metal Oxide Electrodes for Lithium Cells and Batteries」と題されたThackery他による特許文献1および「Lithium Metal Oxide Electrodes for Lithium Cells and Batteries」と題されたThackery他による特許文献5においてさらに記載されており、両明細書は、参照により本明細書に組み込まれる。Thackeryは、M’として特に注目すべきものとしてMn、Ti、およびZrを識別し、MについてはNiを識別している。
いくつかの具体的な層状構造の構造が、Thackery他による非特許文献1においてさらに記載されており、かかる文献は、参照により本明細書に組み込まれる。この論文において報告されている研究は、式Li1+x[Mn0.5Ni0.5]1−xO2およびLi1+x[Mn0.333Ni0.333Co0.333]1−xO2を有する組成物について考察している。また、論文は、層状材料の構造上の複雑性について記載している。
昨今、Kangおよび共同研究者は、式Li1+xNiαMnβCoγM’δO2−zFzを有する二次電池において用いるための組成物であって、M’=Mg、Zn、Al、Ga、B、Zr、Ti、xは約0〜0.3、αは約0.2〜0.6、βは約0.2〜0.6、γは約0〜0.3、δは約0〜0.15、zは約0〜0.2である組成物について記載している。これらの金属およびフッ素は、電気化学サイクル中の結果的に得られる層状構造の電池容量および安定性を改善させるものとして提案されている。参照により本明細書に組み込まれる「Layered cathode materials for lithium ion rechargeable batteries」と題されたKang他による特許文献6を参照のこと。この文献は、10サイクル後の室温での容量が250mAh/g(ミリアンペア時毎グラム)を下回るカソード材料を報告している。なお、酸素をフッ素で置換すれば、多価金属の酸化状態は、フッ素を有さない組成物の酸化物組成物よりも低くなる。Kang他は、以下の実施例において検討する組成物であるLi1.2Ni0.15Mn0.55Co0.10O2を含む様々な具体的な組成物について検討している。この特許において得られた結果は、匹敵するサイクル容量を達成しない材料の固相合成に関わるものであった。
合成方法
本明細書に記載の合成アプローチを用いることにより、サイクル後の比容量が改善された層状のリチウムリッチなカソード活物質を形成することが可能である。合成方法は、式Li1+xNiαMnβCoγMδO2−zFzを有する組成物の合成に適合されており、式中、xは約0.05〜約0.25の範囲、αは約0.1〜約0.4の範囲、βは約0.4〜約0.65の範囲、γは約0.05〜約0.3の範囲、δは約0〜約0.1の範囲、zは約0〜約0.1の範囲であり、MはMg、Zn、Al、Ga、B、Zr、Ti、Ca、Ce、Y、Nb、またはそれらの組み合わせである。また、合成アプローチは、商業的スケールアップにも好適である。具体的には、共沈プロセスおよびゾル−ゲルプロセスを用いることにより、望ましい結果を有する所望されるリチウムリッチな正極材料を合成することが可能である。フッ化リチウム反応物を、一般には適量の水酸化リチウムとともに、反応物に添加することにより、フッ素ドーパントを導入することが可能である。
本明細書に記載の合成アプローチを用いることにより、サイクル後の比容量が改善された層状のリチウムリッチなカソード活物質を形成することが可能である。合成方法は、式Li1+xNiαMnβCoγMδO2−zFzを有する組成物の合成に適合されており、式中、xは約0.05〜約0.25の範囲、αは約0.1〜約0.4の範囲、βは約0.4〜約0.65の範囲、γは約0.05〜約0.3の範囲、δは約0〜約0.1の範囲、zは約0〜約0.1の範囲であり、MはMg、Zn、Al、Ga、B、Zr、Ti、Ca、Ce、Y、Nb、またはそれらの組み合わせである。また、合成アプローチは、商業的スケールアップにも好適である。具体的には、共沈プロセスおよびゾル−ゲルプロセスを用いることにより、望ましい結果を有する所望されるリチウムリッチな正極材料を合成することが可能である。フッ化リチウム反応物を、一般には適量の水酸化リチウムとともに、反応物に添加することにより、フッ素ドーパントを導入することが可能である。
共沈プロセスでは、金属塩を、所望されるモル比で精製水などの水性溶媒に溶解させる。好適な金属塩は、例えば、金属酢酸塩、金属硫酸塩、金属硝酸塩、およびそれらの組み合わせを含む。溶液の濃度は、一般に、0.1M〜2Mから選択する。金属塩の相対モル量は、生成物質についての所望される式に基づいて選択することが可能である。次いで、溶液のpHを、水酸化リチウムおよび/または水酸化アンモニウムの添加などで調整することにより、所望される量の金属元素を有する金属水酸化物を沈殿させる。一般に、pHを約10〜約12pH単位の値に調整することにより、沈殿を行うことが可能である。溶液を加熱および攪拌することにより、水酸化物の沈殿を容易にすることが可能である。次いで、沈殿した金属水酸化物を溶液から分離させ、洗浄し、乾燥させることにより粉末を形成し、さらなる処理を行うことが可能である。例えば、乾燥は、約110℃のオーブン中で約4〜約12時間行うことが可能である。
次いで、収集された金属水酸化物粉末に熱処理を施すことにより、水酸化物組成物から水を除去して対応する酸化物組成物に変換することが可能である。一般に、熱処理は、オーブン、炉などにおいて行うことが可能である。熱処理は、不活性雰囲気中または酸素が存在する雰囲気中で行うことが可能である。いくつかの実施形態では、材料を少なくとも約300℃、いくつかの実施形態では約350℃〜約1000℃の温度に加熱することにより、水酸化物を酸化物に変換することが可能である。熱処理は、一般に、少なくとも約15分間、さらなる実施形態では約30分〜24時間以上、追加の実施形態では約45分間〜約15時間行うことが可能である。さらなる熱処理を行うことにより、生成物質の結晶性を改善することが可能である。結晶性生成物を形成するためのこの焼成ステップは、一般に、少なくとも約650℃の温度、いくつかの実施形態では約700℃〜約1200℃、さらなる実施形態では約750℃〜約1100℃で行われる。粉末の構造特性を改善する焼成ステップは、一般に、少なくとも約15分間、さらなる実施形態では約20分間〜約30時間以上、他の実施形態では約30分間〜約24時間行うことが可能である。加熱ステップは、所望される場合、温度を適切にランピングするステップと組み合わせることにより、所望される材料を産生することが可能である。上で明記した範囲内で温度および時間のさらなる範囲が考えられ、それらの範囲も本開示内であることを、当業者は認識するであろう。
プロセスにおける1つ以上の選択されたステップにおいて、リチウム元素を材料に組み入れることが可能である。例えば、沈殿ステップを行う前または行った後に、水酸化リチウム塩を添加するステップによりリチウム塩を溶液に組み入れることが可能である。このアプローチでは、リチウム種がその他の金属と同じように材料に組み入れられる。また、リチウムの特性のため、生成物組成物の結果的に得られる特性に悪影響を与えることなく、固相反応においてリチウム元素を材料に組み入れることが可能である。従って、例えば、LiOH・H2O、LiOH、またはそれらの組み合わせなどの一般に粉末としての適量のリチウムソースを、沈殿した金属水酸化物と混合させることが可能である。次いで、粉末混合物に加熱ステップを行って酸化物を形成し、次いで、結晶性最終生成物質を形成する。
ゾル−ゲルアプローチでは、金属酢酸塩または他の可溶性金属化合物などの金属塩を、やはり精製水などの水性溶媒に溶解させる。一般に、アニオンが系から除去されるように、後続の加熱ステップ中に塩のアニオンを分解するように選択することが望ましい。いくつかの実施形態では、酢酸塩または硝酸塩のいずれかを可溶性金属化合物として用いることが可能である。しかし、酢酸金属塩は、酸化物を形成する分解プロセス中にいずれの有毒ガスも発生しないため、より環境に優しい。対照的に、硝酸塩は、分解プロセス中にNOxガスを形成する。酸を添加することにより金属溶液を加水分解し、水酸化物ネットワークを形成することが可能である。例えば、グリコール酸/酒石酸溶液を用いることが可能である。水酸化アンモニウムを用いることにより、pHを約7の値に調整することが可能である。酸の量および対応するpHを選択することにより、ゲル形成プロセスを制御することが可能である。溶液をいくらか加熱することにより、ゲルの形成を容易にすることが可能である。結果的に得られるゲルは、採取し、乾燥させることが可能である。採取されたゲルを、まずは約300℃〜約600℃の温度で15分間〜約24時間熱処理することにより、ゲルを分解することが可能である。熱処理により、原理的には、水酸化物が酸化物に変換されることに加え、ゲルのカルボン酸および他の揮発性成分が除去され得る。Fey他(非特許文献2、かかる文献は、参照により本明細書に組み込まれる)により検討されているように、カルボン酸は、一般に加熱処理中に分解するため、酸化物形成のためのエンタルピーに影響を及ぼす。次いで、約800℃〜約1200℃における30分間〜約48時間の焼成ステップを行うことにより、最終層状組成物を形成することが可能である。ゾル−ゲル材料を処理するための温度および時間のさらなる範囲が考えられ、それらの範囲も本開示内であることを、当業者は認識するであろう。
被覆および被覆を形成するための方法
金属フッ化物被覆が、本明細書に記載のリチウムリッチな層状正極活物質の性能を著しく改善することが見出されている。特に、サイクル特性が著しく改善することが見出されている。しかし、フッ化物被覆により総容量も望ましい特性を示し、第1サイクル不可逆的容量損失も減少する。被覆により、本明細書に記載の高容量のリチウムリッチな組成物の性能における驚くべき改善が提供される。一般に、選択された金属フッ化物または半金属フッ化物を被覆に用いることが可能である。同様に、金属および/または半金属元素の組み合わせを有する被覆を用いることが可能である。
金属フッ化物被覆が、本明細書に記載のリチウムリッチな層状正極活物質の性能を著しく改善することが見出されている。特に、サイクル特性が著しく改善することが見出されている。しかし、フッ化物被覆により総容量も望ましい特性を示し、第1サイクル不可逆的容量損失も減少する。被覆により、本明細書に記載の高容量のリチウムリッチな組成物の性能における驚くべき改善が提供される。一般に、選択された金属フッ化物または半金属フッ化物を被覆に用いることが可能である。同様に、金属および/または半金属元素の組み合わせを有する被覆を用いることが可能である。
リチウム二次電池用の一般的な材料用の正極活物質の性能を安定化させる金属/半金属フッ化物被覆が提案されている。フッ化物被覆に好適な金属および半金属元素は、例えば、Al、Bi、Ga、Ge、In、Mg、Pb、Si、Sn、Ti、Tl、Zn、Zr、およびそれらの組み合わせを含む。フッ化アルミニウムは、合理的なコストを有するとともに環境に優しいと考えられるため、望ましい被覆材料であり得る。金属フッ化物被覆は、「Cathode Active Materials Coated With Fluorine Compound for Lithium Secondary Batteries and Method for Preparing the Same」と題されたSun他による公開PCT出願の特許文献2において一般に記載されており、当該明細書は、参照により本明細書に組み込まれる。この特許出願は、LiF、ZnF2、またはAlF3で被覆されたLiCoO2についての結果を提供している。上で参照したSunによるPCT出願は、具体的には、以下のフッ化物組成物に言及している:CsF、KF、LiF、NaF、RbF、TiF、AgF、AgF2、BaF2、CaF2、CuF2、CdF2、FeF2、HgF2、Hg2F2、MnF2、MgF2、NiF2、PbF2、SnF2、SrF2、XeF2、ZnF2、AlF3、BF3、BiF3、CeF3、CrF3、DyF3、EuF3、GaF3、GdF3、FeF3、HoF3、InF3、LaF3、LuF3、MnF3、NdF3、VOF3、PrF3、SbF3、ScF3、SmF3、TbF3、TiF3、TmF3、YF3、YbF3、TlF3、CeF4、GeF4、HfF4、SiF4、SnF4、TiF4、VF4、ZrF4、NbF5、SbF5、TaF5、BiF5、MoF6、ReF6、SF6、およびWF6。
LiN1/3Co1/3Mn1/3O2のサイクル性能に対するAlF3被覆の効果が、Sun他による非特許文献3との論文においてさらに記載されている。また、LiNi0.8Co0.1Mn0.1O2のサイクル性能に対するAlF3被覆の効果が、Woo他による非特許文献4との論文においてさらに記載されており、かかる文献は、参照により本明細書に組み込まれる。Al2O3被覆による不可逆的容量損失における減少が、Wu他により非特許文献4において言及されており、かかる文献は、参照により本明細書に組み込まれる。
以下の実施例において実証されるように、金属/半金属フッ化物被覆は、リチウムイオン二次電池用のリチウムリッチな層状組成物の性能を著しく改善することが可能であることが見出されている。一般に、被覆の量は、被覆により得られる有益な安定化を、材料の高い比容量に直接寄与しないのが一般的な被覆材料の重量による比容量の損失と平衡化させるように選択することが可能である。一般に、被覆材料の量は、約0.005モルパーセント〜約10モルパーセント、さらなる実施形態では約0.5モルパーセント〜約7モルパーセント、他の実施形態では約2.0モルパーセント〜約3.5モルパーセントの範囲である。上で明記した範囲内で被覆材料のさらなる範囲が考えられ、それらの範囲も本開示内であることを、当業者は認識するであろう。無被覆材料の容量を改善するために有効なAlF3被覆金属酸化物材料におけるAlF3の量は、無被覆材料の粒子サイズおよび表面積に関する。特に、より大きい表面積の粉末については、一般に、より高いモル百分率の金属フッ化物被覆を用いることにより、より小さい表面積の粉末に対する被覆と同等の効果を達成することが可能である。
フッ化物被覆は、沈殿アプローチを用いて堆積させることが可能である。正極材料の粉末を、水性溶媒などの好適な溶媒中に混合することが可能である。所望される金属/半金属の可溶性組成物を、溶媒に溶解させることが可能である。次いで、NH4Fを分散/溶液に徐々に添加することにより、金属フッ化物を沈殿させることが可能である。被覆反応体の総量は、所望される量の被覆が形成されるように選択することが可能であり、被覆反応体の比は、被覆材料の化学量論に基づかせることが可能である。被覆プロセス中、被覆混合物を、水溶液については約60℃〜約100℃の範囲などの合理的な温度に約20分間〜約48時間加熱することにより、被覆プロセスを容易にすることが可能である。被覆電気活性材料を溶液から除去した後、材料を乾燥させ、一般に約250℃〜約600℃の温度に約20分間〜約48時間加熱することにより、被覆材料の形成を完了させることが可能である。加熱は、窒素雰囲気下または他の実質的に無酸素の雰囲気下で行うことが可能である。
電池性能
本明細書に記載の改善された正極活物質から形成された電池は、中程度の電流のアプリケーションのための現実的な放電条件下で優れた性能を示している。具体的には、活物質は、中程度の放電レートにおけるセルのサイクル後に、改善された比容量を示している。さらにその上、被覆材料は、多くのサイクル数まで改善されたサイクルを示している。いくつかの実施形態では、被覆電気活性材料は、無被覆材料に対して、第1サイクル不可逆的容量損失における著しい減少を示す。
本明細書に記載の改善された正極活物質から形成された電池は、中程度の電流のアプリケーションのための現実的な放電条件下で優れた性能を示している。具体的には、活物質は、中程度の放電レートにおけるセルのサイクル後に、改善された比容量を示している。さらにその上、被覆材料は、多くのサイクル数まで改善されたサイクルを示している。いくつかの実施形態では、被覆電気活性材料は、無被覆材料に対して、第1サイクル不可逆的容量損失における著しい減少を示す。
一般に、様々な類似の試験手順を用いて電池性能を評価することが可能である。本明細書に記載の性能値を評価するための具体的な試験手順について説明する。試験手順は、以下の実施例においてより詳細に説明する。具体的には、セルは、室温で4.6ボルトと2.0ボルトとの間でサイクルさせることが可能であるが、他の範囲を用いることにより対応する異なる結果を得ることも可能である。セルは、一般に、4.6ボルト〜2.0ボルトの範囲にわたり安定したサイクルを有するため、この範囲にわたり評価を行うことが商業的使用のために望ましい。最初の3サイクルについては、セルをレートC/10で放電させて不可逆的容量損失を生じさせる。続く3サイクルは、セルをC/5でサイクルさせる。サイクル7以降については、セルを、中電流アプリケーションのための合理的な試験レートであるレートC/3でサイクルさせる。繰り返すが、C/xとの表記は、セルをx時間で選択された最小電圧まで十分に放電させるレートで、セルを放電させることを示唆する。セル容量は放電レートに大きく依存し、放電レートが増加するにつれて容量が失われる。
いくつかの実施形態では、正極活物質は、放電レートC/3における第10サイクル中の比容量が少なくとも約240ミリアンペア時毎グラム(mAh/g)であり、追加の実施形態では、約245mAh/g〜約270mAh/gである。被覆電気活性材料についての不可逆的容量損失は、無被覆材料の同様の性能に対して少なくとも約25%、さらなる実施形態では約30%〜約60%減少させることが可能である。比容量および不可逆的容量損失における減少のさらなる範囲が考えられ、それらの範囲も本開示内であることを、当業者は認識するであろう。
実施例1〜8において試験したコイン型セルは、すべて、ここで概説する手順に従い生産したものを用いた。リチウム金属酸化物(LMO)粉末を、アセチレンブラック(Timcal,Ltd,SwitzerlandのSuper P(商標))およびグラファイト(Timcal,LtdのKS 6(商標))とよく混合して、均質な粉末混合物を形成した。別に、ポリフッ化ビニリデンPVDF(日本の株式会社クレハのKF1300(商標))を、N−メチル−ピロリドン(Honeywell−Riedel−de−Haen)と混合し、一晩攪拌してPVDF−NMP溶液を形成した。次いで、均質な粉末混合物をPVDF−NMP溶液に添加し、約2時間混合させて均質なスラリを形成した。ドクターブレード被覆プロセスを用いてスラリをアルミニウム箔集電体上に塗布することにより濡れた薄膜を形成した。
濡れた薄膜を有するアルミニウム箔集電体を110℃の真空オーブン中で約2時間乾燥させることによりNMPを除去し、正極材料を形成した。シートミルのローラの間で正極材料をプレス処理し、所望の厚さを有する正極を得た。上記のプロセスを用いて作成された80:5:5:10のLMO:アセチレンブラック:グラファイト:PVDF比を有する正極組成物の例を、以下で提示する。
コイン型セルを製作するため、アルゴンを充填したグローブボックス内に正極を配置した。125ミクロンの厚さを有するリチウム箔(FMC Lithium)を負極として用いた。電解質は、体積比1:1:1の炭酸エチレン、炭酸ジエチル、および炭酸ジメチル(Ferro Corp.,Ohio USA)の混合物にLiPF6塩を溶解させることにより形成されたLiPF6の1M溶液とした。正極と負極との間に、電解質を浸した三層(ポリプロピレン/ポリエチレン/ポリプロピレン)微孔性セパレータ(Celgard,LLC,NC,USAの2320)を配置した。さらに数滴の電解質を電極間に添加した。次いで、かしめプロセスにより電極を2032コイン型セルハードウェア(宝泉株式会社、日本)に封入して、コイン型セルを形成した。結果的に得られるコイン型セルをMaccorサイクル試験器で試験して、一定数のサイクルにわたる充放電曲線およびサイクル安定性を得た。本明細書に含まれるすべての電気化学的データは、0.1C(C/10)、0.2C(C/5)、または0.33C(C/3)の3つのレートでのサイクルによるものである。
実施例1:金属酢酸塩のLiOH/NH4OHとの反応によるリチウム金属酸化物の形成
本実施例は、後に所望の酸化物に処理される水酸化物として沈殿した金属酢酸塩に基づく共沈プロセスを実証するものである。リチウムは、最初の沈殿ステップにおいて組み入れられる。
本実施例は、後に所望の酸化物に処理される水酸化物として沈殿した金属酢酸塩に基づく共沈プロセスを実証するものである。リチウムは、最初の沈殿ステップにおいて組み入れられる。
本実施例における処理は、無酸素雰囲気中で行った。適切なモル比の化学量論量の酢酸リチウム、酢酸ニッケル、酢酸コバルト、および酢酸マンガンを水に溶解させ、Ni、Co、Mnイオンを含有する飽和遷移金属酢酸塩溶液を形成した。また、要求されるモル比の水酸化リチウム(LiOH)および少なくとも2倍の濃度の水酸化アンモニウム(NH4OH)を含む飽和溶液も調製した。遷移金属酢酸塩溶液をLiOH/NH4OH溶液にゆっくりと滴下させ、遷移金属水酸化物の沈殿物を形成させた。遷移金属酢酸塩溶液の添加完了後、反応混合物をゆっくりと110℃まで短時間温めた。続いて、反応混合物を140℃まで温め、蒸発により水を除去した。反応混合物から水が実質的に除去されると、混合物は粘性を有する半固体物質となった。半固体物質を大容量るつぼに移動させ、ゆっくりと480℃に10時間加熱した。焼成後に得られた固体を穏やかに粉砕して茶色がかった黒色のLMO粉末を形成し、それを800〜1000℃で焼成して電気化学的性能を改善させた。生成物組成物はLi1.2Ni0.175Co0.10Mn0.525O2であった。
LMO粉末をX線により測定し、粉末のX線回析パターンを図2に示す。上で概説した手順に従い、LMO粉末を用いてコイン型セルを形成した。コイン型セルを試験し、電圧対比容量および比容量対サイクル寿命のプロットをそれぞれ図3aおよび図3bに示す。
実施例2:金属酢酸塩のLiOHとの反応によるリチウム金属酸化物の形成
本実施例は、混合金属水酸化物に関わる固相反応においてリチウムが導入される水酸化物共沈アプローチを用いる正極材料の合成を実証するものである。
本実施例は、混合金属水酸化物に関わる固相反応においてリチウムが導入される水酸化物共沈アプローチを用いる正極材料の合成を実証するものである。
乾燥した沈殿物の形成による本実施例における処理は、無酸素雰囲気中で行った。化学量論量の酢酸ニッケル(Ni(CH3COO)2・xH2O)、酢酸コバルト(Co(CH3COO)2・xH2O)、および酢酸マンガン(Mn(CH3COO)2・xH2O)を蒸留水に溶解させ、金属酢酸塩溶液を形成した。金属酢酸塩溶液をLiOH水溶液の攪拌溶液に連続的に添加し、金属水酸化物を沈殿させた。反応混合物を10〜12程度のpHで室温〜80℃に保った。金属酢酸塩の添加レート、攪拌速度、反応混合物の温度およびpH値を調整して、沈殿する粒子のモーフォロジ、サイズ、および電子特性を制御した。いくつかの実施形態では、金属酢酸塩水溶液の濃度は1M〜3Mであり、LiOH水溶液の濃度は1M〜3Mであった。プロセス中、水酸化リチウム溶液を用いてOH−イオンを提供することにより、金属水酸化物沈殿物を形成した。以下で検討する後続の濾過ステップおよび洗浄ステップ後にLiOHの残留分が金属水酸化物中に存在してもよいが、リチウムの大部分は可溶性塩として洗い落とされた。
金属水酸化物沈殿物を濾過し、蒸留水で複数回洗浄し、110℃の窒素雰囲気下の真空オーブン中で16時間乾燥させることにより、乾燥した金属水酸化物粉末を産出させた。適量のLiOH粉末を乾燥した金属水酸化物粉末と組み合わせ、ジャーミル、二重遊星ミキサ、または乾燥粉末ミキサでよく混合させた。混合粉末を空気中で400℃で8時間焼成し、続いて、さらなる混合ステップを行うことにより、形成された粉末をさらに均質化させた。均質化された粉末を、再度、空気中で900℃で12時間焼成することにより、リチウム組成物酸化物粉末(LMO)を形成した。生成物組成物はLi1.2Ni0.175Co0.10Mn0.525O2であった。
LMO粉末をX線により測定し、粉末のX線回析パターンを図4に示す。上で概説した手順に従い、LMO粉末を用いてコイン型セルを形成した。形成されたコイン型セルを試験し、電圧対比容量および比容量対サイクル寿命のプロットをそれぞれ図5aおよび図5bに示す。最初の3サイクルは、放電レート0.1Cで得た。次の3サイクルは、レート0.2Cで測定した。それ以降のサイクルは、レート0.33Cで測定した。
実施例3:金属硫酸塩のNaOH/NH4OHとの反応によるリチウム金属酸化物の形成
本実施例は、水酸化ナトリウムと水酸化アンモニウムとの混合物として提供される塩基を有する金属硫酸塩出発物質に基づく共沈プロセスを実証するものである。
本実施例は、水酸化ナトリウムと水酸化アンモニウムとの混合物として提供される塩基を有する金属硫酸塩出発物質に基づく共沈プロセスを実証するものである。
乾燥した沈殿物の形成による本実施例における処理は、無酸素雰囲気中で行った。化学量論量の金属硫酸塩(NiSO4・xH2O、CoSO4・xH2O、およびMnSO4・xH2O)を蒸留水に溶解させ、金属硫酸塩水溶液を形成した。別に、NaOHとNH4OHとの混合物を有する水溶液を調製した。2つの溶液を反応容器に徐々に添加して金属水酸化物沈殿物を形成した。沈殿ステップ中、反応混合物の温度を室温〜80℃に保ちながら、反応混合物を攪拌した。反応混合物のpHは約10〜12であった。金属硫酸塩水溶液の濃度は1M〜3Mであり、NaOH/NH4OH水溶液のNaOH濃度は1M〜3M、NH4OH濃度は0.2〜2Mであった。金属水酸化物沈殿物を濾過し、蒸留水で複数回洗浄し、110℃で16時間乾燥させることにより、金属水酸化物粉末を形成した。
適量のLiOH粉末を乾燥した金属水酸化物粉末と組み合わせ、ジャーミル、二重遊星ミキサ、または乾燥粉末ミキサでよく混合させることにより、均質な粉末混合物を形成した。均質化された粉末を空気中で500℃で10時間焼成し、続いて、さらなる混合ステップを行うことにより、結果的に得られる粉末をさらに均質化させた。均質化された粉末を、再度、空気中で900℃で12時間焼成することにより、リチウム組成物酸化物粉末(LMO)を形成した。生成物組成物はLi1.2Ni0.175Co0.10Mn0.525O2であった。
LMO粉末をX線により測定し、粉末のX線回析パターンを図6に示す。上で概説した手順に従い、LMO粉末を用いてコイン型セルを形成した。形成されたコイン型セルを試験し、電圧対比容量および比容量対サイクル寿命のプロットをそれぞれ図7aおよび図7bに示す。最初の3サイクルは、放電レート0.1Cで測定した。次の3サイクルは、レート0.2Cで測定した。それ以降のサイクルは、レート0.33Cで測定した。
実施例4:金属酢酸塩のNaOH/NH4OHとの反応によるリチウム金属酸化物の形成
金属硫酸塩の代わりに化学量論量の酢酸ニッケル(Ni(CH3COO)2・xH2O)、酢酸コバルト(Co(CH3COO)2・xH2O)、および酢酸マンガン(Mn(CH3COO)2・xH2O)を用いて実施例3で説明したプロセスを繰り返すことにより、金属水酸化物沈殿物を形成した。水酸化リチウムとの反応後、リチウム組成物酸化物粉末(LMO)が形成された。均質化された粉末を、再度、空気中で900℃で12時間焼成することにより、リチウム組成物酸化物粉末(LMO)を形成した。生成物組成物はLi1.2Ni0.175Co0.10Mn0.525O2であった。
金属硫酸塩の代わりに化学量論量の酢酸ニッケル(Ni(CH3COO)2・xH2O)、酢酸コバルト(Co(CH3COO)2・xH2O)、および酢酸マンガン(Mn(CH3COO)2・xH2O)を用いて実施例3で説明したプロセスを繰り返すことにより、金属水酸化物沈殿物を形成した。水酸化リチウムとの反応後、リチウム組成物酸化物粉末(LMO)が形成された。均質化された粉末を、再度、空気中で900℃で12時間焼成することにより、リチウム組成物酸化物粉末(LMO)を形成した。生成物組成物はLi1.2Ni0.175Co0.10Mn0.525O2であった。
本実施例における処理は、無酸素雰囲気中で行った。LMO粉末をX線により測定し、粉末のX線回析パターンを図8に示す。上で概説した手順に従い、LMO粉末を用いてコイン型セルを形成した。形成されたコイン型セルを試験し、電圧対比容量および比容量対サイクル寿命のプロットをそれぞれ図9aおよび図9bに示す。最初の3サイクルは、放電レート0.1Cで測定した。次の3サイクルは、レート0.2Cで測定した。それ以降のサイクルは、レート0.33Cで測定した。
実施例5:金属酢酸塩のLiOH/NH4OHとの反応によるリチウム金属酸化物の形成
本実施例は、リチウムを金属水酸化物沈殿物に組み入れない点を除いて実施例1に類似の水酸化物ベースの共沈プロセスを実証するものである。
本実施例は、リチウムを金属水酸化物沈殿物に組み入れない点を除いて実施例1に類似の水酸化物ベースの共沈プロセスを実証するものである。
乾燥した沈殿物の形成による本実施例における処理は、無酸素雰囲気中で行った。化学量論量の酢酸ニッケル(Ni(CH3COO)2・xH2O)、酢酸コバルト(Co(CH3COO)2・xH2O)、および酢酸マンガン(Mn(CH3COO)2・xH2O)を蒸留水に溶解させ、金属酢酸塩溶液を形成した。別に、LiOHおよびNH4OHの水溶液を調製した。2つの溶液を反応容器に徐々に添加して金属水酸化物沈殿物を形成した。反応混合物の温度を室温〜80℃に保ちながら、反応混合物を攪拌した。反応混合物のpHは約10〜12であった。一般に、金属硫酸塩水溶液の濃度は1M〜3Mであり、LiOH/NH4OH水溶液のLiOH濃度は1M〜3M、NH4OH濃度は0.2〜2Mであった。金属水酸化物沈殿物を濾過し、蒸留水で複数回洗浄し、110℃で16時間乾燥させることにより、金属水酸化物粉末を形成した。
適量のLiOH粉末を乾燥した金属水酸化物粉末と組み合わせ、ジャーミル、二重遊星ミキサ、または乾燥粉末ミキサでよく混合させることにより、均質な粉末混合物を形成した。均質化された粉末を空気中で400℃で8時間焼成し、続いてさらなる混合ステップを行うことにより、形成された粉末をさらに均質化させた。均質化された粉末を、再度、空気中で900℃で12時間焼成することにより、リチウム組成物酸化物粉末(LMO)を形成した。生成物組成物はLi1.2Ni0.175Co0.10Mn0.525O2であった。
LMO粉末をX線により測定し、粉末のX線回析パターンを図10に示す。上で概説した手順に従い、LMO粉末を用いてコイン型セルを形成した。形成されたコイン型セルを試験し、電圧対比容量および比容量対サイクル寿命のプロットをそれぞれ図11aおよび図11bに示す。最初の3サイクルは、放電レート0.1Cで測定した。次の3サイクルは、レート0.2Cで測定した。それ以降のサイクルは、レート0.33Cで測定した。
実施例6:ゾル−ゲルプロセス
本実施例は、ゾル−ゲルプロセスを用いる所望されるリチウム金属酸化物組成物の合成を実証するものである。
本実施例は、ゾル−ゲルプロセスを用いる所望されるリチウム金属酸化物組成物の合成を実証するものである。
化学量論量の金属酢酸塩を水に溶解させ、金属酢酸塩溶液を形成した。別に、マレイン酸溶液も調製した。定速で攪拌しながら、金属酢酸塩溶液をマレイン酸溶液に滴下によりゆっくりと添加した。好適な量の塩基を滴下により添加することにより反応混合物のpHを調整して、反応中ずっといずれの浮遊物も生じさせることなく反応混合物を当初の清澄性に維持した。金属酢酸塩溶液の添加後、反応混合物の温度を85℃に上昇させ、反応混合物から水をゆっくりと蒸発させることにより、「ゾル」を形成した。「ゾル」をさらに110℃で加熱することにより、「ゲル」の形成を容易にした。次いで、ゲルを収集し、空気中で480℃で12時間予備焼成してカルボン酸を除去することにより、ターゲット組成物を形成した。さらに、ターゲット組成物を800〜1000℃で焼成することにより、結晶性を改善させた。ターゲット組成物の結晶性は、その電気化学的性能にとって重要である。生成物組成物はLi1.2Ni0.175Co0.10Mn0.525O2であった。
生成物組成物をX線により測定し、粉末のX線回析パターンを図12に示す。上で概説した手順に従い、組成物を用いてコイン型セルを形成した。コイン型セルを試験し、電圧対比容量および比容量対サイクル寿命のプロットをそれぞれ図13aおよび図13bに示す。最初の3サイクルは、放電レート0.1Cで測定した。次の3サイクルは、レート0.2Cで測定した。
実施例7:AlF3被覆金属酸化物材料の形成
上記実施例において調製した金属酸化物粒子は、溶液補助法を用いてフッ化アルミニウム(AlF3)の薄層で被覆することが可能である。選択された量のフッ化アルミニウム被覆のため、適量の硝酸アルミニウムの飽和溶液を水性溶媒中で調製した。次いで、金属酸化物粒子を硝酸アルミニウム溶液に添加することにより、混合物を形成した。混合物を一定期間激しく混合することにより均質化させた。混合の長さは、混合物の体積に依存する。均質化後、化学量論量のフッ化アンモニウムを均質化された混合物に添加することにより、フッ素ソースを保持しながら金属水酸化物沈殿物を形成した。沈殿の完了後、混合物を80℃で5時間攪拌した。次いで、混合物を濾過し、得られた固体を繰り返し洗浄することにより、いずれの未反応材料も除去した。固体を400℃で窒素雰囲気中で5時間焼成することにより、AlF3被覆金属酸化物材料を形成した。
上記実施例において調製した金属酸化物粒子は、溶液補助法を用いてフッ化アルミニウム(AlF3)の薄層で被覆することが可能である。選択された量のフッ化アルミニウム被覆のため、適量の硝酸アルミニウムの飽和溶液を水性溶媒中で調製した。次いで、金属酸化物粒子を硝酸アルミニウム溶液に添加することにより、混合物を形成した。混合物を一定期間激しく混合することにより均質化させた。混合の長さは、混合物の体積に依存する。均質化後、化学量論量のフッ化アンモニウムを均質化された混合物に添加することにより、フッ素ソースを保持しながら金属水酸化物沈殿物を形成した。沈殿の完了後、混合物を80℃で5時間攪拌した。次いで、混合物を濾過し、得られた固体を繰り返し洗浄することにより、いずれの未反応材料も除去した。固体を400℃で窒素雰囲気中で5時間焼成することにより、AlF3被覆金属酸化物材料を形成した。
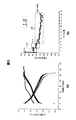
具体的には、実施例2において合成したリチウム金属酸化物(LMO)粒子を、本実施例において説明したプロセスを用いて3モル%のフッ化アルミニウムで被覆した。次いで、上で概説した手順に従い、フッ化アルミニウムで被覆されたLMOを用いてコイン型セルを形成した。コイン型セルを試験し、比容量対サイクル寿命のプロットを図14に示す。図14は、実施例2のフッ化アルミニウム被覆LMOから形成されたコイン型セルからのデータを示す。図15および図16は、それぞれ放電レート0.1Cおよび0.33における3モル%のフッ化アルミニウムで被覆された金属酸化物の電圧対比容量のプロットである。
実施例8:AlF3被覆金属酸化物材料における異なる被覆量についての性能結果
本実施例は、性能がAlF3被覆材料の量に大きく依存することを実証している。
本実施例は、性能がAlF3被覆材料の量に大きく依存することを実証している。
組成物Li[Li0.2Ni0.175Co0.10Mn0.525]O2を有するカソード材料を、実施例4において説明した金属酢酸塩、水酸化ナトリウム、および水酸化アンモニウムの間の共沈プロセスを用いて合成した。続いて、材料をフッ化アルミニウムで被覆することにより、フッ化アルミニウムのモル百分率が1%、2%、および4%であるAlF3被覆Li[Li0.2Ni0.175Co0.10Mn0.525]O2(AlF3−LMO)組成物を形成した。次いで、上で概説した手順に従い、AlF3−LMO材料を用いてコイン型セルを形成した。
コイン型セルを試験し、比容量対サイクル寿命のプロットを図17に示す。セルの最初の3サイクルは、放電レートC/10で試験を行った。サイクル4〜6は放電レートC/5で試験を行い、それ以降は放電レートC/3でセルをサイクルさせた。図17は、AlF3被覆がより高い放電レートC/3においてセルの容量を改善させることを示す。C/3放電レートでは、1モル%および2モル%のAlF3で被覆されたサンプルの容量が無被覆サンプルよりも高い。しかし、4モル%のAlF3で被覆されたサンプルの容量は、無被覆サンプルよりも低い。フッ化アルミニウム自体は、電気化学的に活性ではない。サンプルに添加されるフッ化アルミニウムの量による比容量の損失が、フッ化アルミニウム被覆を追加する利点がその電気化学的不活性により相殺される点を超えるときは、セル容量の低下が観測される。Li[Li0.2Ni0.175Co0.10Mn0.525]O2材料について用いるフッ化アルミニウムの量の閾値は、2〜4モル%のようである。
さらなる合成プロセスを行ってAlF3含有量を最適化した。組成物Li[Li0.2Ni0.175Co0.10Mn0.525]O2を有するカソード材料を、実施例2において説明した金属酢酸塩と水酸化リチウムとの間の共沈プロセスを用いて合成した。続いて、材料をフッ化アルミニウムで被覆することにより、フッ化アルミニウムのモル百分率が2%および3%であるAlF3被覆Li[Li0.2Ni0.175Co0.10Mn0.525]O2(AlF3−LMO)組成物を形成した。次いで、上で概説した手順に従い、AlF3−LMO材料を用いてコイン型セルを形成した。コイン型セルを試験し、比容量対サイクル寿命のプロットを図18に示す。2モル%および3モル%のフッ化アルミニウムで被覆されたサンプルは、無被覆粉末よりも高い容量を示した。また、AlF3被覆サンプルの不可逆的容量損失は32mAh/gであり、無被覆粉末の65mAh/gよりも低かった。
上記実施形態は、説明を意図するものであって、限定を意図していない。さらなる実施形態も請求項の範囲である。加えて、本発明を特定の実施形態を参照して説明してきたが、本発明の精神および範囲を逸脱することなく形態および詳細における変更を行うことが可能であることが、当業者には理解されよう。上記文書のいずれの参照による引用も、本明細書中の明示的開示に反するいずれの主題も組み込まれないように限定される。
Claims (26)
- 4.6ボルトから2.0ボルトへの放電時の放電レートC/3における室温での第10放電サイクル放電容量が、少なくとも240mAh/gである、リチウムイオンセル用正極活物質。
- 式xLiMO2・(1−x)Li2M’O3を有し、式中、Mは平均原子価が+3である1つ以上の金属イオンを表し、M’は平均原子価が+4である1つ以上の金属イオンであり、0<x<1である、請求項1に記載の正極活物質。
- M’はMnを含み、MはMn、Co、およびNiを含む、請求項2に記載の正極活物質。
- 式Li1+xNiαMnβCoγMδO2−zFzを有し、式中、xは約0.05〜約0.25の範囲、αは約0.1〜約0.4の範囲、βは約0.4〜約0.65の範囲、γは約0.05〜約0.3の範囲、δは約0〜約0.1の範囲、zは約0〜約0.1の範囲であり、MはMg、Zn、Al、Ga、B、Zr、Ti、Ca、Ce、Y、Nb、またはそれらの組み合わせである、請求項1に記載の正極活物質。
- 式Li1+xNiαMnβCoγO2を有し、式中、xは約0.05〜約0.25の範囲、αは約0.1〜約0.4の範囲、βは約0.4〜約0.65の範囲、γは約0.05〜約0.3の範囲である、請求項1に記載の正極活物質。
- 式Li1.2Ni0.175Co0.10Mn0.525O2を有する、請求項1に記載の正極活物質。
- 4.6ボルトから2.0ボルトへの放電時の放電レートC/3における室温での第10放電サイクル放電容量が、少なくとも245mAh/gである、請求項1に記載の正極活物質。
- 4.6ボルトから約2.0ボルトへの放電時の放電レートC/3における室温での第10放電サイクル放電容量が、約250〜約275mAh/gである、請求項1に記載の正極活物質。
- 金属フッ化物の被覆を含む、請求項1に記載の正極活物質。
- 請求項1に記載の正極活物質を含む正極と、リチウムインターカレーション組成物を含む負極と、前記正極と前記負極との間のセパレータとを備える、二次リチウムイオン電池。
- 結晶格子内に+4金属カチオン、+3金属カチオン、および+2金属カチオンを含む層状リチウム金属酸化物を含むリチウムイオンセル用正極活物質であって、前記活物質は金属/半金属フッ化物被覆を有し、前記正極活物質は、放電レートC/10における第1サイクル不可逆的容量損失が、無被覆材料の第1サイクル不可逆的容量損失の約2/3以下であり、放電レートC/3における室温での放電時の第20サイクル放電容量が、第5サイクル放電容量の少なくとも約98%である、正極活物質。
- 式xLiMO2・(1−x)Li2M’O3を有し、式中、Mは平均原子価が+3である1つ以上の金属イオンを表し、M’は平均原子価が+4である1つ以上の金属イオンであり、0<x<1である、請求項11に記載の正極活物質。
- 式Li1+xNiαMnβCoγO2を有し、式中、xは約0.05〜約0.25の範囲、αは約0.1〜約0.4の範囲、βは約0.4〜約0.65の範囲、γは約0.05〜約0.3の範囲である、請求項11に記載の正極活物質。
- 前記材料は約0.5モルパーセント〜約4モルパーセントの金属フッ化物を含む、請求項11に記載の正極活物質。
- 前記金属フッ化物はAlF3を含む、請求項11に記載の正極活物質。
- 前記電極材料は、レートC/3における室温での放電時の第20サイクル放電容量が、第5サイクル放電容量の少なくとも約98.5%である、請求項11に記載の正極活物質。
- 前記電極活物質は、4.6ボルトから2.0ボルトへの放電時の放電レートC/3における室温での第10サイクル放電容量が、約250mAh/g〜約275mAh/gである、請求項11に記載の正極活物質。
- 請求項11に記載の正極活物質を含む正極と、リチウムインターカレーション組成物を含む負極と、前記正極と前記負極との間のセパレータとを備える、二次リチウムイオン電池。
- 層状リチウム金属酸化物組成物を合成するための方法であって、前記方法は、+2金属カチオンを含む溶液から混合金属水酸化物組成物を沈殿させるステップを含み、前記水酸化物組成物は選択された組成物を有する、方法。
- 前記溶液は酢酸アニオン、硫酸アニオン、硝酸アニオン、またはそれらの組み合わせを含む、請求項19に記載の方法。
- 前記水酸化物組成物を加熱して対応する結晶性リチウム金属酸化物組成物を形成するステップをさらに含む、請求項19に記載の方法。
- 前記組成物は式Li1+xNiαMnβCoγO2を有し、式中、xは約0.05〜約0.25の範囲、αは約0.1〜約0.4の範囲、βは約0.4〜約0.65の範囲、γは約0.05〜約0.3の範囲である、請求項21に記載の方法。
- 粉末形態のリチウムソースを前記金属水酸化物組成物に添加して混合物を形成するステップと、前記混合物を加熱して対応する結晶性リチウム金属酸化物組成物を形成するステップとをさらに含む、請求項19に記載の方法。
- 層状リチウム金属酸化物組成物を合成するための方法であって、前記方法は、リチウムイオンおよび+2金属カチオンを含むゾル−ゲル組成物を少なくとも約750℃の温度で焼成して結晶性層状リチウム金属酸化物組成物を形成するステップを含む、方法。
- 前記組成物は式Li1+xNiαMnβCoγO2を有し、式中、xは約0.05〜約0.25の範囲、αは約0.1〜約0.4の範囲、βは約0.4〜約0.65の範囲、γは約0.05〜約0.3の範囲である、請求項24に記載の方法。
- 前記ゾル−ゲルは、カルボン酸を金属酢酸塩溶液に添加することにより形成される、請求項24に記載の方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US12/246,814 US8389160B2 (en) | 2008-10-07 | 2008-10-07 | Positive electrode materials for lithium ion batteries having a high specific discharge capacity and processes for the synthesis of these materials |
| US12/246,814 | 2008-10-07 | ||
| PCT/US2009/059519 WO2010042434A2 (en) | 2008-10-07 | 2009-10-05 | Positive electrode materials for lithium ion batteries having a high specific discharge capacity and processes for the synthesis of these materials |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2012505520A true JP2012505520A (ja) | 2012-03-01 |
| JP2012505520A5 JP2012505520A5 (ja) | 2012-11-29 |
Family
ID=42076074
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011531092A Pending JP2012505520A (ja) | 2008-10-07 | 2009-10-05 | 高い比放電容量を有するリチウムイオン電池用正極材料およびこれらの材料を合成するためのプロセス |
Country Status (7)
| Country | Link |
|---|---|
| US (2) | US8389160B2 (ja) |
| EP (1) | EP2351122A4 (ja) |
| JP (1) | JP2012505520A (ja) |
| KR (1) | KR20110084200A (ja) |
| CN (1) | CN102177605A (ja) |
| TW (1) | TWI384669B (ja) |
| WO (1) | WO2010042434A2 (ja) |
Cited By (18)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2013511129A (ja) * | 2009-11-11 | 2013-03-28 | エンビア・システムズ・インコーポレイテッド | リチウムイオン電池用のコーティングを施した正極材料 |
| JP2013206685A (ja) * | 2012-03-28 | 2013-10-07 | National Institute Of Advanced Industrial & Technology | 高結晶性のaLi2MnO3−(1−a)Li(Nix,Coy,Mnz)O2系ナノ構造電極材料、および、エレクトロスピニング法によるその製造方法 |
| JP2013206558A (ja) * | 2012-03-27 | 2013-10-07 | Tdk Corp | 活物質及びリチウムイオン二次電池 |
| WO2014076946A1 (ja) * | 2012-11-13 | 2014-05-22 | Jx日鉱日石エネルギー株式会社 | 正極材、正極材の製造方法、および非水電解質電池 |
| JP2014116308A (ja) * | 2012-12-06 | 2014-06-26 | Samsung Fine Chemicals Co Ltd | 正極活物質、その製造方法およびそれを含むリチウム二次電池 |
| JP2014531718A (ja) * | 2011-09-26 | 2014-11-27 | コリア エレクトロニクス テクノロジ インスティチュート | リチウム二次電池用正極活物質、その製造方法及びそれを含むリチウム二次電池 |
| JP2015533257A (ja) * | 2013-06-18 | 2015-11-19 | エルジー・ケム・リミテッド | リチウム二次電池用正極活物質及びその製造方法 |
| JP2015213054A (ja) * | 2014-04-15 | 2015-11-26 | ワイルドキャット・ディスカバリー・テクノロジーズ・インコーポレイテッドWildcat Discovery Technologies, Inc. | 金属抽出によって作製した材料 |
| JP2016058316A (ja) * | 2014-09-11 | 2016-04-21 | トヨタ自動車株式会社 | リチウムイオン二次電池及びその製造方法 |
| JP2016516267A (ja) * | 2013-03-15 | 2016-06-02 | ナノ ワン マテリアルズ コーポレーション | 電池用途の層状リチウム混合酸化物の微細粉体及び超微細粉体、並びにナノ粉体の工業生産に関する錯形成前駆体配合方法論 |
| JP2016524576A (ja) * | 2013-03-15 | 2016-08-18 | ナノ ワン マテリアルズ コーポレーション | 電池用途のリチウム金属酸化物の微細粉体及び超微細粉体、並びにナノ粉体の工業生産に関する錯形成前駆体配合方法論 |
| US9570739B2 (en) | 2013-02-28 | 2017-02-14 | Samsung Sdi Co., Ltd. | Composite positive active material, method of preparing the same, and positive electrode and lithium battery containing the material |
| JP2017037713A (ja) * | 2015-08-06 | 2017-02-16 | トヨタ自動車株式会社 | 非水電解質二次電池用正極活物質の製造方法 |
| WO2017094416A1 (ja) * | 2015-12-02 | 2017-06-08 | 日本電気株式会社 | リチウム二次電池用正極活物質、リチウム二次電池用正極及びリチウム二次電池、並びにそれらの製造方法 |
| US9685657B2 (en) | 2013-08-08 | 2017-06-20 | Samsung Sdi Co., Ltd. | Composite precursor, composite prepared therefrom, a method of preparing a composite precursor and a composite, positive electrode for lithium secondary battery including the same, and lithium secondary battery employing the same |
| JP2018529198A (ja) * | 2015-09-16 | 2018-10-04 | ローベルト ボツシユ ゲゼルシヤフト ミツト ベシユレンクテル ハフツングRobert Bosch Gmbh | バッテリーセルの正極用の活物質、正極、およびバッテリーセル |
| JP2018529197A (ja) * | 2015-09-16 | 2018-10-04 | ローベルト ボツシユ ゲゼルシヤフト ミツト ベシユレンクテル ハフツングRobert Bosch Gmbh | バッテリーセルの正極用の活物質、正極、およびバッテリーセル |
| JP2020513653A (ja) * | 2016-11-24 | 2020-05-14 | ローベルト ボツシユ ゲゼルシヤフト ミツト ベシユレンクテル ハフツングRobert Bosch Gmbh | 電池セルの正極用の活物質、正極および電池セル |
Families Citing this family (144)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8404376B2 (en) | 2002-08-09 | 2013-03-26 | Infinite Power Solutions, Inc. | Metal film encapsulation |
| US8445130B2 (en) | 2002-08-09 | 2013-05-21 | Infinite Power Solutions, Inc. | Hybrid thin-film battery |
| US8394522B2 (en) | 2002-08-09 | 2013-03-12 | Infinite Power Solutions, Inc. | Robust metal film encapsulation |
| US8236443B2 (en) | 2002-08-09 | 2012-08-07 | Infinite Power Solutions, Inc. | Metal film encapsulation |
| US8535396B2 (en) | 2002-08-09 | 2013-09-17 | Infinite Power Solutions, Inc. | Electrochemical apparatus with barrier layer protected substrate |
| US20070264564A1 (en) | 2006-03-16 | 2007-11-15 | Infinite Power Solutions, Inc. | Thin film battery on an integrated circuit or circuit board and method thereof |
| US8431264B2 (en) | 2002-08-09 | 2013-04-30 | Infinite Power Solutions, Inc. | Hybrid thin-film battery |
| US8021778B2 (en) | 2002-08-09 | 2011-09-20 | Infinite Power Solutions, Inc. | Electrochemical apparatus with barrier layer protected substrate |
| US8728285B2 (en) | 2003-05-23 | 2014-05-20 | Demaray, Llc | Transparent conductive oxides |
| US8636876B2 (en) | 2004-12-08 | 2014-01-28 | R. Ernest Demaray | Deposition of LiCoO2 |
| US7959769B2 (en) | 2004-12-08 | 2011-06-14 | Infinite Power Solutions, Inc. | Deposition of LiCoO2 |
| US8062708B2 (en) | 2006-09-29 | 2011-11-22 | Infinite Power Solutions, Inc. | Masking of and material constraint for depositing battery layers on flexible substrates |
| US8197781B2 (en) | 2006-11-07 | 2012-06-12 | Infinite Power Solutions, Inc. | Sputtering target of Li3PO4 and method for producing same |
| US9334557B2 (en) | 2007-12-21 | 2016-05-10 | Sapurast Research Llc | Method for sputter targets for electrolyte films |
| US8268488B2 (en) * | 2007-12-21 | 2012-09-18 | Infinite Power Solutions, Inc. | Thin film electrolyte for thin film batteries |
| JP5705549B2 (ja) | 2008-01-11 | 2015-04-22 | インフィニット パワー ソリューションズ, インコーポレイテッド | 薄膜電池および他のデバイスのための薄膜カプセル化 |
| CN101983469B (zh) | 2008-04-02 | 2014-06-04 | 无穷动力解决方案股份有限公司 | 与能量采集关联的储能装置的无源过电压/欠电压控制和保护 |
| US8187752B2 (en) | 2008-04-16 | 2012-05-29 | Envia Systems, Inc. | High energy lithium ion secondary batteries |
| WO2009131700A2 (en) | 2008-04-25 | 2009-10-29 | Envia Systems, Inc. | High energy lithium ion batteries with particular negative electrode compositions |
| EP2319101B1 (en) * | 2008-08-11 | 2015-11-04 | Sapurast Research LLC | Energy device with integral collector surface for electromagnetic energy harvesting and method thereof |
| JP5650646B2 (ja) | 2008-09-12 | 2015-01-07 | インフィニット パワー ソリューションズ, インコーポレイテッド | 電磁エネルギーを介したデータ通信のための一体型伝導性表面を有するエネルギーデバイスおよび電磁エネルギーを介したデータ通信のための方法 |
| US8916294B2 (en) * | 2008-09-30 | 2014-12-23 | Envia Systems, Inc. | Fluorine doped lithium rich metal oxide positive electrode battery materials with high specific capacity and corresponding batteries |
| KR20110082035A (ko) * | 2008-10-08 | 2011-07-15 | 인피니트 파워 솔루션스, 인크. | 발에 의해 동력 공급되는 신발 삽입형 센서-트랜시버 |
| US8508193B2 (en) | 2008-10-08 | 2013-08-13 | Infinite Power Solutions, Inc. | Environmentally-powered wireless sensor module |
| US9012073B2 (en) * | 2008-11-11 | 2015-04-21 | Envia Systems, Inc. | Composite compositions, negative electrodes with composite compositions and corresponding batteries |
| US8465873B2 (en) | 2008-12-11 | 2013-06-18 | Envia Systems, Inc. | Positive electrode materials for high discharge capacity lithium ion batteries |
| KR101115416B1 (ko) * | 2009-06-08 | 2012-02-15 | 한양대학교 산학협력단 | 리튬 이차 전지용 양극 활물질, 이의 제조 방법 및 이를 포함하는 리튬 이차 전지 |
| US10056644B2 (en) * | 2009-07-24 | 2018-08-21 | Zenlabs Energy, Inc. | Lithium ion batteries with long cycling performance |
| JP6162402B2 (ja) | 2009-08-27 | 2017-07-12 | エンビア・システムズ・インコーポレイテッドEnvia Systems, Inc. | 高い比容量および優れたサイクルを有する積層リチウムリッチ錯体金属酸化物 |
| TWI437753B (zh) * | 2009-08-27 | 2014-05-11 | Envia Systems Inc | 鋰基電池之經金屬氧化物塗佈之正電極材料 |
| EP2474056B1 (en) | 2009-09-01 | 2016-05-04 | Sapurast Research LLC | Printed circuit board with integrated thin film battery |
| WO2011056847A2 (en) * | 2009-11-03 | 2011-05-12 | Envia Systems, Inc. | High capacity anode materials for lithium ion batteries |
| US8993177B2 (en) | 2009-12-04 | 2015-03-31 | Envia Systems, Inc. | Lithium ion battery with high voltage electrolytes and additives |
| US8765306B2 (en) | 2010-03-26 | 2014-07-01 | Envia Systems, Inc. | High voltage battery formation protocols and control of charging and discharging for desirable long term cycling performance |
| US8741484B2 (en) | 2010-04-02 | 2014-06-03 | Envia Systems, Inc. | Doped positive electrode active materials and lithium ion secondary battery constructed therefrom |
| US20110300432A1 (en) | 2010-06-07 | 2011-12-08 | Snyder Shawn W | Rechargeable, High-Density Electrochemical Device |
| US9083062B2 (en) | 2010-08-02 | 2015-07-14 | Envia Systems, Inc. | Battery packs for vehicles and high capacity pouch secondary batteries for incorporation into compact battery packs |
| US8928286B2 (en) | 2010-09-03 | 2015-01-06 | Envia Systems, Inc. | Very long cycling of lithium ion batteries with lithium rich cathode materials |
| US8663849B2 (en) | 2010-09-22 | 2014-03-04 | Envia Systems, Inc. | Metal halide coatings on lithium ion battery positive electrode materials and corresponding batteries |
| US9166222B2 (en) | 2010-11-02 | 2015-10-20 | Envia Systems, Inc. | Lithium ion batteries with supplemental lithium |
| WO2012067675A1 (en) * | 2010-11-17 | 2012-05-24 | Uchicago Argonne, Llc, Operator Of Argonne National Laboratory | Electrode structures and surfaces for li batteries |
| EP2695225B1 (en) * | 2011-04-06 | 2014-12-10 | Umicore | Glass-coated cathode powders for rechargeable batteries |
| US9601228B2 (en) * | 2011-05-16 | 2017-03-21 | Envia Systems, Inc. | Silicon oxide based high capacity anode materials for lithium ion batteries |
| KR101292754B1 (ko) * | 2011-07-07 | 2013-08-02 | 한양대학교 산학협력단 | 리튬 이차 전지용 활물질, 이의 제조 방법 및 이를 포함하는 리튬 이차 전지 |
| US9159990B2 (en) | 2011-08-19 | 2015-10-13 | Envia Systems, Inc. | High capacity lithium ion battery formation protocol and corresponding batteries |
| WO2013033579A1 (en) | 2011-09-02 | 2013-03-07 | E. I. Du Pont De Nemours And Company | Fluorinated electrolyte compositions |
| WO2013033595A1 (en) | 2011-09-02 | 2013-03-07 | E. I. Du Pont De Nemours And Company | Lithium ion battery |
| KR101920485B1 (ko) * | 2011-09-26 | 2018-11-21 | 전자부품연구원 | 리튬 이차전지용 양극 활물질의 전구체, 양극 활물질, 이의 제조 방법 및 이를 포함하는 리튬 이차전지 |
| CN103137960B (zh) * | 2011-11-25 | 2016-01-20 | 清华大学 | 锂离子电池正极材料及其制备方法以及锂离子电池 |
| WO2013090263A1 (en) | 2011-12-12 | 2013-06-20 | Envia Systems, Inc. | Lithium metal oxides with multiple phases and stable high energy electrochemical cycling |
| CN102437323B (zh) * | 2011-12-12 | 2015-03-18 | 江南大学 | 锂离子电池正极材料及其制备方法 |
| US9139441B2 (en) | 2012-01-19 | 2015-09-22 | Envia Systems, Inc. | Porous silicon based anode material formed using metal reduction |
| US9070489B2 (en) | 2012-02-07 | 2015-06-30 | Envia Systems, Inc. | Mixed phase lithium metal oxide compositions with desirable battery performance |
| EP2814778B1 (de) * | 2012-02-15 | 2016-02-03 | Basf Se | Partikel, verfahren zu ihrer herstellung und ihre verwendung |
| US9437865B2 (en) * | 2012-03-27 | 2016-09-06 | Tdk Corporation | Active material for lithium ion secondary battery, and lithium ion secondary battery |
| US10553871B2 (en) | 2012-05-04 | 2020-02-04 | Zenlabs Energy, Inc. | Battery cell engineering and design to reach high energy |
| US9780358B2 (en) | 2012-05-04 | 2017-10-03 | Zenlabs Energy, Inc. | Battery designs with high capacity anode materials and cathode materials |
| US10044066B2 (en) | 2012-06-01 | 2018-08-07 | Solvary SA | Fluorinated electrolyte compositions |
| KR102064194B1 (ko) | 2012-06-01 | 2020-01-09 | 솔베이(소시에떼아노님) | 리튬 이온 배터리 |
| US9692039B2 (en) | 2012-07-24 | 2017-06-27 | Quantumscape Corporation | Nanostructured materials for electrochemical conversion reactions |
| US9552901B2 (en) | 2012-08-17 | 2017-01-24 | Envia Systems, Inc. | Lithium ion batteries with high energy density, excellent cycling capability and low internal impedance |
| KR101835586B1 (ko) * | 2012-08-23 | 2018-03-07 | 삼성에스디아이 주식회사 | 복합양극활물질, 이를 채용한 양극 및 리튬 전지 |
| KR101975394B1 (ko) | 2012-09-12 | 2019-05-07 | 삼성에스디아이 주식회사 | 복합양극활물질, 이를 채용한 양극과 리튬전지 및 그 제조방법 |
| KR20140066052A (ko) * | 2012-11-22 | 2014-05-30 | 삼성정밀화학 주식회사 | 양극 활물질, 이의 제조방법 및 이를 포함하는 리튬 이차 전지 |
| US10115962B2 (en) | 2012-12-20 | 2018-10-30 | Envia Systems, Inc. | High capacity cathode material with stabilizing nanocoatings |
| US9040203B2 (en) * | 2013-01-16 | 2015-05-26 | Samsung Sdi Co., Ltd. | Lithium battery |
| JP6293256B2 (ja) | 2013-03-12 | 2018-03-14 | アップル インコーポレイテッド | 先進のカソード材料を用いた高電圧、高体積エネルギー密度のリチウムイオンバッテリ |
| US9698419B1 (en) | 2013-03-15 | 2017-07-04 | Nano One Materials Corp. | Complexometric precursor formulation methodology for industrial production of fine and ultrafine powders and nanopowders of layered lithium mixed metal oxides for battery applications |
| US9136534B2 (en) | 2013-03-15 | 2015-09-15 | Nano One Materials Corp. | Complexometric precursors formulation methodology for industrial production of high performance fine and ultrafine powders and nanopowders for specialized applications |
| US9159999B2 (en) | 2013-03-15 | 2015-10-13 | Nano One Materials Corp. | Complexometric precursor formulation methodology for industrial production of fine and ultrafine powders and nanopowders for lithium metal oxides for battery applications |
| CA2908044C (en) | 2013-04-04 | 2022-08-23 | E. I. Du Pont De Nemours And Company | Nonaqueous electrolyte compositions |
| US10020491B2 (en) | 2013-04-16 | 2018-07-10 | Zenlabs Energy, Inc. | Silicon-based active materials for lithium ion batteries and synthesis with solution processing |
| US20140328729A1 (en) | 2013-05-06 | 2014-11-06 | Liang-Yuh Chen | Apparatus for Preparing a Material of a Battery Cell |
| US10886526B2 (en) | 2013-06-13 | 2021-01-05 | Zenlabs Energy, Inc. | Silicon-silicon oxide-carbon composites for lithium battery electrodes and methods for forming the composites |
| CN104253273A (zh) * | 2013-06-28 | 2014-12-31 | 江南大学 | 阴、阳离子复合掺杂改性的锂离子电池(4:4:2)型三元正极材料及其制备方法 |
| KR101794097B1 (ko) * | 2013-07-03 | 2017-11-06 | 삼성에스디아이 주식회사 | 리튬 이차 전지용 양극 활물질, 이의 제조 방법, 그리고 이를 포함하는 리튬 이차 전지용 양극 및 리튬 이차 전지 |
| US10411299B2 (en) | 2013-08-02 | 2019-09-10 | Zenlabs Energy, Inc. | Electrolytes for stable cycling of high capacity lithium based batteries |
| US11476494B2 (en) | 2013-08-16 | 2022-10-18 | Zenlabs Energy, Inc. | Lithium ion batteries with high capacity anode active material and good cycling for consumer electronics |
| DE102013218078A1 (de) * | 2013-09-10 | 2015-03-12 | Volkswagen Aktiengesellschaft | Neues Regenerationsverfahren für Lithium-Ionen-Batterien |
| US10069143B2 (en) | 2013-12-23 | 2018-09-04 | Uchicago Argonne, Llc | Cobalt-stabilized lithium metal oxide electrodes for lithium batteries |
| US20150243974A1 (en) * | 2014-02-25 | 2015-08-27 | Quantumscape Corporation | Hybrid electrodes with both intercalation and conversion materials |
| KR20160126036A (ko) * | 2014-02-27 | 2016-11-01 | 바스프 에스이 | 플루오르화 리튬화 혼합 전이금속 산화물의 제조 방법 |
| KR102509895B1 (ko) | 2014-05-23 | 2023-03-15 | 솔베이(소시에떼아노님) | 환형 설페이트 및 리튬 보레이트를 포함하는 비수성 전해질 조성물 |
| US10559850B2 (en) | 2014-05-23 | 2020-02-11 | Solvay Sa | Nonaqueous electrolyte compositions comprising cyclic sulfates |
| WO2016003532A1 (en) * | 2014-06-30 | 2016-01-07 | University Of Southern California | Free-standing active material/carbon nanomaterial network |
| US9716265B2 (en) | 2014-08-01 | 2017-07-25 | Apple Inc. | High-density precursor for manufacture of composite metal oxide cathodes for Li-ion batteries |
| KR20170042324A (ko) | 2014-08-14 | 2017-04-18 | 솔베이(소시에떼아노님) | 술톤 및 플루오린화된 용매를 포함하는 비수성 전해질 조성물 |
| US10326135B2 (en) | 2014-08-15 | 2019-06-18 | Quantumscape Corporation | Doped conversion materials for secondary battery cathodes |
| US10535898B2 (en) | 2014-12-17 | 2020-01-14 | Solvay Sa | Nonaqueous electrolyte compositions comprising lithium malonatoborate and fluorinated solvent |
| US10199684B2 (en) | 2014-12-17 | 2019-02-05 | Solvay Sa | Nonaqueous electrolyte compositions comprising lithium glycolatoborate and fluorinated solvent |
| WO2016115404A1 (en) | 2015-01-15 | 2016-07-21 | Envia Systems, Inc. | Positive electrode active materials with composite coatings for high energy density secondary batteries and corresponding processes |
| KR102570264B1 (ko) * | 2015-05-15 | 2023-08-25 | 삼성에스디아이 주식회사 | 양극 활물질 및 그 제조방법, 상기 양극 활물질을 채용한 양극과 리튬 전지 |
| JP6788661B2 (ja) | 2015-08-04 | 2020-11-25 | ソルヴェイ(ソシエテ アノニム) | リチウムオキサラトホスフェートを含んでなる非水系電解質組成物 |
| US10305103B2 (en) | 2015-08-11 | 2019-05-28 | Uchicago Argonne, Llc | Stabilized electrodes for lithium batteries |
| WO2017058650A1 (en) | 2015-09-30 | 2017-04-06 | Hongli Dai | Cathode-active materials, their precursors, and methods of preparation |
| EP3369125B1 (en) | 2015-10-26 | 2020-04-29 | Solvay Sa | Nonaqueous electrolyte compositions comprising a fluorinated solvent and a 2-furanone |
| US10862106B2 (en) | 2015-10-28 | 2020-12-08 | Samsung Electronics Co., Ltd. | Composite positive electrode active material, positive electrode including the same, and lithium battery including the positive electrode |
| EP3163656B1 (en) * | 2015-10-28 | 2018-12-12 | Samsung Electronics Co., Ltd. | Composite positive electrode active material, positive electrode including the same, and lithium battery including the positive electrode |
| US10987735B2 (en) | 2015-12-16 | 2021-04-27 | 6K Inc. | Spheroidal titanium metallic powders with custom microstructures |
| EP3389862B1 (en) | 2015-12-16 | 2023-12-06 | 6K Inc. | Method of producing spheroidal dehydrogenated titanium alloy particles |
| WO2017112424A1 (en) | 2015-12-22 | 2017-06-29 | E. I. Du Pont De Nemours And Company | Electrolyte compositions comprising metal fluoride particles |
| CN109328409A (zh) | 2016-03-14 | 2019-02-12 | 苹果公司 | 用于锂离子电池的阴极活性材料 |
| PL235260B1 (pl) * | 2016-05-23 | 2020-06-15 | Univ Jagiellonski | Materiały katodowe LKMNO i sposób ich wytwarzania |
| EP3984629A1 (en) * | 2016-06-23 | 2022-04-20 | 6K Inc. | Lithium ion battery materials |
| EP3485527A2 (en) | 2016-07-15 | 2019-05-22 | Solvay SA | Nonaqueous electrolyte compositions |
| US11489198B2 (en) | 2016-08-19 | 2022-11-01 | Solvay Sa | Nonaqueous electrolyte compositions comprising silyl oxalates |
| KR102488908B1 (ko) | 2016-09-14 | 2023-01-17 | 솔베이(소시에떼아노님) | 6원 고리 사이클릭 설페이트를 함유하는 전해질 |
| CN112158891B (zh) | 2016-09-20 | 2023-03-31 | 苹果公司 | 具有改善的颗粒形态的阴极活性材料 |
| KR102223565B1 (ko) | 2016-09-21 | 2021-03-04 | 애플 인크. | 리튬 이온 배터리용 표면 안정화된 캐소드 재료 및 이의 합성 방법 |
| KR20230116968A (ko) * | 2016-09-21 | 2023-08-04 | 바스프 에스이 | 이작용성 포스폰산 실릴에스터를 포함하는 전기화학셀 |
| CN106654251A (zh) * | 2016-11-30 | 2017-05-10 | 浙江天能能源科技股份有限公司 | 一种改性富锂锰基正极材料及其制备方法 |
| CN110495025B (zh) * | 2017-01-18 | 2023-09-05 | 纳诺万材料公司 | 用于锂离子电池阴极材料前体的一锅合成法 |
| US10741839B2 (en) | 2017-03-02 | 2020-08-11 | Uchicago Argonne, Llc | Surface treatment for lithium battery electrode materials |
| US10705129B2 (en) * | 2017-09-13 | 2020-07-07 | Toshiba Memory Corporation | Techniques for testing PLP capacitors |
| US11623875B2 (en) * | 2017-10-03 | 2023-04-11 | The Government Of The United States, As Represented By The Secretary Of The Army | Stabilized lithium, manganese AB2O4 spinel for rechargeable lithium electrochemical systems through A and B site doping, method of preparing the same, and Li electrochemical cell containing the same |
| JP6852653B2 (ja) * | 2017-11-07 | 2021-03-31 | トヨタ自動車株式会社 | 正極活物質およびフッ化物イオン電池 |
| US11094925B2 (en) | 2017-12-22 | 2021-08-17 | Zenlabs Energy, Inc. | Electrodes with silicon oxide active materials for lithium ion cells achieving high capacity, high energy density and long cycle life performance |
| KR20200105482A (ko) | 2018-01-12 | 2020-09-07 | 솔베이(소시에떼아노님) | 리튬 비스(플루오로설포닐)이미드를 포함하는 비수성 전해질 조성물 |
| WO2019246257A1 (en) | 2018-06-19 | 2019-12-26 | Amastan Technologies Inc. | Process for producing spheroidized powder from feedstock materials |
| WO2020025502A1 (en) | 2018-07-31 | 2020-02-06 | Solvay Sa | New components for electrolyte compositions |
| EP3605699A1 (en) | 2018-07-31 | 2020-02-05 | Solvay Sa | New components for electrolyte compositions |
| EP3605698A1 (en) | 2018-07-31 | 2020-02-05 | Solvay Sa | New components for electrolyte compositions |
| EP3605700A1 (en) | 2018-07-31 | 2020-02-05 | Solvay Sa | New components for electrolyte compositions |
| WO2020025501A1 (en) | 2018-07-31 | 2020-02-06 | Solvay Sa | New components for electrolyte compositions |
| WO2020025499A1 (en) | 2018-07-31 | 2020-02-06 | Solvay Sa | New components for electrolyte compositions |
| EP3604276A1 (en) | 2018-07-31 | 2020-02-05 | Solvay Sa | New components for electrolyte compositions |
| US11695108B2 (en) | 2018-08-02 | 2023-07-04 | Apple Inc. | Oxide mixture and complex oxide coatings for cathode materials |
| US11749799B2 (en) | 2018-08-17 | 2023-09-05 | Apple Inc. | Coatings for cathode active materials |
| US11289745B2 (en) | 2019-01-09 | 2022-03-29 | GM Global Technology Operations LLC | Elimination of gaseous reactants in lithium ion batteries |
| CN114007782A (zh) | 2019-04-30 | 2022-02-01 | 6K有限公司 | 机械合金化的粉末原料 |
| SG11202111578UA (en) | 2019-04-30 | 2021-11-29 | 6K Inc | Lithium lanthanum zirconium oxide (llzo) powder |
| CN110165167A (zh) * | 2019-05-14 | 2019-08-23 | 上海汉行科技有限公司 | 一种表面改性亚铁氰基材料及其制备方法 |
| US11376559B2 (en) | 2019-06-28 | 2022-07-05 | eJoule, Inc. | Processing system and method for producing a particulate material |
| US11121354B2 (en) | 2019-06-28 | 2021-09-14 | eJoule, Inc. | System with power jet modules and method thereof |
| US11673112B2 (en) | 2020-06-28 | 2023-06-13 | eJoule, Inc. | System and process with assisted gas flow inside a reaction chamber |
| US11757096B2 (en) | 2019-08-21 | 2023-09-12 | Apple Inc. | Aluminum-doped lithium cobalt manganese oxide batteries |
| CN114641462A (zh) | 2019-11-18 | 2022-06-17 | 6K有限公司 | 用于球形粉末的独特原料及制造方法 |
| US11590568B2 (en) | 2019-12-19 | 2023-02-28 | 6K Inc. | Process for producing spheroidized powder from feedstock materials |
| CN110970668B (zh) * | 2019-12-23 | 2021-10-08 | 中国科学院过程工程研究所 | 一种全固态电池复合结构、其制备方法和用途 |
| WO2021263273A1 (en) | 2020-06-25 | 2021-12-30 | 6K Inc. | Microcomposite alloy structure |
| KR20230073182A (ko) | 2020-09-24 | 2023-05-25 | 6케이 인크. | 플라즈마를 개시하기 위한 시스템, 디바이스 및 방법 |
| JP2023548325A (ja) | 2020-10-30 | 2023-11-16 | シックスケー インコーポレイテッド | 球状化金属粉末の合成のためのシステムおよび方法 |
| CN113044890A (zh) * | 2021-02-02 | 2021-06-29 | 江汉大学 | 一种正极材料及其制备方法和锂离子电池 |
| WO2023137022A1 (en) * | 2022-01-12 | 2023-07-20 | Tesla, Inc. | Doped cathode active materials and methods thereof |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2007503102A (ja) * | 2003-05-28 | 2007-02-15 | ナショナル・リサーチ・カウンシル・オブ・カナダ | リチウムセルおよびバッテリー用の酸化リチウム電極 |
| WO2008081839A1 (ja) * | 2006-12-27 | 2008-07-10 | Sanyo Electric Co., Ltd. | 非水電解質二次電池およびその製造方法 |
| JP2008536285A (ja) * | 2005-04-15 | 2008-09-04 | エナーセラミック インコーポレイテッド | フッ素化合物でコーティングされたリチウム二次電池用正極活物質及びその製造方法 |
| JP2010103086A (ja) * | 2008-09-26 | 2010-05-06 | Nissan Motor Co Ltd | リチウムイオン電池用正極 |
Family Cites Families (110)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2699176B2 (ja) * | 1988-05-20 | 1998-01-19 | 日立マクセル 株式会社 | リチウム二次電池 |
| US4957543A (en) | 1989-06-16 | 1990-09-18 | Inco Limited | Method of forming nickel foam |
| CA2068015A1 (en) | 1991-06-17 | 1992-12-18 | Michael M. Thackeray | Electrode material |
| US5393622A (en) * | 1992-02-07 | 1995-02-28 | Matsushita Electric Industrial Co., Ltd. | Process for production of positive electrode active material |
| US5374491A (en) | 1993-01-27 | 1994-12-20 | Eltech Systems Corporation | High density, high capacity battery electrode |
| JP3276451B2 (ja) | 1993-05-20 | 2002-04-22 | 新神戸電機株式会社 | リチウム電池 |
| JP3112138B2 (ja) | 1993-07-20 | 2000-11-27 | セントラル硝子株式会社 | 含リチウム金属ハロゲン化酸化物およびその製造法 |
| JP3506397B2 (ja) | 1995-03-28 | 2004-03-15 | 三井金属鉱業株式会社 | リチウム二次電池用正極材料およびその製造方法、並びにこれを用いたリチウム二次電池 |
| US5738907A (en) | 1995-08-04 | 1998-04-14 | Eltech Systems Corporation | Conductive metal porous sheet production |
| US5674645A (en) | 1996-09-06 | 1997-10-07 | Bell Communications Research, Inc. | Lithium manganese oxy-fluorides for li-ion rechargeable battery electrodes |
| US6087042A (en) | 1996-10-18 | 2000-07-11 | Kabushiki Kaisha Toyota Chuo Kenkyusho | Positive electrode material for secondary lithium battery |
| US6183718B1 (en) | 1996-12-09 | 2001-02-06 | Valence Technology, Inc. | Method of making stabilized electrochemical cell active material of lithium manganese oxide |
| US6037095A (en) | 1997-03-28 | 2000-03-14 | Fuji Photo Film Co., Ltd. | Non-aqueous lithium ion secondary battery |
| US6749648B1 (en) | 2000-06-19 | 2004-06-15 | Nanagram Corporation | Lithium metal oxides |
| US6337156B1 (en) | 1997-12-23 | 2002-01-08 | Sri International | Ion battery using high aspect ratio electrodes |
| CN1146062C (zh) | 1998-02-10 | 2004-04-14 | 三星电管株式会社 | 正极活性材料及其制造方法以及使用该材料的锂二次电池 |
| WO1999060638A2 (en) | 1998-05-15 | 1999-11-25 | Duracell Inc. | Battery cathode materials |
| ATE288819T1 (de) | 1998-06-29 | 2005-02-15 | Stork Screens Bv | Produktion eines porösen schaumproduktes für batterieelektroden |
| US6528208B1 (en) | 1998-07-09 | 2003-03-04 | The University Of Chicago | Anodes for rechargeable lithium batteries |
| WO2000004992A1 (en) | 1998-07-20 | 2000-02-03 | Corning Incorporated | Method of making activated carbon derived from pitches |
| US6428766B1 (en) | 1998-10-27 | 2002-08-06 | Toda Kogyo Corporation | Manganese oxide, lithium manganese complex oxide and cobalt-coated lithium manganese complex oxide, and preparation processes thereof |
| CA2350710C (en) | 1998-11-13 | 2005-09-13 | Fmc Corporation | Layered lithium metal oxides free of localized cubic spinel-like structural phases and methods of making same |
| US6168887B1 (en) | 1999-01-15 | 2001-01-02 | Chemetals Technology Corporation | Layered lithium manganese oxide bronze and electrodes thereof |
| US6322744B1 (en) | 1999-02-17 | 2001-11-27 | Valence Technology, Inc. | Lithium manganese oxide-based active material |
| US6489060B1 (en) | 1999-05-26 | 2002-12-03 | E-One Moli Energy (Canada) Limited | Rechargeable spinel lithium batteries with greatly improved elevated temperature cycle life |
| US6248477B1 (en) | 1999-09-29 | 2001-06-19 | Kerr-Mcgee Chemical Llc | Cathode intercalation compositions, production methods and rechargeable lithium batteries containing the same |
| JP2003514353A (ja) | 1999-11-08 | 2003-04-15 | ネオフォトニクス・コーポレイション | 特定サイズの粒子を含む電極 |
| JP4383681B2 (ja) * | 2000-02-28 | 2009-12-16 | 三星エスディアイ株式会社 | リチウム二次電池用正極活物質及びその製造方法 |
| US6737195B2 (en) | 2000-03-13 | 2004-05-18 | Samsung Sdi Co., Ltd. | Positive active material for rechargeable lithium battery and method of preparing same |
| US6420071B1 (en) | 2000-03-21 | 2002-07-16 | Midwest Research Institute | Method for improving the durability of ion insertion materials |
| KR20030007651A (ko) | 2000-05-24 | 2003-01-23 | 텔코디아 테크놀로지스, 인코포레이티드 | 이중 양이온 재충전가능 전기화학 전지 |
| US6677082B2 (en) | 2000-06-22 | 2004-01-13 | The University Of Chicago | Lithium metal oxide electrodes for lithium cells and batteries |
| US7468223B2 (en) | 2000-06-22 | 2008-12-23 | Uchicago Argonne, Llc | Lithium metal oxide electrodes for lithium cells and batteries |
| US6680143B2 (en) | 2000-06-22 | 2004-01-20 | The University Of Chicago | Lithium metal oxide electrodes for lithium cells and batteries |
| US6660432B2 (en) | 2000-09-14 | 2003-12-09 | Ilion Technology Corporation | Lithiated oxide materials and methods of manufacture |
| US6730429B2 (en) | 2000-11-10 | 2004-05-04 | The University Of Chicago | Intermetallic negative electrodes for non-aqueous lithium cells and batteries |
| WO2002054525A1 (fr) | 2000-12-28 | 2002-07-11 | Matsushita Electric Industrial Co., Ltd. | Batterie a electrolyte non aqueux et son procede de production |
| KR100470287B1 (ko) | 2000-12-28 | 2005-02-05 | 마쯔시다덴기산교 가부시키가이샤 | 비수전해질(非水電解質) 이차전지 |
| CA2369030C (en) | 2001-01-23 | 2006-02-21 | Kabushiki Kaisha Toshiba | Positive electrode active material and lithium ion secondary battery |
| US6855460B2 (en) | 2001-02-08 | 2005-02-15 | The University Of Chicago | Negative electrodes for lithium cells and batteries |
| JP3615491B2 (ja) | 2001-03-05 | 2005-02-02 | 松下電器産業株式会社 | 非水電解質二次電池およびその製造法 |
| US6964828B2 (en) | 2001-04-27 | 2005-11-15 | 3M Innovative Properties Company | Cathode compositions for lithium-ion batteries |
| US7135251B2 (en) | 2001-06-14 | 2006-11-14 | Samsung Sdi Co., Ltd. | Active material for battery and method of preparing the same |
| WO2003015198A2 (en) | 2001-08-07 | 2003-02-20 | 3M Innovative Properties Company | Cathode compositions for lithium ion batteries |
| DE10142622A1 (de) | 2001-08-31 | 2003-03-20 | Creavis Tech & Innovation Gmbh | Elektrischer Separator, Verfahren zu dessen Herstellung und Verwendung |
| KR100413816B1 (ko) | 2001-10-16 | 2004-01-03 | 학교법인 한양학원 | 리튬 2차 전지용 전극 활물질, 그의 제조방법, 및 그를포함하는 리튬 2차 전지 |
| KR100399642B1 (ko) | 2001-10-24 | 2003-09-29 | 삼성에스디아이 주식회사 | 리튬 이차 전지용 양극 활물질 및 그 제조방법 |
| US7393476B2 (en) | 2001-11-22 | 2008-07-01 | Gs Yuasa Corporation | Positive electrode active material for lithium secondary cell and lithium secondary cell |
| US20030108790A1 (en) | 2001-12-05 | 2003-06-12 | Arumugam Manthiram | Surface/chemically modified oxide cathodes for lithium-ion batteries |
| TW563266B (en) | 2002-10-18 | 2003-11-21 | Ind Tech Res Inst | Modified lithium cobalt oxide for lithium ion battery as cathode, preparation thereof, and lithium ion battery |
| US7435402B2 (en) | 2002-11-01 | 2008-10-14 | U Chicago Argonne Llc | Method and apparatus for preparation of spherical metal carbonates and lithium metal oxides for lithium rechargeable batteries |
| US7205072B2 (en) * | 2002-11-01 | 2007-04-17 | The University Of Chicago | Layered cathode materials for lithium ion rechargeable batteries |
| JP4030443B2 (ja) | 2003-02-27 | 2008-01-09 | 三洋電機株式会社 | 非水電解質二次電池 |
| US7556655B2 (en) | 2003-03-14 | 2009-07-07 | 3M Innovative Properties Company | Method of producing lithium ion cathode materials |
| US7732096B2 (en) | 2003-04-24 | 2010-06-08 | Uchicago Argonne, Llc | Lithium metal oxide electrodes for lithium batteries |
| KR100739921B1 (ko) | 2003-06-03 | 2007-07-16 | 가부시키가이샤 유아사코오포레이션 | 비수 전해질 전지 |
| FR2860922B1 (fr) | 2003-10-10 | 2009-07-31 | Cit Alcatel | Matiere electrochimiquement active pour electrode positive de generateur electrochimique rechargeable au lithium |
| KR100548988B1 (ko) | 2003-11-26 | 2006-02-02 | 학교법인 한양학원 | 리튬이차전지용 양극활물질 제조방법, 그 방법에 사용되는반응기 및 그 방법으로 제조되는 리튬이차전지용 양극활물질 |
| JP4100341B2 (ja) | 2003-12-26 | 2008-06-11 | 新神戸電機株式会社 | リチウム二次電池用正極材料及びそれを用いたリチウム二次電池 |
| KR20060042201A (ko) | 2004-02-27 | 2006-05-12 | 산요덴키가부시키가이샤 | 리튬 2차 전지 |
| KR100578877B1 (ko) | 2004-03-12 | 2006-05-11 | 삼성에스디아이 주식회사 | 리튬 이차 전지 |
| EP1742281B1 (en) | 2004-04-27 | 2011-09-07 | Mitsubishi Chemical Corporation | Layered lithium nickel manganese cobalt composite oxide powder for material of positive electrode of lithium secondary battery, process for producing the same, positive electrode of lithium secondary battery therefrom, and lithium secondary battery |
| JP4841116B2 (ja) | 2004-05-28 | 2011-12-21 | 三洋電機株式会社 | 非水電解質二次電池 |
| US9012096B2 (en) | 2004-05-28 | 2015-04-21 | Uchicago Argonne, Llc | Long life lithium batteries with stabilized electrodes |
| TWI290781B (en) | 2004-09-02 | 2007-12-01 | Lg Chemical Ltd | Electrode active material with multi-element based oxide layers and preparation method thereof |
| ES2620809T3 (es) | 2004-09-03 | 2017-06-29 | Uchicago Argonne, Llc | Electrodos compuestos de óxido de manganeso par baterías de litio |
| US7635536B2 (en) | 2004-09-03 | 2009-12-22 | Uchicago Argonne, Llc | Manganese oxide composite electrodes for lithium batteries |
| US7364793B2 (en) | 2004-09-24 | 2008-04-29 | Lg Chem, Ltd. | Powdered lithium transition metal oxide having doped interface layer and outer layer and method for preparation of the same |
| JP4051686B2 (ja) | 2004-09-30 | 2008-02-27 | ソニー株式会社 | 負極活物質およびそれを用いた電池 |
| JP4752244B2 (ja) | 2004-11-09 | 2011-08-17 | 三菱化学株式会社 | リチウム二次電池正極材料用層状リチウムニッケルマンガン系複合酸化物粉体及びそれを用いたリチウム二次電池正極、並びにリチウム二次電池 |
| KR100796953B1 (ko) | 2005-01-20 | 2008-01-22 | 주식회사 에코프로 | 2차 전지용 양극 활물질, 그 제조방법 및 이를 포함하는리튬이차전지 |
| KR100674287B1 (ko) | 2005-04-01 | 2007-01-24 | 에스케이 주식회사 | 핵·껍질 다층구조를 가지는 리튬이차전지용 양극 활물질,그 제조 방법 및 이를 사용한 리튬이차전지 |
| EP1880435A4 (en) * | 2005-04-15 | 2009-07-15 | Enerceramic Inc | KATHODEN ACTIVE MATERIAL COATED WITH A FLUORIC COMPOUND FOR LITHIUM SECONDARY BATTERIES AND METHOD OF MANUFACTURING THEREOF |
| CN101176226B (zh) | 2005-05-17 | 2010-07-21 | Agc清美化学股份有限公司 | 锂二次电池正极用的含锂复合氧化物的制造方法 |
| US8445129B2 (en) | 2005-05-27 | 2013-05-21 | Sony Corporation | Cathode active material, method of manufacturing it, cathode, and battery |
| JP5099398B2 (ja) | 2005-06-07 | 2012-12-19 | ソニー株式会社 | 二次電池用正極活物質、二次電池用正極および二次電池 |
| KR100701532B1 (ko) | 2005-06-21 | 2007-03-29 | 대정화금주식회사 | 불소화합물이 첨가된 리튬이차전지 양극 활물질 및 그제조방법 |
| FR2890241B1 (fr) | 2005-08-25 | 2009-05-22 | Commissariat Energie Atomique | Materiau d'electrode positive haute tension de structure spinelle a base de nickel et de manganese pour accumulateurs au lithium |
| JP4625744B2 (ja) | 2005-09-29 | 2011-02-02 | 株式会社東芝 | 非水電解質電池および電池パック |
| US7906238B2 (en) | 2005-12-23 | 2011-03-15 | 3M Innovative Properties Company | Silicon-containing alloys useful as electrodes for lithium-ion batteries |
| JP5315591B2 (ja) | 2006-02-20 | 2013-10-16 | ソニー株式会社 | 正極活物質および電池 |
| US7906239B2 (en) | 2006-03-06 | 2011-03-15 | Sony Corporation | Cathode active material, method for producing the same, and nonaqueous electrolyte secondary battery |
| JP5023541B2 (ja) | 2006-04-14 | 2012-09-12 | 日産自動車株式会社 | 二次電池の製造方法 |
| EP2067198A2 (en) | 2006-09-25 | 2009-06-10 | Board of Regents, The University of Texas System | Cation-substituted spinel oxide and oxyfluoride cathodes for lithium ion batteries |
| US7935270B2 (en) | 2006-10-04 | 2011-05-03 | Samsung Sdi Co., Ltd | Cathode active material and lithium battery using the same |
| US7927506B2 (en) | 2006-10-04 | 2011-04-19 | Samsung Sdi Co., Ltd. | Cathode active material and lithium battery using the same |
| JP4936440B2 (ja) | 2006-10-26 | 2012-05-23 | 日立マクセルエナジー株式会社 | 非水二次電池 |
| KR100814826B1 (ko) | 2006-11-20 | 2008-03-20 | 삼성에스디아이 주식회사 | 리튬 이차 전지 |
| US10665892B2 (en) | 2007-01-10 | 2020-05-26 | Eocell Limited | Lithium batteries with nano-composite positive electrode material |
| EP2071650A4 (en) | 2007-03-30 | 2013-04-03 | Panasonic Corp | ACTIVE MATERIAL FOR A NON-AQUEOUS ELECTROLYTE SECONDARY BATTERY AND METHOD FOR THE PRODUCTION THEREOF |
| US20080241693A1 (en) | 2007-03-30 | 2008-10-02 | Minoru Fukuchi | Lithium transition metal complex oxide for lithium ion secondary battery cathode active material and method for producing the same, lithium ion secondary battery cathode active material, and lithium ion secondary battery |
| KR101430616B1 (ko) | 2007-12-18 | 2014-08-14 | 삼성에스디아이 주식회사 | 캐소드 및 이를 채용한 리튬 전지 |
| US8187752B2 (en) | 2008-04-16 | 2012-05-29 | Envia Systems, Inc. | High energy lithium ion secondary batteries |
| EP2264814A4 (en) | 2008-04-17 | 2016-08-17 | Jx Nippon Mining & Metals Corp | POSITIVE ELECTRODE ACTIVE MATERIAL FOR LITHIUM-ION BATTERY, POSITIVE ELECTRODE FOR RECHARGEABLE BATTERY, AND LITHIUM-ION BATTERY |
| WO2009131700A2 (en) | 2008-04-25 | 2009-10-29 | Envia Systems, Inc. | High energy lithium ion batteries with particular negative electrode compositions |
| US8277683B2 (en) | 2008-05-30 | 2012-10-02 | Uchicago Argonne, Llc | Nano-sized structured layered positive electrode materials to enable high energy density and high rate capability lithium batteries |
| US8916294B2 (en) | 2008-09-30 | 2014-12-23 | Envia Systems, Inc. | Fluorine doped lithium rich metal oxide positive electrode battery materials with high specific capacity and corresponding batteries |
| US9012073B2 (en) | 2008-11-11 | 2015-04-21 | Envia Systems, Inc. | Composite compositions, negative electrodes with composite compositions and corresponding batteries |
| US8465873B2 (en) | 2008-12-11 | 2013-06-18 | Envia Systems, Inc. | Positive electrode materials for high discharge capacity lithium ion batteries |
| US10056644B2 (en) | 2009-07-24 | 2018-08-21 | Zenlabs Energy, Inc. | Lithium ion batteries with long cycling performance |
| JP6162402B2 (ja) | 2009-08-27 | 2017-07-12 | エンビア・システムズ・インコーポレイテッドEnvia Systems, Inc. | 高い比容量および優れたサイクルを有する積層リチウムリッチ錯体金属酸化物 |
| TWI437753B (zh) | 2009-08-27 | 2014-05-11 | Envia Systems Inc | 鋰基電池之經金屬氧化物塗佈之正電極材料 |
| WO2011056847A2 (en) | 2009-11-03 | 2011-05-12 | Envia Systems, Inc. | High capacity anode materials for lithium ion batteries |
| US9843041B2 (en) | 2009-11-11 | 2017-12-12 | Zenlabs Energy, Inc. | Coated positive electrode materials for lithium ion batteries |
| US8993177B2 (en) | 2009-12-04 | 2015-03-31 | Envia Systems, Inc. | Lithium ion battery with high voltage electrolytes and additives |
| US8765306B2 (en) | 2010-03-26 | 2014-07-01 | Envia Systems, Inc. | High voltage battery formation protocols and control of charging and discharging for desirable long term cycling performance |
| US8741484B2 (en) | 2010-04-02 | 2014-06-03 | Envia Systems, Inc. | Doped positive electrode active materials and lithium ion secondary battery constructed therefrom |
| US9083062B2 (en) | 2010-08-02 | 2015-07-14 | Envia Systems, Inc. | Battery packs for vehicles and high capacity pouch secondary batteries for incorporation into compact battery packs |
| US8928286B2 (en) | 2010-09-03 | 2015-01-06 | Envia Systems, Inc. | Very long cycling of lithium ion batteries with lithium rich cathode materials |
| US8663849B2 (en) | 2010-09-22 | 2014-03-04 | Envia Systems, Inc. | Metal halide coatings on lithium ion battery positive electrode materials and corresponding batteries |
-
2008
- 2008-10-07 US US12/246,814 patent/US8389160B2/en active Active
-
2009
- 2009-10-05 WO PCT/US2009/059519 patent/WO2010042434A2/en active Application Filing
- 2009-10-05 JP JP2011531092A patent/JP2012505520A/ja active Pending
- 2009-10-05 CN CN2009801398691A patent/CN102177605A/zh active Pending
- 2009-10-05 KR KR1020117009503A patent/KR20110084200A/ko not_active Application Discontinuation
- 2009-10-05 EP EP09819712A patent/EP2351122A4/en not_active Withdrawn
- 2009-10-07 TW TW098134024A patent/TWI384669B/zh not_active IP Right Cessation
-
2013
- 2013-01-31 US US13/755,263 patent/US20130142944A1/en not_active Abandoned
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2007503102A (ja) * | 2003-05-28 | 2007-02-15 | ナショナル・リサーチ・カウンシル・オブ・カナダ | リチウムセルおよびバッテリー用の酸化リチウム電極 |
| JP2008536285A (ja) * | 2005-04-15 | 2008-09-04 | エナーセラミック インコーポレイテッド | フッ素化合物でコーティングされたリチウム二次電池用正極活物質及びその製造方法 |
| WO2008081839A1 (ja) * | 2006-12-27 | 2008-07-10 | Sanyo Electric Co., Ltd. | 非水電解質二次電池およびその製造方法 |
| JP2010103086A (ja) * | 2008-09-26 | 2010-05-06 | Nissan Motor Co Ltd | リチウムイオン電池用正極 |
Non-Patent Citations (4)
| Title |
|---|
| JPN6013054196; Journal of Materials chemistry 17, 2007, 3112-3125 * |
| JPN6013054198; Journal of the electrochemical society 152(9), 2005, A1879-A1889 * |
| JPN6013054201; Journal of Power Sources 112, 2002, 634-638 * |
| JPN6013054204; Journal of the electrochemical society 154(3), 2007, A168-A172 * |
Cited By (26)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2013511129A (ja) * | 2009-11-11 | 2013-03-28 | エンビア・システムズ・インコーポレイテッド | リチウムイオン電池用のコーティングを施した正極材料 |
| JP2014531718A (ja) * | 2011-09-26 | 2014-11-27 | コリア エレクトロニクス テクノロジ インスティチュート | リチウム二次電池用正極活物質、その製造方法及びそれを含むリチウム二次電池 |
| JP2013206558A (ja) * | 2012-03-27 | 2013-10-07 | Tdk Corp | 活物質及びリチウムイオン二次電池 |
| JP2013206685A (ja) * | 2012-03-28 | 2013-10-07 | National Institute Of Advanced Industrial & Technology | 高結晶性のaLi2MnO3−(1−a)Li(Nix,Coy,Mnz)O2系ナノ構造電極材料、および、エレクトロスピニング法によるその製造方法 |
| WO2014076946A1 (ja) * | 2012-11-13 | 2014-05-22 | Jx日鉱日石エネルギー株式会社 | 正極材、正極材の製造方法、および非水電解質電池 |
| JP2014116308A (ja) * | 2012-12-06 | 2014-06-26 | Samsung Fine Chemicals Co Ltd | 正極活物質、その製造方法およびそれを含むリチウム二次電池 |
| US9570739B2 (en) | 2013-02-28 | 2017-02-14 | Samsung Sdi Co., Ltd. | Composite positive active material, method of preparing the same, and positive electrode and lithium battery containing the material |
| KR101771086B1 (ko) * | 2013-02-28 | 2017-09-05 | 삼성에스디아이 주식회사 | 복합 양극 활물질 및 그 제조방법, 상기 복합 양극 활물질을 채용한 양극과 리튬 전지 |
| JP2016516267A (ja) * | 2013-03-15 | 2016-06-02 | ナノ ワン マテリアルズ コーポレーション | 電池用途の層状リチウム混合酸化物の微細粉体及び超微細粉体、並びにナノ粉体の工業生産に関する錯形成前駆体配合方法論 |
| JP2016524576A (ja) * | 2013-03-15 | 2016-08-18 | ナノ ワン マテリアルズ コーポレーション | 電池用途のリチウム金属酸化物の微細粉体及び超微細粉体、並びにナノ粉体の工業生産に関する錯形成前駆体配合方法論 |
| JP2019023159A (ja) * | 2013-03-15 | 2019-02-14 | ナノ ワン マテリアルズ コーポレーション | 電池用途のリチウム金属酸化物の微細粉体及び超微細粉体、並びにナノ粉体の工業生産に関する錯形成前駆体配合方法論 |
| US10374232B2 (en) | 2013-03-15 | 2019-08-06 | Nano One Materials Corp. | Complexometric precursor formulation methodology for industrial production of fine and ultrafine powders and nanopowders for lithium metal oxides for battery applications |
| JP2018081925A (ja) * | 2013-03-15 | 2018-05-24 | ナノ ワン マテリアルズ コーポレーション | 電池用途の層状リチウム混合酸化物の微細粉体及び超微細粉体、並びにナノ粉体の工業生産に関する錯形成前駆体配合方法論 |
| JP2015533257A (ja) * | 2013-06-18 | 2015-11-19 | エルジー・ケム・リミテッド | リチウム二次電池用正極活物質及びその製造方法 |
| US9685657B2 (en) | 2013-08-08 | 2017-06-20 | Samsung Sdi Co., Ltd. | Composite precursor, composite prepared therefrom, a method of preparing a composite precursor and a composite, positive electrode for lithium secondary battery including the same, and lithium secondary battery employing the same |
| KR101785264B1 (ko) * | 2013-08-08 | 2017-10-16 | 삼성에스디아이 주식회사 | 복합체 전구체, 이로부터 형성된 복합체, 그 제조방법, 이를 포함하는 리튬 이차 전지용 양극 및 이를 구비한 리튬 이차 전지 |
| JP2015213054A (ja) * | 2014-04-15 | 2015-11-26 | ワイルドキャット・ディスカバリー・テクノロジーズ・インコーポレイテッドWildcat Discovery Technologies, Inc. | 金属抽出によって作製した材料 |
| JP2016058316A (ja) * | 2014-09-11 | 2016-04-21 | トヨタ自動車株式会社 | リチウムイオン二次電池及びその製造方法 |
| JP2017037713A (ja) * | 2015-08-06 | 2017-02-16 | トヨタ自動車株式会社 | 非水電解質二次電池用正極活物質の製造方法 |
| JP2018529197A (ja) * | 2015-09-16 | 2018-10-04 | ローベルト ボツシユ ゲゼルシヤフト ミツト ベシユレンクテル ハフツングRobert Bosch Gmbh | バッテリーセルの正極用の活物質、正極、およびバッテリーセル |
| JP2018529198A (ja) * | 2015-09-16 | 2018-10-04 | ローベルト ボツシユ ゲゼルシヤフト ミツト ベシユレンクテル ハフツングRobert Bosch Gmbh | バッテリーセルの正極用の活物質、正極、およびバッテリーセル |
| US10763502B2 (en) | 2015-09-16 | 2020-09-01 | Robert Bosch Gmbh | Active material for a positive electrode of a battery cell, positive electrode, and battery cell |
| US10790502B2 (en) | 2015-09-16 | 2020-09-29 | Robert Bosch Gmbh | Active material for a positive electrode of a battery cell, positive electrode, and battery cell |
| WO2017094416A1 (ja) * | 2015-12-02 | 2017-06-08 | 日本電気株式会社 | リチウム二次電池用正極活物質、リチウム二次電池用正極及びリチウム二次電池、並びにそれらの製造方法 |
| US10833369B2 (en) | 2015-12-02 | 2020-11-10 | Nec Corporation | Positive electrode active substance for lithium secondary battery, positive electrode for lithium secondary battery and lithium secondary battery, and methods for producing these |
| JP2020513653A (ja) * | 2016-11-24 | 2020-05-14 | ローベルト ボツシユ ゲゼルシヤフト ミツト ベシユレンクテル ハフツングRobert Bosch Gmbh | 電池セルの正極用の活物質、正極および電池セル |
Also Published As
| Publication number | Publication date |
|---|---|
| EP2351122A2 (en) | 2011-08-03 |
| WO2010042434A2 (en) | 2010-04-15 |
| US20130142944A1 (en) | 2013-06-06 |
| CN102177605A (zh) | 2011-09-07 |
| US20100086853A1 (en) | 2010-04-08 |
| WO2010042434A3 (en) | 2010-07-08 |
| KR20110084200A (ko) | 2011-07-21 |
| US8389160B2 (en) | 2013-03-05 |
| TWI384669B (zh) | 2013-02-01 |
| TW201023416A (en) | 2010-06-16 |
| EP2351122A4 (en) | 2012-05-09 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US8389160B2 (en) | Positive electrode materials for lithium ion batteries having a high specific discharge capacity and processes for the synthesis of these materials | |
| US9960424B2 (en) | Positive electrode materials for high discharge capacity lithium ion batteries | |
| US20180062170A1 (en) | Coated positive electrode materials for lithium ion batteries | |
| EP2619828B1 (en) | Metal halide coatings on lithium ion battery positive electrode materials and corresponding batteries | |
| US8741485B2 (en) | Layer-layer lithium rich complex metal oxides with high specific capacity and excellent cycling | |
| US8916294B2 (en) | Fluorine doped lithium rich metal oxide positive electrode battery materials with high specific capacity and corresponding batteries | |
| US8535832B2 (en) | Metal oxide coated positive electrode materials for lithium-based batteries | |
| JP2013524440A (ja) | ドープされた正極活物質、およびそれより構成されるリチウムイオン二次電池 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20121004 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20121004 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20131008 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20140401 |