RU2745977C2 - Способ получения циклоалкилкарбоксамидо-индольных соединений - Google Patents
Способ получения циклоалкилкарбоксамидо-индольных соединений Download PDFInfo
- Publication number
- RU2745977C2 RU2745977C2 RU2015145784A RU2015145784A RU2745977C2 RU 2745977 C2 RU2745977 C2 RU 2745977C2 RU 2015145784 A RU2015145784 A RU 2015145784A RU 2015145784 A RU2015145784 A RU 2015145784A RU 2745977 C2 RU2745977 C2 RU 2745977C2
- Authority
- RU
- Russia
- Prior art keywords
- compound
- another embodiment
- cftr
- vol
- present
- Prior art date
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D317/00—Heterocyclic compounds containing five-membered rings having two oxygen atoms as the only ring hetero atoms
- C07D317/08—Heterocyclic compounds containing five-membered rings having two oxygen atoms as the only ring hetero atoms having the hetero atoms in positions 1 and 3
- C07D317/44—Heterocyclic compounds containing five-membered rings having two oxygen atoms as the only ring hetero atoms having the hetero atoms in positions 1 and 3 ortho- or peri-condensed with carbocyclic rings or ring systems
- C07D317/46—Heterocyclic compounds containing five-membered rings having two oxygen atoms as the only ring hetero atoms having the hetero atoms in positions 1 and 3 ortho- or peri-condensed with carbocyclic rings or ring systems condensed with one six-membered ring
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/40—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil
- A61K31/403—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil condensed with carbocyclic rings, e.g. carbazole
- A61K31/404—Indoles, e.g. pindolol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/40—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil
- A61K31/403—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil condensed with carbocyclic rings, e.g. carbazole
- A61K31/404—Indoles, e.g. pindolol
- A61K31/4045—Indole-alkylamines; Amides thereof, e.g. serotonin, melatonin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/40—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil
- A61K31/403—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil condensed with carbocyclic rings, e.g. carbazole
- A61K31/404—Indoles, e.g. pindolol
- A61K31/405—Indole-alkanecarboxylic acids; Derivatives thereof, e.g. tryptophan, indomethacin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/16—Drugs for disorders of the alimentary tract or the digestive system for liver or gallbladder disorders, e.g. hepatoprotective agents, cholagogues, litholytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/18—Drugs for disorders of the alimentary tract or the digestive system for pancreatic disorders, e.g. pancreatic enzymes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/02—Nasal agents, e.g. decongestants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/06—Antiasthmatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/10—Expectorants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/12—Mucolytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P15/00—Drugs for genital or sexual disorders; Contraceptives
- A61P15/08—Drugs for genital or sexual disorders; Contraceptives for gonadal disorders or for enhancing fertility, e.g. inducers of ovulation or of spermatogenesis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/08—Drugs for skeletal disorders for bone diseases, e.g. rachitism, Paget's disease
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/08—Drugs for skeletal disorders for bone diseases, e.g. rachitism, Paget's disease
- A61P19/10—Drugs for skeletal disorders for bone diseases, e.g. rachitism, Paget's disease for osteoporosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/08—Antiepileptics; Anticonvulsants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
- A61P25/16—Anti-Parkinson drugs
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/06—Antihyperlipidemics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C209/00—Preparation of compounds containing amino groups bound to a carbon skeleton
- C07C209/68—Preparation of compounds containing amino groups bound to a carbon skeleton from amines, by reactions not involving amino groups, e.g. reduction of unsaturated amines, aromatisation, or substitution of the carbon skeleton
- C07C209/74—Preparation of compounds containing amino groups bound to a carbon skeleton from amines, by reactions not involving amino groups, e.g. reduction of unsaturated amines, aromatisation, or substitution of the carbon skeleton by halogenation, hydrohalogenation, dehalogenation, or dehydrohalogenation
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C225/00—Compounds containing amino groups and doubly—bound oxygen atoms bound to the same carbon skeleton, at least one of the doubly—bound oxygen atoms not being part of a —CHO group, e.g. amino ketones
- C07C225/02—Compounds containing amino groups and doubly—bound oxygen atoms bound to the same carbon skeleton, at least one of the doubly—bound oxygen atoms not being part of a —CHO group, e.g. amino ketones having amino groups bound to acyclic carbon atoms of the carbon skeleton
- C07C225/04—Compounds containing amino groups and doubly—bound oxygen atoms bound to the same carbon skeleton, at least one of the doubly—bound oxygen atoms not being part of a —CHO group, e.g. amino ketones having amino groups bound to acyclic carbon atoms of the carbon skeleton the carbon skeleton being saturated
- C07C225/06—Compounds containing amino groups and doubly—bound oxygen atoms bound to the same carbon skeleton, at least one of the doubly—bound oxygen atoms not being part of a —CHO group, e.g. amino ketones having amino groups bound to acyclic carbon atoms of the carbon skeleton the carbon skeleton being saturated and acyclic
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D209/00—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D209/02—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom condensed with one carbocyclic ring
- C07D209/04—Indoles; Hydrogenated indoles
- C07D209/10—Indoles; Hydrogenated indoles with substituted hydrocarbon radicals attached to carbon atoms of the hetero ring
- C07D209/12—Radicals substituted by oxygen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D209/00—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D209/02—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom condensed with one carbocyclic ring
- C07D209/04—Indoles; Hydrogenated indoles
- C07D209/30—Indoles; Hydrogenated indoles with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, directly attached to carbon atoms of the hetero ring
- C07D209/40—Nitrogen atoms, not forming part of a nitro radical, e.g. isatin semicarbazone
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D317/00—Heterocyclic compounds containing five-membered rings having two oxygen atoms as the only ring hetero atoms
- C07D317/08—Heterocyclic compounds containing five-membered rings having two oxygen atoms as the only ring hetero atoms having the hetero atoms in positions 1 and 3
- C07D317/44—Heterocyclic compounds containing five-membered rings having two oxygen atoms as the only ring hetero atoms having the hetero atoms in positions 1 and 3 ortho- or peri-condensed with carbocyclic rings or ring systems
- C07D317/46—Heterocyclic compounds containing five-membered rings having two oxygen atoms as the only ring hetero atoms having the hetero atoms in positions 1 and 3 ortho- or peri-condensed with carbocyclic rings or ring systems condensed with one six-membered ring
- C07D317/48—Methylenedioxybenzenes or hydrogenated methylenedioxybenzenes, unsubstituted on the hetero ring
- C07D317/50—Methylenedioxybenzenes or hydrogenated methylenedioxybenzenes, unsubstituted on the hetero ring with only hydrogen atoms, hydrocarbon or substituted hydrocarbon radicals, directly attached to atoms of the carbocyclic ring
- C07D317/60—Radicals substituted by carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/12—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings linked by a chain containing hetero atoms as chain links
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Pulmonology (AREA)
- Neurosurgery (AREA)
- Physical Education & Sports Medicine (AREA)
- Diabetes (AREA)
- Neurology (AREA)
- Biomedical Technology (AREA)
- Rheumatology (AREA)
- Epidemiology (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Hematology (AREA)
- Psychology (AREA)
- Obesity (AREA)
- Pain & Pain Management (AREA)
- Reproductive Health (AREA)
- Endocrinology (AREA)
- Pregnancy & Childbirth (AREA)
- Gynecology & Obstetrics (AREA)
- Otolaryngology (AREA)
- Gastroenterology & Hepatology (AREA)
- Ophthalmology & Optometry (AREA)
- Emergency Medicine (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Plural Heterocyclic Compounds (AREA)
- Indole Compounds (AREA)
- Low-Molecular Organic Synthesis Reactions Using Catalysts (AREA)
Abstract
Изобретение относится к соединению формулы III, где независимо для каждого случая R2 представляет собой галоген; R3 представляет собой C1-6алифатическую группу, замещенную OP; P представляет собой ацетил, бензоил, бензил, β-метоксиэтоксиметиловый эфир, диметокситритил, метоксиметиловый эфир, метокситритил, пара-метоксибензиловый эфир, пивалоил, тетрагидропиранил, тритил и триметилсилил; и o представляет собой 1. Технический результат – получено новое промежуточное соединение, которое применимо для получения (R)-1-(2,2-дифторбензо[d][1,3]диоксол-5-ил)-N-(1-(2,3-дигидроксипропил)-6-фтор-2-(1-гидрокси-2-метилпропан-2-ил)-1H-индол-5-ил)циклопропанкарбоксамида, которое в свою очередь может найти применение в медицине для лечения заболеваний, опосредованных CFTR, таких как кистозный фиброз. 2 з.п. ф-лы, 6 табл.
Description
Перекрестная ссылка на родственные заявки
[001] По настоящей заявке испрашивается приоритет на основании предварительных патентных заявок США с серийными номерами 61/333870, подана 12 мая 2010 года; 61/327095, подана 22 апреля 2010 года; 61/327057, подана 22 апреля 2010 года; 61/329493, подана 29 апреля 2010 года; 61/327091, подана 22 апреля 2010 года; 61/329510, подана 29 апреля 2010 года; 61/327099, подана 22 апреля 2010 года и 61/329500, подана 29 апреля 2010 года, полное содержание всех этих патентных заявок включено в настоящую заявку посредством ссылки.
Область техники, к которой относится изобретение
[002] Настоящее изобретение раскрывает способы получения соединений, полезных для лечения заболеваний, опосредованных CFTR, таких как кистозный фиброз.
Предпосылки создания изобретения
[003] CFTR представляет собой cAMP/ATP-опосредованный анионный канал, который экспрессируется в различных типах клеток, включая абсорбирующие и секреторные клетки эпителия, где он регулирует поток анионов через мембрану, а также активность других ионных каналов и белков. В клетках эпителия нормальное функционирование CFTR имеет решающее значение для поддержания транспорта электролитов по всему организму, включая респираторную и пищеварительную ткани. CFTR состоит примерно из 1480 аминокислот, которые кодируют белок, состоящий из тандемного повтора трансмембранных доменов, каждый из которых содержит шесть трансмембранных спиралей и нуклеотид-связывающий домен. Эти два трансмембранных домена связаны посредством большого полярного регуляторного (R)-домена с несколькими сайтами фосфорилирования, которые регулируют активность канала и направленную миграцию клеток.
[004] Ген, кодирующий CFTR, был идентифицирован и секвенирован (см. Gregory, R. J. et al. (1990) Nature 347:382-386; Rich, D. P. et al. (1990) Nature 347:358-362), (Riordan, J. R. et al. (1989) Science 245: 1066-1073). Дефект этого гена вызывает мутации в CFTR, в результате приводящие к кистозному фиброзу ("CF"), наиболее распространенному генетическому заболеванию со смертельным исходом у людей. Кистозный фиброз поражает примерно одного из каждых 2500 новорожденных в Соединенных Штатах. Из общей численности населения США до 10 миллионов человек имеют одну копию дефектного гена без видимых эффектов заболевания. Напротив, люди с двумя копиями CF-ассоциируемого гена страдают от изнурительных и фатальных последствий CF, включая хроническое заболевание легких.
[005] У пациентов с кистозным фиброзом мутации в CFTR, эндогенно экспрессированного в респираторном эпителии, приводят к пониженной апикальной анионной секреции, вызывающей дисбаланс транспорта ионов и жидкостей. Полученное в результате снижение анионного транспорта способствует повышению накопления слизи в легких и сопутствующим микробным инфекциям, что в конечном итоге приводит к смерти больных CF. Помимо респираторного заболевания, пациенты с CF обычно страдают от желудочно-кишечных проблем и недостаточной функции поджелудочной железы, которые, если их не лечить, приводят к смерти. Кроме того, большинство мужчин с кистозным фиброзом являются бесплодными, и среди женщин с кистозным фиброзом уменьшается рождаемость. В отличие от тяжелых последствий двух копий CF-ассоциированного гена, лица с одной копией CF-ассоциированного гена демонстрируют повышенную резистентность к холере и обезвоживанию в результате диареи - это, возможно, объясняет относительно высокую распространенность CF гена у населения.
[006] Анализ последовательности CFTR гена CF хромосом выявил ряд вызывающих заболевание мутаций (Cutting, G. R. et al. (1990) Nature 346:366-369; Dean, M. et al. (1990) Cell 61:863:870; и Kerem, B-S. et al. (1989) Science 245: 1073-1080; Kerem, B-S. et al. (1990) Proc. Natl. Acad. Sci. USA 87:8447-8451). На сегодняшний день идентифицировано >1000 вызывающих заболевание мутаций в CF гене (http://www.genet.sickkids.on.ca/cftr/). Наиболее распространенной мутацией является делеция фенилаланина в положении 508 аминокислотной последовательности CFTR, и ее обычно обозначают как ΔF508-CFTR. Эта мутация встречается примерно в 70% случаев кистозного фиброза и связана с тяжелым заболеванием. Другие мутации включают R117H и G551D.
[007] Делеция остатка 508 в ΔF508-CFTR препятствует правильной укладке зарождающегося белка. Это приводит к неспособности мутантного белка выходить из ER и перемещаться к плазменной мембране. В результате количество каналов, присутствующих в мембране, намного меньше, чем наблюдается в клетках, экспрессирующих CFTR дикого типа. В дополнение к нарушению направленной миграции эта мутация приводит к нарушению воротного механизма ионных каналов. Взятые вместе, уменьшение количества каналов в мембране и нарушение воротного механизма приводят к снижению анионного транспорта через эпителий, приводящее к нарушению транспорта ионов и жидкостей. (Quinton, P. M. (1990), FASEB J. 4: 2709-2727). Исследования, однако, показали, что уменьшенные количества ΔF508-CFTR в мембране являются функциональными, хотя и меньше, чем CFTR дикого типа. (Dalemans et al. (1991), Nature Lond. 354: 526-528; Denning et al., supra; Pasyk and Foskett (1995), J. Cell. Biochem. 270: 12347-50). В дополнение к ΔF508-CFTR, другие вызывающие заболевание мутации в CFTR, которые приводят к нарушению направленной миграции, синтеза и/или воротного механизма ионных каналов, могут активироваться или подавляться для изменения анионной секреции и модификации прогрессирования и/или тяжести заболевания.
[008] Хотя CFTR транспортирует различные молекулы помимо анионов, ясно, что эта роль (транспорт анионов) представляет собой один элемент в важном механизме транспорта ионов и воды через эпителий. Другие элементы включают эпителиальный Na+ канал, ENaC, совместный транспортер Na+/2C1-/K+, Na+-K+-АТФазный насос и базолатеральные мембранные K+ каналы, которые отвечают за поглощение хлорида в клетках.
[009] Эти элементы работают вместе для достижения направленного транспорта через эпителий посредством их селективной экспрессии и локализации в клетке. Абсорбция хлорида происходит за счет скоординированной активности ENaC и CFTR, присутствующих на апикальной мембране, и Na+-K+-АТФазного насоса и Cl- каналов, экспрессируемых на базолатеральной поверхности клетки. Вторичный активный транспорт хлорида с люминальной стороны приводит к накоплению внутриклеточного хлорида, который затем может пассивно выходить из клетки через Cl- каналы, что приводит к векторному транспорту. Расположение Na+/2C1-/K+ ко-транспортера, Na+-K+-АТФазного насоса и базолатеральных мембранных K+ каналов на базолатеральной поверхности и CFTR на люминальной стороне координирует секрецию хлорида через CFTR на люминальной стороне. Поскольку вода вероятно никогда активно не транспортируется сама по себе, ее поток через эпителий зависит от ничтожно малых трансэпителиальных осмотических градиентов, генерируемых объемным потоком натрия и хлоридов.
[0010] Как обсуждается выше, считается, что делеция остатка 508 в ΔF508-CFTR препятствует правильной укладке зарождающегося белка, что приводит к неспособности такого мутантного белка выходить из ER и перемещаться к плазменной мембране. В результате на плазменной мембране присутствуют недостаточные количества зрелого белка и хлоридный транспорт в тканях эпителия существенно снижается. Действительно, было показано, что этот клеточный феномен дефектного ER процессинга ABC транспортеров посредством ER механизма является причиной, лежащей в основе не только CF заболевания, но также широкого ряда других обособленных и наследственных заболеваний. Два пути неправильной работы ER механизма представляют собой либо потерю связывания с ER экспортом белков, приводящую к деградации, либо ER аккумуляцию этих дефектных/имеющих неправильную укладку белков [Aridor M, et al., Nature Med., 5(7), pp 745-751 (1999); Shastry, B.S., et al., Neurochem. International, 43, pp 1-7 (2003); Rutishauser, J., et al., Swiss Med Wkly, 132, pp 211-222 (2002); Morello, JP et al., TIPS, 21, pp. 466-469 (2000); Bross P., et al., Human Mut., 14, pp. 186-198 (1999)].
[0011] (R)-1-(2,2-дифторбензо[d][1,3]диоксол-5-ил)-N-(1-(2,3-дигидроксипропил)-6-фтор-2-(1-гидрокси-2-метилпропан-2-ил)-1H-индол-5-ил)циклопропанкарбоксамид раскрывается в опубликованной патентной заявке США US20090131492 (указанная публикация включена в настоящую заявку посредством ссылки в полном объеме) в качестве модулятора активности CFTR и, таким образом, полезен при лечении CFTR-опосредованных заболеваний, таких как кистозный фиброз. Однако остается необходимость в экономичных способах для получения циклоалкилкарбоксамидо-индольных соединений, описанных в настоящей заявке.
КРАТКОЕ СОДЕРЖАНИЕ ИЗОБРЕТЕНИЯ
[0012] Как описано в настоящей заявке, настоящее изобретение обеспечивает способы получения CFTR корректоров, полезных в лечении CFTR опосредованных заболеваний, таких как кистозный фиброз. Такие соединения включают (R)-1-(2,2-дифторбензо[d][1,3]диоксол-5-ил)-N-(1-(2,3-дигидроксипропил)-6-фтор-2-(1-гидрокси-2-метилпропан-2-ил)-1H-индол-5-ил)циклопропанкарбоксамид (в дальнейшем "Соединение 1"), который имеет представленную ниже структуру:
Соединение 1
[0013] Соединение 1 и его фармацевтически приемлемые композиции являются полезными для лечения или уменьшения тяжести CFTR-опосредованных заболеваний, таких как, например, кистозный фиброз. Соединение 1 может существовать в нескольких различных твердых формах, таких как по существу кристаллические формы или аморфные формы.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0014] Определения
[0015] Как используется в настоящей заявке, применяются следующие определения, если не указано иное.
[0016] Термин "CFTR", как используется в настоящей заявке, означает регулятор трансмембранной проводимости кистозного фиброза или его мутацию в состоянии регуляторной активности, включая, но не ограничиваясь этим, ΔF508 CFTR и G551D CFTR (мутации CFTR см., например, на http://www.genet.sickkids.on.ca/cftr/).
[0017] Термин "модуляция", как используется в настоящей заявке, означает увеличение или уменьшение, например, активности, на измеримое количество.
[0018] Термин " химически стабильный", как используется в настоящей заявке, означает, что твердая форма Соединения 1 не разлагается на одно или несколько различных химических соединений при воздействии определенных условий, например, 40°C/75% относительной влажности, в течение определенного периода времени, например, 1 дня, 2 дней, 3 дней, 1 недели, 2 недель или дольше. В некоторых вариантах воплощения менее чем 25% твердой формы Соединения 1 разлагается, в некоторых вариантах воплощения менее чем приблизительно 20%, менее чем приблизительно 15%, менее чем приблизительно 10%, менее чем приблизительно 5%, менее чем приблизительно 3%, менее чем приблизительно 1%, менее чем приблизительно 0,5% формы Соединения 1 разлагается при воздействии указанных условий. В некоторых вариантах воплощения никакое обнаруживаемое количество твердой формы Соединения 1 не разлагается.
[0019] Термин "физически стабильный", как используется в настоящей заявке, означает, что твердая форма Соединения 1 не преобразуется в одну или несколько других физических форм Соединения 1 (например, других твердых форм, согласно определению методом XRPD, DSC и др.) при воздействии определенных условий, например, 40°C/75% относительной влажности, в течение определенного периода времени, например, 1 дня, 2 дней, 3 дней, 1 недели, 2 недель или дольше. В некоторых вариантах воплощения менее чем 25% твердой формы Соединения 1 преобразуется в одну или несколько других физических форм при воздействии указанных условий. В некоторых вариантах воплощения менее чем приблизительно 20%, менее чем приблизительно 15%, менее чем приблизительно 10%, менее чем приблизительно 5%, менее чем приблизительно 3%, менее чем приблизительно 1%, менее чем приблизительно 0,5% твердой формы Соединения 1 преобразуется в одну или несколько других физических форм Соединения 1 при воздействии определенных условий. В некоторых вариантах воплощения никакое обнаруживаемое количество твердой формы Соединения 1 не преобразуется в одну или несколько других физических форм Соединения 1.
[0020] Как используется в настоящей заявке, термины "около" и "приблизительно", при использовании в связи с дозами, количествами или массовыми процентами ингредиентов композиции или лекарственной формы, означает дозу, количество или массовый процент, которые признаны специалистом в данной области техники как обеспечивающие фармакологическоий эффект, эквивалентный эффекту, получаемому при использовании указанной дозы, количества или массового процента. Конкретно, термин "около" или "приблизительно" означает допустимую погрешность для конкретного значения, как определено специалистом в данной области техники, которая частично зависит от того, как значение измеряется или определяется. В некоторых вариантах воплощения термин "около" или "приблизительно" означает стандартные отклонения в пределах 1, 2, 3 или 4. В некоторых вариантах воплощения термин "около" или "приблизительно" означает в пределах 30%, 25%, 20%, 15%, 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2%, 1%, 0,5%, 0,1% или 0,05% от данного значения или диапазона.
[0021] Если не указано иное, структуры, представленные в настоящем описании, также должны включать все изомерные (например, энантиомерные, диастереомерные и геометрические (или конформационные)) формы структуры; например, R- и S-конфигурации для каждого центра асимметрии, (Z)- и (E)-изомеры по двойной связи и (Z)- и (E)-конформационные изомеры. Таким образом, отдельные стереохимические изомеры, а также энантиомерные, диастереомерные и геометрические (или конформационные) смеси соединений по настоящему изобретению находятся в пределах объема изобретения. Все таутомерные формы Соединения 1 включены в настоящую заявку. Например, Соединение 1 может существовать в виде таутомеров, оба из которых включены в настоящую заявку:
[0022] Кроме того, если не указано иное, структуры, представленные в настоящей заявке, также должны включать соединения, которые отличаются только наличием одного или более изотопно обогащенных атомов. Например, Соединение 1, в котором один или несколько атомов водорода замещены дейтерием или тритием или один или более атомов углерода замещены 13C- или 14C- обогащенным углеродом, находится в пределах объема настоящего изобретения. Такие соединения являются полезными, например, в качестве аналитических инструментов, зондов в биологических анализах или соединений с улучшенным терапевтическим профилем.
[0023] Термин "защитная группа", сокращенно P, как используется в настоящей заявке, относится к любой химической группе, введенной в молекулу путем химической модификации функциональной группы с целью получения химической селективности в последующей химической реакции. Неограничивающие примеры спиртовых защитных групп включают ацетил (Ac), бензоил (Bz), бензил (Bn), β-метоксиэтоксиметиловый эфир (MEM), диметокситритил (DMT), метоксиметиловый эфир (MOM), метокситритил (MMT), пара-метоксибензиловый эфир (PMB), пивалоил (Piv), тетрагидропиранил (THP), тритил (Tr) и триметилсилил (TMS). В одном варианте воплощения защитная группа представляет собой Bn, который имеет структуру -CH2C6H5.
[0024] Аббревиатура "DCM" означает дихлорметан. Аббревиатура "IPA" означает изопропиловый спирт. Аббревиатура "DMSO" означает диметилсульфоксид. Аббревиатура "MTBE" означает метил-трет-бутиловый эфир. Аббревиатура "THF" означает тетрагидрофуран. Аббревиатура "TEA" означает триэтиламин. Аббревиатура "dba" как в Pd(dba)2 означает дибензилиденацетон. Аббревиатура "dppf" как в Pd(dppf)Cl2 означает 1,1'-бис(дифенилфосфино)ферроцен.
[0025] В одном аспекте настоящее изобретение представляет собой способ получения соединения формулы I:
где независимо для каждого случая
кольцо А представляет собой конденсированное циклоалкильное, гетероциклоалкильное, арильное или гетероарильное кольцо;
R1 независимо выбран из -RJ, -ORJ, -N(RJ)2, -NО2, галогена, -CN, -C1-4галогеналкила, -C1-4галогеналкокси, -C(О)N(RJ)2, -NRJC(О)RJ, -SORJ, -SО2RJ, -SО2N(RJ)2, -NRJSO2RJ, -CORJ, -СО2RJ, -NRJSO2N(RJ)2, -COCORJ;
RJ представляет собой водород или C1-6 алифатическую группу;
X представляет собой CN или СО2R;
R представляет собой C1-6 алифатическую группу или арил; и
m представляет собой целое число от 0 до 3 включительно;
включающий стадии
a) взаимодействия соединения формулы IA в первом органическом растворителе
где независимо для каждого случая
кольцо А представляет собой конденсированное циклоалкильное, гетероциклоалкильное, арильное или гетероарильное кольцо;
R1 независимо выбран из -RJ, -ORJ, -N(RJ)2, -NО2, галогена, -CN, -C1-4галогеналкила, -C1-4галогеналкокси, -C(О)N(RJ)2, -NRJC(О)RJ, -SORJ, -SО2RJ, -SО2N(RJ)2, -NRJSO2RJ, -CORJ, -СО2RJ, -NRJSO2N(RJ)2, -COCORJ;
RJ представляет собой водород или C1-6 алифатическую группу;
m представляет собой целое число от 0 до 3 включительно; и
Hal представляет собой галогенид;
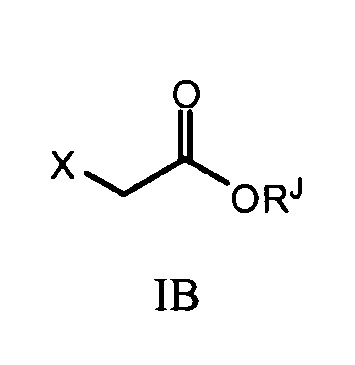
с соединением формулы IB:
где RJ представляет собой водород или C1-6 алифатическую группу, с образованием соединения формулы IC:
где независимо для каждого случая
кольцо А представляет собой конденсированное циклоалкильное, гетероциклоалкильное, арильное или гетероарильное кольцо;
R1 независимо выбран из -RJ, -ORJ, -N(RJ)2, -NО2, галогена, -CN, -C1-4галогеналкила, -C1-4галогеналкокси, -C(О)N(RJ)2, -NRJC(О)RJ, -SORJ, -SО2RJ, -SО2N(RJ)2, -NRJSO2RJ, -CORJ, -СО2RJ, -NRJSO2N(RJ)2, -COCORJ;
RJ представляет собой водород или C1-6 алифатическую группу;
X представляет собой CN или СО2R;
R представляет собой C1-6 алифатическую группу или арил; и
m представляет собой целое число от 0 до 3 включительно; и
b) удаления -СО2RJ группы из соединения IC во втором органическом растворителе с образованием соединения формулы I.
[0026] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где кольцо А представляет собой конденсированный гетероциклоалкил или гетероарил. В другом варианте воплощения кольцо А выбрано из
В другом варианте воплощения кольцо А представляет собой
[0027] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где X представляет собой CN. В другом варианте воплощения X представляет собой СО2Et.
[0028] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где m имеет значение 0.
[0029] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где RJ представляет собой C1-6 алифатическую группу. В другом варианте воплощения RJ представляет собой -CH2CH3.
[0030] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где Hal представляет собой Br.
[0031] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где первый органический растворитель представляет собой апротонный растворитель. В другом варианте воплощения первый органический растворитель выбран из 1,2-диметоксиэтана, диоксана, ацетонитрила, толуола, бензола, ксилолов, метил-трет-бутилового эфира, метилэтилкетона, метилизобутилкетона, ацетона, N,N-диметилформамида, N,N-диметилацетамида, N-метилпирролидинона, этилацетата, дихлорметана или диметилсульфоксида. В другом варианте воплощения первый органический растворитель выбран из ацетонитрила, толуола, бензола или ксилолов. В другом варианте воплощения первый органический растворитель представляет собой толуол.
[0032] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где стадию а) осуществляют в присутствии катализатора на основе переходного металла. В другом варианте воплощения стадию а) осуществляют в присутствии палладиевого катализатора. В другом варианте воплощения стадию а) осуществляют в присутствии палладиевого катализатора, выбранного из ацетата палладия(II), Pd(dppf)Cl2, Pd(dba)2, тетракис(трифенилфосфин)палладия(0) или трис(дибензилиденацетон)дипалладия(0). В другом варианте воплощения стадию а) осуществляют в присутствии Pd(dba)2.
[0033] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где стадию а) осуществляют при температуре от около 50°C до 90°C. В другом варианте воплощения стадию а) осуществляют при температуре от около 60°C до 80°C. В другом варианте воплощения стадию а) осуществляют при температуре около 70°C.
[0034] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где второй органический растворитель представляет собой апротонный растворитель. В другом варианте воплощения второй органический растворитель выбран из 1,2-диметоксиэтана, диоксана, ацетонитрила, толуола, бензола, ксилолов, метил-трет-бутилового эфира, метилэтилкетона, метилизобутилкетона, ацетона, N,N-диметилформамида, N,N-диметилацетамида, N-метилпирролидинона, этилацетата, дихлорметана или диметилсульфоксида. В другом варианте воплощения второй органический растворитель представляет собой диметилсульфоксид.
[0035] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где стадию b) осуществляют в присутствии неорганической кислоты. В другом варианте воплощения стадию b) осуществляют в присутствии неорганической кислоты, выбранной из хлористоводородной, серной, азотной, фосфорной или борной кислоты. В другом варианте воплощения стадию b) осуществляют в присутствии хлористоводородной кислоты.
[0036] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где стадию b) осуществляют при температуре от около 55°C до 95°C. В другом варианте воплощения стадию b) осуществляют при температуре от около 65°C до 85°C. В другом варианте воплощения стадию b) осуществляют при температуре около 75°C.
[0037] В другом аспекте настоящее изобретение представляет способ получения соединения формулы II:
где независимо для каждого случая
кольцо А представляет собой конденсированное циклоалкильное, гетероциклоалкильное, арильное или гетероарильное кольцо;
Hal представляет собой галогенид;
R1 независимо выбран из -RJ, -ORJ, -N(RJ)2, -NО2, галогена, -CN, -C1-4галогеналкила, -C1-4галогеналкокси, -C(О)N(RJ)2, -NRJC(О)RJ, -SORJ, -SО2RJ, -SО2N(RJ)2, -NRJSO2RJ, -CORJ, -СО2RJ, -NRJSO2N(RJ)2, -COCORJ;
RJ представляет собой водород или C1-6 алифатическую группу;
m представляет собой целое число от 0 до 3 включительно; и
n представляет собой целое число от 1 до 4 включительно;
включающий стадии
a) взаимодействия соединения формулы IIA в первом органическом растворителе
где независимо для каждого случая
кольцо А представляет собой конденсированное циклоалкильное, гетероциклоалкильное, арильное или гетероарильное кольцо;
R1 независимо выбран из -RJ, -ORJ, -N(RJ)2, -NО2, галогена, -CN, -C1-4галогеналкила, -C1-4галогеналкокси, -C(О)N(RJ)2, -NRJC(О)RJ, -SORJ, -SО2RJ, -SО2N(RJ)2, -NRJSO2RJ, -CORJ, -СО2RJ, -NRJSO2N(RJ)2, -COCORJ;
RJ представляет собой водород или C1-6 алифатическую группу;
m представляет собой целое число от 0 до 3 включительно; и
Hal представляет собой галогенид;
с соединением формулы IIB:
где
X представляет собой CN или СО2R;
R представляет собой C1-6 алифатическую группу или арил; и
RJ представляет собой водород или C1-6 алифатическую группу, с образованием соединения формулы IIC:
где независимо для каждого случая
кольцо А представляет собой конденсированное циклоалкильное, гетероциклоалкильное, арильное или гетероарильное кольцо;
R1 независимо выбран из -RJ, -ORJ, -N(RJ)2, -NО2, галогена, -CN, -C1-4галогеналкила, -C1-4галогеналкокси, -C(О)N(RJ)2, -NRJC(О)RJ, -SORJ, -SО2RJ, -SО2N(RJ)2, -NRJSO2RJ, -CORJ, -СО2RJ, -NRJSO2N(RJ)2, -COCORJ;
RJ представляет собой водород или C1-6 алифатическую группу;
X представляет собой CN или СО2R;
R представляет собой С1-6 алифатическую группу или арил; и
m представляет собой целое число от 0 до 3 включительно;
b) удаления -СО2RJ группы из соединения IIC во втором органическом растворителе с образованием соединения формулы I:
где независимо для каждого случая
кольцо А представляет собой конденсированное циклоалкильное, гетероциклоалкильное, арильное или гетероарильное кольцо;
R1 независимо выбран из -RJ, -ORJ, -N(RJ)2, -NО2, галогена, -CN, -C1-4галогеналкила, -C1-4галогеналкокси, -C(О)N(RJ)2, -NRJC(О)RJ, -SORJ, -SО2RJ, -SО2N(RJ)2, -NRJSO2RJ, -CORJ, -СО2RJ, -NRJSO2N(RJ)2, -COCORJ;
RJ представляет собой водород или C1-6 алифатическую группу;
X представляет собой CN или СО2R;
R представляет собой С1-6 алифатическую группу или арил; и
m представляет собой целое число от 0 до 3 включительно;
c) взаимодействия соединения формулы I с соединением формулы IID в присутствии основания:
где независимо для каждого случая
Hal представляет собой галогенид; и
q представляет собой целое число от 0 до 3 включительно; с получением соединения формулы IIE:
где независимо для каждого случая
кольцо А представляет собой конденсированное циклоалкильное, гетероциклоалкильное, арильное или гетероарильное кольцо;
R1 независимо выбран из -RJ, -ORJ, -N(RJ)2, -NО2, галогена, -CN, -C1-4галогеналкила, -C1-4галогеналкокси, -C(О)N(RJ)2, -NRJC(О)RJ, -SORJ, -SО2RJ, -SО2N(RJ)2, -NRJSO2RJ, -CORJ, -СО2RJ, -NRJSO2N(RJ)2, -COCORJ;
RJ представляет собой водород или C1-6 алифатическую группу;
m представляет собой целое число от 0 до 3 включительно;
X представляет собой CN или СО2R;
R представляет собой С1-6 алифатическую группу или арил; и
n представляет собой целое число от 1 до 4 включительно;
d) последовательного взаимодействия соединения формулы IIE с гидроксидным основанием и кислотой с образованием соединения формулы IIF:
где независимо для каждого случая
кольцо А представляет собой конденсированное циклоалкильное, гетероциклоалкильное, арильное или гетероарильное кольцо;
R1 независимо выбран из -RJ, -ORJ, -N(RJ)2, -NО2, галогена, -CN, -C1-4галогеналкила, -C1-4галогеналкокси, -C(О)N(RJ)2, -NRJC(О)RJ, -SORJ, -SО2RJ, -SО2N(RJ)2, -NRJSO2RJ, -CORJ, -СО2RJ, -NRJSO2N(RJ)2, -COCORJ;
RJ представляет собой водород или C1-6 алифатическую группу;
m представляет собой целое число от 0 до 3 включительно; и
n представляет собой целое число от 1 до 4 включительно; и
e) взаимодействия соединения формулы IIF с галогенирующим агентом в третьем органическом растворителе с образованием соединения формулы II.
[0038] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где на стадии a) первый органический растворитель представляет собой апротонный растворитель. В другом варианте воплощения первый органический растворитель выбран из 1,2-диметоксиэтана, диоксана, ацетонитрила, толуола, бензола, ксилолов, метил-трет-бутилового эфира, метилэтилкетона, метилизобутилкетона, ацетона, N,N-диметилформамида, N,N-диметилацетамида, N-метилпирролидинона, этилацетата, дихлорметана или диметилсульфоксида. В другом варианте воплощения первый органический растворитель представляет собой толуол.
[0039] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где на стадии a) m имеет значение 0.
[0040] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где на стадии a) Hal представляет собой Br.
[0041] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где на стадии a) кольцо А представляет собой конденсированное гетероциклическое или гетероарильное кольцо. В другом варианте воплощения кольцо А выбрано из
В другом варианте воплощения кольцо А представляет собой
[0042] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где на стадии a) X представляет собой CN. В другом варианте воплощения X представляет собой СО2Et.
[0043] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где на стадии a) RJ представляет собой Et.
[0044] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где в формуле IIC кольцо А представляет собой
m имеет значение 0, X представляет собой CN и RJ представляет собой Et.
[0045] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где на стадии b) второй растворитель представляет собой апротонный растворитель. В другом варианте воплощения второй органический растворитель выбран из 1,2-диметоксиэтана, диоксана, ацетонитрила, толуола, бензола, ксилолов, метил-трет-бутилового эфира, метилэтилкетона, метилизобутилкетона, ацетона, N,N-диметилформамида, N,N-диметилацетамида, N-метилпирролидинона, этилацетата, дихлорметана или диметилсульфоксида. В другом варианте воплощения второй растворитель представляет собой диметилсульфоксид.
[0046] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где в формуле I кольцо А представляет собой
m имеет значение 0 и X представляет собой CN.
[0047] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где на стадии c) основание представляет собой неорганическое основание. В другом варианте воплощения основание представляет собой гидроксид. В другом варианте воплощения основание представляет собой NaOH.
[0048] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где в формуле IID q имеет значение 1.
[0049] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где в формуле IID один Hal представляет собой Cl, а другой Hal представляет собой Br.
[0050] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где на стадии d) основание представляет собой NaOH. В другом варианте воплощения на стадии d) кислота представляет собой HCl.
[0051] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где на стадии d) взаимодействие с гидроксидным основанием происходит при температуре от около 60°C до 100°C. В другом варианте воплощения взаимодействие с гидроксидом происходит при температуре от около 70°C до 90°C. В другом варианте воплощения взаимодействие с гидроксидом происходит при температуре около 80°C.
[0052] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где в формуле IIE кольцо А представляет собой
m имеет значение 0, n имеет значение 1 и X представляет собой CN.
[0053] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где на стадии e), третий органический растворитель представляет собой апротонный растворитель. В другом варианте воплощения на стадии e), третий органический растворитель выбран из 1,2-диметоксиэтана, диоксана, ацетонитрила, толуола, бензола, ксилолов, метил-трет-бутилового эфира, метилэтилкетона, метилизобутилкетона, ацетона, N,N-диметилформамида, N,N-диметилацетамида, N-метилпирролидинона, этилацетата, дихлорметана или диметилсульфоксида. В другом варианте воплощения на стадии e), третий органический растворитель представляет собой толуол.
[0054] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где на стадии e), галогенирующий агент представляет собой SOCl2.
[0055] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где стадию е) осуществляют при температуре от около 40°C до 80°C. В другом варианте воплощения стадию е) осуществляют при температуре от около 50°C до 70°C. В другом варианте воплощения стадию е) осуществляют при температуре около 60°C.
[0056] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где в формуле IIF кольцо А представляет собой
m имеет значение 0 и n имеет значение 1.
[0057] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где в формуле II кольцо А представляет собой
m имеет значение 0, n имеет значение 1 и Hal представляет собой Cl.
[0058] В другом аспекте, настоящее изобретение представляет способ получения соединения формулы III:
где независимо для каждого случая
R2 представляет собой -RJ, -ORJ, -N(RJ)2, -NO2, галоген, -CN, -C1-4галогеналкил, -C1-4галогеналкокси, -C(О)N(RJ)2, -NRJC(О)RJ, -SORJ, -SO2RJ, -SO2N(RJ)2, -NRJSO2RJ, -CORJ, -СО2RJ, -NRJSO2N(RJ)2, -COCORJ;
RJ представляет собой водород или C1-6 алифатическую группу;
R3 представляет собой C1-6 алифатическую группу, необязательно замещенную OH, OP, -О-C1-6 алифатической группой, арилом, гетероарилом, -O-арилом или -O-гетероарилом;
P представляет собой защитную группу; и
o представляет собой целое число от 0 до 3;
включающий стадии
a) взаимодействия соединения формулы IIIA:
где независимо для каждого случая
R2 представляет собой -RJ, -ORJ, -N(RJ)2, -NO2, галоген, -CN, -C1-4галогеналкил, -C1-4галогеналкокси, -C(О)N(RJ)2, -NRJC(О)RJ, -SORJ, -SO2RJ, -SO2N(RJ)2, -NRJSO2RJ, -CORJ, -СО2RJ, -NRJSO2N(RJ)2, -COCORJ;
RJ представляет собой водород или C1-6 алифатическую группу; и
o представляет собой целое число от 0 до 3;
с галогенирующим реагентом в первом органическом растворителе с образованием соединения формулы IIIB:
где независимо для каждого случая
R2 представляет собой -RJ, -ORJ, -N(RJ)2, -NO2, галоген, -CN, -C1-4галогеналкил, -C1-4галогеналкокси, -C(О)N(RJ)2, -NRJC(О)RJ, -SORJ, -SO2RJ, -SO2N(RJ)2, -NRJSO2RJ, -CORJ, -СО2RJ, -NRJSO2N(RJ)2, -COCORJ;
RJ представляет собой водород или C1-6 алифатическую группу;
o представляет собой целое число от 0 до 3; и
Hal представляет собой галогенид;
b) взаимодействия соединения формулы IIIB во втором органическом растворителе с соединением формулы IIIC:
где
P представляет собой защитную группу;
с последующим восстановлением и обработкой кислотой с образованием соединения формулы IIID:
где
R2 представляет собой -RJ, -ORJ, -N(RJ)2, -NO2, галоген, -CN, -C1-4галогеналкил, -C1-4галогеналкокси, -C(О)N(RJ)2, -NRJC(О)RJ, -SORJ, -SO2RJ, -SO2N(RJ)2, -NRJSO2RJ, -CORJ, -СО2RJ, -NRJSO2N(RJ)2, -COCORJ;
RJ представляет собой водород или C1-6 алифатическую группу;
o представляет собой целое число от 0 до 3;
Hal представляет собой галогенид;
P представляет собой защитную группу; и
AӨ представляет собой анион;
c) нейтрализации соединения формулы IIID в присутствии основания с образованием соединения формулы IIID-a:
где
R2 представляет собой -RJ, -ORJ, -N(RJ)2, -NO2, галоген, -CN, -C1-4галогеналкил, -C1-4галогеналкокси, -C(О)N(RJ)2, -NRJC(О)RJ, -SORJ, -SO2RJ, -SO2N(RJ)2, -NRJSO2RJ, -CORJ, -СО2RJ, -NRJSO2N(RJ)2, -COCORJ;
RJ представляет собой водород или C1-6 алифатическую группу;
o представляет собой целое число от 0 до 3;
Hal представляет собой галогенид; и
P представляет собой защитную группу;
d) взаимодействия соединения формулы IIID-a в третьем органическом растворителе с соединением формулы IIIE:
где независимо для каждого случая
R3 представляет собой C1-6 алифатическую группу, необязательно замещенную OH, OP, -О-C1-6 алифатической группой, арилом, гетероарилом, -O-арилом или -O-гетероарилом;
в присутствии катализатора с образованием соединения формулы III.
[0059] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где в формуле IIIA o имеет значение 1. В другом варианте воплощения o имеет значение 1 и R2 представляет собой F.
[0060] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где на стадии a) галогенирующий реагент представляет собой N-бромсукцинимид.
[0061] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где на стадии a) первый органический растворитель представляет собой апротонный растворитель. В другом варианте воплощения первый органический растворитель выбран из 1,2-диметоксиэтана, диоксана, ацетонитрила, толуола, бензола, ксилолов, метил-трет-бутилового эфира, метилэтилкетона, метилизобутилкетона, ацетона, N,N-диметилформамида, N,N-диметилацетамида, N-метилпирролидинона, этилацетата, дихлорметана или диметилсульфоксида. В другом варианте воплощения первый органический растворитель представляет собой этилацетат.
[0062] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где стадию а) осуществляют при температуре от около 2°C до 42°C. В другом варианте воплощения стадию а) осуществляют при температуре от около 12°C до 32°C. В другом варианте воплощения стадию а) осуществляют при температуре около 22°C.
[0063] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где в формуле IIIB o имеет значение 1, R2 представляет собой F, и Hal представляет собой Br.
[0064] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где в формуле IIIC P представляет собой бензил.
[0065] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где на стадии b) второй органический растворитель представляет собой апротонный растворитель. В другом варианте воплощения на стадии b) второй органический растворитель выбран из 1,2-диметоксиэтана, диоксана, ацетонитрила, толуола, бензола, ксилолов, метил-трет-бутилового эфира, метилэтилкетона, метилизобутилкетона, ацетона, N,N-диметилформамида, N,N-диметилацетамида, N-метилпирролидинона, этилацетата, дихлорметана или диметилсульфоксида. В другом варианте воплощения на стадии b) второй органический растворитель представляет собой толуол.
[0066] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где на стадии b) взаимодействие с соединением формулы IIIC происходит при температуре от около 60°C до 100°C. В другом варианте воплощения на стадии b) взаимодействие с соединением формулы IIIC происходит при температуре от около 70°C до 90°C. В другом варианте воплощения на стадии b) взаимодействие с соединением формулы IIIC происходит при температуре около 80°C.
[0067] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где на стадии b) восстановление осуществляют при помощи водорода.
[0068] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где на стадии b) кислота представляет собой пара-толуолсульфоновую кислоту.
[0069] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где в формуле IIID, o имеет значение 1, R2 представляет собой F, Hal представляет собой Br, AӨ представляет собой Tos-, и P представляет собой бензил.
[0070] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где в формуле IIIE, R3 представляет собой C(CH3)2CH2О(бензил).
[0071] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где на стадии c) основание представляет собой неорганическое основание.
[0072] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где на стадии c) основание представляет собой NaHСО3.
[0073] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где на стадии d) третий органический растворитель представляет собой апротонный растворитель. В другом варианте воплощения на стадии d) третий органический растворитель выбран из 1,2-диметоксиэтана, диоксана, ацетонитрила, толуола, бензола, ксилолов, метил-трет-бутилового эфира, метилэтилкетона, метилизобутилкетона, ацетона, N,N-диметилформамида, N,N-диметилацетамида, N-метилпирролидинона, этилацетата, дихлорметана или диметилсульфоксида. В другом варианте воплощения на стадии d) третий органический растворитель представляет собой ацетонитрил.
[0074] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где стадию d) осуществляют при температуре от около 60°C до 100°C. В другом варианте воплощения стадию d) осуществляют при температуре от около 70°C до 90°C. В другом варианте воплощения стадию d) осуществляют при температуре около 80°C.
[0075] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где на стадии d) катализатор представляет собой палладиевый катализатор. В другом варианте воплощения на стадии d) катализатор выбран из ацетата палладия(II), Pd(dppf)Cl2, Pd(dba)2, (MeCN)2PdCl2, тетракис(трифенилфосфин)палладия(0) или трис(дибензилиденацетон)дипалладия(0). В другом варианте воплощения на стадии d) катализатор представляет собой ацетат палладия(II).
[0076] В другом аспекте, настоящее изобретение представляет способ получения соединения формулы IV:
где независимо для каждого случая
кольцо А представляет собой конденсированное циклоалкильное, гетероциклоалкильное, арильное или гетероарильное кольцо;
R1 и R2 независимо выбраны из -RJ, -ORJ, -N(RJ)2, -NО2, галогена, -CN, -C1-4галогеналкила, -C1-4галогеналкокси, -C(О)N(RJ)2, -NRJC(О)RJ, -SORJ, -SO2RJ, -SO2N(RJ)2, -NRJSO2RJ, -CORJ, -СО2RJ, -NRJSO2N(RJ)2, -COCORJ;
RJ представляет собой водород или C1-6 алифатическую группу;
R3 представляет собой C1-6 алифатическую группу, необязательно замещенную OH, OP, -О-C1-6 алифатической группой, арилом, гетероарилом, -O-арилом или -O-гетероарилом;
P представляет собой защитную группу;
m представляет собой целое число от 0 до 3 включительно;
n представляет собой целое число от 1 до 4 включительно; и
o представляет собой целое число от 1 до 3 включительно;
включающий стадии
a) взаимодействия соединения формулы IIIA:
где независимо для каждого случая
R2 представляет собой -RJ, -ORJ, -N(RJ)2, -NO2, галоген, -CN, -C1-4галогеналкил, -C1-4галогеналкокси, -C(О)N(RJ)2, -NRJC(О)RJ, -SORJ, -SO2RJ, -SO2N(RJ)2, -NRJSO2RJ, -CORJ, -СО2RJ, -NRJSO2N(RJ)2, -COCORJ;
RJ представляет собой водород или C1-6 алифатическую группу; и
o представляет собой целое число от 0 до 3;
с галогенирующим реагентом в первом органическом растворителе с образованием соединения формулы IIIB:
где независимо для каждого случая
R2 представляет собой -RJ, -ORJ, -N(RJ)2, -NO2, галоген, -CN, -C1-4галогеналкил, -C1-4галогеналкокси, -C(О)N(RJ)2, -NRJC(О)RJ, -SORJ, -SO2RJ, -SO2N(RJ)2, -NRJSO2RJ, -CORJ, -СО2RJ, -NRJSO2N(RJ)2, -COCORJ;
RJ представляет собой водород или C1-6 алифатическую группу;
o представляет собой целое число от 0 до 3; и
Hal представляет собой галогенид;
b) взаимодействия соединения формулы IIIB во втором органическом растворителе с соединением формулы IIIC:
где
P представляет собой защитную группу;
с последующим восстановлением и обработкой кислотой с образованием соединения формулы IIID:
где
R2 представляет собой -RJ, -ORJ, -N(RJ)2, -NO2, галоген, -CN, -C1-4галогеналкил, -C1-4галогеналкокси, -C(О)N(RJ)2, -NRJC(О)RJ, -SORJ, -SO2RJ, -SO2N(RJ)2, -NRJSO2RJ, -CORJ, -СО2RJ, -NRJSO2N(RJ)2, -COCORJ;
RJ представляет собой водород или C1-6 алифатическую группу;
o представляет собой целое число от 0 до 3;
Hal представляет собой галогенид;
P представляет собой защитную группу; и
AӨ представляет собой анион;
c) нейтрализации соединения формулы IIID в присутствии основания с образованием соединения формулы IIID-a:
где
R2 представляет собой -RJ, -ORJ, -N(RJ)2, -NO2, галоген, -CN, -C1-4галогеналкил, -C1-4галогеналкокси, -C(О)N(RJ)2, -NRJC(О)RJ, -SORJ, -SO2RJ, -SO2N(RJ)2, -NRJSO2RJ, -CORJ, -СО2RJ, -NRJSO2N(RJ)2, -COCORJ;
RJ представляет собой водород или C1-6 алифатическую группу;
o представляет собой целое число от 0 до 3;
Hal представляет собой галогенид; и
P представляет собой защитную группу;
d) взаимодействия соединения формулы IIID в третьем органическом растворителе с соединением формулы IIIE:
где независимо для каждого случая
R3 представляет собой C1-6 алифатическую группу, необязательно замещенную OH, OP, -О-C1-6 алифатической группой, арилом, гетероарилом, -O-арилом или -O-гетероарилом;
в присутствии катализатора с образованием соединения формулы III:
где независимо для каждого случая
R2 представляет собой -RJ, -ORJ, -N(RJ)2, -NO2, галоген, -CN, -C1-4галогеналкил, -C1-4галогеналкокси, -C(О)N(RJ)2, -NRJC(О)RJ, -SORJ, -SO2RJ, -SO2N(RJ)2, -NRJSO2RJ, -CORJ, -СО2RJ, -NRJSO2N(RJ)2, -COCORJ;
RJ представляет собой водород или C1-6 алифатическую группу;
R3 представляет собой C1-6 алифатическую группу, необязательно замещенную OH, OP, -О-C1-6 алифатической группой, арилом, гетероарилом, -O-арилом или -O-гетероарилом;
P представляет собой защитную группу; и
o представляет собой целое число от 0 до 3;
e) взаимодействия соединения формулы III в четвертом органическом растворителе с соединением формулы II:
где независимо для каждого случая
кольцо А представляет собой конденсированное циклоалкильное, гетероциклоалкильное, арильное или гетероарильное кольцо;
Hal представляет собой галогенид;
R1 независимо выбран из -RJ, -ORJ, -N(RJ)2, -NО2, галогена, -CN, -C1-4галогеналкила, -C1-4галогеналкокси, -C(О)N(RJ)2, -NRJC(О)RJ, -SORJ, -SО2RJ, -SО2N(RJ)2, -NRJSO2RJ, -CORJ, -СО2RJ, -NRJSO2N(RJ)2, -COCORJ;
RJ представляет собой водород или C1-6 алифатическую группу;
m представляет собой целое число от 0 до 3 включительно; и
n представляет собой целое число от 1 до 4 включительно;
с образованием соединения формулы IV.
[0077] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где в формуле IV кольцо А выбрано из
В другом варианте воплощения в формуле IV кольцо А представляет собой
[0078] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где в формуле IV m имеет значение 0. В другом варианте воплощения в формуле IV n имеет значение 1. В другом варианте воплощения в формуле IV o имеет значение 1 и R2 представляет собой F.
[0079] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где в формуле IV P представляет собой бензил.
[0080] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где в формуле IV R3 представляет собой C4 алифатическую группу, необязательно замещенную группой OP. В другом варианте воплощения в формуле IV R3 представляет собой
В другом варианте воплощения в формуле IV R3 представляет собой
[0081] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где в формуле IV кольцо А представляет собой
m имеет значение 0, n имеет значение 1, o имеет значение 1 и R2 представляет собой F, P представляет собой бензил и R3 представляет собой
[0082] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где на стадии a) галогенирующий реагент представляет собой N-бромсукцинимид.
[0083] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где на стадии a) первый органический растворитель представляет собой апротонный растворитель. В другом варианте воплощения на стадии a) первый органический растворитель выбран из 1,2-диметоксиэтана, диоксана, ацетонитрила, толуола, бензола, ксилолов, метил-трет-бутилового эфира, метилэтилкетона, метилизобутилкетона, ацетона, N,N-диметилформамида, N,N-диметилацетамида, N-метилпирролидинона, этилацетата, дихлорметана или диметилсульфоксида. В другом варианте воплощения на стадии a) первый органический растворитель представляет собой этилацетат.
[0084] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где стадию а) осуществляют при температуре от около 2°C до 42°C. В другом варианте воплощения стадию а) осуществляют при температуре от около 12°C до 32°C. В другом варианте воплощения стадию а) осуществляют при температуре около 22°C.
[0085] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где в формуле IIIB o имеет значение 1, R2 представляет собой F, и Hal представляет собой Br.
[0086] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где в формуле IIIC P представляет собой бензил.
[0087] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где на стадии b) второй органический растворитель представляет собой апротонный растворитель. В другом варианте воплощения на стадии b) второй органический растворитель выбран из 1,2-диметоксиэтана, диоксана, ацетонитрила, толуола, бензола, ксилолов, метил-трет-бутилового эфира, метилэтилкетона, метилизобутилкетона, ацетона, N,N-диметилформамида, N,N-диметилацетамида, N-метилпирролидинона, этилацетата, дихлорметана или диметилсульфоксида. В другом варианте воплощения на стадии b) второй органический растворитель представляет собой толуол.
[0088] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где на стадии b) взаимодействие с соединением формулы IIIC происходит при температуре от около 60°C до 100°C. В другом варианте воплощения на стадии b) взаимодействие с соединением формулы IIIC происходит при температуре от около 70°C до 90°C. В другом варианте воплощения на стадии b) взаимодействие с соединением формулы IIIC происходит при температуре около 80°C.
[0089] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где на стадии b) восстановление осуществляют при помощи водорода.
[0090] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где на стадии b) кислота представляет собой пара-толуолсульфоновую кислоту.
[0091] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где в формуле IIID o имеет значение 1, R2 представляет собой F, Hal представляет собой Br, A- представляет собой Tos-, и P представляет собой бензил.
[0092] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где в формуле IIIE R3 представляет собой C(CH3)2CH2О(бензил).
[0093] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где на стадии c) основание представляет собой неорганическое основание.
[0094] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где на стадии c) основание представляет собой NaHСО3.
[0095] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где на стадии d) третий органический растворитель представляет собой апротонный растворитель. В другом варианте воплощения на стадии d) третий органический растворитель выбран из 1,2-диметоксиэтана, диоксана, ацетонитрила, толуола, бензола, ксилолов, метил-трет-бутилового эфира, метилэтилкетона, метилизобутилкетона, ацетона, N,N-диметилформамида, N,N-диметилацетамида, N-метилпирролидинона, этилацетата, дихлорметана или диметилсульфоксида. В другом варианте воплощения на стадии d) третий органический растворитель представляет собой ацетонитрил.
[0096] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где стадию d) осуществляют при температуре от около 60°C до 100°C. В другом варианте воплощения стадию d) осуществляют при температуре от около 70°C до 90°C. В другом варианте воплощения стадию d) осуществляют при температуре около 80°C.
[0097] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где на стадии d) катализатор представляет собой палладиевый катализатор. В другом варианте воплощения на стадии d) катализатор выбран из ацетата палладия(II), Pd(dppf)Cl2, Pd(dba)2, тетракис(трифенилфосфин)палладия(0) или трис(дибензилиденацетон)дипалладия(0). В другом варианте воплощения на стадии d) катализатор представляет собой ацетат палладия(II).
[0098] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где на стадии е) кольцо А представляет собой
m имеет значение 0, n имеет значение 1 и Hal представляет собой Cl.
[0099] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где на стадии e) четвертый органический растворитель представляет собой апротонный растворитель. В другом варианте воплощения на стадии e) четвертый органический растворитель выбран из 1,2-диметоксиэтана, диоксана, ацетонитрила, толуола, бензола, ксилолов, метил-трет-бутилового эфира, метилэтилкетона, метилизобутилкетона, ацетона, N,N-диметилформамида, N,N-диметилацетамида, N-метилпирролидинона, этилацетата, дихлорметана или диметилсульфоксида. В другом варианте воплощения на стадии e) четвертый органический растворитель представляет собой дихлорметан.
[00100] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где стадию е) осуществляют при температуре от около -20°C до 20°C. В другом варианте воплощения стадию е) осуществляют при температуре от около -10°C до 10°C. В другом варианте воплощения стадию е) осуществляют при температуре около 0°C.
[00101] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где на стадии e) соединение формулы II получают in situ путем галогенирования кислотного предшественника и подвергают взаимодействию с соединением формулы III без выделения.
[00102] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, дополнительно включающий удаление двух защитных групп из соединения формулы IV с образованием соединения формулы IVA:
[00103] В другом варианте воплощения защитные группы удаляют путем гидрирования.
[00104] В другом аспекте настоящее изобретение представляет собой способ получения соединения 1:
включающий стадии
a) взаимодействия соединения 2:
с бромирующим реагентом с образованием соединения 3:
b) взаимодействия соединения 3 с соединением 4:
с последующим восстановлением с образованием соединения 5:
с последующей нейтрализацией соединения 5 при помощи основания с получением соединения 5a:
c) взаимодействия соединения 5 с соединением 6:
в присутствии катализатора с образованием соединения 7:
d) взаимодействия соединения 7 с соединением 8:
с образованием соединения 9:
и
e) удаления двух Bn защитных групп с образованием соединения 1.
[00105] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где на стадии a) бромирующий агент представляет собой N-бромсукцинимид.
[00106] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где на стадии b) восстановление осуществляют при помощи водорода.
[00107] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где на стадии b) основание представляет собой неорганическое основание.
[00108] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где на стадии b) основание представляет собой NaHСО3.
[00109] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где на стадии c) катализатор представляет собой палладиевый катализатор. В другом варианте воплощения на стадии c) катализатор выбран из ацетата палладия(II), Pd(dppf)Cl2, Pd(dba)2, тетракис(трифенилфосфин)палладия(0) или трис(дибензилиденацетон)дипалладия(0). В другом варианте воплощения на стадии c) катализатор представляет собой ацетат палладия(II).
[00110] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где на стадии d) соединение 8 получают in situ путем галогенирования кислотного предшественника без выделения.
[00111] В другом варианте воплощения настоящее изобретение представляет вышеописанный способ, где на стадии e) Bn защитные группы удаляют путем гидрирования.
[00112] В другом аспекте настоящее изобретение представляет собой соединение формулы 23:
где
кольцо А представляет собой конденсированное циклоалкильное, гетероциклоалкильное, арильное или гетероарильное кольцо;
R1 независимо выбран из -RJ, -ORJ, -N(RJ)2, -NО2, галогена, -CN, -C1-4галогеналкила, -C1-4галогеналкокси, -C(О)N(RJ)2, -NRJC(О)RJ, -SORJ, -SО2RJ, -SО2N(RJ)2, -NRJSO2RJ, -CORJ, -СО2RJ, -NRJSO2N(RJ)2, -COCORJ;
RJ представляет собой водород или C1-6 алифатическую группу;
X представляет собой CN или СО2R;
R представляет собой С1-6 алифатическую группу или арил; и
m представляет собой целое число от 0 до 3 включительно.
[00113] В другом варианте воплощения настоящее изобретение представляет соединение формулы 23 и сопутствующие определения, где кольцо А представляет собой конденсированный гетероциклоалкил или гетероарил. В другом варианте воплощения кольцо А выбрано из
В другом варианте воплощения кольцо А представляет собой
[00114] В другом варианте воплощения настоящее изобретение представляет соединение формулы 23 и сопутствующие определения, где X представляет собой CN. В другом варианте воплощения X представляет собой СО2Et.
[00115] В другом варианте воплощения настоящее изобретение представляет соединение формулы 23 и сопутствующие определения, где m имеет значение 0.
[00116] В другом варианте воплощения настоящее изобретение представляет соединение формулы 23 и сопутствующие определения, где RJ представляет собой C1-6 алифатическую группу. В другом варианте воплощения RJ представляет собой -CH2CH3.
[00117] В другом аспекте настоящее изобретение представляет соединение
[00118] В другом аспекте настоящее изобретение представляет соединение
[00119] Способы получения соединений формул I, II, III и IV
[00120] Соединения формул I, II, II и IV могут быть получены при помощи способов, представленных на Схемах 1-3.
[00121] Схема 1. Соединения формул I и II
[00122] a = Pd(0) катализатор; b = кислота; c = основание; d = гидроксидное основание; e = кислота; f = галогенирующий агент;
[00123] где кольцо A, R1, m, X, RJ, Hal, q и n имеют значения, указанные выше.
[00124] На Схеме 1, арилгалогенид IA подвергают взаимодействию со сложным эфиром IB в присутствии катализатора на основе переходного металла в подходящем растворителе (например, толуоле) с получением сложного эфира IC. В сложных эфирах IB и IC, X может представлять собой либо CN, либо СО2R. Обработка соединения IC кислотой в подходящем растворителе (например, диметилсульфоксиде (DMSO)) дает соединение I. Взаимодействие соединения I с дигалогенидом IID в присутствии основания дает циклоалкилиден IIE. Гидролиз цианида или оставшейся сложноэфирной группы, в зависимости от особенностей группы X, дает карбоновую кислоту IIF, которую подвергают галогенированию с получением галогенангидрида II.
[00125] В одном варианте воплощения соединение IA является коммерчески доступным. В одном варианте воплощения кольцо А представляет собой 5-членное диоксильное кольцо. В одном варианте воплощения Hal в соединении IA представляет собой Br. В одном варианте воплощения взаимодействие соединений IA и IIB осуществляют в толуоле в присутствии Pd(0) катализатора, например, Pd(dba)2. В другом варианте воплощения взаимодействие осуществляют в присутствии алкилфосфина, например, t-Bu3P и фосфатной соли, например, Na3PО4. В другом варианте воплощения взаимодействие соединений IA и IIB осуществляют при температуре около 70°C. В другом варианте воплощения RJ представляет собой Et.
[00126] В одном варианте воплощения деэтерификацию соединения IC до соединения I осуществляют в неорганической кислоте. В другом варианте воплощения неорганическая кислота представляет собой HCl. Преобразование осуществляют в соответствующем апротонном растворителе (например, DMSO) при температуре около 75°C.
[00127] В одном варианте воплощения соединение I подвергают взаимодействию с NaOH и алкилдигалогенидом с получением циклоалкилидена в подходящем растворителе (например, MTBE). Этот способ можно адаптировать для нескольких спироциклических колец путем выбора соответствующего алкилдигалогенида. Например, спироциклическое бутановое кольцо может быть получено путем взаимодействия соединения I с, например, 1-бром-3-хлорпропаном. Было установлено, что смешанный бром- и хлордигалогенид лучше всего работает в экономическом масштабе, так как считается, что термодинамика взаимодействия является более благоприятной.
[00128] В одном варианте воплощения соединение IIE подвергают гидролизу до карбоновой кислоты IIF в присутствии воды и основания (например, NaOH) в подходящем растворителе (например, этаноле). Последующая обработка кислотой, такой как HCl, приводит к получению соединения IIF. В другом варианте воплощения соединение IIF обрабатывают путем его перекристаллизации из толуола.
[00129] В одном варианте воплощения галогенирующий агент, который преобразует соединение IIF в соединение II, представляет собой тионилхлорид. В другом варианте воплощения тионилхлорид добавляют к соединению IIF в толуоле при температуре около 60°C. В одном варианте воплощения эта стадия непосредственно продолжает связывание между соединением II и амином III (см. ниже), и ее осуществляют в том же реакционном сосуде.
[00130] Существует несколько неограничивающих преимуществ образования соединения II в соответствии со Схемой 1 и описанными выше и где-либо в заявке вариантами воплощения. Эти преимущества еще более очевидны при получении соединения II в экономическом масштабе и включают следующие. В целом реакция требует всего лишь 5 стадий, и это меньше, чем сообщалось ранее (т.е. исходя из арилкарбоновой кислоты, которую восстанавливают до метилового спирта, который преобразовывают в метилхлорид, который подвергают взаимодействию с NaCN). Этот путь синтеза вводит группу CN или сложноэфирную группу (т.е. X) без отдельной реакции хлорирования. Использование этанола в качестве со-растворителя в гидролизе соединения IIE до соединения IIF приводит в результате к однородной реакционной смеси, что упрощает отбор проб и контроль реакции. Перекристаллизация соединения IIF из толуола устраняет необходимость в формировании дициклогексиламиновой (DCA) соли, как сообщалось ранее.
[00131] Схема 2. Соединения формулы III.
[00132] a = галогенирующий агент; b = Zn(II) катализатор; c = H2, Pt; d = кислота; e = основание; f = Pd(II) катализатор;
[00133] где R2, o, Hal, AӨ и P определены выше.
[00134] В одном варианте воплощения в соединении IIIA R2 представляет собой F и находится в мета-положении относительно группы амина. В другом варианте воплощения соединение IIIA подвергают бромированию при помощи N-бромсукцинимида в подходящем растворителе (например, этилацетате) при температуре около 22°C.
[00135] В другом варианте воплощения соединение IIIB подвергают взаимодействию с эпоксидом IIIC, осуществляя реакцию раскрытия кольца с аминовой группой соединения IIIB с образованием соединения IIID. В одном варианте воплощения защитная группа P в соединении IIIC представляет собой бензил (Bn). В другом варианте воплощения эпоксид IIIC является хиральным. В одном варианте воплощения соединение IIIC представляет собой (R) соединение IIIC. В другом варианте воплощения соединение IIIC представляет собой (S) соединение IIIC. В одном варианте воплощения реакцию раскрытия цикла осуществляют в подходящем растворителе (например, толуоле) при температуре около 80°C. В другом варианте воплощения реакцию раскрытия кольца осуществляют в присутствии Zn(II) катализатора (например, Zn(ClО4)2). В другом варианте воплощения преобразование из соединения IIIB в соединение IIID включает реакцию раскрытия цикла с эпоксидом IIIC, с последующим гидрированием и затем обработкой кислотой с образованием соединения IIID. В другом варианте воплощения гидрирование осуществляют при помощи H2/Pt(S)/C. В другом варианте воплощения кислота представляет собой толуолсульфоновую кислоту, такую, где AӨ представляет собой тозилатный анион.
[00136] В другом варианте воплощения алкин IIIE подвергают реакции сочетания с соединением IIID в подходящем растворителе (например, ацетонитриле) при температуре около 80°C. В другом варианте воплощения реакцию сочетания осуществляют в присутствии катализатора Pd(II), такого как Pd(OAc)2. Первоначальная реакция не приводит к замыканию кольца, а только к замещению галогенида в IIID. Замыкание кольца осуществляют посредством реакции с другим катализатором Pd(II), таким как (MeCN)2PdCl2, в подходящем растворителе (например, ацетонитриле). В одном варианте воплощения замыкание кольца осуществляют при температуре от около 80°C. В одном варианте воплощения R3 в алкиновом соединении IIIE представляет собой -C(CH3)2CH2OBn. В одном варианте воплощения продукт реакции сочетания не выделяют, а осуществляют его поглощение в ацетонитрил и подвергают взаимодействию с (MeCN)2PdCl2.
[00137] Есть несколько неограничивающих преимуществ образования соединения III в соответствии со Схемой 2 и вариантами воплощения, описанными выше и в любом месте настоящей заявки. Эти преимущества еще более очевидны при получении соединения III в экономическом масштабе и включают следующие. Общее число стадий снижено по сравнению с тем, что было раскрыто ранее, всего до 3 стадий. Другие преимущества включают исключение хроматографии и образования побочных продуктов от защитных групп.
[00138] Схема 3. Соединения формулы IV
[00139] a = галогенирующий агент; b = апротонный растворитель;
[00140] где кольцо A, R1, m, n, hal, R2, o, P и R3 имеют значения, указанные выше.
[00141] Взаимодействие кислоты и основания между соединением II и соединением III в подходящем растворителе (например, дихлорметане (DCM)) дает защищенный аналог Соединения 1. В одном варианте воплощения галогенангидрид II получают из соединения IIF, как показано на Схеме 1, в том же реакционном сосуде, без выделения. В другом варианте воплощения реакцию между кислотой и основанием осуществляют в присутствии основания, такого как триэтиламин (TEA). В одном варианте воплощения количество TEA составляет 2 эквивалента относительно соединения II. В одном варианте воплощения после взаимодействия в течение 4 часов при температуре около 0°C и нагревания до комнатной температуры в течение ночи к смеси добавляют воду и перемешивают в течение дополнительных 30 минут. Органическую фазу отделяют и соединение IV выделяют отгонкой реакционного растворителя. В одном варианте воплощения соединение IV собирают при помощи фильтрации на диоксиде кремния.
[00142] В другом варианте воплощения соединения формулы IV можно подвергнуть процедуре удаления защиты с образованием соединения формулы IVa в соответствии со Схемой 4.
[00143] Схема 4. Удаление защиты у соединений формулы IV
[00144] a=H2/Pd/C;
[00145] где кольцо A, R1, m, n, R2, o, R3 и P определены выше.
[00146] В одном варианте воплощения давление водорода составляет 3 бар (3,059 кг/см2). В другом варианте воплощения скорость перемешивания в процессе гидрирования увеличивают до 800 оборотов в минуту. В другом варианте воплощения после того, как быстрое поглощение водорода становится менее интенсивным, сосуд для гидрирования нагревают до приблизительно 50°C в течение 2 дней. В другом варианте воплощения через 2 дня добавляют дополнительное количество катализатора и гидрирование продолжают еще в течение 4 дней. В другом варианте воплощения соединение IV растворяют в подходящем растворителе (например, THF).
[00147] В другом варианте воплощения Соединение 1 может быть получено путем сочетания группы галогенангидрида кислоты 7 с группой амина 8 с образованием соединения 9 с последующим удалением защиты в соответствии со Схемой 5.
[00148] Схема 5. Получение соединения 1
[00149] Где Соединение 7 получают в соответствии со Схемой 6.
[00150] Схема 6
[00151] Где соединение 8 получают в соответствии со Схемой 7.
[00152] Схема 7
[00153] Применения, композиция и введение
[00154] Фармацевтически приемлемые композиции
[00155] В другом аспекте настоящего изобретения обеспечиваются фармацевтически приемлемые композиции, при этом такие композиции включают соединение 1 форму A или аморфное соединение 1, описанное в настоящей заявке, и необязательно включают фармацевтически приемлемый носитель, адъювант или наполнитель. В некоторых вариантах воплощения эти композиции необязательно дополнительно включают одно или несколько дополнительных терапевтических средств.
[00156] Как описано выше, фармацевтически приемлемые композиции по настоящему изобретению дополнительно включают фармацевтически приемлемый носитель, адъювант или наполнитель, который, как используется в настоящей заявке, включает любой и все растворители, разбавители или другие жидкие наполнители, диспергирующие или суспендирующие вспомогательные вещества, поверхностно-активные вещества, изотонические вещества, загустители или эмульгаторы, консерванты, твердые связующие, смазывающие вещества и подобные, подходящие для конкретной лекарственной формы, которая является желательной. Remington's Pharmaceutical Sciences, Sixteenth Edition, E. W. Martin (Mack Publishing Co., Easton, Pa., 1980) раскрывает различные носители для использования в формулировании фармацевтически приемлемых композиций и известные способы их получения. За исключением только тех случаев, когда какая-либо среда, традиционно используемая в качестве носителя, несовместима с соединениями по настоящему изобретению, например, дает какой-либо нежелательный биологический эффект или иным образом вступает в нежелательное взаимодействие с каким-либо другим компонентом(ами) фармацевтически приемлемой композиции, ее использование предусматривается как охватываемое объемом настоящего изобретения. Некоторые примеры веществ, которые могут служить в качестве фармацевтически приемлемых носителей, включают, но не ограничиваются этим, ионообменники, оксид алюминия, стеарат алюминия, лецитин, белки сыворотки, такие как человеческий сывороточный альбумин, буферные вещества, такие как фосфаты, глицин, сорбиновая кислота или сорбат калия, смеси неполных глицеридов насыщенных растительных жирных кислот, воду, соли или электролиты, такие как протамин сульфат, вторичный кислый натрия гидрофосфат, гидрофосфат калия, хлорид натрия, цинковые соли, коллоидный диоксид кремния, трисиликат магния, поливинилпирролидон, полиакрилаты, воски, полиэтилен-полиоксипропиленовые блок-полимеры, ланолин, сахара, такие как лактоза, глюкоза и сахароза; крахмалы, такие как кукурузный крахмал и картофельный крахмал; целлюлозу и ее производные, такие как натрий-карбоксиметилцеллюлоза, этилцеллюлоза и ацетат целлюлозы; порошкообразный трагакант; солод; желатин; тальк; эксципиенты, такие как масло какао и воски для суппозиториев; масла, такие как арахисовое масло, масло семян хлопчатника; саффлоровое масло; кунжутное масло; оливковое масло; кукурузное масло и соевое масло; гликоли, такие как пропиленгликоль или полиэтиленгликоль; сложные эфиры, такие как этилолеат и этиллаурат; агар; буферные вещества, такие как гидроксид магния и гидроксид алюминия; альгиновую кислоту; апирогенную воду; изотонический солевой раствор; раствор Рингера; этиловый спирт и фосфатно-буферные растворы, а также другие нетоксичные совместимые смазывающие вещества, такие как лаурилсульфат натрия и стеарат магния, а также красители, агенты высвобождения, вещества покрытий, подсластители, отдушки и ароматизаторы, консерванты и антиоксиданты также могут присутствовать в композиции, в соответствии с решением специалиста, занимающегося формулированием композиций.
[00157] Применения соединений и фармацевтически приемлемые композиции
[00158] Еще в одном аспекте настоящее изобретение обеспечивает способ лечения состояния, заболевания или расстройства, связанного с CFTR. В некоторых вариантах воплощения настоящее изобретение обеспечивает способ лечения состояния, заболевания или расстройства, связанного с дефицитом CFTR активности, при этом такой способ включает введение композиции, включающей соединение 1, описанное в настоящей заявке, субъекту, предпочтительно млекопитающему, нуждающемуся в этом.
[00159] "CFTR-опосредованное заболевание", как используется в настоящей заявке, представляет собой заболевание, выбранное из таких как кистозный фиброз, астма, вызванное курением COPD, хронический бронхит, риносинусит, запор, панкреатит, недостаточность поджелудочной железы, мужское бесплодие, вызванное врожденным двусторонним отсутствием семявыводящих протоков (CBAVD), легочное заболевание средней тяжести, идиопатический панкреатит, аллергический бронхопульмонарный аспергиллез (ABPA), заболевание печени, наследственная эмфизема, наследственный гемохроматоз, дефициты коагуляции-фибринолиза, такие как дефицит белка C, наследственная ангиоэдема типа 1, дефициты липидного процессинга, такие как семейная гиперхолестеринемия, хиломикронемия типа 1, абеталипопротеинемия, болезни лизосомального накопления, такие как I-клеточное заболевание/псевдо-Hurler, мукополисахаридозы, болезнь Сандофа/Тея-Сакса, синдром Криглера-Найяра типа II, полиэндокринопатия/гиперинсулинемия, сахарный диабет, карликовость Ларона, дефицит милеопероксидазы, первичный гипопаратиреоидизм, меланома, гликаноз CDG типа 1, врожденный гипертиреоидизм, несовершенный остеогенез, наследственная гипофибриногенемия, дефицит ACT, несахарный диабет (DI), нейрофизеальный DI, нефрогенный DI, синдром Шарко-Мари Тута, болезнь Perlizaeus-Merzbacher, нейродегенеративные заболевания, такие как болезнь Альцгеймера, болезнь Паркинсона, амиотрофический боковой склероз, прогрессирующий супрануклеарный паралич, болезнь Пика, некоторые полиглутаминные неврологические расстройства, такие как болезнь Гентингтона, спинномозговая-мозжечковая атаксия типа I, спинальная и бульбарная мышечная атрофия, dentatorubal pallidoluysian и миотоническая дистрофия, а также спонгиформные энцефалопатии, такие как наследственная болезнь Крейтцфельдта-Якоба (из-за дефекта процессинга прионового белка), болезнь Фабри, синдром Страусслера-Шейнкера, COPD, болезнь сухих глаз или болезнь Шегрена, остеопороз, остеопения, заживление кости и рост кости (включая репарацию кости, регенерацию кости, уменьшение резорбции кости и увеличение отложения костной массы), синдром Горэма, хлоридные каналопатии, такие как врожденная миотония (формы Томсона и Бэккера), синдром Бартера типа III, болезнь Дента, гиперэксплексия, эпилепсия, гиперэксплексия, болезнь лизосомального накопления, синдром Ангельмана и первичная цилиарная дискинезия (PCD), термин для наследственных расстройств цилиарной структуры и/или функции, включая PCD с situs inversus (заболевание, известное также как синдром Картагенера), PCD без situs inversus и цилиарную аплазию. В другом варианте воплощения CFTR-опосредованное заболевание представляет собой кистозный фиброз, эмфизему, COPD или остеопороз. В другом варианте воплощения CFTR-опосредованное заболевание представляет собой кистозный фиброз.
[00160] В некоторых вариантах воплощения настоящее изобретение обеспечивает способ лечения CFTR-опосредованного заболевания у человека, включающий стадию введения указанному человеку эффективного количества композиции, включающей соединение 1, описанное в настоящей заявке.
[00161] В соответствии с настоящим изобретением, "эффективное количество" соединения 1 формы A или аморфного соединения 1, или фармацевтически приемлемой композиции такого соединения представляет собой такое количество, которое является эффективным для лечения или ослабления тяжести любого из заболеваний, перечисленных выше.
[00162] Соединение 1 или фармацевтически приемлемую композицию такого соединения можно вводить с использованием любого количества и любого пути введения, эффективного для лечения или ослабления тяжести одного или нескольких из заболеваний, перечисленных выше.
[00163] В некоторых вариантах воплощения соединение 1, описанное в настоящей заявке, или фармацевтически приемлемая композиция такого соединения являются полезными для лечения или ослабления тяжести кистозного фиброза у пациентов, которые демонстрируют остаточную CFTR активность в апикальной мембране респираторного и не респираторного эпителия. Присутствие остаточной CFTR активности на эпителиальной поверхности легко можно определить с использованием способов, известных из уровня техники, например, стандартных электрофизиологических, биохимических или гистохимических методов. Такие способы определяют CFTR активность с использованием in vivo или ex vivo электрофизиологических процедур, измерения концентраций Cl- в потовых или слюнных выделениях, или ex vivo биохимических или гистохимических процедур для контроля плотности клеточной поверхности. С использованием таких способов легко можно определить остаточную CFTR активность у пациентов гетерозиготных или гомозиготных в отношении множества различных мутаций, включая пациентов гомозиготных или гетерозиготных в отношении наиболее распространенной мутации ΔF508.
[00164] В одном варианте воплощения соединение 1, описанное в настоящей заявке, или фармацевтически приемлемая композиция такого соединения являются полезными для лечения или ослабления тяжести кистозного фиброза у пациентов в рамках определенных генотипов, демонстрирующих остаточную CFTR активность, например, класс III мутаций (нарушенная регуляция или воротный механизм), класс IV мутаций (изменение проводимости) или класс V мутаций (уменьшенный синтез) (Lee R. Choo-Kang, Pamela L., Zeitlin, Type I, II, III, IV and V cystic fibrosis Tansmembrane Conductance Regulator Defects and Opportunities of Therapy; Current Opinion in Pulmonary Medicine 6:521-529, 2000). Другие генотипы пациентов, которые демонстрируют остаточную CFTR активность, включают пациентов, гомозиготных в отношении одного из этих классов или гетерозиготных в отношении любого другого класса мутаций, включая класс I мутаций, класс II мутаций или мутацию, которая не классифицирована.
[00165] В одном варианте воплощения соединение 1, описанное в настоящей заявке, или фармацевтически приемлемая композиция такого соединения являются полезными для лечения или ослабления тяжести кистозного фиброза у пациентов в рамках определенных клинических фенотипов, например, от умеренно до слабовыраженного клинического фенотипа, который типично коррелирует с количеством остаточной CFTR активности в апикальной мембране эпителия. Такие фенотипы включают пациентов, демонстрирующих панкреатическую недостаточность, или пациентов, у которых диагностирован идиопатический панкреатит и врожденное двустороннее отсутствие семявыводящих протоков или легочное заболевание умеренной тяжести.
[00166] Точное необходимое количество будет изменяться от субъекта к субъекту, в зависимости от видов, возраста и общего состояния субъекта, тяжести инфекции, конкретного используемого средства, способа его введения и подобных факторов. Соединения по настоящему изобретению предпочтительно формулируют в стандартную лекарственную форму для простоты введения и равномерного дозирования. Выражение "стандартная лекарственная форма", как оно используется в настоящей заявке, относится физически дискретной единице средства, подходящей для пациента, подлежащего лечению. Однако должно быть понятно, что общее суточное количество соединений и композиций по настоящему изобретению определяет лечащий врач согласно взвешенной медицинской оценке. Конкретный эффективный уровень доз для любого конкретного пациента или организма зависит от различных факторов, включая расстройство, подлежащее лечению, и тяжесть этого расстройства; активность конкретного используемого соединения; конкретную используемую композицию; возраст, массу тела, общее состояние здоровья, пол и режим питания пациента; время введения, путь введения и скорость выведения из организма конкретного используемого соединения; продолжительность лечения; лекарственные средства, используемые в комбинации или одновременно с конкретным используемым соединением, и подобные факторы, хорошо известные в медицине. Термин "пациент" или "субъект", как он используется в настоящей заявке, означает животное, предпочтительно млекопитающее, и наиболее предпочтительно человека.
[00167] Фармацевтически приемлемые композиции по настоящему изобретению можно вводить человеку и другим животным перорально, ректально, парентерально, интрацистернально, интравагинально, внутрибрюшинно, местно (в виде порошков, мазей или капель), буккально, в виде перорального или назального спрея или т.п., в зависимости от тяжести инфекции, подлежащей лечению. В некоторых вариантах воплощения соединения по настоящему изобретению можно вводить перорально или парентерально при уровне доз от около 0,01 мг/кг до около 50 мг/кг, и предпочтительно от около 1 мг/кг до около 25 мг/кг массы тела субъекта в день, один или несколько раз в день, для получения желательного терапевтического эффекта.
[00168] В некоторых вариантах воплощения дозируемое количество соединения 1 в стандартной лекарственной форме составляет от 100 мг до 1000 мг. В другом варианте воплощения дозируемое количество соединения 1 составляет от 200 мг до 900 мг. В другом варианте воплощения дозируемое количество соединения 1 составляет от 300 мг до 800 мг. В другом варианте воплощения дозируемое количество соединения 1 составляет от 400 мг до 700 мг. В другом варианте воплощения дозируемое количество соединения 1 составляет от 500 мг до 600 мг.
[00169] Препараты для инъекций, например стерильные водные или масляные суспензии для инъекций, можно сформулировать в соответствии с известными из уровня техники способами, с использованием подходящих диспергирующих или смачивающих веществ и суспендирующих веществ. Стерильный препарат для инъекций также может представлять собой стерильный раствор, суспензию или эмульсию для инъекций в нетоксичном парентерально приемлемом разбавителе или растворителе, например, в виде раствора в 1,3-бутандиоле. Из приемлемых наполнителей и растворителей, которые можно использовать, можно указать воду, раствор Рингера, U.S.P. и изотонический раствор хлорида натрия. Кроме того, традиционно используют стерильные нелетучие масла в качестве растворителя или среды для суспендирования. Для этих целей можно использовать любое светлое нелетучее масло, включая синтетические моно- или диглицериды. Кроме того, жирные кислоты, такие как олеиновая кислота, используют для получения препаратов для инъекций.
[00170] Композиции для инъекций можно стерилизовать, например, путем фильтрования через удерживающий бактерии фильтр или путем включения стерилизующих средств в форме стерильных твердых композиций, которые можно растворять или диспергировать в стерильной воде или другой стерильной среде для инъекций перед применением.
[00171] Композиции для ректального или вагинального введения предпочтительно представляют собой суппозитории, которые можно получить путем смешивания соединения по настоящему изобретению с подходящими нераздражающими эксципиентами или носителями, такими как масло какао, полиэтиленгликоль или воск для суппозиториев, которые являются твердыми при температуре окружающей среды, но жидкими при температуре тела и поэтому плавятся в прямой кишке или вагинальной полости и высвобождают активное соединение.
[00172] Твердые лекарственные формы для перорального введения включают капсулы, таблетки, пилюли, порошки и гранулы. В таких твердых лекарственных формах активное соединение смешивают с по меньшей мере одним инертным, фармацевтически приемлемым эксципиентом или носителем, таким как цитрат натрия или дикальцийфосфат, и/или a) наполнителями или объемными веществами, такими как крахмалы, лактоза, сахароза, глюкоза, маннит и кремневая кислота, b) связующими, такими как, например, карбоксиметилцеллюлоза, альгинаты, желатин, поливинилпирролидинон, сахароза и аравийская камедь, c) увлажнителями, такими как глицерин, d) разрыхлителями, такими как агар-агар, карбонат кальция, картофельный или тапиоковый крахмал, альгиновая кислота, некоторые силикаты и карбонат натрия, e) замедляющими растворение веществами, такими как парафин, f) ускорителями вбсорбции, такими как четвертичные аммониевые соединения, g) смачивающими веществами, такими как, например, цетиловый спирт и глицеринмоностеарат, h) абсорбентами, такими как каолин и бентонитовая глина, и i) смазывающими веществами, такими как тальк, стеарат кальция, стеарат магния, твердые полиэтиленгликоли, лаурилсульфат натрия, и смесями таких веществ. В случае капсул, таблеток и пилюль лекарственная форма также может включать буферные вещества.
[00173] Твердые композиции подобного типа также можно использовать в качестве наполнителей в мягких и твердых заполняемых желатиновых капсулах с использованием таких эксципиентов, как лактоза или молочный сахар, а также высокомолекулярные полиэтиленгликоли и подобные. Такие твердые лекарственные формы, как таблетки, драже, капсулы, пилюли и гранулы, можно получить с покрытиями и оболочками, такими как энтеросолюбильные покрытия и другие покрытия, хорошо известные в области фармацевтического формулирования. Они, необязательно, могут содержать вещества, делающие композицию непрозрачной, и также могут иметь такую композицию, чтобы они высвобождали активный ингредиент(ы) только или преимущественно в определенной части пищеварительного тракта, необязательно замедленным образом. Примеры композиций оболочек, которые можно использовать, включают полимерные вещества и воски. Твердые композиции подобного типа также можно использовать в качестве наполнителей в мягких и твердых заполняемых желатиновых капсулах с использованием таких эксципиентов, как лактоза или молочный сахар, а также высокомолекулярные полиэтиленгликоли и подобные.
[00174] Активные соединения также могут быть в микроинкапсулированной форме с одним или несколькими эксципиентами, указанными выше. Такие твердые лекарственные формы, как таблетки, драже, капсулы, пилюли и гранулы, можно получить с покрытиями и оболочками, такими как энтеросолюбильные покрытия, контролирующие высвобождение покрытия и другие покрытия, хорошо известные в области фармацевтического формулирования. В таких твердых лекарственных формах активное соединение может быть смешано с по меньшей мере одним инертным разбавителем, таким как сахароза, лактоза или крахмал. Такие лекарственные формы также могут включать, как это имеет место в обычной практике, дополнительные вещества, отличные от инертных разбавителей, например, смазывающие вещества для таблетирования и другие вспомогательные вещества для таблетирования, такие как стеарат магния и микрокристаллическая целлюлоза. В случае капсул, таблеток и пилюль лекарственные формы также могут включать буферные вещества. Они, необязательно, могут содержать вещества, делающие композицию непрозрачной, и также могут иметь такую композицию, чтобы они высвобождали активный ингредиент(ы) только или преимущественно в определенной части пищеварительного тракта, необязательно замедленным образом. Примеры композиций оболочек, которые можно использовать, включают полимерные вещества и воски.
[00175] Также предусматривается, что соединение 1, описанное в настоящей заявке, или фармацевтически приемлемую композицию такого соединения можно использовать в комбинированных терапиях, т.е. соединение 1 можно вводить одновременно с, до или после одного или нескольких других желательных терапевтических средств или медицинских процедур. Конкретная комбинация терапий (терапевтических средств или процедур) для использования в комбинированной схеме лечения должна учитывать совместимость желательных терапевтических средств и/или процедур и желательный для достижения терапевтический эффект. Также должно быть понятно, что применяемые терапии могут достигать желательного эффекта для того же самого расстройства (например, соединение по настоящему изобретению можно вводить одновременно с другим средством, используемым для лечения того же самого расстройства), или они могут достигать разных эффектов (например, контроль каких-либо побочных эффектов). Как используется в настоящей заявке, дополнительные терапевтические средства, которые обычно вводят для лечения или профилактики конкретного заболевания или состояния, известны как "подходящие при заболевании или состоянии, подлежащем лечению".
[00176] В одном варианте воплощения дополнительное средство выбрано из муколитического средства, бронходилататора, антибиотика, противоинфекционного средства, противовоспалительного средства, модулятора CFTR, отличного от соединения по настоящему изобретению, или питательного вещества.
[00177] В одном варианте воплощения дополнительное терапевтическое средство представляет собой антибиотик. Примеры антибиотиков, полезных в настоящем изобретении, включают тобрамицин, включая тобрамицин в форме порошка для ингаляций (TIP), азитромицин, азтреонам, включая аэрозольные формы азтреонама, амикацин, включая липосомные композиции такого средства, ципрофлоксацин, включая его композиции, подходящие для введения путем ингаляции, левофлаксацин, включая его аэрозольные композиции, и комбинации двух антибиотиков, например, фосфомицина и тобрамицина.
[00178] В другом варианте воплощения дополнительное средство представляет собой муколитическое средство. Примеры муколитических средств, полезных в настоящем изобретении, включают Pulmozyme®.
[00179] В другом варианте воплощения дополнительное средство представляет собой бронходилататор.
Примеры бронходилататоров включают альбутерол, метапротенерол сульфат, пирбутерол ацетат, салметерол или тетрабулин сульфат.
[00180] В другом варианте воплощения дополнительное средство является эффективным для восстановления поверхностной жидкости в дыхательных путях и легких. Такие средства улучшают перемещение соли в клетки и из клеток, делая слизь в дыхательных путях и легких более гидратированной, и поэтому их очищение происходит гораздо легче. Примеры таких средств включают гипертонический солевой раствор, денуфосол тетранатрий ([[(3S, 5R)-5-(4-амино-2-оксопиримидин-1-ил)-3-гидроксиоксолан-2-ил]метокси-гидроксифосфорил] [[[(2R,3S,4R,5R)-5-(2,4-диоксопиримидин-1-ил)-3,4-дигидроксиоксолан-2-ил]метокси-гидроксифосфорил]окси-гидроксифосфорил]гидрофосфат) или бронхитол (предназначенная для ингаляций композиция маннита).
[00181] В другом варианте воплощения дополнительное средство представляет собой противовоспалительное средство, т.е. средство, которое снижает воспаление в легких. Примеры таких средств, полезных в настоящем изобретении, включают ибупрофен, докозагексановую кислоту (DHA), силденафил, глутатион для ингаляций, пиоглитазон, гидроксихлорохин или симвастатин.
[00182] В другом варианте воплощения дополнительное средство представляет собой модулятор CFTR, отличный от соединения 1, т.е. средство, которое обладает эффектом модуляции CFTR активности. Примеры таких средств включают аталурен ("PTC 124®"; 3-[5-(2-фторфенил)-l,2,4-оксадиазол-3-ил]бензойная кислота), синапултид, ланковутид, депелестат (ингибитор человеческой рекомбинантной нейтрофил-эластазы), кобипростон (7-{(2R,4aR,5R,7aR)-2-[(3S)-1,1-дифтор-3-метилпентил]-2-гидрокси-6-оксооктагидроциклопента[b]пиран-5-ил}гептановая кислота) и N-(5-гидрокси-2,4-дитрет-бутилфенил)-4-оксо-1H-хинолин-3-карбоксамид.
[00183] В другом варианте воплощения дополнительное средство представляет собой питательное вещество. Примеры питательных веществ включают панкрелипазу (заменитель панкреатических ферментов), включая Pancrease®, Pancrecarb®, Ultrase® или Creon®, Liprotomase® (прежнее торговое наименование Trizytek®), Aquadeks® или глутатион для ингаляций. В одном варианте воплощения дополнительное питательное вещество представляет собой панкрелипазу.
[00184] В другом варианте воплощения дополнительное средство представляет собой соединение, выбранное из гентамицина, куркумина, циклофосфамида, 4-фенилбутирата, миглустата, фелодипина, нимодипина, Филоксина B, гениестейна, Апигенина, модуляторов cAMP/cGMP, таких как ролипрам, силденафил, милринон, тадалафил, амринон, изопротеренол, албутерол и алметерол, дезоксиспергуалина, ингибиторов HSP 90, ингибиторов HSP 70, ингибиторов протеосомы, таких как эпоксомицин, лактацистин, и т.п.
[00185] В другом варианте воплощения дополнительное средство представляет собой соединение, раскрытое в WO 2004028480, WO 2004110352, WO 2005094374, WO 2005120497 или WO 2006101740.
[00186] В другом варианте воплощения дополнительное средство представляет собой производное бензо(c)хинолизиния, которое демонстрирует CFTR-модулирующую активность, или бензопирановое производное, которое демонстрирует CFTR-модулирующую активность.
[00187] В другом варианте воплощения дополнительное средство представляет собой соединение, раскрытое в US7202262, US6992096, US20060148864, US20060148863, US20060035943, US20050164973, WO2006110483, WO2006044456, WO2006044682, WO2006044505, WO2006044503, WO2006044502 или WO2004091502.
[00188] В другом варианте воплощения дополнительное средство представляет собой соединение, раскрытое в WO2004080972, WO2004111014, WO2005035514, WO2005049018, WO2006099256, WO2006127588 или WO2007044560.
[00189] Эти комбинации являются полезными для лечения заболеваний, описанных в настоящей заявке, включая кистозный фиброз. Эти комбинации также являются полезными в наборах, описанных в настоящей заявке.
[00190] Количество дополнительного терапевтического средства, присутствующего в композициях по настоящему изобретению, не должно превышать обычно предназначенное для введения количество в композиции, включающей такое терапевтическое средство в качестве единственного активного вещества. Предпочтительно, количество дополнительного терапевтического средства в композициях, раскрытых в настоящем изобретении, находится в пределах от приблизительно 50% до 100% от количества, обычно присутствующего в композиции, включающей такое средство в качестве единственного терапевтически активного вещества.
[00191] Чтобы лучше понять изобретение, описанное в настоящей заявке, далее представлены следующие примеры. Должно быть понятно, что эти примеры предназначены исключительно для иллюстративных целей, и их не следует рассматривать как каким-либо образом ограничивающие настоящее изобретение.
ПРИМЕРЫ
[00192] Методы и Материалы
[00193] Vitride® (натрий бис(2-метоксиэтокси)алюминий гидрид [или NaAlH2(OCH2CH2OCFl3)2], 65% масс. раствор в толуоле) закупали у компании Aldrich Chemicals. 3-Фтор-4-нитроанилин закупали у компании Capot Chemicals. 5-Бром-2,2-дифтор-1,3-бензодиоксол закупали у компании Alfa Aesar. 2,2-Дифтор-1,3-бензодиоксол-5-карбоновую кислоту закупали у компании Saltigo (филиал компании Lanxess Corporation).
[00194] В любом разделе настоящей заявке, в случае, если название соединения неправильно описывает структуру этого соединения, структура отменяет это название и имеет преимущество.
[00195] Синтез соединения 1
[00196] Кислотная группа
[00197] Синтез (2,2-дифтор-l,3-бензодиоксол-5-ил)-1-этилацетат-ацетонитрила
[00198] Реактор продували азотом и загружали 900 мл толуола. Растворитель дегазировали путем барботирования азотом в течение не менее 16 часов. В реактор затем загружали Na3PО4 (155,7 г, 949,5 ммоль), с последующим добавлением бис(дибензилиденацетон) палладия(0) (7,28 г, 12,66 ммоль). Загружали 10% масс./масс. раствор трет-бутилфосфина в гексанах (51,23 г, 25,32 ммоль) в течение 10 минут при 23°C через продутую азотом капельную воронку. Смесь оставляли для перемешивания в течение 50 минут, и затем добавляли 5-бром-2,2-дифтор-1,3-бензодиоксол (75 г, 316,5 ммоль) в течение 1 минуты. После перемешивания еще в течение 50 минут в смесь загружали этилцианоацетат (71,6 г, 633,0 ммоль) в течение 5 минут с последующим добавлением воды (4,5 мл) одной порцией. Смесь нагревали до 70°C в течение 40 минут и анализировали методом ВЭЖХ каждые 1-2 часа для определения, произошло или нет преобразование участвующих в реакции веществ в продукт. После завершения преобразования (типично 100% конверсия через 5-8 часов) смесь охлаждали до 20-25°C и фильтровали через слой целита. Слой целита промывали толуолом (2×450 мл) и объединенные органические слои концентрировали до 300 мл в условиях вакуума при 60-65°C. К концентрату добавляли 225 мл DMSO и концентрировали в условиях вакуума при 70-80°C вплоть до прекращения активной отгонки растворителя. Раствор охлаждали до 20-25°C и разбавляли до 900 мл при помощи DMSO для подготовки для стадии 2. 1H ЯМР (500 MГц, CDCl3) δ 7,16-7,10 (м, 2H), 7,03 (д, J=8,2 Гц, 1H), 4,63 (с, 1H), 4,19 (м, 2H), 1,23 (т, J=7,1 Гц, 3H).
[00199] Синтез (2,2-дифтор-1,3-бензодиоксол-5-ил)ацетонитрила
[00200] В DMSO раствор (2,2-дифтор-1,3-бензодиоксол-5-ил)-1-этилацетат-ацетонитрила с предыдущей стадии загружали 3 н раствор HCl (617,3 мл, 1,85 моль) в течение 20 минут, поддерживая при этом внутреннюю температуру <40°C. Смесь затем нагревали до 75°C в течение 1 часа и анализировали методом ВЭЖХ каждые 1-2 часа для определения % конверсии. Когда наблюдали конверсию >99% (типично через 5-6 часов), реакционную смесь охлаждали до 20-25°C и экстрагировали при помощи MTBE (2×525 мл), при достаточном времени, обеспечивающем полное фазовое разделение в процессе экстракций. Объединенные органические экстракты промывали при помощи 5% NaCl (2×375 мл). Раствор затем переносили в оборудование, подходящее для 1,5-2,5 торр вакуумной дистилляции, снабженное охлажденной приемной колбой. Раствор концентрировали в условиях вакуума при <60°C для удаления растворителей. (2,2-Дифтор-1,3-бензодиоксол-5-ил)ацетонитрил затем отгоняли из полученного масла при 125-130°C (температура печи) и 1,5-2,0 тор. (2,2-Дифтор-1,3-бензодиоксол-5-ил)ацетонитрил выделяли в виде прозрачного масла с выходом 66% из 5-бром-2,2-дифтор-1,3-бензодиоксола (2 стадии) и с ВЭЖХ чистотой 91,5% AUC (соответствует масс./масс. анализу 95%). 1H ЯМР (500 MГц, ДМСО) δ 7,44 (уш.с, 1H), 7,43 (д, J=8,4 Гц, 1H), 7,22 (дд, J=8,2, 1,8 Гц, 1H), 4,07 (с, 2H).
[00201] Синтез (2,2-дифтор-1,3-бензодиоксол-5-ил)циклопропанкарбонитрила
[00202] Исходный раствор 50% масс./масс. NaOH дегазировали путем барботирования азотом в течение не менее 16 часов. Аналогичным образом дегазировали соответствующее количество MTBE в течение нескольких часов. В реактор после продувки азотом загружали дегазированный MTBE (143 мл) с последующим добавлением (2,2-дифтор-1,3-бензодиоксол-5-ил)ацетонитрила (40,95 г, 207,7 ммоль) и тетрабутиламмонийбромида (2,25 г, 10,38 ммоль). Объем смеси регистрировали и смесь дегазировали путем барботирования азотом в течение 30 минут. Достаточно дегазированный MTBE загружали для возвращения смеси к исходному объему, отмеченному до дегазирования. К перемешиваемой смеси при 23,0°C добавляли дегазированный 50% масс./масс. NaOH (143 мл) в течение 10 минут с последующим добавлением 1-бром-2-хлорэтана (44,7 г, 311,6 ммоль) в течение 30 минут. Реакционную смесь анализировали методом ВЭЖХ с 1-часовыми интервалами для определения % конверсии. Перед отбором проб перемешивание останавливали, чтобы произошло разделение фаз. Из верхней органической фазы отбирали пробы для анализа. Когда наблюдали % конверсии >99% (типично через 2,5-3 часа), реакционную смесь охлаждали до 10°C и добавляли воду (461 мл) с такой скоростью, чтобы поддерживать температуру <25°C. Температуру регулировали на уровне 20-25°C и фазы разделяли. Примечание: для полного фазового разделения необходимо достаточное количество времени. Водную фазу экстрагировали при помощи MTBE (123 мл) и объединенную органическую фазу промывали 1 н раствором HCl (163 мл) и 5% раствором NaCl (163 мл). Раствор (2,2-дифтор-1,3-бензодиоксол-5-ил)циклопропанкарбонитрила в MTBE концентрировали до 164 мл в условиях вакуума при 40-50°C. В раствор загружали этанол (256 мл) и снова концентрировали до 164 мл в условиях вакуума при 50-60°C. Загружали этанол (256 мл) и смесь концентрировали до 164 мл в условиях вакуума при 50-60°C. Полученную смесь охлаждали до 20-25°C и разбавляли этанолом до 266 мл для подготовки для следующей стадии. 1H ЯМР (500 MГц, ДМСО) δ 7,43 (д, J=8,4 Гц, 1H), 7,40 (д, J=1,9 Гц, 1H), 7,30 (дд, J=8,4, 1,9 Гц, 1H), 1,75 (м, 2H), 1,53 (м, 2H).
[00203] Синтез 1-(2,2-дифтор-1,3-бензодиоксол-5-ил)циклопропанкарбоновой кислоты
[00204] В раствор (2,2-дифтор-1,3-бензодиоксол-5-ил)циклопропанкарбонитрила в этаноле с предыдущей стадии загружали 6 н раствор NaOH (277 мл) в течение 20 минут и нагревали до внутренней температуры 77-78°C в течение 45 минут. Развитие реакции отслеживали методом ВЭЖХ через 16 часов. Примечание: контролировали поглощение как (2,2-дифтор-1,3-бензодиоксол-5-ил)циклопропанкарбонитрила, так и первичного амида, являющегося результатом частичного гидролиза (2,2-дифтор-1,3-бензодиоксол-5-ил)циклопропанкарбонитрила. Когда наблюдали % конверсии >99% (типично 100% конверсия через 16 часов), реакционную смесь охлаждали до 25°C и загружали этанол (41 мл) и DCM (164 мл). Раствор охлаждали до 10°C и загружали 6 н раствор HCl (290 мл) с такой скоростью, чтобы поддерживать температуру <25°C. После нагревания до 20-25°C фазы разделяли. Нижнюю органическую фазу собирали, и верхнюю водную фазу обратно экстрагировали в DCM (164 мл). Примечание: водная фаза была несколько мутной до и после экстракции из-за высокой концентрации неорганических солей. Органические слои объединяли и концентрировали в условиях вакуума до 164 мл. Добавляли толуол (328 мл) и смесь конденсировали до 164 мл при 70-75°C. Смесь охлаждали до 45°C, загружали MTBE (364 мл) и перемешивали при 60°C в течение 20 минут. Раствор охлаждали до 25°C и осветляли фильтрованием, удаляя остаточные неорганические соли. MTBE (123 мл) использовали для промывки реактора и собранных твердых частиц. Объединенные органические слои переносили в чистый реактор для подготовки для следующей стадии.
[00205] Выделение 1-(2,2-дифтор-1,3-бензодиоксол-5-ил)циклопропанкарбоновой кислоты
[00206] Раствор 1-(2,2-дифтор-1,3-бензодиоксол-5-ил)циклопропанкарбоновой кислоты с предыдущей стадии концентрировали в условиях вакуума до 164 мл, загружали толуол (328 мл) и концентрировали до 164 мл при 70-75°C. Смесь затем нагревали до 100-105°C с получением гомогенного раствора. После перемешивания при этой температуре в течение 30 минут раствор охлаждали до 5°C в течение 2 часов и поддерживали при 5°C в течение 3 часов. Смесь затем фильтровали и реактор и собранное твердое вещество промывали охлажденной смесью 1:1 толуол/н-гептан (2×123 мл). Вещество сушили в условиях вакуума при 55°C в течение 17 часов с получением 1-(2,2-дифтор-1,3-бензодиоксол-5-ил)циклопропанкарбоновой кислоты в виде не совсем белого кристаллического твердого вещества. 1-(2,2-дифтор-1,3-бензодиоксол-5-ил)циклопропанкарбоновую кислоту выделяли с выходом 79% из (2,2-дифтор-1,3-бензодиоксол-5-ил)ацетонитрила (3 стадии, включая выделение) и с ВЭЖХ чистотой 99,0% AUC. ESI-MS m/z рассчитано 242,04, найдено 241,58 (M+1)+; 1H ЯМР (500 MГц, ДМСО) δ 12,40 (с, 1H), 7,40 (д, J=1,6 Гц, 1H), 7,30 (д, J=8,3 Гц, 1H), 7,17 (дд, J=8,3, 1,7 Гц, 1H), 1,46 (м, 2H), 1,17 (м, 2H).
[00207] Альтернативный синтез кислотной группы
[00208] Синтез (2,2-дифтор-1,3-бензодиоксол-5-ил)метанола
[00209] Коммерчески доступную 2,2-дифтор-1,3-бензодиоксол-5-карбоновую кислоту (1,0 экв.) суспендировали в толуоле (10 об.). Vitride® (2 экв.) добавляли через капельную воронку с такой скоростью, чтобы поддерживать температуру при 15-25°C. По окончании добавления температуру повышали до 40°C в течение 2 часов, затем 10% (масс./масс.) водный раствор NaOH (4,0 экв.) осторожно добавляли через капельную воронку, поддерживая температуру при 40-50°C. После перемешивания еще в течение 30 минут слоям давали разделиться при 40°C. Органическую фазу охлаждали до 20°C, затем промывали водой (2×1,5 об.), сушили (Na2SO4), фильтровали и концентрировали с получением неочищенного (2,2-дифтор-1,3-бензодиоксол-5-ил)метанола, который использовали непосредственно на следующей стадии.
[00210] Синтез 5-хлорметил-2,2-дифтор-1,3-бензодиоксола
[00211] (2,2-дифтор-1,3-бензодиоксол-5-ил)метанол (1,0 экв.) растворяли в MTBE (5 об.). Добавляли каталитическое количество DMAP (1% моль) и добавляли SOCl2 (1,2 экв.) через капельную воронку. SOCl2 добавляли с такой скоростью, чтобы поддерживать температуру в реакторе при 15-25°C. Температуру повышали до 30°C в течение 1 часа, затем охлаждали до 20°C, затем добавляли воду (4 об.) через капельную воронку, поддерживая температуру ниже 30°C. После перемешивания еще в течение 30 минут слоям давали разделиться. Органический слой перемешивали и добавляли 10% (масс./об.) водный раствор NaOH (4,4 об.). После перемешивания в течение 15-20 минут, слоям давали разделиться. Органическую фазу затем сушили (Na2SO4), фильтровали и концентрировали с получением неочищенного 5-хлорметил-2,2-дифтор-1,3-бензодиоксола, который использовали непосредственно на следующей стадии.
[00212] Синтез (2,2-дифтор-1,3-бензодиоксол-5-ил)ацетонитрила
[00213] Раствор 5-хлорметил-2,2-дифтор-1,3-бензодиоксола (1 экв.) в DMSO (ДМСО) (1,25 об.) добавляли к суспензии NaCN (1,4 экв.) в DMSO (3 об.), поддерживая температуру в пределах 30-40°C. Смесь перемешивали в течение 1 часа, затем добавляли воду (6 об.) с последующим добавлением MTBE (4 об.). После перемешивания в течение 30 минут слои разделяли. Водный слой экстрагировали при помощи MTBE (1,8 об.). Объединенные органические слои промывали водой (1,8 об.), сушили (Na2SO4), фильтровали и концентрировали с получением неочищенного (2,2-дифтор-1,3-бензодиоксол-5-ил)ацетонитрила (95%), который использовали непосредственно на следующей стадии.
[00214] Остальные стадии такие же, как описано выше для синтеза кислотной группы.
[00215] Группа амина
[00216] Синтез 2-бром-5-фтор-4-нитроанилина
В колбу загружали 3-фтор-4-нитроанилин (1,0 экв.) с последующим добавлением этилацетата (10 об.) и перемешивали для растворения всех твердых частиц. Добавляли N-бромсукцинимид (1,0 экв.) по порциям так, чтобы поддерживать внутреннюю температуру 22°C. После завершения реакции реакционную смесь концентрировали в вакууме на роторном испарителе. Остаток суспендировали в дистиллированной воде (5 об.) для растворения и удаления сукцинимида. (Сукцинимид также можно удалить с использованием процедуры обработки водой). Воду декантировали и твердое вещество суспендировали в 2-пропаноле (5 об.) в течение ночи. Полученную суспензию фильтровали и мокрую лепешку промывали 2-пропанолом, сушили в вакуумной печи при 50°C в течение ночи под потоком N2 до достижения постоянной массы. Выделяли желтовато-коричневое твердое вещество (50% выход, 97,5% AUC). Другие примеси представляли собой бром-региоизомер (1,4% AUC) и ди-бром аддукт (1,1% AUC). 1H ЯМР (500 MГц, ДМСО) δ 8,19 (1H, д, J=8,1 Гц), 7,06 (уш. с, 2H), 6,64 (д, 1H, J=14,3 Гц).
[00217] Синтез соли п-толуолсульфоновой кислоты и (R)-1-((4-амино-2-бром-5-фторфенил)амино)-3-(бензилокси)пропан-2-ола
[00218] В тщательно высушенную колбу под потоком N2 загружали следующие вещества: активированные порошкообразные 4Ǻ молекулярные сита (50% масс. в расчете на 2-бром-5-фтор-4-нитроанилин), 2-бром-5-фтор-4-нитроанилин (1,0 экв.), перхлорат цинка дигидрат (20% моль) и толуол (8 об.). Смесь перемешивали при комнатной температуре в течение 30 минут (NMT). В конце добавляли (R)-бензилглицидиловый эфир (2,0 экв.) в толуоле (2 об.) равномерным потоком. Реакционную смесь нагревали до 80°C (внутренняя температура) и перемешивали в течение приблизительно 7 часов или до тех пор, пока содержание 2-бром-5-фтор-4-нитроанилина не достигало <5% AUC.
[00219] Реакционную смесь охлаждали до комнатной температуры и добавляли Целит (50% масс.) с последующим добавлением этилацетата (10 об.). Полученную смесь фильтровали для удаления Целита и сита и промывали этилацетатом (2 об.). Фильтрат промывали раствором хлорида аммония (4 об., 20% масс./об.). Органический слой промывали раствором бикарбоната натрия (4 об.×2,5% масс./об.). Органический слой концентрировали в вакууме на роторном испарителе. Полученную суспензию растворяли в изопропилацетате (10 об.) и этот раствор переносили в гидрогенизатор Buchi.
[00220] В гидрогенизатор загружали 5% масс. Pt(S)/C (1,5% моль) и смесь перемешивали под потоком N2 при 30°C (внутренняя температура). Реакционную смесь продували потоком N2, затем водородом. Давление в гидрогенизаторе доводили до 1 бар водорода и смесь быстро перемешивали (>1200 об./мин). После завершения реакции катализатор фильтровали через слой Целита и промывали дихлорметаном (10 об.). Фильтрат концентрировали в вакууме. Любой оставшийся изопропилацетат отгоняли при помощи дихлорметана (2 об.) и концентрировали на роторном испарителе досуха.
[00221] Полученный остаток растворяли в дихлорметане (10 об.), добавляли моногидрат пара-толуолсульфоновой кислоты (1,2 экв.) и перемешивали в течение ночи. Продукт фильтровали и промывали дихлорметаном (2 об.) и сушили в какууме. Мокрую лепешку переносили в сушильные лотки и помещали в вакуумную печь и сушили при 45°C с N2 продувкой до достижения постоянной массы. Соль п-толуолсульфоновой кислоты и (R)-1-((4-амино-2-бром-5-фторфенил)амино)-3-(бензилокси)пропан-2-ола выделяли в виде не совсем белого твердого вещества.
[00222] Хиральная чистота согласно определениям составляла >97%эи.
[00223] Синтез (3-хлор-3-метилбут-1-инил)триметилсилана
[00224] Пропаргиловый спирт (1,0 экв.) загружали в реакционный сосуд. Добавляли водный раствор хлористоводородной кислоты (37%, 3,75 об.) и начинали перемешивание. В процессе растворения твердого спирта наблюдали умеренную эндотерму (5-6°C). Полученную смесь перемешивали в течение ночи (16 часов), смесь постепенно становилась темно-красной. В 30-л снабженный кожухом реакционный сосуд загружали воду (5 об.), затем охлаждали до 10°C. Реакционную смесь медленно переносили в воду под вакуумом, поддерживая внутреннюю температуру смеси ниже 25°C. Добавляли гексаны (3 об.) и полученную смесь перемешивали в течение 0,5 часов. Фазы осаждали и водную фазу (pH <1) сливали и далее не использовали. Органическую фазу концентрировали в вакууме с использованием роторного испарителя с получением продукта в виде красного масла.
[00225] Синтез (4-(бензилокси)-3,3-диметилбут-1-инил)триметилсилана
[00226] Способ A
[00227] Все указанные эквиваленты и объемы в этой части указаны в расчете на 250-г реакцию. Магниевые стружки (69,5 г, 2,86 моль, 2,0 экв.) загружали в 3-л 4-горлый реакционный сосуд и перемешивали при помощи магнитной мешалки под потоком азота в течение 0,5 часов. Реакционный сосуд погружали в баню лед-вода. В реакционный сосуд медленно добавляли пропаргилхлорид (250 г, 1,43 моль, 1,0 экв.) в ТГФ (1,8 л, 7,2 об.) при перемешивании до тех пор, пока не наблюдали начальную экзотерму (~10°C). Образование реагента Гриньяра подтверждали при помощи IPC с использованием 1H-ЯМР спектроскопии. Как только экзотерма спадала, медленно добавляли оставшийся раствор, поддерживая температуру партии <15°C. Процедура добавления требовала ~3,5 часов. Полученную темно-зеленую смесь сливали в 2-л снабженную крышкой бутыль.
[00228] Все указанные эквиваленты и объемы в этой части указаны в расчете на 500-г реакцию. В 22-л реактор загружали раствор бензилхлорметилового эфира (95%, 375 г, 2,31 моль, 0,8 экв.) в ТГФ (1,5 л, 3 об.). Реактор охлаждали на бане лед-вода. Полученные, как описано выше, две партии реагента Гриньяра объединяли и затем добавляли медленно к раствору бензилхлорметилового эфира через капельную воронку, поддерживая температуру партии ниже 25°C. Процедура добавления требовала 1,5 часов. Реакционную смесь перемешивали в течение ночи (16 часов).
[00229] Все указанные эквиваленты и объемы в этой части указаны в расчете на 1-кг реакцию. Раствор 15% хлорида аммония получали в 30-л снабженном кожухом реакторе (1,5 кг в 8,5 кг воды, 10 об.). Раствор охлаждали до 5°C. Полученные, как описано выше, две смеси реагента Гриньяра объединяли и затем переносили в раствор хлорида аммония через приемный сосуд. При таком гашении наблюдали экзотерму, и эту процедуру осуществляли с такой скоростью, чтобы поддерживать внутреннюю температуру ниже 25°C. После завершения переноса температуру кожуха реакционного сосуда устанавливали на 25°C. Добавляли гексаны (8 л, 8 об.) и смесь перемешивали в течение 0,5 часов. После отстаивания фаз водную фазу (pH 9) сливали и далее не использовали. Оставшуюся органическую фазу промывали водой (2 л, 2 об.). Органическую фазу концентрировали в вакууме с использованием 22-л роторного испарителя, с получением неочищенного продукта в виде оранжевого масла.
[00230] Способ B
[00231] Магниевые стружки (106 г, 4,35 моль, 1,0 экв.) загружали в 22-л реактор и затем суспендировали в ТГФ (760 мл, 1 об.). Реакционный сосуд охлаждали на бане лед-вода таким образом, чтобы температура партии достигала 2°C. В реактор медленно добавляли раствор пропаргилхлорида (760 г, 4,35 моль, 1,0 экв.) в ТГФ (4,5 л, 6 об.). После добавления 100 мл процедуру добавления останавливали и смесь перемешивали до тех пор, пока не наблюдали 13°C экзотерму, указывающую на начало образования реагента Гриньяра. После угасания экзотермы медленно добавляли еще 500 мл раствора пропаргилхлорида, поддерживая температуру партии <20°C. Образование реагента Гриньяра подтверждали при помощи IPC с использованием 1H-ЯМР спектроскопии. Медленно добавляли оставшийся раствор пропаргилхлорида, поддерживая температуру партии <20°C. Процедура добавления требовала ~1,5 часов. Полученный темно- зеленый раствор перемешивали в течение 0,5 часов. Образование реагента Гриньяра подтверждали при помощи IPC с использованием 1H-ЯМР спектроскопии. Чистый бензилхлорметиловый эфир загружали в подсоединенную к реактору капельную воронку и затем добавляли по каплям в реактор, поддерживая температуру партии ниже 25°C. Процедура добавления требовала 1,0 часа. Реакционную смесь перемешивали в течение ночи. Водную обработку и концентрирование осуществляли с использованием такой же процедуры и соответствующих количеств веществ, как в Способе A, с получением продукта в виде оранжевого масла.
[00232] Синтез 4-бензилокси-3,3-диметилбут-1-ина
[00233] В 30-л снабженный кожухом реактор загружали метанол (6 об.), затем охлаждали до 5°C. В реактор добавляли гидроксид калия (85%, 1,3 экв.). По мере растворения гидроксида калия наблюдали 15-20°C экзотерму. Температуру кожуха устанавливали на 25°C. Добавляли раствор 4-бензилокси-3,3-диметил-1-триметилсилилбут-1-ина (1,0 экв.) в метаноле (2 об.) и полученную смесь перемешивали до завершения реакции, которую отслеживали методом ВЭЖХ. Типично время реакции при 25°C составляло 3-4 часов. Реакционную смесь разбавляли водой (8 об.) и затем перемешивали в течение 0,5 часов. Добавляли гексаны (6 об.) и полученную смесь перемешивали в течение 0,5 часов. Фазам давали отстояться и затем водную фазу (pH 10-11) сливали и далее не использовали. Органическую фазу промывали раствором KOH (85%, 0,4 экв.) в воде (8 об.), затем водой (8 об.). Органическую фазу затем концентрировали с использованием роторного испарителя, с получением указанного в заголовке соединения в виде желто-оранжевого масла. Типичная чистота этого вещества находится в пределах 80%, и, в основном, присутствует одна примесь. 1H ЯМР (400 MГц, C6D6) δ 7,28 (д, 2H, J=7,4 Гц), 7,18 (т, 2H, J=7,2 Гц), 7,10 (д, 1H, J=7,2 Гц), 4,35 (с, 2H), 3,24 (с, 2H), 1,91 (с, 1H), 1,25 (с, 6H).
[00234] Синтез N-бензилгликолированный-5-амино-2-(2-бензилокси-1,1-диметилэтил)-6-фториндола
[00235] Способ A
[00236] Синтез (R)-1-((4-амино-2-(4-(бензилокси)-3,3-диметилбут-1-ин-1-ил)-5-фторфенил)амино)-3-(бензилокси)пропан-2-ола
[00237] Соль п-толуолсульфоновой кислоты и (R)-1-((4-амино-2-бром-5-фторфенил)амино)-3-(бензилокси)пропан-2-ола преобразовывали в форму свободного основания путем перемешивания твердого вещества в дихлорметане (5 об.) и насыщенном растворе NaHСО3 (5 об.) до получения прозрачного органического слоя. Полученные слои разделяли и органический слой промывали насыщенным раствором NaHСО3 (5 об.), с затем насыщенным солевым раствором и концентрировали в вакууме с получением (R)-1-((4-амино-2-бром-5-фторфенил)амино)-3-(бензилокси)пропан-2-ола в форме свободного основания в виде масла.
[00238] Ацетат палладия (0,01 экв.), dppb (0,015 экв.), CuI (0,015 экв.) и карбонат калия (3 экв.) суспендировали в ацетонитриле (1,2 об.). После перемешивания в течение 15 минут добавляли раствор 4-бензилокси-3,3-диметилбут-1-ина (1,1 экв.) в ацетонитриле (0,2 об.). Смесь барботировали газообразным азотом в течение 1 часа и затем добавляли раствор (R)-1-((4-амино-2-бром-5-фторфенил)амино)-3-(бензилокси)пропан-2-ола в форме свободного основания (1 экв.) в ацетонитриле (4,1 об.). Смесь барботировали газообразным азотом еще в течение одного часа и затем нагревали до 80°C. Развитие реакции отслеживали методом ВЭЖХ, и обычно через 3-5 часов реакция была полностью завершена. Смесь охлаждали до комнатной температуры и затем фильтровали через Целит. Лепешку промывали ацетонитрилом (4 об.). Объединенные фильтраты подвергали азеотропной сушке досуха и затем смесь осветляли фильтрованием в следующем реакторе. Ацетонитрильный раствор (R)-1-((4-амино-2-(4-(бензилокси)-3,3-диметилбут-1-ин-1-ил)-5-фторфенил)амино)-3-(бензилокси)пропан-2-ола, полученный таким образом, использовали непосредственно в следующей процедуре (циклизации) без дополнительной обработки.
[00239] Синтез N-бензилгликолированный-5-амино-2-(2-бензилокси-1,1-диметилэтил)-6-фториндола
[00240] Бис-ацетонитрилдихлорпалладий (0,1 экв.) и CuI (0,1 экв.) загружали в реактор и затем суспендировали в растворе (R)-1-((4-амино-2-(4-(бензилокси)-3,3-диметилбут-1-ин-1-ил)-5-фторфенил)амино)-3-(бензилокси)пропан-2-ола, полченного выше (1 экв.), в ацетонитриле (9,5 об. в целом). Смесь барботировали газообразным азотом в течение 1 часа и затем нагревали до 80°C. Развитие реакции отслеживали методом ВЭЖХ, и реакция типично полностью завершалась через 1-3 часа. Смесь фильтровали через Целит и лепешку промывали ацетонитрилом. Осуществляли замену растворителя на этилацетат (7,5 об.). Этилацетатный раствор промывали водным раствором NH3-NH4Cl (2×2,5 об.), затем 10% насыщенным солевым раствором (2,5 об.). Этилацетатный раствор затем перемешивали с силикагелем (1,8 масс. экв.) и Si-TMT (0,1 масс. экв.) в течение 6 часов. После фильтрования полученный раствор концентрировали. Остаточное масло растворяли в DCM/гептане (4 об.) и затем очищали колоночной хроматографией. Масло, полученное таким образом, затем кристаллизовали из 25% EtOAc/гептан (4 об.). Кристаллический (R)-1-(5-амино-2-(1-(бензилокси)-2-метилпропан-2-ил)-6-фтор-1H-индол-1-ил)-3-(бензилокси)пропан-2-ол типично получали с выходом 27-38%. 1H ЯМР (400 MГц, ДМСО) δ 7,38-7,34 (м, 4H), 7,32-7,23 (м, 6H), 7,21 (д, 1H, J=12,8 Гц), 6,77 (д, 1H, J=9,0 Гц), 6,06 (с, 1H), 5,13 (д, 1H, J=4,9 Гц), 4,54 (с, 2H), 4,46 (уш. с, 2H), 4,45 (с, 2H), 4,33 (д, 1H, J=12,4 Гц), 4,09-4,04 (м, 2H), 3,63 (д, 1Н, J=9,2 Гц), 3,56 (д, 1H, J=9,2 Гц), 3,49 (дд, 1H, J=9,8, 4,4 Гц), 3,43 (дд, 1H, J=9,8, 5,7 Гц), 1,40 (с, 6H).
[00241] Синтез N-бензилгликолированный-5-амино-2-(2-бензилокси-1,1-диметилэтил)-6-фториндола
[00242] Способ B
[00243] Ацетат палладия (33 г, 0,04 экв.), dppb (94 г, 0,06 экв.) и карбонат калия (1,5 кг, 3,0 экв.) загружали в реактор. Масло, представляющее собой бензилгликолированный 4-аммоний-2-бром-5-фторанилин в форме свободного основания (1,5 кг, 1,0 экв.) растворяли в ацетонитриле (8,2 л, 4,1 об.) и затем добавляли в реактор. Смесь барботировали газообразным азотом в течение 1 часа (NLT). К смеси добавляли раствор 4-бензилокси-3,3-диметилбут-1-ина (70%, 1,1 кг, 1,05 экв.) в ацетонитриле, затем барботировали газообразным азотом в течение 1 часа (NLT). Смесь нагревали до 80°C и затем перемешивали в течение ночи. Осуществляли IPC методом ВЭЖХ и через 16 часов определяли завершение реакции. Смесь охлаждали до температуры окружающей среды и затем фильтровали через слой Целита (228 г). Реактор и слой Целита промывали ацетонитрилом (2×2 л, 2 об.). Объединенные фазы концентрировали на 22-л роторном испарителе до тех пор, пока не собирали 8 л растворителя, оставляя неочищенный продукт в 7 л (3,5 об.) ацетонитрила.
[00244] Бис-ацетонитрилдихлорпалладий (144 г, 0,15 экв.) загружали в реактор. Неочищенный раствор переносили обратно в реактор и колбу роторного испарителя промывали ацетонитрилом (4 л, 2 об.). Объединенные растворы барботировали газообразным азотом в течение 1 часа (NLT). Реакционную смесь нагревали до 80°C в течение 16 часов (NLT). Контроль в процессе реакции методом ВЭЖХ показал полное расходование исходного вещества. Реакционную смесь фильтровали через Целит (300 г). Реактор и фильтровальную лепешку промывали ацетонитрилом (3 л, 1,5 об.). Объединенные фильтраты концентрировали до масла при помощи роторного испарителя. Масло растворяли в этилацетате (8,8 л, 4,4 об.). Раствор промывали 20% раствором хлорида аммония (5 л, 2,5 об.), затем 5% насыщенным солевым раствором (5 л, 2,5 об.). Силикагель (3,5 кг, 1,8 масс. экв.) добавляли к органической фазе, которую перемешивали в течение ночи. Добавляли Deloxan THP II металлический очиститель (358 г) и гептан (17,6 л) и полученную смесь перемешивали в течение 3 часов (NLT). Смесь фильтровали через воронку из спеченного стекла. Фильтровальную лепешку промывали 30% раствором этилацетата в гептане (25 л). Объединенные фильтраты концентрировали при пониженном давлении с получением N-бензилгликолированный-5-амино-2-(2-бензилокси-1,1-диметилэтил)-6-фториндола в виде коричневой пасты (1,4 кг).
[00245] Синтез соединения 1
[00246] Синтез бензил-защищенного соединения 1
[00247] 1-(2,2-Дифтор-1,3-бензодиоксол-5-ил)циклопропанкарбоновую кислоту (1,3 экв.) суспендировали в толуоле (2,5 об., в расчете на 1-(2,2-дифтор-1,3-бензодиоксол-5-ил)циклопропанкарбоновую кислоту). Добавляли тионилхлорид (SOCl2, 1,7 экв.) через капельную воронку и смесь нагревали до 60°C. Полученную смесь перемешивали в течение 2 часов. Толуол и избыток SOCl2 отгоняли с использованием роторного испарителя. Добавляли дополнительное количество толуола (2,5 об. в расчете на 1-(2,2-дифтор-1,3-бензодиоксол-5-ил)циклопропанкарбоновую кислоту) и смесь подвергали дистилляции до 1 об. толуола. Раствор (R)-1-(5-амино-2-(1-(бензилокси)-2-метилпропан-2-ил)-6-фтор-1H-индол-1-ил)-3-(бензилокси)пропан-2-ола (1 экв.) и триэтиламина (3 экв.) в DCM (4 об.) охлаждали до 0°C. Добавляли раствор хлорангидрида кислоты в толуоле (1 об.), поддерживая при этом температуру партии ниже 10°C. Развитие реакции отслеживали методом ВЭЖХ, и обычно реакция была полностью завершена через минуту. После нагревания до 25°C реакционную смесь промывали 5% раствором NaHСО3 (3,5 об.), 1 M NaOH (3,5 об.) и 1 M HCl (5 об.). Осуществляли замену растворителя на метанол (2 об.) и полученный раствор (R)-N-(1-(3-(бензилокси)-2-гидроксипропил)-2-(1-(бензилокси)-2-метилпропан-2-ил)-6-фтор-1H-индол-5-ил)-1-(2,2-дифторбензо[d][1,3]диоксол-5-ил)циклопропанкарбоксамида в метаноле использовали без дополнительной обработки на следующей стадии (гидрогенолиз).
[00248] Синтез соединения 1
[00249] 5% палладий-на-угле (~50% влажности, 0,01 экв.) загружали в соответствующий аппарат для гидрирования. Осторожно добавляли раствор (R)-N-(1-(3-(бензилокси)-2-гидроксипропил)-2-(1-(бензилокси)-2-метилпропан-2-ил)-6-фтор-1H-индол-5-ил)-1-(2,2-дифторбензо[d][1,3]диоксол-5-ил)циклопропанкарбоксамида в метаноле (2 об.), полученный на предыдущей стадии, с последующим добавлением 3 M раствора HCl в метаноле. Реакционный сосуд продували газообразным азотом и затем газообразным водородом. Смесь интенсивно перемешивали до полного завершения реакции, как было определено ВЭЖХ анализом. Типичное время реакции составляло 3-5 часов. Реакционную смесь фильтровали через Целит и лепешку промывали метанолом (2 об.). Осуществляли замену растворителя на изопропанол (3 об.). Неочищенное Соединение 1 кристаллизовали из смеси 75% IPA-гептан (4 об., т.е. 1 об. гептана добавляли к 3 об. IPA), и полученные кристаллы вызревали в 50% IPA-гептане (т.е. 2 об. гептана добавляли к смеси). Типичные выходы Соединения 4 в результате двухстадийной процедуры ацилирования/гидрогенолиза составляют от 68% до 84%. Соединение 4 можно подвергнуть перекристаллизации из IPA-гептана, следуя процедуре, описанной непосредственно выше.
[00250] Соединение 1 также можно получить с использованием одного или нескольких путей синтеза, раскрытых в опубликованной патентной заявке США № US20090131492, включенной в настоящую заявку посредством ссылки.
[00251] В таблице 10 ниже представлены аналитические данные для соединения 1.
| Таблица 10 | |||
| Соед № | ЖХ/МС М+1 |
ЖХ/RT мин |
ЯМР |
| 1 | 521,5 | 1,69 | 1H ЯМР (400,0 MГц, CD3CN) δ 7 69 (д, J=7,7 Гц, 1H), 7,44 (д, J=1,6 Гц, 1H), 7,39 (дд, J=1,7, 8,3 Гц, 1H), 7,31 (с, 1H), 7,27 (д, J=8,3 Гц, 1H), 7,20 (д, J=12,0 Гц, 1H), 6,34 (с, 1H), 4,32 (д, J=6,8 Гц, 2H), 4,15-4,09 (м, 1H), 3,89 (дд, J=6,0, 11,5 Гц, 1H), 3,63-3,52 (м, 3H), 3,42 (д, J=4,6 Гц, 1H), 3,21 (дд, J=6,2, 7,2 Гц, 1H), 3,04 (т, J=5,8 Гц, 1H), 1,59 (дд, J=3,8, 6,8 Гц, 2H), 1,44 (с, 3H), 1,33 (с, 3H) и 1,18 (дд, J=3,7, 6,8 Гц, 2H) ч/млн. |
[00252] АНАЛИЗЫ
[00253] Анализы для определения и измерения ΔF508-CFTR корректирующих свойств соединений
[00254] Оптические способы определения мембранного потенциала для анализа ΔF508-CFTR-модулирующих свойств соединений
[00255] В оптическом анализе мембранного потенциала использовали потенциал-чувствительные FRET сенсоры, описанные Gonzalez и Tsien (см. Gonzalez, J. E. and R. Y. Tsien (1995) "Voltage sensing by fluorescence resonance energy transfer in single cells" Biophys J 69(4): 1272-80; и Gonzalez, J. E. and R. Y. Tsien (1997) "Improved indicators of cell membrane potential that use fluorescence resonance energy transfer" Chem Biol 4(4): 269-77), в комбинации с инструментами для измерения изменений флуоресценции, такими как Потенциал/Ионный Зонд-Ридер (VIPR) (см. Gonzalez, J. E., K. Oades, et al. (1999) "Cell-based assays and instrumentation for screening ion-channel targets" Drug Discov Today 4(9): 431-439).
[00256] Эти потенциал-чувствительные анализы основаны на изменении передачи резонансной энергии флуоресценции (FRET) между мембрано-растворимым потенциал-чувствительным красителем, DiSBAC2(3), и флуоресцентным фосфолипидом, CC2-DMPE, который присоединен к внешней стороне плазменной мембраны и действует как FRET донор. Изменения мембранного потенциала (Vm) вызывают редистрибуцию отрицательно заряженного DiSBAC2(3) через плазменную мембрану, и количество переносимой энергии из CC2-DMPE изменяется соответственно. Изменения эмиссии флуоресценции отслеживали с использованием VIPR™ II, которое представляет собой интегрированное устройство для манипуляции с жидкостями и детекции флуоресценции, разработанное для осуществления клеточных скрининговых анализов в 96- или 384-луночных микротитровальных планшетах.
[00257] I. Идентификация корректирующих соединений
[00258] Для идентификации малых молекул, которые корректируют нарушение трафика, связанное с ΔF508-CFTR, был разработан HTS анализ в формате одного добавления. Клетки инкубировали в бессывороточной среде в течение 16 часов при 37°C в присутствии или в отсутствие (отрицательный контроль) испытываемого соединения. В качестве положительного контроля, клетки высевали в 384-луночные планшеты и инкубировали в течение 16 часов при 27°C для "температурной коррекции" ΔF508-CFTR. Клетки затем промывали 3X раствором Кребса и Рингера и нагружали потенциал-чувствительными красителями. Для активации ΔF508-CFTR, 10 мкМ форсколина и потенциирующее средство для CFTR, генистеин (20 мкМ), добавляли вместе с не содержащей Cl- средой в каждую лунку. Добавление не содержащей Cl- среды промотировало отток Cl- в ответ на активацию ΔF508-CFTR, и полученную деполяризацию мембраны оптически отслеживали с использованием FRET-основанных потенциал-чувствительных красителей.
[00259] 2. Идентификация потенциирующих соединений
[00260] Для идентификации потенциирующих средств для ΔF508-CFTR был разработан HTS анализ в формате двойного добавления. В процессе первого добавления в каждую лунку добавляли не содержащую Cl- среду с или без испытываемого соединения. Через 22 секунды осуществляли второе добавление не содержащей Cl- среды, содержащей 2-10 мкМ форсколина, для активации ΔF508-CFTR. Внеклеточная концентрация Cl- после обоих добавлений была 28 мМ, что промотировало отток Cl- в ответ на активацию ΔF508-CFTR, и полученную деполяризацию мембраны оптически отслеживали с использованием FRET-основанных потенциал-чувствительных красителей.
3. Растворы
| Раствор в ванночке #1: (в мМ) | NaCl 160, KCl 4,5, CaCl2 2, MgCl2 1, HEPES 10, pH 7,4 при помощи NaOH. |
| Не содержащий хлориды раствор в ванночке: | Хлоридные соли в растворе в ванночке #1 заменяли глюконатными солями. |
| CC2-DMPE: | Получали в виде 10 мМ исходного раствора в DMSO и хранили при -20°C. |
| DiSBAC2(3): | Получали в виде 10 мМ исходного раствора в DMSO и хранили при -20°C. |
[00262] 4. Клеточная культура
[00263] NIH3T3 мышиные фибробласты, стабильно экспрессирующие ΔF508-CFTR, использовали для оптических измерений мембранного потенциала. Клетки поддерживали при 37°C в 5% СО2 и 90% влажности в модифицированной Дульбекко среде Игла, дополненной 2 мМ глутамина, 10% фетальной бычьей сыворотки, 1×NEAA, β-ΜΕ, 1×пенициллина/стрептомицина и 25 мМ HEPES в 175 см2 колбах для культивирования. Для всех оптических анализов клетки высевали при плотности 30000/лунка в 384-луночные покрытые матригелем планшеты и культивировали в течение 2 часов при 37°C, затем культивировали при 27°C в течение 24 часов для анализа потенциирующего средства. Для анализов корректирующего средства клетки культивировали при 27°C или 37°C с и без соединения в течение 16-24 часов.
[00264] Электрофизиологические анализы для определения ΔF508-CFTR-модулирующих свойств соединений
[00265] 1. Анализ с использованием камеры Ussing
[00266] эксперименты с использованием камеры Ussing осуществляли на поляризованных эпителиальных клетках, экспрессирующих ΔF508-CFTR, для дополнительной характеризации модуляторов ΔF508-CFTR, идентифицированных в оптических анализах. FRTΔF508-CFTR эпителиальные клетки, которые выращивали на Costar Snapwell включениях клеточной культуры, закрепляли в камере Ussing (Physiologic Instruments, Inc., San Diego, CA) и монослои постоянно подвергали короткому замыканию с использованием Вольт-кламп Системы (Department of Bioengineering, University of Iowa, IA, and Physiologic Instruments, Inc., San Diego, CA). Трансэпителиальное сопротивление измеряли путем приложения 2-мВ импульса. В этих условиях FRT эпителии демонстрировали сопротивления 4 ΚΩ/см2 или больше. Растворы поддерживали при 27°C и барботировали воздухом. Отклонения напряжения на электродах и сопротивление жидкости корректировали с использованием не содержащих клетки включений. В этих условиях ток отражает поток Cl- через ΔF508-CFTR, экспрессируемые в апикальной мембране. ISC получали в цифровом формате с использованием MP100A-CE интерфейса и программы AcqKnowledge (v3.2.6; BIOPAC Systems, Santa Barbara, CA).
[00267] 2. Идентификация корректирующих соединений
[00268] Типичный протокол, использующий градиент концентрации Cl- от базолатеральной к апикальной мембране. Для установления этого градиента на базолатеральной мембране использовали нормальный раствор Рингера, тогда как апикальный NaCl заменяли эквимолярным количеством глюконата натрия (оттитрованный до pH 7,4 при помощи NaOH) с получением большого градиента Cl- концентрации через эпителий. Все эксперименты осуществляли с интактными монослоями. Для полной активации ΔF508-CFTR, использовали форсколин (10 мкМ) и ингибитор PDE, IBMX (100 мкМ), с последующим добавлением потенциирующего средства для CFTR генистеина (50 мкМ).
[00269] Как наблюдали в других клеточных типах, инкубация при более низких температурах FRT клеток, стабильно экспрессирующих ΔF508-CFTR, повышает функциональную плотность CFTR в плазменной мембране. Для определения активности корректирующих соединений, клетки инкубировали с 10 мкМ испытываемого соединения в течение 24 часов при 37°C и затем промывали 3X перед регистрацией. cAMP- и генистеин-опосредованный ISC в обработанных соединением клетках нормализовали к 27°C и 37°C контролям и выражали как процент активности. Предварительная инкубация клеток с корректирующим соединением существенно повышала cAMP- и генистеин-опосредованный ISC по сравнению с 37°C контролями.
[00270] 3. Идентификация потенциирующих соединений
[00271] Типичный протокол, использующий градиент концентрации Cl- от базолатеральной к апикальной мембране. Для установления этого градиента на базолатеральной мембране использовали нормальный раствор Рингера и осуществляли пермеабилизацию нистатином (360 мкг/мл), тогда как апикальный NaCl заменяли эквимолярным количеством глюконата натрия (оттитрованный до pH 7,4 при помощи NaOH) с получением большого градиента Cl- концентрации через эпителий. Все эксперименты осуществляли через 30 минут после пермеабилизации нистатином. Форсколин (10 мкМ) и все испытываемые соединения добавляли к обеим сторонам включений клеточной культуры. Эффективность предполагаемых ΔF508-CFTR-потенциирующих средств сравнивали с эффективностью известного потенциирующего средства генистеина.
[00272] 4. Растворы
| Базолатеральный раствор (в мМ): | NaCl (135), CaCl2 (1,2), MgCl2 (1,2), K2HPО4 (2,4), KHPО4 (0,6), N-2-гидроксиэтилпиперазин- N'-2-этансульфоновая кислота (HEPES) (10) и декстроза (10). Раствор оттитрованный до pH 7,4 при помощи NaOH. |
| Апикальный раствор (в мМ): | Такой же, как базолатеральный раствор, где NaCl заменен Na глюконатом (135). |
[00273] 5. Клеточная культура
[00274] Эпителиальные клетки крыс Fisher (FRT), экспрессирующие ΔF508-CFTR (FRTΔF508-CFTR) использовали для экспериментов с камерой Ussing для предполагаемых модуляторов ΔF508-CFTR, идентифицированных в оптических анализах. Клетки культивировали на Costar Snapwell включениях клеточной культуры и культивировали в течение пяти дней при 37°C и 5% СО2 в модифицированной Куном среде Хэма F-12, дополненной 5% фетальной телячьей сывороткой, 100 Ед./мл пенициллина и 100 мкг/мл стрептомицина. Перед использованием для характеризации активности соединений как потенцирующих средств клетки инкубировали при 27°C в течение 16-48 часов для коррекции на ΔF508-CFTR. Для определения активности корректирующих соединений, клетки инкубировали при 27°C или 37°C с и без соединения в течение 24 часов.
[00275] 6. Регистрации в формате “целая клетка”
Макроскопический ΔF508-CFTR ток (IΔF508) в температура- и испытываемое соединение-скорректированных NIH3T3 клетках, стабильно экспрессирующих ΔF508-CFTR, отслеживали путем регистрации с использованием перфорированного “пэтча”, в формате “целая клетка”. Вкратце, вольт-кламп регистрации IΔF508 осуществляли при комнатной температуре с использованием Axopatch 200B пэтч-кламп усилителя (Axon Instruments Inc., Foster City, CA). Все регистрации осуществляли при частоте выборки 10 кГц и низкочастотной фильтрации при 1 кГц. Пипетки имели сопротивление 5-6 ΜΩ при заполнении внутриклеточным раствором. В этих условиях регистрации рассчитанный потенциал реверсии для Cl- (ECI) при комнатной температуре был -28 мВ. Все регистрации имели изоляционное сопротивление >20 GQ и последовательное сопротивление <15 ΜΩ. Генерацию импульсов, сбор данных и анализ осуществляли с использованием персонального компьютера, снабженного Digidata 1320 A/D интерфейсом в сочетании с Clampex 8 (Axon Instruments Inc.). Ванночка содержала <250 мкл солевого раствора, и постоянно осуществляли перфузию со скоростью 2 мл/мин с использованием перфузионной системы с гравитационным режимом систем.
[00276] 7. Идентификация корректирующих соединений
[00277] Для определения активности корректирующих соединений для повышения плотности функционального ΔF508-CFTR в плазменной мембране использовали вышеописанный способ “перфорированный пэтч” регистрации для измерения плотности тока после 24-часовой обработки корректирующими соединениями. Для полной активации ΔF508-CFTR к клеткам добавляли 10 мкМ форсколина и 20 мкМ генистеин. В таких условиях регистрации плотность тока после 24-часовой инкубации при 27°C была выше, чем та, которую наблюдали после 24-часовой инкубации при 37°C. Эти результаты согласуются с известными эффектами низкотемпературной инкубации на плотность ΔF508-CFTR в плазменной мембране. Для определения эффектов корректирующих соединений на CFTR плотность тока клетки инкубировали с 10 мкМ испытываемого соединения в течение 24 часов при 37°C и плотность тока сравнивали с 27°C и 37°C контролями (% активности). Перед регистрацией клетки промывали 3X внеклеточной регистрационной средой для удаления какого-либо оставшегося количества испытываемого соединения. Предварительная инкубация с 10 мкМ корректирующих соединений существенно повышала cAMP- и генистеин-зависимый ток по сравнению с 37°C контролями.
[00278] 8. Идентификация потенциирующих соединений
[00279] Способность ΔF508-CFTR-потенциирующих средств увеличивать макроскопический ΔF508-CFTR Cl- ток (IΔF508) в NIH3T3 клетках, стабильно экспрессирующих ΔF508-CFTR, также исследовали с использованием способа “перфорированный пэтч” регистрации. Потенциирующие средства, идентифицированные в оптических анализах, вызывали дозозависимое повышение в IΔF508 с такой же активностью и эффективностью, которые наблюдали в оптических анализах. Во всех исследованных клетках потенциал реверсии до и в процессе применения потенциирующего средства был около -30 мВ, что представляет собой рассчитанное значение ECI (-28 мВ).
[00280] 9. Растворы
| Внутриклеточный раствор (в мМ): | Cs-аспартат (90), CsCl (50), MgCl2 (1), HEPES (10) и 240 мкг/мл амфотерицина-B (pH доводили до 7,35 при помощи CsOH). |
| Внеклеточный раствор (в мМ): | N-метил-D-глюкамин (NMDG)-Cl (150), MgCl 2 (2), CaCl2 (2), HEPES (10) (pH доводили до 7,35 при помощи HCl). |
[00281] 10. Клеточная культура
[00282] NIH3T3 мышиные фибробласты, стабильно экспрессирующие ΔF508-CFTR, использовали для регистраций в формате “целая клетка”. Клетки поддерживали при 37°C в 5% СО2 и 90% влажности в модифицированной Дульбекко среде Игла, дополненной 2 мМ глутамина, 10% фетальной бычьей сыворотки, 1×NEAA, β-ΜΕ, 1×пенициллина/стрептомицина и 25 мМ HEPES, в 175 см2 колбах для культивирования. Для регистраций в формате “целая клетка”, 2500-5000 клеток высевали на покрытые поли-L-лизином предметные стекла и культивировали в течение 24-48 часов при 27°C перед использованием для испытания активности потенциирующих средств; и инкубировали с или без корректирующего соединения при 37°C для измерения активности корректирующих средств.
[00283] 11. Регистрации одиночных каналов
[00284] Активности одиночных каналов температура-скорректированных ΔF508-CFTR, стабильно экспрессируемых в NIH3T3 клетках, и активности потенциирующих соединений наблюдали с использованием вырезанного мембранного “пэтча” в конфигурации “внутренняя сторона наружу”. Вкратце, вольт-кламп регистрации активности одиночных каналов осуществляли при комнатной температуре с использованием Axopatch 200B пэтч-кламп усилителя (Axon Instruments Inc.). Все регистрации осуществляли при частоте выборки 10 кГц и низкочастотной фильтрации при 400 Гц. Пэтч-пипетки были изготовлены из Corning Kovar Sealing #7052 стекла (World Precision Instruments, Inc., Sarasota, FL) и имели сопротивление 5-8 ΜΩ при заполнении внеклеточным раствором. ΔF508-CFTR активировался после эксцизии путем добавления 1 мМ Мg-ATP и 75 нМ cAMP-зависимой протеинкиназы, каталитической субъединицы (PKA; Promega Corp. Madison, WI). После стабилизации активности канала “пэтч” подвергали перфузии с использованием микроперфузионной системы с гравитационным режимом. Входящий поток помещали рядом с “пэтчем”, что обеспечивало полный обмен растворами в течение 1-2 секунд. Чтобы поддерживать ΔF508-CFTR активность в процессе быстрой перфузии неспецифический ингибитор фосфатазы F- (10 мМ NaF) добавляли к раствору в ванночке. В этих условиях регистрации активность канала оставалась постоянной в течение всего процесса пэтч-регистрации (до 60 минут). Токи, генерируемые положительным зарядом, перемещающимся изнутри во внеклеточные растворы (анионы перемещаются в обратном направлении) показаны как положительные токи. Потенциал на кончике пипетки (Vp) поддерживали при 80 мВ.
[00285] Активность каналов анализировали из мембранных “пэтчей”, содержащих ≤2 активных канала. Максимальное количество одновременных открытий определяло количество активных каналов в процессе эксперимента. Для определения амплитуды тока одиночного канала данные, зарегистрированные за 120 секунд ΔF508-CFTR активности, фильтровали "офлайн" при 100 Гц и затем использовали для построения гистограмм амплитуды по всем точкам, которые подгоняли к множеству функций Гаусса с использованием программы Bio-Patch Analysis (Bio-Logic Comp. France). Общий микроскопический ток и вероятность открытия (Pо) определяли на основании 120 с активности канала. Pо определяли с использованием Bio-Patch программы или из соотношения Pо=I/i(N), где I = средний ток, i = амплитуда тока одиночного канала, и N = количество активных каналов в “пэтче”.
[00286] 12. Растворы
| Внеклеточный раствор (в мМ): | NMDG (150), аспарагиновая кислота (150), CaCl2 (5), MgCl2 (2) и HEPES (10) (pH доводили до 7,35 при помощи Tris основания). |
| Внутриклеточный раствор (в мМ): | NMDG-Cl (150), MgCl2 (2), EGTA (5), TES (10) и Tris основание (14) (pH доводили до 7,35 при помощи HCl). |
[00287] 13. Клеточная культура
[00288] NIH3T3 мышиные фибробласты, стабильно экспрессирующие ΔF508-CFTR, использовали для пэтч-кламп регистраций в вырезанной мембране. Клетки поддерживали при 37°C в 5% СО2 и 90% влажности в модифицированной Дульбекко среде Игла, дополненной 2 мМ глутамина, 10% фетальной бычьей сыворотки, 1×NEAA, β-ΜΕ, 1×пенициллина/стрептомицина и 25 мМ HEPES, в 175 см2 колбах для культивирования. Для регистраций одиночных каналов 2500-5000 клеток высевали на покрытые поли-L-лизином предметные стекла и культивировали в течение 24-48 часов при 27°C перед использованием.
[00289] С использованием процедур, описанных выше, была измерена активность, т.е. значения EC50, соединения 1, результаты представлены в Таблице 11.
| Таблица 11 | ||
| ЕС50, столбцы гистограммы: +++<=2,0<++<=5,0<+ | ||
| Процент активности, столбцы гистограммы: +<=25,0<++<=100,0<+++ | ||
| Соед. № | ЕС50 (на основании столбцов гистограммы) | Максимальная эффективность (на основании столбцов гистограммы) |
| 1 | +++ | +++ |
Claims (9)
1. Соединение формулы III:
где независимо для каждого случая
R2 представляет собой галоген;
R3 представляет собой C1-6алифатическую группу, замещенную OP;
P представляет собой ацетил, бензоил, бензил, β-метоксиэтоксиметиловый эфир, диметокситритил, метоксиметиловый эфир, метокситритил, пара-метоксибензиловый эфир, пивалоил, тетрагидропиранил, тритил и триметилсилил; и
o представляет собой 1.
2. Соединение по п.1, где R2 представляет собой F.
3. Соединение по п.1 или 2, где R3 представляет собой C(CH3)2CH2O(бензил).
Applications Claiming Priority (16)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US32705710P | 2010-04-22 | 2010-04-22 | |
| US32709510P | 2010-04-22 | 2010-04-22 | |
| US32709110P | 2010-04-22 | 2010-04-22 | |
| US32709910P | 2010-04-22 | 2010-04-22 | |
| US11/327,099 | 2010-04-22 | ||
| US61/327,091 | 2010-04-22 | ||
| US61/327,057 | 2010-04-22 | ||
| US61/327,095 | 2010-04-22 | ||
| US32950010P | 2010-04-29 | 2010-04-29 | |
| US32949310P | 2010-04-29 | 2010-04-29 | |
| US32951010P | 2010-04-29 | 2010-04-29 | |
| US61/329,510 | 2010-04-29 | ||
| US61/329,500 | 2010-04-29 | ||
| US61/329,493 | 2010-04-29 | ||
| US33387010P | 2010-05-12 | 2010-05-12 | |
| US61/333,870 | 2010-05-12 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2012149691/04A Division RU2569678C2 (ru) | 2010-04-22 | 2011-04-21 | Способ получения циклоалкилкарбоксамидо-индольных соединений |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| RU2015145784A RU2015145784A (ru) | 2019-01-11 |
| RU2015145784A3 RU2015145784A3 (ru) | 2019-04-29 |
| RU2745977C2 true RU2745977C2 (ru) | 2021-04-05 |
Family
ID=44278819
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2015145784A RU2745977C2 (ru) | 2010-04-22 | 2011-04-21 | Способ получения циклоалкилкарбоксамидо-индольных соединений |
| RU2012149691/04A RU2569678C2 (ru) | 2010-04-22 | 2011-04-21 | Способ получения циклоалкилкарбоксамидо-индольных соединений |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2012149691/04A RU2569678C2 (ru) | 2010-04-22 | 2011-04-21 | Способ получения циклоалкилкарбоксамидо-индольных соединений |
Country Status (18)
| Country | Link |
|---|---|
| US (4) | US9035072B2 (ru) |
| EP (3) | EP3381899B1 (ru) |
| JP (4) | JP2013525371A (ru) |
| KR (3) | KR20130056244A (ru) |
| CN (2) | CN105130948A (ru) |
| AR (1) | AR081333A1 (ru) |
| AU (2) | AU2011242712B2 (ru) |
| BR (1) | BR112012027056B8 (ru) |
| CA (2) | CA2797118C (ru) |
| ES (2) | ES2608474T3 (ru) |
| HK (2) | HK1218419A1 (ru) |
| IL (3) | IL222539A0 (ru) |
| MX (3) | MX342288B (ru) |
| NZ (2) | NZ734535A (ru) |
| RU (2) | RU2745977C2 (ru) |
| SG (3) | SG184987A1 (ru) |
| TW (3) | TWI620744B (ru) |
| WO (1) | WO2011133751A2 (ru) |
Families Citing this family (89)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20100074949A1 (en) | 2008-08-13 | 2010-03-25 | William Rowe | Pharmaceutical composition and administration thereof |
| KR20060088537A (ko) | 2003-09-06 | 2006-08-04 | 버텍스 파마슈티칼스 인코포레이티드 | Atp-결합 카세트 수송체의 조절자 |
| US7977322B2 (en) | 2004-08-20 | 2011-07-12 | Vertex Pharmaceuticals Incorporated | Modulators of ATP-binding cassette transporters |
| CN101006076B (zh) | 2004-06-24 | 2010-09-29 | 沃泰克斯药物股份有限公司 | Atp-结合弹夹转运蛋白的调控剂 |
| AU2006279810B2 (en) | 2005-08-11 | 2011-10-27 | Vertex Pharmaceuticals Incorporated | Modulators of cystic fibrosis transmembrane conductance regulator |
| EP2404919B1 (en) | 2005-11-08 | 2013-08-21 | Vertex Pharmaceuticals Incorporated | Heterocyclic compound useful as a modulator of ATP-binding cassette transporters. |
| DK3219705T3 (da) | 2005-12-28 | 2020-04-14 | Vertex Pharma | Farmaceutiske sammensætninger af den amorfe form af n-[2,4-bis(1,1-dimethylethyl)-5-hydroxyphenyl]-1,4-dihydro-4-oxoquinolin-3-carboxamid |
| US7645789B2 (en) | 2006-04-07 | 2010-01-12 | Vertex Pharmaceuticals Incorporated | Indole derivatives as CFTR modulators |
| PL2007756T3 (pl) | 2006-04-07 | 2016-01-29 | Vertex Pharma | Modulatory transporterów posiadających kasetę wiążącą ATP |
| US10022352B2 (en) | 2006-04-07 | 2018-07-17 | Vertex Pharmaceuticals Incorporated | Modulators of ATP-binding cassette transporters |
| US8563573B2 (en) | 2007-11-02 | 2013-10-22 | Vertex Pharmaceuticals Incorporated | Azaindole derivatives as CFTR modulators |
| US8969386B2 (en) | 2007-05-09 | 2015-03-03 | Vertex Pharmaceuticals Incorporated | Modulators of CFTR |
| WO2009038913A2 (en) | 2007-08-24 | 2009-03-26 | Vertex Pharmaceuticals Incorporated | Isothiazolopyridinones useful for the treatment of (inter alia) cystic fibrosis |
| EP2217572B1 (en) | 2007-11-16 | 2013-11-06 | Vertex Pharmaceuticals Incorporated | Isoquinoline modulators of atp-binding cassette transporters |
| PL2225230T3 (pl) | 2007-12-07 | 2017-08-31 | Vertex Pharmaceuticals Incorporated | Stałe postacie kwasu 3-(6-(1-(2,2-difluorobenzo[d][1,3]dioksol-5-ilo)cyklopropanokarboksyamido)-3-metylopirydyn-2-ylo)benzoesowego |
| MX364936B (es) | 2007-12-07 | 2019-05-15 | Vertex Pharma | Procesos para producir acidos cicloalquilcarboxamido-piridin benzoicos. |
| US20100036130A1 (en) | 2007-12-07 | 2010-02-11 | Vertex Pharmaceuticals Incorporated | Processes for producing cycloalkylcarboxamido-pyridine benzoic acids |
| ES2647531T3 (es) | 2008-02-28 | 2017-12-22 | Vertex Pharmaceuticals Incorporated | Derivados de heteroarilo como moduladores de CFTR |
| EP2271621B1 (en) | 2008-03-31 | 2013-11-20 | Vertex Pharmaceuticals Incorporated | Pyridyl derivatives as cftr modulators |
| AR073709A1 (es) | 2008-09-29 | 2010-11-24 | Vertex Pharma | Unidades de dosis de acido 3-(6-(1-(2,2-difluorobenzeno (d) (1,3) dioxol-5-il) ciclopropancarboxamido)-3-metilpiridin-2-il) benzoico |
| PT2408750E (pt) | 2009-03-20 | 2015-10-15 | Vertex Pharma | Processo para a produção de modeladores do regulador de condutância transmembranar da fibrose cística |
| US8802868B2 (en) | 2010-03-25 | 2014-08-12 | Vertex Pharmaceuticals Incorporated | Solid forms of (R)-1(2,2-difluorobenzo[D][1,3]dioxo1-5-yl)-N-(1-(2,3-dihydroxypropyl-6-fluoro-2-(1-hydroxy-2-methylpropan2-yl)-1H-Indol-5-yl)-Cyclopropanecarboxamide |
| RS61314B1 (sr) * | 2010-03-25 | 2021-02-26 | Vertex Pharma | Čvrsta disperzija amorfnog oblika (r)-1(2,2-difluorobenzo(d)(1,3)dioksol-5-il)-n-(1-(2,3-dihidroksipropil)-6-fluoro-2-(1-hidroksi-2-metilpropan-2-il)-1h-indol-5-il)-ciklopropankarboksamida |
| NZ602838A (en) | 2010-04-07 | 2015-06-26 | Vertex Pharma | Pharmaceutical compositions of 3-(6-(1-(2,2-difluorobenzo[d][1,3]dioxol-5-yl) cyclopropanecarboxamido)-3-methylpyridin-2-yl)benzoic acid and administration thereof |
| RS54783B1 (sr) | 2010-04-07 | 2016-10-31 | Vertex Pharma | Čvrste forme 3-(6-(1-(2,2-difluorobenzo[d][1,3]dioksol-5-il)ciklopropankarboksiamido)-3-metilpiridin-2-il)benzoeve kiseline |
| SG184987A1 (en) * | 2010-04-22 | 2012-11-29 | Vertex Pharma | Process of producing cycloalkylcarboxamido-indole compounds |
| MX357328B (es) | 2011-11-08 | 2018-07-05 | Vertex Pharma | Moduladores de trasportadores de casete enlazante de atp. |
| EP2819670A1 (en) | 2012-02-27 | 2015-01-07 | Vertex Pharmaceuticals Incorporated | Pharmaceutical composition and administration thereof |
| AU2013290444B2 (en) | 2012-07-16 | 2018-04-26 | Vertex Pharmaceuticals Incorporated | Pharmaceutical compositions of (R)-1-(2,2-diflurorbenzo[d][1,3]dioxol-5-yl)-N-(1-(2,3-dihydroxypropyl)-6-fluoro-2-(1-hydroxy-2-methylpropan-2-yl)-1H-indol-5-yl) cyclopropanecarboxamide and administration thereof |
| MX365950B (es) | 2013-03-13 | 2019-06-19 | Flatley Discovery Lab Llc | Compuestos de piridazinona y metodos para el tratamiento de la fibrosis quistica. |
| MX2016006118A (es) | 2013-11-12 | 2016-07-21 | Vertex Pharma | Proceso para preparar composiciones farmaceuticas para el tratamiento de enfermedades mediadas por regulador de la conductancia transmembrana de la fibrosis quistica (cftr). |
| US10206877B2 (en) | 2014-04-15 | 2019-02-19 | Vertex Pharmaceuticals Incorporated | Pharmaceutical compositions for the treatment of cystic fibrosis transmembrane conductance regulator mediated diseases |
| GB201415381D0 (en) | 2014-08-29 | 2014-10-15 | Algipharma As | Inhalable powder formulations of alginate oligomers |
| TWI735416B (zh) | 2014-10-06 | 2021-08-11 | 美商維泰克斯製藥公司 | 囊腫纖維化症跨膜傳導調節蛋白之調節劑 |
| RU2749213C2 (ru) | 2014-10-07 | 2021-06-07 | Вертекс Фармасьютикалз Инкорпорейтед | Сокристаллы модуляторов регулятора трансмембранной проводимости при кистозном фиброзе |
| US10302602B2 (en) | 2014-11-18 | 2019-05-28 | Vertex Pharmaceuticals Incorporated | Process of conducting high throughput testing high performance liquid chromatography |
| EP3240539A4 (en) | 2014-12-31 | 2018-07-25 | Auspex Pharmaceuticals, Inc. | Cyclopropanecarboxamide modulators of cystic fibrosis transmembrane conductance regulator |
| GB201504878D0 (en) | 2015-03-23 | 2015-05-06 | Algipharma As | Use of alginate oligomers and CFTR modulators in the treatment of conditions associated with CFTR dysfuntion |
| CA2981495C (en) | 2015-03-31 | 2023-09-26 | Vertex Pharmaceuticals (Europe) Limited | Deuterated vx-661 |
| GB201517639D0 (en) | 2015-10-06 | 2015-11-18 | Algipharma As | Use of alginate oligomers to treat or prevent microbial overgrowth in the intestinal tract |
| PL3394040T3 (pl) * | 2015-12-24 | 2022-05-02 | The Regents Of The University Of California | Regulatory cftr i sposoby ich zastosowania |
| US10047077B2 (en) | 2016-04-13 | 2018-08-14 | Skyline Antiinfectives, Inc. | Deuterated O-sulfated beta-lactam hydroxamic acids and deuterated N-sulfated beta-lactams |
| CN109803962B (zh) | 2016-09-30 | 2022-04-29 | 弗特克斯药品有限公司 | 囊性纤维化跨膜传导调控蛋白的调节剂、以及药物组合物 |
| MA54847A (fr) | 2016-12-09 | 2021-12-08 | Vertex Pharma | Forme crystalline d'un n-(pyrazol-4-yl)sulfonyl-6-(pyrazol-1-yl)-2-(pyrrolidin-1-yl)pyridine-3-carboxamide pour traiter la mucoviscidose |
| US20180280349A1 (en) | 2017-03-28 | 2018-10-04 | Vertex Pharmaceuticals Incorporated | Methods of treating cystic fibrosis in patients with residual function mutations |
| EP3634402A1 (en) | 2017-06-08 | 2020-04-15 | Vertex Pharmaceuticals Incorporated | Methods of treatment for cystic fibrosis |
| US20210069174A1 (en) | 2017-07-01 | 2021-03-11 | Vertex Pharmaceuticals Incorporated | Compositions and methods for treatment of cystic fibrosis |
| WO2019018353A1 (en) | 2017-07-17 | 2019-01-24 | Vertex Pharmaceuticals Incorporated | METHODS OF TREATING CYSTIC FIBROSIS |
| WO2019018395A1 (en) | 2017-07-17 | 2019-01-24 | Vertex Pharmaceuticals Incorporated | METHODS OF TREATING CYSTIC FIBROSIS |
| ES2912657T3 (es) | 2017-08-02 | 2022-05-26 | Vertex Pharma | Procesos para preparar compuestos de pirrolidina |
| KR20200044873A (ko) | 2017-08-24 | 2020-04-29 | 더 리젠츠 오브 더 유니버시티 오브 캘리포니아 | 안구 제약학적 조성물 |
| AU2018351533B2 (en) | 2017-10-19 | 2023-02-02 | Vertex Pharmaceuticals Incorporated | Crystalline forms and compositions of CFTR modulators |
| KR20200097293A (ko) | 2017-12-08 | 2020-08-18 | 버텍스 파마슈티칼스 인코포레이티드 | 낭포성 섬유증 막횡단 전도 조절자의 조정제의 제조 방법 |
| TWI810243B (zh) | 2018-02-05 | 2023-08-01 | 美商維泰克斯製藥公司 | 用於治療囊腫纖化症之醫藥組合物 |
| CN112004817B (zh) | 2018-02-15 | 2023-06-23 | 弗特克斯药品有限公司 | 作为cftr的调节剂的大环化合物、其药物组合物、它们的用途和制备方法 |
| US11414439B2 (en) | 2018-04-13 | 2022-08-16 | Vertex Pharmaceuticals Incorporated | Modulators of cystic fibrosis transmembrane conductance regulator, pharmaceutical compositions, methods of treatment, and process for making the modulator |
| LT3880197T (lt) | 2018-11-14 | 2023-05-10 | Vertex Pharmaceuticals Incorporated | Cistinės fibrozės gydymo būdai |
| CA3067611A1 (en) | 2019-01-15 | 2020-07-15 | Apotex Inc. | Processes for the preparation of tezacaftor and intermediates thereof |
| WO2020214921A1 (en) | 2019-04-17 | 2020-10-22 | Vertex Pharmaceuticals Incorporated | Solid forms of modulators of cftr |
| WO2020256437A1 (ko) * | 2019-06-19 | 2020-12-24 | 주식회사 엘지화학 | 인돌 또는 인다졸 화합물의 제조방법 |
| CN114080383B (zh) * | 2019-06-19 | 2024-07-23 | 株式会社Lg化学 | 制备吲哚或吲唑化合物的方法 |
| CN114599657A (zh) | 2019-08-14 | 2022-06-07 | 弗特克斯药品有限公司 | Cftr调节剂的结晶形式 |
| US20220313698A1 (en) | 2019-08-14 | 2022-10-06 | Vertex Pharmaceuticals Incorporated | Modulators of cystic fibrosis transmembrane conductance regulator |
| TW202115092A (zh) | 2019-08-14 | 2021-04-16 | 美商維泰克斯製藥公司 | 囊腫纖維化跨膜傳導調節蛋白之調節劑 |
| TW202120517A (zh) | 2019-08-14 | 2021-06-01 | 美商維泰克斯製藥公司 | 製備cftr調節劑之方法 |
| CN110437125B (zh) * | 2019-09-06 | 2021-03-12 | 苏州旺山旺水生物医药有限公司 | 一种Tezacaftor中间体II的制备方法 |
| CN113121358A (zh) * | 2019-12-31 | 2021-07-16 | 阜新金特莱氟化学有限责任公司 | 2-溴-5-氟-4-硝基苯胺的制备方法 |
| CN111187197B (zh) * | 2020-01-13 | 2021-10-01 | 苏州旺山旺水生物医药有限公司 | 一种Tezacaftor中间体的合成方法 |
| US20230057246A1 (en) * | 2020-02-05 | 2023-02-23 | Laurus Labs Limited | Novel processes for preparation of tezacaftor |
| CR20230120A (es) | 2020-08-07 | 2023-09-01 | Vertex Pharma | Moduladores del regulador de la conductancia transmembrana de la fibrosis quística |
| IL300413A (en) | 2020-08-13 | 2023-04-01 | Vertex Pharma | Crystal forms of CFTR modulators |
| IL301756A (en) | 2020-10-07 | 2023-05-01 | Vertex Pharma | Cystic fibrosis transmembrane regulator conductance modulators |
| US20230374038A1 (en) | 2020-10-07 | 2023-11-23 | Vertex Pharmaceuticals Incorporated | Modulators of cystic fibrosis transmembrane conductance regulator |
| WO2022076624A1 (en) | 2020-10-07 | 2022-04-14 | Vertex Pharmaceuticals Incorporated | Modulators of cystic fibrosis transmembrane conductance regulator |
| WO2022076628A1 (en) | 2020-10-07 | 2022-04-14 | Vertex Pharmaceuticals Incorporated | Modulators of cystic fibrosis transmembrane conductance regulator |
| US20230373974A1 (en) | 2020-10-07 | 2023-11-23 | Vertex Pharmaceuticals Incorporated | Modulators of cystic fibrosis transmembrane conductance regulator |
| EP4225762A1 (en) | 2020-10-07 | 2023-08-16 | Vertex Pharmaceuticals Incorporated | Modulators of cystic fibrosis transmembrane conductance regulator |
| WO2022076622A2 (en) | 2020-10-07 | 2022-04-14 | Vertex Pharmaceuticals Incorporated | Modulators of cystic fibrosis transmembrane conductance regulator |
| WO2022076626A1 (en) | 2020-10-07 | 2022-04-14 | Vertex Pharmaceuticals Incorporated | Modulators of cystic fibrosis transmembrane conductance regulator |
| EP4225748A1 (en) | 2020-10-07 | 2023-08-16 | Vertex Pharmaceuticals Incorporated | Modulators of cystic fibrosis transmembrane conductance regulator |
| US20230382924A1 (en) | 2020-10-07 | 2023-11-30 | Vertex Pharmaceuticals Incorporated | Modulators of cystic fibrosis transmembrane conductance regulator |
| MX2023006770A (es) | 2020-12-10 | 2023-08-14 | Vertex Pharma | Metodos de tratamiento para fibrosis quistica. |
| CN113657599B (zh) * | 2021-08-20 | 2024-05-28 | 北京航空航天大学 | 事故因果推理方法、装置、电子设备及可读存储介质 |
| IL314449A (en) | 2022-02-03 | 2024-09-01 | Vertex Pharma | Cystic fibrosis treatment methods |
| AU2023215372A1 (en) | 2022-02-03 | 2024-08-22 | Vertex Pharmaceuticals Incorporated | Methods of preparing and crystalline forms of (6a,12a)-17-amino-12-methyl-6,15-bis(trifluoromethyl)-13,19-dioxa-3,4,18-triazatricyclo[ 12.3.1.12,5]nonadeca-1(18),2,4,14,16-pentaen-6-ol |
| WO2023154291A1 (en) | 2022-02-08 | 2023-08-17 | Vertex Pharmaceuticals Incorporated | Modulators of cystic fibrosis transmembrane conductance regulator |
| WO2023196429A1 (en) | 2022-04-06 | 2023-10-12 | Vertex Pharmaceuticals Incorporated | Modulators of cystic fibrosis transmembrane conductance regulator |
| WO2023224924A1 (en) | 2022-05-16 | 2023-11-23 | Vertex Pharmaceuticals Incorporated | Solid forms of a macrocyclic compounds as cftr modulators and their preparation |
| WO2023224931A1 (en) | 2022-05-16 | 2023-11-23 | Vertex Pharmaceuticals Incorporated | Methods of treatment for cystic fibrosis |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| SU620208A3 (ru) * | 1975-06-04 | 1978-08-15 | Сумитомо Кемикал Компани, Лимитед, (Фирма) | Способ получени производных индола |
| US20090131492A1 (en) * | 2006-04-07 | 2009-05-21 | Ruah Sara S Hadida | Indole derivatives as CFTR modulators |
Family Cites Families (326)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS5328173A (en) * | 1976-08-06 | 1978-03-16 | Zenyaku Kogyo Kk | Novel phenylmethanenitro compound and its preparation |
| DE2735133C2 (de) | 1977-08-04 | 1981-10-15 | Universität Karlsruhe Institut für Elektrotechnische Grundlagen der Informatik, 7500 Karlsruhe | Speicherzelle für zerstörungsfreies Auslesen mit 2 Josephson-Kontakten |
| US4138397A (en) | 1978-02-27 | 1979-02-06 | Richardson-Merrell Inc. | 6-(2,3-Dihydro-5-benzofuranyl)acetamido penicillin derivatives |
| GB8524157D0 (en) | 1984-10-19 | 1985-11-06 | Ici America Inc | Heterocyclic amides |
| JPS61103861A (ja) * | 1984-10-27 | 1986-05-22 | Nitto Kasei Kk | アリ−ル置換シアン酢酸エステルの製造方法 |
| US5304121A (en) | 1990-12-28 | 1994-04-19 | Boston Scientific Corporation | Drug delivery system making use of a hydrogel polymer coating |
| US5886026A (en) | 1993-07-19 | 1999-03-23 | Angiotech Pharmaceuticals Inc. | Anti-angiogenic compositions and methods of use |
| GB9317764D0 (en) | 1993-08-26 | 1993-10-13 | Pfizer Ltd | Therapeutic compound |
| US5510379A (en) | 1994-12-19 | 1996-04-23 | Warner-Lambert Company | Sulfonate ACAT inhibitors |
| US6099562A (en) | 1996-06-13 | 2000-08-08 | Schneider (Usa) Inc. | Drug coating with topcoat |
| JPH10213820A (ja) | 1997-01-31 | 1998-08-11 | Canon Inc | 液晶素子及び液晶装置 |
| WO1998047868A1 (en) | 1997-04-18 | 1998-10-29 | Smithkline Beecham Plc | Heterocycle-containing urea derivatives as 5ht1a, 5ht1b and 5ht1d receptor antagonists |
| DE69831233T2 (de) * | 1997-06-21 | 2006-06-01 | Roche Diagnostics Gmbh | Barbitursaure derivaten mit antimetastatischer und antitumorischer wirkung |
| DK0901786T3 (da) | 1997-08-11 | 2007-10-08 | Pfizer Prod Inc | Faste farmaceutiske dispersioner med foröget biotilgængelighed |
| US20020017295A1 (en) | 2000-07-07 | 2002-02-14 | Weers Jeffry G. | Phospholipid-based powders for inhalation |
| ATE249219T1 (de) | 1997-12-11 | 2003-09-15 | Iaf Biochem Int | Antivirale verbindungen |
| US6426331B1 (en) | 1998-07-08 | 2002-07-30 | Tularik Inc. | Inhibitors of STAT function |
| AUPP609198A0 (en) | 1998-09-22 | 1998-10-15 | Curtin University Of Technology | Use of non-peptidyl compounds for the treatment of insulin related ailments |
| EP1035115B1 (en) | 1999-02-24 | 2004-09-29 | F. Hoffmann-La Roche Ag | 4-Phenylpyridine derivatives and their use as NK-1 receptor antagonists |
| ATE329920T1 (de) | 1999-09-10 | 2006-07-15 | Novo Nordisk As | Modulatoren der protein tyrosin phosphatase (ptpases) |
| WO2001019831A1 (en) | 1999-09-10 | 2001-03-22 | Novo Nordisk A/S | MODULATORS OF PROTEIN TYROSINE PHOSPHATASES (PTPases) |
| AUPQ288499A0 (en) | 1999-09-16 | 1999-10-07 | Biota Scientific Management Pty Ltd | Antiviral agents |
| US6514964B1 (en) | 1999-09-27 | 2003-02-04 | Amgen Inc. | Fused cycloheptane and fused azacycloheptane compounds and their methods of use |
| IT1315267B1 (it) | 1999-12-23 | 2003-02-03 | Novuspharma Spa | Derivati di 2-(1h-indol-3-il)-2-oxo-acetammidi ad attivita'antitumorale |
| TWI284639B (en) | 2000-01-24 | 2007-08-01 | Shionogi & Co | A compound having thrombopoietin receptor agonistic effect |
| DE10038019A1 (de) * | 2000-08-04 | 2002-02-14 | Bayer Ag | Substituierte Triazolopyrid(az)ine |
| US6777400B2 (en) | 2000-08-05 | 2004-08-17 | Smithkline Beecham Corporation | Anti-inflammatory androstane derivative compositions |
| US6562989B2 (en) * | 2000-08-07 | 2003-05-13 | Yale University | Catalyst for aromatic C—O, C—N, and C—C bond formation |
| TWI259180B (en) | 2000-08-08 | 2006-08-01 | Hoffmann La Roche | 4-Phenyl-pyridine derivatives |
| AR030357A1 (es) | 2000-08-18 | 2003-08-20 | Lundbeck & Co As H | Derivados 4 -, 5 -, 6 - y 7-indol |
| US6550895B1 (en) | 2000-10-20 | 2003-04-22 | Silverbrook Research Pty Ltd | Moving nozzle ink jet with inlet restriction |
| DE60134679D1 (de) | 2000-10-20 | 2008-08-14 | Eisai R&D Man Co Ltd | Stickstoff enthaltende aromatische Heterozyklen |
| EP1217000A1 (en) | 2000-12-23 | 2002-06-26 | Aventis Pharma Deutschland GmbH | Inhibitors of factor Xa and factor VIIa |
| GB0102109D0 (en) | 2001-01-26 | 2001-03-14 | Syngenta Ltd | Chemical process |
| US20100074949A1 (en) | 2008-08-13 | 2010-03-25 | William Rowe | Pharmaceutical composition and administration thereof |
| EP1383799A4 (en) | 2001-04-10 | 2008-08-06 | Transtech Pharma Inc | PROBES, SYSTEMS AND METHODS FOR DISCOVERING MEDICAMENTS |
| JP4535680B2 (ja) | 2001-04-16 | 2010-09-01 | エーザイ・アール・アンド・ディー・マネジメント株式会社 | 新規1h−インダゾール化合物 |
| NZ528752A (en) | 2001-06-28 | 2006-06-30 | Pfizer Prod Inc | Triamide-substituted indoles, benzofuranes and benzothiophenes as inhibitors of microsomal triglyceride transfer protein (MTP) and/or apolipoprotein B (APO B) secretion |
| WO2003007945A1 (en) | 2001-07-20 | 2003-01-30 | Boehringer Ingelheim (Canada) Ltd. | Viral polymerase inhibitors |
| AUPR738301A0 (en) | 2001-08-30 | 2001-09-20 | Starpharma Limited | Chemotherapeutic agents |
| JP4343690B2 (ja) | 2001-11-13 | 2009-10-14 | メルク フロスト カナダ リミテツド | プロテアーゼ阻害薬としてのシアノアルキルアミノ誘導体 |
| CZ2004747A3 (cs) | 2001-12-21 | 2004-11-10 | Novo Nordisk A/S | Deriváty amidů jako GK aktivátory |
| US7074805B2 (en) | 2002-02-20 | 2006-07-11 | Abbott Laboratories | Fused azabicyclic compounds that inhibit vanilloid receptor subtype 1 (VR1) receptor |
| US20030158188A1 (en) | 2002-02-20 | 2003-08-21 | Chih-Hung Lee | Fused azabicyclic compounds that inhibit vanilloid receptor subtype 1 (VR1) receptor |
| AU2003228744A1 (en) | 2002-04-29 | 2003-11-17 | The Ohio State University | Inhibition of protein tyrosine phosphatases and sh2 domains by a neutral phosphotyrosine mimetic |
| MXPA05000130A (es) | 2002-06-27 | 2005-02-17 | Novo Nordisk As | Derivados de aril-carbonilo como agentes terapeuticos. |
| WO2004007472A1 (ja) | 2002-07-10 | 2004-01-22 | Ono Pharmaceutical Co., Ltd. | Ccr4アンタゴニストおよびその医薬用途 |
| TWI244393B (en) | 2002-08-06 | 2005-12-01 | Idenix Pharmaceuticals Inc | Crystalline and amorphous forms of beta-L-2'-deoxythymidine |
| RU2005111225A (ru) | 2002-09-18 | 2005-08-27 | Оно Фармасьютикал Ко., Лтд. (Jp) | Производные триазаспиро[5.5]ундекана и лекарственные средства, содержащие их в качестве активного ингредиента |
| MXPA05003366A (es) | 2002-09-30 | 2005-10-05 | Univ California | Inhibidores de la proteina reguladora de conductancia transmembranal de la fibrosis quistica y usos de los mismos. |
| JP2004131393A (ja) | 2002-10-08 | 2004-04-30 | Kowa Co | 易溶出性製剤 |
| US20050215614A1 (en) | 2002-10-15 | 2005-09-29 | Rigel Pharmaceuticals, Inc. | Substituted indoles and their use as hcv inhibitors |
| FR2846327B1 (fr) | 2002-10-25 | 2006-03-24 | Merck Sante Sas | Derives de n-benzodioxolyl, n-benzodioxanyl et n-benzodioxepinyl arylcarboxamides utilisables dans le traitement de dyslipidemies et compositions pharmaceutiques les contenant. |
| CA2504044A1 (en) | 2002-11-01 | 2004-05-21 | Merck & Co., Inc. | Carbonylamino-benzimidazole derivatives as androgen receptor modulators |
| DE10251019A1 (de) | 2002-11-02 | 2004-05-19 | Aventis Pharma Deutschland Gmbh | Neue Pyrimidin-4,6-dicarbonsäurediamide zur selektiven Inhibierung von Kollagenasen |
| PL375044A1 (en) | 2002-11-02 | 2005-11-14 | Sanofi-Aventis Deutschland Gmbh | Novel pyrimidine-4,6-dicarboxamides for the selective inhibition of collagenases |
| US20040146941A1 (en) | 2002-11-04 | 2004-07-29 | Biliang Zhang | Chemical encoding technology for combinatorial synthesis |
| WO2004056744A1 (en) | 2002-12-23 | 2004-07-08 | Janssen Pharmaceutica N.V. | Adamantyl acetamides as hydroxysteroid dehydrogenase inhibitors |
| DE10300017A1 (de) | 2003-01-03 | 2004-07-15 | Aventis Pharma Deutschland Gmbh | Selektive MMP 13 Inhibitoren |
| CA2512582C (en) | 2003-01-08 | 2014-07-08 | University Of Washington | Antibacterial agents |
| US6933311B2 (en) | 2003-02-11 | 2005-08-23 | Abbott Laboratories | Fused azabicyclic compounds that inhibit vanilloid receptor subtype 1 (VR1) receptor |
| ATE450533T1 (de) | 2003-02-14 | 2009-12-15 | Glaxo Group Ltd | Carboxamidderivate |
| DE10306941A1 (de) | 2003-02-18 | 2004-08-26 | Merck Patent Gmbh | Benzofuranoxyethylamine |
| EP1601657A1 (en) | 2003-03-12 | 2005-12-07 | Vertex Pharmaceuticals Incorporated | Pyrazole modulators of atp-binding cassette transporters |
| DE10315377A1 (de) | 2003-04-03 | 2004-10-14 | Merck Patent Gmbh | Carbonylverbindungen |
| WO2004087646A2 (de) | 2003-04-03 | 2004-10-14 | Merck Patent Gmbh | Pyrrolidin -1,2-dicarbonsäure-1-(phenylamid) -2- (4-(3-oxo-morpholin-4-yl)-phenylamid) derivate und verwandte verbindungen als inhibitoren des koagulationsfaktors xa zur behandlung von thromboembolischen erkrankungen |
| US20050164951A1 (en) | 2003-04-03 | 2005-07-28 | The Regents Of The University Of California | Inhibitors for the soluble epoxide hydrolase |
| ATE482747T1 (de) | 2003-04-11 | 2010-10-15 | High Point Pharmaceuticals Llc | Neue amide derivate und deren pharmazeutische verwendungen |
| ES2770035T3 (es) | 2003-04-11 | 2020-06-30 | Ptc Therapeutics Inc | Compuesto de ácido 1,2,4-oxadiazol benzoico y su uso para la supresión sin sentido y el tratamiento de enfermedades |
| WO2004110352A2 (en) | 2003-05-16 | 2004-12-23 | The Regents Of The University Of California | Compounds having activity in increasing ion transport by mutant-cftr and uses thereof |
| EP1646615B1 (en) | 2003-06-06 | 2009-08-26 | Vertex Pharmaceuticals Incorporated | Pyrimidine derivatives as modulators of atp-binding cassette transporters |
| WO2005002519A2 (en) | 2003-06-27 | 2005-01-13 | Henry M.Jackson Foundation For The Advancement Of Military Medicine, Inc. | Amphiphilic pyridinium compounds, method of making and use thereof |
| US20050113576A1 (en) | 2003-08-05 | 2005-05-26 | Chih-Hung Lee | Fused azabicyclic compounds that inhibit vanilloid receptor subtype 1 (VR1) receptor |
| MXPA06001738A (es) | 2003-08-15 | 2006-05-12 | Lundbeck & Co As H | Derivados de ciclopropilo como antagonistas del receptor nk3. |
| KR20060088537A (ko) | 2003-09-06 | 2006-08-04 | 버텍스 파마슈티칼스 인코포레이티드 | Atp-결합 카세트 수송체의 조절자 |
| US20050070718A1 (en) | 2003-09-30 | 2005-03-31 | Abbott Gmbh & Co. Kg | Heteroaryl-substituted 1,3-dihydroindol-2-one derivatives and medicaments containing them |
| JP2007509044A (ja) | 2003-10-08 | 2007-04-12 | バーテックス ファーマシューティカルズ インコーポレイテッド | シクロアルキルピラニル基を含むatp結合カセットトランスポーターのモジュレータ |
| WO2005037802A1 (ja) * | 2003-10-16 | 2005-04-28 | Sankyo Company, Limited | 5-アリールピリミジン誘導体 |
| JPWO2005040135A1 (ja) | 2003-10-24 | 2007-03-08 | 小野薬品工業株式会社 | 抗ストレス薬およびその医薬用途 |
| JP4869072B2 (ja) | 2003-11-14 | 2012-02-01 | バーテックス ファーマシューティカルズ インコーポレイテッド | Atp結合カセットトランスポーターのモジュレーターとして有用なチアゾールおよびオキサゾール |
| GB0330043D0 (en) | 2003-12-24 | 2004-01-28 | Pharmacia Italia Spa | Pyrrolo [2,3-b] pyridine derivatives active as kinase inhibitors process for their preparation and pharmaceutical compositions comprising them |
| US8759335B2 (en) | 2004-01-30 | 2014-06-24 | Vertex Pharmaceuticals Incorporated | Modulators of ATP-binding cassette transporters |
| US7977322B2 (en) | 2004-08-20 | 2011-07-12 | Vertex Pharmaceuticals Incorporated | Modulators of ATP-binding cassette transporters |
| CA2553040A1 (en) | 2004-02-02 | 2005-08-18 | Ambrx, Inc. | Modified human four helical bundle polypeptides and their uses |
| WO2005094374A2 (en) | 2004-03-30 | 2005-10-13 | The Regents Of The University Of California | Hydrazide-containing cftr inhibitor compounds and uses thereof |
| US20050222271A1 (en) | 2004-03-31 | 2005-10-06 | Le Huang | Novel amorphous form of memantine hydrochloride |
| FR2868417B1 (fr) | 2004-04-02 | 2006-06-23 | Rhodia Chimie Sa | Procede de formation d'une liaison carbone-carbone |
| CA2568499A1 (en) | 2004-06-01 | 2005-12-15 | Tm Bioscience Corporation | Method of detecting cystic fibrosis associated mutations |
| EP1765347A4 (en) | 2004-06-04 | 2008-10-01 | Univ California | COMPOUNDS WITH ION TRANSPORTER HEALING EFFECT BY MUTANT CFTR AND ITS USE |
| US20140343098A1 (en) | 2004-06-24 | 2014-11-20 | Vertex Pharmaceuticals Incorporated | Modulators of atp-binding cassette transporters |
| US8354427B2 (en) | 2004-06-24 | 2013-01-15 | Vertex Pharmaceutical Incorporated | Modulators of ATP-binding cassette transporters |
| CN101006076B (zh) | 2004-06-24 | 2010-09-29 | 沃泰克斯药物股份有限公司 | Atp-结合弹夹转运蛋白的调控剂 |
| CA2572292A1 (en) | 2004-07-02 | 2006-02-09 | Advancis Pharmaceutical Corporation | Tablet for pulsed delivery |
| GB0416730D0 (en) | 2004-07-27 | 2004-09-01 | Novartis Ag | Organic compounds |
| MX2007001215A (es) | 2004-08-06 | 2007-04-17 | Otsuka Pharma Co Ltd | Compuestos aromaticos. |
| DE102004047254A1 (de) | 2004-09-29 | 2006-04-13 | Merck Patent Gmbh | Carbonylverbindungen |
| CA2583177A1 (en) | 2004-10-13 | 2006-04-27 | Ptc Therapeutics, Inc. | Compounds for nonsense suppression, and methods for their use |
| NZ554555A (en) | 2004-10-20 | 2011-09-30 | Univ California | Cyclohexyl-urea derivatives as improved inhibitors for the soluble epoxide hydrolase |
| US20080051418A1 (en) | 2004-11-26 | 2008-02-28 | Tsuyoshi Maekawa | Arylalkanoic Acid Derivative |
| NZ560513A (en) | 2005-02-25 | 2010-07-30 | Ono Pharmaceutical Co | Indole compound and use thereof |
| EP1865949B1 (en) | 2005-03-11 | 2012-11-14 | Vertex Pharmaceuticals Incorporated | Modulators of ATP-binding cassette transporters |
| KR20070114820A (ko) | 2005-03-18 | 2007-12-04 | 더 리젠츠 오브 더 유니버시티 오브 캘리포니아 | 돌연변이-cftr 처리를 보정하는데 활성을 가지는화합물 및 이것의 사용 |
| US20100120789A1 (en) | 2005-03-24 | 2010-05-13 | Nigel Vicker | Compound |
| US7402596B2 (en) | 2005-03-24 | 2008-07-22 | Renovis, Inc. | Bicycloheteroaryl compounds as P2X7 modulators and uses thereof |
| GB0506133D0 (en) | 2005-03-24 | 2005-05-04 | Sterix Ltd | Compound |
| EP1864978A4 (en) | 2005-03-28 | 2009-07-01 | Toyama Chemical Co Ltd | PROCESS FOR PRODUCING 1- (3- (2- (1-BENZOTHIOPHEN-5-YL) -ETHOXY) PROPYL) AZETIDIN-3-OL OR ITS SALTS |
| JP2006282534A (ja) | 2005-03-31 | 2006-10-19 | Fuji Photo Film Co Ltd | アミド類の製造方法 |
| NZ562197A (en) | 2005-04-08 | 2010-09-30 | Ptc Therapeutics Inc | Compositions of an orally active 1,2,4-oxadiazole for nonsense mutation suppression therapy |
| US20070032475A1 (en) | 2005-04-15 | 2007-02-08 | Ye Xiaocong M | Novel compounds useful for bradykinin B1 receptor antagonism |
| CA2609392A1 (en) | 2005-05-24 | 2006-11-30 | Vertex Pharmaceuticals Incorporated | Modulators of atp-binding cassette transporters |
| AU2006279810B2 (en) | 2005-08-11 | 2011-10-27 | Vertex Pharmaceuticals Incorporated | Modulators of cystic fibrosis transmembrane conductance regulator |
| CN101287732A (zh) | 2005-08-11 | 2008-10-15 | 沃泰克斯药物股份有限公司 | 囊性纤维化跨膜电导调节剂的调控剂 |
| AU2006297414A1 (en) * | 2005-09-29 | 2007-04-12 | Wyeth | 1- (1H- indol- 1-yl) -3- (methylamino) -1- phenylpropan-2-ol derivatives and related compounds as modulators of the monoamine reuptake for the treatment of vasomotor symptoms (VMS) |
| US8314256B2 (en) | 2005-10-06 | 2012-11-20 | Vertex Pharmaceuticals Incorporated | Modulators of ATP-binding cassette transporters |
| JP2009514875A (ja) | 2005-11-02 | 2009-04-09 | サイトキネティクス・インコーポレーテッド | 化学物質、組成物、および方法 |
| EP2404919B1 (en) | 2005-11-08 | 2013-08-21 | Vertex Pharmaceuticals Incorporated | Heterocyclic compound useful as a modulator of ATP-binding cassette transporters. |
| US20120232059A1 (en) | 2005-11-08 | 2012-09-13 | Vertex Pharmaceuticals Incorporated | Modulators of ATP-Binding Cassette Transporters |
| GB0525144D0 (en) | 2005-12-09 | 2006-01-18 | Novartis Ag | Organic compounds |
| DK1966214T3 (en) * | 2005-12-21 | 2017-02-13 | Janssen Pharmaceutica Nv | TRIAZOLPYRIDAZINES AS TYROSINKINASA MODULATORS |
| JP2009521468A (ja) | 2005-12-24 | 2009-06-04 | バーテックス ファーマシューティカルズ インコーポレイテッド | Abc輸送体の調節因子としてのキノリン−4−オン誘導体 |
| EP1974212A1 (en) | 2005-12-27 | 2008-10-01 | Vertex Pharmaceuticals Incorporated | Compounds useful in cftr assays and methods therewith |
| JP5165586B2 (ja) | 2005-12-28 | 2013-03-21 | バーテックス ファーマシューティカルズ インコーポレイテッド | 嚢胞性線維症の処置のためのATP結合カセットトランスポーターのモジュレーターとしての、1−(ベンゾ[d][1,3]ジオキソール−5−イル)−N−(フェニル)シクロプロパン−カルボキサミド誘導体および関連化合物 |
| DK3219705T3 (da) | 2005-12-28 | 2020-04-14 | Vertex Pharma | Farmaceutiske sammensætninger af den amorfe form af n-[2,4-bis(1,1-dimethylethyl)-5-hydroxyphenyl]-1,4-dihydro-4-oxoquinolin-3-carboxamid |
| US7671221B2 (en) | 2005-12-28 | 2010-03-02 | Vertex Pharmaceuticals Incorporated | Modulators of ATP-Binding Cassette transporters |
| TW200808723A (en) | 2006-03-13 | 2008-02-16 | Univ California | Conformationally restricted urea inhibitors of soluble epoxide hydrolase |
| RS20090406A (en) | 2006-03-20 | 2010-12-31 | Vertex Pharmaceuticals Incorporated | Pharmaceutical compositions |
| EP2001498A4 (en) | 2006-03-20 | 2013-01-23 | Vertex Pharma | PHARMACEUTICAL COMPOSITIONS |
| WO2007111994A2 (en) | 2006-03-22 | 2007-10-04 | Syndexa Pharmaceuticals Corporation | Compounds and methods for treatment of disorders associated with er stress |
| US10022352B2 (en) | 2006-04-07 | 2018-07-17 | Vertex Pharmaceuticals Incorporated | Modulators of ATP-binding cassette transporters |
| PL2007756T3 (pl) | 2006-04-07 | 2016-01-29 | Vertex Pharma | Modulatory transporterów posiadających kasetę wiążącą ATP |
| ATE534383T1 (de) | 2006-05-12 | 2011-12-15 | Vertex Pharma | Zusammensetzungen aus n-ä2,4-bis(1,1- dimethylethyl)-5-hydroxyphenylü-1,4-dihydro-4- oxochinolin-3-carboxamid |
| WO2007146712A2 (en) | 2006-06-09 | 2007-12-21 | Kemia, Inc. | Therapy using cytokine inhibitors |
| WO2008020227A2 (en) | 2006-08-17 | 2008-02-21 | Astrazeneca Ab | Antibacterial pyrrolecarboxamides |
| WO2008029168A2 (en) | 2006-09-08 | 2008-03-13 | Summit Corporation Plc | Treatment of duchenne muscular dystrophy |
| WO2008029152A2 (en) | 2006-09-08 | 2008-03-13 | Summit Corporation Plc | Treatment of duchenne muscular dystrophy |
| BRPI0717317A2 (pt) * | 2006-10-23 | 2013-10-22 | Sgx Pharmaceuticals Inc | Modularoes da proteína cinase triazalopiridazina |
| US8563573B2 (en) | 2007-11-02 | 2013-10-22 | Vertex Pharmaceuticals Incorporated | Azaindole derivatives as CFTR modulators |
| CN103159760B (zh) | 2006-11-03 | 2016-06-08 | 沃泰克斯药物股份有限公司 | 作为cftr调控剂的氮杂吲哚衍生物 |
| US7754739B2 (en) | 2007-05-09 | 2010-07-13 | Vertex Pharmaceuticals Incorporated | Modulators of CFTR |
| US20080132560A1 (en) | 2006-11-21 | 2008-06-05 | San-Laung Chow | Solid dispersion composition |
| WO2008065732A1 (fr) | 2006-11-27 | 2008-06-05 | Nippon Polyurethane Industry Co., Ltd. | Procédé de production d'un mélange à base d'isocyanate modifié contenant une liaison allophanate et une liaison isocyanurate |
| US20080260820A1 (en) | 2007-04-19 | 2008-10-23 | Gilles Borrelly | Oral dosage formulations of protease-resistant polypeptides |
| US8969386B2 (en) | 2007-05-09 | 2015-03-03 | Vertex Pharmaceuticals Incorporated | Modulators of CFTR |
| CN101687883B (zh) | 2007-05-25 | 2012-05-23 | 沃泰克斯药物股份有限公司 | 囊性纤维化跨膜传导调节因子的调节剂 |
| US8557823B2 (en) | 2007-06-18 | 2013-10-15 | Advanced Cancer Therapeutics, Llc | Family of PFKFB3 inhibitors with anti-neoplastic activities |
| WO2008156783A2 (en) | 2007-06-18 | 2008-12-24 | University Of Louisville Research Foundation, Inc. | Family of pfkfb3 inhibitors with anti-neoplastic activities |
| ES2551095T3 (es) | 2007-07-19 | 2015-11-16 | Lundbeck, H., A/S | Amidas heterocíclicas de 5 miembros y compuestos relacionados |
| US20110177999A1 (en) | 2007-08-09 | 2011-07-21 | Vertex Pharmaceuticals Incorporated | Therapeutic Combinations Useful in Treating CFTR Related Diseases |
| WO2009038913A2 (en) | 2007-08-24 | 2009-03-26 | Vertex Pharmaceuticals Incorporated | Isothiazolopyridinones useful for the treatment of (inter alia) cystic fibrosis |
| JP5461405B2 (ja) | 2007-09-14 | 2014-04-02 | バーテックス ファーマシューティカルズ インコーポレイテッド | 嚢胞性線維症膜コンダクタンス制御因子の調節因子 |
| NZ583848A (en) | 2007-09-14 | 2012-07-27 | Vertex Pharma | Solid forms of n-[2,4-bis(1,1-dimethylethyl)-5-hydroxyphenyl]-1,4-dihydro-4-oxoquinoline-3-carboxamide |
| WO2009055917A1 (en) | 2007-11-02 | 2009-05-07 | Methylgene Inc. | Inhibitors of histone deacetylase |
| EP2217572B1 (en) | 2007-11-16 | 2013-11-06 | Vertex Pharmaceuticals Incorporated | Isoquinoline modulators of atp-binding cassette transporters |
| EP2218718A1 (en) | 2007-11-22 | 2010-08-18 | Zenyaku Kogyo Kabushikikaisha | Amorphous form of heterocyclic compound, solid dispersion and medicinal preparation each comprising the same, and process for production of the same |
| PL2225230T3 (pl) | 2007-12-07 | 2017-08-31 | Vertex Pharmaceuticals Incorporated | Stałe postacie kwasu 3-(6-(1-(2,2-difluorobenzo[d][1,3]dioksol-5-ilo)cyklopropanokarboksyamido)-3-metylopirydyn-2-ylo)benzoesowego |
| MX364936B (es) | 2007-12-07 | 2019-05-15 | Vertex Pharma | Procesos para producir acidos cicloalquilcarboxamido-piridin benzoicos. |
| US20100036130A1 (en) | 2007-12-07 | 2010-02-11 | Vertex Pharmaceuticals Incorporated | Processes for producing cycloalkylcarboxamido-pyridine benzoic acids |
| EP2237768A2 (en) | 2007-12-07 | 2010-10-13 | Vertex Pharmaceuticals Incorporated | Formulations of 3-(6-(1-(2,2-difluorobenzo[d][1,3]dioxol-5-yl) cyclopropanecarboxamido)-3-methylpyridin-2-yl)benzoic acid |
| EP2231671B1 (en) | 2007-12-13 | 2013-04-24 | Vertex Pharmaceuticals Incorporated | Modulators of cystic fibrosis transmembrane conductance regulator |
| US20090247521A1 (en) | 2007-12-28 | 2009-10-01 | Arete Therapeutics, Inc. | Soluble epoxide hydrolase inhibitors for the treatment of endothelial dysfunction |
| ES2647531T3 (es) | 2008-02-28 | 2017-12-22 | Vertex Pharmaceuticals Incorporated | Derivados de heteroarilo como moduladores de CFTR |
| EP2271621B1 (en) | 2008-03-31 | 2013-11-20 | Vertex Pharmaceuticals Incorporated | Pyridyl derivatives as cftr modulators |
| US20110071197A1 (en) | 2008-04-16 | 2011-03-24 | Peter Nilsson | Bis-aryl compounds for use as medicaments |
| WO2009129501A1 (en) | 2008-04-18 | 2009-10-22 | Arete Therapeutics, Inc. | Use of soluble epoxide hydrolase inhibitors in the treatment of smooth muscle disorders |
| PT2276485E (pt) | 2008-04-24 | 2014-10-20 | Bristol Myers Squibb Co | Utilização de epotilona d no tratamento de doenças tauassociadas que compreendem a doença de alzheimer |
| US20110112193A1 (en) | 2008-05-14 | 2011-05-12 | Peter Nilsson | Bis-aryl compounds for use as medicaments |
| US9447049B2 (en) | 2010-03-01 | 2016-09-20 | University Of Tennessee Research Foundation | Compounds for treatment of cancer |
| US8822513B2 (en) | 2010-03-01 | 2014-09-02 | Gtx, Inc. | Compounds for treatment of cancer |
| US20100256184A1 (en) | 2008-08-13 | 2010-10-07 | Vertex Pharmaceuticals Incorporated | Pharmaceutical composition and administrations thereof |
| CA2733908C (en) | 2008-08-13 | 2017-05-30 | Vertex Pharmaceuticals Incorporated | Pharmaceutical composition comprising a solid dispersion of n-[2,4-bis(1,1-dimethylethyl)-5-hydroxyphenyl]-1,4-dihydro-4-oxoquinoline-3-carboxamide |
| US8895781B2 (en) | 2008-09-04 | 2014-11-25 | Georgetown University | Transition metal-catalyzed C—H amination using unactivated amines |
| AR073578A1 (es) | 2008-09-15 | 2010-11-17 | Priaxon Ag | Pirrolidin-2-onas |
| AR073709A1 (es) | 2008-09-29 | 2010-11-24 | Vertex Pharma | Unidades de dosis de acido 3-(6-(1-(2,2-difluorobenzeno (d) (1,3) dioxol-5-il) ciclopropancarboxamido)-3-metilpiridin-2-il) benzoico |
| WO2010048149A2 (en) | 2008-10-20 | 2010-04-29 | Kalypsys, Inc. | Heterocyclic modulators of gpr119 for treatment of disease |
| US20110257223A1 (en) * | 2008-10-23 | 2011-10-20 | Vertex Pharmaceuticals Incorporated | Modulators of Cystic Fibrosis Transmembrane Conductance Regulator |
| ES2532138T3 (es) | 2008-10-23 | 2015-03-24 | Vertex Pharmaceuticals Incorporated | Moduladores del regulador de la conductancia transmembrana de la fibrosis quística |
| TWI465449B (zh) * | 2008-10-23 | 2014-12-21 | Vertex Pharma | 囊腫性纖維化跨膜傳導調節因子之調控因子 |
| EP2358680B1 (en) | 2008-10-23 | 2013-03-20 | Vertex Pharmaceuticals Incorporated | Solid forms of n-(4-(7-azabicyclo[2.2.1]heptan-7-yl)-2-(trifluoromethyl)phenyl)-4-oxo-5-(trifluoromethyl)-1,4-dihydroquinoline-3-carboxamide |
| UA104876C2 (ru) | 2008-11-06 | 2014-03-25 | Вертекс Фармасьютікалз Інкорпорейтед | Модуляторы атф-связывающих кассетных транспортеров |
| ES2532753T3 (es) | 2008-11-06 | 2015-03-31 | Vertex Pharmaceuticals Incorporated | Moduladores de transportadores del casete de unión a ATP |
| CA2743241A1 (en) | 2008-11-27 | 2010-06-03 | Boehringer Ingelheim International Gmbh | 6,7,8,9-tetrahydro-5h-1,4,7,10a-tetraaza-cyclohept[f]indene derivatives, pharmaceutical compositions containing these compounds, their use and processes for preparing them |
| BRPI0922364A2 (pt) | 2008-12-03 | 2017-08-29 | Presidio Pharmaceuticals Inc | Composto, composição farmacêutica e uso de um composto |
| US8367660B2 (en) | 2008-12-30 | 2013-02-05 | Vertex Pharmaceuticals Incorporated | Modulators of cystic fibrosis transmembrane conductance regulator |
| US8946419B2 (en) | 2009-02-23 | 2015-02-03 | Mallinckrodt Llc | (+)-6-hydroxy-morphinan or (+)-6-amino-morphinan derivatives |
| WO2010104307A2 (ko) | 2009-03-07 | 2010-09-16 | 주식회사 메디젠텍 | 세포핵에서 세포질로의 gsk3의 이동을 억제하는 화합물을 함유하는 세포핵에서 세포질로의 gsk3 이동에 의해 발생되는 질환의 치료 또는 예방용 약학적 조성물 |
| AU2010226393B2 (en) | 2009-03-20 | 2016-08-11 | Vertex Pharmaceuticals Incorporated | Modulators of cystic fibrosis transmembrane conductance regulator |
| PT2408750E (pt) | 2009-03-20 | 2015-10-15 | Vertex Pharma | Processo para a produção de modeladores do regulador de condutância transmembranar da fibrose cística |
| GB0905641D0 (en) | 2009-04-01 | 2009-05-13 | Serodus As | Compounds |
| DK2419429T3 (da) | 2009-04-16 | 2014-06-23 | Ct Nac De Investigaciones Oncológicas Cnio | Imidazopyraziner som inhibitorer af proteinkinaser |
| WO2011005355A1 (en) | 2009-05-07 | 2011-01-13 | Achaogen, Inc. | Combinations comprising a lpxc inhibitor and an antibiotic for use in the treatment of infections caused by gram-negative bacteria |
| CN105254557A (zh) | 2009-05-29 | 2016-01-20 | 拉夸里亚创药株式会社 | 作为钙或钠通道阻滞剂的芳基取代羧酰胺衍生物 |
| EP2264012A1 (de) | 2009-06-03 | 2010-12-22 | Bayer CropScience AG | Heteroarylamidine und deren Verwendung als Fungizide |
| KR101256018B1 (ko) | 2009-08-20 | 2013-04-18 | 한국과학기술연구원 | 단백질 키나아제 저해활성을 갖는 1,3,6-치환된 인돌 화합물 |
| WO2011029832A1 (de) | 2009-09-09 | 2011-03-17 | Vifor (International) Ag | Neue thiazol- und oxazol-hepcidin-antagonisten |
| CN102498112B (zh) | 2009-09-17 | 2015-05-20 | 沃泰克斯药物股份有限公司 | 制备氮杂二环化合物的方法 |
| US9334230B2 (en) | 2009-09-18 | 2016-05-10 | Nanyang Technological University | Process of forming an amide |
| EP2490687A1 (en) | 2009-10-22 | 2012-08-29 | Vertex Pharmaceuticals Incorporated | Compositions for treatment of cystic fibrosis and other chronic diseases |
| BR112012009583A2 (pt) | 2009-10-23 | 2015-09-29 | Vertex Pharma | processo para preparação de moduladores de regulador de condutância de transmembrana de fibrose cística |
| MX2012004791A (es) | 2009-10-23 | 2013-02-01 | Vertex Pharma | Formas sólidas de n-(4-(7-azabiciclo[2.2.1]heptan-7-il)-2-(trifluo rometil)fenil)-4-oxo-5-(trifluorometil)-1,4-dihidroquinolina-3-ca rboxamida. |
| WO2011094890A1 (en) | 2010-02-02 | 2011-08-11 | Argusina Inc. | Phenylalanine derivatives and their use as non-peptide glp-1 receptor modulators |
| RU2581367C2 (ru) | 2010-03-01 | 2016-04-20 | Джи Ти Икс, ИНК. | Соединения для лечения рака |
| WO2011115892A1 (en) | 2010-03-15 | 2011-09-22 | Griffin Patrick R | Modulators of the retinoic acid receptor-related orphan receptors |
| EP3037415A1 (en) | 2010-03-19 | 2016-06-29 | Vertex Pharmaceuticals Inc. | Solid form of n-[2,4-bis(1,1-dimethylethyl)-5-hydroxyphenyl]-1,4-dihydro-4-oxoquinoline-3-carboxamide |
| US8802868B2 (en) * | 2010-03-25 | 2014-08-12 | Vertex Pharmaceuticals Incorporated | Solid forms of (R)-1(2,2-difluorobenzo[D][1,3]dioxo1-5-yl)-N-(1-(2,3-dihydroxypropyl-6-fluoro-2-(1-hydroxy-2-methylpropan2-yl)-1H-Indol-5-yl)-Cyclopropanecarboxamide |
| RS61314B1 (sr) * | 2010-03-25 | 2021-02-26 | Vertex Pharma | Čvrsta disperzija amorfnog oblika (r)-1(2,2-difluorobenzo(d)(1,3)dioksol-5-il)-n-(1-(2,3-dihidroksipropil)-6-fluoro-2-(1-hidroksi-2-metilpropan-2-il)-1h-indol-5-il)-ciklopropankarboksamida |
| RS54783B1 (sr) | 2010-04-07 | 2016-10-31 | Vertex Pharma | Čvrste forme 3-(6-(1-(2,2-difluorobenzo[d][1,3]dioksol-5-il)ciklopropankarboksiamido)-3-metilpiridin-2-il)benzoeve kiseline |
| NZ602838A (en) | 2010-04-07 | 2015-06-26 | Vertex Pharma | Pharmaceutical compositions of 3-(6-(1-(2,2-difluorobenzo[d][1,3]dioxol-5-yl) cyclopropanecarboxamido)-3-methylpyridin-2-yl)benzoic acid and administration thereof |
| WO2011133951A1 (en) | 2010-04-22 | 2011-10-27 | Vertex Pharmaceuticals Incorporated | Pharmaceutical compositions and administrations thereof |
| SG184987A1 (en) * | 2010-04-22 | 2012-11-29 | Vertex Pharma | Process of producing cycloalkylcarboxamido-indole compounds |
| CA2796602A1 (en) * | 2010-04-22 | 2011-10-27 | Vertex Pharmaceuticals Incorporated | Pharmaceutical compositions and administrations thereof |
| NZ603044A (en) * | 2010-04-22 | 2015-08-28 | Vertex Pharma | Pharmaceutical compositions comprising cftr modulators and administrations thereof |
| EP2386606B1 (fr) | 2010-04-30 | 2018-03-21 | Total Marketing Services | Utilisation de dérivés organogelateurs dans des compositions bitumineuses pour améliorer leur résistance aux agressions chimiques |
| EP2571506B1 (en) | 2010-05-20 | 2017-05-10 | Cempra Pharmaceuticals, Inc. | Processes for preparing macrolides and ketolides and intermediates therefor |
| WO2011146886A1 (en) | 2010-05-20 | 2011-11-24 | Vertex Pharmaceuticals Incorporated | Processes for producing modulators of cystic fibrosis transmembrane conductance regulator |
| CA2798412A1 (en) | 2010-05-20 | 2011-11-24 | Vertex Pharmaceuticals Incorporated | Pharmaceutical compositions and administrations thereof |
| US8563593B2 (en) * | 2010-06-08 | 2013-10-22 | Vertex Pharmaceuticals Incorporated | Formulations of (R)-1-(2,2-difluorobenzo[D] [1,3] dioxol-5-yl)-N-(1-(2,3-dihydroxypropyl)-6-fluoro-2-(1-hydroxy-2-methylpropan-2-yl)-1H-indol-5-yl)cyclopropanecarboxamide |
| US20120149708A1 (en) | 2010-06-17 | 2012-06-14 | George Mason University | Modulators of viral transcription, and methods and compositions therewith |
| UA110113C2 (xx) | 2010-07-29 | 2015-11-25 | Біциклічні азагетероциклічні карбоксаміди | |
| WO2012016133A2 (en) | 2010-07-29 | 2012-02-02 | President And Fellows Of Harvard College | Ros1 kinase inhibitors for the treatment of glioblastoma and other p53-deficient cancers |
| CA2808501A1 (en) * | 2010-08-23 | 2012-03-01 | Vertex Pharmaceuticals Incorporated | Pharmaceutical composition of (r)-1-(2,2-difluorobenzo[d][1,3]dioxol-5-yl)-n-(1-(2,3-dihydroxy propyl)-6-fluoro-2-(1-hydroxy-2-methylpropan-2-yl)-1h-indol-5-yl) cyclopropanecarboxamide and administration therof |
| MX2013002353A (es) | 2010-08-27 | 2013-09-26 | Vertex Pharma | Composicion farmaceutica y administraciones de la misma. |
| WO2012049555A1 (en) | 2010-10-13 | 2012-04-19 | Lupin Limited | Spirocyclic compounds as voltage-gated sodium channel modulators |
| WO2012052540A1 (en) | 2010-10-21 | 2012-04-26 | Universitaet Des Saarlandes | Selective cyp11b1 inhibitors for the treatment of cortisol dependent diseases |
| US8802700B2 (en) | 2010-12-10 | 2014-08-12 | Vertex Pharmaceuticals Incorporated | Modulators of ATP-Binding Cassette transporters |
| WO2012079583A1 (en) | 2010-12-15 | 2012-06-21 | Aarhus Universitet | System providing controlled delivery of gaseous co for carbonylation reactions |
| CA2827392A1 (en) | 2011-02-24 | 2012-08-30 | Emory University | Noggin blocking compositions for ossification and methods related thereto |
| WO2012129562A2 (en) | 2011-03-24 | 2012-09-27 | The Scripps Research Institute | Compounds and methods for inducing chondrogenesis |
| CN102731492B (zh) | 2011-03-30 | 2016-06-29 | 江苏恒瑞医药股份有限公司 | 环己烷类衍生物、其制备方法及其在医药上的应用 |
| HUE047354T2 (hu) | 2011-05-18 | 2020-04-28 | Vertex Pharmaceuticals Europe Ltd | Ivacaftor deuterizált származékai |
| US8945605B2 (en) | 2011-06-07 | 2015-02-03 | Parion Sciences, Inc. | Aerosol delivery systems, compositions and methods |
| WO2013005057A1 (en) | 2011-07-07 | 2013-01-10 | Centro Nacional De Investigaciones Oncológicas (Cnio) | New compounds |
| BR112014005286B1 (pt) | 2011-09-09 | 2022-08-23 | Lantheus Medical Imaging, Inc | Compostos de um primeiro e um segundo agente de imageamento para determinar incompatibilidade de inervação e perfusão na parte do indivíduo |
| WO2013038373A1 (en) | 2011-09-16 | 2013-03-21 | Novartis Ag | Pyridine amide derivatives |
| WO2013038381A1 (en) | 2011-09-16 | 2013-03-21 | Novartis Ag | Pyridine/pyrazine amide derivatives |
| WO2013038386A1 (en) | 2011-09-16 | 2013-03-21 | Novartis Ag | Heterocyclic compounds for the treatment of cystic fibrosis |
| JP6165733B2 (ja) | 2011-09-16 | 2017-07-19 | ノバルティス アーゲー | N−置換ヘテロシクリルカルボキサミド類 |
| WO2013038378A1 (en) | 2011-09-16 | 2013-03-21 | Novartis Ag | Pyridine amide derivatives |
| GB201116559D0 (en) | 2011-09-26 | 2011-11-09 | Univ Leuven Kath | Novel viral replication inhibitors |
| CA2853299A1 (en) | 2011-11-02 | 2013-05-10 | Vertex Pharmaceuticals Incorporated | Use of (n-[2,4-bis(1,1-dimethylethyl)-5-hydroxyphenyl]-1,4-dihydro-4-oxoquinoline-3-carboxamide) for treating cftr mediated diseases |
| MX357328B (es) * | 2011-11-08 | 2018-07-05 | Vertex Pharma | Moduladores de trasportadores de casete enlazante de atp. |
| US20140127901A1 (en) * | 2012-11-08 | 2014-05-08 | Taiwan Semiconductor Manufacturing Company, Ltd. | Low-k damage free integration scheme for copper interconnects |
| WO2013086131A1 (en) | 2011-12-06 | 2013-06-13 | The Trustees Of The University Of Pennsylvania | Inhibitors targeting drug-resistant influenza a |
| US8772541B2 (en) | 2011-12-15 | 2014-07-08 | University of Pittsburgh—of the Commonwealth System of Higher Education | Cannabinoid receptor 2 (CB2) inverse agonists and therapeutic potential for multiple myeloma and osteoporosis bone diseases |
| EP2606726A1 (de) | 2011-12-21 | 2013-06-26 | Bayer CropScience AG | N-Arylamidine-substituierte trifluoroethylsulfid-Derivate als Akarizide und Insektizide |
| KR20140117612A (ko) | 2012-01-25 | 2014-10-07 | 버텍스 파마슈티칼스 인코포레이티드 | 3-(6-(1-(2,2-다이플루오로벤조[d][1,3]다이옥솔-5-일) 사이클로프로판카르복사미도)-3-메틸피리딘-2-일)벤조산의 제형 |
| EP2819670A1 (en) | 2012-02-27 | 2015-01-07 | Vertex Pharmaceuticals Incorporated | Pharmaceutical composition and administration thereof |
| JP2015518504A (ja) | 2012-04-03 | 2015-07-02 | スリーエム イノベイティブ プロパティズ カンパニー | 光塩基発生剤を含む架橋性組成物 |
| US8674108B2 (en) | 2012-04-20 | 2014-03-18 | Vertex Pharmaceuticals Incorporated | Solid forms of N-[2,4-bis(1,1-dimethylethy)-5-hydroxyphenyl]-1,4-dihydro-4-oxoquinoline-3-carboxamide |
| US9528016B2 (en) | 2012-04-26 | 2016-12-27 | Xerox Corporation | Phase change inks comprising crystalline amides |
| US8888905B2 (en) | 2012-04-26 | 2014-11-18 | Xerox Corporation | Fast crystallizing crystalline-amorphous ink compositions and methods for making the same |
| CA2813472A1 (en) | 2012-04-26 | 2013-10-26 | Xerox Corporation | Rapid solidifying crystalline-amorphous inks |
| US9228101B2 (en) | 2012-04-26 | 2016-01-05 | Xerox Corporation | Rapidly crystallizing phase change inks and methods for forming the same |
| US20130284054A1 (en) | 2012-04-26 | 2013-10-31 | Xerox Corporation | Rapid solidifying crystalline-amorphous inks |
| GB2502624A (en) | 2012-06-01 | 2013-12-04 | Univ East Anglia | Phosphoramide and phosphoramide-based catalysts and their use in intermolecular aziridination |
| EP2859005B1 (en) | 2012-06-08 | 2018-10-31 | Massachusetts Institute of Technology | Phosphine-ligated palladium sulfonate palladacycles |
| AU2013270681A1 (en) * | 2012-06-08 | 2014-12-18 | Vertex Pharmaceuticals Incorporated | Pharmaceutical compositions for the treatment of CFTR -mediated disorders |
| FR2992317B1 (fr) | 2012-06-22 | 2016-05-13 | Diverchim | Procede de preparation de peptides chiraux |
| WO2014002106A1 (en) | 2012-06-25 | 2014-01-03 | Cadila Healthcare Limited | Novel compounds for the treatment of dyslipidemia and related diseases |
| NZ703824A (en) | 2012-07-12 | 2018-06-29 | Proqr Therapeutics Ii Bv | Oligonucleotides for making a change in the sequence of a target rna molecule present in a living cell |
| WO2014011050A1 (en) | 2012-07-12 | 2014-01-16 | Proqr Therapeutics B.V. | Exon replacement with stabilized artificial rnas |
| AU2013290444B2 (en) | 2012-07-16 | 2018-04-26 | Vertex Pharmaceuticals Incorporated | Pharmaceutical compositions of (R)-1-(2,2-diflurorbenzo[d][1,3]dioxol-5-yl)-N-(1-(2,3-dihydroxypropyl)-6-fluoro-2-(1-hydroxy-2-methylpropan-2-yl)-1H-indol-5-yl) cyclopropanecarboxamide and administration thereof |
| US10207989B2 (en) | 2012-09-20 | 2019-02-19 | Temple University—Of the Commonwealth System of Higher Education | Substituted alkyl diaryl derivatives, methods of preparation and uses |
| WO2014068893A1 (ja) | 2012-10-29 | 2014-05-08 | コニカミノルタ株式会社 | 位相差フィルム、円偏光板、及び画像表示装置 |
| HRP20181740T4 (hr) | 2012-11-02 | 2024-01-05 | Vertex Pharmaceuticals Incorporated | Farmaceutski pripravci za liječenje bolesti koje su posredovane s cftr |
| US9757379B2 (en) | 2012-11-14 | 2017-09-12 | The Board Of Regents Of The University Of Texas System | Inhibition of HIF-2α heterodimerization with HIF1β (ARNT) |
| JP6146990B2 (ja) | 2012-11-16 | 2017-06-14 | コンサート ファーマシューティカルズ インコーポレイテッド | 重水素化されたcftr増強物質 |
| SG11201503959VA (en) | 2012-11-20 | 2015-06-29 | Merial Inc | Anthelmintic compounds and compositions and method of using thereof |
| ITMI20122065A1 (it) | 2012-12-03 | 2014-06-04 | Univ Padova | Uso dei correttori del cftr nel trattamento delle patologie del muscolo striato |
| EP2929346A1 (en) | 2012-12-05 | 2015-10-14 | Institut National de la Santé et de la Recherche Médicale (INSERM) | Diagnosis of cystic fibrosis |
| US20140158127A1 (en) | 2012-12-07 | 2014-06-12 | Parion Sciences, Inc. | Nasal cannula for delivery of aerosolized medicaments |
| US20140221424A1 (en) | 2013-01-30 | 2014-08-07 | Vertex Pharmaceuticals Incorporated | Pharmaceutical compositions for use in the treatment of cystic fibrosis |
| US9452139B2 (en) | 2013-03-14 | 2016-09-27 | Novartis Ag | Respirable agglomerates of porous carrier particles and micronized drug |
| US20140296164A1 (en) | 2013-03-29 | 2014-10-02 | Calista Therapeutics, Inc. | Compositions and methods of use for cell targeted inhibitors of the Cystic Fibrosis transmembrane regulator associated ligand |
| AU2014264936B2 (en) | 2013-05-07 | 2018-09-27 | Galapagos Nv | Novel compounds and pharmaceutical compositions thereof for the treatment of cystic fibrosis |
| AU2014268477A1 (en) | 2013-05-24 | 2015-11-12 | The California Institute For Biomedical Research | Compounds for treatment of drug resistant and persistent tuberculosis |
| JP2014232188A (ja) | 2013-05-29 | 2014-12-11 | コニカミノルタ株式会社 | セルロースアシレートフィルム、円偏光板及び画像表示装置 |
| AU2014302458A1 (en) | 2013-06-26 | 2015-12-24 | Proteostasis Therapeutics, Inc. | Methods of modulating CFTR activity |
| DK3030568T3 (en) | 2013-08-08 | 2019-01-07 | Galapagos Nv | THIENO [2,3-C] PYRANES AS CFTR MODULATORS |
| US9688990B2 (en) | 2013-09-12 | 2017-06-27 | Institut National De La Sante Et De La Recherche Medicale (Inserm) | Methods and pharmaceutical compositions for treatment of cystic fibrosis |
| JP6564380B2 (ja) | 2013-09-20 | 2019-08-21 | ユニバーシティ オブ ピッツバーグ − オブ ザ コモンウェルス システム オブ ハイヤー エデュケイション | 前立腺癌を治療するための化合物 |
| EP3052190A4 (en) | 2013-10-01 | 2017-07-19 | New York University | Amino, amido, and heterocyclic compounds as modulators of rage activity and uses thereof |
| US9700881B2 (en) | 2013-10-09 | 2017-07-11 | Emory University | Heterocyclic coupling catalysts and methods related thereto |
| MX2016006118A (es) | 2013-11-12 | 2016-07-21 | Vertex Pharma | Proceso para preparar composiciones farmaceuticas para el tratamiento de enfermedades mediadas por regulador de la conductancia transmembrana de la fibrosis quistica (cftr). |
| KR20150062652A (ko) | 2013-11-29 | 2015-06-08 | 삼성전자주식회사 | 초음파 감응성 리포좀, 그를 포함한 약제학적 조성물 및 그를 이용하여 개체의 체내에 활성제를 전달하는 방법 |
| JP6759100B2 (ja) | 2013-12-30 | 2020-09-23 | ライフサイ ファーマシューティカルズ,インク. | 治療用阻害化合物 |
| US20170029366A1 (en) | 2014-03-07 | 2017-02-02 | The Johns Hopkins University | Inhibitors of histone lysine specific demethylase (lsd1) and histone deacetylases (hdacs) |
| JP2015172005A (ja) | 2014-03-11 | 2015-10-01 | 国立大学法人 東京大学 | 鉄触媒によるカップリング化合物の製造方法 |
| US9790219B2 (en) | 2014-03-13 | 2017-10-17 | Proteostasis Therapeutics, Inc. | Compounds, compositions, and methods for increasing CFTR activity |
| WO2015138934A1 (en) | 2014-03-13 | 2015-09-17 | Proteostasis Therapeutics, Inc. | Compounds, compositions, and methods for increasing cftr activity |
| US10206877B2 (en) | 2014-04-15 | 2019-02-19 | Vertex Pharmaceuticals Incorporated | Pharmaceutical compositions for the treatment of cystic fibrosis transmembrane conductance regulator mediated diseases |
| JP5932881B2 (ja) * | 2014-05-08 | 2016-06-08 | 株式会社フジクラ | マルチコアファイバ及びそのマルチコアファイバの製造方法 |
| AU2015255752B2 (en) | 2014-05-08 | 2020-07-23 | Immunoforge Co., Ltd. | Methods and compositions for treating Cystic Fibrosis |
| RU2688191C2 (ru) | 2014-05-12 | 2019-05-21 | ВЕРОНА ФАРМА ПиэЛСи | Новое лечение |
| MY199033A (en) | 2014-05-16 | 2023-10-10 | Olaplex Inc | Keratin treatment formulations and methods |
| WO2015179414A1 (en) | 2014-05-19 | 2015-11-26 | Merial, Inc. | Anthelmintic compounds |
| AR100724A1 (es) | 2014-06-05 | 2016-10-26 | Merck Patent Gmbh | Derivados de quinolina y su uso en enfermedades neurodegenerativas |
| WO2015196071A1 (en) | 2014-06-19 | 2015-12-23 | Proteostasis Therapeutics, Inc. | Compounds, compositions and methods of increasing cftr activity |
| CN107105749A (zh) | 2014-08-13 | 2017-08-29 | 阿克索生物医药公司 | 抗微生物化合物和组合物及其用途 |
| GB201415381D0 (en) | 2014-08-29 | 2014-10-15 | Algipharma As | Inhalable powder formulations of alginate oligomers |
| JP2017538659A (ja) | 2014-09-10 | 2017-12-28 | エピザイム インコーポレイテッド | Smyd阻害剤 |
| WO2016050209A1 (zh) | 2014-10-01 | 2016-04-07 | 厦门赛诺邦格生物科技有限公司 | 一种异官能化聚乙二醇衍生物、制备方法及其生物相关物质 |
| WO2016050208A1 (zh) | 2014-10-01 | 2016-04-07 | 厦门赛诺邦格生物科技有限公司 | 一种多官能化聚乙二醇衍生物修饰的生物相关物质 |
| US11324827B2 (en) | 2014-10-01 | 2022-05-10 | Xiamen Sinopeg Biotech Co., Ltd. | Multifunctionalized polyethylene glycol derivative and preparation method therefor |
| CN104725628B (zh) | 2014-10-01 | 2018-04-17 | 厦门赛诺邦格生物科技股份有限公司 | 一种含可降解基团的单一官能化支化聚乙二醇、制备方法及其生物相关物质 |
| WO2016054560A1 (en) | 2014-10-02 | 2016-04-07 | Flatley Discovery Lab | Isoxazole compounds and methods for the treatment of cystic fibrosis |
| US9573948B2 (en) | 2014-10-06 | 2017-02-21 | Flatley Discovery Lab | Triazolopyridine compounds and methods for the treatment of cystic fibrosis |
| TWI735416B (zh) | 2014-10-06 | 2021-08-11 | 美商維泰克斯製藥公司 | 囊腫纖維化症跨膜傳導調節蛋白之調節劑 |
| RU2749213C2 (ru) | 2014-10-07 | 2021-06-07 | Вертекс Фармасьютикалз Инкорпорейтед | Сокристаллы модуляторов регулятора трансмембранной проводимости при кистозном фиброзе |
| US20170281612A1 (en) | 2014-10-08 | 2017-10-05 | Nivalis Therapeutics, Inc. | Methods for the Treatment of Cystic Fibrosis |
| US20160108406A1 (en) | 2014-10-08 | 2016-04-21 | University Of Iowa Research Foundation | Method of regulating cftr expression and processing |
| GB201418892D0 (en) | 2014-10-23 | 2014-12-10 | Proqr Therapeutics B V | DNA editing |
| WO2016066582A1 (en) | 2014-10-28 | 2016-05-06 | Bci Pharma | Nucleoside kinase inhibitors |
| EP3212189B1 (en) | 2014-10-31 | 2020-09-09 | AbbVie Overseas S.à r.l. | Substituted chromanes and method of use |
| BR112017009194A2 (pt) | 2014-10-31 | 2017-12-26 | Abbvie Sarl | tetra-hidropiranos substituídos e método de uso |
| WO2016086015A1 (en) | 2014-11-25 | 2016-06-02 | University Of Rochester | Myoglobin-based catalysts for carbene transfer reactions |
| MA41031A (fr) | 2014-11-26 | 2017-10-03 | Catabasis Pharmaceuticals Inc | Conjugués cystéamine-acide gras et leur utilisation comme activateurs de l'autophagie |
| WO2016086136A1 (en) | 2014-11-26 | 2016-06-02 | Catabasis Pharmaceuticals, Inc. | Fatty acid cysteamine conjugates of cftr modulators and their use in treating medical disorders |
| US10344023B2 (en) | 2014-12-23 | 2019-07-09 | Proteostasis Therapeutics, Inc. | Derivatives of 3-heteroarylisoxazol-5-carboxylic amide useful for the treatment of inter alia cystic fibrosis |
| MA41253A (fr) | 2014-12-23 | 2017-10-31 | Proteostasis Therapeutics Inc | Composés, compositions et procédés pour augmenter l'activité du cftr |
| CA2971850A1 (en) | 2014-12-23 | 2016-06-30 | Proteostasis Therapeutics, Inc. | Derivatives of 5-phenyl- or 5-heteroarylthiazol-2-carboxylic amide useful for the treatment of inter alia cystic fibrosis |
| US10738011B2 (en) | 2014-12-23 | 2020-08-11 | Proteostasis Therapeutics, Inc. | Derivatives of 5-(hetero)arylpyrazol-3-carboxylic amide or 1-(hetero)aryltriazol-4-carboxylic amide useful for the treatment of inter alia cystic fibrosis |
| ES2737227T3 (es) | 2014-12-24 | 2020-01-10 | Kither Biotech S R L | Péptido inhibidor de gamma PI3K novedoso para el tratamiento de enfermedades del sistema respiratorio |
| EP3240539A4 (en) | 2014-12-31 | 2018-07-25 | Auspex Pharmaceuticals, Inc. | Cyclopropanecarboxamide modulators of cystic fibrosis transmembrane conductance regulator |
| WO2016107603A1 (zh) | 2015-01-01 | 2016-07-07 | 成都贝斯凯瑞生物科技有限公司 | 取代氮杂环衍生物及其应用 |
| US20180147187A1 (en) | 2015-01-12 | 2018-05-31 | Proteostasis Therapeutics, Inc. | Compounds, compositions, and methods for increasing cftr activity |
| CA2981495C (en) | 2015-03-31 | 2023-09-26 | Vertex Pharmaceuticals (Europe) Limited | Deuterated vx-661 |
-
2011
- 2011-04-21 SG SG2012078374A patent/SG184987A1/en unknown
- 2011-04-21 EP EP18173910.3A patent/EP3381899B1/en active Active
- 2011-04-21 CA CA2797118A patent/CA2797118C/en active Active
- 2011-04-21 RU RU2015145784A patent/RU2745977C2/ru active
- 2011-04-21 WO PCT/US2011/033396 patent/WO2011133751A2/en active Application Filing
- 2011-04-21 CN CN201510526116.3A patent/CN105130948A/zh active Pending
- 2011-04-21 KR KR1020127030452A patent/KR20130056244A/ko not_active Application Discontinuation
- 2011-04-21 US US13/642,642 patent/US9035072B2/en active Active
- 2011-04-21 SG SG10201913594UA patent/SG10201913594UA/en unknown
- 2011-04-21 MX MX2015003252A patent/MX342288B/es unknown
- 2011-04-21 CN CN201180031319.5A patent/CN103038214B/zh active Active
- 2011-04-21 KR KR1020167010394A patent/KR101984225B1/ko active IP Right Grant
- 2011-04-21 EP EP16154612.2A patent/EP3045452A1/en not_active Withdrawn
- 2011-04-21 MX MX2012012204A patent/MX2012012204A/es active IP Right Grant
- 2011-04-21 AU AU2011242712A patent/AU2011242712B2/en active Active
- 2011-04-21 NZ NZ734535A patent/NZ734535A/en unknown
- 2011-04-21 JP JP2013506299A patent/JP2013525371A/ja active Pending
- 2011-04-21 ES ES11729195.5T patent/ES2608474T3/es active Active
- 2011-04-21 ES ES18173910T patent/ES2858351T3/es active Active
- 2011-04-21 RU RU2012149691/04A patent/RU2569678C2/ru active
- 2011-04-21 MX MX2016009018A patent/MX353408B/es unknown
- 2011-04-21 CA CA3108488A patent/CA3108488A1/en not_active Abandoned
- 2011-04-21 KR KR1020197015032A patent/KR20190061096A/ko not_active Application Discontinuation
- 2011-04-21 NZ NZ603721A patent/NZ603721A/en unknown
- 2011-04-21 SG SG10201505700QA patent/SG10201505700QA/en unknown
- 2011-04-21 EP EP11729195.5A patent/EP2560954B1/en active Active
- 2011-04-21 BR BR112012027056A patent/BR112012027056B8/pt not_active IP Right Cessation
- 2011-04-22 TW TW105122115A patent/TWI620744B/zh active
- 2011-04-22 TW TW100114198A patent/TWI518082B/zh active
- 2011-04-22 TW TW104142162A patent/TWI561518B/zh active
- 2011-04-25 AR ARP110101412A patent/AR081333A1/es not_active Application Discontinuation
-
2012
- 2012-10-18 IL IL222539A patent/IL222539A0/en unknown
-
2014
- 2014-12-11 IL IL236209A patent/IL236209B/en active IP Right Grant
-
2015
- 2015-04-15 US US14/687,286 patent/US10071979B2/en active Active
- 2015-05-22 JP JP2015104812A patent/JP2015166382A/ja not_active Withdrawn
-
2016
- 2016-04-22 AU AU2016202569A patent/AU2016202569B2/en active Active
- 2016-06-07 HK HK16106480.6A patent/HK1218419A1/zh unknown
- 2016-12-07 HK HK16113950A patent/HK1225721A1/zh unknown
-
2017
- 2017-01-25 JP JP2017011298A patent/JP6484652B2/ja active Active
-
2018
- 2018-08-09 US US16/059,724 patent/US20190210991A1/en not_active Abandoned
- 2018-11-09 JP JP2018210982A patent/JP6714673B2/ja active Active
-
2019
- 2019-08-27 IL IL268953A patent/IL268953B/en active IP Right Grant
-
2020
- 2020-08-26 US US17/003,051 patent/US20210238158A1/en not_active Abandoned
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| SU620208A3 (ru) * | 1975-06-04 | 1978-08-15 | Сумитомо Кемикал Компани, Лимитед, (Фирма) | Способ получени производных индола |
| US20090131492A1 (en) * | 2006-04-07 | 2009-05-21 | Ruah Sara S Hadida | Indole derivatives as CFTR modulators |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2745977C2 (ru) | Способ получения циклоалкилкарбоксамидо-индольных соединений | |
| US9314455B2 (en) | Solid forms of 3-(6-(1-(2,2-difluorobenzo[d][1,3]dioxol-5-yl)cyclopropanecarboxamido)-3-methylpyridin-2-yl)benzoic acid | |
| AU2015221470B2 (en) | Solid forms of 3-(6-(1-(2,2-difluorobenzo[d][1,3]dioxol-5-yl) cyclopropanecarboxamido)-3-methylpyridin-2-yl)benzoic acid |