ES2750243T3 - Composición de vacuna que comprende polisacáridos capsulares naturales conjugados de N. Meningitidis - Google Patents
Composición de vacuna que comprende polisacáridos capsulares naturales conjugados de N. Meningitidis Download PDFInfo
- Publication number
- ES2750243T3 ES2750243T3 ES10177832T ES10177832T ES2750243T3 ES 2750243 T3 ES2750243 T3 ES 2750243T3 ES 10177832 T ES10177832 T ES 10177832T ES 10177832 T ES10177832 T ES 10177832T ES 2750243 T3 ES2750243 T3 ES 2750243T3
- Authority
- ES
- Spain
- Prior art keywords
- kda
- capsular polysaccharide
- polysaccharide
- menc
- meningitidis
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/0016—Combination vaccines based on diphtheria-tetanus-pertussis
- A61K39/0017—Combination vaccines based on whole cell diphtheria-tetanus-pertussis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/0016—Combination vaccines based on diphtheria-tetanus-pertussis
- A61K39/0018—Combination vaccines based on acellular diphtheria-tetanus-pertussis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/02—Bacterial antigens
- A61K39/05—Actinobacteria, e.g. Actinomyces, Streptomyces, Nocardia, Bifidobacterium, Gardnerella, Corynebacterium; Propionibacterium
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/02—Bacterial antigens
- A61K39/08—Clostridium, e.g. Clostridium tetani
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/02—Bacterial antigens
- A61K39/09—Lactobacillales, e.g. aerococcus, enterococcus, lactobacillus, lactococcus, streptococcus
- A61K39/092—Streptococcus
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/02—Bacterial antigens
- A61K39/095—Neisseria
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/02—Bacterial antigens
- A61K39/099—Bordetella
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/02—Bacterial antigens
- A61K39/102—Pasteurellales, e.g. Actinobacillus, Pasteurella; Haemophilus
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/02—Bacterial antigens
- A61K39/116—Polyvalent bacterial antigens
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/12—Viral antigens
- A61K39/145—Orthomyxoviridae, e.g. influenza virus
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/12—Viral antigens
- A61K39/29—Hepatitis virus
- A61K39/292—Serum hepatitis virus, hepatitis B virus, e.g. Australia antigen
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/385—Haptens or antigens, bound to carriers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/04—Drugs for disorders of the respiratory system for throat disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/14—Antitussive agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/20—Antivirals for DNA viruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/04—Immunostimulants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H3/00—Compounds containing only hydrogen atoms and saccharide radicals having only carbon, hydrogen, and oxygen atoms
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N7/00—Viruses; Bacteriophages; Compositions thereof; Preparation or purification thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/545—Medicinal preparations containing antigens or antibodies characterised by the dose, timing or administration schedule
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/55—Medicinal preparations containing antigens or antibodies characterised by the host/recipient, e.g. newborn with maternal antibodies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/57—Medicinal preparations containing antigens or antibodies characterised by the type of response, e.g. Th1, Th2
- A61K2039/575—Medicinal preparations containing antigens or antibodies characterised by the type of response, e.g. Th1, Th2 humoral response
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/60—Medicinal preparations containing antigens or antibodies characteristics by the carrier linked to the antigen
- A61K2039/6031—Proteins
- A61K2039/6037—Bacterial toxins, e.g. diphteria toxoid [DT], tetanus toxoid [TT]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/62—Medicinal preparations containing antigens or antibodies characterised by the link between antigen and carrier
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/62—Medicinal preparations containing antigens or antibodies characterised by the link between antigen and carrier
- A61K2039/627—Medicinal preparations containing antigens or antibodies characterised by the link between antigen and carrier characterised by the linker
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/70—Multivalent vaccine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/12—Viral antigens
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2730/00—Reverse transcribing DNA viruses
- C12N2730/00011—Details
- C12N2730/10011—Hepadnaviridae
- C12N2730/10111—Orthohepadnavirus, e.g. hepatitis B virus
- C12N2730/10134—Use of virus or viral component as vaccine, e.g. live-attenuated or inactivated virus, VLP, viral protein
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2760/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA ssRNA viruses negative-sense
- C12N2760/00011—Details
- C12N2760/16011—Orthomyxoviridae
- C12N2760/16211—Influenzavirus B, i.e. influenza B virus
- C12N2760/16234—Use of virus or viral component as vaccine, e.g. live-attenuated or inactivated virus, VLP, viral protein
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2760/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA ssRNA viruses negative-sense
- C12N2760/00011—Details
- C12N2760/16011—Orthomyxoviridae
- C12N2760/16211—Influenzavirus B, i.e. influenza B virus
- C12N2760/16271—Demonstrated in vivo effect
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2770/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA ssRNA viruses positive-sense
- C12N2770/00011—Details
- C12N2770/32011—Picornaviridae
- C12N2770/32611—Poliovirus
- C12N2770/32634—Use of virus or viral component as vaccine, e.g. live-attenuated or inactivated virus, VLP, viral protein
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02A—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE
- Y02A50/00—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE in human health protection, e.g. against extreme weather
- Y02A50/30—Against vector-borne diseases, e.g. mosquito-borne, fly-borne, tick-borne or waterborne diseases whose impact is exacerbated by climate change
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Immunology (AREA)
- Mycology (AREA)
- Microbiology (AREA)
- Epidemiology (AREA)
- Virology (AREA)
- Organic Chemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Communicable Diseases (AREA)
- Pulmonology (AREA)
- Oncology (AREA)
- Genetics & Genomics (AREA)
- Biotechnology (AREA)
- Biochemistry (AREA)
- Molecular Biology (AREA)
- Wood Science & Technology (AREA)
- Zoology (AREA)
- Otolaryngology (AREA)
- Biomedical Technology (AREA)
- General Engineering & Computer Science (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Medicinal Preparation (AREA)
- Peptides Or Proteins (AREA)
- Surgical Instruments (AREA)
Abstract
Una composición inmunogénica que comprende polisacáridos capsulares de N. meningitidis de los serogrupos A, C, W135 e Y, en donde cada polisacárido capsular de N. meningitidis está conjugado con una proteína vehículo de toxoide tetánico (TT) para producir un conjugado de polisacárido capsular de N. meningitidis, en el que: - el polisacárido capsular MenA presente en el conjugado de sacárido capsular MenA tiene un tamaño promedio de más de 60 kDa y es polisacárido capsular MenA natural o microfluidizado; - el polisacárido capsular MenC presente en el conjugado de sacárido capsular MenC tiene un tamaño promedio de más de 150 kDa y es un polisacárido capsular MenC natural; - el polisacárido capsular MenW presente en en conjugado de polisacárido capsular es un polisacárido capsular MenW dimensionado por microfluidización y tiene un tamaño promedio de 100-200 kDa, y - el polisacárido capsular MenY presente en el conjugado de polisacárido capsular MenY es un polisacárido capsular MenY dimensionado por microfluidización y tiene un tamaño promedio de 100-200 kDa.
Description
DESCRIPCIÓN
Composición de vacuna que comprende polisacáridos capsulares naturales conjugados de N. Meningitidis
La presente invención se refiere a composiciones inmunogénicas que comprenden polisacáridos capsulares de N. meningitidis conjugados con una proteína vehículo. También se refiere a vacunas y kits de vacunas que comprenden conjugados de polisacárido de N. meningitidis, procesos para fabricar las composiciones inmunogénicas y vacunas y el uso de las vacunas y composiciones inmunogénicas de la invención en terapia. También se refiere a las composiciones inmunogénicas proporcionadas para su uso en métodos de inmunización frente a la infección por Neisseria.
Neisseria meningitidis es un patógeno humano Gram-negativo que causa meningitis bacteriana. Basándose en el polisacárido capsular del organismo, se han identificado doce serogrupos de N. meningitidis (A, B, C, H, I, K, L, 29E, W135, X, Y y Z). El serogrupo A (MenA) es la causa más común de enfermedad epidémica en África subsahariana. Los serogrupos B y C son responsables de la mayoría de los casos en los países en desarrollo, y los casos restantes son causados por W135 e Y).
En la técnica se conocen composiciones inmunogénicas que comprenden sacáridos de N. meningitidis conjugados con proteínas transportadoras. Por ejemplo, el documento WO 02/58737 desvela una vacuna que comprende polisacáridos capsulares purificados de los serogrupos A, C, W135 e Y de N. meningitidis conjugados con una proteína vehículo. Sin embargo, la presente solicitud enseña que los polisacáridos capsulares de N. meningitidis extraídos se deberían despolimerizar calentándolos en una solución de peróxido de hidrógeno antes de la conjugación.
El documento WO 03/07985 desvela vacunas conjugadas que comprenden sacárido de N. meningitidis seleccionado entre los serogrupos A, C, W135 e Y. Los polisacáridos capsulares meningocócicos se extraen y a continuación se hidrolizan de modo que se usa una selección de oligosacáridos obtenidos a partir de los polisacáridos capsulares para su conjugación con una proteína vehículo.
El documento WO 04/103400 también desvela conjugado de polisacárido-proteína obtenido a partir de meningococo multivalente que contiene polisacáridos capsulares obtenidos a partir de los serogrupos A, C, W135 e Y de N. meningitidis. La presente solicitud enseña que, en lugar de usar el polisacárido capsular nativo grande, se prefiere el uso de polisacáridos meningocócicos de un tamaño más pequeño. Sugiere que los polisacáridos capsulares se despolimerizan parcialmente usando condiciones oxidantes suaves para dar un tamaño promedio de menos de 100.000 daltons, preferentemente de 12.000 a 25.000 daltons.
Sigue existiendo la necesidad de desarrollar vacunas conjugadas mejoradas frente a la meningitis por neisseria. La presente invención se refiere a la provisión de una vacuna conjugada de polisacárido meningocócico en la que el tamaño de los polisacáridos es mayor que el que se enseña en la bibliografía. El enfoque de la técnica ha sido usar oligosacáridos para facilitar la producción de conjugados. Los inventores han descubierto que mediante el uso de conjugados de polisacárido nativos o de tamaño pequeño, se pueden obtener una o más de las siguientes ventajas: 1) un conjugado que tiene alta inmungenicidad que se puede filtrar; 2) se puede mejorar la memoria inmunológica (al igual que en el ejemplo tres); 3) la alteración de la proporción de polisacárido con respecto a proteína en el conjugado de un modo tal que la proporción de polisacárido con respecto a proteína (p/p) en el conjugado se pueda aumentar (esto puede dar como resultado una reducción del efecto de supresión del vehículo); 4) los conjugados inmunogénicos susceptibles de hidrólisis (tal como los conjugados MenA) se pueden estabilizar mediante el uso de polisacáridos más grandes para la conjugación. El uso de polisacáridos más grandes puede dar como resultado una mayor reticulación con el vehículo conjugado y, por lo tanto, menos escisión del sacárido libre del conjugado. Las vacunas conjugadas que se han descrito en la técnica anterior tienden a despolimerizar los polisacáridos antes de la conjugación para mejorar la conjugación. La presente invención se dirige a una estrategia diferente y muestra sorprendentemente que las vacunas conjugadas meningocócicas que retienen un tamaño mayor de polisacárido proporcionan una buena respuesta inmunológica frente a la enfermedad meningocócica.
Por lo tanto, en un aspecto de la presente invención, se proporciona una composición inmunogénica que comprende polisacáridos capsulares de N. meningitidis de los serogrupos A, C , W135 e Y, en donde cada polisacárido capsular de N. meningitidis se conjuga con una proteína vehículo de toxoide del tétano (TT) para producir un conjugado de polisacárido capsular de N. meningitidis, en el que:
- el polisacárido capsular MenA presente en el conjugado de sacárido capsular MenA tiene un tamaño promedio de más de 60 kDa y es polisacárido capsular MenA natural o microfluidizado;
- el polisacárido capsular MenC presente en el conjugado de sacárido capsular MenC tiene un tamaño promedio de más de 150 kDa y es un polisacárido capsular MenC natural;
- el polisacárido capsular MenW presente en en conjugado de polisacárido capsular es un polisacárido capsular MenW dimensionado por microfluidización y tiene un tamaño promedio de 100-200 kDa, y
el polisacárido capsular MenY presente en el conjugado de polisacárido capsular MenY es un polisacárido capsular
MenY dimensionado por microfluidización y tiene un tamaño promedio de 100-200 kDa.
De acuerdo con un aspecto adicional de la invención se proporciona una vacuna que comprende la composición inmunogénica de la invención y un vehículo farmacéuticamente aceptable.
De acuerdo con un aspecto adicional de la invención se proporciona un kit de vacuna para administración simultánea o secuencial que comprende dos composiciones inmunogénicas multivalentes para proporcionar protección en un hospedador frente a una enfermedad causada por Bordetella pertussis, Clostridium tetani, Corynebacterium diphtheriae, Haemophilus influenzae y Neisseria meningitidis, comprendiendo dicho kit un primer recipiente que comprende:
toxoide del tétano (TT),
toxoide de difteria (DT), y
componentes de células completas o acelulares de pertussis
y un segundo recipiente que comprende:
la composición inmunogénica de la invención.
De acuerdo con un aspecto adicional de la invención se proporciona un proceso para preparar la vacuna de la invención que comprende la etapa de mezclar la composición inmunogénica de la invención con un vehículo farmacéuticamente aceptable.
De acuerdo con un aspecto adicional de la invención, se proporciona un proceso para crear la vacuna de la invención que comprende la etapa de mezclar la composición inmunogénica de la invención con un vehículo farmacéuticamente aceptable.
De acuerdo con un aspecto adicional de la invención se proporciona una composición inmunogénica de la invención para su uso en el tratamiento o prevención de una enfermedad causada por Neisseria meningitidis.
Descripción de las figuras
Figura 1 - A - Gráfico de barras que muestra respuestas de GMC en un ELISA anti-MenY. ENYTT012 es un conjugado de MenY-TT preparado a partir del polisacárido MenY nativo. ENYTT014 es un conjugado de MenY-TT preparado a partir del polisacárido MenY microfluidizado que se había sometido a 40 ciclos de microfluidización. ENYTT015bis es un conjugado de MenY-TT preparado a partir del polisacárido MenY microfluidizado que se había sometido a 20 ciclos de microfluidización.
- B - Gráfico de barras que muestra respuestas de GMT en un ensayo anti-MenY SBA. ENYTT012 es un conjugado de MenY-TT preparado a partir del polisacárido MenY nativo. ENYTT014 es un conjugado de MenY-TT preparado a partir del polisacárido MenY microfluidizado que se había sometido a 40 ciclos de microfluidización. ENYTT015bis es un conjugado de MenY-TT preparado a partir del polisacárido MenY microfluidizado que se había sometido a 20 ciclos de microfluidización.
Descripción detallada
Una composición inmunogénica de la invención es una que comprende polisacáridos capsulares de N. meningitidis de los serogrupos A, C, W135 e Y, en donde cada polisacárido capsular de N. meningitidis está conjugado con una proteína vehículo de Toxoide Tetánico (TT) para producir un conjugado de polisacárido capsular de N. meningitidis, en el que:
- el polisacárido capsular MenA presente en el conjugado de sacárido capsular MenA tiene un tamaño promedio de más de 60 kDa y es polisacárido capsular MenA natural o microfluidizado;
- el polisacárido capsular MenC presente en el conjugado de sacárido capsular MenC tiene un tamaño promedio de más de 150 kDa y es un polisacárido capsular MenC natural;
- el polisacárido capsular MenW presente en en conjugado de polisacárido capsular es un polisacárido capsular MenW dimensionado por microfluidización y tiene un tamaño promedio de 100-200 kDa, y
- el polisacárido capsular MenY presente en el conjugado de polisacárido capsular MenY es un polisacárido capsular MenY dimensionado por microfluidización y tiene un tamaño promedio de 100-200 kDa.
También se desvela una composición inmunogénica que comprende polisacáridos capsulares de N. meningitidis de al menos uno, dos, tres o cuatro de los serogrupos A, C, W e Y conjugados con una proteína vehículo , en la que al menos un, dos, tres o cuatro de cada polisacárido de N. meningitidis es cualquiera de un polisacárido nativo o se dimensiona en un factor de hasta x1,5, x2, x3, x4, x5, x6, x7, x8, x9 o x10 con respecto al peso molecular promedio en peso del polisacárido nativo.
Para los fines de la invención, "polisacárido nativo" se refiere a un polisacárido que no se ha sometido a un proceso, cuya finalidad es reducir el tamaño del polisacárido. El tamaño de un polisacárido se puede llegar a reducir ligeramente durante los procedimientos de purificación normales. Un polisacárido de ese tipo aún es nativo. Solo se
podría considerar que el polisacárido no es nativo si el polisacárido se ha sometido a técnicas de dimensionamiento. Para los fines de la invención, "dimensionado en un factor de hasta x2" se refiere a que el polisacárido está sujeto un proceso destinado a reducir el tamaño del polisacárido pero que retiene un tamaño superior a la mitad del tamaño del polisacárido nativo. X3, x4 etc., se deben interpretar del mismo modo, es decir, el polisacárido está sujeto a un proceso destinado a reducir el tamaño del polisacárido pero retiene un tamaño de más de un tercio, un cuarto, etc., del tamaño del polisacárido nativos respectivamente.
También se desvela una composición inmunogénica que comprende polisacáridos capsulares de N. meningitidis de al menos uno, dos, tres o cuatro de los serogrupos A, C, W e Y conjugado con una proteína de vehículo en donde al menos uno, dos, tres o cuatro de cada uno de los polisacáridos de N. meningitidis es un polisacárido natural.
También se desvela una composición inmunogénica que comprende polisacáridos capsulares de N. meningitidis de al menos uno, dos, tres o cuatro de los serogrupos A, C, W e Y conjugados con una proteína vehículo, en la que al menos un, dos, tres o cuatro de cada polisacárido de N. meningitidis se dimensiona en un factor de x1,5, x2, x3, x4, x5, x6, x7, x8, x9 o x10.
También se desvelan composiciones inmunogénicas que opcionalmente comprenden conjugados de: polisacárido capsular del serogrupo C (MenC), polisacárido capsular del serogrupo A (MenA), polisacárido capsular del serogrupo W135 (MenW), polisacárido capsular del serogrupo Y (MenY), polisacáridos capsulares de los serogrupos C e Y (MenCY), polisacáridos capsulares de los serogrupos C y A (MenAC), polisacáridos capsulares de los serogrupos C y W (MenCW), polisacáridos capsulares de los serogrupos A e Y (MenAY), polisacáridos capsulares de los serogrupos A y W (MenAW), polisacáridos capsulares de los serogrupos W e Y (Men WY), polisacáridos capsulares de los serogrupos A, C y W (MenACW), polisacáridos capsulares de los serogrupos A, C e Y (MenACY); polisacáridos capsulares de los serogrupos A, W135 e Y (MenAWY), polisacáridos capsulares C, W135 e Y de los serogrupos (MenCWY); o polisacáridos capsulares A, C, W135 e Y de los serogrupos (MenACWY) de N. meningitidis. Esta es la definición de "un, dos, tres o cuatro", o "al menos uno de "los serogrupos A, C, W e Y, o de cada uno de polisacárido de N. meningitidis cuando se menciona en el presente documento.
En un caso, el tamaño promedio (o peso molecular) de al menos uno, dos, tres, cuatro de cada polisacárido de N. meningitidis es 50 KDa - 1500 kDa, 50 kDa - 500 kDa, 50 kDa - 300 KDa, 101 kDa - 1500 kDa, 101 kDa - 500 kDa, o 101 kDa - 300 kDa tal como se determina por MALLS.
En una realización, el polisacárido MenA tiene un peso molecular de 60-70 kDa o 60-80 kDa tal como se determina por MALLS.
En una realización, el polisacárido MenC tiene un peso molecular de 150-210 kDa o 180-210 kDa tal como se determina por MALLS.
En una realización el polisacárido MenY tiene un peso molecular de 100-150 kDa o 110-140 kDa, 100-140 kDa, 140 170 kDa o 150-160 kDa tal como se determina por MALLS.
En una realización el polisacárido MenW tiene un peso molecular de 100-150 kDa, 110-140 kDa, 120-140 kDa tal como se determina por MALLS.
En el presente documento el peso molecular o peso molecular promedio de un polisacárido se refiere al peso molecular promedio en peso (Pm) del polisacárido medido antes de su conjugación y se mide por MALLS.
La técnica MALLS se conoce bien la técnica y generalmente se lleva a cabo como se describe en el ejemplo 2. Para el análisis MALLS de sacáridos meningocócicos, se pueden usar dos columnas (TSKG6000 y 5000pWxI TOSOH Bioscience) en combinación y los sacáridos se diluyen en agua. Los sacáridos se detectan usando un detector de dispersión de luz (por ejemplo Wyatt Dawn DSP equipado con un láser de argón de 10 mW a 488 nm) y un refractómetro inferométrico (por ejemplo Wyatt Otilab DSP equipado con una celda P100 y un filtro de color rojo a 498 nm).
En una composición de la invención: el sacárido MenA es natural o microfluidizado; el sacárido MenC es un sacárido natural; el sacárido MenW es microfluidizado; y el sacárido MenY es microfluidizado.
La microfluidización tiene la ventaja de disminuir el tamaño de los polisacáridos nativos más grandes lo suficiente como para proporcionar un conjugado que se puede filtrar. El dimensionamiento se realiza en un factor no superior a x20, x10, x8, x6, x5, x4, x3, x2 o x1,5.
También se describe una composición inmunogénica que comprende conjugados de N. meningitidis que se preparan a partir de una mezcla de polisacáridos nativos y polisacáridos que se dimensiona en un factor no superior a x20. Por ejemplo, los polisacáridos de MenC y/o MenA son nativos. Por ejemplo, los polisacáridos de MenY y/o MenW se dimensionan en un factor no superior a x20, x10, x8, x6, x5, x4, x3 , x2 o x1,5. Por ejemplo, una composición
inmunogénica contiene un conjugado preparado a partir de MenY y/o MenW y/o MenC y/o MenA que está dimensionado en un factor no superior a x20, x10, x8, x6, x5, x4, x3 , x2 o x1,5 y/o está microfluidizado. Por ejemplo, una composición inmunogénica contiene un conjugado preparado a partir de MenA y/o MenC y/o MenW y/o MenY nativos. Por ejemplo, una composición inmunogénica comprende un conjugado preparado a partir de MenC nativo. Por ejemplo, una composición inmunogénica comprende un conjugado preparado a partir de MenC y MenA nativos que se dimensiona en un factor no superior a x20, x10, x8, x6, x5, x4, x3, x2 o x1,5 y/o se microfluidiza. Por ejemplo, una composición inmunogénica comprende un conjugado preparado a partir de MenC y MenY nativos que se dimensionan en un factor no superior a x20, x10, x8, x6, x5, x4, x3, x2 o x1,5 y/o se microfluidiza.
En una realización, la polidispersión del polisacárido es 1-1,5, 1-1,3, 1-1,2, 1-1,1 o 1-1,05 y después de su conjugación a una proteína vehículo, la polidispersión del conjugado es 1,0-2,5, 1,0-2,0. 1,0-1,5, 1,0-1,2, 1,5-2,5, 1,7 2,2 o 1,5-2,0. Todas las mediciones de polidispersión se realizan por MALLS.
En una realización, la composición inmunogénica de la invención además comprende un antígeno del serogrupo B de N. meningitidis. El antígeno es opcionalmente un polisacárido capsular del serogrupo B (MenB) de N. meningitidis o un polisacárido u oligosacárido dimensionado obtenido a partir del mismo. El antígeno es opcionalmente una preparación de vesículas de membrana externa del serogrupo B de N. meningitidis como se describe en los documentos EP301992, WO 01/09350, WO 04/14417, WO 04/14418 y WO 04/14419.
En una realización, la composición inmunogénica de la invención comprende además un sacárido capsular b (Hib) de H. influenzae conjugado a una proteína vehículo.
El polisacárido o polisacáridos de N. meningitidis (y opcionalmente el sacárido capsular Hib) incluidos en las composiciones farmacéuticas de la invención cada uno se conjuga al vehículo de toxoide del tétano. Opcionalmente el Hib se puede conjugar al fragmento C de toxoide del tétano, mutantes no tóxicos de la toxina del tétano, toxoide de difteria, CRM197, otros mutantes no tóxicos de la toxina de difteria [tal como CRM176, CRM 197, CRM228, CRM 45 (Uchida et al J. Biol. Chem. 218; 3838-3844, 1973); CRM 9, CRM 45, CRM102, CRM 103 y CRM107 y otras mutaciones descritas por Nicholls y Youle en Genetically Engineered Toxins, Ed: Frankel, Maecel Dekker Inc, 1992; deleción o mutación de Glu-148 a Asp, Gln o Ser y/o Ala 158 a Gly y otras mutaciones desveladas en los documentos US 4709017 o US 4950740; mutación de al menos una o más restos de Lys 516, Lys 526, Phe 530 Y/o Lys 534 y otras mutaciones desveladas en los documentos US 5917017 o US 6455673; o fragmento desvelado en el documento US 5843711], neumolisina neumocócica, OMPC (proteínas de membrana externa meningocócica -normalmente extraída del serogrupo B de N. meningitidis - documento EP0372501), péptidos sintéticos (documentos EP0378881, EP0427347), proteínas de choque térmico (documentos WO 93/17712, WO 94/03208), proteínas de pertussis (documentos WO 98/58668, EP0471177), citoquinas, linfoquinas, factores u hormonas de crecimiento (documento WO 91/01146), proteínas artificiales que comprenden múltiples epítopos de linfocitos T CD4+ humanos de diversos antígenos obtenidos a partir de patógenos (Falugi et al (2001) Eur J Immunol 31; 3816 3824) tal como proteína N19 (Baraldoi et al (2004) Infect Immun 72; 4884-7) proteína PspA de superficie neumocócica (documento WO 02/091998) neumolisina (Kuo et al (1995) Infect Immun 63; 2706-13), proteínas de absorción de hierro (documento WO 01/72337), toxinas A o B de C. difficile (documento WO 00/61761) o Proteína D (documentos EP594610 y WO 00/56360).
La composición inmunogénica de la invención usa Toxoides del Tétano para cada polisacárido de N. meningitidis (independientemente). En una realización cuando Hib está presente, Hib se puede conjugar con la misma proteína vehículo.
En una realización, una sola proteína vehículo puede llevar más de un antígeno sacárido (documento WO 04/083251). Por ejemplo, una sola proteína vehículo se podría conjugar con MenA y MenC; MenA y MenW; MenA y MenY; MenC y MenW; MenC y MenY; Men W y MenY; MenA, MenC y MenW; MenA, MenC y MenY; MenA, MenW y MenY; MenC, MenW y MenY; MenA, MenC, MenW y MenY; Hib y MenA; Hib y MenC; Hib y MenW; o Hib y MenY. En una realización, la composición inmunogénica de la invención comprende un sacárido Hib conjugado con una proteína vehículo seleccionada entre el grupo que consiste en TT, DT, CRM197, fragmento C de TT y proteína D. También se desvela una composición inmunogénica que comprende al menos un conjugado de sacárido meningocócico (por ejemplo MenA; MenC; MenW; MenY; MenA y MenC; MenA y MenW; MenA y MenY; MenC y Men W; Men C y MenY; Men W y MenY; MenA, MenC y MenW; MenA, MenC y MenY; MenA, MenW y MwnY; MenC, MenW y MenY o MenA, MenC, MenW y MenY) que tiene una proporción de sacárido Men con respecto a proteína vehículo entre 1:5 y 5:1, entre 1:2 y 5:1, entre 1:0,5 y 1:2,5 o entre 1:1,25 y 1:2,5 (p/p).
La composición inmunogénica de la invención comprende opcionalmente un conjugado de sacárido Hib que tiene una proporción de Hib con respecto a proteína vehículo entre 1:5 y 5:1; 1:2 y 2:1; 1:1 y 1:4; 1:2 y 1:3,5; o aproximadamente o exactamente 1:2,5 o 1:3 (p/p). Por 'aproximadamente' se hace referencia a dentro de un 10 % de la proporción indicada.
La proporción de sacárido con respecto a proteína vehículo (p/p) en un conjugado se puede determinar usando el
conjugado esterilizado. La cantidad de proteína se determina usando un ensayo de Lowry (por ejemplo Lowry et al (195l) J. Biol. Chem. 193, 265-275 o Peterson et al Analytical Biochemistry 100, 201-220 (1979)) y la cantidad de sacárido se determina usando ICP-OES (espectroscopia de emisión óptica con plasma inductivamente Acoplado) para MenA, ensayo de DMAP para MenC y ensayo de Resorcinol para MenW y MenY (Monsigny et al (1988) Anal. Biochem. 175, 525-530).
En una realización, la composición inmunogénica de la invención el polisacárido o polisacáridos de N. meningitidis y/o el sacárido Hib se conjuga con la proteína vehículo a través de un conector, por ejemplo un conector difuncional. El conector es opcionalmente heterobifuncional u homobifuncional, que tiene por ejemplo un grupo amino reactivo y un grupo ácido carboxílico reactivo, 2 grupos amino reactivos o dos grupos ha sido carboxílico reactivos. El conector tiene por ejemplo entre 4 y 20, 4 y 12, 5 y 10 átomos de carbono. Un posible conector es ADH. Otros conectores incluyen B-propionamido (documento WO 00/10599), nitrofenil-etilamina (Gever et al (1979) Med. Microbiol. Immunol. 165; 171-288), haluros de haloalquilo (documento US4057685), enlaces glicosídicos (documentos US4673574, US4808700), hexano diamina y ácido 6-aminocaproico (documento US4459286).
Los conjugados de polisacárido presentes en las composiciones inmunogénicas de la invención se pueden preparar mediante cualquier técnica de acoplamiento conocida. El método de conjugación puede depender de la activación del sacárido con tetrafluoroborato de 1-ciano-4-dimetilamino piridinio (CDAp ) para formar un éster de cianato. Por lo tanto el sacárido activado se puede acoplar directamente o a través de un grupo espaciador (conector) a un grupo amino en la proteína vehículo. Por ejemplo, el espaciador podría ser cistamina o cisteamina para dar un polisacárido tiolado que se podría acoplar al vehículo a través del enlace tioéter obtenido después de reacción con una proteína vehículo activada por maleimida (por ejemplo usando GMBS) o una proteína vehículo holoacetilada (por ejemplo usando yodoacetimida o bromoacetatobromoacetato de N-succinimidilo). Opcionalmente, el éster de cianato (preparado opcionalmente mediante química de CDAP) se acopla con hexano diamina o ADH y el sacárido derivatizado con amino se conjuga con la proteína vehículo usando química de carbodiimida (por ejemplo, EDAC o EDC). Los conjugados de ese tipo se describen en la solicitud publicada de PCT WO 93/15760 Uniformed Services University y WO 95/08348 y WO 96/29094.
Otras técnicas adecuadas usan carbiinidas, hidrazidas, ésteres activos, norborano, ácido p-nitrobenzoico, N-hidroxisuccinimida, S-NHS, EDC, TSTU. Muchos se describen en el documento WO 98/42721. La conjugación puede implicar un conector de carbonilo que se puede formar por reacción de un grupo hidroxilo libre del sacárido con CDI (Bethell et al J. Biol. Chem. 1979, 254; 2572-4, Hearn et al J. Chromatogr. 1981. 218; 509-18) seguido por la reacción con una proteína para formar un enlace carbamato. Esto puede implicar la reducción del término anomérico a un grupo hidroxilo primario, protección/desprotección opcional de la reacción del grupo hidroxilo primario del grupo hidroxilo primario con CDI para formar un compuesto intermedio de carbamato CDI y acoplar el compuesto intermedio de carbamato CDI con un grupo amino en una proteína.
Los conjugados también se pueden preparar mediante métodos de aminación reductora directa como se describe en los documentos US 4365170 (Jennings) y US 4673574 (Anderson). Otros métodos se describen en los documentos EP-0-161-188, EP-208375 y EP-0-477508.
Un método adicional implica el acoplamiento de un sacárido activado con bromuro de cianógeno (o CDAP) derivatizado con hidrazida de ácido adípico (ADH) al vehículo de proteína por condensación de carbodiimida (Chu C. et al Infect. Immunity, 1983245256), por ejemplo usando EDAC.
En una realización, un grupo hidroxilo (opcionalmente un grupo hidroxilo activado, por ejemplo, un grupo hidroxilo activado por un éster de cianato) en un sacárido está unido a un grupo amino o carboxílico en una proteína, ya sea directa o indirectamente (a través de un conector). Cuando está presente un conectó, un grupo hidroxilo en un sacárido está opcionalmente unido a un grupo amino en un conector, por ejemplo mediante el uso de conjugación CDAP. Un grupo amino adicional en el conector (por ejemplo ADH) se puede conjugar con un grupo de ácido carboxílico en una proteína, por ejemplo usando química de carbodiimida, por ejemplo usando EDAC. En una realización, el polisacárido o polisacáridos capsular(es) Hib o de N. meningitidis se conjuga con el conectó primero antes de que el conector se conjugue con la proteína vehículo.
En una realización, el sacárido Hib, cuando está presente, se conjuga con la proteína vehículo usando CNBr, o CDAP, o una combinación de CDAP y química de carbodiimida (tal como EDAC), o una combinación de CNBr y química de carbodiimida (tal como EDAC). Opcionalmente, Hib se conjuga usando química de CNBr y carbodiimida, opcionalmente EDAC. Por ejemplo, CNBr se usa para unir el sacárido y el conectó en la continuación la química de la carbodiimida se usa para unir el conectó al vehículo de proteína.
En una realización, al menos uno de los polisacáridos capsulares de N. meningitidis se conjuga directamente con una proteína vehículo; opcionalmente el sacárido o sacáridos Men W y/o MenY y/o MenC se conjuga directamente con una proteína vehículo. Por ejemplo MenW; MenY; MenC; MenW y MenY; MenW y MenC; MenY y MenC; o MenW, MenY y MenC se unen directamente a la proteína vehículo. Opcionalmente el al menos uno de los polisacáridos capsulares de N. meningitidis se conjuga directamente por CDAP. Por ejemplo MenW; MenY; MenC; MenW y MenY; MenW y MenC; MenY y MenC; o MenW, MenY y MenC se unen directamente a la proteína vehículo
por CDAP (véanse los documentos WO 95/08348 y WO 96/29094). En una realización, todos los polisacáridos capsulares de N. meningitidis están conjugados con toxoide del tétano.
Opcionalmente la proporción de Men W y/o Y sacárido con respecto a proteína vehículo está entre 1:0,5 y 1:2 (p/p) y/o la proporción de MenC sacárido con respecto a proteína vehículo está entre 1:0,5 y 1:4 o 1:1,25-1:1,5 o 1:0,5 y 1:1,5 (p/p), especialmente cuando éstos sacáridos se unen directamente a la proteína, opcionalmente usan CDAP. En una realización, al menos uno del polisacárido o polisacáridos capsulares de N. meningitidis se conjuga con la proteína vehículo a través de un conector, por ejemplo un conector difuncional. El conector es opcionalmente heterobifuncional u homobifuncional, que tienen por ejemplo un grupo amino reactivo y un grupo ácido carboxílico reactivo, 2 grupos amino reactivos o 2 grupos acilo carboxílico reactivos. El conector tiene por ejemplo entre 4 y 20, 4 y 12, 5 y 10 átomos de carbono. Un conector posible es ADH.
En una realización, MenA; MenC; o MenA y MenC se conjuga con una proteína vehículo (por ejemplo toxoide del tétano) a través de un conector.
En una realización, al menos un polisacárido de N. meningitidis se conjuga con una proteína vehículo a través de un conector usando CDAP y EDAC. Por ejemplo, MenA; MenC; o MenA y MenC se conjugan con una proteína a través de un conector (por ejemplo los que tienen dos grupos hidrozino en sus extremos tal como ADH) usando CDAP y EDAC como se ha descrito anteriormente. Por ejemplo, CDAP se usa para conjugar el sacárido a un conector y EDAC se usa para conjugar el conector a una proteína. Opcionalmente, la conjugación a través de un conector da como resultado una proporción de polisacárido con respecto a proteína vehículo entre 1:0,5 y 1:6; 1:1 y 1:5 o 1:2 y 1:4, para MenA; MenC; o MenA y MenC.
En una realización, el polisacárido capsular MenA está al menos parcialmente O-acilado de modo que al menos un 50 %, 60 %, 70 %, 80 %, 90 %, 95 % o un 98 % de las unidades de repetición están O-acetiladas en al menos una posición. La O-acetilación está presente por ejemplo al menos en la posición O-3 de al menos un 50 %, 60 %, 70 %, 80 %, 90 %, 95 % o un 98 % de las unidades de repetición.
En una realización, el polisacárido capsular MenC está al menos parcialmente O-acetilado de modo que al menos un 30 %, 40 %, 50 %, 60 %, 70 %, 80 %, 90 %, 95 % o un 98 % de las unidades de repetición de unido en NeuNAc (a2^9) están O-acetiladas en al menos una o dos posiciones. La O-acetilación está presente por ejemplo en la posición O-7 y/o O-8 de al menos un 30 %, 40 %, 50 %, 60 %, 70 %, 80 %, 90 %, 95 % o un 98 %de las unidades de repetición.
En una realización, el polisacárido capsular MenW está al menos parcialmente O-acetilado de modo que al menos un 30 %, 40 %, 50 %, 60 %, 70 %, 80 %, 90 %, 95 % o un 98 % de las unidades de repetición están O-acetiladas en al menos una o dos posiciones. La O-acetilación está presente por ejemplo en la posición O-7 y/o O-9 de al menos un 30 %, 40 %, 50 %, 60 %, 70 %, 80 %, 90 %, 95 % o un 98 % de las unidades de repetición.
En una realización, el polisacárido capsular MenY está al menos parcialmente O-acetilado de modo que al menos un 20 %, 30 %, 40 %, 50 %, 60 %, 70 %, 80 %, 90 %, 95 % o 98 % de las unidades de repetición están O-acetiladas en al menos una o dos posiciones. La O-acetilación está presente en la posición 7 y/o 9 de al menos un 20 %, 30 %, 40 %, 50 %, 60 %, 70 %, 80 %, 90 %, 95 % o un 98 % de las unidades de repetición.
El porcentaje de O-acetilación se refiere al porcentaje de las unidades de repetición que contienen O-acetilación. Esto se puede medir en el polisacárido antes de la conjugación y/o después de la conjugación.
En una realización adicional, la composición inmunogénica de la invención comprende un conjugado de sacárido Hib y al menos dos conjugados de polisacárido de N. meningitidis en la que el conjugado de Hib está presente en una dosis de sacárido más baja que la dosis de sacárido media de los al menos dos conjugados de polisacárido de N. meningitidis. Como alternativa, el conjugado de Hib está presente en una dosis de sacárido más baja que la dosis de sacárido de cada uno de los al menos dos conjugados de polisacárido de N. meningitidis. Por ejemplo, la dosis del conjugados de conjugado Hib puede ser al menos un 10 %, 20 %, 30 %, 40 %, 50 %, 60 %, 70 % o un 80 % más baja que la dosis de sacárido media o más baja de los al menos dos conjugados de polisacárido de N. meningitidis adicionales.
El término "sacárido" incluye polisacáridos u oligosacáridos. Los polisacáridos se aíslan de bacterias o se aíslan de bacterias y se dimensionan en cierto grado mediante métodos conocidos (véanse por ejemplo los documentos EP497524 y EP497525) y opcionalmente mediante microfluidización. Los polisacáridos se pueden dimensionar con el fin de reducir la viscosidad de las muestras de polisacárido y/o para mejorar la capacidad de filtración de productos conjugados. Los oligosacáridos se caracterizan porque generalmente son polisacáridos hidrolizados con un bajo número de unidades de repetición (por lo general 5-30 unidades de repetición).
La dosis media se determina mediante adición de las dosis de todos los polisacáridos adicionales y dividiendo entre el número de polisacáridos adicionales. Los polisacáridos adicionales en todos los polisacáridos dentro de la
composición inmunogénica excepto Hib y pueden incluir polisacáridos capsulares de N. meningitidis. La "dosis" está en la cantidad de la composición inmunogénica o vacuna que se administra a un ser humano.
Un sacárido Hib es el polisacárido capsular fosfato de polirribosilo (PRP) de Haemophilus influenzae de tipo b o un oligosacárido obtenido a partir del mismo.
'Al menos dos conjugados de sacárido bacteriano adicionales' se debe tomar como haciendo referencia al menos dos conjugados de sacárido bacterianos adicionales bacterial además de un conjugado de Hib. Los al menos dos conjugados bacterianos adicionales pueden incluir conjugados de polisacárido capsular de N. meningitidis.
Las composiciones inmunogénicas de la invención pueden comprender conjugados de sacárido adicionales obtenidos a partir de uno o más de of Neisseria meningitidis, Streptococcus pneumoniae, Streptococci del Grupo A, Streptococci del Grupo B, S. typhi, Staphylococcus aureus o Staphylococcus epidermidis. En una realización, la composición inmunogénica comprende polisacáridos u oligosacáridos capsulares obtenidos a partir de uno o más de los serogrupos A, C, W135 y Y de Neisseria meningitidis. Una realización adicional comprende polisacáridos u oligosacáridos capsulares obtenidos a partir de Streptococcus pneumoniae. Los antígenos de polisacárido u oligosacárido capsular neumocócico se seleccionan opcionalmente entre los serotipos 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20, 22F, 23F y 33F (opcionalmente entre los serotipos 1, 3, 4, 5, 6B, 7F, 9V, 14, 18C, 19F y 23F). una realización adicional comprende el Tipo 5, Tipo 8 o 336 de polisacáridos u oligosacáridos capsulares de Staphylococcus aureus. Una realización adicional comprende el Tipo I, Tipo II o Tipo III de polisacáridos capsulares de Staphylococcus epidermidis. Una realización adicional comprende el sacárido Vi (poli u oligosacárido) de S. typhi. Una realización adicional comprende el Tipo la, Tipo Ic, Tipo II, Tipo III o Tipo V de polisacáridos u oligosacáridos capsulares de Streptococcus del Grupo B. Una realización adicional comprende los polisacáridos u oligosacáridos capsulares de Streptococcus del Grupo A, comprendiendo además opcionalmente al menos una proteína M y opcionalmente múltiples tipos de proteína M.
En una realización, la composición inmunogénica de la invención contiene cada polisacárido capsular de N. meningitidis a una dosis entre 0,1-20 |jg; 1-10 |jg; 2-10 |jg, 2,5-5 |jg, aproximada o exactamente 5 |jg; o aproximada o exactamente 2,5 jig.
En una realización, la composición inmunogénica de la invención por ejemplo contiene el conjugado de sacárido Hib a una dosis de sacárido entre 0,1 y 9 jig; 1 y 5 jig o 2 y 3 jig o aproximada o exactamente 2,5 jig y cada uno de los conjugados de polisacárido de N. meningitidis a una dosis de sacárido entre 2 y 20 jig, 3 y 10 jig, o entre 4 y 7 jig o aproximada o exactamente 5 jig.
"Alrededor de" o "aproximadamente" son tal como se definen dentro de un 10 % más o menos del número dado para los fines de la invención.
En una realización, la composición inmunogénica de la invención contiene una dosis de sacárido del conjugado de sacárido Hib que es por ejemplo inferior a un 90 %, 80 %, 75 %, 70 %, 60 %, 50 %, 40 %, 30 %, 20 % o un 10 % de la dosis media de sacárido de al menos dos, tres, cuatro o cada uno de los conjugados de polisacárido de N. meningitidis. La dosis de sacárido del sacárido Hib está por ejemplo entre un 20 % y 60 %, 30 % y 60 %, 40 % y un 60 % o aproximada o exactamente un 50 % de la dosis media de sacárido de al menos dos, tres, cuatro o cada uno de los conjugados de polisacárido de N. meningitidis.
En una realización, la composición inmunogénica de la invención contiene una dosis de sacárido del conjugado de sacárido Hib que es por ejemplo inferior a un 90 %, 80 %, 75 %, 70 %, 60 %, 50 %, 40 %, 30 %, 20 % o un 10 % de la dosis de sacárido más baja de al menos dos, tres, cuatro o cada uno de los conjugados de polisacárido de N. meningitidis. La dosis de sacárido del sacárido Hib está por ejemplo entre un 20 % y 60 %, 30 % y 60 %, 40 % y 60 % o aproximada o exactamente 50 % de la dosis de sacárido más baja de al menos dos, tres, cuatro o cada uno de los conjugados de polisacárido de N. meningitidis.
En una realización de la invención, la dosis de sacárido de cada uno de al menos dos, tres, cuatro o cada uno de los conjugados de polisacárido de N. meningitidis estacionalmente la misma, o aproximadamente la misma.
Como ejemplos de una composición inmunogénica de la invención está una composición que consiste en o que comprende:
MenA, MenC, MenW y MenY a proporciones de dosis de sacárido de 1:1:1:1 o 2:1:1:1 o 1:2:1:1 o 2:2:1:1 o 1:3:1:1 o 1:4:1:1 (p/p).
Un aspecto adicional de la invención es una vacuna que comprende la composición inmunogénica de la invención y un excipiente farmacéuticamente aceptable.
En una realización, la composición inmunogénica de la invención se tampona a, o se ajusta a, entre pH 7,0 y 8,0, pH 7,2 y 7,6 o aproximada o exactamente pH 7,4.
La composición o vacunas inmunogénicas de la invención se liofilizan opcionalmente en presencia de un agente estabilizante por ejemplo un poliol tal como sacarosa o trehalosa.
Opcionalmente, la composición o vacuna inmunogénica de la invención contiene la cantidad de un adyuvante suficiente para aumentar la respuesta inmunológica al agente inmunógeno. Los ayudantes adecuados incluyen, pero no se limitan a sales de aluminio (fosfato de aluminio o hidróxido de aluminio), mezclas de escualeno (SAF-1), péptido de muramilo, derivados de saponina, preparaciones de pared celular de micobacterias, monofosforil lípido A, derivados de ácido micólico, tensioactivos de copolímero de bloque no iónico, Quil A, subunidad de toxina B del cólera, polifosfaceno y derivados, y complejos inmunoestimulantes (los ISCOM) tal como los descritos por Takahashi et al. (1990) Nature 344: 873-875.
Para las combinaciones de N. meningitidis o HibMen discutidas anteriormente, puede ser ventajoso no usar ningún adyuvante de sal de aluminio o ningún adyuvante.
Como con todas las composiciones o vacunas inmunogénicas, las cantidades inmunológicamente eficaces de los inmunógenos se deben determinar por vía empírica. Los factores a considerar incluyen la inmunogenicidad, tanto si el inmunógeno forma complejo con o se une covalente mente a un adyuvante o proteína vehículo u otro vehículo, vías de administración y el número de dosificaciones de inmunización que se van a administrar. Los factores de ese tipo se conocen en la técnica de la vacuna y bien dentro de la habilidad de los inmunólogos está hacer tales determinaciones sin experimentación excesiva.
El agente activo puede estar presente en concentraciones variables en la composición farmacéutica de la vacuna de la invención. Por lo general, la concentración mínima de la sustancia es una cantidad necesaria para conseguir su uso previsto, mientras que la concentración máxima es la cantidad máxima que permanecerá en solución o suspendida homogéneamente dentro de la mezcla inicial. Por ejemplo, la cantidad mínima de un agente terapéutico es opcionalmente una que proporcionará una única dosificación terapéuticamente eficaz. Para las sustancias bioactivas, la concentración mínima es una cantidad necesaria para la bioactividad tras la reconstitución y la concentración máxima está en el punto en el que no se puede mantener una suspensión homogénea. En el caso de unidades de dosificación única, la cantidad es la de una sola aplicación terapéutica. En general, se espera que cada dosis comprenda 1-100 |jg de antígeno de proteína, opcionalmente 5-50 |jg o 5-25 |jg. Los ejemplos de dosis de sacáridos bacterianos son 10-20 jg, 5-10 jg, 2,5-5 jg o 1-2,5 jg. La cantidad preferente de la sustancia varía de una sustancia a otra, pero la puede determinar fácilmente alguien con experiencia en la materia.
Las preparaciones de vacuna de la presente invención se pueden usar en métodos para proteger o tratar a un mamífero (por ejemplo, un paciente humano) susceptible de infección, mediante la administración de dicha vacuna por vía sistémica o mucosa. Un paciente humano es opcionalmente un bebé (menos de 12 meses), un niño pequeño (12-24, 12-16 o 12-14 meses), un niño (2-10, 3-8 o 3-5 años) y un adolescente (12 -25, 14-21 o 15-19 años) o un adulto (cualquier edad mayor de 12, 15, 18 o 21). Estas administraciones pueden incluir inyección por vía intramuscular, intraperitoneal, intradérmica o subcutánea; o vía administración mucosa a los tractos oral/alimentario, respiratorio, genitourinario. Se prefiere la administración intranasal de vacunas para el tratamiento de la neumonía o la otitis media (ya que el transporte nasofaríngeo de neumococos se puede prevenir de manera más eficaz, lo que atenúa la infección en su etapa más temprana). Aunque la vacuna de la invención se puede administrar como una dosis única, sus componentes también se pueden administrar en conjunto al mismo tiempo o en diferentes momentos (por ejemplo, si los sacáridos están presentes en una vacuna, estos se podrían administrar por separado al mismo tiempo o 1-2 semanas después de la administración de una vacuna de proteína bacteriana para una coordinación óptima de las respuestas inmunes entre sí). Además de una vía de administración única, se pueden usar 2 días de administración diferentes. Por ejemplo, los antígenos virales se pueden administrar por vía ID (intradérmica), mientras que las proteínas bacterianas se pueden administrar por vía IM (intramuscular) o por vía IN (intranasal). Si los sacáridos están presentes, se pueden administrar por vía iM (o ID) y las proteínas bacterianas se pueden administrar por vía IN (o ID). Además, las vacunas de la invención se pueden administrar por vía IM para dosis de cebado y por vía IN para dosis de refuerzo.
La preparación de vacuna se describe generalmente en Vaccine Design ("The subunit and adjuvant approach" (eds Powell M.F. y Newman M.J.) (1995) Plenum Press New York). La encapsulación dentro de liposomas se describe en Fullerton, documento de Patente de Estados Unidos N.° 4.235.877.
Un aspecto adicional de la invención es un kit de vacuna para administración simultánea o secuencial que comprende dos composiciones inmunogénicas multivalentes para proporcionar protección en un hospedador frente a una enfermedad causada por Bordetella pertussis, Clostridium tetani, Corynebacterium diphtheriae y Neisseria meningitidis y opcionalmente Haemophilus influenzae. Por ejemplo, el kit comprende opcionalmente un primer recipiente que comprende uno o más de:
toxoide del tétano (TT),
toxoide de difteria (DT), y
componentes de células completas o acelulares de pertussis
y un segundo recipiente que comprende cualquiera de:
una composición inmunogénica de la invención, opcionalmente liofilizada.
o
conjugado de sacárido Hib, y
una composición inmunogénica de la invención, opcionalmente liofilizada.
Los ejemplos de formulación del conjugado Hib y los conjugados de polisacárido de N. meningitidis son como se han descrito anteriormente.
Un aspecto adicional de la invención es un kit de vacuna para administración simultánea o secuencial que comprende dos composiciones inmunogénicas multivalentes para proporcionar protección en un hospedador frente a una enfermedad causada por Streptococcus pneumoniae y Neisseria meningitidis y opcionalmente Haemophilus influenzae. Por ejemplo, el kit comprende opcionalmente un primer recipiente que comprende uno o más de:
uno o más conjugados de una proteína vehículo y un sacárido capsular de Streptococcus pneumoniae [en el que el sacárido capsular es opcionalmente de un serotipo neumocócico seleccionado entre el grupo que consiste en 1,2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20, 22F, 23F y 33F].
y un segundo recipiente que comprende cualquiera de:
una composición inmunogénica de la invención, opcionalmente liofilizada.
o
conjugado de sacárido de Hib, y
una composición inmunogénica de la invención, opcionalmente liofilizada.
Los ejemplos del conjugado Hib y los conjugados de polisacárido de N. meningitidis son como se han descrito anteriormente.
Por lo general la vacuna de Streptococcus pneumoniae en el kit de vacuna de la presente invención comprenderá antígenos de sacárido (o finalmente conjugados), en el que los polisacárido se tienen a partir de al menos cuatro serotipos de neumococos elegidos entre el grupo que consiste en 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15b , 17F, 18C, 19A, 19F, 20, 22F, 23F y 33F. Opcionalmente los cuatro serotipos incluyen 6B, 14, 19F y 23F. Opcionalmente, al menos 7 serotipos están incluidos en la composición, por ejemplo los obtenidos a partir de los serotipos 4, 6B, 9V, 14, 18C, 19F, y 23F. Opcionalmente más de 7 serotipos están incluidos en la composición, por ejemplo al menos 10, 11, 12, 13 o 14 serotipos. Por ejemplo la composición en una realización incluye 11 polisacáridos capsulares obtenidos a partir de los serotipos 1, 3, 4, 5, 6B, 7F, 9V, 14, 18C, 19F y 23F (opcionalmente conjugados). En una realización de la invención al menos 13 antígenos de polisacárido (opcionalmente conjugados) están incluidos, aunque en la invención además también se contemplan antígenos de polisacárido, por ejemplo 23 valentes (tal como los serotipos 1, 2, 3, 4, 5, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20, 22F, 23F y 33F).
También se desvela un kit de vacuna que comprende un tercer componente. Por ejemplo, el kit comprende opcionalmente un primer recipiente que comprende uno o más de:
toxoide del tétano (TT),
toxoide de difteria (DT), y
componentes de células completas o acelulares de pertussis
y un segundo recipiente que comprende:
uno o más conjugados de una proteína vehículo y un sacárido capsular de Streptococcus pneumoniae [en el que el sacárido capsular es opcionalmente de un serotipo de pneumocócico seleccionar entre el grupo que consiste en 1, 2, 3, 4, 5, 6A, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20, 22F, 23F y 33F].
y un tercer recipiente que comprende:
una composición inmunogénica de la invención, opcionalmente liofilizada.
o
conjugado de sacárido de Hib, y
una composición inmunogénica de la invención, opcionalmente liofilizada.
Las composiciones inmunogénicas de la invención pueden comprender además opcionalmente antígenos de sarampión y/o paperas y/o rubéola y/o varicela. Por ejemplo, la composición inmunogénica meningocócica contiene antígenos de sarampión, paperas y rubéola o sarampión, paperas, rubéola y varicela. En una realización, estos antígenos virales están opcionalmente presentes en el mismo recipiente que el conjugado o conjugados meningocócico y/o de sacárido Hib. En una realización, estos antígenos virales están liofilizados.
Un aspecto adicional de la invención es un proceso para preparar la vacuna de la invención que comprende la etapa de mezclar la composición inmunogénica de la invención con un vehículo farmacéuticamente aceptable.
La preparación de vacuna generalmente se describe en Vaccine Design ("The subunit and adjuvant approach" (eds Powell M.F. y Newman M.J.) (1995) Plenum Press New York). La encapsulación dentro de liposomas se describe en Fullerton, documento de Patente de Estados Unidos N.° 4.235.877.
Un aspecto adicional de la invención es una composición inmunogénica de la invención para su uso en el método de inmunización de un hospedador humano frente a una enfermedad causada por N. meningitidis y opcionalmente una infección por Haemophilus influenzae que comprende la administración al hospedador de una dosis inmunoprotectora de la composición o vacuna inmunogénica o kit de la invención.
Un aspecto adicional de la invención es una composición inmunogénica de la invención para su uso en el tratamiento o prevención de una enfermedad causada por N. meningitidis y opcionalmente una infección por Haemophilus influenzae.
La invención se ilustra en los ejemplos adjuntos. Los ejemplos que siguen a continuación se llevan a cabo usando técnicas convencionales, que son bien conocidas y de rutina para los expertos en la materia, excepto cuando se describe de otro modo con detalle en cualquier parte. Los ejemplos son ilustrativos, pero no limitan la invención. Ejemplos
Ejemplo 1 - preparación de conjugados de polisacárido
La unión covalente del polisacárido PRP de Haemophilus influenzae (Hib) a TT se llevó a cabo mediante una química de acoplamiento desarrollada por Chu et al (Infection and Immunity 1983, 40 (1); 245-256). El polisacárido pRP de Hib si activo mediante adición de CNBr e incubando a pH 10,5 durante los seis minutos. El pH se disminuyó a pH 8,75 y se añadió dihidrazida del ácido adípico (ADH) y la incubación continuó durante un periodo adicional de 90 minutos. El PRP activado se acopló a toxoide del tétano unificado a través de condensación de carbodiimida usando 1-etil-3-(3-dimetilaminopropil)carbodiimida (EDAC). La EDAC se añadió al PRP activado para alcanzar una proporción final de 0,6 mg de EDAC/mg de PRP activado. El pH se ajustó a 5,0 y el toxoide del tétano purificado se añadió para alcanzar 2 mg de TT/mg de PRP activado. La solución resultante se dejó durante tres días con agitación suave. Después de filtración a través de una membrana de 0,45 pm, el conjugado se purificó en una columna sephacryl S500HR (Pharmacia, Suecia) equilibrada en NaCl 0,2 M.
Los conjugados de MenC -TT se produjeron usando polisacáridos nativos (de aproximadamente 150 kDa tal como se mide por MALLS). Los conjugados de MenA-TT se produjeron usando cualquiera de polisacárido nativo o polisacárido ligeramente microfluidizado de aproximadamente 60 kDa tal como se mire con el método de MALLS del ejemplo 2. Los conjugados MenW y MenY-TT se produjeron usando polisacáridos dimensionado es de aproximadamente 100-200 kDa tal como se mide por MALLS (véase el ejemplo 2). La dimensión en que se realizó mediante microfluidización usando un aparato homogeneizador Emulsiflex C-50. los polisacáridos a continuación se filtraron a través de un filtro de 0,2 pm.
La activación y el acoplamiento se llevaron a cabo como se describe en los documentos WO 96/29094 y WO 00/56360. En resumen, el polisacárido a una concentración de 10-20 mg/ml en NaCl 2 M a pH 5,5-6,0 se mezcló con la solución CDAP (100 mg/ml recién preparados en acetonitrilo/WFI, 50/50) hasta una proporción final de CDAP/polisacárido de 0,75/1 o 1,5/1. Después de 1,5 minutos, el pH se elevó con hidróxido sódico a pH 10,0. Después de tres minutos, el toxoide del tétano se añadió para alcanzar una proporción de proteína/polisacárido de 1,5/1 para MenW, 1,2/1 para MenY, 1,5/1 para MenA o 1,5/1 para MenC. La reacción continuó de una a dos horas. Después de la etapa de acoplamiento, se añadió glicina a una proporción final de glicina/PS (p/p) de 7,5/1 y el pH se ajustó a pH 9,0. La mezcla se dejó durante 30 minutos. El conjugado se aclaró usando un filtro Kleenpak de 10 pm a continuación se cargó sobre una columna Sephacryl S400HR usando un tampón de elución de NaCl 150 mM, Tris 10 mM o 5 mM a PHP,5. Los lotes clínicos se filtraron en una membrana esterilizante Opticap 4. los conjugados resultantes presentaban una proporción media de polisacárido:proteína de 1:1-1:5 (p/p).
Con el fin de conjugar el polisacárido capsular MenA al toxoide del tétano a través de un espaciado, se usó el siguiente método. La unión covalente del polisacárido y el espaciador (ADH) se lleva a cabo mediante química de acoplamiento mediante la cual el polisacárido se activa en condiciones controladas mediante un agente de
cianilación, tetrafluoroborato de 1-ciano-4-dimetilamino-piridinio (CDAP). El espaciador reacciona con el PS cianilado a través de sus grupos hidrazino, para formar un enlace de isourea estable entre el espaciador y el polisacárido. Una solución de 10 mg/ml de MenA se trató con una solución recién preparada de 100 mg/ml de CDAP en acetonitrilo/agua (50/50 (v/v)) para obtener una proporción de CDAP/MenA de 0,75 (p/p). la lista inicial después de 1,5 minutos, el pH se aumentó a pH 10,0. Tres minutos más tarde, se añadió ADH para obtener una proporción de ADH/MenA de 8,9. El pH de la solución se disminuyó hasta 8,75 y la reacción evolucionó durante 2 horas.
Antes de la reacción de conjugación, la solución de TT purificada y la solución de PSAah se diluyeron para alcanzar una concentración de 10 mg/ml para PSAah y 10 mg/ml para TT.
EDAC se añadió a la solución de PSah con el fin de alcanzar una proporción final de 0,9 mg de EDAC/mg de PSAah. El pH se ajustó a 5,0. El toxoide del tétano purificado se añadió con una bomba peristáltica (en 60 minutos) para alcanzar 2 mg de TT/mg de PSAah. La solución resultante se dejó 60 min a 25 °C con agitación para obtener un tiempo de acoplamiento final de 120 min. El conjugado se aclaró usando un filtro de 10 pm y se purificó usando una columna Sephacryl S400HR.
Ejemplo 2 - determinación del peso molecular usando MALLS
Los detectores se acoplaron a una columna de exclusión por tamaño de HPLC a partir de la cual se eluyeron las muestras. Por un lado, el detector de dispersión de luz láser midió las intensidades de luz dispersadas a 16 ángulos mediante la solución macromolecular y por otro lado, un refractómetro interferométrico colocado en línea permitió la determinación de la cantidad de muestra eludida. A partir de estas intensidades, se puede determinar el tamaño de la forma de las macromoléculas en solución.
El peso molecular medio en peso (Pm) se define como la suma de los pesos de todas las especies, multiplicado por su respectivo peso molecular y dividido entre la suma de los pesos de todas las especies.
a) Peso molecular promedio en peso: -Pm-
b) Peso molecular promedio en número: -Mn-
c) raíz cuadrada media del radio: -Rw- y R2w es el cuadrado del radio definido por:
(-mi- es la masa de un centro de dispersión i y -ri- esa distancia entre el centro de dispersión i y el centro de gravedad de la macromolécula).
d) La polidispersión se define como la proporción -Pm / Mn-.
Los polisacáridos meningocócicos se analizaron por MALLS mediante carga sobre dos columnas de HPLC (TSKG6000 y 5000PWxl) usadas en combinación. Sobre la columna se cargaron 25 pl del polisacárido y se eludieron con 0,75 ml de agua filtrada. Los polisacáridos se detectan usando un detector de dispersión de luz (Wyatt Dawn DSP equipado con un láser de argón de 10 mW a 488 nm) y un refractómetro inferométrico (Wyatt Otilab DSP equipado con una celda P100 y un filtro rojo a 498 nm).
Las polidispersiones y recuperaciones de peso molecular de todas las fuerzas se calcularon con el método de Debye usando un ajuste polinómico del orden de 1 en el software Astra 4.72.
Ejemplo 3 - ensayo clínico que compara la inmunización con Meningitec o un conjugado de MenC-TT de mayor tamaño
Se llevó a cabo un estudio controlado, de fase II, abierto para comparar la vacuna de conjugado de serogrupo C meningocócico (MenC) de GSK Biologicals con la vacuna de conjugado de serogrupo C b-meningocócico de Haemophilus influenzae (Hib-MenC) de GSK Biological o Meningitec®. Cada dosis de Meningitec® contiene 10 |jg de conjugados de oligosacárido de serogrupo C meningocócico con 15 jg de CRM197 y la produce Wyeth. Los conjugados de MenC de GSK contenían polisacáridos nativos de aproximadamente 200 kDa conjugado con toxoide del tétano (TT).
El estudio consistió en cinco grupos, cada uno planificado para contener 100 sujetos, situados en dos ramas paralelas o sigue a continuación: En el presente estudio, todos los sujetos en ambas ramas recibieron un quinto (1/5) de una dosis de Mencevax™ ACWY y una dosis simultánea de Infanrix™ hexa a los 12-15 meses de edad (Mes del Estudio 0). Se recogieron dos muestras de sangre de todos los sujetos (Mes del Estudio 0 y Mes del Estudio 1). La rama 1 consistió en cuatro grupos de estudio de vacunación primaria que se cebaron a las edades de 3, 4 y 5 meses con las siguientes vacunas:
• Grupo K: MenC (10 jg), no adsorbido sobre sales de aluminio (no ads.), conjugado de toxoide del tétano (TT) e Infanrix™ hexa (MenC10-TT Infanrix™ hexa)
• Grupo L: Hib (10 jg)-MenC (10 jg), conjugado de TT no ads. e Infanrix™ penta (Hib10-MenC10-TT Infanrix™ penta)
• Grupo M: Hib (5 jg)-MenC (5 jg), no ads., conjugado de TT e Infanrix™ penta (Hib5-MenC5-TT Infanrix™ penta)
• Grupo N: Meningitec™ e Infanrix™ hexa (Meningitec™ Infanrix™ hexa)
Los dos grupos de vacuna Hib-MenC-TT (Grupos L y M) se mantuvieron con ocultación en el estudio de estimulación como la formulación exacta de la vacuna candidata.
La rama 2-(Grupo O) consistió en sujetos emparejados por edades no vacunados previamente con una vacuna de serogrupo C meningocócico (sin tratamiento previo) pero que habían recibido vacunas pediátricas de rutina de acuerdo con la German Permanent Commission on Immunization.
Criterios para evaluación:
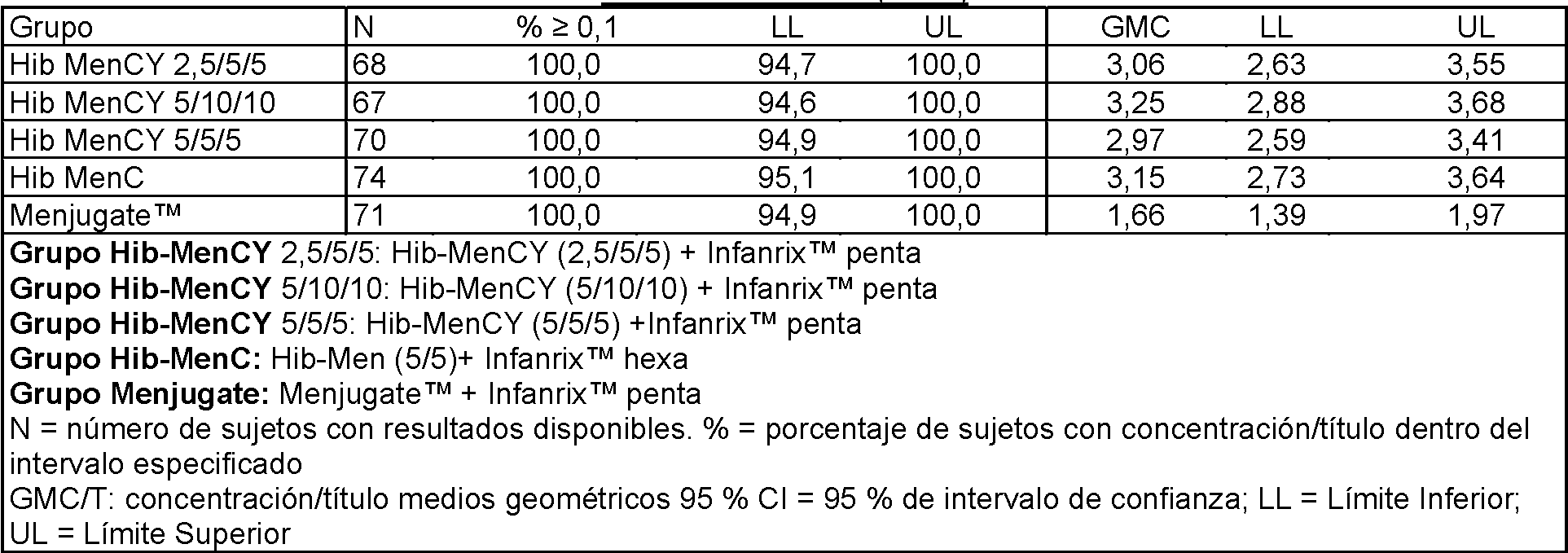
Inmunogenicidad: Determinación de títulos de anticuerpos bactericida frente a meningococo C (SBA-MenC) mediante un ensayo bactericida (punto de corte: una dilución de 1:8) y medición de ELISA de anticuerpos frente al serogrupo C meningocócico (punto de corte de ensayo: 0,3 jg/ml), el PRP del polisacárido Hib (punto de corte del ensayo: 0,15 jg/ml) y toxoide del tétano (punto de corte del ensayo: 0,1 IU/ml) en muestras de sangre obtenidas antes de la vacunación y aproximadamente un mes después de la vacunación en todos los sujetos.
Métodos estadísticos:
Demografía: Determinación de la edad media en meses (con mediana, intervalo y desviación estándar [DT]), y composición racial y género de las cohortes vacunadas de ATP y Total.
Inmunogenicidad:
Se llevaron a cabo dos análisis de inmunogenicidad basándose en la cohorte de ATP para inmunogenicidad (para análisis de memoria inmunológica y respuesta a estimulación) o la cohorte de ATP para seguridad (para análisis de persistencia). Estos incluyeron: Evaluación de la memoria inmunológica para MenC y respuesta a estimulación para Hib y Tétano (antes y un mes después de la administración de 1/5 de dosis de la vacuna de polisacárido sencillo): • Determinación de los títulos de media geométrica y concentraciones (GMT y GMC) con intervalos de confianza de un 95 % (95 % de Cl)
• Determinación el porcentaje de sujetos con título/concentración de anticuerpo por encima de los puntos de corte propuestos con un 95 % de Cl exacto (tasas de seropositividad/seroprotección)
• Investigación de títulos/concentración de anticuerpos después de vacunación usando curvas acumulativas inversas
• Computación de un 95 % de Cl asintótico estandarizado para la diferencia de la tasa de seropositividad/seroprotección
• entre el grupo cebado (Grupos K, L, M y N) y el grupo no cebado (Grupo O)
• Determinación de la media geométrica de la proporción individual de títulos de SBA-MenC con respecto a la
concentración de anti-PSC, con un 95 % de CI
• Determinación del 95 % de CI para la proporción de GMT/C después de la vacunación entre los grupos K, L, M y el grupo de control N para anti-PRP y anti-tétano y entre cada grupo cebado (Grupos K, L, M y N) y el grupo no cebado (Grupo O) para SBA-MenC y anti-PSC usando un modelo de ANOVA.
Resultados
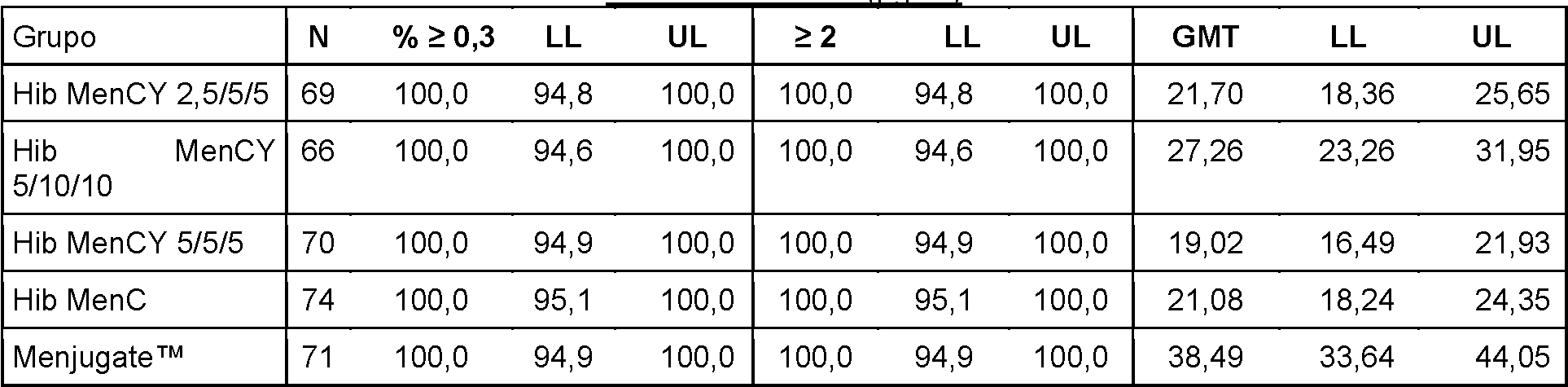
T l 1. T í BA-Mn n nr in ni r ni-P v n i n rf rz
Se consiguieron títulos más elevados de anticuerpos frente a MenC y títulos de SBA más elevados cebando con las vacunas de conjugado de polisacárido MenC de tamaño más grande (grupos K, L y M) en comparación con la vacuna de conjugado de oligosacárido Meningitec.
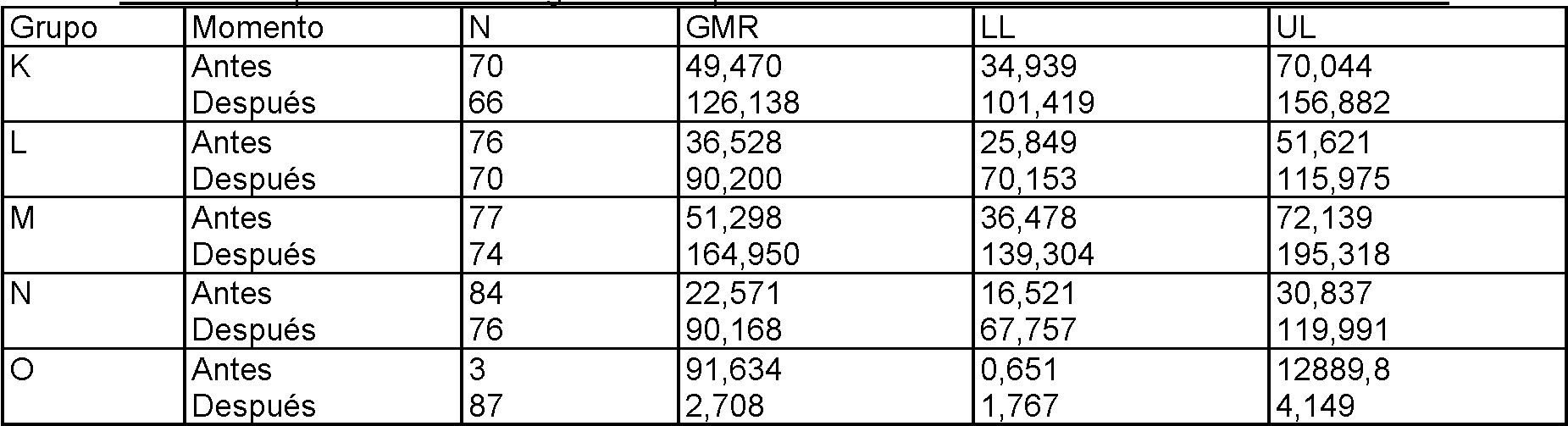
T l 2: Pr ri n m i m ri r í l Mn BA n nr in ni-P
En los cuatro grupos cebados (Grupos K, L, M y N), el GMR aumentó de forma significativa a partir de la vacunación de refuerzo de antes a después indicando la presencia de maduración y funcionalidad de anticuerpo. El GMR en el Grupo M (cebado con Hib5-MenC5-TT) era más elevado que en el Grupo N (cebado con Meningitec™).
-
nin i n
Se consiguieron títulos más elevados de SBA frente a MenC cebando con el tamaño más grande de MenC (grupos K, L y M) en comparación con el cebado con el conjugado de MenC-oligosacárido Meningitec.
Memoria inmunológica (cohorte de ATP para inmunogenicidad)
La administración de 1/5 dosis de la vacuna ACWY de polisacárido puro provocó un título de SBA-MenC muy elevado en los cuatro grupos privados con un 98,7-100 % y un 97,5-100 % de los sujetos cebados con un régimen de vacuna candidata representaba los >1:8 y > 1:128, respectivamente. En el grupo cebado con el régimen de Meningitec™, había una tendencia para porcentaje de sujetos menor con títulos > 1:128 (91,8 %). En comparación, un 17,6 % de los sujetos sin cebar presentaban títulos de SBA MenC > 1:8 y > 1:128.
Ejemplo 4 Ensayo clínico en fase II con vacuna de conjugado de HibMenAC -TT mezclada con DTPw-HepB Diseño del estudio: Estudio de un solo centro, abierto, aleatorio (1:1:1:1:1), con cinco grupos. Los cinco grupos recibieron el siguiente régimen de vacunación respectivamente, a las 6, 10 y 14 semanas de edad.
Tritanrix.-HepB/Hib-MenAC 2,5 pg/2,5 pg/2,5 pg: en lo sucesivo denominado 2,5/2,5/2,5
• Tritanrix.-HepB/Hib-MenAC 2,5 pg/5 pg/5 pg: en lo sucesivo denominado 2,5/5/5
• Tritanrix.-HepB/Hib-MenAC 5 pg/5 pg/5 pg: en lo sucesivo denominado 5/5/5
• Tritanrix.-HepB Hiberix.: en lo sucesivo denominado Hiberix
• Tritanrix.-HepB/Hiberix. Meningitec: en lo sucesivo denominado Meningitec
Las muestras de sangre se extrajeron en el momento de la primera dosis de vacuna (Antes) y un mes después de la tercera dosis de vacuna (Después de la dosis 3).
Tritanrix es una vacuna DTPw comercializada por GlaxoSmithKline Biologicals S.A.
Se usaron 105 sujetos en cada uno de los cinco grupos proporcionando un total de 525 sujetos en el estudio.
Tabla 4 Contenido de formulaciones de vacuna GSK
Las formulaciones de la vacuna Hib-MenAC se mezclaron de forma extemporánea con Tritanirix-HepB. La vacuna combinada frente a difteria-tétano-células completas de Bordetella pertussis - hepatitis B (DTPw-HB) de GSK Biologicals (Tritanrix-HepB) contiene no menos de 30 Unidades Internacionales (UI) de toxoide de difteria, no menos de 60 UI de toxoide del tétano, no menos de 4 UI de Bordetella pertussis muerta y 10 pg de antígeno de superficie de hepatitis B recombinante.
Terapia de referencia, dosis, modo de administración, número de lote:
Programa/sitio de vacunación: Un grupo recibió la vacuna Tritanrix.-HepB por vía intramuscular en el muslo izquierdo e Hiberix™ por vía intramuscular en el muslo derecho a las 6, 10 y 14 semanas de edad.
Otro grupo recibió la vacuna Tritanrix™ -HepB / Hiberix™ por vía intramuscular en el muslo izquierdo y la vacuna
Meningitec por vía intramuscular en el muslo derecho a las 6, 10 y 14 semanas de edad.
Vacuna/composición/dosis/número de lote: La vacuna Tritanrix™-HepB usada fue como se ha descrito anteriormente. Una dosis (0,5 ml) de la vacuna de conjugado de tipo b de Haemophilus influenzae de GSK Biologicals: Hiberix™ contenía 10 |jg de PRP conjugado con toxoide del tétano. En el Grupo de Hiberix™, se mezcló con diluyente estéril y el Grupo de Meningitec™ se mezcló con Tritanrix™-HepB.
Una dosis (0,5 ml) de la vacuna MENINGITEC™ de Wyeth Lederle contenía: 10 jg de oligosacárido capsular del grupo C meningocócico conjugado con 15 jg de proteína de CRM197 Corynebacterium diphtheria y aluminio en forma de sales.
Resultados - respuestas inmunológicas generadas frente a Hib, MenA y MenC
Conclusión
Una comparación de los resultados de inmunogenicidad conseguidos usando la vacuna de conjugado de MenC-CRM197 de oligosacáridos y las tres formulaciones GSK que contienen los conjugados de polisacárido MenA-TT y MenC -TT mostraron que los conjugados de polisacárido Men fueron capaces de provocar una buena respuesta inmunogénica similar a la conseguida usando la vacuna conjugada de oligosacáridos Meningitec. Todas las formulaciones sometidas a ensayo dieron una respuesta a MenC en el 100 % de los pacientes.
Ejemplo 5 - Ensayo clínico de fase II que administra Hib MenCY de forma simultánea con Infanrix penta de acuerdo con una programación de 2, 3 y 4 meses
Diseño del estudio: un estudio multicéntrico controlado aleatorio abierto (parcialmente con doble ocultación*), de Fase II con 5 grupos que recibieron una programación primaria de tres dosis con vacunas de la siguiente manera: Grupo Hib-MenCY 2,5/5/5: Hib-MenCY (2,5/5/5) Infanrix™ penta Grupo Hib-MenCY 5/10/10: Hib-MenCY (5/10/10) Infanrix™ penta Grupo Hib-MenCY 5/5/5: Hib-MenCY (5/5/5) Infanrix™ penta Grupo Hib-MenC: Hib-MenC (5/5) Infanrix™ penta Grupo Menjugate: Menjugate™** Infanrix™ hexa (control).
*Hib-MenCY 2,5/5/5, Hib-MenCY 5/10/10 y Hib-MenC se administraron con doble ocultación mientras el grupo de Hib-MenCY 5/5/5 y el grupo de Menjugate eran abiertos. Las formulaciones de 2,5/5/5, 5/10/10 y 5/5/5 de Hib-MenCY contienen polisacáridos MenC y polisacáridos MenY nativos que se microfluidizan. **Menjugate™ contiene 10 pg de oligosacáridos MenC conjugados con 12,5-25 pg de CRM197 por dosis y la produce Chiron. Vacunación a los /- 2, 3, 4 meses de edad (Mes del estudio 0, Mes 1 y Mes 2), y muestras de sangre (3,5 ml) de todos los sujetos antes y un mes después de la vacunación primaria (Mes del estudio 0 y Mes 3).
Vacuna de estudio, dosis, modo de administración, número de lote: Tres dosis inyectadas por vía intramuscular a intervalos de un mes, aproximadamente a los 2, 3 y 4 meses de edad como sigue a continuación:
T l : V n mini r i n r l r r r m i n i i i
Inmunogenicidad: Medición de los títulos/concentraciones de anticuerpos frente a cada antígeno de vacuna:
Antes de la primera dosis (Mes 0) y aproximadamente un mes después de la tercera dosis (Mes 3) en todos los sujetos para: SBA-MenC y SBA-MenY, anti-PSC y anti-PSY, anti-PRp, anti-T, anti-FHA, anti-pRN y anti-PT. Usando la actividad bactericida de suero frente a los serogrupos C y Y de N. meningitidis (. De corte de SBA-MenC y SBA-MenY: 1:8 y 1:128); ensayos de ELISA conjuntos de corte: > 0,3 pg/ml y > 2 pg/ml para los polisacáridos de los serogrupos C y Y anti- N. meningitidis (IgG anti-PSC y IgG anti-PSY); > 0,15 pg/ml y > 1,0 pg/ml para polirribosilribitol-fosfato de polisacárido Hib (IgG anti-PRP); 5EL.U/ml para anti-FHA, anti-pRN, anti-PT; > 0,1 IU/ml anti-toxoide del tétano (anti-TT). Solo un mes después de la tercera dosis (Mes 3) en todos los sujetos para: anti-D, los anti-HB y anti-polio 1, 2 y 3. Usando ensayos de ELISA con puntos de corte: 0,1 IU/ml para anti-difteria (anti-D); > 10 mlU/ml para antihepatitis B (anti-HBs); y punto de corte de ensayo de microneutralización: 1:8 para tipos de 1, 2 y 3 anti polio (anti-polio 1, 2 y 3).
Métodos estadísticos:
Las tasas de seroprotección/seropositividad y las concentraciones/títulos de media geométrica (los GMC/GMT) con intervalos de confianza de un 95 % (95 % de CI) se calcularon por grupo, para SBA-MenC, anti-PSC, SBA-MenY, anti-PSY, anti-PRP, anti-Tétano, anti-PT, anti-FHA y anti-PRN antes de y un mes después de la vacunación; para anti-Difteria, anti-HBs, anti-Polio 1, anti-Polio 2 y anti-Polio 3 un mes después de la vacunación. La respuesta a la vacuna (aparición de anticuerpos en sujetos inicialmente seronegativos o al menos mantenimiento de concentraciones de anticuerpos sujetos inicialmente seropositivos) con un 95 % de Cl para anti-PT, anti-PRN y anti-FHA también se calcularon un mes después de la vacunación. Las curvas acumulativas inversas para cada anticuerpo en el Mes 3 también se presentan. Las diferencias entre los grupos Hib-MenCY y los grupos Hib- MenC, en comparación con el grupo de control de Menjugate™ se evaluaron de una manera exploratoria para cada
anticuerpo, excepto para SBA-MenY y anti-PSY, en términos de (1) la diferencia entre el grupo de Menjugate™ (menos) los grupos Hib-MenCY y Hib-MenC al porcentaje de sujetos por encima de los puntos de corte especificados o con una respuesta a la vacuna con su asiento está estandarizada en un 95 % de CI, (2) las proporciones de GMC o GMT del grupo de Menjugate™ con respecto a los grupos Hib-MenCY y Hib-MenC con su 95 % de CI. Las mismas comparaciones se llevaron a cabo para evaluar la diferencia entre cada par de formulaciones de Hib-MenCY para anticuerpos anti-PRP, SBA-MenC, anti-PSC, SBA-MenY, anti-PSY y anti-TT. Tasas de seroprotección/seropositividad y los GMC/T (cohorte de ATP para inmunogenicidad)
-
T l 7 BA -M n Tí l
-
T l 7 BA-M nY Tí l
-
continuación
-
Conclusión
Los conjugados de polisacáridos MenC y Y produjeron una buena respuesta inmunológica en todos los sujetos con un 100 % de los objetos produciendo respuestas de más de 0,3 pg/ml frente a MenC y MenY.
Ejemplo 6 - Ensayo clínico de fase II que compara tres formulaciones de MenACWY-TT con vacuna de conjugado de oligosacárido Meningitec MenC-CRM197
Este ejemplo informa un estudio de rango controlado de dosis controlada de fase II, abierto (parcialmente con ocultación), aleatorio, para evaluar la inmunogenicidad de tres formulaciones diferentes de vacuna de conjugado de toxoide del tétano (MenACWY-TT) de los serogrupos A, C, W-135, Y meningocócicos de GlaxoSmithKline Biological en comparación con una vacuna de conjugado de oligosacárido MenC-CRM197 (Meningitec) cuando se administra una dosis a niños con edades entre 12-14 meses.
El ensayo clínico fue un estudio multicéntrico, abierto (parcialmente con doble ocultación*), controlado en el que los sujetos idóneos de 12-14 meses de edad se clasificaron de forma aleatoria (1:1:1:1) a uno de cuatro grupos paralelos de 50 sujetos para recibir una dosis primaria única en el momento de la Visita 1 como sigue a continuación: Forma 1T: MenACWY-TT a una dosis de 2,5 pg de polisacárido MenA conjugado con toxoide del tétano (TT), 2,5 pg de polisacárido MenC conjugado con tT, 2,5 pg de polisacárido MenW conjugado con TT y 2,5 pg de polisacárido MenY conjugado con TT.
Forma 2T: MenACWY-TT a una dosis de 5 pg de polisacárido MenA conjugado con TT, 5 pg de polisacárido MenC conjugado con TT, 5 pg de polisacárido MenW conjugado con TT y 5 pg de polisacárido MenY conjugado con TT.
Forma 3T: MenACWY-TT a una dosis de 2,5 pg de polisacárido MenA conjugado con TT, 10 pg de polisacárido MenC conjugado con TT, 2,5 pg de polisacárido MenW conjugado con TT y 2,5 pg de polisacárido MenY conjugado con TT.
Ctrl T: 10 pg de oligosacárido MenC conjugado con 12,5-25 pg de CRM197 (Meningitec™).
* Las tres formulaciones de MenACWY-TT diferentes se administraron de una manera con doble ocultación. Programación/sitio de vacunación: Una sola dosis de vacuna se administra por vía intramuscular en el deltoides izquierdo en el momento de la maestra inicia visita 1 (Mes del Estudio 0) de acuerdo con la asignación aleatoria. Todas las vacunas candidatas se suministraron como un gránulo liofilizado en un vial de monodosis (0,5 ml después de su reconstitución con el diluyente suministrado de solución salina).
Inmunogenicidad: Medición de títulos/concentraciones de anticuerpos frente a componentes de antígeno de vacuna meningocócica en muestras de sangre obtenidas antes de la dosis de vacuna del estudio (Mes 0) y aproximadamente un mes después de la dosis de vacuna del estudio (Mes 1) en todos los sujetos. La determinación de los títulos de anticuerpo bactericida frente a los serogrupos A, C, W-135 y Y (SBA-MenA, SBA-MenC, SBA-MenW y SBA-MenY) de N. meningitidis mediante un ensayo bactericida (puntos de corte del ensayo: una dilución de 1:8 y
1:128) y medición de anticuerpos con ELISA frente a los serogrupos A, C, W-135 y Y (anti-PSA, anti-PSC, anti-PSW y anti-PSY, puntos de corte del ensayo > 0,3 |jg/ml y > 2 |jg/ml) de N. meningitidis, y toxoide del tétano (antitetánico, punto de corte del ensayo 0,1 lU/ml).
Resultados
La respuesta al anticuerpo en términos del porcentaje de individuos sensibles a SBA-MenA, SBA-MenC, SBA-MenW y SBA-MenY un mes después de la vacunación (el punto final primario) se muestra en la Tabla 8. Una respuesta se define como mayor o igual que un aumento de 4 veces para sujetos seropositivos o seroconversión para sujetos seronegativos antes de la vacunación.
T l : R l v n r ni r BA n m l v n in
La Tabla 9 muestran los números de sujetos que consiguen títulos de SBA superiores a los puntos de corte de 1:8 y 1:128 así como los GMT.
T l : T r iiv l MT r ni r BA n m l v n in
La vacunación con las formulaciones del conjugado de polisacárido ACWY-TT condujo a buenas respuestas de SBA frente a MenA, MenC, MenW y MenY con un 95-100 % de los sujetos con títulos superiores a 1:8. En particular, las formulaciones de 5/5/5/5 y 2,5/10/2,5/2,5 de los conjugados de polisacárido produjeron una respuesta más elevada frente a MenC que la vacuna Meningitic de oligosacárido en una proporción más elevada de sujetos con títulos superior a 1:128 y las lecturas de GMT.
T l 1 T r iivi l M r ni r ni li ri n m l v n i n
continuación
Las tres formulaciones de vacuna de conjugado de polisacárido ACWY-TT produjeron buenas respetas inmunológicas frente a MenA, MenC, MenW y MenY con entre un 93 % y un 100 % de los sujetos consiguiendo títulos superiores a 0,3 pg/ml. Las lecturas de GMC más elevada se consiguieron usando las poblaciones de 5/5/5/5 y 2/5/10/2,5/2,5 de la vacuna de conjugado de polisacárido ACWY-TT en comparación con Meningitec™.
Ejemplo 7 - comparación de la inmunogenicidad de conjugados de polisacárido MenY nativo y dimensionado
Los ratones (DBA/2 hembra de 6-8 semanas) recibieron dos inyecciones, con una separación de 2 semanas, de PSY-TT por vía subcutánea. Las muestras de sangre se extrajeron 14 días después de la segunda inyección con el fin de llevar a cabo un ELISA anti-PSY y SBA usando la cepa S1975 menY. Por inyección, los ratones recibieron 1 pg de PSY-TT (formulación sin ads. lio.).
Se usaron los conjugados que se describen en la tabla 11.
Tabla 11
Resultados
Los resultados (Figura 1) muestran una tendencia hacia una inmunogenicidad más elevada para conjugados preparados usando el PSY dimensionado. La Figura 1A muestra los resultados de GMC obtenidos en un ensayo ELISA para antisueros proporcionados frente a conjugados preparados a partir de MenY nativo (ENYTT012), MenY microfluidizado - 40 ciclos (ENYTT014) y MenY microfluidizado - 20 ciclos (ENYTT015 bis). Los GMC más elevados se obtuvieron cuando el MenY-TT se preparó a partir de MenY microfluidizado.
Se obtuvieron resultados similares cuando los antisueros se evaluaron con el ensayo SBA (Figura 1B). De nuevo los valores de GMT más elevado se consiguieron usando conjugados preparados a partir de MenY microfluidizado.
Claims (10)
1. Una composición inmunogénica que comprende polisacáridos capsulares de N. meningitidis de los serogrupos A, C, W135 e Y, en donde cada polisacárido capsular de N. meningitidis está conjugado con una proteína vehículo de toxoide tetánico (TT) para producir un conjugado de polisacárido capsular de N. meningitidis, en el que:
- el polisacárido capsular MenA presente en el conjugado de sacárido capsular MenA tiene un tamaño promedio de más de 60 kDa y es polisacárido capsular MenA natural o microfluidizado;
- el polisacárido capsular MenC presente en el conjugado de sacárido capsular MenC tiene un tamaño promedio de más de 150 kDa y es un polisacárido capsular MenC natural;
- el polisacárido capsular MenW presente en en conjugado de polisacárido capsular es un polisacárido capsular MenW dimensionado por microfluidización y tiene un tamaño promedio de 100-200 kDa, y
- el polisacárido capsular MenY presente en el conjugado de polisacárido capsular MenY es un polisacárido capsular MenY dimensionado por microfluidización y tiene un tamaño promedio de 100-200 kDa.
2. La composición inmunogénica de la reivindicación 1, en la que dicho polisacárido capsular MenA tiene un tamaño promedio de más de 75 kDa, 100 kDa o un tamaño promedio de entre 60-80 kDa.
3. La composición inmunogénica de la reivindicación 1 o 2, en la que dicho polisacárido capsular MenC tiene un tamaño promedio de entre 150-200 kDa, 160-200 kDa o 190-200 kDa.
4. La composición inmunogénica de una cualquiera de las reivindicaciones 1-3, en la que dicho polisacárido capsular MenY tiene un tamaño promedio de entre 120-140 kDa.
5. La composición inmunogénica de una cualquiera de las reivindicaciones 1-4 en la que dicho polisacárido capsular MenW tiene un tamaño promedio de entre 100-150 kDa, 140-180 kDa, 150-170 kDa o 110-140 kDa.
6. La composición inmunogénica de cualquier reivindicación 1-5 que comprende una preparación de vesícula de membrana externa o sacárido capsular del serogrupo B de N. meningitidis.
7. Una vacuna que comprende la composición inmunogénica de una cualquiera de las reivindicaciones 1-6 y un vehículo farmacéuticamente aceptable.
8. Un kit de vacuna para administración simultánea o secuencial que comprende dos composiciones inmunogénicas multivalentes para proporcionar protección en un hospedador frente a una enfermedad causada por Bordetella pertussis, Clostridium tetani, Corynebacterium diphtheriae, Haemophilus influenzae y Neisseria meningitidis, comprendiendo dicho kit un primer recipiente que comprende:
toxoide del tétano (TT),
toxoide de difteria (DT), y
componentes de células completas o acelulares de pertussis
y un segundo recipiente que comprende:
la composición inmunogénica de una cualquiera de las reivindicaciones 1-6.
9. Un proceso para preparar la vacuna de la reivindicación 8 que comprende la etapa de mezclar la composición inmunogénica de una cualquiera de las reivindicaciones 1-6 con un vehículo farmacéuticamente aceptable.
10. La composición inmunogénica de las reivindicaciones 1-6 para su uso en el tratamiento o prevención de una enfermedad causada por infección por Neisseria meningitidis.
Applications Claiming Priority (6)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| GBGB0513071.1A GB0513071D0 (en) | 2005-06-27 | 2005-06-27 | Immunogenic composition |
| GBGB0513069.5A GB0513069D0 (en) | 2005-06-27 | 2005-06-27 | Immunogenic composition |
| GB0515556A GB0515556D0 (en) | 2005-07-28 | 2005-07-28 | Immunogenic composition |
| GB0524204A GB0524204D0 (en) | 2005-11-28 | 2005-11-28 | Immunogenic composition |
| GB0526041A GB0526041D0 (en) | 2005-12-21 | 2005-12-21 | Immunogenic composition |
| GB0526040A GB0526040D0 (en) | 2005-12-21 | 2005-12-21 | Immunogenic composition |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2750243T3 true ES2750243T3 (es) | 2020-03-25 |
Family
ID=36716943
Family Applications (9)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES06754599.6T Active ES2377075T5 (es) | 2005-06-27 | 2006-06-23 | Composición inmunogénica |
| ES06754596T Active ES2340711T3 (es) | 2005-06-27 | 2006-06-23 | Composicion inmunogena. |
| ES10177832T Active ES2750243T3 (es) | 2005-06-27 | 2006-06-23 | Composición de vacuna que comprende polisacáridos capsulares naturales conjugados de N. Meningitidis |
| ES14198052T Active ES2747025T3 (es) | 2005-06-27 | 2006-06-23 | Composición inmunógena |
| ES06754582T Active ES2741529T3 (es) | 2005-06-27 | 2006-06-23 | Composición inmunogénica |
| ES10179820.5T Active ES2621780T3 (es) | 2005-06-27 | 2006-06-23 | Procedimiento de fabricación de vacunas |
| ES10158046.2T Active ES2662651T3 (es) | 2005-06-27 | 2006-06-23 | Composición inmunógena |
| ES06762248T Active ES2901378T3 (es) | 2005-06-27 | 2006-06-23 | Composición inmunogénica |
| ES15189397T Active ES2898451T3 (es) | 2005-06-27 | 2006-06-23 | Composición inmunogénica |
Family Applications Before (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES06754599.6T Active ES2377075T5 (es) | 2005-06-27 | 2006-06-23 | Composición inmunogénica |
| ES06754596T Active ES2340711T3 (es) | 2005-06-27 | 2006-06-23 | Composicion inmunogena. |
Family Applications After (6)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES14198052T Active ES2747025T3 (es) | 2005-06-27 | 2006-06-23 | Composición inmunógena |
| ES06754582T Active ES2741529T3 (es) | 2005-06-27 | 2006-06-23 | Composición inmunogénica |
| ES10179820.5T Active ES2621780T3 (es) | 2005-06-27 | 2006-06-23 | Procedimiento de fabricación de vacunas |
| ES10158046.2T Active ES2662651T3 (es) | 2005-06-27 | 2006-06-23 | Composición inmunógena |
| ES06762248T Active ES2901378T3 (es) | 2005-06-27 | 2006-06-23 | Composición inmunogénica |
| ES15189397T Active ES2898451T3 (es) | 2005-06-27 | 2006-06-23 | Composición inmunogénica |
Country Status (36)
| Country | Link |
|---|---|
| US (13) | US9486515B2 (es) |
| EP (11) | EP1896062B1 (es) |
| JP (9) | JP5280199B2 (es) |
| KR (7) | KR101532068B1 (es) |
| CN (3) | CN102218138A (es) |
| AP (1) | AP2436A (es) |
| AR (3) | AR053935A1 (es) |
| AT (3) | ATE536884T1 (es) |
| AU (7) | AU2006263963B2 (es) |
| BE (1) | BE2012C042I2 (es) |
| BR (5) | BRPI0612670B8 (es) |
| CA (5) | CA2612957C (es) |
| CY (5) | CY1109996T1 (es) |
| DE (1) | DE602006013313D1 (es) |
| DK (7) | DK2351578T3 (es) |
| EA (4) | EA012214B1 (es) |
| ES (9) | ES2377075T5 (es) |
| FR (1) | FR22C1008I2 (es) |
| HR (4) | HRP20100211T1 (es) |
| HU (7) | HUE047211T2 (es) |
| IL (8) | IL187924A (es) |
| LT (2) | LT2351578T (es) |
| LU (2) | LU92085I2 (es) |
| MA (4) | MA29603B1 (es) |
| MX (5) | MX2007016402A (es) |
| MY (3) | MY148110A (es) |
| NL (2) | NL300549I2 (es) |
| NO (4) | NO345422B1 (es) |
| NZ (6) | NZ564606A (es) |
| PE (6) | PE20110096A1 (es) |
| PL (8) | PL1896061T3 (es) |
| PT (8) | PT3009146T (es) |
| SI (8) | SI1896063T1 (es) |
| TW (5) | TWI407970B (es) |
| UA (2) | UA95237C2 (es) |
| WO (6) | WO2007000343A2 (es) |
Families Citing this family (104)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| OA12302A (en) * | 2000-06-29 | 2003-10-24 | Glaxosmithkline Biolog Sa | Multivalent vaccine composition. |
| MX339524B (es) | 2001-10-11 | 2016-05-30 | Wyeth Corp | Composiciones inmunogenicas novedosas para la prevencion y tratamiento de enfermedad meningococica. |
| DK1587537T3 (da) | 2003-01-30 | 2012-07-16 | Novartis Ag | Injicerbare vacciner mod multiple meningococ-serogrupper |
| GB0408977D0 (en) * | 2004-04-22 | 2004-05-26 | Chiron Srl | Immunising against meningococcal serogroup Y using proteins |
| GB0505518D0 (en) * | 2005-03-17 | 2005-04-27 | Chiron Srl | Combination vaccines with whole cell pertussis antigen |
| US7955605B2 (en) * | 2005-04-08 | 2011-06-07 | Wyeth Llc | Multivalent pneumococcal polysaccharide-protein conjugate composition |
| US9486515B2 (en) | 2005-06-27 | 2016-11-08 | Glaxosmithkline Biologicals S.A. | Immunogenic composition |
| CA2621023C (en) | 2005-09-01 | 2019-07-02 | Novartis Vaccines And Diagnostics Gmbh & Co. Kg | Multiple vaccination including serogroup c meningococcus |
| AU2012261764B2 (en) * | 2005-09-01 | 2016-09-08 | Novartis Vaccines And Diagnostics Gmbh & Co. Kg | Multiple vaccination including serogroup C meningococcus |
| CN103251940A (zh) | 2005-12-22 | 2013-08-21 | 葛兰素史密丝克莱恩生物有限公司 | 疫苗 |
| US10828361B2 (en) * | 2006-03-22 | 2020-11-10 | Glaxosmithkline Biologicals Sa | Regimens for immunisation with meningococcal conjugates |
| AU2007229449A1 (en) | 2006-03-22 | 2007-10-04 | Novartis Ag | Regimens for immunisation with meningococcal conjugates |
| GB0612854D0 (en) | 2006-06-28 | 2006-08-09 | Novartis Ag | Saccharide analysis |
| EP2491947A3 (en) | 2006-09-07 | 2012-10-17 | GlaxoSmithKline Biologicals S.A. | Vaccine |
| AR064642A1 (es) | 2006-12-22 | 2009-04-15 | Wyeth Corp | Polinucleotido vector que lo comprende celula recombinante que comprende el vector polipeptido , anticuerpo , composicion que comprende el polinucleotido , vector , celula recombinante polipeptido o anticuerpo , uso de la composicion y metodo para preparar la composicion misma y preparar una composi |
| GB0700135D0 (en) * | 2007-01-04 | 2007-02-14 | Glaxosmithkline Biolog Sa | Vaccine |
| GB0700136D0 (en) * | 2007-01-04 | 2007-02-14 | Glaxosmithkline Biolog Sa | Process for manufacturing vaccines |
| MX2009013949A (es) | 2007-06-26 | 2010-05-24 | Glaxosmithkline Biolog Sa | Vacuna que comprende conjugados de polisacárido capsular de streptococcus pneumoniae. |
| GB0713880D0 (en) | 2007-07-17 | 2007-08-29 | Novartis Ag | Conjugate purification |
| US20160228500A9 (en) * | 2007-07-23 | 2016-08-11 | Martina Ochs | Immunogenic Polypeptides and Monoclonal Antibodies |
| GB0714963D0 (en) | 2007-08-01 | 2007-09-12 | Novartis Ag | Compositions comprising antigens |
| BRPI0818545A2 (pt) | 2007-10-19 | 2017-07-04 | Novartis Ag | formulações de vacinais meningocócicas |
| CN102202689A (zh) * | 2008-08-28 | 2011-09-28 | 葛兰素史密丝克莱恩生物有限公司 | 疫苗 |
| US11065323B2 (en) | 2008-10-27 | 2021-07-20 | Glaxosmithkline Biologicals Sa | Purification method |
| GB0822633D0 (en) | 2008-12-11 | 2009-01-21 | Novartis Ag | Formulation |
| GB0822634D0 (en) | 2008-12-11 | 2009-01-21 | Novartis Ag | Meningitis vaccines |
| EP2367568A2 (en) | 2008-12-17 | 2011-09-28 | Novartis AG | Meningococcal vaccines including hemoglobin receptor |
| AU2010227220B2 (en) | 2009-03-24 | 2014-11-13 | Glaxosmithkline Biologicals S.A. | Combinations of meningococcal factor H binding protein and pneumococcal saccharide conjugates |
| CA2756522C (en) | 2009-03-24 | 2018-06-26 | Novartis Ag | Adjuvanting meningococcal factor h binding protein |
| JP5593626B2 (ja) * | 2009-03-31 | 2014-09-24 | 凸版印刷株式会社 | 計量スプーン |
| WO2010119343A2 (en) | 2009-04-14 | 2010-10-21 | Novartis Ag | Compositions for immunising against staphylococcus aureus |
| BRPI1014494A2 (pt) * | 2009-04-30 | 2016-08-02 | Coley Pharm Group Inc | vacina pneumocócica e usos da mesma |
| GB0910046D0 (en) * | 2009-06-10 | 2009-07-22 | Glaxosmithkline Biolog Sa | Novel compositions |
| TWI505834B (zh) * | 2009-06-22 | 2015-11-01 | Wyeth Llc | 組合物及製備金黃色葡萄球菌血清型5及8莢膜多醣結合物之免疫原性組合物之方法 |
| BRPI1015567A2 (pt) | 2009-06-22 | 2021-08-31 | Wyeth Llc | Composições imunogênicas de antígenos de staphylococcus aureus |
| SG178954A1 (en) | 2009-09-02 | 2012-04-27 | Novartis Ag | Immunogenic compositions including tlr activity modulators |
| CA2773637A1 (en) | 2009-09-10 | 2011-03-17 | Novartis Ag | Combination vaccines against respiratory tract diseases |
| MX345967B (es) * | 2009-10-30 | 2017-02-28 | Novartis Ag | Purificacion de sacaridos capsulares de staphylococcus aureus tipo 5 y tipo 8. |
| GB0919690D0 (en) | 2009-11-10 | 2009-12-23 | Guy S And St Thomas S Nhs Foun | compositions for immunising against staphylococcus aureus |
| JP5781542B2 (ja) | 2009-12-30 | 2015-09-24 | ノバルティス アーゲー | E.coliキャリアタンパク質に結合体化した多糖免疫原 |
| TW201136603A (en) * | 2010-02-09 | 2011-11-01 | Merck Sharp & Amp Dohme Corp | 15-valent pneumococcal polysaccharide-protein conjugate vaccine composition |
| GB201003333D0 (en) | 2010-02-26 | 2010-04-14 | Novartis Ag | Immunogenic proteins and compositions |
| GB201003922D0 (en) * | 2010-03-09 | 2010-04-21 | Glaxosmithkline Biolog Sa | Conjugation process |
| GB201003924D0 (en) * | 2010-03-09 | 2010-04-21 | Glaxosmithkline Biolog Sa | Immunogenic composition |
| GB201005625D0 (en) | 2010-04-01 | 2010-05-19 | Novartis Ag | Immunogenic proteins and compositions |
| US10478483B2 (en) | 2010-06-25 | 2019-11-19 | Glaxosmithkline Biologicals Sa | Combinations of meningococcal factor H binding proteins |
| PL3831406T3 (pl) | 2010-08-23 | 2024-09-09 | Wyeth Llc | Stabilne preparaty antygenów rLP2086 Neisseria meningitidis |
| CN103313725B (zh) | 2010-09-01 | 2016-06-29 | 诺华有限公司 | 免疫增强剂吸附不溶性金属离子 |
| ES2759484T3 (es) | 2010-09-10 | 2020-05-11 | Glaxosmithkline Biologicals Sa | Meningococo que sobreexpresa NadA y/o NHBA y vesículas de la membrana externa derivadas del mismo |
| RU2546873C2 (ru) | 2010-09-10 | 2015-04-10 | УАЙТ ЭлЭлСи | Нелипидизированные варианты антигенов neisseria meningitidis orf2086 |
| WO2012072769A1 (en) | 2010-12-01 | 2012-06-07 | Novartis Ag | Pneumococcal rrgb epitopes and clade combinations |
| KR20140026392A (ko) | 2011-03-02 | 2014-03-05 | 노파르티스 아게 | 저용량의 항원 및/또는 보조제를 갖는 조합 백신 |
| GB201114923D0 (en) | 2011-08-30 | 2011-10-12 | Novartis Ag | Immunogenic proteins and compositions |
| US9493517B2 (en) | 2011-11-07 | 2016-11-15 | Glaxosmithkline Biologicals Sa | Conjugates comprising an antigen and a carrier molecule |
| JP2013112653A (ja) * | 2011-11-30 | 2013-06-10 | Jnc Corp | 新規重合体およびその製造方法 |
| GB201121301D0 (en) | 2011-12-12 | 2012-01-25 | Novartis Ag | Method |
| CA2862247A1 (en) | 2011-12-29 | 2013-07-04 | Novartis Ag | Adjuvanted combinations of meningococcal factor h binding proteins |
| HUE040914T4 (hu) * | 2012-01-30 | 2019-05-28 | Serum Institute Of India Pvt Ltd | Immunogén készítmény |
| BR112014019166A2 (pt) | 2012-02-02 | 2017-07-04 | Novartis Ag | promotores para expressão aumentada de proteína em meningococos |
| CN102569723A (zh) * | 2012-02-13 | 2012-07-11 | 华为技术有限公司 | 锂离子电池正极材料及其制备方法、正极及锂离子电池 |
| EP2822586A1 (en) | 2012-03-07 | 2015-01-14 | Novartis AG | Adjuvanted formulations of streptococcus pneumoniae antigens |
| AU2013229432A1 (en) | 2012-03-08 | 2014-10-16 | Novartis Ag | Adjuvanted formulations of booster vaccines |
| CN104159603A (zh) | 2012-03-08 | 2014-11-19 | 诺华股份有限公司 | 带有tlr4激动剂的联合疫苗 |
| SA115360586B1 (ar) | 2012-03-09 | 2017-04-12 | فايزر انك | تركيبات لعلاج الالتهاب السحائي البكتيري وطرق لتحضيرها |
| MY167723A (en) | 2012-03-09 | 2018-09-21 | Pfizer | Neisseria meningitidis compositions and methods thereof |
| KR102057217B1 (ko) * | 2012-06-20 | 2020-01-22 | 에스케이바이오사이언스 주식회사 | 다가 폐렴구균 다당류-단백질 접합체 조성물 |
| BR112015005056A2 (pt) | 2012-09-06 | 2017-11-21 | Novartis Ag | vacinas de combinação com sorogrupo b meningococcus e d/t/p |
| ITMI20121597A1 (it) * | 2012-09-25 | 2014-03-26 | Beta Pharma S A | Coniugato tra frammento di parete cellulare batterica ed un veicolo mucopolisaccaridico e suoi usi in ambito medico |
| CA2885625A1 (en) | 2012-10-02 | 2014-04-10 | Glaxosmithkline Biologicals S.A. | Nonlinear saccharide conjugates |
| SMT201800011T1 (it) | 2012-11-30 | 2018-05-02 | Glaxosmithkline Biologicals Sa | Antigeni e combinazioni di antigeni di pseudomonas |
| KR20140075196A (ko) | 2012-12-11 | 2014-06-19 | 에스케이케미칼주식회사 | 다가 폐렴구균 다당류-단백질 접합체 조성물 |
| BR112015014250A2 (pt) | 2012-12-18 | 2017-07-11 | Glaxosmithkline Biologicals Sa | método para imunizar um bebê, vacina de combinação e, kit |
| TR201807340T4 (tr) | 2013-02-01 | 2018-06-21 | Glaxosmithkline Biologicals Sa | Çan benzeri reseptör agonistleri içeren immünolojik kompozisyonların intradermal yoldan verilmesi. |
| US9802987B2 (en) | 2013-03-08 | 2017-10-31 | Pfizer Inc. | Immunogenic fusion polypeptides |
| AU2014234408B2 (en) | 2013-03-18 | 2017-04-20 | Glaxosmithkline Biologicals S.A. | Method of treatment |
| EP4098276A1 (en) | 2013-09-08 | 2022-12-07 | Pfizer Inc. | Neisseria meningitidis compositions and methods thereof |
| IN2014DE02450A (es) | 2013-09-25 | 2015-06-26 | Suzuki Motor Corp | |
| RU2535122C1 (ru) * | 2013-11-06 | 2014-12-10 | Федеральное казенное учреждение здравоохранения "Российский научно-исследовательский противочумный институт "Микроб" Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека ("РосНИПЧИ "Микроб") | Способ получения холерогена-анатоксина |
| US11160855B2 (en) | 2014-01-21 | 2021-11-02 | Pfizer Inc. | Immunogenic compositions comprising conjugated capsular saccharide antigens and uses thereof |
| CA3206112A1 (en) * | 2014-01-21 | 2015-07-30 | Pfizer Inc. | Immunogenic compositions comprising conjugated capsular saccharide antigens and uses thereof |
| EP2921856B1 (en) | 2014-03-18 | 2016-09-14 | Serum Institute Of India Private Limited | A quantitative assay for 4-pyrrolidinopyridine (4-ppy) in polysaccharide-protein conjugate vaccines |
| EP3131576B1 (en) | 2014-04-17 | 2021-06-30 | Medizinische Hochschule Hannover | Means and methods for producing neisseria meningitidis capsular polysaccharides of low dispersity |
| US10888611B2 (en) | 2015-02-19 | 2021-01-12 | Pfizer Inc. | Neisseria meningitidis compositions and methods thereof |
| EP3325008B1 (en) * | 2015-07-21 | 2025-09-10 | Pfizer Inc. | Immunogenic compositions comprising conjugated capsular saccharide antigens, kits comprising the same and uses thereof |
| US20170333546A1 (en) * | 2015-12-08 | 2017-11-23 | Jl Medical Corporation | Method for Producing and Vaccine Composition of Neisseria Meningitidis Serogroups A, C, Y, and W-135 Oligosaccharides Conjugated to Glycan-Free Carrier Protein |
| WO2017158480A1 (en) * | 2016-03-15 | 2017-09-21 | Msd Wellcome Trust Hilleman Laboratories Pvt. Ltd. | Novel polysaccharide-protein conjugates and process to obtain thereof |
| CA3035320A1 (en) | 2016-09-02 | 2018-03-08 | Glaxosmithkline Biologicals Sa | Vaccines for neisseria gonorrhoeae |
| AU2017321863B2 (en) * | 2016-09-02 | 2024-07-11 | Sanofi Vaccines US Inc. | Neisseria meningitidis vaccine |
| IL308091B1 (en) | 2016-09-13 | 2026-01-01 | Allergan Inc | Protein-free stabilized Clostridium toxin preparations |
| WO2018074296A1 (ja) * | 2016-10-20 | 2018-04-26 | 一般財団法人化学及血清療法研究所 | 低分子化PRPを用いたHibコンジュゲートワクチンの製造方法 |
| US11951165B2 (en) | 2016-12-30 | 2024-04-09 | Vaxcyte, Inc. | Conjugated vaccine carrier proteins |
| DK3562503T3 (da) | 2016-12-30 | 2025-05-26 | Vaxcyte Inc | Polypeptid-antigen-konjugater med ikke-naturlige aminosyrer |
| PE20191107A1 (es) | 2017-01-31 | 2019-08-26 | Pfizer | Composiciones de neisseria meningitidis y metodos respectivos |
| US11389540B2 (en) | 2017-09-07 | 2022-07-19 | Merck Sharp & Dohme Llc | Pneumococcal polysaccharides and their use in immunogenic polysaccharide-carrier protein conjugates |
| US11524076B2 (en) | 2017-09-07 | 2022-12-13 | Merck Sharp & Dohme Llc | Pneumococcal polysaccharides and their use in immunogenic polysaccharide-carrier protein conjugates |
| US20200353064A1 (en) * | 2018-01-29 | 2020-11-12 | Msd Wellcome Trust Hilleman Laboratories Pvt. Ltd. | Novel meningococcal vaccine composition and process thereof |
| WO2019198096A1 (en) * | 2018-04-11 | 2019-10-17 | Msd Wellcome Trust Hilleman Laboratories Pvt. Ltd. | Tetravalent meningococcal vaccine composition and process to prepare thereof |
| JOP20200214A1 (ar) | 2019-09-03 | 2021-03-03 | Serum Institute Of India Pvt Ltd | تركيبات مولدة للمناعة ضد الأمراض المعوية وطرق لتحضيرها |
| WO2021059181A1 (en) | 2019-09-27 | 2021-04-01 | Pfizer Inc. | Neisseria meningitidis compositions and methods thereof |
| WO2021099982A1 (en) | 2019-11-22 | 2021-05-27 | Glaxosmithkline Biologicals Sa | Dosage and administration of a bacterial saccharide glycoconjugate vaccine |
| US20240000958A1 (en) | 2020-11-13 | 2024-01-04 | Glaxosmithkline Biologicals Sa | Novel carriers and conjugation methods |
| RU2770877C1 (ru) * | 2021-04-08 | 2022-04-22 | Федеральное бюджетное учреждение науки "Ростовский научно-исследовательский институт микробиологии и паразитологии" | Способ получения антигенной конъюгированной субстанции гемофильного типа b микроба для создания вакцинных препаратов |
| GB202215414D0 (en) | 2022-10-18 | 2022-11-30 | Glaxosmithkline Biologicals Sa | Vaccine |
| WO2025021704A1 (en) | 2023-07-21 | 2025-01-30 | Glaxosmithkline Biologicals Sa | Vaccine |
Family Cites Families (184)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB513069A (en) | 1937-04-24 | 1939-10-03 | Linde Air Prod Co | Improvements in method of and apparatus for the treatment of metallic bodies by oxidising gas |
| GB505518A (en) | 1938-02-03 | 1939-05-12 | Daniel Morgan Skeins | Improvements in or relating to envelopes |
| US4057685A (en) | 1972-02-02 | 1977-11-08 | Abbott Laboratories | Chemically modified endotoxin immunizing agent |
| US4123520A (en) * | 1977-08-01 | 1978-10-31 | Merck & Co., Inc. | Method for preparing high molecular weight meningococcal Group C vaccine |
| DE2748132A1 (de) * | 1977-10-27 | 1979-05-03 | Behringwerke Ag | Stabilisator fuer polysaccharid |
| US4235994A (en) * | 1978-06-26 | 1980-11-25 | Merck & Co., Inc. | High molecular weight meningococcal group C vaccine and method for preparation thereof |
| US4235877A (en) | 1979-06-27 | 1980-11-25 | Merck & Co., Inc. | Liposome particle containing viral or bacterial antigenic subunit |
| EP0027888B1 (en) * | 1979-09-21 | 1986-04-16 | Hitachi, Ltd. | Semiconductor switch |
| DE3040825A1 (de) * | 1980-10-30 | 1982-09-09 | Dr. Karl Thomae Gmbh, 7950 Biberach | Neues tridekapeptid, verfahren zu seiner herstellung und verwendung |
| US4673574A (en) | 1981-08-31 | 1987-06-16 | Anderson Porter W | Immunogenic conjugates |
| US4459286A (en) | 1983-01-31 | 1984-07-10 | Merck & Co., Inc. | Coupled H. influenzae type B vaccine |
| HU193083B (en) * | 1984-02-22 | 1987-08-28 | Sandoz Ag | Process for preparing diazepinoindole derivatives further pharmaceutical compositions containing such compounds |
| US4695624A (en) | 1984-05-10 | 1987-09-22 | Merck & Co., Inc. | Covalently-modified polyanionic bacterial polysaccharides, stable covalent conjugates of such polysaccharides and immunogenic proteins with bigeneric spacers, and methods of preparing such polysaccharides and conjugates and of confirming covalency |
| US4808700A (en) * | 1984-07-09 | 1989-02-28 | Praxis Biologics, Inc. | Immunogenic conjugates of non-toxic E. coli LT-B enterotoxin subunit and capsular polymers |
| US4709017A (en) * | 1985-06-07 | 1987-11-24 | President And Fellows Of Harvard College | Modified toxic vaccines |
| IT1187753B (it) | 1985-07-05 | 1987-12-23 | Sclavo Spa | Coniugati glicoproteici ad attivita' immunogenica trivalente |
| DE3526940A1 (de) | 1985-07-27 | 1987-02-12 | Siegfried Fricker | Anker zum einbetonieren in schwere lasten |
| IL78929A0 (en) | 1985-07-29 | 1986-09-30 | Abbott Lab | Microemulsion compositions for parenteral administration |
| US4727136A (en) * | 1985-10-01 | 1988-02-23 | Canadian Patents And Development Ltd. | Modified meningococcal group B polysaccharide for conjugate vaccine |
| US4950740A (en) | 1987-03-17 | 1990-08-21 | Cetus Corporation | Recombinant diphtheria vaccines |
| JPH01125328A (ja) | 1987-07-30 | 1989-05-17 | Centro Natl De Biopreparados | 髄膜炎菌ワクチン |
| US5180815A (en) * | 1988-04-13 | 1993-01-19 | Fuji Photo Film Co., Ltd. | Modified protein for carrying hapten |
| US5115924A (en) | 1988-05-31 | 1992-05-26 | Beatrice Konig-Haug | Shelf system |
| DE3841091A1 (de) | 1988-12-07 | 1990-06-13 | Behringwerke Ag | Synthetische antigene, verfahren zu ihrer herstellung und ihre verwendung |
| EP0378881B1 (en) | 1989-01-17 | 1993-06-09 | ENIRICERCHE S.p.A. | Synthetic peptides and their use as universal carriers for the preparation of immunogenic conjugates suitable for the development of synthetic vaccines |
| FI920131A0 (fi) | 1989-07-14 | 1992-01-13 | Praxis Biolog Inc | Cytokin- och hormonbaerare foer konjugatvaccin. |
| IT1237764B (it) | 1989-11-10 | 1993-06-17 | Eniricerche Spa | Peptidi sintetici utili come carriers universali per la preparazione di coniugati immunogenici e loro impiego per lo sviluppo di vaccini sintetici. |
| WO1991008772A1 (en) | 1989-12-14 | 1991-06-27 | National Research Council Of Canada | Improved meningococcal polysaccharide conjugate vaccine |
| SE466259B (sv) | 1990-05-31 | 1992-01-20 | Arne Forsgren | Protein d - ett igd-bindande protein fraan haemophilus influenzae, samt anvaendning av detta foer analys, vacciner och uppreningsaendamaal |
| DE69113564T2 (de) | 1990-08-13 | 1996-05-30 | American Cyanamid Co | Faser-Hemagglutinin von Bordetella pertussis als Träger für konjugierten Impfstoff. |
| US5153312A (en) | 1990-09-28 | 1992-10-06 | American Cyanamid Company | Oligosaccharide conjugate vaccines |
| CA2059693C (en) | 1991-01-28 | 2003-08-19 | Peter J. Kniskern | Polysaccharide antigens from streptococcus pneumoniae |
| CA2059692C (en) | 1991-01-28 | 2004-11-16 | Peter J. Kniskern | Pneumoccoccal polysaccharide conjugate vaccine |
| GB2264352A (en) | 1992-01-31 | 1993-08-25 | Richards Eng Ltd | Incineration apparatus |
| WO1993015760A1 (en) | 1992-02-11 | 1993-08-19 | U.S. Government, As Represented By The Secretary Of The Army | Dual carrier immunogenic construct |
| IT1262896B (it) | 1992-03-06 | 1996-07-22 | Composti coniugati formati da proteine heat shock (hsp) e oligo-poli- saccaridi, loro uso per la produzione di vaccini. | |
| ES2130265T3 (es) | 1992-05-06 | 1999-07-01 | Harvard College | Region de union al receptor de la toxina difterica. |
| JP3626996B2 (ja) | 1992-05-23 | 2005-03-09 | グラクソスミスクライン・バイオロジカルス・ソシエテ・アノニム | B型肝炎表面抗原および他の抗原からなる複合ワクチン |
| IL102687A (en) | 1992-07-30 | 1997-06-10 | Yeda Res & Dev | Conjugates of poorly immunogenic antigens and synthetic pepide carriers and vaccines comprising them |
| SG47725A1 (en) | 1992-10-27 | 1998-04-17 | American Cyanamid Co | Combination pediatric vaccine with enhanced immunogenicity of each vaccine component |
| DE69317556T2 (de) | 1992-12-14 | 1998-07-09 | I/O Exploration Products (Usa), Inc., Stafford, Tex. | Hydraulischer seismischer aktuator |
| US5849301A (en) * | 1993-09-22 | 1998-12-15 | Henry M. Jackson Foundation For The Advancement Of Military Medicine | Producing immunogenic constructs using soluable carbohydrates activated via organic cyanylating reagents |
| DE69433341T2 (de) | 1993-09-22 | 2004-04-15 | Henry M. Jackson Foundation For The Advancement Of Military Medicine | Verfahren zur aktivierung von löslichem kohlenhydraten durch verwendung von neuen cyanylierungsreagenzien, zur herstellung von immunogenischen konstrukten |
| DE4416166C2 (de) * | 1994-05-06 | 1997-11-20 | Immuno Ag | Stabiles Präparat zur Behandlung von Blutgerinnungsstörungen |
| US5869058A (en) | 1994-05-25 | 1999-02-09 | Yeda Research And Development Co. Ltd. | Peptides used as carriers in immunogenic constructs suitable for development of synthetic vaccines |
| US5917017A (en) | 1994-06-08 | 1999-06-29 | President And Fellows Of Harvard College | Diphtheria toxin vaccines bearing a mutated R domain |
| US6455673B1 (en) | 1994-06-08 | 2002-09-24 | President And Fellows Of Harvard College | Multi-mutant diphtheria toxin vaccines |
| GB9422096D0 (en) * | 1994-11-02 | 1994-12-21 | Biocine Spa | Combined meningitis vaccine |
| ATE241384T1 (de) | 1995-03-22 | 2003-06-15 | Jackson H M Found Military Med | Herstellung von immunogenen konstrukten unter verwendung von löslichen kohlehydraten, die durch organische cyanylierungs-reagenzien aktiviert wurden |
| DE69615362T3 (de) | 1995-06-07 | 2006-07-20 | Smithkline Beecham Biologicals S.A. | Impfstoff mit einem polysaccharidantigen-trägerprotein-konjugat und einem trägerprotein |
| IL122588A (en) | 1995-06-23 | 2001-12-23 | Smithkline Beecham Biolog | A combination vaccine containing a polysaccharide conjugated antigen attached to a phosphate aluminum and one or more additional antibodies |
| SE9601158D0 (sv) | 1996-03-26 | 1996-03-26 | Stefan Svenson | Method of producing immunogenic products and vaccines |
| EP1271490B1 (en) | 1996-10-23 | 2011-12-21 | Panasonic Corporation | Optical disk |
| PT942983E (pt) | 1996-10-31 | 2007-02-28 | Human Genome Sciences Inc | Antigénios e vacinas de streptococcus pneumoniae |
| WO1998026799A1 (en) | 1996-12-18 | 1998-06-25 | The Government Of The United States Of America, Represented By The Secretary, Department Of Health And Human Services | Conjugate vaccine for salmonella paratyphi a |
| US6299881B1 (en) | 1997-03-24 | 2001-10-09 | Henry M. Jackson Foundation For The Advancement Of Military Medicine | Uronium salts for activating hydroxyls, carboxyls, and polysaccharides, and conjugate vaccines, immunogens, and other useful immunological reagents produced using uronium salts |
| FR2763244B1 (fr) | 1997-05-14 | 2003-08-01 | Pasteur Merieux Serums Vacc | Composition vaccinale multivalente a porteur mixte |
| GB9713156D0 (en) | 1997-06-20 | 1997-08-27 | Microbiological Res Authority | Vaccines |
| GB9717953D0 (en) | 1997-08-22 | 1997-10-29 | Smithkline Beecham Biolog | Vaccine |
| AU4707097A (en) | 1997-09-15 | 1999-04-05 | Pasteur Merieux Serums Et Vaccins | Multivalent vaccines |
| WO1999013905A1 (en) | 1997-09-18 | 1999-03-25 | The Trustees Of The University Of Pennsylvania | Receptor-binding pocket mutants of influenza a virus hemagglutinin for use in targeted gene delivery |
| US5965714A (en) | 1997-10-02 | 1999-10-12 | Connaught Laboratories, Inc. | Method for the covalent attachment of polysaccharides to protein molecules |
| US7018637B2 (en) | 1998-02-23 | 2006-03-28 | Aventis Pasteur, Inc | Multi-oligosaccharide glycoconjugate bacterial meningitis vaccines |
| CA2264970A1 (en) | 1998-03-10 | 1999-09-10 | American Cyanamid Company | Antigenic conjugates of conserved lipolysaccharides of gram negative bacteria |
| GB9806456D0 (en) | 1998-03-25 | 1998-05-27 | Smithkline Beecham Biolog | Vaccine composition |
| GB9808932D0 (en) * | 1998-04-27 | 1998-06-24 | Chiron Spa | Polyepitope carrier protein |
| EP1073667A2 (en) * | 1998-04-28 | 2001-02-07 | Galenica Pharmaceuticals, Inc. | Polysaccharide-antigen conjugates |
| NZ509986A (en) | 1998-08-19 | 2003-10-31 | Baxter Healthcare S | Immunogenic beta-propionamido-linked polysaccharide and oligosaccharide protein conjugates as vaccines |
| AU1626199A (en) † | 1998-12-04 | 2000-06-26 | Government Of The United States Of America, As Represented By The Secretary Of The Department Of Health And Human Services, The | A vi-repa conjugate vaccine for immunization against salmonella typhi |
| DK1140157T3 (da) | 1998-12-21 | 2009-06-08 | Medimmune Inc | Streptococcus pneumoniae-proteiner og immunogene fragmenter til vacciner |
| US6146902A (en) | 1998-12-29 | 2000-11-14 | Aventis Pasteur, Inc. | Purification of polysaccharide-protein conjugate vaccines by ultrafiltration with ammonium sulfate solutions |
| CA2363141C (en) | 1999-02-26 | 2010-04-06 | Novartis Vaccines And Diagnostics, Inc. | Microemulsions with adsorbed macromolecules and microparticles |
| KR100642044B1 (ko) | 1999-03-19 | 2006-11-10 | 글락소스미스클라인 바이오로지칼즈 에스.에이. | 백신 |
| EP1165796A2 (en) | 1999-04-09 | 2002-01-02 | Techlab, Inc. | Recombinant clostridium toxin a protein carrier for polysaccharide conjugate vaccines |
| JP4660043B2 (ja) | 1999-06-25 | 2011-03-30 | ワイス・ホールディングズ・コーポレイション | グラム陰性細菌のペプチドグリカン結合リポタンパク質の脂質化された形態の製造 |
| GB9918319D0 (en) | 1999-08-03 | 1999-10-06 | Smithkline Beecham Biolog | Vaccine composition |
| GB9925559D0 (en) | 1999-10-28 | 1999-12-29 | Smithkline Beecham Biolog | Novel method |
| ES2307553T3 (es) | 1999-12-02 | 2008-12-01 | Novartis Vaccines And Diagnostics, Inc. | Composiciones y procedimientos para estabilizar moleculas biologicas tras liofilizacion. |
| FR2806304B1 (fr) | 2000-03-17 | 2002-05-10 | Aventis Pasteur | Conjugues polysaccharidiques du pneumocoque a usage vaccinal contre le tetanos et la diphterie |
| GB0007432D0 (en) | 2000-03-27 | 2000-05-17 | Microbiological Res Authority | Proteins for use as carriers in conjugate vaccines |
| OA12302A (en) | 2000-06-29 | 2003-10-24 | Glaxosmithkline Biolog Sa | Multivalent vaccine composition. |
| GB0108364D0 (en) | 2001-04-03 | 2001-05-23 | Glaxosmithkline Biolog Sa | Vaccine composition |
| JP5511117B2 (ja) * | 2000-07-27 | 2014-06-04 | チルドレンズ ホスピタル アンド リサーチ センター アット オークランド | 髄膜炎菌に起因する疾患に対する広域防御のためのワクチン |
| GB0103170D0 (en) * | 2001-02-08 | 2001-03-28 | Smithkline Beecham Biolog | Vaccine composition |
| US7939087B2 (en) * | 2000-10-27 | 2011-05-10 | Novartis Vaccines And Diagnostics, Inc. | Nucleic acids and proteins from Streptococcus groups A & B |
| EP2957300B1 (en) | 2001-01-23 | 2021-07-14 | Sanofi Pasteur Inc. | Multivalent meningococcal polysaccharide-protein conjugate vaccine |
| GB0107661D0 (en) * | 2001-03-27 | 2001-05-16 | Chiron Spa | Staphylococcus aureus |
| GB0107658D0 (en) * | 2001-03-27 | 2001-05-16 | Chiron Spa | Streptococcus pneumoniae |
| AU2002309706A1 (en) | 2001-05-11 | 2002-11-25 | Aventis Pasteur, Inc. | Novel meningitis conjugate vaccine |
| US6615062B2 (en) | 2001-05-31 | 2003-09-02 | Infraredx, Inc. | Referencing optical catheters |
| GB0115176D0 (en) * | 2001-06-20 | 2001-08-15 | Chiron Spa | Capular polysaccharide solubilisation and combination vaccines |
| GB0118249D0 (en) * | 2001-07-26 | 2001-09-19 | Chiron Spa | Histidine vaccines |
| AR045702A1 (es) * | 2001-10-03 | 2005-11-09 | Chiron Corp | Composiciones de adyuvantes. |
| MX339524B (es) | 2001-10-11 | 2016-05-30 | Wyeth Corp | Composiciones inmunogenicas novedosas para la prevencion y tratamiento de enfermedad meningococica. |
| CU23031A1 (es) * | 2002-01-24 | 2005-02-23 | Ct Ingenieria Genetica Biotech | Antigeno de superficie del virus de la hepatitis b como inmunopotenciador mucosal, formulaciones resultantes |
| US7615229B2 (en) | 2002-03-15 | 2009-11-10 | Wyeth Holdings Corporation | Mutants of the P4 protein of nontypable Haemophilus influenzae with reduced enzymatic activity |
| WO2003080678A1 (en) * | 2002-03-26 | 2003-10-02 | Chiron Srl | Modified saccharides having improved stability in water |
| GB0210128D0 (en) * | 2002-05-02 | 2002-06-12 | Chiron Spa | Nucleic acids and proteins from streptococcus groups A & B |
| DE60328481D1 (de) | 2002-05-14 | 2009-09-03 | Novartis Vaccines & Diagnostic | Schleimhautapplizierter impfstoff, der das adjuvanz chitosan und menigokokkenantigene enthält |
| MXPA04011248A (es) | 2002-05-14 | 2005-02-17 | Chiron Srl | Vacunas mucosales en combinacion para la meningitis bacteriana. |
| GB0302218D0 (en) * | 2003-01-30 | 2003-03-05 | Chiron Sri | Vaccine formulation & Mucosal delivery |
| GB0211118D0 (en) * | 2002-05-15 | 2002-06-26 | Polonelli Luciano | Vaccines |
| AU2003257003A1 (en) | 2002-07-30 | 2004-02-16 | Baxter Healthcare S.A. | Chimeric multivalent polysaccharide conjugate vaccines |
| DE20321889U1 (de) | 2002-08-02 | 2012-03-12 | Glaxosmithkline Biologicals S.A. | Impfstoffzusammensetzung |
| GB0220199D0 (en) * | 2002-08-30 | 2002-10-09 | Univ Utrecht | Mutant protein and refolding method |
| GB0220194D0 (en) | 2002-08-30 | 2002-10-09 | Chiron Spa | Improved vesicles |
| DK2353608T3 (da) * | 2002-10-11 | 2020-02-10 | Novartis Vaccines And Diagnostics S R L | Polypeptid-vacciner til bred beskyttelse mod hypervirulente meningokok-linjer |
| CN1401328A (zh) | 2002-10-18 | 2003-03-12 | 北京绿竹生物技术有限责任公司 | 流行性脑脊髓膜炎多糖-蛋白结合疫苗 |
| DK1556477T3 (en) * | 2002-11-01 | 2017-10-23 | Glaxosmithkline Biologicals Sa | Process for drying |
| GB0227346D0 (en) * | 2002-11-22 | 2002-12-31 | Chiron Spa | 741 |
| CN1168501C (zh) | 2002-12-27 | 2004-09-29 | 北京绿竹生物技术有限责任公司 | 一种多糖-蛋白结合疫苗 |
| DK1587537T3 (da) * | 2003-01-30 | 2012-07-16 | Novartis Ag | Injicerbare vacciner mod multiple meningococ-serogrupper |
| PT1601689E (pt) * | 2003-03-13 | 2008-01-04 | Glaxosmithkline Biolog Sa | Processo de purificação para citolisina bacteriana |
| US20060251675A1 (en) | 2003-03-17 | 2006-11-09 | Michael Hagen | Mutant cholera holotoxin as an adjuvant and an antigen carrier protein |
| JP2006528936A (ja) * | 2003-05-07 | 2006-12-28 | アヴェンティス パストゥール インコーポレイテッド | 多価髄膜炎菌誘導体化多糖−タンパク質複合体およびワクチン |
| CA2528007C (en) | 2003-06-02 | 2012-03-27 | Chiron Corporation | Immunogenic compositions based on microparticles comprising adsorbed toxoid and a polysaccharide-containing antigen |
| GB0313916D0 (en) | 2003-06-16 | 2003-07-23 | Glaxosmithkline Biolog Sa | Vaccine composition |
| JP2007516181A (ja) | 2003-06-23 | 2007-06-21 | アヴェンティス パストゥール インコーポレイテッド | 髄膜炎菌血清群aおよびcに対する免疫方法 |
| KR101034055B1 (ko) | 2003-07-18 | 2011-05-12 | 엘지이노텍 주식회사 | 발광 다이오드 및 그 제조방법 |
| AU2004281630A1 (en) * | 2003-08-06 | 2005-04-28 | Bio-Manguinhos/Fiocruz | Process for preparing polysaccharide-protein conjugate vaccines |
| US8048432B2 (en) * | 2003-08-06 | 2011-11-01 | The United States Of America As Represented By The Secretary Of The Department Of Health And Human Services | Polysaccharide-protein conjugate vaccines |
| JP2007502980A (ja) * | 2003-08-21 | 2007-02-15 | アプレラ コーポレイション | Maldi質量分析法のためのマトリックス干渉の軽減 |
| ATE474595T1 (de) * | 2003-10-02 | 2010-08-15 | Glaxosmithkline Biolog Sa | B. pertussis antigene und ihre verwendung bei der vakzinierung |
| SI1670506T1 (sl) * | 2003-10-02 | 2013-03-29 | Novartis Ag | Tekoča cepiva proti multiplim meningokoknim seroskupinam |
| JP5173194B2 (ja) * | 2003-12-23 | 2013-03-27 | グラクソスミスクライン バイオロジカルズ ソシエテ アノニム | ワクチン |
| GB0405787D0 (en) | 2004-03-15 | 2004-04-21 | Chiron Srl | Low dose vaccines |
| WO2005097181A1 (en) * | 2004-04-05 | 2005-10-20 | Pfizer Products Inc. | Microfluidized oil-in-water emulsions and vaccine compositions |
| SI1740217T1 (sl) | 2004-04-30 | 2011-10-28 | Novartis Ag | Konjugirano meningokokno cepljenje |
| GB0409745D0 (en) * | 2004-04-30 | 2004-06-09 | Chiron Srl | Compositions including unconjugated carrier proteins |
| GB0500787D0 (en) | 2005-01-14 | 2005-02-23 | Chiron Srl | Integration of meningococcal conjugate vaccination |
| GB0413868D0 (en) * | 2004-06-21 | 2004-07-21 | Chiron Srl | Dimensional anlaysis of saccharide conjugates |
| JP2008513406A (ja) * | 2004-09-22 | 2008-05-01 | グラクソスミスクライン バイオロジカルズ ソシエテ アノニム | 免疫原性組成物 |
| US20060121055A1 (en) | 2004-12-06 | 2006-06-08 | Becton, Dickinson And Company, Inc. | Compositions with enhanced immunogenicity |
| GB0428394D0 (en) * | 2004-12-24 | 2005-02-02 | Chiron Srl | Saccharide conjugate vaccines |
| GB0502095D0 (en) * | 2005-02-01 | 2005-03-09 | Chiron Srl | Conjugation of streptococcal capsular saccharides |
| SI1858920T1 (sl) * | 2005-02-18 | 2016-07-29 | Glaxosmithkline Biologicals S.A. | Proteini in nukleinske kisline iz escherichia coli, povezane z meningitisom/sepso |
| GB0505518D0 (en) | 2005-03-17 | 2005-04-27 | Chiron Srl | Combination vaccines with whole cell pertussis antigen |
| US20070184072A1 (en) * | 2005-04-08 | 2007-08-09 | Wyeth | Multivalent pneumococcal polysaccharide-protein conjugate composition |
| KR102378962B1 (ko) * | 2005-04-08 | 2022-03-28 | 와이어쓰 엘엘씨 | 다가 폐렴구균 다당류-단백질 접합체 조성물 |
| NZ563940A (en) * | 2005-05-06 | 2010-11-26 | Novartis Vaccines & Diagnostic | Immunogens for meningitidis-A vaccines comprising oligosaccharides linked by a phosphonate |
| US9486515B2 (en) | 2005-06-27 | 2016-11-08 | Glaxosmithkline Biologicals S.A. | Immunogenic composition |
| CN1709505B (zh) | 2005-07-13 | 2010-06-16 | 北京绿竹生物制药有限公司 | 多价细菌荚膜多糖-蛋白质结合物联合疫苗 |
| CA2621023C (en) * | 2005-09-01 | 2019-07-02 | Novartis Vaccines And Diagnostics Gmbh & Co. Kg | Multiple vaccination including serogroup c meningococcus |
| CA2621578C (en) * | 2005-09-05 | 2014-07-22 | Glaxosmithkline Biologicals S.A. | Serum bactericidal assay for n. meningitidis specific antisera |
| GB0522765D0 (en) * | 2005-11-08 | 2005-12-14 | Chiron Srl | Combination vaccine manufacture |
| GB0607088D0 (en) | 2006-04-07 | 2006-05-17 | Glaxosmithkline Biolog Sa | Vaccine |
| CN103251940A (zh) | 2005-12-22 | 2013-08-21 | 葛兰素史密丝克莱恩生物有限公司 | 疫苗 |
| US20080305127A1 (en) | 2005-12-23 | 2008-12-11 | Glaxosmithkline Biologicals S.A. | Conjugate Vaccines |
| CA2644724C (en) * | 2006-03-17 | 2016-05-24 | The Government Of The United States Of America As Represented By The Secretary Of The Department Of Health And Human Services | Methods for preparing complex multivalent immunogenic conjugates |
| AR060187A1 (es) | 2006-03-30 | 2008-05-28 | Glaxosmithkline Biolog Sa | Composicion inmunogenica |
| EP1998802A2 (en) * | 2006-03-30 | 2008-12-10 | GlaxoSmithKline Biologicals S.A. | Immunogenic composition |
| CA2656474A1 (en) | 2006-06-29 | 2008-01-03 | Novartis Ag | Polypeptides from neisseria meningitidis |
| US7491517B2 (en) | 2006-07-19 | 2009-02-17 | Jeeri R Reddy | Method of producing meningococcal meningitis vaccine for Neisseria meningitidis serotypes A,C,Y, and W-135 |
| US20080171061A1 (en) | 2006-07-21 | 2008-07-17 | Douglas Nixon | Human endogenous retrovirus polypeptide compositions and methods of use thereof |
| EP2491947A3 (en) * | 2006-09-07 | 2012-10-17 | GlaxoSmithKline Biologicals S.A. | Vaccine |
| GB0700136D0 (en) * | 2007-01-04 | 2007-02-14 | Glaxosmithkline Biolog Sa | Process for manufacturing vaccines |
| GB0700135D0 (en) | 2007-01-04 | 2007-02-14 | Glaxosmithkline Biolog Sa | Vaccine |
| JP4858611B2 (ja) | 2007-03-14 | 2012-01-18 | コニカミノルタビジネステクノロジーズ株式会社 | 情報埋め込み方法、そのプログラムおよび情報埋め込み装置 |
| WO2008135514A1 (en) * | 2007-05-02 | 2008-11-13 | Glaxosmithkline Biologicals S.A. | Vaccine |
| ES2555786T3 (es) * | 2007-06-04 | 2016-01-08 | Glaxosmithkline Biologicals Sa | Formulación de vacunas contra la meningitis |
| MX2009013949A (es) * | 2007-06-26 | 2010-05-24 | Glaxosmithkline Biolog Sa | Vacuna que comprende conjugados de polisacárido capsular de streptococcus pneumoniae. |
| GB0714963D0 (en) | 2007-08-01 | 2007-09-12 | Novartis Ag | Compositions comprising antigens |
| CN102202689A (zh) | 2008-08-28 | 2011-09-28 | 葛兰素史密丝克莱恩生物有限公司 | 疫苗 |
| GB0816447D0 (en) * | 2008-09-08 | 2008-10-15 | Glaxosmithkline Biolog Sa | Vaccine |
| US8259461B2 (en) * | 2008-11-25 | 2012-09-04 | Micron Technology, Inc. | Apparatus for bypassing faulty connections |
| ES2812523T3 (es) * | 2009-09-30 | 2021-03-17 | Glaxosmithkline Biologicals Sa | Conjugación de polisacáridos capsulares de Staphylococcus aureus de tipo 5 y de tipo 8 |
| TW201136603A (en) * | 2010-02-09 | 2011-11-01 | Merck Sharp & Amp Dohme Corp | 15-valent pneumococcal polysaccharide-protein conjugate vaccine composition |
| GB201003922D0 (en) * | 2010-03-09 | 2010-04-21 | Glaxosmithkline Biolog Sa | Conjugation process |
| US9365624B2 (en) * | 2010-03-11 | 2016-06-14 | Glaxosmithkline Biologicals, S.A. | Vaccine |
| JP5144836B2 (ja) | 2010-06-11 | 2013-02-13 | パナソニック株式会社 | 語音聴取の評価システム、その方法およびそのプログラム |
| US9493517B2 (en) * | 2011-11-07 | 2016-11-15 | Glaxosmithkline Biologicals Sa | Conjugates comprising an antigen and a carrier molecule |
| GB2495341B (en) * | 2011-11-11 | 2013-09-18 | Novartis Ag | Fermentation methods and their products |
| HUE040914T4 (hu) * | 2012-01-30 | 2019-05-28 | Serum Institute Of India Pvt Ltd | Immunogén készítmény |
| EP2852414B9 (en) | 2012-05-22 | 2020-12-09 | GlaxoSmithKline Biologicals SA | Meningococcus serogroup x conjugate |
| WO2014001328A1 (en) | 2012-06-25 | 2014-01-03 | Nadiro A/S | A lifeboat deployment unit |
| ES2939307T3 (es) * | 2012-12-05 | 2023-04-20 | Glaxosmithkline Biologicals Sa | Composición inmunogénica |
| GB201310008D0 (en) * | 2013-06-05 | 2013-07-17 | Glaxosmithkline Biolog Sa | Immunogenic composition for use in therapy |
| JP2017523985A (ja) * | 2014-08-05 | 2017-08-24 | グラクソスミスクライン バイオロジカルズ ソシエテ アノニム | 抗原用担体分子 |
| TWI715617B (zh) * | 2015-08-24 | 2021-01-11 | 比利時商葛蘭素史密斯克藍生物品公司 | 對抗腸道外病原性大腸桿菌之免疫保護之方法及組合物 |
| GB201518684D0 (en) * | 2015-10-21 | 2015-12-02 | Glaxosmithkline Biolog Sa | Vaccine |
| AU2017321863B2 (en) * | 2016-09-02 | 2024-07-11 | Sanofi Vaccines US Inc. | Neisseria meningitidis vaccine |
| US11951165B2 (en) * | 2016-12-30 | 2024-04-09 | Vaxcyte, Inc. | Conjugated vaccine carrier proteins |
| PE20191107A1 (es) * | 2017-01-31 | 2019-08-26 | Pfizer | Composiciones de neisseria meningitidis y metodos respectivos |
| KR102657910B1 (ko) * | 2017-07-18 | 2024-04-18 | 세럼 인스티튜트 오브 인디아 프라이비트 리미티드 | 개선된 안정성, 강화된 면역원성과 감소된 반응원성을 갖는 면역원성 조성물 및 그의 제조 방법 |
-
2006
- 2006-06-23 US US11/917,702 patent/US9486515B2/en active Active
- 2006-06-23 CN CN2011101438611A patent/CN102218138A/zh active Pending
- 2006-06-23 DK DK10179820.5T patent/DK2351578T3/en active
- 2006-06-23 ES ES06754599.6T patent/ES2377075T5/es active Active
- 2006-06-23 PT PT151893971T patent/PT3009146T/pt unknown
- 2006-06-23 PE PE2010000444A patent/PE20110096A1/es active IP Right Grant
- 2006-06-23 HU HUE10177832A patent/HUE047211T2/hu unknown
- 2006-06-23 ES ES06754596T patent/ES2340711T3/es active Active
- 2006-06-23 EP EP06754596A patent/EP1896062B1/en not_active Revoked
- 2006-06-23 DK DK06754611.9T patent/DK1896065T4/da active
- 2006-06-23 EP EP10158046.2A patent/EP2201961B1/en active Active
- 2006-06-23 EA EA200702574A patent/EA012214B1/ru not_active IP Right Cessation
- 2006-06-23 UA UAA200714084A patent/UA95237C2/uk unknown
- 2006-06-23 DK DK06754599.6T patent/DK1896063T3/da active
- 2006-06-23 PT PT06754596T patent/PT1896062E/pt unknown
- 2006-06-23 EP EP14198052.4A patent/EP2878307B1/en active Active
- 2006-06-23 PL PL06754582T patent/PL1896061T3/pl unknown
- 2006-06-23 JP JP2008517436A patent/JP5280199B2/ja active Active
- 2006-06-23 US US11/917,709 patent/US9931397B2/en active Active
- 2006-06-23 MX MX2007016402A patent/MX2007016402A/es active IP Right Grant
- 2006-06-23 CA CA2612957A patent/CA2612957C/en active Active
- 2006-06-23 MX MX2007016236A patent/MX2007016236A/es active IP Right Grant
- 2006-06-23 PL PL06754611T patent/PL1896065T5/pl unknown
- 2006-06-23 EP EP06754610A patent/EP1896064A2/en not_active Ceased
- 2006-06-23 PL PL14198052T patent/PL2878307T3/pl unknown
- 2006-06-23 AR ARP060102725A patent/AR053935A1/es not_active Application Discontinuation
- 2006-06-23 PL PL10179820T patent/PL2351578T3/pl unknown
- 2006-06-23 EP EP06754611.9A patent/EP1896065B2/en active Active
- 2006-06-23 EP EP06754582.2A patent/EP1896061B1/en active Active
- 2006-06-23 PE PE2006000719A patent/PE20070163A1/es active IP Right Grant
- 2006-06-23 PT PT141980524T patent/PT2878307T/pt unknown
- 2006-06-23 ES ES10177832T patent/ES2750243T3/es active Active
- 2006-06-23 MX MX2007016237A patent/MX2007016237A/es active IP Right Grant
- 2006-06-23 AU AU2006263963A patent/AU2006263963B2/en active Active
- 2006-06-23 PT PT06754582T patent/PT1896061T/pt unknown
- 2006-06-23 HR HR20100211T patent/HRP20100211T1/hr unknown
- 2006-06-23 EP EP10177832.2A patent/EP2283857B1/en active Active
- 2006-06-23 KR KR1020137018446A patent/KR101532068B1/ko active Active
- 2006-06-23 KR KR1020087002312A patent/KR101408113B1/ko active Active
- 2006-06-23 ES ES14198052T patent/ES2747025T3/es active Active
- 2006-06-23 AR ARP060102723A patent/AR056396A1/es not_active Application Discontinuation
- 2006-06-23 AR ARP060102724A patent/AR056397A1/es not_active Application Discontinuation
- 2006-06-23 KR KR1020137028209A patent/KR20130122810A/ko not_active Ceased
- 2006-06-23 US US11/917,569 patent/US8431136B2/en active Active
- 2006-06-23 PT PT101798205T patent/PT2351578T/pt unknown
- 2006-06-23 EP EP15189397.1A patent/EP3009146B1/en active Active
- 2006-06-23 HR HRP20110567TT patent/HRP20110567T4/hr unknown
- 2006-06-23 HU HUE15189397A patent/HUE056842T2/hu unknown
- 2006-06-23 CA CA2611960A patent/CA2611960C/en active Active
- 2006-06-23 SI SI200631247T patent/SI1896063T1/sl unknown
- 2006-06-23 SI SI200632356T patent/SI2283857T1/sl unknown
- 2006-06-23 NZ NZ564606A patent/NZ564606A/en unknown
- 2006-06-23 SI SI200630681T patent/SI1896062T1/sl unknown
- 2006-06-23 SI SI200632346T patent/SI1896061T1/sl unknown
- 2006-06-23 WO PCT/EP2006/006270 patent/WO2007000343A2/en not_active Ceased
- 2006-06-23 EP EP06762248.0A patent/EP1896066B8/en active Active
- 2006-06-23 SI SI200632159A patent/SI2351578T1/sl unknown
- 2006-06-23 DK DK06754582.2T patent/DK1896061T3/da active
- 2006-06-23 CA CA2612980A patent/CA2612980C/en active Active
- 2006-06-23 NZ NZ564607A patent/NZ564607A/en unknown
- 2006-06-23 AT AT06754599T patent/ATE536884T1/de active
- 2006-06-23 EP EP10179820.5A patent/EP2351578B1/en active Active
- 2006-06-23 HU HUE06754582A patent/HUE045482T2/hu unknown
- 2006-06-23 ES ES06754582T patent/ES2741529T3/es active Active
- 2006-06-23 EA EA200702577A patent/EA013374B1/ru not_active IP Right Cessation
- 2006-06-23 SI SI200632415T patent/SI3009146T1/sl unknown
- 2006-06-23 WO PCT/EP2006/006210 patent/WO2007000322A1/en not_active Ceased
- 2006-06-23 AU AU2006263965A patent/AU2006263965B2/en active Active
- 2006-06-23 JP JP2008517437A patent/JP5037503B2/ja active Active
- 2006-06-23 MX MX2007016403A patent/MX2007016403A/es active IP Right Grant
- 2006-06-23 LT LTEP10179820.5T patent/LT2351578T/lt unknown
- 2006-06-23 PL PL15189397T patent/PL3009146T3/pl unknown
- 2006-06-23 AP AP2007004274A patent/AP2436A/xx active
- 2006-06-23 AU AU2006263944A patent/AU2006263944B2/en active Active
- 2006-06-23 HU HUE10179820A patent/HUE031380T2/en unknown
- 2006-06-23 CN CN201210028358.6A patent/CN102526723B/zh active Active
- 2006-06-23 KR KR1020087002217A patent/KR101351870B1/ko active Active
- 2006-06-23 PL PL06754599T patent/PL1896063T3/pl unknown
- 2006-06-23 DK DK14198052.4T patent/DK2878307T3/da active
- 2006-06-23 PT PT101778322T patent/PT2283857T/pt unknown
- 2006-06-23 DE DE602006013313T patent/DE602006013313D1/de active Active
- 2006-06-23 ES ES10179820.5T patent/ES2621780T3/es active Active
- 2006-06-23 PL PL10177832T patent/PL2283857T3/pl unknown
- 2006-06-23 AU AU2006263964A patent/AU2006263964B2/en active Active
- 2006-06-23 WO PCT/EP2006/006188 patent/WO2007000314A2/en not_active Ceased
- 2006-06-23 AT AT06754611T patent/ATE516816T1/de active
- 2006-06-23 KR KR1020077030681A patent/KR101321056B1/ko active Active
- 2006-06-23 CN CN201310023297.9A patent/CN103083657B/zh active Active
- 2006-06-23 MX MX2007016405A patent/MX2007016405A/es active IP Right Grant
- 2006-06-23 SI SI200632352T patent/SI2878307T1/sl unknown
- 2006-06-23 US US11/917,726 patent/US8398983B2/en active Active
- 2006-06-23 NZ NZ564371A patent/NZ564371A/en not_active IP Right Cessation
- 2006-06-23 SI SI200631109T patent/SI1896065T2/sl unknown
- 2006-06-23 BR BRPI0612670A patent/BRPI0612670B8/pt active IP Right Grant
- 2006-06-23 BR BRPI0612655-3A patent/BRPI0612655B1/pt active IP Right Grant
- 2006-06-23 KR KR1020077030683A patent/KR101359953B1/ko active Active
- 2006-06-23 EA EA200702575A patent/EA012528B1/ru not_active IP Right Cessation
- 2006-06-23 WO PCT/EP2006/006269 patent/WO2007000342A2/en not_active Ceased
- 2006-06-23 US US11/917,610 patent/US9789179B2/en active Active
- 2006-06-23 JP JP2008517441A patent/JP5297800B2/ja active Active
- 2006-06-23 ES ES10158046.2T patent/ES2662651T3/es active Active
- 2006-06-23 NO NO20076343A patent/NO345422B1/no active Protection Beyond IP Right Term
- 2006-06-23 PL PL06754596T patent/PL1896062T3/pl unknown
- 2006-06-23 NZ NZ564605A patent/NZ564605A/en unknown
- 2006-06-23 CA CA2611964A patent/CA2611964C/en active Active
- 2006-06-23 JP JP2008517442A patent/JP5731737B2/ja active Active
- 2006-06-23 ES ES06762248T patent/ES2901378T3/es active Active
- 2006-06-23 WO PCT/EP2006/006268 patent/WO2007000341A2/en not_active Ceased
- 2006-06-23 BR BRPI0612669A patent/BRPI0612669B8/pt active IP Right Grant
- 2006-06-23 HU HUE14198052A patent/HUE046905T2/hu unknown
- 2006-06-23 DK DK06754596.2T patent/DK1896062T3/da active
- 2006-06-23 KR KR1020077031058A patent/KR101351873B1/ko not_active Expired - Fee Related
- 2006-06-23 UA UAA200714086A patent/UA95238C2/uk unknown
- 2006-06-23 AT AT06754596T patent/ATE462444T1/de active
- 2006-06-23 BR BRPI0612656-1A patent/BRPI0612656B1/pt active IP Right Grant
- 2006-06-23 BR BRPI0612654A patent/BRPI0612654B8/pt active IP Right Grant
- 2006-06-23 NZ NZ564370A patent/NZ564370A/en unknown
- 2006-06-23 PE PE2006000720A patent/PE20070499A1/es active IP Right Grant
- 2006-06-23 EA EA200702576A patent/EA012506B1/ru not_active IP Right Cessation
- 2006-06-23 PE PE2010000450A patent/PE20110072A1/es not_active Application Discontinuation
- 2006-06-23 PT PT06754599T patent/PT1896063E/pt unknown
- 2006-06-23 JP JP2008517440A patent/JP2008543907A/ja active Pending
- 2006-06-23 US US11/917,580 patent/US8329184B2/en active Active
- 2006-06-23 NZ NZ590204A patent/NZ590204A/en unknown
- 2006-06-23 DK DK10177832T patent/DK2283857T3/da active
- 2006-06-23 ES ES15189397T patent/ES2898451T3/es active Active
- 2006-06-23 PT PT06754611T patent/PT1896065E/pt unknown
- 2006-06-23 AU AU2006263936A patent/AU2006263936B2/en active Active
- 2006-06-23 WO PCT/EP2006/006220 patent/WO2007000327A1/en not_active Ceased
- 2006-06-23 PE PE2006000718A patent/PE20070123A1/es not_active Application Discontinuation
- 2006-06-23 EP EP06754599.6A patent/EP1896063B2/en active Active
- 2006-06-23 CA CA2612963A patent/CA2612963C/en active Active
- 2006-06-23 PE PE2014001334A patent/PE20142165A1/es active IP Right Grant
- 2006-06-23 HR HR20120102T patent/HRP20120102T1/hr unknown
- 2006-06-26 TW TW095122979A patent/TWI407970B/zh active
- 2006-06-26 MY MYPI20063023A patent/MY148110A/en unknown
- 2006-06-26 TW TW102148542A patent/TWI537001B/zh active
- 2006-06-26 MY MYPI20063024A patent/MY147783A/en unknown
- 2006-06-26 TW TW102118476A patent/TW201336507A/zh unknown
- 2006-06-26 TW TW095122993A patent/TWI477283B/zh active
- 2006-06-26 TW TW095122969A patent/TWI422386B/zh active
- 2006-06-26 MY MYPI20063025A patent/MY147490A/en unknown
-
2007
- 2007-12-06 IL IL187924A patent/IL187924A/en active IP Right Grant
- 2007-12-07 NO NO20076302A patent/NO344452B1/no unknown
- 2007-12-11 NO NO20076350A patent/NO342815B1/no unknown
- 2007-12-11 IL IL188046A patent/IL188046A/en active IP Right Grant
- 2007-12-11 IL IL188045A patent/IL188045A0/en active IP Right Grant
- 2007-12-12 IL IL188072A patent/IL188072A/en active IP Right Grant
- 2007-12-12 NO NO20076363A patent/NO345305B1/no unknown
- 2007-12-26 MA MA30512A patent/MA29603B1/fr unknown
- 2007-12-26 MA MA30511A patent/MA29602B1/fr unknown
- 2007-12-27 MA MA30521A patent/MA29569B1/fr unknown
- 2007-12-27 MA MA30522A patent/MA29993B1/fr unknown
-
2010
- 2010-04-30 CY CY20101100387T patent/CY1109996T1/el unknown
- 2010-07-21 AU AU2010203115A patent/AU2010203115C1/en active Active
- 2010-08-18 AU AU2010212417A patent/AU2010212417A1/en not_active Abandoned
-
2011
- 2011-06-22 IL IL213718A patent/IL213718A/en active IP Right Grant
- 2011-06-28 IL IL213795A patent/IL213795A/en active IP Right Grant
- 2011-08-15 IL IL214657A patent/IL214657A0/en unknown
- 2011-09-15 CY CY20111100883T patent/CY1111827T1/el unknown
-
2012
- 2012-02-21 CY CY20121100175T patent/CY1112698T1/el unknown
- 2012-04-27 US US13/457,891 patent/US8846049B2/en active Active
- 2012-10-11 IL IL222346A patent/IL222346A/en active IP Right Grant
- 2012-10-16 CY CY2012027C patent/CY2012027I1/el unknown
- 2012-10-16 LT LTPA2012019C patent/LTC1896065I2/lt unknown
- 2012-10-18 BE BE2012C042C patent/BE2012C042I2/fr unknown
- 2012-10-19 NL NL300549C patent/NL300549I2/nl unknown
- 2012-10-19 HU HUS1200023C patent/HUS1200023I1/hu unknown
- 2012-10-19 LU LU92085C patent/LU92085I2/fr unknown
- 2012-11-01 JP JP2012241817A patent/JP5769688B2/ja active Active
-
2013
- 2013-02-27 US US13/778,633 patent/US8883163B2/en active Active
- 2013-03-13 JP JP2013050333A patent/JP5718960B2/ja active Active
- 2013-05-14 JP JP2013102249A patent/JP2013209395A/ja active Pending
-
2014
- 2014-10-28 US US14/525,883 patent/US9358279B2/en active Active
-
2015
- 2015-04-28 JP JP2015091394A patent/JP5965512B2/ja active Active
-
2016
- 2016-09-14 US US15/265,597 patent/US10245317B2/en active Active
-
2017
- 2017-02-21 CY CY20171100234T patent/CY1118646T1/el unknown
- 2017-03-20 HR HRP20170457TT patent/HRP20170457T1/hr unknown
- 2017-08-30 US US15/691,440 patent/US10166287B2/en active Active
-
2018
- 2018-11-02 US US16/179,476 patent/US11241495B2/en active Active
-
2019
- 2019-02-05 US US16/268,287 patent/US20200000911A1/en not_active Abandoned
-
2021
- 2021-12-07 NL NL301151C patent/NL301151I2/nl unknown
- 2021-12-29 LU LU00247C patent/LUC00247I2/fr unknown
-
2022
- 2022-01-13 HU HUS2200002C patent/HUS2200002I1/hu unknown
- 2022-02-21 FR FR22C1008C patent/FR22C1008I2/fr active Active
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2750243T3 (es) | Composición de vacuna que comprende polisacáridos capsulares naturales conjugados de N. Meningitidis | |
| CN101222935B (zh) | 免疫原性组合物 | |
| HK1206587B (en) | Immunogenic composition | |
| HK1116082A (en) | Immunogenic composition |