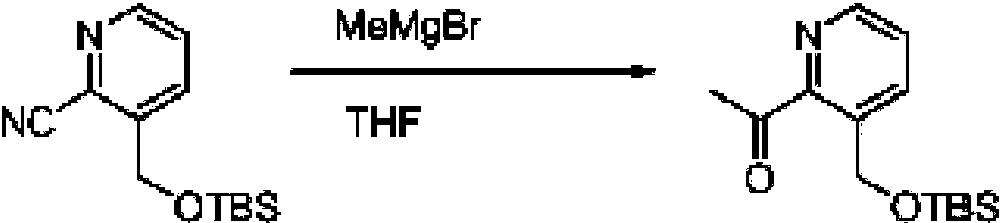ES2811129T3 - Compuestos de benzaldehído sustituidos y métodos para su uso en el aumento de la oxigenación tisular - Google Patents
Compuestos de benzaldehído sustituidos y métodos para su uso en el aumento de la oxigenación tisular Download PDFInfo
- Publication number
- ES2811129T3 ES2811129T3 ES16194019T ES16194019T ES2811129T3 ES 2811129 T3 ES2811129 T3 ES 2811129T3 ES 16194019 T ES16194019 T ES 16194019T ES 16194019 T ES16194019 T ES 16194019T ES 2811129 T3 ES2811129 T3 ES 2811129T3
- Authority
- ES
- Spain
- Prior art keywords
- group
- halo
- alkyl
- compound
- alkynyl
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 0 CC1=NC*C=C1C(O)O Chemical compound CC1=NC*C=C1C(O)O 0.000 description 1
- LLDXUQCATZMIQS-UHFFFAOYSA-N CCC/[O]=C/c1cc(OC)ccc1OC(C(C)[n]1nccc1-1)c2c-1nccc2 Chemical compound CCC/[O]=C/c1cc(OC)ccc1OC(C(C)[n]1nccc1-1)c2c-1nccc2 LLDXUQCATZMIQS-UHFFFAOYSA-N 0.000 description 1
- OPMFFAOEPFATTG-UHFFFAOYSA-N NNCC(F)(F)F Chemical compound NNCC(F)(F)F OPMFFAOEPFATTG-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/4985—Pyrazines or piperazines ortho- or peri-condensed with heterocyclic ring systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/19—Carboxylic acids, e.g. valproic acid
- A61K31/192—Carboxylic acids, e.g. valproic acid having aromatic groups, e.g. sulindac, 2-aryl-propionic acids, ethacrynic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/21—Esters, e.g. nitroglycerine, selenocyanates
- A61K31/215—Esters, e.g. nitroglycerine, selenocyanates of carboxylic acids
- A61K31/235—Esters, e.g. nitroglycerine, selenocyanates of carboxylic acids having an aromatic ring attached to a carboxyl group
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/415—1,2-Diazoles
- A61K31/416—1,2-Diazoles condensed with carbocyclic ring systems, e.g. indazole
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/4353—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems
- A61K31/437—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems the heterocyclic ring system containing a five-membered ring having nitrogen as a ring hetero atom, e.g. indolizine, beta-carboline
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/4406—Non condensed pyridines; Hydrogenated derivatives thereof only substituted in position 3, e.g. zimeldine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/4427—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems
- A61K31/4439—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems containing a five-membered ring with nitrogen as a ring hetero atom, e.g. omeprazole
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/445—Non condensed piperidines, e.g. piperocaine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/04—Drugs for disorders of the alimentary tract or the digestive system for ulcers, gastritis or reflux esophagitis, e.g. antacids, inhibitors of acid secretion, mucosal protectants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/02—Drugs for dermatological disorders for treating wounds, ulcers, burns, scars, keloids, or the like
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
- A61P7/06—Antianaemics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C65/00—Compounds having carboxyl groups bound to carbon atoms of six—membered aromatic rings and containing any of the groups OH, O—metal, —CHO, keto, ether, groups, groups, or groups
- C07C65/21—Compounds having carboxyl groups bound to carbon atoms of six—membered aromatic rings and containing any of the groups OH, O—metal, —CHO, keto, ether, groups, groups, or groups containing ether groups, groups, groups, or groups
- C07C65/24—Compounds having carboxyl groups bound to carbon atoms of six—membered aromatic rings and containing any of the groups OH, O—metal, —CHO, keto, ether, groups, groups, or groups containing ether groups, groups, groups, or groups polycyclic
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C65/00—Compounds having carboxyl groups bound to carbon atoms of six—membered aromatic rings and containing any of the groups OH, O—metal, —CHO, keto, ether, groups, groups, or groups
- C07C65/30—Compounds having carboxyl groups bound to carbon atoms of six—membered aromatic rings and containing any of the groups OH, O—metal, —CHO, keto, ether, groups, groups, or groups containing —CHO groups
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C69/00—Esters of carboxylic acids; Esters of carbonic or haloformic acids
- C07C69/66—Esters of carboxylic acids having esterified carboxylic groups bound to acyclic carbon atoms and having any of the groups OH, O—metal, —CHO, keto, ether, acyloxy, groups, groups, or in the acid moiety
- C07C69/73—Esters of carboxylic acids having esterified carboxylic groups bound to acyclic carbon atoms and having any of the groups OH, O—metal, —CHO, keto, ether, acyloxy, groups, groups, or in the acid moiety of unsaturated acids
- C07C69/734—Ethers
- C07C69/736—Ethers the hydroxy group of the ester being etherified with a hydroxy compound having the hydroxy group bound to a carbon atom of a six-membered aromatic ring
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C69/00—Esters of carboxylic acids; Esters of carbonic or haloformic acids
- C07C69/76—Esters of carboxylic acids having a carboxyl group bound to a carbon atom of a six-membered aromatic ring
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D211/00—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings
- C07D211/04—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings with only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D211/06—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having no double bonds between ring members or between ring members and non-ring members
- C07D211/36—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having no double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D211/60—Carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals
- C07D211/62—Carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals attached in position 4
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D213/00—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members
- C07D213/02—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members
- C07D213/04—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D213/24—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom with substituted hydrocarbon radicals attached to ring carbon atoms
- C07D213/28—Radicals substituted by singly-bound oxygen or sulphur atoms
- C07D213/30—Oxygen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D213/00—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members
- C07D213/02—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members
- C07D213/04—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D213/60—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D213/78—Carbon atoms having three bonds to hetero atoms, with at the most one bond to halogen, e.g. ester or nitrile radicals
- C07D213/79—Acids; Esters
- C07D213/80—Acids; Esters in position 3
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D215/00—Heterocyclic compounds containing quinoline or hydrogenated quinoline ring systems
- C07D215/02—Heterocyclic compounds containing quinoline or hydrogenated quinoline ring systems having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen atoms or carbon atoms directly attached to the ring nitrogen atom
- C07D215/12—Heterocyclic compounds containing quinoline or hydrogenated quinoline ring systems having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen atoms or carbon atoms directly attached to the ring nitrogen atom with substituted hydrocarbon radicals attached to ring carbon atoms
- C07D215/14—Radicals substituted by oxygen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D231/00—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings
- C07D231/54—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings condensed with carbocyclic rings or ring systems
- C07D231/56—Benzopyrazoles; Hydrogenated benzopyrazoles
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D257/00—Heterocyclic compounds containing rings having four nitrogen atoms as the only ring hetero atoms
- C07D257/02—Heterocyclic compounds containing rings having four nitrogen atoms as the only ring hetero atoms not condensed with other rings
- C07D257/04—Five-membered rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/04—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains two hetero rings
- C07D487/04—Ortho-condensed systems
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02P—CLIMATE CHANGE MITIGATION TECHNOLOGIES IN THE PRODUCTION OR PROCESSING OF GOODS
- Y02P20/00—Technologies relating to chemical industry
- Y02P20/50—Improvements relating to the production of bulk chemicals
- Y02P20/55—Design of synthesis routes, e.g. reducing the use of auxiliary or protecting groups
Landscapes
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Epidemiology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Neurology (AREA)
- Biomedical Technology (AREA)
- Neurosurgery (AREA)
- Diabetes (AREA)
- Dermatology (AREA)
- Heart & Thoracic Surgery (AREA)
- Cardiology (AREA)
- Communicable Diseases (AREA)
- Oncology (AREA)
- Hematology (AREA)
- Virology (AREA)
- Emergency Medicine (AREA)
- Psychiatry (AREA)
- Pulmonology (AREA)
- Hospice & Palliative Care (AREA)
- Urology & Nephrology (AREA)
- Vascular Medicine (AREA)
- Molecular Biology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Pyridine Compounds (AREA)
- Plural Heterocyclic Compounds (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Abstract
Un compuesto de Fórmula (I): **(Ver fórmula)** o un tautómero o una sal farmacéuticamente aceptable del mismo, para su uso en el tratamiento del cuerpo humano o animal, en donde Q es piridin-2-ilo, piridin-3-ilo o piridin-4-ilo, estando dicho Q sustituido con uno a tres Ra en donde al menos un Ra es heteroarilo opcionalmente sustituido con uno a tres Rc; Y es CR1aR1b, en donde R1a es H o halo y R1b es H o halo, opcionalmente en donde al menos uno de R1a y R1b es F; X es O; R2, R3, R4 y R5 se seleccionan independientemente del grupo que consiste en hidrógeno, halo, Rb, ORd, OC(O)Re, SRd, CN, NO2, CO2Rd, CONRdRd, C(O)Rd, OC(O)NRdRd, NRdRd, NRdC(O)Re, NRdC(O)2Re, NRdC(O)NRdRd, S(O)Re, S(O)2Re, NRdS(O)2Re, S(O)2NRdRd y N3; o R5 es -(CH2)pR5a en donde p es 0 o 1 y R5a es OH; R6 y R7 forman juntos oxo; cada Ra se selecciona independientemente del grupo que consiste en halo, Rb, ORd, OC(O)Re, SRd, CN, NO2, CO2Rd, CONRdRd, C(O)Rd, OC(O)NRdRd, NRdC(O)Re, NRdC(O)2Re, NRdC(O)NRdRd, S(O)Re, S(O)2Re, NRdS(O)2Re, S(O)2NRdRd, N3, arilo opcionalmente sustituido con de uno a tres Rc, heteroarilo opcionalmente sustituido con de uno a tres Rc y heterocicloalquilo opcionalmente sustituido con de uno a tres Rc; cada Rb se selecciona independientemente del grupo que consiste en alquilo C1-8, alquenilo C2-8 y alquinilo C2-8, cada uno opcionalmente sustituido independientemente con uno a tres halo, ORd o NRdRd; cada Rc se selecciona independientemente del grupo que consiste en halo, alquilo C1-8, halo-alquilo C1-8, alquenilo C2-8, halo-alquenilo C2-8, alquinilo C2-8, halo-alquinilo C2-8, (CH2)mORf, OC(O)Rg, SRf, CN, NO2, CO2Rf, CONRfRf, C(O)Rf, OC(O)NRfRf, (CH2)mNRfRf, NRfC(O)Rg, NRfC(O)2Rg, NRfC(O)NRfRf, S(O)Rg, S(O)2Rg, NRfS(O)2Rg, S(O)2NRfRf y N3 en donde m se selecciona del grupo que consiste en 0, 1, 2, 3, 4, 5 y 6; cada Rd y Rf se selecciona independientemente del grupo que consiste en hidrógeno, alquilo C1-8, halo-alquilo C1- 8, alquenilo C2-8, halo-alquenilo C2-8, alquinilo C2-8 y halo-alquinilo C2-8; y cada Re y Rg se selecciona independientemente del grupo que consiste en alquilo C1-8, halo-alquilo C1-8, alquenilo C2-8, halo-alquenilo C2-8, alquinilo C2-8 y halo-alquinilo C2-8.
Description
DESCRIPCIÓN
Compuestos de benzaldehído sustituidos y métodos para su uso en el aumento de la oxigenación tisular
Campo de la invención
La presente invención se refiere, en general, a benzaldehídos sustituidos y a tautómeros o sales farmacéuticamente aceptables del mismo que actúan como moduladores alostéricos de la hemoglobina, a métodos y a productos intermedios para su preparación, a composiciones farmacéuticas que comprenden los moduladores, y a dichos benzaldehídos sustituidos y a tautómeros o sales farmacéuticamente aceptables del mismo para su uso en el tratamiento de trastornos mediados por la hemoglobina y trastornos que se beneficiarían de un aumento de la oxigenación tisular.
Antecedentes de la invención
La hemoglobina (Hb) es una proteína tetramérica de los glóbulos rojos que transporta hasta cuatro moléculas de oxígeno desde los pulmones a diversos tejidos y órganos a través del cuerpo. La hemoglobina se une y libera oxígeno a través de cambios de configuración, y se encuentra en estado tenso (T) cuando no está unida al oxígeno y en estado relajado (R) cuando está unida al oxígeno. El equilibrio entre los dos estados de configuración está bajo regulación alostérica. Los compuestos naturales tales como el 2,3-bisfosfoglicerato (2,3-BPG), los protones y el dióxido de carbono estabilizan la hemoglobina en su estado T desoxigenado, mientras que el oxígeno estabiliza la hemoglobina en su estado R oxigenado. También se han encontrado otros estados R relajados; sin embargo, su papel en la regulación alostérica no ha sido completamente dilucidado.
La anemia de células falciformes es una enfermedad frecuente, en particular, entre las personas de ascendencia africana y mediterránea. La hemoglobina falciforme (HbS) contiene una mutación puntual en donde el ácido glutámico se reemplaza por valina, permitiendo que el estado T sea susceptible a la polimerización, dando a los glóbulos rojos que contienen HbS su forma característica de hoz. Las células falciformes también son más rígidas que los glóbulos rojos normales, y su falta de flexibilidad puede conducir al bloqueo de los vasos sanguíneos. Se ha descubierto que ciertos aldehídos sintéticos desplazan el equilibrio del estado T formador de polímeros al estado R no formador de polímeros (Nnamani et al. Chemistry & Biodiversity Vol. 5, 2008 pág. 1762-1769) actuando como moduladores alostéricos para estabilizar el estado R mediante la formación de una base de Schiff con un grupo amino sobre la hemoglobina.
El documento US 7.160.910 desvela 2-furfuraldehídos y compuestos relacionados que también son moduladores alostéricos de la hemoglobina. Se encontró que un compuesto en particular, el 5-hidroximetil-2-furfuraldehído (5HMF), era un potente modulador de la hemoglobina tanto in vitro como in vivo. Se encontró que ratones transgénicos productores de HbS humana que se trataron con 5HMF resultaron tener tiempos de supervivencia significativamente mejorados al exponerse a hipoxia extrema (5 % de oxígeno). En estas condiciones hipóxicas, también se encontró que los ratones tratados con 5HMF tenían cantidades reducidas de glóbulos rojos falciformes inducidos por hipoxia en comparación con los ratones no tratados.
Existe una necesidad de agentes terapéuticos que puedan desplazar el equilibrio entre los estados desoxigenado y oxigenado de la Hb para tratar trastornos que están mediados por la Hb o por la Hb anómala tal como la HbS. También existe una necesidad terapéutica de tratar trastornos que se beneficiarían de tener Hb en el estado R con una mayor afinidad por el oxígeno. Dichos agentes terapéuticos tendrían aplicaciones que varían desde, por ejemplo, la sensibilización de células tumorales hipóxicas que son resistentes a la radioterapia o quimioterapia convencional debido a los bajos niveles de oxígeno en la célula, al tratamiento de trastornos pulmonares e hipertensivos, y a la potenciación de la cicatrización de las heridas.
Rolan, P. E et al., British Journal Of Clinical Pharmacology, vol. 35, n.° 4, páginas 419 - 425 (1993), describen el tucaresol para su uso en el tratamiento de la anemia de células falciformes. Osheiza Abdulmalik et al., "Acta Crystallographica Section D Biological Crystallography", vol. 125, n.° 11, páginas 788-928 (2011), describen derivados de vanilina para su uso en el tratamiento de la anemia de células falciformes. Nnamani I N et al., Chemistry & Biodiversity, Helvetica Chimica Acta, vol. 5, n.° 9, páginas 1762-1769 (2008), describen derivados de piridilo de benzaldehído para su uso en el tratamiento de la anemia de células falciformes. Glasson, C R K et al., Australian Journal of Chemistry, vol. 65, páginas 1371*1376 (2012) desvelan el compuesto 2-((5'-metil-[2,2'-bipiridin]-5il)metoxi)benzaldehído como un precursor sintético para un compuesto "pseudo jaula" que quela iones metálicos.
Breve sumario de la invención
La presente invención proporciona, en un aspecto, moduladores alostéricos de hemoglobina. En otro aspecto, se proporcionan composiciones farmacéuticas que comprenden dichos moduladores alostéricos. En otros aspectos, se proporcionan moduladores alostéricos de hemoglobina para su uso en el tratamiento del cuerpo humano o animal. En algunos aspectos, los moduladores alostéricos de hemoglobina son para su uso en el tratamiento de trastornos que se beneficiarían de la oxigenación aumentada, comprendiendo dichos métodos administrar los moduladores
alostéricos a un sujeto que lo necesite.
Descripción detallada de la invención
I. Definiciones
Como se usan en el presente documento, los siguientes términos y expresiones tienen los siguientes significados, a menos que se especifique lo contrario.
Las abreviaturas usadas en el presente documento son convencionales, a menos que se defina lo contrario: ac = acuoso; Boc = f-butilcarboxi; (Boc)2O = di-ferc-butil-dicarbonato; °C = grados Celsius; mCPBA = ácido mcloroperoxibenzoico; DCM = diclorometano (CH2O 2); DIBAL = hidruro de diisobutilaluminio; DMF = dimetilformamida; EtOAc = acetato de etilo; g = gramo; H2 = hidrógeno; H2O = agua; HBr = bromuro de hidrógeno; HCl = cloruro de hidrógeno; HPLC = cromatografía de líquidos de alta presión; h = hora; LAH = hidruro de litio y aluminio (LiAlH4); MeCN = acetonitrilo; MS = espectro de masas; m/z = proporción de la masa con respecto a la carga; MHz = Mega hercio; MeOH = metanol; pM = micromolar; pl = microlitro; mg = miligramo; mM = milimolar; mmol = milimol; ml = mililitro; min = minuto; M = molar; Na2CO3 = carbonato sódico; ng = nanogramo; N = Normal; RMN = resonancia magnética nuclear; Pd/C = paladio sobre carbono; RP = fase inversa; sat = saturado/a; TA = temperatura ambiente; TEA = trietilamina; THF = tetrahidrofurano; TFA = ácido trifluoroacético; TLC = cromatografía de capa fina; y TMS = trimetilsililo.
Se observa en el presente documento que, como se usa en la presente memoria descriptiva y en las reivindicaciones adjuntas, las formas en singular "un", "una", "el" y "la" incluyen los referentes en plural a menos que el contexto indique claramente lo contrario.
"Alcoxi" se refiere a -O(alquilo), en donde alquilo es como se define en el presente documento. Los ejemplos representativos de grupos alcoxi incluyen metoxi, etoxi, f-butoxi, y similares.
"Alquilo", por sí mismo o como parte de otro sustituyente, significa, a menos que se indique lo contrario, un radical de hidrocarburo alifático completamente saturado, de cadena lineal o ramificada, que tiene el número de átomos de carbono designado. Por ejemplo, "alquilo C1-8" se refiere a un radical de hidrocarburo lineal o ramificado, que contiene de 1 a 8 átomos de carbono que se deriva por la eliminación de un átomo de hidrógeno de un solo átomo de carbono de un alcano precursor. Alquilo incluye isómeros de cadena ramificada de grupos alquilo de cadena lineal tales como isopropilo, f-butilo, isobutilo, sec-butilo y similares. Los grupos alquilo representativos incluyen grupos alquilo de cadena lineal y ramificada que tienen 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 o 12 átomos de carbono. Otros grupos alquilo representativos incluyen grupos alquilo de cadena lineal y ramificada que tienen 1, 2, 3, 4, 5, 6, 7 u 8 átomos de carbono.
"Alquenilo" se refiere a un radical de hidrocarburo monovalente lineal o a un radical de hidrocarburo monovalente ramificado que tiene el número de átomos de carbono indicado en el prefijo y que contiene al menos un doble enlace, pero no más de tres dobles enlaces. Por ejemplo, se entiende que alquenilo C2-8 incluye etenilo, propenilo, 1,3-butadienilo y similares.
"Alquinilo" significa un radical de hidrocarburo monovalente lineal o un radical de hidrocarburo monovalente ramificado que contiene al menos un triple enlace y que tiene el número de átomos de carbono indicado en el prefijo. El término "alquinilo" también pretende incluir aquellos grupos alquilo que tienen un triple enlace y un doble enlace. Por ejemplo, alquinilo C2-8 pretende incluir etinilo, propinilo y similares.
La expresión "moduladores alostéricos" se refiere a compuestos que se unen a la hemoglobina para modular su afinidad por el oxígeno. En un grupo de realizaciones, los moduladores alostéricos actúan para estabilizar o desestabilizar una determinada configuración de hemoglobina. En un grupo de realizaciones, los moduladores estabilizan el estado R relajado. En otras realizaciones, los moduladores desestabilizan el estado T tenso. En un grupo de realizaciones, los moduladores alostéricos pueden desestabilizar una configuración mientras estabilizan otra. En algunas de dichas realizaciones, los moduladores estabilizan un estado R relajado y desestabilizan el estado T tenso. Los moduladores, además de modular la afinidad de la hemoglobina por el oxígeno, también pueden conferir propiedades adicionales a la hemoglobina, tales como el aumento de su solubilidad. La presente divulgación no pretende limitarse al mecanismo mediante el que los moduladores alostéricos interactúan con y regulan la hemoglobina. En un grupo de realizaciones, los moduladores alostéricos inhiben la polimerización de HbS y la formación en forma de hoz de los glóbulos rojos. En un grupo de realizaciones, la unión de los moduladores alostéricos proporcionados en el presente documento a la hemoglobina puede ocurrir a través de interacciones covalentes o no covalentes. En una realización, los moduladores alostéricos reaccionan a través de su sustituyente aldehído con un grupo amina en una cadena lateral de aminoácidos de hemoglobina para formar una base de Schiff.
"Amino" se refiere a un radical monovalente -NH2.
"Arilo" por sí mismo o como parte de otro sustituyente se refiere a un grupo de hidrocarburo poliinsaturado, aromático, que contiene de 6 a 14 átomos de carbono, que puede ser un solo anillo o múltiples anillos (hasta tres anillos) que
están condensados o enlazados covalentemente. Por lo tanto, el término incluye, pero sin limitación, grupos tales como fenilo, bifenilo, antracenilo, naftilo a modo de ejemplo. Los ejemplos no limitantes de grupos arilo incluyen fenilo, 1-naftilo, 2-naftilo y 4-bifenilo.
"Cicloalquilo" se refiere a un grupo cíclico saturado o parcialmente saturado de 3 a 14 átomos de carbono y sin heteroátomos en el anillo, y que tiene un solo anillo o múltiples anillos que incluyen sistemas de anillos condensados, puenteados y espiro. El término "cicloalquilo" incluye grupos cicloalquenilo, un anillo de cicloalquilo parcialmente saturado que tiene al menos un sitio de insaturación de anillo >C=C<. Los ejemplos de grupos cicloalquilo incluyen, por ejemplo, adamantilo, ciclopropilo, ciclobutilo, ciclopentilo, ciclooctilo y ciclohexenilo. "cicloalquilo Cu -v " se refiere a grupos cicloalquilo que tienen de u' a v' átomos de carbono como miembros de anillo. "cicloalquenilo Cu -v " se refiere a grupos cicloalquenilo que tienen de u' a v' átomos de carbono como miembros de anillo.
El término "hemoglobina", como se usa en el presente documento, se refiere a cualquier proteína de hemoglobina, incluyendo hemoglobina normal (Hb) y hemoglobina falciforme (HbS).
"Heteroarilo" se refiere a un radical cíclico o policíclico que tiene al menos un anillo aromático y de uno a cinco heteroátomos del anillo seleccionados entre N, O y S, y, opcionalmente, uno o más sustituyentes oxo (=O) unidos a uno o más átomos de carbono del anillo, y en donde los átomos de nitrógeno y de azufre del anillo están opcionalmente oxidados. Un grupo heteroarilo puede estar unido al resto de la molécula a través de un heteroátomo o a través de un átomo de carbono, y puede contener de 5 a 10 átomos de carbono. Los grupos heteroarilo incluyen anillo/s aromático/s policíclico/s condensado/s a grupos cicloalquilo o heterocicloalquilo no aromáticos, y en donde el punto de unión al resto de la molécula puede ser a través de cualquier átomo de anillo adecuado de cualquier anillo. En un grupo heteroarilo policíclico, el/los heteroátomo/s del anillo puede/n estar bien en un anillo aromático o no aromático o ambos. La expresión "anillo aromático" incluye cualquier anillo que tenga al menos una estructura de resonancia plana en donde 2n 2 pi electrones están deslocalizados alrededor del anillo. Los ejemplos de grupos heteroarilo incluyen, pero sin limitación, grupos imidazopiridinilo, grupos pirrolopiridinilo, grupos pirazolopiridinilo, grupos triazolopiridinilo, grupos pirazolopirazinilo, grupos piridinilo, grupos pirazinilo, grupos oxazolilo, grupos imidazolilo, grupos triazolilo, grupos tetrazolilo, grupos pirazolilo, grupos quinolinilo, grupos isoquinolinilo, grupos indazolilo, grupos benzooxazolilo, grupos naftiridinilo y grupos quinoxalinilo. Otros ejemplos no limitantes de grupos heteroarilo incluyen xantina, hipoxantina, 5-benzotiazolilo, purinilo, 2-benzimidazolilo, benzopirazolilo, 5-indolilo, azaindol, 1 -isoquinolilo, 5-isoquinolilo, 2-quinoxalinilo, 5-quinoxalinilo, 3-quinolilo, 6-quinolilo, 1-pirrolilo, 2-pirrolilo, 3-pirrolilo, 1-pirazolilo, 3-pirazolilo, 2-imidazolilo, 4-imidazolilo, pirazinilo, 2-oxazolilo, 4-oxazolilo, 5-oxazolilo, 3-isoxazolilo, 4-isoxazolilo, 5-isoxazolilo, 2-tiazolilo, 4-tiazolilo, 5-tiazolilo, 2-furilo, 3-furilo, 2-tienilo, 3-tienilo, 2-piridilo, 3-piridilo, 4-piridilo, 2-pirimidilo y 4-pirimidilo. "Heteroarilo bicíclico" se refiere a un radical heteroarilo que contiene dos anillos.
El término "heterocicloalquilo" se refiere a un grupo cicloalquilo que contiene al menos un heteroátomo de anillo y opcionalmente uno o más sustituyentes oxo. Como se usa en el presente documento, el término "heteroátomo" pretende incluir oxígeno (O), nitrógeno (N) y azufre (S), en donde los heteroátomos están opcionalmente oxidados y el/los átomo/s de nitrógeno están opcionalmente cuaternizados. Cada heterociclo puede unirse a cualquier carbono o heteroátomo disponible en el anillo. Cada heterociclo puede tener uno o más anillos. Cuando están presentes varios anillos, pueden condensarse entre sí. Cada heterociclo contiene normalmente 1, 2, 3, 4 o 5 heteroátomos seleccionados independientemente. Preferentemente, estos grupos contienen 1, 2, 3, 4, 5, 6, 7, 8, 9 o 10 átomos de carbono, 0, 1, 2, 3, 4 o 5 átomos de nitrógeno, 0, 1 o 2 átomos de azufre y 0 , 1 o 2 átomos de oxígeno. Más preferentemente, estos grupos contienen 1,2 o 3 átomos de nitrógeno, 0-1 átomos de azufre y 0-1 átomos de oxígeno. Los ejemplos no limitantes de grupos heterociclo incluyen morfolin-3-ona, piperazin-2-ona, piperazin-1-óxido, piperidina, morfolina, piperazina, isoxazolina, pirazolina, imidazolina, pirrolidina y similares.
"Halo" o "halógeno", por sí mismos o como parte de otro sustituyente, significan, a menos que se indique lo contrario, un átomo de flúor, cloro, bromo o yodo. Además, términos tales como "haloalquilo" pretenden incluir alquilo en donde uno o más átomos de hidrógeno están sustituidos con átomos de halógeno que pueden ser iguales o diferentes, en un número que varía de uno hasta el número máximo de halógenos permitidos, por ejemplo, para alquilo, (2m' 1), donde m' es el número total de átomos de carbono del grupo alquilo. Por ejemplo, el término "haloalquilo C1-C8" pretende incluir difluorometilo, trifluorometilo, 2,2,2-trifluoroetilo, 4-clorobutilo, 3-bromopropilo y similares. El término "haloalquenilo" y "haloalquinilo" se refiere a radicales alquenilo y alquinilo que tienen uno o más átomos de halógeno. Además, el término "haloalcoxi" se refiere a un radical alcoxi sustituido con uno o más átomos de halógeno. En un grupo de realizaciones, los grupos haloalquilo, haloalquenilo, haloalquinilo y haloalcoxi tienen de uno a 5 o de uno a 3 átomos de halógeno. Los ejemplos de grupos haloalcoxi incluyen difluorometoxi y trifluorometoxi. En un grupo de realizaciones, los átomos de halógeno de los grupos haloalquenilo y haloalquinilo están unidos a las partes alifáticas de estos grupos.
Los términos "opcional" u "opcionalmente", como se usan a lo largo de la memoria descriptiva, significan que el suceso o la circunstancia que se describe posteriormente puede, pero no necesita, ocurrir, y que la descripción incluye casos en donde ocurre el suceso o la circunstancia y casos en donde no. Por ejemplo, "grupo heteroarilo opcionalmente sustituido con un grupo alquilo" significa que el alquilo puede, pero no necesita, estar presente, y la descripción incluye situaciones en donde el grupo heteroarilo está sustituido con un grupo alquilo y situaciones en donde el grupo heteroarilo no está sustituido con el grupo alquilo.
"Oxo" se refiere al átomo divalente =O.
En cada una de las realizaciones anteriores que designan un número de átomos, por ejemplo, "C W se entiende que incluye todas las realizaciones posibles que tienen un átomo menos. Los ejemplos no limitantes incluyen C1-4, C1-5, C1-6 , C1-7, C2-8, C2-7, C3-8, C3-7 y similares.
La expresión "sales farmacéuticamente aceptables" pretende incluir sales de los compuestos activos que se preparan con ácidos o bases relativamente no tóxicos, dependiendo de los sustituyentes particulares encontrados en los compuestos descritos en el presente documento. Cuando los compuestos de la presente invención contienen funcionalidades relativamente ácidas, se pueden obtener sales de adición de bases poniendo en contacto la forma neutra de dichos compuestos con una cantidad suficiente de la base deseada, bien pura o en un disolvente inerte adecuado. Los ejemplos de sales derivadas de bases inorgánicas farmacéuticamente aceptables incluyen sales de aluminio, amonio, calcio, cobre, férrica, ferrosa, litio, magnesio, mangánica, manganosa, potasio, sodio, cinc y similares. Las sales derivadas de bases orgánicas farmacéuticamente aceptables incluyen sales de aminas primarias, secundarias y terciarias, incluyendo aminas sustituidas, aminas cíclicas, aminas de origen natural y similares, tales como arginina, betaína, cafeína, colina, W,W-dibenciletilendiamina, dietilamina, 2-dietilaminoetanol, 2-dimetilaminoetanol, etanolamina, etilendiamina, W-etilmorfolina, W-etilpiperidina, glucamina, glucosamina, histidina, hidrabamina, isopropilamina, lisina, metilglucamina, morfolina, piperazina, piperidina, resinas de poliamina, procaína, purinas, teobromina , trietilamina, trimetilamina, tripropilamina, trometamina y similares. Cuando los compuestos de la presente invención contienen funcionalidades relativamente básicas, se pueden obtener sales de adición de ácido poniendo en contacto la forma neutra de dichos compuestos con una cantidad suficiente del ácido deseado, ya sea puro o en un disolvente inerte adecuado. Los ejemplos de sales de adición de ácido farmacéuticamente aceptables incluyen las derivadas de ácidos inorgánicos como ácido clorhídrico, bromhídrico, nítrico, carbónico, monohidrogenocarbónico, fosfórico, monohidrogenofosfórico, dihidrogenofosfórico, sulfúrico, monohidrogensulfúrico, hidriódico o fosforoso y similares, así como las sales derivadas de ácidos orgánicos relativamente no tóxicos, tales como ácido acético, propiónico, isobutírico, malónico, benzoico, succínico, subérico, fumárico, mandélico, ftálico, bencenosulfónico, p-tolilsulfónico, cítrico, tartárico, metanosulfónico y similares. También se incluyen sales de aminoácidos tales como arginato y similares, y sales de ácidos orgánicos como ácidos glucurónicos o galactunóricos y similares (véase, por ejemplo, Berge, S. M. et al., "Pharmaceutical Salts", Journal of Pharmaceutical Science, 66:1-19, 1977). Ciertos compuestos específicos de la presente invención contienen funciones básicas y ácidas que permiten que los compuestos se conviertan en sales de adición de base o de ácido.
Las formas neutras de los compuestos pueden regenerarse poniendo en contacto la sal con una base o un ácido, y aislando el compuesto precursor de la manera convencional. La forma precursora del compuesto difiere de las diversas formas de sal en ciertas propiedades físicas, tales como la solubilidad en disolventes polares, pero, por lo demás, las sales son equivalentes a la forma precursora del compuesto para los fines de la presente invención.
La expresión "vehículo o excipiente farmacéuticamente aceptable" significa un vehículo o un excipiente que es útil para preparar una composición farmacéutica que, en general, es segura, no tóxica y ni biológicamente ni de otro modo indeseable, e incluye un vehículo o excipiente que es aceptable para un uso veterinario, así como un uso farmacéutico humano. Un "vehículo o excipiente farmacéuticamente aceptable", como se usa en la memoria descriptiva y en las reivindicaciones, incluye tanto uno como más de uno de dichos vehículos o excipientes.
Las expresiones "cantidad farmacéuticamente eficaz", "cantidad terapéuticamente eficaz" o "dosis terapéuticamente eficaz" se refieren a la cantidad del compuesto en cuestión que inducirá la respuesta biológica o médica de un tejido, sistema, animal o ser humano que el investigador, veterinario, médico u otro profesional clínico esté buscando. La expresión "cantidad terapéuticamente eficaz" incluye la cantidad de un compuesto que, cuando se administra, es suficiente para prevenir el desarrollo de, o aliviar hasta cierto punto, uno o más de los síntomas de la afección o del trastorno que se está tratando. La cantidad terapéuticamente eficaz variará dependiendo del compuesto, del trastorno o de la afección, y de su gravedad y de la edad, del peso, etc., del mamífero que se vaya a tratar.
"Grupo protector" se refiere a un grupo de átomos que, cuando se unen a un grupo funcional reactivo en una molécula, enmascaran, reducen o previenen la reactividad del grupo funcional. Por lo general, un grupo protector puede eliminarse selectivamente como se desee en el transcurso de una síntesis. Los ejemplos de grupos protectores se pueden encontrar en Greene y Wuts, "Protective Groups in Organic Chemistry", 3a Ed., 1999, John Wiley & Sons, NY y Harrison et al., "Compendium of Synthetic Organic Methods", Vol. 1-8, 1971-1996, John Wiley & Sons, NY. Los grupos protectores de amino representativos incluyen, pero sin limitación, formilo, acetilo, trifluoroacetilo, bencilo, benciloxicarbonilo ("CBZ"), terc-butoxicarbonilo ("Boc"), trimetilsililo ("TMS"), 2-trimetilsilil-etanosulfonilo ("TES"), grupos tritilo y tritilo sustituidos, aliloxicarbonilo, 9-fluorenilmetiloxicarbonilo ("FMOC"), nitroveratriloxicarbonilo ("NVOC") y similares. Los grupos protectores de hidroxi representativos incluyen, pero sin limitación, aquellos en donde el grupo hidroxi está acilado o alquilado tal como bencil- y tritil-éteres, así como alquiléteres, tetrahidropiraniléteres, trialquilsililéteres (por ejemplo, grupos TMS o TIPPS) y aliléteres.
La expresión "grupo protector de aldehído" se refiere a cualquier grupo protector conocido usado para enmascarar la funcionalidad aldehído. Los grupos protectores de aldehído incluyen acetales y hemiacetales. Los acetales y
hemiacetales se pueden preparar a partir de alcoholes Ci-8o dioles C2-8. Un grupo protector de aldehido puede ser un acetal cíclico de cinco o seis miembros formado por condensación del aldehido con etileno o propilenglicol. Un grupo protector de aldehído puede ser una imina o hidroxiimina. La frase "grupos protectores de aldehído" también incluye grupos de profármacos que convierten el aldehído en un profármaco, donde el aldehído se forma in vivo como el agente activo en condiciones fisiológicas tras la administración del profármaco. El grupo de profármaco también puede servir para aumentar la biodisponibilidad del aldehído. Un grupo de profármaco puede hidrolizarse in vivo al aldehído. Un grupo protector de aldehído puede ser un grupo de profármaco de tiazolidina o /V-acetiltiazolidina. Un grupo protector de aldehído puede ser un grupo de profármaco de tiazolidina desvelado en el documento US 6.355.661. Los moduladores proporcionados en el presente documento pueden condensarse con L-cisteína o un derivado de L-cisteína para formar el profármaco de aldehído protegido con tiazolidina correspondiente. La tiazolidina puede tener la fórmula:
en donde R11 se selecciona del grupo que consiste en OH, alcoxi, alcoxi sustituido, cicloalcoxi, cicloalcoxi sustituido, ariloxi, ariloxi sustituido, heteroariloxi, heteroariloxi sustituido, N(R13)2, en donde R13 es independientemente H, alquilo, alquilo sustituido, alquenilo, alquenilo sustituido, arilo, arilo sustituido, heteroarilo y heteroarilo sustituido; R12 es H o -L-R14, en donde L es carbonilo o sulfonilo; R14 se selecciona del grupo que consiste en alquilo, alquilo sustituido, arilo, arilo sustituido, heteroarilo y heteroarilo sustituido; la línea ondulada significa el punto de unión al anillo de fenilo de los moduladores alostéricos desvelados en el presente documento; y el término "sustituido" se refiere a la sustitución con uno o más sustituyentes seleccionados del grupo que consiste en COOH, CHO, oxiacilo, aciloxi, cicloaciloxi, fenol, fenoxi, piridinilo, pirrolidinilo, amino, amido, hidroxi, alcoxi, cicloalcoxi, F, CI, Br, NO2, ciano, sulfurilo y similares. También se desvelan en el presente documento moduladores que tienen un grupo protector de tiazolidina en donde R11 es alcoxi y R12 es H, o en donde R11 es OH y R12 es -C(O)alquilo, o en donde R11 es NH(heteroarilo) y R12 es -C(O)alquilo.
La expresión "anemia de células falciformes" se refiere a enfermedades mediadas por la hemoglobina falciforme (HbS) que se produce de una sola mutación puntual en la hemoglobina (Hb). Las enfermedades de las células falciformes incluyen anemia de células falciformes, enfermedad de la hemoglobina C falciforme (HbSC), talasemia beta plus falciforme (HbS/p+) y talasemia beta cero falciforme (HbS/p°).
El "sujeto" se define en el presente documento para incluir animales tales como mamíferos, incluyendo, pero sin limitación, primates (por ejemplo, seres humanos), vacas, ovejas, cabras, caballos, perros, gatos, conejos, ratas, ratones y similares. En realizaciones preferidas, el sujeto es un ser humano.
"Tautómero" se refiere a formas alternativas de una molécula que difieren en la posición de un protón, tales como tautómeros de enol-ceto y de imina-enamina, o las formas tautoméricas de grupos heteroarilo que contienen una disposición de átomos anular -N=C(H)-NH-, tales como pirazoles, imidazoles, bencimidazoles, triazoles y tetrazoles. El experto habitual en la materia reconocería que son posibles otras disposiciones de átomos anulares tautoméricas.
Los términos "tratar", "tratando", "tratamiento" y sus variaciones gramaticales, como se usan en el presente documento, incluyen retrasar parcial o totalmente, aliviar, mitigar o reducir la intensidad, progresión o empeoramiento de uno o más síntomas asociados de un trastorno o afección y/o aliviar, mitigar o impedir una o más causas de un trastorno o de una afección. Los tratamientos de acuerdo con la invención pueden aplicarse preventivamente, profiláctica, paliativa o terapéuticamente.
El símbolo > cuando se usa en relación con un sustituyente significa que el sustituyente es un sustituyente divalente unido a dos átomos diferentes a través de un solo átomo en el sustituyente.
Los compuestos que tienen la misma fórmula molecular, pero difieren en la naturaleza o secuencia de unión de sus átomos o la disposición de sus átomos en el espacio se denominan "isómeros". Los isómeros que difieren en la disposición de sus átomos en el espacio se denominan "estereoisómeros". Los términos "estereoisómero" y "estereoisómeros" se refieren a compuestos que existen en diferentes formas estereoisoméricas si poseen uno o más centros asimétricos o un doble enlace con sustitución asimétrica y, por lo tanto, pueden producirse como estereoisómeros individuales o como mezclas. Los estereoisómeros incluyen enantiómeros y diastereómeros. Los estereoisómeros que no son imágenes especulares entre sí se denominan "diastereómeros" y los que son imágenes especulares no superponibles entre sí se denominan "enantiómeros". Cuando un compuesto tiene un centro asimétrico, por ejemplo, está unido a cuatro grupos diferentes, es posible un par de enantiómeros. Un enantiómero
puede caracterizarse por la configuración absoluta de su centro asimétrico y está descrito por las reglas de
secuenciación R y S de Cahn y Prelog, o por la manera en donde la molécula gira el plano de luz polarizada, y se
designa como dextrógiro o levógiro (es decir, como isómeros (+) o (-), respectivamente). Un compuesto quiral puede
existir bien como enantiómero individual o como una mezcla de los mismos. Una mezcla que contiene proporciones
iguales de los enantiómeros se denomina "mezcla racémica". A menos que se indique lo contrario, la descripción
pretende incluir estereoisómeros individuales así como mezclas. Los métodos para la determinación de la
estereoquímica y la separación de estereoisómeros son bien conocidos en la técnica (véase la descripción del capítulo
4 de "ADVANCED ORGANIC CHEMISTRY", 4a edición, J. March, John Wiley and Sons, Nueva York, 1992) difieren
en la quiralidad de uno o más estereocentros.
Los compuestos de la presente invención también pueden contener proporciones no naturales de isótopos atómicos
en uno o más de los átomos que constituyen dichos compuestos. Por ejemplo, los compuestos pueden radiomarcarse
con isótopos tales como, por ejemplo, deuterio (2H), tritio (3H), yodo-125 (125I) o carbono-14 (14C). Se pretende que
todas las variaciones isotópicas de los compuestos de la presente invención, ya sean radiactivos o no, estén incluidas
dentro del alcance de la presente invención.
A menos que se indique lo contrario, la nomenclatura de los sustituyentes que no se definen explícitamente en el
presente documento se realiza nombrando la parte terminal de la funcionalidad seguida por la funcionalidad adyacente
hacia el punto de unión. Por ejemplo, el sustituyente "alcoxialquilo" se refiere a un grupo alquilo que está sustituido
con alcoxi, e "hidroxialquilo" se refiere a un grupo alquilo que está sustituido con hidroxi. Para ambos de estos
sustituyentes, el punto de unión está en el grupo alquilo.
Se entiende que las definiciones y las fórmulas proporcionadas en el presente documento no pretenden incluir
patrones de sustitución no admisibles (por ejemplo, metilo sustituido con 5 grupos fluoro). Dichos patrones de
sustitución no admisibles son bien conocidos por los expertos en la materia.
II. Moduladores de hemoglobina
En un grupo de realizaciones, se proporciona un compuesto de Fórmula (I):
o un tautómero o una sal farmacéuticamente aceptable del mismo, para su uso en el tratamiento del cuerpo humano
o animal,
en donde Q es piridin-2-ilo, piridin-3-ilo o piridin-4-ilo, estando dicho Q sustituido con uno a tres Ra en donde al
menos un Ra es heteroarilo opcionalmente sustituido con uno a tres Rc;
Y es CR1aR1b, en donde R1a es H o halo y R1b es H o halo, opcionalmente en donde al menos uno de R1a y R1b es
F;
X es O;
R2 , R3 , R4 y R5 se seleccionan independientemente del grupo que consiste en hidrógeno, halo, Rb, ORd , OC(O)Re ,
SRd , CN, NO2 , CO2Rd , CONRdRd , C(O)Rd , OC(O)NRdRd , NRdRd , NRdC(O)Re , NRdC(O)2Re , NRdC(O)NRdRd ,
S(O)Re , S(O)2Re , NRdS(O)2Re , S(O)2NRdRd y N3 ; o R5 es -(CH2)pR5a en donde p es 0 o 1 y R5a es OH;
R6 y R7 forman juntos oxo;
cada Ra se selecciona independientemente del grupo que consiste en halo, Rb, ORd , OC(O)Re , SRd , CN, NO2 ,
CO2Rd , CONRdRd , C(O)Rd , OC(O)NRdRd , NRdC(O)Re , NRdC(O)2Re, NRdC(O)NRdRd , S(O)Re , S(O)2Re ,
NRdS(O)2Re , S(O)2NRdRd , N3, arilo opcionalmente sustituido con de uno a tres Rc, heteroarilo opcionalmente
sustituido con de uno a tres Rc y heterocicloalquilo opcionalmente sustituido con de uno a tres Rc ;
cada Rb se selecciona independientemente del grupo que consiste en alquilo C1-8, alquenilo C2-8 y alquinilo C2-8,
cada uno opcionalmente sustituido independientemente con uno a tres halo, ORd o NRdRd ;
cada Rc se selecciona independientemente del grupo que consiste en halo, alquilo C1-8, halo-alquilo C1-8, alquenilo
C2-8, halo-alquenilo C2-8, alquinilo C2-8, halo-alquinilo C2-8, (CH2)mORf , OC(O)Rg , SRf , CN, NO2 ,
C(O)Rf , OC(O)NRfRf , (CH2)mNRfRf , NRfC(O)Rg , NRfC(O)2Rg , NRfC(O)NRfRf , S(O)Rg , S(O)2Rg , NRfS(O)2Rg , S(O)2NRfRf y N3 en donde m se selecciona del grupo que consiste en 0, 1, 2, 3, 4, 5 y 6;
cada Rd y Rf se selecciona independientemente del grupo que consiste en hidrógeno, alquilo C1-8, halo-alquilo C1-8 , alquenilo C2-8, halo-alquenilo C2-8, alquinilo C2-8 y halo-alquinilo C2-8; y
cada Re y Rg se selecciona independientemente del grupo que consiste en alquilo C1-8, halo-alquilo C1-8, alquenilo C2-8, halo-alquenilo C2-8, alquinilo C2-8 y halo-alquinilo C2-8.
En un grupo de realizaciones, Y es CH2 y R5 es H, halo, OH, CHO u OCH3.
En un grupo de realizaciones, Q está sustituido con CONRdRd , NRdRd o heteroarilo opcionalmente sustituido con uno a tres Rc En un grupo de realizaciones, Q está sustituido con heteroarilo que tiene uno o dos átomos de anillo de nitrógeno.
En un grupo de realizaciones, Q se selecciona del grupo que consiste en
En un grupo de realizaciones, al menos un Ra es heteroarilo unido a Q en el átomo del anillo adyacente al átomo del anillo que lleva Y.
En un grupo de realizaciones al menos un Ra es heteroarilo unido a dicho Q en el átomo del anillo adyacente al átomo del anillo que lleva Y. En un grupo de realizaciones al menos un Ra es heteroarilo sustituido con al menos un alquilo C1-8. En un grupo de realizaciones al menos un Ra es heteroarilo sustituido con al menos un metilo. En un grupo de realizaciones al menos un Ra es pirazolilo sustituido con al menos un alquilo C1-8. En un grupo de realizaciones al menos un Ra es pirazolilo sustituido con al menos un metilo. En un grupo de realizaciones, Ra es pirazol-5-ilo. En un grupo de realizaciones, Ra es 4-metil-pirazol-5-ilo.
En un grupo de realizaciones, Q está sustituido con al menos un Ra seleccionado del grupo que consiste en OH, NHC(O)(alquilo C1-8), N(alquilo C1-8)C(O)(alquilo C1-8), -NHC(O)2(alquilo C1-8), -N(alquilo C1-8)C(O)2(alquilo C1-8), NHS(O)2(alquilo C1-8), N(alquilo C1-8)S(O)2(alquilo C1-8) y heterocicloalquilo opcionalmente sustituido con uno a tres Rc . En algunas realizaciones el grupo heterocicloalquilo es morfolino o piperazinilo opcionalmente sustituido con alquilo C1-8, -C(O)alquilo C1-8, -C(O)2alquilo C1-8 o -S(O)2alquilo C1-8.
En un grupo de realizaciones, Q está sustituido con CN o CONRdRd .
En un grupo de realizaciones, R2 es H.
En un grupo de realizaciones, R3 es H.
En un grupo de realizaciones, R5 es H.
En un grupo de realizaciones, R4 es alcoxi C1-8.
En un grupo de realizaciones, R2 , R3 , R5 son H y es alcoxi C1-8.
En un grupo de realizaciones, R4 es metoxi.
En un grupo de realizaciones, R4 es haloalcoxi. En un grupo de realizaciones, R4 es OCHF2. En un grupo de realizaciones, R4 es OCF3.
En un grupo de realizaciones, R2 , R3 , R4 y R5 son H.
En un grupo de realizaciones, Y es CH2.
En un grupo de realizaciones, Y es CR1aR1b y al menos uno de R1a o R1b es F.
En otras realizaciones, la invención proporciona un compuesto de Fórmula (I) o un tautómero o una sal farmacéuticamente aceptable del mismo, para su uso en el tratamiento del cuerpo humano o animal, en donde: Y es CH2 ;
R4 es hidrógeno;
R5 se selecciona del grupo que consiste en hidrógeno, halo y ORd; y
Con la condición de que si R5 es ORd, entonces Ra no es oxo, óxido o halo.
En este grupo de realizaciones, R5 puede seleccionarse del grupo que consiste en hidrógeno y ORd.
En este grupo de realizaciones, R5 puede seleccionarse del grupo que consiste en hidroxi y fluoro.
En este grupo de realizaciones, R2 y R3 pueden seleccionarse independientemente del grupo que consiste en hidrógeno, Rb, ORd, OC(O)Re, CO2Rd, CONRdRd y C(O)Rd.
En este grupo de realizaciones, R2 y R3 pueden ser H.
En otras realizaciones, la invención proporciona un compuesto de acuerdo con la Fórmula (I), o un tautómero o una sal farmacéuticamente aceptable del mismo, para su uso en el tratamiento del cuerpo humano o animal, en donde: Y es CH2; y
R5 se selecciona del grupo que consiste en halo y ORd.
En este grupo de realizaciones, R4 puede ser metoxi.
En este grupo de realizaciones, Q puede ser piridin-3-ilo.
En este grupo de realizaciones, R5 puede seleccionarse del grupo que consiste en hidroxi y fluoro.
La invención proporciona además un compuesto de Fórmula (I):
o un tautómero o una sal farmacéuticamente aceptable del mismo, en donde
Q es piridin-2-ilo, piridin-3-ilo o piridin-4-ilo, estando dicho Q sustituido con uno a tres Ra en donde al menos un Ra es heteroarilo opcionalmente sustituido con uno a tres Rc ;
Y es CR1aR1b, en donde R1a es H o halo y R1b es H o halo, opcionalmente en donde al menos uno de R1a y R1b es F;
X es O;
R2 , R3 , R4 y R5 se seleccionan independientemente del grupo que consiste en hidrógeno, halo, Rb, ORd , OC(O)Re , SRd , CN, NO2 , CO2Rd , CONRdRd , C(O)Rd , OC(O)NRdRd , NRdRd , NRdC(O)Re , NRdC(O)2Re , NRdC(O)NRdRd , S(O)Re , S(O)2Re , NRdS(O)2Re , S(O)2NRdRd y N3 ; o R5 es -(CH2)pR5a en donde p es 0 o 1 y R5a es OH;
R6 y R7 forman juntos oxo;
cada Ra se selecciona independientemente del grupo que consiste en halo, Rb, ORd , OC(O)Re , SRd , CN, NO2 , CO2Rd , CONRdRd , C(O)Rd , OC(O)NRdRd , NRdC(O)Re , NRdC(O)2Re, NRdC(O)NRdRd , S(O)Re , S(O)2Re , NRdS(O)2Re , S(O)2NRdRd , N3, arilo opcionalmente sustituido con de uno a tres Rc, heteroarilo opcionalmente sustituido con de uno a tres Rc y heterocicloalquilo opcionalmente sustituido con de uno a tres Rc ;
cada Rb se selecciona independientemente del grupo que consiste en alquilo C1-8, alquenilo C2-8 y alquinilo C2-8, cada uno opcionalmente sustituido independientemente con uno a tres halo, ORd o NRdRd ;
cada Rc se selecciona independientemente del grupo que consiste en halo, alquilo C1-8, halo-alquilo C1-8, alquenilo C2-8, halo-alquenilo C2-8, alquinilo C2-8, halo-alquinilo C2-8, (CH2)mORf , OC(O)Rg , SRf , CN, NO2 , CO2Rf , CONRfRf ,
C(O)Rf , OC(O)NRfRf , (CH2)mNRfRf , NRfC(O)Rg , NRfC(O)2Rg , NRfC(O)NRfRf , S(O)Rg , S(O)2Rg , NRfS(O)2Rg , S(O)2NRfRf y N3 en donde m se selecciona del grupo que consiste en 0, 1, 2, 3, 4, 5 y 6;
cada Rd y Rf se selecciona independientemente del grupo que consiste en hidrógeno, alquilo C1-8, halo-alquilo C1-8 , alquenilo C2-8, halo-alquenilo C2-8, alquinilo C2-8 y halo-alquinilo C2-8; y
cada Re y Rg se selecciona independientemente del grupo que consiste en alquilo C1-8, halo-alquilo C1-8, alquenilo C2-8, halo-alquenilo C2-8, alquinilo C2-8 y halo-alquinilo C2-8,
con la condición de que el compuesto sea distinto de 2-((5'-metil-[2,2'-bipiridin]-5-il)metoxi)benzaldehído.
En esta realización, las identidades preferidas de los restos Q, Y, R2 , R3 , R4 , R5 , Ra , Rc y Rd son como se expone en cualquiera de las realizaciones anteriores.
En un grupo de realizaciones, un compuesto se selecciona de la Tabla 1 a continuación o un tautómero o sal farmacéuticamente aceptable del mismo.
Tabla 1
continuación
En un grupo de realizaciones, el compuesto se selecciona de:
2-hidroxi-6-((2-(1-isopropil-1H-pirazol-5-il)piridin-3-il)metoxi)benzaldehído,
2-hidroxi-6-((2-(1-(2,2,2-trifluoroetil)-1H-pirazol-5-il)piridin-3-il)metoxi)benzaldehído,
2-hidroxi-6-((2-(1-(3,3,3-trifluoroetil)-1H-pirazol-5-il)piridin-3-il)metoxi)benzaldehído,
2-fluoro-6-((2-( 1-(2,2,2-trifluoroetil)-1H-pirazol-5-il)piridin-3-il)metoxi)benzaldehído,
2-fluoro-6-((2-( 1-(3,3,3-trifluoropropil)-1 H-pirazol-5-il)piridin-3-il)metoxi)benzaldehído y
2-fluoro-6-((2-(1-isopropil-1H-pirazol-5-il)piridin-3-il)metoxi)benzaldehído
o un tautómero o una sal farmacéuticamente aceptable.
En un grupo de realizaciones, se proporciona un compuesto en cualquiera de los Ejemplos o Tablas. En otro grupo de realizaciones, se proporciona cualquier combinación de subrealizaciones como se desvelan en el presente documento incluyendo cualquier combinación de elementos desvelada en el presente documento incluyendo una selección de cualquier elemento único.
En un grupo de realizaciones, se proporciona una composición farmacéutica que comprende un compuesto de cualquiera de las realizaciones anteriores o un tautómero o sal farmacéuticamente aceptable del mismo.
Los compuestos de la presente invención pueden prepararse mediante técnicas de síntesis orgánica conocidas, incluyendo los métodos descritos con más detalle en los Ejemplos.
También se desvelan en el presente documento compuestos intermedios usados en la preparación de los compuestos desvelados en el presente documento.
También se desvelan en el presente documento métodos para preparar los compuestos desvelados en el presente documento.
Por ejemplo, el Esquema I muestra una vía sintética para la síntesis de los compuestos de Fórmula (I) donde X es O e Y es CH2. Se pone en contacto fenol 1.1 con el producto intermedio 1.2 en presencia de base en condiciones de formación de éter para dar éter 1.3, donde Lg representa un grupo saliente tal como un grupo saliente de halógeno. Por el contrario, cuando X es O e Y es CH2 , los compuestos de Fórmula (I) pueden prepararse usando los materiales de partida apropiados donde el resto OH del intermedio 1.1 se reemplaza por un grupo saliente y el grupo Lg del intermedio 1.2 se reemplaza por un grupo OH.
Esquema I
El Esquema II muestra un ejemplo de síntesis de los compuestos de Fórmula (I) donde Q es piridin-3-ilo y Ra es heteroarilo. El ácido 4.1 se reduce a alcohol 4.2 usando métodos conocidos tales como formando el anhídrido (por ejemplo, tratamiento con trietilamina y/o cloroformiato de /-butilo) seguido de la reducción con NaBH4. El alcohol 4.2 se convierte en cloruro 4.3 tal como mediante el tratamiento con cloruro de tionilo. El acoplamiento del haluro con alcohol 4.4 en condiciones de formación de éter da el precursor 4.5 que puede ser funcionalizado con una variedad a grupos heteroarilo Ra. Por ejemplo, 4.5 puede acoplarse con pirazol 4.6 en condiciones de acoplamiento organometálico conocidas (por ejemplo, Pd(PPh3)4) para dar 4.7, donde PG es un grupo protector de nitrógeno tal como un grupo protector de sililo que se puede eliminar, dando el producto 4.8.
Esquema II
Un experto en la materia reconocerá que, en ciertas realizaciones, puede ser ventajoso usar una estrategia de grupo protector. El grupo protector se puede eliminar usando métodos conocidos por los expertos en la materia.
En un grupo de realizaciones, algunos de los compuestos desvelados en el presente documento pueden usarse en general como la base libre. Como alternativa, se pueden usar algunos de los compuestos en forma de sales de adición de ácido.
Se entiende que en otro grupo de realizaciones, cualquiera de las realizaciones anteriores también se puede combinar con otras realizaciones enumeradas en el presente documento, para formar otras realizaciones de la invención. De forma similar, se entiende que, en otras realizaciones, el listado de grupos incluye realizaciones en donde uno o más de los elementos de dichos grupos no están incluidos.
III. Compos/c/ones y métodos de adm/n/strac/ón
Dependiendo del modo de administración deseado, las composiciones farmacéuticas pueden estar en forma de formas
farmacéuticas sólidas, semisólidas o líquidas, preferentemente en forma de dosificación unitaria adecuada para una sola administración de una dosis exacta. Además de una cantidad eficaz del/de los compuesto/s activo/s, las composiciones pueden contener excipientes farmacéuticamente aceptables adecuados, incluyendo adyuvantes que faciliten el procesamiento de los compuestos activos en preparaciones que se puedan usar farmacéuticamente. "Excipiente farmacéuticamente aceptable" se refiere a un excipiente o a una mezcla de excipientes que no interfiere con la eficacia de la actividad biológica del/de los compuesto/s activo/s y que no es tóxico ni indeseable para el sujeto al que se administra.
Para las composiciones sólidas, los excipientes convencionales incluyen, por ejemplo, calidades farmacéuticas de manitol, lactosa, almidón, estearato de magnesio, sacarina sódica, talco, celulosa, glucosa, sacarosa, carbonato de magnesio y similares. Se pueden preparar composiciones líquidas farmacológicamente administrables, por ejemplo, disolviendo, dispersando, etc., un compuesto activo como se describe en el presente documento y adyuvantes farmacéuticos opcionales en agua o un excipiente acuoso, tal como, por ejemplo, agua, solución salina, dextrosa acuosa y similares, para formar una solución o una suspensión. Si se desea, la composición farmacéutica que se vaya a administrar también puede contener cantidades menores de excipientes auxiliares no tóxicos tales como agentes humectantes o emulsionantes, agentes tampón de pH y similares, por ejemplo, acetato de sodio, monolaurato de sorbitán, acetato de sodio de trietanolamina, oleato de trietanolamina, etc.
Para la administración oral, la composición, en general, adoptará la forma de un comprimido o de una cápsula, o puede ser una solución acuosa o no acuosa, suspensión o jarabe. Los comprimidos y las cápsulas son formas de administración oral preferidas. Los comprimidos y las cápsulas para uso oral incluirán, en general, uno o más excipientes comúnmente usados tales como lactosa y almidón de maíz. Por lo general, también se añaden agentes lubricantes tales como estearato de magnesio. Cuando se usan suspensiones líquidas, el agente activo puede combinarse con excipientes de emulsión y suspensión. Si se desea, también se pueden añadir agentes aromatizantes, colorantes y/o edulcorantes. Otros excipientes opcionales para la incorporación en una formulación oral incluyen conservantes, agentes de suspensión, agentes espesantes y similares.
Las formulaciones inyectables se pueden preparar en formas convencionales, ya sea como soluciones o suspensiones líquidas, formas sólidas adecuadas para la solubilización o suspensión en líquido antes de la inyección, o como emulsiones o formulaciones liposomales. La formulación inyectable estéril también puede ser una solución inyectable estéril o una suspensión en un diluyente o disolvente no tóxico aceptable por vía parenteral. Entre los vehículos y disolventes aceptables que pueden emplearse están agua, solución de Ringer y solución isotónica de cloruro sódico. Además, se emplean convencionalmente aceites no volátiles, ésteres grasos o polioles estériles como disolventes o medios de suspensión.
Las composiciones farmacéuticas de la presente invención también pueden formularse en forma liofilizada para la administración parenteral. Las formulaciones liofilizadas se pueden reconstituir mediante la adición de agua u otro medio acuoso, y diluirse después más con un diluyente adecuado antes de su uso. La formulación líquida, en general, es una solución acuosa tamponada, isotónica. Los ejemplos de diluyentes adecuados son solución salina isotónica, dextrosa al 5 % en agua y solución de acetato de sodio o amonio tamponada. Pueden añadirse excipientes sólidos o líquidos farmacéuticamente aceptables para mejorar o estabilizar la composición, o para facilitar la preparación de la composición.
Por lo general, una composición farmacéutica de la presente invención se envasa en un recipiente con una etiqueta, o instrucciones, o ambas, indicando el uso de la composición farmacéutica en el tratamiento de la enfermedad indicada.
La composición farmacéutica puede contener además uno o más agentes farmacológicamente activos además de un compuesto de la presente invención.
Las formas farmacéuticas que contienen cantidades eficaces de los moduladores están dentro de los límites de la experimentación rutinaria y dentro del alcance de la invención. Una dosis terapéuticamente eficaz puede variar dependiendo de la vía de administración y de la forma de dosificación. El compuesto o los compuestos representativos de la invención son una formulación que presenta un alto índice terapéutico. El índice terapéutico es la relación de la dosis entre los efectos tóxicos y terapéuticos que puede expresarse como el cociente entre la DL50 y la DE50. La DL50 es la dosis letal para el 50 % de la población y la DE50 es la dosis terapéuticamente eficaz para el 50 % de la población. La DL50 y la DE50 se determinan mediante procedimientos farmacéuticos convencionales en cultivos de células animales o animales de experimentación. Se ha de entender que una dosis específica y un régimen de tratamiento para cualquier paciente en particular dependerá de una variedad de factores, incluyendo la actividad del compuesto específico empleado, la edad, el peso corporal, el estado de salud general, el sexo y la dieta del paciente, y al momento de la administración, la velocidad de excreción, la combinación de fármacos, el criterio del médico tratante y la gravedad de la enfermedad particular que se está tratando. La cantidad de principio/s activo/s también dependerá del compuesto en particular y del otro agente terapéutico, si está presente, en la composición.
IV. Métodos
La presente invención también proporciona un compuesto de Fórmula (I) según lo desvelado en el presente documento para su uso en un método para aumentar la oxigenación tisular, comprendiendo el método administrar a un sujeto que lo necesite una cantidad terapéuticamente eficaz de un compuesto de cualquiera de las realizaciones anteriores o un tautómero o una sal farmacéuticamente aceptable del mismo.
La presente invención también proporciona un compuesto de Fórmula (I) según lo desvelado en el presente documento para su uso en un método para tratar una afección asociada con la deficiencia de oxígeno, comprendiendo el método administrar a un sujeto que lo necesite una cantidad terapéuticamente eficaz de un compuesto de cualquiera de las realizaciones anteriores o un tautómero o una sal farmacéuticamente aceptable del mismo.
La presente invención también proporciona un compuesto de Fórmula (I) según lo desvelado en el presente documento para su uso en un método para tratar la anemia de células falciformes, el cáncer, un trastorno pulmonar, la ictus, el mal de las alturas, una úlcera, una úlcera de presión, la enfermedad de Alzheimer, el síndrome respiratorio agudo y una herida, comprendiendo el método administrar a un sujeto que lo necesite una cantidad terapéuticamente eficaz de un compuesto de cualquiera de las realizaciones anteriores o un tautómero o una sal farmacéuticamente aceptable del mismo.
V. Ejemplos
Los siguientes ejemplos se ofrecen para ilustrar, pero no para limitar, la invención reivindicada. Los compuestos que no pertenecen al alcance de las reivindicaciones se incluyen solamente con fines de referencia.
EJEMPLOS PREPARATIVOS
Los materiales de partida y los reactivos usados en la preparación de estos compuestos, en general, se pueden adquirir de proveedores comerciales tales como Aldrich Chemical Co., o se preparan mediante métodos conocidos por los expertos en la materia siguiendo procedimientos expuestos en referencias tales como "Fieser and Fieser's Reagents for Organic Synthesis"; Wiley & Sons: Nueva York, 1967-2004, volúmenes 1-22; "Rodd's Chemistry of Carbon Compounds", Elsevier Science Publishers, 1989, volúmenes 1-5 y suplementos; y "Organic Reactions", Wiley & Sons: Nueva York, 2005, Volúmenes 1-65.
Los materiales de partida y los productos intermedios de los esquemas de reacción sintéticos se pueden aislar y purificar si se desea usando técnicas convencionales, incluyendo pero sin limitación, filtración, destilación, cristalización, cromatografía y similares. Dichos materiales se pueden caracterizar usando medios convencionales, incluyendo constantes físicas y datos espectrales.
A menos que se especifique lo contrario, las reacciones descritas en el presente documento se realizan preferentemente bajo una atmósfera inerte a presión atmosférica a un intervalo de temperaturas de reacción de aproximadamente -78 °C a aproximadamente 150 °C, más preferentemente de aproximadamente 0 °C a aproximadamente 125 °C, y lo más preferente y convenientemente a aproximadamente la temperatura ambiente, por ejemplo, de aproximadamente 20 °C a aproximadamente 75 °C.
Haciendo referencia a los siguientes ejemplos, se sintetizaron los compuestos de la presente invención desvelados en el presente documento usando los métodos descritos en el presente documento, u otros métodos conocidos en la técnica.
Ejemplo 1. Preparación de 2-hidroxi-6-((2-(1-isopropil-1H-pirazol-5-il)piridin-3-il)metoxi)benzaldehído (Compuesto 43).
Se agitó una mezcla de 2,6-dihidroxibenzaldehído (1,96 g, 14,2 mmol, 2 eq.) y Cs2CO3 (7,5 g, 21,3 mmol, 3 eq.) en DMF (180 ml) a TA durante 30 min. A esta mezcla, se añadió clorhidrato de 3-(clorometil)-2-(1-isopropil-1H-pirazol-5-il)piridina (1,93 g, 7,1 mmol, 1eq.) a TA. Se siguió agitando la mezcla a TA O/N, se filtró, se concentró y se purificó sobre gel de sílice usando una mezcla de EtOAc y hexanos como eluyente, dando 2-hidroxi-6-((2-(1-isopropil-1H
pirazol- 5-il)piridin-3-il)metoxi)benzaldehído (920 mg, 37%) en forma de un aceite amarillo pálido. RMN de 1H (400 MHz, CDCls) 811,96 (s, 1H), 10,40 (s, 1H), 8,77 (dd, J = 4,8; 1,5 Hz, 1H), 8,00 (d, J = 7,8 Hz, 1H), 7,63 (d, J = 1,8 Hz, 1H), 7,49-7,34 (m, 2H), 6,59 (d, J = 8,5 Hz, 1H), 6,37 (d, J = 1,8 Hz, 1H), 6,29 (d, J= 8,2 Hz, 1H), 5,10 (s, 2H), 4,67 (sep, J= 6,7 Hz, 1H), 1,50 (d, J= 6,6 Hz, 6H). LRMS (M+H+) m/z 338,1.
Ejemplo 2. Preparación alternativa de 2-Hidroxi-6-((2-(1-isopropil-1H-pirazol-5-il)piridin-3-il)metoxi)benzaldehído
Se agitó una mezcla de 2,6-dihidroxibenzaldehído (1,58 g, 11,47 mmol, 2 eq.) y K2CO3 (2,4 g, 17,22 mmol, 3 eq.) en DMF (150 ml) a TA durante 10 min. A esta mezcla, se añadió clorhidrato de 3-(clorometil)-2-(1-isopropil-1H-pirazol-5-il)piridina (1,56 g, 5,74 mmol, 1eq.) a TA. Se calentó la mezcla a 50 °C durante 2 h, se filtró, se concentró y se purificó sobre gel de sílice usando una mezcla de EtOAc y hexanos como eluyente, dando 2-hidroxi-6-((2-(1-isopropil-1H-pirazol- 5-il)pi ridin-3-il)metoxi)benzaldehído (1,71 g, 88%) en forma de un sólido amarillo pálido. Rm N de 1H (400 MHz, CDCls) 811,96 (s, 1H), 10,40 (s, 1H), 8,77 (dd, J = 4,8, 1,5 Hz, 1H), 8,00 (d, J = 7,8 Hz, 1H), 7,63 (d, J = 1,8 Hz, 1H), 7,49-7,34 (m, 2H), 6,59 (d, J = 8,5 Hz, 1H), 6,37 (d, J = 1,8 Hz, 1H), 6,29 (d, J = 8,2 Hz, 1H), 5,10 (s, 2H), 4,67 (sep, J = 6,7 Hz, 1H), 1,50 (d, J = 6,6 Hz, 6H). LRMS (M+H+) m/z 338,1.
Ejemplo 3. Preparación de 5-((2-(1-isopropil-1 H-pirazol-5-il)piridin-3-il)metoxi)-2-metoxibenzaldehído.
Etapa 1:
A una solución de ácido 2-bromonicotínico (4,0 g, 20 mmol) y trietilamina (3,34 ml, 24 mmol, 1,2 eq.) en THF (100 ml), se añadió cloroformiato de i-butilo (3,12 ml, 24 mmol, 1,2 eq.) a 0 °C. Se agitó la mezcla a 0 °C durante 10 min y se filtró. A esta fracción filtrada, se añadió una suspensión de NaBH4 (1,52 g, 40 mmol, 2 eq.) en agua (1,0 ml) a 0 °C. Se agitó la mezcla durante 30 min, se añadió agua (3 ml), se siguió agitando durante 2 h y se concentró a sequedad. Se purificó el producto en bruto sobre gel de sílice usando una mezcla de acetato de etilo y hexanos como eluyente, dando (2-bromopiridin-3-il)metanol (3,4 g, 90 %) en forma de un sólido blanco. LRMS (M+H+) m/z 188,0.
Etapa 2
A una mezcla de (2-bromopiridin-3-il)metanol (20,0 g, 106,4 mmol, 1 eq.) e imidazol (14,5 g, 212,8 mmol, 2 eq.) en DMF (50,0 ml), se añadió TBSCl (19,2 g, 150,7 mmol, 1,2 eq.) a TA. Se agitó la mezcla a TA durante 1 h y se diluyó con una mezcla de agua (100 ml) y EtOAc (300 ml). Se lavó la capa orgánica con solución saturada de NH4Cl y salmuera, se secó sobre Na2SO4, se concentró y se purificó sobre gel de sílice usando EtOAc al 10 %/hexanos como eluyente, dando 2-bromo-3-((terc-butildimetilsililoxi)metil)piridina (30,1 g, 94 %) en forma de un aceite incoloro. LRMS (M+H+) m/z 302,0.
Etapa 3
Se purgó una mezcla de 2-bromo-3-((terc-butildimetMsililoxi)metil)piridina (30,1 g, 100,0 mmol, 1 eq.) y Zn(CN)2 (23,5 g, 200,0 mmol, 2,0 eq.) en DMF (100,0 ml) con N2 durante 5 min y se añadió Pd(PPh3)4 (5,78 g, 5,0 mmol, 0,05 eq.). Se calentó la mezcla a 120 °C durante 2 h bajo N2, se enfrió, se filtró, se concentró y se purificó sobre gel de sílice usando una mezcla de EtOAc y hexanos como eluyente, dando 3-((íerc-butildimetilsililoxi)metil)picolinonitrilo (20,4 g, 82 %) en forma de un aceite incoloro. LRMS (M+H+) m/z 249,1.
Etapa 4:
Se añadió bromuro de metilmagnesio (3 M/éter, 41,0 ml, 123,4 mmol) a una solución agitada de 3-((terc-butildimetilsililoxi)metil)picolinonitrilo (20,4 g, 82,25 mmol) en THF (100,0 ml) a -78 °C. Se calentó la mezcla de reacción hasta la TA, se inactivó con solución acuosa de ácido cítrico y se extrajo con EtOAc (50 ml) dos veces. Se lavaron las capas orgánicas combinadas con solución (sat) de NaHCO3 y salmuera, se secaron sobre Na2SO4, se concentraron y se purificaron sobre gel de sílice usando una mezcla de EtOAc/hexanos como eluyente, dando 1-(3-((tercbutildimetilsililoxi)metil)piridin-2-il)etanona (12,9 g, 59 %) en forma de un aceite incoloro. LRMS (M+H+) m/z 266,2.
Etapa 5:
Se calentó 1-(3-((terc-butildimetilsililoxi)metil)piridin-2-il)etanona (10,8 g, 40,75 mmol) en dimetoxi-W,W-dimetilmetanamina (15,0 ml) a reflujo durante 3 días. Se concentró la mezcla y se usó para la siguiente etapa sin purificación adicional. LRMS (M+H+) m/z 321,1.
Etapa 6:
A (£)-1-(3-((terc-butildimetilsililoxi)metil)piridin-2-il)-3-(dimetilamino)prop-2-en-1-ona (en bruto, 1,03 g, 3,22 mmol, 1 eq.) en EtOH (10 ml), se añadió clorhidrato de isopropilhidrazina (430 mg, 3,86 mmol, 1,2 eq.). Se calentó la mezcla a 80 °C durante 2 h, se enfrió, se añadió HCl (6 N, 0,5 ml) y se agitó O/N. Se concentró la mezcla y se diluyó con EtOAc (80 ml) y solución (sat) de NaHCO3 (10 ml). Se separaron las capas y se extrajo la capa acuosa con EtOAc tres veces. Se secaron las capas orgánicas combinadas sobre Na2SO4, se concentraron y se purificaron sobre gel de
sílice usando EtOAc como eluyente, dando (2-(1-isopropil-1 H-pirazol-5-il)piridin-3-il)metanol (500 mg, 71 %) y (2-(1-isopropil-1 W-pirazol-3-M)piridin-5-M)metanol (55 mg, 25 %) en forma de aceites de color amarillo pálido. Datos para 2-(1-isopropil-1H-pirazol-5-il)pindin-3-il)metanol: RMN de 1H (400 MHz, CDCla) 88,67 (dd, J = 4,7; 1,5 Hz, 1H), 8,0 (d, J = 7,8 Hz, 1H), 7,61 (d, J = 1,8 Hz, 1H), 7,39 (dd, J = 7,8; 4,8 Hz, 1H), 6,37 (d, J = 1,8 Hz, 1H), 4,67 (s, 2H), 4,55 (sep, J = 6,6 Hz, 1H), 1,98-2,05 (ancho, 1H), 1,47 (d, J = 6,6 Hz, 6H). LRMS (M+H+) m/z 218,1. Datos para (2-(1-isopropil-1H-pirazol-3-il)piridin-5-il)metanol: RMN de 1H (400 MHz, CDCla) 88,62 (dd, J = 4,8; 1,6 Hz, 1H), 7,72 (d, J = 7,6 Hz, 1H), 7,55 (d, J = 2,4 Hz, 1H), 7,23 (dd, J = 7,6; 4,8 Hz, 1H), 6,99 (dd, J = 8,0; 6,5 Hz, 1H), 6,07 (t, J = 7,6 Hz, 1H), 4,67 (d, J = 7,6 Hz, 2H), 4,58 (sep, J = 6,7 Hz, 1H), 1,60 (d, J = 6,7 Hz, 1H). LRMS (M+H+) m/z 218,1.
Etapa 7:
A (2-(1-iospropil-1H-pirazol-5-il)piridin-3-il)metanol (560 mg, 2,58 mmol) en DCM (10 ml), se añadió SOCh (3,0 ml) a TA. Se agitó la mezcla de reacción a TA durante 4 h y se concentró a sequedad. Se suspendió el sólido en bruto en tolueno y se concentró a sequedad. El proceso se repitió tres veces y se secó al vacío, dando clorhidrato de 3-(clorometil)-2-(1-isopropil-1H-pirazol-5-N)pindina (700 mg) en forma de un sólido blanquecino, que se usó para la siguiente etapa sin purificación adicional.
Etapa 8:
Una mezcla de 5-hidroxi-2-metoxibenzaldehído (395 mg, 2,58 mmol, 1 eq.), clorhidrato de 3-(clorometil)-2-(1-isopropil-1H-pirazol-5-il)piridina (700 mg, 2,58 mmol, 1 eq.) y K2CO3 (1,4 g, 10,32 mmol, 4 eq.) en DMF (10,0 ml) se calentó a 70 °C durante 2 h. La mezcla se enfrió, se filtró, se concentró y se purificó sobre gel de sílice usando una mezcla de EtOAc y hexanos como eluyente para dar 5-((2-(1-isopropil-1H-pirazol-5-il)piridin-3-il)metoxi)-2-metoxibenzaldehído (590 mg, 65 %) en forma de un sólido blanquecino.
Etapa 9:
5-((2-(1-isopropil-1H-pirazol-5-il)piridin-3-il)metoxi)-2-metoxibenzaldehído (980 mg, 2,78 mmol., 1 eq.) en solución de HCl (6 N, 9,2 ml, 20 eq.) se congeló a -78 °C. La mezcla se liofilizó durante la noche para dar 5-((2-(1-isopropil-1H-pirazol-5-il)piridin-3-il)metoxi)-2-metoxibenzaldehído como un sólido amarillo.
Ejemplo 4. Preparación de 2-hidroxi-6-((2-(1-(2,2,2-trifluoroetil)-1H-pirazol-5-il)piridin-3-il)metoxi)benzaldehído Etapa 1:
A (3,3,3-trifluoroetil)hidrazina (25 g, 50 % en peso en agua, 153,5 mmol, 1 eq.) en un matraz RB (250 ml) se añadió HCl (12 N, 25,6 ml, 307,0 mmol, 2 eq.). La mezcla se concentró para dar clorhidrato de (3,3,3-trifluoroetil)hidrazin a (1,07 g) como un sólido amarillo. LRMS (M+H) m/z 129,1.
Etapa 2:
A ('E)-1-(3-((terc-butildimetilsililoxi)metil)pindin-2-il)-3-(dimetilamino)prop-2-en-1-ona (bruto anteriormente, 5,91 g, 18,44 mmol, 1 eq.) en EtOH (20 ml) se añadió clorhidrato de (3,3,3-trifluoroetil)hidrazina (4,13 g, bruto anteriormente, 22,13 mmol, 1,2 eq.) a ta. La mezcla se calentó a 80 °C durante 1 h, se concentró y se diluyó con EtOAc (50 ml) y solución de NaHCOa (sat) (10 ml). Las capas se separaron y la capa acuosa se extrajo con EtOAc tres veces. Las capas orgánicas combinadas se secaron sobre Na2SO4, se concentraron y se purificaron sobre gel de sílice usando una mezcla de EtOAc y hexanos como eluyente para dar 3-((terc-butildimetilsililoxi)metil)-2-(1-(3,3,3-trifluoroetil)-1H-pirazol-5-il)piridina (5,90 g; 86 % para 2 etapas). Lr MS (M+H+) m/z 372,2.
Etapa 3:
A 3-((terc-butildimetilsililoxi)metil)-2-(1-(3,3,3-trifluoroetil)-1H-pirazol-5-il)piridina (5,91 g, 15,93 mmol) en MeOH (20 ml) se añadió HCl (4 N, 8,0 ml). La mezcla se agitó a ta durante 1 h, se concentró y se diluyó con EtOAc (50 ml) y solución de NaHCO3 (sat) (10 ml). Las capas se separaron y la capa acuosa se extrajo con EtOAc tres veces. Las capas orgánicas combinadas se secaron sobre Na2SO4 y se concentraron para dar 2-(1-(3,3,3-trifluoroetil)-1 H-pirazol-5-il)piridin-3-il)metanol (4,1 g, rendimiento cuantitativo) como líquido incoloro. RMN 1H (400 MHz, CDCb) 88,54 (dd, J = 4,7, 1,5 Hz, 1H), 7,92 (dd, J = 7,9, 1,2 Hz, 1H), 7,57 (d, J = 1,9 Hz, 1H), 7,30 (dd, J = 7,8, 4,8 Hz, 1H), 6,50 (d, J= 1,9 Hz, 1H), 5,09 (q, J = 8,6 Hz, 2H), 4,63 (s, 2H), 1,76 (s, 1H). LRMS (M+H+) m/z 272,1
Etapa 4:
A 2-(1-(2,2,2-trifluoroetil)-1H-pirazol-5-il)piridin-3-il)metanol (408 mg, 1,59 mmol) en DCM (5 ml) se añadió SOCb (1,5 ml) a ta. La mezcla de reacción se agitó a ta durante 4 h y se concentró a sequedad. El sólido bruto se suspendió en tolueno y se concentró a sequedad. El proceso se repitió tres veces y se secó al vacío para dar clorhidrato de 3(clorometil)-2-(1-(2,2,2-trifluoroetil)-1 H-pirazol-5-M)piridina (498 mg) como un sólido blanquecino, que se usó para la siguiente etapa sin purificación adicional.
Etapa 5:
Una mezcla de 2,6-dihidroxibenzaldehido (438 mg, 11,47 mmol, 2 eq.) y K2CO3 (2,4 g, 17,22 mmol, 3 eq.) en DMF (150 ml) se agitó a ta durante 10 min. A esta mezcla se añadió clorhidrato de 3-(clorometil)-2-(1-(2,2,2-trifluoroetil)-1H-pirazol-5-il)piridina (498 mg, 1,59 mmol, 1 eq.) a ta. La mezcla se calentó a 50 °C durante 2 h, se filtró, se concentró y se purificó sobre gel de sílice usando una mezcla de EtOAc y hexanos como eluyente para 2-hidroxi-6-((2-(1-(2,2,2-trifluoroetil)-1 H-pirazol-5-il)piridin-3-il)metoxi)benzaldehído (338,4 mg, 56 %) como un sólido amarillo pálido. RMN 1H (400 MHz, CDCla) 811,99 (s, 1H), 10,41 (s, 1H), 8,76 (dd, J = 4,7, 1,6 Hz, 1H), 8,01 (dd, J = 7,9, 1,4 Hz, 1H), 7,69 (d, J = 1,9 Hz, 1H), 7,49 - 7,39 (m, 2H), 6,61 (d, J = 8,5 Hz, 1H), 6,53 (d, J = 1,9 Hz, 1H), 6,32 (d, J = 8,3 Hz, 1H), 5,30 (q, J = 8,6 Hz, 2H), 5,17 (s, 2H). LRMS (M+H+) m/z 378,1.
Ejemplo 5. Preparación de 2-hidroxi-6-((2-(1-(3,3,3-trifluoropropil)-1H-pirazol-5-il)piridin-3-il)metoxi)benzaldehído (Compuesto 51).
Etapa 1:
A una mezcla de hidrazincarboxilato de bencilo (5,0 g, 30,3 mmol, 1 eq.) y DIEA (15,0 ml, 90,0 mmol, 3 eq.) en DMF (20 ml) se añadió bromuro de 3,3,3-trifluoropropilo (10,7 g, 60,6 mmol, 2 eq.) a ta. La mezcla se calentó a 80 °C durante 20 h, se concentró y se purificó sobre gel de sílice usando una mezcla de EtOAc y hexanos como eluyente a 2-(3,3,3-trifluoropropil)hidrazincarboxilato de bencilo (4,2 g; 53 %) como un sólido blanco. RMN 1H (400 MHz, CDCb) 87,33 -7,17 (m, 5H), 6,11 (s, 1H), 5,01 (s, 2H), 4,00 (s, 1H), 3,00 (dd, J= 12,2, 7,1 Hz, 2H), 2,17 (qt, J= 10,8, 7,3 Hz, 2H). LRMS (M+H+) m/z 263.1
Etapa 2:
A 2-(3,3,3-trifluoropropil)hidrazincarboxilato de bencilo (1,7 g, 6,49 mmol, 1 eq.) en una mezcla de EtOH (30 ml) se añadieron Pd/C (1,0 g) y HCl (12 N, 2,0 ml). La mezcla se cargó con H2 (60 psi), se agitó a ta durante 1 h, se filtró y se concentró para dar diclorhidrato de (3,3,3-trifluoropropil)hidrazina (1,07 g) como un sólido amarillo. LRMS (M+H) m/z 129,1.
Etapa 3:
A (E)-1-(3-((terc-but¡ld¡met¡ls¡l¡lox¡)met¡l)p¡r¡d¡n-2-¡l)-3-(d¡met¡lam¡no)prop-2-en-1-ona (bruto anteriormente, 1,73 g, 5,41 mmol, 1 eq.) en EtOH (10 ml) se añadió diclorhidrato de (3,3,3-tr¡fluoropropil)h¡drazina (1,30 g, bruto anteriormente, 6,49 mmol, 1,2 eq.) a ta. La mezcla se calentó a 80 °C durante 1 h, se concentró y se diluyó con EtOAc (50 ml) y solución de NaHCO3 (sat) (10 ml). Las capas se separaron y la capa acuosa se extrajo con EtOAc tres veces. Las capas orgánicas combinadas se secaron sobre Na2SO4, se concentraron y se purificaron sobre gel de sílice usando una mezcla de EtOAc y hexanos como eluyente para dar 3-((terc-but¡ld¡met¡ls¡l¡lox¡)met¡l)-2-(1-(3,3,3-tr¡fluoroprop¡l)-1H-pirazol-5-il)piridina (1,58 g; 76 % durante 2 etapas). RMN 1H (400 MHz, CDCla) 88,53 (dd, J = 4,7, 1,6 Hz, 1H), 7,96-7,88 (m, 1H), 7,51 (d, J = 1,9 Hz, 1H), 7,29 (dd, J = 7,9, 4,7 Hz, 1H), 6,34 (d, J= 1,9 Hz, 1H), 4,62 (s, 2H), 4,45 -4,33 (m, 2H), 2,82 - 2,61 (m, 2H), 0,85 (s, 8H), -0,00 (s, 5H). LRMS (M+H+) m/z 386,2.
Etapa 4:
A 3-((terc-but¡ld¡met¡ls¡l¡lox¡)met¡l)-2-(1-(3,3,3-tr¡fluoroprop¡l)-1H-p¡razol-5-¡l)p¡r¡d¡na (,158 g, 4,1 mmol) en MeOH (20 ml) se añadió HCl (4 N, 4,0 ml). La mezcla se agitó a ta durante 1 h, se concentró y se diluyó con EtOAc (50 ml) y solución de NaHCO3 (sat) (10 ml). Las capas se separaron y la capa acuosa se extrajo con EtOAc tres veces. Las capas orgánicas combinadas se secaron sobre Na2SO4 y se concentraron para dar (2-(1-(3,3,3-tr¡fluoroprop¡l)-1H-pirazol-5-¡l)p¡rid¡n-3-¡l)metanol (1,1 g, 99 %) como aceite incoloro. RMN 1H (400 MHz, Cd CI3) 88,64 (dd, J = 4,7, 1,7 Hz, 1H), 8,00 (dd, J = 7,9, 1,7 Hz, 1H), 7,57 (d, J= 1,9 Hz, 1H), 7,38 (dd, J = 7,9, 4,8 Hz, 1H), 6,48 (d, J= 1,9 Hz, 1H), 4,69 (s, 2H), 4,51 -4,43 (m, 2H), 2,85-2,72 (m, 2H), 2,70 (s, 1H). LRMS (M+H+) m/z 272,1.
Etapa 5:
A (2-(1-(2,2,2-tr¡fluoroprop¡l)-1H-p¡razol-5-¡l)p¡r¡d¡n-3-¡l)metanol (140 mg, 0,52 mmol) en DCM (5 ml) se añadió SOCI2 (2,0 ml) a ta. La mezcla de reacción se agitó a ta durante 4 h y se concentró a sequedad. El sólido bruto se suspendió en tolueno y se concentró a sequedad. El proceso se repitió tres veces y se secó al vacío para dar clorhidrato de 3-(clorometil)-2-(1-(2,2,2-trifluoropropil)-1 H-pirazol-5-¡l)p¡ridina (498 mg) como un sólido blanquecino, que se usó para la siguiente etapa sin purificación adicional.
Etapa 6:
Una mezcla de 2,6-dihidroxibenzaldehído (144 mg, 1,04 mmol, 2 eq.) y K2CO3 (214 mg, 1,56 mmol, 3 eq.) en DMF (20 ml) se agitó a ta durante 10 min. A esta mezcla se añadió clorhidrato de 3-(clorometil)-2-(1-(2,2,2-trifluoropropil)-1H-pirazol-5-M)piridina (168 mg, 0,52 mmol, 1 eq.) a ta. La mezcla se calentó a 50 °C durante 2 h, se filtró, se concentró y se purificó y eh RP-HPLC (Gemini 21,2 x 150 mm) usando una mezcla de CH3CN y agua como eluyente para 2-hidroxi-6-((2-(1-(3,3,3-trifluoropropil)-1H-pirazol-5-il)piridin-3-il)metoxi)benzaldehído (53,5 mg, 26 %) como un sólido blanquecino. RMN 1H (400 MHz, CDCls ) 811,98 (s, 1H), 10,38 (s, 1H), 8,77 (dd, J = 4,7, 1,6 Hz, 1H), 8,01 (dd, J = 7,9, 1,6 Hz, 1H), 7,61 (d, J = 1,9 Hz, 1H), 7,49 - 7,39 (m, 2H), 6,61 (d, J = 8,5 Hz, 1H), 6,44 (d, J = 1,9 Hz, 1H), 6,34 (d, J = 8,2 Hz, 1H), 5,15 (s, 2H), 4,56 (dd, J = 8,3, 6,7 Hz, 2H), 3,02-2,72 (m, 2H). LRMS (M+H+) m/z 392,1.
Ejemplo 6: Preparación de derivados de benzaldehído.
Los compuestos 52-54 se prepararon de acuerdo con los métodos descritos anteriormente.
2-Fluoro-6-((2-(1-(2,2,2-trifluoroetil)-1H-pirazol-5-il)piridin-3-il)metoxi)benzaldehído (Compuesto 52). RMN 1H (400 MHz, CDCla) 8 10,51 (s, 1H), 8,74 (dd, J = 4,7, 1,6 Hz, 1H), 8,21 (dd, J = 7,9, 1,6 Hz, 1H), 7,70 (d, J = 1,9 Hz, 1H), 7,54-7,41 (m, 2H), 6,82 (dd, J = 10,0, 8,6 Hz, 1H), 6,70 (d, J= 8,5 Hz, 1H), 6,56 (d, J= 1,9 Hz, 1H), 5,28 (q, J = 8,6 Hz, 2H), 5,20 (s, 2H).
2-Fluoro-6-((2-(1-(3,3,3-trifluoropropil)-1H-pirazol-5-il)piridin-3-il)metoxi)benzaldehído (Compuesto 53). RMN 1H (400 MHz, CDCls ) 8 10,50 (s, 1H), 8,75 (dd, J = 4,7, 1,6 Hz, 1H), 8,22 (dd, J = 7,9, 1,6 Hz, 1H), 7,62 (d, J = 1,9 Hz, 1H), 7,54 - 7,42 (m, 2H), 6,83 (dd, J = 10,0, 8,7 Hz, 1H), 6,73 (d, J = 8,5 Hz, 1H), 6,46 (d, J= 1,9 Hz, 1H), 5,19 (s, 2H), 4,59 - 4,51 (m, 2H), 2,96 - 2,76 (m, 2H).
2-Fluoro-6-((2-(1-isopropil-1H-pirazol-5-il)piridin-3-il)metoxi)benzaldehído (Compuesto 54). RMN 1H (400 MHz, CDCb ) 8 10,41 (s, 1H), 8,66 (dd, J = 4,7, 1,6 Hz, 1H), 8,13 (dd, J = 7,9, 1,4 Hz, 1H), 7,55 (d, J= 1,8 Hz, 1H), 7,46 - 7,29 (m, 2H), 6,72 (dd, J = 10,0, 8,7 Hz, 1H), 6,59 (d, J = 8,5 Hz, 1H), 6,29 (d, J = 1,8 Hz, 1H), 5,03 (s, 2H), 4,56 (sep, J = 6,7 Hz, 1H), 1,40 (d, J = 6,6 Hz, 6H).
ENSAYO IN VITRO
Ejemplo 7. Modulación de la afinidad hacia el oxígeno de la hemoglobina por compuestos de benzaldehído sustituidos-Procedimiento de ensayo
Se midieron las curvas de equilibrio de oxígeno (OEC) en hemoglobina S purificada (HbS) mediante el cambio en p50, la presión parcial de oxígeno a la que los sitios de unión de hemo en la muestra de HbS están saturados al 50 % con oxígeno. Se purificó la HbS mediante un procedimiento modificado (Antonini y Brunori, 1971; "Heomoglobin and Myoglobin in their Reactions with Ligands"; North Holland Publishing Company; Amsterdam, Londres) a partir de sangre obtenida de pacientes con anemia de células falciformes homocigótica a través del Centro de Hemoglobinopatía del Instituto de Investigación del Hospital Infantil de Oakland (CHORI) con la aprobación de la Junta de Revisión Institucional. Las curvas de equilibrio de oxígeno se llevaron a cabo con un analizador HEMOX, (TCS Scientific, New Hope, PA). Se diluyeron quinientos pl de HbS purificada de 250 pM en 4,5 ml de tampón HEMOX (TES 30 mM, NaCl 130 mM, KCl 5 mM, pH = 7,4) dando lugar a una concentración final de hemoglobina de 25 pM. Se añadieron los compuestos a las concentraciones finales deseadas. La mezcla se incubó durante 45 min a 37 °C y luego se transfirió a la cámara de muestra de Hemox. Se saturaron las muestras con oxígeno mediante purgado con aire comprimido durante 10 minutos. A continuación, se purgaron las muestras con nitrógeno puro y se registró la absorbancia de desoxi-Hb en función del pO2 de la solución. A continuación, se ajustaron los datos de equilibrio de oxígeno al modelo de Hill, obteniéndose valores para p50. Las curvas de desoxigenación para HbS solo (control) y HbS en presencia de compuesto se recogieron con el software TCS. El p50 para HbS purificada normalmente era de 13,8 ± 1,6. Se obtuvieron los valores de Delta p50 a partir del valor de p50 para el control menos el valor de p50 para HbS tratada con compuesto dividido entre el valor de p50 para el control. Un valor de delta p50 positivo corresponde a una curva desplazada hacia la izquierda y un valor de p50 inferior con respecto al control, lo que indica que el compuesto actúa para modular la HbS para aumentar su afinidad por el oxígeno.
Ejemplo 8. Modulación de a afinidad de hemoglobina por oxígeno por compuestos de benzaldehído sustituidos-Resultados de ensayos.
Los compuestos de la Tabla 1 que se probaron en el ensayo anterior se encontró que todos tenían valores p50 delta positivos. Delta p50 % se calcula a partir de [[p50(HbS) - p50(HbS tratado con compuesto)]/p50(HbS)] X 100.
Ejemplo 9. Ensayo de polimerización
Los ensayos de polimerización se llevan a cabo in vitro usando HbS purificada intercambiada en tampón de fosfato de potasio 1,8 M a pH 7,4. Usando un protocolo ligeramente modificado (Antonini y Brunori, 1971), se purificó la HbS mediante CRO VIRUSYS, de sangre obtenida de pacientes con anemia de células falciformes homocigótica a través del Centro de Hemoglobinopatía del Instituto de Investigación del Hospital Infantil de Oakland (CHORI) con la aprobación de la Junta de Revisión Institucional. Los compuestos se preparan en DMSO al 100 % y se añade una cantidad deseada a 50 pM de HbS purificada a una concentración final de DMSO del 0,3 %. Se ajusta la concentración final de fosfato de potasio a 1,8 M usando una combinación de solución madre de fosfato de potasio 2,5 M y agua a pH 7,4. Se incuba la mezcla de reacción durante una hora a 37 °C y después se transfiere a una placa de 24 pocillos para la desoxigenación en una caja de manipulación con guantes que contiene nitrógeno al 99,5 % y oxígeno al 0,5 %. La placa de 24 pocillos no se cubre y se incuba a 4 °C en un refrigerador de placas dentro de la caja de manipulación con guantes durante una hora y media. Se transfieren cincuenta pl de la mezcla de reacción a una placa de 96 pocillos y se mide la absorbancia a 700 nm cada minuto durante una hora a 37 °C en un lector de placas situado dentro de la caja de manipulación con guantes. Se ajusta un gráfico de la absorbancia frente al tiempo usando un ajuste sigmoideo de Boltzman y se mide el tiempo de retardo (de cero al tiempo de la Vmáx media). Para comparar y clasificar compuestos, se expresan los tiempos de retardo como el porcentaje de retardo (% DT), que se define como la diferencia en los tiempos de retardo para HbS/compuesto y HbS sola multiplicado por 100 y dividido entre el tiempo de retardo para HbS sola.
Los compuestos enumerados a continuación se han ensayado en el ensayo de polimerización. Los intervalos de actividad se definen por el número de símbolos de cruz ( f) indicados. f denota actividad > 40 % pero < 80 %; f f denota actividad > 80 %, pero < 120 %; f f f denota actividad > 120 %, pero < 140 %; f f f f denota actividad > 160 %.
Ejemplo 10. Ensayo de R/T
Se usó un ensayo de transición de estado relajado a tenso ("ensayo R/T") para determinar la capacidad de los compuestos de benzaldehído sustituidos para mantener el estado relajado (R) de afinidad por el alto contenido de oxígeno de la hemoglobina en condiciones desoxigenadas. Esta capacidad se puede expresar como un valor "delta R" (es decir, el cambio en el período de tiempo del estado R después de que la hemoglobina se trata con un compuesto, en comparación con el período sin tratamiento con el compuesto). Delta R es el % de R restante después del tratamiento con los compuestos en comparación con la ausencia de tratamiento (por ejemplo, si el % de R sin tratamiento es del 8 % mientras que con el tratamiento con un compuesto diana es del 48 % de R a 30 pM, entonces el % de R es del 40 % para ese compuesto).
Se purificó una mezcla de HbS/A de sangre obtenida de pacientes con anemia de células falciformes homocigótica a través del Centro de Hemoglobinopatía del Instituto de Investigación del Hospital Infantil de Oakland (CHORI) con la aprobación de la Junta de Revisión Institucional. Se incubó HbS/A (a una concentración final de 3 pM) durante 1 hora a 37 °C en presencia o ausencia de compuestos en tampón de fosfato de potasio de 50 pM, pH = 7,4 y 2,3-diposfoglicerato (DPG) 30 pM en placas de 96 pocillos en un volumen final de 160 pl. Se añadieron los compuestos a diferentes concentraciones (concentraciones finales de 3 pM a 100 pM). Se cubrieron las placas con una película de Mylar. Una vez completada la incubación, se retiró la cubierta de Mylar y se colocaron las placas en un lector de placas Spectrostar Nano previamente calentado a 37 °C. Cinco minutos después, se hizo fluir N2 (caudal = 20 l/min) a través del espectrofotómetro. Se tomaron mediciones espectroscópicas (de 300 nm a 700 nm) cada 5 min durante 2 horas. El análisis de los datos se realizó mediante el uso de regresión lineal de los datos recuperados para todas las longitudes de onda.
En la siguiente Tabla 2, se enumeran los valores de delta R en donde indica un delta R entre 0 y 30, + indica un delta R de entre 30 y 50 y ++ indica un delta R de 50 o superior. A menos que se indique lo contrario, los compuestos de la Tabla 2 se ensayaron a 9 pM.
Tabla 2. Delta R
Ejemplo 11. Ensayo de sangre entera
Se realizaron las curvas de equilibrio de oxígeno (OEC) de sangre entera antes y después del tratamiento con diferentes concentraciones de compuestos de benzaldehído sustituido de la siguiente manera usando un analizador HEMOX (TCS Scientific, New Hope, PA). Se obtuvieron muestras de sangre de pacientes con anemia de células falciformes homocigótica a través del Centro de Hemoglobinopatía del Instituto de Investigación de1Hospital Infantil de Oakland (CHORI) con la aprobación de la Junta de Revisión Institucional. El hematocrito se ajustó al 20 % usando plasma autólogo, y las muestras de sangre se incubaron durante 1 hora a 37 °C en ausencia o presencia de compuestos. Se añadieron 100 pl de estas muestras a 5 ml de tampón de Hemox (TES 30 mM, NaCl 130 mM, KCl 5 mM, pH= 7,4) a 37 °C y después se transfirieron a la cámara de muestras de Hemox. Las muestras se saturaron con oxígeno mediante purgado con aire comprimido durante 10 minutos. A continuación, se purgaron las muestras con nitrógeno puro y se registraron las respectivas absorbancias de oxi y desoxi-Hb en función de la solución de pO2. A continuación, se ajustaron los datos de equilibrio de oxígeno al modelo de Hill, Obteniéndose valores para p50. Las curvas de desoxigenación tanto para la sangre completa sola (control) como para la sangre entera en presencia del compuesto se recogieron con el software TCS.
En la siguiente Tabla 3, se enumeran los valores del % de delta p50 en donde indica un % de delta p50 de entre 0 y 29, + indica un % de delta p50 de entre 30 y 50, y ++ indica un % de delta p50 de 50 o superior. Los compuestos de la Tabla 3 se ensayaron a 1.000 pM. Un valor de delta p50 positivo corresponde a una curva desplazada hacia la izquierda y un valor de p50 inferior con respecto al control, lo que indica que el compuesto actúa para modular la HbS para aumentar su afinidad por el oxígeno.
T l . V l r l l r l n l l n r
Ejemplo 12. Estudio farmacocinético del Compuesto 43 (sal de HCl)
ESTUDIO IV
Se trataron ratas Sprague Dawley con 7,8 mg/kg del Compuesto 43 disuelto en DMA al 10 %: PEG al 50 %: vitron al aprox. 16 %. En los puntos temporales especificados, se extrajeron 10 pl de sangre entera/plasma de ratas y se trataron con ml pl de tampón a pH 3 500 pl de ACN/IS, luego se agitaron durante 1 hora, y se centrifugaron durante 10 minutos a 57 rpm a 4 °C. Se transfirió el sobrenadante a una placa filtrante y se centrifugó a 2.000 rpm durante 1 minuto a 4 °C. A continuación, se analizaron las muestras mediante la monitorización por LC-MS/MS del aldehído precursor. Las concentraciones en sangre y plasma se muestran en la Tabla 4. Los parámetros P/K clave se muestran en la Tabla 5.
Tabla 4
continuación
Tabla 5
ESTUDIO ORAL
Se trataron ratas SD por sonda con 44 mg/kg y 100 mg/kg disueltos en DMA al 10 %: PEG al 90 %. En los puntos de tiempo especificados, se extrajo sangre y se trató como se ha descrito anteriormente en el estudio IV. Los parámetros clave se muestran en la Tabla 5.
Tabla 6
Cualquier conflicto entre cualquier referencia citada en el presente documento y la enseñanza de la presente memoria descriptiva se resolverá a favor de esta última. Del mismo modo, cualquier conflicto entre una definición reconocida por la técnica de un término o de una expresión, y una definición del término o de la expresión proporcionada en la presente memoria descriptiva se ha de resolver a favor de esta última.
Claims (18)
1. Un compuesto de Fórmula (I):
o un tautómero o una sal farmacéuticamente aceptable del mismo, para su uso en el tratamiento del cuerpo humano o animal,
en donde Q es piridin-2-ilo, piridin-3-ilo o piridin-4-ilo, estando dicho Q sustituido con uno a tres Ra en donde al menos un Ra es heteroarilo opcionalmente sustituido con uno a tres Rc;
Y es CR1aR1b, en donde R1a es H o halo y R1b es H o halo, opcionalmente en donde al menos uno de R1a y R1b es F;
X es O;
R2 , R3 , R4 y R5 se seleccionan independientemente del grupo que consiste en hidrógeno, halo, Rb, ORd , OC(O)Re , SRd , CN, NO2 , CO2Rd , CONRdRd , C(O)Rd , OC(O)NRdRd , NRdRd , NRdC(O)Re , NRdC(O)2Re , NRdC(O)NRdRd , S(O)Re , S(O)2Re , NRdS(O)2Re , S(O)2NRdRd y N3 ; o R5 es -(CH2)pR5a en donde p es 0 o 1 y R5a es OH;
R6 y R7 forman juntos oxo;
cada Ra se selecciona independientemente del grupo que consiste en halo, Rb, ORd , OC(O)Re , SRd , CN, NO2 , CO2Rd , CONRdRd , C(O)Rd , OC(O)NRdRd , NRdC(O)Re , NRdC(O)2Re, NRdC(O)NRdRd , S(O)Re , S(O)2Re , NRdS(O)2Re , S(O)2NRdRd , N3, arilo opcionalmente sustituido con de uno a tres Rc, heteroarilo opcionalmente sustituido con de uno a tres Rc y heterocicloalquilo opcionalmente sustituido con de uno a tres Rc ;
cada Rb se selecciona independientemente del grupo que consiste en alquilo C1-8, alquenilo C2-8 y alquinilo C2-8, cada uno opcionalmente sustituido independientemente con uno a tres halo, ORd o NRdRd ;
cada Rc se selecciona independientemente del grupo que consiste en halo, alquilo C1-8, halo-alquilo C1-8, alquenilo C2-8, halo-alquenilo C2-8, alquinilo C2-8, halo-alquinilo C2-8, (CH2)mORf , OC(O)Rg , SRf , CN, NO2 , CO2Rf , CONRfRf , C(O)Rf , OC(O)NRfRf , (CH2)mNRfRf , NRfC(O)Rg , NRfC(O)2Rg , NRfC(O)NRfRf , S(O)Rg , S(O)2Rg , NRfS(O)2Rg , S(O)2NRfRf y N3 en donde m se selecciona del grupo que consiste en 0, 1, 2, 3, 4, 5 y 6;
cada Rd y Rf se selecciona independientemente del grupo que consiste en hidrógeno, alquilo C1-8, halo-alquilo C1-8 , alquenilo C2-8, halo-alquenilo C2-8, alquinilo C2-8 y halo-alquinilo C2-8; y
cada Re y Rg se selecciona independientemente del grupo que consiste en alquilo C1-8, halo-alquilo C1-8, alquenilo C2-8, halo-alquenilo C2-8, alquinilo C2-8 y halo-alquinilo C2-8.
2. El compuesto para su uso de acuerdo con la reivindicación 1, o un tautómero o una sal farmacéuticamente aceptable del mismo, en donde Q está sustituido con uno a tres Ra en donde al menos un Ra es heteroarilo opcionalmente sustituido con de uno a tres Rc y en donde dicho resto heteroarilo está unido a Q en el átomo del anillo adyacente al átomo del anillo que lleva Y.
3. El compuesto para su uso de acuerdo con la reivindicación 1 o 2, o un tautómero o una sal farmacéuticamente aceptable del mismo, en donde Q está sustituido con heteroarilo que tiene uno a dos átomos del anillo de nitrógeno.
4. El compuesto para su uso de acuerdo con la reivindicación 1, o un tautómero o una sal farmacéuticamente aceptable del mismo, en donde
Q es piridin-3-ilo sustituido con uno a tres Ra ;
Y es CR1aR1b, donde R1a es H y R1b es H;
R2 , R3 , R4 y R5 se seleccionan independientemente del grupo que consiste en hidrógeno, halo y ORd ;
al menos un Ra es heteroarilo opcionalmente sustituido con uno a tres Rc ; y
cada Rc se selecciona independientemente del grupo que consiste en alquilo C1-4 y haloalquilo C1-4.
5. El compuesto para su uso de acuerdo con la reivindicación 4, o un tautómero o una sal farmacéuticamente aceptable del mismo, en donde Q está sustituido con heteroarilo que tiene uno o dos átomos del anillo de nitrógeno.
6. El compuesto para su uso de acuerdo con la reivindicación 4 o 5, o un tautómero o una sal farmacéuticamente aceptable del mismo, en donde al menos un Ra está unido a Q en el átomo del anillo adyacente al átomo del anillo que lleva Y.
7. El compuesto para su uso de acuerdo con cualquiera de las reivindicaciones 4-6, o un tautómero o una sal
farmacéuticamente aceptable del mismo, en donde al menos un Ra es heteroarilo sustituido con al menos un alquilo Cl - 4.
8. Un compuesto para su uso de acuerdo con la reivindicación 7, o un tautómero o una sal farmacéuticamente aceptable del mismo, en donde al menos un Ra es pirazolilo sustituido con un alquilo C1-4.
9. El compuesto para su uso de acuerdo con la reivindicación 4 seleccionado del grupo que consiste en:
2-hidroxi-6-((2-(1-(2,2,2-trifluoroetil)-1H-pirazol-5-il)piridin-3-il)metoxi)benzaldehído,
2-hidroxi-6-((2-(1-(3,3,3-trifluoroetil)-1H-pirazol-5-il)piridin-3-il)metoxi)benzaldehído,
2-fluoro-6-((2-(1-(2,2,2-trifluoroetil)-1H-pirazol-5-il)piridin-3-il)metoxi)benzaldehído,
2-fluoro-6-((2-(1-(3,3,3-trifluoropropil)-1H-pirazol-5-il)piridin-3-il)metoxi)benzaldehído y
2-fluoro-6-((2-(1-isopropil-1H-pirazol-5-il)piridin-3-il)metoxi)benzaldehído,
o un tautómero o una sal farmacéuticamente aceptable del mismo.
10. El compuesto para su uso de acuerdo con la reivindicación 1, o un tautómero o una sal farmacéuticamente aceptable del mismo, en donde dicho heteroarilo se selecciona del grupo que consiste en un grupo imidazopiridinilo, un grupo pirrolopiridinilo, un grupo pirazolopiridinilo, un grupo triazolopiridinilo, un grupo pirazolopirazinilo, un grupo piridinilo, un grupo pirazinilo, un grupo oxazolilo, un grupo imidazolilo, un grupo triazolilo, un grupo tetrazolilo, un grupo pirazolilo, un grupo quinolinilo, un grupo isoquinolinilo, un grupo indazolilo, un grupo benzooxazolilo, un grupo naftiridinilo y un grupo quinoxalinilo.
11. Un compuesto para su uso de acuerdo con cualquiera de las reivindicaciones 1-10, o un tautómero o una sal farmacéuticamente aceptable del mismo, que es para su uso en un método para aumentar la oxigenación tisular.
12. Un compuesto para su uso de acuerdo con cualquiera de las reivindicaciones 1-10, o un tautómero o una sal farmacéuticamente aceptable del mismo, que es para su uso en un método para tratar una afección asociada a la deficiencia de oxígeno.
13. El compuesto para su uso de acuerdo con la reivindicación 12, o un tautómero o una sal farmacéuticamente aceptable del mismo, en donde la afección se selecciona del grupo que consiste en cáncer, un trastorno pulmonar, la ictus, el mal de las alturas, una úlcera, una úlcera de presión, la enfermedad de Alzheimer, el síndrome respiratorio agudo y una herida.
14. Un compuesto para su uso de acuerdo con cualquiera de las reivindicaciones 1-10, o un tautómero o una sal farmacéuticamente aceptable del mismo, que es para su uso en un método para tratar enfermedad de células falciformes.
15. El compuesto para su uso de acuerdo con la reivindicación 13, o un tautómero o una sal farmacéuticamente aceptable del mismo, en donde la afección es un trastorno pulmonar.
16. Un compuesto de Fórmula (I):
Q es piridin-2-ilo, piridin-3-ilo o piridin-4-ilo, estando dicho Q sustituido con uno a tres Ra en donde al menos un Ra es heteroarilo opcionalmente sustituido con uno a tres Rc ;
Y es CR1aR1b, en donde R1a es H o halo y R1b es H o halo, opcionalmente en donde al menos uno de R1a y R1b es F;
X es O;
R2 , R3 , R4 y R5 se seleccionan independientemente del grupo que consiste en hidrógeno, halo, Rb, ORd , OC(O)Re , SRd , CN, NO2 , CO2Rd , CONRdRd , C(O)Rd , OC(O)NRdRd , NRdRd , NRdC(O)Re , NRdC(O)2Re , NRdC(O)NRdRd , S(O)Re , S(O)2Re , NRdS(O)2Re , S(O)2NRdRd y N3 ; o R5 es -(CH2)pR5a en donde p es 0 o 1 y R5a es OH;
R6 y R7 forman juntos oxo;
cada Ra se selecciona independientemente del grupo que consiste en halo, Rb, ORd , OC(O)Re , SRd , CN, NO2 , CO2Rd , CONRdRd , C(O)Rd , OC(O)NRdRd , NRdC(O)Re , NRdC(O)2Re, NRdC(O)NRdRd , S(O)Re , S(O)2Re , NRdS(O)2Re , S(O)2NRdRd , N3, arilo opcionalmente sustituido con de uno a tres Rc, heteroarilo opcionalmente sustituido con de uno a tres Rc y heterocicloalquilo opcionalmente sustituido con de uno a tres Rc ;
cada Rb se selecciona independientemente del grupo que consiste en alquilo C1-8, alquenilo C2-8 y alquinilo C2-8, cada uno opcionalmente sustituido independientemente con uno a tres halo, ORd o NRdRd ;
cada Rc se selecciona independientemente del grupo que consiste en halo, alquilo C1-8, halo-alquilo C1-8, alquenilo C2-8, halo-alquenilo C2-8, alquinilo C2-8, halo-alquinilo C2-8, (CH2)mORf , OC(O)Rg , SRf , CN, NO2 , C(O)Rf , OC(O)NRfRf , (CH2)mNRfRf , NRfC(O)Rg , NRfC(O)2Rg , NRfC(O)NRfRf , S(O)Rg , S(O)2Rg , NRfS(O)2Rg , S(O)2NRfRf y N3 en donde m se selecciona del grupo que consiste en 0, 1, 2, 3, 4, 5 y 6;
cada Rd y Rf se selecciona independientemente del grupo que consiste en hidrógeno, alquilo C1-8, halo-alquilo C1-8 , alquenilo C2-8, halo-alquenilo C2-8, alquinilo C2-8 y halo-alquinilo C2-8; y
cada Re y Rg se selecciona independientemente del grupo que consiste en alquilo C1-8, halo-alquilo C1-8, alquenilo C2-8, halo-alquenilo C2-8, alquinilo C2-8 y halo-alquinilo C2-8,
con la condición de que el compuesto sea distinto de 2-((5'-metil-[2,2'-bipiridin]-il)metoxi)benzaldehído.
17. Un compuesto de acuerdo con la reivindicación 16, o un tautómero o una sal farmacéuticamente aceptable del mismo, en donde Q, Y, R2 , R3 , R4 , R5 , Ra y Rc son como se define en una cualquiera de las reivindicaciones 2-10.
18. Una composición farmacéutica que comprende un compuesto de acuerdo con la reivindicación 16 o 17, o un tautómero o una sal farmacéuticamente aceptable del mismo, y un excipiente farmacéuticamente aceptable.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201161581053P | 2011-12-28 | 2011-12-28 | |
| US201261661320P | 2012-06-18 | 2012-06-18 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2811129T3 true ES2811129T3 (es) | 2021-03-10 |
Family
ID=48698669
Family Applications (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES12862525.8T Active ES2643403T3 (es) | 2011-12-28 | 2012-12-28 | Compuestos de benzaldehído sustituidos y métodos para su uso en el aumento de la oxigenación tisular |
| ES16194019T Active ES2811129T3 (es) | 2011-12-28 | 2012-12-28 | Compuestos de benzaldehído sustituidos y métodos para su uso en el aumento de la oxigenación tisular |
| ES20167746T Active ES2963218T3 (es) | 2011-12-28 | 2012-12-28 | Productos intermedios para obtener compuestos de benzaldehído sustituidos y métodos para su uso en el aumento de la oxigenación tisular |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES12862525.8T Active ES2643403T3 (es) | 2011-12-28 | 2012-12-28 | Compuestos de benzaldehído sustituidos y métodos para su uso en el aumento de la oxigenación tisular |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES20167746T Active ES2963218T3 (es) | 2011-12-28 | 2012-12-28 | Productos intermedios para obtener compuestos de benzaldehído sustituidos y métodos para su uso en el aumento de la oxigenación tisular |
Country Status (33)
| Country | Link |
|---|---|
| US (8) | US9018210B2 (es) |
| EP (4) | EP4289813A3 (es) |
| JP (7) | JP6242810B2 (es) |
| CN (2) | CN107176953B (es) |
| AP (1) | AP2014007805A0 (es) |
| AU (6) | AU2012362236B2 (es) |
| BR (1) | BR112014016165B1 (es) |
| CA (2) | CA2860323C (es) |
| CL (1) | CL2014001762A1 (es) |
| CO (1) | CO7101245A2 (es) |
| CY (3) | CY1119575T1 (es) |
| DK (3) | DK3141542T3 (es) |
| ES (3) | ES2643403T3 (es) |
| FI (1) | FI3738434T3 (es) |
| FR (1) | FR22C1042I2 (es) |
| GT (1) | GT201400136A (es) |
| HR (2) | HRP20171665T1 (es) |
| HU (4) | HUE050189T2 (es) |
| IL (4) | IL292366A (es) |
| LT (3) | LT2797416T (es) |
| LU (1) | LUC00276I2 (es) |
| MX (4) | MX372804B (es) |
| NI (1) | NI201400070A (es) |
| NL (1) | NL301191I2 (es) |
| NO (1) | NO2022031I1 (es) |
| PE (3) | PE20181519A1 (es) |
| PL (3) | PL3738434T3 (es) |
| PT (3) | PT3738434T (es) |
| RS (2) | RS56388B1 (es) |
| SG (4) | SG11201403645VA (es) |
| SI (3) | SI3141542T1 (es) |
| SM (2) | SMT201700483T1 (es) |
| WO (1) | WO2013102142A1 (es) |
Families Citing this family (63)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| HK1203412A1 (en) | 2011-12-28 | 2015-10-30 | Global Blood Therapeutics, Inc. | Substituted heteroaryl aldehyde compounds and methods for their use in increasing tissue oxygenation |
| ES2643403T3 (es) * | 2011-12-28 | 2017-11-22 | Global Blood Therapeutics, Inc. | Compuestos de benzaldehído sustituidos y métodos para su uso en el aumento de la oxigenación tisular |
| US9802900B2 (en) | 2013-03-15 | 2017-10-31 | Global Blood Therapeutics, Inc. | Bicyclic heteroaryl compounds and uses thereof for the modulation of hemoglobin |
| MX379235B (es) | 2013-03-15 | 2025-03-11 | Global Blood Therapeutics Inc | Compuestos y sus usos para modular la hemoglobina. |
| US10266551B2 (en) | 2013-03-15 | 2019-04-23 | Global Blood Therapeutics, Inc. | Compounds and uses thereof for the modulation of hemoglobin |
| US9604999B2 (en) | 2013-03-15 | 2017-03-28 | Global Blood Therapeutics, Inc. | Compounds and uses thereof for the modulation of hemoglobin |
| US9422279B2 (en) | 2013-03-15 | 2016-08-23 | Global Blood Therapeutics, Inc. | Compounds and uses thereof for the modulation of hemoglobin |
| EP2968295A1 (en) * | 2013-03-15 | 2016-01-20 | Global Blood Therapeutics, Inc. | Compositions and methods for the modulation of hemoglobin (s) |
| CN105073728A (zh) | 2013-03-15 | 2015-11-18 | 全球血液疗法股份有限公司 | 化合物及其用于调节血红蛋白的用途 |
| US10100043B2 (en) | 2013-03-15 | 2018-10-16 | Global Blood Therapeutics, Inc. | Substituted aldehyde compounds and methods for their use in increasing tissue oxygenation |
| US9458139B2 (en) | 2013-03-15 | 2016-10-04 | Global Blood Therapeutics, Inc. | Compounds and uses thereof for the modulation of hemoglobin |
| WO2014150261A1 (en) * | 2013-03-15 | 2014-09-25 | Global Blood Therapeutics, Inc. | Compounds and uses thereof for the modulaton of hemoglobin |
| US20140274961A1 (en) * | 2013-03-15 | 2014-09-18 | Global Blood Therapeutics, Inc. | Compounds and uses thereof for the modulation of hemoglobin |
| US8952171B2 (en) | 2013-03-15 | 2015-02-10 | Global Blood Therapeutics, Inc. | Compounds and uses thereof for the modulation of hemoglobin |
| WO2014150289A1 (en) * | 2013-03-15 | 2014-09-25 | Global Blood Therapeutics, Inc. | Compounds and uses thereof for the modulation of hemoglobin |
| WO2014150258A1 (en) * | 2013-03-15 | 2014-09-25 | Global Blood Therapeutics, Inc. | Compounds and uses thereof for the modulation of hemoglobin |
| WO2015027067A2 (en) * | 2013-08-23 | 2015-02-26 | Virginia Commonwealth University | Ester nitrates derivatives of aromatic aldehydes with multiple pharmalogic properties to treat sickle cell disease |
| WO2015031284A1 (en) * | 2013-08-26 | 2015-03-05 | Global Blood Therapeutics, Inc. | Formulations comprising wetting agents and compounds for the modulation of hemoglobin (s) |
| US20160207904A1 (en) * | 2013-08-27 | 2016-07-21 | Global Blood Therapeutics, Inc. | Crystalline 2-hydroxy-6-((2-(1-isopropyl-1h-pyrazol-5-yl)pyridin-3-yl)methoxy)benzaldehyde ansolvate salts |
| WO2015031285A1 (en) * | 2013-08-27 | 2015-03-05 | Global Blood Therapeutics, Inc. | Crystalline 2-hydroxy-6-((2-(1-isopropyl-1h-pyrazol-5-yl)pyridin-3-yl)methoxy)benzaldehyde ansolvate salts |
| EA201992707A1 (ru) | 2013-11-18 | 2020-06-30 | Глобал Блад Терапьютикс, Инк. | Соединения и их применения для модуляции гемоглобина |
| WO2015116061A1 (en) * | 2014-01-29 | 2015-08-06 | Global Blood Therapeutics, Inc. | 1:1 adducts of sickle hemoglobin |
| US9248199B2 (en) | 2014-01-29 | 2016-02-02 | Global Blood Therapeutics, Inc. | 1:1 adducts of sickle hemoglobin |
| CN114181195A (zh) * | 2014-02-07 | 2022-03-15 | 全球血液疗法股份有限公司 | 一种化合物的结晶多晶型物 |
| WO2016043849A2 (en) * | 2014-07-24 | 2016-03-24 | Global Blood Therapeutics, Inc. | Compounds for treating acute respiratory distress syndrome or a negative effect thereof |
| MA41841A (fr) | 2015-03-30 | 2018-02-06 | Global Blood Therapeutics Inc | Composés aldéhyde pour le traitement de la fibrose pulmonaire, de l'hypoxie, et de maladies auto-immunes et des tissus conjonctifs |
| WO2016161572A1 (en) * | 2015-04-08 | 2016-10-13 | Merck Sharp & Dohme Corp. | TrkA KINASE INHIBITORS, COMPOSITIONS AND METHODS THEREOF |
| AU2016254049A1 (en) | 2015-04-30 | 2017-11-02 | Musc Foundation For Research Development | Oxindole compounds and pharmaceutical compositions thereof |
| SG11201804647TA (en) | 2015-12-04 | 2018-06-28 | Global Blood Therapeutics Inc | Dosing regimens for 2-hydroxy-6-((2-(1-isopropyl-1h-pyrazol-5-yl)pyridin-3-yl)methoxy)benzaldehyde |
| TWI663160B (zh) * | 2016-05-12 | 2019-06-21 | 全球血液治療公司 | 用於合成2-羥基-6-((2-(1-異丙基-1h-吡唑-5-基)-吡啶-3-基)甲氧基)苯甲醛之方法 |
| EP3472150A1 (en) | 2016-06-17 | 2019-04-24 | Fronthera U.S. Pharmaceuticals LLC | Hemoglobin modifier compounds and uses thereof |
| TW202332423A (zh) | 2016-10-12 | 2023-08-16 | 美商全球血液治療公司 | 包含2-羥基-6-((2-(1-異丙基-1h-吡唑-5-基)吡啶-3-基)甲氧基)-苯甲醛之片劑 |
| ES2747768T3 (es) | 2017-03-20 | 2020-03-11 | Forma Therapeutics Inc | Composiciones de pirrolopirrol como activadores de quinasa de piruvato (PKR) |
| WO2018211474A1 (en) | 2017-05-19 | 2018-11-22 | Trudell Medical International | Positive expiratory pressure device |
| CN108276405A (zh) * | 2018-03-12 | 2018-07-13 | 南安市创培电子科技有限公司 | 一种医药中间体咪唑并[1,2-a]吡啶-2-羧酸乙酯的合成工艺 |
| WO2019182938A1 (en) * | 2018-03-22 | 2019-09-26 | Virginia Commonwealth University | Aromatic aldehydes with sustained and enhanced in vitro and in vivo pharmacologic activity to treat sickle cell disease |
| USD874064S1 (en) | 2018-05-18 | 2020-01-28 | Trudell Medical International | Mask |
| USD903097S1 (en) | 2018-05-18 | 2020-11-24 | Trudell Medical International | Mask |
| US12053458B2 (en) | 2018-09-19 | 2024-08-06 | Novo Nordisk Health Care Ag | Treating sickle cell disease with a pyruvate kinase R activating compound |
| ES2989438T3 (es) | 2018-09-19 | 2024-11-26 | Novo Nordisk Healthcare Ag | Activación de la piruvato cinasa R |
| US11014884B2 (en) | 2018-10-01 | 2021-05-25 | Global Blood Therapeutics, Inc. | Modulators of hemoglobin |
| USD893806S1 (en) | 2018-11-09 | 2020-08-18 | Trudell Medical Internationl | Mask and shroud |
| PT3880654T (pt) | 2018-11-19 | 2022-04-08 | Global Blood Therapeutics Inc | Compostos de 2-formil-3-hidroxifeniloximetil capazes de modular hemoglobina |
| CU20210044A7 (es) * | 2018-11-29 | 2022-01-13 | Pfizer | Pirazoles como moduladores de hemoglobina |
| CN113365992B (zh) * | 2018-12-21 | 2024-05-28 | 晶体制药独资有限公司 | 用于沃塞洛托的制备的方法和中间体 |
| CN113272290A (zh) | 2018-12-21 | 2021-08-17 | 晶体制药独资有限公司 | 用于沃塞洛托合成的方法和中间体 |
| US12479816B2 (en) | 2019-02-08 | 2025-11-25 | University of Pittsburgh—of the Commonwealth System of Higher Education | 20-HETE formation inhibitors |
| EP3693364A1 (en) | 2019-02-11 | 2020-08-12 | Sandoz Ag | Crystalline salts of a hemoglobin s allosteric modulator |
| US20220378756A1 (en) | 2019-09-19 | 2022-12-01 | Forma Therapeutics, Inc. | Activating pyruvate kinase r |
| BR112022009522A2 (pt) | 2019-11-19 | 2022-08-16 | Global Blood Therapeutics Inc | Métodos de administração de voxelotor |
| GB202002560D0 (en) | 2020-02-24 | 2020-04-08 | Johnson Matthey Plc | Crystalline forms of voxelotor, and processes for the preparation thereof |
| EP3888750A1 (en) | 2020-04-02 | 2021-10-06 | Sandoz AG | Crystalline form of voxelotor |
| IT202000025135A1 (it) | 2020-10-23 | 2022-04-23 | Dipharma Francis Srl | Procedimento per la preparazione di un farmaco per il trattamento dell’anemia falciforme |
| IT202000009970A1 (it) * | 2020-05-05 | 2021-11-05 | Dipharma Francis Srl | Procedimento per la preparazione di un farmaco per il trattamento dell’anemia falciforme |
| WO2021224280A1 (en) * | 2020-05-05 | 2021-11-11 | Dipharma Francis S.R.L. | Synthesis of a sickle cell disease agent and intermediates thereof |
| WO2022013052A1 (en) | 2020-07-15 | 2022-01-20 | Sandoz Ag | Compounds comprising voxelotor and 2,5-dihydroxybenzoic acid and crystal forms |
| CN112047924B (zh) * | 2020-10-10 | 2023-04-18 | 山东汇海医药化工有限公司 | 一种沃克洛多的制备方法 |
| TW202233589A (zh) | 2020-11-06 | 2022-09-01 | 美商全球血液治療公司 | 2-羥基-6-((2-(1-異丙基-1h-吡唑-5-基)吡啶-3-基)甲氧基)苯甲醛之製備方法 |
| CN116710441A (zh) * | 2020-11-06 | 2023-09-05 | 全球血液疗法公司 | 制备2-羟基-6-((2-(1-异丙基-1h-吡唑-5-基)吡啶-3-基)甲氧基)苯甲醛的方法 |
| US12128035B2 (en) | 2021-03-19 | 2024-10-29 | Novo Nordisk Health Care Ag | Activating pyruvate kinase R |
| EP4426300A2 (en) | 2021-11-05 | 2024-09-11 | Global Blood Therapeutics, Inc. | Methods of administering voxelotor |
| WO2024102304A1 (en) * | 2022-11-07 | 2024-05-16 | Virginia Commonwealth University | Benzaldehyde compounds with direct polymer destabilizing effects to treat sickle cell disease |
| WO2025106877A1 (en) * | 2023-11-16 | 2025-05-22 | The J. David Gladstone Institutes, A Testamentary Trust Established Under The Will Of J. David Gladstone | Inhaled hypoxia and small molecule forms of hypoxia as novel anticancer agents |
Family Cites Families (257)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| BE558821A (es) | 1956-02-13 | 1900-01-01 | ||
| BE787580A (fr) | 1971-08-13 | 1973-02-14 | Hoechst Ag | Procede de preparation de derives du furanne |
| BE787576A (fr) | 1971-08-13 | 1973-02-14 | Hoechst Ag | Derives de benzofuranne et leur utilisation comme azureurs optiques |
| GB1409865A (en) | 1973-02-13 | 1975-10-15 | Science Union & Cie | Dihydropyridines derivatives their preparation and pharmaceu tical compositions containing them |
| GB1593417A (en) | 1976-12-22 | 1981-07-15 | Squibb & Sons Inc | Carbocyclic-fused pyrazolopyridine derivatives |
| US4062858A (en) | 1976-12-22 | 1977-12-13 | E. R. Squibb & Sons, Inc. | Derivatives of 5,6-dihydrobenzo[5,6]cyclohepta[1,2-b]pyrazolo[4,3-e]pyridin-11(1H)-ones and 11(1H)-imines |
| DE2964427D1 (en) | 1978-10-04 | 1983-02-03 | Ciba Geigy Ag | Process for the preparation of furanyl-benzazoles |
| DE2853765A1 (de) | 1978-12-13 | 1980-06-26 | Bayer Ag | Verfahren zur herstellung von benzimidazolylbenzofuranen |
| DE2904829A1 (de) | 1979-02-08 | 1980-08-14 | Bayer Ag | Verfahren zur herstellung von benzimidazolylbenzofuran |
| ZW14480A1 (en) * | 1979-06-29 | 1982-03-17 | Wellcome Found | Pharmaceutical ethers preparation use and intermediates therefore and their preparation |
| IT1193786B (it) | 1980-12-18 | 1988-08-24 | Wellcome Found | Composti eterei dotati di attivita' mitigatrice delle emoglobinopatie intermedi e procedimento per la loro preparazione |
| JPS5929667A (ja) | 1982-08-13 | 1984-02-16 | Otsuka Pharmaceut Co Ltd | カルボスチリル誘導体および強心剤 |
| US4478834A (en) | 1983-02-11 | 1984-10-23 | Usv Pharmaceutical Corporation | Dihydropyridines and their use in the treatment of asthma |
| GB8402740D0 (en) | 1984-02-02 | 1984-03-07 | Scras | Furo-(3 4-c)-pyridine derivatives |
| JPS6140236A (ja) | 1984-08-02 | 1986-02-26 | Yamanouchi Pharmaceut Co Ltd | ハイドロキノン誘導体 |
| DE3431004A1 (de) | 1984-08-23 | 1986-03-06 | Hoechst Ag, 6230 Frankfurt | Neue 3-pyridylverbindungen und verfahren zu ihrer herstellung |
| DD226590A1 (de) | 1984-09-07 | 1985-08-28 | Univ Leipzig | Mittel zur phagenhemmung in mikrobiellen produktionsprozessen |
| GB8603475D0 (en) | 1986-02-12 | 1986-03-19 | Glaxo Group Ltd | Chemical compounds |
| DK111387A (da) | 1986-03-05 | 1987-09-06 | Otsuka Pharma Co Ltd | Carbostyrilderivater og salte deraf, laegemiddel indeholdende saadanne derivater samt fremgangsmaade til fremstilling af derivaterne |
| GB8628262D0 (en) * | 1986-11-26 | 1986-12-31 | Fujisawa Pharmaceutical Co | Imidazopyridine compounds |
| US4831041A (en) * | 1986-11-26 | 1989-05-16 | Fujisawa Pharmaceutical Co., Ltd. | Imidazopyridine compounds and processes for preparation thereof |
| AU598093B2 (en) | 1987-02-07 | 1990-06-14 | Wellcome Foundation Limited, The | Pyridopyrimidines, methods for their preparation and pharmaceutical formulations thereof |
| DD258226A1 (de) | 1987-03-05 | 1988-07-13 | Fahlberg List Veb | Verfahren zur herstellung von aroxymethylchinoxalinen |
| JPH07121937B2 (ja) | 1987-03-18 | 1995-12-25 | 大塚製薬株式会社 | カルボスチリル誘導体 |
| JPS63258463A (ja) | 1987-04-14 | 1988-10-25 | Kumiai Chem Ind Co Ltd | 2−フエノキシピリミジン誘導体及び除草剤 |
| GB8711802D0 (en) | 1987-05-19 | 1987-06-24 | Fujisawa Pharmaceutical Co | Dithioacetal compounds |
| GB8718940D0 (en) | 1987-08-11 | 1987-09-16 | Glaxo Group Ltd | Chemical compounds |
| US4920131A (en) | 1987-11-03 | 1990-04-24 | Rorer Pharmaceutical Corp. | Quinoline derivatives and use thereof as antagonists of leukotriene D4 |
| JP2650038B2 (ja) | 1988-01-27 | 1997-09-03 | サントリー株式会社 | ピロリチジン化合物およびその用途 |
| EP0336369A1 (en) | 1988-04-04 | 1989-10-11 | E.R. Squibb & Sons, Inc. | 3-Acylamino-1-[[[(substituted sulfonyl)amino]carbonyl]amino]2-azetidinones |
| US4952574A (en) | 1988-09-26 | 1990-08-28 | Riker Laboratories, Inc. | Antiarrhythmic substituted N-(2-piperidylmethyl)benzamides |
| IE81170B1 (en) * | 1988-10-21 | 2000-05-31 | Zeneca Ltd | Pyridine derivatives |
| DD276480A1 (de) | 1988-10-26 | 1990-02-28 | Fahlberg List Veb | Verfahren zur herstellung von naphtho/2,1-b/fur-2-ylchinoxalinen |
| DD276479A1 (de) | 1988-10-26 | 1990-02-28 | Fahlberg List Veb | Verfahren zur herstellung von benzo/b/fur-2-ylchinoxalinen |
| US5236917A (en) | 1989-05-04 | 1993-08-17 | Sterling Winthrop Inc. | Saccharin derivatives useful as proteolytic enzyme inhibitors and compositions and method of use thereof |
| IT1230859B (it) | 1989-06-05 | 1991-11-08 | Corvi Camillo Spa | 2 alchinilfenoli sostituiti ad azione anti infiammatoria, procedimento per la loro preparazione e composizioni farmaceutiche che li contengono. |
| EP0453210A3 (en) | 1990-04-19 | 1993-01-13 | Imperial Chemical Industries Plc | Pyridine derivatives |
| IL98526A0 (en) | 1990-06-18 | 1992-07-15 | Merck & Co Inc | Pyridones,processes for their preparation and pharmaceutical compositions containing them |
| CN1034934C (zh) | 1990-06-19 | 1997-05-21 | 明治制果株式会社 | 血管紧张素ii拮抗性吡啶衍生物的制备方法 |
| NL9001752A (nl) | 1990-08-02 | 1992-03-02 | Cedona Pharm Bv | Nieuwe 1,4-dihydropyridinederivaten. |
| IL99731A0 (en) | 1990-10-18 | 1992-08-18 | Merck & Co Inc | Hydroxylated pyridine derivatives,their preparation and pharmaceutical compositions containing them |
| JPH05301872A (ja) | 1992-04-23 | 1993-11-16 | Kumiai Chem Ind Co Ltd | ピコリン酸誘導体及び除草剤 |
| US5403816A (en) | 1990-10-25 | 1995-04-04 | Kumiai Chemical Industry Co., Ltd. | Picolinic acid derivative and herbicidal composition |
| WO1992013841A1 (de) | 1991-02-08 | 1992-08-20 | Byk Gulden Lomberg Chemische Fabrik Gmbh | Komplexbildner |
| JPH0641118A (ja) | 1991-05-31 | 1994-02-15 | Kumiai Chem Ind Co Ltd | ピコリン酸誘導体及び除草剤 |
| US5185251A (en) | 1991-06-07 | 1993-02-09 | Merck & Co., Inc. | Microbial transformation of a substituted pyridinone using actinoplanacete sp. MA 6559 |
| JP2600644B2 (ja) | 1991-08-16 | 1997-04-16 | 藤沢薬品工業株式会社 | チアゾリルベンゾフラン誘導体 |
| FR2680512B1 (fr) | 1991-08-20 | 1995-01-20 | Adir | Nouveaux derives de 2,4-thiazolidinedione, leur procede de preparation et les compositions pharmaceutiques qui les contiennent. |
| US5202243A (en) | 1991-10-04 | 1993-04-13 | Merck & Co., Inc. | Method of hydroxylating 3-[2-(benzoxazol-2-yl)ethyl]-5-ethyl-6-methyl-2-(1H)-pyridinone by incubation with liver slices |
| GB9203798D0 (en) * | 1992-02-21 | 1992-04-08 | Fujisawa Pharmaceutical Co | Quinolylbenzofuran derivatives,processes for preparation thereof and pharmaceutical composition comprising the same |
| WO1994001406A1 (de) | 1992-07-01 | 1994-01-20 | Byk Gulden Lomberg Chemische Fabrik Gmbh | Kontrastmittel für die mr diagnostik |
| US5290941A (en) | 1992-10-14 | 1994-03-01 | Merck & Co., Inc. | Facile condensation of methylbenzoxazoles with aromatic aldehydes |
| US5521202A (en) | 1993-04-07 | 1996-05-28 | Taiho Pharmaceutical Co., Ltd. | Thiazolidine derivatives and pharmaceutical compositions containing the same |
| DE4318550A1 (de) | 1993-06-04 | 1994-12-08 | Boehringer Mannheim Gmbh | Aryliden-4-oxo-2-thioxo-3- thiazolidincarbonsäuren, Verfahren zu ihrer Herstellung und diese Verbindungen enthaltende Arzneimittel |
| US5534529A (en) | 1993-06-30 | 1996-07-09 | Sankyo Company, Limited | Substituted aromatic amides and ureas derivatives having anti-hypercholesteremic activity, their preparation and their therapeutic uses |
| JPH0725882A (ja) | 1993-07-07 | 1995-01-27 | Res Dev Corp Of Japan | アクロメリン酸bおよびeを製造するための中間体と、その製造方法 |
| ATE180780T1 (de) * | 1993-08-05 | 1999-06-15 | Hoechst Marion Roussel Inc | 2-(piperidin-4-yl, pyridin-4-yl und tetrahydropyridin-4-yl)-benzofuran-7-carbamat derivate, ihre herstellung und verwendung als acetylcholinesterase inhibitoren |
| EP0640609A1 (en) | 1993-08-24 | 1995-03-01 | Ono Pharmaceutical Co., Ltd. | Fused phenol derivatives having inhibitory activity on TXA2 synthetase, and 5-lipoxygenase and scavenging activity on oxygen species |
| US5880131A (en) | 1993-10-20 | 1999-03-09 | Enzon, Inc. | High molecular weight polymer-based prodrugs |
| US5965566A (en) | 1993-10-20 | 1999-10-12 | Enzon, Inc. | High molecular weight polymer-based prodrugs |
| US5840900A (en) | 1993-10-20 | 1998-11-24 | Enzon, Inc. | High molecular weight polymer-based prodrugs |
| US5605976A (en) | 1995-05-15 | 1997-02-25 | Enzon, Inc. | Method of preparing polyalkylene oxide carboxylic acids |
| WO1995014015A1 (en) | 1993-11-19 | 1995-05-26 | Ciba-Geigy Ag | Benzothiophene derivatives possessing a methoxyimino substituent as microbicides |
| EP0658559A1 (de) * | 1993-12-14 | 1995-06-21 | Chemisch Pharmazeutische Forschungsgesellschaft m.b.H. | Thienothiazinderivate, Verfahren zu ihrer Herstellung und ihre Verwendung als 5-dipoxygenase und Cyclooxygenaseinhibitoren |
| JPH09508906A (ja) | 1994-02-14 | 1997-09-09 | メレル ファーマスーティカルズ インコーポレーテッド | エンケファリナーゼ及びaceの阻害剤として有用な新規なメルカプトアセチルアミド1,3,4,5−テトラヒドロベンゾ[c]アゼピン−3−オンジスルフィド誘導体類 |
| GB9420557D0 (en) | 1994-10-12 | 1994-11-30 | Zeneca Ltd | Aromatic compounds |
| DE4442050A1 (de) | 1994-11-25 | 1996-05-30 | Hoechst Ag | Heterospiroverbindungen und ihre Verwendung als Elektrolumineszenzmaterialien |
| US5650408A (en) | 1995-06-07 | 1997-07-22 | Karanewsky; Donald S. | Thiazolo benzazepine containing dual action inhibitors |
| TW434240B (en) | 1995-06-20 | 2001-05-16 | Zeneca Ltd | Aromatic compounds, preparation thereof and pharmaceutical composition comprising same |
| JP3895404B2 (ja) | 1996-05-17 | 2007-03-22 | 興和株式会社 | カルコン誘導体及びこれを含有する医薬 |
| CN1221417A (zh) | 1996-07-26 | 1999-06-30 | 雷迪博士研究基金会 | 具有抗糖尿病、降低血脂、抗高血压性能的噻唑烷二酮化合物,其制备方法及其药物组合物 |
| EP0922028A1 (en) | 1996-08-26 | 1999-06-16 | Genetics Institute, Inc. | Inhibitors of phospholipase enzymes |
| US6630496B1 (en) | 1996-08-26 | 2003-10-07 | Genetics Institute Llc | Inhibitors of phospholipase enzymes |
| AU4136197A (en) | 1996-09-09 | 1998-03-26 | Kyowa Hakko Kogyo Co. Ltd. | Pyrrolocarbazole derivatives |
| ID21482A (id) | 1996-11-12 | 1999-06-17 | Novartis Ag | Turunan-turunan pirazol yang berguna sebagai herbisida |
| US6043389A (en) | 1997-03-11 | 2000-03-28 | Mor Research Applications, Ltd. | Hydroxy and ether-containing oxyalkylene esters and uses thereof |
| US5760232A (en) | 1997-06-16 | 1998-06-02 | Schering Corporation | Synthesis of intermediates useful in preparing bromo-substituted tricyclic compounds |
| US6214817B1 (en) | 1997-06-20 | 2001-04-10 | Monsanto Company | Substituted pyridino pentaazamacrocyle complexes having superoxide dismutase activity |
| US6011042A (en) | 1997-10-10 | 2000-01-04 | Enzon, Inc. | Acyl polymeric derivatives of aromatic hydroxyl-containing compounds |
| US6111107A (en) | 1997-11-20 | 2000-08-29 | Enzon, Inc. | High yield method for stereoselective acylation of tertiary alcohols |
| DE19882892T1 (de) | 1997-12-12 | 2001-02-22 | Euro Celtique Sa | Herstellung von 3-substituierten Adeninen und Imidazopyridinen |
| EP1062216A1 (en) | 1998-02-25 | 2000-12-27 | Genetics Institute, Inc. | Inhibitors of phospholipase a2 |
| EP1064289A1 (en) | 1998-03-18 | 2001-01-03 | Ariad Pharmaceuticals, Inc. | Heterocyclic signal transduction inhibitors, compositions containing them |
| US6214879B1 (en) | 1998-03-24 | 2001-04-10 | Virginia Commonwealth University | Allosteric inhibitors of pyruvate kinase |
| US6153655A (en) | 1998-04-17 | 2000-11-28 | Enzon, Inc. | Terminally-branched polymeric linkers and polymeric conjugates containing the same |
| GB9810860D0 (en) | 1998-05-20 | 1998-07-22 | Hoechst Schering Agrevo Gmbh | Substituted pyridine and pyrimidines, processes for their preparation and their use as pesticides |
| US6232320B1 (en) | 1998-06-04 | 2001-05-15 | Abbott Laboratories | Cell adhesion-inhibiting antiinflammatory compounds |
| CA2333770A1 (en) | 1998-06-04 | 1999-12-09 | Abbott Laboratories | Cell adhesion-inhibiting antinflammatory compounds |
| GB9818627D0 (en) | 1998-08-26 | 1998-10-21 | Glaxo Group Ltd | Improvements in dva vaccination |
| GB9823871D0 (en) | 1998-10-30 | 1998-12-23 | Pharmacia & Upjohn Spa | 2-Amino-thiazole derivatives, process for their preparation, and their use as antitumour agents |
| US20030060425A1 (en) | 1998-11-24 | 2003-03-27 | Ahlem Clarence N. | Immune modulation method using steroid compounds |
| YU41801A (sh) | 1998-12-14 | 2003-12-31 | F. Hofman - La Roche Ag. | Derivati fenilglicina |
| US6544980B2 (en) | 1998-12-31 | 2003-04-08 | Aventis Pharmaceuticals Inc. | N-carboxymethyl substituted benzolactams as inhibitors of matrix metalloproteinase |
| WO2000040564A1 (en) | 1998-12-31 | 2000-07-13 | Aventis Pharmaceuticals Inc. | N-carboxymethyl substituted benzolactams as inhibitors of matrix metalloproteinase |
| US6472349B1 (en) | 1999-03-31 | 2002-10-29 | Basf Aktiengesellschaft | Pyridine-2,3-dicarboxylic acid diamides |
| US6251927B1 (en) | 1999-04-20 | 2001-06-26 | Medinox, Inc. | Methods for treatment of sickle cell anemia |
| CA2370245A1 (en) | 1999-05-14 | 2000-11-23 | Boehringer Ingelheim Pharmaceuticals, Inc. | Enzyme-activated anti-tumor prodrug compounds |
| US6184228B1 (en) | 1999-05-25 | 2001-02-06 | Anadys Pharmaceuticals, Inc. | Anti-sickling agents: selection methods and effective compounds |
| WO2000075145A1 (en) | 1999-06-03 | 2000-12-14 | Abbott Laboratories | Cell adhesion-inhibiting antiinflammatory compounds |
| AUPQ105499A0 (en) | 1999-06-18 | 1999-07-08 | Biota Scientific Management Pty Ltd | Antiviral agents |
| EA005027B1 (ru) | 1999-06-28 | 2004-10-28 | Янссен Фармацевтика Н.В. | Ингибиторы репликации респираторно-синцитиального вируса |
| ES2252063T3 (es) | 1999-09-28 | 2006-05-16 | Eisai Co., Ltd. | Compuesto de quinuclidina y medicamento que comprende el compuesto como principio activo. |
| KR100788970B1 (ko) | 1999-11-05 | 2007-12-27 | 에미스페어 테크놀로지스, 인코포레이티드 | 활성제 전달용 페녹시 카르복시산 화합물 및 조성물 |
| AUPQ407699A0 (en) | 1999-11-16 | 1999-12-09 | Fujisawa Pharmaceutical Co., Ltd. | Aminoalcohol derivatives |
| AU2001230537A1 (en) | 2000-02-01 | 2001-08-14 | Daiichi Pharmaceutical Co., Ltd. | Pyridoxazine derivatives |
| US6506755B2 (en) | 2000-02-03 | 2003-01-14 | Hoffmann-La Roche Inc. | Thiazolidinecarboxyl acids |
| AUPQ585000A0 (en) | 2000-02-28 | 2000-03-16 | Fujisawa Pharmaceutical Co., Ltd. | Aminoalcohol derivatives |
| CN1311198A (zh) | 2000-03-02 | 2001-09-05 | 上海博德基因开发有限公司 | 一种新的多肽——网格蛋白轻链37和编码这种多肽的多核苷酸 |
| AU2001245823A1 (en) | 2000-03-17 | 2001-10-03 | Corixa Corporation | Novel amphipathic aldehydes and their use as adjuvants and immunoeffectors |
| AUPQ841300A0 (en) | 2000-06-27 | 2000-07-20 | Fujisawa Pharmaceutical Co., Ltd. | New aminoalcohol derivatives |
| PT1303490E (pt) | 2000-07-14 | 2008-09-04 | Hoffmann La Roche | Óxidos de aminas como pró-fármacos de antagonistas dosreceptores nk1, de derivados de 4-fenil-piridina |
| US20020142995A1 (en) * | 2000-08-01 | 2002-10-03 | Nicolau Yves Claude | Ammonium salts of hemoglobin allosteric effectors, and uses thereof |
| US6653313B2 (en) | 2000-08-10 | 2003-11-25 | Warner-Lambert Company Llc | 1,4-dihydropyridine compounds as bradykinin antagonists |
| JP4272338B2 (ja) | 2000-09-22 | 2009-06-03 | バイエル アクチェンゲゼルシャフト | ピリジン誘導体 |
| AUPR034000A0 (en) | 2000-09-25 | 2000-10-19 | Fujisawa Pharmaceutical Co., Ltd. | Aminoalcohol derivatives |
| BR0115400A (pt) * | 2000-11-20 | 2003-09-30 | Biovitrum Ab | Compostos de piperazinilpirazina atuando como agonistas ou antagonistas do receptor 5ht-2 de serotonina |
| JPWO2002051849A1 (ja) | 2000-12-26 | 2004-04-22 | 第一製薬株式会社 | Cdk4活性阻害剤 |
| CA2433573A1 (en) | 2000-12-28 | 2002-07-11 | Takeda Chemical Industries, Ltd. | Alkanoic acid derivatives, process for their production and use thereof |
| US20030022923A1 (en) | 2001-03-01 | 2003-01-30 | Medinox, Inc. | Methods for treatment of sickle cell anemia |
| US6627646B2 (en) | 2001-07-17 | 2003-09-30 | Sepracor Inc. | Norastemizole polymorphs |
| US20030073712A1 (en) * | 2001-07-23 | 2003-04-17 | Bing Wang | Cytoprotective compounds, pharmaceutical and cosmetic formulations, and methods |
| JP2003075970A (ja) | 2001-08-31 | 2003-03-12 | Konica Corp | ハロゲン化銀カラー写真感光材料、カラー写真感光材料、その画像形成方法及びデジタル画像情報作製方法 |
| KR100467313B1 (ko) | 2001-11-22 | 2005-01-24 | 한국전자통신연구원 | 적색 유기 전기발광 화합물 및 그 제조 방법과 전기발광소자 |
| US20030187026A1 (en) | 2001-12-13 | 2003-10-02 | Qun Li | Kinase inhibitors |
| CN1596240A (zh) | 2001-12-19 | 2005-03-16 | 阿特罗吉尼克斯公司 | 查耳酮衍生物及其治疗疾病的用途 |
| US20030190333A1 (en) | 2002-02-04 | 2003-10-09 | Corixa Corporation | Immunostimulant compositions comprising aminoalkyl glucosaminide phosphates and saponins |
| EP1542704A1 (en) | 2002-04-18 | 2005-06-22 | Stephen H. Embury | Method and composition for preventing pain in sickle cell patients |
| US6608076B1 (en) | 2002-05-16 | 2003-08-19 | Enzon, Inc. | Camptothecin derivatives and polymeric conjugates thereof |
| GB0212785D0 (en) | 2002-05-31 | 2002-07-10 | Glaxo Group Ltd | Compounds |
| MXPA05001544A (es) * | 2002-08-08 | 2005-04-19 | Smithkline Beecham Corp | Compuestos de tiofeno. |
| EP1548008A4 (en) | 2002-08-23 | 2008-08-06 | Kirin Pharma Kk | COMPOUND WITH TGF-BETA-HEMMENDER EFFECT AND THIS MEDICAL COMPOSITION CONTAINING |
| US7368578B2 (en) | 2002-09-10 | 2008-05-06 | Takeda Pharmaceutical Company Limited | Five-membered heterocyclic compounds |
| CA2507545C (en) | 2002-12-04 | 2011-06-21 | Virginia Commonwealth University | Use of furfural derivatives as anti-sickling agents |
| US20040181075A1 (en) | 2002-12-19 | 2004-09-16 | Weingarten M. David | Process of making chalcone derivatives |
| AU2003289440A1 (en) | 2002-12-25 | 2004-07-22 | Kissei Pharmaceutical Co., Ltd. | Nitrogen-containing heterocycic derivatives, medicinal compositions containing the same and medicinal use thereof |
| EP1596818B1 (de) | 2003-02-24 | 2006-05-03 | Randolph Dr. Dr. Prof. Riemschneider | Kosmetische zusammensetzung mit whitening-effekt, verfahren zu ihrer herstellung und ihre verwendung |
| US20040186077A1 (en) | 2003-03-17 | 2004-09-23 | Medicure International Inc. | Novel heteroaryl phosphonates as cardioprotective agents |
| ZA200507752B (en) | 2003-03-28 | 2007-01-31 | Threshold Pharmaceuticals Inc | Compositions and methods for treating cancer |
| EP1613613B1 (en) | 2003-04-11 | 2021-06-02 | Genzyme Corporation | Cxcr4 chemokine receptor binding compounds |
| BRPI0411255A (pt) | 2003-06-12 | 2006-08-01 | Novo Nordisk As | composto, composição farmacêutica, uso de um composto, métodos de tratar um distúrbio de um paciente, e, processo para a preparação de um composto |
| US7259164B2 (en) * | 2003-08-11 | 2007-08-21 | Cgi Pharmaceuticals, Inc. | Certain substituted imidazo[1,2-a]pyrazines, as modulators of kinase activity |
| US7411083B2 (en) | 2003-09-25 | 2008-08-12 | Wyeth | Substituted acetic acid derivatives |
| CN1875002B (zh) | 2003-11-05 | 2011-08-03 | 霍夫曼-拉罗奇有限公司 | 作为ppar激动剂的苯基衍生物 |
| JP2007513082A (ja) * | 2003-11-10 | 2007-05-24 | シエーリング アクチエンゲゼルシャフト | Ccr−5アンタゴニストとして有用なベンジルエーテルアミン化合物 |
| KR20120039065A (ko) | 2003-12-02 | 2012-04-24 | 셀진 코포레이션 | 혈색소병증 및 빈혈의 치료 및 관리를 위한 방법및 조성물 |
| US7378439B2 (en) | 2004-01-20 | 2008-05-27 | Usv, Ltd. | Process for the preparation of 4-(2-dipropylaminoethyl)-1,3-dihydro-2H-indol-2-one hydrochloride |
| JP2007519735A (ja) | 2004-01-30 | 2007-07-19 | メルク エンド カムパニー インコーポレーテッド | Hivインテグラーゼ阻害剤として有用であるn−ベンジル−3,4−ジヒドロキシピリジン−2−カルボキサミド及びn−ベンジル−2,3−ジヒドロキシピリジン−4−カルボキサミド化合物 |
| GB0403038D0 (en) | 2004-02-11 | 2004-03-17 | Novartis Ag | Organic compounds |
| WO2005087766A1 (en) | 2004-03-09 | 2005-09-22 | Istituto Di Ricerche Di Biologia Molecolare P Angeletti Spa | Hiv integrase inhibitors |
| WO2005086951A2 (en) | 2004-03-10 | 2005-09-22 | Threshold Pharmaceuticals, Inc. | Hypoxia-activated anti-cancer agents |
| DE102004015226B3 (de) | 2004-03-24 | 2005-08-25 | Siemens Ag | Verfahren zum Plasmareinigen eines Werkstücks und zu dessen Durchführung geeignete Vorrichtung |
| JP2007534691A (ja) | 2004-04-22 | 2007-11-29 | アロス・セラピューティクス・インコーポレーテッド | アロステリックヘモグロビン修飾体の組成物および前記組成物の製造法 |
| TW200606133A (en) * | 2004-06-30 | 2006-02-16 | Sankyo Co | Substituted benzene compounds |
| TW200606129A (en) | 2004-07-26 | 2006-02-16 | Chugai Pharmaceutical Co Ltd | Novel cyclohexane derivative, its prodrug, its salt and diabetic therapeutic agent containing the same |
| GB0420722D0 (en) | 2004-09-17 | 2004-10-20 | Addex Pharmaceuticals Sa | Novel allosteric modulators |
| WO2006050598A1 (en) | 2004-10-28 | 2006-05-18 | Medicure International Inc. | Dual antiplatelet/anticoagulant pyridoxine analogs |
| EP1831170A4 (en) | 2004-12-14 | 2009-10-14 | Astrazeneca Ab | SUBSTITUTED AMINOPYRIDINES AND THEIR USE |
| ATE516026T1 (de) | 2005-02-21 | 2011-07-15 | Shionogi & Co | Bicyclisches carbamoylpyridonderivat mit hiv- integrase-hemmender wirkung |
| KR101304981B1 (ko) | 2005-03-19 | 2013-09-06 | (주)아모레퍼시픽 | 바닐로이드 수용체 길항물질로서의 신규 화합물, 이의이성체 또는 이의 약학적으로 허용가능한 염, 및 이를함유하는 약학 조성물 |
| JP4874958B2 (ja) | 2005-03-30 | 2012-02-15 | エーザイ・アール・アンド・ディー・マネジメント株式会社 | ピリジン誘導体を含有する抗真菌剤 |
| GB0506677D0 (en) | 2005-04-01 | 2005-05-11 | Btg Int Ltd | Iron modulators |
| US8129385B2 (en) | 2005-04-28 | 2012-03-06 | Shionogi & Co., Ltd. | Substituted 5-hydroxy-3,4,6,9,9a, 10-hexanhydro-2h-1-oxa04a,8a-diaza-anthracene-6,10-dioness |
| DE102005025989A1 (de) | 2005-06-07 | 2007-01-11 | Bayer Cropscience Ag | Carboxamide |
| JP2006342115A (ja) | 2005-06-10 | 2006-12-21 | Shionogi & Co Ltd | Hivインテグラーゼ阻害活性を有する多環性化合物 |
| EP1910290A2 (en) | 2005-06-30 | 2008-04-16 | Prosidion Limited | Gpcr agonists |
| CN100562514C (zh) | 2005-07-22 | 2009-11-25 | 中国科学院上海药物研究所 | 一类取代丙酰胺衍生物、其制备方法和用途 |
| GB0516270D0 (en) | 2005-08-08 | 2005-09-14 | Glaxo Group Ltd | Novel compounds |
| WO2007047204A1 (en) | 2005-10-11 | 2007-04-26 | University Of Pittsburgh | Isotopically-labeled benzofuran compounds as imagingagents foramyloidogenic proteins |
| EA200801144A1 (ru) | 2005-10-27 | 2008-10-30 | Сионоги Энд Ко., Лтд. | Полициклическое карбамоилпиридоновое производное, обладающее ингибиторной активностью в отношении интегразы вич |
| JP2009515997A (ja) * | 2005-11-18 | 2009-04-16 | タケダ サン ディエゴ インコーポレイテッド | グルコキナーゼ活性剤 |
| WO2007084914A2 (en) | 2006-01-17 | 2007-07-26 | Neurocrine Biosciences, Inc. | Phenoxy-substituted pyrimidines as adenosine receptor antagonists |
| WO2007095495A2 (en) * | 2006-02-13 | 2007-08-23 | Pharmacopeia, Inc. | Benzodiazepine gcnf modulators for stem cell modulation |
| RU2318818C1 (ru) | 2006-04-12 | 2008-03-10 | Общество С Ограниченной Ответственностью "Исследовательский Институт Химического Разнообразия" | Азагетероциклы, комбинаторная библиотека, фокусированная библиотека, фармацевтическая композиция и способ получения (варианты) |
| GB0614586D0 (en) | 2006-07-22 | 2006-08-30 | Pliva Istrazivacki Inst D O O | Pharmaceutical Formulation |
| CN101113148A (zh) | 2006-07-26 | 2008-01-30 | 中国海洋大学 | 二氧哌嗪类化合物及其制备方法和用途 |
| PL2054411T3 (pl) | 2006-07-27 | 2015-02-27 | Amorepacific Corp | Nowe związki, ich izomery lub ich farmaceutycznie dopuszczalne sole jako antagoniści receptora waniloidowego oraz zawierające je kompozycje farmaceutyczne |
| TW200817424A (en) | 2006-08-04 | 2008-04-16 | Daiichi Sankyo Co Ltd | Benzylphenyl glucopyranoside derivatives |
| TWI389895B (zh) | 2006-08-21 | 2013-03-21 | Infinity Discovery Inc | 抑制bcl蛋白質與結合夥伴間之交互作用的化合物及方法 |
| JP5466006B2 (ja) | 2006-09-03 | 2014-04-09 | テックフィールズ バイオケム カンパニー リミテッド | 非常に速い皮膚浸透率を有するアセトアミノフェン及び関連化合物の正荷電水溶性プロドラッグ |
| WO2008041118A2 (en) | 2006-10-04 | 2008-04-10 | Pfizer Products Inc. | Pyrido[4,3-d]pyrimidin-4(3h)-one derivatives as calcium receptor antagonists |
| EA200970401A1 (ru) | 2006-10-23 | 2009-10-30 | Мерк Энд Ко., Инк. | 2-[1-ФЕНИЛ-5-ГИДРОКСИ ИЛИ МЕТОКСИ-4-АЛЬФА-МЕТИЛГЕКСАГИДРОЦИКЛОПЕНТА[f]ИНДАЗОЛ-5-ИЛ] ЭТИЛФЕНИЛЬНЫЕ ПРОИЗВОДНЫЕ В КАЧЕСТВЕ ЛИГАНДОВ ГЛЮКОКОРТИКОИДНОГО РЕЦЕПТОРА |
| EP2123637A4 (en) * | 2006-11-30 | 2011-12-21 | Tokyo Inst Tech | NEW CURCUMIN DERIVATIVES |
| FR2909379B1 (fr) | 2006-11-30 | 2009-01-16 | Servier Lab | Nouveaux derives heterocycliques,leur procede de preparation et les compositions pharmaceutiques qui les contiennent. |
| WO2008066145A1 (en) | 2006-11-30 | 2008-06-05 | R-Tech Ueno, Ltd. | Thiazole derivative and use thereof as vap-1 inhibitor |
| MX2009008798A (es) | 2007-02-22 | 2009-08-24 | Syngenta Participations Ag | Derivados de iminipiridina y sus usos como microbicidas. |
| TWI407960B (zh) | 2007-03-23 | 2013-09-11 | Jerini Ag | 小分子緩激肽b2受體調節劑 |
| US7994367B2 (en) * | 2007-05-22 | 2011-08-09 | Sumitomo Chemical Company, Limited | Method for producing benzaldehyde compound |
| WO2009001214A2 (en) | 2007-06-28 | 2008-12-31 | Pfizer Products Inc. | Thieno[2,3-d]pyrimidin-4(3h)-one, isoxazolo[5,4-d]pyrimidin-4(5h)-one and isothiazolo[5,4-d]pyrimidin-4(5h)-one derivatives as calcium receptor antagonists |
| US20090069288A1 (en) | 2007-07-16 | 2009-03-12 | Breinlinger Eric C | Novel therapeutic compounds |
| AU2008277783B2 (en) | 2007-07-17 | 2012-09-20 | F. Hoffmann-La Roche Ag | Inhibitors of 11beta-hydroxysteroid dehydrogenase |
| ES2375425T3 (es) * | 2007-07-26 | 2012-02-29 | Novartis Ag | Compuestos org�?nicos. |
| TW200918521A (en) | 2007-08-31 | 2009-05-01 | Astrazeneca Ab | Heterocyclic amides and methods of use thereof |
| BRPI0817434A2 (pt) * | 2007-10-17 | 2015-06-16 | Novartis Ag | Composto orgânicos |
| KR101237576B1 (ko) | 2007-12-04 | 2013-03-04 | 에프. 호프만-라 로슈 아게 | 아이속사졸로-피리딘 유도체 |
| US7776875B2 (en) | 2007-12-19 | 2010-08-17 | Hoffman-La Roche Inc. | Spiroindolinone derivatives |
| JP2009203230A (ja) | 2008-01-31 | 2009-09-10 | Daiichi Sankyo Co Ltd | ベンジルフェニルグルコピラノシド誘導体を含有する医薬組成物 |
| US8633245B2 (en) | 2008-04-11 | 2014-01-21 | Institute Of Medicinal Molecular Design, Inc. | PAI-1 inhibitor |
| EP2272817A4 (en) | 2008-04-11 | 2011-12-14 | Inst Med Molecular Design Inc | PAI-1 INHIBITORS |
| JP2011136906A (ja) | 2008-04-18 | 2011-07-14 | Otsuka Pharmaceut Co Ltd | 複素環化合物 |
| US8119647B2 (en) | 2008-04-23 | 2012-02-21 | Glenmark Pharmaceuticals S.A. | Fused pyrimidineone compounds as TRPV3 modulators |
| WO2009136889A1 (en) | 2008-05-08 | 2009-11-12 | Nova Southeastern University | Specific inhibitors for vascular endothelial growth factor receptors |
| AU2009253812A1 (en) | 2008-06-04 | 2009-12-10 | Ambrilia Biopharma Inc. | HIV integrase inhibitors from pyridoxine |
| DE102008027574A1 (de) | 2008-06-10 | 2009-12-17 | Merck Patent Gmbh | Neue Pyrrolidinderivate als MetAP-2 Inhibitoren |
| JP5314330B2 (ja) | 2008-06-16 | 2013-10-16 | 住友化学株式会社 | 2−(アリールオキシメチル)ベンズアルデヒドの製造方法およびその中間体 |
| GB0811451D0 (en) | 2008-06-20 | 2008-07-30 | Syngenta Participations Ag | Novel microbiocides |
| WO2010001946A1 (ja) * | 2008-07-03 | 2010-01-07 | アステラス製薬株式会社 | トリアゾール誘導体またはその塩 |
| AR073304A1 (es) | 2008-09-22 | 2010-10-28 | Jerini Ag | Moduladores del receptor de bradiquinina b2 de molecula pequena |
| EP2358716B1 (en) | 2008-11-12 | 2016-01-06 | Merck Sharp & Dohme Corp. | Inhibitors of fatty acid binding protein (fabp) |
| TW201033201A (en) | 2009-02-19 | 2010-09-16 | Hoffmann La Roche | Isoxazole-isoxazole and isoxazole-isothiazole derivatives |
| EP3708163A1 (en) | 2009-03-31 | 2020-09-16 | Ligand Pharmaceuticals, Inc. | Use of sparsentan for the treatment of chronic inflammatory diseases |
| ES2440000T3 (es) | 2009-05-08 | 2014-01-27 | Tetraphase Pharmaceuticals, Inc. | Compuestos de 8-aza-tetraciclina |
| EP2471789B9 (en) | 2009-08-26 | 2015-03-25 | Takeda Pharmaceutical Company Limited | Fused heterocyclic ring derivative and use thereof |
| US20120245344A1 (en) | 2009-08-31 | 2012-09-27 | Nippon Chemiphar Co., Ltd. | Gpr119 agonist |
| AU2010297290A1 (en) | 2009-09-21 | 2012-03-15 | F. Hoffmann-La Roche Ag | Heterocyclic antiviral compounds |
| AU2010316683B2 (en) | 2009-11-09 | 2015-10-08 | Wyeth Llc | Tablet formulations of neratinib maleate |
| TW201139406A (en) | 2010-01-14 | 2011-11-16 | Glaxo Group Ltd | Voltage-gated sodium channel blockers |
| KR101698153B1 (ko) | 2010-04-26 | 2017-01-23 | 광주과학기술원 | P2x1 및 p2x3 수용체 길항제로 사용되는 신규한 피리딘 카르복실산계 화합물, 이의 제조방법 및 이를 포함하는 조성물 |
| CN102232949A (zh) | 2010-04-27 | 2011-11-09 | 孙远 | 提高药物溶出度的组合物及其制备方法 |
| TWI535442B (zh) | 2010-05-10 | 2016-06-01 | Kyowa Hakko Kirin Co Ltd | A nitrogen-containing heterocyclic compound having an action of inhibiting the production of canine erythritine |
| US20120122928A1 (en) | 2010-08-11 | 2012-05-17 | Bayer Cropscience Ag | Heteroarylpiperidine and -Piperazine Derivatives as Fungicides |
| CN102116772B (zh) | 2010-09-28 | 2013-08-28 | 上海大学 | 二氢查尔酮化合物的筛选方法 |
| BR112013014875A2 (pt) | 2010-12-27 | 2016-10-18 | Takeda Pharmaceutical | tablete oralmente desintegrável |
| CA2832570A1 (en) | 2011-04-06 | 2012-10-11 | Teva Pharmaceutical Industries Ltd. | New intermediates and processes for preparing ticagrelor |
| KR101952222B1 (ko) | 2011-04-11 | 2019-02-26 | 그린 테크 가부시키가이샤 | 신규 피라졸 유도체 |
| CN102952062B (zh) | 2011-08-12 | 2016-06-08 | 中国医学科学院医药生物技术研究所 | 取代苯并杂环类化合物及其制备方法和应用 |
| WO2013040471A2 (en) | 2011-09-15 | 2013-03-21 | Demerx, Inc. | Noribogaine salt ansolvates |
| US20140308260A1 (en) | 2011-10-07 | 2014-10-16 | Radiorx, Inc. | Methods and compositions comprising a nitrite-reductase promoter for treatment of medical disorders and preservation of blood products |
| HK1203412A1 (en) | 2011-12-28 | 2015-10-30 | Global Blood Therapeutics, Inc. | Substituted heteroaryl aldehyde compounds and methods for their use in increasing tissue oxygenation |
| ES2643403T3 (es) * | 2011-12-28 | 2017-11-22 | Global Blood Therapeutics, Inc. | Compuestos de benzaldehído sustituidos y métodos para su uso en el aumento de la oxigenación tisular |
| BR112015015216B1 (pt) | 2012-12-27 | 2020-01-07 | Sumitomo Chemical Company, Limited | Composto de tetrazolinona, agente e método de controle de peste |
| US10100043B2 (en) | 2013-03-15 | 2018-10-16 | Global Blood Therapeutics, Inc. | Substituted aldehyde compounds and methods for their use in increasing tissue oxygenation |
| US9422279B2 (en) | 2013-03-15 | 2016-08-23 | Global Blood Therapeutics, Inc. | Compounds and uses thereof for the modulation of hemoglobin |
| US20150057251A1 (en) | 2013-08-26 | 2015-02-26 | Global Blood Therapeutics, Inc. | Compounds and uses thereof for the modulation of hemoglobin |
| WO2014150258A1 (en) | 2013-03-15 | 2014-09-25 | Global Blood Therapeutics, Inc. | Compounds and uses thereof for the modulation of hemoglobin |
| US10266551B2 (en) | 2013-03-15 | 2019-04-23 | Global Blood Therapeutics, Inc. | Compounds and uses thereof for the modulation of hemoglobin |
| US9458139B2 (en) | 2013-03-15 | 2016-10-04 | Global Blood Therapeutics, Inc. | Compounds and uses thereof for the modulation of hemoglobin |
| WO2014150289A1 (en) | 2013-03-15 | 2014-09-25 | Global Blood Therapeutics, Inc. | Compounds and uses thereof for the modulation of hemoglobin |
| MX379235B (es) | 2013-03-15 | 2025-03-11 | Global Blood Therapeutics Inc | Compuestos y sus usos para modular la hemoglobina. |
| US9604999B2 (en) | 2013-03-15 | 2017-03-28 | Global Blood Therapeutics, Inc. | Compounds and uses thereof for the modulation of hemoglobin |
| CN105073728A (zh) | 2013-03-15 | 2015-11-18 | 全球血液疗法股份有限公司 | 化合物及其用于调节血红蛋白的用途 |
| US8952171B2 (en) | 2013-03-15 | 2015-02-10 | Global Blood Therapeutics, Inc. | Compounds and uses thereof for the modulation of hemoglobin |
| EP2968295A1 (en) | 2013-03-15 | 2016-01-20 | Global Blood Therapeutics, Inc. | Compositions and methods for the modulation of hemoglobin (s) |
| US9802900B2 (en) | 2013-03-15 | 2017-10-31 | Global Blood Therapeutics, Inc. | Bicyclic heteroaryl compounds and uses thereof for the modulation of hemoglobin |
| US20140271591A1 (en) | 2013-03-15 | 2014-09-18 | Global Blood Therapeutics, Inc. | Compositions and methods for the modulation of hemoglobin (s) |
| US20140274961A1 (en) | 2013-03-15 | 2014-09-18 | Global Blood Therapeutics, Inc. | Compounds and uses thereof for the modulation of hemoglobin |
| WO2014150261A1 (en) | 2013-03-15 | 2014-09-25 | Global Blood Therapeutics, Inc. | Compounds and uses thereof for the modulaton of hemoglobin |
| WO2015031284A1 (en) | 2013-08-26 | 2015-03-05 | Global Blood Therapeutics, Inc. | Formulations comprising wetting agents and compounds for the modulation of hemoglobin (s) |
| WO2015031285A1 (en) | 2013-08-27 | 2015-03-05 | Global Blood Therapeutics, Inc. | Crystalline 2-hydroxy-6-((2-(1-isopropyl-1h-pyrazol-5-yl)pyridin-3-yl)methoxy)benzaldehyde ansolvate salts |
| US20160207904A1 (en) | 2013-08-27 | 2016-07-21 | Global Blood Therapeutics, Inc. | Crystalline 2-hydroxy-6-((2-(1-isopropyl-1h-pyrazol-5-yl)pyridin-3-yl)methoxy)benzaldehyde ansolvate salts |
| EA201992707A1 (ru) | 2013-11-18 | 2020-06-30 | Глобал Блад Терапьютикс, Инк. | Соединения и их применения для модуляции гемоглобина |
| US20150141465A1 (en) | 2013-11-18 | 2015-05-21 | Global Blood Therapeutics, Inc. | Compounds and uses thereof for the modulation of hemoglobin |
| US9248199B2 (en) | 2014-01-29 | 2016-02-02 | Global Blood Therapeutics, Inc. | 1:1 adducts of sickle hemoglobin |
| CN114181195A (zh) | 2014-02-07 | 2022-03-15 | 全球血液疗法股份有限公司 | 一种化合物的结晶多晶型物 |
| MA41841A (fr) | 2015-03-30 | 2018-02-06 | Global Blood Therapeutics Inc | Composés aldéhyde pour le traitement de la fibrose pulmonaire, de l'hypoxie, et de maladies auto-immunes et des tissus conjonctifs |
| SG11201804647TA (en) | 2015-12-04 | 2018-06-28 | Global Blood Therapeutics Inc | Dosing regimens for 2-hydroxy-6-((2-(1-isopropyl-1h-pyrazol-5-yl)pyridin-3-yl)methoxy)benzaldehyde |
| TWI663160B (zh) | 2016-05-12 | 2019-06-21 | 全球血液治療公司 | 用於合成2-羥基-6-((2-(1-異丙基-1h-吡唑-5-基)-吡啶-3-基)甲氧基)苯甲醛之方法 |
| TW202332423A (zh) | 2016-10-12 | 2023-08-16 | 美商全球血液治療公司 | 包含2-羥基-6-((2-(1-異丙基-1h-吡唑-5-基)吡啶-3-基)甲氧基)-苯甲醛之片劑 |
-
2012
- 2012-12-28 ES ES12862525.8T patent/ES2643403T3/es active Active
- 2012-12-28 MX MX2018009537A patent/MX372804B/es unknown
- 2012-12-28 ES ES16194019T patent/ES2811129T3/es active Active
- 2012-12-28 AP AP2014007805A patent/AP2014007805A0/xx unknown
- 2012-12-28 CA CA2860323A patent/CA2860323C/en active Active
- 2012-12-28 DK DK16194019.2T patent/DK3141542T3/da active
- 2012-12-28 SG SG11201403645VA patent/SG11201403645VA/en unknown
- 2012-12-28 SI SI201231797T patent/SI3141542T1/sl unknown
- 2012-12-28 EP EP23190105.9A patent/EP4289813A3/en not_active Withdrawn
- 2012-12-28 EP EP12862525.8A patent/EP2797416B1/en active Active
- 2012-12-28 HR HRP20171665TT patent/HRP20171665T1/hr unknown
- 2012-12-28 CN CN201710403045.7A patent/CN107176953B/zh active Active
- 2012-12-28 ES ES20167746T patent/ES2963218T3/es active Active
- 2012-12-28 JP JP2014550525A patent/JP6242810B2/ja active Active
- 2012-12-28 LT LTEP12862525.8T patent/LT2797416T/lt unknown
- 2012-12-28 SI SI201231103T patent/SI2797416T1/sl unknown
- 2012-12-28 EP EP16194019.2A patent/EP3141542B1/en active Active
- 2012-12-28 PE PE2018001322A patent/PE20181519A1/es unknown
- 2012-12-28 HU HUE16194019A patent/HUE050189T2/hu unknown
- 2012-12-28 SG SG10201912409XA patent/SG10201912409XA/en unknown
- 2012-12-28 PE PE2022001477A patent/PE20221914A1/es unknown
- 2012-12-28 DK DK12862525.8T patent/DK2797416T3/en active
- 2012-12-28 CA CA3142817A patent/CA3142817A1/en active Pending
- 2012-12-28 US US13/730,674 patent/US9018210B2/en active Active
- 2012-12-28 MX MX2014007971A patent/MX358992B/es active IP Right Grant
- 2012-12-28 PE PE2014001050A patent/PE20142454A1/es active IP Right Grant
- 2012-12-28 PT PT201677465T patent/PT3738434T/pt unknown
- 2012-12-28 HU HUE20167746A patent/HUE064226T2/hu unknown
- 2012-12-28 EP EP20167746.5A patent/EP3738434B1/en active Active
- 2012-12-28 PL PL20167746.5T patent/PL3738434T3/pl unknown
- 2012-12-28 PT PT161940192T patent/PT3141542T/pt unknown
- 2012-12-28 WO PCT/US2012/072177 patent/WO2013102142A1/en not_active Ceased
- 2012-12-28 PT PT128625258T patent/PT2797416T/pt unknown
- 2012-12-28 SM SM20170483T patent/SMT201700483T1/it unknown
- 2012-12-28 HU HUE12862525A patent/HUE035069T2/en unknown
- 2012-12-28 CN CN201280070743.5A patent/CN104135859B/zh active Active
- 2012-12-28 RS RS20170968A patent/RS56388B1/sr unknown
- 2012-12-28 FI FIEP20167746.5T patent/FI3738434T3/fi active
- 2012-12-28 IL IL292366A patent/IL292366A/en unknown
- 2012-12-28 PL PL12862525T patent/PL2797416T3/pl unknown
- 2012-12-28 LT LTEP16194019.2T patent/LT3141542T/lt unknown
- 2012-12-28 DK DK20167746.5T patent/DK3738434T3/da active
- 2012-12-28 SG SG10201912411RA patent/SG10201912411RA/en unknown
- 2012-12-28 PL PL16194019T patent/PL3141542T3/pl unknown
- 2012-12-28 BR BR112014016165-8A patent/BR112014016165B1/pt active IP Right Grant
- 2012-12-28 SI SI201232045T patent/SI3738434T1/sl unknown
- 2012-12-28 AU AU2012362236A patent/AU2012362236B2/en active Active
- 2012-12-28 SG SG10201702513SA patent/SG10201702513SA/en unknown
- 2012-12-28 RS RS20201021A patent/RS60740B1/sr unknown
- 2012-12-28 SM SM20200370T patent/SMT202000370T1/it unknown
-
2014
- 2014-06-23 IL IL233329A patent/IL233329A0/en active IP Right Grant
- 2014-06-27 NI NI201400070A patent/NI201400070A/es unknown
- 2014-06-27 GT GT201400136A patent/GT201400136A/es unknown
- 2014-06-27 MX MX2022008867A patent/MX2022008867A/es unknown
- 2014-06-27 MX MX2020005645A patent/MX2020005645A/es unknown
- 2014-06-30 CL CL2014001762A patent/CL2014001762A1/es unknown
- 2014-07-28 CO CO14163228A patent/CO7101245A2/es unknown
-
2015
- 2015-03-18 US US14/662,156 patent/US20150344472A1/en not_active Abandoned
-
2016
- 2016-03-16 IL IL24462616A patent/IL244626B/en active IP Right Grant
- 2016-03-25 US US15/081,704 patent/US20160206614A1/en not_active Abandoned
- 2016-06-06 AU AU2016203755A patent/AU2016203755B2/en active Active
-
2017
- 2017-04-10 JP JP2017077318A patent/JP6424399B2/ja active Active
- 2017-09-22 AU AU2017232206A patent/AU2017232206C1/en active Active
- 2017-10-18 CY CY20171101090T patent/CY1119575T1/el unknown
- 2017-12-22 US US15/852,406 patent/US10034879B2/en active Active
-
2018
- 2018-06-25 US US16/017,248 patent/US10806733B2/en active Active
- 2018-10-04 JP JP2018189280A patent/JP6585261B2/ja active Active
-
2019
- 2019-09-04 JP JP2019161066A patent/JP6848026B2/ja active Active
- 2019-10-15 IL IL269977A patent/IL269977B/en unknown
- 2019-12-04 AU AU2019275607A patent/AU2019275607B2/en active Active
-
2020
- 2020-07-01 HR HRP20201045TT patent/HRP20201045T1/hr unknown
- 2020-08-18 CY CY20201100773T patent/CY1123270T1/el unknown
-
2021
- 2021-03-03 JP JP2021033123A patent/JP2021104996A/ja active Pending
- 2021-05-28 US US17/334,213 patent/US20210290619A1/en not_active Abandoned
- 2021-09-17 AU AU2021232806A patent/AU2021232806B2/en active Active
-
2022
- 2022-01-07 US US17/571,183 patent/US20220125786A1/en not_active Abandoned
- 2022-07-20 NO NO2022031C patent/NO2022031I1/no unknown
- 2022-08-01 LU LU00276C patent/LUC00276I2/en unknown
- 2022-08-02 HU HUS2200037C patent/HUS2200037I1/hu unknown
- 2022-08-03 NL NL301191C patent/NL301191I2/nl unknown
- 2022-08-03 FR FR22C1042C patent/FR22C1042I2/fr active Active
- 2022-08-10 CY CY2022025C patent/CY2022025I1/el unknown
- 2022-08-11 LT LTPA2022517C patent/LTPA2022517I1/lt unknown
- 2022-09-27 JP JP2022154128A patent/JP2022191281A/ja active Pending
-
2023
- 2023-04-20 US US18/137,210 patent/US20230255963A1/en not_active Abandoned
-
2024
- 2024-01-24 JP JP2024008428A patent/JP2024050663A/ja active Pending
- 2024-01-29 AU AU2024200515A patent/AU2024200515A1/en not_active Abandoned
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2811129T3 (es) | Compuestos de benzaldehído sustituidos y métodos para su uso en el aumento de la oxigenación tisular | |
| ES2790358T3 (es) | Compuestos de heteroaril aldehído sustituido y métodos para su uso en el aumento de la oxigenación tisular | |
| HK1235055B (en) | Substituted benzaldehyde compounds and methods for their use in increasing tissue oxygenation | |
| HK1203308B (en) | Substituted benzaldehyde compounds and methods for their use in increasing tissue oxygenation | |
| HK1235055A1 (en) | Substituted benzaldehyde compounds and methods for their use in increasing tissue oxygenation |