KR20170032414A - 전자 소자용 재료 - Google Patents
전자 소자용 재료 Download PDFInfo
- Publication number
- KR20170032414A KR20170032414A KR1020177004335A KR20177004335A KR20170032414A KR 20170032414 A KR20170032414 A KR 20170032414A KR 1020177004335 A KR1020177004335 A KR 1020177004335A KR 20177004335 A KR20177004335 A KR 20177004335A KR 20170032414 A KR20170032414 A KR 20170032414A
- Authority
- KR
- South Korea
- Prior art keywords
- group
- atoms
- compound
- radicals
- aromatic ring
- Prior art date
Links
- 239000000463 material Substances 0.000 title claims description 71
- 150000001875 compounds Chemical class 0.000 claims abstract description 190
- 239000000203 mixture Substances 0.000 claims abstract description 41
- 238000009472 formulation Methods 0.000 claims abstract description 6
- 125000003118 aryl group Chemical group 0.000 claims description 101
- 239000010410 layer Substances 0.000 claims description 81
- 125000004432 carbon atom Chemical group C* 0.000 claims description 46
- 239000011159 matrix material Substances 0.000 claims description 42
- -1 NR 2 Inorganic materials 0.000 claims description 41
- 229910052799 carbon Inorganic materials 0.000 claims description 36
- 125000001931 aliphatic group Chemical group 0.000 claims description 30
- 239000002019 doping agent Substances 0.000 claims description 29
- 125000003367 polycyclic group Chemical group 0.000 claims description 28
- 125000002950 monocyclic group Chemical group 0.000 claims description 27
- 229910052731 fluorine Inorganic materials 0.000 claims description 26
- 229910052717 sulfur Inorganic materials 0.000 claims description 25
- 125000003342 alkenyl group Chemical group 0.000 claims description 23
- 125000000304 alkynyl group Chemical group 0.000 claims description 22
- 229910052760 oxygen Inorganic materials 0.000 claims description 22
- 125000001424 substituent group Chemical group 0.000 claims description 22
- 125000003545 alkoxy group Chemical group 0.000 claims description 21
- 125000005309 thioalkoxy group Chemical group 0.000 claims description 18
- 229910052794 bromium Inorganic materials 0.000 claims description 17
- 229910052801 chlorine Inorganic materials 0.000 claims description 17
- 125000000217 alkyl group Chemical group 0.000 claims description 16
- 229910052740 iodine Inorganic materials 0.000 claims description 15
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims description 14
- 125000001072 heteroaryl group Chemical group 0.000 claims description 13
- 125000006165 cyclic alkyl group Chemical group 0.000 claims description 12
- 229910052739 hydrogen Inorganic materials 0.000 claims description 11
- 125000004104 aryloxy group Chemical group 0.000 claims description 10
- 239000002904 solvent Substances 0.000 claims description 9
- 229910052805 deuterium Inorganic materials 0.000 claims description 8
- 229910052757 nitrogen Inorganic materials 0.000 claims description 7
- 238000004519 manufacturing process Methods 0.000 claims description 6
- 239000012044 organic layer Substances 0.000 claims description 6
- 125000006413 ring segment Chemical group 0.000 claims description 5
- 125000005553 heteroaryloxy group Chemical group 0.000 claims description 4
- 125000000623 heterocyclic group Chemical group 0.000 claims description 3
- 239000004215 Carbon black (E152) Substances 0.000 claims description 2
- 125000005055 alkyl alkoxy group Chemical group 0.000 claims description 2
- 125000003710 aryl alkyl group Chemical group 0.000 claims description 2
- 125000004986 diarylamino group Chemical group 0.000 claims description 2
- 125000005240 diheteroarylamino group Chemical group 0.000 claims description 2
- 230000005669 field effect Effects 0.000 claims description 2
- 229930195733 hydrocarbon Natural products 0.000 claims description 2
- 238000010791 quenching Methods 0.000 claims description 2
- 239000010409 thin film Substances 0.000 claims description 2
- 125000004149 thio group Chemical group *S* 0.000 claims description 2
- 238000005401 electroluminescence Methods 0.000 claims 1
- 150000003384 small molecules Chemical class 0.000 claims 1
- 238000007740 vapor deposition Methods 0.000 claims 1
- 150000003254 radicals Chemical class 0.000 description 62
- 238000000034 method Methods 0.000 description 31
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 27
- NFHFRUOZVGFOOS-UHFFFAOYSA-N palladium;triphenylphosphane Chemical compound [Pd].C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 NFHFRUOZVGFOOS-UHFFFAOYSA-N 0.000 description 22
- 239000000243 solution Substances 0.000 description 16
- 229910052751 metal Inorganic materials 0.000 description 14
- 239000002184 metal Substances 0.000 description 14
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 12
- BBEAQIROQSPTKN-UHFFFAOYSA-N pyrene Chemical compound C1=CC=C2C=CC3=CC=CC4=CC=C1C2=C43 BBEAQIROQSPTKN-UHFFFAOYSA-N 0.000 description 12
- 238000004770 highest occupied molecular orbital Methods 0.000 description 11
- SMWDFEZZVXVKRB-UHFFFAOYSA-N Quinoline Chemical compound N1=CC=CC2=CC=CC=C21 SMWDFEZZVXVKRB-UHFFFAOYSA-N 0.000 description 10
- MWPLVEDNUUSJAV-UHFFFAOYSA-N anthracene Chemical compound C1=CC=CC2=CC3=CC=CC=C3C=C21 MWPLVEDNUUSJAV-UHFFFAOYSA-N 0.000 description 10
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 10
- 238000004768 lowest unoccupied molecular orbital Methods 0.000 description 10
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 10
- 239000007787 solid Substances 0.000 description 10
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 9
- GVEPBJHOBDJJJI-UHFFFAOYSA-N fluoranthrene Natural products C1=CC(C2=CC=CC=C22)=C3C2=CC=CC3=C1 GVEPBJHOBDJJJI-UHFFFAOYSA-N 0.000 description 8
- NIHNNTQXNPWCJQ-UHFFFAOYSA-N fluorene Chemical compound C1=CC=C2CC3=CC=CC=C3C2=C1 NIHNNTQXNPWCJQ-UHFFFAOYSA-N 0.000 description 8
- JYEUMXHLPRZUAT-UHFFFAOYSA-N 1,2,3-triazine Chemical compound C1=CN=NN=C1 JYEUMXHLPRZUAT-UHFFFAOYSA-N 0.000 description 7
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 description 7
- 125000003983 fluorenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3CC12)* 0.000 description 7
- 239000011737 fluorine Substances 0.000 description 7
- 230000006872 improvement Effects 0.000 description 7
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Chemical compound [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 description 7
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 6
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 6
- IMNFDUFMRHMDMM-UHFFFAOYSA-N N-Heptane Chemical compound CCCCCCC IMNFDUFMRHMDMM-UHFFFAOYSA-N 0.000 description 6
- UFWIBTONFRDIAS-UHFFFAOYSA-N Naphthalene Chemical compound C1=CC=CC2=CC=CC=C21 UFWIBTONFRDIAS-UHFFFAOYSA-N 0.000 description 6
- PCNDJXKNXGMECE-UHFFFAOYSA-N Phenazine Natural products C1=CC=CC2=NC3=CC=CC=C3N=C21 PCNDJXKNXGMECE-UHFFFAOYSA-N 0.000 description 6
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 6
- DZBUGLKDJFMEHC-UHFFFAOYSA-N acridine Chemical compound C1=CC=CC2=CC3=CC=CC=C3N=C21 DZBUGLKDJFMEHC-UHFFFAOYSA-N 0.000 description 6
- 229910052783 alkali metal Inorganic materials 0.000 description 6
- 150000001340 alkali metals Chemical class 0.000 description 6
- ZUOUZKKEUPVFJK-UHFFFAOYSA-N diphenyl Chemical compound C1=CC=CC=C1C1=CC=CC=C1 ZUOUZKKEUPVFJK-UHFFFAOYSA-N 0.000 description 6
- CTAPFRYPJLPFDF-UHFFFAOYSA-N isoxazole Chemical compound C=1C=NOC=1 CTAPFRYPJLPFDF-UHFFFAOYSA-N 0.000 description 6
- 150000002739 metals Chemical class 0.000 description 6
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 6
- DXBHBZVCASKNBY-UHFFFAOYSA-N 1,2-Benz(a)anthracene Chemical compound C1=CC=C2C3=CC4=CC=CC=C4C=C3C=CC2=C1 DXBHBZVCASKNBY-UHFFFAOYSA-N 0.000 description 5
- 239000005711 Benzoic acid Substances 0.000 description 5
- 125000004429 atom Chemical group 0.000 description 5
- 230000008901 benefit Effects 0.000 description 5
- 235000010233 benzoic acid Nutrition 0.000 description 5
- 238000006243 chemical reaction Methods 0.000 description 5
- 125000004122 cyclic group Chemical group 0.000 description 5
- 125000005842 heteroatom Chemical group 0.000 description 5
- 239000011368 organic material Substances 0.000 description 5
- LXNAVEXFUKBNMK-UHFFFAOYSA-N palladium(II) acetate Substances [Pd].CC(O)=O.CC(O)=O LXNAVEXFUKBNMK-UHFFFAOYSA-N 0.000 description 5
- YJVFFLUZDVXJQI-UHFFFAOYSA-L palladium(ii) acetate Chemical compound [Pd+2].CC([O-])=O.CC([O-])=O YJVFFLUZDVXJQI-UHFFFAOYSA-L 0.000 description 5
- 125000000843 phenylene group Chemical group C1(=C(C=CC=C1)*)* 0.000 description 5
- 239000002243 precursor Substances 0.000 description 5
- 229910052709 silver Inorganic materials 0.000 description 5
- VNFWTIYUKDMAOP-UHFFFAOYSA-N sphos Chemical compound COC1=CC=CC(OC)=C1C1=CC=CC=C1P(C1CCCCC1)C1CCCCC1 VNFWTIYUKDMAOP-UHFFFAOYSA-N 0.000 description 5
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 5
- ICPSWZFVWAPUKF-UHFFFAOYSA-N 1,1'-spirobi[fluorene] Chemical compound C1=CC=C2C=C3C4(C=5C(C6=CC=CC=C6C=5)=CC=C4)C=CC=C3C2=C1 ICPSWZFVWAPUKF-UHFFFAOYSA-N 0.000 description 4
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 4
- HYZJCKYKOHLVJF-UHFFFAOYSA-N 1H-benzimidazole Chemical compound C1=CC=C2NC=NC2=C1 HYZJCKYKOHLVJF-UHFFFAOYSA-N 0.000 description 4
- VEPOHXYIFQMVHW-XOZOLZJESA-N 2,3-dihydroxybutanedioic acid (2S,3S)-3,4-dimethyl-2-phenylmorpholine Chemical compound OC(C(O)C(O)=O)C(O)=O.C[C@H]1[C@@H](OCCN1C)c1ccccc1 VEPOHXYIFQMVHW-XOZOLZJESA-N 0.000 description 4
- XYFCBTPGUUZFHI-UHFFFAOYSA-N Phosphine Chemical compound P XYFCBTPGUUZFHI-UHFFFAOYSA-N 0.000 description 4
- KYQCOXFCLRTKLS-UHFFFAOYSA-N Pyrazine Chemical compound C1=CN=CC=N1 KYQCOXFCLRTKLS-UHFFFAOYSA-N 0.000 description 4
- CZPWVGJYEJSRLH-UHFFFAOYSA-N Pyrimidine Chemical compound C1=CN=CN=C1 CZPWVGJYEJSRLH-UHFFFAOYSA-N 0.000 description 4
- YTPLMLYBLZKORZ-UHFFFAOYSA-N Thiophene Chemical compound C=1C=CSC=1 YTPLMLYBLZKORZ-UHFFFAOYSA-N 0.000 description 4
- IOJUPLGTWVMSFF-UHFFFAOYSA-N benzothiazole Chemical compound C1=CC=C2SC=NC2=C1 IOJUPLGTWVMSFF-UHFFFAOYSA-N 0.000 description 4
- 230000015572 biosynthetic process Effects 0.000 description 4
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 4
- 239000011229 interlayer Substances 0.000 description 4
- 229910052697 platinum Inorganic materials 0.000 description 4
- 238000007639 printing Methods 0.000 description 4
- 238000010992 reflux Methods 0.000 description 4
- 239000010944 silver (metal) Substances 0.000 description 4
- 238000000859 sublimation Methods 0.000 description 4
- 230000008022 sublimation Effects 0.000 description 4
- 238000003786 synthesis reaction Methods 0.000 description 4
- KZPYGQFFRCFCPP-UHFFFAOYSA-N 1,1'-bis(diphenylphosphino)ferrocene Chemical compound [Fe+2].C1=CC=C[C-]1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=C[C-]1P(C=1C=CC=CC=1)C1=CC=CC=C1 KZPYGQFFRCFCPP-UHFFFAOYSA-N 0.000 description 3
- YJTKZCDBKVTVBY-UHFFFAOYSA-N 1,3-Diphenylbenzene Chemical group C1=CC=CC=C1C1=CC=CC(C=2C=CC=CC=2)=C1 YJTKZCDBKVTVBY-UHFFFAOYSA-N 0.000 description 3
- FCEHBMOGCRZNNI-UHFFFAOYSA-N 1-benzothiophene Chemical group C1=CC=C2SC=CC2=C1 FCEHBMOGCRZNNI-UHFFFAOYSA-N 0.000 description 3
- UXGVMFHEKMGWMA-UHFFFAOYSA-N 2-benzofuran Chemical compound C1=CC=CC2=COC=C21 UXGVMFHEKMGWMA-UHFFFAOYSA-N 0.000 description 3
- 0 CC*(C(*)=*1)c2c1cccc2 Chemical compound CC*(C(*)=*1)c2c1cccc2 0.000 description 3
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 3
- CPLXHLVBOLITMK-UHFFFAOYSA-N Magnesium oxide Chemical compound [Mg]=O CPLXHLVBOLITMK-UHFFFAOYSA-N 0.000 description 3
- JGFZNNIVVJXRND-UHFFFAOYSA-N N,N-Diisopropylethylamine (DIPEA) Chemical compound CCN(C(C)C)C(C)C JGFZNNIVVJXRND-UHFFFAOYSA-N 0.000 description 3
- BQCADISMDOOEFD-UHFFFAOYSA-N Silver Chemical compound [Ag] BQCADISMDOOEFD-UHFFFAOYSA-N 0.000 description 3
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 3
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 3
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 3
- 125000003785 benzimidazolyl group Chemical group N1=C(NC2=C1C=CC=C2)* 0.000 description 3
- 235000010290 biphenyl Nutrition 0.000 description 3
- 239000004305 biphenyl Substances 0.000 description 3
- 238000004364 calculation method Methods 0.000 description 3
- 125000000609 carbazolyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3NC12)* 0.000 description 3
- 239000007789 gas Substances 0.000 description 3
- 239000001257 hydrogen Substances 0.000 description 3
- RAXXELZNTBOGNW-UHFFFAOYSA-N imidazole Natural products C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 description 3
- 238000002347 injection Methods 0.000 description 3
- 239000007924 injection Substances 0.000 description 3
- 229910052741 iridium Inorganic materials 0.000 description 3
- GKOZUEZYRPOHIO-UHFFFAOYSA-N iridium atom Chemical compound [Ir] GKOZUEZYRPOHIO-UHFFFAOYSA-N 0.000 description 3
- 150000003951 lactams Chemical class 0.000 description 3
- 238000004020 luminiscence type Methods 0.000 description 3
- 239000011777 magnesium Substances 0.000 description 3
- 229910044991 metal oxide Inorganic materials 0.000 description 3
- 150000004706 metal oxides Chemical class 0.000 description 3
- 125000004433 nitrogen atom Chemical group N* 0.000 description 3
- PIBWKRNGBLPSSY-UHFFFAOYSA-L palladium(II) chloride Chemical compound Cl[Pd]Cl PIBWKRNGBLPSSY-UHFFFAOYSA-L 0.000 description 3
- 230000008569 process Effects 0.000 description 3
- 239000000047 product Substances 0.000 description 3
- 230000001681 protective effect Effects 0.000 description 3
- 239000004332 silver Substances 0.000 description 3
- 229910000029 sodium carbonate Inorganic materials 0.000 description 3
- 229910052938 sodium sulfate Inorganic materials 0.000 description 3
- 235000011152 sodium sulphate Nutrition 0.000 description 3
- 150000003462 sulfoxides Chemical class 0.000 description 3
- CXWXQJXEFPUFDZ-UHFFFAOYSA-N tetralin Chemical compound C1=CC=C2CCCCC2=C1 CXWXQJXEFPUFDZ-UHFFFAOYSA-N 0.000 description 3
- 230000007704 transition Effects 0.000 description 3
- BFIMMTCNYPIMRN-UHFFFAOYSA-N 1,2,3,5-tetramethylbenzene Chemical compound CC1=CC(C)=C(C)C(C)=C1 BFIMMTCNYPIMRN-UHFFFAOYSA-N 0.000 description 2
- IVSZLXZYQVIEFR-UHFFFAOYSA-N 1,3-Dimethylbenzene Natural products CC1=CC=CC(C)=C1 IVSZLXZYQVIEFR-UHFFFAOYSA-N 0.000 description 2
- CHLICZRVGGXEOD-UHFFFAOYSA-N 1-Methoxy-4-methylbenzene Chemical compound COC1=CC=C(C)C=C1 CHLICZRVGGXEOD-UHFFFAOYSA-N 0.000 description 2
- QPUYECUOLPXSFR-UHFFFAOYSA-N 1-methylnaphthalene Chemical compound C1=CC=C2C(C)=CC=CC2=C1 QPUYECUOLPXSFR-UHFFFAOYSA-N 0.000 description 2
- WJFKNYWRSNBZNX-UHFFFAOYSA-N 10H-phenothiazine Chemical compound C1=CC=C2NC3=CC=CC=C3SC2=C1 WJFKNYWRSNBZNX-UHFFFAOYSA-N 0.000 description 2
- TZMSYXZUNZXBOL-UHFFFAOYSA-N 10H-phenoxazine Chemical compound C1=CC=C2NC3=CC=CC=C3OC2=C1 TZMSYXZUNZXBOL-UHFFFAOYSA-N 0.000 description 2
- DXYYSGDWQCSKKO-UHFFFAOYSA-N 2-methylbenzothiazole Chemical compound C1=CC=C2SC(C)=NC2=C1 DXYYSGDWQCSKKO-UHFFFAOYSA-N 0.000 description 2
- KDCGOANMDULRCW-UHFFFAOYSA-N 7H-purine Chemical compound N1=CNC2=NC=NC2=C1 KDCGOANMDULRCW-UHFFFAOYSA-N 0.000 description 2
- BPMFPOGUJAAYHL-UHFFFAOYSA-N 9H-Pyrido[2,3-b]indole Chemical compound C1=CC=C2C3=CC=CC=C3NC2=N1 BPMFPOGUJAAYHL-UHFFFAOYSA-N 0.000 description 2
- KWOLFJPFCHCOCG-UHFFFAOYSA-N Acetophenone Chemical compound CC(=O)C1=CC=CC=C1 KWOLFJPFCHCOCG-UHFFFAOYSA-N 0.000 description 2
- 208000002874 Acne Vulgaris Diseases 0.000 description 2
- 229910016036 BaF 2 Inorganic materials 0.000 description 2
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 2
- 206010012438 Dermatitis atopic Diseases 0.000 description 2
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 2
- LTEQMZWBSYACLV-UHFFFAOYSA-N Hexylbenzene Chemical compound CCCCCCC1=CC=CC=C1 LTEQMZWBSYACLV-UHFFFAOYSA-N 0.000 description 2
- SIKJAQJRHWYJAI-UHFFFAOYSA-N Indole Chemical compound C1=CC=C2NC=CC2=C1 SIKJAQJRHWYJAI-UHFFFAOYSA-N 0.000 description 2
- 229910018068 Li 2 O Inorganic materials 0.000 description 2
- KDLHZDBZIXYQEI-UHFFFAOYSA-N Palladium Chemical compound [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 2
- URLKBWYHVLBVBO-UHFFFAOYSA-N Para-Xylene Chemical group CC1=CC=C(C)C=C1 URLKBWYHVLBVBO-UHFFFAOYSA-N 0.000 description 2
- PWATWSYOIIXYMA-UHFFFAOYSA-N Pentylbenzene Chemical compound CCCCCC1=CC=CC=C1 PWATWSYOIIXYMA-UHFFFAOYSA-N 0.000 description 2
- 229920001609 Poly(3,4-ethylenedioxythiophene) Polymers 0.000 description 2
- 201000004681 Psoriasis Diseases 0.000 description 2
- KAESVJOAVNADME-UHFFFAOYSA-N Pyrrole Chemical compound C=1C=CNC=1 KAESVJOAVNADME-UHFFFAOYSA-N 0.000 description 2
- 208000000453 Skin Neoplasms Diseases 0.000 description 2
- 238000006069 Suzuki reaction reaction Methods 0.000 description 2
- DGEZNRSVGBDHLK-UHFFFAOYSA-N [1,10]phenanthroline Chemical compound C1=CN=C2C3=NC=CC=C3C=CC2=C1 DGEZNRSVGBDHLK-UHFFFAOYSA-N 0.000 description 2
- 206010000496 acne Diseases 0.000 description 2
- 230000004913 activation Effects 0.000 description 2
- 150000001342 alkaline earth metals Chemical class 0.000 description 2
- 229910045601 alloy Inorganic materials 0.000 description 2
- 239000000956 alloy Substances 0.000 description 2
- AZDRQVAHHNSJOQ-UHFFFAOYSA-N alumane Chemical class [AlH3] AZDRQVAHHNSJOQ-UHFFFAOYSA-N 0.000 description 2
- 229910052782 aluminium Inorganic materials 0.000 description 2
- RDOXTESZEPMUJZ-UHFFFAOYSA-N anisole Chemical compound COC1=CC=CC=C1 RDOXTESZEPMUJZ-UHFFFAOYSA-N 0.000 description 2
- 201000008937 atopic dermatitis Diseases 0.000 description 2
- 229910052788 barium Inorganic materials 0.000 description 2
- 239000002585 base Substances 0.000 description 2
- WZJYKHNJTSNBHV-UHFFFAOYSA-N benzo[h]quinoline Chemical compound C1=CN=C2C3=CC=CC=C3C=CC2=C1 WZJYKHNJTSNBHV-UHFFFAOYSA-N 0.000 description 2
- 125000002529 biphenylenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3C12)* 0.000 description 2
- 229910052796 boron Inorganic materials 0.000 description 2
- XSIFPSYPOVKYCO-UHFFFAOYSA-N butyl benzoate Chemical compound CCCCOC(=O)C1=CC=CC=C1 XSIFPSYPOVKYCO-UHFFFAOYSA-N 0.000 description 2
- MVPPADPHJFYWMZ-UHFFFAOYSA-N chlorobenzene Chemical compound ClC1=CC=CC=C1 MVPPADPHJFYWMZ-UHFFFAOYSA-N 0.000 description 2
- WDECIBYCCFPHNR-UHFFFAOYSA-N chrysene Chemical compound C1=CC=CC2=CC=C3C4=CC=CC=C4C=CC3=C21 WDECIBYCCFPHNR-UHFFFAOYSA-N 0.000 description 2
- 150000004696 coordination complex Chemical class 0.000 description 2
- 229910052802 copper Inorganic materials 0.000 description 2
- 239000010949 copper Substances 0.000 description 2
- 239000002537 cosmetic Substances 0.000 description 2
- RWGFKTVRMDUZSP-UHFFFAOYSA-N cumene Chemical compound CC(C)C1=CC=CC=C1 RWGFKTVRMDUZSP-UHFFFAOYSA-N 0.000 description 2
- JHIVVAPYMSGYDF-UHFFFAOYSA-N cyclohexanone Chemical compound O=C1CCCCC1 JHIVVAPYMSGYDF-UHFFFAOYSA-N 0.000 description 2
- NNBZCPXTIHJBJL-UHFFFAOYSA-N decalin Chemical compound C1CCCC2CCCCC21 NNBZCPXTIHJBJL-UHFFFAOYSA-N 0.000 description 2
- IYYZUPMFVPLQIF-UHFFFAOYSA-N dibenzothiophene Chemical compound C1=CC=C2C3=CC=CC=C3SC2=C1 IYYZUPMFVPLQIF-UHFFFAOYSA-N 0.000 description 2
- SQNZJJAZBFDUTD-UHFFFAOYSA-N durene Chemical compound CC1=CC(C)=C(C)C=C1C SQNZJJAZBFDUTD-UHFFFAOYSA-N 0.000 description 2
- 150000002148 esters Chemical class 0.000 description 2
- MTZQAGJQAFMTAQ-UHFFFAOYSA-N ethyl benzoate Chemical compound CCOC(=O)C1=CC=CC=C1 MTZQAGJQAFMTAQ-UHFFFAOYSA-N 0.000 description 2
- 230000005284 excitation Effects 0.000 description 2
- 230000001747 exhibiting effect Effects 0.000 description 2
- 239000011521 glass Substances 0.000 description 2
- 229910052737 gold Inorganic materials 0.000 description 2
- 239000010931 gold Substances 0.000 description 2
- 230000005283 ground state Effects 0.000 description 2
- 238000004128 high performance liquid chromatography Methods 0.000 description 2
- 230000005525 hole transport Effects 0.000 description 2
- 229910052738 indium Inorganic materials 0.000 description 2
- AMGQUBHHOARCQH-UHFFFAOYSA-N indium;oxotin Chemical compound [In].[Sn]=O AMGQUBHHOARCQH-UHFFFAOYSA-N 0.000 description 2
- AWJUIBRHMBBTKR-UHFFFAOYSA-N isoquinoline Chemical compound C1=NC=CC2=CC=CC=C21 AWJUIBRHMBBTKR-UHFFFAOYSA-N 0.000 description 2
- 150000002576 ketones Chemical class 0.000 description 2
- 229910052749 magnesium Inorganic materials 0.000 description 2
- QPJVMBTYPHYUOC-UHFFFAOYSA-N methyl benzoate Chemical compound COC(=O)C1=CC=CC=C1 QPJVMBTYPHYUOC-UHFFFAOYSA-N 0.000 description 2
- 230000007935 neutral effect Effects 0.000 description 2
- CTQNGGLPUBDAKN-UHFFFAOYSA-N o-dimethylbenzene Natural products CC1=CC=CC=C1C CTQNGGLPUBDAKN-UHFFFAOYSA-N 0.000 description 2
- 150000002894 organic compounds Chemical class 0.000 description 2
- 150000002902 organometallic compounds Chemical class 0.000 description 2
- 125000002524 organometallic group Chemical group 0.000 description 2
- MPQXHAGKBWFSNV-UHFFFAOYSA-N oxidophosphanium Chemical class [PH3]=O MPQXHAGKBWFSNV-UHFFFAOYSA-N 0.000 description 2
- AUONHKJOIZSQGR-UHFFFAOYSA-N oxophosphane Chemical compound P=O AUONHKJOIZSQGR-UHFFFAOYSA-N 0.000 description 2
- 125000002080 perylenyl group Chemical group C1(=CC=C2C=CC=C3C4=CC=CC5=CC=CC(C1=C23)=C45)* 0.000 description 2
- CSHWQDPOILHKBI-UHFFFAOYSA-N peryrene Natural products C1=CC(C2=CC=CC=3C2=C2C=CC=3)=C3C2=CC=CC3=C1 CSHWQDPOILHKBI-UHFFFAOYSA-N 0.000 description 2
- 239000012071 phase Substances 0.000 description 2
- YNPNZTXNASCQKK-UHFFFAOYSA-N phenanthrene Chemical compound C1=CC=C2C3=CC=CC=C3C=CC2=C1 YNPNZTXNASCQKK-UHFFFAOYSA-N 0.000 description 2
- 150000002988 phenazines Chemical class 0.000 description 2
- 229950000688 phenothiazine Drugs 0.000 description 2
- 229910000073 phosphorus hydride Inorganic materials 0.000 description 2
- 229920000642 polymer Polymers 0.000 description 2
- SCVFZCLFOSHCOH-UHFFFAOYSA-M potassium acetate Chemical compound [K+].CC([O-])=O SCVFZCLFOSHCOH-UHFFFAOYSA-M 0.000 description 2
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 2
- 238000002360 preparation method Methods 0.000 description 2
- PBMFSQRYOILNGV-UHFFFAOYSA-N pyridazine Chemical compound C1=CC=NN=C1 PBMFSQRYOILNGV-UHFFFAOYSA-N 0.000 description 2
- 238000003077 quantum chemistry computational method Methods 0.000 description 2
- XSCHRSMBECNVNS-UHFFFAOYSA-N quinoxaline Chemical compound N1=CC=NC2=CC=CC=C21 XSCHRSMBECNVNS-UHFFFAOYSA-N 0.000 description 2
- 239000004065 semiconductor Substances 0.000 description 2
- 230000009759 skin aging Effects 0.000 description 2
- 201000000849 skin cancer Diseases 0.000 description 2
- 238000004528 spin coating Methods 0.000 description 2
- 238000003756 stirring Methods 0.000 description 2
- 238000006467 substitution reaction Methods 0.000 description 2
- 239000000758 substrate Substances 0.000 description 2
- ZUHZGEOKBKGPSW-UHFFFAOYSA-N tetraglyme Chemical compound COCCOCCOCCOCCOC ZUHZGEOKBKGPSW-UHFFFAOYSA-N 0.000 description 2
- 238000001931 thermography Methods 0.000 description 2
- 229930192474 thiophene Natural products 0.000 description 2
- 125000005259 triarylamine group Chemical group 0.000 description 2
- SLGBZMMZGDRARJ-UHFFFAOYSA-N triphenylene Chemical compound C1=CC=C2C3=CC=CC=C3C3=CC=CC=C3C2=C1 SLGBZMMZGDRARJ-UHFFFAOYSA-N 0.000 description 2
- 238000001771 vacuum deposition Methods 0.000 description 2
- FIDRAVVQGKNYQK-UHFFFAOYSA-N 1,2,3,4-tetrahydrotriazine Chemical compound C1NNNC=C1 FIDRAVVQGKNYQK-UHFFFAOYSA-N 0.000 description 1
- ZFXBERJDEUDDMX-UHFFFAOYSA-N 1,2,3,5-tetrazine Chemical compound C1=NC=NN=N1 ZFXBERJDEUDDMX-UHFFFAOYSA-N 0.000 description 1
- FNQJDLTXOVEEFB-UHFFFAOYSA-N 1,2,3-benzothiadiazole Chemical compound C1=CC=C2SN=NC2=C1 FNQJDLTXOVEEFB-UHFFFAOYSA-N 0.000 description 1
- UGUHFDPGDQDVGX-UHFFFAOYSA-N 1,2,3-thiadiazole Chemical compound C1=CSN=N1 UGUHFDPGDQDVGX-UHFFFAOYSA-N 0.000 description 1
- HTJMXYRLEDBSLT-UHFFFAOYSA-N 1,2,4,5-tetrazine Chemical compound C1=NN=CN=N1 HTJMXYRLEDBSLT-UHFFFAOYSA-N 0.000 description 1
- BBVIDBNAYOIXOE-UHFFFAOYSA-N 1,2,4-oxadiazole Chemical compound C=1N=CON=1 BBVIDBNAYOIXOE-UHFFFAOYSA-N 0.000 description 1
- YGTAZGSLCXNBQL-UHFFFAOYSA-N 1,2,4-thiadiazole Chemical compound C=1N=CSN=1 YGTAZGSLCXNBQL-UHFFFAOYSA-N 0.000 description 1
- FYADHXFMURLYQI-UHFFFAOYSA-N 1,2,4-triazine Chemical compound C1=CN=NC=N1 FYADHXFMURLYQI-UHFFFAOYSA-N 0.000 description 1
- UDGKZGLPXCRRAM-UHFFFAOYSA-N 1,2,5-thiadiazole Chemical compound C=1C=NSN=1 UDGKZGLPXCRRAM-UHFFFAOYSA-N 0.000 description 1
- FKASFBLJDCHBNZ-UHFFFAOYSA-N 1,3,4-oxadiazole Chemical compound C1=NN=CO1 FKASFBLJDCHBNZ-UHFFFAOYSA-N 0.000 description 1
- MBIZXFATKUQOOA-UHFFFAOYSA-N 1,3,4-thiadiazole Chemical compound C1=NN=CS1 MBIZXFATKUQOOA-UHFFFAOYSA-N 0.000 description 1
- JIHQDMXYYFUGFV-UHFFFAOYSA-N 1,3,5-triazine Chemical compound C1=NC=NC=N1 JIHQDMXYYFUGFV-UHFFFAOYSA-N 0.000 description 1
- FLBAYUMRQUHISI-UHFFFAOYSA-N 1,8-naphthyridine Chemical compound N1=CC=CC2=CC=CN=C21 FLBAYUMRQUHISI-UHFFFAOYSA-N 0.000 description 1
- UHXOHPVVEHBKKT-UHFFFAOYSA-N 1-(2,2-diphenylethenyl)-4-[4-(2,2-diphenylethenyl)phenyl]benzene Chemical compound C=1C=C(C=2C=CC(C=C(C=3C=CC=CC=3)C=3C=CC=CC=3)=CC=2)C=CC=1C=C(C=1C=CC=CC=1)C1=CC=CC=C1 UHXOHPVVEHBKKT-UHFFFAOYSA-N 0.000 description 1
- OSIGJGFTADMDOB-UHFFFAOYSA-N 1-Methoxy-3-methylbenzene Chemical compound COC1=CC=CC(C)=C1 OSIGJGFTADMDOB-UHFFFAOYSA-N 0.000 description 1
- LBNXAWYDQUGHGX-UHFFFAOYSA-N 1-Phenylheptane Chemical compound CCCCCCCC1=CC=CC=C1 LBNXAWYDQUGHGX-UHFFFAOYSA-N 0.000 description 1
- HYLLZXPMJRMUHH-UHFFFAOYSA-N 1-[2-(2-methoxyethoxy)ethoxy]butane Chemical compound CCCCOCCOCCOC HYLLZXPMJRMUHH-UHFFFAOYSA-N 0.000 description 1
- SNAQINZKMQFYFV-UHFFFAOYSA-N 1-[2-[2-(2-methoxyethoxy)ethoxy]ethoxy]butane Chemical compound CCCCOCCOCCOCCOC SNAQINZKMQFYFV-UHFFFAOYSA-N 0.000 description 1
- RERATEUBWLKDFE-UHFFFAOYSA-N 1-methoxy-2-[2-(2-methoxypropoxy)propoxy]propane Chemical compound COCC(C)OCC(C)OCC(C)OC RERATEUBWLKDFE-UHFFFAOYSA-N 0.000 description 1
- JCHJBEZBHANKGA-UHFFFAOYSA-N 1-methoxy-3,5-dimethylbenzene Chemical compound COC1=CC(C)=CC(C)=C1 JCHJBEZBHANKGA-UHFFFAOYSA-N 0.000 description 1
- WCOYPFBMFKXWBM-UHFFFAOYSA-N 1-methyl-2-phenoxybenzene Chemical compound CC1=CC=CC=C1OC1=CC=CC=C1 WCOYPFBMFKXWBM-UHFFFAOYSA-N 0.000 description 1
- UDONPJKEOAWFGI-UHFFFAOYSA-N 1-methyl-3-phenoxybenzene Chemical compound CC1=CC=CC(OC=2C=CC=CC=2)=C1 UDONPJKEOAWFGI-UHFFFAOYSA-N 0.000 description 1
- QWENRTYMTSOGBR-UHFFFAOYSA-N 1H-1,2,3-Triazole Chemical compound C=1C=NNN=1 QWENRTYMTSOGBR-UHFFFAOYSA-N 0.000 description 1
- BAXOFTOLAUCFNW-UHFFFAOYSA-N 1H-indazole Chemical compound C1=CC=C2C=NNC2=C1 BAXOFTOLAUCFNW-UHFFFAOYSA-N 0.000 description 1
- LPHIYKWSEYTCLW-UHFFFAOYSA-N 1h-azaborole Chemical compound N1B=CC=C1 LPHIYKWSEYTCLW-UHFFFAOYSA-N 0.000 description 1
- USYCQABRSUEURP-UHFFFAOYSA-N 1h-benzo[f]benzimidazole Chemical compound C1=CC=C2C=C(NC=N3)C3=CC2=C1 USYCQABRSUEURP-UHFFFAOYSA-N 0.000 description 1
- IGHOZKDBCCFNNC-UHFFFAOYSA-N 1h-imidazole;quinoxaline Chemical compound C1=CNC=N1.N1=CC=NC2=CC=CC=C21 IGHOZKDBCCFNNC-UHFFFAOYSA-N 0.000 description 1
- UPJLZKCEPFAKSH-UHFFFAOYSA-N 2',7'-dibromo-9,9'-spirobi[fluorene] Chemical compound C12=CC=CC=C2C2=CC=CC=C2C21C1=CC(Br)=CC=C1C1=CC=C(Br)C=C12 UPJLZKCEPFAKSH-UHFFFAOYSA-N 0.000 description 1
- PLJDGKPRGUMSAA-UHFFFAOYSA-N 2,2',7,7'-tetraphenyl-1,1'-spirobi[fluorene] Chemical compound C12=CC=C(C=3C=CC=CC=3)C=C2C=C(C23C(=CC=C4C5=CC=C(C=C5C=C43)C=3C=CC=CC=3)C=3C=CC=CC=3)C1=CC=C2C1=CC=CC=C1 PLJDGKPRGUMSAA-UHFFFAOYSA-N 0.000 description 1
- AMEVJOWOWQPPJQ-UHFFFAOYSA-N 2,4-dichloro-6-phenyl-1,3,5-triazine Chemical compound ClC1=NC(Cl)=NC(C=2C=CC=CC=2)=N1 AMEVJOWOWQPPJQ-UHFFFAOYSA-N 0.000 description 1
- RICKKZXCGCSLIU-UHFFFAOYSA-N 2-[2-[carboxymethyl-[[3-hydroxy-5-(hydroxymethyl)-2-methylpyridin-4-yl]methyl]amino]ethyl-[[3-hydroxy-5-(hydroxymethyl)-2-methylpyridin-4-yl]methyl]amino]acetic acid Chemical compound CC1=NC=C(CO)C(CN(CCN(CC(O)=O)CC=2C(=C(C)N=CC=2CO)O)CC(O)=O)=C1O RICKKZXCGCSLIU-UHFFFAOYSA-N 0.000 description 1
- UFWYLYLAKMJSCC-UHFFFAOYSA-N 2-[3-(7'-bromo-9,9'-spirobi[fluorene]-2'-yl)phenyl]-1-phenylbenzimidazole Chemical compound BrC1=CC=C2C=3C=CC(=CC=3C3(C4=CC=CC=C4C=4C=CC=CC3=4)C2=C1)C=1C=C(C=CC=1)C1=NC2=C(N1C1=CC=CC=C1)C=CC=C2 UFWYLYLAKMJSCC-UHFFFAOYSA-N 0.000 description 1
- LYTMVABTDYMBQK-UHFFFAOYSA-N 2-benzothiophene Chemical compound C1=CC=CC2=CSC=C21 LYTMVABTDYMBQK-UHFFFAOYSA-N 0.000 description 1
- ONCCVJKFWKAZAE-UHFFFAOYSA-N 2-bromo-9,9'-spirobi[fluorene] Chemical compound C12=CC=CC=C2C2=CC=CC=C2C21C1=CC=CC=C1C1=CC=C(Br)C=C12 ONCCVJKFWKAZAE-UHFFFAOYSA-N 0.000 description 1
- DDGPPAMADXTGTN-UHFFFAOYSA-N 2-chloro-4,6-diphenyl-1,3,5-triazine Chemical compound N=1C(Cl)=NC(C=2C=CC=CC=2)=NC=1C1=CC=CC=C1 DDGPPAMADXTGTN-UHFFFAOYSA-N 0.000 description 1
- OCCHPYMDRVQDQG-UHFFFAOYSA-N 2-chloro-4-phenyl-6-(9,9'-spirobi[fluorene]-2-yl)-1,3,5-triazine Chemical compound ClC1=NC(=NC(=N1)C1=CC=CC=C1)C1=CC2=C(C=C1)C1=CC=CC=C1C21C2=CC=CC=C2C2=C1C=CC=C2 OCCHPYMDRVQDQG-UHFFFAOYSA-N 0.000 description 1
- CRWNQZTZTZWPOF-UHFFFAOYSA-N 2-methyl-4-phenylpyridine Chemical compound C1=NC(C)=CC(C=2C=CC=CC=2)=C1 CRWNQZTZTZWPOF-UHFFFAOYSA-N 0.000 description 1
- QCDWFXQBSFUVSP-UHFFFAOYSA-N 2-phenoxyethanol Chemical compound OCCOC1=CC=CC=C1 QCDWFXQBSFUVSP-UHFFFAOYSA-N 0.000 description 1
- DWYHDSLIWMUSOO-UHFFFAOYSA-N 2-phenyl-1h-benzimidazole Chemical compound C1=CC=CC=C1C1=NC2=CC=CC=C2N1 DWYHDSLIWMUSOO-UHFFFAOYSA-N 0.000 description 1
- TVYVQNHYIHAJTD-UHFFFAOYSA-N 2-propan-2-ylnaphthalene Chemical compound C1=CC=CC2=CC(C(C)C)=CC=C21 TVYVQNHYIHAJTD-UHFFFAOYSA-N 0.000 description 1
- VHMICKWLTGFITH-UHFFFAOYSA-N 2H-isoindole Chemical compound C1=CC=CC2=CNC=C21 VHMICKWLTGFITH-UHFFFAOYSA-N 0.000 description 1
- YFCSASDLEBELEU-UHFFFAOYSA-N 3,4,5,6,9,10-hexazatetracyclo[12.4.0.02,7.08,13]octadeca-1(18),2(7),3,5,8(13),9,11,14,16-nonaene-11,12,15,16,17,18-hexacarbonitrile Chemical group N#CC1=C(C#N)C(C#N)=C2C3=C(C#N)C(C#N)=NN=C3C3=NN=NN=C3C2=C1C#N YFCSASDLEBELEU-UHFFFAOYSA-N 0.000 description 1
- WHKZBVQIMVUGIH-UHFFFAOYSA-N 3-hydroxyquinoline-2-carboxylic acid Chemical compound C1=CC=C2C=C(O)C(C(=O)O)=NC2=C1 WHKZBVQIMVUGIH-UHFFFAOYSA-N 0.000 description 1
- HHVGZHHLRBNWAD-UHFFFAOYSA-N 4,6-diphenyltriazine Chemical compound C1=CC=CC=C1C1=CC(C=2C=CC=CC=2)=NN=N1 HHVGZHHLRBNWAD-UHFFFAOYSA-N 0.000 description 1
- LVUBSVWMOWKPDJ-UHFFFAOYSA-N 4-methoxy-1,2-dimethylbenzene Chemical compound COC1=CC=C(C)C(C)=C1 LVUBSVWMOWKPDJ-UHFFFAOYSA-N 0.000 description 1
- 229940077398 4-methyl anisole Drugs 0.000 description 1
- NSPMIYGKQJPBQR-UHFFFAOYSA-N 4H-1,2,4-triazole Chemical compound C=1N=CNN=1 NSPMIYGKQJPBQR-UHFFFAOYSA-N 0.000 description 1
- SNFCXVRWFNAHQX-UHFFFAOYSA-N 9,9'-spirobi[fluorene] Chemical compound C12=CC=CC=C2C2=CC=CC=C2C21C1=CC=CC=C1C1=CC=CC=C21 SNFCXVRWFNAHQX-UHFFFAOYSA-N 0.000 description 1
- WDDLHUWVLROJLA-UHFFFAOYSA-N 9,9'-spirobi[fluorene]-2-ylboronic acid Chemical compound C12=CC=CC=C2C2=CC=CC=C2C21C1=CC=CC=C1C1=CC=C(B(O)O)C=C12 WDDLHUWVLROJLA-UHFFFAOYSA-N 0.000 description 1
- 239000005964 Acibenzolar-S-methyl Substances 0.000 description 1
- VPLRCJUDJZSLKO-UHFFFAOYSA-N C(N=C1)=C[S+]1C1=CC=CC=C1 Chemical compound C(N=C1)=C[S+]1C1=CC=CC=C1 VPLRCJUDJZSLKO-UHFFFAOYSA-N 0.000 description 1
- RPNGXEZWXXDFDE-UHFFFAOYSA-N CC1(C)c2cccc(-c3nc(-c4cc(-[n]5c(-c6ccccc6)nc6ccccc56)ccc4)nc(-c4cc(-[n]5c(-c6ccccc6)nc6c5cccc6)ccc4)n3)c2-c2ccccc12 Chemical compound CC1(C)c2cccc(-c3nc(-c4cc(-[n]5c(-c6ccccc6)nc6ccccc56)ccc4)nc(-c4cc(-[n]5c(-c6ccccc6)nc6c5cccc6)ccc4)n3)c2-c2ccccc12 RPNGXEZWXXDFDE-UHFFFAOYSA-N 0.000 description 1
- 208000035484 Cellulite Diseases 0.000 description 1
- OTMSDBZUPAUEDD-UHFFFAOYSA-N Ethane Chemical compound CC OTMSDBZUPAUEDD-UHFFFAOYSA-N 0.000 description 1
- 229910052693 Europium Inorganic materials 0.000 description 1
- YLQBMQCUIZJEEH-UHFFFAOYSA-N Furan Chemical compound C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 1
- 102100040907 Glycerol kinase 3 Human genes 0.000 description 1
- 101710181614 Glycerol kinase 3 Proteins 0.000 description 1
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 1
- 206010061218 Inflammation Diseases 0.000 description 1
- 206010023126 Jaundice Diseases 0.000 description 1
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 1
- ZOKXTWBITQBERF-UHFFFAOYSA-N Molybdenum Chemical compound [Mo] ZOKXTWBITQBERF-UHFFFAOYSA-N 0.000 description 1
- ZCQWOFVYLHDMMC-UHFFFAOYSA-N Oxazole Chemical compound C1=COC=N1 ZCQWOFVYLHDMMC-UHFFFAOYSA-N 0.000 description 1
- 229920000144 PEDOT:PSS Polymers 0.000 description 1
- 206010049752 Peau d'orange Diseases 0.000 description 1
- OFBQJSOFQDEBGM-UHFFFAOYSA-N Pentane Chemical compound CCCCC OFBQJSOFQDEBGM-UHFFFAOYSA-N 0.000 description 1
- CWRVKFFCRWGWCS-UHFFFAOYSA-N Pentrazole Chemical compound C1CCCCC2=NN=NN21 CWRVKFFCRWGWCS-UHFFFAOYSA-N 0.000 description 1
- 102100040908 Putative glycerol kinase 5 Human genes 0.000 description 1
- 101710111071 Putative glycerol kinase 5 Proteins 0.000 description 1
- WTKZEGDFNFYCGP-UHFFFAOYSA-N Pyrazole Chemical compound C=1C=NNC=1 WTKZEGDFNFYCGP-UHFFFAOYSA-N 0.000 description 1
- KJTLSVCANCCWHF-UHFFFAOYSA-N Ruthenium Chemical compound [Ru] KJTLSVCANCCWHF-UHFFFAOYSA-N 0.000 description 1
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 1
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical class [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 1
- PJANXHGTPQOBST-VAWYXSNFSA-N Stilbene Natural products C=1C=CC=CC=1/C=C/C1=CC=CC=C1 PJANXHGTPQOBST-VAWYXSNFSA-N 0.000 description 1
- DHXVGJBLRPWPCS-UHFFFAOYSA-N Tetrahydropyran Chemical compound C1CCOCC1 DHXVGJBLRPWPCS-UHFFFAOYSA-N 0.000 description 1
- DPOPAJRDYZGTIR-UHFFFAOYSA-N Tetrazine Chemical compound C1=CN=NN=N1 DPOPAJRDYZGTIR-UHFFFAOYSA-N 0.000 description 1
- 229910052770 Uranium Inorganic materials 0.000 description 1
- 206010047642 Vitiligo Diseases 0.000 description 1
- CHPDCDRDTOQRAG-UHFFFAOYSA-N [2-(2,6-dimethoxyphenyl)phenyl]phosphane Chemical compound COC1=CC=CC(OC)=C1C1=CC=CC=C1P CHPDCDRDTOQRAG-UHFFFAOYSA-N 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 150000007513 acids Chemical class 0.000 description 1
- 150000001251 acridines Chemical class 0.000 description 1
- 229910001515 alkali metal fluoride Inorganic materials 0.000 description 1
- 229910001618 alkaline earth metal fluoride Inorganic materials 0.000 description 1
- HSFWRNGVRCDJHI-UHFFFAOYSA-N alpha-acetylene Natural products C#C HSFWRNGVRCDJHI-UHFFFAOYSA-N 0.000 description 1
- WUOACPNHFRMFPN-UHFFFAOYSA-N alpha-terpineol Chemical compound CC1=CCC(C(C)(C)O)CC1 WUOACPNHFRMFPN-UHFFFAOYSA-N 0.000 description 1
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 1
- 150000001450 anions Chemical class 0.000 description 1
- 239000010405 anode material Substances 0.000 description 1
- 239000008346 aqueous phase Substances 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 150000004982 aromatic amines Chemical class 0.000 description 1
- 150000001491 aromatic compounds Chemical class 0.000 description 1
- 150000003851 azoles Chemical class 0.000 description 1
- QRUDEWIWKLJBPS-UHFFFAOYSA-N benzotriazole Chemical compound C1=CC=C2N[N][N]C2=C1 QRUDEWIWKLJBPS-UHFFFAOYSA-N 0.000 description 1
- 239000012964 benzotriazole Substances 0.000 description 1
- UFVXQDWNSAGPHN-UHFFFAOYSA-K bis[(2-methylquinolin-8-yl)oxy]-(4-phenylphenoxy)alumane Chemical compound [Al+3].C1=CC=C([O-])C2=NC(C)=CC=C21.C1=CC=C([O-])C2=NC(C)=CC=C21.C1=CC([O-])=CC=C1C1=CC=CC=C1 UFVXQDWNSAGPHN-UHFFFAOYSA-K 0.000 description 1
- 230000000903 blocking effect Effects 0.000 description 1
- 150000001638 boron Chemical class 0.000 description 1
- 150000001639 boron compounds Chemical class 0.000 description 1
- 150000001642 boronic acid derivatives Chemical class 0.000 description 1
- 125000005620 boronic acid group Chemical class 0.000 description 1
- 125000004369 butenyl group Chemical group C(=CCC)* 0.000 description 1
- 125000000480 butynyl group Chemical group [*]C#CC([H])([H])C([H])([H])[H] 0.000 description 1
- 239000006227 byproduct Substances 0.000 description 1
- QRWVLIQWMJWSRT-UHFFFAOYSA-N c(cc1)ccc1-[n]1c(-c2cccc(-c(cc3C45c6ccccc6-c6ccccc46)ccc3-c(cc3)c5cc3-c3nc(-c4cccc5c4c(cccc4)c4[o]5)nc(-c4cccc5c4c(cccc4)c4[o]5)n3)c2)nc2ccccc12 Chemical compound c(cc1)ccc1-[n]1c(-c2cccc(-c(cc3C45c6ccccc6-c6ccccc46)ccc3-c(cc3)c5cc3-c3nc(-c4cccc5c4c(cccc4)c4[o]5)nc(-c4cccc5c4c(cccc4)c4[o]5)n3)c2)nc2ccccc12 QRWVLIQWMJWSRT-UHFFFAOYSA-N 0.000 description 1
- DSIFFSZMZWXZMX-UHFFFAOYSA-N c(cc1)ccc1-[n]1c(-c2cccc(-c3nc(-c4cc(-c5nc(cccc6)c6[n]5-c5ccccc5)ccc4)nc(-c4ccc5-c6ccccc6C6(c7ccccc7-c7c6cccc7)c5c4)n3)c2)nc2c1cccc2 Chemical compound c(cc1)ccc1-[n]1c(-c2cccc(-c3nc(-c4cc(-c5nc(cccc6)c6[n]5-c5ccccc5)ccc4)nc(-c4ccc5-c6ccccc6C6(c7ccccc7-c7c6cccc7)c5c4)n3)c2)nc2c1cccc2 DSIFFSZMZWXZMX-UHFFFAOYSA-N 0.000 description 1
- YDBJHUAXGLRZME-UHFFFAOYSA-N c(cc1)ccc1-[n]1c(ccc(-c2nc(-c(cc3C45c6ccccc6-c6c4cccc6)ccc3-c3c5cccc3)nc(-c3cccc(-c4nc(cccc5)c5[n]4-c4ccccc4)c3)n2)c2)c2c2ccccc12 Chemical compound c(cc1)ccc1-[n]1c(ccc(-c2nc(-c(cc3C45c6ccccc6-c6c4cccc6)ccc3-c3c5cccc3)nc(-c3cccc(-c4nc(cccc5)c5[n]4-c4ccccc4)c3)n2)c2)c2c2ccccc12 YDBJHUAXGLRZME-UHFFFAOYSA-N 0.000 description 1
- OWSGLBQSRXAQLJ-UHFFFAOYSA-N c(cc1)ccc1-c(cc1)ccc1-c(cc1)ccc1-c1nc(-c2cc(-c3nc(cccc4)c4[n]3-c3ccccc3)ccc2)nc(-c2ccc3-c4ccccc4C4(c(cccc5)c5-c5ccccc45)c3c2)n1 Chemical compound c(cc1)ccc1-c(cc1)ccc1-c(cc1)ccc1-c1nc(-c2cc(-c3nc(cccc4)c4[n]3-c3ccccc3)ccc2)nc(-c2ccc3-c4ccccc4C4(c(cccc5)c5-c5ccccc45)c3c2)n1 OWSGLBQSRXAQLJ-UHFFFAOYSA-N 0.000 description 1
- VZXBNVCNLFCMNT-UHFFFAOYSA-N c(cc1)ccc1-c1nc(cccc2)c2[n]1-c1cc(-c2nc(-c(cccc34)c3-c3ccccc3C43c4cc(-c5ccccc5)ccc4-c(cc4)c3cc4-c3ccccc3)nc(-c3ccccc3)n2)ccc1 Chemical compound c(cc1)ccc1-c1nc(cccc2)c2[n]1-c1cc(-c2nc(-c(cccc34)c3-c3ccccc3C43c4cc(-c5ccccc5)ccc4-c(cc4)c3cc4-c3ccccc3)nc(-c3ccccc3)n2)ccc1 VZXBNVCNLFCMNT-UHFFFAOYSA-N 0.000 description 1
- BFUZQENTTYTBPA-UHFFFAOYSA-N c(cc1)ccc1-c1nc(cccc2)c2[n]1-c1cc(-c2nc(-c3cc(-[n]4c(-c5ccccc5)nc5c4cccc5)ccc3)nc(-c3c4-c5ccccc5C5(c6ccccc6-c6ccccc56)c4ccc3)n2)ccc1 Chemical compound c(cc1)ccc1-c1nc(cccc2)c2[n]1-c1cc(-c2nc(-c3cc(-[n]4c(-c5ccccc5)nc5c4cccc5)ccc3)nc(-c3c4-c5ccccc5C5(c6ccccc6-c6ccccc56)c4ccc3)n2)ccc1 BFUZQENTTYTBPA-UHFFFAOYSA-N 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- VPKDCDLSJZCGKE-UHFFFAOYSA-N carbodiimide group Chemical group N=C=N VPKDCDLSJZCGKE-UHFFFAOYSA-N 0.000 description 1
- 150000004649 carbonic acid derivatives Chemical class 0.000 description 1
- 239000012159 carrier gas Substances 0.000 description 1
- 230000001413 cellular effect Effects 0.000 description 1
- 230000036232 cellulite Effects 0.000 description 1
- 238000012512 characterization method Methods 0.000 description 1
- 239000003638 chemical reducing agent Substances 0.000 description 1
- WCZVZNOTHYJIEI-UHFFFAOYSA-N cinnoline Chemical compound N1=NC=CC2=CC=CC=C21 WCZVZNOTHYJIEI-UHFFFAOYSA-N 0.000 description 1
- 238000004440 column chromatography Methods 0.000 description 1
- 230000000052 comparative effect Effects 0.000 description 1
- 238000009833 condensation Methods 0.000 description 1
- 230000005494 condensation Effects 0.000 description 1
- 239000004020 conductor Substances 0.000 description 1
- 239000000470 constituent Substances 0.000 description 1
- 150000001879 copper Chemical class 0.000 description 1
- 239000012043 crude product Substances 0.000 description 1
- 150000001923 cyclic compounds Chemical class 0.000 description 1
- 238000002484 cyclic voltammetry Methods 0.000 description 1
- 125000001162 cycloheptenyl group Chemical group C1(=CCCCCC1)* 0.000 description 1
- 125000000582 cycloheptyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- HPXRVTGHNJAIIH-UHFFFAOYSA-N cyclohexanol Chemical compound OC1CCCCC1 HPXRVTGHNJAIIH-UHFFFAOYSA-N 0.000 description 1
- 125000000596 cyclohexenyl group Chemical group C1(=CCCCC1)* 0.000 description 1
- HHNHBFLGXIUXCM-GFCCVEGCSA-N cyclohexylbenzene Chemical compound [CH]1CCCC[C@@H]1C1=CC=CC=C1 HHNHBFLGXIUXCM-GFCCVEGCSA-N 0.000 description 1
- 125000000522 cyclooctenyl group Chemical group C1(=CCCCCCC1)* 0.000 description 1
- 125000002433 cyclopentenyl group Chemical group C1(=CCCC1)* 0.000 description 1
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- GGRQLKPIJPFWEZ-UHFFFAOYSA-N cycloprop-2-en-1-one Chemical compound O=C1C=C1 GGRQLKPIJPFWEZ-UHFFFAOYSA-N 0.000 description 1
- 230000002950 deficient Effects 0.000 description 1
- SQIFACVGCPWBQZ-UHFFFAOYSA-N delta-terpineol Natural products CC(C)(O)C1CCC(=C)CC1 SQIFACVGCPWBQZ-UHFFFAOYSA-N 0.000 description 1
- 238000000151 deposition Methods 0.000 description 1
- 230000008021 deposition Effects 0.000 description 1
- 150000001987 diarylethers Chemical class 0.000 description 1
- 125000005509 dibenzothiophenyl group Chemical group 0.000 description 1
- MHDVGSVTJDSBDK-UHFFFAOYSA-N dibenzyl ether Chemical compound C=1C=CC=CC=1COCC1=CC=CC=C1 MHDVGSVTJDSBDK-UHFFFAOYSA-N 0.000 description 1
- ZOCHARZZJNPSEU-UHFFFAOYSA-N diboron Chemical compound B#B ZOCHARZZJNPSEU-UHFFFAOYSA-N 0.000 description 1
- 229940028356 diethylene glycol monobutyl ether Drugs 0.000 description 1
- DKHNGUNXLDCATP-UHFFFAOYSA-N dipyrazino[2,3-f:2',3'-h]quinoxaline-2,3,6,7,10,11-hexacarbonitrile Chemical group C12=NC(C#N)=C(C#N)N=C2C2=NC(C#N)=C(C#N)N=C2C2=C1N=C(C#N)C(C#N)=N2 DKHNGUNXLDCATP-UHFFFAOYSA-N 0.000 description 1
- 201000010099 disease Diseases 0.000 description 1
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- KWKXNDCHNDYVRT-UHFFFAOYSA-N dodecylbenzene Chemical compound CCCCCCCCCCCCC1=CC=CC=C1 KWKXNDCHNDYVRT-UHFFFAOYSA-N 0.000 description 1
- 230000005684 electric field Effects 0.000 description 1
- 238000001194 electroluminescence spectrum Methods 0.000 description 1
- 239000003480 eluent Substances 0.000 description 1
- 238000000295 emission spectrum Methods 0.000 description 1
- 239000000839 emulsion Substances 0.000 description 1
- 125000005678 ethenylene group Chemical class [H]C([*:1])=C([H])[*:2] 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 125000002534 ethynyl group Chemical group [H]C#C* 0.000 description 1
- OGPBJKLSAFTDLK-UHFFFAOYSA-N europium atom Chemical compound [Eu] OGPBJKLSAFTDLK-UHFFFAOYSA-N 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 239000000706 filtrate Substances 0.000 description 1
- 150000002222 fluorine compounds Chemical class 0.000 description 1
- 238000011010 flushing procedure Methods 0.000 description 1
- 235000013305 food Nutrition 0.000 description 1
- JKFAIQOWCVVSKC-UHFFFAOYSA-N furazan Chemical compound C=1C=NON=1 JKFAIQOWCVVSKC-UHFFFAOYSA-N 0.000 description 1
- 238000007429 general method Methods 0.000 description 1
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 1
- 125000006038 hexenyl group Chemical group 0.000 description 1
- 125000005980 hexynyl group Chemical group 0.000 description 1
- PZOUSPYUWWUPPK-UHFFFAOYSA-N indole Natural products CC1=CC=CC2=C1C=CN2 PZOUSPYUWWUPPK-UHFFFAOYSA-N 0.000 description 1
- RKJUIXBNRJVNHR-UHFFFAOYSA-N indolenine Natural products C1=CC=C2CC=NC2=C1 RKJUIXBNRJVNHR-UHFFFAOYSA-N 0.000 description 1
- HOBCFUWDNJPFHB-UHFFFAOYSA-N indolizine Chemical compound C1=CC=CN2C=CC=C21 HOBCFUWDNJPFHB-UHFFFAOYSA-N 0.000 description 1
- 230000001939 inductive effect Effects 0.000 description 1
- 208000027866 inflammatory disease Diseases 0.000 description 1
- 230000004054 inflammatory process Effects 0.000 description 1
- 238000007641 inkjet printing Methods 0.000 description 1
- 150000002484 inorganic compounds Chemical class 0.000 description 1
- 229910010272 inorganic material Inorganic materials 0.000 description 1
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 229910052747 lanthanoid Inorganic materials 0.000 description 1
- 150000002602 lanthanoids Chemical class 0.000 description 1
- 239000003446 ligand Substances 0.000 description 1
- PQXKHYXIUOZZFA-UHFFFAOYSA-M lithium fluoride Inorganic materials [Li+].[F-] PQXKHYXIUOZZFA-UHFFFAOYSA-M 0.000 description 1
- COLNWNFTWHPORY-UHFFFAOYSA-M lithium;8-hydroxyquinoline-2-carboxylate Chemical class [Li+].C1=C(C([O-])=O)N=C2C(O)=CC=CC2=C1 COLNWNFTWHPORY-UHFFFAOYSA-M 0.000 description 1
- IMKMFBIYHXBKRX-UHFFFAOYSA-M lithium;quinoline-2-carboxylate Chemical compound [Li+].C1=CC=CC2=NC(C(=O)[O-])=CC=C21 IMKMFBIYHXBKRX-UHFFFAOYSA-M 0.000 description 1
- 238000012423 maintenance Methods 0.000 description 1
- 235000012054 meals Nutrition 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- AUHZEENZYGFFBQ-UHFFFAOYSA-N mesitylene Substances CC1=CC(C)=CC(C)=C1 AUHZEENZYGFFBQ-UHFFFAOYSA-N 0.000 description 1
- 125000001827 mesitylenyl group Chemical group [H]C1=C(C(*)=C(C([H])=C1C([H])([H])[H])C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 229910001092 metal group alloy Inorganic materials 0.000 description 1
- UZKWTJUDCOPSNM-UHFFFAOYSA-N methoxybenzene Substances CCCCOC=C UZKWTJUDCOPSNM-UHFFFAOYSA-N 0.000 description 1
- 229940095102 methyl benzoate Drugs 0.000 description 1
- 229910003455 mixed metal oxide Inorganic materials 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 238000004776 molecular orbital Methods 0.000 description 1
- 229910052750 molybdenum Inorganic materials 0.000 description 1
- 239000011733 molybdenum Substances 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000003136 n-heptyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000001280 n-hexyl group Chemical group C(CCCCC)* 0.000 description 1
- 125000000740 n-pentyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000004957 naphthylene group Chemical group 0.000 description 1
- 125000005244 neohexyl group Chemical group [H]C([H])([H])C(C([H])([H])[H])(C([H])([H])[H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000001971 neopentyl group Chemical group [H]C([*])([H])C(C([H])([H])[H])(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 125000004365 octenyl group Chemical group C(=CCCCCCC)* 0.000 description 1
- VXNSQGRKHCZUSU-UHFFFAOYSA-N octylbenzene Chemical compound [CH2]CCCCCCCC1=CC=CC=C1 VXNSQGRKHCZUSU-UHFFFAOYSA-N 0.000 description 1
- 125000005069 octynyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C#C* 0.000 description 1
- 238000007645 offset printing Methods 0.000 description 1
- 230000003287 optical effect Effects 0.000 description 1
- 238000005457 optimization Methods 0.000 description 1
- 125000000962 organic group Chemical group 0.000 description 1
- 239000012074 organic phase Substances 0.000 description 1
- 229910052762 osmium Inorganic materials 0.000 description 1
- SYQBFIAQOQZEGI-UHFFFAOYSA-N osmium atom Chemical compound [Os] SYQBFIAQOQZEGI-UHFFFAOYSA-N 0.000 description 1
- WCPAKWJPBJAGKN-UHFFFAOYSA-N oxadiazole Chemical compound C1=CON=N1 WCPAKWJPBJAGKN-UHFFFAOYSA-N 0.000 description 1
- JCGNDDUYTRNOFT-UHFFFAOYSA-N oxolane-2,4-dione Chemical compound O=C1COC(=O)C1 JCGNDDUYTRNOFT-UHFFFAOYSA-N 0.000 description 1
- 125000004430 oxygen atom Chemical group O* 0.000 description 1
- 229910052763 palladium Inorganic materials 0.000 description 1
- SLIUAWYAILUBJU-UHFFFAOYSA-N pentacene Chemical compound C1=CC=CC2=CC3=CC4=CC5=CC=CC=C5C=C4C=C3C=C21 SLIUAWYAILUBJU-UHFFFAOYSA-N 0.000 description 1
- 125000002255 pentenyl group Chemical group C(=CCCC)* 0.000 description 1
- 125000005981 pentynyl group Chemical group 0.000 description 1
- 239000008194 pharmaceutical composition Substances 0.000 description 1
- 229960005323 phenoxyethanol Drugs 0.000 description 1
- 108091008695 photoreceptors Proteins 0.000 description 1
- 238000001126 phototherapy Methods 0.000 description 1
- 229920001467 poly(styrenesulfonates) Polymers 0.000 description 1
- 229920000767 polyaniline Polymers 0.000 description 1
- 235000011056 potassium acetate Nutrition 0.000 description 1
- 229910000027 potassium carbonate Inorganic materials 0.000 description 1
- 239000010970 precious metal Substances 0.000 description 1
- 239000002244 precipitate Substances 0.000 description 1
- 230000000750 progressive effect Effects 0.000 description 1
- 125000002568 propynyl group Chemical group [*]C#CC([H])([H])[H] 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- GDISDVBCNPLSDU-UHFFFAOYSA-N pyrido[2,3-g]quinoline Chemical compound C1=CC=NC2=CC3=CC=CN=C3C=C21 GDISDVBCNPLSDU-UHFFFAOYSA-N 0.000 description 1
- HNJBEVLQSNELDL-UHFFFAOYSA-N pyrrolidin-2-one Chemical compound O=C1CCCN1 HNJBEVLQSNELDL-UHFFFAOYSA-N 0.000 description 1
- JWVCLYRUEFBMGU-UHFFFAOYSA-N quinazoline Chemical compound N1=CN=CC2=CC=CC=C21 JWVCLYRUEFBMGU-UHFFFAOYSA-N 0.000 description 1
- 229910052761 rare earth metal Inorganic materials 0.000 description 1
- 150000002910 rare earth metals Chemical class 0.000 description 1
- 239000011541 reaction mixture Substances 0.000 description 1
- 238000001953 recrystallisation Methods 0.000 description 1
- 229910052702 rhenium Inorganic materials 0.000 description 1
- WUAPFZMCVAUBPE-UHFFFAOYSA-N rhenium atom Chemical compound [Re] WUAPFZMCVAUBPE-UHFFFAOYSA-N 0.000 description 1
- 229910052703 rhodium Inorganic materials 0.000 description 1
- 239000010948 rhodium Substances 0.000 description 1
- MHOVAHRLVXNVSD-UHFFFAOYSA-N rhodium atom Chemical compound [Rh] MHOVAHRLVXNVSD-UHFFFAOYSA-N 0.000 description 1
- 238000006798 ring closing metathesis reaction Methods 0.000 description 1
- 229910052707 ruthenium Inorganic materials 0.000 description 1
- 229920006395 saturated elastomer Polymers 0.000 description 1
- 238000007650 screen-printing Methods 0.000 description 1
- 229910052710 silicon Inorganic materials 0.000 description 1
- 125000003808 silyl group Chemical group [H][Si]([H])([H])[*] 0.000 description 1
- 208000017520 skin disease Diseases 0.000 description 1
- PUZPDOWCWNUUKD-UHFFFAOYSA-M sodium fluoride Inorganic materials [F-].[Na+] PUZPDOWCWNUUKD-UHFFFAOYSA-M 0.000 description 1
- FNXKBSAUKFCXIK-UHFFFAOYSA-M sodium;hydrogen carbonate;8-hydroxy-7-iodoquinoline-5-sulfonic acid Chemical class [Na+].OC([O-])=O.C1=CN=C2C(O)=C(I)C=C(S(O)(=O)=O)C2=C1 FNXKBSAUKFCXIK-UHFFFAOYSA-M 0.000 description 1
- 238000010561 standard procedure Methods 0.000 description 1
- 230000001954 sterilising effect Effects 0.000 description 1
- 238000004659 sterilization and disinfection Methods 0.000 description 1
- PJANXHGTPQOBST-UHFFFAOYSA-N stilbene Chemical compound C=1C=CC=CC=1C=CC1=CC=CC=C1 PJANXHGTPQOBST-UHFFFAOYSA-N 0.000 description 1
- 235000021286 stilbenes Nutrition 0.000 description 1
- 238000005092 sublimation method Methods 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 150000003457 sulfones Chemical class 0.000 description 1
- 125000006836 terphenylene group Chemical group 0.000 description 1
- 229940116411 terpineol Drugs 0.000 description 1
- IFLREYGFSNHWGE-UHFFFAOYSA-N tetracene Chemical compound C1=CC=CC2=CC3=CC4=CC=CC=C4C=C3C=C21 IFLREYGFSNHWGE-UHFFFAOYSA-N 0.000 description 1
- 238000002207 thermal evaporation Methods 0.000 description 1
- 125000004001 thioalkyl group Chemical group 0.000 description 1
- 238000010023 transfer printing Methods 0.000 description 1
- 150000003918 triazines Chemical class 0.000 description 1
- ZIBGPFATKBEMQZ-UHFFFAOYSA-N triethylene glycol Chemical compound OCCOCCOCCO ZIBGPFATKBEMQZ-UHFFFAOYSA-N 0.000 description 1
- ITMCEJHCFYSIIV-UHFFFAOYSA-M triflate Chemical compound [O-]S(=O)(=O)C(F)(F)F ITMCEJHCFYSIIV-UHFFFAOYSA-M 0.000 description 1
- WFKWXMTUELFFGS-UHFFFAOYSA-N tungsten Chemical compound [W] WFKWXMTUELFFGS-UHFFFAOYSA-N 0.000 description 1
- 229910052721 tungsten Inorganic materials 0.000 description 1
- 239000010937 tungsten Substances 0.000 description 1
- 229910052720 vanadium Inorganic materials 0.000 description 1
- 238000001947 vapour-phase growth Methods 0.000 description 1
- ABDKAPXRBAPSQN-UHFFFAOYSA-N veratrole Chemical compound COC1=CC=CC=C1OC ABDKAPXRBAPSQN-UHFFFAOYSA-N 0.000 description 1
- PXXNTAGJWPJAGM-UHFFFAOYSA-N vertaline Natural products C1C2C=3C=C(OC)C(OC)=CC=3OC(C=C3)=CC=C3CCC(=O)OC1CC1N2CCCC1 PXXNTAGJWPJAGM-UHFFFAOYSA-N 0.000 description 1
- 230000029663 wound healing Effects 0.000 description 1
- 230000037303 wrinkles Effects 0.000 description 1
- 150000003751 zinc Chemical class 0.000 description 1
- YVTHLONGBIQYBO-UHFFFAOYSA-N zinc indium(3+) oxygen(2-) Chemical compound [O--].[Zn++].[In+3] YVTHLONGBIQYBO-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/14—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D235/00—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, condensed with other rings
- C07D235/02—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, condensed with other rings condensed with carbocyclic rings or ring systems
- C07D235/04—Benzimidazoles; Hydrogenated benzimidazoles
- C07D235/18—Benzimidazoles; Hydrogenated benzimidazoles with aryl radicals directly attached in position 2
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/10—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/04—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/10—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/14—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/10—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/14—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D409/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms
- C07D409/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent, e.g. electroluminescent, chemiluminescent materials
- C09K11/02—Use of particular materials as binders, particle coatings or suspension media therefor
- C09K11/025—Use of particular materials as binders, particle coatings or suspension media therefor non-luminescent particle coatings or suspension media
-
- H01L51/0052—
-
- H01L51/0067—
-
- H01L51/0072—
-
- H01L51/5012—
-
- H01L51/5072—
-
- H01L51/5096—
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/11—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/14—Carrier transporting layers
- H10K50/16—Electron transporting layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/18—Carrier blocking layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
- H10K85/624—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene containing six or more rings
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
- H10K85/626—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene containing more than one polycyclic condensed aromatic rings, e.g. bis-anthracene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/654—Aromatic compounds comprising a hetero atom comprising only nitrogen as heteroatom
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6572—Polycyclic condensed heteroaromatic hydrocarbons comprising only nitrogen in the heteroaromatic polycondensed ring system, e.g. phenanthroline or carbazole
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6574—Polycyclic condensed heteroaromatic hydrocarbons comprising only oxygen in the heteroaromatic polycondensed ring system, e.g. cumarine dyes
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K2101/00—Properties of the organic materials covered by group H10K85/00
- H10K2101/10—Triplet emission
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K2101/00—Properties of the organic materials covered by group H10K85/00
- H10K2101/90—Multiple hosts in the emissive layer
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/17—Carrier injection layers
- H10K50/171—Electron injection layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K71/00—Manufacture or treatment specially adapted for the organic devices covered by this subclass
- H10K71/10—Deposition of organic active material
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K71/00—Manufacture or treatment specially adapted for the organic devices covered by this subclass
- H10K71/10—Deposition of organic active material
- H10K71/12—Deposition of organic active material using liquid deposition, e.g. spin coating
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E10/00—Energy generation through renewable energy sources
- Y02E10/50—Photovoltaic [PV] energy
- Y02E10/549—Organic PV cells
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Physics & Mathematics (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Optics & Photonics (AREA)
- Electroluminescent Light Sources (AREA)
- Plural Heterocyclic Compounds (AREA)
- Heterocyclic Carbon Compounds Containing A Hetero Ring Having Oxygen Or Sulfur (AREA)
- Photovoltaic Devices (AREA)
- Semiconductor Lasers (AREA)
- Compositions Of Oxide Ceramics (AREA)
Abstract
본 발명은 화합물, 조성물, 및 청구된 화합물 또는 조성물을 함유하는 제형 및 전자 소자에 관한 것이다.
Description
본 발명은 화합물, 조성물, 화합물 또는 조성물을 포함하는 제형 및 전자 소자에 관한 것이다.
유기 반도체가 유기 기능성 재료로서 활용되는 유기 전계발광 소자 (예를 들어, OLED (유기 발광 다이오드) 또는 OLEC (유기 발광 전기화학 전지)) 의 구조가, 예를 들어 US 4539507, US 5151629, EP 0676461 및 WO 98/27136 에 기재되어 있다. 여기서 활용되는 발광 재료는 형광 발광체 외에도 점점더 인광을 나타내는 유기금속 착물이다 (M. A. Baldo et al., Appl. Phys. Lett. 1999, 75, 4-6). 양자-역학적 이유로, 인광 발광체로서 유기금속 화합물을 사용해 에너지 및 전력 효율에 있어서 4 배까지의 증가가 가능하다. 일반적으로, 단일선 발광을 나타내는 OLED 의 경우 및 또한 삼중선 발광을 나타내는 OLED 의 경우 둘 모두에서 특히 효율, 작동 전압 및 수명에 있어서 개선의 필요성이 여전히 존재한다.
유기 전계발광 소자의 특성은 단지 활용되는 발광체에 의해서만 결정되지 않는다. 특히, 사용되는 기타 재료, 예컨대 호스트 및 매트릭스 재료, 정공-차단 재료, 전자-수송 재료, 정공-수송 재료 및 전자- 또는 여기자-차단 재료가 또한 여기서 특히 중요하다. 이들 재료의 개선은 전계발광 소자의 상당한 개선을 유도할 수 있다.
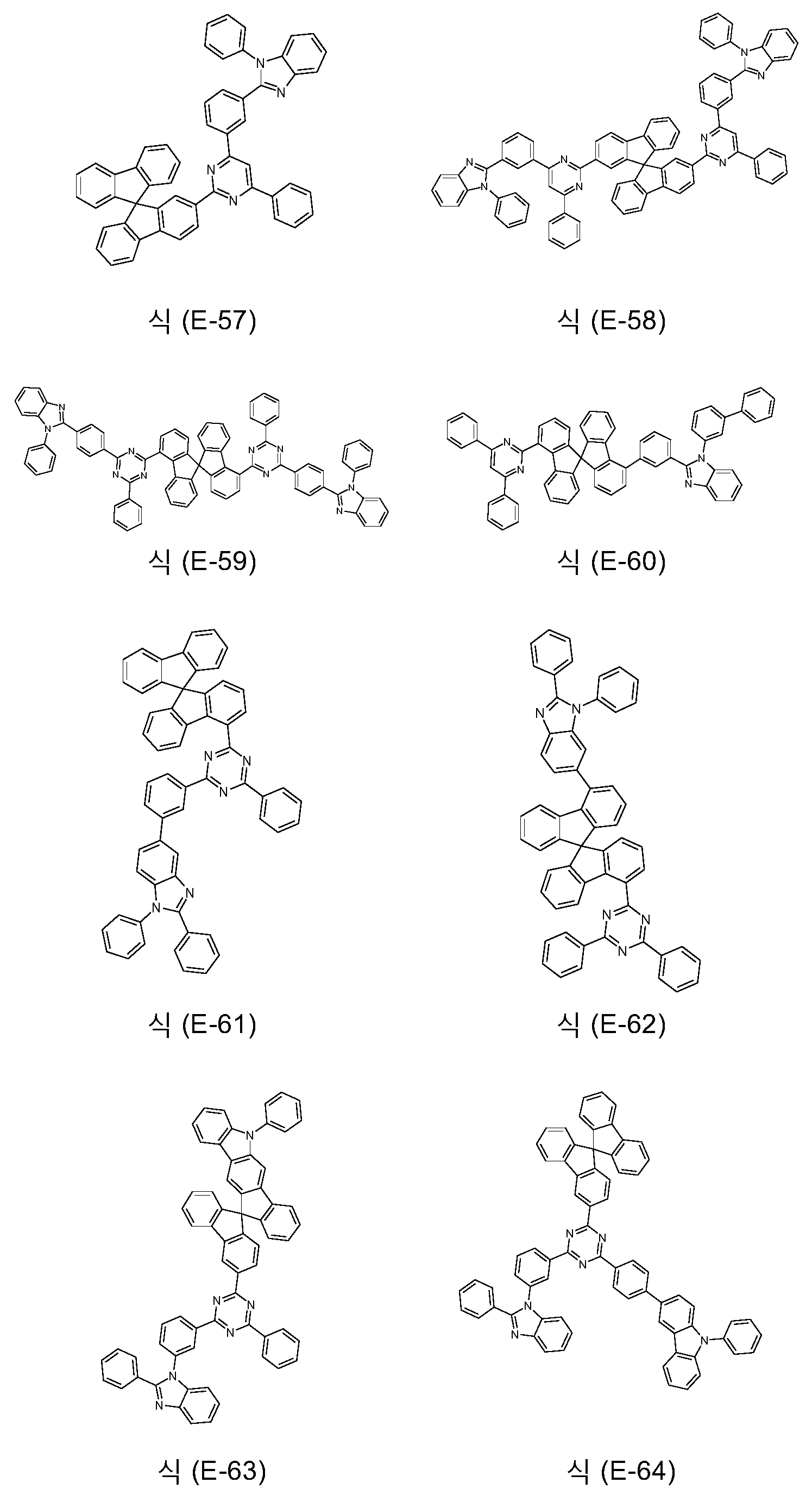
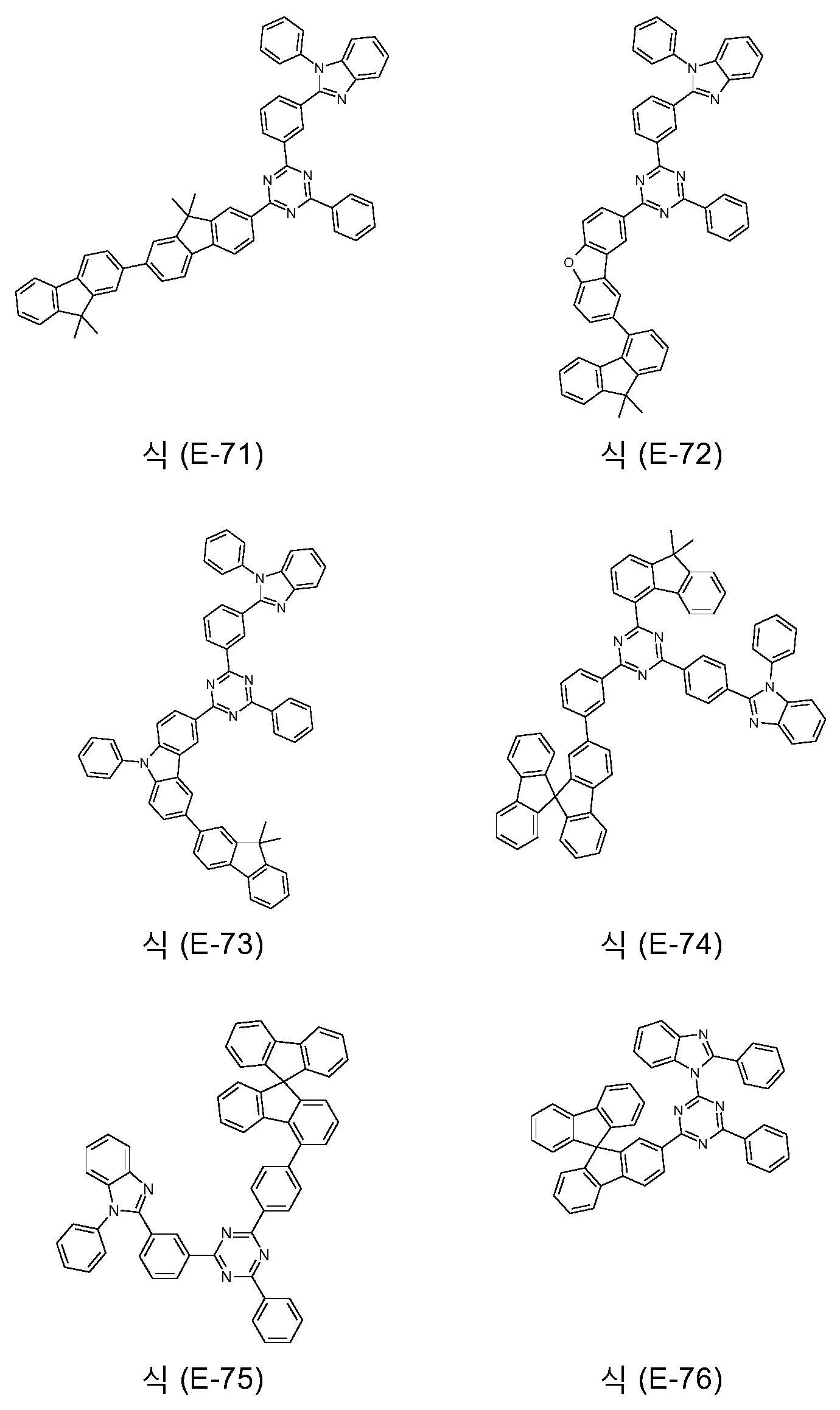
전자-수송 재료로서 트리아진 및 벤즈이미다졸기 둘 모두를 함유하는 화합물이 선행기술로부터 공지되어 있다. WO 2010/126270 은 상기 유형의 화합물을 개시한다. 둘 모두의 기는 플루오렌 골격에 결합되는데, 이때 플루오렌의 2 개의 방향족 고리는 추가의 방향족 축합 형태이다.
KR 101257695 는 또한 트리아진기 및 벤즈이미다졸기를 함유하는 플루오렌을 개시한다. 그러나, 트리아진기는 단지 3 개의 탄소-함유 위치 중 2 개에서 치환된다.
WO 2013/100464 는 벤즈이미다졸기 및 또한 트리아진기 둘 모두를 함유하는 스피로바이플루오렌을 개시한다. 그러나, 트리아진은 미치환된다. 추가로, 벤조티오펜기는 스피로바이플루오렌 상에 축합되었다.
그러나, 기타 재료의 경우와 같이 특히 이들 재료의 사용의 경우 유기 전자 소자의 효율, 작동 전압 및 수명에 있어서 개선의 필요성이 여전히 존재한다.
따라서, 본 발명의 목적은 유기 전자 소자, 특히 유기 전계발광 소자에서의 사용에 적합하고 상기 소자에서의 사용시 양호한 소자 특성을 유도하는 화합물을 제공하고, 상응하는 전자 소자를 제공하는 것이다.
놀랍게도, 하기에 보다 상세히 기재된 특정 화합물이 이들 목적을 달성하고, 선행기술로부터의 단점을 극복한다는 것을 발견하였다. 화합물의 사용은, 특히 수명, 효율 및 작동 전압에 있어서 유기 전자 소자, 특히 유기 전계발광 소자의 매우 양호한 특성을 유도한다. 따라서, 본 발명은 상기 유형의 화합물을 포함하는 전자 소자, 특히 유기 전계발광 소자, 및 상응하는 바람직한 구현예에 관한 것이다.
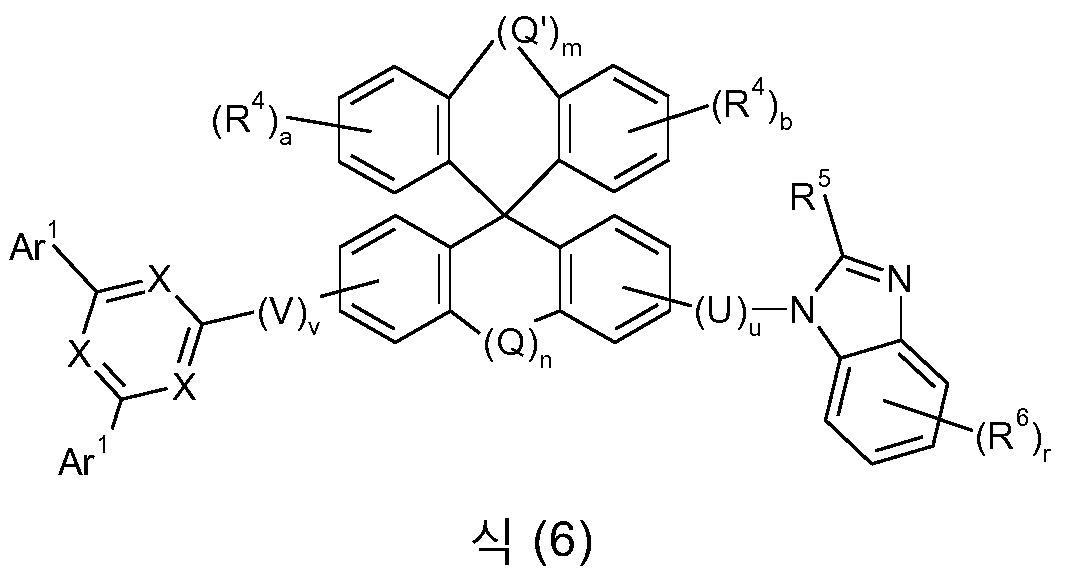
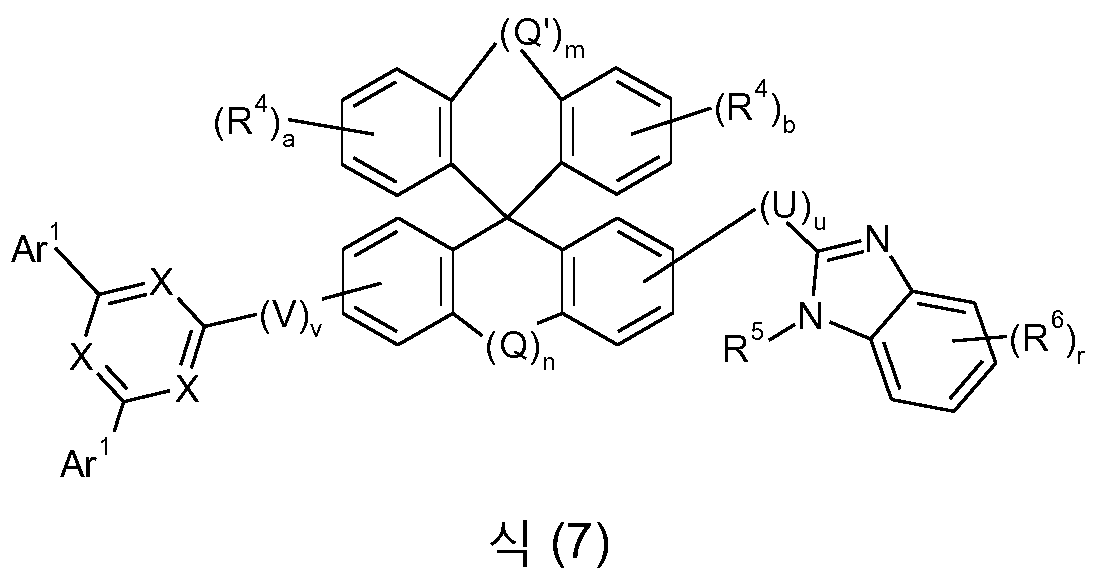
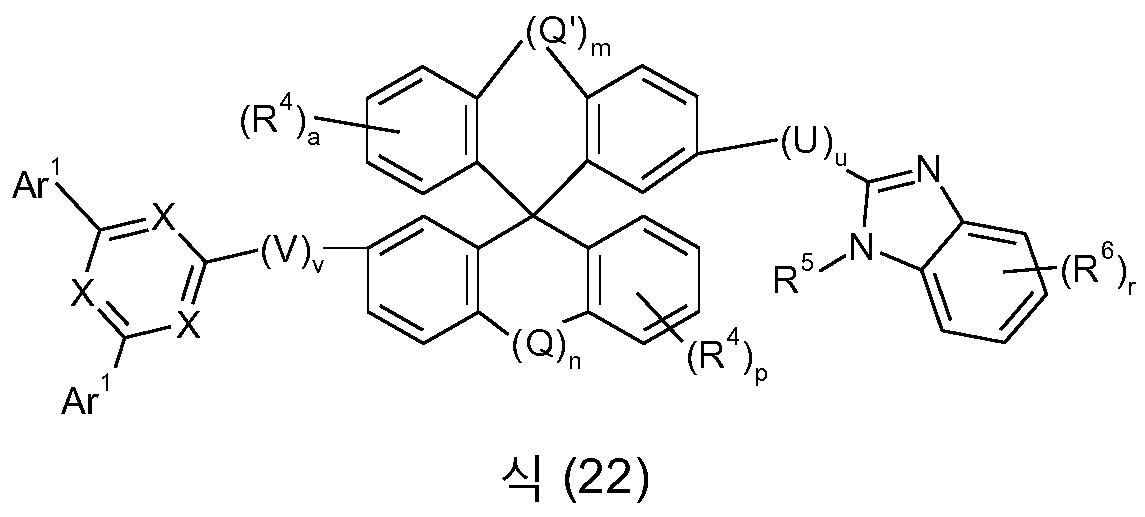
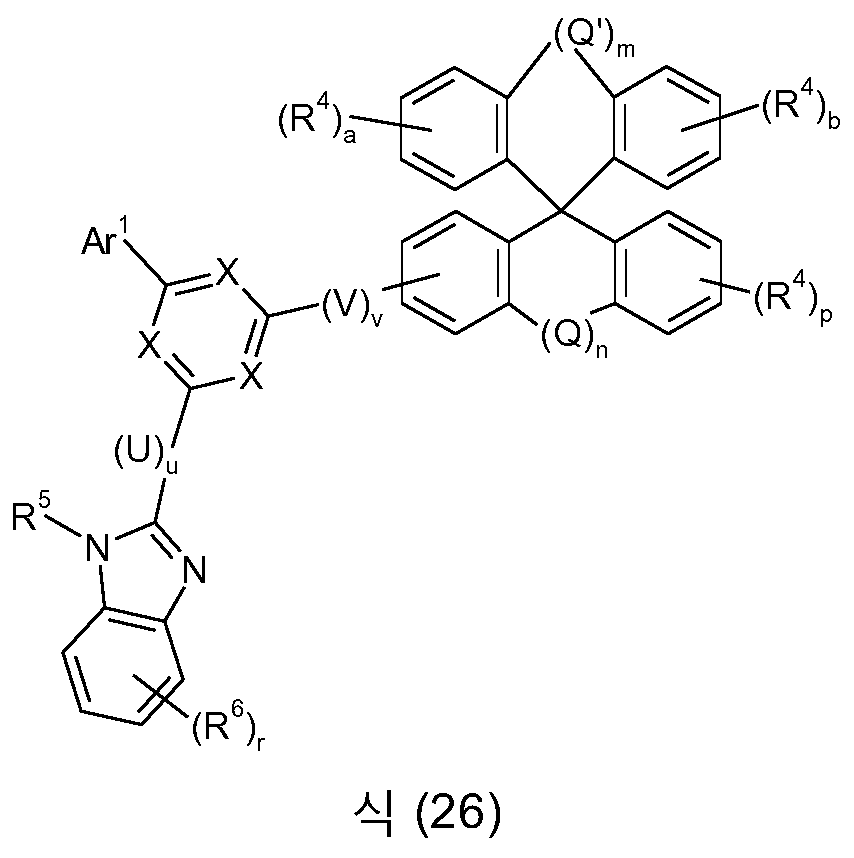
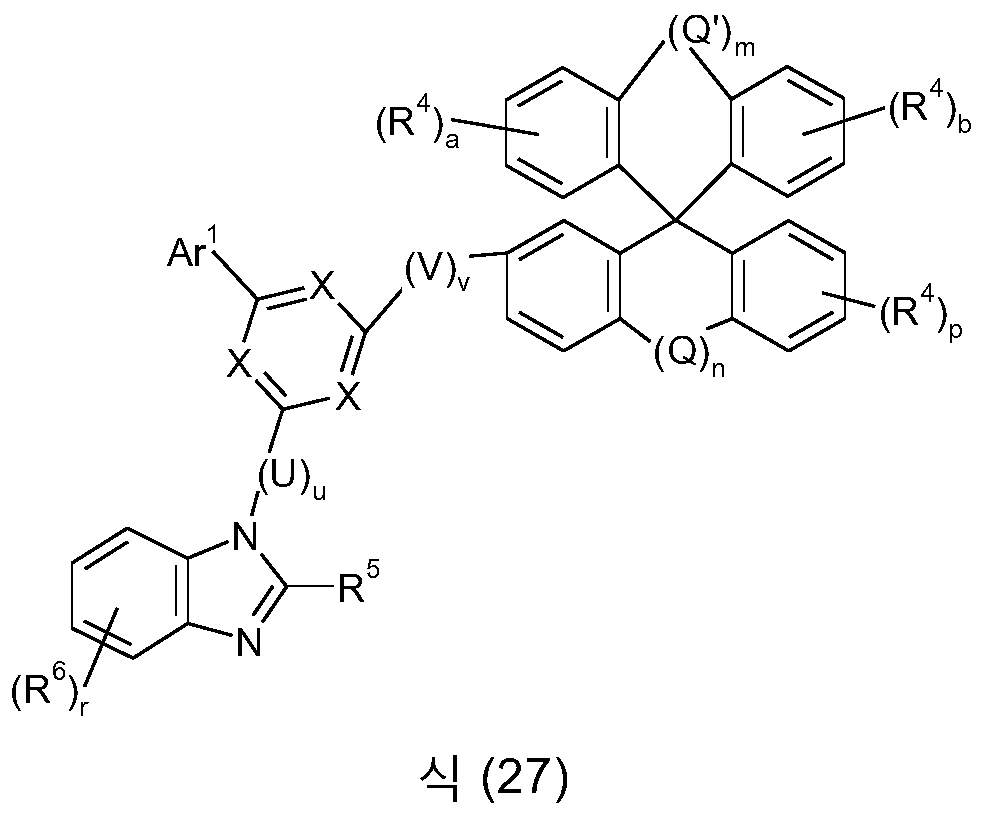
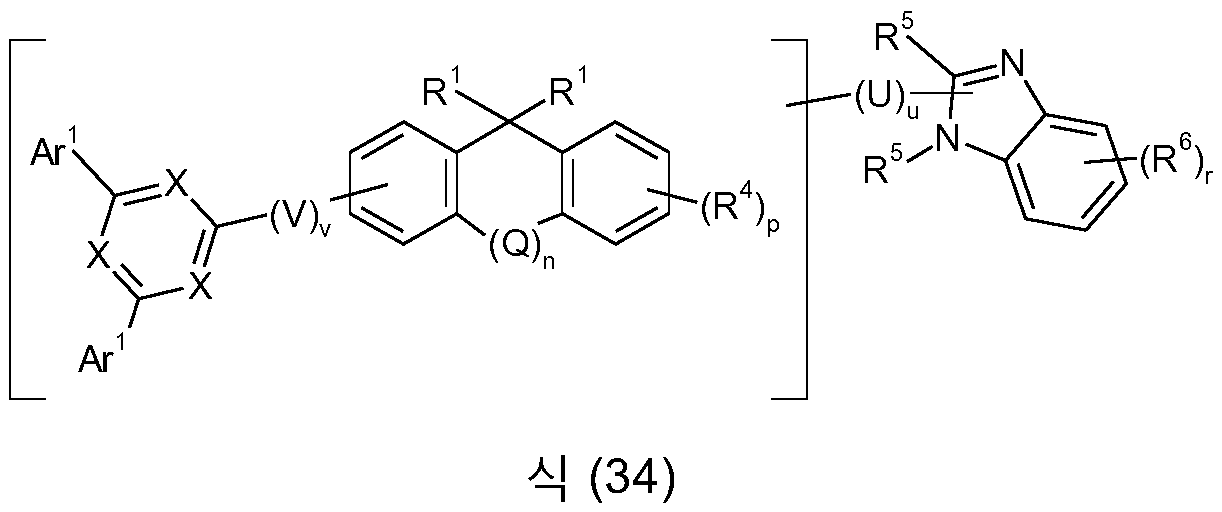
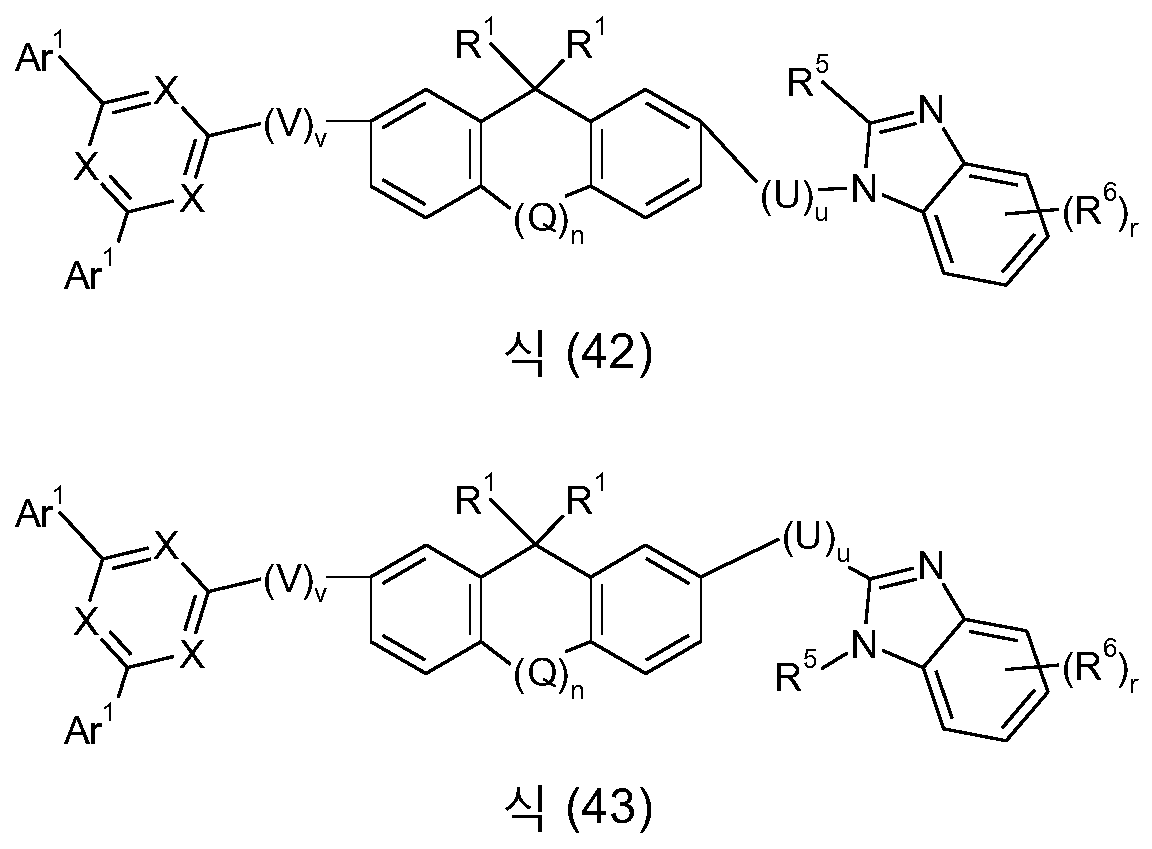
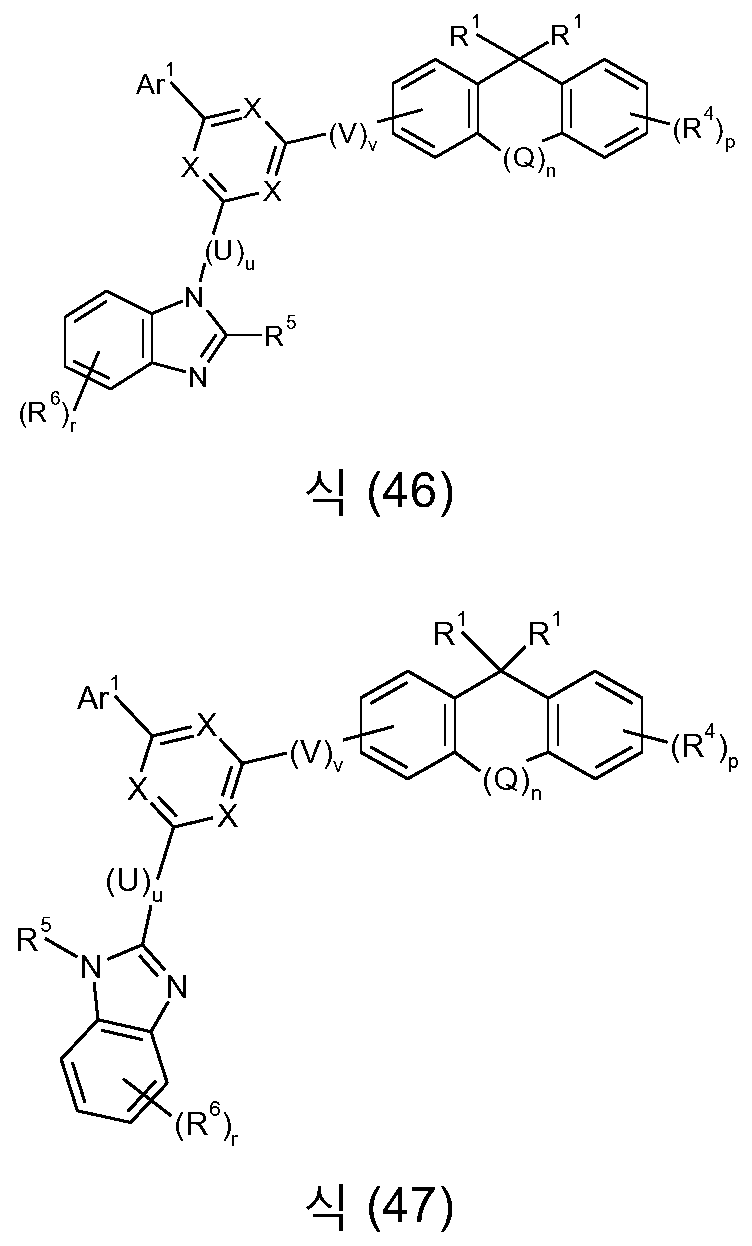
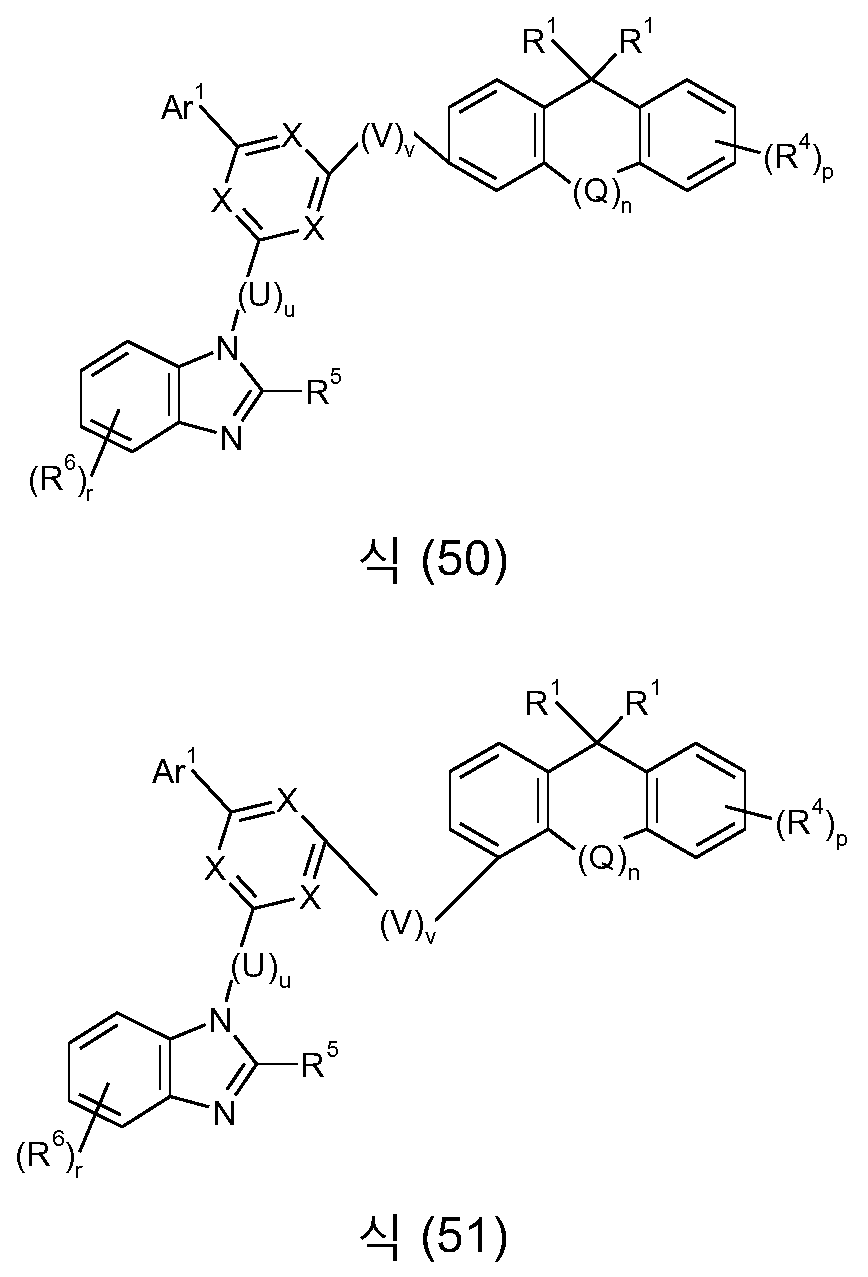
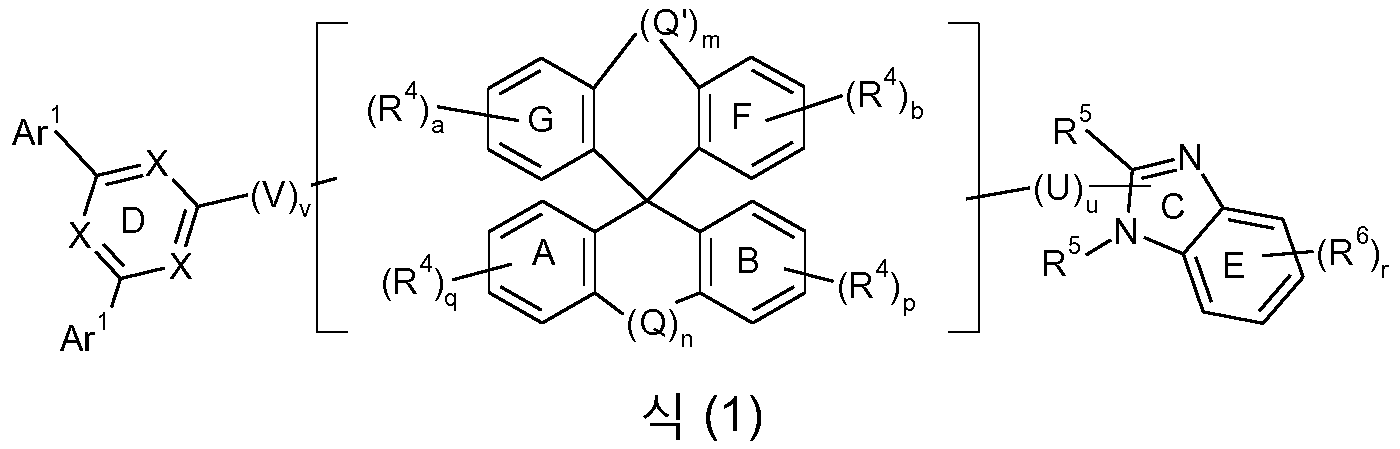
본 발명은 식 (GK-1) 의 골격 또는 대안적으로 식 (GK-2) 의 골격 및 적어도 하나 이상의 식 (G-2) 의 기 및 적어도 하나 이상의 식 (G-3) 의 기를 함유하는 화학 화합물에 관한 것이다:
[식 중, 본 발명에 따른 화합물이 단 하나의 식 (GK-1) 의 기 또는 대안적으로 단 하나의 식 (GK-2) 의 기를 함유하는 경우가 바람직하고;
식 (GK-1) 의 골격 및 식 (G-2) 및 (G-3) 의 기가 서로 공유 결합되거나,
또는 대안적으로 식 (GK-2) 의 골격 및 식 (G-2) 및 (G-3) 의 기가 서로 공유 결합되고;
사용되는 기호 및 지수에 하기 정의가 적용됨:
R1
은 각 경우에 동일 또는 상이하게 H, D, F, Cl, Br, I, CHO, N(Ar1)2, C(=O)Ar1, P(=O)(Ar1)2, S(=O)Ar1, S(=O)2Ar1, CR2=CR2Ar1, CN, NO2, Si(R2)3, B(OR2)2, B(R2)2, B(N(R2)2)2, OSO2R2, 1 내지 40 개의 C 원자를 갖는 직쇄 알킬, 알콕시 또는 티오알콕시기, 또는 2 내지 40 개의 C 원자를 갖는 직쇄 알케닐 또는 알키닐기, 또는 3 내지 40 개의 C 원자를 갖는 분지형 또는 시클릭 알킬, 알케닐, 알키닐, 알콕시 또는 티오알콕시기 (이들 각각은 하나 이상의 라디칼 R2 에 의해 치환될 수 있고, 하나 이상의, 바람직하게는 비인접한 CH2 기는 R2C=CR2, C≡C, Si(R2)2, Ge(R2)2, Sn(R2)2, C=O, C=S, C=Se, C=NR2, P(=O)(R2), SO, SO2, NR2, O, S 또는 CONR2 에 의해 대체될 수 있고, 하나 이상의 H 원자는 D, F, Cl, Br, I, CN 또는 NO2 에 의해 대체될 수 있음), 또는 5 내지 60 개의 방향족 고리 원자를 갖는 방향족 또는 헤테로방향족 고리계 (이는 각 경우에 하나 이상의 라디칼 R2 에 의해 치환될 수 있음), 또는 5 내지 60 개의 방향족 고리 원자를 갖는 아릴옥시 또는 헤테로아릴옥시기 (이는 하나 이상의 라디칼 R2 에 의해 치환될 수 있음), 또는 이들 계의 조합이고; 2 개 이상의 인접한 치환기 R1 은 여기서 서로 모노- 또는 폴리시클릭, 지방족 또는 방향족 고리계를 형성할 수 있고;
R2
는 동일 또는 상이하게 각 경우에 H, D, F, Cl, Br, I, N(R3)2, CN, NO2, Si(R3)3, B(OR3)2, C(=O)R3, P(=O)(R3)2, S(=O)R3, S(=O)2R3, OSO2R3, 1 내지 40 개의 C 원자를 갖는 직쇄 알킬, 알콕시 또는 티오알콕시기, 또는 2 내지 40 개의 C 원자를 갖는 직쇄 알케닐 또는 알키닐기, 또는 3 내지 40 개의 C 원자를 갖는 분지형 또는 시클릭 알킬, 알케닐, 알키닐, 알콕시, 알킬알콕시 또는 티오알콕시기 (이들 각각은 하나 이상의 라디칼 R3 에 의해 치환될 수 있고, 하나 이상의 비인접한 CH2 기는 R3C=CR3, C≡C, Si(R3)2, Ge(R3)2, Sn(R3)2, C=O, C=S, C=Se, C=NR3, P(=O)(R3), SO, SO2, NR3, O, S 또는 CONR3 에 의해 대체될 수 있고, 하나 이상의 H 원자는 D, F, Cl, Br, I, CN 또는 NO2 에 의해 대체될 수 있음), 또는 5 내지 60 개의 방향족 고리 원자를 갖는 방향족 또는 헤테로방향족 고리계 (이는 각 경우에 하나 이상의 라디칼 R3 에 의해 치환될 수 있음), 또는 5 내지 60 개의 방향족 고리 원자를 갖는 아릴옥시, 아릴알콕시 또는 헤테로아릴옥시기 (이는 하나 이상의 라디칼 R3 에 의해 치환될 수 있음), 또는 10 내지 40 개의 방향족 고리 원자를 갖는 디아릴아미노기, 디헤테로아릴아미노기 또는 아릴헤테로아릴아미노기 (이는 하나 이상의 라디칼 R3 에 의해 치환될 수 있음), 또는 이들 기의 2 개 이상의 조합이고; 2 개 이상의 인접한 라디칼 R2 는 여기서 서로 모노- 또는 폴리시클릭, 지방족 또는 방향족 고리계를 형성할 수 있고; 2 개 이상의 인접한 치환기 R2 가 서로 모노- 또는 폴리시클릭, 지방족 또는 방향족 고리계를 형성하지 않은 경우가 바람직하고;
R3
은 동일 또는 상이하게 각 경우에 H, D, F 또는 1 내지 20 개의 C 원자를 갖는 지방족, 방향족 및/또는 헤테로방향족 탄화수소 라디칼 (이때, 추가로 하나 이상의 H 원자는 F 에 의해 대체될 수 있음) 이고; 2 개 이상의 치환기 R3 은 여기서 또한 서로 모노- 또는 폴리시클릭, 지방족 또는 방향족 고리계를 형성할 수 있고; 2 개 이상의 인접한 치환기 R3 이 서로 모노- 또는 폴리시클릭, 지방족 또는 방향족 고리계를 형성하지 않은 경우가 바람직하고;
R5
는 각 경우에 동일 또는 상이하게 F, Cl, Br, I, CHO, N(Ar1)2, C(=O)Ar1, P(=O)(Ar1)2, S(=O)Ar1, S(=O)2Ar1, CR2=CR2Ar1, CN, NO2, Si(R2)3, B(OR2)2, B(R2)2, B(N(R2)2)2, OSO2R2, 1 내지 40 개의 C 원자를 갖는 직쇄 알킬, 알콕시 또는 티오알콕시기, 또는 2 내지 40 개의 C 원자를 갖는 직쇄 알케닐 또는 알키닐기, 또는 3 내지 40 개의 C 원자를 갖는 분지형 또는 시클릭 알킬, 알케닐, 알키닐, 알콕시 또는 티오알콕시기 (이들 각각은 하나 이상의 라디칼 R2 에 의해 치환될 수 있고, 하나 이상의, 바람직하게는 비인접한 CH2 기는 R2C=CR2, C≡C, Si(R2)2, Ge(R2)2, Sn(R2)2, C=O, C=S, C=Se, C=NR2, P(=O)(R2), SO, SO2, NR2, O, S 또는 CONR2 에 의해 대체될 수 있고, 하나 이상의 H 원자는 D, F, Cl, Br, I, CN 또는 NO2 에 의해 대체될 수 있음), 또는 5 내지 60 개의 방향족 고리 원자를 갖는 방향족 또는 헤테로-방향족 고리계 (이는 각 경우에 하나 이상의 라디칼 R2 에 의해 치환될 수 있음), 또는 5 내지 60 개의 방향족 고리 원자를 갖는 아릴옥시 또는 헤테로아릴옥시기 (이는 하나 이상의 라디칼 R2 에 의해 치환될 수 있음), 또는 이들 계의 조합이고; 2 개 이상의 인접한 치환기 R5 는 서로 모노- 또는 폴리시클릭, 지방족 또는 방향족 고리계를 형성할 수 없고;
R4 및 R6
은 각 경우에 동일 또는 상이하게 H, D, F, Cl, Br, I, CHO, N(Ar1)2, C(=O)Ar1, P(=O)(Ar1)2, S(=O)Ar1, S(=O)2Ar1, CR2=CR2Ar1, CN, NO2, Si(R2)3, B(OR2)2, B(R2)2, B(N(R2)2)2, OSO2R2, 1 내지 40 개의 C 원자를 갖는 직쇄 알킬, 알콕시 또는 티오알콕시기, 또는 2 내지 40 개의 C 원자를 갖는 직쇄 알케닐 또는 알키닐기, 또는 3 내지 40 개의 C 원자를 갖는 분지형 또는 시클릭 알킬, 알케닐, 알키닐, 알콕시 또는 티오알콕시기 (이들 각각은 하나 이상의 라디칼 R2 에 의해 치환될 수 있고, 하나 이상의, 바람직하게는 비인접한 CH2 기는 R2C=CR2, C≡C, Si(R2)2, Ge(R2)2, Sn(R2)2, C=O, C=S, C=Se, C=NR2, P(=O)(R2), SO, SO2, NR2, O, S 또는 CONR2 에 의해 대체될 수 있고, 하나 이상의 H 원자는 D, F, Cl, Br, I, CN 또는 NO2 에 의해 대체될 수 있음), 또는 5 내지 60 개의 방향족 고리 원자를 갖는 방향족 또는 헤테로방향족 고리계 (이는 각 경우에 하나 이상의 라디칼 R2 에 의해 치환될 수 있음), 또는 5 내지 60 개의 방향족 고리 원자를 갖는 아릴옥시 또는 헤테로아릴옥시기 (이는 하나 이상의 라디칼 R2 에 의해 치환될 수 있음), 또는 이들 계의 조합이고; 2 개 이상의 인접한 치환기 R4 는 서로 모노- 또는 폴리시클릭, 지방족 또는 방향족 고리계를 형성할 수 없고; 2 개 이상의 인접한 치환기 R6 은 서로 모노- 또는 폴리시클릭, 지방족 또는 방향족 고리계를 형성할 수 있고, 2 개 이상의 인접한 치환기 R6 이 서로 모노- 또는 폴리시클릭, 지방족 또는 방향족 고리계를 형성할 수 없는 경우가 바람직하고;
Q, Q'
는 서로 동일 또는 상이하게 C=O, C=S, S, C(R2)2, NR2 또는 O, 바람직하게는 C(R2)2, NR2 또는 O, 매우 바람직하게는 C(R2)2 또는 NR2, 특히 바람직하게는 C(R2)2 이고;
n
은 0 또는 1 이며, 이때 n = 0 인 것이 바람직하고, n = 0 인 것은 2 개의 방향족 고리 A 및 B 가 기 Q 를 통해 서로 연결되지 않지만 대신에 단일 결합에 의해 연결되는 것을 의미하고;
m
은 0 또는 1 이며, 이때 m = 0 인 것이 바람직하고, m = 0 인 것은 2 개의 방향족 고리가 기 Q' 를 통해 서로 연결되지 않지만 대신에 단일 결합에 의해 연결되는 것을 의미하고;
p
는 0, 1, 2, 3 또는 4, 바람직하게는 0, 1 또는 2, 매우 바람직하게는 0 또는 1, 특히 바람직하게는 0 이고;
q
는 0, 1, 2, 3 또는 4, 바람직하게는 0, 1 또는 2, 매우 바람직하게는 0 또는 1, 특히 바람직하게는 0 이고;
p+q
는 항상 7 이하이고, p+q 는 바람직하게는 0, 1, 2 또는 3 이고, p+q 는 매우 바람직하게는 0, 1 또는 2 이고, p+q 는 특히 바람직하게는 0 또는 1 이고, p+q 는 매우 특히 바람직하게는 0 이고;
a
는 0, 1, 2, 3 또는 4, 바람직하게는 0, 1 또는 2, 매우 바람직하게는 0 또는 1, 특히 바람직하게는 0 이고;
b
는 0, 1, 2, 3 또는 4, 바람직하게는 0, 1 또는 2, 매우 바람직하게는 0 또는 1, 특히 바람직하게는 0 이고;
a+b
는 항상 7 이하이고, a+b 는 바람직하게는 0, 1, 2 또는 3 이고, a+b 는 매우 바람직하게는 0, 1 또는 2 이고, a+b 는 특히 바람직하게는 0 또는 1 이고, a+b 는 매우 특히 바람직하게는 0 이고;
r
은 0, 1, 2, 3 또는 4, 바람직하게는 0, 1 또는 2, 매우 바람직하게는 0 또는 1 이고, r 은 특히 바람직하게는 0 이고;
X
는 동일 또는 상이하게 각 경우에 N 또는 CR1 이고, 하나 이상의 X 는 N 이고, 바람직하게는 X 중 2 개 이상은 N 이고, 매우 바람직하게는 X 3 개 모두는 N 이고;
Ar1
은 각 경우에 동일 또는 상이하게 5 내지 30 개의 방향족 고리 원자를 갖는 방향족 또는 헤테로방향족 고리계 (이는 하나 이상의 라디칼 R2 에 의해 치환될 수 있음) 이고; 라디칼 Ar1 중 2 개는 여기서 또한 B(R2), C(R2)2, Si(R2)2, C=O, C=NR2, C=C(R2)2, O, S, S=O, SO2, N(R2), P(R2) 및 P(=O)R2 로부터 선택되는 브릿지 또는 단일 결합에 의해 서로 연결될 수 있고; 2 개의 라디칼 Ar1 이 서로 연결되지 않은 경우가 바람직함].
식 (GK-1) 의 골격 및 2 개의 식 (G-2) 및 (G-3) 의 기를 함유하는 화합물이 추가의 스피로바이플루오렌기를 함유하지 않고 추가의 플루오렌기를 함유하지 않은 경우가 바람직하다.
식 (GK-2) 의 골격 및 2 개의 식 (G-2) 및 (G-3) 의 기를 함유하는 화합물이 추가의 스피로바이플루오렌기를 함유하지 않고 추가의 플루오렌기를 함유하지 않는 경우 나아가 바람직하다.
바람직한 구현예에서, 식 (G-2) 의 기 및 또한 식 (G-3) 의 기 둘 모두는 단지 골격 (GK-1) 또는 (GK-2) 의 방향족 또는 헤테로방향족 고리에 결합된다.
식 (GK-1) 의 골격 또는 대안적으로 식 (GK-2) 의 골격 및 각 경우에 적어도 하나 이상의 식 (G-2) 의 기 및 각 경우에 적어도 하나 이상의 식 (G-3) 의 기를 함유하는 본 발명에 따른 화합물의 분자량이 최대 3000 g/mol 이하, 바람직하게는 최대 2000 g/mol 이하, 매우 바람직하게는 최대 1500 g/mol 이하, 매우 특히 바람직하게는 최대 1000 g/mol 이하인 경우가 바람직하다.
2 개 이상의 인접한 라디칼 R1 내지 R6 중 어느 것도 서로 모노- 또는 폴리-시클릭, 지방족 또는 방향족 고리계를 형성할 수 없는 경우 본 발명의 목적상 나아가 바람직하다.
2 개 이상의 인접한 라디칼이 서로 모노- 또는 폴리시클릭, 지방족 또는 방향족 고리계를 형성할 수 있다는 점은, 2 개 이상의 인접한 라디칼이 고리 또는 고리계의 부분이 된다는 것을 의미한다. 예를 들어, 라디칼 R4 의 경우와 같이 2 개 이상의 인접한 라디칼이 서로 모노- 또는 폴리시클릭, 지방족 또는 방향족 고리계를 형성할 수 없는 것이 요구된다면, 2 개 이상의 라디칼 R4 는 고리 또는 고리계의 부분일 수 없다. 하기 경우는 식 (GK-1) 및 라디칼 R4, R2 및 R3 의 정의를 참조해 이를 도식으로 예시한다. 상기 정의에 따라, 고리 폐쇄는 2 개 이상의 라디칼 R4 에서 허용되지 않는다 (사례 1). 그러나, R4 는 상기 지시된 바와 같이 R2 로 추가 치환될 수 있으며, 이때 2 개 이상의 인접한 라디칼 R2 는 서로 모노- 또는 폴리시클릭, 지방족 또는 방향족 고리계를 형성할 수 있다. 이는, 2 개 이상의 라디칼 R2 가 고리 또는 고리계를 형성할 수 있을지라도 (사례 2), 다양한 라디칼 R4 가 고리 또는 고리계의 부분이 되는 방식으로 실시될 수 없는 것 (사례 3) 을 의미한다. 라디칼 R2 의 정의에 따라, 이는 라디칼 R3 에 의해 치환될 수 있으며, 이때 2 개 이상의 인접한 라디칼 R3 은 서로 모노- 또는 폴리시클릭, 지방족 또는 방향족 고리계를 형성할 수 있다. 그러나, 이는 라디칼 R4 중 2 개 이상이 고리의 부분이 되지 않는 방식으로만 단지 허용가능하다 (사례 4).
골격이 일반식 (GK-3) 을 갖는 경우 매우 바람직하다:
골격이 일반식 (GK-4) 를 갖는 경우 매우 특히 바람직하다:
마지막으로, 골격이 일반식 (GK-5) 를 갖는 경우 특히 바람직하다:
골격이 일반식 (GK-6) 을 갖는 경우 나아가 매우 바람직하다:
골격이 일반식 (GK-7) 을 갖는 경우 나아가 매우 특히 바람직하다:
바람직한 구현예에서, 본 발명은 일반식 (1) 의 화합물에 관한 것이다:
[식 중, 상기 지시된 바와 같이 지수 및 기호가 정의되고, 나아가:
V
는 2 가기이고;
U
는 2 가기이고;
v
는 0 또는 1 이며, 이때 v = 0 인 것은 고리 D 가 단일 공유 결합을 통해 화합물의 나머지에 직접 연결되는 것을 의미하고;
u
는 0 또는 1 이며, 이때 u = 0 인 것은 고리 C 가 단일 공유 결합을 통해 화합물의 나머지에 직접 연결되는 것을 의미함].
식 (1) 에 따라, 고리 D 는 예를 들어 V 를 통해 고리 A 에 결합될 수 있지만, 고리 C 는 U 를 통해 임의의 목적하는 다른 부위에 결합될 수 있다.
고리 D 가 V 를 통해 지시된 고리 A, B, C, E, F 또는 G 중 하나에 공유 결합되는 경우 및 고리 C 가 U 를 통해 지시된 고리 A, B, D, F 또는 G 중 하나에 공유 결합되는 경우가 바람직하며, 이때 2 개의 고리 C 및 D 중 하나 이상은 2 가기 U 또는 V 를 통해 고리 A, B, F 또는 G 중 하나에 공유 결합된다.
고리 C 를 함유하는 치환기는 여기서 하기 나타낸 2 개의 식 중 하나에 따라 결합되고, 따라서 각 경우에 고리 C 에서 라디칼 R5 중 하나를 대체한다.
V 및 U 가 동일 또는 상이하게 각 경우에 5 내지 60 개의 고리 원자를 함유하는 방향족 또는 헤테로방향족 고리계를 나타내는 경우가 바람직하다. U 및 V 가 페닐렌, 바이페닐렌 또는 터페닐렌기, 매우 특히 바람직하게는 페닐렌 또는 바이페닐렌기, 특히 바람직하게는 페닐렌기인 경우 매우 바람직하다.
고리 D 가 브릿지 V 를 통해 고리 A 에 직접 결합되는 경우가 바람직하며, 이때 q 는 최대 3 일 수 있다. 고리 C 가 마찬가지로 브릿지 U 를 통해 A 에 직접 결합되는 경우, q 는 최대 2 이다. 나아가, 고리 C 가 브릿지 U 를 통해 고리 B 에 직접 결합되는 경우 p 가 최대 3 일 수 있는 것은 말할 것도 없다. 전체적으로 유사하게, 파라미터 a 및 b 의 최대 값은 식 (G-2) 및 (G-3) 의 기에 의한 고리 G 및 F 의 치환에 따라 다르다.
따라서 또한 식 (1) 의 화합물에 대한 표기는, 예를 들어 고리 D 를 함유하는 기가 우선 골격의 고리 A 에 결합되고 고리 C 를 함유하는 기가 고리 D 를 함유하는 기에 결합될 수 있는 것을 의미한다.
바람직한 것은 나아가 일반식 (4) 의 화합물이다:
식 중, 사용된 기호 및 지수에 상기 정의가 적용되고, 그 바람직한 구현예는 또한 식 (4) 의 화합물의 바람직한 구현예를 나타냄.
바람직한 것은 나아가 일반식 (5) 의 화합물이다:
식 중, 사용된 기호 및 지수에 상기 정의가 적용되고, 그 바람직한 구현예는 또한 식 (5) 의 화합물의 바람직한 구현예를 나타냄.
바람직한 것은 나아가 일반식 (6) 의 화합물이다:
식 중, 사용된 기호 및 지수에 상기 정의가 적용되고, 그 바람직한 구현예는 또한 식 (6) 의 화합물의 바람직한 구현예를 나타냄.
바람직한 것은 나아가 일반식 (7) 의 화합물이다:
식 중, 사용된 기호 및 지수에 상기 정의가 적용되고, 그 바람직한 구현예는 또한 식 (7) 의 화합물의 바람직한 구현예를 나타냄.
크게 바람직한 것은 하기 일반식 (8) 내지 (10) 의 화합물로서, 이때 사용된 기호 및 지수에 상기 정의가 적용되고, 그 바람직한 구현예는 또한 식 (8) 내지 (10) 의 화합물의 바람직한 구현예를 나타낸다:
이때, 식 (8) 내지 (10) 의 화합물 중에서, 식 (8) 및 (10) 의 화합물이 특히 바람직함.
특히 바람직한 것은 하기 일반식 (11) 의 화합물로서, 이때 상기 정의는 사용된 기호 및 지수에 적용되고, 그 바람직한 구현예는 또한 식 (11) 의 화합물의 바람직한 구현예를 나타낸다:
매우 특히 바람직한 것은 하기 일반식 (12) 및 (13) 의 화합물로서, 이때 사용된 기호 및 지수에 상기 정의가 적용되고, 그 바람직한 구현예는 또한 식 (12) 및 (13) 의 화합물의 바람직한 구현예를 나타낸다:
추가의 바람직한 구현예에서, 화합물은 일반식 (14) 를 갖는다:
식 중, 사용된 기호 및 지수에 상기 정의가 적용되고, 그 바람직한 구현예는 또한 식 (14) 의 화합물의 바람직한 구현예를 나타냄.
바람직한 것은 나아가 일반식 (15) 의 화합물이다:
식 중, 사용된 기호 및 지수에 상기 정의가 적용되고, 그 바람직한 구현예는 또한 식 (15) 의 화합물의 바람직한 구현예를 나타냄.
바람직한 것은 나아가 일반식 (16) 의 화합물이다:
식 중, 사용된 기호 및 지수에 상기 정의가 적용되고, 그 바람직한 구현예는 또한 식 (16) 의 화합물의 바람직한 구현예를 나타냄.
크게 바람직한 것은 하기 일반식 (17) 내지 (19) 의 화합물로서, 이때 사용된 기호 및 지수에 상기 정의가 적용되고, 그 바람직한 구현예는 또한 식 (17) 내지 (19) 의 화합물의 바람직한 구현예를 나타낸다:
이때, 일반식 (17) 내지 (19) 의 화합물 중에서, 식 (17) 및 (19) 의 화합물이 특히 바람직함.
특히 바람직한 것은 하기 일반식 (20) 의 화합물로서, 이때 사용된 기호 및 지수에 상기 정의가 적용되고, 그 바람직한 구현예는 또한 식 (20) 의 화합물의 바람직한 구현예를 나타낸다:
매우 특히 바람직한 것은 하기 일반식 (21) 및 (22) 의 화합물로서, 이때 사용된 기호 및 지수에 상기 정의가 적용되고, 그 바람직한 구현예는 또한 식 (21) 및 (22) 의 화합물의 바람직한 구현예를 나타낸다:
추가의 바람직한 구현예에서, 화합물은 일반식 (23) 을 갖는다:
식 중, 사용된 기호 및 지수에 상기 정의가 적용되고, 그 바람직한 구현예는 또한 식 (23) 의 화합물의 바람직한 구현예를 나타냄.
바람직한 것은 나아가 일반식 (23a) 의 화합물이다:
식 중, 사용된 기호 및 지수에 상기 정의가 적용되고, 그 바람직한 구현예는 또한 식 (23a) 의 화합물의 바람직한 구현예를 나타냄.
크게 바람직한 것은 여기서 일반식 (24) 의 화합물로서, 이때 사용된 기호 및 지수에 상기 정의가 적용되고, 그 바람직한 구현예는 또한 식 (24) 의 화합물의 바람직한 구현예를 나타낸다:
크게 바람직한 것은 나아가 여기서 일반식 (24a) 의 화합물로서, 이때 사용된 기호 및 지수에 상기 정의가 적용되고, 그 바람직한 구현예는 또한 식 (24a) 의 화합물의 바람직한 구현예를 나타낸다:
특히 바람직한 것은 여기서 일반식 (25) 및 (26) 의 화합물로서, 이때 사용된 기호 및 지수에 상기 정의가 적용되고, 그 바람직한 구현예는 또한 식 (25) 및 (26) 의 화합물의 바람직한 구현예를 나타낸다:
매우 특히 바람직한 것은 여기서 일반식 (27) 내지 (29) 의 화합물로서, 이때 사용된 기호 및 지수에 상기 정의가 적용되고, 그 바람직한 구현예는 또한 식 (27) 내지 (29) 의 화합물의 바람직한 구현예를 나타낸다:
매우 특히 바람직한 것은 나아가 여기서 일반식 (30) 내지 (32) 의 화합물로서, 이때 사용된 기호 및 지수에 상기 정의가 적용되고, 그 바람직한 구현예는 또한 식 (30) 내지 (32) 의 화합물의 바람직한 구현예를 나타낸다:
추가의 바람직한 구현예에서, 본 발명은 일반식 (33) 의 화합물에 관한 것이다:
식 중, 지수 및 기호 및 그 바람직한 구현예는 상기 지시된 바와 같이 정의됨.
식 (1) 에 따라, 고리 D 는 예를 들어 V 를 통해 고리 A 에 결합될 수 있지만, 고리 C 를 U 를 통해 임의의 목적하는 다른 부위에 결합될 수 있다.
고리 D 가 V 를 통해 지시된 고리 A, B, C 또는 E 중 하나에 공유 결합되는 경우 및 고리 C 가 U 를 통해 지시된 고리 A, B 또는 D 중 하나에 공유 결합되는 경우가 바람직하며, 이때 2 개의 고리 C 및 D 중 하나 이상은 각각 2 가기 U 또는 V 를 통해 고리 A 또는 B 중 하나에 공유 결합된다.
바람직한 것은 나아가 일반식 (34) 의 화합물이다:
식 중, 사용된 기호 및 지수에 상기 정의가 적용되고, 그 바람직한 구현예는 또한 식 (34) 의 화합물의 바람직한 구현예를 나타냄.
바람직한 것은 나아가 일반식 (35) 의 화합물이다:
식 중, 사용된 기호 및 지수에 상기 정의가 적용되고, 그 바람직한 구현예는 또한 식 (35) 의 화합물의 바람직한 구현예를 나타냄.
바람직한 것은 나아가 일반식 (36) 의 화합물이다:
식 중, 사용된 기호 및 지수에 상기 정의가 적용되고, 그 바람직한 구현예는 또한 식 (36) 의 화합물의 바람직한 구현예를 나타냄.
바람직한 것은 나아가 일반식 (37) 의 화합물이다:
식 중, 사용된 기호 및 지수에 상기 정의가 적용되고, 그 바람직한 구현예는 또한 식 (37) 의 화합물의 바람직한 구현예를 나타냄.
크게 바람직한 것은 하기 일반식 (38) 내지 (40) 의 화합물로서, 이때 사용된 기호 및 지수에 상기 정의가 적용되고, 그 바람직한 구현예는 또한 식 (38) 내지 (40) 의 화합물의 바람직한 구현예를 나타낸다:
이때, 일반식 (38) 내지 (40) 의 화합물 중에서, 식 (38) 및 (40) 의 화합물이 특히 바람직함.
크게 바람직한 것은 하기 일반식 (41) 의 화합물로서, 이때 사용된 기호 및 지수에 상기 정의가 적용되고, 그 바람직한 구현예는 또한 식 (41) 의 화합물의 바람직한 구현예를 나타낸다:
크게 바람직한 것은 하기 일반식 (42) 및 (43) 의 화합물로서, 이때 사용된 기호 및 지수에 상기 정의가 적용되고, 그 바람직한 구현예는 또한 식 (42) 및 (43) 의 화합물의 바람직한 구현예를 나타낸다:
추가의 바람직한 구현예에서, 화합물은 일반식 (44) 를 갖는다:
식 중, 사용된 기호 및 지수에 상기 정의가 적용되고, 그 바람직한 구현예는 또한 식 (44) 의 화합물의 바람직한 구현예를 나타냄.
바람직한 것은 나아가 일반식 (44a) 의 화합물이다:
식 중, 사용된 기호 및 지수에 상기 정의가 적용되고, 그 바람직한 구현예는 또한 식 (44a) 의 화합물의 바람직한 구현예를 나타냄.
크게 바람직한 것은 여기서 일반식 (45) 의 화합물로서, 이때 사용된 기호 및 지수에 상기 정의가 적용되고, 그 바람직한 구현예는 또한 식 (45) 의 화합물의 바람직한 구현예를 나타낸다:
크게 바람직한 것은 나아가 여기서 일반식 (45a) 의 화합물로서, 이때 사용된 기호 및 지수에 상기 정의가 적용되고, 그 바람직한 구현예는 또한 식 (45a) 의 화합물의 바람직한 구현예를 나타낸다:
특히 바람직한 것은 여기서 일반식 (46) 및 (47) 의 화합물로서, 이때 사용된 기호 및 지수에 상기 정의가 적용되고, 그 바람직한 구현예는 또한 식 (46) 및 (47) 의 화합물의 바람직한 구현예를 나타낸다:
매우 특히 바람직한 것은 여기서 일반식 (48) 내지 (51) 의 화합물로서, 이때 사용된 기호 및 지수에 상기 정의가 적용되고, 그 바람직한 구현예는 또한 식 (48) 내지 (51) 의 화합물의 바람직한 구현예를 나타낸다:
매우 특히 바람직한 것은 나아가 여기서 일반식 (52) 내지 (55) 의 화합물로서, 이때 사용된 기호 및 지수에 상기 정의가 적용되고, 그 바람직한 구현예는 또한 식 (52) 내지 (55) 의 화합물의 바람직한 구현예를 나타낸다:
상기 언급된 식의 화합물에서 n 또는 m 이 0 인 경우 특히 바람직하고, n 및 m 둘 모두가 0 인 경우 훨씬 더 바람직하다.
a, b, q 및 p 가 0 이고 u 및 v 가 서로 독립적으로 0 또는 1 인 경우 본 발명의 목적상 가장 바람직하며, 이때 v 가 1 인 경우 기 V 는 페닐렌기이고, u 가 1 인 경우 기 U 는 페닐렌기이다.
라디칼 R1 이 각 경우에 동일 또는 상이하게 1 내지 40 개의 C 원자를 갖는 직쇄 알킬, 알콕시 또는 티오알콕시기, 또는 2 내지 40 개의 C 원자를 갖는 직쇄 알케닐 또는 알키닐기, 또는 3 내지 40 개의 C 원자를 갖는 분지형 또는 시클릭 알킬, 알케닐, 알키닐, 알콕시 또는 티오알콕시기 (이들 각각은 하나 이상의 라디칼 R2 에 의해 치환될 수 있음), 또는 5 내지 60 개의 방향족 고리 원자를 갖는 방향족 또는 헤테로방향족 고리계 (이는 각 경우에 하나 이상의 라디칼 R2 에 의해 치환될 수 있음), 또는 5 내지 60 개의 방향족 고리 원자를 갖는 아릴옥시 또는 헤테로아릴옥시기 (이는 하나 이상의 라디칼 R2 에 의해 치환될 수 있음), 또는 이들 계의 조합인 경우 나아가 바람직하다.
라디칼 R1 이 각 경우에 동일 또는 상이하게 1 내지 40 개의 C 원자를 갖는 직쇄 알킬기, 또는 3 내지 40 개의 C 원자를 갖는 분지형 또는 시클릭 알킬기 (이들 각각은 하나 이상의 라디칼 R2 에 의해 치환될 수 있음), 또는 5 내지 60 개의 방향족 고리 원자를 갖는 방향족 또는 헤테로방향족 고리계 (이는 각 경우에 하나 이상의 라디칼 R2 에 의해 치환될 수 있음) 인 경우 매우 바람직하다.
라디칼 R1 이 각 경우에 동일 또는 상이하게 1 내지 40 개의 C 원자를 갖는 직쇄 알킬기 (이는 각 경우에 하나 이상의 라디칼 R2 에 의해 치환될 수 있음), 또는 5 내지 60 개의 방향족 고리 원자를 갖는 방향족 또는 헤테로방향족 고리계 (이는 각 경우에 하나 이상의 라디칼 R2 에 의해 치환될 수 있음) 인 경우 특히 바람직하다.
라디칼 R1 이 각 경우에 동일 또는 상이하게 1 내지 40 개의 C 원자를 갖는 직쇄 알킬기인 경우 매우 특히 바람직하며, 이때 라디칼 R1 이 각 경우에 동일 또는 상이하게 1 내지 15 개의 C 원자를 갖는 직쇄 알킬기인 경우 특히 바람직하다.
R5 가 각 경우에 동일 또는 상이하게 1 내지 40 개의 C 원자를 갖는 직쇄 알킬, 알콕시 또는 티오알콕시기, 또는 2 내지 40 개의 C 원자를 갖는 직쇄 알케닐 또는 알키닐기, 또는 3 내지 40 개의 C 원자를 갖는 분지형 또는 시클릭 알킬, 알케닐, 알키닐, 알콕시 또는 티오알콕시기 (이들 각각은 하나 이상의 라디칼 R2 에 의해 치환될 수 있음), 또는 5 내지 60 개의 방향족 고리 원자를 갖는 방향족 또는 헤테로방향족 고리계 (이는 각 경우에 하나 이상의 라디칼 R2 에 의해 치환될 수 있음), 또는 5 내지 60 개의 방향족 고리 원자를 갖는 아릴옥시 또는 헤테로아릴옥시기 (이는 하나 이상의 라디칼 R2 에 의해 치환될 수 있음), 또는 이들 계의 조합인데; 2 개 이상의 인접한 치환기 R5 가 서로 모노- 또는 폴리시클릭, 지방족 또는 방향족 고리계를 형성할 수 없는 경우 나아가 바람직하다.
R5 가 각 경우에 동일 또는 상이하게 1 내지 40 개의 C 원자를 갖는 직쇄 알킬기, 또는 3 내지 40 개의 C 원자를 갖는 분지형 또는 시클릭 알킬기 (이들 각각은 하나 이상의 라디칼 R2 에 의해 치환될 수 있음), 또는 5 내지 60 개의 방향족 고리 원자를 갖는 방향족 또는 헤테로방향족 고리계 (이는 각 경우에 하나 이상의 라디칼 R2 에 의해 치환될 수 있음) 인데, 2 개 이상의 인접한 치환기 R5 가 서로 모노- 또는 폴리시클릭, 지방족 또는 방향족 고리계를 형성할 수 없는 경우 매우 바람직하다.
R5 가 각 경우에 동일 또는 상이하게 1 내지 40 개의 C 원자를 갖는 직쇄 알킬기 (이는 각 경우에 하나 이상의 라디칼 R2 에 의해 치환될 수 있음), 또는 5 내지 60 개의 방향족 고리 원자를 갖는 방향족 또는 헤테로방향족 고리계 (이는 각 경우에 하나 이상의 라디칼 R2 에 의해 치환될 수 있음) 인데, 2 개 이상의 인접한 치환기 R5 가 서로 모노- 또는 폴리시클릭, 지방족 또는 방향족 고리계를 형성할 수 없는 경우 특히 바람직하다.
R5 가 각 경우에 동일 또는 상이하게 1 내지 40 개의 C 원자를 갖는 직쇄 알킬기, 또는 5 내지 60 개의 방향족 고리 원자를 갖는 방향족 고리계 (이들 각각은 하나 이상의 라디칼 R2 에 의해 치환될 수 있음) 인데, 2 개 이상의 인접한 치환기 R5 가 서로 모노- 또는 폴리시클릭, 지방족 또는 방향족 고리계를 형성할 수 없는 경우 매우 특히 바람직하다. 매우 특히 바람직한 방향족 고리계는 여기서 페닐, 바이페닐 및 터페닐기로 이루어진 군으로부터 선택된다.
Ar1 이 각 경우에 동일 또는 상이하게 5 내지 30 개의 방향족 고리 원자를 갖는 방향족 또는 헤테로방향족 고리계 (이는 하나 이상의 라디칼 R2 에 의해 치환될 수 있음) 인데; 2 개의 라디칼 Ar1 이 여기서 또한 C(R2)2, O 및 S 로부터 선택되는 브릿지 또는 단일 결합에 의해 서로 연결될 수 있는 경우 나아가 바람직하고; 2 개의 라디칼 Ar1 이 서로 연결되지 않은 경우가 바람직하다.
Ar1 에서 매우 바람직한 기는 페닐, 바이페닐, 터페닐, 쿼터페닐, 디벤조푸라닐, 디벤조티오-페닐, 플루오레닐, 벤즈이미다졸릴, 카르바졸릴, 인데노카르바졸릴 및 인돌로카르바졸릴기로 이루어진 군으로부터 선택되며, 이때 기는 하나 이상의 동일 또는 상이한 라디칼 R2 에 의해 치환될 수 있고, 상기 페닐기가 가장 바람직하다.
2 개 이상의 라디칼이 서로 고리를 형성할 수 있는 공식은 본 출원의 목적상 그 중에서도 2 개의 라디칼이 화학 결합에 의해 서로 연결되는 것을 의미한다. 이는 하기 반응식에 의해 예시된다:
나아가, 그러나 상기 언급된 공식은, 2 개의 라디칼 중 하나가 수소를 나타내는 경우 제 2 라디칼이 수소 원자가 결합된 위치에서 결합되어 고리가 형성되는 것을 또한 의미한다. 이는 하기 반응식에 의해 예시된다:
아릴기는 본 발명의 의미에서 6 개 이상의 C 원자를 함유하고; 헤테로아릴기는 본 발명의 의미에서 2 개 이상의 C 원자 및 1 개 이상의 헤테로원자를 함유하는데, 단 C 원자 및 헤테로원자의 합계는 5 이상이다. 헤테로원자는 바람직하게는 N, O 및 S 로부터 선택된다. 아릴기 또는 헤테로아릴기는 여기서 단순 방향족 고리, 즉 벤젠, 또는 단순 헤테로방향족 고리, 예를 들어 피리딘, 피리미딘, 티오펜 등, 또는 축합 아릴 또는 헤테로아릴기, 예를 들어 나프탈렌, 안트라센, 피렌, 퀴놀린, 이소퀴놀린 등을 의미한다.
방향족 고리계는 본 발명의 의미에서 고리계에서 6 내지 60 개의 C 원자를 함유한다. 헤테로방향족 고리계는 본 발명의 의미에서 5 내지 60 개의 방향족 고리 원자를 함유하며, 이들 중 하나 이상은 헤테로원자이다. 헤테로원자는 바람직하게는 N, O 및/또는 S 로부터 선택된다. 방향족 또는 헤테로방향족 고리계는 본 발명의 의미에서 단지 아릴 또는 헤테로아릴기를 함유할 필요는 없지만 대신에 추가로 복수의 아릴 또는 헤테로아릴기가 비(非)방향족 단위 (바람직하게는, H 이외의 원자 10% 미만), 예를 들어 sp3-혼성화 C, Si, N 또는 O 원자, sp2-혼성화 C 또는 N 원자 또는 sp-혼성화 C 원자에 의해 연결될 수 있는 계를 의미한다. 따라서, 예를 들어 9,9'-스피로바이플루오렌, 9,9'-디아릴-플루오렌, 트리아릴아민, 디아릴 에테르, 스틸벤 등과 같은 계는 또한 2 개 이상의 아릴기가 예를 들어 선형 또는 시클릭 알킬, 알케닐 또는 알키닐기, 또는 실릴기에 의해 연결되는 계인 것과 같이 본 발명의 의미에서 방향족 고리계인 것으로 본다. 나아가, 2 개 이상의 아릴 또는 헤테로아릴기가 단일 결합을 통해 서로 연결되는 계는 또한 예를 들어 바이페닐, 터페닐 또는 디페닐트리아진과 같은 계와 같이 본 발명의 의미에서 방향족 또는 헤테로방향족 고리계인 것으로 본다.
5 - 60 개의 방향족 고리 원자를 갖는 방향족 또는 헤테로방향족 고리계 (이는 각 경우에 또한 상기 정의된 바와 같은 라디칼에 의해 치환될 수 있고, 임의의 목적하는 위치를 통해 방향족 또는 헤테로방향족기에 연결될 수 있음) 는 특히 하기 유래의 기를 의미한다: 벤젠, 나프탈렌, 안트라센, 벤즈안트라센, 페난트렌, 벤조페난트렌, 피렌, 크리센, 페릴렌, 플루오란텐, 나프타센, 펜타센, 벤조피렌, 바이페닐, 바이페닐렌, 터페닐, 터페닐렌, 쿼터페닐, 플루오렌, 스피로바이플루오렌, 디히드로페난트렌, 디히드로피렌, 테트라히드로피렌, 시스- 또는 트랜스-인데노플루오렌, 트룩센, 이소트룩센, 스피로트룩센, 스피로이소트룩센, 푸란, 벤조푸란, 이소벤조-푸란, 디벤조푸란, 티오펜, 벤조티오펜, 이소벤조티오펜, 디벤조티오펜, 피롤, 인돌, 이소인돌, 카르바졸, 인돌로카르바졸, 인데노카르바졸, 피리딘, 퀴놀린, 이소퀴놀린, 아크리딘, 페난트리딘, 벤조-5,6-퀴놀린, 벤조-6,7-퀴놀린, 벤조-7,8-퀴놀린, 페노티아진, 페녹사진, 피라졸, 인다졸, 이미다졸, 벤즈이미다졸, 나프티미다졸, 페난트리미다졸, 피리디미다졸, 피라진이미다졸, 퀴녹살린이미다졸, 옥사졸, 벤족사졸, 나프톡사졸, 안트록사졸, 펜안트록사졸, 이속사졸, 1,2-티아졸, 1,3-티아졸, 벤조티아졸, 피리다진, 벤조피리다진, 피리미딘, 벤조피리미딘, 퀴녹살린, 1,5-디아자-안트라센, 2,7-디아자피렌, 2,3-디아자피렌, 1,6-디아자피렌, 1,8-디아자피렌, 4,5-디아자-피렌, 4,5,9,10-테트라아자페릴렌, 피라진, 페나진, 페녹사진, 페노티아진, 플루오루빈, 나프티리딘, 아자카르바졸, 벤조카르볼린, 페난트롤린, 1,2,3-트리아졸, 1,2,4-트리아졸, 벤조트리아졸, 1,2,3-옥사디아졸, 1,2,4-옥사디아졸, 1,2,5-옥사디아졸, 1,3,4-옥사디아졸, 1,2,3-티아디아졸, 1,2,4-티아디아졸, 1,2,5-티아디아졸, 1,3,4-티아디아졸, 1,3,5-트리아진, 1,2,4-트리아진, 1,2,3-트리아진, 테트라졸, 1,2,4,5-테트라진, 1,2,3,4-테트라진, 1,2,3,5-테트라진, 퓨린, 프테리딘, 인돌리진 및 벤조티아디아졸, 또는 이들 기의 조합.
본 발명의 목적을 위해, 1 내지 40 개의 C 원자를 갖는 직쇄 알킬기, 또는 3 내지 40 개의 C 원자를 갖는 분지형 또는 시클릭 알킬기, 또는 2 내지 40 개의 C 원자를 갖는 알케닐 또는 알키닐기 (이때, 추가로 별개의 H 원자 또는 CH2 기는 라디칼의 정의 하에 상기 언급된 기에 의해 치환될 수 있음) 는 바람직하게는 라디칼 메틸, 에틸, n-프로필, i-프로필, n-부틸, i-부틸, s-부틸, t-부틸, 2-메틸부틸, n-펜틸, s-펜틸, 시클로펜틸, 네오펜틸, n-헥실, 시클로헥실, 네오헥실, n-헵틸, 시클로헵틸, n-옥틸, 시클로옥틸, 2-에틸헥실, 트리플루오로메틸, 펜타플루오로에틸, 2,2,2-트리플루오로에틸, 에테닐, 프로페닐, 부테닐, 펜테닐, 시클로펜테닐, 헥세닐, 시클로헥세닐, 헵테닐, 시클로헵테닐, 옥테닐, 시클로옥테닐, 에티닐, 프로피닐, 부티닐, 펜티닐, 헥시닐 또는 옥티닐을 의미한다. 1 내지 40 개의 C 원자를 갖는 알콕시 또는 티오알킬기는 바람직하게는 메톡시, 트리플루오로메톡시, 에톡시, n-프로폭시, i-프로폭시, n-부톡시, i-부톡시, s-부톡시, t-부톡시, n-펜톡시, s-펜톡시, 2-메틸부톡시, n-헥속시, 시클로헥실옥시, n-헵톡시, 시클로헵틸옥시, n-옥틸옥시, 시클로옥틸옥시, 2-에틸헥실옥시, 펜타플루오로에톡시, 2,2,2-트리플루오로에톡시, 메틸티오, 에틸티오, n-프로필티오, i-프로필티오, n-부틸티오, i-부틸티오, s-부틸티오, t-부틸티오, n-펜틸티오, s-펜틸티오, n-헥실티오, 시클로헥실티오, n-헵틸티오, 시클로헵틸티오, n-옥틸티오, 시클로-옥틸티오, 2-에틸헥실티오, 트리플루오로메틸티오, 펜타플루오로에틸티오, 2,2,2-트리플루오로에틸티오, 에테닐티오, 프로페닐티오, 부테닐티오, 펜테닐티오, 시클로펜테닐티오, 헥세닐티오, 시클로헥세닐티오, 헵테닐티오, 시클로헵테닐티오, 옥테닐티오, 시클로옥테닐티오, 에티닐티오, 프로피닐티오, 부티닐티오, 펜티닐티오, 헥시닐티오, 헵티닐티오 또는 옥티닐티오를 의미한다.
본 발명에 따른 화합물은 반응식 1 및 2 에 따라 제조될 수 있다. 상응하는 모노보론산은 시판되고, Suzuki 커플링에 의해 상응하는 표적 분자로 전환될 수 있다.
식 중, Ab 는 이탈기를 나타내며, 이는 바람직하게는 Cl, Br, I 및 트리플레이트로부터 선택되고; 이는 매우 바람직하게는 Br 임. 보론 피나콜 에스테르 외에도, 기타 에스테르 또는 보론산 그 자체가 또한 여기서 활용될 수 있다. 이들은 당업자에게 매우 친숙하다.
본 발명에 따른 플루오렌은 Suzuki 커플링에 의해 전체적으로 유사하게 제조될 수 있다. 기타 보론 화합물이 또한 여기서 활용될 수 있다. 이들은 당업자에게 매우 친숙하다.
본 발명에 따른 화합물의 합성에서 나타내는 일반 방법이 예시된다. 당업자는 그의 일반적 전문 지식의 한도 내에서 대안적 합성 경로를 개발할 수 있을 것이다.
하기 개요는 본원에 기재된 방법 중 하나에 의해 제조될 수 있는 본 발명에 따른 화합물의 예시적 도를 함유한다.
본 발명에 따른 화합물은 유기 전자 소자에서 사용될 수 있다. 본 발명에 따른 화합물은 여기서 전자-주입, 전자-수송 및/또는 발광층에 활용된다.
본 발명은 따라서 나아가 전자 소자, 바람직하게는 전자-주입, 전자-수송 및/또는 발광층에서의, 본 발명에 따른 화합물의 용도에 관한 것이다.
본 발명에 따른 화합물은 여기서 단지 층의 성분일 수 있거나, 또는 층에서 하나 이상의 기타 재료와의 조합으로 사용될 수 있다.
본 발명에 따른 화합물이 기타 재료와 함께 조성물로 활용되는 경우, 화합물을 포함하는 전자 소자의 효율 데이터의 추가의 개선이 여기서 달성될 수 있다.
본 발명에 따른 화합물은 바람직하게는 소자, 특히 전자 소자, 예컨대 전계발광 소자에서 전형적으로 활용되는 재료와 함께 조성물로 활용된다.
본 발명은 따라서 또한 형광 발광체, 인광 발광체, 매트릭스 재료, 전자-수송 재료, 전자-주입 재료, 정공-전도 재료, 정공-주입 재료, 전자-차단 재료, 정공-차단 재료 및 n-도펀트로 이루어진 군으로부터 선택되는 하나 이상의 추가의 기능성 분자 및 하나 이상의 본 발명에 따른 화합물을 포함하는 조성물에 관한 것이다.
문헌에서, 용어 호스트 재료는 용어 매트릭스 재료 대신에 흔히 또한 사용된다. 일부 저자들은 형광 발광체용 매트릭스 재료에 있어서 용어 호스트 재료를 사용하지만, 용어 매트릭스 재료는 발광층에서 인광 발광체와 함께 사용되는 재료를 나타낸다. 본 경우에, 용어 매트릭스 재료 (호스트 재료) 는 발광체와 독립적으로 사용되고 형광 또는 인광 발광체와 함께 발광층에서 활용될 수 있는 재료를 나타낸다.
별개의 재료가 당업자에 익히 알려져 있고, 넓은 범위로부터 적합한 화합물을 선택하는데 있어서 절대적으로 어려움 없이 제시된다.
본 발명의 바람직한 구현예에서, 유기 전자 소자는 전자-수송 층 (ETL) 에서 본 발명에 따른 화합물 중 하나 이상을 포함한다. ETL 은 여기서 본 발명에 따른 화합물로 이루어진 순수 층일 수 있거나, 또는 이는 또한 하나 이상의 전자-수송 재료를 포함할 수 있다. 당업자는 여기서 다양한 공지된 전자-수송 재료로부터 선택할 수 있을 것이다. ETL 에서 전자-수송 재료와 본 발명에 따른 화합물과의 병용은 특히 양호한 수행성 데이터를 갖는 유기 전자 소자를 유도한다.
본 발명은 따라서 하나 이상의 ETM 및 본 발명에 따른 화합물 중 하나 이상을 포함하는 조성물에 관한 것이다. ETM 은 바람직하게는 비금속 전자-수송 재료의 군으로부터 선택된다.
본 발명에 따른 조성물을 위한 바람직한 전자-수송 재료는 피리딘, 피리미딘, 피리다진, 피라진, 옥사디아졸, 퀴놀린, 퀴녹살린, 안트라센, 벤즈안트라센, 피렌, 페릴렌, 벤즈이미다졸, 트리아진, 케톤, 락탐, 옥사졸, 페난트롤린, 포스핀 옥시드 및 페나진으로부터 선택된다. 트리아진 및 락탐이 여기서 매우 바람직하다.
ETL 의 층 두께는 바람직하게는 5 내지 150 nm 이다.
ETL 에서 본 발명에 따른 화합물의 농도는 전체 전자-수송 층을 기준으로 바람직하게는 10 부피% 내지 90 부피% 범위, 매우 바람직하게는 20 부피% 내지 80 부피% 범위, 매우 특히 바람직하게는 30 부피% 내지 70 부피% 범위, 특히 바람직하게는 40 부피% 내지 60 부피% 범위이다.
전자-수송 층 외에도, 본 발명에 따른 소자는 또한 캐소드 및 전자-수송 층 사이에 위치한 전자-주입 층 (EIL) 을 가질 수 있다. EIL 에서 전자-주입 재료 (EIM) 로서 활용되는 바람직한 재료는 알칼리 금속, 알칼리-금속 착물, 특히 알칼리-금속 옥시네이트 (특히, 치환 또는 미치환된 Li 히드록시퀴놀린), 및 알칼리-금속 또는 알칼리-토금속 플루오라이드, 및 또한 그 옥시드 또는 카르보네이트의 군으로부터 선택된다. 매우 바람직한 전자-주입 재료는 Li, LiF, Li2O, BaF2, MgO, NaF, Cs, CsF, Cs2CO3, Liq 이며, 이때 LiF 및 Liq 가 특히 바람직하고, LiF 는 매우 특히 바람직한 전자-주입 재료를 나타낸다.
EIL 의 층 두께는 바람직하게는 0.5 내지 5 nm 이다.
나아가 바람직한 EIM 는 치환된 리튬 8-히드록시퀴놀리네이트, 특히 DE 102013013876.0 에서 개시된 것들, 매우 특히 하기 식 (C-1) 내지 (C-34) 의 것들이다:
유기 전자 소자의 수행성의 추가의 증가는, 본 발명에 따른 화합물이 n-도펀트와의 조합으로 전자-수송 층에서 활용되는 경우 달성될 수 있다. n-도펀트는 여기서 무기 및 또한 유기 재료 둘 모두일 수 있다.
n-도펀트는 본 출원에서 전자를 방출할 수 있는 유기 또는 무기 화합물 (전자 공여체), 즉 환원제로서 작용되는 화합물을 의미한다.
n-도핑에 활용되는 화합물은 전구체로서 활용될 수 있는데, 이때 이들 전구체 화합물은 활성화에 의해 n-도펀트를 유리시킨다.
바람직한 n-도펀트는 전자-풍부 금속 착물; P=N 화합물; N-헤테로시클릭 화합물, 특히 바람직하게는 나프틸렌카르보디이미드, 피리딘, 아크리딘 및 페나진; 플루오렌 및 자유-라디칼 화합물로부터 선택된다.
특히 바람직한 전자-풍부 금속 착물은 그 중에서도 WO 2005/86251 A2 에 기재되어 있으며, 이때 상기 명세서는 개시 목적으로 참조의 방식으로 본 출원에 포함되어 있다. 뉴트럴 전자-풍부 금속 착물이 여기서 바람직하다.
특히 바람직한 P=N 화합물이 그 중에서도 WO 2012/175535 A1 에 개시되어 있으며, 이때 상기 명세서는 개시 목적으로 참조의 방식으로 본 출원에 포함되어 있다.
n-도펀트의 추가의 기는 N-헤테로시클릭 화합물로 나타낸다. N-헤테로시클릭 화합물은 고리 구조가 수소 및 탄소 외에도 하나 이상의 질소 원자를 함유하는 시클릭 화합물이다. 이들 화합물은 포화, 부분 불포화 또는 헤테로방향족일 수 있다.
N-헤테로시클릭 화합물은 바람직하게는 전구체로서 활용될 수 있으며, 이때 전구체 화합물은 n-도펀트로서 그 기능이 단지 활성화 후에 개시된다는 점에서 구별된다. 특히 전구체로서 활용될 수 있는 바람직한 N-헤테로-시클릭 화합물이 그 중에서도 WO 2009/00237 A1 에 기재되어 있으며, 이때 상기 명세서는 개시 목적으로 참조의 방식으로 본 출원에 포함되어 있다.
n-도펀트로서 적합한 N-헤테로시클릭 화합물의 추가의 기는 나프틸렌카르보디이미드로 나타낸다. 나프틸렌카르보디이미드는 하나 이상의 카르보디이미드기 (N=C=N) 및 나프틸렌기를 함유한다.
놀라운 이점은 WO 2012/168358 A1 에 기재된 나프틸렌카르보디이미드에 의해 달성될 수 있으며, 이때 상기 명세서는 개시 목적으로 참조의 방식으로 본 출원에 포함되어 있다.
n-도펀트로서 활용될 수 있는 바람직한 N-헤테로시클릭 화합물은 나아가 피리딘, 아크리딘 및 페나진 유도체를 포함한다. 이들 화합물은 피리딘, 아크리딘 및 페나진 구조 요소를 함유하고, 당업계에 공지되어 있다. 바람직한 아크리딘 및 페나진이 그 중에서도 US 2007/0145355 A1 에 기재되어 있으며, 이때 상기 명세서는 개시 목적으로 참조의 방식으로 본 출원에 포함되어 있다.
놀라운 이점은 EP 2 452 946 A1 및 EP 2 463 927 A1 에 기재된 피리딘에 의해 달성될 수 있으며, 이때 상기 명세서는 개시 목적으로 참조의 방식으로 본 출원에 포함되어 있다.
본 발명의 특정 구현예에 따라, 플루오렌은 n-도펀트로서 활용될 수 있다. 바람직한 플루오렌이 그 중에서도 WO 2012/031735 A1 에 기재되어 있으며, 이때 상기 명세서는 개시 목적으로 참조의 방식으로 본 출원에 포함되어 있다.
바람직한 n-도펀트는 당업계에 공지된 자유-라디칼 화합물을 포함한다. 바람직한 자유-라디칼 화합물은 헤테로시클릭기를 함유한다. 특히 바람직한 자유-라디칼 화합물이 그 중에서도 EP 1 837 926 A1 및 WO 2007/107306 A1 에 개시되어 있으며, 이때 상기 명세서는 개시 목적으로 참조의 방식으로 본 출원에 포함되어 있다.
상기 n-도펀트 중에서, WO 2005/86251 A2 에 기재된 전자-풍부 금속 착물이 특히 바람직하며, 이때 hpp 가 1,3,4,6,7,8-헥사히드로-2H-피리미도[1,2-a]피리미딘의 음이온을 나타내는 식 W2(hpp)4 의 금속 착물이 매우 특히 바람직하다. 뉴트럴 전자-풍부 금속 착물이 여기서 특히 바람직하다.
n-도핑의 경우, 전자 전이는 n-도펀트의 HOMO (최고 점유 분자 오비탈) 수준에서 매트릭스 재료의 LUMO (최저 비점유 분자 오비탈) 수준으로 실시되며, 이때 전자는 일반적으로 강하게 국소화되지 않지만 대신에 전하 캐리어 중에서 계수된다.
본 발명의 개선은, 본 발명에 따른 화합물의 LUMO 및 n-도펀트의 HOMO 간의 차이 값이 바람직하게는 약 1 eV 미만이고, 추가로 바람직하게는 차이 값이 약 0.5 eV 미만인 것을 제안한다.
본 발명에 따른 화합물은 바람직하게는 약 1 eV 이상, 매우 바람직하게는 1.5 eV 이상의 LUMO 수준을 갖는다.
분자 오비탈, 특히 또한 최고 점유 분자 오비탈 (HOMO) 및 최저 비점유 분자 오비탈 (LUMO), 그 에너지 수준 및 재료의 최저 삼중선 상태 T1 또는 최저 여기된 단일선 상태 S1 의 에너지는 양자 역학 산출법의 도움으로 본 출원에서 측정된다. 금속이 없는 유기 물질의 산출을 위해, 우선 "Ground State/Semi-empirical/Default Spin/AM1/Charge 0/Spin Singlet" 방법을 사용해 기하구조 최적화를 수행한다. 이어서, 에너지 산출을 최적화된 기하구조를 기준으로 수행한다. "6-31G(d)" 기본 세트 (전하 0, 스핀 단일선) 를 사용한 "TD-SCF/DFT/Default Spin/B3PW91" 방법을 여기서 사용한다. 금속-함유 화합물의 경우, "Ground State/Hartree-Fock/Default Spin/LanL2MB/Charge 0/Spin Singlet" 방법을 통해 기하구조를 최적화한다. 에너지 산출은 유기 물질에서 상기 기재된 방법과 유사하게 수행되는데, 그 차이는 금속 원자의 경우 "LanL2DZ" 기본 세트가 사용되고 리간드의 경우 "6-31G(d)" 기본 세트가 사용된다는 점이다. 에너지 산출을 통해 hartree 단위의 HOMO 에너지 수준 HEh 또는 LUMO 에너지 수준 LEh 를 제시한다. 순환 전압전류 측정을 참조해 칼리브레이션된, 전자 볼트로서 HOMO 및 LUMO 에너지 수준은 하기와 같이 그로부터 측정된다:
HOMO(eV) = ((HEh*27.212)-0.9899)/1.1206
LUMO(eV) = ((LEh*27.212)-2.0041)/1.385
상기 적용의 목적을 위해, 이들 값은 재료의 HOMO 또는 LUMO 에너지 수준 각각으로서 간주된다.
최저 삼중선 상태 T1 은 기재된 양자-화학 산출로부터 나온 최저 에너지를 갖는 삼중선 상태의 에너지로 정의된다.
최저 여기 단일선 상태 S1 은 기재된 양자-화학 산출로부터 나온 최저 에너지를 갖는 여기 단일선 상태의 에너지로 정의된다.
본원에 기재된 방법은 사용된 소프트웨어 패키지와 독립적이고, 항상 동일한 결과를 제공한다. 상기 목적을 위해 흔히 사용되는 프로그램의 예는 "Gaussian09W" (Gaussian Inc.) 및 Q Chem 4.1 (Q Chem, Inc.) 이다.
본 발명의 추가의 바람직한 구현예에서, 유기 전자 소자는 발광층 (EML) 에서 본 발명에 따른 화합물 중 하나 이상을 포함한다. 본 발명에 따른 화합물은 여기서 하나 이상의 발광체와 함께 EML 에서 매트릭스 재료로서 활용된다. 가능한 발광체는 여기서 형광 및 인광 발광체 둘 모두이며, 이때 인광 발광체가 바람직하다.
용어 인광 발광체 (인광 도펀트로도 칭함) 는 전형적으로 스핀-금지 전이를 통해, 예를 들어 삼중선 상태 또는 보다 높은 스핀 양자 수를 갖는 상태, 예를 들어 오중선 상태로부터의 전이를 통해 대개 발광이 나타나는 화합물을 포함한다.
적합한 인광 도펀트는 특히 적합한 여기로 바람직하게는 가시 영역에서 발광하고, 추가로 20 초과, 바람직하게는 38 초과 84 미만, 특히 바람직하게는 56 초과 80 미만의 원자수를 갖는 하나 이상의 원자를 함유하는 화합물이다. 사용되는 인광 발광체는 바람직하게는 구리, 몰리브덴, 텅스텐, 레늄, 루테늄, 오스뮴, 로듐, 이리듐, 팔라듐, 백금, 은, 금 또는 유로퓸을 함유하는 화합물, 특히 이리듐, 백금 또는 구리를 함유하는 화합물이다.
모든 발광 이리듐, 백금 또는 구리 착물은 본 출원의 의미에서 인광 화합물로서 간주된다.
인광 화합물은 바람직하게는 삼중선 상태로부터 발광하는 것들이다.
용어 형광 발광체 (또한 형광 도펀트) 는 대개 여기된 단일선 상태로부터의 전이를 통해 발광이 나타나는 화합물을 포함한다.
형광 및 또한 인광 발광체 둘 모두는 선행기술로부터 당업자에 익히 공지되어 있고, 적합한 발광체를 선택하는데 있어서 절대적으로 어떠한 어려움 없이 제시된다.
인광 도펀트의 예가 출원 WO 2000/70655, WO 2001/41512, WO 2002/02714, WO 2002/15645, EP 1191613, EP 1191612, EP 1191614, WO 2005/033244, WO 2005/019373 및 US 2005/0258742 에 의해 밝혀져 있다. 일반적으로, 인광 OLED 에 관한 선행기술에 따라 사용되는 바 및 유기 전계발광 소자 분야의 당업자에 알려져 있는 바와 같이 모든 인광 착물은 본 발명에 따른 소자에서 사용하기에 적합하다.
인광 도펀트의 분명한 예가 하기 표에 나타나 있다:
본 발명의 추가의 바람직한 구현예에서, 화합물은 혼합-매트릭스 시스템의 매트릭스 성분으로서 사용된다. 혼합-매트릭스 시스템은 바람직하게는 2 또는 3 개의 상이한 매트릭스 재료, 특히 바람직하게는 2 개의 상이한 매트릭스 재료를 포함한다. 2 개의 재료 중 하나는 여기서 바람직하게는 정공-수송 특성을 갖는 재료이고, 기타 재료는 전자-수송 특성을 갖는 재료이다. 그러나, 혼합-매트릭스 성분의 목적하는 전자-수송 및 정공-수송 특성은 또한 단일 혼합-매트릭스 성분으로 주로 또는 완전히 조합될 수 있으며, 이때 추가의 혼합-매트릭스 성분(들) 은 기타 기능을 이행한다. 여기서, 2 개의 상이한 매트릭스 재료는 1:50 내지 1:1, 바람직하게는 1:20 내지 1:1, 특히 바람직하게는 1:10 내지 1:1, 매우 특히 바람직하게는 1:4 내지 1:1 의 비로 제시될 수 있다. 혼합-매트릭스 시스템은 바람직하게는 인광 유기 전계발광 소자로 활용된다. 혼합-매트릭스 시스템에 관한 더 세부적인 사항은 그 중에서도 출원 WO 2010/108579 에 제시되어 있다.
혼합-매트릭스 시스템의 매트릭스 성분으로서 본 발명에 따른 화합물과의 조합으로 사용될 수 있는 특히 적합한 매트릭스 재료는 어떠한 유형의 도펀트가 혼합-매트릭스 시스템에서 활용되는지에 따라 인광 도펀트용 하기 나타내는 바람직한 매트릭스 재료, 또는 형광 도펀트용 바람직한 매트릭스 재료로부터 선택된다.
바람직하게는 형광 도펀트용의 적합한 매트릭스 재료는 각종 부류의 물질로부터의 재료이다. 바람직한 매트릭스 재료는 하기 부류로부터 선택된다: 락탐 (예를 들어, WO 2011/116865, WO 2011/137951, WO 2013/064206, WO 2014/056567, EP 13003343.4, EP 14000729.5), 올리고아릴렌 (예를 들어, 2,2',7,7'-테트라페닐스피로바이플루오렌 (EP 676461 에 따름) 또는 디나프틸안트라센), 특히 축합 방향족기를 함유하는 올리고아릴렌, 올리고아릴렌비닐렌 (예를 들어, DPVBi 또는 스피로-DPVBi (EP 676461 에 따름), 폴리포달 금속 착물 (예를 들어, WO 2004/081017 에 따름), 정공-전도 화합물 (예를 들어, WO 2004/058911 에 따름), 전자-전도 화합물, 특히 케톤, 포스핀 옥시드, 술폭시드 등 (예를 들어, WO 2005/084081 및 WO 2005/084082 에 따름), 회전장애이성질체 (예를 들어, WO 2006/048268 에 따름), 보론산 유도체 (예를 들어, WO 2006/117052 에 따름) 또는 벤즈안트라센 (예를 들어, WO 2008/145239 에 따름). 특히 바람직한 매트릭스 재료는 나프탈렌, 안트라센, 벤즈안트라센 및/또는 피렌 또는 이들 화합물의 회전장애이성질체를 포함하는 올리고-아릴렌, 올리고아릴렌비닐렌, 케톤, 포스핀 옥시드 및 술폭시드 부류로부터 선택된다. 매우 특히 바람직한 매트릭스 재료는 안트라센, 벤즈안트라센, 벤조페난트렌 및/또는 피렌 또는 이들 화합물의 회전장애이성질체를 포함하는 올리고-아릴렌 부류로부터 선택된다. 올리고아릴렌은 본 발명의 의미에서 3 개 이상의 아릴 또는 아릴렌기가 서로 결합되는 화합물을 의미한다.
인광 도펀트용의 바람직한 매트릭스 재료는 하기이다: 방향족 아민, 특히 트리아릴아민 (예를 들어, US 2005/0069729 에 따름), 카르바졸 유도체 (예를 들어, CBP, N,N-비스카르바졸릴바이페닐) 또는 WO 2005/039246, US 2005/0069729, JP 2004/288381, EP 1205527 또는 WO 2008/086851 에 따른 화합물, 브릿지 카르바졸 유도체 (예를 들어, WO 2011/088877 및 WO 2011/128017 에 따름), 인데노카르바졸 유도체 (예를 들어, WO 2010/136109 및 WO 2011/000455 에 따름), 아자카르바졸 유도체 (예를 들어, EP 1617710, EP 1617711, EP 1731584, JP 2005/347160 에 따름), 인돌로카르바졸 유도체 (예를 들어, WO 2007/063754 또는 WO 2008/056746 에 따름), 케톤 (예를 들어, WO 2004/093207 또는 WO 2010/006680 에 따름), 포스핀 옥시드, 술폭시드 및 술폰 (예를 들어, WO 2005/003253 에 따름), 올리고페닐렌, 이극성 매트릭스 재료 (예를 들어, WO 2007/137725 에 따름), 실란 (예를 들어, WO 2005/111172 에 따름), 아자보롤 또는 보론 에스테르 (예를 들어, WO 2006/117052 에 따름), 트리아진 유도체 (예를 들어, WO 2010/015306, WO 2007/063754 또는 WO 2008/056746 에 따름), 아연 착물 (예를 들어, EP 652273 또는 WO 2009/062578 에 따름), 알루미늄 착물, 예를 들어 BAlq, 디아자실롤 및 테트라아자실롤 유도체 (예를 들어, WO 2010/054729 에 따름), 디아자포스폴 유도체 (예를 들어, WO 2010/054730 에 따름), 및 알루미늄 착물, 예를 들어 BAlQ.
본 발명은 따라서 또한 하나 이상의 본 발명에 따른 화합물 및 하나 이상의 추가의 매트릭스 재료를 포함하는 조성물에 관한 것이다.
본 발명은 나아가 또한 하나 이상의 본 발명에 따른 화합물 및 하나 이상의 추가의 매트릭스 재료 및 나아가 하나 이상의 형광 또는 인광 발광체, 바람직하게는 인광 발광체를 포함하는 조성물에 관한 것이다.
본 발명은 또한 하나 이상의 본 발명에 따른 화합물 및 하나 이상의 넓은 대역 간격 재료를 포함하는 조성물로서, 이때 넓은 대역 간격 재료가 US 7,294,849 의 개시 내용의 의미에서의 재료를 의미하는 것에 관한 것이다. 이들 시스템은 특히 전계발광 소자에서 특히 유리한 수행성 데이터를 나타낸다.
복수의 매트릭스 재료를 포함하는 시스템 (혼합-매트릭스 시스템) 은 유기 전계발광 소자의 발광 층에서 활용된다. 발광 층은 나아가 또한 하나 이상의 도펀트를 포함한다.
본 발명에 따른 화합물 및 조성물은 유기 전자 소자에서 활용될 수 있다. 본 발명은 따라서 또한 본 발명에 따른 화합물 또는 조성물 중 하나 이상을 포함하는 유기 전자 소자에 관한 것이다.
본 발명에 따른 유기 전자 소자는 바람직하게는 유기 집적 회로 (OIC), 유기 전계-효과 트랜지스터 (OFET), 유기 박막 트랜지스터 (OTFT), 유기 발광 트랜지스터 (OLET), 유기 태양 전지 (OSC), 유기 광학 검출기, 유기 광수용기, 유기 전계-켄치 소자 (OFQD), 유기 발광 전기화학 전지 (OLEC, LEC 또는 LEEC), 유기 레이저 다이오드 (O-레이저) 및 유기 발광 다이오드 (OLED) 로 이루어진 군으로부터 선택된다. 특히 바람직한 것은 여기서 유기 전계발광 소자, 매우 특히 바람직한 것은 OLEC 및 OLED, 특히 바람직한 것은 OLED 이다.
OLED 는 본 발명의 의미에서 소형 유기 분자를 포함하는 유기 발광 다이오드 (SMOLED) 및 또한 폴리머성 발광 다이오드 (PLED) 를 의미하며, 이때 SMOLED 는 바람직한 OLED 를 나타낸다.
이미 상기 언급된 바와 같이, 본 발명에 따른 화합물 또는 조성물을 포함하는 유기 층은 바람직하게는 전자-수송 기능을 갖는 소자의 층이다. 이는 특히 바람직하게는 전자-주입 층 (EIL), 전자-수송 층 (ETL), 정공-차단 층 (HBL) 또는 발광층 (EML) 이다.
본 출원에 따른 정공-수송 층 (HTL) 은 애노드 및 발광 층 (EML) 사이에 위치한 정공-수송 기능을 갖는 층이다.
본 출원에 따른 전자-수송 층 (ETL) 은 캐소드 및 발광 층 (EML) 사이에 위치한 전자-수송 기능을 갖는 층이다.
유기 전자 소자, 특히 또한 유기 전계발광 소자의 구조는 선행기술로부터 당업자에 익히 공지되어 있다.
본 발명에 따른 전자, 특히 전계발광, 유기 소자는 하나 이상의 식 (1) 의 화합물을 포함하는 하나 이상의 유기 층을 포함한다. 유기 층은 하나 이상의 유기 또는 유기금속 화합물을 포함한다는 점에서 구별된다. 유기 소자는 반드시 유기 또는 유기금속 재료로부터 구축되는 층만을 포함할 필요는 없다.
본 발명에 따른 전자 소자는 애노드, 캐소드 및 하나 이상의 본 발명에 따른 화합물을 포함하는 하나 이상의 유기 층을 포함한다.
이미 언급된 바와 같이, 특히 바람직한 유기 전자 소자는 본 발명의 의미에서 유기 전계발광 소자, 및 여기서는 특히 OLED 이다.
캐소드는 바람직하게는 각종 금속, 예를 들어 알칼리 토금속, 알칼리 금속, 주족 금속 또는 란탄족 (예를 들어, Ca, Ba, Mg, Al, In, Mg, Yb, Sm 등) 을 포함하는 다층 구조, 금속 합금 또는 낮은 일 함수를 갖는 금속을 포함한다. 또한, 알칼리 금속 또는 알칼리 토금속 및 은을 포함하는 합금, 예를 들어 마그네슘 및 은을 포함하는 합금이 적합하다. 다층 구조의 경우에, 비교적 높은 일 함수를 갖는 추가 금속, 예를 들어 Ag 는 또한 상기 금속 이외에 사용될 수 있으며, 상기 경우에 예를 들어 Mg/Ag, Ca/Ag 또는 Ba/Ag 와 같은 금속의 조합이 일반적으로 사용된다. 또한, 금속성 캐소드 및 유기 반도체 사이에 높은 유전 상수를 갖는 재료의 얇은 사이층을 도입시키는 것이 바람직할 수 있다. 예를 들어, 알칼리 금속 플루오라이드 또는 알칼리 토금속 플루오라이드, 뿐만 아니라 상응하는 옥시드 또는 카르보네이트 (예를 들어, LiF, Li2O, BaF2, MgO, NaF, CsF, Cs2CO3 등) 가 상기 목적에 적합하다. 마찬가지로, 유기 알칼리-금속 착물, 예를 들어 Liq (리튬 퀴놀리네이트) 또는 치환된 Li 히드록시퀴놀리네이트가 상기 목적에 적합하다.
애노드는 바람직하게는 높은 일 함수를 갖는 재료를 포함한다. 애노드는 바람직하게는 진공에 대하여 4.5 eV 초과의 일 함수를 갖는다. 한편으로, 예를 들어 Ag, Pt 또는 Au 와 같은 높은 산화환원 전위를 갖는 금속이 상기 목적에 적합하다. 다른 한편으로, 금속/금속 옥시드 전극 (예를 들어, Al/Ni/NiOx, Al/PtOx) 가 또한 바람직할 수 있다. 일부 적용을 위해, 전극 중 하나 이상은 광의 커플링-아웃 (OLED/PLED, O-레이저) 또는 유기 재료의 조사 (O-SC) 를 가능케 하기 위해 투명 또는 부분 투명해야 한다. 바람직한 애노드 재료는 여기서 전도성 혼합된 금속 옥시드이다. 특히 바람직한 것은 인듐 주석 옥시드 (ITO) 또는 인듐 아연 옥시드 (IZO) 이다. 나아가, 바람직한 것은 전도성의 도핑된 유기 재료, 특히 전도성의 도핑된 폴리머, 예를 들어 PEDOT, PANI 또는 이들 폴리머의 유도체이다. 이는 p-도핑된 정공-수송 재료가 정공-주입 층으로서 애노드에 적용되는 것이 나아가 바람직한데, 이때 금속 옥시드, 예를 들어 MoO3 또는 WO3, 또는 (퍼)플루오르화 전자-결핍 방향족 화합물이 p-도펀트로서 적합하다. 추가의 적합한 p-도펀트는 HAT-CN (헥사시아노헥사아자트리페닐렌) 또는 화합물 NPD9 (Novaled) 이다. 상기 유형의 층은 저 HOMO, 즉 큰 모듈러스를 갖는 HOMO 를 갖는 재료에서 정공 주입을 단순화한다.
바람직한 구현예에 따라, 2 개 이상의 유기 층은 애노드 및 캐소드 사이에 배열될 수 있다.
추가의 층에서, 일반적으로 층에 있어서 선행기술에 따라 사용되는바 모든 재료를 사용할 수 있고, 당업자는 진보성 없이 전자 소자에 본 발명에 따른 재료와 이들 재료 각각을 조합할 수 있을 것이다. 전형적인 ETM, EIM, 발광체 및 매트릭스 재료가 이미 상기 개시되어 있다.
유기 전계발광 소자는 캐소드, 애노드 및 하나 이상의 발광층 (EML) 을 포함한다. 이들 층 외에도, 이는 또한 추가의 층, 예를 들어 각 경우에 하나 이상의 정공-주입 층 (HIL), 정공-수송 층 (HTL), 정공-차단 층 (HBL), 전자-수송 층 (ETL), 전자-주입 층 (EIL), 여기자-차단 층 (ExBL), 전자-차단 층 (EBL), 전하-발생 층 및/또는 유기 또는 무기 p/n 접합부를 포함할 수 있다. 유기 전계발광 소자의 전형적인 구조는 하기이다: 애노드/HIL/HTL/EML/ETL/EIL/캐소드.
여기서 하나 이상의 정공-수송 층이 예를 들어 금속 옥시드, 예컨대 MoO3 또는 WO3, 또는 (퍼)플루오르화 전자-결핍 방향족 화합물로 p-도핑되고/거나 하나 이상의 전자-수송 층이 n-도핑될 수 있다. 마찬가지로, 예를 들어 전계발광 소자에서 전하 밸런스를 조절하고/거나 여기자-차단 기능을 갖는 사이층(interlayer) 은 2 개의 발광층 사이에 도입될 수 있다. 그러나, 이들 층 각각이 반드시 존재할 필요는 없다는 것에 주목되어야 한다.
유기 전계발광 소자는 하나의 발광층 또는 복수의 발광층을 포함할 수 있다. 복수의 발광층이 존재하는 경우, 이들은 바람직하게는 전체적으로 380 nm 및 750 nm 사이의 복수의 발광 최대치를 가져 전반적으로 백색 발광을 유도하는데, 즉 형광 또는 인광을 낼 수 있는 각종 발광 화합물이 발광 층에 사용된다. 특히 바람직한 것은 3 개의 층이 청색, 녹색 및 주황색 또는 적색 발광을 나타내는 3-층 시스템 (기본 구조에 대해서는, 예를 들어 WO 2005/011013 참조), 또는 3 개 초과의 발광층을 갖는 시스템이다. 하이브리드 시스템이 또한 가능하며, 이때 하나 이상의 층은 형광을 발하고, 하나 이상의 기타 층을 인광을 발한다.
소자의 수명이 물 및/또는 공기의 존재 하에 극적으로 단축되기 때문에, 소자는 상응하게는 (적용에 따라) 구조화되고, 접촉부가 제공되고, 마지막으로는 밀봉된다.
바람직한 것은 나아가 하나 이상의 층이 승화 공정에 의해 적용되며, 이때 재료가 통상적으로 10-5 mbar 미만, 바람직하게는 10-6 mbar 미만의 초기 압력에서 진공 승화기의 증착에 의해 적용되는 것을 특징으로 하는 전자 소자, 특히 유기 전계발광 소자이다. 또한, 초기 압력을, 예를 들어 10-7 mbar 미만과 같이 훨씬 더 낮게 또는 훨씬 더 높게할 수 있다.
바람직한 것은 마찬가지로, 하나 이상의 층이 OVPD (유기 증기상 침착) 방법에 의해 또는 캐리어-가스 승화의 도움으로 적용되며, 이때 재료가 10-5 mbar 내지 1 bar 의 압력에서 적용되는 것을 특징으로 하는 전자 소자, 특히 유기 전계발광 소자이다. 상기 방법의 특별한 경우는 OVJP (유기 증기 제트 인쇄) 방법으로서, 이때 재료가 노즐을 통해 직접 적용되고 따라서 구조화되는 것이다 (예를 들어, M. S. Arnold et al., Appl. Phys. Lett. 2008, 92, 053301).
바람직한 것은 나아가 하나 이상의 층이 예를 들어 스핀 코팅에 의해, 또는 임의의 목적하는 인쇄 방법, 예를 들어 스크린 인쇄, 플렉소그래픽 인쇄, 오프셋 인쇄 또는 노즐 인쇄, 그러나 특히 바람직하게는 LITI (광 유도된 열 이미징, 열 전이 인쇄) 또는 잉크젯 인쇄에 의해, 용액으로부터 제조되는 것을 특징으로 하는 전자 소자, 특히 유기 전계발광 소자이다. 예를 들어 적합한 치환에 의해 수득되는 가용성 화합물은 상기 목적에 필수적이다.
전자 소자, 특히 유기 전계발광 소자는 또한 용액으로부터 하나 이상의 층을 적용하고 증착에 의해 하나 이상의 기타 층을 적용함으로써 하이브리드 시스템으로서 제조될 수 있다. 따라서, 예를 들어 용액으로부터 하나 이상의 발광체 및 매트릭스 재료를 포함하는 발광층을 적용하고, 진공 증착에 의해 정공-차단 층 및/또는 전자-수송 층을 그에 적용할 수 있다.
이들 방법은 일반적으로 당업자에 공지되어 있고, 본 발명에 따른 화합물을 포함하는 전자 소자, 특히 유기 전계발광 소자에 어려움 없이 적용될 수 있다.
용액으로부터 유기 전자 소자의 제조를 위해, 본 발명에 따른 화합물 또는 본 발명에 따른 조성물을 포함하는 제형이 필수적이다.
본 발명은 따라서 또한 하나 이상의 본 발명에 따른 화합물 또는 하나 이상의 본 발명에 따른 조성물 및 하나 이상의 용매를 포함하는 제형에 관한 것이다.
상기 제형은, 예를 들어 용액, 분산물 또는 에멀션일 수 있다. 상기 목적을 위해 2 개 이상의 용매의 혼합물을 사용하는 것이 바람직할 수 있다. 적합하고 바람직한 용매는, 예를 들어 톨루엔, 아니솔, o-, m- 또는 p-자일렌, 메틸 벤조에이트, 메시틸렌, 테트랄린, 베라트롤, THF, 메틸-THF, THP, 클로로벤젠, 디옥산, 페녹시톨루엔, 특히 3-페녹시톨루엔, (-)-펜촌, 1,2,3,5-테트라메틸벤젠, 1,2,4,5-테트라메틸벤젠, 1-메틸나프탈렌, 2-메틸벤조티아졸, 2-페녹시에탄올, 2-피롤리디논, 3-메틸아니솔, 4-메틸아니솔, 3,4-디메틸아니솔, 3,5-디메틸아니솔, 아세토페논, α-테르피네올, 벤조티아졸, 부틸 벤조에이트, 큐멘, 시클로헥산올, 시클로헥사논, 시클로헥실벤젠, 데칼린, 도데실벤젠, 에틸 벤조에이트, 인단, 메틸 벤조에이트, NMP, p-시멘, 페네톨, 1,4-디이소프로필벤젠, 디벤질 에테르, 디에틸렌 글리콜 부틸 메틸 에테르, 트리에틸렌 글리콜 부틸 메틸 에테르, 디에틸렌 글리콜 디부틸 에테르, 트리에틸렌 글리콜 디메틸 에테르, 디에틸렌 글리콜 모노부틸 에테르, 트리프로필렌 글리콜 디메틸 에테르, 테트라에틸렌 글리콜 디메틸 에테르, 2-이소프로필나프탈렌, 펜틸벤젠, 헥실벤젠, 헵틸-벤젠, 옥틸벤젠, 1,1-비스(3,4-디메틸페닐)에탄 또는 이들 용매의 혼합물이다.
본 발명에 따른 화합물을 포함하는 소자는 매우 다양한 방식으로 활용될 수 있다. 따라서, 예를 들어 전계발광 소자는 텔레비전, 휴대폰, 컴퓨터 및 카메라용 디스플레이에 활용될 수 있다. 그러나, 소자가 또한 광 적용에 사용될 수 있다. 나아가, 전계발광 소자는 의료 또는 화장 분야에서 광선 요법을 위해 사용될 수 있다. 따라서, 다수의 질환 (건선, 아토피성 피부염, 염증, 좌창, 피부암 등) 이 치료될 수 있거나, 또는 피부 주름, 피부 홍조 및 피부 노화가 방지 또는 저하될 수 있다. 나아가, 발광 소자는 음료, 식사류 또는 신선 식품의 유지 또는 기기 (예를 들어, 의료 기구) 의 살균을 위해 사용될 수 있다.
본 발명은 따라서 의료에서 광선 요법을 위해 사용되는, 하나 이상의 본 발명에 따른 화합물 또는 하나 이상의 본 발명에 따른 조성물을 포함하는, 전자 소자, 바람직하게는 유기 전계발광 소자, 매우 바람직하게는 OLED 또는 OLEC, 매우 특히 바람직하게는 OLED 에 관한 것이다.
본 발명은 나아가 바람직하게는 피부 질환의 광선 요법적 치료에 사용되는, 하나 이상의 본 발명에 따른 화합물 또는 하나 이상의 본 발명에 따른 조성물을 포함하는, 전자 소자, 바람직하게는 유기 전계발광 소자, 매우 바람직하게는 OLED 또는 OLEC, 매우 특히 바람직하게는 OLED 에 관한 것이다.
본 발명은 나아가 매우 바람직하게는 건선, 아토피성 피부염, 염증 질환, 백반증, 상처 치유, 피부암 및 황달, 특히 신생아의 황달의 광선 요법적 치료에 사용되는, 하나 이상의 본 발명에 따른 화합물 또는 하나 이상의 본 발명에 따른 조성물을 포함하는, 전자 소자, 바람직하게는 유기 전계발광 소자, 매우 바람직하게는 OLED 또는 OLEC, 매우 특히 바람직하게는 OLED 에 관한 것이다.
본 발명은 나아가 화장품 분야에서, 바람직하게는 좌창, 피부 노화 및 셀룰라이트의 치료를 위한, 하나 이상의 본 발명에 따른 화합물 또는 하나 이상의 본 발명에 따른 조성물을 포함하는, 전자 소자, 바람직하게는 유기 전계발광 소자, 매우 바람직하게는 OLED 또는 OLEC, 매우 특히 바람직하게는 OLED 의 용도에 관한 것이다.
본 발명에 따른 전자 소자, 특히 유기 전계발광 소자는 선행기술에 비해 하기 놀라운 이점들로 구별된다:
1.
본 발명에 따른 유기 전계발광 소자는 매우 높은 효율을 가짐.
2.
본 발명에 따른 유기 전계발광 소자는 동시에 개선된 수명을 가짐.
3.
본 발명에 따른 유기 전계발광 소자는 동시에 감소된 작동 전압을 가짐.
4.
본 발명에 따른 화합물이 유기 전자 소자, 특히 유기 전계발광 소자의 상업적 대량 생산에 매우 크게 적합하도록 본 발명에 따른 화합물은 매우 용이하고 저렴하게 제조될 수 있고, 잘 가공될 수 있고, 매우 잘 증발될 수 있음.
상기 언급된 바람직한 구현예는 목적하는바 서로 조합될 수 있다. 본 발명의 특히 바람직한 구현예에서, 상기 언급된 바람직한 구현예가 동시에 적용된다.
본 발명에 기재된 다양한 구현예가 본 발명의 범위 내에 있는 것에 주목되어야 한다. 본 발명에 개시된 각 특성은 명백히 배제되지 않는한 동일하거나, 동등하거나, 또는 유사한 목적을 기여하는 대안 특성으로 대체될 수 있다. 따라서, 본 발명에 개시된 각 특성은 달리 언급되지 않는한 일반 시리즈의 예로서 또는 동등하거나 또는 유사한 특성으로 간주되어야 한다.
본 발명의 모든 특성은 특정한 특성 및/또는 단계가 상호 배타적이지 않는한 임의의 방식으로 서로 조합될 수 있다. 특히, 본 발명의 바람직한 특성에 상기가 적용된다. 동등하게, 비본질적인 조합의 특성이 별개로 (조합이 아니라) 사용될 수 있다.
나아가, 수많은 특성들, 특히 본 발명의 바람직한 구현예의 특성들 그 자체가 진보적이라는 것에 주목되어야 하고, 본 발명의 구현예의 부분으로서 단지 간주되지 않아야 한다. 이들 특성의 경우, 독립적 보호가 현재 청구되는 각 발명에 부가하여 또는 그에 대한 대안으로서 추구될 수 있다.
본 발명과 함께 개시된 기술적 조치에 대한 교시가 추출될 수 있고, 기타 예들과 조합될 수 있다.
당업자는 진보성 없이 추가의 본 발명에 따른 전자 소자를 제조하는데 설명을 사용함으로써 청구범위를 통틀어 본 발명을 수행할 수 있을 것이다.
실시예
실시예 1
2-[3-[7'-(4,6-디페닐-1,3,5-트리아진-2-일)-9,9'-스피로바이-[플루오렌]-2'-일]페닐]-1-페닐벤즈이미다졸 6a 의 합성
2-[3-(7'-브로모-9,9'-스피로바이[플루오렌]-2'-일)페닐]-1-페닐-벤즈이미다졸 (3a) 의 합성
변형법 A
400 ml 의 톨루엔, 400 ml 의 1,4-디옥산 및 200 ml 의 DI 수 중의 50.0 g (105 mmol, 1.00 eq.) 의 2,7-디브로모-9,9'-스피로바이플루오렌 1a, 41.7 g (105 mmol, 1.00 eq.) 의 1-페닐-2-[3-(4,4,5,5-테트라메틸-1,3,2-디옥사-보롤란-2-일)페닐]-1H-벤즈이미다졸 2a 및 36.4 g (263 mmol, 2.50 eq.) 의 탄산칼륨을 우선 2 l 4-구 플라스크에 보호 기체 하에 도입시키고, 탈기시킨다. 이후, 1.22 g (1.05 mmol, 0.01 eq.) 의 테트라키스(트리-페닐포스핀)팔라듐(0) 을 첨가하고, 혼합물을 환류 하에 밤새 가열한다. 반응 완료시, 배치(batch) 를 냉각하고, Celite 를 통해 여과하고, 1 l 의 톨루엔으로 희석한다. 용액을 각 경우에 300 ml 의 반-포화 염화나트륨 용액으로 3x 세정하고, 황산나트륨으로 건조시킨 후 회전 증발기에서 약 200 ml 로 증발시킨다. 침전된 고체를 여과해내고, 진공에서 건조시킨다. 2 치환된 부산물을 승화로 분리해내어 22.0 g (33.1 mmol, 32%) 의 목적하는 생성물 3a 를 수득한다.
변형법 B
절차를 변형법 A 의 절차와 유사하게 수행하는데, 이때 테트라키스(트리페닐포스핀)팔라듐(0) 을 0.01 eq. 의 팔라듐(II) 아세테이트 및 0.01 eq. 의 디시클로헥실-(2',6'-디메톡시바이페닐-2-일)포스핀 (SPhos) 로 대체한다.
하기를 유사하게 반응시킨다:
1-페닐-2-[3-[7'-(4,4,5,5-테트라메틸-1,3,2-디옥사보롤란-2-일)-9,9'-스피로바이[플루오렌]-2'-일]페닐]벤즈이미다졸 4a 의 합성
500 ml 의 건조된 1,4-디옥산 중의 22.0 g (33.1 mmol, 1.00 eq.) 의 2-[3-(7'-브로모-9,9'-스피로바이[플루오렌]-2'-일)-페닐]-1-페닐벤즈이미다졸 3a, 8.84 g (30.1 mmol, 0.91 eq.) 의 비스-(피나콜레이토)디보론 및 26.0 g (265 mmol, 8.00 eq.) 의 칼륨 아세테이트를 우선 1 l 4-구 플라스크에 도입시키고, 30 분 동안 탈기시킨다. 이후, DCM 과의 1,1-비스(디페닐포스피노)페로센팔라듐(II) 디클로라이드 착물 812 mg (0.995 mmol, 0.0300 eq.) 을 첨가하고, 혼합물을 80℃ 의 내부 온도로 가열한다. 밤새 교반한 후, 배치를 냉각하고, 침전된 고체를 흡입으로 여과해낸다. 여과물을 회전 증발기에서 약 50 ml 로 증발시키고, 침전된 고체를 마찬가지로 흡입으로 여과해낸다. 고체를 수합하고, 건조시켜 21.0 g (29.5 mmol, 89%) 의 보론 에스테르 4a 를 수득한다.
하기를 유사하게 반응시킨다:
2-[3-[7'-(4,6-디페닐-1,3,5-트리아진-2-일)-9,9'-스피로바이-[플루오렌]-2'-일]페닐]-1-페닐벤즈이미다졸 6a 의 합성
변형법 A
200 ml 의 톨루엔, 200 ml 의 1,4-디옥산 및 100 ml 의 DI 수 중에서 3.75 g (35.4 mmol, 1.20 eq.) 의 탄산나트륨과 함께 21.0 g (29.5 mmol, 1.00 eq.) 의 1-페닐-2-[3-[7'-(4,4,5,5-테트라메틸-1,3,2-디옥사보롤란-2-일)-9,9'-스피로바이[플루오렌]-2'-일]페닐]벤즈이미다졸 4a 및 7.90 g (29.5 mmol, 1.00 eq.) 의 2-클로로-4,6-디페닐-1,3,5-트리아진 5a 를 우선 1 l 3-구 플라스크에 도입시키고, 20 분 동안 탈기시킨다. 1.02 g (0.885 mmol, 0.0300 eq.) 의 테트라키스(트리페닐포스핀)-팔라듐(0) 의 첨가 후, 배치를 환류 하에 2 일 동안 가열하고, 반응 완료시에 냉각시킨다. 침전된 고체를 흡입으로 여과해내고, 물 및 약간의 톨루엔으로 세정한 후, HPLC 순도 > 99.9% 에 도달할 때까지 톨루엔/헵탄으로부터 수 회 재결정화한다. 승화를 통해 11.5 g (14.0 mmol, 43%) 의 무색 고체 6a 를 수득한다.
변형법 B
절차를 변형법 A 의 절차와 유사하게 수행하는데, 이때 테트라키스(트리페닐포스핀)팔라듐(0) 을 0.01 eq. 의 팔라듐(II) 아세테이트 및 0.04 eq. 의 트리(o-톨릴)포스핀으로 대체한다.
변형법 C
절차를 변형법 A 의 절차와 유사하게 수행하는데, 이때 테트라키스(트리페닐포스핀)팔라듐(0) 을 0.01 eq. 의 팔라듐(II) 아세테이트 및 0.01 eq. 의 디시클로헥실-(2',6'-디메톡시-바이페닐-2-일)포스핀 (SPhos) 으로 대체한다.
하기를 유사하게 제조한다:
실시예 2
2-(3-[1-페닐-1H-벤즈이미다졸-2-일]페닐)-4-페닐-6-(9,9'-스피로-바이[9H-플루오렌]-2-일)-1,3,5-트리아진 11a
2-클로로-4-페닐-6-(9,9'-스피로바이[9H-플루오렌]-2-일)-1,3,5-트리아진 9a 의 합성
변형법 A
300 ml 의 톨루엔, 300 ml 의 1,4-디옥산 및 300 ml 의 DI 수 중의 24.5 g (67.9 mmol, 1.00 eq.) 의 9,9'-스피로바이플루오렌-2'-일보론산 7a, 15.4 g (68.3 mmol, 1.01 eq.) 의 2,4-디클로로-6-페닐-1,3,5-트리아진 8a 및 9.04 g (85.3 mmol, 1.26 eq.) 의 탄산나트륨을 2 l 4-구 플라스크에 보호 기체 하에 도입시키고, 탈기시킨다. 이후, 0.850 g (0.736 mmol, 0.01 eq.) 의 테트라키스(트리페닐포스핀)팔라듐(0) 을 첨가하고, 혼합물을 환류 하에 24 시간 동안 가열한다. 반응 완료시, 배치를 냉각하고, 100 ml 의 에틸 아세테이트로 희석한다. 상을 분별 깔때기로 분리시키고, 수성상을 에틸 아세테이트로 3 회 추출하고, 수합한 유기상을 물로 한 번 더 세정한다. 이후, 혼합물을 황산나트륨으로 건조시키고, 용액을 갈색빛 고체가 침전될 때까지 증발시킨다. 고체를 여과해내고, 고온 에탄올로 교반 하에 세정하고, 재여과 후 진공에서 건조시킨다. 생성물을 용리액으로서 헵탄/디클로로-메탄 5:1 을 사용하는 컬럼 크로마토그래피로 정제하여 9.90 g (19.6 mmol, 29%) 의 무색 고체를 수득한다.
변형법 B
절차를 변형법 A 의 절차와 유사하게 수행하는데, 이때 테트라키스(트리페닐포스핀)팔라듐(0) 을 0.01 eq. 의 팔라듐(II) 아세테이트 및 0.04 eq. 의 트리(o-톨릴)포스핀으로 대체한다.
변형법 C
절차를 변형법 A 의 절차와 유사하게 수행하는데, 이때 테트라키스(트리페닐포스핀)팔라듐(0) 을 0.01 eq. 의 팔라듐(II) 아세테이트 및 0.01 eq. 의 디시클로헥실-(2',6'-디메톡시바이페닐-2-일)포스핀 (SPhos) 으로 대체한다.
변형법 D
절차를 변형법 A 의 절차와 유사하게 수행하는데, 이때 테트라키스(트리페닐포스핀)팔라듐(0) 을 DCM 과의 1,1-비스-(디페닐포스피노)페로센팔라듐(II) 디클로라이드 착물 0.02 eq. 로 대체하고, 건조된 톨루엔을 용매로서 사용한다.
하기를 유사하게 제조한다:
2-(3-[1-페닐-1H-벤즈이미다졸-2-일]페닐)-4-페닐-6-(9,9'-스피로바이[9H-플루오렌]-2-일)-1,3,5-트리아진 11a 의 합성
변형법 A
35 ml 의 톨루엔, 35 ml 의 1,4-디옥산 및 35 ml 의 DI 수 중의 9.90 g (19.6 mmol, 1.00 eq.) 의 2-클로로-4-페닐-6-(9,9'-스피로바이[9H-플루오렌]-2-일)-1,3,5-트리아진 9a, 8.53 g (21.5 mmol, 1.10 eq.) 의 1-페닐-2-[3-(4,4,5,5-테트라메틸-1,3,2-디옥사보롤란-2-일)페닐]-1H-벤즈이미다졸 10a 및 4.57 g (43.1 mmol, 2.20 eq.) 의 탄산나트륨을 우선 250 ml 3-구 플라스크에 보호 기체 하에 도입시키고, 탈기시킨다. 이후, 1.13 g (0.980 mmol, 0.05 eq.) 의 테트라키스(트리페닐포스핀)팔라듐(0) 을 첨가하고, 혼합물을 환류 하에 48 시간 동안 가열한다. 반응 완료시, 배치를 냉각하고, 침전된 고체를 흡입으로 여과해낸다. 수득한 미정제물을 추출, 헵탄/톨루엔으로부터의 삼중 재결정화 및 승화로 정제하여 HPLC 순도 > 99.9% 인 4.83 g (6.54 mmol, 33%) 의 고체를 수득한다.
변형법 B
절차를 변형법 A 의 절차와 유사하게 수행하는데, 이때 테트라키스(트리페닐포스핀)팔라듐(0) 을 DCM 과의 1,1-비스-(디페닐포스피노)페로센팔라듐(II) 디클로라이드 착물 0.02 eq. 로 대체하고, 건조된 톨루엔을 용매로서 사용한다.
변형법 C
4.15 ml (24.4 mmol, 1.10 eq.) 의 디이소프로필에틸아민 (Hunig 염기) 을 실온에서 150 ml 의 THF 중의 10.2 g (22.2 mmol, 1.00 eq.) 의 2-바이페닐-3-일-4-클로로-6-(9,9-디메틸-9H-플루오렌-2-일)-1,3,5-트리아진 9k 및 4.31 g (22.2 mmol, 1.00 eq.) 의 2-페닐-1H-벤즈이미다졸 10k 의 용액에 첨가한다. 반응 혼합물을 밤새 교반하고, 반응 완료시 용매를 진공에서 제거한다. 200 ml 의 디클로로메탄의 첨가 후, 용액을 물로 3 회 추출하고, 황산나트륨으로 건조시키고, 용매를 회전 증발기에서 제거한다. 정제를 변형법 A 와 유사하게 수행하여 5.57 g (9.02 mmol, 41%) 의 목적하는 생성물 11k 를 수득한다.
하기를 유사하게 제조한다:
실시예 3
OLED 의 제조 및 특성화
각종 OLED 의 데이터가 하기 실시예 V1 내지 E16 (표 1 및 2 참조) 에 제시되어 있다.
실시예 V1-E16 에 대한 사전처리: 두께 50 nm 의, 구조화 ITO (인듐 주석 옥시드) 로 코팅된 유리판을 공정 개선을 위해 20 nm 의 PEDOT:PSS (폴리(3,4-에틸렌디옥시티오펜) 폴리(스티렌술포네이트), Heraeus Precious Metals GmbH, Germany 로부터 CLEVIOS™ P VP AI 4083 로서 입수, 수용액으로부터 스핀 코팅에 의해 적용) 로 코팅시킨다. 이들 코팅된 유리판은 OLED 가 적용되는 기판을 형성한다.
OLED 는 이론상 하기 층 구조를 갖는다: 기판 / 정공-수송 층 (HTL) / 임의의 사이층 (IL) / 전자-차단 층 (EBL) / 발광 층 (EML) / 임의의 정공-차단 층 (HBL) / 전자-수송 층 (ETL) / 임의의 전자-주입 층 (EIL) 및 최종적으로 캐소드. 캐소드는 두께 100 nm 로 알루미늄 층에 의해 형성된다. OLED 의 정확한 구조가 표 1 에 나타나 있다. OLED 의 제조에 요구되는 재료가 표 3 에 나타나 있다.
모든 재료를 진공 챔버에서 열 증착으로 적용한다. 여기서, 발광 층은 항상 공증발에 의해 특정한 부피비로 매트릭스 재료 또는 매트릭스 재료들과 부가혼합되는 하나 이상의 매트릭스 재료 (호스트 재료) 및 발광 도펀트 (발광체) 로 이루어진다. 여기서, IC1:IC3:TEG1 (55%:35%:10%) 과 같은 표현은, 재료 IC1 이 55% 의 부피비로 층에 존재하고, IC3 이 35% 의 비로 층에 존재하고, TEG1 이 10% 의 비로 층에 존재하는 것을 의미한다. 유사하게, 전자-수송 층은 또한 2 개의 재료의 혼합물로 이루어질 수 있다.
OLED 는 표준 방법에 의해 특징지어진다. 이 목적을 위해, 람베르트 (Lambert) 발광 특성을 추정하는, 전류/전압/발광 밀도 특성 선 (IUL 특성 선) 으로부터 산출되는, 발광 밀도의 함수로서 전계발광 스펙트럼, 전류 효율 (cd/A 로 측정됨), 전력 효율 (lm/W 로 측정됨) 및 외부 양자 효율 (EQE, % 로 측정됨), 및 수명을 측정한다. 전계발광 스펙트럼은 발광 밀도 1000 cd/m2 에서 측정되고, 이로부터 CIE 1931 x 및 y 색 좌표가 산출된다. 표 2 의 용어 U1000 은 1000 cd/m2 의 발광 밀도에 요구되는 전압을 나타낸다. CE1000 및 PE1000 은 1000 cd/m2 에서 달성되는 전류 및 전력 효율을 각각 나타낸다. 최종적으로, EQE1000 은 1000 cd/m2 의 작업 발광 밀도에서의 외부 양자 효율을 나타낸다. 수명 LT 는 발광 밀도가 일정한 전류 하에 작업시 초기 발광 밀도로부터 특정한 비 L1 로 떨어진 후의 시간으로 정의된다. 표 2 에서 L0;j0 = 4000 cd/m2 및 L1 = 70% 의 표현은, 컬럼 LT 에서 나타낸 수명이 초기 발광 밀도가 4000 cd/m2 에서 2800 cd/m2 로 떨어진 후의 시간에 상응하는 것을 의미한다. 유사하게는, L0;j0 = 20 mA/cm2, L1 = 80% 은 발광 밀도가 20 mA/cm2 에서 작업시 시간 LT 후 그 초기 값의 80% 로 떨어진 것을 의미한다.
각종 OLED 의 데이터가 표 2 에 요약되어 있다. 실시예 V1-V3 은 선행기술에 따른 비교예이고, 실시예 E1-E16 은 본 발명에 따른 OLED 의 데이터를 나타낸다.
실시예의 일부는 본 발명에 따른 OLED 의 이점을 예시하기 위해 하기에 보다 상세히 설명된다.
OLED 의 전자-수송 층 (ETL 또는 EIL) 에서의, 본 발명에 따른 혼합물의 용도
OLED 에서의 전자-주입 및 전자-수송 층에서 사용시, 본 발명에 따른 재료는 성분의 수명 및/또는 효율에 있어서 선행기술에 비해 상당한 개선을 유도한다. 본 발명에 따른 화합물 EG1 의 사용은 선행기술과 비교시 관찰되는 수명을 20% 내지 40% 로 증가시키는 것을 가능케 한다 (실시예 V1 및 V2 와 E1 과의 비교, 및 V3 과 E2 와의 비교). 본 발명에 따른 화합물의 추가의 기술적 이점은 선행기술과 비교시 약 10% 까지 효율을 증가시킨다 (실험 V1 과 E1 과의 비교).
Claims (20)
- 일반식 (GK-1) 의 골격 및 하나 이상의 식 (G-2) 의 기 및 하나 이상의 식 (G-3) 의 기를 함유하는 화합물로서, 이때 식 (G-2) 및 (G-3) 의 기 및 골격이 서로 공유 결합되는 화합물:
[식 중, 사용되는 기호 및 지수에 하기 정의가 적용됨:
R1 은 각 경우에 동일 또는 상이하게 H, D, F, Cl, Br, I, CHO, N(Ar1)2, C(=O)Ar1, P(=O)(Ar1)2, S(=O)Ar1, S(=O)2Ar1, CR2=CR2Ar1, CN, NO2, Si(R2)3, B(OR2)2, B(R2)2, B(N(R2)2)2, OSO2R2, 1 내지 40 개의 C 원자를 갖는 직쇄 알킬, 알콕시 또는 티오알콕시기, 또는 2 내지 40 개의 C 원자를 갖는 직쇄 알케닐 또는 알키닐기, 또는 3 내지 40 개의 C 원자를 갖는 분지형 또는 시클릭 알킬, 알케닐, 알키닐, 알콕시 또는 티오알콕시기 (이들 각각은 하나 이상의 라디칼 R2 에 의해 치환될 수 있고, 하나 이상의, 바람직하게는 비인접한 CH2 기는 R2C=CR2, C≡C, Si(R2)2, Ge(R2)2, Sn(R2)2, C=O, C=S, C=Se, C=NR2, P(=O)(R2), SO, SO2, NR2, O, S 또는 CONR2 에 의해 대체될 수 있고, 하나 이상의 H 원자는 D, F, Cl, Br, I, CN 또는 NO2 에 의해 대체될 수 있음), 또는 5 내지 60 개의 방향족 고리 원자를 갖는 방향족 또는 헤테로방향족 고리계 (이는 각 경우에 하나 이상의 라디칼 R2 에 의해 치환될 수 있음), 또는 5 내지 60 개의 방향족 고리 원자를 갖는 아릴옥시 또는 헤테로아릴옥시기 (이는 하나 이상의 라디칼 R2 에 의해 치환될 수 있음), 또는 이들 계의 조합이고; 2 개 이상의 인접한 치환기 R1 은 여기서 서로 모노- 또는 폴리시클릭, 지방족 또는 방향족 고리계를 형성할 수 있고;
R2 는 동일 또는 상이하게 각 경우에 H, D, F, Cl, Br, I, N(R3)2, CN, NO2, Si(R3)3, B(OR3)2, C(=O)R3, P(=O)(R3)2, S(=O)R3, S(=O)2R3, OSO2R3, 1 내지 40 개의 C 원자를 갖는 직쇄 알킬, 알콕시 또는 티오알콕시기, 또는 2 내지 40 개의 C 원자를 갖는 직쇄 알케닐 또는 알키닐기, 또는 3 내지 40 개의 C 원자를 갖는 분지형 또는 시클릭 알킬, 알케닐, 알키닐, 알콕시, 알킬알콕시 또는 티오알콕시기 (이들 각각은 하나 이상의 라디칼 R3 에 의해 치환될 수 있고, 하나 이상의 비인접한 CH2 기는 R3C=CR3, C≡C, Si(R3)2, Ge(R3)2, Sn(R3)2, C=O, C=S, C=Se, C=NR3, P(=O)(R3), SO, SO2, NR3, O, S 또는 CONR3 에 의해 대체될 수 있고, 하나 이상의 H 원자는 D, F, Cl, Br, I, CN 또는 NO2 에 의해 대체될 수 있음), 또는 5 내지 60 개의 방향족 고리 원자를 갖는 방향족 또는 헤테로방향족 고리계 (이는 각 경우에 하나 이상의 라디칼 R3 에 의해 치환될 수 있음), 또는 5 내지 60 개의 방향족 고리 원자를 갖는 아릴옥시, 아릴알콕시 또는 헤테로아릴옥시기 (이는 하나 이상의 라디칼 R3 에 의해 치환될 수 있음), 또는 10 내지 40 개의 방향족 고리 원자를 갖는 디아릴아미노기, 디헤테로아릴아미노기 또는 아릴헤테로아릴아미노기 (이는 하나 이상의 라디칼 R3 에 의해 치환될 수 있음), 또는 이들 기의 2 개 이상의 조합이고; 2 개 이상의 인접한 라디칼 R2 는 여기서 서로 모노- 또는 폴리시클릭, 지방족 또는 방향족 고리계를 형성할 수 있고; 2 개 이상의 인접한 치환기 R2 가 서로 모노- 또는 폴리시클릭, 지방족 또는 방향족 고리계를 형성하지 않은 경우가 바람직하고;
R3 은 동일 또는 상이하게 각 경우에 H, D, F 또는 1 내지 20 개의 C 원자를 갖는 지방족, 방향족 및/또는 헤테로방향족 탄화수소 라디칼 (이때, 추가로 하나 이상의 H 원자는 F 에 의해 대체될 수 있음) 이고; 2 개 이상의 치환기 R3 은 여기서 또한 서로 모노- 또는 폴리시클릭, 지방족 또는 방향족 고리계를 형성할 수 있고; 2 개 이상의 인접한 치환기 R3 이 서로 모노- 또는 폴리시클릭, 지방족 또는 방향족 고리계를 형성하지 않은 경우가 바람직하고;
R5 는 각 경우에 동일 또는 상이하게 F, Cl, Br, I, CHO, N(Ar1)2, C(=O)Ar1, P(=O)(Ar1)2, S(=O)Ar1, S(=O)2Ar1, CR2=CR2Ar1, CN, NO2, Si(R2)3, B(OR2)2, B(R2)2, B(N(R2)2)2, OSO2R2, 1 내지 40 개의 C 원자를 갖는 직쇄 알킬, 알콕시 또는 티오알콕시기, 또는 2 내지 40 개의 C 원자를 갖는 직쇄 알케닐 또는 알키닐기, 또는 3 내지 40 개의 C 원자를 갖는 분지형 또는 시클릭 알킬, 알케닐, 알키닐, 알콕시 또는 티오알콕시기 (이들 각각은 하나 이상의 라디칼 R2 에 의해 치환될 수 있고, 하나 이상의, 바람직하게는 비인접한 CH2 기는 R2C=CR2, C≡C, Si(R2)2, Ge(R2)2, Sn(R2)2, C=O, C=S, C=Se, C=NR2, P(=O)(R2), SO, SO2, NR2, O, S 또는 CONR2 에 의해 대체될 수 있고, 하나 이상의 H 원자는 D, F, Cl, Br, I, CN 또는 NO2 에 의해 대체될 수 있음), 또는 5 내지 60 개의 방향족 고리 원자를 갖는 방향족 또는 헤테로-방향족 고리계 (이는 각 경우에 하나 이상의 라디칼 R2 에 의해 치환될 수 있음), 또는 5 내지 60 개의 방향족 고리 원자를 갖는 아릴옥시 또는 헤테로아릴옥시기 (이는 하나 이상의 라디칼 R2 에 의해 치환될 수 있음), 또는 이들 계의 조합이고; 2 개 이상의 인접한 치환기 R5 는 서로 모노- 또는 폴리시클릭, 지방족 또는 방향족 고리계를 형성할 수 없고;
R4 및 R6 은 각 경우에 동일 또는 상이하게 H, D, F, Cl, Br, I, CHO, N(Ar1)2, C(=O)Ar1, P(=O)(Ar1)2, S(=O)Ar1, S(=O)2Ar1, CR2=CR2Ar1, CN, NO2, Si(R2)3, B(OR2)2, B(R2)2, B(N(R2)2)2, OSO2R2, 1 내지 40 개의 C 원자를 갖는 직쇄 알킬, 알콕시 또는 티오알콕시기, 또는 2 내지 40 개의 C 원자를 갖는 직쇄 알케닐 또는 알키닐기, 또는 3 내지 40 개의 C 원자를 갖는 분지형 또는 시클릭 알킬, 알케닐, 알키닐, 알콕시 또는 티오알콕시기 (이들 각각은 하나 이상의 라디칼 R2 에 의해 치환될 수 있고, 하나 이상의, 바람직하게는 비인접한 CH2 기는 R2C=CR2, C≡C, Si(R2)2, Ge(R2)2, Sn(R2)2, C=O, C=S, C=Se, C=NR2, P(=O)(R2), SO, SO2, NR2, O, S 또는 CONR2 에 의해 대체될 수 있고, 하나 이상의 H 원자는 D, F, Cl, Br, I, CN 또는 NO2 에 의해 대체될 수 있음), 또는 5 내지 60 개의 방향족 고리 원자를 갖는 방향족 또는 헤테로방향족 고리계 (이는 각 경우에 하나 이상의 라디칼 R2 에 의해 치환될 수 있음), 또는 5 내지 60 개의 방향족 고리 원자를 갖는 아릴옥시 또는 헤테로아릴옥시기 (이는 하나 이상의 라디칼 R2 에 의해 치환될 수 있음), 또는 이들 계의 조합이고; 2 개 이상의 인접한 치환기 R4 는 서로 모노- 또는 폴리시클릭, 지방족 또는 방향족 고리계를 형성할 수 없고; 2 개 이상의 인접한 치환기 R6 은 서로 모노- 또는 폴리시클릭, 지방족 또는 방향족 고리계를 형성할 수 있고, 2 개 이상의 인접한 치환기 R6 이 서로 모노- 또는 폴리시클릭, 지방족 또는 방향족 고리계를 형성할 수 없는 경우가 바람직하고;
Q 는 C=O, C=S, S, C(R2)2, NR2 또는 O, 바람직하게는 C(R2)2, NR2 또는 O, 매우 바람직하게는 C(R2)2 또는 NR2, 특히 바람직하게는 C(R2)2 이고;
n 은 0 또는 1 이며, 이때 n = 0 인 것이 바람직하고, n = 0 인 것은 2 개의 방향족 고리 A 및 B 가 기 Q 를 통해 서로 연결되지 않지만 대신에 단일 결합에 의해 연결되는 것을 의미하고;
p 는 0, 1, 2, 3 또는 4, 바람직하게는 0, 1 또는 2, 매우 바람직하게는 0 또는 1, 특히 바람직하게는 0 이고;
q 는 0, 1, 2, 3 또는 4, 바람직하게는 0, 1 또는 2, 매우 바람직하게는 0 또는 1, 특히 바람직하게는 0 이고;
r 은 0, 1, 2, 3 또는 4, 바람직하게는 0, 1 또는 2, 매우 바람직하게는 0 또는 1 이고, r 은 특히 바람직하게는 0 이고;
X 는 동일 또는 상이하게 각 경우에 N 또는 CR1 이고, 하나 이상의 X 는 N 이고, 바람직하게는 X 중 2 개 이상은 N 이고, 매우 바람직하게는 X 3 개 모두는 N 이고;
Ar1 은 각 경우에 동일 또는 상이하게 5 내지 30 개의 방향족 고리 원자를 갖는 방향족 또는 헤테로방향족 고리계 (이는 하나 이상의 라디칼 R2 에 의해 치환될 수 있음) 이고; 라디칼 Ar1 중 2 개는 여기서 또한 B(R2), C(R2)2, Si(R2)2, C=O, C=NR2, C=C(R2)2, O, S, S=O, SO2, N(R2), P(R2) 및 P(=O)R2 로부터 선택되는 브릿지 또는 단일 결합에 의해 서로 연결될 수 있고; 2 개의 라디칼 Ar1 이 서로 연결되지 않은 경우가 바람직함]. - 제 1 항에 있어서, 화합물이 최대 3000 g/mol 의 분자량을 갖는 소분자인 것을 특징으로 하는 화합물.
- 제 1 항 내지 제 3 항 중 어느 한 항에 있어서, 화합물이 하기 일반식 (1) 을 갖는 것을 특징으로 하는 화합물:
[식 중, 상기 정의가 적용되고, 나아가:
Q' 는 서로 동일 또는 상이하게 C=O, C=S, S, C(R2)2, NR2 또는 O, 바람직하게는 C(R2)2, NR2 또는 O, 매우 바람직하게는 C(R2)2 또는 NR2, 특히 바람직하게는 C(R2)2 이고;
a 는 0, 1, 2, 3 또는 4, 바람직하게는 0, 1 또는 2, 매우 바람직하게는 0 또는 1, 특히 바람직하게는 0 이고;
b 는 0, 1, 2, 3 또는 4, 바람직하게는 0, 1 또는 2, 매우 바람직하게는 0 또는 1, 특히 바람직하게는 0 이고;
a+b 는 여기서 항상 7 이하이고, a+b 는 바람직하게는 0, 1, 2 또는 3 이고, a+b 는 매우 바람직하게는 0, 1 또는 2 이고, a+b 는 특히 바람직하게는 0 또는 1 이고, a+b 는 매우 특히 바람직하게는 0 이고;
m 은 0 또는 1 이며, 이때 m = 0 인 것이 바람직하고, m = 0 인 것은 2 개의 방향족 고리가 기 Q' 를 통해 서로 연결되지 않지만 대신에 단일 결합에 의해 연결되는 것을 의미하고;
V 는 2 가기이고;
U 는 2 가기이고;
v 는 0 또는 1 이며, 이때 v = 0 인 것은 고리 D 가 단일 공유 결합을 통해 화합물의 나머지에 직접 연결된 것을 의미하고;
u 는 0 또는 1 이며, 이때 u = 0 인 것은 고리 C 가 단일 공유 결합을 통해 화합물의 나머지에 직접 연결된 것을 의미함]. - 제 1 항 내지 제 3 항 중 어느 한 항에 있어서, 2 개 이상의 인접한 치환기 R1 이 서로 모노- 또는 폴리시클릭, 지방족 또는 방향족 고리계를 형성하지 않는 것을 특징으로 하는 화합물.
- 하나 이상의 제 1 항 내지 제 12 항 중 어느 한 항에 따른 화합물, 및 형광 발광체, 인광 발광체, 매트릭스 재료, 전자-수송 재료, 전자-주입 재료, 정공-전도 재료, 정공-주입 재료, 전자-차단 재료 및 정공-차단 재료, 넓은 대역 간격 재료 및 n-도펀트로 이루어진 군으로부터 선택되는 하나 이상의 추가의 화합물을 포함하는 조성물.
- 제 13 항에 있어서, 추가의 화합물이 전자-수송 재료 또는 매트릭스 재료인 것을 특징으로 하는 조성물.
- 하나 이상의 제 1 항 내지 제 12 항 중 어느 한 항에 따른 화합물, 또는 하나 이상의 제 13 항 또는 제 14 항에 따른 조성물, 및 하나 이상의 용매를 포함하는 제형.
- 전자 소자, 바람직하게는 유기 전계발광 소자, 매우 바람직하게는 유기 발광 다이오드 (OLED) 또는 유기 발광 전기화학 전지 (OLEC, LEEC, LEC), 매우 특히 바람직하게는 OLED, 바람직하게는 발광층 (EML), 전자-수송 층 (ETL) 및 정공-차단 층 (HBL), 매우 바람직하게는 EML 및 ETL 에서의, 하나 이상의 제 1 항 내지 제 12 항 중 어느 한 항에 따른 화합물, 또는 하나 이상의 제 13 항 또는 제 14 항에 따른 조성물의 용도.
- 바람직하게는 발광층 (EML), 전자-수송 층 (ETL) 및 정공-차단 층 (HBL), 매우 바람직하게는 EML 또는 ETL, 매우 특히 바람직하게는 ETL 에서 하나 이상의 제 1 항 내지 제 12 항 중 어느 한 항에 따른 화합물, 또는 하나 이상의 제 13 항 또는 제 14 항에 따른 조성물을 포함하는 전자 소자.
- 제 17 항에 있어서, 유기 집적 회로 (OIC), 유기 전계-효과 트랜지스터 (OFET), 유기 박막 트랜지스터 (OTFT), 유기 전계발광 소자, 유기 태양 전지 (OSC), 유기 광학 검출기, 유기 광수용기, 바람직하게는 유기 전계발광 소자로부터 선택되는 것을 특징으로 하는 전자 소자.
- 제 17 항 또는 제 18 항에 있어서, 유기 발광 트랜지스터 (OLET), 유기 전계-켄치 소자 (OFQD), 유기 발광 전기화학 전지 (OLEC, LEC, LEEC), 유기 레이저 다이오드 (O-레이저) 및 유기 발광 다이오드 (OLED), 바람직하게는 OLEC 및 OLED, 매우 바람직하게는 OLED 로 이루어진 군으로부터 선택되는 유기 전계발광 소자인 것을 특징으로 하는 전자 소자.
- 제 17 항 내지 제 19 항 중 어느 한 항에 따른 전자 소자의 제조 방법으로서, 하나 이상의 유기 층이 기상 침착에 의해 또는 용액으로부터 적용되는 것을 특징으로 하는 방법.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020227043687A KR102657649B1 (ko) | 2014-07-21 | 2015-06-30 | 전자 소자용 재료 |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP14002528 | 2014-07-21 | ||
| EP14002528.9 | 2014-07-21 | ||
| PCT/EP2015/001315 WO2016012075A1 (de) | 2014-07-21 | 2015-06-30 | Materialien für elektronische vorrichtungen |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020227043687A Division KR102657649B1 (ko) | 2014-07-21 | 2015-06-30 | 전자 소자용 재료 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20170032414A true KR20170032414A (ko) | 2017-03-22 |
| KR102479149B1 KR102479149B1 (ko) | 2022-12-19 |
Family
ID=51220375
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020227043687A KR102657649B1 (ko) | 2014-07-21 | 2015-06-30 | 전자 소자용 재료 |
| KR1020177004335A KR102479149B1 (ko) | 2014-07-21 | 2015-06-30 | 전자 소자용 재료 |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020227043687A KR102657649B1 (ko) | 2014-07-21 | 2015-06-30 | 전자 소자용 재료 |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US10903430B2 (ko) |
| EP (2) | EP3172775B1 (ko) |
| JP (3) | JP6629291B2 (ko) |
| KR (2) | KR102657649B1 (ko) |
| CN (3) | CN106536485A (ko) |
| TW (3) | TWI703140B (ko) |
| WO (1) | WO2016012075A1 (ko) |
Cited By (34)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE102018101398A1 (de) | 2017-03-15 | 2018-09-20 | Hyundai Motor Company | Vibrationssensitives Aufhängungssystem und Steuerverfahren davon |
| WO2018182259A1 (ko) * | 2017-03-30 | 2018-10-04 | 주식회사 엘지화학 | 유기 발광 소자 |
| WO2018190666A1 (ko) * | 2017-04-13 | 2018-10-18 | 주식회사 엘지화학 | 헤테로고리 화합물 및 이를 포함하는 유기 발광 소자 |
| WO2018216913A1 (ko) * | 2017-05-22 | 2018-11-29 | 주식회사 엘지화학 | 신규한 헤테로고리 화합물 및 이를 이용한 유기발광 소자 |
| WO2018216887A1 (ko) * | 2017-05-22 | 2018-11-29 | 주식회사 엘지화학 | 신규한 화합물 및 이를 이용한 유기발광 소자 |
| WO2018230854A1 (ko) * | 2017-06-16 | 2018-12-20 | 경상대학교산학협력단 | 신규한 아크리딘 유도체 및 이를 포함하는 유기전계발광소자 |
| WO2018236066A1 (ko) * | 2017-06-21 | 2018-12-27 | 주식회사 엘지화학 | 신규한 헤테로 고리 화합물 및 이를 이용한 유기 발광 소자 |
| WO2018236040A1 (ko) * | 2017-06-21 | 2018-12-27 | 주식회사 엘지화학 | 신규한 헤테로 고리 화합물 및 이를 이용한 유기발광 소자 |
| WO2019004790A1 (ko) * | 2017-06-30 | 2019-01-03 | 주식회사 엘지화학 | 헤테로고리 화합물 및 이를 포함하는 유기 발광 소자 |
| WO2019004796A1 (ko) * | 2017-06-30 | 2019-01-03 | 주식회사 엘지화학 | 신규한 헤테로 고리 화합물 및 이를 이용한 유기 발광 소자 |
| WO2019004612A1 (ko) * | 2017-06-29 | 2019-01-03 | 주식회사 엘지화학 | 신규한 헤테로 고리 화합물 및 이를 이용한 유기 발광 소자 |
| KR20190002299A (ko) * | 2017-06-29 | 2019-01-08 | 주식회사 엘지화학 | 신규한 헤테로 고리 화합물 및 이를 이용한 유기 발광 소자 |
| WO2019013542A1 (ko) * | 2017-07-11 | 2019-01-17 | 주식회사 엘지화학 | 헤테로고리 화합물 및 이를 포함하는 유기 발광 소자 |
| WO2019013526A1 (ko) * | 2017-07-10 | 2019-01-17 | 주식회사 엘지화학 | 신규한 화합물 및 이를 포함하는 유기 발광 소자 |
| WO2019027263A1 (ko) * | 2017-08-02 | 2019-02-07 | 주식회사 엘지화학 | 헤테로고리 화합물 및 이를 포함하는 유기 발광 소자 |
| WO2019027189A1 (ko) * | 2017-08-02 | 2019-02-07 | 주식회사 엘지화학 | 유기 전계 발광 소자 |
| KR20190014485A (ko) * | 2017-08-02 | 2019-02-12 | 주식회사 엘지화학 | 헤테로고리 화합물 및 이를 포함하는 유기 발광 소자 |
| KR20190044975A (ko) * | 2017-10-23 | 2019-05-02 | 주식회사 엘지화학 | 신규한 고리 화합물 및 이를 이용한 유기발광 소자 |
| KR20190044973A (ko) * | 2017-10-23 | 2019-05-02 | 주식회사 엘지화학 | 신규한 고리 화합물 및 이를 이용한 유기발광 소자 |
| KR20190087259A (ko) * | 2018-01-16 | 2019-07-24 | 삼성전자주식회사 | 축합환 화합물, 이를 포함하는 조성물 및 이를 포함하는 유기 발광 소자 |
| WO2019172699A1 (ko) * | 2018-03-09 | 2019-09-12 | 주식회사 엘지화학 | 화합물 및 이를 포함하는 유기 발광 소자 |
| KR20190114519A (ko) * | 2018-03-30 | 2019-10-10 | 주식회사 엘지화학 | 스피로 화합물 및 이를 포함하는 유기 발광 소자 |
| KR20190114518A (ko) * | 2018-03-30 | 2019-10-10 | 주식회사 엘지화학 | 스피로화합물 및 이를 포함하는 유기 발광 소자 |
| WO2020022768A1 (ko) * | 2018-07-24 | 2020-01-30 | 주식회사 엘지화학 | 유기 발광 소자 |
| WO2020022771A1 (ko) * | 2018-07-24 | 2020-01-30 | 주식회사 엘지화학 | 유기 발광 소자 |
| KR20200079377A (ko) * | 2018-12-24 | 2020-07-03 | 엘지디스플레이 주식회사 | 유기 화합물, 이를 포함하는 유기발광다이오드 및 유기발광장치 |
| WO2020231214A1 (ko) * | 2019-05-15 | 2020-11-19 | 주식회사 엘지화학 | 유기발광소자 |
| WO2021256880A1 (ko) * | 2020-06-18 | 2021-12-23 | 솔루스첨단소재 주식회사 | 유기 발광 화합물 및 이를 이용한 유기 전계 발광 소자 |
| WO2022015047A1 (ko) * | 2020-07-14 | 2022-01-20 | 솔루스첨단소재 주식회사 | 유기 발광 화합물 및 이를 이용한 유기 전계 발광 소자 |
| WO2022019536A1 (ko) * | 2020-07-24 | 2022-01-27 | 주식회사 엘지화학 | 화합물 및 이를 포함하는 유기 발광 소자 |
| WO2022131743A1 (ko) * | 2020-12-14 | 2022-06-23 | 솔루스첨단소재 주식회사 | 유기 발광 화합물 및 이를 이용한 유기 전계 발광 소자 |
| WO2022173203A1 (ko) * | 2021-02-09 | 2022-08-18 | 주식회사 엘지화학 | 화합물 및 이를 포함하는 유기전자소자 |
| US11926607B2 (en) | 2018-08-17 | 2024-03-12 | Lg Chem, Ltd. | Compound and organic light emitting device comprising the same |
| US12004423B2 (en) | 2018-07-25 | 2024-06-04 | Lg Chem, Ltd. | Organic light emitting device |
Families Citing this family (47)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP6629291B2 (ja) * | 2014-07-21 | 2020-01-15 | メルク、パテント、ゲゼルシャフト、ミット、ベシュレンクテル、ハフツングMerck Patent GmbH | 電子素子用材料 |
| US11476426B2 (en) | 2016-02-03 | 2022-10-18 | Sfc Co., Ltd. | Organic light emitting compounds and organic light emitting devices including the same |
| KR20170097820A (ko) | 2016-02-18 | 2017-08-29 | 삼성디스플레이 주식회사 | 유기 발광 소자 |
| KR101755986B1 (ko) * | 2016-02-23 | 2017-07-07 | 주식회사 엘지화학 | 헤테로고리 화합물 및 이를 포함하는 유기 발광 소자 |
| WO2017151535A1 (en) * | 2016-03-04 | 2017-09-08 | Solvay Usa Inc. | Spirobifluorene derivatives and their use in electron injection layers of organic electronic devices |
| WO2017151537A1 (en) * | 2016-03-04 | 2017-09-08 | Solvay Usa Inc. | Spirobifluorene derivatives and their use in electron transport layers of organic electronic devices |
| CN114805337B (zh) * | 2016-03-15 | 2024-07-23 | 陶氏环球技术有限责任公司 | 有机电致发光化合物和其有机电致发光器件 |
| CN107188883A (zh) * | 2016-03-15 | 2017-09-22 | 上海和辉光电有限公司 | 一种应用于oled领域的化合物 |
| JP6859587B2 (ja) * | 2016-03-28 | 2021-04-14 | エルジー・ケム・リミテッド | 化合物およびこれを含む有機電子素子 |
| JP6750783B2 (ja) * | 2016-03-30 | 2020-09-02 | エルジー・ケム・リミテッド | 化合物およびこれを用いる有機発光素子 |
| US10680184B2 (en) | 2016-07-11 | 2020-06-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| KR101939152B1 (ko) * | 2016-09-12 | 2019-01-16 | (주)씨엠디엘 | 플루오렌닐 트리아진 유도체 유기화합물 및 이를 포함하는 유기 전계 발광 소자 |
| KR101956790B1 (ko) * | 2016-10-20 | 2019-03-13 | 주식회사 엘지화학 | 다중고리 화합물 및 이를 포함하는 유기 발광 소자 |
| KR102041398B1 (ko) * | 2017-04-12 | 2019-11-06 | 주식회사 엘지화학 | 신규한 화합물 및 이를 포함하는 유기발광 소자 |
| WO2018190522A1 (ko) * | 2017-04-12 | 2018-10-18 | 주식회사 엘지화학 | 신규한 화합물 및 이를 포함하는 유기발광 소자 |
| KR102055979B1 (ko) * | 2017-05-29 | 2019-12-13 | 주식회사 엘지화학 | 유기 발광 소자 |
| KR102064415B1 (ko) * | 2017-06-30 | 2020-01-09 | 주식회사 엘지화학 | 신규한 헤테로 고리 화합물 및 이를 이용한 유기 발광 소자 |
| KR102132350B1 (ko) | 2017-07-20 | 2020-07-09 | 주식회사 엘지화학 | 신규한 헤테로 고리 화합물 및 이를 이용한 유기 발광 소자 |
| KR102170386B1 (ko) | 2017-09-29 | 2020-10-27 | 주식회사 엘지화학 | 화합물, 이를 포함하는 코팅 조성물, 이를 이용한 유기 발광 소자 및 이의 제조방법 |
| US20200328355A1 (en) * | 2017-11-06 | 2020-10-15 | Hodogaya Chemical Co., Ltd. | Compound having indenocarbazole ring structure, and organic electroluminescence device |
| US11233200B2 (en) | 2018-01-16 | 2022-01-25 | Samsung Electronics Co., Ltd. | Condensed cyclic compound, composition including the same, and organic light-emitting device including the condensed cyclic compound |
| KR20190101739A (ko) * | 2018-02-23 | 2019-09-02 | 주식회사 엘지화학 | 유기 발광 소자 |
| KR102199112B1 (ko) * | 2018-07-31 | 2021-01-06 | 솔루스첨단소재 주식회사 | 유기 화합물 및 이를 이용한 유기 전계 발광 소자 |
| KR102331323B1 (ko) * | 2018-11-13 | 2021-11-25 | 주식회사 엘지화학 | 신규한 화합물 및 이를 이용한 유기발광 소자 |
| KR101987256B1 (ko) * | 2018-12-14 | 2019-06-10 | 주식회사 엘지화학 | 축합환 화합물 및 이를 포함하는 유기 발광 소자 |
| CN109503466A (zh) * | 2018-12-24 | 2019-03-22 | 武汉天马微电子有限公司 | 有机化合物、显示面板及显示装置 |
| CN113233988B (zh) * | 2019-01-23 | 2023-05-02 | 苏州久显新材料有限公司 | 芴类衍生物和电子器件 |
| EP3696179B1 (en) * | 2019-02-15 | 2024-07-17 | Novaled GmbH | Compound and an organic semiconducting layer, an organic electronic device and a display or lighting device comprising the same |
| WO2020197170A1 (ko) * | 2019-03-28 | 2020-10-01 | 주식회사 엘지화학 | 신규한 화합물 및 이를 포함하는 유기발광 소자 |
| KR20200115159A (ko) * | 2019-03-28 | 2020-10-07 | 주식회사 엘지화학 | 신규한 화합물 및 이를 포함하는 유기발광 소자 |
| CN111747933B (zh) * | 2019-03-29 | 2022-03-01 | 吉林省元合电子材料有限公司 | 一种取代的1,3,5-三嗪化合物、组合物及其应用 |
| TW202110808A (zh) | 2019-06-27 | 2021-03-16 | 日商關東化學股份有限公司 | 螺環二氫吖啶系化合物、含有該化合物之電洞傳輸材料、及在電洞傳輸層中包含該化合物之有機電子裝置 |
| US20220359831A1 (en) * | 2019-08-19 | 2022-11-10 | Idemitsu Kosan Co.,Ltd. | Compound, material for organic electroluminescent elements, organic electroluminescent element, and electronic device |
| KR20210043993A (ko) * | 2019-10-14 | 2021-04-22 | 솔루스첨단소재 주식회사 | 유기 화합물 및 이를 포함하는 유기 전계 발광 소자 |
| AU2021267373A1 (en) | 2020-05-06 | 2022-12-08 | Ajax Therapeutics, Inc. | 6-heteroaryloxy benzimidazoles and azabenzimidazoles as JAK2 inhibitors |
| JP2022025483A (ja) * | 2020-07-29 | 2022-02-10 | 出光興産株式会社 | 化合物、有機エレクトロルミネッセンス素子及び電子機器 |
| CN112442023B (zh) * | 2020-11-30 | 2021-08-24 | 长春海谱润斯科技股份有限公司 | 一种杂环衍生物及其有机电致发光器件 |
| CN112661714B (zh) * | 2020-12-22 | 2022-01-07 | 长春海谱润斯科技股份有限公司 | 一种杂环化合物和包含该杂环化合物的有机电致发光器件 |
| WO2022140527A1 (en) | 2020-12-23 | 2022-06-30 | Ajax Therapeutics, Inc. | 6-heteroaryloxy benzimidazoles and azabenzimidazoles as jak2 inhibitors |
| CN112961147B (zh) * | 2021-02-09 | 2022-01-18 | 长春海谱润斯科技股份有限公司 | 一种含氮化合物及其有机电致发光器件 |
| WO2022243403A1 (de) | 2021-05-21 | 2022-11-24 | Merck Patent Gmbh | Verfahren zur kontinuierlichen aufreinigung von mindestens einem funktionalen material und vorrichtung zur kontinuierlichen aufreinigung von mindestens einem funktionalen material |
| CN117480156A (zh) * | 2021-06-04 | 2024-01-30 | 三菱化学株式会社 | 芳香族化合物、有机电致发光元件、组合物及有机电致发光元件的制造方法 |
| CN115322189B (zh) * | 2021-09-28 | 2023-11-28 | 四川阿格瑞新材料有限公司 | 一种螺环化合物及其应用 |
| EP4430042A1 (en) | 2021-11-09 | 2024-09-18 | Ajax Therapeutics, Inc. | 6-he tero aryloxy benzimidazoles and azabenzimidazoles as jak2 inhibitors |
| CN114560840B (zh) * | 2022-03-11 | 2023-10-03 | 常州南京大学高新技术研究院 | 2,7-二芳基呫吨螺芴二醇衍生物及其制备方法 |
| CN114716418B (zh) * | 2022-03-14 | 2024-06-07 | 上海钥熠电子科技有限公司 | 杂环烷烃衍生物、有机光电器件和显示或照明装置 |
| WO2024133211A1 (de) | 2022-12-21 | 2024-06-27 | Merck Patent Gmbh | Neue materialien für organische elektrolumineszenzvorrichtungen |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2010126270A1 (en) * | 2009-04-29 | 2010-11-04 | Dow Advanced Display Materials,Ltd. | Novel organic electroluminescent compounds and organic electroluminescent device using the same |
| KR20130115160A (ko) * | 2012-04-10 | 2013-10-21 | 에스에프씨 주식회사 | 이형고리 화합물 및 이를 포함하는 유기전계발광소자 |
| KR20140014956A (ko) * | 2012-07-27 | 2014-02-06 | (주)피엔에이치테크 | 새로운 유기전계발광소자용 화합물 및 그를 포함하는 유기전계발광소자 |
Family Cites Families (75)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4539507A (en) | 1983-03-25 | 1985-09-03 | Eastman Kodak Company | Organic electroluminescent devices having improved power conversion efficiencies |
| US5151629A (en) | 1991-08-01 | 1992-09-29 | Eastman Kodak Company | Blue emitting internal junction organic electroluminescent device (I) |
| JPH07133483A (ja) | 1993-11-09 | 1995-05-23 | Shinko Electric Ind Co Ltd | El素子用有機発光材料及びel素子 |
| DE59510315D1 (de) | 1994-04-07 | 2002-09-19 | Covion Organic Semiconductors | Spiroverbindungen und ihre Verwendung als Elektrolumineszenzmaterialien |
| DE19652261A1 (de) | 1996-12-16 | 1998-06-18 | Hoechst Ag | Arylsubstituierte Poly(p-arylenvinylene), Verfahren zur Herstellung und deren Verwendung in Elektroluminszenzbauelementen |
| KR100913568B1 (ko) | 1999-05-13 | 2009-08-26 | 더 트러스티즈 오브 프린스턴 유니버시티 | 전계인광에 기초한 고 효율의 유기 발광장치 |
| CN1840607B (zh) | 1999-12-01 | 2010-06-09 | 普林斯顿大学理事会 | 作为有机发光器件的磷光掺杂剂的l2mx形式的络合物 |
| US6660410B2 (en) | 2000-03-27 | 2003-12-09 | Idemitsu Kosan Co., Ltd. | Organic electroluminescence element |
| US20020121638A1 (en) | 2000-06-30 | 2002-09-05 | Vladimir Grushin | Electroluminescent iridium compounds with fluorinated phenylpyridines, phenylpyrimidines, and phenylquinolines and devices made with such compounds |
| CN100505375C (zh) | 2000-08-11 | 2009-06-24 | 普林斯顿大学理事会 | 有机金属化合物和发射转换有机电致磷光 |
| KR100916231B1 (ko) | 2001-03-14 | 2009-09-08 | 더 트러스티즈 오브 프린스턴 유니버시티 | 청색 인광계 유기발광다이오드용 재료 및 장치 |
| US20060063027A1 (en) | 2002-12-23 | 2006-03-23 | Covion Organic Semiconductors Gmbh | Organic electroluminescent element |
| DE10310887A1 (de) | 2003-03-11 | 2004-09-30 | Covion Organic Semiconductors Gmbh | Matallkomplexe |
| JP4411851B2 (ja) | 2003-03-19 | 2010-02-10 | コニカミノルタホールディングス株式会社 | 有機エレクトロルミネッセンス素子 |
| EP1618170A2 (de) | 2003-04-15 | 2006-01-25 | Covion Organic Semiconductors GmbH | Mischungen von organischen zur emission befähigten halbleitern und matrixmaterialien, deren verwendung und elektronikbauteile enthaltend diese mischungen |
| US7740955B2 (en) | 2003-04-23 | 2010-06-22 | Konica Minolta Holdings, Inc. | Organic electroluminescent device and display |
| EP1644459B1 (de) | 2003-07-07 | 2017-08-23 | Merck Patent GmbH | Mischungen von organischen zur emission befähigten halbleitern und matrixmaterialien,sowie elektronikbauteile diese enthaltend |
| DE10333232A1 (de) | 2003-07-21 | 2007-10-11 | Merck Patent Gmbh | Organisches Elektrolumineszenzelement |
| DE10338550A1 (de) | 2003-08-19 | 2005-03-31 | Basf Ag | Übergangsmetallkomplexe mit Carbenliganden als Emitter für organische Licht-emittierende Dioden (OLEDs) |
| US7795801B2 (en) | 2003-09-30 | 2010-09-14 | Konica Minolta Holdings, Inc. | Organic electroluminescent element, illuminator, display and compound |
| DE102004008304A1 (de) | 2004-02-20 | 2005-09-08 | Covion Organic Semiconductors Gmbh | Organische elektronische Vorrichtungen |
| DE102004010954A1 (de) | 2004-03-03 | 2005-10-06 | Novaled Gmbh | Verwendung eines Metallkomplexes als n-Dotand für ein organisches halbleitendes Matrixmaterial, organisches Halbleitermaterial und elektronisches Bauteil |
| US7790890B2 (en) | 2004-03-31 | 2010-09-07 | Konica Minolta Holdings, Inc. | Organic electroluminescence element material, organic electroluminescence element, display device and illumination device |
| DE102004023277A1 (de) | 2004-05-11 | 2005-12-01 | Covion Organic Semiconductors Gmbh | Neue Materialmischungen für die Elektrolumineszenz |
| US7598388B2 (en) | 2004-05-18 | 2009-10-06 | The University Of Southern California | Carbene containing metal complexes as OLEDs |
| JP4862248B2 (ja) | 2004-06-04 | 2012-01-25 | コニカミノルタホールディングス株式会社 | 有機エレクトロルミネッセンス素子、照明装置及び表示装置 |
| EP1655359A1 (de) | 2004-11-06 | 2006-05-10 | Covion Organic Semiconductors GmbH | Organische Elektrolumineszenzvorrichtung |
| CN103204996B (zh) | 2005-05-03 | 2015-12-09 | 默克专利有限公司 | 有机电致发光器件 |
| JP2007049055A (ja) * | 2005-08-12 | 2007-02-22 | Toyo Ink Mfg Co Ltd | 有機エレクトロルミネッセンス素子用材料および有機エレクトロルミネッセンス素子 |
| CN102633820B (zh) | 2005-12-01 | 2015-01-21 | 新日铁住金化学株式会社 | 有机电致发光元件用化合物及有机电致发光元件 |
| US7919010B2 (en) | 2005-12-22 | 2011-04-05 | Novaled Ag | Doped organic semiconductor material |
| EP1837927A1 (de) | 2006-03-22 | 2007-09-26 | Novaled AG | Verwendung von heterocyclischen Radikalen zur Dotierung von organischen Halbleitern |
| ATE394800T1 (de) | 2006-03-21 | 2008-05-15 | Novaled Ag | Heterocyclisches radikal oder diradikal, deren dimere, oligomere, polymere, dispiroverbindungen und polycyclen, deren verwendung, organisches halbleitendes material sowie elektronisches bauelement |
| DE102006025777A1 (de) | 2006-05-31 | 2007-12-06 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| US8062769B2 (en) | 2006-11-09 | 2011-11-22 | Nippon Steel Chemical Co., Ltd. | Indolocarbazole compound for use in organic electroluminescent device and organic electroluminescent device |
| DE102007002714A1 (de) | 2007-01-18 | 2008-07-31 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102007024850A1 (de) | 2007-05-29 | 2008-12-04 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| EP2009014B1 (de) | 2007-06-22 | 2018-10-24 | Novaled GmbH | Verwendung eines Precursors eines n-Dotanden zur Dotierung eines organischen halbleitenden Materials, Precursor und elektronisches oder optoelektronisches Bauelement |
| DE102007053771A1 (de) | 2007-11-12 | 2009-05-14 | Merck Patent Gmbh | Organische Elektrolumineszenzvorrichtungen |
| DE102008033943A1 (de) | 2008-07-18 | 2010-01-21 | Merck Patent Gmbh | Neue Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102008036982A1 (de) | 2008-08-08 | 2010-02-11 | Merck Patent Gmbh | Organische Elektrolumineszenzvorrichtung |
| DE102008056688A1 (de) | 2008-11-11 | 2010-05-12 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| CN102076813B (zh) | 2008-11-11 | 2016-05-18 | 默克专利有限公司 | 有机电致发光器件 |
| KR101257695B1 (ko) | 2008-12-24 | 2013-04-24 | 제일모직주식회사 | 신규한 유기광전소자용 화합물 및 이를 포함하는 유기광전소자 |
| KR101233367B1 (ko) | 2008-12-29 | 2013-02-15 | 제일모직주식회사 | 신규한 유기광전소자용 화합물 및 이를 포함하는 유기광전소자 |
| DE102009014513A1 (de) | 2009-03-23 | 2010-09-30 | Merck Patent Gmbh | Organische Elektrolumineszenzvorrichtung |
| DE102009023155A1 (de) | 2009-05-29 | 2010-12-02 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| EP2436679B1 (en) * | 2009-05-29 | 2016-01-06 | Idemitsu Kosan Co., Ltd. | Anthracene derivative and organic electroluminescent element using the same |
| DE102009031021A1 (de) | 2009-06-30 | 2011-01-05 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| JP5764500B2 (ja) * | 2009-12-14 | 2015-08-19 | 凸版印刷株式会社 | アントラセン誘導体および発光素子 |
| DE102010005697A1 (de) | 2010-01-25 | 2011-07-28 | Merck Patent GmbH, 64293 | Verbindungen für elektronische Vorrichtungen |
| DE102010012738A1 (de) | 2010-03-25 | 2011-09-29 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102010014933A1 (de) | 2010-04-14 | 2011-10-20 | Merck Patent Gmbh | Materialien für elektronische Vorrichtungen |
| DE102010019306B4 (de) | 2010-05-04 | 2021-05-20 | Merck Patent Gmbh | Organische Elektrolumineszenzvorrichtungen |
| DE102010033080A1 (de) | 2010-08-02 | 2012-02-02 | Merck Patent Gmbh | Polymere mit Struktureinheiten, die Elektronen-Transport-Eigenschaften aufweisen |
| JP2013541837A (ja) | 2010-09-10 | 2013-11-14 | ノヴァレッド・アクチエンゲゼルシャフト | 有機光電変換素子用化合物 |
| EP2452946B1 (en) | 2010-11-16 | 2014-05-07 | Novaled AG | Pyridylphosphinoxides for organic electronic device and organic electronic device |
| EP2463927B1 (en) | 2010-12-08 | 2013-08-21 | Novaled AG | Material for organic electronic device and organic electronic device |
| KR101466150B1 (ko) * | 2010-12-31 | 2014-11-27 | 제일모직 주식회사 | 유기광전소자용 화합물 및 이를 포함하는 유기광전소자 |
| CN102126963B (zh) * | 2011-01-11 | 2013-10-16 | 上海师范大学 | 一类螺二芴胺基化合物及其制备方法 |
| WO2012168358A1 (en) | 2011-06-09 | 2012-12-13 | Novaled Ag | Compound for organic electronic device |
| EP2724389B1 (de) | 2011-06-22 | 2018-05-16 | Novaled GmbH | Organisches elektronisches bauelement |
| JP6054394B2 (ja) * | 2011-08-10 | 2016-12-27 | メルク パテント ゲーエムベーハー | 金属錯体 |
| EP2773721B1 (de) | 2011-11-01 | 2015-11-25 | Merck Patent GmbH | Organische elektrolumineszenzvorrichtung |
| KR101497134B1 (ko) * | 2011-12-29 | 2015-03-02 | 제일모직 주식회사 | 유기광전자소자용 화합물, 이를 포함하는 유기발광소자 및 상기 유기발광소자를 포함하는 표시장치 |
| CN102633726B (zh) * | 2012-03-29 | 2014-04-23 | 上海师范大学 | 一种螺二芴类荧光探针及其制备方法与用途 |
| TWI504592B (zh) * | 2012-04-13 | 2015-10-21 | Lg Chemical Ltd | 新穎含氮雜環化合物及使用其之有機電子裝置 |
| CN102659688B (zh) * | 2012-05-09 | 2014-04-02 | 上海师范大学 | 一种螺二芴化合物2-甲基-7-苯并咪唑基螺二芴及其制备方法与用途 |
| KR101401639B1 (ko) * | 2012-07-27 | 2014-06-02 | (주)피엔에이치테크 | 새로운 유기전계발광소자용 화합물 및 그를 포함하는 유기전계발광소자 |
| US9741942B2 (en) | 2012-10-11 | 2017-08-22 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| JP6342419B2 (ja) * | 2012-12-21 | 2018-06-13 | メルク パテント ゲーエムベーハー | 有機エレクトロルミネッセント素子のための材料 |
| WO2015197156A1 (de) * | 2014-06-25 | 2015-12-30 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| JP6629291B2 (ja) | 2014-07-21 | 2020-01-15 | メルク、パテント、ゲゼルシャフト、ミット、ベシュレンクテル、ハフツングMerck Patent GmbH | 電子素子用材料 |
| US10680187B2 (en) * | 2016-09-23 | 2020-06-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2018083053A1 (de) * | 2016-11-02 | 2018-05-11 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
-
2015
- 2015-06-30 JP JP2017503578A patent/JP6629291B2/ja active Active
- 2015-06-30 CN CN201580039205.3A patent/CN106536485A/zh active Pending
- 2015-06-30 EP EP15733629.8A patent/EP3172775B1/de active Active
- 2015-06-30 KR KR1020227043687A patent/KR102657649B1/ko active IP Right Grant
- 2015-06-30 KR KR1020177004335A patent/KR102479149B1/ko active IP Right Grant
- 2015-06-30 CN CN202010787633.7A patent/CN112010842A/zh active Pending
- 2015-06-30 US US15/327,790 patent/US10903430B2/en active Active
- 2015-06-30 CN CN202310552689.8A patent/CN116655603A/zh active Pending
- 2015-06-30 EP EP22163122.9A patent/EP4037000A1/de active Pending
- 2015-06-30 WO PCT/EP2015/001315 patent/WO2016012075A1/de active Application Filing
- 2015-07-20 TW TW104123413A patent/TWI703140B/zh active
- 2015-07-20 TW TW111111458A patent/TW202227400A/zh unknown
- 2015-07-20 TW TW109128650A patent/TWI763011B/zh active
-
2019
- 2019-10-04 JP JP2019183811A patent/JP6893964B2/ja active Active
-
2021
- 2021-05-14 JP JP2021082659A patent/JP7339982B2/ja active Active
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2010126270A1 (en) * | 2009-04-29 | 2010-11-04 | Dow Advanced Display Materials,Ltd. | Novel organic electroluminescent compounds and organic electroluminescent device using the same |
| KR20100118690A (ko) * | 2009-04-29 | 2010-11-08 | 다우어드밴스드디스플레이머티리얼 유한회사 | 신규한 유기 발광 화합물 및 이를 채용하고 있는 유기 전계 발광 소자 |
| KR20130115160A (ko) * | 2012-04-10 | 2013-10-21 | 에스에프씨 주식회사 | 이형고리 화합물 및 이를 포함하는 유기전계발광소자 |
| KR20140014956A (ko) * | 2012-07-27 | 2014-02-06 | (주)피엔에이치테크 | 새로운 유기전계발광소자용 화합물 및 그를 포함하는 유기전계발광소자 |
Cited By (57)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE102018101398A1 (de) | 2017-03-15 | 2018-09-20 | Hyundai Motor Company | Vibrationssensitives Aufhängungssystem und Steuerverfahren davon |
| US11594685B2 (en) | 2017-03-30 | 2023-02-28 | Lg Chem, Ltd. | Organic light emitting device |
| WO2018182259A1 (ko) * | 2017-03-30 | 2018-10-04 | 주식회사 엘지화학 | 유기 발광 소자 |
| CN109564982A (zh) * | 2017-03-30 | 2019-04-02 | 株式会社Lg化学 | 有机发光器件 |
| WO2018190666A1 (ko) * | 2017-04-13 | 2018-10-18 | 주식회사 엘지화학 | 헤테로고리 화합물 및 이를 포함하는 유기 발광 소자 |
| US11450819B2 (en) | 2017-04-13 | 2022-09-20 | Lg Chem, Ltd. | Heterocyclic compound and organic light-emitting element including same |
| WO2018216913A1 (ko) * | 2017-05-22 | 2018-11-29 | 주식회사 엘지화학 | 신규한 헤테로고리 화합물 및 이를 이용한 유기발광 소자 |
| WO2018216887A1 (ko) * | 2017-05-22 | 2018-11-29 | 주식회사 엘지화학 | 신규한 화합물 및 이를 이용한 유기발광 소자 |
| CN110023314A (zh) * | 2017-05-22 | 2019-07-16 | 株式会社Lg化学 | 新型杂环化合物及利用其的有机发光器件 |
| CN110023314B (zh) * | 2017-05-22 | 2022-02-08 | 株式会社Lg化学 | 新型杂环化合物及利用其的有机发光器件 |
| US11515478B2 (en) | 2017-05-22 | 2022-11-29 | Lg Chem Ltd. | Compound and organic light emitting device using the same |
| WO2018230854A1 (ko) * | 2017-06-16 | 2018-12-20 | 경상대학교산학협력단 | 신규한 아크리딘 유도체 및 이를 포함하는 유기전계발광소자 |
| WO2018236066A1 (ko) * | 2017-06-21 | 2018-12-27 | 주식회사 엘지화학 | 신규한 헤테로 고리 화합물 및 이를 이용한 유기 발광 소자 |
| US11407718B2 (en) | 2017-06-21 | 2022-08-09 | Lg Chem, Ltd. | Heterocyclic compound and organic light emitting device comprising the same |
| KR20180138457A (ko) * | 2017-06-21 | 2018-12-31 | 주식회사 엘지화학 | 신규한 헤테로 고리 화합물 및 이를 이용한 유기 발광 소자 |
| WO2018236040A1 (ko) * | 2017-06-21 | 2018-12-27 | 주식회사 엘지화학 | 신규한 헤테로 고리 화합물 및 이를 이용한 유기발광 소자 |
| KR20190002299A (ko) * | 2017-06-29 | 2019-01-08 | 주식회사 엘지화학 | 신규한 헤테로 고리 화합물 및 이를 이용한 유기 발광 소자 |
| WO2019004612A1 (ko) * | 2017-06-29 | 2019-01-03 | 주식회사 엘지화학 | 신규한 헤테로 고리 화합물 및 이를 이용한 유기 발광 소자 |
| US11542258B2 (en) | 2017-06-29 | 2023-01-03 | Lg Chem, Ltd. | Heterocyclic compound and organic light emitting device comprising the same |
| CN110475769B (zh) * | 2017-06-30 | 2023-04-04 | 株式会社Lg化学 | 杂环化合物和包含其的有机发光元件 |
| WO2019004796A1 (ko) * | 2017-06-30 | 2019-01-03 | 주식회사 엘지화학 | 신규한 헤테로 고리 화합물 및 이를 이용한 유기 발광 소자 |
| WO2019004790A1 (ko) * | 2017-06-30 | 2019-01-03 | 주식회사 엘지화학 | 헤테로고리 화합물 및 이를 포함하는 유기 발광 소자 |
| US11427572B2 (en) | 2017-06-30 | 2022-08-30 | Lg Chem, Ltd. | Heterocyclic compound and organic light emitting element including same |
| CN110475769A (zh) * | 2017-06-30 | 2019-11-19 | 株式会社Lg化学 | 杂环化合物和包含其的有机发光元件 |
| KR20190006464A (ko) * | 2017-07-10 | 2019-01-18 | 주식회사 엘지화학 | 신규한 화합물 및 이를 포함하는 유기 발광 소자 |
| US11641778B2 (en) | 2017-07-10 | 2023-05-02 | Lg Chem, Ltd. | Compound and organic light emitting device comprising same |
| WO2019013526A1 (ko) * | 2017-07-10 | 2019-01-17 | 주식회사 엘지화학 | 신규한 화합물 및 이를 포함하는 유기 발광 소자 |
| WO2019013542A1 (ko) * | 2017-07-11 | 2019-01-17 | 주식회사 엘지화학 | 헤테로고리 화합물 및 이를 포함하는 유기 발광 소자 |
| US11563184B2 (en) | 2017-07-11 | 2023-01-24 | Lg Chem, Ltd. | Heterocyclic compound and organic light emitting element containing same |
| KR20190006927A (ko) * | 2017-07-11 | 2019-01-21 | 주식회사 엘지화학 | 헤테로고리 화합물 및 이를 포함하는 유기 발광 소자 |
| KR20190014485A (ko) * | 2017-08-02 | 2019-02-12 | 주식회사 엘지화학 | 헤테로고리 화합물 및 이를 포함하는 유기 발광 소자 |
| US11634414B2 (en) | 2017-08-02 | 2023-04-25 | Lg Chem, Ltd. | Heterocyclic compound and organic light-emitting element including same |
| WO2019027263A1 (ko) * | 2017-08-02 | 2019-02-07 | 주식회사 엘지화학 | 헤테로고리 화합물 및 이를 포함하는 유기 발광 소자 |
| WO2019027189A1 (ko) * | 2017-08-02 | 2019-02-07 | 주식회사 엘지화학 | 유기 전계 발광 소자 |
| KR20190014472A (ko) * | 2017-08-02 | 2019-02-12 | 주식회사 엘지화학 | 유기 전계 발광 소자 |
| KR20190044975A (ko) * | 2017-10-23 | 2019-05-02 | 주식회사 엘지화학 | 신규한 고리 화합물 및 이를 이용한 유기발광 소자 |
| WO2019083178A1 (ko) * | 2017-10-23 | 2019-05-02 | 주식회사 엘지화학 | 신규한 고리 화합물 및 이를 이용한유기발광 소자 |
| KR20190044973A (ko) * | 2017-10-23 | 2019-05-02 | 주식회사 엘지화학 | 신규한 고리 화합물 및 이를 이용한 유기발광 소자 |
| KR20190087259A (ko) * | 2018-01-16 | 2019-07-24 | 삼성전자주식회사 | 축합환 화합물, 이를 포함하는 조성물 및 이를 포함하는 유기 발광 소자 |
| US11878962B2 (en) | 2018-03-09 | 2024-01-23 | Lg Chem, Ltd. | Compound and organic light emitting device comprising same |
| WO2019172699A1 (ko) * | 2018-03-09 | 2019-09-12 | 주식회사 엘지화학 | 화합물 및 이를 포함하는 유기 발광 소자 |
| KR20190114519A (ko) * | 2018-03-30 | 2019-10-10 | 주식회사 엘지화학 | 스피로 화합물 및 이를 포함하는 유기 발광 소자 |
| KR20190114518A (ko) * | 2018-03-30 | 2019-10-10 | 주식회사 엘지화학 | 스피로화합물 및 이를 포함하는 유기 발광 소자 |
| WO2020022768A1 (ko) * | 2018-07-24 | 2020-01-30 | 주식회사 엘지화학 | 유기 발광 소자 |
| WO2020022771A1 (ko) * | 2018-07-24 | 2020-01-30 | 주식회사 엘지화학 | 유기 발광 소자 |
| US12004423B2 (en) | 2018-07-25 | 2024-06-04 | Lg Chem, Ltd. | Organic light emitting device |
| US11926607B2 (en) | 2018-08-17 | 2024-03-12 | Lg Chem, Ltd. | Compound and organic light emitting device comprising the same |
| KR20200079377A (ko) * | 2018-12-24 | 2020-07-03 | 엘지디스플레이 주식회사 | 유기 화합물, 이를 포함하는 유기발광다이오드 및 유기발광장치 |
| WO2020231214A1 (ko) * | 2019-05-15 | 2020-11-19 | 주식회사 엘지화학 | 유기발광소자 |
| KR20210060406A (ko) * | 2019-05-15 | 2021-05-26 | 주식회사 엘지화학 | 유기발광소자 |
| KR20210060407A (ko) * | 2019-05-15 | 2021-05-26 | 주식회사 엘지화학 | 유기발광소자 |
| KR20200132752A (ko) * | 2019-05-15 | 2020-11-25 | 주식회사 엘지화학 | 유기발광소자 |
| WO2021256880A1 (ko) * | 2020-06-18 | 2021-12-23 | 솔루스첨단소재 주식회사 | 유기 발광 화합물 및 이를 이용한 유기 전계 발광 소자 |
| WO2022015047A1 (ko) * | 2020-07-14 | 2022-01-20 | 솔루스첨단소재 주식회사 | 유기 발광 화합물 및 이를 이용한 유기 전계 발광 소자 |
| WO2022019536A1 (ko) * | 2020-07-24 | 2022-01-27 | 주식회사 엘지화학 | 화합물 및 이를 포함하는 유기 발광 소자 |
| WO2022131743A1 (ko) * | 2020-12-14 | 2022-06-23 | 솔루스첨단소재 주식회사 | 유기 발광 화합물 및 이를 이용한 유기 전계 발광 소자 |
| WO2022173203A1 (ko) * | 2021-02-09 | 2022-08-18 | 주식회사 엘지화학 | 화합물 및 이를 포함하는 유기전자소자 |
Also Published As
| Publication number | Publication date |
|---|---|
| CN116655603A (zh) | 2023-08-29 |
| US20170222157A1 (en) | 2017-08-03 |
| CN106536485A (zh) | 2017-03-22 |
| KR102479149B1 (ko) | 2022-12-19 |
| KR20230006918A (ko) | 2023-01-11 |
| TWI763011B (zh) | 2022-05-01 |
| TWI703140B (zh) | 2020-09-01 |
| JP7339982B2 (ja) | 2023-09-06 |
| US10903430B2 (en) | 2021-01-26 |
| EP3172775A1 (de) | 2017-05-31 |
| JP2020033356A (ja) | 2020-03-05 |
| CN112010842A (zh) | 2020-12-01 |
| TW202100521A (zh) | 2021-01-01 |
| JP2017524699A (ja) | 2017-08-31 |
| KR102657649B1 (ko) | 2024-04-15 |
| JP2021155420A (ja) | 2021-10-07 |
| EP4037000A1 (de) | 2022-08-03 |
| JP6893964B2 (ja) | 2021-06-23 |
| WO2016012075A1 (de) | 2016-01-28 |
| EP3172775B1 (de) | 2022-04-20 |
| TW201615635A (zh) | 2016-05-01 |
| TW202227400A (zh) | 2022-07-16 |
| JP6629291B2 (ja) | 2020-01-15 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR102657649B1 (ko) | 전자 소자용 재료 | |
| KR102540425B1 (ko) | 유기 전계발광 소자 (oled) 용 재료로서 비스벤조푸란-융합된 2,8-디아미노인데노[1,2-b]플루오렌 유도체 및 관련 화합물 | |
| KR102202756B1 (ko) | 전자 소자용 물질 | |
| KR102380808B1 (ko) | 치환 옥세핀 | |
| KR102006621B1 (ko) | 화합물 및 유기 전계 발광 디바이스 | |
| KR102363484B1 (ko) | 전자 소자용 물질 | |
| KR102318974B1 (ko) | 전자 소자용 재료 | |
| KR102434545B1 (ko) | 전자 소자용 재료 | |
| KR20160078506A (ko) | 화합물 및 유기 전자 소자 | |
| KR20150038193A (ko) | 2-디아릴아미노플루오렌의 유도체 및 이를 함유하는 유기 전자 화합물 | |
| KR20220054693A (ko) | 헤테로시클릭 스피로 화합물 | |
| KR20170106481A (ko) | 유기 전자 소자용 페난트렌 화합물 | |
| KR20170110641A (ko) | 전자 디바이스용 재료 | |
| KR20180039680A (ko) | 헥사메틸인단 | |
| KR102717935B1 (ko) | 전자 소자용 물질 | |
| KR20240151881A (ko) | 전자 소자용 물질 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A201 | Request for examination | ||
| E902 | Notification of reason for refusal | ||
| E601 | Decision to refuse application | ||
| A107 | Divisional application of patent | ||
| GRNT | Written decision to grant |