JP2015519375A - Pd−l1に結合する抗原結合蛋白質 - Google Patents
Pd−l1に結合する抗原結合蛋白質 Download PDFInfo
- Publication number
- JP2015519375A JP2015519375A JP2015515271A JP2015515271A JP2015519375A JP 2015519375 A JP2015519375 A JP 2015519375A JP 2015515271 A JP2015515271 A JP 2015515271A JP 2015515271 A JP2015515271 A JP 2015515271A JP 2015519375 A JP2015519375 A JP 2015519375A
- Authority
- JP
- Japan
- Prior art keywords
- seq
- sequence number
- referred
- sequence
- variable region
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
- A61K39/39533—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals
- A61K39/39541—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals against normal tissues, cells
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2803—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily
- C07K16/2818—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily against CD28 or CD152
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2803—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily
- C07K16/2827—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily against B7 molecules, e.g. CD80, CD86
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2896—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against molecules with a "CD"-designation, not provided for elsewhere
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2121/00—Preparations for use in therapy
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/21—Immunoglobulins specific features characterized by taxonomic origin from primates, e.g. man
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/55—Fab or Fab'
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
- C07K2317/565—Complementarity determining region [CDR]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
- C07K2317/569—Single domain, e.g. dAb, sdAb, VHH, VNAR or nanobody®
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/60—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments
- C07K2317/62—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments comprising only variable region components
- C07K2317/622—Single chain antibody (scFv)
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/73—Inducing cell death, e.g. apoptosis, necrosis or inhibition of cell proliferation
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/76—Antagonist effect on antigen, e.g. neutralization or inhibition of binding
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/92—Affinity (KD), association rate (Ka), dissociation rate (Kd) or EC50 value
Abstract
Description
配列番号2、配列番号4、配列番号6、配列番号8、配列番号10、配列番号12、配列番号14、配列番号16、配列番号18、配列番号20、配列番号22、配列番号24、配列番号26、配列番号28、配列番号30、配列番号32、配列番号34、配列番号36、配列番号38、配列番号40、配列番号42、配列番号44、配列番号46、配列番号48、配列番号50、配列番号52、配列番号54、配列番号56、配列番号58、配列番号60、配列番号62、配列番号64、配列番号66、配列番号68、配列番号70、配列番号72、配列番号74、配列番号76、配列番号78、配列番号80、配列番号82、配列番号84、配列番号86、配列番号88、配列番号90、配列番号92、配列番号94、配列番号96、配列番号98、配列番号100、配列番号102、配列番号104、配列番号106、配列番号108、配列番号110、配列番号112、配列番号114、配列番号116、配列番号118、配列番号120、配列番号122、配列番号124、配列番号126、配列番号128、配列番号130、配列番号132、配列番号134、配列番号136、配列番号138、配列番号140、配列番号142、配列番号144、配列番号146、配列番号148、配列番号150、配列番号152、配列番号154、配列番号156、配列番号158、配列番号160、配列番号162、配列番号164、配列番号166、配列番号168、配列番号170、配列番号172、配列番号174、配列番号176、配列番号178、配列番号180、配列番号182、配列番号184、配列番号186、配列番号188、配列番号190、配列番号192、配列番号194、配列番号196、配列番号198、配列番号200、配列番号202、配列番号204、配列番号206、配列番号208、配列番号210、配列番号212、配列番号214、配列番号216、配列番号218、配列番号220、配列番号222、配列番号224、配列番号226、配列番号228、配列番号230、配列番号232、配列番号234、配列番号236、配列番号238、配列番号240、配列番号242およびその組み合わせからなる群から選択されるアミノ酸配列と少なくとも95%同一であるL鎖可変領域配列を有する、完全ヒト抗体を提供する。好ましくは、該完全ヒト抗体は、H鎖とL鎖の両方を有し、配列番号1/配列番号2 (本明細書中でE6と称する)、配列番号3/配列番号4 (本明細書中でE7と称する)、配列番号5/配列番号6 (本明細書中でE9と称する)、配列番号7/配列番号8 (本明細書中でE11と称する)、配列番号9/配列番号10 (本明細書中でF1と称する)、配列番号11/配列番号12 (本明細書中でF4と称する)、配列番号13/配列番号14 (本明細書中でF7と称する)、配列番号15/配列番号16 (本明細書中でF8と称する)、配列番号17/配列番号18 (本明細書中でF11と称する)、配列番号19/配列番号20 (本明細書中でG4と称する)、配列番号21/配列番号22 (本明細書中でG9と称する)、配列番号23/配列番号24 (本明細書中でG11と称する)、配列番号25/配列番号26 (本明細書中でG12と称する)、配列番号27/配列番号28 (本明細書中でH1と称する)、配列番号29/配列番号30 (本明細書中でH3と称する)、配列番号31/配列番号32 (本明細書中でH4と称する)、配列番号33/配列番号34 (本明細書中でH5と称する)、配列番号35/配列番号36 (本明細書中でH6と称する)、配列番号37/配列番号38 (本明細書中でH10と称する)、配列番号39/配列番号40 (本明細書中でH12と称する)、配列番号41/配列番号42 (本明細書中でPDL−D2と称する)、配列番号43/配列番号44 (本明細書中でPDL−D11と称する)、配列番号45/配列番号46 (本明細書中でPDL−H1と称する)、配列番号47/配列番号48 (本明細書中でRB4と称する)、配列番号49/配列番号50 (本明細書中でRB11と称する)、配列番号51/配列番号52 (本明細書中でRC5と称する)、配列番号53/配列番号54 (本明細書中でRF5と称する)、配列番号55/配列番号56 (本明細書中でRG9と称する)、配列番号57/配列番号58 (本明細書中でRD1と称する)、配列番号59/配列番号60 (本明細書中でRF11と称する)、配列番号61/配列番号62 (本明細書中でRH11と称する)、配列番号63/配列番号64 (本明細書中でRD9と称する)、配列番号65/配列番号66 (本明細書中でRE10と称する)、配列番号67/配列番号68 (本明細書中でRA3と称する)、配列番号69/配列番号70 (本明細書中でRG1と称する)、配列番号71/配列番号72 (本明細書中でRB1と称する)、配列番号73/配列番号74 (本明細書中でRG7と称する)、配列番号75/配列番号76 (本明細書中でRA6と称する)、配列番号77/配列番号78 (本明細書中でRA8と称する)、配列番号79/配列番号80 (本明細書中でRA9と称する)、配列番号81/配列番号82 (本明細書中でRB5と称する)、配列番号83/配列番号84 (本明細書中でRB8と称する)、配列番号85/配列番号86 (本明細書中でRC8と称する)、配列番号87/配列番号88 (本明細書中でRC10と称する)、配列番号89/配列番号90 (本明細書中でRD2と称する)、配列番号91/配列番号92 (本明細書中でRE8と称する)、配列番号93/配列番号94 (本明細書中でRE9と称する)、配列番号95/配列番号96(本明細書中でRG12と称する)、配列番号97/配列番号98 (本明細書中でRSA1と称する)、配列番号99/配列番号100 (本明細書中でR2A7と称する)、配列番号101/配列番号102 (本明細書中でR2B12と称する)、配列番号103/配列番号104 (本明細書中でR2C9と称する)、配列番号105/配列番号106 (本明細書中でR2D5と称する)、配列番号107/配列番号108 (本明細書中でR2D7と称する)、配列番号109/配列番号110 (本明細書中でR2F4と称する)、配列番号111/配列番号112 (本明細書中でR2A10と称する)、配列番号113/配列番号114 (本明細書中でR2E2と称する)、配列番号115/配列番号116 (本明細書中でR3B8と称する)、配列番号117/配列番号118 (本明細書中でR3C3と称する)、配列番号119/配列番号120 (本明細書中でR3E9と称する)、配列番号121/配列番号122 (本明細書中でR3E10と称する)、配列番号123/配列番号124 (本明細書中でR3F7と称する)、配列番号125/配列番号126 (本明細書中でR3F10と称する)、配列番号127/配列番号128 (本明細書中でR4B10と称する)、配列番号129/配列番号130 (本明細書中でR4H1と称する)、配列番号131/配列番号132 (本明細書中でR4A11と称する)、配列番号133/配列番号134 (本明細書中でR3D2と称する)、配列番号135/配列番号136 (本明細書中でR5B8と称する)、配列番号137/配列番号138 (本明細書中でSH1A1Qと称する)、配列番号139/配列番号140 (本明細書中で SH1B7B(K)と称する)、配列番号141/配列番号142 (本明細書中でSH1C1と称する)、配列番号143/配列番号144 (本明細書中でSH1C8と称する)、配列番号145/配列番号146 (本明細書中でSH1E10と称する)、配列番号147/配列番号148 (本明細書中でSH1E2と称する)、配列番号149/配列番号150 (本明細書中でSH1A9と称する)、配列番号151/配列番号152 (本明細書中でSH1B11と称する)、配列番号153/配列番号154 (本明細書中でSH1E4と称する)、配列番号155/配列番号156 (本明細書中でSH1B3と称する)、配列番号157/配列番号158 (本明細書中でSH1D1と称する)、配列番号159/配列番号160 (本明細書中でSH1D2と称する)、配列番号161/配列番号162 (本明細書中でSH1D12と称する)、配列番号163/配列番号164 (本明細書中でSH1E1と称する)、配列番号165/配列番号166 (本明細書中でSH1G9と称する)、配列番号167/配列番号168 (本明細書中でSH1A11と称する)、配列番号169/配列番号170 (本明細書中でSH1C2と称する)、配列番号171/配列番号172 (本明細書中でSH1G8と称する)、配列番号173/配列番号174 (本明細書中でSH1H2と称する)、配列番号175/配列番号176 (本明細書中でSH1B10と称する)、配列番号177/配列番号178 (本明細書中で SH1B7A(L)と称する)、配列番号179/配列番号180 (本明細書中でSH1E6と称する)、配列番号181/配列番号182 (本明細書中でSH1C11と称する)、配列番号183/配列番号184 (本明細書中でSH1A2と称する)、配列番号185/配列番号186 (本明細書中でSH1B1と称する)、配列番号187/配列番号188 (本明細書中でR6B2と称する)、配列番号189/配列番号190 (本明細書中でR6B7と称する)、配列番号191/配列番号192 (本明細書中でR6B11と称する)、配列番号193/配列番号194 (本明細書中でR6D1と称する)、配列番号195/配列番号196 (本明細書中でR6C8と称する)、配列番号197/配列番号198 (本明細書中でR9G8と称する)、配列番号199/配列番号200 (本明細書中でR7D1と称する)、配列番号201/配列番号202 (本明細書中でR7D2と称する)、配列番号203/配列番号204 (本明細書中でR7E7と称する)、配列番号205/配列番号206 (本明細書中でR7F2と称する)、配列番号207/配列番号208 (本明細書中でR7F7と称する)、配列番号209/配列番号210 (本明細書中でR9H2と称する)、配列番号211/配列番号212 (本明細書中でR9H6と称する)、配列番号213/配列番号214 (本明細書中でH6B1Lと称する)、配列番号215/配列番号216 (本明細書中でH6A1と称する)、配列番号217/配列番号218 (本明細書中でH6B1と称する)、配列番号219/配列番号220 (本明細書中でH6B2と称する)、配列番号221/配列番号222 (本明細書中でH19Cと称する)、配列番号223/配列番号224 (本明細書中でH110Dと称する)、配列番号225/配列番号226 (本明細書中でH11Fと称する)、配列番号227/配列番号228 (本明細書中でH1C1と称する)、配列番号229/配列番号230 (本明細書中でGPG1A2と称する)、配列番号231/配列番号232 (本明細書中でGPGG8と称する)、配列番号233/配列番号234 (本明細書中でGPGG10と称する)、配列番号235/配列番号236 (本明細書中でGPGH7と称する)、配列番号237/配列番号238 (本明細書中でGPGH10と称する)、配列番号239/配列番号240 (本明細書中でGPGH11と称する)、配列番号241/配列番号242 (本明細書中でGPGH10Pと称する)およびその組み合わせからなる群から選択されるH鎖/L鎖可変領域の配列を有する。
配列番号2、配列番号4、配列番号6、配列番号8、配列番号10、配列番号12、配列番号14、配列番号16、配列番号18、配列番号20、配列番号22、配列番号24、配列番号26、配列番号28、配列番号30、配列番号32、配列番号34、配列番号36、配列番号38、配列番号40、配列番号42、配列番号44、配列番号46、配列番号48、配列番号50、配列番号52、配列番号54、配列番号56、配列番号58、配列番号60、配列番号62、配列番号64、配列番号66、配列番号68、配列番号70、配列番号72、配列番号74、配列番号76、配列番号78、配列番号80、配列番号82、配列番号84、配列番号86、配列番号88、配列番号90、配列番号92、配列番号94、配列番号96、配列番号98、配列番号100、配列番号102、配列番号104、配列番号106、配列番号108、配列番号110、配列番号112、配列番号114、配列番号116、配列番号118、配列番号120、配列番号122、配列番号124、配列番号126、配列番号128、配列番号130、配列番号132、配列番号134、配列番号136、配列番号138、配列番号140、配列番号142、配列番号144、配列番号146、配列番号148、配列番号150、配列番号152、配列番号154、配列番号156、配列番号158、配列番号160、配列番号162、配列番号164、配列番号166、配列番号168、配列番号170、配列番号172、配列番号174、配列番号176、配列番号178、配列番号180、配列番号182、配列番号184、配列番号186、配列番号188、配列番号190、配列番号192、配列番号194、配列番号196、配列番号198、配列番号200、配列番号202、配列番号204、配列番号206、配列番号208、配列番号210、配列番号212、配列番号214、配列番号216、配列番号218、配列番号220、配列番号222、配列番号224、配列番号226、配列番号228、配列番号230、配列番号232、配列番号234、配列番号236、配列番号238、配列番号240、配列番号242およびその組み合わせからなる群から選択されるアミノ酸配列と少なくとも95%同一であるL鎖可変領域配列を有する、Fab完全ヒト抗体断片を提供する。好ましくは、該完全ヒト抗体Fab断片は、H鎖可変領域とL鎖可変領域の両方を有し、該抗体は、配列番号1/配列番号2、配列番号3/配列番号4、配列番号5/配列番号6、配列番号7/配列番号8、配列番号9/配列番号10、配列番号11/配列番号12、配列番号13/配列番号14、配列番号15/配列番号16、配列番号17/配列番号18、配列番号19/配列番号20、配列番号21/配列番号22、配列番号23/配列番号24、配列番号25/配列番号26、配列番号27/配列番号28、配列番号29/配列番号30、配列番号31/配列番号32、配列番号33/配列番号34、配列番号35/配列番号36、配列番号37/配列番号38、配列番号39/配列番号40、配列番号41/配列番号42、配列番号43/配列番号44、配列番号45/配列番号46、配列番号47/配列番号48、配列番号49/配列番号50、配列番号51/配列番号52、配列番号53/配列番号54、配列番号55/配列番号56、配列番号57/配列番号58、配列番号59/配列番号60、配列番号61/配列番号62、配列番号63/配列番号64、配列番号65/配列番号66、配列番号67/配列番号68、配列番号69/配列番号70、配列番号71/配列番号72、配列番号73/配列番号74、配列番号75/配列番号76、配列番号77/配列番号78、配列番号79/配列番号80、配列番号81/配列番号82、配列番号83/配列番号84、配列番号85/配列番号86、配列番号87/配列番号88、配列番号89/配列番号90、配列番号91/配列番号92、配列番号93/配列番号94、配列番号95/配列番号96、配列番号97/配列番号98、配列番号99/配列番号100、配列番号101/配列番号102、配列番号103/配列番号104、配列番号105/配列番号106、配列番号107/配列番号108、配列番号109/配列番号110、配列番号111/配列番号112、配列番号113/配列番号114、配列番号115/配列番号116、配列番号117/配列番号118、配列番号119/配列番号120、配列番号121/配列番号122、配列番号123/配列番号124、配列番号125/配列番号126、配列番号127/配列番号128、配列番号129/配列番号130、配列番号131/配列番号132、配列番号133/配列番号134、配列番号135/配列番号136、配列番号137/配列番号138、配列番号139/配列番号140、配列番号141/配列番号142、配列番号143/配列番号144、配列番号145/配列番号146、配列番号147/配列番号148、配列番号149/配列番号150、配列番号151/配列番号152、配列番号153/配列番号154、配列番号155/配列番号156、配列番号157/配列番号158、配列番号159/配列番号160、配列番号161/配列番号162、配列番号163/配列番号164、配列番号165/配列番号166、配列番号167/配列番号168、配列番号169/配列番号170、配列番号171/配列番号172、配列番号173/配列番号174、配列番号175/配列番号176、配列番号177/配列番号178、配列番号179/配列番号180、配列番号181/配列番号182、配列番号183/配列番号184、配列番号185/配列番号186、配列番号187/配列番号188、配列番号189/配列番号190、配列番号191/配列番号192、配列番号193/配列番号194、配列番号195/配列番号196、配列番号197/配列番号198、配列番号199/配列番号200、配列番号201/配列番号202、配列番号203/配列番号204、配列番号205/配列番号206、配列番号207/配列番号208、配列番号209/配列番号210、配列番号211/配列番号212、配列番号213/配列番号214、配列番号215/配列番号216、配列番号217/配列番号218、配列番号219/配列番号220、配列番号221/配列番号222、配列番号223/配列番号224、配列番号225/配列番号226、配列番号227/配列番号228、配列番号229/配列番号230、配列番号231/配列番号232、配列番号233/配列番号234、配列番号235/配列番号236、配列番号237/配列番号238、配列番号239/配列番号240、配列番号241/配列番号242およびその組み合わせからなる群から選択されるH鎖/L鎖可変領域配列を有する。
配列番号2、配列番号4、配列番号6、配列番号8、配列番号10、配列番号12、配列番号14、配列番号16、配列番号18、配列番号20、配列番号22、配列番号24、配列番号26、配列番号28、配列番号30、配列番号32、配列番号34、配列番号36、配列番号38、配列番号40、配列番号42、配列番号44、配列番号46、配列番号48、配列番号50、配列番号52、配列番号54、配列番号56、配列番号58、配列番号60、配列番号62、配列番号64、配列番号66、配列番号68、配列番号70、配列番号72、配列番号74、配列番号76、配列番号78、配列番号80、配列番号82、配列番号84、配列番号86、配列番号88、配列番号90、配列番号92、配列番号94、配列番号96、配列番号98、配列番号100、配列番号102、配列番号104、配列番号106、配列番号108、配列番号110、配列番号112、配列番号114、配列番号116、配列番号118、配列番号120、配列番号122、配列番号124、配列番号126、配列番号128、配列番号130、配列番号132、配列番号134、配列番号136、配列番号138、配列番号140、配列番号142、配列番号144、配列番号146、配列番号148、配列番号150、配列番号152、配列番号154、配列番号156、配列番号158、配列番号160、配列番号162、配列番号164、配列番号166、配列番号168、配列番号170、配列番号172、配列番号174、配列番号176、配列番号178、配列番号180、配列番号182、配列番号184、配列番号186、配列番号188、配列番号190、配列番号192、配列番号194、配列番号196、配列番号198、配列番号200、配列番号202、配列番号204、配列番号206、配列番号208、配列番号210、配列番号212、配列番号214、配列番号216、配列番号218、配列番号220、配列番号222、配列番号224、配列番号226、配列番号228、配列番号230、配列番号232、配列番号234、配列番号236、配列番号238、配列番号240、配列番号242およびその組み合わせからなる群から選択されるアミノ酸配列と少なくとも95%同一であるL鎖可変領域配列を有する、一本鎖ヒト抗体を提供する。好ましくは、該完全ヒト一本鎖抗体は、H鎖可変領域とL鎖可変領域の両方を有し、配列番号1/配列番号2、配列番号3/配列番号4、配列番号5/配列番号6、配列番号7/配列番号8、配列番号9/配列番号10、配列番号11/配列番号12、配列番号13/配列番号14、配列番号15/配列番号16、配列番号17/配列番号18、配列番号19/配列番号20、配列番号21/配列番号22、配列番号23/配列番号24、配列番号25/配列番号26、配列番号27/配列番号28、配列番号29/配列番号30、配列番号31/配列番号32、配列番号33/配列番号34、配列番号35/配列番号36、配列番号37/配列番号38、配列番号39/配列番号40、配列番号41/配列番号42、配列番号43/配列番号44、配列番号45/配列番号46、配列番号47/配列番号48、配列番号49/配列番号50、配列番号51/配列番号52、配列番号53/配列番号54、配列番号55/配列番号56、配列番号57/配列番号58、配列番号59/配列番号60、配列番号61/配列番号62、配列番号63/配列番号64、配列番号65/配列番号66、配列番号67/配列番号68、配列番号69/配列番号70、配列番号71/配列番号72、配列番号73/配列番号74、配列番号75/配列番号76、配列番号77/配列番号78、配列番号79/配列番号80、配列番号81/配列番号82、配列番号83/配列番号84、配列番号85/配列番号86、配列番号87/配列番号88、配列番号89/配列番号90、配列番号91/配列番号92、配列番号93/配列番号94、配列番号95/配列番号96、配列番号97/配列番号98、配列番号99/配列番号100、配列番号101/配列番号102、配列番号103/配列番号104、配列番号105/配列番号106、配列番号107/配列番号108、配列番号109/配列番号110、配列番号111/配列番号112、配列番号113/配列番号114、配列番号115/配列番号116、配列番号117/配列番号118、配列番号119/配列番号120、配列番号121/配列番号122、配列番号123/配列番号124、配列番号125/配列番号126、配列番号127/配列番号128、配列番号129/配列番号130、配列番号131/配列番号132、配列番号133/配列番号134、配列番号135/配列番号136、配列番号137/配列番号138、配列番号139/配列番号140、配列番号141/配列番号142、配列番号143/配列番号144、配列番号145/配列番号146、配列番号147/配列番号148、配列番号149/配列番号150、配列番号151/配列番号152、配列番号153/配列番号154、配列番号155/配列番号156、配列番号157/配列番号158、配列番号159/配列番号160、配列番号161/配列番号162、配列番号163/配列番号164、配列番号165/配列番号166、配列番号167/配列番号168、配列番号169/配列番号170、配列番号171/配列番号172、配列番号173/配列番号174、配列番号175/配列番号176、配列番号177/配列番号178、配列番号179/配列番号180、配列番号181/配列番号182、配列番号183/配列番号184、配列番号185/配列番号186、配列番号187/配列番号188、配列番号189/配列番号190、配列番号191/配列番号192、配列番号193/配列番号194、配列番号195/配列番号196、配列番号197/配列番号198、配列番号199/配列番号200、配列番号201/配列番号202、配列番号203/配列番号204、配列番号205/配列番号206、配列番号207/配列番号208、配列番号209/配列番号210、配列番号211/配列番号212、配列番号213/配列番号214、配列番号215/配列番号216、配列番号217/配列番号218、配列番号219/配列番号220、配列番号221/配列番号222、配列番号223/配列番号224、配列番号225/配列番号226、配列番号227/配列番号228、配列番号229/配列番号230、配列番号231/配列番号232、配列番号233/配列番号234、配列番号235/配列番号236、配列番号237/配列番号238、配列番号239/配列番号240、配列番号241/配列番号242およびその組み合わせからなる群から選択されるH鎖/L鎖可変領域配列を有する。
該完全ヒト抗体は、配列番号1、配列番号3、配列番号5、配列番号7、配列番号9、配列番号11、配列番号13、配列番号15、配列番号17、配列番号19、配列番号21、配列番号23、配列番号25、配列番号27、配列番号29、配列番号31、配列番号33、配列番号35、配列番号37、配列番号39、配列番号41、配列番号43、配列番号45、配列番号47、配列番号49、配列番号51、配列番号53、配列番号55、配列番号57、配列番号59、配列番号61、配列番号63、配列番号65、配列番号67、配列番号69、配列番号71、配列番号73、配列番号75、配列番号77、配列番号79、配列番号81、配列番号83、配列番号85、配列番号87、配列番号89、配列番号91、配列番号93、配列番号95、配列番号97、配列番号99、配列番号101、配列番号103、配列番号105、配列番号107、配列番号109、配列番号111、配列番号113、配列番号115、配列番号117、配列番号119、配列番号121、配列番号123、配列番号125、配列番号127、配列番号129、配列番号131、配列番号133、配列番号135、配列番号137、配列番号139、配列番号141、配列番号143、配列番号145、配列番号147、配列番号149、配列番号151、配列番号153、配列番号155、配列番号157、配列番号159、配列番号161、配列番号163、配列番号165、配列番号167、配列番号169、配列番号171、配列番号173、配列番号175、配列番号177、配列番号179、配列番号181、配列番号183、配列番号185、配列番号187、配列番号189、配列番号191、配列番号193、配列番号195、配列番号197、配列番号199、配列番号201、配列番号203、配列番号205、配列番号207、配列番号209、配列番号211、配列番号213、配列番号215、配列番号217、配列番号219、配列番号221、配列番号223、配列番号225、配列番号227、配列番号229、配列番号231、配列番号233、配列番号235、配列番号237、配列番号239、配列番号241およびその組み合わせからなる群から選択されるアミノ酸配列と少なくとも95%同一であるH鎖可変領域配列を有し、
配列番号2、配列番号4、配列番号6、配列番号8、配列番号10、配列番号12、配列番号14、配列番号16、配列番号18、配列番号20、配列番号22、配列番号24、配列番号26、配列番号28、配列番号30、配列番号32、配列番号34、配列番号36、配列番号38、配列番号40、配列番号42、配列番号44、配列番号46、配列番号48、配列番号50、配列番号52、配列番号54、配列番号56、配列番号58、配列番号60、配列番号62、配列番号64、配列番号66、配列番号68、配列番号70、配列番号72、配列番号74、配列番号76、配列番号78、配列番号80、配列番号82、配列番号84、配列番号86、配列番号88、配列番号90、配列番号92、配列番号94、配列番号96、配列番号98、配列番号100、配列番号102、配列番号104、配列番号106、配列番号108、配列番号110、配列番号112、配列番号114、配列番号116、配列番号118、配列番号120、配列番号122、配列番号124、配列番号126、配列番号128、配列番号130、配列番号132、配列番号134、配列番号136、配列番号138、配列番号140、配列番号142、配列番号144、配列番号146、配列番号148、配列番号150、配列番号152、配列番号154、配列番号156、配列番号158、配列番号160、配列番号162、配列番号164、配列番号166、配列番号168、配列番号170、配列番号172、配列番号174、配列番号176、配列番号178、配列番号180、配列番号182、配列番号184、配列番号186、配列番号188、配列番号190、配列番号192、配列番号194、配列番号196、配列番号198、配列番号200、配列番号202、配列番号204、配列番号206、配列番号208、配列番号210、配列番号212、配列番号214、配列番号216、配列番号218、配列番号220、配列番号222、配列番号224、配列番号226、配列番号228、配列番号230、配列番号232、配列番号234、配列番号236、配列番号238、配列番号240、配列番号242およびその組み合わせからなる群から選択されるアミノ酸配列と少なくとも95%同一であるL鎖可変領域配列を有し;
該Fab完全ヒト抗体断片は、配列番号1、配列番号3、配列番号5、配列番号7、配列番号9、配列番号11、配列番号13、配列番号15、配列番号17、配列番号19、配列番号21、配列番号23、配列番号25、配列番号27、配列番号29、配列番号31、配列番号33、配列番号35、配列番号37、配列番号39、配列番号41、配列番号43、配列番号45、配列番号47、配列番号49、配列番号51、配列番号53、配列番号55、配列番号57、配列番号59、配列番号61、配列番号63、配列番号65、配列番号67、配列番号69、配列番号71、配列番号73、配列番号75、配列番号77、配列番号79、配列番号81、配列番号83、配列番号85、配列番号87、配列番号89、配列番号91、配列番号93、配列番号95、配列番号97、配列番号99、配列番号101、配列番号103、配列番号105、配列番号107、配列番号109、配列番号111、配列番号113、配列番号115、配列番号117、配列番号119、配列番号121、配列番号123、配列番号125、配列番号127、配列番号129、配列番号131、配列番号133、配列番号135、配列番号137、配列番号139、配列番号141、配列番号143、配列番号145、配列番号147、配列番号149、配列番号151、配列番号153、配列番号155、配列番号157、配列番号159、配列番号161、配列番号163、配列番号165、配列番号167、配列番号169、配列番号171、配列番号173、配列番号175、配列番号177、配列番号179、配列番号181、配列番号183、配列番号185、配列番号187、配列番号189、配列番号191、配列番号193、配列番号195、配列番号197、配列番号199、配列番号201、配列番号203、配列番号205、配列番号207、配列番号209、配列番号211、配列番号213、配列番号215、配列番号217、配列番号219、配列番号221、配列番号223、配列番号225、配列番号227、配列番号229、配列番号231、配列番号233、配列番号235、配列番号237、配列番号239、配列番号241およびその組み合わせからなる群から選択されるアミノ酸配列と少なくとも95%同一であるH鎖可変領域配列を有し、
配列番号2、配列番号4、配列番号6、配列番号8、配列番号10、配列番号12、配列番号14、配列番号16、配列番号18、配列番号20、配列番号22、配列番号24、配列番号26、配列番号28、配列番号30、配列番号32、配列番号34、配列番号36、配列番号38、配列番号40、配列番号42、配列番号44、配列番号46、配列番号48、配列番号50、配列番号52、配列番号54、配列番号56、配列番号58、配列番号60、配列番号62、配列番号64、配列番号66、配列番号68、配列番号70、配列番号72、配列番号74、配列番号76、配列番号78、配列番号80、配列番号82、配列番号84、配列番号86、配列番号88、配列番号90、配列番号92、配列番号94、配列番号96、配列番号98、配列番号100、配列番号102、配列番号104、配列番号106、配列番号108、配列番号110、配列番号112、配列番号114、配列番号116、配列番号118、配列番号120、配列番号122、配列番号124、配列番号126、配列番号128、配列番号130、配列番号132、配列番号134、配列番号136、配列番号138、配列番号140、配列番号142、配列番号144、配列番号146、配列番号148、配列番号150、配列番号152、配列番号154、配列番号156、配列番号158、配列番号160、配列番号162、配列番号164、配列番号166、配列番号168、配列番号170、配列番号172、配列番号174、配列番号176、配列番号178、配列番号180、配列番号182、配列番号184、配列番号186、配列番号188、配列番号190、配列番号192、配列番号194、配列番号196、配列番号198、配列番号200、配列番号202、配列番号204、配列番号206、配列番号208、配列番号210、配列番号212、配列番号214、配列番号216、配列番号218、配列番号220、配列番号222、配列番号224、配列番号226、配列番号228、配列番号230、配列番号232、配列番号234、配列番号236、配列番号238、配列番号240、配列番号242およびその組み合わせからなる群から選択されるアミノ酸配列と少なくとも95%同一であるL鎖可変領域配列を有し;
該一本鎖ヒト抗体は、配列番号1、配列番号3、配列番号5、配列番号7、配列番号9、配列番号11、配列番号13、配列番号15、配列番号17、配列番号19、配列番号21、配列番号23、配列番号25、配列番号27、配列番号29、配列番号31、配列番号33、配列番号35、配列番号37、配列番号39、配列番号41、配列番号43、配列番号45、配列番号47、配列番号49、配列番号51、配列番号53、配列番号55、配列番号57、配列番号59、配列番号61、配列番号63、配列番号65、配列番号67、配列番号69、配列番号71、配列番号73、配列番号75、配列番号77、配列番号79、配列番号81、配列番号83、配列番号85、配列番号87、配列番号89、配列番号91、配列番号93、配列番号95、配列番号97、配列番号99、配列番号101、配列番号103、配列番号105、配列番号107、配列番号109、配列番号111、配列番号113、配列番号115、配列番号117、配列番号119、配列番号121、配列番号123、配列番号125、配列番号127、配列番号129、配列番号131、配列番号133、配列番号135、配列番号137、配列番号139、配列番号141、配列番号143、配列番号145、配列番号147、配列番号149、配列番号151、配列番号153、配列番号155、配列番号157、配列番号159、配列番号161、配列番号163、配列番号165、配列番号167、配列番号169、配列番号171、配列番号173、配列番号175、配列番号177、配列番号179、配列番号181、配列番号183、配列番号185、配列番号187、配列番号189、配列番号191、配列番号193、配列番号195、配列番号197、配列番号199、配列番号201、配列番号203、配列番号205、配列番号207、配列番号209、配列番号211、配列番号213、配列番号215、配列番号217、配列番号219、配列番号221、配列番号223、配列番号225、配列番号227、配列番号229、配列番号231、配列番号233、配列番号235、配列番号237、配列番号239、配列番号241およびその組み合わせからなる群から選択されるアミノ酸配列と少なくとも95%同一であるH鎖可変領域配列を有し、
配列番号2、配列番号4、配列番号6、配列番号8、配列番号10、配列番号12、配列番号14、配列番号16、配列番号18、配列番号20、配列番号22、配列番号24、配列番号26、配列番号28、配列番号30、配列番号32、配列番号34、配列番号36、配列番号38、配列番号40、配列番号42、配列番号44、配列番号46、配列番号48、配列番号50、配列番号52、配列番号54、配列番号56、配列番号58、配列番号60、配列番号62、配列番号64、配列番号66、配列番号68、配列番号70、配列番号72、配列番号74、配列番号76、配列番号78、配列番号80、配列番号82、配列番号84、配列番号86、配列番号88、配列番号90、配列番号92、配列番号94、配列番号96、配列番号98、配列番号100、配列番号102、配列番号104、配列番号106、配列番号108、配列番号110、配列番号112、配列番号114、配列番号116、配列番号118、配列番号120、配列番号122、配列番号124、配列番号126、配列番号128、配列番号130、配列番号132、配列番号134、配列番号136、配列番号138、配列番号140、配列番号142、配列番号144、配列番号146、配列番号148、配列番号150、配列番号152、配列番号154、配列番号156、配列番号158、配列番号160、配列番号162、配列番号164、配列番号166、配列番号168、配列番号170、配列番号172、配列番号174、配列番号176、配列番号178、配列番号180、配列番号182、配列番号184、配列番号186、配列番号188、配列番号190、配列番号192、配列番号194、配列番号196、配列番号198、配列番号200、配列番号202、配列番号204、配列番号206、配列番号208、配列番号210、配列番号212、配列番号214、配列番号216、配列番号218、配列番号220、配列番号222、配列番号224、配列番号226、配列番号228、配列番号230、配列番号232、配列番号234、配列番号236、配列番号238、配列番号240、配列番号242およびその組み合わせからなる群から選択されるアミノ酸配列と少なくとも95%同一であるL鎖可変領域配列を有する。
(本明細書中でRG12と称する)、配列番号97/配列番号98(本明細書中でRSA1と称する)、配列番号99/配列番号100 (本明細書中でR2A7と称する)、配列番号101/配列番号102 (本明細書中でR2B12と称する)、配列番号103/配列番号104 (本明細書中でR2C9と称する)、配列番号105/配列番号106 (本明細書中でR2D5と称する)、配列番号107/配列番号108 (本明細書中でR2D7と称する)、配列番号109/配列番号110 (本明細書中でR2F4と称する)、配列番号111/配列番号112 (本明細書中でR2A10と称する)、配列番号113/配列番号114 (本明細書中でR2E2と称する)、配列番号115/配列番号116 (本明細書中でR3B8と称する)、配列番号117/配列番号118 (本明細書中でR3C3と称する)、配列番号119/配列番号120 (本明細書中でR3E9と称する)、配列番号121/配列番号122 (本明細書中でR3E10と称する)、配列番号123/配列番号124 (本明細書中でR3F7と称する)、配列番号125/配列番号126 (本明細書中でR3F10と称する)、配列番号127/配列番号128 (本明細書中でR4B10と称する)、配列番号129/配列番号130 (本明細書中でR4H1と称する)、配列番号131/配列番号132 (本明細書中でR4A11と称する)、配列番号133/配列番号134 (本明細書中でR3D2と称する)、配列番号135/配列番号136 (本明細書中でR5B8と称する)、配列番号137/配列番号138 (本明細書中でSH1A1Qと称する)、配列番号139/配列番号140 (本明細書中で SH1B7B(K)と称する)、配列番号141/配列番号142 (本明細書中でSH1C1と称する)、配列番号143/配列番号144 (本明細書中でSH1C8と称する)、配列番号145/配列番号146 (本明細書中でSH1E10と称する)、配列番号147/配列番号148 (本明細書中でSH1E2と称する)、配列番号149/配列番号150 (本明細書中でSH1A9と称する)、配列番号151/配列番号152 (本明細書中でSH1B11と称する)、配列番号153/配列番号154 (本明細書中でSH1E4と称する)、配列番号155/配列番号156 (本明細書中でSH1B3と称する)、配列番号157/配列番号158 (本明細書中でSH1D1と称する)、配列番号159/配列番号160 (本明細書中でSH1D2と称する)、配列番号161/配列番号162 (本明細書中でSH1D12と称する)、配列番号163/配列番号164 (本明細書中でSH1E1と称する)、配列番号165/配列番号166 (本明細書中でSH1G9と称する)、配列番号167/配列番号168 (本明細書中でSH1A11と称する)、配列番号169/配列番号170 (本明細書中でSH1C2と称する)、配列番号171/配列番号172 (本明細書中でSH1G8と称する)、配列番号173/配列番号174 (本明細書中でSH1H2と称する)、配列番号175/配列番号176 (本明細書中でSH1B10と称する)、配列番号177/配列番号178 (本明細書中で SH1B7A(L)と称する)、配列番号179/配列番号180 (本明細書中でSH1E6と称する)、配列番号181/配列番号182 (本明細書中でSH1C11と称する)、配列番号183/配列番号184 (本明細書中でSH1A2と称する)、配列番号185/配列番号186 (本明細書中でSH1B1と称する)、配列番号187/配列番号188 (本明細書中でR6B2と称する)、配列番号189/配列番号190 (本明細書中でR6B7と称する)、配列番号191/配列番号192 (本明細書中でR6B11と称する)、配列番号193/配列番号194 (本明細書中でR6D1と称する)、配列番号195/配列番号196 (本明細書中でR6C8と称する)、配列番号197/配列番号198 (本明細書中でR9G8と称する)、配列番号199/配列番号200 (本明細書中でR7D1と称する)、配列番号201/配列番号202 (本明細書中でR7D2と称する)、配列番号203/配列番号204 (本明細書中でR7E7と称する)、配列番号205/配列番号206 (本明細書中でR7F2と称する)、配列番号207/配列番号208 (本明細書中でR7F7と称する)、配列番号209/配列番号210 (本明細書中でR9H2と称する)、配列番号211/配列番号212 (本明細書中でR9H6と称する)、配列番号213/配列番号214 (本明細書中でH6B1Lと称する)、配列番号215/配列番号216 (本明細書中でH6A1と称する)、配列番号217/配列番号218 (本明細書中でH6B1と称する)、配列番号219/配列番号220 (本明細書中でH6B2と称する)、配列番号221/配列番号222 (本明細書中でH19Cと称する)、配列番号223/配列番号224 (本明細書中でH110Dと称する)、配列番号225/配列番号226 (本明細書中でH11Fと称する)、配列番号227/配列番号228 (本明細書中でH1C1と称する)、配列番号229/配列番号230 (本明細書中でGPG1A2と称する)、配列番号231/配列番号232 (本明細書中でGPGG8と称する)、配列番号233/配列番号234 (本明細書中でGPGG10と称する)、配列番号235/配列番号236 (本明細書中でGPGH7と称する)、配列番号237/配列番号238 (本明細書中でGPGH10と称する)、配列番号239/配列番号240 (本明細書中でGPGH11と称する)、配列番号241/配列番号242 (本明細書中でGPGH10Pと称する)およびその組み合わせからなる群から選択されるH鎖/L鎖可変領域配列を有する。好ましくは、該完全ヒト一本鎖抗体は、H鎖可変領域とL鎖可変領域の両方を有し、配列番号1/配列番号2、配列番号3/配列番号4、配列番号5/配列番号6、配列番号7/配列番号8、配列番号9/配列番号10、配列番号11/配列番号12、配列番号13/配列番号14、配列番号15/配列番号16、配列番号17/配列番号18、配列番号19/配列番号20、配列番号21/配列番号22、配列番号23/配列番号24、配列番号25/配列番号26、配列番号27/配列番号28、配列番号29/配列番号30、配列番号31/配列番号32、配列番号33/配列番号34、配列番号35/配列番号36、配列番号37/配列番号38、配列番号39/配列番号40、配列番号41/配列番号42、配列番号43/配列番号44、配列番号45/配列番号46、配列番号47/配列番号48、配列番号49/配列番号50、配列番号51/配列番号52、配列番号53/配列番号54、配列番号55/配列番号56、配列番号57/配列番号58、配列番号59/配列番号60、配列番号61/配列番号62、配列番号63/配列番号64、配列番号65/配列番号66、配列番号67/配列番号68、配列番号69/配列番号70、配列番号71/配列番号72、配列番号73/配列番号74、配列番号75/配列番号76、配列番号77/配列番号78、配列番号79/配列番号80、配列番号81/配列番号82、配列番号83/配列番号84、配列番号85/配列番号86、配列番号87/配列番号88、配列番号89/配列番号90、配列番号91/配列番号92、配列番号93/配列番号94、配列番号95/配列番号96、配列番号97/配列番号98、配列番号99/配列番号100、配列番号101/配列番号102、配列番号103/配列番号104、配列番号105/配列番号106、配列番号107/配列番号108、配列番号109/配列番号110、配列番号111/配列番号112、配列番号113/配列番号114、配列番号115/配列番号116、配列番号117/配列番号118、配列番号119/配列番号120、配列番号121/配列番号122、配列番号123/配列番号124、配列番号125/配列番号126、配列番号127/配列番号128、配列番号129/配列番号130、配列番号131/配列番号132、配列番号133/配列番号134、配列番号135/配列番号136、配列番号137/配列番号138、配列番号139/配列番号140、配列番号141/配列番号142、配列番号143/配列番号144、配列番号145/配列番号146、配列番号147/配列番号148、配列番号149/配列番号150、配列番号151/配列番号152、配列番号153/配列番号154、配列番号155/配列番号156、配列番号157/配列番号158、配列番号159/配列番号160、配列番号161/配列番号162、配列番号163/配列番号164、配列番号165/配列番号166、配列番号167/配列番号168、配列番号169/配列番号170、配列番号171/配列番号172、配列番号173/配列番号174、配列番号175/配列番号176、配列番号177/配列番号178、配列番号179/配列番号180、配列番号181/配列番号182、配列番号183/配列番号184、配列番号185/配列番号186、配列番号187/配列番号188、配列番号189/配列番号190、配列番号191/配列番号192、配列番号193/配列番号194、配列番号195/配列番号196、配列番号197/配列番号198、配列番号199/配列番号200、配列番号201/配列番号202、配列番号203/配列番号204、配列番号205/配列番号206、配列番号207/配列番号208、配列番号209/配列番号210、配列番号211/配列番号212、配列番号213/配列番号214、配列番号215/配列番号216、配列番号217/配列番号218、配列番号219/配列番号220、配列番号221/配列番号222、配列番号223/配列番号224、配列番号225/配列番号226、配列番号227/配列番号228、配列番号229/配列番号230、配列番号231/配列番号232、配列番号233/配列番号234、配列番号235/配列番号236、配列番号237/配列番号238、配列番号239/配列番号240、配列番号241/配列番号242およびその組み合わせからなる群から選択されるH鎖/L鎖可変領域配列を有する。
配列番号2、配列番号4、配列番号6、配列番号8、配列番号10、配列番号12、配列番号14、配列番号16、配列番号18、配列番号20、配列番号22、配列番号24、配列番号26、配列番号28、配列番号30、配列番号32、配列番号34、配列番号36、配列番号38、配列番号40、配列番号42、配列番号44、配列番号46、配列番号48、配列番号50、配列番号52、配列番号54、配列番号56、配列番号58、配列番号60、配列番号62、配列番号64、配列番号66、配列番号68、配列番号70、配列番号72、配列番号74、配列番号76、配列番号78、配列番号80、配列番号82、配列番号84、配列番号86、配列番号88、配列番号90、配列番号92、配列番号94、配列番号96、配列番号98、配列番号100、配列番号102、配列番号104、配列番号106、配列番号108、配列番号110、配列番号112、配列番号114、配列番号116、配列番号118、配列番号120、配列番号122、配列番号124、配列番号126、配列番号128、配列番号130、配列番号132、配列番号134、配列番号136、配列番号138、配列番号140、配列番号142、配列番号144、配列番号146、配列番号148、配列番号150、配列番号152、配列番号154、配列番号156、配列番号158、配列番号160、配列番号162、配列番号164、配列番号166、配列番号168、配列番号170、配列番号172、配列番号174、配列番号176、配列番号178、配列番号180、配列番号182、配列番号184、配列番号186、配列番号188、配列番号190、配列番号192、配列番号194、配列番号196、配列番号198、配列番号200、配列番号202、配列番号204、配列番号206、配列番号208、配列番号210、配列番号212、配列番号214、配列番号216、配列番号218、配列番号220、配列番号222、配列番号224、配列番号226、配列番号228、配列番号230、配列番号232、配列番号234、配列番号236、配列番号238、配列番号240、配列番号242およびその組み合わせからなる群から選択されるアミノ酸配列と少なくとも95%同一であるL鎖可変領域配列を有する、完全ヒト抗体を提供する。好ましくは、該完全ヒト抗体は、H鎖とL鎖の両方を有し、配列番号1/配列番号2 (E6と称する)、配列番号3/配列番号4 (E7と称する)、配列番号5/配列番号6 (E9と称する)、配列番号7/配列番号8 (E11と称する)、配列番号9/配列番号10 (F1と称する)、配列番号11/配列番号12 (F4と称する)、配列番号13/配列番号14 (F7と称する)、配列番号15/配列番号16 (F8と称する)、配列番号17/配列番号18 (F11と称する)、配列番号19/配列番号20 (G4と称する)、配列番号21/配列番号22 (G9と称する)、配列番号23/配列番号24 (G11と称する)、配列番号25/配列番号26 (G12と称する)、配列番号27/配列番号28 (H1と称する)、配列番号29/配列番号30 (H3と称する)、配列番号31/配列番号32 (H4と称する)、配列番号33/配列番号34 (H5と称する)、配列番号35/配列番号36 (H6と称する)、配列番号37/配列番号38 (H10と称する)、配列番号39/配列番号40 (H12と称する)、配列番号41/配列番号42 (PDL−D2と称する)、配列番号43/配列番号44 (PDL−D11と称する)、配列番号45/配列番号46 (PDL−H1と称する)、配列番号47/配列番号48 (RB4と称する)、配列番号49/配列番号50 (RB11と称する)、配列番号51/配列番号52 (RC5と称する)、配列番号53/配列番号54 (RF5と称する)、配列番号55/配列番号56 (RG9と称する)、配列番号57/配列番号58 (RD1と称する)、配列番号59/配列番号60 (RF11と称する)、配列番号61/配列番号62 (RH11と称する)、配列番号63/配列番号64 (RD9と称する)、配列番号65/配列番号66 (RE10と称する)、配列番号67/配列番号68 (RA3と称する)、配列番号69/配列番号70 (RG1と称する)、配列番号71/配列番号72 (RB1と称する)、配列番号73/配列番号74 (RG7と称する)、配列番号75/配列番号76 (RA6と称する)、配列番号77/配列番号78 (RA8と称する)、配列番号79/配列番号80 (RA9と称する)、配列番号81/配列番号82 (RB5と称する)、配列番号83/配列番号84 (RB8と称する)、配列番号85/配列番号86 (RC8と称する)、配列番号87/配列番号88 (RC10と称する)、配列番号89/配列番号90 (RD2と称する)、配列番号91/配列番号92 (RE8と称する)、配列番号93/配列番号94 (RE9と称する)、配列番号95/配列番号96 (RG12と称する)、配列番号97/配列番号98 (RSA1と称する)、配列番号99/配列番号100 (R2A7と称する)、配列番号101/配列番号102 (R2B12と称する)、配列番号103/配列番号104 (R2C9と称する)、配列番号105/配列番号106 (R2D5と称する)、配列番号107/配列番号108 (R2D7と称する)、配列番号109/配列番号110 (R2F4と称する)、配列番号111/配列番号112 (R2A10と称する)、配列番号113/配列番号114 (でR2E2と称する)、配列番号115/配列番号116 (R3B8と称する)、配列番号117/配列番号118 (R3C3と称する)、配列番号119/配列番号120 (R3E9と称する)、配列番号121/配列番号122 (R3E10と称する)、配列番号123/配列番号124 (R3F7と称する)、配列番号125/配列番号126 (R3F10と称する)、配列番号127/配列番号128 (R4B10と称する)、配列番号129/配列番号130 (R4H1と称する)、配列番号131/配列番号132 (R4A11と称する)、配列番号133/配列番号134 (R3D2と称する)、配列番号135/配列番号136 (R5B8と称する)、配列番号137/配列番号138 (SH1A1Qと称する)、配列番号139/配列番号140 (SH1B7B(K)と称する)、配列番号141/配列番号142 (SH1C1と称する)、配列番号143/配列番号144 (SH1C8と称する)、配列番号145/配列番号146 (SH1E10と称する)、配列番号147/配列番号148 (SH1E2と称する)、配列番号149/配列番号150 (SH1A9と称する)、配列番号151/配列番号152 (SH1B11と称する)、配列番号153/配列番号154 (SH1E4と称する)、配列番号155/配列番号156 (SH1B3と称する)、配列番号157/配列番号158 (SH1D1と称する)、配列番号159/配列番号160 (SH1D2と称する)、配列番号161/配列番号162 (SH1D12と称する)、配列番号163/配列番号164 (SH1E1と称する)、配列番号165/配列番号166 (SH1G9と称する)、配列番号167/配列番号168 (SH1A11と称する)、配列番号169/配列番号170 (SH1C2と称する)、配列番号171/配列番号172 (SH1G8と称する)、配列番号173/配列番号174 (SH1H2と称する)、配列番号175/配列番号176 (SH1B10と称する)、配列番号177/配列番号178 (SH1B7A(L)と称する)、配列番号179/配列番号180 (SH1E6と称する)、配列番号181/配列番号182 (SH1C11と称する)、配列番号183/配列番号184 (SH1A2と称する)、配列番号185/配列番号186 (SH1B1と称する)、配列番号187/配列番号188 (R6B2と称する)、配列番号189/配列番号190 (R6B7と称する)、配列番号191/配列番号192 (R6B11と称する)、配列番号193/配列番号194 (R6D1と称する)、配列番号195/配列番号196 (R6C8と称する)、配列番号197/配列番号198 (R9G8と称する)、配列番号199/配列番号200 (R7D1と称する)、配列番号201/配列番号202 (R7D2と称する)、配列番号203/配列番号204 (R7E7と称する)、配列番号205/配列番号206 (R7F2と称する)、配列番号207/配列番号208 (R7F7と称する)、配列番号209/配列番号210 (R9H2と称する)、配列番号211/配列番号212 (R9H6と称する)、配列番号213/配列番号214 (H6B1Lと称する)、配列番号215/配列番号216 (H6A1と称する)、配列番号217/配列番号218 (H6B1と称する)、配列番号219/配列番号220 (H6B2と称する)、配列番号221/配列番号222 (H19Cと称する)、配列番号223/配列番号224 (H110Dと称する)、配列番号225/配列番号226 (H11Fと称する)、配列番号227/配列番号228 (H1C1と称する)、配列番号229/配列番号230 (GPG1A2と称する)、配列番号231/配列番号232 (GPGG8と称する)、配列番号233/配列番号234 (GPGG10と称する)、配列番号235/配列番号236 (GPGH7と称する)、配列番号237/配列番号238 (GPGH10と称する)、配列番号239/配列番号240 (GPGH11と称する)、配列番号241/配列番号242 (GPGH10Pと称する)およびその組み合わせからなる群から選択されるH鎖/L鎖可変領域配列を有する。
配列番号2、配列番号4、配列番号6、配列番号8、配列番号10、配列番号12、配列番号14、配列番号16、配列番号18、配列番号20、配列番号22、配列番号24、配列番号26、配列番号28、配列番号30、配列番号32、配列番号34、配列番号36、配列番号38、配列番号40、配列番号42、配列番号44、配列番号46、配列番号48、配列番号50、配列番号52、配列番号54、配列番号56、配列番号58、配列番号60、配列番号62、配列番号64、配列番号66、配列番号68、配列番号70、配列番号72、配列番号74、配列番号76、配列番号78、配列番号80、配列番号82、配列番号84、配列番号86、配列番号88、配列番号90、配列番号92、配列番号94、配列番号96、配列番号98、配列番号100、配列番号102、配列番号104、配列番号106、配列番号108、配列番号110、配列番号112、配列番号114、配列番号116、配列番号118、配列番号120、配列番号122、配列番号124、配列番号126、配列番号128、配列番号130、配列番号132、配列番号134、配列番号136、配列番号138、配列番号140、配列番号142、配列番号144、配列番号146、配列番号148、配列番号150、配列番号152、配列番号154、配列番号156、配列番号158、配列番号160、配列番号162、配列番号164、配列番号166、配列番号168、配列番号170、配列番号172、配列番号174、配列番号176、配列番号178、配列番号180、配列番号182、配列番号184、配列番号186、配列番号188、配列番号190、配列番号192、配列番号194、配列番号196、配列番号198、配列番号200、配列番号202、配列番号204、配列番号206、配列番号208、配列番号210、配列番号212、配列番号214、配列番号216、配列番号218、配列番号220、配列番号222、配列番号224、配列番号226、配列番号228、配列番号230、配列番号232、配列番号234、配列番号236、配列番号238、配列番号240、配列番号242およびその組み合わせからなる群から選択されるアミノ酸配列と少なくとも95%同一であるL鎖可変領域配列を有する、Fab完全ヒト抗体断片を提供する。好ましくは、該完全ヒト抗体Fab断片は、H鎖可変領域とL鎖可変領域配列の両方を有し、該抗体は、配列番号1/配列番号2、配列番号3/配列番号4、配列番号5/配列番号6、配列番号7/配列番号8、配列番号9/配列番号10、配列番号11/配列番号12、配列番号13/配列番号14、配列番号15/配列番号16、配列番号17/配列番号18、配列番号19/配列番号20、配列番号21/配列番号22、配列番号23/配列番号24、配列番号25/配列番号26、配列番号27/配列番号28、配列番号29/配列番号30、配列番号31/配列番号32、配列番号33/配列番号34、配列番号35/配列番号36、配列番号37/配列番号38、配列番号39/配列番号40、配列番号41/配列番号42、配列番号43/配列番号44、配列番号45/配列番号46、配列番号47/配列番号48、配列番号49/配列番号50、配列番号51/配列番号52、配列番号53/配列番号54、配列番号55/配列番号56、配列番号57/配列番号58、配列番号59/配列番号60、配列番号61/配列番号62、配列番号63/配列番号64、配列番号65/配列番号66、配列番号67/配列番号68、配列番号69/配列番号70、配列番号71/配列番号72、配列番号73/配列番号74、配列番号75/配列番号76、配列番号77/配列番号78、配列番号79/配列番号80、配列番号81/配列番号82、配列番号83/配列番号84、配列番号85/配列番号86、配列番号87/配列番号88、配列番号89/配列番号90、配列番号91/配列番号92、配列番号93/配列番号94、配列番号95/配列番号96、配列番号97/配列番号98、配列番号99/配列番号100、配列番号101/配列番号102、配列番号103/配列番号104、配列番号105/配列番号106、配列番号107/配列番号108、配列番号109/配列番号110、配列番号111/配列番号112、配列番号113/配列番号114、配列番号115/配列番号116、配列番号117/配列番号118、配列番号119/配列番号120、配列番号121/配列番号122、配列番号123/配列番号124、配列番号125/配列番号126、配列番号127/配列番号128、配列番号129/配列番号130、配列番号131/配列番号132、配列番号133/配列番号134、配列番号135/配列番号136、配列番号137/配列番号138、配列番号139/配列番号140、配列番号141/配列番号142、配列番号143/配列番号144、配列番号145/配列番号146、配列番号147/配列番号148、配列番号149/配列番号150、配列番号151/配列番号152、配列番号153/配列番号154、配列番号155/配列番号156、配列番号157/配列番号158、配列番号159/配列番号160、配列番号161/配列番号162、配列番号163/配列番号164、配列番号165/配列番号166、配列番号167/配列番号168、配列番号169/配列番号170、配列番号171/配列番号172、配列番号173/配列番号174、配列番号175/配列番号176、配列番号177/配列番号178、配列番号179/配列番号180、配列番号181/配列番号182、配列番号183/配列番号184、配列番号185/配列番号186、配列番号187/配列番号188、配列番号189/配列番号190、配列番号191/配列番号192、配列番号193/配列番号194、配列番号195/配列番号196、配列番号197/配列番号198、配列番号199/配列番号200、配列番号201/配列番号202、配列番号203/配列番号204、配列番号205/配列番号206、配列番号207/配列番号208、配列番号209/配列番号210、配列番号211/配列番号212、配列番号213/配列番号214、配列番号215/配列番号216、配列番号217/配列番号218、配列番号219/配列番号220、配列番号221/配列番号222、配列番号223/配列番号224、配列番号225/配列番号226、配列番号227/配列番号228、配列番号229/配列番号230、配列番号231/配列番号232、配列番号233/配列番号234、配列番号235/配列番号236、配列番号237/配列番号238、配列番号239/配列番号240、配列番号241/配列番号242およびその組み合わせからなる群から選択されるH鎖/L鎖可変領域配列を有する。
配列番号1、配列番号3、配列番号5、配列番号7、配列番号9、配列番号11、配列番号13、配列番号15、配列番号17、配列番号19、配列番号21、配列番号23、配列番号25、配列番号27、配列番号29、配列番号31、配列番号33、配列番号35、配列番号37、配列番号39、配列番号41、配列番号43、配列番号45、配列番号47、配列番号49、配列番号51、配列番号53、配列番号55、配列番号57、配列番号59、配列番号61、配列番号63、配列番号65、配列番号67、配列番号69、配列番号71、配列番号73、配列番号75、配列番号77、配列番号79、配列番号81、配列番号83、配列番号85、配列番号87、配列番号89、配列番号91、配列番号93、配列番号95、配列番号97、配列番号99、配列番号101、配列番号103、配列番号105、配列番号107、配列番号109、配列番号111、配列番号113、配列番号115、配列番号117、配列番号119、配列番号121、配列番号123、配列番号125、配列番号127、配列番号129、配列番号131、配列番号133、配列番号135、配列番号137、配列番号139、配列番号141、配列番号143、配列番号145、配列番号147、配列番号149、配列番号151、配列番号153、配列番号155、配列番号157、配列番号159、配列番号161、配列番号163、配列番号165、配列番号167、配列番号169、配列番号171、配列番号173、配列番号175、配列番号177、配列番号179、配列番号181、配列番号183、配列番号185、配列番号187、配列番号189、配列番号191、配列番号193、配列番号195、配列番号197、配列番号199、配列番号201、配列番号203、配列番号205、配列番号207、配列番号209、配列番号211、配列番号213、配列番号215、配列番号217、配列番号219、配列番号221、配列番号223、配列番号225、配列番号227、配列番号229、配列番号231、配列番号233、配列番号235、配列番号237、配列番号239、配列番号241およびその組み合わせからなる群から選択されるアミノ酸配列と少なくとも95%同一であるH鎖可変領域配列を有し、
配列番号2、配列番号4、配列番号6、配列番号8、配列番号10、配列番号12、配列番号14、配列番号16、配列番号18、配列番号20、配列番号22、配列番号24、配列番号26、配列番号28、配列番号30、配列番号32、配列番号34、配列番号36、配列番号38、配列番号40、配列番号42、配列番号44、配列番号46、配列番号48、配列番号50、配列番号52、配列番号54、配列番号56、配列番号58、配列番号60、配列番号62、配列番号64、配列番号66、配列番号68、配列番号70、配列番号72、配列番号74、配列番号76、配列番号78、配列番号80、配列番号82、配列番号84、配列番号86、配列番号88、配列番号90、配列番号92、配列番号94、配列番号96、配列番号98、配列番号100、配列番号102、配列番号104、配列番号106、配列番号108、配列番号110、配列番号112、配列番号114、配列番号116、配列番号118、配列番号120、配列番号122、配列番号124、配列番号126、配列番号128、配列番号130、配列番号132、配列番号134、配列番号136、配列番号138、配列番号140、配列番号142、配列番号144、配列番号146、配列番号148、配列番号150、配列番号152、配列番号154、配列番号156、配列番号158、配列番号160、配列番号162、配列番号164、配列番号166、配列番号168、配列番号170、配列番号172、配列番号174、配列番号176、配列番号178、配列番号180、配列番号182、配列番号184、配列番号186、配列番号188、配列番号190、配列番号192、配列番号194、配列番号196、配列番号198、配列番号200、配列番号202、配列番号204、配列番号206、配列番号208、配列番号210、配列番号212、配列番号214、配列番号216、配列番号218、配列番号220、配列番号222、配列番号224、配列番号226、配列番号228、配列番号230、配列番号232、配列番号234、配列番号236、配列番号238、配列番号240、配列番号242およびその組み合わせからなる群から選択されるアミノ酸配列と少なくとも95%同一であるL鎖可変領域配列を有する、一本鎖ヒト抗体を提供する。好ましくは、該完全ヒト一本鎖抗体は、H鎖可変領域とL鎖可変領域の両方を有し、配列番号1/配列番号2、配列番号3/配列番号4、配列番号5/配列番号6、配列番号7/配列番号8、配列番号9/配列番号10、配列番号11/配列番号12、配列番号13/配列番号14、配列番号15/配列番号16、配列番号17/配列番号18、配列番号19/配列番号20、配列番号21/配列番号22、配列番号23/配列番号24、配列番号25/配列番号26、配列番号27/配列番号28、配列番号29/配列番号30、配列番号31/配列番号32、配列番号33/配列番号34、配列番号35/配列番号36、配列番号37/配列番号38、配列番号39/配列番号40、配列番号41/配列番号42、配列番号43/配列番号44、配列番号45/配列番号46、配列番号47/配列番号48、配列番号49/配列番号50、配列番号51/配列番号52、配列番号53/配列番号54、配列番号55/配列番号56、配列番号57/配列番号58、配列番号59/配列番号60、配列番号61/配列番号62、配列番号63/配列番号64、配列番号65/配列番号66、配列番号67/配列番号68、配列番号69/配列番号70、配列番号71/配列番号72、配列番号73/配列番号74、配列番号75/配列番号76、配列番号77/配列番号78、配列番号79/配列番号80、配列番号81/配列番号82、配列番号83/配列番号84、配列番号85/配列番号86、配列番号87/配列番号88、配列番号89/配列番号90、配列番号91/配列番号92、配列番号93/配列番号94、配列番号95/配列番号96、配列番号97/配列番号98、配列番号99/配列番号100、配列番号101/配列番号102、配列番号103/配列番号104、配列番号105/配列番号106、配列番号107/配列番号108、配列番号109/配列番号110、配列番号111/配列番号112、配列番号113/配列番号114、配列番号115/配列番号116、配列番号117/配列番号118、配列番号119/配列番号120、配列番号121/配列番号122、配列番号123/配列番号124、配列番号125/配列番号126、配列番号127/配列番号128、配列番号129/配列番号130、配列番号131/配列番号132、配列番号133/配列番号134、配列番号135/配列番号136、配列番号137/配列番号138、配列番号139/配列番号140、配列番号141/配列番号142、配列番号143/配列番号144、配列番号145/配列番号146、配列番号147/配列番号148、配列番号149/配列番号150、配列番号151/配列番号152、配列番号153/配列番号154、配列番号155/配列番号156、配列番号157/配列番号158、配列番号159/配列番号160、配列番号161/配列番号162、配列番号163/配列番号164、配列番号165/配列番号166、配列番号167/配列番号168、配列番号169/配列番号170、配列番号171/配列番号172、配列番号173/配列番号174、配列番号175/配列番号176、配列番号177/配列番号178、配列番号179/配列番号180、配列番号181/配列番号182、配列番号183/配列番号184、配列番号185/配列番号186、配列番号187/配列番号188、配列番号189/配列番号190、配列番号191/配列番号192、配列番号193/配列番号194、配列番号195/配列番号196、配列番号197/配列番号198、配列番号199/配列番号200、配列番号201/配列番号202、配列番号203/配列番号204、配列番号205/配列番号206、配列番号207/配列番号208、配列番号209/配列番号210、配列番号211/配列番号212、配列番号213/配列番号214、配列番号215/配列番号216、配列番号217/配列番号218、配列番号219/配列番号220、配列番号221/配列番号222、配列番号223/配列番号224、配列番号225/配列番号226、配列番号227/配列番号228、配列番号229/配列番号230、配列番号231/配列番号232、配列番号233/配列番号234、配列番号235/配列番号236、配列番号237/配列番号238、配列番号239/配列番号240、配列番号241/配列番号242およびその組み合わせからなる群から選択されるH鎖/L鎖可変領域配列を有する。
該完全ヒト抗体は、配列番号1、配列番号3、配列番号5、配列番号7、配列番号9、配列番号11、配列番号13、配列番号15、配列番号17、配列番号19、配列番号21、配列番号23、配列番号25、配列番号27、配列番号29、配列番号31、配列番号33、配列番号35、配列番号37、配列番号39、配列番号41、配列番号43、配列番号45、配列番号47、配列番号49、配列番号51、配列番号53、配列番号55、配列番号57、配列番号59、配列番号61、配列番号63、配列番号65、配列番号67、配列番号69、配列番号71、配列番号73、配列番号75、配列番号77、配列番号79、配列番号81、配列番号83、配列番号85、配列番号87、配列番号89、配列番号91、配列番号93、配列番号95、配列番号97、配列番号99、配列番号101、配列番号103、配列番号105、配列番号107、配列番号109、配列番号111、配列番号113、配列番号115、配列番号117、配列番号119、配列番号121、配列番号123、配列番号125、配列番号127、配列番号129、配列番号131、配列番号133、配列番号135、配列番号137、配列番号139、配列番号141、配列番号143、配列番号145、配列番号147、配列番号149、配列番号151、配列番号153、配列番号155、配列番号157、配列番号159、配列番号161、配列番号163、配列番号165、配列番号167、配列番号169、配列番号171、配列番号173、配列番号175、配列番号177、配列番号179、配列番号181、配列番号183、配列番号185、配列番号187、配列番号189、配列番号191、配列番号193、配列番号195、配列番号197、配列番号199、配列番号201、配列番号203、配列番号205、配列番号207、配列番号209、配列番号211、配列番号213、配列番号215、配列番号217、配列番号219、配列番号221、配列番号223、配列番号225、配列番号227、配列番号229、配列番号231、配列番号233、配列番号235、配列番号237、配列番号239、配列番号241およびその組み合わせからなる群から選択されるアミノ酸配列と少なくとも95%同一であるH鎖可変領域を有し、
配列番号2、配列番号4、配列番号6、配列番号8、配列番号10、配列番号12、配列番号14、配列番号16、配列番号18、配列番号20、配列番号22、配列番号24、配列番号26、配列番号28、配列番号30、配列番号32、配列番号34、配列番号36、配列番号38、配列番号40、配列番号42、配列番号44、配列番号46、配列番号48、配列番号50、配列番号52、配列番号54、配列番号56、配列番号58、配列番号60、配列番号62、配列番号64、配列番号66、配列番号68、配列番号70、配列番号72、配列番号74、配列番号76、配列番号78、配列番号80、配列番号82、配列番号84、配列番号86、配列番号88、配列番号90、配列番号92、配列番号94、配列番号96、配列番号98、配列番号100、配列番号102、配列番号104、配列番号106、配列番号108、配列番号110、配列番号112、配列番号114、配列番号116、配列番号118、配列番号120、配列番号122、配列番号124、配列番号126、配列番号128、配列番号130、配列番号132、配列番号134、配列番号136、配列番号138、配列番号140、配列番号142、配列番号144、配列番号146、配列番号148、配列番号150、配列番号152、配列番号154、配列番号156、配列番号158、配列番号160、配列番号162、配列番号164、配列番号166、配列番号168、配列番号170、配列番号172、配列番号174、配列番号176、配列番号178、配列番号180、配列番号182、配列番号184、配列番号186、配列番号188、配列番号190、配列番号192、配列番号194、配列番号196、配列番号198、配列番号200、配列番号202、配列番号204、配列番号206、配列番号208、配列番号210、配列番号212、配列番号214、配列番号216、配列番号218、配列番号220、配列番号222、配列番号224、配列番号226、配列番号228、配列番号230、配列番号232、配列番号234、配列番号236、配列番号238、配列番号240、配列番号242およびその組み合わせからなる群から選択されるアミノ酸配列と少なくとも95%同一のL鎖可変領域配列を有し;
該Fab完全ヒト抗体断片は、配列番号1、配列番号3、配列番号5、配列番号7、配列番号9、配列番号11、配列番号13、配列番号15、配列番号17、配列番号19、配列番号21、配列番号23、配列番号25、配列番号27、配列番号29、配列番号31、配列番号33、配列番号35、配列番号37、配列番号39、配列番号41、配列番号43、配列番号45、配列番号47、配列番号49、配列番号51、配列番号53、配列番号55、配列番号57、配列番号59、配列番号61、配列番号63、配列番号65、配列番号67、配列番号69、配列番号71、配列番号73、配列番号75、配列番号77、配列番号79、配列番号81、配列番号83、配列番号85、配列番号87、配列番号89、配列番号91、配列番号93、配列番号95、配列番号97、配列番号99、配列番号101、配列番号103、配列番号105、配列番号107、配列番号109、配列番号111、配列番号113、配列番号115、配列番号117、配列番号119、配列番号121、配列番号123、配列番号125、配列番号127、配列番号129、配列番号131、配列番号133、配列番号135、配列番号137、配列番号139、配列番号141、配列番号143、配列番号145、配列番号147、配列番号149、配列番号151、配列番号153、配列番号155、配列番号157、配列番号159、配列番号161、配列番号163、配列番号165、配列番号167、配列番号169、配列番号171、配列番号173、配列番号175、配列番号177、配列番号179、配列番号181、配列番号183、配列番号185、配列番号187、配列番号189、配列番号191、配列番号193、配列番号195、配列番号197、配列番号199、配列番号201、配列番号203、配列番号205、配列番号207、配列番号209、配列番号211、配列番号213、配列番号215、配列番号217、配列番号219、配列番号221、配列番号223、配列番号225、配列番号227、配列番号229、配列番号231、配列番号233、配列番号235、配列番号237、配列番号239、配列番号241およびその組み合わせからなる群から選択されるアミノ酸配列と少なくとも95%同一であるH鎖可変領域配列を有し、
配列番号2、配列番号4、配列番号6、配列番号8、配列番号10、配列番号12、配列番号14、配列番号16、配列番号18、配列番号20、配列番号22、配列番号24、配列番号26、配列番号28、配列番号30、配列番号32、配列番号34、配列番号36、配列番号38、配列番号40、配列番号42、配列番号44、配列番号46、配列番号48、配列番号50、配列番号52、配列番号54、配列番号56、配列番号58、配列番号60、配列番号62、配列番号64、配列番号66、配列番号68、配列番号70、配列番号72、配列番号74、配列番号76、配列番号78、配列番号80、配列番号82、配列番号84、配列番号86、配列番号88、配列番号90、配列番号92、配列番号94、配列番号96、配列番号98、配列番号100、配列番号102、配列番号104、配列番号106、配列番号108、配列番号110、配列番号112、配列番号114、配列番号116、配列番号118、配列番号120、配列番号122、配列番号124、配列番号126、配列番号128、配列番号130、配列番号132、配列番号134、配列番号136、配列番号138、配列番号140、配列番号142、配列番号144、配列番号146、配列番号148、配列番号150、配列番号152、配列番号154、配列番号156、配列番号158、配列番号160、配列番号162、配列番号164、配列番号166、配列番号168、配列番号170、配列番号172、配列番号174、配列番号176、配列番号178、配列番号180、配列番号182、配列番号184、配列番号186、配列番号188、配列番号190、配列番号192、配列番号194、配列番号196、配列番号198、配列番号200、配列番号202、配列番号204、配列番号206、配列番号208、配列番号210、配列番号212、配列番号214、配列番号216、配列番号218、配列番号220、配列番号222、配列番号224、配列番号226、配列番号228、配列番号230、配列番号232、配列番号234、配列番号236、配列番号238、配列番号240、配列番号242およびその組み合わせからなる群から選択されるアミノ酸配列と少なくとも95%同一であるL鎖可変領域配列を有し;
該一本鎖ヒト抗体は、配列番号1、配列番号3、配列番号5、配列番号7、配列番号9、配列番号11、配列番号13、配列番号15、配列番号17、配列番号19、配列番号21、配列番号23、配列番号25、配列番号27、配列番号29、配列番号31、配列番号33、配列番号35、配列番号37、配列番号39、配列番号41、配列番号43、配列番号45、配列番号47、配列番号49、配列番号51、配列番号53、配列番号55、配列番号57、配列番号59、配列番号61、配列番号63、配列番号65、配列番号67、配列番号69、配列番号71、配列番号73、配列番号75、配列番号77、配列番号79、配列番号81、配列番号83、配列番号85、配列番号87、配列番号89、配列番号91、配列番号93、配列番号95、配列番号97、配列番号99、配列番号101、配列番号103、配列番号105、配列番号107、配列番号109、配列番号111、配列番号113、配列番号115、配列番号117、配列番号119、配列番号121、配列番号123、配列番号125、配列番号127、配列番号129、配列番号131、配列番号133、配列番号135、配列番号137、配列番号139、配列番号141、配列番号143、配列番号145、配列番号147、配列番号149、配列番号151、配列番号153、配列番号155、配列番号157、配列番号159、配列番号161、配列番号163、配列番号165、配列番号167、配列番号169、配列番号171、配列番号173、配列番号175、配列番号177、配列番号179、配列番号181、配列番号183、配列番号185、配列番号187、配列番号189、配列番号191、配列番号193、配列番号195、配列番号197、配列番号199、配列番号201、配列番号203、配列番号205、配列番号207、配列番号209、配列番号211、配列番号213、配列番号215、配列番号217、配列番号219、配列番号221、配列番号223、配列番号225、配列番号227、配列番号229、配列番号231、配列番号233、配列番号235、配列番号237、配列番号239、配列番号241およびその組み合わせからなる群から選択されるアミノ酸配列と少なくとも95%同一であるH鎖可変領域配列を有し、
配列番号2、配列番号4、配列番号6、配列番号8、配列番号10、配列番号12、配列番号14、配列番号16、配列番号18、配列番号20、配列番号22、配列番号24、配列番号26、配列番号28、配列番号30、配列番号32、配列番号34、配列番号36、配列番号38、配列番号40、配列番号42、配列番号44、配列番号46、配列番号48、配列番号50、配列番号52、配列番号54、配列番号56、配列番号58、配列番号60、配列番号62、配列番号64、配列番号66、配列番号68、配列番号70、配列番号72、配列番号74、配列番号76、配列番号78、配列番号80、配列番号82、配列番号84、配列番号86、配列番号88、配列番号90、配列番号92、配列番号94、配列番号96、配列番号98、配列番号100、配列番号102、配列番号104、配列番号106、配列番号108、配列番号110、配列番号112、配列番号114、配列番号116、配列番号118、配列番号120、配列番号122、配列番号124、配列番号126、配列番号128、配列番号130、配列番号132、配列番号134、配列番号136、配列番号138、配列番号140、配列番号142、配列番号144、配列番号146、配列番号148、配列番号150、配列番号152、配列番号154、配列番号156、配列番号158、配列番号160、配列番号162、配列番号164、配列番号166、配列番号168、配列番号170、配列番号172、配列番号174、配列番号176、配列番号178、配列番号180、配列番号182、配列番号184、配列番号186、配列番号188、配列番号190、配列番号192、配列番号194、配列番号196、配列番号198、配列番号200、配列番号202、配列番号204、配列番号206、配列番号208、配列番号210、配列番号212、配列番号214、配列番号216、配列番号218、配列番号220、配列番号222、配列番号224、配列番号226、配列番号228、配列番号230、配列番号232、配列番号234、配列番号236、配列番号238、配列番号240、配列番号242およびその組み合わせからなる群から選択されるアミノ酸配列と少なくとも95%同一であるL鎖可変領域配列を有する。
配列番号195/配列番号196、配列番号197/配列番号198、配列番号199/配列番号200、配列番号201/配列番号202、配列番号203/配列番号204、配列番号205/配列番号206、配列番号207/配列番号208、配列番号209/配列番号210、配列番号211/配列番号212、配列番号213/配列番号214、配列番号215/配列番号216、配列番号217/配列番号218、配列番号219/配列番号220、配列番号221/配列番号222、配列番号223/配列番号224、配列番号225/配列番号226、配列番号227/配列番号228、配列番号229/配列番号230、配列番号231/配列番号232、配列番号233/配列番号234、配列番号235/配列番号236、配列番号237/配列番号238、配列番号239/配列番号240、配列番号241/配列番号242およびその組み合わせからなる群から選択されるH鎖/L鎖可変領域配列を有する。
特定の態様において、本発明の結合ポリペプチドは、さらに、翻訳後修飾を含んでいてもよい。翻訳後の蛋白質修飾の例としては、リン酸化、アセチル化、メチル化、ADP-リボース化、ユビキチン化、グリコシル化、カルボニル化、SUMO化、ビオチン化またはポリペプチド側鎖もしくは疎水性基の付加が挙げられる。結果として、修飾された可溶ポリペプチドには、非アミノ酸エレメント、例えば脂質、多糖もしくは単糖、およびリン酸が含まれていてよい。グリコシル化の好ましい形態は、該ポリペプチドに1つ以上のシアル酸部分を結合させる、シアル酸付加である。シアル酸部分は、該蛋白質の溶解度および血清半減期を改善する一方で、免疫原性を低下させる。Raju et al. Biochemistry. 2001 31; 40(30):8868-76を参照のこと。該非アミノ酸エレメントのポリペプチドの官能性に対する影響は、そのPD−L1またはPD−1の機能に対する拮抗作用、例えば血管新生または腫瘍成長に対する阻害効果について試験してよい。
式: X--O(CH2CH2O)n-1CH2CH2OH (1)
で表され、式中で、nは20〜2300であり、XはHまたは末端修飾、例えばC1-4アルキルである。態様の一において、本発明のPEGは、一方の末端がヒドロキシまたはメトキシである、すなわち、XがHまたはCH3である(「メトキシPEG」)。PEGは、さらに、結合反応に必要な化学基を含んでいてよく; それは、該分子の化学合成により生じたものか、または;分子の距離が最適になるためのスペーサーである。さらに、該PEGは、互いに結合している1つ以上のPEG側鎖からなっていてよい。2つ以上のPEG鎖を有するPEGは、多アーム(multiarmed)または分枝PEGと呼ばれる。分枝PEGは、例えば、ポリエチレンオキシドを種々のポリオール、例えば、グリセロール、ペンタエリトリトール(pentaerythriol)およびソルビトールに添加することにより作製し得る。例えば、4分枝PEGは、ペンタエリトリトール(pentaerythriol)とエチレンオキシドから作製し得る。分枝PEGは、例えば欧州特許公開第0 473 084号および米国特許第5,932,462号に記載されている。PEGの形態の一つには、リジンの第一級アミノ基を介して結合した2PEG側鎖 (PEG2) が挙げられる(Monfardini et al., Bioconjugate Chem. 6 (1995) 62-69)。
式:--CO--(CH2)x--(OCH2CH2)m--OR
のポリ(エチレングリコール)基の1つに、該ポリ(エチレングリコール) 基の--CO (すなわちカルボニル)が、結合ポリペプチドのアミノ基の1つとアミド結合を形成するように、共有結合しており;Rは低級アルキルであり; xは2または3であり; mは約450〜約950であり; nおよびmは、結合体から結合性のポリペプチドを引いた分子量が約10〜40 kDaになるように選択される。態様の一において、結合ポリペプチドのリジンの6-アミノ基は、利用可能な (遊離の) アミノ基である。
P--NHCO--(CH2)x--(OCH2CH2)m--OR (II)
によって表され、式中、Pは本明細書に記載の結合ポリペプチドの基であり(すなわち式(II)に示すカルボニルとアミド結合を形成するアミノ基を含まない); Rは低級アルキルであり; xは2または3であり; mは約450〜約950であり、結合体から結合ポリペプチドを引いた分子量が約10〜約40kDaになるように選択される。本明細書において、「m」の特定の範囲は、配向について意味を持つ。「m」の範囲は、いずれの場合においても、PEG基の分子量によって厳密に決定される。
本発明は、PD−L1の生物活性の阻害に応答する症状の処置または前症状の予防方法を特徴づける。好ましい例は、炎症または細胞の過剰増殖により特徴づけられる症状である。投与技術および用量は、具体的なポリペプチドの種類および処置する具体的な症状によって変わるが、これは当業者によって容易に決定し得るものである。一般的に、規制当局は、治療剤として用いる蛋白質製剤は、発熱物質が許容できる程度に低いレベルになるように製剤することを要求している。したがって、一般的に治療剤は、本質的に発熱性物質を含まないか、または適当な規制当局(例えばFDA)により決定された許容されるレベル以下の発熱性物質しか含まないという点において、他の製剤と異なる。
本明細書に記載の抗PD−L1抗体と治療用ワクチンの組み合わせ治療製品または製剤は、相乗的な腫瘍治療上の利点をもたらす。例えば、本発明は、本明細書に記載の抗PD−L1抗体と、米国特許第8,222,214号に記載されている、アジュバントとしてGM-CSFを組み合わせた、HER2/neuから単離されたE75由来の9merの合成ペプチドである「Neuvax」との組合せ剤を提供し、該文献の記載内容は、引用により本明細書に包含される。さらに、本発明は、本明細書に記載の抗PD−L1抗体と、がん胎児抗原と組み合わせたカナリアポックスウイルスであるALVAC-CEAワクチンとの組合せ剤を提供する。
本明細書に記載のPD−L1結合蛋白質およびその関連する変異体は、多数の治療および診断への適用に有用である。これらには、PD−L1への結合の競合または遮断によるPD−L1の生物活性の阻害ならびに、細胞、特にPD−L1発現細胞への細胞毒性またはイメージング剤の送達が含まれる。これらの分子のサイズが小さく、構造が安定していることは、薬物の製造、急速なクリアランスが望ましい特定の適用における、体内からの急速なクリアランスまたは、適当な、またはかかる特徴を有する分子を用いて改善される新規の送達系への製剤について特に有用であり得る。
抗原結合蛋白質 (例えば、抗体、抗体断片、抗体誘導体、抗体ムテインおよび抗体変異体) は、PD−L1 (好ましくはヒトPD−L1)に結合するポリペプチドである。抗原結合蛋白質には、PD−L1の生物活性を阻害する抗原結合蛋白質が含まれる。
局面の一において、本発明は、対象の処置方法を提供する。該方法は、例えば、対象に対して一般的に健康によい影響を及ぼし得る、例えば、対象の期待寿命を延長し得る。あるいは、該方法は、例えば、疾患、障害、症状または疾病(「症状」)を処置、予防、治療、軽減または改善し得る。処置する症状には、PD−L1の不適当な発現または活性に特徴づけられる症状が含まれる。かかる症状には、発現または活性のレベルが高すぎるものがあり、処置には本明細書に記載するPD−L1拮抗剤を投与することが含まれる。該障害または症状はがんと関連するものである。特に、それらのがんには、肺がん、卵巣がんおよび結腸がんおよび種々の骨髄腫が含まれるが、これらに限定されるものではない。
本明細書に記載の特定の方法には、PD−L1結合性の抗原結合蛋白質を対象に投与し、それにより、PD−L1誘発性の、特定の症状において機能する生物応答を低下させることが含まれる。特定の態様において、本発明の方法は、内在性のPD−L1をPD−L1 結合性の抗原結合蛋白質と、例えば対象への投与または生体外手法により接触させることを含む。
他の局面において、本発明は、PD−L1阻害性抗原結合蛋白質と1種以上の他の処置を用いて対象を処置する方法を提供する。態様の一において、かかる組み合わせ療法により、例えば、腫瘍中の複数の部位または複数の標的を攻撃することにより、相乗効果または相加効果が達成される。本発明に用い得る組み合わせ療法の種類としては、標的細胞および標的組織内の複数の種類の細胞において、単一の疾患関連性経路、複数の経路の複数のノードを阻害または(適当であれば)活性化することが挙げられる。
この実施例は、ヒトリンパ球に発現するヒトPD−L1に結合する、本明細書に記載する抗PD−L1抗体の特徴を示す。ヒト末梢血単核球を、抗CD3とともに3日間培養して活性化させ、PD−L1の発現を促進した。結合は、該活性化リンパ球に連続希釈した該抗体を添加することにより評価した。洗浄後、フィコエリトリン標識抗ヒトIg試薬による染色の後に、FACS Aria (Becton Dickinson, San Jose, CA)を用いた解析を行って結合を検出した。抗ヒトIgGは、Bリンパ球上の免疫グロブリンと反応するため、細胞を、抗ヒトCD19 APC-Cy5試薬を用いて共染色した。データは、CD19陰性のリンパ球をゲーティングすることにより得、結果は図1に示す。H6抗体およびH10抗体はともに、100pMの範囲のEC50で、強力な結合活性を示す。
この実施例により、本明細書に記載する抗PD−L1抗体のヒトリンパ球への結合の結果を示す。抗PD−L1抗体を、非活性化リンパ球への結合について評価した。末梢血単核球を、抗PD−L1抗体 (1μg/ml)とともにインキュベーションした後、洗浄した。抗PD−L1抗体の結合を、フィコエリトリン結合型ヒトIg試薬を用いて染色して検出した。染色された集団を特定するため、細胞を抗CD3 FITCまたは抗CD56 APC試薬で共染色した。抗ヒトIg試薬は、Bリンパ球上の免疫グロブリンと反応するため、細胞を、抗ヒトCD19 APC-Cy5試薬でも染色した。図2に示すデータは、FACSAria (Becton Dickinson, San Jose, CA)を用いて、続けて解析したCD19陰性リンパ球より得られたものである。結果は、CD56陽性NK細胞は、抗PD−L1抗体と反応するが、CD3+T細胞は反応しないことを示す。
この実施例により、本明細書に記載する抗PD−L1抗体が、リンパ球の増殖に対して及ぼす影響を示す。抗PD−L1抗体を、刺激に対するリンパ球の応答の調節能について評価した。抗PD−L1抗体であるH1、H6およびH10を10μg/mlにて、蛍光色素カルボキシフルオセイン(CFSE)で標識し、抗CD3(1ng/ml)で刺激した末梢血単核球の培養物に添加した。3日間培養した後、FACS Aria (Becton Dickinson, San Jose, CA)を用いたフローサイトメトリーにより、増殖活性について該細胞を評価した。図3に示す結果により、抗PD−L1抗体が、リンパ球の増殖を阻害したことが示される。
この実施例により、NK細胞の、本明細書に記載する抗PD−L1抗体が介在する細胞増殖阻害についての影響を示す。優先的にNK細胞への結合を示す抗PD−L1抗体を用いて、増殖阻害におけるこのことの意義を試験した。FACS Aria (Becton Dickinson, Dan Jose, CA)を用いたセルソーティングにより、精製したCD4+、CD8+、CD56+ (NK)および単球の集団を得た。基本の培養として、1.5 x 105個のCD4+細胞と3 x 104個の単球を、抗PD−L1抗体H10(10μg/ml)を添加して、または添加せずに抗CD3 (1 ng/ml)で刺激した。別々の培養において、CD8+細胞またはNK細胞 (ともに3 x 104個)を、この基本培養物に添加した。3日間培養した後、フローサイトメトリーにより測定するリンパ球活性化の指標として、CD25の発現について細胞染色を行った。図4に示す結果を、分画していない全PBMC (1.5 x 105個)と比較した。抗PD−L1抗体は、全PBMCを含む培養物中およびNK細胞を添加した培養物のリンパ球の活性を阻害したが、NK細胞が存在しない場合は阻害しなかった。
この実施例により、抗PD−L1のNK細胞活性化への影響を示す。本明細書に記載する抗PD−L1抗体を、リンパ球の活性化促進能について評価した。末梢血単核細胞またはセルソーティングにより単離したリンパ球サブセットの単離集団を、抗PD−L1抗体(10μg/ml)の存在下もしくは非存在下にて、IL-2 (100 U/ml) を添加して培養した。5日間培養した後、細胞の活性化の指標としてCD25の発現について細胞を染色し、フローサイトメトリーによって解析した。図5に示す結果により、H6およびH10が、細胞の活性化を亢進し、応答性のリンパ球集団がNK細胞であることが示される。
この実施例により、本明細書に記載する抗PD−L1抗体の、多発性硬化症(MS)のマウスモデルにおける、疾患の進行に対する影響を示す。抗PD−L1抗体を、MSのモデルとして実験的自己免疫性脳炎(EAE) を発症するように誘導したマウスの疾患の過程の調節能について評価した。疾患の誘導は、C57Bl/6マウスにおいて、ミエリンオリゴデンドロサイト糖蛋白質(MOG) ペプチドおよび百日咳毒素の注射により行った。疾患の症候が見られるようになると、該マウスに対して、1日おきに抗PD−L1抗体(0.1mg)の腹腔内注射を行った。図6より、抗PD−L1抗体H6およびH10は、いずれも、疾患の発症過程に影響を及ぼし、H6は疾患の重症度を大きく低下させたことが示される。
この実施例により、本明細書に記載する抗PD−L1抗体G12の特徴付けを示す。標準的なNHS/EDCカップリング方法を用いて、rhPD−L1をCM5センサーチップに固定した。全ての測定を、HBS-EPバッファー中で、流速30μL/分にて行った。抗体の濃度を連続的に希釈した。該データに当てはめるのに、1:1 (ラングミュア) 結合モデルを用いた。
この実施例により、G12が、rhPD-1とrhPD−L1間の相互作用を遮断することを示す実験の結果を示す。96ウェル ELISAプレートを、PD1/His 1ng/μLで4℃にて一晩コーティングした後、PBS中のカゼインでブロッキングを行った。2倍に連続希釈したIgG (20μg/mlから開始)20μlと0.25μl/ml PD−L1/Fc 20μlを予め混合し、該混合物を30分間インキュベーションした。該プレートをPBS-Tween (PBST) で3回洗浄した。該混合物25μlをELISAプレートに移し、振盪しながら30分間インキュベーションした。PBSTで3回洗浄した。HRP結合型ヤギ抗ヒトFc (カゼイン中1:500)を添加し、基質としてTMBを使用して30分間発色させた。2M H2SO4 を添加して反応を停止した。ODを450nmにて読み取った。
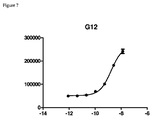
この実施例により、CHO細胞の表面に発現するヒトPD−L1に対するG12の結合についての試験管内EC50データを示す。この実施例により、細胞結合の最大化という観点による、この抗体の結合特性および50%結合飽和 (EC50)が達成される濃度が示される。この実施例における実験手法は以下の通りである: 50,000個のCHO-PD−L1細胞を、v底の96ウェルプレートのウェル中に、 FACSバッファー (PBS + 2% FBS) 100μl中にて一定量入れた。図7に示す濃度を含む、抗体の希釈曲線をFACSバッファー中で作製した。細胞をスピンダウンし、FACSバッファーで1回洗浄した後、抗体溶液25μlでの再懸濁を3つ組みで行った。0.5時間インキュベーションした後、細胞をFACSバッファーで1回洗浄し、PE結合型のヤギ抗ヒトIgG (γ鎖特異的) 二次抗体 (Southern Biotech カタログ番号2040-09) 50μlで再懸濁した。細胞をさらに0.5時間インキュベーションした後、FACSバッファーで1回洗浄した。細胞をFACSバッファー25μl中で再懸濁した後、FL2-Hチャンネルの蛍光強度中央値(MFI: median fluorescence intensity)を、Intellicyt HTFCフローサイトメーターを用いて決定した。
この実施例により、組み換えヒトPD-1 (PD-1-Fcキメラ; Sino Biologics) およびCHO細胞に発現するヒトPD−L1の間の相互作用の、抗PD−L1抗体G12による遮断についての試験管内IC50データを示す。ここで、PD−L1を発現するCHO細胞を、rhPD-1-Fcキメラ蛋白質を添加する前にG12と共インキュベーションした。インキュベーションして洗浄した後、細胞の表面に発現したPD−L1へのPD-1の結合を、Alexa-Fluor 647タグ化抗PD-1抗体を用いて、フローサイトメトリー(Intellicyt HTFC; FL-4H)により検出した。この実施例により、抗PD−L1モノクローナル抗体G12が、CHO細胞の表面上に発現しているPD−L1へのPD-1の結合を効率的に阻害することができたことを示している。
この実施例により、ES-2ヒト卵巣がん細胞の表面に発現するPD−L1へのG12の結合についての試験管内EC50データを示す。この実施例により、細胞結合の最大化という点についての抗体の結合特性および50% 結合飽和 (EC50)が達成される濃度が示される。この実施例において、実験手法は以下の通りである:ES−2細胞を、IFNγ500IU/mlで18時間処理して、PD−L1のレベルをベースの発現より上昇させた。誘導後、50,000個のES−2細胞をv底96プレートのウェルに、FACS Buffer (PBS + 2% FBS) 100μl中にて一定量入れた。図9に示す濃度を含む、抗体の希釈曲線を、FACSバッファー中で作製した。細胞をスピンダウンし、FACSバッファーで1回洗浄した後、3つ組みで抗体溶液25μl中に再懸濁した。0.5時間インキュベーションした後、細胞をFACSバッファーで1回洗浄し、PE結合型ヤギ抗ヒトIgG (γ鎖特異的)二次抗体(Southern Biotech カタログ番号2040-09) 50μlで再懸濁した。細胞をさらに0.5時間インキュベーションした後、FACSバッファーで1回洗浄した。細胞をFACSバッファー25μlで再懸濁し、Intellicyt HTFCフローサイトメーターを用いてFL2-HチャンネルのMFIを決定した。
この実施例により、リンパ球エフェクター細胞中のリンパ球の活性に対する抗体の影響を評価するための混合リンパ球反応(MLR) を示す。抗PD−L1ヒトモノクローナル抗体の存在下または非存在下にて、IL-2分泌を測定した (図10)。抗体の機能的な活性を、精製CD4+Tリンパ球と、同種の樹状細胞からなる混合リンパ球反応(MLR) にて評価した。本明細書に記載する抗体G12抗体を用い、以前に開示されていた抗体配列からの自家作製により得られた、開示されている抗体10A5および12A4 (Bristol-Myers/Medarex) (米国特許出願第2009/0055944号、当該文献の内容は引用により本明細書中に包含される)と比較した。樹状細胞を調製するために、不連続パーコール勾配を用いて精製した単球を、GM-CSF (1,000U/ml)とIL−4 (500U/ml) を添加して7日間培養した。CD4+細胞は、CD8、CD16、CD19およびCD20に対して応答を示すビオチン化抗体を用いてネガティブセレクションにより調製した。応答性の細胞の除去は、ビオチン結合磁気ビーズを用いて達成した。抗体を、表記する濃度にて、カルボキシフルオセイン(CFSE)標識した105個のCD4+細胞と104個の樹状細胞を含むウェルに添加した。5日間培養した後、サイトカイン定量用に上清を回収した。
この実施例により、抗PD−L1抗体によるPD−L1/PD−1経路の遮断の、リンパ球エフェクター細胞に対する影響を示すために用いた、混合リンパ球反応(MLR) を示す。T細胞の活性化は、抗PD−L1ヒトモノクローナル抗体の存在下もしくは非存在下にて測定した(図12)。抗体の機能性活性を、精製CD4+Tリンパ球と同種樹状細胞からなる同種混合リンパ球反応(MLR) にて評価した。本明細書に記載する抗体 H6B1L、RSA1、RA3、RC5、SH1E2、SH1E4、SH1B11およびSH1C8を用い、以前に開示されている抗体配列からの自家作製により得られた、開示されている抗体である10A5 (Bristol-Myers-Squibb/Medarex) およびYW243.55S70 (Roche/Genentech) (米国特許出願第2009/0055944号および第2010/0203056号; 当該文献の内容は引用により本明細書中に包含される)と比較した。樹状細胞を調製するために、不連続パーコール勾配を用いて精製した単球を、GM-CSF (1,000 U/ml)およびIL−4 (500 U/ml)を添加して7日間培養した。CD4+細胞は、CD8、CD16、CD19およびCD20に対して応答を示すビオチン化抗体を用いて、ネガティブセレクションにより調製した。応答性の細胞の除去は、ビオチン結合磁気ビーズを用いて達成した。抗体を表記する濃度にて、105個のカルボキシフルオレセイン(CFSE)標識したCD4+細胞と104個の樹状細胞を含むウェルに添加した。5日間培養した後、細胞を回収し、細胞活性化の指標としてCD25発現について染色した。細胞の活性化をフローサイトメトリーにより測定した。
抗PD−L1抗体の免疫応答の調節能を、混合リンパ球反応(MLR)を用いて評価した。このアッセイにおいて、抗PD−L1抗体の細胞の活性化およびIL−2産生に対する影響を測定した。MLRは、一人のドナー由来の105個の精製ヒトCD4+細胞を、他のドナーから調製した104個の単球由来の樹状細胞とともに培養することにより行った。樹状細胞の調製のために、単離した単球を、GM-CSF (1,000U/ml) とIL−4 (500 U/ml) とともに7日間培養した。特にことわらない限り、抗PD−L1抗体または対照抗体を同種MLR培養物に10μg/mlにて添加した。市販のELISAキット(Biolegend)を用いてIL−2を測定するために、3日目および5日目に上清を回収できるように、プレートを並行して準備した。抗体は、本明細書に記載する抗体H6B1L、RSA1、RA3、RC5、SH1E2、SH1E4、SH1B11およびSH1C8を用い、以前に開示されている抗体配列から自家作製された、開示されている抗体である10A5 (Bristol-Myers-Squibb/Medarex) およびYW243.55S70 (Roche/Genentech) (米国特許出願第2009/0055944 号および第2010/0203056号; 当該文献の内容は引用により本明細書中に包含される)と比較した。
この実施例により、抗PD−L1抗体によるPD−L1/PD−1経路の遮断の、リンパ球エフェクター細胞に対する影響を示すための混合リンパ球反応(MLR)を示す。IFN−γ分泌を、抗PD−L1ヒトモノクローナル抗体の存在下もしくは非存在下にて測定した (図11)。該抗体の機能的な活性は、精製したCD4+Tリンパ球と同種の樹状細胞からなる同種の混合リンパ球反応(MLR) にて評価した。本明細書に開示する抗体H6B1L、RSA1、RA3、RC5、SH1E2、SH1E4、SH1B11およびSH1C8を用い、以前に開示されていた抗体配列から自家作製された、開示されている抗体である10A5 (Bristol-Myers-Squibb/Medarex) およびYW243.55S70 (Roche/Genentech) (米国特許出願第2009/0055944号および第2010/0203056号; 当該文献の内容は引用により本明細書中に包含される)と比較した。
Claims (13)
- PD−L1エピトープに、少なくとも10-6Mの結合親和性にて結合するIgGクラスの完全ヒト抗体であって、配列番号1、配列番号3、配列番号5、配列番号7、配列番号9、配列番号11、配列番号13、配列番号15、配列番号17、配列番号19、配列番号21、配列番号23、配列番号25、配列番号27、配列番号29、配列番号31、配列番号33、配列番号35、配列番号37、配列番号39、配列番号41、配列番号43、配列番号45、配列番号47、配列番号49、配列番号51、配列番号53、配列番号55、配列番号57、配列番号59、配列番号61、配列番号63、配列番号65、配列番号67、配列番号69、配列番号71、配列番号73、配列番号75、配列番号77、配列番号79、配列番号81、配列番号83、配列番号85、配列番号87、配列番号89、配列番号91、配列番号93、配列番号95、配列番号97、配列番号99、配列番号101、配列番号103、配列番号105、配列番号107、配列番号109、配列番号111、配列番号113、配列番号115、配列番号117、配列番号119、配列番号121、配列番号123、配列番号125、配列番号127、配列番号129、配列番号131、配列番号133、配列番号135、配列番号137、配列番号139、配列番号141、配列番号143、配列番号145、配列番号147、配列番号149、配列番号151、配列番号153、配列番号155、配列番号157、配列番号159、配列番号161、配列番号163、配列番号165、配列番号167、配列番号169、配列番号171、配列番号173、配列番号175、配列番号177、配列番号179、配列番号181、配列番号183、配列番号185、配列番号187、配列番号189、配列番号191、配列番号193、配列番号195、配列番号197、配列番号199、配列番号201、配列番号203、配列番号205、配列番号207、配列番号209、配列番号211、配列番号213、配列番号215、配列番号217、配列番号219、配列番号221、配列番号223、配列番号225、配列番号227、配列番号229、配列番号231、配列番号233、配列番号235、配列番号237、配列番号239、配列番号241およびその組み合わせからなる群から選択されるアミノ酸配列と少なくとも95%同一であるH鎖可変領域配列を有し、
配列番号2、配列番号4、配列番号6、配列番号8、配列番号10、配列番号12、配列番号14、配列番号16、配列番号18、配列番号20、配列番号22、配列番号24、配列番号26、配列番号28、配列番号30、配列番号32、配列番号34、配列番号36、配列番号38、配列番号40、配列番号42、配列番号44、配列番号46、配列番号48、配列番号50、配列番号52、配列番号54、配列番号56、配列番号58、配列番号60、配列番号62、配列番号64、配列番号66、配列番号68、配列番号70、配列番号72、配列番号74、配列番号76、配列番号78、配列番号80、配列番号82、配列番号84、配列番号86、配列番号88、配列番号90、配列番号92、配列番号94、配列番号96、配列番号98、配列番号100、配列番号102、配列番号104、配列番号106、配列番号108、配列番号110、配列番号112、配列番号114、配列番号116、配列番号118、配列番号120、配列番号122、配列番号124、配列番号126、配列番号128、配列番号130、配列番号132、配列番号134、配列番号136、配列番号138、配列番号140、配列番号142、配列番号144、配列番号146、配列番号148、配列番号150、配列番号152、配列番号154、配列番号156、配列番号158、配列番号160、配列番号162、配列番号164、配列番号166、配列番号168、配列番号170、配列番号172、配列番号174、配列番号176、配列番号178、配列番号180、配列番号182、配列番号184、配列番号186、配列番号188、配列番号190、配列番号192、配列番号194、配列番号196、配列番号198、配列番号200、配列番号202、配列番号204、配列番号206、配列番号208、配列番号210、配列番号212、配列番号214、配列番号216、配列番号218、配列番号220、配列番号222、配列番号224、配列番号226、配列番号228、配列番号230、配列番号232、配列番号234、配列番号236、配列番号238、配列番号240、配列番号242およびその組み合わせからなる群から選択されるアミノ酸配列と少なくとも95%同一であるL鎖可変領域配列を有する、完全ヒト抗体。 - 請求項1に記載の完全ヒト抗体であって、配列番号1/配列番号2 (E6と称する)、配列番号3/配列番号4 (E7と称する)、配列番号5/配列番号6 (E9と称する)、配列番号7/配列番号8 (E11と称する)、配列番号9/配列番号10 (F1と称する)、配列番号11/配列番号12 (F4と称する)、配列番号13/配列番号14 (F7と称する)、配列番号15/配列番号16 (F8と称する)、配列番号17/配列番号18 (F11と称する)、配列番号19/配列番号20 (G4と称する)、配列番号21/配列番号22 (G9と称する)、配列番号23/配列番号24 (G11と称する)、配列番号25/配列番号26 (G12と称する)、配列番号27/配列番号28 (H1と称する)、配列番号29/配列番号30 (H3と称する)、配列番号31/配列番号32 (H4と称する)、配列番号33/配列番号34 (H5と称する)、配列番号35/配列番号36 (H6と称する)、配列番号37/配列番号38 (H10と称する)、配列番号39/配列番号40 (H12と称する)、配列番号41/配列番号42 (PDL−D2と称する)、配列番号43/配列番号44 (PDL−D11と称する)、配列番号45/配列番号46 (PDL−H1と称する)、配列番号47/配列番号48 (RB4と称する)、配列番号49/配列番号50 (RB11と称する)、配列番号51/配列番号52 (RC5と称する)、配列番号53/配列番号54 (RF5と称する)、配列番号55/配列番号56 (RG9と称する)、配列番号57/配列番号58 (RD1と称する)、配列番号59/配列番号60 (RF11と称する)、配列番号61/配列番号62 (RH11と称する)、配列番号63/配列番号64 (RD9と称する)、配列番号65/配列番号66 (RE10と称する)、配列番号67/配列番号68 (RA3と称する)、配列番号69/配列番号70 (RG1と称する)、配列番号71/配列番号72 (RB1と称する)、配列番号73/配列番号74 (RG7と称する)、配列番号75/配列番号76 (RA6と称する)、配列番号77/配列番号78 (RA8と称する)、配列番号79/配列番号80 (RA9と称する)、配列番号81/配列番号82 (RB5と称する)、配列番号83/配列番号84 (RB8と称する)、配列番号85/配列番号86 (RC8と称する)、配列番号87/配列番号88 (RC10と称する)、配列番号89/配列番号90 (RD2と称する)、配列番号91/配列番号92 (RE8と称する)、配列番号93/配列番号94 (RE9と称する)、配列番号95/配列番号96 (RG12と称する)、配列番号97/配列番号98 (RSA1と称する)、配列番号99/配列番号100 (R2A7と称する)、配列番号101/配列番号102 (R2B12と称する)、配列番号103/配列番号104 (R2C9と称する)、配列番号105/配列番号106 (R2D5と称する)、配列番号107/配列番号108 (R2D7と称する)、配列番号109/配列番号110 (R2F4と称する)、配列番号111/配列番号112 (R2A10と称する)、配列番号113/配列番号114 (R2E2と称する)、配列番号115/配列番号116 (R3B8と称する)、配列番号117/配列番号118 (R3C3と称する)、配列番号119/配列番号120 (R3E9と称する)、配列番号121/配列番号122 (R3E10と称する)、配列番号123/配列番号124 (R3F7と称する)、配列番号125/配列番号126 (R3F10と称する)、配列番号127/配列番号128 (R4B10と称する)、配列番号129/配列番号130 (R4H1と称する)、配列番号131/配列番号132 (R4A11と称する)、配列番号133/配列番号134 (R3D2と称する)、配列番号135/配列番号136 (R5B8と称する)、配列番号137/配列番号138 (SH1A1Qと称する)、配列番号139/配列番号140 (SH1B7B(K)と称する)、配列番号141/配列番号142 (SH1C1と称する)、配列番号143/配列番号144 (SH1C8と称する)、配列番号145/配列番号146 (SH1E10と称する)、配列番号147/配列番号148 (SH1E2と称する)、配列番号149/配列番号150 (SH1A9と称する)、配列番号151/配列番号152 (SH1B11と称する)、配列番号153/配列番号154 (SH1E4と称する)、配列番号155/配列番号156 (SH1B3と称する)、配列番号157/配列番号158 (SH1D1と称する)、配列番号159/配列番号160 (SH1D2と称する)、配列番号161/配列番号162 (SH1D12と称する)、配列番号163/配列番号164 (SH1E1と称する)、配列番号165/配列番号166 (SH1G9と称する)、配列番号167/配列番号168 (SH1A11と称する)、配列番号169/配列番号170 (SH1C2と称する)、配列番号171/配列番号172 (SH1G8と称する)、配列番号173/配列番号174 (SH1H2と称する)、配列番号175/配列番号176 (SH1B10と称する)、配列番号177/配列番号178 (SH1B7A(L)と称する)、配列番号179/配列番号180 (SH1E6と称する)、配列番号181/配列番号182 (SH1C11と称する)、配列番号183/配列番号184 (SH1A2と称する)、配列番号185/配列番号186 (SH1B1と称する)、配列番号187/配列番号188 (R6B2と称する)、配列番号189/配列番号190 (R6B7と称する)、配列番号191/配列番号192 (R6B11と称する)、配列番号193/配列番号194 (R6D1と称する)、配列番号195/配列番号196 (R6C8と称する)、配列番号197/配列番号198 (R9G8と称する)、配列番号199/配列番号200 (R7D1と称する)、配列番号201/配列番号202 (R7D2と称する)、配列番号203/配列番号204 (R7E7と称する)、配列番号205/配列番号206 (R7F2と称する)、配列番号207/配列番号208 (R7F7と称する)、配列番号209/配列番号210 (R9H2と称する)、配列番号211/配列番号212 (R9H6と称する)、配列番号213/配列番号214 (H6B1Lと称する)、配列番号215/配列番号216 (H6A1と称する)、配列番号217/配列番号218 (H6B1と称する)、配列番号219/配列番号220 (H6B2と称する)、配列番号221/配列番号222 (H19Cと称する)、配列番号223/配列番号224 (H110Dと称する)、配列番号225/配列番号226 (H11Fと称する)、配列番号227/配列番号228 (H1C1と称する)、配列番号229/配列番号230 (GPG1A2と称する)、配列番号231/配列番号232 (GPGG8と称する)、配列番号233/配列番号234 (GPGG10と称する)、配列番号235/配列番号236 (GPGH7と称する)、配列番号237/配列番号238 (GPGH10と称する)、配列番号239/配列番号240 (GPGH11と称する)、配列番号241/配列番号242 (GPGH10Pと称する)およびその組み合わせからなる群から選択される、H鎖/L鎖可変領域配列を有する、完全ヒト抗体。
- H鎖由来の可変領域とL鎖由来の可変領域配列を有するFab完全ヒト抗体断片であって、配列番号1、配列番号3、配列番号5、配列番号7、配列番号9、配列番号11、配列番号13、配列番号15、配列番号17、配列番号19、配列番号21、配列番号23、配列番号25、配列番号27、配列番号29、配列番号31、配列番号33、配列番号35、配列番号37、配列番号39、配列番号41、配列番号43、配列番号45、配列番号47、配列番号49、配列番号51、配列番号53、配列番号55、配列番号57、配列番号59、配列番号61、配列番号63、配列番号65、配列番号67、配列番号69、配列番号71、配列番号73、配列番号75、配列番号77、配列番号79、配列番号81、配列番号83、配列番号85、配列番号87、配列番号89、配列番号91、配列番号93、配列番号95、配列番号97、配列番号99、配列番号101、配列番号103、配列番号105、配列番号107、配列番号109、配列番号111、配列番号113、配列番号115、配列番号117、配列番号119、配列番号121、配列番号123、配列番号125、配列番号127、配列番号129、配列番号131、配列番号133、配列番号135、配列番号137、配列番号139、配列番号141、配列番号143、配列番号145、配列番号147、配列番号149、配列番号151、配列番号153、配列番号155、配列番号157、配列番号159、配列番号161、配列番号163、配列番号165、配列番号167、配列番号169、配列番号171、配列番号173、配列番号175、配列番号177、配列番号179、配列番号181、配列番号183、配列番号185、配列番号187、配列番号189、配列番号191、配列番号193、配列番号195、配列番号197、配列番号199、配列番号201、配列番号203、配列番号205、配列番号207、配列番号209、配列番号211、配列番号213、配列番号215、配列番号217、配列番号219、配列番号221、配列番号223、配列番号225、配列番号227、配列番号229、配列番号231、配列番号233、配列番号235、配列番号237、配列番号239、配列番号241およびその組み合わせからなる群から選択されるアミノ酸配列と少なくとも95%同一であるH鎖可変領域配列を有し、
配列番号2、配列番号4、配列番号6、配列番号8、配列番号10、配列番号12、配列番号14、配列番号16、配列番号18、配列番号20、配列番号22、配列番号24、配列番号26、配列番号28、配列番号30、配列番号32、配列番号34、配列番号36、配列番号38、配列番号40、配列番号42、配列番号44、配列番号46、配列番号48、配列番号50、配列番号52、配列番号54、配列番号56、配列番号58、配列番号60、配列番号62、配列番号64、配列番号66、配列番号68、配列番号70、配列番号72、配列番号74、配列番号76、配列番号78、配列番号80、配列番号82、配列番号84、配列番号86、配列番号88、配列番号90、配列番号92、配列番号94、配列番号96、配列番号98、配列番号100、配列番号102、配列番号104、配列番号106、配列番号108、配列番号110、配列番号112、配列番号114、配列番号116、配列番号118、配列番号120、配列番号122、配列番号124、配列番号126、配列番号128、配列番号130、配列番号132、配列番号134、配列番号136、配列番号138、配列番号140、配列番号142、配列番号144、配列番号146、配列番号148、配列番号150、配列番号152、配列番号154、配列番号156、配列番号158、配列番号160、配列番号162、配列番号164、配列番号166、配列番号168、配列番号170、配列番号172、配列番号174、配列番号176、配列番号178、配列番号180、配列番号182、配列番号184、配列番号186、配列番号188、配列番号190、配列番号192、配列番号194、配列番号196、配列番号198、配列番号200、配列番号202、配列番号204、配列番号206、配列番号208、配列番号210、配列番号212、配列番号214、配列番号216、配列番号218、配列番号220、配列番号222、配列番号224、配列番号226、配列番号228、配列番号230、配列番号232、配列番号234、配列番号236、配列番号238、配列番号240、配列番号242およびその組み合わせからなる群から選択されるアミノ酸配列と少なくとも95%同一であるL鎖可変領域配列を有する、Fab完全ヒト抗体断片。 - 請求項3記載の完全ヒト抗体Fab断片であって、該抗体が、配列番号1/配列番号2、配列番号3/配列番号4、配列番号5/配列番号6、配列番号7/配列番号8、配列番号9/配列番号10、配列番号11/配列番号12、配列番号13/配列番号14、配列番号15/配列番号16、配列番号17/配列番号18、配列番号19/配列番号20、配列番号21/配列番号22、配列番号23/配列番号24、配列番号25/配列番号26、配列番号27/配列番号28、配列番号29/配列番号30、配列番号31/配列番号32、配列番号33/配列番号34、配列番号35/配列番号36、配列番号37/配列番号38、配列番号39/配列番号40、配列番号41/配列番号42、配列番号43/配列番号44、配列番号45/配列番号46、配列番号47/配列番号48、配列番号49/配列番号50、配列番号51/配列番号52、配列番号53/配列番号54、配列番号55/配列番号56、配列番号57/配列番号58、配列番号59/配列番号60、配列番号61/配列番号62、配列番号63/配列番号64、配列番号65/配列番号66、配列番号67/配列番号68、配列番号69/配列番号70、配列番号71/配列番号72、配列番号73/配列番号74、配列番号75/配列番号76、配列番号77/配列番号78、配列番号79/配列番号80、配列番号81/配列番号82、配列番号83/配列番号84、配列番号85/配列番号86、配列番号87/配列番号88、配列番号89/配列番号90、配列番号91/配列番号92、配列番号93/配列番号94、配列番号95/配列番号96、配列番号97/配列番号98、配列番号99/配列番号100、配列番号101/配列番号102、配列番号103/配列番号104、配列番号105/配列番号106、配列番号107/配列番号108、配列番号109/配列番号110、配列番号111/配列番号112、配列番号113/配列番号114、配列番号115/配列番号116、配列番号117/配列番号118、配列番号119/配列番号120、配列番号121/配列番号122、配列番号123/配列番号124、配列番号125/配列番号126、配列番号127/配列番号128、配列番号129/配列番号130、配列番号131/配列番号132、配列番号133/配列番号134、配列番号135/配列番号136、配列番号137/配列番号138、配列番号139/配列番号140、配列番号141/配列番号142、配列番号143/配列番号144、配列番号145/配列番号146、配列番号147/配列番号148、配列番号149/配列番号150、配列番号151/配列番号152、配列番号153/配列番号154、配列番号155/配列番号156、配列番号157/配列番号158、配列番号159/配列番号160、配列番号161/配列番号162、配列番号163/配列番号164、配列番号165/配列番号166、配列番号167/配列番号168、配列番号169/配列番号170、配列番号171/配列番号172、配列番号173/配列番号174、配列番号175/配列番号176、配列番号177/配列番号178、配列番号179/配列番号180、配列番号181/配列番号182、配列番号183/配列番号184、配列番号185/配列番号186、配列番号187/配列番号188、配列番号189/配列番号190、配列番号191/配列番号192、配列番号193/配列番号194、配列番号195/配列番号196、配列番号197/配列番号198、配列番号199/配列番号200、配列番号201/配列番号202、配列番号203/配列番号204、配列番号205/配列番号206、配列番号207/配列番号208、配列番号209/配列番号210、配列番号211/配列番号212、配列番号213/配列番号214、配列番号215/配列番号216、配列番号217/配列番号218、配列番号219/配列番号220、配列番号221/配列番号222、配列番号223/配列番号224、配列番号225/配列番号226、配列番号227/配列番号228、配列番号229/配列番号230、配列番号231/配列番号232、配列番号233/配列番号234、配列番号235/配列番号236、配列番号237/配列番号238、配列番号239/配列番号240、配列番号241/配列番号242およびその組み合わせからなる群から選択されるH鎖/L鎖可変領域配列を有する、完全ヒト抗体Fab断片。
- H鎖由来の可変領域とL鎖由来の可変領域およびH鎖とL鎖の可変領域配列をつなぐペプチドリンカーを有する一本鎖ヒト抗体であって、配列番号1、配列番号3、配列番号5、配列番号7、配列番号9、配列番号11、配列番号13、配列番号15、配列番号17、配列番号19、配列番号21、配列番号23、配列番号25、配列番号27、配列番号29、配列番号31、配列番号33、配列番号35、配列番号37、配列番号39、配列番号41、配列番号43、配列番号45、配列番号47、配列番号49、配列番号51、配列番号53、配列番号55、配列番号57、配列番号59、配列番号61、配列番号63、配列番号65、配列番号67、配列番号69、配列番号71、配列番号73、配列番号75、配列番号77、配列番号79、配列番号81、配列番号83、配列番号85、配列番号87、配列番号89、配列番号91、配列番号93、配列番号95、配列番号97、配列番号99、配列番号101、配列番号103、配列番号105、配列番号107、配列番号109、配列番号111、配列番号113、配列番号115、配列番号117、配列番号119、配列番号121、配列番号123、配列番号125、配列番号127、配列番号129、配列番号131、配列番号133、配列番号135、配列番号137、配列番号139、配列番号141、配列番号143、配列番号145、配列番号147、配列番号149、配列番号151、配列番号153、配列番号155、配列番号157、配列番号159、配列番号161、配列番号163、配列番号165、配列番号167、配列番号169、配列番号171、配列番号173、配列番号175、配列番号177、配列番号179、配列番号181、配列番号183、配列番号185、配列番号187、配列番号189、配列番号191、配列番号193、配列番号195、配列番号197、配列番号199、配列番号201、配列番号203、配列番号205、配列番号207、配列番号209、配列番号211、配列番号213、配列番号215、配列番号217、配列番号219、配列番号221、配列番号223、配列番号225、配列番号227、配列番号229、配列番号231、配列番号233、配列番号235、配列番号237、配列番号239、配列番号241およびその組み合わせからなる群から選択されるアミノ酸配列と少なくとも95%同一であるH鎖可変領域配列を有し、
配列番号2、配列番号4、配列番号6、配列番号8、配列番号10、配列番号12、配列番号14、配列番号16、配列番号18、配列番号20、配列番号22、配列番号24、配列番号26、配列番号28、配列番号30、配列番号32、配列番号34、配列番号36、配列番号38、配列番号40、配列番号42、配列番号44、配列番号46、配列番号48、配列番号50、配列番号52、配列番号54、配列番号56、配列番号58、配列番号60、配列番号62、配列番号64、配列番号66、配列番号68、配列番号70、配列番号72、配列番号74、配列番号76、配列番号78、配列番号80、配列番号82、配列番号84、配列番号86、配列番号88、配列番号90、配列番号92、配列番号94、配列番号96、配列番号98、配列番号100、配列番号102、配列番号104、配列番号106、配列番号108、配列番号110、配列番号112、配列番号114、配列番号116、配列番号118、配列番号120、配列番号122、配列番号124、配列番号126、配列番号128、配列番号130、配列番号132、配列番号134、配列番号136、配列番号138、配列番号140、配列番号142、配列番号144、配列番号146、配列番号148、配列番号150、配列番号152、配列番号154、配列番号156、配列番号158、配列番号160、配列番号162、配列番号164、配列番号166、配列番号168、配列番号170、配列番号172、配列番号174、配列番号176、配列番号178、配列番号180、配列番号182、配列番号184、配列番号186、配列番号188、配列番号190、配列番号192、配列番号194、配列番号196、配列番号198、配列番号200、配列番号202、配列番号204、配列番号206、配列番号208、配列番号210、配列番号212、配列番号214、配列番号216、配列番号218、配列番号220、配列番号222、配列番号224、配列番号226、配列番号228、配列番号230、配列番号232、配列番号234、配列番号236、配列番号238、配列番号240、配列番号242およびその組み合わせからなる群から選択されるアミノ酸配列と少なくとも95%同一であるL鎖可変領域配列を有する、一本鎖ヒト抗体。 - 請求項5記載の完全ヒト一本鎖抗体であって、配列番号1/配列番号2、配列番号3/配列番号4、配列番号5/配列番号6、配列番号7/配列番号8、配列番号9/配列番号10、配列番号11/配列番号12、配列番号13/配列番号14、配列番号15/配列番号16、配列番号17/配列番号18、配列番号19/配列番号20、配列番号21/配列番号22、配列番号23/配列番号24、配列番号25/配列番号26、配列番号27/配列番号28、配列番号29/配列番号30、配列番号31/配列番号32、配列番号33/配列番号34、配列番号35/配列番号36、配列番号37/配列番号38、配列番号39/配列番号40、配列番号41/配列番号42、配列番号43/配列番号44、配列番号45/配列番号46、配列番号47/配列番号48、配列番号49/配列番号50、配列番号51/配列番号52、配列番号53/配列番号54、配列番号55/配列番号56、配列番号57/配列番号58、配列番号59/配列番号60、配列番号61/配列番号62、配列番号63/配列番号64、配列番号65/配列番号66、配列番号67/配列番号68、配列番号69/配列番号70、配列番号71/配列番号72、配列番号73/配列番号74、配列番号75/配列番号76、配列番号77/配列番号78、配列番号79/配列番号80、配列番号81/配列番号82、配列番号83/配列番号84、配列番号85/配列番号86、配列番号87/配列番号88、配列番号89/配列番号90、配列番号91/配列番号92、配列番号93/配列番号94、配列番号95/配列番号96、配列番号97/配列番号98、配列番号99/配列番号100、配列番号101/配列番号102、配列番号103/配列番号104、配列番号105/配列番号106、配列番号107/配列番号108、配列番号109/配列番号110、配列番号111/配列番号112、配列番号113/配列番号114、配列番号115/配列番号116、配列番号117/配列番号118、配列番号119/配列番号120、配列番号121/配列番号122、配列番号123/配列番号124、配列番号125/配列番号126、配列番号127/配列番号128、配列番号129/配列番号130、配列番号131/配列番号132、配列番号133/配列番号134、配列番号135/配列番号136、配列番号137/配列番号138、配列番号139/配列番号140、配列番号141/配列番号142、配列番号143/配列番号144、配列番号145/配列番号146、配列番号147/配列番号148、配列番号149/配列番号150、配列番号151/配列番号152、配列番号153/配列番号154、配列番号155/配列番号156、配列番号157/配列番号158、配列番号159/配列番号160、配列番号161/配列番号162、配列番号163/配列番号164、配列番号165/配列番号166、配列番号167/配列番号168、配列番号169/配列番号170、配列番号171/配列番号172、配列番号173/配列番号174、配列番号175/配列番号176、配列番号177/配列番号178、配列番号179/配列番号180、配列番号181/配列番号182、配列番号183/配列番号184、配列番号185/配列番号186、配列番号187/配列番号188、配列番号189/配列番号190、配列番号191/配列番号192、配列番号193/配列番号194、配列番号195/配列番号196、配列番号197/配列番号198、配列番号199/配列番号200、配列番号201/配列番号202、配列番号203/配列番号204、配列番号205/配列番号206、配列番号207/配列番号208、配列番号209/配列番号210、配列番号211/配列番号212、配列番号213/配列番号214、配列番号215/配列番号216、配列番号217/配列番号218、配列番号219/配列番号220、配列番号221/配列番号222、配列番号223/配列番号224、配列番号225/配列番号226、配列番号227/配列番号228、配列番号229/配列番号230、配列番号231/配列番号232、配列番号233/配列番号234、配列番号235/配列番号236、配列番号237/配列番号238、配列番号239/配列番号240、配列番号241/配列番号242、およびその組み合わせからなる群から選択されるH鎖/L鎖可変領域配列を有する、完全一本鎖ヒト抗体。
- H鎖可変領域とL鎖可変領域の両方を有する請求項5記載の完全ヒト一本鎖抗体であって、配列番号1/配列番号2、配列番号3/配列番号4、配列番号5/配列番号6、配列番号7/配列番号8、配列番号9/配列番号10、配列番号11/配列番号12、配列番号13/配列番号14、配列番号15/配列番号16、配列番号17/配列番号18、配列番号19/配列番号20、配列番号21/配列番号22、配列番号23/配列番号24、配列番号25/配列番号26、配列番号27/配列番号28、配列番号29/配列番号30、配列番号31/配列番号32、配列番号33/配列番号34、配列番号35/配列番号36、配列番号37/配列番号38、配列番号39/配列番号40、配列番号41/配列番号42、配列番号43/配列番号44、配列番号45/配列番号46、配列番号47/配列番号48、配列番号49/配列番号50、配列番号51/配列番号52、配列番号53/配列番号54、配列番号55/配列番号56、配列番号57/配列番号58、配列番号59/配列番号60、配列番号61/配列番号62、配列番号63/配列番号64、配列番号65/配列番号66、配列番号67/配列番号68、配列番号69/配列番号70、配列番号71/配列番号72、配列番号73/配列番号74、配列番号75/配列番号76、配列番号77/配列番号78、配列番号79/配列番号80、配列番号81/配列番号82、配列番号83/配列番号84、配列番号85/配列番号86、配列番号87/配列番号88、配列番号89/配列番号90、配列番号91/配列番号92、配列番号93/配列番号94、配列番号95/配列番号96、配列番号97/配列番号98、配列番号99/配列番号100、配列番号101/配列番号102、配列番号103/配列番号104、配列番号105/配列番号106、配列番号107/配列番号108、配列番号109/配列番号110、配列番号111/配列番号112、配列番号113/配列番号114、配列番号115/配列番号116、配列番号117/配列番号118、配列番号119/配列番号120、配列番号121/配列番号122、配列番号123/配列番号124、配列番号125/配列番号126、配列番号127/配列番号128、配列番号129/配列番号130、配列番号131/配列番号132、配列番号133/配列番号134、配列番号135/配列番号136、配列番号137/配列番号138、配列番号139/配列番号140、配列番号141/配列番号142、配列番号143/配列番号144、配列番号145/配列番号146、配列番号147/配列番号148、配列番号149/配列番号150、配列番号151/配列番号152、配列番号153/配列番号154、配列番号155/配列番号156、配列番号157/配列番号158、配列番号159/配列番号160、配列番号161/配列番号162、配列番号163/配列番号164、配列番号165/配列番号166、配列番号167/配列番号168、配列番号169/配列番号170、配列番号171/配列番号172、配列番号173/配列番号174、配列番号175/配列番号176、配列番号177/配列番号178、配列番号179/配列番号180、配列番号181/配列番号182、配列番号183/配列番号184、配列番号185/配列番号186、配列番号187/配列番号188、配列番号189/配列番号190、配列番号191/配列番号192、配列番号193/配列番号194、配列番号195/配列番号196、配列番号197/配列番号198、配列番号199/配列番号200、配列番号201/配列番号202、配列番号203/配列番号204、配列番号205/配列番号206、配列番号207/配列番号208、配列番号209/配列番号210、配列番号211/配列番号212、配列番号213/配列番号214、配列番号215/配列番号216、配列番号217/配列番号218、配列番号219/配列番号220、配列番号221/配列番号222、配列番号223/配列番号224、配列番号225/配列番号226、配列番号227/配列番号228、配列番号229/配列番号230、配列番号231/配列番号232、配列番号233/配列番号234、配列番号235/配列番号236、配列番号237/配列番号238、配列番号239/配列番号240、配列番号241/配列番号242およびその組み合わせからなる群から選択されるH鎖/L鎖可変領域配列を有する、完全ヒト一本鎖抗体。
- 有効量の抗PD−L1ポリペプチドを投与することを含む広範囲の哺乳類のがんまたは炎症性疾患もしくは自己免疫性疾患の処置方法であって、
該抗PD−L1ポリペプチドが、PD−L1エピトープに少なくとも10-6Mの結合親和性で結合する、IgGクラスの完全ヒト抗体、H鎖由来の可変領域配列とL鎖由来の可変領域配列を有するFab完全ヒト抗体断片、H鎖由来の可変領域とL鎖由来の可変領域およびH鎖とL鎖の可変領域をつなぐペプチドリンカーを有する一本鎖ヒト抗体およびその組み合わせから選択され;ここで、
該完全ヒト抗体が、配列番号1、配列番号3、配列番号5、配列番号7、配列番号9、配列番号11、配列番号13、配列番号15、配列番号17、配列番号19、配列番号21、配列番号23、配列番号25、配列番号27、配列番号29、配列番号31、配列番号33、配列番号35、配列番号37、配列番号39、配列番号41、配列番号43、配列番号45、配列番号47、配列番号49、配列番号51、配列番号53、配列番号55、配列番号57、配列番号59、配列番号61、配列番号63、配列番号65、配列番号67、配列番号69、配列番号71、配列番号73、配列番号75、配列番号77、配列番号79、配列番号81、配列番号83、配列番号85、配列番号87、配列番号89、配列番号91、配列番号93、配列番号95、配列番号97、配列番号99、配列番号101、配列番号103、配列番号105、配列番号107、配列番号109、配列番号111、配列番号113、配列番号115、配列番号117、配列番号119、配列番号121、配列番号123、配列番号125、配列番号127、配列番号129、配列番号131、配列番号133、配列番号135、配列番号137、配列番号139、配列番号141、配列番号143、配列番号145、配列番号147、配列番号149、配列番号151、配列番号153、配列番号155、配列番号157、配列番号159、配列番号161、配列番号163、配列番号165、配列番号167、配列番号169、配列番号171、配列番号173、配列番号175、配列番号177、配列番号179、配列番号181、配列番号183、配列番号185、配列番号187、配列番号189、配列番号191、配列番号193、配列番号195、配列番号197、配列番号199、配列番号201、配列番号203、配列番号205、配列番号207、配列番号209、配列番号211、配列番号213、配列番号215、配列番号217、配列番号219、配列番号221、配列番号223、配列番号225、配列番号227、配列番号229、配列番号231、配列番号233、配列番号235、配列番号237、配列番号239、配列番号241およびその組み合わせからなる群から選択されるアミノ酸配列と少なくとも95%同一であるH鎖可変領域を有し、
配列番号2、配列番号4、配列番号6、配列番号8、配列番号10、配列番号12、配列番号14、配列番号16、配列番号18、配列番号20、配列番号22、配列番号24、配列番号26、配列番号28、配列番号30、配列番号32、配列番号34、配列番号36、配列番号38、配列番号40、配列番号42、配列番号44、配列番号46、配列番号48、配列番号50、配列番号52、配列番号54、配列番号56、配列番号58、配列番号60、配列番号62、配列番号64、配列番号66、配列番号68、配列番号70、配列番号72、配列番号74、配列番号76、配列番号78、配列番号80、配列番号82、配列番号84、配列番号86、配列番号88、配列番号90、配列番号92、配列番号94、配列番号96、配列番号98、配列番号100、配列番号102、配列番号104、配列番号106、配列番号108、配列番号110、配列番号112、配列番号114、配列番号116、配列番号118、配列番号120、配列番号122、配列番号124、配列番号126、配列番号128、配列番号130、配列番号132、配列番号134、配列番号136、配列番号138、配列番号140、配列番号142、配列番号144、配列番号146、配列番号148、配列番号150、配列番号152、配列番号154、配列番号156、配列番号158、配列番号160、配列番号162、配列番号164、配列番号166、配列番号168、配列番号170、配列番号172、配列番号174、配列番号176、配列番号178、配列番号180、配列番号182、配列番号184、配列番号186、配列番号188、配列番号190、配列番号192、配列番号194、配列番号196、配列番号198、配列番号200、配列番号202、配列番号204、配列番号206、配列番号208、配列番号210、配列番号212、配列番号214、配列番号216、配列番号218、配列番号220、配列番号222、配列番号224、配列番号226、配列番号228、配列番号230、配列番号232、配列番号234、配列番号236、配列番号238、配列番号240、配列番号242およびその組み合わせからなる群から選択されるアミノ酸配列と少なくとも95%同一であるL鎖可変領域配列を有しており;
該Fab完全ヒト抗体断片が、配列番号1、配列番号3、配列番号5、配列番号7、配列番号9、配列番号11、配列番号13、配列番号15、配列番号17、配列番号19、配列番号21、配列番号23、配列番号25、配列番号27、配列番号29、配列番号31、配列番号33、配列番号35、配列番号37、配列番号39、配列番号41、配列番号43、配列番号45、配列番号47、配列番号49、配列番号51、配列番号53、配列番号55、配列番号57、配列番号59、配列番号61、配列番号63、配列番号65、配列番号67、配列番号69、配列番号71、配列番号73、配列番号75、配列番号77、配列番号79、配列番号81、配列番号83、配列番号85、配列番号87、配列番号89、配列番号91、配列番号93、配列番号95、配列番号97、配列番号99、配列番号101、配列番号103、配列番号105、配列番号107、配列番号109、配列番号111、配列番号113、配列番号115、配列番号117、配列番号119、配列番号121、配列番号123、配列番号125、配列番号127、配列番号129、配列番号131、配列番号133、配列番号135、配列番号137、配列番号139、配列番号141、配列番号143、配列番号145、配列番号147、配列番号149、配列番号151、配列番号153、配列番号155、配列番号157、配列番号159、配列番号161、配列番号163、配列番号165、配列番号167、配列番号169、配列番号171、配列番号173、配列番号175、配列番号177、配列番号179、配列番号181、配列番号183、配列番号185、配列番号187、配列番号189、配列番号191、配列番号193、配列番号195、配列番号197、配列番号199、配列番号201、配列番号203、配列番号205、配列番号207、配列番号209、配列番号211、配列番号213、配列番号215、配列番号217、配列番号219、配列番号221、配列番号223、配列番号225、配列番号227およびその組み合わせからなる群から選択されるアミノ酸配列と少なくとも95%同一であるH鎖可変領域配列を有し、
配列番号2、配列番号4、配列番号6、配列番号8、配列番号10、配列番号12、配列番号14、配列番号16、配列番号18、配列番号20、配列番号22、配列番号24、配列番号26、配列番号28、配列番号30、配列番号32、配列番号34、配列番号36、配列番号38、配列番号40、配列番号42、配列番号44、配列番号46、配列番号48、配列番号50、配列番号52、配列番号54、配列番号56、配列番号58、配列番号60、配列番号62、配列番号64、配列番号66、配列番号68、配列番号70、配列番号72、配列番号74、配列番号76、配列番号78、配列番号80、配列番号82、配列番号84、配列番号86、配列番号88、配列番号90、配列番号92、配列番号94、配列番号96、配列番号98、配列番号100、配列番号102、配列番号104、配列番号106、配列番号108、配列番号110、配列番号112、配列番号114、配列番号116、配列番号118、配列番号120、配列番号122、配列番号124、配列番号126、配列番号128、配列番号130、配列番号132、配列番号134、配列番号136、配列番号138、配列番号140、配列番号142、配列番号144、配列番号146、配列番号148、配列番号150、配列番号152、配列番号154、配列番号156、配列番号158、配列番号160、配列番号162、配列番号164、配列番号166、配列番号168、配列番号170、配列番号172、配列番号174、配列番号176、配列番号178、配列番号180、配列番号182、配列番号184、配列番号186、配列番号188、配列番号190、配列番号192、配列番号194、配列番号196、配列番号198、配列番号200、配列番号202、配列番号204、配列番号206、配列番号208、配列番号210、配列番号212、配列番号214、配列番号216、配列番号218、配列番号220、配列番号222、配列番号224、配列番号226、配列番号228、配列番号230、配列番号232、配列番号234、配列番号236、配列番号238、配列番号240、配列番号242およびその組み合わせからなる群から選択されるアミノ酸配列と少なくとも95%同一であるL鎖可変領域配列を有しており;
該一本鎖ヒト抗体が、配列番号1、配列番号3、配列番号5、配列番号7、配列番号9、配列番号11、配列番号13、配列番号15、配列番号17、配列番号19、配列番号21、配列番号23、配列番号25、配列番号27、配列番号29、配列番号31、配列番号33、配列番号35、配列番号37、配列番号39、配列番号41、配列番号43、配列番号45、配列番号47、配列番号49、配列番号51、配列番号53、配列番号55、配列番号57、配列番号59、配列番号61、配列番号63、配列番号65、配列番号67、配列番号69、配列番号71、配列番号73、配列番号75、配列番号77、配列番号79、配列番号81、配列番号83、配列番号85、配列番号87、配列番号89、配列番号91、配列番号93、配列番号95、配列番号97、配列番号99、配列番号101、配列番号103、配列番号105、配列番号107、配列番号109、配列番号111、配列番号113、配列番号115、配列番号117、配列番号119、配列番号121、配列番号123、配列番号125、配列番号127、配列番号129、配列番号131、配列番号133、配列番号135、配列番号137、配列番号139、配列番号141、配列番号143、配列番号145、配列番号147、配列番号149、配列番号151、配列番号153、配列番号155、配列番号157、配列番号159、配列番号161、配列番号163、配列番号165、配列番号167、配列番号169、配列番号171、配列番号173、配列番号175、配列番号177、配列番号179、配列番号181、配列番号183、配列番号185、配列番号187、配列番号189、配列番号191、配列番号193、配列番号195、配列番号197、配列番号199、配列番号201、配列番号203、配列番号205、配列番号207、配列番号209、配列番号211、配列番号213、配列番号215、配列番号217、配列番号219、配列番号221、配列番号223、配列番号225、配列番号227、配列番号229、配列番号231、配列番号233、配列番号235、配列番号237、配列番号239、配列番号241およびその組み合わせからなる群から選択されるアミノ酸配列と少なくとも95%同一であるH鎖可変領域配列を有し、
配列番号2、配列番号4、配列番号6、配列番号8、配列番号10、配列番号12、配列番号14、配列番号16、配列番号18、配列番号20、配列番号22、配列番号24、配列番号26、配列番号28、配列番号30、配列番号32、配列番号34、配列番号36、配列番号38、配列番号40、配列番号42、配列番号44、配列番号46、配列番号48、配列番号50、配列番号52、配列番号54、配列番号56、配列番号58、配列番号60、配列番号62、配列番号64、配列番号66、配列番号68、配列番号70、配列番号72、配列番号74、配列番号76、配列番号78、配列番号80、配列番号82、配列番号84、配列番号86、配列番号88、配列番号90、配列番号92、配列番号94、配列番号96、配列番号98、配列番号100、配列番号102、配列番号104、配列番号106、配列番号108、配列番号110、配列番号112、配列番号114、配列番号116、配列番号118、配列番号120、配列番号122、配列番号124、配列番号126、配列番号128、配列番号130、配列番号132、配列番号134、配列番号136、配列番号138、配列番号140、配列番号142、配列番号144、配列番号146、配列番号148、配列番号150、配列番号152、配列番号154、配列番号156、配列番号158、配列番号160、配列番号162、配列番号164、配列番号166、配列番号168、配列番号170、配列番号172、配列番号174、配列番号176、配列番号178、配列番号180、配列番号182、配列番号184、配列番号186、配列番号188、配列番号190、配列番号192、配列番号194、配列番号196、配列番号198、配列番号200、配列番号202、配列番号204、配列番号206、配列番号208、配列番号210、配列番号212、配列番号214、配列番号216、配列番号218、配列番号220、配列番号222、配列番号224、配列番号226、配列番号228、配列番号230、配列番号232、配列番号234、配列番号236、配列番号238、配列番号240、配列番号242およびその組み合わせからなる群から選択されるアミノ酸配列と少なくとも95%同一であるL鎖可変領域配列を有する、処置方法。 - 請求項8記載の広範囲の哺乳類のがんの処置方法であって、
該完全ヒト抗体が、配列番号1/配列番号2、配列番号3/配列番号4、配列番号5/配列番号6、配列番号7/配列番号8、配列番号9/配列番号10、配列番号11/配列番号12、配列番号13/配列番号14、配列番号15/配列番号16、配列番号17/配列番号18、配列番号19/配列番号20、配列番号21/配列番号22、配列番号23/配列番号24、配列番号25/配列番号26、配列番号27/配列番号28、配列番号29/配列番号30、配列番号31/配列番号32、配列番号33/配列番号34、配列番号35/配列番号36、配列番号37/配列番号38、配列番号39/配列番号40、配列番号41/配列番号42、配列番号43/配列番号44、配列番号45/配列番号46、配列番号47/配列番号48、配列番号49/配列番号50、配列番号51/配列番号52、配列番号53/配列番号54、配列番号55/配列番号56、配列番号57/配列番号58、配列番号59/配列番号60、配列番号61/配列番号62、配列番号63/配列番号64、配列番号65/配列番号66、配列番号67/配列番号68、配列番号69/配列番号70、配列番号71/配列番号72、配列番号73/配列番号74、配列番号75/配列番号76、配列番号77/配列番号78、配列番号79/配列番号80、配列番号81/配列番号82、配列番号83/配列番号84、配列番号85/配列番号86、配列番号87/配列番号88、配列番号89/配列番号90、配列番号91/配列番号92、配列番号93/配列番号94、配列番号95/配列番号96、配列番号97/配列番号98、配列番号99/配列番号100、配列番号101/配列番号102、配列番号103/配列番号104、配列番号105/配列番号106、配列番号107/配列番号108、配列番号109/配列番号110、配列番号111/配列番号112、配列番号113/配列番号114、配列番号115/配列番号116、配列番号117/配列番号118、配列番号119/配列番号120、配列番号121/配列番号122、配列番号123/配列番号124、配列番号125/配列番号126、配列番号127/配列番号128、配列番号129/配列番号130、配列番号131/配列番号132、配列番号133/配列番号134、配列番号135/配列番号136、配列番号137/配列番号138、配列番号139/配列番号140、配列番号141/配列番号142、配列番号143/配列番号144、配列番号145/配列番号146、配列番号147/配列番号148、配列番号149/配列番号150、配列番号151/配列番号152、配列番号153/配列番号154、配列番号155/配列番号156、配列番号157/配列番号158、配列番号159/配列番号160、配列番号161/配列番号162、配列番号163/配列番号164、配列番号165/配列番号166、配列番号167/配列番号168、配列番号169/配列番号170、配列番号171/配列番号172、配列番号173/配列番号174、配列番号175/配列番号176、配列番号177/配列番号178、配列番号179/配列番号180、配列番号181/配列番号182、配列番号183/配列番号184、配列番号185/配列番号186、配列番号187/配列番号188、配列番号189/配列番号190、配列番号191/配列番号192、配列番号193/配列番号194、配列番号195/配列番号196、配列番号197/配列番号198、配列番号199/配列番号200、配列番号201/配列番号202、配列番号203/配列番号204、配列番号205/配列番号206、配列番号207/配列番号208、配列番号209/配列番号210、配列番号211/配列番号212、配列番号213/配列番号214、配列番号215/配列番号216、配列番号217/配列番号218、配列番号219/配列番号220、配列番号221/配列番号222、配列番号223/配列番号224、配列番号225/配列番号226、配列番号227/配列番号228、配列番号229/配列番号230、配列番号231/配列番号232、配列番号233/配列番号234、配列番号235/配列番号236、配列番号237/配列番号238、配列番号239/配列番号240、配列番号241/配列番号242およびその組み合わせからなる群から選択されるH鎖/L鎖可変領域配列を有する、処置方法。 - 請求項8記載の広範囲の哺乳類のがんの処置方法であって、
該完全ヒト抗体Fab断片が、H鎖可変領域とL鎖可変領域の両方を有し、該抗体が、配列番号1/配列番号2、配列番号3/配列番号4、配列番号5/配列番号6、配列番号7/配列番号8、配列番号9/配列番号10、配列番号11/配列番号12、配列番号13/配列番号14、配列番号15/配列番号16、配列番号17/配列番号18、配列番号19/配列番号20、配列番号21/配列番号22、配列番号23/配列番号24、配列番号25/配列番号26、配列番号27/配列番号28、配列番号29/配列番号30、配列番号31/配列番号32、配列番号33/配列番号34、配列番号35/配列番号36、配列番号37/配列番号38、配列番号39/配列番号40、配列番号41/配列番号42、配列番号43/配列番号44、配列番号45/配列番号46、配列番号47/配列番号48、配列番号49/配列番号50、配列番号51/配列番号52、配列番号53/配列番号54、配列番号55/配列番号56、配列番号57/配列番号58、配列番号59/配列番号60、配列番号61/配列番号62、配列番号63/配列番号64、配列番号65/配列番号66、配列番号67/配列番号68、配列番号69/配列番号70、配列番号71/配列番号72、配列番号73/配列番号74、配列番号75/配列番号76、配列番号77/配列番号78、配列番号79/配列番号80、配列番号81/配列番号82、配列番号83/配列番号84、配列番号85/配列番号86、配列番号87/配列番号88、配列番号89/配列番号90、配列番号91/配列番号92、配列番号93/配列番号94、配列番号95/配列番号96、配列番号97/配列番号98、配列番号99/配列番号100、配列番号101/配列番号102、配列番号103/配列番号104、配列番号105/配列番号106、配列番号107/配列番号108、配列番号109/配列番号110、配列番号111/配列番号112、配列番号113/配列番号114、配列番号115/配列番号116、配列番号117/配列番号118、配列番号119/配列番号120、配列番号121/配列番号122、配列番号123/配列番号124、配列番号125/配列番号126、配列番号127/配列番号128、配列番号129/配列番号130、配列番号131/配列番号132、配列番号133/配列番号134、配列番号135/配列番号136、配列番号137/配列番号138、配列番号139/配列番号140、配列番号141/配列番号142、配列番号143/配列番号144、配列番号145/配列番号146、配列番号147/配列番号148、配列番号149/配列番号150、配列番号151/配列番号152、配列番号153/配列番号154、配列番号155/配列番号156、配列番号157/配列番号158、配列番号159/配列番号160、配列番号161/配列番号162、配列番号163/配列番号164、配列番号165/配列番号166、配列番号167/配列番号168、配列番号169/配列番号170、配列番号171/配列番号172、配列番号173/配列番号174、配列番号175/配列番号176、配列番号177/配列番号178、配列番号179/配列番号180、配列番号181/配列番号182、配列番号183/配列番号184、配列番号185/配列番号186、配列番号187/配列番号188、配列番号189/配列番号190、配列番号191/配列番号192、配列番号193/配列番号194、配列番号195/配列番号196、配列番号197/配列番号198、配列番号199/配列番号200、配列番号201/配列番号202、配列番号203/配列番号204、配列番号205/配列番号206、配列番号207/配列番号208、配列番号209/配列番号210、配列番号211/配列番号212、配列番号213/配列番号214、配列番号215/配列番号216、配列番号217/配列番号218、配列番号219/配列番号220、配列番号221/配列番号222、配列番号223/配列番号224、配列番号225/配列番号226、配列番号227/配列番号228、配列番号229/配列番号230、配列番号231/配列番号232、配列番号233/配列番号234、配列番号235/配列番号236、配列番号237/配列番号238、配列番号239/配列番号240、配列番号241/配列番号242およびその組み合わせからなる群から選択されるH鎖/L鎖可変領域配列を有する、処置方法。 - 請求項8記載の広範囲の哺乳類のがんの処置方法であって、
該ヒト完全一本鎖抗体がH鎖可変領域およびL鎖可変領域の両方を有し、配列番号1/配列番号2、配列番号3/配列番号4、配列番号5/配列番号6、配列番号7/配列番号8、配列番号9/配列番号10、配列番号11/配列番号12、配列番号13/配列番号14、配列番号15/配列番号16、配列番号17/配列番号18、配列番号19/配列番号20、配列番号21/配列番号22、配列番号23/配列番号24、配列番号25/配列番号26、配列番号27/配列番号28、配列番号29/配列番号30、配列番号31/配列番号32、配列番号33/配列番号34、配列番号35/配列番号36、配列番号37/配列番号38、配列番号39/配列番号40、配列番号41/配列番号42、配列番号43/配列番号44、配列番号45/配列番号46、配列番号47/配列番号48、配列番号49/配列番号50、配列番号51/配列番号52、配列番号53/配列番号54、配列番号55/配列番号56、配列番号57/配列番号58、配列番号59/配列番号60、配列番号61/配列番号62、配列番号63/配列番号64、配列番号65/配列番号66、配列番号67/配列番号68、配列番号69/配列番号70、配列番号71/配列番号72、配列番号73/配列番号74、配列番号75/配列番号76、配列番号77/配列番号78、配列番号79/配列番号80、配列番号81/配列番号82、配列番号83/配列番号84、配列番号85/配列番号86、配列番号87/配列番号88、配列番号89/配列番号90、配列番号91/配列番号92、配列番号93/配列番号94、配列番号95/配列番号96、配列番号97/配列番号98、配列番号99/配列番号100、配列番号101/配列番号102、配列番号103/配列番号104、配列番号105/配列番号106、配列番号107/配列番号108、配列番号109/配列番号110、配列番号111/配列番号112、配列番号113/配列番号114、配列番号115/配列番号116、配列番号117/配列番号118、配列番号119/配列番号120、配列番号121/配列番号122、配列番号123/配列番号124、配列番号125/配列番号126、配列番号127/配列番号128、配列番号129/配列番号130、配列番号131/配列番号132、配列番号133/配列番号134、配列番号135/配列番号136、配列番号137/配列番号138、配列番号139/配列番号140、配列番号141/配列番号142、配列番号143/配列番号144、配列番号145/配列番号146、配列番号147/配列番号148、配列番号149/配列番号150、配列番号151/配列番号152、配列番号153/配列番号154、配列番号155/配列番号156、配列番号157/配列番号158、配列番号159/配列番号160、配列番号161/配列番号162、配列番号163/配列番号164、配列番号165/配列番号166、配列番号167/配列番号168、配列番号169/配列番号170、配列番号171/配列番号172、配列番号173/配列番号174、配列番号175/配列番号176、配列番号177/配列番号178、配列番号179/配列番号180、配列番号181/配列番号182、配列番号183/配列番号184、配列番号185/配列番号186、配列番号187/配列番号188、配列番号189/配列番号190、配列番号191/配列番号192、配列番号193/配列番号194、配列番号195/配列番号196、配列番号197/配列番号198、配列番号199/配列番号200、配列番号201/配列番号202、配列番号203/配列番号204、配列番号205/配列番号206、配列番号207/配列番号208、配列番号209/配列番号210、配列番号211/配列番号212、配列番号213/配列番号214、配列番号215/配列番号216、配列番号217/配列番号218、配列番号219/配列番号220、配列番号221/配列番号222、配列番号223/配列番号224、配列番号225/配列番号226、配列番号227/配列番号228、配列番号229/配列番号230、配列番号231/配列番号232、配列番号233/配列番号234、配列番号235/配列番号236、配列番号237/配列番号238、配列番号239/配列番号240、配列番号241/配列番号242およびその組み合わせからなる群から選択されるH鎖/L鎖可変領域配列を有する、処置方法。 - 請求項8記載の広範囲の哺乳類のがんまたは炎症性疾患もしくは自己免疫性疾患の処置方法であって、処置する広範囲の哺乳類のがんが、卵巣がん、結腸がん、乳がん、肺がん、骨髄腫、神経芽腫由来CNS腫瘍、単球性白血病、B細胞由来白血病、T細胞由来白血病、B細胞由来リンパ腫、T細胞由来リンパ腫、脂肪細胞由来腫瘍およびその組み合わせからなる群から選択される、処置方法。
- 請求項8記載の広範囲の哺乳類のがんまたは炎症性疾患もしくは自己免疫性疾患の処置方法であって、広範囲の自己免疫性疾患または炎症性疾患が、腸粘膜炎症、大腸炎に伴う消耗性疾患、多発性硬化症、全身性エリテマトーデス、ウイルス感染症、関節リウマチ、変形性関節症、乾癬、クローン病および炎症性腸疾患からなる群から選択される、処置方法。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201261654022P | 2012-05-31 | 2012-05-31 | |
| US61/654,022 | 2012-05-31 | ||
| US201261739982P | 2012-12-20 | 2012-12-20 | |
| US61/739,982 | 2012-12-20 | ||
| PCT/US2013/043775 WO2013181634A2 (en) | 2012-05-31 | 2013-05-31 | Antigen binding proteins that bind pd-l1 |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2017155655A Division JP6648080B2 (ja) | 2012-05-31 | 2017-08-10 | Pd−l1に結合する抗原結合蛋白質 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2015519375A true JP2015519375A (ja) | 2015-07-09 |
| JP2015519375A5 JP2015519375A5 (ja) | 2016-07-14 |
Family
ID=49670536
Family Applications (5)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2015515271A Pending JP2015519375A (ja) | 2012-05-31 | 2013-05-31 | Pd−l1に結合する抗原結合蛋白質 |
| JP2017155655A Active JP6648080B2 (ja) | 2012-05-31 | 2017-08-10 | Pd−l1に結合する抗原結合蛋白質 |
| JP2020004101A Active JP6829330B2 (ja) | 2012-05-31 | 2020-01-15 | Pd−l1に結合する抗原結合蛋白質 |
| JP2021008088A Pending JP2021061862A (ja) | 2012-05-31 | 2021-01-21 | Pd−l1に結合する抗原結合蛋白質 |
| JP2022017798A Pending JP2022058932A (ja) | 2012-05-31 | 2022-02-08 | Pd-l1に結合する抗原結合蛋白質 |
Family Applications After (4)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2017155655A Active JP6648080B2 (ja) | 2012-05-31 | 2017-08-10 | Pd−l1に結合する抗原結合蛋白質 |
| JP2020004101A Active JP6829330B2 (ja) | 2012-05-31 | 2020-01-15 | Pd−l1に結合する抗原結合蛋白質 |
| JP2021008088A Pending JP2021061862A (ja) | 2012-05-31 | 2021-01-21 | Pd−l1に結合する抗原結合蛋白質 |
| JP2022017798A Pending JP2022058932A (ja) | 2012-05-31 | 2022-02-08 | Pd-l1に結合する抗原結合蛋白質 |
Country Status (11)
| Country | Link |
|---|---|
| US (5) | US9175082B2 (ja) |
| EP (2) | EP3553086A1 (ja) |
| JP (5) | JP2015519375A (ja) |
| KR (4) | KR102284247B1 (ja) |
| CN (3) | CN104736168B (ja) |
| AU (4) | AU2013267161A1 (ja) |
| BR (1) | BR112014029883B1 (ja) |
| CA (2) | CA2872030A1 (ja) |
| CO (1) | CO7160115A2 (ja) |
| HK (1) | HK1204557A1 (ja) |
| WO (1) | WO2013181634A2 (ja) |
Cited By (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2018526974A (ja) * | 2016-03-04 | 2018-09-20 | シチュアン ケルン−バイオテック バイオファーマシューティカル カンパニー リミテッド | Pdl−1抗体、その医薬組成物及びその使用 |
| JP2018531219A (ja) * | 2015-08-24 | 2018-10-25 | イーライ リリー アンド カンパニー | Pd−l1抗体 |
| JP2019503687A (ja) * | 2016-01-04 | 2019-02-14 | ジアンスー ヒャマブ ファーマシューティカル カンパニー リミテッド | 抗pd−l1抗体およびその使用 |
| JP2019510041A (ja) * | 2016-03-30 | 2019-04-11 | マイクロバイオ カンパニー, リミテッド | 免疫チェックポイントモジュレーターおよび共生微生物叢による発酵産物の併用がん療法 |
| JP2019514853A (ja) * | 2016-05-20 | 2019-06-06 | ルェヤン(スーツォ)バイオロジー サイエンス アンド テクノロジー シーオー.,エルティーディー | 抗人pd−l1人源化単クローン抗体及び応用 |
| JP2019516394A (ja) * | 2016-03-23 | 2019-06-20 | マブスペース バイオサイエンシズ (スーチョウ) カンパニー,リミテッド | 新規抗pd−l1抗体 |
| JP2021509258A (ja) * | 2017-12-29 | 2021-03-25 | エーピー バイオサイエンスィズ インコーポレイテッド | 癌治療のために免疫チェックポイントを調節する単一特異性および二重特異性タンパク質 |
| JP2021102633A (ja) * | 2016-01-29 | 2021-07-15 | ソレント・セラピューティクス・インコーポレイテッドSorrento Therapeutics, Inc. | Pd−l1に結合する抗原結合性タンパク質 |
| JP2021534750A (ja) * | 2018-08-20 | 2021-12-16 | 1グローブ バイオメディカル カンパニー, リミテッド | 新規ながん免疫療法抗体組成物 |
| JP2022511311A (ja) * | 2019-04-26 | 2022-01-31 | アイ-エムエービー バイオファーマ ユーエス リミテッド | ヒトpd‐l1抗体 |
| JP2022528007A (ja) * | 2019-06-10 | 2022-06-07 | 山東博安生物技術股▲ふん▼有限公司 | PDL1及びTGFβに対する二機能性融合タンパク質並びにその使用 |
Families Citing this family (335)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| BRPI0917592B1 (pt) | 2008-12-09 | 2021-08-17 | Genentech, Inc | Anticorpo anti-pd-l1, composição, artigos manufaturados e usos de uma composição |
| HUE052198T2 (hu) | 2011-07-21 | 2021-04-28 | Sumitomo Dainippon Pharma Oncology Inc | Heterociklusos protein kináz inhibitorok |
| CA2863658C (en) * | 2012-02-03 | 2023-03-14 | Emory University | Immunostimulatory compositions, particles, and uses related thereto |
| EP3553086A1 (en) | 2012-05-31 | 2019-10-16 | Sorrento Therapeutics Inc. | Antigen binding proteins that bind pd-l1 |
| LT2964638T (lt) | 2013-03-06 | 2017-12-27 | Astrazeneca Ab | Epidermio augimo faktoriaus receptoriaus aktyvinančių mutacijų formų chinazolino inhibitoriai |
| PL3702373T3 (pl) | 2013-09-13 | 2022-12-05 | Beigene Switzerland Gmbh | Przeciwciała anty-PD1 i ich zastosowanie jako środki terapeutyczne i diagnostyczne |
| EP3757130A1 (en) | 2013-09-26 | 2020-12-30 | Costim Pharmaceuticals Inc. | Methods for treating hematologic cancers |
| AU2014339900B2 (en) * | 2013-10-25 | 2019-10-24 | Dana-Farber Cancer Institute, Inc. | Anti-PD-L1 monoclonal antibodies and fragments thereof |
| CN105899535A (zh) * | 2013-12-17 | 2016-08-24 | 豪夫迈·罗氏有限公司 | 用pd-1轴结合拮抗剂和抗cd20抗体治疗癌症的方法 |
| NZ720515A (en) * | 2013-12-17 | 2022-12-23 | Genentech Inc | Methods of treating cancers using pd-1 axis binding antagonists and taxanes |
| DE202014010499U1 (de) | 2013-12-17 | 2015-10-20 | Kymab Limited | Targeting von humaner PCSK9 zur Cholesterinbehandlung |
| EP3659624B1 (en) * | 2014-01-15 | 2022-11-16 | The U.S.A. as represented by the Secretary, Department of Health and Human Services | Cartilage targeting agents and their use |
| HUE057917T2 (hu) * | 2014-01-15 | 2022-06-28 | Kadmon Corp Llc | Immunmodulátor szerek |
| JOP20200094A1 (ar) | 2014-01-24 | 2017-06-16 | Dana Farber Cancer Inst Inc | جزيئات جسم مضاد لـ pd-1 واستخداماتها |
| JOP20200096A1 (ar) | 2014-01-31 | 2017-06-16 | Children’S Medical Center Corp | جزيئات جسم مضاد لـ tim-3 واستخداماتها |
| GB201403775D0 (en) | 2014-03-04 | 2014-04-16 | Kymab Ltd | Antibodies, uses & methods |
| KR20160138309A (ko) * | 2014-04-16 | 2016-12-02 | 소렌토 쎄라퓨틱스, 인코포레이티드 | Cd147에 결합하는 항체 치료제 |
| KR102003754B1 (ko) * | 2014-07-03 | 2019-07-25 | 베이진 엘티디 | Pd-l1 항체와 이를 이용한 치료 및 진단 |
| CA2955788C (en) | 2014-07-22 | 2024-01-16 | Ziyong Sun | Anti-pd-1 antibodies |
| WO2016022630A1 (en) | 2014-08-05 | 2016-02-11 | Jiping Zha | Anti-pd-l1 antibodies |
| EA201790489A1 (ru) | 2014-08-29 | 2017-08-31 | Сорренто Терапьютикс, Инк. | ТЕРАПЕВТИЧЕСКИЕ СРЕДСТВА НА ОСНОВЕ АНТИТЕЛ, СВЯЗЫВАЮЩИЕ OprF И OprI |
| EP3191097B1 (en) | 2014-09-13 | 2019-10-23 | Novartis AG | Combination therapies |
| AU2015330731B2 (en) | 2014-10-10 | 2020-07-09 | Idera Pharmaceuticals, Inc. | Treatment of cancer using TLR9 agonist with checkpoint inhibitors |
| MX2017004810A (es) | 2014-10-14 | 2017-10-16 | Novartis Ag | Moleculas de anticuerpo que se unen a pd-l1 y usos de las mismas. |
| KR102632418B1 (ko) * | 2014-11-25 | 2024-01-31 | 브리스톨-마이어스 스큅 컴퍼니 | 영상화를 위한 신규 pd-l1 결합 폴리펩티드 |
| JP6701217B2 (ja) | 2014-11-25 | 2020-05-27 | ブリストル−マイヤーズ スクイブ カンパニーBristol−Myers Squibb Company | 生物学的製剤の18f−放射性標識方法および組成物 |
| CA2974237C (en) | 2015-01-09 | 2021-07-20 | Etubics Corporation | Methods and compositions for combination immunotherapy |
| GB201500319D0 (en) | 2015-01-09 | 2015-02-25 | Agency Science Tech & Res | Anti-PD-L1 antibodies |
| IL292449B2 (en) | 2015-03-13 | 2024-02-01 | Cytomx Therapeutics Inc | Nucleic acids encoding antibodies against PDL1 and methods for their preparation |
| US11933786B2 (en) | 2015-03-30 | 2024-03-19 | Stcube, Inc. | Antibodies specific to glycosylated PD-L1 and methods of use thereof |
| US11149087B2 (en) * | 2015-04-20 | 2021-10-19 | Etubics Corporation | Methods and compositions for combination immunotherapy |
| CN113603784A (zh) | 2015-05-29 | 2021-11-05 | 艾吉纳斯公司 | 抗-ctla-4抗体及其使用方法 |
| WO2016197367A1 (en) | 2015-06-11 | 2016-12-15 | Wuxi Biologics (Shanghai) Co. Ltd. | Novel anti-pd-l1 antibodies |
| CN108026173A (zh) | 2015-06-12 | 2018-05-11 | 百时美施贵宝公司 | 通过联合阻断pd-1和cxcr4信号传导途径治疗癌症 |
| EP3310815A1 (en) | 2015-06-17 | 2018-04-25 | F. Hoffmann-La Roche AG | Methods of treating locally advanced or metastatic breast cancers using pd-1 axis binding antagonists and taxanes |
| CN106397592A (zh) * | 2015-07-31 | 2017-02-15 | 苏州康宁杰瑞生物科技有限公司 | 针对程序性死亡配体(pd-l1)的单域抗体及其衍生蛋白 |
| EA201890434A1 (ru) | 2015-08-05 | 2018-10-31 | Янссен Байотек, Инк. | Антитела к cd154 и способы их применения |
| WO2017020291A1 (en) * | 2015-08-06 | 2017-02-09 | Wuxi Biologics (Shanghai) Co. Ltd. | Novel anti-pd-l1 antibodies |
| CN106480022B (zh) * | 2015-08-27 | 2020-07-10 | 杨光华 | 干涉片段及其应用 |
| CN106480023B (zh) * | 2015-08-27 | 2020-07-10 | 杨光华 | 干涉片段及其应用 |
| CN109608544B (zh) | 2015-11-17 | 2022-09-16 | 苏州盛迪亚生物医药有限公司 | Pd-l1抗体、其抗原结合片段及其医药用途 |
| KR20180093010A (ko) | 2015-12-04 | 2018-08-20 | 더 리전트 오브 더 유니버시티 오브 캘리포니아 | 새로운 암 치료용 항체 |
| JP6893639B2 (ja) * | 2015-12-28 | 2021-06-23 | 国立大学法人京都大学 | がんの判定方法、がんの判定のための装置及びコンピュータプログラム |
| JP7022067B2 (ja) * | 2016-01-14 | 2022-02-17 | メモリアル スローン ケタリング キャンサー センター | Foxp3由来のペプチドに特異的なt細胞受容体様抗体 |
| US20190048085A1 (en) * | 2016-02-25 | 2019-02-14 | Cell Medica Switzerland Ag | Modified cells for immunotherapy |
| CN109310885B (zh) | 2016-03-15 | 2022-05-31 | 梅尔莎纳医疗公司 | NaPi2b靶向抗体-药物缀合物及其使用方法 |
| CN107216389B (zh) * | 2016-03-18 | 2022-03-29 | 和迈生物科技有限公司 | 抗pd-l1纳米抗体及其编码序列和用途 |
| JP2019518068A (ja) * | 2016-03-29 | 2019-06-27 | エスティーキューブ アンド カンパニー,インコーポレイテッド | グリコシル化免疫チェックポイントタンパク質に特異的に結合する抗体を選択する方法 |
| CN109195991B (zh) | 2016-03-29 | 2023-10-31 | 斯特库比股份有限公司 | 对糖基化pd-l1特异的双重功能抗体及其使用方法 |
| CA3022915A1 (en) * | 2016-05-03 | 2017-11-09 | The Scripps Research Institute | Trkb agonist antibodies for treating neurodegenerative disorders |
| TWI781934B (zh) | 2016-05-27 | 2022-11-01 | 美商艾吉納斯公司 | 抗-tim-3抗體及其使用方法 |
| CN109562195A (zh) * | 2016-06-01 | 2019-04-02 | 百时美施贵宝公司 | 用pd-l1结合多肽进行pet成像 |
| WO2017210335A1 (en) | 2016-06-01 | 2017-12-07 | Bristol-Myers Squibb Company | Imaging methods using 18f-radiolabeled biologics |
| CN109715196A (zh) | 2016-06-13 | 2019-05-03 | 转矩医疗股份有限公司 | 用于促进免疫细胞功能的组合物和方法 |
| WO2018029474A2 (en) | 2016-08-09 | 2018-02-15 | Kymab Limited | Anti-icos antibodies |
| RU2769282C2 (ru) | 2016-06-20 | 2022-03-30 | Кимаб Лимитед | Анти-PD-L1 и IL-2 цитокины |
| US9567399B1 (en) | 2016-06-20 | 2017-02-14 | Kymab Limited | Antibodies and immunocytokines |
| CA3027204A1 (en) * | 2016-06-29 | 2018-01-04 | Checkpoint Therapeutics, Inc. | Pd-l1-specific antibodies and methods of using the same |
| CA3029426A1 (en) | 2016-06-30 | 2018-01-04 | Oncorus, Inc. | Pseudotyped oncolytic viral delivery of therapeutic polypeptides |
| WO2018007885A1 (en) | 2016-07-05 | 2018-01-11 | Beigene, Ltd. | COMBINATION OF A PD-l ANTAGONIST AND A RAF INHIBITOR FOR TREATING CANCER |
| GB201612520D0 (en) | 2016-07-19 | 2016-08-31 | F-Star Beta Ltd | Binding molecules |
| US11746152B2 (en) | 2016-07-20 | 2023-09-05 | Stcube, Inc. | Methods of cancer treatment and therapy using a combination of antibodies that bind glycosylated PD-L1 |
| UA125395C2 (uk) * | 2016-08-05 | 2022-03-02 | І-Байолоджікс Інк. | Антитіло проти білка-1 запрограмованої клітинної смерті (pd-1) і його застосування |
| JP7198752B2 (ja) | 2016-08-09 | 2023-01-04 | カイマブ・リミテッド | 抗icos抗体 |
| TWI739887B (zh) | 2016-08-19 | 2021-09-21 | 英屬開曼群島商百濟神州有限公司 | 使用包含btk抑制劑的組合產品治療癌症 |
| TW202246349A (zh) | 2016-10-11 | 2022-12-01 | 美商艾吉納斯公司 | 抗lag-3抗體及其使用方法 |
| KR102634093B1 (ko) | 2016-10-28 | 2024-02-07 | 브리스톨-마이어스 스큅 컴퍼니 | 항-pd-1 항체를 사용하여 요로상피 암종을 치료하는 방법 |
| EA201990875A1 (ru) | 2016-11-03 | 2019-09-30 | Бристол-Маерс Сквибб Компани | Активируемые антитела против ctla-4 и их применение |
| US11779604B2 (en) | 2016-11-03 | 2023-10-10 | Kymab Limited | Antibodies, combinations comprising antibodies, biomarkers, uses and methods |
| WO2018094275A1 (en) | 2016-11-18 | 2018-05-24 | Tolero Pharmaceuticals, Inc. | Alvocidib prodrugs and their use as protein kinase inhibitors |
| US11135307B2 (en) | 2016-11-23 | 2021-10-05 | Mersana Therapeutics, Inc. | Peptide-containing linkers for antibody-drug conjugates |
| MD3551660T2 (ro) | 2016-12-07 | 2024-03-31 | Agenus Inc | Anticorpi anti-CTLA-4 și procedee de utilizare a acestora |
| BR112019011582A2 (pt) | 2016-12-07 | 2019-10-22 | Agenus Inc. | anticorpos e métodos de utilização dos mesmos |
| AU2017378226A1 (en) | 2016-12-14 | 2019-06-20 | Janssen Biotech, Inc. | CD8A-binding fibronectin type III domains |
| US10597438B2 (en) | 2016-12-14 | 2020-03-24 | Janssen Biotech, Inc. | PD-L1 binding fibronectin type III domains |
| US10611823B2 (en) | 2016-12-14 | 2020-04-07 | Hanssen Biotech, Inc | CD137 binding fibronectin type III domains |
| JP2020503883A (ja) | 2017-01-13 | 2020-02-06 | アジェナス インコーポレイテッド | Ny−eso−1に結合するt細胞受容体およびその使用方法 |
| EP3573989A4 (en) | 2017-01-25 | 2020-11-18 | Beigene, Ltd. | CRYSTALLINE FORMS OF (S) -7- (1- (BUT-2-YNOYL) -PIPERIDINE-4-YL) -2- (4-PHENOXYPHENYL) -4,5,6,7-TETRAHYDROPYRAZOLO [1,5-A ] PYRIMIDINE-3-CARBOXAMIDE, MANUFACTURING AND USES THEREOF |
| TWI674261B (zh) | 2017-02-17 | 2019-10-11 | 美商英能腫瘤免疫股份有限公司 | Nlrp3 調節劑 |
| CN108456251A (zh) * | 2017-02-21 | 2018-08-28 | 上海君实生物医药科技股份有限公司 | 抗pd-l1抗体及其应用 |
| WO2018160538A1 (en) | 2017-02-28 | 2018-09-07 | Mersana Therapeutics, Inc. | Combination therapies of her2-targeted antibody-drug conjugates |
| CA3058175A1 (en) | 2017-03-31 | 2018-10-04 | Bristol-Myers Squibb Company | Methods of treating tumor |
| TWI788340B (zh) | 2017-04-07 | 2023-01-01 | 美商必治妥美雅史谷比公司 | 抗icos促效劑抗體及其用途 |
| TW201841942A (zh) | 2017-04-13 | 2018-12-01 | 美商艾吉納斯公司 | 抗cd137抗體及其使用方法 |
| RU2665790C1 (ru) * | 2017-04-17 | 2018-09-04 | Закрытое Акционерное Общество "Биокад" | Моноклональное антитело к pd-l1 |
| AR111651A1 (es) | 2017-04-28 | 2019-08-07 | Novartis Ag | Conjugados de anticuerpos que comprenden agonistas del receptor de tipo toll y terapias de combinación |
| RS64576B1 (sr) | 2017-05-01 | 2023-10-31 | Agenus Inc | Anti-tigit antitela i postupci njihove primene |
| EP3630842A2 (en) | 2017-05-30 | 2020-04-08 | Bristol-Myers Squibb Company | Compositions comprising a combination of an anti-lag-3 antibody, a pd-1 pathway inhibitor, and an immunotherapeutic agent |
| US11723975B2 (en) | 2017-05-30 | 2023-08-15 | Bristol-Myers Squibb Company | Compositions comprising an anti-LAG-3 antibody or an anti-LAG-3 antibody and an anti-PD-1 or anti-PD-L1 antibody |
| CN110720039A (zh) | 2017-05-30 | 2020-01-21 | 百时美施贵宝公司 | Lag-3阳性肿瘤的治疗 |
| CN110678483B (zh) | 2017-06-01 | 2023-09-22 | 百时美施贵宝公司 | 用抗pd-1抗体治疗肿瘤的方法 |
| AU2018278327B2 (en) | 2017-06-01 | 2023-03-16 | Cytomx Therapeutics, Inc. | Activatable anti-pdl1 antibodies and methods of use thereof |
| WO2018229715A1 (en) | 2017-06-16 | 2018-12-20 | Novartis Ag | Compositions comprising anti-cd32b antibodies and methods of use thereof |
| GB201709808D0 (en) | 2017-06-20 | 2017-08-02 | Kymab Ltd | Antibodies |
| WO2018235056A1 (en) | 2017-06-22 | 2018-12-27 | Novartis Ag | IL-1BETA BINDING ANTIBODIES FOR USE IN THE TREATMENT OF CANCER |
| US20200172628A1 (en) | 2017-06-22 | 2020-06-04 | Novartis Ag | Antibody molecules to cd73 and uses thereof |
| CN110785187B (zh) | 2017-06-22 | 2024-04-05 | 诺华股份有限公司 | 针对cd73的抗体分子及其用途 |
| US20190048072A1 (en) | 2017-06-22 | 2019-02-14 | Novartis Ag | USE OF IL-1beta BINDING ANTIBODIES |
| CA3066518A1 (en) | 2017-06-26 | 2019-01-03 | Beigene, Ltd. | Immunotherapy for hepatocellular carcinoma |
| JP2020525483A (ja) | 2017-06-27 | 2020-08-27 | ノバルティス アーゲー | 抗tim−3抗体のための投与レジメンおよびその使用 |
| AU2018301681B2 (en) | 2017-07-14 | 2022-07-14 | Innate Tumor Immunity, Inc. | NLRP3 modulators |
| AU2018302283A1 (en) | 2017-07-20 | 2020-02-06 | Novartis Ag | Dosage regimens of anti-LAG-3 antibodies and uses thereof |
| CN110997691B (zh) | 2017-07-28 | 2023-11-07 | 百时美施贵宝公司 | 作为抗癌剂的环二核苷酸 |
| AR112405A1 (es) | 2017-08-07 | 2019-10-23 | Amgen Inc | Tratamiento de cáncer de mama triple negativo o cáncer colorrectal con metástasis hepáticas |
| CN111051328B (zh) | 2017-08-31 | 2023-11-03 | 百时美施贵宝公司 | 作为抗癌剂的环二核苷酸 |
| ES2945140T3 (es) | 2017-08-31 | 2023-06-28 | Bristol Myers Squibb Co | Dinucleótidos cíclicos como agentes anticancerosos |
| WO2019046496A1 (en) | 2017-08-31 | 2019-03-07 | Bristol-Myers Squibb Company | CYCLIC DINUCLEOTIDES AS ANTICANCER AGENTS |
| SG11202001319QA (en) | 2017-09-04 | 2020-03-30 | Agenus Inc | T cell receptors that bind to mixed lineage leukemia (mll)-specific phosphopeptides and methods of use thereof |
| US11497756B2 (en) | 2017-09-12 | 2022-11-15 | Sumitomo Pharma Oncology, Inc. | Treatment regimen for cancers that are insensitive to BCL-2 inhibitors using the MCL-1 inhibitor alvocidib |
| US11660311B2 (en) | 2017-10-10 | 2023-05-30 | Bristol-Myers Squibb Company | Cyclic dinucleotides as anticancer agents |
| CN111247169A (zh) | 2017-10-15 | 2020-06-05 | 百时美施贵宝公司 | 治疗肿瘤的方法 |
| CN111406063B (zh) | 2017-10-16 | 2023-09-15 | 百时美施贵宝公司 | 作为抗癌剂的环二核苷酸 |
| US20210040205A1 (en) | 2017-10-25 | 2021-02-11 | Novartis Ag | Antibodies targeting cd32b and methods of use thereof |
| MX2020004567A (es) | 2017-11-06 | 2020-08-13 | Genentech Inc | Metodos diagnosticos y terapeuticos para el cancer. |
| BR112020008316A2 (pt) | 2017-11-06 | 2020-10-20 | Bristol-Myers Squibb Company | métodos para o tratamento de um tumor |
| WO2019104289A1 (en) | 2017-11-27 | 2019-05-31 | Mersana Therapeutics, Inc. | Pyrrolobenzodiazepine antibody conjugates |
| US11786529B2 (en) | 2017-11-29 | 2023-10-17 | Beigene Switzerland Gmbh | Treatment of indolent or aggressive B-cell lymphomas using a combination comprising BTK inhibitors |
| WO2019122882A1 (en) | 2017-12-19 | 2019-06-27 | Kymab Limited | Bispecific antibody for icos and pd-l1 |
| GB201721338D0 (en) | 2017-12-19 | 2018-01-31 | Kymab Ltd | Anti-icos Antibodies |
| CN111757757A (zh) | 2017-12-21 | 2020-10-09 | 梅尔莎纳医疗公司 | 吡咯并苯并二氮呯抗体共轭物 |
| EP3731850A4 (en) | 2017-12-29 | 2021-12-01 | Oncorus, Inc. | ONCOLYTIC VIRUS DELIVERY OF THERAPEUTIC POLYPEPTIDES |
| EP3737408A1 (en) | 2018-01-08 | 2020-11-18 | Novartis AG | Immune-enhancing rnas for combination with chimeric antigen receptor therapy |
| BR112020013475A2 (pt) | 2018-01-10 | 2020-12-08 | Jiangsu Hengrui Medicine Co., Ltd. | Anticorpo de pd-l1, fragmento de ligação ao antígeno do mesmo, e uso farmacêutico do mesmo |
| KR20200109339A (ko) | 2018-01-16 | 2020-09-22 | 브리스톨-마이어스 스큅 컴퍼니 | Tim3에 대한 항체를 사용하여 암을 치료하는 방법 |
| BR112020014574A2 (pt) | 2018-01-22 | 2020-12-08 | Bristol-Myers Squibb Company | Composições e métodos para o tratamento do câncer |
| WO2019144126A1 (en) | 2018-01-22 | 2019-07-25 | Pascal Biosciences Inc. | Cannabinoids and derivatives for promoting immunogenicity of tumor and infected cells |
| WO2019152660A1 (en) | 2018-01-31 | 2019-08-08 | Novartis Ag | Combination therapy using a chimeric antigen receptor |
| WO2019160956A1 (en) | 2018-02-13 | 2019-08-22 | Novartis Ag | Chimeric antigen receptor therapy in combination with il-15r and il15 |
| US10519187B2 (en) | 2018-02-13 | 2019-12-31 | Bristol-Myers Squibb Company | Cyclic dinucleotides as anticancer agents |
| SG11202005290QA (en) * | 2018-02-28 | 2020-07-29 | Ap Biosciences Inc | Bifunctional proteins combining checkpoint blockade for targeted therapy |
| JP7250808B2 (ja) | 2018-03-08 | 2023-04-03 | ブリストル-マイヤーズ スクイブ カンパニー | 抗がん剤としての環状ジヌクレオチド |
| CN108484761B (zh) * | 2018-03-10 | 2021-04-30 | 吉林大学 | 一种特异性识别并诱导Aβ42的寡聚体及原纤维解聚的单链抗体、单链抗体基因及其应用 |
| AU2019237212A1 (en) * | 2018-03-22 | 2020-09-24 | Keires Ag | Antagonistic PD-1, PD-L1 and LAG-3 binding proteins |
| CN111886256A (zh) | 2018-03-23 | 2020-11-03 | 百时美施贵宝公司 | 抗mica和/或micb抗体及其用途 |
| KR20200139724A (ko) | 2018-03-30 | 2020-12-14 | 브리스톨-마이어스 스큅 컴퍼니 | 종양을 치료하는 방법 |
| CN111936514A (zh) | 2018-03-30 | 2020-11-13 | 美勒斯公司 | 多价抗体 |
| WO2019195452A1 (en) | 2018-04-04 | 2019-10-10 | Bristol-Myers Squibb Company | Anti-cd27 antibodies and uses thereof |
| US20210147547A1 (en) | 2018-04-13 | 2021-05-20 | Novartis Ag | Dosage Regimens For Anti-Pd-L1 Antibodies And Uses Thereof |
| EP4353235A2 (en) | 2018-04-25 | 2024-04-17 | Innate Tumor Immunity, Inc. | Nlrp3 modulators |
| CA3096909A1 (en) | 2018-04-26 | 2019-10-31 | Agenus Inc. | Heat shock protein-binding peptide compositions and methods of use thereof |
| TW202015726A (zh) | 2018-05-30 | 2020-05-01 | 瑞士商諾華公司 | Entpd2抗體、組合療法、及使用該等抗體和組合療法之方法 |
| WO2019232244A2 (en) | 2018-05-31 | 2019-12-05 | Novartis Ag | Antibody molecules to cd73 and uses thereof |
| EP3802611A2 (en) | 2018-06-01 | 2021-04-14 | Novartis AG | Binding molecules against bcma and uses thereof |
| MA52889A (fr) | 2018-06-15 | 2021-04-21 | Flagship Pioneering Innovations V Inc | Augmentation de l'activité immunitaire par modulation de facteurs de signalisation post-cellulaires |
| BR112020026384A2 (pt) | 2018-06-23 | 2021-03-30 | Genentech, Inc. | Métodos para tratar um indivíduo com câncer de pulmão e para tratar um indivíduo com câncer de pulmão de pequenas células, kits, anticorpo anti-pd-l1 e composição |
| WO2020001526A1 (zh) * | 2018-06-29 | 2020-01-02 | 苏州智核生物医药科技有限公司 | Pd-l1结合多肽及其用途 |
| CA3099176A1 (en) * | 2018-06-29 | 2020-01-02 | Alector Llc | Anti-sirp-beta1 antibodies and methods of use thereof |
| IL278951B (en) | 2018-07-10 | 2022-08-01 | Novartis Ag | History of 3-(5-hydroxy-1-oxoisoindolin-2-yl)piperidine-6,2-dione and their use in the treatment of ikzf2-dependent diseases |
| AR116109A1 (es) | 2018-07-10 | 2021-03-31 | Novartis Ag | Derivados de 3-(5-amino-1-oxoisoindolin-2-il)piperidina-2,6-diona y usos de los mismos |
| GB201811403D0 (en) | 2018-07-12 | 2018-08-29 | F Star Beta Ltd | Antibody molecules |
| CA3104147A1 (en) | 2018-07-18 | 2020-01-23 | Genentech, Inc. | Methods of treating lung cancer with a pd-1 axis binding antagonist, an antimetabolite, and a platinum agent |
| SG11202100693UA (en) | 2018-07-26 | 2021-02-25 | Bristol Myers Squibb Co | Lag-3 combination therapy for the treatment of cancer |
| ES2930171T3 (es) | 2018-08-16 | 2022-12-07 | Innate Tumor Immunity Inc | Moduladores de NLRP3 derivados de imidazo[4,5-C]quinolina |
| US20210317118A1 (en) | 2018-08-16 | 2021-10-14 | Innate Tumor Immunity, Inc. | Nlrp3 modulators |
| BR112021002642A2 (pt) | 2018-08-16 | 2021-05-04 | Innate Tumor Immunity, Inc. | compostos de 4-amino-1h-imidazo[4,5-c]quinolina substituídos e métodos aprimorados para a preparação dos mesmos |
| WO2020051099A1 (en) | 2018-09-03 | 2020-03-12 | Genentech, Inc. | Carboxamide and sulfonamide derivatives useful as tead modulators |
| KR20210072059A (ko) | 2018-10-09 | 2021-06-16 | 브리스톨-마이어스 스큅 컴퍼니 | 암을 치료하기 위한 항-MerTK 항체 |
| CA3117016A1 (en) | 2018-10-19 | 2020-04-23 | Bristol-Myers Squibb Company | Combination therapy for melanoma |
| WO2020086724A1 (en) | 2018-10-23 | 2020-04-30 | Bristol-Myers Squibb Company | Methods of treating tumor |
| MX2021004906A (es) | 2018-10-29 | 2021-09-10 | Mersana Therapeutics Inc | Conjugados de anticuerpo modificado con cisteína-fármaco con enlazadores que contienen péptidos. |
| WO2020089811A1 (en) | 2018-10-31 | 2020-05-07 | Novartis Ag | Dc-sign antibody drug conjugates |
| JP2022513029A (ja) | 2018-11-14 | 2022-02-07 | リジェネロン・ファーマシューティカルズ・インコーポレイテッド | 皮膚がんを治療するためのpd-1阻害剤の病変内投与 |
| TW202033555A (zh) | 2018-11-16 | 2020-09-16 | 美商必治妥美雅史谷比公司 | 抗nkg2a抗體及其用途 |
| CN113490499A (zh) | 2018-12-04 | 2021-10-08 | 大日本住友制药肿瘤公司 | 用作治疗癌症的活性剂的cdk9抑制剂及其多晶型物 |
| WO2020117849A1 (en) | 2018-12-04 | 2020-06-11 | Bristol-Myers Squibb Company | Methods of analysis using in-sample calibration curve by multiple isotopologue reaction monitoring |
| MX2021007392A (es) | 2018-12-20 | 2021-08-24 | Novartis Ag | Regimen de dosificacion y combinacion farmaceutica que comprende derivados de 3-(1-oxoisoindolin-2-il)piperidina-2,6-diona. |
| JP2022514087A (ja) | 2018-12-21 | 2022-02-09 | ノバルティス アーゲー | IL-1β結合抗体の使用 |
| US20220025036A1 (en) | 2018-12-21 | 2022-01-27 | Novartis Ag | Use of il-1beta binding antibodies |
| WO2020128637A1 (en) | 2018-12-21 | 2020-06-25 | Novartis Ag | Use of il-1 binding antibodies in the treatment of a msi-h cancer |
| AU2019408408A1 (en) | 2018-12-21 | 2021-06-03 | Valerio Therapeutics | New conjugated nucleic acid molecules and their uses |
| SG11202104699TA (en) | 2018-12-21 | 2021-07-29 | Novartis Ag | Use of il-1 beta antibodies in the treatment or prevention of myelodysplastic syndrome |
| WO2020136235A1 (en) | 2018-12-28 | 2020-07-02 | Transgene Sa | M2-defective poxvirus |
| JP7335341B2 (ja) | 2019-01-14 | 2023-08-29 | イネイト・テューマー・イミュニティ・インコーポレイテッド | Nlrp3モジュレーター |
| KR20210114983A (ko) | 2019-01-14 | 2021-09-24 | 인네이트 튜머 이뮤니티, 인코포레이티드 | Nlrp3 조정제 |
| KR20210114982A (ko) | 2019-01-14 | 2021-09-24 | 인네이트 튜머 이뮤니티, 인코포레이티드 | 암의 치료에 사용하기 위한 헤테로시클릭 nlrp3 조정제 |
| TW202043272A (zh) | 2019-01-14 | 2020-12-01 | 美商建南德克公司 | 使用pd-1軸結合拮抗劑及rna疫苗治療癌症之方法 |
| EP3911416A1 (en) | 2019-01-14 | 2021-11-24 | Innate Tumor Immunity, Inc. | Substituted quinazolines as nlrp3 modulators, for use in the treatment of cancer |
| US20220098304A1 (en) | 2019-02-03 | 2022-03-31 | Jiangsu Hengrui Medicine Co., Ltd. | Anti-pd-1 antibody, antigen-binding fragment thereof and pharmaceutical use thereof |
| JP2022520361A (ja) | 2019-02-12 | 2022-03-30 | スミトモ ダイニッポン ファーマ オンコロジー, インコーポレイテッド | 複素環式タンパク質キナーゼ阻害剤を含む製剤 |
| US20220107320A1 (en) | 2019-02-15 | 2022-04-07 | Incelldx, Inc. | Assaying Bladder-Associated Samples, Identifying and Treating Bladder-Associated Neoplasia, and Kits for Use Therein |
| KR20210129672A (ko) | 2019-02-15 | 2021-10-28 | 노파르티스 아게 | 치환된 3-(1-옥소이소인돌린-2-일)피페리딘-2,6-디온 유도체 및 이의 용도 |
| JP2022520811A (ja) | 2019-02-15 | 2022-04-01 | ノバルティス アーゲー | 3-(1-オキソ-5-(ピペリジン-4-イル)イソインドリン-2-イル)ピペリジン-2,6-ジオン誘導体及びその使用 |
| CN113490529A (zh) | 2019-02-28 | 2021-10-08 | 瑞泽恩制药公司 | 用于治疗皮肤癌的pd-1抑制剂的施用 |
| CA3129963A1 (en) | 2019-03-06 | 2020-09-10 | Regeneron Pharmaceuticals, Inc. | Il-4/il-13 pathway inhibitors for enhanced efficacy in treating cancer |
| WO2020191326A1 (en) | 2019-03-20 | 2020-09-24 | Sumitomo Dainippon Pharma Oncology, Inc. | Treatment of acute myeloid leukemia (aml) with venetoclax failure |
| AU2020245437A1 (en) | 2019-03-22 | 2021-09-30 | Sumitomo Pharma Oncology, Inc. | Compositions comprising PKM2 modulators and methods of treatment using the same |
| KR20210146348A (ko) | 2019-03-28 | 2021-12-03 | 브리스톨-마이어스 스큅 컴퍼니 | 종양을 치료하는 방법 |
| US20220195046A1 (en) | 2019-03-28 | 2022-06-23 | Bristol-Myers Squibb Company | Methods of treating tumor |
| WO2020215020A1 (en) * | 2019-04-18 | 2020-10-22 | Qlsf Biotherapeutics Inc. | Humanized anti-pd-l1 antibodies |
| WO2020214995A1 (en) | 2019-04-19 | 2020-10-22 | Genentech, Inc. | Anti-mertk antibodies and their methods of use |
| EP3962493A2 (en) | 2019-05-03 | 2022-03-09 | Flagship Pioneering Innovations V, Inc. | Methods of modulating immune activity/level of irf or sting or of treating cancer, comprising the administration of a sting modulator and/or purinergic receptor modulator or postcellular signaling factor |
| EP3962947A2 (en) | 2019-05-03 | 2022-03-09 | F. Hoffmann-La Roche AG | Methods of treating cancer with an anti-pd-l1 antibody |
| WO2020231766A1 (en) | 2019-05-13 | 2020-11-19 | Bristol-Myers Squibb Company | AGONISTS OF ROR GAMMAt |
| US20230242478A1 (en) | 2019-05-13 | 2023-08-03 | Bristol-Myers Squibb Company | AGONISTS OF ROR GAMMAt |
| JP2022534967A (ja) | 2019-05-30 | 2022-08-04 | ブリストル-マイヤーズ スクイブ カンパニー | 多腫瘍遺伝子シグネチャーおよびその使用 |
| CN110156895B (zh) * | 2019-05-30 | 2020-11-20 | 上海甲贝生物医药技术股份有限公司 | 一种抗pd-l1抗体或其功能性片段及其用途 |
| KR20220016157A (ko) | 2019-05-30 | 2022-02-08 | 브리스톨-마이어스 스큅 컴퍼니 | 세포 국재화 시그너쳐 및 조합 요법 |
| CN114127315A (zh) | 2019-05-30 | 2022-03-01 | 百时美施贵宝公司 | 鉴定适合于免疫肿瘤学(i-o)疗法的受试者的方法 |
| US11246906B2 (en) | 2019-06-11 | 2022-02-15 | Alkermes Pharma Ireland Limited | Compositions and methods for subcutaneous administration of cancer immunotherapy |
| WO2020264410A1 (en) * | 2019-06-26 | 2020-12-30 | Sensor-Kinesis Corporation | Troponin t binding agents and uses thereof |
| CA3145864A1 (en) | 2019-07-03 | 2021-01-07 | Sumitomo Dainippon Pharma Oncology, Inc. | Tyrosine kinase non-receptor 1 (tnk1) inhibitors and uses thereof |
| US20220306630A1 (en) | 2019-08-06 | 2022-09-29 | Bristol-Myers Squibb Company | AGONISTS OF ROR GAMMAt |
| WO2021024020A1 (en) | 2019-08-06 | 2021-02-11 | Astellas Pharma Inc. | Combination therapy involving antibodies against claudin 18.2 and immune checkpoint inhibitors for treatment of cancer |
| JP2022545741A (ja) | 2019-08-30 | 2022-10-28 | アジェナス インコーポレイテッド | 抗cd96抗体およびその使用方法 |
| CA3151022A1 (en) | 2019-09-17 | 2021-03-25 | Bial - R&D Investments, S.A. | Substituted n-heterocyclic carboxamides as acid ceramidase inhibitors and their use as medicaments |
| CN114901652A (zh) | 2019-09-17 | 2022-08-12 | 比亚尔R&D投资股份公司 | 用于治疗医学病症的经取代的饱和和不饱和n-杂环甲酰胺及相关化合物 |
| AU2020349516A1 (en) | 2019-09-17 | 2022-03-17 | Bial-R&D Investments, S.A. | Substituted imidazole carboxamides and their use in the treatment of medical disorders |
| US20220348651A1 (en) | 2019-09-18 | 2022-11-03 | Novartis Ag | Entpd2 antibodies, combination therapies, and methods of using the antibodies and combination therapies |
| TW202124446A (zh) | 2019-09-18 | 2021-07-01 | 瑞士商諾華公司 | 與entpd2抗體之組合療法 |
| KR20220066334A (ko) | 2019-09-22 | 2022-05-24 | 브리스톨-마이어스 스큅 컴퍼니 | Lag-3 길항제 요법에 대한 정량적 공간 프로파일링 |
| BR112022005655A2 (pt) | 2019-09-25 | 2022-09-06 | Bristol Myers Squibb Co | Biomarcador compósito para terapia para câncer |
| US11628222B2 (en) | 2019-10-14 | 2023-04-18 | Aro Biotherapeutics Company | CD71 binding fibronectin type III domains |
| US11781138B2 (en) | 2019-10-14 | 2023-10-10 | Aro Biotherapeutics Company | FN3 domain-siRNA conjugates and uses thereof |
| TW202128191A (zh) | 2019-10-21 | 2021-08-01 | 瑞士商諾華公司 | Tim-3抑制劑及其用途 |
| CN114786679A (zh) | 2019-10-21 | 2022-07-22 | 诺华股份有限公司 | 具有维奈托克和tim-3抑制剂的组合疗法 |
| WO2021092220A1 (en) | 2019-11-06 | 2021-05-14 | Bristol-Myers Squibb Company | Methods of identifying a subject with a tumor suitable for a checkpoint inhibitor therapy |
| WO2021092221A1 (en) | 2019-11-06 | 2021-05-14 | Bristol-Myers Squibb Company | Methods of identifying a subject with a tumor suitable for a checkpoint inhibitor therapy |
| JP2022553851A (ja) | 2019-11-08 | 2022-12-26 | ブリストル-マイヤーズ スクイブ カンパニー | 黒色腫の処置のためのlag-3アンタゴニスト |
| CA3155989A1 (en) | 2019-11-13 | 2021-05-20 | Jason Robert ZBIEG | Therapeutic compounds and methods of use |
| US20220395553A1 (en) | 2019-11-14 | 2022-12-15 | Cohbar, Inc. | Cxcr4 antagonist peptides |
| WO2021102343A1 (en) | 2019-11-22 | 2021-05-27 | Sumitomo Dainippon Pharma Oncology, Inc. | Solid dose pharmaceutical composition |
| JP2023505256A (ja) | 2019-12-05 | 2023-02-08 | ソレント・セラピューティクス・インコーポレイテッド | 腫瘍ターゲティング抗体と組み合わせた抗cd47抗体を含む組成物および方法 |
| US20230114107A1 (en) | 2019-12-17 | 2023-04-13 | Flagship Pioneering Innovations V, Inc. | Combination anti-cancer therapies with inducers of iron-dependent cellular disassembly |
| CA3158532A1 (en) | 2019-12-19 | 2021-06-24 | Susan Wee | Combinations of dgk inhibitors and checkpoint antagonists |
| WO2021123902A1 (en) | 2019-12-20 | 2021-06-24 | Novartis Ag | Combination of anti tim-3 antibody mbg453 and anti tgf-beta antibody nis793, with or without decitabine or the anti pd-1 antibody spartalizumab, for treating myelofibrosis and myelodysplastic syndrome |
| CN113121686A (zh) * | 2019-12-31 | 2021-07-16 | 迈威(上海)生物科技股份有限公司 | 抗pd-l1抗体及其应用 |
| WO2021142203A1 (en) | 2020-01-10 | 2021-07-15 | Innate Tumor Immunity, Inc. | Nlrp3 modulators |
| IL293752A (en) | 2020-01-17 | 2022-08-01 | Novartis Ag | A combination containing a tim-3 inhibitor and a substance that causes hypomethylation for use in the treatment of myeloplastic syndrome or chronic myelomonocytic leukemia |
| KR20210095781A (ko) | 2020-01-24 | 2021-08-03 | 주식회사 에이프릴바이오 | 항원결합 단편 및 생리활성 이펙터 모이어티로 구성된 융합 컨스트럭트를 포함하는 다중결합항체 및 이를 포함하는 약학조성물 |
| CA3161513A1 (en) | 2020-01-28 | 2021-08-05 | Irwin DAVIDSON | Antisense oligonucleotide targeting linc00518 for treating melanoma |
| CN114945596A (zh) | 2020-01-29 | 2022-08-26 | 美勒斯公司 | 用于调节免疫细胞衔接效应的手段和方法 |
| KR20220133996A (ko) | 2020-01-30 | 2022-10-05 | 오엔에이 테라퓨틱스 에스.엘. | 암 및 암 전이를 치료하기 위한 병용 요법 |
| CN116650628A (zh) | 2020-01-31 | 2023-08-29 | 基因泰克公司 | 用pd-1轴结合拮抗剂和rna疫苗诱导新表位特异性t细胞的方法 |
| WO2021158938A1 (en) | 2020-02-06 | 2021-08-12 | Bristol-Myers Squibb Company | Il-10 and uses thereof |
| JP2023515633A (ja) | 2020-02-28 | 2023-04-13 | ブリストル-マイヤーズ スクイブ カンパニー | 放射性標識されたフィブロネクチンに基づく足場および抗体ならびにそのセラノスティクス的使用 |
| JP2023517011A (ja) | 2020-03-05 | 2023-04-21 | ネオティーエックス セラピューティクス リミテッド | 免疫細胞を用いて癌を治療するための方法および組成物 |
| MX2022010912A (es) | 2020-03-06 | 2022-11-09 | Celgene Quanticel Res Inc | Combinacion de un inhibidor de desmetilasa-1 especifica de lisina (lsd-1) y nivolumab para usarse en el tratamiento de cancer de pulmon de celulas peque?as (sclc) o cancer de pulmon de celulas no peque?as escamosas (sqnsclc). |
| CA3174442A1 (en) | 2020-03-06 | 2021-09-10 | ONA Therapeutics S.L. | Anti-cd36 antibodies and their use to treat cancer |
| CA3172697A1 (en) | 2020-03-23 | 2021-09-30 | Ruth Yin-Zong LAN | Anti-ccr8 antibodies for treating cancer |
| JP7240512B2 (ja) | 2020-05-26 | 2023-03-15 | リジェネロン・ファーマシューティカルズ・インコーポレイテッド | Pd-1阻害剤を投与することにより子宮頸がんを処置する方法 |
| TW202214857A (zh) | 2020-06-19 | 2022-04-16 | 法商昂席歐公司 | 新型結合核酸分子及其用途 |
| JP2023531676A (ja) | 2020-06-23 | 2023-07-25 | ノバルティス アーゲー | 3-(1-オキソイソインドリン-2-イル)ピぺリジン-2,6-ジオン誘導体を含む投与レジメン |
| JP2023532339A (ja) | 2020-06-29 | 2023-07-27 | フラグシップ パイオニアリング イノベーションズ ブイ,インコーポレーテッド | サノトランスミッションを促進するためにエンジニアリングされたウイルス及び癌の処置におけるそれらの使用 |
| US20220023405A1 (en) | 2020-06-30 | 2022-01-27 | Dcprime B.V. | Use of leukemia-derived cells in ovarian cancer vaccines |
| EP4178611A1 (en) | 2020-07-07 | 2023-05-17 | BioNTech SE | Therapeutic rna for hpv-positive cancer |
| US11787775B2 (en) | 2020-07-24 | 2023-10-17 | Genentech, Inc. | Therapeutic compounds and methods of use |
| JP2023536164A (ja) | 2020-08-03 | 2023-08-23 | ノバルティス アーゲー | ヘテロアリール置換3-(1-オキソイソインドリン-2-イル)ピペリジン-2,6-ジオン誘導体及びその使用 |
| MX2023002123A (es) | 2020-08-26 | 2023-03-15 | Regeneron Pharma | Metodos de tratamiento de cancer mediante la administracion de un inhibidor de pd-1. |
| EP4204095A1 (en) | 2020-08-28 | 2023-07-05 | Bristol-Myers Squibb Company | Lag-3 antagonist therapy for hepatocellular carcinoma |
| AU2021334361A1 (en) | 2020-08-31 | 2023-05-11 | Bristol-Myers Squibb Company | Cell localization signature and immunotherapy |
| WO2022051448A1 (en) | 2020-09-03 | 2022-03-10 | Regeneron Pharmaceuticals, Inc. | Methods of treating cancer pain by administering a pd-1 inhibitor |
| WO2022076318A1 (en) | 2020-10-05 | 2022-04-14 | Bristol-Myers Squibb Company | Methods for concentrating proteins |
| US20230364127A1 (en) | 2020-10-06 | 2023-11-16 | Codiak Biosciences, Inc. | Extracellular vesicle-aso constructs targeting stat6 |
| AR123855A1 (es) | 2020-10-20 | 2023-01-18 | Genentech Inc | Anticuerpos anti-mertk conjugados con peg y métodos de uso |
| EP4232019A1 (en) | 2020-10-23 | 2023-08-30 | Bristol-Myers Squibb Company | Lag-3 antagonist therapy for lung cancer |
| WO2022093981A1 (en) | 2020-10-28 | 2022-05-05 | Genentech, Inc. | Combination therapy comprising ptpn22 inhibitors and pd-l1 binding antagonists |
| EP4236960A1 (en) | 2020-10-28 | 2023-09-06 | Ikena Oncology, Inc. | Combination of an ahr inhibitor with a pdx inhibitor or doxorubicine |
| WO2022098628A2 (en) | 2020-11-04 | 2022-05-12 | Genentech, Inc. | Subcutaneous dosing of anti-cd20/anti-cd3 bispecific antibodies |
| WO2022098638A2 (en) | 2020-11-04 | 2022-05-12 | Genentech, Inc. | Dosing for treatment with anti-cd20/anti-cd3 bispecific antibodies |
| IL302217A (en) | 2020-11-04 | 2023-06-01 | Genentech Inc | Dosage for treatment with bispecific anti-CD20/anti-CD3 antibodies and anti-CD79B drug antibody conjugates |
| EP4240491A1 (en) | 2020-11-06 | 2023-09-13 | Novartis AG | Cd19 binding molecules and uses thereof |
| CA3201519A1 (en) | 2020-11-13 | 2022-05-19 | Genentech, Inc. | Methods and compositions comprising a krasg12c inhibitor and a pd-l1 binding antagonist for treating lung cancer |
| WO2022119830A1 (en) | 2020-12-02 | 2022-06-09 | Genentech, Inc. | Methods and compositions for neoadjuvant and adjuvant urothelial carcinoma therapy |
| WO2022120179A1 (en) | 2020-12-03 | 2022-06-09 | Bristol-Myers Squibb Company | Multi-tumor gene signatures and uses thereof |
| CA3201219A1 (en) | 2020-12-04 | 2022-06-09 | Mir Ali | Ionizable cationic lipids and lipid nanoparticles, and methods of synthesis and use thereof |
| TW202237119A (zh) | 2020-12-10 | 2022-10-01 | 美商住友製藥腫瘤公司 | Alk﹘5抑制劑和彼之用途 |
| WO2022135667A1 (en) | 2020-12-21 | 2022-06-30 | BioNTech SE | Therapeutic rna for treating cancer |
| WO2022135666A1 (en) | 2020-12-21 | 2022-06-30 | BioNTech SE | Treatment schedule for cytokine proteins |
| TW202245808A (zh) | 2020-12-21 | 2022-12-01 | 德商拜恩迪克公司 | 用於治療癌症之治療性rna |
| US20220233689A1 (en) | 2020-12-28 | 2022-07-28 | Bristol-Myers Squibb Company | Methods of treating tumors |
| US20220233693A1 (en) | 2020-12-28 | 2022-07-28 | Bristol-Myers Squibb Company | Antibody Compositions and Methods of Use Thereof |
| AU2022211682A1 (en) | 2021-01-22 | 2023-08-03 | Mendus B.V. | Methods of tumor vaccination |
| EP4284510A1 (en) | 2021-01-29 | 2023-12-06 | Novartis AG | Dosage regimes for anti-cd73 and anti-entpd2 antibodies and uses thereof |
| TW202241508A (zh) | 2021-01-29 | 2022-11-01 | 美商艾歐凡斯生物治療公司 | 細胞介素相關之腫瘤浸潤性淋巴球組合物及方法 |
| WO2022169921A1 (en) | 2021-02-04 | 2022-08-11 | Bristol-Myers Squibb Company | Benzofuran compounds as sting agonists |
| EP4304633A1 (en) | 2021-03-12 | 2024-01-17 | Mendus B.V. | Methods of vaccination and use of cd47 blockade |
| JP2024511373A (ja) | 2021-03-18 | 2024-03-13 | ノバルティス アーゲー | がんのためのバイオマーカーおよびその使用 |
| JP2024511106A (ja) | 2021-03-23 | 2024-03-12 | リジェネロン・ファーマシューティカルズ・インコーポレイテッド | Pd-1阻害剤を投与することにより免疫抑制または免疫不全患者におけるがんを処置する方法 |
| TW202304506A (zh) | 2021-03-25 | 2023-02-01 | 日商安斯泰來製藥公司 | 涉及抗claudin 18.2抗體的組合治療以治療癌症 |
| CN117858719A (zh) | 2021-03-29 | 2024-04-09 | 朱诺治疗学股份有限公司 | 使用检查点抑制剂疗法和car t细胞疗法的组合进行给药和治疗的方法 |
| US20220325287A1 (en) | 2021-03-31 | 2022-10-13 | Flagship Pioneering Innovations V, Inc. | Thanotransmission polypeptides and their use in treating cancer |
| JP2024514530A (ja) | 2021-04-02 | 2024-04-02 | ザ リージェンツ オブ ザ ユニバーシティ オブ カリフォルニア | 切断型cdcp1に対する抗体およびその使用 |
| TW202304979A (zh) | 2021-04-07 | 2023-02-01 | 瑞士商諾華公司 | 抗TGFβ抗體及其他治療劑用於治療增殖性疾病之用途 |
| TW202309022A (zh) | 2021-04-13 | 2023-03-01 | 美商努法倫特公司 | 用於治療具egfr突變之癌症之胺基取代雜環 |
| CN117321078A (zh) | 2021-04-30 | 2023-12-29 | 豪夫迈·罗氏有限公司 | 针对用抗cd20/抗cd3双特异性抗体和抗cd79b抗体药物缀合物进行组合治疗的给药 |
| EP4330436A1 (en) | 2021-04-30 | 2024-03-06 | Genentech, Inc. | Therapeutic and diagnostic methods and compositions for cancer |
| WO2022243378A1 (en) | 2021-05-18 | 2022-11-24 | Kymab Limited | Uses of anti-icos antibodies |
| AR125874A1 (es) | 2021-05-18 | 2023-08-23 | Novartis Ag | Terapias de combinación |
| GB202107994D0 (en) | 2021-06-04 | 2021-07-21 | Kymab Ltd | Treatment of cancer |
| EP4352100A1 (en) | 2021-06-09 | 2024-04-17 | Sorrento Therapeutics, Inc. | Method of treating cancer by administration of an anti-pd-1 or anti-pd-l1 therapeutic agent via a lymphatic microneedle delivery device |
| WO2023278641A1 (en) | 2021-06-29 | 2023-01-05 | Flagship Pioneering Innovations V, Inc. | Immune cells engineered to promote thanotransmission and uses thereof |
| KR20240028452A (ko) | 2021-07-02 | 2024-03-05 | 제넨테크, 인크. | 암을 치료하기 위한 방법 및 조성물 |
| AU2022312698A1 (en) | 2021-07-13 | 2024-01-25 | BioNTech SE | Multispecific binding agents against cd40 and cd137 in combination therapy for cancer |
| US20230139492A1 (en) | 2021-07-19 | 2023-05-04 | Regeneron Pharmaceuticals, Inc. | Combination of checkpoint inhibitors and an oncolytic virus for treating cancer |
| WO2023010094A2 (en) | 2021-07-28 | 2023-02-02 | Genentech, Inc. | Methods and compositions for treating cancer |
| AU2022317820A1 (en) | 2021-07-28 | 2023-12-14 | F. Hoffmann-La Roche Ag | Methods and compositions for treating cancer |
| CA3226281A1 (en) | 2021-07-30 | 2023-02-02 | ONA Therapeutics S.L. | Anti-cd36 antibodies and their use to treat cancer |
| CA3229448A1 (en) | 2021-08-23 | 2023-03-02 | Immunitas Therapeutics, Inc. | Anti-cd161 antibodies and uses thereof |
| WO2023051926A1 (en) | 2021-09-30 | 2023-04-06 | BioNTech SE | Treatment involving non-immunogenic rna for antigen vaccination and pd-1 axis binding antagonists |
| TW202321308A (zh) | 2021-09-30 | 2023-06-01 | 美商建南德克公司 | 使用抗tigit抗體、抗cd38抗體及pd—1軸結合拮抗劑治療血液癌症的方法 |
| TW202333802A (zh) | 2021-10-11 | 2023-09-01 | 德商拜恩迪克公司 | 用於肺癌之治療性rna(二) |
| IL309227A (en) | 2021-10-29 | 2024-02-01 | Bristol Myers Squibb Co | LAG-3 antagonist therapy for hematological cancer |
| WO2023080900A1 (en) | 2021-11-05 | 2023-05-11 | Genentech, Inc. | Methods and compositions for classifying and treating kidney cancer |
| WO2023083439A1 (en) | 2021-11-09 | 2023-05-19 | BioNTech SE | Tlr7 agonist and combinations for cancer treatment |
| TW202340212A (zh) | 2021-11-24 | 2023-10-16 | 美商建南德克公司 | 治療性化合物及其使用方法 |
| WO2023097195A1 (en) | 2021-11-24 | 2023-06-01 | Genentech, Inc. | Therapeutic indazole compounds and methods of use in the treatment of cancer |
| WO2023111203A1 (en) | 2021-12-16 | 2023-06-22 | Onxeo | New conjugated nucleic acid molecules and their uses |
| WO2023137161A1 (en) | 2022-01-14 | 2023-07-20 | Amgen Inc. | Triple blockade of tigit, cd112r, and pd-l1 |
| WO2023147371A1 (en) | 2022-01-26 | 2023-08-03 | Bristol-Myers Squibb Company | Combination therapy for hepatocellular carcinoma |
| WO2023147488A1 (en) | 2022-01-28 | 2023-08-03 | Iovance Biotherapeutics, Inc. | Cytokine associated tumor infiltrating lymphocytes compositions and methods |
| WO2023159102A1 (en) | 2022-02-17 | 2023-08-24 | Regeneron Pharmaceuticals, Inc. | Combinations of checkpoint inhibitors and oncolytic virus for treating cancer |
| WO2023164638A1 (en) | 2022-02-25 | 2023-08-31 | Bristol-Myers Squibb Company | Combination therapy for colorectal carcinoma |
| WO2023168404A1 (en) | 2022-03-04 | 2023-09-07 | Bristol-Myers Squibb Company | Methods of treating a tumor |
| WO2023170606A1 (en) | 2022-03-08 | 2023-09-14 | Alentis Therapeutics Ag | Use of anti-claudin-1 antibodies to increase t cell availability |
| WO2023174210A1 (en) | 2022-03-14 | 2023-09-21 | Laekna Limited | Combination treatment for cancer |
| WO2023178329A1 (en) | 2022-03-18 | 2023-09-21 | Bristol-Myers Squibb Company | Methods of isolating polypeptides |
| WO2023191816A1 (en) | 2022-04-01 | 2023-10-05 | Genentech, Inc. | Dosing for treatment with anti-fcrh5/anti-cd3 bispecific antibodies |
| WO2023196987A1 (en) | 2022-04-07 | 2023-10-12 | Bristol-Myers Squibb Company | Methods of treating tumor |
| US20230326022A1 (en) | 2022-04-08 | 2023-10-12 | Bristol-Myers Squibb Company | Machine Learning Identification, Classification, and Quantification of Tertiary Lymphoid Structures |
| WO2023214325A1 (en) | 2022-05-05 | 2023-11-09 | Novartis Ag | Pyrazolopyrimidine derivatives and uses thereof as tet2 inhibitors |
| WO2023219613A1 (en) | 2022-05-11 | 2023-11-16 | Genentech, Inc. | Dosing for treatment with anti-fcrh5/anti-cd3 bispecific antibodies |
| WO2023220703A1 (en) | 2022-05-12 | 2023-11-16 | Genentech, Inc. | Methods and compositions comprising a shp2 inhibitor and a pd-l1 binding antagonist |
| WO2023222854A1 (en) | 2022-05-18 | 2023-11-23 | Kymab Limited | Uses of anti-icos antibodies |
| WO2023235847A1 (en) | 2022-06-02 | 2023-12-07 | Bristol-Myers Squibb Company | Antibody compositions and methods of use thereof |
| WO2023240058A2 (en) | 2022-06-07 | 2023-12-14 | Genentech, Inc. | Prognostic and therapeutic methods for cancer |
| WO2023240156A1 (en) | 2022-06-08 | 2023-12-14 | Tidal Therapeutics, Inc. | Ionizable cationic lipids and lipid nanoparticles, and methods of synthesis and use thereof |
| WO2024015897A1 (en) | 2022-07-13 | 2024-01-18 | Genentech, Inc. | Dosing for treatment with anti-fcrh5/anti-cd3 bispecific antibodies |
| WO2024020432A1 (en) | 2022-07-19 | 2024-01-25 | Genentech, Inc. | Dosing for treatment with anti-fcrh5/anti-cd3 bispecific antibodies |
| WO2024023740A1 (en) | 2022-07-27 | 2024-02-01 | Astrazeneca Ab | Combinations of recombinant virus expressing interleukin-12 with pd-1/pd-l1 inhibitors |
| WO2024049949A1 (en) | 2022-09-01 | 2024-03-07 | Genentech, Inc. | Therapeutic and diagnostic methods for bladder cancer |
| WO2024054992A1 (en) | 2022-09-09 | 2024-03-14 | Bristol-Myers Squibb Company | Methods of separating chelator |
| WO2024069009A1 (en) | 2022-09-30 | 2024-04-04 | Alentis Therapeutics Ag | Treatment of drug-resistant hepatocellular carcinoma |
| WO2024077191A1 (en) | 2022-10-05 | 2024-04-11 | Flagship Pioneering Innovations V, Inc. | Nucleic acid molecules encoding trif and additionalpolypeptides and their use in treating cancer |
| WO2024077166A1 (en) | 2022-10-05 | 2024-04-11 | Genentech, Inc. | Methods and compositions for classifying and treating lung cancer |
| WO2024077095A1 (en) | 2022-10-05 | 2024-04-11 | Genentech, Inc. | Methods and compositions for classifying and treating bladder cancer |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2004526740A (ja) * | 2001-04-02 | 2004-09-02 | ワイス | Pd−1の、そのリガンドとの相互作用の調節 |
| JP2008544755A (ja) * | 2005-07-01 | 2008-12-11 | メダレックス インコーポレーティッド | プログラム死リガンド1(pd−l1)に対するヒトモノクローナル抗体 |
| WO2011066389A1 (en) * | 2009-11-24 | 2011-06-03 | Medimmmune, Limited | Targeted binding agents against b7-h1 |
| JP2012511329A (ja) * | 2008-12-09 | 2012-05-24 | ジェネンテック, インコーポレイテッド | 抗pd−l1抗体およびt細胞機能を増強するためのそれらの使用 |
Family Cites Families (50)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| NL154598B (nl) | 1970-11-10 | 1977-09-15 | Organon Nv | Werkwijze voor het aantonen en bepalen van laagmoleculire verbindingen en van eiwitten die deze verbindingen specifiek kunnen binden, alsmede testverpakking. |
| US3901654A (en) | 1971-06-21 | 1975-08-26 | Biological Developments | Receptor assays of biologically active compounds employing biologically specific receptors |
| US3817827A (en) | 1972-03-30 | 1974-06-18 | Scott Paper Co | Soft absorbent fibrous webs containing elastomeric bonding material and formed by creping and embossing |
| US4179337A (en) | 1973-07-20 | 1979-12-18 | Davis Frank F | Non-immunogenic polypeptides |
| US4002531A (en) | 1976-01-22 | 1977-01-11 | Pierce Chemical Company | Modifying enzymes with polyethylene glycol and product produced thereby |
| US4098876A (en) | 1976-10-26 | 1978-07-04 | Corning Glass Works | Reverse sandwich immunoassay |
| JPS6023084B2 (ja) | 1979-07-11 | 1985-06-05 | 味の素株式会社 | 代用血液 |
| US4640835A (en) | 1981-10-30 | 1987-02-03 | Nippon Chemiphar Company, Ltd. | Plasminogen activator derivatives |
| US4496689A (en) | 1983-12-27 | 1985-01-29 | Miles Laboratories, Inc. | Covalently attached complex of alpha-1-proteinase inhibitor with a water soluble polymer |
| DE3675588D1 (de) | 1985-06-19 | 1990-12-20 | Ajinomoto Kk | Haemoglobin, das an ein poly(alkenylenoxid) gebunden ist. |
| US4791192A (en) | 1986-06-26 | 1988-12-13 | Takeda Chemical Industries, Ltd. | Chemically modified protein with polyethyleneglycol |
| US4946778A (en) | 1987-09-21 | 1990-08-07 | Genex Corporation | Single polypeptide chain binding molecules |
| US6010902A (en) | 1988-04-04 | 2000-01-04 | Bristol-Meyers Squibb Company | Antibody heteroconjugates and bispecific antibodies for use in regulation of lymphocyte activity |
| US5859205A (en) * | 1989-12-21 | 1999-01-12 | Celltech Limited | Humanised antibodies |
| US5766897A (en) | 1990-06-21 | 1998-06-16 | Incyte Pharmaceuticals, Inc. | Cysteine-pegylated proteins |
| GB9014932D0 (en) | 1990-07-05 | 1990-08-22 | Celltech Ltd | Recombinant dna product and method |
| JP3051145B2 (ja) | 1990-08-28 | 2000-06-12 | 住友製薬株式会社 | 新規なポリエチレングリコール誘導体修飾ペプチド |
| US5582996A (en) | 1990-12-04 | 1996-12-10 | The Wistar Institute Of Anatomy & Biology | Bifunctional antibodies and method of preparing same |
| DE4118120A1 (de) | 1991-06-03 | 1992-12-10 | Behringwerke Ag | Tetravalente bispezifische rezeptoren, ihre herstellung und verwendung |
| WO1994004679A1 (en) | 1991-06-14 | 1994-03-03 | Genentech, Inc. | Method for making humanized antibodies |
| US5281698A (en) | 1991-07-23 | 1994-01-25 | Cetus Oncology Corporation | Preparation of an activated polymer ester for protein conjugation |
| JPH05244982A (ja) | 1991-12-06 | 1993-09-24 | Sumitomo Chem Co Ltd | 擬人化b−b10 |
| AU673190B2 (en) | 1992-07-13 | 1996-10-31 | Bionebraska, Inc. | Method for modification of recombinant polypeptides |
| US5382657A (en) | 1992-08-26 | 1995-01-17 | Hoffmann-La Roche Inc. | Peg-interferon conjugates |
| WO1994010308A1 (en) | 1992-10-23 | 1994-05-11 | Immunex Corporation | Methods of preparing soluble, oligomeric proteins |
| US5446090A (en) | 1993-11-12 | 1995-08-29 | Shearwater Polymers, Inc. | Isolatable, water soluble, and hydrolytically stable active sulfones of poly(ethylene glycol) and related polymers for modification of surfaces and molecules |
| US5594409A (en) | 1994-01-31 | 1997-01-14 | Shank; Edward J. | Customer activated device |
| US5824784A (en) | 1994-10-12 | 1998-10-20 | Amgen Inc. | N-terminally chemically modified protein compositions and methods |
| US5932462A (en) | 1995-01-10 | 1999-08-03 | Shearwater Polymers, Inc. | Multiarmed, monofunctional, polymer for coupling to molecules and surfaces |
| US5731168A (en) | 1995-03-01 | 1998-03-24 | Genentech, Inc. | Method for making heteromultimeric polypeptides |
| GB9722131D0 (en) | 1997-10-20 | 1997-12-17 | Medical Res Council | Method |
| GB9928787D0 (en) | 1999-12-03 | 2000-02-02 | Medical Res Council | Direct screening method |
| US6938003B2 (en) | 2000-06-30 | 2005-08-30 | Mahesh Harpale | Method and apparatus for a credibility reporting system to augment an online exchange |
| WO2002026265A2 (en) | 2000-09-29 | 2002-04-04 | Schering Corporation | Pegylated interleukin-10 |
| GB0025144D0 (en) | 2000-10-13 | 2000-11-29 | Medical Res Council | Concatenated nucleic acid sequences |
| CN1753912B (zh) * | 2002-12-23 | 2011-11-02 | 惠氏公司 | 抗pd-1抗体及其用途 |
| US20040202995A1 (en) | 2003-04-09 | 2004-10-14 | Domantis | Nucleic acids, proteins, and screening methods |
| AU2004279441B2 (en) | 2003-10-08 | 2010-07-01 | The Feinstein Institute For Medical Research | Methods and compositions for diagnosis and treatment of B cell chronic lymphocytic leukemia |
| EP4174179A3 (en) * | 2005-08-23 | 2023-09-27 | The Trustees of the University of Pennsylvania | Rna containing modified nucleosides and methods of use thereof |
| CN101104640A (zh) * | 2006-07-10 | 2008-01-16 | 苏州大学 | 抗人pd-l1单克隆抗体制备及应用 |
| CN101122603A (zh) * | 2006-08-08 | 2008-02-13 | 中国科学院上海生命科学研究院 | 可溶性协同信号分子在检测类风湿关节炎中的用途 |
| EP2162149B1 (en) | 2007-06-01 | 2013-11-06 | The Henry M. Jackson Foundation for the Advancement of Military Medicine, Inc. | Vaccine for the prevention of breast cancer relapse |
| WO2009111315A2 (en) | 2008-02-29 | 2009-09-11 | Mayo Foundation For Medical Education And Research | Methods for reducing granulomatous inflammation |
| CA2732003A1 (en) | 2008-07-31 | 2010-02-04 | James D. Marks | Antibodies that neutralize botulinum neurotoxins |
| US20130108641A1 (en) * | 2011-09-14 | 2013-05-02 | Sanofi | Anti-gitr antibodies |
| EP3553086A1 (en) | 2012-05-31 | 2019-10-16 | Sorrento Therapeutics Inc. | Antigen binding proteins that bind pd-l1 |
| IL292449B2 (en) * | 2015-03-13 | 2024-02-01 | Cytomx Therapeutics Inc | Nucleic acids encoding antibodies against PDL1 and methods for their preparation |
| SG11201805422WA (en) * | 2016-01-11 | 2018-07-30 | Inhibrx Inc | Multivalent and multispecific ox40-binding fusion proteins |
| WO2017123650A2 (en) * | 2016-01-11 | 2017-07-20 | Inhibrx Lp | Multivalent and multispecific 41bb-binding fusion proteins |
| CN116333124A (zh) * | 2016-01-29 | 2023-06-27 | 索伦托药业有限公司 | 与pd-l1结合的抗原结合蛋白 |
-
2013
- 2013-05-31 EP EP19155701.6A patent/EP3553086A1/en active Pending
- 2013-05-31 CN CN201380040060.XA patent/CN104736168B/zh active Active
- 2013-05-31 CA CA2872030A patent/CA2872030A1/en active Pending
- 2013-05-31 BR BR112014029883-1A patent/BR112014029883B1/pt active IP Right Grant
- 2013-05-31 CN CN202210723361.3A patent/CN115093480A/zh active Pending
- 2013-05-31 KR KR1020207028069A patent/KR102284247B1/ko active IP Right Grant
- 2013-05-31 KR KR1020147037096A patent/KR102163408B1/ko active IP Right Grant
- 2013-05-31 AU AU2013267161A patent/AU2013267161A1/en not_active Abandoned
- 2013-05-31 KR KR1020227019920A patent/KR20220084444A/ko active Application Filing
- 2013-05-31 KR KR1020217023721A patent/KR102410078B1/ko active IP Right Grant
- 2013-05-31 CA CA3175758A patent/CA3175758A1/en active Pending
- 2013-05-31 CN CN201810955588.4A patent/CN109467601B/zh active Active
- 2013-05-31 EP EP13796457.3A patent/EP2854843A4/en not_active Withdrawn
- 2013-05-31 US US13/907,685 patent/US9175082B2/en active Active
- 2013-05-31 JP JP2015515271A patent/JP2015519375A/ja active Pending
- 2013-05-31 WO PCT/US2013/043775 patent/WO2013181634A2/en active Application Filing
-
2014
- 2014-12-30 CO CO14286019A patent/CO7160115A2/es unknown
-
2015
- 2015-05-28 HK HK15105082.1A patent/HK1204557A1/xx unknown
- 2015-09-24 US US14/864,677 patent/US20170182161A1/en not_active Abandoned
-
2017
- 2017-06-09 US US15/619,389 patent/US10058609B2/en active Active
- 2017-08-10 JP JP2017155655A patent/JP6648080B2/ja active Active
-
2018
- 2018-04-06 AU AU2018202465A patent/AU2018202465B2/en active Active
- 2018-08-24 US US16/111,995 patent/US11027012B2/en active Active
-
2020
- 2020-01-15 JP JP2020004101A patent/JP6829330B2/ja active Active
- 2020-06-19 AU AU2020204113A patent/AU2020204113B2/en active Active
-
2021
- 2021-01-21 JP JP2021008088A patent/JP2021061862A/ja active Pending
- 2021-05-03 US US17/306,395 patent/US11878058B2/en active Active
-
2022
- 2022-02-08 JP JP2022017798A patent/JP2022058932A/ja active Pending
- 2022-06-27 AU AU2022204504A patent/AU2022204504A1/en active Pending
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2004526740A (ja) * | 2001-04-02 | 2004-09-02 | ワイス | Pd−1の、そのリガンドとの相互作用の調節 |
| JP2008544755A (ja) * | 2005-07-01 | 2008-12-11 | メダレックス インコーポレーティッド | プログラム死リガンド1(pd−l1)に対するヒトモノクローナル抗体 |
| JP2012511329A (ja) * | 2008-12-09 | 2012-05-24 | ジェネンテック, インコーポレイテッド | 抗pd−l1抗体およびt細胞機能を増強するためのそれらの使用 |
| WO2011066389A1 (en) * | 2009-11-24 | 2011-06-03 | Medimmmune, Limited | Targeted binding agents against b7-h1 |
Cited By (22)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2018531219A (ja) * | 2015-08-24 | 2018-10-25 | イーライ リリー アンド カンパニー | Pd−l1抗体 |
| JP2019503687A (ja) * | 2016-01-04 | 2019-02-14 | ジアンスー ヒャマブ ファーマシューティカル カンパニー リミテッド | 抗pd−l1抗体およびその使用 |
| US10889648B2 (en) | 2016-01-04 | 2021-01-12 | Jiangsu Hyamab Pharmaceutical Co., Ltd. | Anti-PD-L1 antibodies and uses thereof |
| JP2021102633A (ja) * | 2016-01-29 | 2021-07-15 | ソレント・セラピューティクス・インコーポレイテッドSorrento Therapeutics, Inc. | Pd−l1に結合する抗原結合性タンパク質 |
| JP7140867B2 (ja) | 2016-01-29 | 2022-09-21 | ソレント・セラピューティクス・インコーポレイテッド | Pd-l1に結合する抗原結合性タンパク質 |
| US11136413B2 (en) | 2016-03-04 | 2021-10-05 | Sichuan Kelun-Biotech Biopharmaceutical Co., Ltd. | PDL-1 antibody, pharmaceutical composition thereof, and uses thereof |
| JP2018526974A (ja) * | 2016-03-04 | 2018-09-20 | シチュアン ケルン−バイオテック バイオファーマシューティカル カンパニー リミテッド | Pdl−1抗体、その医薬組成物及びその使用 |
| US10465014B2 (en) | 2016-03-04 | 2019-11-05 | Sichuan Kelun-Biotech Biopharmaceutical Co., Ltd. | PDL-1 antibody, pharmaceutical composition thereof, and uses thereof |
| JP2019516394A (ja) * | 2016-03-23 | 2019-06-20 | マブスペース バイオサイエンシズ (スーチョウ) カンパニー,リミテッド | 新規抗pd−l1抗体 |
| US11753473B2 (en) | 2016-03-23 | 2023-09-12 | Suzhou Transcenta Therapeutics Co., Ltd. | Anti-PD-L1 antibodies |
| JP2022068161A (ja) * | 2016-03-23 | 2022-05-09 | スーチョウ トランセンタ セラピューティクス カンパニー,リミテッド | 新規抗pd-l1抗体 |
| JP7345578B2 (ja) | 2016-03-23 | 2023-09-15 | スーチョウ トランセンタ セラピューティクス カンパニー,リミテッド | 新規抗pd-l1抗体 |
| JP2022058740A (ja) * | 2016-03-30 | 2022-04-12 | マイクロバイオ カンパニー, リミテッド | 免疫チェックポイントモジュレーターおよび共生微生物叢による発酵産物の併用がん療法 |
| JP7442555B2 (ja) | 2016-03-30 | 2024-03-04 | マイクロバイオ カンパニー, リミテッド | 免疫チェックポイントモジュレーターおよび共生微生物叢による発酵産物の併用がん療法 |
| JP2019510041A (ja) * | 2016-03-30 | 2019-04-11 | マイクロバイオ カンパニー, リミテッド | 免疫チェックポイントモジュレーターおよび共生微生物叢による発酵産物の併用がん療法 |
| JP2019514853A (ja) * | 2016-05-20 | 2019-06-06 | ルェヤン(スーツォ)バイオロジー サイエンス アンド テクノロジー シーオー.,エルティーディー | 抗人pd−l1人源化単クローン抗体及び応用 |
| JP2021509258A (ja) * | 2017-12-29 | 2021-03-25 | エーピー バイオサイエンスィズ インコーポレイテッド | 癌治療のために免疫チェックポイントを調節する単一特異性および二重特異性タンパク質 |
| US11643470B2 (en) | 2017-12-29 | 2023-05-09 | Ap Biosciences, Inc. | PD-L1 and OX40 binding proteins for cancer Regulation |
| JP2021534750A (ja) * | 2018-08-20 | 2021-12-16 | 1グローブ バイオメディカル カンパニー, リミテッド | 新規ながん免疫療法抗体組成物 |
| JP2022511311A (ja) * | 2019-04-26 | 2022-01-31 | アイ-エムエービー バイオファーマ ユーエス リミテッド | ヒトpd‐l1抗体 |
| JP7212990B2 (ja) | 2019-04-26 | 2023-01-26 | アイ-エムエービー バイオファーマ ユーエス リミテッド | ヒトpd‐l1抗体 |
| JP2022528007A (ja) * | 2019-06-10 | 2022-06-07 | 山東博安生物技術股▲ふん▼有限公司 | PDL1及びTGFβに対する二機能性融合タンパク質並びにその使用 |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6829330B2 (ja) | Pd−l1に結合する抗原結合蛋白質 | |
| JP6997743B2 (ja) | Pd-1に結合する抗原結合蛋白質 | |
| JP7140867B2 (ja) | Pd-l1に結合する抗原結合性タンパク質 | |
| JP2015520172A (ja) | Dll−4に結合する抗原結合蛋白質 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20160527 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20160527 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20170314 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20170613 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20171205 |