JP7307723B2 - Pad阻害剤としてのイミダゾ-ピリジン化合物 - Google Patents
Pad阻害剤としてのイミダゾ-ピリジン化合物 Download PDFInfo
- Publication number
- JP7307723B2 JP7307723B2 JP2020521516A JP2020521516A JP7307723B2 JP 7307723 B2 JP7307723 B2 JP 7307723B2 JP 2020521516 A JP2020521516 A JP 2020521516A JP 2020521516 A JP2020521516 A JP 2020521516A JP 7307723 B2 JP7307723 B2 JP 7307723B2
- Authority
- JP
- Japan
- Prior art keywords
- alkyl
- alkoxy
- aryl
- heteroaryl
- indol
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/535—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one oxygen as the ring hetero atoms, e.g. 1,2-oxazines
- A61K31/5375—1,4-Oxazines, e.g. morpholine
- A61K31/5383—1,4-Oxazines, e.g. morpholine ortho- or peri-condensed with heterocyclic ring systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/04—Ortho-condensed systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/4353—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems
- A61K31/437—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems the heterocyclic ring system containing a five-membered ring having nitrogen as a ring hetero atom, e.g. indolizine, beta-carboline
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/445—Non condensed piperidines, e.g. piperocaine
- A61K31/4523—Non condensed piperidines, e.g. piperocaine containing further heterocyclic ring systems
- A61K31/4545—Non condensed piperidines, e.g. piperocaine containing further heterocyclic ring systems containing a six-membered ring with nitrogen as a ring hetero atom, e.g. pipamperone, anabasine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/06—Antiasthmatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/06—Antipsoriatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D498/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D498/02—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and oxygen atoms as the only ring hetero atoms in which the condensed system contains two hetero rings
- C07D498/04—Ortho-condensed systems
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Medicinal Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Epidemiology (AREA)
- Pulmonology (AREA)
- Rheumatology (AREA)
- Immunology (AREA)
- Dermatology (AREA)
- Physical Education & Sports Medicine (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Pain & Pain Management (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
- Nitrogen And Oxygen Or Sulfur-Condensed Heterocyclic Ring Systems (AREA)
- Medicinal Preparation (AREA)
Description
本開示は、PAD4酵素を阻害する式(I)、(II)、および(III)のイミダゾ-ピリジン化合物、並びにそれらの多形体、立体異性体、プロドラッグ、溶媒和化合物、共結晶、中間体、薬学的に許容できる塩、およびそれらの代謝産物に関する。
PAD(タンパク質アルギニンデイミナーゼ)は、生組織におけるシトルリン化のプロセスをもたらす酵素のファミリーから成っている。(J. E. Jones, et al. Curr. Opin. Drug Discov. Devel., 2009, 12, 616-627)。PADファミリーは、PAD1、PAD2、PAD3、PAD4、およびPAD6という個々の酵素からなる。PADファミリーの酵素は、人体における種々の生理学的および病理学的プロセスに影響を与え、制御するため、重要である。
本開示は、式Iの化合物であって、
BはNまたはCR2から選択され;DはNまたはCR3から選択され;R1、R2、R3およびR4はそれぞれ独立して、水素、ヒドロキシル、シアノ、アミノ、ハロゲン、C1-6アルキル、C1-6アルコキシ、C3-6シクロアルキル、C1-6ハロアルキル、C1-6ハロアルコキシ、C1-6アシルアミノ、C1-6アルキルアミノ、C5-10アリール、C1-6ヘテロシクリル、C1-6ヘテロアリール、C(O)NR15、C(O)C1-6アルキルアミノ、C(O)C5-6アリール、C(O)C1-6ヘテロアリール、C(O)C1-6アルキル、C(O)C1-6ハロアルキル、SO2C1-6アルキル、SO2C1-6ハロアルキル、SO2C3-6シクロアルキル、SO2NR15、SO2NC1-6アルキルアミノ、SO2C5-6アリール、またはSO2C1-6ヘテロアリールから選択され、ここで、C1-6アルキル、C1-6アルコキシ、C1-6ヘテロアリール、およびC1-6ハロアルコキシは、水素、オキソ、C1-6アルキル、C1-6アルコキシ、C1-6ハロアルキル、C3-6シクロアルキル、C5-10アリール、C1-6ヘテロシクリル、C1-6ヘテロアリール、シアノ、およびヒドロキシルから選択される基(groups)の1つまたは複数で任意に置換され;R11は水素であり;R12はC1-6アルキルアミノ、およびN、SまたはOから選択される1~3個のヘテロ原子を有する5~10員の単環式または二環式の飽和複素環であり、あるいは、R11およびR12を合わせてN、SまたはOから選択される1~5個のヘテロ原子を有する5~10員の単環式または二環式の飽和または不飽和の複素環を形成することができ、ここで、5~10員の単環式または二環式の飽和または不飽和の複素環は、アミノ、C1-6アルキルアミノ、C1-6アシルアミノ、-NHC(NH)CH2Cl、-NH(CO)CH=CH-CH2-N(CH3)2、C1-6アルキル、ハロゲン、C1-6アルコキシ、またはヒドロキシルから選択される置換基で任意に置換され;R13は、水素、5~10員の単環式または二環式のアリール、およびN、SまたはOから選択される1~5個のヘテロ原子を有する5~10員の単環式または二環式のヘテロアリールから選択され、ここで、5~10員の単環式または二環式のアリール、および5~10員の単環式または二環式のヘテロアリールは、ヒドロキシル、シアノ、ハロゲン、C1-6アルキル、C1-6アルコキシ、C3-6シクロアルキル、C1-6ハロアルキル、C1-6ハロアルコキシ、C1-6アシルアミノ、C1-6アルキルアミノ、C5-10アリール、C1-10ヘテロシクリル、C1-10ヘテロアリール、C(O)C1-6アルキル、C(O)C1-6ハロアルキル、C(O)NR15、C(O)C1-6アルキルアミノ、C(O)C5-6アリール、C(O)C1-6ヘテロアリール、SO2C1-6アルキル、SO2C1-6ハロアルキル、SO2C3-6シクロアルキル、SO2NR15、SO2NC1-6アルキルアミノ、SO2C5-6アリール、またはSO2C1-6ヘテロアリールから選択される1~5個の置換基で任意に置換され、ここで、C1-6アルキル、C1-6アルコキシ、C3-6シクロアルキル、C5-10アリール、C1-10ヘテロシクリル、およびC1-10ヘテロアリールは、水素、C1-6アルキル、C1-6ハロアルキル、C1-6アルコキシ、C3-6シクロアルキル、C5-6アリール、C1-6ヘテロアリール、C1-6ヘテロシクリル、オキソ、ハロゲン、ヒドロキシル、およびシアノから選択される基の1つまたは複数で任意に置換され、ここで、C5-6アリール、C1-6ヘテロアリール、およびC1-6ヘテロシクリルは、水素、C1-6アルキル、C1-6アルコキシ、オキソ、ハロゲン、ヒドロキシル、-CH2OH、およびシアノから選択される基の1つまたは複数で任意に置換され;R15は、水素、C1-6アルキル、およびそれらの組み合わせから成る群から選択される、式Iの化合物を開示する。
R11およびR12を合わせてN、SまたはOから選択される1~5個のヘテロ原子を有する5~10員の単環式または二環式の飽和または不飽和の複素環を形成することができ、ここで、5~10員の単環式または二環式の飽和または不飽和の複素環は、アミノ、C1-6アルキルアミノ、C1-6アシルアミノ、-NHC(NH)CH2Cl、-NH(CO)CH=CH-CH2-N(CH3)2、C1-6アルキル、ハロゲン、C1-6アルコキシ、またはヒドロキシルから選択される置換基で任意に置換され;R15は、水素、C1-6アルキル、およびそれらの組み合わせから成る群から選択される、式IIの化合物を記載する。
R11およびR12を合わせてN、SまたはOから選択される1~5個のヘテロ原子を有する5~10員の単環式または二環式の飽和または不飽和の複素環を形成することができ、ここで、5~10員の単環式または二環式の飽和または不飽和の複素環は、アミノ、C1-6アルキルアミノ、C1-6アシルアミノ、-NHC(NH)CH2Cl、-NH(CO)CH=CH-CH2-N(CH3)2、C1-6アルキル、ハロゲン、C1-6アルコキシ、またはヒドロキシルから選択される置換基で任意に置換され;R15は、水素、C1-6アルキル、およびそれらの組み合わせから成る群から選択される、式IIIの化合物を記載する。
当業者ならば、本開示は、具体的に記載された例以外の変形例や修正例の対象となり得ると理解するであろう。本開示はそのような変形例および修正例すべてを含むと理解されたい。本開示はまた、本明細書中で個別にまたは集合的に言及されたまたは示されたすべての工程、特徴、組成物、および化合物、およびそのような工程または特徴の任意または複数の、任意かつすべての組み合わせを含む。
便宜上、本開示のさらなる説明の前に、本明細書および実施例で使用される特定の用語をここにまとめる。これらの定義は本開示の残りの部分に照らして読まれるべきであり、当業者によって理解されているように理解されるべきである。本明細書で使用される用語は当業者に認識され、知られている意味を有するが、利便性および完全性のために、特定の用語およびそれらの意味を以下に記載する。
BはNまたはCR2から選択され;DはNまたはCR3から選択され;R1、R2、R3およびR4はそれぞれ独立して、水素、ヒドロキシル、シアノ、アミノ、ハロゲン、C1-6アルキル、C1-6アルコキシ、C3-6シクロアルキル、C1-6ハロアルキル、C1-6ハロアルコキシ、C1-6アシルアミノ、C1-6アルキルアミノ、C5-10アリール、C1-6ヘテロシクリル、C1-6ヘテロアリール、C(O)NR15、C(O)C1-6アルキルアミノ、C(O)C5-6アリール、C(O)C1-6ヘテロアリール、C(O)C1-6アルキル、C(O)C1-6ハロアルキル、SO2C1-6アルキル、SO2C1-6ハロアルキル、SO2C3-6シクロアルキル、SO2NR15、SO2NC1-6アルキルアミノ、SO2C5-6アリール、またはSO2C1-6ヘテロアリールから選択され、ここで、C1-6アルキル、C1-6アルコキシ、C1-6ヘテロアリール、およびC1-6ハロアルコキシは、水素、オキソ、C1-6アルキル、C1-6アルコキシ、C1-6ハロアルキル、C3-6シクロアルキル、C5-10アリール、C1-6ヘテロシクリル、C1-6ヘテロアリール、シアノ、およびヒドロキシルから選択される基の1つまたは複数で任意に置換され;R11は水素であり;R12はC1-6アルキルアミノ、およびN、SまたはOから選択される1~3個のヘテロ原子を有する5~10員の単環式または二環式の飽和複素環であり、あるいは、R11およびR12を合わせてN、SまたはOから選択される1~5個のヘテロ原子を有する5~10員の単環式または二環式の飽和または不飽和の複素環を形成することができ、ここで、5~10員の単環式または二環式の飽和または不飽和の複素環は、アミノ、C1-6アルキルアミノ、C1-6アシルアミノ、-NHC(NH)CH2Cl、-NH(CO)CH=CH-CH2-N(CH3)2、C1-6アルキル、ハロゲン、C1-6アルコキシ、またはヒドロキシルから選択される置換基で任意に置換され;R13は、水素、5~10員の単環式または二環式のアリール、およびN、SまたはOから選択される1~5個のヘテロ原子を有する5~10員の単環式または二環式のヘテロアリールから選択され、ここで、5~10員の単環式または二環式のアリール、および5~10員の単環式または二環式のヘテロアリールは、ヒドロキシル、シアノ、ハロゲン、C1-6アルキル、C1-6アルコキシ、C3-6シクロアルキル、C1-6ハロアルキル、C1-6ハロアルコキシ、C1-6アシルアミノ、C1-6アルキルアミノ、C5-10アリール、C1-10ヘテロシクリル、C1-10ヘテロアリール、C(O)C1-6アルキル、C(O)C1-6ハロアルキル、C(O)NR15、C(O)C1-6アルキルアミノ、C(O)C5-6アリール、C(O)C1-6ヘテロアリール、SO2C1-6アルキル、SO2C1-6ハロアルキル、SO2C3-6シクロアルキル、SO2NR15、SO2NC1-6アルキルアミノ、SO2C5-6アリール、またはSO2C1-6ヘテロアリールから選択される1~5個の置換基で任意に置換され、ここで、C1-6アルキル、C1-6アルコキシ、C3-6シクロアルキル、C5-10アリール、C1-10ヘテロシクリル、およびC1-10ヘテロアリールは、水素、C1-6アルキル、C1-6ハロアルキル、C1-6アルコキシ、C3-6シクロアルキル、C5-6アリール、C1-6ヘテロアリール、C1-6ヘテロシクリル、オキソ、ハロゲン、ヒドロキシル、およびシアノから選択される基の1つまたは複数で任意に置換され、ここで、C5-6アリール、C1-6ヘテロアリール、およびC1-6ヘテロシクリルは、水素、C1-6アルキル、C1-6アルコキシ、オキソ、ハロゲン、ヒドロキシル、-CH2OH、およびシアノから選択される基の1つまたは複数で任意に置換され;R15は、水素、C1-6アルキル、およびそれらの組み合わせから成る群から選択される、式Iの化合物、その多形体、立体異性体、プロドラッグ、溶媒和化合物、共結晶、中間体、薬学的に許容できる塩、およびその代謝産物が提供される。
R11およびR12を合わせてN、SまたはOから選択される1~5個のヘテロ原子を有する5~10員の単環式または二環式の飽和または不飽和の複素環を形成することができ、ここで、5~10員の単環式または二環式の飽和または不飽和の複素環は、アミノ、C1-6アルキルアミノ、C1-6アシルアミノ、-NHC(NH)CH2Cl、-NH(CO)CH=CH-CH2-N(CH3)2、C1-6アルキル、ハロゲン、C1-6アルコキシ、またはヒドロキシルから選択される置換基で任意に置換され;R15は、水素、C1-6アルキル、およびそれらの組み合わせから成る群から選択される、式IIの化合物、その多形体、立体異性体、プロドラッグ、溶媒和化合物、共結晶、中間体、薬学的に許容できる塩、およびその代謝産物が提供される。
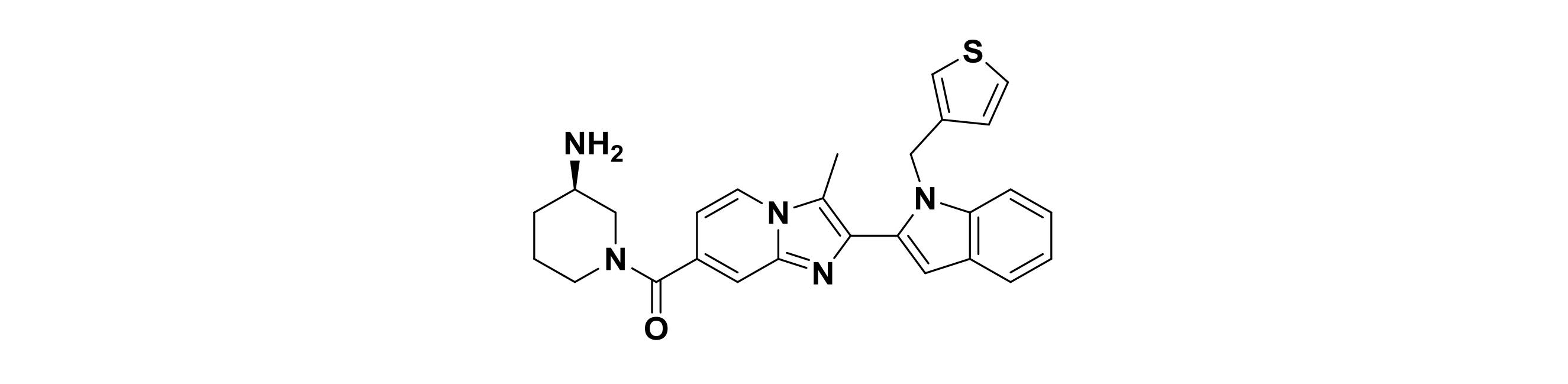
1)(R)-(3-アミノピペリジン-1-イル)(2-(3-ブロモ-1-(シクロプロピルメチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
2)(R)-(3-アミノピペリジン-1-イル)(2-(1-(シクロプロピルメチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
3)(R)-(3-アミノピペリジン-1-イル)(2-(1-ベンジル-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
4)(R)-(3-アミノピペリジン-1-イル)(2-(1-エチル-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
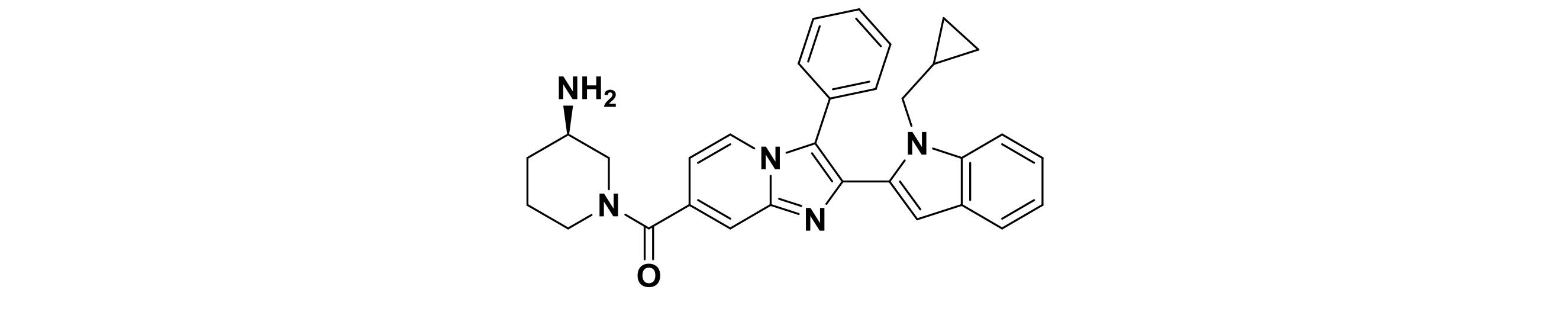
5)(R)-(3-アミノピペリジン-1-イル)(2-(1-エチル-3-フェニル-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
6)(R)-(3-アミノピロリジン-1-イル)(2-(1-エチル-3-フェニル-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
7)(R)-(3-アミノピロリジン-1-イル)(2-(1-エチル-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
8)(R)-(3-アミノピロリジン-1-イル)(2-(1-(シクロプロピルメチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
9)(2-(1-(シクロプロピルメチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)(ヘキサヒドロ-2H-ピリド[4,3-b][1,4]オキサジン-6(5H)-イル)メタノン、
10)(R)-(3-アミノピペリジン-1-イル)(3-メチル-2-(1-(ピリジン-4-イルメチル)-1H-インドール-2-イル)イミダゾ[1,2a]ピリジン-7-イル)メタノン、
11)(R)-(3-アミノピペリジン-1-イル)(3-メチル-2-(1-((テトラヒドロ-2H-ピラン-4-イル)メチル)-1H-インドール-2-イル)イミダゾ[1,2a]ピリジン-7-イル)メタノン、
12)(R)-(3-アミノピペリジン-1-イル)(2-(1-(4-メトキシベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
13)(R)-(3-アミノピペリジン-1-イル)(2-(1-(4-フルオロベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
14)(R)-4-((2-(7-(3-アミノピペリジン-1-カルボニル)-3-メチルイミダゾ[1,2a]ピリジン-2-イル)-1H-インドール-1-イル)メチル)ベンゾニトリル、
15)(R)-(3-アミノピペリジン-1-イル)(3-メチル-2-(1-(ピリジン-3-イルメチル)-1H-インドール-2-イル)イミダゾ[1,2a]ピリジン-7-イル)メタノン、
16)(R)-(3-アミノピペリジン-1-イル)(3-メチル-2-(1-(ピリジン-2-イルメチル)-1H-インドール-2-イル)イミダゾ[1,2a]ピリジン-7-イル)メタノン、
17)(R)-(3-アミノピペリジン-1-イル)(3-メチル-2-(1-(2,2,2-トリフルオロエチル)-1H-インドール-2-イル)イミダゾ[1,2a]ピリジン-7-イル)メタノン、
18)(R)-4-((2-(7-(3-アミノピペリジン-1-カルボニル)-3-メチルイミダゾ[1,2a]ピリジン-2-イル)-1H-インドール-1-イル)メチル)-1-メチルピリジン-2(1H)-オン、
19)(R)-(3-アミノピペリジン-1-イル)(2-(3-エチルベンゾ[b]チオフェン-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
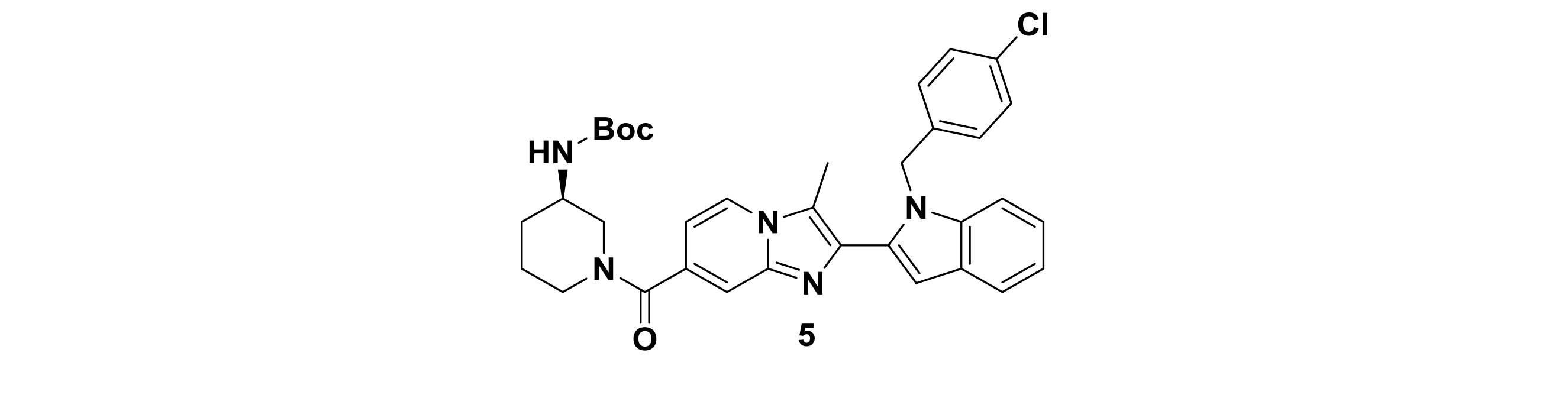
20)(R)-(3-アミノピペリジン-1-イル)(2-(1-(4-クロロベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
21)(R)-(3-アミノピペリジン-1-イル)(2-(1-(2-フルオロベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
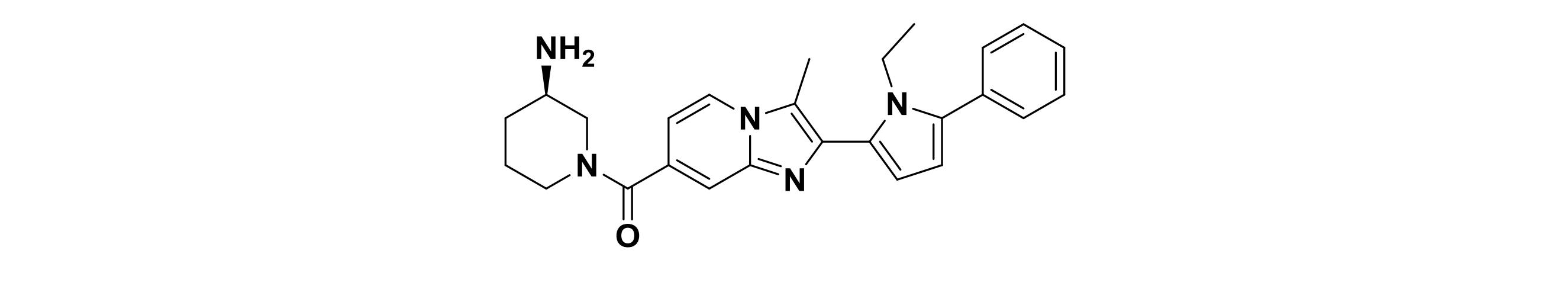
22)(R)-(3-アミノピペリジン-1-イル)(2-(1-エチル-5-フェニル-1H-ピロール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
23)(R)-(3-アミノピペリジン-1-イル)(2-(1-(シクロプロピルメチル)-6-メトキシ-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
24)(R)-(3-アミノピペリジン-1-イル)(2-(1-エチル-1H-ピロロ[2,3-b]ピリジン-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
25)(R)-(3-アミノピペリジン-1-イル)(2-(1-(シクロプロピルメチル)-1H-インドール-2-イル)-3,5-ジメチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
26)(R)-(3-アミノピペリジン-1-イル)(2-(1-ベンジル-1H-インドール-2-イル)-3,5-ジメチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
27)(R)-(3-アミノピペリジン-1-イル)(3,5-ジメチル-2-(1-(ピリジン-2-イルメチル)-1H-インドール-2-イル)イミダゾ[1,2a]ピリジン-7-イル)メタノン、
28)(R)-(3-アミノピペリジン-1-イル)(2-(1-(シクロプロピルメチル)-6-フルオロ-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
29)(R)-(3-アミノピペリジン-1-イル)(2-(1-(シクロプロピルメチル)-5-フルオロ-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
30)(R)-(3-アミノピペリジン-1-イル)(2-(1-(シクロプロピルメチル)-7-メチル-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
31)(R)-(3-アミノピペリジン-1-イル)(2-(2-エチルフェニル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
32)(R)-(3-アミノピペリジン-1-イル)(2-(1-(シクロプロピルメチル)-1H-インドール-2-イル)-3-フェニルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
33)(R)-(3-アミノピペリジン-1-イル)(3-シクロプロピルメチル-2-(1-(シクロプロピルメチル)-1H-インドール-2-イル)イミダゾ[1,2a]ピリジン-7-イル)メタノン、
34)(R)-(3-アミノピペリジン-1-イル)(2-(1-(シクロプロピルメチル)-1H-インドール-2-イル)-3-(メトキシメチル)イミダゾ[1,2a]ピリジン-7-イル)メタノン、
35)(R)-(3-アミノピペリジン-1-イル)(2-(1-(3-フルオロベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
36)(R)-(3-アミノピペリジン-1-イル)(3-メチル-2-(1-(チオフェン-3-イルメチル)-1H-インドール-2-イル)イミダゾ[1,2a]ピリジン-7-イル)メタノン、
37)(R)-(3-アミノピペリジン-1-イル)(2-(1-(フラン-3-イルメチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
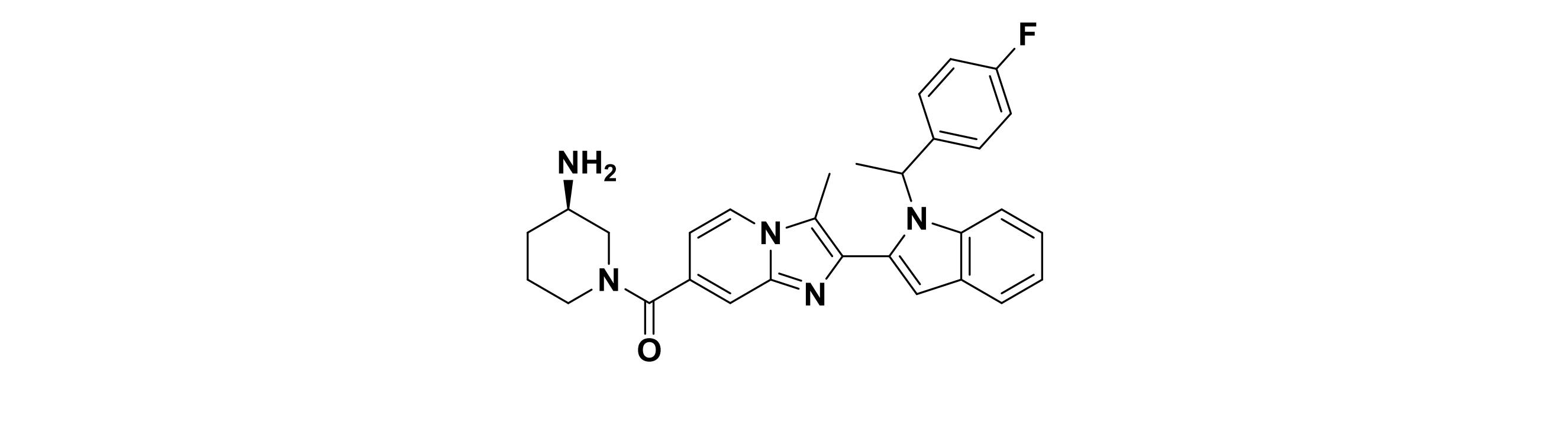
38)(R)-(3-アミノピペリジン-1-イル)(2-(1-(1-(4-フルオロフェニル)エチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
39)(R)-(3-アミノピペリジン-1-イル)(2-(1-エチル-5-フルオロ-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
40)(R)-(3-アミノピペリジン-1-イル)(2-(1-(シクロプロピルメチル)4-フルオロ-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
41)(R)-(3-アミノピペリジン-1-イル)(3-メチル-2-(1-((4-メチルチアゾール-2-イル)メチル)-1H-インドール-2-イル)イミダゾ[1,2a]ピリジン-7-イル)メタノン、
42)(R)-(3-アミノピペリジン-1-イル)(2-(1-(3-メトキシベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
43)(R)-(3-アミノピペリジン-1-イル)(2-(5-ブロモ-1-(シクロプロピルメチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
44)(R)-(3-アミノピペリジン-1-イル)(2-(7-クロロ-1-(シクロプロピルメチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
45)(R)-(3-アミノピペリジン-1-イル)(2-(1-(4-フルオロベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
46)(R)-(3-アミノピペリジン-1-イル)(3-メチル-2-(1-メチル-1H-インドール-2-イル)イミダゾ[1,2a]ピリジン-7-イル)メタノン、
47)(R)-(3-アミノピペリジン-1-イル)(2-(1-(シクロプロピルメチル)-7-メトキシ-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
48)(R)-(3-アミノピペリジン-1-イル)(2-(1-((2,4-ジメチルチアゾール-5-イル)メチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
49)(R)-(3-アミノピペリジン-1-イル)(3-メチル-2-(1-((2-メチルチアゾール-5-イル)メチル)-1H-インドール-2-イル)イミダゾ[1,2a]ピリジン-7-イル)メタノン、
50)(R)-(3-アミノピペリジン-1-イル)(2-(1-(3-メトキシベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノントリフルオロ酢酸塩、
51)(R)-(3-アミノピペリジン-1-イル)(2-(6-メトキシ-1-(ピリジン-3-イルメチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
52)(R)-(3-アミノピペリジン-1-イル)(2-(1-(シクロプロピルメチル)-6-フルオロ-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノントリフルオロ酢酸塩、
53)(R)-(3-アミノピペリジン-1-イル)(2-(5-フルオロ-1-(3-メトキシベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
54)(R)-(3-アミノピペリジン-1-イル)(2-(6-フルオロ-1-(4-フルオロベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
55)(R)-(3-アミノピペリジン-1-イル)(2-(5,6-ジフルオロ-1-(3-メトキシベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
56)(R,E)-4-(ジメチルアミノ)-N-(1-(2-(1-(4-フルオロベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-カルボニル)ピペリジン-3-イル)ブタ-2-エンアミド、
57)(R)-(3-アミノピペリジン-1-イル)(3-メチル-2-(1-(ピラジン-2-イルメチル)-1H-インドール-2-イル)イミダゾ[1,2a]ピリジン-7-イル)メタノン、
58)(R)-(3-アミノピペリジン-1-イル)(3-メチル-2-(1-(ピリミジン-5-イルメチル)-1H-インドール-2-イル)イミダゾ[1,2a]ピリジン-7-イル)メタノントリフルオロ酢酸塩、
59)(R)-(3-アミノピペリジン-1-イル)(3-メチル-2-(1-(ピリダジン-3-イルメチル)-1H-インドール-2-イル)イミダゾ[1,2a]ピリジン-7-イル)メタノン、
60)(R)-(3-アミノピペリジン-1-イル)(2-(1-イソブチル-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
61)(R)-(3-アミノピペリジン-1-イル)(2-(1-(シクロブチルメチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
62)(R)-(3-アミノピペリジン-1-イル)(2-(1-((3-フルオロピリジン-2-イル)メチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
63)(R)-(3-アミノピペリジン-1-イル)(2-(1-((5-メトキシピリジン-2-イル)メチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
64)(R)-(3-アミノピペリジン-1-イル)(2-(1-(2-メトキシエチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
65)(R)-(3-アミノピペリジン-1-イル)(2-(1-(2-ヒドロキシエチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
66)(R)-(3-アミノピペリジン-1-イル)(2-(6-メトキシ-1-(ピリジン-4-イルメチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
67)(R)-(3-アミノピペリジン-1-イル)(2-(1-エチル-6-メトキシ-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
68)(R)-(3-アミノピペリジン-1-イル)(2-(6-フルオロ-1-(ピリジン-4-イルメチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
69)(R)-(3-アミノピペリジン-1-イル)(2-(6-フルオロ-1-(ピリジン-3-イルメチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
70)(R)-(3-アミノピペリジン-1-イル)(2-(6-フルオロ-1-(3-メトキシベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
71)(R)-(3-アミノピペリジン-1-イル)(2-(6-フルオロ-1-(4-メトキシベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
72)(R)-(3-アミノピペリジン-1-イル)(2-(1-エチル-6-フルオロ-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
73)(R)-(3-アミノピペリジン-1-イル)(2-(6-フルオロ-1-イソブチル-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
74)(R)-(3-アミノピペリジン-1-イル)(2-(5-フルオロ-1-(ピリジン-4-イルメチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
75)(R)-(3-アミノピペリジン-1-イル)(2-(5-フルオロ-1-(4-メトキシベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
76)(R)-(3-アミノピペリジン-1-イル)(2-(5-フルオロ-1-(4-フルオロベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
77)(R)-(3-アミノピペリジン-1-イル)(2-(7-クロロ-1-(4-フルオロベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
78)(R)-(3-アミノピペリジン-1-イル)(2-(1-(2,2-ジフルオロエチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノントリフルオロ酢酸塩、
79)(R)-(3-アミノピペリジン-1-イル)(2-(1-((5-フルオロピリジン-2-イル)メチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
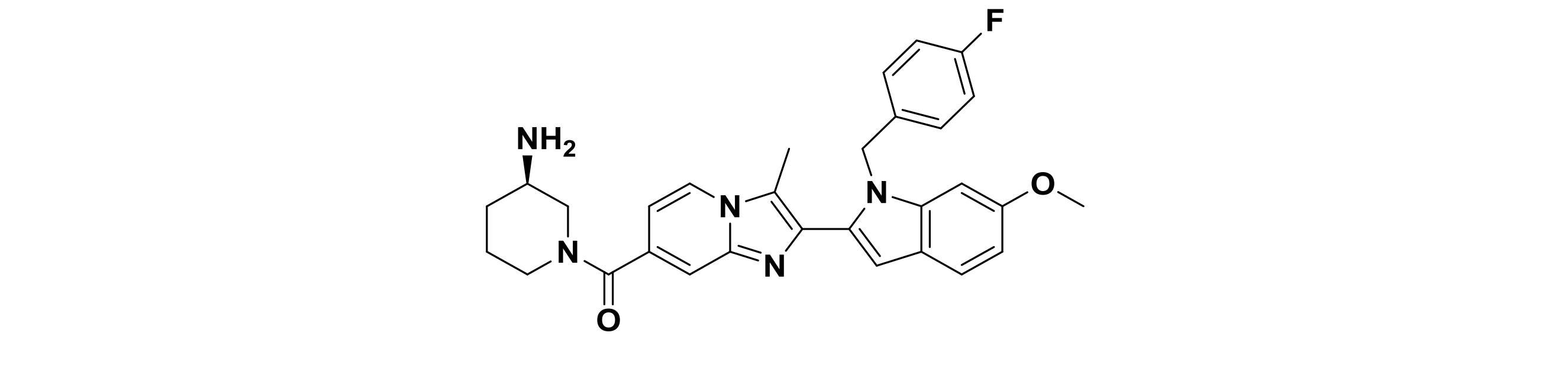
80)(R)-(3-アミノピペリジン-1-イル)(2-(1-(4-フルオロベンジル)-6-メトキシ-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
81)(R)-(3-アミノピペリジン-1-イル)(2-(1-(4-(ヒドロキシメチル)ベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
82)(R)-(3-アミノピペリジン-1-イル)(2-(1-イソブチル-6-メトキシ-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
83)(R)-(3-アミノピペリジン-1-イル)(2-(1-(2,2-ジフルオロエチル)-6-メトキシ-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、
84)(R)-(3-アミノピペリジン-1-イル)(2-(5-フルオロ-1-イソブチル-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、および、
85)(R)-(3-アミノピペリジン-1-イル)(2-(1-(4-フルオロ-3-メトキシベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン、および、
86)(R)-(3-アミノピペリジン-1-イル)(2-(1-(シクロプロピルメチル)-6-メトキシ-1H-インドール-2-イル)-3-(メトキシメチル)イミダゾ[1,2a]ピリジン-7-イル)メタノン、から成る群から選択される、式(I)の化合物、またはその多形体、立体異性体、プロドラッグ、溶媒和化合物、共結晶、中間体、薬学的に許容できる塩、およびその代謝産物が提供される。
本明細書中で使用される、これらのプロセス、スキームおよび実施例において使用される記号および慣例は現代の科学文献(例えば、the Journal of the American Chemical Society)において使用されるものと一致する。特に明記しない限り、全ての出発物質は商業的供給者から入手し、さらに精製することなく使用した。具体的には、以下の略語が実施例において、および本明細書全体を通して使用され得る。
AcOH 酢酸
BOC2O ジ-tert-ブチルジカルボネート
nBuLi n-ブチルリチウム
BuOH ブタノール
Bz ベンジル
Cbz カルボキシベンジル
cHex シクロヘキサン
Cs2CO3 炭酸セシウム
DCM/CH2Cl2 ジクロロメタン
DIAD アゾジカルボン酸ジイソプロピル
ジオキサン 1,4-ジオキサン
DIPEA N、N-ジイソプロピルエチルアミン
DMSO ジメチルスルホキシド
DMF N,N-ジメチルホルムアミド
Et3N トリエチルアミン
エーテル ジエチルエーテル
EtOAc 酢酸エチル
HATU o-(7-アザベンゾトリアゾル1-イル)-N,N,N’,Ν’-テトラメチルウロニウムヘキサフルオロホスフェート
HPLC 高速液体クロマトグラフィー
IPA イソプロピルアルコール
K2CO3 炭酸カリウム
KOH 水酸化カリウム
LiOH 水酸化リチウム
LCMSまたはLC/MS 液体クロマトグラフィー質量分析
MeOH メタノール
min 分
Na2SO4 硫酸ナトリウム
NaHCO3 重炭酸ナトリウム
NH4Cl 塩化アンモニウム
パラジウムテトラキス パラジウムテトラキストリフェニルホスフィン
Pd/C パラジウム炭素
PTSA p-トルエンスルホン酸
rb 丸底(フラスコ)
r.t/rt. 室温
Rt 保持時間
TFA トリフルオロ酢酸
TFAA トリフルオロ酢酸無水物
THF/thf テトラヒドロフラン
TLC/tic 薄層クロマトグラフィー
TMEDA テトラメチルエチレンジアミン
HOBt ヒドロキシベンゾトリアゾール
EDC.HCl 1-エチル-3-(3-ジメチルアミノプロピル)カルボジイミド塩酸塩
以下の実施例は、本開示の化合物の合成、活性、および適用に関する詳細を提供する。以下は代表的なものにすぎず、本発明はこれらの実施例に記載された詳細によって限定されないことを理解されたい。
式I、式II、および式IIIの化合物の合成のための一般的な手順
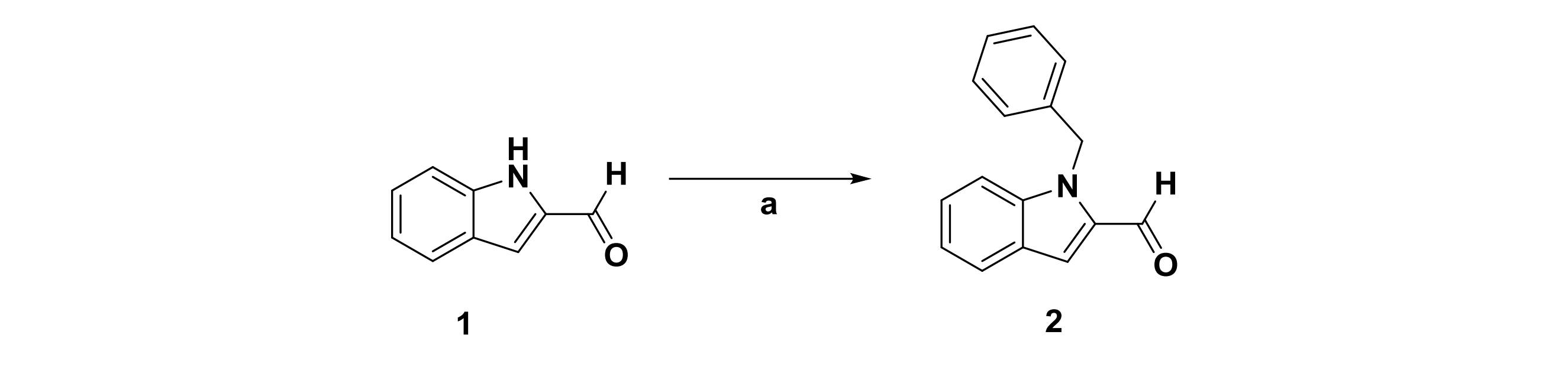
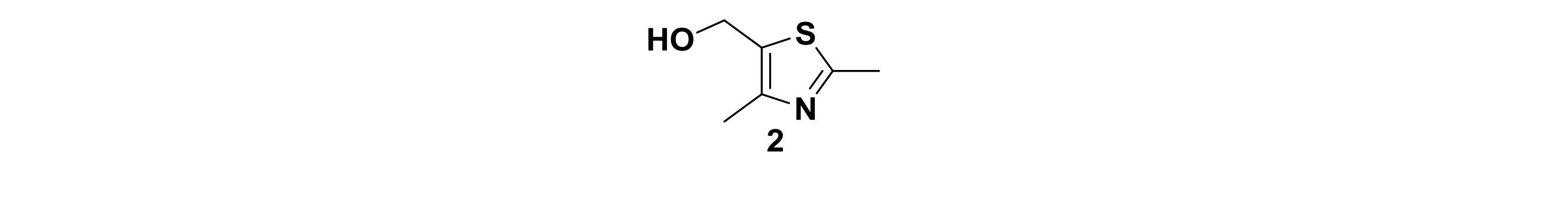
工程1:N,O-ジメチルヒドロキシルアミン塩酸塩、トリエチルアミン、HOBtおよびEDC.HClを用いて、化合物1を標準状態で化合物2に変換した(反応条件a)。
工程2:化合物2をエチルマグネシウムブロミドで処理し(反応条件b)、中間体3を得た。
工程3:フェニルトリメチルアンモニウムトリブロミドを用いて中間体3を化合物4に変換した(反応条件c)。
工程4:化合物4をメチル2-アミノイソニコチネートまたはエチル2-クロロ-6-メチルイソニコチネートおよびNaHCO3で処理して(反応条件d)、中間体5を得た。
工程5:置換臭化物(ブロモメチルシクロプロパン)およびCs2CO3と反応させることにより、中間体5を化合物6に変換した(反応条件e)。
工程6:反応条件f下で、化合物6を加水分解して化合物7を得た。
工程7:化合物7と、tert-ブチル(R)-ピペリジン-3-イルカルバメート等の置換カルバメートとのカップリング(反応条件g)により、化合物8を得た。
工程8:Boc脱保護により化合物8を最終化合物9に変換した(反応条件h)。
反応プロセスにおいて使用される化合物は特に言及しない限り、商業的に入手可能であり、Combi-Blocks,Indiaから購入した。NMRデータは、Varian 400MHz分光計で得た。すべての化合物は質量分析(MS-ESI、エレクトロスプレーイオン化質量分析)と同様に1H NMRで特徴づけられた。全ての1H化学シフトを百万分率(ppm)で報告し、溶媒としてのTMSまたは残留重水素化DMSOに対して測定した。MS(ESI)測定は、Waters Mass spectrometerで行った。提供される化合物の収率は、単離された化合物を指す。
(R)-(3-アミノピペリジン-1-イル)(2-(3-ブロモ-1-(シクロプロピルメチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン(化合物-1)の合成
工程3:2-ブロモ-1-(3-ブロモ-1H-インドール-2-イル)プロパン-1-オン(4)の調製
(R)-(3-アミノピペリジン-1-イル)(2-(1-(シクロプロピルメチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン(化合物-2)
上記スキーム-2に概説した手順を用いて、中間体8を合成した。
(R)-(3-アミノピペリジン-1-イル)(2-(1-ベンジル-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(1-エチル-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(1-エチル-3-フェニル-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン(化合物-5)の合成
中間体1を、上記スキーム-2の中間体6について概説した手順を用いて合成する。
(R)(3-アミノピロリジン-1-イル)(2-(1-エチル-3-フェニル-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピロリジン-1-イル)(2-(1-エチル-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)3-(アミノピロリジン-1-イル)(2-(1-(シクロプロピルメチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(2-(1-(シクロプロピルメチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)(ヘキサヒドロ-2H-ピリド[4,3-b][1,4]オキサジン-6(5H)-イル)メタノン
(R)(3-アミノピペリジン-1-イル)(3-メチル-2-(1-(ピリジン-4-イルメチル)-1H-インドール-2-イル)イミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(3-メチル-2-(1-((テトラヒドロ-2H-ピラン-4-イル)メチル)-1H-インドール-2-イル)イミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(1-(4-メトキシベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(1-(4-フルオロベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-4-((2-(7-(3-アミノピペリジン-1-カルボニル)-3-メチルイミダゾ[1,2a]ピリジン-2-イル)-1H-インドール-1-イル)メチル)ベンゾニトリル
(R)(3-アミノピペリジン-1-イル)(3-メチル-2-(1-(ピリジン-3-イルメチル)-1H-インドール-2-イル)イミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)(3-アミノピペリジン-1-イル)(3-メチル-2-(1-(ピリジン-2-イルメチル)-1H-インドール-2-イル)イミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(3-メチル-2-(1-(2,2,2-トリフルオロエチル)-1H-インドール-2-イル)イミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-4-((2-(7-(3-アミノピペリジン-1-カルボニル)-3-メチルイミダゾ[1,2-a]ピリジン-2-イル)-1H-インド-ル-1-イル)メチル)-1-メチルピリジン-2(1H)-オン
(R)-(3-アミノピペリジン-1-イル)(2-(3-エチルベンゾ[b]チオフェン-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(1-(4-クロロベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン(化合物-20)の合成
(R)-(3-アミノピペリジン-1-イル)(2-(1-(2-フルオロベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(1-エチル-5-フェニル-1H-ピロール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(1-(シクロプロピルメチル)-6-メトキシ-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(1-エチル-1H-ピロロ[2,3-b]ピリジン-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(1-(シクロプロピルメチル)-1H-インドール-2-イル)-3,5-ジメチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(1-ベンジル-1H-インドール-2-イル)-3,5-ジメチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(3,5-ジメチル-2-(1-(ピリジン-2-イルメチル)-1H-インドール-2-イル)イミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(1-(シクロプロピルメチル)-6-フルオロ-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(1-(シクロプロピルメチル)-5-フルオロ-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(1-(シクロプロピルメチル)-7-メチル-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(2-エチルフェニル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン(化合物-31)の合成
(R)-(3-アミノピペリジン-1-イル)(2-(1-(シクロプロピルメチル)-1H-インドール-2-イル)-3-フェニルイミダゾ[1,2-a]ピリジン-7-イル)メタノン(化合物-32)の合成
(R)-(3-アミノピペリジン-1-イル)(3-シクロプロピル-2-(1-(シクロプロピルメチル)-1H-インドール-2-イル)イミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(1-(シクロプロピルメチル)-1H-インドール-2-イル)-3(メトキシメチル)イミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(1-(3-フルオロベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(3-メチル-2-(1-(チオフェン-3-イルメチル)-1H-インドール-2-イル)イミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(1-(フラン-3-イルメチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-3-アミノピペリジン-1-イル(2-(1-(1-(4-フルオロフェニル)エチル)-1H-インドール-2-イル)-3メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(1-エチル-5-フルオロ-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(1-(シクロプロピルメチル)-4-フルオロ-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(3-メチル-2-(1-((4-メチルチアゾール-2-イル)メチル)-1H-インドール-2-イル)イミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(1-(3-メトキシベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(5-ブロモ-1-(シクロプロピルメチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(7-クロロ-1-(シクロプロピルメチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(1-(4-フルオロベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタンチオンの合成
化合物-45は、以下に提供される工程に従って化合物-13から調製した。
(R)-(3-アミノピペリジン-1-イル)(3-メチル-2-(1-メチル-1H-インドール-2-イル)イミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(1-(シクロプロピルメチル)-7-メトキシ-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(1-((2,4-ジメチルチアゾール-5-イル)メチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(3-メチル-2-(1-((2-メチルチアゾール-5-イル)メチル)-1H-インドール-2-イル)イミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(1-(3-メトキシベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノントリフルオロ酢酸塩(化合物50)の合成
(R)-(3-アミノピペリジン-1-イル)(2-(6-メトキシ-1-(ピリジン-3-イルメチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(1-(シクロプロピルメチル)-6-フルオロ-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノントリフルオロ酢酸塩
(R)-(3-アミノピペリジン-1-イル)(2-(5-フルオロ-1-(3-メトキシベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(6-フルオロ-1-(4-フルオロベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(5,6-ジフルオロ-1-(3-メトキシベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R,E)-4-(ジメチルアミノ)-N-(1-(2-(1-(4-フルオロベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-カルボニル)ピペリジン-3-イル)ブタ-2-エンアミドの合成
(R)-(3-アミノピペリジン-1-イル)(3-メチル-2-(1-(ピラジン-2-イルメチル)-1H-インドール-2-イル)イミダゾ[1,2-a]ピリジン-7-イル)メタノン(化合物-57)の合成
(R)(3-アミノピペリジン-1-イル)(3-メチル-2-(1-(ピリミジン-5-イルメチル)-1H-インドール-2-イル)イミダゾ[1,2-a]ピリジン-7-イル)メタノントリフルオロ酢酸塩
(R)-(3-アミノピペリジン-1-イル)(3-メチル-2-(1-(ピリダジン-3-イルメチル)-1H-インドール-2-イル)イミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(1-イソブチル-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(1-(シクロブチルメチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(1-((3-フルオロピリジン-2-イル)メチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(1-((5-メトキシピリジン-2-イル)メチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(1-(2-メトキシエチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(1-(2-ヒドロキシエチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノンの合成
(R)-(3-アミノピペリジン-1-イル)(2-(6-メトキシ-1-(ピリジン-4-イルメチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(1-エチル-6-メトキシ-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(6-フルオロ-1-(ピリジン-4-イルメチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(6-フルオロ-1-(ピリジン-3-イルメチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(6-フルオロ-1-(3-メトキシベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(6-フルオロ-1-(4-メトキシベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(1-エチル-6-フルオロ-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(6-フルオロ-1-イソブチル-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(5-フルオロ-1-(ピリジン-4-イルメチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(5-フルオロ-1-(4-メトキシベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(5-フルオロ-1-(4-フルオロベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(7-クロロ-1-(4-フルオロベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(1-(2,2-ジフルオロエチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノントリフルオロ酢酸塩の合成
(R)-(3-アミノピペリジン-1-イル)(2-(1-((5-フルオロピリジン-2-イル)メチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(1-(4-フルオロベンジル)-6-メトキシ-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(1-(4-(ヒドロキシメチル)ベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(1-イソブチル-6-メトキシ-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(1-(2,2-ジフルオロエチル)-6-メトキシ-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(5-フルオロ-1-イソブチル-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(1-(4-フルオロ-3-メトキシベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2-a]ピリジン-7-イル)メタノン
(R)-(3-アミノピペリジン-1-イル)(2-(1-(シクロプロピルメチル)-6-メトキシ-1H-インドール-2-イル)-3-(メトキシメチル)イミダゾ[1,2-a]ピリジン-7-イル)メタノン
2-ブロモ-1-(3-エチルベンゾ[b]チオフェン-2-イル)プロパン-1-オン(化合物-19の中間体)の合成:
工程3:7-メトキシ-1H-インドール-2-カルバルデヒドの調製
生物学的評価のための一般的手順
FP結合アッセイ
化合物のPAD4との結合をFPアッセイによって検出した。PAD4をアッセイ緩衝液(100mM HEPES、50mM NaCl、1mM DTT、5%グリセロールおよび1mM CHAPS)中で1uMに希釈し、384ウェルブラックプレート中の種々の濃度の化合物またはDMSOビヒクル(1%)を含有するウェルに添加した。10nMのフルオレセイン標識プローブ(JPAD-00085)をプレートに添加した。アッセイプレートを室温で60分間インキュベートした後、Pherastar上のFPモジュール(λex 485/λem 535nm)でFP読み取りを測定した。IC50はXLフィットソフトウェアモデル205を用いて計算した。(Lewis et. al, Nat Chem Biol. 2015, 11(3), 189-91)。
アンモニア放出を介して、シトルリン化アッセイを検出した。PAD4を、アッセイ緩衝液(100mM HEPES、50mM NaCl、2mM DDT、0.6mg/mL BSA、pH7.4)中で120nMに希釈し、ブラック384ウェルプレート中の種々の濃度の化合物またはDMSOビヒクル(最終1%)を含むウェルに添加した。室温での60分間のプレインキュベーション後、基板(200mM HEPES、50mM NaCl、350uM CaCl2中の1.5mM BAEE、2mM、pH7.4)の添加によって反応を開始した。60分後、50mMのEDTA、2.6mMのo-フタルアルデヒドおよび2.6mMのDTTを含有する停止/検出緩衝液を添加することによって、反応を停止させた。アッセイは、室温で90分間インキュベートした後、Tecanリーダーで蛍光(例えばλex 405/λem 460nm)を測定した。IC50はXLフィットソフトウェアモデル205を用いて計算した。(Lewis et. al, Nat Chem Biol. 2015, 11(3), 189-91)。
以下の表1は、上記のPAD4アッセイにおける本発明の選択された化合物の活性を示す。「A」と指定された活性を有する化合物はIC50≦1uMを提供し、「B」と指定された活性を有する化合物はIC501~10uMを提供し、「C」と指定された活性を有する化合物はIC50≧10 uMを提供した。
Claims (25)
- 式(I)の化合物、
その立体異性体または薬学的に許容できる塩であって、
XはOまたはSから選択され;
ZはNであり;
AはCR1であり;
BはCR2であり;
DはCR3であり;
R1、R2およびR3はそれぞれ独立して、水素またはC1-6アルキルから選択され;
R4は、水素、C1-6アルキル、C1-6アルコキシ、C3-6シクロアルキル、またはC6-10アリールから選択され、
ここで、C1-6アルキルおよびC1-6アルコキシは、C1-6アルキルまたはC1-6アルコキシから選択される基の1つまたは複数で任意に置換され;
R11およびR12を合わせてN、SまたはOから選択される1~5個のヘテロ原子を有する5~10員の単環式または二環式の飽和の複素環を形成しており、
ここで、5~10員の単環式または二環式の飽和の複素環は、アミノ、C1-6アルキルアミノまたは-NH(CO)CH=CH-CH2-N(CH3)2から選択される置換基で任意に置換され;および
R13は、6員の単環式のアリール、およびN、SまたはOから選択される1~5個のヘテロ原子を有する5~10員の単環式または二環式のヘテロアリールから選択され、
ここで、6員の単環式のアリール、および5~10員の単環式または二環式のヘテロアリールは、ヒドロキシル、シアノ、ハロゲン、C1-6アルキル、C1-6アルコキシ、C3-6シクロアルキル、C1-6ハロアルキル、C6-10アリール、C1-10ヘテロシクリル、またはC1-10ヘテロアリールから選択される1~5個の置換基で任意に置換され、ここで、C1-6アルキル、C1-6アルコキシ、C3-6シクロアルキル、C6-10アリール、C1-10ヘテロシクリル、およびC1-10ヘテロアリールは、水素、C1-6アルキル、C1-6ハロアルキル、C1-6アルコキシ、C3-6シクロアルキル、C6アリール、C1-6ヘテロアリール、C1-6ヘテロシクリル、オキソ、ハロゲン、ヒドロキシル、およびシアノから選択される基の1つまたは複数で任意に置換され、ここで、C6アリール、C1-6ヘテロアリール、およびC1-6ヘテロシクリルは、水素、C1-6アルキル、C1-6アルコキシ、オキソ、ハロゲン、ヒドロキシル、-CH2OH、およびシアノから選択される基の1つまたは複数で任意に置換される、式(I)の化合物、その立体異性体または薬学的に許容できる塩。 - 式(I)の化合物、その立体異性体または薬学的に許容できる塩であって、
XはOまたはSから選択され;
ZはNであり;
AはCR1であり;
BはCR2であり;
DはCR3であり;
R1、R2およびR3はそれぞれ独立して、水素またはC1-4アルキルから選択され、
R4は、水素、C1-4アルキル、C1-4アルコキシ、C3-5シクロアルキル、またはC6アリールから選択され、
ここで、C1-4アルキルおよびC1-4アルコキシは、C1-4アルキルまたはC1-4アルコキシから選択される基の1つまたは複数で任意に置換され;
R11およびR12を合わせてN、SまたはOから選択される1~5個のヘテロ原子を有する5~10員の単環式または二環式の飽和の複素環を形成しており、
ここで、5~10員の単環式または二環式の飽和の複素環は、アミノ、C1-6アルキルアミノ、または-NH(CO)CH=CH-CH2-N(CH3)2から選択される置換基で任意に置換され;および
R13は、6員の単環式のアリール、およびN、SまたはOから選択される1~5個のヘテロ原子を有する5~10員の単環式または二環式のヘテロアリールから選択され、
ここで、6員の単環式のアリール、および5~10員の単環式または二環式のヘテロアリールは、ヒドロキシル、シアノ、ハロゲン、C1-6アルキル、C1-6アルコキシ、C3-6シクロアルキル、C1-6ハロアルキル、C6-10アリール、C1-10ヘテロシクリル、またはC1-10ヘテロアリールから選択される1~5個の置換基で任意に置換され、ここで、C1-6アルキル、C1-6アルコキシ、C3-6シクロアルキル、C6-10アリール、C1-10ヘテロシクリル、およびC1-10ヘテロアリールは、水素、C1-6アルキル、C1-6ハロアルキル、C1-6アルコキシ、C3-6シクロアルキル、C6アリール、C1-6ヘテロアリール、C1-6ヘテロシクリル、オキソ、ハロゲン、ヒドロキシル、およびシアノから選択される基の1つまたは複数で任意に置換され、ここで、C6アリール、C1-6ヘテロアリール、およびC1-6ヘテロシクリルは、水素、C1-6アルキル、C1-6アルコキシ、オキソ、ハロゲン、ヒドロキシル、-CH2OH、およびシアノから選択される基の1つまたは複数で任意に置換される、請求項1に記載の式(I)の化合物、その立体異性体または薬学的に許容できる塩。 - 式(I)の化合物、その立体異性体または薬学的に許容できる塩であって、
XはOまたはSから選択され;
ZはNであり;
AはCR1であり;
BはCR2であり;
DはCR3であり;
R1、R2およびR3はそれぞれ独立して、水素またはC1-4アルキルから選択され、
R4は、水素、C1-4アルキル、C1-4アルコキシ、C3-5シクロアルキル、またはC6アリールから選択され、
ここで、C1-4アルキルおよびC1-4アルコキシは、C1-4アルキルまたはC1-4アルコキシから選択される基の1つまたは複数で任意に置換され;
R11およびR12を合わせてNまたはOから選択される1~5個のヘテロ原子を有する5~10員の単環式または二環式の飽和の複素環を形成しており、
ここで、5~10員の単環式または二環式の飽和の複素環は、アミノ、C1-4アルキルアミノ、または-NH(CO)CH=CH-CH2-N(CH3)2から選択される置換基で任意に置換され;および
R13は、6員の単環式のアリール、およびN、SまたはOから選択される1~5個のヘテロ原子を有する5~10員の単環式または二環式のヘテロアリールから選択され、
ここで、6員の単環式のアリール、および5~10員の単環式または二環式のヘテロアリールは、ハロゲン、C1-4アルキル、C1-4アルコキシ、C3-6シクロアルキル、C1-4ハロアルキル、C6-9アリール、C1-9ヘテロシクリル、またはC1-9ヘテロアリールから選択される1~5個の置換基で任意に置換され、ここで、C1-4アルキル、C1-4アルコキシ、C3-6シクロアルキル、C6-9アリール、C1-9ヘテロシクリル、およびC1-9ヘテロアリールは、水素、C1-4アルキル、C1-4ハロアルキル、C1-4アルコキシ、C3-6シクロアルキル、C6アリール、C1-6ヘテロアリール、C1-6ヘテロシクリル、オキソ、ハロゲン、ヒドロキシル、およびシアノから選択される基の1つまたは複数で任意に置換され、ここで、C6アリール、C1-6ヘテロアリール、およびC1-6ヘテロシクリルは、水素、C1-6アルキル、C1-6アルコキシ、オキソ、ハロゲン、ヒドロキシル、-CH2OH、およびシアノから選択される基の1つまたは複数で任意に置換される、請求項1に記載の式(I)の化合物、その立体異性体または薬学的に許容できる塩。 - 式(I)の化合物、その立体異性体または薬学的に許容できる塩であって、
XはOまたはSから選択され;
ZはNであり;
AはCR1であり;
BはCR2であり;
DはCR3であり;
R1、R2およびR3はそれぞれ独立して、水素またはC1-2アルキルから選択され;
R4は、水素、C1-4アルキル、C1-4アルコキシ、C3-5シクロアルキル、またはC6アリールから選択され、
ここで、C1-4アルキル、およびC1-4アルコキシは、C1-4アルキル、およびC1-4アルコキシから選択される基の1つまたは複数で任意に置換され;
R11およびR12を合わせてN、SまたはOから選択される1~5個のヘテロ原子を有する5~10員の単環式または二環式の飽和の複素環を形成しており、
ここで、5~10員の単環式または二環式の飽和の複素環は、アミノ、C1-2アルキルアミノ、または-NH(CO)CH=CH-CH2-N(CH3)2から選択される置換基で任意に置換され;
R13は、6員の単環式のアリール、およびN、SまたはOから選択される1~5個のヘテロ原子を有する5~9員の単環式または二環式のヘテロアリールから選択され、
ここで、6員の単環式のアリール、および5~9員の単環式または二環式のヘテロアリールは、ヒドロキシル、シアノ、フルオロ、ブロモ、クロロ、C1-4アルキル、C1-4アルコキシ、C1-4ハロアルキル、C3-5シクロアルキル、C6-9アリール、C1-9ヘテロシクリル、またはC1-9ヘテロアリールから選択される1~5個の置換基で任意に置換され、ここで、C1-4アルキル、C1-4アルコキシ、C3-5シクロアルキル、C6-9アリール、C1-9ヘテロシクリル、およびC1-9ヘテロアリールは、水素、ヒドロキシル、C1-4アルキル、C1-4アルコキシ、C1-4ハロアルキル、C3-5シクロアルキル、C6アリール、C1-6ヘテロアリール、C1-6ヘテロシクリル、オキソ、ハロゲン、およびシアノから選択される基の1つまたは複数で任意に置換され、ここで、C6アリール、C1-6ヘテロアリール、およびC1-6ヘテロシクリルは、水素、C1-6アルキル、C1-6アルコキシ、オキソ、ハロゲン、ヒドロキシル、-CH2OH、およびシアノから選択される基の1つまたは複数で任意に置換される、請求項1に記載の式(I)の化合物、その立体異性体または薬学的に許容できる塩。 - 式(II)の化合物、
その立体異性体または薬学的に許容できる塩であって、
XはOまたはSから選択され;
ZはNであり;
AはCR1であり;
BはCR2であり;
DはCR3であり;
EはNまたはCR6から選択され;
FはCR7であり;
GはCR8であり;
HはCR9であり;
R1、R2およびR3はそれぞれ独立して、水素またはC1-6アルキルから選択され;
R4は水素、C1-6アルキル、C1-6アルコキシ、C3-6シクロアルキル、またはC6-10アリールから選択され、
ここで、C1-6アルキルおよびC1-6アルコキシは、C1-6アルキルまたはC1-6アルコキシから選択される基の1つまたは複数で任意に置換され;
R5、R6、R7、R8、R9およびR10はそれぞれ独立して、水素、ヒドロキシル、シアノ、ハロゲン、C1-6アルキル、C1-6アルコキシ、C3-6シクロアルキル、C1-6ハロアルキル、C6-10アリール、C1-10ヘテロシクリル、またはC1-10ヘテロアリールから選択され、
ここで、C1-6アルキル、C1-6アルコキシ、およびC1-10ヘテロアリールは、水素、オキソ、C1-6アルキル、C1-6アルコキシ、C1-6ハロアルキル、C3-6シクロアルキル、C6-9アリール、C1-6ヘテロシクリル、C1-6ヘテロアリール、シアノ、ハロゲン、およびヒドロキシルから選択される基の1つまたは複数で任意に置換され、ここで、C6-9アリール、C1-6ヘテロアリール、およびC1-6ヘテロシクリルは、水素、C1-6アルキル、C1-6アルコキシ、オキソ、ハロゲン、ヒドロキシル、-CH2OH、およびシアノから選択される基の1つまたは複数で任意に置換され;および
R11およびR12を合わせてN、SまたはOから選択される1~5個のヘテロ原子を有する5~10員の単環式または二環式の飽和の複素環を形成しており、
ここで、5~10員の単環式または二環式の飽和の複素環は、アミノ、C1-6アルキルアミノ、または-NH(CO)CH=CH-CH2-N(CH3)2から選択される置換基で任意に置換される、式(II)の化合物、その立体異性体または薬学的に許容できる塩。 - 式(II)の化合物、その立体異性体または薬学的に許容できる塩であって、
XはOまたはSから選択され;
ZはNであり;
AはCR1であり;
BはCR2であり;
DはCR3であり;
EはNまたはCR6から選択され;
FはCR7であり;
GはCR8であり;
HはCR9であり;
R1、R2およびR3はそれぞれ独立して、水素またはC1-6アルキルから選択され;
R6、R7、R8、R9およびR10はそれぞれ独立して、水素、ヒドロキシル、ハロゲン、C1-4アルキル、C1-4アルコキシ、C1-4ハロアルキル、C3-5シクロアルキル、またはC6アリールから選択され;
R4は水素、C1-4アルキル、C1-4アルコキシ、C3-6シクロアルキル、またはC6-9アリールから選択され、
ここで、C1-4アルキルおよびC1-4アルコキシは、C1-4アルキルまたはC1-4アルコキシから選択される基の1つまたは複数で任意に置換され;
R5は水素、ヒドロキシル、シアノ、ハロゲン、C1-4アルキル、C1-4アルコキシ、C3-6シクロアルキル、C1-4ハロアルキル、C6-9アリール、C1-9ヘテロシクリル、またはC1-9ヘテロアリールから選択され、
ここで、C1-4アルキル、C1-4アルコキシ、およびC1-9ヘテロアリールは、水素、オキソ、C1-4アルキル、C1-4アルコキシ、C1-4ハロアルキル、C3-6シクロアルキル、C6アリール、C1-6ヘテロシクリル、C1-6ヘテロアリール、シアノ、ハロゲン、およびヒドロキシルから選択される基の1つまたは複数で任意に置換され、ここで、C6アリール、C1-6ヘテロアリール、およびC1-6ヘテロシクリルは、水素、C1-4アルキル、C1-4アルコキシ、オキソ、ハロゲン、ヒドロキシル、-CH2OH、およびシアノから選択される基の1つまたは複数で任意に置換され;および
R11およびR12を合わせてN、SまたはOから選択される1~5個のヘテロ原子を有する5~10員の単環式または二環式の飽和の複素環を形成しており、
ここで、5~10員の単環式または二環式の飽和の複素環は、アミノ、C1-6アルキルアミノ、または-NH(CO)CH=CH-CH2-N(CH3)2から選択される置換基で任意に置換される、請求項5に記載の式(II)の化合物、その立体異性体または薬学的に許容できる塩。 - 式(II)の化合物、その立体異性体または薬学的に許容できる塩であって、
XはOまたはSから選択され;
ZはNであり;
AはCR1であり;
BはCR2であり;
DはCR3であり;
EはNまたはCR6から選択され;
FはCR7であり;
GはCR8であり;
HはCR9であり;
R1、R2およびR3はそれぞれ独立して、水素またはC1-2アルキルから選択され;
R6、R7、R8、R9およびR10はそれぞれ独立して、水素、ハロゲン、C1-2アルキル、C1-2アルコキシ、またはC6アリールから選択され;
R4は水素、C1-4アルキル、C1-4アルコキシ、C3-6シクロアルキル、またはC6-9アリールから選択され、
ここで、C1-4アルキルおよびC1-4アルコキシは、C1-4アルキルまたはC1-4アルコキシから選択される基の1つまたは複数で任意に置換され;
R5は水素、C1-4アルキル、C1-4アルコキシ、C3-6シクロアルキル、C1-4ハロアルキル、C6-9アリール、C1-9ヘテロシクリル、またはC1-9ヘテロアリールから選択され、
ここで、C1-4アルキル、C1-4アルコキシ、およびC1-9ヘテロアリールは、水素、オキソ、C1-4アルキル、C1-4アルコキシ、C1-4ハロアルキル、C3-6シクロアルキル、C6アリール、C1-6ヘテロシクリル、C1-6ヘテロアリール、シアノ、ハロゲン、およびヒドロキシルから選択される基の1つまたは複数で任意に置換され、ここで、C6アリール、C1-6ヘテロアリール、およびC1-6ヘテロシクリルは、水素、C1-6アルキル、C1-6アルコキシ、オキソ、ハロゲン、ヒドロキシル、-CH2OH、およびシアノから選択される基の1つまたは複数で任意に置換され;および
R11およびR12を合わせてN、SまたはOから選択される1~5個のヘテロ原子を有する5~10員の単環式または二環式の飽和複素環を形成しており、
ここで、5~10員の単環式または二環式の飽和複素環は、アミノ、C1-2アルキルアミノ、または-NH(CO)CH=CH-CH2-N(CH3)2から選択される置換基で任意に置換される、請求項5に記載の式(II)の化合物、その立体異性体または薬学的に許容できる塩。 - 式(III)の化合物、
その立体異性体または薬学的に許容できる塩であって、
XはOまたはSから選択され;
ZはNであり;
R1、R2およびR3はそれぞれ独立して、水素またはC1-6アルキルから選択され;
R4は水素、C1-6アルキル、C1-6アルコキシ、C3-6シクロアルキル、またはC6-10アリールから選択され、
ここで、C1-6アルキルおよびC1-6アルコキシは、C1-6アルキルまたはC1-6アルコキシから選択される基の1つまたは複数で任意に置換され;
R5、R6、R7、R8、R9およびR10はそれぞれ独立して、水素、ヒドロキシル、シアノ、ハロゲン、C1-6アルキル、C1-6アルコキシ、C3-6シクロアルキル、C1-6ハロアルキル、C6-10アリール、C1-10ヘテロシクリル、またはC1-10ヘテロアリールから選択され、
ここで、C1-6アルキル、C1-6アルコキシ、およびC1-10ヘテロアリールは、水素、オキソ、C1-6アルキル、C1-6アルコキシ、C1-6ハロアルキル、C3-6シクロアルキル、C6-9アリール、C1-6ヘテロシクリル、C1-6ヘテロアリール、シアノ、ハロゲン、およびヒドロキシルから選択される基の1つまたは複数で任意に置換され、ここで、C6-9アリール、C1-6ヘテロアリール、およびC1-6ヘテロシクリルは、水素、C1-6アルキル、C1-6アルコキシ、オキソ、ハロゲン、ヒドロキシル、-CH2OH、およびシアノから選択される基の1つまたは複数で任意に置換され;および
R11およびR12を合わせてN、SまたはOから選択される1~5個のヘテロ原子を有する5~10員の単環式または二環式の飽和の複素環を形成しており、
ここで、5~10員の単環式または二環式の飽和の複素環は、アミノ、C1-6アルキルアミノ、または-NH(CO)CH=CH-CH2-N(CH3)2から選択される置換基で任意に置換される、式(III)の化合物、その立体異性体または薬学的に許容できる塩。 - 式(III)の化合物、その立体異性体または薬学的に許容できる塩であって、
XはOまたはSから選択され;
ZはNであり;
R1、R2およびR3はそれぞれ独立して、水素またはC1-6アルキルから選択され;
R6、R7、R8、R9、およびR10はそれぞれ独立して、水素、ヒドロキシル、ハロゲン、C1-4アルキル、C1-4アルコキシまたはC6アリールから選択され;
R4は水素、C1-4アルキル、C1-4アルコキシ、C3-6シクロアルキル、またはC6-9アリールから選択され、
ここで、C1-4アルキル、およびC1-4アルコキシは、C1-4アルキル、またはC1-4アルコキシから選択される基の1つまたは複数で任意に置換され;
R5は水素、ヒドロキシル、シアノ、ハロゲン、C1-4アルキル、C1-4アルコキシ、C3-6シクロアルキル、C1-4ハロアルキル、C6-9アリール、C1-9ヘテロシクリル、またはC1-9ヘテロアリールから選択され、
ここで、C1-4アルキル、C1-4アルコキシ、およびC1-9ヘテロアリールは、水素、オキソ、C1-4アルキル、C1-4アルコキシ、C1-4ハロアルキル、C3-6シクロアルキル、C6アリール、C1-6ヘテロシクリル、C1-6ヘテロアリール、シアノ、ハロゲン、およびヒドロキシルから選択される基の1つまたは複数で任意に置換され、ここで、C6アリール、C1-6ヘテロアリール、およびC1-6ヘテロシクリルは、水素、C1-6アルキル、C1-6アルコキシ、オキソ、ハロゲン、ヒドロキシル、-CH2OH、およびシアノから選択される基の1つまたは複数で任意に置換され;および
R11およびR12を合わせてN、SまたはOから選択される1~5個のヘテロ原子を有する5~10員の単環式または二環式の飽和の複素環を形成しており、
ここで、5~10員の単環式または二環式の飽和の複素環は、アミノ、C1-6アルキルアミノ、または-NH(CO)CH=CH-CH2-N(CH3)2から選択される置換基で任意に置換される、請求項8に記載の式(III)の化合物、その立体異性体または薬学的に許容できる塩。 - 式(III)の化合物、その立体異性体または薬学的に許容できる塩であって、
XはOまたはSから選択され;
ZはNであり;
R1、R2およびR3はそれぞれ独立して、水素またはC1-4アルキルであり;
R6、R7、R8、R9およびR10はそれぞれ独立して、水素、ハロゲン、C1-4アルキル、C1-4アルコキシ、またはC6アリールから選択され、
R4は水素、C1-4アルキル、C1-4アルコキシ、C3-6シクロアルキル、またはC6-9アリールから選択され、
ここで、C1-4アルキル、およびC1-4アルコキシはC1-4アルキル、またはC1-4アルコキシから選択される基の1つまたは複数で任意に置換され;
R5は水素、C1-4アルキル、C1-4アルコキシ、C3-6シクロアルキル、C6-9アリール、C1-9ヘテロシクリル、またはC1-9ヘテロアリールから選択され、ここで、C1-4アルキル、C1-4アルコキシ、およびC1-9ヘテロアリールは、水素、オキソ、C1-4アルキル、C1-4アルコキシ、C1-4ハロアルキル、C3-6シクロアルキル、C6アリール、C1-6ヘテロシクリル、C1-6ヘテロアリール、シアノ、ハロゲン、およびヒドロキシルから選択される基の1つまたは複数で任意に置換され、ここで、C6アリール、C1-6ヘテロアリール、およびC1-6ヘテロシクリルは、水素、C1-6アルキル、C1-6アルコキシ、オキソ、ハロゲン、ヒドロキシル、-CH2OH、およびシアノから選択される基の1つまたは複数で任意に置換され;
R11およびR12を合わせてN、SまたはOから選択される1~5個のヘテロ原子を有する5~10員の単環式または二環式の飽和複素環を形成し、
ここで、5~10員の単環式または二環式の飽和の複素環は、アミノ、C1-4アルキルアミノ、または-NH(CO)CH=CH-CH2-N(CH3)2から選択される置換基で任意に置換される、請求項8に記載の式(III)の化合物、その立体異性体または薬学的に許容できる塩。 - (R)-(3-アミノピペリジン-1-イル)(2-(3-ブロモ-1-(シクロプロピルメチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(1)、
(R)-(3-アミノピペリジン-1-イル)(2-(1-(シクロプロピルメチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(2)、
(R)-(3-アミノピペリジン-1-イル)(2-(1-ベンジル-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(3)、
(R)-(3-アミノピペリジン-1-イル)(2-(1-エチル-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(4)、
(R)-(3-アミノピペリジン-1-イル)(2-(1-エチル-3-フェニル-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(5)、
(R)-(3-アミノピロリジン-1-イル)(2-(1-エチル-3-フェニル-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(6)、
(R)-(3-アミノピロリジン-1-イル)(2-(1-エチル-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(7)、
(R)-(3-アミノピロリジン-1-イル)(2-(1-(シクロプロピルメチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(8)、
(2-(1-(シクロプロピルメチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)(ヘキサヒドロ-2H-ピリド[4,3-b][1,4]オキサジン-6(5H)-イル)メタノン(9)、
(R)-(3-アミノピペリジン-1-イル)(3-メチル-2-(1-(ピリジン-4-イルメチル)-1H-インドール-2-イル)イミダゾ[1,2a]ピリジン-7-イル)メタノン(10)、
(R)-(3-アミノピペリジン-1-イル)(3-メチル-2-(1-((テトラヒドロ-2H-ピラン-4-イル)メチル)-1H-インドール-2-イル)イミダゾ[1,2a]ピリジン-7-イル)メタノン(11)、
(R)-(3-アミノピペリジン-1-イル)(2-(1-(4-メトキシベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(12)、
(R)-(3-アミノピペリジン-1-イル)(2-(1-(4-フルオロベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(13)、
(R)-4-((2-(7-(3-アミノピペリジン-1-カルボニル)-3-メチルイミダゾ[1,2a]ピリジン-2-イル)-1H-インドール-1-イル)メチル)ベンゾニトリル(14)、
(R)-(3-アミノピペリジン-1-イル)(3-メチル-2-(1-(ピリジン-3-イルメチル)-1H-インドール-2-イル)イミダゾ[1,2a]ピリジン-7-イル)メタノン(15)、
(R)-(3-アミノピペリジン-1-イル)(3-メチル-2-(1-(ピリジン-2-イルメチル)-1H-インドール-2-イル)イミダゾ[1,2a]ピリジン-7-イル)メタノン(16)、
(R)-(3-アミノピペリジン-1-イル)(3-メチル-2-(1-(2,2,2-トリフルオロエチル)-1H-インドール-2-イル)イミダゾ[1,2a]ピリジン-7-イル)メタノン(17)、
(R)-4-((2-(7-(3-アミノピペリジン-1-カルボニル)-3-メチルイミダゾ[1,2a]ピリジン-2-イル)-1H-インドール-1-イル)メチル)-1-メチルピリジン-2(1H)-オン(18)、
(R)-(3-アミノピペリジン-1-イル)(2-(3-エチルベンゾ[b]チオフェン-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(19)、
(R)-(3-アミノピペリジン-1-イル)(2-(1-(4-クロロベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(20)、
(R)-(3-アミノピペリジン-1-イル)(2-(1-(2-フルオロベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(21)、
(R)-(3-アミノピペリジン-1-イル)(2-(1-エチル-5-フェニル-1H-ピロール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(22)、
(R)-(3-アミノピペリジン-1-イル)(2-(1-(シクロプロピルメチル)-6-メトキシ-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(23)、
(R)-(3-アミノピペリジン-1-イル)(2-(1-エチル-1H-ピロロ[2,3-b]ピリジン-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(24)、
(R)-(3-アミノピペリジン-1-イル)(2-(1-(シクロプロピルメチル)-1H-インドール-2-イル)-3,5-ジメチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(25)、
(R)-(3-アミノピペリジン-1-イル)(2-(1-ベンジル-1H-インドール-2-イル)-3,5-ジメチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(26)、
(R)-(3-アミノピペリジン-1-イル)(3,5-ジメチル-2-(1-(ピリジン-2-イルメチル)-1H-インドール-2-イル)イミダゾ[1,2a]ピリジン-7-イル)メタノン(27)、
(R)-(3-アミノピペリジン-1-イル)(2-(1-(シクロプロピルメチル)-6-フルオロ-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(28)、
(R)-(3-アミノピペリジン-1-イル)(2-(1-(シクロプロピルメチル)-5-フルオロ-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(29)、
(R)-(3-アミノピペリジン-1-イル)(2-(1-(シクロプロピルメチル)-7-メチル-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(30)、
(R)-(3-アミノピペリジン-1-イル)(2-(2-エチルフェニル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(31)、
(R)-(3-アミノピペリジン-1-イル)(2-(1-(シクロプロピルメチル)-1H-インドール-2-イル)-3-フェニルイミダゾ[1,2a]ピリジン-7-イル)メタノン(32)、
(R)-(3-アミノピペリジン-1-イル)(3-シクロプロピルメチル-2-(1-(シクロプロピルメチル)-1H-インドール-2-イル)イミダゾ[1,2a]ピリジン-7-イル)メタノン(33)、
(R)-(3-アミノピペリジン-1-イル)(2-(1-(シクロプロピルメチル)-1H-インドール-2-イル)-3-(メトキシメチル)イミダゾ[1,2a]ピリジン-7-イル)メタノン(34)、
(R)-(3-アミノピペリジン-1-イル)(2-(1-(3-フルオロベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(35)、
(R)-(3-アミノピペリジン-1-イル)(3-メチル-2-(1-(チオフェン-3-イルメチル)-1H-インドール-2-イル)イミダゾ[1,2a]ピリジン-7-イル)メタノン(36)、
(R)-(3-アミノピペリジン-1-イル)(2-(1-(フラン-3-イルメチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(37)、
(R)-(3-アミノピペリジン-1-イル)(2-(1-(1-(4-フルオロフェニル)エチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(38)、
(R)-(3-アミノピペリジン-1-イル)(2-(1-エチル-5-フルオロ-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(39)、
(R)-(3-アミノピペリジン-1-イル)(2-(1-(シクロプロピルメチル)4-フルオロ-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(40)、
(R)-(3-アミノピペリジン-1-イル)(3-メチル-2-(1-((4-メチルチアゾール-2-イル)メチル)-1H-インドール-2-イル)イミダゾ[1,2a]ピリジン-7-イル)メタノン(41)、
(R)-(3-アミノピペリジン-1-イル)(2-(1-(3-メトキシベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(42)、
(R)-(3-アミノピペリジン-1-イル)(2-(5-ブロモ-1-(シクロプロピルメチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(43)、
(R)-(3-アミノピペリジン-1-イル)(2-(7-クロロ-1-(シクロプロピルメチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(44)、
(R)-(3-アミノピペリジン-1-イル)(2-(1-(4-フルオロベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(45)、
(R)-(3-アミノピペリジン-1-イル)(3-メチル-2-(1-メチル-1H-インドール-2-イル)イミダゾ[1,2a]ピリジン-7-イル)メタノン(46)、
(R)-(3-アミノピペリジン-1-イル)(2-(1-(シクロプロピルメチル)-7-メトキシ-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(47)、
(R)-(3-アミノピペリジン-1-イル)(2-(1-((2,4-ジメチルチアゾール-5-イル)メチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(48)、
(R)-(3-アミノピペリジン-1-イル)(3-メチル-2-(1-((2-メチルチアゾール-5-イル)メチル)-1H-インドール-2-イル)イミダゾ[1,2a]ピリジン-7-イル)メタノン(49)、
(R)-(3-アミノピペリジン-1-イル)(2-(1-(3-メトキシベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノントリフルオロ酢酸塩(50)、
(R)-(3-アミノピペリジン-1-イル)(2-(6-メトキシ-1-(ピリジン-3-イルメチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(51)、
(R)-(3-アミノピペリジン-1-イル)(2-(1-(シクロプロピルメチル)-6-フルオロ-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノントリフルオロ酢酸塩(52)、
(R)-(3-アミノピペリジン-1-イル)(2-(5-フルオロ-1-(3-メトキシベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(53)、
(R)-(3-アミノピペリジン-1-イル)(2-(6-フルオロ-1-(4-フルオロベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(54)、
(R)-(3-アミノピペリジン-1-イル)(2-(5,6-ジフルオロ-1-(3-メトキシベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(55)、
(R,E)-4-(ジメチルアミノ)-N-(1-(2-(1-(4-フルオロベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-カルボニル)ピペリジン-3-イル)ブタ-2-エンアミド(56)、
(R)-(3-アミノピペリジン-1-イル)(3-メチル-2-(1-(ピラジン-2-イルメチル)-1H-インドール-2-イル)イミダゾ[1,2a]ピリジン-7-イル)メタノン(57)、
(R)-(3-アミノピペリジン-1-イル)(3-メチル-2-(1-(ピリミジン-5-イルメチル)-1H-インドール-2-イル)イミダゾ[1,2a]ピリジン-7-イル)メタノントリフルオロ酢酸塩(58)、
(R)-(3-アミノピペリジン-1-イル)(3-メチル-2-(1-(ピリダジン-3-イルメチル)-1H-インドール-2-イル)イミダゾ[1,2a]ピリジン-7-イル)メタノン(59)、
(R)-(3-アミノピペリジン-1-イル)(2-(1-イソブチル-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(60)、
(R)-(3-アミノピペリジン-1-イル)(2-(1-(シクロブチルメチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(61)、
(R)-(3-アミノピペリジン-1-イル)(2-(1-((3-フルオロピリジン-2-イル)メチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(62)、
(R)-(3-アミノピペリジン-1-イル)(2-(1-((5-メトキシピリジン-2-イル)メチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(63)、
(R)-(3-アミノピペリジン-1-イル)(2-(1-(2-メトキシエチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(64)、
(R)-(3-アミノピペリジン-1-イル)(2-(1-(2-ヒドロキシエチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(65)、
(R)-(3-アミノピペリジン-1-イル)(2-(6-メトキシ-1-(ピリジン-4-イルメチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(66)、
(R)-(3-アミノピペリジン-1-イル)(2-(1-エチル-6-メトキシ-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(67)、
(R)-(3-アミノピペリジン-1-イル)(2-(6-フルオロ-1-(ピリジン-4-イルメチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(68)、
(R)-(3-アミノピペリジン-1-イル)(2-(6-フルオロ-1-(ピリジン-3-イルメチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(69)、
(R)-(3-アミノピペリジン-1-イル)(2-(6-フルオロ-1-(3-メトキシベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(70)、
(R)-(3-アミノピペリジン-1-イル)(2-(6-フルオロ-1-(4-メトキシベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(71)、
(R)-(3-アミノピペリジン-1-イル)(2-(1-エチル-6-フルオロ-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(72)、
(R)-(3-アミノピペリジン-1-イル)(2-(6-フルオロ-1-イソブチル-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(73)、
(R)-(3-アミノピペリジン-1-イル)(2-(5-フルオロ-1-(ピリジン-4-イルメチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(74)、
(R)-(3-アミノピペリジン-1-イル)(2-(5-フルオロ-1-(4-メトキシベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(75)、
(R)-(3-アミノピペリジン-1-イル)(2-(5-フルオロ-1-(4-フルオロベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(76)、
(R)-(3-アミノピペリジン-1-イル)(2-(7-クロロ-1-(4-フルオロベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(77)、
(R)-(3-アミノピペリジン-1-イル)(2-(1-(2,2-ジフルオロエチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノントリフルオロ酢酸塩(78)、
(R)-(3-アミノピペリジン-1-イル)(2-(1-((5-フルオロピリジン-2-イル)メチル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(79)、
(R)-(3-アミノピペリジン-1-イル)(2-(1-(4-フルオロベンジル)-6-メトキシ-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(80)、
(R)-(3-アミノピペリジン-1-イル)(2-(1-(4-(ヒドロキシメチル)ベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(81)、
(R)-(3-アミノピペリジン-1-イル)(2-(1-イソブチル-6-メトキシ-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(82)、
(R)-(3-アミノピペリジン-1-イル)(2-(1-(2,2-ジフルオロエチル)-6-メトキシ-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(83)、
(R)-(3-アミノピペリジン-1-イル)(2-(5-フルオロ-1-イソブチル-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(84)、および、
(R)-(3-アミノピペリジン-1-イル)(2-(1-(4-フルオロ-3-メトキシベンジル)-1H-インドール-2-イル)-3-メチルイミダゾ[1,2a]ピリジン-7-イル)メタノン(85)から成る群から選択される、請求項1に記載の式(I)の化合物、またはその立体異性体もしくは薬学的に許容できる塩。 - 請求項1~4、11のいずれか1項に記載の式(I)の化合物、その立体異性体または薬学的に許容できる塩の調製方法であって、
R13CH(O)およびR4CH2NO2を、式(IVA)または式(IV)から選択される化合物と反応させる工程を含み、
R13CH(O)のR13は、6員の単環式のアリール、およびN、SまたはOから選択される1~5個のヘテロ原子を有する5~10員の単環式または二環式のヘテロアリールから選択され、ここで、6員の単環式のアリール、および5~10員の単環式または二環式のヘテロアリールは、ヒドロキシル、シアノ、ハロゲン、C1-6アルキル、C1-6アルコキシ、C3-6シクロアルキル、C1-6ハロアルキル、C6-10アリール、C1-10ヘテロシクリル、またはC1-10ヘテロアリールから成る群から選択される1~5個の置換基で任意に置換され、ここで、C1-6アルキル、C1-6アルコキシ、C3-6シクロアルキル、C6-10アリール、C1-10ヘテロシクリル、およびC1-10ヘテロアリールは、水素、C1-6アルキル、C1-6ハロアルキル、C1-6アルコキシ、C3-6シクロアルキル、C6アリール、C1-6ヘテロアリール、C1-6ヘテロシクリル、オキソ、ハロゲン、ヒドロキシル、およびシアノから選択される基の1つまたは複数で任意に置換され、ここで、C6アリール、C1-6ヘテロアリール、およびC1-6ヘテロシクリルは、水素、C1-6アルキル、C1-6アルコキシ、オキソ、ハロゲン、ヒドロキシル、-CH2OH、およびシアノから選択される基の1つまたは複数で任意に置換され;式(IVA)および式(IV)のAはCR1であり;BはCR2であり;DはCR3であり;R11およびR12を合わせてN、SまたはOから選択される1~5個のヘテロ原子を有する5~10員の単環式または二環式の飽和の複素環を形成しており、ここで、5~10員の単環式または二環式の飽和の複素環は、アミノ、C1-6アルキルアミノ、または-NH(CO)CH=CH-CH2-N(CH3)2から選択される置換基で任意に置換され;R4CH2NO2のR4は、水素、C1-6アルキル、C1-6アルコキシ、C3-6シクロアルキル、またはC6-10アリールから選択され、ここで、C1-6アルキル、およびC1-6アルコキシは、C1-6アルキル、またはC1-6アルコキシから選択される基の1つまたは複数で任意に置換され;式(I)のXはOまたはSから選択され;ZはNであり;AはCR1であり;BはCR2であり;DはCR3であり;R1、R2およびR3はそれぞれ独立して、水素またはC1-6アルキルから選択され;R4は水素、C1-6アルキル、C1-6アルコキシ、C3-6シクロアルキル、またはC6-10アリールから選択され、ここで、C1-6アルキル、およびC1-6アルコキシは、C1-6アルキル、またはC1-6アルコキシから選択される基の1つまたは複数で任意に置換され;R11およびR12を合わせてN、SまたはOから選択される1~5個のヘテロ原子を有する5~10員の単環式または二環式の飽和の複素環を形成しており、ここで、5~10員の単環式または二環式の飽和の複素環は、アミノ、C1-6アルキルアミノ、または-NH(CO)CH=CH-CH2-N(CH3)2から選択される置換基で任意に置換され;およびR13は、6員の単環式のアリール、およびN、SまたはOから選択される1~5個のヘテロ原子を有する5~10員の単環式または二環式のヘテロアリールから選択され、
ここで、6員の単環式のアリール、および5~10員の単環式または二環式のヘテロアリールは、ヒドロキシル、シアノ、ハロゲン、C1-6アルキル、C1-6アルコキシ、C3-6シクロアルキル、C1-6ハロアルキル、C6-10アリール、C1-10ヘテロシクリル、またはC1-10ヘテロアリールから選択される1~5個の置換基で任意に置換され、ここで、C1-6アルキル、C1-6アルコキシ、C3-6シクロアルキル、C6-10アリール、C1-10ヘテロシクリル、およびC1-10ヘテロアリールは、水素、C1-6アルキル、C1-6ハロアルキル、C1-6アルコキシ、C3-6シクロアルキル、C6アリール、C1-6ヘテロアリール、C1-6ヘテロシクリル、オキソ、ハロゲン、ヒドロキシル、およびシアノから選択される基の1つまたは複数で任意に置換され、ここで、C6アリール、C1-6ヘテロアリール、およびC1-6ヘテロシクリルは、水素、C1-6アルキル、C1-6アルコキシ、オキソ、ハロゲン、ヒドロキシル、-CH2OH、およびシアノから選択される基の1つまたは複数で任意に置換される、調製方法。 - 請求項5~7のいずれか1項に記載の式(II)の化合物、その立体異性体または薬学的に許容できる塩の調製方法であって、
R4CH2NO2および式(V)を、式(IVA)または式(IV)から選択される化合物と反応させる工程を含み、
式(IVA)および式(IV)のAはCR1であり;BはCR2であり;DはCR3であり;R11およびR12を合わせてN、SまたはOから選択される1~5個のヘテロ原子を有する5~10員の単環式または二環式の飽和の複素環を形成しており、ここで、5~10員の単環式または二環式の飽和の複素環は、アミノ、C1-6アルキルアミノ、または-NH(CO)CH=CH-CH2-N(CH3)2から選択される置換基で任意に置換され;R4CH2NO2のR4は、水素、C1-6アルキル、C1-6アルコキシ、C3-6シクロアルキル、またはC6-10アリールから選択され、ここで、C1-6アルキル、およびC1-6アルコキシは、C1-6アルキル、またはC1-6アルコキシから選択される基の1つまたは複数で任意に置換され;式(V)のEはNまたはCR6から選択され;FはCR7であり;GはCR8であり;HはCR9であり;R1、R2およびR3はそれぞれ独立して、水素またはC1-6アルキルから選択され;
R5、R6、R7、R8、R9およびR10はそれぞれ独立して、水素、ヒドロキシル、シアノ、ハロゲン、C1-6アルキル、C1-6アルコキシ、C3-6シクロアルキル、C1-6ハロアルキル、C6-10アリール、C1-10ヘテロシクリル、またはC1-10ヘテロアリールから選択され、ここで、C1-6アルキル、C1-6アルコキシ、およびC1-10ヘテロアリールは、水素、オキソ、C1-6アルキル、C1-6アルコキシ、C1-6ハロアルキル、C3-6シクロアルキル、C6-9アリール、C1-6ヘテロシクリル、C1-6ヘテロアリール、シアノ、ハロゲン、およびヒドロキシルから選択される基の1つまたは複数で任意に置換され、ここで、C6-9アリール、C1-6ヘテロアリール、およびC1-6ヘテロシクリルは、水素、C1-6アルキル、C1-6アルコキシ、オキソ、ハロゲン、ヒドロキシル、-CH2OH、およびシアノから選択される基の1つまたは複数で任意に置換され;式(II)のXはOまたはSから選択され;ZはNであり;AはCR1であり;BはCR2であり;DはCR3であり;EはNまたはCR6から選択され;FはCR7であり;GはCR8であり;HはCR9であり;R1、R2およびR3はそれぞれ独立して、水素またはC1-6アルキルから選択され;R4は水素、C1-6アルキル、C1-6アルコキシ、C3-6シクロアルキル、またはC6-10アリールから選択され、ここで、C1-6アルキル、およびC1-6アルコキシは、C1-6アルキル、またはC1-6アルコキシから選択される基の1つまたは複数で任意に置換され;R5、R6、R7、R8、R9およびR10はそれぞれ独立して、水素、ヒドロキシル、シアノ、ハロゲン、C1-6アルキル、C1-6アルコキシ、C3-6シクロアルキル、C1-6ハロアルキル、C6-10アリール、C1-10ヘテロシクリル、またはC1-10ヘテロアリールから選択され、ここで、C1-6アルキル、C1-6アルコキシ、およびC1-10ヘテロアリールは、水素、オキソ、C1-6アルキル、C1-6アルコキシ、C1-6ハロアルキル、C3-6シクロアルキル、C6-9アリール、C1-6ヘテロシクリル、C1-6ヘテロアリール、シアノ、ハロゲン、およびヒドロキシルから選択される基の1つまたは複数で任意に置換され、ここで、C6-9アリール、C1-6ヘテロアリール、およびC1-6ヘテロシクリルは、水素、C1-6アルキル、C1-6アルコキシ、オキソ、ハロゲン、ヒドロキシル、-CH2OH、およびシアノから選択される基の1つまたは複数で任意に置換され;およびR11およびR12を合わせてN、SまたはOから選択される1~5個のヘテロ原子を任意に有する5~10員の単環式または二環式の飽和の複素環を形成しており、ここで、5~10員の単環式または二環式の飽和の複素環は、アミノ、C1-6アルキルアミノ、または-NH(CO)CH=CH-CH2-N(CH3)2から選択される置換基で任意に置換される、調製方法。 - 請求項8~10のいずれか1項に記載の式(III)の化合物、またはその立体異性体もしくは薬学的に許容できる塩の調製方法であって、
式(VII)、R4CH2NO2を、式(VIA)または式(VI)から選択される化合物と反応させる工程を含み、
式(VIA)および式(VI)のR1、R2およびR3はそれぞれ独立して、水素またはC1-6アルキルから選択され;R4CH2NO2のR4は水素、C1-6アルキル、C1-6アルコキシ、C3-6シクロアルキル、またはC6-10アリールから選択され、ここで、C1-6アルキル、およびC1-6アルコキシは、C1-6アルキル、またはC1-6アルコキシから選択される基の1つまたは複数で任意に置換され;式(VII)のR5、R6、R7、R8、R9およびR10はそれぞれ独立して、水素、ヒドロキシル、シアノ、ハロゲン、C1-6アルキル、C1-6アルコキシ、C3-6シクロアルキル、C1-6ハロアルキル、C6-10アリール、C1-10ヘテロシクリル、またはC1-10ヘテロアリールから選択され、ここで、C1-6アルキル、C1-6アルコキシ、およびC1-10ヘテロアリールは、水素、オキソ、C1-6アルキル、C1-6アルコキシ、C1-6ハロアルキル、C3-6シクロアルキル、C6-9アリール、C1-6ヘテロシクリル、C1-6ヘテロアリール、シアノ、ハロゲン、およびヒドロキシルから選択される基の1つまたは複数で任意に置換され、ここで、C6-9アリール、C1-6ヘテロアリール、およびC1-6ヘテロシクリルは、水素、C1-6アルキル、C1-6アルコキシ、オキソ、ハロゲン、ヒドロキシル、-CH2OH、およびシアノから選択される基の1つまたは複数で任意に置換され;式(III)のXはOまたはSから選択され;ZはNであり;R1、R2およびR3はそれぞれ独立して、水素またはC1-6アルキルから選択され;R4は水素、C1-6アルキル、C1-6アルコキシ、C3-6シクロアルキル、またはC6-10アリールから選択され、ここで、C1-6アルキル、およびC1-6アルコキシは、C1-6アルキル、またはC1-6アルコキシから選択される基の1つまたは複数で任意に置換され;R5、R6、R7、R8、R9およびR10はそれぞれ独立して、水素、ヒドロキシル、シアノ、ハロゲン、C1-6アルキル、C1-6アルコキシ、C3-6シクロアルキル、C1-6ハロアルキル、C6-10アリール、C1-10ヘテロシクリル、またはC1-10ヘテロアリールから選択され、ここで、C1-6アルキル、C1-6アルコキシ、およびC1-10ヘテロアリールは、水素、オキソ、C1-6アルキル、C1-6アルコキシ、C1-6ハロアルキル、C3-6シクロアルキル、C6-9アリール、C1-6ヘテロシクリル、C1-6ヘテロアリール、シアノ、ハロゲン、およびヒドロキシルから選択される基の1つまたは複数で任意に置換され、ここで、C6-9アリール、C1-6ヘテロアリール、およびC1-6ヘテロシクリルは、水素、C1-6アルキル、C1-6アルコキシ、オキソ、ハロゲン、ヒドロキシル、-CH2OH、およびシアノから選択される基の1つまたは複数で任意に置換され;およびR11およびR12を合わせてN、SまたはOから選択される1~5個のヘテロ原子を有する5~10員の単環式または二環式の飽和の複素環を形成しており、ここで、5~10員の単環式または二環式の飽和の複素環は、アミノ、C1-6アルキルアミノ、または-NH(CO)CH=CH-CH2-N(CH3)2から選択される置換基で任意に置換される、調製方法。 - 請求項1~11のいずれか1項に記載の式(I)、式(II)、式(III)の化合物またはその薬学的に許容できる塩と、薬学的に許容できる担体とを含み、任意で1つまたは複数の他の医薬組成物を含む、医薬組成物。
- 上記組成物は、錠剤、カプセル、粉末、シロップ、溶液、エアロゾル、および懸濁液から選択される形態である、請求項15に記載の医薬組成物。
- 細胞内で1つまたは複数のPADを阻害する薬物の製造に用いられる、請求項1~11のいずれか1項に記載の化合物またはその薬学的に許容できる塩。
- 細胞内で1つまたは複数のPADファミリーを阻害するための薬物の製造における、請求項1~11のいずれか1項に記載の化合物の使用。
- 1つまたは複数のPADファミリーによって媒介される症状を患う対象に、化合物または医薬組成物を、治療上有効な量、投与する工程を含む、1つまたは複数のPADによって媒介される症状の治療のための薬剤の製造における、請求項1~11のいずれか1項に記載の化合物、または請求項15もしくは16に記載の医薬組成物の使用。
- 関節リウマチ、血管炎、全身性紅斑性狼瘡、潰瘍性大腸炎、癌、嚢胞性線維症、喘息、皮膚エリテマトーデス、および乾癬の治療に用いられる、請求項1~11のいずれか1項に記載の化合物。
- 他の臨床的に関連する薬剤または生物学的薬剤と併用して、1つまたは複数のPADファミリーによって媒介される症状を治療する、または、血管炎、全身性紅斑性狼瘡、癌、喘息、および皮膚エリテマトーデスを治療する、および/または治療の予防をするための薬物の製造における、請求項1~11のいずれか1項に記載の化合物の使用、または請求項15もしくは16に記載の医薬組成物の使用。
- 他の臨床的に関連する薬剤または生物学的薬剤と併用して、1つまたは複数のPADファミリーによって媒介される症状を治療する、または、酸誘発肺損傷、呼吸窮迫症候群、アレルゲン誘発喘息、アレルギー性気管支肺疾患、未熟児慢性肺疾患、慢性閉塞性肺疾患、大腸炎、嚢胞性線維症、通風性関節炎、炎症性腸疾患、炎症性肺疾患、炎症性疼痛、若年性関節リウマチ、腎臓病、寄生虫感染症による腎障害、腎移植拒絶反応予防、肺障害、狼瘡、ループス腎炎、多発性硬化症、筋ジストロフィー、非アレルゲン誘発喘息、変形性関節症、歯周炎、腹膜子宮内膜症、乾癬、肺疾患、肺線維症、化膿性無菌性関節炎、腎疾患、リウマチ性疾患、関節リウマチ、敗血症、激痛、潰瘍性大腸炎を治療および/または予防するための薬物の製造における、請求項1~11のいずれか1項に記載の化合物の使用、または請求項15もしくは16に記載の医薬組成物の使用。
- 1つまたは複数のPADファミリーによって媒介される症状を患う対象に、化合物または医薬組成物を治療に有効な量、投与する工程を含む、1つまたは複数のPADファミリーの不調によって媒介される上記症状の治療および/または予防のための薬剤の製造における、請求項1~11のいずれか1項に記載の化合物、または請求項15もしくは16に記載の医薬組成物の使用。
- 他の臨床的に関連する薬剤または生物学的薬剤と併用して、化合物または医薬組成物を、それを必要とする対象に投与する工程を含む、関節リウマチの治療のための薬剤の製造における、請求項1~11のいずれか1項に記載の化合物、または請求項15もしくは16に記載の医薬組成物の使用。
- 他の臨床的に関連する免疫調節剤と併用して、化合物または医薬組成物を、それを必要とする対象に投与する工程を含む、癌の治療のための薬剤の製造における、請求項1~11のいずれか1項に記載の化合物、または請求項15もしくは16に記載の医薬組成物の使用。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| IN201741037110 | 2017-10-18 | ||
| IN201741037110 | 2017-10-18 | ||
| PCT/IN2018/050671 WO2019077631A1 (en) | 2017-10-18 | 2018-10-16 | IMIDAZO-PYRIDINE COMPOUNDS FOR USE AS PAD INHIBITORS |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2021500330A JP2021500330A (ja) | 2021-01-07 |
| JP7307723B2 true JP7307723B2 (ja) | 2023-07-12 |
Family
ID=64051641
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020521516A Active JP7307723B2 (ja) | 2017-10-18 | 2018-10-16 | Pad阻害剤としてのイミダゾ-ピリジン化合物 |
Country Status (20)
| Country | Link |
|---|---|
| US (1) | US11426412B2 (ja) |
| EP (1) | EP3697785B1 (ja) |
| JP (1) | JP7307723B2 (ja) |
| KR (1) | KR20200071752A (ja) |
| CN (1) | CN111225915B (ja) |
| AU (1) | AU2018352142B2 (ja) |
| BR (1) | BR112020007607A2 (ja) |
| CA (1) | CA3076476A1 (ja) |
| DK (1) | DK3697785T3 (ja) |
| ES (1) | ES2941512T3 (ja) |
| FI (1) | FI3697785T3 (ja) |
| HU (1) | HUE061607T2 (ja) |
| IL (1) | IL272667B (ja) |
| MX (1) | MX2020003341A (ja) |
| PL (1) | PL3697785T3 (ja) |
| PT (1) | PT3697785T (ja) |
| RS (1) | RS64104B1 (ja) |
| SG (1) | SG11202003463XA (ja) |
| WO (1) | WO2019077631A1 (ja) |
| ZA (1) | ZA202002770B (ja) |
Families Citing this family (22)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA3073656C (en) | 2017-09-22 | 2024-03-05 | Jubilant Epipad LLC | Heterocyclic compounds as pad inhibitors |
| DK3697785T3 (da) | 2017-10-18 | 2023-04-03 | Jubilant Epipad LLC | Imidazo-pyridine forbindelser som pad-inhibitorer |
| WO2019087214A1 (en) | 2017-11-06 | 2019-05-09 | Jubilant Biosys Limited | Pyrimidine derivatives as inhibitors of pd1/pd-l1 activation |
| US11459338B2 (en) | 2017-11-24 | 2022-10-04 | Jubilant Episcribe Llc | Heterocyclic compounds as PRMT5 inhibitors |
| KR20200131845A (ko) | 2018-03-13 | 2020-11-24 | 주빌런트 프로델 엘엘씨 | Pd1/pd-l1 상호작용/활성화 억제제로서의 비사이클릭 화합물 |
| JP7447080B2 (ja) | 2018-08-08 | 2024-03-11 | ブリストル-マイヤーズ スクイブ カンパニー | Pad4阻害剤としての置換チエノピロール |
| AU2019319835A1 (en) | 2018-08-08 | 2021-03-25 | Bristol-Myers Squibb Company | Indole and azaindole inhibitors of PAD enzymes |
| JP7451419B2 (ja) | 2018-10-26 | 2024-03-18 | 大鵬薬品工業株式会社 | 新規なインダゾール化合物又はその塩 |
| MX2021011302A (es) | 2019-03-19 | 2022-01-19 | Boehringer Ingelheim Animal Health Usa Inc | Compuestos de aza-benzotiofeno y aza-benzofurano como antihelminticos. |
| CN112574230B (zh) * | 2019-09-27 | 2022-10-28 | 药捷安康(南京)科技股份有限公司 | 肽酰精氨酸脱亚胺酶抑制剂及其用途 |
| AU2020372881A1 (en) | 2019-10-28 | 2022-06-09 | Merck Sharp & Dohme Llc | Small molecule inhibitors of KRAS G12C mutant |
| WO2021084765A1 (en) * | 2019-10-31 | 2021-05-06 | Taiho Pharmaceutical Co., Ltd | 4-aminobut-2-enamide derivatives and salts thereof |
| TW202140477A (zh) * | 2020-02-12 | 2021-11-01 | 美商必治妥美雅史谷比公司 | 雜環pad4抑制劑 |
| US20230107927A1 (en) | 2020-02-28 | 2023-04-06 | First Wave Bio, Inc. | Methods of treating iatrogenic autoimmune colitis |
| MX2022013615A (es) | 2020-04-30 | 2022-11-16 | Gilead Sciences Inc | Inhibidores de macrociclo de peptidilarginina deiminasas. |
| EP4185589A1 (en) | 2020-05-29 | 2023-05-31 | Boehringer Ingelheim Animal Health USA Inc. | Anthelmintic heterocyclic compounds |
| EP4196476A4 (en) * | 2020-08-12 | 2024-08-07 | Jubilant Epipad LLC | METHOD AND COMPOUND FOR USE IN THE TREATMENT AND/OR PREVENTION OF NETOSIS |
| TW202233174A (zh) * | 2020-12-22 | 2022-09-01 | 美商基利科學股份有限公司 | 肽基精胺酸去亞胺酶之抑制劑 |
| US11878965B2 (en) | 2020-12-22 | 2024-01-23 | Gilead Sciences, Inc. | Inhibitors of peptidylarginine deiminases |
| AU2022234499A1 (en) * | 2021-03-11 | 2023-10-26 | Zhejiang University | Fused ring heterocyclic compound and application thereof, and pharmaceutical composition containing same and application thereof |
| WO2022232320A1 (en) * | 2021-04-27 | 2022-11-03 | Merck Sharp & Dohme Corp. | Small molecule inhibitors of kras g12c mutant |
| CA3236894A1 (en) | 2021-11-01 | 2023-05-04 | Boehringer Ingelheim Vetmedica Gmbh | Anthelmintic pyrrolopyridazine compounds |
Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2005523288A (ja) | 2002-02-19 | 2005-08-04 | ファルマシア・アンド・アップジョン・カンパニー・エルエルシー | 疾病治療用の縮合した二環式−n−架橋−複素環式芳香族カルボキサミド |
| JP2006502164A (ja) | 2002-09-06 | 2006-01-19 | バイオジェン・アイデック・エムエイ・インコーポレイテッド | イミダゾロピリジンならびにその生成および使用方法 |
| JP2009523752A (ja) | 2006-01-17 | 2009-06-25 | エフ.ホフマン−ラ ロシュ アーゲー | GABAレセプター経由でのアルツハイマー病の処置に有用なアリール−イソオキサゾール−4−イル−イミダゾ[1,2−a]ピリジン誘導体 |
| JP2011500544A (ja) | 2007-10-12 | 2011-01-06 | アステックス、セラピューティックス、リミテッド | タンパク質チロシンキナーゼインヒビターとしての二環式ヘテロ環式化合物 |
| JP2015522628A (ja) | 2012-07-26 | 2015-08-06 | グラクソ グループ リミテッドGlaxo Group L | Pad4阻害剤としての2−(アザインドール−2−イル)ベンズイミダゾール |
| WO2016185279A1 (en) | 2015-05-21 | 2016-11-24 | Glaxosmithkline Intellectual Property Development Limited | Benzoimidazole derivatives as pad4 inhibitors |
Family Cites Families (273)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB1230663A (ja) | 1968-12-10 | 1971-05-05 | ||
| GB1356789A (en) | 1970-08-06 | 1974-06-12 | Prodotti Antibiotici Spa | Derivatives of theophylline |
| DE2050657C3 (de) | 1970-10-15 | 1974-06-20 | Basf Ag, 6700 Ludwigshafen | Azofarbstoffe, Verfahren zu ihrer Herstellung und deren Verwendung |
| US3970753A (en) | 1973-06-12 | 1976-07-20 | Smith Kline & French Laboratories Limited | Imidazo[1,2-a]pyridines |
| DE2361390A1 (de) | 1973-12-10 | 1975-06-19 | Merck Patent Gmbh | Isochinolinderivate und verfahren zu ihrer herstellung |
| US4246274A (en) | 1978-05-10 | 1981-01-20 | Bayer Aktiengesellschaft | Antimycotic hydroxypropyl-imidazoles |
| DE2832677A1 (de) | 1978-07-26 | 1980-02-07 | Bayer Ag | Hydroxypropyl-imidazole, verfahren zu ihrer herstellung sowie ihre verwendung als arzneimittel |
| DE3210570A1 (de) | 1982-03-23 | 1983-10-06 | Hoechst Ag | 3-azolyl-1,2-diaryl-1-halogen-1-propene, ihre herstellung, ihre verwendung als pflanzenschutzmittel und diese verbindungen enthaltende praeparate |
| WO1984002907A1 (en) | 1983-01-21 | 1984-08-02 | Alkaloida Vegyeszeti Gyar | New alkyl diamine derivatives |
| AU5698186A (en) | 1985-03-15 | 1986-10-13 | Summerton, J. | Polynucleotide assay reagent and method |
| DE3628545A1 (de) | 1985-09-23 | 1987-04-23 | Hoechst Ag | Arylmethylazole und deren salze, verfahren zu ihrer herstellung, sie enthaltende mittel und ihre verwendung |
| JPH07100688B2 (ja) | 1986-02-12 | 1995-11-01 | 大日本製薬株式会社 | 環状アミン誘導体 |
| JPH07121911B2 (ja) | 1986-03-26 | 1995-12-25 | クミアイ化学工業株式会社 | 4(1h)−ピリジノン誘導体および農園芸用殺菌剤 |
| DE3631013A1 (de) | 1986-09-12 | 1988-03-24 | Thomae Gmbh Dr K | Neue naphthylderivate, diese verbindungen enthaltende arzneimittel und verfahren zu ihrer herstellung |
| DE3879024T2 (de) | 1987-07-31 | 1993-10-07 | Takeda Chemical Industries Ltd | Pyridinium-Derivate, ihre Herstellung und Verwendung. |
| US5210266A (en) | 1987-12-03 | 1993-05-11 | Dainippon Pharmaceutical Co., Ltd. | N-substituted mercaptopropanamide derivatives |
| US5179125A (en) | 1987-12-03 | 1993-01-12 | Dainippon Pharmaceutical Co., Ltd. | N-substituted mercaptopropanamide derivatives |
| GB8820231D0 (en) * | 1988-08-25 | 1988-09-28 | Fujisawa Pharmaceutical Co | New benzazole compounds processes for preparation thereof & pharmaceutical composition comprising same |
| FR2638747B1 (fr) | 1988-11-08 | 1993-12-24 | Synthelabo | Derives de phenyloxypropanolamines, leur preparation et leur application en therapeutique |
| DE3901723A1 (de) | 1989-01-21 | 1990-07-26 | Bayer Ag | Azolyl-derivate |
| JP2769711B2 (ja) | 1989-02-17 | 1998-06-25 | 昭和電工株式会社 | オレフィン重合用触媒成分の製造方法及びオレフィンの重合方法 |
| WO1991000537A1 (de) | 1989-07-04 | 1991-01-10 | Kumpf, Ursula | Verfahren und einrichtung zum einziehen von insbesondere lichtwellenleiterkabeln in schutzrohre |
| US5420289A (en) | 1989-10-27 | 1995-05-30 | American Home Products Corporation | Substituted indole-, indene-, pyranoindole- and tetrahydrocarbazole-alkanoic acid derivatives as inhibitors of PLA2 and lipoxygenase |
| PT95692A (pt) | 1989-10-27 | 1991-09-13 | American Home Prod | Processo para a preparacao de derivados de acidos indole-,indeno-,piranoindole- e tetra-hidrocarbazole-alcanoicos, ou quais sao uteis como inibidores de pla2 e da lipoxigenase |
| US5229516A (en) | 1989-10-27 | 1993-07-20 | American Home Products Corporation | Substituted indole-, indene-, pyranoindole- and tetrahydrocarbazole-alkanoic acid derivatives as inhibitors of PLA2 and lipoxygenase |
| DE69108138T2 (de) | 1990-07-30 | 1995-07-06 | Takeda Chemical Industries Ltd | Imidazopyridinderivate und ihre Verwendung. |
| CA2090434A1 (en) | 1991-07-03 | 1993-01-04 | Mitsuaki Ohtani | Phospholipase a2 inhibitor |
| EP0533056A3 (en) | 1991-09-14 | 1993-06-16 | Hoechst Aktiengesellschaft | Substituted aminopropanes, process for their preparation and their use as antimycotic agents |
| US5273980A (en) | 1991-09-30 | 1993-12-28 | Merck Frosst Canada Inc. | Bicyclic-azaarylmethoxy) indoles as inhibitors of leukotriene biosynthesis |
| CA2079374C (en) | 1991-09-30 | 2003-08-05 | Merck Frosst Canada Incorporated | (bicyclic-azaarylmethoxy)indoles as inhibitors of leukotriene biosynthesis |
| US5330989A (en) | 1991-10-24 | 1994-07-19 | American Home Products Corporation | Heterocycles substituted with biphenyl-3-cyclobutene-1,2-dione derivatives |
| CA2125570A1 (en) | 1991-12-10 | 1993-06-24 | Frank Zurmuhlen | Pyrimidinyl- or triazinyl-oxy(or thio)aldehyde derivatives and their use as herbicides or plant-growth regulators |
| GB9206757D0 (en) | 1992-03-27 | 1992-05-13 | Ferring Bv | Novel peptide receptor ligands |
| DE4227522A1 (de) | 1992-08-20 | 1994-02-24 | Bayer Ag | Lichtpolarisierende Folien und neue dichroitische Farbstoffe hierfür |
| JP3298954B2 (ja) | 1992-12-16 | 2002-07-08 | 三共株式会社 | 新規n,n’−ジベンゾイルヒドラジン誘導体及び殺虫組成物 |
| US5484926A (en) | 1993-10-07 | 1996-01-16 | Agouron Pharmaceuticals, Inc. | HIV protease inhibitors |
| DK0691959T3 (da) | 1993-03-29 | 1999-04-26 | Zeneca Ltd | Heterocykliske derivater som blodpladeaggregations-inhibitorer |
| IL109220A0 (en) | 1993-04-05 | 1994-07-31 | Synaptic Pharma Corp | Dihydropyridines and new uses thereof |
| JPH09501405A (ja) | 1993-05-27 | 1997-02-10 | スミスクライン・ビーチャム・ラボラトワール・ファルマソーティク | 抗不整脈用n−置換3−ベンズアゼピンまたはイソキノリン |
| FR2706895A1 (en) | 1993-06-22 | 1994-12-30 | Synthelabo | Tetrahydroisoquinoline derivatives, their preparation and their application in therapeutics |
| JPH07179402A (ja) | 1993-10-20 | 1995-07-18 | Ishihara Sangyo Kaisha Ltd | 置換ベンゼン誘導体、その製造方法及びそれを含有する有害生物防除剤 |
| US5461154A (en) | 1994-02-02 | 1995-10-24 | Eli Lilly And Company | Intermediate and process for making |
| TW281667B (ja) | 1994-02-03 | 1996-07-21 | Synthelabo | |
| GB9402807D0 (en) | 1994-02-14 | 1994-04-06 | Xenova Ltd | Pharmaceutical compounds |
| JPH07304770A (ja) | 1994-05-11 | 1995-11-21 | Kanebo Ltd | 新規ベンゾアゼピノン誘導体 |
| US5593994A (en) | 1994-09-29 | 1997-01-14 | The Dupont Merck Pharmaceutical Company | Prostaglandin synthase inhibitors |
| AU4368996A (en) | 1994-11-23 | 1996-06-17 | Neurogen Corporation | Certain 4-aminomethyl-2-substituted imidazole derivatives and 2-aminomethyl-4-substituted imidazole derivatives; new classes of dopamine receptor subtype specific ligands |
| US5541033A (en) | 1995-02-01 | 1996-07-30 | Ocg Microelectronic Materials, Inc. | Selected o-quinonediazide sulfonic acid esters of phenolic compounds and their use in radiation-sensitive compositions |
| US20030018025A1 (en) | 1995-06-07 | 2003-01-23 | Neurogen Corporation, Corporation Of The State Of Delaware | Certain 4-aminomethyl-2-substituted imidazole derivatives and 2-aminomethyl-4-substituted imidazole derivatives: new classes of dopamine receptor subtype specific ligands |
| US5554621A (en) | 1995-06-07 | 1996-09-10 | Bristol-Myers Squibb Company | Dihydropyridine NPY antagonists: nitrogen heterocyclic derivatives |
| EP0848957A1 (en) | 1995-09-08 | 1998-06-24 | Kanebo Ltd. | Fas LIGAND SOLUBILIZATION INHIBITOR |
| IL125033A0 (en) | 1995-12-29 | 1999-01-26 | Smithkline Beecham Corp | Vitronectin receptor antagonists |
| EP0915888A1 (en) | 1996-04-24 | 1999-05-19 | Takeda Chemical Industries, Ltd. | Fused imidazopyridine derivatives as antihyperlipidemic agents |
| DE69737376T2 (de) | 1996-07-17 | 2007-06-06 | Fuji Photo Film Co., Ltd., Minami-Ashigara | Verfahren zur Synthese einer Oxonolverbindung |
| GB9717576D0 (en) | 1997-08-19 | 1997-10-22 | Xenova Ltd | Pharmaceutical compounds |
| HN1997000027A (es) | 1996-12-06 | 1997-06-05 | Pfizer Prod Inc | Derivados de 6-fenil piridil - 2 amina |
| HUP9700392A1 (hu) | 1997-02-10 | 1999-09-28 | ICN Magyarország Részvénytársaság | Egy vagy két hatóanyagot tartalmazó kardioprotektív hatású gyógyszerkészítmények |
| US6048877A (en) | 1997-02-21 | 2000-04-11 | Bristol-Myers Squibb Company | Tetralone derivatives as antiarrhythmic agents |
| DK0971878T3 (da) | 1997-02-27 | 2008-06-30 | Takeda Pharmaceutical | Aminforbindelser, fremstillingen og anvendelsen deraf som inhibitorer af amyloid-beta-produktion |
| DE19717371A1 (de) | 1997-04-24 | 1998-10-29 | Basf Ag | Propargyl-terminierte, nematische oder cholesterische Polymere |
| KR100343067B1 (ko) | 1997-07-31 | 2002-07-03 | 프리돌린 클라우스너, 롤란드 비. 보레르 | 항종양제 및 항전이제로서 산소-치환된하이드록시쿠마라논 유도체 |
| JPH11119379A (ja) | 1997-10-08 | 1999-04-30 | Fuji Photo Film Co Ltd | ハロゲン化銀カラー写真感光材料および画像形成方法 |
| AU3352899A (en) | 1997-12-11 | 1999-07-12 | American Home Products Corporation | 2,4,6-trisubstituted pyridines with estrogenic activity and methods for the solid phase synthesis thereof |
| TW555757B (en) | 1998-07-31 | 2003-10-01 | Akzo Nobel Nv | Aminomethylcarboxylic acid derivatives |
| DE19834751A1 (de) | 1998-08-01 | 2000-02-03 | Boehringer Ingelheim Pharma | Disubstituierte bicyclische Heterocyclen, ihre Herstellung und ihre Verwendung als Arzneimittel |
| DE69924132T2 (de) | 1998-10-20 | 2006-04-06 | Takeda Pharmaceutical Co. Ltd. | Aromatische aminderivate, verfahren zu ihrer herstellung und mittel, die diese enthalten |
| GB9823873D0 (en) | 1998-10-30 | 1998-12-30 | Pharmacia & Upjohn Spa | 2-ureido-thiazole derivatives,process for their preparation,and their use as antitumour agents |
| US6357758B1 (en) | 1999-06-30 | 2002-03-19 | Federal-Mogul World Wide, Inc. | Metal gasket and method of manufacturing |
| JP4603679B2 (ja) | 1999-12-14 | 2010-12-22 | 日本化薬株式会社 | 害虫防除剤 |
| GB0007108D0 (en) | 2000-03-23 | 2000-05-17 | Novartis Ag | Organic compounds |
| US6534651B2 (en) | 2000-04-06 | 2003-03-18 | Inotek Pharmaceuticals Corp. | 7-Substituted isoindolinone inhibitors of inflammation and reperfusion injury and methods of use thereof |
| KR20020097484A (ko) | 2000-05-19 | 2002-12-31 | 다케다 야쿠힌 고교 가부시키가이샤 | β-씨크리타아제 억제제 |
| US6846813B2 (en) | 2000-06-30 | 2005-01-25 | Pharmacia & Upjohn Company | Compounds to treat alzheimer's disease |
| MXPA02012560A (es) | 2000-06-30 | 2003-05-14 | Elan Pharm Inc | Compuestos para tratar la enfermedad de alzheimer. |
| US20020094989A1 (en) | 2000-10-11 | 2002-07-18 | Hale Jeffrey J. | Pyrrolidine modulators of CCR5 chemokine receptor activity |
| WO2002034716A2 (en) | 2000-10-11 | 2002-05-02 | Merck & Co., Inc. | Pyrrolidine modulators of ccr5 chemokine receptor activity |
| SE0100568D0 (sv) | 2001-02-20 | 2001-02-20 | Astrazeneca Ab | Compounds |
| DE10110750A1 (de) | 2001-03-07 | 2002-09-12 | Bayer Ag | Neuartige Aminodicarbonsäurederivate mit pharmazeutischen Eigenschaften |
| FR2822153B1 (fr) | 2001-03-19 | 2003-10-31 | Servier Lab | Nouveaux derives d'indenoindolones, leur procede de preparation et les compositions pharmaceutiques qui les contiennent |
| NZ527276A (en) | 2001-03-27 | 2004-11-26 | Actelion Pharmaceuticals Ltd | 1,2,3,4-tetrahydroisoquinoline derivatives as urotensin II receptor antagonists |
| FR2822827B1 (fr) | 2001-03-28 | 2003-05-16 | Sanofi Synthelabo | Nouveaux derives de n-(arylsulfonyl) beta-aminoacides comportant un groupe aminomethyle substitue, leur procede de preparation et les compositions pharmaceutiques en contenant |
| MXPA03009239A (es) | 2001-04-10 | 2004-11-12 | Johnson & Johnson | Derivados de 1,3,8-triazapiro[4,5]decan-4-ona utiles para el tratamiento de trastornos mediados por el receptor orl-1. |
| WO2002088089A1 (fr) | 2001-04-19 | 2002-11-07 | Banyu Pharmaceutical Co., Ltd. | Derives de spiropiperidine, antagonistes du recepteur de nociceptine les contenant en tant qu'ingredient actif et compositions medicinales |
| US6720321B2 (en) | 2001-06-05 | 2004-04-13 | Boehringer Ingelheim Pharmaceuticals, Inc. | 1,4-disubstituted benzo-fused cycloalkyl urea compounds |
| BR0210190A (pt) | 2001-06-07 | 2004-04-06 | Lilly Co Eli | Moduladores de receptores ativados de proliferador de peroxissomo |
| EP1429776A2 (en) | 2001-09-21 | 2004-06-23 | PHARMACIA & UPJOHN COMPANY | Tricyclic indole derivatives as 5-ht ligands |
| SI1441734T1 (sl) | 2001-10-26 | 2007-08-31 | Angeletti P Ist Richerche Bio | Dihidropirimidin karboksamidni inhibitorji HIV-integraze |
| SE0103644D0 (sv) | 2001-11-01 | 2001-11-01 | Astrazeneca Ab | Therapeutic isoquinoline compounds |
| ES2242890T3 (es) | 2001-11-20 | 2005-11-16 | Eli Lilly And Company | Agonistas beta 3 de oxindol 3-sustituido. |
| ATE386740T1 (de) | 2001-11-20 | 2008-03-15 | Lilly Co Eli | Beta-3 adrenergische agonisten |
| GB0202873D0 (en) | 2002-02-07 | 2002-03-27 | Novartis Ag | Organic compounds |
| US6875780B2 (en) | 2002-04-05 | 2005-04-05 | Warner-Lambert Company | Compounds that modulate PPAR activity and methods for their preparation |
| AU2003248122A1 (en) | 2002-07-25 | 2004-02-16 | Kotobuki Pharmaceutical Co., Ltd. | Sodium channel inhibitor |
| EP1388342A1 (en) | 2002-08-07 | 2004-02-11 | Aventis Pharma Deutschland GmbH | Acylated, heteroaryl-condensed cycloalkenylamines and their use as pharmaceuticals |
| BR0306309A (pt) | 2002-09-09 | 2004-10-19 | Janssen Pharmaceutica Nv | Derivados de 1,3,8-triazaespiro[4.5]decan-4-ona substituìda com hidroxialquila úteis para o tratamento de distúrbios mediados pelo receptor orl-1 |
| WO2004035579A1 (ja) | 2002-10-15 | 2004-04-29 | Takeda Pharmaceutical Company Limited | イミダゾピリジン誘導体、その製造法および用途 |
| AU2003284596A1 (en) | 2002-11-22 | 2004-06-18 | Takeda Pharmaceutical Company Limited | Imidazole derivative, process for producing the same, and use |
| JP4422034B2 (ja) | 2002-12-06 | 2010-02-24 | バイエル・ヘルスケア・アクチェンゲゼルシャフト | テトラヒドロ−ナフタレン誘導体 |
| MXPA05006798A (es) | 2002-12-20 | 2006-03-09 | Migenix Corp | Ligandos de adenina nucleotido translocasa (ant) y composiciones y metodos relacionados a estos. |
| WO2004078731A1 (fr) | 2003-03-06 | 2004-09-16 | 'chemical Diversity Research Institute', Ltd. | Acides quinoline-carboxyliques et leurs derives et bibliotheque focalisee |
| WO2004109400A2 (en) | 2003-03-11 | 2004-12-16 | Arch Speciality Chemicals, Inc. | Novel photosensitive resin compositions |
| JP4226395B2 (ja) | 2003-06-16 | 2009-02-18 | アルパイン株式会社 | 音声補正装置 |
| US7504401B2 (en) | 2003-08-29 | 2009-03-17 | Locus Pharmaceuticals, Inc. | Anti-cancer agents and uses thereof |
| CA2550012A1 (en) | 2003-12-17 | 2005-06-30 | Takeda Pharmaceutical Company Limited | Urea derivative, process for producing the same and use |
| US20050159334A1 (en) | 2004-01-16 | 2005-07-21 | Gluck Oscar S. | Method for treating rheumatoid arthritis by inhibiting peptidylarginine deiminase |
| EP1735319B1 (en) | 2004-03-26 | 2017-05-03 | MethylGene Inc. | Inhibitors of histone deacetylase |
| TWI351282B (en) | 2004-04-07 | 2011-11-01 | Theravance Inc | Quinolinone-carboxamide compounds as 5-ht4 recepto |
| RU2266906C1 (ru) | 2004-04-29 | 2005-12-27 | Общество с ограниченной ответственностью "Исследовательский Институт Химического Разнообразия" (ООО "Исследовательский Институт Химического Разнообразия") | Анелированные карбамоилазагетероциклы, способы их получения (варианты), фармацевтическая композиция, фокусированная библиотека |
| GB0413605D0 (en) | 2004-06-17 | 2004-07-21 | Addex Pharmaceuticals Sa | Novel compounds |
| US7488745B2 (en) | 2004-07-16 | 2009-02-10 | Schering Corporation | Compounds for the treatment of inflammatory disorders |
| EP1655283A1 (en) | 2004-11-08 | 2006-05-10 | Evotec OAI AG | 11beta-HSD1 Inhibitors |
| JP2008007405A (ja) | 2004-12-07 | 2008-01-17 | Takeda Chem Ind Ltd | カルボキサミド誘導体 |
| KR20070091665A (ko) | 2004-12-22 | 2007-09-11 | 세라밴스 인코포레이티드 | 인다졸-카르복사미드 화합물 |
| US7297700B2 (en) | 2005-03-24 | 2007-11-20 | Renovis, Inc. | Bicycloheteroaryl compounds as P2X7 modulators and uses thereof |
| DE102005016547A1 (de) | 2005-04-08 | 2006-10-12 | Grünenthal GmbH | Substituierte 5,6,7,8-Tetrahydro-imidazo(1,2-a)pyridin-2-ylamin-Verbindungen und deren Verwendung zur Herstellung von Arzneimitteln |
| AR054363A1 (es) | 2005-05-23 | 2007-06-20 | Astrazeneca Ab | Compuestos que exhiben actividad moduladora en el receptor 5-hidroxi-triptamina 6 |
| US7800123B2 (en) | 2005-05-25 | 2010-09-21 | Koninklijke Philips Electronics N.V. | Electroluminescence device |
| EP1890690A4 (en) | 2005-06-02 | 2010-06-02 | Jenrin Discovery | MAO-B INHIBITORS FOR TREATING OBESITY |
| DE602006019595D1 (de) | 2005-06-07 | 2011-02-24 | Theravance Inc | Benzimidazoloncarbonsäureamidverbindungen als agonisten des 5-ht4-rezeptors |
| US7592461B2 (en) | 2005-12-21 | 2009-09-22 | Bristol-Myers Squibb Company | Indane modulators of glucocorticoid receptor, AP-1, and/or NF-κB activity and use thereof |
| CN102499921A (zh) | 2005-12-22 | 2012-06-20 | 海德拉生物科学公司 | 治疗疼痛的方法和组合物 |
| JP2009524689A (ja) | 2006-01-25 | 2009-07-02 | スミスクライン ビーチャム コーポレーション | 化合物 |
| US20070191371A1 (en) | 2006-02-14 | 2007-08-16 | Kalypsys, Inc. | Heterocyclic modulators of ppar |
| RU2302417C1 (ru) | 2006-03-14 | 2007-07-10 | Иващенко Андрей Александрович | 1-оксо-3-(1н-индол-3-ил)-1,2,3,4-тетрагидроизохинолины, способы их получения, комбинаторная библиотека и фокусированная библиотека |
| CA2646430A1 (en) | 2006-03-14 | 2007-09-20 | Amgen Inc. | Bicyclic carboxylic acid derivatives useful for treating metabolic disorders |
| CA2540218A1 (en) | 2006-03-17 | 2007-09-17 | Hafedh Trigui | Asymmetric beams for spectrum efficiency |
| DE102006015449A1 (de) | 2006-03-31 | 2007-10-04 | Eads Deutschland Gmbh | Selbstleuchtender Körper und Verfahren zu seiner Herstellung |
| RU2303597C1 (ru) | 2006-05-12 | 2007-07-27 | Иващенко Андрей Александрович | Фармацевтическая композиция, способы ее получения и применения |
| US20080280891A1 (en) | 2006-06-27 | 2008-11-13 | Locus Pharmaceuticals, Inc. | Anti-cancer agents and uses thereof |
| JP5352454B2 (ja) | 2006-06-28 | 2013-11-27 | サノフイ | Cxcr2アンンタゴニスト |
| WO2008008059A1 (en) | 2006-07-12 | 2008-01-17 | Locus Pharmaceuticals, Inc. | Anti-cancer agents ans uses thereof |
| DE102006039003A1 (de) | 2006-08-19 | 2008-02-21 | Boehringer Ingelheim Pharma Gmbh & Co. Kg | Neue Verbindungen |
| JP2010506948A (ja) | 2006-10-20 | 2010-03-04 | アイアールエム・リミテッド・ライアビリティ・カンパニー | C−kitおよびpdgfr受容体を調節するための組成物および方法 |
| WO2008064320A2 (en) | 2006-11-21 | 2008-05-29 | University Of Virginia Patent Foundation | Hydrindane analogs having sphingosine 1-phosphate receptor agonist activity |
| KR20090094336A (ko) | 2006-11-27 | 2009-09-04 | 하. 룬트벡 아크티에 셀스카브 | 헤테로아릴 아미드 유도체 |
| WO2008065500A2 (en) | 2006-11-30 | 2008-06-05 | Pfizer Products Inc. | Heteroaryl amides as type i glycine transport inhibitors |
| CA2673003A1 (en) | 2006-12-22 | 2008-07-03 | Novartis Ag | Quinazolines for pdk1 inhibition |
| US8338437B2 (en) | 2007-02-28 | 2012-12-25 | Methylgene Inc. | Amines as small molecule inhibitors |
| CN101686952A (zh) | 2007-03-12 | 2010-03-31 | Vm生物医药公司 | 新型钙离子通道调节剂 |
| CN101679422A (zh) | 2007-03-28 | 2010-03-24 | 阵列生物制药公司 | 作为受体酪氨酸激酶抑制剂的咪唑并[1,2-a]吡啶化合物 |
| JP5313881B2 (ja) | 2007-04-04 | 2013-10-09 | 興和株式会社 | テトラヒドロイソキノリン化合物 |
| JP2008280344A (ja) | 2007-04-12 | 2008-11-20 | Sumitomo Chemical Co Ltd | ヒドラジド化合物及びそれを含有する有害節足動物防除剤 |
| TW200902533A (en) | 2007-05-02 | 2009-01-16 | Boehringer Ingelheim Int | Carboxylic acid amides, manufacturing and use thereof as medicaments |
| AU2008302667B2 (en) | 2007-06-15 | 2014-07-10 | Board Of Regents, The University Of Texas System | Methods and compositions to inhibit edema factor and adenylyl cyclase |
| CN101784520B (zh) | 2007-06-20 | 2014-07-02 | 田边三菱制药株式会社 | 磺酰基丙二酰胺衍生物和其药物用途 |
| RU2345996C1 (ru) | 2007-07-17 | 2009-02-10 | Андрей Александрович Иващенко | Аннелированные азагетероциклические амиды, включающие пиримидиновый фрагмент, способ их получения и применения |
| MX2010001650A (es) | 2007-08-10 | 2010-08-02 | Glaxosmithkline Llc | Entidades quimicas biciclicas que contienen nitrogeno para el tratamiento de infecciones virales. |
| WO2009048152A2 (en) | 2007-10-11 | 2009-04-16 | Sumitomo Chemical Company, Limited | Unsaturated imine compound and use thereof for pest control |
| ES2830024T3 (es) | 2007-10-19 | 2021-06-02 | Novartis Ag | Composiciones y métodos para el tratamiento del edema macular |
| EP2072050A1 (en) | 2007-12-21 | 2009-06-24 | Santhera Pharmaceuticals (Schweiz) AG | Compounds with anti-emetic effect |
| JP2011507910A (ja) | 2007-12-21 | 2011-03-10 | ユニバーシティー オブ ロチェスター | 真核生物の寿命を変更するための方法 |
| FR2925902B1 (fr) | 2008-01-02 | 2011-01-07 | Sanofi Aventis | DERIVES D'IMIDAZO°1,2-a!PYRIDINE-2-CARBOXAMIDES, LEUR PREPARATION ET LEUR APPLICATION EN THERAPEUTIQUE |
| RU2371444C1 (ru) | 2008-01-24 | 2009-10-27 | Андрей Александрович Иващенко | ФУРО- И ТИЕНО[2,3-b]-ХИНОЛИН-2-КАРБОКСАМИДЫ, СПОСОБ ПОЛУЧЕНИЯ И ПРОТИВОТУБЕРКУЛЕЗНАЯ АКТИВНОСТЬ |
| US8338406B2 (en) | 2008-02-22 | 2012-12-25 | Otsuka Pharmaceutical Co., Ltd. | Benzodiazepine compound and pharmaceutical composition |
| JP2009209090A (ja) | 2008-03-04 | 2009-09-17 | Mitsui Chemicals Inc | 殺虫剤及び該殺虫剤に含まれる化合物、並びに該化合物の使用方法 |
| US20090276250A1 (en) | 2008-05-01 | 2009-11-05 | Travel Tech Systems, Llc | Process and system to determine commercial airline arrivals |
| US8148408B2 (en) | 2008-05-09 | 2012-04-03 | Abbott Laboratories | Selective substituted pyridine ligands for neuronal nicotinic receptors |
| WO2009140101A2 (en) | 2008-05-12 | 2009-11-19 | Boehringer Ingelheim International Gmbh | Imidazopyridine compounds useful as mmp-13 inhibitors |
| JP2009274984A (ja) | 2008-05-14 | 2009-11-26 | Sumitomo Chemical Co Ltd | 化合物、光学フィルムおよび光学フィルムの製造方法 |
| US20100121052A1 (en) | 2008-06-20 | 2010-05-13 | Rama Jain | Novel compounds for treating proliferative diseases |
| AR073949A1 (es) | 2008-10-21 | 2010-12-15 | Metabolex Inc | Agonistas del receptor aril-gpr120 y usos de los mismos |
| DE102008060958A1 (de) | 2008-12-06 | 2010-07-08 | Saltigo Gmbh | Hydroxytetralone |
| NZ593937A (en) | 2008-12-08 | 2014-05-30 | Vm Pharma Llc | Compositions of protein receptor tyrosine kinase inhibitors |
| US8367700B2 (en) | 2008-12-17 | 2013-02-05 | Gruenenthal Gmbh | Substituted 4-(1.2,3,4-tetrahydroisoquinolin-2-yl)-4-oxobutyric acid amide as KCNQ2/3 modulators |
| US20100204265A1 (en) | 2009-02-09 | 2010-08-12 | Genelabs Technologies, Inc. | Certain Nitrogen Containing Bicyclic Chemical Entities for Treating Viral Infections |
| JP2012051806A (ja) | 2009-02-26 | 2012-03-15 | Eisai R & D Management Co Ltd | イミダゾリルピラジン誘導体 |
| CN104592219B (zh) | 2009-03-16 | 2017-04-12 | 住友化学株式会社 | 化合物、光学膜和光学膜的制造方法 |
| JP5899607B2 (ja) | 2009-03-16 | 2016-04-06 | 住友化学株式会社 | 化合物、光学フィルム及び光学フィルムの製造方法 |
| AU2010232729A1 (en) | 2009-03-31 | 2011-10-20 | Arqule, Inc. | Substituted indolo-pyridinone compounds |
| US20110077250A1 (en) | 2009-06-26 | 2011-03-31 | Ryder Sean | Compounds for modulating rna binding proteins and uses therefor |
| JP5669481B2 (ja) | 2009-08-21 | 2015-02-12 | 大塚製薬株式会社 | 医薬組成物 |
| GB0914767D0 (en) | 2009-08-24 | 2009-09-30 | Sterix Ltd | Compound |
| EP2357176A1 (en) | 2010-01-15 | 2011-08-17 | Hybrigenics S.A. | Amidoacridine derivatives useful as selective inhibitors of ubiquitin specific protease 7 |
| EP3106460B1 (en) | 2010-02-11 | 2019-04-10 | Celgene Corporation | Arylmethoxy isoindoline derivatives and compositions comprising and methods of using the same |
| UY33304A (es) | 2010-04-02 | 2011-10-31 | Amgen Inc | Compuestos heterocíclicos y sus usos |
| US8697911B2 (en) | 2010-07-07 | 2014-04-15 | Boehringer Ingelheim International Gmbh | Rho kinase inhibitors |
| US9079880B2 (en) | 2010-07-07 | 2015-07-14 | Boehringer Ingelheim International Gmbh | Rho kinase inhibitors |
| RU2563644C2 (ru) | 2010-08-20 | 2015-09-20 | Хатчисон Медифарма Лимитед | Пирролопиримидиновые соединения и их применения |
| WO2012022045A1 (en) | 2010-08-20 | 2012-02-23 | Hutchison Medipharma Limited | Pyrrolopyrimidine compounds and uses thereof |
| US20130203756A1 (en) | 2010-10-29 | 2013-08-08 | Jamie L. Bunda | Isoindoline pde10 inhibitors |
| CN106986862A (zh) | 2010-12-22 | 2017-07-28 | Abbvie 公司 | 丙型肝炎抑制剂及其用途 |
| US8975235B2 (en) | 2011-03-20 | 2015-03-10 | Intermune, Inc. | Lysophosphatidic acid receptor antagonists |
| JP6284475B2 (ja) | 2011-06-29 | 2018-02-28 | ザ ジェネラル ホスピタル コーポレイション | 雌性生殖細胞における生体エネルギー状態を増強するための組成物及び方法 |
| EP2726477A4 (en) | 2011-06-29 | 2015-08-26 | Harvard College | SMALL MOLECULAR CD38 HEMMER AND USE METHOD THEREFOR |
| US9938269B2 (en) | 2011-06-30 | 2018-04-10 | Abbvie Inc. | Inhibitor compounds of phosphodiesterase type 10A |
| JP2014198669A (ja) | 2011-08-03 | 2014-10-23 | 杏林製薬株式会社 | ビアリールエステル誘導体、及びそれらを有効成分とする医薬 |
| US20130116241A1 (en) | 2011-11-09 | 2013-05-09 | Abbvie Inc. | Novel inhibitor compounds of phosphodiesterase type 10a |
| AU2012358805B2 (en) | 2011-12-22 | 2017-07-20 | Gilead Sciences, Inc. | Pyrazolo[1,5-a]pyrimidines as antiviral agents |
| CA2859869A1 (en) | 2011-12-23 | 2013-06-27 | Novartis Ag | Compounds for inhibiting the interaction of bcl2 with binding partners |
| MX2014007732A (es) | 2011-12-23 | 2015-01-12 | Novartis Ag | Compuestos para inhibir la interaccion de bcl2 con los mismos componentes de enlace. |
| EP2794592A1 (en) | 2011-12-23 | 2014-10-29 | Novartis AG | Compounds for inhibiting the interaction of bcl2 with binding partners |
| WO2013096049A1 (en) | 2011-12-23 | 2013-06-27 | Novartis Ag | Compounds for inhibiting the interaction of bcl2 with binding partners |
| CZ2012114A3 (cs) | 2012-02-17 | 2013-02-20 | Zentiva, K.S. | Zpusob prípravy rivaroxabanu zalozený na úspore 1,1´ -karbonyldiimidazolu |
| US8859541B2 (en) | 2012-02-27 | 2014-10-14 | Boehringer Ingelheim International Gmbh | 6-alkynylpyridines |
| JP6197031B2 (ja) | 2012-05-24 | 2017-09-13 | セルゾーム リミティッド | Tyk2阻害剤としてのヘテロシクリルピリミジン類似体 |
| EP2669276A1 (en) | 2012-05-31 | 2013-12-04 | Université de Strasbourg | Ornithine- and lysine-derivatives for the treatment of pain |
| EP2864349A4 (en) | 2012-06-20 | 2016-02-24 | Univ California | DYNAMIC BIOMIMETIC SYNZYM CATALYST, CATALYSIS AND CATALYST SYSTEMS |
| FR2993564B1 (fr) | 2012-07-20 | 2014-08-22 | Metabrain Res | Derives d'imidazopyridine utiles dans le traitement du diabete |
| WO2014031872A2 (en) | 2012-08-23 | 2014-02-27 | The Broad Institute, Inc. | Small molecule inhibitors for treating parasitic infections |
| WO2014031986A1 (en) | 2012-08-24 | 2014-02-27 | Board Of Regents Of The University Of Texas System | Pro-neurogenic compounds |
| JP6196233B2 (ja) | 2012-11-15 | 2017-09-13 | 高砂香料工業株式会社 | アルミニウム触媒 |
| WO2014100764A2 (en) | 2012-12-21 | 2014-06-26 | Epizyme, Inc. | Methods of inhibiting prmt5 |
| KR102024417B1 (ko) | 2012-12-21 | 2019-11-07 | 에피자임, 인코포레이티드 | 테트라하이드로- 및 디하이드로-이소퀴놀린 prmt5 억제제 및 이의 용도 |
| US9637450B2 (en) | 2013-03-14 | 2017-05-02 | The Trustees Of Columbia University In The City Of New York | Octahydrocyclopentapyrroles, their preparation and use |
| FR3008976A1 (fr) | 2013-07-23 | 2015-01-30 | Servier Lab | "nouveaux derives d'indolizine, leur procede de preparation et les compositions pharmaceutiques qui les contiennent" |
| EA029981B1 (ru) | 2013-08-27 | 2018-06-29 | Бристол-Майерс Сквибб Компани | Ингибиторы ido |
| KR102276644B1 (ko) | 2013-09-04 | 2021-07-13 | 브리스톨-마이어스 스큅 컴퍼니 | 면역조절제로서 유용한 화합물 |
| GB201321730D0 (en) | 2013-12-09 | 2014-01-22 | Ucb Pharma Sa | Therapeutic agents |
| GB201321746D0 (en) | 2013-12-09 | 2014-01-22 | Ucb Pharma Sa | Therapeutic agents |
| WO2015108038A1 (ja) | 2014-01-17 | 2015-07-23 | 第一三共株式会社 | エチレングリコール化合物 |
| ES2693255T3 (es) | 2014-02-27 | 2018-12-10 | Ono Pharmaceutical Co., Ltd. | Compuesto que presenta actividad agonista de EP2 selectiva |
| US9067898B1 (en) | 2014-03-07 | 2015-06-30 | Janssen Pharmaceutica Nv | Isothiazole derivatives as GPR120 agonists for the treatment of type II diabetes |
| CN110713489B (zh) | 2014-03-19 | 2022-05-31 | 勃林格殷格翰国际有限公司 | 杂芳基syk抑制剂 |
| WO2015197028A1 (en) | 2014-06-28 | 2015-12-30 | Sunshine Lake Pharma Co., Ltd. | Compounds as hepatitis c virus (hcv) inhibitors and uses thereof in medicine |
| EP3169671B1 (en) | 2014-07-17 | 2019-08-21 | Sunshine Lake Pharma Co., Ltd. | 1-(5-(tert.-butyl)isoxazol-3-yl)-3-(4-((phenyl)ethynyl)phenyl)urea derivatives and related compounds as flt3 inhibitors for treating cancer |
| WO2016031815A1 (ja) | 2014-08-26 | 2016-03-03 | 武田薬品工業株式会社 | 複素環化合物 |
| GB201415573D0 (en) | 2014-09-03 | 2014-10-15 | Cancer Therapeutics Crc Pty Ltd | Compounds |
| WO2016036636A1 (en) | 2014-09-05 | 2016-03-10 | Merck Sharp & Dohme Corp. | Tetrahydroisoquinoline derivatives useful as inhibitors of diacylglyceride o-acyltransferase 2 |
| CN105461693B (zh) | 2014-09-26 | 2019-10-25 | 广东东阳光药业有限公司 | Crth2拮抗剂化合物及其用途 |
| AU2015326506B2 (en) | 2014-10-03 | 2021-02-25 | Divya MAHESHWARI | Novel anthranilic acid derivatives |
| ES2578377B1 (es) | 2014-12-22 | 2017-05-04 | Consejo Superior De Investigaciones Científicas (Csic) | Compuestos moduladores del sensor neuronal de calcio dream y sus usos terapéuticos. |
| CA2994798A1 (en) | 2015-07-03 | 2017-01-12 | Anca CATRINA | Methods and compounds for the alleviation and/or prevention of bone loss |
| WO2017024180A1 (en) | 2015-08-06 | 2017-02-09 | Amgen Inc. | Vinyl fluoride cyclopropyl fused thiazin-2-amine compounds as beta-secretase inhibitors and methods of use |
| WO2017025510A1 (en) | 2015-08-12 | 2017-02-16 | Syngenta Participations Ag | Microbiocidal heterobicyclic derivatives |
| WO2017042182A1 (en) | 2015-09-08 | 2017-03-16 | F. Hoffmann-La Roche Ag | Tricyclic pi3k inhibitor compounds and methods of use |
| MA47013A (fr) | 2015-10-21 | 2018-08-29 | Otsuka Pharma Co Ltd | Composés benzolactames utilisés en tant qu'inhibiteurs de protéine kinase |
| US20170174671A1 (en) | 2015-12-17 | 2017-06-22 | Incyte Corporation | Heterocyclic compounds as immunomodulators |
| WO2017109095A1 (en) | 2015-12-22 | 2017-06-29 | AbbVie Deutschland GmbH & Co. KG | Fused (hetero)cyclic compounds as s1p modulators |
| EP3190103A1 (en) | 2016-01-08 | 2017-07-12 | Rijksuniversiteit Groningen | Inhibitors of the pd-1/pd-l1 protein/protein interaction |
| AR107694A1 (es) | 2016-02-23 | 2018-05-23 | Padlock Therapeutics Inc | Heteroarilos inhibidores de pad4 |
| CN109476657A (zh) | 2016-06-16 | 2019-03-15 | 爱尔兰詹森科学公司 | 作为抗细菌剂的杂环化合物 |
| JP6936820B2 (ja) | 2016-06-30 | 2021-09-22 | ヴィーブ ヘルスケア ユーケー(ナンバー5)リミテッド | ヒト免疫不全ウイルス複製の阻害剤としてのアザデカリン誘導体 |
| CN110818690B (zh) | 2016-07-26 | 2021-08-10 | 深圳市塔吉瑞生物医药有限公司 | 用于抑制蛋白酪氨酸激酶活性的氨基嘧啶类化合物 |
| AU2017305399A1 (en) | 2016-08-03 | 2019-01-31 | Arising International, Inc. | Symmetric or semi-symmetric compounds useful as immunomodulators |
| TWI795381B (zh) | 2016-12-21 | 2023-03-11 | 比利時商健生藥品公司 | 作為malt1抑制劑之吡唑衍生物 |
| WO2018112843A1 (en) | 2016-12-22 | 2018-06-28 | Merck Sharp & Dohme Corp. | Heteroaryl piperidine ether allosteric modulators of the m4 muscarinic acetylcholine receptor |
| CN110099900B (zh) | 2016-12-27 | 2022-12-02 | 山东大学 | 针对Smoothened突变株的刺猬通路抑制剂 |
| CN107056630B (zh) | 2017-01-23 | 2020-01-17 | 合肥工业大学 | 一种茚满类衍生物及其合成方法和在医药上的用途 |
| US12012467B2 (en) | 2017-03-28 | 2024-06-18 | Regents Of The University Of Michigan | Small molecule DCN1 inhibitors and therapeutic methods using the same |
| US11021471B2 (en) | 2017-05-10 | 2021-06-01 | Forge Therapeutics, Inc. | Antibacterial compounds |
| CN107163044B (zh) | 2017-06-19 | 2021-04-23 | 广东药科大学 | 一类具有蛋白酶修饰活性的萘乙二酮化合物及其衍生物 |
| WO2018234342A1 (en) | 2017-06-21 | 2018-12-27 | F. Hoffmann-La Roche Ag | ISOINDOLINONE DERIVATIVES AS MODULATORS OF IRAK4 |
| GB201710851D0 (en) | 2017-07-06 | 2017-08-23 | Galápagos Nv | Novel compounds and pharmaceutical compositions thereof for the treatment of fibrosis |
| CA3073656C (en) | 2017-09-22 | 2024-03-05 | Jubilant Epipad LLC | Heterocyclic compounds as pad inhibitors |
| DK3697785T3 (da) | 2017-10-18 | 2023-04-03 | Jubilant Epipad LLC | Imidazo-pyridine forbindelser som pad-inhibitorer |
| CN111491920B (zh) | 2017-10-20 | 2024-01-30 | 范德比尔特大学 | 毒蕈碱性乙酰胆碱受体m4的拮抗剂 |
| WO2019087214A1 (en) | 2017-11-06 | 2019-05-09 | Jubilant Biosys Limited | Pyrimidine derivatives as inhibitors of pd1/pd-l1 activation |
| US11459338B2 (en) | 2017-11-24 | 2022-10-04 | Jubilant Episcribe Llc | Heterocyclic compounds as PRMT5 inhibitors |
| US11420973B2 (en) | 2017-12-19 | 2022-08-23 | Bristol-Myers Squibb Company | Amide substituted indole compounds useful as TLR inhibitors |
| CN110117278B (zh) | 2018-02-07 | 2022-07-19 | 石家庄以岭药业股份有限公司 | 烷氧基苯并五元(六元)杂环胺类化合物及其药物用途 |
| KR102351458B1 (ko) | 2018-02-14 | 2022-01-13 | 후지필름 가부시키가이샤 | 중합성 액정 조성물, 광학 이방성막, 광학 필름, 편광판 및 화상 표시 장치 |
| KR20200131845A (ko) | 2018-03-13 | 2020-11-24 | 주빌런트 프로델 엘엘씨 | Pd1/pd-l1 상호작용/활성화 억제제로서의 비사이클릭 화합물 |
| JP6956033B2 (ja) | 2018-03-14 | 2021-10-27 | 日本化薬株式会社 | ベンゾアゾール化合物、並びにこれを含んだ顔料組成物 |
| CN108358917B (zh) | 2018-04-24 | 2020-06-19 | 北京市结核病胸部肿瘤研究所 | 含有碱性稠环片段的咪唑并[1,2-a]吡啶-3-酰胺类化合物及其制备方法 |
| WO2019205147A1 (zh) | 2018-04-28 | 2019-10-31 | 上海璃道医药科技有限公司 | 包含苯并含氧脂肪环结构的氨基乙酰胺类化合物及其用途 |
| WO2019213234A1 (en) | 2018-05-01 | 2019-11-07 | The Trustees Of Columbia University In The City Of New York | Triazolopyrimidines, their preparation and use |
| EP3829575A4 (en) | 2018-08-01 | 2022-07-20 | The Trustees of Columbia University in the City of New York | RBP4 ANTAGONISTS FOR THE TREATMENT AND PREVENTION OF NON-ALCOHOLIC LIVER DISEASE AND GOUT |
| AU2019316858B2 (en) | 2018-08-06 | 2024-03-28 | Moexa Pharmaceuticals Limited | Smad3 inhibitors |
| CN112654903B (zh) | 2018-08-28 | 2022-09-27 | 富士胶片株式会社 | 层叠体及图像显示装置 |
| CN110963997A (zh) | 2018-09-28 | 2020-04-07 | 四川科伦博泰生物医药股份有限公司 | 杂环酰胺类化合物、包含其的药物组合物及其制备方法和用途 |
| EP3643711A1 (en) | 2018-10-24 | 2020-04-29 | Bayer Animal Health GmbH | New anthelmintic compounds |
| KR102641718B1 (ko) | 2018-10-30 | 2024-02-29 | 길리애드 사이언시즈, 인코포레이티드 | 알파4베타7 인테그린 억제제로서의 이미다조피리딘 유도체 |
| CN110105299B (zh) | 2019-01-23 | 2023-01-03 | 中山大学 | 一种含芳醚取代恶唑烷酮羧酸酯类衍生物及其制备方法和应用 |
| JP2022528562A (ja) | 2019-04-05 | 2022-06-14 | ストーム・セラピューティクス・リミテッド | Mettl3阻害化合物 |
| RU2717101C1 (ru) | 2019-06-03 | 2020-03-18 | Андрей Александрович Иващенко | Анелированные 9-гидрокси-1,8-диоксо-1,3,4,8-тетрагидро-2Н-пиридо[1,2-a]пиразин-7-карбоксамиды - ингибиторы интегразы ВИЧ, способы их получения и применения |
| JP7420502B2 (ja) | 2019-07-24 | 2024-01-23 | 住友化学株式会社 | 重合性液晶混合組成物、位相差板、楕円偏光板および有機el表示装置 |
| AR119494A1 (es) | 2019-07-29 | 2021-12-22 | Servier Lab | DERIVADOS DE 6,7-DIHIDRO-5H-PIRIDO[2,3-c]PIRIDAZIN-8-ILO, COMPOSICIONES FARMACÉUTICAS QUE LOS CONTIENEN Y SUS USOS COMO AGENTES PROAPOPTÓTICOS |
| WO2021028810A1 (en) | 2019-08-09 | 2021-02-18 | Inorbit Therapeutics Ab | Sulfinic acid compounds as free fatty acid receptor agonists |
| JP7182533B2 (ja) | 2019-09-27 | 2022-12-02 | 富士フイルム株式会社 | 液晶組成物、光学異方性層、光学フィルム、偏光板および画像表示装置 |
| CN114521212B (zh) | 2019-09-27 | 2024-06-21 | 富士胶片株式会社 | 液晶组合物、光学各向异性层、光学膜、偏振片及图像显示装置 |
| CN114829361B (zh) | 2019-11-15 | 2024-07-16 | 柳韩洋行 | 具有2,3-二氢-1h-茚或2,3-二氢苯并呋喃部分的衍生物或其药学上可接受盐及含其的药物组合物 |
| US11811624B2 (en) | 2019-11-15 | 2023-11-07 | Mitsubishi Electric Corporation | Edge device linking system, edge device linking method, and recording medium |
| CN111606904B (zh) | 2020-04-07 | 2021-10-15 | 广州医科大学 | 氮杂吲哚类化合物及其应用 |
-
2018
- 2018-10-16 DK DK18796135.4T patent/DK3697785T3/da active
- 2018-10-16 PT PT187961354T patent/PT3697785T/pt unknown
- 2018-10-16 AU AU2018352142A patent/AU2018352142B2/en active Active
- 2018-10-16 BR BR112020007607-4A patent/BR112020007607A2/pt unknown
- 2018-10-16 SG SG11202003463XA patent/SG11202003463XA/en unknown
- 2018-10-16 MX MX2020003341A patent/MX2020003341A/es unknown
- 2018-10-16 HU HUE18796135A patent/HUE061607T2/hu unknown
- 2018-10-16 JP JP2020521516A patent/JP7307723B2/ja active Active
- 2018-10-16 KR KR1020207013652A patent/KR20200071752A/ko not_active Application Discontinuation
- 2018-10-16 CN CN201880067592.5A patent/CN111225915B/zh active Active
- 2018-10-16 RS RS20230226A patent/RS64104B1/sr unknown
- 2018-10-16 IL IL272667A patent/IL272667B/en unknown
- 2018-10-16 EP EP18796135.4A patent/EP3697785B1/en active Active
- 2018-10-16 PL PL18796135.4T patent/PL3697785T3/pl unknown
- 2018-10-16 WO PCT/IN2018/050671 patent/WO2019077631A1/en unknown
- 2018-10-16 CA CA3076476A patent/CA3076476A1/en active Pending
- 2018-10-16 ES ES18796135T patent/ES2941512T3/es active Active
- 2018-10-16 US US16/757,120 patent/US11426412B2/en active Active
- 2018-10-16 FI FIEP18796135.4T patent/FI3697785T3/fi active
-
2020
- 2020-05-14 ZA ZA2020/02770A patent/ZA202002770B/en unknown
Patent Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2005523288A (ja) | 2002-02-19 | 2005-08-04 | ファルマシア・アンド・アップジョン・カンパニー・エルエルシー | 疾病治療用の縮合した二環式−n−架橋−複素環式芳香族カルボキサミド |
| JP2006502164A (ja) | 2002-09-06 | 2006-01-19 | バイオジェン・アイデック・エムエイ・インコーポレイテッド | イミダゾロピリジンならびにその生成および使用方法 |
| JP2009523752A (ja) | 2006-01-17 | 2009-06-25 | エフ.ホフマン−ラ ロシュ アーゲー | GABAレセプター経由でのアルツハイマー病の処置に有用なアリール−イソオキサゾール−4−イル−イミダゾ[1,2−a]ピリジン誘導体 |
| JP2011500544A (ja) | 2007-10-12 | 2011-01-06 | アステックス、セラピューティックス、リミテッド | タンパク質チロシンキナーゼインヒビターとしての二環式ヘテロ環式化合物 |
| JP2015522628A (ja) | 2012-07-26 | 2015-08-06 | グラクソ グループ リミテッドGlaxo Group L | Pad4阻害剤としての2−(アザインドール−2−イル)ベンズイミダゾール |
| WO2016185279A1 (en) | 2015-05-21 | 2016-11-24 | Glaxosmithkline Intellectual Property Development Limited | Benzoimidazole derivatives as pad4 inhibitors |
Non-Patent Citations (4)
| Title |
|---|
| REGISTRY(STN)[online],2013年10月29日,[検索日 2022.08.25],CAS Registry Number: 1465348-20-2 |
| REGISTRY(STN)[online],2014年02月06日,[検索日 2022.08.25],CAS Registry Number: 1538490-40-2 |
| REGISTRY(STN)[online],2015年02月08日,[検索日 2022.08.25],CAS Registry Number: 1645471-61-9 |
| REGISTRY(STN)[online],2017年05月03日,[検索日 2022.08.25],CAS Registry Number:2094867-86-2 |
Also Published As
| Publication number | Publication date |
|---|---|
| EP3697785A1 (en) | 2020-08-26 |
| PT3697785T (pt) | 2023-04-03 |
| DK3697785T3 (da) | 2023-04-03 |
| AU2018352142A1 (en) | 2020-03-05 |
| RU2020114991A (ru) | 2021-11-18 |
| IL272667A (en) | 2020-03-31 |
| AU2018352142B2 (en) | 2022-08-25 |
| BR112020007607A2 (pt) | 2020-09-29 |
| CA3076476A1 (en) | 2019-04-25 |
| US11426412B2 (en) | 2022-08-30 |
| EP3697785B1 (en) | 2022-12-28 |
| RS64104B1 (sr) | 2023-04-28 |
| US20200237771A1 (en) | 2020-07-30 |
| WO2019077631A1 (en) | 2019-04-25 |
| JP2021500330A (ja) | 2021-01-07 |
| ZA202002770B (en) | 2021-10-27 |
| IL272667B (en) | 2022-09-01 |
| HUE061607T2 (hu) | 2023-07-28 |
| ES2941512T3 (es) | 2023-05-23 |
| RU2020114991A3 (ja) | 2022-03-30 |
| FI3697785T3 (fi) | 2023-04-03 |
| PL3697785T3 (pl) | 2023-08-07 |
| CN111225915A (zh) | 2020-06-02 |
| CN111225915B (zh) | 2023-03-07 |
| SG11202003463XA (en) | 2020-05-28 |
| MX2020003341A (es) | 2020-09-17 |
| KR20200071752A (ko) | 2020-06-19 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7307723B2 (ja) | Pad阻害剤としてのイミダゾ-ピリジン化合物 | |
| RU2764243C2 (ru) | Гетероциклические соединения в качестве ингибиторов PAD | |
| JP5989805B2 (ja) | メチル基変更酵素の調節物質、組成物及びその使用 | |
| KR102359993B1 (ko) | 피리미도[5,4-b]인돌리진 또는 피리미도[5,4-b]피롤리진 화합물, 그의 제조방법 및 용도 | |
| TWI768156B (zh) | 新穎緩激肽b2受體拮抗劑及其用途 | |
| PT1765795E (pt) | Derivados alcinilo como moduladores de receptores metabotrópicos de glutamato | |
| EP2331541B1 (en) | Indolizine inhibitors of leukotriene production | |
| JP6837072B2 (ja) | 6,7−ジヒドロ−5H−ピラゾロ[5,1−b][1,3]オキサジン−2−カルボキサミド化合物 | |
| RU2782743C2 (ru) | Имидазопиридиновые соединения в качестве ингибиторов PAD | |
| RU2782743C9 (ru) | Имидазопиридиновые соединения в качестве ингибиторов PAD | |
| JP2006169138A (ja) | ピラゾロピリジンピラゾロン誘導体とその付加塩及びpde阻害剤 | |
| WO2021121420A1 (zh) | 苯并吡唑类化合物及其中间体、制备方法和应用 | |
| CN116217543A (zh) | 一种新的ccr3抑制剂化合物及其用途 | |
| CA3202328A1 (en) | Chemical compounds useful for inhibiting nav1.8 voltage-gated sodium channels and treating nav1.8 mediated diseases | |
| WO2022155111A1 (en) | Indole derivatives as kinase inhibitors | |
| WO2007067904A2 (en) | Peptide deformylase inhibitors |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20211012 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20220915 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20220920 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20221220 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20230307 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20230529 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20230613 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20230630 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7307723 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |