JP4153303B2 - 走査型電子顕微鏡を用いた非真空環境内のサンプルの検査のための装置および方法 - Google Patents
走査型電子顕微鏡を用いた非真空環境内のサンプルの検査のための装置および方法 Download PDFInfo
- Publication number
- JP4153303B2 JP4153303B2 JP2002547196A JP2002547196A JP4153303B2 JP 4153303 B2 JP4153303 B2 JP 4153303B2 JP 2002547196 A JP2002547196 A JP 2002547196A JP 2002547196 A JP2002547196 A JP 2002547196A JP 4153303 B2 JP4153303 B2 JP 4153303B2
- Authority
- JP
- Japan
- Prior art keywords
- sample
- membrane
- cells
- chamber
- electrons
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 238000000034 method Methods 0.000 title description 49
- 238000007689 inspection Methods 0.000 title description 13
- 239000000463 material Substances 0.000 claims description 67
- 238000010894 electron beam technology Methods 0.000 claims description 29
- 229920001721 polyimide Polymers 0.000 claims description 15
- 239000012530 fluid Substances 0.000 claims description 14
- 239000004642 Polyimide Substances 0.000 claims description 13
- 230000003993 interaction Effects 0.000 claims description 12
- 239000012298 atmosphere Substances 0.000 claims description 7
- 239000010410 layer Substances 0.000 claims description 7
- -1 polyethylene Polymers 0.000 claims description 5
- 239000004952 Polyamide Substances 0.000 claims description 4
- 239000004962 Polyamide-imide Substances 0.000 claims description 4
- 229920002647 polyamide Polymers 0.000 claims description 4
- 229920002312 polyamide-imide Polymers 0.000 claims description 4
- 239000004698 Polyethylene Substances 0.000 claims description 3
- 238000009434 installation Methods 0.000 claims description 3
- 229920003223 poly(pyromellitimide-1,4-diphenyl ether) Polymers 0.000 claims description 3
- 229920000573 polyethylene Polymers 0.000 claims description 3
- 229920000128 polypyrrole Polymers 0.000 claims description 3
- 229920002037 poly(vinyl butyral) polymer Polymers 0.000 claims 1
- WQGWDDDVZFFDIG-UHFFFAOYSA-N pyrogallol Chemical group OC1=CC=CC(O)=C1O WQGWDDDVZFFDIG-UHFFFAOYSA-N 0.000 claims 1
- 239000012528 membrane Substances 0.000 abstract description 149
- 239000000523 sample Substances 0.000 description 147
- 210000004027 cell Anatomy 0.000 description 132
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Chemical compound O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 51
- 229910001868 water Inorganic materials 0.000 description 43
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 38
- 229910052737 gold Inorganic materials 0.000 description 32
- 239000010931 gold Substances 0.000 description 32
- 238000002372 labelling Methods 0.000 description 27
- 239000002245 particle Substances 0.000 description 21
- 238000005192 partition Methods 0.000 description 20
- 229910052799 carbon Inorganic materials 0.000 description 19
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 17
- 238000003384 imaging method Methods 0.000 description 15
- 238000010586 diagram Methods 0.000 description 13
- 239000000243 solution Substances 0.000 description 13
- 230000004888 barrier function Effects 0.000 description 12
- 239000011324 bead Substances 0.000 description 12
- 230000001464 adherent effect Effects 0.000 description 11
- 239000002609 medium Substances 0.000 description 11
- 238000002360 preparation method Methods 0.000 description 11
- 239000008055 phosphate buffer solution Substances 0.000 description 10
- 239000011248 coating agent Substances 0.000 description 9
- 238000000576 coating method Methods 0.000 description 9
- 230000000694 effects Effects 0.000 description 9
- 238000001514 detection method Methods 0.000 description 8
- 238000001493 electron microscopy Methods 0.000 description 8
- 238000005259 measurement Methods 0.000 description 8
- 239000012472 biological sample Substances 0.000 description 7
- 238000004364 calculation method Methods 0.000 description 7
- 238000002474 experimental method Methods 0.000 description 7
- 230000003287 optical effect Effects 0.000 description 7
- 230000005855 radiation Effects 0.000 description 7
- YBJHBAHKTGYVGT-ZKWXMUAHSA-N (+)-Biotin Chemical compound N1C(=O)N[C@@H]2[C@H](CCCCC(=O)O)SC[C@@H]21 YBJHBAHKTGYVGT-ZKWXMUAHSA-N 0.000 description 6
- 239000000839 emulsion Substances 0.000 description 6
- 238000005516 engineering process Methods 0.000 description 6
- 229940079593 drug Drugs 0.000 description 5
- 239000003814 drug Substances 0.000 description 5
- 239000003921 oil Substances 0.000 description 5
- 230000008569 process Effects 0.000 description 5
- 108010090804 Streptavidin Proteins 0.000 description 4
- 238000009825 accumulation Methods 0.000 description 4
- 239000012736 aqueous medium Substances 0.000 description 4
- 125000004429 atom Chemical group 0.000 description 4
- 230000008901 benefit Effects 0.000 description 4
- 238000004422 calculation algorithm Methods 0.000 description 4
- 150000001875 compounds Chemical class 0.000 description 4
- 238000001727 in vivo Methods 0.000 description 4
- 239000003562 lightweight material Substances 0.000 description 4
- 239000007788 liquid Substances 0.000 description 4
- PQXKHYXIUOZZFA-UHFFFAOYSA-M lithium fluoride Chemical compound [Li+].[F-] PQXKHYXIUOZZFA-UHFFFAOYSA-M 0.000 description 4
- 239000003550 marker Substances 0.000 description 4
- 239000000203 mixture Substances 0.000 description 4
- 239000013307 optical fiber Substances 0.000 description 4
- 229920000642 polymer Polymers 0.000 description 4
- 238000005070 sampling Methods 0.000 description 4
- LIVNPJMFVYWSIS-UHFFFAOYSA-N silicon monoxide Chemical compound [Si-]#[O+] LIVNPJMFVYWSIS-UHFFFAOYSA-N 0.000 description 4
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 3
- 102000016359 Fibronectins Human genes 0.000 description 3
- 108010067306 Fibronectins Proteins 0.000 description 3
- 108010052285 Membrane Proteins Proteins 0.000 description 3
- BQCADISMDOOEFD-UHFFFAOYSA-N Silver Chemical compound [Ag] BQCADISMDOOEFD-UHFFFAOYSA-N 0.000 description 3
- 238000004458 analytical method Methods 0.000 description 3
- 230000015572 biosynthetic process Effects 0.000 description 3
- 229960002685 biotin Drugs 0.000 description 3
- 235000020958 biotin Nutrition 0.000 description 3
- 239000011616 biotin Substances 0.000 description 3
- 210000000170 cell membrane Anatomy 0.000 description 3
- 230000001413 cellular effect Effects 0.000 description 3
- 239000000084 colloidal system Substances 0.000 description 3
- 238000013461 design Methods 0.000 description 3
- 238000011161 development Methods 0.000 description 3
- 230000018109 developmental process Effects 0.000 description 3
- 238000000635 electron micrograph Methods 0.000 description 3
- 238000000605 extraction Methods 0.000 description 3
- 239000006260 foam Substances 0.000 description 3
- 239000007789 gas Substances 0.000 description 3
- 235000003642 hunger Nutrition 0.000 description 3
- 230000001965 increasing effect Effects 0.000 description 3
- 238000003780 insertion Methods 0.000 description 3
- 230000037431 insertion Effects 0.000 description 3
- 230000003834 intracellular effect Effects 0.000 description 3
- 210000003098 myoblast Anatomy 0.000 description 3
- 230000008823 permeabilization Effects 0.000 description 3
- 239000008194 pharmaceutical composition Substances 0.000 description 3
- 239000004033 plastic Substances 0.000 description 3
- 229920003023 plastic Polymers 0.000 description 3
- 150000003254 radicals Chemical class 0.000 description 3
- 230000004044 response Effects 0.000 description 3
- 238000004626 scanning electron microscopy Methods 0.000 description 3
- 238000007789 sealing Methods 0.000 description 3
- 229910052709 silver Inorganic materials 0.000 description 3
- 239000004332 silver Substances 0.000 description 3
- 238000001228 spectrum Methods 0.000 description 3
- 239000006228 supernatant Substances 0.000 description 3
- WWJZWCUNLNYYAU-UHFFFAOYSA-N temephos Chemical compound C1=CC(OP(=S)(OC)OC)=CC=C1SC1=CC=C(OP(=S)(OC)OC)C=C1 WWJZWCUNLNYYAU-UHFFFAOYSA-N 0.000 description 3
- 238000005406 washing Methods 0.000 description 3
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 2
- 108091008794 FGF receptors Proteins 0.000 description 2
- 102000044168 Fibroblast Growth Factor Receptor Human genes 0.000 description 2
- 102000010789 Interleukin-2 Receptors Human genes 0.000 description 2
- 108010038453 Interleukin-2 Receptors Proteins 0.000 description 2
- 102000018697 Membrane Proteins Human genes 0.000 description 2
- 238000000342 Monte Carlo simulation Methods 0.000 description 2
- 229930040373 Paraformaldehyde Natural products 0.000 description 2
- 206010057249 Phagocytosis Diseases 0.000 description 2
- 108010039918 Polylysine Proteins 0.000 description 2
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 2
- 238000004125 X-ray microanalysis Methods 0.000 description 2
- 239000000654 additive Substances 0.000 description 2
- 238000013459 approach Methods 0.000 description 2
- 230000005540 biological transmission Effects 0.000 description 2
- 230000003833 cell viability Effects 0.000 description 2
- 230000008859 change Effects 0.000 description 2
- 210000004978 chinese hamster ovary cell Anatomy 0.000 description 2
- 229920001940 conductive polymer Polymers 0.000 description 2
- 239000004020 conductor Substances 0.000 description 2
- 230000007423 decrease Effects 0.000 description 2
- 238000009826 distribution Methods 0.000 description 2
- 238000011156 evaluation Methods 0.000 description 2
- 238000001506 fluorescence spectroscopy Methods 0.000 description 2
- 239000012737 fresh medium Substances 0.000 description 2
- 238000010191 image analysis Methods 0.000 description 2
- 230000004941 influx Effects 0.000 description 2
- 239000012212 insulator Substances 0.000 description 2
- 210000004698 lymphocyte Anatomy 0.000 description 2
- 238000004519 manufacturing process Methods 0.000 description 2
- 230000007246 mechanism Effects 0.000 description 2
- 238000005374 membrane filtration Methods 0.000 description 2
- 238000004377 microelectronic Methods 0.000 description 2
- 239000003068 molecular probe Substances 0.000 description 2
- 229910052757 nitrogen Inorganic materials 0.000 description 2
- 238000012634 optical imaging Methods 0.000 description 2
- 238000000399 optical microscopy Methods 0.000 description 2
- 210000003463 organelle Anatomy 0.000 description 2
- 239000011368 organic material Substances 0.000 description 2
- 229920002866 paraformaldehyde Polymers 0.000 description 2
- 239000003208 petroleum Substances 0.000 description 2
- 230000008782 phagocytosis Effects 0.000 description 2
- 229920000656 polylysine Polymers 0.000 description 2
- 102000004169 proteins and genes Human genes 0.000 description 2
- 108090000623 proteins and genes Proteins 0.000 description 2
- 238000011002 quantification Methods 0.000 description 2
- 239000002096 quantum dot Substances 0.000 description 2
- 102000005962 receptors Human genes 0.000 description 2
- 108020003175 receptors Proteins 0.000 description 2
- 239000004065 semiconductor Substances 0.000 description 2
- 210000002966 serum Anatomy 0.000 description 2
- JJGWLCLUQNFDIS-GTSONSFRSA-M sodium;1-[6-[5-[(3as,4s,6ar)-2-oxo-1,3,3a,4,6,6a-hexahydrothieno[3,4-d]imidazol-4-yl]pentanoylamino]hexanoyloxy]-2,5-dioxopyrrolidine-3-sulfonate Chemical compound [Na+].O=C1C(S(=O)(=O)[O-])CC(=O)N1OC(=O)CCCCCNC(=O)CCCC[C@H]1[C@H]2NC(=O)N[C@H]2CS1 JJGWLCLUQNFDIS-GTSONSFRSA-M 0.000 description 2
- 239000000758 substrate Substances 0.000 description 2
- 210000001519 tissue Anatomy 0.000 description 2
- WFKWXMTUELFFGS-UHFFFAOYSA-N tungsten Chemical compound [W] WFKWXMTUELFFGS-UHFFFAOYSA-N 0.000 description 2
- 229910052721 tungsten Inorganic materials 0.000 description 2
- 239000010937 tungsten Substances 0.000 description 2
- 238000009736 wetting Methods 0.000 description 2
- 241000212384 Bifora Species 0.000 description 1
- 229920000742 Cotton Polymers 0.000 description 1
- 108060006698 EGF receptor Proteins 0.000 description 1
- 102000001301 EGF receptor Human genes 0.000 description 1
- 102000009465 Growth Factor Receptors Human genes 0.000 description 1
- 108010009202 Growth Factor Receptors Proteins 0.000 description 1
- 239000004677 Nylon Substances 0.000 description 1
- 230000002292 Radical scavenging effect Effects 0.000 description 1
- 241000220317 Rosa Species 0.000 description 1
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical compound [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 description 1
- 229930006000 Sucrose Natural products 0.000 description 1
- 239000006096 absorbing agent Substances 0.000 description 1
- 230000000996 additive effect Effects 0.000 description 1
- 230000003321 amplification Effects 0.000 description 1
- 201000009310 astigmatism Diseases 0.000 description 1
- 239000000227 bioadhesive Substances 0.000 description 1
- 230000004071 biological effect Effects 0.000 description 1
- 230000031018 biological processes and functions Effects 0.000 description 1
- 230000000903 blocking effect Effects 0.000 description 1
- 150000001722 carbon compounds Chemical class 0.000 description 1
- 238000005136 cathodoluminescence Methods 0.000 description 1
- 239000006143 cell culture medium Substances 0.000 description 1
- 230000030833 cell death Effects 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- 238000012512 characterization method Methods 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 239000013065 commercial product Substances 0.000 description 1
- 230000006835 compression Effects 0.000 description 1
- 238000007906 compression Methods 0.000 description 1
- 238000011109 contamination Methods 0.000 description 1
- 239000002872 contrast media Substances 0.000 description 1
- 238000001816 cooling Methods 0.000 description 1
- 238000012937 correction Methods 0.000 description 1
- 230000008878 coupling Effects 0.000 description 1
- 238000010168 coupling process Methods 0.000 description 1
- 238000005859 coupling reaction Methods 0.000 description 1
- 230000009089 cytolysis Effects 0.000 description 1
- 210000000805 cytoplasm Anatomy 0.000 description 1
- 210000004292 cytoskeleton Anatomy 0.000 description 1
- 210000000172 cytosol Anatomy 0.000 description 1
- 238000000354 decomposition reaction Methods 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 230000018044 dehydration Effects 0.000 description 1
- 238000006297 dehydration reaction Methods 0.000 description 1
- 230000008021 deposition Effects 0.000 description 1
- 230000023077 detection of light stimulus Effects 0.000 description 1
- 238000006073 displacement reaction Methods 0.000 description 1
- 238000004090 dissolution Methods 0.000 description 1
- 238000007876 drug discovery Methods 0.000 description 1
- 238000001035 drying Methods 0.000 description 1
- 239000008151 electrolyte solution Substances 0.000 description 1
- 238000001803 electron scattering Methods 0.000 description 1
- 230000002708 enhancing effect Effects 0.000 description 1
- 230000007613 environmental effect Effects 0.000 description 1
- 210000003743 erythrocyte Anatomy 0.000 description 1
- 238000001704 evaporation Methods 0.000 description 1
- 230000005284 excitation Effects 0.000 description 1
- 238000011049 filling Methods 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 239000007850 fluorescent dye Substances 0.000 description 1
- 238000001215 fluorescent labelling Methods 0.000 description 1
- 102000034287 fluorescent proteins Human genes 0.000 description 1
- 108091006047 fluorescent proteins Proteins 0.000 description 1
- 230000004907 flux Effects 0.000 description 1
- 239000011888 foil Substances 0.000 description 1
- 230000007274 generation of a signal involved in cell-cell signaling Effects 0.000 description 1
- 229910052739 hydrogen Inorganic materials 0.000 description 1
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 238000011534 incubation Methods 0.000 description 1
- 230000002452 interceptive effect Effects 0.000 description 1
- 238000011068 loading method Methods 0.000 description 1
- 238000004020 luminiscence type Methods 0.000 description 1
- 238000012423 maintenance Methods 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- 238000004452 microanalysis Methods 0.000 description 1
- 238000000386 microscopy Methods 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 239000002105 nanoparticle Substances 0.000 description 1
- 125000004433 nitrogen atom Chemical group N* 0.000 description 1
- 231100000252 nontoxic Toxicity 0.000 description 1
- 230000003000 nontoxic effect Effects 0.000 description 1
- 238000003199 nucleic acid amplification method Methods 0.000 description 1
- 210000004940 nucleus Anatomy 0.000 description 1
- 229920001778 nylon Polymers 0.000 description 1
- 239000007764 o/w emulsion Substances 0.000 description 1
- 150000002894 organic compounds Chemical class 0.000 description 1
- 230000000242 pagocytic effect Effects 0.000 description 1
- 229920006254 polymer film Polymers 0.000 description 1
- 239000001194 polyoxyethylene (40) stearate Substances 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 239000000047 product Substances 0.000 description 1
- 239000002516 radical scavenger Substances 0.000 description 1
- 238000011084 recovery Methods 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 230000003014 reinforcing effect Effects 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 238000001878 scanning electron micrograph Methods 0.000 description 1
- 239000012679 serum free medium Substances 0.000 description 1
- 229910052710 silicon Inorganic materials 0.000 description 1
- 239000010703 silicon Substances 0.000 description 1
- 235000012239 silicon dioxide Nutrition 0.000 description 1
- 239000000377 silicon dioxide Substances 0.000 description 1
- 238000004088 simulation Methods 0.000 description 1
- 238000004557 single molecule detection Methods 0.000 description 1
- 125000006850 spacer group Chemical group 0.000 description 1
- 229910001220 stainless steel Inorganic materials 0.000 description 1
- 239000010935 stainless steel Substances 0.000 description 1
- 239000010421 standard material Substances 0.000 description 1
- 230000000638 stimulation Effects 0.000 description 1
- 238000003756 stirring Methods 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 239000005720 sucrose Substances 0.000 description 1
- 125000000185 sucrose group Chemical group 0.000 description 1
- 238000004381 surface treatment Methods 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 230000009747 swallowing Effects 0.000 description 1
- 230000008961 swelling Effects 0.000 description 1
- 229920002994 synthetic fiber Polymers 0.000 description 1
- 239000012209 synthetic fiber Substances 0.000 description 1
- 238000012360 testing method Methods 0.000 description 1
- 239000004753 textile Substances 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- 210000002268 wool Anatomy 0.000 description 1
- 238000004846 x-ray emission Methods 0.000 description 1
Images
Classifications
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01J—ELECTRIC DISCHARGE TUBES OR DISCHARGE LAMPS
- H01J37/00—Discharge tubes with provision for introducing objects or material to be exposed to the discharge, e.g. for the purpose of examination or processing thereof
- H01J37/26—Electron or ion microscopes; Electron or ion diffraction tubes
- H01J37/28—Electron or ion microscopes; Electron or ion diffraction tubes with scanning beams
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01J—ELECTRIC DISCHARGE TUBES OR DISCHARGE LAMPS
- H01J37/00—Discharge tubes with provision for introducing objects or material to be exposed to the discharge, e.g. for the purpose of examination or processing thereof
- H01J37/02—Details
- H01J37/20—Means for supporting or positioning the object or the material; Means for adjusting diaphragms or lenses associated with the support
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01J—ELECTRIC DISCHARGE TUBES OR DISCHARGE LAMPS
- H01J2237/00—Discharge tubes exposing object to beam, e.g. for analysis treatment, etching, imaging
- H01J2237/006—Details of gas supplies, e.g. in an ion source, to a beam line, to a specimen or to a workpiece
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01J—ELECTRIC DISCHARGE TUBES OR DISCHARGE LAMPS
- H01J2237/00—Discharge tubes exposing object to beam, e.g. for analysis treatment, etching, imaging
- H01J2237/20—Positioning, supporting, modifying or maintaining the physical state of objects being observed or treated
- H01J2237/2002—Controlling environment of sample
- H01J2237/2003—Environmental cells
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01J—ELECTRIC DISCHARGE TUBES OR DISCHARGE LAMPS
- H01J2237/00—Discharge tubes exposing object to beam, e.g. for analysis treatment, etching, imaging
- H01J2237/26—Electron or ion microscopes
- H01J2237/28—Scanning microscopes
- H01J2237/2803—Scanning microscopes characterised by the imaging method
- H01J2237/2807—X-rays
Landscapes
- Chemical & Material Sciences (AREA)
- Analytical Chemistry (AREA)
- Analysing Materials By The Use Of Radiation (AREA)
- Sampling And Sample Adjustment (AREA)
- Investigating Or Analysing Biological Materials (AREA)
Description
発明の分野
本発明は、走査型電子顕微鏡を用いた非真空環境内のサンプルの検査のための装置および方法、そして更に特定的には(ただし限定的ではなく)、湿潤環境内での物体の検査のためのこのような器具および方法の使用に関する。
発明の背景
光学顕微鏡は、光の波長のために百、通常は数百ナノメートルの範囲内の解像度に制限されている。走査型電子顕微鏡はこの制限をもたず、数ナノメートルの範囲内の著しく高い解像度に到達することができる。
【0002】
SEMの欠点の1つは、サンプルを真空下に維持しなければならず、このため、in vivoプロセスの研究又は湿潤材料の研究が不可能である、という点にある。その上、有機材料から成る電気絶縁性サンプルには、電荷の蓄積を回避するためのコーティングが必要となる。
【0003】
1960年という早い時期に、Thornleyの論文(ケンブリッジ大学、1960年)が、水蒸気雰囲気内に電子顕微鏡検査用に意図されたサンプルを維持する試みの失敗を開示した。電子ビームの真空からチャンバを密封するためには、膜が用いられ、チャンバ自体は、水蒸気供給源からの入口を有している。
【0004】
生きた試料用に電子顕微鏡を使用する試みは、1970年代にまでさかのぼる。SwiftおよびBrownの論文(J. Phys. E:Sci. Instrum. 3,914,1970)が、例えば水中で大気圧での試料を検査するための透過型電子顕微鏡(TEM)の使用について開示した。サンプルを取付けるためには、コロジオン−炭素フィルムで密封されたアパーチャをもつセルが用いられる。電子ビームがアパーチャを通過してサンプルを打撃し、サンプルにより停止させられなかった電子はシンチレータまで進行を続け、そこで光子が生成される。大気圧で、0.1μmの解像度が要求されていたにも関わらず、結果は「かなりノイズが多い」ことがわかった。
【0005】
米国特許第4,071,766号は、非真空環境内の材料を見るために電子顕微鏡を用いる試みについて記述しており、「永久にくり返し発生する問題」として生きた物体の検査に言及している。米国特許第4,720,633号は、非真空環境内の材料を見るために電子顕微鏡検査法を用いるさらなる試みについて記述している。これらの特許の両方において、電子ビームは器具を通って湿潤な試料まで走行する。しかしながら、これらの試みはいずれも、湿潤物体をうまく検分することに成功していない。これらの文書の両方の内容が本書に参考として内含されている。
【0006】
上述の問題を解決しようとしている市販製品が、電子ビームの経路に沿って真空勾配を維持するPhilips Electron Optics社(オランダ、Eindhoven)から市販されている環境走査型電子顕微鏡(ESEM)である。しかしながら、ESEMは、水蒸気平衡の臨界点でサンプルについて作業を行なうことを必要とし、又、4℃前後までサンプルを冷却することをも必要としている。5トールまでの圧力での試料の検査が可能であると言われている。しかしながら、これまでのところ、湿潤でかつ/又は生きた物体を10nm以下の解像度で検分できるという証拠は全く無い。この製品およびその作動方法についてのさらなる情報は、本書にその内容が参考として内含されている米国特許第5,250,808号、5,362,964号および5,412,211号の中に見い出すことができる。
【0007】
有機物質の高解像度検査を達成する一般的方法は、透過型電子顕微鏡(TEM)である。TEMは、50nmの範囲内の標準的厚みをもつ特別に調製された試料を必要とする。サンプル中を通過する平行ビームを作り出すために、非常に高い電圧が印加される。本書にその内容が参考として内含されている米国特許第5,406,087号は、TEMで使用するための試料保持装置を開示している。電子ビームを透過させることのできる2枚のフィルムの間に試料が密封される。装置の内部は、水分が満たされ、TEMの真空環境内に設置され得る。非常に高いエネルギーのビームが、試料および周囲流体を通って走行し、低い信号雑音比と同時にサンプルに対する著しい損傷も導く。
【0008】
EMにより利用可能となった情報は通常、その他の技術によっては利用できない(Griffiths(2001)細胞生物学における傾向、11;4;153−154で再考されている)。EMが一般に充分活用されていない理由は、労働集約的で時間がかかるのみならず結果の生物学的妥当性に関する懸念も発生させるサンプル調製の複雑さにある。水性環境内でEMを実施することができれば、これらの問題の多いサンプル調製段階は不要となるだろう。
【0009】
従って、現在のところ、長い間感じられてきたニーズにも関わらず、高分子および分子レベルの細部を示す解像度での湿潤サンプルの研究を可能にする顕微鏡は全く存在しない。かかる能力は、細胞生物学および重合体科学ならびに石油、食品およびマイクロエレクトロニクスなどの産業といった多様な分野で必要とされている。特に、細胞生物学の分野においては、かかる顕微鏡は、分子レベルのプロセスの測定を導くと同時に医薬品の発見および診断用測定における新しい分野全体を開く細胞の分析を可能にすることだろう。例えば、かかる顕微鏡は、薬物と生きた細胞の間の相互作用の詳細な研究および直接的観察を可能にすることだろう。
発明の概要
本発明の目的は、湿潤サンプルの電子顕微鏡検査を可能にすることになる、走査型電子顕微鏡と共に使用するように適合されたチャンバを提供する。
【0010】
本発明の第1の態様に従うと、走査型電子顕微鏡と共に使用するのに適したチャンバにおいて、膜で密封された少なくとも1つのアパーチャを含み、前記膜が真空に耐えるように適合されており、かつ電子に対する透過性を有し、内部が前記真空から隔離されているチャンバが提供されている。
【0011】
好ましくはチャンバは、水又は制限的な意味なく細胞培地を含めたあらゆる水性媒質を実質的に大気圧に保つように適合されている。
【0012】
好ましくは、膜で密封されたアパーチャは、0.1〜4mmの範囲内の直径を有している。
【0013】
好ましくは、膜は、実質的に200〜5000Åの範囲内、より好ましくは500〜2000Åの、そして最も好ましくは、500〜1500Åの厚みを有している。
【0014】
本発明の主要な要素を構成する膜に必要とされる特性としては、エネルギー電子がそれを貫通してチャンバ内に備えられたサンプルと相互作用するのに充分なほど薄い一方で、EMの真空と前記膜により密封されたチャンバ内に収納された環境の間のおよそ1気圧の圧力差に耐えるという能力が含まれる。これらの属性をもつあらゆる材料が、本発明の原理に従った使用に適したものでありうる。現在好まれている態様に従うと、膜材料は、ポリイミド、ポリアミド、ポリアミド−イミド、ポリエチレン、ポリピロールおよび付加的な導電性重合体、パルロジオン、コロジオン、カプトン、フォームバー、ビニレック、ブトバー、ピロフォーム、二酸化ケイ素、一酸化ケイ素および炭素から成るグループの中から選択される。
【0015】
好ましくは、サンプルは膜の近くに置かれる。代替的には、サンプルは前記膜と接触した状態で取付けられ、こうして、電子ビームがサンプルに到達するのに(真空ではなく)物質の中を最小距離だけ通過する必要しかなくなるという利点が得られる。膜は、好ましくは、膜と真空の間に設置された支持用格子によって支持されている。
【0016】
一般に、チャンバは、サンプルを流体内か又は実質的に大気圧に、又はその両方の条件に封じ込めながら、真空内に位置づけされる。前記チャンバの壁の少なくとも一部分は、1気圧力の圧力勾配に対する耐性をもち、2keVを超えるエネルギーをもつ電子に対する透過性を有している。
【0017】
本発明の第2の態様に従うと、電子ビーム用の真空通路および物体と結びつけて設置された真空耐性バリヤを含んで成り、前記真空耐性バリヤが、真空から物体を隔離するように設置されている、走査型電子ビームを用いたチャンバ内の物体の高解像度検査のための器具が提供されている。物体の上には、螢光および電子発光マーカーが備わっていてよく、かくして電子ビームは光電子放射を励起することができる。マーカーは、問題の特定の分子と会合させられていてよく、この方法は、個々の分子についての情報を含む光ベースの画像を可能にする。かかる態様は好ましくは又、光検知ユニットを含み、チャンバは、光導体の一部分として構築されていてよい。光検知ユニットは、光電子増倍管を含んでいてよい。
【0018】
光検知ユニットは、個々の光子を検知するように適合されていてよく、かくして前記器具は、単一の分子の刺激の結果として得られる光放出を検知するように適合されている。
【0019】
バリヤ又は膜は、より好ましい態様においては、ポリイミド、ポリアミド、ポリアミド−イミド、カプトン、フォームバーおよびブトバーのうちのいずれかであってよい。
【0020】
バリヤ又は膜は、前記膜と前記真空の間に設置された補強用格子で補強されていてよく、又、実質的に200〜5000Åの範囲内、より好ましくは500〜2000Åの範囲内、最も好ましくは500〜1500Åの範囲内にある厚みを有する。
【0021】
好ましくは、バリヤ又は膜は、実質的に0.1〜4mmの範囲内の直径をもつアパーチャを横断して設置されている。特に好ましい態様においては、この直径は実質的に1mmである。
【0022】
バリヤ又は膜は好ましくは、エネルギー電子すなわち、2keVを超えるエネルギーをもつ電子に対する透過性を有する。
【0023】
1つの態様に従うと、バリヤは、高い2次電子収量、標準的にはフッ化リチウムをもつ材料の層でコーティングされている。
【0024】
1つの態様においては、ラジカルスカベンジャ分子が前記物体と結びつけて位置設定されている。
【0025】
1つの態様においては、該物体又はサンプルは、前記真空耐性バリヤに隣接して又はそれと接触した状態で設置されている。
【0026】
本発明の第3の態様に従うと、1気圧の圧力勾配に対する耐性をもつ直径1mmの露呈部域を有しかつ高エネルギー電子に対する透過性をもつ膜の、実質的に100nmより優れた解像度で走査型電子ビームの下で湿潤サンプルを検分できるようにするためのチャンバを構築することを目的とした使用、が提供されている。
【0027】
本発明の第4の態様に従うと、バリヤを用いて真空チャンバからそのチャンバを分離することにより1つのチャンバ内の湿潤物体を隔離する段階、前記真空チャンバから前記バリヤを通して前記サンプルを打撃するべく電子ビームを提供する段階および、前記チャンバから出現する2次電子および後方散乱電子のうちの少なくとも1つを観察する段階を含む、ナノメートル範囲の解像度で湿潤物体を観察する方法が提供されている。
【0028】
好ましくは、バリヤは、実質的に1気圧の圧力に耐え、2keVを超えるエネルギーをもつ電子に対する透過性をもつように選択されている膜を含む。
【0029】
好ましくは、湿潤物体は、医薬組成物を含む。
【0030】
好ましくは、湿潤物体は更に、医薬組成物と相互作用する生きた細胞を含む。
【0031】
好ましくは、チャンバは、流体入口を含み、医薬組成物は、観察中動的に入口を通して、濃度およびタイプを含むグループのうちの1つに関して変更される。
【0032】
本発明をより良く理解し、本発明をいかに有効に実施できるかを示すために、ここで純粋に一例として、添付図面を参照する。
発明の詳細な説明
本発明は、湿潤なサンプルの研究に適合されている走査型電子顕微鏡の新技術を提供する。湿潤な環境は、エネルギー電子が研究対象のサンプルの中を通過しこれと相互作用するのに充分薄い膜によって封じ込められた小型チャンバの中に提供される。
【0033】
ここでは、膜を通した走査型電子顕微鏡内のサンプルの画像形成における信号形成の技術および機構の両方を開示する。更に我々は、この方法における主要な要素である膜の機械的および空間的セットアップおよびその必要とされる特性をも開示する。
【0034】
我々は、材料および厚みの選択に対する指針を与える膜の特徴づけのため単純な測定について開示している。更に、さまざまな異なるサンプルの画像を形成する上での該技術の能力についても開示している。アクセス可能なコントラストおよび解像度、これらを得るのに必要な電流も評価されている。我々は、10nm前後の解像度で水中の全粒子を観察することが可能であるが、一方それより低いコントラストの材料は、100nm前後という著しく低い解像度を提供しうるということを示している。この新しい技術は、材料調査および細胞生物学といったようなさまざまな分野において数多くの応用に適合させることが可能である。
【0035】
本発明は、膜様仕切りの導入により真空から流体サンプルを隔離することに基づいている。重合体技術における最近の開発は、片側では大気圧、もう1方の側では高真空に耐えるほど充分強靱でありながらエネルギー電子に対しては事実上透過性をもつ薄い膜の生産を可能にしている。画像形成対象体積は、膜のすぐ近く、標準的には流体内へ数μmの範囲内にある。これは、生体粘着細胞といった膜表面又はその近くにある物体の検査のために理想的である。開示されている技術は、更に、既存の全ての走査型電子顕微鏡に容易に適合でき、室温および大気圧での測定を可能にする。
【0036】
A.実験用セットアップ
我々は、高真空モードでJEOL6400SEMおよびフィリップス(Philips)ESEMの両方で作業するよう本発明の装置および方法をうまく応用したが、我々が提示する装置はあらゆるSEMで使用することができる。本発明の現在好まれているいくつかの態様について、添付図面および図との関係において以下で完全に詳細を記述することにする。
【0037】
サンプルは、標準的SEMサンプルマウントインサートのラインに沿って設計されたチャンバの内側に保持される。主として強調されるのは、外部圧力差に対するサンプルの密封であり、これは一連のOリングを用いて行なわれる。膜が所定の位置にある状態で我々がサンプルを閉じる時点で人がチャンバ内部の流体を試しに圧縮したとすると著しい変形がひき起こされることになるため、サンプルの閉鎖は膜にとっての一つの危険性を提示する。これを回避するために、インサートの軸を通して小さい放出用溝路が開放状態に保たれ、流体のわずかな放出により内側の圧力を平衡化している。この溝路に対する開口部は、所定の位置にネジ込まれているもう1つのOリングで、その後密封される。
【0038】
膜は、いくつかの重要な特性を有していなくてはならない。まず最初にそれは可能なかぎり電子に対する透過性をもっている必要がある。これには、低い平均原子数(低いZ)および低い密度が関与する。従って、重合体フィルムが最も適した選択肢である。
【0039】
膜には非常にすぐれた機械的特性も必要とされる。電子が問題のゾーンに達する前の電子の散乱を可能なかぎり小さく保ちながら、膜は、観察に必要とされるだけの大きさの表面について1気圧の圧力差に耐えなくてはならない。それは又、サンプルの調製の際の多大な取扱い量を可能にするのに充分な可とう性も有していなくてはならず、かくして炭素フィルムは非常に脆いためその可能性が排除されることになる。サンプル内部のおよびサンプルホルダーを構成する材料に対する多孔性は、チャンバの適切な密封を確保するため、できるかぎり低減されなくてはならない。
【0040】
理想的には、膜の電気伝導率は、入射電子ビームを摂動させ画像を不鮮明にさせる可能性のある膜の外部表面の局所的帯電を防ぐのに充分高くなくてはならない。実際には、我々は、膜の外側で薄い炭素フィルムを蒸発させ、かくして帯電効果を削除している。
【0041】
最後に、観察される物体に対する膜の親和性が重要な要因となりうる。標準的には、電子顕微鏡においては、電子は上部領域から底面まで進み、そのため我々が観察したい物体は膜の下に位置設定されることになる。開発された方法においては、物体が膜にきわめて近いところにある場合そして最もよいのはそれらが膜に付着されている場合に最高の結果が得られる。
【0042】
膜を構築するためには、さまざまな材料がテストされてきており、全ては炭素化合物に基づくものである。TEMにおいて支持用フィルムを構築するのに一般に用いられているフォームバー(Formvar)およびブトバー〔DavisonおよびColquhoun、J. Elec. Microsc. Tech.2,35,1985;HandleyおよびOlsen、Ultra-microscopy4,479,1979〕,およびポリイミドがテストされてきた。これまでにテストされてきたこれらの材料のうち、ポリイミドのみが、全ての機械的および密封必要条件を満たした。現在好まれている1つの態様に従うと、Moxtex、Incにより供給されている厚さ1450’のポリイミド膜が使用される。ポリイミド膜は水に対する測定可能な多孔性を全く示さない;サンプルは、SEMへの挿入に先立ち数時間約10−7バールの真空下に置かれても、検出可能な損失を示さない。サンプルは、1mm2以上のウインドウ内で大気圧により生成される力に耐えることができる。膜に対するこの力そしてその結果としての破断のリスクを最小限におさえるため、表面は通常、膜の外側に付着されたTEMNi格子の使用により削減された(125〜330μmのメッシュが用いられた)。電気伝導度については、外部表面上の50’の炭素被着で充分であるということがわかった。親和性特性が必要な場合、それは、内部表面処理によって達成される。
【0043】
B.コントラスト形成メカニズム
検出器上の信号の形成に対する貢献としては、2つの異なるものが存在する。第1のものは、均等な雑音の供給源であり、一方第2のものには信号が含まれる。
1.ビームが膜を打撃すると、後方散乱電子(BSE)および2次電子(SE)が膜自身によって生成される。最初の数ナノメートル(2次電子の平均自由経路)内で生成されたSEのみが膜から逃れることができる〔ゴールドスタイン(Goldstein)ら、走査型電子顕微鏡検査法およびX線微量分析p113,Plenum press、New York、London、1992〕。それらの平均自由経路は、導体(薄い炭素層)中1nm前後であり、(ポリイミドおよびそれを超える流体のように)絶縁体の中で最高10nmである。SEは膜内および炭素コーティング遮へい物内の両方で作り出される。
【0044】
従って、BSEおよびSEの両方で構成された、膜に起因する信号に対する第1の貢献が得られる。この貢献は、我々が使用する膜の組成および厚みの両方が至る所で同じであることから均質である。以下では、(膜を表わす)下付き文字「m」がこの貢献を意味するものとする。
2.膜を横断するときに後方散乱されないビームからの電子の部分は、サンプル上にぶつかる。ここでも又、2次電子および後方散乱電子が生成される。
【0045】
ここで生成されたSEは、逃がれる機会がなく、膜(絶縁体)又は薄い炭素コーティング遮へい物(導体)により停止させられた状態となる。これとは対照的に、サンプル内に作り出されたBSEは、膜を通って戻るように退出する可能性がある。それらは、膜を通過するにつれて、2次電子を生成する可能性があり、これらの電子はその平均自由経路より低い表面からの距離のところで作り出された場合、検出器に逃れることができる。
【0046】
かくして、EMおよびBSE検出器の両方に到達する、問題のゾーン内の後方散乱事象に起因する信号に対するこの第2の貢献が得られる。以下では、(サンプルを表わす)下付き文字「s」がこの貢献を意味することになる。
【0047】
第2の貢献(s)は明らかに、問題の貢献である。これは、我々が求めている情報を担持しているが、一方第1のものは膜のみ(m)に関係している。2つの隣接点間のコントラストは、それらの間のサンプル信号の差が膜信号内の変動よりも高い場合に観察可能となる。
【0048】
かくして、画像を形成する我々の能力は、大きい信号対雑音比を得る可能性によって決定される。これは、それ自体、サンプル内部にある材料の後方散乱係数(「材料コントラスト」)の差によって決定され、膜にも左右される。
【0049】
後方散乱係数がわかっている2つの異なる材料を仮定して、特定の膜について、1つの画像を形成するために満たす必要のある条件を決定したいと思う。
【0050】
収集された合計信号Sは、2次電子と後方散乱電子の両方で構成されている:
【0051】
【数1】
【0052】
ηおよびδは、それぞれ、ビーム電流に対するBSEおよびSEの比を表わす。係数εは、検出される2種類の電子についての収集効率を表わす。
【0053】
後方散乱係数ηはそれ自体、2つの貢献すなわち膜(m)内部からのBSEおよびサンプル(s)内部からのBSEから成る。η=ηmtηs。
【0054】
同様にして、SE散乱係数δは2つの貢献を有する、δ=δm+ηsΔm。
【0055】
その差は、δmが膜内に入るビームの電子により生成される2次電子を表わす一方、Δmは、サンプル内部の関連する後方散乱事象の後に退出中の電子により膜内で生成される2次電子を表わす、という点にある。
【0056】
かくして、膜を通って戻るエネルギービーム電子の流束は1からηsだけ削減されることから、後方散乱係数ηsはΔmだけ増す。
【0057】
δmおよびΔmが両方共、膜の表面に近いところからの2次電子の放出を説明しているという点に留意されたい。δmについて、2次電子を生成する高エネルギー電子は、大部分が、入射ビーム電子であり、膜内部で後方散乱した電子からの貢献は小さい。Δmについては、2次電子を生成する電子はサンプル内部で後方散乱事象を経験している。この理由から、Δmは低速材料依存性を含む可能性がある。膜の下にある材料に応じて、この領域内のBSEのエネルギースペクトルは異なるものであり得、BSEの異なるエネルギーが異なるSE放出を生成し得る。
【0058】
我々が使用している後方散乱および2次係数および文献内で通常記述されている係数の定義がわずかに異なっているという点に留意されたい。後者は、半無限の媒質について定義されており、材料(金、炭素、ナイロンなど)に特徴的なものである。ここで、係数は、その特定の厚みをもつ1つの膜およびその炭素遮へい物の電荷放出を記述している。これらの係数は、ポリイミド材料の半無限のサンプルの電荷放出を記述するものではない。同じ要領で、サンプル係数は、膜で覆われたサンプルの内部の材料から来る信号を記述している。以下における我々の目標の1つは、測定上の係数を材料(例えば水、金など)の特徴である古典的な理論上の係数と実験的関連づけすることにある。
【0059】
信号SAおよびSBを与える2つの隣接する点を考慮してみよう。それらの間の材料コントラストは次のように定義づけされる。
【0060】
【数2】
【0061】
(SA>SBと仮定する)。
【0062】
信号Sを修正する方法としては基本的に2つのものが存在する。1つは、それに定数を乗じること(増幅)である。もう1つは、信号に対し正又は負の定数を加えること(これは「ブラックレベル」である)。信号に対する膜の貢献は、至る所で同じである。その厚みおよびその組成は、きわめて明確である。従って、組成コントラストもトポグラフィックコントラストも、膜のために、点AおよびBの間に現われない。
【0063】
かくして、貢献mは、ブラックレベルを適切に選択することによって除去され得る定数である。それでも、nを膜から散乱した電子の数としておよそpnの雑音が測定に干渉しうるものの、それについては以下で立ち戻ることとして、当面それを無視する、ということに留意されたい。この選択より、点AとBの間のコントラストは大幅に単純化される:
【0064】
【数3】
【0065】
材料コントラストは、点AとBで膜の下にある材料内に発生した後方散乱事象の数の差にのみ関係づけられる。
【0066】
貢献mに立ち戻ると、それは、それがおおよそサンプル内部の事象により生成された信号の振幅をもつものである場合、画像を完全に破壊しうる雑音を生成する。このような理由から、我々は、膜特性を研究し、膜のみに関係づけられかつブラックレベルの適切な選択によりコントラストの式(等式3)内では削除された信号の部分を定量化しなくてはならない。
【0067】
C.膜を通しての電子の通過
ここで、信号に対する膜の貢献を実験的に定量化することにする。これは、エネルギーの一関数としてその表面から放出されたBSEおよびSEを単位として行なわれる。我々が用いる方法は、異なる状況でサンプルを横断する合計電流を測定し、次に減産を行ってBSEおよびSE内への損失を得ることにある。我々は、サンプルにおいてSEMが提供する全電流を推定するべく妨害の無い電流を測定し、次にこの電流に対する膜の効果を測定する。最後に我々は、ここでは金および水である与えられた材料まで膜を通って進む電流を測定する。
【0068】
この目的のために、我々は4つの異なるサンプルおよび、異なるサンプルが顕微鏡内部に同時に挿入され得るようにする1つのアセンブリを使用した(我々がもっていた4つのサンプルのうち、3つは一緒に挿入でき、従って我々は重複する三ツ揃いおよび同一の条件で実験をくり返した)。異なるエネルギーについて、ビームを連続して各サンプル上に位置づけし、大地とサンプルの間の電流を測定した。
【0069】
サンプル1は、単に、ビームの全ての電荷を収集することによりビーム電流I(ビーム)を測定するために使用されたファラデーカップである〔ゴールドスタインら、走査型電子顕微鏡検査法とX線微量分析、p65,Plenum press、New York、London、1992〕。それは、中央に直径が10mのアパーチャをもつNiプレートで閉じられたキャビティ(直径2mm,深さ3mm)をその上面に伴う、大地に接続された大量の炭素で構成されている。ビームは、アパーチャを通って入り、炭素キャビティの底面を打撃し、かくして、主要ビームおよび実際には全ての散乱した電子が収集されることになる。
【0070】
サンプル2は、アパーチャが膜で覆われているという点を除いて、同一の設計である。我々はこれを測定I(膜)と呼ぶ。
【0071】
サンプル3は、大地に接続され膜で覆われた純金サンプルから成る。金はまず最初に、膜との「直接的」接触が達成された大きい部域が得られるようその表面が充分平滑となるように、融解させられた。最後にサンプル4は、水が入り膜で密封された我々の実験用チャンバである。サンプル3およびサンプル4は、I(材料)+I(膜)について2つの値を定義する。
【0072】
サンプル1および2について測定した電流の差(サンプル1のものにより正規化されている)は、膜との相互作用によって放出された電子の百分率を与える。これは、膜の2次および後方散乱係数の貢献を測定する:
【0073】
【数4】
【0074】
S3又は4について測定した電流からのビーム電流(サンプル1)の差は、外側に到達するサンプルから放出された電子の百分率を与える。これらには、膜および材料(それぞれ金又は水のいずれか)の両方と相互作用した電子が含まれている:
【0075】
【数5】
【0076】
下付き文字Sは、ここでは金又は水である材料を意味する。
【0077】
5keV未満のエネルギーについては、金および水曲線は、膜曲線上に重なることがわかる。これはすなわち、ビームが、サンプルに到達すると同時にBSEを検出器に送り戻すのに充分なほどのエネルギーは有していないことを意味する。
【0078】
5keVを上回るエネルギーについては、3本の曲線は、その勾配が異なっている。検出された信号の成長しつつある部分は、考慮対象の材料との相互作用に起因する。エネルギーが増大するにつれて、この差は増大する。信号の材料成分は支配的なものとなる。
【0079】
水サンプルおよび10keVの電子エネルギーについては、ビーム−膜相互作用は、電荷放出の50%に貢献する。その貢献は15keVで35%まで減少する。
【0080】
金の場合、原子番号が高いために、割合は劇的に小さくなる。10keVで、放出された電荷のわずか4%が膜の特徴である。15keVでは、膜の貢献は2%まで下がる。
【0081】
この段階で、我々は合計電子放出から膜成分を差し引き信号に対する材料貢献を得ることができる。これには、問題の材料とそれらの相互作用により散乱させられる電子のみが内含される。
【0082】
低エネルギーでは、ビームの電子はサンプルに到達せず、曲線はゼロになるはずである。非常に高いエネルギーでは、曲線は、膜が事実上透過性となることから、材料の後方散乱係数の挙動に追従するはずである。これが実際2本の曲線について我々が観察することである。水曲線の減少勾配は、HungerおよびKuchlerの微分演算〔Phys、Status. Solidi A. 56,K45,1979;ゴールドスタイン前掲書p95も参照のこと〕から計算されるような、後方散乱係数の理論上の挙動に追従する。全曲線の増加勾配も同じく、(同じ式から導出されるような)計算上の後方散乱係数の推移に直接追従する。
【0083】
それぞれの材料の後方散乱係数によりこれらの曲線を正規化することによって(その該当するエネルギー依存性を伴って)低い材料依存性のみが残っている曲線が得られる。
【0084】
水についての結果は、HungerおよびKuchlerにより予測された理論的曲線よりも約25%低い後方散乱係数を表わしている。この差の原因が何であるかは定かでないが、我々のサンプルは完全に封じ込められ、汚染の機会は最少限しかないことから、我々は、我々が実験的に決定した値がこの数量について現時点で利用可能な最も偽りのない結果であると考えている。
【0085】
我々はこれを直接測定したわけではないが、膜より下の材料の特性は明らかに、放出されているBSEのエネルギースペクトルにも影響を及ぼす。エネルギーは、E0を入射電子のエネルギーとして、0〜E0の範囲内にある。軽い材料(例えば炭素)は、E0/2の値をほぼ中心とする分布をもち対称である〔Hermannにより編集された第4回国際X線光学および微量分析会議議事録(Paris、1966)中、Bishop;ゴールドスタイン前掲書p100も参照のこと〕。重い材料(例えば金)は、非対称性の強いBSEのエネルギー分析をもち、ピークはE0により近くなっている。この差は、2つの効果を誘発する。まず第1に、膜を横断して戻ることのできるBSEと生成された合計BSEの比は、軽い材料の場合よりも重い材料の場合に高くなる。膜は、実際には低エネルギーBSEをろ過により除去するように作用しており、かくして軽い要素と重い要素の間のコントラストを人工的に増強している。第2に、BSEのエネルギースペクトルの差は、低いエネルギーのBSEが退出する途中でSEを生成する確率がより高いことから、SE放出Δmにも影響を及ぼす可能性がある。
【0086】
水と金の原子番号の間の電子番号のその他の材料については、対応する曲線は、示された2つの端部の間にあることになる。これまでの結果からの我々の結論は以下のようにまとめられる。
a) 4〜5keV以下のエネルギーについては、サンプルからいかなる信号も検出できない。この閾値は、より薄い膜を使用することによって減少させることができる。
b) エネルギー中間領域は、次のような複数の理由で興味深いものである:まず第1に、低エネルギーのBSEに対する膜ろ過効果は、重量材料と軽量材料の間のコントラストを増強する。第2に、この領域におけるSEの放出は重要であり、SE検出器で容易に画像形成することが可能である。全曲線上のピークは、1より高い値に達し、SEの高い放出を実証している。
c) 高いエネルギーについては、放出された電荷は、理論的に予測されたBSE係数に近づいている。その理由は、より高い電子エネルギー(ビームの電子および後方散乱電子の両方について)では、BSEが膜を横断する確率が更に高く、退出中のSEに対する確率はより低いものである、ということにある。2次放出はΔmの減少に関係しており、従って、実験的に観察された通り、BSE検出器を通して画像形成することが更に容易になる。
【0087】
BSEに対する膜ろ過効果は、高エネルギーで無視できるものとなる。コントラストの式(等式3)の中で、後方散乱係数を、考慮対象の材料(水、金、炭素など)の後方散乱係数で差し換えることができる。水平域に達するエネルギーは、それ以上になるとこの近似が有効となる最小のエネルギーを示している。本書で例示されている膜については、この値は15keV前後である。
D.一定の与えられた材料コントラストの観察のため最小プローブ電流を演繹する。
【0088】
2つの点の間に小さな組成差(平均原子番号の差)が存在する場合直ちに、それを観察することは理論的に可能である。問題は、その観察を行なうために、これらの点にどれだけの電子がぶつかる必要があるかである。
【0089】
このような推定は、複数の理由から有用である。まず第1に、選択された電流は、解像度に影響を及ぼす。高い電流は、ビームの集束度を低くする。これは、顕微鏡の電子源がタングステンフィラメントである場合に、問題がより大きく、電界放出顕微鏡の場合についてはさほど注意が必要な問題ではない。第2に、電子源は制限された数の電荷しか生成できず、第3に、高い放射線線量が試料に損傷を与える可能性がある。
【0090】
我々は、一般に、大部分の場合低コントラストのサンプルであることが判明するエマルジョン、生体試料,重合体溶液などといったような試料含有液体に関心を寄せている。
【0091】
充分な可視性についての幾分か恣意的ではあるものの有用な基準は、「ローズ基準」〔ゴールドスタイン前掲書中、p215〕。これには、2点AおよびB間の差を観察するためには、これらの点の間の信号振幅差は雑音レベルの5倍より高くなくてはならないと記述されている:
(SA−SB)>5N
異なる走査においてビームが点Aにあるときに検出器に入る電子の数を測定することで、その標準偏差が〜η1/2によって求められ平均値nに中心をおく分布が得られる。かくして信号はηに比例し、雑音はη1/2に比例する。信号対雑音比はS/N〜η1/2であり、観察できる材料コントラストの最小レベルはCmin=5/η1/2である。
【0092】
かくして、特定の材料コントラストCを観察するために収集すべき電子の平均数は、一般的な形でη>(5/C)2により求められる。(検出器における)対応する電流はIs>(q/t)(5/C)2であり,ここでqは、電子の電荷であり、tはビームが各点に存在する時間である。tは同様に、t=T/npとして表現することもでき、この場合式中の
Tは走査時間、npはフレームあたりの画素数である。高品質の画像については、標準的にnp=106画素が存在する。ピコアンペア単位でIsを、又秒単位でTを測定すると、一定の与えられた材料コントラストCを得るために検出器において必要とされる電流が、
Is=4/TC2 (4)
であることが見い出される。
【0093】
最後に、信号電流Isおよびビーム電流IBはIS=ηs(εBS+εSEΔm)IBを通して関係づけされる。Everhart−Thomley検出器のようなSE検出器は、BSEの除去率が優れ、非常に効率が良い〔ゴールドスタイン前掲書〕。BSE検出器はSEを収集せず、通常小さなシグニチュアを有することから、中程度の収集効率しかもたない。実験により、我々は、10keV前後のエネルギーで、BSEおよびSEの両方のモードでの画像が同じコントラストで現われ、一方、より高いエネルギーでは、BSEの方がすぐれているということを発見した。25%での収集効率の適正な推定値を取り上げると、コントラストCを得るのに必要とされるビーム電流が〔19〕(同じく〔ゴールドスタイン p217〕中)であることがわかる。
【0094】
IB=16/nηTC2 (5)
高いエネルギーでは、コントラストCは単純に等式3により膜の下の材料の後方散乱係数に関係づけされる。表1は、細胞、油/水エマルジョンおよび水中金粒子といったような生体試料の観察のために必要とされる最小電流の計算の結果を示している。
【0095】
4つの元素C、H、NおよびOは、細胞といったような生体試料の重量のほぼ99%を作り上げている。細胞は、70%の水と29%の有機化合物で構成されている。これらの化合物中の原子の約50%がH原子であり、24%がC,24%がOそして1%がN原子である〔20〕。これらの値がわかっていることから、標準的有機分子の平均原子番号は6.72である。水の原子番号は7.22であり、生きた細胞については、それは7.07である。20keVでの対応する後方散乱係数を計算すると、水については0.075、細胞については0.073となる。かくして、水性媒質により取り囲まれた細胞は、低いコントラストC=2:5%を提示し、更に後方散乱係数は低い。この計算は、ナノアンペアの範囲内の最小電流が100sという標準走査のために必要とされるということを示している。
【0096】
【表1】
【0097】
表I.水を含む異なるサンプルの観察に必要とされる最小電流の評価。Iは等式5から求められる。ηの値は、指示された平均原子番号値Zを用いて、エネルギーE=20keVでHungerおよびKuchlerの式から計算される。走査時間T=100sは、精細な低速走査に典型的なものである。
【0098】
油/水エマルジョンは、より容易に観察可能であり得、10倍高いコントラストC=26:7%を呈する。最小電流は、その場合、数十ピコアンペアまで降下する。水中に浸漬された金粒子については、コントラストは非常に高い(C=90%)。それを画像形成するには、数分の1ピコアンペアしか必要ではない(表I)。
【0099】
細胞といったような生体サンプルは、適正な蓄積時間内で画像形成するために高い電流を必要とする。有利には、細胞を飾るためにコロイド金粒子といったような重量マーカーでの標識づけを使用することができる。油/水のエマルジョンは、標準的な電流および蓄積時間条件下で直接観察することができる。
【0100】
低エネルギー(10keV以下)では、膜の影響が重要となる。その結果として、低コントラストサンプルは、画像形成されるのにより一層多くの電流を必要とする。
【0101】
E.当該技術の解像度の評価
あらゆる電子顕微鏡測定においてそうであるように、解像度の問題は究極的に、高い電子含有量をもつ散乱原子の存在に要約される。強く散乱する原子の不在下では、ビームはサンプル中の深いところまで到達し、それにつれて拡幅し、戻されるのに充分な相互作用を受けないうちに、解像度を喪失する。高い電子密度をもつ材料で、ビームは戻され吸収される前に短かい距離しか走行せず、かくして散乱する体積は小さく解像度は高くなる。
【0102】
解像度に対する膜の効果を見るためには、直径deffにより特徴づけられる有効信号生成体積を評価する必要がある〔ゴールドスタイン、前掲書中、p162〕:
【0103】
【数6】
【0104】
なお、式中、dBは、膜に入るビームの直径を表わす。ビームが膜を横断するにつれて、幾分かの散乱が発生し、これは低エネルギーにおいては特に重要で、高いエネルギーでは無視できる傾向をもつ。dmは、膜との相互作用の結果としてのビームの拡幅を表わす。ゼロの初期幅dB=0をもつビームは、直径dmをもつ膜から出現することになる。
【0105】
距離dBSEは、BSEとして戻る前にサンプル中で電子により覆われている体積の平均直径である。dBSEは、文献〔ゴールドスタイン前掲書中、p105〕内に見い出すことができ、Kanaya-Okayama(KO)範囲に関係する。KO範囲により全ての特徴的長さを再度スケーリングすると、材料依存性の大部分が除去され、小さい原子番号Zの依存性のみが残される。金のサンプルの場合、BSEの90%が直径dBSE=0.3RKOの体積に由来している。炭素については、同じ関係から、dBSE=0.6RKOが得られる。
【0106】
KO範囲は、材料内部の電子の相互作用の体積の標準的サイズを与える。これは、その周囲が相互作用体積の制限的包絡線を包含するビーム衝撃点を表面上の中心とする円の半径と等価である:
【0107】
【数7】
【0108】
RKOはμm単位で表現され、E0はkeV単位の入射ビームエネルギーであり、Aはg/モル単位の原子量であり、βはg/cm3単位の密度、Zは原子番号である。
【0109】
3つの異なる層(炭素膜−材料)という一般的ケースでは、理論上の解像度を計算することは、重要である。しかしながら、非常に低いか又は非常に高い原子番号をもつ材料という2つの制限的ケースでは、かかる推定が可能である。
A.低エネルギーでの低コントラストサンプルの解像度
水、油又は膜を構成する材料といったような軽量材料は、原子番号に関し充分近いものであり、そのため単純な推定というのは、それらを同じものとみなすことである。このとき、解像度の推定は、単純に次のようなものである:
【0110】
【数8】
【0111】
なお式中、dBSEは、平均軽量材料の中で計算される。この評価は、dBSEが膜の厚みよりも大きいかぎり意味がある。
【0112】
ビームdBの直径は、顕微鏡内で用いられる電子源によって左右される。電界放出源は、最良の条件(低電流、高エネルギー)下で1nmのサイズのビームを生成し、一方、最も困難な条件下では、サイズは10nm前後である。タングステンフィラメント顕微鏡については、ビームの直径は10〜100nmまで変動しうる。
【0113】
かくして、軽量サンプルの場合に得られた解像度は、およそ200nmである。10keV,低電流および電界放出源では、推定から、deff=170nmが得られ、一方20keVでは、最高deff=500nmとなる。
【0114】
実験により、我々は、膜厚みよりも優れた解像度を得るのが困難である、ということを発見した。エネルギーを低下させた時点で、膜の下でサンプル採取された体積が低減することから、解像度は改善する。しかし、実際には、エネルギーが低減されるにつれて、コントラストは、トレードオフとして減少する。サンプルから後方散乱される電子は更に少なくなり、サンプル信号対膜信号の比は減少する。かくして、解像度の真の限界は、検出可能な最小コントラストにより与えられる。膜の厚みを低減させることができる場合には、サンプルを画像形成するための最小のエネルギーは減少し、解像度は著しく改善することになる。
【0115】
この解像度の推定値は、この段階でなぜ水中油型エマルジョンといったような低コントラストのサンプルについて、我々の技術が光学顕微鏡に関し著しく改善を示さないのかを表わしている。これは、より薄い膜といったような技術的進歩により改善可能である。しかしながら、水中金粒子、更に一般的には重量材料で作られ軽量材料中に浸漬された小さな物体を考慮したとき、状況は完全に変わる。
【0116】
B.高エネルギーでの高コントラストサンプルの解像度
水の内部での金粒子のケースは非常に興味深いものである。高エネルギーで実験的に得た解像度は数10ナノメートルの範囲内にある。エネルギーが高くなればなるほど、得られる解像度は良くなる。実際の直径40nmのビーズは、30keVで50nm前後の直径であるように見え、これは(dBSEにより与えられる)BSEの相互作用体積よりも1ケタ以上小さいものである。このことは、解像度が相互作用範囲と関係づけされないということを実証している。この場合、解像度は、粒子の深さに到達したときのビーズの直径にリンクされる。
【0117】
高エネルギーでは、ビームは、それを妨害するビーズが全くない場合、水の内側で拡散することができ、BSEによりサンプル採取される体積は深くかつ幅広である(1〜数μm(ミクロン))。BSEが生成する信号は、非常に幅の広い体積全体にわたる蓄積の結果であり、このような理由から、ビームが走査されるとき著しく変動しない。その上、高い倍率では、画像サイズ自体が、おおよそBSEでサンプル採取された体積のサイズである場合、この深いBSE信号は、ブラックレベルの適切な選択によって除去することのできる定数である。一方、電子ビームが重量材料ビーズを横断する場合、ビームの有意な部分が妨害され得、直ちに、はるかに多くのBSEが放出される(高い後方散乱係数)。かくして、得られる解像度は、ビーズの深さにおける電子ビームの空間的拡がりによって左右される。
【0118】
膜のすぐ下にあるビーズは、最高の解像度で画像形成される。サンプルの内部深くに粒子があればあるほど、それを画像形成できる解像度は低くなる。
【0119】
ビームの拡張は、モンテカルロシミュレーションに充分適合された問題である。我々は、かかる計算を行なうために、D.C. Jayが考案したコードを使用した〔電子顕微鏡検査および微量分析のためのモンテカルロモデリング(Oxford University Press. New York、London 1995)〕。シミュレーションのための入力値は、ポリイミド化学量論構造式C22O5H10N2,平均原子番号6:4および平均原子量9.8g/モルである。材料の密度は1.4g/ccである。
【0120】
20keVでは、解像度の限界は、膜より下60nmと推定される。30keVでは、計算されたビーム直径は35nmであり、これはビーズが膜と接触している場合に実験的に得られる解像度と相容性ある値である。
【0121】
計算は、2倍の薄さの膜を使用した場合、高エネルギーで10nmの解像度での画像形成が可能であることを示している。
【0122】
サンプルの内部深くにあるビーズについては、間にある水に起因するビームの拡張を考慮に入れなくてはならない。解像度の近似は、モンテカルロシミュレーションから計算されたdeff=V(d2(ビーム)+d2(膜)+d2(水)・d(水)から得られる。
【0123】
膜を使用した状態で、かつ30keVで、膜より下100nmにある金粒子は、45nmの解像度で画像形成可能である。200nmの深さのビーズは、同じエネルギーで80nmの解像度で画像形成できる。
【0124】
F.サンプル採取深度
完全さを期して、サンプル内部でどれほど深く重量粒子を検出できるかを評価することが有利である。
【0125】
軽量材料中では、脱出するBSEのほぼ50%が、表面に戻る前に0.2RKOに等しい深さに到達する(ゴールドスタイン前掲書p105)。数値的係数0.2は炭素についてのものであるが、係数は原子番号と共に非常にゆっくりと推移することから、水および膜を構成する材料についても非常に類似しているはずである。
【0126】
その値を我々の推定上のサンプル採取深度として考慮すると、6keVで、サンプル採取深度は150nm前後である。この値は、我々の厚み145nmの膜ではこのエネルギー未満では画像形成がほとんど不可能であったという我々の観察と相容性あるものである。
【0127】
水中では、サンプル採取深度は10keVで約0.4μmであり、20keVで1.2μm,35keVでは3.1μmであり、これは、多くの走査型電子顕微鏡上で利用可能な最大エネルギーである。これらの値は、水の内部で全粒子を検出できる深度範囲の推定値を与えている。
【0128】
G.チャンバ内部の圧力の推定
以下に記すのは、湿潤チャンバ内部の圧力の単純な計算である。この計算は、大部分が、きわめてわずかの空気しか(例えば小さな気泡)内部にない状態でチャンバに水が充填されたと仮定されているセットアップを基準としている。
【0129】
計算を単純化するために、以下の仮定が考慮される。
1.大気圧でほとんど水が充填されている閉鎖されたチャンバで開始する。内部には、実際小さな体積の空気Va(大気圧で測定)が入っており、この体積はチャンバを真空内に置いた後の体積膨張Vに比べて小さいものである。
2.膜は、バネ定数kをもつバネにより保持されたピストンとしてモデリングされる。このモデリングは、膜上の力と膜の変位Xの間の線形関係しか仮定していないことから、恐らくは適切なものである。この有効な定数は、実験により容易に推定される。膜(ピストン)の表面積はSで記されている。
3.水は、圧縮不能であると仮定される。チャンバがひとたび真空下に置かれたならば、ピストンは、平衡に達するまでシフトする。膨張した体積Veは、平衡条件により決定され、空気および水蒸気により充填される。水蒸気圧PH2Oは温度のみによって決定され、体積とは無関係である(Kittleyの熱物理学を参照のこと)。空気および水蒸気は両方共理想気体であるものと仮定されている。
【0130】
水蒸気分子の数は、以下の式から得られる;
【0131】
【数9】
【0132】
なお式中Tは温度である。
【0133】
真空内に挿入した後のチャンバ内の合計圧力は以下の通りである:
【0134】
【数10】
【0135】
なお式中、
【0136】
【数11】
【0137】
は、空気(窒素)分子の数である。(1)および(2)において、我々は、Ve>Vaという仮定1を用いた。
【0138】
圧力についてのもう1つの等式は、平衡条件によって与えられる:
【0139】
【数12】
【0140】
Ve=XSを用いて、体積Veについての等式が得られる。
【0141】
【数13】
【0142】
(4)を(1)および(2)に代入すると、幾分かの操作の後、初期パラメータによって左右されるPtotについての等式が得られる:
【0143】
【数14】
【0144】
この等式は、(最後の項で除することによって)次の式に変換できる:
【0145】
【数15】
【0146】
又は
【0147】
【数16】
【0148】
等式(7)は、Ptotの推定のために有用である。右側の最初の項は約0.025である。第2項についての比率がこの値よりもはるかに小さい場合には、気泡を無視することができ、チャンバ内の圧力は水蒸気圧である。それが大きい場合には、この比率は大気圧からの合計圧力の分数を与える。この等式は、Ve>Vaを条件として導出されたものであることに留意されたい。Va>Veである場合には、圧力は大気圧に近いものにとどまり、水蒸気圧は不適切である。
好ましい態様の説明
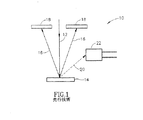
ここで、先行技術のSEM10のサンプル部域の縦断面を示す一般化されたダイヤグラムである図1を参照する。一次電子ビーム12は、真空経路を通って走行し、サンプル14に達する。それはサンプル14を打撃して後方散乱した電子6の流れを形成し、これらの電子は後方散乱した電子の検出器18を打撃する。後方散乱した電子に加えて、サンプルにより放出された2次電子20が2次電子検出器22に向かって加速される。
【0149】
雰囲気を通しての電子の平均自由経路は非常に小さく、かくして、エミッタからサンプルを介し検出器に至るまでの電子経路全体は真空中にあり、湿潤サンプル又はin vivoプロセスを研究することは不可能になっている。
【0150】
ここで、本発明の第1の態様に従った走査型電子顕微鏡の縦断面を示す一般化されたダイヤグラムである図2を参照する。前述の図の中に示されたものと同じである部分には同じ参照番号が付され、当該態様の理解に必要な場合を除き、再度説明はしない。
【0151】
図2では、1次電子ビーム12が、真空チャンバ30を通って、チャンバ34内に置かれたサンプル32に向かって走行する。チャンバ34内に密封されているのは、湿潤で生きた組織の保持に適した雰囲気であり、この雰囲気中でin vivoプロセスを行なうことができる。最も適した環境には水性媒質が含まれる。
【0152】
真空チャンバからチャンバを密封するために、標準的には膜であるバリヤ36が、リング38により画定されたアパーチャを横断して伸張させられる。リング38は、以下の図3に関連して更に詳細に示されるように気密な形で膜36を端部で保持するように設計されている。サンプル32は、好ましくは、膜36まで近接して設置され、電子ビームがサンプルに到達するのにチャンバ内部の雰囲気を通って走行しなくてすむようになっている。好ましい一態様においては、サンプル32は、膜と実際に物理的に接触した状態にあり、生きた組織の場合には、膜上で成長させられてもよいし、又は、以下で例示するように既知の方法を用いて膜に取付けられていてもよい。
【0153】
好ましくは、チャンバ34は、以下で図3に関連して詳述されるように、逃し出口40を含んでいる。チャンバは更に、試料のための適切な条件を維持する流体用の入口41および出口42を含む。例えば、研究対象の試料の化学環境を変えるべく入口41および出口42を利用することも可能である。この特長は、薬物の研究において特に有用であり、この場合、与えられた薬物の濃度が変わるにつれての細胞の動的反応を見守ることができる。
【0154】
膜36は、ホイル又はフィルムであってよく、好ましくは、同時に電子ビームに対する透過性をもちながら最高1気圧の圧力勾配に耐えることができなくてはならない。1つの実施例においては、圧力勾配に耐えることができかつ3keV以上の領域内のエネルギーをもつ電子ビームに対する透過性を有することから、実質的に厚み1500Åのポリイミド層が使用される。より薄い膜は、2keVに対する透過性をもつ。より一般的には、厚みは、必要な圧力勾配に耐えかつ同時に利用可能なビームエネルギーで電子に対する透過性を有するように、200〜5000Åの範囲内にあってよい。好ましい材料は、例えば分子構造式C12H12N2Oのポリイミド、ポリアミド、ポリアミド−イミド、ポリエチレン、ポリピロールおよび付加的な導電性重合体、パルロジオン、コロジオン、二酸化ケイ素、一酸化ケイ素、炭素およびカプトン(商標),フォームバー(商標),ビニレック(商標),ピロフォーム(商標)およびブトバー(商標)を含む商標付き材料である。上述のようなポリイミドで構成された膜は、一次ビームおよび結果として得られた後方散乱電子16の通過を可能にする。
【0155】
2次電子(SE)は一般に、上述のものよりも低いエネルギーを有し、通常水中で吸収される傾向をもつ。かくして、サンプルから放出されるSEは通常検出されない。しかしながら、好ましい態様においては、SE信号は、高い2次電子収量をもつ材料の単数又は複数の層37で膜をコーティングすることによって増強される。標準的材料としては、フッ化リチウムがある。
【0156】
ここで認識できるように、SEは、SE検出器22により検出され、かくして全体的信号を増強するのに役立つ。
【0157】
好ましい態様においては、アパーチャ内の膜36の露出された部域の直径は、実質的に1〜3mmである。膜は標準的に、格子上に支持され、格子内部の各開口の最大直径は実質的に0.1mmである。格子は、圧力勾配に耐える膜の能力を増強させる。格子は、図3に概略的に示されている。
【0158】
膜は好ましくは、チャンバ34内部の通常の大気条件の維持を可能にし、かくして、生きた細胞、オルガネラ又はその一部分およびタンパク質を内含する一範囲のサンプルの検査を可能にする。膜は更に、表面活性剤、コロイド、油粒子、エマルジョンおよび重合体又はミセル性溶液の検査を可能にする。製薬業界では、チャンバは、例えば、膨潤、溶解および崩壊といったような薬物の動的特性更には或る種の薬物に対する細胞の耐性を検査するために使用可能である。繊維業界では、チャンバは、羊毛、木綿および合成繊維の加湿および乾燥を調査するために使用することができる。本発明を応用できるその他の分子としては、石油、食品、地質学、マイクロエレクトロニクス、ペーパーコーティングおよび材料科学があると考えられる。
【0159】
チャンバ34自体には、望みに応じて気体又は液体を充填することができ、電子ビームのナノメートル範囲の解像度に起因して、分子レベルでサンプルを監視することが可能である。膜に起因する解像度の損失は、その中で発生する散乱事象がきわめて少ないことから、無視できるものである。チャンバに気体が充填される場合、好ましくは、バネ43および付加的な膜44を含む圧縮除去装置をチャンバ内に具備して、膜が破裂するのを防ぐことができる。
【0160】
本発明の態様に従うと、チャンバ34を、図3に関して以下で論述するように、標準的SEM内に内蔵することができる。チャンバ34は、標準的試料ホルダー又は試料マウントと相容性がある。試料ホルダーは、試料チャンバ内すなわち試料ホルダーの設置のための顕微鏡のエンクロージャ内に容易に内臓できるような形で、標準的な市販の試料ホルダーの寸法に従って設計されている。
【0161】
以上では、大気圧を含むものとしてチャンバが記述されてきたが、このことは全てのサンプルについて必要ではなく、場合によっては、より低い圧力も適切であることが判明することもあり、従って、膜36を横断する圧力勾配は削減される。
【0162】
生きた細胞又はin vivoプロセスを観察するのに電子ビームを使用するにあたっての問題点は、電子ビーム自体がサンプルに損傷を与えるという点にある。例えば、DNAに対するピーク損傷は、4keVで発生する。3keV/1500Åのポリイミド膜の選択は、安全なことに、ピーク損傷レベルより低いものである。
【0163】
損傷レベルは更に、個々のサンプルに対する損傷を最小限におさえるエネルギーレベルを見い出すことで最適化することができる。
【0164】
ここで、図2のチャンバのさらなる1態様のわずかに分解された簡略化した断面図でありさらなる詳細を示す図3を参照する。好ましくは従来のサンプルホルダーにはめ込まれるサイズのチャンバ50は、サンプル保持アセンブリ51を含んで成り、このアセンブリはそれ自体、開放した表面55をもつサンプル領域54を封じ込める本体部材52を含む。図3の例においては、本体部材52は、標準的SEM試料マウントである。サンプル領域は、サンプル領域54の露出側全体にわたりはめ合わされる上述のタイプの膜56によって封じ込められている。格子59が、膜より上に位置づけられ、そこからスペーサ57により分離されている。閉鎖用部材58が、膜56をその縁部のまわりでグリップするような形で本体部材52全体にはめ合わさっている。閉鎖用部材は、本体部材52内のネジ穴60と連続している封じ込め部材58内の対応する穴の中にはまり込むネジ63を介して本体に取付けられている。サンプル領域54の密封を提供するため、サンプル領域54のまわりで本体部材52の中にOリングシール66がはめ込まれている。
【0165】
サンプル64は、膜56と近接した状態で示されている。好ましくはサンプルは、電子ビームが任意の多大な量の雰囲気内を走行する必要がないように、膜と実際に接触しているか又はそれからナノメートル以内のところにあるべきである。
【0166】
サンプル領域が、ネジ62の締付けによって密封されている場合には、サンプル領域内に圧力の上昇が存在する可能性がある。かくして、余剰の流体を逃がすことができるようにする圧力除去装置が具備される。このアセンブリ68は、流路72を封じ込めるステム70を含む。流路72は、ステム70の遠方端部にあるさらなる開口部14とサンプル領域54を連結している。ステム70のまわりには、第2のOリングシール78に対し内向きにプレスするべく下部部分79とはめ合わさる上部部分77を含む滑動する円筒形閉鎖部材76がある。閉鎖部材76は好ましくは、サンプル領域自体が密封された後で初めて開口部を密封するために使用され、かくしてサンプル保持アセンブリ51の余剰の流体のための経路を可能にしている。
【0167】
インサート73は、サンプルホルダー(図示せず)内への挿入を可能にする。
【0168】
ここで、光学手段による付加的なサンプル採取のために適合された図2および3のチャンバの1態様である図4を参照する。図4では、チャンバ80が光導体82の一部として作られている。閉鎖用部材86により保持された膜84がチャンバ80を真空に対し密封する。反射性コーティング90が好ましくは、光導体82の片端を被覆し、もう一方の端部は、矢印92の方向に光電子増倍管(図示せず)まで導いている。サンプル94には、電子ビームにより励起される電子発光(螢光)マーカーでマーキングが施されている。光は、光電子増倍管(図示せず)により増幅されるべく、矢印92の方向に偏向させられる。かくして、単光子で検出することが可能であり、好ましくは、SEMのナノ規模の解像度における光学的検出のための手段が具備されている。
【0169】
ここで、図3に示された態様を用いた湿潤試料の検査を示す電子顕微鏡写真である図5を参照する。サンプルは、本書にその内容が参考として内含されているMatthews(Institute of Physics 議事録、EMAG99,p95,Sheffield、1999)により記述されている、ESEMコントラストを実証するために前述の実験において用いられているような水中油形エマルジョンである。電子顕微鏡写真は、低解像度をもつJEOL8400SEMで撮影され、目盛マーカーが示されている。本発明に従って膜を用いて得られる解像度は、膜無しの従来の要領でSEMを用いて達成される解像度レベルとほとんど同じである。優れたコントラストが得られ、全体的結果は、湿潤試料の検査にとって充分なものである。
【0170】
明確さを期して個々の複数の態様の状況下で記述されている本発明のさまざまな特長を単一の態様の中に組合せた形で提供することも可能である、ということがわかる。換言すると、簡潔さを期して単一の態様の状況下で記されている本発明のさまざまな特長を、個別に、又は任意の適切なサブコンビネーションの形で提供することも又可能である。
発明の好ましい方法の詳細な説明
理想的には、生存可能な未定着細胞を含めた(ただしこれに制限されるわけではない)湿潤サンプルの画像を形成するための技術は、以下の能力を提供すべきである:
1.画像形成特性
− 少なくとも100nm、好ましくは1〜20ナノメートルの範囲の解像度。
− 高い信号対雑音および信号対バックグラウンド比。
2.細胞の生理学的環境:
− 湿潤未定着細胞の湿潤環境内で作業できる能力
− 最小限の放射線損傷(画像形成に対する最小限の妨害、結果の生物学的妥当性に対する最小限の効果)
3.処理能力:
− 最少限のサンプル調製段階
− 自動化戦略
本発明は、以上で概略的に記した仕様に合致するように我々が修正している走査型電子顕微鏡に基づくものである。
【0171】
最少限のサンプル調製の段階
従来のSEM手順では、帯電を防ぐべくサンプルのコーティングが必要とされている。ここでは、細胞をとり囲む電解質水溶液(媒質)は、帯電を防ぐのに充分なものである。かくして、サンプル調製は、コーティングを必要とせず、生きた細胞での作業を可能にしている。サンプル調製に定着、脱水又はコーティングが不要であることから、従来のSEMに比べてサンプル調製手順は徹底的に短縮され単純化され、結果の質は著しく高まる。ここで示すのは、制限的な意味のない例としてのサンプル調製手順である。この例は、膜タンパク質の細胞外部分のような細胞外細胞成分を標識づけするために適している。細胞内細胞成分の標識づけを含めたその他の標識づけ技術は、以下の例の節で記述されている。細胞の標識づけは、普通の免疫標識付け手順によって行なわれる。
【0172】
我々の結果は、この湿潤SEM技術が、定着された細胞および生きた細胞の両方に、そして粘着細胞、および非粘着細胞の両方のために適しているということを実証している。その上、これらの結果は、単一の分子検出を得るのに標識づけが必要とされる一方で細胞を標識付け無しで画像形成することもできるということを実証している。
【0173】
自動化戦略
本発明は同様に、実験室用SEMの低い処理能力をも解決している。本発明は、生体サンプルのために、ウェーハ検査用に半導体業界向けに開発されたSEM自動化を利用している。ウェーハ検査用に開発されたSEM自動化を生物学において利用するというこの考えは、「生体分子の同定および定量化方法およびそのための器具」という題の同時係属PCT出願(PCT/IL01/00764)の中で詳細に記述されている。そこでは、サンプルは乾燥しており、ウェーハ検査走査型電子顕微鏡(WISEM)又はWISEM様の顕微鏡の直接的使用を可能にしている。この考え方は、WISEMを含めた従来の電子顕微鏡の真空必要条件との相容性をもつようにサンプルを調製するためには、自動化の実行可能性を妨げる徹底的かつ複雑な段階が課せられることから、天然の水性環境内で得られた生体サンプルには適用できなかった。本発明は、これらの問題のサンプル調製段階を必要とすることなく、水性サンプルの画像形成を可能にし、かくして、ウェーハ検査用に半導体業界向けに開発されたSEM自動化を生物学で利用することを可能にしている。この利用により、該方法を実施するのに必要とされる計装コストが大幅に削減されることになる。
【0174】
自動化戦略は、WETSEM技術での生きた細胞の自動化された画像形成において使用すべき手順を記述する一組の指針である。本発明の好ましい態様においては、自動化手順には、湿潤SEM画像形成のために調製された1つのサンプルを各々が収納している多数の隔離されたチャンバを収納する「セルチップ」が内含される。かかる小分割(隔離されたチャンバ)は各々、上で細胞サンプル(同一の又は異なるものであってよい)が成長させられる仕切り膜を収納している。
【0175】
サンプルの調製においては、標準の自動化された流体制御を使用することができる。
【0176】
画像形成のためのセルチップの準備がひとたび完了した時点で、これをSEM内に一体化された標準光学顕微鏡検査又は光ファイバなどのような特殊なセットアップを用いて自動化された光学画像形成(又は代替的には低倍率SEM走査)へともっていくことができる。この走査は、各チャンバ内の細胞の全体像、それらの位置および実験のための他のあらゆる関連情報を提供することになる。この走査における細胞に関する情報は、特定的に開発されたアルゴリズムを用いて自動的に検出されることになる。
【0177】
仕切り膜は、機械的安定性のため、金属格子上に取付けられる。この格子は、各々全ての画像の座標のための便利できわめて安定した基準を提供する。
【0178】
光学的走査がSEMの外側で実施される場合、セルチップは、SEMart画像形成のためSEMチャンバに移送される。光学顕微鏡およびSEMの座標間の整合を行なうため、アラインメントアルゴリズムが使用されることになる。
【0179】
これら2つの座標系がひとたび整合されると、SEMは光学走査(又は低倍率SEM走査)から自動的に選択された問題の特定的領域(ROI)の画像を形成する。かかるROIには、重要な生物活性が発生する細胞内の特定の領域、又は、その細胞内の特定の亜局在化に関係する領域、又は、細胞内のその他の領域の統計的表示を提供する領域が含まれる可能性がある。金コロイドは、各々のこのような領域の中で画像を形成すべきである。
【0180】
かかるROIは、異なるサイズを有する可能性があり、従ってSEMの異なる倍率を必要とする。画像形成された視野と観察できる標識づけのサイズの間にはトレードオフが存在するという点を留意されたい。従って、異なる視野で画像形成するためには、異なるサイズの標識付けが必要となる。特定的には、単細胞全体の画像のためには、大きな視野が必要とされる。かかる大きな視野は、低い倍率および走査の解像度に応じて大きな金コロイドのみを観察する能力を意味している。代替的には、より高い倍率で撮られた数多くの小視野画像を組合わせて、細胞全体の高解像度ピクチャを提供することもできる。
【0181】
SEM画像は自動的に撮られる。これには、SEM載物台の自動化された位置づけ、自動焦点および非点収差補正、自動化された輝度およびコントラストが含まれる。
【0182】
SEMにより撮られた画像は、画像分析アルゴリズムを用いて自動的に分析可能である。これには、観察された金コロイドの位置およびサイズの識別、計数および比較が含まれる。
【0183】
その他の信号も同様に、SEM撮像において測定可能である。これらには、(以下で例示されているような)陰極発光マーカーからの信号又は、サンプルの分析化学分析を提供できるサンプルからのX線放出が含まれる。
【0184】
1つのセルチップをSEMで走査する一方でもう1つのセルチップを光学的に走査することができる。
【0185】
SEM内での非常に高い解像度の光学画像形成
非常に興味深い1つのオプションは、サンプル中の光放出を励起するべく狭い電子ビームを使用することにある。かかる光放出は、陰極発光(CL)と呼ばれ、過去においては、脱水されたサンプルに対して研究されてきた(Hough PVC,SEMI 257,1977で再考されている)。これは、光学顕微鏡検査での理論的限界よりもはるかに優れた解像度での光放出の検出を可能にすることになる。この解決法は、SEM画像形成の高い解像度として良く知られている螢光標識付けを組合せている。このオプションは、SEM内で湿潤および生きたサンプルが画像形成される場合に非常に有利である。この画像形成システムにおいては、電子ビームは、それ自体可視光を放出するCL(螢光)標識づけ分子を励起する2次電子(SE)を生成する。この放出された光は、次の通常の電子検出とは別の収集経路内で収集される。2次電子による励起は、広帯域UV放射線と等価であることが示される可能性がある(Hough PVC、SEMI,257 1977参照)。この方法には数多くの利点がある:すなわち
1.螢光および金標識づけの組合せは、生物学的利点を数多く有している。
2.標識づけされた分子の高解像度画像形成を得ることにより、新しい重要な生物学的情報を提供することが可能である。
3.単光子検出は管理が容易で、放出された光子のかなり大きな割合が確実に回収される。
4.DNAコードされた螢光タンパク質が利用できることで、電子顕微鏡検査のための新しい標識づけの機会が開かれる。
5.この技術では、量子ドットおよび螢光ビーズといったような独特のプローブをマーカーとして使用することができ、その他の技術においては達成できない汎用性および利点が提供される。
【0186】
湿潤CL器具の態様は、既存のCL検出器に基づいていてもよいし、新規の収集幾何形状および構成の開発がこれに関与していてもよい。既存の検出器は、例えば、上部半平面(サンプルより上)から光を収集するものである。この鏡構成では、楕円形の鏡がサンプルより上に設置され、電子ビームの通過を可能にするためその中に小さい穴が備わっている。光は、鏡により収集され、光子検出器がその向こうにある顕微鏡の中のウィンドウに向かって導かれる。このような収集構成は、例えばGatan(前Oxford Instruments)から市販されている。以下では、光子がサンプルの下で収集され光導体により顕微鏡の外側の検出器まで導かれる。下半分平面内での収集のための2つの構成例について説明する。
【0187】
器具は以下のように作られる:すなわち、(ステンレス鋼で作られた)サンプルチャンバは、膜がレンズの焦平面に位置づけされるような形で、上部部分では仕切り膜により、又下部部分では小さなレンズにより閉鎖されている。かくして、膜の近くで放出されたレンズにより収集された光は、レンズから離れるときに視準された状態で出てくる。サンプルチャンバは、載物台の内側に置かれ、ここでプリズムが90度で(すなわち水平に)レンズから出てくる光を再度方向づけする。
【0188】
載物台は同様に、光ファイバの入口で光を再度集束するのに用いられるレンズを収納している。光ファイバは、載物台から顕微鏡の外側にある検出器まで至る。使用される検出器は、単光子モジュール検出システムである。検出された各光子について、出力信号はTTL信号である(0〜5Vの方形信号)。
【0189】
検出器の出力端はコンピュータカードに接続され、このコンピュータカードが受信したTTL信号(光子)の数を計数する。コンピュータカードは同様に、顕微鏡からいくつかの信号、すなわち画像獲得開始、新フレームの開始、新しいラインの開始、といったような信号を受信する。特別に設計された適切なソフトウェアを用いて、画像は、収集されたデータから実時間で再構築される。
【0190】
図6は、異なる構成要素部品A−Eが合わせて組立てられた状態のサンプルチャンバを示している。個々の部品については図7A−Eに詳しく描かれている。
【0191】
螢光実験用セットアップを組立てる
図7(A−E)は、螢光実験のために用いられるアセンブリの第1の態様を示している。
【0192】
側面に直径数ミリメートルの穴(図示せず)を含む部品Aがテーブル上に上下逆さまにして置かれている。部品Bは、部品AとBのネジ穴を整列させるべく注意しながら内側に置かれる。2つのOリングが部品B内に挿入される。膜は、所定の場所に置かれている。膜は、厚み0.1mmのプラスチック製支持体上にとりつけられる。プラスチック製支持体の直径は、使用されるOリングの2つの直径の間で選択されなくてはならない。直径3mmの穴は、プラスチック製支持体の中央に予め予備成形されており、これは、膜の無い領域である。TEM格子は膜の片面(外側面)の中央に貼りつけられている。次に、部品Cが挿入される。水平導管が、部品Aの側面穴と整列させられていることが重要である。6本のネジが挿入される。膜、部品A,BおよびCは、合わせてネジ留めされる。このときサンプルは、いつでも水又はその他のあらゆる水性媒質が満たされてよい状態となる。液体媒質は、部品Cの中央にある自由空間の内部に、(それがなおも上下逆さまである状態で)入れられる。部品AおよびCの側面上に設けられた穴を通して、細いピン(直径0.1mm)が挿入される。ピンは、その端部が湿潤チャンバに到達するまで、内側に深く挿入される。ピンのもう1方の端部は、外側に進む。最後のOリングは部品C内でその場所に置かれる(この段階で、ピンがそこのちょうど下にあることから、Oリングは完全に所定の場所に設置され得ない。これは正常であり、後続する段階にとって有用なことである)。(中央に光を視準させるためのレンズ(図示せず)を収納している)部品Dが、アセンブリの中に置かれる。レンズの内側は、チャンバを満たす媒質によって湿っている。最終的に部品Eが挿入される。部品Eをアセンブリ内部で回すと、部品D(レンズ付き)は漸進的にOリング(部品Cの)上にプレスされる。Oリングはピンのために完全に所定の場所にないことから、それはなおチャンバを外部から隔離しない。部品Eをネジ込むと、湿潤チャンバの体積は減少し、かくして余剰の媒質は、ピンに近いところでOリングの下を流出することができる。通常は、部品C内の流路から、幾分かの液滴が流出する。Oリングが充分にプレスされレンズが正しく設置された時点で、ピンはゆっくりと引き抜かれる。組立てのこの段階で、部品B内のOリングは、自由に全ての空間を占有することができる。Oリングは、チャンバを密封するその自然の位置に入る。かくして、チャンバは、最終的にその段階で完全に密封される。このアセンブリ(部品A〜E)はこのときその正常位置(上面が上)に回転され、専用に設計された顕微鏡の載物台の内側に挿入される。
【0193】
図8は、アセンブリと共に使用するのに適した顕微鏡の載物台を示している。載物台(2)の上面キャビティは、サンプルチャンバが挿入されるリセスである。そのすぐ下にはプリズムがある。プリズム(1)は、穴の方向に光を再度導くために使用される。この穴の中で、レンズ(図示せず)が、光ファイバの入口で光を集束する。
【0194】
光の収集効率をより良くするために、生体サンプルと光導体の間の直接的カップリングが樹立される代替的なセットアップが設計された。この代替的セットアップは、図9に示されている。それは、光が直接サンプル領域から上述の単光子検出器セットアップまで進む、真空気密チャンバを収納している。この図面では、ハウジング(I)が、ネジ(6,7)を用いて支持体(2)およびカバー(3)に取付けられ、内部には、Oリング(8)で密封された光導体(5)に更に連結された膜(9)を伴うキャビティディスク(4)が位置づけされている。
【0195】
標識づけ技術
本発明は、1つの細胞の細胞内又は細胞外部分のいずれかにおいて細胞成分を画像形成するのに適している。
【0196】
細胞の細胞内部分を標識づけするのに異なるアプローチを考慮することができる。
【0197】
細胞を定着後に使用できる場合、一般的方法には、細胞膜の易透化又はその抽出が関与する。
【0198】
生きた細胞に適した1つの代替的方法は、飲作用反応を通してマーカーを挿入することである。細胞をその後定着させるか生きている間に観察することができる。飲作用反応は、適切な条件下で行なわれた場合、細胞の生存可能性を保存する。それは、分子(当該技術分野における既知の応用の大部分において螢光マーカー)又は(本出願にとって特に適しているような)ナノ規模の粒子を挿入することを可能にする。一部の研究者は、細胞内部にμm(ミクロン)規模でビーズを導入する上での成功も報告している。
【0199】
易透化および抽出の手順は、定着された細胞に適している。作業者が細胞膜を完全に除去したいのかそれとも幾分かの間隙を作り出したいだけなのかに応じて、いくつかの手順を採用することができる。
【0200】
抽出および定着は、細胞の外部膜がまず最初に完全に除去されることを意味する。そのとき、すぐ後で、細胞は定着される。この種の手順は、細胞質、核又は細胞骨格の中の構造を視覚化するために優れている。
【0201】
定着および易透化は、細胞がまず最初に定着され更に細胞膜が易透化されることを意味する。
【0202】
飲作用反応は、生きた細胞のために適している。例えば、市販のInflux(細胞内部に粒子を導入するためのMolecular Probe I−14402)といったような作用物質を使用することができる。Influx細胞投入技術は、飲小胞の浸透圧溶解に基づいている。簡単に言うと、投入すべき化合物を、高張媒質と高濃度で混合し、飲小胞を介して細胞内に材料を運び込むことを可能にする。次に、細胞は低張媒質に移送され、その結果、細胞内の飲小胞から捕獲された材料が放出され、細胞質ゾルを化合物で満たすことになる。
【0203】
Molecular Probeにより与えられたプロトコルに従って、我々は、細胞内部に、Colloidal Gold、100ナノメートルサイズの金粒子、μm(ミクロン)規模の螢光ビーズおよび量子ドットを導入した。細胞を定着し、観察に先立ち金又は銀を増強させることができる。この方法を用いる場合、或る程度の百分率で細胞が死滅する。実施された実験の大部分において、10〜20%未満の細胞が失なわれた。
【0204】
生きた細胞の細胞表面を、細胞に対する損傷が低い状態で、金粒子で標識づけすることができる。本発明と合わせて使用するために開発されたプロトコル例では、当該技術分野において既知であるように、ストレプトアビジン−ビチオン標識づけ方法が利用される。考え方は、細胞表面上の一定の百分率のタンパク質に付着することになるビチオンと共に細胞をインキュベートするというものである。このとき、細胞は、ビチオンに付着することになる金粒子にリンクされたストレプトアビジンとインキュベートされる。インキュベーションのためのビオチンの用量は、膜タンパク質上の過度に多くのビチオンがその活性を混乱させ細胞死を誘発し得ることから、入念に制御されなくてはならない。異なる研究から、ビチオンを細胞トラッキングの応用分野のために使用することができる、ということが示された。複数の研究が、赤血球を扱った(例えばHoffmann-Fezerら、Annals of Hematology、74,231−238,1997;Ault、K.A. and C. Knowles、 Exp Hematology、23,996−1001,1995,およびその中の参考文献)。ビチオンは、その生物学にほとんど又は全く変化をもたらすことなく、数多くの細胞を標識づけし、必要とあらばそれらの検出および回収の両方を可能にする。
【0205】
マイクロカラム。処理能力を増大させることになるさらなる開発が、マイクロカラムでの並行検査である。そのサイズのため、マイクロカラムは、並行して作動することができ、走査時間およびSEMをベースとするシステムのかさ高さを著しく削減する。マイクロカラムのさらなる詳細は、その内容が、あたかも本書で完全に開示されているかのように参考として本書に内含されている、FeinermanおよびCrewe「小型電子光学」、Advances in Imaging and Electron Physics、第102巻、187(1998)ならびに米国特許第5,122,663号の中で提供されている。マイクロカラムベースの電子顕微鏡を生物学的応用分野で利用するという考え方は、「生体分子の同定および定量化方法およびそのための器具」という題の同時係属PCT出願の中で詳細に記述されている(PCT/IL01/00764)。
【0206】
本発明の原理についての以下の例は、単に、制限的な意味のないものとしてみなされるよう意図された、単に例示を目的として提供されるものである。
例
仕切り膜上で細胞を成長させる
以下に記すのは、非制限的な例として提供される、膜上で細胞を成長させるための手順例である。ポリイミド仕切り膜をまず最初に、15分間フィブロネクチン(0.1mg/ml)でコーティングする。PBSおよび培地で洗浄した後、チャンバ1個あたり12〜15μl中800〜1500個の細胞という濃度で、通常のやり方で細胞を平板固定する。24時間後に、細胞はいつでも操作/標識づけできる状態となる。大部分の細胞型は、付加的な基質様のフィブロネクチンの支持無しで、ただし大規模な洗浄手順中により洗い出される確率が更に高くなるような条件下で、仕切り膜自体の上で成長することができる。細胞の生存可能性は、これらの手順のいずれによっても影響されない。
【0207】
本発明は、粘着および非粘着細胞の両方と相容性がある(以下で例示される通り)。非粘着細胞(例えばリンパ球)を画像形成する目的で、まず最初に細胞を懸濁状態で標識づけし、その後、1〜3時間0.4%のポリリシンで前処理された仕切り膜上に、30分間粘着させる。
放射線損傷を最小限におさえる
現在、我々は、短時間規模(秒)でのみ、混乱を受けていないプロセスの画像動力学を例示している。注意する必要のある一種の放射線損傷は、水分子を打撃する電子ビームにより形成された遊離ラジカルによって生成される損傷である。
【0208】
かかる損傷に対する考えられる1つの戦略は、放射線によって生成される遊離ラジカルを吸収し、かくして細胞に対する放射線の損傷を最小限におさえると思われる添加剤を細胞の媒質に内含させることである。細胞にとって非毒性であるかぎり、ラジカルスカベンジングに適した既知のあらゆる化合物を使用することが可能である。かかる添加物の1つの候補例は、遊離ラジカル吸収物質として同定されてきたスクロースである。従来の電子ビーム技術が湿潤環境内で機能しないことから、この解決法は、本発明の場合にのみ可能である。
【0209】
免疫標識づけによる細胞の標識づけ
細胞の標識づけは、普通の免疫標識づけ手順によって行なわれる。細胞を洗浄し、任意には7分間2%のパラホルムアルデヒドによって定着させた。適切な血清での遮断の後、細胞を1時間特異的モノ又はポリクロナール抗体と共にインキュベートした。洗浄後、第1の特異的抗体を認識する第2の抗体と共にサンプルをインキュベートする。この第2の抗体は、5,10,20又は40nmの金クラスタにリンクされる。このとき、各コロイドについて入念に較正した条件を用いて、銀増強により、金標識づけを更に増幅させることができる。
【0210】
仕切り膜下の定着させられた湿潤細胞
定着させたA431細胞およびC2C12マウス筋芽細胞上で標識づけされた成長因子レセプタ
2%のパラホルムアルデヒドで細胞を定着させ、抗FGFレセプタモノクローナル抗体(C2C12筋芽細胞上)又は抗−EGFモノクローナル抗体(A431細胞)とそれに続く直径20nmの金コロイドにリンクされた抗マウスIgGで標識づけした。細胞を定着させ、標識づけ粒子のサイズを増大させるために銀増強を用いた。画像形成のためにXL30ESEMを用い、細胞を後方散乱電子(BSE)モードで検査した。FGFレセプタ金標識づけは、図10Aに示されている両方の細胞上で明るいスポットとして見ることができる。EGFレセプタは、図10B−DのA431細胞上で目に見える。核部域のまわりの標識づけの不鮮明さは、金粒子間のトポグラフィ差の結果である。仕切り膜に近い金標識づけは、明確でピントが合っているが、核を超えたおよび核のまわりのより遠位の標識づけは不鮮明である。核の領域内の標識の不鮮明さは、この領域内の標識が仕切り膜から更に離れているという事実の証拠である。この不鮮明さは実際、仕切り膜の平面からの標識の距離の決定用の手段を提供し、かくして三次元情報を提供する。仕切り膜と標識の間の付加的な媒質の効果を逆重畳する能力をもつ画像分析アルゴリズムを用いること、この距離のかなり精確な推定が提供できる。
【0211】
細胞(膜下層に付着された側とは反対にある)の遠位側で標識のより高い解像度を達成するために、もう1つのチャンバ設計を適用することができる。このような設計においては、細胞は、薄い液体層のみがそれらをカバーしている状態で、平らな基盤上で成長させられる。その後、細胞をカバーするこの基盤の上面に仕切り膜が設置される。このようにして、細胞の上面側が画像形成され、細胞はなお湿潤環境内にある。
【0212】
膜の下の生きた標識付けされていない粘着細胞
生きたC2C12マウス筋芽細胞
その通常の培地内でフィブロネクチン上に平板固定した。24時間後に、BSEモードで細胞を検査した。生きたC2C12細胞(図11A−D)およびCHO細胞(図12)は、細胞およびその核ならびにいくつかの核下オルガネラの輪郭を明確に示している。
【0213】
ジャーカットヒトリンパ球上でアルファ標識づけされたIL−2レセプタ
抗ヒトIL−2レセプタモノクローナル抗体およびそれに続く直径20nmの金コロイドにリンクされた抗マウスIgGで、細胞を標識づけした。30分間、ポリリシンで予備コーティングされた仕切り膜上に細胞を粘着させ、その後BSEモードで検査した。図13は、定着させたC2C12のFGFレセプタ標識づけ(図10A)およびA431細胞のEGFレセプタ標識づけ(図10B−D)において以前に見られた通りの金粒子の間のトポグラフィ差の結果としてもたらされるピントの合ったおよびピント外れの金標識づけを示している。
【0214】
この陰極発光(CL)セットアップで撮影された画像
信号がかなり微弱でも(おそらくは、集光効率が低いことに起因して)、細胞は明確に観察される。細胞は、CLマーカー無しでも観察される(すなわち、細胞の幾分かの部分は内部発光をもつ)。CLマーカーを用い、収集効率が改善された場合、はるかに高い解像度が予想される。
【0215】
定着された細胞NIH3T3の陰極発光画像
細胞内にはいかなる発光マーカーも挿入されなかった。従って、放出された光は、図14A−Cに示されているように、細胞の「自然の」陰極発光の結果である。細胞の幅は約20μm(ミクロン)である。
【0216】
NTH3T3細胞上でのビオチンベースの標識づけ
材料:
スルフォ−NHS−LCビオチン(SigmaB1022)(DMSO中に10mg/mg溶解させ4℃に保つ)。
【0217】
直径10mmから40nmの金粒子にリンクされたストレプトアビジン
37℃で予め温められたリン酸緩衝溶液(PBS)(その細胞系統のための培養温度で予め温められた)細胞系統用培地。
【0218】
予め温められた血清を含まない培地。
【0219】
調製すべき溶液:
溶液A: 予め温めたPBS中の0.5mg/mlのスルフォ−NHS−LC−ビオチン。水中で分解が発生することから使用直前に溶液を作らなくてはならない。
【0220】
溶液B: PBS中に溶解させたストレプトアビジン金(1/10〜1/100)+血清を含まない培地(1対5の体積比)。
【0221】
溶液C: 完全培地−PBS溶液(1対5の体積比)。
【0222】
手順:
1.細胞のトリプシン処理
2.4分間1250回転/分での遠心分離
3.上清を除去し、10mlの新鮮培地内で再懸濁させる。
4.1.5ml入りのエッペンドルフ管2本に分けて3mlを取る。
5.3分間1600回転/分で遠心分離する。
6.上清を可能なかぎり多く除去する。
7.管の中に1.5mlとなるよう37度のPBSを穏やかに添加する(洗浄)。細胞を再懸濁させる。
8.3分間再び遠心分離する。
9.PBSを除去し、ビオチン(溶液A)を添加する。細胞を再度懸濁させ、充分にただし穏やかに混合する。
10.20分間37度でインキュベートする(3分毎に撹拌する)。
11.遠心分離する。
12.上清を除去し、1.5mlの新鮮培地中で再懸濁させる。
13.ペトリ皿又は膜に移し、数時間〜一晩インキュベートさせる。
14.PBSで1〜2回洗浄する。
15.1時間溶液Bを用いてインキュベートし、可能ならば時々混ぜる。
16.PBSで1〜2回洗う。
17.PBSを除去し溶液Cと交換する。
18.電子顕微鏡内での観察にとりかかる。
【0223】
生きたNIHT3細胞。細胞表面タンパク質をビオチニル化し、図15に示されているように40nmの金粒子に付着させたストレプトアビジンにリンクさせた。
【0224】
当業者であれば、本発明が以上で特定的に示し記述したものに制限されるものではないということがわかるだろう。むしろ、本発明の範囲は、上述のさまざまな特長のコンビネーションおよびサブコンビネーションの両方ならびに、以上の説明を読んだ時点で当業者が思いつき先行技術には無いその変形形態および修正を内含するものである。
【図面の簡単な説明】
【図1】 図1は、先行技術の走査型電子顕微鏡のサンプル部域の縦断面を示す一般化されたダイヤグラムである。
【図2】 図2は、本発明の1態様に従ったチャンバを内蔵する走査型電子顕微鏡の縦断面である。
【図3】 図3は、本発明の1態様に従ったチャンバの一般化された断面図である。
【図4】 図4は、光導体内に埋込まれた本発明のもう1つの態様に従ったチャンバの一般化された断面図である。
【図5】 図5は、図3の態様を用いて撮られた電子顕微鏡写真である。
【図6】 図6は、螢光用の組立てられたサンプルチャンバユニットのダイヤグラムである。
【図7】 図7A−Eは、図6のチャンバの構成要素A−Eのダイヤグラムである。
【図7A】 図7Aは、図6のチャンバの構成要素Aのダイヤグラムである。
【図7B】 図7Bは、図6のチャンバの構成要素Bのダイヤグラムである。
【図7C】 図7Cは、図6のチャンバの構成要素Cのダイヤグラムである。
【図7D】 図7Dは、図6のチャンバの構成要素Dのダイヤグラムである。
【図7E】 図7Eは、図6のチャンバの構成要素Eのダイヤグラムである。
【図8A】 図8Aは、チャンバと共に使用するための顕微鏡載物台アダプタのダイヤグラムである。
【図8B】 図8Bは、チャンバと共に使用するための顕微鏡載物台アダプタのダイヤグラムである。
【図9】 図9は、(電子)発光用の1変形態様のダイヤグラムである。
【図10A】 図10Aは、仕切り膜の下の定着された湿潤細胞の画像を示す。
【図10B】 図10Bは、仕切り膜の下の定着された湿潤細胞の画像を示す。
【図10C】 図10Cは、仕切り膜の下の定着された湿潤細胞の画像を示す。
【図10D】 図10Dは、仕切り膜の下の定着された湿潤細胞の画像を示す。
【図10E】 図10Eは、仕切り膜の下の定着された湿潤細胞の画像を示す。
【図11A】 図11Aは、膜の下の生きた標識付けの無い粘着細胞の画像である。
【図11B】 図11Bは、膜の下の生きた標識付けの無い粘着細胞の画像である。
【図11C】 図11Cは、膜の下の生きた標識付けの無い粘着細胞の画像である。
【図11D】 図11Dは、膜の下の生きた標識付けの無い粘着細胞の画像である。
【図12】 図12は、膜の下のまだ標識付けされていないインタクトのCHO細胞の画像である。
【図13】 図13は、膜の下の生きた非粘着細胞の画像である。
【図14A】 図14Aは、定着されたNIH3T3細胞の陰極発光画像である。
【図14B】 図14Bは、定着されたNIH3T3細胞の陰極発光画像である。
【図14C】 図14Cは、定着されたNIH3T3細胞の陰極発光画像である。
【図15】 図15は、インタクトのNIH3T3細胞の画像である。
Claims (6)
- −閉鎖された試料設置体積を画定する試料構造;
−前記試料設置体積の外側の体積から前記試料設置体積を密封する少なくとも電子ビーム透過性、流体不透過性かつ最高1気圧の圧力勾配に耐えることができる層、および
−前記閉鎖された試料設置体積内の1つの場所で電子と試料の相互作用から生成された光を収集するように作動する集光装置、を含む試料エンクロージャアセンブリ。 - 前記層が、ポリイミド、ポリアミド、ポリアミド−イミド、ポリエチレン、ポリピロール、パルロジオン、コロジオン,カプトン,フォームバー,ビニレック,ブトバー,およびピロフォームからなる群から選択された材料で形成されている、請求項1に記載の試料エンクロージャアセンブリ。
- 100μm(ミクロン)以上の少なくとも1つの寸法をもつ開口部を画定する、前記少なくとも1つの層用のアパーチャ付き機械的支持体をも含む、請求項1または2に記載の試料エンクロージャアセンブリ。
- 前記少なくとも1つの層が、少なくとも1気圧の圧力勾配までは流体不透過性である、請求項1〜3のいずれか1項に記載の試料エンクロージャアセンブリ。
- 前記層が、2−30KeVの範囲内のエネルギーをもつ電子に対する透過性をもつ、請求項1〜4のいずれか1項に記載の試料エンクロージャアセンブリ。
- 前記閉鎖された試料設置体積と連絡する圧力除去装置をも含む、請求項1〜5のいずれか1項に記載の試料エンクロージャアセンブリ。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US25087900P | 2000-12-01 | 2000-12-01 | |
| US30645801P | 2001-07-20 | 2001-07-20 | |
| PCT/IL2001/001108 WO2002045125A1 (en) | 2000-12-01 | 2001-11-30 | Device and method for the examination of samples in a non-vacuum environment using a scanning electron microscope |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2008097275A Division JP2008171830A (ja) | 2000-12-01 | 2008-04-03 | 走査型電子顕微鏡を用いた非真空環境内のサンプルの検査のための装置および方法 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2004515049A JP2004515049A (ja) | 2004-05-20 |
| JP2004515049A5 JP2004515049A5 (ja) | 2005-12-22 |
| JP4153303B2 true JP4153303B2 (ja) | 2008-09-24 |
Family
ID=26941209
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2002547196A Expired - Fee Related JP4153303B2 (ja) | 2000-12-01 | 2001-11-30 | 走査型電子顕微鏡を用いた非真空環境内のサンプルの検査のための装置および方法 |
| JP2008097275A Pending JP2008171830A (ja) | 2000-12-01 | 2008-04-03 | 走査型電子顕微鏡を用いた非真空環境内のサンプルの検査のための装置および方法 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2008097275A Pending JP2008171830A (ja) | 2000-12-01 | 2008-04-03 | 走査型電子顕微鏡を用いた非真空環境内のサンプルの検査のための装置および方法 |
Country Status (10)
| Country | Link |
|---|---|
| US (3) | US6992300B2 (ja) |
| EP (1) | EP1340241B1 (ja) |
| JP (2) | JP4153303B2 (ja) |
| CN (1) | CN1511332A (ja) |
| AT (1) | ATE510298T1 (ja) |
| AU (2) | AU2002221019B2 (ja) |
| CA (1) | CA2436237A1 (ja) |
| CZ (1) | CZ20031455A3 (ja) |
| IL (1) | IL156027A0 (ja) |
| WO (1) | WO2002045125A1 (ja) |
Families Citing this family (141)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB2367686B (en) * | 2000-08-10 | 2002-12-11 | Leo Electron Microscopy Ltd | Improvements in or relating to particle detectors |
| AU2003231893A1 (en) | 2002-06-05 | 2003-12-22 | Quantomix Ltd. | A sample enclosure for a scanning electron microscope and methods of use thereof |
| IL150056A0 (en) * | 2002-06-05 | 2002-12-01 | Yeda Res & Dev | Low-pressure chamber for scanning electron microscopy in a wet environment |
| US11243494B2 (en) | 2002-07-31 | 2022-02-08 | Abs Global, Inc. | Multiple laminar flow-based particle and cellular separation with laser steering |
| US20070125947A1 (en) * | 2003-02-20 | 2007-06-07 | David Sprinzak | Sample enclosure for a scanning electron microscope and methods of use thereof |
| US20050017173A1 (en) * | 2003-07-15 | 2005-01-27 | Nalin Kumar | Individually addressable nanoelectrode array |
| US7274447B2 (en) * | 2004-06-21 | 2007-09-25 | Swce | Material porosity pressure impulse testing system |
| US20060144778A1 (en) * | 2004-07-29 | 2006-07-06 | Grunthaner Frank J | Low stress, ultra-thin, uniform membrane, methods of fabricating same and incorporation into detection devices |
| US7626179B2 (en) * | 2005-09-30 | 2009-12-01 | Virgin Island Microsystems, Inc. | Electron beam induced resonance |
| US7791290B2 (en) | 2005-09-30 | 2010-09-07 | Virgin Islands Microsystems, Inc. | Ultra-small resonating charged particle beam modulator |
| US7586097B2 (en) | 2006-01-05 | 2009-09-08 | Virgin Islands Microsystems, Inc. | Switching micro-resonant structures using at least one director |
| EP1794772A2 (en) * | 2004-08-26 | 2007-06-13 | Quantomix Ltd. | Sample enclosure for inspection and methods of use thereof |
| NL1027025C2 (nl) | 2004-09-13 | 2006-03-14 | Univ Delft Tech | Microreactor voor een transmissie elektronenmicroscoop en verwarmingselement en werkwijze voor vervaardiging daarvan. |
| US7381970B2 (en) * | 2005-01-31 | 2008-06-03 | Summer Schneider | Specimen stage for charged-particle scanning microscopy |
| US20060172315A1 (en) * | 2005-02-01 | 2006-08-03 | Anderson Amy L | Methods for staining cells for identification and sorting |
| CN100511568C (zh) * | 2005-05-09 | 2009-07-08 | 东捷科技股份有限公司 | 在真空或低压环境中操作高压腔室且供观测的方法及装置 |
| TWI277734B (en) * | 2005-10-26 | 2007-04-01 | Li Bing Huan | Method for observing living bodies using an electron microscopy |
| TWI275118B (en) * | 2005-12-09 | 2007-03-01 | Li Bing Huan | Sample box of electron microscope for observing a general sample/live cell |
| JP2007163447A (ja) * | 2005-12-09 | 2007-06-28 | Lee Bing Huan | 電子顕微鏡用の超薄液体制御板 |
| EP1982346A4 (en) * | 2006-02-02 | 2014-05-07 | Cebt Co Ltd | DEVICE FOR MAINTAINING DIFFERENTIAL PRESSURE GRADES FOR AN ELECTRONIC COLUMN |
| US7443358B2 (en) | 2006-02-28 | 2008-10-28 | Virgin Island Microsystems, Inc. | Integrated filter in antenna-based detector |
| US7646991B2 (en) | 2006-04-26 | 2010-01-12 | Virgin Island Microsystems, Inc. | Selectable frequency EMR emitter |
| US7876793B2 (en) | 2006-04-26 | 2011-01-25 | Virgin Islands Microsystems, Inc. | Micro free electron laser (FEL) |
| JP2007294365A (ja) * | 2006-04-27 | 2007-11-08 | Jeol Ltd | 試料検査方法、試料保持体、及び試料検査装置並びに試料検査システム |
| JP2007292702A (ja) * | 2006-04-27 | 2007-11-08 | Jeol Ltd | 試料検査装置及び試料検査方法並びに試料検査システム |
| US7728702B2 (en) | 2006-05-05 | 2010-06-01 | Virgin Islands Microsystems, Inc. | Shielding of integrated circuit package with high-permeability magnetic material |
| US7718977B2 (en) | 2006-05-05 | 2010-05-18 | Virgin Island Microsystems, Inc. | Stray charged particle removal device |
| US8188431B2 (en) | 2006-05-05 | 2012-05-29 | Jonathan Gorrell | Integration of vacuum microelectronic device with integrated circuit |
| US7436177B2 (en) * | 2006-05-05 | 2008-10-14 | Virgin Islands Microsystems, Inc. | SEM test apparatus |
| US7732786B2 (en) | 2006-05-05 | 2010-06-08 | Virgin Islands Microsystems, Inc. | Coupling energy in a plasmon wave to an electron beam |
| US7359589B2 (en) | 2006-05-05 | 2008-04-15 | Virgin Islands Microsystems, Inc. | Coupling electromagnetic wave through microcircuit |
| US7656094B2 (en) * | 2006-05-05 | 2010-02-02 | Virgin Islands Microsystems, Inc. | Electron accelerator for ultra-small resonant structures |
| US7746532B2 (en) | 2006-05-05 | 2010-06-29 | Virgin Island Microsystems, Inc. | Electro-optical switching system and method |
| US7728397B2 (en) | 2006-05-05 | 2010-06-01 | Virgin Islands Microsystems, Inc. | Coupled nano-resonating energy emitting structures |
| US7710040B2 (en) | 2006-05-05 | 2010-05-04 | Virgin Islands Microsystems, Inc. | Single layer construction for ultra small devices |
| US7723698B2 (en) | 2006-05-05 | 2010-05-25 | Virgin Islands Microsystems, Inc. | Top metal layer shield for ultra-small resonant structures |
| US7986113B2 (en) | 2006-05-05 | 2011-07-26 | Virgin Islands Microsystems, Inc. | Selectable frequency light emitter |
| US7741934B2 (en) | 2006-05-05 | 2010-06-22 | Virgin Islands Microsystems, Inc. | Coupling a signal through a window |
| US7679067B2 (en) | 2006-05-26 | 2010-03-16 | Virgin Island Microsystems, Inc. | Receiver array using shared electron beam |
| US7655934B2 (en) | 2006-06-28 | 2010-02-02 | Virgin Island Microsystems, Inc. | Data on light bulb |
| JP5084188B2 (ja) * | 2006-07-04 | 2012-11-28 | 日本電子株式会社 | 試料保持体、試料検査方法及び試料検査装置並びに試料検査システム |
| US7450794B2 (en) | 2006-09-19 | 2008-11-11 | Virgin Islands Microsystems, Inc. | Microcircuit using electromagnetic wave routing |
| JP4850654B2 (ja) * | 2006-10-23 | 2012-01-11 | 株式会社日立ハイテクノロジーズ | 荷電粒子線装置および荷電粒子線装置用試料保持装置 |
| WO2008050321A2 (en) | 2006-10-24 | 2008-05-02 | B-Nano Ltd. | An interface, a methof for observing an object within a non-vacuum environment and a scanning electron microscope |
| JP5002251B2 (ja) | 2006-12-06 | 2012-08-15 | 日本電子株式会社 | 試料検査方法及び試料検査装置 |
| TWI330380B (en) * | 2006-12-07 | 2010-09-11 | Nat Univ Tsing Hua | A specimen kit for electron microscope and its fabrication process |
| JP2008153086A (ja) * | 2006-12-19 | 2008-07-03 | Jeol Ltd | 試料検査装置及び試料検査方法並びに試料検査システム |
| EP2365321B1 (en) | 2006-12-19 | 2013-10-02 | JEOL Ltd. | Sample inspection apparatus, sample inspection method, and sample inspection system |
| US7659513B2 (en) | 2006-12-20 | 2010-02-09 | Virgin Islands Microsystems, Inc. | Low terahertz source and detector |
| JP5318364B2 (ja) | 2007-01-31 | 2013-10-16 | 日本電子株式会社 | 試料保持体、試料検査装置及び試料検査方法、並びに試料保持体の製造方法 |
| EP1953793B1 (en) | 2007-01-31 | 2012-05-16 | JEOL Ltd. | Specimen holder, specimen inspection apparatus, specimen inspection method, and method of fabricating specimen holder |
| JP2008210715A (ja) * | 2007-02-27 | 2008-09-11 | Ebara Corp | 荷電粒子線装置及びこれを用いた試料表面観察方法 |
| EP2130086A4 (en) | 2007-03-02 | 2012-03-14 | Protochips Inc | MEMBRANE SUPPORTS WITH REINFORCING FUNCTIONS |
| US7990336B2 (en) | 2007-06-19 | 2011-08-02 | Virgin Islands Microsystems, Inc. | Microwave coupled excitation of solid state resonant arrays |
| US9134307B2 (en) | 2007-07-11 | 2015-09-15 | X-Body, Inc. | Method for determining ion channel modulating properties of a test reagent |
| WO2009009718A1 (en) | 2007-07-11 | 2009-01-15 | Sru Biosystems, Inc. | Methods of identifying modulators of ion channels |
| US7791053B2 (en) | 2007-10-10 | 2010-09-07 | Virgin Islands Microsystems, Inc. | Depressed anode with plasmon-enabled devices such as ultra-small resonant structures |
| EP2565900B1 (en) | 2007-11-13 | 2016-02-03 | Carl Zeiss Microscopy Limited | Beam device and system comprising a particle beam device and an optical microscope |
| JP5253800B2 (ja) * | 2007-12-26 | 2013-07-31 | 日本電子株式会社 | 試料保持体及び観察・検査方法並びに観察・検査装置 |
| JP5215701B2 (ja) | 2008-03-26 | 2013-06-19 | 日本電子株式会社 | 試料検査装置及び試料検査方法 |
| EP2105944A1 (en) * | 2008-03-28 | 2009-09-30 | FEI Company | Environmental cell for a particle-optical apparatus |
| JP5314317B2 (ja) * | 2008-04-08 | 2013-10-16 | 日本電子株式会社 | 検査方法及び試液 |
| JP2010002300A (ja) | 2008-06-20 | 2010-01-07 | Jeol Ltd | 試料保持体、試料検査装置及び試料検査方法 |
| WO2010001399A1 (en) * | 2008-07-03 | 2010-01-07 | B-Nano | A scanning electron microscope, an interface and a method for observing an object within a non-vacuum environment |
| US8981294B2 (en) | 2008-07-03 | 2015-03-17 | B-Nano Ltd. | Scanning electron microscope, an interface and a method for observing an object within a non-vacuum environment |
| JP2010027488A (ja) | 2008-07-23 | 2010-02-04 | Jeol Ltd | 試料保持体、試料検査装置及び試料検査方法 |
| US8492716B2 (en) * | 2008-09-28 | 2013-07-23 | B-Nano Ltd. | Vacuumed device and a scanning electron microscope |
| JP5205234B2 (ja) * | 2008-12-02 | 2013-06-05 | 株式会社日立ハイテクノロジーズ | 微小試料採取装置,検査解析システム、および検査解析方法 |
| US8059271B2 (en) | 2009-02-04 | 2011-11-15 | The United States Of America As Represented By The Secretary Of The Army | Reusable sample holding device permitting ready loading of very small wet samples |
| JP5124507B2 (ja) | 2009-02-16 | 2013-01-23 | 株式会社日立ハイテクノロジーズ | 電子線装置および電子線装置用試料保持装置 |
| JP2010230417A (ja) | 2009-03-26 | 2010-10-14 | Jeol Ltd | 試料の検査装置及び検査方法 |
| US8087309B2 (en) | 2009-05-22 | 2012-01-03 | Sion Power Corporation | Hermetic sample holder and method for performing microanalysis under controlled atmosphere environment |
| NL2004888A (en) * | 2009-06-29 | 2010-12-30 | Asml Netherlands Bv | Deposition method and apparatus. |
| CA2768873A1 (en) * | 2009-07-23 | 2011-01-27 | Insight Nanofluidics Inc. | Nanofluidic cell |
| DE112010005188B4 (de) * | 2010-01-27 | 2016-04-07 | Hitachi High-Technologies Corp. | Vorrichtung zum Bestrahlen mit geladenen Teilchen |
| JP2011243483A (ja) | 2010-05-20 | 2011-12-01 | Jeol Ltd | 試料保持体、検査装置、及び検査方法 |
| JP5065516B2 (ja) * | 2010-08-04 | 2012-11-07 | エフ イー アイ カンパニ | 薄い電子検出器における後方散乱の減少 |
| JP5218503B2 (ja) * | 2010-09-01 | 2013-06-26 | コニカミノルタビジネステクノロジーズ株式会社 | 光走査装置および画像形成装置 |
| WO2012041721A1 (en) | 2010-10-01 | 2012-04-05 | Attolight Sa | Deconvolution of time-gated cathodoluminescence images |
| US10908066B2 (en) | 2010-11-16 | 2021-02-02 | 1087 Systems, Inc. | Use of vibrational spectroscopy for microfluidic liquid measurement |
| US20120190137A1 (en) * | 2011-01-24 | 2012-07-26 | Sumitomo Electric Industries, Ltd. | Cross section observation method |
| US10505234B2 (en) | 2011-03-14 | 2019-12-10 | Battelle Memorial Institute | Battery cell and n situ battery electrode analysis method |
| US10598609B2 (en) * | 2011-03-14 | 2020-03-24 | Battelle Memorial Institute | Universal liquid sample device and process for high resolution transmission electron microscope imaging and multimodal analyses of liquid sample materials |
| US9274059B2 (en) | 2011-03-14 | 2016-03-01 | Battelle Memorial Institute | Microfluidic electrochemical device and process for chemical imaging and electrochemical analysis at the electrode-liquid interface in-situ |
| US8555710B2 (en) * | 2011-03-14 | 2013-10-15 | Battelle Memorial Institute | Systems and methods for analyzing liquids under vacuum |
| JP5699023B2 (ja) | 2011-04-11 | 2015-04-08 | 株式会社日立ハイテクノロジーズ | 荷電粒子線装置 |
| CN103493171B (zh) * | 2011-04-28 | 2016-02-17 | 株式会社日立高新技术 | 电子显微镜用试样保持装置以及电子显微镜装置 |
| EP3528276A3 (en) | 2011-05-13 | 2019-09-04 | Fibics Incorporated | Microscopy imaging method |
| EP2732299A4 (en) | 2011-07-15 | 2015-03-25 | Orbotech Ltd | ELECTRICAL TESTING OF ELECTRONIC DEVICES BY MEANS OF ELECTRON BEAM-INDUCED PLASMA STONES |
| EP2734836A4 (en) | 2011-07-21 | 2015-07-22 | Univ Columbia | METHOD OF COLLECTING AND PROCESSING ELECTRON DIFFACTION DATA |
| JP5896708B2 (ja) | 2011-12-06 | 2016-03-30 | 株式会社日立ハイテクノロジーズ | 走査イオン顕微鏡および二次粒子制御方法 |
| JP5115997B1 (ja) * | 2011-12-27 | 2013-01-09 | 独立行政法人産業技術総合研究所 | 走査型電子顕微鏡像観察用の試料支持部材及び走査型電子顕微鏡像の観察方法 |
| JP2013187096A (ja) * | 2012-03-09 | 2013-09-19 | Hitachi Ltd | 電子顕微鏡の液体試料ホルダ及びその製造方法 |
| US8809783B2 (en) * | 2012-06-19 | 2014-08-19 | Rensselaer Polytechnic Institute | High spatial resolution non-contact temperature measurement |
| JP6002946B2 (ja) | 2012-07-23 | 2016-10-05 | 国立研究開発法人産業技術総合研究所 | 試料ホルダおよび電子顕微鏡像の観察方法 |
| JP5936484B2 (ja) | 2012-08-20 | 2016-06-22 | 株式会社日立ハイテクノロジーズ | 荷電粒子線装置及び試料観察方法 |
| JP5923412B2 (ja) | 2012-08-24 | 2016-05-24 | 株式会社日立ハイテクノロジーズ | 観察装置および光軸調整方法 |
| JP5930922B2 (ja) | 2012-09-14 | 2016-06-08 | 株式会社日立ハイテクノロジーズ | 荷電粒子線装置及び試料観察方法 |
| JP6207824B2 (ja) | 2012-10-01 | 2017-10-04 | 株式会社日立ハイテクノロジーズ | 荷電粒子線装置、隔膜の位置調整方法および隔膜位置調整ジグ |
| JP6051014B2 (ja) | 2012-10-29 | 2016-12-21 | 株式会社日立ハイテクノロジーズ | 試料格納用容器、荷電粒子線装置、及び画像取得方法 |
| JP6035602B2 (ja) * | 2012-11-21 | 2016-11-30 | 株式会社日立ハイテクノロジーズ | 荷電粒子線装置、試料台ユニット、及び試料観察方法 |
| US8872105B2 (en) * | 2013-02-19 | 2014-10-28 | Fei Company | In situ reactivation of fluorescence marker |
| EP2959287A4 (en) | 2013-02-20 | 2016-10-19 | Nano Ltd B | scanning Electron Microscope |
| KR102026936B1 (ko) * | 2013-03-26 | 2019-10-01 | 삼성디스플레이 주식회사 | 주사 전자 현미경을 이용한 검사 시스템 |
| JP6112553B2 (ja) | 2013-04-08 | 2017-04-12 | 国立研究開発法人産業技術総合研究所 | 観察システム及び観察方法 |
| DE112014001109B4 (de) * | 2013-04-12 | 2019-11-14 | Hitachi High-Technologies Corporation | Mit einem Strahl geladener Teilchen arbeitende Vorrichtung und Filterelement |
| US8961904B2 (en) | 2013-07-16 | 2015-02-24 | Premium Genetics (Uk) Ltd. | Microfluidic chip |
| DE102013012609B4 (de) * | 2013-07-26 | 2024-06-27 | Carl Zeiss Microscopy Gmbh | Optoelektronischer Detektor, insbesondere für hochauflösende Lichtrastermikroskope und Lichtrastermikroskop |
| DE112014003268B4 (de) | 2013-08-23 | 2018-05-30 | Hitachi High-Technologies Corporation | Membrananbringungselement, mit einem strahl geladener teilchen arbeitende vorrichtung, system, membrananbringungsverfahren sowie verfahren zum inspizieren der qualität |
| US9741526B2 (en) | 2013-09-06 | 2017-08-22 | Hitachi High-Technologies Corporation | Charged particle beam apparatus and sample image acquiring method |
| JP6364167B2 (ja) * | 2013-09-30 | 2018-07-25 | 株式会社日立ハイテクノロジーズ | 環境制御型荷電粒子観察システム |
| USD794816S1 (en) * | 2013-10-24 | 2017-08-15 | Hitachi High-Technologies Corporation | Sample holder for an electron microscope |
| US11796449B2 (en) | 2013-10-30 | 2023-10-24 | Abs Global, Inc. | Microfluidic system and method with focused energy apparatus |
| US10410338B2 (en) * | 2013-11-04 | 2019-09-10 | Kla-Tencor Corporation | Method and system for correlating optical images with scanning electron microscopy images |
| US9997331B1 (en) | 2014-01-27 | 2018-06-12 | Mochii, Inc. | Charged-particle beam microscopy |
| JP6047508B2 (ja) | 2014-01-27 | 2016-12-21 | 株式会社日立ハイテクノロジーズ | 荷電粒子線装置、試料画像取得方法、およびプログラム記録媒体 |
| US9564291B1 (en) * | 2014-01-27 | 2017-02-07 | Mochii, Inc. | Hybrid charged-particle beam and light beam microscopy |
| US20160032281A1 (en) * | 2014-07-31 | 2016-02-04 | Fei Company | Functionalized grids for locating and imaging biological specimens and methods of using the same |
| GB2537579A (en) * | 2014-11-07 | 2016-10-26 | Linkam Scient Instr Ltd | Microscopic sample preparation |
| TWI546841B (zh) | 2014-12-10 | 2016-08-21 | 財團法人工業技術研究院 | 具有載台的電子顯微鏡 |
| WO2016132222A2 (en) | 2015-02-19 | 2016-08-25 | Premium Genetics (Uk) Ltd. | Scanning infrared measurement system |
| WO2017033219A1 (ja) | 2015-08-21 | 2017-03-02 | 株式会社 日立ハイテクノロジーズ | 荷電粒子顕微鏡の観察支援ユニットおよびこれを用いた試料観察方法 |
| TWI597481B (zh) * | 2015-12-22 | 2017-09-01 | 閤康生物科技股份有限公司 | 樣本收集元件及其製作方法 |
| TWI594288B (zh) * | 2016-03-14 | 2017-08-01 | 台灣電鏡儀器股份有限公司 | 電子顯微鏡 |
| CN106525845B (zh) * | 2016-10-11 | 2023-11-03 | 聚束科技(北京)有限公司 | 一种带电粒子束系统、光电联合探测系统及方法 |
| CN106783493B (zh) * | 2016-12-01 | 2018-07-10 | 聚束科技(北京)有限公司 | 一种真空气氛处理装置、样品观测系统及方法 |
| US11051390B2 (en) * | 2017-03-22 | 2021-06-29 | Japan Atomic Energy Agency | Functional membrane for ion beam transmission, beam line device and filter device each having the same, and method of adjusting filter device |
| WO2019226790A1 (en) | 2018-05-23 | 2019-11-28 | Abs Global, Inc. | Systems and methods for particle focusing in microchannels |
| CN109187595B (zh) * | 2018-09-27 | 2021-05-11 | 南京宁智高新材料研究院有限公司 | 一种测量透射电镜中微气体束引起的局部等效压强的装置 |
| JP7189529B2 (ja) * | 2018-10-15 | 2022-12-14 | 国立大学法人 筑波大学 | 環境セルとその製造方法 |
| US11538659B2 (en) * | 2018-10-25 | 2022-12-27 | Hitachi High-Tech Corporation | Charged particle beam device, autofocus processing method of charged particle beam device, and detector |
| US10777379B1 (en) * | 2019-03-19 | 2020-09-15 | Hitachi High-Tech Corporation | Holder and charged particle beam apparatus |
| KR102198707B1 (ko) * | 2019-03-25 | 2021-01-05 | (주)코셈 | 착탈 가능한 컬럼을 구비하는 주사 전자 현미경 및, 이를 이용한 영상 획득 방법 |
| CN117413819A (zh) | 2019-04-18 | 2024-01-19 | 艾步思国际有限责任公司 | 用于连续添加冷冻保护剂的系统和工艺 |
| US11738312B2 (en) * | 2019-08-01 | 2023-08-29 | Government Of The United States Of America, As Represented By The Secretary Of Commerce | Multidimensional printer |
| US11628439B2 (en) | 2020-01-13 | 2023-04-18 | Abs Global, Inc. | Single-sheath microfluidic chip |
| NL2024861B1 (en) * | 2020-02-07 | 2021-09-13 | Univ Delft Tech | Method for recording and correlating light and charged particle microscopy images |
| US11410838B2 (en) | 2020-09-03 | 2022-08-09 | Thermo Finnigan Llc | Long life electron multiplier |
| CN112461807B (zh) * | 2020-11-26 | 2021-11-19 | 山西大学 | 碳量子点在靶向细胞核仁免洗成像中的应用 |
| DE102021101982A1 (de) | 2021-01-28 | 2022-07-28 | ebm-papst neo GmbH & Co. KG | Vorrichtung und Verfahren zur Erfassung einer Konzentration von vorbestimmten Partikeln anhand ihrer morphologischen Eigenschaften in Luft |
| CN114113182A (zh) * | 2021-10-22 | 2022-03-01 | 合肥国轩高科动力能源有限公司 | 一种用于扫描电镜拍摄硅基负极材料的定位处理方法 |
Family Cites Families (50)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FR1345670A (fr) * | 1962-10-25 | 1963-12-13 | Radiologie Cie Gle | Perfectionnements aux porte-échantillons liquides pour spectromètres à rayons chious vide |
| US3657596A (en) * | 1965-05-20 | 1972-04-18 | Westinghouse Electric Corp | Electron image device having target comprising porous region adjacent conductive layer and outer, denser region |
| US3378684A (en) * | 1965-06-16 | 1968-04-16 | Gen Electric | Fluid sample cell with means to keep constant pressure on the sample fluid |
| US4071766A (en) * | 1974-03-28 | 1978-01-31 | Mta Kozponti Kemiai Kutato Intezet | Micro-chamber for electron optical examinations particularly for the electron microscopic examination of biological objects |
| JPS5168585U (ja) * | 1974-11-26 | 1976-05-31 | ||
| US4115689A (en) * | 1977-07-06 | 1978-09-19 | Won Vann Y | Leveling device for forming X-ray specimen |
| US4308547A (en) * | 1978-04-13 | 1981-12-29 | Recognition Equipment Incorporated | Liquid drop emitter |
| DE2921151C2 (de) * | 1979-05-25 | 1982-12-02 | Ernst Leitz Wetzlar Gmbh, 6330 Wetzlar | Vorrichtung zum Nachweis von in einem Abtast-Elektronenstrahlmikroskop von einer Probe ausgehenden Rückstreuelektronen |
| AU534811B2 (en) * | 1979-07-03 | 1984-02-16 | Unisearch Limited | Atmospheric scanning electron microscope |
| US4448311A (en) * | 1983-01-24 | 1984-05-15 | Tech Ref, Inc. | Sample cell |
| JPS59168652A (ja) * | 1983-03-16 | 1984-09-22 | Hitachi Ltd | 素子修正方法及びその装置 |
| US4618938A (en) * | 1984-02-22 | 1986-10-21 | Kla Instruments Corporation | Method and apparatus for automatic wafer inspection |
| US4587666A (en) * | 1984-05-03 | 1986-05-06 | Angelo M. Torrisi | System and a method for mounting film to a sample holder for X-ray spectroscopic fluorescence analysis |
| US4720622A (en) * | 1985-03-11 | 1988-01-19 | Sanyo Electric Co., Ltd | Wall-mounted type cooking apparatus |
| US4705949A (en) * | 1985-11-25 | 1987-11-10 | The United States Of America As Represented By The Secretary Of Commerce | Method and apparatus relating to specimen cells for scanning electron microscopes |
| US4720633A (en) * | 1986-01-17 | 1988-01-19 | Electro-Scan Corporation | Scanning electron microscope for visualization of wet samples |
| JPH0687410B2 (ja) * | 1986-08-01 | 1994-11-02 | エレクトロ‐スキャン コーポレーション | 走査電子顕微鏡及び試料の表面を電子顕微鏡的に像形成する方法 |
| US4880976A (en) * | 1987-05-21 | 1989-11-14 | Electroscan Corporation | Secondary electron detector for use in a gaseous atmosphere |
| US5250808A (en) * | 1987-05-21 | 1993-10-05 | Electroscan Corporation | Integrated electron optical/differential pumping/imaging signal system for an environmental scanning electron microscope |
| JPH0614461B2 (ja) | 1987-05-22 | 1994-02-23 | 日本電子株式会社 | 電子顕微鏡におけるガス雰囲気試料ホルダ |
| US4929831A (en) * | 1988-12-08 | 1990-05-29 | The United States Of America As Represented By The Secretary Of The Navy | Electron beam apparatus for testing infrared detectors in a cryogenically shielded environment |
| US4912330A (en) * | 1988-12-27 | 1990-03-27 | United States Of America As Represented By The Secretary Of The Navy | Apparatus for X-ray testing long wave infrared radiation detectors |
| US4929041A (en) * | 1989-01-09 | 1990-05-29 | Johnston Pump/General Valve, Inc. | Cathodoluminescence system for use in a scanning electron microscope including means for controlling optical fiber aperture |
| US5103102A (en) * | 1989-02-24 | 1992-04-07 | Micrion Corporation | Localized vacuum apparatus and method |
| JP2794471B2 (ja) * | 1989-11-24 | 1998-09-03 | 日本電子テクニクス株式会社 | 電子顕微鏡 |
| US5866904A (en) * | 1990-10-12 | 1999-02-02 | Hitachi, Ltd. | Scanning electron microscope and method for dimension measuring by using the same |
| JP3148353B2 (ja) * | 1991-05-30 | 2001-03-19 | ケーエルエー・インストルメンツ・コーポレーション | 電子ビーム検査方法とそのシステム |
| US5470757A (en) * | 1991-06-25 | 1995-11-28 | Minnesota Mining And Manufacturing Company | Spectroscopic sample holder and method for using same |
| US5122663A (en) * | 1991-07-24 | 1992-06-16 | International Business Machine Corporation | Compact, integrated electron beam imaging system |
| US5323441A (en) * | 1992-12-15 | 1994-06-21 | Angelo M. Torrisi | Sample holder for spectroscopic analysis and method for mounting film to sample holder |
| JP2781320B2 (ja) | 1993-01-18 | 1998-07-30 | 株式会社蛋白工学研究所 | 電子顕微鏡等の試料ホルダ |
| US5326971A (en) * | 1993-05-17 | 1994-07-05 | Motorola, Inc. | Transmission electron microscope environmental specimen holder |
| US5412211A (en) * | 1993-07-30 | 1995-05-02 | Electroscan Corporation | Environmental scanning electron microscope |
| US5362964A (en) * | 1993-07-30 | 1994-11-08 | Electroscan Corporation | Environmental scanning electron microscope |
| US5644132A (en) * | 1994-06-20 | 1997-07-01 | Opan Technologies Ltd. | System for high resolution imaging and measurement of topographic and material features on a specimen |
| US5466940A (en) * | 1994-06-20 | 1995-11-14 | Opal Technologies Ltd. | Electron detector with high backscattered electron acceptance for particle beam apparatus |
| US6025592A (en) * | 1995-08-11 | 2000-02-15 | Philips Electronics North America | High temperature specimen stage and detector for an environmental scanning electron microscope |
| US5898261A (en) * | 1996-01-31 | 1999-04-27 | The United States Of America As Represented By The Secretary Of The Air Force | Fluid-cooled particle-beam transmission window |
| EP0865454B1 (en) * | 1996-03-20 | 2001-01-03 | Celanese International Corporation | Addition of amine to improve paraformaldehyde |
| US5667791A (en) * | 1996-05-31 | 1997-09-16 | Thione International, Inc. | X-ray induced skin damage protective composition |
| JPH1064467A (ja) * | 1996-08-23 | 1998-03-06 | Toshiba Corp | 電子顕微鏡 |
| JP3500264B2 (ja) * | 1997-01-29 | 2004-02-23 | 株式会社日立製作所 | 試料分析装置 |
| US5859699A (en) * | 1997-02-07 | 1999-01-12 | Arcturus Engineering, Inc. | Laser capture microdissection analysis vessel |
| US5789748A (en) * | 1997-05-29 | 1998-08-04 | Stanford University | Low voltage electron beam system |
| US5945672A (en) * | 1998-01-29 | 1999-08-31 | Fei Company | Gaseous backscattered electron detector for an environmental scanning electron microscope |
| IL139743A0 (en) * | 1998-05-22 | 2002-02-10 | Euro Celtique Sa | Dissolution stage for an environmental scanning electron microscope |
| US6452177B1 (en) * | 1998-09-04 | 2002-09-17 | California Institute Of Technology | Atmospheric electron x-ray spectrometer |
| JP3610245B2 (ja) | 1998-10-27 | 2005-01-12 | 日本電子株式会社 | ガス雰囲気試料ホルダ |
| WO2002014830A2 (en) | 2000-08-17 | 2002-02-21 | Yeda Research And Development Co. Ltd. | Method of identification and quantification of biological molecules and apparatus therefore |
| JP2002273446A (ja) | 2001-03-19 | 2002-09-24 | Sanyo Electric Co Ltd | 汚水処理装置用電解槽 |
-
2001
- 2001-11-30 AU AU2002221019A patent/AU2002221019B2/en not_active Ceased
- 2001-11-30 EP EP01998987A patent/EP1340241B1/en not_active Expired - Lifetime
- 2001-11-30 JP JP2002547196A patent/JP4153303B2/ja not_active Expired - Fee Related
- 2001-11-30 CA CA002436237A patent/CA2436237A1/en not_active Abandoned
- 2001-11-30 CZ CZ20031455A patent/CZ20031455A3/cs unknown
- 2001-11-30 AT AT01998987T patent/ATE510298T1/de not_active IP Right Cessation
- 2001-11-30 IL IL15602701A patent/IL156027A0/xx active IP Right Grant
- 2001-11-30 AU AU2101902A patent/AU2101902A/xx active Pending
- 2001-11-30 CN CNA018199062A patent/CN1511332A/zh active Pending
- 2001-11-30 WO PCT/IL2001/001108 patent/WO2002045125A1/en active Application Filing
-
2003
- 2003-05-27 US US10/448,313 patent/US6992300B2/en not_active Expired - Lifetime
-
2004
- 2004-05-06 US US10/841,769 patent/US6989542B2/en not_active Expired - Lifetime
-
2005
- 2005-08-19 US US11/207,611 patent/US7253418B2/en not_active Expired - Fee Related
-
2008
- 2008-04-03 JP JP2008097275A patent/JP2008171830A/ja active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| CZ20031455A3 (cs) | 2003-10-15 |
| IL156027A0 (en) | 2003-12-23 |
| JP2004515049A (ja) | 2004-05-20 |
| ATE510298T1 (de) | 2011-06-15 |
| US20060033038A1 (en) | 2006-02-16 |
| US7253418B2 (en) | 2007-08-07 |
| AU2101902A (en) | 2002-06-11 |
| US6989542B2 (en) | 2006-01-24 |
| EP1340241B1 (en) | 2011-05-18 |
| WO2002045125A1 (en) | 2002-06-06 |
| CA2436237A1 (en) | 2002-06-06 |
| US20040217297A1 (en) | 2004-11-04 |
| JP2008171830A (ja) | 2008-07-24 |
| EP1340241A4 (en) | 2009-01-14 |
| AU2002221019B2 (en) | 2007-02-08 |
| CN1511332A (zh) | 2004-07-07 |
| US6992300B2 (en) | 2006-01-31 |
| US20040046120A1 (en) | 2004-03-11 |
| EP1340241A1 (en) | 2003-09-03 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4153303B2 (ja) | 走査型電子顕微鏡を用いた非真空環境内のサンプルの検査のための装置および方法 | |
| AU2002221019A1 (en) | Device and method for the examination of samples in a non-vacuum environment using a scanning electron microscope | |
| US9207196B2 (en) | Transmission electron microscopy for imaging live cells | |
| US7745802B2 (en) | Specimen holder, specimen inspection apparatus, specimen inspection method, and method of fabricating specimen holder | |
| Peckys et al. | Nanoscale imaging of whole cells using a liquid enclosure and a scanning transmission electron microscope | |
| EP2312302A1 (en) | Apparatus and method for inspecting samples | |
| EP2388575A1 (en) | Sample holder, inspection apparatus and inspection method | |
| US8119994B2 (en) | Apparatus and method for inspecting sample | |
| US7906760B2 (en) | Inspection method and reagent solution | |
| US7968843B2 (en) | Method and apparatus for simultaneous SEM and optical examination | |
| JP2008047411A (ja) | 試料保持体及び試料検査方法並びに試料検査装置 | |
| Kaech | An introduction to electron microscopy instrumentation, imaging and preparation | |
| de Jonge et al. | Practical aspects of transmission electron microscopy in liquid | |
| Griffith et al. | Photoelectron imaging in cell biology | |
| Griffith et al. | A high vacuum photoelectron microscope for the study of biological specimens | |
| Pawley | LVSEM for biology | |
| Setou et al. | Mammalian cell nano structures visualized by cryo Hilbert differential contrast transmission electron microscopy | |
| IL156027A (en) | Device and method for the examination of samples in a non-vacuum environment using a scanning electron microscope | |
| EP1953793B1 (en) | Specimen holder, specimen inspection apparatus, specimen inspection method, and method of fabricating specimen holder | |
| Tousimis | Electron probe microanalysis of biological structures | |
| Stegmann et al. | 13 Electron Microscopic Image Acquisition | |
| JPH0665014B2 (ja) | 自然状態試料観察可能走査型電子顕微鏡 | |
| JP2024081144A (ja) | 荷電粒子顕微鏡法を使用して試料を評価する方法 | |
| KR960011065B1 (ko) | 습윤 표본을 관찰 가능한 주사형 전자 현미경 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20041122 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20041122 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20060213 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20060228 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20060530 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20060607 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20060831 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20070522 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20070820 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20071217 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20080311 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20080403 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20080603 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20080703 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 4153303 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20110711 Year of fee payment: 3 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20110711 Year of fee payment: 3 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20120711 Year of fee payment: 4 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20130711 Year of fee payment: 5 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |