RU2523201C2 - Способ получения изоцианатов с использованием диарилкарбоната - Google Patents
Способ получения изоцианатов с использованием диарилкарбоната Download PDFInfo
- Publication number
- RU2523201C2 RU2523201C2 RU2010146077/04A RU2010146077A RU2523201C2 RU 2523201 C2 RU2523201 C2 RU 2523201C2 RU 2010146077/04 A RU2010146077/04 A RU 2010146077/04A RU 2010146077 A RU2010146077 A RU 2010146077A RU 2523201 C2 RU2523201 C2 RU 2523201C2
- Authority
- RU
- Russia
- Prior art keywords
- including isomers
- reaction
- reactor
- thermal decomposition
- diaryl carbonate
- Prior art date
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C263/00—Preparation of derivatives of isocyanic acid
- C07C263/04—Preparation of derivatives of isocyanic acid from or via carbamates or carbamoyl halides
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C265/00—Derivatives of isocyanic acid
- C07C265/14—Derivatives of isocyanic acid containing at least two isocyanate groups bound to the same carbon skeleton
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2601/00—Systems containing only non-condensed rings
- C07C2601/12—Systems containing only non-condensed rings with a six-membered ring
- C07C2601/14—The ring being saturated
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Abstract
Изобретение относится к способу получения изоцианата. Способ включает несколько стадий. Сначала получают реакционную смесь, содержащую арилкарбамат, содержащий арильную группу, образующуюся из диарилкарбоната, ароматическое гидроксисоединение, образующееся из диарилкарбоната, и диарилкарбонат, путем осуществления взаимодействия диарилкарбоната и соединения амина в реакторе, в котором осуществляют реакцию между диарилкарбонатом и соединением амина. Затем переносят реакционную смесь в реактор термического разложения, соединенный линией с реактором, в котором осуществляют реакцию между диарилкарбонатом и соединением амина. После этого получают изоцианат в результате реакции термического разложения арилкарбамата. При этом диарилкарбонат включает атом металла в концентрации от 0,001 м.д. до 10%. Диарилкарбонат представляет собой соединение формулы (1), где R1 представляет собой ароматическую группу, содержащую от 6 до 12 атомов углерода. Соединение амина представляет собой соединение формулы (2), где R2 представляет собой группу, выбранную из алифатической группы, содержащей от 1 до 20 атомов углерода, и ароматической группы, содержащей от 6 до 20 атомов углерода, при этом вышеуказанная группа содержит атом, выбранный из атома углерода и атома кислорода, ее валентность равна n и n представляет собой целое число от 2 до 10. Предлагаемый способ позволяет ингибировать реакции денатурирования арилкарбамата, тем самым обеспечивая стабильное получение изоцианата в течение длительного времени с высоким выходом. 29 з.п. ф-лы, 16 ил., 1 табл., 27 пр.
Description
Область техники, к которой относится изобретение
Настоящее изобретение относится к способу получения изоцианатов с использованием диарилкарбоната в качестве исходного материала.
Уровень техники
Изоцианаты широко используются в качестве исходных материалов при получении таких продуктов, как полиуретановая пена, краски, адгезивы и тому подобное. Основной промышленный способ получения изоцианатов включает осуществление взаимодействия соединений амина с фосгеном (фосгеновый способ), и почти все количество изоцианатов, производимое во всем мире, получают в соответствии с указанным фосгеновым способом. Однако фосгеновый способ создает множество проблем.
Во-первых, указанный способ требует использования большого количества фосгена в качестве исходного материала. Фосген является высокотоксичным соединением и требует специальных предосторожностей при обращении с ним, чтобы предотвратить соприкосновение работающего персонала с фосгеном, и также требует специальной аппаратуры для обезвреживания отработанного материала.
Во-вторых, так как в фосгеновом способе в больших количествах в качестве побочного продукта образуется обладающий высокой коррозионной способностью хлористый водород, то кроме необходимости использовать способ обезвреживания хлористого водорода, во многих случаях в получаемых изоцианатах содержится гидролитический хлор, который может плохо влиять на устойчивость к погодным условиям и термостойкость полиуретановых изделий в случае использования изоцианатов, получаемых с использованием фосгенового способа.
На основании представленного уровня техники велись поиски такого способа получения соединений изоцианата, в котором не использовался бы фосген. Один пример предложенного способа получения соединений изоцианата без использования фосгена включает термическое разложение эфиров карбаминовой кислоты. Давно было известно, что изоцианаты и гидроксисоединения можно получить при термическом разложении эфиров карбаминовой кислоты (см., например, непатентный документ 1). Основная реакция иллюстрируется следующей формулой:
(где R представляет собой органический остаток с валентностью a, R' представляет собой одновалентный органический остаток и a представляет собой целое число 1 или более).
Среди эфиров карбаминовой кислоты арилкарбаматы, которые представляют собой эфиры карбаминовой кислоты, в которых эфирная группа представляет собой ароматическую группу, обладают тем преимуществом, что позволяют вести реакцию термического разложения при более низких температурах, чем температуры в реакции алкилкарбаматов, где эфирная группа представляет собой алкильную группу (см. патентный документ 1).
До настоящего времени были раскрыты различные способы получения арилкарбаматов.
В описании патентного документа 2 раскрыто, что соответствующие арилалкилмонокарбаматы получают с выходом от 90 до 95% за счет осуществления взаимодействия алкилмоноаминов с диарилкарбонатами в присутствии растворителя, такого как бензол, диоксан или четыреххлористый углерод. Кроме того, в патентном документе 3 был предложен способ непрерывного получения фенилового эфира метилкарбаминовой кислоты из метиламина и дифенилкарбоната.
Однако все эти способы представляют собой способы получения алкиларилкарбаматов с использованием низших алкилмоноаминов в качестве аминов, но не арилалкилполикарбаматов. В случае получения соответствующих эфиров арилалкилполикарбаминовой кислоты из алкилполиаминов, таких как алкилдиамины или алкилтриамины, из-за использования алкилмоноаминов возникают совершенно другие проблемы. Это происходит потому, что, хотя только соединения мочевины образуются в качестве побочных продуктов побочных реакций, представленных следующей формулой (3) и/или формулой (4), в дополнение к реакции, представленной следующей формулой (2), в случае использования алкилмоноаминов, в случае алкилполиаминов, таких как алкилдиамины или алкилтриамины, в качестве побочных продуктов образуется чрезвычайно много различных типов соединений мочевины, таких как соединения, представленные следующей формулой (5), формулой (6) и/или формулой (7).
(где R' представляет собой одновалентную алкильную группу или ароматическую группу, Ar представляет собой одновалентную ароматическую группу и p, q и r соответственно представляют собой целое число 1 или более).
А именно реакции, приводящие к образованию побочных продуктов в форме таких различных соединений мочевины, создают проблему снижения выхода целевого соединения в форме арилалкилполикарбаматов, также как и проблему, состоящую в крайне затруднительном выделении и очистке целевого продукта от смеси указанных соединений мочевины и полимерных соединений мочевины.
Поэтому, хотя было предпринято крайне мало попыток получения эфиров арилалкилполикарбаминовой кислоты из алкилполиаминов и диарилкарбонатов, существует очень мало сообщений об этих попытках. Например, в соответствии с описанием патентного документа 4 был предложен способ получения фенилового эфира 1,6-гексаметилендикарбаминовой кислоты в реакционной системе, в которой раствор, в котором 1 моль 1,6-гексаметилендиамина растворен в 5-кратном количестве молей бензола, добавляют по каплям в раствор, в котором 1 моль дифенилкарбоната растворен в 5-кратном количестве молей бензола, при перемешивании при 80°C. В соответствии с указанным патентным описанием важно использовать такие растворители, в которых фениловый эфир 1,6-гексаметилендикарбаминовой кислоты как можно меньше растворяется в реакционном растворителе, чтобы обеспечить наиболее выгодные условия протекания реакции, и указывается, что наиболее предпочтительными примерами таких растворителей являются бензол или хлорбензол.
С этой точки зрения, целевой фениловый эфир 1,6-гексаметилендикарбаминовой кислоты получен в непатентном документе 3 в результате реакции 0,01 моль дифенилкарбоната и 0,005 моль 1,6-гексаметилендиамина, с использованием 40 мл толуола в качестве реакционного растворителя в течение длительного промежутка времени в 20 часов. Однако выход составляет только 93%, несмотря на использование столь большого количества толуола, и проблема получения побочных продуктов в виде соединений мочевины и соединений полимочевины, которые необходимо удалить, остается.
Кроме того, в патентном документе 5 раскрыт способ получения соединений диуретана, в котором диарилкарбонаты и соединения амина подвергают взаимодействию в присутствии протонсодержащих кислот. Однако в случае осуществления способа получения, раскрытого в указанной патентной публикации, в промышленном масштабе, нельзя сказать, что выход диуретанового соединения является адекватным, и необходимо вести реакцию при низкой температуре, чтобы ингибировать побочные реакции, что, тем самым, приводит к такому недостатку, как большая длительность реакции.
В патентном документе 6 раскрыт способ, в котором диарилкарбонаты и ароматические полиамины подвергают взаимодействию в присутствии гетероциклических третичных аминов, таких как 2-гидроксипиридин. Кроме того, что указанный способ требует дорогостоящего катализатора в количествах, равных или больше, чем эквимолярные количества, в расчете на субстрат реакции, его проблемой является также низкая скорость реакции.
В соответствии с патентным документом 7, хотя указанный способ раскрыт для синтеза ароматических уретанов при температурах от 140 до 230°C в присутствии ароматических аминов, диарилкарбонат и кислота Льюиса в качестве катализатора, в случае осуществления указанного способа, также как использование кислоты Льюиса, вызывают коррозию аппаратуры, и выделение и извлечение продукта оказываются затруднительными.
В патентном документе 8 раскрыт способ получения ариловых эфиров алкилполикарбаминовой кислоты, включающий осуществление еакции в практически гомогенном растворе, с использованием от 1 до 3 эквивалентов диарилкарбоната на эквивалент аминогрупп алкилполиамина, и с использованием ароматических гидроксисоединений в качестве растворителя в реакции, когда ариловые эфиры алкилполикарбаминовой кислоты получают путем осуществления взаимодействия алкилполиаминов и диарилкарбонатов. В соответствии с указанной патентной публикацией, ариловые эфиры алкилполикарбаминовой кислоты получают с высокой селективностью и высоким выходом, обычно 96% или более и 98% или более в его предпочтительном варианте. Однако, так как образование соединений мочевины было подтверждено, хотя и в небольшом количестве, образования соединений мочевины невозможно избежать полностью.
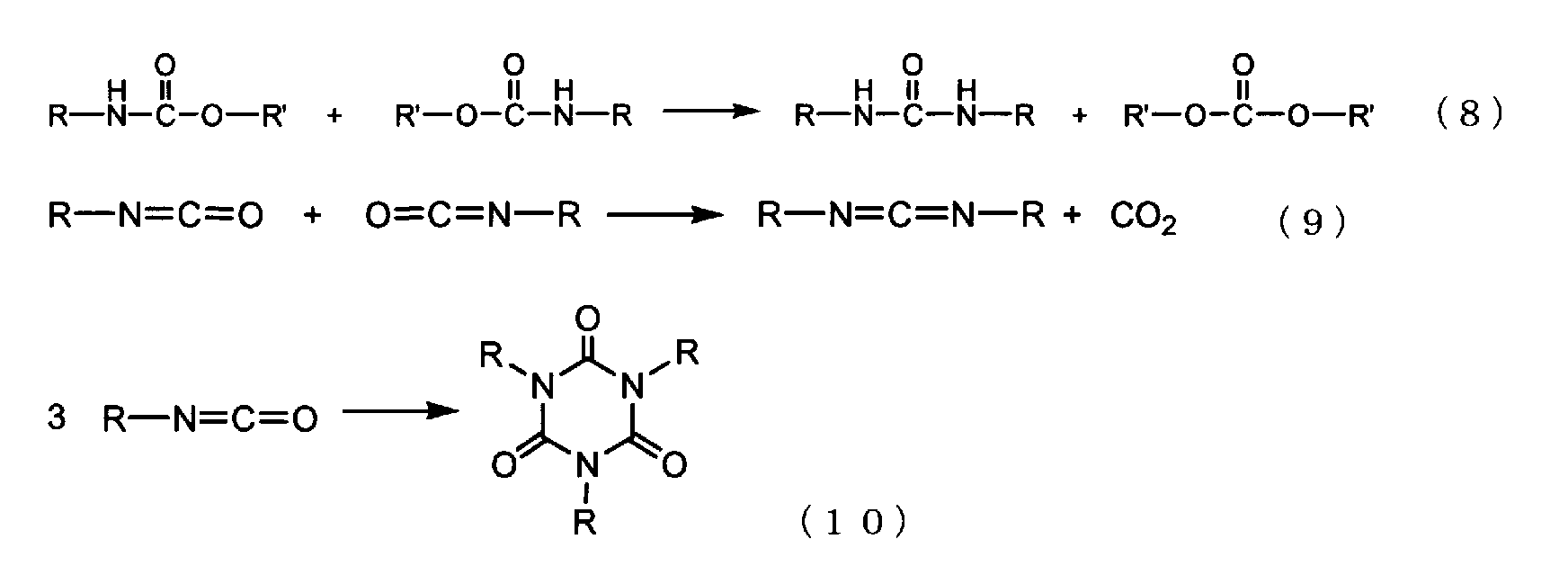
С другой стороны, при термическом разложении эфиров карбаминовой кислоты происходит одновременное протекание различных необратимых побочных реакций, таких как реакции термического денатурирования для эфиров карбаминовой кислоты или конденсация изоцианатов, образующихся при термическом разложении. Примеры таких побочных реакций включают реакцию, в которой происходит образование мочевинных связей, как представлено следующей формулой (8), реакцию, в которой происходит образование карбодиимидов, как представлено следующей формулой (9), и реакцию, в которой происходит образование изоциануратов, как представлено следующей формулой (10) (см. непатентный документ 1 и непатентный документ 2).
Помимо указанных побочных реакций, приводящих к снижению выходов целевых изоцианатов и селективности реакции при производстве полиизоцианатов, в частности, указанные реакции могут создать длительные эксплуатационные трудности в результате, например, осаждения твердых полимерных частиц, которые забивают реактор.
Были предложены различные способы получения изоцианатов с использованием эфиров карбаминовой кислоты в качестве исходных материалов.
В соответствии с патентным документом 9 ароматические диизоцианаты и/или полиизоцианаты получают на протяжении следующих двух стадий. Более конкретно, на первой стадии ароматические первичные амины и/или ароматические первичные полиамины подвергают взаимодействию с O-алкилкарбаматами в присутствии или в отсутствие катализатора и в присутствии или отсутствие мочевины и спирта для образования арилдиуретанов и/или арилполиуретанов с последующим удалением образующегося аммиака при необходимости. На второй стадии ароматические изоцианаты и/или ароматические полиизоцианаты получают путем термического разложения арилдиуретанов и/или арилполиуретанов.
Известно несколько способов образования соответствующих изоцианатов и спиртов за счет термического разложения (циклических) алифатических, и особенно ароматических моноуретанов и диуретанов, примеры которых включают способ, осуществляемый при высокой температуре в газовой фазе, и способ, осуществляемый в условиях при низкой температуре в жидкой фазе. Однако, так как существуют ситуации, в которых, например, реакционная смесь вызывает образование осадков, полимерных веществ и циклических соединений в реакторах и регенерационных установках за счет протекания побочных реакций, как было раскрыто ранее, или указанные вещества образуют вещества, которые прилипают к стенкам реактора, экономическая эффективность весьма низкая в случае получения изоцианатов в течение длительного промежутка времени.
Таким образом, химические способы, такие как использование специального катализатора (см. патентный документ 10 и патентный документ 11) или катализатора, скомбинированного с инертным растворителем (см. патентный документ 12), раскрыты как повышающие выходы при термическом разложении уретана.
Более конкретно, в патентном документе 13 раскрыт способ получения гексаметилендиизоцианата, включающий термическое разложение гексаметилендиэтилуретана в присутствии дибензилтолуола, используемого в качестве растворителя, и в присутствии смеси катализаторов, содержащей метилтолуолсульфонат и дихлорид дифенилолова. Однако оценить экономическую эффективность указанного способа невозможно, так как отсутствует подробное описание получения исходных компонентов, их выделения или очистки и необязательной регенерации растворителя и смеси катализаторов.
В соответствии с процессом, раскрытым в патентном документе 14 уретан можно легко разложить на изоцианат и спирт в содержащем углерод псевдоожиженном слое без использования катализатора. Кроме того, в соответствии с описанием патентного документа 15, гексаметилендиалкилуретан можно разложить в газовой фазе при температуре, превышающей 300°C, в присутствии или в отсутствие газопроницаемого упаковочного материала, состоящего из, например, углерода, меди, бронзы, стали, цинка, алюминия, титана, хрома, кобальта или кварца, получая в результате гексаметилендиизоцианат. В соответствии с описанием патентного документа 14, указанный процесс осуществляют в присутствии галогеноводорода и/или донора галогеноводорода. Однако указанный способ не позволяет достичь выхода гексаметилендиизоцианата в 90% или более. Это связано с тем, что продукты разложения частично снова связываются друг с другом, образуя уретановые связи. Поэтому все еще требуется очистка гексаметилендиизоцианата путем перегонки, и существует множество случаев, когда потери выходов возрастают.
Кроме того, в патентном документе 16 раскрыто, что монокарбаматы можно с успехом разлагать с высоким выходом без использования растворителя при пониженном давлении и/или в отсутствие стабилизатора и при сравнительно низкой температуре. Указанные продукты разложения (моноизоцианаты и спирты) удаляют путем перегонки из кипящей реакционной смеси и отбирают отдельно за счет фракционной конденсации. Обычно описывают способ частичного удаления реакционной смеси для удаления побочных продуктов, образующихся в процессе термического разложения. Так, хотя имеется возможность удалять побочные продукты из нижней части реактора, описанная выше проблема, связанная с прилипанием вещества к стенкам реактора, остается, и проблемы, связанные с длительными процессами, остаются нерешенными. Кроме того, отсутствует описание, касающееся промышленного использования удаленных остаточных веществ (содержащих значительные количества полезных компонентов).
В соответствии с описанием патентного документа 17 термическое разложение алифатических, алициклических или ароматических поликарбаматов осуществляют при температуре от 150 до 350°C и при давлении от 0,001 до 20 бар, в присутствии инертного растворителя и в присутствии или отсутствии катализатора и вспомогательных веществ в виде хлористого водорода, органического хлорангидрида, алкилирующего агента или оловоорганического соединения. Образующиеся побочные продукты можно непрерывно удалять из реактора вместе с реакционным раствором, например, и одновременно добавлять соответствующие количества свежего растворителя или регенерированного растворителя. Примеры недостатков указанного способа включают снижение объемной производительности полиизоцианата, связанное с использованием циркулирующего растворителя, и высокие энергетические затраты, включая регенерацию растворителя. Кроме того, так как используемое вспомогательное вещество является летучим в условиях реакции, может происходить загрязнение продуктов разложения. Кроме того, так как существует большое количество образующихся остаточных веществ относительно образующегося полиизоцианата, возникают сомнения, касающиеся экономической эффективности и надежности указанного способа как промышленного процесса.
В патентном документе 18 раскрыт способ непрерывного термического разложения карбаматов, подаваемых вдоль внутренних стенок трубчатого реактора в виде жидкости, в присутствии растворителя с высокой температурой кипения, примеры которого могут включать 5-(этоксикарбониламино)-1-(этоксикарбониламинометил)-1,3,3-триметилциклогексан как алициклический диуретан. Указанный способ имеет такие недостатки, как низкий выход и низкая селективность в процессе получения (циклических) алифатических диизоцианатов. Кроме того, отсутствует описание непрерывного способа сопровождающего регенерацию повторно связанных или частично разложившихся карбаматов, нет также никаких указаний на последующую обработку растворителя, содержащего побочные продукты и катализатор.
Можно легко себе представить возможность получения изоцианатов с использованием диарилкарбонатов и аминосоединений в качестве исходных материалов путем комбинирования арилкарбаматного способа получения и изоцианатного способа получения с использованием термического разложения эфиров карбаминовой кислоты, как раскрыто выше. Однако для комбинирования указанных арилкарбаматного способа получения и изоцианатного способа получения с использованием термического разложения арилкарбаматов, как раскрыто выше, необходимо использовать способы, включающие сложные процедуры, состоящие из осуществления термического разложения арилкарбамата путем осуществления взаимодействия диарилкарбонатов и соединений амина и выделения арилкарбаматов из полученного реакционного раствора с последующим термическим разложением арилкарбаматов, или способы с использованием реакционного раствора, полученного в процессе получения арилкарбаматов непосредственно в реакции термического разложения.
В этой связи в патентном документе 19 раскрыт способ синтеза ароматических изоцианатов путем синтеза уретановых соединений путем осуществления взаимодействия ароматических аминов и диарилкарбонатов в присутствии катализатора кислоты Льюиса и продолжения термического разложение уретановых соединений в диарилкарбонаты, используемые для синтеза уретановых соединений. В указанной патентной публикации изоцианаты получают, подвергая уретансодержащий реакционный раствор, полученный путем осуществления взаимодействия соединений амина и диарилкарбонатов в присутствии катализатора кислоты Льюиса, реакции термического разложения в реакторах, которые используют для синтеза уретана.
Патентный документ 1: патент США № 3992430
Патентный документ 2: опубликованная заявка на патент Японии № S52-71443
Патентный документ 3: опубликованная заявка на патент Японии № S61-183257
Патентный документ 4: патент Германии № 925496
Патентный документ 5: опубликованная заявка на патент Японии № H10-316645
Патентный документ 6: опубликованная заявка на патент Японии № S52-136147
Патентный документ 7: опубликованная заявка на патент Японии № 2004-262834
Патентный документ 8: опубликованная заявка на патент Японии № H1-230550
Патентный документ 9: патент США № 4290970
Патентный документ 10: патент США № 2692275
Патентный документ 11: патент США № 3734941
Патентный документ 12: патент США № 4081472
Патентный документ 13: патент США № 4388426
Патентный документ 14: патент США № 4482499
Патентный документ 15: патент США № 4613466
Патентный документ 16: патент США № 4386033
Патентный документ 17: патент США № 4388246
Патентный документ 18: патент США № 4692550
Патентный документ 19: опубликованная заявка на патент Японии № 2004-262835
Непатентный документ 1: Berchte der Deutechen Chemischen Gesellschaft, Vol. 3, p. 653, 1870
Непатентный документ 2: Journal of American Chemical Society, Vol. 81, p. 2138, 1959
Непатентный документ 3: Journal of Polymer Science, Polymer Chemistry Edition, Vol. 17, p. 835, 1979
Сущность изобретения
Проблемы, которые должно решить рассматриваемое изобретение
Однако невозможно выбрать реакторы и условия реакций, каждое из которых подходит для реакции синтеза уретанового соединения и реакции термического разложения, так как осуществляют реакцию синтеза уретанового соединения и реакцию термического разложения в одном и том же реакторе. В соответствии с примерами патентного документа 19 выход изоцианатов фактически снижается. Кроме того, в указанной патентной публикации не представлено подробного описания способа непрерывного получения изоцианатов, и он не удовлетворителен с точки зрения промышленной эффективности процесса получения изоцианата.
Таким образом, способ получения изоцианатов с использованием диарилкарбонатов и соединений амина в качестве исходных материалов для получения арилкарбаматов с последующим получением изоцианатов через арилкарбаматы все еще имеет множество проблем, которые необходимо решить, и указанный способ до сих пор не был использован в промышленном масштабе.
Целью настоящего изобретения является создание способа получения изоцианата, который преодолел бы различные проблемы известного уровня техники, как раскрыто выше, используя диарилкарбонаты и соединения амина.
Средства для решения проблемы
В результате непрерывных интенсивных исследований вышеуказанных проблем авторы настоящего изобретения нашли способ получения изоцианатов путем переноса смеси, полученной при осуществлении взаимодействия диарилкарбонатов и соединений амина в специфических условиях, в реактор термического разложения в специфических условиях и путем осуществления реакции термического разложения содержащегося в смеси эфира карбаминовой кислоты, тем самым, осуществив завершение настоящего изобретения.
Коротко, в настоящем изобретении предложено следующее:
[1] способ получения изоцианата, включающий стадии:
получения реакционной смеси, содержащей арилкарбамат, содержащий арильную группу, образующуюся из диарилкарбоната, ароматическое гидроксисоединение, образующееся из диарилкарбоната, и диарилкарбонат, путем осуществления взаимодействия диарилкарбоната и соединения амина, в реакторе, в котором осуществляют реакцию между диарилкарбонатом и соединением амина;
переноса реакционной смеси в реактор термического разложения, соединенный линией с реактором, в котором осуществляют реакцию между указанным диарилкарбонатом и указанным соединением амина; и
получения изоцианата путем осуществления реакции термического разложения арилкарбамата.
[2] Указанный способ в соответствии пунктом [1], включающий далее очистку кислотой побочного продукта с высокой температурой кипения, прилипшего к реактору термического разложения.
[3] Указанный способ в соответствии с пунктом [1] или [2], где реакцию между диарилкарбонатом и соединением амина осуществляют при стехиометрическом отношении диарилкарбоната к аминогруппам, содержащимся в соединении амина, 1 или более.
[4] Указанный способ в соответствии с любым одним из пунктов [1]-[3], где диарилкарбонат и соединение амина подвергают взаимодействию в присутствии ароматического гидроксисоединения в качестве реакционного растворителя.
[5] Указанный способ в соответствии с пунктом [4], где указанное ароматическое гидроксисоединение, используемое в качестве реакционного растворителя, представляет собой ароматическое гидроксисоединение того же типа, что и соединение ArOH, имеющее структуру, в которой атом водорода добавлен к группе ArO, составляющей диарилкарбонат ArOCOOAr (где Ar представляет собой ароматическую группу и O представляет собой атом кислорода).
[6] Указанный способ в соответствии с любым одним из пунктов [1]-[5], где реакционную смесь подают в реактор термического разложения в виде жидкости.
[7] Указанный способ в соответствии с пунктом [6], где реакционную смесь подают в указанный реактор термического разложения, поддерживая при этом температуру в интервале от 10 до 180°C.
[8] Указанный способ в соответствии с любым одним из пунктов [1]-[7], где реакционную смесь непрерывно подают в реактор термического разложения.
[9] Указанный способ в соответствии с любым одним из пунктов [1]-[8], где компонент с низкой температурой кипения, образующийся в указанной реакции термического разложения, выделяют из указанного реактора термического разложения в виде газофазного компонента, и жидкофазный компонент выделяют из нижней части реактора.
[10] Указанный способ в соответствии с пунктом [9], где регенерацию газофазного компонента и регенерацию жидкофазного компонента осуществляют непрерывно.
[11] Указанный способ в соответствии с пунктом [9] или [10], где указанный изоцианат, полученный в реакции термического разложения арилкарбамата, выделяют из указанного реактора термического разложения в виде газофазного компонента и жидкофазный компонент, содержащий указанный диарилкарбонат, выделяют из нижней части реактора.
[12] Указанный способ в соответствии с пунктом [11], дополнительно включающий регенерацию изоцианата путем дистилляционного разделения в ректификационной колонне газофазного компонента, содержащего изоцианат, выделенный из указанного реактора термического разложения, и подачу газофазного компонента, содержащего указанный изоцианат, выделенный из указанного реактора термического разложения, в дистилляционную колонну в газообразной фазе.
[13] Указанный способ в соответствии с пунктом [11] или [12], где указанный жидкофазный компонент, содержащий указанный диарилкарбонат, представляет собой смесь, содержащую арилкарбамат, и всю смесь или часть смеси подают в верхнюю часть реактора.
[14] Указанный способ в соответствии с пунктом [9] или [10], где указанный изоцианат, полученный в указанной реакции термического разложения арилкарбамата, выделяют из нижней части реактора, в котором осуществляют указанную реакцию термического разложения, в виде жидкофазного компонента.
[15] Указанный способ в соответствии с пунктом [14], где жидкофазный компонент, выделенный из нижней части реактора, включает изоцианат и арилкарбамат, причем весь или часть указанного изоцианата выделяют из жидкофазного компонента, и все или часть из оставшегося подают в верхнюю часть реактора.
[16] Указанный способ в соответствии с пунктом [14] или [15], где указанный изоцианат выделяют путем дистилляционного разделения смеси, содержащей изоцианат, выделенный из указанного реактора термического разложения.
[17] Указанный способ в соответствии с любым одним из пунктов [1]-[16], где тип реактора, в котором осуществляют реакцию между диарилкарбонатом и соединением амина, и тип реактора термического разложения могут быть одинаковыми или различными, и реактор, в котором осуществляют реакцию между указанным диарилкарбонатом и соединением амина, и реактор термического разложения представляют собой, по меньшей мере, один реактор, выбранный из группы, состоящей из реактора колонного типа и реактора корпусного типа.
[18] Указанный способ в соответствии с пунктом [17], где указанный реактор термического разложения состоит из, по меньшей мере, одного реактора, выбранного из группы, состоящей из выпаривателя, непрерывной многоступенчатой ректификационной колонны, насадочной колонны, тонкопленочного выпаривателя и выпаривателя с падающей пленкой жидкости.
[19] Указанный способ в соответствии с любым одним из пунктов [1]-[18], где реакцию между указанным диарилкарбонатом и соединением амина осуществляют в присутствии катализатора.
[20] Указанный способ в соответствии с любым одним из пунктов [1]-[19], где указанную реакцию термического разложения осуществляют в жидкой фазе.
[21] Указанный способ в соответствии с любым одним из пунктов [1]-[20], где указанный диарилкарбонат представляет собой соединение, представленное следующей формулой (1):
(где R1 представляет собой ароматическую группу, содержащую от 6 до 12 атомов углерода).
[22] Указанный способ в соответствии с пунктом [21], где указанный диарилкарбонат включает атом металла в количестве от 0,001 м.д. до 10%.
[23] Указанный способ в соответствии с пунктом [22], где указанный атом металла представляет собой один тип или несколько типов атомов металлов, выбранных из группы, состоящей из атомов железа, никеля, кобальта, цинка, олова, меди и титана.
[24] Указанный способ в соответствии с любым одним из пунктов [1]-[23], где указанный диарилкарбонат представляет собой диарилкарбонат, полученный способом, который включает следующие стадии (1)-(3):
стадия (1): получение реакционной смеси, содержащей диалкилкарбонат, путем осуществления взаимодействия оловоорганического соединения, содержащего олово-кислород-углеродную связь, и двуокиси углерода;
стадия (2): получение указанного диалкилкарбоната и остаточной жидкости при разделении реакционной смеси; и
стадия (3): получение указанного диарилкарбоната путем осуществления взаимодействия диалкилкарбоната, выделенного на стадии (2), и ароматического гидроксисоединения A с последующим удалением побочного продукта спирта.
[25] Указанный способ в соответствии с пунктом [24], где ароматическое гидроксисоединение A представляет собой ароматическое гидроксисоединение, содержащее от 6 до 12 атомов углерода.
[26] Указанный способ в соответствии с пунктом [24] или [25], где указанный диарилкарбонат представляет собой диарилкарбонат, полученный способом, который дополнительно включает следующие стадии (4) и (5):
стадия (4): образование оловоорганического соединения, содержащего олово-кислород-углеродную связь и воду, путем осуществления взаимодействия остаточной жидкости, полученной на стадии (2), со спиртом с последующим удалением воды из реакционной системы; и
стадия (5): повторное использование указанного оловоорганического соединения, содержащего олово-кислород-углеродную связь, полученного на стадии (4), в качестве оловоорганического соединения, содержащего олово-кислород-углеродную связь, стадии (1).
[27] Указанный способ в соответствии с пунктом [24], где спирт, выделенный на стадии (3), используют как весь спирт или часть спирта стадии (4).
[28] Указанный способ в соответствии с любым одним из пунктов [9]-[27], где указанный диарилкарбонат выделяют и регенерируют из жидкофазного компонента или газофазного компонента, выделенного из указанного реактора термического разложения, и указанный диарилкарбонат повторно используют в качестве диарилкарбоната, используемого в качестве исходного материала.
[29] Указанный способ в соответствии с пунктом [1] или [24], где ароматическое гидроксисоединение выделяют и регенерируют из указанного жидкофазного компонента или газофазного компонента, выделенного из указанной реакции термического разложения, и ароматическое гидроксисоединение возвращают в оборот для использования в качестве ароматического гидроксисоединения A стадии (3) или в качестве ароматического гидроксисоединения, используемого в качестве реакционного растворителя.
[30] Указанный способ в соответствии с любым одним из пунктов [1]-[29], где соединение амина представляет собой соединение полиамина.
[31] Указанный способ в соответствии с пунктом [30], где соединение амина представляет собой соединение, представленное следующей формулой (2):
(где R2 представляет собой группу, выбранную из группы, состоящей из алифатической группы, содержащей от 1 до 20 атомов углерода, и ароматической группы, содержащей от 6 до 20 атомов углерода, причем вышеуказанная группа содержит атом, выбранный из атома углерода и атома кислорода, и с валентностью равной n, и n представляет собой целое число от 2 до 10).
[32] Указанный способ в соответствии с пунктом [31], где соединение амина представляет собой соединение диамина, в котором n представляет собой 2 в формуле (2).
[33] Указанный способ в соответствии с любым одним из пунктов [1]-[32], где подачу соединения амина в реактор, в котором подвергают взаимодействию эфир карбоновой кислоты и соединение амина, осуществляют в жидкой фазе.
[34] Указанный способ в соответствии с любым одним из пунктов [1]-[33], где подачу соединения амина в реактор, в котором подвергают взаимодействию эфир карбоновой кислоты и соединение амина, осуществляют в виде смеси, включающей спирт, воду или эфир карбоновой кислоты.
Преимущества настоящего изобретения
В соответствии с указанным способом по настоящему изобретению изоцианаты можно с успехом получать непрерывно в течение длительного промежутка времени, используя диарилкарбонаты и соединения амина в качестве исходных материалов.
Краткое описание чертежей
Фиг. 1 представляет собой концептуальное изображение устройства для непрерывного получения эфира карбоновой кислоты в соответствии с вариантом настоящего изобретения;
фиг. 2 представляет собой концептуальное изображение устройства для получения ароматического эфира карбоновой кислоты в соответствии с вариантом настоящего изобретения;
фиг. 3 представляет собой концептуальное изображение устройства для получения ароматического эфира карбоновой кислоты в соответствии с вариантом настоящего изобретения;
фиг. 4 представляет собой концептуальное изображение устройства для очистки спирта в соответствии с вариантом настоящего изобретения;
фиг. 5 представляет собой концептуальное изображение устройства для очистки диарилкарбоната в соответствии с вариантом настоящего изобретения;
фиг. 6 представляет собой концептуальное изображение устройства для очистки диарилкарбоната в соответствии с вариантом настоящего изобретения;
фиг. 7 представляет собой концептуальное изображение устройства для получения арилкарбамата в соответствии с вариантом настоящего изобретения;
фиг. 8 представляет собой концептуальное изображение устройства для получения изоцианата в соответствии с вариантом настоящего изобретения;
фиг. 9 представляет собой концептуальное изображение устройства для получения изоцианата в соответствии с вариантом настоящего изобретения;
фиг. 10 представляет собой концептуальное изображение устройства для получения изоцианата в соответствии с вариантом настоящего изобретения;
фиг. 11 представляет собой концептуальное изображение устройства для получения изоцианата в соответствии с вариантом настоящего изобретения;
фиг. 12 представляет собой концептуальное изображение устройства для получения изоцианата в соответствии с вариантом настоящего изобретения;
фиг. 13 представляет собой концептуальное изображение устройства для получения изоцианата в соответствии с вариантом настоящего изобретения;
фиг. 14 представляет собой концептуальное изображение устройства для получения изоцианата в соответствии с вариантом настоящего изобретения;
фиг. 15 представляет собой концептуальное изображение устройства для получения изоцианата в соответствии с вариантом настоящего изобретения; и
фиг. 16 представляет собой концептуальное изображение устройства для получения арилкарбамата в соответствии с вариантом настоящего изобретения.
Краткое описание номеров ссылок
(на фиг. 1)
101, 107: ректификационная колонна
102: реактор колонного типа
103, 106: тонкопленочный выпариватель
104: автоклав
105: декарбонизационный резервуар
111, 112, 117: ребойлер
121, 123, 126, 127: холодильник
1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17: линии
(на фиг. 2)
202: непрерывная многоступенчатая ректификационная колонна
205, 206: резервуар-хранилище
201: подогреватель
203: холодильник
204: ребойлер
21, 22, 23, 24, 25: линии
(на фиг. 3)
302: непрерывная многоступенчатая ректификационная колонна
305, 306: резервуар-хранилище
301: подогреватель
303: холодильник
304: ребойлер
31, 32, 33, 34, 35: линии
(на фиг. 4)
402: непрерывная многоступенчатая ректификационная колонна
405, 406: резервуар-хранилище
401: подогреватель
403: холодильник
404: ребойлер
41, 42, 43, 44, 45: линии
(на фиг. 5)
502: непрерывная многоступенчатая ректификационная колонна
505, 506: резервуар-хранилище
501: подогреватель
503: холодильник
504: ребойлер
51, 52, 53, 54, 55: линии
(на фиг. 6)
602: непрерывная многоступенчатая ректификационная колонна
605, 606: резервуар-хранилище
601: подогреватель
603: холодильник
604: ребойлер
61, 62, 63, 64, 65: линии
(на фиг. 7)
701, 702, 703, 705: резервуар-хранилище
704: реактор с разделительными перегородками
71, 72, 73, 74: линии
(на фиг. 8)
801: тонкопленочный выпариватель
802, 803: непрерывная многоступенчатая ректификационная колонна
808, 809, 810: резервуар-хранилище
803, 806: холодильник
804, 807: ребойлер
81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94: линии
(на фиг. 9)
902: непрерывная многоступенчатая ректификационная колонна
905, 906: резервуар-хранилище
901: подогреватель
903: холодильник
904: ребойлер
95, 96, 97, 98, 99: линии
(на фиг. 10)
1002: непрерывная многоступенчатая ректификационная колонна
1005, 1006: резервуар-хранилище
1001: подогреватель
1003: холодильник
1004: ребойлер
A1, A2, A3, A4, A5: линии
(на фиг. 11)
1102: непрерывная многоступенчатая ректификационная колонна
1105, 1106: резервуар-хранилище
1101: подогреватель
1103: холодильник
1104: ребойлер
B1, B2, B3, B4, B5: линии
(на фиг. 12)
1201: тонкопленочный выпариватель
1202, 1205, 1208: непрерывная многоступенчатая ректификационная колонна
1203, 1206, 1209: холодильник
1204, 1207, 1210: ребойлер
C1, C2, C3, C4, C5, C6, C7, C8, C9, C10, C11, C12, C13, C14, C15, C16, C17, C18: линии
(на фиг. 13)
1301, 1304, 1307: непрерывная многоступенчатая ректификационная колонна
1302, 1305, 1308: холодильник
1303, 1306, 1309: ребойлер
D1, D2, D3, D4, D5, D6, D7, D8, D9, D10, D11, D12, D13, D14, D15: линии
(на фиг. 14)
1401, 1402, 1403, 1409, 1411: резервуар-хранилище
1404: реактор с разделительными перегородками
1405, 1406: непрерывная многоступенчатая ректификационная колонна
1407, 1410: холодильник
1408, 1412: ребойлер
E1, E2, E3, E4, E5, E6, E7, E8, E9, E10, E11, E12, E13: линии
(на фиг. 15)
1501, 1502, 1503: резервуар-хранилище
1504: реактор с разделительными перегородками
1506, 1509, 1512: непрерывная многоступенчатая ректификационная колонна
1505, 1508, 1511: холодильник
1507, 1510, 1513: ребойлер
F1, F2, F3, F4, F5, F6, F7, F8, F9, F10, F11, F12, F13, F14, F15, F16, F17, F18: линии
(на фиг. 16)
1601, 1602, 1603, 1606: резервуар-хранилище
1604: реактор с разделительными перегородками
1605: колонна
1607: холодильник
G1, G2, G3, G4, G5, G6: линии
Предпочтительный вариант осуществления изобретения
Далее предложено подробное объяснение предпочтительного варианта способа осуществления по настоящему изобретению (здесь и далее именуемого как “настоящий вариант”). Кроме того, настоящее изобретение не ограничено следующим рассматриваемым вариантом, но скорее может быть модифицировано различными способами в рамках объема сущности настоящего изобретения.
Способ получения в рассматриваемом варианте представляет собой способ получения изоцианата, который включает стадии:
получения реакционной смеси, содержащей арилкарбамат, содержащий арильную группу, образовавшуюся из диарилкарбоната, ароматическое гидроксисоединение, образовавшееся из диарилкарбоната, и диарилкарбонат, путем осуществления взаимодействия диарилкарбоната и соединения амина в присутствии ароматического гидроксисоединения в качестве реакционного растворителя, переноса реакционной смеси в реактор термического разложения и получения изоцианата путем осуществления реакции термического разложения арилкарбамата; где
реактор, в котором осуществляют реакцию между диарилкарбонатом и соединением амина, и реактор термического разложения арилкарбамата различны.
Описание приведено, во-первых, при условии, что диарилкарбонат и соединение амина, используемые в указанном способе, получают в соответствии с рассматриваемым вариантом.
Диарилкарбонат, используемый в способе получения в соответствии с рассматриваемым вариантом, представляет собой соединение представленное следующей формулой (13):
(где R1 представляет собой ароматическую группу, содержащую от 6 до 20 атомов углерода).
R1 в вышеприведенной формуле (13) является предпочтительно ароматической углеводородной группой, содержащей от 6 до 20 атомов углерода, и более предпочтительно ароматической углеводородной группой, содержащей от 6 до 12 атомов углерода. Хотя можно использовать диарилкарбонат, в котором R1 представляет собой ароматическую углеводородную группу, содержащую 21 или более атомов углерода, с точки зрения простоты выделения изоцианата, образованного в указанной реакции термического разложения эфира карбаминовой кислоты, что будет раскрыто далее, предпочтительно, чтобы число атомов углерода, составляющих R1, было 20 или менее.
Конкретные примеры таких R1 могут включать фенильную группу, метилфенильную группу (включая изомеры), этилфенильную группу (включая изомеры), пропилфенильную группу (включая изомеры), бутилфенильную группу (включая изомеры), пентилфенильную группу (включая изомеры), гексилфенильную группу (включая изомеры), диметилфенильную группу (включая изомеры), метилэтилфенильную группу (включая изомеры), метилпропилфенильную группу (включая изомеры), метилбутилфенильную группу (включая изомеры), метилпентилфенильную группу (включая изомеры), диэтилфенильную группу (включая изомеры), этилпропилфенильную группу (включая изомеры), этилбутилфенильную группу (включая изомеры), дипропилфенильную группу (включая изомеры), триметилфенильную группу (включая изомеры), триэтилфенильную группу (включая изомеры) и нафтильную группу (включая изомеры). Среди указанных диарилкарбонатов предпочтительны диарилкарбонаты, в которых R1 представляет собой ароматическую углеводородную группу, содержащую от 6 до 8 атомов углерода, и примеры таких диарилкарбонатов могут включать дифенилкарбонат, ди(метилфенил)карбонат (включая изомеры), ди(диэтилфенил)карбонат (включая изомеры) и ди(метилэтилфенил)карбонат (включая изомеры).
Указанные диарилкарбонаты содержат атомы металлов предпочтительно в интервале количественных значений от 0,001 м.д. до 10%, более предпочтительно в интервале количественных значений от 0,001 м.д. до 5% и еще более предпочтительно в интервале количественных значений от 0,002 м.д. до 3%. Кроме того, атомы металлов могут присутствовать в форме ионов металла или в форме отдельных атомов металла. Атомы металла предпочтительно являются атомами металлов с валентностями от 2 до 4 и предпочтительно одного типа или нескольких типов металлов, выбранных из группы, состоящей из железа, кобальта, никеля, цинка, олова, меди и титана. Авторы настоящего изобретения неожиданно обнаружили, что, если используют диарилкарбонат, содержащий атомы металла в вышеуказанных пределах концентрации, наблюдается эффект ингибирования реакции денатурирования арилкарбамата, образующегося в реакциях между диарилкарбонатом и соединением амина. Хотя механизм возникновения указанного эффекта не ясен, авторы настоящего изобретения предположили, что указанные атомы металла координируют с уретановыми связями (-NHCOO-) эфира карбаминовой кислоты, образующегося в реакции, тем самым, стабилизируя уретановые связи и ингибируя побочные реакции, указанные, например, выше в формулах (4) и (8). Кроме того, хотя эффект, который вызывают указанные атомы металла в отношении ингибирования реакции денатурирования арилкарбаматов, наблюдался также при переносе реакционных растворов, содержащих арилкарбаматы, как будет раскрыто далее, предполагают, что это тот же механизм, который раскрыт выше.
Хотя ожидается, что аналогичные эффекты будут происходить, даже если смесь получена путем смешивания диарилкарбоната и соединения амина и к смеси будут добавлены указанные ранее примеры атомов металлов в вышеуказанных интервалах концентраций, в результате проведенных авторами настоящего изобретения интенсивных исследований было обнаружено, что вышеописанных эффектов трудно достичь, если просто добавлять атомы металла к смеси диарилкарбоната и соединения амина. Хотя причина получения такого результата непонятна, авторы настоящего изобретения предположили, что, в противоположность диарилкарбонату, координированному с атомами металла, содержащимися в диарилкарбонате, так как взаимодействие между атомами металла и соединением амина больше, чем взаимодействие между атомами металла и диарилкарбоната, атомы металла, добавленные к смеси диарилкарбоната и соединения амина, в значительной степени координируют с соединением амина, тем самым, затрудняя координацию с уретановой связью образовавшегося арилкарбамата.
Хотя эфир карбаминовой кислоты в рассматриваемом варианте предпочтительно получают, используя раскрытый далее способ, в том случае, если указанные ранее примеры атомов металлов содержатся в диарилкарбонате, полученном в соответствии с указанным способом в раскрытом выше предпочтительном варианте, диарилкарбонат можно использовать, как он есть. В том случае, если количество атомов металла, содержащееся в указанном диарилкарбонате, меньше, чем значения указанного выше интервала, можно добавить другие атомы металла в форме органической соли, такой как ацетат или нафтенаты, хлорид или комплекс ацетилацетона. Кроме того, в том случае, если количество атомов металла больше, чем указанный выше количественный интервал, атомы металла можно использовать после уменьшения количества диарилкарбоната до указанных ранее пределов за счет удаления, например, путем очистки растворителем, очистки перегонкой, кристаллизацией или с использованием ионообменной смолы, или удаления с помощью хелатообразующей смолы.
Кроме того, так как известно, что атомы металла, содержащиеся в вышеуказанном концентрационном интервале в диарилкарбонатах, не обладают каталитической активностью в реакции между диарилкарбонатами и соединениями амина почти во всех случаях, в этом смысле, они четко отличаются от катализаторов, используемых для получения арилкарбаматов, что будет раскрыто далее.
Так как количество компонентов металла, содержащееся в диарилкарбонате, можно количественно определить различными известными способами, такими как атомно-абсорбционный анализ, спектрометрия с индуктивно связанной плазмой - спектрометрия с атомным излучением, масс-спектрометрия с индуктивно связанной плазмой, флуоресцентный рентгеновский анализ, рентгеновская фотоэлектронная спектроскопия, электронно-лучевой микроанализ или масс-спектрометрия вторичных ионов, способ можно выбрать с учетом формы образца и количества содержащихся в нем металлических компонентов.
Хотя известный процесс можно использовать для получения диарилкарбоната, предпочтительно используют способ, в котором подвергают взаимодействию оловоорганическое соединение, содержащее олово-кислород-углеродную связь, с двуокисью углерода для получения эфира карбоновой кислоты с последующим получением диарилкарбоната из эфира карбоновой кислоты и ароматического гидроксисоединения. А именно эфир карбоновой кислоты можно получить в соответствии со способом, включающим стадии:
стадия (1): (стадия получения диалкилкарбоната) получения реакционной смеси, содержащей диалкилкарбонат, путем осуществления взаимодействия оловоорганического соединения, содержащего олово-кислород-углеродную связь, и двуокиси углерода;
стадия (2): (стадия выделения диалкилкарбоната) получения диалкилкарбоната и остаточной жидкости путем разделения реакционной смеси; и
стадия (3): (стадия получения диарилкарбоната) получения диарилкарбоната путем осуществления взаимодействия диалкилкарбоната, выделенного на стадии (2), и ароматического гидроксисоединения A с последующим выделением побочного продукта спирта.
Кроме того, следующие стадии (4) и (5) можно осуществить помимо стадий (1)-(3), причем стадии (4) и (5) включают следующие стадии:
стадия (4): (стадия регенерации оловоорганического соединения) получение оловоорганического соединения, содержащего олово-кислород-углеродную связь и воду, путем осуществления взаимодействия остаточной жидкости, полученной на стадии (2), со спиртом с последующим удалением воды из реакционной системы; и
стадия (5): (стадия рециркуляции) повторное использование оловоорганического соединения, содержащего олово-кислород-углеродную связь, полученного на стадии (4), в качестве оловоорганического соединения, содержащего олово-кислород-углеродную связь стадии (1).
Указанные соединения диалкилолова предпочтительно используют в качестве оловоорганических соединений, используемых на стадии (1). Указанное соединение диалкилолова относится к оловоорганическому соединению, в котором две алкильные группы связаны с одним атомом олова.
Примеры указанных соединений диалкилолова могут включать соединения, выбранные из, по меньшей мере, одного типа соединений, выбранных из группы, состоящей из соединений диалкилолова, представленных следующей формулой (14), и соединений тетраалкилдистанноксана, представленных следующей формулой (15):
(каждый из R3 и R4 независимо представляет собой неразветвленную или разветвленную алкильную группу, содержащую от 1 до 12 атомов углерода,
каждый из X1 и X2 независимо представляет собой, по меньшей мере, один тип заместителя, выбранный из группы, состоящей из алкоксигруппы, ацилоксигруппы и атома галогена,
каждый из a и b представляет собой целое число от 0 до 2, и a+b=2, и
каждый из c и d представляет собой целое число от 0 до 2, и c+d=2);
(каждый из R5, R6, R7 и R8 независимо представляет собой неразветвленную или разветвленную алкильную группу, содержащую от 1 до 12 атомов углерода,
X3 и X4 представляют собой, по меньшей мере, один тип заместителя, выбранный из группы, состоящей из алкоксигруппы, ацилоксигруппы и атома галогена, и
каждый из e, f, g и h представляет собой целое число от 0 до 2, e+f=2 и g+h=2).
Примеры R3 и R4 в катализаторе диалкилолова, представленного в вышеприведенной формуле (14), также как примеры R5, R6, R7 и R8 в соединении тетраалкилдистанноксана, представленном выше в формуле (15), могут включать алкильные группы в форме алифатических углеводородных групп, в которых число атомов углерода, составляющих указанную группу, является числом, выбранным из группы, состоящей из целых чисел от 1 до 12, таких как метильная группа, этильная группа, пропильная группа (включая изомеры), бутильная группа (включая изомеры), пентильная группа (включая изомеры), гексильная группа (включая изомеры), гептильная группа (включая изомеры), октильная группа (включая изомеры), нонильная группа (включая изомеры), децильная группа (включая изомеры) или додецильная группа (включая изомеры). Более предпочтительные примеры могут включать неразветвленные или разветвленные алкильные группы, в которых число атомов углерода составляющих указанную группу, является числом, выбранным из группы, состоящей из целых чисел от 1 до 8, и, хотя можно использовать соединения диалкилолова, в алкильных группах которых число атомов углерода, составляющих группу, находится вне указанного интервала значений, существуют случаи, в которых текучесть может быть недостаточной или производительность может быть снижена. Кроме того, н-бутильная группа или н-октильная группа являются более предпочтительными с учетом производства в промышленных масштабах.
X1 и X2 соединения диалкилолова, представленного вышеприведенной формулой (14), и X3 и X4 соединения тетраалкилдистанноксана, представленного вышеприведенной формулой (15), представляют, по меньшей мере, один тип заместителей, выбранных из группы, состоящей из алкоксигруппы, ацилоксигруппы и атома галогена, и в случае, если указанная группа представляет собой алкоксигруппу и/или ацилоксигруппу, число атомов углерода, составляющих группу, предпочтительно представляет собой число, выбранное из группы, состоящей из целых чисел от 0 до 12. Примеры таких групп могут включать алкоксигруппы, состоящие из неразветвленной или разветвленной насыщенной алкильной группы и атома кислорода, такие как метоксигруппа, этоксигруппа, пропоксигруппа (включая изомеры), бутоксигруппа (включая изомеры), пентилоксигруппа (включая изомеры), гексилоксигруппа (включая изомеры), гептилоксигруппа (включая изомеры), октилоксигруппа (включая изомеры), нонилоксигруппа (включая изомеры) или децилоксигруппа (включая изомеры); ацилоксируппы, состоящие из неразветвленной или разветвленной насыщенной алкильной группы, карбонильной группы и атома кислорода, такие как ацетоксигруппа, пропионилоксигруппа, бутирилоксигруппа, валерилоксигруппа или лауроилоксигруппа; и атом галогена, такой как группа хлора или группа брома. Более предпочтительные примеры могут включать алкоксигруппы, содержащие от 4 до 6 атомов углерода, с учетом текучести и растворимости, также как использования катализатора получения эфира карбоновой кислоты.
Примеры соединений диалкилолова, представленных формулой (14), могут включать соединения диалкил-диалкоксиолова, такие как диметил-диметоксиолово, диметил-диэтоксиолово, диметил-дипропоксиолово (включая изомеры), диметил-дибутоксиолово (включая изомеры), диметил-дипентилоксиолово (включая изомеры), диметил-дигексилоксиолово (включая изомеры), диметил-дигептилоксиолово (включая изомеры), диметил-диоктилоксиолово (включая изомеры), диметил-динонилоксиолово (включая изомеры), диметил-дидецилоксиолово (включая изомеры), дибутил-диметоксиолово (включая изомеры), дибутил-диэтоксиолово (включая изомеры), дибутил-дипропоксиолово (включая изомеры), дибутил-дибутилоксиолово (включая изомеры), дибутил-дипентилоксиолово (включая изомеры), дибутил-дигексилоксиолово (включая изомеры), дибутил-дигептилоксиолово (включая изомеры), дибутил-диоктилоксиолово (включая изомеры), дибутил-динонилоксиолово (включая изомеры), дибутил-дидецилоксиолово (включая изомеры), диоктил-диметоксиолово (включая изомеры), диоктил-диэтоксиолово (включая изомеры), диоктил-дипропоксиолово (включая изомеры), диоктил-дибутилоксиолово (включая изомеры), диоктил-дипентилоксиолово (включая изомеры), диоктил-дигексилоксиолово (включая изомеры), диоктил-дигептилоксиолово (включая изомеры), диоктил-диоктилоксиолово (включая изомеры), диоктил-динонилоксиолово (включая изомеры) или диоктил-дидецилоксиолово (включая изомеры); соединения диалкил-диацилоксиолова, такие как диметил-диацетоксиолово, диметил-дипропионилоксиолово (включая изомеры), диметил-дибутирилоксиолово (включая изомеры), диметил-валерилоксиолово (включая изомеры), диметил-дилауроилоксиолово (включая изомеры), дибутил-диацетоксиолово (включая изомеры), дибутил-дипропионилоксиолово (включая изомеры), дибутил-дибутирилоксиолово (включая изомеры), дибутил-дивалерилоксиолово (включая изомеры), дибутил-дилауроилоксиолово (включая изомеры), диоктил-диацетоксиолово (включая изомеры), диоктил-дипропионилоксиолово (включая изомеры), диоктил-дибутирилоксиолово (включая изомеры), диоктил-валерилоксиолово (включая изомеры) или диоктил-дилауроилокси олово (включая изомеры); и диалкил-дигалогениды олова, такие как диметил-дихлоролово, диметил-дибромолово, дибутил-дихлоролово (включая изомеры), дибутил-дибромолово (включая изомеры), диоктил-дихлоролово (включая изомеры) или диоктил-дибромолово (включая изомеры).
Среди них предпочтительны диалкоксиды диалкилолова, такие как диметил-диметоксиолово, диметил-диэтоксиолово, диметил-дипропоксиолово (включая изомеры), диметил-дибутоксиолово (включая изомеры), диметил-дипентилоксиолово (включая изомеры), диметил-дигексилоксиолово (включая изомеры), диметил-дигептилоксиолово (включая изомеры), диметил-диоктилоксиолово (включая изомеры), диметил-динонилоксиолово (включая изомеры), диметил-дидецилоксиолово (включая изомеры), дибутил-диметоксиолово (включая изомеры), дибутил-диэтоксиолово (включая изомеры), дибутил-дипропоксиолово (включая изомеры), дибутил-дибутилоксиолово (включая изомеры), дибутил-дипентилоксиолово (включая изомеры), дибутил-дигексилоксиолово (включая изомеры), дибутил-дигептилоксиолово (включая изомеры), дибутил-диоктилоксиолово (включая изомеры), дибутил-динонилоксиолово (включая изомеры), дибутил-дидецилоксиолово (включая изомеры), диоктил-диметоксиолово (включая изомеры), диоктил-диэтоксиолово (включая изомеры), диоктил-дипропоксиолово (включая изомеры), диоктил-дибутилоксиолово (включая изомеры), диоктил-дипентилоксиолово (включая изомеры), диоктил-дигексилоксиолово (включая изомеры), диоктил-дигептилоксиолово (включая изомеры), диоктил-диоктилоксиолово (включая изомеры), диоктил-динонилоксиолово (включая изомеры) или диоктил-дидецилоксиолово (включая изомеры), более предпочтительны соединения диалкил-диалкоксиолова, такие как дибутил-дипропоксиолово (включая изомеры), дибутил-дибутирилоксиолово (включая изомеры), дибутил-дипентилоксиолово (включая изомеры), дибутил-дигексилоксиолово (включая изомеры), дибутил-дигептилоксиолово (включая изомеры), диоктил-дипропоксиолово (включая изомеры), диоктил-дибутоксиолово (включая изомеры), диоктил-дипентилоксиолово (включая изомеры), диоктил-дигексилоксиолово (включая изомеры) или диоктил-дигептилоксиолово (включая изомеры), и еще более предпочтительны дибутил-дибутилоксиолово (включая изомеры), дибутил-дипентилоксиолово (включая изомеры), дибутил-дигексилоксиолово (включая изомеры), дибутил-дигептилоксиолово (включая изомеры), дибутил-диоктилоксиолово (включая изомеры), диоктил-дибутилоксиолово (включая изомеры), диоктил-дипентилоксиолово (включая изомеры), диоктил-дигексилоксиолово (включая изомеры), диоктил-дигептилоксиолово (включая изомеры) или диоктил-диоктилоксиолово (включая изомеры).
Хотя соединения диалкилолова, представленные формулой (14), демонстрируют мономерную структуру, они могут иметь полимерную структуру или быть в форме ассоциатов.
Примеры тетраалкилдиалкоксидистанноксанов, представленных формулой (15), могут включать 1,1,3,3-тетраалкил-1,3-диалкоксидистанноксаны, такие как 1,1,3,3-тетраметил-1,3-диметоксидистанноксан, 1,1,3,3-тетраметил-1,3-диэтоксидистанноксан, 1,1,3,3-тетраметил-1,3-дипропоксидистанноксан (включая изомеры), 1,1,3,3-тетраметил-1,3-дибутоксидистанноксан (включая изомеры), 1,1,3,3-тетраметил-1,3-дипентилоксидистанноксан (включая изомеры), 1,1,3,3- тетраметил-1,3-дигексилоксидистанноксан (включая изомеры), 1,1,3,3-тетраметил-1,3-дигептилоксидистанноксан (включая изомеры), 1,1,3,3-тетраметил-1,3-диоктилоксидистанноксан (включая изомеры), 1,1,3,3-тетраметил-1,3-динонилоксидистанноксан (включая изомеры), 1,1,3,3-тетраметил-1,3-дидецилоксидистанноксан (включая изомеры), 1,1,3,3-тетрабутил-1,3-диметоксидистанноксан (включая изомеры), 1,1,3,3-тетрабутил-1,3-диэтоксидистанноксан (включая изомеры), 1,1,3,3-тетрабутил-1,3-дипропоксидистанноксан (включая изомеры), 1,1,3,3-тетрабутил-1,3-дибутоксидистанноксан (включая изомеры), 1,1,3,3-тетрабутил-1,3-дипентилоксидистанноксан (включая изомеры), 1,1,3,3-тетрабутил-1,3-дигексилоксидистанноксан (включая изомеры), 1,1,3,3-тетрабутил-1,3-дигептилоксидистанноксан (включая изомеры), 1,1,3,3-тетрабутил-1,3-диоктилоксидистанноксан (включая изомеры), 1,1,3,3-тетрабутил-1,3-динонилоксидистанноксан (включая изомеры), 1,1,3,3-тетрабутил-1,3-дидецилоксидистанноксан (включая изомеры), 1,1,3,3-тетраоктил-1,3-диметоксидистанноксан (включая изомеры), 1,1,3,3-тетраоктил-1,3-диэтоксидистанноксан (включая изомеры), 1,1,3,3-тетраоктил-1,3-дипропоксидистанноксан (включая изомеры), 1,1,3,3-тетраоктил-1,3-дибутоксидистанноксан (включая изомеры), 1,1,3,3-тетраоктил-1,3-дипентилоксидистанноксан (включая изомеры), 1,1,3,3-тетраоктил-1,3-дигексилоксидистанноксан (включая изомеры), 1,1,3,3-тетраоктил-1,3-дигептилоксидистанноксан (включая изомеры), 1,1,3,3-тетраоктил-1,3-диоктилоксидистанноксан (включая изомеры), 1,1,3,3-тетраоктил-1,3-динонилоксидистанноксан (включая изомеры) или 1,1,3,3-тетраоктил-1,3-дидецилоксидистанноксан (включая изомеры);
1,1,3,3-тетраалкил-1,3-диацилоксидистанноксаны, такие как 1,1,3,3-тетраметил-1,3-диацетоксидистанноксан, 1,1,3,3-тетраметил-1,3-дипропионилоксидистанноксан (включая изомеры), 1,1,3,3-тетраметил-1,3-дибутирилоксидистанноксан (включая изомеры), 1,1,3,3-тетраметил-1,3-дивалерилоксидистанноксан (включая изомеры), 1,1,3,3-тетраметил-1,3-дилауроилоксидистанноксан (включая изомеры), 1,1,3,3-тетрабутил-1,3-диацетоксидистанноксан (включая изомеры), 1,1,3,3-тетрабутил-1,3-дипропионилоксидистанноксан (включая изомеры), 1,1,3,3-тетрабутил-1,3-дибутирилоксидистанноксан (включая изомеры), 1,1,3,3-тетрабутил-1,3-дивалерилоксидистанноксан (включая изомеры), 1,1,3,3-тетрабутил-1,3-дилауроилоксидистанноксан (включая изомеры), 1,1,3,3-тетраоктил-1,3-диацетоксидистанноксан (включая изомеры), 1,1,3,3-тетраоктил-1,3-дипропионилоксидистанноксан (включая изомеры), 1,1,3,3-тетраоктил-1,3-дибутирилоксидистанноксан (включая изомеры), 1,1,3,3-тетраоктил-1,3-дивалерилоксидистанноксан (включая изомеры) или 1,1,3,3-тетраоктил-1,3-дилауроилоксидистанноксан (включая изомеры); и
1,1,3,3-тетраалкил-1,3-дигалогениды дистанноксаны, такие как 1,1,3,3-тетраметил-1,3-дихлордистанноксан, 1,1,3,3-тетраметил-1,3-дибромдистанноксан, 1,1,3,3-тетрабутил-1,3-дихлордистанноксан (включая изомеры), 1,1,3,3-тетрабутил-1,3- дибромдистанноксан (включая изомеры), 1,1,3,3-тетраоктил-1,3-дихлордистанноксан (включая изомеры) или 1,1,3,3-тетраоктил-1,3-дибромдистанноксан (включая изомеры).
Среди них предпочтительны 1,1,3,3-тетраалкил-1,3-диалкоксидистанноксаны, такие как 1,1,3,3-тетраметил-1,3-диметоксидистанноксан, 1,1,3,3-тетраметил-1,3-диэтоксидистанноксан, 1,1,3,3-тетраметил-1,3-дипропоксидистанноксан (включая изомеры), 1,1,3,3-тетраметил-1,3-дибутоксидистанноксан (включая изомеры), 1,1,3,3-тетраметил-1,3-дипентилоксидистанноксан (включая изомеры), 1,1,3,3- тетраметил-1,3-дигексилоксидистанноксан (включая изомеры), 1,1,3,3-тетраметил-1,3-дигептилоксидистанноксан (включая изомеры), 1,1,3,3-тетраметил-1,3-диоктилоксидистанноксан (включая изомеры), 1,1,3,3-тетраметил-1,3-динонилоксидистанноксан (включая изомеры), 1,1,3,3-тетраметил-1,3-дидецилоксидистанноксан (включая изомеры), 1,1,3,3-тетрабутил-1,3-диметоксидистанноксан (включая изомеры), 1,1,3,3-тетрабутил-1,3-диэтоксидистанноксан (включая изомеры), 1,1,3,3-тетрабутил-1,3-дипропоксидистанноксан (включая изомеры), 1,1,3,3-тетрабутил-1,3-дибутоксидистанноксан (включая изомеры), 1,1,3,3-тетрабутил-1,3-дипентилоксидистанноксан (включая изомеры), 1,1,3,3-тетрабутил-1,3-дигексилоксидистанноксан (включая изомеры), 1,1,3,3-тетрабутил-1,3-дигептилоксидистанноксан (включая изомеры), 1,1,3,3-тетрабутил-1,3-диоктилоксидистанноксан (включая изомеры), 1,1,3,3-тетрабутил-1,3-динонилоксидистанноксан (включая изомеры), 1,1,3,3-тетрабутил-1,3-дидецилоксидистанноксан (включая изомеры), 1,1,3,3-тетраоктил-1,3-диметоксидистанноксан (включая изомеры), 1,1,3,3-тетраоктил-1,3-диэтоксидистанноксан (включая изомеры), 1,1,3,3-тетраоктил-1,3-дипропоксидистанноксан (включая изомеры), 1,1,3,3-тетраоктил-1,3-дибутоксидистанноксан (включая изомеры), 1,1,3,3-тетраоктил-1,3-дипентилоксидистанноксан (включая изомеры), 1,1,3,3-тетраоктил-1,3-дигексилоксидистанноксан (включая изомеры), 1,1,3,3-тетраоктил-1,3-дигептилоксидистанноксан (включая изомеры), 1,1,3,3-тетраоктил-1,3-диоктилоксидистанноксан (включая изомеры), 1,1,3,3-тетраоктил-1,3-динонилоксидистанноксан (включая изомеры) или 1,1,3,3-тетраоктил-1,3-дидецилоксидистанноксан (включая изомеры), и более предпочтительны 1,1,3,3-тетрабутил-1,3-дибутоксидистанноксан (включая изомеры), 1,1,3,3-тетрабутил-1,3-дипентилоксидистанноксан (включая изомеры), 1,1,3,3-тетрабутил-1,3-дигексилоксидистанноксан (включая изомеры), 1,1,3,3-тетрабутил-1,3-дигептилоксидистанноксан (включая изомеры), 1,1,3,3-тетрабутил-1,3-диоктилоксидистанноксан (включая изомеры), 1,1,3,3-тетраоктил-1,3-дибутоксидистанноксан (включая изомеры), 1,1,3,3-тетраоктил-1,3-дипентилоксидистанноксан (включая изомеры), 1,1,3,3-тетраоктил-1,3-дигексилоксидистанноксан (включая изомеры), 1,1,3,3-тетраоктил-1,3-дигептилоксидистанноксан (включая изомеры) или 1,1,3,3-тетраоктил-1,3-диоктилоксидистанноксан (включая изомеры).
Хотя тетраалкилдиалкоксидистанноксаны, представленные формулой (15), демонстрируют мономерную структуру, они также могут иметь полимерную структуру или могут быть в форме ассоциатов.
Обычно органические соединения олова легко образуют ассоциативные структуры, и хотя, например, известно, что диалкилдиалкоксиолово образует димерную структуру, и известно, что присутствующие тетраалкилдиалкоксидистанноксаны образуют лестничную структуру, в которой ассоциированы две или три молекулы, даже в тех случаях, когда происходят изменения в указанном ассоциативном состоянии, представление соединения в форме мономерной структуры является обычным для специалистов в указанной области.
Кроме того, указанные ранее соединения диалкилолова можно использовать отдельно или их можно использовать в виде смеси двух или более типов соединений.
Раскрытый ранее способ получения (такой как те, что раскрыты в WO 2005/111049) можно предпочтительно использовать как способ получения соединений диалкилолова. Указанный способ представляет собой способ получения соединений диалкилолова из оксидов диалкилолова и спиртов.
Примеры спиртов, используемых в рассматриваемом варианте, могут включать спирты, такие как метанол, этанол, пропанол (включая изомеры), бутанол (включая изомеры), пентанол (включая изомеры), гексанол (включая изомеры), гептанол (включая изомеры), октанол (включая изомеры), нонанол (включая изомеры) или деканол (включая изомеры), и предпочтительно использовать спирт, в котором число атомов углерода, составляющих спирт, является числом, выбранным из группы, состоящей из целых чисел от 1 до 12.
Оксиды диалкилолова, представленные следующей формулой (16), используют в качестве оксида диалкилолова, используемого в процессе синтеза алкоксида алкилолова:
(каждый из R9 и R10 независимо представляет собой неразветвленную или разветвленную алкильную группу, содержащую от 1 до 12 атомов углерода).
Примеры R9 и R10 могут включать алкильные группы в форме алифатических углеводородных групп, содержащих от 1 до 12 атомов углерода, таких как метильная группа, этильная группа, пропильная группа (включая изомеры), бутильная группа (включая изомеры), пентильная группа (включая изомеры), гексильная группа (включая изомеры), гептильная группа (включая изомеры), октильная группа (включая изомеры), нонильная группа (включая изомеры), децильная группа (включая изомеры), ундецильная группа (включая изомеры) или додецильная группа (включая изомеры). Более предпочтительные примеры могут включать неразветвленные или разветвленные насыщенные алкильные группы, содержащие от 1 до 8 атомов углерода, тогда как еще более предпочтительные примеры могут включать н-бутильную группу и н-октильную группу.
Тетраалкилдиалкоксидистанноксаны и/или диалкоксиды диалкилолова получают в реакции дегидратации спирта и оксида диалкилолова, при этом удаляя из системы образующуюся воду. Температура, при которой осуществляют реакцию, находится, например, в интервале значений от 80 до 180°C, и для удаления из системы образующейся воды предпочтительны температуры от 100 до 180°C, хотя они меняются в зависимости от давления. Хотя высокая температура реакции предпочтительна для увеличения скорости реакции, так как нежелательные реакции, такие как разложение, также могут происходить при высоких температурах, тем самым, уменьшая выход, более предпочтительны температуры реакций в интервале значений от 100 до 160°C. Давление реакции представляет собой давление, которое позволяет удалять из системы образующуюся воду, и реакцию осуществляют при давлении от 20 до 1×106 Па, хотя и варьируя ее в соответствии с температурой реакции. Конкретных ограничений на время реакции дегидратации не существует, и обычно оно составляет от 0,001 до 50 часов, предпочтительно от 0,01 до 10 часов и более предпочтительно от 0,1 до 2 часов. Реакцию можно закончить после того, как достигают необходимой композиции алкоксида алкилолова. За ходом реакции также следят, измеряя количество воды, экстрагируемой из системы, и также определяя способом, в котором используют 119Sn-ЯМР, отбирая образцы реакционной жидкости. Для того чтобы получить смесь в соответствии с рассматриваемым вариантом настоящего изобретения на стадии (1), реакцию заканчивают после подтверждения факта получения композиции, в которой молярное отношение тетраалкилдиалкоксидистанноксана и диалкоксида диалкилолова, содержащихся в композиции алкоксида алкилолова, полученной в вышеуказанной реакции, если они выражены как объединенный молярный процент обоих, находится в интервале значений от 0:100 до 80:20 и более предпочтительно в интервале значений от 10:90 до 70:30. Используемый спирт можно использовать, пока он все еще присутствует в реакционной системе, и указанный спирт можно также использовать, отгоняя спирт, в зависимости от ситуации. Так как очень выгодно иметь возможность уменьшения размеров реакторов для следующих стадий, предпочтительно удалить как можно больше спирта. Удаление известным способом перегонки предпочтительно для способа удаления, и известное дистилляционное оборудование можно использовать в качестве дистиллятора, используемого для дистилляции. Тонкопленочные дистилляционные аппараты предпочтительно использовать в качестве дистилляционных аппаратов, так как спирт можно удалить за короткий промежуток времени. Относительно типа реакторов для проведения реакции дегидратации не существует конкретных ограничений, и можно использовать известные реакторы корпусного типа или типа колонны. Реакционную смесь с низкой температурой кипения, содержащую воду, экстрагируют в газообразной фазе из реактора путем перегонки, тогда как реакционную смесь с высокой температурой кипения, содержащую полученный алкоксид алкилолова или смесь алкоксидов алкилолова, отводят в форме жидкости из нижней части реактора. Для таких реакторов используют различные известные способы, примеры которых могут включать реакторы, содержащие резервуар перемешивания, многоступенчатый резервуар перемешивания, ректификационную колонну, многоступенчатую ректификационную колонну, многотрубчатый реактор, непрерывную многоступенчатую ректификационную колонну, насадочную колонну, тонкопленочный выпариватель, реактор, снабженный внутренней подложкой, реактор с принудительной циркуляцией, выпариватель с падающей пленкой, выпариватель с падающими каплями, струйный реактор или барботируемый колонный реактор, и типы реакторов, в которых используют их комбинации. Предпочтительны способы с использованием реактора типа колонны с точки зрения эффективности сдвига равновесия в сторону получения продуктов, хотя предпочтительна структура с высокой площадью контакта газ-жидкость для быстрого перевода образующейся воды в газообразную фазу. Хотя можно также использовать непрерывные способы с использованием многотрубчатого реактора, многоступенчатой ректификационной колонны или насадочной колонны, заполненной насадкой, так как оксид диалкилолова, используемый на этой стадии, обычно является твердым, предпочтительно использовать способ, в котором реакцию вначале ведут в реакторе корпусного типа, с последующим повышением содержания диалкоксида диалкилолова в реакторе колонного типа. Хотя в качестве материалов для реактора и линий можно использовать известные материалы, при условии, что они не оказывают вредного воздействия, предпочтительно использовать такие недорогие материалы, как SUS304, SUS316 или SUS316L. При необходимости можно добавить известную аппаратуру, используемую в процессе, такую как счетчик для жидкостей и газов, термометр и другие измерительные приборы или ребойлер, насос или холодильник и тому подобное; такие известные способы для нагревания, как пар или обогреватель, можно использовать для нагревания, и для охлаждения можно использовать такие известные способы, как воздушное охлаждение, охлаждение водой или солевым раствором.
Стадия (1) представляет собой стадию получения эфиров карбоновой кислоты путем осуществления взаимодействия соединения диалкилолова, полученного в соответствии с раскрытым выше процессом, с газообразной двуокисью углерода. Ранее раскрытые способы получения (такие как раскрытые в WO 03/055840 или WO 04/014840) эфира карбоновой кислоты предпочтительно использовать на этой стадии.
Соединения алкилолова, подаваемые на эту стадию, можно подавать со стадии синтеза алкоксида алкилолова в начале процесса получения или со стадии получения соединения диалкилолова стадии (4), что будет раскрыто далее, до стадии (5) в процессе непрерывного производства.
На стадии (1) вышеуказанные алкоксид диалкилолова и газообразная двуокись углерода абсорбируются и претерпевают химическую реакцию до получения смеси, содержащей связанную с двуокисью углерода форму алкоксида диалкилолова. Во время указанной химической реакции алкоксид диалкилолова реагирует в форме жидкости. Алкоксид диалкилолова предпочтительно переводят в форму жидкости путем нагревания для получения алкоксида диалкилолова в форме жидкости в случае, если алкоксид диалкилолова находится в твердой форме. Кроме того, его можно также перевести в жидкую форму, используя растворитель и тому подобное. Хотя, изменяясь в соответствии с температурой реакции, давление реакции предпочтительно находится в интервале значений от нормального давления до 1 МПа и более предпочтительно в интервале значений от нормального давления до 0,6 МПа. Хотя возможны изменения в соответствии с давлением реакции, температура реакции предпочтительно находится в интервале значений от -40 до 80°C, и с учетом проблемы текучести во время переноса более предпочтительна температура от 0 до 80°C, и наиболее предпочтительна температура в интервале значений от нормальной температура (например, 20°C) до 80°C. Время реакции может быть в интервале значений от нескольких секунд до 100 часов, и с учетом проблемы производительности и тому подобного оно предпочтительно составляет от нескольких минут до 10 часов. В качестве реактора можно использовать известный реактор корпусного типа или реактор колонного типа. Кроме того, несколько реакторов можно использовать в комбинации. Так как указанная реакция представляет собой реакцию между газообразной двуокисью углерода (газ) и композицией алкоксида алкилолова (жидкость), для эффективности осуществления реакции предпочтительно увеличить площадь поверхности контакта между газом и жидкостью за счет увеличения поверхности соприкосновения газ-жидкость. Известные находки можно использовать для способа осуществления взаимодействия, увеличивая, таким образом, поверхность соприкосновения газ-жидкость, и примеры таких предпочтительных способов могут включать увеличение скорости перемешивания или осуществление барботирования в жидкость в случае реактора корпусного типа и использование насадочной колонны или использование тарельчатой колонны в случае реактора колонного типа. Примеры таких реакторов колонного типа могут включать тарельчатые типы колонн, использующие такие тарелки, как барботажная тарелка, тарелка абсорбционной колонны, пористая тарелка, клапанная тарелка или тарелка в противотоке, и типы насадочных колонн, заполненные различными типами насадочных материалов, таких как кольца Рашига, кольца Лессинга, pole ring, седла Берля, Interlock saddle, насадку Диксона, насадку МакМагона, Helipack, насадку Sulzer или Mellapak. Хотя в качестве материала для реакторов и линий можно использовать известные материалы, при условии, что они не оказывают вредного воздействия, предпочтительно использовать такие недорогие материалы, как SUS304, SUS316 или SUS316L. Известные аппараты, используемые в процессе, такие как счетчики для жидкостей и газов, термометр и другие измерительные приборы или ребойлер, насос или холодильник и тому подобные, можно добавить при необходимости, можно использовать такие известные способы нагревания, как нагревание паром или за счет нагревателя, и можно использовать такие известные способы охлаждения, как воздушное охлаждение, охлаждение водой или солевым раствором. Так как реакция обычно является экзотермической реакцией, реактор можно охлаждать, или он может охлаждаться за счет рассеивания тепла. Альтернативно реактор может быть также нагреваемым, если целью является комбинация с реакцией этерификации карбоновой кислоты. Такие известные способы, как способ с использованием нагревательной рубашки или способ с использованием внутреннего змеевика, можно использовать для нагревания и охлаждения реактора. Композицию, состоящую из газообразной двуокиси углерода и алкоксида алкилолова, подаваемую в реактор, можно подавать в реактор раздельно, или их можно смешать до подачи в реактор. Указанные компоненты можно также подавать через различные места в реакторах. Завершение реакции можно определить с помощью, например, 119Sn-ЯМР анализа.
Далее, реакцонную жидкость, содержащую эфир карбоновой кислоты, получают из алкоксида диалкилолова, связанного с двуокисью углерода, полученного вышеуказанным способом.
Хотя температура реакции находится в интервале значений от 110 до 200°C и высокая температура реакции предпочтительна для увеличения скорости реакции, так как нежелательные реакции, такие как реакции разложения, также происходят при высоких температурах, тем самым, снижая выход, температура реакции более предпочтительна в интервале значений от 120 до 180°C, время реакции предпочтительно находится в интервале значений от 0,1 до 10 часов, и давление реакции находится в интервале значений от 1,5 до 20 МПа и предпочтительно от 2,0 до 10 МПа. Реакцию заканчивают после того, как в реакторах образуется необходимый эфир карбоновой кислоты. За ходом реакции можно следить, например, отбирая образцы реакционной жидкости в реакторах и анализируя образующийся эфир карбоновой кислоты такими способами, как 1H-ЯМР или газовая хроматография. Например, реакцию можно остановить после того, как эфир карбоновой кислоты образовался в молярном отношении 10% или более относительно алкоксида диалкилолова и/или формы алкоксида диалкилолова, связанного с двуокисью углерода, содержащейся в алкоксиде диалкилолова, и/или в форме алкоксида диалкилолова, связанного с двуокисью углерода, и в случае необходимости повысить выход эфира карбоновой кислоты реакцию можно остановить после достижения указанного значения 90% или более. В качестве реактора можно использовать известный реактор и предпочтительно использовать реактор колонного типа или реактор корпусного типа. Хотя в качестве материалов реактора и линий можно использовать известные материалы, при условии, что они не оказывают вредного воздействия, предпочтительно использовать такие недорогие материалы, как SUS304, SUS316 или SUS316L. При необходимости можно добавить известные технологические приборы, такие как счетчики для жидкостей и газов, термометр и другие измерительные приборы или ребойлер, насос или холодильник и тому подобное, для нагревания можно использовать такие известные способы, как пар или нагреватель, и для охлаждения можно использовать такие известные способы, как воздушное охлаждение, охлаждение водой или солевым раствором.
Стадия (2) в рассматриваемом варианте представляет собой стадию получения остаточной жидкости из реакционной жидкости, содержащей эфир карбоновой кислоты, полученной на вышеуказанной стадии (1) вместе с выделением и регенерацией эфира карбоновой кислоты. Известный способ или аппаратуру можно предпочтительно использовать в способе выделения, и предпочтительным способом является дистилляция.
Эфир карбоновой кислоты и оставшуюся жидкость получают путем периодической, полупериодической или непрерывной дистилляции реакционной жидкости, перенесенной с вышеуказанной стадии (1). Предпочтительный пример способа дистилляции состоит в подаче реакционной жидкости в дистиллятор, в выделении эфира карбоновой кислоты в форме газофазного компонента из верхней части дистиллятора и удалении из системы и в удалении оставшейся жидкости в форме жидкого компонента из нижней части дистиллятора. Хотя, изменяясь в соответствии с температурой кипения эфира карбоновой кислоты и давления, температура на этой стадии находится в интервале значений от нормальной температуры (например, 20°C) до 200°C и так как встречаются случаи, в которых может происходить денатурирование соединения олова в остаточной жидкости, или количество эфира карбоновой кислоты может уменьшаться за счет обратной реакции при высоких температурах, предпочтительны температуры в интервале значений от нормальной температуры (например, 20°C) до 150°C. Хотя изменяясь в соответствии с типом эфира карбоновой кислоты и температурой, при которой осуществляют реакцию, реакцию обычно осуществляют в условиях от нормального давления до пониженного давления, и с учетом производительности давление более предпочтительно в интервале значений от 100 Па до 80 кПа и наиболее предпочтительно в интервале значений от 100 Па до 50 кПа. Реакцию можно осуществить за время в интервале значений от 0,01 до 10 часов, и так как встречаются случаи, в которых соединения олова, содержащиеся в реакционной жидкости, денатурированы, и случаи, в которых количество эфира карбоновой кислоты уменьшается за счет обратной реакции, если реакцию осуществляют в течение длительного промежутка времени при высоких температурах, время реакции предпочтительно составляет от 0,01 до 0,5 часа и наиболее предпочтительно в интервале значений от 0,01 до 0,3 часа. В качестве дистиллятора можно использовать известный дистиллятор, дистиллятор колонного типа или дистиллятор корпусного типа предпочтительно, или несколько типов можно использовать в комбинации. Более предпочтительные дистилляторы состоят из тонкопленочного выпаривателя и тонкопленочного дистиллятора, и тонкопленочный выпариватель с дистилляционной колонной или тонкопленочный дистиллятор наиболее предпочтительны. Хотя известные материалы можно использовать в качестве материалов реактора и линий при условии, что они не оказывают вредного воздействия, то предпочтительно можно использовать такие недорогие материалы, как SUS304, SUS316 или SUS316L. Известные технологические приборы, такие как счетчики для жидкостей и газов, термометр и другие измерительные приборы или ребойлер, насос или холодильник и тому подобные, можно добавить, при необходимости, такие известные способы, как пар или нагреватель, можно использовать для нагревания и такие известные способы, как воздушное охлаждение, охлаждение водой или солевым раствором, можно использовать для охлаждения.
Стадия (3) представляет собой стадию получения диарилкарбоната путем осуществления взаимодействия диалкилкарбоната, выделенного на стадии (2), и ароматического гидроксисоединения A с последующим выделением побочного продукта спирта. Ароматическое гидроксисоединение, как здесь указано, относится к соединению R1OH, в котором атом водорода добавлен к группе R1O, составляющей диарилкарбонат, представленный вышеуказанной формулой (1) (где R1 представляет собой ароматическую группу, как определено ранее, и O представляет собой атом кислорода). Конкретные примеры предпочтительно используемых ароматических гидроксисоединений A могут включать фенол, монозамещенные фенолы, такие как метилфенол (включая изомеры), этилфенол (включая изомеры), пропилфенол (включая изомеры), бутилфенол (включая изомеры), пентилфенол (включая изомеры) или гексилфенол (включая изомеры); дизамещенные фенолы, такие как диметилфенол (включая изомеры), диэтилфенол (включая изомеры), дипропилфенол (включая изомеры), метилэтилфенол (включая изомеры), метилпропилфенол (включая изомеры), метилбутилфенол (включая изомеры), метилпентилфенол (включая изомеры), этилпропилфенол (включая изомеры) или этилбутилфенол (включая изомеры); тризамещенные фенолы, такие как триметилфенол (включая изомеры), триэтилфенол (включая изомеры), диметилэтилфенол (включая изомеры), диметилпропилфенол (включая изомеры) или диметилбутилфенол (включая изомеры); и нафтол (включая изомеры).
Стадия (3) в рассматриваемом варианте представляет собой стадию получения диарилкарбоната путем осуществления взаимодействия компонента, содержащего, главным образом, эфир карбоновой кислоты, выделенного на стадии (2), и ароматического гидроксисоединения A. Ранее были предложены многочисленные способы получения алкиларилкарбонатов и диарилкарбонатов из диалкилкарбонатов и ароматических гидроксисоединений, и указанные технологии также можно предпочтительно использовать в рассматриваемом варианте.
Реакция стадии (3) включает реакцию переэтерификации между эфирами карбоновой кислоты и ароматическими гидроксисоединениями, и реакцию диспропорционирования алкиларилкарбоната, полученного в результате реакции переэтерификации.
Реакция переэтерификации является равновесной реакцией, и для того чтобы реакция протекала успешно, предпочтительно при осуществлении реакции удалять спирт, образующийся в реакции переэтерификации, и в указанном случае температура кипения ароматического гидроксисоединения, используемого на стадии (3), предпочтительно выше, чем температура кипения алкилового спирта, составляющего алкилкарбонат, полученный на стадии (2). В частности, в случае непрерывного осуществления стадий (1)-(3) путем повтора один или более раз температура кипения алкилового спирта предпочтительно ниже, чем стандартная температура кипения ароматического гидроксисоединения, и разница между их температурами кипения составляет предпочтительно 2°C и более, предпочтительно 10°C с учетом легкости выделения.
Примеры диалкилкарбонатов, использованных на стадии (3), могут включать диметилкарбонат, диэтилкарбонат, дипропилкарбонат (включая изомеры), дибутилкарбонат (включая изомеры), дипентилкарбонат (включая изомеры), дигексилкарбонат (включая изомеры), дигептилкарбонат (включая изомеры), диоктилкарбонат (включая изомеры), динонилкарбонат (включая изомеры), дидецил карбонат (включая изомеры), дициклопентилкарбонат (включая изомеры), дициклогексилкарбонат (включая изомеры), дициклогептилкарбонат (включая изомеры), дибензилкарбонат, дифенэтилкарбонат (включая изомеры), ди(фенилпропил)карбонат (включая изомеры), ди(фенилбутил)карбонат (включая изомеры), ди(хлорбензил)карбонат (включая изомеры), ди(метоксибензил)карбонат (включая изомеры), ди(метоксиметил)карбонат (включая изомеры), ди(метоксиэтил)карбонат (включая изомеры), ди(хлорэтил)карбонат (включая изомеры), ди(цианоэтил)карбонат (включая изомеры), метилэтилкарбонат, метилпропилкарбонат (включая изомеры), метилбутилкарбонат (включая изомеры), этилпропилкарбонат (включая изомеры), этилбутилкарбонат (включая изомеры), этиленкарбонат и пропиленкарбонат. Используемым эфиром карбоновой кислоты может быть один из указанных типов алкилкарбонатов или их смесь.
Среди указанных диалкилкарбонатов, те диалкилкарбонаты, которые предпочтительно используют в рассматриваемом варианте, представляют собой диарилкарбонаты, у которых стандартная температура кипения спирта, составляющего эфир карбоновой кислоты, выше, чем стандартная температура кипения воды, например, алкиловые спирты, содержащие алкильную группу, содержащую от 4 до 12 атомов углерода, алкенильные спирты, содержащие неразветвленную или разветвленную алкенильную группу, содержащую от 4 до 12 атомов углерода, циклоалкильные спирты и аралкильные спирты. Для того чтобы реакция, осуществляемая на стадии (3), проходила более выгодно, спирт, у которого стандартная температура кипения ниже, чем стандартная температура кипения ароматического гидроксисоединения, используемого на стадии (3), являются более предпочтительными с учетом удаления спирта, образующегося на стадии реакции (3). А именно предпочтителен диалкилкарбонат, который состоит из спирта, стандартная температура кипения которого выше, чем стандартная температура кипения воды, но ниже, чем стандартная температура кипения ароматического гидроксисоединения.
Количество ароматического гидроксисоединения, используемого на стадии (3), выделяют на стадии (2), и его можно использовать в интервале значений стехиометрического отношения от 0,1 до 10000-кратного количества диалкилкарбоната, используемого на стадии (3). Так как реакция на стадии (3) является, в основном, равновесной реакцией, то, хотя использование большого количества ароматического гидроксисоединения является выгодным, так как увеличение используемого количества приводит к необходимости реактора больших размеров, также как и к более крупной ректификационной колонне для последующего разделения продукта, количество ароматического гидроксисоединения находится предпочтительно в интервале значений от 1 до 1000-кратного, и более предпочтительно в интервале значений от 1 до 100-кратного количества диалкилкарбоната.
Хотя соединения, которые подают на стадию (3), главным образом, состоят из диалкилкарбоната, ароматического гидроксисоединения и, при необходимости, катализатора, примеси могут присутствовать при условии, что они не оказывают вредного воздействия на реакцию.
Хотя продукты в виде спирта, алкиларилкарбоната и диарилкарбоната и тому подобного могут содержаться среди указанных загружаемых сырьевых материалов, так как реакция является обратимой, скорость реакции для сырых материалов снижается в том случае, если концентрации указанных продуктов чрезмерно высоки, тем самым, делая это нежелательным. Хотя возможны изменения в соответствии с типом и количеством катализатора и условиями реакции, весовое отношение подаваемого диалкилкарбоната и ароматического гидроксисоединения обычно является таким, что ароматическое гидроксисоединение предпочтительно подают в молярном отношении в интервале значений от 0,01 до 1000-кратного к диалкилкарбонату в подаваемых сырых материалах.
Хотя возможны изменения в соответствии с условиями реакции и типом и внутренней структурой реактора, время реакции переэтерификации стадии (3) обычно составляет от 0,001 до 50 часов, предпочтительно от 0,01 до 10 часов и более предпочтительно от 0,05 до 5 часов. Термин температура реакции относится к температуре внутри реактора, и хотя возможны изменения в соответствии с типами сырых материалов, используемых в форме диалкилкарбоната и ароматического гидроксисоединения, температура обычно составляет величину в интервале от 50 до 350°C и предпочтительно от 100 до 280°C. Кроме того, хотя возможны изменения в соответствии с типами используемых сырых материалов, температурой реакции и тому подобным, давление в реакции может быть пониженным давлением, нормальным давлением или повышенным давлением, и реакцию обычно осуществляют при давлении в интервале значений от 10 Па до 20 мПа.
Хотя в рассматриваемом варианте использование растворителя необязательно, подходящий инертный растворитель можно использовать в качестве реакционного растворителя с целью, например, облегчения протекания реакции, примеры которого могут включать простые эфиры, алифатические углеводороды, ароматические углеводороды, алифатические углеводородные галогениды и ароматические углеводородные галогениды. Кроме того, в реакционной системе могут также присутствовать инертные газы, такие как азот, гелий или аргон, в качестве инертного вещества в реакции, и вышеуказанные инертные газы и неактивные в реакции органические соединения с низкой температурой кипения можно вводить в газообразной форме в нижнюю часть непрерывной многоступенчатой ректификационной колонны с целью ускорения удаления побочных продуктов с низкой температурой кипения, образующихся в процессе перегонки.
Катализатор можно добавить в процессе осуществления реакции переэтерификации стадии (3). Хотя алкиларилкарбонат и диарилкарбонат получают из эфира карбоновой кислоты в реакции переэтерификации, как было раскрыто ранее, так как равновесие указанной реакции переэтерификации смещается в направлении реагентов, и так как скорость реакции низка, при получении диарилкарбоната указанным способом, были сделаны несколько предложений для его усовершенствования, и известный процесс можно предпочтительно использовать в рассматриваемом варианте.
Хотя возможны изменения в соответствии с типом используемого катализатора, типом реактора, типом и весовыми отношениями эфира карбоновой кислоты и ароматического гидроксисоединения и условиями реакции, такими как температура реакции и давление реакции, количество катализатора в случае использования катализатора в рассматриваемом варианте обычно составляет от 0,0001 до 50% по весу, будучи выражено как отношение к полному количеству эфира карбоновой кислоты и ароматического гидроксисоединения, как подаваемых сырых материалов. Кроме того, в случае использования твердого катализатора катализатор предпочтительно используют в количестве от 0,01 до 75% по объему, в расчете на объем пустой колонны реактора.
Известны многочисленные металлосодержащие катализаторы, предложенные в качестве катализаторов для повышения скорости реакции, и известные катализаторы реакции переэтерификации можно также использовать в рассматриваемом варианте. В способе получения алкиларилкарбоната и/или смеси алкиларилкарбоната и диарилкарбоната путем осуществления взаимодействия эфира карбоновой кислоты и ароматического гидроксисоединения, были предложены в качестве катализаторов кислоты Льюиса, такие как гидриды переходных металлов или соединения, из которых образуются кислоты Льюиса, соединения олова, такие как оловоорганические алкоксиды или оловоорганические оксиды, соли и алкоксиды щелочноземельных металлов или щелочных металлов, соединения свинца, комплексы металлов, такие как комплексы меди, железа или циркония, эфиры титановой кислоты, смеси кислот Льюиса и протонсодержащих кислот, соединения Sc, Mo, Mn, Bi или Te и ацетат железа были предложены как примеры таких катализаторов. Хотя образование диарилкарбоната может происходить только в результате реакции переэтерификации, он может также образовываться в результате реакции диспропорционирования алкиларилкарбонатов, образующихся в реакции переэтерификации. Здесь реакция диспропорционирования относится к реакции, в которой диалкилкарбонат и диарилкарбонат образуются из двух молекул алкиларилкарбоната. Хотя алкиларилкарбонат далее реагирует с ароматическим гидроксисоединением, превращаясь в диарилкарбонат, так как реакция диспропорционирования протекает быстрее, в случае необходимости получения диарилкарбоната диарилкарбонат получают в реакции диспропорционирования алкиларилкарбоната. Обе указанные реакции являются равновесными реакциями. Выгодно, чтобы реакция протекала во время экстрагирования алкилового спирта в реакции переэтерификации для получения алкиларилкарбоната, и выгодно, чтобы реакция протекала во время экстрагирования диалкилкарбоната на стадии реакции диспропорционирования. Таким образом, предпочтительные условия реакции отличаются на каждой стадии. Хотя необходимо осуществлять реакцию, разделяя на две стадии в случае осуществления непрерывной реакции, в случае осуществления реакции периодически, реакцию можно также осуществлять последовательно в одном и том же реакторе.
Таким образом, катализатор реакции диспропорционирования может также присутствовать вместе с ранее раскрытым катализатором трансэтерификации. Были предложены многочисленные примеры таких катализаторов, примеры которых могут включать кислоты Льюиса и соединения переходных металлов, из которых образуются кислоты Льюиса, полимерные соединения олова, соединения, представленные общей формулой R-X(=O)OH (где X выбран из группы, состоящей из Sn и Ti, где R выбран из группы, состоящей из одновалентных углеводородных групп), смеси кислот Льюиса и протонсодержащих кислот, свинцовых катализаторов, соединений титана и циркония, соединений олова и соединений Sc, Mo, Mn, Bi или Te.
Стадия диспропорционирования представляет собой стадию, в которой диалкилкарбонат и диарилкарбонат получают в реакции диспропорционирования алкиларилкарбоната, полученного на стадии трансэтерификации. Как было раскрыто ранее, катализатор диспропорционирования можно добавить, если реакцию переэтерификации и реакцию диспропорционирования осуществляют одновременно, или реакцию переэтерификации и реакцию диспропорционирования можно осуществлять отдельно и последовательно или периодически. Кроме того, хотя бывают ситуации, в которых диарилкарбонат получают одновременно с алкиларилкарбонатом в реакции переэтерификации, также как в случае осуществления реакции переэтерификации и реакции диспропорционирования отдельно, также как в случае, если реакцию диспропорционирования можно осуществить отдельно. Как было указано ранее, реакция диспропорционирования представляет собой стадию, на которой алкиларилкарбонат получают в реакции переэтерификации между диалкилкарбонатом и ароматическим гидроксисоединением, и для того чтобы указанная равновесная реакция протекала выгодно, выгодно также использовать способ, который дает возможность протекать реакции при одновременном удалении спирта. Так как указанная реакция диспропорционирования также подчиняется ограничению равновесия, в попытках предоставить реакции протекать с успехом выгоден способ, который позволяет реакции протекать при одновременном удалении из системы или диалкилкарбоната, или диарилкарбоната, образующихся в реакции диспропорционирования. В рассматриваемом варианте предпочтительно осуществлять реакцию диспропорционирования при одновременном удалении диалкилкарбоната из системы путем выбора соответствующих алкоксигрупп и арильных групп, так что полученный диалкилкарбонат кипит при более низкой температуре, чем диарилкарбонат. Отводимый диалкилкарбонат можно использовать, возвращая на стадию, предшествующую реакции диспропорционирования. Если количество полученного диарилкарбоната необходимо увеличить, предпочтительно использовать экстрагированный диалкилкарбонат, возвращая его на стадию трансэтерификации.
Катализатор реакции диспропорционирования можно использовать в реакции диспропорционирования. Были предложены многочисленные примеры таких катализаторов. Примеры таких предложенных катализаторов могут включать кислоты Льюиса и соединения переходных металлов, которые участвуют в получении кислот Льюиса, полимерные соединения олова, соединения, представленные общей формулой R-X(=O)OH (где X выбран из группы, состоящей из Sn и Ti, где R выбран из группы, состоящей из одновалентных углеводородных групп), смеси кислот Льюиса и протонсодержащих кислот, свинцовые катализаторы, соединения титана и циркония, соединения олова и Sc, Mo, Mn, Bi или Te.
Те же самые катализаторы, что и катализаторы трансэтерификации, используемые на стадии трансэтерификации, можно использовать в качестве катализаторов реакции диспропорционирования в рассматриваемом варианте.
Алкиларилкарбонат, используемый на стадии реакции диспропорционирования, представляет собой алкилариловый эфир карбоновой кислоты. Примеры алкиларилкарбонатов могут включать метилфенилкарбонат, этилфенилкарбонат, пропилфенилкарбонат (включая изомеры), бутилфенилкарбонат (включая изомеры), аллилфенилкарбонат (включая изомеры), пентилфенилкарбонат (включая изомеры), гексилфенилкарбонат (включая изомеры), гептилфенилкарбонат (включая изомеры), октилтолилкарбонат (включая изомеры), нонил(этилфенил)карбонат (включая изомеры), децил (бутилфенил)карбонат (включая изомеры), метилтолилкарбонат (включая изомеры), этилтолилкарбонат (включая изомеры), пропилтолилкарбонат (включая изомеры), бутилтолилкарбонат (включая изомеры), аллилтолилкарбонат (включая изомеры), метилксилилкарбонат (включая изомеры), метил(триметилфенил)карбонат (включая изомеры), метил(хлорфенил)карбонат (включая изомеры), метил(нитрофенил)карбонат (включая изомеры), метил(метоксифенил)карбонат (включая изомеры), метил(пиридил)карбонат (включая изомеры), этилкумилкарбонат (включая изомеры), метил(бензоилфенил)карбонат (включая изомеры), этилксилилкарбонат (включая изомеры) и бензилксилилкарбонат (включая изомеры). Указанные алкиларилкарбонаты могут представлять собой один тип или смесь двух или более типов.
Среди указанных алкиларилкарбонатов те, которые предпочтительно используют в рассматриваемом варианте, представляют собой алкиларилкарбонаты, в которых спирт, составляющий алкиларилкарбонат, представляет собой спирт, температура кипения которого выше, чем воды, температура кипения спирта, составляющего алкиларилкарбонат, ниже, чем температура кипения ароматического гидроксисоединения, составляющего алкиларилкарбонат, выбирают из, например, алкиловых спиртов, содержащих неразветвленную или разветвленную алкильную группу, содержащую от 4 до 12 атомов углерода, алкенильных спиртов, содержащих неразветвленную или разветвленную алкенильную группу, содержащую от 4 до 12 атомов углерода, циклоалкильных спиртов и аралкильных спиртов, и с учетом удаления диалкилкарбоната, образующегося в реакции диспропорционирования, предпочтительно, чтобы температура кипения диалкилкарбоната была ниже, чем диарилкарбоната, полученного в реакции диспропорционирования, чтобы реакция диспропорционирования протекала с выгодой. В качестве примеров таких оптимальных комбинаций, спирт, спирт, соответствующий алкоксигруппе соединения металла, содержащего металл-углерод-кислородную связь, представленную упомянутыми ранее формулами (14) и (15), и спирты, составляющие диалкилкарбонат, представляют собой спирты, выбранные из группы, состоящей из пентанола (включая изомеры), гексанола (включая изомеры) и гептанола (включая изомеры), тогда как ароматическое гидроксисоединение представляет собой ароматическое гидроксисоединение, выбранное из фенола и крезола.
Хотя соединения, подаваемые в реакцию диспропорционирования, главным образом, состоят из алкиларилкарбоната и катализатора при необходимости, примеси также могут присутствовать при условии, что они практически не оказывают вредного воздействия на ход реакции.
Хотя возможны изменения в соответствии с типом используемого катализатора, типом реактора, типом и количеством алкиларилкарбоната и условиями реакции, такими как температура реакции и давление реакции, количество катализатора в случае использования катализатора в рассматриваемом варианте обычно составляет от 0,0001 до 50% по весу, будучи выражено как отношение к полному количеству алкиларилкарбоната, как подаваемого сырого материала. Кроме того, в случае использования твердого катализатора катализатор предпочтительно используют в количестве от 0,01 до 75% по объему в расчете на объем пустой колонны реактора.
Хотя спирт, ароматическое гидроксисоединение и диарилкарбонат и тому подобное могут содержаться в указанных подаваемых сырых материалах, так как реакция является обратимой, скорость реакции сырых материалов снижается в случае, если концентрации указанных компонентов избыточно высоки, тем самым, делая это нежелательным.
Хотя возможны изменения в соответствии с условиями реакции и типом и внутренней структурой реактора, время реакции диспропорционирования обычно составляет от 0,001 до 50 часов, предпочтительно от 0,01 до 10 часов и более предпочтительно от 0,05 до 5 часов. Хотя возможны изменения в соответствии с типом используемого алкиларилкарбоната, температура реакции обычно находится в интервале значений от 50 до 350°C и предпочтительно от 100 до 280°C. Кроме того, хотя возможны изменения в соответствии с типами используемых соединений сырого материала, температурой реакции и тому подобного, давление реакции может быть пониженным давлением, нормальным давлением или повышенным давлением, и реакцию обычно осуществляют при давлении в интервале значений от 10 Па до 20 мПа.
Хотя использование растворителя не является обязательно необходимым на стадии диспропорционирования в рассматриваемом варианте, подходящий инертный растворитель можно использовать как реакционный растворитель с целью, например, облегчения протекания реакции, примеры которого могут включать простые эфиры, алифатические углеводороды, ароматические углеводороды, алифатические углеводородные галогениды и ароматические углеводородные галогениды. Кроме того, в реакционной системе могут также присутствовать инертные газы, такие как азот, гелий или аргон, в качестве инертного вещества в реакции, и вышеуказанные инертные газы и органические соединения с низкой температурой кипения, неактивные в реакции, можно вводить в газообразной форме из нижней части непрерывной многоступенчатой ректификационной колонны с целью ускорения дистилляции образующихся побочных продуктов с низкой температурой кипения.
После завершения реакции диспропорционирования диарилкарбонат получают путем удаления известными способами катализатора, алкиларилкарбоната, ароматического гидроксисоединения и спирта.
Не существует конкретных ограничений относительно типа реактора, используемого на стадиях трансэтерификации и диспропорционирования, и используют различные известные способы, примеры которых могут включать типы реакторов с использованием перемешиваемого резервуара, многоступенчатого перемешиваемого резервуара или многоступенчатой ректификационной колонны и их комбинаций. В качестве таких реакторов можно использовать реакторы периодического типа или непрерывного типа. Способы использования многоступенчатой ректификационной колонны предпочтительны с точки зрения эффективности сдвига равновесия в сторону получения продуктов, и особенно предпочтителен непрерывный способ с использованием многоступенчатой ректификационной колонны. Многоступенчатая ректификационная колонна относится к ректификационной колонне, включающей множество стадий, в которой число теоретических пластин дистилляции составляет две или более, и любую многоступенчатую ректификационную колонну можно использовать при условии, что она обеспечивает непрерывную дистилляцию. Любую многоступенчатую ректификационную колонну можно использовать в качестве многоступенчатой ректификационной колонны при условии, что она обычно используется в качестве многоступенчатой ректификационной колонны, примеры которых могут включать тарельчатые типы колонн, использующие такие тарелки, как барботажная тарелка, тарелка абсорбционной колонны, пористая тарелка, клапанная тарелка или тарелка в противотоке, и типы насадочных колонн, заполненные различными типами насадочных материалов, таких как кольца Рашига, кольца Лессинга, кольца pole, седла Берля, седла Interlock, насадку Диксона, насадку МакМагона, Helipack, насадку Sulzer или Mellapak. Кроме того, предпочтительно также использовать колонну тарельчато-насадочного типа, которая объединяет тарельчатую часть с насадочной частью, заполненную насадочным материалом. В случае осуществления непрерывного способа с использованием многоступенчатой ректификационной колонны исходные вещества и реагенты непрерывно подают в непрерывную многоступенчатую ректификационную колонну и одновременно осуществляют реакцию переэтерификации и/или реакцию диспропорционирования между обоими веществами в жидкой фазе или фазе газ-жидкость в присутствии металлосодержащего катализатора внутри ректификационной колонны, причем реакционную смесь с высокой температурой кипения, содержащую полученный алкиларилкарбонат и/или диарилкарбонат, отводят в жидкой форме из нижней части ректификационной колонны, а реакционную смесь с низкой температурой кипения, содержащую образующиеся побочные продукты, непрерывно отводят в газообразном состоянии из верхней части ректификационной колонны путем дистилляции, тем самым, получая в результате диарилкарбонат.
Хотя в предшествующем описании был приведен пример получения диарилкарбоната с использованием соединения диалкилолова, следующие стадии (4) и (5) можно осуществить, кроме вышеуказанных стадий (1)-(3), причем стадии (4) и (5) включают стадии:
стадия (4): образования оловоорганического соединения, содержащего олово-кислород-углеродную связь и воду, путем осуществления взаимодействия остаточной жидкости, полученной на стадии (2), со спиртом с последующим удалением воды из реакционной системы; и
стадия (5): повторного использования оловоорганического соединения, содержащего олово-кислород-углеродную связь, полученного на стадии (4), в качестве оловоорганического соединения, содержащего олово-кислород-углеродную связь, стадии (1).
Стадия (4) представляет собой стадию регенерации соединения диалкилолова путем осуществления взаимодействия остаточной жидкости, полученной на стадии (2), со спиртом.
Примеры спиртов, использованных на этой стадии, могут включать спирты, такие как метанол, этанол, пропанол (включая изомеры), бутанол (включая изомеры), пентанол (включая изомеры), гексанол (включая изомеры), гептанол (включая изомеры), октанол (включая изомеры), нонанол (включая изомеры) или деканол (включая изомеры), и хотя предпочтительно использовать спирт, в котором число атомов углерода, составляющих спирт, представляет собой число, выбранное из группы, состоящей из целых чисел от 1 до 12, более предпочтительно использовать тот же самый спирт, который используют на вышеуказанной стадии синтеза алкоксида алкилолова.
Предпочтительно, чтобы условия реакции дегидратации были такими же, что и условия на вышеуказанной стадии синтеза алкоксида алкилолова. Реакцию можно остановить после получения необходимой композиции алкоксида алкилолова. За ходом реакции можно также следить, измеряя количество воды, отводимой из системы, и можно также определить способом, в котором используют 119Sn-ЯМР, отбирая образцы реакционной жидкости. Для того чтобы получить смесь в рассматриваемом варианте на стадии (1), реакцию заканчивают после подтверждения получения композиции, в которой молярное отношение тетраалкилдиалкоксидистанноксана и диалкоксида диалкилолова, содержащихся в композиции алкоксида алкилолова, полученной в вышеуказанной реакции, будучи выражено как объединенное молярное отношение обоих, находится в интервале значений от 0:100 до 80:20 и более предпочтительно в интервале значений от 10:90 до 70:30. Использумый спирт может быть спиртом, присутствующим в реакционной системе, и спирт можно также удалять путем дистилляции, в зависимости от конкретного случая. Так как существенным преимуществом является возможность уменьшения реакторов на других стадиях, предпочтительно удалять как можно больше спирта. Удаление его известным способом дистилляции является предпочтительным способом удаления, и в качестве дистиллятора, используемого для дистилляции спирта, можно использовать известное оборудование для дистилляции. В качестве дистилляционного оборудования предпочтительно использовать тонкопленочные дистилляторы, так как спирт можно удалить за короткий промежуток времени. В отличие от стадии синтеза алкоксида алкилолова, так как оксид диалкилолова в твердом состоянии обычно не используют на этой стадии, в отношении реактора существует несколько ограничений. А именно, так как конкретных ограничений относительно типа реактора дегидратации не существует, можно использовать реактор известного корпусного типа или колонного типа. Реакционную смесь с низкой температурой кипения, содержащую воду, удаляют в газообразной форме из реактора путем перегонки, тогда как реакционную смесь с высокой температурой кипения, содержащую полученный алкоксид алкилолова или смесь алкоксида алкилолова, отводят в форме жидкости из нижней части реактора. Различные известные способы используют в таких реакторах, примеры которых могут включать используемые типы реакторов, содержащих перемешиваемый резервуар, многоступенчатый перемешиваемый резервуар, ректификационную колонну, многоступенчатую ректификационную колонну, многотрубный реактор, непрерывную многоступенчатую ректификационную колонну, насадочную колонну, тонкопленочный выпариватель, реактор, снабженный внутри носителем, реактор с принудительной циркуляцией, выпариватель с падающей пленкой, выпариватель с падающими каплями, реактор со струйным течением жидкости или барботажную колонну, и различные типы, в которых используют их комбинации. Способы с использованием колонного реактора предпочтительны с точки зрения эффективности сдвига равновесия в сторону получения продукта, причем устройство реактора с большой площадью контакта газ-жидкость предпочтительно, так как оно обеспечивает возможность быстрого перехода образующейся воды в газообразную фазу. Непрерывные способы с использованием многотрубного реактора, многоступенчатой ректификационной колонны или насадочной колонны, заполненной насадкой, наиболее предпочтительны. Хотя известные материалы можно использовать в качестве материалов реакторов и линий при условии, что они не оказывают вредного воздействия, и предпочтительно можно использовать такие недорогие материалы, как SUS304, SUS316 или SUS316L. Известные аппараты технологических процессов, такие как счетчики для жидкостей и газов, термометры и другие измерительные приборы или ребойлер, насос или холодильник и тому подобное, можно добавить, при необходимости, такие известные способы, как пар или нагреватель можно использовать для нагревания, и такие известные способы, как воздушное охлаждение, охлаждение водой или солевым раствором можно использовать для охлаждения.
Соединение диалкилолова, полученное на стадии (4), как раскрыто выше, повторно используют в качестве соединения диалкилолова, используемого на стадии (1), в соответствии со следующей стадией (5) (стадия рециркуляции), в которой оловоорганические соединения, содержащие олово-кислород-углеродную связь, полученные на стадии (4), повторно используют в качестве оловоорганических соединений, содержащих олово-кислород-углеродную связь стадии (1).
Соединения амина
С другой стороны, соединения амина, представленные следующей формулой (17), используют в качестве соединений амина, используемых в способе получения в соответствии с рассматриваемым вариантом:
(где R2 представляет собой группу, выбранную из группы, состоящей из алифатической группы, содержащей от 1 до 20 атомов углерода, и ароматической группы, содержащей от 6 до 20 атомов углерода, причем указанная группа содержит атом, выбранный из атомов углерода и кислорода, и имеющую валентность, равную n, и
n представляет собой целое число от 2 до 10).
В вышеприведенной формуле (17) предпочтительно используют полиамин, в котором n равно 2 или более, и более предпочтительно используют соединение диамина, в котором n равно 2.
В вышеприведенной формуле (17) R2 представляет собой более предпочтительно алкильную группу, содержащую от 1 до 20 атомов углерода, или циклоалкильную группу, содержащую от 5 до 20 атомов углерода, и примеры R2 могут включать линейные углеводороды, такие как метилен, диметилен, триметилен, тетраметилен, пентаметилен, гексаметилен или октаметилен; незамещенные алициклические углеводороды, такие как циклопентан, циклогексан, циклогептан, циклооктан или бис(циклогексил)алкан; алкилзамещенные циклогексаны, такие как метилциклопентан, этилциклопентан, метилциклогексан (включая изомеры), этилциклогексан (включая изомеры), пропилциклогексан (включая изомеры), бутилциклогексан (включая изомеры), пентилциклогексан (включая изомеры) или гексилциклогексан (включая изомеры); диалкилзамещенные циклогексаны, такие как диметилциклогексан (включая изомеры), диэтилциклогексан (включая изомеры) или дибутилциклогексан (включая изомеры); триалкилзамещенные циклогексаны, такие как 1,5,5-триметилциклогексан, 1,5,5-триэтилциклогексан, 1,5,5-трипропилциклогексан (включая изомеры) или 1,5,5-трибутилциклогексан (включая изомеры); моноалкилзамещенные бензолы, такие как толуол, этилбензол или пропилбензол; диалкилзамещенные бензолы, такие как ксилол, диэтилбензол или дипропилбензол; и ароматические углеводороды, такие как дифенилалкан или бензол. Особенно предпочтительно использовать гексаметиленовые, фениленовые, дифенилметановые, толуольные, циклогексановые, ксилольные, метилциклогексановые, изофороновые и дициклогексилметановые группы.
Примеры таких полимерных соединений амина могут включать алифатические диамины, такие как гексаметилендиамин, 4,4'-метиленбис(циклогексиламин) (включая изомеры), циклогександиамин (включая изомеры) или 3-аминометил-3,5,5-триметилциклогексиламин (включая изомеры); и ароматически диамины, такие как фенилендиамин (включая изомеры), толуолдиамин (включая изомеры) или 4,4'-метилендианилин (включая изомеры). Среди них более предпочтительно использовать алифатические диамины, такие как гексаметилендиамин, 4,4'-метиленбис(циклогексиламин) (включая изомеры), циклогександиамин (включая изомеры) и 3-аминометил-3,5,5-триметилциклогексиламин (включая изомеры), хотя более предпочтительно использовать гексаметилендиамин, 4,4'-метиленбис(циклогексиламин) и 3-аминометил-3,5,5-триметилциклогексиламин.
Реакция диарилкарбоната и соединения амина
Далее представлено объяснение реакции между раскрытым ранее диарилкарбонатом и соединением амина.
Реакцию диарилкарбоната и соединения амина ведут в присутствии ароматического гидроксисоединения. Соединения, содержащие одну гидроксильную группу, непосредственно связанную с ароматическим углеводородным кольцом, составляющим ароматическое гидроксисоединение, предпочтительны в качестве ароматических гидроксисоединений. Хотя ароматическое гидроксисоединение, содержащее две или более гидроксильные группы, непосредственно связанные с ароматическим углеводородным кольцом, составляющим ароматическое гидроксисоединение, можно также использовать в качестве ароматического гидроксисоединения, составляющего композицию в соответствии с рассматриваемым вариантом, так как встречаются случаи, в которых вязкость раствора может быть высокой в реакции между диарилкарбонатом и соединением амина, и это может привести к уменьшению эффективности реакции или привести к уменьшению эффективности во время переноса реакционной жидкости, как будет раскрыто позднее.
Примеры ароматических гидроксисоединений, используемых в реакции между диарилкарбонатом и соединением амина, могут включать фенол; монозамещенные фенолы, такие как метилфенол (включая изомеры), этилфенол (включая изомеры), пропилфенол (включая изомеры), бутилфенол (включая изомеры), пентилфенол (включая изомеры), гексилфенол (включая изомеры), гептилфенол (включая изомеры), октилфенол (включая изомеры), нонилфенол (включая изомеры), децилфенол (включая изомеры), додецилфенол (включая изомеры), фенилфенол (включая изомеры), феноксифенол (включая изомеры) или кумилфенол (включая изомеры); дизамещенные фенолы, такие как диметилфенол (включая изомеры), диэтилфенол (включая изомеры), дипропилфенол (включая изомеры), дибутилфенол (включая изомеры), дипентилфенол (включая изомеры), дигексилфенол (включая изомеры), дигептилфенол (включая изомеры), диоктилфенол (включая изомеры), динонилфенол (включая изомеры), дидецилфенол (включая изомеры), дидодецилфенол (включая изомеры), дифенилфенол (включая изомеры), дифеноксифенол (включая изомеры), дикумилфенол (включая изомеры), метилэтилфенол (включая изомеры), метилпропилфенол (включая изомеры), метилбутилфенол (включая изомеры), метилпентилфенол (включая изомеры), метилгексилфенол (включая изомеры), метилгептилфенол (включая изомеры), метилоктилфенол (включая изомеры), метилнонилфенол (включая изомеры), метилдецилфенол (включая изомеры), метилдодецилфенол (включая изомеры), метилфенилфенол (включая изомеры), метилфеноксифенол (включая изомеры), метилкумилфенол (включая изомеры), этилпропилфенол (включая изомеры), этилбутилфенол (включая изомеры), этилпентилфенол (включая изомеры), этилгексилфенол (включая изомеры), этилгептилфенол (включая изомеры), этилоктилфенол (включая изомеры), этилнонилфенол (включая изомеры), этилдецилфенол (включая изомеры), этилдодецилфенол (включая изомеры), этилфенилфенол (включая изомеры), этилфеноксифенол (включая изомеры), этилкумилфенол (включая изомеры), пропилбутилфенол (включая изомеры), пропилпентилфенол (включая изомеры), пропилгексилфенол (включая изомеры), пропилгептилфенол (включая изомеры), пропилоктилфенол (включая изомеры), пропилнонилфенол (включая изомеры), пропилдецилфенол (включая изомеры), пропилдодецилфенол (включая изомеры), пропилфенилфенол (включая изомеры), пропилфеноксифенол (включая изомеры), пропилкумилфенол (включая изомеры), бутилпентилфенол (включая изомеры), бутилгексилфенол (включая изомеры), бутилгептилфенол (включая изомеры), бутилоктилфенол (включая изомеры), бутилнонилфенол (включая изомеры), бутилдецилфенол (включая изомеры), бутилдодецилфенол (включая изомеры), бутилфенилфенол (включая изомеры), бутилфеноксифенол (включая изомеры), бутилкумилфенол (включая изомеры), пентилгексилфенол (включая изомеры), пентилгептилфенол (включая изомеры), пентилоктилфенол (включая изомеры), пентилнонилфенол (включая изомеры), пентилдецилфенол (включая изомеры), пентилдодецилфенол (включая изомеры), пентилфенилфенол (включая изомеры), пентилфеноксифенол (включая изомеры), пентилкумилфенол (включая изомеры), гексилгептилфенол (включая изомеры), гексилоктилфенол (включая изомеры), гексилнонилфенол (включая изомеры), гексилдецилфенол (включая изомеры), гексилдодецилфенол (включая изомеры), гексилфенилфенол (включая изомеры), гексилфеноксифенол (включая изомеры), гексилкумилфенол (включая изомеры), гептилоктилфенол (включая изомеры), гептилнонилфенол (включая изомеры), гептилдецилфенол (включая изомеры), гептилдодецилфенол (включая изомеры), гептилфенилфенол (включая изомеры), гептилфеноксифенол (включая изомеры), гептилкумилфенол (включая изомеры), октилнонилфенол (включая изомеры), октилдецилфенол (включая изомеры), октилдодецилфенол (включая изомеры), октилфенилфенол (включая изомеры), октилфеноксифенол (включая изомеры), октилкумилфенол (включая изомеры), нонилдецилфенол (включая изомеры), нонилдодецилфенол (включая изомеры), нонилфенилфенол (включая изомеры), нонилфеноксифенол (включая изомеры), нонилкумилфенол (включая изомеры), додецилфенилфенол (включая изомеры), додецилфеноксифенол (включая изомеры) или додецилкумилфенол (включая изомеры); и тризамещенные фенолы, такие как триметилфенол (включая изомеры), триэтилфенол (включая изомеры), трипропилфенол (включая изомеры), трибутилфенол (включая изомеры), трипентилфенол (включая изомеры), тригексилфенол (включая изомеры), тригептилфенол (включая изомеры), триоктилфенол (включая изомеры), тринонилфенол (включая изомеры), тридецилфенол (включая изомеры), тридодецилфенол (включая изомеры), трифенилфенол (включая изомеры), трифеноксифенол (включая изомеры), трикумилфенол (включая изомеры), диметилэтилфенол (включая изомеры), диметилпропилфенол (включая изомеры), диметилбутилфенол (включая изомеры), диметилпентилфенол (включая изомеры), диметилгексилфенол (включая изомеры), диметилгептилфенол (включая изомеры), диметилоктилфенол (включая изомеры), диметилнонилфенол (включая изомеры), диметилдецилфенол (включая изомеры), диметилдодецилфенол (включая изомеры), диметилфенилфенол (включая изомеры), диметилфеноксифенол (включая изомеры), диметилкумилфенол (включая изомеры), диэтилметилфенол (включая изомеры), диэтилпропилфенол (включая изомеры), диэтилбутилфенол (включая изомеры), диэтилпентилфенол (включая изомеры), диэтилгексилфенол (включая изомеры), диэтилгептилфенол (включая изомеры), диэтилоктилфенол (включая изомеры), диэтилнонилфенол (включая изомеры), диэтилдецилфенол (включая изомеры), диэтилдодецилфенол (включая изомеры), диэтилфенилфенол (включая изомеры), диэтилфеноксифенол (включая изомеры), диэтилкумилфенол (включая изомеры), дипропилметилфенол (включая изомеры), дипропилэтилфенол (включая изомеры), дипропилбутилфенол (включая изомеры), дипропилпентилфенол (включая изомеры), дипропилгексилфенол (включая изомеры), дипропилгептилфенол (включая изомеры), дипропилоктилфенол (включая изомеры), дипропилнонилфенол (включая изомеры), дипропилдецилфенол (включая изомеры), дипропилдодецилфенол (включая изомеры), дипропилфенилфенол (включая изомеры), дипропилфеноксифенол (включая изомеры), дипропилкумилфенол (включая изомеры), дибутилметилфенол (включая изомеры), дибутилэтилфенол (включая изомеры), дибутилпропилфенол (включая изомеры), дибутилпентилфенол (включая изомеры), дибутилгексилфенол (включая изомеры), дибутилгептилфенол (включая изомеры), дибутилоктилфенол (включая изомеры), дибутилнонилфенол (включая изомеры), дибутилдецилфенол (включая изомеры), дибутилдодецилфенол (включая изомеры), дибутилфенилфенол (включая изомеры), дибутилфеноксифенол (включая изомеры), дибутилкумилфенол (включая изомеры), дипентилметилфенол (включая изомеры), дипентилэтилфенол (включая изомеры), дипентилпропилфенол (включая изомеры), дипентилбутилфенол (включая изомеры), дипентилгексилфенол (включая изомеры), дипентилгептилфенол (включая изомеры), дипентилоктилфенол (включая изомеры), дипентилнонилфенол (включая изомеры), дипентилдецилфенол (включая изомеры), дипентилдодецилфенол (включая изомеры), дипентилфенилфенол (включая изомеры), дипентилфеноксифенол (включая изомеры), дипентилкумилфенол (включая изомеры), дигексилметилфенол (включая изомеры), дигексилэтилфенол (включая изомеры), дигексилпропилфенол (включая изомеры), дигексилбутилфенол (включая изомеры), дигексилпентилфенол (включая изомеры), дигексилгептилфенол (включая изомеры), дигексилоктилфенол (включая изомеры), дигексилнонилфенол (включая изомеры), дигексилдецилфенол (включая изомеры), дигексилдодецилфенол (включая изомеры), дигексилфенилфенол (включая изомеры), дигексилфеноксифенол (включая изомеры), дигексилкумилфенол (включая изомеры), дигептилметилфенол (включая изомеры), дигептилэтилфенол (включая изомеры), дигептилпропилфенол (включая изомеры), дигептилбутилфенол (включая изомеры), дигептилпентилфенол (включая изомеры), дигептилгексилфенол (включая изомеры), дигептилоктилфенол (включая изомеры), дигептилнонилфенол (включая изомеры), дигептилдецилфенол (включая изомеры), дигептилдодецилфенол (включая изомеры), дигептилфенилфенол (включая изомеры), дигептилфеноксифенол (включая изомеры), дигептилкумилфенол (включая изомеры), диоктилметилфенол (включая изомеры), диоктилэтилфенол (включая изомеры), диоктилпропилфенол (включая изомеры), диоктилбутилфенол (включая изомеры), диоктилпентилфенол (включая изомеры), диоктилгексилфенол (включая изомеры), диоктилгептилфенол (включая изомеры), диоктилнонилфенол (включая изомеры), диоктилдецилфенол (включая изомеры), диоктилдодецилфенол (включая изомеры), диоктилфенилфенол (включая изомеры), диоктилфеноксифенол (включая изомеры), диоктилкумилфенол (включая изомеры), динонилметилфенол (включая изомеры), динонилэтилфенол (включая изомеры), динонилпропилфенол (включая изомеры), динонилбутилфенол (включая изомеры), динонилпентилфенол (включая изомеры), динонилгексилфенол (включая изомеры), динонилгептилфенол (включая изомеры), динонилоктилфенол (включая изомеры), динонилдецилфенол (включая изомеры), динонилдодецилфенол (включая изомеры), динонилфенилфенол (включая изомеры), динонилфеноксифенол (включая изомеры), динонилкумилфенол (включая изомеры), дидецилметилфенол (включая изомеры), дидецилэтилфенол (включая изомеры), дидецилпропилфенол (включая изомеры), дидецилбутилфенол (включая изомеры), дидецилпентилфенол (включая изомеры), дидецилгексилфенол (включая изомеры), дидецилгептилфенол (включая изомеры), дидецилоктилфенол (включая изомеры), дидецилнонилфенол (включая изомеры), дидецилдодецилфенол (включая изомеры), дидецилфенилфенол (включая изомеры), дидецилфеноксифенол (включая изомеры), дидецилкумилфенол (включая изомеры), дидодецилметилфенол (включая изомеры), дидодецилэтилфенол (включая изомеры), дидодецилпропилфенол (включая изомеры), дидодецилбутилфенол (включая изомеры), дидодецилпентилфенол (включая изомеры), дидодецилгексилфенол (включая изомеры), дидодецилгептилфенол (включая изомеры), дидодецилоктилфенол (включая изомеры), дидодецилнонилфенол (включая изомеры), дидодецилдецилфенол (включая изомеры), дидодецилдодецилфенол (включая изомеры), дидодецилфенилфенол (включая изомеры), дидодецилфеноксифенол (включая изомеры), дидодецилкумилфенол (включая изомеры), дифенилметилфенол (включая изомеры), дифенилэтилфенол (включая изомеры), дифенилпропилфенол (включая изомеры), дифенилбутилфенол (включая изомеры), дифенилпентилфенол (включая изомеры), дифенилгексилфенол (включая изомеры), дифенилгептилфенол (включая изомеры), дифенилоктилфенол (включая изомеры), дифенилнонилфенол (включая изомеры), дифенилдецилфенол (включая изомеры), дифенилдодецилфенол (включая изомеры), дифенилфеноксифенол (включая изомеры), дифенилкумилфенол (включая изомеры), дифеноксиметилфенол (включая изомеры), дифеноксиэтилфенол (включая изомеры), дифеноксипропилфенол (включая изомеры), дифеноксибутилфенол (включая изомеры), дифеноксипентилфенол (включая изомеры), дифеноксигексилфенол (включая изомеры), дифеноксигептилфенол (включая изомеры), дифеноксиоктилфенол (включая изомеры), дифеноксинонилфенол (включая изомеры), дифеноксидецилфенол (включая изомеры), дифеноксидодецилфенол (включая изомеры), дифеноксифенилфенол (включая изомеры), дифеноксикумилфенол (включая изомеры), дикумилметилфенол (включая изомеры), дикумилэтилфенол (включая изомеры), дикумилпропилфенол (включая изомеры), дикумилбутилфенол (включая изомеры), дикумилпентилфенол (включая изомеры), дикумилгексилфенол (включая изомеры), дикумилгептилфенол (включая изомеры), дикумилоктилфенол (включая изомеры), дикумилнонилфенол (включая изомеры), дикумилдецилфенол (включая изомеры), дикумилдодецилфенол (включая изомеры), дикумилфенилфенол (включая изомеры), дикумилфеноксифенол (включая изомеры), метилэтилпропилфенол (включая изомеры), метилэтилбутилфенол (включая изомеры), метилэтилпентилфенол (включая изомеры), метилэтилгексилфенол (включая изомеры), метилэтилгептилфенол (включая изомеры), метилэтилоктилфенол (включая изомеры), метилэтилнонилфенол (включая изомеры), метилэтилдецилфенол (включая изомеры), метилэтилдодецилфенол (включая изомеры), метилэтилфенилфенол (включая изомеры), метилэтилфеноксифенол (включая изомеры), метилэтилкумилфенол (включая изомеры), метилпропилбутилфенол (включая изомеры), метилпропилпентилфенол (включая изомеры), метилпропилгексилфенол (включая изомеры), метилпропилгептилфенол (включая изомеры), метилпропилоктилфенол (включая изомеры), метилпропилнонилфенол (включая изомеры), метилпропилдецилфенол (включая изомеры), метилпропилдодецилфенол (включая изомеры), метилпропилфенилфенол (включая изомеры), метилпропилфеноксифенол (включая изомеры), метилпропилкумилфенол (включая изомеры), метилбутилпентилфенол (включая изомеры), метилбутилгексилфенол (включая изомеры), метилбутилгептилфенол (включая изомеры), метилбутилоктилфенол (включая изомеры), метилбутилнонилфенол (включая изомеры), метилбутилдецилфенол (включая изомеры), метилбутилдодецилфенол (включая изомеры), метилбутилфенилфенол (включая изомеры), метилбутилфеноксифенол (включая изомеры), метилбутилкумилфенол (включая изомеры), метилпентилгексилфенол, метилпентилгептилфенол (включая изомеры), метилпентилоктилфенол (включая изомеры), метилпентилнонилфенол (включая изомеры), метилпентилдецилфенол (включая изомеры), метилпентилдодецилфенол (включая изомеры), метилпентилфенилфенол (включая изомеры), метилпентилфеноксифенол (включая изомеры), метилпентилкумилфенол (включая изомеры), метилгексилгептилфенол (включая изомеры), метилгексилоктилфенол (включая изомеры), метилгексилнонилфенол (включая изомеры), метилгексилдецилфенол (включая изомеры), метилгексилдодецилфенол (включая изомеры), метилгексилфенилфенол (включая изомеры), метилгексилфеноксифенол (включая изомеры), метилгексилкумилфенол (включая изомеры), этилпропилбутилфенол (включая изомеры), этилпропилпентилфенол (включая изомеры), этилпропилгексилфенол (включая изомеры), этилпропилгептилфенол (включая изомеры), этилпропилоктилфенол (включая изомеры), этилпропилнонилфенол (включая изомеры), этилпропилдецилфенол (включая изомеры), этилпропилдодецилфенол (включая изомеры), этилпропилфенилфенол (включая изомеры), этилпропилфеноксифенол (включая изомеры), этилпропилкумилфенол (включая изомеры), этилбутилфенол (включая изомеры), этилбутилпентилфенол (включая изомеры), этилбутилгексилфенол (включая изомеры), этилбутилгептилфенол (включая изомеры), этилбутилоктилфенол (включая изомеры), этилбутилнонилфенол (включая изомеры), этилбутилдецилфенол (включая изомеры), этилбутилдодецилфенол (включая изомеры), этилбутилфенилфенол (включая изомеры), этилбутилфеноксифенол (включая изомеры), этилбутилкумилфенол (включая изомеры), этилпентилгексилфенол (включая изомеры), этилпентилгептилфенол (включая изомеры), этилпентилоктилфенол (включая изомеры), этилпентилнонилфенол (включая изомеры), этилпентилдецилфенол (включая изомеры), этилпентилдодецилфенол (включая изомеры), этилпентилфенилфенол (включая изомеры), этилпентилфеноксифенол (включая изомеры), этилпентилкумилфенол (включая изомеры), этилгексилгептилфенол (включая изомеры), этилгексилоктилфенол (включая изомеры), этилгексилнонилфенол (включая изомеры), этилгексилдецилфенол (включая изомеры), этилгексилдодецилфенол (включая изомеры), этилгексилфенилфенол (включая изомеры), этилгексилфеноксифенол (включая изомеры), этилгексилкумилфенол (включая изомеры), этилгептилоктилфенол (включая изомеры), этилгептилнонилфенол (включая изомеры), этилгептилдецилфенол (включая изомеры), этилгептилдодецилфенол (включая изомеры), этилгептилфенилфенол (включая изомеры), этилгептилфеноксифенол (включая изомеры), этилгептилкумилфенол (включая изомеры), этилоктилфенол (включая изомеры), этилоктилнонилфенол (включая изомеры), этилоктилдецилфенол (включая изомеры), этилоктилдодецилфенол (включая изомеры), этилоктилфенилфенол (включая изомеры), этилоктилфеноксифенол (включая изомеры), этилоктилкумилфенол (включая изомеры), этилнонилдецилфенол (включая изомеры), этилнонилдодецилфенол (включая изомеры), этилнонилфенилфенол (включая изомеры), этилнонилфеноксифенол (включая изомеры), этилнонилкумилфенол (включая изомеры), этилдецилдодецилфенол (включая изомеры), этилдецилфенилфенол (включая изомеры), этилдецилфеноксифенол (включая изомеры), этилдецилкумилфенол (включая изомеры), этилдодецилфенилфенол (включая изомеры), этилдодецилфеноксифенол (включая изомеры), этилдодецилкумилфенол (включая изомеры), этилфенилфеноксифенол (включая изомеры), этилфенилкумилфенол (включая изомеры), пропилбутилфенол (включая изомеры), пропилбутилпентилфенол (включая изомеры), пропилбутилгексилфенол (включая изомеры), пропилбутилгептилфенол (включая изомеры), пропилбутилоктилфенол (включая изомеры), пропилбутилнонилфенол (включая изомеры), пропилбутилдецилфенол (включая изомеры), пропилбутилдодецилфенол (включая изомеры), пропилбутилфенилфенол (включая изомеры), пропилбутилфеноксифенол (включая изомеры), пропилбутилкумилфенол (включая изомеры), пропилпентилфенол (включая изомеры), пропилпентилгексилфенол (включая изомеры), пропилпентилгептилфенол (включая изомеры), пропилпентилоктилфенол (включая изомеры), пропилпентилнонилфенол (включая изомеры), пропилпентилдецилфенол (включая изомеры), пропилпентилдодецилфенол (включая изомеры), пропилпентилфенилфенол (включая изомеры), пропилпентилфеноксифенол (включая изомеры), пропилпентилкумилфенол (включая изомеры), пропилгексилфенол (включая изомеры), пропилгексилгептилфенол (включая изомеры), пропилгексилоктилфенол (включая изомеры), пропилгексилнонилфенол (включая изомеры), пропилгексилдецилфенол (включая изомеры), пропилгексилдодецилфенол (включая изомеры), пропилгексилфенилфенол (включая изомеры), пропилгексилфеноксифенол (включая изомеры), пропилгексилкумилфенол (включая изомеры), пропилгептилоктилфенол (включая изомеры), пропилгептилнонилфенол (включая изомеры), пропилгептилдецилфенол (включая изомеры), пропилгептилдодецилфенол (включая изомеры), пропилгептилфенилфенол (включая изомеры), пропилгептилфеноксифенол (включая изомеры), пропилгептилкумилфенол (включая изомеры), пропилоктилнонилфенол (включая изомеры), пропилоктилдецилфенол (включая изомеры), пропилоктилдодецилфенол (включая изомеры), пропилоктилфенилфенол (включая изомеры), пропилоктилфеноксифенол (включая изомеры), пропилоктилкумилфенол (включая изомеры), пропилнонилдецилфенол (включая изомеры), пропилнонилдодецилфенол (включая изомеры), пропилнонилфенилфенол (включая изомеры), пропилнонилфеноксифенол (включая изомеры), пропилнонилкумилфенол (включая изомеры), пропилдецилдодецилфенол (включая изомеры), пропилдецилфенилфенол (включая изомеры), пропилдецилфеноксифенол (включая изомеры), пропилдецилкумилфенол (включая изомеры), пропилдодецилфенилфенол (включая изомеры), пропилдодецилфеноксифенол (включая изомеры), пропилдодецилкумилфенол (включая изомеры), метилфенол (включая изомеры), этилфенол (включая изомеры), пропилфенол (включая изомеры), бутилфенол (включая изомеры), пентилфенол (включая изомеры), гексилфенол (включая изомеры), гептилфенол (включая изомеры), октилфенол (включая изомеры), нонилфенол (включая изомеры), децилфенол (включая изомеры), додецилфенол (включая изомеры), фенилфенол (включая изомеры), феноксифенол (включая изомеры), кумилфенол (включая изомеры), пропилфенилфеноксифенол (включая изомеры), пропилфенилкумилфенол (включая изомеры), пропилфеноксикумилфенол (включая изомеры), пропилбутилпентилфенол (включая изомеры), пропилбутилгексилфенол (включая изомеры), пропилбутилгептилфенол (включая изомеры), пропилбутилоктилфенол (включая изомеры), пропилбутилнонилфенол (включая изомеры), пропилбутилдецилфенол (включая изомеры), пропилбутилдодецилфенол (включая изомеры), пропилбутилфенилфенол (включая изомеры), пропилбутилфеноксифенол (включая изомеры), пропилбутилкумилфенол (включая изомеры), пропилпентилфенол (включая изомеры), пропилпентилгексилфенол (включая изомеры), пропилпентилгептилфенол (включая изомеры), пропилпентилоктилфенол (включая изомеры), пропилпентилнонилфенол (включая изомеры), пропилпентилдецилфенол (включая изомеры), пропилпентилдодецилфенол (включая изомеры), пропилпентилфенилфенол (включая изомеры), пропилпентилфеноксифенол (включая изомеры), пропилпентилкумилфенол (включая изомеры), пропилгексилгептилфенол (включая изомеры), пропилгексилоктилфенол (включая изомеры), пропилгексилнонилфенол (включая изомеры), пропилгексилдецилфенол (включая изомеры), пропилгексилдодецилфенол (включая изомеры), пропилгексилфенилфенол (включая изомеры), пропилгексилфеноксифенол (включая изомеры), пропилгексилкумилфенол (включая изомеры), пропилгептилоктилфенол (включая изомеры), пропилгептилнонилфенол (включая изомеры), пропилгептилдецилфенол (включая изомеры), пропилгептилдодецилфенол (включая изомеры), пропилгептилфенилфенол (включая изомеры), пропилгептилфеноксифенол (включая изомеры), пропилгептилкумилфенол (включая изомеры), пропилоктилнонилфенол (включая изомеры), пропилоктилдецилфенол (включая изомеры), пропилоктилдодецилфенол (включая изомеры), пропилоктилфенилфенол (включая изомеры), пропилоктилфеноксифенол (включая изомеры), пропилоктилкумилфенол (включая изомеры), пропилнонилдецилфенол (включая изомеры), пропилнонилдодецилфенол (включая изомеры), пропилнонилфенилфенол (включая изомеры), пропилнонилфеноксифенол (включая изомеры), пропилнонилкумилфенол (включая изомеры), пропилдецилдодецилфенол (включая изомеры), пропилдецилфенилфенол (включая изомеры), пропилдецилфеноксифенол (включая изомеры), пропилдецилкумилфенол (включая изомеры), пропилдодецилфенилфенол (включая изомеры), пропилдодецилфеноксифенол (включая изомеры), пропилфенилфеноксифенол (включая изомеры), пропилфенилкумилфенол (включая изомеры), бутилпентилгексилфенол (включая изомеры), бутилпентилгептилфенол (включая изомеры), бутилпентилоктилфенол (включая изомеры), бутилпентилнонилфенол (включая изомеры), бутилпентилдецилфенол (включая изомеры), бутилпентилдодецилфенол (включая изомеры), бутилпентилфенилфенол (включая изомеры), бутилпентилфеноксифенол (включая изомеры), бутилпентилкумилфенол (включая изомеры), бутилгексилгептилфенол (включая изомеры), бутилгексилоктилфенол (включая изомеры), бутилгексилнонилфенол (включая изомеры), бутилгексилдецилфенол (включая изомеры), бутилгексилдодецилфенол (включая изомеры), бутилгексилфенилфенол (включая изомеры), бутилгексилфеноксифенол (включая изомеры), бутилгексилкумилфенол (включая изомеры), бутилгептилоктилфенол (включая изомеры), бутилгептилнонилфенол (включая изомеры), бутилгептилдецилфенол (включая изомеры), бутилгептилдодецилфенол (включая изомеры), бутилгептилфенилфенол (включая изомеры), бутилгептилфеноксифенол (включая изомеры), бутилгептилкумилфенол (включая изомеры), бутилоктилнонилфенол (включая изомеры), бутилоктилдецилфенол (включая изомеры), бутилоктилдодецилфенол (включая изомеры), бутилоктилфенилфенол (включая изомеры), бутилоктилфеноксифенол (включая изомеры), бутилоктилкумилфенол (включая изомеры), бутилнонилдецилфенол (включая изомеры), бутилнонилдодецилфенол (включая изомеры), бутилнонилфенилфенол (включая изомеры), бутилнонилфеноксифенол (включая изомеры), бутилнонилкумилфенол (включая изомеры), бутилдецилдодецилфенол (включая изомеры), бутилдецилфенилфенол (включая изомеры), бутилдецилфеноксифенол (включая изомеры), бутилдецилкумилфенол (включая изомеры), бутилдодецилфенол (включая изомеры), бутилдодецилфенилфенол (включая изомеры), бутилдодецилфеноксифенол (включая изомеры), бутилдодецилкумилфенол (включая изомеры), бутилфенилфенол (включая изомеры), бутилфенилфеноксифенол (включая изомеры), бутилфенилкумилфенол (включая изомеры), пентилгексилгептилфенол (включая изомеры), пентилгексилоктилфенол (включая изомеры), пентилгексилнонилфенол (включая изомеры), пентилгексилдецилфенол (включая изомеры), пентилгексилдодецилфенол (включая изомеры), пентилгексилфенилфенол (включая изомеры), пентилгексилфеноксифенол (включая изомеры), пентилгексилкумилфенол (включая изомеры), пентилгептилоктилфенол (включая изомеры), пентилгептилнонилфенол (включая изомеры), пентилгептилдецилфенол (включая изомеры), пентилгептилдодецилфенол (включая изомеры), пентилгептилфенилфенол (включая изомеры), пентилгептилфеноксифенол (включая изомеры), пентилгептилкумилфенол (включая изомеры), пентилоктилнонилфенол (включая изомеры), пентилоктилдецилфенол (включая изомеры), пентилоктилдодецилфенол (включая изомеры), пентилоктилфенилфенол (включая изомеры), пентилоктилфеноксифенол (включая изомеры), пентилоктилкумилфенол (включая изомеры), пентилнонилдецилфенол (включая изомеры), пентилнонилдодецилфенол (включая изомеры), пентилнонилфенилфенол (включая изомеры), пентилнонилфеноксифенол (включая изомеры), пентилнонилкумилфенол (включая изомеры), пентилдецилдодецилфенол (включая изомеры), пентилдецилфенилфенол (включая изомеры), пентилдецилфеноксифенол (включая изомеры), пентилдецилкумилфенол (включая изомеры), пентилдодецилфенилфенол (включая изомеры), пентилдодецилфеноксифенол (включая изомеры), пентилдодецилкумилфенол (включая изомеры), пентилфенилфеноксифенол (включая изомеры), пентилфенилкумилфенол (включая изомеры), гексилгептилоктилфенол (включая изомеры), гексилгептилнонилфенол (включая изомеры), гексилгептилдецилфенол (включая изомеры), гексилгептилдодецилфенол (включая изомеры), гексилгептилфенилфенол (включая изомеры), гексилгептилфеноксифенол (включая изомеры), гексилгептилкумилфенол (включая изомеры), гексилоктилнонилфенол (включая изомеры), гексилоктилдецилфенол (включая изомеры), гексилоктилдодецилфенол (включая изомеры), гексилоктилфенилфенол (включая изомеры), гексилоктилфеноксифенол (включая изомеры), гексилоктилкумилфенол (включая изомеры), гексилнонилдецилфенол (включая изомеры), гексилнонилдодецилфенол (включая изомеры), гексилнонилфенилфенол (включая изомеры), гексилнонилфеноксифенол (включая изомеры), гексилдецилфенилфенол (включая изомеры), гексилдецилфеноксифенол (включая изомеры), гексилдецилкумилфенол (включая изомеры), гексилдодецилфенилфенол (включая изомеры), гексилдодецилфеноксифенол (включая изомеры), гексилдодецилкумилфенол (включая изомеры), гексилфенилфеноксифенол (включая изомеры), гексилфенилкумилфенол (включая изомеры), гептилоктилнонилфенол (включая изомеры), гептилоктилдецилфенол (включая изомеры), гептилоктилдодецилфенол (включая изомеры), гептилоктилфенилфенол (включая изомеры), гептилоктилфеноксифенол (включая изомеры), гептилоктилкумилфенол (включая изомеры), гептилнонилдецилфенол (включая изомеры), гептилнонилдодецилфенол (включая изомеры), гептилнонилфенилфенол (включая изомеры), гептилнонилфеноксифенол (включая изомеры), гептилнонилкумилфенол (включая изомеры), гептилдецилдодецилфенол (включая изомеры), гептилдецилфенилфенол (включая изомеры), гептилдецилфеноксифенол (включая изомеры), гептилдецилкумилфенол (включая изомеры), гептилдодецилфенилфенол (включая изомеры), гептилдодецилфеноксифенол (включая изомеры), гептилдодецилкумилфенол (включая изомеры), гептилфенилфеноксифенол (включая изомеры), гептилфенилкумилфенол (включая изомеры), октилнонилдецилфенол (включая изомеры), октилнонилдодецилфенол (включая изомеры), октилнонилфенилфенол (включая изомеры), октилнонилфеноксифенол (включая изомеры), октилнонилкумилфенол (включая изомеры), октилдецилдодецилфенол (включая изомеры), октилдецилфенилфенол (включая изомеры), октилдецилфеноксифенол (включая изомеры), октилдецилкумилфенол (включая изомеры), октилдодецилфенилфенол (включая изомеры), октилдодецилфеноксифенол (включая изомеры), октилдодецилкумилфенол (включая изомеры), октилфенилфеноксифенол (включая изомеры), октилфенилкумилфенол (включая изомеры), нонилдецилдодецилфенол (включая изомеры), нонилдецилфенилфенол (включая изомеры), нонилдецилфеноксифенол (включая изомеры), нонилдецилкумилфенол (включая изомеры), нонилдодецилфенилфенол (включая изомеры), нонилдодецилфеноксифенол (включая изомеры), нонилдодецилкумилфенол (включая изомеры), нонилфенилфеноксифенол (включая изомеры), нонилфенилкумилфенол (включая изомеры), децилдодецилфенилфенол (включая изомеры), децилдодецилфеноксифенол (включая изомеры), децилдодецилкумилфенол (включая изомеры), децилфенилфеноксифенол (включая изомеры), децилфенилкумилфенол (включая изомеры), додецилфенилфеноксифенол (включая изомеры), додецилфенилкумилфенол (включая изомеры) или фенилфеноксикумилфенол (включая изомеры). Среди указанных ароматических гидроксисоединений более предпочтительно использовать ароматические гидроксисоединения, соответствующие соединению R1OH, в котором атом водорода добавлен к группе R1O, составляющей диарилкарбонат (где R1 представляет собой ароматическую группу, как определено ранее, и O представляет собой атом кислорода). Это происходит потому, что количество типов соединений в реакционной смеси, полученной при осуществлении взаимодействия диарилкарбоната и соединения амина, можно уменьшить, тем самым, облегчая процедуру выделения.
Соединение амина подают предпочтительно в жидком состоянии в реактор, в котором осуществляют получение арилкарбамата. Обычно большинство соединений амина, как представлено выше, являются твердыми при обычной температуре (например, 20°C), и в таких случаях, хотя соединение амина можно подавать в жидком состоянии за счет нагревания до температуры, равной или выше, чем температура плавления соединения амина, если соединение амина подают при избыточно высокой температуре, встречаются случаи, в которых могут происходить побочные реакции, такие как реакции термического денатурирования, вызываемые нагреванием, соединение амина предпочтительно подают в жидком состоянии при относительно низкой темперауте в виде смеси с вышеуказанным ароматическим гидроксисоединением, диарилкарбонатом или водой.
Хотя возможны изменения в соответствии с участвующими в реакции соединениями, условия реакций, в которых осуществляют взаимодействие диарилкарбоната и соединений амина, таковы, что стехиометрическое отношение диарилкарбоната к аминогруппам в соединениях амина находится в интервале значений от 1 до 1000-кратного, и хотя диарилкарбонат находится предпочтительно в избытке относительно аминогрупп соединений амина для быстрого завершения реакции путем повышения скорости реакции, с учетом размеров реактора стехиометрическое отношение предпочтительно находится в интервале значений от 1,1 до 50-кратного, и более предпочтительно в интервале значений от 1,5 до 10-кратного. Количество используемого ароматического гидроксисоединения таково, что стехиометрическое отношение ароматического гидроксисоединения к аминогруппам соединения амина находится в интервале значений от 1 до 100-кратного, предпочтительно в интервале значений от 1,2 до 50-кратного и более предпочтительно в интервале значений от 1,5 до 10-кратного. Температура реакции обычно находится в интервале значений от 0 до 150°C. Хотя высокая температура предпочтительна для повышения скорости реакции, с другой стороны, так как нежелательные реакции также происходят при высоких температурах, температура реакции предпочтительно находится в интервале значений от 10 до 100°C. В реакторах могут быть установлены известные охлаждающие аппараты или нагревательные аппараты для поддержания постоянной температуры реакции. Кроме того, хотя возможны изменения в соответствии с типами используемых соединений и температурами реакций, давление реакции может быть пониженным давлением, нормальным давлением или повышенным давлением, и реакцию обычно ведут при давлении в интервале значений от 20 до 1×106 Па. Ограничений по времени реакции практически не существует (время пребывания в случае непрерывного процесса), и обычно оно составляет от 0,001 до 50 часов, предпочтительно от 0,01 до 20 часов и более предпочтительно от 0,1 до 10 часов. Кроме того, реакцию можно также закончить, подтверждая, что образовалось нужное количество арилкарбамата, например, с помощью жидкостной хроматографии после отбора образцов реакционной жидкости.
В рассматриваемом варианте изобретения предпочтительно не использовать катализатор в реакции диарилкарбоната и соединения амина. Во время переноса реакционной смеси и во время реакции термического разложения эфира карбаминовой кислоты, содержащегося в реакционной смеси (что будет раскрыто далее), если арилкарбамат нагревают в присутствии металлического компонента, источником которого является катализатор, может происходить реакция термического денатурирования и так далее до арилкарбамата. Хотя катализатор можно использовать при проведении реакции между диарилкарбонатом и соединением амина с последующим осуществлением переноса или реакции термического разложения реакционной смеси после прохождения стадии удаления катализатора, это приводит к увеличению количества стадий, что нежелательно.
Однако катализатор можно использовать с целью, например, завершения реакции за короткий промежуток времени или для снижения температуры реакции. Обычнно, так как ароматические соединения амина обладают более низкой реакционной способностью, чем алифатические соединения амина, в случае использования ароматических соединений амина в качестве соединения амина, встречаются случаи, в которых эффективно использовать катализатор. В случае использования катализатора примеры катализаторов, которые можно использовать, могут включать металлоорганические соединения и неорганические соединения металлов, такие как соединения олова, свинца, меди или титана, и основные катализаторы, такие как алкоголяты щелочных металлов или щелочноземельных металлов в форме метилатов, этилатов и бутиратов (включая изомеры) лития, натрия, калия, кальция или бария.
В рассматриваемом варианте предпочтительно не использовать реакционные растворители, отличающиеся от вышеуказанных ароматических гидроксисоединений, и/или избыток диарилкарбоната. Хотя существуют варианты, в которых были раскрыты способы известного уровня техники, в которых используют инертный реакционный растворитель в отношении изоцианатов и эфиров карбаминовой кислоты образующихся в реакции термического разложения диарилкарбаматов, использование таковых в качестве инертного растворителя делает сложным разделение и так далее до изоцианатов и ароматических гидроксисоединений, образующихся в указанной реакции термического разложения эфира карбаминовой кислоты, раскрытой далее, тем самым, делая указанный способ нежелательным.
Реактор известного корпусного типа, реактор колонного типа или ректификационную колонну можно использовать в качестве реактора, используемого для реакции между диарилкарбонатами и соединениями амина, и хотя известные материалы можно использовать для реакторов и линий при условии, что они не оказывают вредного воздействия на исходные вещества или реагенты, предпочтительно можно использовать недорогие SUS304, SUS316 или SUS316L и тому подобные.
Арилкарбамат
Смесь, содержащую арилкарбамат, избыток диарилкарбоната и ароматическое гидроксисоединение, получают в рассматриваемой реакции.
Арилкарбамат представляет собой соединение, представленное следующей формулой (18):
(где R2 имеет определенные ранее значения и представляет собой группу, источником которой является соединение амина,
R1 имеет определенные ранее значения и представляет собой группу, источником которой является диарилкарбонат, и
n представляет собой целое число от 2 до 10, и оно такое же, как число аминогрупп в соединении амина).
Примеры эфиров карбаминовой кислоты, представленные выше формулой (18), могут включать арилкарбаматы, такие как дифениловый эфир N,N'-гександиил-бис-карбаминовой кислоты, ди(метилфенил)овый эфир N,N'-гександиил-бис-карбаминовой кислоты (включая изомеры), ди(этилфенил)овый эфир N,N'-гександиил-бис-карбаминовой кислоты (включая изомеры), ди(пропилфенил)овый эфир N,N'-гександиил-бис-карбаминовой кислоты (включая изомеры), ди(бутилфенил)овый эфир N,N'-гександиил-бис-карбаминовой кислоты (включая изомеры), ди(пентилфенил)овый эфир N,N'-гександиил-бис-карбаминовой кислоты (включая изомеры), дифенил-4,4'-метилендициклогексилкарбамат, ди(метилфенил)-4,4'-метилендициклогексилкарбамат, ди(этилфенил)-4,4'-метилендициклогексилкарбамат, ди(пропилфенил)-4,4'-метилендициклогексилкарбамат (включая изомеры), ди(бутилфенил)-4,4'-метилендициклогексилкарбамат (включая изомеры), ди(пентилфенил)-4,4'-метилендициклогексилкарбамат (включая изомеры), ди(гексилфенил)-4,4'-метилендициклогексилкарбамат (включая изомеры), ди(гептилфенил)-4,4'-метилендициклогексилкарбамат (включая изомеры), ди(октилфенил)-4,4'-метилендициклогексилкарбамат (включая изомеры), фениловый эфир 3-(феноксикарбониламинометил)-3,5,5-триметилциклогексил карбаминовой кислоты, (метилфенокси)эфир 3-(метилфеноксикарбониламинометил)-3,5,5-триметилциклогексил карбаминовой кислоты (включая изомеры), (этилфенил)овый эфир 3-(этилфеноксикарбониламинометил)-3,5,5-триметилциклогексил карбаминовой кислоты (включая изомеры), (пропилфенил)овый эфир 3-(пропилфеноксикарбониламинометил)-3,5,5-триметилциклогексил карбаминовой кислоты (включая изомеры), (бутилфенил)овый эфир 3-(бутилфеноксикарбониламинометил)-3,5,5-триметилциклогексил карбаминовой кислоты (включая изомеры), (пентилфенил)овый эфир 3-(пентилфеноксикарбониламинометил)-3,5,5-триметилциклогексил карбаминовой кислоты (включая изомеры), (гексилфенил)овый эфир 3-(гексилфеноксикарбониламинометил)-3,5,5-триметилциклогексил карбаминовой кислоты (включая изомеры), (гептилфенил)овый эфир 3-(гептилфеноксикарбониламинометил)-3,5,5-триметилциклогексил карбаминовой кислоты (включая изомеры), (октилфенил)овый эфир 3-(октилфеноксикарбониламинометил)-3,5,5-триметилциклогексил карбаминовой кислоты (включая изомеры), дифениловый эфир толуолдикарбаминовой кислоты (включая изомеры), ди(метилфенил)овый эфир толуолдикарбаминовой кислоты (включая изомеры), ди(этилфенил)овый эфир толуолдикарбаминовой кислоты (включая изомеры), ди(пропилфенил)овый эфир толуолдикарбаминовой кислоты (включая изомеры), ди(бутилфенил)овый эфир толуолдикарбаминовой кислоты (включая изомеры), ди(пентилфенил)овый эфир толуолдикарбаминовой кислоты (включая изомеры), ди(гексилфенил)овый эфир толуолдикарбаминовой кислоты (включая изомеры), ди(гептилфенил)овый эфир толуолдикарбаминовой кислоты (включая изомеры), ди(октилфенил)овый эфир толуолдикарбаминовой кислоты (включая изомеры), дифениловый эфир N,N'-(4,4'-метандиилдифенил)-бискарбаминовой кислоты, ди(метилфенил)овый эфир N,N'-(4,4'-метандиилдифенил)-бискарбаминовой кислоты, ди(этилфенил)овый эфир N,N'-(4,4'-метандиилдифенил)-бискарбаминовой кислоты, ди(пропилфенил)овый эфир N,N'-(4,4'-метандиилдифенил)-бискарбаминовой кислоты, ди(бутилфенил)овый эфир N,N'-(4,4'-метандиилдифенил)-бискарбаминовой кислоты, ди(пентилфенил)овый эфир N,N'-(4,4'-метандиилдифенил)-бискарбаминовой кислоты, ди(гексилфенил)овый эфир N,N'-(4,4'-метандиилдифенил)бискарбаминовой кислоты, ди(гептилфенил)овый эфир N,N'-(4,4'-метандиилдифенил)бискарбаминовой кислоты или ди(октилфенил)овый эфир N,N'-(4,4'-метандиилдифенил)бискарбаминовой кислоты (включая изомеры).
Перенос реакционной жидкости после уретанирования
Реакционную жидкость, содержащую арилкарбамат, полученный в соответствии с раскрытым выше способом, предпочтительно удаляют из реактора, в котором ведут реакцию, и переносят в реактор, в котором осущестляют реакцию термического разложения для арилкарбамата (здесь и далее именуемый как “реактор термического разложения”), с последующим осуществлением реакции термического разложения арилкарбамата. Таким образом, используя отдельный реактор для получения арилкарбамата и отдельный реактор термического разложения, можно выбрать подходящие для каждой из реакций реакторы и можно установить гибкие условия реакций, тем самым, создавая возможность повысить выход в каждой из реакций.
Так как указанные арилкарбаматы легко образуют водородные связи между молекулами за счет уретановых связей арилкарбамата, они часто характеризуются высокими температурами плавления. При переносе указанных арилкарбаматов, перед переносом твердый эфир карбаминовой кислоты, например, измельчают или обрабатывают носителем для превращения в таблетки и тому подобное. Однако, в случае переноса твердого арилкарбамата, который был обработан носителем, часто возникает необходимость в сложной аппаратуре, чтобы обеспечить стабильный перенос фиксированного количества арилкарбамата, или возникает необходимость в создании способа поддержания формы арилкарбамата в определенных рамках в случае риска закупорки линии переноса или частых изменений в форме арилкарбамата. Поэтому арилкарбамат предпочтительно подают в реактор термического разложения в форме жидкости.
В качестве способа подачи арилкарбамата в реактор термического разложения в форме жидкости предпочтительно использует способ, в котором арилкарбамат подают в форме реакционной смеси, полученной путем осуществления взаимодействия диарилкарбоната и соединения амина.
Хотя арилкарбамат можно также переносить путем нагревания арилкарбамата до температуры, которая выше, чем его температура плавления, с учетом предотвращения отверждения во время переноса необходимо нагревать арилкарбамат до температуры, которая выше, чем его температура плавления (например, 200°C). В случае поддержания столь высокой температуры арилкарбамата часто происходит термическое разложение арилкарбамата в нежелательных участках, приводя к образованию изоцианатов, или часто происходит реакция термического денатурирования арилкарбамата, как было раскрыто ранее.
В противоположность этому, так как реакционная смесь, полученная путем осуществления взаимодействия диарилкарбоната и соединения амина, представляет собой жидкость при нормальной температуре (20°C), или даже если она является твердой при нормальной температуре, так как она часто становится гомогенным раствором при температуре, которая ниже, чем температура плавления арилкарбамата, можно ингибировать термическое денатурирование арилкарбамата и тому подобное.
Кроме того, авторы настоящего изобретения неожиданно обнаружили, что если арилкарбамат переносят в форме реакционной смеси, полученной путем осуществления взаимодействия диарилкарбоната и соединения амина, ингибируется уменьшение количества арилкарбамата, вызываемое термическим денатурированием и так далее до арилкарбамата. Хотя механизм возникновения такого эффекта неясен, авторы настоящего изобретения предполагают, что в результате содержания ароматического гидроксисоединения в реакционной смеси и уретановых связей (-NHCOO-) эфира карбаминовой кислоты, образующих водородные связи в реакции, за счет которой образуются мочевинные связи, как представлено вышеприведенной формулой (2), уретановые связи находятся в таком состоянии, в котором они не могут приблизиться друг к другу, и реакция образования мочевинных связей затруднена.
Перенос реакционной смеси предпочтительно осуществляют в интервале температур от 10 до 180°C, более предпочтительно от 30 до 170°C и еще более предпочтительно от 50 до 150°C.
В способе, с помощью которого арилкарбамат переносят в реакцию термического разложения в форме реакционной смеси, полученной путем осуществления взаимодействия диарилкарбоната и соединения амина, так как реакционную смесь переносят без процедуры осуществления дистилляционного разделения и тому подобного, существует преимущество возможности упростить указанный процесс. Кроме того, в случае способа, с помощью которого арилкарбамат подают в форме смеси, в которой вся или часть ароматического гидроксисоединения была удалена из реакционной смеси, указанный процесс можно также упростить, так как отсутствует необходимость в осуществлении процедуры выделения только арилкарбамата из реакционной смеси.
Реакция термического разложения арилкарбамата
Затем приводится объяснение получения изоцианата путем осуществления реакции термического разложения арилкарбамата.
Указанная реакция термического разложения в рассматриваемом варианте представляет собой реакцию, в которой соответствующие изоцианат и ароматическое гидроксисоединение образуются из арилкарбамата.
Температура реакции обычно находится в интервале значений от 100 до 300°C, и хотя высокая температура предпочтительна для повышения скорости реакции, так как побочные реакции, как раскрыто выше, могут привести к восстановлению арилкарбамата и/или образованию продукта реакции в форме изоцианата при высоких температурах, температура реакции предпочтительно находится в интервале значений от 150 до 250°C. В реакторах можно установить известные охлаждающие аппараты или нагревательные аппараты для поддержания постоянной температуры реакции. Кроме того, хотя возможны изменения в соответствии с типами используемых соединений и температурами реакций, давление в реакции может быть пониженным давлением, нормальным давлением или повышенным давлением, реакцию обычно осуществляют при давлении в интервале значений от 20 до 1×106 Па. Не существует конкретных ограничений относительно времени реакции (время пребывания в случае непрерывного способа), и обычно оно составляет от 0,001 до 100 часов, предпочтительно от 0,005 до 50 часов и более предпочтительно от 0,01 до 10 часов.
В рассматриваемом варианте катализатор предпочтительно не используют. Хотя катализатор можно использовать для промотирования указанной реакции термического разложения, существует множество случаев, в которых побочные реакции, вызванные арилкарбаматом и/или изоцианатом, протекают легко, тем самым, делая использование катализатора нежелательным.
Существуют случаи, в которых могут происходить побочные реакции, как раскрыто выше, если выдерживать арилкарбамат при высоких температурах в течение длительного промежутка времени. Кроме того, изоцианаты, образующиеся в указанной реакции термического разложения, могут также вызывать такие побочные реакции. Таким образом, промежуток времени, в течение которого арилкарбамат и изоцианат находятся в условиях высокой температуры, должен быть как можно более коротким, предпочтительно насколько возможно коротким, и указанную реакцию термического разложения предпочтительно осуществляют в непрерывном процессе. Непрерывный процесс относится к способу, в котором смесь, содержащую арилкарбамат, непрерывно подают в реактор и подвергают указанной реакции термического разложения с последующим непрерывным удалением образующихся изоцианата и ароматического гидроксисоединения из указанного реактора термического разложения. В указанном непрерывном процессе компонент с низкой температурой кипения, образующийся при термическом разложении арилкарбамата, предпочтительно удаляют из верхней части реактора термического разложения в форме газофазного компонента, тогда как оставшееся удаляют из нижней части реактора термического разложения в форме жидкофазного компонента. Хотя все соединения, присутствующие в указанном реакторе термического разложения, можно отводить в форме газофазного компонента, при этом оставляя жидкофазные компоненты в указанном реакторе термического разложения, полимерные соединения, образующиеся за счет побочных реакций, вызываемых арилкарбаматом и/или изоцианатом, растворяют, тем самым, демонстрируя эффект предотвращения прилипания и накопления полимерных соединений в указанном реакторе термического разложения. Хотя изоцианат и ароматическое гидроксисоединение образуются в результате термического разложения арилкарбамата, по меньшей мере, одно из указанных соединений регенерируют в форме газофазного компонента. Какое именно из указанных соединений регенерируют в форме газофазного компонента, зависит от условий указанной реакции термического разложения.
Здесь термин "компонент с низкой температурой кипения, образующийся в результате термического разложения арилкарбамата", используемый в рассматриваемом варианте, соответствует ароматическому гидроксисоединению и/или изоцианату, образующимся в результате термического разложения эфира карбаминовой кислоты, это, в частности, относится к соединениям, способным существовать в газовой фазе в условиях, в которых осуществляют указанную реакцию термического разложения.
Например, можно использовать способ, в котором изоцианат и ароматическое гидроксисоединение, образовавшиеся в результате указанной реакции термического разложения, удаляют в форме газофазного компонента, тогда как в жидкой фазе удаляют компонент, содержащий диарилкарбонат и/или эфир карбаминовой кислоты. В указанном способе изоцианат и ароматическое гидроксисоединение можно отводить отдельно в реактор термического разложения. Удаленный газообразный компонент, содержащий изоцианат, предпочтительно подают в газообразной фазе в дистилляционный аппарат для выделения и очистки изоцианата. Хотя отведенный газообразный компонент, содержащий изоцианат, можно подавать в дистилляционный аппарат после перевода в жидкую фазу с помощью холодильника и тому подобного, встречается много случаев, в которых аппаратура становится сложной, и возрастает расход энергии, что делает такой способ нежелательным. С другой стороны, жидкофазный компонент, содержащий диарилкарбонат и/или арилкарбамат, отводят из нижней части реактора термического разложения, и в случае, если жидкофазный компонент содержит диарилкарбонат, указанный диарилкарбонат предпочтительно выделяют и регенерируют из жидкофазного компонента и снова используют. Кроме того, в случае, если жидкофазный компонент содержит арилкарбамат, часть его или весь жидкофазный компонент предпочтительно подают в верхнюю часть реактора термического разложения и арилкарбамат снова подвергают указанной реакции термического разложения. Термин "верхняя часть реактора термического разложения" в том смысле, как здесь использован, относится к, например, второй тарелке и выше нижней части в терминах числа теоретических тарелок, в случае, если указанный реактор термического разложения представляет собой ректификационную колонну, или относится к части, которая выше, чем нагреваемая теплопроводящая поверхность, в случае, если указанный реактор термического разложения представляет собой тонкопленочный дистиллятор. Если подают весь или часть жидкофазного компонента в реактор термического разложения, жидкофазный компонент предпочтительно переносят, поддерживая температуру от 50 до 180°C, более предпочтительно от 70 до 170°C и еще более предпочтительно от 100 до 150°C.
Кроме того, можно также использовать способ, в котором, например, изоцианат, ароматическое гидроксисоединение и диарилкарбонат, образующиеся в указанной реакции термического разложения, отводят в форме газофазного компонента и жидкофазный компонент, содержащий арилкарбамат, отводят из нижней части реактора термического разложения. В указанном способе также отводимый газообразный компонент, содержащий изоцианат, предпочтительно подают в дистилляционный аппарат в газообразной фазе для очистки и выделения изоцианата. С другой стороны, весь или часть жидкофазного компонента, содержащего арилкарбамат, подают в верхнюю часть реактора термического разложения и арилкарбамат снова подвергают указанной реакции термического разложения. Если подают весь или часть жидкофазного компонента в верхнюю часть реактора термического разложения, жидкофазный компонент предпочтительно переносят, поддерживая температуру от 50 до 180°C, более предпочтительно от 70 до 170°C и еще более предпочтительно от 100 до 150°C.
Кроме того, можно также использовать способ, в котором, например, ароматическое гидроксисоединение, изоцианат и ароматическое гидроксисоединение, образующиеся в указанной реакции термического разложения, отводят в форме газофазного компонента, тогда как смесь, содержащую изоцианат, отводят в форме жидкофазного компонента из нижней части реактора термического разложения. В таком случае изоцианат регенерируют, подавая жидкофазный компонент в дистилляционный аппарат. В случае если диарилкарбонат содержится в жидкофазном компоненте, диарилкарбонат предпочтительно выделяют и регенерируют для повторного использования. Кроме того, в случае если арилкарбамат содержится в жидкофазном компоненте, всю или часть содержащей арилкарбамат смеси предпочтительно подают в верхнюю часть реактора термического разложения и арилкарбамат снова подвергают указанной реакции термического разложения. Если подают весь или часть жидкофазного компонента в верхнюю часть реактора термического разложения, жидкофазный компонент предпочтительно переносят, поддерживая температуру в диапазоне от 50 до 180°C, более предпочтительно от 70 до 170°C и еще более предпочтительно от 100 до 150°C.
Как было раскрыто ранее, в указанной реакции термического разложения жидкофазный компонент предпочтительно отводят из нижней части реактора термического разложения. Это происходит потому, что в результате присутствия жидкофазного компонента в реакторе термического разложения полимерные побочные продукты, образующиеся в побочных реакциях за счет арилкарбамата и/или изоцианата, растворяются и могут быть удалены из указанного реактора термического разложения в форме жидкофазного компонента, тем самым, обеспечивая эффект уменьшения адгезии и накопления указанных полимерных соединений в указанном реакторе термического разложения.
В том случае, если арилкарбамат содержится в жидкофазном компоненте, хотя весь или часть жидкофазного компонента подают в верхнюю часть реактора термического разложения, и арилкарбамат вновь подвергается указанной реакции термического разложения, существуют случаи, в которых полимерные побочные продукты накапливаются в жидкофазном компоненте, если указанную стадию повторяют. В таких случаях весь или часть жидкофазного компонента можно удалить из реакционной системы для уменьшения накопления полимерных побочных продуктов или поддержания их постоянной концентрации.
Каждое из ароматического гидроксисоединения и/или диарилкарбоната, содержащееся в газообразном компоненте и/или в жидкофазном компоненте, полученном в указанной реакции термического разложения, как раскрыто выше, можно выделить и регенерировть для повторного использования. Более конкретно, ароматическое гидроксисоединение можно повторно использовать в качестве реакционного растворителя в реакции между диарилкарбонатом и соединением амина и/или в качестве ароматического гидроксисоединения A стадии (3) получения диарилкарбоната, тогда как диарилкарбонат можно повторно использовать в качестве сырого материала в реакции получения арилкарбамата.
Хотя нет конкретных ограничений относительно типа реактора термического разложения, используют известный дистилляционный аппарат, предпочтительно для эффективной регенерации газофазного компонента. Используют различные известные способы, примеры которых могут включать ректификационную колонну, многоступенчатую ректификационную колонну, многотрубный реактор, непрерывную многоступенчатую ректификационную колонну, насадочную колонну, тонкопленочный выпариватель, реактор, снабженный внутренней подложкой, реактор с принудительной циркуляцией, выпариватель с падающей пленкой, выпариватель с падающими каплями и способы, в которых используют их комбинации. С точки зрения быстроты удаления из реакционной системы компоненты с низкой температурой кипения предпочтителен трубчатый реактор, хотя такие реакторы, как трубчатый тонкопленочный выпариватель, трубчатый выпариватель с падающей пленкой, используют более предпочтительно, и предпочтительны конструкции с большой площадью контакта газ-жидкость, чтобы обеспечить быстрый переход образующихся компонентов с низкой температурой кипения в газообразную фазу.
Хотя известные материалы можно использовать для реакторов термического разложения и линий при условии, что они не оказывают вредного воздействия на арилкарбамат или продукты в форме ароматического гидроксисоединения, изоцианата и тому подобного, предпочтительно использовать SUS304, SUS316 или SUS316L и тому подобное, так как они недороги.
Очистка реактора термического разложения
В рассматриваемом варианте реакционная жидкость, содержащая арилкарбамат, полученная путем осуществления взаимодействия диарилкарбоната и соединения амина, содержит полимерные продукты побочных реакций, как представлено, например, вышеуказанными формулами (5), (6) и (7). Так как указанные продукты побочных реакций легко растворяются в ароматическом гидроксисоединении во многих случаях, их растворяют в реакционной жидкости, содержащей арилкарбамат. Однако, если большую часть ароматического гидроксисоединения отводят из указанного реактора термического разложения в форме газофазного компонента, существует много случаев, в которых продукты побочных реакций прилипают к реактору термического разложения. Кроме того, хотя образуются полимерные продукты побочных реакций, возникающие из побочных реакций, представленных, например, в вышеуказанных формулах (8), (9) и (10), сопровождающих термическое разложение арилкарбамата, существует много случаев, в которых побочные продукты, полученные в результате указанной реакции термического разложения, также прилипают к реактору термического разложения. Если указанные соединения, прилипающие к реактору термического разложения, накапливаются до некоторой степени, функционирование реактора термического разложения нарушается, и так как часто возможны случаи, в которых указанное затрудняет длительные операции, возникает необходимость в проведении работ, состоящих в разборке и очистке реактора термического разложения.
Авторы настоящего изобретения неожиданно обнаружили, что соединения, прилипшие к реактору термического разложения, легко растворяются в кислоте. На основании указанных открытий, в случае, когда вещества с высокой температурой кипения прилипают к реактору термического разложения, авторы настоящего изобретения обдумали и усовершенствовали способ сохранения внутренней поверхности реактора термического разложения (и частично его стенок) чистыми путем очищения стенок реактора термического разложения кислотой для растворения указанных веществ с высокой температурой кипения и удаления их из указанного реактора термического разложения. Так как указанный способ обеспечивает очистку стенок реактора термического разложения без его разборки и отдельного очищения реактора термического разложения, время простоя реактора термического разложения можно значительно сократить, тем самым, повышая производительность изоцианата.
Не существует конкретных ограничений относительно кислот, используемых для очистки, при условии, что они способны растворять полимерные побочные продукты, и можно использовать органические кислоты или неорганические кислоты, хотя предпочтительно использовать органические кислоты. Хотя примеры используемых органических кислот могут включать угольную кислоту, сульфоновую кислоту, сульфиновую кислоту, фенолы, енолы, тиофенолы, имиды, оксимы и ароматические сульфонамиды, предпочтительно использовать угольную кислоту и фенолы. Примеры таких соединений могут включать насыщенные или ненасыщенные соединения алифатической монокарбоновой кислоты, такие как муравьиная кислота, уксусная кислота, пропионовая кислота, н-масляная кислота, изомасляная кислота, валериановая кислота, изовалериановая кислота, 2-метилбутановая кислота, триметилуксусная кислота, гексановая кислота, изокапроевая кислота, 2-этилбутановая кислота, 2,2-диметилбутановая кислота, гептановая кислота (включая изомеры), октановая кислота (включая изомеры), нонановая кислота (включая изомеры), декановая кислота (включая изомеры), ундекановая кислота (включая изомеры), додекановая кислота (включая изомеры), тетрадекановая кислота (включая изомеры), гексадекановая кислота (включая изомеры), акриловая кислота, кротоновая кислота, изокротоновая кислота, винилацетат, метакриловая кислота, ангеликовая кислота, тиглиновая кислота, аллилацетат или ундеценовая кислота (включая изомеры); насыщенные или ненасыщенные алифатические дикарбоновые кислоты, такие как щавелевая кислота, малоновая кислота, янтарная кислота, глутаровая кислота, адипиновая кислота, гептандикарбоновая кислота (включая изомеры), октандикарбоновая кислота (включая изомеры), нонандикарбоновая кислота (включая изомеры), октандикарбоновая кислота (включая изомеры), малеиновая кислота, фумаровая кислота, метилмалеиновая кислота, метилфумаровая кислота, пентендикарбоновая кислота (включая изомеры), итаконовая кислота или аллилмалоновая кислота; насыщенные или ненасыщенные алифатические трикарбоновые кислоты, такие как 1,2,3-пропантрикарбоновая кислота, 1,2,3-пропентрикарбоновая кислота или 2,3-диметилбутан-1,2,3-трикарбоновая кислота; соединения ароматической монокарбоновой кислоты, такие как бензойная кислота, метилбензойная кислота (включая изомеры), этилбензойная кислота (включая изомеры), пропилбензойная кислота (включая изомеры), диметилбензойная кислота (включая изомеры) или триметилбензойная кислота (включая изомеры); соединения ароматических дикарбоновых кислот, такие как фталевая кислота, изофталевая кислота, терефталевая кислота или метилизофталевая кислота (включая изомеры); соединения ароматических трикарбоновых кислот, такие как гемимеллитовая кислота, тримеллитовая кислота или тримезиновая кислота; монозамещенные фенолы, такие как фенол, метилфенол (включая изомеры), этилфенол (включая изомеры), пропилфенол (включая изомеры), бутилфенол (включая изомеры), пентилфенол (включая изомеры), гексилфенол (включая изомеры), гептилфенол (включая изомеры), октилфенол (включая изомеры), нонилфенол (включая изомеры), децилфенол (включая изомеры), додецилфенол (включая изомеры), фенилфенол (включая изомеры), феноксифенол (включая изомеры) или кумилфенол (включая изомеры); дизамещенные фенолы, такие как диметилфенол (включая изомеры), диэтилфенол (включая изомеры), дипропилфенол (включая изомеры), дибутилфенол (включая изомеры), дипентилфенол (включая изомеры), дигексилфенол (включая изомеры), дигептилфенол (включая изомеры), диоктилфенол (включая изомеры), динонилфенол (включая изомеры), дидецилфенол (включая изомеры), дидодецилфенол (включая изомеры), дифенилфенол (включая изомеры), дифеноксифенол (включая изомеры), дикумилфенол (включая изомеры), метилэтилфенол (включая изомеры), метилпропилфенол (включая изомеры), метилбутилфенол (включая изомеры), метилпентилфенол (включая изомеры), метилгексилфенол (включая изомеры), метилгептилфенол (включая изомеры), метилоктилфенол (включая изомеры), метилнонилфенол (включая изомеры), метилдецилфенол (включая изомеры), метилдодецилфенол (включая изомеры), метилфенилфенол (включая изомеры), метилфеноксифенол (включая изомеры), метилкумилфенол (включая изомеры), этилпропилфенол (включая изомеры), этилбутилфенол (включая изомеры), этилпентилфенол (включая изомеры), этилгексилфенол (включая изомеры), этилгептилфенол (включая изомеры), этилоктилфенол (включая изомеры), этилнонилфенол (включая изомеры), этилдецилфенол (включая изомеры), этилдодецилфенол (включая изомеры), этилфенилфенол (включая изомеры), этилфеноксифенол (включая изомеры), этилкумилфенол (включая изомеры), пропилбутилфенол (включая изомеры), пропилпентилфенол (включая изомеры), пропилгексилфенол (включая изомеры), пропилгептилфенол (включая изомеры), пропилоктилфенол (включая изомеры), пропилнонилфенол (включая изомеры), пропилдецилфенол (включая изомеры), пропилдодецилфенол (включая изомеры), пропилфенилфенол (включая изомеры), пропилфеноксифенол (включая изомеры), пропилкумилфенол (включая изомеры), бутилпентилфенол (включая изомеры), бутилгексилфенол (включая изомеры), бутилгептилфенол (включая изомеры), бутилоктилфенол (включая изомеры), бутилнонилфенол (включая изомеры), бутилдецилфенол (включая изомеры), бутилдодецилфенол (включая изомеры), бутилфенилфенол (включая изомеры), бутилфеноксифенол (включая изомеры), бутилкумилфенол (включая изомеры), пентилгексилфенол (включая изомеры), пентилгептилфенол (включая изомеры), пентилоктилфенол (включая изомеры), пентилнонилфенол (включая изомеры), пентилдецилфенол (включая изомеры), пентилдодецилфенол (включая изомеры), пентилфенилфенол (включая изомеры), пентилфеноксифенол (включая изомеры), пентилкумилфенол (включая изомеры), гексилгептилфенол (включая изомеры), гексилоктилфенол (включая изомеры), гексилнонилфенол (включая изомеры), гексилдецилфенол (включая изомеры), гексилдодецилфенол (включая изомеры), гексилфенилфенол (включая изомеры), гексилфеноксифенол (включая изомеры), гексилкумилфенол (включая изомеры), гептилоктилфенол (включая изомеры), гептилнонилфенол (включая изомеры), гептилдецилфенол (включая изомеры), гептилдодецилфенол (включая изомеры), гептилфенилфенол (включая изомеры), гептилфеноксифенол (включая изомеры), гептилкумилфенол (включая изомеры), октилнонилфенол (включая изомеры), октилдецилфенол (включая изомеры), октилдодецилфенол (включая изомеры), октилфенилфенол (включая изомеры), октилфеноксифенол (включая изомеры), октилкумилфенол (включая изомеры), нонилдецилфенол (включая изомеры), нонилдодецилфенол (включая изомеры), нонилфенилфенол (включая изомеры), нонилфеноксифенол (включая изомеры), нонилкумилфенол (включая изомеры), додецилфенилфенол (включая изомеры), додецилфеноксифенол (включая изомеры) или додецилкумилфенол (включая изомеры); и тризамещенные фенолы, такие как триметилфенол (включая изомеры), триэтилфенол (включая изомеры), трипропилфенол (включая изомеры), трибутилфенол (включая изомеры), трипентилфенол (включая изомеры), тригексилфенол (включая изомеры), тригептилфенол (включая изомеры), триоктилфенол (включая изомеры), тринонилфенол (включая изомеры), тридецилфенол (включая изомеры), тридодецилфенол (включая изомеры), трифенилфенол (включая изомеры), трифеноксифенол (включая изомеры), трикумилфенол (включая изомеры), диметилэтилфенол (включая изомеры), диметилпропилфенол (включая изомеры), диметилбутилфенол (включая изомеры), диметилпентилфенол (включая изомеры), диметилгексилфенол (включая изомеры), диметилгептилфенол (включая изомеры), диметилоктилфенол (включая изомеры), диметилнонилфенол (включая изомеры), диметилдецилфенол (включая изомеры), диметилдодецилфенол (включая изомеры), диметилфенилфенол (включая изомеры), диметилфеноксифенол (включая изомеры), диметилкумилфенол (включая изомеры), диэтилметилфенол (включая изомеры), диэтилпропилфенол (включая изомеры), диэтилбутилфенол (включая изомеры), диэтилпентилфенол (включая изомеры), диэтилгексилфенол (включая изомеры), диэтилгептилфенол (включая изомеры), диэтилоктилфенол (включая изомеры), диэтилнонилфенол (включая изомеры), диэтилдецилфенол (включая изомеры), диэтилдодецилфенол (включая изомеры), диэтилфенилфенол (включая изомеры), диэтилфеноксифенол (включая изомеры), диэтилкумилфенол (включая изомеры), дипропилметилфенол (включая изомеры), дипропилэтилфенол (включая изомеры), дипропилбутилфенол (включая изомеры), дипропилпентилфенол (включая изомеры), дипропилгексилфенол (включая изомеры), дипропилгептилфенол (включая изомеры), дипропилоктилфенол (включая изомеры), дипропилнонилфенол (включая изомеры), дипропилдецилфенол (включая изомеры), дипропилдодецилфенол (включая изомеры), дипропилфенилфенол (включая изомеры), дипропилфеноксифенол (включая изомеры), дипропилкумилфенол (включая изомеры), дибутилметилфенол (включая изомеры), дибутилэтилфенол (включая изомеры), дибутилпропилфенол (включая изомеры), дибутилпентилфенол (включая изомеры), дибутилгексилфенол (включая изомеры), дибутилгептилфенол (включая изомеры), дибутилоктилфенол (включая изомеры), дибутилнонилфенол (включая изомеры), дибутилдецилфенол (включая изомеры), дибутилдодецилфенол (включая изомеры), дибутилфенилфенол (включая изомеры), дибутилфеноксифенол (включая изомеры), дибутилкумилфенол (включая изомеры), дипентилметилфенол (включая изомеры), дипентилэтилфенол (включая изомеры), дипентилпропилфенол (включая изомеры), дипентилбутилфенол (включая изомеры), дипентилгексилфенол (включая изомеры), дипентилгептилфенол (включая изомеры), дипентилоктилфенол (включая изомеры), дипентилнонилфенол (включая изомеры), дипентилдецилфенол (включая изомеры), дипентилдодецилфенол (включая изомеры), дипентилфенилфенол (включая изомеры), дипентилфеноксифенол (включая изомеры), дипентилкумилфенол (включая изомеры), дигексилметилфенол (включая изомеры), дигексилэтилфенол (включая изомеры), дигексилпропилфенол (включая изомеры), дигексилбутилфенол (включая изомеры), дигексилпентилфенол (включая изомеры), дигексилгептилфенол (включая изомеры), дигексилоктилфенол (включая изомеры), дигексилнонилфенол (включая изомеры), дигексилдецилфенол (включая изомеры), дигексилдодецилфенол (включая изомеры), дигексилфенилфенол (включая изомеры), дигексилфеноксифенол (включая изомеры), дигексилкумилфенол (включая изомеры), дигептилметилфенол (включая изомеры), дигептилэтилфенол (включая изомеры), дигептилпропилфенол (включая изомеры), дигептилбутилфенол (включая изомеры), дигептилпентилфенол (включая изомеры), дигептилгексилфенол (включая изомеры), дигептилоктилфенол (включая изомеры), дигептилнонилфенол (включая изомеры), дигептилдецилфенол (включая изомеры), дигептилдодецилфенол (включая изомеры), дигептилфенилфенол (включая изомеры), дигептилфеноксифенол (включая изомеры), дигептилкумилфенол (включая изомеры), диоктилметилфенол (включая изомеры), диоктилэтилфенол (включая изомеры), диоктилпропилфенол (включая изомеры), диоктилбутилфенол (включая изомеры), диоктилпентилфенол (включая изомеры), диоктилгексилфенол (включая изомеры), диоктилгептилфенол (включая изомеры), диоктилнонилфенол (включая изомеры), диоктилдецилфенол (включая изомеры), диоктилдодецилфенол (включая изомеры), диоктилфенилфенол (включая изомеры), диоктилфеноксифенол (включая изомеры), диоктилкумилфенол (включая изомеры), динонилметилфенол (включая изомеры), динонилэтилфенол (включая изомеры), динонилпропилфенол (включая изомеры), динонилбутилфенол (включая изомеры), динонилпентилфенол (включая изомеры), динонилгексилфенол (включая изомеры), динонилгептилфенол (включая изомеры), динонилоктилфенол (включая изомеры), динонилдецилфенол (включая изомеры), динонилдодецилфенол (включая изомеры), динонилфенилфенол (включая изомеры), динонилфеноксифенол (включая изомеры), динонилкумилфенол (включая изомеры), дидецилметилфенол (включая изомеры), дидецилэтилфенол (включая изомеры), дидецилпропилфенол (включая изомеры), дидецилбутилфенол (включая изомеры), дидецилпентилфенол (включая изомеры), дидецилгексилфенол (включая изомеры), дидецилгептилфенол (включая изомеры), дидецилоктилфенол (включая изомеры), дидецилнонилфенол (включая изомеры), дидецилдодецилфенол (включая изомеры), дидецилфенилфенол (включая изомеры), дидецилфеноксифенол (включая изомеры), дидецилкумилфенол (включая изомеры), дидодецилметилфенол (включая изомеры), дидодецилэтилфенол (включая изомеры), дидодецилпропилфенол (включая изомеры), дидодецилбутилфенол (включая изомеры), дидодецилпентилфенол (включая изомеры), дидодецилгексилфенол (включая изомеры), дидодецилгептилфенол (включая изомеры), дидодецилоктилфенол (включая изомеры), дидодецилнонилфенол (включая изомеры), дидодецилдецилфенол (включая изомеры), дидодецилдодецилфенол (включая изомеры), дидодецилфенилфенол (включая изомеры), дидодецилфеноксифенол (включая изомеры), дидодецилкумилфенол (включая изомеры), дифенилметилфенол (включая изомеры), дифенилэтилфенол (включая изомеры), дифенилпропилфенол (включая изомеры), дифенилбутилфенол (включая изомеры), дифенилпентилфенол (включая изомеры), дифенилгексилфенол (включая изомеры), дифенилгептилфенол (включая изомеры), дифенилоктилфенол (включая изомеры), дифенилнонилфенол (включая изомеры), дифенилдецилфенол (включая изомеры), дифенилдодецилфенол (включая изомеры), дифенилфеноксифенол (включая изомеры), дифенилкумилфенол (включая изомеры), дифеноксиметилфенол (включая изомеры), дифеноксиэтилфенол (включая изомеры), дифеноксипропилфенол (включая изомеры), дифеноксибутилфенол (включая изомеры), дифеноксипентилфенол (включая изомеры), дифеноксигексилфенол (включая изомеры), дифеноксигептилфенол (включая изомеры), дифеноксиоктилфенол (включая изомеры), дифеноксинонилфенол (включая изомеры), дифеноксидецилфенол (включая изомеры), дифеноксидодецилфенол (включая изомеры), дифеноксифенилфенол (включая изомеры), дифеноксикумилфенол (включая изомеры), дикумилметилфенол (включая изомеры), дикумилэтилфенол (включая изомеры), дикумилпропилфенол (включая изомеры), дикумилбутилфенол (включая изомеры), дикумилпентилфенол (включая изомеры), дикумилгексилфенол (включая изомеры), дикумилгептилфенол (включая изомеры), дикумилоктилфенол (включая изомеры), дикумилнонилфенол (включая изомеры), дикумилдецилфенол (включая изомеры), дикумилдодецилфенол (включая изомеры), дикумилфенилфенол (включая изомеры), дикумилфеноксифенол (включая изомеры), метилэтилпропилфенол (включая изомеры), метилэтилбутилфенол (включая изомеры), метилэтилпентилфенол (включая изомеры), метилэтилгексилфенол (включая изомеры), метилэтилгептилфенол (включая изомеры), метилэтилоктилфенол (включая изомеры), метилэтилнонилфенол (включая изомеры), метилэтилдецилфенол (включая изомеры), метилэтилдодецилфенол (включая изомеры), метилэтилфенилфенол (включая изомеры), метилэтилфеноксифенол (включая изомеры), метилэтилкумилфенол (включая изомеры), метилпропилбутилфенол (включая изомеры), метилпропилпентилфенол (включая изомеры), метилпропилгексилфенол (включая изомеры), метилпропилгептилфенол (включая изомеры), метилпропилоктилфенол (включая изомеры), метилпропилнонилфенол (включая изомеры), метилпропилдецилфенол (включая изомеры), метилпропилдодецилфенол (включая изомеры), метилпропилфенилфенол (включая изомеры), метилпропилфеноксифенол (включая изомеры), метилпропилкумилфенол (включая изомеры), метилбутилпентилфенол (включая изомеры), метилбутилгексилфенол (включая изомеры), метилбутилгептилфенол (включая изомеры), метилбутилоктилфенол (включая изомеры), метилбутилнонилфенол (включая изомеры), метилбутилдецилфенол (включая изомеры), метилбутилдодецилфенол (включая изомеры), метилбутилфенилфенол (включая изомеры), метилбутилфеноксифенол (включая изомеры), метилбутилкумилфенол (включая изомеры), метилпентилгексилфенол, метилпентилгептилфенол (включая изомеры), метилпентилоктилфенол (включая изомеры), метилпентилнонилфенол (включая изомеры), метилпентилдецилфенол (включая изомеры), метилпентилдодецилфенол (включая изомеры), метилпентилфенилфенол (включая изомеры), метилпентилфеноксифенол (включая изомеры), метилпентилкумилфенол (включая изомеры), метилгексилгептилфенол (включая изомеры), метилгексилоктилфенол (включая изомеры), метилгексилнонилфенол (включая изомеры), метилгексилдецилфенол (включая изомеры), метилгексилдодецилфенол (включая изомеры), метилгексилфенилфенол (включая изомеры), метилгексилфеноксифенол (включая изомеры), метилгексилкумилфенол (включая изомеры), этилпропилбутилфенол (включая изомеры), этилпропилпентилфенол (включая изомеры), этилпропилгексилфенол (включая изомеры), этилпропилгептилфенол (включая изомеры), этилпропилоктилфенол (включая изомеры), этилпропилнонилфенол (включая изомеры), этилпропилдецилфенол (включая изомеры), этилпропилдодецилфенол (включая изомеры), этилпропилфенилфенол (включая изомеры), этилпропилфеноксифенол (включая изомеры), этилпропилкумилфенол (включая изомеры), этилбутилфенол (включая изомеры), этилбутилпентилфенол (включая изомеры), этилбутилгексилфенол (включая изомеры), этилбутилгептилфенол (включая изомеры), этилбутилоктилфенол (включая изомеры), этилбутилнонилфенол (включая изомеры), этилбутилдецилфенол (включая изомеры), этилбутилдодецилфенол (включая изомеры), этилбутилфенилфенол (включая изомеры), этилбутилфеноксифенол (включая изомеры), этилбутилкумилфенол (включая изомеры), этилпентилгексилфенол (включая изомеры), этилпентилгептилфенол (включая изомеры), этилпентилоктилфенол (включая изомеры), этилпентилнонилфенол (включая изомеры), этилпентилдецилфенол (включая изомеры), этилпентилдодецилфенол (включая изомеры), этилпентилфенилфенол (включая изомеры), этилпентилфеноксифенол (включая изомеры), этилпентилкумилфенол (включая изомеры), этилгексилгептилфенол (включая изомеры), этилгексилоктилфенол (включая изомеры), этилгексилнонилфенол (включая изомеры), этилгексилдецилфенол (включая изомеры), этилгексилдодецилфенол (включая изомеры), этилгексилфенилфенол (включая изомеры), этилгексилфеноксифенол (включая изомеры), этилгексилкумилфенол (включая изомеры), этилгептилоктилфенол (включая изомеры), этилгептилнонилфенол (включая изомеры), этилгептилдецилфенол (включая изомеры), этилгептилдодецилфенол (включая изомеры), этилгептилфенилфенол (включая изомеры), этилгептилфеноксифенол (включая изомеры), этилгептилкумилфенол (включая изомеры), этилоктилфенол (включая изомеры), этилоктилнонилфенол (включая изомеры), этилоктилдецилфенол (включая изомеры), этилоктилдодецилфенол (включая изомеры), этилоктилфенилфенол (включая изомеры), этилоктилфеноксифенол (включая изомеры), этилоктилкумилфенол (включая изомеры), этилнонилдецилфенол (включая изомеры), этилнонилдодецилфенол (включая изомеры), этилнонилфенилфенол (включая изомеры), этилнонилфеноксифенол (включая изомеры), этилнонилкумилфенол (включая изомеры), этилдецилдодецилфенол (включая изомеры), этилдецилфенилфенол (включая изомеры), этилдецилфеноксифенол (включая изомеры), этилдецилкумилфенол (включая изомеры), этилдодецилфенилфенол (включая изомеры), этилдодецилфеноксифенол (включая изомеры), этилдодецилкумилфенол (включая изомеры), этилфенилфеноксифенол (включая изомеры), этилфенилкумилфенол (включая изомеры), пропилбутилфенол (включая изомеры), пропилбутилпентилфенол (включая изомеры), пропилбутилгексилфенол (включая изомеры), пропилбутилгептилфенол (включая изомеры), пропилбутилоктилфенол (включая изомеры), пропилбутилнонилфенол (включая изомеры), пропилбутилдецилфенол (включая изомеры), пропилбутилдодецилфенол (включая изомеры), пропилбутилфенилфенол (включая изомеры), пропилбутилфеноксифенол (включая изомеры), пропилбутилкумилфенол (включая изомеры), пропилпентилфенол (включая изомеры), пропилпентилгексилфенол (включая изомеры), пропилпентилгептилфенол (включая изомеры), пропилпентилоктилфенол (включая изомеры), пропилпентилнонилфенол (включая изомеры), пропилпентилдецилфенол (включая изомеры), пропилпентилдодецилфенол (включая изомеры), пропилпентилфенилфенол (включая изомеры), пропилпентилфеноксифенол (включая изомеры), пропилпентилкумилфенол (включая изомеры), пропилгексилфенол (включая изомеры), пропилгексилгептилфенол (включая изомеры), пропилгексилоктилфенол (включая изомеры), пропилгексилнонилфенол (включая изомеры), пропилгексилдецилфенол (включая изомеры), пропилгексилдодецилфенол (включая изомеры), пропилгексилфенилфенол (включая изомеры), пропилгексилфеноксифенол (включая изомеры), пропилгексилкумилфенол (включая изомеры), пропилгептилоктилфенол (включая изомеры), пропилгептилнонилфенол (включая изомеры), пропилгептилдецилфенол (включая изомеры), пропилгептилдодецилфенол (включая изомеры), пропилгептилфенилфенол (включая изомеры), пропилгептилфеноксифенол (включая изомеры), пропилгептилкумилфенол (включая изомеры), пропилоктилнонилфенол (включая изомеры), пропилоктилдецилфенол (включая изомеры), пропилоктилдодецилфенол (включая изомеры), пропилоктилфенилфенол (включая изомеры), пропилоктилфеноксифенол (включая изомеры), пропилоктилкумилфенол (включая изомеры), пропилнонилдецилфенол (включая изомеры), пропилнонилдодецилфенол (включая изомеры), пропилнонилфенилфенол (включая изомеры), пропилнонилфеноксифенол (включая изомеры), пропилнонилкумилфенол (включая изомеры), пропилдецилдодецилфенол (включая изомеры), пропилдецилфенилфенол (включая изомеры), пропилдецилфеноксифенол (включая изомеры), пропилдецилкумилфенол (включая изомеры), пропилдодецилфенилфенол (включая изомеры), пропилдодецилфеноксифенол (включая изомеры), пропилдодецилкумилфенол (включая изомеры), метилфенол (включая изомеры), этилфенол (включая изомеры), пропилфенол (включая изомеры), бутилфенол (включая изомеры), пентилфенол (включая изомеры), гексилфенол (включая изомеры), гептилфенол (включая изомеры), октилфенол (включая изомеры), нонилфенол (включая изомеры), децилфенол (включая изомеры), додецилфенол (включая изомеры), фенилфенол (включая изомеры), феноксифенол (включая изомеры), кумилфенол (включая изомеры), пропилфенилфеноксифенол (включая изомеры), пропилфенилкумилфенол (включая изомеры), пропилфеноксикумилфенол (включая изомеры), пропилбутилпентилфенол (включая изомеры), пропилбутилгексилфенол (включая изомеры), пропилбутилгептилфенол (включая изомеры), пропилбутилоктилфенол (включая изомеры), пропилбутилнонилфенол (включая изомеры), пропилбутилдецилфенол (включая изомеры), пропилбутилдодецилфенол (включая изомеры), пропилбутилфенилфенол (включая изомеры), пропилбутилфеноксифенол (включая изомеры), пропилбутилкумилфенол (включая изомеры), пропилпентилфенол (включая изомеры), пропилпентилгексилфенол (включая изомеры), пропилпентилгептилфенол (включая изомеры), пропилпентилоктилфенол (включая изомеры), пропилпентилнонилфенол (включая изомеры), пропилпентилдецилфенол (включая изомеры), пропилпентилдодецилфенол (включая изомеры), пропилпентилфенилфенол (включая изомеры), пропилпентилфеноксифенол (включая изомеры), пропилпентилкумилфенол (включая изомеры), пропилгексилгептилфенол (включая изомеры), пропилгексилоктилфенол (включая изомеры), пропилгексилнонилфенол (включая изомеры), пропилгексилдецилфенол (включая изомеры), пропилгексилдодецилфенол (включая изомеры), пропилгексилфенилфенол (включая изомеры), пропилгексилфеноксифенол (включая изомеры), пропилгексилкумилфенол (включая изомеры), пропилгептилоктилфенол (включая изомеры), пропилгептилнонилфенол (включая изомеры), пропилгептилдецилфенол (включая изомеры), пропилгептилдодецилфенол (включая изомеры), пропилгептилфенилфенол (включая изомеры), пропилгептилфеноксифенол (включая изомеры), пропилгептилкумилфенол (включая изомеры), пропилоктилнонилфенол (включая изомеры), пропилоктилдецилфенол (включая изомеры), пропилоктилдодецилфенол (включая изомеры), пропилоктилфенилфенол (включая изомеры), пропилоктилфеноксифенол (включая изомеры), пропилоктилкумилфенол (включая изомеры), пропилнонилдецилфенол (включая изомеры), пропилнонилдодецилфенол (включая изомеры), пропилнонилфенилфенол (включая изомеры), пропилнонилфеноксифенол (включая изомеры), пропилнонилкумилфенол (включая изомеры), пропилдецилдодецилфенол (включая изомеры), пропилдецилфенилфенол (включая изомеры), пропилдецилфеноксифенол (включая изомеры), пропилдецилкумилфенол (включая изомеры), пропилдодецилфенилфенол (включая изомеры), пропилдодецилфеноксифенол (включая изомеры), пропилфенилфеноксифенол (включая изомеры), пропилфенилкумилфенол (включая изомеры), бутилпентилгексилфенол (включая изомеры), бутилпентилгептилфенол (включая изомеры), бутилпентилоктилфенол (включая изомеры), бутилпентилнонилфенол (включая изомеры), бутилпентилдецилфенол (включая изомеры), бутилпентилдодецилфенол (включая изомеры), бутилпентилфенилфенол (включая изомеры), бутилпентилфеноксифенол (включая изомеры), бутилпентилкумилфенол (включая изомеры), бутилгексилгептилфенол (включая изомеры), бутилгексилоктилфенол (включая изомеры), бутилгексилнонилфенол (включая изомеры), бутилгексилдецилфенол (включая изомеры), бутилгексилдодецилфенол (включая изомеры), бутилгексилфенилфенол (включая изомеры), бутилгексилфеноксифенол (включая изомеры), бутилгексилкумилфенол (включая изомеры), бутилгептилоктилфенол (включая изомеры), бутилгептилнонилфенол (включая изомеры), бутилгептилдецилфенол (включая изомеры), бутилгептилдодецилфенол (включая изомеры), бутилгептилфенилфенол (включая изомеры), бутилгептилфеноксифенол (включая изомеры), бутилгептилкумилфенол (включая изомеры), бутилоктилнонилфенол (включая изомеры), бутилоктилдецилфенол (включая изомеры), бутилоктилдодецилфенол (включая изомеры), бутилоктилфенилфенол (включая изомеры), бутилоктилфеноксифенол (включая изомеры), бутилоктилкумилфенол (включая изомеры), бутилнонилдецилфенол (включая изомеры), бутилнонилдодецилфенол (включая изомеры), бутилнонилфенилфенол (включая изомеры), бутилнонилфеноксифенол (включая изомеры), бутилнонилкумилфенол (включая изомеры), бутилдецилдодецилфенол (включая изомеры), бутилдецилфенилфенол (включая изомеры), бутилдецилфеноксифенол (включая изомеры), бутилдецилкумилфенол (включая изомеры), бутилдодецилфенол (включая изомеры), бутилдодецилфенилфенол (включая изомеры), бутилдодецилфеноксифенол (включая изомеры), бутилдодецилкумилфенол (включая изомеры), бутилфенилфенол (включая изомеры), бутилфенилфеноксифенол (включая изомеры), бутилфенилкумилфенол (включая изомеры), пентилгексилгептилфенол (включая изомеры), пентилгексилоктилфенол (включая изомеры), пентилгексилнонилфенол (включая изомеры), пентилгексилдецилфенол (включая изомеры), пентилгексилдодецилфенол (включая изомеры), пентилгексилфенилфенол (включая изомеры), пентилгексилфеноксифенол (включая изомеры), пентилгексилкумилфенол (включая изомеры), пентилгептилоктилфенол (включая изомеры), пентилгептилнонилфенол (включая изомеры), пентилгептилдецилфенол (включая изомеры), пентилгептилдодецилфенол (включая изомеры), пентилгептилфенилфенол (включая изомеры), пентилгептилфеноксифенол (включая изомеры), пентилгептилкумилфенол (включая изомеры), пентилоктилнонилфенол (включая изомеры), пентилоктилдецилфенол (включая изомеры), пентилоктилдодецилфенол (включая изомеры), пентилоктилфенилфенол (включая изомеры), пентилоктилфеноксифенол (включая изомеры), пентилоктилкумилфенол (включая изомеры), пентилнонилдецилфенол (включая изомеры), пентилнонилдодецилфенол (включая изомеры), пентилнонилфенилфенол (включая изомеры), пентилнонилфеноксифенол (включая изомеры), пентилнонилкумилфенол (включая изомеры), пентилдецилдодецилфенол (включая изомеры), пентилдецилфенилфенол (включая изомеры), пентилдецилфеноксифенол (включая изомеры), пентилдецилкумилфенол (включая изомеры), пентилдодецилфенилфенол (включая изомеры), пентилдодецилфеноксифенол (включая изомеры), пентилдодецилкумилфенол (включая изомеры), пентилфенилфеноксифенол (включая изомеры), пентилфенилкумилфенол (включая изомеры), гексилгептилоктилфенол (включая изомеры), гексилгептилнонилфенол (включая изомеры), гексилгептилдецилфенол (включая изомеры), гексилгептилдодецилфенол (включая изомеры), гексилгептилфенилфенол (включая изомеры), гексилгептилфеноксифенол (включая изомеры), гексилгептилкумилфенол (включая изомеры), гексилоктилнонилфенол (включая изомеры), гексилоктилдецилфенол (включая изомеры), гексилоктилдодецилфенол (включая изомеры), гексилоктилфенилфенол (включая изомеры), гексилоктилфеноксифенол (включая изомеры), гексилоктилкумилфенол (включая изомеры), гексилнонилдецилфенол (включая изомеры), гексилнонилдодецилфенол (включая изомеры), гексилнонилфенилфенол (включая изомеры), гексилнонилфеноксифенол (включая изомеры), гексилдецилфенилфенол (включая изомеры), гексилдецилфеноксифенол (включая изомеры), гексилдецилкумилфенол (включая изомеры), гексилдодецилфенилфенол (включая изомеры), гексилдодецилфеноксифенол (включая изомеры), гексилдодецилкумилфенол (включая изомеры), гексилфенилфеноксифенол (включая изомеры), гексилфенилкумилфенол (включая изомеры), гептилоктилнонилфенол (включая изомеры), гептилоктилдецилфенол (включая изомеры), гептилоктилдодецилфенол (включая изомеры), гептилоктилфенилфенол (включая изомеры), гептилоктилфеноксифенол (включая изомеры), гептилоктилкумилфенол (включая изомеры), гептилнонилдецилфенол (включая изомеры), гептилнонилдодецилфенол (включая изомеры), гептилнонилфенилфенол (включая изомеры), гептилнонилфеноксифенол (включая изомеры), гептилнонилкумилфенол (включая изомеры), гептилдецилдодецилфенол (включая изомеры), гептилдецилфенилфенол (включая изомеры), гептилдецилфеноксифенол (включая изомеры), гептилдецилкумилфенол (включая изомеры), гептилдодецилфенилфенол (включая изомеры), гептилдодецилфеноксифенол (включая изомеры), гептилдодецилкумилфенол (включая изомеры), гептилфенилфеноксифенол (включая изомеры), гептилфенилкумилфенол (включая изомеры), октилнонилдецилфенол (включая изомеры), октилнонилдодецилфенол (включая изомеры), октилнонилфенилфенол (включая изомеры), октилнонилфеноксифенол (включая изомеры), октилнонилкумилфенол (включая изомеры), октилдецилдодецилфенол (включая изомеры), октилдецилфенилфенол (включая изомеры), октилдецилфеноксифенол (включая изомеры), октилдецилкумилфенол (включая изомеры), октилдодецилфенилфенол (включая изомеры), октилдодецилфеноксифенол (включая изомеры), октилдодецилкумилфенол (включая изомеры), октилфенилфеноксифенол (включая изомеры), октилфенилкумилфенол (включая изомеры), нонилдецилдодецилфенол (включая изомеры), нонилдецилфенилфенол (включая изомеры), нонилдецилфеноксифенол (включая изомеры), нонилдецилкумилфенол (включая изомеры), нонилдодецилфенилфенол (включая изомеры), нонилдодецилфеноксифенол (включая изомеры), нонилдодецилкумилфенол (включая изомеры), нонилфенилфеноксифенол (включая изомеры), нонилфенилкумилфенол (включая изомеры), децилдодецилфенилфенол (включая изомеры), децилдодецилфеноксифенол (включая изомеры), децилдодецилкумилфенол (включая изомеры), децилфенилфеноксифенол (включая изомеры), децилфенилкумилфенол (включая изомеры), додецилфенилфеноксифенол (включая изомеры), додецилфенилкумилфенол (включая изомеры) или фенилфеноксикумилфенол (включая изомеры). Среди указанных органических кислот, с учетом эффектов в случае очистки растворителя, остающегося в реакторе термического разложения после процедуры очистки, ароматические гидроксисоединения более предпочтительны, хотя еще более предпочтительны соединения, аналогичные ароматическим гидроксисоединениям, которые используют в реакции диарилкарбоната и соединения амина.
Обратите внимание на то, что в случае использования ароматического гидроксисоединения в качестве кислоты, используемой в процессе очистки, разница между стандартной температурой кипения ароматического гидроксисоединения и стандартными температурами кипения соединения, соответствующего изоцианату, образующемуся в процессе раскрытого выше термического разложения арилкарбамата и ароматического гидроксисоединения, образующегося в процессе термического разложения арилкарбамата, составляет предпочтительно 10°C или более с точки зрения очищающего эффекта.
Различные способы можно использовать для очистки реактора термического разложения, используя вышеуказанный очищающий растворитель, примеры которых могут включать очистку реактора термического разложения путем введения очищающего растворителя из верхней части реактора термического разложения, и очистку внутренней поверхности реактора термического разложения путем введения очищающего растворителя из нижней части реактора термического разложения и осуществления его кипячения внутри реактора термического разложения.
Нет необходимости проводить процедуру очистки каждый раз, когда осуществляют указанную реакцию термического разложения, скорее частота проведения процедур очистки произвольно определяется в соответствии с используемыми соединениями, производительностью и так далее, и процедуру очистки предпочтительно осуществляют один раз в каждые 1-20000 часов работы, более предпочтительно от одного раза в день до одного раза в год рабочего времени и еще более предпочтительно от одного раза в месяц до одного раза в год рабочего времени. Реактор термического разложения может быть снабжен линией для подачи очищающего растворителя.
Кроме того, если термическое разложение арилкарбамата осуществляют с целью очистки реактора термического разложения, очищающий растворитель может также присутствовать в условиях указанной реакции термического разложения. Это отличается от требования к инертному растворителю, как указано в известном ранее способе (см., например, патент США № 4081472). Например, в соответствии с указанным патентным документом, хотя термин инертный растворитель относится к соединению, которое не реагирует с изоцианатом, образующимся при термическом разложении эфира карбаминовой кислоты, в противоположность этому, как указано в литературе (Journal of the American Chemical Society, Vol. 64, p. 2229, 1942), например, что уретан образуется в результате реакции между ароматическим гидроксисоединением и фенилизоцианатом, ароматические гидроксисоединения способны реагировать с изоцианатами. Ароматическое гидроксисоединение можно переносить в реактор термического разложения после перемешивания, при переносе реакционной смеси, полученной в реакции между диарилкарбонатом и соединением амина, в реактор термического разложения, или можно подавать, обеспечив линию подачи ароматического гидроксисоединения, отдельную от линии подачи реакционной смеси.
Изоцианаты, полученные в соответствии с представленным вариантом способа получения, можно предпочтительно использовать как исходный материал для получения полиуретановой пены, красок, адгезивов и тому подобного. Так как изоцианаты можно получить в соответствии со способом получения в рассматриваемом варианте с хорошим выходом без использования токсичного фосгена, настоящее изобретение чрезвычайно важно для промышленности.
ПРИМЕРЫ
Хотя далее предложено подробное разъяснение настоящего изобретения на основе его примеров, объем настоящего изобретения не ограничен указанными примерами.
Аналитические способы
1) ЯМР анализ
Прибор: JNM-A400 FT-NMR system, JEOL Ltd., Япония
(1) Приготовление образцов для 1H- и 13C-ЯМР анализа
Взвешивают около 0,3 г образцового раствора, добавляя затем около 0,7 г дейтерохлороформа (99,8%, Aldrich Corp., USA) и 0,05 г тетраметилолова (реагентной степени чистоты, Wako Pure Chemical Industries, Ltd., Japan) в качестве внутреннего стандарта и перемешивают до однородности, получая растворы, используемые в качестве образцов для ЯМР анализа.
(2) Количественный анализ
Анализы осуществляют для каждого стандарта и количественные анализы осуществляют, анализируя растворы образцов, на основании полученной калибровочной кривой.
2) Жидкостная хроматография
Прибор: LC-10AT system, Shimadzu Corp., Japan
Колонка: колонка Silica-60, Tosoh Corp., Japan, две колонки, соединенные последовательно
Проявляющий растворитель: жидкость, состоящая из смеси гексана и тетрагидрофурана (80/20) (объем/объем)
Скорость потока растворителя: 2 мл/мин
Температура колонки: 35°C
Детектор: R.I. (рефрактометр)
(1) Аналитические образцы для жидкостной хроматографии
Взвешивают около 0,1 г образца с последующим добавлением около 1 г тетрагидрофурана (обезвоженного, Wako Pure Chemical Industries, Ltd., Japan) и около 0,02 г бисфенола A (гарантированный реагент, Wako Pure Chemical Industries, Ltd., Japan) в качестве внутреннего стандарта и перемешивают до однородности, получая растворы, используемые в качестве аналитических образцов для жидкостной хроматографии.
(2) Количественный анализ
Анализы осуществляют для каждого стандарта, и количественные анализы осуществляют для растворов аналитических образцов на основании полученной калибровочной кривой.
3) Газовая хроматография
Прибор: GC-2010, Shimadzu Corp., Japan
Колонка: DB-1 колонка, Agilent Technologies Corp., USA, длина: 30 м, внутренний диаметр: 0,250 мм, толщина пленки: 1,00 мкм
Температура колонки: выдерживают при 50°C в течение 5 минут с последующим повышением температуры со скоростью 10°C/мин до 200°C; выдерживают при 200°C в течение 5 минут с последующим повышением температуры со скоростью 10°C/мин до 300°C
Детектор: FID
(1) Аналитические образцы для газовой хроматографии
Взвешивают около 0,05 г образца с последующим добавлением около 1 г ацетона (обезвоженного, Wako Pure Chemical Industries, Ltd., Japan) и около 0,02 г толуола (обезвоженного, Wako Pure Chemical Industries, Ltd., Japan) в качестве внутреннего стандарта и перемешивают до однородности, получая растворы, используемые в качестве аналитических образцов для газовой хроматографии.
(2) Количественный анализ
Анализы осуществляют для каждого стандарта, и количественные анализы осуществляют для растворов аналитических образцов на основании полученной калибровочной кривой.
4) Масс-спектрометрия с индуктивно связанной плазмой
Прибор: SPQ-8000, Seiko Epson Corp., Japan
(1) Аналитические образцы для масс-спектрометрии с индуктивно связанной плазмой
Около 0,15 г образца превращают в золу разбавленной серной кислотой с последующим растворением в разбавленной азотной кислоте.
(2) Количественный анализ
Анализы осуществляют для каждого стандарта, и количественные анализы осуществляют для растворов аналитических образцов на основании полученной калибровочной кривой.
Справочный пример 1. Получение дифенилкарбоната
Стадия (I-1): Получение катализаторов диалкилолова
692 г (2,78 моль) оксида ди-н-бутилолова и 2000 г (27 моль) 1-бутанола (Wako Pure Chemical Industries, Ltd., Japan) помещают в 3000-мл волюметрическую грушевидную колбу. Колбу, содержащую смесь в виде белой суспензии, соединяют с выпаривателем, к которому присоединена масляная баня, снабженная регулятором температуры, вакуумным насосом и вакуумным регулятором. Выход продувочного клапана указанного выпаривателя соединяют с линией, содержащей газофазный азот, поступающий под нормальным давлением. После закрытия продувочного клапана выпаривателя для уменьшения давления внутри системы продувочный клапан открывают постепенно, чтобы обеспечить поступление азота в систему и возвращение к нормальному давлению. Температуру масляной бани устанавливают при 126°C, колбу погружают в масляную баню и начинают вращение выпаривателя. После нагревания и перемешивания путем вращения в течение около 30 минут при нормальном давлении при открытом продувочном клапане выпаривателя начинается кипение и дистилляция низкокипящих компонентов смеси. После поддержания указанного состояния в течение 8 часов, продувочный клапан закрывают, давление внутри системы постепенно уменьшают, и оставшиеся низкокипящие компоненты перегоняют при давлении внутри системы от 76 до 54 Кпа. После того как низкокипящие компоненты больше не появляются, колбу вынимают из масляной бани. Реакционная жидкость имеет вид прозрачной жидкости. Затем колбу вынимают из масляной бани, продувочный клапан постепенно открывают и давление внутри системы возвращают к нормальным значениям давления. В колбе получают 952 г реакционной жидкости. По результатам 119Sn-, 1H- и 13C-ЯМР анализов получают продукт в виде 1,1,3,3-тетра-н-бутил-1,3-ди(н-бутилокси)дистанноксан с выходом 99% в расчете на оксид ди-н-бутилолова. Затем ту же самую процедуру повторяют 12 раз до получения всего 11480 г 1,1,3,3-тетра-н-бутил-1,3-ди(н-бутилокси)дистанноксана.
Стадия (I-2): Получение дибутилкарбоната
Эфир карбоновой кислоты получают в аппарате непрерывного получения, подобном тому, который представлен на фиг. 1. 1,1,3,3-тетра-н-бутил-1,3-ди(н-бутилокси)дистанноксан, полученный на стадии (I-1), подают со скоростью 4201 г/час по линии 4 в реактор колонного типа с насадкой Mellapak 750Y (Sulzer Chemtech Ltd., Switzerland) с внутренним диаметром 151 мм и эффективной длиной 5040 мм, и 1-бутанол, очищенный с помощью дистилляционной колонны 101, подают в реактор колонного типа 102 со скоростью 24717 г/час по линии 2. Температуру жидкости внутри реактора устанавливают при 160°C, за счет нагревателя и ребойлера 112, и давление доводят до около 150 кПа, используя клапан управления давлением. Время пребывания в реакторе составляет около 10 минут. 1-Бутанол, содержащий воду, со скоростью 24715 г/час из верхней части реактора по линии 6 и 1-бутанол со скоростью 824 г/час по линии 1 закачивают в дистилляционную колонну 101, набитую насадкой Metal Gauze CY Packing (Sulzer Chemtech Ltd., Switzerland) и снабженную ребойлером 111 и холодильником 121 для осуществления дистилляционной очистки. В верхней части дистилляционной колонны 101 фракцию с высокой концентрацией воды конденсируют в холодильнике 121 и отводят по линии 3. Очищенный 1-бутанол закачивают по передаточной линии 2, расположенной в нижней части дистилляционной колонны 101. Композицию катализатора алкоксида алкилолова, содержащую ди-н-бутоксид ди-н-бутилолова и 1,1,3,3-тетра-н-бутил-1,3-ди(н-бутилокси)дистанноксан, получают из нижней части реактора колонного типа 102 и подают в тонкопленочный выпариватель 103 (Kobelco Eco-Растворы Co., Ltd., Japan) по линии 5. 1-Бутанол отгоняют в тонкопленочном выпаривателе 103 и возвращают в реактор колонного типа 102 через холодильник 123, линию 8 и линию 4. Композицию катализатора алкоксида алкилолова откачивают из нижней части тонкопленочного выпаривателя 103 по линии 7 и подают в автоклав 104, при этом устанавливая скорость потока активных компонентов в форме дибутоксида дибутилолова и 1,1,3,3-тетра-н-бутил-1,3-ди(н-бутилокси)дистанноксана около 4812 г/час. Двуокись углерода подают в автоклав по линии 9 со скоростью 973 г/час и давление внутри автоклава поддерживают при 4 МПа. Температуру внутри автоклава устанавливают при 120°C, время пребывания устанавливают около 4 часов и осуществляют реакцию между двуокисью углерода и композицией катализатора алкоксида алкилолова до получения реакционной жидкости, содержащей дибутилкарбонат. Указанную реакционную жидкость переносят в резервуар декарбонизации 105 по линии 10 и через контрольный клапан для удаления остаточной двуокиси углерода и двуокись углерода выделяют по линии 11. Затем реакционную жидкость закачивают в тонкопленочный выпариватель 106 (Kobelco Eco-Solutions Co., Ltd., Japan), температура которого 140°C и давление около 1,4 кПа по линии 12, и подают, поддерживая скорость потока 1,1,3,3-тетра-н-бутил-1,3-ди(н-бутилокси)дистанноксана около 4201 г/час до получения фракции, содержащей дибутилкарбонат. С другой стороны, остаток после выпаривания передают в реактор колонного типа 102 по линии 13 и линии 4, устанавливая при этом скорость потока 1,1,3,3-тетра-н-бутил-1,3-ди(н-бутилокси)дистанноксана около 4201 г/час. Фракцию, содержащую дибутилкарбонат, подают в дистилляционную колонну 107 с насадкой Metal Gauze CY (Sulzer Chemtech Ltd., Switzerland) и снабженную ребойлером 117 и холодильником 127, через холодильник 126 и линию 14 со скоростью 830 г/час с последующей дистилляционной очисткой до получения 99 вес.% дибутилкарбоната, поступающего по линии 15 со скоростью 814 г/час. Когда композицию катализатора алкоксида алкилолова в линии 13 проанализировали с помощью 119Sn-, 1H- и 13C-ЯМР анализа, было обнаружено, что он содержат 1,1,3,3-тетра-н-бутил-1,3-ди(н-бутилокси)дистанноксан, но не содержит ди-н-бутилолово-ди-н-бутоксид. После осуществления вышеуказанной непрерывной операции в течение около 600 часов композицию катализатора алкоксида алкилолова отводят по линии 16 со скоростью 16 г/час, при этом 1,1,3,3-тетра-н-бутил-1,3-ди(н-бутилокси)дистанноксан, полученный в соответствии с стадией (I-1), отводят по линии 17 со скоростью 16 г/час.
Стадия (I-3): Получение ароматического эфира карбоновой кислоты
Получение катализатора
79 г фенола и 32 г оксида свинца нагревают в течение 10 часов при 180°C, и образующуюся воду отгоняют с фенолом. Около 2,5 г воды экстрагируют за 10 часов. Затем указанный катализатор получают, отгоняя фенол из верхней части реактора.
Получение ароматического эфира карбоновой кислоты
Используют аппарат, подобный представленному на фиг. 2.
Смесь, включающую дибутилкарбонат, полученный на стадии (I-2), фенол и полученный выше катализатор (составленный так, что весовое отношение дибутилкарбоната и фенола в указанной смеси составляет около 65/35 и концентрация свинца составляет около 1% по весу) непрерывно подают в жидком состоянии через предварительный подогреватель 201 на среднюю ступень многоступенчатой дистилляционной колонны непрерывного действия 202, заполненной насадкой Dickson (диаметр: 6 мм), с внутренним диаметром около 5 см и длиной колонны 2 м, по линии 21 со скоростью около 270 г/час и оставляют реагировать. Количество требуемого тепла для реакции и дистилляции подают, используя циркулирующую жидкость в нижней части колонны, через линию 23 и ребойлер 204. Температура жидкости в нижней части многоступенчатой дистилляционной колонны непрерывного действия 202 составляет 238°C, давление в верхней части колонны составляет около 250 кПа, и флегмовое число устанавливают так, чтобы оно было примерно 2. Газ, отводимый из верхней части многоступенчатой дистилляционной колонны непрерывного действия 202, удаляют по линии 22 и непрерывно передают в резервуар-хранилище 205 через холодильник 203 по линии 24 со скоростью около 67 г/час. Жидкость непрерывно удаляют из нижней части колонны по линии 23 в резервуар-хранилище 206 со скоростью около 204 г/час.
Состав жидкости, отводимой по линии 24, состоит из около 33% вес. 1-бутанола, около 65% вес. фенола и около 2% вес. дибутилкарбоната. Состав жидкости, отводимой в резервуар-хранилище 206, состоит из около 11% вес. фенола, около 60% вес. дибутилкарбоната, около 26% вес. из бутилфенилкарбоната и около 1,6% вес. дифенилкарбоната, и концентрация свинца составляет около 1% вес.
Затем используют аппарат, подобный представленному на фиг. 3.
Жидкость, экстрагированную в резервуар-хранилище 206, непрерывно подают в жидком состоянии через предварительный подогреватель 301 на среднюю ступень многоступенчатой дистилляционной колонны непрерывного действия 302, заполненную насадкой Dickson (диаметр 6 мм), с внутренним диаметром около 5 см и длиной колонны 2 м, по линии 31 со скоростью около 203 г/час. Количество требуемого тепла для реакции и дистилляции обеспечивают с помощью циркулирующей жидкости в нижней части колонны через линию 33 и ребойлер 304. Температура жидкости в нижней части многоступенчатой дистилляционной колонны непрерывного действия 302 составляет 240°C, давление в верхней части колонны составляет около 27 кПа, и флегмовое число устанавливают около 2. Газ, отводимый из верхней части многоступенчатой дистилляционной колонны непрерывного действия 302, поступает по линии 32 и конденсируется в холодильнике 303 и непрерывно отводится по линии 34 в резервуар-хранилище 305 со скоростью около 165 г/час. Жидкость непрерывно удаляют из нижней части колонны по линии 33 в резервуар-хранилище 306 со скоростью около 39 г/час.
Состав жидкости, отводимой по линии 34, состоит из около 500 м.д. 1-бутанола, около 13% вес. фенола, около 85% вес. дибутилкарбоната и около 2% вес. бутилфенилкарбоната. Состав жидкости, отводимой в резервуар-хранилище 306, состоит из около 0,3% вес. дибутилкарбоната, из около 32% вес. бутилфенилкарбоната и около 61% вес. дифенилкарбоната, и концентрация свинца составляет около 7% вес.
Рециркуляция спирта
Спирт рециклизуют, используя аппарат, подобный представленному на фиг. 4.
Жидкость, непрерывно отводимую в резервуар-хранилище 205, непрерывно подают через предварительный подогреватель 401 в положение около 0,7 м от нижней части многоступенчатой дистилляционной колонны непрерывного действия 402, заполненной насадкой Dickson (диаметр: 6 мм), с внутренним диаметром около 5 см и длиной колонны 2 м, по линии 41 со скоростью около 201 г/час для осуществления дистилляционного разделения. Количество требуемого тепла для дистилляционного разделения подают, осуществляя циркуляцию жидкости в нижней части колонны, через линию 43 и ребойлер 404. Температура жидкости в нижней части многоступенчатой дистилляционной колонны непрерывного действия 402 составляет 145°C, давление в верхней части колонны составляет около 13 кПа, и флегмовое число устанавливают около 0,3. Газ, отводимый из верхней части многоступенчатой дистилляционной колонны непрерывного действия 402, конденсируют в холодильнике 403, поступая по линии 42, и отводят по линии 44 в резервуар-хранилище 405 со скоростью около 68 г/час. Жидкость непрерывно удаляют из нижней части колонны по линии 43 в резервуар-хранилище 406 со скоростью около 133 г/час.
Состав жидкости, отводимой по линии 44, состоит из около 99% вес. 1-бутанола и около 100 м.д. фенола. Состав жидкости, отводимой в резервуар-хранилище 406, состоит из около 2% вес. дибутилкарбоната и около 98% вес. фенола.
Очистка диарилкарбоната
Диарилкарбонат очищают, используя аппарат, подобный представленному на фиг. 5 и 6.
Жидкость, экстрагированную в резервуар-хранилище 306, непрерывно подают в жидком состоянии через предварительный подогреватель 501 на среднюю ступень многоступенчатой дистилляционной колонны непрерывного действия 502, заполненной насадкой Dickson (диаметр: 6 мм), с внутренним диаметром около 5 см и длиной колонны 2 м, по линии 51 со скоростью около 195 г/час. Количество требуемого тепла для дистилляционного разделения подают, обеспечивая циркулирование жидкости в нижней части колонны, через линию 53 и ребойлер 504. Температура жидкости в нижней части многоступенчатой дистилляционной колонны непрерывного действия 502 составляет 210°C, давление в верхней части колонны составляет около 1,5 кПа, и флегмовое число устанавливают около 1. Газ, отводимый из верхней части многоступенчатой дистилляционной колонны непрерывного действия 502, конденсируют в холодильнике 503 по линии 52 и непрерывно отводят по линии 54. Жидкость отводят из нижней части колонны по линии 53 в резервуар-хранилище 506 со скоростью около 14 г/час.
Состав жидкости, отводимой по линии 54, состоит из около 0,3% вес. дибутилкарбоната, из около 34% вес. бутилфенилкарбоната и около 66% вес. дифенилкарбоната.
Жидкость, экстрагируемую по линии 54, непрерывно подают через предварительный подогреватель 601 на среднюю ступень многоступенчатой дистилляционной колонны непрерывного действия 602, заполненной насадкой Dickson (диаметр: 6 мм), с внутренним диаметром около 5 см и длиной колонны 2 м, по линии 61 со скоростью около 181 г/час. Количество требуемого тепла для дистилляционного разделения подводят, обеспечивая циркуляцию жидкости в нижней части колонны, через линию 63 и ребойлер 604. Температура жидкости в нижней части многоступенчатой дистилляционной колонны непрерывного действия 602 составляет 232°C, давление в верхней части колонны составляет около 15 кПа, и флегмовое число устанавливают около 2. Газ, отводимый из верхней части многоступенчатой дистилляционной колонны непрерывного действия 602, конденсируют в холодильнике 603 по линии 62 и непрерывно отводят по линии 64. Жидкость экстрагируют из нижней части колонны по линии 63 в резервуар-хранилище 606 со скоростью около 119 г/час.
Состав жидкости, отводимой по линии 64, состоит из около 0,6% вес. дибутилкарбоната, из около 99% вес. бутилфенилкарбоната и около 0,4% вес. дифенилкарбоната. Состав жидкости, отводимой в резервуар-хранилище 606, состоит из 0,1% вес. дибутилкарбоната и около 99,9% вес. дифенилкарбоната. Дифенилкарбонат содержит 22 м.д. металлической компоненты в форме железа.
Пример 1
Стадия (1-1): Получение дифенилового эфира N,N′-гександиил-бис-карбаминовой кислоты
Реакцию осуществляют, используя аппарат, подобный представленному на фиг.7.
1350 г (6,3 моль) дифенилкарбоната справочного примера 1 подают в реактор с разделительными перегородками 704, изготовленный из SUS, с внутренним объемом 5 л, из резервуара-хранилища 701 по линии 71 при закрытой линии 74, и 987 г (10,5 моль) фенола (Aldrich Corp., USA) подают в реактор, изготовленный из SUS, из резервуара-хранилища 702 по линии 72. Температуру жидкости внутри реактора 704 устанавливают около 50°C и 244 г (2,1 моль) гексаметилендиамина (Aldrich Corp., USA) подают в реактор 704 из резервуара-хранилища 703 по линии 73 со скоростью около 200 г/час.
В результате анализа раствора после реакции с помощью жидкостной хроматографии было обнаружено, что дифениловый эфир N,N'-гександиил-бис-карбаминовой кислоты образовался с выходом 99,5%.
Линию 74 открывают и реакционную жидкость переносят в резервуар-хранилище 705 по линии 74.
Стадия (1-2): Получение изоцианата термическим разложением дифенилового эфира N,N'-гександиил-бис-карбаминовой кислоты
Реакцию осуществляют, используя аппарат, подобный представленному на фиг. 8.
Тонкопленочный дистилляционный аппарат 801 (Kobelco Eco-Solutions Co., Ltd., Japan) c теплопроводящей площадью поверхности 0,1 м2 нагревают до 220°C и давление в тонкопленочном дистилляционном аппарате устанавливают около 13 кПа. Смесь, выделенную в резервуар-хранилище 705 на стадии (1-1), нагревают до 150°C и подают в верхнюю часть тонкопленочного дистилляционного аппарата 801 по линии 81 со скоростью около 800 г/час. Жидкофазный компонент отводят из нижней части тонкопленочного дистилляционного аппарата 801 по линии 83 и подают в верхнюю часть тонкопленочного дистилляционного аппарата 801 по линии 84 и линии 81. Газофазный компонент отводят по линии 82.
Газофазный компонент, экстрагированный из тонкопленочного дистилляционного аппарата 801 по линии 82, непрерывно подают на среднюю ступень многоступенчатой дистилляционной колонны непрерывного действия 802, заполненную насадкой Dickson (диаметр: 6 мм), с внутренним диаметром около 5 см и длиной колонны 2 м, для осуществления дистилляционного разделения газофазного компонента. Количество тепла, требуемое для дистилляционного разделения, подают, обеспечивая циркуляцию жидкости в нижней части колонны, через линию 86 и ребойлер 804. Температура жидкости в нижней части многоступенчатой дистилляционной колонны непрерывного действия 802 составляет 150°C, и давление в верхней части колонны составляет около 15 кПа. Газ, отводимый из верхней части многоступенчатой дистилляционной колонны непрерывного действия 802, конденсируют в холодильнике 803 по линии 85 и непрерывно отводят по линии 87. Жидкофазный компонент отводят по линии 89 из многоступенчатой дистилляционной колонны непрерывного действия 802 на участке, расположенном ниже, чем линия 82.
Жидкофазный компонент, экстрагированный по линии 89, непрерывно подают на среднюю ступень многоступенчатой дистилляционной колонны непрерывного действия 805, заполненную насадкой Dickson (диаметр: 6 мм), с внутренним диаметром около 5 см и длиной колонны 2 м, для осуществления дистилляционного разделения жидкофазного компонента. Количество тепла, требуемое для дистилляционного разделения, подводят, обеспечивая циркуляцию жидкости в нижней части колонны, через линию 91 и ребойлер 807. Температура жидкости в нижней части многоступенчатой дистилляционной колонны непрерывного действия 805 составляет 150°C, и давление в верхней части колонны составляет около 1,5 кПа. Газ, отводимый из верхней части многоступенчатой дистилляционной колонны непрерывного действия 805, конденсируют в холодильнике 806 по линии 90 и непрерывно отводят в резервуар-хранилище 809 по линии 92. Выделенное количество в равновесном состоянии составляет около 104 г/час.
Жидкофазный компонент экстрагируют в резервуар-хранилище 810 по линии 94 со скоростью около 140 г/час в равновесном состоянии. Жидкофазный компонент содержит около 97% вес. дифенилкарбоната.
Жидкость, отводимая по линии 92, представляет собой раствор, который содержит около 99,8% вес. гексаметилендиизоцианата. Выход в расчете на гексаметилендиамин составляет 95,3%.
Стадия (1-3): Рециркуляция диарилкарбоната
Диарилкарбонат рециклизуют, используя аппарат, подобный представленному на фиг. 9 и 10.
Жидкость, отводимую по линии 94 на стадии (1-2), непрерывно подают через предварительный подогреватель 901 на среднюю ступень многоступенчатой дистилляционной колонны непрерывного действия 902, заполненную насадкой Dickson (диаметр: 6 мм), с внутренним диаметром около 5 см и длиной колонны 2 м, по линии 95 со скоростью около 195 г/час. Количество тепла, требуемое для дистилляционного разделения, подводят, обеспечивая циркуляцию жидкости в нижней части колонны, через линию 97 и ребойлер 904. Температура жидкости в нижней части многоступенчатой дистилляционной колонны непрерывного действия 902 составляет 210°C, давление в верхней части колонны составляет около 1,5 кПа, и флегмовое число устанавливают около 1. Газ, отводимый из верхней части многоступенчатой дистилляционной колонны непрерывного действия 902, конденсируют в холодильнике 903 по линии 96 и непрерывно отводят по линии 99. Жидкость экстрагируют в резервуар-хранилище 906 из нижней части колонны по линии 97 со скоростью около 14 г/час.
Жидкость, отводимую по линии 99, непрерывно подают через предварительный подогреватель 1001 на среднюю ступень многоступенчатой дистилляционной колонны непрерывного действия 1002, заполненную насадкой Dickson (диаметр: 6 мм) с внутренним диаметром около 5 см и длиной колонны 2 м, по линии A1 со скоростью около 181 г/час. Количество тепла, требуемое для дистилляционного разделения, подводят, обеспечивая циркуляцию жидкости в нижней части колонны, через линию A3 и ребойлер 1004. Температура жидкости в нижней части многоступенчатой дистилляционной колонны непрерывного действия 1002 составляет 232°C, давление в верхней части колонны составляет около 15 кПа, и флегмовое число устанавливают около 2. Газ, отводимый из верхней части многоступенчатой дистилляционной колонны непрерывного действия 1002, конденсируют в холодильнике 1003 по линии A2 и непрерывно отводят по линии A4. Жидкость экстрагируют в резервуар-хранилище 1006 из нижней части колонны по линии A3 со скоростью около 119 г/час. Жидкость, экстрагированная в резервуар-хранилище 1006, содержит около 99,9% вес. дифенилкарбоната.
Стадия (1-4): Рециклизация фенола
Фенол рециклизуют, используя аппарат, подобный представленному на фиг. 11.
Жидкость, отводимую по линии 87 на стадии (1-2), непрерывно подают через предварительный подогреватель 1101 на среднюю ступень многоступенчатой дистилляционной колонны непрерывного действия 1102, заполненную насадкой Dickson (диаметр: 6 мм), с внутренним диаметром около 5 см и длиной колонны 2 м, по линии B1 со скоростью около 200 г/час. Количество тепла, требуемое для дистилляционного разделения, подводят, обеспечивая циркуляцию жидкости в нижней части колонны, через линию B3 и ребойлер 1104. Температура жидкости в нижней части многоступенчатой дистилляционной колонны непрерывного действия 1102 составляет 230°C, давление в верхней части колонны является атмосферным давлением, и флегмовое число устанавливают около 1. Газ, отводимый из верхней части многоступенчатой дистилляционной колонны непрерывного действия 1102, конденсируют в холодильнике 1103 по линии B2 и непрерывно отводят в резервуар-хранилище 1105 по линии A4. Жидкость, отводимая в резервуар-хранилище 1105, содержит около 99,9% вес. фенола. Хотя непрерывную операцию осуществляют в течение 10 дней, на стенках тонкопленочного дистилляционного аппарата 801 не наблюдается накопления прилипших веществ. Более того, когда непрерывную операцию осуществляют в течение 300 дней, на стенках тонкопленочного дистилляционного аппарата 801 наблюдают накопление прилипших веществ.
Пример 2
Стадия (2-1): Получение фенилового эфира 3-(феноксикарбониламинометил)-3,5,5-триметилциклогексилкарбаминовой кислоты
Реакцию осуществляют, используя аппарат, подобный представленному на фиг. 7.
1992 г (9,3 моль) дифенилкарбоната справочного примера 1 подают в реактор с разделительными перегородками 704, изготовленный из SUS, с внутренним объемом 5 л, из резервуара-хранилища 701 по линии 71, при этом линию 74 закрывают, и 1311 г (14,0 моль) фенола подают в реактор, выполненный из SUS, из резервуара-хранилища 702 по линии 72. Температуру жидкости внутри реактора 704 устанавливают около 50°C и 528 г (3,1 моль) 3-аминометил-3,5,5-триметилциклогексиламина (Aldrich Corp., USA) подают в реактор 704 из резервуара-хранилища 703 по линии 73 со скоростью около 250 г/час.
В результате анализа раствора после реакции с помощью жидкостной хроматографии было обнаружено, что образовался фениловый эфир 3-(феноксикарбониламинометил)-3,5,5-триметилциклогексилкарбаминовой кислоты с выходом 99,3%.
Линию 74 открывают и реакционную жидкость переносят в резервуар-хранилище 705 по линии 74.
Стадия (2-2): Получение изоцианата путем термического разложения фенилового эфира 3-(феноксикарбониламинометил)-3,5,5-триметилциклогексилкарбаминовой кислоты
Реакцию осуществляют, используя аппарат, подобный представленному на фиг. 8.
Тонкопленочный дистилляционный аппарат 801 (Kobelco Eco-Solutions Co., Ltd., Japan) с площадью теплопроводящей поверхности 0,1 м2 нагревают до 220°C и давление внутри тонкопленочного дистилляционного аппарата устанавливают около 13 кПа. Полученную смесь, регенерированную в резервуар-хранилище 705 на стадии (2-1), нагревают до 150°C и подают в верхнюю часть тонкопленочного дистилляционного аппарата 801 по линии 81 со скоростью около 780 г/час. Жидкофазный компонент отводят из нижней части тонкопленочного дистилляционного аппарата 801 по линии 83 и подают в верхнюю часть тонкопленочного дистилляционного аппарата 801 по линии 84 и линии 81. Газофазный компонент отводят по линии 82.
Газофазный компонент, отводимый из тонкопленочного дистилляционного аппарата 801 по линии 82, непрерывно подают на среднюю ступень многоступенчатой дистилляционной колонны непрерывного действия 802, заполненную насадкой Dickson (диаметр: 6 мм) с внутренним диаметром около 5 см и длиной колонны 2 м, для осуществления дистилляционного разделения газофазного компонента. Количество тепла, требуемое для дистилляционного разделения, подводят, обеспечивая циркуляцию жидкости в нижней части колонны, через линию 86 и ребойлер 804. Температура жидкости в нижней части многоступенчатой дистилляционной колонны непрерывного действия 802 составляет 150°C, и давление в верхней части колонны составляет около 15 кПа. Газ, отводимый из верхней части многоступенчатой дистилляционной колонны непрерывного действия 802, конденсируют в холодильнике 803 по линии 85 и непрерывно отводят по линии 87. Жидкофазный компонент отводят по линии 89 многоступенчатой дистилляционной колонны непрерывного действия 802, расположенной ниже, чем линия 82.
Жидкофазный компонент, отводимый по линии 89, непрерывно подают на среднюю ступень многоступенчатой дистилляционной колонны непрерывного действия 805, заполненной насадкой Dickson (диаметр: 6 мм) с внутренним диаметром около 5 см и длиной колонны 2 м, для осуществления дистилляционного разделения жидкофазного компонента. Количество тепла, требуемое для дистилляционного разделения, подводят, обеспечивая циркуляцию жидкости в нижней части колонны, через линию 91 и ребойлер 807. Температура жидкости в нижней части многоступенчатой дистилляционной колонны непрерывного действия 805 составляет 150°C, и давление в верхней части колонны составляет около 1,3 кПа. Газ, отводимый из верхней части многоступенчатой дистилляционной колонны непрерывного действия 805, конденсируют в холодильнике 806 по линии 90 и непрерывно отводят в резервуар-хранилище 809 по линии 92 со скоростью около 134 г/час.
Жидкость, отводимая по линии 92, представляет собой раствор, содержащий около 99,8% вес. изофорондиизоцианата. Выход в расчете на 3-аминометил-3,5,5-триметилциклогексиламин составляет 95,0%. Хотя непрерывную операцию осуществляют в течение 10 дней, на стенках тонкопленочного дистилляционного аппарата 801 не наблюдают накопления прилипших веществ.
Пример 3
Стадия (3-1): Получение дифенил-4,4'-метилендициклогексилкарбамата
Ацетилацетонат железа(II) добавляют к дифенилкарбонату справочного примера 1 до получения дифенилкарбоната, содержащего 2,3% атомов металла в виде железа.
Реакцию осуществляют, используя аппарат, подобный представленному на фиг. 7.
1577 г (7,4 моль) дифенилкарбоната подают в реактор с разделительными перегородками 704, изготовленный из SUS, с внутренним объемом 5 л, из резервуара-хранилища 701 по линии 71, причем линию 74 закрывают, и 1189 г (12,7 моль) фенола подают в реактор, изготовленный из SUS, из резервуара-хранилища 702 по линии 72. Температуру жидкости внутри реактора 704 устанавливают около 50°C и 484 г (2,3 моль) 4,4'-метиленбис(циклогексиламина) (Aldrich Corp., USA) подают в реактор 704 из резервуара-хранилища 703 по линии 73 со скоростью около 250 г/час.
В результате анализа раствора после реакции с помощью жидкостной хроматографии было обнаружено, что образуется дифенил-4,4'-метилендициклогексилкарбамат с выходом 99,1%.
Линию 74 открывают и реакционную жидкость переносят в резервуар-хранилище 705 по линии 74.
Стадия (3-2): Получение изоцианата путем термического разложения дифенил-4,4'-метилендициклогексилкарбамата
Реакцию осуществляют, используя аппарат, подобный представленному на фиг. 12.
Тонкопленочный дистилляционный аппарат 1201 (Kobelco Eco-Solutions Co., Ltd., Japan) с теплопроводящей площадью поверхности 0,1 м2 нагревают до 250°C и давление внутри тонкопленочного дистилляционного аппарата устанавливают около 1,3 кПа. Полученную смесь, поступившую в резервуар-хранилище 705 на стадии (3-1), нагревают до 170°C и подают в верхнюю часть тонкопленочного дистилляционного аппарата 1201 по линии C1 со скоростью около 650 г/час. Жидкофазный компонент отводят из нижней части тонкопленочного дистилляционного аппарата 1201 по линии C3 и направляют в верхнюю часть тонкопленочного дистилляционного аппарата 1201 по линии C4 и линии C1. Газофазный компонент отводят по линии C2.
Газофазный компонент, отводимый из тонкопленочного дистилляционного аппарата 1201 по линии C2, непрерывно подают на среднюю ступень многоступенчатой дистилляционной колонны непрерывного действия 1202, заполненную насадкой Dickson (диаметр: 6 мм), с внутренним диаметром около 5 см и длиной колонны 2 м, для осуществления дистилляционного разделения газофазного компонента. Количество тепла, требуемое для дистилляционного разделения, подводят, обеспечивая циркуляцию жидкости в нижней части колонны, через линию C6 и ребойлер 1204. Температура жидкости в нижней части многоступенчатой дистилляционной колонны непрерывного действия 1201 составляет 210°C, и давление в верхней части колонны соответствует атмосферному давлению. Газ, отводимый из верхней части многоступенчатой дистилляционной колонны непрерывного действия 1201, конденсируют в холодильнике 1203 по линии C5 и непрерывно отводят по линии C7. Жидкофазный компонент отводят по линии C8.
Жидкофазный компонент, отводимый по линии C8, непрерывно подают на среднюю ступень многоступенчатой дистилляционной колонны непрерывного действия 1205, заполненную насадкой Dickson (диаметр 6 мм), с внутренним диаметром около 5 см и длиной колонны 2 м, для осуществления дистилляционного разделения жидкофазного компонента. Количество тепла, требуемое для дистилляционного разделения, подводят, обеспечивая циркуляцию жидкости в нижней части колонны, через линию C11 и ребойлер 1207. Температура жидкости в нижней части многоступенчатой дистилляционной колонны непрерывного действия 1205 составляет 210°C, и давление в верхней части колонны составляет около 2,5 кПа. Газ, отводимый из верхней части многоступенчатой дистилляционной колонны непрерывного действия 1205, конденсируют в холодильнике 1206 по линии C10 и непрерывно отводят по линии C12. Жидкофазный компонент отводят по линии C14.
Жидкофазный компонент, отводимый по линии C14, непрерывно подают на среднюю ступень многоступенчатой дистилляционной колонны непрерывного действия 1208, заполненную насадкой Dickson (диаметр: 6 мм), с внутренним диаметром около 5 см и длиной колонны 2 м, для осуществления дистилляционного разделения жидкофазного компонента. Количество тепла, требуемое для дистилляционного разделения, подводят, обеспечивая циркуляцию жидкости в нижней части колонны, через линию C16 и ребойлер 1210. Температура жидкости в нижней части многоступенчатой дистилляционной колонны непрерывного действия 1208 составляет 220°C, и давление в верхней части колонны составляет около 0,5 кПа. Газ, отводимый из верхней части многоступенчатой дистилляционной колонны непрерывного действия 1205, конденсируют в холодильнике 1209 по линии C15 и непрерывно подают по линии C17 со скоростью около 113 г/час. Жидкость, отводимая по линии C17, представляет собой раствор, содержащий около 99,9% вес. 4,4'-метиленбис(циклогексилизоцианата). Выход в расчете на 4,4'-метиленбис(циклогексиламин) составляет 93,2%. Хотя непрерывную операцию осуществляют в течение 10 дней, на стенках тонкопленочного дистилляционного аппарата 1202 не наблюдают накопления прилипших веществ.
Пример 4
Стадия (4-1): Получение дифенил-4,4'-метилендициклогексилкарбамата
Осуществляют тот же самый процесс, что и на стадии (3-1) примера 3, за исключением того, что используют 1344 г (11,0 моль) 2,6-диметилфенола (Aldrich Corp., USA) и 463 г (2,2 моль) 4,4'-метиленбис(циклогексиламина) вместо 1650 г (7,7 моль) дифенилкарбоната справочного примера 1 и фенола. В результате анализа раствора после реакции с помощью жидкостной хроматографии было обнаружено, что образовался дифенил-4,4'-метилендициклогексилкарбамат с выходом 99,3%.
Стадия (4-2): Получение изоцианата путем термического разложения дифенил-4,4'-метилендициклогексилкарбамата
Осуществляют тот же самый процесс, что и на стадии (3-2) примера 3, за исключением того, что используют смесь, полученную на стадии (4-1), вместо смеси, полученной на стадии (3-1), и нагревают указанную смесь до 140°C. Смесь фенола и 2,6-диметилфенола экстрагируют по линии C7. Жидкость, отводимая по линии C17, содержит около 99,9% вес. 4,4'-метиленбис(циклогексилизоцианата). Выход в расчете на 4,4'-метиленбис(циклогексиламин) составляет 92,3%. Хотя непрерывную операцию осуществляют в течение 10 дней, на стенках тонкопленочного дистилляционного аппарата 1202 не наблюдают накопления прилипших веществ.
Пример 5
Стадия (5-1): Получение дифенилового эфира N,N'-гександиил-бис-карбаминовой кислоты
Осуществляют тот же самый процесс, что и на стадии (1-1) примера 1, за исключением того, что подают 1874 г (8,8 моль) дифенилкарбоната, 1246 г (13,3 моль) фенола и 291 г (2,5 моль) гексаметилендиамина справочного примера 1.
В результате анализа раствора после реакции с помощью жидкостной хроматографии было обнаружено, что образовался дифениловый эфир N,N'-гександиил-бис-карбаминовой кислоты с выходом 99,4%.
Стадия (5-2): Получение изоцианата путем термического разложения дифенилового эфира N,N'-гександиил-бис-карбаминовой кислоты
Осуществляют тот же самый процесс, что и на стадии (1-2) примера 1, за исключением того, что используют смесь, полученную на стадии (5-1), вместо смеси, полученной на стадии (1-1), нагревают указанную смесь до 190°C и подают в тонкопленочный дистилляционный аппарат 801. Жидкость непрерывно отводят по линии 92 в резервуар-хранилище 809 со скоростью около 76,5 г/час. Жидкость, отводимая по линии 92, представляет собой раствор, содержащий около 99,8% вес. гексаметилендиизоцианата. Выход в расчете на гексаметилендиамин составляет 77,5%. Хотя осуществляют непрерывную операцию в течение 10 дней, на стенках тонкопленочного дистилляционного аппарата 801 не наблюдают накопления прилипших веществ.
Пример 6
Стадия (6-1): Получение дифенилового эфира N,N'-гександиил-бис-карбаминовой кислоты
Осуществляют тот же самый процесс, что и на стадии (1-1) примера 1, за исключением того, что используют 2056 г (9,6 моль) дифенилкарбоната справочного примера 1, 1504 г (16,0 моль) фенола и 372 г (3,2 моль) гексаметилендиамина.
В результате анализа раствора после реакции с помощью жидкостной хроматографии было обнаружено, что образовался дифениловый эфир N,N'-гександиил-бис-карбаминовой кислоты с выходом 99,4%.
Стадия (6-2): Получение изоцианата путем термического разложения дифенилового эфира N,N'-гександиил-бис-карбаминовой кислоты
Реакцию осуществляют, используя аппарат, подобный представленному на фиг. 8.
Тонкопленочный дистилляционный аппарат 801 с теплопроводящей площадью поверхности 0,1 м2 нагревают до 220°C и давление внутри тонкопленочного дистилляционного аппарата устанавливают около 0,13 кПа. Смесь, поступившую в резервуар-хранилище 705 на стадии (6-1), нагревают до 100°C и подают в верхнюю часть тонкопленочного дистилляционного аппарата 801 по линии 81 со скоростью около 800 г/час. Газофазный компонент отводят из нижней части тонкопленочного дистилляционного аппарата 801 по линии 82. Почти совсем не выделяется жидкофазного компонента по линии 83, расположенной в нижней части тонкопленочного дистилляционного аппарата 801.
Газофазный компонент, отводимый из тонкопленочного дистилляционный аппарат 801 по линии 82, непрерывно подают на среднюю ступень многоступенчатой дистилляционной колонны непрерывного действия 802, заполненную насадкой Dickson (диаметр: 6 мм), с внутренним диаметром около 5 см и длиной колонны 2 м, для осуществления дистилляционного разделения газофазного компонента. Количество тепла, требуемое для дистилляционного разделения, подводят, обеспечивая циркуляцию жидкости в нижней части колонны, через линию 86 и ребойлер 804. Температура жидкости в нижней части многоступенчатой дистилляционной колонны непрерывного действия 802 составляет 150°C, и давление в верхней части колонны составляет около 8 кПа. Газ, отводимый из верхней части многоступенчатой дистилляционной колонны непрерывного действия 802, конденсируют в холодильнике 803 по линии 85 и непрерывно отводят по линии 87. Жидкофазный компонент отводят по линии 89 многоступенчатой дистилляционной колонны непрерывного действия 802, расположенной ниже, чем линия 82.
Жидкофазный компонент, отводимый по линии 89, непрерывно подают на среднюю ступень многоступенчатой дистилляционной колонны непрерывного действия 805, заполненную насадкой Dickson (диаметр: 6 мм), с внутренним диаметром около 5 см и длиной колонны 2 м, для осуществления дистилляционного разделения жидкофазного компонента. Количество тепла, требуемое для дистилляционного разделения, подводят, обеспечивая циркуляцию жидкости в нижней части колонны, через линию 91 и ребойлер 807. Температура жидкости в нижней части многоступенчатой дистилляционной колонны непрерывного действия 805 составляет 150°C, и давление в верхней части колонны составляет около 1,5 кПа. Газ, отводимый из верхней части многоступенчатой дистилляционной колонны непрерывного действия 805, конденсируют в холодильнике 806 по линии 90 и непрерывно отводят в резервуар-хранилище 809 по линии 92. Отводимое количество в равновесном состоянии составляет около 104 г/час.
Жидкость, отводимая по линии 92, представляет собой раствор, содержащий около 99,9% вес. гексаметилендиизоцианата. Выход в расчете на гексаметилендиамин составляет 95,4%. Если непрерывную операцию осуществляют в течение 10 дней, на стенках тонкопленочного дистилляционного аппарата 801 наблюдают накопление прилипших веществ.
Пример 7
Стадия (7-1): Получение дифенил-4,4'-метилендициклогексилкарбамата
Осуществляют тот же самый процесс, что и на стадии (3-1) примера 3, за исключением того, что используют 1874 г (8,8 моль) дифенилкарбоната справочного примера 1, 1175 г (12,5 моль) фенола и 526 г (2,5 моль) 4,4'-метиленбис(циклогексиламина).
В результате анализа раствора после реакции с помощью жидкостной хроматографии было обнаружено, что дифенил-4,4'-метилендициклогексилкарбамат образовался с выходом 99,2%.
Стадия (7-2): Получение изоцианата путем термического разложения дифенил-4,4'-метилендициклогексилкарбамата
Реакцию осуществляют, используя аппарат, подобный представленному на фиг. 13.
Смесь, поступившую в резервуар-хранилище 705 на стадии (7-1), нагревают до 150°C и подают на среднюю ступень многоступенчатой дистилляционной колонны непрерывного действия 1301, заполненную насадкой Dickson (диаметр: 6 мм), с внутренним диаметром около 5 см и длиной колонны 2 м, по линии D1 со скоростью около 510 г/час для осуществления реакции термического разложения. Количество тепла, требуемое для термического разложения, подводят, обеспечивая циркуляцию жидкости в нижней части колонны, через линию D3 и ребойлер 1303. Температура жидкости в нижней части многоступенчатой дистилляционной колонны непрерывного действия 1301 составляет 220°C, и давление в верхней части колонны составляет около 15 кПа. Газ, отводимый из верхней части многоступенчатой дистилляционной колонны непрерывного действия 1301, конденсируют в холодильнике 1302 по линии D2 и непрерывно отводят по линии D4. Жидкофазный компонент отводят из многоступенчатой дистилляционной колонны непрерывного действия 1301 по линии D3.
Жидкофазный компонент, отводимый по линии D6, непрерывно подают на среднюю ступень многоступенчатой дистилляционной колонны непрерывного действия 1304, заполненной насадкой Dickson (диаметр: 6 мм), с внутренним диаметром около 5 см и длиной колонны 2 м, для осуществления дистилляционного разделения жидкофазного компонента. Количество тепла, требуемое для дистилляционного разделения, подводят, обеспечивая циркуляцию жидкости в нижней части колонны, через линию D8 и ребойлер 1306. Температура жидкости в нижней части многоступенчатой дистилляционной колонны непрерывного действия 1304 составляет 220°C, и давление в верхней части колонны составляет около 5,2 кПа. Газ, отводимый из верхней части многоступенчатой дистилляционной колонны непрерывного действия 1304, конденсируют в холодильнике 1305 по линии D7 и непрерывно отводят по линии D9. Жидкофазный компонент отбирают из нижней части многоступенчатой дистилляционной колонны непрерывного действия 1304 по линии D8 и линии D11.
Жидкофазный компонент, отводимый по линии D8, непрерывно подают на среднюю ступень многоступенчатой дистилляционной колонны непрерывного действия 1307, заполненной насадкой Dickson (диаметр: 6 мм), с внутренним диаметром около 5 см и длиной колонны 2 м, для осуществления дистилляционного разделения жидкофазного компонента. Количество тепла, требуемое для дистилляционного разделения, подводят, обеспечивая циркуляцию жидкости в нижней части колонны, через линию D14 и ребойлер 1309. Температура жидкости в нижней части многоступенчатой дистилляционной колонны непрерывного действия 1307 составляет 220°C, и давление в верхней части колонны составляет около 0,40 кПа. Газ, отводимый из верхней части многоступенчатой дистилляционной колонны непрерывного действия 1307, конденсируют в холодильнике 1308 по линии D12 и непрерывно отводят по линии D13. Отводимое количество в равновесном состоянии составляет около 75 г/час.
Жидкость, отводимая по линии D13, представляет собой раствор, содержащий около 99,8% вес. 4,4'-метиленбис(циклогексилизоцианата). Выход в расчете на 4,4'-метиленбис(циклогексиламин) составляет 80,4%. Когда непрерывную операцию осуществляют в течение 10 дней, наблюдают накопление прилипших веществ внутри тонкопленочного дистилляционного аппарата 1301.
Пример 8
Стадия (8-1): Получение дифенилового эфира N,N'-гександиил-бис-карбаминовой кислоты
Осуществляют тот же самый процесс, что и на стадии (1-1) примера 1, за исключением того, что используют 2204 г (8,4 моль) 4-додецилфенола (Aldrich Corp., USA) и 244 г (2,1 моль) гексаметилендиамина вместо 1350 г (6,3 моль) дифенилкарбоната справочного примера 1 и фенола.
В результате анализа раствора после реакции с помощью жидкостной хроматографии было обнаружено, что дифениловый эфир N,N'-гександиил-бис-карбаминовой кислоты образовался с выходом 99,0%.
Стадия (8-2): Получение изоцианата путем термического разложения дифенилового эфира N,N'-гександиил-бис-карбаминовой кислоты
Реакцию осуществляют, используя аппарат, подобный представленному на фиг. 8.
Тонкопленочный дистилляционный аппарат 801 с теплопроводящей площадью поверхности 0,1 м2 нагревают до 220°C и давление внутри тонкопленочного дистилляционный аппарат устанавливают около 5,2 кПа. Смесь, поступившую в резервуар-хранилище 705 на стадии (8-1), нагревают до 150°C и подают в верхнюю часть тонкопленочного дистилляционного аппарата 801 по линии 81 со скоростью около 1200 г/час. Жидкофазный компонент отводят из нижней части тонкопленочного дистилляционного аппарата 801 по линии 83 и подают в верхнюю часть тонкопленочного дистилляционного аппарата 801 по линии 84 и линии 81. Газофазный компонент отводят по линии 82.
Газофазный компонент, отводимый из тонкопленочного дистилляционного аппарата 801 по линии 82, непрерывно подают на среднюю ступень многоступенчатой дистилляционной колонны непрерывного действия 802, заполненной насадкой Dickson (диаметр: 6 мм), с внутренним диаметром около 5 см и длиной колонны 2 м, для осуществления дистилляционного разделения газофазного компонента. Количество тепла, требуемое для дистилляционного разделения, подводят, обеспечивая циркуляцию жидкости в нижней части колонны, через линию 86 и ребойлер 804. Температура жидкости в нижней части многоступенчатой дистилляционной колонны непрерывного действия 802 составляет 150°C, и давление в верхней части колонны составляет около 4,0 кПа. Газ, отводимый из верхней части многоступенчатой дистилляционной колонны непрерывного действия 802, конденсируют в холодильнике 803 по линии 85 и непрерывно отводят по линии 87. Жидкофазный компонент экстрагируют по линии 89 многоступенчатой дистилляционной колонны непрерывного действия 802 на участке, расположенном ниже, чем линия 82.
Жидкофазный компонент, отводимый по линии 89, непрерывно подают на среднюю ступень многоступенчатой дистилляционной колонны непрерывного действия 805, заполненной насадкой Dickson (диаметр: 6 мм), с внутренним диаметром около 5 см и длиной колонны 2 м, для осуществления дистилляционного разделения жидкофазного компонента. Количество тепла, требуемое для дистилляционного разделения, подводят, обеспечивая циркуляцию жидкости в нижней части колонны, через линию 91 и ребойлер 807. Температура жидкости в нижней части многоступенчатой дистилляционной колонны непрерывного действия 805 составляет 150°C, и давление в верхней части колонны составляет около 0,8 кПа. Газ, отводимый из верхней части многоступенчатой дистилляционной колонны непрерывного действия 805, конденсируют в холодильнике 806 по линии 90 и непрерывно отводят в резервуар-хранилище 809 по линии 92. Экстрагируемое количество в равновесном состоянии составляет около 104 г/час.
Жидкофазный компонент отводят в резервуар-хранилище 810 по линии 94 со скоростью около 690 г/час в равновесном состоянии. Жидкофазный компонент содержит около 97% вес. 4-додецилфенола.
Жидкость, отводимая по линии 92, представляет собой раствор, который содержит около 99,8% по весу гексаметилендиизоцианата. Выход в расчете на гексаметилендиамин составляет 93,1%. Хотя непрерывную операцию осуществляют в течение 10 дней, на стенках тонкопленочного дистилляционного аппарата 801 не наблюдают накопления прилипших веществ.
Пример 9
Стадия (9-1): Получение фенилового эфира 3-(феноксикарбониламинометил)-3,5,5-триметилциклогексилкарбаминовой кислоты
Осуществляют тот же самый процесс, что и на стадии (2-1) примера 2, за исключением того, что используют 2643 г (8,0 моль) 2,4-(α,α-диметилбензил)фенола (Tokyo Chemical Industry Co., Ltd., Japan) и 273 г (1,6 моль) 3-аминометил-3,5,5-триметилциклогексиламина вместо 1028 г (4,8 моль) дифенилкарбоната справочного примера 1, и фенол.
В результате анализа раствора после реакции с помощью жидкостной хроматографии было обнаружено, что фениловый эфир 3-(феноксикарбониламинометил)-3,5,5-триметилциклогексилкарбаминовой кислоты образовался с выходом 99,0%.
Стадия (9-2): Получение изоцианата путем термического разложения фенилового эфира 3-(феноксикарбониламинометил)-3,5,5-триметилциклогексилкарбаминовой кислоты
Осуществляют тот же самый процесс, что и на стадии (8-2) примера 8, за исключением того, что используют смесь, полученную на стадии (9-1), вместо смеси, полученной на стадии (8-1), нагревая смесь до 150°C и подавая со скоростью около 1310 г/час.
Газ, отводимый из верхней части многоступенчатой дистилляционной колонны непрерывного действия 805, конденсируют в холодильнике 806 по линии 90 и непрерывно отводят в резервуар-хранилище 809 по линии 92 со скоростью около 112 г/час.
Жидкость, отводимая по линии 92, представляет собой раствор, который содержит около 99,8% вес. изофорондиизоцианата. Выход в расчете на 3-аминометил-3,5,5-триметилциклогексиламин составляет 94,5%. Хотя непрерывную операцию осуществляют в течение 10 дней, на стенках тонкопленочного дистилляционного аппарата 801 не наблюдают накопления прилипших веществ.
Пример 10
Стадия (10-1): Получение дифенилового эфира N,N'-(4,4'-метандиилдифенил)бискарбаминовой кислоты
Реакцию осуществляют, используя аппарат, подобный представленному на фиг. 7.
Смесь 1478 г (6,9 моль) дифенилкарбоната справочного примера 1 и 50,5 г (0,2 моль) дигидрата ацетата цинка (Aldrich Corp., USA) подают в реактор с разделительными перегородками 704, изготовленный из SUS, и с внутренним объемом 5 л, из резервуара-хранилища 701 по линии 71, при этом линию 74 закрывают, и 1297 г (13,8 моль) фенола подают в реактор, изготовленный из SUS, из резервуара-хранилища 702 по линии 72. Температуру жидкости внутри реактора 704 устанавливают около 50°C и 456 г (2,3 моль) 4,4'-метилендианилина (Aldrich Corp., USA) подают в реактор 704 из резервуара-хранилища 703 по линии 73 со скоростью около 200 г/час.
В результате анализа раствора после реакции с помощью жидкостной хроматографии было обнаружено, что дифениловый эфир N,N'-(4,4'-метандиилдифенил)бискарбаминовой кислоты образовался с выходом 98,8%.
Линию 74 открывают, и реакционную жидкость переносят в резервуар-хранилище 705 по линии 74.
Стадия (10-2): Получение изоцианата путем термического разложения дифенилового эфира N,N'-(4,4'-метандиилдифенил)-бискарбаминовой кислоты
Реакцию осуществляют, используя аппарат, подобный представленному на фиг. 12.
Тонкопленочный дистилляционный аппарат 1201 с теплопроводящей площадью поверхности 0,1 м2 нагревают до 230°C и давление внутри тонкопленочного дистилляционного аппарата устанавливают около 1,3 кПа. Смесь, поступившую в резервуар-хранилище 705 на стадии (10-1), нагревают до 130°C и подают в верхнюю часть тонкопленочного дистилляционного аппарата 1201 по линии C1 со скоростью около 690 г/час. Жидкофазный компонент отводят из нижней части тонкопленочного дистилляционного аппарата 1201 по линии C3 и подают в верхнюю часть тонкопленочного дистилляционного аппарата 1201 по линии C4 и линии C1. Газофазный компонент отводят по линии C2.
Газофазный компонент, отводимый из тонкопленочного дистилляционного аппарата 1201 по линии C2, непрерывно подают на среднюю ступень многоступенчатой дистилляционной колонны непрерывного действия 1202, заполненной насадкой Dickson (диаметр: 6 мм), с внутренним диаметром около 5 см и длиной колонны 2 м, для осуществления дистилляционного разделения газофазного компонента. Количество тепла, требуемое для дистилляционного разделения, подводят, обеспечивая циркуляцию жидкости в нижней части колонны, через линию 86 и ребойлер 804. Температура жидкости в нижней части многоступенчатой дистилляционной колонны непрерывного действия 1201 составляет 200°C, и давление в верхней части колонны составляет 60 кПа. Газ, отводимый из верхней части многоступенчатой дистилляционной колонны непрерывного действия 1201, конденсируют в холодильнике 1203 по линии C5 и непрерывно отводят по линии C7. Жидкофазный компонент экстрагируют по линии C8.
Жидкофазный компонент, отводимый по линии C8, непрерывно подают на среднюю ступень многоступенчатой дистилляционной колонны непрерывного действия 1205, заполненной насадкой Dickson (диаметр: 6 мм), с внутренним диаметром около 5 см и длиной колонны 2 м, для осуществления дистилляционного разделения жидкофазного компонента. Количество тепла, требуемое для дистилляционного разделения, подводят, обеспечивая циркуляцию жидкости в нижней части колонны, через линию C11 и ребойлер 1207. Температура жидкости в нижней части многоступенчатой дистилляционной колонны непрерывного действия 1205 составляет 210°C, и давление в верхней части колонны составляет около 2,5 кПа. Газ, отводимый из верхней части многоступенчатой дистилляционной колонны непрерывного действия 1205, конденсируют в холодильнике 1206 по линии C10 и непрерывно отводят по линии C12. Жидкофазный компонент отводят по линии C14.
Жидкофазный компонент, отводимый по линии C14, непрерывно подают на среднюю ступень многоступенчатой дистилляционной колонны непрерывного действия 1208, заполненной насадкой Dickson (диаметр 6 мм), с внутренним диаметром около 5 см и длиной колонны 2 м, для осуществления дистилляционного разделения жидкофазного компонента. Количество тепла, требуемое для дистилляционного разделения, подводят, обеспечивая циркуляцию жидкости в нижней части колонны, через линию C16 и ребойлер 1210. Температура жидкости в нижней части многоступенчатой дистилляционной колонны непрерывного действия 1208 составляет 220°C, и давление в верхней части колонны составляет около 0,5 кПа. Газ, отводимый из верхней части многоступенчатой дистилляционной колонны непрерывного действия 1205, конденсируют в холодильнике 1209 по линии C15 и непрерывно отводят по линии C17 со скоростью около 99,6 г/час. Жидкость, отводимая по линии C17, содержит около 99,9% вес. 4,4'-дифенилметандиизоцианата. Выход в расчете на 4,4'-метилендианилин составляет 82,3%. Хотя непрерывную операцию осуществляют в течение 10 дней, на стенках тонкопленочного дистилляционного аппарата 1202 не наблюдают накопления прилипших веществ.
Пример 11
Стадия (11-1): Получение дифенилового эфира толуол-2,4-дикарбаминовой кислоты
Реакцию осуществляют, используя аппарат, подобный представленному на ФИГ. 7.
Смесь 2125 г (9,9 моль) дифенилкарбоната справочного примера 1 и 35,1 г (0,2 моль) дигидрата ацетата цинка подают в реактор с разделительными перегородками 704, изготовленный из SUS, и с внутренним объемом 5 л, из резервуара-хранилища 701 по линии 71, причем линию 74 закрывают, и 1534 г (16,3 моль) фенола подают в реактор, изготовленный из SUS, из резервуара-хранилища 702 по линии 72. Температуру жидкости внутри реактора 704 устанавливают около 50°C и 391 г (3,2 моль) 2,4-толуолдиамина (Aldrich Corp., USA) подают в реактор 704 из резервуара-хранилища 703 по линии 73 со скоростью около 230 г/час.
В результате анализа раствора после реакции с помощью жидкостной хроматографии было обнаружено, что дифениловый эфир толуол-2,4-дикарбаминовой кислоты образовался с выходом 98,1%.
Линию 74 открывают и реакционную жидкость переносят в резервуар-хранилище 705 по линии 74.
Стадия (11-2): Получение изоцианата путем термического разложения дифенилового эфира толуол-2,4-дикарбаминовой кислоты
Реакцию осуществляют, используя аппарат, подобный представленному на фиг. 8.
Тонкопленочный дистилляционный аппарат 801 с теплопроводящей площадью поверхности 0,1 м2 нагревают до 220°C и давление внутри тонкопленочного дистилляционного аппарата устанавливают около 13 кПа. Смесь, поступившую в резервуар-хранилище 705 на стадии (11-1), нагревают до 130°C и подают в верхнюю часть тонкопленочного дистилляционного аппарата 801 по линии 81 со скоростью около 820 г/час. Жидкофазный компонент отводят из нижней части тонкопленочного дистилляционного аппарата 801 по линии 83 и подают в верхнюю часть тонкопленочного дистилляционного аппарата 801 по линии 84 и линии 81. Газофазный компонент экстрагируют по линии 82.
Газофазный компонент, отводимый из тонкопленочного дистилляционного аппарата 801 по линии 82, непрерывно подают на среднюю ступень многоступенчатой дистилляционной колонны непрерывного действия 802, заполненной насадкой Dickson (диаметр: 6 мм), с внутренним диаметром около 5 см и длиной колонны 2 м, для осуществления дистилляционного разделения газофазного компонента. Количество тепла, требуемое для дистилляционного разделения, подводят, обеспечивая циркуляцию жидкости в нижней части колонны, через линию 86 и ребойлер 804. Температура жидкости в нижней части многоступенчатой дистилляционной колонны непрерывного действия 802 составляет 150°C, и давление в верхней части колонны составляет около 15 кПа. Газ, отводимый из верхней части многоступенчатой дистилляционной колонны непрерывного действия 802, конденсируют в холодильнике 803 по линии 85 и непрерывно отводят по линии 87. Жидкофазный компонент экстрагируют по линии 89 многоступенчатой дистилляционной колонны непрерывного действия 802 на участке, расположенном ниже, чем линия 82.
Жидкофазный компонент, отводимый по линии 89, непрерывно подают на среднюю ступень многоступенчатой дистилляционной колонны непрерывного действия 805, заполненной насадкой Dickson (диаметр: 6 мм), с внутренним диаметром около 5 см и длиной колонны 2 м, для осуществления дистилляционного разделения жидкофазного компонента. Количество тепла, требуемое для дистилляционного разделения, подводят, обеспечивая циркуляцию жидкости в нижней части колонны, через линию 91 и ребойлер 807. Температура жидкости в нижней части многоступенчатой дистилляционной колонны непрерывного действия 805 составляет 150°C, и давление в верхней части колонны составляет около 1,3 кПа. Газ, отводимый из верхней части многоступенчатой дистилляционной колонны непрерывного действия 805, конденсируют в холодильнике 806 по линии 90 и непрерывно отводят в резервуар-хранилище 809 по линии 92 со скоростью около 93 г/час.
Жидкость, отводимая по линии 92, представляет собой раствор, содержащий около 99,7% вес. 2,4-толуолдиизоцианата. Выход в расчете на 2,4-толуолдиамин составляет 83,4%. Хотя непрерывную операцию осуществляют в течение 10 дней, на стенках тонкопленочного дистилляционного аппарата 801 не наблюдают накопления прилипших веществ.
Пример 12
Стадия (12-1): Получение дифенилового эфира N,N'-(4,4'-метандиилдифенил)бискарбаминовой кислоты
Осуществляют тот же самый процесс, что и на стадии (10-1) примера 10, за исключением того, что используют 1293 г (13,8 моль) смеси 2055 г (9,5 моль) дифенилкарбоната справочного примера 1 и 54,9 г (0,3 моль) дигидрата ацетата цинка, 1293 г (13,8 моль) фенола и 496 г (2,5 моль) 4,4'-метилендианилина.
В результате анализа раствора после реакции с помощью жидкостной хроматографии было обнаружено, что дифениловый эфир N,N'-(4,4'-метандиилдифенил)бискарбаминовой кислоты образовался с выходом 98,6%.
Стадия (12-2): Получение изоцианата путем термического разложения дифенилового эфира N,N'-(4,4'-метандиилдифенил)бискарбаминовой кислоты
Используют смесь, полученную на стадии (12-1), вместо смеси, полученной на стадии (7-1), указанную смесь нагревают до 130°C и подают по линии D1 со скоростью около 700 г/час для осуществления реакции термического разложения. Количество тепла, требуемое для термического разложения, подводят, обеспечивая циркуляцию жидкости в нижней части колонны, через линию D3 и ребойлер 1303. Температура жидкости в нижней части многоступенчатой дистилляционной колонны непрерывного действия 1301 составляет 220°C, и давление в верхней части колонны составляет около 15 кПа. Газ, отводимый из верхней части многоступенчатой дистилляционной колонны непрерывного действия 1301, конденсируют в холодильнике 1302 по линии D2 и непрерывно отводят по линии D4. Жидкофазный компонент отводят из многоступенчатой дистилляционной колонны непрерывного действия 1301 по линии D3.
Жидкофазный компонент, отводимый по линии D6, непрерывно подают на среднюю ступень многоступенчатой дистилляционной колонны непрерывного действия 1304, заполненной насадкой Dickson (диаметр: 6 мм), с внутренним диаметром около 5 см и длиной колонны 2 м, для осуществления дистилляционного разделения жидкофазного компонента. Количество тепла, требуемое для дистилляционного разделения, подводят, обеспечивая циркуляцию жидкости в нижней части колонны, через линию D8 и ребойлер 1306. Температура жидкости в нижней части многоступенчатой дистилляционной колонны непрерывного действия 1304 составляет 220°C, и давление в верхней части колонны составляет около 5,2 кПа. Газ, отводимый из верхней части многоступенчатой дистилляционной колонны непрерывного действия 1304, конденсируют в холодильнике 1305 по линии D7 и непрерывно отводят по линии D9. Жидкофазный компонент отводят из нижней части многоступенчатой дистилляционной колонны непрерывного действия 1304 по линии D8 и линии D11.
Жидкофазный компонент, отводимый по линии D8, непрерывно подают на среднюю ступень многоступенчатой дистилляционной колонны непрерывного действия 1307, заполненной насадкой Dickson (диаметр: 6 мм), с внутренним диаметром около 5 см и длиной колонны 2 м, для осуществления дистилляционного разделения жидкофазного компонента. Количество тепла, требуемое для дистилляционного разделения, подводят, обеспечивая циркуляцию жидкости в нижней части колонны, через линию D14 и ребойлер 1309. Температура жидкости в нижней части многоступенчатой дистилляционной колонны непрерывного действия 1307 составляет 220°C, и давление в верхней части колонны составляет около 0,40 кПа. Газ, отводимый из верхней части многоступенчатой дистилляционной колонны непрерывного действия 1307, конденсируют в холодильнике 1308 по линии D12 и непрерывно отводят по линии D13. Отводимое количество в равновесном состоянии составляет около 92 г/час.
Жидкость, отводимая по линии D13, представляет собой раствор, содержащий около 99,8% вес. 4,4'-дифенилметандиизоцианата. Выход в расчете на 4,4'-метилендианилин составляет 76,9%. Когда непрерывную операцию осуществляют в течение 10 дней, внутри тонкопленочного дистилляционного аппарата 1301 наблюдают накопление прилипших веществ.
Пример 13
Стадия (13-1): Получение дифенилового эфира N,N'-гександиил-бис-карбаминовой кислоты
Дифенилкарбонат справочного примера 1 помещают в грушевидную колбу с внутренним объемом 10 л, снабженную трехходовым вентилем, дистилляционной колонной, заполненной Helipak No. 3, фракционирующей колонной, снабженной обратным холодильником и соединенной со сборником дистиллята, и термометром, прикрепленными к грушевидной колбе, и внутренний объем системы заполняют азотом в вакууме для осуществления дистилляционной очистки дифенилкарбоната. При осуществлении 1H-ЯМР анализа продукта дистилляционной очистки было обнаружено, что он содержит около 99,9% вес. дифенилкарбоната. Кроме того, он также содержит 0,002 м.д. атомов металла в виде железа.
Осуществляют тот же самый процесс, что и на стадии (1-1) примера 1, за исключением того, что используют 1414 г (6,6 моль) дифенилкарбоната, 1034 г (11,0 моль) фенола и 256 г (2,2 моль) гексаметилендиамина.
В результате анализа раствора после реакции с помощью жидкостной хроматографии было обнаружено, что образовался дифениловый эфир N,N'-гександиил-бис-карбаминовой кислоты с выходом 99,0%.
Стадия (13-2): Получение изоцианата путем термического разложения дифенилового эфира N,N'-гександиил-бис-карбаминовой кислоты
Осуществляют тот же самый процесс, что и на стадии (1-2) примера 1, за исключением того, что используют смесь, полученную на стадии (13-1), вместо смеси, полученной на стадии (1-1). Жидкость непрерывно удаляют по линии 92 в резервуар-хранилище 809 со скоростью около 104 г/час. Жидкость, отводимая по линии 92, представляет собой раствор, содержащий около 99,8% вес. гексаметилендиизоцианата. Выход в расчете на гексаметилендиамин составляет 95,0%. Хотя непрерывную операцию осуществляют в течение 10 дней, не наблюдают накопления прилипших веществ на стенках тонкопленочного дистилляционного аппарата 801.
Пример 14
Стадия (14-1): Получение дифенилового эфира N,N'-гександиил-бис-карбаминовой кислоты
Ацетилацетонат железа(II) добавляют к дифенилкарбонату справочного примера 1 для получения дифенилкарбоната с содержанием атомов металла в форме железа 8%. Осуществляют тот же самый процесс, что и на стадии (1-1) примера 1, за исключением того, что используют 1371 г (6,4 моль) дифенилкарбоната, 940 г (10,0 моль) фенола и 232 г (2,0 моль) гексаметилендиамина.
В результате анализа раствора после реакции с помощью жидкостной хроматографии было обнаружено, что образовался дифениловый эфир N,N'-гександиил-бис-карбаминовой кислоты с выходом 98,9%.
Стадия (14-2): Получение изоцианата путем термического разложения дифенилового эфира N,N'-гександиил-бис-карбаминовой кислоты
Осуществляют тот же самый процесс, что и на стадии (1-2) примера 1, за исключением того, что используют смесь, полученную на стадии (14-1), вместо смеси, полученной на стадии (1-1). Жидкость непрерывно удаляют в резервуар-хранилище 809 по линии 92 со скоростью около 101 г/час. Жидкость, отводимая по линии 92, представляет собой раствор, содержащий около 99,8% вес. гексаметилендиизоцианата. Выход в расчете на гексаметилендиамин составляет 95,2%. Хотя непрерывную операцию осуществляют в течение 10 дней, не наблюдают накопления прилипших веществ на стенках тонкопленочного дистилляционного аппарата 801.
Пример 15
Стадия (15-1): Получение дифенилового эфира N,N'-гександиил-бис-карбаминовой кислоты
Дифенилкарбонат справочного примера 1 помещают в грушевидную колбу с внутренним объемом 10 л, снабженную трехходовым вентилем, дистилляционной колонной, заполненной Helipak No. 3, фракционирующей колонной, снабженной обратным холодильником и соединенной со сборником дистиллята, и термометром, прикрепленными к грушевидной колбе, и внутренний объем системы заполняют азотом в вакууме для осуществления дистилляционной очистки дифенилкарбоната. Колбу охлаждают для прекращения дистилляционной очистки, когда получают количество дистиллята, равное примерно одной четвертой части от загрузки. В результате 1H-ЯМР анализа дистиллята было обнаружено, что он содержит около 99,9% вес. дифенилкарбоната. Кроме того, уровни содержания атомов металлов в виде железа, кобальта, никеля, цинка, олова, меди и титана в указанном дистилляте оказались ниже предела определения (0,001 м.д.).
Осуществляют тот же самый процесс, что и на стадии (1-1) примера 1, за исключением того, что используют 1553 г (7,3 моль) дифенилкарбоната, 1175 г (12,5 моль) фенола и 291 г (2,5 моль) гексаметилендиамина.
В результате анализа раствора после реакции с помощью жидкостной хроматографии было обнаружено, что образовался дифениловый эфир N,N'-гександиил-бис-карбаминовой кислоты с выходом 95,6%.
Стадия (15-2): Получение изоцианата путем термического разложения дифенилового эфира N,N'-гександиил-бис-карбаминовой кислоты
Осуществляют тот же самый процесс, что и на стадии (1-2) примера 1, за исключением того, что используют смесь, полученную на стадии (15-1), вместо смеси, полученной на стадии (1-1). Жидкость непрерывно удаляют по линии 92 в резервуар-хранилище 809 со скоростью около 99,1 г/час. Жидкость, отводимая по линии 92, представляет собой раствор, содержащий около 99,8% вес. гексаметилендиизоцианата. Выход в расчете на гексаметилендиамин составляет 88,9%. Хотя непрерывную операцию осуществляют в течение 10 дней, не наблюдают накопления прилипших веществ на стенках тонкопленочного дистилляционного аппарата 801.
Пример 16
Стадия (16-1): Получение дифенилового эфира N,N'-гександиил-бис-карбаминовой кислоты
Ацетилацетонат железа(II) добавляют к дифенилкарбонату справочного примера 1 для получения дифенилкарбоната с содержанием атомов металла в виде железа 13%. Осуществляют тот же самый процесс, что и на стадии (1-1) примера 1, за исключением того, что используют 1527 г (7,1 моль) дифенилкарбоната, 1081 г (11,5 моль) фенола и 267 г (2,3 моль) гексаметилендиамина.
В результате анализа раствора после реакции с помощью жидкостной хроматографии было обнаружено, что образовался дифениловый эфир N,N'-гександиил-бис-карбаминовой кислоты с выходом 94,5%.
Стадия (16-2): Получение изоцианата путем термического разложения дифенилового эфира N,N'-гександиил-бис-карбаминовой кислоты
Осуществляют тот же самый процесс, что и на стадии (1-2) примера 1, за исключением того, что используют смесь, полученную на стадии (16-1), вместо смеси, полученной на стадии (1-1). Жидкость непрерывно удаляют в резервуар-хранилище 809 по линии 92 со скоростью около 95,1 г/час. Жидкость, отводимая по линии 92, представляет собой раствор, содержащий около 99,8% вес. гексаметилендиизоцианата. Выход в расчете на гексаметилендиамин составляет 88,0%. Когда непрерывную операцию осуществляют в течение 10 дней, наблюдают накопление прилипших веществ на стенках тонкопленочного дистилляционного аппарата 801.
Пример 17
Стадия (17-1): Получение дифенилового эфира N,N'-гександиил-бис-карбаминовой кислоты
Осуществляют тот же самый процесс, что и на стадии (1-1) примера 1, за исключением того, что используют 1350 г (6,3 моль) дифенилкарбоната и 790 г (8,4 моль) фенола и используют смесь 244 г (2,1 моль) гексаметилендиамина и 197 г (2,1 моль) фенола вместо гексаметилендиамина.
В результате анализа раствора после реакции с помощью жидкостной хроматографии было обнаружено, что образовался дифениловый эфир N,N'-гександиил-бис-карбаминовой кислоты с выходом 99,0%.
Стадия (17-2): Получение изоцианата путем термического разложения дифенилового эфира N,N'-гександиил-бис-карбаминовой кислоты
Осуществляют тот же самый процесс, что и на стадии (1-2) примера 1, за исключением того, что используют смесь, полученную на стадии (17-1), вместо смеси, полученной на стадии (1-1). Жидкость непрерывно удаляют по линии 92 в резервуар-хранилище 809 со скоростью около 106 г/час. Жидкость, отводимая по линии 92, представляет собой раствор, содержащий около 99,8% вес. гексаметилендиизоцианата. Выход в расчете на гексаметилендиамин составляет 97,0%. Хотя непрерывную операцию осуществляют в течение 10 дней, не наблюдают накопления прилипших веществ на стенках тонкопленочного дистилляционного аппарата 801.
Пример 18
Стадия (18-1): Получение бис(3-метилбутилового) эфира N,N'-гександиил-бис-карбаминовой кислоты
Реакцию осуществляют, используя аппарат, подобный представленному на фиг. 16.
1660 г (7,8 моль) дифенилкарбоната подают в реактор с разделительными перегородками 1604, изготовленный из SUS, и с внутренним объемом 5 л из резервуара-хранилища 1601 по линии G1, при этом линию G4 закрывают, и 1175 г (12,5 моль) фенола подают в реактор, изготовленный из SUS, из резервуара-хранилища 1602 по линии G2. Температуру жидкости внутри реактора 1604 устанавливают около 50°C и смесь 291 г (2,5 моль) гексаметилендиамина и воды подают из резервуара-хранилища 1603 по линии G3 в реактор 1604 со скоростью около 200 г/час.
После завершения реакции давление внутри реактора 1604 снижают до 10 кПа и воду отгоняют. Воду конденсируют в холодильнике 1607 и удаляют по линии G6.
В результате анализа раствора после реакции с помощью жидкостной хроматографии было обнаружено, что образовался дифениловый эфир N,N'-гександиил-бис-карбаминовой кислоты с выходом 99,0%.
Линию G4 открывают и реакционную жидкость переносят в резервуар-хранилище 1605 по линии G4.
Стадия (18-2): Получение изоцианата путем термического разложения дифенилового эфира N,N'-гександиил-бис-карбаминовой кислоты
Осуществляют тот же самый процесс, что и на стадии (1-2) примера 1, за исключением того, что используют смесь, полученную на стадии (18-1), вместо смеси, полученной на стадии (1-1). Нагреваемая площадь поверхности тонкопленочного дистилляционного аппарата 801 относительно объема реактора больше, чем в случае реактора 1604 на фиг. 16. Жидкость непрерывно удаляют по линии 92 в резервуар-хранилище 809 со скоростью около 104 г/час. Жидкость, отводимая по линии 92, представляет собой раствор, содержащий около 99,8% вес. гексаметилендиизоцианата. Выход в расчете на гексаметилендиамин составляет 96,5%. Хотя непрерывную операцию осуществляют в течение 10 дней, не наблюдают накопления прилипших веществ на стенках тонкопленочного дистилляционного аппарата 801.
Пример 19 Очистка реактора
Осуществляют процедуру очистки тонкопленочного дистилляционного аппарата 801, в котором наблюдалось накопление прилипшего вещества в примере 6. Тонкопленочный дистилляционный аппарат 801 нагревают до 180°C, и внутренний объем тонкопленочного дистилляционного аппарата 801 наполняют азотом при атмосферном давлении. Фенол, подаваемый по линии 81 со скоростью около 1200 г/час, отводят по линии 83, и жидкофазный компонент удаляют по линии 94 в резервуар-хранилище 810. Когда указанную процедуру осуществляют в течение 1 часа, прилипшее вещество внутри тонкопленочного дистилляционного аппарата 801 не наблюдают.
Примеры 20-27
Процедуру примера 6 осуществляют непрерывно, и различные очищающие растворители используют каждые 10 дней для осуществления процедуры очистки, используя способ примера 19. Полученные результаты представлены в таблице 1.
Сравнительный пример 1
Стадия (A-1): Получение дифенилового эфира N,N'-гександиил-бис-карбаминовой кислоты
Реакцию осуществляют, используя аппарат, подобный представленному на фиг. 14.
1979 г (9,2 моль) дифенилкарбоната подают в реактор с разделительными перегородками 1404, изготовленный из SUS, и с внутренним объемом 5 л из резервуара-хранилища 1401 по линии E1, при этом линию E4 закрывают, и 1316 г (14,0 моль) фенола подают в реактор, изготовленный из SUS, из резервуара-хранилища 1402 по линии E2. Температуру жидкости внутри реактора 1404 устанавливают около 50°C, и 325 г (2,8 моль) гексаметилендиамина подают в реактор 1404 из резервуара-хранилища 1403 по линии E3 со скоростью около 190 г/час.
В результате анализа раствора после реакции с помощью жидкостной хроматографии было обнаружено, что образовался дифениловый эфир N,N'-гександиил-бис-карбаминовой кислоты с выходом 99,3%.
Стадия (A-2): Получение изоцианата путем термического разложения дифенилового эфира N,N'-гександиил-бис-карбаминовой кислоты
Непрерывную реакцию осуществляют, используя аппарат, подобный представленному на фиг. 14.
SUS-реактор 1404 нагревают до 220°C и давление внутри реактора снижают до 1,3 кПа. Газофазный компонент экстрагируют по линии E4, и газофазный компонент непрерывно подают на среднюю ступень многоступенчатой дистилляционной колонны непрерывного действия 1405, заполненную насадкой Dickson (диаметр: 6 мм), с внутренним диаметром около 5 см и длиной колонны 2 м, для осуществления дистилляционного разделения газофазного компонента. Количество тепла, требуемое для дистилляционного разделения, подводят, обеспечивая циркуляцию жидкости в нижней части колонны, через линию E6 и ребойлер 1408. Температура жидкости в нижней части многоступенчатой дистилляционной колонны непрерывного действия 1405 составляет 150°C, и давление в верхней части колонны составляет около 15 кПа. Газ, отводимый из верхней части многоступенчатой дистилляционной колонны непрерывного действия 1405, конденсируют в холодильнике 1407 по линии E5 и непрерывно отводят по линии E7. Жидкофазный компонент экстрагируют по линии E9 многоступенчатой дистилляционной колонны непрерывного действия 1405, расположенной ниже, чем линия E4.
Жидкофазный компонент, отводимый по линии E9, непрерывно подают на среднюю ступень многоступенчатой дистилляционной колонны непрерывного действия 1406, заполненную насадкой Dickson (диаметр 6 мм), с внутренним диаметром около 5 см и длиной колонны 2 м, для осуществления дистилляционного разделения жидкофазного компонента. Количество тепла, требуемое для дистилляционного разделения, подводят, обеспечивая циркуляцию жидкости в нижней части колонны, через линию E11 и ребойлер 1412. Температура жидкости в нижней части многоступенчатой дистилляционной колонны непрерывного действия 1406 составляет 150°C, и давление в верхней части колонны составляет около 1,5 кПа. Газ, отводимый из верхней части многоступенчатой дистилляционной колонны непрерывного действия 1406, конденсируют в холодильнике 1410 по линии E10 и непрерывно отводят в резервуар-хранилище 1411 по линии E12. Количество жидкости, поступившей в резервуар-хранилище 1411, составляет около 304 г. Полученная жидкость представляет собой раствор, содержащий около 99,8% вес. гексаметилендиизоцианата. Выход в расчете на гексаметилендиамин составляет 64,5%.
Сравнительный пример 2
Стадия (B-1): Получение дифенилового эфира N,N'-(4,4'-метандиилдифенил)бискарбаминовой кислоты
Реакцию осуществляют, используя аппарат, подобный представленному на фиг. 15.
Смесь 1527 г (7,1 моль) дифенилкарбоната и 50,5 г (0,2 моль) дигидрата ацетата цинка подают в реактор с разделительными перегородками 1504, изготовленный из SUS, и с внутренним объемом 5 л из резервуара-хранилища 1501 по линии F1, причем линию F4 закрывают, и 1146 г (1,2 моль) фенола подают в реактор, изготовленный из SUS, из резервуара-хранилища 1502 по линии F2. Температуру жидкости внутри реактора 1504 устанавливают около 50°C и 456 г (2,3 моль) 4,4'-метилендианилина подают в реактор 1504 из резервуара-хранилища 1503 по линии F3 со скоростью около 200 г/час.
В результате анализа раствора после реакции с помощью жидкостной хроматографии было обнаружено, что образовался дифениловый эфир N,N'-(4,4'-метандиилдифенил)бискарбаминовой кислоты с выходом 98,3%.
Стадия (B-2): Получение изоцианата путем термического разложения дифенилового эфира N,N'-(4,4'-метандиилдифенил)-бискарбаминовой кислоты
Непрерывную реакцию осуществляют, используя аппарат, подобный представленному на фиг. 15.
SUS-реактор 1504 нагревают до 220°C и давление внутри реактора снижают до 1,3 кПа. Газофазный компонент отводят по линии F4 и газофазный компонент непрерывно подают на среднюю ступень многоступенчатой дистилляционной колонны непрерывного действия 1506, заполненную насадкой Dickson (диаметр 6 мм), с внутренним диаметром около 5 см и длиной колонны 2 м, для осуществления дистилляционного разделения газофазного компонента. Количество тепла, требуемое для дистилляционного разделения, подводят, обеспечивая циркуляцию жидкости в нижней части колонны, через линию F6 и ребойлер 1507. Температура жидкости в нижней части многоступенчатой дистилляционной колонны непрерывного действия 1506 составляет 200°C, и давление в верхней части колонны составляет 60 кПа. Газ, отводимый из верхней части многоступенчатой дистилляционной колонны непрерывного действия 1506, конденсируют в холодильнике 1505 по линии F5 и непрерывно отводят по линии F7. Жидкофазный компонент отводят по линии F6.
Жидкофазный компонент, отводимый по линии F6, непрерывно подают на среднюю ступень многоступенчатой дистилляционной колонны непрерывного действия 1509, заполненную насадкой Dickson (диаметр 6 мм), с внутренним диаметром около 5 см и длиной колонны 2 м, для осуществления дистилляционного разделения жидкофазного компонента. Количество тепла, требуемое для дистилляционного разделения, подводят, обеспечивая циркуляцию жидкости в нижней части колонны, через линию F11 и ребойлер 1510. Температура жидкости в нижней части многоступенчатой дистилляционной колонны непрерывного действия 1509 составляет 210°C, и давление в верхней части колонны составляет около 2,5 кПа. Газ, отводимый из верхней части многоступенчатой дистилляционной колонны непрерывного действия 1509, конденсируют в холодильнике 1508 по линии F10 и непрерывно отводят по линии F12. Жидкофазный компонент отводят по линии F11.
Жидкофазный компонент, отводимый по линии F14, непрерывно подают на среднюю ступень многоступенчатой дистилляционной колонны непрерывного действия 1512, заполненную насадкой Dickson (диаметр 6 мм), с внутренним диаметром около 5 см и длиной колонны 2 м, для осуществления дистилляционного разделения жидкофазного компонента. Количество тепла, требуемое для дистилляционного разделения, подводят, обеспечивая циркуляцию жидкости в нижней части колонны, через линию F16 и ребойлер 1513. Температура жидкости в нижней части многоступенчатой дистилляционной колонны непрерывного действия 1512 составляет 220°C, и давление в верхней части колонны составляет около 0,5 кПа. Газ, отводимый из верхней части многоступенчатой дистилляционной колонны непрерывного действия 1512, конденсируют в холодильнике 1511 по линии F15 и непрерывно отводят по линии F17. Количество жидкости, отводимой по линии F17, составляет около 70 г, и она содержит около 99,9% вес. 4,4'-дифенилметандиизоцианата. Выход в расчете на 4,4'-метилендианилин составляет 56,0%.
Сравнительный пример 3
Стадия (C-1): Получение дифенилового эфира N,N'-гександиил-бис-карбаминовой кислоты
Реакцию осуществляют, используя аппарат, подобный представленному на фиг. 7.
2454 г (11,5 моль) дифенилкарбоната подают в реактор с разделительными перегородками 704, изготовленный из SUS, и с внутренним объемом 5 л из резервуара-хранилища 701 по линии 71, причем линию 74 закрывают. Температуру жидкости внутри реактора 704 устанавливают около 80°C, чтобы расплавить дифенилкарбонат, и 372 г (3,2 моль) гексаметилендиамина подают в реактор 704 из резервуара-хранилища 703 по линии 73 со скоростью около 100 г/час.
В результате анализа раствора после реакции с помощью жидкостной хроматографии было обнаружено, что образовался дифениловый эфир N,N'-гександиил-бис-карбаминовой кислоты с выходом 77,5%.
Линию 74 открывают и реакционную жидкость переносят в резервуар-хранилище 705 по линии 74.
Стадия (C-2): Получение изоцианата путем термического разложения дифенилового эфира N,N'-гександиил-бис-карбаминовой кислоты
Реакцию осуществляют, используя аппарат, подобный представленному на фиг. 8.
Способ осуществляют так же, как на стадии (1-2) примера 1, за исключением того, что используют смесь, полученную на стадии (C-1), вместо смеси, полученной на стадии (1-1).
Жидкость непрерывно удаляют в резервуар-хранилище 809 по линии 92 со скоростью около 113 г/час.
Жидкость, отводимая по линии 92, представляет собой раствор, содержащий около 99,8% вес. гексаметилендиизоцианата. Выход в расчете на гексаметилендиамин составляет 74,4%.
Сравнительные примеры 4-6
Непрерывно осуществляют процедуру примера 6 и каждые 10 дней используют различные растворители для осуществления процедуры очистки, используя способ примера 13. Полученные результаты представлены в таблице.
| Таблица 1 Результаты осуществления процедуры очистки |
|||||
| Температура в тонкопленочном дистилляционном аппарате | Очищающий растворитель | Скорость подачи очищающего растворителя | Время очистки | Результаты | |
| Пр. 20 | 200°C | 2,6-диметилфенол | 1000 г/час | 2 час | Ο |
| Пр. 21 | 210°C | 2,4,6-триметилфенол | 800 г/час | 2 час | Ο |
| Пр. 22 | 250°C | 2-фенилфенол | 1000 г/час | 3 час | Ο |
| Пр. 23 | 280°C | 2,4(α,α-диметил- бензил)фенол |
1200 г/час | 1 час | Ο |
| Пр. 24 | 200°C | 4-этоксифенол | 1100 г/час | 2 час | Ο |
| Пр. 25 | 270°C | 4-додецилфенол | 1300 г/час | 1 час | Ο |
| Пр. 26 | 200°C | Салициловая кислота | 800 г/час | 2 час | Ο |
| Пр. 27 | 220°C | Бензойная кислота | 800 г/час | 4 час | Ο |
| Сравн. Пр. 4 | 200°C | н-додекан | 1000 г/час | 4 час | × |
| Сравн. Пр. 45 |
200°C | Нафталин | 1000 г/час | 4 час | × |
| Сравн. Пр. 6 |
180°C | 1-фенилэтанол | 1000 г/час | 4 час | × |
| Ο: после процедуры очистки прилипших веществ не наблюдается. ×: после процедуры очистки наблюдаются прилипшие вещества. |
|||||
Промышленная применимость
Так как способ получения изоцианата в соответствии с настоящим изобретением позволяет эффективно получать изоцианат без использования высокотоксичного фосгена, указанный способ получения по настоящему изобретению является полезным промышленным способом и отличается высокой промышленной ценностью.
Claims (30)
1. Способ получения изоцианата, включающий стадии
получения реакционной смеси, содержащей арилкарбамат, содержащий арильную группу, образующуюся из диарилкарбоната, ароматическое гидроксисоединение, образующееся из диарилкарбоната, и диарилкарбонат, путем осуществления взаимодействия диарилкарбоната и соединения амина в реакторе, в котором осуществляют реакцию между диарилкарбонатом и соединением амина;
переноса реакционной смеси в реактор термического разложения, соединенный линией с реактором, в котором осуществляют реакцию между диарилкарбонатом и соединением амина; и
получения изоцианата в результате реакции термического разложения арилкарбамата;
где диарилкарбонат представляет собой соединение следующей формулы (1):
(где R1 представляет собой ароматическую группу, содержащую от 6 до 12 атомов углерода),
где соединение амина представляет собой соединение, представленное формулой (2):
(где R2 представляет собой группу, выбранную из группы, состоящей из алифатической группы, содержащей от 1 до 20 атомов углерода, и ароматической группы, содержащей от 6 до 20 атомов углерода, при этом вышеуказанная группа содержит атом, выбранный из атома углерода и атома кислорода, и ее валентность равна n и n представляет собой целое число от 2 до 10) и
где диарилкарбонат включает атом металла в концентрации от 0,001 м.д. до 10%.
получения реакционной смеси, содержащей арилкарбамат, содержащий арильную группу, образующуюся из диарилкарбоната, ароматическое гидроксисоединение, образующееся из диарилкарбоната, и диарилкарбонат, путем осуществления взаимодействия диарилкарбоната и соединения амина в реакторе, в котором осуществляют реакцию между диарилкарбонатом и соединением амина;
переноса реакционной смеси в реактор термического разложения, соединенный линией с реактором, в котором осуществляют реакцию между диарилкарбонатом и соединением амина; и
получения изоцианата в результате реакции термического разложения арилкарбамата;
где диарилкарбонат представляет собой соединение следующей формулы (1):
(где R1 представляет собой ароматическую группу, содержащую от 6 до 12 атомов углерода),
где соединение амина представляет собой соединение, представленное формулой (2):
(где R2 представляет собой группу, выбранную из группы, состоящей из алифатической группы, содержащей от 1 до 20 атомов углерода, и ароматической группы, содержащей от 6 до 20 атомов углерода, при этом вышеуказанная группа содержит атом, выбранный из атома углерода и атома кислорода, и ее валентность равна n и n представляет собой целое число от 2 до 10) и
где диарилкарбонат включает атом металла в концентрации от 0,001 м.д. до 10%.
2. Способ по п.1, дополнительно включающий очистку кислотой побочного продукта с высокой температурой кипения, прилипшего к реактору термического разложения.
3. Способ по п.1, где реакцию между диарилкарбонатом и соединением амина осуществляют при стехиометрическом отношении указанного диарилкарбоната к аминогруппам, входящим в соединение амина, 1 или более.
4. Способ по п.1, где диарилкарбонат и соединение амина подвергают взаимодействию в присутствии ароматического гидроксисоединения в качестве реакционного растворителя.
5. Способ по п.4, где ароматическое гидроксисоединение, используемое в качестве реакционного растворителя, представляет собой ароматическое гидроксисоединение того же типа, что и соединение АrОН, имеющее структуру, в которой атом водорода добавлен к АrО группе, составляющей диарилкарбонат АrОСООАr (где Аr представляет собой ароматическую группу и O представляет собой атом кислорода).
6. Способ по п.1, где реакционную смесь подают в реактор термического разложения в виде жидкости.
7. Способ по п.6, где реакционную смесь подают в реактор термического разложения, поддерживая при этом температуру в интервале от 10 до 180°С.
8. Способ по п.1, где реакционную смесь непрерывно подают в реактор термического разложения.
9. Способ по п.1, где компонент с низкой температурой кипения, образовавшийся в реакции термического разложения, выделяют из реактора термического разложения в форме газофазного компонента и жидкофазный компонент выделяют из нижней части реактора.
10. Способ по п.9, где регенерацию газофазного компонента и регенерацию жидкофазного компонента осуществляют непрерывно.
11. Способ по п.9, где изоцианат, полученный в результате реакции термического разложения арилкарбамата, выделяют из реактора термического разложения в форме газофазного компонента и жидкофазный компонент, содержащий диарилкарбонат, выделяют из нижней части реактора.
12. Способ по п.11, дополнительно включающий регенерацию изоцианата путем дистилляционного разделения, используя дистилляционную колонну, газофазного компонента, содержащего изоцианат, выделенный из реактора термического разложения, и подавая газофазный компонент, содержащий изоцианат, выделенный из реактора термического разложения, в дистилляционную колонну в виде газовой фазы.
13. Способ по п.11, где жидкофазный компонент, содержащий диарилкарбонат, представляет собой смесь, содержащую арилкарбамат, и всю или часть смеси подают в верхнюю часть реактора.
14. Способ по п.9, где изоцианат, полученный в реакции термического разложения арилкарбамата, выделяют из нижней части реактора, в котором осуществляют реакцию термического разложения, в форме жидкофазного компонента.
15. Способ по п.14, где жидкофазный компонент, выделяемый из нижней части реактора, включает изоцианат и арилкарбамат, при этом весь или часть изоцианата выделяют из жидкофазного компонента и все или часть оставшегося подают в верхнюю часть реактора.
16. Способ по п.14, где изоцианат выделяют путем дистилляционного разделения смеси, содержащей изоцианат, выделенный из реактора термического разложения.
17. Способ по п.1, где тип реактора, в котором осуществляют реакцию между диарилкарбонатом и соединением амина, и тип реактора термического разложения могут быть одинаковыми или различными, и реактор, в котором осуществляют реакцию между диарилкарбонатом и соединением амина, и реактор термического разложения представляют собой реактор, выбранный из группы, состоящей из реактора колонного типа и реактора корпусного типа.
18. Способ по п.17, где реактор термического разложения состоит из реактора, выбранного из группы, состоящей из выпаривателя, непрерывной многоступенчатой ректификационной колонны, насадочной колонны, тонкопленочного выпаривателя и выпарного аппарата с падающей пленкой жидкости.
19. Способ по п.1, где реакцию между диарилкарбонатом и соединением амина осуществляют в присутствии катализатора.
20. Способ по п.1, где реакцию термического разложения осуществляют в жидкой фазе.
21. Способ по п.1, где атом металла представляет собой один тип или несколько типов атомов металлов, выбранных из группы, состоящей из атомов железа, никеля, кобальта, цинка, олова, меди и титана.
22. Способ по п.1, где диарилкарбонат представляет собой диарилкарбонат, полученный способом, который включает следующие стадии (1)-(3):
стадия (1): получение реакционной смеси, содержащей диалкилкарбонат, путем осуществления взаимодействия органического соединения олова, содержащего олово-кислород-углеродную связь, и диоксида углерода;
стадия (2): получение диалкилкарбоната и остаточной жидкости путем разделения реакционной смеси; и
стадия (3): получение диарилкарбоната путем осуществления взаимодействия диалкилкарбоната, выделенного на стадии (2), и ароматического гидроксисоединения А с последующим выделением побочного продукта спирта.
стадия (1): получение реакционной смеси, содержащей диалкилкарбонат, путем осуществления взаимодействия органического соединения олова, содержащего олово-кислород-углеродную связь, и диоксида углерода;
стадия (2): получение диалкилкарбоната и остаточной жидкости путем разделения реакционной смеси; и
стадия (3): получение диарилкарбоната путем осуществления взаимодействия диалкилкарбоната, выделенного на стадии (2), и ароматического гидроксисоединения А с последующим выделением побочного продукта спирта.
23. Способ по п.22, где ароматическое гидроксисоединение А представляет собой ароматическое гидроксисоединение, содержащее от 6 до 12 атомов углерода.
24. Способ по п.22, где диарилкарбонат представляет собой диарилкарбонат, полученный способом, который дополнительно включает следующие стадии (4) и (5):
стадия (4): получение органического соединения олова, содержащего олово-кислород-углеродную связь и воду, путем осуществления взаимодействия остаточной жидкости, полученной на стадии (2), со спиртом с последующим удалением воды из реакционной системы; и
стадия (5): повторное использование органического соединения олова, содержащего олово-кислород-углеродную связь, полученного на стадии (4), как органического соединения олова, содержащего олово-кислород-углеродную связь, стадии (1).
стадия (4): получение органического соединения олова, содержащего олово-кислород-углеродную связь и воду, путем осуществления взаимодействия остаточной жидкости, полученной на стадии (2), со спиртом с последующим удалением воды из реакционной системы; и
стадия (5): повторное использование органического соединения олова, содержащего олово-кислород-углеродную связь, полученного на стадии (4), как органического соединения олова, содержащего олово-кислород-углеродную связь, стадии (1).
25. Способ по п.22, где спирт, выделенный на стадии (3), используют как весь или часть спирта стадии (4).
26. Способ по п.9, где диарилкарбонат отделяют и выделяют из жидкофазного компонента или газофазного компонента, выделенных из реактора термического разложения, и указанный диарилкарбонат снова используют в качестве диарилкарбоната, используемого в качестве исходного материала.
27. Способ по п.1 или 22, где ароматическое гидроксисоединение отделяют и выделяют из жидкофазного компонента или газофазного компонента, выделенных в результате реакции термического разложения, и ароматическое гидроксисоединение возвращают в процесс для использования в качестве ароматического гидроксисоединения А на стадии (3) или в качестве ароматического гидроксисоединения, используемого в качестве реакционного растворителя.
28. Способ по п.1, где соединение амина представляет собой соединение диамина, в котором n равно 2 в формуле (2).
29. Способ по п.1, где подачу соединения амина в реактор, в котором эфир карбоновой кислоты и соединение амина подвергают взаимодействию, осуществляют в жидком состоянии.
30. Способ по п.1, где подачу соединения амина в реактор, в котором эфир карбоновой кислоты и соединение амина подвергают взаимодействию, осуществляют в виде смеси, включающей спирт, воду или эфир карбоновой кислоты.
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| PCT/JP2008/058944 WO2009139061A1 (ja) | 2008-05-15 | 2008-05-15 | 炭酸ジアリールを用いるイソシアネートの製造方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2010146077A RU2010146077A (ru) | 2012-05-20 |
| RU2523201C2 true RU2523201C2 (ru) | 2014-07-20 |
Family
ID=41318443
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2010146077/04A RU2523201C2 (ru) | 2008-05-15 | 2008-05-15 | Способ получения изоцианатов с использованием диарилкарбоната |
Country Status (9)
| Country | Link |
|---|---|
| US (1) | US8895774B2 (ru) |
| EP (1) | EP2275405B1 (ru) |
| JP (1) | JP5242678B2 (ru) |
| KR (2) | KR101363232B1 (ru) |
| CN (1) | CN102026964B (ru) |
| BR (1) | BRPI0822695B1 (ru) |
| CA (1) | CA2721357C (ru) |
| RU (1) | RU2523201C2 (ru) |
| WO (1) | WO2009139061A1 (ru) |
Families Citing this family (21)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| TW200844080A (en) * | 2007-01-11 | 2008-11-16 | Asahi Kasei Chemicals Corp | Process for producing isocyanate |
| CA2705874C (en) | 2007-11-19 | 2013-10-29 | Masaaki Shinohata | Process for producing isocyanates and aromatic hydroxy compounds from aromatic polycarbonate resins |
| RU2523201C2 (ru) | 2008-05-15 | 2014-07-20 | Асахи Касеи Кемикалз Корпорейшн | Способ получения изоцианатов с использованием диарилкарбоната |
| CA2721359C (en) * | 2008-05-15 | 2014-05-06 | Asahi Kasei Chemicals Corporation | Isocyanate production process |
| JP5949563B2 (ja) * | 2011-02-09 | 2016-07-06 | 宇部興産株式会社 | イソシアネート化合物の製造方法 |
| CN102896103B (zh) * | 2011-07-25 | 2014-12-03 | 中国石油天然气股份有限公司 | 一种清洗氨基甲酸酯热分解反应器结焦的方法 |
| US9012676B2 (en) | 2011-09-22 | 2015-04-21 | Great Eastern Resins Industrial Co., Ltd. | Processes for producing aryl carbamates, isocynates and polyureas using diaryl carbonate |
| KR101348229B1 (ko) * | 2011-12-14 | 2014-01-08 | 경희대학교 산학협력단 | 지방족 디이소시아네이트의 제조방법 |
| TWI530510B (zh) * | 2012-11-01 | 2016-04-21 | 旭化成化學股份有限公司 | 聚異氰酸酯組成物及異氰酸酯聚合物組成物 |
| CN107207422B (zh) | 2015-01-30 | 2020-12-11 | 巴斯夫欧洲公司 | 低副产物的多亚苯基多亚甲基多异氰酸酯 |
| CN106146832A (zh) * | 2015-04-01 | 2016-11-23 | 大东树脂化学股份有限公司 | 利用二芳基碳酸酯制造脂肪族胺基二甲酸酯、脂肪族胺基多甲酸酯和聚脲的方法 |
| CN106349110A (zh) * | 2015-07-17 | 2017-01-25 | 大东树脂化学股份有限公司 | 制备脂肪族二异氰酸酯的二步法及一锅化合成法 |
| TWI561504B (en) | 2015-07-17 | 2016-12-11 | Great Eastern Resins Ind Co Ltd | Two-step and one-pot processes for preparation of aliphatic diisocyanates |
| CN108250406B (zh) * | 2016-12-29 | 2021-06-15 | 大东树脂化学股份有限公司 | 含软链段的多胺基甲酸酯、多元异氰酸酯、胺甲酸酯预聚物及聚胺甲酸酯弹性体及制备方法 |
| TWI671324B (zh) | 2016-12-29 | 2019-09-11 | 大東樹脂化學股份有限公司 | 包含軟鏈段之多胺基甲酸酯、非光氣法之接續合成多元異氰酸酯、其衍生之胺甲酸酯預聚物及聚胺甲酸酯彈性體及其製備方法 |
| TWI647253B (zh) | 2016-12-29 | 2019-01-11 | 大東樹脂化學股份有限公司 | 利用芳香族氨甲酸酯透過異氰酸鹽作為前驅物之經催化熱反應路徑以製備醯胺或聚醯胺的方法及由芳香胺製備芳香族氨甲酸酯前驅物的方法 |
| JP6757468B2 (ja) | 2017-05-15 | 2020-09-16 | 旭化成株式会社 | イソシアネートの製造方法 |
| JP6843977B2 (ja) * | 2017-05-15 | 2021-03-17 | 旭化成株式会社 | イソシアネートの製造方法 |
| US11352319B2 (en) | 2018-05-15 | 2022-06-07 | Asahi Kasei Kabushiki Kaisha | Method for producing carbamate and method for producing isocyanate |
| CN110256296A (zh) * | 2019-05-20 | 2019-09-20 | 江苏蓝丰生物化工股份有限公司 | 1,5-萘二异氰酸酯的合成方法 |
| EP4063347A4 (en) * | 2019-11-20 | 2023-03-15 | Asahi Kasei Kabushiki Kaisha | ISOCYANATE PRODUCTION PROCESS |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| SU1433410A3 (ru) * | 1985-02-08 | 1988-10-23 | Эникем Синтези,С.П.А. (Фирма) | Способ получени N-метилкарбаматов |
| EP1640357A1 (en) * | 2003-06-27 | 2006-03-29 | Asahi Kasei Chemicals Corporation | Method for producing aromatic carbonate |
| EP1760085A1 (en) * | 2004-05-19 | 2007-03-07 | Asahi Kasei Chemicals Corporation | Process for production of alkyltin alkoxides |
Family Cites Families (84)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE925496C (de) | 1943-03-27 | 1955-03-24 | Dehydag Gmbh | Verfahren zur Herstellung superpolymerer Verbindungen |
| US2692275A (en) | 1953-01-23 | 1954-10-19 | Rohm & Haas | Preparation of 1, 8-diisocyanato-p-menthane |
| NL246083A (ru) | 1958-12-06 | |||
| US3382289A (en) | 1963-04-01 | 1968-05-07 | Exxon Research Engineering Co | Preparation of isoprene feedstock |
| US3366662A (en) * | 1964-03-02 | 1968-01-30 | Olin Mathieson | Process for preparing isocyanates |
| JPS4627593Y1 (ru) | 1967-11-22 | 1971-09-22 | ||
| FR1601198A (ru) | 1968-01-17 | 1970-08-10 | ||
| DE1768860A1 (de) * | 1968-07-09 | 1972-01-13 | Bayer Ag | Verfahren zur Herstellung von mono- und polyfunktionellen Derivaten der Kohlensaeure |
| US3734941A (en) | 1968-09-06 | 1973-05-22 | American Cyanamid Co | Process for converting urethanes to isocyanates |
| JPS5219624A (en) | 1975-08-07 | 1977-02-15 | Mitsui Toatsu Chem Inc | Process for preparation of isocyanates |
| US3992430A (en) | 1975-09-11 | 1976-11-16 | Chevron Research Company | Process for preparing aromatic isocyanates |
| IT1051034B (it) | 1975-12-03 | 1981-04-21 | Snam Progetti | Procedimento per la preparazione di uretani aromatici |
| JPS6024096B2 (ja) | 1976-05-10 | 1985-06-11 | 日本ポリウレタン工業株式会社 | カルバメ−ト化合物の製造法 |
| JPS5439002A (en) | 1977-08-30 | 1979-03-24 | Mitsubishi Chem Ind Ltd | Preparation of isocyanates |
| US4123450A (en) | 1977-09-22 | 1978-10-31 | Fmc Corporation | Process for preparing alkyl isocyanates |
| DE2917490A1 (de) | 1979-04-30 | 1980-11-13 | Basf Ag | Verfahren zur herstellung von aliphatischen und cycloaliphatischen di- und polyurethanen |
| DE2942503A1 (de) | 1979-10-20 | 1981-05-07 | Basf Ag, 6700 Ludwigshafen | Verfahren zur herstellung von aromatischen di- und/oder polyisocyanaten |
| DE2943480A1 (de) | 1979-10-27 | 1981-05-07 | Bayer Ag, 5090 Leverkusen | Verfahren zur herstellung von n,o-disubstituierten urethanen, sowie ihre verwendung als ausgangsmaterial zur herstellung von isocyanaten |
| DE2943550A1 (de) | 1979-10-27 | 1981-05-14 | Bayer Ag, 5090 Leverkusen | Verfahren zur herstellung von urethanen und ihre verwendung als ausgangsmaterial zur herstellung von isocyanaten |
| DE2943551A1 (de) | 1979-10-27 | 1981-05-07 | Bayer Ag, 5090 Leverkusen | Verfahren zur herstellung von n,o-disubstituierten urethanen, sowie ihre verwendung zur herstellung von isocyanaten |
| DE3035354A1 (de) | 1980-09-19 | 1982-04-29 | Bayer Ag, 5090 Leverkusen | Verfahren zur herstellung von n,o-disubstituierten urethanen und ihre verwendung als ausgangsmaterial zur herstellung von organischen isocyanaten |
| DE3040692A1 (de) | 1980-10-29 | 1982-06-03 | Basf Ag, 6700 Ludwigshafen | Verfahren zur herstellung aliphatischer isocyanate |
| DE3047898A1 (de) | 1980-12-19 | 1982-07-15 | Bayer Ag, 5090 Leverkusen | Verfahren zur kontinuierlichen thermischen spaltung von carbamidsaeureestern und die verwendung von hierbei anfallenden isocyanate und carbamidsaeureester aufweisenden gemischen zur herstellung von isocyanaten |
| DE3108990A1 (de) | 1981-03-10 | 1982-09-23 | Bayer Ag, 5090 Leverkusen | Verfahren zur herstellung von polyisocyanaten |
| US4388426A (en) | 1981-06-26 | 1983-06-14 | Eschem Inc. | Stabilization of epoxy systems in non-flammable solvents |
| DE3142627A1 (de) | 1981-10-28 | 1983-05-05 | Basf Ag, 6700 Ludwigshafen | Verfahren zur herstellung von isocyanaten durch thermische spaltung von urethanen |
| DE3215591A1 (de) | 1982-04-27 | 1983-10-27 | Bayer Ag, 5090 Leverkusen | Verfahren zur kontinuierlichen thermischen spaltung von carbamidsaeureestern |
| EP0100047B1 (de) | 1982-07-24 | 1986-02-12 | BASF Aktiengesellschaft | Verfahren zur Herstellung von Hexamethylen-diisocyanat-1,6 und/oder isomeren Diisocyanaten mit 6 Kohlenstoffatomen im Alkylenrest |
| JPH0645586B2 (ja) | 1982-12-13 | 1994-06-15 | 三菱化成株式会社 | 芳香族ウレタンの熱分解法 |
| DE3314790A1 (de) | 1983-04-23 | 1984-10-25 | Basf Ag, 6700 Ludwigshafen | Mehrstufenverfahren zur herstellung von 3-isocyanatomethyl-3,5,5-trimethyl-cyclohexylisocyanat |
| DE3314788A1 (de) | 1983-04-23 | 1984-10-25 | Basf Ag, 6700 Ludwigshafen | Mehrstufenverfahren zur herstellung von hexamethylendiisocyanat-1,6 und/oder isomeren aliphatischen diisocyanaten mit 6 kohlenstoffatomen im alkylenrest |
| IT1164223B (it) | 1983-05-13 | 1987-04-08 | Anic Spa | Procedimento perfezionato per la produzione di isocianati alchilici |
| JPS60231640A (ja) | 1984-05-02 | 1985-11-18 | Asahi Chem Ind Co Ltd | イソシアナ−トの連続的製法 |
| JPH0627593B2 (ja) | 1985-09-12 | 1994-04-13 | 鐘紡株式会社 | 吸着式ヒ−トポンプ |
| JPS63189572A (ja) | 1987-01-30 | 1988-08-05 | フジテツク株式会社 | 縦列式駐車装置の可動ステップ |
| US4925971A (en) | 1987-12-08 | 1990-05-15 | Asahi Kasei Kogyo Kabushiki Kaisha | Method for producing aliphatic o-arylurethanes |
| JPH01230550A (ja) | 1988-03-11 | 1989-09-14 | Asahi Chem Ind Co Ltd | アルキルポリカルバミン酸アリールエステルの製造方法 |
| JPH026665A (ja) | 1988-06-10 | 1990-01-10 | Kao Corp | 衣料用柔軟仕上剤 |
| DE3828033A1 (de) | 1988-08-18 | 1990-03-08 | Huels Chemische Werke Ag | Kreislaufverfahren zur herstellung von (cyclo)aliphatischen diisocyanaten |
| JPH0613361B2 (ja) | 1990-02-14 | 1994-02-23 | 株式会社アイ・エフ・プランニング | ごみ容器 |
| EP0446514B1 (en) | 1990-03-16 | 1993-03-10 | Council of Scientific and Industrial Research | Process for the preparation of aryl esters of n-alkyl carbamic acids |
| DE4124671A1 (de) | 1991-07-25 | 1993-01-28 | Basf Ag | Reaktor und verfahren zur thermischen spaltung von carbamidsaeureestern |
| DE4213099A1 (de) | 1992-04-21 | 1993-10-28 | Basf Ag | Mehrstufiges Verfahren zur kontinuierlichen Herstellung von organischen Polyisocyanaten |
| IT1255763B (it) | 1992-05-15 | 1995-11-15 | Franco Rivetti | Procedimento per la preparazione di isocianati alchilici |
| JP3100008B2 (ja) * | 1992-08-07 | 2000-10-16 | 旭化成工業株式会社 | 芳香族ポリカーボネートの製法 |
| JP3226997B2 (ja) * | 1992-12-28 | 2001-11-12 | 旭化成株式会社 | ポリカルバミン酸エステル化合物の熱分解方法 |
| US5498319A (en) * | 1993-06-29 | 1996-03-12 | General Electric Company | Process for purifying diaryl carbonates |
| JPH0725830A (ja) | 1993-07-08 | 1995-01-27 | Daicel Chem Ind Ltd | 炭酸ジエステルの精製法及びその精製法によって得られた炭酸ジエステルを用いて製造したポリカーボネート |
| US5457732A (en) | 1994-02-28 | 1995-10-10 | Motorola, Inc. | Method and apparatus for delivery of a response in a messaging system |
| JP3083039B2 (ja) | 1994-03-18 | 2000-09-04 | 三菱瓦斯化学株式会社 | イソシアネート類の製造方法 |
| IT1282023B1 (it) | 1995-07-06 | 1998-03-06 | Mini Ricerca Scient Tecnolog | Procedimento per la produzione di uretani aromatici |
| IT1282022B1 (it) | 1995-07-06 | 1998-03-06 | Mini Ricerca Scient Tecnolog | Procedimento per la produzione di carbammati aromatici |
| JP3674642B2 (ja) | 1995-09-22 | 2005-07-20 | 三菱瓦斯化学株式会社 | イソシアネート類の製造法 |
| DE59705128D1 (de) * | 1996-03-15 | 2001-12-06 | Bayer Ag | Verfahren zur thermischen Spaltung von Carbamidsäureestern |
| EP0902014A1 (en) | 1997-02-14 | 1999-03-17 | Ube Industries Limited | Process for producing aryl carbamates |
| JP4462644B2 (ja) | 1997-05-20 | 2010-05-12 | 宇部興産株式会社 | カルバメートの製造法 |
| IT1292030B1 (it) | 1997-05-29 | 1999-01-25 | Mini Ricerca Scient Tecnolog | Procedimento per la sintesi di uretani aromatici |
| JP2002500654A (ja) | 1997-05-31 | 2002-01-08 | ハンツマン・アイシーアイ・ケミカルズ・エルエルシー | 有機イソシアネート類の製造方法 |
| AU8211798A (en) * | 1997-06-09 | 1998-12-30 | Huntsman Ici Chemicals Llc | Process for the production of organic isocyanates |
| JP4029225B2 (ja) | 1997-06-17 | 2008-01-09 | 三菱瓦斯化学株式会社 | イソシアネート化合物の製造方法 |
| EP0957073A1 (en) | 1998-05-12 | 1999-11-17 | Schwarz Pharma Ag | Novel derivatives of 3,3-diphenylpropylamines |
| JP2000344730A (ja) | 1999-06-03 | 2000-12-12 | Mitsubishi Gas Chem Co Inc | 1,5−ナフチレンジイソシアネートの製造法 |
| JP2001031639A (ja) | 1999-07-15 | 2001-02-06 | Mitsubishi Gas Chem Co Inc | 1,5−ナフチレンジイソシアネートの製造方法 |
| JP2001048855A (ja) * | 1999-08-11 | 2001-02-20 | Takeda Chem Ind Ltd | イソシアネート基含有化合物の製造方法、イソシアネート基含有化合物およびイソシアネート基含有ポリシロキサン化合物 |
| IT1317756B1 (it) | 2000-02-03 | 2003-07-15 | Eni Spa | Procedimento integrato per la preparazione di isocianati aromatici eprocessi per la realizzazione delle relative fasi intermedie. |
| CN1186317C (zh) | 2000-02-29 | 2005-01-26 | 亨茨曼国际有限公司 | 制备有机多异氰酸酯的方法 |
| JP4458620B2 (ja) | 2000-05-12 | 2010-04-28 | 株式会社Adeka | カラーフィルター用耐光性付与剤及びこれを用いたカラーフィルター用感光性樹脂組成物 |
| US6781010B1 (en) * | 2000-09-19 | 2004-08-24 | Lyondell Chemical Company | Non-phosgene route to the manufacture of organic isocyanates |
| JP4993827B2 (ja) | 2001-08-17 | 2012-08-08 | 日本曹達株式会社 | 試料導入管閉塞防止方法 |
| KR100545615B1 (ko) | 2001-12-27 | 2006-01-24 | 아사히 가세이 케미칼즈 가부시키가이샤 | 탄산에스테르의 제조 방법 |
| JP3992178B2 (ja) | 2001-12-27 | 2007-10-17 | 旭化成ケミカルズ株式会社 | 炭酸エステルの製造方法 |
| JP2003201275A (ja) | 2001-12-28 | 2003-07-18 | Mitsui Chemicals Inc | 芳香族ウレタン化合物の製造方法 |
| SG115512A1 (en) | 2001-12-28 | 2005-10-28 | Mitsui Takeda Chemicals Inc | Method for producing carbamates and method for producing isocyanates |
| JP4397810B2 (ja) | 2002-08-07 | 2010-01-13 | 旭化成ケミカルズ株式会社 | 炭酸エステルの製造方法 |
| JP4299020B2 (ja) | 2003-02-13 | 2009-07-22 | 三井化学ポリウレタン株式会社 | アルキルカルバメートの製造方法 |
| JP2004262834A (ja) | 2003-02-28 | 2004-09-24 | Mitsui Chemicals Inc | 芳香族ウレタン化合物の製造方法 |
| JP2004262835A (ja) * | 2003-02-28 | 2004-09-24 | Mitsui Chemicals Inc | 芳香族イソシアネートの製造方法 |
| JP2006069941A (ja) * | 2004-09-01 | 2006-03-16 | Kagawa Industry Support Foundation | イソシアネート系化合物の分解回収方法 |
| CN1324007C (zh) | 2004-09-17 | 2007-07-04 | 中国科学院成都有机化学有限公司 | 一种氨基甲酸酯的合成方法 |
| US8053595B2 (en) | 2006-11-17 | 2011-11-08 | Asahi Kasei Chemicals Corporation | Process for producing isocyanates |
| TW200844080A (en) | 2007-01-11 | 2008-11-16 | Asahi Kasei Chemicals Corp | Process for producing isocyanate |
| CA2705874C (en) | 2007-11-19 | 2013-10-29 | Masaaki Shinohata | Process for producing isocyanates and aromatic hydroxy compounds from aromatic polycarbonate resins |
| CA2721359C (en) | 2008-05-15 | 2014-05-06 | Asahi Kasei Chemicals Corporation | Isocyanate production process |
| RU2523201C2 (ru) | 2008-05-15 | 2014-07-20 | Асахи Касеи Кемикалз Корпорейшн | Способ получения изоцианатов с использованием диарилкарбоната |
-
2008
- 2008-05-15 RU RU2010146077/04A patent/RU2523201C2/ru not_active IP Right Cessation
- 2008-05-15 EP EP08752802.2A patent/EP2275405B1/en active Active
- 2008-05-15 CN CN2008801291473A patent/CN102026964B/zh active Active
- 2008-05-15 KR KR1020107025418A patent/KR101363232B1/ko active IP Right Grant
- 2008-05-15 BR BRPI0822695A patent/BRPI0822695B1/pt not_active IP Right Cessation
- 2008-05-15 US US12/991,586 patent/US8895774B2/en active Active
- 2008-05-15 KR KR1020137028771A patent/KR20130127553A/ko not_active Application Discontinuation
- 2008-05-15 CA CA2721357A patent/CA2721357C/en not_active Expired - Fee Related
- 2008-05-15 JP JP2010511822A patent/JP5242678B2/ja active Active
- 2008-05-15 WO PCT/JP2008/058944 patent/WO2009139061A1/ja active Application Filing
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| SU1433410A3 (ru) * | 1985-02-08 | 1988-10-23 | Эникем Синтези,С.П.А. (Фирма) | Способ получени N-метилкарбаматов |
| EP1640357A1 (en) * | 2003-06-27 | 2006-03-29 | Asahi Kasei Chemicals Corporation | Method for producing aromatic carbonate |
| EP1760085A1 (en) * | 2004-05-19 | 2007-03-07 | Asahi Kasei Chemicals Corporation | Process for production of alkyltin alkoxides |
Also Published As
| Publication number | Publication date |
|---|---|
| EP2275405A1 (en) | 2011-01-19 |
| JPWO2009139061A1 (ja) | 2011-09-15 |
| JP5242678B2 (ja) | 2013-07-24 |
| KR20110007184A (ko) | 2011-01-21 |
| RU2010146077A (ru) | 2012-05-20 |
| CN102026964B (zh) | 2013-12-25 |
| BRPI0822695A2 (pt) | 2015-07-07 |
| KR20130127553A (ko) | 2013-11-22 |
| CA2721357C (en) | 2014-01-07 |
| BRPI0822695B1 (pt) | 2017-05-02 |
| US8895774B2 (en) | 2014-11-25 |
| EP2275405B1 (en) | 2019-04-24 |
| EP2275405A4 (en) | 2015-10-28 |
| CA2721357A1 (en) | 2009-11-19 |
| US20110054211A1 (en) | 2011-03-03 |
| KR101363232B1 (ko) | 2014-02-12 |
| CN102026964A (zh) | 2011-04-20 |
| WO2009139061A1 (ja) | 2009-11-19 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2523201C2 (ru) | Способ получения изоцианатов с использованием диарилкарбоната | |
| KR101525641B1 (ko) | 이소시아네이트의 제조 방법 | |
| KR101347403B1 (ko) | N-치환 카르밤산 에스테르의 제조 방법, 상기 n-치환 카르밤산 에스테르를 이용하는 이소시아네이트의 제조 방법, 및 n-치환 카르밤산 에스테르 및 방향족 히드록시 화합물을 포함하는 n-치환 카르밤산 에스테르의 이송용 및 저장용 조성물 | |
| JP4958971B2 (ja) | カルバミン酸エステルおよび芳香族ヒドロキシ化合物を含む組成物を用いるイソシアネートの製造方法、ならびにカルバミン酸エステル移送用および貯蔵用組成物 | |
| JP5650777B2 (ja) | 炭酸ジアリールを用いるイソシアネートの製造方法 | |
| TWI408120B (zh) | A process for producing isocyanates using diaryl carbonates | |
| TWI496763B (zh) | Preparation of isocyanates | |
| SG190662A1 (en) | Process for producing isocyanates using diaryl carbonate | |
| RU2419603C2 (ru) | Способ получения изоцианатов |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20190516 |