JP2022548309A - Crth2のバリアント核酸ライブラリー - Google Patents
Crth2のバリアント核酸ライブラリー Download PDFInfo
- Publication number
- JP2022548309A JP2022548309A JP2022518006A JP2022518006A JP2022548309A JP 2022548309 A JP2022548309 A JP 2022548309A JP 2022518006 A JP2022518006 A JP 2022518006A JP 2022518006 A JP2022518006 A JP 2022518006A JP 2022548309 A JP2022548309 A JP 2022548309A
- Authority
- JP
- Japan
- Prior art keywords
- antibody
- seq
- crth2r
- nucleic acid
- set forth
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 150000007523 nucleic acids Chemical class 0.000 title claims abstract description 238
- 102000039446 nucleic acids Human genes 0.000 title claims abstract description 219
- 108020004707 nucleic acids Proteins 0.000 title claims abstract description 219
- 108050000258 Prostaglandin D receptors Proteins 0.000 title description 2
- 102000009389 Prostaglandin D receptors Human genes 0.000 title 1
- 230000027455 binding Effects 0.000 claims abstract description 172
- 108060003951 Immunoglobulin Proteins 0.000 claims abstract description 161
- 102000018358 immunoglobulin Human genes 0.000 claims abstract description 161
- 238000000034 method Methods 0.000 claims abstract description 114
- 108090000623 proteins and genes Proteins 0.000 claims abstract description 60
- 102000004169 proteins and genes Human genes 0.000 claims abstract description 43
- 229940072221 immunoglobulins Drugs 0.000 claims abstract description 26
- 108010003723 Single-Domain Antibodies Proteins 0.000 claims abstract description 22
- 150000001413 amino acids Chemical class 0.000 claims description 144
- 108091033319 polynucleotide Proteins 0.000 claims description 142
- 239000002157 polynucleotide Substances 0.000 claims description 142
- 102000040430 polynucleotide Human genes 0.000 claims description 142
- 125000003275 alpha amino acid group Chemical group 0.000 claims description 106
- 102000008394 Immunoglobulin Fragments Human genes 0.000 claims description 105
- 108010021625 Immunoglobulin Fragments Proteins 0.000 claims description 105
- 108010047041 Complementarity Determining Regions Proteins 0.000 claims description 74
- 102000006496 Immunoglobulin Heavy Chains Human genes 0.000 claims description 65
- 108010019476 Immunoglobulin Heavy Chains Proteins 0.000 claims description 65
- 102000013463 Immunoglobulin Light Chains Human genes 0.000 claims description 58
- 108010065825 Immunoglobulin Light Chains Proteins 0.000 claims description 58
- 239000012634 fragment Substances 0.000 claims description 50
- 241000282414 Homo sapiens Species 0.000 claims description 30
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims description 29
- 239000000427 antigen Substances 0.000 claims description 25
- 108091007433 antigens Proteins 0.000 claims description 25
- 102000036639 antigens Human genes 0.000 claims description 25
- 238000013262 cAMP assay Methods 0.000 claims description 22
- 201000010099 disease Diseases 0.000 claims description 19
- 239000003446 ligand Substances 0.000 claims description 17
- 239000013598 vector Substances 0.000 claims description 15
- 108090000765 processed proteins & peptides Proteins 0.000 claims description 13
- 208000035475 disorder Diseases 0.000 claims description 10
- 102000004196 processed proteins & peptides Human genes 0.000 claims description 10
- 206010020751 Hypersensitivity Diseases 0.000 claims description 7
- 201000004384 Alopecia Diseases 0.000 claims description 6
- 108010054477 Immunoglobulin Fab Fragments Proteins 0.000 claims description 6
- 102000001706 Immunoglobulin Fab Fragments Human genes 0.000 claims description 6
- 108010008177 Fd immunoglobulins Proteins 0.000 claims description 5
- 108010067060 Immunoglobulin Variable Region Proteins 0.000 claims description 5
- 102000017727 Immunoglobulin Variable Region Human genes 0.000 claims description 5
- 208000030961 allergic reaction Diseases 0.000 claims description 5
- 210000003734 kidney Anatomy 0.000 claims description 5
- 239000000816 peptidomimetic Substances 0.000 claims description 4
- 206010039085 Rhinitis allergic Diseases 0.000 claims description 3
- 201000010105 allergic rhinitis Diseases 0.000 claims description 3
- 231100000360 alopecia Toxicity 0.000 claims description 3
- 208000006673 asthma Diseases 0.000 claims description 3
- 210000000988 bone and bone Anatomy 0.000 claims description 3
- 210000000845 cartilage Anatomy 0.000 claims description 3
- 210000003169 central nervous system Anatomy 0.000 claims description 3
- 208000030949 chronic idiopathic urticaria Diseases 0.000 claims description 3
- 206010072757 chronic spontaneous urticaria Diseases 0.000 claims description 3
- 208000024376 chronic urticaria Diseases 0.000 claims description 3
- 210000004209 hair Anatomy 0.000 claims description 3
- 230000003676 hair loss Effects 0.000 claims description 3
- 230000028709 inflammatory response Effects 0.000 claims description 3
- 210000000936 intestine Anatomy 0.000 claims description 3
- 210000004072 lung Anatomy 0.000 claims description 3
- 210000003491 skin Anatomy 0.000 claims description 3
- 238000002156 mixing Methods 0.000 claims description 2
- 239000000203 mixture Substances 0.000 abstract description 21
- 108091028043 Nucleic acid sequence Proteins 0.000 abstract description 18
- 102100024218 Prostaglandin D2 receptor 2 Human genes 0.000 abstract description 9
- 101710201263 Prostaglandin D2 receptor 2 Proteins 0.000 abstract description 4
- 235000001014 amino acid Nutrition 0.000 description 138
- 210000004027 cell Anatomy 0.000 description 95
- 239000000758 substrate Substances 0.000 description 79
- 230000015572 biosynthetic process Effects 0.000 description 72
- 238000003786 synthesis reaction Methods 0.000 description 71
- 108020004705 Codon Proteins 0.000 description 57
- 102000003688 G-Protein-Coupled Receptors Human genes 0.000 description 39
- 108090000045 G-Protein-Coupled Receptors Proteins 0.000 description 39
- 235000018102 proteins Nutrition 0.000 description 35
- 230000000694 effects Effects 0.000 description 29
- 238000012163 sequencing technique Methods 0.000 description 29
- 102100035360 Cerebellar degeneration-related antigen 1 Human genes 0.000 description 25
- 101000737793 Homo sapiens Cerebellar degeneration-related antigen 1 Proteins 0.000 description 25
- -1 antibodies Proteins 0.000 description 24
- 239000000463 material Substances 0.000 description 23
- 239000003153 chemical reaction reagent Substances 0.000 description 20
- 238000004458 analytical method Methods 0.000 description 19
- 230000008569 process Effects 0.000 description 18
- 101001037147 Homo sapiens Immunoglobulin heavy variable 1-69 Proteins 0.000 description 17
- 102100040232 Immunoglobulin heavy variable 1-69 Human genes 0.000 description 17
- 230000014509 gene expression Effects 0.000 description 17
- 239000002773 nucleotide Substances 0.000 description 16
- 125000003729 nucleotide group Chemical group 0.000 description 16
- 150000008300 phosphoramidites Chemical class 0.000 description 16
- 102100029100 Hematopoietic prostaglandin D synthase Human genes 0.000 description 15
- 101000988802 Homo sapiens Hematopoietic prostaglandin D synthase Proteins 0.000 description 15
- 108010058731 nopaline synthase Proteins 0.000 description 15
- 230000003647 oxidation Effects 0.000 description 15
- 238000007254 oxidation reaction Methods 0.000 description 15
- BHMBVRSPMRCCGG-OUTUXVNYSA-N prostaglandin D2 Chemical compound CCCCC[C@H](O)\C=C\[C@@H]1[C@@H](C\C=C/CCCC(O)=O)[C@@H](O)CC1=O BHMBVRSPMRCCGG-OUTUXVNYSA-N 0.000 description 15
- BHMBVRSPMRCCGG-UHFFFAOYSA-N prostaglandine D2 Natural products CCCCCC(O)C=CC1C(CC=CCCCC(O)=O)C(O)CC1=O BHMBVRSPMRCCGG-UHFFFAOYSA-N 0.000 description 15
- 239000005557 antagonist Substances 0.000 description 14
- 230000008878 coupling Effects 0.000 description 14
- 238000010168 coupling process Methods 0.000 description 14
- 238000005859 coupling reaction Methods 0.000 description 14
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 14
- 108020004414 DNA Proteins 0.000 description 13
- 241000282324 Felis Species 0.000 description 13
- 238000000151 deposition Methods 0.000 description 13
- 238000013461 design Methods 0.000 description 13
- 230000003993 interaction Effects 0.000 description 13
- 239000002777 nucleoside Substances 0.000 description 13
- 238000011282 treatment Methods 0.000 description 13
- 230000008021 deposition Effects 0.000 description 12
- 230000006870 function Effects 0.000 description 12
- 238000012986 modification Methods 0.000 description 12
- 230000004048 modification Effects 0.000 description 12
- 101001037139 Homo sapiens Immunoglobulin heavy variable 3-30 Proteins 0.000 description 11
- 102100040219 Immunoglobulin heavy variable 3-30 Human genes 0.000 description 11
- 230000001965 increasing effect Effects 0.000 description 11
- 238000012545 processing Methods 0.000 description 11
- 239000000047 product Substances 0.000 description 11
- 239000000126 substance Substances 0.000 description 11
- 101001037140 Homo sapiens Immunoglobulin heavy variable 3-23 Proteins 0.000 description 10
- 101001054839 Homo sapiens Immunoglobulin lambda variable 1-51 Proteins 0.000 description 10
- 102100040220 Immunoglobulin heavy variable 3-23 Human genes 0.000 description 10
- 102100026922 Immunoglobulin lambda variable 1-51 Human genes 0.000 description 10
- 229940125516 allosteric modulator Drugs 0.000 description 10
- 238000003556 assay Methods 0.000 description 10
- 238000006243 chemical reaction Methods 0.000 description 10
- 239000013604 expression vector Substances 0.000 description 10
- 102000005962 receptors Human genes 0.000 description 10
- 108020003175 receptors Proteins 0.000 description 10
- 238000012216 screening Methods 0.000 description 10
- 238000003860 storage Methods 0.000 description 10
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 9
- 241000282465 Canis Species 0.000 description 9
- 230000003281 allosteric effect Effects 0.000 description 9
- OHCQJHSOBUTRHG-KGGHGJDLSA-N FORSKOLIN Chemical compound O=C([C@@]12O)C[C@](C)(C=C)O[C@]1(C)[C@@H](OC(=O)C)[C@@H](O)[C@@H]1[C@]2(C)[C@@H](O)CCC1(C)C OHCQJHSOBUTRHG-KGGHGJDLSA-N 0.000 description 8
- 238000012413 Fluorescence activated cell sorting analysis Methods 0.000 description 8
- 241000283973 Oryctolagus cuniculus Species 0.000 description 8
- 101150117115 V gene Proteins 0.000 description 8
- 102000000072 beta-Arrestins Human genes 0.000 description 8
- 108010080367 beta-Arrestins Proteins 0.000 description 8
- 238000004091 panning Methods 0.000 description 8
- 230000007115 recruitment Effects 0.000 description 8
- 101001138089 Homo sapiens Immunoglobulin kappa variable 1-39 Proteins 0.000 description 7
- 101001047618 Homo sapiens Immunoglobulin kappa variable 3-15 Proteins 0.000 description 7
- 101000956885 Homo sapiens Immunoglobulin lambda variable 2-14 Proteins 0.000 description 7
- 102100020910 Immunoglobulin kappa variable 1-39 Human genes 0.000 description 7
- 102100022965 Immunoglobulin kappa variable 3-15 Human genes 0.000 description 7
- 102100038429 Immunoglobulin lambda variable 2-14 Human genes 0.000 description 7
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical compound [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 description 7
- 238000004891 communication Methods 0.000 description 7
- 230000002093 peripheral effect Effects 0.000 description 7
- 230000001225 therapeutic effect Effects 0.000 description 7
- 108091008875 B cell receptors Proteins 0.000 description 6
- 101710154606 Hemagglutinin Proteins 0.000 description 6
- 101710093908 Outer capsid protein VP4 Proteins 0.000 description 6
- 101710135467 Outer capsid protein sigma-1 Proteins 0.000 description 6
- 101710176177 Protein A56 Proteins 0.000 description 6
- 239000000556 agonist Substances 0.000 description 6
- 230000003321 amplification Effects 0.000 description 6
- 210000004899 c-terminal region Anatomy 0.000 description 6
- 239000003814 drug Substances 0.000 description 6
- 238000001943 fluorescence-activated cell sorting Methods 0.000 description 6
- 239000000185 hemagglutinin Substances 0.000 description 6
- 239000010410 layer Substances 0.000 description 6
- 238000004519 manufacturing process Methods 0.000 description 6
- 239000000178 monomer Substances 0.000 description 6
- 229940126662 negative allosteric modulator Drugs 0.000 description 6
- 238000003199 nucleic acid amplification method Methods 0.000 description 6
- 229920001184 polypeptide Polymers 0.000 description 6
- 229940126027 positive allosteric modulator Drugs 0.000 description 6
- 239000010703 silicon Substances 0.000 description 6
- 229910052710 silicon Inorganic materials 0.000 description 6
- 239000004055 small Interfering RNA Substances 0.000 description 6
- 239000007787 solid Substances 0.000 description 6
- 238000004448 titration Methods 0.000 description 6
- 241000282472 Canis lupus familiaris Species 0.000 description 5
- 101000998951 Homo sapiens Immunoglobulin heavy variable 1-8 Proteins 0.000 description 5
- 101001047627 Homo sapiens Immunoglobulin kappa variable 2-28 Proteins 0.000 description 5
- 102100036885 Immunoglobulin heavy variable 1-8 Human genes 0.000 description 5
- 102100022950 Immunoglobulin kappa variable 2-28 Human genes 0.000 description 5
- 206010028980 Neoplasm Diseases 0.000 description 5
- 241000288906 Primates Species 0.000 description 5
- 241000700159 Rattus Species 0.000 description 5
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 5
- 238000003491 array Methods 0.000 description 5
- 201000011510 cancer Diseases 0.000 description 5
- 230000001413 cellular effect Effects 0.000 description 5
- 238000012937 correction Methods 0.000 description 5
- 238000002474 experimental method Methods 0.000 description 5
- 239000012530 fluid Substances 0.000 description 5
- 230000005714 functional activity Effects 0.000 description 5
- 238000007306 functionalization reaction Methods 0.000 description 5
- 230000000521 hyperimmunizing effect Effects 0.000 description 5
- 239000003112 inhibitor Substances 0.000 description 5
- 230000003834 intracellular effect Effects 0.000 description 5
- 108020004999 messenger RNA Proteins 0.000 description 5
- 210000004160 naive b lymphocyte Anatomy 0.000 description 5
- 238000007481 next generation sequencing Methods 0.000 description 5
- 150000003384 small molecules Chemical class 0.000 description 5
- 238000012916 structural analysis Methods 0.000 description 5
- 238000012546 transfer Methods 0.000 description 5
- 238000013519 translation Methods 0.000 description 5
- 238000005406 washing Methods 0.000 description 5
- QGZKDVFQNNGYKY-UHFFFAOYSA-N Ammonia Chemical compound N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 4
- 241000283690 Bos taurus Species 0.000 description 4
- 241000282836 Camelus dromedarius Species 0.000 description 4
- SUZLHDUTVMZSEV-UHFFFAOYSA-N Deoxycoleonol Natural products C12C(=O)CC(C)(C=C)OC2(C)C(OC(=O)C)C(O)C2C1(C)C(O)CCC2(C)C SUZLHDUTVMZSEV-UHFFFAOYSA-N 0.000 description 4
- 241000196324 Embryophyta Species 0.000 description 4
- 241000282326 Felis catus Species 0.000 description 4
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 4
- 108010043121 Green Fluorescent Proteins Proteins 0.000 description 4
- 102000004144 Green Fluorescent Proteins Human genes 0.000 description 4
- 101000998950 Homo sapiens Immunoglobulin heavy variable 1-18 Proteins 0.000 description 4
- 101000839781 Homo sapiens Immunoglobulin heavy variable 4-59 Proteins 0.000 description 4
- 101000989076 Homo sapiens Immunoglobulin heavy variable 4-61 Proteins 0.000 description 4
- 101001047617 Homo sapiens Immunoglobulin kappa variable 3-11 Proteins 0.000 description 4
- 102100036884 Immunoglobulin heavy variable 1-18 Human genes 0.000 description 4
- 102100028405 Immunoglobulin heavy variable 4-59 Human genes 0.000 description 4
- 102100029419 Immunoglobulin heavy variable 4-61 Human genes 0.000 description 4
- 102100022955 Immunoglobulin kappa variable 3-11 Human genes 0.000 description 4
- 108700011259 MicroRNAs Proteins 0.000 description 4
- 241000699666 Mus <mouse, genus> Species 0.000 description 4
- 241000699670 Mus sp. Species 0.000 description 4
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 4
- 238000012300 Sequence Analysis Methods 0.000 description 4
- 230000008848 allosteric regulation Effects 0.000 description 4
- 239000003795 chemical substances by application Substances 0.000 description 4
- OHCQJHSOBUTRHG-UHFFFAOYSA-N colforsin Natural products OC12C(=O)CC(C)(C=C)OC1(C)C(OC(=O)C)C(O)C1C2(C)C(O)CCC1(C)C OHCQJHSOBUTRHG-UHFFFAOYSA-N 0.000 description 4
- 238000013500 data storage Methods 0.000 description 4
- 238000010586 diagram Methods 0.000 description 4
- 238000009826 distribution Methods 0.000 description 4
- 239000005090 green fluorescent protein Substances 0.000 description 4
- 239000000833 heterodimer Substances 0.000 description 4
- 230000002163 immunogen Effects 0.000 description 4
- 230000000670 limiting effect Effects 0.000 description 4
- 210000001806 memory b lymphocyte Anatomy 0.000 description 4
- 239000002679 microRNA Substances 0.000 description 4
- 238000002515 oligonucleotide synthesis Methods 0.000 description 4
- 230000037361 pathway Effects 0.000 description 4
- 230000000144 pharmacologic effect Effects 0.000 description 4
- 239000013641 positive control Substances 0.000 description 4
- 238000003908 quality control method Methods 0.000 description 4
- 238000007789 sealing Methods 0.000 description 4
- 239000000243 solution Substances 0.000 description 4
- 238000005987 sulfurization reaction Methods 0.000 description 4
- 238000001308 synthesis method Methods 0.000 description 4
- 230000002194 synthesizing effect Effects 0.000 description 4
- QKDAMFXBOUOVMF-UHFFFAOYSA-N 4-hydroxy-n-(3-triethoxysilylpropyl)butanamide Chemical compound CCO[Si](OCC)(OCC)CCCNC(=O)CCCO QKDAMFXBOUOVMF-UHFFFAOYSA-N 0.000 description 3
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 3
- WFDIJRYMOXRFFG-UHFFFAOYSA-N Acetic anhydride Chemical compound CC(=O)OC(C)=O WFDIJRYMOXRFFG-UHFFFAOYSA-N 0.000 description 3
- 244000303258 Annona diversifolia Species 0.000 description 3
- 235000002198 Annona diversifolia Nutrition 0.000 description 3
- 108020004635 Complementary DNA Proteins 0.000 description 3
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 3
- 238000002965 ELISA Methods 0.000 description 3
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 3
- 241000287828 Gallus gallus Species 0.000 description 3
- 241000238631 Hexapoda Species 0.000 description 3
- 101001037141 Homo sapiens Immunoglobulin heavy variable 3-21 Proteins 0.000 description 3
- 101001138130 Homo sapiens Immunoglobulin kappa variable 1-9 Proteins 0.000 description 3
- 101001047619 Homo sapiens Immunoglobulin kappa variable 3-20 Proteins 0.000 description 3
- 101000604674 Homo sapiens Immunoglobulin kappa variable 4-1 Proteins 0.000 description 3
- 102100040217 Immunoglobulin heavy variable 3-21 Human genes 0.000 description 3
- 102100020770 Immunoglobulin kappa variable 1-9 Human genes 0.000 description 3
- 102100022964 Immunoglobulin kappa variable 3-20 Human genes 0.000 description 3
- 102100038198 Immunoglobulin kappa variable 4-1 Human genes 0.000 description 3
- 101150008942 J gene Proteins 0.000 description 3
- 240000007594 Oryza sativa Species 0.000 description 3
- 235000007164 Oryza sativa Nutrition 0.000 description 3
- 108700008625 Reporter Genes Proteins 0.000 description 3
- 108091027967 Small hairpin RNA Proteins 0.000 description 3
- 108020004459 Small interfering RNA Proteins 0.000 description 3
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 3
- 230000003044 adaptive effect Effects 0.000 description 3
- 230000001270 agonistic effect Effects 0.000 description 3
- 238000013459 approach Methods 0.000 description 3
- 238000010804 cDNA synthesis Methods 0.000 description 3
- 230000000295 complement effect Effects 0.000 description 3
- 239000002299 complementary DNA Substances 0.000 description 3
- 238000010511 deprotection reaction Methods 0.000 description 3
- 230000027832 depurination Effects 0.000 description 3
- 238000011161 development Methods 0.000 description 3
- 230000018109 developmental process Effects 0.000 description 3
- 108091006047 fluorescent proteins Proteins 0.000 description 3
- 102000034287 fluorescent proteins Human genes 0.000 description 3
- 239000011521 glass Substances 0.000 description 3
- 239000007788 liquid Substances 0.000 description 3
- 238000002703 mutagenesis Methods 0.000 description 3
- 231100000350 mutagenesis Toxicity 0.000 description 3
- 238000005457 optimization Methods 0.000 description 3
- 125000006239 protecting group Chemical group 0.000 description 3
- 230000002441 reversible effect Effects 0.000 description 3
- 235000009566 rice Nutrition 0.000 description 3
- 230000000638 stimulation Effects 0.000 description 3
- 238000012360 testing method Methods 0.000 description 3
- 238000009736 wetting Methods 0.000 description 3
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 2
- JUDOLRSMWHVKGX-UHFFFAOYSA-N 1,1-dioxo-1$l^{6},2-benzodithiol-3-one Chemical compound C1=CC=C2C(=O)SS(=O)(=O)C2=C1 JUDOLRSMWHVKGX-UHFFFAOYSA-N 0.000 description 2
- KJUGUADJHNHALS-UHFFFAOYSA-N 1H-tetrazole Chemical compound C=1N=NNN=1 KJUGUADJHNHALS-UHFFFAOYSA-N 0.000 description 2
- OISVCGZHLKNMSJ-UHFFFAOYSA-N 2,6-dimethylpyridine Chemical compound CC1=CC=CC(C)=N1 OISVCGZHLKNMSJ-UHFFFAOYSA-N 0.000 description 2
- FWBHETKCLVMNFS-UHFFFAOYSA-N 4',6-Diamino-2-phenylindol Chemical compound C1=CC(C(=N)N)=CC=C1C1=CC2=CC=C(C(N)=N)C=C2N1 FWBHETKCLVMNFS-UHFFFAOYSA-N 0.000 description 2
- 102000002260 Alkaline Phosphatase Human genes 0.000 description 2
- 108020004774 Alkaline Phosphatase Proteins 0.000 description 2
- 241000894006 Bacteria Species 0.000 description 2
- 108091032955 Bacterial small RNA Proteins 0.000 description 2
- 241000283707 Capra Species 0.000 description 2
- 208000024172 Cardiovascular disease Diseases 0.000 description 2
- 102000014914 Carrier Proteins Human genes 0.000 description 2
- 241000282693 Cercopithecidae Species 0.000 description 2
- 108010035563 Chloramphenicol O-acetyltransferase Proteins 0.000 description 2
- 241000251730 Chondrichthyes Species 0.000 description 2
- 108091026890 Coding region Proteins 0.000 description 2
- 108010066133 D-octopine dehydrogenase Proteins 0.000 description 2
- BWGNESOTFCXPMA-UHFFFAOYSA-N Dihydrogen disulfide Chemical compound SS BWGNESOTFCXPMA-UHFFFAOYSA-N 0.000 description 2
- 102000004190 Enzymes Human genes 0.000 description 2
- 108090000790 Enzymes Proteins 0.000 description 2
- 241000283086 Equidae Species 0.000 description 2
- 241000283074 Equus asinus Species 0.000 description 2
- 241000283073 Equus caballus Species 0.000 description 2
- 206010053487 Exposure to toxic agent Diseases 0.000 description 2
- 208000018522 Gastrointestinal disease Diseases 0.000 description 2
- 239000004471 Glycine Substances 0.000 description 2
- 241000282575 Gorilla Species 0.000 description 2
- NYHBQMYGNKIUIF-UUOKFMHZSA-N Guanosine Chemical group C1=NC=2C(=O)NC(N)=NC=2N1[C@@H]1O[C@H](CO)[C@@H](O)[C@H]1O NYHBQMYGNKIUIF-UUOKFMHZSA-N 0.000 description 2
- 241000282412 Homo Species 0.000 description 2
- 101000998947 Homo sapiens Immunoglobulin heavy variable 1-46 Proteins 0.000 description 2
- 101001037153 Homo sapiens Immunoglobulin heavy variable 3-7 Proteins 0.000 description 2
- 101000839687 Homo sapiens Immunoglobulin heavy variable 3-74 Proteins 0.000 description 2
- 101000839682 Homo sapiens Immunoglobulin heavy variable 4-34 Proteins 0.000 description 2
- 101000839679 Homo sapiens Immunoglobulin heavy variable 4-39 Proteins 0.000 description 2
- 101001054843 Homo sapiens Immunoglobulin lambda variable 1-40 Proteins 0.000 description 2
- 101001005360 Homo sapiens Immunoglobulin lambda variable 3-1 Proteins 0.000 description 2
- 102000009786 Immunoglobulin Constant Regions Human genes 0.000 description 2
- 108010009817 Immunoglobulin Constant Regions Proteins 0.000 description 2
- 108010091135 Immunoglobulin Fc Fragments Proteins 0.000 description 2
- 102000018071 Immunoglobulin Fc Fragments Human genes 0.000 description 2
- 102100036888 Immunoglobulin heavy variable 1-46 Human genes 0.000 description 2
- 102100040231 Immunoglobulin heavy variable 3-7 Human genes 0.000 description 2
- 102100028305 Immunoglobulin heavy variable 3-74 Human genes 0.000 description 2
- 102100028306 Immunoglobulin heavy variable 4-34 Human genes 0.000 description 2
- 102100028312 Immunoglobulin heavy variable 4-39 Human genes 0.000 description 2
- 102100026911 Immunoglobulin lambda variable 1-40 Human genes 0.000 description 2
- 102100025921 Immunoglobulin lambda variable 3-1 Human genes 0.000 description 2
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 2
- 108060001084 Luciferase Proteins 0.000 description 2
- 239000005089 Luciferase Substances 0.000 description 2
- 241000124008 Mammalia Species 0.000 description 2
- BAVYZALUXZFZLV-UHFFFAOYSA-N Methylamine Chemical compound NC BAVYZALUXZFZLV-UHFFFAOYSA-N 0.000 description 2
- 108091007491 NSP3 Papain-like protease domains Proteins 0.000 description 2
- 208000012902 Nervous system disease Diseases 0.000 description 2
- 208000025966 Neurological disease Diseases 0.000 description 2
- 238000012408 PCR amplification Methods 0.000 description 2
- 241000282579 Pan Species 0.000 description 2
- 241000282520 Papio Species 0.000 description 2
- 229930040373 Paraformaldehyde Natural products 0.000 description 2
- 241001494479 Pecora Species 0.000 description 2
- 239000004743 Polypropylene Substances 0.000 description 2
- 239000004793 Polystyrene Substances 0.000 description 2
- 241000282405 Pongo abelii Species 0.000 description 2
- 108010019477 S-adenosyl-L-methionine-dependent N-methyltransferase Proteins 0.000 description 2
- BLRPTPMANUNPDV-UHFFFAOYSA-N Silane Chemical compound [SiH4] BLRPTPMANUNPDV-UHFFFAOYSA-N 0.000 description 2
- 241000282887 Suidae Species 0.000 description 2
- 108091007498 Transmembrane domain 2 Proteins 0.000 description 2
- 102000004142 Trypsin Human genes 0.000 description 2
- 108090000631 Trypsin Proteins 0.000 description 2
- DRTQHJPVMGBUCF-XVFCMESISA-N Uridine Chemical compound O[C@@H]1[C@H](O)[C@@H](CO)O[C@H]1N1C(=O)NC(=O)C=C1 DRTQHJPVMGBUCF-XVFCMESISA-N 0.000 description 2
- 238000009825 accumulation Methods 0.000 description 2
- 239000012190 activator Substances 0.000 description 2
- 239000002318 adhesion promoter Substances 0.000 description 2
- 125000000539 amino acid group Chemical group 0.000 description 2
- 229910021529 ammonia Inorganic materials 0.000 description 2
- 230000003042 antagnostic effect Effects 0.000 description 2
- 230000001580 bacterial effect Effects 0.000 description 2
- 108091007497 betacoronavirus-specific marker domains Proteins 0.000 description 2
- 108091008324 binding proteins Proteins 0.000 description 2
- 230000011496 cAMP-mediated signaling Effects 0.000 description 2
- 238000000423 cell based assay Methods 0.000 description 2
- 238000003776 cleavage reaction Methods 0.000 description 2
- 239000011248 coating agent Substances 0.000 description 2
- 238000000576 coating method Methods 0.000 description 2
- 210000004748 cultured cell Anatomy 0.000 description 2
- 108010082025 cyan fluorescent protein Proteins 0.000 description 2
- OPTASPLRGRRNAP-UHFFFAOYSA-N cytosine Chemical compound NC=1C=CNC(=O)N=1 OPTASPLRGRRNAP-UHFFFAOYSA-N 0.000 description 2
- 230000007423 decrease Effects 0.000 description 2
- 230000003247 decreasing effect Effects 0.000 description 2
- 238000001514 detection method Methods 0.000 description 2
- 238000006642 detritylation reaction Methods 0.000 description 2
- JXTHNDFMNIQAHM-UHFFFAOYSA-N dichloroacetic acid Chemical compound OC(=O)C(Cl)Cl JXTHNDFMNIQAHM-UHFFFAOYSA-N 0.000 description 2
- 239000000539 dimer Substances 0.000 description 2
- 239000004205 dimethyl polysiloxane Substances 0.000 description 2
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 2
- 229940079593 drug Drugs 0.000 description 2
- 238000009509 drug development Methods 0.000 description 2
- 238000001035 drying Methods 0.000 description 2
- 238000010228 ex vivo assay Methods 0.000 description 2
- 238000000799 fluorescence microscopy Methods 0.000 description 2
- 238000007672 fourth generation sequencing Methods 0.000 description 2
- UYTPUPDQBNUYGX-UHFFFAOYSA-N guanine Chemical compound O=C1NC(N)=NC2=C1N=CN2 UYTPUPDQBNUYGX-UHFFFAOYSA-N 0.000 description 2
- HNDVDQJCIGZPNO-UHFFFAOYSA-N histidine Natural products OC(=O)C(N)CC1=CN=CN1 HNDVDQJCIGZPNO-UHFFFAOYSA-N 0.000 description 2
- 238000009396 hybridization Methods 0.000 description 2
- 238000000338 in vitro Methods 0.000 description 2
- 238000000099 in vitro assay Methods 0.000 description 2
- 238000005462 in vivo assay Methods 0.000 description 2
- 238000011065 in-situ storage Methods 0.000 description 2
- 238000010348 incorporation Methods 0.000 description 2
- 238000011534 incubation Methods 0.000 description 2
- 230000006698 induction Effects 0.000 description 2
- 208000027866 inflammatory disease Diseases 0.000 description 2
- 150000002500 ions Chemical class 0.000 description 2
- 238000002898 library design Methods 0.000 description 2
- 230000004807 localization Effects 0.000 description 2
- 235000019689 luncheon sausage Nutrition 0.000 description 2
- 208000030159 metabolic disease Diseases 0.000 description 2
- 229910052751 metal Inorganic materials 0.000 description 2
- 239000002184 metal Substances 0.000 description 2
- 150000002739 metals Chemical class 0.000 description 2
- 238000013508 migration Methods 0.000 description 2
- 230000005012 migration Effects 0.000 description 2
- 230000035772 mutation Effects 0.000 description 2
- 108010000785 non-ribosomal peptide synthase Proteins 0.000 description 2
- 238000001668 nucleic acid synthesis Methods 0.000 description 2
- 150000003833 nucleoside derivatives Chemical class 0.000 description 2
- 230000001590 oxidative effect Effects 0.000 description 2
- 229920002866 paraformaldehyde Polymers 0.000 description 2
- 239000002245 particle Substances 0.000 description 2
- 239000002953 phosphate buffered saline Substances 0.000 description 2
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Chemical compound [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 description 2
- 229920000435 poly(dimethylsiloxane) Polymers 0.000 description 2
- 229920002704 polyhistidine Polymers 0.000 description 2
- 229930001118 polyketide hybrid Natural products 0.000 description 2
- 125000003308 polyketide hybrid group Chemical group 0.000 description 2
- 229920000642 polymer Polymers 0.000 description 2
- 229920001155 polypropylene Polymers 0.000 description 2
- 229920002223 polystyrene Polymers 0.000 description 2
- 238000002360 preparation method Methods 0.000 description 2
- 230000002265 prevention Effects 0.000 description 2
- 230000002062 proliferating effect Effects 0.000 description 2
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 2
- 238000012175 pyrosequencing Methods 0.000 description 2
- 230000002285 radioactive effect Effects 0.000 description 2
- 108010054624 red fluorescent protein Proteins 0.000 description 2
- 238000011160 research Methods 0.000 description 2
- 208000023504 respiratory system disease Diseases 0.000 description 2
- 239000000523 sample Substances 0.000 description 2
- 230000007017 scission Effects 0.000 description 2
- 239000004065 semiconductor Substances 0.000 description 2
- 238000000926 separation method Methods 0.000 description 2
- 238000007841 sequencing by ligation Methods 0.000 description 2
- 229910000077 silane Inorganic materials 0.000 description 2
- 239000000377 silicon dioxide Substances 0.000 description 2
- 235000012239 silicon dioxide Nutrition 0.000 description 2
- 238000006467 substitution reaction Methods 0.000 description 2
- 230000008685 targeting Effects 0.000 description 2
- CIHOLLKRGTVIJN-UHFFFAOYSA-N tert‐butyl hydroperoxide Chemical compound CC(C)(C)OO CIHOLLKRGTVIJN-UHFFFAOYSA-N 0.000 description 2
- 229940124597 therapeutic agent Drugs 0.000 description 2
- RWQNBRDOKXIBIV-UHFFFAOYSA-N thymine Chemical compound CC1=CNC(=O)NC1=O RWQNBRDOKXIBIV-UHFFFAOYSA-N 0.000 description 2
- 238000001890 transfection Methods 0.000 description 2
- 239000012588 trypsin Substances 0.000 description 2
- 230000003612 virological effect Effects 0.000 description 2
- 108091005957 yellow fluorescent proteins Proteins 0.000 description 2
- GBBJBUGPGFNISJ-YDQXZVTASA-N (4as,7r,8as)-9,9-dimethyltetrahydro-4h-4a,7-methanobenzo[c][1,2]oxazireno[2,3-b]isothiazole 3,3-dioxide Chemical compound C1S(=O)(=O)N2O[C@@]32C[C@@H]2C(C)(C)[C@]13CC2 GBBJBUGPGFNISJ-YDQXZVTASA-N 0.000 description 1
- MCTWTZJPVLRJOU-UHFFFAOYSA-N 1-methyl-1H-imidazole Chemical compound CN1C=CN=C1 MCTWTZJPVLRJOU-UHFFFAOYSA-N 0.000 description 1
- WUHZCNHGBOHDKN-UHFFFAOYSA-N 11-triethoxysilylundecyl acetate Chemical compound CCO[Si](OCC)(OCC)CCCCCCCCCCCOC(C)=O WUHZCNHGBOHDKN-UHFFFAOYSA-N 0.000 description 1
- GVZJRBAUSGYWJI-UHFFFAOYSA-N 2,5-bis(3-dodecylthiophen-2-yl)thiophene Chemical compound C1=CSC(C=2SC(=CC=2)C2=C(C=CS2)CCCCCCCCCCCC)=C1CCCCCCCCCCCC GVZJRBAUSGYWJI-UHFFFAOYSA-N 0.000 description 1
- FOYWCEUVVIHJKD-UHFFFAOYSA-N 2-methyl-5-(1h-pyrazol-5-yl)pyridine Chemical compound C1=NC(C)=CC=C1C1=CC=NN1 FOYWCEUVVIHJKD-UHFFFAOYSA-N 0.000 description 1
- 125000002103 4,4'-dimethoxytriphenylmethyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C(*)(C1=C([H])C([H])=C(OC([H])([H])[H])C([H])=C1[H])C1=C([H])C([H])=C(OC([H])([H])[H])C([H])=C1[H] 0.000 description 1
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical compound C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 description 1
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 1
- 108010000700 Acetolactate synthase Proteins 0.000 description 1
- 241000251468 Actinopterygii Species 0.000 description 1
- 229930024421 Adenine Natural products 0.000 description 1
- GFFGJBXGBJISGV-UHFFFAOYSA-N Adenine Chemical compound NC1=NC=NC2=C1N=CN2 GFFGJBXGBJISGV-UHFFFAOYSA-N 0.000 description 1
- 229920000936 Agarose Polymers 0.000 description 1
- 241001504639 Alcedo atthis Species 0.000 description 1
- 102000016904 Armadillo Domain Proteins Human genes 0.000 description 1
- 108010014223 Armadillo Domain Proteins Proteins 0.000 description 1
- 102100026189 Beta-galactosidase Human genes 0.000 description 1
- 241000167854 Bourreria succulenta Species 0.000 description 1
- 102100027207 CD27 antigen Human genes 0.000 description 1
- 108090000994 Catalytic RNA Proteins 0.000 description 1
- 102000053642 Catalytic RNA Human genes 0.000 description 1
- 108091005944 Cerulean Proteins 0.000 description 1
- 241000252506 Characiformes Species 0.000 description 1
- 108091005960 Citrine Proteins 0.000 description 1
- 241000699800 Cricetinae Species 0.000 description 1
- 241000699802 Cricetulus griseus Species 0.000 description 1
- MIKUYHXYGGJMLM-GIMIYPNGSA-N Crotonoside Natural products C1=NC2=C(N)NC(=O)N=C2N1[C@H]1O[C@@H](CO)[C@H](O)[C@@H]1O MIKUYHXYGGJMLM-GIMIYPNGSA-N 0.000 description 1
- 108010025905 Cystine-Knot Miniproteins Proteins 0.000 description 1
- 101150097493 D gene Proteins 0.000 description 1
- NYHBQMYGNKIUIF-UHFFFAOYSA-N D-guanosine Natural products C1=2NC(N)=NC(=O)C=2N=CN1C1OC(CO)C(O)C1O NYHBQMYGNKIUIF-UHFFFAOYSA-N 0.000 description 1
- 102000053602 DNA Human genes 0.000 description 1
- 230000006820 DNA synthesis Effects 0.000 description 1
- 241000289632 Dasypodidae Species 0.000 description 1
- 108700022150 Designed Ankyrin Repeat Proteins Proteins 0.000 description 1
- 229920002307 Dextran Polymers 0.000 description 1
- 241000255925 Diptera Species 0.000 description 1
- 108091005942 ECFP Proteins 0.000 description 1
- 208000017701 Endocrine disease Diseases 0.000 description 1
- 241000206602 Eukaryota Species 0.000 description 1
- 108700024394 Exon Proteins 0.000 description 1
- 241000233866 Fungi Species 0.000 description 1
- 102000006395 Globulins Human genes 0.000 description 1
- 108010044091 Globulins Proteins 0.000 description 1
- 102000053187 Glucuronidase Human genes 0.000 description 1
- 108010060309 Glucuronidase Proteins 0.000 description 1
- HVLSXIKZNLPZJJ-TXZCQADKSA-N HA peptide Chemical compound C([C@@H](C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](C(C)C)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N[C@@H](C)C(O)=O)NC(=O)[C@H]1N(CCC1)C(=O)[C@@H](N)CC=1C=CC(O)=CC=1)C1=CC=C(O)C=C1 HVLSXIKZNLPZJJ-TXZCQADKSA-N 0.000 description 1
- 101000914511 Homo sapiens CD27 antigen Proteins 0.000 description 1
- 101001037151 Homo sapiens Immunoglobulin heavy variable 2-70 Proteins 0.000 description 1
- 101001037136 Homo sapiens Immunoglobulin heavy variable 3-15 Proteins 0.000 description 1
- 101000839662 Homo sapiens Immunoglobulin heavy variable 3-48 Proteins 0.000 description 1
- 101000839660 Homo sapiens Immunoglobulin heavy variable 3-53 Proteins 0.000 description 1
- 101000839658 Homo sapiens Immunoglobulin heavy variable 3-66 Proteins 0.000 description 1
- 101000839659 Homo sapiens Immunoglobulin heavy variable 3-72 Proteins 0.000 description 1
- 101000839657 Homo sapiens Immunoglobulin heavy variable 3-73 Proteins 0.000 description 1
- 101000989062 Homo sapiens Immunoglobulin heavy variable 5-51 Proteins 0.000 description 1
- 101001138127 Homo sapiens Immunoglobulin kappa variable 1-13 Proteins 0.000 description 1
- 101001138133 Homo sapiens Immunoglobulin kappa variable 1-5 Proteins 0.000 description 1
- 101001054838 Homo sapiens Immunoglobulin lambda variable 1-44 Proteins 0.000 description 1
- 101001005365 Homo sapiens Immunoglobulin lambda variable 3-21 Proteins 0.000 description 1
- 101000878605 Homo sapiens Low affinity immunoglobulin epsilon Fc receptor Proteins 0.000 description 1
- 101000831007 Homo sapiens T-cell immunoreceptor with Ig and ITIM domains Proteins 0.000 description 1
- 108010001336 Horseradish Peroxidase Proteins 0.000 description 1
- 208000013016 Hypoglycemia Diseases 0.000 description 1
- 102100040233 Immunoglobulin heavy variable 2-70 Human genes 0.000 description 1
- 102100040224 Immunoglobulin heavy variable 3-15 Human genes 0.000 description 1
- 102100028320 Immunoglobulin heavy variable 3-48 Human genes 0.000 description 1
- 102100028317 Immunoglobulin heavy variable 3-53 Human genes 0.000 description 1
- 102100027821 Immunoglobulin heavy variable 3-66 Human genes 0.000 description 1
- 102100027820 Immunoglobulin heavy variable 3-72 Human genes 0.000 description 1
- 102100027822 Immunoglobulin heavy variable 3-73 Human genes 0.000 description 1
- 102100029414 Immunoglobulin heavy variable 5-51 Human genes 0.000 description 1
- 102100020772 Immunoglobulin kappa variable 1-13 Human genes 0.000 description 1
- 102100020769 Immunoglobulin kappa variable 1-5 Human genes 0.000 description 1
- 102100026921 Immunoglobulin lambda variable 1-44 Human genes 0.000 description 1
- 102100025934 Immunoglobulin lambda variable 3-21 Human genes 0.000 description 1
- 108091029795 Intergenic region Proteins 0.000 description 1
- 108091092195 Intron Proteins 0.000 description 1
- 102100038007 Low affinity immunoglobulin epsilon Fc receptor Human genes 0.000 description 1
- 241001465754 Metazoa Species 0.000 description 1
- 241001529936 Murinae Species 0.000 description 1
- KWYHDKDOAIKMQN-UHFFFAOYSA-N N,N,N',N'-tetramethylethylenediamine Chemical compound CN(C)CCN(C)C KWYHDKDOAIKMQN-UHFFFAOYSA-N 0.000 description 1
- 239000000020 Nitrocellulose Substances 0.000 description 1
- 108091092724 Noncoding DNA Proteins 0.000 description 1
- 108020004711 Nucleic Acid Probes Proteins 0.000 description 1
- 108091005461 Nucleic proteins Chemical group 0.000 description 1
- 239000004677 Nylon Substances 0.000 description 1
- NWSOKOJWKWNSAF-UHFFFAOYSA-N O=C(Sc1nnn[nH]1)c1ccccc1 Chemical compound O=C(Sc1nnn[nH]1)c1ccccc1 NWSOKOJWKWNSAF-UHFFFAOYSA-N 0.000 description 1
- 108091034117 Oligonucleotide Proteins 0.000 description 1
- 239000012807 PCR reagent Substances 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- 208000002193 Pain Diseases 0.000 description 1
- 108010067902 Peptide Library Proteins 0.000 description 1
- 241000208474 Protea Species 0.000 description 1
- 108091030071 RNAI Proteins 0.000 description 1
- 240000004808 Saccharomyces cerevisiae Species 0.000 description 1
- 229910052581 Si3N4 Inorganic materials 0.000 description 1
- 108020003224 Small Nucleolar RNA Proteins 0.000 description 1
- 102000042773 Small Nucleolar RNA Human genes 0.000 description 1
- 241000251131 Sphyrna Species 0.000 description 1
- ZSJLQEPLLKMAKR-UHFFFAOYSA-N Streptozotocin Natural products O=NN(C)C(=O)NC1C(O)OC(CO)C(O)C1O ZSJLQEPLLKMAKR-UHFFFAOYSA-N 0.000 description 1
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 1
- 102100024834 T-cell immunoreceptor with Ig and ITIM domains Human genes 0.000 description 1
- 108091023040 Transcription factor Proteins 0.000 description 1
- 102000040945 Transcription factor Human genes 0.000 description 1
- 108020004566 Transfer RNA Proteins 0.000 description 1
- XLYOFNOQVPJJNP-PWCQTSIFSA-N Tritiated water Chemical compound [3H]O[3H] XLYOFNOQVPJJNP-PWCQTSIFSA-N 0.000 description 1
- 230000001133 acceleration Effects 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 239000013543 active substance Substances 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 230000000996 additive effect Effects 0.000 description 1
- 229960000643 adenine Drugs 0.000 description 1
- 230000032683 aging Effects 0.000 description 1
- 230000008850 allosteric inhibition Effects 0.000 description 1
- 230000004075 alteration Effects 0.000 description 1
- HOPRXXXSABQWAV-UHFFFAOYSA-N anhydrous collidine Natural products CC1=CC=NC(C)=C1C HOPRXXXSABQWAV-UHFFFAOYSA-N 0.000 description 1
- 210000004102 animal cell Anatomy 0.000 description 1
- 238000010171 animal model Methods 0.000 description 1
- 230000010056 antibody-dependent cellular cytotoxicity Effects 0.000 description 1
- 230000006907 apoptotic process Effects 0.000 description 1
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 1
- 230000001363 autoimmune Effects 0.000 description 1
- 239000011324 bead Substances 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 108010005774 beta-Galactosidase Proteins 0.000 description 1
- DRTQHJPVMGBUCF-PSQAKQOGSA-N beta-L-uridine Natural products O[C@H]1[C@@H](O)[C@H](CO)O[C@@H]1N1C(=O)NC(=O)C=C1 DRTQHJPVMGBUCF-PSQAKQOGSA-N 0.000 description 1
- 125000002619 bicyclic group Chemical group 0.000 description 1
- 239000011230 binding agent Substances 0.000 description 1
- 238000005842 biochemical reaction Methods 0.000 description 1
- 230000003115 biocidal effect Effects 0.000 description 1
- 230000004071 biological effect Effects 0.000 description 1
- 230000008236 biological pathway Effects 0.000 description 1
- 230000033228 biological regulation Effects 0.000 description 1
- 108091005948 blue fluorescent proteins Proteins 0.000 description 1
- 239000006227 byproduct Substances 0.000 description 1
- 230000030833 cell death Effects 0.000 description 1
- 230000005754 cellular signaling Effects 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 235000019693 cherries Nutrition 0.000 description 1
- 210000004978 chinese hamster ovary cell Anatomy 0.000 description 1
- 231100000313 clinical toxicology Toxicity 0.000 description 1
- UTBIMNXEDGNJFE-UHFFFAOYSA-N collidine Natural products CC1=CC=C(C)C(C)=N1 UTBIMNXEDGNJFE-UHFFFAOYSA-N 0.000 description 1
- 238000002742 combinatorial mutagenesis Methods 0.000 description 1
- 150000001875 compounds Chemical class 0.000 description 1
- 238000010205 computational analysis Methods 0.000 description 1
- 239000004020 conductor Substances 0.000 description 1
- 239000000470 constituent Substances 0.000 description 1
- 238000010276 construction Methods 0.000 description 1
- 238000012864 cross contamination Methods 0.000 description 1
- 230000001351 cycling effect Effects 0.000 description 1
- 229940104302 cytosine Drugs 0.000 description 1
- 230000006378 damage Effects 0.000 description 1
- 238000013499 data model Methods 0.000 description 1
- BAAAEEDPKUHLID-UHFFFAOYSA-N decyl(triethoxy)silane Chemical compound CCCCCCCCCC[Si](OCC)(OCC)OCC BAAAEEDPKUHLID-UHFFFAOYSA-N 0.000 description 1
- 230000007547 defect Effects 0.000 description 1
- 230000002950 deficient Effects 0.000 description 1
- 238000001212 derivatisation Methods 0.000 description 1
- 229960005215 dichloroacetic acid Drugs 0.000 description 1
- HPYNZHMRTTWQTB-UHFFFAOYSA-N dimethylpyridine Natural products CC1=CC=CN=C1C HPYNZHMRTTWQTB-UHFFFAOYSA-N 0.000 description 1
- 208000037765 diseases and disorders Diseases 0.000 description 1
- KPUWHANPEXNPJT-UHFFFAOYSA-N disiloxane Chemical class [SiH3]O[SiH3] KPUWHANPEXNPJT-UHFFFAOYSA-N 0.000 description 1
- 231100000673 dose–response relationship Toxicity 0.000 description 1
- 238000007876 drug discovery Methods 0.000 description 1
- 239000012636 effector Substances 0.000 description 1
- 230000005684 electric field Effects 0.000 description 1
- 208000030172 endocrine system disease Diseases 0.000 description 1
- 239000003623 enhancer Substances 0.000 description 1
- 230000002708 enhancing effect Effects 0.000 description 1
- 238000001976 enzyme digestion Methods 0.000 description 1
- 238000005530 etching Methods 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 230000000763 evoking effect Effects 0.000 description 1
- 238000011049 filling Methods 0.000 description 1
- 238000000684 flow cytometry Methods 0.000 description 1
- 238000001506 fluorescence spectroscopy Methods 0.000 description 1
- 238000013467 fragmentation Methods 0.000 description 1
- 238000006062 fragmentation reaction Methods 0.000 description 1
- 238000010230 functional analysis Methods 0.000 description 1
- 125000000524 functional group Chemical group 0.000 description 1
- 230000002538 fungal effect Effects 0.000 description 1
- 239000005350 fused silica glass Substances 0.000 description 1
- 239000007789 gas Substances 0.000 description 1
- 239000000499 gel Substances 0.000 description 1
- 230000009368 gene silencing by RNA Effects 0.000 description 1
- 102000054767 gene variant Human genes 0.000 description 1
- 230000002068 genetic effect Effects 0.000 description 1
- 210000004602 germ cell Anatomy 0.000 description 1
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 1
- 229910052737 gold Inorganic materials 0.000 description 1
- 239000010931 gold Substances 0.000 description 1
- 230000012010 growth Effects 0.000 description 1
- 229940029575 guanosine Drugs 0.000 description 1
- 230000002489 hematologic effect Effects 0.000 description 1
- 238000012165 high-throughput sequencing Methods 0.000 description 1
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 1
- 230000002218 hypoglycaemic effect Effects 0.000 description 1
- 238000007654 immersion Methods 0.000 description 1
- 230000001900 immune effect Effects 0.000 description 1
- 238000010166 immunofluorescence Methods 0.000 description 1
- 238000000126 in silico method Methods 0.000 description 1
- 238000001727 in vivo Methods 0.000 description 1
- 229910052738 indium Inorganic materials 0.000 description 1
- 230000001939 inductive effect Effects 0.000 description 1
- 230000002401 inhibitory effect Effects 0.000 description 1
- 230000005764 inhibitory process Effects 0.000 description 1
- 238000003780 insertion Methods 0.000 description 1
- 230000037431 insertion Effects 0.000 description 1
- 230000010354 integration Effects 0.000 description 1
- 238000011835 investigation Methods 0.000 description 1
- 239000011630 iodine Substances 0.000 description 1
- 229910052740 iodine Inorganic materials 0.000 description 1
- 229940059904 light mineral oil Drugs 0.000 description 1
- 239000002502 liposome Substances 0.000 description 1
- 230000033001 locomotion Effects 0.000 description 1
- 230000007774 longterm Effects 0.000 description 1
- 238000013178 mathematical model Methods 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 230000002503 metabolic effect Effects 0.000 description 1
- 229910044991 metal oxide Inorganic materials 0.000 description 1
- 150000004706 metal oxides Chemical class 0.000 description 1
- 238000001823 molecular biology technique Methods 0.000 description 1
- 229920001220 nitrocellulos Polymers 0.000 description 1
- 108091027963 non-coding RNA Proteins 0.000 description 1
- 230000009871 nonspecific binding Effects 0.000 description 1
- 239000002853 nucleic acid probe Substances 0.000 description 1
- 125000003835 nucleoside group Chemical group 0.000 description 1
- 229920001778 nylon Polymers 0.000 description 1
- 239000012044 organic layer Substances 0.000 description 1
- 210000001672 ovary Anatomy 0.000 description 1
- 239000007800 oxidant agent Substances 0.000 description 1
- 229910052760 oxygen Inorganic materials 0.000 description 1
- 239000001301 oxygen Substances 0.000 description 1
- 230000036961 partial effect Effects 0.000 description 1
- 230000008506 pathogenesis Effects 0.000 description 1
- 230000007170 pathology Effects 0.000 description 1
- 238000000059 patterning Methods 0.000 description 1
- 230000002085 persistent effect Effects 0.000 description 1
- 238000002823 phage display Methods 0.000 description 1
- 239000008194 pharmaceutical composition Substances 0.000 description 1
- 239000010452 phosphate Substances 0.000 description 1
- 150000004713 phosphodiesters Chemical class 0.000 description 1
- 238000000206 photolithography Methods 0.000 description 1
- 229920002120 photoresistant polymer Polymers 0.000 description 1
- 230000000704 physical effect Effects 0.000 description 1
- 238000001020 plasma etching Methods 0.000 description 1
- 239000013612 plasmid Substances 0.000 description 1
- 239000004033 plastic Substances 0.000 description 1
- 229920003023 plastic Polymers 0.000 description 1
- 229910052697 platinum Inorganic materials 0.000 description 1
- 229920002401 polyacrylamide Polymers 0.000 description 1
- 239000004417 polycarbonate Substances 0.000 description 1
- 229920000515 polycarbonate Polymers 0.000 description 1
- 238000006116 polymerization reaction Methods 0.000 description 1
- 239000004810 polytetrafluoroethylene Substances 0.000 description 1
- 229920001343 polytetrafluoroethylene Polymers 0.000 description 1
- 231100001271 preclinical toxicology Toxicity 0.000 description 1
- 239000002243 precursor Substances 0.000 description 1
- 230000009465 prokaryotic expression Effects 0.000 description 1
- 230000035755 proliferation Effects 0.000 description 1
- 230000012846 protein folding Effects 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 150000003254 radicals Chemical class 0.000 description 1
- 238000010188 recombinant method Methods 0.000 description 1
- 230000006798 recombination Effects 0.000 description 1
- 238000005215 recombination Methods 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 230000012385 regulation of binding Effects 0.000 description 1
- 230000001105 regulatory effect Effects 0.000 description 1
- 230000003252 repetitive effect Effects 0.000 description 1
- 230000033458 reproduction Effects 0.000 description 1
- 208000017443 reproductive system disease Diseases 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 108091008146 restriction endonucleases Proteins 0.000 description 1
- 238000010839 reverse transcription Methods 0.000 description 1
- 238000012552 review Methods 0.000 description 1
- 108020004418 ribosomal RNA Proteins 0.000 description 1
- 108091092562 ribozyme Proteins 0.000 description 1
- 238000005070 sampling Methods 0.000 description 1
- 238000007480 sanger sequencing Methods 0.000 description 1
- 238000001338 self-assembly Methods 0.000 description 1
- 230000011664 signaling Effects 0.000 description 1
- 238000002444 silanisation Methods 0.000 description 1
- HQVNEWCFYHHQES-UHFFFAOYSA-N silicon nitride Chemical compound N12[Si]34N5[Si]62N3[Si]51N64 HQVNEWCFYHHQES-UHFFFAOYSA-N 0.000 description 1
- 238000000527 sonication Methods 0.000 description 1
- 241000894007 species Species 0.000 description 1
- ZSJLQEPLLKMAKR-GKHCUFPYSA-N streptozocin Chemical compound O=NN(C)C(=O)N[C@H]1[C@@H](O)O[C@H](CO)[C@@H](O)[C@@H]1O ZSJLQEPLLKMAKR-GKHCUFPYSA-N 0.000 description 1
- 229960001052 streptozocin Drugs 0.000 description 1
- 238000005486 sulfidation Methods 0.000 description 1
- 229910052717 sulfur Inorganic materials 0.000 description 1
- 239000011593 sulfur Substances 0.000 description 1
- 239000002344 surface layer Substances 0.000 description 1
- 230000003746 surface roughness Effects 0.000 description 1
- GFYHSKONPJXCDE-UHFFFAOYSA-N sym-collidine Natural products CC1=CN=C(C)C(C)=C1 GFYHSKONPJXCDE-UHFFFAOYSA-N 0.000 description 1
- 238000010189 synthetic method Methods 0.000 description 1
- 150000003536 tetrazoles Chemical class 0.000 description 1
- 229940126585 therapeutic drug Drugs 0.000 description 1
- RYYWUUFWQRZTIU-UHFFFAOYSA-K thiophosphate Chemical compound [O-]P([O-])([O-])=S RYYWUUFWQRZTIU-UHFFFAOYSA-K 0.000 description 1
- 229940113082 thymine Drugs 0.000 description 1
- 210000001519 tissue Anatomy 0.000 description 1
- 231100000419 toxicity Toxicity 0.000 description 1
- 230000001988 toxicity Effects 0.000 description 1
- AVXLXFZNRNUCRP-UHFFFAOYSA-N trichloro(1,1,2,2,3,3,4,4,5,5,6,6,7,7,8,8,8-heptadecafluorooctyl)silane Chemical compound FC(F)(F)C(F)(F)C(F)(F)C(F)(F)C(F)(F)C(F)(F)C(F)(F)C(F)(F)[Si](Cl)(Cl)Cl AVXLXFZNRNUCRP-UHFFFAOYSA-N 0.000 description 1
- YNJBWRMUSHSURL-UHFFFAOYSA-N trichloroacetic acid Chemical compound OC(=O)C(Cl)(Cl)Cl YNJBWRMUSHSURL-UHFFFAOYSA-N 0.000 description 1
- 239000010981 turquoise Substances 0.000 description 1
- 235000002374 tyrosine Nutrition 0.000 description 1
- 150000003668 tyrosines Chemical class 0.000 description 1
- DRTQHJPVMGBUCF-UHFFFAOYSA-N uracil arabinoside Natural products OC1C(O)C(CO)OC1N1C(=O)NC(=O)C=C1 DRTQHJPVMGBUCF-UHFFFAOYSA-N 0.000 description 1
- 229940045145 uridine Drugs 0.000 description 1
- 238000001291 vacuum drying Methods 0.000 description 1
- 238000007740 vapor deposition Methods 0.000 description 1
- 239000006200 vaporizer Substances 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C40—COMBINATORIAL TECHNOLOGY
- C40B—COMBINATORIAL CHEMISTRY; LIBRARIES, e.g. CHEMICAL LIBRARIES
- C40B40/00—Libraries per se, e.g. arrays, mixtures
- C40B40/04—Libraries containing only organic compounds
- C40B40/10—Libraries containing peptides or polypeptides, or derivatives thereof
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2869—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against hormone receptors
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/10—Processes for the isolation, preparation or purification of DNA or RNA
- C12N15/1034—Isolating an individual clone by screening libraries
- C12N15/1044—Preparation or screening of libraries displayed on scaffold proteins
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/06—Antiasthmatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/14—Drugs for dermatological disorders for baldness or alopecia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/08—Antiallergic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/005—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies constructed by phage libraries
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2896—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against molecules with a "CD"-designation, not provided for elsewhere
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/10—Processes for the isolation, preparation or purification of DNA or RNA
- C12N15/102—Mutagenizing nucleic acids
- C12N15/1027—Mutagenizing nucleic acids by DNA shuffling, e.g. RSR, STEP, RPR
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/10—Processes for the isolation, preparation or purification of DNA or RNA
- C12N15/1034—Isolating an individual clone by screening libraries
- C12N15/1093—General methods of preparing gene libraries, not provided for in other subgroups
-
- C—CHEMISTRY; METALLURGY
- C40—COMBINATORIAL TECHNOLOGY
- C40B—COMBINATORIAL CHEMISTRY; LIBRARIES, e.g. CHEMICAL LIBRARIES
- C40B40/00—Libraries per se, e.g. arrays, mixtures
- C40B40/04—Libraries containing only organic compounds
- C40B40/06—Libraries containing nucleotides or polynucleotides, or derivatives thereof
- C40B40/08—Libraries containing RNA or DNA which encodes proteins, e.g. gene libraries
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/24—Immunoglobulins specific features characterized by taxonomic origin containing regions, domains or residues from different species, e.g. chimeric, humanized or veneered
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
- C07K2317/565—Complementarity determining region [CDR]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/76—Antagonist effect on antigen, e.g. neutralization or inhibition of binding
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/92—Affinity (KD), association rate (Ka), dissociation rate (Kd) or EC50 value
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- Genetics & Genomics (AREA)
- Engineering & Computer Science (AREA)
- Molecular Biology (AREA)
- General Health & Medical Sciences (AREA)
- Biochemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Medicinal Chemistry (AREA)
- Biomedical Technology (AREA)
- General Engineering & Computer Science (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Biotechnology (AREA)
- Biophysics (AREA)
- Immunology (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Crystallography & Structural Chemistry (AREA)
- Plant Pathology (AREA)
- Physics & Mathematics (AREA)
- Microbiology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Bioinformatics & Computational Biology (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Veterinary Medicine (AREA)
- Pulmonology (AREA)
- Virology (AREA)
- Pain & Pain Management (AREA)
- Rheumatology (AREA)
- Dermatology (AREA)
- Endocrinology (AREA)
- Neurology (AREA)
- Peptides Or Proteins (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
Abstract
【選択図】図17B
Description
本出願は、2019年9月23日に出願された米国仮特許出願第62/904,595号、2019年11月14日に出願された米国仮特許出願第62/935,590号、および2019年12月9日に出願された米国仮特許出願第62/945,752号の利益を主張し、これらの各々は参照によりその全体が組み込まれる。
本明細書において引用されるすべての刊行物、特許、および特許出願は、各々の刊行物、特許、または特許出願が参照により組み込まれることが具体的かつ個別に示された場合と同じ程度に、参照により本明細書に組み込まれる。
本開示は、他に示されない限り、当業者の技術の範囲内である従来の分子生物学技術を使用する。別段の定義がない限り、本明細書で使用されるすべての技術的および科学的用語は、当該技術分野の当業者によって一般的に理解されるのと同じ意味を有する。
本開示を通して、様々な実施形態が範囲形式で提示される。範囲形式での記載は、単に便宜上および簡潔にするためのものであり、任意の実施形態の範囲に対する柔軟性のない制限として解釈されるべきではないことを理解されるべきである。したがって、範囲の記載は、文脈で明確に別段の指示がない限り、すべての可能なサブ範囲と、その範囲内の下限の単位の10分の1までの個々の数値を具体的に開示すと見なされるべきである。例えば、1~6などの範囲の記述は、1~3、1~4、1~5、2~4、2~6、3~6などのサブ範囲およびその範囲内の個々の値(1.1、2、2.3、5、および5.9など)を具体的に開示すると見なされるべきである。これは、範囲の幅に関係なく適用される。これらの介在する範囲の上限および下限は、独立して、より小さな範囲に含まれ得、これらはまた本開示にも含まれ、言及された範囲内の任意の具体的に除外された制限に供される。言及された範囲が制限の一方または両方を含む場合、文脈が明確に別段の指示をしない限り、それらの含まれる制限のいずれかまたは両方を除外する範囲もまた本開示に含まれる。
本明細書で提供されるのは、CRTH2R結合ドメインを含む足場をコードする核酸を含む、プロスタグランジンD2受容体2(DP2またはCRTH2R)のためのGタンパク質共役受容体(GPCR)結合ライブラリーに関する方法および組成物である。本明細書に記載の足場は、CRTH2R結合ドメインを安定して支持することができる。CRTH2R結合ドメインは、CRTH2RリガンドとCRTH2Rの表面相互作用に基づいて設計され得る。本明細書に記載のライブラリーは、少なくとも1つの所定の参照核酸配列の所定のバリアントをそれぞれコードする核酸を含むバリアントライブラリーを提供するためにさらに多様化され得る。本明細書でさらに説明されるのは、核酸ライブラリーが翻訳されるときに生成され得るタンパク質ライブラリーである。いくつかの場合において、本明細書に記載の核酸ライブラリーを細胞に移して、細胞ライブラリーを生成する。本明細書に記載の方法を使用して合成されたライブラリーの下流のアプリケーションも本明細書に提供される。下流のアプリケーションには、生物学的に関連する機能の増強、例えば、安定性、親和性、結合、機能的活性の改善を伴い、およびCRTH2Rシグナル伝達に関連する病状の治療または予防のためである、バリアント核酸またはタンパク質配列の同定が含まれる。
本明細書で提供されるのは、足場をコードする核酸を含むライブラリーであり、ここで、CRTH2R結合ドメインの配列は、足場に配置される。本明細書に記載の足場は、未修飾の足場と比較して、足場に挿入された場合に、一連のCRTH2R結合ドメインをコードする配列の安定性の改善を可能にする。例示的な足場には、タンパク質、ペプチド、免疫グロブリン、それらの誘導体、またはそれらの組み合わせが含まれるが、これらに限定されない。いくつかの場合において、足場は免疫グロブリンである。本明細書に記載の足場は、改善された機能的活性、構造的安定性、発現、特異性、またはそれらの組み合わせを含む。いくつかの場合において、足場は、CRTH2R結合ドメインをサポートするための長い領域を含む。
本明細書で提供されるのは、CRTH2R結合ドメインの配列を含む足場をコードする核酸を含むCRTH2R結合ライブラリーである。いくつかの場合において、足場は免疫グロブリンである。いくつかの場合において、CRTH2R結合ドメインの配列を含む足場は、CRTH2R結合ドメインとCRTH2Rの間の相互作用によって決定される。
本明細書で提供されるのは、CRTH2R結合ドメインを含む足場をコードする核酸を含むライブラリーであって、ライブラリーは、改善された特異性、安定性、発現、折り畳み、または下流の活性を有する。いくつかの場合において、本明細書に記載のライブラリーは、スクリーニングおよび分析に使用される。
本明細書で提供されるのは、治療効果を有し得るCRTH2R結合ドメインを含む足場をコードする核酸を含むCRTH2R結合ライブラリーである。いくつかの場合において、CRTH2R結合ライブラリーは、翻訳されると、疾患または障害の治療のために使用されるタンパク質をもたらす。いくつかの場合において、タンパク質は免疫グロブリンである。いくつかの場合において、タンパク質はペプチド模倣物である。例示的な疾患には、癌、炎症性疾患または障害、代謝性疾患または障害、心血管疾患または障害、呼吸器疾患または障害、疼痛、消化器疾患または障害、生殖性疾患または障害、内分泌疾患または障害、あるいは神経学的疾患または障害が含まれるがこれらに限定されない。いくつかの場合において、癌は固形癌または血液癌である。いくつかの場合において、本明細書に記載のプロスタグランジンD2受容体2(DP2またはCRTH2R)の阻害剤は、中枢神経系、腎臓、腸、肺、毛、皮膚、骨、または軟骨の疾患または障害の治療のために使用される。いくつかの場合において、本明細書に記載のCRTH2Rの阻害剤またはアンタゴニストは、炎症反応を特徴とする疾患または障害の治療のために使用される。いくつかの場合において、本明細書に記載のCRTH2Rの阻害剤またはアンタゴニストは、アレルギー反応の治療のために使用される。いくつかの場合において、アレルギー反応は慢性特発性蕁麻疹である。いくつかの場合において、アレルギー反応はアレルギー性鼻炎である。いくつかの場合において、本明細書に記載のCRTH2Rの阻害剤またはアンタゴニストは、喘息の治療のために使用される。いくつかの場合において、本明細書に記載のCRTH2Rの阻害剤またはアンタゴニストは、脱毛症または禿頭症の治療のために使用される。いくつかの場合において、対象は哺乳動物である。いくつかの場合において、対象は、マウス、ウサギ、イヌ、またはヒトである。本明細書に記載の方法によって治療される対象は、乳児、成人、または小児であり得る。本明細書に記載の抗体または抗体フラグメントを含む医薬組成物は、静脈内または皮下に投与され得る。
コドンのバリエーション
本明細書に記載のバリアント核酸ライブラリーは、複数の核酸を含み得、ここで、各核酸は、参照核酸配列と比較して、バリアントコドン配列をコードする。いくつかの場合において、第1の核酸集団の各核酸は、単一のバリアント部位にバリアントを含む。いくつかの場合において、第1の核酸集団は、単一のバリアント部位に複数のバリアントを含み、その結果、第1の核酸集団は、同じバリアント部位に複数のバリアントを含む。第1の核酸集団は、同じバリアント部位において複数のコドンバリアントを集合的にコードする核酸を含み得る。第1の核酸集団は、同じ位置に最大19個以上のコドンを集合的にコードする核酸を含み得る。第1の核酸集団は、同じ位置で最大60個のバリアントトリプレットを集合的にコードする核酸を含み得るか、または第1の核酸集団は、同じ位置に最大61個の異なるコドンのトリプレットを集合的にコードする核酸を含み得る。各バリアントは、翻訳の間に異なるアミノ酸を生じるコドンをコードし得る。表3は、バリアント部位において可能な各コドン(および代表的なアミノ酸)のリストを示す。
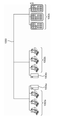
本明細書で提供されるのは、革新的な合成プラットフォームを作成するための、ポリヌクレオチド合成からシリコン上の、ナノウェル内での遺伝子アセンブリまでのエンドツーエンドプロセスの小型化、並列化、および垂直統合を利用するプラットフォームアプローチである。本明細書に記載のデバイスは、96ウェルプレートと同じフットプリントを提供し、シリコン合成プラットフォームは、従来の合成方法と比較して最大1,000倍以上のスループットの増大が可能であり、1回の高度に並列化された実行で、最大約1,000,000以上のポリヌクレオチド、または10,000以上の遺伝子の生成を伴う。
ポリヌクレオチド合成のための表面として使用されるデバイスは、均質なアレイ表面、パターン化されたアレイ表面、チャネル、ビーズ、ゲルなどを含むがこれらに限定されない基材の形態であり得る。本明細書で提供されるのは、複数のクラスターを含む基質であり、各クラスターは、ポリヌクレオチドの付着および合成を支持する複数の遺伝子座を含む。いくつかの場合において、基材は均質なアレイ表面を含む。例えば、均質なアレイ表面は均質なプレートである。本明細書で使用される「遺伝子座」という用語は、表面から延びる単一の所定の配列をコードするポリヌクレオチドの支持を提供する構造上の別個の領域を指す。いくつかの場合において、遺伝子座は二次元表面、例えば実質的に平面の表面上にある。いくつかの場合において、遺伝子座は、ウェル、マイクロウェル、チャネル、またはポストなどの三次元表面上にある。いくつかの場合において、遺伝子座の表面は、ポリヌクレオチド合成のために少なくとも1つのヌクレオチド、または好ましくは、ポリヌクレオチドの集団の合成のための同一のヌクレオチドの集団に付着するように能動的に機能化される材料を含む。いくつかの場合において、ポリヌクレオチドは、同じ核酸配列をコードするポリヌクレオチドの集団を指す。いくつかの場合において、基材の表面は、基材の1つまたは複数の表面を含めている。提供されるシステムおよび方法を使用して本明細書に記載のライブラリー内で合成されたポリヌクレオチドの平均エラー率は、多くの場合、エラー修正なしで、多くの場合、1000分の1未満、約2000分の1未満、約3000分の1未満、またはそれ以下である。
本明細書で提供される基材、デバイス、および反応器は、本明細書に記載される方法、組成物、およびシステムに適した任意の様々な材料から製造される。特定の例において、基材材料は、低レベルのヌクレオチド結合を示すように製造される。いくつかの場合において、基材材料は、高レベルのヌクレオチド結合を示す別個の表面を生成するように修飾される。いくつかの場合において、基材材料は可視光および/またはUV光に対して透明である。いくつかの場合において、基材材料は十分に導電性であり、例えば、基材の全部または一部にわたって均一な電界を形成することができる。いくつかの場合において、導電性材料は電気アースに接続される。いくつかの場合において、基材は熱伝導性または断熱性である。いくつかの場合において、材料は、化学的または生化学的反応、例えば、ポリヌクレオチド合成反応プロセスをサポートするために、耐薬品性および耐熱性である。いくつかの場合において、基材は柔軟な材料を含む。柔軟な材料の場合、材料には、修飾と非修飾の両方である、ナイロン、ニトロセルロース、ポリプロピレンなどが含まれるが、これらに限定されない。いくつかの場合において、基材は剛性材料を含む。剛性材料の場合、材料には、ガラス、フューズシリカ、シリコン、プラスチック(例えば、ポリテトラフルオロエチレン、ポリプロピレン、ポリスチレン、ポリカーボネート、およびそれらのブレンドなど)、金属(例えば、金、プラチナなど)が含まれ得るが、これらに限定されない。基材、固体支持体または反応器は、シリコン、ポリスチレン、アガロース、デキストラン、セルロース系ポリマー、ポリアクリルアミド、ポリジメチルシロキサン(PDMS)、およびガラスからなる群より選択される材料から製造することができる。基材/固体支持体またはその中の微細構造、反応器は、本明細書に列挙される材料または当該技術分野において知られている他の任意の適切な材料の組み合わせで製造され得る。
本明細書で提供されるのは、本明細書に記載される方法、組成物、およびシステムのための基材であり、基材は、本明細書に記載される方法、組成物、およびシステムに適した表面構造を有する。いくつかの場合において、基材は、隆起したおよび/または下降した特徴を含む。そのような特徴を有することの1つの利点は、ポリヌクレオチド合成をサポートするための表面積の増加である。いくつかの場合において、隆起および/または下降した特徴を有する基材は、三次元基材と呼ばれる。いくつかの事例において、三次元基材は1つ以上のチャネルを含む。いくつかの場合において、1つ以上の遺伝子座がチャネルを構成する。いくつかの事例において、チャネルは、材料沈着装置などの沈着装置を介して試薬沈着にアクセス可能である。いくつかの事例において、試薬および/または流体は、流体通信の1つ以上のチャネルのより大きなウェルに集まる。例えば、基材は、クラスターを伴う複数の遺伝子座に対応する複数のチャネルを含み、複数のチャネルは、クラスターの1つのウェルと流体連結している。いくつかの方法において、ポリヌクレオチドのライブラリーは、複数の遺伝子座のクラスターにおいて合成される。
本明細書で提供されるのは、表面上でのポリヌクレオチド合成のための方法であり、ここで、表面は、様々な表面修飾を含む。いくつかの場合において、表面修飾は、基材表面、または基材表面の選択された部位もしくは領域の1つ以上の化学的および/もしくは物理的特性を変更するための加法または減法プロセスによる表面の化学的および/または物理的変更に使用される。例えば、表面修飾には、(1)表面の濡れ特性の変更、(2)表面の機能化、すなわち、表面官能基の提供、修飾、または置換、(3)表面の非機能化、すなわち、表面官能基の除去、(4)他の方法で、例えば、エッチングを通して表面の化学組成を変化させること、(5)表面粗さを増加または減少させること、(6)表面にコーティングを提供すること、例えば、表面の濡れ特性とは異なる濡れ特性を示すコーティングを提供すること、および/または(7)表面に粒子を沈着させることが含まれるが、これらに限定されない。
ポリヌクレオチド合成のための現在の開示の方法は、ホスホルアミダイト化学を含むプロセスを含み得る。いくつかの場合において、ポリヌクレオチド合成は、塩基をホスホルアミダイトとカップリングすることを含む。ポリヌクレオチド合成は、カップリング条件下でのホスホルアミダイトの沈着による塩基のカップリングを含み得、ここで、同じ塩基が、任意選択で、ホスホルアミダイトと共に1回より多く沈着され、すなわち、二重カップリングである。ポリヌクレオチド合成は、未反応部位のキャッピングを含み得る。いくつかの場合において、キャッピングは任意選択である。ポリヌクレオチド合成はまた、酸化または1回の酸化工程または複数の酸化工程を含み得る。ポリヌクレオチド合成は、脱ブロック化、脱トリチル化、および硫化を含み得る。いくつかの場合において、ポリヌクレオチド合成は、酸化または硫化のいずれかを含む。いくつかの場合において、ポリヌクレオチド合成反応中の1つまたは各工程の間に、例えば、テトラゾールまたはアセトニトリルを使用して、デバイスを洗浄する。ホスホルアミダイト合成法の任意の1工程の時間枠は、約2分、1分、50秒、40秒、30秒、20秒、および10秒未満であり得る。
本明細書に記載されるシステムのいずれかは、コンピュータに動作可能に連結され得、ローカルまたはリモートのいずれかでコンピュータを介して自動化され得る。様々な例において、本開示の方法およびシステムは、コンピュータシステム上のソフトウェアプログラムおよびその使用をさらに含み得る。したがって、材料沈着装置の動き、分配動作、および真空作動の調整および同期化などの分配/真空/補充機能の同期化のためのコンピュータ制御は、本開示の範囲内である。コンピュータシステムは、基材の指定された領域に正しい試薬を送達するために、ユーザが指定した塩基配列と材料沈着装置の位置との間のインターフェースをとるようにプログラムすることができる。
ポリヌクレオチドのライブラリーの結合および合成をサポートするようにデバイスを機能化した。デバイスの表面は、最初に90%H2SO4と10%H2O2を含むピラニア溶液を使用して20分間ウェットクリーニングした。デバイスをいくつかのビーカーでDI水を用いてすすぎ、DI水がん首蛇口の下に5分間保持し、そしてN2で乾燥させた。続いて、デバイスをNH4OH(1:100;3mL:300mL)に5分間浸し、ハンドガンを使用してDI水ですすぎ、3つの連続するビーカーにDI水でそれぞれ1分間浸し、次にハンドガンを使用してDI水で再度すすいだ。次に、デバイスの表面をO2にさらすことにより、デバイスをプラズマ洗浄した。SAMCO PC-300機器を使用して、ダウンストリームモードで250ワットで1分間、O2プラズマエッチングを行った。
二次元オリゴヌクレオチド合成デバイスは、フローセルに組み立てられ、これは、フローセル(Applied Biosystems(ABI394 DNAシンセサイザー))に接続された。二次元オリゴヌクレオチド合成デバイスは、N-(3-トリエトキシシリルプロピル)-4-ヒドロキシブチラミド(Gelest)で均一に官能化し、これを使用して、本明細書に記載のポリヌクレオチド合成法を使用して、50bpの例示的なポリヌクレオチド(「50量体ポリヌクレオチド」)を合成した。
5’AGACAATCAACCATTTGGGGTGGACAGCCTTGACCTCTAGACTTCGGCAT##TTTTTTTTTT3’(配列番号2)、ここで#はチミジン-スクシニルヘキサミドCEDホスホルアミダイト(ChemGenesのCLP-2244)を示し、これは脱保護中に表面からオリゴを放出できるようにする切断可能なリンカーである。
50量体配列の合成について実施例2に記載されたのと同じプロセスを、100量体ポリヌクレオチド(「100量体ポリヌクレオチド」;5’CGGGATCCTTATCGTCATCGTCGTACAGATCCCGACCCATTTGCTGTCCACCAGTCATGCTAGCCATACCATGATGATGATGATGATGAGAACCCCGCAT##TTTTTTTTTT3’)の合成に使用し、#は2つの異なるシリコンチップ上のチミジン-スクシニルヘキサミドCEDホスホルアミダイト(ChemGenesのCLP-2244、配列番号3)を示し、1つ目はN-(3-トリエトキシシリルプロピル)-4-ヒドロキシブチラミドで均一に官能化され、2つ目は11-アセトキシウンデシルトリエトキシシランとn-デシルトリエトキシシランの5/95混合物で官能化され、そして表面から抽出されたポリヌクレオチドをBioAnalyzer装置で分析した。
98℃、30秒
98℃、10秒;63℃、10秒;72℃、10秒;12サイクル繰り返す
72℃、2分。
を使用して、さらにPCR増幅した。
足場を生成するために、構造分析、重鎖のレパートリー配列決定分析、およびヘテロ二量体ハイスループット配列決定データセットの特異的分析を実施した。各重鎖は、各軽鎖足場に関連付けられていた。各重鎖足場には、5つの異なる長いCDRH3ループオプションが割り当てられた。各軽鎖足場には、5つの異なるL3足場が割り当てられた。重鎖CDRH3ステムは、個体間とV遺伝子セグメント全体の両方で見られる頻繁に観察される長いH3ループステム(N末端およびC末端に10アミノ酸)から選択された。軽鎖足場L3は、長いH3を含むヘテロダイマーから選択された。タンパク質データバンク(Protein Data Bank)(PDB)、ならびに、CDR H1、H2、L1、L2、L3、およびCDRH3ステムが固定された、ディープ配列データセットからの情報に基づく直接ヘテロダイマーを使用した。次に、様々な足場を、発現を評価するためにファージ上に表示するためにフォーマットした。
約2,017個の抗体構造が分析され、そこから、少なくとも25アミノ酸の長さの長いCDRH3を有する22個の構造が観察された。重鎖には、IGHV1-69、IGHV3-30、IGHV4-49、およびIGHV3-21が含まれていた。同定された軽鎖には、IGLV3-21、IGKV3-11、IGKV2-28、IGKV1-5、IGLV1-51、IGLV1-44、およびIGKV1-13が含まれていた。分析では、IGHV4-59/61-IGLV3-21、IGHV3-21-IGKV2-28、IGHV1-69-IGKV3-11、およびIGHV1-69-IGKV1-5を含む4つのヘテロダイマーの組み合わせが複数回観察された。配列と構造の分析により、いくつかの構造でCDRH3内ジスルフィド結合が特定され、ステムにチロシンなどのかさばる側鎖が充填され、H3の長期的な安定性のサポートを提供する。ベータ-ターン-ベータシートと「ハンマーヘッド」サブドメインを含む二次構造も観察された。
レパートリー分析は、12人の健康な対照からの偏りのない5’RACEによって得られた、1,083,875個のIgM+/CD27ナイーブB細胞受容体(BCR)配列、および1,433,011個のCD27+配列で実施された。12人の健康な対照は、同数の男性と女性を含み、4人の白人、4人のアジア人、および4人のヒスパニックの固体で構成されていた。レパートリー分析は、ヒトレパートリーの1%未満が21アミノ酸より長いCDRH3を有するBCRを含むことを実証した。長いCDR3サブレパートリーにおいてV遺伝子バイアスが観察され、IGHV1-69、IGHV4-34、IGHV1-18、およびIGHV1-8は、長いH3ループを有するBCRで優先的な富化を示した。IGHV3-23、IGHV4-59/61、IGHV5-51、IGHV3-48、IGHV3-53/66、IGHV3-15、IGHV3-74、IGHV3-73、IGHV3-72、およびIGHV2-70では、長いループに対するバイアスが観察された。IGHV4-34足場は自己反応性であり、半減期が短いことが実証された。
足場についてヘテロ二量体分析を実施し、バリアント配列および足場の長さをアッセイした。
バリアント配列のGPCR足場を使用して構造分析を実施し、長さをアッセイした。
GPCR-リガンド相互作用表面および足場配置に基づいて、ライブラリーが設計され、そしてデノボ合成された。実施例4を参照されたい。実施例5を参照すると、10のバリアント配列が可変ドメイン、重鎖503のために設計され、237個のバリアント配列が重鎖相補性決定領域3 507のために設計され、44個のバリアント配列が可変ドメイン、軽鎖513のために設計された。実施例1~3に記載されると同様の方法に従って、図6に見られるように、フラグメントは3つの断片として合成された。
GPCR抗体ライブラリーの生成に続いて、約47個のGPCRがスクリーニングのために選択された。サイズが約1.8kbから約4.5kbのGPCR構築物をpCDNA3.1ベクター中で設計した。次に、GPCR構築物は、階層的アセンブリを含む実施例4~5に記載されたのと同様の方法に従って合成された。47個のGPCR構築物のうち、46個のGPCR構築物が合成された。
免疫グロブリン足場ライブラリーは、GPCR結合ドメインの配置のために、および一連のGPCR結合ドメインをコードする配列の安定性を改善するために設計された。免疫グロブリン足場には、リンカーを備えたVLドメインに結合したVHドメインが含まれていた。VHドメインとVLドメインのフレームワークエレメントとCDRエレメントのバリアント核酸配列が生成された。設計の構造は図12Aに示す。フルドメイン構造は図12Bに示す。リーダー、リンカー、およびpIIIの配列を表7に示す。
GPCR結合タンパク質について、ファージ選択からの上位100~200scFvは、完全長免疫グロブリンに変換された。免疫グロブリン変換後、クローンをExpiCHOで一過性にトランスフェクトして、免疫グロブリンを生成した。KingfisherおよびHamiltonをバッチIgG精製に使用し、続いてラボチップを使用して、精製されたすべての免疫グロブリンの純度データを収集した。図13および表11に見られるように、10mLの培養物から高い収率および純度が得られた。
合成VHHライブラリーが開発された。調整されたCDR多様性を備えた「VHH Ratio」ライブラリーの場合、2391個のVHH配列(iCANデータベース)がClustal Omegaを使用して整列され、各位置でのコンセンサスが決定され、フレームワークは各位置でのコンセンサスから導出された。2391個の配列のすべてのCDRは、位置固有の変動について分析され、この多様性はライブラリー設計に導入された。シャッフルされたCDR多様性を備えた「VHH Shuffle」ライブラリーの場合、ナノボディ配列内のユニークなCDRについて、iCANデータベースをスキャンした。1239個のユニークなCDR1、1600個のユニークなCDR2、および1608個のユニークなCDR3が識別され、フレームワークは、iCANデータベースの2391個の配列内の各フレームワーク位置でのコンセンサスから導出された。ユニークなCDRのそれぞれは、コンセンサスフレームワーク中で個別に合成およびシャッフルされ、理論上の多様性が3.2×10^9のライブラリーを生成した。次に、制限酵素消化を使用して、ライブラリーをファージミドベクターにクローニングした。「VHH hShuffle」ライブラリー(シャッフルされたCDR多様性を備えた合成「ヒト」VHHライブラリー)の場合、iCANデータベースをスキャンしてナノボディ配列内のユニークなCDRを探した。1239個のユニークなCDR1、1600個のユニークなCDR2、および1608個のユニークなCDR3が識別され、フレームワーク1、3、および4がヒト生殖細胞系列DP-47フレームワークから導出された。フレームワーク2は、iCANデータベースの2391個の配列内の各フレームワーク位置でのコンセンサスから導出された。ユニークなCDRはそれぞれ、NUGEツールを使用して部分的にヒト化されたフレームワークで個別に合成およびシャッフルされ、理論上の多様性が3.2×10^9のライブラリーを生成した。次に、NUGEツールを使用してライブラリーをファージミドベクターにクローニングした。
CRTH2RのためのVHHライブラリーは、実施例9に記載された方法と同様に開発された。簡単に述べると、CRTH2Rを発現する安定な細胞株が生成され、標的発現がFACSによって確認された。次に、標的の80%より多くを発現する細胞を、細胞ベースの選択のために使用した。目的の標的を安定して過剰発現している細胞に対して、5ラウンドの細胞ベースの選択を実行した。選択の各ラウンドに108個の細胞を使用した。標的発現細胞で選択する前に、各ラウンドからのファージを最初に108個のCHOバックグラウンド細胞で枯渇させた。選択のストリンジェンシーは、選択の後続のラウンドでの洗浄の数を増やすことによって増加した。次に、トリプシンを使用して細胞をファージから溶出し、次のパニングラウンドのためにファージを増幅した。ラウンド4とラウンド5からの合計1000個のクローンがNGSによって配列決定され、VHH-Fcとして再フォーマットするためのユニークなクローンが識別される。
抗CRTH2R抗体の細胞結合は、CHO CRTH2R陽性細胞(GFP+)および親CHO細胞(GFP-)で試験し、親陰性細胞および標的陽性細胞を比較して偽陽性を除外することによって決定された。表14Aに列挙されている抗体は、100nM(15μg/mL)から開始し、合計8点について、3倍のタイトレーションを行った。CRTH2R IgG抗体の重鎖および軽鎖配列を表14Bに示す。濃度による平均蛍光強度(MFI)によって検出される結合を図20A-20Eに示す。CRTH2-27を用いる100nMでの例示的なゲートドットプロットとAPCヒストグラムを図21A-21Bに示す。2つの抗体(gPCR-51およびgPCR-52)をポジティブ対照として使用した。2つのポジティブ対照の結合プロファイルを図22A-22Bに示す。
CRTH2R IgG抗体のライブラリーをアッセイして、PGD2誘導性cAMPシグナルにおけるアンタゴニスト機能を決定した。簡単に説明すると、細胞をIgG(タイトレーション1:3)と室温で1時間プレインキュベートした。続いて、CRTH2RはGαi共役しているため、フォルスコリンの存在下、細胞をPGD2(0.59nM)で37℃にて30分間刺激した。
CRTH2R IgG抗体をアロステリック活性についてアッセイした。アロステリック調節は、PGD2誘導cAMPシグナルにおけるCRTH2R IgG抗体をアッセイすることによって決定された。簡単に説明すると、細胞をIgG抗体なしまたは100nMのCRTH2R IgG抗体とともに再インキュベートした。続いて、フォルスコリンの存在下で細胞を様々な濃度のPGD2で刺激し、続いてcAMP活性をアッセイした。
CRTH2R IgG抗体をアゴニスト機能についてアッセイした。アゴニスト活性は、PGD2誘導cAMPシグナルにおいて実施例11に記載されているCRTH2R IgG抗体をアッセイすることによって決定された。
アロステリック調節は、既知のCRTH2Rアンタゴニスト(小分子OC000459)および2つの対照抗体について決定された。実験は、実施例13に記載されたものと同様に実施された。簡単に言えば、細胞を、OC000459、コンパレーターCRTH2R AB51抗体、またはコンパレーターCRTH2R AB52抗体で処理した。次に、フォルスコリンの存在下で細胞をPGD2で刺激した。
9個のCRTH2R IgG抗体によるアンタゴニスト調節が決定された。9個のCRTH2R IgG抗体には、CRTH2-9、CRTH2-27、CRTH2-50、CRTH2-32、CRTH2-42、CRTH2-74、CRTH2-55、CRTH2-28、およびCRTH2-39が含まれた。OC000459と比較したこれらの9個の抗体のアンタゴニスト機能は、PGD2によって誘導されるβ-アレスチン動員を使用して決定された。小分子OC000459を使用したポジティブ対照を含む結果を図27A-27Dに示す。
9個のCRTH2R IgGによるアロステリック調節が決定された。9個のCRTH2R IgGには、CRTH2-9、CRTH2-27、CRTH2-50、CRTH2-32、CRTH2-42、CRTH2-74、CRTH2-55、CRTH2-28、およびCRTH2-39が含まれた。OC000459と比較したこれらの9個の抗体のアロステリック調節は、PGD2によって誘導されるβ-アレスチンの動員を使用して決定された。
過免疫免疫グロブリン(IgG)ライブラリーは、実施例9に記載されたのと同様の方法を使用して作製された。簡単に説明すると、過免疫IgGライブラリーは、3人の健康なドナーのそれぞれからの3700万を超えるユニークなIgH配列からなるヒトナイーブおよび記憶B細胞受容体配列のデータベースの分析から生成された。200万を超えるCDRH3配列がこの分析から収集され、実施例1~3と同様の方法を使用して個別に構築された。重複するCDRH3と、開発において頻繁に問題を引き起こす可能性のある不利な原因となる(liability)モチーフは、ライブラリー合成工程で削除された。次に、これらのCDRH3配列の多様性をコンビナトリアルに組み立て、DP47ヒトフレームワークに組み込んで、1×1010サイズの高機能抗体Fabライブラリーを構築した。設計の概略図は図28に見ることができる。
GPCRライブラリーは、CDRランダム化スキームを使用して作成された。
CRTH2Rライブラリーは、実施例19に同様に記載されているCDRランダム化スキームを使用して作成される。
Claims (77)
- 複数の核酸を含む核酸ライブラリーであって、ここで、各核酸は、翻訳される場合、CRTH2R結合免疫グロブリンをコードする配列をコードし、前記CRTH2R結合免疫グロブリンは、CRTH2R結合ドメインのバリアントを含み、前記CRTH2R結合ドメインは、CRTH2Rのリガンドであり、前記核酸ライブラリーは、少なくとも10,000個のバリアント免疫グロブリン重鎖および少なくとも10,000個のバリアント免疫グロブリン軽鎖を含む、核酸ライブラリー。
- 前記核酸ライブラリーが、少なくとも50,000個のバリアント免疫グロブリン重鎖および少なくとも50,000個のバリアント免疫グロブリン軽鎖を含む、請求項1に記載の核酸ライブラリー。
- 前記核酸ライブラリーが、少なくとも100,000個のバリアント免疫グロブリン重鎖および少なくとも100,000個のバリアント免疫グロブリン軽鎖を含む、請求項1に記載の核酸ライブラリー。
- 前記核酸ライブラリーが、少なくとも105個の同一でない核酸を含む、請求項1に記載の核酸ライブラリー。
- 翻訳される場合の前記免疫グロブリン重鎖の長さが約90~約100アミノ酸である、請求項1に記載の核酸ライブラリー。
- 翻訳される場合の前記免疫グロブリン重鎖の長さが約100~約400アミノ酸である、請求項1に記載の核酸ライブラリー。
- 翻訳される場合の前記バリアント免疫グロブリン重鎖が、配列番号2338~2360または2403~2405のいずれか1つに対して少なくとも80%の配列同一性を含む、請求項1に記載の核酸ライブラリー。
- 翻訳される場合の前記バリアント免疫グロブリン軽鎖が、配列番号2361~2381または2406-2408のいずれか1つに対して少なくとも80%の配列同一性を含む、請求項1に記載の核酸ライブラリー。
- 複数の核酸を含む核酸ライブラリーであって、前記複数の核酸の各核酸は、翻訳される場合、抗体またはその抗体フラグメントをコードする配列をコードし、ここで、前記抗体またはその抗体フラグメントは、CRTH2R結合ドメインを含む重鎖(VH)の可変領域を含み、前記複数の核酸の各核酸が、CRTH2R結合ドメインの配列バリアントをコードする配列を含み、前記抗体または抗体フラグメントが、100nM未満のKDでその抗原に結合する、核酸ライブラリー。
- 前記VHの長さが約90~約100アミノ酸である、請求項9に記載の核酸ライブラリー。
- 前記VHの長さが約100~約400アミノ酸である、請求項9に記載の核酸ライブラリー。
- 前記VHの長さが約270~約300塩基対である、請求項9に記載の核酸ライブラリー。
- 前記VHの長さが約300~約1200塩基対である、請求項9に記載の核酸ライブラリー。
- 少なくとも105個の同一でない核酸を含む、請求項9に記載の核酸ライブラリー。
- 複数の核酸を含む核酸ライブラリーであって、各核酸は、翻訳される場合、CRTH2R単一ドメイン抗体をコードする配列をコードし、前記複数の配列の各配列は、重鎖(VH)の可変領域上のCDR1、CDR2、またはCDR3をコードするバリアント配列を含み、前記核酸ライブラリーは少なくとも30,000個のバリアント配列を含み、前記CRTH2R単一ドメイン抗体は100nM未満のKDでその抗原に結合する、核酸ライブラリー。
- 翻訳されたときの前記VHの長さが約90~約100アミノ酸である、請求項15に記載の核酸ライブラリー。
- 翻訳されたときの前記VHの長さが約100~約400アミノ酸である、請求項15に記載の核酸ライブラリー。
- 前記VHの長さが約270~約300塩基対である、請求項15に記載の核酸ライブラリー。
- 前記VHの長さが約300~約1200塩基対である、請求項15に記載の核酸ライブラリー。
- 翻訳されたときの前記VHが、配列番号2338-2360または2403-2405のいずれか1つに対して少なくとも80%の配列同一性を含む、請求項15に記載の核酸ライブラリー。
- 免疫グロブリン重鎖および免疫グロブリン軽鎖を含む、CRTH2Rに結合する抗体または抗体フラグメントであって、
a.前記免疫グロブリン重鎖は、配列番号2338-2360または2403-2405のいずれか1つに記載されるものと少なくとも約90%同一であるアミノ酸配列を含み、および
b.前記免疫グロブリン軽鎖は、配列番号2361-2381または2406-2408のいずれか1つに記載されるものと少なくとも約90%同一であるアミノ酸配列を含む、抗体または抗体フラグメント。 - 前記免疫グロブリン重鎖が、配列番号2338に記載されるものと少なくとも約90%同一であるアミノ酸配列を含み、前記免疫グロブリン軽鎖が、配列番号2361に記載されるものと少なくとも約90%同一であるアミノ酸配列を含む、請求項21に記載の抗体または抗体フラグメント。
- 前記免疫グロブリン重鎖が、配列番号2339に記載されるものと少なくとも約90%同一であるアミノ酸配列を含み、前記免疫グロブリン軽鎖が、配列番号2362に記載されるものと少なくとも約90%同一であるアミノ酸配列を含む、請求項21に記載の抗体または抗体フラグメント。
- 前記免疫グロブリン重鎖が、配列番号2340に記載されるものと少なくとも約90%同一であるアミノ酸配列を含み、前記免疫グロブリン軽鎖が、配列番号2363に記載されるものと少なくとも約90%同一であるアミノ酸配列を含む、請求項21に記載の抗体または抗体フラグメント。
- 前記免疫グロブリン重鎖が、配列番号2341に記載されるものと少なくとも約90%同一であるアミノ酸配列を含み、前記免疫グロブリン軽鎖が、配列番号2364に記載されるものと少なくとも約90%同一であるアミノ酸配列を含む、請求項21に記載の抗体または抗体フラグメント。
- 前記免疫グロブリン重鎖が、配列番号2342に記載されるものと少なくとも約90%同一であるアミノ酸配列を含み、前記免疫グロブリン軽鎖が、配列番号2365に記載されるものと少なくとも約90%同一であるアミノ酸配列を含む、請求項21に記載の抗体または抗体フラグメント。
- 前記免疫グロブリン重鎖が、配列番号2343に記載されるものと少なくとも約90%同一であるアミノ酸配列を含み、前記免疫グロブリン軽鎖が、配列番号2366に記載されるものと少なくとも約90%同一であるアミノ酸配列を含む、請求項21に記載の抗体または抗体フラグメント。
- 前記免疫グロブリン重鎖が、配列番号2344に記載されるものと少なくとも約90%同一であるアミノ酸配列を含み、前記免疫グロブリン軽鎖が、配列番号2367に記載されるものと少なくとも約90%同一であるアミノ酸配列を含む、請求項21に記載の抗体または抗体フラグメント。
- 前記免疫グロブリン重鎖が、配列番号2345に記載されるものと少なくとも約90%同一であるアミノ酸配列を含み、前記免疫グロブリン軽鎖が、配列番号2368に記載されるものと少なくとも約90%同一であるアミノ酸配列を含む、請求項21に記載の抗体または抗体フラグメント。
- 前記免疫グロブリン重鎖が、配列番号2346に記載されるものと少なくとも約90%同一であるアミノ酸配列を含み、前記免疫グロブリン軽鎖が、配列番号2369に記載されるものと少なくとも約90%同一であるアミノ酸配列を含む、請求項21に記載の抗体または抗体フラグメント。
- 前記免疫グロブリン重鎖が、配列番号2347に記載されるものと少なくとも約90%同一であるアミノ酸配列を含み、前記免疫グロブリン軽鎖が、配列番号2370に記載されるものと少なくとも約90%同一であるアミノ酸配列を含む、請求項21に記載の抗体または抗体フラグメント。
- 前記免疫グロブリン重鎖が、配列番号2348に記載されるものと少なくとも約90%同一であるアミノ酸配列を含み、前記免疫グロブリン軽鎖が、配列番号2371に記載されるものと少なくとも約90%同一であるアミノ酸配列を含む、請求項21に記載の抗体または抗体フラグメント。
- 前記免疫グロブリン重鎖が、配列番号2349に記載されるものと少なくとも約90%同一であるアミノ酸配列を含み、前記免疫グロブリン軽鎖が、配列番号2372に記載されるものと少なくとも約90%同一であるアミノ酸配列を含む、請求項21に記載の抗体または抗体フラグメント。
- 前記免疫グロブリン重鎖が、配列番号2350に記載されるものと少なくとも約90%同一であるアミノ酸配列を含み、前記免疫グロブリン軽鎖が、配列番号2373に記載されるものと少なくとも約90%同一であるアミノ酸配列を含む、請求項21に記載の抗体または抗体フラグメント。
- 前記免疫グロブリン重鎖が、配列番号2351に記載されるものと少なくとも約90%同一であるアミノ酸配列を含み、前記免疫グロブリン軽鎖が、配列番号2374に記載されるものと少なくとも約90%同一であるアミノ酸配列を含む、請求項21に記載の抗体または抗体フラグメント。
- 前記免疫グロブリン重鎖が、配列番号2352に記載されるものと少なくとも約90%同一であるアミノ酸配列を含み、前記免疫グロブリン軽鎖が、配列番号2375に記載されるものと少なくとも約90%同一であるアミノ酸配列を含む、請求項21に記載の抗体または抗体フラグメント。
- 前記免疫グロブリン重鎖が、配列番号2353に記載されるものと少なくとも約90%同一であるアミノ酸配列を含み、前記免疫グロブリン軽鎖が、配列番号2376に記載されるものと少なくとも約90%同一であるアミノ酸配列を含む、請求項21に記載の抗体または抗体フラグメント。
- 前記免疫グロブリン重鎖が、配列番号2354に記載されるものと少なくとも約90%同一であるアミノ酸配列を含み、前記免疫グロブリン軽鎖が、配列番号2377に記載されるものと少なくとも約90%同一であるアミノ酸配列を含む、請求項21に記載の抗体または抗体フラグメント。
- 前記免疫グロブリン重鎖が、配列番号2355に記載されるものと少なくとも約90%同一であるアミノ酸配列を含み、前記免疫グロブリン軽鎖が、配列番号2378に記載されるものと少なくとも約90%同一であるアミノ酸配列を含む、請求項21に記載の抗体または抗体フラグメント。
- 前記免疫グロブリン重鎖が、配列番号2356に記載されるものと少なくとも約90%同一であるアミノ酸配列を含み、前記免疫グロブリン軽鎖が、配列番号2379に記載されるものと少なくとも約90%同一であるアミノ酸配列を含む、請求項21に記載の抗体または抗体フラグメント。
- 前記免疫グロブリン重鎖が、配列番号2357に記載されるものと少なくとも約90%同一であるアミノ酸配列を含み、前記免疫グロブリン軽鎖が、配列番号2380に記載されるものと少なくとも約90%同一であるアミノ酸配列を含む、請求項21に記載の抗体または抗体フラグメント。
- 前記免疫グロブリン重鎖が、配列番号2358に記載されるものと少なくとも約90%同一であるアミノ酸配列を含み、前記免疫グロブリン軽鎖が、配列番号2381に記載されるものと少なくとも約90%同一であるアミノ酸配列を含む、請求項21に記載の抗体または抗体フラグメント。
- 前記免疫グロブリン重鎖が、配列番号2403に記載されるものと少なくとも約90%同一であるアミノ酸配列を含み、前記免疫グロブリン軽鎖が、配列番号2406に記載されるものと少なくとも約90%同一であるアミノ酸配列を含む、請求項21に記載の抗体または抗体フラグメント。
- 前記免疫グロブリン重鎖が、配列番号2404に記載されるものと少なくとも約90%同一であるアミノ酸配列を含み、前記免疫グロブリン軽鎖が、配列番号2407に記載されるものと少なくとも約90%同一であるアミノ酸配列を含む、請求項21記載の抗体または抗体フラグメント。
- 前記免疫グロブリン重鎖が、配列番号2405に記載されるものと少なくとも約90%同一であるアミノ酸配列を含み、前記免疫グロブリン軽鎖が、配列番号2408に記載されるものと少なくとも約90%同一であるアミノ酸配列を含む、請求項21記載の抗体または抗体フラグメント。
- 前記抗体が、モノクローナル抗体、ポリクローナル抗体、二重特異性抗体、多重特異性抗体、グラフト化抗体、ヒト抗体、ヒト化抗体、合成抗体、キメラ抗体、ラクダ化抗体、単鎖Fvs(scFv)、単鎖抗体、Fabフラグメント、F(ab’)2フラグメント、Fdフラグメント、Fvフラグメント、単鎖ドメイン抗体、単離相補性決定領域(CDR)、ダイアボディ、単一の単鎖可変ドメインのみから構成されるフラグメント、ジスルフィド結合Fv(sdFv)、イントラボディ、抗イディオタイプ(anti-Id)抗体、またはそれらのab抗原結合フラグメントである、請求項21に記載の抗体または抗体フラグメント。
- 前記抗体またはその抗体フラグメントがキメラであるかまたはヒト化されている、請求項21に記載の抗体または抗体フラグメント。
- 前記抗体が、cAMPアッセイにおいて約25ナノモル未満のEC50を有する、請求項21に記載の抗体または抗体フラグメント。
- 前記抗体が、cAMPアッセイにおいて約20ナノモル未満のEC50を有する、請求項21に記載の抗体または抗体フラグメント。
- 前記抗体が、cAMPアッセイにおいて約10ナノモル未満のEC50を有する、請求項21に記載の抗体または抗体フラグメント。
- 配列番号2382-2402のいずれか1つに記載されるものと少なくとも約90%同一であるアミノ酸配列を含む相補性決定領域(CDR)を含む、抗体または抗体フラグメント。
- 抗体または抗体フラグメントであって、前記抗体または抗体フラグメントが、配列番号2382-2402のいずれか1つの配列を含み、前記抗体が、モノクローナル抗体、ポリクローナル抗体、二重特異性抗体、多重特異性抗体、グラフト化抗体、ヒト抗体、ヒト化抗体、合成抗体、キメラ抗体、ラクダ化抗体、単鎖Fvs(scFv)、単鎖抗体、Fabフラグメント、F(ab’)2フラグメント、Fdフラグメント、Fvフラグメント、単鎖ドメイン抗体、単離相補性決定領域(CDR)、ダイアボディ、単一の単鎖可変ドメインのみから構成されるフラグメント、ジスルフィド結合Fv(sdFv)、イントラボディ、抗イディオタイプ(anti-Id)抗体、またはそれらのab抗原結合フラグメントである、抗体または抗体フラグメント。
- 請求項21-52のいずれか一項に記載の抗体または抗体フラグメントを投与する工程を含む、中枢神経系、腎臓、腸、肺、毛、皮膚、骨、または軟骨の疾患または障害を治療する方法。
- 請求項21-52のいずれか一項に記載の抗体または抗体フラグメントを投与する工程を含む、炎症反応によって特徴付けられる疾患または障害を治療する方法。
- 請求項21-52のいずれか一項に記載の抗体または抗体フラグメントを投与する工程を含む、アレルギー反応を治療する方法。
- 前記アレルギー反応が慢性特発性蕁麻疹またはアレルギー性鼻炎である、請求項55に記載の方法。
- 請求項21-52のいずれか一項に記載の抗体または抗体フラグメントを投与する工程を含む、喘息を治療する方法。
- 請求項21-52のいずれか一項に記載の抗体または抗体フラグメントを投与する工程を含む、脱毛症または禿頭症を治療する方法。
- CRTH2R抗体またはその抗体フラグメントをコードする核酸ライブラリーを生成するための方法であって、前記方法は、
(a)所定の配列を提供する工程であって、前記所定の配列は、
i.第1の複数のポリヌクレオチドであって、前記第1の複数のポリヌクレオチドの各ポリヌクレオチドは、重鎖上のCDR1をコードする少なくとも1000個のバリアント配列をコードする、第1の複数のポリヌクレオチド、
ii.第2の複数のポリヌクレオチドであって、前記第2の複数のポリヌクレオチドの各ポリヌクレオチドは、重鎖上のCDR2をコードする少なくとも1000個のバリアント配列をコードする、第2の複数のポリヌクレオチド、
iii.第3の複数のポリヌクレオチドであって、前記第3の複数のポリヌクレオチドの各ポリヌクレオチドは、重鎖上のCDR3をコードする少なくとも1000個のバリアント配列をコードする、第3の複数のポリヌクレオチド
をコードする、所定の配列を提供する工程、
(b)前記第1の複数のポリヌクレオチド、前記第2の複数のポリヌクレオチド、および前記第3の複数のポリヌクレオチドを混合して、CRTH2R抗体またはその抗体フラグメントをコードするバリアント核酸の核酸ライブラリーを形成する工程であって、前記バリアント核酸の少なくとも70%は、100nM未満のKDでその抗原に結合する抗体または抗体フラグメントをコードする、工程
を含む、方法。 - 前記CRTH2R抗体またはその抗体フラグメントが単一ドメイン抗体である、請求項59に記載の方法。
- 前記単一ドメイン抗体が1つの重鎖可変ドメインを含む、請求項60に記載の方法。
- 前記単一ドメイン抗体がVHH抗体である、請求項60に記載の方法。
- 前記核酸ライブラリーが少なくとも50,000個のバリアント配列を含む、請求項59に記載の方法。
- 前記核酸ライブラリーが少なくとも100,000個のバリアント配列を含む、請求項59に記載の方法。
- 前記核酸ライブラリーが少なくとも105個の同一でない核酸を含む、請求項59に記載の方法。
- 前記核酸ライブラリーが、75nM未満のKDでCRTH2Rに結合するCRTH2R抗体または抗体フラグメントをコードする少なくとも1つの配列を含む、請求項59に記載の方法。
- 前記核酸ライブラリーが、50nM未満のKDでCRTH2Rに結合するCRTH2R抗体または抗体フラグメントをコードする少なくとも1つの配列を含む、請求項59に記載の方法。
- 前記核酸ライブラリーが、10nM未満のKDでCRTH2Rに結合するCRTH2R抗体または抗体フラグメントをコードする少なくとも1つの配列を含む、請求項59に記載の方法。
- 前記核酸ライブラリーが少なくとも500個のバリアント配列を含む、請求項68に記載の方法。
- 前記核酸ライブラリーが、75nM未満のKDでCRTH2Rに結合するCRTH2R抗体または抗体フラグメントをコードする少なくとも5つの配列を含む、請求項59に記載の方法。
- 請求項1-20のいずれか一項に記載の核酸ライブラリーによってコードされるタンパク質ライブラリーであって、ペプチドを含む、タンパク質ライブラリー。
- 免疫グロブリンを含む、請求項71に記載のタンパク質ライブラリー。
- 抗体を含む、請求項71に記載のタンパク質ライブラリー。
- ペプチド模倣物ライブラリーである、請求項71に記載のタンパク質ライブラリー。
- 請求項1-20のいずれか一項に記載の核酸ライブラリーを含むベクターライブラリー。
- 請求項1-20のいずれか一項に記載の核酸ライブラリーを含む細胞ライブラリー。
- 請求項71-74のいずれか一項に記載のタンパク質ライブラリーを含む細胞ライブラリー。
Applications Claiming Priority (7)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201962904595P | 2019-09-23 | 2019-09-23 | |
| US62/904,595 | 2019-09-23 | ||
| US201962935590P | 2019-11-14 | 2019-11-14 | |
| US62/935,590 | 2019-11-14 | ||
| US201962945752P | 2019-12-09 | 2019-12-09 | |
| US62/945,752 | 2019-12-09 | ||
| PCT/US2020/052291 WO2021061829A1 (en) | 2019-09-23 | 2020-09-23 | Variant nucleic acid libraries for crth2 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2022548309A true JP2022548309A (ja) | 2022-11-17 |
| JPWO2021061829A5 JPWO2021061829A5 (ja) | 2023-07-20 |
Family
ID=75166117
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2022518006A Pending JP2022548309A (ja) | 2019-09-23 | 2020-09-23 | Crth2のバリアント核酸ライブラリー |
Country Status (9)
| Country | Link |
|---|---|
| US (1) | US12091777B2 (ja) |
| EP (1) | EP4034566A4 (ja) |
| JP (1) | JP2022548309A (ja) |
| KR (1) | KR20220066151A (ja) |
| CN (1) | CN115003697A (ja) |
| AU (1) | AU2020356471A1 (ja) |
| CA (1) | CA3155629A1 (ja) |
| IL (1) | IL291515A (ja) |
| WO (1) | WO2021061829A1 (ja) |
Families Citing this family (19)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ES2815099T3 (es) | 2013-08-05 | 2021-03-29 | Twist Bioscience Corp | Genotecas sintetizadas de novo |
| CA2975852A1 (en) | 2015-02-04 | 2016-08-11 | Twist Bioscience Corporation | Methods and devices for de novo oligonucleic acid assembly |
| WO2016172377A1 (en) | 2015-04-21 | 2016-10-27 | Twist Bioscience Corporation | Devices and methods for oligonucleic acid library synthesis |
| IL258164B (en) | 2015-09-18 | 2022-09-01 | Twist Bioscience Corp | Methods to regulate the activity of proteins and cells and a method for the production of nucleic acids |
| US11512347B2 (en) | 2015-09-22 | 2022-11-29 | Twist Bioscience Corporation | Flexible substrates for nucleic acid synthesis |
| JP6871364B2 (ja) | 2016-09-21 | 2021-05-12 | ツイスト バイオサイエンス コーポレーション | 核酸に基づくデータ保存 |
| CN110892485B (zh) | 2017-02-22 | 2024-03-22 | 特韦斯特生物科学公司 | 基于核酸的数据存储 |
| GB2578844A (en) | 2017-06-12 | 2020-05-27 | Twist Bioscience Corp | Methods for seamless nucleic acid assembly |
| WO2018231864A1 (en) | 2017-06-12 | 2018-12-20 | Twist Bioscience Corporation | Methods for seamless nucleic acid assembly |
| GB2581620A (en) | 2017-09-11 | 2020-08-26 | Twist Bioscience Corp | GPCR binding proteins and synthesis thereof |
| CN111565834B (zh) | 2017-10-20 | 2022-08-26 | 特韦斯特生物科学公司 | 用于多核苷酸合成的加热的纳米孔 |
| AU2019205269A1 (en) | 2018-01-04 | 2020-07-30 | Twist Bioscience Corporation | DNA-based digital information storage |
| CN112639130B (zh) | 2018-05-18 | 2024-08-09 | 特韦斯特生物科学公司 | 用于核酸杂交的多核苷酸、试剂和方法 |
| SG11202109283UA (en) | 2019-02-26 | 2021-09-29 | Twist Bioscience Corp | Variant nucleic acid libraries for antibody optimization |
| CN114729342A (zh) | 2019-06-21 | 2022-07-08 | 特韦斯特生物科学公司 | 基于条形码的核酸序列装配 |
| CA3155629A1 (en) | 2019-09-23 | 2021-04-01 | Twist Bioscience Corporation | Variant nucleic acid libraries for crth2 |
| AU2020355027A1 (en) * | 2019-09-23 | 2022-04-21 | Twist Bioscience Corporation | Antibodies that bind CD3 Epsilon |
| JP2023523335A (ja) | 2020-04-27 | 2023-06-02 | ツイスト バイオサイエンス コーポレーション | コロナウイルス用の変異体核酸ライブラリー相互参照 |
| EP4229210A1 (en) | 2020-10-19 | 2023-08-23 | Twist Bioscience Corporation | Methods of synthesizing oligonucleotides using tethered nucleotides |
Family Cites Families (957)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3549368A (en) | 1968-07-02 | 1970-12-22 | Ibm | Process for improving photoresist adhesion |
| US3920714A (en) | 1972-11-16 | 1975-11-18 | Weber Heinrich | Process for the production of polymeric hydrocarbons with reactive silyl side groups |
| GB1550867A (en) | 1975-08-04 | 1979-08-22 | Hughes Aircraft Co | Positioning method and apparatus for fabricating microcircuit devices |
| US4415732A (en) | 1981-03-27 | 1983-11-15 | University Patents, Inc. | Phosphoramidite compounds and processes |
| EP0090789A1 (en) | 1982-03-26 | 1983-10-05 | Monsanto Company | Chemical DNA synthesis |
| US4994373A (en) | 1983-01-27 | 1991-02-19 | Enzo Biochem, Inc. | Method and structures employing chemically-labelled polynucleotide probes |
| JPS59224123A (ja) | 1983-05-20 | 1984-12-17 | Oki Electric Ind Co Ltd | ウエハアライメントマ−ク |
| US5118605A (en) | 1984-10-16 | 1992-06-02 | Chiron Corporation | Polynucleotide determination with selectable cleavage sites |
| JPS61141761A (ja) | 1984-12-12 | 1986-06-28 | Kanegafuchi Chem Ind Co Ltd | 硬化性組成物 |
| US5242794A (en) | 1984-12-13 | 1993-09-07 | Applied Biosystems, Inc. | Detection of specific sequences in nucleic acids |
| US4613398A (en) | 1985-06-06 | 1986-09-23 | International Business Machines Corporation | Formation of etch-resistant resists through preferential permeation |
| US4981797A (en) | 1985-08-08 | 1991-01-01 | Life Technologies, Inc. | Process of producing highly transformable cells and cells produced thereby |
| US4726877A (en) | 1986-01-22 | 1988-02-23 | E. I. Du Pont De Nemours And Company | Methods of using photosensitive compositions containing microgels |
| US5763192A (en) | 1986-11-20 | 1998-06-09 | Ixsys, Incorporated | Process for obtaining DNA, RNA, peptides, polypeptides, or protein, by recombinant DNA technique |
| US4808511A (en) | 1987-05-19 | 1989-02-28 | International Business Machines Corporation | Vapor phase photoresist silylation process |
| JPH07113774B2 (ja) | 1987-05-29 | 1995-12-06 | 株式会社日立製作所 | パタ−ンの形成方法 |
| US4988617A (en) | 1988-03-25 | 1991-01-29 | California Institute Of Technology | Method of detecting a nucleotide change in nucleic acids |
| US5700637A (en) | 1988-05-03 | 1997-12-23 | Isis Innovation Limited | Apparatus and method for analyzing polynucleotide sequences and method of generating oligonucleotide arrays |
| EP0385410B1 (en) | 1989-02-28 | 1996-10-02 | Canon Kabushiki Kaisha | Partially double-stranded oligonucleotide and method for forming oligonucleotide |
| US5556750A (en) | 1989-05-12 | 1996-09-17 | Duke University | Methods and kits for fractionating a population of DNA molecules based on the presence or absence of a base-pair mismatch utilizing mismatch repair systems |
| US6008031A (en) | 1989-05-12 | 1999-12-28 | Duke University | Method of analysis and manipulation of DNA utilizing mismatch repair systems |
| US5459039A (en) | 1989-05-12 | 1995-10-17 | Duke University | Methods for mapping genetic mutations |
| US5102797A (en) | 1989-05-26 | 1992-04-07 | Dna Plant Technology Corporation | Introduction of heterologous genes into bacteria using transposon flanked expression cassette and a binary vector system |
| US6309822B1 (en) | 1989-06-07 | 2001-10-30 | Affymetrix, Inc. | Method for comparing copy number of nucleic acid sequences |
| US6919211B1 (en) | 1989-06-07 | 2005-07-19 | Affymetrix, Inc. | Polypeptide arrays |
| US5527681A (en) | 1989-06-07 | 1996-06-18 | Affymax Technologies N.V. | Immobilized molecular synthesis of systematically substituted compounds |
| US6040138A (en) | 1995-09-15 | 2000-03-21 | Affymetrix, Inc. | Expression monitoring by hybridization to high density oligonucleotide arrays |
| US5143854A (en) | 1989-06-07 | 1992-09-01 | Affymax Technologies N.V. | Large scale photolithographic solid phase synthesis of polypeptides and receptor binding screening thereof |
| US5242974A (en) | 1991-11-22 | 1993-09-07 | Affymax Technologies N.V. | Polymer reversal on solid surfaces |
| US5744101A (en) | 1989-06-07 | 1998-04-28 | Affymax Technologies N.V. | Photolabile nucleoside protecting groups |
| CA2036946C (en) | 1990-04-06 | 2001-10-16 | Kenneth V. Deugau | Indexing linkers |
| US5494810A (en) | 1990-05-03 | 1996-02-27 | Cornell Research Foundation, Inc. | Thermostable ligase-mediated DNA amplifications system for the detection of genetic disease |
| US6087482A (en) | 1990-07-27 | 2000-07-11 | Isis Pharmaceuticals, Inc. | Heteroatomic oligonucleoside linkages |
| FI87886C (fi) | 1990-09-06 | 1993-03-10 | Instrumentarium Oy | Faestorgan |
| DE69133559T2 (de) | 1990-09-27 | 2007-11-22 | Invitrogen Corp., Carlsbad | Direkte Klonierung von PCR amplifizierten Nucleinsäuren |
| GB9025236D0 (en) | 1990-11-20 | 1991-01-02 | Secr Defence | Silicon-on porous-silicon;method of production |
| DE69133293T2 (de) | 1990-12-06 | 2004-05-27 | Affymetrix, Inc., Santa Clara | Verfahren und Reagenzien für immobilisierten Polymersynthese in sehr grossem Masstab |
| DE69132843T2 (de) | 1990-12-06 | 2002-09-12 | Affymetrix, Inc. (N.D.Ges.D.Staates Delaware) | Identifizierung von Nukleinsäuren in Proben |
| US6582908B2 (en) | 1990-12-06 | 2003-06-24 | Affymetrix, Inc. | Oligonucleotides |
| US5455166A (en) | 1991-01-31 | 1995-10-03 | Becton, Dickinson And Company | Strand displacement amplification |
| US5137814A (en) | 1991-06-14 | 1992-08-11 | Life Technologies, Inc. | Use of exo-sample nucleotides in gene cloning |
| US5449754A (en) | 1991-08-07 | 1995-09-12 | H & N Instruments, Inc. | Generation of combinatorial libraries |
| US5474796A (en) | 1991-09-04 | 1995-12-12 | Protogene Laboratories, Inc. | Method and apparatus for conducting an array of chemical reactions on a support surface |
| US5846717A (en) | 1996-01-24 | 1998-12-08 | Third Wave Technologies, Inc. | Detection of nucleic acid sequences by invader-directed cleavage |
| US5994069A (en) | 1996-01-24 | 1999-11-30 | Third Wave Technologies, Inc. | Detection of nucleic acids by multiple sequential invasive cleavages |
| US7150982B2 (en) | 1991-09-09 | 2006-12-19 | Third Wave Technologies, Inc. | RNA detection assays |
| US7045289B2 (en) | 1991-09-09 | 2006-05-16 | Third Wave Technologies, Inc. | Detection of RNA Sequences |
| US6759226B1 (en) | 2000-05-24 | 2004-07-06 | Third Wave Technologies, Inc. | Enzymes for the detection of specific nucleic acid sequences |
| US5384261A (en) | 1991-11-22 | 1995-01-24 | Affymax Technologies N.V. | Very large scale immobilized polymer synthesis using mechanically directed flow paths |
| ATE262374T1 (de) | 1991-11-22 | 2004-04-15 | Affymetrix Inc | Kombinatorische strategien für polymersynthese |
| US5573905A (en) | 1992-03-30 | 1996-11-12 | The Scripps Research Institute | Encoded combinatorial chemical libraries |
| JP2775346B2 (ja) | 1992-04-03 | 1998-07-16 | アプライド バイオシステムズ,インコーポレイテッド | プローブ構成物および方法 |
| JP2553322Y2 (ja) | 1992-05-11 | 1997-11-05 | サンデン株式会社 | 飲料抽出装置のフィルタ送り機構 |
| JPH07509365A (ja) | 1992-07-31 | 1995-10-19 | デイド・ベーリング・マルブルク・ゲゼルシヤフト・ミツト・ベシユレンクテル・ハフツング | ポリヌクレオチド類の3’末端に特定配列を導入する方法 |
| US5288514A (en) | 1992-09-14 | 1994-02-22 | The Regents Of The University Of California | Solid phase and combinatorial synthesis of benzodiazepine compounds on a solid support |
| JP3176444B2 (ja) | 1992-10-01 | 2001-06-18 | 株式会社リコー | 水性インク及びこれを用いた記録方法 |
| DE4241045C1 (de) | 1992-12-05 | 1994-05-26 | Bosch Gmbh Robert | Verfahren zum anisotropen Ätzen von Silicium |
| US5368823A (en) | 1993-02-11 | 1994-11-29 | University Of Georgia Research Foundation, Inc. | Automated synthesis of oligonucleotides |
| US5395753A (en) | 1993-02-19 | 1995-03-07 | Theratech, Inc. | Method for diagnosing rheumatoid arthritis |
| ATE246702T1 (de) | 1993-04-12 | 2003-08-15 | Univ Northwestern | Verfahren zur darstellung von oligonukleotiden |
| US7135312B2 (en) | 1993-04-15 | 2006-11-14 | University Of Rochester | Circular DNA vectors for synthesis of RNA and DNA |
| US5455239A (en) | 1993-08-05 | 1995-10-03 | Merck & Co. Inc. | 3-aryl of heteroaryl-7-heteroaralkylamido cephalosporin compounds, compositions and methods of use |
| US5482845A (en) | 1993-09-24 | 1996-01-09 | The Trustees Of Columbia University In The City Of New York | Method for construction of normalized cDNA libraries |
| CN1039623C (zh) | 1993-10-22 | 1998-09-02 | 中国人民解放军军事医学科学院毒物药物研究所 | 一种防治运动病综合征的药物组合物及其制备方法 |
| ES2176308T3 (es) | 1993-10-28 | 2002-12-01 | Houston Advanced Res Ct | Dispositivo de microestructura porosa que permite un flujo. |
| US6893816B1 (en) | 1993-10-28 | 2005-05-17 | Houston Advanced Research Center | Microfabricated, flowthrough porous apparatus for discrete detection of binding reactions |
| US6027877A (en) | 1993-11-04 | 2000-02-22 | Gene Check, Inc. | Use of immobilized mismatch binding protein for detection of mutations and polymorphisms, purification of amplified DNA samples and allele identification |
| US5834252A (en) | 1995-04-18 | 1998-11-10 | Glaxo Group Limited | End-complementary polymerase reaction |
| US6015880A (en) | 1994-03-16 | 2000-01-18 | California Institute Of Technology | Method and substrate for performing multiple sequential reactions on a matrix |
| CN1326994C (zh) | 1994-03-29 | 2007-07-18 | 诺沃奇梅兹有限公司 | 碱性芽孢杆菌淀粉酶 |
| US5514789A (en) | 1994-04-21 | 1996-05-07 | Barrskogen, Inc. | Recovery of oligonucleotides by gas phase cleavage |
| SE512382C2 (sv) | 1994-04-26 | 2000-03-06 | Ericsson Telefon Ab L M | Anordning och förfarande för att placera långsträckta element mot eller invid en yta |
| ATE198511T1 (de) | 1994-04-29 | 2001-01-15 | Perkin Elmer Corp | Verfahren und vorrichtung zur echtzeiterfassung der produkte von nukleinsäureamplifikation |
| US6287850B1 (en) | 1995-06-07 | 2001-09-11 | Affymetrix, Inc. | Bioarray chip reaction apparatus and its manufacture |
| AU689924B2 (en) | 1994-06-23 | 1998-04-09 | Affymax Technologies N.V. | Photolabile compounds and methods for their use |
| US5641658A (en) | 1994-08-03 | 1997-06-24 | Mosaic Technologies, Inc. | Method for performing amplification of nucleic acid with two primers bound to a single solid support |
| US5530516A (en) | 1994-10-04 | 1996-06-25 | Tamarack Scientific Co., Inc. | Large-area projection exposure system |
| US6635226B1 (en) | 1994-10-19 | 2003-10-21 | Agilent Technologies, Inc. | Microanalytical device and use thereof for conducting chemical processes |
| US6613560B1 (en) | 1994-10-19 | 2003-09-02 | Agilent Technologies, Inc. | PCR microreactor for amplifying DNA using microquantities of sample fluid |
| US5556752A (en) | 1994-10-24 | 1996-09-17 | Affymetrix, Inc. | Surface-bound, unimolecular, double-stranded DNA |
| EP0792195A4 (en) | 1994-11-22 | 1999-05-26 | Complex Fluid Systems Inc | NON-AMINIC PHOTOSENSITIVE RESIN ADHESION PROMOTERS FOR MICROELECTRONIC APPLICATIONS |
| US5688642A (en) | 1994-12-01 | 1997-11-18 | The United States Of America As Represented By The Secretary Of The Navy | Selective attachment of nucleic acid molecules to patterned self-assembled surfaces |
| US6017434A (en) | 1995-05-09 | 2000-01-25 | Curagen Corporation | Apparatus and method for the generation, separation, detection, and recognition of biopolymer fragments |
| US5830655A (en) | 1995-05-22 | 1998-11-03 | Sri International | Oligonucleotide sizing using cleavable primers |
| US5700642A (en) | 1995-05-22 | 1997-12-23 | Sri International | Oligonucleotide sizing using immobilized cleavable primers |
| US5877280A (en) | 1995-06-06 | 1999-03-02 | The Mount Sinai School Of Medicine Of The City University Of New York | Thermostable muts proteins |
| US6446682B1 (en) | 1995-06-06 | 2002-09-10 | James P. Viken | Auto-loading fluid exchanger and method of use |
| US5707806A (en) | 1995-06-07 | 1998-01-13 | Genzyme Corporation | Direct sequence identification of mutations by cleavage- and ligation-associated mutation-specific sequencing |
| US5712126A (en) | 1995-08-01 | 1998-01-27 | Yale University | Analysis of gene expression by display of 3-end restriction fragments of CDNA |
| US5780613A (en) | 1995-08-01 | 1998-07-14 | Northwestern University | Covalent lock for self-assembled oligonucleotide constructs |
| US5854033A (en) | 1995-11-21 | 1998-12-29 | Yale University | Rolling circle replication reporter systems |
| US6537776B1 (en) | 1999-06-14 | 2003-03-25 | Diversa Corporation | Synthetic ligation reassembly in directed evolution |
| US6352842B1 (en) | 1995-12-07 | 2002-03-05 | Diversa Corporation | Exonucease-mediated gene assembly in directed evolution |
| DE69627189T2 (de) | 1995-12-15 | 2004-02-05 | Duke University | Verfahren zum nachweis und zur entfernung von mutantsequenzen, die während enzymatischer amplifikation entstehen |
| US5962271A (en) | 1996-01-03 | 1999-10-05 | Cloutech Laboratories, Inc. | Methods and compositions for generating full-length cDNA having arbitrary nucleotide sequence at the 3'-end |
| US5976846A (en) | 1996-01-13 | 1999-11-02 | Passmore; Steven E. | Method for multifragment in vivo cloning and mutation mapping |
| US7527928B2 (en) | 1996-11-29 | 2009-05-05 | Third Wave Technologies, Inc. | Reactions on a solid surface |
| US7122364B1 (en) | 1998-03-24 | 2006-10-17 | Third Wave Technologies, Inc. | FEN endonucleases |
| US6562611B1 (en) | 1996-11-29 | 2003-05-13 | Third Wave Technologies, Ins. | FEN-1 endonucleases, mixtures and cleavage methods |
| US7432048B2 (en) | 1996-11-29 | 2008-10-07 | Third Wave Technologies, Inc. | Reactions on a solid surface |
| US5985557A (en) | 1996-01-24 | 1999-11-16 | Third Wave Technologies, Inc. | Invasive cleavage of nucleic acids |
| US6706471B1 (en) | 1996-01-24 | 2004-03-16 | Third Wave Technologies, Inc. | Detection of nucleic acid sequences by invader-directed cleavage |
| US6090606A (en) | 1996-01-24 | 2000-07-18 | Third Wave Technologies, Inc. | Cleavage agents |
| US6274369B1 (en) | 1996-02-02 | 2001-08-14 | Invitrogen Corporation | Method capable of increasing competency of bacterial cell transformation |
| US6013440A (en) | 1996-03-11 | 2000-01-11 | Affymetrix, Inc. | Nucleic acid affinity columns |
| US6020481A (en) | 1996-04-01 | 2000-02-01 | The Perkin-Elmer Corporation | Asymmetric benzoxanthene dyes |
| US6706875B1 (en) | 1996-04-17 | 2004-03-16 | Affyemtrix, Inc. | Substrate preparation process |
| US5869245A (en) | 1996-06-05 | 1999-02-09 | Fox Chase Cancer Center | Mismatch endonuclease and its use in identifying mutations in targeted polynucleotide strands |
| US5863801A (en) | 1996-06-14 | 1999-01-26 | Sarnoff Corporation | Automated nucleic acid isolation |
| US6780982B2 (en) | 1996-07-12 | 2004-08-24 | Third Wave Technologies, Inc. | Charge tags and the separation of nucleic acid molecules |
| US5853993A (en) | 1996-10-21 | 1998-12-29 | Hewlett-Packard Company | Signal enhancement method and kit |
| WO1998022541A2 (en) | 1996-11-08 | 1998-05-28 | Ikonos Corporation | Method for coating substrates |
| US5750672A (en) | 1996-11-22 | 1998-05-12 | Barrskogen, Inc. | Anhydrous amine cleavage of oligonucleotides |
| CA2276462C (en) | 1996-12-31 | 2007-06-12 | Genometrix Incorporated | Multiplexed molecular analysis system apparatus and method |
| EP1005529B1 (en) | 1997-02-12 | 2005-04-27 | Invitrogen Corporation | Methods for lyophilizing competent cells |
| US5882496A (en) | 1997-02-27 | 1999-03-16 | The Regents Of The University Of California | Porous silicon structures with high surface area/specific pore size |
| US6770748B2 (en) | 1997-03-07 | 2004-08-03 | Takeshi Imanishi | Bicyclonucleoside and oligonucleotide analogue |
| US6028189A (en) | 1997-03-20 | 2000-02-22 | University Of Washington | Solvent for oligonucleotide synthesis and methods of use |
| US6384210B1 (en) | 1997-03-20 | 2002-05-07 | University Of Washington | Solvent for biopolymer synthesis, solvent microdroplets and methods of use |
| US6419883B1 (en) | 1998-01-16 | 2002-07-16 | University Of Washington | Chemical synthesis using solvent microdroplets |
| ATE378417T1 (de) | 1997-03-21 | 2007-11-15 | Stratagene California | Polymerase-verbessernder faktor (pef)-enthaltende extrakte, pef proteinkomplexe, isoliertes pef protein und verfahren zur reinigung und identifizierung |
| US5922593A (en) | 1997-05-23 | 1999-07-13 | Becton, Dickinson And Company | Microbiological test panel and method therefor |
| US6969488B2 (en) | 1998-05-22 | 2005-11-29 | Solexa, Inc. | System and apparatus for sequential processing of analytes |
| DE69824586T2 (de) | 1997-06-26 | 2005-06-23 | PerSeptive Biosystems, Inc., Framingham | Probenträger hoher dichte für die analyse biologischer proben |
| GB9714716D0 (en) | 1997-07-11 | 1997-09-17 | Brax Genomics Ltd | Characterising nucleic acids |
| US5989872A (en) | 1997-08-12 | 1999-11-23 | Clontech Laboratories, Inc. | Methods and compositions for transferring DNA sequence information among vectors |
| US6027898A (en) | 1997-08-18 | 2000-02-22 | Transgenomic, Inc. | Chromatographic method for mutation detection using mutation site specifically acting enzymes and chemicals |
| US6794499B2 (en) | 1997-09-12 | 2004-09-21 | Exiqon A/S | Oligonucleotide analogues |
| US6136568A (en) | 1997-09-15 | 2000-10-24 | Hiatt; Andrew C. | De novo polynucleotide synthesis using rolling templates |
| DE69841578D1 (de) | 1997-09-16 | 2010-05-06 | Centocor Inc | Methoden zur kompletten chemischen Synthese und Zusammensetzung von Genen und Genomen |
| US6670127B2 (en) | 1997-09-16 | 2003-12-30 | Egea Biosciences, Inc. | Method for assembly of a polynucleotide encoding a target polypeptide |
| US5976842A (en) | 1997-10-30 | 1999-11-02 | Clontech Laboratories, Inc. | Methods and compositions for use in high fidelity polymerase chain reaction |
| US8182991B1 (en) | 1997-11-26 | 2012-05-22 | Third Wave Technologies, Inc. | FEN-1 endonucleases, mixtures and cleavage methods |
| US6408308B1 (en) | 1998-01-29 | 2002-06-18 | Incyte Pharmaceuticals, Inc. | System and method for generating, analyzing and storing normalized expression datasets from raw expression datasets derived from microarray includes nucleic acid probe sequences |
| US6287776B1 (en) | 1998-02-02 | 2001-09-11 | Signature Bioscience, Inc. | Method for detecting and classifying nucleic acid hybridization |
| US6251588B1 (en) | 1998-02-10 | 2001-06-26 | Agilent Technologies, Inc. | Method for evaluating oligonucleotide probe sequences |
| ATE246041T1 (de) | 1998-02-11 | 2003-08-15 | Univ Houston Office Of Technol | Vorrichtung zur durchführung chemischer und biochemischer reaktionen unter anwendung von photoerzeugten reagenzien |
| US6375903B1 (en) | 1998-02-23 | 2002-04-23 | Wisconsin Alumni Research Foundation | Method and apparatus for synthesis of arrays of DNA probes |
| CA2325468C (en) | 1998-03-25 | 2008-11-18 | Ulf Landegren | Rolling circle replication of padlock probes |
| US6284497B1 (en) | 1998-04-09 | 2001-09-04 | Trustees Of Boston University | Nucleic acid arrays and methods of synthesis |
| US7321828B2 (en) | 1998-04-13 | 2008-01-22 | Isis Pharmaceuticals, Inc. | System of components for preparing oligonucleotides |
| AU762397B2 (en) | 1998-04-13 | 2003-06-26 | Isis Pharmaceuticals, Inc. | Identification of genetic targets for modulation by oligonucleotides and generation of oligonucleotides for gene modulation |
| US6376285B1 (en) | 1998-05-28 | 2002-04-23 | Texas Instruments Incorporated | Annealed porous silicon with epitaxial layer for SOI |
| US6274725B1 (en) | 1998-06-02 | 2001-08-14 | Isis Pharmaceuticals, Inc. | Activators for oligonucleotide synthesis |
| US6130045A (en) | 1998-06-11 | 2000-10-10 | Clontech Laboratories, Inc. | Thermostable polymerase |
| US6251595B1 (en) | 1998-06-18 | 2001-06-26 | Agilent Technologies, Inc. | Methods and devices for carrying out chemical reactions |
| ATE313548T1 (de) | 1998-06-22 | 2006-01-15 | Affymetrix Inc | Reagenz und verfahren zu fester phase synthese |
| US6218118B1 (en) | 1998-07-09 | 2001-04-17 | Agilent Technologies, Inc. | Method and mixture reagents for analyzing the nucleotide sequence of nucleic acids by mass spectrometry |
| US7399844B2 (en) | 1998-07-09 | 2008-07-15 | Agilent Technologies, Inc. | Method and reagents for analyzing the nucleotide sequence of nucleic acids |
| US20030022207A1 (en) | 1998-10-16 | 2003-01-30 | Solexa, Ltd. | Arrayed polynucleotides and their use in genome analysis |
| US6787308B2 (en) | 1998-07-30 | 2004-09-07 | Solexa Ltd. | Arrayed biomolecules and their use in sequencing |
| US6222030B1 (en) | 1998-08-03 | 2001-04-24 | Agilent Technologies, Inc. | Solid phase synthesis of oligonucleotides using carbonate protecting groups and alpha-effect nucleophile deprotection |
| US6991922B2 (en) | 1998-08-12 | 2006-01-31 | Proteus S.A. | Process for in vitro creation of recombinant polynucleotide sequences by oriented ligation |
| US6951719B1 (en) | 1999-08-11 | 2005-10-04 | Proteus S.A. | Process for obtaining recombined nucleotide sequences in vitro, libraries of sequences and sequences thus obtained |
| US6107038A (en) | 1998-08-14 | 2000-08-22 | Agilent Technologies Inc. | Method of binding a plurality of chemicals on a substrate by electrophoretic self-assembly |
| EP2273270A1 (de) | 1998-08-28 | 2011-01-12 | febit holding GmbH | Verfahren und Vorrichtung zur Herstellung und/oder Analyse von biochemischen Reaktionsträgern |
| US6258454B1 (en) | 1998-09-01 | 2001-07-10 | Agilent Technologies Inc. | Functionalization of substrate surfaces with silane mixtures |
| US6461812B2 (en) | 1998-09-09 | 2002-10-08 | Agilent Technologies, Inc. | Method and multiple reservoir apparatus for fabrication of biomolecular arrays |
| US6458583B1 (en) | 1998-09-09 | 2002-10-01 | Agilent Technologies, Inc. | Method and apparatus for making nucleic acid arrays |
| EP1114184A2 (en) | 1998-09-15 | 2001-07-11 | Yale University | Molecular cloning using rolling circle amplification |
| AR021833A1 (es) | 1998-09-30 | 2002-08-07 | Applied Research Systems | Metodos de amplificacion y secuenciacion de acido nucleico |
| US6399516B1 (en) | 1998-10-30 | 2002-06-04 | Massachusetts Institute Of Technology | Plasma etch techniques for fabricating silicon structures from a substrate |
| US6309828B1 (en) | 1998-11-18 | 2001-10-30 | Agilent Technologies, Inc. | Method and apparatus for fabricating replicate arrays of nucleic acid molecules |
| GB9900298D0 (en) | 1999-01-07 | 1999-02-24 | Medical Res Council | Optical sorting method |
| AU2415200A (en) | 1999-01-18 | 2000-08-01 | Maxygen, Inc. | Methods of populating data structures for use in evolutionary simulations |
| US6376246B1 (en) | 1999-02-05 | 2002-04-23 | Maxygen, Inc. | Oligonucleotide mediated nucleic acid recombination |
| US20070065838A1 (en) | 1999-01-19 | 2007-03-22 | Maxygen, Inc. | Oligonucleotide mediated nucleic acid recombination |
| EP2253704B1 (en) | 1999-01-19 | 2015-08-19 | Codexis Mayflower Holdings, LLC | Oligonucleotide mediated nucleic acid recombination |
| US6251685B1 (en) | 1999-02-18 | 2001-06-26 | Agilent Technologies, Inc. | Readout method for molecular biological electronically addressable arrays |
| CA2362939C (en) | 1999-02-19 | 2010-07-27 | Febit Ferrarius Biotechnology Gmbh | Method for producing polymers |
| ATE508200T1 (de) | 1999-02-23 | 2011-05-15 | Caliper Life Sciences Inc | Sequenzierung durch inkorporation |
| ATE296310T1 (de) | 1999-03-08 | 2005-06-15 | Metrigen Inc | Syntheseverfahren zum ökonomischen aufbau langer dna-sequenzen und zusammensetzungen hierfür |
| US6824866B1 (en) | 1999-04-08 | 2004-11-30 | Affymetrix, Inc. | Porous silica substrates for polymer synthesis and assays |
| US6284465B1 (en) | 1999-04-15 | 2001-09-04 | Agilent Technologies, Inc. | Apparatus, systems and method for locating nucleic acids bound to surfaces |
| US6469156B1 (en) | 1999-04-20 | 2002-10-22 | The United States Of America As Represented By The Department Of Health And Human Services | Rapid and sensitive method for detecting histoplasma capsulatum |
| US6518056B2 (en) | 1999-04-27 | 2003-02-11 | Agilent Technologies Inc. | Apparatus, systems and method for assaying biological materials using an annular format |
| US6221653B1 (en) | 1999-04-27 | 2001-04-24 | Agilent Technologies, Inc. | Method of performing array-based hybridization assays using thermal inkjet deposition of sample fluids |
| US6773676B2 (en) | 1999-04-27 | 2004-08-10 | Agilent Technologies, Inc. | Devices for performing array hybridization assays and methods of using the same |
| US6300137B1 (en) | 1999-04-28 | 2001-10-09 | Agilent Technologies Inc. | Method for synthesizing a specific, surface-bound polymer uniformly over an element of a molecular array |
| US6242266B1 (en) | 1999-04-30 | 2001-06-05 | Agilent Technologies Inc. | Preparation of biopolymer arrays |
| US7276336B1 (en) | 1999-07-22 | 2007-10-02 | Agilent Technologies, Inc. | Methods of fabricating an addressable array of biopolymer probes |
| US6323043B1 (en) | 1999-04-30 | 2001-11-27 | Agilent Technologies, Inc. | Fabricating biopolymer arrays |
| DE60008517T2 (de) | 1999-05-01 | 2004-12-16 | Psimedica Ltd., Malvern | Derivatisiertes poröses silicium |
| CA2395874C (en) | 1999-05-06 | 2011-09-20 | Frank Carter Bancroft | Dna-based steganography |
| US7056661B2 (en) | 1999-05-19 | 2006-06-06 | Cornell Research Foundation, Inc. | Method for sequencing nucleic acid molecules |
| ATE415409T1 (de) | 1999-05-24 | 2008-12-15 | Invitrogen Corp | Ein verfahren zum entschützen markierter oligonukleotide |
| US6472147B1 (en) | 1999-05-25 | 2002-10-29 | The Scripps Research Institute | Methods for display of heterodimeric proteins on filamentous phage using pVII and pIX, compositions, vectors and combinatorial libraries |
| US6132997A (en) | 1999-05-28 | 2000-10-17 | Agilent Technologies | Method for linear mRNA amplification |
| US6815218B1 (en) | 1999-06-09 | 2004-11-09 | Massachusetts Institute Of Technology | Methods for manufacturing bioelectronic devices |
| DE19928410C2 (de) | 1999-06-22 | 2002-11-28 | Agilent Technologies Inc | Gerätegehäuse mit einer Einrichtung zum Betrieb eines Labor-Mikrochips |
| US6709852B1 (en) | 1999-06-22 | 2004-03-23 | Invitrogen Corporation | Rapid growing microorganisms for biotechnology applications |
| US7537886B1 (en) | 1999-06-22 | 2009-05-26 | Life Technologies Corporation | Primers and methods for the detection and discrimination of nucleic acids |
| US6399394B1 (en) | 1999-06-30 | 2002-06-04 | Agilent Technologies, Inc. | Testing multiple fluid samples with multiple biopolymer arrays |
| US6465183B2 (en) | 1999-07-01 | 2002-10-15 | Agilent Technologies, Inc. | Multidentate arrays |
| US7504213B2 (en) | 1999-07-09 | 2009-03-17 | Agilent Technologies, Inc. | Methods and apparatus for preparing arrays comprising features having degenerate biopolymers |
| US6461816B1 (en) | 1999-07-09 | 2002-10-08 | Agilent Technologies, Inc. | Methods for controlling cross-hybridization in analysis of nucleic acid sequences |
| US6346423B1 (en) | 1999-07-16 | 2002-02-12 | Agilent Technologies, Inc. | Methods and compositions for producing biopolymeric arrays |
| US6306599B1 (en) | 1999-07-16 | 2001-10-23 | Agilent Technologies Inc. | Biopolymer arrays and their fabrication |
| US6201112B1 (en) | 1999-07-22 | 2001-03-13 | Agilent Technologies Inc. | Method for 3′ end-labeling ribonucleic acids |
| US6180351B1 (en) | 1999-07-22 | 2001-01-30 | Agilent Technologies Inc. | Chemical array fabrication with identifier |
| AU775380B2 (en) | 1999-08-18 | 2004-07-29 | Illumina, Inc. | Compositions and methods for preparing oligonucleotide solutions |
| US6262490B1 (en) | 1999-11-05 | 2001-07-17 | Advanced Semiconductor Engineering, Inc. | Substrate strip for use in packaging semiconductor chips |
| US6319674B1 (en) | 1999-09-16 | 2001-11-20 | Agilent Technologies, Inc. | Methods for attaching substances to surfaces |
| US7244559B2 (en) | 1999-09-16 | 2007-07-17 | 454 Life Sciences Corporation | Method of sequencing a nucleic acid |
| US6743585B2 (en) | 1999-09-16 | 2004-06-01 | Agilent Technologies, Inc. | Methods for preparing conjugates |
| US7211390B2 (en) | 1999-09-16 | 2007-05-01 | 454 Life Sciences Corporation | Method of sequencing a nucleic acid |
| US7122303B2 (en) | 1999-09-17 | 2006-10-17 | Agilent Technologies, Inc. | Arrays comprising background features that provide for a measure of a non-specific binding and methods for using the same |
| US7078167B2 (en) | 1999-09-17 | 2006-07-18 | Agilent Technologies, Inc. | Arrays having background features and methods for using the same |
| AU7537200A (en) | 1999-09-29 | 2001-04-30 | Solexa Ltd. | Polynucleotide sequencing |
| DE19947495C2 (de) | 1999-10-01 | 2003-05-28 | Agilent Technologies Inc | Mikrofluidischer Mikrochip |
| AU1075701A (en) | 1999-10-08 | 2001-04-23 | Protogene Laboratories, Inc. | Method and apparatus for performing large numbers of reactions using array assembly |
| US6232072B1 (en) | 1999-10-15 | 2001-05-15 | Agilent Technologies, Inc. | Biopolymer array inspection |
| US6451998B1 (en) | 1999-10-18 | 2002-09-17 | Agilent Technologies, Inc. | Capping and de-capping during oligonucleotide synthesis |
| US6171797B1 (en) | 1999-10-20 | 2001-01-09 | Agilent Technologies Inc. | Methods of making polymeric arrays |
| US6387636B1 (en) | 1999-10-22 | 2002-05-14 | Agilent Technologies, Inc. | Method of shielding biosynthesis reactions from the ambient environment on an array |
| US7115423B1 (en) | 1999-10-22 | 2006-10-03 | Agilent Technologies, Inc. | Fluidic structures within an array package |
| US6077674A (en) | 1999-10-27 | 2000-06-20 | Agilent Technologies Inc. | Method of producing oligonucleotide arrays with features of high purity |
| US20010055761A1 (en) | 1999-10-29 | 2001-12-27 | Agilent Technologies | Small scale dna synthesis using polymeric solid support with functionalized regions |
| US8268605B2 (en) | 1999-10-29 | 2012-09-18 | Agilent Technologies, Inc. | Compositions and methods utilizing DNA polymerases |
| US6329210B1 (en) | 1999-10-29 | 2001-12-11 | Agilent Technologies, Inc. | Method and apparatus for high volume polymer synthesis |
| US6689319B1 (en) | 1999-10-29 | 2004-02-10 | Agilent Technologies, Ind. | Apparatus for deposition and inspection of chemical and biological fluids |
| US6406849B1 (en) | 1999-10-29 | 2002-06-18 | Agilent Technologies, Inc. | Interrogating multi-featured arrays |
| US6428957B1 (en) | 1999-11-08 | 2002-08-06 | Agilent Technologies, Inc. | Systems tools and methods of assaying biological materials using spatially-addressable arrays |
| US6440669B1 (en) | 1999-11-10 | 2002-08-27 | Agilent Technologies, Inc. | Methods for applying small volumes of reagents |
| US7041445B2 (en) | 1999-11-15 | 2006-05-09 | Clontech Laboratories, Inc. | Long oligonucleotide arrays |
| US6446642B1 (en) | 1999-11-22 | 2002-09-10 | Agilent Technologies, Inc. | Method and apparatus to clean an inkjet reagent deposition device |
| US6582938B1 (en) | 2001-05-11 | 2003-06-24 | Affymetrix, Inc. | Amplification of nucleic acids |
| US6800439B1 (en) | 2000-01-06 | 2004-10-05 | Affymetrix, Inc. | Methods for improved array preparation |
| JP2003519495A (ja) | 2000-01-11 | 2003-06-24 | マキシジェン, インコーポレイテッド | 多様性生成およびスクリーニングのための一体化されたシステムおよび方法 |
| EP1118661A1 (en) | 2000-01-13 | 2001-07-25 | Het Nederlands Kanker Instituut | T cell receptor libraries |
| WO2001056216A2 (en) | 2000-01-25 | 2001-08-02 | Affymetrix, Inc. | Method, system and computer software for providing a genomic web portal |
| US6587579B1 (en) | 2000-01-26 | 2003-07-01 | Agilent Technologies Inc. | Feature quality in array fabrication |
| US7198939B2 (en) | 2000-01-28 | 2007-04-03 | Agilent Technologies, Inc. | Apparatus for interrogating an addressable array |
| US6406851B1 (en) | 2000-01-28 | 2002-06-18 | Agilent Technologies, Inc. | Method for coating a substrate quickly and uniformly with a small volume of fluid |
| US6458526B1 (en) | 2000-01-28 | 2002-10-01 | Agilent Technologies, Inc. | Method and apparatus to inhibit bubble formation in a fluid |
| US6235483B1 (en) | 2000-01-31 | 2001-05-22 | Agilent Technologies, Inc. | Methods and kits for indirect labeling of nucleic acids |
| GB0002389D0 (en) | 2000-02-02 | 2000-03-22 | Solexa Ltd | Molecular arrays |
| US6403314B1 (en) | 2000-02-04 | 2002-06-11 | Agilent Technologies, Inc. | Computational method and system for predicting fragmented hybridization and for identifying potential cross-hybridization |
| US6833450B1 (en) | 2000-03-17 | 2004-12-21 | Affymetrix, Inc. | Phosphite ester oxidation in nucleic acid array preparation |
| US6365355B1 (en) | 2000-03-28 | 2002-04-02 | The Regents Of The University Of California | Chimeric proteins for detection and quantitation of DNA mutations, DNA sequence variations, DNA damage and DNA mismatches |
| US20020025561A1 (en) | 2000-04-17 | 2002-02-28 | Hodgson Clague Pitman | Vectors for gene-self-assembly |
| US7776021B2 (en) | 2000-04-28 | 2010-08-17 | The Charles Stark Draper Laboratory | Micromachined bilayer unit for filtration of small molecules |
| US7163660B2 (en) | 2000-05-31 | 2007-01-16 | Infineon Technologies Ag | Arrangement for taking up liquid analytes |
| US6716634B1 (en) | 2000-05-31 | 2004-04-06 | Agilent Technologies, Inc. | Increasing ionization efficiency in mass spectrometry |
| EP1287010A1 (en) | 2000-06-02 | 2003-03-05 | Blue Heron Biotechnology, Inc. | Methods for improving the sequence fidelity of synthetic double-stranded oligonucleotides |
| US6686193B2 (en) | 2000-07-10 | 2004-02-03 | Vertex Pharmaceuticals, Inc. | High throughput method and system for screening candidate compounds for activity against target ion channels |
| WO2002010443A1 (en) | 2000-07-27 | 2002-02-07 | The Australian National University | Combinatorial probes and uses therefor |
| EP1176151B1 (en) | 2000-07-28 | 2014-08-20 | Agilent Technologies, Inc. | Synthesis of polynucleotides using combined oxidation/deprotection chemistry |
| EP1180548B1 (en) | 2000-07-31 | 2005-11-02 | Agilent Technologies, Inc. (a Delaware corporation) | Array based methods for synthesizing nucleic acid mixtures |
| US6599693B1 (en) | 2000-07-31 | 2003-07-29 | Agilent Technologies Inc. | Array fabrication |
| US6890760B1 (en) | 2000-07-31 | 2005-05-10 | Agilent Technologies, Inc. | Array fabrication |
| US7205400B2 (en) | 2000-07-31 | 2007-04-17 | Agilent Technologies, Inc. | Array fabrication |
| US6613893B1 (en) | 2000-07-31 | 2003-09-02 | Agilent Technologies Inc. | Array fabrication |
| GB0018876D0 (en) | 2000-08-01 | 2000-09-20 | Applied Research Systems | Method of producing polypeptides |
| JP2004527215A (ja) | 2000-08-24 | 2004-09-09 | マキシジェン, インコーポレイテッド | 構築物、および代謝経路操作におけるそれらの使用 |
| AU2001291540A1 (en) | 2000-09-08 | 2002-03-22 | University Technologies International, Inc. | Linker phosphoramidites for oligonucleotide synthesis |
| US6966945B1 (en) | 2000-09-20 | 2005-11-22 | Goodrich Corporation | Inorganic matrix compositions, composites and process of making the same |
| WO2002027029A2 (en) | 2000-09-27 | 2002-04-04 | Lynx Therapeutics, Inc. | Method for determining relative abundance of nucleic acid sequences |
| NO20004869D0 (no) | 2000-09-28 | 2000-09-28 | Torbjoern Rognes | Metode for hurtig optimal lokal sekvensjustering ved bruk av parallell prosessering |
| US7097809B2 (en) | 2000-10-03 | 2006-08-29 | California Institute Of Technology | Combinatorial synthesis system |
| JP4361271B2 (ja) | 2000-10-10 | 2009-11-11 | バイオトローブ・インコーポレイテツド | アッセイ、合成、および保存用の器具、ならびに、その作製、使用、および操作の方法 |
| DE10051396A1 (de) | 2000-10-17 | 2002-04-18 | Febit Ferrarius Biotech Gmbh | Verfahren und Vorrichtung zur integrierten Synthese und Analytbestimmung an einem Träger |
| US6693187B1 (en) | 2000-10-17 | 2004-02-17 | Lievre Cornu Llc | Phosphinoamidite carboxlates and analogs thereof in the synthesis of oligonucleotides having reduced internucleotide charge |
| SI1327230T1 (ja) | 2000-10-18 | 2005-08-31 | Ultra Proizv Elektronskih Napr | |
| EP1203945B1 (en) | 2000-10-26 | 2006-12-20 | Agilent Technologies, Inc. (a Delaware corporation) | Microarray |
| US6905816B2 (en) | 2000-11-27 | 2005-06-14 | Intelligent Medical Devices, Inc. | Clinically intelligent diagnostic devices and methods |
| US20020155439A1 (en) | 2000-12-04 | 2002-10-24 | Ana Rodriguez | Method for generating a library of mutant oligonucleotides using the linear cyclic amplification reaction |
| DE10060433B4 (de) | 2000-12-05 | 2006-05-11 | Hahn-Schickard-Gesellschaft für angewandte Forschung e.V. | Verfahren zur Herstellung eines Fluidbauelements, Fluidbauelement und Analysevorrichtung |
| US6768005B2 (en) | 2000-12-20 | 2004-07-27 | Avecia Limited | Process |
| CA2437040C (en) | 2000-12-05 | 2011-01-25 | Avecia Limited | Process for the preparation of phosphorothioate oligonucleotides |
| US20040253242A1 (en) | 2000-12-05 | 2004-12-16 | Bowdish Katherine S. | Rationally designed antibodies |
| US6660475B2 (en) | 2000-12-15 | 2003-12-09 | New England Biolabs, Inc. | Use of site-specific nicking endonucleases to create single-stranded regions and applications thereof |
| AUPR259301A0 (en) | 2001-01-18 | 2001-02-15 | Polymerat Pty Ltd | Polymers having co-continuous architecture |
| DE60227361D1 (de) | 2001-01-19 | 2008-08-14 | Centocor Inc | Computer vermitteltes assembly von polynucleotiden kodierend für ein zielgerichtetes polypeptide |
| US6958217B2 (en) | 2001-01-24 | 2005-10-25 | Genomic Expression Aps | Single-stranded polynucleotide tags |
| US7027930B2 (en) | 2001-01-31 | 2006-04-11 | Agilent Technologies, Inc. | Reading chemical arrays |
| US6879915B2 (en) | 2001-01-31 | 2005-04-12 | Agilent Technologies, Inc. | Chemical array fabrication and use |
| US7166258B2 (en) | 2001-01-31 | 2007-01-23 | Agilent Technologies, Inc. | Automation-optimized microarray package |
| US20020164824A1 (en) | 2001-02-16 | 2002-11-07 | Jianming Xiao | Method and apparatus based on bundled capillaries for high throughput screening |
| US6660338B1 (en) | 2001-03-08 | 2003-12-09 | Agilent Technologies, Inc. | Functionalization of substrate surfaces with silane mixtures |
| WO2002072864A2 (en) | 2001-03-08 | 2002-09-19 | Applera Corporation | Reagents for oligonucleotide cleavage and deprotection |
| US7211654B2 (en) | 2001-03-14 | 2007-05-01 | Regents Of The University Of Michigan | Linkers and co-coupling agents for optimization of oligonucleotide synthesis and purification on solid supports |
| EP2801624B1 (en) | 2001-03-16 | 2019-03-06 | Singular Bio, Inc | Arrays and methods of use |
| US6610978B2 (en) | 2001-03-27 | 2003-08-26 | Agilent Technologies, Inc. | Integrated sample preparation, separation and introduction microdevice for inductively coupled plasma mass spectrometry |
| WO2002078947A1 (en) | 2001-04-02 | 2002-10-10 | Prolinx Incorporated | Sensor surfaces for detecting analytes |
| US20030022240A1 (en) | 2001-04-17 | 2003-01-30 | Peizhi Luo | Generation and affinity maturation of antibody library in silico |
| US6943036B2 (en) | 2001-04-30 | 2005-09-13 | Agilent Technologies, Inc. | Error detection in chemical array fabrication |
| WO2002090923A2 (en) | 2001-05-03 | 2002-11-14 | Sigma-Genosys, Ltd. | Methods for assembling protein microarrays |
| EP1392868B2 (en) | 2001-05-18 | 2013-09-04 | Wisconsin Alumni Research Foundation | Method for the synthesis of dna sequences using photo-labile linkers |
| WO2002094846A2 (en) | 2001-05-22 | 2002-11-28 | Parallel Synthesis Technologies, Inc. | Method for in situ, on-chip chemical synthesis |
| US6880576B2 (en) | 2001-06-07 | 2005-04-19 | Nanostream, Inc. | Microfluidic devices for methods development |
| US6613523B2 (en) | 2001-06-29 | 2003-09-02 | Agilent Technologies, Inc. | Method of DNA sequencing using cleavable tags |
| US6649348B2 (en) | 2001-06-29 | 2003-11-18 | Agilent Technologies Inc. | Methods for manufacturing arrays |
| US20040161741A1 (en) | 2001-06-30 | 2004-08-19 | Elazar Rabani | Novel compositions and processes for analyte detection, quantification and amplification |
| US6989267B2 (en) | 2001-07-02 | 2006-01-24 | Agilent Technologies, Inc. | Methods of making microarrays with substrate surfaces having covalently bound polyelectrolyte films |
| US6753145B2 (en) | 2001-07-05 | 2004-06-22 | Agilent Technologies, Inc. | Buffer composition and method for hybridization of microarrays on adsorbed polymer siliceous surfaces |
| US7205399B1 (en) | 2001-07-06 | 2007-04-17 | Sirna Therapeutics, Inc. | Methods and reagents for oligonucleotide synthesis |
| US7128876B2 (en) | 2001-07-17 | 2006-10-31 | Agilent Technologies, Inc. | Microdevice and method for component separation in a fluid |
| US7314599B2 (en) | 2001-07-17 | 2008-01-01 | Agilent Technologies, Inc. | Paek embossing and adhesion for microfluidic devices |
| US6702256B2 (en) | 2001-07-17 | 2004-03-09 | Agilent Technologies, Inc. | Flow-switching microdevice |
| US20030108903A1 (en) | 2001-07-19 | 2003-06-12 | Liman Wang | Multiple word DNA computing on surfaces |
| US8067556B2 (en) | 2001-07-26 | 2011-11-29 | Agilent Technologies, Inc. | Multi-site mutagenesis |
| WO2003014325A2 (en) | 2001-08-10 | 2003-02-20 | Xencor | Protein design automation for protein libraries |
| US7371580B2 (en) | 2001-08-24 | 2008-05-13 | Agilent Technologies, Inc. | Use of unstructured nucleic acids in assaying nucleic acid molecules |
| US6682702B2 (en) | 2001-08-24 | 2004-01-27 | Agilent Technologies, Inc. | Apparatus and method for simultaneously conducting multiple chemical reactions |
| JP2003101204A (ja) | 2001-09-25 | 2003-04-04 | Nec Kansai Ltd | 配線基板及び配線基板の製造方法並びに電子部品 |
| US20030082618A1 (en) | 2001-10-15 | 2003-05-01 | Guangshan Li | Methods for detecting genetic aberrations |
| US20050124022A1 (en) | 2001-10-30 | 2005-06-09 | Maithreyan Srinivasan | Novel sulfurylase-luciferase fusion proteins and thermostable sulfurylase |
| US6902921B2 (en) | 2001-10-30 | 2005-06-07 | 454 Corporation | Sulfurylase-luciferase fusion proteins and thermostable sulfurylase |
| US7524950B2 (en) | 2001-10-31 | 2009-04-28 | Agilent Technologies, Inc. | Uses of cationic salts for polynucleotide synthesis |
| US6852850B2 (en) | 2001-10-31 | 2005-02-08 | Agilent Technologies, Inc. | Use of ionic liquids for fabrication of polynucleotide arrays |
| US6858720B2 (en) | 2001-10-31 | 2005-02-22 | Agilent Technologies, Inc. | Method of synthesizing polynucleotides using ionic liquids |
| WO2003040410A1 (en) | 2001-11-02 | 2003-05-15 | Nimblegen Systems, Inc. | Detection of hybridization oligonucleotide microarray through covalently labeling microarray probe |
| ATE509272T1 (de) | 2001-11-09 | 2011-05-15 | 3Dbiosurfaces Technologies Llc | Substrate mit hochliegendem oberflächenbereich für mikroarrays sowie verfahren zur herstellung davon |
| US7482118B2 (en) | 2001-11-15 | 2009-01-27 | Third Wave Technologies, Inc. | Endonuclease-substrate complexes |
| ATE414767T1 (de) | 2001-11-22 | 2008-12-15 | Sloning Biotechnology Gmbh | Nukleinsäure-linker und deren verwendung in der gensynthese |
| US20030099952A1 (en) | 2001-11-26 | 2003-05-29 | Roland Green | Microarrays with visible pattern detection |
| WO2003048395A1 (en) | 2001-12-03 | 2003-06-12 | Zymogenetics, Inc. | Methods for the selection and cloning of nucleic acid molecules free of unwanted nucleotide sequence alterations |
| US6927029B2 (en) | 2001-12-03 | 2005-08-09 | Agilent Technologies, Inc. | Surface with tethered polymeric species for binding biomolecules |
| WO2003054232A2 (en) | 2001-12-13 | 2003-07-03 | Blue Heron Biotechnology, Inc. | Methods for removal of double-stranded oligonucleotides containing sequence errors using mismatch recognition proteins |
| US6838888B2 (en) | 2001-12-13 | 2005-01-04 | Agilent Technologies, Inc. | Flow cell humidity sensor system |
| US7932070B2 (en) | 2001-12-21 | 2011-04-26 | Agilent Technologies, Inc. | High fidelity DNA polymerase compositions and uses therefor |
| US6846454B2 (en) | 2001-12-24 | 2005-01-25 | Agilent Technologies, Inc. | Fluid exit in reaction chambers |
| US6790620B2 (en) | 2001-12-24 | 2004-09-14 | Agilent Technologies, Inc. | Small volume chambers |
| US7282183B2 (en) | 2001-12-24 | 2007-10-16 | Agilent Technologies, Inc. | Atmospheric control in reaction chambers |
| AU2003207448A1 (en) | 2002-01-04 | 2003-07-24 | Board Of Regents, The University Of Texas System | Proofreading, error deletion, and ligation method for synthesis of high-fidelity polynucleotide sequences |
| US7025324B1 (en) | 2002-01-04 | 2006-04-11 | Massachusetts Institute Of Technology | Gating apparatus and method of manufacture |
| US6673552B2 (en) | 2002-01-14 | 2004-01-06 | Diversa Corporation | Methods for purifying annealed double-stranded oligonucleotides lacking base pair mismatches or nucleotide gaps |
| AU2003217207A1 (en) | 2002-01-14 | 2003-07-30 | Verenium Corporation | Methods for making polynucleotides and purifying double-stranded polynucleotides |
| US20040009498A1 (en) | 2002-01-14 | 2004-01-15 | Diversa Corporation | Chimeric antigen binding molecules and methods for making and using them |
| US7141368B2 (en) | 2002-01-30 | 2006-11-28 | Agilent Technologies, Inc. | Multi-directional deposition in array fabrication |
| US20040126757A1 (en) | 2002-01-31 | 2004-07-01 | Francesco Cerrina | Method and apparatus for synthesis of arrays of DNA probes |
| US7157229B2 (en) | 2002-01-31 | 2007-01-02 | Nimblegen Systems, Inc. | Prepatterned substrate for optical synthesis of DNA probes |
| US7422851B2 (en) | 2002-01-31 | 2008-09-09 | Nimblegen Systems, Inc. | Correction for illumination non-uniformity during the synthesis of arrays of oligomers |
| US7037659B2 (en) | 2002-01-31 | 2006-05-02 | Nimblegen Systems Inc. | Apparatus for constructing DNA probes having a prismatic and kaleidoscopic light homogenizer |
| US7083975B2 (en) | 2002-02-01 | 2006-08-01 | Roland Green | Microarray synthesis instrument and method |
| US20030148291A1 (en) | 2002-02-05 | 2003-08-07 | Karla Robotti | Method of immobilizing biologically active molecules for assay purposes in a microfluidic format |
| US6728129B2 (en) | 2002-02-19 | 2004-04-27 | The Regents Of The University Of California | Multistate triple-decker dyads in three distinct architectures for information storage applications |
| US6958119B2 (en) | 2002-02-26 | 2005-10-25 | Agilent Technologies, Inc. | Mobile phase gradient generation microfluidic device |
| US6914229B2 (en) | 2002-02-28 | 2005-07-05 | Agilent Technologies, Inc. | Signal offset for prevention of data clipping in a molecular array scanner |
| US6929951B2 (en) | 2002-02-28 | 2005-08-16 | Agilent Technologies, Inc. | Method and system for molecular array scanner calibration |
| US6770892B2 (en) | 2002-02-28 | 2004-08-03 | Agilent Technologies, Inc. | Method and system for automated focus-distance determination for molecular array scanners |
| US20050084907A1 (en) | 2002-03-01 | 2005-04-21 | Maxygen, Inc. | Methods, systems, and software for identifying functional biomolecules |
| US6919181B2 (en) | 2002-03-25 | 2005-07-19 | Agilent Technologies, Inc. | Methods for generating ligand arrays |
| JP2005521419A (ja) | 2002-04-01 | 2005-07-21 | ブルー ヘロン バイオテクノロジー インコーポレイテッド | ポリヌクレオチド作製のための固相方法 |
| EP1350853A1 (en) | 2002-04-05 | 2003-10-08 | ID-Lelystad, Instituut voor Dierhouderij en Diergezondheid B.V. | Detection of polymorphisms |
| US6773888B2 (en) | 2002-04-08 | 2004-08-10 | Affymetrix, Inc. | Photoactivatable silane compounds and methods for their synthesis and use |
| CA2483338C (en) | 2002-04-22 | 2014-10-14 | Genencor International, Inc. | Method of creating a library of bacterial clones with varying levels of gene expression |
| GB0209539D0 (en) | 2002-04-26 | 2002-06-05 | Avecia Ltd | Monomer Polymer and process |
| US6946285B2 (en) | 2002-04-29 | 2005-09-20 | Agilent Technologies, Inc. | Arrays with elongated features |
| US7125523B2 (en) | 2002-04-29 | 2006-10-24 | Agilent Technologies, Inc. | Holders for arrays |
| US6621076B1 (en) | 2002-04-30 | 2003-09-16 | Agilent Technologies, Inc. | Flexible assembly for transporting sample fluids into a mass spectrometer |
| US7094537B2 (en) | 2002-04-30 | 2006-08-22 | Agilent Technologies, Inc. | Micro arrays with structured and unstructured probes |
| WO2003093504A1 (de) | 2002-05-06 | 2003-11-13 | Noxxon Pharma Ag | Verfahren zur amplifikation von nukleinsäuren |
| US20030211478A1 (en) | 2002-05-08 | 2003-11-13 | Gentel Corporation | Transcription factor profiling on a solid surface |
| US7221785B2 (en) | 2002-05-21 | 2007-05-22 | Agilent Technologies, Inc. | Method and system for measuring a molecular array background signal from a continuous background region of specified size |
| WO2003100012A2 (en) | 2002-05-24 | 2003-12-04 | Nimblegen Systems, Inc. | Microarrays and method for running hybridization reaction for multiple samples on a single microarray |
| AU2003240795A1 (en) | 2002-05-24 | 2003-12-12 | Invitrogen Corporation | Nested pcr employing degradable primers |
| US6789965B2 (en) | 2002-05-31 | 2004-09-14 | Agilent Technologies, Inc. | Dot printer with off-axis loading |
| US7537936B2 (en) | 2002-05-31 | 2009-05-26 | Agilent Technologies, Inc. | Method of testing multiple fluid samples with multiple biopolymer arrays |
| US7078505B2 (en) | 2002-06-06 | 2006-07-18 | Agilent Technologies, Inc. | Manufacture of arrays with varying deposition parameters |
| US7919308B2 (en) | 2002-06-14 | 2011-04-05 | Agilent Technologies, Inc. | Form in place gaskets for assays |
| US7351379B2 (en) | 2002-06-14 | 2008-04-01 | Agilent Technologies, Inc. | Fluid containment structure |
| US7371348B2 (en) | 2002-06-14 | 2008-05-13 | Agilent Technologies | Multiple array format |
| US6939673B2 (en) | 2002-06-14 | 2005-09-06 | Agilent Technologies, Inc. | Manufacture of arrays with reduced error impact |
| US20070275411A1 (en) | 2006-05-25 | 2007-11-29 | Mcgall Glenn H | Silane mixtures |
| US7220573B2 (en) | 2002-06-21 | 2007-05-22 | Agilent Technologies, Inc. | Array assay devices and methods of using the same |
| US6713262B2 (en) | 2002-06-25 | 2004-03-30 | Agilent Technologies, Inc. | Methods and compositions for high throughput identification of protein/nucleic acid binding pairs |
| US7894998B2 (en) | 2002-06-26 | 2011-02-22 | Agilent Technologies, Inc. | Method for identifying suitable nucleic acid probe sequences for use in nucleic acid arrays |
| US7202358B2 (en) | 2002-07-25 | 2007-04-10 | Agilent Technologies, Inc. | Methods for producing ligand arrays |
| US7452712B2 (en) | 2002-07-30 | 2008-11-18 | Applied Biosystems Inc. | Sample block apparatus and method of maintaining a microcard on a sample block |
| US6835938B2 (en) | 2002-07-31 | 2004-12-28 | Agilent Technologies, Inc. | Biopolymer array substrate thickness dependent automated focus-distance determination method for biopolymer array scanners |
| US7101508B2 (en) | 2002-07-31 | 2006-09-05 | Agilent Technologies, Inc. | Chemical array fabrication errors |
| US7153689B2 (en) | 2002-08-01 | 2006-12-26 | Agilent Technologies, Inc. | Apparatus and methods for cleaning and priming droplet dispensing devices |
| US8946387B2 (en) | 2002-08-14 | 2015-02-03 | Macrogenics, Inc. | FcγRIIB specific antibodies and methods of use thereof |
| US7205128B2 (en) | 2002-08-16 | 2007-04-17 | Agilent Technologies, Inc. | Method for synthesis of the second strand of cDNA |
| US7563600B2 (en) | 2002-09-12 | 2009-07-21 | Combimatrix Corporation | Microarray synthesis and assembly of gene-length polynucleotides |
| JP2006517090A (ja) | 2002-09-26 | 2006-07-20 | コーサン バイオサイエンシーズ, インコーポレイテッド | 合成遺伝子 |
| US7498176B2 (en) | 2002-09-27 | 2009-03-03 | Roche Nimblegen, Inc. | Microarray with hydrophobic barriers |
| CA2500936C (en) | 2002-09-30 | 2012-10-30 | Nimblegen Systems, Inc. | Parallel loading of arrays |
| CA2500783C (en) | 2002-10-01 | 2012-07-17 | Nimblegen Systems, Inc. | Microarrays having multiple oligonucleotides in single array features |
| US7129075B2 (en) | 2002-10-18 | 2006-10-31 | Transgenomic, Inc. | Isolated CEL II endonuclease |
| US8283148B2 (en) | 2002-10-25 | 2012-10-09 | Agilent Technologies, Inc. | DNA polymerase compositions for quantitative PCR and methods thereof |
| WO2004039953A2 (en) | 2002-10-28 | 2004-05-13 | Xeotron Corporation | Array oligomer synthesis and use. |
| US7402279B2 (en) | 2002-10-31 | 2008-07-22 | Agilent Technologies, Inc. | Device with integrated microfluidic and electronic components |
| US7390457B2 (en) | 2002-10-31 | 2008-06-24 | Agilent Technologies, Inc. | Integrated microfluidic array device |
| US7364896B2 (en) | 2002-10-31 | 2008-04-29 | Agilent Technologies, Inc. | Test strips including flexible array substrates and method of hybridization |
| US7422911B2 (en) | 2002-10-31 | 2008-09-09 | Agilent Technologies, Inc. | Composite flexible array substrate having flexible support |
| US7629120B2 (en) | 2002-10-31 | 2009-12-08 | Rice University | Method for assembling PCR fragments of DNA |
| AU2003287449A1 (en) | 2002-10-31 | 2004-05-25 | Nanostream, Inc. | Parallel detection chromatography systems |
| US20040086892A1 (en) | 2002-11-06 | 2004-05-06 | Crothers Donald M. | Universal tag assay |
| US7029854B2 (en) | 2002-11-22 | 2006-04-18 | Agilent Technologies, Inc. | Methods designing multiple mRNA transcript nucleic acid probe sequences for use in nucleic acid arrays |
| US7062385B2 (en) | 2002-11-25 | 2006-06-13 | Tufts University | Intelligent electro-optical nucleic acid-based sensor array and method for detecting volatile compounds in ambient air |
| RU2377253C2 (ru) | 2002-12-02 | 2009-12-27 | Амген Фремонт,Инк. | Антитела, специфичные к фактору некроза опухолей, и их применение |
| US20040110133A1 (en) | 2002-12-06 | 2004-06-10 | Affymetrix, Inc. | Functionated photoacid generator for biological microarray synthesis |
| US7879580B2 (en) | 2002-12-10 | 2011-02-01 | Massachusetts Institute Of Technology | Methods for high fidelity production of long nucleic acid molecules |
| US7932025B2 (en) | 2002-12-10 | 2011-04-26 | Massachusetts Institute Of Technology | Methods for high fidelity production of long nucleic acid molecules with error control |
| US6987263B2 (en) | 2002-12-13 | 2006-01-17 | Nanostream, Inc. | High throughput systems and methods for parallel sample analysis |
| US20060076482A1 (en) | 2002-12-13 | 2006-04-13 | Hobbs Steven E | High throughput systems and methods for parallel sample analysis |
| US7247337B1 (en) | 2002-12-16 | 2007-07-24 | Agilent Technologies, Inc. | Method and apparatus for microarray fabrication |
| US20040191810A1 (en) | 2002-12-17 | 2004-09-30 | Affymetrix, Inc. | Immersed microarrays in conical wells |
| GB0229443D0 (en) | 2002-12-18 | 2003-01-22 | Avecia Ltd | Process |
| US7960157B2 (en) | 2002-12-20 | 2011-06-14 | Agilent Technologies, Inc. | DNA polymerase blends and uses thereof |
| DE03808546T1 (de) | 2002-12-23 | 2006-01-26 | Agilent Technologies, Inc., Palo Alto | Vergleichende genomischehybridisierungstests unter verwendung von merkmalen immobilisierteroligonukleotide sowie zusammensetzungen zur durchführung davon |
| DE10260805A1 (de) | 2002-12-23 | 2004-07-22 | Geneart Gmbh | Verfahren und Vorrichtung zum Optimieren einer Nucleotidsequenz zur Expression eines Proteins |
| BR0316880A (pt) | 2002-12-23 | 2005-10-25 | Wyeth Corp | Anticorpos contra pd-1 e usos dos mesmos |
| WO2004058391A2 (de) | 2002-12-23 | 2004-07-15 | Febit Biotech Gmbh | Photoaktivierbare zweistufige schutzgruppen für die synthese von biopolymeren |
| US7372982B2 (en) | 2003-01-14 | 2008-05-13 | Agilent Technologies, Inc. | User interface for molecular array feature analysis |
| US6809277B2 (en) | 2003-01-22 | 2004-10-26 | Agilent Technologies, Inc. | Method for registering a deposited material with channel plate channels, and switch produced using same |
| EP1594950A4 (en) | 2003-01-29 | 2007-07-25 | 454 Corp | PRODUCT FOR THE PREPARATION OF SIMPLE STRANDED DNA BANKS |
| US8073626B2 (en) | 2003-01-31 | 2011-12-06 | Agilent Technologies, Inc. | Biopolymer array reading |
| US7202264B2 (en) | 2003-01-31 | 2007-04-10 | Isis Pharmaceuticals, Inc. | Supports for oligomer synthesis |
| US6950756B2 (en) | 2003-02-05 | 2005-09-27 | Agilent Technologies, Inc. | Rearrangement of microarray scan images to form virtual arrays |
| GB2398383B (en) | 2003-02-12 | 2005-03-09 | Global Genomics Ab | Method and means for nucleic acid sequencing |
| US7413709B2 (en) | 2003-02-12 | 2008-08-19 | Agilent Technologies, Inc. | PAEK-based microfluidic device with integrated electrospray emitter |
| US7244513B2 (en) | 2003-02-21 | 2007-07-17 | Nano-Proprietary, Inc. | Stain-etched silicon powder |
| US7070932B2 (en) | 2003-02-25 | 2006-07-04 | Agilent Technologies, Inc. | Methods and devices for detecting printhead misalignment of an in situ polymeric array synthesis device |
| US7252938B2 (en) | 2003-02-25 | 2007-08-07 | Agilent Technologies, Inc. | Methods and devices for producing a polymer at a location of a substrate |
| JP2004268394A (ja) | 2003-03-07 | 2004-09-30 | Canon Inc | インクジェット記録装置及びその制御方法 |
| WO2004080887A1 (en) | 2003-03-07 | 2004-09-23 | Massachusetts Institute Of Technology | Three dimensional mecrofabrication |
| US20050053968A1 (en) | 2003-03-31 | 2005-03-10 | Council Of Scientific And Industrial Research | Method for storing information in DNA |
| US7534561B2 (en) | 2003-04-02 | 2009-05-19 | Agilent Technologies, Inc. | Nucleic acid array in situ fabrication methods and arrays produced using the same |
| WO2004090170A1 (en) | 2003-04-02 | 2004-10-21 | Blue Heron Biotechnology, Inc. | Error reduction in automated gene synthesis |
| US20040219663A1 (en) | 2003-04-30 | 2004-11-04 | Page Robert D. | Biopolymer array fabrication using different drop deposition heads |
| US7269518B2 (en) | 2003-04-30 | 2007-09-11 | Agilent Technologies, Inc. | Chemical array reading |
| US7206439B2 (en) | 2003-04-30 | 2007-04-17 | Agilent Technologies, Inc. | Feature locations in array reading |
| US6916113B2 (en) | 2003-05-16 | 2005-07-12 | Agilent Technologies, Inc. | Devices and methods for fluid mixing |
| CA2526368A1 (en) | 2003-05-20 | 2004-12-02 | Fluidigm Corporation | Method and system for microfluidic device and imaging thereof |
| DE602004028933D1 (de) | 2003-05-30 | 2010-10-14 | Univ Illinois | Genexpressionsprofile zur identifizierung von genetisch bevorzugten huftieren |
| WO2004108081A2 (en) | 2003-06-02 | 2004-12-16 | Isis Pharmaceuticals, Inc. | Oligonucleotide synthesis with alternative solvents |
| US8133670B2 (en) | 2003-06-13 | 2012-03-13 | Cold Spring Harbor Laboratory | Method for making populations of defined nucleic acid molecules |
| US6938476B2 (en) | 2003-06-25 | 2005-09-06 | Agilent Technologies, Inc. | Apparatus and methods for sensing fluid levels |
| US7534563B2 (en) | 2003-06-30 | 2009-05-19 | Agilent Technologies, Inc. | Methods for producing ligand arrays |
| US20050016851A1 (en) | 2003-07-24 | 2005-01-27 | Jensen Klavs F. | Microchemical method and apparatus for synthesis and coating of colloidal nanoparticles |
| US6843281B1 (en) | 2003-07-30 | 2005-01-18 | Agilent Techinologies, Inc. | Methods and apparatus for introducing liquids into microfluidic chambers |
| US7353116B2 (en) | 2003-07-31 | 2008-04-01 | Agilent Technologies, Inc. | Chemical array with test dependent signal reading or processing |
| WO2005014850A2 (en) | 2003-08-06 | 2005-02-17 | University Of Massachusetts | Systems and methods for analyzing nucleic acid sequences |
| US7028536B2 (en) | 2004-06-29 | 2006-04-18 | Nanostream, Inc. | Sealing interface for microfluidic device |
| US7348144B2 (en) | 2003-08-13 | 2008-03-25 | Agilent Technologies, Inc. | Methods and system for multi-drug treatment discovery |
| US7229497B2 (en) | 2003-08-26 | 2007-06-12 | Massachusetts Institute Of Technology | Method of preparing nanocrystals |
| US7427679B2 (en) | 2003-08-30 | 2008-09-23 | Agilent Technologies, Inc. | Precursors for two-step polynucleotide synthesis |
| US7193077B2 (en) | 2003-08-30 | 2007-03-20 | Agilent Technologies, Inc. | Exocyclic amine triaryl methyl protecting groups in two-step polynucleotide synthesis |
| US7417139B2 (en) | 2003-08-30 | 2008-08-26 | Agilent Technologies, Inc. | Method for polynucleotide synthesis |
| US7585970B2 (en) | 2003-08-30 | 2009-09-08 | Agilent Technologies, Inc. | Method of polynucleotide synthesis using modified support |
| US7385050B2 (en) | 2003-08-30 | 2008-06-10 | Agilent Technologies, Inc. | Cleavable linker for polynucleotide synthesis |
| US20050049796A1 (en) | 2003-09-03 | 2005-03-03 | Webb Peter G. | Methods for encoding non-biological information on microarrays |
| US20120202710A1 (en) | 2003-09-09 | 2012-08-09 | Integrigen, Inc. | Methods and compositions for generation of germline human antibody genes |
| WO2005030929A2 (en) | 2003-09-23 | 2005-04-07 | Atom Sciences, Inc. | Polymeric nucleic acid hybridization probes |
| US7488607B2 (en) | 2003-09-30 | 2009-02-10 | Agilent Technologies, Inc. | Electronically readable microarray with electronic addressing function |
| US7147362B2 (en) | 2003-10-15 | 2006-12-12 | Agilent Technologies, Inc. | Method of mixing by intermittent centrifugal force |
| US7075161B2 (en) | 2003-10-23 | 2006-07-11 | Agilent Technologies, Inc. | Apparatus and method for making a low capacitance artificial nanopore |
| WO2005043154A2 (en) | 2003-10-27 | 2005-05-12 | Massachusetts Institute Of Technology | High density reaction chambers and methods of use |
| US7169560B2 (en) | 2003-11-12 | 2007-01-30 | Helicos Biosciences Corporation | Short cycle methods for sequencing polynucleotides |
| US7276338B2 (en) | 2003-11-17 | 2007-10-02 | Jacobson Joseph M | Nucleotide sequencing via repetitive single molecule hybridization |
| DE10353887A1 (de) | 2003-11-18 | 2005-06-16 | Febit Ag | Hochparalleler DNA-Synthesizer auf Matrizenbasis |
| US7851192B2 (en) | 2004-11-22 | 2010-12-14 | New England Biolabs, Inc. | Modified DNA cleavage enzymes and methods for use |
| US7282705B2 (en) | 2003-12-19 | 2007-10-16 | Agilent Technologies, Inc. | Microdevice having an annular lining for producing an electrospray emitter |
| EP2789383B1 (en) | 2004-01-07 | 2023-05-03 | Illumina Cambridge Limited | Molecular arrays |
| ES2432040T3 (es) | 2004-01-28 | 2013-11-29 | 454 Life Sciences Corporation | Amplificación de ácido nucleico con emulsión de flujo continuo |
| US7084180B2 (en) | 2004-01-28 | 2006-08-01 | Velocys, Inc. | Fischer-tropsch synthesis using microchannel technology and novel catalyst and microchannel reactor |
| AU2005214329A1 (en) | 2004-02-12 | 2005-09-01 | Population Genetics Technologies Ltd | Genetic analysis by sequence-specific sorting |
| US7125488B2 (en) | 2004-02-12 | 2006-10-24 | Varian, Inc. | Polar-modified bonded phase materials for chromatographic separations |
| EP1733055A4 (en) | 2004-02-27 | 2009-03-11 | Harvard College | polynucleotide |
| WO2005093092A2 (en) | 2004-03-26 | 2005-10-06 | Bayer Healthcare Ag | Diagnostics and therapeutics for diseases associated with g-protein coupled receptor 44 (gpr44) |
| US7875463B2 (en) | 2004-03-26 | 2011-01-25 | Agilent Technologies, Inc. | Generalized pulse jet ejection head control model |
| US20050214778A1 (en) | 2004-03-29 | 2005-09-29 | Peck Bill J | Methods for in situ generation of nucleic acid arrays |
| US20050214779A1 (en) | 2004-03-29 | 2005-09-29 | Peck Bill J | Methods for in situ generation of nucleic acid arrays |
| US8825411B2 (en) | 2004-05-04 | 2014-09-02 | Dna Twopointo, Inc. | Design, synthesis and assembly of synthetic nucleic acids |
| US20060003958A1 (en) | 2004-05-11 | 2006-01-05 | Melville Mark W | Novel polynucleotides related to oligonucleotide arrays to monitor gene expression |
| ES2459367T3 (es) | 2004-05-19 | 2014-05-09 | Massachusetts Institute Of Technology | Modelos tridimensionales de enfermedades de células/tejidos perfundidos |
| US7302348B2 (en) | 2004-06-02 | 2007-11-27 | Agilent Technologies, Inc. | Method and system for quantifying and removing spatial-intensity trends in microarray data |
| US20060024711A1 (en) | 2004-07-02 | 2006-02-02 | Helicos Biosciences Corporation | Methods for nucleic acid amplification and sequence determination |
| MX2007000105A (es) | 2004-07-06 | 2007-07-18 | Bioren Inc | Mutagenesis look-through para crear polipeptidos alterados con propiedades mejoradas. |
| US7811753B2 (en) | 2004-07-14 | 2010-10-12 | Ibis Biosciences, Inc. | Methods for repairing degraded DNA |
| US7276720B2 (en) | 2004-07-19 | 2007-10-02 | Helicos Biosciences Corporation | Apparatus and methods for analyzing samples |
| US20060012793A1 (en) | 2004-07-19 | 2006-01-19 | Helicos Biosciences Corporation | Apparatus and methods for analyzing samples |
| US20060019084A1 (en) | 2004-07-23 | 2006-01-26 | Pearson Laurence T | Monolithic composition and method |
| US20060024678A1 (en) | 2004-07-28 | 2006-02-02 | Helicos Biosciences Corporation | Use of single-stranded nucleic acid binding proteins in sequencing |
| JP4550115B2 (ja) | 2004-08-03 | 2010-09-22 | ジーンアート・アクチエンゲゼルシャフト | CpG含量を変化させることにより遺伝子発現を調整する方法 |
| WO2006073504A2 (en) | 2004-08-04 | 2006-07-13 | President And Fellows Of Harvard College | Wobble sequencing |
| WO2006018044A1 (en) | 2004-08-18 | 2006-02-23 | Agilent Technologies, Inc. | Microfluidic assembly with coupled microfluidic devices |
| US7034290B2 (en) | 2004-09-24 | 2006-04-25 | Agilent Technologies, Inc. | Target support with pattern recognition sites |
| US7943046B2 (en) | 2004-10-01 | 2011-05-17 | Agilent Technologies, Inc | Methods and systems for on-column protein delipidation |
| US20070122817A1 (en) | 2005-02-28 | 2007-05-31 | George Church | Methods for assembly of high fidelity synthetic polynucleotides |
| JP2008523786A (ja) | 2004-10-18 | 2008-07-10 | コドン デバイシズ インコーポレイテッド | 高忠実度合成ポリヌクレオチドのアセンブリ方法 |
| US7141807B2 (en) | 2004-10-22 | 2006-11-28 | Agilent Technologies, Inc. | Nanowire capillaries for mass spectrometry |
| US20060110744A1 (en) | 2004-11-23 | 2006-05-25 | Sampas Nicolas M | Probe design methods and microarrays for comparative genomic hybridization and location analysis |
| US8380441B2 (en) | 2004-11-30 | 2013-02-19 | Agilent Technologies, Inc. | Systems for producing chemical array layouts |
| US7977119B2 (en) | 2004-12-08 | 2011-07-12 | Agilent Technologies, Inc. | Chemical arrays and methods of using the same |
| US11268149B2 (en) | 2004-12-08 | 2022-03-08 | Cedars-Sinai Medical Center | Diagnosis and treatment of inflammatory bowel disease |
| US7439272B2 (en) | 2004-12-20 | 2008-10-21 | Varian, Inc. | Ultraporous sol gel monoliths |
| WO2006068625A1 (en) | 2004-12-22 | 2006-06-29 | National University Of Singapore | Novel snake toxin |
| WO2006069584A2 (en) | 2004-12-29 | 2006-07-06 | Exiqon A/S | NOVEL OLIGONUCLEOTIDE COMPOSITIONS AND PROBE SEQUENCES USEFUL FOR DETECTION AND ANALYSIS OF microRNAs AND THEIR TARGET mRNAs |
| US20060160138A1 (en) | 2005-01-13 | 2006-07-20 | George Church | Compositions and methods for protein design |
| US20060171855A1 (en) | 2005-02-03 | 2006-08-03 | Hongfeng Yin | Devices,systems and methods for multi-dimensional separation |
| US20090088679A1 (en) | 2005-02-07 | 2009-04-02 | Massachusetts Institute Of Technology | Electronically-Degradable Layer-by-Layer Thin Films |
| US7393665B2 (en) | 2005-02-10 | 2008-07-01 | Population Genetics Technologies Ltd | Methods and compositions for tagging and identifying polynucleotides |
| JP4641199B2 (ja) | 2005-02-28 | 2011-03-02 | 国立感染症研究所長 | Rna干渉ポリヌクレオチド混合物の設計装置、rna干渉ポリヌクレオチド混合物の作製方法、及びrna干渉ポリヌクレオチド混合物の設計プログラム |
| US20060203236A1 (en) | 2005-03-08 | 2006-09-14 | Zhenghua Ji | Sample cell |
| WO2007086890A2 (en) | 2005-03-10 | 2007-08-02 | Genemark Inc. | Method, apparatus, and system for authentication using labels containing nucleotide seouences |
| EP1623763A1 (en) | 2005-03-11 | 2006-02-08 | Agilent Technologies, Inc. | Chip with cleaning cavity |
| US7618777B2 (en) | 2005-03-16 | 2009-11-17 | Agilent Technologies, Inc. | Composition and method for array hybridization |
| US20060219637A1 (en) | 2005-03-29 | 2006-10-05 | Killeen Kevin P | Devices, systems and methods for liquid chromatography |
| WO2006116476A1 (en) | 2005-04-27 | 2006-11-02 | Sigma-Aldrich Co. | Activators for oligonucleotide and phosphoramidite synthesis |
| US7572907B2 (en) | 2005-04-29 | 2009-08-11 | Agilent Technologies, Inc. | Methods and compounds for polynucleotide synthesis |
| US8497069B2 (en) | 2005-04-29 | 2013-07-30 | Synthetic Genomics, Inc. | Amplification and cloning of single DNA molecules using rolling circle amplification |
| US8945680B2 (en) | 2005-05-12 | 2015-02-03 | Hempel A/S | Method for the establishment of a crack resistant epoxy paint coat and paint compositions suitable for said method |
| US7396676B2 (en) | 2005-05-31 | 2008-07-08 | Agilent Technologies, Inc. | Evanescent wave sensor with attached ligand |
| EP2620510B2 (en) | 2005-06-15 | 2020-02-19 | Complete Genomics Inc. | Single molecule arrays for genetic and chemical analysis |
| US7919239B2 (en) | 2005-07-01 | 2011-04-05 | Agilent Technologies, Inc. | Increasing hybridization efficiencies |
| US8076064B2 (en) | 2005-07-09 | 2011-12-13 | Agilent Technologies, Inc. | Method of treatment of RNA sample |
| US7718365B2 (en) | 2005-07-09 | 2010-05-18 | Agilent Technologies, Inc. | Microarray analysis of RNA |
| ATE510930T1 (de) | 2005-08-02 | 2011-06-15 | Rubicon Genomics Inc | Zusammensetzungen und verfahren zur bearbeitung und amplifikation von dna mit verwendung mehrerer enzyme in einer einzigen reaktion |
| DE102005037351B3 (de) | 2005-08-08 | 2007-01-11 | Geneart Ag | Verfahren für die kontinuierliche zielgerichtete Evolution von Proteinen in vitro |
| US9404882B2 (en) | 2005-08-11 | 2016-08-02 | New Mexico Tech Research Foundation | Method of producing a multi-microchannel, flow-through element and device using same |
| US7749701B2 (en) | 2005-08-11 | 2010-07-06 | Agilent Technologies, Inc. | Controlling use of oligonucleotide sequences released from arrays |
| CA2618665C (en) | 2005-08-11 | 2012-11-13 | J. Craig Venter Institute | Method for in vitro recombination |
| EP1915446B1 (en) | 2005-08-11 | 2017-06-14 | Synthetic Genomics, Inc. | In vitro recombination method |
| US7805252B2 (en) | 2005-08-16 | 2010-09-28 | Dna Twopointo, Inc. | Systems and methods for designing and ordering polynucleotides |
| US20070054127A1 (en) | 2005-08-26 | 2007-03-08 | Hergenrother Robert W | Silane coating compositions, coating systems, and methods |
| US20070196834A1 (en) | 2005-09-09 | 2007-08-23 | Francesco Cerrina | Method and system for the generation of large double stranded DNA fragments |
| WO2007033176A2 (en) | 2005-09-14 | 2007-03-22 | Illumina, Inc. | Continuous polymer synthesizer |
| EP1939621B1 (en) | 2005-09-16 | 2014-11-19 | Azbil Corporation | Method for manufacturing substrate for biochip, and method for manufacturing biochip |
| US20080308884A1 (en) | 2005-10-13 | 2008-12-18 | Silex Microsystems Ab | Fabrication of Inlet and Outlet Connections for Microfluidic Chips |
| US7759471B2 (en) | 2005-10-31 | 2010-07-20 | Agilent Technologies, Inc. | Monomer compositions for the synthesis of RNA, methods of synthesis, and methods of deprotection |
| US8202985B2 (en) | 2005-10-31 | 2012-06-19 | Agilent Technologies, Inc. | Monomer compositions for the synthesis of polynucleotides, methods of synthesis, and methods of deprotection |
| US8552174B2 (en) | 2005-10-31 | 2013-10-08 | Agilent Technologies, Inc. | Solutions, methods, and processes for deprotection of polynucleotides |
| US7368550B2 (en) | 2005-10-31 | 2008-05-06 | Agilent Technologies, Inc. | Phosphorus protecting groups |
| GB0522310D0 (en) | 2005-11-01 | 2005-12-07 | Solexa Ltd | Methods of preparing libraries of template polynucleotides |
| US7291471B2 (en) | 2005-11-21 | 2007-11-06 | Agilent Technologies, Inc. | Cleavable oligonucleotide arrays |
| GB0524069D0 (en) | 2005-11-25 | 2006-01-04 | Solexa Ltd | Preparation of templates for solid phase amplification |
| US8137936B2 (en) | 2005-11-29 | 2012-03-20 | Macevicz Stephen C | Selected amplification of polynucleotides |
| EP1966394B1 (en) | 2005-12-22 | 2012-07-25 | Keygene N.V. | Improved strategies for transcript profiling using high throughput sequencing technologies |
| US7939645B2 (en) | 2006-01-06 | 2011-05-10 | Agilent Technologies, Inc | Reaction buffer composition for nucleic acid replication with packed DNA polymerases |
| WO2007081386A2 (en) | 2006-01-11 | 2007-07-19 | Raindance Technologies, Inc. | Microfluidic devices and methods of use |
| US7544473B2 (en) | 2006-01-23 | 2009-06-09 | Population Genetics Technologies Ltd. | Nucleic acid analysis using sequence tokens |
| WO2007087377A2 (en) | 2006-01-25 | 2007-08-02 | Massachusetts Institute Of Technology | Photoelectrochemical synthesis of high density combinatorial polymer arrays |
| US9274108B2 (en) | 2006-02-06 | 2016-03-01 | Massachusetts Institute Of Technology | Self-assembly of macromolecules on multilayered polymer surfaces |
| US8809876B2 (en) | 2006-02-14 | 2014-08-19 | Massachusetts Institute Of Technology | Absorbing film |
| US7807356B2 (en) | 2006-03-09 | 2010-10-05 | Agilent Technologies, Inc. | Labeled nucleotide composition |
| TW200806317A (en) | 2006-03-20 | 2008-02-01 | Wyeth Corp | Methods for reducing protein aggregation |
| US7855281B2 (en) | 2006-03-23 | 2010-12-21 | Agilent Technologies, Inc. | Cleavable thiocarbonate linkers for polynucleotide synthesis |
| US7572908B2 (en) | 2006-03-23 | 2009-08-11 | Agilent Technologies, Inc. | Cleavable linkers for polynucleotides |
| US20070231800A1 (en) | 2006-03-28 | 2007-10-04 | Agilent Technologies, Inc. | Determination of methylated DNA |
| EP3722409A1 (en) | 2006-03-31 | 2020-10-14 | Illumina, Inc. | Systems and devices for sequence by synthesis analysis |
| EP2010567A2 (en) | 2006-04-07 | 2009-01-07 | The Government of the United States of America as Represented by The Department of Health and Human Services | Antibody compositions and methods for treatment of neoplastic disease |
| US20070238104A1 (en) | 2006-04-07 | 2007-10-11 | Agilent Technologies, Inc. | Competitive oligonucleotides |
| US20070238106A1 (en) | 2006-04-07 | 2007-10-11 | Agilent Technologies, Inc. | Systems and methods of determining alleles and/or copy numbers |
| US20070238108A1 (en) | 2006-04-07 | 2007-10-11 | Agilent Technologies, Inc. | Validation of comparative genomic hybridization |
| US8058055B2 (en) | 2006-04-07 | 2011-11-15 | Agilent Technologies, Inc. | High resolution chromosomal mapping |
| US20100173364A1 (en) | 2006-04-11 | 2010-07-08 | New England Biolabs, Inc. | Repair of Nucleic Acids for Improved Amplification |
| CN101495654A (zh) | 2006-04-19 | 2009-07-29 | 阿普里拉股份有限公司 | 无凝胶珠基测序的试剂、方法和文库 |
| US8383338B2 (en) | 2006-04-24 | 2013-02-26 | Roche Nimblegen, Inc. | Methods and systems for uniform enrichment of genomic regions |
| US20070259346A1 (en) | 2006-05-03 | 2007-11-08 | Agilent Technologies, Inc. | Analysis of arrays |
| US20070259344A1 (en) | 2006-05-03 | 2007-11-08 | Agilent Technologies, Inc. | Compound probes and methods of increasing the effective probe densities of arrays |
| US20070259347A1 (en) | 2006-05-03 | 2007-11-08 | Agilent Technologies, Inc. | Methods of increasing the effective probe densities of arrays |
| US20070259345A1 (en) | 2006-05-03 | 2007-11-08 | Agilent Technologies, Inc. | Target determination using compound probes |
| WO2007136834A2 (en) | 2006-05-19 | 2007-11-29 | Codon Devices, Inc. | Combined extension and ligation for nucleic acid assembly |
| US20070281309A1 (en) | 2006-05-19 | 2007-12-06 | Massachusetts Institute Of Technology | Microfluidic-based Gene Synthesis |
| WO2008054543A2 (en) | 2006-05-20 | 2008-05-08 | Codon Devices, Inc. | Oligonucleotides for multiplex nucleic acid assembly |
| EP2035984A4 (en) | 2006-06-19 | 2010-03-31 | Yeda Res & Dev | PROGRAMMABLE ITERATED ELONGATION: PROCESS FOR THE MANUFACTURE OF SYNTHETIC GENES AND COMBINATORY DNA AND PROTEIN LIBRARIES |
| AT503902B1 (de) | 2006-07-05 | 2008-06-15 | F Star Biotech Forsch & Entw | Verfahren zur manipulation von immunglobulinen |
| AT503861B1 (de) | 2006-07-05 | 2008-06-15 | F Star Biotech Forsch & Entw | Verfahren zur manipulation von t-zell-rezeptoren |
| US20080193772A1 (en) | 2006-07-07 | 2008-08-14 | Bio-Rad Laboratories, Inc | Mass spectrometry probes having hydrophobic coatiings |
| US7524942B2 (en) | 2006-07-31 | 2009-04-28 | Agilent Technologies, Inc. | Labeled nucleotide composition |
| US7572585B2 (en) | 2006-07-31 | 2009-08-11 | Agilent Technologies, Inc. | Enzymatic labeling of RNA |
| EP2049682A2 (en) | 2006-07-31 | 2009-04-22 | Illumina Cambridge Limited | Method of library preparation avoiding the formation of adaptor dimers |
| WO2008017473A2 (en) | 2006-08-08 | 2008-02-14 | Gunther Hartmann | Structure and use of 5' phosphate oligonucleotides |
| DE102006039479A1 (de) | 2006-08-23 | 2008-03-06 | Febit Biotech Gmbh | Programmierbare Oligonukleotidsynthese |
| EP2061909A2 (en) | 2006-08-24 | 2009-05-27 | Illumina Cambridge Limited | Method for retaining even coverage of short insert libraries |
| WO2008027558A2 (en) | 2006-08-31 | 2008-03-06 | Codon Devices, Inc. | Iterative nucleic acid assembly using activation of vector-encoded traits |
| US8415138B2 (en) | 2006-08-31 | 2013-04-09 | Agilent Technologies, Inc. | Apparatuses and methods for oligonucleotide preparation |
| US8097711B2 (en) | 2006-09-02 | 2012-01-17 | Agilent Technologies, Inc. | Thioether substituted aryl carbonate protecting groups |
| US20080311628A1 (en) | 2006-10-03 | 2008-12-18 | Ghc Technologies, Inc. | Methods and compositions for rapid amplification and capture of nucleic acid sequences |
| WO2008045380A2 (en) | 2006-10-04 | 2008-04-17 | Codon Devices, Inc. | Nucleic acid libraries and their design and assembly |
| US20080085511A1 (en) | 2006-10-05 | 2008-04-10 | Peck Bill J | Preparation of biopolymer arrays |
| JP2008097189A (ja) | 2006-10-10 | 2008-04-24 | National Institute Of Advanced Industrial & Technology | 塩基配列断片の転写物特異性又は遺伝子特異性を判定する方法 |
| US20080085514A1 (en) | 2006-10-10 | 2008-04-10 | Peck Bill J | Methods and devices for array synthesis |
| US7867782B2 (en) | 2006-10-19 | 2011-01-11 | Agilent Technologies, Inc. | Nanoscale moiety placement methods |
| US7999087B2 (en) | 2006-11-15 | 2011-08-16 | Agilent Technologies, Inc. | 2′-silyl containing thiocarbonate protecting groups for RNA synthesis |
| WO2008063134A1 (en) | 2006-11-24 | 2008-05-29 | Agency For Science, Technology And Research | Method of producing a pattern of discriminative wettability |
| WO2008063135A1 (en) | 2006-11-24 | 2008-05-29 | Agency For Science, Technology And Research | Apparatus for processing a sample in a liquid droplet and method of using the same |
| US8242258B2 (en) | 2006-12-03 | 2012-08-14 | Agilent Technologies, Inc. | Protecting groups for RNA synthesis |
| AU2007328900A1 (en) | 2006-12-05 | 2008-06-12 | Ablynx N.V. | Peptides capable of binding to serum proteins |
| US7989396B2 (en) | 2006-12-05 | 2011-08-02 | The Board Of Trustees Of The Leland Stanford Junior University | Biomolecule immobilization on biosensors |
| US7862999B2 (en) | 2007-01-17 | 2011-01-04 | Affymetrix, Inc. | Multiplex targeted amplification using flap nuclease |
| US8314220B2 (en) | 2007-01-26 | 2012-11-20 | Agilent Technologies, Inc. | Methods compositions, and kits for detection of microRNA |
| US20080182296A1 (en) | 2007-01-31 | 2008-07-31 | Chanda Pranab K | Pcr-directed gene synthesis from large number of overlapping oligodeoxyribonucleotides |
| KR100827449B1 (ko) | 2007-02-07 | 2008-05-07 | 삼성전자주식회사 | 광분해성 화합물과 상기 화합물이 커플링된 올리고머프로브 어레이용 기판, 올리고머 프로브 어레이 및 이의제조 방법 |
| US20100323404A1 (en) | 2007-02-09 | 2010-12-23 | Richard Lathrop | Method for recombining dna sequences and compositions related thereto |
| WO2008103475A1 (en) | 2007-02-20 | 2008-08-28 | Anaptysbio, Inc. | Somatic hypermutation systems |
| JP2008218579A (ja) | 2007-03-01 | 2008-09-18 | Denki Kagaku Kogyo Kk | 金属ベース回路基板 |
| US9029085B2 (en) | 2007-03-07 | 2015-05-12 | President And Fellows Of Harvard College | Assays and other reactions involving droplets |
| US7651762B2 (en) | 2007-03-13 | 2010-01-26 | Varian, Inc. | Methods and devices using a shrinkable support for porous monolithic materials |
| CA2684801C (en) | 2007-04-04 | 2017-10-10 | The Regents Of The University Of California | Compositions, devices, systems, and methods for using a nanopore |
| DK2476689T3 (en) | 2007-05-10 | 2016-01-18 | Agilent Technologies Inc | Thiocarbonbeskyttende groups for RNA synthesis |
| US20100286290A1 (en) | 2007-06-04 | 2010-11-11 | Jakob Schwalbe Lohmann | Enzyme activity assay using rolling circle amplification |
| US20080318334A1 (en) | 2007-06-20 | 2008-12-25 | Robotti Karla M | Microfluidic devices comprising fluid flow paths having a monolithic chromatographic material |
| US20090023190A1 (en) | 2007-06-20 | 2009-01-22 | Kai Qin Lao | Sequence amplification with loopable primers |
| US8194244B2 (en) | 2007-06-29 | 2012-06-05 | Intel Corporation | Solution sample plate with wells designed for improved Raman scattering signal detection efficiency |
| US7659069B2 (en) | 2007-08-31 | 2010-02-09 | Agilent Technologies, Inc. | Binary signaling assay using a split-polymerase |
| US7979215B2 (en) | 2007-07-30 | 2011-07-12 | Agilent Technologies, Inc. | Methods and systems for evaluating CGH candidate probe nucleic acid sequences |
| US8685642B2 (en) | 2007-07-30 | 2014-04-01 | Agilent Technologies, Inc. | Allele-specific copy number measurement using single nucleotide polymorphism and DNA arrays |
| US20090036664A1 (en) | 2007-07-31 | 2009-02-05 | Brian Jon Peter | Complex oligonucleotide primer mix |
| US20110124049A1 (en) | 2007-08-07 | 2011-05-26 | Mo-Huang Li | Integrated microfluidic device for gene synthesis |
| WO2009023547A2 (en) | 2007-08-14 | 2009-02-19 | Arcxis Biotechnologies | Polymer microfluidic biochip fabrication |
| US20110126929A1 (en) | 2007-08-15 | 2011-06-02 | Massachusetts Institute Of Technology | Microstructures For Fluidic Ballasting and Flow Control |
| US20090053704A1 (en) | 2007-08-24 | 2009-02-26 | Natalia Novoradovskaya | Stabilization of nucleic acids on solid supports |
| US9598737B2 (en) | 2012-05-09 | 2017-03-21 | Longhorn Vaccines And Diagnostics, Llc | Next generation genomic sequencing methods |
| US8877688B2 (en) | 2007-09-14 | 2014-11-04 | Adimab, Llc | Rationally designed, synthetic antibody libraries and uses therefor |
| WO2009039208A1 (en) | 2007-09-17 | 2009-03-26 | Twof, Inc. | Supramolecular nanostamping printing device |
| US7790387B2 (en) | 2007-09-24 | 2010-09-07 | Agilent Technologies, Inc. | Thiocarbonate linkers for polynucleotides |
| US8003330B2 (en) | 2007-09-28 | 2011-08-23 | Pacific Biosciences Of California, Inc. | Error-free amplification of DNA for clonal sequencing |
| EP2053132A1 (en) | 2007-10-23 | 2009-04-29 | Roche Diagnostics GmbH | Enrichment and sequence analysis of geomic regions |
| US8617811B2 (en) | 2008-01-28 | 2013-12-31 | Complete Genomics, Inc. | Methods and compositions for efficient base calling in sequencing reactions |
| WO2009070665A1 (en) | 2007-11-27 | 2009-06-04 | Massachusetts Institute Of Technology | Near field detector for integrated surface plasmon resonance biosensor applications |
| US20100272711A1 (en) | 2007-12-12 | 2010-10-28 | Thomas Jefferson University | Compositions and methods for the treatment and prevention of cardiovascular diseases |
| US9286439B2 (en) | 2007-12-17 | 2016-03-15 | Yeda Research And Development Co Ltd | System and method for editing and manipulating DNA |
| CN102016068A (zh) | 2008-01-09 | 2011-04-13 | 生命科技公司 | 制备用于核酸测序的配对标签文库的方法 |
| US9540637B2 (en) | 2008-01-09 | 2017-01-10 | Life Technologies Corporation | Nucleic acid adaptors and uses thereof |
| US7682809B2 (en) | 2008-01-11 | 2010-03-23 | Agilent Technologies, Inc. | Direct ATP release sequencing |
| WO2009092564A2 (en) | 2008-01-23 | 2009-07-30 | Roche Diagnostics Gmbh | Integrated instrument performing synthesis and amplification |
| WO2009131724A2 (en) | 2008-01-24 | 2009-10-29 | Massachusetts Institute Of Technology | Insulated nanogap devices and methods of use thereof |
| US20090194483A1 (en) | 2008-01-31 | 2009-08-06 | Robotti Karla M | Microfluidic device having monolithic separation medium and method of use |
| JP5725540B2 (ja) | 2008-02-15 | 2015-05-27 | シンセティック ジェノミクス インコーポレーテッド | 核酸分子のインビトロでの連結および組み合わせアセンブリのための方法 |
| US20110009607A1 (en) | 2008-03-11 | 2011-01-13 | Makoto Komiyama | Method for preparing dna fragment having sticky end |
| US20090230044A1 (en) | 2008-03-13 | 2009-09-17 | Agilent Technologies, Inc. | Microfluid Chip Cleaning |
| US20090238722A1 (en) | 2008-03-18 | 2009-09-24 | Agilent Technologies, Inc. | Pressure-Reinforced Fluidic Chip |
| CA2720247C (en) | 2008-03-31 | 2020-07-14 | Pacific Biosciences Of California, Inc. | Single molecule loading methods and compositions |
| US20090246788A1 (en) | 2008-04-01 | 2009-10-01 | Roche Nimblegen, Inc. | Methods and Assays for Capture of Nucleic Acids |
| US8853185B2 (en) | 2008-04-09 | 2014-10-07 | Cornell University | Coferons and methods of making and using them |
| US8911948B2 (en) | 2008-04-30 | 2014-12-16 | Integrated Dna Technologies, Inc. | RNase H-based assays utilizing modified RNA monomers |
| EP2113255A1 (en) | 2008-05-02 | 2009-11-04 | f-star Biotechnologische Forschungs- und Entwicklungsges.m.b.H. | Cytotoxic immunoglobulin |
| JP4582224B2 (ja) | 2008-05-02 | 2010-11-17 | ソニー株式会社 | マイクロビーズ作製方法及びマイクロビーズ |
| WO2009147537A2 (en) | 2008-05-27 | 2009-12-10 | Dako Denmark A/S | Compositions and methods for detection of chromosomal aberrations with novel hybridization buffers |
| EP2310416A1 (en) | 2008-06-30 | 2011-04-20 | Morphotek, Inc. | Anti-gd2 antibodies and methods and uses related thereto |
| GB2461546B (en) | 2008-07-02 | 2010-07-07 | Argen X Bv | Antigen binding polypeptides |
| JP4667490B2 (ja) | 2008-07-09 | 2011-04-13 | 三菱電機株式会社 | 加熱調理器 |
| WO2010014903A1 (en) | 2008-07-31 | 2010-02-04 | Massachusetts Institute Of Technology | Multiplexed olfactory receptor-based microsurface plasmon polariton detector |
| US20100069250A1 (en) | 2008-08-16 | 2010-03-18 | The Board Of Trustees Of The Leland Stanford Junior University | Digital PCR Calibration for High Throughput Sequencing |
| KR101759586B1 (ko) | 2008-08-22 | 2017-07-19 | 상가모 테라퓨틱스, 인코포레이티드 | 표적화된 단일가닥 분할 및 표적화된 통합을 위한 방법 및 조성물 |
| WO2010025310A2 (en) | 2008-08-27 | 2010-03-04 | Westend Asset Clearinghouse Company, Llc | Methods and devices for high fidelity polynucleotide synthesis |
| US8034917B2 (en) | 2008-08-28 | 2011-10-11 | Agilent Technologies, Inc. | Primer-directed chromosome painting |
| US8586310B2 (en) | 2008-09-05 | 2013-11-19 | Washington University | Method for multiplexed nucleic acid patch polymerase chain reaction |
| WO2010028366A2 (en) | 2008-09-05 | 2010-03-11 | Life Technologies Corporation | Methods and systems for nucleic acid sequencing validation, calibration and normalization |
| CA2772434C (en) | 2008-09-05 | 2017-11-21 | Masad Damha | Rna monomers containing o-acetal levulinyl ester groups and their use in rna microarrays |
| KR101718406B1 (ko) | 2008-09-06 | 2017-03-21 | 켐진스 코포레이션 | 역방향 합성 rna용 rna 합성-포스포라미디트, 및 리간드, 크로모포어의 용이한 도입, 및 합성 rna 3´-말단에서의 변형에서의 적용 |
| US8541569B2 (en) | 2008-09-06 | 2013-09-24 | Chemgenes Corporation | Phosphoramidites for synthetic RNA in the reverse direction, efficient RNA synthesis and convenient introduction of 3'-end ligands, chromophores and modifications of synthetic RNA |
| WO2010030776A1 (en) | 2008-09-10 | 2010-03-18 | Genscript Corporation | Homologous recombination-based dna cloning methods and compositions |
| US20100076183A1 (en) | 2008-09-22 | 2010-03-25 | Dellinger Douglas J | Protected monomer and method of final deprotection for rna synthesis |
| US8213015B2 (en) | 2008-09-25 | 2012-07-03 | Agilent Technologies, Inc. | Integrated flow cell with semiconductor oxide tubing |
| AU2009298501A1 (en) | 2008-09-30 | 2010-04-08 | Abbvie Inc. | Improved antibody libraries |
| US20100090341A1 (en) | 2008-10-14 | 2010-04-15 | Molecular Imprints, Inc. | Nano-patterned active layers formed by nano-imprint lithography |
| US20100301398A1 (en) | 2009-05-29 | 2010-12-02 | Ion Torrent Systems Incorporated | Methods and apparatus for measuring analytes |
| US9080211B2 (en) | 2008-10-24 | 2015-07-14 | Epicentre Technologies Corporation | Transposon end compositions and methods for modifying nucleic acids |
| WO2010053443A1 (en) | 2008-11-06 | 2010-05-14 | Agency For Science, Technology And Research | Apparatus for biopolymer synthesis |
| EP2356146A1 (en) | 2008-11-07 | 2011-08-17 | Fabrus Llc | Anti-dll4 antibodies and uses thereof |
| US8357489B2 (en) | 2008-11-13 | 2013-01-22 | The Board Of Trustees Of The Leland Stanford Junior University | Methods for detecting hepatocellular carcinoma |
| US20110229471A1 (en) | 2008-11-26 | 2011-09-22 | Cedars-Sinai Medical Center | Methods of determining responsiveness to anti-tnf alpha therapy in inflammatory bowel disease |
| BRPI0923225A2 (pt) | 2008-12-02 | 2016-10-04 | Chiralgen Ltd | metodo para sintese de acidos nucleicos modificados no atomo de fosforo |
| US8963262B2 (en) | 2009-08-07 | 2015-02-24 | Massachusettes Institute Of Technology | Method and apparatus for forming MEMS device |
| JO3382B1 (ar) | 2008-12-23 | 2019-03-13 | Amgen Inc | أجسام مضادة ترتبط مع مستقبل cgrp بشري |
| TW201104253A (en) | 2008-12-31 | 2011-02-01 | Nat Health Research Institutes | Microarray chip and method of fabricating for the same |
| EP2393833A1 (en) | 2009-02-09 | 2011-12-14 | Helmholtz Zentrum München Deutsches Forschungszentrum für Gesundheit und Umwelt (GmbH) | Repertoire of allo-restricted peptide-specific t cell receptor sequences and use thereof |
| US8569046B2 (en) | 2009-02-20 | 2013-10-29 | Massachusetts Institute Of Technology | Microarray with microchannels |
| US20100216648A1 (en) | 2009-02-20 | 2010-08-26 | Febit Holding Gmbh | Synthesis of sequence-verified nucleic acids |
| US9464284B2 (en) | 2009-03-09 | 2016-10-11 | Bioatla, Llc | Mirac proteins |
| WO2010115122A2 (en) | 2009-04-03 | 2010-10-07 | Illumina, Inc. | Generation of uniform fragments of nucleic acids using patterned substrates |
| JP2010248084A (ja) | 2009-04-10 | 2010-11-04 | Invitrogen Japan Kk | 新規洗浄溶媒を用いるオリゴヌクレオチド合成法 |
| US7862716B2 (en) | 2009-04-13 | 2011-01-04 | Sielc Technologies Corporation | HPLC schematic with integrated sample cleaning system |
| US8993040B2 (en) | 2009-04-29 | 2015-03-31 | Sicpa Holding Sa | Method and apparatus for depositing a biological fluid onto a substrate |
| US9085798B2 (en) | 2009-04-30 | 2015-07-21 | Prognosys Biosciences, Inc. | Nucleic acid constructs and methods of use |
| EP2248914A1 (en) | 2009-05-05 | 2010-11-10 | Max-Planck-Gesellschaft zur Förderung der Wissenschaften e.V. | The use of class IIB restriction endonucleases in 2nd generation sequencing applications |
| US9309557B2 (en) | 2010-12-17 | 2016-04-12 | Life Technologies Corporation | Nucleic acid amplification |
| US20100292102A1 (en) | 2009-05-14 | 2010-11-18 | Ali Nouri | System and Method For Preventing Synthesis of Dangerous Biological Sequences |
| US20100300882A1 (en) | 2009-05-26 | 2010-12-02 | General Electric Company | Devices and methods for in-line sample preparation of materials |
| WO2010141249A2 (en) | 2009-06-02 | 2010-12-09 | Merck Sharp & Dohme Corp. | Generation, characterization and uses thereof of anti-notch3 antibodies |
| WO2010141433A2 (en) | 2009-06-02 | 2010-12-09 | The Regents Of The University Of California | Virus discovery by sequencing and assembly of virus-derived sirnas, mirnas, pirnas |
| US8309710B2 (en) | 2009-06-29 | 2012-11-13 | Agilent Technologies, Inc. | Use of N-alkyl imidazole for sulfurization of oligonucleotides with an acetyl disulfide |
| US8642755B2 (en) | 2009-06-30 | 2014-02-04 | Agilent Technologies, Inc. | Use of thioacetic acid derivatives in the sulfurization of oligonucleotides with phenylacetyl disulfide |
| GB0912909D0 (en) | 2009-07-23 | 2009-08-26 | Olink Genomics Ab | Probes for specific analysis of nucleic acids |
| US8329208B2 (en) | 2009-07-28 | 2012-12-11 | Methylation Sciences International Srl | Pharmacokinetics of S-adenosylmethionine formulations |
| CN102482714B (zh) | 2009-07-30 | 2018-04-06 | 霍夫曼-拉罗奇有限公司 | 寡核苷酸探针组以及与其相关的方法和用途 |
| WO2011020529A2 (en) | 2009-08-19 | 2011-02-24 | Merck Patent Gmbh | Antibodies for the detection of integrin complexes in ffpe material |
| ES2562159T3 (es) | 2009-08-20 | 2016-03-02 | Population Genetics Technologies Ltd. | Composiciones y métodos para el reordenamiento de ácido nucleico molecular |
| US8476598B1 (en) | 2009-08-31 | 2013-07-02 | Sionyx, Inc. | Electromagnetic radiation imaging devices and associated methods |
| US20110082055A1 (en) | 2009-09-18 | 2011-04-07 | Codexis, Inc. | Reduced codon mutagenesis |
| US20120184724A1 (en) | 2009-09-22 | 2012-07-19 | Agilent Technologies, Inc. | Protected monomers and methods of deprotection for rna synthesis |
| WO2011038241A1 (en) | 2009-09-25 | 2011-03-31 | President And Fellows Of Harvard College | Nucleic acid amplification and sequencing by synthesis with fluorogenic nucleotides |
| US8975019B2 (en) | 2009-10-19 | 2015-03-10 | University Of Massachusetts | Deducing exon connectivity by RNA-templated DNA ligation/sequencing |
| EP2494062B1 (en) | 2009-10-28 | 2016-12-28 | Janssen Biotech, Inc. | Anti-glp-1r antibodies and their uses |
| WO2011053957A2 (en) | 2009-11-02 | 2011-05-05 | Gen9, Inc. | Compositions and methods for the regulation of multiple genes of interest in a cell |
| WO2011056872A2 (en) | 2009-11-03 | 2011-05-12 | Gen9, Inc. | Methods and microfluidic devices for the manipulation of droplets in high fidelity polynucleotide assembly |
| US20110114549A1 (en) | 2009-11-13 | 2011-05-19 | Agilent Technolgies, Inc. | Microfluidic device comprising separation columns |
| EP3085791A1 (en) | 2009-11-25 | 2016-10-26 | Gen9, Inc. | Methods and apparatuses for chip-based dna error reduction |
| WO2011066185A1 (en) | 2009-11-25 | 2011-06-03 | Gen9, Inc. | Microfluidic devices and methods for gene synthesis |
| US8500979B2 (en) | 2009-12-31 | 2013-08-06 | Intel Corporation | Nanogap chemical and biochemical sensors |
| WO2011085075A2 (en) | 2010-01-07 | 2011-07-14 | Gen9, Inc. | Assembly of high fidelity polynucleotides |
| US9758817B2 (en) | 2010-01-13 | 2017-09-12 | Agilent Technologies, Inc. | Method for identifying a nucleic acid in a sample |
| KR101230350B1 (ko) | 2010-01-27 | 2013-02-06 | 주식회사 엘지화학 | 구조적 안정성이 우수한 전지팩 |
| KR20110094878A (ko) | 2010-02-18 | 2011-08-24 | 삼성전자주식회사 | 올리고머 어레이 제조용 조성물 및 올리고머 어레이 제조 방법 |
| US20120027786A1 (en) | 2010-02-23 | 2012-02-02 | Massachusetts Institute Of Technology | Genetically programmable pathogen sense and destroy |
| GB201003036D0 (en) | 2010-02-23 | 2010-04-07 | Fermentas Uab | Restriction endonucleases and their applications |
| US8716467B2 (en) | 2010-03-03 | 2014-05-06 | Gen9, Inc. | Methods and devices for nucleic acid synthesis |
| EP2542676A1 (en) | 2010-03-05 | 2013-01-09 | Synthetic Genomics, Inc. | Methods for cloning and manipulating genomes |
| US20130085472A1 (en) | 2010-03-09 | 2013-04-04 | Toxcure, LLC | Microneedle nasal delivery device |
| EP2703491B1 (en) | 2010-04-09 | 2017-03-08 | The Catholic University Of America | Protein and nucleic acid delivery vehicles, components and mechanisms thereof |
| WO2011143556A1 (en) | 2010-05-13 | 2011-11-17 | Gen9, Inc. | Methods for nucleotide sequencing and high fidelity polynucleotide synthesis |
| WO2011150168A1 (en) | 2010-05-28 | 2011-12-01 | Gen9, Inc. | Methods and devices for in situ nucleic acid synthesis |
| KR101339064B1 (ko) | 2010-05-28 | 2014-01-06 | 한양대학교 에리카산학협력단 | 바이오칩을 이용하여 암호를 해독하는 방법 및 이를 이용하여 바코드의 위조 여부를 확인하는 방법 |
| GB2481425A (en) | 2010-06-23 | 2011-12-28 | Iti Scotland Ltd | Method and device for assembling polynucleic acid sequences |
| EP2598528A1 (en) | 2010-07-28 | 2013-06-05 | Immunocore Ltd. | T cell receptors |
| EP3115468B1 (en) | 2010-09-21 | 2018-07-25 | Agilent Technologies, Inc. | Increasing confidence of allele calls with molecular counting |
| US8715933B2 (en) | 2010-09-27 | 2014-05-06 | Nabsys, Inc. | Assay methods using nicking endonucleases |
| WO2012045001A2 (en) * | 2010-09-30 | 2012-04-05 | Vanderbilt University | Influenza virus antibodies and immunogens and uses therefor |
| WO2012051327A2 (en) | 2010-10-12 | 2012-04-19 | Cornell University | Method of dual-adapter recombination for efficient concatenation of multiple dna fragments in shuffled or specified arrangements |
| WO2012154201A1 (en) | 2010-10-22 | 2012-11-15 | President And Fellows Of Harvard College | Orthogonal amplification and assembly of nucleic acid sequences |
| EP2635679B1 (en) | 2010-11-05 | 2017-04-19 | Illumina, Inc. | Linking sequence reads using paired code tags |
| EP4039363A1 (en) | 2010-11-12 | 2022-08-10 | Gen9, Inc. | Protein arrays and methods of using and making the same |
| IL280133B2 (en) | 2010-11-12 | 2023-04-01 | Gen9 Inc | Methods and devices for the synthesis of nucleic acids |
| CN103370425B (zh) | 2010-12-17 | 2019-03-19 | 生命技术公司 | 用于核酸扩增的方法、组合物、系统、仪器和试剂盒 |
| US20120164633A1 (en) | 2010-12-27 | 2012-06-28 | Ibis Biosciences, Inc. | Digital droplet sequencing |
| US9487807B2 (en) | 2010-12-27 | 2016-11-08 | Ibis Biosciences, Inc. | Compositions and methods for producing single-stranded circular DNA |
| US9683054B2 (en) | 2010-12-31 | 2017-06-20 | BioAlta, LLC | Express humanization of antibodies |
| JP6016785B2 (ja) | 2011-03-30 | 2016-10-26 | 国立研究開発法人国立長寿医療研究センター | 膜分取培養器、膜分取培養キット、およびこれを用いた幹細胞分取方法、ならびに分離膜 |
| US10131903B2 (en) | 2011-04-01 | 2018-11-20 | The Regents Of The University Of California | Microfluidic platform for synthetic biology applications |
| US9384920B1 (en) | 2011-04-04 | 2016-07-05 | Eric J. Bakulich | Locking knob |
| US20140357497A1 (en) | 2011-04-27 | 2014-12-04 | Kun Zhang | Designing padlock probes for targeted genomic sequencing |
| US8722585B2 (en) | 2011-05-08 | 2014-05-13 | Yan Wang | Methods of making di-tagged DNA libraries from DNA or RNA using double-tagged oligonucleotides |
| CN112592960B (zh) | 2011-05-20 | 2024-08-27 | 富鲁达公司 | 核酸编码反应 |
| US9752176B2 (en) | 2011-06-15 | 2017-09-05 | Ginkgo Bioworks, Inc. | Methods for preparative in vitro cloning |
| ES2662372T3 (es) | 2011-06-21 | 2018-04-06 | Vib Vzw | Dominios de unión dirigidos contra complejos GPCR:proteína G y usos derivados de los mismos |
| WO2013003630A2 (en) | 2011-06-28 | 2013-01-03 | Igor Kutyavin | Methods and compositions for enrichment of nucleic acids in mixtures of highly homologous sequences |
| US20130045483A1 (en) | 2011-07-01 | 2013-02-21 | Whitehead Institute For Biomedical Research | Yeast cells expressing amyloid beta and uses therefor |
| WO2013019361A1 (en) | 2011-07-07 | 2013-02-07 | Life Technologies Corporation | Sequencing methods |
| US20130017978A1 (en) | 2011-07-11 | 2013-01-17 | Finnzymes Oy | Methods and transposon nucleic acids for generating a dna library |
| WO2013010062A2 (en) | 2011-07-14 | 2013-01-17 | Life Technologies Corporation | Nucleic acid complexity reduction |
| ES2737957T3 (es) | 2011-08-26 | 2020-01-17 | Gen9 Inc | Composiciones y métodos para el ensamblaje de alta fidelidad de ácidos nucleicos |
| US20150203839A1 (en) | 2011-08-26 | 2015-07-23 | Gen9, Inc. | Compositions and Methods for High Fidelity Assembly of Nucleic Acids |
| ES2844529T3 (es) | 2011-09-01 | 2021-07-22 | Genome Compiler Corp | Sistema de diseño, visualización y transacciones de construcciones polinucleotídicas para fabricar las mismas |
| US10752944B2 (en) | 2011-09-06 | 2020-08-25 | Gen-Probe Incorporated | Circularized templates for sequencing |
| US8840981B2 (en) | 2011-09-09 | 2014-09-23 | Eastman Kodak Company | Microfluidic device with multilayer coating |
| LT2768607T (lt) | 2011-09-26 | 2021-12-27 | Thermo Fisher Scientific Geneart Gmbh | Daugiašulininė plokštelė didelio efektyvumo, mažo tūrio nukleorūgščių sintezei atlikti |
| US20130091126A1 (en) | 2011-10-11 | 2013-04-11 | Life Technologies Corporation | Systems and methods for analysis and interpretation of nucleic acid sequence data |
| CA2852949A1 (en) | 2011-10-19 | 2013-04-25 | Nugen Technologies, Inc. | Compositions and methods for directional nucleic acid amplification and sequencing |
| US8987174B2 (en) | 2011-10-28 | 2015-03-24 | Prognosys Biosciences, Inc. | Methods for manufacturing molecular arrays |
| US8815782B2 (en) | 2011-11-11 | 2014-08-26 | Agilent Technologies, Inc. | Use of DNAzymes for analysis of an RNA sample |
| US20130137173A1 (en) | 2011-11-30 | 2013-05-30 | Feng Zhang | Nucleotide-specific recognition sequences for designer tal effectors |
| US8450107B1 (en) | 2011-11-30 | 2013-05-28 | The Broad Institute Inc. | Nucleotide-specific recognition sequences for designer TAL effectors |
| JP2013151468A (ja) | 2011-11-30 | 2013-08-08 | Agilent Technologies Inc | オリゴマーの合成及び精製の新規方法 |
| WO2013096692A1 (en) | 2011-12-21 | 2013-06-27 | Illumina, Inc. | Apparatus and methods for kinetic analysis and determination of nucleic acid sequences |
| WO2013093693A1 (en) | 2011-12-22 | 2013-06-27 | Rinat Neuroscience Corp. | Staphylococcus aureus specific antibodies and uses thereof |
| CA2862364C (en) | 2011-12-30 | 2021-02-23 | Quest Diagnostics Investments Incorporated | Nucleic acid analysis using emulsion pcr |
| WO2013101783A2 (en) | 2011-12-30 | 2013-07-04 | Bio-Rad Laboratories, Inc. | Methods and compositions for performing nucleic acid amplification reactions |
| JP2015509005A (ja) | 2012-02-01 | 2015-03-26 | シンセティック ジェノミクス インコーポレーテッド | エラーを最少限に抑える核酸分子の合成のための材料及び方法 |
| ES2776673T3 (es) | 2012-02-27 | 2020-07-31 | Univ North Carolina Chapel Hill | Métodos y usos para etiquetas moleculares |
| WO2013128281A1 (en) | 2012-02-28 | 2013-09-06 | Population Genetics Technologies Ltd | Method for attaching a counter sequence to a nucleic acid sample |
| EP2825653A4 (en) | 2012-03-14 | 2016-01-20 | Innovative Targeting Solutions Inc | PRODUCTION OF TARGETED SEQUENCE DIVERSITY IN FUSION PROTEINS |
| US9150853B2 (en) | 2012-03-21 | 2015-10-06 | Gen9, Inc. | Methods for screening proteins using DNA encoded chemical libraries as templates for enzyme catalysis |
| AU2013237989B2 (en) | 2012-03-28 | 2017-07-20 | 3M Innovative Properties Company | Reduced-pressure systems, dressings, and methods facilitating separation of electronic and clinical component parts |
| US9732384B2 (en) | 2012-04-02 | 2017-08-15 | Lux Bio Group, Inc. | Apparatus and method for molecular separation, purification, and sensing |
| WO2013154770A1 (en) | 2012-04-10 | 2013-10-17 | The Trustees Of Princeton University | Ultra-sensitive sensor |
| US20150353921A9 (en) | 2012-04-16 | 2015-12-10 | Jingdong Tian | Method of on-chip nucleic acid molecule synthesis |
| US20130281308A1 (en) | 2012-04-24 | 2013-10-24 | Gen9, Inc. | Methods for sorting nucleic acids and preparative in vitro cloning |
| CN104603286B (zh) | 2012-04-24 | 2020-07-31 | Gen9股份有限公司 | 在体外克隆中分选核酸和多重制备物的方法 |
| CA2872908C (en) | 2012-05-10 | 2023-11-14 | Gerhard Frey | Multi-specific monoclonal antibodies |
| EP3514243B1 (en) | 2012-05-21 | 2022-08-17 | The Scripps Research Institute | Methods of sample preparation |
| EP2856375B1 (en) | 2012-06-01 | 2018-07-18 | European Molecular Biology Laboratory | High-capacity storage of digital information in dna |
| US10308979B2 (en) | 2012-06-01 | 2019-06-04 | Agilent Technologies, Inc. | Target enrichment and labeling for multi-kilobase DNA |
| WO2013188037A2 (en) | 2012-06-11 | 2013-12-19 | Agilent Technologies, Inc | Method of adaptor-dimer subtraction using a crispr cas6 protein |
| CA2875666A1 (en) | 2012-06-14 | 2013-12-19 | Fred Hutchinson Cancer Research Center | Compositions and methods for sensitive mutation detection in nucleic acid molecules |
| JP6509727B2 (ja) | 2012-06-25 | 2019-05-15 | ギンゴー バイオワークス, インコーポレイテッド | 核酸アセンブリおよび高処理シークエンシングのための方法 |
| SG11201408807YA (en) | 2012-07-03 | 2015-01-29 | Integrated Dna Tech Inc | Tm-enhanced blocking oligonucleotides and baits for improved target enrichment and reduced off-target selection |
| US9255245B2 (en) | 2012-07-03 | 2016-02-09 | Agilent Technologies, Inc. | Sample probes and methods for sampling intracellular material |
| US20140038240A1 (en) | 2012-07-10 | 2014-02-06 | Pivot Bio, Inc. | Methods for multipart, modular and scarless assembly of dna molecules |
| WO2014012071A1 (en) | 2012-07-12 | 2014-01-16 | Massachusetts Institute Of Technology | Methods and apparatus for assembly |
| JP6239813B2 (ja) | 2012-07-18 | 2017-11-29 | 株式会社Screenセミコンダクターソリューションズ | 基板処理装置および基板処理方法 |
| US9384320B2 (en) | 2012-07-19 | 2016-07-05 | President And Fellows Of Harvard College | Methods of storing information using nucleic acids |
| RU2015106749A (ru) | 2012-07-27 | 2016-09-20 | Дзе Борд Оф Трастиз Оф Дзе Юниверсити Оф Иллинойс | Конструирование т-клеточных рецепторов |
| WO2014021938A1 (en) | 2012-08-02 | 2014-02-06 | The Board Of Trustees Of The Leland Stanford Junior University | Methods and apparatus for nucleic acid synthesis using oligo-templated polymerization |
| EP4219706A1 (en) | 2012-08-16 | 2023-08-02 | Synthetic Genomics, Inc. | Automated dsdna synthesis using a digital to biological converter |
| WO2014035693A2 (en) | 2012-08-31 | 2014-03-06 | The Scripps Research Institute | Methods and compositions related to modulators of eukaryotic cells |
| WO2014039587A1 (en) | 2012-09-05 | 2014-03-13 | Bio-Rad Laboratories, Inc. | Systems and methods for stabilizing droplets |
| CN107541546B (zh) | 2012-10-15 | 2021-06-15 | 生命技术公司 | 用于标靶核酸富集的组合物、方法、系统和试剂盒 |
| KR20140048733A (ko) | 2012-10-16 | 2014-04-24 | 삼성전자주식회사 | 다중 웰 플레이트 및 상기 다중 웰 플레이트를 이용한 표적 물질 분석 방법 |
| US9410173B2 (en) | 2012-10-24 | 2016-08-09 | Clontech Laboratories, Inc. | Template switch-based methods for producing a product nucleic acid |
| CA2932532C (en) | 2012-12-04 | 2021-06-22 | Phosphorex, Inc. | Microparticles and nanoparticles having negative surface charges |
| US10662424B2 (en) | 2012-12-06 | 2020-05-26 | Agilent Technologies, Inc. | Molecular fabrication |
| WO2014088694A1 (en) | 2012-12-06 | 2014-06-12 | Agilent Technologies, Inc. | Restriction enzyme-free target enrichment |
| JP6410726B2 (ja) | 2012-12-10 | 2018-10-24 | レゾリューション バイオサイエンス, インコーポレイテッド | 標的化ゲノム解析のための方法 |
| WO2014092886A2 (en) | 2012-12-10 | 2014-06-19 | Agilent Technologies, Inc. | Pairing code directed assembly |
| US20140310830A1 (en) | 2012-12-12 | 2014-10-16 | Feng Zhang | CRISPR-Cas Nickase Systems, Methods And Compositions For Sequence Manipulation in Eukaryotes |
| SG11201506750QA (en) | 2013-02-28 | 2015-09-29 | Univ Nanyang Tech | Method of manufacturing a device for supporting biological material growth and device therefrom |
| US9580746B2 (en) | 2013-03-05 | 2017-02-28 | Agilent Technologies, Inc. | Synthesis of long fish probes |
| WO2014137328A1 (en) | 2013-03-05 | 2014-09-12 | Agilent Technologies, Inc. | Detection of genomic rearrangements by sequence capture |
| EP3828277B1 (en) | 2013-03-13 | 2023-06-07 | Gen9, Inc. | Compositions, methods and apparatus for oligonucleotides synthesis |
| WO2014160059A1 (en) | 2013-03-13 | 2014-10-02 | Gen9, Inc. | Compositions and methods for synthesis of high fidelity oligonucleotides |
| AR095517A1 (es) * | 2013-03-15 | 2015-10-21 | Genentech Inc | ANTICUERPOS CONTRA EL RECEPTOR QUIMIOATRAYENTE EXPRESADO EN CÉLULAS T HELPER 2 (ANTI-CRTh2) Y MÉTODOS DE USO |
| EP2971152B1 (en) | 2013-03-15 | 2018-08-01 | The Board Of Trustees Of The Leland Stanford Junior University | Identification and use of circulating nucleic acid tumor markers |
| US20140274741A1 (en) | 2013-03-15 | 2014-09-18 | The Translational Genomics Research Institute | Methods to capture and sequence large fragments of dna and diagnostic methods for neuromuscular disease |
| US20140274729A1 (en) | 2013-03-15 | 2014-09-18 | Nugen Technologies, Inc. | Methods, compositions and kits for generation of stranded rna or dna libraries |
| WO2014151696A1 (en) | 2013-03-15 | 2014-09-25 | Gen9, Inc. | Compositions and methods for multiplex nucleic acids synthesis |
| US10683536B2 (en) | 2013-04-02 | 2020-06-16 | Molecular Assemblies, Inc. | Reusable initiators for synthesizing nucleic acids |
| US9279149B2 (en) | 2013-04-02 | 2016-03-08 | Molecular Assemblies, Inc. | Methods and apparatus for synthesizing nucleic acids |
| US9771613B2 (en) | 2013-04-02 | 2017-09-26 | Molecular Assemblies, Inc. | Methods and apparatus for synthesizing nucleic acid |
| US20150293102A1 (en) | 2013-04-13 | 2015-10-15 | Jung-Uk Shim | Detecting low-abundant analyte in microfluidic droplets |
| ITRM20130278A1 (it) | 2013-05-10 | 2014-11-11 | Consiglio Nazionale Ricerche | Procedimento di fabbricazione di film autoassemblati di copolimeri a blocchi |
| MX2016000231A (es) | 2013-06-26 | 2016-10-05 | Guangzhou Xiangxue Pharmaceutical Co Ltd | Receptor de celulas t de la alta estabilidad y metodo de preparacion y aplicacion del mismo. |
| US20150010953A1 (en) | 2013-07-03 | 2015-01-08 | Agilent Technologies, Inc. | Method for producing a population of oligonucleotides that has reduced synthesis errors |
| KR20150005062A (ko) | 2013-07-04 | 2015-01-14 | 삼성전자주식회사 | 미니-코어를 사용하는 프로세서 |
| US10421957B2 (en) | 2013-07-29 | 2019-09-24 | Agilent Technologies, Inc. | DNA assembly using an RNA-programmable nickase |
| US20160168564A1 (en) | 2013-07-30 | 2016-06-16 | Gen9, Inc. | Methods for the Production of Long Length Clonal Sequence Verified Nucleic Acid Constructs |
| ES2815099T3 (es) | 2013-08-05 | 2021-03-29 | Twist Bioscience Corp | Genotecas sintetizadas de novo |
| US9595180B2 (en) | 2013-08-07 | 2017-03-14 | Nike, Inc. | Activity recognition with activity reminders |
| CN104371019B (zh) | 2013-08-13 | 2019-09-10 | 鸿运华宁(杭州)生物医药有限公司 | 一种能与glp-1r特异性结合的抗体及其与glp-1的融合蛋白质 |
| GB201314721D0 (en) | 2013-08-16 | 2013-10-02 | Almagen Ltd | A method of selectively masking one or more sites on a surface and a method of synthesising an array of molecules |
| WO2015031689A1 (en) | 2013-08-30 | 2015-03-05 | Personalis, Inc. | Methods and systems for genomic analysis |
| KR102362030B1 (ko) | 2013-09-14 | 2022-02-10 | 켐진스 코포레이션 | 역방향 접근법을 사용한 긴 rna의 고효율 합성 |
| WO2015040075A1 (en) | 2013-09-18 | 2015-03-26 | Genome Research Limited | Genomic screening methods using rna-guided endonucleases |
| US9422325B2 (en) | 2013-10-04 | 2016-08-23 | Trustees Of Tufts College | Glycosylation reactions using phenyl(trifluoroethyl)iodonium salts |
| EP3055676A1 (en) | 2013-10-07 | 2016-08-17 | Cellular Research, Inc. | Methods and systems for digitally counting features on arrays |
| EP3063301A4 (en) | 2013-10-29 | 2017-07-19 | Longhorn Vaccines and Diagnostics, LLC | Next generation genomic sequencing methods |
| WO2015081142A1 (en) | 2013-11-26 | 2015-06-04 | Xenco Medical, Llc | Lock and release implant delivery system |
| CN105934541B (zh) | 2013-11-27 | 2019-07-12 | Gen9股份有限公司 | 核酸文库及其制造方法 |
| US20160297883A1 (en) | 2013-12-04 | 2016-10-13 | Innovative Targeting Solutions, Inc. | G-protein coupled receptor agonists and methods |
| CA2931296C (en) | 2013-12-04 | 2024-04-23 | Chugai Seiyaku Kabushiki Kaisha | Antigen-binding molecules, the antigen-binding activity of which varies according to the concentration of compounds, and libraries of said molecules |
| EP3102676A1 (en) | 2013-12-09 | 2016-12-14 | Integrated DNA Technologies Inc. | Long nucleic acid sequences containing variable regions |
| JP6841656B2 (ja) | 2013-12-17 | 2021-03-10 | ジェネンテック, インコーポレイテッド | Pd−1軸結合アンタゴニスト及びタキサンを使用する癌の治療方法 |
| GB2521387B (en) | 2013-12-18 | 2020-05-27 | Ge Healthcare Uk Ltd | Oligonucleotide data storage on solid supports |
| US10537889B2 (en) | 2013-12-31 | 2020-01-21 | Illumina, Inc. | Addressable flow cell using patterned electrodes |
| US9587268B2 (en) | 2014-01-29 | 2017-03-07 | Agilent Technologies Inc. | Fast hybridization for next generation sequencing target enrichment |
| US10287627B2 (en) | 2014-02-08 | 2019-05-14 | The Regents Of The University Of Colorado, A Body Corporate | Multiplexed linking PCR |
| US10208338B2 (en) | 2014-03-03 | 2019-02-19 | Swift Biosciences, Inc. | Enhanced adaptor ligation |
| RU2722696C2 (ru) | 2014-03-14 | 2020-06-03 | Иммунокор Лимитед | Библиотеки tcr |
| WO2015195178A2 (en) | 2014-03-27 | 2015-12-23 | Canon U.S. Life Sciences, Inc. | Integration of ex situ fabricated porous polymer monoliths into fluidic chips |
| US10190161B2 (en) | 2014-04-03 | 2019-01-29 | Stmicroelectronics S.R.L. | Apparatus and method for nucleic acid sequencing based on nanowire detectors |
| US20170037790A1 (en) | 2014-04-15 | 2017-02-09 | Volvo Construction Equipment Ab | Device for controlling engine and hydraulic pump of construction equipment and control method therefor |
| GB201407852D0 (en) | 2014-05-02 | 2014-06-18 | Iontas Ltd | Preparation of libraries od protein variants expressed in eukaryotic cells and use for selecting binding molecules |
| EP3143161B1 (en) | 2014-05-16 | 2021-04-21 | Illumina, Inc. | Nucleic acid synthesis techniques |
| US20150361423A1 (en) | 2014-06-16 | 2015-12-17 | Agilent Technologies, Inc. | High throughput gene assembly in droplets |
| US20150361422A1 (en) | 2014-06-16 | 2015-12-17 | Agilent Technologies, Inc. | High throughput gene assembly in droplets |
| US10870845B2 (en) | 2014-07-01 | 2020-12-22 | Global Life Sciences Solutions Operations UK Ltd | Methods for capturing nucleic acids |
| US10472620B2 (en) | 2014-07-01 | 2019-11-12 | General Electric Company | Method, substrate and device for separating nucleic acids |
| US20170198268A1 (en) | 2014-07-09 | 2017-07-13 | Gen9, Inc. | Compositions and Methods for Site-Directed DNA Nicking and Cleaving |
| US11254933B2 (en) | 2014-07-14 | 2022-02-22 | The Regents Of The University Of California | CRISPR/Cas transcriptional modulation |
| US20160017394A1 (en) | 2014-07-15 | 2016-01-21 | Life Technologies Corporation | Compositions and methods for nucleic acid assembly |
| WO2016022557A1 (en) | 2014-08-05 | 2016-02-11 | Twist Bioscience Corporation | Cell free cloning of nucleic acids |
| EP3191604B1 (en) | 2014-09-09 | 2021-04-14 | Igenomx International Genomics Corporation | Methods and compositions for rapid nucleic acid library preparation |
| WO2016053881A1 (en) | 2014-10-03 | 2016-04-07 | Life Technologies Corporation | Genetic sequence verification compositions, methods and kits |
| CN113930455A (zh) | 2014-10-09 | 2022-01-14 | 生命技术公司 | Crispr寡核苷酸和基因剪辑 |
| EP3204518B1 (en) | 2014-10-10 | 2019-07-10 | Invitae Corporation | Universal blocking oligo system and improved hybridization capture methods for multiplexed capture reactions |
| US20170249345A1 (en) | 2014-10-18 | 2017-08-31 | Girik Malik | A biomolecule based data storage system |
| CN107107058B (zh) | 2014-10-22 | 2021-08-10 | 加利福尼亚大学董事会 | 高清晰度微液滴打印机 |
| US9890417B2 (en) | 2014-11-03 | 2018-02-13 | Agilent Technologies, Inc. | Signal amplification of fluorescence in situ hybridization |
| WO2016076345A1 (ja) | 2014-11-11 | 2016-05-19 | 中外製薬株式会社 | 改変された抗体可変領域を含む抗原結合分子のライブラリ |
| US10233490B2 (en) | 2014-11-21 | 2019-03-19 | Metabiotech Corporation | Methods for assembling and reading nucleic acid sequences from mixed populations |
| CN104562213A (zh) | 2014-12-26 | 2015-04-29 | 北京诺禾致源生物信息科技有限公司 | 扩增子文库及其构建方法 |
| CA2975852A1 (en) | 2015-02-04 | 2016-08-11 | Twist Bioscience Corporation | Methods and devices for de novo oligonucleic acid assembly |
| CA2975855A1 (en) | 2015-02-04 | 2016-08-11 | Twist Bioscience Corporation | Compositions and methods for synthetic gene assembly |
| US9834774B2 (en) | 2015-02-11 | 2017-12-05 | Agilent Technologies, Inc. | Methods and compositions for rapid seamless DNA assembly |
| EP3256624A4 (en) | 2015-02-13 | 2018-07-25 | Vaccine Research Institute of San Diego | Materials and methods to analyze rna isoforms in transcriptomes |
| CN104734848A (zh) | 2015-03-02 | 2015-06-24 | 郑州轻工业学院 | 基于重组dna技术对信息进行加密与隐藏的方法及应用 |
| US10745456B2 (en) | 2015-04-01 | 2020-08-18 | The Scripps Research Institute | Methods and compositions related to GPCR agonist polypeptides |
| WO2016162127A1 (en) | 2015-04-08 | 2016-10-13 | Polyphor Ag | Backbone-cyclized peptidomimetics |
| US11164661B2 (en) | 2015-04-10 | 2021-11-02 | University Of Washington | Integrated system for nucleic acid-based storage and retrieval of digital data using keys |
| EP3283512A4 (en) | 2015-04-17 | 2018-10-03 | Distributed Bio Inc | Method for mass humanization of non-human antibodies |
| WO2016172377A1 (en) | 2015-04-21 | 2016-10-27 | Twist Bioscience Corporation | Devices and methods for oligonucleic acid library synthesis |
| EP3288973B1 (en) | 2015-04-30 | 2021-10-20 | AbCheck s.r.o. | Method for mass humanization of rabbit antibodies |
| WO2016183100A1 (en) | 2015-05-11 | 2016-11-17 | Twist Bioscience Corporation | Compositions and methods for nucleic acid amplification |
| EP3322812B1 (en) | 2015-07-13 | 2022-05-18 | President and Fellows of Harvard College | Methods for retrievable information storage using nucleic acids |
| GB201513113D0 (en) | 2015-07-24 | 2015-09-09 | Genome Res Ltd | Nasal sampling methods |
| IL258164B (en) | 2015-09-18 | 2022-09-01 | Twist Bioscience Corp | Methods to regulate the activity of proteins and cells and a method for the production of nucleic acids |
| US11512347B2 (en) | 2015-09-22 | 2022-11-29 | Twist Bioscience Corporation | Flexible substrates for nucleic acid synthesis |
| CN108026137A (zh) | 2015-10-01 | 2018-05-11 | 华盛顿大学 | Dna寡核苷酸的多对组装 |
| US20170141793A1 (en) | 2015-11-13 | 2017-05-18 | Microsoft Technology Licensing, Llc | Error correction for nucleotide data stores |
| CN115920796A (zh) | 2015-12-01 | 2023-04-07 | 特韦斯特生物科学公司 | 功能化表面及其制备 |
| EP3387152B1 (en) | 2015-12-08 | 2022-01-26 | Twinstrand Biosciences, Inc. | Improved adapters, methods, and compositions for duplex sequencing |
| GB2562933B (en) | 2016-01-08 | 2022-06-29 | Maxion Therapeutics Ltd | Binding members with altered diversity scaffold domains |
| GB201604492D0 (en) | 2016-03-16 | 2016-04-27 | Immatics Biotechnologies Gmbh | Transfected t-cells and t-cell receptors for use in immunotherapy against cancers |
| US11708574B2 (en) | 2016-06-10 | 2023-07-25 | Myriad Women's Health, Inc. | Nucleic acid sequencing adapters and uses thereof |
| WO2017214574A1 (en) | 2016-06-10 | 2017-12-14 | Twist Bioscience Corporation | Systems and methods for automated annotation and screening of biological sequences |
| WO2018026920A1 (en) | 2016-08-03 | 2018-02-08 | Twist Bioscience Corporation | Textured surfaces for polynucleotide synthesis |
| GB2568444A (en) | 2016-08-22 | 2019-05-15 | Twist Bioscience Corp | De novo synthesized nucleic acid libraries |
| US11453712B2 (en) | 2016-09-02 | 2022-09-27 | Lentigen Technology Inc. | Compositions and methods for treating cancer with DuoCARs |
| JP6871364B2 (ja) | 2016-09-21 | 2021-05-12 | ツイスト バイオサイエンス コーポレーション | 核酸に基づくデータ保存 |
| EP3541973B1 (en) | 2016-11-18 | 2024-03-27 | Twist Bioscience Corporation | Polynucleotide libraries having controlled stoichiometry and synthesis thereof |
| JP7169975B2 (ja) | 2016-12-16 | 2022-11-11 | ツイスト バイオサイエンス コーポレーション | 免疫シナプスの変異体ライブラリーおよびその合成 |
| IL267113B2 (en) | 2016-12-21 | 2024-09-01 | Cephalon Llc | Antibodies that bind specifically to human IL-15 and their uses |
| CN110892485B (zh) | 2017-02-22 | 2024-03-22 | 特韦斯特生物科学公司 | 基于核酸的数据存储 |
| EP3596258A4 (en) | 2017-03-15 | 2020-12-30 | Twist Bioscience Corporation | NOVO SYNTHEIZED NUCLEIC ACID COMBINATORIAL BANKS |
| WO2018170169A1 (en) | 2017-03-15 | 2018-09-20 | Twist Bioscience Corporation | Variant libraries of the immunological synapse and synthesis thereof |
| PL3600281T3 (pl) | 2017-03-23 | 2023-09-11 | QBiotics Pty Ltd | Terapia skojarzona w leczeniu i profilaktyce nowotworów |
| WO2018183918A1 (en) | 2017-03-30 | 2018-10-04 | Grail, Inc. | Enhanced ligation in sequencing library preparation |
| CN111094584A (zh) | 2017-04-23 | 2020-05-01 | 伊鲁米那股份有限公司 | 用于改进编索引的核酸文库中的样品鉴定的组合物和方法 |
| AU2018266377B2 (en) | 2017-05-08 | 2024-06-20 | Illumina, Inc. | Universal short adapters for indexing of polynucleotide samples |
| GB2578844A (en) | 2017-06-12 | 2020-05-27 | Twist Bioscience Corp | Methods for seamless nucleic acid assembly |
| WO2018231864A1 (en) | 2017-06-12 | 2018-12-20 | Twist Bioscience Corporation | Methods for seamless nucleic acid assembly |
| IL272100B2 (en) | 2017-07-18 | 2024-02-01 | Investig Forestales Bioforest S A | Method and device for asymmetric polarity reversal in electro-membrane processes |
| GB2581620A (en) | 2017-09-11 | 2020-08-26 | Twist Bioscience Corp | GPCR binding proteins and synthesis thereof |
| CN111565834B (zh) | 2017-10-20 | 2022-08-26 | 特韦斯特生物科学公司 | 用于多核苷酸合成的加热的纳米孔 |
| US20200299684A1 (en) | 2017-10-27 | 2020-09-24 | Twist Bioscience Corporation | Systems and methods for polynucleotide scoring |
| US11427867B2 (en) | 2017-11-29 | 2022-08-30 | Xgenomes Corp. | Sequencing by emergence |
| AU2019205269A1 (en) | 2018-01-04 | 2020-07-30 | Twist Bioscience Corporation | DNA-based digital information storage |
| US10722916B2 (en) | 2018-01-19 | 2020-07-28 | Caulk Garbage Can LLC | Caulk gun attachment for wiping excess caulk |
| SG11202006898TA (en) | 2018-01-26 | 2020-08-28 | Regeneron Pharma Inc | Anti-tmprss2 antibodies and antigen-binding fragments |
| CN112639130B (zh) | 2018-05-18 | 2024-08-09 | 特韦斯特生物科学公司 | 用于核酸杂交的多核苷酸、试剂和方法 |
| US20210147830A1 (en) | 2018-06-29 | 2021-05-20 | Thermo Fisher Scientific Geneart Gmbh | High throughput assembly of nucleic acid molecules |
| US10963953B2 (en) | 2018-10-10 | 2021-03-30 | Alliance Inspection Management, LLC | Reserve management for continuous bidding portal |
| US10969965B2 (en) | 2018-12-24 | 2021-04-06 | Western Digital Technologies, Inc. | Dynamic performance density tuning for data storage device |
| US20200222875A1 (en) | 2018-12-26 | 2020-07-16 | Twist Bioscience Corporation | Highly accurate de novo polynucleotide synthesis |
| JP2022521766A (ja) | 2019-02-25 | 2022-04-12 | ツイスト バイオサイエンス コーポレーション | 次世代シーケンシングのための組成物および方法 |
| CN113766930A (zh) | 2019-02-26 | 2021-12-07 | 特韦斯特生物科学公司 | Glp1受体的变异核酸文库 |
| SG11202109283UA (en) | 2019-02-26 | 2021-09-29 | Twist Bioscience Corp | Variant nucleic acid libraries for antibody optimization |
| US20220243195A1 (en) | 2019-06-21 | 2022-08-04 | Twist Bioscience Corporation | Barcode-based nucleic acid sequence assembly |
| CN114729342A (zh) | 2019-06-21 | 2022-07-08 | 特韦斯特生物科学公司 | 基于条形码的核酸序列装配 |
| AU2020315955A1 (en) | 2019-07-22 | 2022-03-03 | Igenomx International Genomics Corporation | Methods and compositions for high throughput sample preparation using double unique dual indexing |
| WO2021046655A1 (en) | 2019-09-13 | 2021-03-18 | University Health Network | Detection of circulating tumor dna using double stranded hybrid capture |
| AU2020355027A1 (en) | 2019-09-23 | 2022-04-21 | Twist Bioscience Corporation | Antibodies that bind CD3 Epsilon |
| CA3155629A1 (en) | 2019-09-23 | 2021-04-01 | Twist Bioscience Corporation | Variant nucleic acid libraries for crth2 |
| CA3164146A1 (en) | 2019-12-09 | 2021-06-17 | Twist Bioscience Corporation | Variant nucleic acid libraries for adenosine receptors |
| JP2023523335A (ja) | 2020-04-27 | 2023-06-02 | ツイスト バイオサイエンス コーポレーション | コロナウイルス用の変異体核酸ライブラリー相互参照 |
| WO2022010934A2 (en) | 2020-07-07 | 2022-01-13 | Twist Bioscience Corporation | Devices and methods for light-directed polymer synthesis |
| WO2022046797A1 (en) | 2020-08-25 | 2022-03-03 | Twist Bioscience Corporation | Compositions and methods for library sequencing |
| CA3190667A1 (en) | 2020-08-26 | 2022-03-03 | Aaron Sato | Methods and compositions relating to glp1r variants |
| US20220064206A1 (en) | 2020-08-28 | 2022-03-03 | Twist Bioscience Corporation | Devices and methods for synthesis |
| US20220106590A1 (en) | 2020-10-05 | 2022-04-07 | Twist Bioscience Corporation | Hybridization methods and reagents |
| EP4229210A1 (en) | 2020-10-19 | 2023-08-23 | Twist Bioscience Corporation | Methods of synthesizing oligonucleotides using tethered nucleotides |
| WO2022087293A1 (en) | 2020-10-22 | 2022-04-28 | Twist Bioscience Corporation | Methods and systems for detecting coronavirus |
| US20220135965A1 (en) | 2020-10-26 | 2022-05-05 | Twist Bioscience Corporation | Libraries for next generation sequencing |
| US20220135690A1 (en) | 2020-11-03 | 2022-05-05 | Twist Bioscience Corporation | Methods and compositions relating to chemokine receptor variants |
| US20220259319A1 (en) | 2021-01-21 | 2022-08-18 | Twist Bioscience Corporation | Methods and compositions relating to adenosine receptors |
| WO2022178137A1 (en) | 2021-02-19 | 2022-08-25 | Twist Bioscience Corporation | Libraries for identification of genomic variants |
| EP4314075A2 (en) | 2021-03-24 | 2024-02-07 | Twist Bioscience Corporation | Variant nucleic acid libraries for cd3 |
| EP4314074A1 (en) | 2021-03-24 | 2024-02-07 | Twist Bioscience Corporation | Variant nucleic acid libraries for tigit |
| US20220323924A1 (en) | 2021-03-24 | 2022-10-13 | Twist Bioscience Corporation | Electrochemical polynucleotide synthesis |
| WO2022217004A1 (en) | 2021-04-09 | 2022-10-13 | Twist Bioscience Corporation | Libraries for mutational analysis |
| EP4334516A1 (en) | 2021-05-03 | 2024-03-13 | Twist Bioscience Corporation | Variant nucleic acid libraries for ion channels |
| WO2022235584A1 (en) | 2021-05-03 | 2022-11-10 | Twist Bioscience Corporation | Variant nucleic acid libraries for glycans |
| US20230002478A1 (en) | 2021-06-22 | 2023-01-05 | Twist Bioscience Corporation | Methods and compositions relating to covid antibody epitopes |
| US20230192819A1 (en) | 2021-08-17 | 2023-06-22 | Twist Bioscience Corporation | Single domain antibodies for sars-cov-2 |
| WO2023023183A2 (en) | 2021-08-17 | 2023-02-23 | Twist Bioscience Corporation | Sars-cov-2 antibodies and related compositions and methods of use |
| US20230115861A1 (en) | 2021-08-19 | 2023-04-13 | Twist Bioscience Corporation | Methods and compositions relating to covalently closed nucleic acids |
| KR20240101595A (ko) | 2021-10-18 | 2024-07-02 | 트위스트 바이오사이언스 코포레이션 | 연속 서열분석에 관한 방법 및 조성물 |
| US20230265217A1 (en) | 2021-10-27 | 2023-08-24 | Twist Bioscience Corporation | Multispecific sars-cov-2 antibodies and methods of use |
| WO2023076419A2 (en) | 2021-10-27 | 2023-05-04 | Twist Bioscience Corporation | Sars-cov-2 antibodies and methods of use |
| CN118525028A (zh) | 2021-11-01 | 2024-08-20 | 特韦斯特生物科学公司 | 用于合成的装置和方法 |
| WO2023091614A2 (en) | 2021-11-18 | 2023-05-25 | Twist Bioscience Corporation | Dickkopf-1 variant antibodies and methods of use |
| US20230265179A1 (en) | 2021-11-18 | 2023-08-24 | Twist Bioscience Corporation | Cytokine variant antibodies and methods of use |
| WO2023102034A2 (en) | 2021-12-01 | 2023-06-08 | Twist Bioscience Corporation | Neuropilin-1 variant antibodies and methods of use |
| KR20240116520A (ko) | 2021-12-08 | 2024-07-29 | 트위스트 바이오사이언스 코포레이션 | 나노전기 디바이스 및 그 용도 |
| WO2023114432A2 (en) | 2021-12-17 | 2023-06-22 | Twist Bioscience Corporation | Compositions and methods for detection of variants |
| WO2023130123A2 (en) | 2022-01-03 | 2023-07-06 | Twist Bioscience Corporation | Bispecific sars-cov-2 antibodies and methods of use |
| US20230340461A1 (en) | 2022-02-14 | 2023-10-26 | Twist Bioscience Corporation | Combinatorial dna assembly for multispecific antibodies |
| US20230407290A1 (en) | 2022-03-07 | 2023-12-21 | Twist Bioscience Corporation | Methylation-mediated adapter removal on nucleic acid sequences |
| WO2023192635A2 (en) | 2022-04-01 | 2023-10-05 | Twist Bioscience Corporation | Libraries for methylation analysis |
| WO2023196499A1 (en) | 2022-04-07 | 2023-10-12 | Twist Bioscience Corporation | Substrate cleavage for nucleic acid synthesis |
| WO2023205345A2 (en) | 2022-04-21 | 2023-10-26 | Twist Bioscience Corporation | Codecs for dna data storage |
-
2020
- 2020-09-23 CA CA3155629A patent/CA3155629A1/en active Pending
- 2020-09-23 AU AU2020356471A patent/AU2020356471A1/en not_active Abandoned
- 2020-09-23 KR KR1020227013500A patent/KR20220066151A/ko unknown
- 2020-09-23 JP JP2022518006A patent/JP2022548309A/ja active Pending
- 2020-09-23 US US17/030,216 patent/US12091777B2/en active Active
- 2020-09-23 WO PCT/US2020/052291 patent/WO2021061829A1/en unknown
- 2020-09-23 EP EP20868003.3A patent/EP4034566A4/en active Pending
- 2020-09-23 CN CN202080081341.XA patent/CN115003697A/zh active Pending
-
2022
- 2022-03-20 IL IL291515A patent/IL291515A/en unknown
Also Published As
| Publication number | Publication date |
|---|---|
| US20210102192A1 (en) | 2021-04-08 |
| US12091777B2 (en) | 2024-09-17 |
| CA3155629A1 (en) | 2021-04-01 |
| EP4034566A1 (en) | 2022-08-03 |
| CN115003697A (zh) | 2022-09-02 |
| IL291515A (en) | 2022-05-01 |
| AU2020356471A1 (en) | 2022-04-21 |
| KR20220066151A (ko) | 2022-05-23 |
| WO2021061829A1 (en) | 2021-04-01 |
| EP4034566A4 (en) | 2024-01-24 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US12091777B2 (en) | Variant nucleic acid libraries for CRTH2 | |
| US20210102195A1 (en) | Variant nucleic acid libraries for single domain antibodies | |
| US20220135690A1 (en) | Methods and compositions relating to chemokine receptor variants | |
| WO2020176678A1 (en) | Variant nucleic acid libraries for glp1 receptor | |
| JP2023504572A (ja) | アデノシン受容体のためのバリアント核酸ライブラリー | |
| US20220356468A1 (en) | Variant nucleic acid libraries for ion channels | |
| US20220348659A1 (en) | Variant nucleic acid libraries for cd3 | |
| WO2022159620A1 (en) | Methods and compositions relating to adenosine receptors | |
| US20220411784A1 (en) | Variant nucleic acid libraries for glycans | |
| EP4314074A1 (en) | Variant nucleic acid libraries for tigit | |
| US20230265198A1 (en) | Neuropilin-1 variant antibodies and methods of use | |
| WO2023076419A2 (en) | Sars-cov-2 antibodies and methods of use | |
| WO2023091614A2 (en) | Dickkopf-1 variant antibodies and methods of use | |
| WO2024064310A2 (en) | Variant nucleic acid libraries for tigit |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20230711 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20230711 |
|
| RD02 | Notification of acceptance of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7422 Effective date: 20240426 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20240426 |
|
| RD14 | Notification of resignation of power of sub attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7434 Effective date: 20240426 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20240426 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20240724 |