KR101406631B1 - 유기 전기 발광 소자 - Google Patents
유기 전기 발광 소자 Download PDFInfo
- Publication number
- KR101406631B1 KR101406631B1 KR1020087021039A KR20087021039A KR101406631B1 KR 101406631 B1 KR101406631 B1 KR 101406631B1 KR 1020087021039 A KR1020087021039 A KR 1020087021039A KR 20087021039 A KR20087021039 A KR 20087021039A KR 101406631 B1 KR101406631 B1 KR 101406631B1
- Authority
- KR
- South Korea
- Prior art keywords
- group
- substituted
- unsubstituted
- carbon atoms
- branched
- Prior art date
Links
- 0 C[C@@](*c(c(*)c(c(*)c1c2c3*)N)c1c1c(c(*)c4-5)c2c(*)c(*)c3I)c1c4-c1c(*)c(*)c(C*)c2c1c-5c(*)c(*=C)c2* Chemical compound C[C@@](*c(c(*)c(c(*)c1c2c3*)N)c1c1c(c(*)c4-5)c2c(*)c(*)c3I)c1c4-c1c(*)c(*)c(C*)c2c1c-5c(*)c(*=C)c2* 0.000 description 13
- FKDVZXHFGNCBKH-UHFFFAOYSA-N C(CC(c1c(C=CCC2)c2ccc1)=CC1)C1c1c(ccc(C2C=CC=CC2)c2)c2c(-c2cc3ccccc3cc2)c(cc2)c1cc2C1=CC=CCC1 Chemical compound C(CC(c1c(C=CCC2)c2ccc1)=CC1)C1c1c(ccc(C2C=CC=CC2)c2)c2c(-c2cc3ccccc3cc2)c(cc2)c1cc2C1=CC=CCC1 FKDVZXHFGNCBKH-UHFFFAOYSA-N 0.000 description 1
- FQUOSBREFMFTBH-UHFFFAOYSA-N c(cc1)ccc1-c1c(-c(c(c-2c3)c4cc3-c3cc5ccccc5cc3)ccc4-c3cccc4c3cccc4)c-2c(-c2ccccc2)c2c1cccc2 Chemical compound c(cc1)ccc1-c1c(-c(c(c-2c3)c4cc3-c3cc5ccccc5cc3)ccc4-c3cccc4c3cccc4)c-2c(-c2ccccc2)c2c1cccc2 FQUOSBREFMFTBH-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent, e.g. electroluminescent, chemiluminescent materials
- C09K11/06—Luminescent, e.g. electroluminescent, chemiluminescent materials containing organic luminescent materials
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
- H10K85/626—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene containing more than one polycyclic condensed aromatic rings, e.g. bis-anthracene
-
- H—ELECTRICITY
- H05—ELECTRIC TECHNIQUES NOT OTHERWISE PROVIDED FOR
- H05B—ELECTRIC HEATING; ELECTRIC LIGHT SOURCES NOT OTHERWISE PROVIDED FOR; CIRCUIT ARRANGEMENTS FOR ELECTRIC LIGHT SOURCES, IN GENERAL
- H05B33/00—Electroluminescent light sources
- H05B33/12—Light sources with substantially two-dimensional radiating surfaces
- H05B33/14—Light sources with substantially two-dimensional radiating surfaces characterised by the chemical or physical composition or the arrangement of the electroluminescent material, or by the simultaneous addition of the electroluminescent material in or onto the light source
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
- H10K85/622—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene containing four rings, e.g. pyrene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
- H10K85/623—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene containing five rings, e.g. pentacene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
- H10K85/625—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene containing at least one aromatic ring having 7 or more carbon atoms, e.g. azulene
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1003—Carbocyclic compounds
- C09K2211/1011—Condensed systems
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1003—Carbocyclic compounds
- C09K2211/1014—Carbocyclic compounds bridged by heteroatoms, e.g. N, P, Si or B
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1029—Heterocyclic compounds characterised by ligands containing one nitrogen atom as the heteroatom
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1029—Heterocyclic compounds characterised by ligands containing one nitrogen atom as the heteroatom
- C09K2211/1037—Heterocyclic compounds characterised by ligands containing one nitrogen atom as the heteroatom with sulfur
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1044—Heterocyclic compounds characterised by ligands containing two nitrogen atoms as heteroatoms
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1044—Heterocyclic compounds characterised by ligands containing two nitrogen atoms as heteroatoms
- C09K2211/1048—Heterocyclic compounds characterised by ligands containing two nitrogen atoms as heteroatoms with oxygen
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1044—Heterocyclic compounds characterised by ligands containing two nitrogen atoms as heteroatoms
- C09K2211/1051—Heterocyclic compounds characterised by ligands containing two nitrogen atoms as heteroatoms with sulfur
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1092—Heterocyclic compounds characterised by ligands containing sulfur as the only heteroatom
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1096—Heterocyclic compounds characterised by ligands containing other heteroatoms
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/11—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/631—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine
Landscapes
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Physics & Mathematics (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Organic Chemistry (AREA)
- Electroluminescent Light Sources (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Abstract
본 발명에 따르면, 음극과 양극 사이에 적어도 발광층을 포함하는 1층 또는 복수 층으로 이루어지는 유기 박막층이 협지되어 있는 유기 전기 발광 소자에 있어서, 상기 발광층이 특정한 플루오란텐 구조를 갖는 화합물로부터 선택되는 적어도 1 종류와, 특정 구조의 축합 환 함유 화합물로부터 선택되는 적어도 1 종류를 함유하는 것에 의해, 수명이 길고, 고 발광 효율이며, 청색 발광이 얻어지는 유기 전기 발광 소자를 제공한다.
Description
본 발명은 플루오란텐 구조를 갖는 화합물과 축합 환 함유 화합물을 함유하는 유기 전기 발광 소자에 관한 것으로, 특히 상기 플루오란텐 구조를 갖는 화합물과 축합 환 함유 화합물을 발광층에 이용하는 것에 의해, 수명이 길고, 고 발광 효율이며, 청색 발광이 얻어지는 유기 전기 발광 소자에 관한 것이다.
유기 전기 발광 소자(이하, "전기 발광"을 "EL"이라고 약기하는 경우가 있음)는, 전계를 인가함으로써, 양극으로부터 주입된 정공과 음극으로부터 주입된 전자의 재결합 에너지에 의해 형광성 물질이 발광하는 원리를 이용한 자발광 소자이다. 이스트맨 코닥사의 C.W.Tang 등에 의한 적층형 소자에 의한 저전압 구동 유기 EL 소자의 보고(C.W.Tang, S.A. Vanslyke, 어플라이드 피직스 레터즈(Applied Physics Letters), 51권, 913 페이지, 1987년 등)가 이루어진 이래, 유기 재료를 구성 재료로 하는 유기 EL 소자에 관한 연구가 왕성하게 행해지고 있다. Tang 등은, 트리스(8-퀴놀리노라토)알루미늄을 발광층에, 트라이페닐다이아민 유도체를 정공 수송층에 이용하고 있다. 적층 구조의 이점으로는, 발광층에의 정공의 주입 효율을 높이는 것, 음극으로부터 주입된 전자를 블로킹하여 재결합에 의해 생성되는 여기자의 생성 효율을 높이는 것, 발광층 내에서 생성된 여기자를 가두는 것 등을 들 수 있다. 이 예와 같이 유기 EL 소자의 소자 구조로서는, 정공 수송(주입)층, 전자 수송 발광층의 2층형, 또는 정공 수송(주입)층, 발광층, 전자 수송(주입)층의 3층형 등이 잘 알려져 있다. 이러한 적층형 구조 소자에서는 주입된 정공과 전자의 재결합 효율을 높이기 위하여, 소자 구조나 형성 방법의 고안이 이루어지고 있다.
또한, 발광 재료로서는 트리스(8-퀴놀리노라토)알루미늄 착체 등의 킬레이트 착체, 쿠마린 유도체, 테트라페닐뷰타다이엔 유도체, 비스스타이릴아릴렌 유도체, 옥사다이아졸 유도체 등의 발광 재료가 알려져 있고, 그것으로부터는 청색부터 적색까지의 가시 영역의 발광이 얻어진다는 것이 보고되어 있으며, 컬러 표시 소자의 실현이 기대되고 있다(예컨대, 특허 문헌 1, 특허 문헌 2, 특허 문헌 3 등).
발광 재료로서 비스안트라센 유도체를 이용한 소자가 특허 문헌 4 및 특허 문헌 5에 개시되어 있다. 비스안트라센은 청색 발광 재료로서 사용되는데, 그 효율이나 수명이 실용 가능한 레벨에까지 도달하지 못하고 불충분하였다.
또한, 발광 재료로서 대칭 피렌 유도체를 이용한 소자가 특허 문헌 6, 특허 문헌 7, 특허 문헌 8, 및 특허 문헌 9에 개시되어 있다. 이러한 대칭 피렌 유도체는 청색 발광 재료로서 사용되는데, 소자 수명의 개선이 요구되고 있었다.
발광 재료로서 플루오란텐 유도체를 이용한 소자가 특허 문헌 10, 특허 문헌 11, 특허 문헌 12, 특허 문헌 13, 특허 문헌 14에 개시되어 있다. 이러한 플루오 란텐 유도체는, 청색 발광 재료로서 사용되는데, 소자 수명의 개선이 요구되고 있었다.
특허 문헌 1 :일본 특허 공개 제1996-239655호 공보
특허 문헌 2 :일본 특허 공개 제1995-183561호 공보
특허 문헌 3 :일본 특허 공개 제1991-200889호 공보
특허 문헌 4 :미국 특허 제3008897호 명세서
특허 문헌 5 :일본 특허 공개 제1996-12600호 공보
특허 문헌 6 :일본 특허 공개 제2001-118682호 공보
특허 문헌 7 :일본 특허 공개 제2002-63988호 공보
특허 문헌 8 :일본 특허 공개 제2004-75567호 공보
특허 문헌 9 :일본 특허 공개 제2004-83481호 공보
특허 문헌 10 :일본 특허 공개 제2002-69044호 공보
특허 문헌 11 :국제 공개 WO 02/085822 공보
특허 문헌 12 :국제 공개 WO 2005/033051 공보
특허 문헌 13 :일본 특허 공개 제1998-189247호 공보
특허 문헌 14 :일본 특허 공개 제2005-68087호 공보
(발명의 개시)
(발명이 해결하고자 하는 과제)
본 발명은 상기 과제를 해결하기 위하여 이루어진 것으로, 수명이 길고, 고 발광 효율이며, 청색 발광이 얻어지는 유기 EL 소자를 제공하는 것을 목적으로 한다.
(과제를 해결하기 위한 수단)
본 발명자 등은, 상기 목적을 달성하기 위하여 예의 연구를 거듭한 결과, 음극과 양극 사이에 적어도 발광층을 포함하는 1층 또는 복수 층으로 이루어지는 유기 박막층이 협지되어 있는 유기 EL 소자에 있어서, 상기 발광층이 하기 화학식 1로 표시되는 축합 환 함유 화합물로부터 선택되는 적어도 1 종류와, 플루오란텐 구조를 갖는 화합물로부터 선택되는 적어도 1 종류를 함유하는 유기 전기 발광 소자는, 수명이 길고, 고 발광 효율이며, 청색 발광이 얻어진다는 것을 발견하고, 본 발명을 완성하기에 이르렀다.
본 발명의 유기 EL 소자는, 발광층이 하기 화학식 1로 표시되는 축합 환 함유 화합물로부터 선택되는 적어도 1 종류와, 플루오란텐 구조를 갖는 화합물로부터 선택되는 적어도 1 종류를 함유한다.
[화학식 1]
G2
식중, G2는 축합 환 함유 화합물이며, 치환 또는 무치환의 안트라센 구조, 치환 또는 무치환의 피렌 구조, 치환 또는 무치환의 아민 구조, 또는 치환 또는 무치환의 벤젠 구조를 갖는 화합물이다.
본 발명의 유기 EL 소자에 이용하는 플루오란텐 구조를 갖는 화합물은, 바람직하게는 하기 화학식 2로 표시된다.
[화학식 2]
FLn-G1
식중, FL은 플루오란텐 구조를 갖는 1가의 기이며, n은 2~4의 정수이다. 복수의 FL은 동일해도 상이해도 좋다.
G1은, n이 1인 경우에는 수소 원자, n이 2 이상인 경우에는 치환 또는 무치환의 탄소 원자수 6~40의 방향족환기, 치환 또는 무치환의 탄소 원자수 6~40의 아릴아미노기, 치환 또는 무치환의 탄소 원자수 6~60의 다이아미노아릴기, 치환 또는 무치환의 탄소 원자수 6~60의 트라이아미노아릴기, 치환 또는 무치환의 탄소 원자수 3~40의 복소환기, 치환 또는 무치환의 에테닐렌기이며, 단일 결합을 포함한다.
(발명의 효과)
발광층이 하기 화학식 1로 표시되는 축합 환 함유 화합물로부터 선택되는 적어도 1 종류와, 플루오란텐 구조를 갖는 화합물로부터 선택되는 적어도 1 종류를 함유하는 본 발명의 유기 전기 발광 소자는, 수명이 길고, 고 발광 효율이며, 청색 발광이 얻어진다.
또한, 본 발명에 의해 얻어지는 유기 EL 소자의, 온도, 습도, 분위기 등에 대한 안정성 향상을 위하여, 소자의 표면에 보호층을 마련하거나, 실리콘 오일, 수 지 등에 의해 소자 전체를 보호하는 것도 가능하다.
(발명을 실시하기 위한 최선의 형태)
본 발명의 유기 EL 소자는, 음극과 양극 사이에 적어도 발광층을 포함하는 1층 또는 복수 층으로 이루어지는 유기 박막층이 협지되어 있는 유기 EL 소자에 있어서, 상기 발광층이 하기 화학식 1로 표시되는 축합 환 함유 화합물로부터 선택되는 적어도 1 종류와, 플루오란텐 구조를 갖는 화합물로부터 선택되는 적어도 1 종류를 함유한다. 이 유기 EL 소자는, 수명이 길고, 고 발광 효율이며, 청색 발광이 얻어진다.
본 발명의 유기 EL 소자에 이용하는 축합 환 함유 화합물은, 하기 화학식 1로 표시된다.
[화학식 1]
G2
식중, G2는 축합 환 함유 화합물이며, 치환 또는 무치환의 안트라센 구조, 치환 또는 무치환의 피렌 구조, 치환 또는 무치환의 아민 구조, 또는 치환 또는 무치환의 벤젠 구조를 갖는 화합물이다.
또한, 본 발명의 유기 EL 소자는, 하기 화학식 1로 표시되는 축합 환 함유 화합물로부터 선택되는 적어도 1 종류와, 하기 화학식 2로 표시되는 플루오란텐 구조를 갖는 화합물로부터 선택되는 적어도 1 종류를 함유한다.
[화학식 1]
G2
식중, G2는 축합 환 함유 화합물이며, 치환 또는 무치환의 안트라센 구조, 치환 또는 무치환의 피렌 구조, 치환 또는 무치환의 아민 구조, 또는 치환 또는 무치환의 벤젠 구조를 갖는 화합물이다.
[화학식 2]
FLn-G1
식중, FL은 플루오란텐 구조를 갖는 1가의 기이며, n은 2~4의 정수이다. 복수의 FL은 동일해도 상이해도 좋다.
G1은, 치환 또는 무치환의 탄소 원자수 6~40의 방향족환기, 치환 또는 무치환의 탄소 원자수 6~40의 아릴아미노기, 치환 또는 무치환의 탄소 원자수 6~60의 다이아미노아릴기, 치환 또는 무치환의 탄소 원자수 6~60의 트라이아미노아릴기, 치환 또는 무치환의 탄소 원자수 3~40의 복소환기, 치환 또는 무치환의 에테닐렌기이며, 단일 결합을 포함한다.
본 발명의 유기 전기 발광 소자에 있어서, 바람직하게는, 상기 플루오란텐 구조를 갖는 화합물이 하기 화학식 1a의 구조를 갖는 화합물이다.
[화학식 1a]
화학식 1a 중, X1~X10은, 각각 독립적으로, 수소 원자, 할로젠 원자, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알콕시기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬싸이오기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일옥시기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일싸이오기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬옥시기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬싸이오기, 치환 또는 무치환의 탄소 원자수 6~20의 아릴기(단, 화학식 1a인 경우는 없음), 치환 또는 무치환의 탄소 원자수 5~20의 복소환기, 치환 또는 무치환의 탄소 원자수 6~20의 아릴옥시기, 치환 또는 무치환의 탄소 원자수 6~20의 아릴싸이오기, 치환 또는 무치환의 탄소 원자수 2~30의 아미노기, 사이아노기, 실릴기, 하이드록실기, -COOR1e기(기 중, R1e는 수소 원자, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 또는 치환 또는 무치환의 탄소 원자수 6~30의 아릴기를 나타냄), -COR2e기(기 중, R2e는 수소 원자, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 치환 또는 무치환의 탄소 원자수 6~30의 아릴기, 또는 아미노기를 나타냄), -OCOR3e기(기 중, R3e는 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 치환 또는 무치환의 탄소 원자수 6~30의 아릴기를 나타냄)를 나타내며, 또한 X1~X10 중, 인접하는 기 및 각 기의 치환기는 서로 결합하여 치환 또는 무치환의 탄소환을 형성하고 있어도 좋다.
바람직하게는, 상기 화학식 1a 중, X3과 X10의 둘 모두가 수소 원자가 되는 경우는 없다.
본 발명의 유기 전기 발광 소자에 있어서, 바람직하게는, 상기 플루오란텐 구조를 갖는 화합물이 하기 화학식 1b의 구조를 갖는 화합물이다.
[화학식 1b]
화학식 1b 중, X1~X12는 각각 독립적으로, 수소 원자, 할로젠 원자, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알콕시기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬싸이오기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일옥시기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일싸이오기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬옥시기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬싸이오기, 치환 또는 무치환의 탄소 원자수 6~20의 아릴기(단, 화학식 1b인 경우는 없음), 치환 또는 무치환의 탄소 원자수 5~20의 복소환기, 치환 또는 무치환의 탄소 원자수 6~20의 아릴옥시기, 치환 또는 무치환의 탄소 원자수 6~20의 아릴싸이오기, 치환 또는 무치환의 탄소 원자수 2~30의 아미노기, 사이아노기, 실릴기, 하이드록실기, -COOR1e기(기 중, R1e는 수소 원자, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 또는 치환 또는 무치환의 탄소 원자수 6~30의 아릴기를 나타냄), -COR2e기(기 중, R2e는 수소 원자, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 치환 또는 무치환의 탄소 원자수 6~30의 아릴기, 또는 아미노기를 나타냄), -OCOR3e기(기 중, R3e는, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 치환 또는 무치환의 탄소 원자수 6~30의 아릴기를 나타냄)를 나타내며, 또한 X1~X12 중, 인접하는 기 및 각 기의 치환기는 서로 결합하여 치환 또는 무치환의 탄소환을 형성하고 있어도 좋다.
단, 상기 화학식 1b 중, X4와 X11의 둘 모두가 수소 원자인 경우는 없다.
단, 플루오란텐 구조를 갖는 화합물이 화학식 1b로 표시되고, 화학식 1의 G2가 9,10-다이페닐안트라센인 경우는 없다.
본 발명의 유기 전기 발광 소자에 있어서, 바람직하게는, 상기 플루오란텐 구조를 갖는 화합물이 하기 화학식 1c의 구조를 갖는 화합물이다.
[화학식 1c]
화학식 1c 중, X1~X12는 각각 독립적으로, 수소 원자, 할로젠 원자, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알콕시기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬싸이오기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일옥시기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일싸이오기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬옥시기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬싸이오기, 치환 또는 무치환의 탄소 원자수 6~20의 아릴기, 치환 또는 무치환의 탄소 원자수 6~20의 아릴옥시기, 치환 또는 무치환의 탄소 원자수 6~20의 아릴싸이오기, 치환 또는 무치환의 탄소 원자수 2~30의 아미노기, 사이아노기, 실릴기, 하이드록실기, -COOR1e기(기 중, R1e는 수소 원자, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 또는 치환 또는 무치환의 탄소 원자수 6~30의 아릴기를 나타냄), -COR2e기(기 중, R2e는 수소 원자, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 치환 또는 무치환의 탄소 원자수 6~30의 아릴기, 또는 아미노기를 나타냄), -OCOR3e기(기 중, R3e는, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 치환 또는 무치환의 탄소 원자수 6~30의 아릴기를 나타냄)를 나타내며, 또한 X1~X12 중, 인접하는 기 및 각 기의 치환기는 서로 결합하여 치환 또는 무치환의 탄소환을 형성하고 있어도 좋다.
단, 상기 화학식 1c 중, X7≠X8이다.
단, 상기 화학식 1c 중, X4와 X11의 둘 모두가 수소 원자인 경우는 없다.
상기 화학식 2에 있어서 n이 2~4이고, FL이 하기 화학식 2a, 2c, 및 2d 중 어느 하나에 나타내는 구조를 갖는 화합물로부터 유도되는 1가의 기이다.
[화학식 2a]
[화학식 2c]
[화학식 2d]
화학식 2a, 2c, 및 2d 중, X1~X16은 각각 독립적으로, 수소 원자, 할로젠 원자, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알콕시기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬싸이오기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일옥시기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일싸이오기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬옥시기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬싸이오기, 치환 또는 무치환의 탄소 원자수 6~20의 아릴기, 치환 또는 무치환의 탄소 원자수 6~20의 아릴옥시기, 치환 또는 무치환의 탄소 원자수 6~20의 아릴싸이오기, 치환 또는 무치환의 탄소 원자수 2~30의 아미노기, 사이아노기, 실릴기, 하이드록실기, -COOR1e기(기 중, R1e는 수소 원자, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 또는 치환 또는 무치환의 탄소 원자수 6~30의 아릴기를 나타냄), -COR2e기(기 중, R2e는 수소 원자, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 치환 또는 무치환의 탄소 원자수 6~30의 아릴기, 또는 아미노기를 나타냄), -OCOR3e기(기 중, R3e는, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 치환 또는 무치환의 탄소 원자수 6~30의 아릴기를 나타냄)를 나타내며, 또한 X1~X16 중, 인접하는 기 및 각 기의 치환기는 서로 결합하여 치환 또는 무치환의 탄소환을 형성하고 있어도 좋다.
상기 화학식 2에 있어서 n이 2~4이고, FL이 하기 화학식 2'b에 나타내는 구조를 갖는 화합물로부터 유도되는 1가의 기이다.
[화학식 2'b]
화학식 2'b 중, X1~X12는 각각 독립적으로, 수소 원자, 할로젠 원자, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알콕시기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬싸이오기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일옥시기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일싸이오기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬옥시기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬싸이오기, 치환 또는 무치환의 탄소 원자수 6~20의 아릴기, 치환 또는 무치환의 탄소 원자수 6~20의 아릴옥시기, 치환 또는 무치환의 탄소 원자수 6~20의 아릴싸이오기, 치환 또는 무치환의 탄소 원자수 2~30의 아미노기, 사이아노기, 실릴기, 하이드록실기, -COOR1e기(기 중, R1e는 수소 원자, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 또는 치환 또는 무치환의 탄소 원자수 6~30의 아릴기를 나타냄), -COR2e기(기 중, R2e는 수소 원자, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 치환 또는 무치환의 탄소 원자수 6~30의 아릴기, 또는 아미노기를 나타냄), -OCOR3e기(기 중, R3e는, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 치환 또는 무치환의 탄소 원자수 6~30의 아릴기를 나타냄)를 나타내며, 또한 X1~X12 중, 인접하는 기 및 각 기의 치환기는 서로 결합하여 치환 또는 무치환의 탄소환을 형성하고 있어도 좋다.
단, 상기 화학식 2에 있어서, n이 2로 표시되고, G1이 페닐렌기로 이루어지는 연결기이며, 화학식 1의 G2가 10,10'-비스(2-페닐페닐)-9,9'-바이안트라센인 경우는 없다.
화학식 1a~1c, 2a~2d 및 2'b 중의 X1~X16의 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기로서는, 예컨대, 메틸기, 에틸기, 프로필기, 아이소프로필기, n-뷰틸기, s-뷰틸기, 아이소뷰틸기, t-뷰틸기, n-펜틸기, n-헥실기, n-헵틸기, n-옥틸기, n-노닐기, n-데실기, n-운데실기, n-도데실기, n-트라이데실기, n-테트라데실기, n-펜타데실기, n-헥사데실기, n-헵타데실기, n-옥타데실기, 네오펜틸기, 1-메틸펜틸기, 2-메틸펜틸기, 1-펜틸헥실기, 1-뷰틸펜틸기, 1-헵틸옥틸기, 3-메틸펜틸기, 하이드록시메틸기, 1-하이드록시에틸기, 2-하이드록시에틸기, 2-하이드록시아이소뷰틸기, 1,2-다이하이드록시에틸기, 1,3-다이하이드록시아이소프로필기, 2,3-다이하이드록시-t-뷰틸기, 1,2,3-트라이하이드록시프로필기, 클로로메틸기, 1-클로로에틸기, 2-클로로에틸기, 2-클로로아이소뷰틸기, 1,2-다이클로로에틸기, 1,3-다이클로로아이소프로필기, 2,3-다이클로로-t-뷰틸기, 1,2,3-트라이클로로프로필기, 브로모메틸기, 1-브로모에틸기, 2-브로모에틸기, 2-브로모아이소뷰틸기, 1,2-다이브로모에틸기, 1,3-다이브로모아이소프로필기, 2,3-다이브로모-t-뷰틸기, 1,2,3-트라이브로모프로필기, 아이오도메틸기, 1-아이오도에틸기, 2-아이오도에틸기, 2-아이오도아이소뷰틸기, 1,2-다이아이오도에틸기, 1,3-다이아이오도아이소프로필기, 2,3-다이아이오도-t-뷰틸기, 1,2,3-트라이아이오도프로필기, 아미노메틸기, 1-아미노에틸기, 2-아미노에틸기, 2-아미노아이소뷰틸기, 1,2-다이아미노에틸기, 1,3-다이아미노아이소프로필기, 2,3-다이아미노-t-뷰틸기, 1,2,3-트라이아미노프로필기, 사이아노메틸기, 1-사이아노에틸기, 2-사이아노에틸기, 2-사이아노아이소뷰틸기, 1,2-다이사이아노에틸기, 1,3-다이사이아노아이소프로필기, 2,3-다이사이아노-t-뷰틸기, 1,2,3-트라이사이아노프로필기, 나이트로메틸기, 1-나이트로에틸기, 2-나이트로에틸기, 1,2-다이나이트로에틸기, 2,3-다이나이트로-t-뷰틸기, 1,2,3-트라이나이트로프로필기, 트라이플루오로메틸기, 퍼플루오로에틸기, 퍼플루오로프로필기, 퍼플루오로뷰틸기, 퍼플루오로펜틸기, 퍼플루오로헥실기, 1H,1H-퍼플루오로에틸기, 1H,1H-퍼플루오로프로필기, 1H,1H-퍼플루오로뷰틸기, 1H,1H-퍼플루오로펜틸기, 1H,1H-퍼플루오로헥실기, 사이클로펜틸기, 사이클로헥실기, 사이클로옥틸기, 3,5-테트라메틸사이클로헥실기 등을 들 수 있다.
이들 중에서도 바람직하게는, 메틸기, 에틸기, 프로필기, 아이소프로필기, n-뷰틸기, s-뷰틸기, 아이소뷰틸기, t-뷰틸기, n-펜틸기, n-헥실기, n-헵틸기, n-옥틸기, n-노닐기, n-데실기, n-운데실기, n-도데실기, n-트라이데실기, n-테트라데실기, n-펜타데실기, n-헥사데실기, n-헵타데실기, n-옥타데실기, 네오펜틸기, 1-메틸펜틸기, 1-펜틸헥실기, 1-뷰틸펜틸기, 1-헵틸옥틸기, 사이클로헥실기, 사이클로옥틸기, 3,5-테트라메틸사이클로헥실기 등을 들 수 있다.
치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알콕시기 및 알킬싸이오기는, 각각 -OY1 및 -SY2로 표시되는 기이며, Y1 및 Y2의 구체예로서는, 상기 알킬기에서 설명한 것과 동일한 것을 들 수 있고, 바람직한 예도 마찬가지이다.
치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기로서는, 예컨대, 바이닐기, 알릴기, 1-뷰텐일기, 2-뷰텐일기, 3-뷰텐일기, 1,3-뷰테인다이엔일기, 1-메틸바이닐기, 스타이릴기, 2,2-다이페닐바이닐기, 1,2-다이페닐바이닐기, 1-메틸알릴기, 1,1-다이메틸알릴기, 2-메틸알릴기, 1-페닐알릴기, 2-페닐알릴기, 3-페닐알릴기, 3,3-다이페닐알릴기, 1,2-다이메틸알릴기, 1-페닐-1-뷰텐일기, 3-페닐-1-뷰텐일기 등을 들 수 있으며, 바람직하게는, 스타이릴기, 2,2-다이페닐바이닐기, 1,2-다이페닐바이닐기 등을 들 수 있다.
치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일옥시기, 및 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일싸이오기는, 각각 -OY3 및-SY4로 표시되는 기이며, Y3 및 Y4의 구체예로서는, 상기 알켄일기에서 설명한 것과 동일한 것을 들 수 있고, 바람직한 예도 마찬가지이다.
치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기로서는, 예컨대, 벤질기, 1-페닐에틸기, 2-페닐에틸기, 1-페닐아이소프로필기, 2-페닐아이소프로필기, 페닐-t-뷰틸기, α-나프틸메틸기, 1-α-나프틸에틸기, 2-α-나프틸에틸기, 1-α-나프틸아이소프로필기, 2-α-나프틸아이소프로필기, β-나프틸메틸기, 1-β-나프틸에틸기, 2-β-나프틸에틸기, 1-β-나프틸아이소프로필기, 2-β-나프틸아이소프로필기, 1-피롤릴메틸기, 2-(1-피롤릴)에틸기, p-메틸벤질기, m-메틸벤질기, o-메틸벤질기, p-클로로벤질기, m-클로로벤질기, o-클로로벤질기, p-브로모벤질기, m-브로모벤질기, o-브로모벤질기, p-아이오도벤질기, m-아이오도벤질기, o-아이오도벤질기, p-하이드록시벤질기, m-하이드록시벤질기, o-하이드록시벤질기, p-아미노벤질기, m-아미노벤질기, o-아미노벤질기, p-나이트로벤질기, m-나이트로벤질기, o-나이트로벤질기, p-사이아노벤질기, m-사이아노벤질기, o-사이아노벤질기, 1-하이드록시-2-페닐아이소프로필기, 1-클로로-2-페닐아이소프로필기 등을 들 수 있다.
이들 중에서도 바람직하게는, 벤질기, p-사이아노벤질기, m-사이아노벤질기, o-사이아노벤질기, 1-페닐에틸기, 2-페닐에틸기, 1-페닐아이소프로필기, 2-페닐아이소프로필기 등을 들 수 있다.
치환 또는 무치환의 탄소 원자수 7~30의 아르알킬옥시기, 및 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬싸이오기는, 각각 -OY5 및-SY6으로 표시되는 기이며, Y5 및 Y6의 구체예로서는, 상기 아르알킬기에서 설명한 것과 동일한 것을 들 수 있고, 바람직한 예도 마찬가지이다.
치환 또는 무치환의 탄소 원자수 6~20의 아릴기로서는, 예컨대, 페닐기, 1-나프틸기, 2-나프틸기, 1-안트릴기, 2-안트릴기, 9-안트릴기, 1-페난트릴기, 2-페난트릴기, 3-페난트릴기, 4-페난트릴기, 9-페난트릴기, 1-나프타센일기, 2-나프타센일기, 9-나프타센일기, 1-피렌일기, 2-피렌일기, 4-피렌일기, 2-바이페닐일기, 3-바이페닐일기, 4-바이페닐일기, p-터페닐-4-일기, p-터페닐-3-일기, p-터페닐-2-일기, m-터페닐-4-일기, m-터페닐-3-일기, m-터페닐-2-일기, o-톨릴기, m-톨릴기, p-톨릴기, p-t-뷰틸페닐기, p-(2-페닐프로필)페닐기, 3-메틸-2-나프틸기, 4-메틸-1-나프틸기, 4-메틸-1-안트릴기, 4'-메틸바이페닐일기, 4"-t-뷰틸-p-터페닐-4-일기, o-큐멘일기, m-큐멘일기, p-큐멘일기, 2,3-자일릴기, 3,4-자일릴기, 2,5-자일릴기, 메시틸기 등을 들 수 있다.
이들 중에서도 바람직하게는, 페닐기, 1-나프틸기, 2-나프틸기, 9-페난트릴기, 2-바이페닐일기, 3-바이페닐일기, 4-바이페닐일기, p-톨릴기, 3,4-자일릴기 등을 들 수 있다.
X1~X16의 치환 또는 무치환의 방향족 복소환기의 예로서는, 1-피롤릴기, 2-피롤릴기, 3-피롤릴기, 피라진일기, 2-피리딘일기, 3-피리딘일기, 4-피리딘일기, 1-인돌릴기, 2-인돌릴기, 3-인돌릴기, 4-인돌릴기, 5-인돌릴기, 6-인돌릴기, 7-인돌릴기, 1-아이소인돌릴기, 2-아이소인돌릴기, 3-아이소인돌릴기, 4-아이소인돌릴기, 5-아이소인돌릴기, 6-아이소인돌릴기, 7-아이소인돌릴기, 2-퓨릴기, 3-퓨릴기, 2-벤조퓨란일기, 3-벤조퓨란일기, 4-벤조퓨란일기, 5-벤조퓨란일기, 6-벤조퓨란일기, 7-벤조퓨란일기, 1-아이소벤조퓨란일기, 3-아이소벤조퓨란일기, 4-아이소벤조퓨란일기, 5-아이소벤조퓨란일기, 6-아이소벤조퓨란일기, 7-아이소벤조퓨란일기, 퀴놀릴기, 3-퀴놀릴기, 4-퀴놀릴기, 5-퀴놀릴기, 6-퀴놀릴기, 7-퀴놀릴기, 8-퀴놀릴기, 1-아이소퀴놀릴기, 3-아이소퀴놀릴기, 4-아이소퀴놀릴기, 5-아이소퀴놀릴기, 6-아이소퀴놀릴기, 7-아이소퀴놀릴기, 8-아이소퀴놀릴기, 2-퀴녹살린일기, 5-퀴녹살린일기, 6-퀴녹살린일기, 1-카바졸릴기, 2-카바졸릴기, 3-카바졸릴기, 4-카바졸릴기, 9-카바졸릴기, 1-페난트리딘일기, 2-페난트리딘일기, 3-페난트리딘일기, 4-페난트리딘일기, 6-페난트리딘일기, 7-페난트리딘일기, 8-페난트리딘일기, 9-페난트리딘일기, 10-페난트리딘일기, 1-아크리딘일기, 2-아크리딘일기, 3-아크리딘일기, 4-아크리딘일기, 9-아크리딘일기, 1,7-페난트롤린-2-일기, 1,7-페난트롤린-3-일기, 1,7-페난트롤린-4-일기, 1,7-페난트롤린-5-일기, 1,7-페난트롤린-6-일기, 1,7-페난트롤린-8-일기, 1,7-페난트롤린-9-일기, 1,7-페난트롤린-10-일기, 1,8-페난트롤린-2-일기, 1,8-페난트롤린-3-일기, 1,8-페난트롤린-4-일기, 1,8-페난트롤린-5-일기, 1,8-페난트롤린-6-일기, 1,8-페난트롤린-7-일기, 1,8-페난트롤린-9-일기, 1,8-페난트롤린-10-일기, 1,9-페난트롤린-2-일기, 1,9-페난트롤린-3-일기, 1,9-페난트롤린-4-일기, 1,9-페난트롤린-5-일기, 1,9-페난트롤린-6-일기, 1,9-페난트롤린-7-일기, 1,9-페난트롤린-8-일기, 1,9-페난트롤린-10-일기, 1,10-페난트롤린-2-일기, 1,10-페난트롤린-3-일기, 1,10-페난트롤린-4-일기, 1,10-페난트롤린-5-일기, 2,9-페난트롤린-1-일기, 2,9-페난트롤린-3-일기, 2,9-페난트롤린-4-일기, 2,9-페난트롤린-5-일기, 2,9-페난트롤린-6-일기, 2,9-페난트롤린-7-일기, 2,9-페난트롤린-8-일기, 2,9-페난트롤린-10-일기, 2,8-페난트롤린-1-일기, 2,8-페난트롤린-3-일기, 2,8-페난트롤린-4-일기, 2,8-페난트롤린-5-일기, 2,8-페난트롤린-6-일기, 2,8-페난트롤린-7-일기, 2,8-페난트롤린-9-일기, 2,8-페난트롤린-10-일기, 2,7-페난트롤린-1-일기, 2,7-페난트롤린-3-일기, 2,7-페난트롤린-4-일기, 2,7-페난트롤린-5-일기, 2,7-페난트롤린-6-일기, 2,7-페난트롤린-8-일기, 2,7-페난트롤린-9-일기, 2,7-페난트롤린-10-일기, 1-페나진일기, 2-페나진일기, 1-페노싸이아진일기, 2-페노싸이아진일기, 3-페노싸이아진일기, 4-페노싸이아진일기, 10-페노싸이아진일기, 1-페녹사진일기, 2-페녹사진일기, 3-페녹사진일기, 4-페녹사진일기, 10-페녹사진일기, 2-옥사졸릴기, 4-옥사졸릴기, 5-옥사졸릴기, 2-옥사다이아졸릴기, 5-옥사다이아졸릴기, 3-퓨라잔일기, 2-싸이엔일기, 3-싸이엔일기, 2-메틸피롤-1-일기, 2-메틸피롤-3-일기, 2-메틸피롤-4-일기, 2-메틸피롤-5-일기, 3-메틸피롤-1-일기, 3-메틸피롤-2-일기, 3-메틸피롤-4-일기, 3-메틸피롤-5-일기, 2-t-뷰틸피롤-4-일기, 3-(2-페닐프로필)피롤-1-일기, 2-메틸-1-인돌릴기, 4-메틸-1-인돌릴기, 2-메틸-3-인돌릴기, 4-메틸-3-인돌릴기, 2-t-뷰틸1-인돌릴기, 4-t-뷰틸1-인돌릴기, 2-t-뷰틸3-인돌릴기, 4-t-뷰틸3-인돌릴기 등을 들 수 있다.
치환 또는 무치환의 탄소 원자수 6~20의 아릴옥시기, 및 치환 또는 무치환의 탄소 원자수 6~20의 아릴싸이오기는, 각각 -OY7 및-SY8로 표시되는 기이며, Y7 및 Y8의 구체예로서는, 상기 아릴기에서 설명한 것과 동일한 것을 들 수 있고, 바람직한 예도 마찬가지이다.
치환 또는 무치환의 탄소 원자수 2~30의 아미노기로서는, 알킬아미노기 및 아르알킬아미노기가 포함되고, -NQ1Q2로 표시되며, Q1, Q2의 구체예로서는 각각 독립적으로, 상기 알킬기, 상기 아릴기, 상기 아르알킬기에서 설명한 것과 동일한 것을 들 수 있고, 바람직한 예도 마찬가지이다.
-COOR1e기, -COR2e기, 및 -OCOR3e기에 있어서의 R1e, R2e 및 R3e인 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 또는 치환 또는 무치환의 탄소 원자수 6~30의 아릴기, 또는 아미노기의 구체예도 상기와 마찬가지의 구체예를 들 수 있다.
X1~X16으로 바람직한 것은 치환 또는 무치환의 탄소 원자수 6~20의 아릴기이다.
본 발명의 유기 전기 발광 소자에 함유되는 플루오란텐 구조를 갖는 화합물이, 상기 화학식 2에 있어서 n이 2이고, 2개의 FL이 서로 상이하면 바람직하다.
본 발명의 유기 전기 발광 소자에 함유되는 플루오란텐 구조를 갖는 화합물이, 상기 화학식 2에 있어서 n이 2이고, 2개의 FL이 상기 화학식 2a~2d 및 2'b 중 어느 하나로 표시되고, 또한 서로 상이하면 더 바람직하다.
화학식 2에 있어서의 G1은, 치환 또는 무치환의 탄소 원자수 6~40의 방향족환기, 치환 또는 무치환의 탄소 원자수 6~40의 아릴아미노기, 치환 또는 무치환의 탄소 원자수 6~60의 다이아미노아릴기, 치환 또는 무치환의 탄소 원자수 6~60의 트라이아미노아릴기, 치환 또는 무치환의 탄소 원자수 3~40의 복소환기, 또는 치환 또는 무치환의 에테닐렌기이다. 한편, n이 2 이상인 경우에는, G1은 단일 결합인 경우를 포함한다.
G1은 바람직하게는, 치환 또는 비치환의 페닐렌, 바이페닐렌, 나프타센, 안트레센, 에테닐렌, 플루오렌, 싸이오펜, 싸이아다이아졸, 피라진, 아민, 아릴아민, 트라이아릴아민, 카바졸, 피롤, 싸이아졸, 벤조싸이아졸, 벤조싸이아다이아졸, 페난트롤린, 퀴놀린, 및 퀴녹살린으로 이루어지는 연결기를 나타낸다.
G1은 바람직하게는 하기 구조의 2가 또는 3가의 기로부터 선택된다.
상기 화학식 2에 있어서 n이 2~4이고, FL이 하기 화학식 2'b에 나타내는 구조를 갖는 화합물로부터 유도되는 1가의 기이다.
[화학식 2'b]
화학식 2'b 중, X1~X12는 각각 독립적으로, 수소 원자, 할로젠 원자, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알콕시기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬싸이오기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일옥시기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일싸이오기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬옥시기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬싸이오기, 치환 또는 무치환의 탄소 원자수 6~20의 아릴기, 치환 또는 무치환의 탄소 원자수 6~20의 아릴옥시기, 치환 또는 무치환의 탄소 원자수 6~20의 아릴싸이오기, 치환 또는 무치환의 탄소 원자수 2~30의 아미노기, 사이아노기, 실릴기, 하이드록실기, -COOR1e기(기 중, R1e는 수소 원자, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 또는 치환 또는 무치환의 탄소 원자수 6~30의 아릴기를 나타냄), -COR2e기(기 중, R2e는 수소 원자, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 치환 또는 무치환의 탄소 원자수 6~30의 아릴기, 또는 아미노기를 나타냄), -OCOR3e기(기 중, R3e는, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 치환 또는 무치환의 탄소 원자수 6~30의 아릴기를 나타냄)를 나타내며, 또한 X1~X12 중, 인접하는 기 및 각 기의 치환기는 서로 결합하여 치환 또는 무치환의 탄소환을 형성하고 있어도 좋다.
단, 복수의 FL은 n=2일 때에는 서로 상이하고, n=3~4일 때, 적어도 하나의 FL은 다른 FL과 상이하다.
또한, 화학식 2'b 중, X1~X12의 구체예는 상기의 것과 동일하다.
상기 화학식 2에 있어서 n이 2~4이고, FL이 하기 화학식 2'b에 나타내는 구조를 갖는 화합물로부터 유도되는 1가의 기이다.
[화학식 2'b]
화학식 2'b 중, X1~X12는 각각 독립적으로, 수소 원자, 할로젠 원자, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알콕시기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬싸이오기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일옥시기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일싸이오기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬옥시기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬싸이오기, 치환 또는 무치환의 탄소 원자수 6~20의 아릴기, 치환 또는 무치환의 탄소 원자수 6~20의 아릴옥시기, 치환 또는 무치환의 탄소 원자수 6~20의 아릴싸이오기, 치환 또는 무치환의 탄소 원자수 2~30의 아미노기, 사이아노기, 실릴기, 하이드록실기, -COOR1e기(기 중, R1e는 수소 원자, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 또는 치환 또는 무치환의 탄소 원자수 6~30의 아릴기를 나타냄), -COR2e기(기 중, R2e는 수소 원자, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 치환 또는 무치환의 탄소 원자수 6~30의 아릴기, 또는 아미노기를 나타냄), -OCOR3e기(기 중, R3e는, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 치환 또는 무치환의 탄소 원자수 6~30의 아릴기를 나타냄)를 나타내며, 또한 X1~X12 중, 인접하는 기 및 각 기의 치환기는 서로 결합하여 치환 또는 무치환의 탄소환을 형성하고 있어도 좋다.
단, 복수의 FL은 n=2일 때는 서로 상이하고, n=3~4일 때, 적어도 하나의 FL은 다른 FL과 상이하다. 상기 G1이 단일 결합 및 하기 구조의 기로부터 선택되는 1종이다. 또한, 화학식 2'b 중, X1~X12의 구체예는 상기의 것과 동일하다.
본 발명의 유기 EL 소자 재료로서 화학식 2로 표시되는 플루오란텐 구조를 갖는 화합물과 함께 사용되는 축합 환 함유 화합물은, 하기 화학식 1로 표시된다.
[화학식 1]
G2
식중, G2는 축합 환 함유 화합물이며, 치환 또는 무치환의 안트라센 구조, 치환 또는 무치환의 피렌 구조, 치환 또는 무치환의 아민 구조, 또는 치환 또는 무치환의 벤젠 구조를 갖는 화합물이다.
G2는 하기 치환 또는 무치환의 안트라센 구조이면 바람직하다.
[화학식 3a]
화학식 3a 중, A1 및 A2는 각각 독립적으로, 치환 또는 무치환의 핵탄소수 10~20의 축합 방향족환기이다.
화학식 3a에 있어서의, A1 및 A2의 치환 또는 무치환의 축합 방향족환기로서는, 예컨대, 1-나프틸기, 2-나프틸기, 1-안트릴기, 2-안트릴기, 9-안트릴기, 1-페난트릴기, 2-페난트릴기, 3-페난트릴기, 4-페난트릴기, 9-페난트릴기, 1-나프타센일기, 2-나프타센일기, 9-나프타센일기, 1-피렌일기, 2-피렌일기, 4-피렌일기, 3-메틸-2-나프틸기, 4-메틸-1-나프틸기, 4-메틸-1-안트릴기 등을 들 수 있다.
이들 중에서도 바람직하게는, 1-나프틸기, 2-나프틸기, 9-페난트릴기이다.
화학식 3a에 있어서의 Ar1 및 Ar2는 각각 독립적으로, 수소 원자, 또는 치환 또는 무치환의 핵탄소수 6~50의 방향족환기이다.
Ar1 및 Ar2의 치환 또는 무치환의 방향족환기로서는, 예컨대, 페닐기, 1-나프틸기, 2-나프틸기, 1-안트릴기, 2-안트릴기, 9-안트릴기, 1-페난트릴기, 2-페난트릴기, 3-페난트릴기, 4-페난트릴기, 9-페난트릴기, 1-나프타센일기, 2-나프타센일기, 9-나프타센일기, 1-피렌일기, 2-피렌일기, 4-피렌일기, 2-바이페닐일기, 3-바이페닐일기, 4-바이페닐일기, p-터페닐-4-일기, p-터페닐-3-일기, p-터페닐-2-일기, m-터페닐-4-일기, m-터페닐-3-일기, m-터페닐-2-일기, o-톨릴기, m-톨릴기, p-톨릴기, p-t-뷰틸페닐기, p-(2-페닐프로필)페닐기, 3-메틸-2-나프틸기, 4-메틸-1-나프틸기, 4-메틸-1-안트릴기, 4'-메틸바이페닐일기, 4"-t-뷰틸-p-터페닐-4-일기 등을 들 수 있다.
이들 중에서도 바람직하게는, 페닐기, 1-나프틸기, 2-나프틸기, 9-페난트릴기, 1-나프타센일기, 2-나프타센일기, 9-나프타센일기, 1-피렌일기, 2-피렌일기, 4-피렌일기, 2-바이페닐일기, 3-바이페닐일기, 4-바이페닐일기, o-톨릴기, m-톨릴기, p-톨릴기, p-t-뷰틸페닐기이다.
화학식 3a에 있어서의, R1~R10은 각각 독립적으로, 수소 원자, 치환 또는 무치환의 핵탄소수 6~50의 방향족환기, 치환 또는 무치환의 핵원자수 5~50의 방향족 복소환기, 치환 또는 무치환의 탄소수 1~50의 알킬기, 치환 또는 무치환의 사이클로알킬기, 치환 또는 무치환의 탄소수 1~50의 알콕시기, 치환 또는 무치환의 탄소수 6~50의 아르알킬기, 치환 또는 무치환의 핵원자수 5~50의 아릴옥시기, 치환 또는 무치환의 핵원자수 5~50의 아릴싸이오기, 치환 또는 무치환의 탄소수 1~50의 알콕시카보닐기, 치환 또는 무치환의 실릴기, 카복실기, 할로젠 원자, 사이아노기, 나이트로기 또는 하이드록실기이다.
R1~R10의 치환 또는 무치환의 방향족환기의 예로서는, 페닐기, 1-나프틸기, 2-나프틸기, 1-안트릴기, 2-안트릴기, 9-안트릴기, 1-페난트릴기, 2-페난트릴기, 3-페난트릴기, 4-페난트릴기, 9-페난트릴기, 1-나프타센일기, 2-나프타센일기, 9-나프타센일기, 1-피렌일기, 2-피렌일기, 4-피렌일기, 2-바이페닐일기, 3-바이페닐일기, 4-바이페닐일기, p-터페닐-4-일기, p-터페닐-3-일기, p-터페닐-2-일기, m-터페닐-4-일기, m-터페닐-3-일기, m-터페닐-2-일기, o-톨릴기, m-톨릴기, p-톨릴기, p-t-뷰틸페닐기, p-(2-페닐프로필)페닐기, 3-메틸-2-나프틸기, 4-메틸-1-나프틸기, 4-메틸-1-안트릴기, 4'-메틸바이페닐일기, 4"-t-뷰틸-p-터페닐-4-일기 등을 들 수 있다.
R1~R10의 치환 또는 무치환의 방향족 복소환기의 예로서는, 1-피롤릴기, 2-피롤릴기, 3-피롤릴기, 피라진일기, 2-피리딘일기, 3-피리딘일기, 4-피리딘일기, 1-인돌릴기, 2-인돌릴기, 3-인돌릴기, 4-인돌릴기, 5-인돌릴기, 6-인돌릴기, 7-인돌릴기, 1-아이소인돌릴기, 2-아이소인돌릴기, 3-아이소인돌릴기, 4-아이소인돌릴기, 5-아이소인돌릴기, 6-아이소인돌릴기, 7-아이소인돌릴기, 2-퓨릴기, 3-퓨릴기, 2-벤조퓨란일기, 3-벤조퓨란일기, 4-벤조퓨란일기, 5-벤조퓨란일기, 6-벤조퓨란일기, 7-벤조퓨란일기, 1-아이소벤조퓨란일기, 3-아이소벤조퓨란일기, 4-아이소벤조퓨란일기, 5-아이소벤조퓨란일기, 6-아이소벤조퓨란일기, 7-아이소벤조퓨란일기, 퀴놀릴기, 3-퀴놀릴기, 4-퀴놀릴기, 5-퀴놀릴기, 6-퀴놀릴기, 7-퀴놀릴기, 8-퀴놀릴기, 1-아이소퀴놀릴기, 3-아이소퀴놀릴기, 4-아이소퀴놀릴기, 5-아이소퀴놀릴기, 6-아이소퀴놀릴기, 7-아이소퀴놀릴기, 8-아이소퀴놀릴기, 2-퀴녹살린일기, 5-퀴녹살린일기, 6-퀴녹살린일기, 1-카바졸릴기, 2-카바졸릴기, 3-카바졸릴기, 4-카바졸릴기, 9-카바졸릴기, 1-페난트리딘일기, 2-페난트리딘일기, 3-페난트리딘일기, 4-페난트리딘일기, 6-페난트리딘일기, 7-페난트리딘일기, 8-페난트리딘일기, 9-페난트리딘일기, 10-페난트리딘일기, 1-아크리딘일기, 2-아크리딘일기, 3-아크리딘일기, 4-아크리딘일기, 9-아크리딘일기, 1,7-페난트롤린-2-일기, 1,7-페난트롤린-3-일기, 1,7-페난트롤린-4-일기, 1,7-페난트롤린-5-일기, 1,7-페난트롤린-6-일기, 1,7-페난트롤린-8-일기, 1,7-페난트롤린-9-일기, 1,7-페난트롤린-10-일기, 1,8-페난트롤린-2-일기, 1,8-페난트롤린-3-일기, 1,8-페난트롤린-4-일기, 1,8-페난트롤린-5-일기, 1,8-페난트롤린-6-일기, 1,8-페난트롤린-7-일기, 1,8-페난트롤린-9-일기, 1,8-페난트롤린-10-일기, 1,9-페난트롤린-2-일기, 1,9-페난트롤린-3-일기, 1,9-페난트롤린-4-일기, 1,9-페난트롤린-5-일기, 1,9-페난트롤린-6-일기, 1,9-페난트롤린-7-일기, 1,9-페난트롤린-8-일기, 1,9-페난트롤린-10-일기, 1,10-페난트롤린-2-일기, 1,10-페난트롤린-3-일기, 1,10-페난트롤린-4-일기, 1,10-페난트롤린-5-일기, 2,9-페난트롤린-1-일기, 2,9-페난트롤린-3-일기, 2,9-페난트롤린-4-일기, 2,9-페난트롤린-5-일기, 2,9-페난트롤린-6-일기, 2,9-페난트롤린-7-일기, 2,9-페난트롤린-8-일기, 2,9-페난트롤린-10-일기, 2,8-페난트롤린-1-일기, 2,8-페난트롤린-3-일기, 2,8-페난트롤린-4-일기, 2,8-페난트롤린-5-일기, 2,8-페난트롤린-6-일기, 2,8-페난트롤린-7-일기, 2,8-페난트롤린-9-일기, 2,8-페난트롤린-10-일기, 2,7-페난트롤린-1-일기, 2,7-페난트롤린-3-일기, 2,7-페난트롤린-4-일기, 2,7-페난트롤린-5-일기, 2,7-페난트롤린-6-일기, 2,7-페난트롤린-8-일기, 2,7-페난트롤린-9-일기, 2,7-페난트롤린-10-일기, 1-페나진일기, 2-페나진일기, 1-페노싸이아진일기, 2-페노싸이아진일기, 3-페노싸이아진일기, 4-페노싸이아진일기, 10-페노싸이아진일기, 1-페녹사진일기, 2-페녹사진일기, 3-페녹사진일기, 4-페녹사진일기, 10-페녹사진일기, 2-옥사졸릴기, 4-옥사졸릴기, 5-옥사졸릴기, 2-옥사다이아졸릴기, 5-옥사다이아졸릴기, 3-퓨라잔일기, 2-싸이엔일기, 3-싸이엔일기, 2-메틸피롤-1-일기, 2-메틸피롤-3-일기, 2-메틸피롤-4-일기, 2-메틸피롤-5-일기, 3-메틸피롤-1-일기, 3-메틸피롤-2-일기, 3-메틸피롤-4-일기, 3-메틸피롤-5-일기, 2-t-뷰틸피롤-4-일기, 3-(2-페닐프로필)피롤-1-일기, 2-메틸-1-인돌릴기, 4-메틸-1-인돌릴기, 2-메틸-3-인돌릴기, 4-메틸-3-인돌릴기, 2-t-뷰틸1-인돌릴기, 4-t-뷰틸1-인돌릴기, 2-t-뷰틸3-인돌릴기, 4-t-뷰틸3-인돌릴기 등을 들 수 있다.
R1~R10의 치환 또는 무치환의 알킬기의 예로서는, 메틸기, 에틸기, 프로필기, 아이소프로필기, n-뷰틸기, s-뷰틸기, 아이소뷰틸기, t-뷰틸기, n-펜틸기, n-헥실기, n-헵틸기, n-옥틸기, 하이드록시메틸기, 1-하이드록시에틸기, 2-하이드록시에틸기, 2-하이드록시아이소뷰틸기, 1,2-다이하이드록시에틸기, 1,3-다이하이드록시아이소프로필기, 2,3-다이하이드록시-t-뷰틸기, 1,2,3-트라이하이드록시프로필기, 클로로메틸기, 1-클로로에틸기, 2-클로로에틸기, 2-클로로아이소뷰틸기, 1,2-다이클로로에틸기, 1,3-다이클로로아이소프로필기, 2,3-다이클로로-t-뷰틸기, 1,2,3-트라이클로로프로필기, 브로모메틸기, 1-브로모에틸기, 2-브로모에틸기, 2-브로모아이소뷰틸기, 1,2-다이브로모에틸기, 1,3-다이브로모아이소프로필기, 2,3-다이브로모-t-뷰틸기, 1,2,3-트라이브로모프로필기, 아이오도메틸기, 1-아이오도에틸기, 2-아이오도에틸기, 2-아이오도아이소뷰틸기, 1,2-다이아이오도에틸기, 1,3-다이아이오도아이소프로필기, 2,3-다이아이오도-t-뷰틸기, 1,2,3-트라이아이오도프로필기, 아미노메틸기, 1-아미노에틸기, 2-아미노에틸기, 2-아미노아이소뷰틸기, 1,2-다이아미노에틸기, 1,3-다이아미노아이소프로필기, 2,3-다이아미노-t-뷰틸기, 1,2,3-트라이아미노프로필기, 사이아노메틸기, 1-사이아노에틸기, 2-사이아노에틸기, 2-사이아노아이소뷰틸기, 1,2-다이사이아노에틸기, 1,3-다이사이아노아이소프로필기, 2,3-다이사이아노-t-뷰틸기, 1,2,3-트라이사이아노프로필기, 나이트로메틸기, 1-나이트로에틸기, 2-나이트로에틸기, 2-나이트로아이소뷰틸기, 1,2-다이나이트로에틸기, 1,3-다이나이트로아이소프로필기, 2,3-다이나이트로-t-뷰틸기, 1,2,3-트라이나이트로프로필기 등을 들 수 있다.
R1~R10의 치환 또는 무치환의 사이클로알킬기의 예로서는, 예컨대, 사이클로프로필기, 사이클로뷰틸기, 사이클로펜틸기, 사이클로헥실기, 4-메틸사이클로헥실기, 1-아다만틸기, 2-아다만틸기, 1-노보닐기, 2-노보닐기 등을 들 수 있다.
R1~R10의 치환 또는 무치환의 알콕시기는, -OY로 표시되는 기이며, Y의 예로서는, 상기 R1~R10의 치환 또는 무치환의 알킬기와 마찬가지의 예를 들 수 있다.
R1~R10의 치환 또는 무치환의 아르알킬기의 예로서는, 벤질기, 1-페닐에틸기, 2-페닐에틸기, 1-페닐아이소프로필기, 2-페닐아이소프로필기, 페닐-t-뷰틸기, α-나프틸메틸기, 1-α-나프틸에틸기, 2-α-나프틸에틸기, 1-α-나프틸아이소프로필기, 2-α-나프틸아이소프로필기, β-나프틸메틸기, 1-β-나프틸에틸기, 2-β-나프틸에틸기, 1-β-나프틸아이소프로필기, 2-β-나프틸아이소프로필기, 1-피롤릴메틸기, 2-(1-피롤릴)에틸기, p-메틸벤질기, m-메틸벤질기, o-메틸벤질기, p-클로로벤질기, m-클로로벤질기, o-클로로벤질기, p-브로모벤질기, m-브로모벤질기, o-브로모벤질기, p-아이오도벤질기, m-아이오도벤질기, o-아이오도벤질기, p-하이드록시벤질기, m-하이드록시벤질기, o-하이드록시벤질기, p-아미노벤질기, m-아미노벤질기, o-아미노벤질기, p-나이트로벤질기, m-나이트로벤질기, o-나이트로벤질기, p-사이아노벤질기, m-사이아노벤질기, o-사이아노벤질기, 1-하이드록시-2-페닐아이소프로필기, 1-클로로-2-페닐아이소프로필기 등을 들 수 있다.
R1~R10의 치환 또는 무치환의 아릴옥시기 및 아릴싸이오기는, 각각 -OY' 및 -SY"으로 표시되고, Y' 및 Y"의 예로서는, 상기 R1~R10의 치환 또는 무치환의 방향족환기, 및 R1~R10의 치환 또는 무치환의 방향족 복소환기와 마찬가지의 예를 들 수 있다.
R1~R10의 치환 또는 무치환의 알콕시카보닐기는 -COOZ로 표시되고, Z의 예로서는 상기 R1~R10의 치환 또는 무치환의 알킬기와 마찬가지의 예를 들 수 있다.
R1~R10의 할로젠 원자로서는, 불소, 염소, 브롬, 요오드 등을 들 수 있다. 바람직하게는 불소 원자이다.
상기 Ar1, Ar2 및 R1~R10이 나타내는 기에 있어서의 치환기로서는, 할로젠 원자, 하이드록실기, 나이트로기, 사이아노기, 알킬기, 아릴기, 사이클로알킬기, 알콕시기, 방향족 복소환기, 아르알킬기, 아릴옥시기, 아릴싸이오기, 알콕시카보닐기, 또는 카복실기 등을 들 수 있다.
Ar1, Ar2, R9 및 R10은, 각각 복수이어도 좋고, 인접하는 것끼리 포화 또는 불포화의 환상 구조를 형성하고 있어도 좋다.
상기 G2가 하기 화학식 3a"에 나타내는 구조를 갖는 화합물이면 바람직하다.
[화학식 3a"]
식중, Ar1 및 Ar2는 각각 독립적으로, 치환 또는 무치환의 핵탄소수 10~30의 방향족환기(단, 안트라센 잔기를 제외함)이다. R1~R8은 각각 독립적으로, 수소 원자, 치환 또는 무치환의 핵탄소수 6~50의 방향족환기, 치환 또는 무치환의 핵원자수 5~50의 방향족 복소환기, 치환 또는 무치환의 탄소수 1~50의 알킬기, 치환 또는 무치환의 사이클로알킬기, 치환 또는 무치환의 탄소수 1~50의 알콕시기, 치환 또는 무치환의 탄소수 6~50의 아르알킬기, 치환 또는 무치환의 핵원자수 5~50의 아릴옥시기, 치환 또는 무치환의 핵원자수 5~50의 아릴싸이오기, 치환 또는 무치환의 탄소수 1~50의 알콕시카보닐기, 치환 또는 무치환의 실릴기, 카복실기, 할로젠 원자, 사이아노기, 나이트로기 또는 하이드록실기이다.
화학식 3a"에 있어서의 Ar1 및 Ar2의 핵탄소수 10~30의 방향족환기(단, 안트라센 잔기를 제외함)의 예로서는, 치환 또는 무치환의 α-나프틸기 및 β-나프틸기, 치환 또는 무치환의 페난트렌일기, 치환 또는 무치환의 크라이센일기, 치환 또는 무치환의 테트라센일기, 치환 또는 무치환의 피렌일기, 치환 또는 무치환의 페닐나프틸기, 치환 또는 무치환의 나프틸나프틸기, 치환 또는 무치환의 나프틸페닐기, 치환 또는 무치환의 페닐피렌일기, 치환 또는 무치환의 피렌일페닐기, 치환 또는 무치환의 나프틸나프틸나프틸기, 치환 또는 무치환의 나프틸나프틸페닐기, 치환 또는 무치환의 나프틸페닐페닐기, 치환 또는 무치환의 나프틸페닐나프틸기, 치환 또는 무치환의 페닐나프틸나프틸기, 치환 또는 무치환의 페닐나프틸페닐기, 치환 또는 무치환의 페닐페닐나프틸기 등을 들 수 있다. 이들 중에서도 치환 또는 무치환의 α-나프틸기 및 β-나프틸기, 치환 또는 무치환의 페닐나프틸기, 치환 또는 무치환의 나프틸나프틸기, 또는 치환 또는 무치환의 나프틸페닐기이면 바람직하다.
화학식 3a"에 있어서, 무치환의 핵탄소수 10~30의 방향족환기가 나프탈렌 잔기를 포함하는 방향족 잔기이면 바람직하다.
화학식 3a"에 있어서의 R1~R8의 치환 또는 무치환의 핵탄소수 6~50의 방향족환기, 치환 또는 무치환의 핵원자수 5~50의 방향족 복소환기, 치환 또는 무치환의 탄소수 1~50의 알킬기, 치환 또는 무치환의 사이클로알킬기, 치환 또는 무치환의 탄소수 1~50의 알콕시기, 치환 또는 무치환의 탄소수 6~50의 아르알킬기, 치환 또는 무치환의 핵원자수 5~50의 아릴옥시기, 치환 또는 무치환의 핵원자수 5~50의 아릴싸이오기, 치환 또는 무치환의 탄소수 1~50의 알콕시카보닐기, 및 치환 또는 무치환의 실릴기의 구체예는, 각각 상기의 것과 동일하다.
G2가 하기 화학식 3a'에 나타내는 구조를 갖는 화합물이면 바람직하다.
[화학식 3a']
식중, A1 및 A2는 각각 독립적으로, 수소 원자, 또는 치환 또는 무치환의 핵탄소수 6~50의 방향족환기이다.
R1~R10은 각각 독립적으로, 수소 원자, 치환 또는 무치환의 핵탄소수 6~50의 방향족환기, 치환 또는 무치환의 핵원자수 5~50의 방향족 복소환기, 치환 또는 무치환의 탄소수 1~50의 알킬기, 치환 또는 무치환의 사이클로알킬기, 치환 또는 무치환의 탄소수 1~50의 알콕시기, 치환 또는 무치환의 탄소수 6~50의 아르알킬기, 치환 또는 무치환의 핵원자수 5~50의 아릴옥시기, 치환 또는 무치환의 핵원자수 5~50의 아릴싸이오기, 치환 또는 무치환의 탄소수 1~50의 알콕시카보닐기, 치환 또는 무치환의 실릴기, 카복실기, 할로젠 원자, 사이아노기, 나이트로기 또는 하이드록실기이다.
Ar1, Ar2, R9 및 R10은, 각각 복수여도 좋고, 인접하는 것끼리 포화 또는 불포화의 환상 구조를 형성하고 있어도 좋다.
단, 화학식 3a'에 있어서, 중심의 안트라센의 9위치 및 10위치에, 해당 안트라센 상에 나타내는 X-Y축에 대하여 대칭형으로 되는 기가 결합하는 경우는 없다.
A1, A2 및 R1~R10의 구체예로서는 화학식 3a와 마찬가지의 것을 들 수 있다.
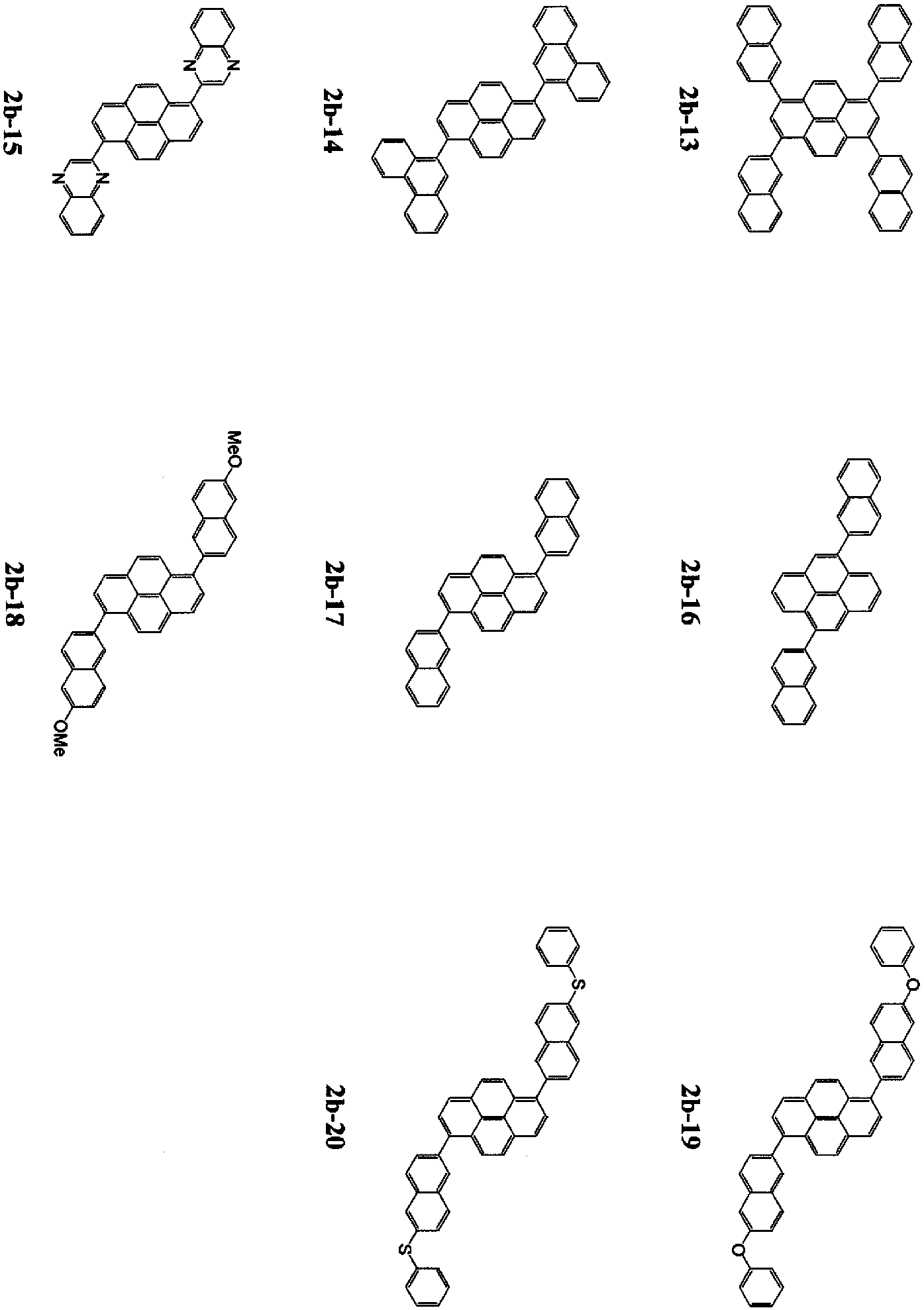
상기 화학식 1로 표시되는 G2의 축합 환 함유 화합물은, 하기 치환 또는 무치환의 피렌 구조이면 바람직하다.
[화학식 3b]
식중, Ar1b 및 Ar2b는, 각각 치환 또는 무치환의 핵탄소수 6~50의 방향족기이다.
이 방향족기의 예로서는, 페닐기, 1-나프틸기, 2-나프틸기, 1-안트릴기, 2-안트릴기, 9-안트릴기, 9-(10-페닐)안트릴기, 9-(10-나프틸-1-일)안트릴기, 9-(10-나프틸-2-일)안트릴기, 1-페난트릴기, 2-페난트릴기, 3-페난트릴기, 4-페난트릴기, 9-페난트릴기, 1-나프타센일기, 2-나프타센일기, 9-나프타센일기, 1-피렌일기, 2-피렌일기, 4-피렌일기, 2-바이페닐일기, 3-바이페닐일기, 4-바이페닐일기, p-터페닐-4-일기, p-터페닐-3-일기, p-터페닐-2-일기, m-터페닐-4-일기, m-터페닐-3-일기, m-터페닐-2-일기, o-톨릴기, m-톨릴기, p-톨릴기, p-t-뷰틸페닐기, 3-메틸-2-나프틸기, 4-메틸-1-나프틸기, 4-메틸-1-안트릴기 등을 들 수 있다.
이들 중에서도 바람직하게는, 페닐기, 1-나프틸기, 2-나프틸기, 9-(10-페닐)안트릴기, 9-(10-나프틸-1-일)안트릴기, 9-(10-나프틸-2-일)안트릴기, 9-페난트릴기, 1-피렌일기, 2-피렌일기, 4-피렌일기, 2-바이페닐일기, 3-바이페닐일기, 4-바이페닐일기, o-톨릴기, m-톨릴기, p-톨릴기, p-t-뷰틸페닐기 등을 들 수 있다.
또한, 상기 방향족기는 치환기로 더 치환되어 있어도 좋으며, 예컨대, 알킬기(메틸기, 에틸기, 프로필기, 아이소프로필기, n-뷰틸기, s-뷰틸기, 아이소뷰틸기, t-뷰틸기, n-펜틸기, n-헥실기, n-헵틸기, n-옥틸기, 하이드록시메틸기, 1-하이드록시에틸기, 2-하이드록시에틸기, 2-하이드록시아이소뷰틸기, 1,2-다이하이드록시에틸기, 1,3-다이하이드록시아이소프로필기, 2,3-다이하이드록시-t-뷰틸기, 1,2,3-트라이하이드록시프로필기, 클로로메틸기, 1-클로로에틸기, 2-클로로에틸기, 2-클로로아이소뷰틸기, 1,2-다이클로로에틸기, 1,3-다이클로로아이소프로필기, 2,3-다이클로로-t-뷰틸기, 1,2,3-트라이클로로프로필기, 브로모메틸기, 1-브로모에틸기, 2-브로모에틸기, 2-브로모아이소뷰틸기, 1,2-다이브로모에틸기, 1,3-다이브로모아이소프로필기, 2,3-다이브로모-t-뷰틸기, 1,2,3-트라이브로모프로필기, 아이오도메틸기, 1-아이오도에틸기, 2-아이오도에틸기, 2-아이오도아이소뷰틸기, 1,2-다이아이오도에틸기, 1,3-다이아이오도아이소프로필기, 2,3-다이아이오도-t-뷰틸기, 1,2,3-트라이아이오도프로필기, 아미노메틸기, 1-아미노에틸기, 2-아미노에틸기, 2-아미노아이소뷰틸기, 1,2-다이아미노에틸기, 1,3-다이아미노아이소프로필기, 2,3-다이아미노-t-뷰틸기, 1,2,3-트라이아미노프로필기, 사이아노메틸기, 1-사이아노에틸기, 2-사이아노에틸기, 2-사이아노아이소뷰틸기, 1,2-다이사이아노에틸기, 1,3-다이사이아노아이소프로필기, 2,3-다이사이아노-t-뷰틸기, 1,2,3-트라이사이아노프로필기, 나이트로메틸기, 1-나이트로에틸기, 2-나이트로에틸기, 2-나이트로아이소뷰틸기, 1,2-다이나이트로에틸기, 1,3-다이나이트로아이소프로필기, 2,3-다이나이트로-t-뷰틸기, 1,2,3-트라이나이트로프로필기, 사이클로프로필기, 사이클로뷰틸기, 사이클로펜틸기, 사이클로헥실기, 4-메틸사이클로헥실기, 1-아다만틸기, 2-아다만틸기, 1-노보닐기, 2-노보닐기 등), 탄소수 1~6의 알콕시기(에톡시기, 메톡시기, i-프로폭시기, n-프로폭시기, s-뷰톡시기, t-뷰톡시기, 펜톡시기, 헥실옥시기, 사이클로펜톡시기, 사이클로헥실옥시기 등), 핵원자수 5~40의 아릴기, 핵원자수 5~40의 아릴기로 치환된 아미노기, 핵원자수 5~40의 아릴기를 갖는 에스터기, 탄소수 1~6의 알킬기를 갖는 에스터기, 사이아노기, 나이트로기, 할로젠 원자 등을 들 수 있다.
상기 화학식 3b 중의 "L"은, 각각 치환 또는 무치환의 페닐렌기, 치환 또는 무치환의 나프탈렌일렌기, 치환 또는 무치환의 플루오렌일렌기, 또는 치환 또는 무치환의 다이벤조실롤릴렌기이며, 치환 또는 무치환의 페닐렌기, 또는 치환 또는 무치환의 플루오렌일렌기가 바람직하다.
또한, 이 치환기로서는, 상기 방향족기에서 예시한 것과 마찬가지의 것을 들 수 있다.
상기 화학식 3b 중, m은 0~2(바람직하게는 0~1)의 정수, nb는 1~4(바람직하게는 1~2)의 정수, s는 0~2(바람직하게는 0~1)의 정수, t는 0~4(바람직하게는 0~2)의 정수이다.
또한, 화학식 2b에 있어서, L 또는 Ar1b는 피렌의 1~5위치 중 어느 하나에 결합하고, L 또는 Ar2b는 피렌의 6~10위치 중 어느 하나에 결합한다.
단, nb+t가 짝수일 때, Ar1b, Ar2b, L은 하기 (1) 또는 (2)를 만족한다.
(1) Ar1b≠Ar2b(여기서 "≠"는 상이한 구조의 기인 것을 나타냄)
(2) Ar1b=Ar2b일 때
(2-1) m≠s 및/또는 nb≠t, 또는
(2-2) m=s 또한, nb=t일 때,
(2-2-1) L, 또는 피렌이, 각각 Ar1b 및 Ar2b 상의 상이한 결합 위치에 결합하고 있거나, (2-2-2) L, 또는 피렌이, Ar1b 및 Ar2b 상의 동일한 결합 위치에서 결합하고 있는 경우, L 또는 Ar1b 및 Ar2b의 피렌에 있어서의 치환 위치가 1위치와 6위치, 또는 2위치와 7위치인 경우는 없다.
상기 화학식 1로 표시되는 G2의 축합 환 함유 화합물은, 하기 치환 또는 무치환의 아민 구조이면 바람직하다.
[화학식 3c]
식중, Ar1c, Ar2c 및 Ar3c는 각각 독립적으로, 안트라센 구조, 페난트렌 구조, 또는 피렌 구조를 갖는 기를 나타낸다. R1c, R2c, 및 R3c는 각각 독립적으로, 수소 원자 또는 치환기를 나타낸다.
상기 Ar1c, Ar2c, Ar3c는, 치환 또는 무치환의 안트릴페닐기, 안트릴기, 페난트렌일기, 피렌일기가 바람직하고, 알킬 치환 또는 무치환의 안트릴페닐기, 페난트릴기, 피렌일기가 보다 바람직하며, 피렌일기, 페난트릴기가 특히 바람직하다.
상기 R1c, R2c 및 R3c인 치환기로서는, 알킬기(바람직하게는 탄소수 1~30, 보다 바람직하게는 탄소수 1~20, 특히 바람직하게는 탄소수 1~10이며, 예컨대 메틸, 에틸, 아이소프로필, t-뷰틸, n-옥틸, n-데실, n-헥사데실, 사이클로프로필, 사이클로펜틸, 사이클로헥실 등을 들 수 있음), 알켄일기(바람직하게는 탄소수 2~30, 보다 바람직하게는 탄소수 2~20, 특히 바람직하게는 탄소수 2~10이며, 예컨대 바이닐, 알릴, 2-뷰텐일, 3-펜텐일 등을 들 수 있음), 알킨일기(바람직하게는 탄소수 2~30, 보다 바람직하게는 탄소수 2~20, 특히 바람직하게는 탄소수 2~10이며, 예컨대 프로파길, 3-펜틴일 등을 들 수 있음), 아릴기(바람직하게는 탄소수 6~30, 보다 바람직하게는 탄소수 6~20, 특히 바람직하게는 탄소수 6~12이며, 예컨대 페닐, p-메틸페닐, 나프틸, 안트라닐 등을 들 수 있음), 아미노기(바람직하게는 탄소수 0~30, 보다 바람직하게는 탄소수 0~20, 특히 바람직하게는 탄소수 0~10이며, 예컨대 아미노, 메틸아미노, 다이메틸아미노, 다이에틸아미노, 다이벤질아미노, 다이페닐아미노, 다이톨릴아미노 등을 들 수 있음), 알콕시기(바람직하게는 탄소수 1~30, 보다 바람직하게는 탄소수 1~20, 특히 바람직하게는 탄소수 1~10이며, 예컨대 메톡시, 에톡시, 뷰톡시, 2-에틸헥실옥시 등을 들 수 있음),
아릴옥시기(바람직하게는 탄소수 6~30, 보다 바람직하게는 탄소수 6~20, 특히 바람직하게는 탄소수 6~12이며, 예컨대 페닐옥시, 1-나프틸옥시, 2-나프틸옥시 등을 들 수 있음), 헤테로아릴옥시기(바람직하게는 탄소수 1~30, 보다 바람직하게는 탄소수 1~20, 특히 바람직하게는 탄소수 1~12이며, 예컨대 피리딜옥시, 피라질옥시, 피리미딜옥시, 퀴놀릴옥시 등을 들 수 있음), 아실기(바람직하게는 탄소수 1~30, 보다 바람직하게는 탄소수 1~20, 특히 바람직하게는 탄소수 1~12이며, 예컨대 아세틸, 벤조일, 폼일, 피발로일 등을 들 수 있음), 알콕시카보닐기(바람직하게는 탄소수 2~30, 보다 바람직하게는 탄소수 2~20, 특히 바람직하게는 탄소수 2~12이며, 예컨대 메톡시카보닐, 에톡시카보닐 등을 들 수 있음), 아릴옥시카보닐기(바람직하게는 탄소수 7~30, 보다 바람직하게는 탄소수 7~20, 특히 바람직하게는 탄소수 7~12이며, 예컨대 페닐옥시카보닐 등을 들 수 있음), 아실옥시기(바람직하게는 탄소수 2~30, 보다 바람직하게는 탄소수 2~20, 특히 바람직하게는 탄소수 2~10이며, 예컨대 아세트옥시, 벤조일옥시 등을 들 수 있음), 아실아미노기(바람직하게는 탄소수 2~30, 보다 바람직하게는 탄소수 2~20, 특히 바람직하게는 탄소수 2~10이며, 예컨대 아세틸아미노, 벤조일아미노 등을 들 수 있음),
알콕시카보닐아미노기(바람직하게는 탄소수 2~30, 보다 바람직하게는 탄소수 2~20, 특히 바람직하게는 탄소수 2~12이며, 예컨대 메톡시카보닐아미노 등을 들 수 있음), 아릴옥시카보닐아미노기(바람직하게는 탄소수 7~30, 보다 바람직하게는 탄소수 7~20, 특히 바람직하게는 탄소수 7~12이며, 예컨대 페닐옥시카보닐아미노 등을 들 수 있음), 설폰일아미노기(바람직하게는 탄소수 1~30, 보다 바람직하게는 탄소수 1~20, 특히 바람직하게는 탄소수 1~12이며, 예컨대 메테인설폰일아미노, 벤젠설폰일아미노 등을 들 수 있음), 설팜오일기(바람직하게는 탄소수 0~30, 보다 바람직하게는 탄소수 0~20, 특히 바람직하게는 탄소수 0~12이며, 예컨대 설팜오일, 메틸설팜오일, 다이메틸설팜오일, 페닐설팜오일 등을 들 수 있음), 카밤오일기(바람직하게는 탄소수 1~30, 보다 바람직하게는 탄소수 1~20, 특히 바람직하게는 탄소수 1~12이며, 예컨대 카밤오일, 메틸카밤오일, 다이에틸카밤오일, 페닐카밤오일 등을 들 수 있음),
알킬싸이오기(바람직하게는 탄소수 1~30, 보다 바람직하게는 탄소수 1~20, 특히 바람직하게는 탄소수 1~12이며, 예컨대 메틸싸이오, 에틸싸이오 등을 들 수 있음), 아릴싸이오기(바람직하게는 탄소수 6~30, 보다 바람직하게는 탄소수 6~20, 특히 바람직하게는 탄소수 6~12이며, 예컨대 페닐싸이오 등을 들 수 있음), 헤테로아릴싸이오기(바람직하게는 탄소수 1~30, 보다 바람직하게는 탄소수 1~20, 특히 바람직하게는 탄소수 1~12이며, 예컨대 피리딜싸이오, 2-벤즈이미다졸릴싸이오, 2-벤즈옥사졸릴싸이오, 2-벤즈싸이아졸릴싸이오 등을 들 수 있음), 설폰일기(바람직하게는 탄소수 1~30, 보다 바람직하게는 탄소수 1~20, 특히 바람직하게는 탄소수 1~12이며, 예컨대 메실, 토실 등을 들 수 있음), 설핀일기(바람직하게는 탄소수 1~30, 보다 바람직하게는 탄소수 1~20, 특히 바람직하게는 탄소수 1~12이며, 예컨대 메테인설핀일, 벤젠설핀일 등을 들 수 있음), 유레이도기(바람직하게는 탄소수 1~30, 보다 바람직하게는 탄소수 1~20, 특히 바람직하게는 탄소수 1~12이며, 예컨대 유레이도, 메틸유레이도, 페닐유레이도 등을 들 수 있음),
인산아마이드기(바람직하게는 탄소수 1~30, 보다 바람직하게는 탄소수 1~20, 특히 바람직하게는 탄소수 1~12이며, 예컨대 다이에틸인산아마이드, 페닐인산아마이드 등을 들 수 있음), 하이드록시기, 머캅토기, 할로젠 원자(예컨대 불소 원자, 염소 원자, 브롬 원자, 요오드 원자), 사이아노기, 설포기, 카복실기, 나이트로기, 하이드록삼산기, 설피노기, 하이드라지노기, 이미노기, 헤테로환기(바람직하게는 탄소수 1~30, 보다 바람직하게는 탄소수 1~12이며, 헤테로 원자로서는, 예컨대 질소 원자, 산소 원자, 황 원자, 구체적으로는 예컨대 이미다졸릴, 피리딜, 퀴놀릴, 퓨릴, 싸이엔일, 피페리딜, 모폴리노, 벤즈옥사졸릴, 벤즈이미다졸릴, 벤즈싸이아졸릴 등을 들 수 있음), 실릴기(바람직하게는 탄소수 3~40, 보다 바람직하게는 탄소수 3~30, 특히 바람직하게는 탄소수 3~24이며, 예컨대 트라이메틸실릴, 트라이페닐실릴 등을 들 수 있음) 등을 들 수 있다. 이들의 치환기는 더 치환되어도 좋다.
상기 R1c, R2c 및 R3c는 알킬기 또는 아릴기가 바람직하다.
상기 화학식 1로 표시되는 G2의 축합 환 함유 화합물은, 하기 치환 또는 무치환의 벤젠 구조이면 바람직하다.
[화학식 3d]
식중, Ar11, Ar21 및 Ar31은 각각 아릴렌기를 나타내며, Ar12, Ar22 및 Ar32는 각각 독립적으로, 치환기 또는 수소 원자를 나타낸다. Ar11, Ar21, Ar31, Ar12, Ar22, 및 Ar32 중 적어도 하나는 축환 아릴 구조 또는 축환 헤테로아릴 구조이다. Ar은 아릴렌기 또는 헤테로아릴렌기를 나타낸다.
화학식 3d에 대하여 설명한다. Ar11, Ar21, Ar31은 각각 아릴렌기를 나타낸다. 아릴렌기의 탄소수는 6~30이 바람직하고, 6~20이 보다 바람직하며, 6~16이 더욱 바람직하다. 아릴렌기로서는, 예컨대, 페닐렌기, 나프틸렌기, 안트릴렌기, 페난트레닐렌기, 피레닐렌기, 페릴레닐렌기, 플루오렌일렌기, 바이페닐렌기, 터페닐렌기, 루브레닐렌기, 크리센일렌기, 트라이페닐레닐렌기, 벤조안트릴렌기, 벤조페난트레닐렌기, 다이페닐안트릴렌기 등을 들 수 있으며, 이들의 아릴렌기는 치환기를 더 갖고 있어도 좋다.
아릴렌기 상의 치환기로서는, 예컨대, 알킬기(바람직하게는 탄소수 1~30, 보다 바람직하게는 탄소수 1~20, 특히 바람직하게는 탄소수 1~10이며, 예컨대 메틸, 에틸, 아이소프로필, t-뷰틸, n-옥틸, n-데실, n-헥사데실, 사이클로프로필, 사이클로펜틸, 사이클로헥실 등을 들 수 있음), 알켄일기(바람직하게는 탄소수 2~30, 보다 바람직하게는 탄소수 2~20, 특히 바람직하게는 탄소수 2~10이며, 예컨대 바이닐, 알릴, 2-뷰텐일, 3-펜텐일 등을 들 수 있음), 알킨일기(바람직하게는 탄소수 2~30, 보다 바람직하게는 탄소수 2~20, 특히 바람직하게는 탄소수 2~10이며, 예컨대 프로파길, 3-펜틴일 등을 들 수 있음), 아릴기(바람직하게는 탄소수 6~30, 보다 바람직하게는 탄소수 6~20, 특히 바람직하게는 탄소수 6~12이며, 예컨대 페닐, p-메틸페닐, 나프틸, 안트라닐 등을 들 수 있음), 아미노기(바람직하게는 탄소수 0~30, 보다 바람직하게는 탄소수 0~20, 특히 바람직하게는 탄소수 0~10이며, 예컨대 아미노, 메틸아미노, 다이메틸아미노, 다이에틸아미노, 다이벤질아미노, 다이페닐아미노, 다이톨릴아미노 등을 들 수 있음), 알콕시기(바람직하게는 탄소수 1~30, 보다 바람직하게는 탄소수 1~20, 특히 바람직하게는 탄소수 1~10이며, 예컨대 메톡시, 에톡시, 뷰톡시, 2-에틸헥실옥시 등을 들 수 있음), 아릴옥시기(바람직하게는 탄소수 6~30, 보다 바람직하게는 탄소수 6~20, 특히 바람직하게는 탄소수 6~12이며, 예컨대 페닐옥시, 1-나프틸옥시, 2-나프틸옥시 등을 들 수 있음), 헤테로아릴옥시기(바람직하게는 탄소수 1~30, 보다 바람직하게는 탄소수 1~20, 특히 바람직하게는 탄소수 1~12이며, 예컨대 피리딜옥시, 피라질옥시, 피리미딜옥시, 퀴놀릴옥시 등을 들 수 있음),
아실기(바람직하게는 탄소수 1~30, 보다 바람직하게는 탄소수 1~20, 특히 바람직하게는 탄소수 1~12이며, 예컨대 아세틸, 벤조일, 폼일, 피발로일 등을 들 수 있음), 알콕시카보닐기(바람직하게는 탄소수 2~30, 보다 바람직하게는 탄소수 2~20, 특히 바람직하게는 탄소수 2~12이며, 예컨대 메톡시카보닐, 에톡시카보닐 등을 들 수 있음), 아릴옥시카보닐기(바람직하게는 탄소수 7~30, 보다 바람직하게는 탄소수 7~20, 특히 바람직하게는 탄소수 7~12이며, 예컨대 페닐옥시카보닐 등을 들 수 있음), 아실옥시기(바람직하게는 탄소수 2~30, 보다 바람직하게는 탄소수 2~20, 특히 바람직하게는 탄소수 2~10이며, 예컨대 아세트옥시, 벤조일옥시 등을 들 수 있음), 아실아미노기(바람직하게는 탄소수 2~30, 보다 바람직하게는 탄소수 2~20, 특히 바람직하게는 탄소수 2~10이며, 예컨대 아세틸아미노, 벤조일아미노 등을 들 수 있음), 알콕시카보닐아미노기(바람직하게는 탄소수 2~30, 보다 바람직하게는 탄소수 2~20, 특히 바람직하게는 탄소수 2~12이며, 예컨대 메톡시카보닐아미노 등을 들 수 있음), 아릴옥시카보닐아미노기(바람직하게는 탄소수 7~30, 보다 바람직하게는 탄소수 7~20, 특히 바람직하게는 탄소수 7~12이며, 예컨대 페닐옥시카보닐아미노 등을 들 수 있음), 설폰일아미노기(바람직하게는 탄소수 1~30, 보다 바람직하게는 탄소수 1~20, 특히 바람직하게는 탄소수 1~12이며, 예컨대 메테인설폰일아미노, 벤젠설폰일아미노 등을 들 수 있음), 설팜오일기(바람직하게는 탄소수 0~30, 보다 바람직하게는 탄소수 0~20, 특히 바람직하게는 탄소수 0~12이며, 예컨대 설팜오일, 메틸설팜오일, 다이메틸설팜오일, 페닐설팜오일 등을 들 수 있음), 카밤오일기(바람직하게는 탄소수 1~30, 보다 바람직하게는 탄소수 1~20, 특히 바람직하게는 탄소수 1~12이며, 예컨대 카밤오일, 메틸카밤오일, 다이에틸카밤오일, 페닐카밤오일 등을 들 수 있음), 알킬싸이오기(바람직하게는 탄소수 1~30, 보다 바람직하게는 탄소수 1~20, 특히 바람직하게는 탄소수 1~12이며, 예컨대 메틸싸이오, 에틸싸이오 등을 들 수 있음), 아릴싸이오기(바람직하게는 탄소수 6~30, 보다 바람직하게는 탄소수 6~20, 특히 바람직하게는 탄소수 6~12이며, 예컨대 페닐싸이오 등을 들 수 있음),
헤테로아릴싸이오기(바람직하게는 탄소수 1~30, 보다 바람직하게는 탄소수 1~20, 특히 바람직하게는 탄소수 1~12이며, 예컨대 피리딜싸이오, 2-벤즈이미다졸릴싸이오, 2-벤즈옥사졸릴싸이오, 2-벤즈싸이아졸릴싸이오 등을 들 수 있음), 설폰일기(바람직하게는 탄소수 1~30, 보다 바람직하게는 탄소수 1~20, 특히 바람직하게는 탄소수 1~12이며, 예컨대 메실, 토실 등을 들 수 있음), 설핀일기(바람직하게는 탄소수 1~30, 보다 바람직하게는 탄소수 1~20, 특히 바람직하게는 탄소수 1~12이며, 예컨대 메테인설핀일, 벤젠설핀일 등을 들 수 있음), 유레이도기(바람직하게는 탄소수 1~30, 보다 바람직하게는 탄소수 1~20, 특히 바람직하게는 탄소수 1~12이며, 예컨대 유레이도, 메틸유레이도, 페닐유레이도 등을 들 수 있음), 인산아마이드기(바람직하게는 탄소수 1~30, 보다 바람직하게는 탄소수 1~20, 특히 바람직하게는 탄소수 1~12이며, 예컨대 다이에틸인산아마이드, 페닐인산아마이드 등을 들 수 있음), 하이드록시기, 머캅토기, 할로젠 원자(예컨대 불소 원자, 염소 원자, 브롬원자, 요오드 원자), 사이아노기, 설포기, 카복실기, 나이트로기, 하이드록삼산기, 설피노기, 하이드라지노기, 이미노기, 헤테로환기(바람직하게는 탄소수 1~30, 보다 바람직하게는 탄소수 1~12이며, 헤테로 원자로서는, 예컨대 질소 원자, 산소 원자, 황 원자, 구체적으로는 예컨대 이미다졸릴, 피리딜, 퀴놀릴, 퓨릴, 싸이엔일, 피페리딜, 모폴리노, 벤즈옥사졸릴, 벤즈이미다졸릴, 벤즈싸이아졸릴, 카바졸릴기, 아제핀일기 등을 들 수 있음), 실릴기(바람직하게는 탄소수 3~40, 보다 바람직하게는 탄소수 3~30, 특히 바람직하게는 탄소수 3~24이며, 예컨대 트라이메틸실릴, 트라이페닐실릴 등을 들 수 있음) 등을 들 수 있다. 이들의 치환기는 더 치환되어도 좋다.
상기 Ar11, Ar21, Ar31, Ar12, Ar22, 및 Ar32 중 적어도 하나는 축환 아릴 구조 또는 축환 헤테로 아릴 구조이다. Ar11, Ar21, Ar31, Ar12, Ar22, 및 Ar32 중 적어도 하나가 축환 아릴 구조인 것이 바람직하다.
상기 축환 아릴 구조로서는, 바람직하게는, 나프탈렌 구조, 안트라센 구조, 페난트렌 구조, 피렌 구조, 페릴렌 구조, 보다 바람직하게는, 나프탈렌 구조, 안트라센 구조, 피렌 구조, 페난트렌 구조이고, 더 바람직하게는, 페난트렌 구조, 4환 이상의 아릴 구조이며, 특히 바람직하게는, 피렌 구조이다.
상기 축환 헤테로아릴 구조로서는, 바람직하게는, 퀴놀린 구조, 퀴녹살린 구조, 퀴나졸린 구조, 아크리딘 구조, 페난트리딘 구조, 프탈라진 구조, 페난트롤린 구조이며, 보다 바람직하게는, 퀴놀린 구조, 퀴녹살린 구조, 퀴나졸린 구조, 프탈라진 구조, 페난트롤린 구조이다.
상기 Ar은, 3가의 기인 아릴렌기(바람직하게는 탄소수 6~30, 보다 바람직하게는 6~20, 더 바람직하게는 탄소수 6~16, 예컨대 페닐렌기, 나프틸렌기, 안트라세닐렌기, 페난트렌기, 피레닐렌기, 트라이페닐렌기 등을 들 수 있음), 헤테로아릴렌기(헤테로 원자로서 바람직하게는 질소 원자, 황 원자, 산소 원자, 보다 바람직하게는 질소 원자, 바람직하게는 탄소수 2~30, 보다 바람직하게는 탄소수 3~20, 더 바람직하게는 탄소수 3~16, 예컨대 피리딜렌기, 피라질렌기, 싸이오페닐렌기, 퀴놀릴렌기, 퀴녹살릴렌기, 트리아질렌기 등을 들 수 있음)를 나타내며, 이들 기는 치환기를 갖고 있어도 좋다. 치환기로서는 예컨대, 상기 Ar11 상의 치환기에서 설명한 기를 들 수 있다. Ar은 각각 3가의 기인, 페닐렌기(벤젠트라이일), 나프틸렌기(나프탈렌트라이일), 안트라세닐렌기(안트라센트라이일), 피레닐렌기(피렌트라이일), 트라이페닐렌기인 것이 바람직하고, 페닐렌기인 것이 보다 바람직하며, 무치환(Ar11, Ar21, Ar31은 치환되어 있음) 페닐렌기, 알킬 치환 페닐렌기인 것이 더 바람직하다.
상기 화학식 1로 표시되는 G2의 축합 환 함유 화합물은, 하기 화학식 3'a~3'd로 표시되는 화합물로부터 선택되는 1종 이상이면 바람직하다.
화학식 3'a
[화학식 3'a]
(식 3'a 중, Ar1a 및 Ar2a는 각각 독립적으로, 치환 또는 무치환의 핵탄소수 6~20의 방향족환으로부터 유도되는 기이다. 상기 방향족환은 1 또는 2 이상의 치환기로 치환되어 있어도 좋다. 상기 치환기는 치환 또는 무치환의 핵탄소수 6~50의 아릴기, 치환 또는 무치환의 탄소수 1~50의 알킬기, 치환 또는 무치환의 탄소수 3~50의 사이클로알킬기, 치환 또는 무치환의 탄소수 1~50의 알콕시기, 치환 또는 무치환의 탄소수 6~50의 아르알킬기, 치환 또는 무치환의 핵원자수 5~50의 아릴옥시기, 치환 또는 무치환의 핵원자수 5~50의 아릴싸이오기, 치환 또는 무치환의 탄소수 1~50의 알콕시카보닐기, 치환 또는 무치환의 실릴기, 카복실기, 할로젠 원자, 사이아노기, 나이트로기 및 하이드록시기로부터 선택된다. 상기 방향족환이 2 이상의 치환기로 치환되어 있는 경우, 상기 치환기는 동일해도, 상이해도 좋으며, 인접하는 치환기끼리는 서로 결합하여 포화 또는 불포화의 환상 구조를 형성하고 있어도 좋다.
R1a~R8a는 각각 독립적으로, 수소 원자, 치환 또는 무치환의 핵탄소수 6~50의 아릴기, 치환 또는 무치환의 핵원자수 5~50의 헤테로아릴기, 치환 또는 무치환의 탄소수 1~50의 알킬기, 치환 또는 무치환의 탄소수 3~50의 사이클로알킬기, 치환 또는 무치환의 탄소수 1~50의 알콕시기, 치환 또는 무치환의 탄소수 6~50의 아르알킬기, 치환 또는 무치환의 핵원자수 5~50의 아릴옥시기, 치환 또는 무치환의 핵원자수 5~50의 아릴싸이오기, 치환 또는 무치환의 탄소수 1~50의 알콕시카보닐기, 치환 또는 무치환의 실릴기, 카복실기, 할로젠 원자, 사이아노기, 나이트로기 및 하이드록시기로부터 선택된다)
화학식 3'b
[화학식 3'b]
(화학식 3'b 중, Ar1b 및 Ar2b는 각각 독립적으로, 치환 또는 무치환의 핵탄소수 6~50의 아릴기이다.
L1 및 L2는 각각 독립적으로, 치환 또는 무치환의 페닐렌기, 치환 또는 무치환의 나프탈렌일렌기, 치환 또는 무치환의 플루오렌일렌기, 및 치환 또는 무치환의 다이벤조실롤릴렌기로부터 선택된다.
p 및 q는 0~2의 정수, r은 1~4의 정수, s는 0~4의 정수이다.
또한, L1 또는 Ar1b는 피렌의 1~5위치 중 어느 하나에 결합하고, L2 또는 Ar2b는 피렌의 6~10위치 중 어느 하나에 결합한다.)
화학식 3'c
[화학식 3'c]
(화학식 3'c 중, Ar1c, Ar2c 및 Ar3c는 각각 독립적으로, 안트라센 구조를 갖는 기, 페난트렌 구조를 갖는 기, 피렌 구조를 갖는 기 및 페릴렌 구조를 갖는 기로부터 선택된다.
R1c, R2c 및 R3c는 각각 독립적으로, 수소 원자 또는 치환기를 나타낸다)
화학식 3'd
[화학식 3'd]
(화학식 3'd 중, Ar1d, Ar2d 및 Ar3d는 각각 독립적으로, 핵탄소수 6~50의 아릴기를 나타낸다. 상기 아릴기는 1 또는 2 이상의 치환기로 치환되어 있어도 좋다.
Ar1d, Ar2d, Ar3d 및 이들의 아릴기가 갖는 치환기 중 적어도 하나는 핵탄소수 10~20의 축환 아릴 구조 또는 핵탄소수 6~20의 축환 헤테로아릴 구조를 갖는다.
Ar은 방향환 또는 복소방향환으로부터 유도되는 3가의 기를 나타낸다)
상기 화학식 3'a~3'd에 있어서의 치환기의 예는 상기 화학식 3a~3d에서 든 예와 동일하며, 바람직한 예도 마찬가지이다.
본 발명의 유기 EL 소자에 사용되는 화학식 2로 표시되는 플루오란텐 구조를 갖는 화합물의 구체예를 이하에 나타내겠지만, 이들 예시 화합물에 한정되는 것은 아니다.
본 발명의 유기 EL 소자에 사용되는 화학식 3a로 표시되는 G2인 안트라센 유도체의 구체예로서는, 일본 특허 공개 제2004-356033호 공보 [0043]~[0063]에 나타나 있는 분자 중에 안트라센 골격을 2개 갖는 것이나, 국제 공개 WO2005/061656의 27~28페이지에 나타나 있는 안트라센 골격을 1개 갖는 화합물 등 공지의 각종 안트라센 유도체를 들 수 있다. 대표적인 구체예를 하기에 나타낸다.
본 발명의 유기 EL 소자에 사용되는 화학식 3b로 표시되는 G2인 피렌 유도체의 공지된 구체예로서, 국제 공개 WO2005/115950 공보 [0020]~[0023]에 나타나 있는 비대칭 피렌 유도체가 있지만, 그 밖에 대칭 피렌 유도체도 본 발명의 유기 EL 소자 재료로서 이용할 수 있다. 대표적인 구체예를 하기에 나타낸다.
본 발명의 유기 EL 소자에 사용되는 화학식 3c로 표시되는 G2인 아민 유도체의 공지된 구체예로서는, 일본 특허 공개 제2002-324678호 공보 [0079]~[0083]에 나타나 있는 아민 유도체가 있지만, 그 이외에 하기와 같은 아민 유도체도 본 발명의 유기 EL 소자 재료로서 이용할 수 있다.
본 발명의 유기 EL 소자에 사용되는 화학식 3d로 표시되는 G2인 벤젠 유도체의 공지된 구체예로서는 일본 특허 공개 제2002-324678호 공보 [0079]~[0083]에 나타나 있지만, 본 발명의 유기 EL 소자에 사용되는 벤젠 유도체의 구체예는 하기와 같은 것이 포함된다.
본 발명의 유기 EL 소자는 발광층 중에, 플루오란텐 구조를 갖는 상기 화합물이 0.01~20중량%, 바람직하게는 0.5~20중량% 함유되어 있다.
본 발명의 유기 EL 소자는, 한 쌍의 전극 중 적어도 한 쪽의 표면에, 칼코게나이드층, 할로젠화 금속층 또는 금속 산화물층을 마련한 것이다.
본 발명의 유기 전기 발광 재료 함유 용액은, 유기 전기 발광 재료와 용매로 이루어지는 것으로, 상기 유기 전기 발광 재료가 호스트 재료와 도펀트 재료로 이루어지며, 해당 도펀트 재료는 상기 화학식 2로 표시되는 플루오란텐 구조를 갖는 화합물 중 적어도 1종이고, 해당 호스트 재료는 화학식 3a, 3a', 3b~3d, 3'a~3'd, 3a" 및 화학식 1로 표시되는 축합 환 함유 화합물로부터 선택되는 적어도 1종인 것을 특징으로 한다.
이하, 본 발명의 유기 EL 소자의 소자 구성에 대하여 설명한다.
(1) 유기 EL 소자의 구성
본 발명의 유기 EL 소자의 대표적인 소자 구성으로서는,
(1) 양극/발광층/음극
(2) 양극/정공 주입층/발광층/음극
(3) 양극/발광층/전자 주입층/음극
(4) 양극/정공 주입층/발광층/전자 주입층/음극
(5) 양극/유기 반도체층/발광층/음극
(6) 양극/유기 반도체층/전자 장벽층/발광층/음극
(7) 양극/유기 반도체층/발광층/부착 개선층/음극
(8) 양극/정공 주입층/정공 수송층/발광층/전자 주입층/음극
(9) 양극/절연층/발광층/절연층/음극
(10) 양극/무기 반도체층/절연층/발광층/절연층/음극
(11) 양극/유기 반도체층/절연층/발광층/절연층/음극
(12) 양극/절연층/정공 주입층/정공 수송층/발광층/절연층/음극
(13) 양극/절연층/정공 주입층/정공 수송층/발광층/전자 주입층/음극
등의 구조를 들 수 있다.
이들 중에서 통상 (8)의 구성이 바람직하게 사용된다.
본 발명의 화합물은 상기의 어떠한 유기층에 사용되어도 좋지만, 이들 구성 요소 중의 발광 대역에 함유되어 있는 것이 바람직하다.
(2) 투광성 기판
본 발명의 유기 EL 소자는 투광성의 기판 상에 제작한다. 여기서 말하는 투광성 기판은 유기 EL 소자를 지지하는 기판으로, 400~700㎚의 가시 영역의 광의 투과율이 50% 이상이고 평활한 기판이 바람직하다.
구체적으로는, 유리판, 폴리머판 등을 들 수 있다. 유리판으로서는, 특히 소다석회 유리, 바륨·스트론튬 함유 유리, 납 유리, 알루미노규산 유리, 붕규산 유리, 바륨붕규산 유리, 석영 등을 들 수 있다. 또한 폴리머판으로서는, 폴리카보네이트, 아크릴, 폴리에틸렌테레프탈레이트, 폴리에터설파이드, 폴리설폰 등을 들 수 있다.
(3) 양극
본 발명의 유기 EL 소자의 양극은, 정공을 정공 수송층 또는 발광층에 주입하는 역할을 담당하는 것으로, 4.5eV 이상의 일함수를 갖는 것이 효과적이다. 본 발명에 사용되는 양극 재료의 구체예로서는, 산화인듐주석합금(ITO), 산화주석(NESA), 금, 은, 백금, 구리 등을 적용할 수 있다. 또한, 양극으로서는, 전자 수송층 또는 발광층에 전자를 주입할 목적으로, 일함수가 작은 재료가 바람직하다.
양극은 이들의 전극 물질을 증착법이나 스퍼터링법 등의 방법으로 박막을 형성시키는 것에 의해 제작할 수 있다.
이와 같이 발광층으로부터의 발광을 양극으로부터 취출하는 경우, 양극의 발광에 대한 투과율이 10%보다 크게 하는 것이 바람직하다. 또한, 양극의 시트 저항은, 수백 Ω/□ 이하가 바람직하다. 양극의 막 두께는 재료에도 의존하지만, 통상 10㎚~1㎛, 바람직하게는 10~200㎚의 범위에서 선택된다.
(4) 발광층
유기 EL 소자의 발광층은 이하의 기능을 아울러 갖는 것이다. 즉,
(1) 주입 기능 ; 전계 인가시에 양극 또는 정공 주입층으로부터 정공을 주입할 수 있으며,
음극 또는 전자 주입층으로부터 전자를 주입할 수 있는 기능
(2) 수송 기능 ; 주입한 전하(전자와 정공)를 전계의 힘으로 이동시키는 기능
(3) 발광 기능 ; 전자와 정공의 재결합의 장을 제공하고, 이것을 발광으로 연결시키는 기능
이 있다. 단, 정공의 주입 용이성과 전자의 주입 용이성에 차이가 있어도 좋고, 또한, 정공과 전자의 이동도로 표시되는 수송능에 대소가 있어도 좋지만, 어느 한 쪽의 전하를 이동하는 것이 바람직하다.
이 발광층을 형성하는 방법으로서는, 예컨대 증착법, 스핀 코팅법, LB법 등의 공지된 방법을 적용할 수 있다. 발광층은, 특히 분자 퇴적막인 것이 바람직하다.
여기서 분자 퇴적막이란, 기상 상태의 재료 화합물로부터 침착되어 형성된 박막이나, 용액 상태 또는 액상 상태의 재료 화합물로부터 고체화되어 형성된 막을 말하며, 통상 이 분자 퇴적막은, LB법에 의해 형성된 박막(분자 누적막)과는 응집 구조, 고차 구조의 차이나, 그것에 기인하는 기능적인 차이에 의해 구분할 수 있다.
또한, 일본 특허 공개 제1982-51781호 공보에 개시되어 있는 바와 같이, 수지 등의 결착제와 재료 화합물을 용제에 녹여 용액으로 한 후, 이것을 스핀 코팅법 등에 의해 박막화하는 것에 의해서도 발광층을 형성할 수 있다.
본 발명에 있어서는, 본 발명의 목적이 손상되지 않는 범위에서, 소망에 따라 발광층에, 본 발명의 플루오란텐 구조를 갖는 화합물 및 축합 환 함유 화합물로 이루어지는 발광 재료 이외의 다른 공지된 발광 재료를 함유시켜도 좋으며, 또한 본 발명의 발광 재료를 포함하는 발광층에, 다른 공지된 발광 재료를 포함하는 발광층을 적층하여도 좋다.
또한, 발광층의 막 두께는, 바람직하게는 5~50㎚, 보다 바람직하게는 7~50㎚, 가장 바람직하게는 10~50㎚이다. 5㎚ 미만에서는 발광층 형성이 곤란하게 되어, 색도의 조정이 곤란하게 될 우려가 있고, 50㎚를 초과하면 구동 전압이 상승할 우려가 있다.
(5) 정공 주입·수송층(정공 수송 대역)
정공 주입·수송층은 발광층에의 정공 주입을 돕고, 발광 영역까지 수송하는 층으로서, 정공 이동도가 크고, 이온화 에너지가 통상 5.5eV 이하로 작다. 이러한 정공 주입·수송층으로서는, 보다 낮은 전계 강도로 정공을 발광층에 수송하는 재료가 바람직하며, 또 정공의 이동도가, 예컨대 104~106V/㎝의 전계 인가시에, 적어도 10-4㎠/V·초이면 바람직하다.
본 발명의 방향족 아민 유도체를 정공 수송 대역에 이용하는 경우, 본 발명의 방향족 아민 유도체 단독으로 정공 주입, 수송층을 형성하여도 좋고, 다른 재료와 혼합하여 이용하여도 좋다.
본 발명의 방향족 아민 유도체와 혼합하여 정공 주입·수송층을 형성하는 재료로서는, 상기의 바람직한 성질을 갖는 것이면 특별히 제한은 없으며, 종래, 광 도전 재료에 있어서 정공의 전하 수송 재료로서 관용되고 있는 것이나, 유기 EL 소자의 정공 주입·수송층에 사용되는 공지된 것 중에서 임의의 것을 선택하여 이용할 수 있다.
구체예로서는, 트라이아졸 유도체(미국특허 3,112,197호 명세서 등 참조), 옥사다이아졸 유도체(미국 특허 3,189,447호 명세서 등 참조), 이미다졸 유도체(일본 특허 공고 제1962-16096호 공보 등 참조), 폴리아릴알케인 유도체(미국 특허 3,615,402호 명세서, 동 제3,820,989호 명세서, 동 제3,542,544호 명세서, 일본 특허 공고 제1970-555호 공보, 동 제1976-10983호 공보, 일본 특허 공개 제1976-93224호 공보, 동 제1980-17105호 공보, 동 제1981-4148호 공보, 동 제1980-108667호 공보, 동 제1980-156953호 공보, 동 제1981-36656호 공보 등 참조), 피라졸린 유도체 및 피라졸론 유도체(미국 특허 제3,180,729호 명세서, 동 제4,278,746호 명세서, 일본 특허 공개 제1980-88064호 공보, 동 제1980-88065호 공보, 동 제1974-105537호 공보, 동 제1980-51086호 공보, 동 제1981-80051호 공보, 동 제1981-88141호 공보, 동 제1982-45545호 공보, 동 제1979-112637호 공보, 동 제1980-74546호 공보 등 참조), 페닐렌다이아민 유도체(미국 특허 제3,615,404호 명세서, 일본 특허 공고 제1976-10105호 공보, 동 제1971-3712호 공보, 동 제1972-25336호 공보, 일본 특허 공개 제1979-53435호 공보, 동 제1979-110536호 공보, 동 제1979-119925호 공보 등 참조), 아릴아민 유도체(미국 특허 제3,567,450호 명세서, 동 제3,180,703호 명세서, 동 제3,240,597호 명세서, 동 제3,658,520호 명세서, 동 제4,232,103호 명세서, 동 제4,175,961호 명세서, 동 제4,012,376호 명세서, 일본 특허 공고 제1974-35702호 공보, 동 제1964-27577호 공보, 일본 특허 공개 제1980-144250호 공보, 동 제1981-119132호 공보, 동 제1981-22437호 공보, 서독 특허 제1,110,518호 명세서 등 참조), 아미노치환 칼콘 유도체(미국 특허 제3,526,501호 명세서 등 참조), 옥사졸 유도체(미국 특허 제3,257,203호 명세서 등에 개시된 것), 스타이릴안트라센 유도체(일본 특허 공개 제1981-46234호 공보 등 참조), 플루오레논 유도체(일본 특허 공개 제1979-110837호 공보 등 참조), 하이드라존 유도체(미국 특허 제3,717,462호 명세서, 일본 특허 공개 제1979-59143호 공보, 동 제1980-52063호 공보, 동 제1980-52064호 공보, 동 제1980-46760호 공보, 동 제1980-85495호 공보, 동 제1982-11350호 공보, 동 제1982-148749호 공보, 일본 특허 공개 제1990-311591호 공보 등 참조), 스틸벤 유도체(일본 특허 공개 제1986-210363호 공보, 동 제1986-228451호 공보, 동 제1986-14642호 공보, 동 제1986-72255호 공보, 동 제1987-47646호 공보, 동 제1987-36674호 공보, 동 제1987-10652호 공보, 동 제1987-30255호 공보, 동 제1985-93455호 공보, 동 제1985-94462호 공보, 동 제1985-174749호 공보, 동 제1985-175052호 공보 등 참조), 실라잔 유도체(미국 특허 제4,950,950호 명세서), 폴리실레인계(일본 특허 공개 제1990-204996호 공보), 아닐린계 공중합체(일본 특허 공개 제1990-282263호 공보), 일본 특허 공개 제1989-211399호 공보에 개시되어 있는 도전성 고분자 올리고머(특히, 싸이오펜올리고머) 등을 들 수 있다.
정공 주입·수송층의 재료로서는 상기의 것을 사용할 수 있지만, 포르피린 화합물(일본 특허 공개 제1988-295695호 공보 등에 개시된 것), 방향족 제3급 아민 화합물 및 스타이릴아민 화합물(미국 특허 제4,127,412호 명세서, 일본 특허 공개 제1978-27033호 공보, 동 제1979-58445호 공보, 동 제1979-149634호 공보, 동 제1979-64299호 공보, 동 제1980-79450호 공보, 동 제1980-144250호 공보, 동 제1981-119132호 공보, 동 제1986-295558호 공보, 동 제1986-98353호 공보, 동 제1988-295695호 공보 등 참조), 특히 방향족 제3급 아민 화합물을 이용하는 것이 바람직하다.
또한, 미국 특허 제5,061,569호에 기재되어 있는 2개의 축합 방향족환을 분자 내에 갖는, 예컨대, 4,4'-비스(N-(1-나프틸)-N-페닐아미노)바이페닐(이하, "NPD"라고 약기함), 또한 일본 특허 공개 제1992-308688호 공보에 기재되어 있는 트라이페닐아민 유닛이 3개의 스타버스트형으로 연결된 4,4',4"-트리스(N-(3-메틸페닐)-N-페닐아미노)트라이페닐아민(이하, "MTDATA"라고 약기함) 등을 들 수 있다.
또한, 발광층의 재료로서 나타낸 전술한 방향족 다이메틸리덴계 화합물 외에, p형 Si, p형 SiC 등의 무기 화합물도 정공 주입층의 재료로서 사용할 수 있다.
정공 주입·수송층은 상술한 화합물을, 예컨대, 진공 증착법, 스핀 코팅법, 캐스팅법, LB법 등의 공지된 방법에 의해 박막화함으로써 형성할 수 있다. 정공 주입·수송층으로서의 막 두께는 특별히 제한은 없지만, 통상은 5㎚~5㎛이다. 이 정공 주입·수송층은, 정공 수송 대역에 본 발명의 화합물을 함유하고 있으면, 전술한 재료의 1종 또는 2종 이상으로 이루어지는 1 층으로 구성되어도 좋고, 또는 상기 정공 주입·수송층과는 다른 종류의 화합물로 이루어지는 정공 주입·수송층을 적층한 것이어도 좋다.
또한, 발광층에의 정공 주입 또는 전자 주입을 돕는 층으로서, 10-10S/㎝ 이상의 도전율을 갖는 것이 적합하다. 이러한 유기 반도체층의 재료로서는, 싸이오펜 함유 올리고머나 일본 특허 공개 제1996-193191호 공보에 개시되어 있는 아릴아민 함유 올리고머 등의 도전성 올리고머, 아릴아민 함유 덴드리머 등의 도전성 덴드리머 등을 이용할 수 있다.
(6) 전자 주입층
전자 주입층은, 발광층에의 전자의 주입을 돕는 층으로서, 전자 이동도가 크고, 또한 부착 개선층은 이 전자 주입층 중에서 특히 음극과의 부착이 좋은 재료로 이루어지는 층이다. 전자 주입층에 사용되는 재료로서는, 8-하이드록시퀴놀린 또는 그 유도체의 금속착체가 바람직하다.
상기 8-하이드록시퀴놀린 또는 그 유도체의 금속착체의 구체예로서는, 옥신(일반적으로 8-퀴놀린올 또는 8-하이드록시퀴놀린)의 킬레이트를 포함하는 금속 킬레이트옥시노이드 화합물을 들 수 있다.
예컨대, 발광 재료의 항목에서 기재한 Alq를 전자 주입층으로서 이용할 수 있다.
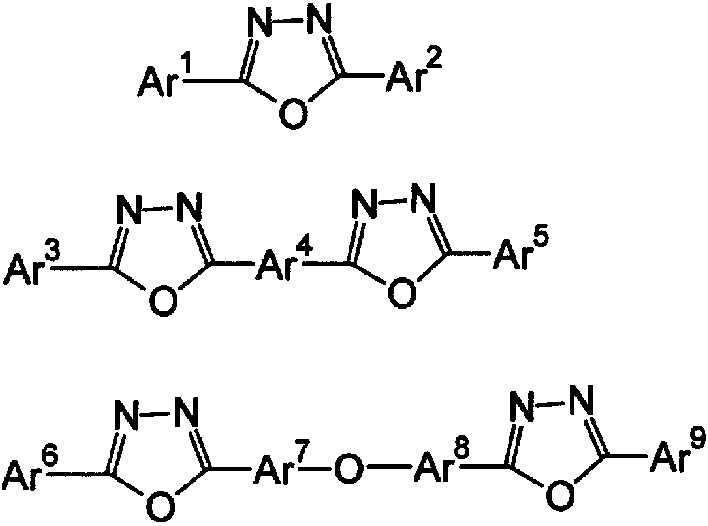
한편, 옥사다이아졸 유도체로서는, 이하의 화학식으로 표시되는 전자 전달 화합물을 들 수 있다.
(식중, Ar1, Ar2, Ar3, Ar5, Ar6, Ar9는 각각 치환 또는 무치환의 아릴기를 나타내며, 각각 서로 동일해도, 상이해도 좋다. 또한 Ar4, Ar7, Ar8은 치환 또는 무치환의 아릴렌기를 나타내며, 각각 동일해도, 상이해도 좋다)
여기서 아릴기로서는 페닐기, 바이페닐기, 안트라닐기, 페릴레닐기, 피렌일기를 들 수 있다. 또한, 아릴렌기로서는 페닐렌기, 나프틸렌기, 바이페닐렌기, 안트라닐렌기, 페리레닐렌기, 피레닐렌기 등을 들 수 있다. 또한, 치환기로서는 탄소수 1~10의 알킬기, 탄소수 1~10의 알콕시기 또는 사이아노기 등을 들 수 있다. 이 전자 전달 화합물은 박막 형성성인 것이 바람직하다.
상기 전자 전달성 화합물의 구체예로서는 하기의 것을 들 수 있다.
본 발명의 유기 EL 소자의 바람직한 형태로, 전자를 수송하는 영역 또는 음극과 유기층의 계면 영역에, 환원성 도펀트를 함유하는 소자가 있다. 여기서, 환원성 도펀트란, 전자 수송성 화합물을 환원할 수 있는 물질로 정의된다. 따라서, 일정한 환원성을 갖는 것이면 다양한 것을 사용할 수 있으며, 예컨대, 알칼리 금속, 알칼리 토류 금속, 희토류 금속, 알칼리 금속의 산화물, 알칼리 금속의 할로젠화물, 알칼리 토류 금속의 산화물, 알칼리 토류 금속의 할로젠화물, 희토류 금속의 산화물 또는 희토류 금속의 할로젠화물, 알칼리 금속의 유기착체, 알칼리 토류 금속의 유기착체, 희토류 금속의 유기착체로 이루어지는 군으로부터 선택되는 적어도 하나의 물질을 적합하게 사용할 수 있다.
또한, 보다 구체적으로, 바람직한 환원성 도펀트로서는, Na(일함수:2.36eV), K(일함수:2.28eV), Rb(일함수:2.16eV) 및 Cs(일함수:1.95eV)로 이루어지는 군으로부터 선택되는 적어도 하나의 알칼리 금속이나, Ca(일함수:2.9eV), Sr(일함수:2.0~2.5eV), 및 Ba(일함수:2.52eV)로 이루어지는 군으로부터 선택되는 적어도 하나의 알칼리 토류 금속을 들 수 있는 일함수가 2.9eV 이하인 것이 특히 바람직하다. 이들 중, 보다 바람직한 환원성 도펀트는, K, Rb 및 Cs로 이루어지는 군으로부터 선택되는 적어도 하나의 알칼리 금속이고, 더 바람직하게는, Rb 또는 Cs이며, 가장 바람직한 것은 Cs이다. 이들의 알칼리 금속은, 특히 환원 능력이 높고, 전자 주입역에의 비교적 소량의 첨가에 의해, 유기 EL 소자에 있어서의 발광 휘도의 향상이나 장수명화가 도모된다. 또한, 일함수가 2.9eV 이하인 환원성 도펀트로서, 이들 2종 이상의 알칼리 금속의 조합도 바람직하며, 특히 Cs를 포함한 조합, 예컨대, Cs와 Na, Cs와 K, Cs와 Rb 혹은 Cs와 Na와 K의 조합인 것이 바람직하다. Cs를 조합하여 포함하는 것에 의해, 환원 능력을 효율적으로 발휘할 수 있으며, 전자 주입역에의 첨가에 의해, 유기 EL 소자에 있어서의 발광 휘도의 향상이나 장수명화를 도모할 수 있다.
본 발명에 있어서는 음극과 유기층 사이에 절연체나 반도체로 구성되는 전자 주입층을 더 설치하여도 좋다. 이 때, 전류의 누출을 유효하게 방지하여, 전자 주입성을 향상시킬 수 있다. 이러한 절연체로서는, 알칼리 금속 칼코게나이드, 알칼리 토류 금속 칼코게나이드, 알칼리 금속의 할로젠화물 및 알칼리 토류 금속의 할로젠화물로 이루어지는 군으로부터 선택되는 적어도 하나의 금속 화합물을 사용하는 것이 바람직하다. 전자 주입층이 이들의 알칼리 금속 칼코게나이드 등으로 구성되어 있으면, 전자 주입성을 더욱 향상시킬 수 있다는 점에서 바람직하다. 구체적으로, 바람직한 알칼리 금속 칼코게나이드로서는, 예컨대, Li2O, K2O, Na2S, Na2Se 및 Na2O를 들 수 있으며, 바람직한 알칼리 토류 금속 칼코게나이드로서는, 예컨대, CaO, BaO, SrO, BeO, BaS, 및 CaSe를 들 수 있다. 또한, 바람직한 알칼리 금속의 할로젠화물로서는, 예컨대, LiF, NaF, KF, LiCl, KCl및 NaCl 등을 들 수 있다. 또한, 바람직한 알칼리 토류 금속의 할로젠화물로서는, 예컨대, CaF2, BaF2, SrF2, MgF2 및 BeF2와 같은 불화물이나, 불화물 이외의 할로젠화물을 들 수 있다.
또한, 전자 수송층을 구성하는 반도체로서는, Ba, Ca, Sr, Yb, Al, Ga, In, Li, Na, Cd, Mg, Si, Ta, Sb 및 Zn 중 적어도 하나의 원소를 포함하는 산화물, 질화물 또는 산화 질화물 등의 1종 단독 또는 2종 이상의 조합을 들 수 있다. 또한, 전자 수송층을 구성하는 무기 화합물이, 미결정 또는 비정질의 절연성 박막인 것이 바람직하다. 전자 수송층이 이들의 절연성 박막으로 구성되어 있으면, 보다 균질한 박막이 형성되기 때문에, 다크 스폿 등의 화소 결함을 감소시킬 수 있다. 또, 이러한 무기 화합물로서는, 전술한 알칼리 금속 칼코게나이드, 알칼리 토류 금속 칼코게나이드, 알칼리 금속의 할로젠화물 및 알칼리 토류 금속의 할로젠화물 등을 들 수 있다.
(7) 음극
음극으로서는, 전자 주입·수송층 또는 발광층에 전자를 주입하기 위하여, 일함수가 작은(4eV 이하) 금속, 합금, 전기 전도성 화합물 및 이들의 혼합물을 전극 물질로 하는 것이 이용된다. 이러한 전극 물질의 구체예로서는, 나트륨, 나트륨·칼륨 합금, 마그네슘, 리튬, 마그네슘·은 합금, 알루미늄/산화알루미늄, 알루미늄·리튬 합금, 인듐, 희토류 금속 등을 들 수 있다.
이 음극은 이들의 전극 물질을 증착이나 스퍼터링 등의 방법에 의해 박막을 형성시킴으로써 제작할 수 있다.
여기서 발광층으로부터의 발광을 음극으로부터 취출하는 경우, 음극의 발광에 대한 투과율은 10%보다 크게 하는 것이 바람직하다.
또한, 음극으로서의 시트 저항은 수백Ω/□ 이하가 바람직하며, 막 두께는 통상 10㎚~1㎛, 바람직하게는 50~200㎚이다.
(8) 절연층
유기 EL 소자는 초박막에 전계를 인가하기 때문에, 누출이나 단락에 의한 화소 결함이 발생하기 쉽다. 이것을 방지하기 위하여, 한 쌍의 전극 사이에 절연성의 박막층을 삽입하는 것이 바람직하다.
절연층에 사용되는 재료로서는 예컨대 산화알루미늄, 불화리튬, 산화리튬, 불화세슘, 산화세슘, 산화마그네슘, 불화마그네슘, 산화칼슘, 불화칼슘, 질화알루미늄, 산화타이타늄, 산화규소, 산화게르마늄, 질화규소, 질화붕소, 산화몰리브덴, 산화루테늄, 산화바나듐 등을 들 수 있다.
이들의 혼합물이나 적층물을 이용해도 좋다.
(9) 유기 EL 소자의 제조 방법
이상 예시한 재료 및 형성 방법에 의해 양극, 발광층, 필요에 따라 정공 주입층, 및 필요에 따라 전자 주입층을 형성하고, 추가로 음극을 형성하는 것에 의해 유기 EL 소자를 제작할 수 있다. 또, 음극으로부터 양극으로, 상기와 반대의 순서로 유기 EL 소자를 제작하는 것도 가능하다.
이하, 투광성 기판 상에 양극/정공 주입층/발광층/전자 주입층/음극이 순차적으로 설치된 구성의 유기 EL 소자의 제작예를 기재한다.
우선, 적당한 투광성 기판 상에 양극 재료로 이루어지는 박막을 1㎛ 이하, 바람직하게는 10~200㎚ 범위의 막 두께로 되도록 증착이나 스퍼터링 등의 방법에 의해 형성하여 양극을 제작한다. 다음에, 이 양극 상에 정공 주입층을 마련한다. 정공 주입층의 형성은, 전술한 바와 같이 진공 증착법, 스핀 코팅법, 캐스팅법, LB법 등의 방법에 의해 행하는 것이 가능하지만, 균질한 막의 수득이 용이하고, 또한 핀홀이 잘 발생하지 않는다는 등의 점에서 진공 증착법에 의해 형성하는 것이 바람직하다. 진공 증착법에 의해 정공 주입층을 형성하는 경우, 그 증착 조건은 사용하는 화합물(정공 주입층의 재료), 목적으로 하는 정공 주입층의 결정 구조나 재결합 구조 등에 따라 다르지만, 일반적으로 증착원 온도 50~450℃, 진공도 10-7~10-3Torr, 증착 속도 0.01~50㎚/초, 기판 온도 -50~300℃, 막 두께 5㎚~5㎛의 범위에서 적절히 선택하는 것이 바람직하다.
다음에, 정공 주입층 상에 발광층을 마련하는 발광층의 형성도, 원하는 유기 발광 재료를 이용하여 진공 증착법, 스퍼터링, 스핀 코팅법, 캐스팅법 등의 방법에 의해 유기 발광 재료를 박막화함으로써 형성할 수 있지만, 균질한 막의 수득이 용이하고, 또한 핀홀이 잘 발생하지 않는다는 등의 점에서 진공 증착법에 의해 형성하는 것이 바람직하다. 진공 증착법에 의해 발광층을 형성하는 경우, 그 증착 조건은 사용하는 화합물에 따라 다르지만, 일반적으로 정공 주입층과 동일한 조건 범위 중에서 선택할 수 있다.
본 발명의 EL 소자의 발광층은, 상기 발광 재료를 증착뿐만 아니라, 습식으로도 성막할 수 있다. 이 발광층의 각 유기층의 형성은, 진공 증착, 스퍼터링, 플라즈마, 이온 플레이팅 등의 건식 성막법이나 스핀 코팅, 딥핑, 캐스팅, 바코팅, 롤코팅, 플로우코팅, 잉크젯 등의 도포법을 적용할 수 있다.
습식 성막법의 경우, 각 층을 형성하는 재료를 적절한 용매에 용해 또는 분산시켜서 발광성 유기 용액을 조제하여 박막을 형성하는데, 그 용매는 어떠한 것이라도 좋다. 용매로서는, 예컨대, 다이클로로메테인, 다이클로로에테인, 클로로폼, 사염화탄소, 테트라클로로에테인, 트라이클로로에테인, 클로로벤젠, 다이클로로벤젠, 클로로톨루엔, 트라이플루오로톨루엔 등의 할로젠계 탄화 수소계 용매나, 다이뷰틸에터, 테트라하이드로퓨란, 테트라하이드로피란, 다이옥세인, 아니솔, 다이메톡시에테인 등의 에터계 용매, 메탄올이나 에탄올, 프로판올, 아이소프로판올, 뷰탄올, 펜탄올, 헥산올, 사이클로헥산올, 메틸셀로솔브, 에틸셀로솔브, 에틸렌글라이콜 등의 알코올계 용매, 아세톤, 메틸에틸케톤, 다이에틸케톤, 2-헥산온, 메틸아이소뷰틸케톤, 2-헵탄온, 4-헵탄온, 다이아이소뷰틸케톤, 아세토닐아세톤, 아이소포론, 사이클로헥산온, 메틸헥산온, 아세토페논 등의 케톤계 용매, 벤젠, 톨루엔, 자일렌, 에틸벤젠, 헥세인, 사이클로헥세인, 옥테인, 데칸, 테트라린 등의 탄화수소계 용매, 아세트산에틸, 아세트산뷰틸, 아세트산아밀 등의 에스터계 용매, 다이메틸카보네이트, 메틸에틸카보네이트, 다이에틸카보네이트 등의 쇄상 탄산에스터계 용매, 에틸렌카보네이트, 프로필렌카보네이트 등의 환상 탄산에스터계 용매 등을 들 수 있다. 그 중에서도, 톨루엔, 다이옥세인 등의 탄화수소계 용매나 에터계 용매가 바람직하다. 또한, 이들의 용매는 1종을 단독으로 사용해도 좋고 2종 이상을 혼합하여 사용해도 좋다. 또, 사용할 수 있는 용매는 이들에 한정되는 것은 아니다.
다음에, 이 발광층 상에 전자 주입층을 마련한다. 정공 주입층, 발광층과 마찬가지로 균질한 막을 얻을 필요에서 진공 증착법에 의해 형성하는 것이 바람직하다. 증착 조건은 정공 주입층, 발광층과 마찬가지의 조건 범위에서 선택할 수 있다.
본 발명의 화합물은, 발광 대역이나 정공 수송 대역 중 어느 하나의 층에 함유시킬 것인가에 따라 다르지만, 진공 증착법을 이용하는 경우에는 다른 재료와의 공증착을 할 수 있다. 또한, 스핀 코팅법을 이용하는 경우에는, 다른 재료와 혼합함으로써 함유시킬 수 있다.
마지막으로 음극을 적층하여 유기 EL 소자를 얻을 수 있다.
음극은 금속으로 구성되는 것으로서, 증착법, 스퍼터링을 이용할 수 있다. 그러나, 하지의 유기물층을 제막시의 손상으로부터 지키기 위해서는 진공 증착법이 바람직하다.
지금까지 기재해 온 유기 EL 소자의 제작은 1회의 진공 흡인으로 일관하여 양극에서 음극까지 제작하는 것이 바람직하다.
본 발명의 유기 EL 소자의 각 층의 형성 방법은 특별히 한정되지 않는다. 종래 공지된 진공 증착법, 스핀 코팅법 등에 의한 형성 방법을 이용할 수 있다. 본 발명의 유기 EL 소자에 이용하는 유기 박막층은, 진공 증착법, 분자선 증착법(MBE법) 또는 용매에 녹인 용액의 딥핑법, 스핀 코팅법, 캐스팅법, 바코팅법, 롤코팅법 등의 도포법에 의한 공지된 방법으로 형성할 수 있다.
또한, 어떠한 유기 박막층에 있어서도, 성막성 향상, 막의 핀홀 방지 등을 위하여 적절한 수지나 첨가제를 사용해도 좋다. 사용이 가능한 수지로서는, 폴리스타이렌, 폴리카보네이트, 폴리알릴레이트, 폴리에스터, 폴리아마이드, 폴리우레탄, 폴리설폰, 폴리메틸메타크릴레이트, 폴리메틸아크릴레이트, 셀룰로스 등의 절연성 수지 및 그들의 공중합체, 폴리-N-바이닐카바졸, 폴리실레인 등의 광 도전성 수지, 폴리아닐린, 폴리싸이오펜, 폴리피롤 등의 도전성 수지 등을 들 수 있다. 또한, 첨가제로서는, 산화 방지제, 자외선 흡수제, 가소제 등을 들 수 있다.
본 발명의 유기 EL 소자의 각 유기층의 막 두께는 특별히 한정되는 것은 아니지만, 적절한 막 두께로 설정할 필요가 있다. 일반적으로 막 두께가 지나치게 얇으면 핀홀 등이 발생하여, 전계를 인가하더라도 충분한 발광 휘도를 얻을 수 없게 될 우려가 있고, 반대로 지나치게 두꺼우면 일정한 광 출력을 얻기 위하여 높은 인가 전압이 필요하게 되어 효율이 나빠지기 때문에, 통상, 막 두께는 5㎚~10㎛의 범위가 적합하지만, 10㎚~0.2㎛의 범위가 더욱 바람직하다.
본 발명에 의해 수득된 유기 EL 소자의, 온도, 습도, 분위기 등에 대한 안정성의 향상을 위해, 소자의 표면에 보호층을 마련하거나, 실리콘 오일, 수지 등에 의해 소자 전체를 보호하는 것도 가능하다.
또, 유기 EL 소자에 직류 전압을 인가하는 경우, 양극을 +, 음극을 -의 극성으로 하고, 5~40V의 전압을 인가하면 발광을 관측할 수 있다. 또한, 반대의 극성으로 전압을 인가하더라도 전류는 흐르지 않고, 발광은 전혀 발생하지 않는다. 또, 교류 전압을 인가한 경우에는 양극이 +, 음극이 -의 극성이 되었을 때에만 균일한 발광이 관측된다. 인가하는 교류의 파형은 임의적이어도 좋다.
이하, 본 발명을 실시예에 기초하여 상세히 설명하지만, 본 발명은 그 요지를 벗어나지 않는 한, 이하의 실시예에 한정되지 않는다.
(실시예 1)
(1) 유기 EL 소자의 제조
25㎜×75㎜×1.1㎜ 두께의 유리 기판 상에 막 두께 120㎚의 인듐주석산화물로 이루어지는 투명 전극을 마련하였다. 이 유리 기판을 아이소프로필알코올로 초음파 세정하고, 자외선 및 오존을 조사하여 세정하였다.
이어서, 투명 전극 부착 유리 기판을, 진공 증착 장치의 증착조 내의 기판 홀더에 장착하는 동시에, 진공조 내의 진공도를 1×10-3㎩로 감압하였다.
우선, 투명 전극이 형성되어 있는 측의 면 상에 상기 투명 전극을 덮도록 하여 N', N"-비스[4-(다이페닐아미노)페닐]-N', N"-다이페닐바이페닐-4,4'-다이아민의 층을 증착 속도 2㎚/sec, 막 두께 60㎚로 성막하였다. 이 막은 정공 주입층으로서 기능한다.
다음에, 이 정공 주입층 위에 N, N-비스[4'-{N-(나프틸-1-일)-N-페닐}아미노바이페닐-4-일]-N-페닐아민의 층을 증착 속도 2㎚/sec, 막 두께 20㎚로 성막하였다. 이 막은 정공 수송층으로서 기능한다.
정공 수송층 위에 화합물(2a'-55)와 화합물(1-3)을 각각 증착 속도 2㎚/sec 및 0.2㎚/sec, 막 두께 40㎚로, 중량비가 (2a'-55):(1-3)=40:2로 되도록 동시 증착하였다. 이 막은 발광층으로서 기능한다.
그 위에, 트리스(8-하이드록시퀴놀리노)알루미늄을 증착 속도 2㎚/sec, 막 두께 20㎚로 증착하여, 전자 수송층을 성막하였다.
또한, 불화리튬을 증착 속도 0.1㎚/sec, 막 두께 1㎚로 전자 주입층을 성막하였다.
마지막으로, 알루미늄을 증착 속도 2㎚/sec, 막 두께 200㎚로 음극층을 형성하였다.
(2) 유기 EL 소자의 평가
다음에, 이 소자에 통전 시험을 실시한 바, 전압 6.5V에서 발광 휘도가 750cd/㎡이고, 발광색은 청색인 것을 확인하였다. 또한, 초기 발광 휘도를 100cd/㎡로 하여 정전류 구동시킨 바, 반감 수명은 10,000시간 이상이며, 충분히 실용 영역인 것을 확인하였다. 수득된 결과를 표 1에 나타낸다.
(실시예 2~5)
실시예 2~5에 있어서는, 발광층에, 실시예 1의 화합물(2a'-55)와 화합물(1-3) 대신에, 각각 실시예 2에서는 화합물(2a'-59)와 화합물(1-3)을 중량비 40:2로, 실시예 3에서는 화합물(2a'-59)와 화합물(1-7)을 중량비 40:2로, 실시예 4에서는 화합물(2a'-101)과 화합물(1-79)를 중량비 40:2로, 또한 실시예 5에서는 화합물(2a-7)과 화합물(1-27)을 중량비 40:2로 이용한 것 외에는, 실시예 1과 마찬가지로 유기 EL 소자를 제작하였다.
그 결과, 표 1에 나타낸 바와 같이 모두 청색 발광이 관찰되고, 발광 휘도는 670~760cd/㎡이고, 반감 수명은 모두 10,000 시간 이상이며, 충분히 실용 영역이 었다.
(실시예 6~10)
실시예 6~10에 있어서는, 발광층에, 실시예 1의 화합물(2a'-55)와 화합물(1-3) 대신에, 각각 실시예 6에서는 화합물(2a'-57)과 화합물(1-36)을 중량비 40:2로, 실시예 7에서는 화합물(2b-9)와 화합물(1-5)를 중량비 40:2로, 실시예 8에서는 화합물(2b-26)과 화합물(1-97)을 중량비 40:2로, 실시예 9에서는 화합물(2c-1)과 화합물(1-8)을 중량비 40:2로, 실시예 10에서는 화합물(2d-1)과 화합물(1-3)을 중량비 40:2로 이용한 것 외에는, 실시예 1과 마찬가지로 유기 EL 소자를 제작하였다.
그 결과, 표 2에 나타낸 바와 같이 모두 청색 발광이 관찰되고, 발광 휘도는 675~710cd/㎡이고, 반감 수명은 모두 10,000 시간 이상이며, 충분히 실용 영역이었다.
(비교예 1~3)
비교예 1~3에 있어서는, 발광층에, 실시예 1의 화합물(2a'-55)와 화합물(1-3) 대신에, 각각, 비교예 1에서는 화합물(2a'-59)만을 막 두께 40㎚로, 비교예 2에서는 하기 화합물(A)와 화합물(1-3)을 막 두께 40㎚(A:1-3=40:2)로, 또한 비교예 3에서는 화합물(2a'-59)와 하기 화합물(B)를 막 두께 40㎚(중량비 (2a'-59):B=40:2)로 이용한 것 외에는, 실시예 1과 마찬가지로 유기 EL 소자를 제작하였다.
여기서 화합물(A)는 비스(2-메틸-8-퀴놀리노라토)알루미늄-μ-옥소-비스(2-메틸-8-퀴놀리노라토)알루미늄이며, 화합물(B)는 2,5,8,11-테트라-t-뷰틸페릴렌이다.
그 결과, 표 3에 나타낸 바와 같이 모두 청색 발광이 관찰되었지만, 발광 휘도는 100~300cd/㎡이고, 반감 수명은 3000~5000 시간으로 짧았다.
(실시예 11)
(1) 유기 EL 소자의 제조
25㎜×75㎜×1.1㎜ 두께의 유리 기판 상에, 막 두께 120㎚의 인듐주석산화물로 이루어지는 투명 전극을 마련하였다. 이 유리 기판을 아이소프로필알코올로 초음파 세정하고, 자외선 및 오존을 조사하여 세정하였다.
이어서, 투명 전극 부착 유리 기판을, 진공 증착 장치의 증착조 내의 기판 홀더에 장착하는 동시에, 진공조 내의 진공도를 1×10-3㎩로 감압하였다.
우선, 투명 전극이 형성되어 있는 측의 면 상에 상기 투명 전극을 덮도록 하여 N', N"-비스[4-(다이페닐아미노)페닐]-N', N"-다이페닐바이페닐-4,4'-다이아민의 층을 증착 속도 2㎚/sec, 막 두께 60㎚로 성막하였다. 이 막은 정공 주입층으로서 기능한다.
다음에, 이 정공 주입층 위에 N, N, N', N'-테트라(4-바이페닐릴)벤지딘의 층을 증착 속도 2㎚/sec, 막 두께 20㎚로 성막하였다. 이 막은 정공 수송층으로서 기능한다.
정공 수송층 위에, 상기 화합물(2a'-55)[발광 재료 1]와 상기 화합물(2-21)[발광 재료 2]을 각각 증착 속도 2㎚/sec 및 0.2㎚/sec, 막 두께 40㎚로, 중량비가 (2a'-55):(2-21)=40:2가 되도록 동시 증착하였다. 이 막은 발광층으로서 기능한다.
그 위에, 트리스(8-하이드록시퀴놀리노)알루미늄을 증착 속도 2㎚/sec, 막 두께 20㎚로 증착하여, 전자 수송층을 성막하였다.
또한, 불화리튬을 증착 속도 0.1㎚/sec, 막 두께 1㎚로 전자 주입층을 성막하였다.
마지막으로, 알루미늄을 증착 속도 2㎚/sec, 막 두께 200㎚로 음극층을 형성하고, 유기 EL 소자를 제조하였다.
(2) 유기 EL 소자의 평가
다음에, 이 소자에 통전 시험을 실시한 바, 전압 6.3V에서 발광 휘도가 445cd/㎡이고, 발광 피크 파장(ELλmax) 및 색도를 측정한 바 발광색은 청색인 것을 확인하였다. 또한, 초기 발광 휘도를 100cd/㎡으로 하여 정전류 구동시킨 바, 반감 수명은 10,000 시간 이상이며, 충분히 실용 영역인 것을 확인하였다. 수득된 결과를 표 4-1에 나타낸다.
(실시예 12~20)
실시예 11의 발광 재료 1과 발광 재료 2를, 표 4-1 및 표 4-2에 나타낸 바와 같이 변경한 것 이외에는 마찬가지로 하여 유기 EL 소자를 제조하였다.
다음에 소자의 각각에 대하여 통전 시험을 실시한 바, 전압 6.3V에서 발광 휘도가 180~550cd/㎡이고, 발광 피크 파장(ELλmax) 및 색도를 측정한 바 발광색은 청색인 것을 확인하였다. 또한, 초기 발광 휘도를 100cd/㎡으로 하여 정전류 구동시킨 바, 반감 수명은 5,500 시간 이상이며, 충분히 실용 영역인 것을 확인하였다. 수득된 결과를 표 4-1 및 표 4-2에 나타낸다.
표 1, 표 2, 표 4-1 및 표 4-2에 나타내는 실시예 1~20의 평가 결과로부터, 본 발명의 유기 EL 소자에 의해, 청색 발광이며 우수한 발광 휘도와, 실용 영역에 있는 반감 수명을 달성할 수 있다. 특히, 축합 환 함유 G2로서 안트라센 구조를, 플루오란텐 구조로서 화학식 1b 구조 화합물을 이용함으로써, 발광 효율, 반감 수명이 가장 우수하다.
(비교예 4)
비교예 4에 있어서는, 발광층에, 실시예 11의 화합물(2a'-55)와 화합물(2-21) 대신에, 화합물(2a'-55)와 하기 화합물(C)을 막 두께 40㎚(중량비 (2a'-55):C=40:2)를 이용한 것 외에는, 실시예 11과 마찬가지로 유기 EL 소자를 제작하였다.
여기서 화합물(C)은 벤조[k]플루오란텐이다.
그 결과, 발광색은 청색 발광이 관찰되었지만, 발광 휘도는 105cd/㎡이고, 반감 수명은 3000 시간으로 짧았다.
(실시예 21)
25㎜×75㎜×1.1㎜ 두께의 ITO 투명 전극 부착 유리 기판(지오마틱사 제품)을 아이소프로필알코올 중에서 초음파 세정을 5분간 실시한 후, UV 오존 세정을 30분간 실시하였다.
이 기판 위에 적층 구조의 정공 주입·수송층을 형성하였다. 우선, 스핀 코팅법으로 폴리에틸렌다이옥시싸이오펜·폴리스타이렌설폰산(PEDOT·PSS)을 100㎚의 막 두께로 성막하였다. 이어서, 하기에 나타내는 폴리머 1(분자량(Mw):145000)의 톨루엔 용액(0.6중량%)을 스핀 코팅법으로 20㎚의 막 두께로 성막하고, 170℃에서 30분간 건조하였다.
다음에, 발광층을, 발광 재료로서 상기 화합물(2a'-55) 및 상기 화합물(2-21)((2a'-55):(2-21)=20:2(중량비))을 1중량% 포함하는 톨루엔 용액을 이용하여, 스핀 코팅법으로 성막하였다. 이 발광층의 막 두께는 50㎚였다.
이 발광층 상에, 막 두께 10㎚의 트리스(8-퀴놀린올)알루미늄막(이하, 「Alq막」이라고 약기함)을 성막하였다. 이 Alq막은 전자 수송층으로서 기능한다.
그 후, 환원성 도펀트인 Li(Li원:사에스게터사 제품)와 Alq를 이원 증착시켜, 전자 주입층(음극)으로서 Alq:Li막을 형성하였다. 이 Alq:Li막 상에 금속 Al을 증착시켜 금속 음극을 형성하고, 유기 EL 소자를 형성하였다.
이 소자는 청색 발광하고, 발광면은 균일하였다. 이 때의 발광 효율은 2.9cd/A였다.
(실시예 22)
25㎜×75㎜×1.1㎜ 두께의 유리 기판 상에 막 두께 120㎚의 인듐주석산화물로 이루어지는 투명 전극을 마련하였다. 이 유리 기판을 아이소프로필알코올로 초음파 세정하고, 자외선 및 오존을 조사하여 세정하였다. 이어서, 투명 전극 부착 유리 기판을 진공 증착 장치의 증착조 내의 기판 홀더에 장착하는 동시에, 진공조 내의 진공도를 1×10-3㎩로 감압하였다.
우선, 투명 전극이 형성되어 있는 측의 면 상에 상기 투명 전극을 덮도록 하여 N', N"-비스[4-(다이페닐아미노)페닐]-N', N"-다이페닐바이페닐-4,4'-다이아민의 층을 증착 속도 2㎚/sec, 막 두께 60㎚로 성막하였다. 이 막은 정공 주입층으로서 기능한다. 다음에, 이 정공 주입층 위에 N, N, N', N'-테트라(4-바이페닐릴)벤지딘의 층을 증착 속도 2㎚/sec, 막 두께 20㎚로 성막하였다. 이 막은 정공 수송층으로서 기능한다.
정공 수송층 위에, 상기 화합물(2a-2)[발광 재료 1]와 상기 화합물(2-28)[발광 재료 2]을, 각각 증착 속도 2㎚/sec 및 0.2㎚/sec, 막 두께 40㎚로, 중량비가 (2a-2):(2-28)=40:2로 되도록 동시 증착하였다. 이 막은 발광층으로서 기능한다. 그 위에, 트리스(8-하이드록시퀴놀리노)알루미늄을 증착 속도 2㎚/sec, 막 두께 20㎚로 증착하여, 전자 수송층을 성막하였다. 또, 불화리튬을 증착 속도 0.1㎚/sec, 막 두께 1㎚로, 전자 주입층을 성막하였다. 마지막으로, 알루미늄을 증착 속도 2㎚/sec, 막 두께 200㎚로 음극층을 형성하여, 유기 EL 소자를 제조하였다.
다음에 이 소자에 통전 시험을 실시한 바, 전압 6.5V에서 발광 휘도가 250cd/㎡이고, 발광 피크 파장(ELλmax)은 446이었다. 초기 발광 휘도를 100cd/㎡로 하여 정전류 구동시킨 바, 반감 수명은 10,000 시간 이상이며, 충분히 실용 영역인 것을 확인하였다.
이상 상세히 설명한 바와 같이, 발광층이 상기 화학식 1로 표시되는 플루오란텐 구조를 갖는 화합물로부터 선택되는 적어도 1 종류와, 상기 화학식 2로 표시되는 축합 환 함유 화합물로부터 선택되는 적어도 1 종류를 함유하는 본 발명의 유기 전기 발광 소자는, 발광 휘도가 높고, 수명이 길다. 또한, 본 발명에 의해 수득된 유기 EL 소자의, 온도, 습도, 분위기 등에 대한 안정성의 향상을 위하여, 소자의 표면에 보호층을 마련하거나, 실리콘 오일, 수지 등에 의해 소자 전체를 보호 하는 것도 가능하다. 이 때문에, 본 발명의 유기 EL 소자는, 실용성이 높아, 벽걸이 텔레비전의 평면 발광체나 디스플레이의 백라이트 등의 광원으로서 유용하다. 유기 EL 소자, 정공 주입·수송 재료, 또한 전자 사진 감광체나 유기 반도체의 전하 수송 재료로서도 이용할 수 있다.
Claims (20)
- 음극과 양극 사이에 적어도 발광층을 포함하는 1층 또는 복수 층으로 이루어지는 유기 박막층이 협지되어 있는 유기 전기 발광 소자에 있어서,상기 발광층이,(A) 하기 화학식 1로 표시되는 축합 환 함유 화합물로부터 선택되는 적어도 1 종류와,(B) 하기 화학식 1a, 화학식 1b 및 화학식 1c로 이루어지는 군으로부터 선택되는 화합물로부터 선택되는 적어도 1 종류를 함유하는 유기 전기 발광 소자.[화학식 1]G2{(식중, G2는 하기 화학식 3a로 나타내는 구조를 갖는 화합물, 하기 화학식 3b로 나타내는 구조를 갖는 화합물, 하기 화학식 3c로 나타내는 구조를 갖는 화합물, 하기 화학식 3d로 나타내는 구조를 갖는 화합물, 하기 화학식 3a'으로 나타내는 구조를 갖는 화합물, 하기 화학식 3a''으로 나타내는 구조를 갖는 화합물, 하기 화학식 3'a로 나타내는 구조를 갖는 화합물, 하기 화학식 3'b로 나타내는 구조를 갖는 화합물, 하기 화학식 3'c로 나타내는 구조를 갖는 화합물 및 하기 화학식 3'd로 나타내는 구조를 갖는 화합물로 이루어진 군으로부터 선택되는 화합물을 나타냄)[화학식 3a](식중, A1 은 1-나프틸기, 2-나프틸기, 1-페난트릴기, 2-페난트릴기, 3-페난트릴기, 4-페난트릴기, 9-페난트릴기, 1-나프타센일기, 2-나프타센일기, 9-나프타센일기, 1-피렌일기, 2-피렌일기, 4-피렌일기, 3-메틸-2-나프틸기 또는 4-메틸-1-나프틸기이며,A2는 1-나프틸기, 2-나프틸기, 1-페난트릴기, 2-페난트릴기, 3-페난트릴기, 4-페난트릴기, 9-페난트릴기, 1-나프타센일기, 2-나프타센일기, 9-나프타센일기, 1-피렌일기, 2-피렌일기, 4-피렌일기, 3-메틸-2-나프틸기 또는 4-메틸-1-나프틸기이고,Ar1 및 Ar2는 각각 독립적으로, 수소 원자, 또는 치환 또는 무치환의 핵탄소수 6~50의 방향족환기이며,R1~R10은 각각 독립적으로, 수소 원자, 치환 또는 무치환의 핵탄소수 6~50의 방향족환기, 치환 또는 무치환의 핵원자수 5~50의 방향족 복소환기, 치환 또는 무치환의 탄소수 1~50의 알킬기, 치환 또는 무치환의 사이클로알킬기, 치환 또는 무치환의 탄소수 1~50의 알콕시기, 치환 또는 무치환의 탄소수 6~50의 아르알킬기, 치환 또는 무치환의 핵원자수 5~50의 아릴옥시기, 치환 또는 무치환의 핵원자수 5~50의 아릴싸이오기, 치환 또는 무치환의 탄소수 1~50의 알콕시카보닐기, 치환 또는 무치환의 실릴기, 카복실기, 할로젠 원자, 사이아노기, 나이트로기 또는 하이드록실기이고,Ar1, Ar2, R9 및 R10은, 각각 복수이어도 좋고, 인접하는 것끼리 포화 또는 불포화의 환상 구조를 형성하고 있어도 좋음)[화학식 3b](식중, Ar1b 및 Ar2b는 각각 치환 또는 무치환의 핵탄소수 6~50의 방향족기이고,L은, 각각 치환 또는 무치환의 페닐렌기, 치환 또는 무치환의 나프탈렌일렌기, 치환 또는 무치환의 플루오렌일렌기, 또는 치환 또는 무치환의 다이벤조실롤릴렌기이며,m은 0~2의 정수, nb는 1~4의 정수, s는 0~2의 정수, t는 0~4의 정수이고,또한, L 또는 Ar1b는 피렌의 1~5위치 중 어느 하나에 결합하고, L 또는 Ar2b는 피렌의 6~10위치 중 어느 하나에 결합하며,단, nb+t가 짝수일 때, Ar1b, Ar2b, L은 하기 (1) 또는 (2)를 만족시키고,(1) Ar1b≠Ar2b(여기서 ≠는, 상이한 구조의 기인 것을 나타냄)(2) Ar1b=Ar2b일 때(2-1) m≠s 및/또는 nb≠t, 또는(2-2) m=s 또한 nb=t일 때,(2-2-1) L, 또는 피렌이, 각각 Ar1b 및 Ar2b 상의 상이한 결합 위치에 결합하고 있거나,(2-2-2) L, 또는 피렌이, Ar1b 및 Ar2b 상의 동일한 결합 위치에서 결합하고 있는 경우,L 또는 Ar1b 및 Ar2b의 피렌에 있어서의 치환 위치가 1위치와 6위치, 또는 2위치와 7위치인 경우는 없음)[화학식 3c](식중, Ar1c, Ar2c 및 Ar3c는 각각 독립적으로, 페난트렌 구조, 또는 피렌 구조를 갖는 기를 나타내고, R1c, R2c, 및 R3c는 각각 독립적으로, 수소 원자 또는 치환기를 나타냄)[화학식 3d](식중, Ar11, Ar21 및 Ar31은 각각 아릴렌기를 나타내고, Ar12, Ar22 및 Ar32는 각각 독립적으로, 치환기 또는 수소 원자를 나타내며, Ar11, Ar21, Ar31, Ar12, Ar22, 및 Ar32중 적어도 하나는 나프탈렌 구조, 페난트렌 구조, 피렌 구조, 페릴렌 구조 또는 축환 헤테로 아릴 구조이고, Ar는 아릴렌기 또는 헤테로아릴렌기를 나타냄)[화학식 3a'](식중, A1 은 1-나프틸기, 2-나프틸기, 1-페난트릴기, 2-페난트릴기, 3-페난트릴기, 4-페난트릴기, 9-페난트릴기, 1-나프타센일기, 2-나프타센일기, 9-나프타센일기, 1-피렌일기, 2-피렌일기, 4-피렌일기, 3-메틸-2-나프틸기, 4-메틸-1-나프틸기 또는 4-메틸-1-안트릴기이며,A2는 수소 원자, 또는 치환 또는 무치환의 핵탄소수 6~50의 방향족환기이고,Ar1 및 Ar2는 각각 독립적으로, 수소 원자, 또는 치환 또는 무치환의 핵탄소수 6~50의 방향족환기이며,R1~R10은 각각 독립적으로, 수소 원자, 치환 또는 무치환의 핵탄소수 6~50의 방향족환기, 치환 또는 무치환의 핵원자수 5~50의 방향족 복소환기, 치환 또는 무치환의 탄소수 1~50의 알킬기, 치환 또는 무치환의 사이클로알킬기, 치환 또는 무치환의 탄소수 1~50의 알콕시기, 치환 또는 무치환의 탄소수 6~50의 아르알킬기, 치환 또는 무치환의 핵원자수 5~50의 아릴옥시기, 치환 또는 무치환의 핵원자수 5~50의 아릴싸이오기, 치환 또는 무치환의 탄소수 1~50의 알콕시카보닐기, 치환 또는 무치환의 실릴기, 카복실기, 할로젠 원자, 사이아노기, 나이트로기 또는 하이드록실기이고,Ar1, Ar2, R9 및 R10은 각각 복수이어도 좋고, 인접하는 것끼리 포화 또는 불포화의 환상 구조를 형성하고 있어도 좋으며,단, 화학식 3a'에 있어서, 중심의 안트라센의 9위치 및 10위치에, 상기 안트라센 상에 나타내는 X-Y축에 대하여 대칭형으로 되는 기가 결합하는 경우는 없음)[화학식 3a"](식중, Ar1 및 Ar2는 각각 독립적으로, 치환 또는 무치환의 핵탄소수 10~30의 방향족환기(단, 안트라센 잔기를 제외함)이고,R1~R8은 각각 독립적으로, 수소 원자, 치환 또는 무치환의 핵탄소수 6~50의 방향족환기, 치환 또는 무치환의 핵원자수 5~50의 방향족 복소환기, 치환 또는 무치환의 탄소수 1~50의 알킬기, 치환 또는 무치환의 사이클로알킬기, 치환 또는 무치환의 탄소수 1~50의 알콕시기, 치환 또는 무치환의 탄소수 6~50의 아르알킬기, 치환 또는 무치환의 핵원자수 5~50의 아릴옥시기, 치환 또는 무치환의 핵원자수 5~50의 아릴싸이오기, 치환 또는 무치환의 탄소수 1~50의 알콕시카보닐기, 치환 또는 무치환의 실릴기, 카복실기, 할로젠 원자, 사이아노기, 나이트로기 또는 하이드록실기임)[화학식 3'a](식 3'a 중, Ar1a 및 Ar2a는 각각 독립적으로, 치환 또는 무치환의 핵탄소수 6~20의 방향족환으로부터 유도되는 기이고, 상기 방향족환은 1 또는 2 이상의 치환기로 치환되어 있고, 상기 치환기는 1-나프틸기, 2-나프틸기, 9-페난트릴기, 1-나프타센일기, 2-나프타센일기, 9-나프타센일기, 1-피렌일기, 2-피렌일기, 4-피렌일기, 2-바이페닐일기, 3-바이페닐일기, 4-바이페닐일기, o-톨릴기, m-톨릴기, p-톨릴기, p-t-뷰틸페닐기, 치환 또는 무치환의 탄소수 1~50의 알킬기, 치환 또는 무치환의 탄소수 3~50의 사이클로알킬기, 치환 또는 무치환의 탄소수 1~50의 알콕시기, 치환 또는 무치환의 탄소수 6~50의 아르알킬기, 치환 또는 무치환의 핵원자수 5~50의 아릴옥시기, 치환 또는 무치환의 핵원자수 5~50의 아릴싸이오기, 치환 또는 무치환의 탄소수 1~50의 알콕시카보닐기, 치환 또는 무치환의 실릴기, 카복실기, 할로젠 원자, 사이아노기, 나이트로기 및 하이드록시기로부터 선택되고, 상기 방향족환이 2 이상의 치환기로 치환되어 있는 경우, 상기 치환기는 동일하여도, 상이하여도 좋으며, 인접하는 치환기끼리는 서로 결합하여 포화 또는 불포화의 환상 구조를 형성하고 있어도 좋으며,R1a~R8a는 각각 독립적으로, 수소 원자, 치환 또는 무치환의 핵탄소수 6~50의 아릴기, 치환 또는 무치환의 핵원자수 5~50의 헤테로아릴기, 치환 또는 무치환의 탄소수 1~50의 알킬기, 치환 또는 무치환의 탄소수 3~50의 사이클로알킬기, 치환 또는 무치환의 탄소수 1~50의 알콕시기, 치환 또는 무치환의 탄소수 6~50의 아르알킬기, 치환 또는 무치환의 핵원자수 5~50의 아릴옥시기, 치환 또는 무치환의 핵원자수 5~50의 아릴싸이오기, 치환 또는 무치환의 탄소수 1~50의 알콕시카보닐기, 치환 또는 무치환의 실릴기, 카복실기, 할로젠 원자, 사이아노기, 나이트로기 및 하이드록시기로부터 선택됨)[화학식 3'b](식 3'b 중, Ar1b 및 Ar2b는 각각 독립적으로, 치환 또는 무치환의 핵탄소수 6~50의 아릴기이고,L1 및 L2는 각각 독립적으로, 치환 또는 무치환의 페닐렌기, 치환 또는 무치환의 나프탈렌일렌기, 치환 또는 무치환의 플루오렌일렌기 및 치환 또는 무치환의 다이벤조실롤릴렌기로부터 선택되며,p 및 q는 0~2의 정수, r은 1~4의 정수, s는 0~4의 정수이고,또한, L1 또는 Ar1b는 피렌의 1~5위치 중 어느 하나에 결합하고, L2 또는 Ar2b는 피렌의 6~10위치 중 어느 하나에 결합함)[화학식 3'c](식 3'c 중, Ar1c, Ar2c 및 Ar3c는 각각 독립적으로, 안트라센 구조를 갖는 기, 피렌 구조를 갖는 기 및 페릴렌 구조를 갖는 기로부터 선택되고,R1c, R2c 및 R3c는 각각 독립적으로, 수소 원자 또는 치환기를 나타냄)[화학식 3'd](식 3'd 중, Ar1d, Ar2d 및 Ar3d는 각각 독립적으로, 핵탄소수 6~50의 아릴기를 나타내고, 상기 아릴기는 1 또는 2 이상의 치환기로 치환되어 있어도 좋으며,Ar1d, Ar2d, Ar3d 및 이들의 아릴기가 갖는 치환기중 적어도 하나는 나프탈렌 구조, 페난트렌 구조, 피렌 구조, 페릴렌 구조 또는 핵탄소수 6~20의 축환 헤테로 아릴 구조를 가지며,Ar은 방향환 또는 복소방향환으로부터 유도되는 3가의 기를 나타냄)}[화학식 1a](화학식 1a 중, X1~X10은 각각 독립적으로, 수소 원자, 할로젠 원자, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알콕시기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬싸이오기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일옥시기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일싸이오기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬옥시기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬싸이오기, 치환 또는 무치환의 탄소 원자수 6~20의 아릴기, 치환 또는 무치환의 탄소 원자수 5~20의 복소환기, 치환 또는 무치환의 탄소 원자수 6~20의 아릴옥시기, 치환 또는 무치환의 탄소 원자수 6~20의 아릴싸이오기, 사이아노기, 실릴기, 하이드록실기, -COOR1e기(기 중, R1e는 수소 원자, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 또는 치환 또는 무치환의 탄소 원자수 6~30의 아릴기를 나타냄), -COR2e기(기 중, R2e는 수소 원자, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 치환 또는 무치환의 탄소 원자수 6~30의 아릴기, 또는 아미노기를 나타냄), -OCOR3e기(기 중, R3e는 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 치환 또는 무치환의 탄소 원자수 6~30의 아릴기를 나타냄)를 나타내며,단, 상기 치환 또는 무치환의 탄소 원자수 6~20의 아릴기는 상기 화학식 1a(식중, X1~X10은 각각 독립적으로, 수소 원자, 할로젠 원자, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알콕시기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬싸이오기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일옥시기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일싸이오기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬옥시기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬싸이오기, 치환 또는 무치환의 탄소 원자수 6~20의 아릴기, 치환 또는 무치환의 탄소 원자수 5~20의 복소환기, 치환 또는 무치환의 탄소 원자수 6~20의 아릴옥시기, 치환 또는 무치환의 탄소 원자수 6~20의 아릴싸이오기, 치환 또는 무치환의 탄소 원자수 2~30의 아미노기, 사이아노기, 실릴기, 하이드록실기, -COOR1e기(기 중, R1e는 수소 원자, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 또는 치환 또는 무치환의 탄소 원자수 6~30의 아릴기를 나타냄), -COR2e기(기 중, R2e는 수소 원자, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 치환 또는 무치환의 탄소 원자수 6~30의 아릴기, 또는 아미노기를 나타냄), -OCOR3e기(기 중, R3e는 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 치환 또는 무치환의 탄소 원자수 6~30의 아릴기를 나타냄))인 경우는 없음)[화학식 1b](화학식 1b중, X1~X12는 화학식 1a의 X1~X10과 동일하되,단, 상기 화학식 1b 중 X1~X12는, 치환 또는 무치환의 탄소 원자수 2~30의 아미노기여도 좋고, 또한, 상기 치환 또는 무치환의 탄소 원자수 6~20의 아릴기는 상기 화학식 1b인 경우는 없고, 또한 X1~X12 중, 인접하는 기 및 각 기의 치환기는 서로 결합하여 치환 또는 무치환의 탄소환을 형성하는 경우는 없고, X4와 X11의 둘 모두가 수소 원자인 경우는 없음)[화학식 1c](화학식 1c중, X1~X12는 화학식 1a의 X1~X10과 동일하되,단, 상기 화학식 1c 중, X1~X12는, 치환 또는 무치환의 탄소 원자수 5~20의 복소환기는 아니고, 또한, X1~X12는, 치환 또는 무치환의 탄소 원자수 2~30의 아미노기여도 좋고, X1~X12 중 인접하는 기 및 각 기의 치환기는 서로 결합하여 치환 또는 무치환의 탄소환을 형성하는 경우는 없고,또한, 상기 화학식 1c 중, X7≠X8 이고,상기 화학식 1c 중, X4와 X11의 둘 모두가 수소 원자인 경우는 없고,플루오란텐 구조를 갖는 화합물이 화학식 1b로 표시되고, 화학식 1의 G2가 9,10-다이페닐안트라센인 경우는 없음)
- 음극과 양극 사이에 적어도 발광층을 포함하는 1층 또는 복수 층으로 이루어지는 유기 박막층이 협지되어 있는 유기 전기 발광 소자에 있어서,상기 발광층이,(A) 하기 화학식 1로 표시되는 축합 환 함유 화합물로부터 선택되는 적어도 1 종류와,(B) 하기 화학식 2로 표시되는 플루오란텐 구조를 갖는 화합물로부터 선택되는 적어도 1 종류를 함유하는 유기 전기 발광 소자.[화학식 1]G2{(식중, G2는 하기 화학식 3a로 나타내는 구조를 갖는 화합물, 하기 화학식 3b로 나타내는 구조를 갖는 화합물, 하기 화학식 3c로 나타내는 구조를 갖는 화합물, 하기 화학식 3d로 나타내는 구조를 갖는 화합물, 하기 화학식 3a'으로 나타내는 구조를 갖는 화합물, 하기 화학식 3a''으로 나타내는 구조를 갖는 화합물, 하기 화학식 3'a로 나타내는 구조를 갖는 화합물, 하기 화학식 3'b로 나타내는 구조를 갖는 화합물, 하기 화학식 3'c로 나타내는 구조를 갖는 화합물 및 하기 화학식 3'd로 나타내는 구조를 갖는 화합물로 이루어지는 군으로부터 선택되는 화합물을 나타냄)[화학식 3a](식중, A1 은 1-나프틸기, 2-나프틸기, 1-페난트릴기, 2-페난트릴기, 3-페난트릴기, 4-페난트릴기, 9-페난트릴기, 1-나프타센일기, 2-나프타센일기, 9-나프타센일기, 1-피렌일기, 2-피렌일기, 4-피렌일기, 3-메틸-2-나프틸기 또는 4-메틸-1-나프틸기이며,A2는 1-나프틸기, 2-나프틸기, 1-페난트릴기, 2-페난트릴기, 3-페난트릴기, 4-페난트릴기, 9-페난트릴기, 1-나프타센일기, 2-나프타센일기, 9-나프타센일기, 1-피렌일기, 2-피렌일기, 4-피렌일기, 3-메틸-2-나프틸기 또는 4-메틸-1-나프틸기이고,Ar1 및 Ar2는 각각 독립적으로, 수소 원자, 또는 치환 또는 무치환의 핵탄소수 6~50의 방향족환기이며,R1~R10은 각각 독립적으로, 수소 원자, 치환 또는 무치환의 핵탄소수 6~50의 방향족환기, 치환 또는 무치환의 핵원자수 5~50의 방향족 복소환기, 치환 또는 무치환의 탄소수 1~50의 알킬기, 치환 또는 무치환의 사이클로알킬기, 치환 또는 무치환의 탄소수 1~50의 알콕시기, 치환 또는 무치환의 탄소수 6~50의 아르알킬기, 치환 또는 무치환의 핵원자수 5~50의 아릴옥시기, 치환 또는 무치환의 핵원자수 5~50의 아릴싸이오기, 치환 또는 무치환의 탄소수 1~50의 알콕시카보닐기, 치환 또는 무치환의 실릴기, 카복실기, 할로젠 원자, 사이아노기, 나이트로기 또는 하이드록실기이고,Ar1, Ar2, R9 및 R10은, 각각 복수이어도 좋고, 인접하는 것끼리 포화 또는 불포화의 환상 구조를 형성하고 있어도 좋음)[화학식 3b](식중, Ar1b 및 Ar2b는 각각 치환 또는 무치환의 핵탄소수 6~50의 방향족기이고,L은, 각각 치환 또는 무치환의 페닐렌기, 치환 또는 무치환의 나프탈렌일렌기, 치환 또는 무치환의 플루오렌일렌기, 또는 치환 또는 무치환의 다이벤조실롤릴렌기이며,m은 0~2의 정수, nb는 1~4의 정수, s는 0~2의 정수, t는 0~4의 정수이고,또한, L 또는 Ar1b는 피렌의 1~5위치 중 어느 하나에 결합하고, L 또는 Ar2b는 피렌의 6~10위치 중 어느 하나에 결합하며,단, nb+t가 짝수일 때, Ar1b, Ar2b, L은 하기 (1) 또는 (2)를 만족시키고,(1) Ar1b≠Ar2b(여기서 ≠는, 상이한 구조의 기인 것을 나타냄)(2) Ar1b=Ar2b일 때(2-1) m≠s 및/또는 nb≠t, 또는(2-2) m=s 또한 nb=t일 때,(2-2-1) L, 또는 피렌이, 각각 Ar1b 및 Ar2b 상의 상이한 결합 위치에 결합하고 있거나,(2-2-2) L, 또는 피렌이, Ar1b 및 Ar2b 상의 동일한 결합 위치에서 결합하고 있는 경우,L 또는 Ar1b 및 Ar2b의 피렌에 있어서의 치환 위치가 1위치와 6위치, 또는 2위치와 7위치인 경우는 없음)[화학식 3c](식중, Ar1c, Ar2c 및 Ar3c는 각각 독립적으로, 페난트렌 구조, 또는 피렌 구조를 갖는 기를 나타내고, R1c, R2c, 및 R3c는 각각 독립적으로, 수소 원자 또는 치환기를 나타냄)[화학식 3d](식중, Ar11, Ar21 및 Ar31은 각각 아릴렌기를 나타내고, Ar12, Ar22 및 Ar32는 각각 독립적으로, 치환기 또는 수소 원자를 나타내며, Ar11, Ar21, Ar31, Ar12, Ar22, 및 Ar32중 적어도 하나는 나프탈렌 구조, 페난트렌 구조, 피렌 구조, 페릴렌 구조 또는 축환 헤테로 아릴 구조이고, Ar는 아릴렌기 또는 헤테로아릴렌기를 나타냄)[화학식 3a'](식중, A1 은 1-나프틸기, 2-나프틸기, 1-페난트릴기, 2-페난트릴기, 3-페난트릴기, 4-페난트릴기, 9-페난트릴기, 1-나프타센일기, 2-나프타센일기, 9-나프타센일기, 1-피렌일기, 2-피렌일기, 4-피렌일기, 3-메틸-2-나프틸기, 4-메틸-1-나프틸기 또는 4-메틸-1-안트릴기이며,A2는 수소 원자, 또는 치환 또는 무치환의 핵탄소수 6~50의 방향족환기이고,Ar1 및 Ar2는 각각 독립적으로, 수소 원자, 또는 치환 또는 무치환의 핵탄소수 6~50의 방향족환기이며,R1~R10은 각각 독립적으로, 수소 원자, 치환 또는 무치환의 핵탄소수 6~50의 방향족환기, 치환 또는 무치환의 핵원자수 5~50의 방향족 복소환기, 치환 또는 무치환의 탄소수 1~50의 알킬기, 치환 또는 무치환의 사이클로알킬기, 치환 또는 무치환의 탄소수 1~50의 알콕시기, 치환 또는 무치환의 탄소수 6~50의 아르알킬기, 치환 또는 무치환의 핵원자수 5~50의 아릴옥시기, 치환 또는 무치환의 핵원자수 5~50의 아릴싸이오기, 치환 또는 무치환의 탄소수 1~50의 알콕시카보닐기, 치환 또는 무치환의 실릴기, 카복실기, 할로젠 원자, 사이아노기, 나이트로기 또는 하이드록실기이고,Ar1, Ar2, R9 및 R10은 각각 복수이어도 좋고, 인접하는 것끼리 포화 또는 불포화의 환상 구조를 형성하고 있어도 좋으며,단, 화학식 3a'에 있어서, 중심의 안트라센의 9위치 및 10위치에, 상기 안트라센 상에 나타내는 X-Y축에 대하여 대칭형으로 되는 기가 결합하는 경우는 없음)[화학식 3a"](식중, Ar1 및 Ar2는 각각 독립적으로, 치환 또는 무치환의 핵탄소수 10~30의 방향족환기(단, 안트라센 잔기를 제외함)이고,R1~R8은 각각 독립적으로, 수소 원자, 치환 또는 무치환의 핵탄소수 6~50의 방향족환기, 치환 또는 무치환의 핵원자수 5~50의 방향족 복소환기, 치환 또는 무치환의 탄소수 1~50의 알킬기, 치환 또는 무치환의 사이클로알킬기, 치환 또는 무치환의 탄소수 1~50의 알콕시기, 치환 또는 무치환의 탄소수 6~50의 아르알킬기, 치환 또는 무치환의 핵원자수 5~50의 아릴옥시기, 치환 또는 무치환의 핵원자수 5~50의 아릴싸이오기, 치환 또는 무치환의 탄소수 1~50의 알콕시카보닐기, 치환 또는 무치환의 실릴기, 카복실기, 할로젠 원자, 사이아노기, 나이트로기 또는 하이드록실기임)[화학식 3'a](식 3'a 중, Ar1a 및 Ar2a는 각각 독립적으로, 치환 또는 무치환의 핵탄소수 6~20의 방향족환으로부터 유도되는 기이고, 상기 방향족환은 1 또는 2 이상의 치환기로 치환되어 있고, 상기 치환기는 1-나프틸기, 2-나프틸기, 9-페난트릴기, 1-나프타센일기, 2-나프타센일기, 9-나프타센일기, 1-피렌일기, 2-피렌일기, 4-피렌일기, 2-바이페닐일기, 3-바이페닐일기, 4-바이페닐일기, o-톨릴기, m-톨릴기, p-톨릴기, p-t-뷰틸페닐기, 치환 또는 무치환의 탄소수 1~50의 알킬기, 치환 또는 무치환의 탄소수 3~50의 사이클로알킬기, 치환 또는 무치환의 탄소수 1~50의 알콕시기, 치환 또는 무치환의 탄소수 6~50의 아르알킬기, 치환 또는 무치환의 핵원자수 5~50의 아릴옥시기, 치환 또는 무치환의 핵원자수 5~50의 아릴싸이오기, 치환 또는 무치환의 탄소수 1~50의 알콕시카보닐기, 치환 또는 무치환의 실릴기, 카복실기, 할로젠 원자, 사이아노기, 나이트로기 및 하이드록시기로부터 선택되고, 상기 방향족환이 2 이상의 치환기로 치환되어 있는 경우, 상기 치환기는 동일하여도, 상이하여도 좋으며, 인접하는 치환기끼리는 서로 결합하여 포화 또는 불포화의 환상 구조를 형성하고 있어도 좋으며,R1a~R8a는 각각 독립적으로, 수소 원자, 치환 또는 무치환의 핵탄소수 6~50의 아릴기, 치환 또는 무치환의 핵원자수 5~50의 헤테로아릴기, 치환 또는 무치환의 탄소수 1~50의 알킬기, 치환 또는 무치환의 탄소수 3~50의 사이클로알킬기, 치환 또는 무치환의 탄소수 1~50의 알콕시기, 치환 또는 무치환의 탄소수 6~50의 아르알킬기, 치환 또는 무치환의 핵원자수 5~50의 아릴옥시기, 치환 또는 무치환의 핵원자수 5~50의 아릴싸이오기, 치환 또는 무치환의 탄소수 1~50의 알콕시카보닐기, 치환 또는 무치환의 실릴기, 카복실기, 할로젠 원자, 사이아노기, 나이트로기 및 하이드록시기로부터 선택됨)[화학식 3'b](식 3'b 중, Ar1b 및 Ar2b는 각각 독립적으로, 치환 또는 무치환의 핵탄소수 6~50의 아릴기이고,L1 및 L2는 각각 독립적으로, 치환 또는 무치환의 페닐렌기, 치환 또는 무치환의 나프탈렌일렌기, 치환 또는 무치환의 플루오렌일렌기 및 치환 또는 무치환의 다이벤조실롤릴렌기로부터 선택되며,p 및 q는 0~2의 정수, r은 1~4의 정수, s는 0~4의 정수이고,또한, L1 또는 Ar1b는 피렌의 1~5위치 중 어느 하나에 결합하고, L2 또는 Ar2b는 피렌의 6~10위치 중 어느 하나에 결합함)[화학식 3'c](식 3'c 중, Ar1c, Ar2c 및 Ar3c는 각각 독립적으로, 안트라센 구조를 갖는 기, 피렌 구조를 갖는 기 및 페릴렌 구조를 갖는 기로부터 선택되고,R1c, R2c 및 R3c는 각각 독립적으로, 수소 원자 또는 치환기를 나타냄)[화학식 3'd](식 3'd 중, Ar1d, Ar2d 및 Ar3d는 각각 독립적으로, 핵탄소수 6~50의 아릴기를 나타내고, 상기 아릴기는 1 또는 2 이상의 치환기로 치환되어 있어도 좋으며,Ar1d, Ar2d, Ar3d 및 이들의 아릴기가 갖는 치환기중 적어도 하나는 나프탈렌 구조, 페난트렌 구조, 피렌 구조, 페릴렌 구조 또는 핵탄소수 6~20의 축환 헤테로 아릴 구조를 가지며,Ar은 방향환 또는 복소방향환으로부터 유도되는 3가의 기를 나타냄)}[화학식 2]FLn-G1{(식중, FL은 플루오란텐 구조를 갖는 1가의 기이고, n은 2~4의 정수이며, 상기 FL은 하기 화학식 1a, 하기 화학식 1b 및 하기 화학식 1c의 구조를 갖는 어느 하나의 화합물로부터 선택되는 1가의 기이고, 복수의 FL은 동일해도 상이해도 좋으며,G1은, 치환 또는 무치환의 탄소 원자수 6~40의 방향족환기, 치환 또는 무치환의 탄소 원자수 6~40의 아릴아미노기, 치환 또는 무치환의 탄소 원자수 6~60의 다이아미노아릴기, 치환 또는 무치환의 탄소 원자수 6~60의 트라이아미노아릴기, 치환 또는 무치환의 탄소 원자수 3~40의 복소환기, 치환 또는 무치환의 에테닐렌기이며, 단일 결합을 포함함)[화학식 1a](화학식 1a 중, X1~X10은 각각 독립적으로, 수소 원자, 할로젠 원자, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알콕시기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬싸이오기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일옥시기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일싸이오기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬옥시기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬싸이오기, 치환 또는 무치환의 탄소 원자수 6~20의 아릴기, 치환 또는 무치환의 탄소 원자수 5~20의 복소환기, 치환 또는 무치환의 탄소 원자수 6~20의 아릴옥시기, 치환 또는 무치환의 탄소 원자수 6~20의 아릴싸이오기, 사이아노기, 실릴기, 하이드록실기, -COOR1e기(기 중, R1e는 수소 원자, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 또는 치환 또는 무치환의 탄소 원자수 6~30의 아릴기를 나타냄), -COR2e기(기 중, R2e는 수소 원자, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 치환 또는 무치환의 탄소 원자수 6~30의 아릴기, 또는 아미노기를 나타냄), -OCOR3e기(기 중, R3e는 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 치환 또는 무치환의 탄소 원자수 6~30의 아릴기를 나타냄)를 나타내며,단, 상기 치환 또는 무치환의 탄소 원자수 6~20의 아릴기는 상기 화학식 1a(식중, X1~X10은 각각 독립적으로, 수소 원자, 할로젠 원자, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알콕시기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬싸이오기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일옥시기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일싸이오기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬옥시기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬싸이오기, 치환 또는 무치환의 탄소 원자수 6~20의 아릴기, 치환 또는 무치환의 탄소 원자수 5~20의 복소환기, 치환 또는 무치환의 탄소 원자수 6~20의 아릴옥시기, 치환 또는 무치환의 탄소 원자수 6~20의 아릴싸이오기, 치환 또는 무치환의 탄소 원자수 2~30의 아미노기, 사이아노기, 실릴기, 하이드록실기, -COOR1e기(기 중, R1e는 수소 원자, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 또는 치환 또는 무치환의 탄소 원자수 6~30의 아릴기를 나타냄), -COR2e기(기 중, R2e는 수소 원자, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 치환 또는 무치환의 탄소 원자수 6~30의 아릴기, 또는 아미노기를 나타냄), -OCOR3e기(기 중, R3e는 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 치환 또는 무치환의 탄소 원자수 6~30의 아릴기를 나타냄))인 경우는 없음)[화학식 1b](화학식 1b중, X1~X12는 화학식 1a의 X1~X10과 동일하되,단, 상기 화학식 1b 중 X1~X12는, 치환 또는 무치환의 탄소 원자수 2~30의 아미노기여도 좋고, 또한, 상기 치환 또는 무치환의 탄소 원자수 6~20의 아릴기는 상기 화학식 1b인 경우는 없고, X4와 X11의 둘 모두가 수소 원자인 경우는 없음)[화학식 1c](화학식 1c중, X1~X12는 화학식 1a의 X1~X10과 동일하되,단, 상기 화학식 1c 중, X1~X12는, 치환 또는 무치환의 탄소 원자수 5~20의 복소환기는 아니고, 또한, X1~X12는, 치환 또는 무치환의 탄소 원자수 2~30의 아미노기여도 좋고, X1~X12 중 인접하는 기 및 각 기의 치환기는 서로 결합하여 치환 또는 무치환의 탄소환을 형성하는 경우는 없고,또한, 상기 화학식 1c 중, X7≠X8 이고,상기 화학식 1c 중, X4와 X11의 둘 모두가 수소 원자인 경우는 없고,플루오란텐 구조를 갖는 화합물이 화학식 1b로 표시되고, 화학식 1의 G2가 9,10-다이페닐안트라센인 경우는 없음)}
- 제 1 항에 있어서,플루오란텐 구조를 갖는 화합물이 화학식 1c의 구조를 갖는 화합물인 유기 전기 발광 소자.
- 제 2 항에 있어서,상기 화학식 2에 있어서 n이 2이고,두개의 FL이 서로 상이한 유기 전기 발광 소자.
- 제 1 항 내지 제 5 항 중 어느 한 항에 있어서,상기 G2가 화학식 3a으로 나타내는 구조를 갖는 화합물인 유기 전기 발광 소자.
- 제 1 항 내지 제 5 항 중 어느 한 항에 있어서,상기 G2가 화학식 3a''으로 나타내는 구조를 갖는 화합물인 유기 전기 발광 소자.
- 제 7 항에 있어서,무치환의 핵탄소수 10~30의 방향족환기가 나프탈렌 잔기를 포함하는 방향족 잔기인 유기 전기 발광 소자.
- 제 1 항 내지 제 5 항 중 어느 한 항에 있어서,상기 G2가 화학식 3a'으로 나타내는 구조를 갖는 화합물인 유기 전기 발광 소자.
- 제 1 항 내지 제 5 항 중 어느 한 항에 있어서,상기 G2가 화학식 3b~3d 중 어느 하나로 나타내는 구조를 갖는 화합물인 유기 전기 발광 소자.
- 제 1 항 내지 제 5 항 중 어느 한 항에 있어서,상기 G2가 화학식 3'a~3'd 중 어느 하나로 나타내는 화합물로부터 선택되는 적어도 1종인 유기 전기 발광 소자.
- 제 1 항 내지 제 5 항 중 어느 한 항에 있어서,상기 발광층 중에, 플루오란텐 구조를 갖는 상기 화합물이 0.01~20중량% 함유되어 있는 유기 전기 발광 소자.
- 제 1 항 내지 제 5 항 중 어느 한 항에 있어서,한 쌍의 전극 중 적어도 한 쪽의 표면에, 칼코게나이드층, 할로젠화 금속층 또는 금속 산화물층을 마련하는 유기 전기 발광 소자.
- 유기 전기 발광 재료와 용매로 이루어지는 유기 전기 발광 재료 함유 용액에 있어서,상기 유기 전기 발광 재료가 호스트 재료와 도펀트 재료로 이루어지고, 상기 도펀트 재료는 하기 화학식 2로 표시되는 플루오란텐 구조를 갖는 화합물 중 적어도 1종이고, 상기 호스트 재료는 하기 화학식 3a, 3a', 3b~3d, 3'a~3'd 및 화학식 1로 표시되는 축합 환 함유 화합물로부터 선택되는 적어도 1종인 것을 특징으로 하는 유기 전기 발광 재료 함유 용액.[화학식 1]G2{(식중, G2는 하기 화학식 3a로 나타내는 구조를 갖는 화합물, 하기 화학식 3b로 나타내는 구조를 갖는 화합물, 하기 화학식 3c로 나타내는 구조를 갖는 화합물, 하기 화학식 3d로 나타내는 구조를 갖는 화합물, 하기 화학식 3a'으로 나타내는 구조를 갖는 화합물, 하기 화학식 3a''으로 나타내는 구조를 갖는 화합물, 하기 화학식 3'a로 나타내는 구조를 갖는 화합물, 하기 화학식 3'b로 나타내는 구조를 갖는 화합물, 하기 화학식 3'c로 나타내는 구조를 갖는 화합물 및 하기 화학식 3'd로 나타내는 구조를 갖는 화합물로 이루어지는 군으로부터 선택되는 화합물을 나타냄)[화학식 3a](식중, A1 은 1-나프틸기, 2-나프틸기, 1-페난트릴기, 2-페난트릴기, 3-페난트릴기, 4-페난트릴기, 9-페난트릴기, 1-나프타센일기, 2-나프타센일기, 9-나프타센일기, 1-피렌일기, 2-피렌일기, 4-피렌일기, 3-메틸-2-나프틸기 또는 4-메틸-1-나프틸기이며,A2는 1-나프틸기, 2-나프틸기, 1-페난트릴기, 2-페난트릴기, 3-페난트릴기, 4-페난트릴기, 9-페난트릴기, 1-나프타센일기, 2-나프타센일기, 9-나프타센일기, 1-피렌일기, 2-피렌일기, 4-피렌일기, 3-메틸-2-나프틸기 또는 4-메틸-1-나프틸기이고,Ar1 및 Ar2는 각각 독립적으로, 수소 원자, 또는 치환 또는 무치환의 핵탄소수 6~50의 방향족환기이며,R1~R10은 각각 독립적으로, 수소 원자, 치환 또는 무치환의 핵탄소수 6~50의 방향족환기, 치환 또는 무치환의 핵원자수 5~50의 방향족 복소환기, 치환 또는 무치환의 탄소수 1~50의 알킬기, 치환 또는 무치환의 사이클로알킬기, 치환 또는 무치환의 탄소수 1~50의 알콕시기, 치환 또는 무치환의 탄소수 6~50의 아르알킬기, 치환 또는 무치환의 핵원자수 5~50의 아릴옥시기, 치환 또는 무치환의 핵원자수 5~50의 아릴싸이오기, 치환 또는 무치환의 탄소수 1~50의 알콕시카보닐기, 치환 또는 무치환의 실릴기, 카복실기, 할로젠 원자, 사이아노기, 나이트로기 또는 하이드록실기이고,Ar1, Ar2, R9 및 R10은, 각각 복수이어도 좋고, 인접하는 것끼리 포화 또는 불포화의 환상 구조를 형성하고 있어도 좋음)[화학식 3b](식중, Ar1b 및 Ar2b는 각각 치환 또는 무치환의 핵탄소수 6~50의 방향족기이고,L은, 각각 치환 또는 무치환의 페닐렌기, 치환 또는 무치환의 나프탈렌일렌기, 치환 또는 무치환의 플루오렌일렌기, 또는 치환 또는 무치환의 다이벤조실롤릴렌기이며,m은 0~2의 정수, nb는 1~4의 정수, s는 0~2의 정수, t는 0~4의 정수이고,또한, L 또는 Ar1b는 피렌의 1~5위치 중 어느 하나에 결합하고, L 또는 Ar2b는 피렌의 6~10위치 중 어느 하나에 결합하며,단, nb+t가 짝수일 때, Ar1b, Ar2b, L은 하기 (1) 또는 (2)를 만족시키고,(1) Ar1b≠Ar2b(여기서 ≠는, 상이한 구조의 기인 것을 나타냄)(2) Ar1b=Ar2b일 때(2-1) m≠s 및/또는 nb≠t, 또는(2-2) m=s 또한 nb=t일 때,(2-2-1) L, 또는 피렌이, 각각 Ar1b 및 Ar2b 상의 상이한 결합 위치에 결합하고 있거나,(2-2-2) L, 또는 피렌이, Ar1b 및 Ar2b 상의 동일한 결합 위치에서 결합하고 있는 경우,L 또는 Ar1b 및 Ar2b의 피렌에 있어서의 치환 위치가 1위치와 6위치, 또는 2위치와 7위치인 경우는 없음)[화학식 3c](식중, Ar1c, Ar2c 및 Ar3c는 각각 독립적으로, 페난트렌 구조, 또는 피렌 구조를 갖는 기를 나타내고, R1c, R2c, 및 R3c는 각각 독립적으로, 수소 원자 또는 치환기를 나타냄)[화학식 3d](식중, Ar11, Ar21 및 Ar31은 각각 아릴렌기를 나타내고, Ar12, Ar22 및 Ar32는 각각 독립적으로, 치환기 또는 수소 원자를 나타내며, Ar11, Ar21, Ar31, Ar12, Ar22, 및 Ar32중 적어도 하나는 나프탈렌 구조, 페난트렌 구조, 피렌 구조, 페릴렌 구조 또는 축환 헤테로 아릴 구조이고, Ar는 아릴렌기 또는 헤테로아릴렌기를 나타냄)[화학식 3a'](식중, A1 은 1-나프틸기, 2-나프틸기, 1-페난트릴기, 2-페난트릴기, 3-페난트릴기, 4-페난트릴기, 9-페난트릴기, 1-나프타센일기, 2-나프타센일기, 9-나프타센일기, 1-피렌일기, 2-피렌일기, 4-피렌일기, 3-메틸-2-나프틸기, 4-메틸-1-나프틸기 또는 4-메틸-1-안트릴기이며,A2는 수소 원자, 또는 치환 또는 무치환의 핵탄소수 6~50의 방향족환기이고,Ar1 및 Ar2는 각각 독립적으로, 수소 원자, 또는 치환 또는 무치환의 핵탄소수 6~50의 방향족환기이며,R1~R10은 각각 독립적으로, 수소 원자, 치환 또는 무치환의 핵탄소수 6~50의 방향족환기, 치환 또는 무치환의 핵원자수 5~50의 방향족 복소환기, 치환 또는 무치환의 탄소수 1~50의 알킬기, 치환 또는 무치환의 사이클로알킬기, 치환 또는 무치환의 탄소수 1~50의 알콕시기, 치환 또는 무치환의 탄소수 6~50의 아르알킬기, 치환 또는 무치환의 핵원자수 5~50의 아릴옥시기, 치환 또는 무치환의 핵원자수 5~50의 아릴싸이오기, 치환 또는 무치환의 탄소수 1~50의 알콕시카보닐기, 치환 또는 무치환의 실릴기, 카복실기, 할로젠 원자, 사이아노기, 나이트로기 또는 하이드록실기이고,Ar1, Ar2, R9 및 R10은 각각 복수이어도 좋고, 인접하는 것끼리 포화 또는 불포화의 환상 구조를 형성하고 있어도 좋으며,단, 화학식 3a'에 있어서, 중심의 안트라센의 9위치 및 10위치에, 상기 안트라센 상에 나타내는 X-Y축에 대하여 대칭형으로 되는 기가 결합하는 경우는 없음)[화학식 3a"](식중, Ar1 및 Ar2는 각각 독립적으로, 치환 또는 무치환의 핵탄소수 10~30의 방향족환기(단, 안트라센 잔기를 제외함)이고,R1~R8은 각각 독립적으로, 수소 원자, 치환 또는 무치환의 핵탄소수 6~50의 방향족환기, 치환 또는 무치환의 핵원자수 5~50의 방향족 복소환기, 치환 또는 무치환의 탄소수 1~50의 알킬기, 치환 또는 무치환의 사이클로알킬기, 치환 또는 무치환의 탄소수 1~50의 알콕시기, 치환 또는 무치환의 탄소수 6~50의 아르알킬기, 치환 또는 무치환의 핵원자수 5~50의 아릴옥시기, 치환 또는 무치환의 핵원자수 5~50의 아릴싸이오기, 치환 또는 무치환의 탄소수 1~50의 알콕시카보닐기, 치환 또는 무치환의 실릴기, 카복실기, 할로젠 원자, 사이아노기, 나이트로기 또는 하이드록실기임)[화학식 3'a](식 3'a 중, Ar1a 및 Ar2a는 각각 독립적으로, 치환 또는 무치환의 핵탄소수 6~20의 방향족환으로부터 유도되는 기이고, 상기 방향족환은 1 또는 2 이상의 치환기로 치환되어 있고, 상기 치환기는 1-나프틸기, 2-나프틸기, 9-페난트릴기, 1-나프타센일기, 2-나프타센일기, 9-나프타센일기, 1-피렌일기, 2-피렌일기, 4-피렌일기, 2-바이페닐일기, 3-바이페닐일기, 4-바이페닐일기, o-톨릴기, m-톨릴기, p-톨릴기, p-t-뷰틸페닐기, 치환 또는 무치환의 탄소수 1~50의 알킬기, 치환 또는 무치환의 탄소수 3~50의 사이클로알킬기, 치환 또는 무치환의 탄소수 1~50의 알콕시기, 치환 또는 무치환의 탄소수 6~50의 아르알킬기, 치환 또는 무치환의 핵원자수 5~50의 아릴옥시기, 치환 또는 무치환의 핵원자수 5~50의 아릴싸이오기, 치환 또는 무치환의 탄소수 1~50의 알콕시카보닐기, 치환 또는 무치환의 실릴기, 카복실기, 할로젠 원자, 사이아노기, 나이트로기 및 하이드록시기로부터 선택되고, 상기 방향족환이 2 이상의 치환기로 치환되어 있는 경우, 상기 치환기는 동일하여도, 상이하여도 좋으며, 인접하는 치환기끼리는 서로 결합하여 포화 또는 불포화의 환상 구조를 형성하고 있어도 좋으며,R1a~R8a는 각각 독립적으로, 수소 원자, 치환 또는 무치환의 핵탄소수 6~50의 아릴기, 치환 또는 무치환의 핵원자수 5~50의 헤테로아릴기, 치환 또는 무치환의 탄소수 1~50의 알킬기, 치환 또는 무치환의 탄소수 3~50의 사이클로알킬기, 치환 또는 무치환의 탄소수 1~50의 알콕시기, 치환 또는 무치환의 탄소수 6~50의 아르알킬기, 치환 또는 무치환의 핵원자수 5~50의 아릴옥시기, 치환 또는 무치환의 핵원자수 5~50의 아릴싸이오기, 치환 또는 무치환의 탄소수 1~50의 알콕시카보닐기, 치환 또는 무치환의 실릴기, 카복실기, 할로젠 원자, 사이아노기, 나이트로기 및 하이드록시기로부터 선택됨)[화학식 3'b](식 3'b 중, Ar1b 및 Ar2b는 각각 독립적으로, 치환 또는 무치환의 핵탄소수 6~50의 아릴기이고,L1 및 L2는 각각 독립적으로, 치환 또는 무치환의 페닐렌기, 치환 또는 무치환의 나프탈렌일렌기, 치환 또는 무치환의 플루오렌일렌기 및 치환 또는 무치환의 다이벤조실롤릴렌기로부터 선택되며,p 및 q는 0~2의 정수, r은 1~4의 정수, s는 0~4의 정수이고,또한, L1 또는 Ar1b는 피렌의 1~5위치 중 어느 하나에 결합하고, L2 또는 Ar2b는 피렌의 6~10위치 중 어느 하나에 결합함)[화학식 3'c](식 3'c 중, Ar1c, Ar2c 및 Ar3c는 각각 독립적으로, 안트라센 구조를 갖는 기, 피렌 구조를 갖는 기 및 페릴렌 구조를 갖는 기로부터 선택되고,R1c, R2c 및 R3c는 각각 독립적으로, 수소 원자 또는 치환기를 나타냄)[화학식 3'd](식 3'd 중, Ar1d, Ar2d 및 Ar3d는 각각 독립적으로, 핵탄소수 6~50의 아릴기를 나타내고, 상기 아릴기는 1 또는 2 이상의 치환기로 치환되어 있어도 좋으며,Ar1d, Ar2d, Ar3d 및 이들의 아릴기가 갖는 치환기중 적어도 하나는 나프탈렌 구조, 페난트렌 구조, 피렌 구조, 페릴렌 구조 또는 핵탄소수 6~20의 축환 헤테로 아릴 구조를 가지며,Ar은 방향환 또는 복소방향환으로부터 유도되는 3가의 기를 나타냄)}[화학식 2]FLn-G1{(식중, FL은 플루오란텐 구조를 갖는 1가의 기이고, n은 2~4의 정수이며, 상기 FL은 하기 화학식 1a, 하기 화학식 1b 및 하기 화학식 1c의 구조를 갖는 어느 하나의 화합물로부터 선택되는 1가의 기이고, 복수의 FL은 동일해도 상이해도 좋으며,G1은, 치환 또는 무치환의 탄소 원자수 6~40의 방향족환기, 치환 또는 무치환의 탄소 원자수 6~40의 아릴아미노기, 치환 또는 무치환의 탄소 원자수 6~60의 다이아미노아릴기, 치환 또는 무치환의 탄소 원자수 6~60의 트라이아미노아릴기, 치환 또는 무치환의 탄소 원자수 3~40의 복소환기, 치환 또는 무치환의 에테닐렌기이며, 단일 결합을 포함함)[화학식 1a](화학식 1a 중, X1~X10은 각각 독립적으로, 수소 원자, 할로젠 원자, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알콕시기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬싸이오기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일옥시기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일싸이오기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬옥시기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬싸이오기, 치환 또는 무치환의 탄소 원자수 6~20의 아릴기, 치환 또는 무치환의 탄소 원자수 5~20의 복소환기, 치환 또는 무치환의 탄소 원자수 6~20의 아릴옥시기, 치환 또는 무치환의 탄소 원자수 6~20의 아릴싸이오기, 사이아노기, 실릴기, 하이드록실기, -COOR1e기(기 중, R1e는 수소 원자, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 또는 치환 또는 무치환의 탄소 원자수 6~30의 아릴기를 나타냄), -COR2e기(기 중, R2e는 수소 원자, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 치환 또는 무치환의 탄소 원자수 6~30의 아릴기, 또는 아미노기를 나타냄), -OCOR3e기(기 중, R3e는 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 치환 또는 무치환의 탄소 원자수 6~30의 아릴기를 나타냄)를 나타내며,단, 상기 치환 또는 무치환의 탄소 원자수 6~20의 아릴기는 상기 화학식 1a(식중, X1~X10은 각각 독립적으로, 수소 원자, 할로젠 원자, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알콕시기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬싸이오기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일옥시기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일싸이오기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬옥시기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬싸이오기, 치환 또는 무치환의 탄소 원자수 6~20의 아릴기, 치환 또는 무치환의 탄소 원자수 5~20의 복소환기, 치환 또는 무치환의 탄소 원자수 6~20의 아릴옥시기, 치환 또는 무치환의 탄소 원자수 6~20의 아릴싸이오기, 치환 또는 무치환의 탄소 원자수 2~30의 아미노기, 사이아노기, 실릴기, 하이드록실기, -COOR1e기(기 중, R1e는 수소 원자, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 또는 치환 또는 무치환의 탄소 원자수 6~30의 아릴기를 나타냄), -COR2e기(기 중, R2e는 수소 원자, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 치환 또는 무치환의 탄소 원자수 6~30의 아릴기, 또는 아미노기를 나타냄), -OCOR3e기(기 중, R3e는 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 1~30의 알킬기, 치환 또는 무치환의 직쇄, 분기 또는 환상의 탄소 원자수 2~30의 알켄일기, 치환 또는 무치환의 탄소 원자수 7~30의 아르알킬기, 치환 또는 무치환의 탄소 원자수 6~30의 아릴기를 나타냄))인 경우는 없음)[화학식 1b](화학식 1b중, X1~X12는 화학식 1a의 X1~X10과 동일하되,단, 상기 화학식 1b 중 X1~X12는, 치환 또는 무치환의 탄소 원자수 2~30의 아미노기여도 좋고, 또한, 상기 치환 또는 무치환의 탄소 원자수 6~20의 아릴기는 상기 화학식 1b인 경우는 없고, X4와 X11의 둘 모두가 수소 원자인 경우는 없음)[화학식 1c](화학식 1c중, X1~X12는 화학식 1a의 X1~X10과 동일하되,단, 상기 화학식 1c 중, X1~X12는, 치환 또는 무치환의 탄소 원자수 5~20의 복소환기는 아니고, 또한, X1~X12는, 치환 또는 무치환의 탄소 원자수 2~30의 아미노기여도 좋고, X1~X12 중 인접하는 기 및 각 기의 치환기는 서로 결합하여 치환 또는 무치환의 탄소환을 형성하는 경우는 없고,또한, 상기 화학식 1c 중, X7≠X8 이고,상기 화학식 1c 중, X4와 X11의 둘 모두가 수소 원자인 경우는 없고,플루오란텐 구조를 갖는 화합물이 화학식 1b로 표시되고, 화학식 1의 G2가 9,10-다이페닐안트라센인 경우는 없음)}
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JPJP-P-2006-00053942 | 2006-02-28 | ||
| JP2006053942 | 2006-02-28 | ||
| JP2006312023 | 2006-11-17 | ||
| JPJP-P-2006-00312023 | 2006-11-17 | ||
| PCT/JP2007/053806 WO2007100010A1 (ja) | 2006-02-28 | 2007-02-28 | 有機エレクトロルミネッセンス素子 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20080114702A KR20080114702A (ko) | 2008-12-31 |
| KR101406631B1 true KR101406631B1 (ko) | 2014-06-11 |
Family
ID=38459111
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020087021039A KR101406631B1 (ko) | 2006-02-28 | 2007-02-28 | 유기 전기 발광 소자 |
Country Status (7)
| Country | Link |
|---|---|
| US (2) | US9214636B2 (ko) |
| EP (1) | EP1990844B1 (ko) |
| JP (1) | JP5199066B2 (ko) |
| KR (1) | KR101406631B1 (ko) |
| CN (2) | CN102394273A (ko) |
| TW (1) | TWI433595B (ko) |
| WO (1) | WO2007100010A1 (ko) |
Families Citing this family (55)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP1757670A3 (en) * | 1999-09-30 | 2007-03-21 | Idemitsu Kosan Company Limited | Organic electroluminescent element |
| JP5122482B2 (ja) * | 2006-01-27 | 2013-01-16 | エルジー・ケム・リミテッド | 新規なアントラセン誘導体、その製造方法およびこれを用いた有機電気素子 |
| US7977869B2 (en) | 2006-08-04 | 2011-07-12 | Canon Kabushiki Kaisha | Organic luminescent device and benzo[k]fluoranthene compound |
| WO2008059713A1 (en) * | 2006-11-15 | 2008-05-22 | Idemitsu Kosan Co., Ltd. | Fluoranthene compound, organic electroluminescent device using the fluoranthene compound, and organic electroluminescent material-containing solution |
| JP2008137978A (ja) * | 2006-12-05 | 2008-06-19 | Canon Inc | カルバゾール誘導体及びこれを用いた有機発光素子 |
| KR100874472B1 (ko) * | 2007-02-28 | 2008-12-18 | 에스에프씨 주식회사 | 청색발광화합물 및 이를 이용한 유기전계발광소자 |
| JP5110919B2 (ja) * | 2007-03-07 | 2012-12-26 | キヤノン株式会社 | 縮合環化合物及びこれを用いた有機発光素子 |
| US8154195B2 (en) | 2007-07-07 | 2012-04-10 | Idemitsu Kosan Co., Ltd. | Organic electroluminescence device and material for organic electroluminescence device |
| JP2010245061A (ja) * | 2007-07-07 | 2010-10-28 | Idemitsu Kosan Co Ltd | 有機el素子 |
| WO2009066600A1 (ja) * | 2007-11-19 | 2009-05-28 | Idemitsu Kosan Co., Ltd. | モノベンゾクリセン誘導体、及びそれを含む有機エレクトロルミネッセンス素子用材料、並びにそれを用いた有機エレクトロルミネッセンス素子 |
| KR101528241B1 (ko) * | 2007-12-07 | 2015-06-15 | 삼성디스플레이 주식회사 | 방향족 복소환 화합물, 이를 포함한 유기막을 구비한 유기발광 소자 및 상기 유기발광 소자의 제조 방법 |
| CN103107284A (zh) | 2007-12-28 | 2013-05-15 | 出光兴产株式会社 | 芳胺衍生物及使用该芳胺衍生物的有机电致发光元件 |
| KR101099753B1 (ko) | 2008-02-02 | 2011-12-28 | 에스에프씨 주식회사 | 플루오란텐 유도체 및 이를 포함하는 유기전계발광소자 |
| KR100901887B1 (ko) * | 2008-03-14 | 2009-06-09 | (주)그라쎌 | 신규한 유기 발광 화합물 및 이를 채용하고 있는 유기 발광소자 |
| JP5424681B2 (ja) * | 2008-04-01 | 2014-02-26 | キヤノン株式会社 | 有機発光素子 |
| JP2010121036A (ja) * | 2008-11-19 | 2010-06-03 | Canon Inc | 発光素子及び画像表示装置および新規有機化合物 |
| JP2010121035A (ja) * | 2008-11-19 | 2010-06-03 | Canon Inc | 新規有機化合物、発光素子及び画像表示装置 |
| US20100244677A1 (en) * | 2009-03-31 | 2010-09-30 | Begley William J | Oled device containing a silyl-fluoranthene derivative |
| US8039129B2 (en) * | 2009-04-06 | 2011-10-18 | Idemitsu Kosan Co., Ltd. | Organic electroluminescence device and material for organic electroluminescence device |
| US8039127B2 (en) * | 2009-04-06 | 2011-10-18 | Idemitsu Kosan Co., Ltd. | Organic electroluminescence device and material for organic electroluminescence device |
| US8431250B2 (en) | 2009-04-24 | 2013-04-30 | Idemitsu Kosan Co., Ltd. | Aromatic amine derivative, and organic electroluminescent element comprising the same |
| US20100295445A1 (en) * | 2009-05-22 | 2010-11-25 | Idemitsu Kosan Co., Ltd. | Organic electroluminescent device |
| US20100295444A1 (en) * | 2009-05-22 | 2010-11-25 | Idemitsu Kosan Co., Ltd. | Organic electroluminescence device |
| US9153790B2 (en) * | 2009-05-22 | 2015-10-06 | Idemitsu Kosan Co., Ltd. | Organic electroluminescent device |
| US8476823B2 (en) * | 2009-05-22 | 2013-07-02 | Idemitsu Kosan Co., Ltd. | Organic electroluminescent device |
| US20100314644A1 (en) | 2009-06-12 | 2010-12-16 | Idemitsu Kosan Co., Ltd. | Organic electroluminescent device |
| US20120013244A1 (en) * | 2009-12-16 | 2012-01-19 | Idemitsu Kosan Co., Ltd. | Organic luminescent medium |
| JP5645849B2 (ja) * | 2009-12-21 | 2014-12-24 | 出光興産株式会社 | ピレン誘導体及びそれを用いた有機エレクトロルミネッセンス素子 |
| EP2518787A1 (en) * | 2009-12-21 | 2012-10-31 | Idemitsu Kosan Co., Ltd. | Organic electroluminescent element using pyrene derivative |
| JP5575547B2 (ja) * | 2010-05-28 | 2014-08-20 | 双葉電子工業株式会社 | 有機el素子 |
| CN103012163B (zh) * | 2011-09-28 | 2015-07-08 | 海洋王照明科技股份有限公司 | 双荧蒽有机半导体材料及其制备方法和应用 |
| CN103012206B (zh) * | 2011-09-28 | 2014-10-01 | 海洋王照明科技股份有限公司 | 双荧蒽有机半导体材料及其制备方法和应用 |
| CN103044386B (zh) * | 2011-10-17 | 2014-10-01 | 海洋王照明科技股份有限公司 | 含双荧蒽有机半导体材料、其制备方法及应用 |
| KR101946891B1 (ko) | 2012-07-05 | 2019-02-12 | 도레이 카부시키가이샤 | 발광 소자 재료 및 발광 소자 |
| WO2014034891A1 (ja) * | 2012-08-31 | 2014-03-06 | 出光興産株式会社 | 有機エレクトロルミネッセンス素子 |
| JP2015233023A (ja) * | 2012-08-31 | 2015-12-24 | 出光興産株式会社 | 有機エレクトロルミネッセンス素子 |
| JPWO2014057873A1 (ja) * | 2012-10-10 | 2016-09-05 | 東レ株式会社 | ホスフィンオキサイド誘導体およびそれを有する発光素子 |
| JP6183214B2 (ja) | 2012-10-12 | 2017-08-23 | 東レ株式会社 | フルオランテン誘導体、それを含有する発光素子材料および発光素子 |
| JP2014096417A (ja) * | 2012-11-07 | 2014-05-22 | Idemitsu Kosan Co Ltd | 有機エレクトロルミネッセンス素子および電子機器 |
| JP2014096418A (ja) * | 2012-11-07 | 2014-05-22 | Idemitsu Kosan Co Ltd | 有機エレクトロルミネッセンス素子および電子機器 |
| WO2014081168A1 (ko) * | 2012-11-21 | 2014-05-30 | 주식회사 엘지화학 | 플루오란텐 화합물 및 이를 포함하는 유기 전자 소자 |
| CN105308022B (zh) * | 2013-05-31 | 2019-03-15 | 出光兴产株式会社 | 稠合荧蒽化合物、含有该化合物的有机电致发光元件用材料、以及使用了该化合物的有机电致发光元件及电子设备 |
| KR101621801B1 (ko) * | 2015-01-14 | 2016-05-17 | 삼성디스플레이 주식회사 | 방향족 복소환 화합물 및 이를 포함한 유기막을 구비한 유기 발광 소자 |
| CN106356452B (zh) * | 2015-12-09 | 2018-09-18 | 广东阿格蕾雅光电材料有限公司 | 仅电子有机半导体二极管器件 |
| JP7033397B2 (ja) * | 2016-03-29 | 2022-03-10 | 住友化学株式会社 | 発光素子 |
| WO2017170313A1 (ja) | 2016-03-29 | 2017-10-05 | 住友化学株式会社 | 発光素子 |
| EP3478030A4 (en) | 2016-06-24 | 2020-01-22 | Sumitomo Chemical Company, Limited | LIGHT EMITTING ELEMENT |
| KR20230117645A (ko) | 2017-04-26 | 2023-08-08 | 오티아이 루미오닉스 인크. | 표면의 코팅을 패턴화하는 방법 및 패턴화된 코팅을포함하는 장치 |
| US11751415B2 (en) | 2018-02-02 | 2023-09-05 | Oti Lumionics Inc. | Materials for forming a nucleation-inhibiting coating and devices incorporating same |
| CN108383693A (zh) * | 2018-02-06 | 2018-08-10 | 陕西师范大学 | 一种有机蓝色荧光材料及其制备方法和应用 |
| WO2020178804A1 (en) | 2019-03-07 | 2020-09-10 | Oti Lumionics Inc. | Materials for forming a nucleation-inhibiting coating and devices incorporating same |
| WO2021090932A1 (ja) * | 2019-11-08 | 2021-05-14 | 出光興産株式会社 | 有機エレクトロルミネッセンス素子及び電子機器 |
| WO2021201176A1 (ja) * | 2020-04-01 | 2021-10-07 | 出光興産株式会社 | 有機エレクトロルミネッセンス素子、化合物及び電子機器 |
| WO2021210304A1 (ja) * | 2020-04-15 | 2021-10-21 | 出光興産株式会社 | 化合物、有機エレクトロルミネッセンス素子及び電子機器 |
| KR20230116914A (ko) | 2020-12-07 | 2023-08-04 | 오티아이 루미오닉스 인크. | 핵 생성 억제 코팅 및 하부 금속 코팅을 사용한 전도성 증착 층의 패턴화 |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2003026616A (ja) * | 2001-04-19 | 2003-01-29 | Tdk Corp | 有機el素子用化合物、有機el素子 |
Family Cites Families (133)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| NL217825A (ko) | 1956-06-04 | |||
| NL100993C (ko) | 1956-06-27 | |||
| US3180729A (en) | 1956-12-22 | 1965-04-27 | Azoplate Corp | Material for electrophotographic reproduction |
| NL126440C (ko) | 1958-08-20 | |||
| NL250330A (ko) | 1959-04-09 | |||
| US3008897A (en) | 1959-08-07 | 1961-11-14 | Sinclair Refining Co | Hydrocarbon demetallization process |
| US3240597A (en) | 1961-08-21 | 1966-03-15 | Eastman Kodak Co | Photoconducting polymers for preparing electrophotographic materials |
| US3180703A (en) | 1963-01-15 | 1965-04-27 | Kerr Mc Gee Oil Ind Inc | Recovery process |
| JPS45555B1 (ko) | 1966-03-24 | 1970-01-09 | ||
| JPS463712B1 (ko) | 1966-04-14 | 1971-01-29 | ||
| US3526501A (en) | 1967-02-03 | 1970-09-01 | Eastman Kodak Co | 4-diarylamino-substituted chalcone containing photoconductive compositions for use in electrophotography |
| US3542544A (en) | 1967-04-03 | 1970-11-24 | Eastman Kodak Co | Photoconductive elements containing organic photoconductors of the triarylalkane and tetraarylmethane types |
| US3658520A (en) | 1968-02-20 | 1972-04-25 | Eastman Kodak Co | Photoconductive elements containing as photoconductors triarylamines substituted by active hydrogen-containing groups |
| US3567450A (en) | 1968-02-20 | 1971-03-02 | Eastman Kodak Co | Photoconductive elements containing substituted triarylamine photoconductors |
| US3615404A (en) | 1968-04-25 | 1971-10-26 | Scott Paper Co | 1 3-phenylenediamine containing photoconductive materials |
| CA917980A (en) | 1969-06-20 | 1973-01-02 | J. Fox Charles | Alkylaminoaromatic organic photoconductors |
| US3717462A (en) | 1969-07-28 | 1973-02-20 | Canon Kk | Heat treatment of an electrophotographic photosensitive member |
| BE756375A (fr) | 1969-09-30 | 1971-03-01 | Eastman Kodak Co | Nouvelle composition photoconductrice et produit la contenant utilisables en electrophotographie |
| BE756943A (fr) | 1969-10-01 | 1971-03-16 | Eastman Kodak Co | Nouvelles compositions photoconductrices et produits les contenant, utilisables notamment en electrophotographie |
| JPS4725336B1 (ko) | 1969-11-26 | 1972-07-11 | ||
| JPS5110983B2 (ko) | 1971-09-10 | 1976-04-08 | ||
| GB1413352A (en) | 1972-02-09 | 1975-11-12 | Scott Paper Co | Electrophotographic material |
| US3837851A (en) | 1973-01-15 | 1974-09-24 | Ibm | Photoconductor overcoated with triarylpyrazoline charge transport layer |
| GB1505409A (en) | 1974-12-20 | 1978-03-30 | Eastman Kodak Co | Photoconductive compositions |
| US4127412A (en) | 1975-12-09 | 1978-11-28 | Eastman Kodak Company | Photoconductive compositions and elements |
| US4012376A (en) | 1975-12-29 | 1977-03-15 | Eastman Kodak Company | Photosensitive colorant materials |
| CA1104866A (en) | 1976-08-23 | 1981-07-14 | Milan Stolka | Imaging member containing a substituted n,n,n',n',- tetraphenyl-[1,1'-biphenyl]-4,4'-diamine in the chargge transport layer |
| US4175961A (en) | 1976-12-22 | 1979-11-27 | Eastman Kodak Company | Multi-active photoconductive elements |
| US4123269A (en) | 1977-09-29 | 1978-10-31 | Xerox Corporation | Electrostatographic photosensitive device comprising hole injecting and hole transport layers |
| JPS5453435A (en) | 1977-10-01 | 1979-04-26 | Yoshikatsu Kume | Portable bicycle equipped with foldable type triangle frame |
| US4150987A (en) | 1977-10-17 | 1979-04-24 | International Business Machines Corporation | Hydrazone containing charge transport element and photoconductive process of using same |
| JPS5464299A (en) | 1977-10-29 | 1979-05-23 | Toshiba Corp | Beam deflector for charged particles |
| JPS54112637A (en) | 1978-02-06 | 1979-09-03 | Ricoh Co Ltd | Electrophotographic photoreceptor |
| JPS54110837A (en) | 1978-02-17 | 1979-08-30 | Ricoh Co Ltd | Electrophotographic photoreceptor |
| JPS54110536A (en) | 1978-02-20 | 1979-08-30 | Ichikoh Ind Ltd | Device for time-lag putting out room lamp for motorcar |
| JPS54119925A (en) | 1978-03-10 | 1979-09-18 | Ricoh Co Ltd | Photosensitive material for electrophotography |
| US4251612A (en) | 1978-05-12 | 1981-02-17 | Xerox Corporation | Dielectric overcoated photoresponsive imaging member |
| JPS6028342B2 (ja) | 1978-06-21 | 1985-07-04 | コニカ株式会社 | 電子写真感光体 |
| JPS6060052B2 (ja) | 1978-07-21 | 1985-12-27 | コニカ株式会社 | 電子写真感光体 |
| JPS5551086A (en) | 1978-09-04 | 1980-04-14 | Copyer Co Ltd | Novel pyrazoline compound, its preparation, and electrophotographic photosensitive substance comprising it |
| JPS5546760A (en) | 1978-09-29 | 1980-04-02 | Ricoh Co Ltd | Electrophotographic photoreceptor |
| JPS5552063A (en) | 1978-10-13 | 1980-04-16 | Ricoh Co Ltd | Electrophotographic receptor |
| JPS5552064A (en) | 1978-10-13 | 1980-04-16 | Ricoh Co Ltd | Electrophotographic receptor |
| JPS5574546A (en) | 1978-11-30 | 1980-06-05 | Ricoh Co Ltd | Electrophotographic photoreceptor |
| US4306008A (en) | 1978-12-04 | 1981-12-15 | Xerox Corporation | Imaging system with a diamine charge transport material in a polycarbonate resin |
| JPS5588064A (en) | 1978-12-05 | 1980-07-03 | Konishiroku Photo Ind Co Ltd | Electrophotographic receptor |
| JPS5588065A (en) | 1978-12-12 | 1980-07-03 | Konishiroku Photo Ind Co Ltd | Electrophotographic receptor |
| JPS5585495A (en) | 1978-12-18 | 1980-06-27 | Pacific Metals Co Ltd | Method of composting organic waste |
| JPS55108667A (en) | 1979-02-13 | 1980-08-21 | Ricoh Co Ltd | Electrophotographic receptor |
| US4233384A (en) | 1979-04-30 | 1980-11-11 | Xerox Corporation | Imaging system using novel charge transport layer |
| JPS6035058B2 (ja) | 1979-05-17 | 1985-08-12 | 三菱製紙株式会社 | 有機光半導体電子写真材料 |
| JPS564148A (en) | 1979-06-21 | 1981-01-17 | Konishiroku Photo Ind Co Ltd | Electrophotographic receptor |
| JPS5622437A (en) | 1979-08-01 | 1981-03-03 | Ricoh Co Ltd | Electrophotographic receptor |
| US4232103A (en) | 1979-08-27 | 1980-11-04 | Xerox Corporation | Phenyl benzotriazole stabilized photosensitive device |
| JPS5636656A (en) | 1979-09-03 | 1981-04-09 | Mitsubishi Paper Mills Ltd | Electrophotographic material |
| JPS5646234A (en) | 1979-09-21 | 1981-04-27 | Ricoh Co Ltd | Electrophotographic receptor |
| US4273846A (en) | 1979-11-23 | 1981-06-16 | Xerox Corporation | Imaging member having a charge transport layer of a terphenyl diamine and a polycarbonate resin |
| JPS5680051A (en) | 1979-12-04 | 1981-07-01 | Ricoh Co Ltd | Electrophotographic receptor |
| JPS5688141A (en) | 1979-12-20 | 1981-07-17 | Konishiroku Photo Ind Co Ltd | Electrophotographic receptor |
| JPS6034099B2 (ja) | 1980-06-24 | 1985-08-07 | 富士写真フイルム株式会社 | 電子写真感光体 |
| US4356429A (en) | 1980-07-17 | 1982-10-26 | Eastman Kodak Company | Organic electroluminescent cell |
| JPS6059590B2 (ja) | 1980-09-03 | 1985-12-25 | 三菱製紙株式会社 | 電子写真感光体 |
| JPS57148749A (en) | 1981-03-11 | 1982-09-14 | Fuji Photo Film Co Ltd | Electrophotographic receptor |
| JPS6093445A (ja) | 1983-10-28 | 1985-05-25 | Ricoh Co Ltd | 電子写真用感光体 |
| JPS6094462A (ja) | 1983-10-28 | 1985-05-27 | Ricoh Co Ltd | スチルベン誘導体及びその製造法 |
| JPS60175052A (ja) | 1984-02-21 | 1985-09-09 | Ricoh Co Ltd | 電子写真用感光体 |
| JPS60174749A (ja) | 1984-02-21 | 1985-09-09 | Ricoh Co Ltd | スチリル化合物及びその製造法 |
| JPS6114642A (ja) | 1984-06-29 | 1986-01-22 | Konishiroku Photo Ind Co Ltd | 電子写真感光体 |
| JPS6172255A (ja) | 1984-09-14 | 1986-04-14 | Konishiroku Photo Ind Co Ltd | 電子写真感光体 |
| US4665000A (en) | 1984-10-19 | 1987-05-12 | Xerox Corporation | Photoresponsive devices containing aromatic ether hole transport layers |
| JPS61210363A (ja) | 1985-03-15 | 1986-09-18 | Canon Inc | 電子写真感光体 |
| JPS61228451A (ja) | 1985-04-03 | 1986-10-11 | Canon Inc | 電子写真感光体 |
| US4588666A (en) | 1985-06-24 | 1986-05-13 | Xerox Corporation | Photoconductive imaging members with alkoxy amine charge transport molecules |
| JPS6210652A (ja) | 1985-07-08 | 1987-01-19 | Minolta Camera Co Ltd | 感光体 |
| JPS6230255A (ja) | 1985-07-31 | 1987-02-09 | Minolta Camera Co Ltd | 電子写真感光体 |
| JPS6236674A (ja) | 1985-08-05 | 1987-02-17 | Fuji Photo Film Co Ltd | 電子写真感光体 |
| JPS6247646A (ja) | 1985-08-27 | 1987-03-02 | Konishiroku Photo Ind Co Ltd | 感光体 |
| US4720432A (en) | 1987-02-11 | 1988-01-19 | Eastman Kodak Company | Electroluminescent device with organic luminescent medium |
| JPS63256965A (ja) | 1987-04-15 | 1988-10-24 | Canon Inc | 静電荷像現像用トナ− |
| JPH01211399A (ja) | 1988-02-19 | 1989-08-24 | Toshiba Corp | スキャン機能付きダイナミックシフトレジスタ |
| JPH02282263A (ja) | 1988-12-09 | 1990-11-19 | Nippon Oil Co Ltd | ホール輸送材料 |
| JP2727620B2 (ja) | 1989-02-01 | 1998-03-11 | 日本電気株式会社 | 有機薄膜el素子 |
| US5653713A (en) | 1989-04-24 | 1997-08-05 | Michelson; Gary Karlin | Surgical rongeur |
| US4950950A (en) | 1989-05-18 | 1990-08-21 | Eastman Kodak Company | Electroluminescent device with silazane-containing luminescent zone |
| JPH02311591A (ja) | 1989-05-25 | 1990-12-27 | Mitsubishi Kasei Corp | 有機電界発光素子 |
| JP2897138B2 (ja) | 1989-06-30 | 1999-05-31 | 株式会社リコー | 電界発光素子 |
| US5061569A (en) | 1990-07-26 | 1991-10-29 | Eastman Kodak Company | Electroluminescent device with organic electroluminescent medium |
| JP3016896B2 (ja) | 1991-04-08 | 2000-03-06 | パイオニア株式会社 | 有機エレクトロルミネッセンス素子 |
| JPH07138561A (ja) | 1993-11-17 | 1995-05-30 | Idemitsu Kosan Co Ltd | 有機エレクトロルミネッセンス素子 |
| JP2988819B2 (ja) | 1993-12-24 | 1999-12-13 | シャープ株式会社 | 回路内蔵受光素子の作製方法 |
| JP3816969B2 (ja) | 1994-04-26 | 2006-08-30 | Tdk株式会社 | 有機el素子 |
| JP3306735B2 (ja) | 1995-01-19 | 2002-07-24 | 出光興産株式会社 | 有機電界発光素子及び有機薄膜 |
| JP3724833B2 (ja) | 1995-03-06 | 2005-12-07 | 出光興産株式会社 | 有機エレクトロルミネッセンス素子 |
| JP4070274B2 (ja) | 1996-11-07 | 2008-04-02 | 三井化学株式会社 | 有機電界発光素子 |
| JP3853042B2 (ja) | 1996-11-07 | 2006-12-06 | 三井化学株式会社 | 有機電界発光素子 |
| JP3899566B2 (ja) | 1996-11-25 | 2007-03-28 | セイコーエプソン株式会社 | 有機el表示装置の製造方法 |
| JP3794819B2 (ja) | 1997-04-18 | 2006-07-12 | 三井化学株式会社 | フルオランテン誘導体および有機電界発光素子 |
| US5935721A (en) * | 1998-03-20 | 1999-08-10 | Eastman Kodak Company | Organic electroluminescent elements for stable electroluminescent |
| JP3716096B2 (ja) | 1998-04-02 | 2005-11-16 | 三菱重工業株式会社 | 微粉炭セパレータ装置 |
| JP3794846B2 (ja) | 1998-12-17 | 2006-07-12 | 三井化学株式会社 | 炭化水素化合物および有機電界発光素子 |
| JP3794847B2 (ja) | 1998-12-21 | 2006-07-12 | 三井化学株式会社 | 炭化水素化合物および有機電界発光素子 |
| EP1757670A3 (en) * | 1999-09-30 | 2007-03-21 | Idemitsu Kosan Company Limited | Organic electroluminescent element |
| JP3905265B2 (ja) | 1999-10-21 | 2007-04-18 | 富士フイルム株式会社 | 有機エレクトロルミネッセンス素子 |
| US6866947B1 (en) * | 1999-12-28 | 2005-03-15 | Idemitsu Kosan Co., Ltd. | Organic electroluminescence device emitting white light |
| JP4255610B2 (ja) * | 1999-12-28 | 2009-04-15 | 出光興産株式会社 | 白色系有機エレクトロルミネッセンス素子 |
| JP4473413B2 (ja) | 2000-06-06 | 2010-06-02 | 三井化学株式会社 | 炭化水素化合物および有機電界発光素子 |
| JP4536880B2 (ja) | 2000-07-18 | 2010-09-01 | キヤノン株式会社 | 情報処理システム及びその制御方法、情報処理装置及び方法、並びに記憶媒体 |
| JP3961200B2 (ja) | 2000-07-25 | 2007-08-22 | 三星エスディアイ株式会社 | 有機エレクトロルミネッセンス素子 |
| JP2002063988A (ja) | 2000-08-22 | 2002-02-28 | Toray Ind Inc | 発光素子 |
| JP4562884B2 (ja) | 2000-08-25 | 2010-10-13 | 出光興産株式会社 | 有機エレクトロルミネッセンス素子 |
| EP1347031A4 (en) | 2000-09-07 | 2007-07-04 | Idemitsu Kosan Co | ORGANIC ELECTROLUMINESCENT ELEMENT |
| US7097917B1 (en) * | 2001-04-19 | 2006-08-29 | Tdk Corporation | Compounds for use in organic EL devices and organic EL devices |
| JP2002324678A (ja) | 2001-04-26 | 2002-11-08 | Fuji Photo Film Co Ltd | 発光素子 |
| JP2003272862A (ja) | 2002-03-13 | 2003-09-26 | Fuji Photo Film Co Ltd | 発光素子 |
| JP2004002351A (ja) | 2002-03-27 | 2004-01-08 | Tdk Corp | 有機el素子 |
| US6841267B2 (en) * | 2002-04-24 | 2005-01-11 | Eastman Kodak Company | Efficient electroluminescent device |
| TWI314947B (en) * | 2002-04-24 | 2009-09-21 | Eastman Kodak Compan | Organic light emitting diode devices with improved operational stability |
| JP2004075567A (ja) | 2002-08-12 | 2004-03-11 | Idemitsu Kosan Co Ltd | オリゴアリーレン誘導体及びそれを利用した有機エレクトロルミネッセンス素子 |
| CN101628847B (zh) | 2002-08-23 | 2013-05-29 | 出光兴产株式会社 | 有机电致发光器件和蒽衍生物 |
| JP4585750B2 (ja) | 2002-08-27 | 2010-11-24 | キヤノン株式会社 | 縮合多環化合物及びそれを用いた有機発光素子 |
| JP3902993B2 (ja) | 2002-08-27 | 2007-04-11 | キヤノン株式会社 | フルオレン化合物及びそれを用いた有機発光素子 |
| US20040049754A1 (en) * | 2002-09-06 | 2004-03-11 | Sun Microsystems, Inc. | Method and apparatus for filling and connecting filler material in a layout |
| WO2004063159A1 (ja) | 2003-01-10 | 2004-07-29 | Idemitsu Kosan Co., Ltd. | 含窒素複素環誘導体及びそれを用いた有機エレクトロルミネッセンス素子 |
| JP3984190B2 (ja) | 2003-05-30 | 2007-10-03 | Tdk株式会社 | 有機el素子 |
| JP4400134B2 (ja) | 2003-07-31 | 2010-01-20 | Tdk株式会社 | 有機el素子用化合物及び有機el素子 |
| JP4059822B2 (ja) | 2003-08-26 | 2008-03-12 | 三井化学株式会社 | ベンゾフルオランテン化合物、および該ベンゾフルオランテン化合物を含有する有機電界発光素子 |
| DE10345583A1 (de) | 2003-09-29 | 2005-05-19 | Basf Ag | Synthese von phenylsubstituierten Fluoranthenen durch Diels-Alder-Reaktion und ihre Verwendung |
| JPWO2005061656A1 (ja) | 2003-12-19 | 2007-07-12 | 出光興産株式会社 | 有機エレクトロルミネッセンス素子用発光材料、それを利用した有機エレクトロルミネッセンス素子及び有機エレクトロルミネッセンス素子用材料 |
| JP4674454B2 (ja) | 2004-01-27 | 2011-04-20 | ソニー株式会社 | 有機発光材料および有機電界発光素子 |
| US7368624B2 (en) | 2004-03-30 | 2008-05-06 | Eastman Kodak Company | Synthesis for polycyclic aromatic hydrocarbon compounds |
| CN1960957A (zh) | 2004-05-27 | 2007-05-09 | 出光兴产株式会社 | 不对称芘衍生物以及使用该衍生物的有机电致发光器件 |
| JP5084208B2 (ja) * | 2006-09-15 | 2012-11-28 | 出光興産株式会社 | 有機エレクトロルミネッセンス素子及び有機エレクトロルミネッセンス素子用材料 |
| US8294142B2 (en) * | 2007-07-07 | 2012-10-23 | Idemitsu Kosan Co., Ltd. | Organic EL device |
-
2007
- 2007-02-27 US US11/679,531 patent/US9214636B2/en active Active
- 2007-02-28 JP JP2008502825A patent/JP5199066B2/ja not_active Expired - Fee Related
- 2007-02-28 EP EP07737525.1A patent/EP1990844B1/en not_active Not-in-force
- 2007-02-28 CN CN2011103730708A patent/CN102394273A/zh active Pending
- 2007-02-28 KR KR1020087021039A patent/KR101406631B1/ko active IP Right Grant
- 2007-02-28 CN CN2007800068553A patent/CN101390230B/zh not_active Expired - Fee Related
- 2007-02-28 WO PCT/JP2007/053806 patent/WO2007100010A1/ja active Application Filing
- 2007-03-01 TW TW096107028A patent/TWI433595B/zh not_active IP Right Cessation
-
2013
- 2013-01-10 US US13/738,372 patent/US20130221333A1/en not_active Abandoned
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2003026616A (ja) * | 2001-04-19 | 2003-01-29 | Tdk Corp | 有機el素子用化合物、有機el素子 |
Also Published As
| Publication number | Publication date |
|---|---|
| CN102394273A (zh) | 2012-03-28 |
| TW200746895A (en) | 2007-12-16 |
| JP5199066B2 (ja) | 2013-05-15 |
| US20070243411A1 (en) | 2007-10-18 |
| EP1990844B1 (en) | 2016-07-20 |
| EP1990844A1 (en) | 2008-11-12 |
| KR20080114702A (ko) | 2008-12-31 |
| JPWO2007100010A1 (ja) | 2009-07-23 |
| EP1990844A4 (en) | 2010-05-26 |
| CN101390230A (zh) | 2009-03-18 |
| US20130221333A1 (en) | 2013-08-29 |
| WO2007100010A1 (ja) | 2007-09-07 |
| CN101390230B (zh) | 2011-12-14 |
| TWI433595B (zh) | 2014-04-01 |
| US9214636B2 (en) | 2015-12-15 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR101406631B1 (ko) | 유기 전기 발광 소자 | |
| KR101422864B1 (ko) | 복소환 함유 아릴아민 유도체를 이용한 유기 전계발광 소자 | |
| KR101008769B1 (ko) | 유기 전기발광 소자 | |
| KR101663325B1 (ko) | 유기 일렉트로 루미네선스 소자 및 유기 일렉트로 루미네선스 소자용 재료 | |
| TWI432553B (zh) | Fluoranthene compounds and organic electroluminescent elements using the fluoranthene compounds and solutions containing organic electroluminescent materials | |
| KR101290027B1 (ko) | 질소 함유 헤테로환 유도체 및 그것을 사용한 유기전기발광 소자 | |
| TWI361020B (ko) | ||
| KR101597855B1 (ko) | 유기 발광 소자 및 이에 사용하기 위한 재료 | |
| KR100900375B1 (ko) | 유기 전자발광 소자 | |
| JP4481930B2 (ja) | 白色系有機エレクトロルミネッセンス素子 | |
| KR101026627B1 (ko) | 방향족 아민 유도체 및 이를 이용한 유기 전기발광 소자 | |
| EP1559706A1 (en) | Aromatic amine derivative and organic electroluminescent element employing the same | |
| JP5249654B2 (ja) | フルオランテン誘導体を用いた有機エレクトロルミネッセンス素子 | |
| WO2009102054A1 (ja) | 有機発光媒体および有機el素子 | |
| KR20060014410A (ko) | 유기 전기발광 소자 및 표시 장치 | |
| EP1762553A1 (en) | Polycyclic aromatic compound, material for forming luminescent coating film and organic electroluminescent device using same | |
| WO2010013675A1 (ja) | 有機発光媒体及び有機el素子 | |
| JP2008162921A (ja) | ベンゾチアジアゾール誘導体及びそれを用いた有機エレクトロルミネッセンス素子用 | |
| JP5325484B2 (ja) | 有機エレクトロルミネッセンス素子 | |
| KR20080098376A (ko) | 적색계 유기 전기발광 소자 | |
| JP2008069128A (ja) | 有機エレクトロルミネッセンス素子及び有機エレクトロルミネッセンス素子用材料 | |
| JP5525702B2 (ja) | インデノペリレン誘導体を用いた有機エレクトロルミネッセンス素子 | |
| TW200911017A (en) | Organic electroluminescence device | |
| KR20060009932A (ko) | 스파이로 결합 함유 화합물, 발광성 도막 형성용 재료 및이를 이용한 유기 전기발광 소자 | |
| JP5319287B2 (ja) | 芳香族アミン誘導体及びそれを用いた有機エレクトロルミネッセンス素子 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A201 | Request for examination | ||
| E701 | Decision to grant or registration of patent right | ||
| GRNT | Written decision to grant | ||
| FPAY | Annual fee payment |
Payment date: 20170522 Year of fee payment: 4 |
|
| FPAY | Annual fee payment |
Payment date: 20180517 Year of fee payment: 5 |
|
| FPAY | Annual fee payment |
Payment date: 20190515 Year of fee payment: 6 |