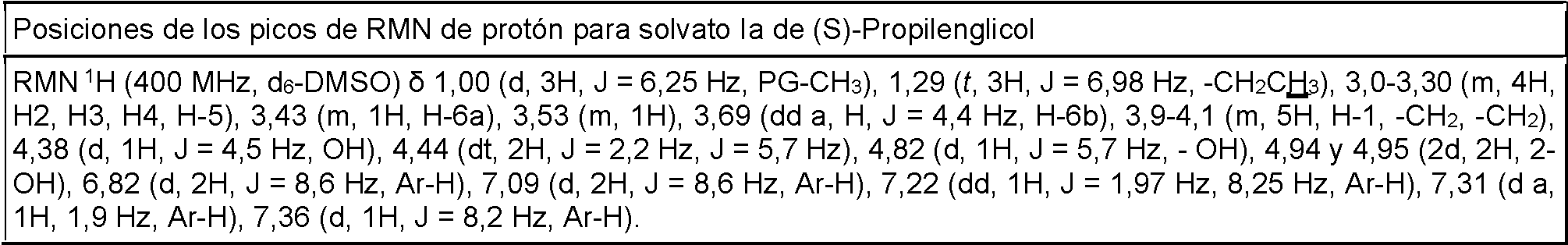
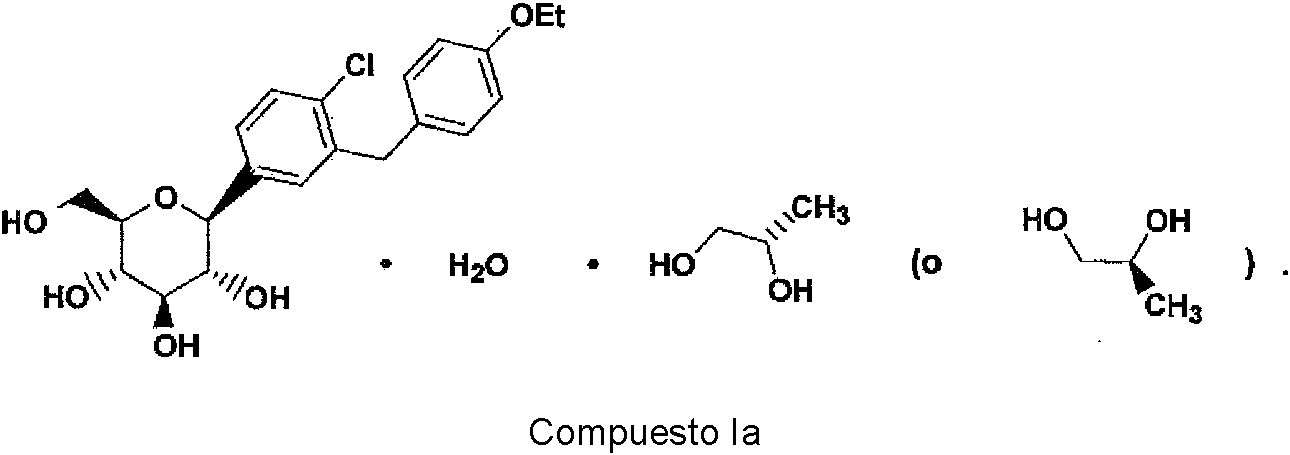
ES2769130T3 - Composición farmacéutica que comprende un solvato de (S)-propilenglicol de (2S,3R,4S,5S,6R)-2-[4-cloro-3-(4-etoxi-bencil)-fenil]-6-hidroximetil-2-metoxi-tetrahidro-piran-3,4,5-triol cristalino. - Google Patents
Composición farmacéutica que comprende un solvato de (S)-propilenglicol de (2S,3R,4S,5S,6R)-2-[4-cloro-3-(4-etoxi-bencil)-fenil]-6-hidroximetil-2-metoxi-tetrahidro-piran-3,4,5-triol cristalino. Download PDFInfo
- Publication number
- ES2769130T3 ES2769130T3 ES17203302T ES17203302T ES2769130T3 ES 2769130 T3 ES2769130 T3 ES 2769130T3 ES 17203302 T ES17203302 T ES 17203302T ES 17203302 T ES17203302 T ES 17203302T ES 2769130 T3 ES2769130 T3 ES 2769130T3
- Authority
- ES
- Spain
- Prior art keywords
- compound
- pharmaceutical composition
- propylene glycol
- crystalline
- solvate
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 239000012453 solvate Substances 0.000 title claims abstract description 66
- DNIAPMSPPWPWGF-VKHMYHEASA-N (+)-propylene glycol Chemical compound C[C@H](O)CO DNIAPMSPPWPWGF-VKHMYHEASA-N 0.000 title claims abstract description 28
- 229960004463 (s)- propylene glycol Drugs 0.000 title claims abstract description 27
- 239000008194 pharmaceutical composition Substances 0.000 title claims abstract description 20
- -1 4-ethoxy-benzyl Chemical group 0.000 title description 34
- 239000013078 crystal Substances 0.000 claims description 64
- 238000000634 powder X-ray diffraction Methods 0.000 claims description 22
- 239000007787 solid Substances 0.000 claims description 17
- 239000003814 drug Substances 0.000 claims description 16
- 238000000113 differential scanning calorimetry Methods 0.000 claims description 11
- 238000005259 measurement Methods 0.000 claims description 11
- 238000001757 thermogravimetry curve Methods 0.000 claims description 7
- 239000003472 antidiabetic agent Substances 0.000 claims description 6
- 229940124597 therapeutic agent Drugs 0.000 claims description 6
- 229910052799 carbon Inorganic materials 0.000 claims description 5
- 229940125708 antidiabetic agent Drugs 0.000 claims description 4
- 239000003795 chemical substances by application Substances 0.000 claims description 4
- 230000000879 anti-atherosclerotic effect Effects 0.000 claims description 3
- 239000000883 anti-obesity agent Substances 0.000 claims description 3
- 229940030600 antihypertensive agent Drugs 0.000 claims description 3
- 239000002220 antihypertensive agent Substances 0.000 claims description 3
- 229940125710 antiobesity agent Drugs 0.000 claims description 3
- 150000002632 lipids Chemical class 0.000 claims description 3
- 230000004580 weight loss Effects 0.000 claims description 2
- 238000001460 carbon-13 nuclear magnetic resonance spectrum Methods 0.000 claims 2
- 239000003085 diluting agent Substances 0.000 claims 1
- 239000003937 drug carrier Substances 0.000 claims 1
- 150000001875 compounds Chemical class 0.000 description 121
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 101
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 92
- 239000000203 mixture Substances 0.000 description 54
- DLDJFQGPPSQZKI-UHFFFAOYSA-N but-2-yne-1,4-diol Chemical compound OCC#CCO DLDJFQGPPSQZKI-UHFFFAOYSA-N 0.000 description 36
- 239000003112 inhibitor Substances 0.000 description 31
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 28
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 27
- 238000000034 method Methods 0.000 description 26
- IMNFDUFMRHMDMM-UHFFFAOYSA-N N-Heptane Chemical compound CCCCCCC IMNFDUFMRHMDMM-UHFFFAOYSA-N 0.000 description 24
- 238000006243 chemical reaction Methods 0.000 description 23
- 239000000047 product Substances 0.000 description 22
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 21
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 18
- 238000002360 preparation method Methods 0.000 description 18
- 229940125890 compound Ia Drugs 0.000 description 16
- 239000000725 suspension Substances 0.000 description 16
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 16
- BXGYYDRIMBPOMN-UHFFFAOYSA-N 2-(hydroxymethoxy)ethoxymethanol Chemical compound OCOCCOCO BXGYYDRIMBPOMN-UHFFFAOYSA-N 0.000 description 15
- 239000011541 reaction mixture Substances 0.000 description 14
- AQRLNPVMDITEJU-UHFFFAOYSA-N triethylsilane Chemical compound CC[SiH](CC)CC AQRLNPVMDITEJU-UHFFFAOYSA-N 0.000 description 14
- 239000012071 phase Substances 0.000 description 13
- 102000001494 Sterol O-Acyltransferase Human genes 0.000 description 12
- 108010054082 Sterol O-acyltransferase Proteins 0.000 description 12
- 238000005859 coupling reaction Methods 0.000 description 12
- 238000002425 crystallisation Methods 0.000 description 12
- 230000008025 crystallization Effects 0.000 description 12
- 239000002904 solvent Substances 0.000 description 12
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 11
- 229940126062 Compound A Drugs 0.000 description 11
- NLDMNSXOCDLTTB-UHFFFAOYSA-N Heterophylliin A Natural products O1C2COC(=O)C3=CC(O)=C(O)C(O)=C3C3=C(O)C(O)=C(O)C=C3C(=O)OC2C(OC(=O)C=2C=C(O)C(O)=C(O)C=2)C(O)C1OC(=O)C1=CC(O)=C(O)C(O)=C1 NLDMNSXOCDLTTB-UHFFFAOYSA-N 0.000 description 11
- 210000004027 cell Anatomy 0.000 description 10
- 235000019439 ethyl acetate Nutrition 0.000 description 10
- GWYFCOCPABKNJV-UHFFFAOYSA-N isovaleric acid Chemical compound CC(C)CC(O)=O GWYFCOCPABKNJV-UHFFFAOYSA-N 0.000 description 10
- 230000008569 process Effects 0.000 description 10
- 238000003756 stirring Methods 0.000 description 10
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 9
- 108091006269 SLC5A2 Proteins 0.000 description 9
- 102000058081 Sodium-Glucose Transporter 2 Human genes 0.000 description 9
- 239000000556 agonist Substances 0.000 description 9
- 229940079593 drug Drugs 0.000 description 9
- 230000000694 effects Effects 0.000 description 9
- 239000008103 glucose Substances 0.000 description 9
- 238000004128 high performance liquid chromatography Methods 0.000 description 9
- 238000002411 thermogravimetry Methods 0.000 description 9
- XDTMQSROBMDMFD-UHFFFAOYSA-N Cyclohexane Chemical compound C1CCCCC1 XDTMQSROBMDMFD-UHFFFAOYSA-N 0.000 description 8
- 239000003153 chemical reaction reagent Substances 0.000 description 8
- 238000006138 lithiation reaction Methods 0.000 description 8
- 230000003068 static effect Effects 0.000 description 8
- CXBDYQVECUFKRK-UHFFFAOYSA-N 1-methoxybutane Chemical compound CCCCOC CXBDYQVECUFKRK-UHFFFAOYSA-N 0.000 description 7
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 7
- 239000000543 intermediate Substances 0.000 description 7
- 239000011734 sodium Substances 0.000 description 7
- 239000000243 solution Substances 0.000 description 7
- DNIAPMSPPWPWGF-GSVOUGTGSA-N (R)-(-)-Propylene glycol Chemical compound C[C@@H](O)CO DNIAPMSPPWPWGF-GSVOUGTGSA-N 0.000 description 6
- 229940095131 (r)- propylene glycol Drugs 0.000 description 6
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 6
- WFDIJRYMOXRFFG-UHFFFAOYSA-N Acetic anhydride Chemical compound CC(=O)OC(C)=O WFDIJRYMOXRFFG-UHFFFAOYSA-N 0.000 description 6
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 6
- DKPFZGUDAPQIHT-UHFFFAOYSA-N Butyl acetate Natural products CCCCOC(C)=O DKPFZGUDAPQIHT-UHFFFAOYSA-N 0.000 description 6
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 6
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 6
- 230000015572 biosynthetic process Effects 0.000 description 6
- 235000012970 cakes Nutrition 0.000 description 6
- 206010012601 diabetes mellitus Diseases 0.000 description 6
- FUZZWVXGSFPDMH-UHFFFAOYSA-N hexanoic acid Chemical compound CCCCCC(O)=O FUZZWVXGSFPDMH-UHFFFAOYSA-N 0.000 description 6
- JMMWKPVZQRWMSS-UHFFFAOYSA-N isopropanol acetate Natural products CC(C)OC(C)=O JMMWKPVZQRWMSS-UHFFFAOYSA-N 0.000 description 6
- 229940011051 isopropyl acetate Drugs 0.000 description 6
- 229910052744 lithium Inorganic materials 0.000 description 6
- 239000003960 organic solvent Substances 0.000 description 6
- 238000001144 powder X-ray diffraction data Methods 0.000 description 6
- 102000009515 Arachidonate 15-Lipoxygenase Human genes 0.000 description 5
- 108010048907 Arachidonate 15-lipoxygenase Proteins 0.000 description 5
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 5
- 239000002841 Lewis acid Substances 0.000 description 5
- BZLVMXJERCGZMT-UHFFFAOYSA-N Methyl tert-butyl ether Chemical compound COC(C)(C)C BZLVMXJERCGZMT-UHFFFAOYSA-N 0.000 description 5
- 239000005557 antagonist Substances 0.000 description 5
- 229910052796 boron Inorganic materials 0.000 description 5
- 230000008878 coupling Effects 0.000 description 5
- 150000007517 lewis acids Chemical class 0.000 description 5
- 238000004519 manufacturing process Methods 0.000 description 5
- 238000010899 nucleation Methods 0.000 description 5
- 238000000371 solid-state nuclear magnetic resonance spectroscopy Methods 0.000 description 5
- 239000011877 solvent mixture Substances 0.000 description 5
- JYVXNLLUYHCIIH-UHFFFAOYSA-N (+/-)-mevalonolactone Natural products CC1(O)CCOC(=O)C1 JYVXNLLUYHCIIH-UHFFFAOYSA-N 0.000 description 4
- VHYFNPMBLIVWCW-UHFFFAOYSA-N 4-Dimethylaminopyridine Chemical compound CN(C)C1=CC=NC=C1 VHYFNPMBLIVWCW-UHFFFAOYSA-N 0.000 description 4
- 201000001320 Atherosclerosis Diseases 0.000 description 4
- 229940121710 HMGCoA reductase inhibitor Drugs 0.000 description 4
- ONIBWKKTOPOVIA-BYPYZUCNSA-N L-Proline Chemical compound OC(=O)[C@@H]1CCCN1 ONIBWKKTOPOVIA-BYPYZUCNSA-N 0.000 description 4
- 229930182821 L-proline Natural products 0.000 description 4
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 4
- 238000002441 X-ray diffraction Methods 0.000 description 4
- 239000003524 antilipemic agent Substances 0.000 description 4
- 239000002585 base Substances 0.000 description 4
- 239000003638 chemical reducing agent Substances 0.000 description 4
- 238000010168 coupling process Methods 0.000 description 4
- 238000013461 design Methods 0.000 description 4
- 201000010099 disease Diseases 0.000 description 4
- VYFYYTLLBUKUHU-UHFFFAOYSA-N dopamine Chemical compound NCCC1=CC=C(O)C(O)=C1 VYFYYTLLBUKUHU-UHFFFAOYSA-N 0.000 description 4
- 230000009977 dual effect Effects 0.000 description 4
- 238000010438 heat treatment Methods 0.000 description 4
- 230000005764 inhibitory process Effects 0.000 description 4
- 210000003734 kidney Anatomy 0.000 description 4
- 239000007788 liquid Substances 0.000 description 4
- 229940057061 mevalonolactone Drugs 0.000 description 4
- 125000000896 monocarboxylic acid group Chemical group 0.000 description 4
- 229910052757 nitrogen Inorganic materials 0.000 description 4
- DHHVAGZRUROJKS-UHFFFAOYSA-N phentermine Chemical compound CC(C)(N)CC1=CC=CC=C1 DHHVAGZRUROJKS-UHFFFAOYSA-N 0.000 description 4
- 238000012545 processing Methods 0.000 description 4
- 229960002429 proline Drugs 0.000 description 4
- 238000010791 quenching Methods 0.000 description 4
- 230000000171 quenching effect Effects 0.000 description 4
- 230000035484 reaction time Effects 0.000 description 4
- 102000005962 receptors Human genes 0.000 description 4
- 108020003175 receptors Proteins 0.000 description 4
- QZAYGJVTTNCVMB-UHFFFAOYSA-N serotonin Chemical compound C1=C(O)C=C2C(CCN)=CNC2=C1 QZAYGJVTTNCVMB-UHFFFAOYSA-N 0.000 description 4
- 239000004059 squalene synthase inhibitor Substances 0.000 description 4
- 208000001072 type 2 diabetes mellitus Diseases 0.000 description 4
- USFZMSVCRYTOJT-UHFFFAOYSA-N Ammonium acetate Chemical compound N.CC(O)=O USFZMSVCRYTOJT-UHFFFAOYSA-N 0.000 description 3
- KZMGYPLQYOPHEL-UHFFFAOYSA-N Boron trifluoride etherate Chemical compound FB(F)F.CCOCC KZMGYPLQYOPHEL-UHFFFAOYSA-N 0.000 description 3
- 208000002249 Diabetes Complications Diseases 0.000 description 3
- 206010012655 Diabetic complications Diseases 0.000 description 3
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 3
- DTHNMHAUYICORS-KTKZVXAJSA-N Glucagon-like peptide 1 Chemical compound C([C@@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](C)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CCCCN)C(=O)NCC(=O)N[C@@H](CCCNC(N)=N)C(N)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCCCN)NC(=O)[C@H](C)NC(=O)[C@H](C)NC(=O)[C@H](CCC(N)=O)NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@@H](NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C)NC(=O)[C@@H](N)CC=1N=CNC=1)[C@@H](C)O)[C@@H](C)O)C(C)C)C1=CC=CC=C1 DTHNMHAUYICORS-KTKZVXAJSA-N 0.000 description 3
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 3
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 3
- 206010022489 Insulin Resistance Diseases 0.000 description 3
- YSDQQAXHVYUZIW-QCIJIYAXSA-N Liraglutide Chemical compound C([C@@H](C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(O)=O)C(=O)NCC(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](C)C(=O)N[C@@H](C)C(=O)N[C@@H](CCCCNC(=O)CC[C@H](NC(=O)CCCCCCCCCCCCCCC)C(O)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](C)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)NCC(=O)N[C@@H](CCCNC(N)=N)C(=O)NCC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@@H](NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C)NC(=O)[C@@H](N)CC=1NC=NC=1)[C@@H](C)O)[C@@H](C)O)C(C)C)C1=CC=C(O)C=C1 YSDQQAXHVYUZIW-QCIJIYAXSA-N 0.000 description 3
- 108010016731 PPAR gamma Proteins 0.000 description 3
- KWYUFKZDYYNOTN-UHFFFAOYSA-M Potassium hydroxide Chemical compound [OH-].[K+] KWYUFKZDYYNOTN-UHFFFAOYSA-M 0.000 description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 3
- 239000002253 acid Substances 0.000 description 3
- 230000004913 activation Effects 0.000 description 3
- 230000001476 alcoholic effect Effects 0.000 description 3
- 238000004458 analytical method Methods 0.000 description 3
- 239000002830 appetite depressant Substances 0.000 description 3
- 238000001875 carbon-13 cross-polarisation magic angle spinning nuclear magnetic resonance spectrum Methods 0.000 description 3
- 230000008859 change Effects 0.000 description 3
- 238000012512 characterization method Methods 0.000 description 3
- 238000001816 cooling Methods 0.000 description 3
- 230000001419 dependent effect Effects 0.000 description 3
- 238000011161 development Methods 0.000 description 3
- 229910001873 dinitrogen Inorganic materials 0.000 description 3
- 208000035475 disorder Diseases 0.000 description 3
- 238000002474 experimental method Methods 0.000 description 3
- 238000001914 filtration Methods 0.000 description 3
- 239000002471 hydroxymethylglutaryl coenzyme A reductase inhibitor Substances 0.000 description 3
- PCZOHLXUXFIOCF-BXMDZJJMSA-N lovastatin Chemical compound C([C@H]1[C@@H](C)C=CC2=C[C@H](C)C[C@@H]([C@H]12)OC(=O)[C@@H](C)CC)C[C@@H]1C[C@@H](O)CC(=O)O1 PCZOHLXUXFIOCF-BXMDZJJMSA-N 0.000 description 3
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 3
- 239000012074 organic phase Substances 0.000 description 3
- AHLBNYSZXLDEJQ-FWEHEUNISA-N orlistat Chemical compound CCCCCCCCCCC[C@H](OC(=O)[C@H](CC(C)C)NC=O)C[C@@H]1OC(=O)[C@H]1CCCCCC AHLBNYSZXLDEJQ-FWEHEUNISA-N 0.000 description 3
- 229960001243 orlistat Drugs 0.000 description 3
- 229940096701 plain lipid modifying drug hmg coa reductase inhibitors Drugs 0.000 description 3
- 210000000512 proximal kidney tubule Anatomy 0.000 description 3
- 230000005855 radiation Effects 0.000 description 3
- 238000001953 recrystallisation Methods 0.000 description 3
- 229910052708 sodium Inorganic materials 0.000 description 3
- 239000007858 starting material Substances 0.000 description 3
- 239000000126 substance Substances 0.000 description 3
- 108090000721 thyroid hormone receptors Proteins 0.000 description 3
- 102000004217 thyroid hormone receptors Human genes 0.000 description 3
- HSINOMROUCMIEA-FGVHQWLLSA-N (2s,4r)-4-[(3r,5s,6r,7r,8s,9s,10s,13r,14s,17r)-6-ethyl-3,7-dihydroxy-10,13-dimethyl-2,3,4,5,6,7,8,9,11,12,14,15,16,17-tetradecahydro-1h-cyclopenta[a]phenanthren-17-yl]-2-methylpentanoic acid Chemical compound C([C@@]12C)C[C@@H](O)C[C@H]1[C@@H](CC)[C@@H](O)[C@@H]1[C@@H]2CC[C@]2(C)[C@@H]([C@H](C)C[C@H](C)C(O)=O)CC[C@H]21 HSINOMROUCMIEA-FGVHQWLLSA-N 0.000 description 2
- ZGGHKIMDNBDHJB-NRFPMOEYSA-M (3R,5S)-fluvastatin sodium Chemical compound [Na+].C12=CC=CC=C2N(C(C)C)C(\C=C\[C@@H](O)C[C@@H](O)CC([O-])=O)=C1C1=CC=C(F)C=C1 ZGGHKIMDNBDHJB-NRFPMOEYSA-M 0.000 description 2
- KWTSXDURSIMDCE-QMMMGPOBSA-N (S)-amphetamine Chemical compound C[C@H](N)CC1=CC=CC=C1 KWTSXDURSIMDCE-QMMMGPOBSA-N 0.000 description 2
- LTMQZVLXCLQPCT-UHFFFAOYSA-N 1,1,6-trimethyltetralin Chemical group C1CCC(C)(C)C=2C1=CC(C)=CC=2 LTMQZVLXCLQPCT-UHFFFAOYSA-N 0.000 description 2
- 238000001644 13C nuclear magnetic resonance spectroscopy Methods 0.000 description 2
- WNZQDUSMALZDQF-UHFFFAOYSA-N 2-benzofuran-1(3H)-one Chemical compound C1=CC=C2C(=O)OCC2=C1 WNZQDUSMALZDQF-UHFFFAOYSA-N 0.000 description 2
- ILPUOPPYSQEBNJ-UHFFFAOYSA-N 2-methyl-2-phenoxypropanoic acid Chemical class OC(=O)C(C)(C)OC1=CC=CC=C1 ILPUOPPYSQEBNJ-UHFFFAOYSA-N 0.000 description 2
- SWLAMJPTOQZTAE-UHFFFAOYSA-N 4-[2-[(5-chloro-2-methoxybenzoyl)amino]ethyl]benzoic acid Chemical class COC1=CC=C(Cl)C=C1C(=O)NCCC1=CC=C(C(O)=O)C=C1 SWLAMJPTOQZTAE-UHFFFAOYSA-N 0.000 description 2
- QBQLYIISSRXYKL-UHFFFAOYSA-N 4-[[4-[2-(5-methyl-2-phenyl-1,3-oxazol-4-yl)ethoxy]phenyl]methyl]-1,2-oxazolidine-3,5-dione Chemical compound CC=1OC(C=2C=CC=CC=2)=NC=1CCOC(C=C1)=CC=C1CC1C(=O)NOC1=O QBQLYIISSRXYKL-UHFFFAOYSA-N 0.000 description 2
- 229960000549 4-dimethylaminophenol Drugs 0.000 description 2
- XUKUURHRXDUEBC-KAYWLYCHSA-N Atorvastatin Chemical compound C=1C=CC=CC=1C1=C(C=2C=CC(F)=CC=2)N(CC[C@@H](O)C[C@@H](O)CC(O)=O)C(C(C)C)=C1C(=O)NC1=CC=CC=C1 XUKUURHRXDUEBC-KAYWLYCHSA-N 0.000 description 2
- XUKUURHRXDUEBC-UHFFFAOYSA-N Atorvastatin Natural products C=1C=CC=CC=1C1=C(C=2C=CC(F)=CC=2)N(CCC(O)CC(O)CC(O)=O)C(C(C)C)=C1C(=O)NC1=CC=CC=C1 XUKUURHRXDUEBC-UHFFFAOYSA-N 0.000 description 2
- 229940123208 Biguanide Drugs 0.000 description 2
- 102000004219 Brain-derived neurotrophic factor Human genes 0.000 description 2
- 108090000715 Brain-derived neurotrophic factor Proteins 0.000 description 2
- JZUFKLXOESDKRF-UHFFFAOYSA-N Chlorothiazide Chemical compound C1=C(Cl)C(S(=O)(=O)N)=CC2=C1NCNS2(=O)=O JZUFKLXOESDKRF-UHFFFAOYSA-N 0.000 description 2
- 108010005939 Ciliary Neurotrophic Factor Proteins 0.000 description 2
- 102100031614 Ciliary neurotrophic factor Human genes 0.000 description 2
- 102000034534 Cotransporters Human genes 0.000 description 2
- 108020003264 Cotransporters Proteins 0.000 description 2
- 229910002483 Cu Ka Inorganic materials 0.000 description 2
- YLQBMQCUIZJEEH-UHFFFAOYSA-N Furan Chemical compound C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 2
- HEMJJKBWTPKOJG-UHFFFAOYSA-N Gemfibrozil Chemical compound CC1=CC=C(C)C(OCCCC(C)(C)C(O)=O)=C1 HEMJJKBWTPKOJG-UHFFFAOYSA-N 0.000 description 2
- 108091052347 Glucose transporter family Proteins 0.000 description 2
- 102000015779 HDL Lipoproteins Human genes 0.000 description 2
- 108010010234 HDL Lipoproteins Proteins 0.000 description 2
- NTYJJOPFIAHURM-UHFFFAOYSA-N Histamine Chemical compound NCCC1=CN=CN1 NTYJJOPFIAHURM-UHFFFAOYSA-N 0.000 description 2
- 229940122355 Insulin sensitizer Drugs 0.000 description 2
- COLNVLDHVKWLRT-QMMMGPOBSA-N L-phenylalanine Chemical compound OC(=O)[C@@H](N)CC1=CC=CC=C1 COLNVLDHVKWLRT-QMMMGPOBSA-N 0.000 description 2
- 239000000867 Lipoxygenase Inhibitor Substances 0.000 description 2
- 108010019598 Liraglutide Proteins 0.000 description 2
- WMFOQBRAJBCJND-UHFFFAOYSA-M Lithium hydroxide Chemical compound [Li+].[OH-] WMFOQBRAJBCJND-UHFFFAOYSA-M 0.000 description 2
- ZPXSCAKFGYXMGA-UHFFFAOYSA-N Mazindol Chemical compound N12CCN=C2C2=CC=CC=C2C1(O)C1=CC=C(Cl)C=C1 ZPXSCAKFGYXMGA-UHFFFAOYSA-N 0.000 description 2
- 102000029828 Melanin-concentrating hormone receptor Human genes 0.000 description 2
- 108010047068 Melanin-concentrating hormone receptor Proteins 0.000 description 2
- PCZOHLXUXFIOCF-UHFFFAOYSA-N Monacolin X Natural products C12C(OC(=O)C(C)CC)CC(C)C=C2C=CC(C)C1CCC1CC(O)CC(=O)O1 PCZOHLXUXFIOCF-UHFFFAOYSA-N 0.000 description 2
- LRHPLDYGYMQRHN-UHFFFAOYSA-N N-Butanol Chemical compound CCCCO LRHPLDYGYMQRHN-UHFFFAOYSA-N 0.000 description 2
- AHLBNYSZXLDEJQ-UHFFFAOYSA-N N-formyl-L-leucylester Natural products CCCCCCCCCCCC(OC(=O)C(CC(C)C)NC=O)CC1OC(=O)C1CCCCCC AHLBNYSZXLDEJQ-UHFFFAOYSA-N 0.000 description 2
- 238000005481 NMR spectroscopy Methods 0.000 description 2
- 102000003729 Neprilysin Human genes 0.000 description 2
- 108090000028 Neprilysin Proteins 0.000 description 2
- PVNIIMVLHYAWGP-UHFFFAOYSA-N Niacin Chemical compound OC(=O)C1=CC=CN=C1 PVNIIMVLHYAWGP-UHFFFAOYSA-N 0.000 description 2
- 108010028924 PPAR alpha Proteins 0.000 description 2
- 102000023984 PPAR alpha Human genes 0.000 description 2
- 229940124754 PPAR-alpha/gamma agonist Drugs 0.000 description 2
- 102100038831 Peroxisome proliferator-activated receptor alpha Human genes 0.000 description 2
- 102100038825 Peroxisome proliferator-activated receptor gamma Human genes 0.000 description 2
- TUZYXOIXSAXUGO-UHFFFAOYSA-N Pravastatin Natural products C1=CC(C)C(CCC(O)CC(O)CC(O)=O)C2C(OC(=O)C(C)CC)CC(O)C=C21 TUZYXOIXSAXUGO-UHFFFAOYSA-N 0.000 description 2
- KAESVJOAVNADME-UHFFFAOYSA-N Pyrrole Chemical compound C=1C=CNC=1 KAESVJOAVNADME-UHFFFAOYSA-N 0.000 description 2
- SMWDFEZZVXVKRB-UHFFFAOYSA-N Quinoline Chemical compound N1=CC=CC2=CC=CC=C21 SMWDFEZZVXVKRB-UHFFFAOYSA-N 0.000 description 2
- 241000700159 Rattus Species 0.000 description 2
- YASAKCUCGLMORW-UHFFFAOYSA-N Rosiglitazone Chemical compound C=1C=CC=NC=1N(C)CCOC(C=C1)=CC=C1CC1SC(=O)NC1=O YASAKCUCGLMORW-UHFFFAOYSA-N 0.000 description 2
- RYMZZMVNJRMUDD-UHFFFAOYSA-N SJ000286063 Natural products C12C(OC(=O)C(C)(C)CC)CC(C)C=C2C=CC(C)C1CCC1CC(O)CC(=O)O1 RYMZZMVNJRMUDD-UHFFFAOYSA-N 0.000 description 2
- 229940123464 Thiazolidinedione Drugs 0.000 description 2
- KJADKKWYZYXHBB-XBWDGYHZSA-N Topiramic acid Chemical compound C1O[C@@]2(COS(N)(=O)=O)OC(C)(C)O[C@H]2[C@@H]2OC(C)(C)O[C@@H]21 KJADKKWYZYXHBB-XBWDGYHZSA-N 0.000 description 2
- ORILYTVJVMAKLC-UHFFFAOYSA-N adamantane Chemical compound C1C(C2)CC3CC1CC2C3 ORILYTVJVMAKLC-UHFFFAOYSA-N 0.000 description 2
- 239000000048 adrenergic agonist Substances 0.000 description 2
- 229940125709 anorectic agent Drugs 0.000 description 2
- 230000002058 anti-hyperglycaemic effect Effects 0.000 description 2
- 239000012296 anti-solvent Substances 0.000 description 2
- 239000003529 anticholesteremic agent Substances 0.000 description 2
- 239000008346 aqueous phase Substances 0.000 description 2
- 125000003118 aryl group Chemical group 0.000 description 2
- 239000012298 atmosphere Substances 0.000 description 2
- 229960005370 atorvastatin Drugs 0.000 description 2
- 108010014210 axokine Proteins 0.000 description 2
- 239000003613 bile acid Substances 0.000 description 2
- 229920000080 bile acid sequestrant Polymers 0.000 description 2
- 229940096699 bile acid sequestrants Drugs 0.000 description 2
- 230000036765 blood level Effects 0.000 description 2
- WTEOIRVLGSZEPR-UHFFFAOYSA-N boron trifluoride Chemical compound FB(F)F WTEOIRVLGSZEPR-UHFFFAOYSA-N 0.000 description 2
- 229940077737 brain-derived neurotrophic factor Drugs 0.000 description 2
- 229960005110 cerivastatin Drugs 0.000 description 2
- SEERZIQQUAZTOL-ANMDKAQQSA-N cerivastatin Chemical compound COCC1=C(C(C)C)N=C(C(C)C)C(\C=C\[C@@H](O)C[C@@H](O)CC(O)=O)=C1C1=CC=C(F)C=C1 SEERZIQQUAZTOL-ANMDKAQQSA-N 0.000 description 2
- JNGZXGGOCLZBFB-IVCQMTBJSA-N compound E Chemical compound N([C@@H](C)C(=O)N[C@@H]1C(N(C)C2=CC=CC=C2C(C=2C=CC=CC=2)=N1)=O)C(=O)CC1=CC(F)=CC(F)=C1 JNGZXGGOCLZBFB-IVCQMTBJSA-N 0.000 description 2
- 238000010924 continuous production Methods 0.000 description 2
- 230000001276 controlling effect Effects 0.000 description 2
- 230000001054 cortical effect Effects 0.000 description 2
- QQKNSPHAFATFNQ-UHFFFAOYSA-N darglitazone Chemical compound CC=1OC(C=2C=CC=CC=2)=NC=1CCC(=O)C(C=C1)=CC=C1CC1SC(=O)NC1=O QQKNSPHAFATFNQ-UHFFFAOYSA-N 0.000 description 2
- 238000013480 data collection Methods 0.000 description 2
- 238000010586 diagram Methods 0.000 description 2
- 238000001938 differential scanning calorimetry curve Methods 0.000 description 2
- 238000002050 diffraction method Methods 0.000 description 2
- 150000002009 diols Chemical class 0.000 description 2
- 235000011180 diphosphates Nutrition 0.000 description 2
- DLNKOYKMWOXYQA-UHFFFAOYSA-N dl-pseudophenylpropanolamine Natural products CC(N)C(O)C1=CC=CC=C1 DLNKOYKMWOXYQA-UHFFFAOYSA-N 0.000 description 2
- 229960003638 dopamine Drugs 0.000 description 2
- 239000002552 dosage form Substances 0.000 description 2
- 235000021463 dry cake Nutrition 0.000 description 2
- PHJMNLZSBSXKJE-UHFFFAOYSA-N ethanol;dihydrate Chemical compound O.O.CCO PHJMNLZSBSXKJE-UHFFFAOYSA-N 0.000 description 2
- 230000029142 excretion Effects 0.000 description 2
- 238000000605 extraction Methods 0.000 description 2
- 229940125753 fibrate Drugs 0.000 description 2
- 229960003765 fluvastatin Drugs 0.000 description 2
- 230000006870 function Effects 0.000 description 2
- 229960003627 gemfibrozil Drugs 0.000 description 2
- 229960004580 glibenclamide Drugs 0.000 description 2
- ZNNLBTZKUZBEKO-UHFFFAOYSA-N glyburide Chemical compound COC1=CC=C(Cl)C=C1C(=O)NCCC1=CC=C(S(=O)(=O)NC(=O)NC2CCCCC2)C=C1 ZNNLBTZKUZBEKO-UHFFFAOYSA-N 0.000 description 2
- 238000005858 glycosidation reaction Methods 0.000 description 2
- 238000000227 grinding Methods 0.000 description 2
- 229910052739 hydrogen Inorganic materials 0.000 description 2
- 230000000055 hyoplipidemic effect Effects 0.000 description 2
- 201000001421 hyperglycemia Diseases 0.000 description 2
- 238000002955 isolation Methods 0.000 description 2
- 238000010902 jet-milling Methods 0.000 description 2
- 239000010410 layer Substances 0.000 description 2
- 229960002701 liraglutide Drugs 0.000 description 2
- DLEDOFVPSDKWEF-UHFFFAOYSA-N lithium butane Chemical compound [Li+].CCC[CH2-] DLEDOFVPSDKWEF-UHFFFAOYSA-N 0.000 description 2
- 210000004185 liver Anatomy 0.000 description 2
- 229960004844 lovastatin Drugs 0.000 description 2
- QLJODMDSTUBWDW-UHFFFAOYSA-N lovastatin hydroxy acid Natural products C1=CC(C)C(CCC(O)CC(O)CC(O)=O)C2C(OC(=O)C(C)CC)CC(C)C=C21 QLJODMDSTUBWDW-UHFFFAOYSA-N 0.000 description 2
- 229960000299 mazindol Drugs 0.000 description 2
- 229950004994 meglitinide Drugs 0.000 description 2
- 239000000336 melanocortin receptor agonist Substances 0.000 description 2
- FWMHZWMPUWAUPL-NDEPHWFRSA-N methyl (4s)-3-[3-[4-(3-acetamidophenyl)piperidin-1-yl]propylcarbamoyl]-4-(3,4-difluorophenyl)-6-(methoxymethyl)-2-oxo-1,4-dihydropyrimidine-5-carboxylate Chemical compound N1([C@H](C(=C(NC1=O)COC)C(=O)OC)C=1C=C(F)C(F)=CC=1)C(=O)NCCCN(CC1)CCC1C1=CC=CC(NC(C)=O)=C1 FWMHZWMPUWAUPL-NDEPHWFRSA-N 0.000 description 2
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 2
- UAEPNZWRGJTJPN-UHFFFAOYSA-N methylcyclohexane Chemical compound CC1CCCCC1 UAEPNZWRGJTJPN-UHFFFAOYSA-N 0.000 description 2
- 230000000407 monoamine reuptake Effects 0.000 description 2
- MZRVEZGGRBJDDB-UHFFFAOYSA-N n-Butyllithium Substances [Li]CCCC MZRVEZGGRBJDDB-UHFFFAOYSA-N 0.000 description 2
- PKWDZWYVIHVNKS-UHFFFAOYSA-N netoglitazone Chemical compound FC1=CC=CC=C1COC1=CC=C(C=C(CC2C(NC(=O)S2)=O)C=C2)C2=C1 PKWDZWYVIHVNKS-UHFFFAOYSA-N 0.000 description 2
- 238000006386 neutralization reaction Methods 0.000 description 2
- 239000012044 organic layer Substances 0.000 description 2
- 125000001979 organolithium group Chemical group 0.000 description 2
- 125000001181 organosilyl group Chemical group [SiH3]* 0.000 description 2
- 239000002245 particle Substances 0.000 description 2
- 108091008725 peroxisome proliferator-activated receptors alpha Proteins 0.000 description 2
- 229960003562 phentermine Drugs 0.000 description 2
- 229960000395 phenylpropanolamine Drugs 0.000 description 2
- DLNKOYKMWOXYQA-APPZFPTMSA-N phenylpropanolamine Chemical compound C[C@@H](N)[C@H](O)C1=CC=CC=C1 DLNKOYKMWOXYQA-APPZFPTMSA-N 0.000 description 2
- RHGYHLPFVJEAOC-FFNUKLMVSA-L pitavastatin calcium Chemical compound [Ca+2].[O-]C(=O)C[C@H](O)C[C@H](O)\C=C\C1=C(C2CC2)N=C2C=CC=CC2=C1C1=CC=C(F)C=C1.[O-]C(=O)C[C@H](O)C[C@H](O)\C=C\C1=C(C2CC2)N=C2C=CC=CC2=C1C1=CC=C(F)C=C1 RHGYHLPFVJEAOC-FFNUKLMVSA-L 0.000 description 2
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Chemical compound [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 description 2
- 229960002965 pravastatin Drugs 0.000 description 2
- TUZYXOIXSAXUGO-PZAWKZKUSA-N pravastatin Chemical compound C1=C[C@H](C)[C@H](CC[C@@H](O)C[C@@H](O)CC(O)=O)[C@H]2[C@@H](OC(=O)[C@@H](C)CC)C[C@H](O)C=C21 TUZYXOIXSAXUGO-PZAWKZKUSA-N 0.000 description 2
- GCYXWQUSHADNBF-AAEALURTSA-N preproglucagon 78-108 Chemical compound C([C@@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](C)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CCCCN)C(=O)NCC(=O)N[C@@H](CCCNC(N)=N)C(=O)NCC(O)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCCCN)NC(=O)[C@H](C)NC(=O)[C@H](C)NC(=O)[C@H](CCC(N)=O)NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@@H](NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C)NC(=O)[C@@H](N)CC=1N=CNC=1)[C@@H](C)O)[C@@H](C)O)C(C)C)C1=CC=CC=C1 GCYXWQUSHADNBF-AAEALURTSA-N 0.000 description 2
- 229960003912 probucol Drugs 0.000 description 2
- FYPMFJGVHOHGLL-UHFFFAOYSA-N probucol Chemical compound C=1C(C(C)(C)C)=C(O)C(C(C)(C)C)=CC=1SC(C)(C)SC1=CC(C(C)(C)C)=C(O)C(C(C)(C)C)=C1 FYPMFJGVHOHGLL-UHFFFAOYSA-N 0.000 description 2
- 230000001105 regulatory effect Effects 0.000 description 2
- 150000003839 salts Chemical class 0.000 description 2
- 229940076279 serotonin Drugs 0.000 description 2
- UNAANXDKBXWMLN-UHFFFAOYSA-N sibutramine Chemical compound C=1C=C(Cl)C=CC=1C1(C(N(C)C)CC(C)C)CCC1 UNAANXDKBXWMLN-UHFFFAOYSA-N 0.000 description 2
- 229960004425 sibutramine Drugs 0.000 description 2
- 229960002855 simvastatin Drugs 0.000 description 2
- RYMZZMVNJRMUDD-HGQWONQESA-N simvastatin Chemical compound C([C@H]1[C@@H](C)C=CC2=C[C@H](C)C[C@@H]([C@H]12)OC(=O)C(C)(C)CC)C[C@@H]1C[C@@H](O)CC(=O)O1 RYMZZMVNJRMUDD-HGQWONQESA-N 0.000 description 2
- 241000894007 species Species 0.000 description 2
- 238000001228 spectrum Methods 0.000 description 2
- 230000000946 synaptic effect Effects 0.000 description 2
- 150000001467 thiazolidinediones Chemical class 0.000 description 2
- 210000001519 tissue Anatomy 0.000 description 2
- 229960004394 topiramate Drugs 0.000 description 2
- CMSGWTNRGKRWGS-NQIIRXRSSA-N torcetrapib Chemical compound COC(=O)N([C@H]1C[C@@H](CC)N(C2=CC=C(C=C21)C(F)(F)F)C(=O)OCC)CC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1 CMSGWTNRGKRWGS-NQIIRXRSSA-N 0.000 description 2
- 210000005239 tubule Anatomy 0.000 description 2
- 150000003672 ureas Chemical class 0.000 description 2
- AHOUBRCZNHFOSL-YOEHRIQHSA-N (+)-Casbol Chemical compound C1=CC(F)=CC=C1[C@H]1[C@H](COC=2C=C3OCOC3=CC=2)CNCC1 AHOUBRCZNHFOSL-YOEHRIQHSA-N 0.000 description 1
- DBGIVFWFUFKIQN-VIFPVBQESA-N (+)-Fenfluramine Chemical compound CCN[C@@H](C)CC1=CC=CC(C(F)(F)F)=C1 DBGIVFWFUFKIQN-VIFPVBQESA-N 0.000 description 1
- DBGIVFWFUFKIQN-UHFFFAOYSA-N (+-)-Fenfluramine Chemical compound CCNC(C)CC1=CC=CC(C(F)(F)F)=C1 DBGIVFWFUFKIQN-UHFFFAOYSA-N 0.000 description 1
- XUFXOAAUWZOOIT-SXARVLRPSA-N (2R,3R,4R,5S,6R)-5-[[(2R,3R,4R,5S,6R)-5-[[(2R,3R,4S,5S,6R)-3,4-dihydroxy-6-methyl-5-[[(1S,4R,5S,6S)-4,5,6-trihydroxy-3-(hydroxymethyl)-1-cyclohex-2-enyl]amino]-2-oxanyl]oxy]-3,4-dihydroxy-6-(hydroxymethyl)-2-oxanyl]oxy]-6-(hydroxymethyl)oxane-2,3,4-triol Chemical compound O([C@H]1O[C@H](CO)[C@H]([C@@H]([C@H]1O)O)O[C@H]1O[C@@H]([C@H]([C@H](O)[C@H]1O)N[C@@H]1[C@@H]([C@@H](O)[C@H](O)C(CO)=C1)O)C)[C@@H]1[C@@H](CO)O[C@@H](O)[C@H](O)[C@H]1O XUFXOAAUWZOOIT-SXARVLRPSA-N 0.000 description 1
- NVXFXLSOGLFXKQ-JMSVASOKSA-N (2s)-1-[(2r,4r)-5-ethoxy-2,4-dimethyl-5-oxopentanoyl]-2,3-dihydroindole-2-carboxylic acid Chemical compound C1=CC=C2N(C(=O)[C@H](C)C[C@@H](C)C(=O)OCC)[C@H](C(O)=O)CC2=C1 NVXFXLSOGLFXKQ-JMSVASOKSA-N 0.000 description 1
- BAVDEDVBIHTHJQ-UVJOBNTFSA-N (2s)-1-[(2s)-6-amino-2-[[(1s)-1-carboxy-3-phenylpropyl]amino]hexanoyl]pyrrolidine-2-carboxylic acid;hydrate Chemical compound O.C([C@H](N[C@@H](CCCCN)C(=O)N1[C@@H](CCC1)C(O)=O)C(O)=O)CC1=CC=CC=C1 BAVDEDVBIHTHJQ-UVJOBNTFSA-N 0.000 description 1
- YDZWHGJRWMQCDP-NKILCQAGSA-N (2s,3s,4s,5r,6r)-6-[[(3s,4ar,6ar,6bs,8as,12as,14ar,14br)-8a-carboxy-4,4,6a,6b,11,11,14b-heptamethyl-1,2,3,4a,5,6,7,8,9,10,12,12a,14,14a-tetradecahydropicen-3-yl]oxy]-3-hydroxy-4-[(2s,3r,4s,5r,6r)-3,4,5-trihydroxy-6-(hydroxymethyl)oxan-2-yl]oxy-5-[(2s,3r,4 Chemical compound O([C@H]1[C@H](O)[C@H](O[C@H]([C@@H]1O[C@H]1[C@@H]([C@@H](O)[C@H](O)[C@@H](CO)O1)O)O[C@H]1CC[C@]2(C)[C@H]3CC=C4[C@@]([C@@]3(CC[C@H]2C1(C)C)C)(C)CC[C@]1(CCC(C[C@H]14)(C)C)C(O)=O)C(O)=O)[C@@H]1O[C@H](CO)[C@H](O)[C@H](O)[C@H]1O YDZWHGJRWMQCDP-NKILCQAGSA-N 0.000 description 1
- BIDNLKIUORFRQP-XYGFDPSESA-N (2s,4s)-4-cyclohexyl-1-[2-[[(1s)-2-methyl-1-propanoyloxypropoxy]-(4-phenylbutyl)phosphoryl]acetyl]pyrrolidine-2-carboxylic acid Chemical compound C([P@@](=O)(O[C@H](OC(=O)CC)C(C)C)CC(=O)N1[C@@H](C[C@H](C1)C1CCCCC1)C(O)=O)CCCC1=CC=CC=C1 BIDNLKIUORFRQP-XYGFDPSESA-N 0.000 description 1
- RICKQPKTSOSCOF-HKUYNNGSSA-N (3s)-2-[(2s)-2-amino-3-(1h-indol-3-yl)propanoyl]-3,4-dihydro-1h-isoquinoline-3-carboxylic acid Chemical compound C1C2=CC=CC=C2C[C@@H](C(O)=O)N1C(=O)[C@@H](N)CC1=CNC2=CC=CC=C12 RICKQPKTSOSCOF-HKUYNNGSSA-N 0.000 description 1
- AXJQVVLKUYCICH-OAQYLSRUSA-N (4s)-5-(4-chlorophenyl)-n-(4-chlorophenyl)sulfonyl-n'-methyl-4-phenyl-3,4-dihydropyrazole-2-carboximidamide Chemical compound C=1C=C(Cl)C=CC=1C([C@H](C1)C=2C=CC=CC=2)=NN1C(=NC)NS(=O)(=O)C1=CC=C(Cl)C=C1 AXJQVVLKUYCICH-OAQYLSRUSA-N 0.000 description 1
- QYIXCDOBOSTCEI-BPAAZKTESA-N (8r,9s,10s,13r,14s,17r)-10,13-dimethyl-17-[(2r)-6-methylheptan-2-yl]-2,3,4,5,6,7,8,9,11,12,14,15,16,17-tetradecahydro-1h-cyclopenta[a]phenanthren-3-ol Chemical compound C1CC2CC(O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@H]([C@H](C)CCCC(C)C)[C@@]1(C)CC2 QYIXCDOBOSTCEI-BPAAZKTESA-N 0.000 description 1
- RWIUTHWKQHRQNP-ZDVGBALWSA-N (9e,12e)-n-(1-phenylethyl)octadeca-9,12-dienamide Chemical compound CCCCC\C=C\C\C=C\CCCCCCCC(=O)NC(C)C1=CC=CC=C1 RWIUTHWKQHRQNP-ZDVGBALWSA-N 0.000 description 1
- RTHCYVBBDHJXIQ-MRXNPFEDSA-N (R)-fluoxetine Chemical compound O([C@H](CCNC)C=1C=CC=CC=1)C1=CC=C(C(F)(F)F)C=C1 RTHCYVBBDHJXIQ-MRXNPFEDSA-N 0.000 description 1
- JLHMJWHSBYZWJJ-UHFFFAOYSA-N 1,2-thiazole 1-oxide Chemical class O=S1C=CC=N1 JLHMJWHSBYZWJJ-UHFFFAOYSA-N 0.000 description 1
- POQMHHDKXWTFHB-UHFFFAOYSA-N 1-[5-[(4,5-diphenyl-1h-imidazol-2-yl)sulfinyl]pentyl]-3,5-dimethylpyrazole Chemical compound N1=C(C)C=C(C)N1CCCCCS(=O)C1=NC(C=2C=CC=CC=2)=C(C=2C=CC=CC=2)N1 POQMHHDKXWTFHB-UHFFFAOYSA-N 0.000 description 1
- 229940123153 15 Lipoxygenase inhibitor Drugs 0.000 description 1
- SGTNSNPWRIOYBX-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-5-{[2-(3,4-dimethoxyphenyl)ethyl](methyl)amino}-2-(propan-2-yl)pentanenitrile Chemical compound C1=C(OC)C(OC)=CC=C1CCN(C)CCCC(C#N)(C(C)C)C1=CC=C(OC)C(OC)=C1 SGTNSNPWRIOYBX-UHFFFAOYSA-N 0.000 description 1
- YZQLWPMZQVHJED-UHFFFAOYSA-N 2-methylpropanethioic acid S-[2-[[[1-(2-ethylbutyl)cyclohexyl]-oxomethyl]amino]phenyl] ester Chemical compound C=1C=CC=C(SC(=O)C(C)C)C=1NC(=O)C1(CC(CC)CC)CCCCC1 YZQLWPMZQVHJED-UHFFFAOYSA-N 0.000 description 1
- 125000003903 2-propenyl group Chemical group [H]C([*])([H])C([H])=C([H])[H] 0.000 description 1
- CZMRCDWAGMRECN-UHFFFAOYSA-N 2-{[3,4-dihydroxy-2,5-bis(hydroxymethyl)oxolan-2-yl]oxy}-6-(hydroxymethyl)oxane-3,4,5-triol Chemical compound OCC1OC(CO)(OC2OC(CO)C(O)C(O)C2O)C(O)C1O CZMRCDWAGMRECN-UHFFFAOYSA-N 0.000 description 1
- ZPSJGADGUYYRKE-UHFFFAOYSA-N 2H-pyran-2-one Chemical compound O=C1C=CC=CO1 ZPSJGADGUYYRKE-UHFFFAOYSA-N 0.000 description 1
- NBYATBIMYLFITE-UHFFFAOYSA-N 3-[decyl(dimethyl)silyl]-n-[2-(4-methylphenyl)-1-phenylethyl]propanamide Chemical compound C=1C=CC=CC=1C(NC(=O)CC[Si](C)(C)CCCCCCCCCC)CC1=CC=C(C)C=C1 NBYATBIMYLFITE-UHFFFAOYSA-N 0.000 description 1
- FUSNOPLQVRUIIM-UHFFFAOYSA-N 4-amino-2-(4,4-dimethyl-2-oxoimidazolidin-1-yl)-n-[3-(trifluoromethyl)phenyl]pyrimidine-5-carboxamide Chemical compound O=C1NC(C)(C)CN1C(N=C1N)=NC=C1C(=O)NC1=CC=CC(C(F)(F)F)=C1 FUSNOPLQVRUIIM-UHFFFAOYSA-N 0.000 description 1
- MXNQOXJLUJUCGE-UHFFFAOYSA-N 4-amino-2-(4,4-dimethyl-2-oxoimidazolidin-1-yl)-n-[3-(trifluoromethyl)phenyl]pyrimidine-5-carboxamide;hydrochloride Chemical compound Cl.O=C1NC(C)(C)CN1C(N=C1N)=NC=C1C(=O)NC1=CC=CC(C(F)(F)F)=C1 MXNQOXJLUJUCGE-UHFFFAOYSA-N 0.000 description 1
- WUBBRNOQWQTFEX-UHFFFAOYSA-N 4-aminosalicylic acid Chemical compound NC1=CC=C(C(O)=O)C(O)=C1 WUBBRNOQWQTFEX-UHFFFAOYSA-N 0.000 description 1
- NFFXEUUOMTXWCX-UHFFFAOYSA-N 5-[(2,4-dioxo-1,3-thiazolidin-5-yl)methyl]-2-methoxy-n-[[4-(trifluoromethyl)phenyl]methyl]benzamide Chemical compound C1=C(C(=O)NCC=2C=CC(=CC=2)C(F)(F)F)C(OC)=CC=C1CC1SC(=O)NC1=O NFFXEUUOMTXWCX-UHFFFAOYSA-N 0.000 description 1
- MVDXXGIBARMXSA-PYUWXLGESA-N 5-[[(2r)-2-benzyl-3,4-dihydro-2h-chromen-6-yl]methyl]-1,3-thiazolidine-2,4-dione Chemical compound S1C(=O)NC(=O)C1CC1=CC=C(O[C@@H](CC=2C=CC=CC=2)CC2)C2=C1 MVDXXGIBARMXSA-PYUWXLGESA-N 0.000 description 1
- HCEQQASHRRPQFE-UHFFFAOYSA-N 5-chloro-n-[2-[4-(cyclohexylcarbamoylsulfamoyl)phenyl]ethyl]-2-methoxybenzamide;3-(diaminomethylidene)-1,1-dimethylguanidine;hydrochloride Chemical compound Cl.CN(C)C(=N)N=C(N)N.COC1=CC=C(Cl)C=C1C(=O)NCCC1=CC=C(S(=O)(=O)NC(=O)NC2CCCCC2)C=C1 HCEQQASHRRPQFE-UHFFFAOYSA-N 0.000 description 1
- VFFZWMWTUSXDCB-ZDUSSCGKSA-N 6-[2-[[2-[(2s)-2-cyanopyrrolidin-1-yl]-2-oxoethyl]amino]ethylamino]pyridine-3-carbonitrile Chemical compound N1([C@@H](CCC1)C#N)C(=O)CNCCNC1=CC=C(C#N)C=N1 VFFZWMWTUSXDCB-ZDUSSCGKSA-N 0.000 description 1
- 239000005541 ACE inhibitor Substances 0.000 description 1
- RZVAJINKPMORJF-UHFFFAOYSA-N Acetaminophen Chemical compound CC(=O)NC1=CC=C(O)C=C1 RZVAJINKPMORJF-UHFFFAOYSA-N 0.000 description 1
- DJQOOSBJCLSSEY-UHFFFAOYSA-N Acipimox Chemical compound CC1=CN=C(C(O)=O)C=[N+]1[O-] DJQOOSBJCLSSEY-UHFFFAOYSA-N 0.000 description 1
- 239000005695 Ammonium acetate Substances 0.000 description 1
- 101100438156 Arabidopsis thaliana CAD7 gene Proteins 0.000 description 1
- 101100460776 Arabidopsis thaliana NPY2 gene Proteins 0.000 description 1
- 101100460782 Arabidopsis thaliana NPY4 gene Proteins 0.000 description 1
- 101100460788 Arabidopsis thaliana NPY5 gene Proteins 0.000 description 1
- BSYNRYMUTXBXSQ-UHFFFAOYSA-N Aspirin Chemical compound CC(=O)OC1=CC=CC=C1C(O)=O BSYNRYMUTXBXSQ-UHFFFAOYSA-N 0.000 description 1
- PTQXTEKSNBVPQJ-UHFFFAOYSA-N Avasimibe Chemical compound CC(C)C1=CC(C(C)C)=CC(C(C)C)=C1CC(=O)NS(=O)(=O)OC1=C(C(C)C)C=CC=C1C(C)C PTQXTEKSNBVPQJ-UHFFFAOYSA-N 0.000 description 1
- 229910015900 BF3 Inorganic materials 0.000 description 1
- XNCOSPRUTUOJCJ-UHFFFAOYSA-N Biguanide Chemical compound NC(N)=NC(N)=N XNCOSPRUTUOJCJ-UHFFFAOYSA-N 0.000 description 1
- PUDZWXPKLIXQKQ-UHFFFAOYSA-N C(=O)(O)C1C(COP1(O)=O)O Chemical compound C(=O)(O)C1C(COP1(O)=O)O PUDZWXPKLIXQKQ-UHFFFAOYSA-N 0.000 description 1
- 239000002083 C09CA01 - Losartan Substances 0.000 description 1
- 239000004072 C09CA03 - Valsartan Substances 0.000 description 1
- 239000002947 C09CA04 - Irbesartan Substances 0.000 description 1
- 101150071647 CAD4 gene Proteins 0.000 description 1
- BLPTXXQGBNMPLZ-BKGXHVDHSA-N CCOc1ccc(C/C(/C)=C(/C=C\C([C@@H]([C@@H]([C@H]2O)[O]#C)O[C@H](CO)[C@H]2O)=C)\Cl)cc1 Chemical compound CCOc1ccc(C/C(/C)=C(/C=C\C([C@@H]([C@@H]([C@H]2O)[O]#C)O[C@H](CO)[C@H]2O)=C)\Cl)cc1 BLPTXXQGBNMPLZ-BKGXHVDHSA-N 0.000 description 1
- JVHXJTBJCFBINQ-ADAARDCZSA-N CCOc1ccc(Cc2cc([C@@H]([C@@H]([C@H]3O)O)O[C@H](CO)[C@H]3O)ccc2Cl)cc1 Chemical compound CCOc1ccc(Cc2cc([C@@H]([C@@H]([C@H]3O)O)O[C@H](CO)[C@H]3O)ccc2Cl)cc1 JVHXJTBJCFBINQ-ADAARDCZSA-N 0.000 description 1
- 108010055448 CJC 1131 Proteins 0.000 description 1
- 229940127291 Calcium channel antagonist Drugs 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- 108010078791 Carrier Proteins Proteins 0.000 description 1
- 208000002177 Cataract Diseases 0.000 description 1
- 101100322652 Catharanthus roseus ADH13 gene Proteins 0.000 description 1
- 101100087088 Catharanthus roseus Redox1 gene Proteins 0.000 description 1
- RKWGIWYCVPQPMF-UHFFFAOYSA-N Chloropropamide Chemical compound CCCNC(=O)NS(=O)(=O)C1=CC=C(Cl)C=C1 RKWGIWYCVPQPMF-UHFFFAOYSA-N 0.000 description 1
- DBAKFASWICGISY-BTJKTKAUSA-N Chlorpheniramine maleate Chemical compound OC(=O)\C=C/C(O)=O.C=1C=CC=NC=1C(CCN(C)C)C1=CC=C(Cl)C=C1 DBAKFASWICGISY-BTJKTKAUSA-N 0.000 description 1
- 108010061846 Cholesterol Ester Transfer Proteins Proteins 0.000 description 1
- 102000012336 Cholesterol Ester Transfer Proteins Human genes 0.000 description 1
- 229940122502 Cholesterol absorption inhibitor Drugs 0.000 description 1
- 229920001268 Cholestyramine Polymers 0.000 description 1
- KPSRODZRAIWAKH-JTQLQIEISA-N Ciprofibrate Natural products C1=CC(OC(C)(C)C(O)=O)=CC=C1[C@H]1C(Cl)(Cl)C1 KPSRODZRAIWAKH-JTQLQIEISA-N 0.000 description 1
- BMOVQUBVGICXQN-UHFFFAOYSA-N Clinofibrate Chemical compound C1=CC(OC(C)(CC)C(O)=O)=CC=C1C1(C=2C=CC(OC(C)(CC)C(O)=O)=CC=2)CCCCC1 BMOVQUBVGICXQN-UHFFFAOYSA-N 0.000 description 1
- 229920002911 Colestipol Polymers 0.000 description 1
- 102000012289 Corticotropin-Releasing Hormone Human genes 0.000 description 1
- 108010022152 Corticotropin-Releasing Hormone Proteins 0.000 description 1
- 239000000055 Corticotropin-Releasing Hormone Substances 0.000 description 1
- 241000699800 Cricetinae Species 0.000 description 1
- 229910016523 CuKa Inorganic materials 0.000 description 1
- XZMCDFZZKTWFGF-UHFFFAOYSA-N Cyanamide Chemical compound NC#N XZMCDFZZKTWFGF-UHFFFAOYSA-N 0.000 description 1
- HPJYKMSFRBJOSW-JHSUYXJUSA-N Damsin Chemical compound C[C@H]1CC[C@H]2C(=C)C(=O)O[C@H]2[C@]2(C)C(=O)CC[C@@H]12 HPJYKMSFRBJOSW-JHSUYXJUSA-N 0.000 description 1
- 102100025012 Dipeptidyl peptidase 4 Human genes 0.000 description 1
- 208000032928 Dyslipidaemia Diseases 0.000 description 1
- 108010061435 Enalapril Proteins 0.000 description 1
- HTQBXNHDCUEHJF-XWLPCZSASA-N Exenatide Chemical compound C([C@@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(N)=O)C(=O)NCC(=O)NCC(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CO)C(=O)N[C@@H](CO)C(=O)NCC(=O)N[C@@H](C)C(=O)N1[C@@H](CCC1)C(=O)N1[C@@H](CCC1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CO)C(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@@H](NC(=O)[C@H](C)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCSC)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CO)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@@H](NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)CNC(=O)[C@@H](N)CC=1NC=NC=1)[C@@H](C)O)[C@@H](C)O)C(C)C)C1=CC=CC=C1 HTQBXNHDCUEHJF-XWLPCZSASA-N 0.000 description 1
- 108010011459 Exenatide Proteins 0.000 description 1
- 102000018711 Facilitative Glucose Transport Proteins Human genes 0.000 description 1
- 102000030914 Fatty Acid-Binding Human genes 0.000 description 1
- MBHNWCYEGXQEIT-UHFFFAOYSA-N Fluphenazine hydrochloride Chemical compound Cl.Cl.C1CN(CCO)CCN1CCCN1C2=CC(C(F)(F)F)=CC=C2SC2=CC=CC=C21 MBHNWCYEGXQEIT-UHFFFAOYSA-N 0.000 description 1
- 102000011392 Galanin receptor Human genes 0.000 description 1
- 108050001605 Galanin receptor Proteins 0.000 description 1
- 101000930822 Giardia intestinalis Dipeptidyl-peptidase 4 Proteins 0.000 description 1
- 102000007446 Glucagon-Like Peptide-1 Receptor Human genes 0.000 description 1
- 108010086246 Glucagon-Like Peptide-1 Receptor Proteins 0.000 description 1
- 101800000224 Glucagon-like peptide 1 Proteins 0.000 description 1
- 102400000322 Glucagon-like peptide 1 Human genes 0.000 description 1
- 101800004266 Glucagon-like peptide 1(7-37) Proteins 0.000 description 1
- FAEKWTJYAYMJKF-QHCPKHFHSA-N GlucoNorm Chemical compound C1=C(C(O)=O)C(OCC)=CC(CC(=O)N[C@@H](CC(C)C)C=2C(=CC=CC=2)N2CCCCC2)=C1 FAEKWTJYAYMJKF-QHCPKHFHSA-N 0.000 description 1
- 208000002705 Glucose Intolerance Diseases 0.000 description 1
- 102000042092 Glucose transporter family Human genes 0.000 description 1
- 102000004366 Glucosidases Human genes 0.000 description 1
- 108010056771 Glucosidases Proteins 0.000 description 1
- 102000007390 Glycogen Phosphorylase Human genes 0.000 description 1
- 108010046163 Glycogen Phosphorylase Proteins 0.000 description 1
- 101000581402 Homo sapiens Melanin-concentrating hormone receptor 1 Proteins 0.000 description 1
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 1
- 102000004286 Hydroxymethylglutaryl CoA Reductases Human genes 0.000 description 1
- 108090000895 Hydroxymethylglutaryl CoA Reductases Proteins 0.000 description 1
- 208000035150 Hypercholesterolemia Diseases 0.000 description 1
- 206010060378 Hyperinsulinaemia Diseases 0.000 description 1
- 208000031226 Hyperlipidaemia Diseases 0.000 description 1
- 206010020772 Hypertension Diseases 0.000 description 1
- 206010061218 Inflammation Diseases 0.000 description 1
- 102000004877 Insulin Human genes 0.000 description 1
- 108090001061 Insulin Proteins 0.000 description 1
- 229940122199 Insulin secretagogue Drugs 0.000 description 1
- 102000036770 Islet Amyloid Polypeptide Human genes 0.000 description 1
- 108010041872 Islet Amyloid Polypeptide Proteins 0.000 description 1
- NHTMVDHEPJAVLT-UHFFFAOYSA-N Isooctane Chemical compound CC(C)CC(C)(C)C NHTMVDHEPJAVLT-UHFFFAOYSA-N 0.000 description 1
- GWESVXSMPKAFAS-UHFFFAOYSA-N Isopropylcyclohexane Natural products CC(C)C1CCCCC1 GWESVXSMPKAFAS-UHFFFAOYSA-N 0.000 description 1
- PMRVFZXOCRHXFE-FMEJWYFOSA-L Kad 1229 Chemical compound [Ca+2].C([C@@H](CC(=O)N1C[C@@H]2CCCC[C@@H]2C1)C(=O)[O-])C1=CC=CC=C1.C([C@@H](CC(=O)N1C[C@@H]2CCCC[C@@H]2C1)C(=O)[O-])C1=CC=CC=C1 PMRVFZXOCRHXFE-FMEJWYFOSA-L 0.000 description 1
- 102000000853 LDL receptors Human genes 0.000 description 1
- 108010001831 LDL receptors Proteins 0.000 description 1
- 108010018112 LY 315902 Proteins 0.000 description 1
- 102000016267 Leptin Human genes 0.000 description 1
- 108010092277 Leptin Proteins 0.000 description 1
- 229940127470 Lipase Inhibitors Drugs 0.000 description 1
- 229940086609 Lipase inhibitor Drugs 0.000 description 1
- 208000017170 Lipid metabolism disease Diseases 0.000 description 1
- 102000004895 Lipoproteins Human genes 0.000 description 1
- 108090001030 Lipoproteins Proteins 0.000 description 1
- 108010007859 Lisinopril Proteins 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- 102100027375 Melanin-concentrating hormone receptor 1 Human genes 0.000 description 1
- 208000001145 Metabolic Syndrome Diseases 0.000 description 1
- 241001465754 Metazoa Species 0.000 description 1
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 1
- CESYKOGBSMNBPD-UHFFFAOYSA-N Methyclothiazide Chemical compound ClC1=C(S(N)(=O)=O)C=C2S(=O)(=O)N(C)C(CCl)NC2=C1 CESYKOGBSMNBPD-UHFFFAOYSA-N 0.000 description 1
- IBAQFPQHRJAVAV-ULAWRXDQSA-N Miglitol Chemical compound OCCN1C[C@H](O)[C@@H](O)[C@H](O)[C@H]1CO IBAQFPQHRJAVAV-ULAWRXDQSA-N 0.000 description 1
- IRLWJILLXJGJTD-UHFFFAOYSA-N Muraglitazar Chemical compound C1=CC(OC)=CC=C1OC(=O)N(CC(O)=O)CC(C=C1)=CC=C1OCCC1=C(C)OC(C=2C=CC=CC=2)=N1 IRLWJILLXJGJTD-UHFFFAOYSA-N 0.000 description 1
- 101150027439 NPY1 gene Proteins 0.000 description 1
- 101150111774 NPY5R gene Proteins 0.000 description 1
- 229930193140 Neomycin Natural products 0.000 description 1
- 208000008589 Obesity Diseases 0.000 description 1
- 108091034117 Oligonucleotide Proteins 0.000 description 1
- 102000002512 Orexin Human genes 0.000 description 1
- 241000283973 Oryctolagus cuniculus Species 0.000 description 1
- 102000000536 PPAR gamma Human genes 0.000 description 1
- AHOUBRCZNHFOSL-UHFFFAOYSA-N Paroxetine hydrochloride Natural products C1=CC(F)=CC=C1C1C(COC=2C=C3OCOC3=CC=2)CNCC1 AHOUBRCZNHFOSL-UHFFFAOYSA-N 0.000 description 1
- 102000003728 Peroxisome Proliferator-Activated Receptors Human genes 0.000 description 1
- 108090000029 Peroxisome Proliferator-Activated Receptors Proteins 0.000 description 1
- CYLWJCABXYDINA-UHFFFAOYSA-N Polythiazide Polymers ClC1=C(S(N)(=O)=O)C=C2S(=O)(=O)N(C)C(CSCC(F)(F)F)NC2=C1 CYLWJCABXYDINA-UHFFFAOYSA-N 0.000 description 1
- XBDQKXXYIPTUBI-UHFFFAOYSA-M Propionate Chemical compound CCC([O-])=O XBDQKXXYIPTUBI-UHFFFAOYSA-M 0.000 description 1
- JYVXNLLUYHCIIH-ZCFIWIBFSA-N R-mevalonolactone, (-)- Chemical compound C[C@@]1(O)CCOC(=O)C1 JYVXNLLUYHCIIH-ZCFIWIBFSA-N 0.000 description 1
- 101100095088 Rattus norvegicus Slc5a2 gene Proteins 0.000 description 1
- 208000017442 Retinal disease Diseases 0.000 description 1
- 206010038923 Retinopathy Diseases 0.000 description 1
- AJLFOPYRIVGYMJ-UHFFFAOYSA-N SJ000287055 Natural products C12C(OC(=O)C(C)CC)CCC=C2C=CC(C)C1CCC1CC(O)CC(=O)O1 AJLFOPYRIVGYMJ-UHFFFAOYSA-N 0.000 description 1
- 229940124639 Selective inhibitor Drugs 0.000 description 1
- BLRPTPMANUNPDV-UHFFFAOYSA-N Silane Chemical compound [SiH4] BLRPTPMANUNPDV-UHFFFAOYSA-N 0.000 description 1
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 1
- 229940123518 Sodium/glucose cotransporter 2 inhibitor Drugs 0.000 description 1
- 229940100389 Sulfonylurea Drugs 0.000 description 1
- 102000003673 Symporters Human genes 0.000 description 1
- 108090000088 Symporters Proteins 0.000 description 1
- ATZKAUGGNMSCCY-VVFNRDJMSA-N [(1r,2r,3r)-2-[(3e)-4,8-dimethylnona-3,7-dienyl]-2-methyl-3-[(1e,5e)-2,6,10-trimethylundeca-1,5,9-trienyl]cyclopropyl]methyl phosphono hydrogen phosphate Chemical class CC(C)=CCC\C(C)=C\CC\C(C)=C\[C@@H]1[C@@H](COP(O)(=O)OP(O)(O)=O)[C@]1(C)CC\C=C(/C)CCC=C(C)C ATZKAUGGNMSCCY-VVFNRDJMSA-N 0.000 description 1
- 201000000690 abdominal obesity-metabolic syndrome Diseases 0.000 description 1
- 230000002159 abnormal effect Effects 0.000 description 1
- 229960002632 acarbose Drugs 0.000 description 1
- XUFXOAAUWZOOIT-UHFFFAOYSA-N acarviostatin I01 Natural products OC1C(O)C(NC2C(C(O)C(O)C(CO)=C2)O)C(C)OC1OC(C(C1O)O)C(CO)OC1OC1C(CO)OC(O)C(O)C1O XUFXOAAUWZOOIT-UHFFFAOYSA-N 0.000 description 1
- KXKVLQRXCPHEJC-UHFFFAOYSA-N acetic acid trimethyl ester Natural products COC(C)=O KXKVLQRXCPHEJC-UHFFFAOYSA-N 0.000 description 1
- LVZGQWKTUCVPBQ-UHFFFAOYSA-N acetic acid;trifluoroborane Chemical compound CC(O)=O.FB(F)F LVZGQWKTUCVPBQ-UHFFFAOYSA-N 0.000 description 1
- 229960001138 acetylsalicylic acid Drugs 0.000 description 1
- 230000002378 acidificating effect Effects 0.000 description 1
- DFDGRKNOFOJBAJ-UHFFFAOYSA-N acifran Chemical compound C=1C=CC=CC=1C1(C)OC(C(O)=O)=CC1=O DFDGRKNOFOJBAJ-UHFFFAOYSA-N 0.000 description 1
- 229950000146 acifran Drugs 0.000 description 1
- 229960003526 acipimox Drugs 0.000 description 1
- 230000003213 activating effect Effects 0.000 description 1
- 239000004480 active ingredient Substances 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 230000000996 additive effect Effects 0.000 description 1
- 150000008044 alkali metal hydroxides Chemical class 0.000 description 1
- 208000026935 allergic disease Diseases 0.000 description 1
- QYIXCDOBOSTCEI-UHFFFAOYSA-N alpha-cholestanol Natural products C1CC2CC(O)CCC2(C)C2C1C1CCC(C(C)CCCC(C)C)C1(C)CC2 QYIXCDOBOSTCEI-UHFFFAOYSA-N 0.000 description 1
- 229910052782 aluminium Inorganic materials 0.000 description 1
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 1
- 150000001408 amides Chemical class 0.000 description 1
- 150000001412 amines Chemical group 0.000 description 1
- 229940024606 amino acid Drugs 0.000 description 1
- 150000001413 amino acids Chemical class 0.000 description 1
- 229960004909 aminosalicylic acid Drugs 0.000 description 1
- HTIQEAQVCYTUBX-UHFFFAOYSA-N amlodipine Chemical compound CCOC(=O)C1=C(COCCN)NC(C)=C(C(=O)OC)C1C1=CC=CC=C1Cl HTIQEAQVCYTUBX-UHFFFAOYSA-N 0.000 description 1
- 229960000528 amlodipine Drugs 0.000 description 1
- 229940043376 ammonium acetate Drugs 0.000 description 1
- 235000019257 ammonium acetate Nutrition 0.000 description 1
- 239000002333 angiotensin II receptor antagonist Substances 0.000 description 1
- 229940044094 angiotensin-converting-enzyme inhibitor Drugs 0.000 description 1
- 238000010171 animal model Methods 0.000 description 1
- 229940127226 anticholesterol agent Drugs 0.000 description 1
- 229940058303 antinematodal benzimidazole derivative Drugs 0.000 description 1
- 230000003078 antioxidant effect Effects 0.000 description 1
- 239000000074 antisense oligonucleotide Substances 0.000 description 1
- 238000012230 antisense oligonucleotides Methods 0.000 description 1
- 125000004429 atom Chemical group 0.000 description 1
- 229950010046 avasimibe Drugs 0.000 description 1
- 210000000227 basophil cell of anterior lobe of hypophysis Anatomy 0.000 description 1
- 229960003515 bendroflumethiazide Drugs 0.000 description 1
- HDWIHXWEUNVBIY-UHFFFAOYSA-N bendroflumethiazidum Chemical compound C1=C(C(F)(F)F)C(S(=O)(=O)N)=CC(S(N2)(=O)=O)=C1NC2CC1=CC=CC=C1 HDWIHXWEUNVBIY-UHFFFAOYSA-N 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 150000001556 benzimidazoles Chemical class 0.000 description 1
- 229960001541 benzthiazide Drugs 0.000 description 1
- NDTSRXAMMQDVSW-UHFFFAOYSA-N benzthiazide Chemical compound C1=C(Cl)C(S(=O)(=O)N)=CC(S(N2)(=O)=O)=C1N=C2CSCC1=CC=CC=C1 NDTSRXAMMQDVSW-UHFFFAOYSA-N 0.000 description 1
- 239000002876 beta blocker Substances 0.000 description 1
- 229960000516 bezafibrate Drugs 0.000 description 1
- IIBYAHWJQTYFKB-UHFFFAOYSA-N bezafibrate Chemical compound C1=CC(OC(C)(C)C(O)=O)=CC=C1CCNC(=O)C1=CC=C(Cl)C=C1 IIBYAHWJQTYFKB-UHFFFAOYSA-N 0.000 description 1
- 150000004283 biguanides Chemical class 0.000 description 1
- 230000002051 biphasic effect Effects 0.000 description 1
- 238000009835 boiling Methods 0.000 description 1
- 229940043232 butyl acetate Drugs 0.000 description 1
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 239000000480 calcium channel blocker Substances 0.000 description 1
- 238000004364 calculation method Methods 0.000 description 1
- 239000003555 cannabinoid 1 receptor antagonist Substances 0.000 description 1
- 229960000830 captopril Drugs 0.000 description 1
- FAKRSMQSSFJEIM-RQJHMYQMSA-N captopril Chemical compound SC[C@@H](C)C(=O)N1CCC[C@H]1C(O)=O FAKRSMQSSFJEIM-RQJHMYQMSA-N 0.000 description 1
- 235000013877 carbamide Nutrition 0.000 description 1
- 238000003889 chemical engineering Methods 0.000 description 1
- 229960002155 chlorothiazide Drugs 0.000 description 1
- 229960003291 chlorphenamine Drugs 0.000 description 1
- 229960001761 chlorpropamide Drugs 0.000 description 1
- HVYWMOMLDIMFJA-DPAQBDIFSA-N cholesterol Chemical compound C1C=C2C[C@@H](O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@H]([C@H](C)CCCC(C)C)[C@@]1(C)CC2 HVYWMOMLDIMFJA-DPAQBDIFSA-N 0.000 description 1
- 230000001906 cholesterol absorption Effects 0.000 description 1
- 239000003354 cholesterol ester transfer protein inhibitor Substances 0.000 description 1
- 238000004587 chromatography analysis Methods 0.000 description 1
- 229960002174 ciprofibrate Drugs 0.000 description 1
- KPSRODZRAIWAKH-UHFFFAOYSA-N ciprofibrate Chemical compound C1=CC(OC(C)(C)C(O)=O)=CC=C1C1C(Cl)(Cl)C1 KPSRODZRAIWAKH-UHFFFAOYSA-N 0.000 description 1
- 229950003072 clinofibrate Drugs 0.000 description 1
- 229960001214 clofibrate Drugs 0.000 description 1
- KNHUKKLJHYUCFP-UHFFFAOYSA-N clofibrate Chemical compound CCOC(=O)C(C)(C)OC1=CC=C(Cl)C=C1 KNHUKKLJHYUCFP-UHFFFAOYSA-N 0.000 description 1
- TZWKUQDQKPYNLL-UHFFFAOYSA-N cloforex Chemical compound CCOC(=O)NC(C)(C)CC1=CC=C(Cl)C=C1 TZWKUQDQKPYNLL-UHFFFAOYSA-N 0.000 description 1
- 229950008294 cloforex Drugs 0.000 description 1
- HXCXASJHZQXCKK-UHFFFAOYSA-N clortermine Chemical compound CC(C)(N)CC1=CC=CC=C1Cl HXCXASJHZQXCKK-UHFFFAOYSA-N 0.000 description 1
- 229950000649 clortermine Drugs 0.000 description 1
- 229960002604 colestipol Drugs 0.000 description 1
- GMRWGQCZJGVHKL-UHFFFAOYSA-N colestipol Chemical compound ClCC1CO1.NCCNCCNCCNCCN GMRWGQCZJGVHKL-UHFFFAOYSA-N 0.000 description 1
- 230000000052 comparative effect Effects 0.000 description 1
- 238000004590 computer program Methods 0.000 description 1
- 238000011109 contamination Methods 0.000 description 1
- 239000013256 coordination polymer Substances 0.000 description 1
- 238000005388 cross polarization Methods 0.000 description 1
- 238000002447 crystallographic data Methods 0.000 description 1
- 150000001942 cyclopropanes Chemical class 0.000 description 1
- 229950006689 darglitazone Drugs 0.000 description 1
- 239000008367 deionised water Substances 0.000 description 1
- 229910021641 deionized water Inorganic materials 0.000 description 1
- 229960005227 delapril Drugs 0.000 description 1
- WOUOLAUOZXOLJQ-MBSDFSHPSA-N delapril Chemical compound C([C@@H](C(=O)OCC)N[C@@H](C)C(=O)N(CC(O)=O)C1CC2=CC=CC=C2C1)CC1=CC=CC=C1 WOUOLAUOZXOLJQ-MBSDFSHPSA-N 0.000 description 1
- 229960004597 dexfenfluramine Drugs 0.000 description 1
- 229940120124 dichloroacetate Drugs 0.000 description 1
- JXTHNDFMNIQAHM-UHFFFAOYSA-N dichloroacetic acid Chemical compound OC(=O)C(Cl)Cl JXTHNDFMNIQAHM-UHFFFAOYSA-N 0.000 description 1
- 230000037213 diet Effects 0.000 description 1
- 235000005911 diet Nutrition 0.000 description 1
- HSUGRBWQSSZJOP-RTWAWAEBSA-N diltiazem Chemical compound C1=CC(OC)=CC=C1[C@H]1[C@@H](OC(C)=O)C(=O)N(CCN(C)C)C2=CC=CC=C2S1 HSUGRBWQSSZJOP-RTWAWAEBSA-N 0.000 description 1
- 229960004166 diltiazem Drugs 0.000 description 1
- JVSWJIKNEAIKJW-UHFFFAOYSA-N dimethyl-hexane Natural products CCCCCC(C)C JVSWJIKNEAIKJW-UHFFFAOYSA-N 0.000 description 1
- 229940090124 dipeptidyl peptidase 4 (dpp-4) inhibitors for blood glucose lowering Drugs 0.000 description 1
- 239000001177 diphosphate Substances 0.000 description 1
- XPPKVPWEQAFLFU-UHFFFAOYSA-J diphosphate(4-) Chemical compound [O-]P([O-])(=O)OP([O-])([O-])=O XPPKVPWEQAFLFU-UHFFFAOYSA-J 0.000 description 1
- 238000004090 dissolution Methods 0.000 description 1
- 238000004821 distillation Methods 0.000 description 1
- 238000009826 distribution Methods 0.000 description 1
- 239000002934 diuretic Substances 0.000 description 1
- 229940030606 diuretics Drugs 0.000 description 1
- 238000001035 drying Methods 0.000 description 1
- 229960000873 enalapril Drugs 0.000 description 1
- GBXSMTUPTTWBMN-XIRDDKMYSA-N enalapril Chemical compound C([C@@H](C(=O)OCC)N[C@@H](C)C(=O)N1[C@@H](CCC1)C(O)=O)CC1=CC=CC=C1 GBXSMTUPTTWBMN-XIRDDKMYSA-N 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 229950002375 englitazone Drugs 0.000 description 1
- 210000002919 epithelial cell Anatomy 0.000 description 1
- 238000001704 evaporation Methods 0.000 description 1
- 230000008020 evaporation Effects 0.000 description 1
- 229960001519 exenatide Drugs 0.000 description 1
- 229950008696 farnesil Drugs 0.000 description 1
- 108091022862 fatty acid binding Proteins 0.000 description 1
- 229960001582 fenfluramine Drugs 0.000 description 1
- 229960002297 fenofibrate Drugs 0.000 description 1
- YMTINGFKWWXKFG-UHFFFAOYSA-N fenofibrate Chemical compound C1=CC(OC(C)(C)C(=O)OC(C)C)=CC=C1C(=O)C1=CC=C(Cl)C=C1 YMTINGFKWWXKFG-UHFFFAOYSA-N 0.000 description 1
- 239000012065 filter cake Substances 0.000 description 1
- 239000012467 final product Substances 0.000 description 1
- 239000012530 fluid Substances 0.000 description 1
- 229960003028 flumethiazide Drugs 0.000 description 1
- RGUQWGXAYZNLMI-UHFFFAOYSA-N flumethiazide Chemical compound C1=C(C(F)(F)F)C(S(=O)(=O)N)=CC2=C1NC=NS2(=O)=O RGUQWGXAYZNLMI-UHFFFAOYSA-N 0.000 description 1
- 229960002464 fluoxetine Drugs 0.000 description 1
- CJOFXWAVKWHTFT-XSFVSMFZSA-N fluvoxamine Chemical compound COCCCC\C(=N/OCCN)C1=CC=C(C(F)(F)F)C=C1 CJOFXWAVKWHTFT-XSFVSMFZSA-N 0.000 description 1
- 229960004038 fluvoxamine Drugs 0.000 description 1
- 229960002490 fosinopril Drugs 0.000 description 1
- 235000021588 free fatty acids Nutrition 0.000 description 1
- 238000004108 freeze drying Methods 0.000 description 1
- ZZUFCTLCJUWOSV-UHFFFAOYSA-N furosemide Chemical compound C1=C(Cl)C(S(=O)(=O)N)=CC(C(O)=O)=C1NCC1=CC=CO1 ZZUFCTLCJUWOSV-UHFFFAOYSA-N 0.000 description 1
- 229960003883 furosemide Drugs 0.000 description 1
- 230000004927 fusion Effects 0.000 description 1
- AIWAEWBZDJARBJ-PXUUZXDZSA-N fz7co35x2s Chemical compound C([C@@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](C)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CCCCN)C(=O)NCC(=O)N[C@@H](CCCN=C(N)N)C(=O)N[C@@H](CCCCNC(=O)COCCOCCNC(=O)CCN1C(C=CC1=O)=O)C(N)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCCCN)NC(=O)[C@H](C)NC(=O)[C@H](C)NC(=O)[C@H](CCC(N)=O)NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@@H](NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)[C@@H](C)NC(=O)[C@@H](N)CC=1N=CNC=1)[C@@H](C)O)[C@@H](C)O)C(C)C)C1=CC=CC=C1 AIWAEWBZDJARBJ-PXUUZXDZSA-N 0.000 description 1
- 230000002496 gastric effect Effects 0.000 description 1
- YRSVDSQRGBYVIY-GJZGRUSLSA-N gemopatrilat Chemical compound O=C1N(CC(O)=O)C(C)(C)CCC[C@@H]1NC(=O)[C@@H](S)CC1=CC=CC=C1 YRSVDSQRGBYVIY-GJZGRUSLSA-N 0.000 description 1
- 229950006480 gemopatrilat Drugs 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- WIGIZIANZCJQQY-RUCARUNLSA-N glimepiride Chemical compound O=C1C(CC)=C(C)CN1C(=O)NCCC1=CC=C(S(=O)(=O)NC(=O)N[C@@H]2CC[C@@H](C)CC2)C=C1 WIGIZIANZCJQQY-RUCARUNLSA-N 0.000 description 1
- 229960004346 glimepiride Drugs 0.000 description 1
- ZJJXGWJIGJFDTL-UHFFFAOYSA-N glipizide Chemical compound C1=NC(C)=CN=C1C(=O)NCCC1=CC=C(S(=O)(=O)NC(=O)NC2CCCCC2)C=C1 ZJJXGWJIGJFDTL-UHFFFAOYSA-N 0.000 description 1
- 229960001381 glipizide Drugs 0.000 description 1
- 108010063245 glucagon-like peptide 1 (7-36)amide Proteins 0.000 description 1
- 230000006377 glucose transport Effects 0.000 description 1
- 229940112611 glucovance Drugs 0.000 description 1
- 229930182470 glycoside Natural products 0.000 description 1
- 150000002338 glycosides Chemical class 0.000 description 1
- 229910052736 halogen Inorganic materials 0.000 description 1
- 150000002367 halogens Chemical class 0.000 description 1
- 238000003306 harvesting Methods 0.000 description 1
- 230000002440 hepatic effect Effects 0.000 description 1
- 229960001340 histamine Drugs 0.000 description 1
- 229960002003 hydrochlorothiazide Drugs 0.000 description 1
- 229960003313 hydroflumethiazide Drugs 0.000 description 1
- DMDGGSIALPNSEE-UHFFFAOYSA-N hydroflumethiazide Chemical compound C1=C(C(F)(F)F)C(S(=O)(=O)N)=CC2=C1NCNS2(=O)=O DMDGGSIALPNSEE-UHFFFAOYSA-N 0.000 description 1
- 239000001257 hydrogen Substances 0.000 description 1
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 1
- 230000003451 hyperinsulinaemic effect Effects 0.000 description 1
- 201000008980 hyperinsulinism Diseases 0.000 description 1
- 208000006575 hypertriglyceridemia Diseases 0.000 description 1
- 230000000871 hypocholesterolemic effect Effects 0.000 description 1
- 229950010293 imanixil Drugs 0.000 description 1
- 150000002460 imidazoles Chemical class 0.000 description 1
- 125000003454 indenyl group Chemical class C1(C=CC2=CC=CC=C12)* 0.000 description 1
- 230000004054 inflammatory process Effects 0.000 description 1
- 230000000977 initiatory effect Effects 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 238000009413 insulation Methods 0.000 description 1
- 239000004026 insulin derivative Substances 0.000 description 1
- 230000010354 integration Effects 0.000 description 1
- 239000013067 intermediate product Substances 0.000 description 1
- 210000000936 intestine Anatomy 0.000 description 1
- 150000002500 ions Chemical class 0.000 description 1
- 229960002198 irbesartan Drugs 0.000 description 1
- YCPOHTHPUREGFM-UHFFFAOYSA-N irbesartan Chemical compound O=C1N(CC=2C=CC(=CC=2)C=2C(=CC=CC=2)C=2[N]N=NN=2)C(CCCC)=NC21CCCC2 YCPOHTHPUREGFM-UHFFFAOYSA-N 0.000 description 1
- 230000007794 irritation Effects 0.000 description 1
- 208000028867 ischemia Diseases 0.000 description 1
- 125000000468 ketone group Chemical group 0.000 description 1
- 208000017169 kidney disease Diseases 0.000 description 1
- 230000003907 kidney function Effects 0.000 description 1
- NRYBAZVQPHGZNS-ZSOCWYAHSA-N leptin Chemical compound O=C([C@H](CO)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CO)NC(=O)CNC(=O)[C@H](CCC(N)=O)NC(=O)[C@@H](N)CC(C)C)CCSC)N1CCC[C@H]1C(=O)NCC(=O)N[C@@H](CS)C(O)=O NRYBAZVQPHGZNS-ZSOCWYAHSA-N 0.000 description 1
- 229940039781 leptin Drugs 0.000 description 1
- 102000005861 leptin receptors Human genes 0.000 description 1
- 108010019813 leptin receptors Proteins 0.000 description 1
- 239000003446 ligand Substances 0.000 description 1
- 230000037356 lipid metabolism Effects 0.000 description 1
- 229960002394 lisinopril Drugs 0.000 description 1
- UBJFKNSINUCEAL-UHFFFAOYSA-N lithium;2-methylpropane Chemical compound [Li+].C[C-](C)C UBJFKNSINUCEAL-UHFFFAOYSA-N 0.000 description 1
- WGOPGODQLGJZGL-UHFFFAOYSA-N lithium;butane Chemical compound [Li+].CC[CH-]C WGOPGODQLGJZGL-UHFFFAOYSA-N 0.000 description 1
- 230000004807 localization Effects 0.000 description 1
- 229960005060 lorcaserin Drugs 0.000 description 1
- XTTZERNUQAFMOF-QMMMGPOBSA-N lorcaserin Chemical compound C[C@H]1CNCCC2=CC=C(Cl)C=C12 XTTZERNUQAFMOF-QMMMGPOBSA-N 0.000 description 1
- KJJZZJSZUJXYEA-UHFFFAOYSA-N losartan Chemical compound CCCCC1=NC(Cl)=C(CO)N1CC1=CC=C(C=2C(=CC=CC=2)C=2[N]N=NN=2)C=C1 KJJZZJSZUJXYEA-UHFFFAOYSA-N 0.000 description 1
- 229960004773 losartan Drugs 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 239000011159 matrix material Substances 0.000 description 1
- 230000001404 mediated effect Effects 0.000 description 1
- 229950008446 melinamide Drugs 0.000 description 1
- 238000002844 melting Methods 0.000 description 1
- 230000008018 melting Effects 0.000 description 1
- 108020004999 messenger RNA Proteins 0.000 description 1
- XZWYZXLIPXDOLR-UHFFFAOYSA-N metformin Chemical compound CN(C)C(=N)NC(N)=N XZWYZXLIPXDOLR-UHFFFAOYSA-N 0.000 description 1
- 229960003105 metformin Drugs 0.000 description 1
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 description 1
- GYNNXHKOJHMOHS-UHFFFAOYSA-N methyl-cycloheptane Natural products CC1CCCCCC1 GYNNXHKOJHMOHS-UHFFFAOYSA-N 0.000 description 1
- AJLFOPYRIVGYMJ-INTXDZFKSA-N mevastatin Chemical compound C([C@H]1[C@@H](C)C=CC2=CCC[C@@H]([C@H]12)OC(=O)[C@@H](C)CC)C[C@@H]1C[C@@H](O)CC(=O)O1 AJLFOPYRIVGYMJ-INTXDZFKSA-N 0.000 description 1
- 229950009116 mevastatin Drugs 0.000 description 1
- BOZILQFLQYBIIY-UHFFFAOYSA-N mevastatin hydroxy acid Natural products C1=CC(C)C(CCC(O)CC(O)CC(O)=O)C2C(OC(=O)C(C)CC)CCC=C21 BOZILQFLQYBIIY-UHFFFAOYSA-N 0.000 description 1
- 229960001110 miglitol Drugs 0.000 description 1
- 229960003365 mitiglinide Drugs 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 238000012544 monitoring process Methods 0.000 description 1
- 150000004682 monohydrates Chemical class 0.000 description 1
- 239000012452 mother liquor Substances 0.000 description 1
- 229950001135 muraglitazar Drugs 0.000 description 1
- 230000035772 mutation Effects 0.000 description 1
- WGESLFUSXZBFQF-UHFFFAOYSA-N n-methyl-n-prop-2-enylprop-2-en-1-amine Chemical class C=CCN(C)CC=C WGESLFUSXZBFQF-UHFFFAOYSA-N 0.000 description 1
- 125000001624 naphthyl group Chemical group 0.000 description 1
- 229960000698 nateglinide Drugs 0.000 description 1
- OELFLUMRDSZNSF-BRWVUGGUSA-N nateglinide Chemical compound C1C[C@@H](C(C)C)CC[C@@H]1C(=O)N[C@@H](C(O)=O)CC1=CC=CC=C1 OELFLUMRDSZNSF-BRWVUGGUSA-N 0.000 description 1
- 229960004927 neomycin Drugs 0.000 description 1
- 201000001119 neuropathy Diseases 0.000 description 1
- 230000007823 neuropathy Effects 0.000 description 1
- 229960003512 nicotinic acid Drugs 0.000 description 1
- 235000001968 nicotinic acid Nutrition 0.000 description 1
- 239000011664 nicotinic acid Substances 0.000 description 1
- 229960001597 nifedipine Drugs 0.000 description 1
- HYIMSNHJOBLJNT-UHFFFAOYSA-N nifedipine Chemical compound COC(=O)C1=C(C)NC(C)=C(C(=O)OC)C1C1=CC=CC=C1[N+]([O-])=O HYIMSNHJOBLJNT-UHFFFAOYSA-N 0.000 description 1
- 150000002823 nitrates Chemical class 0.000 description 1
- 239000012299 nitrogen atmosphere Substances 0.000 description 1
- 235000020824 obesity Nutrition 0.000 description 1
- LVRLSYPNFFBYCZ-VGWMRTNUSA-N omapatrilat Chemical compound C([C@H](S)C(=O)N[C@H]1CCS[C@H]2CCC[C@H](N2C1=O)C(=O)O)C1=CC=CC=C1 LVRLSYPNFFBYCZ-VGWMRTNUSA-N 0.000 description 1
- 229950000973 omapatrilat Drugs 0.000 description 1
- 238000005580 one pot reaction Methods 0.000 description 1
- 108060005714 orexin Proteins 0.000 description 1
- 238000012261 overproduction Methods 0.000 description 1
- QXAMTEJJAZOINB-UHFFFAOYSA-N oxane-3,4,5-triol Chemical compound OC1COCC(O)C1O QXAMTEJJAZOINB-UHFFFAOYSA-N 0.000 description 1
- RVTZCBVAJQQJTK-UHFFFAOYSA-N oxygen(2-);zirconium(4+) Chemical compound [O-2].[O-2].[Zr+4] RVTZCBVAJQQJTK-UHFFFAOYSA-N 0.000 description 1
- 238000004806 packaging method and process Methods 0.000 description 1
- 229960002296 paroxetine Drugs 0.000 description 1
- 230000037361 pathway Effects 0.000 description 1
- 229950008492 pentopril Drugs 0.000 description 1
- 230000002093 peripheral effect Effects 0.000 description 1
- 208000033808 peripheral neuropathy Diseases 0.000 description 1
- 229940083256 peripheral vasodilators nicotinic acid and derivative Drugs 0.000 description 1
- 210000002824 peroxisome Anatomy 0.000 description 1
- 239000008024 pharmaceutical diluent Substances 0.000 description 1
- 230000000144 pharmacologic effect Effects 0.000 description 1
- ICFJFFQQTFMIBG-UHFFFAOYSA-N phenformin Chemical compound NC(=N)NC(=N)NCCC1=CC=CC=C1 ICFJFFQQTFMIBG-UHFFFAOYSA-N 0.000 description 1
- 229960003243 phenformin Drugs 0.000 description 1
- 229960005190 phenylalanine Drugs 0.000 description 1
- ACVYVLVWPXVTIT-UHFFFAOYSA-N phosphinic acid Chemical class O[PH2]=O ACVYVLVWPXVTIT-UHFFFAOYSA-N 0.000 description 1
- 230000000704 physical effect Effects 0.000 description 1
- 230000008288 physiological mechanism Effects 0.000 description 1
- 229950003624 picilorex Drugs 0.000 description 1
- PZJBWSQQDMRZHY-UHFFFAOYSA-N picilorex Chemical compound CC1NC(C2CC2)CC1C1=CC=C(Cl)C=C1 PZJBWSQQDMRZHY-UHFFFAOYSA-N 0.000 description 1
- 229960002797 pitavastatin Drugs 0.000 description 1
- 229910052697 platinum Inorganic materials 0.000 description 1
- 230000010287 polarization Effects 0.000 description 1
- 229920000371 poly(diallyldimethylammonium chloride) polymer Polymers 0.000 description 1
- 229960005483 polythiazide Drugs 0.000 description 1
- 229920000046 polythiazide Polymers 0.000 description 1
- 230000003389 potentiating effect Effects 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 238000001556 precipitation Methods 0.000 description 1
- 201000009104 prediabetes syndrome Diseases 0.000 description 1
- 230000002265 prevention Effects 0.000 description 1
- 230000035755 proliferation Effects 0.000 description 1
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 229960004063 propylene glycol Drugs 0.000 description 1
- 235000013772 propylene glycol Nutrition 0.000 description 1
- 102000004169 proteins and genes Human genes 0.000 description 1
- 108090000623 proteins and genes Proteins 0.000 description 1
- 238000005086 pumping Methods 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 150000003217 pyrazoles Chemical class 0.000 description 1
- 239000005297 pyrex Substances 0.000 description 1
- 150000003222 pyridines Chemical class 0.000 description 1
- 229960001455 quinapril Drugs 0.000 description 1
- JSDRRTOADPPCHY-HSQYWUDLSA-N quinapril Chemical compound C([C@@H](C(=O)OCC)N[C@@H](C)C(=O)N1[C@@H](CC2=CC=CC=C2C1)C(O)=O)CC1=CC=CC=C1 JSDRRTOADPPCHY-HSQYWUDLSA-N 0.000 description 1
- 229960003401 ramipril Drugs 0.000 description 1
- HDACQVRGBOVJII-JBDAPHQKSA-N ramipril Chemical compound C([C@@H](C(=O)OCC)N[C@@H](C)C(=O)N1[C@@H](C[C@@H]2CCC[C@@H]21)C(O)=O)CC1=CC=CC=C1 HDACQVRGBOVJII-JBDAPHQKSA-N 0.000 description 1
- 239000002464 receptor antagonist Substances 0.000 description 1
- 229940044551 receptor antagonist Drugs 0.000 description 1
- 229950005713 reglitazar Drugs 0.000 description 1
- 230000030558 renal glucose absorption Effects 0.000 description 1
- 208000007278 renal glycosuria Diseases 0.000 description 1
- 229960002354 repaglinide Drugs 0.000 description 1
- JZCPYUJPEARBJL-UHFFFAOYSA-N rimonabant Chemical compound CC=1C(C(=O)NN2CCCCC2)=NN(C=2C(=CC(Cl)=CC=2)Cl)C=1C1=CC=C(Cl)C=C1 JZCPYUJPEARBJL-UHFFFAOYSA-N 0.000 description 1
- XMSXOLDPMGMWTH-UHFFFAOYSA-N rivoglitazone Chemical compound CN1C2=CC(OC)=CC=C2N=C1COC(C=C1)=CC=C1CC1SC(=O)NC1=O XMSXOLDPMGMWTH-UHFFFAOYSA-N 0.000 description 1
- 229950010764 rivoglitazone Drugs 0.000 description 1
- 229960004586 rosiglitazone Drugs 0.000 description 1
- IMNTVVOUWFPRSB-JWQCQUIFSA-N sch-48461 Chemical compound C1=CC(OC)=CC=C1[C@H]1N(C=2C=CC(OC)=CC=2)C(=O)[C@@H]1CCCC1=CC=CC=C1 IMNTVVOUWFPRSB-JWQCQUIFSA-N 0.000 description 1
- 230000028327 secretion Effects 0.000 description 1
- 239000000952 serotonin receptor agonist Substances 0.000 description 1
- VGKDLMBJGBXTGI-SJCJKPOMSA-N sertraline Chemical compound C1([C@@H]2CC[C@@H](C3=CC=CC=C32)NC)=CC=C(Cl)C(Cl)=C1 VGKDLMBJGBXTGI-SJCJKPOMSA-N 0.000 description 1
- 229960002073 sertraline Drugs 0.000 description 1
- 238000007873 sieving Methods 0.000 description 1
- 229910052938 sodium sulfate Inorganic materials 0.000 description 1
- 235000011152 sodium sulphate Nutrition 0.000 description 1
- 239000007790 solid phase Substances 0.000 description 1
- 238000000638 solvent extraction Methods 0.000 description 1
- 238000005507 spraying Methods 0.000 description 1
- 238000000859 sublimation Methods 0.000 description 1
- 230000008022 sublimation Effects 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- 230000001629 suppression Effects 0.000 description 1
- 208000011580 syndromic disease Diseases 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 150000003505 terpenes Chemical class 0.000 description 1
- CXGTZJYQWSUFET-IBGZPJMESA-N tesaglitazar Chemical compound C1=CC(C[C@H](OCC)C(O)=O)=CC=C1OCCC1=CC=C(OS(C)(=O)=O)C=C1 CXGTZJYQWSUFET-IBGZPJMESA-N 0.000 description 1
- 229950004704 tesaglitazar Drugs 0.000 description 1
- 238000012360 testing method Methods 0.000 description 1
- 230000001225 therapeutic effect Effects 0.000 description 1
- 150000003577 thiophenes Chemical class 0.000 description 1
- 229950004514 torcetrapib Drugs 0.000 description 1
- 230000001988 toxicity Effects 0.000 description 1
- 231100000419 toxicity Toxicity 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- 230000009466 transformation Effects 0.000 description 1
- 230000007704 transition Effects 0.000 description 1
- GXPHKUHSUJUWKP-UHFFFAOYSA-N troglitazone Chemical compound C1CC=2C(C)=C(O)C(C)=C(C)C=2OC1(C)COC(C=C1)=CC=C1CC1SC(=O)NC1=O GXPHKUHSUJUWKP-UHFFFAOYSA-N 0.000 description 1
- 229960001641 troglitazone Drugs 0.000 description 1
- GXPHKUHSUJUWKP-NTKDMRAZSA-N troglitazone Natural products C([C@@]1(OC=2C(C)=C(C(=C(C)C=2CC1)O)C)C)OC(C=C1)=CC=C1C[C@H]1SC(=O)NC1=O GXPHKUHSUJUWKP-NTKDMRAZSA-N 0.000 description 1
- 238000001622 two pulse phase modulation pulse sequence Methods 0.000 description 1
- 210000002700 urine Anatomy 0.000 description 1
- 229960004699 valsartan Drugs 0.000 description 1
- SJSNUMAYCRRIOM-QFIPXVFZSA-N valsartan Chemical compound C1=CC(CN(C(=O)CCCC)[C@@H](C(C)C)C(O)=O)=CC=C1C1=CC=CC=C1C1=NN=N[N]1 SJSNUMAYCRRIOM-QFIPXVFZSA-N 0.000 description 1
- 208000019553 vascular disease Diseases 0.000 description 1
- 229960001722 verapamil Drugs 0.000 description 1
- 238000004457 water analysis Methods 0.000 description 1
- 230000029663 wound healing Effects 0.000 description 1
- 229910001928 zirconium oxide Inorganic materials 0.000 description 1
- IAIDUHCBNLFXEF-MNEFBYGVSA-N zofenopril Chemical compound C([C@@H](C)C(=O)N1[C@@H](C[C@@H](C1)SC=1C=CC=CC=1)C(O)=O)SC(=O)C1=CC=CC=C1 IAIDUHCBNLFXEF-MNEFBYGVSA-N 0.000 description 1
- 229960002769 zofenopril Drugs 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D309/00—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only ring hetero atom, not condensed with other rings
- C07D309/02—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only ring hetero atom, not condensed with other rings having no double bonds between ring members or between ring members and non-ring members
- C07D309/08—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only ring hetero atom, not condensed with other rings having no double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D309/10—Oxygen atoms
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7028—Compounds having saccharide radicals attached to non-saccharide compounds by glycosidic linkages
- A61K31/7034—Compounds having saccharide radicals attached to non-saccharide compounds by glycosidic linkages attached to a carbocyclic compound, e.g. phloridzin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/335—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin
- A61K31/35—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin having six-membered rings with one oxygen as the only ring hetero atom
- A61K31/351—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin having six-membered rings with one oxygen as the only ring hetero atom not condensed with another ring
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P5/00—Drugs for disorders of the endocrine system
- A61P5/48—Drugs for disorders of the endocrine system of the pancreatic hormones
- A61P5/50—Drugs for disorders of the endocrine system of the pancreatic hormones for increasing or potentiating the activity of insulin
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H15/00—Compounds containing hydrocarbon or substituted hydrocarbon radicals directly attached to hetero atoms of saccharide radicals
- C07H15/20—Carbocyclic rings
- C07H15/207—Cyclohexane rings not substituted by nitrogen atoms, e.g. kasugamycins
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H7/00—Compounds containing non-saccharide radicals linked to saccharide radicals by a carbon-to-carbon bond
- C07H7/04—Carbocyclic radicals
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Medicinal Chemistry (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Diabetes (AREA)
- Molecular Biology (AREA)
- Engineering & Computer Science (AREA)
- Epidemiology (AREA)
- Genetics & Genomics (AREA)
- Biochemistry (AREA)
- Biotechnology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Endocrinology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Obesity (AREA)
- Emergency Medicine (AREA)
- Hematology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Pyrane Compounds (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Pyrrole Compounds (AREA)
- Saccharide Compounds (AREA)
- Peptides Or Proteins (AREA)
Abstract
Una composicion farmaceutica que comprende una cantidad terapeuticamente eficaz de un solvato cristalino de (S)- propilenglicol ((S)-PG) de la estructura (forma SC-3) Ia**Fórmula**
Description
DESCRIPCIÓN
Composición farmacéutica que comprende un solvato de (S)-propilenglicol de (2S,3R,4S,5S,6R)-2-[4-cloro-3-(4-etoxibencil)-fenil]-6-hidroximetil-2-metoxi-tetrahidro-piran-3,4,5-triol cristalino
Campo de la invención
La presente invención se refiere a composiciones farmacéuticas que comprenden estructuras cristalinas polimórficas ácidas libres de inhibidores de SGLT2.
Antecedentes de la invención
Aproximadamente 100 millones de personas en todo el mundo padecen diabetes tipo II (NIDDM), que se caracteriza por hiperglucemia debido a la producción excesiva de glucosa hepática y la resistencia periférica a la insulina, cuyas causas originales aún se desconocen. El control constante de los niveles de glucosa en plasma en pacientes con diabetes puede contrarrestar el desarrollo de complicaciones diabéticas y la falla de las células beta observada en la enfermedad avanzada.
La glucosa plasmática normalmente se filtra en el riñón en el glomérulo y se reabsorbe activamente en el túbulo proximal. El noventa por ciento de la recaptación de glucosa en el riñón ocurre en las células epiteliales del segmento S1 temprano del túbulo proximal cortical renal. SGLT2, una proteína de 672 aminoácidos que contiene 14 segmentos que atraviesan la membrana que se expresa predominantemente en el segmento S1 temprano de los túbulos proximales renales, es probable que sea el principal transportador responsable de esta recaptación. La especificidad del sustrato, la dependencia del sodio y la localización de SGLT2 son consistentes con las propiedades del transportador de glucosa dependiente de sodio de alta capacidad y baja afinidad previamente caracterizado en túbulos proximales corticales de riñón humano. Además, los estudios de agotamiento del híbrido implican SGLT2 como el cotransportador de Na+/glucosa predominante en el segmento S1 del túbulo proximal, ya que prácticamente toda la actividad de transporte de glucosa dependiente de Na codificada en ARNm de la corteza renal de rata es inhibida por un oligonucleótido antisentido específico para SGLT2 de rata. En humanos, las mutaciones en SGLT2 se han asociado con formas familiares de glucosuria renal, lo que proporciona más evidencia del papel principal de SGLT2 en la reabsorción renal de glucosa. En tales pacientes, la morfología renal y la función renal son por lo demás normales. Se predijo que la inhibición de SGLT2 reduciría los niveles de glucosa en plasma a través de una mayor excreción de glucosa en pacientes diabéticos.
La inhibición selectiva de SGLT2 en pacientes diabéticos podría normalizar la glucosa en plasma mejorando la excreción de glucosa en la orina, mejorando así la sensibilidad a la insulina y retrasando el desarrollo de complicaciones diabéticas, en ausencia de efectos secundarios gastrointestinales significativos. El documento WO 2004/063209 describe 1-C-(6-doro-4-etoxidifenilmetano-3-N-p-D-glucopiranosa y el correspondiente complejo de L-fenilalanina del mismo.
Sumario de la invención
Se describen en este documento las estructuras cristalinas de un compuesto de la fórmula I
En un aspecto, la invención proporciona una composición farmacéutica que comprende una cantidad terapéuticamente eficaz de un solvato de (S)-propilenglicol ((S)-PG) cristalino de la estructura (forma SC-3)Ia
Compuesto la
También se describe la estructura (R)-propilenglicol ((R)-PG) Ib que es la forma SD-3
y métodos para tratar la diabetes y enfermedades relacionadas utilizando las estructuras cristalinas del compuesto la. El compuesto de fórmula I en la forma de un sólido no cristalino se describe en la patente de los Estados Unidos N° 6.515.117. También se describe un proceso para la preparación del compuesto cristalino (S)-PG de la estructura Ia (forma SC-3)
Compuesto Ia
que incluye las etapas de proporcionar un compuesto A (preparado como se describe en la solicitud de los Estados Unidos N° de serie 10/745.075 presentada el 23 de diciembre de 2003, ejemplos 17 a 20), de la estructura
tratando el compuesto A con un disolvente alcohólico tal como metanol o etanol y una base acuosa tal como hidróxido de sodio, y agua, si es necesario, bajo una atmósfera inerte, y temperatura elevada, si es necesario, añadiendo un ácido tal como ácido clorhídrico para neutralizar la mezcla de reacción, para formar el compuesto I de la estructura
y tratar la mezcla de reacción que contiene el compuesto I con un disolvente orgánico tal como metil t-butil éter, un acetato de alquilo tal como acetato de etilo, acetato de metilo, acetato de isopropilo o acetato de butilo, y (S)-propilenglicol, opcionalmente añadiendo semillas del compuesto Ia (S)-PG (SC-3) a la mezcla, para formar el compuesto (S)-PG Ia (forma SC-3).
También se describe en este documento un proceso para preparar el compuesto cristalino (R)-PG de la estructura Ib (forma SD-3)
(R)-propMenglicol
que es similar al proceso para preparar (S)-PG la (forma SC-3) descrito anteriormente excepto que se emplea (R)-propilenglicol en lugar de (S)-propilenglicol.
También se describe en este documento un proceso novedoso para preparar el compuesto Ia
que incluye la etapa de reducir un compuesto B de la estructura
para eliminar el grupo metoxi por tratamiento del compuesto B (preparado como se describe en la solicitud de Estados Unidos con N° de Serie 10/745.075 presentada el 23 de diciembre de 2003, Ejemplo 17), o un solvato cristalino tal como el solvato de dimetanol Ig o el solvato 1,4-butino-diol (If), con un agente reductor, tal como hidruro de trietilsililo y un grupo de activación que es un ácido de Lewis tal como BF3^Et2O o BF 3 ^2CH 3 COOH, preferiblemente BF 3 ^2CH a COOH, y un disolvente orgánico tal como CH3CN, y agua añadida, separando el compuesto de la estructura I
y tratando el compuesto I con (S)-propilenglicol en presencia de un disolvente tal como t-butil metil éter, opcionalmente con semillas del compuesto Ia ((S)-PG), para formar una suspensión cristalina del compuesto Ia ((S)-PG) y separando el compuesto Ia ((S)-PG).
El proceso anterior es una operación de un solo recipiente que minimiza la producción de productos intermedios, dando como resultado un rendimiento y una prioridad mejorados del compuesto cristalino Ia final.
El compuesto cristalino Ia, al que también se hace referencia como el solvato de (S)-propilenglicol del compuesto I, es una estructura cristalina novedosa.
El compuesto de fórmula B (forma amorfa) se describe en la solicitud de los Estados Unidos con N.° de serie 10/745.075, presentada el 23 de diciembre de 2003.
El compuesto I se puede preparar disolviendo el compuesto A en etanol preferiblemente calentando a ebullición para formar un producto oleoso que es el compuesto I.
Breve descripción de las figuras
La invención se ilustra por referencia a los dibujos adjuntos descritos a continuación.
La Figura 1 muestra los patrones de difracción de rayos X de polvo calculados (simulados a 25°C) y observados (experimentales a temperatura ambiente) de la estructura cristalina (S)-PG la, forma SC-3.
La Figura 2 muestra el patrón de difracción de rayos X de polvo observado (experimental a temperatura ambiente) de la estructura cristalina Ib (R)-PG.
La Figura 3 muestra el espectro de RMN 13C CPMAS para la estructura cristalina (S)-PG de la forma SC-3.
La Figura 4 muestra el espectro de RMN 13C CPMAS para la estructura cristalina (R)-PG de Ib.
La Figura 5 muestra una curva de análisis termogravimétrico (TGA) de la estructura cristalina (S)-PG de Ia, forma SC-3. La Figura 6 muestra una curva de análisis termogravimétrico (TGA) de la estructura cristalina (R)-PG de lb, forma SD-3. La Figura 7 muestra un termograma de calorimetría diferencial de barrido (DSC) de la estructura cristalina (S)-PG del compuesto de la forma Ia, forma SC-3.
La Figura 8 muestra un termograma de calorimetría diferencial de barrido (DSC) de la estructura cristalina (R)-PG de Ib. La Figura 9 muestra un patrón de difracción de rayos X de polvo observado (experimental a temperatura ambiente) de la estructura cristalina If del solvato de 1,4-butino-diol.
La Figura 10 muestra un patrón de difracción de rayos X de polvo observado (experimental a temperatura ambiente) diagrama de la estructura cristalina Ig del solvato de dimetanol.
La Figura 11 muestra un termograma de calorimetría diferencial de barrido (DSC) de la estructura cristalina If del solvato de 1,4-butino-diol.
La Figura 12 es una representación esquemática de una configuración de reacción continua.
Descripción detallada de la invención
La presente invención proporciona una composición farmacéutica que comprende una cantidad terapéuticamente eficaz de un solvato de (S)-propilenglicol ((S)-PG) cristalino de la estructura (forma SC-3) Ia.
El término "farmacéuticamente aceptable", como se usa en el presente documento, se refiere a aquellos compuestos, materiales, composiciones y/o formas de dosificación que, dentro del alcance de un buen juicio médico, son adecuados para el contacto con los tejidos de seres humanos y animales sin toxicidad excesiva, irritación, respuesta alérgica u otras complicaciones problemáticas acorde con una relación razonable beneficio/riesgo. En ciertas realizaciones preferidas, las estructuras cristalinas del compuesto I de la invención esté en forma sustancialmente pura. El término "sustancialmente pura", como se usa en este documento, significa un compuesto que tiene una pureza aproximadamente mayor al 90% que incluye, por ejemplo, aproximadamente 91%, aproximadamente 92%, aproximadamente 93%, aproximadamente 94%, aproximadamente 95%, aproximadamente 96%, aproximadamente 97%, aproximadamente 98%, aproximadamente 99% y aproximadamente 100%.
La capacidad de un compuesto para existir en diferentes estructuras cristalinas se conoce como polimorfismo. Como se usa en el presente documento, "polimorfo" se refiere a formas cristalinas que tienen la misma composición química pero diferentes disposiciones espaciales de las moléculas, átomos y/o iones que forman el cristal. Aunque los polimorfos tienen la misma composición química, difieren en el empaquetamiento y la disposición geométrica, y pueden exhibir diferentes propiedades físicas tales como punto de fusión, forma, color, densidad, dureza, deformabilidad, estabilidad, disolución y similares. Dependiendo de su relación temperatura-estabilidad, dos polimorfos pueden ser monotrópicos o enantiotrópicos. Para un sistema monotrópico, la estabilidad relativa entre las dos fases sólidas permanece sin cambios a medida que cambia la temperatura. Por el contrario, en un sistema enantiotrópico existe una temperatura de transición a la cual se invierte la estabilidad de las dos fases. (Theory and Origin of Polymorphism en "Polymorphism in Pharmaceutical Solids" (1999) ISBN-8247-0237).
Las muestras de las estructuras cristalinas en las composiciones farmacéuticas de la invención pueden proporcionarse con homogeneidad de fase sustancialmente pura, lo que indica la presencia de una cantidad dominante de una única estructura cristalina y opcionalmente cantidades menores de una o más estructuras cristalinas diferentes. La presencia de más de una estructura cristalina en una muestra puede determinarse mediante técnicas tales como la difracción de rayos X de polvo (PXRD) o espectroscopía de resonancia magnética nuclear en estado sólido (SSNMR). Por ejemplo, la presencia de picos adicionales en la comparación de un patrón de PXRD medido experimentalmente (observado) con un patrón de PXRD simulado (calculado) puede indicar más de una estructura cristalina en la muestra. El PXRD simulado se puede calcular a partir de datos de rayos X de un solo cristal. (Véase Smith, D.K., "A FORTRAN Program for Calculating X-Ray Powder Diffraction Patterns," Lawrence Radiation Laboratory, Livermore, California, UCRL-7196, abril de 1963; véase también Yin. S., Scaringe, R.P., DiMarco, J., Galella, M. and Gougoutas, J.Z., American Pharmaceutical Review, 2003, 6, 2, 80). Preferiblemente, la estructura cristalina tiene una homogeneidad de fase sustancialmente pura como se
indica por menos de 10%, preferiblemente menos de 5% y más preferiblemente menos de 2% del área total del pico en el patrón de PXRD medido experimentalmente que surge de los picos extra que están ausentes del patrón de PXRD simulado. La más preferida es una estructura cristalina de la invención que tiene una homogeneidad de fase sustancialmente pura con menos del 1% del área total del pico en el patrón de PXRD medido experimentalmente que surge de los picos adicionales que están ausentes del patrón de PXRD simulado.
Las diversas estructuras cristalinas descritas en este documento pueden distinguirse entre sí mediante el uso de diversas técnicas analíticas conocidas por los expertos en la técnica. Tales técnicas incluyen, pero no se limitan a, espectroscopía de resonancia magnética nuclear en estado sólido (SSNMR), difracción de rayos X de polvo (PXRD), calorimetría diferencial de barrido (DSC) y/o análisis termogravimétrico (TGA).
Preparación de estructuras cristalinas
Las estructuras cristalinas en las composiciones farmacéuticas de la invención se pueden preparar mediante una diversidad de métodos, que incluyen, por ejemplo, cristalización o recristalización en un disolvente adecuado, sublimación, crecimiento a partir de una fusión, transformación en estado sólido a partir de otra fase, cristalización de un fluido supercrítico, y pulverización por chorro. Las técnicas para la cristalización o recristalización de estructuras cristalinas a partir de una mezcla de disolventes incluyen, por ejemplo, evaporación del disolvente, disminución de la temperatura de la mezcla de disolventes, siembra cristalina de una mezcla disolvente sobresaturada de la molécula y/o sal, liofilización de la mezcla de disolventes, y adición de antidisolventes (contradisolventes) a la mezcla de disolventes. Se pueden emplear técnicas de cristalización de alto rendimiento para preparar estructuras cristalinas, que incluyen polimorfos.
Cristales de fármacos, incluyendo polimorfos, métodos de preparación y caracterización de cristales de fármacos se discuten en Solid-State Chemistry of Drugs, S.R. Byrn, R.R. Pfeiffer, y J.G. Stowell, 2da Edición, SSCI, West Lafayette, Indiana, 1999.
Se pueden agregar cristales semilla a cualquier mezcla de cristalización para promover la cristalización. Como será evidente para el experto en la materia, la siembra se usa como un medio para controlar el crecimiento de una estructura cristalina particular o como un medio para controlar la distribución del tamaño de partícula del producto cristalino. De acuerdo con esto, el cálculo de la cantidad de semillas necesarias depende del tamaño de la semilla disponible y del tamaño deseado de una partícula promedio de producto como se describe, por ejemplo, en "Programmed cooling of batch crystallizers", J.W. Mullin y J. Nyvlt, Chemical Engineering Science, 1971, 26, 369-377. En general, las semillas de pequeño tamaño son necesarias para controlar eficazmente el crecimiento de cristales en el lote. Las semillas de pequeño tamaño pueden generarse mediante tamizando, molienda o micronizado de cristales más grandes o mediante microcristalización de soluciones. Debe tenerse cuidado de que la molienda o micronizado de cristales no dé como resultado ningún cambio en la cristalinidad de la estructura cristalina deseada (es decir, cambio a amorfo o a otro polimorfo).
Como se usa en el presente documento, el término "temperatura ambiente" o "TA" indica una temperatura ambiente de 20 a 25°C (68-77°F).
En general, en la preparación del compuesto cristalino Ia como se describe a continuación, se emplearán disolvente(s) para permitir la formación del compuesto cristalino Ia, preferiblemente que tenga una densidad aparente como se describe a continuación.
El compuesto cristalino de la estructura Ia (S-PG) SC-3 puede prepararse de acuerdo con la siguiente reacción telescópica como se muestra en el Esquema I.
ESQUEMA I
OH B Ciclohexano
Como se observa en el Esquema I, el compuesto B o If o Ig (denominado colectivamente como compuesto B) en el que el compuesto B en forma de un sólido amorfo o sólido cristalino (If o Ig) se trata con un agente reductor tal como hidruro de sililo, preferiblemente un hidruro de alquilsililo, más preferiblemente trietilsilano (o hidruro de trietilsililo), en presencia de un grupo de activación que es un ácido de Lewis, tal como BC b ^Me2S, BBr 3 , BF 3 OEt 2 , BC b o BF 3 ^2CH 3 COOH, preferiblemente BF 3 OEt 2 o BF 3 ^2CH 3 COOH y un disolvente orgánico tal como CH3CN, CH 3 CN/tolueno o CH3CN/ diclorometano, cloruro de metileno o agua, a una temperatura dentro del intervalo de aproximadamente -15 a aproximadamente 25°C, preferiblemente de aproximadamente 5 a aproximadamente 10°C, para reducir el compuesto B y formar el correspondiente compuesto base I
que se separa de la mezcla de reacción y se trata con (S)-propilenglicol ((S)-PG) y un disolvente orgánico tal como un acetato de alquilo como se expuso aquí anteriormente, preferiblemente acetato de isopropilo o t-butil metil éter (MTBE), y opcionalmente semillas del compuesto ((S)-PG) Ia (relación molar de semillas de Ia:compuesto B dentro del intervalo de aproximadamente 0,1 a aproximadamente 10%, preferiblemente de aproximadamente 0,5% a aproximadamente 3%), para formar una suspensión cristalina del compuesto ((S)-PG) Ia y separando el compuesto cristalino ((S)-PG) Ia de la suspensión cristalina.
Al llevar a cabo la reacción controlada anterior del Esquema I, se empleará el agente reductor de sililo en una relación molar al compuesto B dentro del intervalo de aproximadamente 1,2:1 a aproximadamente 4,5:1, preferiblemente de aproximadamente 2:1 a aproximadamente 4:1, mientras que el grupo activador (ácido de Lewis) se empleará en una relación molar respecto al agente reductor de sililo en el intervalo de aproximadamente 1,2:1 a aproximadamente 4,5:1, preferiblemente de aproximadamente 2:1 a aproximadamente 4:1. Se empleará (S)-propilenglicol ((S)-PG) en una relación molar respecto al compuesto B en el intervalo de aproximadamente 0,9:1 a aproximadamente 1,5:1, preferiblemente de aproximadamente 0,98:1 a aproximadamente 1,2:1; se empleará agua en una relación molar respecto a (S)-PG dentro del intervalo de aproximadamente 0,95:1 a aproximadamente 5:1, preferiblemente de aproximadamente 0,99:1 a aproximadamente 2:1.
El compuesto cristalino de la estructura Ia ((S)-PG) forma SC-3 también se puede preparar de acuerdo con el Esquema II de reacción expuesto a continuación.
ESQUEMA II
Compuesto A
(S)-PG
forma SC-3
en el que el compuesto A se trata con un disolvente alcohólico tal como metanol, etanol o alcohol isopropílico, preferiblemente metanol, agua y base acuosa tal como un hidróxido de metal alcalino tal como NaOH, KOH o LiOH, preferiblemente NaOH, preferiblemente bajo una atmósfera inerte tal como nitrógeno, a una temperatura elevada dentro del intervalo de aproximadamente 50 a aproximadamente 85°C, preferiblemente de aproximadamente 60 a aproximadamente 80°C para formar el compuesto I.
La base acuosa se empleará en una relación molar de compuesto A en el intervalo de aproximadamente 3,5:1 a aproximadamente 5,5:1, preferiblemente de aproximadamente 3:1 a aproximadamente 5:1.
La mezcla de reacción que contiene el compuesto I se trata con un disolvente orgánico tal como metil-butil-éter (MTBE) o un acetato de alquilo como se describió anteriormente, preferiblemente acetato de isopropilo, o MTBE, para separar el compuesto I que se trata con (S)-propilenglicol para formar una suspensión espesa que contiene el producto cristalino Ia (S)-PG, forma SC-3. Opcionalmente, las semillas del compuesto ((S)-PG) Ia se agregan a la mezcla de reacción. El compuesto cristalino Ia se separa de la suspensión usando procedimientos convencionales, por ejemplo, se trata la suspensión del compuesto Ia con un disolvente orgánico tal como ciclohexano, isooctano o metil ciclohexano, preferiblemente ciclohexano, y se recupera el compuesto cristalino Ia.
Al llevar a cabo la formación del compuesto Ia, el (S)-PG se emplea en una relación molar respecto al compuesto I con el intervalo de aproximadamente 0,9:1 a aproximadamente 1,5:1, preferiblemente de aproximadamente 0,98:1 a aproximadamente 1,2:1.
Como se indicó anteriormente, el solvato Ib de (R)-propilenglicol del compuesto I se puede preparar de manera similar al correspondiente solvato de (S)-propilenglicol, excepto que se usa (R)-propilenglicol en lugar de (S)-propilenglicol.
El proceso para preparar la forma cristalina del compuesto B, es decir, If, se lleva a cabo de acuerdo con el Esquema IV que se expone a continuación.
El solvato de 1,4-butin-diol cristalino If se puede preparar de acuerdo con el siguiente Esquema IV de reacción.
ESQUEMA IV
en el que el compuesto B no cristalino (que puede prepararse como se describe en la solicitud de patente de Estados Unidos N° de serie 10 / 745.075 presentada el 23 de diciembre de 2003 o en la patente de Estados Unidos N° 6.515.117), preferiblemente en forma sustancialmente pura (por ejemplo 50 a 100% puro ), se mezcla con tolueno / acetato de alquilo (tal como acetato de etilo), y la mezcla se calienta a una temperatura dentro del intervalo de aproximadamente 50 a aproximadamente 70°C, preferiblemente de aproximadamente 55 a aproximadamente 65°C, se agrega 2-butino-1,4-diol y se calienta como se indicó anteriormente hasta que el diol se disuelve, se añaden las semillas del compuesto If y la mezcla se enfría para formar cristales del compuesto If.
En un proceso alternativo para preparar el compuesto cristalino If, el compuesto B se disuelve en acetato de alquilo (tal como acetato de butilo) o una mezcla de acetato de alquilo / heptano (0,5:1 a 1,5:1) a una temperatura elevada dentro del intervalo de aproximadamente 50 a aproximadamente 70°C, preferiblemente de aproximadamente 55 a aproximadamente 65°C, se agrega 1,4-butin-diol, y la mezcla se enfría a temperatura ambiente para formar cristales del compuesto If. El compuesto If puede cristalizarse a partir de una mezcla de compuesto B y tolueno / acetato de alquilo (preferiblemente acetato de etilo) que contiene una relación en volumen de tolueno respecto a acetato de alquilo dentro del intervalo de aproximadamente 1:1 a aproximadamente 19:1, preferiblemente de aproximadamente 4:1 a aproximadamente 9:1. La mezcla de tolueno / acetato de alquilo incluirá suficiente tolueno para proporcionar una relación molar con el compuesto B dentro del intervalo de aproximadamente 40:1 a aproximadamente 90:1, preferiblemente de aproximadamente 60:1 a aproximadamente 80:1, para permitir la formación del solvato If de 1,4-butileno-diol.
La cristalización para formar solvato de 1,4-butin-diol puede realizarse más fácilmente empleando cristales de siembra del compuesto If en una cantidad de aproximadamente 0,1 a aproximadamente 10%, preferiblemente de aproximadamente 0,5 a aproximadamente 3% con base en el peso del compuesto de partida B.
Alternativamente, el compuesto If se puede cristalizar a partir de una mezcla de compuesto B y acetato de alquilo / heptano (preferiblemente acetato de butilo / tolueno) opcionalmente con siembra con semillas de compuesto cristalino If.
El solvato If de 1,4-butin-diol cristalino también se puede preparar en un proceso continuo como se muestra en el Esquema IVA.
La síntesis del solvato If implica dos etapas secuenciales con el compuesto E y el compuesto D: (1) litiación del compuesto E para generar un compuesto intermedio G litiado, y (2) acoplamiento del compuesto intermedio G litiado con el compuesto D.
ESQUEMA IV A
Con referencia ahora a la Figura 12, se muestra un diagrama esquemático de flujo del proceso (similar al descrito en la patente de Estados Unidos N° 7.164.015). El proceso completo para preparar el compuesto If, tal como se muestra en el Esquema IVA, se realiza en condiciones no criogénicas. Un reactivo aromático E que tiene un grupo adecuado para el intercambio de Li y halógeno se almacena en un primer recipiente 1 a temperatura ambiente. Un reactivo de litio Q se alimenta a un segundo recipiente 2, también a temperatura ambiente. El reactivo aromático E y el reactivo de litio Q se transfieren desde los recipientes 1 y 2 a través de las bombas 3 y 4, respectivamente, a un primer mezclador 5 estático encamisado. La temperatura de una reacción para producir una especie de anión litiado está regulada aproximadamente a partir de -30°C hasta aproximadamente 20°C, en el primer mezclador 5 mediante un enfriador 6.
La especie de anión litiado G así formada se alimenta directamente desde el primer mezclador 5 a un segundo mezclador 22 estático a lo largo de una línea 19 de transferencia convencional. Un reactivo D sustituido con carbonilo se alimenta a un tercer recipiente 20 a temperatura ambiente y se transfiere mediante la bomba 21 a través del enfriador 26 donde se enfría a una temperatura dentro del intervalo de aproximadamente -10 a aproximadamente -30°C, y luego pasar al segundo mezclador 22 estático encamisado. Una reacción para producir un producto de glucósido H se regula en el segundo mezclador 22 mediante un segundo enfriador 23.
El procesamiento adicional en condiciones de glicosidación ocurre cuando H se alimenta a un reactor 25 convencional donde se trata con ácido en un disolvente alcohólico, preferiblemente MSA/MeOH o HCl/MeOH, para formar H' (hemicetal desililado) que se convierte adicionalmente en glicósido B. El tratamiento adicional y la nueva extracción y la cristalización con 2-butileno-1,4-diol (J) en tolueno / EtOAc producen producto cristalino If. El reactor 25 puede mantenerse a temperatura ambiente u otra temperatura no criogénica durante el curso de cualquier reacción posterior.
El reactivo de litio utilizado es deseablemente un reactivo de organolitio. Los reactivos de organolitio adecuados incluyen n-BuLi, s-BuLi y t-BuLi. Otros serán evidentes para los expertos en la técnica.
Después de la finalización de la reacción, el producto deseado If puede aislarse y purificarse según técnicas ampliamente conocidas en el campo de la química orgánica (por ejemplo, precipitación, extracción con disolvente, recristalización y cromatografía). El compuesto desprotegido puede ser un compuesto intermedio o producto final útil. El compuesto If
puede hacerse reaccionar adicionalmente para obtener sales básicas o de adición de ácido farmacéuticamente aceptables, usando métodos que serán conocidos por los expertos en la técnica.
La temperatura y el tiempo de reacción son dos parámetros importantes en el diseño de un proceso continuo mostrado en el Esquema IVA: la litiación puede operarse continuamente desde -30°C (o inferior) hasta 20°C (o superior), preferiblemente desde aproximadamente -17° hasta aproximadamente -10°C, con minutos a segundos de tiempo de reacción. Para la posterior reacción de acoplamiento, la corriente del derivado litiado G se mezcla adicionalmente con la corriente del compuesto D (la tercera alimentación) en un mezclador. El flujo mixto puede enviarse luego a un reactor de flujo si se necesita un tiempo de reacción adicional para completarla. La reacción de acoplamiento se puede operar continuamente a temperaturas más altas de -30°C a -10°C (o más), preferiblemente de aproximadamente -30° a aproximadamente -20°C, con minutos a segundos de tiempo de reacción. La corriente de acoplamiento se envía luego a un reactor discontinuo para reacciones adicionales como se describe en este documento. Con el procesamiento continuo, las reacciones de litiación y acoplamiento pueden integrarse y operarse a temperaturas más elevadas utilizando reactores de flujo más pequeños con un control de temperatura eficiente, en comparación con los reactores criogénicos por lotes a escala.
La temperatura de operación de litiación continua en el proceso anterior puede ser tan alta como 20°C (sin limitación), preferiblemente -17 a -10°C, mientras genera > 95 RAP, del compuesto intermedio litiado G deseado.
En la reacción de acoplamiento, el producto de acoplamiento del proceso anterior a -20°C a -30°C, preferiblemente en el intervalo de 70-79 RAP.
El compuesto If se puede emplear para preparar el compuesto intermedio cristalino A como se muestra en el Esquema IVB.
ESQUEMA IVB
Preparación del compuesto intermedio A
Con referencia al Esquema IVB, el compuesto sólido If, DMAP sólido, acetonitrilo líquido y anhídrido acético líquido se calientan a una temperatura dentro del intervalo de aproximadamente 70 a aproximadamente 85°C y se mantienen hasta que se completa la reacción.
El lote se enfría (por ejemplo, 5°C). Se añaden a la mezcla de reacción trietilsilano y el complejo de trifluoruro de boro ácido acético u otro ácido de Lewis (como se describe con respecto al Esquema I). Una vez completada la reacción, se agrega acetona u otro disolvente. El lote se calienta (por ejemplo, desde aproximadamente 20 hasta aproximadamente 30°C) y se mantiene hasta que se consume el trietilsilano. Se agrega NH4OAc acuoso y el lote se mezcla y se deja sedimentar hasta que se forman las fases superior e inferior. El volumen del lote de producto en la fase superior rica se reduce destilando el acetonitrilo con agitación mínima. El SDA3A etanol se agrega a temperatura elevada (> 60°C).
El producto A cristaliza por enfriamiento o enfriamiento con siembra (5% en peso con base en el compuesto si se muele en húmedo, se muele con chorro de nitrógeno o un lote anterior).
El producto se recristaliza como una torta húmeda o seca de SDA3A etanol.
El solvato Ig de dimetanol cristalino se prepara de acuerdo con la siguiente reacción del Esquema V.
ESQUEMA V
en el que el compuesto B no cristalino (que puede prepararse como se describe en la solicitud de patente de los Estados Unidos N° de serie 10 / 745.075 presentada el 23 de diciembre de 2003 o en la patente de los Estados Unidos N° 6.515.117), preferiblemente en forma sustancialmente pura (50 a 100% pura), se disuelve en metanol, una mezcla de metanol/tolueno, o una mezcla de metanol/tolueno/heptano, una mezcla de metanol/metil t-butil éter (MTBE)/heptano, o una mezcla de metanol/tolueno/acetato de etilo u otro acetato de alquilo con agitación, para formar una suspensión blanca que contiene solvato Ig de dimetanol cristalino. El solvato Ig de dimetanol cristalino puede recuperarse de la suspensión usando procedimientos convencionales, tales como filtración.
El proceso anterior puede llevarse a cabo a temperatura ambiente, aunque se pueden emplear temperaturas elevadas de hasta aproximadamente 20-25°C para mejorar la cristalización.
El compuesto Ig puede cristalizarse a partir de una mezcla de metanol/tolueno que contiene una relación en volumen de metanol a tolueno dentro del intervalo de aproximadamente 6:1 a aproximadamente 1:1, preferiblemente de aproximadamente 3:1 a aproximadamente 5:1. La mezcla de metanol/tolueno incluirá suficiente metanol para proporcionar una relación molar con el compuesto B dentro del intervalo de aproximadamente 80:1 a aproximadamente 10:1, preferiblemente de aproximadamente 40:1 a aproximadamente 20:1, para permitir la formación del solvato Ig de dimetanol.
La cristalización para formar solvato Ig de dimetanol puede efectuarse más fácilmente empleando cristales de siembra del compuesto Ig en una cantidad de aproximadamente 0,1 a aproximadamente 10%, preferiblemente de aproximadamente 0,5 a aproximadamente 3% con base en el peso del compuesto de partida B.
El compuesto Ig (que puede o no purificarse) también se puede cristalizar a partir de una mezcla de metanol/tolueno/heptano con siembra con semillas del compuesto cristalino Ig que emplea desde aproximadamente 0,1 hasta aproximadamente 10%, preferiblemente desde aproximadamente 0,5 hasta aproximadamente 3% con base en el peso del compuesto de partida B. El metanol se empleará en una relación en volumen con tolueno dentro del intervalo de aproximadamente 1:0,5 a aproximadamente 1:6, preferiblemente de aproximadamente 1:1,5 a aproximadamente 1:2,5, y una relación en volumen de heptano:tolueno dentro del intervalo de aproximadamente 2:1 a aproximadamente 0,5:1, preferiblemente de aproximadamente 1,3:1 a aproximadamente 0,5:1.
Ejemplos
Preparación de estructuras cristalinas
Ejemplo 1
Preparación de la estructura de (S)-propilenglicol ((S)-PG) - Forma SC-3 - Fórmula Ia
El Compuesto A puede prepararse como se describe en el Ejemplo 1, Parte E de la patente de Estados Unidos N° 6.515.117.
Se cargó un reactor de vidrio de 10 L equipado con un termopar y una entrada de nitrógeno con MeOH (1,25 L), agua desionizada (3,6 L) seguido de NaOH acuoso al 50% (205,9 mL, 3,899 mol). La solución residual de NaOH en el cilindro de medición se transfirió con agua (94 mL) al recipiente de reacción. Se añadió el compuesto A (503,11 g, 0,872 mol) y se agitó y calentó la mezcla a ~ 68°C durante 1,5 h. Después de 1 h, la temperatura del baño de circulación se redujo de 80 a 70°C; la temperatura interna bajó a 65°C. Después de un total de 3 h, la HPLC 1 indicó la finalización de la reacción, el Compuesto I AP ~ 99,5. Después de enfriar la mezcla a 25°C, se añadió acetato de isopropilo (2,5 L). La mezcla se agitó durante 10 minutos y luego se separó la capa acuosa (pH = 12,5) y se lavó la capa orgánica con agua (1 L). Durante este lavado, el pH del sistema bifásico se ajustó a 6,0 con HCl conc. (5,0 mL) y luego se separó la capa acuosa 2 . La capa orgánica se recogió en un recipiente separado. El reactor se lavó con agua (2 L), MeOH (2 L) y se purgó con gas nitrógeno. La solución húmeda del compuesto B se cargó nuevamente en el reactor y se introdujo (S)-propilenglicol ((S)-PG) (67,03 g, 0,872 moles). Opcionalmente, se pueden agregar cristales de siembra de (S)-PG la en esta etapa. La cristalización instantánea produjo una suspensión espesa. Después de agitar durante 1 h, se añadió ciclohexano (2,5 L) rápidamente durante 10 minutos y se continuó la agitación durante 21 h. El producto se filtró a través de un papel de filtro (Whatman # 5, embudo Buchner de 24" de diámetro). La filtración fue rápida y tomó aproximadamente 15 minutos. La torta del filtro se lavó con una mezcla (1:1) de MTBE/ciclohexano (2 x 1L) y se secó bajo succión durante 0,5 h. El sólido se transfirió a una bandeja Pyrex y se secó al vacío (25 mm de Hg) en un horno a 25-30°C durante dos días hasta que el análisis de agua por KF correspondió al monohidrato (3,6% en peso). Se obtuvo el producto la (S)-PG (0,425 kg, rendimiento 97%) en forma de un sólido blanco como la nieve, HPLC 3 AP 99,7.
Los cristales de siembra se pueden preparar disolviendo el compuesto I en un disolvente tal como MTBE y tratando la solución resultante con (S)-propilenglicol y procediendo como se describió anteriormente sin el uso de siembra.
1HPLC: Columna: YMC ODS-A (C-18) S3, 4,6 x 50 mm. Disolvente A: H3PO4 acuso al 0,2%. Disolvente B: 90% de CH3CN / 10% de H2O. Inicio % B = 0, final % B = 100. Tiempo de gradiente 8 min; mantener el tiempo 3 min. Tiempo de parada de integración 11,0 min. Velocidad de flujo 2,5 mL/min. Longitud de onda UV 220 nm.
2 Se realizó la neutralización antes de la división de fases para evitar la contaminación del producto con NaOH. La estructura de (S)-PG preparada sin neutralización era ligeramente básica [pH 8,3 de una suspensión sometida a sonicación en agua (~20 mg/mL)].
3 Método de HPLC: Fase móvil A: 0,05% de TFA en H2O. Fase móvil B: 0,05% de TFA en CAN. Columna: YMC Hydrosphere 4,6 x 150 (3|j). Gradiente: 30-90% de B durante 45 minutos, manteniendo durante 5 minutos; regresar al 30% de B y volver a equilibrar durante 10 min. Longitud de onda: 220 nm. Volumen de inyección: 10 jl. Temperatura: ambiente.
Ejemplo 1A
Estructura de (S)-propilenglicol ((S)-PG) - Forma SC-3 - Fórmula la
Masa Exacta: 502.20
Peso en moles: 502.98
C, 57.31; H, 7.01; Cl, 7.05; O, 28.63
Procedimiento
Se cargaron 20 g del compuesto A en un reactor a temperatura y presión ambiente. Se añadieron 30 mL de metanol y 49,75 mL de NaOH 3 N al reactor y la mezcla de reacción se calentó a 80°C o se sometió a reflujo, y se mantuvo durante aproximadamente 2-3 horas para completar la reacción < 0,5 AP. El lote se enfrió a 20°C y se neutralizó a pH 6,0-7,5 usando HCl concentrado o ácido acético 1 N (se requiere una introducción de ~ 1mL/g).
Extracción
El producto se extrajo de la mezcla de reacción en 100 mL de acetato de isopropilo, la fase acuosa se separó y la fase orgánica se lavó con agua hasta una conductividad <10 mS (introducción de ~ 4 mL/g). La fase acuosa se separó. Cristalización
Se añadieron 2,8 g (1,05 eq) de (S)-(+)-1,2-propanodiol a la mezcla de reacción. El lote se sembró con 0,1 g de compuesto I de siembra. Se añadieron 160 mL de ciclohexano y el lote se enfrió desde temperatura ambiente hasta 5°C. El lote se dejó agitar a temperatura ambiente desde 5°C al menos 1 hora antes del aislamiento.
Aislamiento y secado
Cada carga de torta aislada se lavó con 50/50 en volumen de mezcla de acetato de isopropilo/ciclohexano. La torta se secó a 30°C en un horno de vacío bajo vacío total. (La torta está seca cuando KF = 3,6% - 4,1%).
Rendimiento = 84% (sin corregir)
Pureza típica = 99,81 AP
Contenido típico de PG = 15,1 - 15,8% por GC
Ejemplo 2 ejemplo comparativo
Preparación de la estructura de (R)-propilenglicol - Ib
(R)-propilenglicol Ib
La estructura del (R)-propMengMcol se preparó usando el mismo proceso que el descrito anteriormente para la estructura del (S)-propilenglicol Ia (Ejemplo 1) excepto que se usó (R)-propilenglicol en lugar de (S)-propilenglicol.
Ejemplo 6
Preparación del solvato de (S)-PG forma SC-3 la
Para acetonitrilo (12 mL), a temperatura de lote de 8-10°C bajo atmósfera de nitrógeno, se cargó trifluoruro de boro eterato de dietilo (2,3 mL, 18,4 mmol) y agua (0,82 mL, 4,6 mmol). Después de mantener la mezcla anterior durante aproximadamente 1 hora, se añadió trietilsilano (3 mL, 18,4 mmol). La mezcla resultante se mantuvo durante aproximadamente 1 hora, y luego se añadió el compuesto B (preparado como se describe en el Ejemplo 17) en 10 mL de acetonitrilo. El lote se mantuvo entre 5 y 10°C. Una vez completada la reacción tal como se determinó mediante HPLC, la mezcla de reacción se inactivó con acetato de amonio acuoso (24 mL, 85 g) en 200 mL de agua. Las fases se separaron y la fase orgánica rica en producto se secó sobre sulfato de sodio. La fase orgánica rica en producto se concentró a presión reducida.
Agua (13 mg, 0,7 mmol, con base en la introducción de 0,3 g del compuesto B sin purificar), (S)-propilenglicol (56 mg, 0,7 mmol), t-butil-metil éter (5 mL, ~17 mL/g de compuesto B (entrada)), las semillas del compuesto la (~ 20 mg) se mezclaron y se mantuvieron durante 1 hora, para formar una suspensión cristalina. Se añadió ciclohexano (10 mL, 33 mL/g de compuesto B (entrada)). El producto cristalino (la) se aisló por filtración (4-5%) y se secó al vacío a 20-25°C.
Ejemplo 7
Preparación de solvato Ig de MeOH cristalino
Se obtuvieron cristales de solvato Ig de metanol disolviendo el compuesto B puro en metanol y agitando a temperatura ambiente. Se formó una suspensión blanca después de unos pocos días, y se encontró que era Ig de solvato Ig cristalino de metanol.
El solvato Ig de di-MeOH cristalino así formado se puede usar en lugar del compuesto B en la preparación del compuesto cristalino Ia tal como se describe en el Ejemplo 6.
Ejemplo 8
Preparación de solvato Ig de di-MeOH cristalino a partir del Compuesto B no purificado en metanol/tolueno 80/20 usando semillas
Se disolvieron 6 g del compuesto B (HPLC AP aproximadamente 80%) en 15 mL de metanol/tolueno 80/20.
Se añadieron semillas (aproximadamente 1% del compuesto de partida B) de cristales del compuesto Ig y la mezcla se enfrió para formar una suspensión que contenía cristales.
La suspensión se agitó durante 6 horas antes de aislarla.
Se encontró que la torta húmeda era solvato If de metanol cristalino, pero pierde la cristalinidad si se deja abierta durante unas pocas horas.
Ejemplo 9
Preparación de solvato Ig de di-MeOH cristalino a partir del Compuesto B no purificado en metanol/tolueno/heptano utilizando semillas
Se añadieron 2,5 g de compuesto B (91,5%) a un vial de centelleo con una barra de agitación magnética.
Se añadieron 4 mL de tolueno para disolver el compuesto Ia.
Se añadieron 2 mL de metanol. A continuación, se añadieron semillas de cristales del compuesto Ig (aproximadamente 1%).
Se añadieron 4 mL de heptano durante 30 minutos y la mezcla se agitó durante 12 horas. La torta húmeda se aisló en un embudo Buchner. Se descubrió que la torta húmeda era solvato Ig de metanol cristalino. Se secó al vacío a 30°C. El polvo resultante perdió cristalinidad.
Rendimiento = 1,7 g = 74,5% (corregido). Patrón de XRD de caracterización de cristales: Figura 10.
El solvato Ig de MeOH cristalino así formado puede usarse en lugar del compuesto B en la preparación del compuesto Ia cristalino tal como se describe en el Ejemplo 6.
Ejemplo 10 (no de acuerdo con la invención reivindicada)
Preparación de solvato If de 1,4-butinodiol cristalino a partir del compuesto B en tolueno/acetato de etilo usando semillas El solvato de 1,4-butin-diol se puede cristalizar en un acetato de alquilo (por ejemplo, acetato de etilo, propilo o butilo), alcohol (por ejemplo, isopropanol, butanol) o incluso agua. El tolueno y el heptano actúan como antidisolventes cuando se cristalizan en acetato de alquilo.
Se disolvieron 50 g (90,3% en peso) del Compuesto B en 675 mL de tolueno. La solución se calentó a 60°C y se añadieron 75 mL de acetato de etilo. Se añadieron 1,5 equivalentes de 2-butino-1,4-diol (= 13,3 g) y la mezcla se mantuvo a 60°C hasta que se disolvió el butileno diol. La solución se enfrió a 55°C y se añadió 0,1% de semillas (50 mg) del compuesto If de 1,4-butino-diol. La mezcla se mantuvo durante 1 hora a 55°C. Compuesto If comenzó a cristalizar. La mezcla se enfrió a 25°C durante 6 horas. La suspensión resultante se agitó durante 3 horas antes del aislamiento (el licor madre concentrado era < 3 mg/mL), se filtró y se lavó con 180 mL de tolueno 20 mL de acetato de etilo, y se secó al vacío a 45°C para producir cristales de solvato If de 1,4-butino-diol.
HPLC AP = 99,5%. Potencia = 80,7% en peso (Potencia esperada = 83,6% para el solvato 1:1). Rendimiento = 95%. Ejemplo 11 (no de acuerdo con la invención reivindicada)
Preparación del solvato If de 1,4-butin-diol cristalino a partir del compuesto B en acetato de butilo/heptano
Se disolvieron 0,5 g del Compuesto B (91% en peso) en 3,5 mL de acetato de butilo 3,5 mL de heptano a 60°C. Se añadieron 1,5 equivalentes de 2-butino-1,4-diol y la mezcla se enfrió a temperatura ambiente. La suspensión resultante se agitó durante 12 horas, se filtró y se lavó con 1 mL de acetato de butilo/heptano 1:1 y se secó al vacío a 50°C para producir cristales de solvato If de 1,4-butino-diol. Potencia = 85,1%. Rendimiento = 90%.
El solvato If de 1,4-butin-diol puede emplearse en lugar del compuesto B y empleando el ácido de Lewis BF32CH3COOH en lugar de BF3OEt2 para formar el compuesto cristalino la.
Ejemplo 16
Preparación del compuesto If a través de litiación continua y reacciones de acoplamiento
Se empleó un esquema de reacción similar al que se muestra en el Esquema IVA y la Figura 12.
Se instaló un enfriador de -30°C para el reactor 5 de litiación (mezclador 5 estático encamisado).
Se instaló un enfriador de -30°C para el reactor 22 de acoplamiento (mezclador 22 estático encamisado) y un intercambiador de calor de enfriamiento previo (no mostrado en la Figura 12) para la alimentación del compuesto D / tolueno.
Litiación continua
Las dos alimentaciones de E/THF/tolueno (2,74 mL/min) y Q, es decir, n-BuLi en hexano (0,41 mL/min), se mezclaron y se combinaron a través del mezclador 5 estático encamisado (-30°C).
Antes de bombear la alimentación de D/tolueno, se envió tolueno (2,96 mL/min) al sistema como un flujo de reposición para mantener el flujo total constante a 6,1 mL/min.
Se recogieron muestras a la salida del mezclador 5 estático de litiación para análisis por HPLC. Se tomaron muestras antes (a) del inicio de la reacción de acoplamiento, y (b) después de la recolección de la mezcla de reacción en el reactor de MSA-MeOH.
Reacción de acoplamiento continuo
La alimentación de D/tolueno (2,96 mL/min) se enfrió previamente a través de un intercambiador de calor antes de mezclar con la corriente de litiación.
Las dos corrientes, concretamente G y D, se mezclaron y combinaron a través de un mezclador 22 estático encamisado (entre -24°C y -30°C).
La corriente de reacción apareció de color amarillento.
Se recogieron muestras a la salida del mezclador 22 para análisis por HPLC. Se tomaron muestras antes y después de la recolección en el reactor 25 de MSA-MeOH.
Metil glicosidación
La corriente 24 de reacción de acoplamiento se alimentó a un reactor 25 de 500 mL que contenía MSA y metanol o HCl / MeOH a < -10°C con agitación.
Después de finalizar la recolección, la mezcla de reacción se mantuvo a < -10°C con agitación durante otra hora.
La mezcla de reacción se calentó hasta 35°C. La reacción se consideró completa (aproximadamente 6 horas) hasta que el análisis por HPLC indicó que RAP de hemicetal H' desililado < 0,3%. La reacción se enfrió a temperatura ambiente (20°C) y la mezcla de reacción se mantuvo durante 16 horas para formar el compuesto B.
Formación de cristales de If
B se cristalizó con 2-butino-1,4-diol (J) en tolueno/EtOAc para producir cristales de If.
Ejemplo 17 (no de acuerdo con la invención reivindicada)
Preparación del compuesto intermedio A
Compuesto If sólido (50,0 g), DMAP sólido (1,2 g), acetonitrilo líquido (450 mL) y anhídrido acético líquido (63 mL) se cargaron en un reactor de matraz de 250 mL.
El lote (77°C) se calentó y mantuvo hasta que se completó la reacción.
El lote se enfrió (5°C).
Se cargaron al reactor trietilsilano (72 mL) y complejo de ácido acético trifluoruro de boro (63 mL).
Una vez completada la reacción, se añadió acetona (36 mL).
El lote (21°C) se calentó y se mantuvo hasta que se consumió el trietilsilano.
Se añadió NH4OAc acuoso (33% en peso, 450 mL) y el lote se mezcló, se dejó sedimentar hasta que se formaron las fases superior e inferior.
El volumen del lote de producto en la fase superior rica se redujo mediante destilación de acetonitrilo a agitación mínima. Se cargó etanol SDA3A (1 L) a temperatura elevada (> 60°C).
El producto se cristalizó por enfriamiento o enfriamiento con siembra (5% en peso con base en el compuesto If se molió en húmedo, se molió con chorro de nitrógeno, o un lote previo). El producto típicamente se aisló con > 75% de rendimiento. El producto se recristalizó como una torta húmeda o seca a partir de etanol SDA3A.
Caracterización de la estructura cristalina
Las estructuras cristalinas equivalentes a las estructuras cristalinas descritas a continuación y reivindicadas en este documento pueden demostrar características analíticas similares, aunque no idénticas, dentro de un margen razonable de error, dependiendo de las condiciones de ensayo, pureza, equipamiento y otras variables comunes conocidas por los expertos en la técnica.
Difracción de rayos X de polvo
Un experto en la materia apreciará que se puede obtener un patrón de difracción de rayos X de polvo con un error de medición que depende de las condiciones de medición empleadas. En particular, se sabe generalmente que las intensidades en un patrón de difracción de rayos X de polvo pueden fluctuar dependiendo de las condiciones de medición empleadas. Se debe entender además que las intensidades relativas también pueden variar dependiendo de las condiciones experimentales y, en consecuencia, el orden exacto de intensidad no debe tenerse en cuenta. Adicionalmente, un error de medición del ángulo de difracción para un patrón de difracción de rayos X de polvo convencional es típicamente aproximadamente del 5% o menos, y tal grado de error de medición se debe tener en cuenta como perteneciente a los ángulos de difracción mencionados anteriormente. En consecuencia, debe entenderse que las estructuras cristalinas de la presente invención no están limitadas a las estructuras cristalinas que proporcionan patrones de difracción de rayos X completamente idénticos a los patrones de difracción de rayos X de polvo representados en las Figuras adjuntas descritas aquí. Cualesquiera estructuras cristalinas que proporcionen patrones de difracción de rayos X de polvo sustancialmente idénticos a los descritos en las Figuras adjuntas caen dentro del alcance de la presente invención. La capacidad de determinar identidades sustanciales de los patrones de difracción de rayos X de polvo está dentro del alcance de un experto en la técnica.
(S)-PG (forma SC-3) Ia, (R)-PG Ib, solvato If de 1,4-butino-diol y solvato Ig de dimetanol
Se empaquetaron aproximadamente 200 mg en un soporte de muestras de difracción de rayos X de polvo de Philips (PXRD). La muestra se transfirió a una unidad Philips MPD (45 KV, 40 mA, Cu Kai). Los datos se recogieron a temperatura ambiente en un intervalo de 2 a 322-theta (modo de barrido continuo, velocidad de barrido de 0,03 grados/s, rendijas auto divergencia y antidispersión, rendija de recepción: 0,2 mm, centrifugado de muestras: encendido).
Los patrones de difracción de rayos X de polvo para las estructuras (S)-PG (Ia), (R)-PG (Ib) se ilustran en las Figuras 1 y 2, respectivamente. Los patrones de difracción de rayos X de polvo para el solvato IF de 1,4-butinodiol y el solvato Ig de dimetanol se ilustran en las Figuras 9 y 10, respectivamente. Las posiciones de pico de difracción seleccionadas (grados 20 ± 0,2) para las estructuras (S)-PG (Ia), (R)-PG (Ib) se muestran en la Tabla 1 a continuación. Las posiciones características de los picos de difracción (grados 20 ± 0,1) a TA, se basan en un patrón de alta calidad recogido con un difractómetro (CuKa) con un capilar giratorio con 20 calibrado con una metodología del Instituto Nacional de Estándares y Tecnología, y otro estándar adecuado conocido para los expertos en la técnica. Las intensidades relativas, sin embargo, pueden cambiar dependiendo del tamaño y morfología del cristal.
Tabla 1
Resonancia magnética nuclear en estado sólido
Las estructuras de (S)-PG (Ia), (R)-PG (Ib), solvato If de 1,4-butin-diol y solvato Ig de dimetanol se caracterizaron mediante técnicas de RMN en estado sólido.
Todas las mediciones de RMN 13C en estado sólido se realizaron con un espectrómetro de RMN Bruker DSX-400 de 400 MHz. Se obtuvieron espectros de alta resolución usando desacoplamiento de protones de alta potencia y la secuencia de pulsos TPPM y la polarización cruzada de amplitud de rampa (RAMP-CP) con giro de ángulo mágico (MAS) a aproximadamente 12 kHz (AE Bennett et al., J. Chem. Phys., 1995, 103, 6951; G. Metz, X. Wu y SO Smith, J. Magn. Reson. A, 1994, 110, 219 - 227). Se usaron aproximadamente 70 mg de muestra, empaquetados en un rotor de óxido de zirconio de diseño de cartucho para cada experimento. Los desplazamientos químicos (8) se referenciaron en adamantano externo con la resonancia de alta frecuencia ajustada a 38,56 ppm (W.L. Earl y D.L. VanderHart, J. Magn. Reson., 1982, 48, 35-54).
El espectro de RMN 13C CPMAS resultante para la estructura (S)-PG y (R)-PG se muestra en las Figuras 3 y 4, respectivamente.
Los principales picos de resonancia para el espectro de carbono en estado sólido de (S)-PG y (R)-PG se enumeran a continuación en la Tabla 1A y en la Tabla 2 y para el solvato If de 1,4-butino-diol y el solvato Ig de dimetanol se enumeran a continuación en las Tablas 2A y 2B, respectivamente. Se considera que las estructuras cristalinas que demuestran posiciones de pico de RMN 13C sustancialmente similares, en las que "sustancialmente similar" significa 10 a 15% de valor sin dimensiones, caen dentro del alcance de la invención (es decir, equivalentes a las estructuras ilustradas a continuación).
Tabla 1A
Tabla 2
Estos datos son estrictamente válidos para un espectrofotómetro de 400 MHz.
Tabla 2A
Tabla 2B
Análisis termogravimétrico
Los experimentos de análisis termogravimétrico (TGA) se realizaron en un TA InstrumentsMR modelo Q500. La muestra (aproximadamente 10-30 mg) se colocó en una bandeja de platino previamente tarada. El peso de la muestra se midió con precisión y se registró hasta una milésima de miligramo por el instrumento. El horno se purgó con gas nitrógeno a razón de 100 mL/min. Los datos se recogieron entre la temperatura ambiente y 300°C a una velocidad de calentamiento de 10°C/min.
Las curvas de TGA para las estructuras (S)-PG la y (R)-PG Ib se muestran en las Figuras 5 y 6, respectivamente. La pérdida de peso corresponde a una mol de agua y una mol de propilenglicol por mol de estructura analizada.
Calorimetría de barrido diferencial
El comportamiento térmico en estado sólido del solvato (S)-PG la, (R)-PG Ib, 1,4-butileno-diol If y las estructuras de Ig de solvato de dimetanol se investigaron mediante calorimetría de barrido diferencial (DSC). Las curvas de DSC para las estructuras (S)-PG Ia y (R)-PG Ib se muestran en las Figuras 7 y 8, respectivamente. Las curvas de DSC para el solvato If de 1,4-butino-diol y las estructuras del solvato Ig de dimetanol se muestran en las Figuras 11 y 12, respectivamente.
Se llevaron a cabo experimentos de calorimetría de barrido diferencial (DSC) en un TA InstrumentsMR modelo Q1000. La muestra (aproximadamente 2-6 mg) se pesó en un platillo de aluminio y se registró con precisión hasta una centésima de miligramo, y se transfirió al DSC. El instrumento se purgó con gas nitrógeno a razón de 50 mL/min. Los datos se recogieron entre la temperatura ambiente y 300°C a una velocidad de calentamiento de 10°C/min. La gráfica se hizo con los picos endotérmicos apuntando hacia abajo.
Sin embargo, un experto en la técnica observará que en la medición de DSC hay un cierto grado de variabilidad en el inicio de la medición real y las temperaturas máximas, dependiendo de la velocidad de calentamiento, la forma y pureza del cristal y otros parámetros de medición.
Análisis de rayos X de un solo cristal
Se obtuvieron e investigaron mediante difracción de rayos X un cristal único para la estructura (S)-PG Ia, y para el solvato If de 1,4-butileno-diol, el solvato Ig de dimetanol, L-prolina Ih en proporción 1:2, L-prolina Ii en proporción 1:1 y L-prolina hemihidrato Ij en proporción 1:1.
Los datos se recogieron en un difractómetro en serie CAD4 de Bruker-Nonius1. Los parámetros de célula unitaria se obtuvieron a través del análisis de mínimos cuadrados de los ajustes del difractómetro experimental de 25 reflexiones de ángulo alto. Las intensidades se midieron usando radiación de Cu Ka (A = 1,5418 Á) a una temperatura constante con la técnica de escaneo variable 0-20 y se corrigieron solo para los factores de polarización de Lorentz. Los recuentos de fondo se recopilaron en los extremos del barrido durante la mitad del tiempo del barrido. Alternativamente, los datos de cristal único se recogieron en un sistema Bruker-Nonius Kappa CCD 2000 usando radiación de Cu Ka (A = 1,5418 Á). La indexación y el procesamiento de los datos de intensidad medidos se llevaron a cabo con el paquete de software2 HKL20002 en la suite de programas Collect.3
1 BRUKER AXS, Inc., 5465 East Cheryl Parkway Madison, WI 53711 EE.UU.
2 Otwinowski, Z. & Minor, W. (1997) en Macromolecular Crystallography, eds. Carter, W.C. Jr y Sweet, R.M. (Academic, NY), vol. 276, páginas 307-326
3 Recopilación de la recolección de datos y procesamiento de la interfaz de usuario: Collect: Data collection software, R. Hooft, Nonius B.V., 1998.
Cuando se indicó, los cristales se enfriaron en la corriente fría de un sistema criogénico de Oxford 4 durante la recopilación de datos.4 Oxford Cryosystems Cryostream cooler: J. Cosier y A.M. Glazer, J. Appl. Cryst., 1986, 19, 105
Las estructuras se resolvieron mediante métodos directos y se refinaron sobre la base de las reflexiones observadas usando el paquete de software SDP5 con modificaciones locales menores o el paquete cristalográfico, MAXUS.6 5 SDP, Paquete de Determinación de Estructura, Enraf-Nonius, Bohemia NY 11716. Los factores de dispersión, incluidos f y f'', en el software SDP se tomaron de las "International Tables for Crystallography", Kynoch Press, Birmingham, Inglaterra, 1974; Vol. IV, Tablas 2.2A y 2.3.1
6 Paquete de software de solución y refinamiento maXus: S. Mackay, C.J. Gilmore, C. Edwards, M. Tremayne, N. Stewart, K. Shankland. maXus: un programa de ordenador para la solución y el refinamiento de estructuras cristalinas a partir de datos de difracción.
Los parámetros atómicos derivados (coordenadas y factores de temperatura) se refinaron a través de mínimos cuadrados de matriz completa. La función minimizada en los refinamientos fue ZW(|Fo | - |Fc |)2. R se define como Z||Fo|-|Fc ||/Z|Fo | mientras que Rw = [Zw (|Fo | - |Fc |)2/Zw |Fo |2]1/2 donde w es una función de ponderación apropiada basada en errores en las intensidades observadas. Los mapas de diferencias se examinaron en todas las etapas de refinamiento. Los hidrógenos se introdujeron en posiciones idealizadas con factores de temperatura isotrópicos, pero no se variaron los parámetros de hidrógeno.
Los parámetros de células unitarias para la estructura (S)-PG la forma SC-3 se enumeran a continuación en la Tabla 3. Como se usa en este documento, el parámetro de célula unitaria "moléculas/por célula" se refiere al número de moléculas de Compuesto en la célula unitaria.
Tabla 3
La Tabla 4 a continuación expone los parámetros posicionales para la estructura (S)-PG Ia a 25°C.
Tabla 4
Los parámetros de células unitarias para el dihidrato de monoetanol (estructura de etanol o EtOH) forma SA-1, fórmula Ic, se enumeran a continuación en la Tabla 5.
Tabla 5
La Tabla 6 a continuación establece los parámetros posicionales para la forma SA-1 (monoetanol-dihidrato), Ic a -50°C.
Tabla 6
Los parámetros de célula unitaria para el etilenglicol de SB-1, fórmula Id se enumeran a continuación en la Tabla 7.
Tabla 7
Los parámetros de célula unitaria para el solvato de 1,4-butinodiol se enumeran a continuación en la Tabla 11.
Tabla 11
La Tabla 12 a continuación expone los parámetros posicionales para el solvato If de 1,4-butinodiol a 25°C.
Tabla 12
La Tabla 13 a continuación expone los parámetros de célula unitaria para el solvato Ig de dimetanol.
Tabla 13
La Tabla 14 a continuación expone los parámetros posicionales para el solvato de dimetanol Ig a -50°C.
Tabla 14
La Tabla 15 a continuación expone los parámetros de célula unitaria para la forma 3 del complejo de L-prolina en proporción 1:2, fórmula Ih.
Utilidades y combinaciones
A. Utilidades
El compuesto de la presente que se describe posee actividad como un inhibidor de los transportadores de glucosa dependientes de sodio encontrados en el intestino y el riñón de mamíferos. Preferiblemente, el compuesto de la invención es un inhibidor selectivo de la actividad de SGLT2 renal y, por lo tanto, puede usarse en el tratamiento de enfermedades o trastornos asociados con la actividad de SGLT2.
Por consiguiente, las composiciones farmacéuticas de la presente invención se pueden administrar a mamíferos, preferiblemente seres humanos, para el tratamiento de una variedad de afecciones y trastornos, que incluyen, entre otros, tratar o retrasar la progresión o el inicio de la diabetes (incluyendo Tipo I y Tipo II, tolerancia alterada a la glucosa, resistencia a la insulina y complicaciones diabéticas, como nefropatía, retinopatía, neuropatía y cataratas), hiperglucemia, hiperinsulinemia, hipercolesterolemia, dislipidemia, niveles elevados en sangre de ácidos grasos libres o glicerol, hiperlipidemia, hipertrigliceridemia, obesidad, cicatrización de heridas, isquemia tisular, aterosclerosis e hipertensión. El compuesto de la presente invención también se puede utilizar para aumentar los niveles en sangre de lipoproteína de alta densidad (HDL).
Además, las afecciones, afecciones y enfermedades a las que se hace referencia colectivamente como "Síndrome X" o Síndrome Metabólico como se detalla en Johannsson, J. Clin. Endocrinol. Metab., 82, 727-34 (1997), se pueden tratar empleando el compuesto de la presente invención.
Las composiciones farmacéuticas que comprenden (S)-PG (SC-3) (Ia) cristalino se pueden administrar en formas de dosificación y en dosificaciones como se describe en la patente de Estados Unidos N° 6.515.117.
B. Combinaciones
La presente invención incluye dentro de su alcance composiciones farmacéuticas que comprenden, como ingrediente activo, una cantidad terapéuticamente eficaz de un compuesto de fórmula I, que incluye (S)-PG (forma SC-3, Ia, solo o en combinación con un vehículo o diluyente farmacéutico. Opcionalmente, las composiciones reivindicadas pueden utilizarse como un tratamiento individual, o utilizarse en combinación con uno o más agentes terapéuticos diferentes.
Otro "agente o agentes terapéuticos" adecuados para combinación con las composiciones reivindicadas incluyen, pero no se limitan a, agentes terapéuticos conocidos útiles en el tratamiento de los trastornos mencionados anteriormente que incluyen: agentes antidiabéticos; agentes antihiperglicémicos; agentes hipolipidémicos / reductores de lípidos; agentes contra la obesidad; agentes antihipertensivos y supresores del apetito.
Los ejemplos de agentes antidiabéticos adecuados para uso en combinación con las composiciones reivindicadas incluyen biguanidas (por ejemplo, metformina o fenformina), inhibidores de glucosidasa (por ejemplo, acarbosa o miglitol), insulinas (incluidos secretagogos de insulina o sensibilizadores a insulina), meglitinidas (por ejemplo, repaglinida), sulfonilureas (por ejemplo, glimepirida, gliburida, gliclazida, clorpropamida y glipizida), combinaciones de biguanida/gliburida (por ejemplo, Glucovance®), tiazolidindionas (por ejemplo, troglitazona, rosiglitazona y pioglitazona), agonistas de PPAR-alfa , agonistas de PPAR-gamma, agonistas duales de PPAR alfa / gamma, inhibidores de la glicógeno fosforilasa, inhibidores de la proteína de unión a ácidos grasos (aP2), péptido 1 similar al glucagón (GLP-1) u otros agonistas del receptor de GLP-1 e inhibidores de dipeptidil peptidasa IV (d Pp4).
Se cree que el uso de las composiciones reivindicadas en combinación con al menos uno o más agentes antidiabéticos adicionales proporciona resultados antihiperglicémicos mayores que los posibles a partir de cada uno de estos medicamentos solos y mayores que los efectos antihiperglicémicos aditivos combinados producidos por estos medicamentos.
Otras tiazolidindionas adecuadas incluyen MCC-555 de Mitsubishi (descrita en la patente de Estados Unidos N° 5.594.016), faraglitazar de Glaxo-Wellcome (GI-262570), englitazona (c P-68722, Pfizer) o darglitazona (CP-86325, Pfizer, isaglitazona ( MIT/J&J), reglitazar (JTT-501) (JPNT/P&U), rivoglitazona (R-119702) (Sankyo / WL), liraglutida (NN-2344) (Dr. Reddy / NN), o (Z)-1,4-bis-4-[(3,5-dioxo-1,2,4-oxadiazolidin-2-il-metil)]fenoxibut-2-eno (YM-440, Yamanouchi).
Ejemplos de agonistas de PPAR-alfa, agonistas de PPAR-gamma y agonistas duales de PPAR alfa / gamma incluyen muraglitazar, peliglitazar, tesaglitazar AR-HO39242 Astra/Zeneca, GW-501516 (Glaxo-Wellcome), KRP297 (Kyorin Merck), así como los revelados por Murakami et al., "A Novel Insulin Sensitizer Acts As a Coligand for Peroxisome Proliferation - Activated Receptor Alpha (PPAR alpha) and PPAR gamma. Effect on PPAR alpha Activation on Abnormal Lipid Metabolism in Liver of Zucker Fatty Rats", Diabetes 47, 1841-1847 (1998), WO 01/21602 y en la patente de Estados Unidos N° 6.653.314, cuyos compuestos designados como preferidos son preferidos para uso aquí.
Los inhibidores de aP2 adecuados incluyen los descritos en la solicitud de los Estados Unidos con N° de serie 09 / 391.053, presentada el 7 de septiembre de 1999 y en la solicitud de los Estados Unidos con N° de serie 09 / 519.079, presentada el 6 de marzo de 2000, empleando dosificaciones como se establece en este documento.
Los inhibidores adecuados de DPP4 incluyen los descritos en WO 99/38501, WO 99/46272, WO 99/67279 (PROBIODRUG), WO 99/67278 (PROBIODRUG), WO 99/61431 (PROBIODRUG), NVP-DPP728A (1-[[[2-[(5-cianopiridin-2-il)amino]etil]amino]acetil]-2-ciano-(S)-pirrolidina (Novartis) como se describe por Hughes y col., Biochemistry, 38 (36), 11597-11603, 1999, TSL-225 (ácido tri ptofil-1,2,3,4-tetrahidroisoquinolin-3-carboxílico (descrito por Yamada et al., Bioorg. & Med. Chem. Lett. 8 (1998) 1537-1540), 2-cianopirrolididas y 4-cianopirrolididas, como describen Ashworth et al., Bioorg. & Med. Chem. Lett., Vol. 6, N° 22, páginas 1163-1166 y 2745-2748 (1996), los compuestos descritos en la solicitud de los Estados Unidos serial N° 10 / 899.641, WO 01/68603 y la patente de los Estados Unidos N° 6.395.767, empleando dosificaciones como se expone en las referencias anteriores.
Otras meglitinidas adecuadas incluyen nateglinida (Novartis) o KAD1229 (PF/Kissei).
Los ejemplos de agentes antihiperglicémicos adecuados para uso en combinación con las composiciones reivindicadas incluyen el péptido 1 similar al glucagón (GLP-1) tal como GLP-1 (1-36) amida, GLP-1 ( 7-36) amida, GLP-1 (7-37) (como se describe en la patente de Estados Unidos N° 5.614.492), así como exenatida (Amylin / Lilly), LY-315902 (Lilly), MK-0431 (Merck), liraglutida (NovoNordisk), ZP-10 (Zealand Pharmaceuticals A/S), CJC-1131 (Conjuchem Inc.), y los compuestos descritos en el documento WO 03/033671.
Los ejemplos de agentes hipolipidémicos / reductores de lípidos adecuados para uso en combinación con las composiciones reivindicadas incluyen uno o más inhibidores de MTP, inhibidores de HMG CoA reductasa, inhibidores de escualeno sintetasa, derivados de ácido fíbrico, inhibidores de ACAT, inhibidores de lipoxigenasa, inhibidores de la absorción de colesterol, inhibidores del cotransportador ileal de Na+/ácido biliar, sobrerreguladores de la actividad del receptor de LDL, secuestrantes de ácidos biliares, proteína de transferencia de éster de colesterol (por ejemplo, inhibidores de CETP, tales como torcetrapib (CP-529414, Pfizer) y JTT-705 (Akros Pharma)), agonistas de PPAR (como se describió anteriormente) y/o ácido nicotínico y derivados de los mismos.
Los inhibidores de MTP que pueden emplearse tal como se describió anteriormente incluyen los descritos en la patente de los Estados Unidos N° 5.595.872, la patente de los Estados Unidos N° 5.739.135, la patente de los Estados Unidos N° 5.712.279, la patente de los Estados Unidos N° 5.760.246, la patente de los Estados Unidos N° 5.827.875, la patente de los Estados Unidos N° 5.885.983 y la patente de Estados Unidos N° 5.962.440.
Los inhibidores de la HMG CoA reductasa que se pueden emplear en combinación con las composiciones reivindicadas incluyen mevastatina y compuestos relacionados, como se describe en la patente de los Estados Unidos N° 3.983.140, lovastatina (mevinolina) y compuestos relacionados, como se describe en patente de Estados Unidos N° 4.231.938, pravastatina y compuestos relacionados, tal como se describe en la patente de Estados Unidos N° 4.346.227, simvastatina y compuestos relacionados, como se describe en las patentes de Estados Unidos N° 4.448.784 y 4.450.171. Otros inhibidores de la HMG CoA reductasa que pueden emplearse aquí incluyen, pero no se limitan a, fluvastatina, descrita en la patente de Estados Unidos N° 5.354.772, cerivastatina, como se describe en las patentes de Estados Unidos N° 5.006.530 y 5.177.080, atorvastatina, como se describe en las patentes de Estados Unidos N° 4.681.893, 5.273.995, 5.385.929 y 5.686.104, atavastatina (nisvastatina de Nissan/Sankyo (NK-104)), como se describe en la patente de Estados Unidos N° 5.011.930, visastatin (Shionogi-Astra/Zeneca (ZD-4522)), como se describe en la patente de Estados Unidos N° 5.260.440, y compuestos de estatina relacionados descritos en la patente de Estados Unidos N° 5.753.675, análogos de pirazol de derivados de mevalonolactona, como se describe en la patente de Estados Unidos N° 4.613.610, análogos de indeno de derivados de mevalonolactona, como se describe en la solicitud PCT WO 86/03488, 6-[2-(sustituido-pirrol-1-il)-alquil)piran-2-onas y sus derivados, como se describe en la patente de los Estados Unidos N° 4.647.576, SC-45355 de Searle (un derivado de ácido pentanodioico sustituido en posición 3) dicloroacetato, análogos de imidazol de mevalonolactona, como se describe en la solicitud PCT WO 86/07054, derivados del ácido 3-carboxi-2-hidroxi-propanofosfónico, como se describe en la patente francesa N° 2.596.393, pirrol disustituido en posiciones 2 y 3, furano y derivados de tiofeno, como se describe en la solicitud de patente europea N° 0221025, análogos de naftilo de la mevalonolactona, como se describe en la patente de los Estados Unidos N° 4.686.237, octahidronaftalenos, tal como se describe en la patente de los Estados Unidos N° 4.499.289, cetoanálogos de la mevinolina (lovastatina), como se describe en la solicitud
de patente europea N° 0142146 A2, y derivados de quinolina y piridina, como se describe en la patente de los Estados Unidos N° 5.506.219 y 5.691.322.
Los agentes hipolipidémicos preferidos son pravastatina, lovastatina, simvastatina, atorvastatina, fluvastatina, cerivastatina, atavastatina y ZD-4522.
Además, los compuestos de ácido fosfínico útiles en la inhibición de HMG CoA reductasa, tales como los descritos en el documento GB 2205837, son adecuados para uso en combinación con las composiciones reivindicadas.
Los inhibidores de escualeno sintetasa adecuados para su uso en la presente invención incluyen, pero no se limitan a, a -fosfono-sulfonatos descritos en la patente de Estados Unidos N° 5.712.396, los descritos por Biller et al., J. Med. Chem., 1988, vol. 31, N° 10, páginas 1869-1871, que incluyen isoprenoide (fosfinil-metil)fosfonatos, así como también otros inhibidores conocidos de la escualeno sintetasa, por ejemplo, como se describe en la patente de los Estados Unidos N° 4.871.721 y 4.924.024 y en Biller, SA, Neuenschwander, K., Ponpipom, MM, y Poulter, CD, Current Pharmaceutical Design, 2, 1-40 (1996).
Además, otros inhibidores de escualeno sintetasa adecuados para su uso en la presente invención incluyen los pirofosfatos terpenoides descritos por P. Ortiz de Montellano et al., J. Med. Chem., 1977, 20, 243-249, el análogo A de farnesil difosfato y análogos de pirofosfato de preescualeno (PSQ-PP) como lo describen Corey y Volante, J. Am. Chem. Soc., 1976, 98, 1291-1293, fosfinilfosfonatos informados por McClard, R.W. et al., J.A.C.S., 1987, 109, 5544 y ciclopropanos informados por Capson, T.L., tesis doctoral, junio de 1987, Dept. Med. Chem. U of Utah, Abstract, Tabla de Contenidos, págs. 16, 17, 40-43, 48-51, Resumen.
Los derivados de ácido fíbrico que se pueden emplear en combinación con las composiciones reivindicadas incluyen fenofibrato, gemfibrozil, clofibrato, bezafibrato, ciprofibrato, clinofibrato y similares, probucol y compuestos relacionados, como se describe en la patente de Estados Unidos N° 3.674.836, siendo preferidos probucol y gemfibrozil, secuestrantes de ácidos biliares, tales como colestiramina, colestipol y DEAE-Sefadex (Secholex®, Policexide®), así como lipostabil (Rhone-Poulenc), Eisai E-5050 (un derivado de etanolamina sustituida en N) , imanixil (HOE-402), tetrahidrolipstatina (THL), istigmastanilfosforilcolina (SPC, Roche), aminociclodextrina (Tanabe Seiyoku), Ajinomoto AJ-814 (derivado de azuleno), melinamida (Sumitomo), Sandoz 58-035, American Cyanamid CL-277.082 y CL-283.546 (derivados de urea disustituidos), ácido nicotínico, acipimox, acifrán, neomicina, ácido p-aminosalicílico, aspirina, derivados de poli(dialilmetilamina), tal como se describe en la patente de Estados Unidos N° 4.759.923, poli(cloruro de dialildimetilamonio) de amina cuaternaria y ionenos, tal como se describe en la patente de los Estados Unidos N° 4.027.009, y otros agentes conocidos reductores del colesterol en suero.
El inhibidor de ACAT que puede emplearse en combinación con las composiciones reivindicadas incluye los descritos en Drugs of the Future 24, 9-15 (1999), (Avasimibe); "The ACAT inhibitor, Cl-1011 is effective in the prevention and regression of aortic Fatty streak area in hamsters", Nicolosi et al., Atherosclerosis (Shannon, Irel). (1998), 137 (1), 77-85; "The pharmacological profile of FCE 27677: a novel ACAT inhibitor with potent hypolipidemic activity mediated by selective suppression of the hepatic secretion of ApoB100-containing lipoprotein", Ghiselli, Giancarlo, Cardiovasc. Drug Rev. (1998), 16(1), 16-30; "RP 73163: a bioavailable alkylsulfinyl-diphenylimidazole ACAT inhibitor", Smith, C., et al, Bioorg. Med. Chem. Lett. (1996), 6(1), 47-50; "ACAT inhibitors: physiologic mechanisms for hypolipidemic and anti-atherosclerotic activities in experimental animals", Krause et al, Editor(s): Ruffolo, Robert R., Jr.; Hollinger, Mannfred A., Inflammation: Mediators Pathways (1995), 173-98, Publisher: CRC, Boca Raton, Fla.; "ACAT inhibitors: potential anti-atherosclerotic agents", Sliskovic et al., Curr. Med. Chem. (1994), 1(3), 204-25; "Inhibitors of acyl-CoA: cholesterol O-acyl transferase (ACAT) as hypocholesterolemic agents. 6. The first water-soluble ACAT inhibitor with lipid-regulating activity. Inhibitors of acyl-CoA: cholesterol acyltransferase (ACAT). 7. Development of a series of substituted N-phenyl-N'-[(1-phenylcyclopentyl)methyl]ureas with enhanced hypocholesterolemic activity", Stout et al, Chemtracts: Org. Chem. (1995), 8(6), 359-62, o TS-962 (Taisho Pharmaceutical Co. Ltd).
El agente hipolipidémico puede ser un sobrerregulador de la actividad del receptor de LD2, tal como 1(3H)-isobenzofuranona, 3-(13-hidroxi-10-oxotetradecil)-5,7-dimetoxi-(MD-700, Taisho Pharmaceutical Co. Ltd) y colestan-3-ol, 4-(2-propenil)-(3a, 4a, 5a)-(LY295427, Eli Lilly).
Los ejemplos del inhibidor adecuado de la absorción de colesterol para uso en combinación con las composiciones reivindicadas incluyen SCH48461 (Schering-Plough), así como los descritos en Atherosclerosis 115, 45-63 (1995) y J. Med. Chem. 41, 973 (1998).
Los ejemplos de inhibidores adecuados del cotransportador ileal de Na+/ácido biliar para su uso en combinación con las composiciones reivindicadas incluyen compuestos como se describe en Drugs of the Future, 24, 425-430 (1999).
Los inhibidores de la lipoxigenasa que se pueden emplear en combinación con las composiciones reivindicadas incluyen inhibidores de 15-lipoxigenasa (15-LO), tales como derivados de bencimidazol, como se describe en el documento WO 97/12615, inhibidores de 15-LO, como se describe en el documento WO 97/12613, isotiazolonas, como se describe en el documento WO 96/38144, e inhibidores de 15-LO, como lo describen Sendobry et al. "Attenuation of diet-induced atherosclerosis in rabbits with a highly selective 15-lipoxygenase inhibitor lacking significant antioxidant properties", Brit.
J. Pharmacology (1997) 120, 1199-1206, y Comicelli et al, "15-Lipoxygenase and its Inhibition: A Novel Therapeutic Target for Vascular Disease", Current Pharmaceutical Design, 1999, 5, 11-20.
Los ejemplos de agentes antihipertensivos adecuados para uso en combinación con las composiciones reivindicadas incluyen bloqueadores beta adrenérgicos, bloqueadores del canal de calcio (tipo L y tipo T, por ejemplo, diltiazem, verapamilo, nifedipina, amlodipina y mybefradil), diuréticos (por ejemplo, clorotiazida, hidroclorotiazida, flumetiazida, hidroflumetiazida, bendroflumetiazida, metilclorotiazida, triclorometiazida, politiazida, benztiazida, tricrinafeno de ácido etacrínico, clortalidona, furosemida, musolimina, bumetanida, triamtreneno, amilorida, espironolactona), inhibidores de renina, inhibidores de la ACE (por ejemplo, captopril, zofenopril, fosinopril, enalapril, ceranopril, cilazopril, delapril, pentopril, quinapril, ramipril, lisinopril), antagonistas del receptor de AT-1 (por ejemplo, losartán, irbesartán, valsartán), antagonistas del receptor de ET (por ejemplo, sitaxsentán, atrsentan y compuestos divulgados en las patentes de Estados Unidos N° 5.612.359 y 6.043.265), antagonista dual de ET/AII (por ejemplo, compuestos descritos en el documento WO 00/0 1389), inhibidores de endopeptidasa neutra (NEP), inhibidores de vasopepsidasa (inhibidores duales de NEP-ACE) (por ejemplo, omapatrilat y gemopatrilat) y nitratos.
Los ejemplos de agentes contra la obesidad adecuados para uso en combinación con las composiciones reivindicadas de la presente invención incluyen un agonista beta 3 adrenérgico, un inhibidor de lipasa, un inhibidor de recaptación de serotonina (y dopamina), un fármaco del receptor beta de tiroides, agonistas de 5HT2C, (tal como Arena APD-356); antagonistas de MCHR1 como Synaptic SNAP-7941 y Takeda T-226926, agonistas del receptor de melanocortina (MC4R), antagonistas del receptor de la hormona concentradora de melanina (MCHR) (como Synaptic SNAP-7941 y Takeda T-226926), moduladores del receptor de galanina, antagonistas de orexina, agonistas de CCK, antagonista de NPY1 o NPY5, moduladores de NPY2 y NPY4, agonistas del factor liberador de corticotropina, moduladores del receptor 3 de histamina (H3), inhibidores de la 11-beta-HSD-1, moduladores del receptor de la adinopectina, inhibidores de recaptación de monoamina o agentes liberadores, un factor neurotrófico ciliar (CNTF, tal como AXOKINE® por Regeneron), BDNF (factor neurotrófico derivado del cerebro), leptina y moduladores del receptor de leptina, antagonistas del receptor cannabinoide-1 (como SR-141716 (Sanofi) o SLV-319 (Solvay)) y/o un agente anorexígeno.
Los agonistas beta 3 adrenérgicos que se pueden emplear opcionalmente en combinación con las composiciones reivindicadas incluyen AJ9677 (Takeda / Dainippon), L750355 (Merck) o CP331648 (Pfizer) u otros agonistas beta 3 conocidos, como se divulga en las patentes de los Estados Unidos N° 5.541.204, 5.770.615, 5.491.134, 5.776.983 y 5.488.064.
Los ejemplos de inhibidores de lipasa que se pueden emplear opcionalmente en combinación con las composiciones reivindicadas incluyen orlistat o a TL-962 (Alizyme).
El inhibidor de la recaptación de serotonina (y dopamina) (o agonistas del receptor de serotonina) que se puede emplear opcionalmente en combinación con las composiciones reivindicadas puede ser BVT-933 (Biovitrum), sibutramina, topiramato (Johnson & Johnson) o axokine (Regeneron).
Los ejemplos de compuestos del receptor beta tiroideo que se pueden emplear opcionalmente en combinación con las composiciones reivindicadas incluyen ligandos del receptor tiroideo, tales como los descritos en el documento WO 97/21993 (U. Cal SF), WO 99/00353 (KaroBio) y WO 00/039077 (KaroBio).
Los inhibidores de la recaptación de monoamina que se pueden emplear opcionalmente en combinación con las composiciones reivindicadas incluyen fenfluramina, dexfenfluramina, fluvoxamina, fluoxetina, paroxetina, sertralina, clorofenamina, cloforex, clortermina, picilorex, sibutramina, dexanfetamina, fentermina, fenilpropanolamina o mazindol.
El agente anorexígeno que se puede emplear opcionalmente en combinación con las composiciones reivindicadas incluye topiramato (Johnson & Johnson), dexanfetamina, fentermina, fenilpropanolamina o mazindol.
Los otros agentes terapéuticos anteriores, cuando se emplean en combinación con las composiciones reivindicadas, se pueden usar, por ejemplo, en las cantidades indicadas en Physicians 'Desk Reference, como en las patentes establecidas anteriormente o según lo determine un experto en la técnica.
Claims (9)
2. Una composición farmacéutica de acuerdo con la reivindicación 1, en la que el solvato cristalino de (S)-propilenglicol ((S)-PG se caracteriza por uno o más de los siguientes:
a) parámetros de célula unitaria sustancialmente iguales a los siguientes:
Dimensiones de la célula:
a = 11,2688 (8) A
b = 4,8093 (3) A
c = 46,723 (3) A
a = 90 grados
p = 90 grados
Y = 90 grados
Grupo espacial = P212121
Moléculas / unidad asimétrica = 1
en donde la medición de dicha estructura cristalina es a temperatura ambiente y que se caracteriza por coordenadas atómicas fraccionarias sustancialmente como se enumeran en la Tabla 4;
b) un patrón de difracción de rayos X de polvo que comprende valores 20 (CuKaA = 1,5418 A) seleccionados del grupo que consiste de 3,8 ± 0,1, 7,6 ± 0,1, 8,1 ± 0,1, 8,7 ± 0,1, 15,2 ± 0,1, 15,7,4 ± 0,1, 17,1 ± 0,1, 18,9 ± 0,1 y 20,1 ± 0,1, a temperatura ambiente;
c) un espectro de RMN 13C en estado sólido que tiene posiciones de pico sustancialmente similares en 16,2, 17,6, 39,3, 60,9, 63,3, 69,8, 76,9, 78,7, 79,4, 113,8, 123,6, 129,3, 130,5, 132,0, 135,7, 139,1 y 158,0 ppm, como se determina en un espectrómetro de 400 MHz con respecto a TMS en cero;
d) un termograma de calorimetría de barrido diferencial que tiene una endoterma en el intervalo de aproximadamente 50°C a 78°C o como se muestra en la Figura 7; o
e) una curva de análisis termogravimétrico con aproximadamente 18,7% de pérdida de peso desde aproximadamente temperatura ambiente hasta aproximadamente 240°C o como se muestra en la Figura 5.
3. Una composición farmacéutica de acuerdo con la reivindicación 1 o la reivindicación 2, que comprende además uno o más agentes terapéuticos seleccionados del grupo que consiste en un agente antidiabético, un agente contra la obesidad, un agente antihipertensivo, un agente antiaterosclerótico y un agente reductor de lípidos.
4. Una composición farmacéutica de acuerdo con la reivindicación 1 o la reivindicación 2, que comprende además un vehículo o diluyente farmacéuticamente aceptable.
5. Una composición farmacéutica de acuerdo con una cualquiera de las reivindicaciones precedentes, en la que el solvato cristalino de (S)-propilenglicol ((S)-PG) se encuentra en forma sustancialmente pura.
6. Una composición farmacéutica de acuerdo con una cualquiera de las reivindicaciones precedentes, en la que el solvato cristalino de (S)-propilenglicol ((S)-PG) tiene una homogeneidad de fase sustancialmente pura.7
7. Una composición farmacéutica de acuerdo con una cualquiera de las reivindicaciones 1 a 6 (S)-propilenglicol ((S)-PG), en la que el solvato cristalino de se caracteriza por parámetros de célula unitaria sustancialmente iguales a los siguientes:
Dimensiones de la célula:
a = 11,2688 (8) A
b = 4,8093 (3) A
c = 46,723 (3) A
a = 90 grados
p = 90 grados
y = 90 grados
Grupo espacial = P2i2i2i
Moléculas / unidad asimétrica = 1
en donde la medición de dicha estructura cristalina es a temperatura ambiente y que se caracteriza por coordenadas atómicas fraccionarias sustancialmente como se enumeran en la Tabla 4.
8. Una composición farmacéutica de acuerdo con una cualquiera de las reivindicaciones en la que el solvato de 1 a 6, (S)-PG) se caracteriza por un espectro de RMN 13C en estado sólido que tiene posiciones de pico sustancialmente similares a, 16,2, 17,6, 39,3, 60,9, 63,3, 69,8, 76,9, 78,7, 79,4, 113,8, 123,6, 129,3, 130,5, 132,0, 135,7, 139,1 y 158,0 ppm, como se determina en un espectrómetro de 400 MHz respecto a TMS en cero.
9. Una composición farmacéutica de acuerdo con una cualquiera de las reivindicaciones 1 a 6, en la que el solvato cristalino de (S)-propilenglicol ((S)=PG) se caracteriza por un termograma de calorimetría de barrido diferencial que tiene una endoterma en el intervalo de aproximadamente 50°C a 78°C o como se muestra en la Figura 7.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US81711806P | 2006-06-28 | 2006-06-28 | |
| US11/765,481 US7919598B2 (en) | 2006-06-28 | 2007-06-20 | Crystal structures of SGLT2 inhibitors and processes for preparing same |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2769130T3 true ES2769130T3 (es) | 2020-06-24 |
Family
ID=38581970
Family Applications (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES17203302T Active ES2769130T3 (es) | 2006-06-28 | 2007-06-21 | Composición farmacéutica que comprende un solvato de (S)-propilenglicol de (2S,3R,4S,5S,6R)-2-[4-cloro-3-(4-etoxi-bencil)-fenil]-6-hidroximetil-2-metoxi-tetrahidro-piran-3,4,5-triol cristalino. |
| ES07784499T Active ES2521665T5 (es) | 2006-06-28 | 2007-06-21 | Solvatos cristalinos de derivados de (1S)-1,5-anhidro-1-C-(3-((fenil)metil)fenil)-D-glucitol con alcoholes como inhibidores de SGLT2 para el tratamiento de diabetes |
| ES15181545T Active ES2659862T5 (en) | 2006-06-28 | 2007-06-21 | (2s,3r,4s,5s,6r)-2-[4-chloro-3-(4-ethoxy-benzyl)-phenyl]-6-hydroxymethyl-2-methoxy-tetrahydro-pyran-3,4,5-triol propylene glycol solvate as sgt2 inhibitor for the treatment of diabetes |
Family Applications After (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES07784499T Active ES2521665T5 (es) | 2006-06-28 | 2007-06-21 | Solvatos cristalinos de derivados de (1S)-1,5-anhidro-1-C-(3-((fenil)metil)fenil)-D-glucitol con alcoholes como inhibidores de SGLT2 para el tratamiento de diabetes |
| ES15181545T Active ES2659862T5 (en) | 2006-06-28 | 2007-06-21 | (2s,3r,4s,5s,6r)-2-[4-chloro-3-(4-ethoxy-benzyl)-phenyl]-6-hydroxymethyl-2-methoxy-tetrahydro-pyran-3,4,5-triol propylene glycol solvate as sgt2 inhibitor for the treatment of diabetes |
Country Status (32)
| Country | Link |
|---|---|
| US (3) | US7919598B2 (es) |
| EP (4) | EP2457918A3 (es) |
| JP (6) | JP5313889B2 (es) |
| KR (1) | KR101493102B1 (es) |
| CN (2) | CN101479287B (es) |
| AR (1) | AR061730A1 (es) |
| AU (1) | AU2007265246B2 (es) |
| BR (3) | BR122017021516B8 (es) |
| CA (3) | CA2924318C (es) |
| CL (1) | CL2007001915A1 (es) |
| CO (1) | CO6160299A2 (es) |
| CY (1) | CY1115738T1 (es) |
| DK (1) | DK2069374T4 (es) |
| EA (4) | EA018229B1 (es) |
| ES (3) | ES2769130T3 (es) |
| HR (1) | HRP20141007T4 (es) |
| IL (5) | IL195882A (es) |
| MX (3) | MX339143B (es) |
| MY (2) | MY148566A (es) |
| NO (2) | NO346828B1 (es) |
| NZ (4) | NZ589202A (es) |
| PE (2) | PE20120776A1 (es) |
| PH (1) | PH12012500168B1 (es) |
| PL (1) | PL2069374T5 (es) |
| PT (1) | PT2069374E (es) |
| RS (1) | RS53638B2 (es) |
| SG (2) | SG10201402181SA (es) |
| SI (1) | SI2069374T2 (es) |
| TW (4) | TWI466876B (es) |
| UA (1) | UA96765C2 (es) |
| WO (1) | WO2008002824A1 (es) |
| ZA (1) | ZA200810475B (es) |
Families Citing this family (166)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| UA91341C2 (ru) | 2004-07-15 | 2010-07-26 | Амр Текнолоджи, Інк. | Арил- и гетероарилзамещенные тетрагидроизохинолины и их применение для блокирования обратного захвата норэпинефрина, допамина и серотонина |
| TW200726755A (en) * | 2005-07-07 | 2007-07-16 | Astellas Pharma Inc | A crystalline choline salt of an azulene derivative |
| TWI370818B (en) * | 2006-04-05 | 2012-08-21 | Astellas Pharma Inc | Cocrystal of c-glycoside derivative and l-proline |
| US7919598B2 (en) * | 2006-06-28 | 2011-04-05 | Bristol-Myers Squibb Company | Crystal structures of SGLT2 inhibitors and processes for preparing same |
| KR101100072B1 (ko) * | 2006-12-21 | 2011-12-29 | 고토부키 세이야쿠 가부시키가이샤 | C-글리코시드 유도체의 제조방법 및 이의 합성 중간체 |
| AR065809A1 (es) * | 2007-03-22 | 2009-07-01 | Bristol Myers Squibb Co | Formulaciones farmaceuticas que contienen un inhibidor sglt2 |
| TW200904454A (en) | 2007-03-22 | 2009-02-01 | Bristol Myers Squibb Co | Methods for treating obesity employing an SGLT2 inhibitor and compositions thereof |
| CN101754972A (zh) * | 2007-05-18 | 2010-06-23 | 百时美施贵宝公司 | Sglt2抑制剂的晶体结构及其制备方法 |
| EP2025674A1 (de) | 2007-08-15 | 2009-02-18 | sanofi-aventis | Substituierte Tetrahydronaphthaline, Verfahren zu ihrer Herstellung und ihre Verwendung als Arzneimittel |
| UA101004C2 (en) | 2007-12-13 | 2013-02-25 | Теракос, Инк. | Derivatives of benzylphenylcyclohexane and use thereof |
| CN104387354A (zh) * | 2007-12-27 | 2015-03-04 | 阿斯利康公司 | Sglt2 抑制剂的晶体结构及其制备方法 |
| CN103319445B (zh) * | 2007-12-27 | 2016-01-20 | 阿斯利康公司 | Sglt2抑制剂的晶体结构及其制备方法 |
| ES2541141T3 (es) * | 2008-01-31 | 2015-07-16 | Astellas Pharma Inc. | Composición farmacéutica para el tratamiento de las enfermedades del hígado graso |
| US8450286B2 (en) * | 2008-03-18 | 2013-05-28 | Bristol-Myers Squibb Company | Method for treating cancers having high glucose requirements employing an SGLT2 inhibitor and compositions thereof |
| WO2009143021A1 (en) * | 2008-05-22 | 2009-11-26 | Bristol-Myers Squibb Company | Method for treating and preventing kidney stones employing an sglt2 inhibitor and composition containing same |
| WO2009143010A1 (en) * | 2008-05-22 | 2009-11-26 | Bristol-Myers Squibb Company | Method for treating hyponatremia employing an sglt2 inhibitor and composition containing same |
| US8791077B2 (en) * | 2008-05-22 | 2014-07-29 | Astrazeneca Ab | Method for treating hyperuricemia employing an SGLT2 inhibitor and composition containing same |
| US9156812B2 (en) | 2008-06-04 | 2015-10-13 | Bristol-Myers Squibb Company | Crystalline form of 6-[(4S)-2-methyl-4-(2-naphthyl)-1,2,3,4-tetrahydroisoquinolin-7-yl]pyridazin-3-amine |
| AU2009270936B2 (en) | 2008-07-15 | 2014-12-18 | Theracos, Inc. | Deuterated benzylbenzene derivatives and methods of use |
| AU2014201286B2 (en) * | 2008-08-22 | 2015-07-02 | Theracosbio, Llc | Processes for the preparation of SGLT2 inhibitors |
| MX2011001855A (es) * | 2008-08-22 | 2011-03-24 | Theracos Inc | Procesos para la preparacion de inhibidores de sglt2. |
| MY155418A (en) | 2008-08-28 | 2015-10-15 | Pfizer | Dioxa-bicyclo[3.2.1]octane-2,3,4-triol derivatives |
| BRPI1008560B1 (pt) | 2009-02-13 | 2021-08-31 | Boehringer Ingelheim International Gmbh | Composição farmacêutica compreendendo um inibidor de sglt2, um inibidor de dpp-iv e opcionalmente um outro agente antidiabético e usos dos mesmos |
| EP2429295B1 (en) * | 2009-05-12 | 2013-12-25 | Albany Molecular Research, Inc. | Aryl, heteroaryl, and heterocycle substituted tetrahydroisoquinolines and use thereof |
| US8815894B2 (en) * | 2009-05-12 | 2014-08-26 | Bristol-Myers Squibb Company | Crystalline forms of (S)-7-([1,2,4]triazolo[1,5-a]pyridin-6-yl)-4-(3,4-dichlorophenyl)-1,2,3,4-tetrahydroisoquinoline and use thereof |
| AU2010247763B2 (en) * | 2009-05-12 | 2015-12-24 | Albany Molecular Research, Inc. | 7-([1,2,4,]triazolo[1,5,-a]pyridin-6-yl)-4-(3,4-dichlorophenyl)-1,2,3,4- tetrahydroisoquinoline and use thereof |
| US20110009347A1 (en) | 2009-07-08 | 2011-01-13 | Yin Liang | Combination therapy for the treatment of diabetes |
| EA021983B1 (ru) | 2009-11-02 | 2015-10-30 | Пфайзер Инк. | Производные диоксабицикло[3.2.1]октан-2,3,4-триола |
| EP3315124B1 (en) | 2009-11-13 | 2021-01-06 | Astrazeneca AB | Bilayer tablet formulations |
| JP5784623B2 (ja) | 2009-11-13 | 2015-09-24 | アストラゼネカ・アクチエボラーグAstrazeneca Aktiebolag | 速放性錠剤製剤 |
| WO2011107494A1 (de) | 2010-03-03 | 2011-09-09 | Sanofi | Neue aromatische glykosidderivate, diese verbindungen enthaltende arzneimittel und deren verwendung |
| EP2552442A1 (en) | 2010-03-30 | 2013-02-06 | Boehringer Ingelheim International GmbH | Pharmaceutical composition comprising an sglt2 inhibitor and a ppar- gamma agonist and uses thereof |
| TWI599360B (zh) | 2010-05-11 | 2017-09-21 | 健生藥品公司 | 醫藥調配物 |
| WO2011153712A1 (en) | 2010-06-12 | 2011-12-15 | Theracos, Inc. | Crystalline form of benzylbenzene sglt2 inhibitor |
| WO2011157827A1 (de) | 2010-06-18 | 2011-12-22 | Sanofi | Azolopyridin-3-on-derivate als inhibitoren von lipasen und phospholipasen |
| US8530413B2 (en) | 2010-06-21 | 2013-09-10 | Sanofi | Heterocyclically substituted methoxyphenyl derivatives with an oxo group, processes for preparation thereof and use thereof as medicaments |
| TW201215388A (en) | 2010-07-05 | 2012-04-16 | Sanofi Sa | (2-aryloxyacetylamino)phenylpropionic acid derivatives, processes for preparation thereof and use thereof as medicaments |
| TW201221505A (en) | 2010-07-05 | 2012-06-01 | Sanofi Sa | Aryloxyalkylene-substituted hydroxyphenylhexynoic acids, process for preparation thereof and use thereof as a medicament |
| TW201215387A (en) | 2010-07-05 | 2012-04-16 | Sanofi Aventis | Spirocyclically substituted 1,3-propane dioxide derivatives, processes for preparation thereof and use thereof as a medicament |
| WO2012025857A1 (en) | 2010-08-23 | 2012-03-01 | Hetero Research Foundation | Cycloalkyl methoxybenzyl phenyl pyran derivatives as sodium dependent glucose co transporter (sglt2) inhibitors |
| CN103370064A (zh) | 2010-09-03 | 2013-10-23 | 百时美施贵宝公司 | 使用水溶性抗氧化剂的药物制剂 |
| WO2012041898A1 (en) | 2010-09-29 | 2012-04-05 | Celon Pharma Sp. Z O.O. | Combination of sglt2 inhibitor and a sugar compound for the treatment of diabetes |
| US20120283169A1 (en) | 2010-11-08 | 2012-11-08 | Boehringer Ingelheim International Gmbh | Pharmaceutical composition, methods for treating and uses thereof |
| CA2826391C (en) | 2011-02-01 | 2017-01-24 | Bristol-Myers Squibb Company | Pharmaceutical formulations including an amine compound |
| US20130035281A1 (en) | 2011-02-09 | 2013-02-07 | Boehringer Ingelheim International Gmbh | Pharmaceutical composition, methods for treating and uses thereof |
| RS55056B1 (sr) | 2011-04-13 | 2016-12-30 | Janssen Pharmaceutica Nv | Proces za pripremu jedinjenja koja su korisna kao inhibitori sglt2 |
| TWI542596B (zh) * | 2011-05-09 | 2016-07-21 | 健生藥品公司 | (2s,3r,4r,5s,6r)-2-(3-((5-(4-氟苯基)噻吩-2-基)甲基)-4-甲基苯基)-6-(羥甲基)四氫-2h-哌喃-3,4,5-三醇之l-脯胺酸及檸檬酸共晶體 |
| BR112013031032A2 (pt) | 2011-06-03 | 2016-11-29 | Boehringer Ingelheim Int | inibidores de sglt-2 para o tratamento de distúrbios metabólicos em pacientes tratados com agentes neurolépticos |
| WO2013037390A1 (en) | 2011-09-12 | 2013-03-21 | Sanofi | 6-(4-hydroxy-phenyl)-3-styryl-1h-pyrazolo[3,4-b]pyridine-4-carboxylic acid amide derivatives as kinase inhibitors |
| EP2760862B1 (en) | 2011-09-27 | 2015-10-21 | Sanofi | 6-(4-hydroxy-phenyl)-3-alkyl-1h-pyrazolo[3,4-b]pyridine-4-carboxylic acid amide derivatives as kinase inhibitors |
| CN103889429B (zh) * | 2011-10-31 | 2016-10-19 | 台湾神隆股份有限公司 | Sglt2抑制剂的结晶和非结晶形式 |
| EP2597090A1 (en) | 2011-11-28 | 2013-05-29 | Sandoz AG | Crystalline dapagliflozin hydrate |
| WO2013090550A1 (en) | 2011-12-15 | 2013-06-20 | National Health Research Institutes | Novel glycoside compounds |
| US9193751B2 (en) | 2012-04-10 | 2015-11-24 | Theracos, Inc. | Process for the preparation of benzylbenzene SGLT2 inhibitors |
| US9145434B2 (en) | 2012-07-26 | 2015-09-29 | Boehringer Ingelheim International Gmbh | Crystalline complex of 1-cyano-2-(4-cyclopropyl-benzyl)-4-(ss-d-glucopyranos-1-yl)-benzene, methods for its preparation and the use thereof for preparing medicaments |
| CN103910719B (zh) * | 2012-12-31 | 2018-05-01 | 上海璎黎药业有限公司 | 葡萄糖衍生物与苯丙氨酸复合物、晶体、制备方法及应用 |
| CN103910769B (zh) * | 2012-12-31 | 2018-10-02 | 上海璎黎药业有限公司 | 葡萄糖衍生物和脯氨酸的复合物、晶体、制备方法及应用 |
| EP2968375B1 (en) | 2013-03-14 | 2019-06-12 | MSD International GmbH | Methods for preparing sglt2 inhibitors |
| DK2981269T3 (da) | 2013-04-04 | 2023-10-23 | Boehringer Ingelheim Vetmedica Gmbh | Behandling af stofskifteforstyrrelser hos hestedyr |
| WO2014178040A1 (en) | 2013-04-29 | 2014-11-06 | Mapi Pharma Ltd. | Co-crystals of dapagliflozin |
| US20160214953A1 (en) | 2013-09-23 | 2016-07-28 | Sun Pharmaceutical Industries Limited | Process for the preparation of dapagliflozin |
| EP3049397A1 (en) | 2013-09-27 | 2016-08-03 | Sun Pharmaceutical Industries Ltd | Process for the purification of dapagliflozin |
| WO2015051484A1 (en) | 2013-10-12 | 2015-04-16 | Theracos, Inc. | Preparation of hydroxy-benzylbenzene derivatives |
| WO2015063726A1 (en) | 2013-10-31 | 2015-05-07 | Ranbaxy Laboratories Limited | Process for the preparation of 4-bromo-1-chloro-2-(4-ethoxybenzyl)benzene |
| MX376097B (es) | 2013-12-17 | 2025-03-07 | Boehringer Ingelheim Vetmedica Gmbh | Inhibidores de sglt2 para usarse en el tratamiento o prevención de trastornos metabólicos en animales felinos. |
| CA2932674C (en) | 2014-01-23 | 2023-01-24 | Boehringer Ingelheim Vetmedica Gmbh | Treatment of metabolic disorders in canine animals |
| CN104829572B (zh) * | 2014-02-10 | 2019-01-04 | 江苏豪森药业集团有限公司 | 达格列净新晶型及其制备方法 |
| EP3110402A1 (en) | 2014-02-28 | 2017-01-04 | Sun Pharmaceutical Industries Ltd | Dapagliflozin compositions |
| EP3114115A4 (en) * | 2014-03-06 | 2017-08-23 | MSN Laboratories Private Limited | Process for the preparation of (1s)-1,5-anhydro-1-c-[4-chloro-3-[(4-ethoxyphenyl)methyl]phenyl]-d-glucitol and its solvate thereof |
| FI3721882T3 (fi) | 2014-04-01 | 2024-09-24 | Boehringer Ingelheim Vetmedica Gmbh | Aineenvaihduntahäiriöiden hoito hevoseläimissä |
| KR102149572B1 (ko) | 2014-05-19 | 2020-08-28 | 화이자 인코포레이티드 | 아시알로당단백질 수용체의 표적화제로서 치환된-6,8-다이옥사바이사이클로[3.2.1]옥탄-2,3-다이올 화합물 |
| CN104017031A (zh) * | 2014-06-21 | 2014-09-03 | 李友香 | 降血糖药物和组合物 |
| CN104031098A (zh) * | 2014-06-21 | 2014-09-10 | 李友香 | 降糖药物 |
| EP3229814A4 (en) * | 2014-06-23 | 2018-07-11 | Sun Pharmaceutical Industries Ltd | Co-crystal of dapagliflozin with citric acid |
| KR20160013770A (ko) * | 2014-07-28 | 2016-02-05 | 한미정밀화학주식회사 | 다파글리프로진의 신규 결정질 복합체 및 이의 제조방법 |
| EP4403230A3 (en) | 2014-09-25 | 2025-01-08 | Boehringer Ingelheim Vetmedica GmbH | Combination treatment of sglt2 inhibitors and dopamine agonists for preventing metabolic disorders in equine animals |
| JP2017528499A (ja) | 2014-09-25 | 2017-09-28 | アストラゼネカ・アクチエボラーグAstrazeneca Aktiebolag | 肝臓の疾患を治療するためのオメガ3脂肪酸とsglt−2阻害薬との併用剤 |
| CN104496952B (zh) * | 2014-11-28 | 2017-04-19 | 深圳翰宇药业股份有限公司 | 一种达格列净的合成方法 |
| US20170342100A1 (en) * | 2014-12-03 | 2017-11-30 | Sun Pharmaceutical Industries Limited | Processes for the preparation of ertugliflozin |
| CZ2015110A3 (cs) * | 2015-02-18 | 2016-08-31 | Zentiva, K.S. | Pevné formy empagliflozinu |
| WO2016147197A1 (en) * | 2015-03-17 | 2016-09-22 | Harman Finochem Limited | A novel process for preparing (2s,3r,4r,5s,6r)-2-[4-chloro-3-(4-ethoxybenzyl)pheny 1] -6-(hy droxy methyl)tetrahydro-2h-py ran-3,4,5-triol and its amorphous form |
| WO2016155578A1 (zh) * | 2015-03-27 | 2016-10-06 | 苏州晶云药物科技有限公司 | 达格列净的新晶型及其制备方法 |
| WO2016161995A1 (en) | 2015-04-08 | 2016-10-13 | Zentiva, K.S. | Solid forms of amorphous dapagliflozin |
| CN106146446B (zh) * | 2015-04-17 | 2019-11-08 | 杭州领业医药科技有限公司 | 达格列净半水合物及其晶型、其制备方法及药物组合物 |
| WO2016178148A1 (en) * | 2015-05-05 | 2016-11-10 | Glenmark Pharmaceuticals Limited | Process for preparation of dapagliflozin |
| SG10201911417PA (en) | 2015-06-17 | 2020-01-30 | Otsuka America Pharmaceutical Inc | Crystalline compounds |
| WO2017042683A1 (en) * | 2015-09-07 | 2017-03-16 | Dr. Reddy's Laboratories Limited | Isolated intermediate of dapagliflozin, process for the preparation of isolated intermediate of dapagliflozin, process for the preparation of dapagliflozin |
| ES2896101T3 (es) | 2015-09-15 | 2022-02-23 | Laurus Labs Ltd | Cocristales de inhibidores de SGLT2, procedimiento para su preparación y composiciones farmacéuticas de los mismos |
| WO2017060925A1 (en) * | 2015-10-09 | 2017-04-13 | Harman Finochem Limited | Novel pipecolic acid co-crystals of dapagliflozin and process for the preparation thereof |
| US9845303B2 (en) | 2015-10-19 | 2017-12-19 | Cadila Healthcare Limited | Process for the preparation of dapagliflozin |
| CA3005920C (en) * | 2015-11-27 | 2023-08-22 | Sunshine Lake Pharma Co., Ltd. | A complex of a glucopyranosyl derivative and preparation method and use thereof |
| WO2017099496A1 (ko) * | 2015-12-11 | 2017-06-15 | 동아에스티 주식회사 | 다파글리플로진의 신규 용매화물 및 이의 제조방법 |
| WO2017118945A1 (en) | 2016-01-08 | 2017-07-13 | Lupin Limited | Premix of dapagliflozin and process for the preparation thereof |
| CN105503802A (zh) * | 2016-01-15 | 2016-04-20 | 中山大学 | 一种达格列净-柠檬酸共晶的制备方法 |
| ES3061357T3 (en) | 2016-03-11 | 2026-04-01 | Merck Sharp & Dohme Llc | Ertugliflozin for use in treating heart failure in patients with diabetes |
| MX2018011696A (es) | 2016-03-31 | 2019-06-06 | Lupin Ltd | Composición farmacéutica de dapagliflozina. |
| WO2017191539A1 (en) * | 2016-05-02 | 2017-11-09 | Aurobindo Pharma Limited | Process for the preparation dl-proline co-crystal of dapagliflozin |
| EP3466939B1 (en) * | 2016-05-24 | 2021-02-24 | Jiangsu Hansoh Pharmaceutical Group Co., Ltd. | New dapagliflozin crystal form and preparation method and use thereof |
| WO2017203457A1 (en) * | 2016-05-26 | 2017-11-30 | Dr. Reddy's Laboratories Limited | Solid state forms of empagliflozin |
| WO2017203229A1 (en) | 2016-05-27 | 2017-11-30 | Cipla Limited | Dapagliflozin premixes |
| WO2017206827A1 (zh) * | 2016-05-28 | 2017-12-07 | 山东轩竹医药科技有限公司 | 钠-葡萄糖协同转运蛋白2抑制剂的晶型 |
| CN107445932A (zh) * | 2016-05-30 | 2017-12-08 | 上海医药工业研究院 | 达格列净共晶物的制备工艺 |
| WO2017221211A1 (en) * | 2016-06-24 | 2017-12-28 | Biocon Limited | Process for the preparation of dapagliflozin and its solvate thereof |
| CN107641139A (zh) | 2016-07-22 | 2018-01-30 | 江苏豪森药业集团有限公司 | 达格列净中间体的晶型及其制备方法 |
| BR112019005930A2 (pt) | 2016-10-19 | 2019-06-11 | Boehringer Ingelheim Int | combinações compreendendo um inibidor de ssao/vap-1 e um inibidor de sglt2, e usos das mesmas |
| KR20180058510A (ko) * | 2016-11-24 | 2018-06-01 | 한미약품 주식회사 | 다파글리플로진 l-프롤린을 포함하는 약제학적 제제 |
| KR20180078762A (ko) * | 2016-12-30 | 2018-07-10 | 한미약품 주식회사 | 다파글리플로진 l-프롤린을 포함하는 당뇨병 질환의 예방 또는 치료용 약제학적 조성물 |
| WO2018124497A1 (ko) * | 2016-12-30 | 2018-07-05 | 한미약품 주식회사 | 다파글리플로진 l-프롤린과 항당뇨병제를 포함하는 약제학적 복합 제제 |
| WO2018167589A1 (en) | 2017-03-16 | 2018-09-20 | Inventia Healthcare Private Limited | Pharmaceutical composition comprising dapagliflozin |
| AR112015A1 (es) | 2017-06-09 | 2019-09-11 | Novo Nordisk As | Composiciones sólidas para administración oral |
| CN107488156B (zh) * | 2017-09-04 | 2020-05-26 | 上海现代制药股份有限公司 | 一种无定型葡萄糖醇的合成方法 |
| WO2019066359A2 (ko) * | 2017-09-29 | 2019-04-04 | 한미약품 주식회사 | 다파글리플로진 l-프롤린과 메트포르민을 포함하는 약제학적 복합제제 |
| KR102369679B1 (ko) * | 2017-09-29 | 2022-03-04 | 한미약품 주식회사 | 다파글리플로진 l-프롤린과 메트포르민을 포함하는 약제학적 복합제제 |
| CN108516966A (zh) * | 2017-10-19 | 2018-09-11 | 浙江海正药业股份有限公司 | 达格列净的晶型及其制备方法和用途 |
| KR20190115948A (ko) | 2018-04-04 | 2019-10-14 | 한미약품 주식회사 | 다파글리플로진 l-프롤린을 포함하는 당뇨병 질환의 예방 또는 치료용 약제학적 조성물 |
| US20210113561A1 (en) | 2018-04-17 | 2021-04-22 | Boehringer Ingelheim International Gmbh | Pharmaceutical composition, methods for treating and uses thereof |
| KR102204439B1 (ko) | 2018-05-14 | 2021-01-18 | 에이치케이이노엔 주식회사 | Sglt-2 억제제 및 dpp-iv 억제제를 포함하는 약제학적 조성물 |
| BR112021000139A2 (pt) | 2018-07-19 | 2021-04-06 | Astrazeneca Ab | Métodos de tratamento da hfpef empregando dapagliflozina e composições compreendendo a mesma |
| WO2020039394A1 (en) | 2018-08-24 | 2020-02-27 | Novartis Ag | New drug combinations |
| US10968192B2 (en) * | 2018-09-26 | 2021-04-06 | Lexicon Pharmaceuticals, Inc. | Crystalline solid forms of N-(1-((2-(dimethylamino)ethyl)amino)-2-methyl-1-oxopropan-2-yl)-4-(4-(2-methyl-5-((2S,3R,4R,5S,6R)-3,4,5-trihydroxy-6-(methylthio)tetrahydro-2H-pyran-2-yl)benzyl)phenyl)butanamide and methods of their synthesis |
| MX2021003845A (es) | 2018-10-01 | 2021-05-27 | Astrazeneca Ab | Composiciones para reducir el acido urico serico. |
| DK3873600T5 (da) | 2018-10-29 | 2024-03-18 | Boehringer Ingelheim Int | Pyridinylsulfonamidderivater, farmaceutiske sammensætninger og anvendelser deraf |
| US12213970B2 (en) | 2018-10-29 | 2025-02-04 | Boehringer Ingelheim International Gmbh | Pyridinyl sulfonamide derivatives, pharmaceutical compositions and uses thereof |
| CN109705075B (zh) * | 2018-12-13 | 2022-12-23 | 苏中药业集团股份有限公司 | 一种达格列净的纯化方法 |
| CN109705076B (zh) * | 2019-01-21 | 2023-03-24 | 苏中药业集团股份有限公司 | 一种达格列净晶型、制备方法及其用途 |
| CN111559997A (zh) * | 2019-02-13 | 2020-08-21 | 罗欣药业(上海)有限公司 | 一种达格列净新晶型及其制备方法 |
| CN111689936A (zh) * | 2019-03-15 | 2020-09-22 | 罗欣药业(上海)有限公司 | 达格列净新晶型及其制备方法 |
| CN114641276A (zh) | 2019-11-07 | 2022-06-17 | 诺和诺德股份有限公司 | 包含glp-1激动剂、sglt2抑制剂和n-(8-(2-羟基苯甲酰基)氨基)辛酸的盐的固体组合物 |
| MX2019014226A (es) * | 2019-11-27 | 2022-09-23 | Alparis Sa De Cv | Nuevas fases sólidas de dapagliflozina. |
| EP4064854A1 (en) | 2019-11-28 | 2022-10-05 | Boehringer Ingelheim Vetmedica GmbH | Use of sglt-2 inhibitors in the drying-off of non-human mammals |
| PH12022551449A1 (en) * | 2019-12-24 | 2023-10-16 | Hanmi Pharmaceutical Co Ltd | Complex formulation comprising sitagliptin and dapagliflozin, and preparation method therefor |
| CN119841865A (zh) | 2020-02-07 | 2025-04-18 | 加舒布鲁姆生物公司 | 杂环glp-1激动剂 |
| JP7423800B2 (ja) | 2020-02-17 | 2024-01-29 | ベーリンガー インゲルハイム フェトメディカ ゲーエムベーハー | ネコにおける心臓疾患の予防および/または治療のためのsglt-2阻害剤の使用 |
| UA128665C2 (uk) | 2020-02-21 | 2024-09-18 | Заклади Фармацеутичне Полфарма С.А. | Фармацевтична композиція, яка містить аморфний дапагліфлозин |
| EP4114365A1 (en) | 2020-03-05 | 2023-01-11 | KRKA, d.d., Novo mesto | Pharmaceutical composition comprising sglt2 inhibitor |
| EP4138826A1 (en) | 2020-04-22 | 2023-03-01 | Bayer Aktiengesellschaft | Combination of finerenone and a sglt2 inhibitor for the treatment and/or prevention of cardiovascular and/or renal diseases |
| FI4143183T3 (fi) | 2020-04-29 | 2026-01-07 | Gasherbrum Bio Inc | Heterosyklisiä glp-1-agonisteja |
| US20230165856A1 (en) | 2020-04-29 | 2023-06-01 | Astrazeneca Ab | Dapagliflozin and ambrisentan for the prevention and treatment of covid-19 |
| KR102838283B1 (ko) * | 2020-07-10 | 2025-07-25 | 한미약품 주식회사 | 시타글립틴 및 다파글리플로진을 포함하는 복합제제 및 그 제조방법 |
| TW202220672A (zh) | 2020-07-27 | 2022-06-01 | 瑞典商阿斯特捷利康公司 | 用達格列淨治療慢性腎臟病之方法 |
| AU2021202643B2 (en) | 2020-07-27 | 2023-02-02 | Astrazeneca Ab | Methods of treating chronic kidney disease with dapagliflozin |
| PE20231181A1 (es) | 2020-08-06 | 2023-08-11 | Gasherbrum Bio Inc | Agonistas del glp-1 heterociclicos |
| EP4206212A4 (en) * | 2020-09-30 | 2024-05-22 | Beijing Creatron Institute of Pharmaceutical Research Co., Ltd. | Sglt-2 inhibitor sarcosine co-crystal, preparation method therefor and use thereof |
| MX2024001184A (es) | 2021-07-28 | 2024-02-27 | Boehringer Ingelheim Vetmedica Gmbh | Uso de inhibidores de sglt-2 para la prevencion y/o tratamiento de cardiopatias en mamiferos no humanos, que excluye felinos, en particular, caninos. |
| CN117715639A (zh) | 2021-07-28 | 2024-03-15 | 勃林格殷格翰动物保健有限公司 | Sglt-2抑制剂用于预防和/或治疗非人哺乳动物中的肾脏病的用途 |
| US20240269105A1 (en) | 2021-07-28 | 2024-08-15 | Boehringer Ingelheim Vetmedica Gmbh | Use of sglt-2 inhibitors for the prevention and/or treatment of hypertension in non-human mammals |
| CN114394993B (zh) * | 2021-11-11 | 2023-11-10 | 苏州正济药业有限公司 | 一种达格列净中间体的制备方法 |
| CN114213399B (zh) * | 2021-12-20 | 2024-10-01 | 上海启讯医药科技有限公司 | 一种卡格列净丙酮水合物及其制备方法和用途 |
| AU2022425078A1 (en) | 2021-12-30 | 2024-08-08 | Newamsterdam Pharma B.V. | Obicetrapib and sglt2 inhibitor combination |
| US20250108065A1 (en) | 2022-01-26 | 2025-04-03 | Astrazeneca Ab | Methods of treating prediabetes or reducing the risk of developing type 2 diabetes with dapagliflozin |
| CN119137124A (zh) | 2022-03-09 | 2024-12-13 | 加舒布鲁姆生物公司 | 杂环glp-1激动剂 |
| WO2023179542A1 (en) | 2022-03-21 | 2023-09-28 | Gasherbrum Bio , Inc. | 5,8-dihydro-1,7-naphthyridine derivatives as glp-1 agonists for the treatment of diabetes |
| WO2023198140A1 (en) | 2022-04-14 | 2023-10-19 | Gasherbrum Bio, Inc. | Heterocyclic glp-1 agonists |
| WO2023227492A1 (en) | 2022-05-25 | 2023-11-30 | Boehringer Ingelheim Vetmedica Gmbh | Aqueous pharmaceutical compositions comprising sglt-2 inhibitors |
| CA3264757A1 (en) | 2022-08-12 | 2024-02-15 | Astrazeneca Ab | Polytherapy for the treatment of cirrhosis with portal hypertension |
| CR20250112A (es) | 2022-09-01 | 2025-08-18 | Aztrazeneca Ab | Combinación de ihnibidores de sglt2 y moduladores del receptor mineralcorticoide para usar en el tratamiento de enfermedades cardiorrenales |
| WO2024062310A1 (en) * | 2022-09-22 | 2024-03-28 | Savoi Guilherme | Co-crystals derived from empagliflozin and dapagliflozin with l-proline |
| JP2026508912A (ja) | 2023-03-06 | 2026-03-13 | ベーリンガー インゲルハイム フェトメディカ ゲーエムベーハー | 液体医薬組成物、特に1種又は複数のsglt-2阻害剤を含む液体医薬組成物の送達のためのシステム |
| EP4427742A1 (en) | 2023-03-06 | 2024-09-11 | Galenicum Health S.L.U. | Pharmaceutical compositions comprising dapagliflozin and metformin |
| EP4431088A1 (en) | 2023-03-06 | 2024-09-18 | Galenicum Health S.L.U. | Pharmaceutical compositions comprising dapagliflozin and metformin |
| WO2024226537A1 (en) | 2023-04-24 | 2024-10-31 | Newamsterdam Pharma B.V. | Amorphous obicetrapib and sglt2 inhibitor combination |
| CN121175053A (zh) | 2023-05-24 | 2025-12-19 | 勃林格殷格翰动物保健有限公司 | 包含一或多种sglt-2抑制剂及替米沙坦的非人类哺乳动物中肾脏疾病和/或高血压的组合治疗和/或预防 |
| TW202508593A (zh) | 2023-05-24 | 2025-03-01 | 德商百靈佳殷格翰維美迪加股份有限公司 | 包含一或多種sglt-2抑制劑及匹莫苯坦(pimobendan)及/或替米沙坦(telmisartan)之非人類哺乳動物心臟病之組合治療及/或預防 |
| EP4487910A1 (en) | 2023-07-06 | 2025-01-08 | Zaklady Farmaceutyczne Polpharma S.A. | Process for the preparation of dapagliflozin |
| CN117624100A (zh) * | 2023-10-30 | 2024-03-01 | 宣城美诺华药业有限公司 | 一种达格列净的高效生产工艺 |
| WO2025125513A1 (en) | 2023-12-15 | 2025-06-19 | AstraZeneca Ireland Limited | Sglt2 inhibitors and baxdrostat for treating chronic kidney disease and hypertension |
Family Cites Families (84)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3674836A (en) | 1968-05-21 | 1972-07-04 | Parke Davis & Co | 2,2-dimethyl-{11 -aryloxy-alkanoic acids and salts and esters thereof |
| US4027009A (en) | 1973-06-11 | 1977-05-31 | Merck & Co., Inc. | Compositions and methods for depressing blood serum cholesterol |
| JPS5612114B2 (es) | 1974-06-07 | 1981-03-18 | ||
| US4231938A (en) | 1979-06-15 | 1980-11-04 | Merck & Co., Inc. | Hypocholesteremic fermentation products and process of preparation |
| MX7065E (es) | 1980-06-06 | 1987-04-10 | Sankyo Co | Un procedimiento microbiologico para preparar derivados de ml-236b |
| US4450171A (en) | 1980-08-05 | 1984-05-22 | Merck & Co., Inc. | Antihypercholesterolemic compounds |
| US4448784A (en) | 1982-04-12 | 1984-05-15 | Hoechst-Roussel Pharmaceuticals, Inc. | 1-(Aminoalkylphenyl and aminoalkylbenzyl)-indoles and indolines and analgesic method of use thereof |
| US5354772A (en) | 1982-11-22 | 1994-10-11 | Sandoz Pharm. Corp. | Indole analogs of mevalonolactone and derivatives thereof |
| US4499289A (en) | 1982-12-03 | 1985-02-12 | G. D. Searle & Co. | Octahydronapthalenes |
| CA1327360C (en) | 1983-11-14 | 1994-03-01 | William F. Hoffman | Oxo-analogs of mevinolin-like antihypercholesterolemic agents |
| US4613610A (en) | 1984-06-22 | 1986-09-23 | Sandoz Pharmaceuticals Corp. | Cholesterol biosynthesis inhibiting pyrazole analogs of mevalonolactone and its derivatives |
| US4686237A (en) | 1984-07-24 | 1987-08-11 | Sandoz Pharmaceuticals Corp. | Erythro-(E)-7-[3'-C1-3 alkyl-1'-(3",5"-dimethylphenyl)naphth-2'-yl]-3,5-dihydroxyhept-6-enoic acids and derivatives thereof |
| US4647576A (en) | 1984-09-24 | 1987-03-03 | Warner-Lambert Company | Trans-6-[2-(substitutedpyrrol-1-yl)alkyl]-pyran-2-one inhibitors of cholesterol synthesis |
| EP0216785B1 (en) | 1984-12-04 | 1991-01-30 | Sandoz Ag | Indene analogs of mevalonolactone and derivatives thereof |
| US4668794A (en) | 1985-05-22 | 1987-05-26 | Sandoz Pharm. Corp. | Intermediate imidazole acrolein analogs |
| HUT48208A (en) | 1985-10-25 | 1989-05-29 | Sandoz Ag | Process for producing heterocyclic analogues of mevalolactone derivatives and pharmaceutical compositions comprising such compounds |
| FR2596393B1 (fr) | 1986-04-01 | 1988-06-03 | Sanofi Sa | Derives de l'acide hydroxy-3 dihydroxyoxophosphorio-4 butanoique, leur procede de preparation, leur application comme medicament et les compositions les renfermant |
| US5614492A (en) | 1986-05-05 | 1997-03-25 | The General Hospital Corporation | Insulinotropic hormone GLP-1 (7-36) and uses thereof |
| US4681893A (en) | 1986-05-30 | 1987-07-21 | Warner-Lambert Company | Trans-6-[2-(3- or 4-carboxamido-substituted pyrrol-1-yl)alkyl]-4-hydroxypyran-2-one inhibitors of cholesterol synthesis |
| FI89493C (fi) | 1987-05-22 | 1993-10-11 | Squibb & Sons Inc | Foerfarande foer framstaellning av terapeutiskt aktiva, fosforhaltiga inhibitorer av hmg-coa-reduktas och vid foerfarandet anvaendbar ny mellanprodukt |
| US4759923A (en) | 1987-06-25 | 1988-07-26 | Hercules Incorporated | Process for lowering serum cholesterol using poly(diallylmethylamine) derivatives |
| JP2569746B2 (ja) | 1987-08-20 | 1997-01-08 | 日産化学工業株式会社 | キノリン系メバロノラクトン類 |
| US4924024A (en) | 1988-01-11 | 1990-05-08 | E. R. Squibb & Sons, Inc. | Phosphorus-containing squalene synthetase inhibitors, new intermediates and method |
| US4871721A (en) | 1988-01-11 | 1989-10-03 | E. R. Squibb & Sons, Inc. | Phosphorus-containing squalene synthetase inhibitors |
| NO177005C (no) | 1988-01-20 | 1995-07-05 | Bayer Ag | Analogifremgangsmåte for fremstilling av substituerte pyridiner, samt mellomprodukter til bruk ved fremstillingen |
| US5506219A (en) | 1988-08-29 | 1996-04-09 | E. R. Squibb & Sons, Inc. | Pyridine anchors for HMG-CoA reductase inhibitors |
| US5753675A (en) | 1989-03-03 | 1998-05-19 | Novartis Pharmaceuticals Corporation | Quinoline analogs of mevalonolactone and derivatives thereof |
| FI94339C (fi) | 1989-07-21 | 1995-08-25 | Warner Lambert Co | Menetelmä farmaseuttisesti käyttökelpoisen /R-(R*,R*)/-2-(4-fluorifenyyli)- , -dihydroksi-5-(1-metyylietyyli)-3-fenyyli-4-/(fenyyliamino)karbonyyli/-1H-pyrroli-1-heptaanihapon ja sen farmaseuttisesti hyväksyttävien suolojen valmistamiseksi |
| US5177080A (en) | 1990-12-14 | 1993-01-05 | Bayer Aktiengesellschaft | Substituted pyridyl-dihydroxy-heptenoic acid and its salts |
| JP2648897B2 (ja) | 1991-07-01 | 1997-09-03 | 塩野義製薬株式会社 | ピリミジン誘導体 |
| US5595872A (en) | 1992-03-06 | 1997-01-21 | Bristol-Myers Squibb Company | Nucleic acids encoding microsomal trigyceride transfer protein |
| US5470845A (en) | 1992-10-28 | 1995-11-28 | Bristol-Myers Squibb Company | Methods of using α-phosphonosulfonate squalene synthetase inhibitors including the treatment of atherosclerosis and hypercholesterolemia |
| US5594016A (en) | 1992-12-28 | 1997-01-14 | Mitsubishi Chemical Corporation | Naphthalene derivatives |
| ES2133158T3 (es) | 1993-01-19 | 1999-09-01 | Warner Lambert Co | Formulacion ci-981 oral, estable y proceso de preparacion del mismo. |
| US5340583A (en) | 1993-05-06 | 1994-08-23 | Allergan, Inc. | Antimicrobial lenses and lens care systems |
| US5739135A (en) | 1993-09-03 | 1998-04-14 | Bristol-Myers Squibb Company | Inhibitors of microsomal triglyceride transfer protein and method |
| US5776983A (en) | 1993-12-21 | 1998-07-07 | Bristol-Myers Squibb Company | Catecholamine surrogates useful as β3 agonists |
| US5488064A (en) | 1994-05-02 | 1996-01-30 | Bristol-Myers Squibb Company | Benzo 1,3 dioxole derivatives |
| US5385929A (en) | 1994-05-04 | 1995-01-31 | Warner-Lambert Company | [(Hydroxyphenylamino) carbonyl] pyrroles |
| US5612359A (en) | 1994-08-26 | 1997-03-18 | Bristol-Myers Squibb Company | Substituted biphenyl isoxazole sulfonamides |
| US5491134A (en) | 1994-09-16 | 1996-02-13 | Bristol-Myers Squibb Company | Sulfonic, phosphonic or phosphiniic acid β3 agonist derivatives |
| US5541204A (en) | 1994-12-02 | 1996-07-30 | Bristol-Myers Squibb Company | Aryloxypropanolamine β 3 adrenergic agonists |
| US5620997A (en) | 1995-05-31 | 1997-04-15 | Warner-Lambert Company | Isothiazolones |
| WO1997012613A1 (en) | 1995-10-05 | 1997-04-10 | Warner-Lambert Company | Method for treating and preventing inflammation and atherosclerosis |
| AU717743B2 (en) | 1995-12-13 | 2000-03-30 | Regents Of The University Of California, The | Nuclear receptor ligands and ligand binding domains |
| US5770615A (en) | 1996-04-04 | 1998-06-23 | Bristol-Myers Squibb Company | Catecholamine surrogates useful as β3 agonists |
| US5962440A (en) | 1996-05-09 | 1999-10-05 | Bristol-Myers Squibb Company | Cyclic phosphonate ester inhibitors of microsomal triglyceride transfer protein and method |
| US5885983A (en) | 1996-05-10 | 1999-03-23 | Bristol-Myers Squibb Company | Inhibitors of microsomal triglyceride transfer protein and method |
| US5827875A (en) | 1996-05-10 | 1998-10-27 | Bristol-Myers Squibb Company | Inhibitors of microsomal triglyceride transfer protein and method |
| US5760246A (en) | 1996-12-17 | 1998-06-02 | Biller; Scott A. | Conformationally restricted aromatic inhibitors of microsomal triglyceride transfer protein and method |
| TW536540B (en) | 1997-01-30 | 2003-06-11 | Bristol Myers Squibb Co | Endothelin antagonists: N-[[2'-[[(4,5-dimethyl-3-isoxazolyl)amino]sulfonyl]-4-(2-oxazolyl)[1,1'-biphenyl]-2-yl]methyl]-N,3,3-trimethylbutanamide and N-(4,5-dimethyl-3-isoxazolyl)-2'-[(3,3-dimethyl-2-oxo-1-pyrrolidinyl)methyl]-4'-(2-oxazolyl)[1,1'-biphe |
| GB9713739D0 (en) | 1997-06-27 | 1997-09-03 | Karobio Ab | Thyroid receptor ligands |
| AU766219B2 (en) | 1998-02-02 | 2003-10-09 | 1149336 Ontario Inc. | Method of regulating glucose metabolism, and reagents related thereto |
| AU3034299A (en) | 1998-03-09 | 1999-09-27 | Fondatech Benelux N.V. | Serine peptidase modulators |
| GB9807354D0 (en) * | 1998-04-07 | 1998-06-03 | Glaxo Group Ltd | Antiviral compound |
| DE19823831A1 (de) | 1998-05-28 | 1999-12-02 | Probiodrug Ges Fuer Arzneim | Neue pharmazeutische Verwendung von Isoleucyl Thiazolidid und seinen Salzen |
| DE19828113A1 (de) | 1998-06-24 | 2000-01-05 | Probiodrug Ges Fuer Arzneim | Prodrugs von Inhibitoren der Dipeptidyl Peptidase IV |
| DE19828114A1 (de) | 1998-06-24 | 2000-01-27 | Probiodrug Ges Fuer Arzneim | Produgs instabiler Inhibitoren der Dipeptidyl Peptidase IV |
| WO2000001389A1 (en) | 1998-07-06 | 2000-01-13 | Bristol-Myers Squibb Co. | Biphenyl sulfonamides as dual angiotensin endothelin receptor antagonists |
| US6069238A (en) | 1998-09-30 | 2000-05-30 | Eli Lilly And Company | Spirocyclic C-glycosides |
| GB9828442D0 (en) | 1998-12-24 | 1999-02-17 | Karobio Ab | Novel thyroid receptor ligands and method II |
| US6414002B1 (en) | 1999-09-22 | 2002-07-02 | Bristol-Myers Squibb Company | Substituted acid derivatives useful as antidiabetic and antiobesity agents and method |
| TWI302149B (en) | 1999-09-22 | 2008-10-21 | Bristol Myers Squibb Co | Substituted acid derivatives useful as antiodiabetic and antiobesity agents and method |
| US6515117B2 (en) * | 1999-10-12 | 2003-02-04 | Bristol-Myers Squibb Company | C-aryl glucoside SGLT2 inhibitors and method |
| PH12000002657B1 (en) | 1999-10-12 | 2006-02-21 | Bristol Myers Squibb Co | C-aryl glucoside SGLT2 inhibitors |
| US6395767B2 (en) | 2000-03-10 | 2002-05-28 | Bristol-Myers Squibb Company | Cyclopropyl-fused pyrrolidine-based inhibitors of dipeptidyl peptidase IV and method |
| US6683056B2 (en) | 2000-03-30 | 2004-01-27 | Bristol-Myers Squibb Company | O-aryl glucoside SGLT2 inhibitors and method |
| KR20020014570A (ko) * | 2000-08-18 | 2002-02-25 | 김충섭 | 고체분산화시킨 무정형 이프리플라본의 제조방법 |
| US6936590B2 (en) | 2001-03-13 | 2005-08-30 | Bristol Myers Squibb Company | C-aryl glucoside SGLT2 inhibitors and method |
| WO2002083066A2 (en) | 2001-04-11 | 2002-10-24 | Bristol-Myers Squibb Company | Amino acid complexes of c-aryl glucosides for treatment of diabetes and method |
| DK1390377T3 (da) * | 2001-05-22 | 2006-06-19 | Pfizer Prod Inc | Ny krystalform af azithromycin |
| CA2463908A1 (en) | 2001-10-18 | 2003-04-24 | Bristol-Myers Squibb Company | Human glucagon-like-peptide-1 mimics and their use in the treatment of diabetes and related conditions |
| WO2004061433A1 (en) * | 2002-12-30 | 2004-07-22 | Transform Pharmaceuticals, Inc. | Pharmaceutical compositions with improved dissolution |
| WO2004060347A2 (en) † | 2002-09-03 | 2004-07-22 | Transform Pharmaceuticals, Inc. | Pharmaceutical propylene glycol solvate compositions |
| US7790905B2 (en) * | 2002-02-15 | 2010-09-07 | Mcneil-Ppc, Inc. | Pharmaceutical propylene glycol solvate compositions |
| EP1511490A4 (en) * | 2002-05-31 | 2009-03-11 | Transform Pharmaceuticals Inc | NOVEL CONAZOLE CRYSTALLINE FORMS AND RELATED METHODS, PHARMACEUTICAL COMPOSITIONS AND METHODS |
| BR0317929A (pt) | 2003-01-03 | 2006-04-11 | Bristol Myers Squibb Co | métodos de produzir inibidores de sglt2 de glicosìdeo de c-arila |
| EP1597266A4 (en) | 2003-02-27 | 2008-02-20 | Bristol Myers Squibb Co | NON-CRYOGENIC PROCESS FOR THE PRODUCTION OF GLYCOSIDES |
| ES2567571T3 (es) * | 2003-03-14 | 2016-04-25 | Astellas Pharma Inc. | Derivados de C-glucósido y sales de los mismos |
| EP1595880A1 (en) * | 2004-05-13 | 2005-11-16 | Speedel Pharma AG | Crystalline forms of a pyridinyl-sulfonamide and their use as endothelin receptor antagonists |
| AU2005252110B2 (en) * | 2004-06-11 | 2008-09-04 | Shionogi & Co., Ltd. | 5-amino-2,4,7-trioxo-3,4,7,8-tetrahydro-2H-pyrido[2,3-D] pyrimidine derivatives and related compounds for the treatment of cancer |
| AR051446A1 (es) * | 2004-09-23 | 2007-01-17 | Bristol Myers Squibb Co | Glucosidos de c-arilo como inhibidores selectivos de transportadores de glucosa (sglt2) |
| US7919598B2 (en) * | 2006-06-28 | 2011-04-05 | Bristol-Myers Squibb Company | Crystal structures of SGLT2 inhibitors and processes for preparing same |
| CN104829572B (zh) | 2014-02-10 | 2019-01-04 | 江苏豪森药业集团有限公司 | 达格列净新晶型及其制备方法 |
-
2007
- 2007-06-20 US US11/765,481 patent/US7919598B2/en active Active
- 2007-06-21 MY MYPI20085336A patent/MY148566A/en unknown
- 2007-06-21 NZ NZ589202A patent/NZ589202A/en unknown
- 2007-06-21 HR HRP20141007TT patent/HRP20141007T4/hr unknown
- 2007-06-21 EP EP12152907A patent/EP2457918A3/en not_active Withdrawn
- 2007-06-21 EA EA200900066A patent/EA018229B1/ru not_active IP Right Cessation
- 2007-06-21 SG SG10201402181SA patent/SG10201402181SA/en unknown
- 2007-06-21 NZ NZ589195A patent/NZ589195A/en unknown
- 2007-06-21 RS RS20140570A patent/RS53638B2/sr unknown
- 2007-06-21 EP EP17203302.9A patent/EP3363807B1/en active Active
- 2007-06-21 BR BR122017021516A patent/BR122017021516B8/pt active IP Right Grant
- 2007-06-21 SG SG2011047727A patent/SG172741A1/en unknown
- 2007-06-21 UA UAA200900606A patent/UA96765C2/uk unknown
- 2007-06-21 CN CN200780024135XA patent/CN101479287B/zh active Active
- 2007-06-21 PT PT77844991T patent/PT2069374E/pt unknown
- 2007-06-21 PL PL07784499T patent/PL2069374T5/pl unknown
- 2007-06-21 CA CA2924318A patent/CA2924318C/en active Active
- 2007-06-21 ES ES17203302T patent/ES2769130T3/es active Active
- 2007-06-21 NO NO20085169A patent/NO346828B1/no unknown
- 2007-06-21 DK DK07784499.1T patent/DK2069374T4/da active
- 2007-06-21 JP JP2009518468A patent/JP5313889B2/ja active Active
- 2007-06-21 ES ES07784499T patent/ES2521665T5/es active Active
- 2007-06-21 MX MX2011009646A patent/MX339143B/es unknown
- 2007-06-21 CN CN201310052369.2A patent/CN103145773B/zh active Active
- 2007-06-21 EA EA201791254A patent/EA035999B1/ru not_active IP Right Cessation
- 2007-06-21 BR BR122017015106A patent/BR122017015106B8/pt active IP Right Grant
- 2007-06-21 EP EP15181545.3A patent/EP3045466B2/en active Active
- 2007-06-21 ES ES15181545T patent/ES2659862T5/es active Active
- 2007-06-21 EP EP07784499.1A patent/EP2069374B2/en active Active
- 2007-06-21 MX MX2016006205A patent/MX367155B/es unknown
- 2007-06-21 BR BRPI0713544A patent/BRPI0713544B8/pt active IP Right Grant
- 2007-06-21 NZ NZ574346A patent/NZ574346A/en unknown
- 2007-06-21 EA EA201490902A patent/EA028259B1/ru not_active IP Right Cessation
- 2007-06-21 CA CA2985797A patent/CA2985797A1/en not_active Abandoned
- 2007-06-21 KR KR1020087031643A patent/KR101493102B1/ko not_active Ceased
- 2007-06-21 AU AU2007265246A patent/AU2007265246B2/en active Active
- 2007-06-21 MY MYPI2014001983A patent/MY173930A/en unknown
- 2007-06-21 MX MX2008015377A patent/MX2008015377A/es active IP Right Grant
- 2007-06-21 CA CA2653344A patent/CA2653344C/en active Active
- 2007-06-21 NZ NZ589190A patent/NZ589190A/en unknown
- 2007-06-21 EA EA201171333A patent/EA020428B1/ru not_active IP Right Cessation
- 2007-06-21 SI SI200731535T patent/SI2069374T2/sl unknown
- 2007-06-21 WO PCT/US2007/071749 patent/WO2008002824A1/en not_active Ceased
- 2007-06-28 TW TW102137967A patent/TWI466876B/zh not_active IP Right Cessation
- 2007-06-28 TW TW103140880A patent/TWI519528B/zh not_active IP Right Cessation
- 2007-06-28 TW TW104129264A patent/TW201546054A/zh unknown
- 2007-06-28 TW TW096123519A patent/TWI421245B/zh not_active IP Right Cessation
- 2007-06-28 CL CL2007001915A patent/CL2007001915A1/es unknown
- 2007-06-28 AR ARP070102896A patent/AR061730A1/es not_active Application Discontinuation
- 2007-07-02 PE PE2011001791A patent/PE20120776A1/es not_active Application Discontinuation
- 2007-07-02 PE PE2007000845A patent/PE20080349A1/es not_active Application Discontinuation
-
2008
- 2008-11-10 ZA ZA2008/10475A patent/ZA200810475B/en unknown
- 2008-12-11 IL IL195882A patent/IL195882A/en active IP Right Grant
- 2008-12-24 CO CO08136743A patent/CO6160299A2/es unknown
-
2011
- 2011-03-16 US US13/049,712 patent/US8501698B2/en active Active
- 2011-07-19 IL IL214180A patent/IL214180A/en active IP Right Grant
- 2011-07-19 IL IL214182A patent/IL214182A/en active IP Right Grant
- 2011-07-19 IL IL214181A patent/IL214181A/en active IP Right Grant
-
2012
- 2012-01-26 PH PH12012500168A patent/PH12012500168B1/en unknown
-
2013
- 2013-05-14 JP JP2013102220A patent/JP5666651B2/ja active Active
- 2013-07-10 US US13/938,763 patent/US9453039B2/en active Active
-
2014
- 2014-10-29 CY CY20141100887T patent/CY1115738T1/el unknown
- 2014-12-10 JP JP2014250141A patent/JP5937187B2/ja active Active
-
2016
- 2016-05-11 JP JP2016095472A patent/JP2016172758A/ja active Pending
- 2016-05-17 IL IL245688A patent/IL245688A0/en unknown
-
2017
- 2017-07-07 JP JP2017133952A patent/JP2017222681A/ja active Pending
-
2018
- 2018-12-18 JP JP2018236514A patent/JP2019059779A/ja active Pending
-
2022
- 2022-11-17 NO NO20221233A patent/NO347770B1/no unknown
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2769130T3 (es) | Composición farmacéutica que comprende un solvato de (S)-propilenglicol de (2S,3R,4S,5S,6R)-2-[4-cloro-3-(4-etoxi-bencil)-fenil]-6-hidroximetil-2-metoxi-tetrahidro-piran-3,4,5-triol cristalino. | |
| CN101687793B (zh) | 沙格列汀的晶形及其制备方法 | |
| US20080287529A1 (en) | Crystal structures of sglt2 inhibitors and processes for preparing same | |
| HK1260346B (en) | Pharmaceutical composition comprising crystalline (2s,3r,4s,5s,6r)-2-[4-chloro-3-(4-ethoxy-benzyl)-phenyl]-6-hydroxymethyl-2-methoxy-tetrahydro-pyran-3,4,5-triol (s)-propylene glycol solvate | |
| HK1260346A1 (en) | Pharmaceutical composition comprising crystalline (2s,3r,4s,5s,6r)-2-[4-chloro-3-(4-ethoxy-benzyl)-phenyl]-6-hydroxymethyl-2-methoxy-tetrahydro-pyran-3,4,5-triol (s)-propylene glycol solvate | |
| HK1227878B (en) | (2s,3r,4s,5s,6r)-2-[4-chloro-3-(4-ethoxy-benzyl)-phenyl]-6-hydroxymethyl-2-methoxy-tetrahydro-pyran-3,4,5-triol propylene glycol solvate as sgt2 inhibitor for the treatment of diabetes | |
| HK1127359B (en) | Crystalline solvates of (1s)-1,5-anhydro-1-c-(3-((phenyl) methyl) phenyl)-d-glucitol derivatives with alcohols as sglt2 inhibitors for the treatment of diabetes |