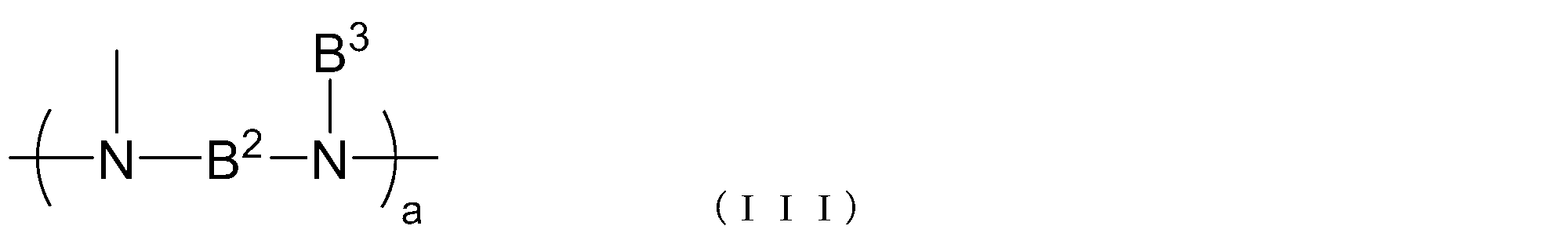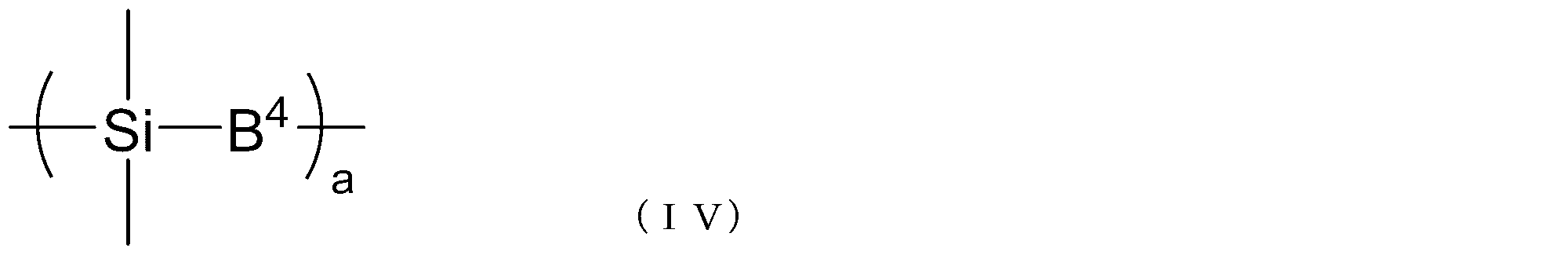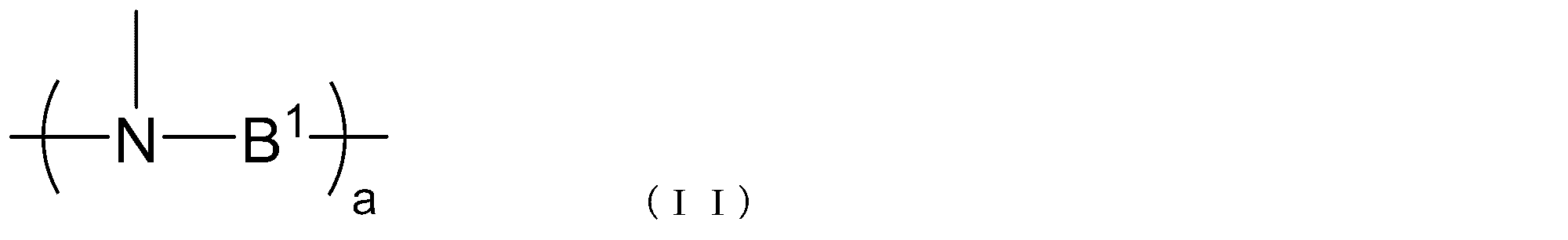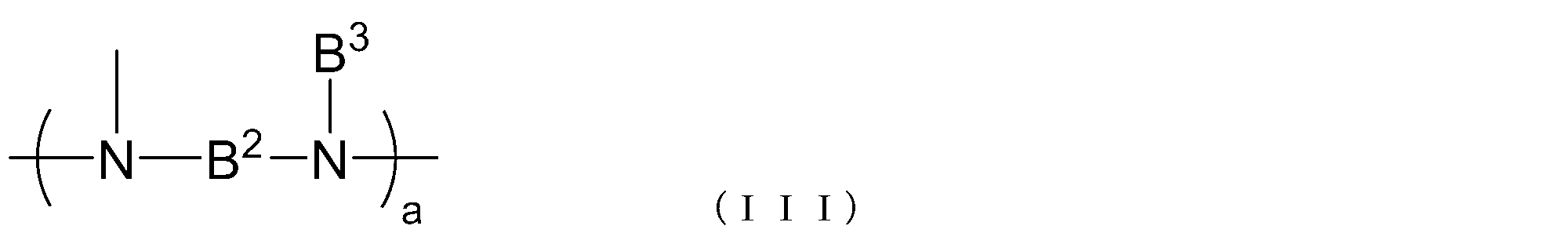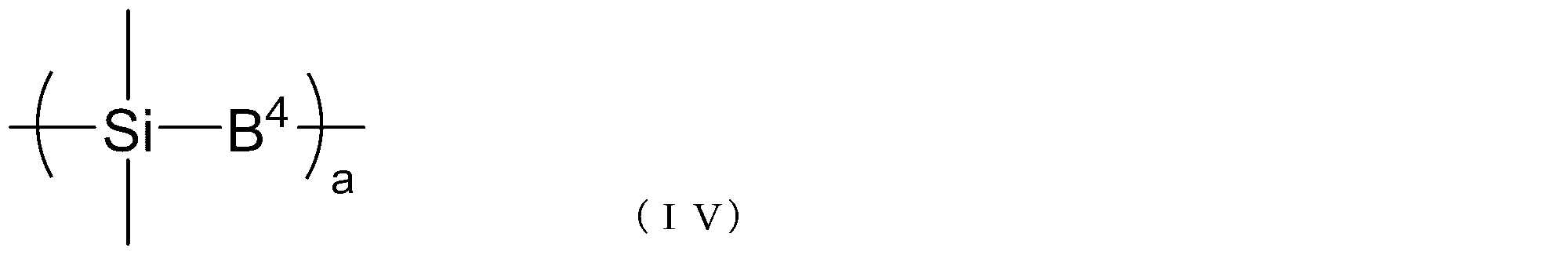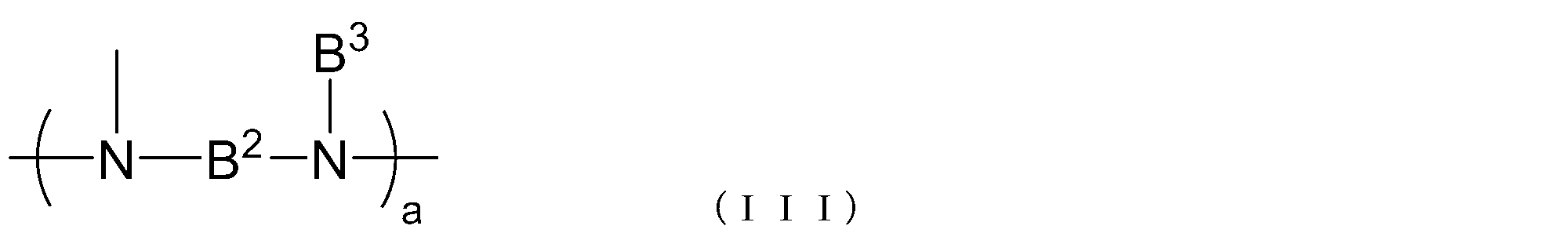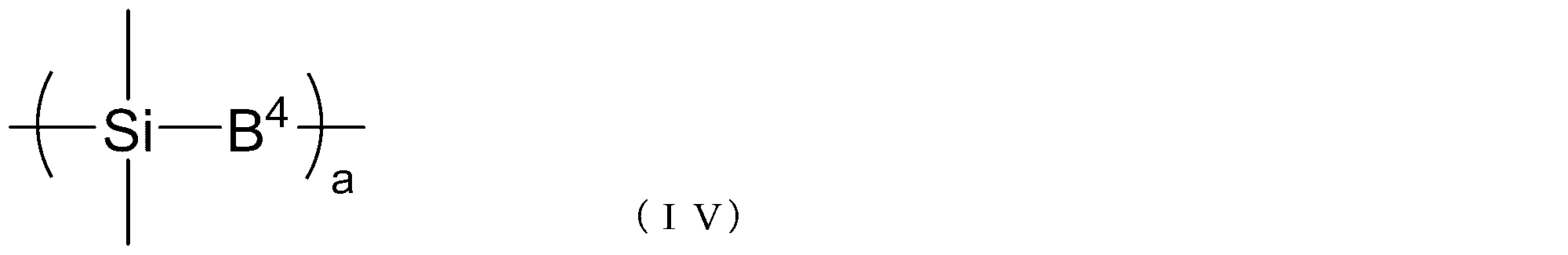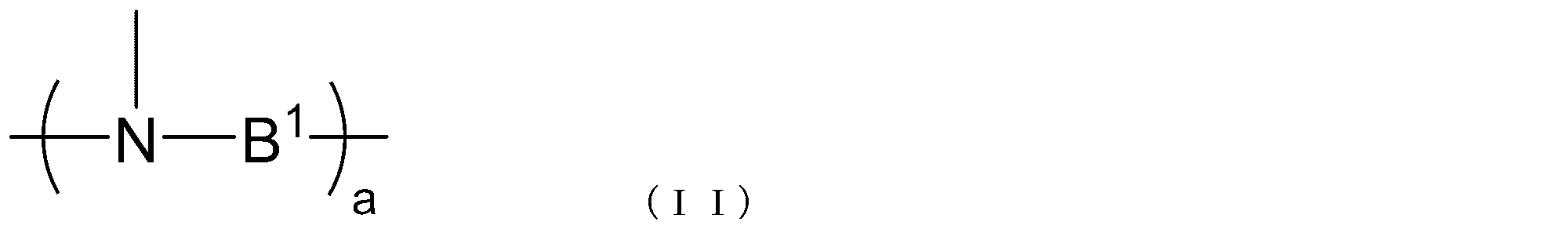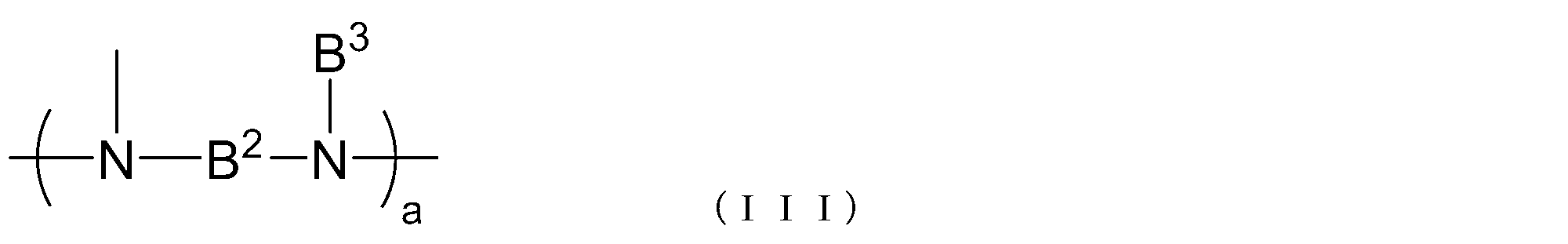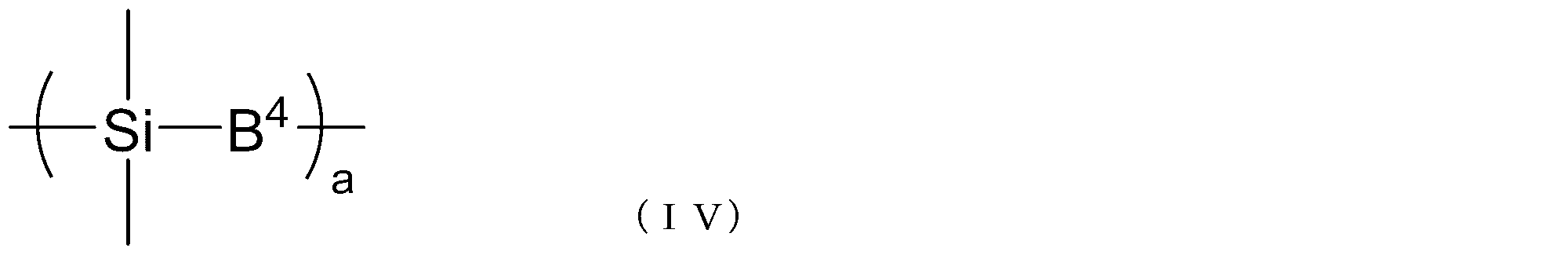WO2016133154A1 - 変性共役ジエン系重合体及びその製造方法、ゴム組成物、並びにタイヤ - Google Patents
変性共役ジエン系重合体及びその製造方法、ゴム組成物、並びにタイヤ Download PDFInfo
- Publication number
- WO2016133154A1 WO2016133154A1 PCT/JP2016/054687 JP2016054687W WO2016133154A1 WO 2016133154 A1 WO2016133154 A1 WO 2016133154A1 JP 2016054687 W JP2016054687 W JP 2016054687W WO 2016133154 A1 WO2016133154 A1 WO 2016133154A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- conjugated diene
- diene polymer
- modified conjugated
- integer
- formula
- Prior art date
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08C—TREATMENT OR CHEMICAL MODIFICATION OF RUBBERS
- C08C19/00—Chemical modification of rubber
- C08C19/22—Incorporating nitrogen atoms into the molecule
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08C—TREATMENT OR CHEMICAL MODIFICATION OF RUBBERS
- C08C19/00—Chemical modification of rubber
- C08C19/25—Incorporating silicon atoms into the molecule
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F8/00—Chemical modification by after-treatment
- C08F8/30—Introducing nitrogen atoms or nitrogen-containing groups
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B60—VEHICLES IN GENERAL
- B60C—VEHICLE TYRES; TYRE INFLATION; TYRE CHANGING; CONNECTING VALVES TO INFLATABLE ELASTIC BODIES IN GENERAL; DEVICES OR ARRANGEMENTS RELATED TO TYRES
- B60C1/00—Tyres characterised by the chemical composition or the physical arrangement or mixture of the composition
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B60—VEHICLES IN GENERAL
- B60C—VEHICLE TYRES; TYRE INFLATION; TYRE CHANGING; CONNECTING VALVES TO INFLATABLE ELASTIC BODIES IN GENERAL; DEVICES OR ARRANGEMENTS RELATED TO TYRES
- B60C1/00—Tyres characterised by the chemical composition or the physical arrangement or mixture of the composition
- B60C1/0016—Compositions of the tread
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08C—TREATMENT OR CHEMICAL MODIFICATION OF RUBBERS
- C08C19/00—Chemical modification of rubber
- C08C19/30—Addition of a reagent which reacts with a hetero atom or a group containing hetero atoms of the macromolecule
- C08C19/42—Addition of a reagent which reacts with a hetero atom or a group containing hetero atoms of the macromolecule reacting with metals or metal-containing groups
- C08C19/44—Addition of a reagent which reacts with a hetero atom or a group containing hetero atoms of the macromolecule reacting with metals or metal-containing groups of polymers containing metal atoms exclusively at one or both ends of the skeleton
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F2/00—Processes of polymerisation
- C08F2/38—Polymerisation using regulators, e.g. chain terminating agents, e.g. telomerisation
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F36/00—Homopolymers and copolymers of compounds having one or more unsaturated aliphatic radicals, at least one having two or more carbon-to-carbon double bonds
- C08F36/02—Homopolymers and copolymers of compounds having one or more unsaturated aliphatic radicals, at least one having two or more carbon-to-carbon double bonds the radical having only two carbon-to-carbon double bonds
- C08F36/04—Homopolymers and copolymers of compounds having one or more unsaturated aliphatic radicals, at least one having two or more carbon-to-carbon double bonds the radical having only two carbon-to-carbon double bonds conjugated
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K3/00—Use of inorganic substances as compounding ingredients
- C08K3/01—Use of inorganic substances as compounding ingredients characterized by their specific function
- C08K3/013—Fillers, pigments or reinforcing additives
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08L—COMPOSITIONS OF MACROMOLECULAR COMPOUNDS
- C08L15/00—Compositions of rubber derivatives
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08L—COMPOSITIONS OF MACROMOLECULAR COMPOUNDS
- C08L47/00—Compositions of homopolymers or copolymers of compounds having one or more unsaturated aliphatic radicals, at least one having two or more carbon-to-carbon double bonds; Compositions of derivatives of such polymers
Definitions
- the present invention relates to a modified conjugated diene polymer, a production method thereof, a rubber composition, and a tire.
- a material containing rubber and a reinforcing filler such as carbon black and silica.
- a material containing silica when used, it is possible to improve the balance between low hysteresis loss and wet skid resistance.
- a functional group having affinity or reactivity with silica into the molecular end of a rubber having high mobility, the dispersibility of silica in the material is improved, and further, Attempts have been made to reduce the hysteresis loss by reducing the mobility of the rubber molecule end by bonding.
- Patent Document 1 proposes a modified diene rubber obtained by reacting a modifier having a glycidylamino group with a polymer active terminal.
- Patent Documents 2 to 4 propose a modified diene rubber obtained by reacting an alkoxysilane containing an amino group with the active terminal of a polymer, and a composition of these with silica.
- Patent Documents 5 and 6 propose polymers in which a cyclic azasilacycle compound is reacted with a polymer active terminal to functionalize the polymer.
- Patent Document 7 proposes a diene rubber obtained by a coupling reaction between a polymer active terminal and a polyfunctional silane compound.
- the silica-containing material has a hydrophilic surface with respect to carbon black having a hydrophobic surface, and has a low affinity with the conjugated diene rubber, compared to carbon black, It has the disadvantage of poor dispersibility. Therefore, the material containing silica needs to contain a silane coupling agent or the like separately in order to impart a bond between silica and rubber and improve dispersibility. In addition, a material in which a functional group having high reactivity with silica is introduced at the molecular terminal of the rubber is kneaded because the reaction with the silica particles proceeds during the kneading process and the viscosity of the composition increases.
- the present invention is excellent in workability when used as a vulcanized product, excellent in balance between low hysteresis loss property and wet skid resistance and used in vulcanized product, and wear resistance, and has practically sufficient fracture characteristics.
- An object of the present invention is to provide a modified conjugated diene polymer having:
- a modified conjugated diene polymer having a weight average molecular weight within a predetermined range the modified conjugated diene having a molecular weight within a predetermined range.
- the modified conjugated diene polymer which contains a predetermined amount of a polymer and the shrinkage factor (g ′) is less than a predetermined value, is excellent in processability when used as a vulcanizate and low when used as a vulcanizate. It has been found that it has excellent balance between hysteresis loss and wet skid resistance and wear resistance, and has practically sufficient fracture characteristics, and has completed the present invention.
- a modified conjugated diene polymer having a weight average molecular weight of 20 ⁇ 10 4 or more and 300 ⁇ 10 4 or less The modified conjugated diene polymer having a molecular weight of 200 ⁇ 10 4 or more and 500 ⁇ 10 4 or less with respect to the total amount of the modified conjugated diene polymer is contained in an amount of 0.25% by mass to 30% by mass, A modified conjugated diene polymer having a shrinkage factor (g ′) of less than 0.64.
- the modified conjugated diene polymer according to [1] which has a nitrogen atom and a silicon atom.
- [3] The modified conjugated diene polymer according to [1] or [2], wherein the weight average molecular weight is 50 ⁇ 10 4 or more and 150 ⁇ 10 4 or less.
- [4] [1] The modified conjugated diene polymer having a molecular weight of 200 ⁇ 10 4 or more and 500 ⁇ 10 4 or less with respect to the total amount of the modified conjugated diene polymer is 1.0% by mass or more and 30% by mass or less. ]
- [5] Has a branch, The modified conjugated diene polymer according to any one of [1] to [4], wherein the degree of branching is 5 or more.
- D 1 represents a diene polymer chain
- R 1 to R 3 each independently represents a single bond or an alkylene group having 1 to 20 carbon atoms
- R 4 and R 7 are Each independently represents an alkyl group having 1 to 20 carbon atoms
- R 5 , R 8 and R 9 each independently represents a hydrogen atom or an alkyl group having 1 to 20 carbon atoms
- R 6 and R 10 Each independently represents an alkylene group having 1 to 20 carbon atoms
- R 11 represents a hydrogen atom or an alkyl group having 1 to 20 carbon atoms
- m and x each independently represents an integer of 1 to 3;
- D 1, R 1 ⁇ R 11 , m in the case of, p, x, y, and z are each independent and different even with the same I represents an integer of 0 to 6
- j represents an integer of 0 to 6
- k represents an integer of 0 to 6
- (i + j + k) represents an integer of 3 to 10
- ((X ⁇ i) + (y ⁇ j) + (z ⁇ k)) is an integer of 5 to 30.
- A is a hydrocarbon group having 1 to 20 carbon atoms, or an oxygen atom, a nitrogen atom,
- A is a modified conjugated diene polymer according to [10], which is represented by any one of the following general formulas (II) to (V).
- B 1 represents a single bond or a hydrocarbon group having 1 to 20 carbon atoms, and a represents an integer of 1 to 10.
- each B 1 independently represents Yes.
- B 2 represents a single bond or a hydrocarbon group having 1 to 20 carbon atoms
- B 3 represents an alkyl group having 1 to 20 carbon atoms
- a represents an integer of 1 to 10
- B 4 represents a single bond or a hydrocarbon group having 1 to 20 carbon atoms
- a represents an integer of 1 to 10.
- each B 4 independently represents Yes.
- B 5 represents a single bond or a hydrocarbon group having a carbon number of 1 ⁇ 20
- a is the B 5 in the case of. Plurality of an integer of 1 to 10, each independently Yes.
- R 12 to R 14 each independently represents a single bond or an alkylene group having 1 to 20 carbon atoms, and R 15 to R 18 and R 20 each independently represents 1 carbon atom
- R 19 and R 22 each independently represent an alkylene group having 1 to 20 carbon atoms
- R 21 represents an alkyl group or trialkylsilyl group having 1 to 20 carbon atoms
- m represents an integer of 1 to 3
- p represents 1 or 2.
- R 12 to R 22 , m, and p when there are a plurality of each are independent and may be the same or different I is an integer from 0 to 6, j is an integer from 0 to 6, k is an integer from 0 to 6, and (i + j + k) is an integer from 3 to 10.
- A is a hydrocarbon group having 1 to 20 carbon atoms, or an oxygen atom, nitrogen atom, silicon atom, sulfur atom And at least one atom selected from the group consisting of a phosphorus atom, an organic group having no active hydrogen.
- A is a method for producing a modified conjugated diene polymer according to [12], which is represented by any one of the following general formulas (II) to (V).
- B 1 represents a single bond or a hydrocarbon group having 1 to 20 carbon atoms, and a represents an integer of 1 to 10.
- each B 4 independently represents Yes.
- B 5 represents a single bond or a hydrocarbon group having a carbon number of 1 ⁇ 20
- a is the B 5 in the case of.
- A is represented by Formula (II) or Formula (III), k shows 0, The manufacturing method of the modified conjugated diene type polymer as described in [13].
- A is represented by formula (II) or formula (III), k represents 0, The process for producing a modified conjugated diene polymer according to [13] or [14], wherein in formula (II) or formula (III), a represents an integer of 2 to 10.
- a represents an integer of 2 to 10.
- a rubber component and 5.0 parts by weight or more and 150 parts by weight of a filler with respect to 100 parts by weight of the rubber component, The rubber composition, wherein the rubber component contains 10% by mass or more of the modified conjugated diene polymer according to any one of [1] to [11] with respect to the total amount of the rubber component.
- a tire comprising the rubber composition according to [18].
- the modified conjugated diene polymer according to the present invention there is a balance between excellent processability when used as a vulcanized product, and excellent low hysteresis loss and wet skid resistance when used as a vulcanized product. Wearability and practically sufficient fracture characteristics can be obtained.
- the present embodiment a mode for carrying out the present invention (hereinafter referred to as “the present embodiment”) will be described in detail.
- the following embodiments are examples for explaining the present invention, and are not intended to limit the present invention to the following contents.
- the present invention can be implemented with appropriate modifications within the scope of the gist thereof.
- the modified conjugated diene polymer of the present embodiment has a weight average molecular weight of 20 ⁇ 10 4 or more and 300 ⁇ 10 4 or less, and a molecular weight of 200 ⁇ with respect to the total amount (100% by mass) of the modified conjugated diene polymer. It comprises 10 4 to 500 ⁇ 10 4 or less is a modified conjugated diene-based polymer 0.25 mass% to 30 mass%, shrinkage factor (g ') is less than 0.64.
- a polymer having a branch tends to have a smaller molecular size when compared with a linear polymer having the same absolute molecular weight.
- the contraction factor (g ′) of the present embodiment is an index of the ratio of the size occupied by the molecule to the linear polymer having the same absolute molecular weight. That is, as the degree of branching of the polymer increases, the shrinkage factor (g ′) tends to decrease.
- intrinsic viscosity is used as an index of molecular size
- the shrinkage factor (g ′) at each absolute molecular weight of the modified conjugated diene polymer was calculated, and the average value of the shrinkage factor (g ′) when the absolute molecular weight was 100 ⁇ 10 4 to 200 ⁇ 10 4 was calculated as The shrinkage factor (g ′) of the modified conjugated diene polymer is used.
- the “branch” is formed by bonding one polymer directly or indirectly with another polymer.
- the “degree of branching” is the number of polymers that are directly or indirectly bonded to one branch. For example, when five conjugated diene polymer chains described later are bonded to each other indirectly via a coupling agent residue described later, the degree of branching is 5.
- the contraction factor (g ′) is less than 0.64, preferably 0.63 or less, more preferably 0.60 or less, still more preferably 0.59 or less, and even more preferably 0.8. 57 or less.
- the lower limit of the contraction factor (g ′) is not particularly limited, and may be the detection limit value or less, but is preferably 0.30 or more, more preferably 0.33 or more, and further preferably 0. .35 or more, more preferably 0.45 or more.
- a modified conjugated diene polymer having a shrinkage factor (g ′) within this range tends to be excellent in processability when used as a vulcanized product.
- the contraction factor (g ′) tends to depend on the degree of branching, for example, the contraction factor (g ′) can be controlled using the degree of branching as an index. Specifically, when a modified conjugated diene polymer having a branching degree of 6 is used, the shrinkage factor (g ′) tends to be 0.59 or more and 0.63 or less. In the case of a modified conjugated diene-based polymer in which is 8, the shrinkage factor (g ′) tends to be 0.45 or more and 0.59 or less.
- the contraction factor (g ′) is measured by the method described in Examples described later.
- the conjugated diene polymer chain of this embodiment is a constituent unit of a modified conjugated diene polymer, and is produced, for example, by reacting a conjugated diene polymer and a coupling agent described later. It is a structural unit derived from.
- the conjugated diene polymer chain of the present embodiment is preferably bonded to one coupling residue described later.
- the coupling residue of this embodiment is a structural unit of a modified conjugated diene polymer bonded to a conjugated diene polymer chain. For example, a conjugated diene polymer and a coupling agent described below are reacted. This is a structural unit derived from a coupling agent.
- the modified conjugated diene polymer of the present embodiment preferably has a branch and the degree of branching is 5 or more.
- the modified conjugated diene polymer has one or more coupling residues and a conjugated diene polymer chain bonded to the coupling residue, and the branch is one of the cups. More preferably, it contains a branch having 5 or more conjugated diene polymer chains bonded to the ring residue.
- the structure of the modified conjugated diene polymer so that the degree of branching is 5 or more, and the branch includes a branch in which 5 or more conjugated diene polymer chains are bonded to one coupling residue.
- the contraction factor (g ′) can be made less than 0.64 more reliably.
- the modified conjugated diene polymer of the present embodiment has a branch and the degree of branching is 6 or more.
- the modified conjugated diene polymer has one or more coupling residues and a conjugated diene polymer chain bonded to the coupling residue, and the branch is one of the cups. More preferably, it contains a branch having 6 or more conjugated diene polymer chains bonded to the ring residue.
- the structure of the modified conjugated diene polymer so that the degree of branching is 6 or more, and the branch includes a branch in which 6 or more conjugated diene polymer chains are bonded to one coupling residue.
- the contraction factor (g ′) can be reduced to 0.63 or less.
- the modified conjugated diene polymer of the present embodiment has a branch, the branching degree is more preferably 7 or more, and the branching degree is more preferably 8 or more.
- the upper limit of the degree of branching is not particularly limited, but is preferably 18 or less.
- the modified conjugated diene polymer has one or more coupling residues and a conjugated diene polymer chain bonded to the coupling residue, and the branch is one of the cups. More preferably, it contains a branch in which 7 or more of the conjugated diene polymer chain is bonded to the ring residue, and 8 or more of the conjugated diene polymer chain to 1 of the coupling residue. Even more preferably, it comprises a branch to which are attached.
- the number of conjugated diene polymer chains bonded to one coupling residue can be confirmed from the contraction factor (g ′), the degree of branching is 8 or more, and By specifying the structure of the modified conjugated diene polymer so that it contains a branch in which 8 or more conjugated diene polymer chains are bonded to one coupling residue, a shrinkage factor (g ′) Can be made 0.59 or less.
- the modified conjugated diene polymer of this embodiment preferably has a nitrogen atom and a silicon atom.
- the effect of the present embodiment which is excellent in workability when making a vulcanized product, tends to be more excellent in the balance between low hysteresis loss and wet skid resistance and abrasion resistance when used as a vulcanized product. is there.
- the modified conjugated diene polymer has a nitrogen atom can be confirmed by the presence or absence of adsorption to a specific column by the method described in the Examples described later. Moreover, it can confirm by a metal analysis by the method of the Example description mentioned later that a modified
- the modified conjugated diene polymer preferably has a silicon atom, and at least one silicon atom of the modified conjugated diene polymer may constitute an alkoxysilyl group or silanol group having 1 to 20 carbon atoms. More preferred. Thereby, there exists a tendency for the effect of this embodiment to become more remarkable. Further, from the viewpoint that hydrogen halide can be generated by reacting with air, the modified conjugated diene polymer preferably does not contain halogen.
- the terminal of the five or more conjugated diene polymer chains is bonded to a silicon atom of each coupling residue.
- the terminal of the some conjugated diene polymer chain may be bonded to one silicon atom.
- the terminal of the conjugated diene polymer chain and the alkoxy group or hydroxyl group having 1 to 20 carbon atoms are bonded to one silicon atom, and as a result, the one silicon atom is alkoxysilyl having 1 to 20 carbon atoms.
- Group or silanol group may be constituted. From the viewpoint that hydrogen halide can be generated by reacting with air, the coupling residue preferably has no halogen.
- all or part of the double bonds are converted to saturated hydrocarbons by further hydrogenating the modified conjugated diene polymer or the conjugated diene polymer described below in an inert solvent.
- Can do In that case, heat resistance and weather resistance are improved, deterioration of the product when processed at high temperature can be prevented, and exercise performance as rubber tends to be improved. As a result, it exhibits even better performance in various applications such as automotive applications.
- the hydrogenation rate of the unsaturated double bond based on the conjugated diene compound can be arbitrarily selected according to the purpose and is not particularly limited. When used as a vulcanizate, it is preferable that the double bond of the conjugated diene part partially remains.
- the hydrogenation rate of the conjugated diene part in the conjugated diene polymer is preferably 3.0% or more and 70% or less, more preferably 5.0 or more and 65% or less, and more preferably 10%. More preferably, it is 60% or less.
- heat resistance and exercise performance tend to be improved by selectively hydrogenating vinyl groups.
- the hydrogenation rate can be determined by a nuclear magnetic resonance apparatus (NMR).
- the modified conjugated diene copolymer of the present embodiment can be an oil-extended polymer to which an extending oil is added.
- the modified conjugated diene copolymer of the present embodiment is non-oil-extended, oil-extended, processability when used as a rubber vulcanizate, and wear resistance when used as a vulcanizate.
- the Mooney viscosity measured at 100 ° C. is preferably 20 or more and 100 or less, and more preferably 30 or more and 80 or less. The Mooney viscosity is measured by the method described in Examples described later.
- the weight average molecular weight of the modified conjugated diene polymer is 20 ⁇ 10 4 or more and 300 ⁇ 10 4 or less, preferably 50 ⁇ 10 4 or more, more preferably 64 ⁇ 10 4 or more, and still more preferably 80 ⁇ 10 4 or more.
- the weight average molecular weight is preferably 250 ⁇ 10 4 or less, preferably 180 ⁇ 10 4 or less, and more preferably 150 ⁇ 10 4 or less.
- the weight average molecular weight is 300 ⁇ 10 4 or less, it is excellent in workability and dispersibility of the filler when used as a vulcanizate, and practically sufficient fracture characteristics can be obtained.
- the weight average molecular weights of the modified conjugated diene polymer and the conjugated diene polymer described later are measured by the method described in the examples described later.
- the modified conjugated diene polymer is a modified conjugated diene polymer (hereinafter referred to as “specific”) having a molecular weight of 200 ⁇ 10 4 to 500 ⁇ 10 4 with respect to the total amount (100% by mass) of the modified conjugated diene. Of 0.25% by mass or more and 30% by mass or less. As a result, the balance between the low hysteresis loss and the wet skid resistance and the wear resistance, which are the effects of the present embodiment, are excellent.
- the modified conjugated diene polymer preferably contains a specific high molecular weight component in an amount of 1.0% by mass or more, more preferably 1.4% by mass or more, further preferably 1.75% by mass or more, and still more preferably.
- the modified conjugated diene polymer preferably contains a specific high molecular weight component in an amount of 28% by mass or less, more preferably 25% by mass or less, still more preferably 20% by mass or less, and 18% by mass or less.
- “molecular weight” is a standard polystyrene conversion molecular weight obtained by GPC (gel permeation chromatography).
- the amount used as a polymerization initiator of the organic monolithium compound described later may be adjusted, and may be as follows.
- a method having a residence time distribution that is, the time distribution of the growth reaction may be widened.
- a continuous type preferably a tank reactor with a stirrer is a backmix reactor of a type in which the mixture is vigorously mixed with a stirrer, and more preferably a tube type reactor used as a complete mixing type reactor.
- a method of recirculating a part a method of providing a polymerization initiator feed place in the middle of the polymerization reactor in addition to or near the monomer inlet, and a tank type and a tube type The method of combining is mentioned.
- These methods are methods in which the residence time distribution is increased so that a polymer component having a long residence time becomes a high molecular weight component.
- a polymerization initiator feed method is used continuously or intermittently from the start of the polymerization to the middle of the polymerization, at the start of the polymerization, and / or during the polymerization.
- the method of feeding continuously or intermittently is mentioned.
- This method is a method in which a polymer polymerized from the polymerization start point at which the polymerization initiator is first fed becomes a high molecular weight component, and a molecular weight difference is generated between the polymer initiated later.
- the amount of the polymerization initiator corresponding to the target molecular weight is continuously fed to the monomer, for example, at a conversion rate of 0% to 95%, the weight having an expanded molecular weight distribution is obtained.
- the activity ratio of the living end of the conjugated diene polymer before the reaction step tends to be high, and the coupling rate after coupling, that is, the modified conjugated diene polymer having a high modification rate.
- a method of a backmix reactor of a type in which a tank reactor with a stirrer is used and vigorously mixed with a stirrer is more preferable.
- the temperature change after a polymerization process until a coupling agent is added becomes like this.
- it is 10 degrees C or less, More preferably, it is 5 degrees C or less.
- the reaction time is preferably 10 seconds or longer, more preferably 30 seconds or longer.
- the time from the end of the polymerization step to the start time of the reaction step is preferably shorter, but more preferably within 5 minutes.
- the amount of coupling agent added in order to produce a predetermined amount of high molecular weight component, it is preferable to appropriately control the amount of coupling agent added.
- the addition amount of the coupling agent for example, a method of adding after diluting the coupling agent is preferable.
- the dilution concentration is preferably 0.1 mmol / L to 1.1 mol / L, and more preferably 1 mmol / L to 0.75 mol / L.
- the water content of the solvent to be diluted is preferably 100 mass ppm or less, more preferably 50 mass ppm or less, still more preferably 30 mass ppm or less, and even more preferably 10 mass ppm or less.
- the water content of the solvent to be diluted is 100 mass ppm or less, the coupling agent and water react with each other, and the functional group in the coupling agent is reduced, resulting in a mole of the conjugated diene polymer.
- the difference between the number and the number of moles of the coupling agent can be suppressed, and a high molecular weight component tends to be obtained.
- the molecular weight distribution (Mw / Mn) represented by the ratio of the weight average molecular weight (Mw) to the number average molecular weight (Mn) is preferably 1.6 or more and 3.0 or less.
- a modified conjugated diene polymer having a molecular weight distribution in this range tends to be more excellent in processability when it is made into a vulcanized product, and tends to be more excellent in wearability when made into a vulcanized product.
- the number average molecular weight, the weight average molecular weight, the molecular weight distribution, and the content of a specific high molecular weight component with respect to the modified conjugated diene polymer and the conjugated diene polymer described later are measured by the methods described in the examples described later.
- the modified conjugated diene polymer of the present embodiment is preferably represented by the following general formula (I).
- D 1 represents a diene polymer chain, and the diene polymer chain preferably has a weight average molecular weight of 10 ⁇ 10 4 to 100 ⁇ 10 4 .
- R 1 to R 3 each independently represents a single bond or an alkylene group having 1 to 20 carbon atoms
- R 4 and R 7 each independently represents an alkyl group having 1 to 20 carbon atoms
- R 5 , R 8, and R 9 each independently represents a hydrogen atom or an alkyl group having a carbon number of 1 to 20
- R 6 and R 10 each independently represents an alkylene group having 1 to 20 carbon atoms
- R 11 Represents a hydrogen atom or an alkyl group having 1 to 20 carbon atoms.
- m and x represent an integer of 1 to 3, x ⁇ m, p represents 1 or 2
- y represents an integer of 1 to 3, y ⁇ (p + 1)
- z is 1 Or the integer of 2 is shown.
- D 1 , R 1 to R 11 , m, p, x, y, and z when there are a plurality of each are independent and may be the same or different.
- i represents an integer of 0 to 6
- j represents an integer of 0 to 6
- k represents an integer of 0 to 6
- (i + j + k) represents an integer of 3 to 10
- ((x ⁇ i) + (Y ⁇ j) + (z ⁇ k)) is an integer of 5 to 30.
- A has a hydrocarbon group having 1 to 20 carbon atoms or at least one atom selected from the group consisting of an oxygen atom, a nitrogen atom, a silicon atom, a sulfur atom, and a phosphorus atom, and an active hydrogen.
- the organic group which does not have is shown.
- the hydrocarbon group represented by A includes saturated, unsaturated, aliphatic, and aromatic hydrocarbon groups.
- the organic group having no active hydrogen is an organic group for inactivating the active terminal of the conjugated diene polymer. Examples of such an organic group include functional groups having active hydrogen such as a hydroxyl group (—OH), a secondary amino group (> NH), a primary amino group (—NH 2 ), and a sulfhydryl group (—SH).
- An organic group having no group is shown.
- the hydrocarbon group represented by A includes saturated, unsaturated, aliphatic, and aromatic hydrocarbon groups.
- the organic group having no active hydrogen is an organic group for inactivating the active terminal of the conjugated diene polymer. Examples of such an organic group include functional groups having active hydrogen such as a hydroxyl group (—OH), a secondary amino group (> NH), a primary amino group (—NH 2 ), and a sulfhydryl group (—SH
- the modified conjugated diene-based polymer represented by the formula (1) tends to be more excellent in processability when used as a vulcanized product, which is an effect of this embodiment, and has low hysteresis loss when used as a vulcanized product. And wet skid resistance and wear resistance.
- A is represented by any one of the following general formulas (II) to (V).
- B 1 represents a single bond or a hydrocarbon group having 1 to 20 carbon atoms, and a represents an integer of 1 to 10. When there are a plurality of B 1 s , each is independent.
- B 2 represents a single bond or a hydrocarbon group having 1 to 20 carbon atoms
- B 3 represents an alkyl group having 1 to 20 carbon atoms
- a represents an integer of 1 to 10 .
- B 2 and B 3 when there are a plurality of each are independent of each other.
- B 4 represents a single bond or a hydrocarbon group having 1 to 20 carbon atoms, and a represents an integer of 1 to 10. When there are a plurality of B 4 s , they are independent of each other.
- B 5 represents a single bond or a hydrocarbon group having 1 to 20 carbon atoms, and a represents an integer of 1 to 10.
- the B 5 when there are a plurality, are each independently.
- A is represented by any one of the formulas (II) to (V)
- the effect of this embodiment tends to be superior to the workability of the vulcanized product. It tends to be superior due to the balance between low hysteresis loss and wet skid resistance and wear resistance. Moreover, it tends to be easily available for practical use.
- the method for producing a modified conjugated diene polymer of the present embodiment comprises an organic monolithium compound as a polymerization initiator, polymerizing at least a conjugated diene compound to obtain a conjugated diene polymer, and the conjugated diene polymer. And a reaction step in which a reactive compound having five or more functional groups (hereinafter also referred to as “coupling agent”) is reacted with the active terminal of the conjugated diene polymer of the present embodiment.
- a reactive compound having five or more functional groups hereinafter also referred to as “coupling agent”
- the coupling agent it is preferable to react a pentafunctional or higher functional compound having a nitrogen atom and a silicon atom.
- R 12 to R 14 each independently represents a single bond or an alkylene group having 1 to 20 carbon atoms
- R 15 to R 18 and R 20 each independently represent 1 to carbon atoms
- 20 represents an alkyl group
- R 19 and R 22 each independently represents an alkylene group having 1 to 20 carbon atoms
- R 21 represents an alkyl group having 1 to 20 carbon atoms or a trialkylsilyl group
- m represents an integer of 1 to 3
- p represents 1 or 2.
- R 12 to R 22 , m, and p when there are a plurality of each are independent and may be the same or different.
- A has a hydrocarbon group having 1 to 20 carbon atoms, or at least one atom selected from the group consisting of an oxygen atom, a nitrogen atom, a silicon atom, a sulfur atom, and a phosphorus atom, and has no active hydrogen.
- An organic group is shown.
- the hydrocarbon group represented by A includes saturated, unsaturated, aliphatic, and aromatic hydrocarbon groups.
- the organic group having no active hydrogen is an organic group that inactivates the active terminal of the conjugated diene polymer.
- Examples of such an organic group include functional groups having active hydrogen such as a hydroxyl group (—OH), a secondary amino group (> NH), a primary amino group (—NH 2 ), and a sulfhydryl group (—SH).
- An organic group having no group include functional groups having active hydrogen such as a hydroxyl group (—OH), a secondary amino group (> NH), a primary amino group (—NH 2 ), and a sulfhydryl group (—SH).
- an organic monolithium compound is used as a polymerization initiator, and at least a conjugated diene compound is polymerized to obtain a conjugated diene polymer.
- the polymerization step is preferably polymerization by a growth reaction by living anion polymerization reaction, whereby a conjugated diene polymer having an active end can be obtained, and a modified diene polymer having a high modification rate tends to be obtained. is there.
- the conjugated diene polymer of this embodiment is obtained by polymerizing at least a conjugated diene compound, and is obtained by copolymerizing both a conjugated diene compound and a vinyl-substituted aromatic compound as necessary.
- the conjugated diene compound of this embodiment is not particularly limited as long as it is a polymerizable monomer, but is preferably a conjugated diene compound containing 4 to 12 carbon atoms per molecule, more preferably 4 to 8 carbon atoms. Is a conjugated diene compound.
- conjugated diene compounds include, but are not limited to, for example, 1,3-butadiene, isoprene, 2,3-dimethyl-1,3-butadiene, 1,3-pentadiene, 3-methyl-1 1,3-pentadiene, 1,3-hexadiene, and 1,3-heptadiene.
- 1,3-butadiene and isoprene are preferable from the viewpoint of industrial availability. These may be used alone or in combination of two or more.
- the vinyl-substituted aromatic compound is not particularly limited as long as it is a monomer copolymerizable with a conjugated diene compound, but a monovinyl aromatic compound is preferable.
- monovinyl aromatic compounds include, but are not limited to, styrene, p-methylstyrene, ⁇ -methylstyrene, vinylethylbenzene, vinylxylene, vinylnaphthalene, and diphenylethylene.
- styrene is preferable from the viewpoint of industrial availability. These may be used alone or in combination of two or more.
- the reaction in the reaction step described later may be hindered. Therefore, the total content concentration (mass) of these impurities is preferably 200 ppm or less, more preferably 100 ppm or less, and even more preferably 50 ppm or less.
- allenes include propadiene and 1,2-butadiene.
- acetylenes include ethyl acetylene and vinyl acetylene.
- the conjugated diene polymer may be a random copolymer or a block copolymer.
- the random copolymer is not limited to the following, but for example, a random copolymer composed of two or more conjugated diene compounds such as butadiene-isoprene random copolymer, butadiene-styrene random copolymer, isoprene-styrene. And a random copolymer comprising a conjugated diene of a random copolymer and a butadiene-isoprene-styrene random copolymer and a vinyl-substituted aromatic compound.
- the composition distribution of each monomer in the copolymer chain is not particularly limited.
- a completely random copolymer close to a statistical random composition a taper (gradient) random in which the composition is distributed in a tapered shape.
- a copolymer is mentioned.
- the bonding mode of the conjugated diene that is, the composition of 1,4-bonds, 1,2-bonds, etc. may be uniform or distributed.
- the block copolymer is not limited to the following, but for example, a 2 type block copolymer (diblock) consisting of 2 blocks, a 3 type block copolymer (triblock) consisting of 3 blocks, 4 4 type block copolymer (tetrablock) which consists of a piece is mentioned.
- the polymer constituting one block may be a polymer composed of one type of monomer or a copolymer composed of two or more types of monomers.
- a polymer block composed of 1,3-butadiene is represented by “B”
- a copolymer of 1,3-butadiene and isoprene is represented by “B / I”
- a copolymer of 1,3-butadiene and styrene is not limited to the following, but for example, a 2 type block copolymer (diblock) consisting of 2 blocks, a 3 type block copolymer (triblock) consisting of 3 blocks, 4 4 type block copolymer (
- each block need not be clearly distinguished. Further, when one polymer block is a copolymer composed of two types of monomers A and B, A and B in the block may be distributed uniformly or in a tapered shape. Good.
- the polymerization initiator of this embodiment uses at least an organic monolithium compound.
- organic monolithium compounds include, but are not limited to, low molecular compounds and solubilized oligomeric organic monolithium compounds.
- examples of the organic monolithium compound include a compound having a carbon-lithium bond, a compound having a nitrogen-lithium bond, and a compound having a tin-lithium bond in the bonding mode between the organic group and the lithium.
- the amount of the organic monolithium compound used as a polymerization initiator is preferably determined by the molecular weight of the target conjugated diene polymer or modified conjugated diene polymer.
- the amount of the monomer such as the conjugated diene compound used relative to the amount of the polymerization initiator is related to the degree of polymerization, that is, tends to be related to the number average molecular weight and / or the weight average molecular weight. Therefore, in order to increase the molecular weight, it is preferable to adjust in the direction of decreasing the polymerization initiator, and in order to decrease the molecular weight, it is preferable to adjust in the direction of increasing the amount of polymerization initiator.
- the organic monolithium compound is preferably an alkyllithium compound having a substituted amino group or a dialkylaminolithium from the viewpoint of being used in one method for introducing a nitrogen atom into a conjugated diene polymer.
- a conjugated diene polymer having a nitrogen atom composed of an amino group at the polymerization initiation terminal is obtained.
- the substituted amino group is an amino group having no active hydrogen or having a structure in which active hydrogen is protected.
- the alkyl lithium compound having an amino group not having active hydrogen is not limited to the following, but examples thereof include 3-dimethylaminopropyl lithium, 3-diethylaminopropyl lithium, 4- (methylpropylamino) butyl lithium, and 4 -Hexamethyleneiminobutyllithium.
- the alkyllithium compound having an amino group having a structure in which active hydrogen is protected is not limited to the following, and examples thereof include 3-bistrimethylsilylaminopropyllithium and 4-trimethylsilylmethylaminobutyllithium.
- dialkylamino lithium examples include, but are not limited to, lithium dimethylamide, lithium diethylamide, lithium dipropylamide, lithium dibutylamide, lithium di-n-hexylamide, lithium diheptylamide, lithium diisopropylamide, lithium dioctylamide Lithium-di-2-ethylhexylamide, lithium didecylamide, lithium ethylpropylamide, lithium ethylbutyramide, lithium ethylbenzylamide, lithium methylphenethylamide, lithium hexamethyleneimide, lithium pyrrolidide, lithium piperidide, Lithium heptamethyleneimide, lithium morpholide, 1-lithioazacyclooctane, 6-lithio-1,3,3-trimethyl-6-azabici B [3.2.1] octane, and 1-lithio-1,2,3,6-tetrahydropyridine and the like.
- organic monolithium compounds having a substituted amino group are obtained by reacting a small amount of a polymerizable monomer, for example, a monomer such as 1,3-butadiene, isoprene, or styrene, solubilized oligomeric organic monolithium. It can also be used as a compound.
- a polymerizable monomer for example, a monomer such as 1,3-butadiene, isoprene, or styrene. It can also be used as a compound.
- the organic monolithium compound is preferably an alkyllithium compound from the viewpoint of industrial availability and ease of control of the polymerization reaction.
- a conjugated diene polymer having an alkyl group at the polymerization initiation terminal is obtained.
- the alkyl lithium compound include, but are not limited to, n-butyl lithium, sec-butyl lithium, tert-butyl lithium, n-hexyl lithium, benzyl lithium, phenyl lithium, and stilbene lithium.
- n-butyllithium and sec-butyllithium are preferable from the viewpoints of industrial availability and ease of control of the polymerization reaction.
- organic monolithium compounds may be used alone or in combination of two or more. Moreover, you may use together with another organometallic compound.
- organometallic compound include alkaline earth metal compounds, other alkali metal compounds, and other organometallic compounds.
- alkaline earth metal compound include, but are not limited to, organic magnesium compounds, organic calcium compounds, and organic strontium compounds. Also included are the alkaline earth metal alkoxides, sulfonates, carbonates, and amide compounds.
- organic magnesium compound include dibutyl magnesium and ethyl butyl magnesium.
- organometallic compounds include organoaluminum compounds.
- the polymerization reaction mode is not limited to the following, and examples thereof include batch type (also referred to as “batch type”) and continuous type polymerization reaction modes.
- batch type also referred to as “batch type”
- continuous type polymerization reaction modes In the continuous mode, one or two or more connected reactors can be used.
- the continuous reactor for example, a tank type with a stirrer or a tube type is used.
- the monomer, the inert solvent, and the polymerization initiator are continuously fed to the reactor, and a polymer solution containing the polymer is obtained in the reactor.
- the coalescence solution is drained.
- the batch reactor for example, a tank type equipped with a stirrer is used.
- the monomer, inert solvent, and polymerization initiator are fed and, if necessary, the monomer is added continuously or intermittently during the polymerization, and the polymer is added in the reactor.
- a polymer solution is obtained, and after completion of the polymerization, the polymer solution is discharged.
- a continuous system is preferred, in which the polymer can be continuously discharged and used for the next reaction in a short time.
- the polymerization step is preferably performed in an inert solvent.
- the solvent include hydrocarbon solvents such as saturated hydrocarbons and aromatic hydrocarbons.
- Specific hydrocarbon solvents include, but are not limited to, for example, aliphatic hydrocarbons such as butane, pentane, hexane, and heptane; alicyclics such as cyclopentane, cyclohexane, methylcyclopentane, and methylcyclohexane Hydrocarbons: Hydrocarbons composed of aromatic hydrocarbons such as benzene, toluene, xylene and mixtures thereof.
- a conjugated diene polymer having a high concentration of active terminals tends to be obtained, and modification with a high modification rate
- a conjugated diene polymer is preferred because it tends to be obtained.
- a polar compound may be added.
- An aromatic vinyl compound can be randomly copolymerized with a conjugated diene compound and tends to be used as a vinylating agent for controlling the microstructure of the conjugated diene portion.
- the polymerization reaction tends to be effective.
- polar compounds include, but are not limited to, tetrahydrofuran, diethyl ether, dioxane, ethylene glycol dimethyl ether, ethylene glycol dibutyl ether, diethylene glycol dimethyl ether, diethylene glycol dibutyl ether, dimethoxybenzene, 2,2-bis (2-oxolanyl).
- Ethers such as propane; Tertiary amine compounds such as tetramethylethylenediamine, dipiperidinoethane, trimethylamine, triethylamine, pyridine, quinuclidine; potassium-tert-amylate, potassium-tert-butyrate, sodium-tert-butyrate, Use alkali metal alkoxide compounds such as sodium amylate; phosphine compounds such as triphenylphosphine Rukoto can. These polar compounds may be used alone or in combination of two or more.
- the amount of the polar compound used is not particularly limited and can be selected according to the purpose, but is preferably 0.01 mol or more and 100 mol or less with respect to 1 mol of the polymerization initiator.
- An appropriate amount of such a polar compound (vinylating agent) can be used as a regulator of the microstructure of the polymer conjugated diene moiety depending on the desired vinyl bond amount.
- Many polar compounds simultaneously have an effective randomizing effect in the copolymerization of conjugated diene compounds and aromatic vinyl compounds, and tend to be used to adjust the distribution of aromatic vinyl compounds and adjust the amount of styrene block It is in.
- the total amount of styrene and a part of 1,3-butadiene may be used together.
- a method in which a polymerization reaction is started and the remaining 1,3-butadiene is intermittently added during the copolymerization reaction may be used.
- the polymerization temperature is preferably a temperature at which living anion polymerization proceeds, more preferably 0 ° C. or more, and further preferably 120 ° C. or less from the viewpoint of productivity.
- a temperature at which living anion polymerization proceeds More preferably, it exists in the tendency which can fully ensure the reaction amount of the coupling agent with respect to the active terminal after completion
- the conjugated diene polymer before the reaction step obtained in the polymerization step preferably has a Mooney viscosity measured at 110 ° C. of 10 or more and 90 or less, more preferably 15 or more and 85 or less, and still more preferably 20 It is 60 or less. Within this range, the modified conjugated diene polymer of this embodiment tends to be excellent in workability and wear resistance.
- the amount of bound conjugated diene in the conjugated diene polymer or modified conjugated diene polymer of the present embodiment is not particularly limited, but is preferably 40% by mass to 100% by mass, and more preferably 55% by mass to 80% by mass. The following is more preferable.
- the amount of bonded aromatic vinyl in the conjugated diene polymer or modified conjugated diene polymer of the present embodiment is not particularly limited, but is preferably 0% by mass or more and 60% by mass or less, and more preferably 20% by mass or more. More preferably, it is 45 mass% or less.
- the amount of bound conjugated diene and amount of bound aromatic vinyl are in the above ranges, the balance between low hysteresis loss and wet skid resistance when used as a vulcanized product, wear resistance, and fracture characteristics tend to be superior.
- the amount of bonded aromatic vinyl can be measured by ultraviolet absorption of a phenyl group, and the amount of bonded conjugated diene can also be obtained from this. Specifically, it measures according to the method as described in the Example mentioned later.
- the vinyl bond amount in the conjugated diene bond unit is not particularly limited, but is preferably 10 mol% or more and 75 mol% or less, and 20 mol. % To 65 mol% is more preferable.
- the vinyl bond amount is in the above range, there is a tendency to be more excellent in the balance of low hysteresis loss and wet skid resistance, wear resistance, and fracture strength when vulcanized.
- the modified diene polymer is a copolymer of butadiene and styrene, it is determined by the method of Hampton (RR Hampton, Analytical Chemistry, 21, 923 (1949)) in the butadiene bond unit.
- the vinyl bond amount (1,2-bond amount) can be determined. Specifically, it is measured by the method described in the examples described later.
- the amount of each bond in the modified conjugated diene polymer is in the above range, and the glass transition temperature of the modified conjugated diene polymer is ⁇ 45 ° C. or more and ⁇ 15 ° C.
- the glass transition temperature is ⁇ 45 ° C. or more and ⁇ 15 ° C.
- the glass transition temperature according to ISO 22768: 2006, a DSC curve is recorded while raising the temperature in a predetermined temperature range, and the peak top (Inflection point) of the DSC differential curve is set as the glass transition temperature. Specifically, it is measured by the method described in the examples described later.
- the number of blocks in which 30 or more aromatic vinyl units are linked may be small or not. preferable. More specifically, when the copolymer is a butadiene-styrene copolymer, the Kolthoff method (method described in IM KOLTHOFF, et al., J. Polym. Sci. 1, 429 (1946)). In the known method for analyzing the amount of polystyrene insoluble in methanol, the block in which 30 or more aromatic vinyl units are linked is preferably 5.0 relative to the total amount of the copolymer. It is not more than mass%, more preferably not more than 3.0 mass%.
- the conjugated diene polymer of the present embodiment is a conjugated diene-aromatic vinyl copolymer
- the ratio of aromatic vinyl units to be present alone is large.
- the copolymer is a butadiene-styrene copolymer
- the copolymer is decomposed by an ozonolysis method known as Tanaka et al. (Polymer, 22, 1721 (1981)).
- Tanaka et al. Polymer, 22, 1721 (1981)
- the isolated styrene amount is 40% by mass or more and the chain styrene structure having 8 or more styrene chains is 5.0% by mass or less based on the total amount of styrene bonded. It is desirable.
- the obtained vulcanized rubber has excellent performance with particularly low hysteresis loss.
- reaction process In the reaction step of the present embodiment, a reactive compound having five or more functional groups (hereinafter also referred to as “coupling agent”) is reacted with the active terminal of the conjugated diene polymer of the present embodiment, and the coupling residue.
- the modified conjugated diene polymer of this embodiment in which a group and a conjugated diene polymer of 5 or more molecules are bonded can be obtained. It is preferable to react a pentafunctional or higher functional reactive compound having a nitrogen atom and a silicon atom.
- the coupling agent used in the reaction step of the present embodiment may have any structure as long as it is a pentafunctional or higher functional compound, but preferably a pentafunctional or higher functional compound having a nitrogen atom and a silicon atom. And preferably has at least three silicon-containing functional groups. Further preferred coupling agents are those in which at least one silicon atom constitutes an alkoxysilyl group or silanol group having 1 to 20 carbon atoms, and more preferably represented by the formula (VI) described above as a coupling agent. A compound.
- the alkoxysilyl group of the coupling agent reacts with, for example, the active terminal of the conjugated diene polymer to dissociate alkoxylithium, and the bond between the terminal of the conjugated diene polymer chain and the coupling residue silicon. Tend to form. A value obtained by subtracting the number of SiORs reduced by the reaction from the total number of SiORs that one molecule of the coupling agent has becomes the number of alkoxysilyl groups that the coupling residue has.
- the azasilacycle group of the coupling agent forms a> N—Li bond and a bond between the conjugated diene polymer terminal and the coupling residue silicon.
- 2 moles of conjugated diene copolymer reacted with 1 mole of trialkoxysilane group is 3 or more in the modified conjugated diene copolymer, that is, the degree of branching is 6 or more, and other reactions.
- the condensation reaction tends to be suppressed.
- Examples of the coupling agent include, but are not limited to, tris (3-trimethoxysilylpropyl) amine, tris (3-triethoxysilylpropyl) amine, tris (3-tripropoxysilylpropyl) amine, bis (3-trimethoxysilylpropyl)-[3- (2,2-dimethoxy-1-aza-2-silacyclopentane) propyl] amine, tetrakis (3-trimethoxysilylpropyl) -1,3-propanediamine, Tris (3-trimethoxysilylpropyl)-[3- (1-methoxy-2-trimethylsilyl-1-sila-2-azacyclopentane) propyl] -1,3-propanediamine, tris (3-trimethoxysilylpropyl) )-[3- (1-Methoxy-2-methyl-1-sila-2-azacyclopentane) Propyl] -1,3-prop
- the reaction temperature in the reaction step is preferably the same as the polymerization temperature of the conjugated diene polymer, more preferably 0 ° C. or more and 120 ° C. or less, and further preferably 50 ° C. or more and 100 ° C. or less. Moreover, the temperature change after a polymerization process until a coupling agent is added becomes like this. Preferably it is 10 degrees C or less, More preferably, it is 5 degrees C or less.
- the reaction time in the reaction step is preferably 10 seconds or more, more preferably 30 seconds or more.
- the time from the end of the polymerization step to the start of the reaction step is preferably shorter, but more preferably within 5 minutes. By doing so, a high coupling rate and a high modification rate tend to be obtained.
- the mixing in the reaction step may be either mechanical stirring or stirring with a static mixer.
- the reaction process is also preferably continuous.
- the reactor in the reaction step for example, a tank type with a stirrer or a tube type is used.
- the coupling agent may be continuously supplied to the reactor after being diluted with an inert solvent.
- the reaction process may be performed by transferring the coupling agent to a polymerization reactor or by transferring it to another reactor.
- A is preferably represented by any one of the following general formulas (II) to (V).
- B 1 represents a single bond or a hydrocarbon group having 1 to 20 carbon atoms, and a represents an integer of 1 to 10. When there are a plurality of B 1 s , each is independent.
- B 2 represents a single bond or a hydrocarbon group having 1 to 20 carbon atoms
- B 3 represents an alkyl group having 1 to 20 carbon atoms
- a represents an integer of 1 to 10 .
- B 2 and B 3 when there are a plurality of each are independent of each other.
- B 4 represents a single bond or a hydrocarbon group having 1 to 20 carbon atoms, and a represents an integer of 1 to 10. When there are a plurality of B 4 s , they are independent of each other.
- B 5 represents a single bond or a hydrocarbon group having 1 to 20 carbon atoms, and a represents an integer of 1 to 10.
- the B 5 when there are a plurality, are each independently.
- A is represented by any one of the formulas (II) to (V), a modified conjugated diene polymer having better performance of the present embodiment tends to be obtained.
- the coupling agent is not limited to the following, but examples include tris (3-trimethoxysilylpropyl) amine, bis (3-trimethoxy Silylpropyl)-[3- (2,2-dimethoxy-1-aza-2-silacyclopentane) propyl] amine, bis [3- (2,2-dimethoxy-1-aza-2-silacyclopentane) propyl ]-(3-trimethoxysilylpropyl) amine, tris [3- (2,2-dimethoxy-1-aza-2-silacyclopentane) propyl] amine, tris (3-ethoxysilylpropyl) amine, bis (3 -Triethoxysilylpropyl)-[3- (2,2-diethoxy-1-aza-2-silacyclopentane) propyl] amine, bis [3- (2,2 Diethoxy-1-aza-2-s
- the coupling agent is not limited to the following.
- the coupling agent is not limited to the following.
- the coupling agent is not limited to the following.
- A is preferably represented by formula (II) or formula (III), and k represents 0.
- Such a coupling agent tends to be easily available, and tends to be more excellent in wear resistance and low hysteresis loss performance when the modified conjugated diene polymer is used as a vulcanizate.
- Such coupling agents are not limited to the following, but include, for example, bis (3-trimethoxysilylpropyl)-[3- (2,2-dimethoxy-1-aza-2-silacyclopentane) propyl.
- A is more preferably represented by formula (II) or formula (III), k represents 0, and in formula (II) or formula (III), a is 2 to 10 Indicates an integer. Thereby, it exists in the tendency for the abrasion resistance and low hysteresis loss performance when vulcanized to become more excellent.
- Examples of such a coupling agent include, but are not limited to, tetrakis [3- (2,2-dimethoxy-1-aza-2-silacyclopentane) propyl] -1,3-propanediamine, Tetrakis (3-trimethoxysilylpropyl) -1,3-propanediamine, tetrakis (3-trimethoxysilylpropyl) -1,3-bisaminomethylcyclohexane, and N 1- (3- (bis (3- (tri trimethoxysilyl) propyl) amino) propyl) -N 1 - methyl -N 3 - (3- (methyl (3- (trimethoxysilyl) propyl) amino) propyl) -N 3 - (3- (trimethoxysilyl) propyl ) -1,3-propanediamine.
- the amount of the compound represented by the formula (VI) as the coupling agent is adjusted so that the number of moles of the conjugated diene polymer to the number of moles of the coupling agent reacts at a desired stoichiometric ratio. Tending to achieve the desired degree of branching.
- the number of moles of the specific polymerization initiator is preferably 5.0 times mole or more, more preferably 6.0 times mole or more, relative to the number of moles of the coupling agent.
- the number of functional groups of the coupling agent ((m ⁇ 1) ⁇ i + p ⁇ j + k) is preferably an integer of 5 to 10, and more preferably an integer of 6 to 10. .
- a method of adding after diluting the coupling agent is preferable.
- the difference in addition amount is the same, the difference between the number of moles of the conjugated diene polymer and the number of moles of the coupling agent tends to be smaller when diluted.
- the water content of the solvent to be diluted is preferably 100 ppm by mass or less, more preferably 50 ppm by mass or less, still more preferably 30 ppm by mass or less, and even more preferably 10 ppm by mass or less.
- the water content of the solvent to be diluted is 100 mass ppm or less, the coupling agent and water react with each other, and the functional group in the coupling agent is reduced, resulting in a mole of the conjugated diene polymer. It tends to be possible to suppress the deviation between the number and the number of moles of the coupling agent.
- the molecular weight distribution (Mw / Mn) of the conjugated diene polymer is preferably 1.5 or more and 2.5 or less, more preferably Is preferably 1.8 or more and 2.2 or less.
- the resulting modified conjugated diene polymer is preferably such that a peak of a molecular weight curve by GPC is detected. In this case, the workability and wear resistance which are the object of the present embodiment tend to be more excellent.
- the ratio of the coupling polymer in the modified conjugated polymer is represented by the modification rate.
- the modification rate is preferably 30% by mass or more, more preferably 50% by mass or more, and further preferably 70% by mass or more.
- the ratio of the coupling polymer is synonymous with the modification rate when the coupling residue has a functional group composed of nitrogen and silicon. The modification rate is measured by the method described in Examples described later.
- a condensation reaction step in which a condensation reaction is performed in the presence of a condensation accelerator may be provided after the reaction step or before the reaction step.
- the method for hydrogenating the conjugated diene part of the modified conjugated diene polymer of the present embodiment is not particularly limited, and a known method can be used.
- a suitable hydrogenation method includes a method of hydrogenating by blowing gaseous hydrogen into the polymer solution in the presence of a catalyst.
- a catalyst for example, a heterogeneous catalyst such as a catalyst in which a noble metal is supported on a porous inorganic substance; a catalyst in which a salt such as nickel or cobalt is solubilized and reacted with organic aluminum or the like, or a metallocene such as titanocene is used. Examples thereof include homogeneous catalysts such as catalysts. Among these, titanocene catalysts are preferable from the viewpoint of selecting mild hydrogenation conditions.
- the hydrogenation of the aromatic group can be performed by using a noble metal supported catalyst.
- the hydrogenation catalyst are not limited to the following.
- hydrogenation catalysts for example, JP-B-42-8704, JP-B-43-6636, JP-B-63-4841, JP-B-1-37970, JP-B-1-53851, Examples also include known hydrogenation catalysts described in Japanese Patent Publication No. 2-9041 and Japanese Patent Application Laid-Open No. 8-109219.
- a preferable hydrogenation catalyst includes a reaction mixture of a titanocene compound and a reducing organometallic compound.
- a deactivator, a neutralizing agent, and the like may be added to the copolymer solution after the reaction step, if necessary.
- the quenching agent include, but are not limited to, water; alcohols such as methanol, ethanol, and isopropanol.
- the neutralizing agent include, but are not limited to, for example, carboxylic acids such as stearic acid, oleic acid, and versatic acid (a mixture of carboxylic acids having 9 to 11 carbon atoms, mainly 10 and having many branches). Acid; An aqueous solution of an inorganic acid, carbon dioxide gas.
- a stabilizer for rubber from the viewpoint of preventing gel formation after polymerization and improving the stability during processing.
- the rubber stabilizer is not limited to the following, and known ones can be used.
- BHT 2,6-di-tert-butyl-4-hydroxytoluene
- n-octadecyl-3 Antioxidants such as — (4′-hydroxy-3 ′, 5′-di-tert-butylphenol) propinate and 2-methyl-4,6-bis [(octylthio) methyl] phenol are preferred.
- an extension oil can be added to the modified conjugated diene copolymer as necessary.
- the method of adding the extender oil to the modified conjugated diene polymer is not limited to the following, but the extender oil is added to the polymer solution and mixed to obtain an oil-extended copolymer solution.
- the extending oil include aroma oil, naphthenic oil, paraffin oil, and the like.
- an aromatic substitute oil having a polycyclic aromatic (PCA) component of 3% by mass or less by the IP346 method is preferable.
- Aroma alternative oils include TDAE (Treated Distillate Aromatic Extracts), MES (Mild Extraction Solvate), and RadE (Rex), which are listed in Kautschuk Kunststoffe 52 (12) 799 (1999).
- TDAE Teated Distillate Aromatic Extracts
- MES Meld Extraction Solvate
- RadE Rex
- the addition amount of extending oil is not specifically limited, 10 mass parts or more and 60 mass parts or less are preferable with respect to 100 mass parts of modified conjugated diene polymers, and 20 mass parts or more and 37.5 mass parts or less are more preferable.
- the modified conjugated diene polymer of the present embodiment is suitably used as a vulcanizate.
- the vulcanizate include tires, hoses, shoe soles, vibration-insulating rubbers, automobile parts, and vibration-insulating rubbers, and also include resin-reinforced rubbers such as impact-resistant polystyrene and ABS resin.
- the modified conjugated diene polymer is suitably used for a tread rubber composition for tires.
- the vulcanized product may be, for example, a modified conjugated diene polymer of the present embodiment, if necessary, an inorganic filler such as a silica-based inorganic filler or carbon black, or a modified conjugated diene polymer of the present embodiment.
- a modified conjugated diene polymer composition is kneaded with a rubber-like polymer, a silane coupling agent, a rubber softener, a vulcanizing agent, a vulcanization accelerator, a vulcanization aid, etc. It can be obtained by sulfuration.
- the rubber composition of the present embodiment includes a rubber component and a filler of 5.0 parts by mass or more and 150 parts by mass or less with respect to 100 parts by mass of the rubber component. Further, the rubber component contains 10% by mass or more of the above-described modified conjugated diene polymer with respect to the total amount (100% by mass) of the rubber component. Moreover, it is preferable that the said filler contains a silica type inorganic filler.
- the rubber composition tends to be more excellent in processability when it is made into a vulcanizate by dispersing a silica-based inorganic filler, and the balance between low hysteresis loss and wet skid resistance when made into a vulcanizate.
- the rubber composition of this embodiment is used for vulcanized rubber applications such as tires, automobile parts such as anti-vibration rubber, and shoes, it is preferable that a silica-based inorganic filler is included.
- a rubbery polymer other than the modified conjugated diene polymer of the present embodiment (hereinafter simply referred to as “rubbery polymer”) is combined with the branched modified diene polymer of the present embodiment.
- rubbery polymers include, but are not limited to, for example, conjugated diene polymers or hydrogenated products thereof, random copolymers of conjugated diene compounds and vinyl aromatic compounds, or hydrogenated products thereof. Products, block copolymers of conjugated diene compounds and vinyl aromatic compounds or hydrogenated products thereof, non-diene polymers, and natural rubber.
- Specific rubbery polymers are not limited to the following, but include, for example, butadiene rubber or hydrogenated product thereof, isoprene rubber or hydrogenated product thereof, styrene-butadiene rubber or hydrogenated product thereof, and styrene-butadiene block.
- examples thereof include styrene elastomers such as copolymers or hydrogenated products thereof, styrene-isoprene block copolymers or hydrogenated products thereof, acrylonitrile-butadiene rubbers or hydrogenated products thereof.
- Non-diene polymers are not limited to the following, but include olefins such as ethylene-propylene rubber, ethylene-propylene-diene rubber, ethylene-butene-diene rubber, ethylene-butene rubber, ethylene-hexene rubber, and ethylene-octene rubber.
- olefins such as ethylene-propylene rubber, ethylene-propylene-diene rubber, ethylene-butene-diene rubber, ethylene-butene rubber, ethylene-hexene rubber, and ethylene-octene rubber.
- Elastomer butyl rubber, brominated butyl rubber, acrylic rubber, fluoro rubber, silicone rubber, chlorinated polyethylene rubber, epichlorohydrin rubber, ⁇ , ⁇ -unsaturated nitrile-acrylate ester-conjugated diene copolymer rubber, urethane rubber, and polysulfide rubber Is mentioned.
- Examples of natural rubber include, but are not limited to, the following: smoked sheet RSS 3-5, SMR, and epoxidized natural rubber.
- the various rubber-like polymers described above may be modified rubbers to which functional groups having polarity such as hydroxyl groups and amino groups are added.
- functional groups having polarity such as hydroxyl groups and amino groups are added.
- butadiene rubber, isoprene rubber, styrene-butadiene rubber, natural rubber, and butyl rubber are preferably used.
- the weight average molecular weight of the rubber-like polymer is preferably from 2,000 to 2,000,000, more preferably from 5,000 to 1,500,000 from the viewpoint of the balance between performance and processing characteristics.
- a low molecular weight rubbery polymer so-called liquid rubber, can also be used.
- These rubber-like polymers may be used individually by 1 type, and may use 2 or more types together.
- the content ratio (mass ratio) of the modified conjugated diene polymer to the rubber-like polymer is (modified conjugated diene).
- System polymer / rubbery polymer) is preferably 10/90 or more and 100/0 or less, more preferably 20/80 or more and 90/10 or less, and even more preferably 50/50 or more and 80/20 or less. Therefore, the rubber component preferably contains the modified conjugated diene polymer in an amount of 10 to 100 parts by weight, more preferably 20 to 90 parts by weight, based on the total amount (100 parts by weight) of the rubber component. Included, more preferably 50 parts by weight or more and 80 parts by weight or less.
- the filler is not limited to the following, and examples thereof include silica-based inorganic filler, carbon black, metal oxide, and metal hydroxide. Among these, a silica type inorganic filler is preferable. These may be used alone or in combination of two or more.
- the content of the filler in the rubber composition is from 5.0 parts by weight to 150 parts by weight, and from 20 parts by weight to 100 parts by weight with respect to 100 parts by weight of the rubber component containing the modified conjugated diene polymer. Preferably there is.
- the content of the filler is 5.0 parts by mass or more from the viewpoint of the effect of adding the filler, and the filler is sufficiently dispersed, so that the workability and mechanical strength of the composition are practically sufficient. From the viewpoint of, it is 150 parts by mass or less.
- the silica-based inorganic filler is not particularly limited, but may be a known, solid particles preferably comprise SiO 2 or Si 3 Al as a constituent unit, the main structural units of SiO 2 or Si 3 Al Solid particles contained as a component are more preferable.
- a main component means the component contained in a silica type inorganic filler 50 mass% or more, Preferably it is 70 mass% or more, More preferably, it is 80 mass% or more.
- silica-based inorganic fillers are not limited to the following, but examples include inorganic fibrous materials such as silica, clay, talc, mica, diatomaceous earth, wollastonite, montmorillonite, zeolite, and glass fiber. . Moreover, the mixture of the silica type inorganic filler which hydrophobized the surface, and a silica type inorganic filler and inorganic fillers other than a silica type is also mentioned. Among these, silica and glass fiber are preferable, and silica is more preferable from the viewpoints of strength and wear resistance. Examples of silica include dry silica, wet silica, and synthetic silicate silica. Among these silicas, wet silica is preferable from the viewpoint of excellent balance between fracture property improvement effect and wet skid resistance.
- the nitrogen adsorption specific surface area determined by the BET adsorption method of the silica-based inorganic filler is 100 m 2 / g or more and 300 m 2 / g or less. preferably, more preferably not more than 170m 2 / g or more 250m 2 / g. If necessary, a silica-based inorganic filler having a relatively small specific surface area (for example, a specific surface area of 200 m 2 / g or less) and a silica-based filler having a relatively large specific surface area (for example, 200 m 2 / g or more). Inorganic fillers) can be used in combination.
- the modified conjugated diene-based polymer improves the dispersibility of silica, There is an effect in improving the wearability, and there is a tendency that good fracture characteristics and low hysteresis loss can be well balanced.
- the content of the silica-based inorganic filler in the rubber composition is 5.0 parts by mass or more and 150 parts by mass, and 20 parts by mass or more and 100 parts by mass with respect to 100 parts by mass of the rubber component containing the modified conjugated diene polymer. Part or less.
- the content of the silica-based inorganic filler is 5.0 parts by mass or more from the viewpoint of manifesting the effect of adding the inorganic filler, and the inorganic filler is sufficiently dispersed to make the processability and mechanical strength of the composition practical. From the viewpoint of making it sufficiently satisfactory, it is 150 parts by mass or less.
- the carbon black is not limited to the following, and examples thereof include carbon blacks of each class such as SRF, FEF, HAF, ISAF, and SAF. Among these, carbon black having a nitrogen adsorption specific surface area of 50 m 2 / g or more and a dibutyl phthalate (DBP) oil absorption of 80 mL / 100 g or less is preferable.
- the content of carbon black is preferably 0.5 parts by mass or more and 100 parts by mass or less, and more preferably 3.0 parts by mass or more and 100 parts by mass or less with respect to 100 parts by mass of the rubber component including the modified conjugated diene polymer. 5.0 parts by mass or more and 50 parts by mass or less are more preferable.
- the content of carbon black is preferably 0.5 parts by mass or more from the viewpoint of expressing the performance required for applications such as dry grip performance and conductivity, and from the viewpoint of dispersibility, 100 parts by mass. The following is preferable.
- the metal oxide refers to solid particles having the chemical formula MxOy (M represents a metal atom, and x and y each independently represents an integer of 1 to 6) as a main component of a structural unit.
- MxOy M represents a metal atom, and x and y each independently represents an integer of 1 to 6
- Examples of the metal oxide include, but are not limited to, alumina, titanium oxide, magnesium oxide, and zinc oxide.
- the metal hydroxide include, but are not limited to, aluminum hydroxide, magnesium hydroxide, and zirconium hydroxide.
- the rubber composition may contain a silane coupling agent.
- the silane coupling agent has a function to close the interaction between the rubber component and the inorganic filler, and has an affinity or binding group for each of the rubber component and the silica-based inorganic filler.
- a compound having a sulfur bond portion and an alkoxysilyl group or silanol group portion in one molecule is preferable. Examples of such compounds include bis- [3- (triethoxysilyl) -propyl] -tetrasulfide, bis- [3- (triethoxysilyl) -propyl] -disulfide, bis- [2- (triethoxy Silyl) -ethyl] -tetrasulfide.
- the content of the silane coupling agent is preferably 0.1 parts by mass or more and 30 parts by mass or less, more preferably 0.5 parts by mass or more and 20 parts by mass or less with respect to 100 parts by mass of the inorganic filler described above. 0 to 15 parts by mass is more preferable. When the content of the silane coupling agent is within the above range, the addition effect of the silane coupling agent tends to be more remarkable.
- the rubber composition may contain a rubber softener from the viewpoint of improving processability.
- a rubber softener mineral oil or a liquid or low molecular weight synthetic softener is suitable.
- Mineral oil-based rubber softeners called process oils or extender oils that are used to soften, increase volume and improve processability of rubbers are mixtures of aromatic, naphthenic and paraffin chains.
- a paraffin chain having 50% or more carbon atoms in the total carbon is called paraffinic, and a naphthenic ring having 30% or more and 45% or less carbon atoms in the total carbon is naphthenic or aromatic. What accounts for over 30% of carbon is called aromatic.
- the conjugated diene polymer of the present embodiment is a copolymer of a conjugated diene compound and a vinyl aromatic compound
- the rubber softener used has a suitable aromatic content and is compatible with the copolymer. Is preferable because it tends to be good.
- silica inorganic fillers for the method of mixing the modified conjugated diene polymer and other rubbery polymers, silica inorganic fillers, carbon black and other fillers, silane coupling agents, rubber softeners, etc.
- silica inorganic fillers for example, an open roll, a Banbury mixer, a kneader, a single screw extruder, a twin screw extruder, a melt kneading method using a general mixer such as a multi-screw extruder, A method of removing the solvent by heating after dissolution and mixing can be mentioned.
- melt kneading method using a roll, a Banbury mixer, a kneader, or an extruder is preferred from the viewpoint of productivity and good kneading properties.
- any of a method of kneading the rubber component and other fillers, silane coupling agents, and additives at a time, and a method of mixing in multiple times can be applied.
- the rubber composition may be a vulcanized composition that has been vulcanized with a vulcanizing agent.
- the vulcanizing agent include, but are not limited to, radical generators such as organic peroxides and azo compounds, oxime compounds, nitroso compounds, polyamine compounds, sulfur, and sulfur compounds.
- Sulfur compounds include sulfur monochloride, sulfur dichloride, disulfide compounds, polymeric polysulfur compounds, and the like.
- the content of the vulcanizing agent is preferably 0.01 parts by mass or more and 20 parts by mass or less, and more preferably 0.1 parts by mass or more and 15 parts by mass or less with respect to 100 parts by mass of the rubber component.
- the vulcanization method a conventionally known method can be applied, and the vulcanization temperature is preferably 120 ° C. or higher and 200 ° C. or lower, more preferably 140 ° C. or higher and 180 ° C. or lower.
- a vulcanization accelerator may be used as necessary.
- the vulcanization accelerator a conventionally known material can be used, and is not limited to the following materials. For example, sulfenamide, guanidine, thiuram, aldehyde-amine, aldehyde-ammonia, thiazole Thiourea and dithiocarbamate vulcanization accelerators.
- cure adjuvant although not limited to the following, For example, zinc white and a stearic acid are mentioned.
- the content of the vulcanization accelerator is preferably 0.01 parts by mass or more and 20 parts by mass or less, and more preferably 0.1 parts by mass or more and 15 parts by mass or less with respect to 100 parts by mass of the rubber component.
- softening agents and fillers heat resistance stabilizers, antistatic agents, weather resistance stabilizers, antiaging agents, colorants, lubricants other than those described above may be used without departing from the object of the present embodiment.
- Various additives such as these may be used.
- known softeners can be used.
- specific examples of other fillers include calcium carbonate, magnesium carbonate, aluminum sulfate, and barium sulfate.
- Known materials can be used as the above heat stabilizer, antistatic agent, weathering stabilizer, anti-aging agent, colorant, and lubricant.
- the modified diene polymer composition of the present embodiment is suitably used as a tire rubber composition. That is, the tire according to the present embodiment uses a rubber composition.
- the tire rubber composition of the present embodiment is not limited to the following.
- various tires such as fuel-saving tires, all-season tires, high-performance tires, studless tires: treads, carcass, sidewalls, bead portions, etc. It can be used for each tire part.
- the rubber composition for tires is excellent in the balance between low hysteresis loss and wet skid resistance and wear resistance when used as a vulcanized product, for fuel-saving tires and treads for high-performance tires, More preferably used.
- Molecular weight measurement condition 1 GPC measuring apparatus (trade name “manufactured by Tosoh Corporation”) using three conjugated diene polymers or modified conjugated diene polymers as a sample and three columns using polystyrene gel as a filler.
- the eluent used was THF (tetrahydrofuran) containing 5 mmol / L triethylamine.
- THF tetrahydrofuran
- TSKguardcolumn SuperMP (HZ) -H was connected as a guard column.
- a 10 mg sample for measurement was dissolved in 10 mL of THF to prepare a measurement solution, and 10 ⁇ L of the measurement solution was injected into a GPC measurement device, and measurement was performed under conditions of an oven temperature of 40 ° C. and a THF flow rate of 0.35 mL / min.
- Measurement condition 2 Using a conjugated diene polymer or modified conjugated diene polymer as a sample, a chromatogram was measured using a GPC measuring apparatus in which three columns using polystyrene gel as a filler were connected, and standard polystyrene Based on the calibration curve using the above, the weight average molecular weight (Mw) and the number average molecular weight (Mn), the peak top molecular weight of the modified conjugated diene polymer (Mp 1 ) and the peak top molecular weight of the conjugated diene polymer (Mp 2 ) And the ratio (Mp 1 / Mp 2 ) and the ratio of the molecular weight of 200 ⁇ 10 4 or more and 500 ⁇ 10 4 or less.
- Mw weight average molecular weight
- Mn number average molecular weight
- Mp 1 peak top molecular weight of the modified conjugated diene polymer
- Mp 2 peak top molecular weight of the conjugated diene polymer
- the eluent used was THF containing 5 mmol / L triethylamine.
- the column used was guard column: trade name “TSKguardcolumn SuperHH” manufactured by Tosoh Corporation, and column: trade name “TSKgel SuperH5000”, “TSKgel SuperH6000”, “TSKgel SuperH7000” manufactured by Tosoh Corporation.
- An RI detector (trade name “HLC8020” manufactured by Tosoh Corporation) was used under the conditions of an oven temperature of 40 ° C. and a THF flow rate of 0.6 mL / min. 10 mg of a sample for measurement was dissolved in 20 mL of THF to prepare a measurement solution, and 20 ⁇ L of the measurement solution was injected into a GPC measurement device and measured.
- Tables 1 and 2 show the results of measurement under measurement condition 2 for samples measured under measurement condition 1 and having a molecular weight distribution value of less than 1.6.
- Peak top molecular weight of the (Mp 1 and Mp 2), in any of the measurement conditions 1 and 2 were also determined as follows. In the GPC curve obtained by measurement, the peak detected as the highest molecular weight component was selected. For the selected peak, the molecular weight corresponding to the maximum value of the peak was calculated and used as the peak top molecular weight.
- the ratio of the molecular weight of 200 ⁇ 10 4 or more and 500 ⁇ 10 4 or less is the molecular weight of 200 ⁇ 10 4 from the ratio of the molecular weight of 500 ⁇ 10 4 or less to the whole from the integral molecular weight distribution curve in both measurement conditions 1 and 2. It was calculated by subtracting the proportion occupied by less than 4 .
- the eluent used was THF containing 5 mmol / L triethylamine.
- Tosoh Corporation trade names “TSKgel G4000HXL”, “TSKgel G5000HXL”, and “TSKgel G6000HXL” were used.
- a 20 mg sample for measurement was dissolved in 10 mL of THF to prepare a measurement solution, and 100 ⁇ L of the measurement solution was injected into a GPC measurement device, and measurement was performed under conditions of an oven temperature of 40 ° C. and a THF flow rate of 1 mL / min.
- Glass transition temperature (Tg) Glass transition temperature (Tg) Using a modified conjugated diene-based polymer as a sample, in accordance with ISO 22768: 2006, a differential scanning calorimeter “DSC3200S” manufactured by Mac Science Co. was used. The DSC curve was recorded while the temperature was raised at, and the peak top (Inflection point) of the DSC differential curve was taken as the glass transition temperature.
- the modified conjugated diene polymer was used as a sample and measured by applying the property of adsorbing the modified basic polymer component to a GPC column using silica gel as a filler.
- the amount of adsorption on the silica column is measured from the difference between the chromatogram measured with the polystyrene column and the chromatogram measured with the silica column of the sample solution containing the sample and the low molecular weight internal standard polystyrene. Asked. Specifically, it is as shown below.
- sample solution 10 mg of sample and 5 mg of standard polystyrene were dissolved in 20 mL of THF to prepare a sample solution.
- GPC measurement conditions using a polystyrene column (measurement condition 3): Using a trade name “HLC-8320GPC” manufactured by Tosoh Corporation, THF containing 5 mmol / L triethylamine was used as an eluent, and 10 ⁇ L of a sample solution was used as an apparatus. The mixture was injected, and a chromatogram was obtained using a RI detector under conditions of a column oven temperature of 40 ° C. and a THF flow rate of 0.35 mL / min. As the column, three Tosoh product names “TSKgel SuperMultiporeHZ-H” were connected, and the Tosoh product name “TSKguardcolumn SuperMP (HZ) -H” was connected as a guard column.
- Measurement condition 4 Using THF containing 5 mmol / L of triethylamine as an eluent, 20 ⁇ L of a sample solution was injected into the apparatus for measurement. As the columns, guard columns: trade names “TSKguardcolumn SuperH-H” manufactured by Tosoh Corporation, and columns: trade names “TSKgel SuperH5000”, “TSKgel SuperH6000”, “TSKgel SuperH7000” manufactured by Tosoh Corporation were used. A chromatogram was obtained by measurement using a RI detector (HLC8020 manufactured by Tosoh Corporation) under conditions of a column oven temperature of 40 ° C. and a THF flow rate of 0.6 mL / min.
- RI detector HCC8020 manufactured by Tosoh Corporation
- GPC measurement conditions using a silica-based column Using a trade name “HLC-8320GPC” manufactured by Tosoh Corporation, using THF as an eluent, 50 ⁇ L of a sample solution was injected into the apparatus, column oven temperature 40 ° C., THF flow rate A chromatogram was obtained using an RI detector at 0.5 ml / min.
- the column uses the product names “Zorbax PSM-1000S”, “PSM-300S”, “PSM-60S” and uses the product name “DIOL 4.6 ⁇ 12.5 mm 5 micron” as the guard column in front of it. Connected and used.
- Example 1 Modified Conjugated Diene Polymer (Sample 1) The internal volume is 10 L, the ratio (L / D) of the internal height (L) to the diameter (D) is 4.0, the inlet is at the bottom, the outlet is at the top, and a tank reactor with a stirrer A tank-type pressure vessel having a stirrer and a temperature control jacket was used as a polymerization reactor. Water was previously removed, and 1,3-butadiene was mixed at 17.9 g / min, styrene at 9.8 g / min, and n-hexane at 145.3 g / min.
- n-butyllithium for residual impurity inactivation treatment was added and mixed at 0.104 mmol / min, and then at the bottom of the reactive group. Continuously fed. Further, polymerization in which 2,2-bis (2-oxolanyl) propane as a polar substance is vigorously mixed with a stirrer at a rate of 0.0194 g / min and n-butyllithium as a polymerization initiator at a rate of 0.255 mmol / min. The reaction was continuously fed to the bottom of the reactor. The temperature was controlled so that the temperature of the polymerization solution at the reactor top outlet was 75 ° C.
- Example 2 Modified Conjugated Diene Polymer (Sample 2) The coupling agent was changed from bis (3-trimethoxysilylpropyl)-[3- (2,2-dimethoxy-1-aza-2-silacyclopentane) propyl] amine to tris (3-trimethoxysilylpropyl) amine (Table A modified conjugated diene polymer (Sample 2) was obtained in the same manner as in Example 1 except that the content was changed to “B”. Table 1 shows the physical properties of Sample 2.
- Example 3 Modified Conjugated Diene Polymer (Sample 3)
- the coupling agent was changed from bis (3-trimethoxysilylpropyl)-[3- (2,2-dimethoxy-1-aza-2-silacyclopentane) propyl] amine to tris (3-triethoxysilylpropyl) amine (Table A modified conjugated diene polymer (Sample 3) was obtained in the same manner as in Example 1 except that the abbreviation “C” was used.
- Table 1 shows the physical properties of Sample 3.
- Example 4 Modified Conjugated Diene Polymer (Sample 4)
- the amount of the treated n-butyllithium added was 0.117 mmol / min
- the amount of the polymerized n-butyllithium added was 0.242 mmol / min
- the coupling agent was bis (3-trimethoxysilylpropyl)-[3- (2 , 2-Dimethoxy-1-aza-2-silacyclopentane) propyl] amine to tris (3-trimethoxysilylpropyl)-[3- (2,2-dimethoxy-1-aza-2-silacyclopentane) propyl ]
- Modified 1,1-propanediamine abbreviated as “D” in the table
- a system polymer (Sample 4) was obtained. Table 1 shows the physical properties of Sample 4.
- Example 5 Modified Conjugated Diene Polymer (Sample 5) The amount of treated n-butyllithium added was 0.108 mmol / min, the amount of polymerized n-butyllithium added was 0.251 mmol / min, and the coupling agent was bis (3-trimethoxysilylpropyl)-[3- (2 , 2-Dimethoxy-1-aza-2-silacyclopentane) propyl] amine to tris (3-trimethoxysilylpropyl)-[3- (1-methoxy-2-trimethylsilyl-1-sila-2-azacyclopentane) ) Propyl] -1,3-propanediamine (abbreviated as “E” in the table), and modified in the same manner as in Example 1 except that the addition amount of the coupling agent was 0.0359 mmol / min.
- a conjugated diene polymer (Sample 5) was obtained. Table 1 shows the physical properties of Sample 5.
- Example 6 Modified Conjugated Diene Polymer (Sample 6)
- the amount of the treated n-butyllithium added was 0.117 mmol / min
- the amount of the polymerized n-butyllithium added was 0.242 mmol / min
- the coupling agent was bis (3-trimethoxysilylpropyl)-[3- (2 , 2-Dimethoxy-1-aza-2-silacyclopentane) propyl] amine to tetrakis [3- (2,2-dimethoxy-1-aza-2-silacyclopentane) propyl] -1,3-propanediamine
- the modified conjugated diene polymer (sample 6) was obtained in the same manner as in Example 1 except that the amount of coupling agent was changed to 0.0302 mmol / min instead of “F” in the table. It was. Table 1 shows the physical properties of Sample 6.
- Example 7 Modified conjugated diene polymer (Sample 7)
- the amount of the treated n-butyllithium added was 0.117 mmol / min
- the amount of the polymerized n-butyllithium added was 0.242 mmol / min
- the coupling agent was bis (3-trimethoxysilylpropyl)-[3- (2 , 2-Dimethoxy-1-aza-2-silacyclopentane) propyl] amine is replaced with tetrakis (3-trimethoxysilylpropyl) -1,3-propanediamine (abbreviated as “G” in the table), and a cup is added.
- a modified conjugated diene polymer (sample 7) was obtained in the same manner as in Example 1 except that the amount of ring agent added was 0.0302 mmol / min. Table 1 shows the physical properties of Sample 7.
- Example 8 Modified Conjugated Diene Polymer (Sample 8)
- the amount of the treated n-butyllithium added was 0.117 mmol / min
- the amount of the polymerized n-butyllithium added was 0.242 mmol / min
- the coupling agent was bis (3-trimethoxysilylpropyl)-[3- (2 , 2-dimethoxy-1-aza-2-silacyclopentane) propyl] amine is replaced with tetrakis (3-trimethoxysilylpropyl) -1,3-bisaminomethylcyclohexane (abbreviated as “H” in the table).
- a modified conjugated diene polymer (Sample 8) was obtained in the same manner as in Example 1 except that the addition amount of the coupling agent was 0.0302 mmol / min. Table 2 shows the physical properties of Sample 8.
- Example 9 Modified Conjugated Diene Polymer (Sample 9) The amount of treated n-butyllithium added was 0.124 mmol / min, the amount of polymerized n-butyllithium added was 0.286 mmol / min, and the polar substance 2,2-bis (2-oxolanyl) propane was 0.0265 g / min.
- the “degree of branching” shown in Tables 1 and 2 is the number of branches assumed from the number of functional groups and the amount added of the coupling agent, and can also be confirmed from the value of the contraction factor.
- the “number of SiOR residues” shown in Tables 1 and 2 is a value obtained by subtracting the number of SiORs reduced by the reaction from the total number of SiORs that one molecule of the coupling agent has.
- the rubber coupled with the coupling agent (I) used in Comparative Example 1 was not adsorbed on the silica column, and the modification rate could not be measured.
- Example 10 to 18 and Comparative Examples 4 to 6 Samples 1 to 12 shown in Table 1 and Table 2 were used as raw rubbers, and rubber compositions containing the respective raw rubbers were obtained according to the formulation shown below.
- Modified conjugated diene polymer (samples 1 to 12): 100 parts by mass (without oil) Silica 1 (trade name “Ultrasil 7000GR” manufactured by Evonik Degussa, Inc., nitrogen adsorption specific surface area 170 m 2 / g): 50.0 parts by mass Silica 2 (trade name “Zeosil Premium 200MP” manufactured by Rhodia, Inc., nitrogen adsorption specific surface area 220 m 2 / g): 25.0 parts by mass Carbon black (trade name “Seast KH (N339)” manufactured by Tokai Carbon Co., Ltd.): 5.0 parts by mass Silane coupling agent (trade name “Si75” manufactured by Evonik Degussa, Triethoxysilylpropyl) disulf
- the above materials were kneaded by the following method to obtain a rubber composition.
- a closed kneading machine (with an internal volume of 0.3 L) equipped with a temperature control device, as the first stage kneading, under the conditions of a filling rate of 65% and a rotor rotation speed of 30 to 50 rpm, raw rubber (samples 1 to 12), A filler (silica 1, silica 2, carbon black), a silane coupling agent, process oil, zinc white, and stearic acid were kneaded.
- the temperature of the closed mixer was controlled, and each rubber composition (compound) was obtained at a discharge temperature of 155 to 160 ° C.
- the mixture obtained above was cooled to room temperature, an anti-aging agent was added, and the mixture was kneaded again to improve silica dispersion. Also in this case, the discharge temperature of the blend was adjusted to 155 to 160 ° C. by controlling the temperature of the mixer.
- sulfur and vulcanization accelerators 1 and 2 were added and kneaded with an open roll set at 70 ° C. Thereafter, it was molded and vulcanized with a vulcanization press at 160 ° C. for 20 minutes.
- the rubber composition before vulcanization and the rubber composition after vulcanization were evaluated. Specifically, the evaluation was performed by the following method. The results are shown in Tables 3 and 4.
- Viscoelastic Parameters Viscoelastic Parameters Viscoelastic parameters were measured in a torsion mode using a viscoelastic tester “ARES” manufactured by Rheometrics Scientific. Each measured value was indexed with the result for the rubber composition of Comparative Example 4 as 100. Tan ⁇ measured at 0 ° C. with a frequency of 10 Hz and a strain of 1% was used as an index of wet grip properties. It shows that wet grip property is so favorable that an index
- the modified conjugated diene polymers of Examples 10 to 18 were compared with the modified conjugated diene polymers of Comparative Examples 4 to 6, and wet grip properties when used as vulcanizates. It has been confirmed that it has an excellent balance of fuel economy and excellent wear resistance. Moreover, it was also confirmed that the compound Mooney viscosity at the time of making a vulcanizate is low and shows good processability. And it was also confirmed that it has practically sufficient fracture strength when it is used as a vulcanizate.
- the modified conjugated diene polymer according to the present invention has industrial applicability in fields such as tire treads, automobile interior / exterior products, anti-vibration rubber, belts, footwear, foams, and various industrial products.
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- General Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Mechanical Engineering (AREA)
- Addition Polymer Or Copolymer, Post-Treatments, Or Chemical Modifications (AREA)
- Compositions Of Macromolecular Compounds (AREA)
- Tires In General (AREA)
- Graft Or Block Polymers (AREA)
Abstract
Description
[1]
重量平均分子量が、20×104以上300×104以下である、変性共役ジエン系重合体であって、
前記変性共役ジエン系重合体の総量に対して、分子量が200×104以上500×104以下である該変性共役ジエン系重合体を、0.25質量%以上30質量%以下含み、
収縮因子(g’)が、0.64未満である、変性共役ジエン系重合体。
[2]
窒素原子と珪素原子とを有する、[1]に記載の変性共役ジエン系重合体。
[3]
前記重量平均分子量は、50×104以上150×104以下である、[1]又は[2]に記載の変性共役ジエン系重合体。
[4]
前記変性共役ジエン系重合体の総量に対して、分子量が200×104以上500×104以下である該変性共役ジエン系重合体を、1.0質量%以上30質量%以下含む、[1]~[3]のいずれかに記載の変性共役ジエン系重合体。
[5]
分岐を有し、
分岐度が、5以上である、[1]~[4]のいずれかに記載の変性共役ジエン系重合体。
[6]
前記分岐度は、6以上である、[5]に記載の変性共役ジエン系重合体。
[7]
1以上のカップリング残基と、該カップリング残基に対して結合する共役ジエン系重合体鎖と、を有し、
前記分岐は、1の前記カップリング残基に対して5以上の前記共役ジエン系重合体鎖が結合している分岐を含む、[5]又は[6]に記載の変性共役ジエン系重合体。
[8]
前記分岐は、1の前記カップリング残基に対して6以上の前記共役ジエン系重合体鎖が結合している分岐を含む、[5]~[7]のいずれかに記載の変性共役ジエン系重合体。
[9]
前記カップリング残基が有する、少なくとも1の珪素原子が、炭素数1~20のアルコキシシリル基又はシラノール基を構成する、[7]又は[8]に記載の変性共役ジエン系重合体。
[10]
下記一般式(I)で表される、[1]~[9]のいずれかに記載の変性共役ジエン系重合体。
[11]
式(I)において、Aは、下記一般式(II)~(V)のいずれかで表される、[10]に記載の変性共役ジエン系重合体。
[12]
[1]~[11]のいずれかに記載の変性共役ジエン系重合体の製造方法であって、
有機モノリチウム化合物を重合開始剤として用い、少なくとも共役ジエン化合物を重合し、共役ジエン系重合体を得る重合工程と、
前記共役ジエン系重合体と、下記一般式(VI)で表される化合物と、を反応させる反応工程と、を有する、変性共役ジエン系重合体の製造方法。
[13]
式(VI)において、Aは、下記一般式(II)~(V)のいずれかで表される、[12]に記載の変性共役ジエン系重合体の製造方法。
[14]
式(VI)において、Aは、式(II)又は式(III)で表され、kは、0を示す、[13]に記載の変性共役ジエン系重合体の製造方法。
[15]
式(VI)において、Aは、式(II)又は式(III)で表され、kは、0を示し、
式(II)又は式(III)において、aは、2~10の整数を示す、[13]又は[14]に記載の変性共役ジエン系重合体の製造方法。
[16]
前記有機モノリチウム化合物は、置換アミノ基を有するアルキルリチウム化合物、又はジアルキルアミノリチウムである、[12]~[15]のいずれか一項に記載の変性共役ジエン系重合体の製造方法。
[17]
前記有機モノリチウム化合物は、アルキルリチウム化合物である、[12]~[15]のいずれかに記載の変性共役ジエン系重合体の製造方法。
[18]
ゴム成分と、該ゴム成分100質量部に対して5.0質量部以上150質量部の充填剤と、を含み、
前記ゴム成分は、該ゴム成分の総量に対して、[1]~[11]のいずれかに記載の変性共役ジエン系重合体を、10質量%以上含む、ゴム組成物。
[19]
[18]に記載のゴム組成物を用いてなる、タイヤ。
本実施形態の変性共役ジエン系重合体は、重量平均分子量が20×104以上300×104以下であり、該変性共役ジエン系重合体の総量(100質量%)に対して分子量が200×104以上500×104以下である該変性共役ジエン系重合体を0.25質量%以上30質量%以下含み、収縮因子(g’)が0.64未満である。
本実施形態の共役ジエン系重合体鎖は、変性共役ジエン系重合体の構成単位であり、例えば、後述する共役ジエン系重合体とカップリング剤とを反応させることによって生じる、共役ジエン系重合体由来の構造単位である。本実施形態の共役ジエン系重合体鎖は、後述する1のカップリング残基に対して結合していることが好ましい。
本実施形態のカップリング残基は、共役ジエン系重合体鎖に結合される、変性共役ジエン系重合体の構成単位であり、例えば、後述する共役ジエン系重合体とカップリング剤とを反応させることによって生じる、カップリング剤由来の構造単位である。
本実施形態の変性共役ジエン系重合体の製造方法は、有機モノリチウム化合物を重合開始剤として用い、少なくとも共役ジエン化合物を重合し、共役ジエン系重合体を得る重合工程と、該共役ジエン系重合体と、本実施形態の共役ジエン系重合体の活性末端に対して、5官能以上の反応性化合物(以下、「カップリング剤」ともいう。)を反応させる反応工程と、を有する。カップリング剤としては、窒素原子と珪素原子とを有する5官能以上の反応性化合物を反応させるのが好ましい。下記一般式(VI)に示す化合物と、を反応させる反応工程と、を有することが好ましい。
本実施形態の重合工程は、有機モノリチウム化合物を重合開始剤とし、少なくとも共役ジエン化合物を重合し、共役ジエン系重合体を得る。重合工程は、リビングアニオン重合反応による成長反応による重合が好ましく、これにより、活性末端を有する共役ジエン系重合体を得ることができ、高変性率の変性ジエン系重合体を得ることができる傾向にある。
本実施形態の共役ジエン系重合体は、少なくとも共役ジエン化合物を重合して得られ、必要に応じて共役ジエン化合物とビニル置換芳香族化合物との両方を共重合して得られる。本実施形態の共役ジエン化合物としては、重合可能な単量体であれば特に限定されないが、1分子当り4~12の炭素原子を含む共役ジエン化合物が好ましく、より好ましくは4~8の炭素原子を含む共役ジエン化合物である。このような共役ジエン化合物としては、以下のものに限定されないが、例えば、1,3-ブタジエン、イソプレン、2,3-ジメチル-1,3-ブタジエン、1,3-ペンタジエン、3-メチル-1,3-ペンタジエン、1,3-ヘキサジエン、及び1,3-ヘプタジエンが挙げられる。これらの中でも、工業的入手の容易さの観点から、1,3-ブタジエン、及びイソプレンが好ましい。これらは1種単独で用いてもよいし、2種以上を併用してもよい。
本実施形態の重合開始剤は、少なくとも有機モノリチウム化合物を用いる。有機モノリチウム化合物としては、以下のものに限定されないが、例えば、低分子化合物、可溶化したオリゴマーの有機モノリチウム化合物が挙げられる。また、有機モノリチウム化合物としては、その有機基とそのリチウムの結合様式において、例えば、炭素-リチウム結合を有する化合物、窒素-リチウム結合を有する化合物、及び錫-リチウム結合を有する化合物が挙げられる。
本実施形態の反応工程は、本実施形態の共役ジエン系重合体の活性末端に対して、5官能以上の反応性化合物(以下、「カップリング剤」ともいう。)を反応させ、カップリング残基と5分子以上の共役ジエン系重合体とが結合した本実施形態の変性共役ジエン系重合体を得られる。窒素原子と珪素原子とを有する5官能以上の反応性化合物を反応させるのが好ましい。
本実施形態の反応工程で用いられるカップリング剤は、5官能以上の反応性化合物であればいかなる構造のものでも良いが、好ましくは、窒素原子と珪素原子とを有する5官能以上の反応性化合物が好ましく、少なくとも3個の珪素含有官能基を有していることが好ましい。さらに好ましいカップリング剤は、少なくとも1の珪素原子が、炭素数1~20のアルコキシシリル基又はシラノール基を構成するものであり、より好ましくはカップリング剤として上述した式(VI)で表される化合物である。
(Mp1/Mp2)<1.8×10-12×(Mp2-120×104)2+2
Mp2は、20×104以上80×104、Mp1は30×104以上150×104以下がより好ましい。Mp1及びMp2は、後述する実施例に記載の方法により求める。
本実施形態のゴム組成物は、ゴム成分と、該ゴム成分100質量部に対して5.0質量部以上150質量部以下の充填剤とを含む。また、当該ゴム成分は、該ゴム成分の総量(100質量%)に対して、上述した変性共役ジエン系重合体を10質量%以上含む。また、当該充填剤は、シリカ系無機充填剤を含むことが好ましい。ゴム組成物は、シリカ系無機充填剤を分散させることで、加硫物とする際の加工性により優れる傾向にあり、加硫物としたときにおける低ヒステリシスロス性とウェットスキッド抵抗性とのバランス及び耐摩耗性と、破壊強度と、により優れる傾向にある。本実施形態のゴム組成物が、タイヤ、防振ゴム等の自動車部品、靴等の加硫ゴム用途に用いられる場合にも、シリカ系無機充填剤を含むことが好ましい。
本実施形態の変性ジエン系重合体組成物は、タイヤ用ゴム組成物として好適に用いられる。すなわち、本実施形態のタイヤは、ゴム組成物を用いてなる。
変性共役ジエン系重合体を試料として、試料100mgを、クロロホルムで100mLにメスアップし、溶解して測定サンプルとした。スチレンのフェニル基による紫外線吸収波長(254nm付近)の吸収量により、試料である変性共役ジエン系重合体100質量%に対しての結合スチレン量(質量%)を測定した(島津製作所社製の分光光度計「UV-2450」)。
変性共役ジエン系重合体を試料として、試料50mgを、10mLの二硫化炭素に溶解して測定サンプルとした。溶液セルを用いて、赤外線スペクトルを600~1000cm-1の範囲で測定して、所定の波数における吸光度によりハンプトンの方法(R.R.Hampton,Analytical Chemistry 21,923(1949)に記載の方法)の計算式に従い、ブタジエン部分のミクロ構造、すなわち、1,2-ビニル結合量(mol%)を求めた(日本分光社製のフーリエ変換赤外分光光度計「FT-IR230」)。
測定条件1:共役ジエン系重合体又は変性共役ジエン系重合体を試料として、ポリスチレン系ゲルを充填剤としたカラムを3本連結したGPC測定装置(東ソー社製の商品名「HLC-8320GPC」)を使用して、RI検出器(東ソー社製の商品名「HLC8020」)を用いてクロマトグラムを測定し、標準ポリスチレンを使用して得られる検量線に基づいて、重量平均分子量(Mw)と数平均分子量(Mn)と分子量分布(Mw/Mn)と、変性共役ジエン系重合体のピークトップ分子量(Mp1)と共役ジエン系重合体のピークトップ分子量(Mp2)とその比率(Mp1/Mp2)と、分子量200×104以上500×104以下の割合と、を求めた。溶離液は5mmol/Lのトリエチルアミン入りTHF(テトラヒドロフラン)を使用した。カラムは、東ソー社製の商品名「TSKgel SuperMultiporeHZ-H」を3本接続し、その前段にガードカラムとして東ソー社製の商品名「TSKguardcolumn SuperMP(HZ)-H」を接続して使用した。測定用の試料10mgを10mLのTHFに溶解して測定溶液とし、測定溶液10μLをGPC測定装置に注入して、オーブン温度40℃、THF流量0.35mL/分の条件で測定した。上記の測定条件1で測定した各種試料の中で、分子量分布(Mw/Mn)の値が1.6未満であった試料は、改めて下記の測定条件2により測定した。測定条件1で測定し、その分子量分布の値が1.6以上であった試料に対しては、測定条件1で測定した結果を表1及び表2に示す。
変性共役ジエン系重合体を試料として、ポリスチレン系ゲルを充填剤としたカラムを3本連結したGPC測定装置(Malvern社製の商品名「GPCmax VE-2001」)を使用して、光散乱検出器、RI検出器、粘度検出器(Malvern社製の商品名「TDA305」)の順番に接続されている3つの検出器を用いて測定し、標準ポリスチレンに基づいて、光散乱検出器とRI検出器結果から絶対分子量を、RI検出器と粘度検出器の結果から固有粘度を求めた。直鎖ポリマーは、固有粘度[η]=-3.883M0.771に従うものとして用い、各分子量に対応する固有粘度の比としての収縮因子(g’)を算出した。溶離液は5mmol/Lのトリエチルアミン入りTHFを使用した。カラムは、東ソー社製の商品名「TSKgel G4000HXL」、「TSKgel G5000HXL」、及び「TSKgel G6000HXL」を接続して使用した。測定用の試料20mgを10mLのTHFに溶解して測定溶液とし、測定溶液100μLをGPC測定装置に注入して、オーブン温度40℃、THF流量1mL/分の条件で測定した。
共役ジエン系重合体又は変性共役ジエン系重合体を試料として、ムーニー粘度計(上島製作所社製の商品名「VR1132」)を用い、JIS K6300に準拠し、L形ローターを用いてムーニー粘度を測定した。測定温度は、共役ジエン系重合体を試料とする場合には110℃とし、変性共役ジエン系重合体を試料とする場合には100℃とした。まず、試料を1分間試験温度で予熱した後、ローターを2rpmで回転させ、4分後のトルクを測定してムーニー粘度(ML(1+4))とした。
変性共役ジエン系重合体を試料として、ISO 22768:2006に準拠して、マックサイエンス社製の示差走査熱量計「DSC3200S」を用い、ヘリウム50mL/分の流通下、-100℃から20℃/分で昇温しながらDSC曲線を記録し、DSC微分曲線のピークトップ(Inflection point)をガラス転移温度とした。
変性共役ジエン系重合体を試料として、シリカ系ゲルを充填剤としたGPCカラムに、変性した塩基性重合体成分が吸着する特性を応用することにより、測定した。試料及び低分子量内部標準ポリスチレンを含む試料溶液を、ポリスチレン系カラムで測定したクロマトグラムと、シリカ系カラムで測定したクロマトグラムと、の差分よりシリカ系カラムへの吸着量を測定し、変性率を求めた。具体的には、以下に示すとおりである。また、上記の(物性3)の測定条件1で測定、その分子量分布の値が1.6以上であった試料に対しては下記の測定条件3、その分子量分布の値が1.6未満であった試料に対しては下記の測定条件4で測定し、その結果を表1及び2に示す。
ポリスチレン系カラムを用いたGPC測定条件(測定条件3):東ソー社製の商品名「HLC-8320GPC」を使用して、5mmol/Lのトリエチルアミン入りTHFを溶離液として用い、試料溶液10μLを装置に注入し、カラムオーブン温度40℃、THF流量0.35mL/分の条件で、RI検出器を用いてクロマトグラムを得た。カラムは、東ソー社製の商品名「TSKgel SuperMultiporeHZ-H」を3本接続し、その前段にガードカラムとして東ソー社製の商品名「TSKguardcolumn SuperMP(HZ)-H」を接続して使用した。
変性率(%)=[1-(P2×P3)/(P1×P4)]×100
(ただし、P1+P2=P3+P4=100)
(物性7)と同様の測定を行い、算出された変性率が10%以上であった場合、窒素原子を有していると判断した。これにより、実施例1~9、及び比較例2、3の変性共役ジエン系重合体が窒素原子を有すること、比較例1の変性共役ジエン系重合体が窒素原子を有しないことを確認した。
変性共役ジエン系重合体0.5gを試料として、JIS K 0101 44.3.1に準拠して、紫外可視分光光度計(島津製作所社製の商品名「UV-1800」)を用いて測定し、モリブデン青吸光光度法により定量した。これにより、珪素原子が検出された場合(検出下限10質量ppm)、珪素原子を有していると判断した。これにより、実施例1~9、及び比較例1~3の変性共役ジエン系重合体が珪素原子を有することを確認した。
内容積が10Lで、内部の高さ(L)と直径(D)との比(L/D)が4.0であり、底部に入口、頂部に出口を有し、攪拌機付槽型反応器である攪拌機及び温度制御用のジャケットを有する槽型圧力容器を重合反応器とした。予め水分除去した、1,3-ブタジエンを17.9g/分、スチレンを9.8g/分、n-ヘキサンを145.3g/分の条件で混合した。この混合溶液を反応基の入口に供給する配管の途中に設けたスタティックミキサーにおいて、残存不純物不活性処理用のn-ブチルリチウムを0.104mmol/分で添加、混合した後、反応基の底部に連続的に供給した。更に、極性物質として2,2-ビス(2-オキソラニル)プロパンを0.0194g/分の速度で、重合開始剤としてn-ブチルリチウムを0.255mmol/分の速度で、攪拌機で激しく混合する重合反応器の底部へ供給し、連続的に重合反応を継続させた。反応器頂部出口における重合溶液の温度が75℃となるように温度を制御した。重合が十分に安定したところで、反応器頂部出口より、カップリング剤添加前の重合体溶液を少量抜出し、酸化防止剤(BHT)を重合体100gあたり0.2gとなるように添加した後に溶媒を除去し、110℃のムーニー粘度及び各種の分子量を測定した。その他の物性も併せて表1に示す。
カップリング剤をビス(3-トリメトキシシリルプロピル)-[3-(2,2-ジメトキシ-1-アザ-2-シラシクロペンタン)プロピル]アミンからトリス(3-トリメトキシシリルプロピル)アミン(表中、「B」と略す。)に替えた以外は、実施例1と同様にして、変性共役ジエン系重合体(試料2)を得た。試料2の物性を表1に示す。
カップリング剤をビス(3-トリメトキシシリルプロピル)-[3-(2,2-ジメトキシ-1-アザ-2-シラシクロペンタン)プロピル]アミンからトリス(3-トリエトキシシリルプロピル)アミン(表中、「C」と略す。)に替えた以外は、実施例1と同様にして、変性共役ジエン系重合体(試料3)を得た。試料3の物性を表1に示す。
処理n-ブチルリチウムの添加量を0.117mmol/分、重合n-ブチルリチウムの添加量を0.242mmol/分とし、カップリング剤をビス(3-トリメトキシシリルプロピル)-[3-(2,2-ジメトキシ-1-アザ-2-シラシクロペンタン)プロピル]アミンからトリス(3-トリメトキシシリルプロピル)-[3-(2,2-ジメトキシ-1-アザ-2-シラシクロペンタン)プロピル]-1,3-プロパンジアミン(表中、「D」と略す。)に替え、カップリング剤の添加量を0.0302mmol/分とした以外は、実施例1と同様にして、変性共役ジエン系重合体(試料4)を得た。試料4の物性を表1に示す。
処理n-ブチルリチウムの添加量を0.108mmol/分、重合n-ブチルリチウムの添加量を0.251mmol/分とし、カップリング剤をビス(3-トリメトキシシリルプロピル)-[3-(2,2-ジメトキシ-1-アザ-2-シラシクロペンタン)プロピル]アミンからトリス(3-トリメトキシシリルプロピル)-[3-(1-メトキシ-2-トリメチルシリル-1-シラ-2-アザシクロペンタン)プロピル]-1,3-プロパンジアミン(表中、「E」と略す。)に替え、カップリング剤の添加量を0.0359mmol/分とした以外は、実施例1と同様にして、変性共役ジエン系重合体(試料5)を得た。試料5の物性を表1に示す。
処理n-ブチルリチウムの添加量を0.117mmol/分、重合n-ブチルリチウムの添加量を0.242mmol/分とし、カップリング剤をビス(3-トリメトキシシリルプロピル)-[3-(2,2-ジメトキシ-1-アザ-2-シラシクロペンタン)プロピル]アミンからテトラキス[3-(2,2-ジメトキシ-1-アザ-2-シラシクロペンタン)プロピル]-1,3-プロパンジアミン(表中、「F」と略す。)に替え、カップリング剤の添加量を0.0302mmol/分とした以外は、実施例1と同様にして、変性共役ジエン系重合体(試料6)を得た。試料6の物性を表1に示す。
処理n-ブチルリチウムの添加量を0.117mmol/分、重合n-ブチルリチウムの添加量を0.242mmol/分とし、カップリング剤をビス(3-トリメトキシシリルプロピル)-[3-(2,2-ジメトキシ-1-アザ-2-シラシクロペンタン)プロピル]アミンからテトラキス(3-トリメトキシシリルプロピル)-1,3-プロパンジアミン(表中、「G」と略す。)に替え、カップリング剤の添加量を0.0302mmol/分とした以外は、実施例1と同様にして、変性共役ジエン系重合体(試料7)を得た。試料7の物性を表1に示す。
処理n-ブチルリチウムの添加量を0.117mmol/分、重合n-ブチルリチウムの添加量を0.242mmol/分とし、カップリング剤をビス(3-トリメトキシシリルプロピル)-[3-(2,2-ジメトキシ-1-アザ-2-シラシクロペンタン)プロピル]アミンからテトラキス(3-トリメトキシシリルプロピル)-1,3-ビスアミノメチルシクロヘキサン(表中、「H」と略す。)に替え、カップリング剤の添加量を0.0302mmol/分とした以外は、実施例1と同様にして、変性共役ジエン系重合体(試料8)を得た。試料8の物性を表2に示す。
処理n-ブチルリチウムの添加量を0.124mmol/分、重合n-ブチルリチウムの添加量を0.286mmol/分、極性物質の2,2-ビス(2-オキソラニル)プロパンを0.0265g/分とし、カップリング剤をビス(3-トリメトキシシリルプロピル)-[3-(2,2-ジメトキシ-1-アザ-2-シラシクロペンタン)プロピル]アミンからトリス(3-トリメトキシシリルプロピル)アミン(B)に替え、カップリング剤の添加量を0.0477mmol/分とした以外は、実施例1と同様にして、変性共役ジエン系重合体(試料9)を得た。試料9の物性を表2に示す。
処理n-ブチルリチウムの添加量を0.114mmol/分、重合n-ブチルリチウムの添加量を0.248mmol/分とし、カップリング剤をビス(3-トリメトキシシリルプロピル)-[3-(2,2-ジメトキシ-1-アザ-2-シラシクロペンタン)プロピル]アミンからビス(トリメトキシシリル)エタン(表中、「I」と略す。)に替え、カップリング剤の添加量を0.0620mmol/分とした以外は、実施例1と同様にして、変性共役ジエン系重合体(試料10)を得た。試料11の物性を表2に示す。
処理n-ブチルリチウムの添加量を0.114mmol/分、重合n-ブチルリチウムの添加量を0.248mmol/分とし、カップリング剤をビス(3-トリメトキシシリルプロピル)-[3-(2,2-ジメトキシ-1-アザ-2-シラシクロペンタン)プロピル]アミンからビス(3-トリメトキシシリルプロピル)メチルアミン(表中、「J」と略す。)に替え、カップリング剤の添加量を0.0620mmol/分とした以外は、実施例1と同様にして、変性共役ジエン系重合体(試料11)を得た。試料11の物性を表2に示す。
内容量30Lで、攪拌機及びジャケットを備える温度制御が可能なオートクレーブを反応器として使用し、予め不純物を除去した、ノルマルヘキサン17200g、スチレン1022g、1,3-ブタジエン1778g、極性物質として2,2-ビス(2-オキソラニル)プロパン1.26gを反応器に入れ、反応器内が48℃のときに重合開始剤n-ブチルリチウム17.0mmolを添加し重合を開始した。重合開始直後から、反応器内の温度は上昇していき、ピーク温度(83℃)を迎え温度の低下が確認されたところでカップリング剤ビス(3-トリメトキシシリルプロピル)メチルアミン(J)を3.48mmol添加し、さらに10分撹拌した。重合停止剤としてエタノール17.0mmolを加え、反応を停止させ、変性共役ジエン系重合体を含有する重合体溶液を得た。得られた重合体溶液に、酸化防止剤(BHT)を重合体100gあたり0.2gとなるように5.6g添加した後、スチームストリッピングにより溶媒を除去して、分岐変性ジエン系重合体(試料12)を得た。試料12の物性を表2に示す。
表1及び表2に示す試料1~12を原料ゴムとして、以下に示す配合に従い、それぞれの原料ゴムを含有するゴム組成物を得た。
変性共役ジエン系重合体(試料1~12):100質量部(オイル抜き)
シリカ1(エボニック デグサ社製の商品名「Ultrasil 7000GR」窒素吸着比表面積170m2/g):50.0質量部
シリカ2(ローディア社製の商品名「Zeosil Premium 200MP」窒素吸着比表面積220m2/g):25.0質量部
カーボンブラック(東海カーボン社製の商品名「シーストKH(N339)」):5.0質量部
シランカップリング剤(エボニック デグサ社製の商品名「Si75」、ビス(トリエトキシシリルプロピル)ジスルフィド):6.0質量部
S-RAEオイル(JX日鉱日石エネルギー社製の商品名「プロセスNC140」):37.5質量部
亜鉛華:2.5質量部
ステアリン酸:1.0質量部
老化防止剤(N-(1,3-ジメチルブチル)-N‘-フェニル-p-フェニレンジアミン):2.0質量部
硫黄:2.2質量部
加硫促進剤1(N-シクロヘキシル-2-ベンゾチアジルスルフィンアミド):1.7質量部
加硫促進剤2(ジフェニルグアニジン):2.0質量部
合計:239.4質量部
上記で得た第二段の混練後、かつ、第三段の混練前の配合物を試料として、ムーニー粘度計を使用し、JIS K6300-1に準拠して、130℃、1分間の予熱を行った後に、ローターを毎分2回転で4分間回転させた後の粘度を測定した。比較例4の結果を100として指数化した。指数が小さいほど加工性が良好であることを示す。
レオメトリックス・サイエンティフィック社製の粘弾性試験機「ARES」を使用し、ねじりモードで粘弾性パラメータを測定した。各々の測定値は、比較例4のゴム組成物に対する結果を100として指数化した。0℃において周波数10Hz、ひずみ1%で測定したtanδをウェットグリップ性の指標とした。指数が大きいほどウェットグリップ性が良好であることを示す。また、50℃において周波数10Hz、ひずみ3%で測定したtanδを省燃費性の指標とした。指数が小さいほど省燃費性が良好であることを示す。
JIS K6251の引張試験法に準拠し、引張強度及び引張伸びを測定し、比較例4の結果を100として指数化した。指数が大きいほど引張強度、引張伸びが良好であることを示す。
アクロン摩耗試験機(安田精機製作所社製)を使用し、JIS K6264-2に準拠して、荷重44.4N、1000回転の摩耗量を測定し、比較例4の結果を100として指数化した。指数が大きいほど耐摩耗性が良好であることを示す。
Claims (19)
- 重量平均分子量が、20×104以上300×104以下である、変性共役ジエン系重合体であって、
前記変性共役ジエン系重合体の総量に対して、分子量が200×104以上500×104以下である該変性共役ジエン系重合体を、0.25質量%以上30質量%以下含み、
収縮因子(g’)が、0.64未満である、変性共役ジエン系重合体。 - 窒素原子と珪素原子とを有する、請求項1に記載の変性共役ジエン系重合体。
- 前記重量平均分子量は、50×104以上150×104以下である、請求項1又は2に記載の変性共役ジエン系重合体。
- 前記変性共役ジエン系重合体の総量に対して、分子量が200×104以上500×104以下である該変性共役ジエン系重合体を、1.0質量%以上30質量%以下含む、請求項1~3のいずれか一項に記載の変性共役ジエン系重合体。
- 分岐を有し、
分岐度が、5以上である、請求項1~4のいずれか一項に記載の変性共役ジエン系重合体。 - 前記分岐度は、6以上である、請求項5に記載の変性共役ジエン系重合体。
- 1以上のカップリング残基と、該カップリング残基に対して結合する共役ジエン系重合体鎖と、を有し、
前記分岐は、1の前記カップリング残基に対して5以上の前記共役ジエン系重合体鎖が結合している分岐を含む、請求項5又は6に記載の変性共役ジエン系重合体。 - 前記分岐は、1の前記カップリング残基に対して6以上の前記共役ジエン系重合体鎖が結合している分岐を含む、請求項5~7のいずれか一項に記載の変性共役ジエン系重合体。
- 前記カップリング残基が有する、少なくとも1の珪素原子が、炭素数1~20のアルコキシシリル基又はシラノール基を構成する、請求項7又は8に記載の変性共役ジエン系重合体。
- 下記一般式(I)で表される、請求項1~9のいずれか一項に記載の変性共役ジエン系重合体。
- 式(I)において、Aは、下記一般式(II)~(V)のいずれかで表される、請求項10に記載の変性共役ジエン系重合体。
- 請求項1~11のいずれか一項に記載の変性共役ジエン系重合体の製造方法であって、
有機モノリチウム化合物を重合開始剤として用い、少なくとも共役ジエン化合物を重合し、共役ジエン系重合体を得る重合工程と、
前記共役ジエン系重合体と、下記一般式(VI)で表される化合物と、を反応させる反応工程と、を有する、変性共役ジエン系重合体の製造方法。
- 式(VI)において、Aは、下記一般式(II)~(V)のいずれかで表される、請求項12に記載の変性共役ジエン系重合体の製造方法。
- 式(VI)において、Aは、式(II)又は式(III)で表され、kは、0を示す、請求項13に記載の変性共役ジエン系重合体の製造方法。
- 式(VI)において、Aは、式(II)又は式(III)で表され、kは、0を示し、
式(II)又は式(III)において、aは、2~10の整数を示す、請求項13又は14に記載の変性共役ジエン系重合体の製造方法。 - 前記有機モノリチウム化合物は、置換アミノ基を有するアルキルリチウム化合物、又はジアルキルアミノリチウムである、請求項12~15のいずれか一項に記載の変性共役ジエン系重合体の製造方法。
- 前記有機モノリチウム化合物は、アルキルリチウム化合物である、請求項12~15のいずれか一項に記載の変性共役ジエン系重合体の製造方法。
- ゴム成分と、該ゴム成分100質量部に対して5.0質量部以上150質量部の充填剤と、を含み、
前記ゴム成分は、該ゴム成分の総量に対して、請求項1~11のいずれか一項に記載の変性共役ジエン系重合体を、10質量%以上含む、ゴム組成物。 - 請求項18に記載のゴム組成物を用いてなる、タイヤ。
Priority Applications (8)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| SG11201706702QA SG11201706702QA (en) | 2015-02-19 | 2016-02-18 | Modified conjugated diene-based polymer and production method therefor, rubber composition and tire |
| JP2017500727A JPWO2016133154A1 (ja) | 2015-02-19 | 2016-02-18 | 変性共役ジエン系重合体及びその製造方法、ゴム組成物、並びにタイヤ |
| CN201680010513.8A CN107250166B (zh) | 2015-02-19 | 2016-02-18 | 改性共轭二烯系聚合物及其制造方法、橡胶组合物以及轮胎 |
| EP16752540.1A EP3260471A4 (en) | 2015-02-19 | 2016-02-18 | Modified conjugated diene polymer and method for producing same, rubber composition, and tire |
| BR112017017631-9A BR112017017631B1 (pt) | 2015-02-19 | 2016-02-18 | Polímero à base de dieno conjugado modificado e método para produzir o mesmo, composição de borracha e pneu |
| KR1020197009831A KR20190039622A (ko) | 2015-02-19 | 2016-02-18 | 변성 공액 디엔계 중합체 및 그의 제조 방법, 고무 조성물, 및 타이어 |
| KR1020177021440A KR101968849B1 (ko) | 2015-02-19 | 2016-02-18 | 변성 공액 디엔계 중합체 및 그의 제조 방법, 고무 조성물, 및 타이어 |
| US15/551,711 US10519254B2 (en) | 2015-02-19 | 2016-02-18 | Modified conjugated diene-based polymer and production method therefor, rubber composition and tire |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2015031098 | 2015-02-19 | ||
| JP2015-031098 | 2015-02-19 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2016133154A1 true WO2016133154A1 (ja) | 2016-08-25 |
Family
ID=56692298
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2016/054687 WO2016133154A1 (ja) | 2015-02-19 | 2016-02-18 | 変性共役ジエン系重合体及びその製造方法、ゴム組成物、並びにタイヤ |
Country Status (9)
| Country | Link |
|---|---|
| US (1) | US10519254B2 (ja) |
| EP (1) | EP3260471A4 (ja) |
| JP (4) | JPWO2016133154A1 (ja) |
| KR (2) | KR20190039622A (ja) |
| CN (1) | CN107250166B (ja) |
| BR (1) | BR112017017631B1 (ja) |
| SG (1) | SG11201706702QA (ja) |
| TW (1) | TWI585114B (ja) |
| WO (1) | WO2016133154A1 (ja) |
Cited By (20)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2017197455A (ja) * | 2016-04-26 | 2017-11-02 | 信越化学工業株式会社 | 含窒素オルガノキシシラン化合物およびその製造方法 |
| WO2018034194A1 (ja) * | 2016-08-19 | 2018-02-22 | 旭化成株式会社 | 変性共役ジエン系重合体、ゴム組成物、及びタイヤ |
| WO2018034217A1 (ja) * | 2016-08-19 | 2018-02-22 | 旭化成株式会社 | 変性共役ジエン系重合体、その製造方法、ゴム組成物、タイヤ |
| JP2018028018A (ja) * | 2016-08-17 | 2018-02-22 | 旭化成株式会社 | 変性共役ジエン系重合体組成物、トレッド用ゴム組成物、及びタイヤ |
| WO2018186367A1 (ja) * | 2017-04-06 | 2018-10-11 | 株式会社ブリヂストン | ゴム組成物及びタイヤ |
| JP2018177894A (ja) * | 2017-04-06 | 2018-11-15 | 株式会社ブリヂストン | ゴム組成物及びタイヤ |
| KR20190092559A (ko) * | 2017-04-28 | 2019-08-07 | 아사히 가세이 가부시키가이샤 | 변성 공액 디엔계 중합체, 중합체 조성물 및 고무 조성물 |
| WO2019244850A1 (ja) * | 2018-06-18 | 2019-12-26 | 株式会社ブリヂストン | ゴム組成物およびタイヤ |
| JP2020012101A (ja) * | 2018-07-04 | 2020-01-23 | 旭化成株式会社 | 変性共役ジエン系重合体、変性共役ジエン系重合体組成物、及びゴム組成物 |
| JP2020059408A (ja) * | 2018-10-10 | 2020-04-16 | 株式会社ブリヂストン | タイヤ |
| WO2020196892A1 (ja) | 2019-03-28 | 2020-10-01 | Zsエラストマー株式会社 | ゴム組成物及びゴム組成物を製造する方法 |
| WO2021024811A1 (ja) * | 2019-08-06 | 2021-02-11 | 旭化成株式会社 | 共役ジエン系重合体、分岐化剤、共役ジエン系重合体の製造方法、油展共役ジエン系重合体、ゴム組成物、及びタイヤ |
| JP2021084932A (ja) * | 2019-11-26 | 2021-06-03 | 旭化成株式会社 | 共役ジエン系重合体組成物、及びタイヤ |
| EP3835325A1 (en) | 2019-12-12 | 2021-06-16 | Asahi Kasei Kabushiki Kaisha | Production method for modified conjugated diene-based polymer, modified conjugated diene-based polymer, rubber composition, production method for rubber composition, and production method for tire |
| KR20210075015A (ko) | 2019-12-12 | 2021-06-22 | 아사히 가세이 가부시키가이샤 | 분지화 공액 디엔계 중합체의 제조 방법, 분지화 공액 디엔계 중합체, 고무 조성물의 제조 방법 및 타이어의 제조 방법 |
| EP3845568A2 (en) | 2019-12-12 | 2021-07-07 | Asahi Kasei Kabushiki Kaisha | Production method for branched conjugated diene-based polymer, production method for rubber composition, production method for tire, branched conjugated diene-based polymer, and branched conjugated diene-based polymer composition |
| JP2022000519A (ja) * | 2017-03-07 | 2022-01-04 | 旭化成株式会社 | 変性共役ジエン系重合体、重合体組成物、及びゴム組成物 |
| US11339240B2 (en) | 2018-10-03 | 2022-05-24 | Asahi Kasei Kabushiki Kaisha | Conjugated diene-based polymer, branching agent, production method for conjugated diene-based polymer, extended conjugated diene-based polymer, rubber composition, and tire |
| US11377539B2 (en) | 2018-02-16 | 2022-07-05 | Sumitomo Chemical Company, Limited | Conjugated diene-based polymer, conjugated diene-based polymer composition, and method for producing conjugated diene-based polymer |
| EP4186911A1 (en) | 2021-11-30 | 2023-05-31 | Trinseo Europe GmbH | Amine-containing vinyldisiloxanes in the manufacture of elastomeric polymers |
Families Citing this family (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| SG11201706702QA (en) * | 2015-02-19 | 2017-09-28 | Asahi Chemical Ind | Modified conjugated diene-based polymer and production method therefor, rubber composition and tire |
| KR101909335B1 (ko) * | 2016-02-29 | 2018-10-17 | 주식회사 엘지화학 | 아자실란계 변성제 및 이를 이용한 변성 공액디엔계 중합체의 제조방법 |
| BR112019002831B1 (pt) * | 2016-08-19 | 2022-10-25 | Asahi Kasei Kabushiki Kaisha | Polímeros de dieno conjugado modificado, composição de borracha e pneu |
| KR20190038344A (ko) * | 2017-09-29 | 2019-04-08 | 주식회사 엘지화학 | 고무 조성물 |
| JP7280115B2 (ja) * | 2018-06-28 | 2023-05-23 | 旭化成株式会社 | 変性共役ジエン系重合体混合物の製造方法 |
| CN110684154B (zh) * | 2018-07-04 | 2022-05-17 | 旭化成株式会社 | 改性共轭二烯系聚合物、改性共轭二烯系聚合物组合物以及橡胶组合物 |
| JP7344709B2 (ja) * | 2018-08-23 | 2023-09-14 | 旭化成株式会社 | 変性共役ジエン系重合体組成物、ゴム組成物及びゴム組成物の製造方法 |
| JP7398901B2 (ja) * | 2018-08-28 | 2023-12-15 | 旭化成株式会社 | 変性共役ジエン系重合体組成物、ゴム組成物、及びゴム組成物の製造方法 |
| CN110872406B (zh) * | 2018-08-30 | 2022-04-12 | 旭化成株式会社 | 改性共轭二烯系聚合物组合物 |
| CN110872405B (zh) * | 2018-08-30 | 2022-04-12 | 旭化成株式会社 | 改性共轭二烯系聚合物组合物、橡胶组合物、橡胶组合物的制造方法以及轮胎 |
| CN110878151B (zh) * | 2018-09-05 | 2022-04-12 | 旭化成株式会社 | 橡胶组合物 |
| JP7315409B2 (ja) * | 2018-09-05 | 2023-07-26 | 旭化成株式会社 | ゴム組成物 |
| JP7357951B2 (ja) * | 2019-07-25 | 2023-10-10 | 三好化成株式会社 | 親水化無機粉体及び当該親水化無機粉体を配合した化粧料 |
| TW202116896A (zh) * | 2019-09-20 | 2021-05-01 | 日商可樂麗股份有限公司 | 橡膠組成物、輪胎用橡膠組成物及鞋底用橡膠組成物 |
| JP2021165370A (ja) * | 2020-04-03 | 2021-10-14 | 旭化成株式会社 | 共役ジエン系重合体、共役ジエン系重合体の製造方法、共役ジエン系重合体組成物、及びゴム組成物 |
| JP2021167407A (ja) * | 2020-04-08 | 2021-10-21 | 旭化成株式会社 | 共役ジエン系重合体及びその製造方法、並びにゴム組成物。 |
| WO2022024219A1 (ja) * | 2020-07-28 | 2022-02-03 | Jsr株式会社 | 重合体組成物、架橋重合体、及びタイヤ |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2009263537A (ja) * | 2008-04-25 | 2009-11-12 | Bridgestone Corp | 空気入りタイヤ |
| JP2013082843A (ja) * | 2011-10-12 | 2013-05-09 | Asahi Kasei Chemicals Corp | 変性共役ジエン系重合体の製造方法、変性共役ジエン系重合体、及び変性共役ジエン系重合体組成物、及びタイヤ |
| WO2013125614A1 (ja) * | 2012-02-22 | 2013-08-29 | 住友ゴム工業株式会社 | タイヤ用ゴム組成物及び空気入りタイヤ |
| US20150045474A1 (en) * | 2013-08-01 | 2015-02-12 | Lg Chem, Ltd. | Modified conjugated diene polymer and method for preparing the same |
Family Cites Families (24)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN1105125C (zh) * | 1997-11-27 | 2003-04-09 | 台橡股份有限公司 | 适用于轮胎胎面的橡胶 |
| JP3895446B2 (ja) | 1997-12-26 | 2007-03-22 | 株式会社ブリヂストン | 重合体の製造方法、得られた重合体、及びそれを用いたゴム組成物 |
| EP1153972B2 (en) | 1999-09-27 | 2012-01-11 | Asahi Kasei Kabushiki Kaisha | Rubber composition |
| JP4129619B2 (ja) | 2001-09-27 | 2008-08-06 | Jsr株式会社 | 共役ジオレフィン(共)重合ゴム、該(共)重合ゴムの製造方法、ゴム組成物およびタイヤ |
| JP2005290355A (ja) | 2004-03-11 | 2005-10-20 | Sumitomo Chemical Co Ltd | 変性ジエン系重合体ゴム及びその製造方法 |
| CN101107294B (zh) | 2005-01-14 | 2011-05-25 | 株式会社普利司通 | 官能化聚合物和从其改进的轮胎 |
| JP5576020B2 (ja) * | 2005-09-22 | 2014-08-20 | 旭化成ケミカルズ株式会社 | 共役ジエン系重合体およびその製造方法 |
| JP5568860B2 (ja) | 2006-03-31 | 2014-08-13 | 日本ゼオン株式会社 | タイヤ用ゴム組成物の製造方法、タイヤ用ゴム組成物、及びタイヤ |
| JP2008285558A (ja) * | 2007-05-16 | 2008-11-27 | Asahi Kasei Chemicals Corp | 油展共役ジエン系重合体組成物 |
| US8425784B2 (en) * | 2007-11-05 | 2013-04-23 | University Of Kansas | Ozonolysis reactions in liquid CO2 and CO2-expanded solvents |
| CN102361886B (zh) * | 2009-05-13 | 2013-07-03 | 旭化成化学株式会社 | 支链状共轭二烯系聚合物的制造方法 |
| EP2559709B1 (en) * | 2010-04-16 | 2016-01-13 | Asahi Kasei Chemicals Corporation | Process for producing modified conjugated diene polymer, modified conjugated diene polymer, and composition of modified conjugated diene polymer |
| JP5761185B2 (ja) * | 2010-06-08 | 2015-08-12 | Jsr株式会社 | 変性共役ジエン系ゴム、その製造方法、及びゴム組成物 |
| MY168416A (en) * | 2011-08-26 | 2018-11-09 | Asahi Kasei Chemicals Corp | Method for producing modified conjugated diene polymer, modified conjugated diene polymer, modified conjugated diene polymer composition, rubber composition and tire |
| IN2014CN01721A (ja) | 2011-09-08 | 2015-05-29 | Asahi Kasei Chemicals Corp | |
| JP5971916B2 (ja) * | 2011-10-12 | 2016-08-17 | 旭化成株式会社 | 変性共役ジエン系重合体、その製造方法、変性共役ジエン系重合体組成物、及びタイヤ |
| JP5850699B2 (ja) * | 2011-10-19 | 2016-02-03 | 旭化成ケミカルズ株式会社 | ベーストレッド用ゴム組成物 |
| KR101455508B1 (ko) * | 2012-02-06 | 2014-10-27 | 주식회사 엘지화학 | 변성 공액 디엔계 중합체 및 이의 제조방법 |
| JP6166066B2 (ja) | 2013-03-13 | 2017-07-19 | 旭化成株式会社 | 変性共役ジエン系重合体組成物、トレッド、サイドウォール及びタイヤ |
| CN104271609B (zh) * | 2013-04-25 | 2016-11-09 | Lg化学株式会社 | 连续制备改性共轭二烯聚合物的方法,由该方法得到的聚合物和包含该聚合物的橡胶组合物 |
| US9988515B2 (en) | 2013-04-25 | 2018-06-05 | Lg Chem, Ltd. | Method for preparing conjugated diene polymer, composition comprising the same and tire comprising the composition |
| JP6516462B2 (ja) | 2013-12-13 | 2019-05-22 | 旭化成株式会社 | 変性共役ジエン系重合体の製造方法、変性共役ジエン系重合体、及び変性共役ジエン系重合体組成物 |
| JP2016079217A (ja) | 2014-10-10 | 2016-05-16 | 旭化成ケミカルズ株式会社 | 変性共役ジエン系重合体の製造方法、変性共役ジエン系重合体、及び変性共役ジエン系重合体組成物 |
| SG11201706702QA (en) | 2015-02-19 | 2017-09-28 | Asahi Chemical Ind | Modified conjugated diene-based polymer and production method therefor, rubber composition and tire |
-
2016
- 2016-02-18 SG SG11201706702QA patent/SG11201706702QA/en unknown
- 2016-02-18 KR KR1020197009831A patent/KR20190039622A/ko not_active Application Discontinuation
- 2016-02-18 JP JP2017500727A patent/JPWO2016133154A1/ja not_active Ceased
- 2016-02-18 CN CN201680010513.8A patent/CN107250166B/zh active Active
- 2016-02-18 KR KR1020177021440A patent/KR101968849B1/ko active IP Right Grant
- 2016-02-18 US US15/551,711 patent/US10519254B2/en active Active
- 2016-02-18 BR BR112017017631-9A patent/BR112017017631B1/pt active IP Right Grant
- 2016-02-18 WO PCT/JP2016/054687 patent/WO2016133154A1/ja active Application Filing
- 2016-02-18 EP EP16752540.1A patent/EP3260471A4/en active Pending
- 2016-02-19 TW TW105105014A patent/TWI585114B/zh active
-
2017
- 2017-10-27 JP JP2017208579A patent/JP6501847B2/ja active Active
-
2018
- 2018-09-14 JP JP2018172679A patent/JP6796903B2/ja active Active
-
2020
- 2020-11-13 JP JP2020189265A patent/JP2021028398A/ja active Pending
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2009263537A (ja) * | 2008-04-25 | 2009-11-12 | Bridgestone Corp | 空気入りタイヤ |
| JP2013082843A (ja) * | 2011-10-12 | 2013-05-09 | Asahi Kasei Chemicals Corp | 変性共役ジエン系重合体の製造方法、変性共役ジエン系重合体、及び変性共役ジエン系重合体組成物、及びタイヤ |
| WO2013125614A1 (ja) * | 2012-02-22 | 2013-08-29 | 住友ゴム工業株式会社 | タイヤ用ゴム組成物及び空気入りタイヤ |
| US20150045474A1 (en) * | 2013-08-01 | 2015-02-12 | Lg Chem, Ltd. | Modified conjugated diene polymer and method for preparing the same |
Non-Patent Citations (1)
| Title |
|---|
| See also references of EP3260471A1 * |
Cited By (43)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2017197455A (ja) * | 2016-04-26 | 2017-11-02 | 信越化学工業株式会社 | 含窒素オルガノキシシラン化合物およびその製造方法 |
| JP2018028018A (ja) * | 2016-08-17 | 2018-02-22 | 旭化成株式会社 | 変性共役ジエン系重合体組成物、トレッド用ゴム組成物、及びタイヤ |
| US11091609B2 (en) | 2016-08-19 | 2021-08-17 | Asahi Kasei Kabushiki Kaisha | Modified conjugated diene-based polymer, production method thereof, rubber composition and tire |
| WO2018034194A1 (ja) * | 2016-08-19 | 2018-02-22 | 旭化成株式会社 | 変性共役ジエン系重合体、ゴム組成物、及びタイヤ |
| WO2018034217A1 (ja) * | 2016-08-19 | 2018-02-22 | 旭化成株式会社 | 変性共役ジエン系重合体、その製造方法、ゴム組成物、タイヤ |
| US11414503B2 (en) | 2016-08-19 | 2022-08-16 | Asahi Kasei Kabushiki Kaisha | Modified conjugated diene-based polymer, rubber composition, and tire |
| JPWO2018034217A1 (ja) * | 2016-08-19 | 2019-06-13 | 旭化成株式会社 | 変性共役ジエン系重合体、その製造方法、ゴム組成物、タイヤ |
| JPWO2018034194A1 (ja) * | 2016-08-19 | 2019-06-13 | 旭化成株式会社 | 変性共役ジエン系重合体、ゴム組成物、及びタイヤ |
| JP7335928B2 (ja) | 2017-03-07 | 2023-08-30 | 旭化成株式会社 | 変性共役ジエン系重合体、重合体組成物、及びゴム組成物 |
| US11292862B2 (en) | 2017-03-07 | 2022-04-05 | Asahi Kasei Kabushiki Kaisha | Modified conjugated diene-based polymer, polymer composition, and rubber composition |
| JP2022000519A (ja) * | 2017-03-07 | 2022-01-04 | 旭化成株式会社 | 変性共役ジエン系重合体、重合体組成物、及びゴム組成物 |
| CN110536922A (zh) * | 2017-04-06 | 2019-12-03 | 株式会社普利司通 | 橡胶组合物和轮胎 |
| WO2018186367A1 (ja) * | 2017-04-06 | 2018-10-11 | 株式会社ブリヂストン | ゴム組成物及びタイヤ |
| JPWO2018186367A1 (ja) * | 2017-04-06 | 2020-05-14 | 株式会社ブリヂストン | ゴム組成物及びタイヤ |
| JP2018177894A (ja) * | 2017-04-06 | 2018-11-15 | 株式会社ブリヂストン | ゴム組成物及びタイヤ |
| EP3608362A4 (en) * | 2017-04-06 | 2020-11-25 | Bridgestone Corporation | COMPOSITION OF RUBBER AND TIRE |
| CN110506062A (zh) * | 2017-04-28 | 2019-11-26 | 旭化成株式会社 | 改性共轭二烯系聚合物、聚合物组合物以及橡胶组合物 |
| EP3617237A4 (en) * | 2017-04-28 | 2020-05-06 | Asahi Kasei Kabushiki Kaisha | MODIFIED CONJUGATED DIENE POLYMER, POLYMER COMPOSITION AND RUBBER COMPOSITION |
| KR102201044B1 (ko) * | 2017-04-28 | 2021-01-11 | 아사히 가세이 가부시키가이샤 | 변성 공액 디엔계 중합체, 중합체 조성물 및 고무 조성물 |
| KR20190092559A (ko) * | 2017-04-28 | 2019-08-07 | 아사히 가세이 가부시키가이샤 | 변성 공액 디엔계 중합체, 중합체 조성물 및 고무 조성물 |
| CN110506062B (zh) * | 2017-04-28 | 2022-02-22 | 旭化成株式会社 | 改性共轭二烯系聚合物、聚合物组合物以及橡胶组合物 |
| US11225534B2 (en) | 2017-04-28 | 2022-01-18 | Asahi Kasei Kabushiki Kaisha | Modified conjugated diene-based polymer, polymer composition, and rubber composition |
| US11377539B2 (en) | 2018-02-16 | 2022-07-05 | Sumitomo Chemical Company, Limited | Conjugated diene-based polymer, conjugated diene-based polymer composition, and method for producing conjugated diene-based polymer |
| WO2019244850A1 (ja) * | 2018-06-18 | 2019-12-26 | 株式会社ブリヂストン | ゴム組成物およびタイヤ |
| JP7405521B2 (ja) | 2018-07-04 | 2023-12-26 | 旭化成株式会社 | 変性共役ジエン系重合体、変性共役ジエン系重合体組成物、及びゴム組成物 |
| JP2020012101A (ja) * | 2018-07-04 | 2020-01-23 | 旭化成株式会社 | 変性共役ジエン系重合体、変性共役ジエン系重合体組成物、及びゴム組成物 |
| US11339240B2 (en) | 2018-10-03 | 2022-05-24 | Asahi Kasei Kabushiki Kaisha | Conjugated diene-based polymer, branching agent, production method for conjugated diene-based polymer, extended conjugated diene-based polymer, rubber composition, and tire |
| JP2020059408A (ja) * | 2018-10-10 | 2020-04-16 | 株式会社ブリヂストン | タイヤ |
| JP7081879B2 (ja) | 2018-10-10 | 2022-06-07 | 株式会社ブリヂストン | タイヤ |
| WO2020196892A1 (ja) | 2019-03-28 | 2020-10-01 | Zsエラストマー株式会社 | ゴム組成物及びゴム組成物を製造する方法 |
| KR20220013407A (ko) * | 2019-08-06 | 2022-02-04 | 아사히 가세이 가부시키가이샤 | 공액 디엔계 중합체, 분지화제, 공액 디엔계 중합체의 제조 방법, 유전 공액 디엔계 중합체, 고무 조성물 및 타이어 |
| WO2021024811A1 (ja) * | 2019-08-06 | 2021-02-11 | 旭化成株式会社 | 共役ジエン系重合体、分岐化剤、共役ジエン系重合体の製造方法、油展共役ジエン系重合体、ゴム組成物、及びタイヤ |
| JPWO2021024811A1 (ja) * | 2019-08-06 | 2021-02-11 | ||
| JP7343589B2 (ja) | 2019-08-06 | 2023-09-12 | 旭化成株式会社 | 共役ジエン系重合体、分岐化剤、共役ジエン系重合体の製造方法、油展共役ジエン系重合体、ゴム組成物、及びタイヤ |
| KR102684932B1 (ko) * | 2019-08-06 | 2024-07-16 | 아사히 가세이 가부시키가이샤 | 공액 디엔계 중합체, 분지화제, 공액 디엔계 중합체의 제조 방법, 유전 공액 디엔계 중합체, 고무 조성물 및 타이어 |
| JP2021084932A (ja) * | 2019-11-26 | 2021-06-03 | 旭化成株式会社 | 共役ジエン系重合体組成物、及びタイヤ |
| JP7356881B2 (ja) | 2019-11-26 | 2023-10-05 | 旭化成株式会社 | 共役ジエン系重合体組成物、及びタイヤ |
| KR20210075015A (ko) | 2019-12-12 | 2021-06-22 | 아사히 가세이 가부시키가이샤 | 분지화 공액 디엔계 중합체의 제조 방법, 분지화 공액 디엔계 중합체, 고무 조성물의 제조 방법 및 타이어의 제조 방법 |
| EP3835325A1 (en) | 2019-12-12 | 2021-06-16 | Asahi Kasei Kabushiki Kaisha | Production method for modified conjugated diene-based polymer, modified conjugated diene-based polymer, rubber composition, production method for rubber composition, and production method for tire |
| EP3845568A2 (en) | 2019-12-12 | 2021-07-07 | Asahi Kasei Kabushiki Kaisha | Production method for branched conjugated diene-based polymer, production method for rubber composition, production method for tire, branched conjugated diene-based polymer, and branched conjugated diene-based polymer composition |
| US11884760B2 (en) | 2019-12-12 | 2024-01-30 | Asahi Kasei Kabushiki Kaisha | Production method for branched conjugated diene-based polymer, production method for rubber composition, production method for tire, branched conjugated diene-based polymer, and branched conjugated diene-based polymer composition |
| EP4186911A1 (en) | 2021-11-30 | 2023-05-31 | Trinseo Europe GmbH | Amine-containing vinyldisiloxanes in the manufacture of elastomeric polymers |
| WO2023099462A1 (en) | 2021-11-30 | 2023-06-08 | Trinseo Europe Gmbh | Amine-containing vinyldisiloxanes in the manufacture of elastomeric polymers |
Also Published As
| Publication number | Publication date |
|---|---|
| SG11201706702QA (en) | 2017-09-28 |
| JPWO2016133154A1 (ja) | 2017-04-27 |
| TW201638121A (zh) | 2016-11-01 |
| TWI585114B (zh) | 2017-06-01 |
| EP3260471A4 (en) | 2018-06-20 |
| KR101968849B1 (ko) | 2019-04-12 |
| KR20170102321A (ko) | 2017-09-08 |
| EP3260471A1 (en) | 2017-12-27 |
| JP2018016814A (ja) | 2018-02-01 |
| BR112017017631B1 (pt) | 2022-08-02 |
| JP2021028398A (ja) | 2021-02-25 |
| KR20190039622A (ko) | 2019-04-12 |
| JP2019002028A (ja) | 2019-01-10 |
| CN107250166B (zh) | 2021-09-24 |
| US10519254B2 (en) | 2019-12-31 |
| US20180066076A1 (en) | 2018-03-08 |
| CN107250166A (zh) | 2017-10-13 |
| BR112017017631A2 (ja) | 2018-05-08 |
| JP6796903B2 (ja) | 2020-12-09 |
| JP6501847B2 (ja) | 2019-04-17 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6501847B2 (ja) | 変性共役ジエン系重合体及びその製造方法、ゴム組成物、並びにタイヤ | |
| KR102143416B1 (ko) | 변성 공액 디엔계 중합체, 그의 제조 방법, 고무 조성물, 타이어 | |
| JP5911524B2 (ja) | 変性共役ジエン系重合体、及び変性共役ジエン系重合体組成物 | |
| WO2016199779A1 (ja) | 変性共役ジエン系重合体及びその製造方法、ゴム組成物、並びにタイヤ | |
| TWI648294B (zh) | Modified conjugated diene polymer, rubber composition, and tire | |
| JP5705120B2 (ja) | 変性共役ジエン系重合体の製造方法、変性共役ジエン系重合体、及び変性共役ジエン系重合体組成物 | |
| JP5898212B2 (ja) | 変性共役ジエン系重合体の製造方法、変性共役ジエン系重合体、変性共役ジエン系重合体組成物、ゴム組成物、及びタイヤ | |
| JP6769780B2 (ja) | 変性共役ジエン系重合体及びそのゴム組成物、並びにタイヤ | |
| KR102141469B1 (ko) | 변성 공액 디엔계 중합체 및 그의 고무 조성물, 그리고 타이어 | |
| JP2018028018A (ja) | 変性共役ジエン系重合体組成物、トレッド用ゴム組成物、及びタイヤ | |
| JP2016079217A (ja) | 変性共役ジエン系重合体の製造方法、変性共役ジエン系重合体、及び変性共役ジエン系重合体組成物 | |
| JP2018002986A (ja) | 変性共役ジエン系重合体組成物、サイドウォール用ゴム組成物、及びタイヤ | |
| WO2018164053A1 (ja) | 変性共役ジエン系重合体、重合体組成物、及びゴム組成物 | |
| JP7381725B2 (ja) | 水添共役ジエン系重合体、水添共役ジエン系重合体組成物、及びゴム組成物並びに水添共役ジエン系重合体の製造方法 | |
| JP7343589B2 (ja) | 共役ジエン系重合体、分岐化剤、共役ジエン系重合体の製造方法、油展共役ジエン系重合体、ゴム組成物、及びタイヤ | |
| JP2013082794A (ja) | 変性共役ジエン系重合体組成物 | |
| WO2020070961A1 (ja) | 共役ジエン系重合体、分岐化剤、共役ジエン系重合体の製造方法、伸展共役ジエン系重合体、ゴム組成物、及びタイヤ | |
| JP7312638B2 (ja) | 変性共役ジエン系重合体組成物の製造方法 | |
| WO2018199267A1 (ja) | 変性共役ジエン系重合体、重合体組成物、及びゴム組成物 | |
| JP2019131723A (ja) | 変性共役ジエン系重合体組成物及び製造方法、並びにタイヤ |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 16752540 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 2017500727 Country of ref document: JP Kind code of ref document: A |
|
| ENP | Entry into the national phase |
Ref document number: 20177021440 Country of ref document: KR Kind code of ref document: A |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 15551711 Country of ref document: US |
|
| REEP | Request for entry into the european phase |
Ref document number: 2016752540 Country of ref document: EP |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| REG | Reference to national code |
Ref country code: BR Ref legal event code: B01A Ref document number: 112017017631 Country of ref document: BR |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 11201706702Q Country of ref document: SG |
|
| ENP | Entry into the national phase |
Ref document number: 112017017631 Country of ref document: BR Kind code of ref document: A2 Effective date: 20170817 |