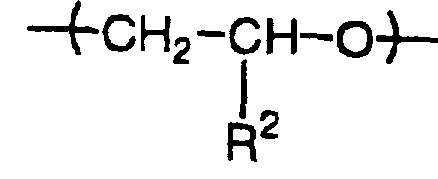WO1997042251A1 - Cross-linked solid polyelectrolyte and use thereof - Google Patents
Cross-linked solid polyelectrolyte and use thereof Download PDFInfo
- Publication number
- WO1997042251A1 WO1997042251A1 PCT/JP1997/001522 JP9701522W WO9742251A1 WO 1997042251 A1 WO1997042251 A1 WO 1997042251A1 JP 9701522 W JP9701522 W JP 9701522W WO 9742251 A1 WO9742251 A1 WO 9742251A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- group
- copolymer
- epoxy
- ion
- monomer
- Prior art date
Links
Classifications
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/056—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes
- H01M10/0564—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes the electrolyte being constituted of organic materials only
- H01M10/0565—Polymeric materials, e.g. gel-type or solid-type
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G65/00—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule
- C08G65/02—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule from cyclic ethers by opening of the heterocyclic ring
- C08G65/04—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule from cyclic ethers by opening of the heterocyclic ring from cyclic ethers only
- C08G65/06—Cyclic ethers having no atoms other than carbon and hydrogen outside the ring
- C08G65/14—Unsaturated oxiranes
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G65/00—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule
- C08G65/02—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule from cyclic ethers by opening of the heterocyclic ring
- C08G65/04—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule from cyclic ethers by opening of the heterocyclic ring from cyclic ethers only
- C08G65/22—Cyclic ethers having at least one atom other than carbon and hydrogen outside the ring
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G65/00—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule
- C08G65/02—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule from cyclic ethers by opening of the heterocyclic ring
- C08G65/04—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule from cyclic ethers by opening of the heterocyclic ring from cyclic ethers only
- C08G65/22—Cyclic ethers having at least one atom other than carbon and hydrogen outside the ring
- C08G65/24—Epihalohydrins
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G65/00—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule
- C08G65/02—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule from cyclic ethers by opening of the heterocyclic ring
- C08G65/32—Polymers modified by chemical after-treatment
- C08G65/329—Polymers modified by chemical after-treatment with organic compounds
- C08G65/336—Polymers modified by chemical after-treatment with organic compounds containing silicon
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M6/00—Primary cells; Manufacture thereof
- H01M6/14—Cells with non-aqueous electrolyte
- H01M6/18—Cells with non-aqueous electrolyte with solid electrolyte
- H01M6/181—Cells with non-aqueous electrolyte with solid electrolyte with polymeric electrolytes
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/052—Li-accumulators
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/10—Energy storage using batteries
Definitions
- the present invention relates to a crosslinkable polyether copolymer, a crosslinked body of the polymer, and a crosslinked polymer solid electrolyte.
- the present invention relates to a solid polymer electrolyte suitable as a material for an electrochemical device such as a battery, a capacitor, and a sensor.
- electrolytes that make up electrochemical devices such as batteries, capacitors, and sensors have been used in the form of solutions or pastes because of their ionic conductivity.
- problems have been pointed out, such as limitations on ultra-small and thin devices.
- solid electrolytes such as inorganic crystalline materials, inorganic glasses, and organic polymer materials have been proposed.
- Organic polymer materials generally have excellent processability and moldability, and the resulting solid electrolyte has flexibility and bendability, which increases the degree of freedom in the design of applied devices. Progress is expected. However, at present, it is inferior to other materials in terms of ion conductivity.
- the polyether copolymer having an oligoquinone ethylene side chain described in Japanese Patent Application No. 7-109616 of the present applicant shows excellent ion conductivity at room temperature (for example, 30 ° C), but has a crosslinked structure. Since it does not have such a structure, if the operating temperature is high (for example, 60 ° C), it will cause inconvenience due to plastic deformation. For example, when used in a thin battery, a short circuit between the positive electrode and the negative electrode is a concern.
- An object of the present invention is to provide an L-solid debris which has excellent ionic conductivity and has plastic deformation or fluidity even at high temperatures.
- Another object of the present invention is to provide a polymer that provides the above solid electrolyte.
- the present invention is a.
- R 1 is an alkyl group having 1 to 12 carbon atoms, an alkyl group having 2 to 8 carbon atoms, a cycloalkyl group having 3 to 8 carbon atoms, an aryl group having 6 to 14 carbon atoms, and 7 carbon atoms.
- To 12 are aralkyl groups and tetrahydrobiranyl groups.
- (C) a polyether copolymer having 0.005 to 15 mol% of a repeating unit derived from a monomer having one epoxy group and at least one reactive functional group, wherein the number average molecular weight is A polyether copolymer having a glass transition temperature of not more than 60 ° C and a heat of fusion of not more than 70 J measured by a differential scanning calorimeter (DSC).
- DSC differential scanning calorimeter
- the present invention also provides a crosslinked product obtained by crosslinking the copolymer.
- the present invention provides a polymer solid electrolyte comprising the crosslinked body and an electrolyte salt compound.
- the present invention provides a battery using the solid polymer electrolyte. Detailed description of the invention
- the repeating unit (C) may be derived from a monomer of the formula (I) I-1) or (I I I-2).
- R 2 and R 3 are reactive functional group-containing groups.
- the polymer of the present invention comprises (A) a repeating unit derived from a monomer of formula (I):
- R 1 is an alkyl group having 1 to 12 carbon atoms, an alkenyl group having 2 to 8 carbon atoms, a cycloalkyl group having 3 to 8 carbon atoms, an aryl group having 6 to 14 carbon atoms, and 7 to 7 carbon atoms. It is a group selected from 12 aralkyl groups and tetrahydrobiranyl group.
- (C) a repeating unit derived from a monomer having one epoxy group and at least one reactive functional group
- the repeating unit (C) derived from the monomer of the formula (III-1-1) or (III-2) is represented by the formula (II-1-1) or (III'-12):
- R 2 and R 3 are reactive functional group-containing groups.
- the reactive functional group in the structural unit (C) is preferably (a) a reactive gayne group, (b) an epoxy group, (c) an ethylenically unsaturated group, or (d) a halogen atom.
- the polymerization method of the polyether copolymer having a side chain capable of forming a bridge according to the present invention is the same as the method described in JP-A-63-154736 and JP-A-62-169823 of the present applicant. It is done.
- the polymerization reaction can be performed as follows. Using a catalyst system mainly composed of organic aluminum, a catalyst system mainly composed of organic zinc, a catalyst system composed of an organic tin-ester phosphate condensate, etc., as a catalyst for ring-opening polymerization, each monomer is used in the presence or absence of a solvent. under a reaction temperature 10 to 80 e C, Polje Ichite alcohol copolymer is obtained by reacting under stirring.
- an organotin-phosphate ester condensate catalyst system is particularly preferred in view of the degree of polymerization or the properties of the copolymer to be produced. Reactive functional groups do not react in the polymerization reaction, copolymerization with reactive functional groups The body is obtained.
- the molar ratio of the repeating unit (A), the repeating unit (B) and the repeating unit (C) is (A) 1 to 98 mol%, preferably 3 to 98 mol%. (B) 95-1 mol%, preferably 95-1 mol%, for example 90-5 mol%, and (C) 0.005-10 mol%, preferably 0.01-5 mol%, For example, it is 0.05 to 5 mol%. If the content of the repeating unit (B) exceeds 95 mol%, the glass transition temperature will increase and the oxishethylene chain will be crystallized, and as a result, the ion conductivity of the solid electrolyte will be significantly deteriorated.
- the ion conductivity is improved by lowering the crystallinity of polyethylene oxide.However, in the case of the polyether copolymer of the present invention, the effect of improving the ion conductivity is remarkably large. all right.
- the molar ratio of the repeating unit (C) is less than 0.005 mol%, the copolymer cannot be sufficiently crosslinked, and it is difficult to obtain a solid electrolyte in a high temperature region (for example, 60 ° C). Becomes If the molar ratio of the repeating unit (C) is as much as 15 mol%, film formation becomes impossible.
- the glass transition temperature and the calorific value of the polyether copolymer were measured by a differential scanning calorimeter (DSC).
- the glass transition temperature of the polyether copolymer is at most 160 ° C, preferably at most 63 eC , for example, at most 65 ° C.
- the heat of fusion of the polyether copolymer is 70 JZg or less, for example, 60 J / g or less, particularly 50 JZg or less.
- the polyether copolymer of the present invention may be any of a block copolymer and a random copolymer. Random copolymers are preferred because they have a greater effect of lowering the crystallinity of polyethylene oxide.
- the polyether copolymer of the present invention has a reactivity capable of forming an oligoxechylene side chain and a bridge. It is a polyether copolymer having a side chain containing a functional group.
- Tel copolymers are usually terpolymers formed from three types of monomers, but may be copolymers formed from four or more types of monomers.
- the monomer having a reactive gay group forming the repeating unit (C) has the formula CHI-a-1):
- R 2 is a reactive gayne-containing group.
- R 3 is a reactive gayne-containing group.
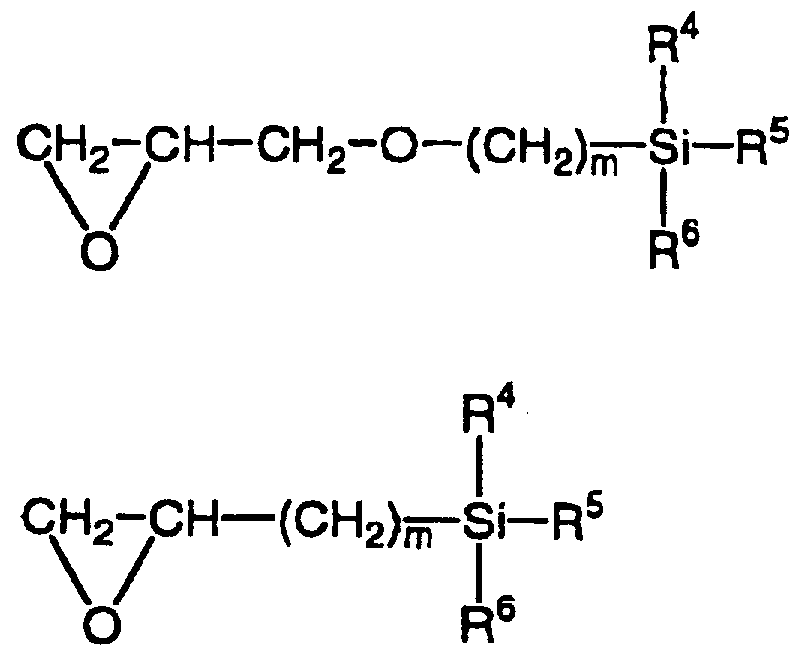
- the reactive gayne group-containing monomer represented by Ia-1) is preferably a compound represented by (III-1a-1-11) or (III-1a-1-2). Even things.
- the reactive gay group-containing monomer represented by the formula (II-1a-2) is preferably a compound represented by the formula (II-1a-2-1).
- R 4 , R 5 and R e are different even if they are the same. However, at least one is an alkoxy group and the rest is an alkyl group. m represents 1 to 6.
- Examples of the monomer represented by the formula (III-a-1-1) include 1-glycidoxymethyltrimethoxin silane, 1-glycidoxymethylmethyldimethoxin lan, 2-glindoxyshethyltrimethoxin lan, Glycidoxyshethyl methyldimethoxysilane, 3-glycidoxypropylmethyldimethoxysilane, 3-glycidoxypropyltrimethoxane, 4-glycidoxybutyl Examples include methyldimethoxysilane, 4-grindoxybutylmethyltrimethoxyquinsilane, 6-glindoquinhexylmethyldimethoxane lan, 6-glindoquinhexylmethyltrimethoxysilane and the like.
- Examples of the monomer represented by the formula (III-a-1-2) include 3- (1,2-epoxy) propyltrimethoxysilane, 3- (1.2-epoxy) propylmethyldimethoxysilane, 3- (1,2- Epoxy) propyldimethylmethoxysilane, 4- (1,2-epoxy) butyltrimethoxysilane, 4- (1,2-epochine) butylmethyldimethoxysilane, 5- (1,2-epochin pentyltrimethoxysilane, 5- (1, 21-epoxy) Pentylmethyldimethoxysilane, 6- (1,2-epoxy) hexyltrimethoxysilane, 6- (1.2-epoxy) hexylmethyldimethoxysilane and the like.
- Examples of the monomer represented by the formula (III-a-2-l) include 1- (3,4-epoxycyclohexyl) methyltrimethoxine lan, 1- (3,4-epoxycyclohexyl) methyl Methyldimethoxysilane, 2- (3,4-epoxycyclohexyl) ethyl limetoxin orchid, 2- (3,4-epoxycyclohexyl) ethylmethyldimethoxysilane, 3- (3,4-epoxycyclohexyl) Toxin orchid, 3- (3,4-epoxycyclohexyl) propylmethyl Dimethoxin orchid, 4- (3,4-epoxycyclohexyl) butyltrimethyoxysilane, 4- (3,4-epoxycyclohexyl) butylmethyldimethyl Toxisilane and the like can be mentioned.
- 3-glycidoxypropyl trimethoxane 3-glycidoxypropyl methyl dimethoxysilane
- 4- (1,2-epoxy) butyl trimethoxysilane 4- (1,2-epoxy) butyl trimethoxysilane
- 5- (1,2-epoxy) pentyltrime Toxicylane 2- (3,4-epoxycyclohexyl) ethyltrimethoxysilane
- 2- (3,4-epoxycyclohexyl) ethyltrimethoxysilane Particularly preferred.
- a monomer having two epoxy groups forming a repeating unit (C) has the formula (III-b):
- R 7 is a divalent organic group.
- a ⁇ and A 2 are hydrogen or a methyl group
- Ph is phenylene
- m is a number from 0 to: L 2.
- the monomer having two epoxy groups is represented by the following formula (I I I-b-1), (I I I), (I I), (I I), (I I), (I I), (I I), (I I), (I I), (I I), (I I), (I I), (I I), (I I), (I I), (I I), (I I), (I I), (I I), (I I), (I I), (I I), (I I), (I I I-b-1), (I I),
- the monomers represented by (III-b-1) include 2,3-epoxypropyl-2 ', 3'-epoxy-2'-methylpropyl ether, ethylene glycol-2.3-epoxypropyl-2', 3'-Epoxy-2'-methylpropyl ether; and diethylene glycol-2,3-epoxypropyl-2'.3'-epoxy-2'-methylpropyl ether.
- the monomers represented by the formula (III-b-2) include 2-methyl-1.2.3, 4-diepoxybutane, 2-methinole-1.2.4.5-diepoxypentane, and 2-methinole-1,2 , 5.6-diepoxyhexane and the like.
- the monomers represented by the formula (III-b-3) include hydroquinone-2.3-epoxypropyl-2 ', 3'-epoxy-2'-methylpropyl ether, and catechol-2.3-epoxypropyl-2', 3'-epoxy-2'-methylpropyl ether and the like.
- 2,3-epoxypropyl-2 ', 3'-epoxy-2'-methylpropylether, and ethylene glycol-2.3-epoxypropyl-2', 3'-epoxy-2'-methylpropylether Is preferred.
- the monomer having an ethylenically unsaturated group forming the repeating unit (C) is Formula (III-c)
- Re is a group having an ethylenically unsaturated group.
- Examples of the ethylenically unsaturated group-containing monomer include arylglycidyl ether,
- aryl glycidyl ether, glycidyl acrylate, and daricidyl methacrylate are used.
- the monomer (C) having a halogen atom is represented by the formula (I I I—d):
- R 9 is a group having at least one halogen atom. ] Is preferable.
- Examples of monomers having a halogen atom include
- X is a halogen atom, especially bromine (Br) or iodine (I). ].
- the degree of polymerization n of the quinethylene unit in the side chain is preferably 1 to 12, for example, 1 to 6. If the degree of polymerization n exceeds 12, the ionic conductivity of the obtained solid electrolyte decreases, which is not preferable.
- R 1 may be a methyl group, an ethyl group, a propyl group, a butyl group, a ventil group, a hexyl group, an aryl group, or a cyclohexyl group.
- the polyether copolymer has a number average molecular weight of 50,000 to 2,000,000, preferably 100,000 to 200,000, in order to obtain processability, moldability, mechanical strength, and flexibility. If the number average molecular weight is less than 50,000, it is necessary to increase the crosslink density in order to maintain mechanical strength and to prevent flow at high temperatures, and the ionic conductivity of the obtained electrolyte decreases. More than 2 million This causes problems in workability and formability.
- the copolymer can be bridged by a reaction between the reactive gay group and water.
- tin compounds such as dibutyltin dilaurate, dibutylsumarate, dibutyltin diacetate, tin octoate, dibutyltin acetyl acetate, titanium compounds such as tetrabutyl titanate and tetrapropyl titanate, aluminum trisacetyl acetate, Organometallic compounds such as aluminum compounds such as aluminum such as aluminum triacetyl acetate and diisopropoxy aluminum acetate acetate; or butylamine, octylamine, laurylamine, dibutylamine, monoethanolamine Amine, diethanolamine, triethanolamine, diethylenetriamine, triethylenetetraamine, cyclohexylamine, benzylamine, Ruami knob opening Piruamin, Guanin may be used etc. amine compounds such as Jifuwe two Ruguanin as a catalyst.
- polyamines examples include diethylenetriamine, dibrovirenetriamine, triethylenetetramine, tetraethylenepentamine, dimethylaminopropylamine, acetylaminopropylamine, dibutylaminobutyramine, hexamethylenediamine, Aliphatic polyamines such as N-aminoethylpiperazine, bis-aminoprovirpiperazine, trimethylhexamethylenediamine, and diphthalic dihydrazide, 4,4'-diaminodiphenyl ether, diaminodiphenyl sulfone, m-phenyl And aromatic polyamines such as penylenediamine, 2,4-toluylenediamine, m-tolylylenediamine, 0-tolylylenediamine and xylylenediamine. Polyamine Although the amount of addition depends on the type of polyamine, it is usually in the range of 0.1 to 10% by weight of the whole composition.
- the acid anhydrides include maleic anhydride, dodecenyl succinic anhydride, chlorendexic anhydride, phthalic anhydride, pyromellitic anhydride, hexahydrohydrophthalic anhydride, methylhexahydrophthalic anhydride, and tetramethylene maleic anhydride. And tetrahydrophthalic anhydride, methyltetrahydrophthalic anhydride, trimellitic anhydride and the like.
- the amount of the acid anhydride varies depending on the type of the acid anhydride, but is usually in the range of 0.1 to 10% by weight of the whole composition. Accelerators may be used for these crosslinks.
- a radical initiator selected from organic peroxides, azo compounds and the like, and active energy rays such as ultraviolet rays and electron beams are used.
- a crosslinker having a hydrogen hydride can also be used.
- Organic peroxides such as ketone peroxides, baroxy ketals, hydroperoxides, dialkyl peroxides, disilver oxides, and peroxyesters, etc., which are usually used for construction purposes, are used. These can be listed as: methylethyl ketone peroxide, cyclohexanone baroxide, 1.1-bis (t-butylperoxy) -3,3,5-trioxide.
- the amount of the organic peroxide varies depending on the type of the organic peroxid
- azo compounds As azo compounds, azonitrile compounds, azomido compounds, azamidine compounds, and the like, which are usually used for cross-linking applications, are used.If these are listed, 2.2'-azobisisobutyronitrile, 2. 2'-azobis (2-methylbutyronitrile), 2,2'-azobis (4-methoxy-2,4-dimethylvaleronitrile), 2,2'-azobis (2,4-dimethylvaleronitrile), 1, ⁇ -azobis (cyclohexane-1-carbonitrile), 2- (carbamoylazo) isobutyronitrile, 2-phenylazo-4-methoxy-2,4-dimethyl-valeronitrile, 1,1- Azobis (2-methyl-N-phenylpropionamidine) dihydrochloride, 2, 2'-azobis [N- (4-chlorophenyl) -2-methylpropionamidine) dihydrochloride, 2, 2 ' -Azobis [N
- crosslinking by irradiation with active energy rays such as ultraviolet rays
- active energy rays such as ultraviolet rays
- glycidyl ether acrylate, glycidyl methacrylate, and glycidyl ether gay cinnamate are particularly preferable among the monomer components represented by the formula (III-c).
- ⁇ ⁇ -ethoxyacetophenone 2-hydroxy-2-methyl-1-furylpropane-1-one, benzyldimethylketal, and 1 (4-isopropylpropyl) -2-hydroxy- 2-Methylpropan-1-one, 4- (2-hydroquinone) quinil- (2-hydroxy-2-propyl) ketone, 2.2-dimethoxy-1.2-diphenylethane-1-one, 1-hydroxy Shikiguchi Heki Roof Acetophenones such as diketone, 2-methyl-2-morpholino (4-thiomethylphenyl) propan-1-one, benzoin, benzoin methyl ether, benzoin ethyl ether, benzoin isopropyl ether, benzoin isobutyl ether, etc.
- Benzoin ethers benzophenone, methyl 0-benzoylbenzoate, 4-funylbenzophenone, hydroxybenzophenone, 4-benzoinole-4'-methyldisulfide I-sulfide, alkylated benzophenone, 3, 3 ' , 4,4'-Tetra (t-butylperoxycarbonyl) benzophenone, 4-benzoyl-N, N-dimethyl-N- [2- ⁇ -oxo-2-probenyloquin) ethyl] benzenemethanamini Benzophthalones such as dimethyl bromide and (4-benzoylbenzyl) trimethylammonium chloride Thioxanthones, such as 2,2-isopropyl propyl xanthone, 2,4-dimethylthioxanthone, 2.4-diethyl thioxanthone, 2.4-dichlorothioxanthone, azidopyren
- a compound having at least two hydrides is used.
- a polysiloxane compound or a polysilane compound is preferable.
- Examples of the polysiloxane compound include a linear polysiloxane compound represented by the formula (a-1) or (a-2) or a cyclic polysiloxane compound represented by the formula (a-3).
- R 11 , R 12 .R 13 , R 14 , R 15 .R 16 .R 17 , R 18 and E 19 each represent a hydrogen atom or a carbon atom.
- a lower alkyl group such as a methyl group or an ethyl group is preferable.
- As the alkoxy group a lower alkoxy group such as a methoxy group or an ethoxyquin group is preferable.
- silane compound a linear silane compound represented by the formula (b-1) is used.
- catalysts for the hydronylation reaction include transition metals such as palladium and platinum, or compounds and complexes thereof. Also, peroxides, amines and phosphines are used. The most common catalysts include dichlorobis (aceto nitrile) palladium (II), chlorotris (triphenylphosphine) rhodium (I), and chloroplatinic acid.
- a cross-linking agent such as polyamines, mercaptoimidazolines, mercaptovirimidines, thiopereas, and polymercapbutanes is used.
- polyamines include hexamethylene diamine carbamate, triethylenetetramine, tetraethylenepentamine, ethylenediaminecarbamate, diethylenetriamine, dipropylenetriamine, dimethylaminopropylamine, and dimethylaminoprom.
- mercaptoimidazolines include 2-mercaptoimidazoline, 4-methyl-2-mercaptoimidazoline, and 5-ethyl-4-4-butyl-12-mercaptoimidazoline.
- Examples of mercaptopyrimidines include 2-mercaptopyrimidine, 4.6-dimethyl-12-mercaptopyrimidine, and 5-butyl-2-mercaptopyrimidine.
- the thioreas include thiorea, ethylene thiorea, dibutyl thiourea, trimethyl thiourea, triethyl thiourea, and trib. Tilthiodialea and the like.
- polymercaptans examples include 2-dibutylamino 4.6-dimethylcapto-1-s-triazine, 2-fuynilamine 4.6-dimercaptotriazine, 2,5-dimercapto1-1,3.4-thiazole, 1,10 —Decanedithiol, 2,3-dimethylcaptovirazine, 2,3-dimercaptoquinoxaline, 6-methylquinoxaline-12,3-dithiocarbonate and the like.
- the amount of the cross-linking agent varies depending on the type of the mulching agent, but is usually in the range of 0.1 to 30% by weight of the whole composition.
- a metallized support serving as an acid acceptor to the composition of the present invention.
- the metal oxide serving as the acid acceptor include oxides, hydroxides, carbonates, carboxylates, silicates, borates, phosphites, and the like of the metals of the periodic table.
- Specific examples include magnesium, magnesium hydroxide, barium hydroxide, magnesium carbonate, barium carbonate, quicklime, slaked lime, calcium carbonate, calcium gayate, calcium stearate, zinc stearate, calcium phthalate, Magnesium phosphite, calcium phosphite, zinc white, tin oxide, litharge, lead tin, lead white, dibasic lead phthalate, dibasic lead carbonate, tin stearate, basic lead phosphite, basic Examples include tin phosphite, basic lead sulfite, tribasic sulfate, and the like.
- the amount of the metal compound serving as the acid acceptor varies depending on the type, but is usually in the range of 0.1 to 30% by weight of the whole composition.
- the electrolyte salt compound used in the present invention is preferably soluble in the polyether copolymer of the present invention or a crosslinked body of the copolymer.
- the following salt compounds are preferably used.
- gold cations, ammonium ions, amidium ions, and Cation selected from guanidium ion, chloride ion, bromide ion, iodine ion, perchlorate ion, thiosuccinate ion, tetrafluorophosphate ion, nitrate ion, AsF 6 —, PF 6 , stearyl sulfonate ion , Okuchirusuruhon acid ion, dodecylbenzenesulfonate I O emissions, naphthalenesulfonic acid ion, dodecyl naphthalenesulfonate ion, 7.2 7.8, 8 - Te Torashiano -P- Keno Jimetan'ion, X 1 S 0 3 -,
- X 1 , X 2 , X 3 and Y are electron-withdrawing groups.
- XX 2 and X 3 are each independently a perfluoroalkyl group or a perfluoroaryl group having 1 to 6 carbon atoms
- Y is a nitrogen atom, a nitroso group, a carbonyl group, a carboxyl group. Or a cyano group.
- XX 2 and X 3 may be the same or different.
- a transition metal cation can be used as the metal cation.
- a cation of a metal selected from Mn, Fe, Co, Ni, Cu, Zn and Ag metals is used.
- a favorable result can be obtained by using a cation of a metal selected from Li, Na, K, Rb, Cs, Mg, Ca and Ba metal. It is free to use two or more of the above compounds as electrolyte salt compounds.
- the amount of the electrolyte salt compound used is 0.0001 of the total number of moles of the electrolyte salt compound and the total number of moles of oxethylene units (the total number of moles of oxyethylene units including the main chain and side chains of the polyether copolymer).
- ⁇ 5 preferably in the range of 0.001 to 0.5. If this value exceeds 5, the workability, the formability, the mechanical strength and the flexibility of the obtained solid electrolyte are reduced, and the ion conductivity is also reduced.
- Flame-retardant compounds include brominated epoxy compounds, tetrabrominated bisphenols, halides such as paraffin chloride, antimony trioxide, antimony pentoxide, aluminum hydroxide, magnesium hydroxide, phosphate esters, An effective amount is selected from polyphosphate and zinc borate.
- the method for producing the solid polymer electrolyte of the present invention is not particularly limited, but usually (1) after mechanically mixing the copolymer and the electrolyte salt compound, or using the copolymer and the electrolyte salt compound in a solvent.
- various kinds of kneaders, oven rolls, extruders and the like can be arbitrarily used.
- polar solvents for example, tetrahydrofuran, acetone, acetonitrile, dimethylformamide, dimethylsulfoxide, dioxane, methylethylketone, methylisobutylketone, etc. are used alone or in combination. .
- concentration of the solution is not particularly limited, but is preferably 1 to 50% by weight.
- the amount of water used in the citrus reaction is not particularly limited because it is easily generated even by moisture in the atmosphere.
- Cross-linking can be achieved by passing the product through a cold or hot water bath for a short time, or by exposing it to steam or air.
- the reaction is carried out at a temperature of 10 to 200 ° C for 10 minutes to 20 hours.
- the Tachibana reaction ends.
- the crosslinking reaction is completed in a temperature of 10 ° C. to 200 ° C. for 1 minute to 20 hours.
- energy rays such as ultraviolet rays
- a sensitizer is used.
- the crosslinking reaction is completed in 0.1 second to 1 hour under the temperature condition of 10 to 15 CTC.
- the cross-linking reaction is completed in a temperature of 10 ° C. to 180 ° C. in 10 minutes to 10 hours.
- the copolymer of the present invention and a crosslinked product of the copolymer are useful precursors as a solid polymer electrolyte.
- the polymer solid electrolyte is excellent in mechanical strength and flexibility, and it is easy to obtain a large-area thin-film solid electrolyte by utilizing its properties.
- a battery using the polymer solid electrolyte of the present invention can be manufactured.
- the cathode material lithium-manganese composite oxide, lithium cobaltate, vanadium pentoxide, polyacene, polypyrene, polyphenylene, polyphenylene, polyphenylene sulfide, polyphenylene oxide, Polyvirol, polyfuran, polyazulene, etc.
- the negative electrode material examples include an interlayer compound in which lithium is occluded between graphite and a carbon layer, lithium metal, lithium-lead alloy, and the like.
- the crosslinked polymer electrolyte of the present invention can be used in a battery.
- cations such as alkali metal ions, Cu ions, Ca ions, and Mg ions can be used as a membrane for ion electrodes.
- the solid polymer electrolyte of the present invention is particularly suitable as a material for electrochemical devices such as batteries, capacitors, and sensors.
- the monomer-converted composition of the copolymer was analyzed by elemental analysis and 1 H NMR spectrum.
- the molecular weight of the copolymer was measured by gel permeation chromatography, and the molecular weight was calculated in terms of standard polystyrene.
- Gel permeation chromatography was performed using Shimadzu Corporation's RID-6A measuring instrument, Showa Denko KK Showdex columns KD-80, KD-806, KD-806M and KD-803, and solvent DMF.
- the reaction was performed at 60 ° C using.
- the glass transition temperature and heat of fusion were measured using a differential scanning calorimeter DSC 8230B manufactured by Rigaku Denki Co., Ltd.
- the conductivity was measured by the complex impedance method using an alternating current method with a voltage of 0.5 V and a frequency of 15 ⁇ 5 ⁇ 1 ⁇ between a platinum electrode and a film dried in vacuum at 2 CT ° C and ImmHg for 72 hours.
- the flexibility of the solid electrolyte film was evaluated based on the presence or absence of breakage when the film was bent at 180 ° at 25 ° C.
- 3-glycidoxy was prepared by purging the inside of a glass four-necked flask with an inner volume of 3 L with nitrogen, using 1 g of the condensed substance obtained in the above-mentioned catalyst production example and water at 10 ppm or less as a to medium. 2.13 g of propyl methyl dimethoxysilane, 224 g of triethylene glycol glycidyl methyl ether and 980 g of n-hexane as a solvent were charged, and 40 g of ethylene oxide was measured by gas chromatography to determine the conversion of triethylene glycol glycidyl methyl ether. While tracking with, added sequentially. The polymerization reaction was performed at 2 CTC for 10 hours.
- the polymerization reaction was stopped with methanol. After removing the polymer by decantation, the polymer was dried under normal pressure at 40 eC for 24 hours and further under reduced pressure at 45 for 10 hours to obtain 220 g of a polymer.
- the glass transfer temperature of this polymer was 170 ° C, the number average molecular weight was 400,000, and the heat of fusion was 3 J / g. The results obtained are shown in Table 1.
- Example 7 After a crosslinked body 1 g obtained in Example 7 was impregnated 20 hours tetra human Dorofuran solution 5 m 1 containing lithium perchlorate 100 mg, 160 ° C, 2 OKgw / cm 2 at a heating for 10 minutes, pressurized, A film was obtained. This film is flexible and has a conductivity of 20. 1.5x10,60 in C. In C, it was 5.1 x 1 ⁇ ' ⁇ S / cm).
- Example 3 In the same manner as in Example 1, a copolymer comprising the structural units shown in Table 3 was synthesized. In Comparative Examples 1 and 3, films were obtained in the same manner as in Example 9. In Comparative Example 2, a film was obtained in the same manner as in Example 9 except that water was not added. The results obtained are shown in Table 3.
- crosslinked polymer solid electrolyte obtained from the polyether copolymer of the present invention has excellent ion conductivity and mechanical properties.
- Katachibana polymer solid electrolyte obtained in Example 9 as the electrolyte, constituted Lithium metal ⁇ , and a secondary battery have use lithium cobalt oxide (L i C o 0 2) as a positive electrode as a negative electrode.
- Crosslinked polymer solid electrolyte size is 10 ⁇ X10 mm x 1 ram.
- the size of the lithium foil is 10 mm X 10 ram X 0.1 mm.
- Lithium cobalt oxide was prepared by mixing a predetermined amount of lithium carbonate and a carbonate powder, followed by firing at 900 ° C. for 5 hours.
- -Epoxy-2'-methylpropyl ether 10.47 g, triethylene glycol glycidyl methyl ether 184 g and n-hexane 900 g as a solvent were charged, and 40 g of ethylene oxide reduced the conversion of triethylene glycol glycidyl methyl ether.
- Sequential addition was performed while tracking by gas chromatography. The polymerization reaction was performed at 20 ° C. for 8 hours. The polymerization reaction was stopped with methanol.
- 1 g of the crosslinked product obtained in Example 22 contains 100 mg of lithium perchlorate After impregnating the tetrahydrofuran solution 5 m 1 20 hours to obtain 16 (TC, 20 1 ⁇ ⁇ Ji 111 2 heated for 10 min, pressurized film.
- the film has a soft ⁇ , conductivity 20 ° 1.3xl 0- 4, was at 60 ° C 4.6 X 10- 4 ( S / cm) at C.
- Example 2 4 obtained crosslinked polymer solid electrolyte as the electrolyte, to constitute a secondary 3 ⁇ 4 pond using lithium metal foil as a negative electrode, and lithium cobaltate as a positive electrode (L i C o 0 2) .
- the size of the crosslinked polymer solid electrolyte is 10 mm X 10 .DUD X 1 mm.
- the size of lithium ⁇ is 10 ⁇ X 10 im X 0.1 mm.
- Lithium cobaltate was prepared by mixing predetermined amounts of lithium carbonate and cobalt carbonate powder ⁇ and then firing at 900 ° C for 5 hours.
- Example 24 12 parts by weight of acetylene black and 3 parts by weight of the crosslinked polymer solid electrolyte obtained in Example 24 were added to 85 parts by weight of the obtained lithium cobaltate, followed by mixing in a mortar. This was press-molded at a pressure of 300 KgW / cm 2 into 10 mm ⁇ 10 mm ⁇ 2 mm to obtain a positive electrode of a battery.
- Scissors EXAMPLE 2 4 obtained crosslinked polymer solid electrolyte lithium metal foil and cobalt lithium DOO acid plate, while applying a pressure of 10 KGW / cm 2 as the interface is in close contact were examined charge-discharge characteristics of the battery .
- the discharge current at an initial terminal voltage of 3.2 V was 0.4 mA / cm 2 , and charging was possible at 0.3 mk / cm 2 . Since the battery of this embodiment can be easily manufactured to be thin, the battery is lightweight and has a large capacity.
- Structural unit of formula (1) 10 10 Ethylene oxide 96 90 60
- Organic peroxyphosphate condensate Polymerized in a solvent system.
- a solution of lithium perchlorate in tetrahydrofuran was mixed so that the total number of moles of the soluble electrolyte salt compound (the total number of moles of ethylene oxide units) was 0.05.
- This mixture was cast on a mold made of polytetrafluoroethylene, dried, heated and pressed at 160 Kg and 20 Kg WZcm 2 for 10 minutes to obtain a film.
- Films were obtained in the same manner as in Examples 31 to 37 using a polyether copolymer shown in Table 8 polymerized with an organotin monophosphate condensate catalyst system without adding a crosslinking agent.
- Example 3 1 to 4 6 & Example of squeezing? Tables 7 and 8 show the results of (1) to (12). No. In Tables 8 to 8, the glass transition point and the heat of fusion were measured using a differential scanning calorimeter DSC 8230B manufactured by Rigaku Denki Co., Ltd., in a nitrogen atmosphere, in a temperature range of 100 to 80 ° C, and heated. speed 1 (measured at TCZniin. measurements of the conductivity ⁇ is sandwiched 2 0 ° C 1 mm H g for 7 2 hours in a vacuum dry film with platinum electrodes, voltage 0. 5 V, the frequency range 5 H z ⁇ 1 MH Calculated by the complex impedance method using the alternating current method of z. The flexibility of the solid electrolyte film was evaluated by bending the film to 180 degrees to check for breakage.
- DSC 8230B manufactured by Rigaku Denki Co., Ltd.
- the size of the crosslinked polymer solid electrolyte is 10 mm ⁇ 10 mm ⁇ 1 mm.
- the size of the lithium foil is 10 ram X 10 mm X 0.1 mm.
- Lithium cobalt oxide was prepared by mixing a predetermined amount of lithium carbonate and cobalt carbonate powder and then firing at 90 CTC for 5 hours.
- Example 33 The crosslinked polymer solid electrolyte obtained in 3 was sandwiched between a lithium gold foil and a lithium cobaltate plate, and the charging and discharging characteristics of the battery were increased while applying a pressure of 10 gw / cra 2 so that the interface was in close contact. Examined. Initial terminal voltage 3.2 V The current was 0.4 mA / cm 2 , and the battery was chargeable at 0.3 DAZCID 2 . Since the battery of this embodiment can be easily made thin, a light-weight and large-capacity battery can be obtained.
- Ethylene oxide 70 Triethylene glycol glycidyl methyl ether 27-epibromohydrin 4
- Ethylene oxide 72 Triethyleneglycol-glycidyl methyl ether 25 Number of molecular weight of epipib-mohydrin 3 Copolymer 370,000 Glass transition point of copolymer (° C)-69 Heat of fusion of copolymer G / g) 18
- Example 48 1 g of the copolymer obtained in 8, 0.015 g of a cross-linking agent ethylene thiopera, and 0.05 g of dibasic lead phthalate were added to acetate nitrile 20 m 1. The solution was dissolved, and an acetonitrile solution of lithium perchlorate was mixed so that the molar ratio (the number of moles of the electrolyte salt compound) / (the total number of moles of the oxhetylene unit of the copolymer) was 0.07. This mixed solution was cast on a polytetrafluoroethylene monohydrate, dried, heated at 170, 60 KgwZcm 2 for 15 minutes, and pressed to obtain a film.
- the polymer solid electrolyte of the present invention is excellent in workability, moldability, mechanical strength, flexibility and heat resistance, and its ion conductivity is remarkably improved. Therefore, it can be applied to solid-state batteries, large-capacity capacitors, and display devices, such as electronic devices such as electoric chromic displays.
Landscapes
- Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Organic Chemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Manufacturing & Machinery (AREA)
- Electrochemistry (AREA)
- Physics & Mathematics (AREA)
- Condensed Matter Physics & Semiconductors (AREA)
- Dispersion Chemistry (AREA)
- General Physics & Mathematics (AREA)
- Inorganic Chemistry (AREA)
- Secondary Cells (AREA)
- Compositions Of Macromolecular Compounds (AREA)
- Polyethers (AREA)
- Conductive Materials (AREA)
- Epoxy Resins (AREA)
- Silicon Polymers (AREA)
- Primary Cells (AREA)
- Macromonomer-Based Addition Polymer (AREA)
Description
Claims
Priority Applications (6)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CA002253863A CA2253863C (en) | 1996-05-08 | 1997-05-06 | Cross-linked solid polyelectrolyte and use thereof |
| EP97918369A EP0897941B1 (en) | 1996-05-08 | 1997-05-06 | Cross-linked solid polyelectrolyte and use thereof |
| DE69737057T DE69737057D1 (de) | 1996-05-08 | 1997-05-06 | Vernetzter fester polyelektrolyt und seine verwendung |
| AU26510/97A AU2651097A (en) | 1996-05-08 | 1997-05-06 | Cross-linked solid polyelectrolyte and use thereof |
| US09/147,159 US6239204B1 (en) | 1996-05-08 | 1997-05-06 | Cross-linked solid polyelectrolyte and use thereof |
| JP53974097A JP3215436B2 (ja) | 1996-05-08 | 1997-05-06 | 架橋高分子固体電解質及びその用途 |
Applications Claiming Priority (8)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP8/113496 | 1996-05-08 | ||
| JP11349696 | 1996-05-08 | ||
| JP17343596 | 1996-07-03 | ||
| JP8/173435 | 1996-07-03 | ||
| JP8/183186 | 1996-07-12 | ||
| JP18318696 | 1996-07-12 | ||
| JP8/246199 | 1996-09-18 | ||
| JP24619996 | 1996-09-18 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO1997042251A1 true WO1997042251A1 (en) | 1997-11-13 |
Family
ID=27470087
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP1997/001522 WO1997042251A1 (en) | 1996-05-08 | 1997-05-06 | Cross-linked solid polyelectrolyte and use thereof |
Country Status (10)
| Country | Link |
|---|---|
| US (1) | US6239204B1 (ja) |
| EP (1) | EP0897941B1 (ja) |
| JP (1) | JP3215436B2 (ja) |
| KR (1) | KR100570949B1 (ja) |
| CN (1) | CN1136250C (ja) |
| AU (1) | AU2651097A (ja) |
| CA (1) | CA2253863C (ja) |
| DE (1) | DE69737057D1 (ja) |
| TW (1) | TW430686B (ja) |
| WO (1) | WO1997042251A1 (ja) |
Cited By (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2000154223A (ja) * | 1998-06-25 | 2000-06-06 | Hydro Quebec | 架橋性ポリマ― |
| WO2000075941A1 (fr) * | 1999-06-04 | 2000-12-14 | Mitsui Chemicals, Inc. | Solution electrolytique non aqueuse, electrode et condensateur ainsi equipe |
| WO2002075748A1 (fr) * | 2001-03-19 | 2002-09-26 | Toyo Boseki Kabushiki Kaisha | Gel polymere pour electrolyte et son procede de preparation |
| WO2003028144A1 (en) * | 2001-09-21 | 2003-04-03 | Daiso Co., Ltd. | Element using polymer gel electrolyte |
| US6677084B1 (en) | 1999-04-19 | 2004-01-13 | Daiso Co., Ltd. | Solid crosslinked-polymer electrolyte and use thereof |
| JP3710749B2 (ja) * | 1999-06-16 | 2005-10-26 | 花王株式会社 | 表面改質剤 |
| JP2006269414A (ja) * | 2005-02-28 | 2006-10-05 | Shin Etsu Chem Co Ltd | 電解質膜用硬化性樹脂組成物、電解質膜の製造方法及び電解質膜・電極接合体の製造方法 |
| JP2011006613A (ja) * | 2009-06-26 | 2011-01-13 | Dainichiseika Color & Chem Mfg Co Ltd | 硬化性樹脂組成物およびハードコートフィルムまたはシート |
| WO2011068209A1 (ja) * | 2009-12-03 | 2011-06-09 | 株式会社日本触媒 | 水溶性単量体用中間体含有組成物及びその製造方法、水溶性単量体含有組成物、水溶性単量体用中間体、水溶性単量体及びその製造方法 |
| JP2011137135A (ja) * | 2009-12-03 | 2011-07-14 | Nippon Shokubai Co Ltd | 水溶性単量体用中間体含有組成物及びその製造方法、水溶性単量体用中間体、カチオン性基含有単量体及びその製造方法 |
| JP2011174019A (ja) * | 2010-02-25 | 2011-09-08 | Daiso Co Ltd | 高分子固体電解質およびその用途 |
| JP2012226937A (ja) * | 2011-04-19 | 2012-11-15 | Daiso Co Ltd | 非水電解質二次電池 |
| JP2020087711A (ja) * | 2018-11-26 | 2020-06-04 | 株式会社大阪ソーダ | 無機固体電解質二次電池 |
Families Citing this family (29)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| BR9706631A (pt) * | 1996-08-20 | 1999-11-23 | Daiso Co Ltd | Eletrólito de polìmero sólido |
| KR100337889B1 (ko) * | 2000-06-22 | 2002-05-24 | 김순택 | 리튬 2차전지 |
| EP1339127A4 (en) * | 2000-10-20 | 2006-07-26 | Dainippon Ink & Chemicals | FESTPOLYMER ELECTROLYTE AND CELL WITH THE ELECTROLYTE |
| US6956083B2 (en) * | 2001-05-31 | 2005-10-18 | The Regents Of The University Of California | Single ion conductor cross-linked polymeric networks |
| US7101643B2 (en) * | 2001-05-31 | 2006-09-05 | The Regents Of The University Of California | Polymeric electrolytes based on hydrosilyation reactions |
| DE10136447A1 (de) * | 2001-07-26 | 2003-02-06 | Bayer Ag | Pfropfpolymerisate auf Basis von Polyalkylenoxiden |
| US6858351B2 (en) * | 2001-11-07 | 2005-02-22 | Daiso Co., Ltd. | Polyethylene oxide-based electrolyte containing silicon compound |
| DE60325047D1 (de) * | 2002-04-26 | 2009-01-15 | Zeon Corp | Formmaterial für hochmolekulare festelektrolyte, formen hochmolekularer festelektrolyte und prozess zu ihrer herstellung und polyetherpolymer und prozess zu seiner herstellung |
| KR100496852B1 (ko) * | 2002-08-23 | 2005-06-23 | 대주전자재료 주식회사 | 이온교환막 및 이를 이용한 직접 메탄올 연료전지 |
| US20050260528A1 (en) * | 2004-05-22 | 2005-11-24 | Hynix Semiconductor Inc. | Liquid composition for immersion lithography and lithography method using the same |
| KR101065374B1 (ko) * | 2004-06-30 | 2011-09-16 | 삼성에스디아이 주식회사 | 연료전지용 고분자 막 및 그 제조방법 |
| WO2008102699A1 (ja) * | 2007-02-21 | 2008-08-28 | Nippon Shokubai Co., Ltd. | エチレンオキシド系共重合体、重合体組成物、及びリチウム二次電池 |
| US20090186177A1 (en) * | 2008-01-22 | 2009-07-23 | Eastman Chemical Company | Polyester melt phase products and process for making the same |
| CN103261390B (zh) * | 2010-12-17 | 2015-09-16 | 宝洁公司 | 具有两性聚羧酸根聚合物的清洁组合物 |
| TWI465503B (zh) * | 2011-07-08 | 2014-12-21 | Eternal Materials Co Ltd | 電解質材料調配物、由此形成之電解質材料組合物及其用途 |
| WO2014050944A1 (ja) * | 2012-09-28 | 2014-04-03 | 日本ゼオン株式会社 | ポリエーテル共重合体、架橋性ポリエーテル共重合体組成物及び電解質 |
| WO2014133024A1 (ja) * | 2013-02-27 | 2014-09-04 | ダイソー株式会社 | 正極および非水電解質二次電池 |
| CN103400989A (zh) * | 2013-07-31 | 2013-11-20 | 东莞新能源科技有限公司 | 锂离子电池负极材料用粘接剂及包含该粘接剂的电极的制备方法 |
| CN103500835A (zh) * | 2013-10-10 | 2014-01-08 | 东莞新能源科技有限公司 | 锂离子二次电池及其负极片 |
| DE102015104439B4 (de) * | 2015-03-24 | 2019-02-21 | Bayerische Motoren Werke Aktiengesellschaft | Elektrochromes Element mit verbesserter Elektrolytschicht, Verfahren zu dessen Herstellung, Fahrzeugverglasung sowie Fahrzeug |
| US9920170B1 (en) * | 2017-01-19 | 2018-03-20 | International Business Machines Corporation | Bio-derived cross-linkers |
| US9920171B1 (en) * | 2017-01-27 | 2018-03-20 | International Business Machines Corporation | Crosslinkers from biorenewable resveratrol |
| US10160838B2 (en) | 2017-03-27 | 2018-12-25 | International Business Machines Corporation | Crosslinking materials from biorenewable aconitic acid |
| CN107863527B (zh) * | 2017-10-09 | 2020-06-12 | 吉林聚能新型炭材料股份有限公司 | 一种复合负极材料及其制备方法和应用 |
| WO2019131476A1 (ja) * | 2017-12-28 | 2019-07-04 | パナソニックIpマネジメント株式会社 | 電解コンデンサおよびその製造方法 |
| CN110760292B (zh) * | 2019-09-24 | 2021-02-09 | 江苏立一新材料科技有限公司 | 耐热摩擦材料及其应用 |
| CN111653822B (zh) * | 2020-06-09 | 2022-02-11 | 北京化工大学 | 一种用于锂离子电池的凝胶型离子液体电解质及其制备方法和用途 |
| US11824156B2 (en) | 2020-11-06 | 2023-11-21 | Nano And Advanced Materials Institute Limited | Secondary lithium-ion batteries comprising in situ thermal curable solid composite electrolyte |
| US20220231333A1 (en) * | 2021-01-18 | 2022-07-21 | Global Graphene Group, Inc. | Quasi-solid and solid-state electrolyte for lithium-ion and lithium metal batteries and manufacturing method |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3297783A (en) * | 1962-11-16 | 1967-01-10 | Union Carbide Corp | Vinyl halide resin plasticized with a linear copolymer of a diepoxide with a 1, 2-alkylene oxide |
| JPS62169823A (ja) * | 1986-01-20 | 1987-07-27 | Osaka Soda Co Ltd | 側鎖にエポキシ基を有するポリエ−テル共重合体およびその製造法 |
| JPH02295004A (ja) * | 1989-05-09 | 1990-12-05 | Hitachi Maxell Ltd | リチウムイオン伝導性ポリマー電解質 |
| JPH0347833A (ja) * | 1989-04-13 | 1991-02-28 | Dai Ichi Kogyo Seiyaku Co Ltd | イオン導伝性ポリマー電解質 |
| JPH05304051A (ja) * | 1992-04-28 | 1993-11-16 | Yuasa Corp | 電気二重層コンデンサ |
Family Cites Families (23)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FR2442512A1 (fr) | 1978-11-22 | 1980-06-20 | Anvar | Nouveaux materiaux elastomeres a conduction ionique |
| US4758483A (en) | 1983-03-11 | 1988-07-19 | Societe Nationale Elf Aquitaine | Novel macromolecular material for use in realizing electrolytes and/or electrodes |
| MA20046A1 (fr) | 1983-03-11 | 1984-10-01 | Elf Aquitaine | Materiau macromoleculaire constitue par un sel en solution dans un copolymere. |
| FR2570224B1 (fr) | 1984-09-11 | 1987-03-20 | Elf Aquitaine | Electrolyte solide polymere constitue par un copolymere reticule |
| US4711950A (en) | 1985-11-05 | 1987-12-08 | Osaka Soda Co., Ltd. | Polyether polymer or copolymer, monomer therefor, and process for production thereof |
| JPS62249361A (ja) | 1986-04-21 | 1987-10-30 | Yuasa Battery Co Ltd | 有機固体電解質 |
| EP0260847A1 (en) | 1986-09-19 | 1988-03-23 | Imperial Chemical Industries Plc | Solid electrolytes |
| FR2606218A1 (fr) | 1986-10-30 | 1988-05-06 | Elf Aquitaine | Nouveau materiau a conduction ionique |
| JPH0768336B2 (ja) | 1986-12-18 | 1995-07-26 | ダイソー株式会社 | オリゴオキシエチレン側鎖を有するポリエーテル共重合体の製法 |
| GB8804860D0 (en) * | 1988-03-01 | 1988-03-30 | Ici Plc | Solid electrolyte devices |
| JP2757004B2 (ja) | 1989-03-08 | 1998-05-25 | ダイソー株式会社 | イオン伝導性固体電解質 |
| US5116541A (en) | 1989-04-13 | 1992-05-26 | Dai-Ichi Kogyo Seiyaku Co., Ltd. | Ion-conductive polymer electrolyte |
| IT1236512B (it) | 1989-10-06 | 1993-03-11 | Eniricerche Spa | Elettrolita polimerico solido a base poliepossidica. |
| JP2813832B2 (ja) | 1989-10-26 | 1998-10-22 | 第一工業製薬株式会社 | イオン導伝性ポリマー電解質 |
| JP2813831B2 (ja) | 1989-10-26 | 1998-10-22 | 第一工業製薬株式会社 | イオン導伝性ポリマー電解質 |
| JP2813834B2 (ja) | 1990-05-31 | 1998-10-22 | 第一工業製薬株式会社 | イオン導伝性ポリマー電解質 |
| JP2923542B2 (ja) | 1990-07-06 | 1999-07-26 | 第一工業製薬株式会社 | イオン導伝性ポリマー電解質 |
| US5268243A (en) | 1992-01-27 | 1993-12-07 | Dai-Ichi Kogyo Seiyaku Co., Ltd. | Galvanic cell |
| EP0585072B1 (en) * | 1992-08-27 | 1997-12-29 | Dai-Ichi Kogyo Seiyaku Co., Ltd. | Ion-conductive polymer electrolyte |
| US5755985A (en) * | 1994-09-06 | 1998-05-26 | Hydro-Quebec | LPB electrolyte compositions based on mixtures of copolymers and interpenetrated networks |
| JP3022317B2 (ja) | 1995-05-08 | 2000-03-21 | ダイソー株式会社 | 高分子固体電解質 |
| CA2175950C (en) * | 1995-05-08 | 2008-12-02 | Shinzo Kohjiya | Polymer solid electrolyte |
| US5968681A (en) * | 1996-10-28 | 1999-10-19 | Daiso Co., Ltd | Polyether copolymer and polymer solid electrolyte |
-
1997
- 1997-05-06 AU AU26510/97A patent/AU2651097A/en not_active Abandoned
- 1997-05-06 DE DE69737057T patent/DE69737057D1/de not_active Expired - Lifetime
- 1997-05-06 KR KR1019980707358A patent/KR100570949B1/ko not_active IP Right Cessation
- 1997-05-06 CN CNB971936641A patent/CN1136250C/zh not_active Expired - Fee Related
- 1997-05-06 WO PCT/JP1997/001522 patent/WO1997042251A1/ja active IP Right Grant
- 1997-05-06 CA CA002253863A patent/CA2253863C/en not_active Expired - Fee Related
- 1997-05-06 JP JP53974097A patent/JP3215436B2/ja not_active Expired - Fee Related
- 1997-05-06 US US09/147,159 patent/US6239204B1/en not_active Expired - Fee Related
- 1997-05-06 EP EP97918369A patent/EP0897941B1/en not_active Expired - Lifetime
- 1997-05-07 TW TW086106052A patent/TW430686B/zh not_active IP Right Cessation
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3297783A (en) * | 1962-11-16 | 1967-01-10 | Union Carbide Corp | Vinyl halide resin plasticized with a linear copolymer of a diepoxide with a 1, 2-alkylene oxide |
| JPS62169823A (ja) * | 1986-01-20 | 1987-07-27 | Osaka Soda Co Ltd | 側鎖にエポキシ基を有するポリエ−テル共重合体およびその製造法 |
| JPH0347833A (ja) * | 1989-04-13 | 1991-02-28 | Dai Ichi Kogyo Seiyaku Co Ltd | イオン導伝性ポリマー電解質 |
| JPH02295004A (ja) * | 1989-05-09 | 1990-12-05 | Hitachi Maxell Ltd | リチウムイオン伝導性ポリマー電解質 |
| JPH05304051A (ja) * | 1992-04-28 | 1993-11-16 | Yuasa Corp | 電気二重層コンデンサ |
Non-Patent Citations (1)
| Title |
|---|
| See also references of EP0897941A4 * |
Cited By (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2000154223A (ja) * | 1998-06-25 | 2000-06-06 | Hydro Quebec | 架橋性ポリマ― |
| US8754138B2 (en) | 1998-06-25 | 2014-06-17 | Hydro-Quebec | Polymers obtained from monomers allowing a sequential polymerization, and their use for preparing ionic conductors |
| US8512899B2 (en) | 1998-06-25 | 2013-08-20 | Hydro-Quebec | Polymers obtained from monomers allowing a sequential polymerization, and their use for preparing ionic conductors |
| US6677084B1 (en) | 1999-04-19 | 2004-01-13 | Daiso Co., Ltd. | Solid crosslinked-polymer electrolyte and use thereof |
| WO2000075941A1 (fr) * | 1999-06-04 | 2000-12-14 | Mitsui Chemicals, Inc. | Solution electrolytique non aqueuse, electrode et condensateur ainsi equipe |
| JP3710749B2 (ja) * | 1999-06-16 | 2005-10-26 | 花王株式会社 | 表面改質剤 |
| WO2002075748A1 (fr) * | 2001-03-19 | 2002-09-26 | Toyo Boseki Kabushiki Kaisha | Gel polymere pour electrolyte et son procede de preparation |
| WO2003028144A1 (en) * | 2001-09-21 | 2003-04-03 | Daiso Co., Ltd. | Element using polymer gel electrolyte |
| JP2006269414A (ja) * | 2005-02-28 | 2006-10-05 | Shin Etsu Chem Co Ltd | 電解質膜用硬化性樹脂組成物、電解質膜の製造方法及び電解質膜・電極接合体の製造方法 |
| JP2011006613A (ja) * | 2009-06-26 | 2011-01-13 | Dainichiseika Color & Chem Mfg Co Ltd | 硬化性樹脂組成物およびハードコートフィルムまたはシート |
| JP2011137135A (ja) * | 2009-12-03 | 2011-07-14 | Nippon Shokubai Co Ltd | 水溶性単量体用中間体含有組成物及びその製造方法、水溶性単量体用中間体、カチオン性基含有単量体及びその製造方法 |
| WO2011068209A1 (ja) * | 2009-12-03 | 2011-06-09 | 株式会社日本触媒 | 水溶性単量体用中間体含有組成物及びその製造方法、水溶性単量体含有組成物、水溶性単量体用中間体、水溶性単量体及びその製造方法 |
| US8921584B2 (en) | 2009-12-03 | 2014-12-30 | Nippon Shokubai Co, Ltd | Composition containing intermediate for water-soluble monomer and process for production thereof, composition containing water-soluble monomer, intermediate for water-soluble monomer, and water-soluble monomer and process for production thereof |
| JP2011174019A (ja) * | 2010-02-25 | 2011-09-08 | Daiso Co Ltd | 高分子固体電解質およびその用途 |
| JP2012226937A (ja) * | 2011-04-19 | 2012-11-15 | Daiso Co Ltd | 非水電解質二次電池 |
| JP2020087711A (ja) * | 2018-11-26 | 2020-06-04 | 株式会社大阪ソーダ | 無機固体電解質二次電池 |
| JP7478508B2 (ja) | 2018-11-26 | 2024-05-07 | 株式会社大阪ソーダ | 無機固体電解質二次電池 |
Also Published As
| Publication number | Publication date |
|---|---|
| CN1136250C (zh) | 2004-01-28 |
| AU2651097A (en) | 1997-11-26 |
| TW430686B (en) | 2001-04-21 |
| EP0897941A1 (en) | 1999-02-24 |
| US6239204B1 (en) | 2001-05-29 |
| CN1215416A (zh) | 1999-04-28 |
| EP0897941B1 (en) | 2006-12-06 |
| KR100570949B1 (ko) | 2006-08-30 |
| CA2253863C (en) | 2005-08-09 |
| CA2253863A1 (en) | 1997-11-13 |
| DE69737057D1 (de) | 2007-01-18 |
| KR19990087822A (ko) | 1999-12-27 |
| EP0897941A4 (en) | 1999-07-21 |
| JP3215436B2 (ja) | 2001-10-09 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| WO1997042251A1 (en) | Cross-linked solid polyelectrolyte and use thereof | |
| JP3223978B2 (ja) | ポリエーテル共重合体および高分子固体電解質 | |
| JP3215440B2 (ja) | 高分子固体電解質 | |
| JP3301378B2 (ja) | ポリエーテル共重合体および架橋高分子固体電解質 | |
| EP0838487B1 (en) | Polyether copolymer and polymer solid electrolyte | |
| JP3491539B2 (ja) | 高分子固体電解質及びその用途 | |
| JP4089221B2 (ja) | 高分子固体電解質および電池 | |
| US20030124432A1 (en) | Electrolyte composition and battery | |
| WO1998058983A1 (fr) | Copolymere de polyether, electrolyte a polymere solide, et batterie | |
| JP3484974B2 (ja) | 新規なリチウムポリマー電池 | |
| JP3282565B2 (ja) | 架橋高分子固体電解質及びその用途 | |
| JP3427730B2 (ja) | リチウムポリマー電池 | |
| JP4269648B2 (ja) | 電解質組成物および電池 | |
| JP4640172B2 (ja) | 電解質組成物および電池 | |
| JP2006134817A (ja) | 電解質組成物および電池 | |
| JP2000150308A (ja) | 電気二重層キャパシタ |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| WWE | Wipo information: entry into national phase |
Ref document number: 97193664.1 Country of ref document: CN |
|
| AK | Designated states |
Kind code of ref document: A1 Designated state(s): AL AM AT AU AZ BA BB BG BR BY CA CH CN CU CZ DE DK EE ES FI GB GE GH HU IL IS JP KE KG KR KZ LC LK LR LS LT LU LV MD MG MK MN MW MX NO NZ PL PT RO RU SD SE SG SI SK TJ TM TR TT UA UG US UZ VN YU AM AZ BY KG KZ MD RU TJ TM |
|
| AL | Designated countries for regional patents |
Kind code of ref document: A1 Designated state(s): GH KE LS MW SD SZ UG AT BE CH DE DK ES FI FR GB GR IE IT LU MC NL PT SE BF BJ |
|
| DFPE | Request for preliminary examination filed prior to expiration of 19th month from priority date (pct application filed before 20040101) | ||
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application | ||
| WWE | Wipo information: entry into national phase |
Ref document number: 1019980707358 Country of ref document: KR |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 09147159 Country of ref document: US |
|
| ENP | Entry into the national phase |
Ref document number: 2253863 Country of ref document: CA Ref document number: 2253863 Country of ref document: CA Kind code of ref document: A |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 1997918369 Country of ref document: EP |
|
| WWP | Wipo information: published in national office |
Ref document number: 1997918369 Country of ref document: EP |
|
| REG | Reference to national code |
Ref country code: DE Ref legal event code: 8642 |
|
| WWP | Wipo information: published in national office |
Ref document number: 1019980707358 Country of ref document: KR |
|
| WWG | Wipo information: grant in national office |
Ref document number: 1019980707358 Country of ref document: KR |
|
| WWG | Wipo information: grant in national office |
Ref document number: 1997918369 Country of ref document: EP |