JP2006347931A - ジアルキルシクロブタン酸二無水物及びその製造法 - Google Patents
ジアルキルシクロブタン酸二無水物及びその製造法 Download PDFInfo
- Publication number
- JP2006347931A JP2006347931A JP2005174685A JP2005174685A JP2006347931A JP 2006347931 A JP2006347931 A JP 2006347931A JP 2005174685 A JP2005174685 A JP 2005174685A JP 2005174685 A JP2005174685 A JP 2005174685A JP 2006347931 A JP2006347931 A JP 2006347931A
- Authority
- JP
- Japan
- Prior art keywords
- tetracarboxylic acid
- formula
- dialkylcyclobutane
- producing
- dianhydride compound
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 0 **(C(C(*(*)C1C(O2)=O)C(O3)=O)C3=O)C1C2=O Chemical compound **(C(C(*(*)C1C(O2)=O)C(O3)=O)C3=O)C1C2=O 0.000 description 3
- JVZWIULKHXXMTQ-UHFFFAOYSA-N CCC(C(C1(C)C(O2)=O)C2=O)(C1C(O1)=O)C1=O Chemical compound CCC(C(C1(C)C(O2)=O)C2=O)(C1C(O1)=O)C1=O JVZWIULKHXXMTQ-UHFFFAOYSA-N 0.000 description 2
Abstract
Description
光学材料用ポリイミドの原料モノマーとなり得る脂環式テトラカルボン酸二無水物及びその製造法に関する。
本発明により得られるテトラカルボン酸二無水物は、芳香族ジアミンとの重縮合反応によりポリアミド酸とした後、熱又は触媒を用いた脱水閉環反応により対応するポリイミドとすることができる。
一般に、ポリイミド樹脂はその特徴である高い機械的強度、耐熱性、絶縁性、耐溶剤性のために、液晶表示素子や半導体における保護材料、絶縁材料などの電子材料として広く用いられている。また、最近では光導波路用材料等の光通信用材料としての用途も期待されている。
近年、この分野の発展は目覚ましく、それに対応して、用いられる材料に対しても益々高度な特性が要求される様になっている。即ち、単に耐熱性、耐溶剤性に優れるだけでなく、用途に応じた性能を多数あわせもつことが期待されている。
しかし、特に、全芳香族ポリイミド樹脂においては、濃い琥珀色を呈し着色するため、高い透明性を要求される用途においては問題が生じてくる。また、透明性を実現する一つの方法として、脂環式テトラカルボン酸二無水物と芳香族ジアミンとの重縮合反応によりポリイミド前駆体を得て、該当前駆体をイミド化しポリイミドを製造すれば、比較的着色が少なく、高透明性のポリイミドが得られることは知られている(特許文献1及び2参照。)。
従来、アルキルシクロブタン酸二無水物の合成例は、下記のスキームで表される様に、シトラコン酸無水物(MMAと略す。)の光二量化反応によって、1,3−ジメチルシクロブタン−1,2,3,4−テトラカルボン酸−1,2:3,4−二無水物(1,3−DMCBDAと略す。)と1,4−ジメチルシクロブタン−1,2,3,4−テトラカルボン酸−1,2:3,4−二無水物(1,4−DMCBDAと略す。)の混合物を得ている(特許文献3参照。)。
一般に、ポリイミド樹脂はその特徴である高い機械的強度、耐熱性、絶縁性、耐溶剤性のために、液晶表示素子や半導体における保護材料、絶縁材料などの電子材料として広く用いられている。また、最近では光導波路用材料等の光通信用材料としての用途も期待されている。
近年、この分野の発展は目覚ましく、それに対応して、用いられる材料に対しても益々高度な特性が要求される様になっている。即ち、単に耐熱性、耐溶剤性に優れるだけでなく、用途に応じた性能を多数あわせもつことが期待されている。
しかし、特に、全芳香族ポリイミド樹脂においては、濃い琥珀色を呈し着色するため、高い透明性を要求される用途においては問題が生じてくる。また、透明性を実現する一つの方法として、脂環式テトラカルボン酸二無水物と芳香族ジアミンとの重縮合反応によりポリイミド前駆体を得て、該当前駆体をイミド化しポリイミドを製造すれば、比較的着色が少なく、高透明性のポリイミドが得られることは知られている(特許文献1及び2参照。)。
従来、アルキルシクロブタン酸二無水物の合成例は、下記のスキームで表される様に、シトラコン酸無水物(MMAと略す。)の光二量化反応によって、1,3−ジメチルシクロブタン−1,2,3,4−テトラカルボン酸−1,2:3,4−二無水物(1,3−DMCBDAと略す。)と1,4−ジメチルシクロブタン−1,2,3,4−テトラカルボン酸−1,2:3,4−二無水物(1,4−DMCBDAと略す。)の混合物を得ている(特許文献3参照。)。
しかし、シトラコン酸無水物以外のアルキルマレイン酸無水物の光二量化反応によるジアルキルシクロブタン−1,2,3,4−テトラカルボン酸−1,2:3,4−二無水物の合成例はない。
近年、光を用いた電子材料分野等にも耐熱性の高いポリイミドの使用が要望されて来た。本発明の目的は、紫外線領域に吸収がなく光透過性が高く、更に溶媒溶解性が改善された液晶配向膜や光通信用光導波路等の光学材料用ポリイミドの原料モノマーとなり得る脂環式テトラカルボン酸二無水物及びその製造法の提供を課題とする。
本発明者らは、上記課題の透明性と溶媒溶解性に注目し、脂環式テトラカルボン酸二無水物部分にアルキル側鎖を導入することにより、溶媒溶解性を改善した。
即ち,本発明は、以下の(1)〜(12)に関する。
(1)式[1]
(式中、Rは炭素数2〜10のアルキル基を表す。)
で表されるジアルキルシクロブタン−1,2,3,4−テトラカルボン酸−1,2:3,4−二無水物化合物。
(2)Rがエチル基である(1)記載のジアルキルシクロブタン−1,2,3,4−テトラカルボン酸−1,2:3,4−二無水物化合物。
(3)式[2]
で表される(1)記載のジアルキルシクロブタン−1,2,3,4−テトラカルボン酸−1,2:3,4−二無水物化合物。
(4)式[3]
で表される(1)記載のジアルキルシクロブタン−1,2,3,4−テトラカルボン酸−1,2:3,4−二無水物化合物。
(5)式[4]
(式中、Rは炭素数2〜10のアルキル基を表す。)
で表されるアルキルマレイン酸無水物化合物を光二量化させることを特徴とする式[1]
(式中、Rは炭素数2〜10のアルキル基を表す。)
で表されるジアルキルシクロブタン−1,2,3,4−テトラカルボン酸−1,2:3,4−二無水物化合物の製造法。
(6)Rがエチル基である(5)記載のジアルキルシクロブタン−1,2,3,4−テトラカルボン酸−1,2:3,4−二無水物化合物の製造法。
(7)式[2]
で表される(5)記載のジアルキルシクロブタン−1,2,3,4−テトラカルボン酸−1,2:3,4−二無水物化合物の製造方法。
(8)式[3]
で表される(5)記載のジアルキルシクロブタン−1,2,3,4−テトラカルボン酸−1,2:3,4−二無水物化合物の製造方法。
(9)光二量化反応溶媒が脂肪族エステルであることを特徴とする(5)記載のジアルキルシクロブタン−1,2,3,4−テトラカルボン酸−1,2:3,4−二無水物化合物の製造法。
(10)光二量化反応溶媒が酢酸エチルであることを特徴とする(9)記載のジアルキルシクロブタン−1,2,3,4−テトラカルボン酸−1,2:3,4−二無水物化合物の製造法。
(11)光二量化反応の光源が高圧水銀灯であることを特徴とする(5)記載のジアルキルシクロブタン−1,2,3,4−テトラカルボン酸−1,2:3,4−二無水物化合物の製造法。
(12)光二量化反応の光源波長が300〜600nmであることを特徴とする(11)記載のジアルキルシクロブタン−1,2,3,4−テトラカルボン酸−1,2:3,4−二無水物化合物の製造法。
即ち,本発明は、以下の(1)〜(12)に関する。
(1)式[1]
(式中、Rは炭素数2〜10のアルキル基を表す。)
で表されるジアルキルシクロブタン−1,2,3,4−テトラカルボン酸−1,2:3,4−二無水物化合物。
(2)Rがエチル基である(1)記載のジアルキルシクロブタン−1,2,3,4−テトラカルボン酸−1,2:3,4−二無水物化合物。
(3)式[2]
で表される(1)記載のジアルキルシクロブタン−1,2,3,4−テトラカルボン酸−1,2:3,4−二無水物化合物。
(4)式[3]
で表される(1)記載のジアルキルシクロブタン−1,2,3,4−テトラカルボン酸−1,2:3,4−二無水物化合物。
(5)式[4]
(式中、Rは炭素数2〜10のアルキル基を表す。)
で表されるアルキルマレイン酸無水物化合物を光二量化させることを特徴とする式[1]
(式中、Rは炭素数2〜10のアルキル基を表す。)
で表されるジアルキルシクロブタン−1,2,3,4−テトラカルボン酸−1,2:3,4−二無水物化合物の製造法。
(6)Rがエチル基である(5)記載のジアルキルシクロブタン−1,2,3,4−テトラカルボン酸−1,2:3,4−二無水物化合物の製造法。
(7)式[2]
で表される(5)記載のジアルキルシクロブタン−1,2,3,4−テトラカルボン酸−1,2:3,4−二無水物化合物の製造方法。
(8)式[3]
で表される(5)記載のジアルキルシクロブタン−1,2,3,4−テトラカルボン酸−1,2:3,4−二無水物化合物の製造方法。
(9)光二量化反応溶媒が脂肪族エステルであることを特徴とする(5)記載のジアルキルシクロブタン−1,2,3,4−テトラカルボン酸−1,2:3,4−二無水物化合物の製造法。
(10)光二量化反応溶媒が酢酸エチルであることを特徴とする(9)記載のジアルキルシクロブタン−1,2,3,4−テトラカルボン酸−1,2:3,4−二無水物化合物の製造法。
(11)光二量化反応の光源が高圧水銀灯であることを特徴とする(5)記載のジアルキルシクロブタン−1,2,3,4−テトラカルボン酸−1,2:3,4−二無水物化合物の製造法。
(12)光二量化反応の光源波長が300〜600nmであることを特徴とする(11)記載のジアルキルシクロブタン−1,2,3,4−テトラカルボン酸−1,2:3,4−二無水物化合物の製造法。
紫外線領域に吸収がなく光透過性が高く、溶媒溶解性が改善された液晶表示素子や半導体における保護材料、絶縁材料などの電子材料、更に光導波路等の光通信用材料としての用途が期待される光学材料用ポリイミドの原料モノマーとなり得る脂環式テトラカルボン酸二無水物及びその製造法を提供できる。
以下、本発明を詳細に説明する。
本発明は、式[1]
本発明は、式[1]
(式中、Rは炭素数2〜10のアルキル基を表す。)
で表されるジアルキルシクロブタン−1,2,3,4−テトラカルボン酸−1,2:3,4−二無水物化合物(DACBDA化合物と略す。)を提供する。
で表されるジアルキルシクロブタン−1,2,3,4−テトラカルボン酸−1,2:3,4−二無水物化合物(DACBDA化合物と略す。)を提供する。
DACBDAは、具体的には、1,3−ジアルキルシクロブタン−1,2,3,4−テトラカルボン酸−1,2:3,4−二無水物化合物(1,3−DACBDA化合物と略す。)及び1,4−ジアルキルシクロブタン−1,2,3,4−テトラカルボン酸−1,2:3,4−二無水物化合物(1,4−DACBDA化合物と略す。)として表される。
(式中、Rは炭素数2〜10のアルキル基を表す。)
ここで、Rの具体例としては、エチル基、n−プロピル基、i−プロピル基、n−ブチル基、i−ブチル基、n−ペンチル基、n−ヘキシル基、n−ヘプチル基、n−オクチル基、n−ノニル基及びn−デシル基等が挙げられる。
なお、nはノルマルを、iはイソを表す。
ここで、Rの具体例としては、エチル基、n−プロピル基、i−プロピル基、n−ブチル基、i−ブチル基、n−ペンチル基、n−ヘキシル基、n−ヘプチル基、n−オクチル基、n−ノニル基及びn−デシル基等が挙げられる。
なお、nはノルマルを、iはイソを表す。
特に、本発明は、式[2]
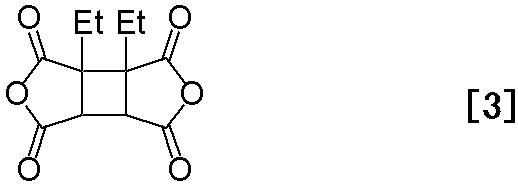
で表される1,3−ジエチルシクロブタン−1,2,3,4−テトラカルボン酸−1,2:3,4−二無水物(1,3−DECBDAと略す。)及び式[3]
で表される1,4−ジエチルシクロブタン−1,2,3,4−テトラカルボン酸−1,2:3,4−二無水物(1,4−DECBDAと略す。)を提供する。
本発明のDACBDA化合物の製造法は、下記のスキームで表される。
本発明のDACBDA化合物の製造法は、下記のスキームで表される。
(式中、Rは炭素数2〜10のアルキル基を表す。)
即ち、式[4]で表される無水アルキルマレイン酸化合物(AMA化合物と略す。)を光二量化して、1,3−DACBDA化合物及び1,4−DACBDA化合物の混合物を得ることができる。
先ず、無水マレイン酸化合物の一例としては、エチルマレイン酸無水物、イソプロピルマレイン酸無水物、n−ブチルマレイン酸無水物、n−ペンチルマレイン酸無水物、n−ヘキシルマレイン酸無水物、n−ヘプチルマレイン酸無水物、n−オクチルマレイン酸無水物、n−ノニルマレイン酸無水物、n−デシルマレイン酸無水物等が挙げられる。
即ち、式[4]で表される無水アルキルマレイン酸化合物(AMA化合物と略す。)を光二量化して、1,3−DACBDA化合物及び1,4−DACBDA化合物の混合物を得ることができる。
先ず、無水マレイン酸化合物の一例としては、エチルマレイン酸無水物、イソプロピルマレイン酸無水物、n−ブチルマレイン酸無水物、n−ペンチルマレイン酸無水物、n−ヘキシルマレイン酸無水物、n−ヘプチルマレイン酸無水物、n−オクチルマレイン酸無水物、n−ノニルマレイン酸無水物、n−デシルマレイン酸無水物等が挙げられる。
ここで本発明の原料の一つであるエチルマレイン酸無水物の製造法は、特に限定されるものではなく、例えば、文献、ジャーナル オブ オルガニック ケミストリー(Journal of Organic Chemistry)、1996年、第61巻、p.6296〜6301に記載されている下記の方法を挙げることができる。
即ち、第一工程でジメチルアセチレンジカルボキシレート(DMADと略す。)とエチルマグネシウムブロマイドを臭化銅とジメチルスルフィドの存在下、テトラヒドロフラン(THF)溶媒中反応させることによりエチルマレイン酸ジメチルエステル(EMMと略す。)を得る。続いて、EMMを水酸化リチウムで加水分解した後、塩酸水で酸性化脱水閉環させることにより、目的のエチルマレイン酸無水物(EMAと略す。)を製造している。
本反応で重要な役割を果たしているのが反応溶媒である。その具体例を挙げると、ギ酸メチル、ギ酸エチル、ギ酸n−プロピル、ギ酸i−プロピル、ギ酸i−ブチル、酢酸メチル、酢酸エチル、酢酸n−プロピル、酢酸i−プロピル、酢酸i−ブチル、プロピオン酸メチル、プロピオン酸エチル、プロピオン酸n−プロピル、プロピオン酸i−プロピル、エチレングリコールジホルメート、エチレングリコールジアセテート、エチレングリコールジプロピオネート等を列記することができる。
これらの中でより好ましい溶媒は、ギ酸エチル、酢酸メチル、酢酸エチル、酢酸i−プロピル、酢酸i−ブチル、エチレングリコールジホルメート、エチレングリコールジアセテート等であり、最も好ましい溶媒は、酢酸エチルである。
これらの中でより好ましい溶媒は、ギ酸エチル、酢酸メチル、酢酸エチル、酢酸i−プロピル、酢酸i−ブチル、エチレングリコールジホルメート、エチレングリコールジアセテート等であり、最も好ましい溶媒は、酢酸エチルである。
酢酸エチルやエチレングリコールジアセテートを溶媒とする方法の優れた特徴は、原料の無水マレイン酸化合物の溶解度が高いにも拘わらず、生成したDACBDA化合物の溶解度が低く結晶として析出するために、DACBDA化合物からのAMA化合物への逆反応やオリゴマー生成等の副反応を抑制することができる。
溶媒の使用量は、AMA化合物に対し3〜50重量倍、より好ましくは5〜20重量倍である。
溶媒の使用量は、AMA化合物に対し3〜50重量倍、より好ましくは5〜20重量倍である。
本反応では、光の波長が重要である。低圧水銀灯(内部照射)、高圧水銀灯(内部照射)、超高圧水銀灯(外部照射)、キセノンランプ(外部照射)の中で高圧水銀灯が、特異的に高収率でDACBDA化合物を与えた。更に、光源冷却管を石英ガラスからパイレックスガラスに変えることにより、光源冷却管への着色ポリマー付着が減少し、DACBDA化合物の収率改善が見られる。即ち、高圧水銀灯の300nm以下の領域の波長が、ポリマー生成やAMA化合物への逆反応に関与し、300〜600nmの波長が好ましいことが判明した。更に、光効率上、内部照射型光源が、DACBDA化合物生成に好ましい結果を与える。
反応温度は、高温になると重合物が副生し、又低温になるとAMA化合物の溶解度が低下し生産効率が減少するところから、−20〜80℃で行うことが好ましい。更に好ましくは−10〜50℃であり、特に0〜20℃間では、副生物の生成が大幅に抑制され、高い選択率及び収率でDACBDA化合物を与える。
反応時間は、1〜100時間で行うことができ、通常5〜50時間で行うのが実用的である。
反応後は、濃縮し生成したDACBDA化合物の結晶を濾過・溶媒洗浄により高純度のDACBDA化合物が得られる。
光二量化反応の代表的製造例は、特開昭59−212495公報に記載がある。
上記各反応及び後処理は、バッチ式又は流通式で行うことが出来、又常圧でも加圧でも行うことができる。
光二量化反応の代表的製造例は、特開昭59−212495公報に記載がある。
上記各反応及び後処理は、バッチ式又は流通式で行うことが出来、又常圧でも加圧でも行うことができる。
以下に実施例を挙げ、本発明を具体的に説明するが、本発明はこれらに限定されるものではない。
尚、実施例で用いた分析法は以下の通りである。
[1] [1H NMR]
機種:ECP500(JEOL),測定溶媒:DMSO−d6
[2] [13C NMR]
機種:ECP500(JEOL),測定溶媒:DMSO−d6
[3][融点(mp.)]
測定機器:自動融点測定装置、FP62 (METTLER TOLEDO)
尚、実施例で用いた分析法は以下の通りである。
[1] [1H NMR]
機種:ECP500(JEOL),測定溶媒:DMSO−d6
[2] [13C NMR]
機種:ECP500(JEOL),測定溶媒:DMSO−d6
[3][融点(mp.)]
測定機器:自動融点測定装置、FP62 (METTLER TOLEDO)
第1の内容積2Lパイレックス(登録商標)ガラス製四つ口反応フラスコに臭化銅・ジメチルスルフィド62g(302mmol)及びテトラヒドロフラン(THF)390gを仕込み、−40℃に冷却下で140〜160rpmの回転速度で攪拌しながら0.97M/Lエチルマグネシウムブロマイド311mL(302mmol)を20分かけて滴下し、同温度で2時間攪拌した。次に−60℃以下に冷却しジメチルアセチレンジカルボキシレート39.0g(274mmol)とTHF78gの混合液を30分かけて滴下し、更に同温度で1時間攪拌し反応混合液を得た。
続いて、第2の内容積2Lパイレックス(登録商標)ガラス製四つ口反応フラスコにトルエン117gと20%塩化アンモニウム507gを仕込み5℃に冷却中に、前記第1反応器で得られた反応混合液を滴下した。この混合液を20℃で30分攪拌すると無機塩が析出した。セライト濾過後分液し有機層を濃縮すると塩が析出したので濾過してから、トルエン195gと1N塩酸水195gの混合液を滴下すると浮遊物が発生し分液後、有機層に水78gを滴下し洗浄後分液し有機層を得た。これを濃縮すると油状物41.1g(GC純度92.9%:得率87.1%)が得られた。この油状物は、以下の1H NMR解析によってエチルマレイン酸ジメチルエステル(EMM)であることを確認した。
続いて、第2の内容積2Lパイレックス(登録商標)ガラス製四つ口反応フラスコにトルエン117gと20%塩化アンモニウム507gを仕込み5℃に冷却中に、前記第1反応器で得られた反応混合液を滴下した。この混合液を20℃で30分攪拌すると無機塩が析出した。セライト濾過後分液し有機層を濃縮すると塩が析出したので濾過してから、トルエン195gと1N塩酸水195gの混合液を滴下すると浮遊物が発生し分液後、有機層に水78gを滴下し洗浄後分液し有機層を得た。これを濃縮すると油状物41.1g(GC純度92.9%:得率87.1%)が得られた。この油状物は、以下の1H NMR解析によってエチルマレイン酸ジメチルエステル(EMM)であることを確認した。
1H NMR(CDCl3,δppm):1.1217(t,J=7.41Hz,3H),2.4033(dd,J1=5.76Hz,J2=8.70Hz,2H),3.7278(s,3H),3.8377(s,3H),5.8138(s,1H)
内容積1Lパイレックス(登録商標)ガラス製四つ口反応フラスコに参考例1で得られたEMM41.1g(GC純度92.9%:239mmol)及びメタノール41.1gを仕込み、40℃で攪拌中に3%水酸化リチウム411g(515mmol)を滴下し1.5時間攪拌した。ここにトルエン82.2gを滴下し分液後、有機層を123gまで濃縮した。続いて残渣を内容積3Lパイレックス(登録商標)ガラス製四つ口反応フラスコに移し、トルエン2055gを滴下し、続いて6N塩酸100g(549mmol)を滴下し60℃で30分攪拌した後分液した。水層にトルエン2055gを滴下し60℃で30分攪拌した後分液した。この抽出操作をもう一度繰り返して得られたトルエン溶液を混合して濃縮し、黒色粗油状物25.1gを得た。これを蒸留すると沸点79℃/667Paの留分18.2g(GC純度92%;収率67.4%)が得られた。
この油状物は、以下の1H NMR及び13C NMR解析によってエチルマレイン酸無水物(EMA)であることを確認した。
この油状物は、以下の1H NMR及び13C NMR解析によってエチルマレイン酸無水物(EMA)であることを確認した。
1H NMR(CDCl3,δppm):1.2545(t,J=7.41Hz,3H),2.5658(dd,J1=5.76Hz,J2=8.70Hz,2H),6.6068(s,1H)
13C NMR(CDCl3,δppm):10.4739,19.3822,128.2133,154.7703,163.9153,165.60899
13C NMR(CDCl3,δppm):10.4739,19.3822,128.2133,154.7703,163.9153,165.60899
内容積300mlパイレックス(登録商標)ガラス製四つ口光反応フラスコにエチルマレイン酸無水物(EMA)9.0g(71.4mmol)及び酢酸エチル90gを仕込み、5℃で攪拌しながら100W高圧水銀灯を25時間照射した。反応終了後18gまで濃縮してから得られた結晶を濾過し、酢酸エチル洗浄してから減圧乾燥することにより白色一次結晶3.0g(1,3−DECBDA:1,4−DECBDA=61.9:38.1)(収率33.3%)が得られた。
又、得られた濾液を濃縮すると粗結晶6.89gが得られた。この結晶にトルエン9gを加えて80℃に加温攪拌してから30℃に冷却してから濾過し、トルエン洗浄した後減圧乾燥することにより白色二次結晶1.8g(1,3−DECBDA:1,4−DECBDA=20.9:79.1)(収率20.0%)が得られた。
この一次結晶は、以下のGC−MASS、1H NMR及び13C NMR解析によって1,3−ジエチルシクロブタン−1,2,3,4−テトラカルボン酸−1,2:3,4−二無水物(1,3−DECBDA)と1,4−ジエチルシクロブタン−1,2,3,4−テトラカルボン酸−1,2:3,4−二無水物(1,4−DECBDA)の混合物であることを確認した。
又、得られた濾液を濃縮すると粗結晶6.89gが得られた。この結晶にトルエン9gを加えて80℃に加温攪拌してから30℃に冷却してから濾過し、トルエン洗浄した後減圧乾燥することにより白色二次結晶1.8g(1,3−DECBDA:1,4−DECBDA=20.9:79.1)(収率20.0%)が得られた。
この一次結晶は、以下のGC−MASS、1H NMR及び13C NMR解析によって1,3−ジエチルシクロブタン−1,2,3,4−テトラカルボン酸−1,2:3,4−二無水物(1,3−DECBDA)と1,4−ジエチルシクロブタン−1,2,3,4−テトラカルボン酸−1,2:3,4−二無水物(1,4−DECBDA)の混合物であることを確認した。
一次結晶解析結果:
GC−MASS(EI+,m/e(%))(主成分):253([M+H]+,1),180(26),152(25),108(55),93(100)
GC−MASS(EI+,m/e(%))(副成分):253([M+H]+,1),206(8),178(13),152(14),108(25),93(100)
1H NMR(DMSO−d6,δppm):0.849−0.908(m,6H),1.762−1.891(m,4H),2.499−2.510(m,2H)、4.115/4.261(積分値:1.00/1.584)
13C NMR(DMSO−d6,δppm)(主成分):7.5461,23.2882,46.4014,48.6143,167.6449,172.0860(各炭素2個分を表す)
13C NMR(DMSO−d6,δppm)(副成分):7.8208,24.1123,40.8231,54.8715,168.8277,170.9414(各炭素2個分を表す):
融点(mp.)191.5℃(白色一次結晶)
GC−MASS(EI+,m/e(%))(主成分):253([M+H]+,1),180(26),152(25),108(55),93(100)
GC−MASS(EI+,m/e(%))(副成分):253([M+H]+,1),206(8),178(13),152(14),108(25),93(100)
1H NMR(DMSO−d6,δppm):0.849−0.908(m,6H),1.762−1.891(m,4H),2.499−2.510(m,2H)、4.115/4.261(積分値:1.00/1.584)
13C NMR(DMSO−d6,δppm)(主成分):7.5461,23.2882,46.4014,48.6143,167.6449,172.0860(各炭素2個分を表す)
13C NMR(DMSO−d6,δppm)(副成分):7.8208,24.1123,40.8231,54.8715,168.8277,170.9414(各炭素2個分を表す):
融点(mp.)191.5℃(白色一次結晶)
内容積300mlパイレックス(登録商標)ガラス製四つ口光反応フラスコにエチルマレイン酸無水物(EMA)8.5g(67.4mmol)及び酢酸エチル85gを仕込み、5℃で攪拌しながら100W高圧水銀灯を25時間照射した。反応終了後17gまで濃縮してから得られた結晶を濾過し、酢酸エチル:トルエン=1:1で洗浄してから減圧乾燥することにより白色結晶2.4g(1,3−DECBDA:1,4−DECBDA=66.9:33.1:mp.197.1〜199.2℃)(収率28.8%)が得られた。
又、得られた濾液を濃縮すると粗結晶6.8gが得られた。この結晶にトルエン8.5gを加えて80℃に加温攪拌してから30℃に冷却ししてから濾過し、トルエン洗浄した後減圧乾燥することにより白色二次結晶2.13g(1,3−DECBDA:1,4−DECBDA=12.2:87.8)(収率25.1%)が得られた。
又、得られた濾液を濃縮すると粗結晶6.8gが得られた。この結晶にトルエン8.5gを加えて80℃に加温攪拌してから30℃に冷却ししてから濾過し、トルエン洗浄した後減圧乾燥することにより白色二次結晶2.13g(1,3−DECBDA:1,4−DECBDA=12.2:87.8)(収率25.1%)が得られた。
Claims (12)
- Rがエチル基である請求項1記載のジアルキルシクロブタン−1,2,3,4−テトラカルボン酸−1,2:3,4−二無水物化合物。
- Rがエチル基である請求項5記載のジアルキルシクロブタン−1,2,3,4−テトラカルボン酸−1,2:3,4−二無水物化合物の製造法。
- 光二量化反応溶媒が脂肪族エステルであることを特徴とする請求項5記載のジアルキルシクロブタン−1,2,3,4−テトラカルボン酸−1,2:3,4−二無水物化合物の製造法。
- 光二量化反応溶媒が酢酸エチルであることを特徴とする請求項9記載のジアルキルシクロブタン−1,2,3,4−テトラカルボン酸−1,2:3,4−二無水物化合物の製造法。
- 光二量化反応の光源が高圧水銀灯であることを特徴とする請求項5記載のジアルキルシクロブタン−1,2,3,4−テトラカルボン酸−1,2:3,4−二無水物化合物の製造法。
- 光二量化反応の光源波長が300〜600nmであることを特徴とする請求項11記載のジアルキルシクロブタン−1,2,3,4−テトラカルボン酸−1,2:3,4−二無水物化合物の製造法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2005174685A JP2006347931A (ja) | 2005-06-15 | 2005-06-15 | ジアルキルシクロブタン酸二無水物及びその製造法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2005174685A JP2006347931A (ja) | 2005-06-15 | 2005-06-15 | ジアルキルシクロブタン酸二無水物及びその製造法 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2006347931A true JP2006347931A (ja) | 2006-12-28 |
Family
ID=37644135
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2005174685A Pending JP2006347931A (ja) | 2005-06-15 | 2005-06-15 | ジアルキルシクロブタン酸二無水物及びその製造法 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2006347931A (ja) |
Cited By (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2015108169A1 (ja) * | 2014-01-17 | 2015-07-23 | 日産化学工業株式会社 | シクロブタンテトラカルボン酸誘導体の製造方法 |
| WO2015108166A1 (ja) * | 2014-01-17 | 2015-07-23 | 日産化学工業株式会社 | シクロブタンテトラカルボン酸誘導体の製造方法 |
| WO2015108167A1 (ja) * | 2014-01-17 | 2015-07-23 | 日産化学工業株式会社 | シクロブタンテトラカルボン酸誘導体の製造方法 |
| WO2015108171A1 (ja) * | 2014-01-17 | 2015-07-23 | 日産化学工業株式会社 | 高純度の1,3-ジアルキルシクロブタン-1,2,3,4-テトラカルボン酸-1,2:3,4-二無水物の製造方法 |
| WO2015108168A1 (ja) * | 2014-01-17 | 2015-07-23 | 日産化学工業株式会社 | シクロブタンテトラカルボン酸誘導体の製造方法 |
| KR20170003949A (ko) | 2014-05-09 | 2017-01-10 | 닛산 가가쿠 고교 가부시키 가이샤 | 1,3-디치환 시클로부탄-1,2,3,4-테트라카르복실산 및 그 산 2 무수물의 신규의 제조 방법 |
| CN109422762A (zh) * | 2017-08-29 | 2019-03-05 | Jsr株式会社 | 环丁烷衍生物的制造方法 |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS58208322A (ja) * | 1982-05-31 | 1983-12-05 | Japan Synthetic Rubber Co Ltd | ポリイミド化合物の製造方法 |
| JPS59212495A (ja) * | 1983-05-19 | 1984-12-01 | Nissan Chem Ind Ltd | 1,2,3,4−シクロブタンテトラカルボン酸−1,2「い」3,4−ジ無水物の製造方法 |
| JPH04106127A (ja) * | 1990-08-28 | 1992-04-08 | Chisso Corp | 溶媒可溶性ポリイミド、その製造法及びカラーフィルター用材料 |
| JPH0980443A (ja) * | 1995-09-08 | 1997-03-28 | Japan Synthetic Rubber Co Ltd | ポリアミック酸、ポリイミドおよび液晶配向剤 |
| JP2003192685A (ja) * | 2001-12-26 | 2003-07-09 | Nissan Chem Ind Ltd | シクロブタンテトラカルボン酸二無水物化合物の製造法 |
-
2005
- 2005-06-15 JP JP2005174685A patent/JP2006347931A/ja active Pending
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS58208322A (ja) * | 1982-05-31 | 1983-12-05 | Japan Synthetic Rubber Co Ltd | ポリイミド化合物の製造方法 |
| JPS59212495A (ja) * | 1983-05-19 | 1984-12-01 | Nissan Chem Ind Ltd | 1,2,3,4−シクロブタンテトラカルボン酸−1,2「い」3,4−ジ無水物の製造方法 |
| JPH04106127A (ja) * | 1990-08-28 | 1992-04-08 | Chisso Corp | 溶媒可溶性ポリイミド、その製造法及びカラーフィルター用材料 |
| JPH0980443A (ja) * | 1995-09-08 | 1997-03-28 | Japan Synthetic Rubber Co Ltd | ポリアミック酸、ポリイミドおよび液晶配向剤 |
| JP2003192685A (ja) * | 2001-12-26 | 2003-07-09 | Nissan Chem Ind Ltd | シクロブタンテトラカルボン酸二無水物化合物の製造法 |
Cited By (29)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPWO2015108167A1 (ja) * | 2014-01-17 | 2017-03-23 | 日産化学工業株式会社 | シクロブタンテトラカルボン酸誘導体の製造方法 |
| WO2015108168A1 (ja) * | 2014-01-17 | 2015-07-23 | 日産化学工業株式会社 | シクロブタンテトラカルボン酸誘導体の製造方法 |
| WO2015108169A1 (ja) * | 2014-01-17 | 2015-07-23 | 日産化学工業株式会社 | シクロブタンテトラカルボン酸誘導体の製造方法 |
| WO2015108171A1 (ja) * | 2014-01-17 | 2015-07-23 | 日産化学工業株式会社 | 高純度の1,3-ジアルキルシクロブタン-1,2,3,4-テトラカルボン酸-1,2:3,4-二無水物の製造方法 |
| JPWO2015108171A1 (ja) * | 2014-01-17 | 2017-03-23 | 日産化学工業株式会社 | 高純度の1,3−ジアルキルシクロブタン−1,2,3,4−テトラカルボン酸−1,2:3,4−二無水物の製造方法 |
| CN105916865A (zh) * | 2014-01-17 | 2016-08-31 | 日产化学工业株式会社 | 环丁烷四羧酸衍生物的制造方法 |
| CN105916863A (zh) * | 2014-01-17 | 2016-08-31 | 日产化学工业株式会社 | 高纯度的1,3-二烷基环丁烷-1,2,3,4-四羧酸-1,2:3,4-二酐的制造方法 |
| CN105916867A (zh) * | 2014-01-17 | 2016-08-31 | 日产化学工业株式会社 | 环丁烷四羧酸衍生物的制造方法 |
| CN105916866A (zh) * | 2014-01-17 | 2016-08-31 | 日产化学工业株式会社 | 环丁烷四羧酸衍生物的制造方法 |
| KR20160107175A (ko) | 2014-01-17 | 2016-09-13 | 닛산 가가쿠 고교 가부시키 가이샤 | 시클로부탄테트라카르복실산 유도체의 제조 방법 |
| KR20160108331A (ko) * | 2014-01-17 | 2016-09-19 | 닛산 가가쿠 고교 가부시키 가이샤 | 고순도의 1,3-디알킬시클로부탄-1,2,3,4-테트라카르복실산-1,2:3,4-2무수물의 제조 방법 |
| TWI648280B (zh) * | 2014-01-17 | 2019-01-21 | 日商日產化學工業股份有限公司 | Method for producing cyclobutane tetracarboxylic acid derivative |
| KR102653978B1 (ko) * | 2014-01-17 | 2024-04-02 | 닛산 가가쿠 가부시키가이샤 | 시클로부탄테트라카르복실산 유도체의 제조 방법 |
| JPWO2015108169A1 (ja) * | 2014-01-17 | 2017-03-23 | 日産化学工業株式会社 | シクロブタンテトラカルボン酸誘導体の製造方法 |
| WO2015108167A1 (ja) * | 2014-01-17 | 2015-07-23 | 日産化学工業株式会社 | シクロブタンテトラカルボン酸誘導体の製造方法 |
| WO2015108166A1 (ja) * | 2014-01-17 | 2015-07-23 | 日産化学工業株式会社 | シクロブタンテトラカルボン酸誘導体の製造方法 |
| KR20160108333A (ko) | 2014-01-17 | 2016-09-19 | 닛산 가가쿠 고교 가부시키 가이샤 | 시클로부탄테트라카르복실산 유도체의 제조 방법 |
| TWI649323B (zh) * | 2014-01-17 | 2019-02-01 | 日商日產化學工業股份有限公司 | Method for producing cyclobutane tetracarboxylic acid derivative |
| TWI649324B (zh) * | 2014-01-17 | 2019-02-01 | 日商日產化學工業股份有限公司 | Method for producing cyclobutane tetracarboxylic acid derivative |
| TWI650304B (zh) * | 2014-01-17 | 2019-02-11 | 日商日產化學工業股份有限公司 | 環丁烷四羧酸衍生物之製造方法 |
| TWI650323B (zh) * | 2014-01-17 | 2019-02-11 | 日商日產化學工業股份有限公司 | 高純度之1,3-二烷基環丁烷-1,2,3,4-四羧酸-1,2:3,4-二酐之製造方法 |
| KR102492874B1 (ko) * | 2014-01-17 | 2023-01-27 | 닛산 가가쿠 가부시키가이샤 | 시클로부탄테트라카르복실산 유도체의 제조 방법 |
| KR102254089B1 (ko) | 2014-01-17 | 2021-05-18 | 닛산 가가쿠 가부시키가이샤 | 시클로부탄테트라카르복실산 유도체의 제조 방법 |
| KR102324576B1 (ko) * | 2014-01-17 | 2021-11-09 | 닛산 가가쿠 가부시키가이샤 | 고순도의 1,3-디알킬시클로부탄-1,2,3,4-테트라카르복실산-1,2:3,4-2무수물의 제조 방법 |
| KR20210149881A (ko) | 2014-01-17 | 2021-12-09 | 닛산 가가쿠 가부시키가이샤 | 시클로부탄테트라카르복실산 유도체의 제조 방법 |
| KR20220063315A (ko) * | 2014-01-17 | 2022-05-17 | 닛산 가가쿠 가부시키가이샤 | 시클로부탄테트라카르복실산 유도체의 제조 방법 |
| KR20170003949A (ko) | 2014-05-09 | 2017-01-10 | 닛산 가가쿠 고교 가부시키 가이샤 | 1,3-디치환 시클로부탄-1,2,3,4-테트라카르복실산 및 그 산 2 무수물의 신규의 제조 방법 |
| CN109422762B (zh) * | 2017-08-29 | 2022-04-05 | Jsr株式会社 | 环丁烷衍生物的制造方法 |
| CN109422762A (zh) * | 2017-08-29 | 2019-03-05 | Jsr株式会社 | 环丁烷衍生物的制造方法 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2006347931A (ja) | ジアルキルシクロブタン酸二無水物及びその製造法 | |
| JP6145571B2 (ja) | 新規酸二無水物、及びこの製造方法 | |
| JP2016179969A (ja) | フルオレン骨格を有するジアミン、ポリアミック酸、及びポリイミド | |
| JP4336933B2 (ja) | 脂環式テトラカルボン酸二無水物、その製造法及びポリイミド | |
| JP2003192685A (ja) | シクロブタンテトラカルボン酸二無水物化合物の製造法 | |
| JP5637132B2 (ja) | ケージ状シクロペンタン酸二無水物化合物、その製造法およびポリイミド | |
| JP2004182962A (ja) | トリプチセン骨格を有するポリイミド樹脂及び光部品 | |
| JP6266940B2 (ja) | アリーレンジオキシ−ビス(無水コハク酸)及びその製造方法 | |
| JP4535233B2 (ja) | 脂環式テトラカルボン酸二無水物、その製造法及びポリイミド | |
| JP4210827B2 (ja) | 脂環式テトラカルボン酸二無水物、その製造法及びポリイミド | |
| WO2020250920A1 (ja) | エステル基含有酸二無水物誘導体の製造方法 | |
| JP4371207B2 (ja) | 脂環式スピロ型ポリイミド | |
| JP7238200B1 (ja) | ビナフチルカルボン酸の製造方法 | |
| JP2013028571A (ja) | ビスフェノールジエステル型酸二無水物、その製造法及びポリイミド | |
| JP5754344B2 (ja) | テトラハイドロペンタレン型酸二無水物、その製造法及びポリイミド | |
| JP2004018422A (ja) | 脂環式スピロ酸二無水物及びその製造法 | |
| JP2010126499A (ja) | ナフタロシアニン化合物及びその製造方法 | |
| WO2015108171A1 (ja) | 高純度の1,3-ジアルキルシクロブタン-1,2,3,4-テトラカルボン酸-1,2:3,4-二無水物の製造方法 | |
| JP4541774B2 (ja) | ビス含フッ素フタル酸無水物の製造方法 | |
| JPH08119939A (ja) | 高純度エーテル型ビスマレイミドの製造方法 | |
| JP2013056869A (ja) | 側鎖置換エチレンジエステル型酸二無水物、その製造法及びポリイミド | |
| WO2013069646A1 (ja) | 4,4'-スルホニルジフェニルエステル型酸二無水物、その製造法及びポリイミド | |
| JP2004203792A (ja) | 4−クロロホルミル−シクロヘキサン−1,2−ジカルボン酸無水物及びその製造方法。 | |
| JP6429357B2 (ja) | 脂環式テトラカルボン酸の製造方法 | |
| JP2013091628A (ja) | m−フェニレンジエステル型酸二無水物、その製造法及びポリイミド |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20080611 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20110420 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20110427 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20110908 |