ES2928202T3 - Compuestos químicos - Google Patents
Compuestos químicos Download PDFInfo
- Publication number
- ES2928202T3 ES2928202T3 ES21180706T ES21180706T ES2928202T3 ES 2928202 T3 ES2928202 T3 ES 2928202T3 ES 21180706 T ES21180706 T ES 21180706T ES 21180706 T ES21180706 T ES 21180706T ES 2928202 T3 ES2928202 T3 ES 2928202T3
- Authority
- ES
- Spain
- Prior art keywords
- oph
- nmr
- mhz
- mmol
- ipso
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H19/00—Compounds containing a hetero ring sharing one ring hetero atom with a saccharide radical; Nucleosides; Mononucleotides; Anhydro-derivatives thereof
- C07H19/02—Compounds containing a hetero ring sharing one ring hetero atom with a saccharide radical; Nucleosides; Mononucleotides; Anhydro-derivatives thereof sharing nitrogen
- C07H19/04—Heterocyclic radicals containing only nitrogen atoms as ring hetero atom
- C07H19/06—Pyrimidine radicals
- C07H19/10—Pyrimidine radicals with the saccharide radical esterified by phosphoric or polyphosphoric acids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
Abstract
Se describen derivados de fosforamidato de nucleótidos y su uso en el tratamiento del cáncer. Los restos básicos de, por ejemplo, cada uno de desoxiuridina, citarabina, gemcitabina y citidina pueden estar sustituidos en la posición 5. El resto de fosforamidato tiene unido al átomo de P un resto de arilo-O y un resto de α-aminoácido. El resto de α-aminoácido puede corresponder o derivar de un aminoácido natural o no natural. (Traducción automática con Google Translate, sin valor legal)
Description
DESCRIPCIÓN
Compuestos químicos
La presente invención se relaciona con derivados de nucleótidos adecuados para su uso en el tratamiento de cáncer.
Los análogos de nucleósidos tales como fluorodesoxiuridina (1), citarabina (2) y gemcitabina (3) están bien constituidos como agentes contra el cáncer. Funcionan como inhibidores de síntesis de ADN después de activación con su forma de 5'-fosfato.
Las formas de fosfatos bioactivos libres no representan en general, fármacos útiles debido a su pobre permeación de membrana. En un esfuerzo para evitar esto se ha reportado una serie de métodos de profármaco de fosfato [Rosowsky et al, J. Med. Chem., 1982, 25, 171-8; Hong et al, J. Med. Chem., 1985, 28, 171-8; Kodama et al, Jpn. J. Cancer Res., 1989, 80, 679-85; Hong et al, 1979, 22, 1428-32; Ji et al, J. Med. Chem., 1990, 33, 2264-70; Jones et al, Nucleic Acids Res., 1989, 17, 7195-7201; Houston et al, J. Med. Chem., 1984, 27, 440-4; Lorey et al, Nucleosides Nucleotides, 1997, 16, 1307-10; Farquhar et al, J. Med. Chem., 1983, 26, 1153-8; Shuto et al, Nucleosides Nucleotides, 1992, 11, 437-46; Le Bec et al, Tet. Letts., 1991, 32, 6553-6; Phelps et al, J. Med. Chem., 1980, 23, 1229-32].
El documento US 2003/109697 A1 divulga compuestos de 5'-fosforamidatilo, pirimidina 1,5-sustituida, derivados, análogos y sales farmacéuticamente aceptables de los mismos para uso en métodos para tratar el cáncer, enfermedades infecciosas, un trastorno autoinmune o una afección inflamatoria. El documento WO 01/07454 A también divulga un método para tratar a un sujeto administrándole un profármaco.
En general, los profármacos de fosfato tienen propiedades biológicas y actividades terapéuticas que son similares a, o algo menores que, el análogo de nucleósido progenitor.
Se ha llevado a cabo un extenso trabajo en esta área desde una perspectiva antiviral, en gran medida sobre nucleósidos didesoxi, y han informado de un método de fosforamidato que se ha adoptado ampliamente para el suministro de fosfatos bio-activos de nucleósidos antivirales.
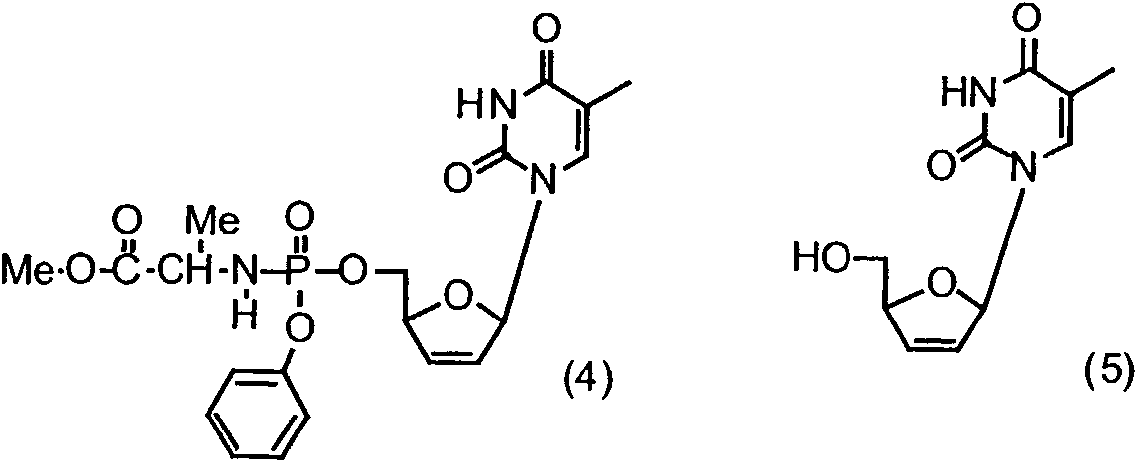
Un ejemplo es el fosforamidato (4) derivado de anti-VIH d4T (5).
Se observó el efecto de variaciones en regiones de éster [McGuigan et al, AVCC, 1998, 9, 473-9], aminoácido [McGuigan et al, Antiviral Res, 1997, 35, 195-204.; AVCC, 2000, 11, 111-6], y arilo [Siddiqui et al, J. Med. Chem., 1999, 42, 393-9] del fosforamidato, así como el efecto de la estereoquímica de aminoácidos [McGuigan et al, AVCC, 1996, 7, 184-8], estereoquímica de fosfato [Allender et al, Analytica Chim . Acta, 2001, 435, 107-13] y nucleósido [Balzarini et al, BBRC, 1996, 225, 363-9; McGuigan et al, Bioorg. Med, Chem. Lett, 1996, 6, 2369-62.; McGuigan et al, Bioorg. Med. Chem. Lett., 2000, 10, 645-7].
Este trabajo ha dado lugar a la descripción óptima de fosforamidato de fenil metoxialaninilo como la pro-unidad estructural prototipo para el suministro intracelular de nucleótidos bioactivos [Balzarini et al, PNAS, 1996, 93, 7295-9; McGuigan et al, J. Med. Chem., 1996, 39, 1748-1753].
Lackey et al [Biochem Pharmacol., 2001,61, 179-89] han reportado la aplicación de nuestro método de profármaco de fosforamidato para nucleósidos antivirales para el agente anti-herpético bromovinil-2’- desoxiuridina (BVDU) (6). En particular, han encontrado que el fosforamidato de fenil metoxialaninilo (7) tiene una actividad significativa contra el cáncer. Esto está en marcado contraste con el nucleósido (antiviral) progenitor (6).
Limited SAR ha sido presentada por este grupo, aunque en sus solicitudes de patentes [WO0239952, EP1200455, CA2317505, US6339151, EP116797, AU2451601] reivindican una serie de variaciones generales en la base, y las regiones de fosfato. Sin embargo, en base a nuestra técnica anterior, el fosforamidato fenil metoxialaninilo (7) se anticiparía que sea entre las más óptimas de las estructuras.
Sorprendentemente, se ha encontrado ahora que otros derivados de análogos de nucleósidos de fosforamidato oxiamino ácido son significativamente más potentes en el tratamiento de cáncer que el fosforamidato de fenil metoxialaninilo (7).
De acuerdo con un primer aspecto de la presente invención se proporciona un compuesto de la fórmula I;
en el que:
R se selecciona del grupo metilo (-CH3), etilo (-C2 H5), n- e i-propilo (-C3H7), n- e i-butilo (-C4H9) y bencilo (-CH2 C6H5); uno de R’ y R" es H y uno de R’ y R" es metilo;
Q es -O-;
X se selecciona independientemente del grupo F, Br y metilo (-CH3);
Y es F;
Ar se selecciona del grupo -C6H5 , PCF3C6H4-, PFC6H4-, PNO2C6H4-, pClC6H4- and oClC6H4-;
Z se selecciona del grupo H, alquilo C1_6acíclico y halógeno; y
n es 0 o 1,
en el que cuando n es 0, Z’ es -NH2 y existe un doble enlace entre la posición 3 y la posición 4, y
cuando n es 1, Z’ es =O;
o una sal farmacéuticamente aceptable de un compuesto de fórmula I
La referencia en la presente especificación a un grupo alquilo significa un radical hidrocarbilo ramificado o no saturado, cíclico.
Los grupos alquilo pueden estar sustituidos o no sustituidos. Donde se sustituye, habrá
generalmente de uno a tres sustituyentes presentes, preferiblemente un sustituyente. Los sustituyentes pueden incluir átomos de halógeno, es decir, átomos de F, Cl, Br e I, y grupos halometilo tales como CF3 y CCh; grupos que contienen oxígeno tales como oxo, hidroxi, carboxi, carhoxialquilo C1 -16 , alcoxi, alcoílo, alcoiloxi, ariloxi, ariloílo y ariloxi; grupos que contienen nitrógeno tales como amino, alquilamino C1 -6, dialquilamino C1 -6, ciano, azida y nitro; grupos que contienen azufre tales como tiol, alquiltiol C1 -6, sulfonilo y sulfóxido; grupos heterocíclicos que pueden estar ellos mismos sustituidos; grupos alquilo como se definen anteriormente, que pueden estar ellos mismos sustituidos; y grupos arilo como se definen anteriormente, que pueden estar sustituidos, tales como fenilo y fenilo sustituido. Los sustituyentes en dichos grupos heterocíclicos, alquilo y arilo son como se definen inmediatamente más arriba.
Preferiblemente, R no está sustituido. Lo más preferiblemente, R es bencilo, especialmente cuando Ar es fenilo no sustituido, n es 0 y cada uno de X e Y es F.
Cuando R' y R" son diferentes, el átomo de C al que están unidos es quiral. Los presentes compuestos pueden ser L o D o una mezcla de estereoisómeros. Preferiblemente son L.
Cuando Z es H, n es 0 y X y Y son cada uno F, la unidad estructural base del compuesto de la fórmula I corresponde a aquel de Gemcitabina es decir el compuesto (3) anterior.
Se prefieren los compuestos de la fórmula I en los que n es 0 y X y Y son F. Particularmente se prefieren los compuestos de la fórmula I en los que n es 0, X y Y son F, y Z es H, que corresponden a gemcitabina.
En una realización preferida alternativa, X se selecciona independientemente de F y metilo.
Por lo tanto, los compuestos que incorporan la presente invención y que tienen variaciones en una o más de la región de éster (R), aminoácido (R', R") y arilo (Ar) de la estructura de fosforamidato en comparación con fosforamidato de fenil metoxialaninilo pueden dar aumentos de potencia sorprendentes y sustanciales de pro-tides derivados de BVDU contra una variedad de tipos de células cancerosas.
De acuerdo con un aspecto adicional de la presente invención se proporciona una composición farmacéutica que comprende un compuesto que tiene la fórmula I de la presente invención en combinación con un excipiente, portador o diluyente farmacéuticamente aceptable.
La presente invención es particularmente aplicable para el tratamiento de un paciente que tiene cáncer de mama, cáncer de colon o cáncer de próstata. Ejemplos de dichos cánceres incluyen mama MDA MB231, colon HT115 y próstata PC-3.
El compuesto que tiene la fórmula I o composición farmacéutica de acuerdo con la presente invención se puede administrar a un paciente, que puede ser humano o animal, mediante cualquier medio adecuado.
Los medicamentos empleados en la presente invención se pueden administrar por ruta oral o parenteral, que incluyen intravenosa, intramuscular, intraperitoneal, subcutánea, transdérmica, vías respiratorias (aerosol), rectal, vaginal y tópica (que incluyen bucal y sublingual).
Para la administración oral, los compuestos de la invención generalmente se proporcionarán en forma de comprimidos o cápsulas, como un polvo o gránulos, o como una solución o suspensión acuosa.
Los comprimidos para uso oral pueden incluir el ingrediente activo mezclado con excipientes farmacéuticamente aceptables tales como diluyentes inertes, agentes disgregantes, agentes aglutinantes, agentes lubricantes, agentes edulcorantes, agentes aromatizantes, agentes colorantes y conservantes. Los diluyentes inertes adecuados incluyen carbonato de sodio y calcio, fosfato de sodio y calcio, y lactosa, mientras que el almidón de maíz y ácido algínico son agentes disgregantes adecuados. Los agentes aglutinantes pueden incluir almidón y gelatina, mientras que el agente lubricante, si está presente, será generalmente estearato de magnesio, ácido esteárico o talco. Si se desea, los comprimidos se pueden recubrir con un material tal como monoestearato de glicerilo o diestearato de glicerilo, para retardar la absorción en el tracto gastrointestinal.
Las cápsulas para uso oral incluyen cápsulas de gelatina dura en las que el ingrediente activo se mezcla con un diluyente sólido, y cápsulas de gelatina blanda en las que el ingrediente activo se mezcla con agua o un aceite tal como aceite de maní, parafina líquida o aceite de oliva.
Las formulaciones para administración rectal pueden estar presentes como un supositorio con una base adecuada que comprende por ejemplo manteca de cacao o un salicilato.
Las formulaciones adecuadas para administración vaginal se pueden presentar como pesarios, tampones, cremas, geles, pastas, espumas o formulaciones de pulverización que contienen además del ingrediente activo dichos portadores que se conocen en la técnica por ser apropiados.
Para uso intramuscular, intraperitoneal, subcutáneo e intravenoso, los compuestos de la invención generalmente se proporcionarán en soluciones o suspensiones acuosas estériles, reguladas a un pH e isotonicidad apropiados. Los vehículos acuosos adecuados incluyen solución de Ringer y cloruro de sodio isotónico. Las suspensiones acuosas de acuerdo con la invención pueden incluir agentes de suspensión tales como derivados de celulosa, alginato de sodio, povidona y goma de tragacanto, y un agente humectante tal como lecitina. Los conservantes adecuados para suspensiones acuosas incluyen p-hidroxibenzoato de etilo y n-propilo.
Los compuestos de la invención también se pueden presentar como formulaciones de liposomas.
En general, una dosis adecuada estará en el intervalo de 0.1 a 300 mg por kilogramo de peso corporal del receptor por día. Una dosis inferior preferido es de 0.5 mg por kilogramo de peso corporal del receptor por día, una dosis inferior más preferida es de 6 mg por kilogramo de peso corporal del receptor por día, una dosis baja aún más preferida es de 10 mg por kilogramo de peso corporal por receptor por día. Una dosis adecuada está preferiblemente en el rango de 6 a 150 mg por kilogramo de peso corporal por día, y más preferiblemente en el rango de 15 a 100 mg por kilogramo de peso corporal por día. La dosis deseada se presenta preferiblemente como dos, tres, cuatro, cinco o seis o más subdosis administradas en intervalos apropiados durante todo el día. Estas subdosis se pueden administrar en formas de dosificación unitaria, por ejemplo, que contiene de 10 a 1500 mg, preferiblemente de 20 a 1000 mg, y aún más preferiblemente de 50 a 700 mg de ingrediente activo por forma de dosificación unitaria.
Ahora se describirán las realizaciones de la presente invención, solo por vía de ejemplo, con referencia a los siguientes ejemplos, procedimientos experimentales y datos experimentales.
Los datos se presentan para un rango de estructuras contra tipos de células tumorales que representan un rango de cánceres comunes en el hombre con la necesidad clínica no satisfecha: MDA MB231 de mama, HT115 de colon, PC-3 de próstata. Los datos de estos ensayos se presentan como la Tabla I.
Procedimiento experimental
Métodos generales
Los siguientes solventes anhidros y reactivos se compraron de Aldrich con tapón seguro: diclorometano (DCM), éter de dietilo (Et2O), tetranhidrofurano THF), N-metilimidazol (NMI), metanol (MeOH), dimetilformamida (DMF), 1,4-dioxano, trietilamina se seca sobre tamices moleculares de 4 Angstrom.
Cromatografía de Capa Delgada
La cromatografía de Capa Delgada (TLC) se realiza sobre placas Kieselgel 60 F254 comercialmente disponibles de Merck y se visualizan los componentes separados utilizando luz ultravioleta (254 nm y 366 nm).
Cromatografía de columna
Se realiza cromatografía de columna utilizando (Kieselgel 60, 35-70 pm, Fluka) como la fase estacionaria. Las muestras se aplican como una solución concentrada en el mismo eluyente, o se adsorbe previamente sobre gel de sílice.
Espectroscopia de RMN
Se registran RMN 1H, 13C y 31P sobre un espectrómetro Bruker Avance DPX300 con frecuencias de operación de 300 MHz, 75 MHz y 121 MHz respectivamente. Los espectros de RMN de 31P se indican en unidades de 8 relacionadas con ácido fosfórico al 85% como estándar externo, los cambios positivos son campo abajo. Se utilizan las siguientes abreviaturas en la asignación de señales de RMN: s (singulete), d (doblete), t (triplete), q (cuarteto), m (multiplete), bs (señal amplia), dd (doblete de doblete), dt (doblete de triplete). Las señales de estrella se dividen debido a mezclas estereoisoméricas.
Procedimientos estándar
Para propósitos prácticos, se proporcionan procedimientos estándar cuando sea aplicable.
Procedimiento estándar 1: Síntesis de Sales de clorhidrato de ésteres de amino.
A una solución de agitación de alcohol anhidro (10 mol eq.) se agrega cloruro de tionilo (2 mol eq.) a 0° C, y la solución resultante agitada durante 1 hr. Después de calentar a temperatura ambiente, se agrega el aminoácido apropiado (1 mol eq) y la reacción se calienta a reflujo durante 6-16 hrs. La eliminación de solvente y recristalización a partir de metanol/éter proporcionan las sales de clorhidrato de ésteres de amino.
Procedimiento estándar 2: Síntesis de Sales de clorhidrato de éster de amino bencilo.
El aminoácido apropiado (1.0 mol eq.), ácido p-tolueno sulfónico (1.0 mol eq.) y alcohol bencílico anhidro (4.1 mol eq.) se calientan a reflujo en tolueno (10 mol eq.) con trampa Dean-Stark durante 24 hrs. En enfriamiento a
temperatura ambiente, se agrega Et2O y la mezcla se deja en baño de hielo durante 1hr luego se filtra y se lava con Et2O. El sólido se disuelve en DCM y se lava con 10% de K2CO3 y agua. La capa orgánica se seca sobre MgSO4, se filtra y el solvente se elimina bajo presión reducida para dar un aceite. Este se solubiliza en acetona y se neutraliza con HCl 1 M. Et2O se agrega y el sólido se filtra y se lava con Et2O para dar un sólido blanco.
Procedimiento estándar 3: Síntesis de Especies de fosforodiclorurato.
Oxicloruro de fósforo (1.0 mol eq.) y el fenol sustituido apropiado (1.0 mol) se agitan con dietiléter anhidro (31 mol eq.). A este se agrega trietilamina anhidra (1.0 mol eq) a -80° C y se deja elevar a temperatura ambiente durante 16 hrs. la sal de clorhidrato de trietilamina se filtra, y el filtrado se reduce hasta secado para dar el producto crudo como un líquido transparente.
Procedimiento estándar 4: Síntesis de Especie de fosforodicloridato.
Fosfodiclorurato (1.0 mol eq.) y la sal de clorhidrato de éster de amino apropiado (1.0 mol eq.) se suspenden en DCM anhidro. Se agrega en forma de gotas trietilamina anhidra a -80° C y después de 1 hr la reacción se deja elevar a temperatura ambiente. La formación de fosfoclorurato se monitoriza por RMN 31P. Después de 2-5 hrs el solvente se elimina bajo presión reducida y el sólido obtenido se lava con éter anhidro (2x20 ml), se filtra, y el filtrado se reduce hasta secado para dar los productos como aceite crudo. Estos aceites usualmente se utilizan sin purificación adicional.
Procedimiento estándar 5: Síntesis de Derivados de fosforoamidato.
A una solución de agitación de (E)-5-(2-bromovinil)-2'-desoxiuridina (1.0 mol eq.) y el fosfoclorurato apropiado (2.0 3.0 mol eq) en THF anhidro a -80° C se agrega en forma de gotas durante 1 min NMI (5.0 mol eq.). Después de 15 mins la reacción se deja elevar a temperatura ambiente y se agita a temperatura ambiente durante 2-19 hrs. El solvente se elimina bajo presión reducida y el aceite amarillo obtenido se disuelve en DCM, se lava con HCl 0.5 M, y agua. La capa orgánica se seca sobre MgSO4, se filtra, se reduce hasta secado y se purifica mediante cromatografía flash (Cloroformo/Metanol 97/3, Diclorometano/Metanol 97/3).
Síntesis de Gemcitabina-[fenil-(benzoxi-L-alaninil)]-fosfato. C255 H27F2 N4O8P, PM =580.47 (CPF 31).
Este se sintetiza de acuerdo con el procedimiento estándar 5, utilizando Gemcitabina (131 mg, 0.5 mmol), Fenil-(benzoxi- L-alaninil)-fosforoclorurato (529 mg, 1.5 mmol), NMI (4.42 mmol, 300 pL) en THF/piridina (4/2 mL) durante 2 hrs. El producto crudo se purifica mediante cromatografía de columna, se eluye con CH2Ch/Metanol 95:5 para dar el producto puro como un sólido espumoso blanco (46 mg, rendimiento 16%).
RMN 31P (MeOD, 121 MHz): 8 5.05, 4.94.
RMN 1H (MeOD, 300 MHz): 8 7.6-7.5 (1H, 2d, 3J=7Hz H-6 ), 7.4-7.2 (10H. m, OPh+CH2 Ph), 6.25 (1H, m, H-1'), 5.95 (1H, 2d, 3J=7Hz, H-5), 5.19 (1H, 2s, CH2 Ph), 4.55-4.1(3H, m, H-3', H-4', CHala), 4.05 (2H, m, H-5'), 1.20 (3H, 2t, 3J= 6 Hz, CH3ala). RMN 13C (MeOD, 75 MHz): 8 20.8, 20.7 (CH3ala), 52.2, 52.0 (CHala), 66.1 (C-5'), 68.4 (CH2 Ph), 71.9, 71.3 (C-3'), 80.6 (C-4'), 85.9 (C-1'), 97.1 (C-5), 121.8, 121.6 ('o', OPh), 123 (C-2'), 126.2 ('p', OPh), 131.8, 130.0, 129.7 ('m' OPh, Bn), 137.9('ipso', CH2 Ph), 142.7, 142.6 (C-6 ), 152.5, 152.4 ('ipso', OPh), 158.2 (C-2), 168.0 (C-4), 175.3, 174.9 (COOBn).
Síntesis de Gemcitabina-[para-clorofenil-(benzoxi-L-alaninil)]-fosfato. C25H26C F 2 N4O8P, PM =614.92 (CPF 40).
Esta se sintetiza de acuerdo con el procedimiento estándar 5, utilizando gemcitabina (131 mg, 0.5 mmol), paraclorofenil-(benzoxi-L-alaninil)-fosforoclorurato (582 mg, 1.5 mmol), NMI (4.42 mmol, 300 j L) en THF/piridina (4/2 mL) durante 2 hrs. El producto crudo se purifica mediante cromatografía de columna, se eluye con CH2Ch/Metanol 95:5 para dar el producto puro como un sólido espumoso blanco (76 mg, rendimiento 25%).
RMN 31P (MeOD, 121 MHz): 85.08.
RMN 1H (MeOD, 300 MHz): 87.65 (1H, 2d, 3J=7Hz H-6), 7.5-7.2 (9H. m, OPh+CH2 Ph), 6.2 (1H, m, H-1'), 5.9 (1H, 2d, 3J=7Hz, H-5), 5.12 (1H, 2s, CH2 Ph), 4.6-4.1 (3H, m, H-3', H-4', CHala), 4.05 (2H, m, H-5'), 1.45-1.35 (3H, 2t, 3J=6 Hz, CHaala).
RMN 13C (MeOD, 75 MHz): 820.9, 20.7 (CHaala), 52.2, 52.0 (CHala), 66.4, 66.2 (C-5'), 68.5 (CH2 Ph), 71.5 (C-3'), 80.7 (C-4'), 86.4 (C-1'), 97.2 (C-5), 123.5 ('o', OPh), 126.9 (C-2'), 131.2, 130.6, 130.3 ('m' OPh, Bn), 131.9 ('p', OPh) 137.5 ('ipso', CH2 Ph), 142.8, 142.7 (C-6), 151.4, 151.0 ('ipso', OPh), 158.2 (C-2), 166.9 (C-4), 175.1, 174.9 (COOBn). Síntesis de Fenil-(metoxi-L-alaninil)-fosforoclorurato. C1 oH1 aClNO4P, PM =277.64.
Este se sintetiza de acuerdo con el procedimiento estándar 4, utilizando clorhidrato de éster de metil L-alanina (2 g, 14.3 mmol), fenildiclorofosfato (3.02 g, 2.14 ml, 14.3 mmol), y TEA (2.9 g, 4.0 ml, 28.7 mmol) en DCM (60 mL), para proporcionar 3.91 g (98%) del producto crudo utilizado sin purificación adicional.
RMN 31P (CDCh, 121 MHz): 89.28, 8.97.
RMN 1H (CDCh; 300 MHz): 87.39-7.34 (2H, m,'o' OPh), 7.29-7.20 (2H, m,'m+p' OPh), 4.98 (1H, bs, NH), 4.27-4.09 (1H, m, CHala), 3.78 (3H, s, O C ^), 1.52-1.49 (3H, 2xd, 3J=7Hz, C ^ala).
RMN 13C (CDCh; 75 MHz): 820.9 (C ^a la), 51.0 (CHala), 53.6 (O C ^), 120.9 ('o' OPh), 126.4 ('p', OPh), 130.2 ('m', OPh), 150.1 ('ipso', OPh), 173.6(COOCH3).
Síntesis de Fenil-(etoxi-L-alaninil)-fosforoclorurato. CnH 15 ClNO4P, PM =291.67.
Este se sintetiza de acuerdo con el procedimiento estándar 4, utilizando clorhidrato de éster de etil L-alanina (770 mg, 5.01 mmol), fenildiclorofosfato (1.12g, 5.01 mmol, 749 j L), y TEA (1.4 mL, 10.02 mmol) en DCM (40 mL). El crudo se purifica mediante cromatografía flash (acetato de etilo/éter de petróleo 7:3) proporcionando 1.02 (69%) de aceite.
RMN 31P (CDCh, 121 MHz): 89.49, 9.07.
RMN 1H (CDCl3 ; 300 MHz): 8 7.39-7.34 (2H, m,'o' OPh), 7.29-7.20 (2H, m, 'm+p' OPh), 4.95 (1H, bs, NH), 4.3-4.1 (3H, m, OCH2CH3 , CHala), 1.50 (3H, 2xd, 3J=7Hz, CHaala), 1.30 (3H, t, 3J=7.1 Hz, OCH2CH3 ).
RMN 13C (CDCla; 75 MHz): 814.5 (CH3CH2), 20.9 (CHaala), 51.0 (CHala), 62.6 CH3CH2 ), 120.9 ('o' OPh), 126.5 ('p', OPh), 130.1 ('m', OPh), 150.1 ('ipso', OPh), 175.1 (COOCH2CH3 ).
Síntesis de Fenil-(benzoxi-L-alaninil)-fosforoclorurato. C16 H17ClNO4P, PM = 353.74.
Este se sintetiza de acuerdo con el procedimiento estándar 4, utilizando clorhidrato de éster de bencil L-alanina (1.0 g, 4.64 mmol), fenil-diclorofosfato (980 mg, 0.69 ml, 4.64 mmol), y TEA (0.94 g, 1290 j L, 9.27 mmol) en DCM (40 mL). El crudo se purifica mediante cromatografía flash (acetato de etilo/éter de petróleo 6:4) proporcionando 1.61 (98%) de aceite.
RMN 31P (CDCh, 121 MHz): 89.41, 9.23.
RMN 1H (CDCh; 300 MHz): 87.41-7.21 (10H, m, OPh+CH2Ph), 5.24 (2H, s, CH2 Ph), 4.95-4.88 (1H, bs, NH), 4.36 4.15 (1H, m, CHala), 1.52-1.49 (3H, 2xd, J=7Hz, CH3ala). RMN 13C (CDCh; 75 MHz): 820.8 (CH3ala), 51.1 (CHala), 68.0 (CH2 Ph), 121.0 ('o' OPh), 126.4 ('p', OPh), 130.3, 129,0, 128.7 ('m' OPh, CH2 Ph), 135.5 ('ipso', CH2 Ph), 150.2 ('ipso', OPh), 172.9 (COOCH2 Ph).
Síntesis de p-nitrofenil-(metoxi-L-alaninil)-fosforoclorurato. C10H12 CIN2O6P, PM =322.64.
Este se sintetiza de acuerdo con el procedimiento estándar 4, utilizando clorhidrato de éster de metil L-alanina (0.70 g, 5.01 mmol), p-nitrofenildiclorofosfato (1.362 g, 5.01 mmol), y TEA (1.4 ml, 10 mmol) en DCM (40 mL), para proporcionar 1.60 g (99%) del producto crudo utilizado sin purificación adicional.
RMN 31P (CDCh, 121 MHz): 89.13, 9.03.
RMN 1H (CDCI3 ; 300 MHz): 58.1 (2H, 2d, 3J=8Hz, OPh), 7.3 (2H, 2d, 3J=8Hz, OPh), 5.0 (1H, bs, NH), 4.1 (1H, m, CHala), 3.75 (3H, s, OCH3 ), 1.5-1.45 (3H, m, CH3ala). RMN 13C (CDCI3 ; 75 MHz): 520.8, 20.7 (CH3ala), 51.1, 50.9 (CHala), 53.2, 53.2 (OCH3), 121.8, 121.6 ('o' OPh), 126.5 ('m', OPh), 145.7 (‘ipso’, OPh), 154.7, 154.6 ('p', OPh), 173.4, 173.2 (COOCH3).
Síntesis de p-nitrofenil-(etoxi-L-alaninil)-fosforoclorurato. C11 H14CIN2O6P, PM =336.67.
Este se sintetiza de acuerdo con el procedimiento estándar 4, utilizando clorhidrato de éster de etil L-alanina (770 mg, 5.01 mmol), p-nitrofenildiclorofosfato (1.362g, 5.01 mmol), y TEA (1.4 mL, 10.02 mmol) en DCM (40 mL), para proporcionar 1.64 g (98%) del producto crudo utilizado sin purificación adicional.
RMN 31P (CDCla, 121 MHz): 59.06, 8.81.
RMN 1H (CDCla; 300 MHz): 58.1 (2H, m, OPh), 7.4 (2H, m, OPh), 4.9-4.7 (1H, bs, NH), 4.3-4.1 (3H, m, OCH2CH3, CHala), 1.55-1.45 (3H, 2xd, 3J=7Hz, CH3ala), 1.40 (3H, t, 3J=7Hz, OCH2CH3).
RMN 13C (CDCh; 75 MHz): 5 14.5 (CH3CH2 ), 21.1, 20.9 (CH3ala), 51.2, 51.0 (CHala), 62.6_CH3CH2), 121.7, 121.3 (‘o' OPh), 126.2, 126.0 (‘m', OPh), 145.7 (‘ipso', OPh), 154.5 (‘p', OPh), 173.4, 173.3 (COOCH2CH3 ).
Síntesis de p-nitrofenil-(benzoxi-L-alaninil)-fosforoclorurato. C16 H16ClN2O6P, PM = 398.04.
Este se sintetiza de acuerdo con el procedimiento estándar 4, utilizando clorhidrato de éster de bencil L-alanina (1.08 g, 5.01 mmol), para-nitrofenil-dicloro fosfato (1.362 g, 5.01 mmol), y TEA (1.4 mL, 1.4 mmol) en DCM (40 mL), para proporcionar 1.85 g (93%) del producto crudo utilizado sin purificación adicional.
RMN 31P (CDCl3, 121 MHz): 59.15, 9.06.
RMN 1H (CDCh; 300 MHz): 58.15 (2H, m, OPh), 7.45 (2H,m,OPh), 7.35-7.25 (5H, m, CH2 Ph), 5.2 (2H, 2s, CH2 Ph), 5.00 (1H, bs, NH), 4.2 (1H, m, CHala), 1.64 (3H, 2xd, 3J=7Hz, CH3ala).
RMN 13C (CDCh; 75 MHz): 5 20.8 (CH3ala), 51.1 (CHala), 68.0 (CH2 Ph), 121.4 (‘o' OPh), 126.1 (‘m'OPh), 130.3, 129.0 (CH2 Ph), 145.7 (‘ipso', CH2 Ph), 150.2 (‘ipso', OPh), 154.6 (‘p', OPh), 172.9 (COOCH2 Ph).
Síntesis de p-fluorofenil-(metoxi-L-alaninil)-fosforoclorurato. C1 qH12 CIFNO4P, PM =295.63.
Este se sintetiza de acuerdo con el procedimiento estándar 4, utilizando clorhidrato de éster de metil L-alanina (0.70 g, 5.01 mmol), p-fluorofenildiclorofosfato (1.210 g, 5.01 mmol), y TEA (1.4 ml, 10 mmol) en DCM (40 mL). El crudo se purifica mediante cromatografía flash (acetato de etilo/éter de petróleo 7:3) proporcionando 1.11 g (75%) de aceite. RMN 31P (CDCla, 121 MHz): 89.98, 9.96.
RMN 1H (CDCh; 300 MHz): 87.1 (2H, m, OPh), 6.95 (2H, m, OPh), 5.0 (1H, bs, NH), 4.25-4.1 (1H, m, CHala), 3.78 (3H, 2s, OCH3), 1.55 (3H, m, CH3ala).
RMN 13C (CDCla; 75 MHz): 820.8 (CH3ala), 51.1, 50.9 (CHala), 53.3 (OCH3 ), 117.1, 117.0 ('o' OPh), 122.6, 122.5 ('m', OPh), 146.0 ('ipso', OPh), 159.1, 159.0 ('p', OPh), 173.4, 173.2 (COOCH3).
Síntesis de p-fluorofenil-(etoxi-L-alaninil)-fosforoclorurato. C11 H14CFNO4P, PM =309.66.
Este se sintetiza de acuerdo con el procedimiento estándar 4, utilizando clorhidrato de éster de etil L-alanina (770 mg, 5.01 mmol), p-fluorofenildiclorofosfato (1.210g, 5.01 mmol), y TEA (1.4 mL, 10.02 mmol) en DCM (40 mL). El crudo se purifica mediante cromatografía flash (acetato de etilo/éter de petróleo 7:3) proporcionando 1.07 (69%) de aceite.
RMN 31P (CDCls, 121 MHz): 810.04, 9.95.
RMN 1H (CDCls; 300 MHz): 8 7.1 (2H, m, OPh), 6.95 (2H, m, OPh), 5.0 (1H, bs, NH), 4.25-4.1 (3H, m, OCH2CH3 , CHala), 1.55 (3H, m, CH3ala), 1.40 (3H, t, 3J=7Hz, OCH2CH3).
RMN 13C (CDCls; 75 MHz): 8 14.5 (CH3CH2), 21.1, 21.0 (CH3ala), 51.2, 51.1 (CHala), 62.6_CH3CH2), 117.3 ('o' OPh), 122.2, 122.0 ('m', OPh), 145.9, 145.8 ('ipso', OPh), 159.0 ('p', OPh), 173.6, 173.5 (COOCH2CH3).
Síntesis de p-fluorofenil-(benzoxi-L-alaninil)-fosforoclorurato. C16 H16CFNO4P, PM = 371.73.
Este se sintetiza de acuerdo con el procedimiento estándar 4, utilizando clorhidrato de éster de bencil L-alanina (1.08 g, 5.01 mmol), para-fluorofenil-dicloro fosfato (1.210 mg, 5.01 mmol), y TEA (1.4 mL, 1.4 mmol) en DCM (40 mL). El crudo se purifica mediante cromatografía flash (acetato de etilo/éter de petróleo 7:3) proporcionando 1.599 (86%) de aceite.
RMN 31P (CDCls, 121 MHz): 89.15, 9.06.
RMN 1H (CDCls; 300 MHz): 87.35-7.25 (5H, m, CH2 Ph), 7.1 (2H, m, OPh), 6.95 (2H,m, OPh), 5.2 (2H, 2s, CH2 Ph), 5.00 (1H, bs, NH), 4.25-4.1 (1H, m, CHala), 1.55 (3H, m, CH3ala).
RMN 13C (CDCls; 75 MHz): 8 20.8 (CH3ala), 51.1, 51.0 (CHala), 68.1 (CH2 Ph), 117.0, 116.9 ('o' OPh), 122.6 ('m'OPh), 130.3, 129.0 (CH2 Ph), 135.7 ('ipso', CH2 Ph), 146.1, 146.0('ipso', OPh), 158.9 ('p', OPh), 173.1 (COOCH2Ph).
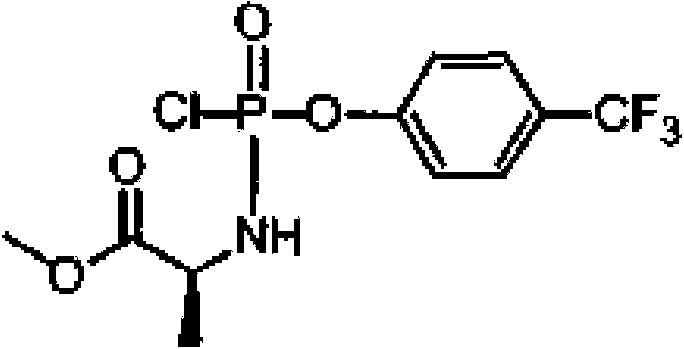
Síntesis de 4-(trifluorometil)-fenil-(metoxi-L-alaninil)-fosforocloridato. C11 H12 ClF3 NO4P, PM =345.64.
Este se sintetiza de acuerdo con el procedimiento estándar 4, utilizando clorhidrato de éster de metil L-alanina (1.0 g, 7.16 mmol), 4-(trifluorometil)-fenil-fosfodidorurato (1.998 g, 7.16 mmol), y TEA (1.449 g, 14.32 mmol, 1916 |jl ) en DCM (30 mL), para proporcionar 2.202 g (89.0%) del producto crudo utilizado sin purificación adicional.
RMN 31P (CDCla, 121 MHz): 8 9.36, 9.22.
RMN 1H (CDCh; 300 MHz): 8 7.66 (2H, d, 3J=8.1 Hz, OPh), 7.44-7.33 (2H, m, OPh), 5.10 (1H, bs, NH), 3.81-3.78 (3H, 2s, CH3O), 3.77-3.68 (1H, m, CH3CH), 1.56-1.52 (3H, m, CHCH3 ).
RMN 13C (CDCh; 75 MHz): 8 20.6, 20.7 (CH3CH), 50.9, 51.1 (CHCH3 ), 53.2 (CH3O), 121.4 ('o', OPh), 124.1 (CF3, J=270 Hz), 128.0 ('m', OPh), 128.6 ('p', J=34 Hz), 152.4, 152.6 ('ipso', OPh), 173.4, 173.5 (COOCH3 ).
Síntesis de 4-(trifluorometil)-fenil-(etoxi-L-alaninil)-fosforoclorurato. C12 H14ClF3NO4, PM =359.67.
Este se sintetiza de acuerdo con el procedimiento estándar 4, utilizando clorhidrato de éster de etil L-alanina (1.0 g, 6.50 mmol), 4-(trifluorometil)-fenil-fosfodiclorurato (1.813 g, 6.50 mmol), y TEA (1.316 g, 13.00 mmol, 1740 j L) en DCM (30 mL), para proporcionar 2.150 g (92.2%) del producto crudo utilizado sin purificación adicional.
RMN 31P (CDCl3, 121 MHz): 8 9.33, 9.28.
RMN 1H (CDCh; 300 MHz): 8 7.70 (2H, d, 3J=8.2 Hz, OPh), 7.46-7.39 (2H, m, OPh), 4.78 (1H, bs, NH), 4.33-4.17 (3H, m, CH3CH2O CHCH3 ), 1.59-1.55 (1H, m, CHCH3 ), 1.56-1.52 (3H, m, CH2CH3 ).
RMN 13C (CDCh; 75 MHz): 8 14.5 (CH3CH2O), 20.8, 20.9 (CH3CH), 50.3, 50.9 (CHCH3 ), 62.3, 62.5 (CH3CH2O), 121.4 ('o', OPh), 124.1 (CF3 , J=270 Hz), 127.7 ('m', OPh), 128.7 ('p', J=33 Hz), 152.4 ('ipso', OPh), 172.9 (COOCH2CH3).
Síntesis de p-trifluorofenil-(benzoxi-L-alaninil)-fosforoclorurato. C17 H16C F 3 NO4P, PM = 421.73.
Este se sintetiza de acuerdo con el procedimiento estándar 4, utilizando clorhidrato de éster de bencil L-alanina (1.08 g, 5.01 mmol), para-trifluorofenil-dicloro fosfato (1.490 mg, 5.01 mmol), y TEA (1.4 mL, 1.4 mmol) en DCM (40 mL). El crudo se purifica mediante cromatografía flash (acetato de etilo/éter de petróleo 6:4) proporcionando 1.80 (85%) de aceite.
RMN 31P (CDCl3, 121 MHz): 89.11, 8.84.
RMN 1H (CDCl3 ; 300 MHz): 87.65 (2H, m, OPh), 7.4-7.2 (7H, m, CH2 Ph 2H OPh), 5.25 (2H, 2s, CH2 Ph), 4.75-4.55 (1H, bs, NH), 4.25-4.1 (1H, m, CHala), 1.60-1.55 (3H, 2d, 3J=7Hz, CH3ala).
RMN 13C (CDCla; 75 MHz): 520.9 (CHsala), 51.3, 51.0 (CHala), 68.2, 68.1 (CH2 Ph), 121.4, 120.9 ('o', OPh), 125.2 (d, J=270Hz, CF3), 126.6 ('m', OPh), 129.1, 128.8, 127.8 (Bn), 130.0 ('p', q, J=32Hz, OPh), 135.4 ('ipso', CH2 Ph), 153.0 ('ipso', OPh), 172.8 (COOCH2 Ph).
Síntesis de 4-clorofenil-(metoxi-L-alaninil)-fosforoclorurato. C10 H12 CI2 NO4P, PM =312.09.
Este se sintetiza de acuerdo con el procedimiento estándar 4, utilizando clorhidrato de éster de metil L-alanina (1.0 g, 7.16 mmol), 4-clorofenilfosforodiclorurato (1.757 g, 7.16 mmol), y TEA (1.449 g, 14.32 mmol, 1995 j L) en DCM (30 mL), para proporcionar 1.621 g (72.5%) del producto crudo utilizado sin purificación adicional.
RMN 31P (CDCl3, 121 MHz): 59.36, 9.07.
RMN 1H (CDCla; 300 MHz): 57.35-7.15 (4H, m, OPh), 4.48-4.36 (1H, bs, NH), 4.22-4.04 (1H, m, CHCH3), 3.76-3.74 (3H, 2s, CH3O), 1.49-1.46 (3H, m, CHCH3 ).
RMN 13C (CDCls; 75 MHz): 521.0 (CH3CH), 50.8, 51.1 (CHCH3 ), 53.4 (CHsO),121.9, 122.1, 122.3, 122.4 ('o', OPh), 130.6, 130.4, 130.2 ('m', OPh), 132.0 ('p', OPh), 148.6 ('ipso', OPh), 173.5 (COOCH3).
Síntesis de 4-clorofenil-(etoxi-L-alaninil)-fosforoclorurato. C11 H-mCI2 NO4P, PM =326.11.
Este se sintetiza de acuerdo con el procedimiento estándar 4, utilizando clorhidrato de éster de etil L-alanina (1.000 g, 6.50 mmol), 4-clorofenilfosforodicloruro (1.595 g, 6.50 mmol), y TEA (1.315 g, 13.00 mmol, 1810 j L) en DCM (20 mL), para proporcionar 1.794 mg (rendimiento 84.7%) del producto.
RMN 31P (CDCls, 121 MHz): 59.54, 9.25.
RMN 1H (CDCls; 300 MHz): 5 7.44-7.21 (4H, m, OPh), 4.59 (1H, bs, NH), 4.33-4.13 (3H, m, OCH2CH3+ CHCH3), 1.57-1.56 (3H, m, CH3CH), 1.43-1.21 (3H, m, OCH2CH3 ).
RMN 13C (CDCls; 75 MHz): 514.5, 14.6 (OCH2CH3), 21.0, 21.5 (CH3CH), 50.9, 51.2 (CHCH3 ), 62.4, 62.5 (OCH2CH3 ), 122.04, 122.3, 122.4 ('o', OPh), 130.4 ('m', OPh), 131.9 ('p', OPh), 148.5, 148.6 ('ipso', OPh), 173.0,173.1 (COOCH2CH3).
Síntesis de 4-nitrofenil-(bencil-2-amino-2-metilpropanoato)-fosforoclorurato. C16 H16Cl2 NO4P, PM =388.18.
Este se sintetiza de acuerdo con el procedimiento estándar 4, utilizando clorhidrato de éster de bencil L-alanina (1.000 g, 4.63 mmol), 4-clorofenilfosfodicloruro (1.136 g, 4.63 mmol), y TEA (937.0 mg, 9.26 mmol, 1290 j L) en DCM (40 mL), para proporcionar 1534 mg (rendimiento 86.5%) del producto crudo utilizado sin purificación adicional.
RMN 31P (CDCI3, 121 MHz): 59.43, 9.16.
RMN 1H (CDCI3 ; 300 MHz): 57.42-7.08 (9H, m, OPh+ CH2 Ph), 5.19 (2H, s, O-hPh), 4.61-4.54 (1H, bs, NH), 4.26 4.10 (1H, m, CHCH3), 1.42-1.38 (3H, m, CH3CH).
RMN 13C (CDCI3 ; 75 MHz): 520.9, 21.0 (CH3CH), 51.0, 51.2 (CHCH3), 68.1, 68.2 (OCH2 Ph), 122.3, 122.4 (‘o', OPh), 128.8, 129.1, 130.4 (‘o', ‘m', ‘p', CH2 Ph+OPh), 131.9 (‘ipso', CH2 Ph), 135.3 (‘p', OPh), 148.5 (‘ipso', OPh), 172.7, 112.8 (COOCH2Ph).
Síntesis de 4-cIorofeniI—fosfodicloridato. C6H4CI3O2 P, PM=245.43.
Esta se sintetiza de acuerdo con el procedimiento estándar 3, utilizando fósforo-oxicloruro (1533 mg, 10.00 mmol, 932 ^L), 4-clorofenol (1.285 g, 10.00 mmol) y TEA (1.011 g, 10.00 mmol, 1394 ^L) en etiléter (100 mL) para dar un aceite (1.897 g, 77.3% de rendimiento).
RMN 31P (CDCh, 121 MHz): 55.18.
RMN 1H (CDCl3 ; 300 MHz): 57.45 (2H, d, 3J=9.0 Hz, OPh), 7.30 (2H, d, 3J=9.0 Hz, OPh).
RMN 13C (CDCh; 75 MHz): 5122.5 (‘o', OPh), 130.6 (‘m', OPh), 133.2 (‘p', OPh), 148.5 (‘ipso', OPh).
Síntesis de 4-(trifluorometil)-fenil-fosfodidorurato. C7H4ClF3O3P, PM =278.98.
Esta se sintetiza de acuerdo con el procedimiento estándar 3, utilizando fósforo-oxicloruro (1.570 mg, 10.24 mmol, 954.5 ^L), 4-trifluorometilfenol (1660 g, 10.24 mmol) y TEA (1.036 g, 10.24 mmol, 1427 ^L) en etiléter (100 mL) para dar un aceite (2.521 g, 88.2% de rendimiento).
RMN 31P (CDCh, 121 MHz): 54.75.
RMN 1H (CDCh; 300 MHz): 57.77 (2H, d, 3J=8.4 Hz, OPh), 7.49 (2H, d, 3J=8.4 Hz, OPh).
RMN 13C (CDCh; 75 MHz): 5 121.6 (‘o', OPh), 123.6 (CF3 , J=271 Hz, OPh), 128.2 (‘m', OPh), 129.7 (‘p', J=33 Hz), 152.7 (‘ipso', OPh).
Síntesis de 4-fluorofenil-fosfodiclorurato. C6H4ChFO2 P, PM =228.97.
Esta se sintetiza de acuerdo con el procedimiento estándar 3, utilizando fósforo-oxicloruro (1.395 mL, 15.00 mmol), 4-clorofenol (1.68 g, 15.00 mmol) y Te a (2.1 mL, 15.00 mmol) en etiléter (140 mL) para dar un aceite (3.96 g, 96 % de rendimiento).
RMN 31P (CDCh, 121 MHz): 55.52.
RMN 1H (CDCh; 300 MHz): 57.15 (2H, d, 3J=8.0 Hz, OPh), 7.05 (2H, d, 3J=8.0 Hz, OPh).
RMN 13C (CDCh; 75 MHz): 5116.8 (‘o', OPh), 122.1 (‘m' OPh), 146.7 (‘p', OPh), 158.7 (‘ipso', OPh).
Los datos experimentales se dan en la Tabla I que ilustra la actividad de los compuestos que se incorporan en la presente invención, y de algunos compuestos comparativos, con respecto a estirpe celular de cáncer de mama humano MDA MB231, estirpe celular de cáncer de colon humana HT115 y estirpe celulade de cáncer de próstata humana PC-3. Los compuestos incluyen aquellos cuyas preparaciones se describieron anteriormente y los compuestos hechos por los métodos preparativos que corresponden a los métodos descritos anteriormente.
Los procedimientos experimentales utilizan estirpe celular de cáncer de colon humana (HT115), estirpe celular de cáncer de próstata humana (PC- 3), estirpe celular de cáncer de mama humana (MDA MB 231) y célula endotelial de vena umbilical humana normal (HuV e C). Los compuestos se diluyen sobre un rango de concentraciones y se agregan a células sobre 1 a 3 días. Se determina la citotoxicidad utilizando un ensayo MTT al final de cada experimento.
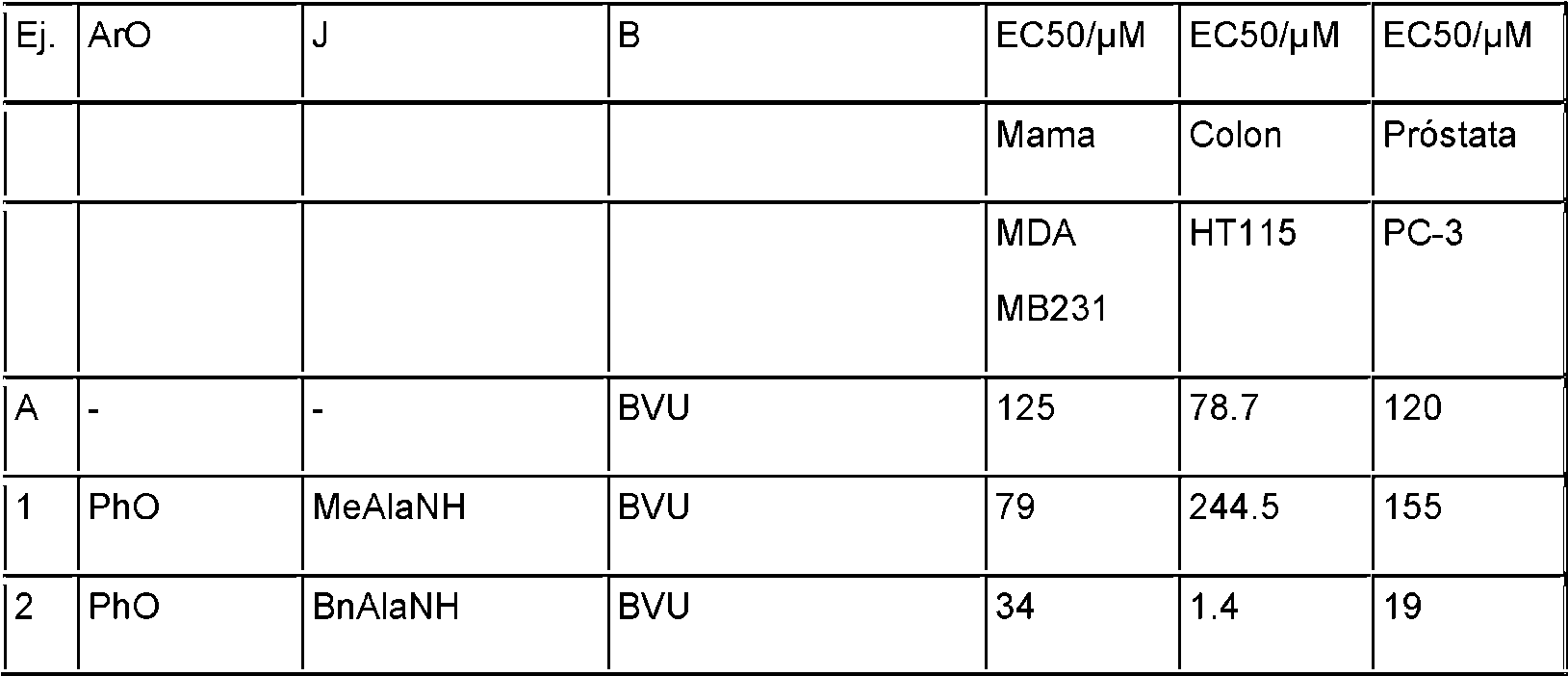
En la Tabla:
"Ar" corresponde al grupo "R" en los compuestos de fórmula I; J se refiere a la unidad estructural representada por, respectivamente, ROCOCR'R"NH-, con respecto a la fórmula I, o, con respecto a los Ejemplos 51, 52 y 53, HOCOCR'R"NH-, con respecto a la fórmula II, a continuación; y
B se refiere a la unidad estructural base con respecto a la fórmula I o la fórmula II.
BVU significa 2-bromovinil uridina.
5-(C=CC[O]O)MeU significa metil propenoato-2'-desoxiuridina.
GemCyt significa gemcitabina.
Los Ejemplos A, 1-30, 32-39, 41-95 y G son ejemplos comparativos.
El Ejemplo A es 5-(2-Bromovinil)-2’-desoxiuridina.
El Ejemplo 1 es el Ejemplo 1 anterior que corresponde al compuesto (7) anterior.
El Ejemplo 67 es propenato-2’-desoxiuridina.
El Ejemplo G is gemcitabina.
Los Ejemplos 51,52 y 53 son compuestos que incorporan la fórmula II anterior.
Los Ejemplos 31 y 40 son compuestos de acuerdo con la presente invención.
TABLA
La gemcitabina (Ejemplo G en la tabla) y el compuesto CPF31 (Ejemplo 31 en la tabla: gemcitabina-[fenil-(benzoxi-L-alaninil)]- fosfato) se compararon en un modelo de ratón con xenoinjertos de cáncer humano (colon HT115 y próstata Pc 3).
Los ratones se dosificaron diariamente en un rango de concentraciones (0.01-10 pM) y el volumen del tumor se evalúo versus control.
Las estadísticas de Kaplan-Meier se calcularon en relación con la supervivencia libre de incidentes.
En los dibujos adjuntos:
La figura 1 muestra para el xenoinjerto de ratón el volumen de tumor para los datos de próstata en día 13 utilizando Gemzar™; (gemcitabina disponible por ejemplo de Lilly).
La figura 2 muestra para el xenoinjerto de ratón el volumen del tumor para los datos de próstata en el día 13 utilizando CPF31;
La Figura 3 muestra las funciones de supervivencia libres de indicencia versus el día para cada uno de CPF31 y gemcitabina; y
La figura 4 muestra para el xenoinjerto de ratón el volumen del tumor para los datos de colon en el día 24 utilizando, respectivamente, compuesto Gemzar y CPF31.
Haciendo referencia a los dibujos, se puede ver que el CPF31 es significativamente menos tóxicos que la gemcitabina.
El CPF31 fue significativamente efectivo en reducir el volumen del tumor de próstata y colon con relación al control en la dosificación diaria de 5 y 10 pM (3 y 6 pg/ml). La gemcitabina no fue efectiva a la concentración más alta no tóxica.
El Gemzar que se ve en la Figura 1 es tóxico por encima de 1 pM. Por el contrario, se ve que el CPF31 en la Figura 2 tiene una toxicidad sustancialmente menor.
La Figura 3 muestra que el CPF31 tiene efectos secundarios significativamente inferiores sobre una base comparable: 3 animales muestran toxicidad grave (10% de pérdida de masa corporal) en GMZ y en CPF31 en el día 10, colectivamente con 4 en GMZ y 1 en CPF31 en el día 11 y 5 en GMZ y 1 en CPF en día 13. Utilizando el análisis de Chi cuadrado al combinar de grupos de 5 y 10 pM, la significación es p = 0.193, 0.078 y 0.0289 en el día 10, 11 y 13. Está claro que en el día 13, el CPF31 exhibe significativamente menos efectos secundarios y los efectos contra el cáncer siguen excediendo a aquel de Gemzar.
La Figura 3 muestra la curva de de supervivencia Kaplan-Meier, la supervivencia libre de incidencia: se basa en la pérdida de acuerdo con la pérdida de peso. Un análisis de proporción Cox muestra que el CPF31 es mucho menos tóxico que el GMZ con base en la pérdida calculada para bajar peso (p = 0.043).
Se encontró que el CPF31 era activo a 5 pM in vitro, mientras que se encontró que el Gemzar era activo a 600 pM, con respecto a la misma estirpe celular de colon. La Figura 4 muestra los resultados de las pruebas in vivo a 5 pM. La mayor actividad de CPF31 en la reducción de volumen del tumor se muestra en la Figura 4.
Claims (3)
1. Un compuesto químico que tiene la fórmula I:
en el que
R se selecciona del grupo metilo (-CH3), etilo (-C2H5), n- e i-propilo (-C3H7), n- e i-butilo (-C4H9) y bencilo (-CH2C6H5); uno de R' y R" es H y uno de R' y R" es metilo;
Q es -O-;
X se selecciona independientemente del grupo F, Br y metilo (-CH3);
Y es F;
Ar se selecciona del grupo -C6H5 , PCF3C6H4-, PFC6H4-, PNO2C6H4-, pClC6H4- and
0 GC6H4-;
Z se selecciona del grupo H, alquilo C i-6 acíclico y halógeno; y
n es 0 o 1,
en el que cuando n es 0, Z' es -NH2 y existe un doble enlace entre la posición 3 y la posición 4, y
cuando n es 1, Z' es =O;
o una sal farmacéuticamente aceptable de un compuesto de fórmula I.
2. Un compuesto de la reivindicación 1, en el que X se selecciona independientemente de F y metilo.
3. Una composición farmacéutica que comprende un compuesto de acuerdo con la reivindicación 1 o la reivindicación 2, en combinación con un vehículo, diluyente o excipiente farmacéuticamente aceptable.
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| GBGB0317009.9A GB0317009D0 (en) | 2003-07-21 | 2003-07-21 | Chemical compounds |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2928202T3 true ES2928202T3 (es) | 2022-11-16 |
Family
ID=27772362
Family Applications (4)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES16155811T Active ES2708570T3 (es) | 2003-07-21 | 2004-07-20 | Compuestos químicos |
| ES04743483.2T Active ES2589738T3 (es) | 2003-07-21 | 2004-07-20 | Fosforamidatos de nucleótidos como agentes contra el cáncer |
| ES21180706T Active ES2928202T3 (es) | 2003-07-21 | 2004-07-20 | Compuestos químicos |
| ES15154759.3T Active ES2667698T3 (es) | 2003-07-21 | 2004-07-20 | Compuestos químicos |
Family Applications Before (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES16155811T Active ES2708570T3 (es) | 2003-07-21 | 2004-07-20 | Compuestos químicos |
| ES04743483.2T Active ES2589738T3 (es) | 2003-07-21 | 2004-07-20 | Fosforamidatos de nucleótidos como agentes contra el cáncer |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES15154759.3T Active ES2667698T3 (es) | 2003-07-21 | 2004-07-20 | Compuestos químicos |
Country Status (20)
| Country | Link |
|---|---|
| US (2) | US7951787B2 (es) |
| EP (5) | EP1646639B8 (es) |
| JP (1) | JP4923216B2 (es) |
| AU (1) | AU2004261455B2 (es) |
| CA (1) | CA2518115C (es) |
| CY (4) | CY1117960T1 (es) |
| DK (4) | DK3904365T3 (es) |
| ES (4) | ES2708570T3 (es) |
| FI (1) | FIC20230013I1 (es) |
| FR (1) | FR23C1014I2 (es) |
| GB (1) | GB0317009D0 (es) |
| HU (4) | HUE059970T2 (es) |
| MX (1) | MXPA05012606A (es) |
| NO (1) | NO333603B1 (es) |
| NZ (1) | NZ541974A (es) |
| PL (4) | PL3904365T3 (es) |
| PT (4) | PT3040340T (es) |
| SI (2) | SI3040340T1 (es) |
| TR (1) | TR201901246T4 (es) |
| WO (1) | WO2005012327A2 (es) |
Families Citing this family (135)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7462605B2 (en) | 1998-01-23 | 2008-12-09 | Celmed Oncology (Usa), Inc. | Phosphoramidate compounds and methods of use |
| MY164523A (en) | 2000-05-23 | 2017-12-29 | Univ Degli Studi Cagliari | Methods and compositions for treating hepatitis c virus |
| EP1294735A2 (en) | 2000-05-26 | 2003-03-26 | Novirio Pharmaceuticals Limited | Methods and compositions for treating flaviviruses and pestiviruses |
| CN1849142A (zh) | 2002-11-15 | 2006-10-18 | 埃迪尼克斯(开曼)有限公司 | 2′-支链核苷和黄病毒突变 |
| EP2345661A1 (en) * | 2003-05-30 | 2011-07-20 | Pharmasset, Inc. | Modified fluorinated nucleoside analogues |
| CN101023094B (zh) * | 2004-07-21 | 2011-05-18 | 法莫赛特股份有限公司 | 烷基取代的2-脱氧-2-氟代-d-呋喃核糖基嘧啶和嘌呤及其衍生物的制备 |
| AU2005285045B2 (en) * | 2004-09-14 | 2011-10-13 | Gilead Pharmasset Llc | Preparation of 2'fluoro-2'- alkyl- substituted or other optionally substituted ribofuranosyl pyrimidines and purines and their derivatives |
| US8399428B2 (en) | 2004-12-09 | 2013-03-19 | Regents Of The University Of Minnesota | Nucleosides with antiviral and anticancer activity |
| GB0505781D0 (en) * | 2005-03-21 | 2005-04-27 | Univ Cardiff | Chemical compounds |
| DE102006037786A1 (de) | 2006-08-11 | 2008-03-20 | Resprotect Gmbh | Nukleoside, diese enthaltendes Arzneimittel und deren Verwendung |
| DK2099461T3 (da) * | 2006-11-13 | 2012-07-02 | Santaris Pharma As | LNA Nukleoside Phosphoramidates |
| GB0623493D0 (en) | 2006-11-24 | 2007-01-03 | Univ Cardiff | Chemical compounds |
| US7964580B2 (en) * | 2007-03-30 | 2011-06-21 | Pharmasset, Inc. | Nucleoside phosphoramidate prodrugs |
| AU2014233579B2 (en) * | 2007-03-30 | 2016-06-23 | Gilead Pharmasset Llc | Nucleoside phosphoramidate prodrugs |
| GB0709791D0 (en) * | 2007-05-22 | 2007-06-27 | Angeletti P Ist Richerche Bio | Antiviral agents |
| FR2922551B1 (fr) * | 2007-10-17 | 2009-12-25 | Univ Claude Bernard Lyon | Prodrogues phosphoesters de la gemcitabine comme agents anticancereux |
| US8173621B2 (en) | 2008-06-11 | 2012-05-08 | Gilead Pharmasset Llc | Nucleoside cyclicphosphates |
| SG172361A1 (en) | 2008-12-23 | 2011-07-28 | Pharmasset Inc | Nucleoside analogs |
| AU2009329872B2 (en) | 2008-12-23 | 2016-07-07 | Gilead Pharmasset Llc | Synthesis of purine nucleosides |
| AR074897A1 (es) | 2008-12-23 | 2011-02-23 | Pharmasset Inc | Fosforamidatos de nucleosidos |
| US8618076B2 (en) | 2009-05-20 | 2013-12-31 | Gilead Pharmasset Llc | Nucleoside phosphoramidates |
| TWI583692B (zh) | 2009-05-20 | 2017-05-21 | 基利法瑪席特有限責任公司 | 核苷磷醯胺 |
| SI2480559T1 (sl) | 2009-09-21 | 2013-10-30 | Gilead Sciences, Inc. | Postopki in intermediati za pripravo 1'-ciano-karbanukleozidnih analogov |
| EP2752422B1 (en) | 2010-03-31 | 2017-08-16 | Gilead Pharmasset LLC | Stereoselective synthesis of phosphorus containing actives |
| US8563530B2 (en) | 2010-03-31 | 2013-10-22 | Gilead Pharmassel LLC | Purine nucleoside phosphoramidate |
| PT2595980E (pt) | 2010-07-22 | 2014-11-27 | Gilead Sciences Inc | Métodos e compostos para tratar infeções pelo vírus da família paramyxoviridae |
| NZ607996A (en) | 2010-09-22 | 2014-07-25 | Alios Biopharma Inc | Substituted nucleotide analogs |
| GB201016855D0 (en) * | 2010-10-06 | 2010-11-17 | Nucana Biomed Ltd | Chemical compounds |
| ES2716158T3 (es) | 2010-11-30 | 2019-06-10 | Gilead Pharmasset Llc | 2'-spiro-nucleótidos para el tratamiento de hepatitis C |
| US9156874B2 (en) | 2011-01-03 | 2015-10-13 | Nanjing Molecular Research, Inc. | Double-liver-targeting phosphoramidate and phosphonoamidate prodrugs |
| US9095599B2 (en) | 2011-01-03 | 2015-08-04 | Nanjing Molecular Research, Inc. | O-(substituted benzyl) phosphoramidate compounds and therapeutic use |
| SG192841A1 (en) * | 2011-03-01 | 2013-09-30 | Nucana Biomed Ltd | Phosphoramidate derivatives of 5 - fluoro - 2 ' - deoxyuridine for use in the treatment of cancer |
| WO2012154321A1 (en) | 2011-03-31 | 2012-11-15 | Idenix Pharmaceuticals, Inc. | Compounds and pharmaceutical compositions for the treatment of viral infections |
| TW201329096A (zh) | 2011-09-12 | 2013-07-16 | Idenix Pharmaceuticals Inc | 經取代羰氧基甲基磷酸醯胺化合物及用於治療病毒感染之藥學組成物 |
| MD4589C1 (ro) | 2011-09-16 | 2019-03-31 | Gilead Pharmasset Llc | Compoziţie farmaceutică cu conţinut de sofosbuvir şi utilizarea acesteia în tratamentul hepatitei virale C |
| EP2768838A1 (en) | 2011-10-14 | 2014-08-27 | IDENIX Pharmaceuticals, Inc. | Substituted 3',5'-cyclic phosphates of purine nucleotide compounds and pharmaceutical compositions for the treatment of viral infections |
| GB2515942A (en) | 2011-10-21 | 2015-01-07 | Abbvie Inc | Combination treatment (e.g. with ABT-072 or ABT-333) of DAAs for use in treating HCV |
| US8492386B2 (en) | 2011-10-21 | 2013-07-23 | Abbvie Inc. | Methods for treating HCV |
| US8466159B2 (en) | 2011-10-21 | 2013-06-18 | Abbvie Inc. | Methods for treating HCV |
| US8853176B2 (en) | 2011-10-21 | 2014-10-07 | Abbvie Inc. | Methods for treating HCV |
| US8889159B2 (en) | 2011-11-29 | 2014-11-18 | Gilead Pharmasset Llc | Compositions and methods for treating hepatitis C virus |
| SI2794628T1 (sl) | 2011-12-20 | 2017-07-31 | Riboscience Llc | 4'-azido-3'-fluoro substituirani nukleozidni derivati kot inhibitorji podvojevanja RNA HCV |
| CA2856179C (en) | 2011-12-20 | 2017-02-28 | F. Hoffmann-La Roche Ag | 2',4'-difluoro-2'-methyl substituted nucleoside derivatives as inhibitors of hcv rna replication |
| EP2794630A4 (en) | 2011-12-22 | 2015-04-01 | Alios Biopharma Inc | SUBSTITUTED PHOSPHORTHIOAT NUCLEOTIDE ANALOGUE |
| CN104321333A (zh) | 2012-03-21 | 2015-01-28 | 沃泰克斯药物股份有限公司 | 硫代氨基磷酸酯核苷酸前药的固体形式 |
| WO2013142157A1 (en) | 2012-03-22 | 2013-09-26 | Alios Biopharma, Inc. | Pharmaceutical combinations comprising a thionucleotide analog |
| TWI637963B (zh) | 2012-03-28 | 2018-10-11 | 富士軟片股份有限公司 | 1-(2-脫氧-2-氟-4-硫-β-D-阿拉伯呋喃糖基)胞嘧啶之鹽 |
| WO2013177195A1 (en) | 2012-05-22 | 2013-11-28 | Idenix Pharmaceuticals, Inc. | 3',5'-cyclic phosphate prodrugs for hcv infection |
| NZ702744A (en) | 2012-05-22 | 2016-12-23 | Idenix Pharmaceuticals Llc | D-amino acid compounds for liver disease |
| EP2852604B1 (en) | 2012-05-22 | 2017-04-12 | Idenix Pharmaceuticals LLC | 3',5'-cyclic phosphoramidate prodrugs for hcv infection |
| UY34824A (es) | 2012-05-25 | 2013-11-29 | Janssen R & D Ireland | Nucleósidos de espirooxetano de uracilo |
| CN104640444B (zh) * | 2012-06-16 | 2016-12-14 | 河南美泰宝生物制药有限公司 | 双肝脏靶向氨基磷酸酯和氨基膦酸酯前药 |
| PL2883866T3 (pl) | 2012-08-13 | 2019-07-31 | Fujifilm Corporation | Produkt pośredni do syntezy 1-(2-deoksy-2-fluoro-4-tio-beta-d-arabinofuranosylo)cytozyny, produkt pośredni do syntezy tionukleozydu i sposoby otrzymywania tych produktów pośrednich |
| CN103665043B (zh) | 2012-08-30 | 2017-11-10 | 江苏豪森药业集团有限公司 | 一种替诺福韦前药及其在医药上的应用 |
| US9192621B2 (en) | 2012-09-27 | 2015-11-24 | Idenix Pharmaceuticals Llc | Esters and malonates of SATE prodrugs |
| EA030189B8 (ru) | 2012-10-08 | 2018-10-31 | Иденикс Фармасьютикалз Ллс | Аналоги 2'-хлоронуклеозидов для инфекции вгс |
| US10723754B2 (en) | 2012-10-22 | 2020-07-28 | Idenix Pharmaceuticals Llc | 2′,4′-bridged nucleosides for HCV infection |
| AU2013346515B2 (en) | 2012-11-16 | 2017-05-25 | NuCana plc | Process for preparing nucleoside prodrugs |
| WO2014099941A1 (en) | 2012-12-19 | 2014-06-26 | Idenix Pharmaceuticals, Inc. | 4'-fluoro nucleosides for the treatment of hcv |
| NZ625087A (en) | 2013-01-31 | 2017-05-26 | Gilead Pharmasset Llc | Combination formulation of two antiviral compounds |
| US10034893B2 (en) | 2013-02-01 | 2018-07-31 | Enanta Pharmaceuticals, Inc. | 5, 6-D2 uridine nucleoside/tide derivatives |
| US9339541B2 (en) | 2013-03-04 | 2016-05-17 | Merck Sharp & Dohme Corp. | Thiophosphate nucleosides for the treatment of HCV |
| US9309275B2 (en) | 2013-03-04 | 2016-04-12 | Idenix Pharmaceuticals Llc | 3′-deoxy nucleosides for the treatment of HCV |
| EP2970357A1 (en) | 2013-03-13 | 2016-01-20 | IDENIX Pharmaceuticals, Inc. | Amino acid phosphoramidate pronucleotides of 2'-cyano, azido and amino nucleosides for the treatment of hcv |
| US9187515B2 (en) | 2013-04-01 | 2015-11-17 | Idenix Pharmaceuticals Llc | 2′,4′-fluoro nucleosides for the treatment of HCV |
| US20140309164A1 (en) | 2013-04-12 | 2014-10-16 | Achillion Pharmaceuticals, Inc. | Deuterated nucleoside prodrugs useful for treating hcv |
| EA035301B1 (ru) | 2013-05-16 | 2020-05-26 | Рибосайенс Ллк | 4'-фтор-2'-метилзамещенные нуклеозидные производные |
| US9249176B2 (en) | 2013-05-16 | 2016-02-02 | Riboscience Llc | 4′-azido, 3′-deoxy-3′-fluoro substituted nucleoside derivatives as inhibitors of HCV RNA replication |
| US20180200280A1 (en) | 2013-05-16 | 2018-07-19 | Riboscience Llc | 4'-Fluoro-2'-Methyl Substituted Nucleoside Derivatives as Inhibitors of HCV RNA Replication |
| US10005779B2 (en) | 2013-06-05 | 2018-06-26 | Idenix Pharmaceuticals Llc | 1′,4′-thio nucleosides for the treatment of HCV |
| WO2015017713A1 (en) | 2013-08-01 | 2015-02-05 | Idenix Pharmaceuticals, Inc. | D-amino acid phosphoramidate pronucleotides of halogeno pyrimidine compounds for liver disease |
| ES2900570T3 (es) | 2013-08-27 | 2022-03-17 | Gilead Pharmasset Llc | Formulación de combinación de dos compuestos antivirales |
| WO2015056213A1 (en) * | 2013-10-17 | 2015-04-23 | Medivir Ab | Hcv polymerase inhibitors |
| KR20160099090A (ko) * | 2013-11-27 | 2016-08-19 | 아이데닉스 파마슈티칼스 엘엘씨 | 간암의 치료를 위한 뉴클레오티드 |
| JP6175553B2 (ja) | 2014-02-18 | 2017-08-09 | 富士フイルム株式会社 | チオラン骨格型糖化合物の製造方法およびチオラン骨格型糖化合物 |
| JP6204223B2 (ja) | 2014-02-19 | 2017-09-27 | 富士フイルム株式会社 | チオピラノース化合物等の製造方法 |
| CN103804446A (zh) * | 2014-02-27 | 2014-05-21 | 苏州东南药业股份有限公司 | 一种3,5-二苯甲酰基-2-去氧-2-氟-2甲基-D-核糖-γ-内酯的制备方法 |
| WO2015161137A1 (en) | 2014-04-16 | 2015-10-22 | Idenix Pharmaceuticals, Inc. | 3'-substituted methyl or alkynyl nucleosides for the treatment of hcv |
| TWI674097B (zh) * | 2014-06-25 | 2019-10-11 | 英商努卡那公眾有限公司 | 磷酸酯衍生物之調配物 |
| TWI695718B (zh) * | 2014-06-25 | 2020-06-11 | 英商努卡那公眾有限公司 | 前藥 |
| US9834577B2 (en) | 2014-07-22 | 2017-12-05 | Laurus Labs Limited | Process for the preparation of gemcitabine-[phenyl(benzoxy-L-alaninyl)] phosphate |
| PT3186244T (pt) * | 2014-08-25 | 2020-05-29 | Medivir Ab | Análogos dioxolano de uridina para o tratamento de cancro |
| US9675632B2 (en) | 2014-08-26 | 2017-06-13 | Enanta Pharmaceuticals, Inc. | Nucleoside and nucleotide derivatives |
| GB201417644D0 (en) * | 2014-10-06 | 2014-11-19 | Nucana Biomed Ltd | Method of separating phosphate diastereoisomers |
| TWI698444B (zh) | 2014-10-29 | 2020-07-11 | 美商基利科學股份有限公司 | 製備核糖苷的方法 |
| TWI678373B (zh) * | 2014-10-31 | 2019-12-01 | 日商富士軟片股份有限公司 | 硫代核苷衍生物或其鹽及醫藥組合物 |
| EP3212658A4 (en) * | 2014-10-31 | 2018-07-25 | Cocrystal Pharma, Inc. | 2',2'-dihalo nucleoside analogs for treatment of the flaviviridae family of viruses and cancer |
| US9718851B2 (en) | 2014-11-06 | 2017-08-01 | Enanta Pharmaceuticals, Inc. | Deuterated nucleoside/tide derivatives |
| LT3224268T (lt) | 2014-11-28 | 2019-09-25 | NuCana plc | Naujieji 2` ir (arba) 5` aminorūgšties esterio fosforamidato 3`-deoksi adenozino dariniai, kaip priešvėžiniai junginiai |
| US9732110B2 (en) | 2014-12-05 | 2017-08-15 | Enanta Pharmaceuticals, Inc. | Nucleoside and nucleotide derivatives |
| JP6735751B2 (ja) | 2014-12-15 | 2020-08-05 | エモリー ユニバーシティー | B型肝炎ウイルスの治療のためのホスホルアミデート |
| WO2016134058A1 (en) | 2015-02-18 | 2016-08-25 | Abbvie Inc. | Combinations useful to treat hepatitis c virus |
| CN109553651B (zh) * | 2015-04-03 | 2021-08-06 | 四川科伦博泰生物医药股份有限公司 | 4’-硫代核苷的新型化合物及其制备方法、药物组合物和应用 |
| MX2017014544A (es) | 2015-05-14 | 2018-09-26 | NuCana plc | Tratamientos del cáncer. |
| TWI687431B (zh) * | 2015-06-22 | 2020-03-11 | 瑞典商米迪維艾克提伯拉公司 | 治療癌症之前藥 |
| CN108350016B (zh) * | 2015-09-02 | 2021-07-27 | 艾伯维公司 | 抗病毒四氢呋喃衍生物 |
| CN106543252A (zh) * | 2015-09-16 | 2017-03-29 | 博瑞生物医药(苏州)股份有限公司 | 核苷氨基磷酸酯类前药的制备方法及其中间体 |
| CN106539810B (zh) * | 2015-09-16 | 2021-03-09 | 济南高合医疗科技有限公司 | 一种富集了nuc-1031单一异构体的组合物及其制备方法和用途 |
| CA2998189C (en) | 2015-09-16 | 2021-08-03 | Gilead Sciences, Inc. | Methods for treating arenaviridae and coronaviridae virus infections |
| CN106543220A (zh) * | 2015-09-16 | 2017-03-29 | 博瑞生物医药(苏州)股份有限公司 | 氨基磷酸酯化合物及其制备方法和晶体 |
| WO2017060661A1 (en) | 2015-10-05 | 2017-04-13 | Nucana Biomed Limited | Combination therapy |
| RS62593B1 (sr) | 2015-12-11 | 2021-12-31 | NuCana plc | Dijastereoselektivna sinteza derivata fosfata i proleka gemcitabina nuc-1031 |
| GB201522771D0 (en) | 2015-12-23 | 2016-02-03 | Nucana Biomed Ltd | Crystalline form of a phosphate derivative |
| US20190381084A1 (en) | 2015-12-23 | 2019-12-19 | Nucana Biomed Limited | Combination therapy |
| MA51576A (fr) * | 2015-12-23 | 2020-11-18 | NuCana plc | Polythérapie |
| WO2017189978A1 (en) | 2016-04-28 | 2017-11-02 | Emory University | Alkyne containing nucleotide and nucleoside therapeutic compositions and uses related thereto |
| GB201609600D0 (en) * | 2016-06-01 | 2016-07-13 | Nucuna Biomed Ltd | Cancer treatments |
| US11364257B2 (en) | 2016-06-24 | 2022-06-21 | Emory University | Phosphoramidates for the treatment of hepatitis B virus |
| US10711029B2 (en) | 2016-07-14 | 2020-07-14 | Atea Pharmaceuticals, Inc. | Beta-d-2′-deoxy-2′-alpha-fluoro-2′-beta-c-substituted-4′fluoro-n6-substituted-6-amino-2-substituted purine nucleotides for the treatment of hepatitis c virus infection |
| MX2019002430A (es) | 2016-08-31 | 2019-07-04 | Fujifilm Corp | Agente antitumoral, mejorador del efecto antitumoral, y kit antitumoral. |
| PL3512863T3 (pl) | 2016-09-07 | 2022-04-04 | Atea Pharmaceuticals, Inc. | 2'-Podstawione-N6-podstawione nukleotydy purynowe do leczenia zakażeń wirusem RNA |
| CN110869028B (zh) | 2017-03-14 | 2023-01-20 | 吉利德科学公司 | 治疗猫冠状病毒感染的方法 |
| CN115403626A (zh) | 2017-05-01 | 2022-11-29 | 吉利德科学公司 | 新结晶形式 |
| GB201709471D0 (en) | 2017-06-14 | 2017-07-26 | Nucana Biomed Ltd | Diastereoselective synthesis of hosphate derivatives |
| CN109134568B (zh) * | 2017-06-15 | 2022-11-22 | 北京美倍他药物研究有限公司 | 核苷磷酸酯/酰胺衍生物及其医药用途 |
| US10675296B2 (en) | 2017-07-11 | 2020-06-09 | Gilead Sciences, Inc. | Compositions comprising an RNA polymerase inhibitor and cyclodextrin for treating viral infections |
| US11266674B2 (en) | 2017-09-01 | 2022-03-08 | Sichuan Kelun-Biotech Biopharmaceutical Co., Ltd. | Pharmaceutical composition for tumor treatment or prevention, method, and use thereof |
| GB201715011D0 (en) | 2017-09-18 | 2017-11-01 | Nucana Biomed Ltd | Floxuridine synthesis |
| EP3684374A4 (en) | 2017-09-21 | 2021-06-16 | Riboscience LLC | 4'-FLUORO-2'-METHYL SUBSTITUTE NUCLEOSIDE DERIVATIVES USED AS HCV RNA REPLICATION INHIBITORS |
| GB201720279D0 (en) | 2017-12-05 | 2018-01-17 | Nucana Biomed Ltd | Anticancer compounds |
| CA3089728C (en) | 2018-01-29 | 2023-01-10 | Fujifilm Corporation | Antitumor agent for biliary tract cancer and method for treating biliary tract cancer |
| AU2019216531A1 (en) | 2018-02-02 | 2020-09-24 | Maverix Oncology, Inc. | Small molecule drug conjugates of gemcitabine monophosphate |
| WO2019152911A1 (en) * | 2018-02-02 | 2019-08-08 | Steven Albert Everett | Novel small molecule drug conjugates of gemcitabine derivatives |
| JP6810763B2 (ja) * | 2019-03-06 | 2021-01-06 | ニューカナ パブリック リミテッド カンパニー | がん治療 |
| GB201904544D0 (en) | 2019-04-01 | 2019-05-15 | NuCana plc | Anticancer compounds |
| WO2021154687A1 (en) | 2020-01-27 | 2021-08-05 | Gilead Sciences, Inc. | Methods for treating sars cov-2 infections |
| WO2021173713A1 (en) | 2020-02-27 | 2021-09-02 | Atea Pharmaceuticals, Inc. | Highly active compounds against covid-19 |
| US10874687B1 (en) | 2020-02-27 | 2020-12-29 | Atea Pharmaceuticals, Inc. | Highly active compounds against COVID-19 |
| CN115298181A (zh) | 2020-03-12 | 2022-11-04 | 吉利德科学公司 | 制备1’-氰基核苷的方法 |
| EP4132651A1 (en) | 2020-04-06 | 2023-02-15 | Gilead Sciences, Inc. | Inhalation formulations of 1'-cyano substituted carbanucleoside analogs |
| CA3179226A1 (en) | 2020-05-29 | 2021-12-02 | Tomas Cihlar | Remdesivir treatment methods |
| CN115996928A (zh) | 2020-06-24 | 2023-04-21 | 吉利德科学公司 | 1’-氰基核苷类似物及其用途 |
| KR20220018954A (ko) * | 2020-08-07 | 2022-02-15 | 주식회사 피노바이오 | 데옥시사이티딘계 항암제 및 실릴 에테르 함유 링커를 포함하는 접합체 및 이의 용도 |
| PE20231983A1 (es) | 2020-08-27 | 2023-12-12 | Gilead Sciences Inc | Compuestos y metodos para el tratamiento de infecciones virales |
| WO2023167944A1 (en) | 2022-03-02 | 2023-09-07 | Gilead Sciences, Inc. | Compounds and methods for treatment of viral infections |
Family Cites Families (32)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2802005A (en) | 1957-08-06 | S-eluorourace | ||
| US2945038A (en) | 1956-09-26 | 1960-07-12 | Hoffmann La Roche | 5-fluorocytosine and preparation thereof |
| US3201387A (en) | 1963-09-18 | 1965-08-17 | Heidelberger Charles | 5-trifluoromethyluracil, derivatives thereof, and processes for preparing the same |
| US4357324A (en) | 1981-02-24 | 1982-11-02 | The United States Of America As Represented By The Department Of Health And Human Services | Prodrug derivatives of 9β-D-arabinofuranosyl-2-fluoroadenine |
| FR2538397A1 (fr) | 1982-12-24 | 1984-06-29 | Charbonnages Ste Chimique | Procede continu de fabrication d'homopolymeres ou de copolymeres de l'ethylene |
| US5204466A (en) | 1990-02-01 | 1993-04-20 | Emory University | Method and compositions for the synthesis of bch-189 and related compounds |
| US5827727A (en) | 1990-02-01 | 1998-10-27 | Emory University | Method of resolution of 1,3-oxathiolane nucleoside enantiomers |
| US5914331A (en) | 1990-02-01 | 1999-06-22 | Emory University | Antiviral activity and resolution of 2-hydroxymethyl-5-(5-fluorocytosin-1-yl)-1,3-oxathiolane |
| US6703396B1 (en) | 1990-02-01 | 2004-03-09 | Emory University | Method of resolution and antiviral activity of 1,3-oxathiolane nuclesoside enantiomers |
| GB9009861D0 (en) | 1990-05-02 | 1990-06-27 | Glaxo Group Ltd | Chemical compounds |
| GB9505025D0 (en) | 1995-03-13 | 1995-05-03 | Medical Res Council | Chemical compounds |
| CN1192102C (zh) | 1998-01-23 | 2005-03-09 | 新生物生物公司 | 酶催化的治疗剂 |
| US7462605B2 (en) * | 1998-01-23 | 2008-12-09 | Celmed Oncology (Usa), Inc. | Phosphoramidate compounds and methods of use |
| US6475985B1 (en) | 1998-03-27 | 2002-11-05 | Regents Of The University Of Minnesota | Nucleosides with antiviral and anticancer activity |
| BR0012677A (pt) * | 1999-07-22 | 2003-07-01 | Newbiotics Inc | Ativação terapêutica catalisada por enzima |
| WO2001045690A2 (en) | 1999-12-23 | 2001-06-28 | Newbiotics, Inc. | Use of bvdu for inhibiting the growth of hyperproliferative cells |
| US20020147175A1 (en) | 2000-11-16 | 2002-10-10 | Shepard H. Michael | Synergistic ECTA compositions |
| JP2004534830A (ja) | 2001-06-21 | 2004-11-18 | グラクソ グループ リミテッド | Hcvにおけるヌクレオシド化合物 |
| GB0129945D0 (en) * | 2001-12-13 | 2002-02-06 | Mrc Technology Ltd | Chemical compounds |
| KR20040094692A (ko) | 2002-02-14 | 2004-11-10 | 파마셋, 리미티드 | 변형된 불소화 뉴클레오사이드 유사체 |
| RS114004A (en) | 2002-06-28 | 2007-02-05 | Idenix (Cayman) Limited, | Modified 2' and 3'-nucleoside produgs for treating flaviridae infections |
| EP1567169A4 (en) | 2002-11-04 | 2009-10-21 | Xenoport Inc | GEMCITABINE PROMOTERS, THEIR PHARMACEUTICAL COMPOSITIONS AND USES THEREOF |
| US7589078B2 (en) * | 2003-02-19 | 2009-09-15 | Yale University | Anti-viral nucleoside analogs and methods for treating viral infections, especially HIV infections |
| EP2345661A1 (en) | 2003-05-30 | 2011-07-20 | Pharmasset, Inc. | Modified fluorinated nucleoside analogues |
| AU2013346515B2 (en) | 2012-11-16 | 2017-05-25 | NuCana plc | Process for preparing nucleoside prodrugs |
| TWI674097B (zh) | 2014-06-25 | 2019-10-11 | 英商努卡那公眾有限公司 | 磷酸酯衍生物之調配物 |
| US9834577B2 (en) | 2014-07-22 | 2017-12-05 | Laurus Labs Limited | Process for the preparation of gemcitabine-[phenyl(benzoxy-L-alaninyl)] phosphate |
| GB201417644D0 (en) * | 2014-10-06 | 2014-11-19 | Nucana Biomed Ltd | Method of separating phosphate diastereoisomers |
| MX2017014544A (es) | 2015-05-14 | 2018-09-26 | NuCana plc | Tratamientos del cáncer. |
| WO2017060661A1 (en) | 2015-10-05 | 2017-04-13 | Nucana Biomed Limited | Combination therapy |
| RS62593B1 (sr) | 2015-12-11 | 2021-12-31 | NuCana plc | Dijastereoselektivna sinteza derivata fosfata i proleka gemcitabina nuc-1031 |
| GB201522764D0 (en) | 2015-12-23 | 2016-02-03 | Nucana Biomed Ltd | Formulations of phosphate derivatives |
-
2003
- 2003-07-21 GB GBGB0317009.9A patent/GB0317009D0/en not_active Ceased
-
2004
- 2004-07-20 HU HUE21180706A patent/HUE059970T2/hu unknown
- 2004-07-20 EP EP04743483.2A patent/EP1646639B8/en active Active
- 2004-07-20 EP EP15154759.3A patent/EP2955190B1/en not_active Revoked
- 2004-07-20 ES ES16155811T patent/ES2708570T3/es active Active
- 2004-07-20 AU AU2004261455A patent/AU2004261455B2/en not_active Ceased
- 2004-07-20 DK DK21180706.0T patent/DK3904365T3/da active
- 2004-07-20 HU HUE04743483A patent/HUE030374T2/en unknown
- 2004-07-20 MX MXPA05012606A patent/MXPA05012606A/es active IP Right Grant
- 2004-07-20 PL PL21180706.0T patent/PL3904365T3/pl unknown
- 2004-07-20 ES ES04743483.2T patent/ES2589738T3/es active Active
- 2004-07-20 EP EP18201295.5A patent/EP3486251A1/en not_active Withdrawn
- 2004-07-20 TR TR2019/01246T patent/TR201901246T4/tr unknown
- 2004-07-20 EP EP21180706.0A patent/EP3904365B1/en active Active
- 2004-07-20 WO PCT/GB2004/003148 patent/WO2005012327A2/en active Application Filing
- 2004-07-20 HU HUE16155811A patent/HUE042282T2/hu unknown
- 2004-07-20 PT PT16155811T patent/PT3040340T/pt unknown
- 2004-07-20 NZ NZ541974A patent/NZ541974A/xx not_active IP Right Cessation
- 2004-07-20 PT PT211807060T patent/PT3904365T/pt unknown
- 2004-07-20 US US10/560,887 patent/US7951787B2/en not_active Ceased
- 2004-07-20 JP JP2006520890A patent/JP4923216B2/ja active Active
- 2004-07-20 SI SI200432460T patent/SI3040340T1/sl unknown
- 2004-07-20 PL PL16155811T patent/PL3040340T3/pl unknown
- 2004-07-20 DK DK04743483.2T patent/DK1646639T3/en active
- 2004-07-20 DK DK16155811.9T patent/DK3040340T3/en active
- 2004-07-20 PT PT151547593T patent/PT2955190T/pt unknown
- 2004-07-20 DK DK15154759.3T patent/DK2955190T3/en active
- 2004-07-20 PL PL04743483.2T patent/PL1646639T3/pl unknown
- 2004-07-20 PL PL15154759T patent/PL2955190T3/pl unknown
- 2004-07-20 PT PT47434832T patent/PT1646639T/pt unknown
- 2004-07-20 US US15/279,611 patent/USRE47589E1/en active Active
- 2004-07-20 ES ES21180706T patent/ES2928202T3/es active Active
- 2004-07-20 SI SI200432439T patent/SI2955190T1/en unknown
- 2004-07-20 ES ES15154759.3T patent/ES2667698T3/es active Active
- 2004-07-20 EP EP16155811.9A patent/EP3040340B1/en active Active
- 2004-07-20 CA CA2518115A patent/CA2518115C/en active Active
-
2005
- 2005-08-26 NO NO20053993A patent/NO333603B1/no not_active IP Right Cessation
-
2016
- 2016-09-05 CY CY20161100875T patent/CY1117960T1/el unknown
-
2018
- 2018-05-03 CY CY20181100460T patent/CY1120202T1/el unknown
-
2019
- 2019-01-30 CY CY20191100124T patent/CY1121218T1/el unknown
-
2022
- 2022-10-07 CY CY20221100667T patent/CY1125603T1/el unknown
-
2023
- 2023-02-28 HU HUS2300012C patent/HUS2300012I1/hu unknown
- 2023-02-28 FR FR23C1014C patent/FR23C1014I2/fr active Active
- 2023-03-01 FI FIC20230013C patent/FIC20230013I1/fi unknown
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2928202T3 (es) | Compuestos químicos | |
| AU2012223012C1 (en) | Phosphoramidate derivatives of 5 - fluoro - 2 ' - deoxyuridine for use in the treatment of cancer | |
| US9156874B2 (en) | Double-liver-targeting phosphoramidate and phosphonoamidate prodrugs | |
| ES2380354T5 (es) | 2'-O,4'-C-metilen biciclonucleósidos | |
| ES2242965T3 (es) | Derivados de aril-ester fosforamidato de 2', 3'-didehidronucleosidos. | |
| ES2264197T3 (es) | Dinucleotidos y sus usos. | |
| AU747196B2 (en) | Method for large-scale production of di(uridine 5'-tetraphosphate) and salts thereof | |
| AU781323B2 (en) | Anti-viral pyrimidine nucleoside analogues | |
| AU610344B2 (en) | 2'-deoxy-5-fluorouridine derivatives | |
| WO2016155593A1 (zh) | 4'-硫代核苷的新型化合物及其制备方法、药物组合物和应用 | |
| WO2011005595A2 (en) | 2-5a analogs and their methods of use | |
| EA017005B1 (ru) | СОЛЬ П-ТОЛУОЛСУЛЬФОКИСЛОТЫ 5-АМИНО-3-(2'-О-АЦЕТИЛ-3'-ДЕЗОКСИ-β-D-РИБОФУРАНОЗИЛ)-3Н-ТИАЗОЛО[4,5-d]ПИРИМИДИН-2-ОНА И СПОСОБЫ ПОЛУЧЕНИЯ | |
| KR100990346B1 (ko) | 상피 및 망막 조직 질환 치료용 조성물 및 방법 | |
| EP2646449B1 (en) | Uridine di- or tri-phosphate derivatives and uses thereof | |
| Lewandowska et al. | Synthesis and anticancer activity of some 5-fluoro-2′-deoxyuridine phosphoramidates | |
| EP0799834A1 (en) | Modified nucleotides | |
| CN114480401B (zh) | 一种氯法拉滨修饰的寡聚核苷酸 | |
| JP2022535386A (ja) | 炭素環ヌクレオシド類似体 |