ES2753386T3 - Derivados de 2-hidroxi-1-{4-[(4-fenil)fenil]carbonil}piperazin-1-il}etano-1-ona y compuestos relacionados como inhibidores de sintasa de ácido graso (FASN) para el tratamiento del cáncer - Google Patents
Derivados de 2-hidroxi-1-{4-[(4-fenil)fenil]carbonil}piperazin-1-il}etano-1-ona y compuestos relacionados como inhibidores de sintasa de ácido graso (FASN) para el tratamiento del cáncer Download PDFInfo
- Publication number
- ES2753386T3 ES2753386T3 ES14779048T ES14779048T ES2753386T3 ES 2753386 T3 ES2753386 T3 ES 2753386T3 ES 14779048 T ES14779048 T ES 14779048T ES 14779048 T ES14779048 T ES 14779048T ES 2753386 T3 ES2753386 T3 ES 2753386T3
- Authority
- ES
- Spain
- Prior art keywords
- alkyl
- aryl
- cycloalkyl
- heteroaryl
- compound
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 150000001875 compounds Chemical class 0.000 title claims abstract description 325
- 102100022089 Acyl-[acyl-carrier-protein] hydrolase Human genes 0.000 title claims description 78
- 108010039731 Fatty Acid Synthases Proteins 0.000 title claims description 75
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 title claims description 43
- 125000002915 carbonyl group Chemical group [*:2]C([*:1])=O 0.000 title claims description 30
- 239000003112 inhibitor Substances 0.000 title description 41
- 206010028980 Neoplasm Diseases 0.000 title description 40
- 201000011510 cancer Diseases 0.000 title description 26
- 238000011282 treatment Methods 0.000 title description 25
- 125000000217 alkyl group Chemical group 0.000 claims abstract description 343
- -1 cyano, hydroxyl Chemical group 0.000 claims abstract description 229
- 125000000753 cycloalkyl group Chemical group 0.000 claims abstract description 214
- 125000003118 aryl group Chemical group 0.000 claims abstract description 194
- 125000001072 heteroaryl group Chemical group 0.000 claims abstract description 184
- 125000000592 heterocycloalkyl group Chemical group 0.000 claims abstract description 140
- 125000002950 monocyclic group Chemical group 0.000 claims abstract description 78
- 125000005843 halogen group Chemical group 0.000 claims abstract description 73
- 125000003545 alkoxy group Chemical group 0.000 claims abstract description 70
- 229910052757 nitrogen Inorganic materials 0.000 claims abstract description 69
- 125000005842 heteroatom Chemical group 0.000 claims abstract description 59
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 claims abstract description 55
- 150000003839 salts Chemical class 0.000 claims abstract description 54
- 125000001424 substituent group Chemical group 0.000 claims abstract description 48
- 229910052717 sulfur Inorganic materials 0.000 claims abstract description 46
- 125000006645 (C3-C4) cycloalkyl group Chemical group 0.000 claims abstract description 42
- 125000002619 bicyclic group Chemical group 0.000 claims abstract description 39
- 125000000304 alkynyl group Chemical group 0.000 claims abstract description 35
- YZCKVEUIGOORGS-OUBTZVSYSA-N Deuterium Chemical compound [2H] YZCKVEUIGOORGS-OUBTZVSYSA-N 0.000 claims abstract description 34
- 229910052805 deuterium Inorganic materials 0.000 claims abstract description 34
- 125000004183 alkoxy alkyl group Chemical group 0.000 claims abstract description 29
- 125000002768 hydroxyalkyl group Chemical group 0.000 claims abstract description 29
- 125000004103 aminoalkyl group Chemical group 0.000 claims abstract description 27
- 229910052760 oxygen Inorganic materials 0.000 claims abstract description 27
- 125000003342 alkenyl group Chemical group 0.000 claims abstract description 25
- 125000004104 aryloxy group Chemical group 0.000 claims abstract description 17
- 125000004404 heteroalkyl group Chemical group 0.000 claims abstract description 8
- 125000000623 heterocyclic group Chemical group 0.000 claims abstract description 8
- 125000006163 5-membered heteroaryl group Chemical class 0.000 claims abstract description 5
- 238000000034 method Methods 0.000 claims description 61
- 239000008194 pharmaceutical composition Substances 0.000 claims description 36
- 239000003814 drug Substances 0.000 claims description 27
- YOXHCYXIAVIFCZ-UHFFFAOYSA-N cyclopropanol Chemical compound OC1CC1 YOXHCYXIAVIFCZ-UHFFFAOYSA-N 0.000 claims description 18
- 229940127089 cytotoxic agent Drugs 0.000 claims description 18
- 125000005350 hydroxycycloalkyl group Chemical group 0.000 claims description 15
- AOJJSUZBOXZQNB-TZSSRYMLSA-N Doxorubicin Chemical compound O([C@H]1C[C@@](O)(CC=2C(O)=C3C(=O)C=4C=CC=C(C=4C(=O)C3=C(O)C=21)OC)C(=O)CO)[C@H]1C[C@H](N)[C@H](O)[C@H](C)O1 AOJJSUZBOXZQNB-TZSSRYMLSA-N 0.000 claims description 10
- 230000002401 inhibitory effect Effects 0.000 claims description 9
- GHASVSINZRGABV-UHFFFAOYSA-N Fluorouracil Chemical compound FC1=CNC(=O)NC1=O GHASVSINZRGABV-UHFFFAOYSA-N 0.000 claims description 8
- 229960002949 fluorouracil Drugs 0.000 claims description 8
- FQISKWAFAHGMGT-SGJOWKDISA-M Methylprednisolone sodium succinate Chemical compound [Na+].C([C@@]12C)=CC(=O)C=C1[C@@H](C)C[C@@H]1[C@@H]2[C@@H](O)C[C@]2(C)[C@@](O)(C(=O)COC(=O)CCC([O-])=O)CC[C@H]21 FQISKWAFAHGMGT-SGJOWKDISA-M 0.000 claims description 7
- 229960004584 methylprednisolone Drugs 0.000 claims description 7
- NKANXQFJJICGDU-QPLCGJKRSA-N Tamoxifen Chemical compound C=1C=CC=CC=1C(/CC)=C(C=1C=CC(OCCN(C)C)=CC=1)/C1=CC=CC=C1 NKANXQFJJICGDU-QPLCGJKRSA-N 0.000 claims description 6
- PLHJCIYEEKOWNM-HHHXNRCGSA-N tipifarnib Chemical compound CN1C=NC=C1[C@](N)(C=1C=C2C(C=3C=C(Cl)C=CC=3)=CC(=O)N(C)C2=CC=1)C1=CC=C(Cl)C=C1 PLHJCIYEEKOWNM-HHHXNRCGSA-N 0.000 claims description 6
- ZDZOTLJHXYCWBA-VCVYQWHSSA-N N-debenzoyl-N-(tert-butoxycarbonyl)-10-deacetyltaxol Chemical compound O([C@H]1[C@H]2[C@@](C([C@H](O)C3=C(C)[C@@H](OC(=O)[C@H](O)[C@@H](NC(=O)OC(C)(C)C)C=4C=CC=CC=4)C[C@]1(O)C3(C)C)=O)(C)[C@@H](O)C[C@H]1OC[C@]12OC(=O)C)C(=O)C1=CC=CC=C1 ZDZOTLJHXYCWBA-VCVYQWHSSA-N 0.000 claims description 5
- 229930012538 Paclitaxel Natural products 0.000 claims description 5
- 229960004316 cisplatin Drugs 0.000 claims description 5
- DQLATGHUWYMOKM-UHFFFAOYSA-L cisplatin Chemical compound N[Pt](N)(Cl)Cl DQLATGHUWYMOKM-UHFFFAOYSA-L 0.000 claims description 5
- 229960001592 paclitaxel Drugs 0.000 claims description 5
- RCINICONZNJXQF-MZXODVADSA-N taxol Chemical compound O([C@@H]1[C@@]2(C[C@@H](C(C)=C(C2(C)C)[C@H](C([C@]2(C)[C@@H](O)C[C@H]3OC[C@]3([C@H]21)OC(C)=O)=O)OC(=O)C)OC(=O)[C@H](O)[C@@H](NC(=O)C=1C=CC=CC=1)C=1C=CC=CC=1)O)C(=O)C1=CC=CC=C1 RCINICONZNJXQF-MZXODVADSA-N 0.000 claims description 5
- 229940124597 therapeutic agent Drugs 0.000 claims description 5
- MUMGGOZAMZWBJJ-DYKIIFRCSA-N Testostosterone Chemical compound O=C1CC[C@]2(C)[C@H]3CC[C@](C)([C@H](CC4)O)[C@@H]4[C@@H]3CCC2=C1 MUMGGOZAMZWBJJ-DYKIIFRCSA-N 0.000 claims description 4
- VSRXQHXAPYXROS-UHFFFAOYSA-N azanide;cyclobutane-1,1-dicarboxylic acid;platinum(2+) Chemical compound [NH2-].[NH2-].[Pt+2].OC(=O)C1(C(O)=O)CCC1 VSRXQHXAPYXROS-UHFFFAOYSA-N 0.000 claims description 4
- 229960004562 carboplatin Drugs 0.000 claims description 4
- 239000002254 cytotoxic agent Substances 0.000 claims description 4
- 231100000599 cytotoxic agent Toxicity 0.000 claims description 4
- 229960003957 dexamethasone Drugs 0.000 claims description 4
- UREBDLICKHMUKA-CXSFZGCWSA-N dexamethasone Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(F)[C@@H]1[C@@H]1C[C@@H](C)[C@@](C(=O)CO)(O)[C@@]1(C)C[C@@H]2O UREBDLICKHMUKA-CXSFZGCWSA-N 0.000 claims description 4
- 239000003937 drug carrier Substances 0.000 claims description 4
- UUVWYPNAQBNQJQ-UHFFFAOYSA-N hexamethylmelamine Chemical compound CN(C)C1=NC(N(C)C)=NC(N(C)C)=N1 UUVWYPNAQBNQJQ-UHFFFAOYSA-N 0.000 claims description 4
- DHMTURDWPRKSOA-RUZDIDTESA-N lonafarnib Chemical compound C1CN(C(=O)N)CCC1CC(=O)N1CCC([C@@H]2C3=C(Br)C=C(Cl)C=C3CCC3=CC(Br)=CN=C32)CC1 DHMTURDWPRKSOA-RUZDIDTESA-N 0.000 claims description 4
- SGDBTWWWUNNDEQ-LBPRGKRZSA-N melphalan Chemical compound OC(=O)[C@@H](N)CC1=CC=C(N(CCCl)CCCl)C=C1 SGDBTWWWUNNDEQ-LBPRGKRZSA-N 0.000 claims description 4
- 229960001924 melphalan Drugs 0.000 claims description 4
- CFCUWKMKBJTWLW-BKHRDMLASA-N mithramycin Chemical compound O([C@@H]1C[C@@H](O[C@H](C)[C@H]1O)OC=1C=C2C=C3C[C@H]([C@@H](C(=O)C3=C(O)C2=C(O)C=1C)O[C@@H]1O[C@H](C)[C@@H](O)[C@H](O[C@@H]2O[C@H](C)[C@H](O)[C@H](O[C@@H]3O[C@H](C)[C@@H](O)[C@@](C)(O)C3)C2)C1)[C@H](OC)C(=O)[C@@H](O)[C@@H](C)O)[C@H]1C[C@@H](O)[C@H](O)[C@@H](C)O1 CFCUWKMKBJTWLW-BKHRDMLASA-N 0.000 claims description 4
- 229960001756 oxaliplatin Drugs 0.000 claims description 4
- DWAFYCQODLXJNR-BNTLRKBRSA-L oxaliplatin Chemical compound O1C(=O)C(=O)O[Pt]11N[C@@H]2CCCC[C@H]2N1 DWAFYCQODLXJNR-BNTLRKBRSA-L 0.000 claims description 4
- 229960002340 pentostatin Drugs 0.000 claims description 4
- FPVKHBSQESCIEP-JQCXWYLXSA-N pentostatin Chemical compound C1[C@H](O)[C@@H](CO)O[C@H]1N1C(N=CNC[C@H]2O)=C2N=C1 FPVKHBSQESCIEP-JQCXWYLXSA-N 0.000 claims description 4
- 125000004194 piperazin-1-yl group Chemical group [H]N1C([H])([H])C([H])([H])N(*)C([H])([H])C1([H])[H] 0.000 claims description 4
- 229960003171 plicamycin Drugs 0.000 claims description 4
- WYWHKKSPHMUBEB-UHFFFAOYSA-N tioguanine Chemical compound N1C(N)=NC(=S)C2=C1N=CN2 WYWHKKSPHMUBEB-UHFFFAOYSA-N 0.000 claims description 4
- NDMPLJNOPCLANR-UHFFFAOYSA-N 3,4-dihydroxy-15-(4-hydroxy-18-methoxycarbonyl-5,18-seco-ibogamin-18-yl)-16-methoxy-1-methyl-6,7-didehydro-aspidospermidine-3-carboxylic acid methyl ester Natural products C1C(CC)(O)CC(CC2(C(=O)OC)C=3C(=CC4=C(C56C(C(C(O)C7(CC)C=CCN(C67)CC5)(O)C(=O)OC)N4C)C=3)OC)CN1CCC1=C2NC2=CC=CC=C12 NDMPLJNOPCLANR-UHFFFAOYSA-N 0.000 claims description 3
- VVIAGPKUTFNRDU-UHFFFAOYSA-N 6S-folinic acid Natural products C1NC=2NC(N)=NC(=O)C=2N(C=O)C1CNC1=CC=C(C(=O)NC(CCC(O)=O)C(O)=O)C=C1 VVIAGPKUTFNRDU-UHFFFAOYSA-N 0.000 claims description 3
- 108010006654 Bleomycin Proteins 0.000 claims description 3
- GAGWJHPBXLXJQN-UORFTKCHSA-N Capecitabine Chemical compound C1=C(F)C(NC(=O)OCCCCC)=NC(=O)N1[C@H]1[C@H](O)[C@H](O)[C@@H](C)O1 GAGWJHPBXLXJQN-UORFTKCHSA-N 0.000 claims description 3
- CMSMOCZEIVJLDB-UHFFFAOYSA-N Cyclophosphamide Chemical compound ClCCN(CCCl)P1(=O)NCCCO1 CMSMOCZEIVJLDB-UHFFFAOYSA-N 0.000 claims description 3
- UHDGCWIWMRVCDJ-CCXZUQQUSA-N Cytarabine Chemical compound O=C1N=C(N)C=CN1[C@H]1[C@@H](O)[C@H](O)[C@@H](CO)O1 UHDGCWIWMRVCDJ-CCXZUQQUSA-N 0.000 claims description 3
- 108010000817 Leuprolide Proteins 0.000 claims description 3
- FOCVUCIESVLUNU-UHFFFAOYSA-N Thiotepa Chemical compound C1CN1P(N1CC1)(=S)N1CC1 FOCVUCIESVLUNU-UHFFFAOYSA-N 0.000 claims description 3
- JXLYSJRDGCGARV-WWYNWVTFSA-N Vinblastine Natural products O=C(O[C@H]1[C@](O)(C(=O)OC)[C@@H]2N(C)c3c(cc(c(OC)c3)[C@]3(C(=O)OC)c4[nH]c5c(c4CCN4C[C@](O)(CC)C[C@H](C3)C4)cccc5)[C@@]32[C@H]2[C@@]1(CC)C=CCN2CC3)C JXLYSJRDGCGARV-WWYNWVTFSA-N 0.000 claims description 3
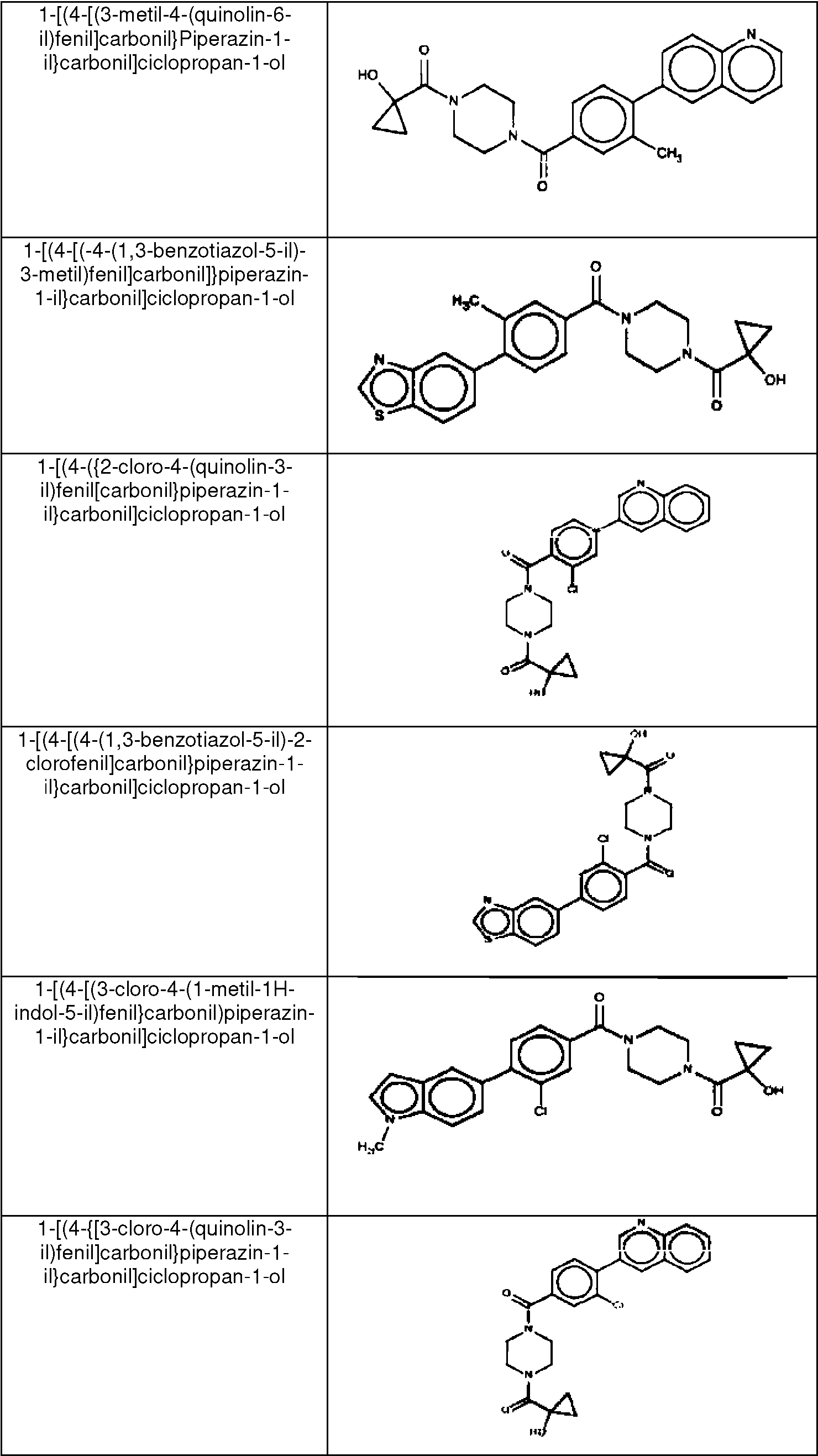
- GBKADBUMPBRZOS-UHFFFAOYSA-N [2-fluoro-4-(1-methylbenzimidazol-5-yl)phenyl]-[4-(1-hydroxycyclopropanecarbonyl)piperazin-1-yl]methanone Chemical compound FC1=C(C(=O)N2CCN(CC2)C(=O)C2(CC2)O)C=CC(=C1)C1=CC2=C(N(C=N2)C)C=C1 GBKADBUMPBRZOS-UHFFFAOYSA-N 0.000 claims description 3
- 229960002932 anastrozole Drugs 0.000 claims description 3
- YBBLVLTVTVSKRW-UHFFFAOYSA-N anastrozole Chemical compound N#CC(C)(C)C1=CC(C(C)(C#N)C)=CC(CN2N=CN=C2)=C1 YBBLVLTVTVSKRW-UHFFFAOYSA-N 0.000 claims description 3
- 229960001561 bleomycin Drugs 0.000 claims description 3
- OYVAGSVQBOHSSS-UAPAGMARSA-O bleomycin A2 Chemical compound N([C@H](C(=O)N[C@H](C)[C@@H](O)[C@H](C)C(=O)N[C@@H]([C@H](O)C)C(=O)NCCC=1SC=C(N=1)C=1SC=C(N=1)C(=O)NCCC[S+](C)C)[C@@H](O[C@H]1[C@H]([C@@H](O)[C@H](O)[C@H](CO)O1)O[C@@H]1[C@H]([C@@H](OC(N)=O)[C@H](O)[C@@H](CO)O1)O)C=1N=CNC=1)C(=O)C1=NC([C@H](CC(N)=O)NC[C@H](N)C(N)=O)=NC(N)=C1C OYVAGSVQBOHSSS-UAPAGMARSA-O 0.000 claims description 3
- JCKYGMPEJWAADB-UHFFFAOYSA-N chlorambucil Chemical compound OC(=O)CCCC1=CC=C(N(CCCl)CCCl)C=C1 JCKYGMPEJWAADB-UHFFFAOYSA-N 0.000 claims description 3
- 229960004630 chlorambucil Drugs 0.000 claims description 3
- 125000004093 cyano group Chemical group *C#N 0.000 claims description 3
- 229960003668 docetaxel Drugs 0.000 claims description 3
- 229960004679 doxorubicin Drugs 0.000 claims description 3
- 229960002074 flutamide Drugs 0.000 claims description 3
- MKXKFYHWDHIYRV-UHFFFAOYSA-N flutamide Chemical compound CC(C)C(=O)NC1=CC=C([N+]([O-])=O)C(C(F)(F)F)=C1 MKXKFYHWDHIYRV-UHFFFAOYSA-N 0.000 claims description 3
- VVIAGPKUTFNRDU-ABLWVSNPSA-N folinic acid Chemical compound C1NC=2NC(N)=NC(=O)C=2N(C=O)C1CNC1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)C=C1 VVIAGPKUTFNRDU-ABLWVSNPSA-N 0.000 claims description 3
- 235000008191 folinic acid Nutrition 0.000 claims description 3
- 239000011672 folinic acid Substances 0.000 claims description 3
- HOMGKSMUEGBAAB-UHFFFAOYSA-N ifosfamide Chemical compound ClCCNP1(=O)OCCCN1CCCl HOMGKSMUEGBAAB-UHFFFAOYSA-N 0.000 claims description 3
- 229960001101 ifosfamide Drugs 0.000 claims description 3
- UWKQSNNFCGGAFS-XIFFEERXSA-N irinotecan Chemical compound C1=C2C(CC)=C3CN(C(C4=C([C@@](C(=O)OC4)(O)CC)C=4)=O)C=4C3=NC2=CC=C1OC(=O)N(CC1)CCC1N1CCCCC1 UWKQSNNFCGGAFS-XIFFEERXSA-N 0.000 claims description 3
- 229960003881 letrozole Drugs 0.000 claims description 3
- HPJKCIUCZWXJDR-UHFFFAOYSA-N letrozole Chemical compound C1=CC(C#N)=CC=C1C(N1N=CN=C1)C1=CC=C(C#N)C=C1 HPJKCIUCZWXJDR-UHFFFAOYSA-N 0.000 claims description 3
- 229960001691 leucovorin Drugs 0.000 claims description 3
- RQZAXGRLVPAYTJ-GQFGMJRRSA-N megestrol acetate Chemical compound C1=C(C)C2=CC(=O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@@](C(C)=O)(OC(=O)C)[C@@]1(C)CC2 RQZAXGRLVPAYTJ-GQFGMJRRSA-N 0.000 claims description 3
- XOFYZVNMUHMLCC-ZPOLXVRWSA-N prednisone Chemical compound O=C1C=C[C@]2(C)[C@H]3C(=O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 XOFYZVNMUHMLCC-ZPOLXVRWSA-N 0.000 claims description 3
- 229960004618 prednisone Drugs 0.000 claims description 3
- 229960001603 tamoxifen Drugs 0.000 claims description 3
- 229960001196 thiotepa Drugs 0.000 claims description 3
- UCFGDBYHRUNTLO-QHCPKHFHSA-N topotecan Chemical compound C1=C(O)C(CN(C)C)=C2C=C(CN3C4=CC5=C(C3=O)COC(=O)[C@]5(O)CC)C4=NC2=C1 UCFGDBYHRUNTLO-QHCPKHFHSA-N 0.000 claims description 3
- 229960000303 topotecan Drugs 0.000 claims description 3
- 229960003048 vinblastine Drugs 0.000 claims description 3
- JXLYSJRDGCGARV-XQKSVPLYSA-N vincaleukoblastine Chemical compound C([C@@H](C[C@]1(C(=O)OC)C=2C(=CC3=C([C@]45[C@H]([C@@]([C@H](OC(C)=O)[C@]6(CC)C=CCN([C@H]56)CC4)(O)C(=O)OC)N3C)C=2)OC)C[C@@](C2)(O)CC)N2CCC2=C1NC1=CC=CC=C21 JXLYSJRDGCGARV-XQKSVPLYSA-N 0.000 claims description 3
- 229960004528 vincristine Drugs 0.000 claims description 3
- OGWKCGZFUXNPDA-XQKSVPLYSA-N vincristine Chemical compound C([N@]1C[C@@H](C[C@]2(C(=O)OC)C=3C(=CC4=C([C@]56[C@H]([C@@]([C@H](OC(C)=O)[C@]7(CC)C=CCN([C@H]67)CC5)(O)C(=O)OC)N4C=O)C=3)OC)C[C@@](C1)(O)CC)CC1=C2NC2=CC=CC=C12 OGWKCGZFUXNPDA-XQKSVPLYSA-N 0.000 claims description 3
- OGWKCGZFUXNPDA-UHFFFAOYSA-N vincristine Natural products C1C(CC)(O)CC(CC2(C(=O)OC)C=3C(=CC4=C(C56C(C(C(OC(C)=O)C7(CC)C=CCN(C67)CC5)(O)C(=O)OC)N4C=O)C=3)OC)CN1CCC1=C2NC2=CC=CC=C12 OGWKCGZFUXNPDA-UHFFFAOYSA-N 0.000 claims description 3
- 229960004355 vindesine Drugs 0.000 claims description 3
- UGGWPQSBPIFKDZ-KOTLKJBCSA-N vindesine Chemical compound C([C@@H](C[C@]1(C(=O)OC)C=2C(=CC3=C([C@]45[C@H]([C@@]([C@H](O)[C@]6(CC)C=CCN([C@H]56)CC4)(O)C(N)=O)N3C)C=2)OC)C[C@@](C2)(O)CC)N2CCC2=C1N=C1[C]2C=CC=C1 UGGWPQSBPIFKDZ-KOTLKJBCSA-N 0.000 claims description 3
- FPVKHBSQESCIEP-UHFFFAOYSA-N (8S)-3-(2-deoxy-beta-D-erythro-pentofuranosyl)-3,6,7,8-tetrahydroimidazo[4,5-d][1,3]diazepin-8-ol Natural products C1C(O)C(CO)OC1N1C(NC=NCC2O)=C2N=C1 FPVKHBSQESCIEP-UHFFFAOYSA-N 0.000 claims description 2
- 102100025573 1-alkyl-2-acetylglycerophosphocholine esterase Human genes 0.000 claims description 2
- VSNHCAURESNICA-NJFSPNSNSA-N 1-oxidanylurea Chemical compound N[14C](=O)NO VSNHCAURESNICA-NJFSPNSNSA-N 0.000 claims description 2
- AOJJSUZBOXZQNB-VTZDEGQISA-N 4'-epidoxorubicin Chemical compound O([C@H]1C[C@@](O)(CC=2C(O)=C3C(=O)C=4C=CC=C(C=4C(=O)C3=C(O)C=21)OC)C(=O)CO)[C@H]1C[C@H](N)[C@@H](O)[C@H](C)O1 AOJJSUZBOXZQNB-VTZDEGQISA-N 0.000 claims description 2
- IDPUKCWIGUEADI-UHFFFAOYSA-N 5-[bis(2-chloroethyl)amino]uracil Chemical compound ClCCN(CCCl)C1=CNC(=O)NC1=O IDPUKCWIGUEADI-UHFFFAOYSA-N 0.000 claims description 2
- BFYIZQONLCFLEV-DAELLWKTSA-N Aromasine Chemical compound O=C1C=C[C@]2(C)[C@H]3CC[C@](C)(C(CC4)=O)[C@@H]4[C@@H]3CC(=C)C2=C1 BFYIZQONLCFLEV-DAELLWKTSA-N 0.000 claims description 2
- 102000014654 Aromatase Human genes 0.000 claims description 2
- 108010078554 Aromatase Proteins 0.000 claims description 2
- GOLCXWYRSKYTSP-UHFFFAOYSA-N Arsenious Acid Chemical compound O1[As]2O[As]1O2 GOLCXWYRSKYTSP-UHFFFAOYSA-N 0.000 claims description 2
- 108010024976 Asparaginase Proteins 0.000 claims description 2
- OLCWFLWEHWLBTO-HSZRJFAPSA-N BMS-214662 Chemical compound C=1C=CSC=1S(=O)(=O)N([C@@H](C1)CC=2C=CC=CC=2)CC2=CC(C#N)=CC=C2N1CC1=CN=CN1 OLCWFLWEHWLBTO-HSZRJFAPSA-N 0.000 claims description 2
- JWBOIMRXGHLCPP-UHFFFAOYSA-N Chloditan Chemical compound C=1C=CC=C(Cl)C=1C(C(Cl)Cl)C1=CC=C(Cl)C=C1 JWBOIMRXGHLCPP-UHFFFAOYSA-N 0.000 claims description 2
- HTIJFSOGRVMCQR-UHFFFAOYSA-N Epirubicin Natural products COc1cccc2C(=O)c3c(O)c4CC(O)(CC(OC5CC(N)C(=O)C(C)O5)c4c(O)c3C(=O)c12)C(=O)CO HTIJFSOGRVMCQR-UHFFFAOYSA-N 0.000 claims description 2
- BFPYWIDHMRZLRN-SLHNCBLASA-N Ethinyl estradiol Chemical compound OC1=CC=C2[C@H]3CC[C@](C)([C@](CC4)(O)C#C)[C@@H]4[C@@H]3CCC2=C1 BFPYWIDHMRZLRN-SLHNCBLASA-N 0.000 claims description 2
- VWUXBMIQPBEWFH-WCCTWKNTSA-N Fulvestrant Chemical compound OC1=CC=C2[C@H]3CC[C@](C)([C@H](CC4)O)[C@@H]4[C@@H]3[C@H](CCCCCCCCCS(=O)CCCC(F)(F)C(F)(F)F)CC2=C1 VWUXBMIQPBEWFH-WCCTWKNTSA-N 0.000 claims description 2
- BLCLNMBMMGCOAS-URPVMXJPSA-N Goserelin Chemical compound C([C@@H](C(=O)N[C@H](COC(C)(C)C)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCN=C(N)N)C(=O)N1[C@@H](CCC1)C(=O)NNC(N)=O)NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC=1NC=NC=1)NC(=O)[C@H]1NC(=O)CC1)C1=CC=C(O)C=C1 BLCLNMBMMGCOAS-URPVMXJPSA-N 0.000 claims description 2
- 108010069236 Goserelin Proteins 0.000 claims description 2
- XDXDZDZNSLXDNA-TZNDIEGXSA-N Idarubicin Chemical compound C1[C@H](N)[C@H](O)[C@H](C)O[C@H]1O[C@@H]1C2=C(O)C(C(=O)C3=CC=CC=C3C3=O)=C3C(O)=C2C[C@@](O)(C(C)=O)C1 XDXDZDZNSLXDNA-TZNDIEGXSA-N 0.000 claims description 2
- XDXDZDZNSLXDNA-UHFFFAOYSA-N Idarubicin Natural products C1C(N)C(O)C(C)OC1OC1C2=C(O)C(C(=O)C3=CC=CC=C3C3=O)=C3C(O)=C2CC(O)(C(C)=O)C1 XDXDZDZNSLXDNA-UHFFFAOYSA-N 0.000 claims description 2
- FBOZXECLQNJBKD-ZDUSSCGKSA-N L-methotrexate Chemical compound C=1N=C2N=C(N)N=C(N)C2=NC=1CN(C)C1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)C=C1 FBOZXECLQNJBKD-ZDUSSCGKSA-N 0.000 claims description 2
- 239000005551 L01XE03 - Erlotinib Substances 0.000 claims description 2
- HLFSDGLLUJUHTE-SNVBAGLBSA-N Levamisole Chemical compound C1([C@H]2CN3CCSC3=N2)=CC=CC=C1 HLFSDGLLUJUHTE-SNVBAGLBSA-N 0.000 claims description 2
- BPEGJWRSRHCHSN-UHFFFAOYSA-N Temozolomide Chemical compound O=C1N(C)N=NC2=C(C(N)=O)N=CN21 BPEGJWRSRHCHSN-UHFFFAOYSA-N 0.000 claims description 2
- 229940009456 adriamycin Drugs 0.000 claims description 2
- 229960000473 altretamine Drugs 0.000 claims description 2
- ROBVIMPUHSLWNV-UHFFFAOYSA-N aminoglutethimide Chemical compound C=1C=C(N)C=CC=1C1(CC)CCC(=O)NC1=O ROBVIMPUHSLWNV-UHFFFAOYSA-N 0.000 claims description 2
- 229960003437 aminoglutethimide Drugs 0.000 claims description 2
- 229960001220 amsacrine Drugs 0.000 claims description 2
- XCPGHVQEEXUHNC-UHFFFAOYSA-N amsacrine Chemical compound COC1=CC(NS(C)(=O)=O)=CC=C1NC1=C(C=CC=C2)C2=NC2=CC=CC=C12 XCPGHVQEEXUHNC-UHFFFAOYSA-N 0.000 claims description 2
- 229940112129 campath Drugs 0.000 claims description 2
- 229960004397 cyclophosphamide Drugs 0.000 claims description 2
- RGLYKWWBQGJZGM-ISLYRVAYSA-N diethylstilbestrol Chemical compound C=1C=C(O)C=CC=1C(/CC)=C(\CC)C1=CC=C(O)C=C1 RGLYKWWBQGJZGM-ISLYRVAYSA-N 0.000 claims description 2
- 229960000452 diethylstilbestrol Drugs 0.000 claims description 2
- 229940120655 eloxatin Drugs 0.000 claims description 2
- 229960001904 epirubicin Drugs 0.000 claims description 2
- 229930013356 epothilone Natural products 0.000 claims description 2
- HESCAJZNRMSMJG-KKQRBIROSA-N epothilone A Chemical class C/C([C@@H]1C[C@@H]2O[C@@H]2CCC[C@@H]([C@@H]([C@@H](C)C(=O)C(C)(C)[C@@H](O)CC(=O)O1)O)C)=C\C1=CSC(C)=N1 HESCAJZNRMSMJG-KKQRBIROSA-N 0.000 claims description 2
- 229940082789 erbitux Drugs 0.000 claims description 2
- AAKJLRGGTJKAMG-UHFFFAOYSA-N erlotinib Chemical compound C=12C=C(OCCOC)C(OCCOC)=CC2=NC=NC=1NC1=CC=CC(C#C)=C1 AAKJLRGGTJKAMG-UHFFFAOYSA-N 0.000 claims description 2
- FRPJXPJMRWBBIH-RBRWEJTLSA-N estramustine Chemical compound ClCCN(CCCl)C(=O)OC1=CC=C2[C@H]3CC[C@](C)([C@H](CC4)O)[C@@H]4[C@@H]3CCC2=C1 FRPJXPJMRWBBIH-RBRWEJTLSA-N 0.000 claims description 2
- 229960001842 estramustine Drugs 0.000 claims description 2
- 229960005420 etoposide Drugs 0.000 claims description 2
- VJJPUSNTGOMMGY-MRVIYFEKSA-N etoposide Chemical compound COC1=C(O)C(OC)=CC([C@@H]2C3=CC=4OCOC=4C=C3[C@@H](O[C@H]3[C@@H]([C@@H](O)[C@@H]4O[C@H](C)OC[C@H]4O3)O)[C@@H]3[C@@H]2C(OC3)=O)=C1 VJJPUSNTGOMMGY-MRVIYFEKSA-N 0.000 claims description 2
- 229960000255 exemestane Drugs 0.000 claims description 2
- GIUYCYHIANZCFB-FJFJXFQQSA-N fludarabine phosphate Chemical compound C1=NC=2C(N)=NC(F)=NC=2N1[C@@H]1O[C@H](COP(O)(O)=O)[C@@H](O)[C@@H]1O GIUYCYHIANZCFB-FJFJXFQQSA-N 0.000 claims description 2
- 229960005304 fludarabine phosphate Drugs 0.000 claims description 2
- YLRFCQOZQXIBAB-RBZZARIASA-N fluoxymesterone Chemical compound C1CC2=CC(=O)CC[C@]2(C)[C@]2(F)[C@@H]1[C@@H]1CC[C@](C)(O)[C@@]1(C)C[C@@H]2O YLRFCQOZQXIBAB-RBZZARIASA-N 0.000 claims description 2
- 229960001751 fluoxymesterone Drugs 0.000 claims description 2
- 229960002258 fulvestrant Drugs 0.000 claims description 2
- XGALLCVXEZPNRQ-UHFFFAOYSA-N gefitinib Chemical compound C=12C=C(OCCCN3CCOCC3)C(OC)=CC2=NC=NC=1NC1=CC=C(F)C(Cl)=C1 XGALLCVXEZPNRQ-UHFFFAOYSA-N 0.000 claims description 2
- 229960005277 gemcitabine Drugs 0.000 claims description 2
- SDUQYLNIPVEERB-QPPQHZFASA-N gemcitabine Chemical compound O=C1N=C(N)C=CN1[C@H]1C(F)(F)[C@H](O)[C@@H](CO)O1 SDUQYLNIPVEERB-QPPQHZFASA-N 0.000 claims description 2
- 229960002913 goserelin Drugs 0.000 claims description 2
- 229960000908 idarubicin Drugs 0.000 claims description 2
- 229940084651 iressa Drugs 0.000 claims description 2
- 229960004768 irinotecan Drugs 0.000 claims description 2
- 229960001614 levamisole Drugs 0.000 claims description 2
- HAWPXGHAZFHHAD-UHFFFAOYSA-N mechlorethamine Chemical compound ClCCN(C)CCCl HAWPXGHAZFHHAD-UHFFFAOYSA-N 0.000 claims description 2
- 229960004961 mechlorethamine Drugs 0.000 claims description 2
- 229960001786 megestrol Drugs 0.000 claims description 2
- 229960000485 methotrexate Drugs 0.000 claims description 2
- 229960000350 mitotane Drugs 0.000 claims description 2
- 229960001156 mitoxantrone Drugs 0.000 claims description 2
- KKZJGLLVHKMTCM-UHFFFAOYSA-N mitoxantrone Chemical compound O=C1C2=C(O)C=CC(O)=C2C(=O)C2=C1C(NCCNCCO)=CC=C2NCCNCCO KKZJGLLVHKMTCM-UHFFFAOYSA-N 0.000 claims description 2
- 229960000624 procarbazine Drugs 0.000 claims description 2
- CPTBDICYNRMXFX-UHFFFAOYSA-N procarbazine Chemical compound CNNCC1=CC=C(C(=O)NC(C)C)C=C1 CPTBDICYNRMXFX-UHFFFAOYSA-N 0.000 claims description 2
- 125000003373 pyrazinyl group Chemical group 0.000 claims description 2
- 125000004076 pyridyl group Chemical group 0.000 claims description 2
- 125000000714 pyrimidinyl group Chemical group 0.000 claims description 2
- 125000004159 quinolin-2-yl group Chemical group [H]C1=C([H])C([H])=C2C([H])=C([H])C(*)=NC2=C1[H] 0.000 claims description 2
- 125000004548 quinolin-3-yl group Chemical group N1=CC(=CC2=CC=CC=C12)* 0.000 claims description 2
- 229940120982 tarceva Drugs 0.000 claims description 2
- 229940063683 taxotere Drugs 0.000 claims description 2
- 229960004964 temozolomide Drugs 0.000 claims description 2
- NRUKOCRGYNPUPR-QBPJDGROSA-N teniposide Chemical compound COC1=C(O)C(OC)=CC([C@@H]2C3=CC=4OCOC=4C=C3[C@@H](O[C@H]3[C@@H]([C@@H](O)[C@@H]4O[C@@H](OC[C@H]4O3)C=3SC=CC=3)O)[C@@H]3[C@@H]2C(OC3)=O)=C1 NRUKOCRGYNPUPR-QBPJDGROSA-N 0.000 claims description 2
- 229960001278 teniposide Drugs 0.000 claims description 2
- 229960003604 testosterone Drugs 0.000 claims description 2
- 229960003087 tioguanine Drugs 0.000 claims description 2
- 229950009158 tipifarnib Drugs 0.000 claims description 2
- XFCLJVABOIYOMF-QPLCGJKRSA-N toremifene Chemical compound C1=CC(OCCN(C)C)=CC=C1C(\C=1C=CC=CC=1)=C(\CCCl)C1=CC=CC=C1 XFCLJVABOIYOMF-QPLCGJKRSA-N 0.000 claims description 2
- 229960005026 toremifene Drugs 0.000 claims description 2
- 229960000575 trastuzumab Drugs 0.000 claims description 2
- 229950001353 tretamine Drugs 0.000 claims description 2
- IUCJMVBFZDHPDX-UHFFFAOYSA-N tretamine Chemical compound C1CN1C1=NC(N2CC2)=NC(N2CC2)=N1 IUCJMVBFZDHPDX-UHFFFAOYSA-N 0.000 claims description 2
- 229940086984 trisenox Drugs 0.000 claims description 2
- 229960001055 uracil mustard Drugs 0.000 claims description 2
- ZOCKGBMQLCSHFP-KQRAQHLDSA-N valrubicin Chemical compound O([C@H]1C[C@](CC2=C(O)C=3C(=O)C4=CC=CC(OC)=C4C(=O)C=3C(O)=C21)(O)C(=O)COC(=O)CCCC)[C@H]1C[C@H](NC(=O)C(F)(F)F)[C@H](O)[C@H](C)O1 ZOCKGBMQLCSHFP-KQRAQHLDSA-N 0.000 claims description 2
- 229960000653 valrubicin Drugs 0.000 claims description 2
- GBABOYUKABKIAF-GHYRFKGUSA-N vinorelbine Chemical compound C1N(CC=2C3=CC=CC=C3NC=22)CC(CC)=C[C@H]1C[C@]2(C(=O)OC)C1=CC([C@]23[C@H]([C@]([C@H](OC(C)=O)[C@]4(CC)C=CCN([C@H]34)CC2)(O)C(=O)OC)N2C)=C2C=C1OC GBABOYUKABKIAF-GHYRFKGUSA-N 0.000 claims description 2
- 229960002066 vinorelbine Drugs 0.000 claims description 2
- 229940053867 xeloda Drugs 0.000 claims description 2
- 101000824278 Homo sapiens Acyl-[acyl-carrier-protein] hydrolase Proteins 0.000 claims 2
- RJURFGZVJUQBHK-UHFFFAOYSA-N actinomycin D Natural products CC1OC(=O)C(C(C)C)N(C)C(=O)CN(C)C(=O)C2CCCN2C(=O)C(C(C)C)NC(=O)C1NC(=O)C1=C(N)C(=O)C(C)=C2OC(C(C)=CC=C3C(=O)NC4C(=O)NC(C(N5CCCC5C(=O)N(C)CC(=O)N(C)C(C(C)C)C(=O)OC4C)=O)C(C)C)=C3N=C21 RJURFGZVJUQBHK-UHFFFAOYSA-N 0.000 claims 2
- 125000006578 monocyclic heterocycloalkyl group Chemical group 0.000 claims 2
- VWKVCALVDOGENI-UHFFFAOYSA-N (3-chloro-4-quinolin-3-ylphenyl)-[4-(1-hydroxycyclopropanecarbonyl)piperazin-1-yl]methanone Chemical compound C1CN(C(=O)C=2C=C(Cl)C(=CC=2)C=2C=C3C=CC=CC3=NC=2)CCN1C(=O)C1(O)CC1 VWKVCALVDOGENI-UHFFFAOYSA-N 0.000 claims 1
- RTQWWZBSTRGEAV-PKHIMPSTSA-N 2-[[(2s)-2-[bis(carboxymethyl)amino]-3-[4-(methylcarbamoylamino)phenyl]propyl]-[2-[bis(carboxymethyl)amino]propyl]amino]acetic acid Chemical compound CNC(=O)NC1=CC=C(C[C@@H](CN(CC(C)N(CC(O)=O)CC(O)=O)CC(O)=O)N(CC(O)=O)CC(O)=O)C=C1 RTQWWZBSTRGEAV-PKHIMPSTSA-N 0.000 claims 1
- ZKQWLVQHVCEMLL-UHFFFAOYSA-N 5-[2-chloro-4-[4-(1-hydroxycyclopropanecarbonyl)piperazine-1-carbonyl]phenyl]-1H-indole-3-carbonitrile Chemical compound ClC1=C(C=CC(=C1)C(=O)N1CCN(CC1)C(=O)C1(CC1)O)C=1C=C2C(=CNC2=CC=1)C#N ZKQWLVQHVCEMLL-UHFFFAOYSA-N 0.000 claims 1
- STQGQHZAVUOBTE-UHFFFAOYSA-N 7-Cyan-hept-2t-en-4,6-diinsaeure Natural products C1=2C(O)=C3C(=O)C=4C(OC)=CC=CC=4C(=O)C3=C(O)C=2CC(O)(C(C)=O)CC1OC1CC(N)C(O)C(C)O1 STQGQHZAVUOBTE-UHFFFAOYSA-N 0.000 claims 1
- 108010092160 Dactinomycin Proteins 0.000 claims 1
- RKHSVDPWIWAXJP-UHFFFAOYSA-N [2-chloro-4-(1-methylindol-5-yl)phenyl]-[4-(1-hydroxycyclopropanecarbonyl)piperazin-1-yl]methanone Chemical compound ClC1=C(C=CC(=C1)C=1C=C2C=CN(C2=CC=1)C)C(=O)N1CCN(CC1)C(=O)C1(CC1)O RKHSVDPWIWAXJP-UHFFFAOYSA-N 0.000 claims 1
- OHXSKYSCNGMXGK-UHFFFAOYSA-N [2-fluoro-4-(1-methylindol-5-yl)phenyl]-[4-(1-hydroxycyclopropanecarbonyl)piperazin-1-yl]methanone Chemical compound FC1=C(C=CC(=C1)C=1C=C2C=CN(C2=CC=1)C)C(=O)N1CCN(CC1)C(=O)C1(CC1)O OHXSKYSCNGMXGK-UHFFFAOYSA-N 0.000 claims 1
- VKZGNDJWTBUMRC-UHFFFAOYSA-N [3-chloro-4-(1-methylindol-5-yl)phenyl]-[4-(1-hydroxycyclopropanecarbonyl)piperazin-1-yl]methanone Chemical compound ClC=1C=C(C=CC=1C=1C=C2C=CN(C2=CC=1)C)C(=O)N1CCN(CC1)C(=O)C1(CC1)O VKZGNDJWTBUMRC-UHFFFAOYSA-N 0.000 claims 1
- SEFIRGUYCMSQKT-UHFFFAOYSA-N [4-(1-hydroxycyclopropanecarbonyl)piperazin-1-yl]-(4-isoquinolin-6-ylphenyl)methanone Chemical compound C1CN(C(=O)C=2C=CC(=CC=2)C=2C=C3C=CN=CC3=CC=2)CCN1C(=O)C1(O)CC1 SEFIRGUYCMSQKT-UHFFFAOYSA-N 0.000 claims 1
- MGWIMGUJYJRYQH-UHFFFAOYSA-N [4-(1-hydroxycyclopropanecarbonyl)piperazin-1-yl]-(4-quinolin-2-ylphenyl)methanone Chemical compound N1=C(C=CC2=CC=CC=C12)C1=CC=C(C=C1)C(=O)N1CCN(CC1)C(=O)C1(CC1)O MGWIMGUJYJRYQH-UHFFFAOYSA-N 0.000 claims 1
- RJURFGZVJUQBHK-IIXSONLDSA-N actinomycin D Chemical compound C[C@H]1OC(=O)[C@H](C(C)C)N(C)C(=O)CN(C)C(=O)[C@@H]2CCCN2C(=O)[C@@H](C(C)C)NC(=O)[C@H]1NC(=O)C1=C(N)C(=O)C(C)=C2OC(C(C)=CC=C3C(=O)N[C@@H]4C(=O)N[C@@H](C(N5CCC[C@H]5C(=O)N(C)CC(=O)N(C)[C@@H](C(C)C)C(=O)O[C@@H]4C)=O)C(C)C)=C3N=C21 RJURFGZVJUQBHK-IIXSONLDSA-N 0.000 claims 1
- GXJABQQUPOEUTA-RDJZCZTQSA-N bortezomib Chemical compound C([C@@H](C(=O)N[C@@H](CC(C)C)B(O)O)NC(=O)C=1N=CC=NC=1)C1=CC=CC=C1 GXJABQQUPOEUTA-RDJZCZTQSA-N 0.000 claims 1
- 229940125904 compound 1 Drugs 0.000 claims 1
- 229960000640 dactinomycin Drugs 0.000 claims 1
- 229960000975 daunorubicin Drugs 0.000 claims 1
- STQGQHZAVUOBTE-VGBVRHCVSA-N daunorubicin Chemical compound O([C@H]1C[C@@](O)(CC=2C(O)=C3C(=O)C=4C=CC=C(C=4C(=O)C3=C(O)C=21)OC)C(C)=O)[C@H]1C[C@H](N)[C@H](O)[C@H](C)O1 STQGQHZAVUOBTE-VGBVRHCVSA-N 0.000 claims 1
- 229960001001 ibritumomab tiuxetan Drugs 0.000 claims 1
- PSGAAPLEWMOORI-PEINSRQWSA-N medroxyprogesterone acetate Chemical compound C([C@@]12C)CC(=O)C=C1[C@@H](C)C[C@@H]1[C@@H]2CC[C@]2(C)[C@@](OC(C)=O)(C(C)=O)CC[C@H]21 PSGAAPLEWMOORI-PEINSRQWSA-N 0.000 claims 1
- 229960002985 medroxyprogesterone acetate Drugs 0.000 claims 1
- 229960004296 megestrol acetate Drugs 0.000 claims 1
- 229960005353 testolactone Drugs 0.000 claims 1
- BPEWUONYVDABNZ-DZBHQSCQSA-N testolactone Chemical compound O=C1C=C[C@]2(C)[C@H]3CC[C@](C)(OC(=O)CC4)[C@@H]4[C@@H]3CCC2=C1 BPEWUONYVDABNZ-DZBHQSCQSA-N 0.000 claims 1
- 229940099039 velcade Drugs 0.000 claims 1
- 125000004178 (C1-C4) alkyl group Chemical group 0.000 abstract 3
- 239000000243 solution Substances 0.000 description 194
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 189
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 170
- 239000000203 mixture Substances 0.000 description 124
- 239000007787 solid Substances 0.000 description 122
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 120
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 101
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 96
- 238000004895 liquid chromatography mass spectrometry Methods 0.000 description 73
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 59
- 235000019439 ethyl acetate Nutrition 0.000 description 58
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 57
- 239000011541 reaction mixture Substances 0.000 description 57
- JGFZNNIVVJXRND-UHFFFAOYSA-N N,N-Diisopropylethylamine (DIPEA) Chemical compound CCN(C(C)C)C(C)C JGFZNNIVVJXRND-UHFFFAOYSA-N 0.000 description 56
- 235000002639 sodium chloride Nutrition 0.000 description 49
- 239000012044 organic layer Substances 0.000 description 48
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 46
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 46
- 239000000741 silica gel Substances 0.000 description 44
- 229910002027 silica gel Inorganic materials 0.000 description 44
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 37
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 36
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 36
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 31
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 31
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 29
- 239000012267 brine Substances 0.000 description 29
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 29
- 231100000614 poison Toxicity 0.000 description 28
- GQXURJDNDYACGE-UHFFFAOYSA-N 1-hydroxycyclopropane-1-carboxylic acid Chemical compound OC(=O)C1(O)CC1 GQXURJDNDYACGE-UHFFFAOYSA-N 0.000 description 27
- 239000003921 oil Substances 0.000 description 27
- 235000019198 oils Nutrition 0.000 description 27
- 238000002360 preparation method Methods 0.000 description 27
- 238000001914 filtration Methods 0.000 description 26
- IXCSERBJSXMMFS-UHFFFAOYSA-N hydrogen chloride Substances Cl.Cl IXCSERBJSXMMFS-UHFFFAOYSA-N 0.000 description 26
- 229910000041 hydrogen chloride Inorganic materials 0.000 description 26
- 238000001816 cooling Methods 0.000 description 24
- 239000003643 water by type Substances 0.000 description 24
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 22
- 239000002246 antineoplastic agent Substances 0.000 description 21
- 201000010099 disease Diseases 0.000 description 20
- 239000000463 material Substances 0.000 description 20
- RFIOZSIHFNEKFF-UHFFFAOYSA-M piperazine-1-carboxylate Chemical compound [O-]C(=O)N1CCNCC1 RFIOZSIHFNEKFF-UHFFFAOYSA-M 0.000 description 20
- FYSNRJHAOHDILO-UHFFFAOYSA-N thionyl chloride Chemical compound ClS(Cl)=O FYSNRJHAOHDILO-UHFFFAOYSA-N 0.000 description 20
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 19
- 229910052799 carbon Inorganic materials 0.000 description 19
- 239000003208 petroleum Substances 0.000 description 19
- 239000012071 phase Substances 0.000 description 19
- 239000011734 sodium Substances 0.000 description 19
- 229910052708 sodium Inorganic materials 0.000 description 19
- 229940083542 sodium Drugs 0.000 description 19
- 235000015424 sodium Nutrition 0.000 description 19
- 230000005764 inhibitory process Effects 0.000 description 18
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 16
- 241000124008 Mammalia Species 0.000 description 16
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 16
- 239000003795 chemical substances by application Substances 0.000 description 16
- 239000007789 gas Substances 0.000 description 16
- NFHFRUOZVGFOOS-UHFFFAOYSA-N palladium;triphenylphosphane Chemical compound [Pd].C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 NFHFRUOZVGFOOS-UHFFFAOYSA-N 0.000 description 16
- 239000012298 atmosphere Substances 0.000 description 15
- WSFSSNUMVMOOMR-BJUDXGSMSA-N methanone Chemical compound O=[11CH2] WSFSSNUMVMOOMR-BJUDXGSMSA-N 0.000 description 15
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 15
- 238000002953 preparative HPLC Methods 0.000 description 15
- 239000002904 solvent Substances 0.000 description 15
- 229910052796 boron Inorganic materials 0.000 description 14
- 239000000543 intermediate Substances 0.000 description 14
- KDLHZDBZIXYQEI-UHFFFAOYSA-N palladium Substances [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 13
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 12
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 12
- DTQVDTLACAAQTR-UHFFFAOYSA-N Trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 12
- 238000010828 elution Methods 0.000 description 12
- 238000004128 high performance liquid chromatography Methods 0.000 description 12
- 239000010410 layer Substances 0.000 description 12
- 239000000546 pharmaceutical excipient Substances 0.000 description 12
- RIOQSEWOXXDEQQ-UHFFFAOYSA-N triphenylphosphine Chemical compound C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 RIOQSEWOXXDEQQ-UHFFFAOYSA-N 0.000 description 12
- 230000008901 benefit Effects 0.000 description 11
- 210000004027 cell Anatomy 0.000 description 11
- 239000012043 crude product Substances 0.000 description 11
- 208000035475 disorder Diseases 0.000 description 11
- 239000012074 organic phase Substances 0.000 description 11
- VHUUQVKOLVNVRT-UHFFFAOYSA-N Ammonium hydroxide Chemical compound [NH4+].[OH-] VHUUQVKOLVNVRT-UHFFFAOYSA-N 0.000 description 10
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 10
- XEEYBQQBJWHFJM-UHFFFAOYSA-N Iron Chemical compound [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 description 10
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 10
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 10
- 239000002671 adjuvant Substances 0.000 description 10
- 239000000908 ammonium hydroxide Substances 0.000 description 10
- 235000011114 ammonium hydroxide Nutrition 0.000 description 10
- 230000000694 effects Effects 0.000 description 10
- DNIAPMSPPWPWGF-UHFFFAOYSA-N propylene glycol Substances CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 10
- WSLDOOZREJYCGB-UHFFFAOYSA-N 1,2-Dichloroethane Chemical compound ClCCCl WSLDOOZREJYCGB-UHFFFAOYSA-N 0.000 description 9
- 125000003236 benzoyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C(*)=O 0.000 description 9
- 230000015572 biosynthetic process Effects 0.000 description 9
- 206010012601 diabetes mellitus Diseases 0.000 description 9
- 230000001965 increasing effect Effects 0.000 description 9
- 239000000047 product Substances 0.000 description 9
- 239000000725 suspension Substances 0.000 description 9
- 206010006187 Breast cancer Diseases 0.000 description 8
- 239000002253 acid Substances 0.000 description 8
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 8
- 238000006243 chemical reaction Methods 0.000 description 8
- ZUOUZKKEUPVFJK-UHFFFAOYSA-N diphenyl Chemical compound C1=CC=CC=C1C1=CC=CC=C1 ZUOUZKKEUPVFJK-UHFFFAOYSA-N 0.000 description 8
- 150000002148 esters Chemical class 0.000 description 8
- 230000002265 prevention Effects 0.000 description 8
- 238000003756 stirring Methods 0.000 description 8
- KXDHJXZQYSOELW-UHFFFAOYSA-M Carbamate Chemical compound NC([O-])=O KXDHJXZQYSOELW-UHFFFAOYSA-M 0.000 description 7
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 7
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 7
- WMFOQBRAJBCJND-UHFFFAOYSA-M Lithium hydroxide Chemical compound [Li+].[OH-] WMFOQBRAJBCJND-UHFFFAOYSA-M 0.000 description 7
- 241001465754 Metazoa Species 0.000 description 7
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 7
- 239000000654 additive Substances 0.000 description 7
- 238000004440 column chromatography Methods 0.000 description 7
- 230000014509 gene expression Effects 0.000 description 7
- LWIHDJKSTIGBAC-UHFFFAOYSA-K potassium phosphate Substances [K+].[K+].[K+].[O-]P([O-])([O-])=O LWIHDJKSTIGBAC-UHFFFAOYSA-K 0.000 description 7
- 125000006413 ring segment Chemical group 0.000 description 7
- 235000017557 sodium bicarbonate Nutrition 0.000 description 7
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 7
- 239000012453 solvate Substances 0.000 description 7
- 208000024891 symptom Diseases 0.000 description 7
- QPYOLSJFOCIOHK-UHFFFAOYSA-N tert-butyl 4-[4-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)benzoyl]piperazine-1-carboxylate Chemical compound C1CN(C(=O)OC(C)(C)C)CCN1C(=O)C1=CC=C(B2OC(C)(C)C(C)(C)O2)C=C1 QPYOLSJFOCIOHK-UHFFFAOYSA-N 0.000 description 7
- HZNVUJQVZSTENZ-UHFFFAOYSA-N 2,3-dichloro-5,6-dicyano-1,4-benzoquinone Chemical compound ClC1=C(Cl)C(=O)C(C#N)=C(C#N)C1=O HZNVUJQVZSTENZ-UHFFFAOYSA-N 0.000 description 6
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 6
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 6
- 108010010803 Gelatin Proteins 0.000 description 6
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 6
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 6
- 101100030361 Neurospora crassa (strain ATCC 24698 / 74-OR23-1A / CBS 708.71 / DSM 1257 / FGSC 987) pph-3 gene Proteins 0.000 description 6
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 6
- 239000002202 Polyethylene glycol Substances 0.000 description 6
- 125000004429 atom Chemical group 0.000 description 6
- 239000002775 capsule Substances 0.000 description 6
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 6
- 238000000132 electrospray ionisation Methods 0.000 description 6
- 230000008030 elimination Effects 0.000 description 6
- 238000003379 elimination reaction Methods 0.000 description 6
- 239000008273 gelatin Substances 0.000 description 6
- 229920000159 gelatin Polymers 0.000 description 6
- 229940014259 gelatin Drugs 0.000 description 6
- 235000019322 gelatine Nutrition 0.000 description 6
- 235000011852 gelatine desserts Nutrition 0.000 description 6
- BDAGIHXWWSANSR-UHFFFAOYSA-N methanoic acid Natural products OC=O BDAGIHXWWSANSR-UHFFFAOYSA-N 0.000 description 6
- 229920001223 polyethylene glycol Polymers 0.000 description 6
- 238000000746 purification Methods 0.000 description 6
- 229920006395 saturated elastomer Polymers 0.000 description 6
- 229910052938 sodium sulfate Inorganic materials 0.000 description 6
- 235000011152 sodium sulphate Nutrition 0.000 description 6
- BKZRMPOYXDWHSH-UHFFFAOYSA-N tert-butyl 4-(4-bromobenzoyl)piperazine-1-carboxylate Chemical compound C1CN(C(=O)OC(C)(C)C)CCN1C(=O)C1=CC=C(Br)C=C1 BKZRMPOYXDWHSH-UHFFFAOYSA-N 0.000 description 6
- CWXPZXBSDSIRCS-UHFFFAOYSA-N tert-butyl piperazine-1-carboxylate Chemical compound CC(C)(C)OC(=O)N1CCNCC1 CWXPZXBSDSIRCS-UHFFFAOYSA-N 0.000 description 6
- HBAQYPYDRFILMT-UHFFFAOYSA-N 8-[3-(1-cyclopropylpyrazol-4-yl)-1H-pyrazolo[4,3-d]pyrimidin-5-yl]-3-methyl-3,8-diazabicyclo[3.2.1]octan-2-one Chemical class C1(CC1)N1N=CC(=C1)C1=NNC2=C1N=C(N=C2)N1C2C(N(CC1CC2)C)=O HBAQYPYDRFILMT-UHFFFAOYSA-N 0.000 description 5
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 5
- 208000026310 Breast neoplasm Diseases 0.000 description 5
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 5
- 206010025323 Lymphomas Diseases 0.000 description 5
- FXHOOIRPVKKKFG-UHFFFAOYSA-N N,N-Dimethylacetamide Chemical compound CN(C)C(C)=O FXHOOIRPVKKKFG-UHFFFAOYSA-N 0.000 description 5
- 208000008589 Obesity Diseases 0.000 description 5
- 206010061535 Ovarian neoplasm Diseases 0.000 description 5
- 208000000236 Prostatic Neoplasms Diseases 0.000 description 5
- 229930006000 Sucrose Natural products 0.000 description 5
- DPXJVFZANSGRMM-UHFFFAOYSA-N acetic acid;2,3,4,5,6-pentahydroxyhexanal;sodium Chemical compound [Na].CC(O)=O.OCC(O)C(O)C(O)C(O)C=O DPXJVFZANSGRMM-UHFFFAOYSA-N 0.000 description 5
- 229940034982 antineoplastic agent Drugs 0.000 description 5
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 5
- 239000000460 chlorine Substances 0.000 description 5
- 229940113088 dimethylacetamide Drugs 0.000 description 5
- 229940079593 drug Drugs 0.000 description 5
- 229960001484 edetic acid Drugs 0.000 description 5
- 239000000839 emulsion Substances 0.000 description 5
- UREBWPXBXRYXRJ-UHFFFAOYSA-N ethyl acetate;methanol Chemical compound OC.CCOC(C)=O UREBWPXBXRYXRJ-UHFFFAOYSA-N 0.000 description 5
- 239000000706 filtrate Substances 0.000 description 5
- 235000011187 glycerol Nutrition 0.000 description 5
- 229910052739 hydrogen Inorganic materials 0.000 description 5
- 239000001257 hydrogen Substances 0.000 description 5
- 208000027866 inflammatory disease Diseases 0.000 description 5
- 208000032839 leukemia Diseases 0.000 description 5
- 239000007788 liquid Substances 0.000 description 5
- 229910052943 magnesium sulfate Inorganic materials 0.000 description 5
- 235000019341 magnesium sulphate Nutrition 0.000 description 5
- 229920000609 methyl cellulose Polymers 0.000 description 5
- 235000010981 methylcellulose Nutrition 0.000 description 5
- 239000001923 methylcellulose Substances 0.000 description 5
- 229960002900 methylcellulose Drugs 0.000 description 5
- 235000020824 obesity Nutrition 0.000 description 5
- 239000002244 precipitate Substances 0.000 description 5
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 5
- 229910000104 sodium hydride Inorganic materials 0.000 description 5
- 239000005720 sucrose Substances 0.000 description 5
- 238000003786 synthesis reaction Methods 0.000 description 5
- 239000003981 vehicle Substances 0.000 description 5
- KZPYGQFFRCFCPP-UHFFFAOYSA-N 1,1'-bis(diphenylphosphino)ferrocene Chemical compound [Fe+2].C1=CC=C[C-]1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=C[C-]1P(C=1C=CC=CC=1)C1=CC=CC=C1 KZPYGQFFRCFCPP-UHFFFAOYSA-N 0.000 description 4
- PEDSSYSZXFKUEG-UHFFFAOYSA-N 1-hydroxycyclopropane-1-carbaldehyde Chemical compound O=CC1(O)CC1 PEDSSYSZXFKUEG-UHFFFAOYSA-N 0.000 description 4
- SVTBMSDMJJWYQN-UHFFFAOYSA-N 2-methylpentane-2,4-diol Chemical compound CC(O)CC(C)(C)O SVTBMSDMJJWYQN-UHFFFAOYSA-N 0.000 description 4
- PCFIABOQFAFDAU-UHFFFAOYSA-N 4-bromo-2-fluorobenzoyl chloride Chemical compound FC1=CC(Br)=CC=C1C(Cl)=O PCFIABOQFAFDAU-UHFFFAOYSA-N 0.000 description 4
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 4
- 206010009944 Colon cancer Diseases 0.000 description 4
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 4
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 4
- 235000010643 Leucaena leucocephala Nutrition 0.000 description 4
- 240000007472 Leucaena leucocephala Species 0.000 description 4
- 206010027476 Metastases Diseases 0.000 description 4
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 4
- 229920000168 Microcrystalline cellulose Polymers 0.000 description 4
- 229920000881 Modified starch Polymers 0.000 description 4
- 239000007832 Na2SO4 Substances 0.000 description 4
- 229920002675 Polyoxyl Polymers 0.000 description 4
- KEAYESYHFKHZAL-UHFFFAOYSA-N Sodium Chemical compound [Na] KEAYESYHFKHZAL-UHFFFAOYSA-N 0.000 description 4
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 4
- 206010046798 Uterine leiomyoma Diseases 0.000 description 4
- 208000036142 Viral infection Diseases 0.000 description 4
- 241000700605 Viruses Species 0.000 description 4
- CLZISMQKJZCZDN-UHFFFAOYSA-N [benzotriazol-1-yloxy(dimethylamino)methylidene]-dimethylazanium Chemical compound C1=CC=C2N(OC(N(C)C)=[N+](C)C)N=NC2=C1 CLZISMQKJZCZDN-UHFFFAOYSA-N 0.000 description 4
- 229960000583 acetic acid Drugs 0.000 description 4
- 125000003710 aryl alkyl group Chemical group 0.000 description 4
- HUMNYLRZRPPJDN-UHFFFAOYSA-N benzaldehyde Chemical compound O=CC1=CC=CC=C1 HUMNYLRZRPPJDN-UHFFFAOYSA-N 0.000 description 4
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 4
- 235000010290 biphenyl Nutrition 0.000 description 4
- FJDQFPXHSGXQBY-UHFFFAOYSA-L caesium carbonate Chemical compound [Cs+].[Cs+].[O-]C([O-])=O FJDQFPXHSGXQBY-UHFFFAOYSA-L 0.000 description 4
- OSGAYBCDTDRGGQ-UHFFFAOYSA-L calcium sulfate Chemical compound [Ca+2].[O-]S([O-])(=O)=O OSGAYBCDTDRGGQ-UHFFFAOYSA-L 0.000 description 4
- 125000004432 carbon atom Chemical group C* 0.000 description 4
- 150000003857 carboxamides Chemical class 0.000 description 4
- 239000001768 carboxy methyl cellulose Substances 0.000 description 4
- 239000004359 castor oil Substances 0.000 description 4
- 235000019438 castor oil Nutrition 0.000 description 4
- 208000029742 colonic neoplasm Diseases 0.000 description 4
- 238000011161 development Methods 0.000 description 4
- 230000018109 developmental process Effects 0.000 description 4
- 239000008121 dextrose Substances 0.000 description 4
- 239000002552 dosage form Substances 0.000 description 4
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 4
- ZEMPKEQAKRGZGQ-XOQCFJPHSA-N glycerol triricinoleate Natural products CCCCCC[C@@H](O)CC=CCCCCCCCC(=O)OC[C@@H](COC(=O)CCCCCCCC=CC[C@@H](O)CCCCCC)OC(=O)CCCCCCCC=CC[C@H](O)CCCCCC ZEMPKEQAKRGZGQ-XOQCFJPHSA-N 0.000 description 4
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 4
- 208000015181 infectious disease Diseases 0.000 description 4
- 229910052740 iodine Inorganic materials 0.000 description 4
- 150000002500 ions Chemical class 0.000 description 4
- 201000010260 leiomyoma Diseases 0.000 description 4
- 239000000314 lubricant Substances 0.000 description 4
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 4
- 238000004519 manufacturing process Methods 0.000 description 4
- 229940016286 microcrystalline cellulose Drugs 0.000 description 4
- 239000008108 microcrystalline cellulose Substances 0.000 description 4
- 235000019813 microcrystalline cellulose Nutrition 0.000 description 4
- 239000012299 nitrogen atmosphere Substances 0.000 description 4
- 229910052700 potassium Inorganic materials 0.000 description 4
- 239000011591 potassium Substances 0.000 description 4
- 229960003975 potassium Drugs 0.000 description 4
- 239000000843 powder Substances 0.000 description 4
- 210000002307 prostate Anatomy 0.000 description 4
- 238000011160 research Methods 0.000 description 4
- 238000010898 silica gel chromatography Methods 0.000 description 4
- 239000012312 sodium hydride Substances 0.000 description 4
- 239000000600 sorbitol Substances 0.000 description 4
- 235000010356 sorbitol Nutrition 0.000 description 4
- 230000000087 stabilizing effect Effects 0.000 description 4
- 239000006188 syrup Substances 0.000 description 4
- 235000020357 syrup Nutrition 0.000 description 4
- RTUUXAWYQSXLDU-UHFFFAOYSA-N tert-butyl 4-(4-bromo-2-fluorobenzoyl)piperazine-1-carboxylate Chemical compound C1CN(C(=O)OC(C)(C)C)CCN1C(=O)C1=CC=C(Br)C=C1F RTUUXAWYQSXLDU-UHFFFAOYSA-N 0.000 description 4
- 230000001225 therapeutic effect Effects 0.000 description 4
- MGSRCZKZVOBKFT-UHFFFAOYSA-N thymol Chemical compound CC(C)C1=CC=C(C)C=C1O MGSRCZKZVOBKFT-UHFFFAOYSA-N 0.000 description 4
- 201000007954 uterine fibroid Diseases 0.000 description 4
- 230000009385 viral infection Effects 0.000 description 4
- CYPYTURSJDMMMP-WVCUSYJESA-N (1e,4e)-1,5-diphenylpenta-1,4-dien-3-one;palladium Chemical compound [Pd].[Pd].C=1C=CC=CC=1\C=C\C(=O)\C=C\C1=CC=CC=C1.C=1C=CC=CC=1\C=C\C(=O)\C=C\C1=CC=CC=C1.C=1C=CC=CC=1\C=C\C(=O)\C=C\C1=CC=CC=C1 CYPYTURSJDMMMP-WVCUSYJESA-N 0.000 description 3
- COXHQSVTIYCSTC-UHFFFAOYSA-N (2-chloro-4-quinolin-6-ylphenyl)-[4-(1-hydroxycyclopropanecarbonyl)piperazin-1-yl]methanone Chemical compound C1CN(C(=O)C=2C(=CC(=CC=2)C=2C=C3C=CC=NC3=CC=2)Cl)CCN1C(=O)C1(O)CC1 COXHQSVTIYCSTC-UHFFFAOYSA-N 0.000 description 3
- KSCFPEMJWULSBW-UHFFFAOYSA-N (4-bromophenyl)-[4-(1-hydroxycyclopropanecarbonyl)piperazin-1-yl]methanone Chemical compound OC1(CC1)C(=O)N1CCN(CC1)C(=O)c1ccc(Br)cc1 KSCFPEMJWULSBW-UHFFFAOYSA-N 0.000 description 3
- DFCOFKUPHDITMO-UHFFFAOYSA-N (4-bromophenyl)-piperazin-1-ylmethanone 2,2,2-trifluoroacetic acid Chemical compound FC(C(=O)O)(F)F.BrC1=CC=C(C=C1)C(=O)N1CCNCC1 DFCOFKUPHDITMO-UHFFFAOYSA-N 0.000 description 3
- NUEZYYBQCMBQOY-UHFFFAOYSA-N 4-(1,3-benzoxazol-2-yl)benzoic acid Chemical compound C1=CC(C(=O)O)=CC=C1C1=NC2=CC=CC=C2O1 NUEZYYBQCMBQOY-UHFFFAOYSA-N 0.000 description 3
- OSWFIVFLDKOXQC-UHFFFAOYSA-N 4-(3-methoxyphenyl)aniline Chemical compound COC1=CC=CC(C=2C=CC(N)=CC=2)=C1 OSWFIVFLDKOXQC-UHFFFAOYSA-N 0.000 description 3
- KMJMDIYGNFGEEO-UHFFFAOYSA-N 5-bromo-1-methylbenzimidazole Chemical compound BrC1=CC=C2N(C)C=NC2=C1 KMJMDIYGNFGEEO-UHFFFAOYSA-N 0.000 description 3
- 201000001320 Atherosclerosis Diseases 0.000 description 3
- 206010005003 Bladder cancer Diseases 0.000 description 3
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 3
- 208000001333 Colorectal Neoplasms Diseases 0.000 description 3
- 241000709675 Coxsackievirus B3 Species 0.000 description 3
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 3
- 239000004375 Dextrin Substances 0.000 description 3
- 229920001353 Dextrin Polymers 0.000 description 3
- 102000004190 Enzymes Human genes 0.000 description 3
- 108090000790 Enzymes Proteins 0.000 description 3
- 102000003951 Erythropoietin Human genes 0.000 description 3
- 108090000394 Erythropoietin Proteins 0.000 description 3
- 108010029961 Filgrastim Proteins 0.000 description 3
- 102100039619 Granulocyte colony-stimulating factor Human genes 0.000 description 3
- 239000007821 HATU Substances 0.000 description 3
- 208000017604 Hodgkin disease Diseases 0.000 description 3
- 208000010747 Hodgkins lymphoma Diseases 0.000 description 3
- 241000282412 Homo Species 0.000 description 3
- 101000610640 Homo sapiens U4/U6 small nuclear ribonucleoprotein Prp3 Proteins 0.000 description 3
- 241000701024 Human betaherpesvirus 5 Species 0.000 description 3
- 241000725303 Human immunodeficiency virus Species 0.000 description 3
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 3
- 229930195725 Mannitol Natural products 0.000 description 3
- BZLVMXJERCGZMT-UHFFFAOYSA-N Methyl tert-butyl ether Chemical compound COC(C)(C)C BZLVMXJERCGZMT-UHFFFAOYSA-N 0.000 description 3
- NWIBSHFKIJFRCO-WUDYKRTCSA-N Mytomycin Chemical compound C1N2C(C(C(C)=C(N)C3=O)=O)=C3[C@@H](COC(N)=O)[C@@]2(OC)[C@@H]2[C@H]1N2 NWIBSHFKIJFRCO-WUDYKRTCSA-N 0.000 description 3
- HSHXDCVZWHOWCS-UHFFFAOYSA-N N'-hexadecylthiophene-2-carbohydrazide Chemical compound CCCCCCCCCCCCCCCCNNC(=O)c1cccs1 HSHXDCVZWHOWCS-UHFFFAOYSA-N 0.000 description 3
- 208000001132 Osteoporosis Diseases 0.000 description 3
- 206010033128 Ovarian cancer Diseases 0.000 description 3
- YNPNZTXNASCQKK-UHFFFAOYSA-N Phenanthrene Natural products C1=CC=C2C3=CC=CC=C3C=CC2=C1 YNPNZTXNASCQKK-UHFFFAOYSA-N 0.000 description 3
- 229920000776 Poly(Adenosine diphosphate-ribose) polymerase Polymers 0.000 description 3
- 239000004698 Polyethylene Substances 0.000 description 3
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 3
- KWYUFKZDYYNOTN-UHFFFAOYSA-M Potassium hydroxide Chemical compound [OH-].[K+] KWYUFKZDYYNOTN-UHFFFAOYSA-M 0.000 description 3
- 101001110823 Saccharomyces cerevisiae (strain ATCC 204508 / S288c) 60S ribosomal protein L6-A Proteins 0.000 description 3
- 101000712176 Saccharomyces cerevisiae (strain ATCC 204508 / S288c) 60S ribosomal protein L6-B Proteins 0.000 description 3
- 102100040374 U4/U6 small nuclear ribonucleoprotein Prp3 Human genes 0.000 description 3
- 208000007097 Urinary Bladder Neoplasms Diseases 0.000 description 3
- DGEZNRSVGBDHLK-UHFFFAOYSA-N [1,10]phenanthroline Chemical compound C1=CN=C2C3=NC=CC=C3C=CC2=C1 DGEZNRSVGBDHLK-UHFFFAOYSA-N 0.000 description 3
- WLLZHCWLKVJBHC-UHFFFAOYSA-N [4-(1,3-benzothiazol-2-yl)phenyl]-piperazin-1-ylmethanone 2,2,2-trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F.O=C(N1CCNCC1)c1ccc(cc1)-c1nc2ccccc2s1 WLLZHCWLKVJBHC-UHFFFAOYSA-N 0.000 description 3
- ZVBLIYQVHBADLA-UHFFFAOYSA-N [4-(1,3-benzoxazol-2-yl)phenyl]-piperazin-1-ylmethanone 2,2,2-trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F.O=C(N1CCNCC1)c1ccc(cc1)-c1nc2ccccc2o1 ZVBLIYQVHBADLA-UHFFFAOYSA-N 0.000 description 3
- FCMVIRJKVFFUQL-UHFFFAOYSA-N [4-(1H-benzimidazol-2-yl)phenyl]-piperazin-1-ylmethanone 2,2,2-trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F.O=C(N1CCNCC1)c1ccc(cc1)-c1nc2ccccc2[nH]1 FCMVIRJKVFFUQL-UHFFFAOYSA-N 0.000 description 3
- SXJIHPAASDDDMB-UHFFFAOYSA-N [4-(4-chloro-2-fluorophenyl)phenyl]-piperazin-1-ylmethanone 2,2,2-trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F.Fc1cc(Cl)ccc1-c1ccc(cc1)C(=O)N1CCNCC1 SXJIHPAASDDDMB-UHFFFAOYSA-N 0.000 description 3
- 235000010443 alginic acid Nutrition 0.000 description 3
- 229920000615 alginic acid Polymers 0.000 description 3
- 239000000783 alginic acid Substances 0.000 description 3
- 229960001126 alginic acid Drugs 0.000 description 3
- 150000004781 alginic acids Chemical class 0.000 description 3
- 150000001447 alkali salts Chemical class 0.000 description 3
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 3
- 150000001412 amines Chemical class 0.000 description 3
- 239000000440 bentonite Substances 0.000 description 3
- 229910000278 bentonite Inorganic materials 0.000 description 3
- SVPXDRXYRYOSEX-UHFFFAOYSA-N bentoquatam Chemical compound O.O=[Si]=O.O=[Al]O[Al]=O SVPXDRXYRYOSEX-UHFFFAOYSA-N 0.000 description 3
- 229960000686 benzalkonium chloride Drugs 0.000 description 3
- 125000005605 benzo group Chemical group 0.000 description 3
- CADWTSSKOVRVJC-UHFFFAOYSA-N benzyl(dimethyl)azanium;chloride Chemical compound [Cl-].C[NH+](C)CC1=CC=CC=C1 CADWTSSKOVRVJC-UHFFFAOYSA-N 0.000 description 3
- 229910052791 calcium Inorganic materials 0.000 description 3
- 239000011575 calcium Substances 0.000 description 3
- 229960005069 calcium Drugs 0.000 description 3
- 229910002092 carbon dioxide Inorganic materials 0.000 description 3
- 230000010261 cell growth Effects 0.000 description 3
- 239000003153 chemical reaction reagent Substances 0.000 description 3
- 230000007423 decrease Effects 0.000 description 3
- 235000019425 dextrin Nutrition 0.000 description 3
- 235000014113 dietary fatty acids Nutrition 0.000 description 3
- 229940088598 enzyme Drugs 0.000 description 3
- 229940105423 erythropoietin Drugs 0.000 description 3
- 229930195729 fatty acid Natural products 0.000 description 3
- 239000000194 fatty acid Substances 0.000 description 3
- 150000004665 fatty acids Chemical class 0.000 description 3
- 229960004177 filgrastim Drugs 0.000 description 3
- 235000019253 formic acid Nutrition 0.000 description 3
- 235000010979 hydroxypropyl methyl cellulose Nutrition 0.000 description 3
- 229920003088 hydroxypropyl methyl cellulose Polymers 0.000 description 3
- 239000001866 hydroxypropyl methyl cellulose Substances 0.000 description 3
- RAXXELZNTBOGNW-UHFFFAOYSA-N imidazole Natural products C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 description 3
- 239000000594 mannitol Substances 0.000 description 3
- 235000010355 mannitol Nutrition 0.000 description 3
- 239000003550 marker Substances 0.000 description 3
- 230000009401 metastasis Effects 0.000 description 3
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 3
- 239000002480 mineral oil Substances 0.000 description 3
- 235000010446 mineral oil Nutrition 0.000 description 3
- GLDOVTGHNKAZLK-UHFFFAOYSA-N n-octadecyl alcohol Natural products CCCCCCCCCCCCCCCCCCO GLDOVTGHNKAZLK-UHFFFAOYSA-N 0.000 description 3
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 3
- 235000011007 phosphoric acid Nutrition 0.000 description 3
- 125000003367 polycyclic group Chemical group 0.000 description 3
- 238000010837 poor prognosis Methods 0.000 description 3
- 229910000160 potassium phosphate Inorganic materials 0.000 description 3
- 229940093916 potassium phosphate Drugs 0.000 description 3
- 235000011009 potassium phosphates Nutrition 0.000 description 3
- OXCMYAYHXIHQOA-UHFFFAOYSA-N potassium;[2-butyl-5-chloro-3-[[4-[2-(1,2,4-triaza-3-azanidacyclopenta-1,4-dien-5-yl)phenyl]phenyl]methyl]imidazol-4-yl]methanol Chemical compound [K+].CCCCC1=NC(Cl)=C(CO)N1CC1=CC=C(C=2C(=CC=CC=2)C2=N[N-]N=N2)C=C1 OXCMYAYHXIHQOA-UHFFFAOYSA-N 0.000 description 3
- 229940002612 prodrug Drugs 0.000 description 3
- 239000000651 prodrug Substances 0.000 description 3
- 235000013772 propylene glycol Nutrition 0.000 description 3
- 238000001959 radiotherapy Methods 0.000 description 3
- 230000002829 reductive effect Effects 0.000 description 3
- 238000002271 resection Methods 0.000 description 3
- 229910052701 rubidium Inorganic materials 0.000 description 3
- 239000000377 silicon dioxide Substances 0.000 description 3
- 235000019812 sodium carboxymethyl cellulose Nutrition 0.000 description 3
- 229920001027 sodium carboxymethylcellulose Polymers 0.000 description 3
- 239000000454 talc Substances 0.000 description 3
- 229910052623 talc Inorganic materials 0.000 description 3
- 235000012222 talc Nutrition 0.000 description 3
- VFZHROUXLCKFCW-UHFFFAOYSA-N tert-butyl 4-[4-(1,3-benzothiazol-2-yl)benzoyl]piperazine-1-carboxylate Chemical compound CC(C)(C)OC(=O)N1CCN(CC1)C(=O)c1ccc(cc1)-c1nc2ccccc2s1 VFZHROUXLCKFCW-UHFFFAOYSA-N 0.000 description 3
- QVTTWCJFQNZKJQ-UHFFFAOYSA-N tert-butyl 4-[4-(1,3-benzoxazol-2-yl)benzoyl]piperazine-1-carboxylate Chemical compound CC(C)(C)OC(=O)N1CCN(CC1)C(=O)c1ccc(cc1)-c1nc2ccccc2o1 QVTTWCJFQNZKJQ-UHFFFAOYSA-N 0.000 description 3
- XCVMWKWLDDZBMV-UHFFFAOYSA-N tert-butyl 4-[4-(1H-benzimidazol-2-yl)benzoyl]piperazine-1-carboxylate Chemical compound CC(C)(C)OC(=O)N1CCN(CC1)C(=O)c1ccc(cc1)-c1nc2ccccc2[nH]1 XCVMWKWLDDZBMV-UHFFFAOYSA-N 0.000 description 3
- 125000005931 tert-butyloxycarbonyl group Chemical group [H]C([H])([H])C(OC(*)=O)(C([H])([H])[H])C([H])([H])[H] 0.000 description 3
- 229940098465 tincture Drugs 0.000 description 3
- 201000005112 urinary bladder cancer Diseases 0.000 description 3
- UGOMMVLRQDMAQQ-UHFFFAOYSA-N xphos Chemical compound CC(C)C1=CC(C(C)C)=CC(C(C)C)=C1C1=CC=CC=C1P(C1CCCCC1)C1CCCCC1 UGOMMVLRQDMAQQ-UHFFFAOYSA-N 0.000 description 3
- JNYAEWCLZODPBN-JGWLITMVSA-N (2r,3r,4s)-2-[(1r)-1,2-dihydroxyethyl]oxolane-3,4-diol Chemical compound OC[C@@H](O)[C@H]1OC[C@H](O)[C@H]1O JNYAEWCLZODPBN-JGWLITMVSA-N 0.000 description 2
- FELGMEQIXOGIFQ-CYBMUJFWSA-N (3r)-9-methyl-3-[(2-methylimidazol-1-yl)methyl]-2,3-dihydro-1h-carbazol-4-one Chemical compound CC1=NC=CN1C[C@@H]1C(=O)C(C=2C(=CC=CC=2)N2C)=C2CC1 FELGMEQIXOGIFQ-CYBMUJFWSA-N 0.000 description 2
- YBNDRTRLXPEWKQ-UHFFFAOYSA-N (4-chloro-2-fluorophenyl)boronic acid Chemical compound OB(O)C1=CC=C(Cl)C=C1F YBNDRTRLXPEWKQ-UHFFFAOYSA-N 0.000 description 2
- ZORQXIQZAOLNGE-UHFFFAOYSA-N 1,1-difluorocyclohexane Chemical compound FC1(F)CCCCC1 ZORQXIQZAOLNGE-UHFFFAOYSA-N 0.000 description 2
- LBUJPTNKIBCYBY-UHFFFAOYSA-N 1,2,3,4-tetrahydroquinoline Chemical compound C1=CC=C2CCCNC2=C1 LBUJPTNKIBCYBY-UHFFFAOYSA-N 0.000 description 2
- REXMVNUOCKTNQJ-UHFFFAOYSA-N 1-(4-bromophenyl)-3-methylindazole Chemical compound Cc1nn(-c2ccc(Br)cc2)c2ccccc12 REXMVNUOCKTNQJ-UHFFFAOYSA-N 0.000 description 2
- MSSDTZLYNMFTKN-UHFFFAOYSA-N 1-Piperazinecarboxaldehyde Chemical compound O=CN1CCNCC1 MSSDTZLYNMFTKN-UHFFFAOYSA-N 0.000 description 2
- PJUPKRYGDFTMTM-UHFFFAOYSA-N 1-hydroxybenzotriazole;hydrate Chemical compound O.C1=CC=C2N(O)N=NC2=C1 PJUPKRYGDFTMTM-UHFFFAOYSA-N 0.000 description 2
- VBICKXHEKHSIBG-UHFFFAOYSA-N 1-monostearoylglycerol Chemical compound CCCCCCCCCCCCCCCCCC(=O)OCC(O)CO VBICKXHEKHSIBG-UHFFFAOYSA-N 0.000 description 2
- WXTMDXOMEHJXQO-UHFFFAOYSA-N 2,5-dihydroxybenzoic acid Chemical compound OC(=O)C1=CC(O)=CC=C1O WXTMDXOMEHJXQO-UHFFFAOYSA-N 0.000 description 2
- CDAWCLOXVUBKRW-UHFFFAOYSA-N 2-aminophenol Chemical compound NC1=CC=CC=C1O CDAWCLOXVUBKRW-UHFFFAOYSA-N 0.000 description 2
- SABSNTHFVVOJMX-UHFFFAOYSA-N 2-chloro-6-fluoro-1,3-benzoxazole Chemical compound FC1=CC=C2N=C(Cl)OC2=C1 SABSNTHFVVOJMX-UHFFFAOYSA-N 0.000 description 2
- BHNHHSOHWZKFOX-UHFFFAOYSA-N 2-methyl-1H-indole Chemical compound C1=CC=C2NC(C)=CC2=C1 BHNHHSOHWZKFOX-UHFFFAOYSA-N 0.000 description 2
- QUVFHVHLCFFINS-UHFFFAOYSA-N 4-(3-aminophenyl)benzoic acid Chemical compound NC1=CC=CC(C=2C=CC(=CC=2)C(O)=O)=C1 QUVFHVHLCFFINS-UHFFFAOYSA-N 0.000 description 2
- IYDKBQIEOBXLTP-UHFFFAOYSA-N 4-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)benzoic acid Chemical compound O1C(C)(C)C(C)(C)OB1C1=CC=C(C(O)=O)C=C1 IYDKBQIEOBXLTP-UHFFFAOYSA-N 0.000 description 2
- WSXXRFWCQRUXTM-UHFFFAOYSA-N 4-(5-cyano-1,3-benzoxazol-2-yl)benzoic acid Chemical compound OC(=O)c1ccc(cc1)-c1nc2cc(ccc2o1)C#N WSXXRFWCQRUXTM-UHFFFAOYSA-N 0.000 description 2
- VHYFNPMBLIVWCW-UHFFFAOYSA-N 4-Dimethylaminopyridine Chemical compound CN(C)C1=CC=NC=C1 VHYFNPMBLIVWCW-UHFFFAOYSA-N 0.000 description 2
- ZQQSRVPOAHYHEL-UHFFFAOYSA-N 4-bromo-2-fluorobenzoic acid Chemical compound OC(=O)C1=CC=C(Br)C=C1F ZQQSRVPOAHYHEL-UHFFFAOYSA-N 0.000 description 2
- 125000004800 4-bromophenyl group Chemical group [H]C1=C([H])C(*)=C([H])C([H])=C1Br 0.000 description 2
- CFKMVGJGLGKFKI-UHFFFAOYSA-N 4-chloro-m-cresol Chemical compound CC1=CC(O)=CC=C1Cl CFKMVGJGLGKFKI-UHFFFAOYSA-N 0.000 description 2
- IVWYPLDIVWVRQE-UHFFFAOYSA-N 5-[4-[4-(1-hydroxycyclopropanecarbonyl)piperazine-1-carbonyl]phenyl]-1H-indole-3-carbonitrile Chemical compound OC1(CC1)C(=O)N1CCN(CC1)C(=O)c1ccc(cc1)-c1ccc2[nH]cc(C#N)c2c1 IVWYPLDIVWVRQE-UHFFFAOYSA-N 0.000 description 2
- IOUHBHPKJTUJKS-UHFFFAOYSA-N 6-bromo-3-methyl-1,2-dihydrobenzotriazole Chemical compound BrC1=CC2=C(N(NN2)C)C=C1 IOUHBHPKJTUJKS-UHFFFAOYSA-N 0.000 description 2
- 244000215068 Acacia senegal Species 0.000 description 2
- 208000024893 Acute lymphoblastic leukemia Diseases 0.000 description 2
- 208000014697 Acute lymphocytic leukaemia Diseases 0.000 description 2
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 2
- 239000005711 Benzoic acid Substances 0.000 description 2
- QFOHBWFCKVYLES-UHFFFAOYSA-N Butylparaben Chemical compound CCCCOC(=O)C1=CC=C(O)C=C1 QFOHBWFCKVYLES-UHFFFAOYSA-N 0.000 description 2
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 2
- 208000005623 Carcinogenesis Diseases 0.000 description 2
- 206010008342 Cervix carcinoma Diseases 0.000 description 2
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 2
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 2
- 239000001692 EU approved anti-caking agent Substances 0.000 description 2
- 239000001856 Ethyl cellulose Substances 0.000 description 2
- ZZSNKZQZMQGXPY-UHFFFAOYSA-N Ethyl cellulose Chemical compound CCOCC1OC(OC)C(OCC)C(OCC)C1OC1C(O)C(O)C(OC)C(CO)O1 ZZSNKZQZMQGXPY-UHFFFAOYSA-N 0.000 description 2
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 2
- 101150003888 FASN gene Proteins 0.000 description 2
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 description 2
- 239000005715 Fructose Substances 0.000 description 2
- 229930091371 Fructose Natural products 0.000 description 2
- RFSUNEUAIZKAJO-ARQDHWQXSA-N Fructose Chemical compound OC[C@H]1O[C@](O)(CO)[C@@H](O)[C@@H]1O RFSUNEUAIZKAJO-ARQDHWQXSA-N 0.000 description 2
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 2
- 229920002907 Guar gum Polymers 0.000 description 2
- 229920000084 Gum arabic Polymers 0.000 description 2
- 241000701044 Human gammaherpesvirus 4 Species 0.000 description 2
- 229920002153 Hydroxypropyl cellulose Polymers 0.000 description 2
- 208000022559 Inflammatory bowel disease Diseases 0.000 description 2
- 241000712431 Influenza A virus Species 0.000 description 2
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 2
- GQYIWUVLTXOXAJ-UHFFFAOYSA-N Lomustine Chemical compound ClCCN(N=O)C(=O)NC1CCCCC1 GQYIWUVLTXOXAJ-UHFFFAOYSA-N 0.000 description 2
- 206010058467 Lung neoplasm malignant Diseases 0.000 description 2
- 244000246386 Mentha pulegium Species 0.000 description 2
- 235000016257 Mentha pulegium Nutrition 0.000 description 2
- 235000004357 Mentha x piperita Nutrition 0.000 description 2
- 208000001145 Metabolic Syndrome Diseases 0.000 description 2
- NTIZESTWPVYFNL-UHFFFAOYSA-N Methyl isobutyl ketone Chemical compound CC(C)CC(C)=O NTIZESTWPVYFNL-UHFFFAOYSA-N 0.000 description 2
- UIHCLUNTQKBZGK-UHFFFAOYSA-N Methyl isobutyl ketone Natural products CCC(C)C(C)=O UIHCLUNTQKBZGK-UHFFFAOYSA-N 0.000 description 2
- LRHPLDYGYMQRHN-UHFFFAOYSA-N N-Butanol Chemical compound CCCCO LRHPLDYGYMQRHN-UHFFFAOYSA-N 0.000 description 2
- WHNWPMSKXPGLAX-UHFFFAOYSA-N N-Vinyl-2-pyrrolidone Chemical compound C=CN1CCCC1=O WHNWPMSKXPGLAX-UHFFFAOYSA-N 0.000 description 2
- XJLXINKUBYWONI-NNYOXOHSSA-N NADP zwitterion Chemical compound NC(=O)C1=CC=C[N+]([C@H]2[C@@H]([C@H](O)[C@@H](COP([O-])(=O)OP(O)(=O)OC[C@@H]3[C@H]([C@@H](OP(O)(O)=O)[C@@H](O3)N3C4=NC=NC(N)=C4N=C3)O)O2)O)=C1 XJLXINKUBYWONI-NNYOXOHSSA-N 0.000 description 2
- 206010028813 Nausea Diseases 0.000 description 2
- 235000019502 Orange oil Nutrition 0.000 description 2
- 206010033307 Overweight Diseases 0.000 description 2
- 206010061902 Pancreatic neoplasm Diseases 0.000 description 2
- 235000019483 Peanut oil Nutrition 0.000 description 2
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N Phenol Chemical compound OC1=CC=CC=C1 ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 description 2
- 241000709664 Picornaviridae Species 0.000 description 2
- 206010035226 Plasma cell myeloma Diseases 0.000 description 2
- RVGRUAULSDPKGF-UHFFFAOYSA-N Poloxamer Chemical compound C1CO1.CC1CO1 RVGRUAULSDPKGF-UHFFFAOYSA-N 0.000 description 2
- 229920003171 Poly (ethylene oxide) Polymers 0.000 description 2
- 102000012338 Poly(ADP-ribose) Polymerases Human genes 0.000 description 2
- 108010061844 Poly(ADP-ribose) Polymerases Proteins 0.000 description 2
- 229920001213 Polysorbate 20 Polymers 0.000 description 2
- 229920001219 Polysorbate 40 Polymers 0.000 description 2
- 229920001214 Polysorbate 60 Polymers 0.000 description 2
- WCUXLLCKKVVCTQ-UHFFFAOYSA-M Potassium chloride Chemical compound [Cl-].[K+] WCUXLLCKKVVCTQ-UHFFFAOYSA-M 0.000 description 2
- 208000006664 Precursor Cell Lymphoblastic Leukemia-Lymphoma Diseases 0.000 description 2
- ATUOYWHBWRKTHZ-UHFFFAOYSA-N Propane Chemical compound CCC ATUOYWHBWRKTHZ-UHFFFAOYSA-N 0.000 description 2
- ZTHYODDOHIVTJV-UHFFFAOYSA-N Propyl gallate Chemical compound CCCOC(=O)C1=CC(O)=C(O)C(O)=C1 ZTHYODDOHIVTJV-UHFFFAOYSA-N 0.000 description 2
- 206010060862 Prostate cancer Diseases 0.000 description 2
- 208000000453 Skin Neoplasms Diseases 0.000 description 2
- DBMJMQXJHONAFJ-UHFFFAOYSA-M Sodium laurylsulphate Chemical compound [Na+].CCCCCCCCCCCCOS([O-])(=O)=O DBMJMQXJHONAFJ-UHFFFAOYSA-M 0.000 description 2
- IYFATESGLOUGBX-YVNJGZBMSA-N Sorbitan monopalmitate Chemical compound CCCCCCCCCCCCCCCC(=O)OC[C@@H](O)[C@H]1OC[C@H](O)[C@H]1O IYFATESGLOUGBX-YVNJGZBMSA-N 0.000 description 2
- 229920002472 Starch Polymers 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- RAHZWNYVWXNFOC-UHFFFAOYSA-N Sulphur dioxide Chemical compound O=S=O RAHZWNYVWXNFOC-UHFFFAOYSA-N 0.000 description 2
- 239000005844 Thymol Substances 0.000 description 2
- GWEVSGVZZGPLCZ-UHFFFAOYSA-N Titan oxide Chemical compound O=[Ti]=O GWEVSGVZZGPLCZ-UHFFFAOYSA-N 0.000 description 2
- GSEJCLTVZPLZKY-UHFFFAOYSA-N Triethanolamine Chemical compound OCCN(CCO)CCO GSEJCLTVZPLZKY-UHFFFAOYSA-N 0.000 description 2
- 208000006105 Uterine Cervical Neoplasms Diseases 0.000 description 2
- 208000002495 Uterine Neoplasms Diseases 0.000 description 2
- 235000009499 Vanilla fragrans Nutrition 0.000 description 2
- 244000263375 Vanilla tahitensis Species 0.000 description 2
- 235000012036 Vanilla tahitensis Nutrition 0.000 description 2
- GZXGSJMCBPIIPX-UHFFFAOYSA-N [3-chloro-4-(1-propan-2-ylindol-5-yl)phenyl]-[4-(1-hydroxycyclopropanecarbonyl)piperazin-1-yl]methanone Chemical compound CC(C)n1ccc2cc(ccc12)-c1ccc(cc1Cl)C(=O)N1CCN(CC1)C(=O)C1(O)CC1 GZXGSJMCBPIIPX-UHFFFAOYSA-N 0.000 description 2
- AGQYWZDFTLTSPF-UHFFFAOYSA-N [4-(1,3-benzothiazol-2-yl)phenyl]-[4-(1-hydroxycyclopropanecarbonyl)piperazin-1-yl]methanone Chemical compound OC1(CC1)C(=O)N1CCN(CC1)C(=O)c1ccc(cc1)-c1nc2ccccc2s1 AGQYWZDFTLTSPF-UHFFFAOYSA-N 0.000 description 2
- FGXGECPNCZCUAJ-UHFFFAOYSA-N [4-(1,3-benzoxazol-2-yl)phenyl]-[4-(1-hydroxycyclopropanecarbonyl)piperazin-1-yl]methanone Chemical compound OC1(CC1)C(=O)N1CCN(CC1)C(=O)c1ccc(cc1)-c1nc2ccccc2o1 FGXGECPNCZCUAJ-UHFFFAOYSA-N 0.000 description 2
- CSXRUXWSMJGACB-UHFFFAOYSA-N [4-(3,4-dihydro-2H-quinolin-1-yl)phenyl]-piperazin-1-ylmethanone Chemical compound O=C(N1CCNCC1)C1=CC=C(C=C1)N1CCCC2=C1C=CC=C2 CSXRUXWSMJGACB-UHFFFAOYSA-N 0.000 description 2
- RDTFIRXDJIMLTB-UHFFFAOYSA-N [4-(5-chloro-1,3-benzoxazol-2-yl)phenyl]-[4-(1-hydroxycyclopropanecarbonyl)piperazin-1-yl]methanone Chemical compound OC1(CC1)C(=O)N1CCN(CC1)C(=O)c1ccc(cc1)-c1nc2cc(Cl)ccc2o1 RDTFIRXDJIMLTB-UHFFFAOYSA-N 0.000 description 2
- 201000000690 abdominal obesity-metabolic syndrome Diseases 0.000 description 2
- 235000010489 acacia gum Nutrition 0.000 description 2
- 239000000205 acacia gum Substances 0.000 description 2
- ZSLZBFCDCINBPY-ZSJPKINUSA-N acetyl-CoA Chemical compound O[C@@H]1[C@H](OP(O)(O)=O)[C@@H](COP(O)(=O)OP(O)(=O)OCC(C)(C)[C@@H](O)C(=O)NCCC(=O)NCCSC(=O)C)O[C@H]1N1C2=NC=NC(N)=C2N=C1 ZSLZBFCDCINBPY-ZSJPKINUSA-N 0.000 description 2
- 229940081735 acetylcellulose Drugs 0.000 description 2
- 230000002378 acidificating effect Effects 0.000 description 2
- 239000013543 active substance Substances 0.000 description 2
- 238000009098 adjuvant therapy Methods 0.000 description 2
- 239000000443 aerosol Substances 0.000 description 2
- 125000003277 amino group Chemical group 0.000 description 2
- 230000001093 anti-cancer Effects 0.000 description 2
- 230000006907 apoptotic process Effects 0.000 description 2
- 239000008346 aqueous phase Substances 0.000 description 2
- 239000007864 aqueous solution Substances 0.000 description 2
- 235000010323 ascorbic acid Nutrition 0.000 description 2
- 238000003556 assay Methods 0.000 description 2
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 2
- 239000002585 base Substances 0.000 description 2
- 229940095076 benzaldehyde Drugs 0.000 description 2
- 235000010233 benzoic acid Nutrition 0.000 description 2
- DUJSUBPWKHTIAG-UHFFFAOYSA-N benzyl 4-[4-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)benzoyl]piperazine-1-carboxylate Chemical compound CC1(C)OB(OC1(C)C)c1ccc(cc1)C(=O)N1CCN(CC1)C(=O)OCc1ccccc1 DUJSUBPWKHTIAG-UHFFFAOYSA-N 0.000 description 2
- XHCNBISSYKFVCY-UHFFFAOYSA-N benzyl 4-[4-(6-fluoro-1,3-benzoxazol-2-yl)benzoyl]-4,7-diazaspiro[2.5]octane-7-carboxylate Chemical compound Fc1ccc2nc(oc2c1)-c1ccc(cc1)C(=O)N1CCN(CC11CC1)C(=O)OCc1ccccc1 XHCNBISSYKFVCY-UHFFFAOYSA-N 0.000 description 2
- SESFRYSPDFLNCH-UHFFFAOYSA-N benzyl benzoate Chemical compound C=1C=CC=CC=1C(=O)OCC1=CC=CC=C1 SESFRYSPDFLNCH-UHFFFAOYSA-N 0.000 description 2
- 239000011230 binding agent Substances 0.000 description 2
- 230000004071 biological effect Effects 0.000 description 2
- 239000004305 biphenyl Substances 0.000 description 2
- 230000000903 blocking effect Effects 0.000 description 2
- 210000000601 blood cell Anatomy 0.000 description 2
- ZADPBFCGQRWHPN-UHFFFAOYSA-N boronic acid Chemical compound OBO ZADPBFCGQRWHPN-UHFFFAOYSA-N 0.000 description 2
- 150000001649 bromium compounds Chemical class 0.000 description 2
- 229910000024 caesium carbonate Inorganic materials 0.000 description 2
- 235000011132 calcium sulphate Nutrition 0.000 description 2
- 230000036952 cancer formation Effects 0.000 description 2
- 239000001569 carbon dioxide Substances 0.000 description 2
- 150000007942 carboxylates Chemical class 0.000 description 2
- 231100000504 carcinogenesis Toxicity 0.000 description 2
- 235000010418 carrageenan Nutrition 0.000 description 2
- 239000000679 carrageenan Substances 0.000 description 2
- 229920001525 carrageenan Polymers 0.000 description 2
- 229940113118 carrageenan Drugs 0.000 description 2
- 239000000969 carrier Substances 0.000 description 2
- 239000012876 carrier material Substances 0.000 description 2
- 230000011748 cell maturation Effects 0.000 description 2
- 229920002301 cellulose acetate Polymers 0.000 description 2
- 210000003169 central nervous system Anatomy 0.000 description 2
- 201000010881 cervical cancer Diseases 0.000 description 2
- 230000002113 chemopreventative effect Effects 0.000 description 2
- 229910052801 chlorine Inorganic materials 0.000 description 2
- OSASVXMJTNOKOY-UHFFFAOYSA-N chlorobutanol Chemical compound CC(C)(O)C(Cl)(Cl)Cl OSASVXMJTNOKOY-UHFFFAOYSA-N 0.000 description 2
- HVYWMOMLDIMFJA-DPAQBDIFSA-N cholesterol Chemical compound C1C=C2C[C@@H](O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@H]([C@H](C)CCCC(C)C)[C@@]1(C)CC2 HVYWMOMLDIMFJA-DPAQBDIFSA-N 0.000 description 2
- 235000015165 citric acid Nutrition 0.000 description 2
- 229940075614 colloidal silicon dioxide Drugs 0.000 description 2
- 238000013329 compounding Methods 0.000 description 2
- 235000005687 corn oil Nutrition 0.000 description 2
- 239000002285 corn oil Substances 0.000 description 2
- 230000008878 coupling Effects 0.000 description 2
- 238000010168 coupling process Methods 0.000 description 2
- 238000005859 coupling reaction Methods 0.000 description 2
- SNRCKKQHDUIRIY-UHFFFAOYSA-L cyclopenta-1,4-dien-1-yl(diphenyl)phosphane;dichloromethane;dichloropalladium;iron(2+) Chemical compound [Fe+2].ClCCl.Cl[Pd]Cl.C1=C[CH-]C(P(C=2C=CC=CC=2)C=2C=CC=CC=2)=C1.C1=C[CH-]C(P(C=2C=CC=CC=2)C=2C=CC=CC=2)=C1 SNRCKKQHDUIRIY-UHFFFAOYSA-L 0.000 description 2
- XRLDSWLMHUQECH-UHFFFAOYSA-N cyclopentanecarboxamide Chemical compound NC(=O)C1CCCC1 XRLDSWLMHUQECH-UHFFFAOYSA-N 0.000 description 2
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 2
- 230000001472 cytotoxic effect Effects 0.000 description 2
- GVJHHUAWPYXKBD-UHFFFAOYSA-N d-alpha-tocopherol Natural products OC1=C(C)C(C)=C2OC(CCCC(C)CCCC(C)CCCC(C)C)(C)CCC2=C1C GVJHHUAWPYXKBD-UHFFFAOYSA-N 0.000 description 2
- 229940096516 dextrates Drugs 0.000 description 2
- ZBCBWPMODOFKDW-UHFFFAOYSA-N diethanolamine Chemical compound OCCNCCO ZBCBWPMODOFKDW-UHFFFAOYSA-N 0.000 description 2
- FLKPEMZONWLCSK-UHFFFAOYSA-N diethyl phthalate Chemical compound CCOC(=O)C1=CC=CC=C1C(=O)OCC FLKPEMZONWLCSK-UHFFFAOYSA-N 0.000 description 2
- 239000003085 diluting agent Substances 0.000 description 2
- 229940008099 dimethicone Drugs 0.000 description 2
- 239000004205 dimethyl polysiloxane Substances 0.000 description 2
- 235000013870 dimethyl polysiloxane Nutrition 0.000 description 2
- AMTWCFIAVKBGOD-UHFFFAOYSA-N dioxosilane;methoxy-dimethyl-trimethylsilyloxysilane Chemical compound O=[Si]=O.CO[Si](C)(C)O[Si](C)(C)C AMTWCFIAVKBGOD-UHFFFAOYSA-N 0.000 description 2
- 239000008387 emulsifying waxe Substances 0.000 description 2
- 102000052116 epidermal growth factor receptor activity proteins Human genes 0.000 description 2
- 108700015053 epidermal growth factor receptor activity proteins Proteins 0.000 description 2
- OAYLNYINCPYISS-UHFFFAOYSA-N ethyl acetate;hexane Chemical compound CCCCCC.CCOC(C)=O OAYLNYINCPYISS-UHFFFAOYSA-N 0.000 description 2
- 235000019325 ethyl cellulose Nutrition 0.000 description 2
- 229920001249 ethyl cellulose Polymers 0.000 description 2
- CBOQJANXLMLOSS-UHFFFAOYSA-N ethyl vanillin Chemical compound CCOC1=CC(C=O)=CC=C1O CBOQJANXLMLOSS-UHFFFAOYSA-N 0.000 description 2
- 239000000796 flavoring agent Substances 0.000 description 2
- 235000019634 flavors Nutrition 0.000 description 2
- 239000011737 fluorine Substances 0.000 description 2
- 229910052731 fluorine Inorganic materials 0.000 description 2
- 235000003599 food sweetener Nutrition 0.000 description 2
- 238000009472 formulation Methods 0.000 description 2
- 230000006870 function Effects 0.000 description 2
- 229960001031 glucose Drugs 0.000 description 2
- MFWNKCLOYSRHCJ-BTTYYORXSA-N granisetron Chemical compound C1=CC=C2C(C(=O)N[C@H]3C[C@H]4CCC[C@@H](C3)N4C)=NN(C)C2=C1 MFWNKCLOYSRHCJ-BTTYYORXSA-N 0.000 description 2
- 229960003727 granisetron Drugs 0.000 description 2
- 235000010417 guar gum Nutrition 0.000 description 2
- 239000000665 guar gum Substances 0.000 description 2
- 229960002154 guar gum Drugs 0.000 description 2
- 201000005787 hematologic cancer Diseases 0.000 description 2
- 208000024200 hematopoietic and lymphoid system neoplasm Diseases 0.000 description 2
- 125000004415 heterocyclylalkyl group Chemical group 0.000 description 2
- BXWNKGSJHAJOGX-UHFFFAOYSA-N hexadecan-1-ol Chemical compound CCCCCCCCCCCCCCCCO BXWNKGSJHAJOGX-UHFFFAOYSA-N 0.000 description 2
- 229940051250 hexylene glycol Drugs 0.000 description 2
- 229940088597 hormone Drugs 0.000 description 2
- 239000005556 hormone Substances 0.000 description 2
- 235000001050 hortel pimenta Nutrition 0.000 description 2
- 150000002430 hydrocarbons Chemical group 0.000 description 2
- NPZTUJOABDZTLV-UHFFFAOYSA-N hydroxybenzotriazole Substances O=C1C=CC=C2NNN=C12 NPZTUJOABDZTLV-UHFFFAOYSA-N 0.000 description 2
- 235000010977 hydroxypropyl cellulose Nutrition 0.000 description 2
- 239000001863 hydroxypropyl cellulose Substances 0.000 description 2
- 230000001939 inductive effect Effects 0.000 description 2
- 239000004615 ingredient Substances 0.000 description 2
- 238000002347 injection Methods 0.000 description 2
- 239000007924 injection Substances 0.000 description 2
- 150000004694 iodide salts Chemical class 0.000 description 2
- INQOMBQAUSQDDS-UHFFFAOYSA-N iodomethane Chemical compound IC INQOMBQAUSQDDS-UHFFFAOYSA-N 0.000 description 2
- 208000002551 irritable bowel syndrome Diseases 0.000 description 2
- NNPPMTNAJDCUHE-UHFFFAOYSA-N isobutane Chemical compound CC(C)C NNPPMTNAJDCUHE-UHFFFAOYSA-N 0.000 description 2
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 2
- 125000001972 isopentyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])C([H])([H])* 0.000 description 2
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 2
- 229940043355 kinase inhibitor Drugs 0.000 description 2
- JVTAAEKCZFNVCJ-UHFFFAOYSA-N lactic acid Chemical compound CC(O)C(O)=O JVTAAEKCZFNVCJ-UHFFFAOYSA-N 0.000 description 2
- 239000008101 lactose Substances 0.000 description 2
- GFIJNRVAKGFPGQ-LIJARHBVSA-N leuprolide Chemical compound CCNC(=O)[C@@H]1CCCN1C(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](CC(C)C)NC(=O)[C@@H](NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC=1N=CNC=1)NC(=O)[C@H]1NC(=O)CC1)CC1=CC=C(O)C=C1 GFIJNRVAKGFPGQ-LIJARHBVSA-N 0.000 description 2
- 229960004338 leuprorelin Drugs 0.000 description 2
- 229940059904 light mineral oil Drugs 0.000 description 2
- 230000000670 limiting effect Effects 0.000 description 2
- 238000004811 liquid chromatography Methods 0.000 description 2
- KWGKDLIKAYFUFQ-UHFFFAOYSA-M lithium chloride Chemical compound [Li+].[Cl-] KWGKDLIKAYFUFQ-UHFFFAOYSA-M 0.000 description 2
- 229960002247 lomustine Drugs 0.000 description 2
- 210000004072 lung Anatomy 0.000 description 2
- 201000005202 lung cancer Diseases 0.000 description 2
- 208000020816 lung neoplasm Diseases 0.000 description 2
- HCWCAKKEBCNQJP-UHFFFAOYSA-N magnesium orthosilicate Chemical compound [Mg+2].[Mg+2].[O-][Si]([O-])([O-])[O-] HCWCAKKEBCNQJP-UHFFFAOYSA-N 0.000 description 2
- 239000000391 magnesium silicate Substances 0.000 description 2
- 235000019792 magnesium silicate Nutrition 0.000 description 2
- 229910052919 magnesium silicate Inorganic materials 0.000 description 2
- 229960002366 magnesium silicate Drugs 0.000 description 2
- 235000019359 magnesium stearate Nutrition 0.000 description 2
- 208000015486 malignant pancreatic neoplasm Diseases 0.000 description 2
- 238000004949 mass spectrometry Methods 0.000 description 2
- GLVAUDGFNGKCSF-UHFFFAOYSA-N mercaptopurine Chemical compound S=C1NC=NC2=C1NC=N2 GLVAUDGFNGKCSF-UHFFFAOYSA-N 0.000 description 2
- 230000002503 metabolic effect Effects 0.000 description 2
- 229940098779 methanesulfonic acid Drugs 0.000 description 2
- KDKBWBVNDADEON-UHFFFAOYSA-N methyl 4-(1,3-benzoxazol-2-yl)benzoate Chemical compound C1=CC(C(=O)OC)=CC=C1C1=NC2=CC=CC=C2O1 KDKBWBVNDADEON-UHFFFAOYSA-N 0.000 description 2
- GTCAXTIRRLKXRU-UHFFFAOYSA-N methyl carbamate Chemical compound COC(N)=O GTCAXTIRRLKXRU-UHFFFAOYSA-N 0.000 description 2
- OSWPMRLSEDHDFF-UHFFFAOYSA-N methyl salicylate Chemical compound COC(=O)C1=CC=CC=C1O OSWPMRLSEDHDFF-UHFFFAOYSA-N 0.000 description 2
- LXCFILQKKLGQFO-UHFFFAOYSA-N methylparaben Chemical compound COC(=O)C1=CC=C(O)C=C1 LXCFILQKKLGQFO-UHFFFAOYSA-N 0.000 description 2
- 230000000813 microbial effect Effects 0.000 description 2
- 229960004857 mitomycin Drugs 0.000 description 2
- YOHYSYJDKVYCJI-UHFFFAOYSA-N n-[3-[[6-[3-(trifluoromethyl)anilino]pyrimidin-4-yl]amino]phenyl]cyclopropanecarboxamide Chemical compound FC(F)(F)C1=CC=CC(NC=2N=CN=C(NC=3C=C(NC(=O)C4CC4)C=CC=3)C=2)=C1 YOHYSYJDKVYCJI-UHFFFAOYSA-N 0.000 description 2
- GOQYKNQRPGWPLP-UHFFFAOYSA-N n-heptadecyl alcohol Natural products CCCCCCCCCCCCCCCCCO GOQYKNQRPGWPLP-UHFFFAOYSA-N 0.000 description 2
- 230000008693 nausea Effects 0.000 description 2
- 125000004433 nitrogen atom Chemical group N* 0.000 description 2
- 208000002154 non-small cell lung carcinoma Diseases 0.000 description 2
- 229960005343 ondansetron Drugs 0.000 description 2
- 239000010502 orange oil Substances 0.000 description 2
- 150000007530 organic bases Chemical class 0.000 description 2
- 230000002018 overexpression Effects 0.000 description 2
- UWOTZNQZPLAURK-UHFFFAOYSA-N oxetane-3-carboxylic acid Chemical compound OC(=O)C1COC1 UWOTZNQZPLAURK-UHFFFAOYSA-N 0.000 description 2
- 239000001301 oxygen Substances 0.000 description 2
- 201000002528 pancreatic cancer Diseases 0.000 description 2
- 208000008443 pancreatic carcinoma Diseases 0.000 description 2
- QNGNSVIICDLXHT-UHFFFAOYSA-N para-ethylbenzaldehyde Natural products CCC1=CC=C(C=O)C=C1 QNGNSVIICDLXHT-UHFFFAOYSA-N 0.000 description 2
- 239000000312 peanut oil Substances 0.000 description 2
- 125000002255 pentenyl group Chemical group C(=CCCC)* 0.000 description 2
- 239000003757 phosphotransferase inhibitor Substances 0.000 description 2
- 229960000502 poloxamer Drugs 0.000 description 2
- 229920001983 poloxamer Polymers 0.000 description 2
- 229920000435 poly(dimethylsiloxane) Polymers 0.000 description 2
- 235000010486 polyoxyethylene sorbitan monolaurate Nutrition 0.000 description 2
- 239000000256 polyoxyethylene sorbitan monolaurate Substances 0.000 description 2
- 235000010482 polyoxyethylene sorbitan monooleate Nutrition 0.000 description 2
- 239000000244 polyoxyethylene sorbitan monooleate Substances 0.000 description 2
- 235000010483 polyoxyethylene sorbitan monopalmitate Nutrition 0.000 description 2
- 239000000249 polyoxyethylene sorbitan monopalmitate Substances 0.000 description 2
- 235000010989 polyoxyethylene sorbitan monostearate Nutrition 0.000 description 2
- 239000001818 polyoxyethylene sorbitan monostearate Substances 0.000 description 2
- 229940068977 polysorbate 20 Drugs 0.000 description 2
- 229940101027 polysorbate 40 Drugs 0.000 description 2
- 229940113124 polysorbate 60 Drugs 0.000 description 2
- 229940068968 polysorbate 80 Drugs 0.000 description 2
- 229920000053 polysorbate 80 Polymers 0.000 description 2
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 2
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 2
- 229940069328 povidone Drugs 0.000 description 2
- 238000001556 precipitation Methods 0.000 description 2
- 230000008569 process Effects 0.000 description 2
- 230000035755 proliferation Effects 0.000 description 2
- QELSKZZBTMNZEB-UHFFFAOYSA-N propylparaben Chemical compound CCCOC(=O)C1=CC=C(O)C=C1 QELSKZZBTMNZEB-UHFFFAOYSA-N 0.000 description 2
- 239000003528 protein farnesyltransferase inhibitor Substances 0.000 description 2
- 108090000623 proteins and genes Proteins 0.000 description 2
- 238000010992 reflux Methods 0.000 description 2
- 230000002441 reversible effect Effects 0.000 description 2
- 239000008159 sesame oil Substances 0.000 description 2
- 235000011803 sesame oil Nutrition 0.000 description 2
- 235000012239 silicon dioxide Nutrition 0.000 description 2
- 229940083037 simethicone Drugs 0.000 description 2
- 201000000849 skin cancer Diseases 0.000 description 2
- 239000011780 sodium chloride Substances 0.000 description 2
- 235000019333 sodium laurylsulphate Nutrition 0.000 description 2
- JQWHASGSAFIOCM-UHFFFAOYSA-M sodium periodate Chemical compound [Na+].[O-]I(=O)(=O)=O JQWHASGSAFIOCM-UHFFFAOYSA-M 0.000 description 2
- 239000002594 sorbent Substances 0.000 description 2
- 235000011069 sorbitan monooleate Nutrition 0.000 description 2
- 239000001593 sorbitan monooleate Substances 0.000 description 2
- 229940035049 sorbitan monooleate Drugs 0.000 description 2
- 235000011071 sorbitan monopalmitate Nutrition 0.000 description 2
- 239000001570 sorbitan monopalmitate Substances 0.000 description 2
- 229940031953 sorbitan monopalmitate Drugs 0.000 description 2
- 239000003381 stabilizer Substances 0.000 description 2
- 239000008107 starch Substances 0.000 description 2
- 229940032147 starch Drugs 0.000 description 2
- 235000019698 starch Nutrition 0.000 description 2
- 239000000126 substance Substances 0.000 description 2
- 230000004083 survival effect Effects 0.000 description 2
- 239000000375 suspending agent Substances 0.000 description 2
- 239000003765 sweetening agent Substances 0.000 description 2
- ZTKXBTXZRJOSMB-INIZCTEOSA-N tert-butyl (2S)-4-[2-fluoro-4-(1-methylbenzimidazol-5-yl)benzoyl]-2-methylpiperazine-1-carboxylate Chemical compound C[C@H]1CN(CCN1C(=O)OC(C)(C)C)C(=O)c1ccc(cc1F)-c1ccc2n(C)cnc2c1 ZTKXBTXZRJOSMB-INIZCTEOSA-N 0.000 description 2
- DATRVIMZZZVHMP-MRVPVSSYSA-N tert-butyl (2r)-2-methylpiperazine-1-carboxylate Chemical compound C[C@@H]1CNCCN1C(=O)OC(C)(C)C DATRVIMZZZVHMP-MRVPVSSYSA-N 0.000 description 2
- MIEUNCGOXURNTQ-UHFFFAOYSA-N tert-butyl 4-(4-pyrazolo[1,5-a]pyridin-2-ylbenzoyl)piperazine-1-carboxylate Chemical compound CC(C)(C)OC(=O)N1CCN(CC1)C(=O)c1ccc(cc1)-c1cc2ccccn2n1 MIEUNCGOXURNTQ-UHFFFAOYSA-N 0.000 description 2
- LDGUEUOPDCRQFT-UHFFFAOYSA-N tert-butyl 4-[4-(2,3-dihydroindol-1-yl)benzoyl]piperazine-1-carboxylate Chemical compound CC(C)(C)OC(=O)N1CCN(CC1)C(=O)c1ccc(cc1)N1CCc2ccccc12 LDGUEUOPDCRQFT-UHFFFAOYSA-N 0.000 description 2
- WGKPBJOFNSLHQX-UHFFFAOYSA-N tert-butyl 4-[4-(3,4-dihydro-2H-quinolin-1-yl)benzoyl]piperazine-1-carboxylate Chemical compound N1(CCCC2=CC=CC=C12)C1=CC=C(C(=O)N2CCN(CC2)C(=O)OC(C)(C)C)C=C1 WGKPBJOFNSLHQX-UHFFFAOYSA-N 0.000 description 2
- CNNPJVNCMBVSNM-UHFFFAOYSA-N tert-butyl 4-[4-(3-amino-1,2-benzoxazol-6-yl)benzoyl]piperazine-1-carboxylate Chemical compound CC(C)(C)OC(=O)N1CCN(CC1)C(=O)c1ccc(cc1)-c1ccc2c(N)noc2c1 CNNPJVNCMBVSNM-UHFFFAOYSA-N 0.000 description 2
- HVWTYDPOWRHSSC-UHFFFAOYSA-N tert-butyl 4-[4-(3-methylindazol-1-yl)benzoyl]piperazine-1-carboxylate Chemical compound Cc1nn(-c2ccc(cc2)C(=O)N2CCN(CC2)C(=O)OC(C)(C)C)c2ccccc12 HVWTYDPOWRHSSC-UHFFFAOYSA-N 0.000 description 2
- XMNADNPAWOEIJP-UHFFFAOYSA-N tert-butyl 4-[4-[3-(cyclopropanecarbonylamino)-1,2-benzoxazol-6-yl]benzoyl]piperazine-1-carboxylate Chemical compound CC(C)(C)OC(=O)N1CCN(CC1)C(=O)c1ccc(cc1)-c1ccc2c(NC(=O)C3CC3)noc2c1 XMNADNPAWOEIJP-UHFFFAOYSA-N 0.000 description 2
- VZGDMQKNWNREIO-UHFFFAOYSA-N tetrachloromethane Chemical compound ClC(Cl)(Cl)Cl VZGDMQKNWNREIO-UHFFFAOYSA-N 0.000 description 2
- HLZKNKRTKFSKGZ-UHFFFAOYSA-N tetradecan-1-ol Chemical compound CCCCCCCCCCCCCCO HLZKNKRTKFSKGZ-UHFFFAOYSA-N 0.000 description 2
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 2
- 238000004809 thin layer chromatography Methods 0.000 description 2
- 229960000790 thymol Drugs 0.000 description 2
- 235000010384 tocopherol Nutrition 0.000 description 2
- 229960001295 tocopherol Drugs 0.000 description 2
- 229930003799 tocopherol Natural products 0.000 description 2
- 239000011732 tocopherol Substances 0.000 description 2
- RUVINXPYWBROJD-ONEGZZNKSA-N trans-anethole Chemical compound COC1=CC=C(\C=C\C)C=C1 RUVINXPYWBROJD-ONEGZZNKSA-N 0.000 description 2
- URAYPUMNDPQOKB-UHFFFAOYSA-N triacetin Chemical compound CC(=O)OCC(OC(C)=O)COC(C)=O URAYPUMNDPQOKB-UHFFFAOYSA-N 0.000 description 2
- QORWJWZARLRLPR-UHFFFAOYSA-H tricalcium bis(phosphate) Chemical compound [Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O QORWJWZARLRLPR-UHFFFAOYSA-H 0.000 description 2
- 235000019731 tricalcium phosphate Nutrition 0.000 description 2
- 229960004418 trolamine Drugs 0.000 description 2
- 208000029729 tumor suppressor gene on chromosome 11 Diseases 0.000 description 2
- 238000000825 ultraviolet detection Methods 0.000 description 2
- 206010046766 uterine cancer Diseases 0.000 description 2
- 230000029812 viral genome replication Effects 0.000 description 2
- 230000003612 virological effect Effects 0.000 description 2
- 239000001993 wax Substances 0.000 description 2
- 239000000080 wetting agent Substances 0.000 description 2
- UHVMMEOXYDMDKI-JKYCWFKZSA-L zinc;1-(5-cyanopyridin-2-yl)-3-[(1s,2s)-2-(6-fluoro-2-hydroxy-3-propanoylphenyl)cyclopropyl]urea;diacetate Chemical compound [Zn+2].CC([O-])=O.CC([O-])=O.CCC(=O)C1=CC=C(F)C([C@H]2[C@H](C2)NC(=O)NC=2N=CC(=CC=2)C#N)=C1O UHVMMEOXYDMDKI-JKYCWFKZSA-L 0.000 description 2
- GVJHHUAWPYXKBD-IEOSBIPESA-N α-tocopherol Chemical compound OC1=C(C)C(C)=C2O[C@@](CCC[C@H](C)CCC[C@H](C)CCCC(C)C)(C)CCC2=C1C GVJHHUAWPYXKBD-IEOSBIPESA-N 0.000 description 2
- NOOLISFMXDJSKH-UTLUCORTSA-N (+)-Neomenthol Chemical compound CC(C)[C@@H]1CC[C@@H](C)C[C@@H]1O NOOLISFMXDJSKH-UTLUCORTSA-N 0.000 description 1
- LSPHULWDVZXLIL-UHFFFAOYSA-N (+/-)-Camphoric acid Chemical class CC1(C)C(C(O)=O)CCC1(C)C(O)=O LSPHULWDVZXLIL-UHFFFAOYSA-N 0.000 description 1
- MFUGHYOIMCMYQV-GJMKNTOUSA-N (1r,2r)-1-n,2-n-dimethylcyclohexane-1,2-diamine Chemical compound CN[C@@H]1CCCC[C@H]1NC.CN[C@@H]1CCCC[C@H]1NC MFUGHYOIMCMYQV-GJMKNTOUSA-N 0.000 description 1
- LNAZSHAWQACDHT-XIYTZBAFSA-N (2r,3r,4s,5r,6s)-4,5-dimethoxy-2-(methoxymethyl)-3-[(2s,3r,4s,5r,6r)-3,4,5-trimethoxy-6-(methoxymethyl)oxan-2-yl]oxy-6-[(2r,3r,4s,5r,6r)-4,5,6-trimethoxy-2-(methoxymethyl)oxan-3-yl]oxyoxane Chemical compound CO[C@@H]1[C@@H](OC)[C@H](OC)[C@@H](COC)O[C@H]1O[C@H]1[C@H](OC)[C@@H](OC)[C@H](O[C@H]2[C@@H]([C@@H](OC)[C@H](OC)O[C@@H]2COC)OC)O[C@@H]1COC LNAZSHAWQACDHT-XIYTZBAFSA-N 0.000 description 1
- PAORVUMOXXAMPL-SECBINFHSA-N (2s)-3,3,3-trifluoro-2-methoxy-2-phenylpropanoyl chloride Chemical compound CO[C@](C(Cl)=O)(C(F)(F)F)C1=CC=CC=C1 PAORVUMOXXAMPL-SECBINFHSA-N 0.000 description 1
- NRESDXFFSNBDGP-UHFFFAOYSA-N (4-bromophenyl)hydrazine Chemical compound NNC1=CC=C(Br)C=C1 NRESDXFFSNBDGP-UHFFFAOYSA-N 0.000 description 1
- YYGNTYWPHWGJRM-UHFFFAOYSA-N (6E,10E,14E,18E)-2,6,10,15,19,23-hexamethyltetracosa-2,6,10,14,18,22-hexaene Chemical compound CC(C)=CCCC(C)=CCCC(C)=CCCC=C(C)CCC=C(C)CCC=C(C)C YYGNTYWPHWGJRM-UHFFFAOYSA-N 0.000 description 1
- ALSTYHKOOCGGFT-KTKRTIGZSA-N (9Z)-octadecen-1-ol Chemical compound CCCCCCCC\C=C/CCCCCCCCO ALSTYHKOOCGGFT-KTKRTIGZSA-N 0.000 description 1
- WRIDQFICGBMAFQ-UHFFFAOYSA-N (E)-8-Octadecenoic acid Natural products CCCCCCCCCC=CCCCCCCC(O)=O WRIDQFICGBMAFQ-UHFFFAOYSA-N 0.000 description 1
- LKJPYSCBVHEWIU-KRWDZBQOSA-N (R)-bicalutamide Chemical compound C([C@@](O)(C)C(=O)NC=1C=C(C(C#N)=CC=1)C(F)(F)F)S(=O)(=O)C1=CC=C(F)C=C1 LKJPYSCBVHEWIU-KRWDZBQOSA-N 0.000 description 1
- BJEPYKJPYRNKOW-REOHCLBHSA-N (S)-malic acid Chemical compound OC(=O)[C@@H](O)CC(O)=O BJEPYKJPYRNKOW-REOHCLBHSA-N 0.000 description 1
- FFJCNSLCJOQHKM-CLFAGFIQSA-N (z)-1-[(z)-octadec-9-enoxy]octadec-9-ene Chemical compound CCCCCCCC\C=C/CCCCCCCCOCCCCCCCC\C=C/CCCCCCCC FFJCNSLCJOQHKM-CLFAGFIQSA-N 0.000 description 1
- DDMOUSALMHHKOS-UHFFFAOYSA-N 1,2-dichloro-1,1,2,2-tetrafluoroethane Chemical compound FC(F)(Cl)C(F)(F)Cl DDMOUSALMHHKOS-UHFFFAOYSA-N 0.000 description 1
- BIXRSCVOWFUPML-UHFFFAOYSA-N 1,3-benzothiazol-2-yl(tributyl)stannane Chemical compound C1=CC=C2SC([Sn](CCCC)(CCCC)CCCC)=NC2=C1 BIXRSCVOWFUPML-UHFFFAOYSA-N 0.000 description 1
- LDVVTQMJQSCDMK-UHFFFAOYSA-N 1,3-dihydroxypropan-2-yl formate Chemical compound OCC(CO)OC=O LDVVTQMJQSCDMK-UHFFFAOYSA-N 0.000 description 1
- BTSMHDXDJYOIJM-UHFFFAOYSA-N 1-(4-bromophenyl)-3-methyl-2,3,4,5,6,7-hexahydroindazole Chemical compound BrC1=CC=C(C=C1)N1NC(C=2CCCCC12)C BTSMHDXDJYOIJM-UHFFFAOYSA-N 0.000 description 1
- GGOIFYXEYJXZSQ-UHFFFAOYSA-N 1-(4-bromophenyl)-3-methyl-4,5,6,7-tetrahydroindazole Chemical compound Cc1nn(c2CCCCc12)-c1ccc(Br)cc1 GGOIFYXEYJXZSQ-UHFFFAOYSA-N 0.000 description 1
- DSKCOVBHIFAJRI-UHFFFAOYSA-N 1-[(2-methylpropan-2-yl)oxycarbonylamino]cyclopropane-1-carboxylic acid Chemical compound CC(C)(C)OC(=O)NC1(C(O)=O)CC1 DSKCOVBHIFAJRI-UHFFFAOYSA-N 0.000 description 1
- PAJPWUMXBYXFCZ-UHFFFAOYSA-N 1-aminocyclopropanecarboxylic acid Chemical compound OC(=O)C1(N)CC1 PAJPWUMXBYXFCZ-UHFFFAOYSA-N 0.000 description 1
- OKMWKBLSFKFYGZ-UHFFFAOYSA-N 1-behenoylglycerol Chemical compound CCCCCCCCCCCCCCCCCCCCCC(=O)OCC(O)CO OKMWKBLSFKFYGZ-UHFFFAOYSA-N 0.000 description 1
- VFWCMGCRMGJXDK-UHFFFAOYSA-N 1-chlorobutane Chemical class CCCCCl VFWCMGCRMGJXDK-UHFFFAOYSA-N 0.000 description 1
- VUQPJRPDRDVQMN-UHFFFAOYSA-N 1-chlorooctadecane Chemical class CCCCCCCCCCCCCCCCCCCl VUQPJRPDRDVQMN-UHFFFAOYSA-N 0.000 description 1
- PZNPLUBHRSSFHT-RRHRGVEJSA-N 1-hexadecanoyl-2-octadecanoyl-sn-glycero-3-phosphocholine Chemical compound CCCCCCCCCCCCCCCCCC(=O)O[C@@H](COP([O-])(=O)OCC[N+](C)(C)C)COC(=O)CCCCCCCCCCCCCCC PZNPLUBHRSSFHT-RRHRGVEJSA-N 0.000 description 1
- IXPNQXFRVYWDDI-UHFFFAOYSA-N 1-methyl-2,4-dioxo-1,3-diazinane-5-carboximidamide Chemical compound CN1CC(C(N)=N)C(=O)NC1=O IXPNQXFRVYWDDI-UHFFFAOYSA-N 0.000 description 1
- IIZPXYDJLKNOIY-JXPKJXOSSA-N 1-palmitoyl-2-arachidonoyl-sn-glycero-3-phosphocholine Chemical compound CCCCCCCCCCCCCCCC(=O)OC[C@H](COP([O-])(=O)OCC[N+](C)(C)C)OC(=O)CCC\C=C/C\C=C/C\C=C/C\C=C/CCCCC IIZPXYDJLKNOIY-JXPKJXOSSA-N 0.000 description 1
- DBPWSSGDRRHUNT-CEGNMAFCSA-N 17α-hydroxyprogesterone Chemical compound C1CC2=CC(=O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@@](C(=O)C)(O)[C@@]1(C)CC2 DBPWSSGDRRHUNT-CEGNMAFCSA-N 0.000 description 1
- URBTWKYNKXLBSU-UHFFFAOYSA-N 18-(18-oxooctadecoxy)octadecanal Chemical compound O=CCCCCCCCCCCCCCCCCCOCCCCCCCCCCCCCCCCCC=O URBTWKYNKXLBSU-UHFFFAOYSA-N 0.000 description 1
- BAXOFTOLAUCFNW-UHFFFAOYSA-N 1H-indazole Chemical compound C1=CC=C2C=NNC2=C1 BAXOFTOLAUCFNW-UHFFFAOYSA-N 0.000 description 1
- CHHHXKFHOYLYRE-UHFFFAOYSA-M 2,4-Hexadienoic acid, potassium salt (1:1), (2E,4E)- Chemical compound [K+].CC=CC=CC([O-])=O CHHHXKFHOYLYRE-UHFFFAOYSA-M 0.000 description 1
- ZEMZPXWZVTUONV-UHFFFAOYSA-N 2-(2-dicyclohexylphosphanylphenyl)-n,n-dimethylaniline Chemical compound CN(C)C1=CC=CC=C1C1=CC=CC=C1P(C1CCCCC1)C1CCCCC1 ZEMZPXWZVTUONV-UHFFFAOYSA-N 0.000 description 1
- YNTJKQDWYXUTLZ-UHFFFAOYSA-N 2-(3-chlorophenoxy)propanoic acid Chemical compound OC(=O)C(C)OC1=CC=CC(Cl)=C1 YNTJKQDWYXUTLZ-UHFFFAOYSA-N 0.000 description 1
- KCODGAGMHNSFLL-UHFFFAOYSA-N 2-(4-bromophenyl)-3-methyl-4,5,6,7-tetrahydroindazole Chemical compound CC1=C2CCCCC2=NN1C1=CC=C(Br)C=C1 KCODGAGMHNSFLL-UHFFFAOYSA-N 0.000 description 1
- HZAXFHJVJLSVMW-UHFFFAOYSA-N 2-Aminoethan-1-ol Chemical compound NCCO HZAXFHJVJLSVMW-UHFFFAOYSA-N 0.000 description 1
- NGNBDVOYPDDBFK-UHFFFAOYSA-N 2-[2,4-di(pentan-2-yl)phenoxy]acetyl chloride Chemical compound CCCC(C)C1=CC=C(OCC(Cl)=O)C(C(C)CCC)=C1 NGNBDVOYPDDBFK-UHFFFAOYSA-N 0.000 description 1
- OIALAIQRYISUEV-UHFFFAOYSA-N 2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-(2-hydroxyethoxy)ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]e Polymers CCCCCCCCCCCCCCCCCC(=O)OCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCO OIALAIQRYISUEV-UHFFFAOYSA-N 0.000 description 1
- HNLXNOZHXNSSPN-UHFFFAOYSA-N 2-[2-[2-[2-[2-[2-[2-[4-(2,4,4-trimethylpentan-2-yl)phenoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethanol Chemical compound CC(C)(C)CC(C)(C)C1=CC=C(OCCOCCOCCOCCOCCOCCOCCO)C=C1 HNLXNOZHXNSSPN-UHFFFAOYSA-N 0.000 description 1
- OEKATORRSPXJHE-UHFFFAOYSA-N 2-acetylcyclohexan-1-one Chemical compound CC(=O)C1CCCCC1=O OEKATORRSPXJHE-UHFFFAOYSA-N 0.000 description 1
- IIDUNAVOCYMUFB-UHFFFAOYSA-N 2-amino-5-fluorophenol Chemical compound NC1=CC=C(F)C=C1O IIDUNAVOCYMUFB-UHFFFAOYSA-N 0.000 description 1
- PHPYXVIHDRDPDI-UHFFFAOYSA-N 2-bromo-1h-benzimidazole Chemical compound C1=CC=C2NC(Br)=NC2=C1 PHPYXVIHDRDPDI-UHFFFAOYSA-N 0.000 description 1
- JBKINHFZTVLNEM-UHFFFAOYSA-N 2-bromoethoxy-tert-butyl-dimethylsilane Chemical compound CC(C)(C)[Si](C)(C)OCCBr JBKINHFZTVLNEM-UHFFFAOYSA-N 0.000 description 1
- FLRVWEZCIVDUPC-UHFFFAOYSA-N 2-chloropyrazolo[1,5-a]pyridine Chemical compound C1=CC=CN2N=C(Cl)C=C21 FLRVWEZCIVDUPC-UHFFFAOYSA-N 0.000 description 1
- LDZYRENCLPUXAX-UHFFFAOYSA-N 2-methyl-1h-benzimidazole Chemical compound C1=CC=C2NC(C)=NC2=C1 LDZYRENCLPUXAX-UHFFFAOYSA-N 0.000 description 1
- 125000004918 2-methyl-2-pentyl group Chemical group CC(C)(CCC)* 0.000 description 1
- YSEQNZOXHCKLOG-UHFFFAOYSA-N 2-methyl-octanoic acid Chemical compound CCCCCCC(C)C(O)=O YSEQNZOXHCKLOG-UHFFFAOYSA-N 0.000 description 1
- 125000004493 2-methylbut-1-yl group Chemical group CC(C*)CC 0.000 description 1
- MSXVEPNJUHWQHW-UHFFFAOYSA-N 2-methylbutan-2-ol Chemical compound CCC(C)(C)O MSXVEPNJUHWQHW-UHFFFAOYSA-N 0.000 description 1
- QTWJRLJHJPIABL-UHFFFAOYSA-N 2-methylphenol;3-methylphenol;4-methylphenol Chemical compound CC1=CC=C(O)C=C1.CC1=CC=CC(O)=C1.CC1=CC=CC=C1O QTWJRLJHJPIABL-UHFFFAOYSA-N 0.000 description 1
- LEACJMVNYZDSKR-UHFFFAOYSA-N 2-octyldodecan-1-ol Chemical compound CCCCCCCCCCC(CO)CCCCCCCC LEACJMVNYZDSKR-UHFFFAOYSA-N 0.000 description 1
- WMPPDTMATNBGJN-UHFFFAOYSA-N 2-phenylethylbromide Chemical class BrCCC1=CC=CC=C1 WMPPDTMATNBGJN-UHFFFAOYSA-N 0.000 description 1
- 125000003903 2-propenyl group Chemical group [H]C([*])([H])C([H])=C([H])[H] 0.000 description 1
- YEYKMVJDLWJFOA-UHFFFAOYSA-N 2-propoxyethanol Chemical compound CCCOCCO YEYKMVJDLWJFOA-UHFFFAOYSA-N 0.000 description 1
- LQJBNNIYVWPHFW-UHFFFAOYSA-N 20:1omega9c fatty acid Natural products CCCCCCCCCCC=CCCCCCCCC(O)=O LQJBNNIYVWPHFW-UHFFFAOYSA-N 0.000 description 1
- CXIISRLRZRAKST-UHFFFAOYSA-N 29‐(4‐nonylphenoxy)‐3,6,9,12,15,18,21,24,27‐ nonaoxanonacosan‐1‐ol Chemical compound CCCCCCCCCC1=CC=C(OCCOCCOCCOCCOCCOCCOCCOCCOCCOCCO)C=C1 CXIISRLRZRAKST-UHFFFAOYSA-N 0.000 description 1
- PLRCVBKYFLWAAT-UHFFFAOYSA-N 3,3-difluorocyclobutane-1-carboxylic acid Chemical compound OC(=O)C1CC(F)(F)C1 PLRCVBKYFLWAAT-UHFFFAOYSA-N 0.000 description 1
- MIDXCONKKJTLDX-UHFFFAOYSA-N 3,5-dimethylcyclopentane-1,2-dione Chemical compound CC1CC(C)C(=O)C1=O MIDXCONKKJTLDX-UHFFFAOYSA-N 0.000 description 1
- JHUUPUMBZGWODW-UHFFFAOYSA-N 3,6-dihydro-1,2-dioxine Chemical compound C1OOCC=C1 JHUUPUMBZGWODW-UHFFFAOYSA-N 0.000 description 1
- QDLXPXDDINSMEW-UHFFFAOYSA-N 3-(3-bromophenyl)-1,2-oxazol-5-amine Chemical compound O1C(N)=CC(C=2C=C(Br)C=CC=2)=N1 QDLXPXDDINSMEW-UHFFFAOYSA-N 0.000 description 1
- FPQQSJJWHUJYPU-UHFFFAOYSA-N 3-(dimethylamino)propyliminomethylidene-ethylazanium;chloride Chemical compound Cl.CCN=C=NCCCN(C)C FPQQSJJWHUJYPU-UHFFFAOYSA-N 0.000 description 1
- 125000006275 3-bromophenyl group Chemical group [H]C1=C([H])C(Br)=C([H])C(*)=C1[H] 0.000 description 1
- 125000004919 3-methyl-2-pentyl group Chemical group CC(C(C)*)CC 0.000 description 1
- YHQXBTXEYZIYOV-UHFFFAOYSA-N 3-methylbut-1-ene Chemical compound CC(C)C=C YHQXBTXEYZIYOV-UHFFFAOYSA-N 0.000 description 1
- 125000003349 3-pyridyl group Chemical group N1=C([H])C([*])=C([H])C([H])=C1[H] 0.000 description 1
- CLEJZSNZYFJMKD-UHFFFAOYSA-N 3h-1,3-oxazole-2-thione Chemical compound SC1=NC=CO1 CLEJZSNZYFJMKD-UHFFFAOYSA-N 0.000 description 1
- UCFSYHMCKWNKAH-UHFFFAOYSA-N 4,4,5,5-tetramethyl-1,3,2-dioxaborolane Chemical compound CC1(C)OBOC1(C)C UCFSYHMCKWNKAH-UHFFFAOYSA-N 0.000 description 1
- GUPRYTGXAKYPMO-UHFFFAOYSA-N 4,7-diazaspiro[2.5]octan-4-yl-[4-(6-fluoro-1,3-benzoxazol-2-yl)phenyl]methanone Chemical compound Fc1ccc2nc(oc2c1)-c1ccc(cc1)C(=O)N1CCNCC11CC1 GUPRYTGXAKYPMO-UHFFFAOYSA-N 0.000 description 1
- GJBSOSHVGKMTOB-UHFFFAOYSA-N 4-(1-methylbenzimidazol-5-yl)benzoic acid Chemical compound C=1C=C2N(C)C=NC2=CC=1C1=CC=C(C(O)=O)C=C1 GJBSOSHVGKMTOB-UHFFFAOYSA-N 0.000 description 1
- CYDQOEWLBCCFJZ-UHFFFAOYSA-N 4-(4-fluorophenyl)oxane-4-carboxylic acid Chemical compound C=1C=C(F)C=CC=1C1(C(=O)O)CCOCC1 CYDQOEWLBCCFJZ-UHFFFAOYSA-N 0.000 description 1
- OKCDZLJMORDXTN-UHFFFAOYSA-N 4-(6-fluoro-1,3-benzoxazol-2-yl)benzoic acid Chemical compound C1=CC(C(=O)O)=CC=C1C1=NC2=CC=C(F)C=C2O1 OKCDZLJMORDXTN-UHFFFAOYSA-N 0.000 description 1
- DANLZOIRUUHIIX-UHFFFAOYSA-N 4-[1-[2-chloro-6-(trifluoromethyl)benzoyl]indazol-3-yl]benzoic acid Chemical compound C1=CC(C(=O)O)=CC=C1C(C1=CC=CC=C11)=NN1C(=O)C1=C(Cl)C=CC=C1C(F)(F)F DANLZOIRUUHIIX-UHFFFAOYSA-N 0.000 description 1
- CZDWJVSOQOMYGC-UHFFFAOYSA-N 4-borono-2-fluorobenzoic acid Chemical compound OB(O)C1=CC=C(C(O)=O)C(F)=C1 CZDWJVSOQOMYGC-UHFFFAOYSA-N 0.000 description 1
- JAVZWSOFJKYSDY-UHFFFAOYSA-N 4-bromo-2-chlorobenzoic acid Chemical compound OC(=O)C1=CC=C(Br)C=C1Cl JAVZWSOFJKYSDY-UHFFFAOYSA-N 0.000 description 1
- 125000002672 4-bromobenzoyl group Chemical group BrC1=CC=C(C(=O)*)C=C1 0.000 description 1
- HIQIXEFWDLTDED-UHFFFAOYSA-N 4-hydroxy-1-piperidin-4-ylpyrrolidin-2-one Chemical compound O=C1CC(O)CN1C1CCNCC1 HIQIXEFWDLTDED-UHFFFAOYSA-N 0.000 description 1
- REIDAMBAPLIATC-UHFFFAOYSA-M 4-methoxycarbonylbenzoate Chemical compound COC(=O)C1=CC=C(C([O-])=O)C=C1 REIDAMBAPLIATC-UHFFFAOYSA-M 0.000 description 1
- 125000004920 4-methyl-2-pentyl group Chemical group CC(CC(C)*)C 0.000 description 1
- RYAQFHLUEMJOMF-UHFFFAOYSA-N 4-phenoxybenzoic acid Chemical compound C1=CC(C(=O)O)=CC=C1OC1=CC=CC=C1 RYAQFHLUEMJOMF-UHFFFAOYSA-N 0.000 description 1
- 125000000339 4-pyridyl group Chemical group N1=C([H])C([H])=C([*])C([H])=C1[H] 0.000 description 1
- MGOKEBHEDJCRQN-UHFFFAOYSA-N 5-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)-1,3-benzothiazole Chemical compound O1C(C)(C)C(C)(C)OB1C1=CC=C(SC=N2)C2=C1 MGOKEBHEDJCRQN-UHFFFAOYSA-N 0.000 description 1
- FATPQDPUKVVCLT-UHFFFAOYSA-N 5-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)-1h-indole Chemical compound O1C(C)(C)C(C)(C)OB1C1=CC=C(NC=C2)C2=C1 FATPQDPUKVVCLT-UHFFFAOYSA-N 0.000 description 1
- 102000035037 5-HT3 receptors Human genes 0.000 description 1
- 108091005477 5-HT3 receptors Proteins 0.000 description 1
- ZPUQCVKBNRGSAP-UHFFFAOYSA-N 5-bromo-1h-indole-3-carbonitrile Chemical compound BrC1=CC=C2NC=C(C#N)C2=C1 ZPUQCVKBNRGSAP-UHFFFAOYSA-N 0.000 description 1
- BQCIJWPKDPZNHD-UHFFFAOYSA-N 5-bromo-2h-benzotriazole Chemical compound C1=C(Br)C=CC2=NNN=C21 BQCIJWPKDPZNHD-UHFFFAOYSA-N 0.000 description 1
- CNLHHYURQCSYLB-UHFFFAOYSA-N 6-bromo-1,2-benzoxazol-3-amine Chemical compound BrC1=CC=C2C(N)=NOC2=C1 CNLHHYURQCSYLB-UHFFFAOYSA-N 0.000 description 1
- XZIIFPSPUDAGJM-UHFFFAOYSA-N 6-chloro-2-n,2-n-diethylpyrimidine-2,4-diamine Chemical compound CCN(CC)C1=NC(N)=CC(Cl)=N1 XZIIFPSPUDAGJM-UHFFFAOYSA-N 0.000 description 1
- RPTXVOBIDXKEFW-UHFFFAOYSA-N 6-fluoro-3h-1,3-benzoxazole-2-thione Chemical compound FC1=CC=C2N=C(S)OC2=C1 RPTXVOBIDXKEFW-UHFFFAOYSA-N 0.000 description 1
- LWZXCEWJPKZISG-UHFFFAOYSA-N 7-O-benzyl 4-O-tert-butyl 4,7-diazaspiro[2.5]octane-4,7-dicarboxylate Chemical compound CC(C)(C)OC(=O)N1CCN(CC11CC1)C(=O)OCc1ccccc1 LWZXCEWJPKZISG-UHFFFAOYSA-N 0.000 description 1
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 1
- QSBYPNXLFMSGKH-UHFFFAOYSA-N 9-Heptadecensaeure Natural products CCCCCCCC=CCCCCCCCC(O)=O QSBYPNXLFMSGKH-UHFFFAOYSA-N 0.000 description 1
- 208000030507 AIDS Diseases 0.000 description 1
- 235000007173 Abies balsamea Nutrition 0.000 description 1
- NIXOWILDQLNWCW-UHFFFAOYSA-N Acrylic acid Chemical compound OC(=O)C=C NIXOWILDQLNWCW-UHFFFAOYSA-N 0.000 description 1
- 241000251468 Actinopterygii Species 0.000 description 1
- 208000031261 Acute myeloid leukaemia Diseases 0.000 description 1
- 208000036762 Acute promyelocytic leukaemia Diseases 0.000 description 1
- 229920001817 Agar Polymers 0.000 description 1
- 235000019489 Almond oil Nutrition 0.000 description 1
- 201000004384 Alopecia Diseases 0.000 description 1
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 1
- 239000005995 Aluminium silicate Substances 0.000 description 1
- QGZKDVFQNNGYKY-UHFFFAOYSA-N Ammonia Chemical compound N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 1
- QGZKDVFQNNGYKY-UHFFFAOYSA-O Ammonium Chemical compound [NH4+] QGZKDVFQNNGYKY-UHFFFAOYSA-O 0.000 description 1
- USFZMSVCRYTOJT-UHFFFAOYSA-N Ammonium acetate Chemical compound N.CC(O)=O USFZMSVCRYTOJT-UHFFFAOYSA-N 0.000 description 1
- 239000005695 Ammonium acetate Substances 0.000 description 1
- 239000004254 Ammonium phosphate Substances 0.000 description 1
- 206010002556 Ankylosing Spondylitis Diseases 0.000 description 1
- 239000004475 Arginine Substances 0.000 description 1
- 108010011485 Aspartame Proteins 0.000 description 1
- 208000023275 Autoimmune disease Diseases 0.000 description 1
- 208000003950 B-cell lymphoma Diseases 0.000 description 1
- 208000032791 BCR-ABL1 positive chronic myelogenous leukemia Diseases 0.000 description 1
- 239000004857 Balsam Substances 0.000 description 1
- 208000020084 Bone disease Diseases 0.000 description 1
- 206010006002 Bone pain Diseases 0.000 description 1
- ZOXJGFHDIHLPTG-UHFFFAOYSA-N Boron Chemical compound [B] ZOXJGFHDIHLPTG-UHFFFAOYSA-N 0.000 description 1
- 241000283690 Bos taurus Species 0.000 description 1
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 1
- COVZYZSDYWQREU-UHFFFAOYSA-N Busulfan Chemical compound CS(=O)(=O)OCCCCOS(C)(=O)=O COVZYZSDYWQREU-UHFFFAOYSA-N 0.000 description 1
- 239000004255 Butylated hydroxyanisole Substances 0.000 description 1
- 239000004322 Butylated hydroxytoluene Substances 0.000 description 1
- NLZUEZXRPGMBCV-UHFFFAOYSA-N Butylhydroxytoluene Chemical compound CC1=CC(C(C)(C)C)=C(O)C(C(C)(C)C)=C1 NLZUEZXRPGMBCV-UHFFFAOYSA-N 0.000 description 1
- MZHXRFLOJSIXKJ-UHFFFAOYSA-N C1CN(CCN1)C(=O)C2=CC=C(C=C2)C3=CC(=CC=C3)C4=NOC=C4 Chemical compound C1CN(CCN1)C(=O)C2=CC=C(C=C2)C3=CC(=CC=C3)C4=NOC=C4 MZHXRFLOJSIXKJ-UHFFFAOYSA-N 0.000 description 1
- 125000003601 C2-C6 alkynyl group Chemical group 0.000 description 1
- 125000004648 C2-C8 alkenyl group Chemical group 0.000 description 1
- KSQKSJNKPVKDOH-UHFFFAOYSA-N CC(C)(C)OC(=O)NC1=CC(=NO1)C2=CC=CC(=C2)C3=CC=CC=C3 Chemical compound CC(C)(C)OC(=O)NC1=CC(=NO1)C2=CC=CC(=C2)C3=CC=CC=C3 KSQKSJNKPVKDOH-UHFFFAOYSA-N 0.000 description 1
- 229940126074 CDK kinase inhibitor Drugs 0.000 description 1
- NONLYMJHKGQHLQ-UHFFFAOYSA-N CS(O)(=O)=O.NC1=CC=CC=C1C1=CC=CC=C1 Chemical compound CS(O)(=O)=O.NC1=CC=CC=C1C1=CC=CC=C1 NONLYMJHKGQHLQ-UHFFFAOYSA-N 0.000 description 1
- UXVMQQNJUSDDNG-UHFFFAOYSA-L Calcium chloride Chemical compound [Cl-].[Cl-].[Ca+2] UXVMQQNJUSDDNG-UHFFFAOYSA-L 0.000 description 1
- 239000001736 Calcium glycerylphosphate Substances 0.000 description 1
- 241000282472 Canis lupus familiaris Species 0.000 description 1
- GAGWJHPBXLXJQN-UHFFFAOYSA-N Capecitabine Natural products C1=C(F)C(NC(=O)OCCCCC)=NC(=O)N1C1C(O)C(O)C(C)O1 GAGWJHPBXLXJQN-UHFFFAOYSA-N 0.000 description 1
- 241000283707 Capra Species 0.000 description 1
- OKTJSMMVPCPJKN-NJFSPNSNSA-N Carbon-14 Chemical compound [14C] OKTJSMMVPCPJKN-NJFSPNSNSA-N 0.000 description 1
- 229920002134 Carboxymethyl cellulose Polymers 0.000 description 1
- 201000009030 Carcinoma Diseases 0.000 description 1
- 208000024172 Cardiovascular disease Diseases 0.000 description 1
- 102000011632 Caseins Human genes 0.000 description 1
- 108010076119 Caseins Proteins 0.000 description 1
- 241000700198 Cavia Species 0.000 description 1
- 229920000623 Cellulose acetate phthalate Polymers 0.000 description 1
- 241000282693 Cercopithecidae Species 0.000 description 1
- KZBUYRJDOAKODT-UHFFFAOYSA-N Chlorine Chemical compound ClCl KZBUYRJDOAKODT-UHFFFAOYSA-N 0.000 description 1
- 208000006545 Chronic Obstructive Pulmonary Disease Diseases 0.000 description 1
- 235000008733 Citrus aurantifolia Nutrition 0.000 description 1
- 208000035473 Communicable disease Diseases 0.000 description 1
- 229910021595 Copper(I) iodide Inorganic materials 0.000 description 1
- 229920000742 Cotton Polymers 0.000 description 1
- 229920002785 Croscarmellose sodium Polymers 0.000 description 1
- 102100034770 Cyclin-dependent kinase inhibitor 3 Human genes 0.000 description 1
- NOOLISFMXDJSKH-UHFFFAOYSA-N DL-menthol Natural products CC(C)C1CCC(C)CC1O NOOLISFMXDJSKH-UHFFFAOYSA-N 0.000 description 1
- 230000004544 DNA amplification Effects 0.000 description 1
- 102100024829 DNA polymerase delta catalytic subunit Human genes 0.000 description 1
- 229940124087 DNA topoisomerase II inhibitor Drugs 0.000 description 1
- XMSXQFUHVRWGNA-UHFFFAOYSA-N Decamethylcyclopentasiloxane Chemical compound C[Si]1(C)O[Si](C)(C)O[Si](C)(C)O[Si](C)(C)O[Si](C)(C)O1 XMSXQFUHVRWGNA-UHFFFAOYSA-N 0.000 description 1
- 239000004287 Dehydroacetic acid Substances 0.000 description 1
- 208000001490 Dengue Diseases 0.000 description 1
- 206010012310 Dengue fever Diseases 0.000 description 1
- 241000725619 Dengue virus Species 0.000 description 1
- 201000004624 Dermatitis Diseases 0.000 description 1
- 206010012438 Dermatitis atopic Diseases 0.000 description 1
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 1
- 239000004338 Dichlorodifluoromethane Substances 0.000 description 1
- XBPCUCUWBYBCDP-UHFFFAOYSA-N Dicyclohexylamine Chemical class C1CCCCC1NC1CCCCC1 XBPCUCUWBYBCDP-UHFFFAOYSA-N 0.000 description 1
- LVGKNOAMLMIIKO-UHFFFAOYSA-N Elaidinsaeure-aethylester Natural products CCCCCCCCC=CCCCCCCCC(=O)OCC LVGKNOAMLMIIKO-UHFFFAOYSA-N 0.000 description 1
- 241000283086 Equidae Species 0.000 description 1
- VGGSQFUCUMXWEO-UHFFFAOYSA-N Ethene Chemical compound C=C VGGSQFUCUMXWEO-UHFFFAOYSA-N 0.000 description 1
- 239000005977 Ethylene Substances 0.000 description 1
- 108010074860 Factor Xa Proteins 0.000 description 1
- 241000282326 Felis catus Species 0.000 description 1
- 229910004373 HOAc Inorganic materials 0.000 description 1
- 241000711549 Hepacivirus C Species 0.000 description 1
- 208000005176 Hepatitis C Diseases 0.000 description 1
- 208000009889 Herpes Simplex Diseases 0.000 description 1
- 208000021519 Hodgkin lymphoma Diseases 0.000 description 1
- 101000868333 Homo sapiens Cyclin-dependent kinase 1 Proteins 0.000 description 1
- 101000945639 Homo sapiens Cyclin-dependent kinase inhibitor 3 Proteins 0.000 description 1
- 101000909198 Homo sapiens DNA polymerase delta catalytic subunit Proteins 0.000 description 1
- 101000991619 Homo sapiens Meprin A subunit alpha Proteins 0.000 description 1
- 101000939500 Homo sapiens UBX domain-containing protein 11 Proteins 0.000 description 1
- CPELXLSAUQHCOX-UHFFFAOYSA-N Hydrogen bromide Chemical class Br CPELXLSAUQHCOX-UHFFFAOYSA-N 0.000 description 1
- 239000004354 Hydroxyethyl cellulose Substances 0.000 description 1
- 229920000663 Hydroxyethyl cellulose Polymers 0.000 description 1
- 244000018716 Impatiens biflora Species 0.000 description 1
- 206010061218 Inflammation Diseases 0.000 description 1
- 108010047761 Interferon-alpha Proteins 0.000 description 1
- 102000006992 Interferon-alpha Human genes 0.000 description 1
- 108010050904 Interferons Proteins 0.000 description 1
- 102000014150 Interferons Human genes 0.000 description 1
- RRHGJUQNOFWUDK-UHFFFAOYSA-N Isoprene Chemical compound CC(=C)C=C RRHGJUQNOFWUDK-UHFFFAOYSA-N 0.000 description 1
- 208000008839 Kidney Neoplasms Diseases 0.000 description 1
- 150000000994 L-ascorbates Chemical class 0.000 description 1
- QAQJMLQRFWZOBN-LAUBAEHRSA-N L-ascorbyl-6-palmitate Chemical compound CCCCCCCCCCCCCCCC(=O)OC[C@H](O)[C@H]1OC(=O)C(O)=C1O QAQJMLQRFWZOBN-LAUBAEHRSA-N 0.000 description 1
- 239000011786 L-ascorbyl-6-palmitate Substances 0.000 description 1
- 239000005517 L01XE01 - Imatinib Substances 0.000 description 1
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 1
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 1
- 239000004472 Lysine Substances 0.000 description 1
- LTYOQGRJFJAKNA-KKIMTKSISA-N Malonyl CoA Natural products S(C(=O)CC(=O)O)CCNC(=O)CCNC(=O)[C@@H](O)C(CO[P@](=O)(O[P@](=O)(OC[C@H]1[C@@H](OP(=O)(O)O)[C@@H](O)[C@@H](n2c3ncnc(N)c3nc2)O1)O)O)(C)C LTYOQGRJFJAKNA-KKIMTKSISA-N 0.000 description 1
- 239000005913 Maltodextrin Substances 0.000 description 1
- 229920002774 Maltodextrin Polymers 0.000 description 1
- 208000025205 Mantle-Cell Lymphoma Diseases 0.000 description 1
- 235000010654 Melissa officinalis Nutrition 0.000 description 1
- 244000062730 Melissa officinalis Species 0.000 description 1
- 235000006679 Mentha X verticillata Nutrition 0.000 description 1
- 235000002899 Mentha suaveolens Nutrition 0.000 description 1
- 235000001636 Mentha x rotundifolia Nutrition 0.000 description 1
- 102100030882 Meprin A subunit alpha Human genes 0.000 description 1
- 229920001410 Microfiber Polymers 0.000 description 1
- 229930192392 Mitomycin Natural products 0.000 description 1
- 208000034578 Multiple myelomas Diseases 0.000 description 1
- 241000699670 Mus sp. Species 0.000 description 1
- 208000031888 Mycoses Diseases 0.000 description 1
- 201000003793 Myelodysplastic syndrome Diseases 0.000 description 1
- 208000033761 Myelogenous Chronic BCR-ABL Positive Leukemia Diseases 0.000 description 1
- 208000033776 Myeloid Acute Leukemia Diseases 0.000 description 1
- ZKGNPQKYVKXMGJ-UHFFFAOYSA-N N,N-dimethylacetamide Chemical compound CN(C)C(C)=O.CN(C)C(C)=O ZKGNPQKYVKXMGJ-UHFFFAOYSA-N 0.000 description 1
- STGAXYQOLVTZAC-UHFFFAOYSA-N N-[3-[4-(piperazine-1-carbonyl)phenyl]phenyl]cyclopentanecarboxamide 2,2,2-trifluoroacetic acid Chemical compound FC(C(=O)O)(F)F.N1(CCNCC1)C(=O)C1=CC=C(C=C1)C1=CC(=CC=C1)NC(=O)C1CCCC1 STGAXYQOLVTZAC-UHFFFAOYSA-N 0.000 description 1
- SFECXPKUPYVYGA-UHFFFAOYSA-N N-[3-[4-[4-(1-hydroxycyclopropanecarbonyl)piperazine-1-carbonyl]phenyl]phenyl]benzenesulfonamide Chemical compound OC1(CC1)C(=O)N1CCN(CC1)C(=O)c1ccc(cc1)-c1cccc(NS(=O)(=O)c2ccccc2)c1 SFECXPKUPYVYGA-UHFFFAOYSA-N 0.000 description 1
- ABIGCEHAQPIQQF-UHFFFAOYSA-N N-[3-[4-[4-(1-hydroxycyclopropanecarbonyl)piperazine-1-carbonyl]phenyl]phenyl]oxetane-3-carboxamide Chemical compound OC1(CC1)C(=O)N1CCN(CC1)C(=O)c1ccc(cc1)-c1cccc(NC(=O)C2COC2)c1 ABIGCEHAQPIQQF-UHFFFAOYSA-N 0.000 description 1
- GGAWQZOUPGIWJO-UHFFFAOYSA-N N-[6-[4-(piperazine-1-carbonyl)phenyl]-1,2-benzoxazol-3-yl]cyclopropanecarboxamide Chemical compound O=C(Nc1noc2cc(ccc12)-c1ccc(cc1)C(=O)N1CCNCC1)C1CC1 GGAWQZOUPGIWJO-UHFFFAOYSA-N 0.000 description 1
- HXKLKALJFKEUER-UHFFFAOYSA-N N-[6-[4-[4-(1-hydroxycyclopropanecarbonyl)piperazine-1-carbonyl]phenyl]-1,2-benzoxazol-3-yl]cyclopropanecarboxamide Chemical compound OC1(CC1)C(=O)N1CCN(CC1)C(=O)c1ccc(cc1)-c1ccc2c(NC(=O)C3CC3)noc2c1 HXKLKALJFKEUER-UHFFFAOYSA-N 0.000 description 1
- 238000005481 NMR spectroscopy Methods 0.000 description 1
- 208000012902 Nervous system disease Diseases 0.000 description 1
- 208000025966 Neurological disease Diseases 0.000 description 1
- GRYLNZFGIOXLOG-UHFFFAOYSA-N Nitric acid Chemical compound O[N+]([O-])=O GRYLNZFGIOXLOG-UHFFFAOYSA-N 0.000 description 1
- 239000005642 Oleic acid Substances 0.000 description 1
- ZQPPMHVWECSIRJ-UHFFFAOYSA-N Oleic acid Natural products CCCCCCCCC=CCCCCCCCC(O)=O ZQPPMHVWECSIRJ-UHFFFAOYSA-N 0.000 description 1
- 241000283973 Oryctolagus cuniculus Species 0.000 description 1
- 208000012868 Overgrowth Diseases 0.000 description 1
- YYVFXSYQSOZCOQ-UHFFFAOYSA-N Oxyquinoline sulfate Chemical compound [O-]S([O-])(=O)=O.C1=C[NH+]=C2C(O)=CC=CC2=C1.C1=C[NH+]=C2C(O)=CC=CC2=C1 YYVFXSYQSOZCOQ-UHFFFAOYSA-N 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- 241000282579 Pan Species 0.000 description 1
- 101150003085 Pdcl gene Proteins 0.000 description 1
- 241001494479 Pecora Species 0.000 description 1
- 101710179684 Poly [ADP-ribose] polymerase Proteins 0.000 description 1
- 102100023712 Poly [ADP-ribose] polymerase 1 Human genes 0.000 description 1
- 229940127397 Poly(ADP-Ribose) Polymerase Inhibitors Drugs 0.000 description 1
- 108010039918 Polylysine Proteins 0.000 description 1
- 229920002685 Polyoxyl 35CastorOil Polymers 0.000 description 1
- 239000004372 Polyvinyl alcohol Substances 0.000 description 1
- XBDQKXXYIPTUBI-UHFFFAOYSA-N Propionic acid Chemical class CCC(O)=O XBDQKXXYIPTUBI-UHFFFAOYSA-N 0.000 description 1
- HDSBZMRLPLPFLQ-UHFFFAOYSA-N Propylene glycol alginate Chemical compound OC1C(O)C(OC)OC(C(O)=O)C1OC1C(O)C(O)C(C)C(C(=O)OCC(C)O)O1 HDSBZMRLPLPFLQ-UHFFFAOYSA-N 0.000 description 1
- 201000004681 Psoriasis Diseases 0.000 description 1
- 201000001263 Psoriatic Arthritis Diseases 0.000 description 1
- 208000036824 Psoriatic arthropathy Diseases 0.000 description 1
- 241000700159 Rattus Species 0.000 description 1
- 206010038389 Renal cancer Diseases 0.000 description 1
- 208000017442 Retinal disease Diseases 0.000 description 1
- 206010038923 Retinopathy Diseases 0.000 description 1
- 206010038997 Retroviral infections Diseases 0.000 description 1
- 241000283984 Rodentia Species 0.000 description 1
- WINXNKPZLFISPD-UHFFFAOYSA-M Saccharin sodium Chemical compound [Na+].C1=CC=C2C(=O)[N-]S(=O)(=O)C2=C1 WINXNKPZLFISPD-UHFFFAOYSA-M 0.000 description 1
- VMHLLURERBWHNL-UHFFFAOYSA-M Sodium acetate Chemical compound [Na+].CC([O-])=O VMHLLURERBWHNL-UHFFFAOYSA-M 0.000 description 1
- UIIMBOGNXHQVGW-DEQYMQKBSA-M Sodium bicarbonate-14C Chemical compound [Na+].O[14C]([O-])=O UIIMBOGNXHQVGW-DEQYMQKBSA-M 0.000 description 1
- 239000004288 Sodium dehydroacetate Substances 0.000 description 1
- 229920002125 Sokalan® Polymers 0.000 description 1
- 235000021355 Stearic acid Nutrition 0.000 description 1
- 208000006011 Stroke Diseases 0.000 description 1
- 241000282887 Suidae Species 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-L Sulfate Chemical compound [O-]S([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 description 1
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical group [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 1
- 206010042971 T-cell lymphoma Diseases 0.000 description 1
- 208000027585 T-cell non-Hodgkin lymphoma Diseases 0.000 description 1
- FEWJPZIEWOKRBE-UHFFFAOYSA-N Tartaric acid Natural products [H+].[H+].[O-]C(=O)C(O)C(O)C([O-])=O FEWJPZIEWOKRBE-UHFFFAOYSA-N 0.000 description 1
- 229940123237 Taxane Drugs 0.000 description 1
- BHEOSNUKNHRBNM-UHFFFAOYSA-N Tetramethylsqualene Natural products CC(=C)C(C)CCC(=C)C(C)CCC(C)=CCCC=C(C)CCC(C)C(=C)CCC(C)C(C)=C BHEOSNUKNHRBNM-UHFFFAOYSA-N 0.000 description 1
- 235000011941 Tilia x europaea Nutrition 0.000 description 1
- 239000000317 Topoisomerase II Inhibitor Substances 0.000 description 1
- 229920001615 Tragacanth Polymers 0.000 description 1
- 102000004357 Transferases Human genes 0.000 description 1
- 108090000992 Transferases Proteins 0.000 description 1
- DOOTYTYQINUNNV-UHFFFAOYSA-N Triethyl citrate Chemical compound CCOC(=O)CC(O)(C(=O)OCC)CC(=O)OCC DOOTYTYQINUNNV-UHFFFAOYSA-N 0.000 description 1
- 102000004243 Tubulin Human genes 0.000 description 1
- 108090000704 Tubulin Proteins 0.000 description 1
- 102100029645 UBX domain-containing protein 11 Human genes 0.000 description 1
- 206010046431 Urethral cancer Diseases 0.000 description 1
- 206010046458 Urethral neoplasms Diseases 0.000 description 1
- 229920002494 Zein Polymers 0.000 description 1
- KQZMDIOMSLHLAO-AWEZNQCLSA-N [(3S)-4-(1-aminocyclopropanecarbonyl)-3-methylpiperazin-1-yl]-[4-(6-fluoro-1,3-benzoxazol-2-yl)phenyl]methanone Chemical compound C[C@H]1CN(CCN1C(=O)C1(N)CC1)C(=O)c1ccc(cc1)-c1nc2ccc(F)cc2o1 KQZMDIOMSLHLAO-AWEZNQCLSA-N 0.000 description 1
- LVMIVPMOEXVLLL-HNNXBMFYSA-N [2-fluoro-4-(1-methylbenzimidazol-5-yl)phenyl]-[(3S)-4-(1-hydroxycyclopropanecarbonyl)-3-methylpiperazin-1-yl]methanone Chemical compound FC1=C(C(=O)N2C[C@@H](N(CC2)C(=O)C2(CC2)O)C)C=CC(=C1)C1=CC2=C(N(C=N2)C)C=C1 LVMIVPMOEXVLLL-HNNXBMFYSA-N 0.000 description 1
- YLUWMFFJWBOBIE-UHFFFAOYSA-N [2-fluoro-4-(6-fluoro-1,3-benzoxazol-2-yl)phenyl]-piperazin-1-ylmethanone Chemical compound Fc1ccc2nc(oc2c1)-c1ccc(C(=O)N2CCNCC2)c(F)c1 YLUWMFFJWBOBIE-UHFFFAOYSA-N 0.000 description 1
- BPBUDVIJYFCWSO-UHFFFAOYSA-N [4-(1,3-benzothiazol-5-yl)phenyl]-[4-(1-hydroxycyclopropanecarbonyl)piperazin-1-yl]methanone Chemical compound C1CN(C(=O)C=2C=CC(=CC=2)C=2C=C3N=CSC3=CC=2)CCN1C(=O)C1(O)CC1 BPBUDVIJYFCWSO-UHFFFAOYSA-N 0.000 description 1
- XJGSRVMXYLPVLR-UHFFFAOYSA-N [4-(1-hydroxycyclopropanecarbonyl)piperazin-1-yl]-[4-[1-(2-hydroxyethyl)benzimidazol-5-yl]phenyl]methanone Chemical compound OCCn1cnc2cc(ccc12)-c1ccc(cc1)C(=O)N1CCN(CC1)C(=O)C1(O)CC1 XJGSRVMXYLPVLR-UHFFFAOYSA-N 0.000 description 1
- MLYISDFOYXANRF-UHFFFAOYSA-N [4-(1-methyl-2,3-dihydrobenzotriazol-5-yl)phenyl]-piperazin-1-ylmethanone Chemical compound CN1NNc2cc(ccc12)-c1ccc(cc1)C(=O)N1CCNCC1 MLYISDFOYXANRF-UHFFFAOYSA-N 0.000 description 1
- PXLXFVMFSLYXNN-UHFFFAOYSA-N [4-(1-methylbenzimidazol-5-yl)phenyl]-piperazin-1-ylmethanone hydrochloride Chemical compound Cl.CN1C=NC2=C1C=CC(=C2)C2=CC=C(C=C2)C(=O)N2CCNCC2 PXLXFVMFSLYXNN-UHFFFAOYSA-N 0.000 description 1
- XMCWEQOJAAPVOB-UHFFFAOYSA-N [4-(1H-benzimidazol-2-yl)phenyl]-[4-(1-hydroxycyclopropanecarbonyl)piperazin-1-yl]methanone Chemical compound OC1(CC1)C(=O)N1CCN(CC1)C(=O)c1ccc(cc1)-c1nc2ccccc2[nH]1 XMCWEQOJAAPVOB-UHFFFAOYSA-N 0.000 description 1
- WCZKKBQNZDWHJU-UHFFFAOYSA-N [4-(2,3-dihydroindol-1-yl)phenyl]-[4-(1-hydroxycyclopropanecarbonyl)piperazin-1-yl]methanone Chemical compound OC1(CC1)C(=O)N1CCN(CC1)C(=O)C1=CC=C(C=C1)N1CCC2=CC=CC=C12 WCZKKBQNZDWHJU-UHFFFAOYSA-N 0.000 description 1
- KOJFSLRUOVKUJT-UHFFFAOYSA-N [4-(2,3-dihydroindol-1-yl)phenyl]-piperazin-1-ylmethanone Chemical compound O=C(N1CCNCC1)C1=CC=C(C=C1)N1CCC2=C1C=CC=C2 KOJFSLRUOVKUJT-UHFFFAOYSA-N 0.000 description 1
- WWHRDJGZCQDBBJ-UHFFFAOYSA-N [4-(2,3-dihydroindol-1-yl)phenyl]-piperazin-1-ylmethanone hydrochloride Chemical compound Cl.O=C(N1CCNCC1)c1ccc(cc1)N1CCc2ccccc12 WWHRDJGZCQDBBJ-UHFFFAOYSA-N 0.000 description 1
- IECDNNCRJOGNKW-UHFFFAOYSA-N [4-(3,4-dihydro-2H-quinolin-1-yl)phenyl]-[4-(1-hydroxycyclopropanecarbonyl)piperazin-1-yl]methanone Chemical compound N1(CCCC2=CC=CC=C12)C1=CC=C(C(=O)N2CCN(CC2)C(=O)C2(CC2)O)C=C1 IECDNNCRJOGNKW-UHFFFAOYSA-N 0.000 description 1
- SKJXFRUJBFGFJS-UHFFFAOYSA-N [4-(3-aminophenyl)phenyl]-[4-(1-hydroxycyclopropanecarbonyl)piperazin-1-yl]methanone Chemical compound Nc1cccc(c1)-c1ccc(cc1)C(=O)N1CCN(CC1)C(=O)C1(O)CC1 SKJXFRUJBFGFJS-UHFFFAOYSA-N 0.000 description 1
- FMJZPEDJPSOLJS-UHFFFAOYSA-N [4-(3-methylindazol-1-yl)phenyl]-piperazin-1-ylmethanone Chemical compound CC1=NN(C2=CC=CC=C12)C1=CC=C(C=C1)C(=O)N1CCNCC1 FMJZPEDJPSOLJS-UHFFFAOYSA-N 0.000 description 1
- DFWSSPIULMTINI-UHFFFAOYSA-N [4-(4-chloro-2-fluorophenyl)-2-fluorophenyl]-piperazin-1-ylmethanone Chemical compound Fc1cc(ccc1C(=O)N1CCNCC1)-c1ccc(Cl)cc1F DFWSSPIULMTINI-UHFFFAOYSA-N 0.000 description 1
- NBLJFIOBIPULHX-UHFFFAOYSA-N [4-(4-chloro-2-fluorophenyl)phenyl]-[4-(1-hydroxycyclopropanecarbonyl)piperazin-1-yl]methanone Chemical compound C1CN(C(=O)C=2C=CC(=CC=2)C=2C(=CC(Cl)=CC=2)F)CCN1C(=O)C1(O)CC1 NBLJFIOBIPULHX-UHFFFAOYSA-N 0.000 description 1
- CEMHUQUXZOHUBY-UHFFFAOYSA-N [4-(5-chloro-1,3-benzoxazol-2-yl)phenyl]-piperazin-1-ylmethanone 2,2,2-trifluoroacetic acid Chemical compound FC(C(=O)O)(F)F.ClC=1C=CC2=C(N=C(O2)C2=CC=C(C=C2)C(=O)N2CCNCC2)C1 CEMHUQUXZOHUBY-UHFFFAOYSA-N 0.000 description 1
- LJJBJECKHAIPNO-UHFFFAOYSA-N [4-[4-[(2-methylpropan-2-yl)oxycarbonyl]piperazine-1-carbonyl]phenyl]boronic acid Chemical compound C1CN(C(=O)OC(C)(C)C)CCN1C(=O)C1=CC=C(B(O)O)C=C1 LJJBJECKHAIPNO-UHFFFAOYSA-N 0.000 description 1
- 150000001242 acetic acid derivatives Chemical class 0.000 description 1
- PHENPABYBHPABM-UHFFFAOYSA-N acetic acid;octane Chemical compound CC(O)=O.CCCCCCCC PHENPABYBHPABM-UHFFFAOYSA-N 0.000 description 1
- 150000008043 acidic salts Chemical class 0.000 description 1
- 239000002535 acidifier Substances 0.000 description 1
- 150000007513 acids Chemical class 0.000 description 1
- 229920006243 acrylic copolymer Polymers 0.000 description 1
- 239000004480 active ingredient Substances 0.000 description 1
- 230000001154 acute effect Effects 0.000 description 1
- 239000008272 agar Substances 0.000 description 1
- 235000010419 agar Nutrition 0.000 description 1
- 229910052783 alkali metal Inorganic materials 0.000 description 1
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 1
- 230000003113 alkalizing effect Effects 0.000 description 1
- 229920013820 alkyl cellulose Polymers 0.000 description 1
- 150000001350 alkyl halides Chemical class 0.000 description 1
- 229940100198 alkylating agent Drugs 0.000 description 1
- 239000002168 alkylating agent Substances 0.000 description 1
- 239000008168 almond oil Substances 0.000 description 1
- 231100000360 alopecia Toxicity 0.000 description 1
- HSFWRNGVRCDJHI-UHFFFAOYSA-N alpha-acetylene Natural products C#C HSFWRNGVRCDJHI-UHFFFAOYSA-N 0.000 description 1
- BJEPYKJPYRNKOW-UHFFFAOYSA-N alpha-hydroxysuccinic acid Natural products OC(=O)C(O)CC(O)=O BJEPYKJPYRNKOW-UHFFFAOYSA-N 0.000 description 1
- 230000004075 alteration Effects 0.000 description 1
- 235000012211 aluminium silicate Nutrition 0.000 description 1
- 229940009868 aluminum magnesium silicate Drugs 0.000 description 1
- WMGSQTMJHBYJMQ-UHFFFAOYSA-N aluminum;magnesium;silicate Chemical compound [Mg+2].[Al+3].[O-][Si]([O-])([O-])[O-] WMGSQTMJHBYJMQ-UHFFFAOYSA-N 0.000 description 1
- 150000001408 amides Chemical class 0.000 description 1
- 150000001413 amino acids Chemical class 0.000 description 1
- 235000019257 ammonium acetate Nutrition 0.000 description 1
- 229940043376 ammonium acetate Drugs 0.000 description 1
- 229910000148 ammonium phosphate Inorganic materials 0.000 description 1
- 235000019289 ammonium phosphates Nutrition 0.000 description 1
- 150000003863 ammonium salts Chemical class 0.000 description 1
- 229940011037 anethole Drugs 0.000 description 1
- 238000010171 animal model Methods 0.000 description 1
- 230000000340 anti-metabolite Effects 0.000 description 1
- 230000000845 anti-microbial effect Effects 0.000 description 1
- 230000000118 anti-neoplastic effect Effects 0.000 description 1
- 230000001028 anti-proliverative effect Effects 0.000 description 1
- 230000000840 anti-viral effect Effects 0.000 description 1
- 239000000729 antidote Substances 0.000 description 1
- 239000002518 antifoaming agent Substances 0.000 description 1
- 229940100197 antimetabolite Drugs 0.000 description 1
- 239000002256 antimetabolite Substances 0.000 description 1
- 229940058303 antinematodal benzimidazole derivative Drugs 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 235000006708 antioxidants Nutrition 0.000 description 1
- 239000012736 aqueous medium Substances 0.000 description 1
- BTFJIXJJCSYFAL-UHFFFAOYSA-N arachidyl alcohol Natural products CCCCCCCCCCCCCCCCCCCCO BTFJIXJJCSYFAL-UHFFFAOYSA-N 0.000 description 1
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 1
- 206010003246 arthritis Diseases 0.000 description 1
- 150000001543 aryl boronic acids Chemical class 0.000 description 1
- 150000001502 aryl halides Chemical class 0.000 description 1
- 239000011668 ascorbic acid Substances 0.000 description 1
- 229960005070 ascorbic acid Drugs 0.000 description 1
- 235000010385 ascorbyl palmitate Nutrition 0.000 description 1
- 239000000605 aspartame Substances 0.000 description 1
- IAOZJIPTCAWIRG-QWRGUYRKSA-N aspartame Chemical compound OC(=O)C[C@H](N)C(=O)N[C@H](C(=O)OC)CC1=CC=CC=C1 IAOZJIPTCAWIRG-QWRGUYRKSA-N 0.000 description 1
- 235000010357 aspartame Nutrition 0.000 description 1
- 229960003438 aspartame Drugs 0.000 description 1
- 208000006673 asthma Diseases 0.000 description 1
- 239000000305 astragalus gummifer gum Substances 0.000 description 1
- 201000008937 atopic dermatitis Diseases 0.000 description 1
- 230000003190 augmentative effect Effects 0.000 description 1
- XLSIIHKGLGJRGO-UHFFFAOYSA-N azane;benzenesulfinic acid Chemical compound [NH4+].[O-]S(=O)C1=CC=CC=C1 XLSIIHKGLGJRGO-UHFFFAOYSA-N 0.000 description 1
- 230000003385 bacteriostatic effect Effects 0.000 description 1
- 239000008228 bacteriostatic water for injection Substances 0.000 description 1
- RQPZNWPYLFFXCP-UHFFFAOYSA-L barium dihydroxide Chemical compound [OH-].[OH-].[Ba+2] RQPZNWPYLFFXCP-UHFFFAOYSA-L 0.000 description 1
- 229910001863 barium hydroxide Inorganic materials 0.000 description 1
- 150000007514 bases Chemical class 0.000 description 1
- SRSXLGNVWSONIS-UHFFFAOYSA-N benzenesulfonic acid Chemical class OS(=O)(=O)C1=CC=CC=C1 SRSXLGNVWSONIS-UHFFFAOYSA-N 0.000 description 1
- CSKNSYBAZOQPLR-UHFFFAOYSA-N benzenesulfonyl chloride Chemical compound ClS(=O)(=O)C1=CC=CC=C1 CSKNSYBAZOQPLR-UHFFFAOYSA-N 0.000 description 1
- 229960003872 benzethonium Drugs 0.000 description 1
- UREZNYTWGJKWBI-UHFFFAOYSA-M benzethonium chloride Chemical compound [Cl-].C1=CC(C(C)(C)CC(C)(C)C)=CC=C1OCCOCC[N+](C)(C)CC1=CC=CC=C1 UREZNYTWGJKWBI-UHFFFAOYSA-M 0.000 description 1
- 150000001556 benzimidazoles Chemical class 0.000 description 1
- 229940050390 benzoate Drugs 0.000 description 1
- 229960004365 benzoic acid Drugs 0.000 description 1
- 150000001558 benzoic acid derivatives Chemical class 0.000 description 1
- BIEORKAUAONTHC-UHFFFAOYSA-N benzyl 4,7-diazaspiro[2.5]octane-7-carboxylate hydrochloride Chemical compound Cl.O=C(OCc1ccccc1)N1CCNC2(CC2)C1 BIEORKAUAONTHC-UHFFFAOYSA-N 0.000 description 1
- 229960002903 benzyl benzoate Drugs 0.000 description 1
- HSDAJNMJOMSNEV-UHFFFAOYSA-N benzyl chloroformate Chemical compound ClC(=O)OCC1=CC=CC=C1 HSDAJNMJOMSNEV-UHFFFAOYSA-N 0.000 description 1
- CTOUWUYDDUSBQE-UHFFFAOYSA-N benzyl piperazine-1-carboxylate Chemical compound C1CNCCN1C(=O)OCC1=CC=CC=C1 CTOUWUYDDUSBQE-UHFFFAOYSA-N 0.000 description 1
- 150000005347 biaryls Chemical class 0.000 description 1
- 229960000997 bicalutamide Drugs 0.000 description 1
- 230000033228 biological regulation Effects 0.000 description 1
- IPWKHHSGDUIRAH-UHFFFAOYSA-N bis(pinacolato)diboron Chemical compound O1C(C)(C)C(C)(C)OB1B1OC(C)(C)C(C)(C)O1 IPWKHHSGDUIRAH-UHFFFAOYSA-N 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-M bisulphate group Chemical group S([O-])(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-M 0.000 description 1
- 210000000988 bone and bone Anatomy 0.000 description 1
- 229910021538 borax Inorganic materials 0.000 description 1
- KGBXLFKZBHKPEV-UHFFFAOYSA-N boric acid Chemical compound OB(O)O KGBXLFKZBHKPEV-UHFFFAOYSA-N 0.000 description 1
- 239000004327 boric acid Substances 0.000 description 1
- 235000010338 boric acid Nutrition 0.000 description 1
- 150000001642 boronic acid derivatives Chemical class 0.000 description 1
- 210000000133 brain stem Anatomy 0.000 description 1
- 210000000481 breast Anatomy 0.000 description 1
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 1
- 229910052794 bromium Inorganic materials 0.000 description 1
- 239000006172 buffering agent Substances 0.000 description 1
- 229960002092 busulfan Drugs 0.000 description 1
- 239000001273 butane Substances 0.000 description 1
- 150000004648 butanoic acid derivatives Chemical class 0.000 description 1
- 125000004369 butenyl group Chemical group C(=CCC)* 0.000 description 1
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 235000019282 butylated hydroxyanisole Nutrition 0.000 description 1
- 229940043253 butylated hydroxyanisole Drugs 0.000 description 1
- CZBZUDVBLSSABA-UHFFFAOYSA-N butylated hydroxyanisole Chemical compound COC1=CC=C(O)C(C(C)(C)C)=C1.COC1=CC=C(O)C=C1C(C)(C)C CZBZUDVBLSSABA-UHFFFAOYSA-N 0.000 description 1
- 235000010354 butylated hydroxytoluene Nutrition 0.000 description 1
- 229940095259 butylated hydroxytoluene Drugs 0.000 description 1
- 229940067596 butylparaben Drugs 0.000 description 1
- 125000000480 butynyl group Chemical group [*]C#CC([H])([H])C([H])([H])[H] 0.000 description 1
- 229910052792 caesium Inorganic materials 0.000 description 1
- 239000001110 calcium chloride Substances 0.000 description 1
- 229910001628 calcium chloride Inorganic materials 0.000 description 1
- UHHRFSOMMCWGSO-UHFFFAOYSA-L calcium glycerophosphate Chemical compound [Ca+2].OCC(CO)OP([O-])([O-])=O UHHRFSOMMCWGSO-UHFFFAOYSA-L 0.000 description 1
- 229940095618 calcium glycerophosphate Drugs 0.000 description 1
- 235000019299 calcium glycerylphosphate Nutrition 0.000 description 1
- FUFJGUQYACFECW-UHFFFAOYSA-L calcium hydrogenphosphate Chemical compound [Ca+2].OP([O-])([O-])=O FUFJGUQYACFECW-UHFFFAOYSA-L 0.000 description 1
- MKJXYGKVIBWPFZ-UHFFFAOYSA-L calcium lactate Chemical compound [Ca+2].CC(O)C([O-])=O.CC(O)C([O-])=O MKJXYGKVIBWPFZ-UHFFFAOYSA-L 0.000 description 1
- 239000001527 calcium lactate Substances 0.000 description 1
- 229960002401 calcium lactate Drugs 0.000 description 1
- 235000011086 calcium lactate Nutrition 0.000 description 1
- 239000001506 calcium phosphate Substances 0.000 description 1
- 239000000378 calcium silicate Substances 0.000 description 1
- 229910052918 calcium silicate Inorganic materials 0.000 description 1
- CJZGTCYPCWQAJB-UHFFFAOYSA-L calcium stearate Chemical compound [Ca+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O CJZGTCYPCWQAJB-UHFFFAOYSA-L 0.000 description 1
- 235000013539 calcium stearate Nutrition 0.000 description 1
- 239000008116 calcium stearate Substances 0.000 description 1
- 229940078456 calcium stearate Drugs 0.000 description 1
- LNMAXKMUGYXKPJ-UHFFFAOYSA-L calcium;1,1-dioxo-1,2-benzothiazol-2-id-3-one Chemical compound [Ca+2].C1=CC=C2C([O-])=NS(=O)(=O)C2=C1.C1=CC=C2C([O-])=NS(=O)(=O)C2=C1 LNMAXKMUGYXKPJ-UHFFFAOYSA-L 0.000 description 1
- OYACROKNLOSFPA-UHFFFAOYSA-N calcium;dioxido(oxo)silane Chemical compound [Ca+2].[O-][Si]([O-])=O OYACROKNLOSFPA-UHFFFAOYSA-N 0.000 description 1
- MIOPJNTWMNEORI-UHFFFAOYSA-N camphorsulfonic acid Chemical class C1CC2(CS(O)(=O)=O)C(=O)CC1C2(C)C MIOPJNTWMNEORI-UHFFFAOYSA-N 0.000 description 1
- 229960004117 capecitabine Drugs 0.000 description 1
- 235000013736 caramel Nutrition 0.000 description 1
- 125000001951 carbamoylamino group Chemical group C(N)(=O)N* 0.000 description 1
- 229960001631 carbomer Drugs 0.000 description 1
- 150000001721 carbon Chemical group 0.000 description 1
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 1
- 235000010948 carboxy methyl cellulose Nutrition 0.000 description 1
- 150000001732 carboxylic acid derivatives Chemical class 0.000 description 1
- 150000001735 carboxylic acids Chemical class 0.000 description 1
- 229920003123 carboxymethyl cellulose sodium Polymers 0.000 description 1
- 239000008112 carboxymethyl-cellulose Substances 0.000 description 1
- 229940105329 carboxymethylcellulose Drugs 0.000 description 1
- 229940063834 carboxymethylcellulose sodium Drugs 0.000 description 1
- 210000000748 cardiovascular system Anatomy 0.000 description 1
- 239000004203 carnauba wax Substances 0.000 description 1
- 235000013869 carnauba wax Nutrition 0.000 description 1
- 239000003054 catalyst Substances 0.000 description 1
- 230000032823 cell division Effects 0.000 description 1
- 230000023549 cell-cell signaling Effects 0.000 description 1
- 230000019522 cellular metabolic process Effects 0.000 description 1
- 235000010980 cellulose Nutrition 0.000 description 1
- 229920002678 cellulose Polymers 0.000 description 1
- 239000001913 cellulose Substances 0.000 description 1
- 229940081734 cellulose acetate phthalate Drugs 0.000 description 1
- 201000007455 central nervous system cancer Diseases 0.000 description 1
- 210000003679 cervix uteri Anatomy 0.000 description 1
- 229960000541 cetyl alcohol Drugs 0.000 description 1
- 229960001927 cetylpyridinium chloride Drugs 0.000 description 1
- YMKDRGPMQRFJGP-UHFFFAOYSA-M cetylpyridinium chloride Chemical compound [Cl-].CCCCCCCCCCCCCCCC[N+]1=CC=CC=C1 YMKDRGPMQRFJGP-UHFFFAOYSA-M 0.000 description 1
- 239000003610 charcoal Substances 0.000 description 1
- 239000002738 chelating agent Substances 0.000 description 1
- 230000000973 chemotherapeutic effect Effects 0.000 description 1
- 238000004296 chiral HPLC Methods 0.000 description 1
- 229960004926 chlorobutanol Drugs 0.000 description 1
- 229960002242 chlorocresol Drugs 0.000 description 1
- 235000012000 cholesterol Nutrition 0.000 description 1
- 238000004587 chromatography analysis Methods 0.000 description 1
- 150000001860 citric acid derivatives Chemical class 0.000 description 1
- 239000011248 coating agent Substances 0.000 description 1
- 210000001072 colon Anatomy 0.000 description 1
- 239000003086 colorant Substances 0.000 description 1
- 239000012230 colorless oil Substances 0.000 description 1
- 238000011284 combination treatment Methods 0.000 description 1
- 239000008139 complexing agent Substances 0.000 description 1
- 235000009508 confectionery Nutrition 0.000 description 1
- 239000000470 constituent Substances 0.000 description 1
- 230000001276 controlling effect Effects 0.000 description 1
- 239000010949 copper Substances 0.000 description 1
- LSXDOTMGLUJQCM-UHFFFAOYSA-M copper(i) iodide Chemical compound I[Cu] LSXDOTMGLUJQCM-UHFFFAOYSA-M 0.000 description 1
- 235000012343 cottonseed oil Nutrition 0.000 description 1
- 239000002385 cottonseed oil Substances 0.000 description 1
- 239000006071 cream Substances 0.000 description 1
- 229930003836 cresol Natural products 0.000 description 1
- 229940013361 cresol Drugs 0.000 description 1
- 229960001681 croscarmellose sodium Drugs 0.000 description 1
- 235000010947 crosslinked sodium carboxy methyl cellulose Nutrition 0.000 description 1
- 239000002875 cyclin dependent kinase inhibitor Substances 0.000 description 1
- 229940043378 cyclin-dependent kinase inhibitor Drugs 0.000 description 1
- 125000000000 cycloalkoxy group Chemical group 0.000 description 1
- 229940086555 cyclomethicone Drugs 0.000 description 1
- NXQGGXCHGDYOHB-UHFFFAOYSA-L cyclopenta-1,4-dien-1-yl(diphenyl)phosphane;dichloropalladium;iron(2+) Chemical compound [Fe+2].Cl[Pd]Cl.[CH-]1C=CC(P(C=2C=CC=CC=2)C=2C=CC=CC=2)=C1.[CH-]1C=CC(P(C=2C=CC=CC=2)C=2C=CC=CC=2)=C1 NXQGGXCHGDYOHB-UHFFFAOYSA-L 0.000 description 1
- WEPUZBYKXNKSDH-UHFFFAOYSA-N cyclopentanecarbonyl chloride Chemical compound ClC(=O)C1CCCC1 WEPUZBYKXNKSDH-UHFFFAOYSA-N 0.000 description 1
- ZOOSILUVXHVRJE-UHFFFAOYSA-N cyclopropanecarbonyl chloride Chemical compound ClC(=O)C1CC1 ZOOSILUVXHVRJE-UHFFFAOYSA-N 0.000 description 1
- AIMMVWOEOZMVMS-UHFFFAOYSA-N cyclopropanecarboxamide Chemical compound NC(=O)C1CC1 AIMMVWOEOZMVMS-UHFFFAOYSA-N 0.000 description 1
- 229960000684 cytarabine Drugs 0.000 description 1
- 231100000433 cytotoxic Toxicity 0.000 description 1
- DEZRYPDIMOWBDS-UHFFFAOYSA-N dcm dichloromethane Chemical compound ClCCl.ClCCl DEZRYPDIMOWBDS-UHFFFAOYSA-N 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 125000002704 decyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 230000007812 deficiency Effects 0.000 description 1
- 235000019258 dehydroacetic acid Nutrition 0.000 description 1
- 229940061632 dehydroacetic acid Drugs 0.000 description 1
- JEQRBTDTEKWZBW-UHFFFAOYSA-N dehydroacetic acid Chemical compound CC(=O)C1=C(O)OC(C)=CC1=O JEQRBTDTEKWZBW-UHFFFAOYSA-N 0.000 description 1
- PGRHXDWITVMQBC-UHFFFAOYSA-N dehydroacetic acid Natural products CC(=O)C1C(=O)OC(C)=CC1=O PGRHXDWITVMQBC-UHFFFAOYSA-N 0.000 description 1
- 229940124447 delivery agent Drugs 0.000 description 1
- VWTINHYPRWEBQY-UHFFFAOYSA-N denatonium Chemical compound [O-]C(=O)C1=CC=CC=C1.C=1C=CC=CC=1C[N+](CC)(CC)CC(=O)NC1=C(C)C=CC=C1C VWTINHYPRWEBQY-UHFFFAOYSA-N 0.000 description 1
- 229960001610 denatonium benzoate Drugs 0.000 description 1
- 239000003398 denaturant Substances 0.000 description 1
- 208000025729 dengue disease Diseases 0.000 description 1
- 210000003298 dental enamel Anatomy 0.000 description 1
- 239000002274 desiccant Substances 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- 229940099371 diacetylated monoglycerides Drugs 0.000 description 1
- 150000008050 dialkyl sulfates Chemical class 0.000 description 1
- MNNHAPBLZZVQHP-UHFFFAOYSA-N diammonium hydrogen phosphate Chemical compound [NH4+].[NH4+].OP([O-])([O-])=O MNNHAPBLZZVQHP-UHFFFAOYSA-N 0.000 description 1
- 229940061607 dibasic sodium phosphate Drugs 0.000 description 1
- LMEDOLJKVASKTP-UHFFFAOYSA-N dibutyl sulfate Chemical class CCCCOS(=O)(=O)OCCCC LMEDOLJKVASKTP-UHFFFAOYSA-N 0.000 description 1
- 235000019700 dicalcium phosphate Nutrition 0.000 description 1
- 229940095079 dicalcium phosphate anhydrous Drugs 0.000 description 1
- PXBRQCKWGAHEHS-UHFFFAOYSA-N dichlorodifluoromethane Chemical compound FC(F)(Cl)Cl PXBRQCKWGAHEHS-UHFFFAOYSA-N 0.000 description 1
- 235000019404 dichlorodifluoromethane Nutrition 0.000 description 1
- WGLUMOCWFMKWIL-UHFFFAOYSA-N dichloromethane;methanol Chemical compound OC.ClCCl WGLUMOCWFMKWIL-UHFFFAOYSA-N 0.000 description 1
- 229940087091 dichlorotetrafluoroethane Drugs 0.000 description 1
- MXFYYFVVIIWKFE-UHFFFAOYSA-N dicyclohexyl-[2-[2,6-di(propan-2-yloxy)phenyl]phenyl]phosphane Chemical compound CC(C)OC1=CC=CC(OC(C)C)=C1C1=CC=CC=C1P(C1CCCCC1)C1CCCCC1 MXFYYFVVIIWKFE-UHFFFAOYSA-N 0.000 description 1
- 125000004177 diethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- UGMCXQCYOVCMTB-UHFFFAOYSA-K dihydroxy(stearato)aluminium Chemical compound CCCCCCCCCCCCCCCCCC(=O)O[Al](O)O UGMCXQCYOVCMTB-UHFFFAOYSA-K 0.000 description 1
- UYAAVKFHBMJOJZ-UHFFFAOYSA-N diimidazo[1,3-b:1',3'-e]pyrazine-5,10-dione Chemical compound O=C1C2=CN=CN2C(=O)C2=CN=CN12 UYAAVKFHBMJOJZ-UHFFFAOYSA-N 0.000 description 1
- LVTYICIALWPMFW-UHFFFAOYSA-N diisopropanolamine Chemical compound CC(O)CNCC(C)O LVTYICIALWPMFW-UHFFFAOYSA-N 0.000 description 1
- 229940043276 diisopropanolamine Drugs 0.000 description 1
- 125000000118 dimethyl group Chemical group [H]C([H])([H])* 0.000 description 1
- 235000019329 dioctyl sodium sulphosuccinate Nutrition 0.000 description 1
- ZPWVASYFFYYZEW-UHFFFAOYSA-L dipotassium hydrogen phosphate Chemical compound [K+].[K+].OP([O-])([O-])=O ZPWVASYFFYYZEW-UHFFFAOYSA-L 0.000 description 1
- 235000019797 dipotassium phosphate Nutrition 0.000 description 1
- 229910000396 dipotassium phosphate Inorganic materials 0.000 description 1
- 230000006806 disease prevention Effects 0.000 description 1
- 208000037765 diseases and disorders Diseases 0.000 description 1
- BNIILDVGGAEEIG-UHFFFAOYSA-L disodium hydrogen phosphate Chemical compound [Na+].[Na+].OP([O-])([O-])=O BNIILDVGGAEEIG-UHFFFAOYSA-L 0.000 description 1
- 238000006073 displacement reaction Methods 0.000 description 1
- 238000009826 distribution Methods 0.000 description 1
- CETRZFQIITUQQL-UHFFFAOYSA-N dmso dimethylsulfoxide Chemical compound CS(C)=O.CS(C)=O CETRZFQIITUQQL-UHFFFAOYSA-N 0.000 description 1
- 229960000878 docusate sodium Drugs 0.000 description 1
- PRAKJMSDJKAYCZ-UHFFFAOYSA-N dodecahydrosqualene Natural products CC(C)CCCC(C)CCCC(C)CCCCC(C)CCCC(C)CCCC(C)C PRAKJMSDJKAYCZ-UHFFFAOYSA-N 0.000 description 1
- 125000003438 dodecyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 238000001647 drug administration Methods 0.000 description 1
- 239000003995 emulsifying agent Substances 0.000 description 1
- 230000001804 emulsifying effect Effects 0.000 description 1
- 230000007613 environmental effect Effects 0.000 description 1
- 239000003248 enzyme activator Substances 0.000 description 1
- 210000003238 esophagus Anatomy 0.000 description 1
- OCLXJTCGWSSVOE-UHFFFAOYSA-N ethanol etoh Chemical compound CCO.CCO OCLXJTCGWSSVOE-UHFFFAOYSA-N 0.000 description 1
- BEFDCLMNVWHSGT-UHFFFAOYSA-N ethenylcyclopentane Chemical compound C=CC1CCCC1 BEFDCLMNVWHSGT-UHFFFAOYSA-N 0.000 description 1
- 125000001301 ethoxy group Chemical group [H]C([H])([H])C([H])([H])O* 0.000 description 1
- DPKMNPWZDCMXQZ-UHFFFAOYSA-N ethyl 2-tert-butylpiperazine-1-carboxylate Chemical compound C(C)OC(=O)N1C(CNCC1)C(C)(C)C DPKMNPWZDCMXQZ-UHFFFAOYSA-N 0.000 description 1
- MVPICKVDHDWCJQ-UHFFFAOYSA-N ethyl 3-pyrrolidin-1-ylpropanoate Chemical compound CCOC(=O)CCN1CCCC1 MVPICKVDHDWCJQ-UHFFFAOYSA-N 0.000 description 1
- 229960004667 ethyl cellulose Drugs 0.000 description 1
- 229960001617 ethyl hydroxybenzoate Drugs 0.000 description 1
- LVGKNOAMLMIIKO-QXMHVHEDSA-N ethyl oleate Chemical compound CCCCCCCC\C=C/CCCCCCCC(=O)OCC LVGKNOAMLMIIKO-QXMHVHEDSA-N 0.000 description 1
- 229940093471 ethyl oleate Drugs 0.000 description 1
- 235000010228 ethyl p-hydroxybenzoate Nutrition 0.000 description 1
- 239000004403 ethyl p-hydroxybenzoate Substances 0.000 description 1
- 229940073505 ethyl vanillin Drugs 0.000 description 1
- NUVBSKCKDOMJSU-UHFFFAOYSA-N ethylparaben Chemical compound CCOC(=O)C1=CC=C(O)C=C1 NUVBSKCKDOMJSU-UHFFFAOYSA-N 0.000 description 1
- 125000002534 ethynyl group Chemical group [H]C#C* 0.000 description 1
- OJCSPXHYDFONPU-UHFFFAOYSA-N etoac etoac Chemical compound CCOC(C)=O.CCOC(C)=O OJCSPXHYDFONPU-UHFFFAOYSA-N 0.000 description 1
- 125000004030 farnesyl group Chemical group [H]C([*])([H])C([H])=C(C([H])([H])[H])C([H])([H])C([H])([H])C([H])=C(C([H])([H])[H])C([H])([H])C([H])([H])C([H])=C(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 230000004136 fatty acid synthesis Effects 0.000 description 1
- 239000000945 filler Substances 0.000 description 1
- 238000003818 flash chromatography Methods 0.000 description 1
- ODKNJVUHOIMIIZ-RRKCRQDMSA-N floxuridine Chemical compound C1[C@H](O)[C@@H](CO)O[C@H]1N1C(=O)NC(=O)C(F)=C1 ODKNJVUHOIMIIZ-RRKCRQDMSA-N 0.000 description 1
- 229960000961 floxuridine Drugs 0.000 description 1
- 239000012530 fluid Substances 0.000 description 1
- QEWYKACRFQMRMB-UHFFFAOYSA-N fluoroacetic acid Chemical compound OC(=O)CF QEWYKACRFQMRMB-UHFFFAOYSA-N 0.000 description 1
- 125000001207 fluorophenyl group Chemical group 0.000 description 1
- 239000011494 foam glass Substances 0.000 description 1
- XVVLAOSRANDVDB-UHFFFAOYSA-N formic acid Chemical compound OC=O.OC=O XVVLAOSRANDVDB-UHFFFAOYSA-N 0.000 description 1
- 238000001640 fractional crystallisation Methods 0.000 description 1
- 238000004108 freeze drying Methods 0.000 description 1
- 229960002737 fructose Drugs 0.000 description 1
- VZCYOOQTPOCHFL-OWOJBTEDSA-L fumarate(2-) Chemical class [O-]C(=O)\C=C\C([O-])=O VZCYOOQTPOCHFL-OWOJBTEDSA-L 0.000 description 1
- 239000001530 fumaric acid Substances 0.000 description 1
- 125000000524 functional group Chemical group 0.000 description 1
- 230000004927 fusion Effects 0.000 description 1
- 210000000232 gallbladder Anatomy 0.000 description 1
- 239000000499 gel Substances 0.000 description 1
- 238000007429 general method Methods 0.000 description 1
- 229960005219 gentisic acid Drugs 0.000 description 1
- 239000012362 glacial acetic acid Substances 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 229940080856 gleevec Drugs 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- 229960005150 glycerol Drugs 0.000 description 1
- 229940049654 glyceryl behenate Drugs 0.000 description 1
- 229940075507 glyceryl monostearate Drugs 0.000 description 1
- 239000001087 glyceryl triacetate Substances 0.000 description 1
- 235000013773 glyceryl triacetate Nutrition 0.000 description 1
- 239000008187 granular material Substances 0.000 description 1
- 230000012010 growth Effects 0.000 description 1
- 229940093915 gynecological organic acid Drugs 0.000 description 1
- 150000004820 halides Chemical class 0.000 description 1
- 229910052736 halogen Inorganic materials 0.000 description 1
- 150000002367 halogens Chemical class 0.000 description 1
- 229940116364 hard fat Drugs 0.000 description 1
- 210000003128 head Anatomy 0.000 description 1
- 201000010536 head and neck cancer Diseases 0.000 description 1
- 208000014829 head and neck neoplasm Diseases 0.000 description 1
- 208000006454 hepatitis Diseases 0.000 description 1
- 231100000283 hepatitis Toxicity 0.000 description 1
- 208000010710 hepatitis C virus infection Diseases 0.000 description 1
- 125000003187 heptyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000004446 heteroarylalkyl group Chemical group 0.000 description 1
- 125000006038 hexenyl group Chemical group 0.000 description 1
- 229940125697 hormonal agent Drugs 0.000 description 1
- 238000001794 hormone therapy Methods 0.000 description 1
- 239000003906 humectant Substances 0.000 description 1
- BHEPBYXIRTUNPN-UHFFFAOYSA-N hydridophosphorus(.) (triplet) Chemical compound [PH] BHEPBYXIRTUNPN-UHFFFAOYSA-N 0.000 description 1
- 150000003840 hydrochlorides Chemical class 0.000 description 1
- 150000002431 hydrogen Chemical class 0.000 description 1
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 1
- XMBWDFGMSWQBCA-UHFFFAOYSA-N hydrogen iodide Chemical class I XMBWDFGMSWQBCA-UHFFFAOYSA-N 0.000 description 1
- 230000003301 hydrolyzing effect Effects 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-M hydroxide Chemical compound [OH-] XLYOFNOQVPJJNP-UHFFFAOYSA-M 0.000 description 1
- 229920013821 hydroxy alkyl cellulose Polymers 0.000 description 1
- 125000005027 hydroxyaryl group Chemical group 0.000 description 1
- 235000019447 hydroxyethyl cellulose Nutrition 0.000 description 1
- 229960002899 hydroxyprogesterone Drugs 0.000 description 1
- 229920003132 hydroxypropyl methylcellulose phthalate Polymers 0.000 description 1
- 229940031704 hydroxypropyl methylcellulose phthalate Drugs 0.000 description 1
- 239000005457 ice water Substances 0.000 description 1
- YLMAHDNUQAMNNX-UHFFFAOYSA-N imatinib methanesulfonate Chemical compound CS(O)(=O)=O.C1CN(C)CCN1CC1=CC=C(C(=O)NC=2C=C(NC=3N=C(C=CN=3)C=3C=NC=CC=3)C(C)=CC=2)C=C1 YLMAHDNUQAMNNX-UHFFFAOYSA-N 0.000 description 1
- 125000002962 imidazol-1-yl group Chemical group [*]N1C([H])=NC([H])=C1[H] 0.000 description 1
- 238000001727 in vivo Methods 0.000 description 1
- LPAGFVYQRIESJQ-UHFFFAOYSA-N indoline Chemical compound C1=CC=C2NCCC2=C1 LPAGFVYQRIESJQ-UHFFFAOYSA-N 0.000 description 1
- 230000002757 inflammatory effect Effects 0.000 description 1
- 230000004054 inflammatory process Effects 0.000 description 1
- 230000000977 initiatory effect Effects 0.000 description 1
- 150000007529 inorganic bases Chemical class 0.000 description 1
- 230000003993 interaction Effects 0.000 description 1
- 230000002452 interceptive effect Effects 0.000 description 1
- 229940047124 interferons Drugs 0.000 description 1
- QWXYZCJEXYQNEI-OSZHWHEXSA-N intermediate I Chemical compound COC(=O)[C@@]1(C=O)[C@H]2CC=[N+](C\C2=C\C)CCc2c1[nH]c1ccccc21 QWXYZCJEXYQNEI-OSZHWHEXSA-N 0.000 description 1
- 238000007918 intramuscular administration Methods 0.000 description 1
- 238000007912 intraperitoneal administration Methods 0.000 description 1
- 238000007913 intrathecal administration Methods 0.000 description 1
- 238000001990 intravenous administration Methods 0.000 description 1
- 239000011630 iodine Substances 0.000 description 1
- UQSXHKLRYXJYBZ-UHFFFAOYSA-N iron oxide Inorganic materials [Fe]=O UQSXHKLRYXJYBZ-UHFFFAOYSA-N 0.000 description 1
- 208000023589 ischemic disease Diseases 0.000 description 1
- 239000001282 iso-butane Substances 0.000 description 1
- QXJSBBXBKPUZAA-UHFFFAOYSA-N isooleic acid Natural products CCCCCCCC=CCCCCCCCCC(O)=O QXJSBBXBKPUZAA-UHFFFAOYSA-N 0.000 description 1
- FMKOJHQHASLBPH-UHFFFAOYSA-N isopropyl iodide Chemical compound CC(C)I FMKOJHQHASLBPH-UHFFFAOYSA-N 0.000 description 1
- 229940074928 isopropyl myristate Drugs 0.000 description 1
- XUGNVMKQXJXZCD-UHFFFAOYSA-N isopropyl palmitate Chemical compound CCCCCCCCCCCCCCCC(=O)OC(C)C XUGNVMKQXJXZCD-UHFFFAOYSA-N 0.000 description 1
- 229940075495 isopropyl palmitate Drugs 0.000 description 1
- NLYAJNPCOHFWQQ-UHFFFAOYSA-N kaolin Chemical compound O.O.O=[Al]O[Si](=O)O[Si](=O)O[Al]=O NLYAJNPCOHFWQQ-UHFFFAOYSA-N 0.000 description 1
- 210000003734 kidney Anatomy 0.000 description 1
- 201000010982 kidney cancer Diseases 0.000 description 1
- 150000003893 lactate salts Chemical class 0.000 description 1
- 235000014655 lactic acid Nutrition 0.000 description 1
- 239000004310 lactic acid Substances 0.000 description 1
- 229940099367 lanolin alcohols Drugs 0.000 description 1
- 235000010445 lecithin Nutrition 0.000 description 1
- 239000000787 lecithin Substances 0.000 description 1
- 229940067606 lecithin Drugs 0.000 description 1
- 239000004571 lime Substances 0.000 description 1
- 239000000865 liniment Substances 0.000 description 1
- 230000003520 lipogenic effect Effects 0.000 description 1
- 229910052744 lithium Inorganic materials 0.000 description 1
- 210000004185 liver Anatomy 0.000 description 1
- 150000004668 long chain fatty acids Chemical class 0.000 description 1
- 239000002171 loop diuretic Substances 0.000 description 1
- 239000006210 lotion Substances 0.000 description 1
- 210000005265 lung cell Anatomy 0.000 description 1
- 230000002101 lytic effect Effects 0.000 description 1
- 229910052749 magnesium Inorganic materials 0.000 description 1
- 239000011777 magnesium Substances 0.000 description 1
- 159000000003 magnesium salts Chemical class 0.000 description 1
- 229940057948 magnesium stearate Drugs 0.000 description 1
- 150000002688 maleic acid derivatives Chemical class 0.000 description 1
- 239000001630 malic acid Substances 0.000 description 1
- 235000011090 malic acid Nutrition 0.000 description 1
- 230000036210 malignancy Effects 0.000 description 1
- 230000003211 malignant effect Effects 0.000 description 1
- LTYOQGRJFJAKNA-DVVLENMVSA-N malonyl-CoA Chemical compound O[C@@H]1[C@H](OP(O)(O)=O)[C@@H](COP(O)(=O)OP(O)(=O)OCC(C)(C)[C@@H](O)C(=O)NCCC(=O)NCCSC(=O)CC(O)=O)O[C@H]1N1C2=NC=NC(N)=C2N=C1 LTYOQGRJFJAKNA-DVVLENMVSA-N 0.000 description 1
- 229940035034 maltodextrin Drugs 0.000 description 1
- 229960001855 mannitol Drugs 0.000 description 1
- 239000011159 matrix material Substances 0.000 description 1
- 239000002609 medium Substances 0.000 description 1
- 239000001525 mentha piperita l. herb oil Substances 0.000 description 1
- 229940041616 menthol Drugs 0.000 description 1
- COTNUBDHGSIOTA-UHFFFAOYSA-N meoh methanol Chemical compound OC.OC COTNUBDHGSIOTA-UHFFFAOYSA-N 0.000 description 1
- 229960001428 mercaptopurine Drugs 0.000 description 1
- 108020004999 messenger RNA Proteins 0.000 description 1
- 229940117841 methacrylic acid copolymer Drugs 0.000 description 1
- 229920003145 methacrylic acid copolymer Polymers 0.000 description 1
- UKVIEHSSVKSQBA-UHFFFAOYSA-N methane;palladium Chemical compound C.[Pd] UKVIEHSSVKSQBA-UHFFFAOYSA-N 0.000 description 1
- AFVFQIVMOAPDHO-UHFFFAOYSA-M methanesulfonate group Chemical class CS(=O)(=O)[O-] AFVFQIVMOAPDHO-UHFFFAOYSA-M 0.000 description 1
- ILFDLYJWQQKAKF-UHFFFAOYSA-N methyl 4-(5-cyano-1,3-benzoxazol-2-yl)benzoate Chemical compound COC(=O)c1ccc(cc1)-c1nc2cc(ccc2o1)C#N ILFDLYJWQQKAKF-UHFFFAOYSA-N 0.000 description 1
- 235000010270 methyl p-hydroxybenzoate Nutrition 0.000 description 1
- 239000004292 methyl p-hydroxybenzoate Substances 0.000 description 1
- 229960001047 methyl salicylate Drugs 0.000 description 1
- 229960002216 methylparaben Drugs 0.000 description 1
- 239000004200 microcrystalline wax Substances 0.000 description 1
- 235000019808 microcrystalline wax Nutrition 0.000 description 1
- 239000003658 microfiber Substances 0.000 description 1
- 150000007522 mineralic acids Chemical class 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 239000002808 molecular sieve Substances 0.000 description 1
- 239000001788 mono and diglycerides of fatty acids Substances 0.000 description 1
- 229940111688 monobasic potassium phosphate Drugs 0.000 description 1
- 229940045641 monobasic sodium phosphate Drugs 0.000 description 1
- 235000019796 monopotassium phosphate Nutrition 0.000 description 1
- LPUQAYUQRXPFSQ-DFWYDOINSA-M monosodium L-glutamate Chemical compound [Na+].[O-]C(=O)[C@@H](N)CCC(O)=O LPUQAYUQRXPFSQ-DFWYDOINSA-M 0.000 description 1
- 235000013923 monosodium glutamate Nutrition 0.000 description 1
- 239000004223 monosodium glutamate Substances 0.000 description 1
- 235000019799 monosodium phosphate Nutrition 0.000 description 1
- 229910000403 monosodium phosphate Inorganic materials 0.000 description 1
- PJUIMOJAAPLTRJ-UHFFFAOYSA-N monothioglycerol Chemical compound OCC(O)CS PJUIMOJAAPLTRJ-UHFFFAOYSA-N 0.000 description 1
- 238000010172 mouse model Methods 0.000 description 1
- 201000006417 multiple sclerosis Diseases 0.000 description 1
- 231100000219 mutagenic Toxicity 0.000 description 1
- 230000003505 mutagenic effect Effects 0.000 description 1
- 201000000050 myeloid neoplasm Diseases 0.000 description 1
- 229940043348 myristyl alcohol Drugs 0.000 description 1
- IJDNQMDRQITEOD-UHFFFAOYSA-N n-butane Chemical compound CCCC IJDNQMDRQITEOD-UHFFFAOYSA-N 0.000 description 1
- 125000001280 n-hexyl group Chemical group C(CCCCC)* 0.000 description 1
- OFBQJSOFQDEBGM-UHFFFAOYSA-N n-pentane Natural products CCCCC OFBQJSOFQDEBGM-UHFFFAOYSA-N 0.000 description 1
- 125000000740 n-pentyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- PSZYNBSKGUBXEH-UHFFFAOYSA-N naphthalene-1-sulfonic acid Chemical class C1=CC=C2C(S(=O)(=O)O)=CC=CC2=C1 PSZYNBSKGUBXEH-UHFFFAOYSA-N 0.000 description 1
- 210000003739 neck Anatomy 0.000 description 1
- 125000001971 neopentyl group Chemical group [H]C([*])([H])C(C([H])([H])[H])(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 230000001537 neural effect Effects 0.000 description 1
- 208000015122 neurodegenerative disease Diseases 0.000 description 1
- 230000000926 neurological effect Effects 0.000 description 1
- 229930027945 nicotinamide-adenine dinucleotide Natural products 0.000 description 1
- 150000002823 nitrates Chemical class 0.000 description 1
- 229910017604 nitric acid Inorganic materials 0.000 description 1
- QJGQUHMNIGDVPM-UHFFFAOYSA-N nitrogen group Chemical group [N] QJGQUHMNIGDVPM-UHFFFAOYSA-N 0.000 description 1
- ODUCDPQEXGNKDN-UHFFFAOYSA-N nitroxyl Chemical compound O=N ODUCDPQEXGNKDN-UHFFFAOYSA-N 0.000 description 1
- 229940073555 nonoxynol-10 Drugs 0.000 description 1
- 229940087419 nonoxynol-9 Drugs 0.000 description 1
- 229920004918 nonoxynol-9 Polymers 0.000 description 1
- 231100000252 nontoxic Toxicity 0.000 description 1
- 230000003000 nontoxic effect Effects 0.000 description 1
- OQCDKBAXFALNLD-UHFFFAOYSA-N octadecanoic acid Natural products CCCCCCCC(C)CCCCCCCCC(O)=O OQCDKBAXFALNLD-UHFFFAOYSA-N 0.000 description 1
- 229940098514 octoxynol-9 Drugs 0.000 description 1
- 229920002114 octoxynol-9 Polymers 0.000 description 1
- 125000002347 octyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 229940060184 oil ingredients Drugs 0.000 description 1
- ZQPPMHVWECSIRJ-KTKRTIGZSA-N oleic acid Chemical compound CCCCCCCC\C=C/CCCCCCCC(O)=O ZQPPMHVWECSIRJ-KTKRTIGZSA-N 0.000 description 1
- 229940055577 oleyl alcohol Drugs 0.000 description 1
- XMLQWXUVTXCDDL-UHFFFAOYSA-N oleyl alcohol Natural products CCCCCCC=CCCCCCCCCCCO XMLQWXUVTXCDDL-UHFFFAOYSA-N 0.000 description 1
- 239000004006 olive oil Substances 0.000 description 1
- 235000008390 olive oil Nutrition 0.000 description 1
- GTVPOLSIJWJJNY-UHFFFAOYSA-N olomoucine Chemical compound N1=C(NCCO)N=C2N(C)C=NC2=C1NCC1=CC=CC=C1 GTVPOLSIJWJJNY-UHFFFAOYSA-N 0.000 description 1
- 239000003605 opacifier Substances 0.000 description 1
- 230000003287 optical effect Effects 0.000 description 1
- 150000007524 organic acids Chemical class 0.000 description 1
- 235000005985 organic acids Nutrition 0.000 description 1
- 201000008482 osteoarthritis Diseases 0.000 description 1
- 229940127084 other anti-cancer agent Drugs 0.000 description 1
- 210000001672 ovary Anatomy 0.000 description 1
- NDLPOXTZKUMGOV-UHFFFAOYSA-N oxo(oxoferriooxy)iron hydrate Chemical compound O.O=[Fe]O[Fe]=O NDLPOXTZKUMGOV-UHFFFAOYSA-N 0.000 description 1
- 125000001820 oxy group Chemical group [*:1]O[*:2] 0.000 description 1
- 229960001257 oxyquinoline sulfate Drugs 0.000 description 1
- 229910052763 palladium Inorganic materials 0.000 description 1
- MUJIDPITZJWBSW-UHFFFAOYSA-N palladium(2+) Chemical compound [Pd+2] MUJIDPITZJWBSW-UHFFFAOYSA-N 0.000 description 1
- 210000000496 pancreas Anatomy 0.000 description 1
- RUVINXPYWBROJD-UHFFFAOYSA-N para-methoxyphenyl Natural products COC1=CC=C(C=CC)C=C1 RUVINXPYWBROJD-UHFFFAOYSA-N 0.000 description 1
- 239000012188 paraffin wax Substances 0.000 description 1
- 238000007911 parenteral administration Methods 0.000 description 1
- 235000014594 pastries Nutrition 0.000 description 1
- 230000008506 pathogenesis Effects 0.000 description 1
- 230000037361 pathway Effects 0.000 description 1
- 229920001277 pectin Polymers 0.000 description 1
- 235000010987 pectin Nutrition 0.000 description 1
- 239000001814 pectin Substances 0.000 description 1
- HQQSBEDKMRHYME-UHFFFAOYSA-N pefloxacin mesylate Chemical compound [H+].CS([O-])(=O)=O.C1=C2N(CC)C=C(C(O)=O)C(=O)C2=CC(F)=C1N1CCN(C)CC1 HQQSBEDKMRHYME-UHFFFAOYSA-N 0.000 description 1
- 108010044644 pegfilgrastim Proteins 0.000 description 1
- 229960001373 pegfilgrastim Drugs 0.000 description 1
- 108010092851 peginterferon alfa-2b Proteins 0.000 description 1
- 229940106366 pegintron Drugs 0.000 description 1
- 125000006194 pentinyl group Chemical group 0.000 description 1
- 235000019477 peppermint oil Nutrition 0.000 description 1
- 239000002304 perfume Substances 0.000 description 1
- 229940124531 pharmaceutical excipient Drugs 0.000 description 1
- 239000000825 pharmaceutical preparation Substances 0.000 description 1
- WVDDGKGOMKODPV-ZQBYOMGUSA-N phenyl(114C)methanol Chemical compound O[14CH2]C1=CC=CC=C1 WVDDGKGOMKODPV-ZQBYOMGUSA-N 0.000 description 1
- PDTFCHSETJBPTR-UHFFFAOYSA-N phenylmercuric nitrate Chemical compound [O-][N+](=O)O[Hg]C1=CC=CC=C1 PDTFCHSETJBPTR-UHFFFAOYSA-N 0.000 description 1
- 235000021317 phosphate Nutrition 0.000 description 1
- ACVYVLVWPXVTIT-UHFFFAOYSA-N phosphinic acid Chemical compound O[PH2]=O ACVYVLVWPXVTIT-UHFFFAOYSA-N 0.000 description 1
- 150000003013 phosphoric acid derivatives Chemical class 0.000 description 1
- BGQLKIRZQYRJPH-UHFFFAOYSA-N piperazine-1-carbaldehyde;hydrochloride Chemical compound Cl.O=CN1CCNCC1 BGQLKIRZQYRJPH-UHFFFAOYSA-N 0.000 description 1
- RFIOZSIHFNEKFF-UHFFFAOYSA-N piperazine-1-carboxylic acid Chemical compound OC(=O)N1CCNCC1 RFIOZSIHFNEKFF-UHFFFAOYSA-N 0.000 description 1
- NJBFOOCLYDNZJN-UHFFFAOYSA-N pipobroman Chemical compound BrCCC(=O)N1CCN(C(=O)CCBr)CC1 NJBFOOCLYDNZJN-UHFFFAOYSA-N 0.000 description 1
- 229960000952 pipobroman Drugs 0.000 description 1
- 239000004014 plasticizer Substances 0.000 description 1
- CSOMAHTTWTVBFL-OFBLZTNGSA-N platensimycin Chemical compound C([C@]1([C@@H]2[C@@H]3C[C@@H]4C[C@@]2(C=CC1=O)C[C@@]4(O3)C)C)CC(=O)NC1=C(O)C=CC(C(O)=O)=C1O CSOMAHTTWTVBFL-OFBLZTNGSA-N 0.000 description 1
- CSOMAHTTWTVBFL-UHFFFAOYSA-N platensimycin Natural products O1C2(C)CC3(C=CC4=O)CC2CC1C3C4(C)CCC(=O)NC1=C(O)C=CC(C(O)=O)=C1O CSOMAHTTWTVBFL-UHFFFAOYSA-N 0.000 description 1
- 229920000058 polyacrylate Polymers 0.000 description 1
- 229920000573 polyethylene Polymers 0.000 description 1
- 229920000656 polylysine Polymers 0.000 description 1
- 229920000642 polymer Polymers 0.000 description 1
- 229920002451 polyvinyl alcohol Polymers 0.000 description 1
- 235000019422 polyvinyl alcohol Nutrition 0.000 description 1
- SCVFZCLFOSHCOH-UHFFFAOYSA-M potassium acetate Chemical compound [K+].CC([O-])=O SCVFZCLFOSHCOH-UHFFFAOYSA-M 0.000 description 1
- XAEFZNCEHLXOMS-UHFFFAOYSA-M potassium benzoate Chemical compound [K+].[O-]C(=O)C1=CC=CC=C1 XAEFZNCEHLXOMS-UHFFFAOYSA-M 0.000 description 1
- 235000010235 potassium benzoate Nutrition 0.000 description 1
- 239000004300 potassium benzoate Substances 0.000 description 1
- 229940103091 potassium benzoate Drugs 0.000 description 1
- 239000001103 potassium chloride Substances 0.000 description 1
- 235000011164 potassium chloride Nutrition 0.000 description 1
- 239000001508 potassium citrate Substances 0.000 description 1
- 229960002635 potassium citrate Drugs 0.000 description 1
- QEEAPRPFLLJWCF-UHFFFAOYSA-K potassium citrate (anhydrous) Chemical compound [K+].[K+].[K+].[O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O QEEAPRPFLLJWCF-UHFFFAOYSA-K 0.000 description 1
- 235000011082 potassium citrates Nutrition 0.000 description 1
- GNSKLFRGEWLPPA-UHFFFAOYSA-M potassium dihydrogen phosphate Chemical compound [K+].OP(O)([O-])=O GNSKLFRGEWLPPA-UHFFFAOYSA-M 0.000 description 1
- 235000011118 potassium hydroxide Nutrition 0.000 description 1
- OQZCJRJRGMMSGK-UHFFFAOYSA-M potassium metaphosphate Chemical compound [K+].[O-]P(=O)=O OQZCJRJRGMMSGK-UHFFFAOYSA-M 0.000 description 1
- 229940099402 potassium metaphosphate Drugs 0.000 description 1
- 159000000001 potassium salts Chemical class 0.000 description 1
- 235000010241 potassium sorbate Nutrition 0.000 description 1
- 239000004302 potassium sorbate Substances 0.000 description 1
- 229940069338 potassium sorbate Drugs 0.000 description 1
- LPNYRYFBWFDTMA-UHFFFAOYSA-N potassium tert-butoxide Chemical compound [K+].CC(C)(C)[O-] LPNYRYFBWFDTMA-UHFFFAOYSA-N 0.000 description 1
- 230000003389 potentiating effect Effects 0.000 description 1
- 238000012746 preparative thin layer chromatography Methods 0.000 description 1
- 239000003755 preservative agent Substances 0.000 description 1
- 230000002062 proliferating effect Effects 0.000 description 1
- ALDITMKAAPLVJK-UHFFFAOYSA-N prop-1-ene;hydrate Chemical group O.CC=C ALDITMKAAPLVJK-UHFFFAOYSA-N 0.000 description 1
- 239000001294 propane Substances 0.000 description 1
- 235000010409 propane-1,2-diol alginate Nutrition 0.000 description 1
- 239000000770 propane-1,2-diol alginate Substances 0.000 description 1
- 239000003380 propellant Substances 0.000 description 1
- 239000000473 propyl gallate Substances 0.000 description 1
- 235000010388 propyl gallate Nutrition 0.000 description 1
- 229940075579 propyl gallate Drugs 0.000 description 1
- 239000004405 propyl p-hydroxybenzoate Substances 0.000 description 1
- 235000010232 propyl p-hydroxybenzoate Nutrition 0.000 description 1
- 229940116423 propylene glycol diacetate Drugs 0.000 description 1
- 229960003415 propylparaben Drugs 0.000 description 1
- 229960005359 propylparaben sodium Drugs 0.000 description 1
- 125000002568 propynyl group Chemical group [*]C#CC([H])([H])[H] 0.000 description 1
- 102000004169 proteins and genes Human genes 0.000 description 1
- 239000008213 purified water Substances 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 238000007430 reference method Methods 0.000 description 1
- 230000001105 regulatory effect Effects 0.000 description 1
- 239000012744 reinforcing agent Substances 0.000 description 1
- 239000005871 repellent Substances 0.000 description 1
- 230000002940 repellent Effects 0.000 description 1
- 230000010076 replication Effects 0.000 description 1
- 238000004007 reversed phase HPLC Methods 0.000 description 1
- 238000012552 review Methods 0.000 description 1
- 206010039073 rheumatoid arthritis Diseases 0.000 description 1
- 229960004641 rituximab Drugs 0.000 description 1
- 235000019719 rose oil Nutrition 0.000 description 1
- 239000010666 rose oil Substances 0.000 description 1
- 239000008132 rose water Substances 0.000 description 1
- 235000019204 saccharin Nutrition 0.000 description 1
- 229940081974 saccharin Drugs 0.000 description 1
- 239000000901 saccharin and its Na,K and Ca salt Substances 0.000 description 1
- 150000003902 salicylic acid esters Chemical class 0.000 description 1
- 239000010703 silicon Substances 0.000 description 1
- 229910052710 silicon Inorganic materials 0.000 description 1
- 210000003491 skin Anatomy 0.000 description 1
- 239000001632 sodium acetate Substances 0.000 description 1
- 235000017281 sodium acetate Nutrition 0.000 description 1
- 229940005550 sodium alginate Drugs 0.000 description 1
- 235000010413 sodium alginate Nutrition 0.000 description 1
- 239000000661 sodium alginate Substances 0.000 description 1
- URGAHOPLAPQHLN-UHFFFAOYSA-N sodium aluminosilicate Chemical compound [Na+].[Al+3].[O-][Si]([O-])=O.[O-][Si]([O-])=O URGAHOPLAPQHLN-UHFFFAOYSA-N 0.000 description 1
- WXMKPNITSTVMEF-UHFFFAOYSA-M sodium benzoate Chemical compound [Na+].[O-]C(=O)C1=CC=CC=C1 WXMKPNITSTVMEF-UHFFFAOYSA-M 0.000 description 1
- 235000010234 sodium benzoate Nutrition 0.000 description 1
- 239000004299 sodium benzoate Substances 0.000 description 1
- 229960003885 sodium benzoate Drugs 0.000 description 1
- 229940080237 sodium caseinate Drugs 0.000 description 1
- 229960002668 sodium chloride Drugs 0.000 description 1
- 239000008354 sodium chloride injection Substances 0.000 description 1
- 239000001509 sodium citrate Substances 0.000 description 1
- NLJMYIDDQXHKNR-UHFFFAOYSA-K sodium citrate Chemical compound O.O.[Na+].[Na+].[Na+].[O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O NLJMYIDDQXHKNR-UHFFFAOYSA-K 0.000 description 1
- 235000011083 sodium citrates Nutrition 0.000 description 1
- 235000019259 sodium dehydroacetate Nutrition 0.000 description 1
- 229940079839 sodium dehydroacetate Drugs 0.000 description 1
- AJPJDKMHJJGVTQ-UHFFFAOYSA-M sodium dihydrogen phosphate Chemical compound [Na+].OP(O)([O-])=O AJPJDKMHJJGVTQ-UHFFFAOYSA-M 0.000 description 1
- APSBXTVYXVQYAB-UHFFFAOYSA-M sodium docusate Chemical compound [Na+].CCCCC(CC)COC(=O)CC(S([O-])(=O)=O)C(=O)OCC(CC)CCCC APSBXTVYXVQYAB-UHFFFAOYSA-M 0.000 description 1
- VYGBQXDNOUHIBZ-UHFFFAOYSA-L sodium formaldehyde sulphoxylate Chemical compound [Na+].[Na+].O=C.[O-]S[O-] VYGBQXDNOUHIBZ-UHFFFAOYSA-L 0.000 description 1
- 239000001540 sodium lactate Substances 0.000 description 1
- 235000011088 sodium lactate Nutrition 0.000 description 1
- 229940005581 sodium lactate Drugs 0.000 description 1
- JXKPEJDQGNYQSM-UHFFFAOYSA-M sodium propionate Chemical compound [Na+].CCC([O-])=O JXKPEJDQGNYQSM-UHFFFAOYSA-M 0.000 description 1
- 235000010334 sodium propionate Nutrition 0.000 description 1
- 239000004324 sodium propionate Substances 0.000 description 1
- 229960003212 sodium propionate Drugs 0.000 description 1
- 229920003109 sodium starch glycolate Polymers 0.000 description 1
- 239000008109 sodium starch glycolate Substances 0.000 description 1
- 229940079832 sodium starch glycolate Drugs 0.000 description 1
- ODFAPIRLUPAQCQ-UHFFFAOYSA-M sodium stearoyl lactylate Chemical compound [Na+].CCCCCCCCCCCCCCCCCC(=O)OC(C)C(=O)OC(C)C([O-])=O ODFAPIRLUPAQCQ-UHFFFAOYSA-M 0.000 description 1
- 229940080352 sodium stearoyl lactylate Drugs 0.000 description 1
- 229940045902 sodium stearyl fumarate Drugs 0.000 description 1
- 235000010339 sodium tetraborate Nutrition 0.000 description 1
- AKHNMLFCWUSKQB-UHFFFAOYSA-L sodium thiosulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=S AKHNMLFCWUSKQB-UHFFFAOYSA-L 0.000 description 1
- 229940001474 sodium thiosulfate Drugs 0.000 description 1
- 235000019345 sodium thiosulphate Nutrition 0.000 description 1
- DSOWAKKSGYUMTF-GZOLSCHFSA-M sodium;(1e)-1-(6-methyl-2,4-dioxopyran-3-ylidene)ethanolate Chemical compound [Na+].C\C([O-])=C1/C(=O)OC(C)=CC1=O DSOWAKKSGYUMTF-GZOLSCHFSA-M 0.000 description 1
- IXMINYBUNCWGER-UHFFFAOYSA-M sodium;4-propoxycarbonylphenolate Chemical compound [Na+].CCCOC(=O)C1=CC=C([O-])C=C1 IXMINYBUNCWGER-UHFFFAOYSA-M 0.000 description 1
- HUAUNKAZQWMVFY-UHFFFAOYSA-M sodium;oxocalcium;hydroxide Chemical compound [OH-].[Na+].[Ca]=O HUAUNKAZQWMVFY-UHFFFAOYSA-M 0.000 description 1
- WGRULTCAYDOGQK-UHFFFAOYSA-M sodium;sodium;hydroxide Chemical compound [OH-].[Na].[Na+] WGRULTCAYDOGQK-UHFFFAOYSA-M 0.000 description 1
- 239000007909 solid dosage form Substances 0.000 description 1
- 235000010199 sorbic acid Nutrition 0.000 description 1
- 239000004334 sorbic acid Substances 0.000 description 1
- 229940075582 sorbic acid Drugs 0.000 description 1
- 229940035044 sorbitan monolaurate Drugs 0.000 description 1
- 239000003549 soybean oil Substances 0.000 description 1
- 235000012424 soybean oil Nutrition 0.000 description 1
- 239000008347 soybean phospholipid Substances 0.000 description 1
- 230000003595 spectral effect Effects 0.000 description 1
- 125000003003 spiro group Chemical group 0.000 description 1
- 229940031439 squalene Drugs 0.000 description 1
- TUHBEKDERLKLEC-UHFFFAOYSA-N squalene Natural products CC(=CCCC(=CCCC(=CCCC=C(/C)CCC=C(/C)CC=C(C)C)C)C)C TUHBEKDERLKLEC-UHFFFAOYSA-N 0.000 description 1
- 206010041823 squamous cell carcinoma Diseases 0.000 description 1
- 208000017572 squamous cell neoplasm Diseases 0.000 description 1
- 239000008117 stearic acid Substances 0.000 description 1
- 239000008227 sterile water for injection Substances 0.000 description 1
- 239000008229 sterile water for irrigation Substances 0.000 description 1
- 210000002784 stomach Anatomy 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- 238000006467 substitution reaction Methods 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- 150000003890 succinate salts Chemical class 0.000 description 1
- 229940124530 sulfonamide Drugs 0.000 description 1
- 150000003456 sulfonamides Chemical class 0.000 description 1
- 125000000472 sulfonyl group Chemical group *S(*)(=O)=O 0.000 description 1
- 229940044609 sulfur dioxide Drugs 0.000 description 1
- 150000003467 sulfuric acid derivatives Chemical class 0.000 description 1
- 235000010269 sulphur dioxide Nutrition 0.000 description 1
- 239000000829 suppository Substances 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 208000011580 syndromic disease Diseases 0.000 description 1
- 230000002194 synthesizing effect Effects 0.000 description 1
- 201000000596 systemic lupus erythematosus Diseases 0.000 description 1
- 239000007885 tablet disintegrant Substances 0.000 description 1
- 239000011975 tartaric acid Substances 0.000 description 1
- 235000002906 tartaric acid Nutrition 0.000 description 1
- 150000003892 tartrate salts Chemical class 0.000 description 1
- FBWNMEQMRUMQSO-UHFFFAOYSA-N tergitol NP-9 Chemical compound CCCCCCCCCC1=CC=C(OCCOCCOCCOCCOCCOCCOCCOCCOCCO)C=C1 FBWNMEQMRUMQSO-UHFFFAOYSA-N 0.000 description 1
- 125000004213 tert-butoxy group Chemical group [H]C([H])([H])C(O*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- FTUUMJLVSHBOTA-QGZVFWFLSA-N tert-butyl (2R)-2-methyl-4-[4-(1-methylbenzimidazol-5-yl)benzoyl]piperazine-1-carboxylate Chemical compound C[C@@H]1CN(CCN1C(=O)OC(C)(C)C)C(=O)c1ccc(cc1)-c1ccc2n(C)cnc2c1 FTUUMJLVSHBOTA-QGZVFWFLSA-N 0.000 description 1
- KHKHHGANZBSHSI-UHFFFAOYSA-N tert-butyl 4-(4-bromo-3-chlorobenzoyl)piperazine-1-carboxylate Chemical compound BrC1=C(C=C(C(=O)N2CCN(CC2)C(=O)OC(C)(C)C)C=C1)Cl KHKHHGANZBSHSI-UHFFFAOYSA-N 0.000 description 1
- VAANXSRYDBHSOU-UHFFFAOYSA-N tert-butyl 4-[4-(1-methylbenzimidazol-5-yl)benzoyl]piperazine-1-carboxylate Chemical compound Cn1cnc2cc(ccc12)-c1ccc(cc1)C(=O)N1CCN(CC1)C(=O)OC(C)(C)C VAANXSRYDBHSOU-UHFFFAOYSA-N 0.000 description 1
- IVANDLPSZQEBCH-UHFFFAOYSA-N tert-butyl 4-[4-(2-methylbenzimidazol-1-yl)benzoyl]piperazine-1-carboxylate Chemical compound Cc1nc2ccccc2n1-c1ccc(cc1)C(=O)N1CCN(CC1)C(=O)OC(C)(C)C IVANDLPSZQEBCH-UHFFFAOYSA-N 0.000 description 1
- IOOKXSDBYPZPHP-UHFFFAOYSA-N tert-butyl 4-[4-[3-[2-[tert-butyl(dimethyl)silyl]oxyethyl]benzimidazol-5-yl]benzoyl]piperazine-1-carboxylate Chemical compound CC(C)(C)OC(=O)N1CCN(CC1)C(=O)c1ccc(cc1)-c1ccc2ncn(CCO[Si](C)(C)C(C)(C)C)c2c1 IOOKXSDBYPZPHP-UHFFFAOYSA-N 0.000 description 1
- CMUDKADWPOXZAJ-KRWDZBQOSA-N tert-butyl N-[1-[(2S)-4-[4-(6-fluoro-1,3-benzoxazol-2-yl)benzoyl]-2-methylpiperazine-1-carbonyl]cyclopropyl]carbamate Chemical compound C[C@H]1CN(CCN1C(=O)C1(CC1)NC(=O)OC(C)(C)C)C(=O)c1ccc(cc1)-c1nc2ccc(F)cc2o1 CMUDKADWPOXZAJ-KRWDZBQOSA-N 0.000 description 1
- JHBKTQCADWRVAT-UHFFFAOYSA-N tert-butyl N-[1-[4-[4-(1-methylbenzimidazol-5-yl)benzoyl]piperazine-1-carbonyl]cyclopropyl]carbamate Chemical compound Cn1cnc2cc(ccc12)-c1ccc(cc1)C(=O)N1CCN(CC1)C(=O)C1(CC1)NC(=O)OC(C)(C)C JHBKTQCADWRVAT-UHFFFAOYSA-N 0.000 description 1
- PJCLTUSLIAKJBR-UHFFFAOYSA-N tert-butyl N-[3-[3-[4-[4-(1-hydroxycyclopropanecarbonyl)piperazine-1-carbonyl]phenyl]phenyl]-1,2-oxazol-5-yl]carbamate Chemical compound CC(C)(C)OC(=O)Nc1cc(no1)-c1cccc(c1)-c1ccc(cc1)C(=O)N1CCN(CC1)C(=O)C1(O)CC1 PJCLTUSLIAKJBR-UHFFFAOYSA-N 0.000 description 1
- OXAMQPMLEJJLDR-UHFFFAOYSA-N tert-butyl N-[5-(3-bromophenyl)-1H-pyrazol-3-yl]carbamate Chemical compound CC(C)(C)OC(=O)Nc1cc(n[nH]1)-c1cccc(Br)c1 OXAMQPMLEJJLDR-UHFFFAOYSA-N 0.000 description 1
- SIXKZGZQCTVLJF-UHFFFAOYSA-N tert-butyl N-[5-[3-[4-(piperazine-1-carbonyl)phenyl]phenyl]-1H-pyrazol-3-yl]carbamate Chemical compound CC(C)(C)OC(=O)Nc1cc(n[nH]1)-c1cccc(c1)-c1ccc(cc1)C(=O)N1CCNCC1 SIXKZGZQCTVLJF-UHFFFAOYSA-N 0.000 description 1
- 238000012360 testing method Methods 0.000 description 1
- WHRNULOCNSKMGB-UHFFFAOYSA-N tetrahydrofuran thf Chemical compound C1CCOC1.C1CCOC1 WHRNULOCNSKMGB-UHFFFAOYSA-N 0.000 description 1
- WROMPOXWARCANT-UHFFFAOYSA-N tfa trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F.OC(=O)C(F)(F)F WROMPOXWARCANT-UHFFFAOYSA-N 0.000 description 1
- 238000002560 therapeutic procedure Methods 0.000 description 1
- RTKIYNMVFMVABJ-UHFFFAOYSA-L thimerosal Chemical compound [Na+].CC[Hg]SC1=CC=CC=C1C([O-])=O RTKIYNMVFMVABJ-UHFFFAOYSA-L 0.000 description 1
- 229940033663 thimerosal Drugs 0.000 description 1
- 150000003567 thiocyanates Chemical class 0.000 description 1
- 230000009424 thromboembolic effect Effects 0.000 description 1
- 239000003734 thymidylate synthase inhibitor Substances 0.000 description 1
- 210000001685 thyroid gland Anatomy 0.000 description 1
- 210000001519 tissue Anatomy 0.000 description 1
- 239000004408 titanium dioxide Substances 0.000 description 1
- 235000010215 titanium dioxide Nutrition 0.000 description 1
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 1
- LBLYYCQCTBFVLH-UHFFFAOYSA-M toluenesulfonate group Chemical group C=1(C(=CC=CC1)S(=O)(=O)[O-])C LBLYYCQCTBFVLH-UHFFFAOYSA-M 0.000 description 1
- 239000012929 tonicity agent Substances 0.000 description 1
- 125000005490 tosylate group Chemical group 0.000 description 1
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 1
- 230000026683 transduction Effects 0.000 description 1
- 238000010361 transduction Methods 0.000 description 1
- 238000011269 treatment regimen Methods 0.000 description 1
- 229960002622 triacetin Drugs 0.000 description 1
- 229940078499 tricalcium phosphate Drugs 0.000 description 1
- 229910000391 tricalcium phosphate Inorganic materials 0.000 description 1
- CYRMSUTZVYGINF-UHFFFAOYSA-N trichlorofluoromethane Chemical compound FC(Cl)(Cl)Cl CYRMSUTZVYGINF-UHFFFAOYSA-N 0.000 description 1
- 229940029284 trichlorofluoromethane Drugs 0.000 description 1
- 239000001069 triethyl citrate Substances 0.000 description 1
- VMYFZRTXGLUXMZ-UHFFFAOYSA-N triethyl citrate Natural products CCOC(=O)C(O)(C(=O)OCC)C(=O)OCC VMYFZRTXGLUXMZ-UHFFFAOYSA-N 0.000 description 1
- 235000013769 triethyl citrate Nutrition 0.000 description 1
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 description 1
- BZVJOYBTLHNRDW-UHFFFAOYSA-N triphenylmethanamine Chemical compound C=1C=CC=CC=1C(C=1C=CC=CC=1)(N)C1=CC=CC=C1 BZVJOYBTLHNRDW-UHFFFAOYSA-N 0.000 description 1
- BSVBQGMMJUBVOD-UHFFFAOYSA-N trisodium borate Chemical compound [Na+].[Na+].[Na+].[O-]B([O-])[O-] BSVBQGMMJUBVOD-UHFFFAOYSA-N 0.000 description 1
- 230000004565 tumor cell growth Effects 0.000 description 1
- 229910052721 tungsten Inorganic materials 0.000 description 1
- MDYZKJNTKZIUSK-UHFFFAOYSA-N tyloxapol Chemical compound O=C.C1CO1.CC(C)(C)CC(C)(C)C1=CC=C(O)C=C1 MDYZKJNTKZIUSK-UHFFFAOYSA-N 0.000 description 1
- 229920001664 tyloxapol Polymers 0.000 description 1
- 229960004224 tyloxapol Drugs 0.000 description 1
- 241001529453 unidentified herpesvirus Species 0.000 description 1
- 210000003932 urinary bladder Anatomy 0.000 description 1
- MWOOGOJBHIARFG-UHFFFAOYSA-N vanillin Chemical compound COC1=CC(C=O)=CC=C1O MWOOGOJBHIARFG-UHFFFAOYSA-N 0.000 description 1
- 235000012141 vanillin Nutrition 0.000 description 1
- FGQOOHJZONJGDT-UHFFFAOYSA-N vanillin Natural products COC1=CC(O)=CC(C=O)=C1 FGQOOHJZONJGDT-UHFFFAOYSA-N 0.000 description 1
- 235000013311 vegetables Nutrition 0.000 description 1
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 1
- 229920002554 vinyl polymer Polymers 0.000 description 1
- 230000007502 viral entry Effects 0.000 description 1
- 230000009447 viral pathogenesis Effects 0.000 description 1
- 230000004580 weight loss Effects 0.000 description 1
- 238000009736 wetting Methods 0.000 description 1
- 229940045860 white wax Drugs 0.000 description 1
- 235000010493 xanthan gum Nutrition 0.000 description 1
- 239000000230 xanthan gum Substances 0.000 description 1
- 229920001285 xanthan gum Polymers 0.000 description 1
- 229940082509 xanthan gum Drugs 0.000 description 1
- 239000005019 zein Substances 0.000 description 1
- 229940093612 zein Drugs 0.000 description 1
- XOOUIPVCVHRTMJ-UHFFFAOYSA-L zinc stearate Chemical compound [Zn+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O XOOUIPVCVHRTMJ-UHFFFAOYSA-L 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D295/00—Heterocyclic compounds containing polymethylene-imine rings with at least five ring members, 3-azabicyclo [3.2.2] nonane, piperazine, morpholine or thiomorpholine rings, having only hydrogen atoms directly attached to the ring carbon atoms
- C07D295/16—Heterocyclic compounds containing polymethylene-imine rings with at least five ring members, 3-azabicyclo [3.2.2] nonane, piperazine, morpholine or thiomorpholine rings, having only hydrogen atoms directly attached to the ring carbon atoms acylated on ring nitrogen atoms
- C07D295/18—Heterocyclic compounds containing polymethylene-imine rings with at least five ring members, 3-azabicyclo [3.2.2] nonane, piperazine, morpholine or thiomorpholine rings, having only hydrogen atoms directly attached to the ring carbon atoms acylated on ring nitrogen atoms by radicals derived from carboxylic acids, or sulfur or nitrogen analogues thereof
- C07D295/182—Radicals derived from carboxylic acids
- C07D295/192—Radicals derived from carboxylic acids from aromatic carboxylic acids
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D295/00—Heterocyclic compounds containing polymethylene-imine rings with at least five ring members, 3-azabicyclo [3.2.2] nonane, piperazine, morpholine or thiomorpholine rings, having only hydrogen atoms directly attached to the ring carbon atoms
- C07D295/16—Heterocyclic compounds containing polymethylene-imine rings with at least five ring members, 3-azabicyclo [3.2.2] nonane, piperazine, morpholine or thiomorpholine rings, having only hydrogen atoms directly attached to the ring carbon atoms acylated on ring nitrogen atoms
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/496—Non-condensed piperazines containing further heterocyclic rings, e.g. rifampin, thiothixene
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/4965—Non-condensed pyrazines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/4965—Non-condensed pyrazines
- A61K31/497—Non-condensed pyrazines containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/4985—Pyrazines or piperazines ortho- or peri-condensed with heterocyclic ring systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/50—Pyridazines; Hydrogenated pyridazines
- A61K31/5025—Pyridazines; Hydrogenated pyridazines ortho- or peri-condensed with heterocyclic ring systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/506—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim not condensed and containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D209/00—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D209/02—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom condensed with one carbocyclic ring
- C07D209/04—Indoles; Hydrogenated indoles
- C07D209/08—Indoles; Hydrogenated indoles with only hydrogen atoms or radicals containing only hydrogen and carbon atoms, directly attached to carbon atoms of the hetero ring
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D209/00—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D209/02—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom condensed with one carbocyclic ring
- C07D209/04—Indoles; Hydrogenated indoles
- C07D209/10—Indoles; Hydrogenated indoles with substituted hydrocarbon radicals attached to carbon atoms of the hetero ring
- C07D209/18—Radicals substituted by carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D213/00—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members
- C07D213/02—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members
- C07D213/04—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D213/24—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom with substituted hydrocarbon radicals attached to ring carbon atoms
- C07D213/54—Radicals substituted by carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals
- C07D213/56—Amides
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D213/00—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members
- C07D213/02—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members
- C07D213/04—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D213/60—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D213/62—Oxygen or sulfur atoms
- C07D213/63—One oxygen atom
- C07D213/65—One oxygen atom attached in position 3 or 5
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D213/00—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members
- C07D213/02—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members
- C07D213/04—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D213/60—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D213/62—Oxygen or sulfur atoms
- C07D213/69—Two or more oxygen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D215/00—Heterocyclic compounds containing quinoline or hydrogenated quinoline ring systems
- C07D215/02—Heterocyclic compounds containing quinoline or hydrogenated quinoline ring systems having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen atoms or carbon atoms directly attached to the ring nitrogen atom
- C07D215/12—Heterocyclic compounds containing quinoline or hydrogenated quinoline ring systems having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen atoms or carbon atoms directly attached to the ring nitrogen atom with substituted hydrocarbon radicals attached to ring carbon atoms
- C07D215/14—Radicals substituted by oxygen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D217/00—Heterocyclic compounds containing isoquinoline or hydrogenated isoquinoline ring systems
- C07D217/12—Heterocyclic compounds containing isoquinoline or hydrogenated isoquinoline ring systems with radicals, substituted by hetero atoms, attached to carbon atoms of the nitrogen-containing ring
- C07D217/14—Heterocyclic compounds containing isoquinoline or hydrogenated isoquinoline ring systems with radicals, substituted by hetero atoms, attached to carbon atoms of the nitrogen-containing ring other than aralkyl radicals
- C07D217/16—Heterocyclic compounds containing isoquinoline or hydrogenated isoquinoline ring systems with radicals, substituted by hetero atoms, attached to carbon atoms of the nitrogen-containing ring other than aralkyl radicals substituted by oxygen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D231/00—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings
- C07D231/02—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings not condensed with other rings
- C07D231/10—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members
- C07D231/12—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members with only hydrogen atoms, hydrocarbon or substituted hydrocarbon radicals, directly attached to ring carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D231/00—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings
- C07D231/54—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings condensed with carbocyclic rings or ring systems
- C07D231/56—Benzopyrazoles; Hydrogenated benzopyrazoles
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D235/00—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, condensed with other rings
- C07D235/02—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, condensed with other rings condensed with carbocyclic rings or ring systems
- C07D235/04—Benzimidazoles; Hydrogenated benzimidazoles
- C07D235/06—Benzimidazoles; Hydrogenated benzimidazoles with only hydrogen atoms, hydrocarbon or substituted hydrocarbon radicals, directly attached in position 2
- C07D235/08—Radicals containing only hydrogen and carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D257/00—Heterocyclic compounds containing rings having four nitrogen atoms as the only ring hetero atoms
- C07D257/02—Heterocyclic compounds containing rings having four nitrogen atoms as the only ring hetero atoms not condensed with other rings
- C07D257/04—Five-membered rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D263/00—Heterocyclic compounds containing 1,3-oxazole or hydrogenated 1,3-oxazole rings
- C07D263/52—Heterocyclic compounds containing 1,3-oxazole or hydrogenated 1,3-oxazole rings condensed with carbocyclic rings or ring systems
- C07D263/54—Benzoxazoles; Hydrogenated benzoxazoles
- C07D263/56—Benzoxazoles; Hydrogenated benzoxazoles with only hydrogen atoms, hydrocarbon or substituted hydrocarbon radicals, directly attached in position 2
- C07D263/57—Aryl or substituted aryl radicals
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D271/00—Heterocyclic compounds containing five-membered rings having two nitrogen atoms and one oxygen atom as the only ring hetero atoms
- C07D271/12—Heterocyclic compounds containing five-membered rings having two nitrogen atoms and one oxygen atom as the only ring hetero atoms condensed with carbocyclic rings or ring systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D277/00—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings
- C07D277/60—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings condensed with carbocyclic rings or ring systems
- C07D277/62—Benzothiazoles
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D277/00—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings
- C07D277/60—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings condensed with carbocyclic rings or ring systems
- C07D277/62—Benzothiazoles
- C07D277/64—Benzothiazoles with only hydrocarbon or substituted hydrocarbon radicals attached in position 2
- C07D277/66—Benzothiazoles with only hydrocarbon or substituted hydrocarbon radicals attached in position 2 with aromatic rings or ring systems directly attached in position 2
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D305/00—Heterocyclic compounds containing four-membered rings having one oxygen atom as the only ring hetero atoms
- C07D305/02—Heterocyclic compounds containing four-membered rings having one oxygen atom as the only ring hetero atoms not condensed with other rings
- C07D305/04—Heterocyclic compounds containing four-membered rings having one oxygen atom as the only ring hetero atoms not condensed with other rings having no double bonds between ring members or between ring members and non-ring members
- C07D305/08—Heterocyclic compounds containing four-membered rings having one oxygen atom as the only ring hetero atoms not condensed with other rings having no double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/04—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/04—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/10—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/12—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/10—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/04—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/10—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains two hetero rings
- C07D487/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D491/00—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00
- C07D491/02—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00 in which the condensed system contains two hetero rings
- C07D491/04—Ortho-condensed systems
- C07D491/044—Ortho-condensed systems with only one oxygen atom as ring hetero atom in the oxygen-containing ring
- C07D491/048—Ortho-condensed systems with only one oxygen atom as ring hetero atom in the oxygen-containing ring the oxygen-containing ring being five-membered
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D495/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having sulfur atoms as the only ring hetero atoms
- C07D495/02—Heterocyclic compounds containing in the condensed system at least one hetero ring having sulfur atoms as the only ring hetero atoms in which the condensed system contains two hetero rings
- C07D495/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D513/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for in groups C07D463/00, C07D477/00 or C07D499/00 - C07D507/00
- C07D513/02—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for in groups C07D463/00, C07D477/00 or C07D499/00 - C07D507/00 in which the condensed system contains two hetero rings
- C07D513/04—Ortho-condensed systems
Abstract
Un compuesto de fórmula I:**Fórmula** en donde: R1 es**Fórmula** L es un anillo monocíclico de 5-10 miembros o alquilo bicíclico o heteroalquilo en donde (i) los miembros del anillo de heteroátomos del heteroalquilo monocíclico o bicíclico de 5-10 miembros se seleccionan independientemente de O, S, o N, y (ii) cada uno del alquilo o heteroalquilo monocíclico o bicíclico de 5-10 miembros o no se sustituye o se sustituye opcionalmente con sustituyentes seleccionados del grupo que consiste de deuterio y -Rb; A y B son independientemente O o S; An es arilo, heteroarilo o heterocicloalquilo monocíclico o bicíclico de 4-10 miembros, en donde (i) dicho heteroarilo o heterocicloalquilo monocíclico o bicíclico de 4-10 miembros tienen 1, 2, 3, o 4 heteroátomos que se seleccionan independientemente de N, S u O, y (ii) cada uno de dichos arilo, heteroarilo o heterocicloalquilo monocíclico o bicíclico de 4-10 miembros, está o bien no sustituido u opcionalmente sustituido independientemente con 1 o más sustituyentes que pueden ser el mismo o diferentes y se seleccionan independientemente del grupo que consiste de deuterio, halo, alquilo, -CHzF3-z, ciano, hidroxilo, hidroxialquilo, amino, aminoalquilo, (amino)alcoxi, -CONH2, -C(O)NH(alquilo), -C(O)N(alquilo)2, - C(O)NH(arilo), -C(O)N(arilo)2, -OCHzF3-z, -alquilo, -alquenilo, alquinilo, alcoxi o (alcoxialquilo)amino -, - N(Rc)-(O)-alquilo, -N(Rc)-C(O)arilo, cicloalquilo, heterocicloalquilo, arilo, y heteroarilo, con la condición de que no hay dos heteroátomos adyacentes en el anillo son ambos S o ambos O; R2 es H o un anillo de arilo, heteroarilo, cicloalquilo, o heterocicloalquilo monocíclico, bicíclico o tricíclico de 4-15 miembros (i) el heteroarilo o heterocicloalquilo monocíclico, bicíclico o tricíclico de 4-15 miembros tiene 1, 2, 3, 4, 5, 6, 7, o 8 heteroátomos que se seleccionan independientemente entre N, S u O, y (ii) en donde cada uno de dicho arilo, heteroarilo, cicloalquilo, y heterocicloalquilo o bien no sustituido o sustituido opcionalmente con 1 o más sustituyentes que pueden ser los mismos o diferentes y se seleccionan independientemente del grupo que consiste en deuterio, halo, ciano, hidroxilo, hidroxilo-alquilo-, hidroxilcicloalquilo-, hidroxilo-heterocicloalquil, aminoalquilo hidroxilo-aril-, hidroxilheteroarilo-, amino, (amino)alcoxi, - CONH2, -C(O)NH(alquilo), -C(O)N(alquilo)2, -C(O)NH(arilo), -C(O)N(arilo)2, -CHzF3-z, - OCHzF3-z, -alquilo, alcoxi, alquenilo, alquinilo, ariloxi, (alcoxialquilo)amino-, cicloalquilo, heterocicloalquilo, (heterocicloalquil)alquilo-, - arilo, heteroarilo, -O(alquilo), -O(cicloalquilo), -O(heterocicloalquilo), -O(arilo), - O(heteroarilo), ONH2, -C(O)NH(alquilo), -C(O)N(arilo)2, -C(O)NH(cicloalquilo), -NH(CO)cicloalquilo, - NH(SO2), -NH(SO2)alquilo, -NH(SO2)arilo, -NH(SO2)heteroarilo, -N(SO2)cicloalquilo, -C(O)N(alquilo)2, (aril)alquilo-, - heteroarilo, (heteroaril)alquilo, -S(O)2alquilo, -S(O)2-arilo, -S(O)2cicloalquilo, -C(O)N(alquilo)2, - (O)alquilo, -NH-C(O)-alquilo, -NH-C(O)-cicloalquilo, NH-(O)heterocicloalquilo, NH-(O)heterocicloalquilo-Rd, -NH-C(O)-Rd-(O)alquilo, -NH-C(O)-arilo, -NH-C(O)-NH-alquilo, NH-C(O)-NH-cicloalquilo, NH2(CO)-alquilo, H-C(O)-NH-arilo, -NH-C(O)-O-alquilo, NH-C(O)-NH-cicloalquilo, -NH-C(O)-O-cicloalquilo, -NH(Rd)-(O)- alquilo, -NH(Rd)-(O)-arilo, -NH(Rd)-SO2)cicloalquilo, -SO2)NH2, -SO2)NH(alquilo), -SO2)N(Rd)cicloalquilo, -SO2)N(alquilo)2, -C(O)N(H)(alquilo), -C(O)N(Rd)(cicloalquilo), metilendioxi, -CHzF3-z, -OCHzF3-z, y alcoxi; Rb es H, halo, C1-C4 alquilo, C1-C3 hidroxilo-alquilo, o C3-C4 cicloalquilo; Rc es H, halo, C1-C4 alquilo, o C3-C4 cicloalquilo; Rd es H, halo, C1-C4 alquilo, o C3-C4 cicloalquilo; y z es 0, 1 ó 2; y las sales farmacéuticamente aceptables de los mismos adicionalmente en donde: R2 no es una forma sustituida o sin sustituir de**Fórmula** en donde X es N o CH; cuando Ar1 es**Fórmula** conectado a**Fórmula** en la posición 1, y X1 y X2 son independientemente N o C-Rz y Ry y Rz son cualquier sustituyente, entonces Rx no incluye alquinilo, alquenilo, arilo, heterocíclico de 5-14 miembros, heteroaromático de 5-14 miembros o carbocíclico de 4-9 miembros; cuando Ar1 es una forma sustituida o no sustituida de un heteroarilo de 5 miembros, Ar1 es una forma sustituida o no sustituida de**Fórmula** y cuando R2 es**Fórmula** A1 no es una forma sustituida o no sustituida de**Fórmula**
Description
DESCRIPCIÓN
Derivados de 2-hidroxi-1-{4-[(4-fenil)fenil]carbonil}piperazin-1-il}etano-1-ona y compuestos relacionados como inhibidores de sintasa de ácido graso (FASN) para el tratamiento del cáncer
Campo de la invención
[0001] La presente invención se refiere a compuestos y composición para la inhibición de la sintasa de ácido graso ("FASN"), su síntesis, aplicaciones y antídoto. Esta aplicación no reclama la prioridad de cualquier otra aplicación.
Antecedentes de la invención
[0002] La sintasa de ácido graso (en adelante "FASN;" también conocido como "FAS") desempeña papeles fundamentales tanto en el metabolismo celular como en la señalización celular. FASN cataliza la formación de ácidos grasos de cadena larga a partir de acetil-CoA, malonil-CoA y nicotinamida adenina dinucleótido fosfato (NADPH), por lo tanto participar en la producción de energía y el almacenamiento, estructura celular y formación de intermediarios en la biosíntesis de las hormonas y otras moléculas biológicamente importantes.
[0003] Una amplia investigación se ha llevado a cabo para estudiar la expresión, función y regulación de ambos genes de codificación de FASN y las diversas formas de proteínas Fasn. Varios estudios indican que FASN está implicado en la oncogénesis andtumor progresión de varios tipos de cáncer. Por ejemplo, FASN amplificación de genes y la sobreexpresión de proteínas se líneas celulares de cáncer de mama humano observedin. (Hunt DA, el carril HM, Zygmont ME, Dervan PA, Hennigar RA (2007), la estabilidad y la sobreexpresión de ARNm de la sintasa de ácido graso en líneas celulares de cáncer de mama humano Anticancer Res 27 (1A): 27-34; Kuhaja FP, (2006) sintasa de ácido graso y el cáncer: Nueva aplicación de una vía antigua Cancer Research, 66 (12) 5977-5980; Menéndez JA, Lupu Rsintasa (2007) Ácidos grasos y el fenotipo lipogénico en la patogénesis del cáncer. Nature Review Cancer, 7, 763-777.) Además, un estudio centrado en los tumores de ovario reveló que los niveles elevados de FASN sirven un indicador de menor supervivencia del sujeto. (Gansler TS, Hardman W, Hunt DA, Schaffel S, Hennigar RA (junio de 1997) El aumento de expresión de la sintasa de ácido graso (OA-519) en tumores de ovario predice una supervivencia más corta Hum Pathol, 28 (6): 686-92). En resumen, la correlación de la expresión de FASN o actividad elevada con alto grado tumoral y etapa avanzada en mama primario, próstata, y cánceres colorrectales ha llamado la atención a la enzima como un posible marcador diana y fármaco de mal pronóstico. 28 (6): 686-92). En resumen, la correlación de la expresión de FASN o actividad elevada con alto grado tumoral y etapa avanzada en mama primario, próstata, y cánceres colorrectales ha llamado la atención a la enzima como un posible marcador diana y fármaco de mal pronóstico. 28 (6): 686-92). En resumen, la correlación de la expresión de FASN o actividad elevada con alto grado tumoral y etapa avanzada en mama primario, próstata, y cánceres colorrectales ha llamado la atención a la enzima como un posible marcador diana y fármaco de mal pronóstico.
[0004] Además de la participación en la oncogénesis, FASN también se ha identificado como un factor que puede influenciar la progresión de enfermedades como la diabetes y los leiomiomas uterinos. En particular, un estudio encontró que un inhibidor de FASN, platensimicina, la reducción de los niveles de glucosa ambientales en modelos de ratón de diabetes. Además, inhibidores de FASN han demostrado ser potencialmente eficaces en la inducción de la pérdida de peso (por ejemplo, EP0869784-A). Del mismo modo, un estudio de todo el genoma sugiere que FASN puede contribuir a la predisposición a leiomiomas uterinos.
[0005] Además, FASN ha sido identificado como una diana para el tratamiento de infecciones microbianas. En particular, síntesis de ácido graso o el nivel de ácido graso se ha reportado ser crítico en la patogénesis viral. Además, FASN ha sido implicado en pathogeneiss de virus humano citomegalovirus (HCMV), los virus de la gripe A y la hepatitis C (Véase, por ejemplo, Mungeret al, Nature Biotechnology, 26: 1179-1186 (2008)). También se ha informado de que la expresión de FASN ha aumentado las células infectadas por virus coxsackie B3 (CVB3), un picornavirus, y la replicación del CVB3 está bloqueada por inhibidores FASN. (Ver Rassmann y otros, Antiviral Research, 76: 150-158 (2007)). Además, FASN se ha informado a ser importante en la replicación viral lítica del virus de Epstein-Barr (EBV). (Li et al, Journal of Virology, 78 (8): 4197 a 4,206 (2004)). FASN también se ha implicado a tener un papel en la replicación del virus del dengue (véase, por ejemplo, Heaton et al, Proc Natl.Acad Sci, 107 (40): 17345-17350 (2010); y Samsa et al., PLoS Pathegens, 5 (10): e1000632 (2009)). Por otra parte, FASN juega un papel importante en la infección por VHC mediante el control de la entrada y la producción viral (Yang W, Capucha BL, Chadwick SL, Watkins, Luo G, Conrads TP, Wang T (2008), sintasa de ácido graso se regula al alza durante la infección de virus de hepatitis C y regula la entrada del virus de la hepatitis C y la producción. Hepatology, 48, 13,967 a 1403)
[0006] Importantes esfuerzos se han centrado en la generación de inhibidores de FASN que pueden ayudar a proporcionar un tratamiento de cáncer y otras enfermedades relacionadas. Un número de inhibidor de familias se han identificado y publicado, como la serie de azabencimidazoles (WO 2011/066211 y las publicaciones relacionadas) y la serie de derivados de sulfonamida (WO2008/075070 y las publicaciones relacionadas) de AstraZeneca Uk Ltd. Sin embargo, debido a la importancia de FASN y las deficiencias en los compuestos publicados, todavía hay una necesidad insatisfecha de inhibidores de FASN potentes y altamente específicos.
[0007] La presente invención introduce un nuevo conjunto de compuestos que inhibe selectivamente actividades FASN y modula el crecimiento y la proliferación de líneas celulares de cáncer. También se incluyen los procesos de síntesis de los nuevos compuestos. Estos compuestos pueden tener implicaciones significativas farmacéuticas en el tratamiento del cáncer, así como otras enfermedades como infecciones virales, obesidad y diabetes.
[0008] WO2013/028495 describe el tratamiento de mieloma múltiple con inhibidores de poli-(ADP-ribosa)polimerasa. CN102627610 describe derivados de bencimidazol para el uso en la supresión de la actividad de poli-(ADP-ribosa)polimerasa y la prevención y tratamiento de tumores, enfermedades isquémicas, diabetes y enfermedades inflamatorias. WO2010/017055 y US2009/197863 divulga inhibidores de actividad poli-(ADP-ribosa) de la polimerasa y el uso de tales compuestos para tratar enfermedades, trastornos y afecciones que mejoran mediante la inhibición de la actividad PARP. WO2005/046685 da a conocer compuestos para uso en la inhibición de la 11betaHSD1, útil en el tratamiento del síndrome metabólico, diabetes y obesity.WO99/16751 describe inhibidores del factor de coagulación Xa, que pueden ser utilizados para prevenir o tratar trastornos tromboembólicos. US2005/043300 describe compuestos que pueden inhibir la interacción de gp120 con CD4, que son de uso en el tratamiento de VIH, una infección retroviral genéticamente relacionada con el VIH, o SIDA. WO2013/028445 da a conocer carboxamidas y carboxamidas inversas y el uso de tales carboxamidas y carboxamidas inversas para la modulación, notablemente la inhibición de la actividad o función de la sintasa de ácido graso (FAS), por ejemplo en el tratamiento de cáncer. Sumario de la invención
[0009] Un aspecto de esta invención es la provisión de compuestos, composiciones, y kits para inhibición de FASN que comprende un compuesto de fórmula I:
en donde
R1 es
L es un anillo monocíclico de 5-10 miembros o alquilo bicíclico o heteroalquilo en donde (i) los miembros del anillo heteroátomo del heteroalquilo monocíclico o bicíclico de 5-10 miembros se seleccionan independientemente de O, S, o N, y (ii) cada uno de los 5-10 miembros monocíclico o bicíclico alquilo o heteroalquilo está o bien sustituido u opcionalmente sustituido con sustituyentes seleccionados del grupo que consiste de deuterio y -Rb;
A y B son independientemente O o S;
Ar1 es
un anillo monocíclico de 4-10 miembros o arilo bicíclico, heteroarilo o heterocicloalquilo, en donde (i) dichos 4-10 miembros monocíclicos o heteroarilo bicíclico o heterocicloalquilo tienen 1, 2, 3 ó 4 heteroátomos que son independientemente seleccionados de N, S u O, y (ii) cada uno de dichos arilo , heteroarilo, o heterocicloalquilo monocíclico o bicíclico de 4-10 miembros es o bien sin sustituir u opcionalmente sustituido independientemente con 1 o más sustituyentes que pueden ser el mismo o diferente y se seleccionan independientemente del grupo que consiste de deuterio, halo, alquilo, - CHzF3-z, ciano, hidroxilo, hidroxialquilo, amino, aminoalquilo, (amino)alcoxi, - CONH2 , -C(O)NH(alquilo), -C(O)N(alquilo)2 , -C(O)NH(arilo), -C(O)N(arilo)2, - OCHzF3-z, -alquilo, -alquenilo, alquinilo, alcoxi o (alcoxialquilo)amino-, -N(Rc)-(O)alquilo, -N(Rc)-C(O)arilo, cicloalquilo, heterocicloalquilo, arilo, y - heteroarilo, con la condición de
que no hay dos heteroátomos de anillo adyacentes son ambos S o ambos O;
R2 es H o un arilo, heteroarilo, cicloalquilo, o heterocicloalquilo monocíclico, bicíclico, o tricíclico de 4-15 miembros, (i) heteroarilo o heterocicloalquilo monocíclico, bicíclico o tricíclico de 4-15 miembros tiene 1, 2, 3, 4, 5, 6, 7, u 8 heteroátomos que se seleccionan independientemente de N, S u O, y (ii) en donde cada uno de dicho arilo, heteroarilo, cicloalquilo, y heterocicloalquilo o bien no sustituido o sustituido opcionalmente con 1 o más sustituyentes que pueden ser el mismo o diferente y se seleccionan independientemente del grupo que consiste de deuterio, halo, ciano, hidroxilo, hidroxilalquil, hidroxilcicloalquilo-, hidroxilo-heterocicloalquilo, hidroxilo-aril-, hidroxilo-heteroaril, amino, aminoalquilo, (amino)alcoxi, - CONH2, -C(O)NH(alquilo), -C(O)N(alquilo)2 , -C(O)NH(arilo), -C(O)N(arilo)2, - CHzF3-z, -OCHzF3-z, -alquilo, alcoxi, alquenilo, alquinilo, ariloxi, (alcoxialquilo)amino-, cicloalquilo, heterocicloalquilo, (heterocicloalquil)alquilo, - arilo, heteroarilo, -O(alquilo), -O(cicloalquilo), -O(heterocicloalquilo), -O(arilo), -O(heteroarilo), ONH2, -C(O)NH(alquilo), -C(O)N(arilo)2 , -C(O)NH(cicloalquilo), -NH(CO)cicloalquilo, -NH(SO2), -NH(SO2)alquilo, -NH(SO2)arilo, -NH(SO2)heteroarilo, -N(SO2)cicloalquilo, -C(O)N(alquilo)2 , (Aril)alquilo, heteroarilo, (heteroaril)alquilo, -S(O)2alquilo, -S(O)2-arilo, -S(O)2cicloalquilo, -C(O)N(alquilo)2 , -C(O)alquilo, -NH-(O)alquilo, -NH-C(O)-cicloalquilo, NH-C(O)heterocicloalquilo, NH-C(O)heterocicloalquilo-Rd, -NH-C(O)-Rd-(O)alquilo, -NH-C(O)-arilo, -NH-C(O)-NH-alquilo, NH-C(O)-NH-cicloalquilo, NH2(CO)-alquilo, NH-C(O)-NH-arilo, -NH-C(O)-O-alquilo, NH-C(O)-NH-cicloalquilo, -NH-C(O)-O-cicloalquilo, -NH(Rd)-(O)-alquilo, -NH(Rd)-(O)-arilo, -NH(Rd)-SO2)cicloalquilo, -S(O2)NH2 , - SO2) NH(alquilo), -S(O2)N(Rd)cicloalquilo, -S(O2)N(alquilo)2 , -C(O)N(H)(alquilo), -C(O)N(Rd)(cicloalquilo), metilendioxi, -CHzF3-z, -Oc HzF3-z, y alcoxi;
Rb es H, halo, C1-C4 alquilo, C1-C3 hidroxilo-alquilo, o C3-C4 cicloalquilo;
Rc es H, halo, C1-C4 alquilo, o C3-C4 cicloalquilo;
Rd es H, halo, C1-C4 alquilo, o C3-C4 cicloalquilo;
y z es 0, 1 ó 2;
y las sales farmacéuticamente aceptables de los mismos;
además en donde:
R2 no es una forma sustituida o sin sustituir de
en donde X es N o CH; cuando An es
conectado a
en la posición 1, y X1 y X2 son independientemente N o C-Rz y Ry y Rz son cualquier sustituyente, entonces Rx no incluye alquinilo, alquenilo, arilo, heterocíclico de 5-14 miembros, heteroaromático de 5-14 miembros o carbocíclico de 4-9 miembros;
cuando Ar1 es una forma sustituida o no sustituida de un heteroarilo de 5 miembros, An es una forma sustituida o no sustituida de
cuando R2 es
Ari no es una forma sustituida o no sustituida de
[0010] Otro aspecto de esta invención es la provisión de compuestos, composiciones, y kits para inhibición de FASN que comprende un compuesto de fórmula I-A:
en donde:
R1 es
Ar1 es un anillo monocíclico de 4-10 miembros o arilo bicíclico, heteroarilo o heterocicloalquilo, en donde (i) dicho heteroarilo o heterocicloalquilo monocíclico o bicíclico de 4-10 miembros tienen 1, 2, 3 ó 4 heteroátomos que son independientemente seleccionados de N, S u O, y (ii) cada uno de dicho arilo , heteroarilo, o heterocicloalquilo monocíclico o bicíclico de 4-10 miembros es o bien sin sustituir u opcionalmente sustituido independientemente con 1 o más sustituyentes que pueden ser el mismo o diferente y se seleccionan independientemente del grupo que consiste de deuterio, halo, alquilo, - CHzF3-z, ciano, hidroxilo, hidroxialquilo, amino, aminoalquilo, (amino)alcoxi, - CONH2 , -C(O)NH(alquilo), -C(O)N(alquilo)2 , -C(O)NH(arilo), -C(O)N(arilo)2 , - OCHzF3-z, -alquilo, -alquenilo, alquinilo, alcoxi o (alcoxialquilo)amino-, -N(Rc)-(O)alquilo, -N(Rc)-C(O)arilo, cicloalquilo, heterocicloalquilo, arilo, y - heteroarilo, con la condición de que no hay dos heteroátomos de anillo adyacente adyacentes son ambos S o ambos O; R2 es H o un arilo, heteroarilo, cicloalquilo, o heterocicloalquilo monocíclico, bicíclico, o tricíclico de 4-15 miembros, (i) heterocicloalquilo o heteroarilo monocíclico, bicíclico o tricíclico de 4-15 miembros tiene 1, 2,
3, 4, 5, 6, 7, o 8 heteroátomos que se seleccionan independientemente de N, S u O, y (ii) en donde cada uno de dichos arilo, heteroarilo, cicloalquilo, y heterocicloalquilo es no sustituido o sustituido opcionalmente con 1 o más sustituyentes que pueden ser los mismos o diferentes y se seleccionan independientemente del grupo que consiste de deuterio, halo, ciano, hidroxilo, hidroxilalquil, hidroxilcicloalquilo-, hidroxiloheterocicloalquilo, hidroxilo-aril-, hidroxilo-heteroaril, amino, aminoalquilo, (amino)alcoxi, - CONH2 , -C(O)NH(alquilo), -C(O)N(alquilo)2 , -C(O)NH(arilo), -C(O)N(arilo)2 , - CHzF3-z, -OCHzF3-z, -alquilo, alcoxi, alquenilo, alquinilo, ariloxi, (alcoxialquilo)amino-, cicloalquilo, heterocicloalquilo, (heterocicloalquil)alquilo, -arilo, heteroarilo, -O(alquilo), -O(cicloalquilo), -O(heterocicloalquilo), -O(arilo), -O(heteroarilo), ONH2 , -C(O)NH(alquilo), -C(O)N(arilo)2 , -C(O)NH(cicloalquilo), -NH(CO)cicloalquilo, -NH(SO2), -NH(SO2)alquilo, -NH(SO2)arilo, -NH(SO2)heteroarilo, -N(SO2)cicloalquilo, -C(O)N(alquilo)2 , (Aril)alquilo, heteroarilo, (heteroaril)alquilo, -S(O)2alquilo, -S(O)2arilo, -S(O)2cicloalquilo, -C(O)N(alquilo)2 , -C(O)alquilo, -NH-(O)alquilo, -NH-C(O)-cicloalquilo, NH-C(O)heterocicloalquilo, NH-C(O)heterocicloalquilo-Rd, -NH-C(O)-Rd-(O)alquilo, -NH-C(O)-arilo, -NH-C(O)-NH-alquilo, NH-C(O)-NH-cicloalquilo, NH2(CO)-alquilo, NH-C(O)-NH-arilo, -NH-C(O)-O-alquilo, NH-C(O)-NH-cicloalquilo, -NH-C(O)-O cicloalquilo, -NH(Rd)-(O)-alquilo, -NH(Rd)-(O)-arilo, -NH(Rd)-SO2)cicloalquilo, -S(O2)NH2 , - SO2)NH(alquilo), -S(O2)N(Rd)cicloalquilo, -S(O2)N(alquilo)2 , -C(O)N(H)(alquilo), -C(O)N(Rd)(cicloalquilo), metilendioxi, -CHzF3-z, -OCHzF3-z, y alcoxi;
Rc es H, halo, C1-C4 alquilo, o C3-C4 cicloalquilo;
Rd es H, halo, C1-C4 alquilo, o C3-C4 cicloalquilo;
y z es 0, 1 ó 2;
y las sales farmacéuticamente aceptables de los mismos.
[0011] Otro aspecto de esta invención es la provisión de compuestos, composiciones, y kits para inhibición de FASN que comprende un compuesto de fórmula I-B:
en donde:
Ar1 es un anillo monocíclico de 4-10 miembros o arilo bicíclico, heteroarilo o heterocicloalquilo, en donde (i) dicho heteroarilo o heterocicloalquilo monocíclico o bicíclico de 4-10 miembros tiene 1, 2, 3, o 4 heteroátomos que se seleccionan independientemente a partir de N, S u O, y (ii) cada uno de dichos arilo, heteroarilo, o heterocicloalquilo monocíclico o bicíclico de 4-10 miembros es o bien no sustituido u opcionalmente sustituido independientemente con 1 o más sustituyentes que pueden ser el mismo o diferente y se seleccionan independientemente del grupo que consiste de deuterio, halo, alquilo, - CHzF3-z, ciano, hidroxilo, hidroxialquilo, amino, aminoalquilo, (amino)alcoxi, - CONH2 , -C(O)NH(alquilo), -C(O)N(alquilo)2 , -C(O)NH(arilo), -C(O)N(arilo)2 , - OCHzF3-z, -alquilo, -alquenilo, alquinilo, alcoxi o (alcoxialquilo)amino-, -N(Rc)-(O)alquilo, -N(Rc)-C(O)arilo, cicloalquilo, heterocicloalquilo, arilo, y - heteroarilo, con la condición de que no hay dos heteroátomos de anillo adyacente adyacentes son ambos S o ambos O; R2 es H o un arilo, heteroarilo, cicloalquilo, o heterocicloalquilo monocíclico, bicíclico, o tricíclico de 4-15 miembros, (i) heterocicloalquilo o heteroarilo monocíclico, bicíclico o tricíclico de 4-15 miembros tiene 1, 2, 3, 4, 5, 6, 7, o 8 heteroátomos que se selecciona independientemente de N, S u O, y (ii) en donde cada uno de dichos arilo, heteroarilo, cicloalquilo, y heterocicloalquilo es no sustituido o sustituido opcionalmente con 1 o más sustituyentes que pueden ser los mismos o diferentes y se seleccionan independientemente del grupo que consiste de deuterio, halo, ciano, hidroxilo, hidroxilalquil, hidroxilcicloalquilo-, hidroxiloheterocicloalquilo, hidroxilo-aril-, hidroxilo-heteroaril, amino, aminoalquilo, (amino)alcoxi, - CONH2 , -C(O)NH(alquilo), -C(O)N(alquilo)2 , -C(O)NH(arilo), -C(O)N(arilo)2 , - CHzF3-z, -OCHzF3-z, -alquilo, alcoxi, alquenilo, alquinilo, ariloxi, (alcoxialquilo)amino-, cicloalquilo, heterocicloalquilo, (heterocicloalquil)alquilo, -arilo, heteroarilo, -O(alquilo), -O(cicloalquilo), -O(heterocicloalquilo), -O(arilo), -O(heteroarilo), ONH2 , -C(O)NH(alquilo), -C(O)N(arilo)2 , -C(O)NH(cicloalquilo), -NH(CO)cicloalquilo, -NH(SO2), -NH(SO2)alquilo, -NH(SO2)arilo, -NH(SO2)heteroarilo, -N(SO2)cicloalquilo, -C(O)N(alquilo)2 , (Aril)alquilo, heteroarilo, (heteroaril)alquilo, -S(O)2alquilo, -S(O)2-arilo, -S(O)2cicloalquilo, -C(O)N(alquilo)2 , -C(O)alquilo, -NH-(O)alquilo, -NH-C(O)-cicloalquilo, NH-C(O)heterocicloalquilo, NH-C(O)heterocicloalquilo-Rd, -NH-C(O)-Rd-(O)alquilo, -NH-C(O)-arilo, -NH-C(O)-NH-alquilo, NH-C(O)-NH-cicloalquilo, NH2 (CO)-alquilo, NH-C(O)-NH-arilo, -NH-C(O)-O-alquilo, NH-C(O)-NH-cicloalquilo, -NH-C(O)-O cicloalquilo, -NH(Rd)-(O)-alquilo, -NH(Rd)-(O)-arilo, -NH(Rd)-SO2)cicloalquilo, -S(O2)NH2 , - SO2)NH(alquilo), -S(O2)N(Rd)cicloalquilo, -S(O2)N(alquilo)2 , -C(O)N(H)(alquilo), -C(O)N(Rd)(cicloalquilo), metilendioxi, -CHzF3-z, -OCzF3-z, y alcoxi;
Rc es H, halo, C1-C4 alquilo, o C3-C4 cicloalquilo;
Rd es H, halo, C1-C4 alquilo, o C3-C4 cicloalquilo;
y z es 0, 1 ó 2;
y las sales farmacéuticamente aceptables de los mismos.
[0012] Otro aspecto de esta invención es la provisión de compuestos, composiciones, y kits para inhibición de FASN que comprende un compuesto de fórmula I-C:
en donde:
R1 es
R2 es H o un anillo monocíclico, bicíclico o tricíclico arilo, heteroarilo, cicloalquilo, o heterocicloalquilo de 4 15 miembros, (i) heteroarilo o heterocicloalquilo monocíclico, bicíclico o tricíclico de 4-15 miembros o tiene 1, 2, 3, 4, 5, 6, 7, o 8 heteroátomos que se seleccionan independientemente de N, S u O, y (ii) en donde cada uno de dichos arilo, heteroarilo, cicloalquilo, y heterocicloalquilo o bien no sustituido o sustituido opcionalmente con 1 o más sustituyentes que pueden ser los mismos o diferentes y se seleccionan independientemente del grupo que consiste en deuterio, halo, ciano, hidroxilo, hidroxilalquil, hidroxilcicloalquilo-, hidroxilo-heterocicloalquil, hidroxilo-aril-, hidroxilo-heteroaril, amino, aminoalquilo, (amino)alcoxi, - CONH2, -C(O)NH(alquilo), -C(O)N(alquilo)2 , -C(O)NH(arilo), -C(O)N(arilo)2, - CHzF3-z, -OCHzF3-z, -alquilo, alcoxi, alquenilo, alquinilo, ariloxi, (alcoxialquilo)amino-, cicloalquilo, heterocicloalquilo, (heterocicloalquil)alquilo, - arilo, heteroarilo, -O(alquilo), -O(cicloalquilo), -O(heterocicloalquilo), -O(arilo), -O(heteroarilo), ONH2 , -C(O)NH(alquilo), -C(O)N(arilo)2 , -C(O)NH(cicloalquilo), -NH(CO)cicloalquilo, -NH(SO2), -NH(SO2)alquilo, -NH(SO2)arilo, -NH(SO2)heteroarilo, -N(SO2)cicloalquilo, -C(O)N(alquilo)2 , (aril)alquilo, heteroarilo, (heteroaril)alquilo, -S(O)2alquilo, -S(O)2-arilo, -S(O)2cicloalquilo, -C(O)N(alquilo)2 , -C(O)alquilo, -NH-(O)alquilo, -NH-C(O)-cicloalquilo, NH-C(O)heterocicloalquilo, NH-C(O)heterocicloalquilo-Rd, -NH-C(O)-Rd-(O)alquilo, -NH-C(O)-arilo, -NH-C(O)-NH-alquilo, NH-C(O)-NH-cicloalquilo, NH2(CO)-alquilo, NH-C(O)-NH-arilo, -NH-C(O)-O-alquilo, NH-C(O)-NH-cicloalquilo, -NH-C(O)-O-cicloalquilo, -NH(Rd)-(O)-alquilo, -NH(Rd)-(O)-arilo, -NH(Rd)-SO2)cicloalquilo, -S(O2)NH2 , - SO2)NH(alquilo), -S(O2)N(Rd)cicloalquilo, -S(O2)N(alquilo)2 , -C(O)N(H)(alquilo), -C(O)N(Rd)(cicloalquilo), metilendioxi, -CHzF3-z, -OCHzF3-z, y alcoxi;
Rd es H, halo, C1-C4 alquilo, o C3-C4 cicloalquilo;
Rq es H, halo, C1-C4 alquilo, o C3-C4 cicloalquilo;
y z es 0, 1 ó 2;
y las sales farmacéuticamente aceptables de los mismos. Otro aspecto de esta invención es la provisión de compuestos, composiciones y kits para la inhibición FASN que comprende un compuesto de fórmula I-D:
(I-D)
en donde:
Ri' es OH o NH2 ;
R2 es H o un arilo, heteroarilo, cicloalquilo, o heterocicloalquilo monocíclico, bicíclico, o tricíclico de 4-15 miembros, (i) heterocicloalquilo o heteroarilo monocíclico, bicíclico o tricíclico de 4-15 miembros tiene 1, 2, 3, 4, 5, 6, 7, o 8 heteroátomos que se seleccionan independientemente de N, S u O, y (ii) en donde cada uno de dichos arilo, heteroarilo, cicloalquilo, y heterocicloalquilo es no sustituido o sustituido opcionalmente con 1 o más sustituyentes que pueden ser los mismos o diferentes y se seleccionan independientemente del grupo que consiste de deuterio, halo, ciano, hidroxilo, hidroxilalquil, hidroxilcicloalquilo-, hidroxiloheterocicloalquilo, hidroxilo-aril-, hidroxilo-heteroaril, amino, aminoalquilo, (amino)alcoxi, - CONH2 , -C(O)NH(alquilo), -C(O)N(alquilo)2 , -C(O)NH(arilo), -C(O)N(arilo)2 , - CHzF3-z, -OCHzF3-z, -alquilo, alcoxi, alquenilo, alquinilo, ariloxi, (alcoxialquilo)amino-, cicloalquilo, heterocicloalquilo, (heterocicloalquil)alquilo, -arilo, heteroarilo, -O(alquilo), -O(cicloalquilo), -O(heterocicloalquilo), -O(arilo), -O(heteroarilo), ONH2 , -C(O)NH(alquilo), -C(O)N(arilo)2 , -C(O)NH(cicloalquilo), -NH(CO)cicloalquilo, -NH(SO2), -NH(SO2)alquilo, -NH(SO2)arilo, -NH(SO2)heteroarilo, -N(SO2)cicloalquilo, -C(O)N(alquilo)2 , (aril)alquilo, heteroarilo, (heteroaril)alquilo, -S(O)2alquilo, -S(O)2-arilo, -S(O)2cicloalquilo, -C(O)N(alquilo)2 , -C(O)alquilo, -NH-(O)alquilo, -NH-C(O)-cicloalquilo, NH-C(O)heterocicloalquilo, NH-C(O)heterocicloalquilo-Rd, -NH-C(O)-Rd-(O)alquilo, -NH-C(O)-arilo, -NH-C(O)-NH-alquilo, NH-C(O)-NH-cicloalquilo, NH2 (CO)-alquilo, NH-C(O)-NH-arilo, -NH-C(O)-O-alquilo, NH-C(O)-NH-cicloalquilo, -NH-C(O)-O cicloalquilo, -NH(Rd)-(O)-alquilo, -NH(Rd)-(O)-arilo, -NH(Rd)-SO2)cicloalquilo, -S(O2)NH2 , - SO2)NH(alquilo), -S(O2)N(Rd)cicloalquilo, -S(O2)N(alquilo)2 , -C(O)N(H)(alquilo), -C(O)N(Rd)(cicloalquilo), metilendioxi, -CHzF3-z, -OCHzF3-z, y alcoxi;
Rd es H, halo, C1-C4 alquilo, o C3-C4 cicloalquilo;
y z es 0, 1 o 2;
y sales farmacéuticamente aceptables de los mismos.
[0013] Otro aspecto de esta invención es la provisión de un compuesto o composición farmacéutica para uso en métodos de tratamiento de una enfermedad a través de la inhibición de FASN en un sujeto (por ejemplo, un humano) en necesidad del mismo administrando al sujeto una cantidad eficaz del compuesto o de la formulación farmacéutica de la presente invención.
[0014] Otra realización preferida es una formulación farmacéutica que comprende un compuesto farmacéuticamente aceptable de la presente invención, que proporciona, tras la administración a un ser humano, una disminución de la carga tumoral y/o metástasis. La formulación farmacéutica se puede administrar por vía oral u otros medios adecuados, por ejemplo, por vía intravenosa o por inyección.
[0015] Sin embargo, otra realización de la descripción es un método de tratamiento de cáncer de ovario en un sujeto (por ejemplo, un humano) en necesidad del mismo mediante la administración al sujeto de una cantidad terapéuticamente eficaz del compuesto o la formulación farmacéutica de la presente invención.
[0016] Sin embargo, otra realización de la descripción es un método de tratamiento de cáncer de colon en un sujeto (por ejemplo, un humano) en necesidad del mismo mediante la administración al sujeto de una cantidad eficaz del compuesto o la formulación farmacéutica de la presente invención.
[0017] Sin embargo, otra realización de la descripción es un método de tratamiento de cáncer de mama en un sujeto (por ejemplo, un humano) en necesidad del mismo mediante la administración al sujeto de una cantidad eficaz de la formulación farmacéutica de la presente invención.
[0018] Sin embargo, otra realización de la descripción es un método de tratamiento de la leucemia en un sujeto (por ejemplo, un humano) en en necesidad del mismo mediante la administración al sujeto de una cantidad eficaz del compuesto o la formulación farmacéutica de la presente invención.
[0019] Sin embargo, otra realización de la descripción es un método de tratamiento de cáncer de colon, antes o después de la resección quirúrgica y/o terapia de radiación, en un sujeto (por ejemplo, un ser humano) en necesidad del mismo mediante la administración al sujeto de una cantidad eficaz del compuesto o la formulación farmacéutica de la presente invención.
[0020] Sin embargo, otra realización de la descripción es un método de tratamiento del cáncer, antes o después de la resección quirúrgica y/o terapia de radiación, en un sujeto (por ejemplo, un ser humano) en necesidad del mismo mediante la administración al sujeto de una cantidad eficaz del compuesto o la formulación farmacéutica de la presente invención, incluyendo terapia coadyuvante para tratar las náuseas, con o sin dexametasona.
[0021] Sin embargo, otra realización de la descripción es un método de tratamiento del cáncer, antes o después de
la resección quirúrgica y/o radioterapia, en un sujeto (por ejemplo, un ser humano) en necesidad del mismo mediante la administración al sujeto de una cantidad eficaz del compuesto o la formulación farmacéutica de la presente invención, incluyendo la terapia adyuvante con uno o más agentes terapéuticos adicionales, o sus sales farmacéuticamente aceptables de los mismos. Los ejemplos no limitantes de tales agentes terapéuticos adicionales incluyen agentes citotóxicos (tales como por ejemplo, pero no limitados a, agentes interactivos de ADN (tales como cisplatin o doxorrubicina)); taxanos (por ejemplo, taxotere, taxol); inhibidores de la topoisomerasa II (tales como etopósido); inhibidores topoisomeraseI (tales como irinotecan (o CPT-11), camptostar, o topotecan); agentes de interacción de tubulina (tales como paclitaxel, docetaxel o las epotilonas); agentes hormonales (tales como tamoxifeno); inhibidores de sintasa de timidilato (tales como 5-fluorouracil o 5-FU); antimetabolitos (tales como metotrexato); agentes alquilantes (tales como temozolomida, ciclofosfamida); inhibidores de transferasa de proteína de farnesil (tales como, SARASAR™ (4-[2-[4-[(11R)-3,10-dibromo-8-cloro-6,11-dihidro-5H-benzo[5,-6]ciclohepta[1,2-b]piridin-11 -il-]-1 -piperidinil]-2-oxoetil]-1 -piperidina-carboxamida, o SCH 66336), tipifarnib (Zarnestra® o R115777 de Janssen Pharmaceuticals), L778, 123 (un inhibidor de la transferasa de proteína de farnesil de Merck & Company, Whitehouse Station, NJ), BMS 214662 (a la transferasa de proteína de farnesil de Bristol-Myers Squibb Pharmaceuticals, Princeton, NJ); inhibidores de transducción de señal (tales como, Iressa® (desde productos farmacéuticos Astra Zeneca, Inglaterra), Tarceva® (inhibidores de cinasa de EGFR), anticuerpos contra EGFR (por ejemplo, C225), GLEEVEC® (inhibidor de quinasa C-abl de Novartis Pharmaceuticals, East Hanover, NJ); interferones tales como, por ejemplo, INTRON® (de Merck & Company), Peg-Intron® (de Merck & Company); combinaciones de terapia hormonal; combinaciones de aromatasa; ara-C, adriamicina, citoxano, y gemcitabina.
[0022] Otros agentes anti-cáncer (también conocido como anti-neoplásicos) incluyen, pero no se limitan a mostaza de uracilo, clormetina, ifosfamida, melfalán, clorambucilo, pipobromán, trietilenmelamina, trietilentiofosforamina, busulfán, carmustina, lomustina, estreptozocina, dacarbazina, floxuridina, citarabina, 6-mercaptopurina, 6-tioguanina, fosfato de fludarabina, oxaliplatino, leucovirina, oxaliplatino (ELOXATIN®. de Sanofi-Synthelabo Pharmaceuticals, Francia), pentostatina, vinblastina, vincristina, vindesina, bleomicina, dactinomicina, daunorubicina, doxorubicina, epirubicina, idarubicina, mitramicina, desoxicoformicina, mitomicina-C, L-asparaginasa, tenipósido 17a-Etinilestradiol, dietilestilbestrol, testosterona, prednisona, fluoximesterona, propionato de dromostanolona, testolactona, acetato de megestrol, metilprednisolona, metiltestosterona, prednisolona, triamcinolona, clorotrianiseno, hidroxiprogesterona, aminoglutetimida, estramustina, acetato de medroxiprogesterona, leuprolida, flutamida, toremifeno, goserelina, cisplatino, carboplatino, hidroxiurea, amsacrina, procarbazina, mitotano, mitoxantrona, levamisol, Navelbeno, anastrazol, Letrazol, capecitabina, Reloxafina, Droloxafina, Hexametilmelamina, Avastin, Herceptin, Bexxar, Velcade, Zevalin, Trisenox, Xeloda, vinorelbina, Porfimer, Erbitux, liposomal, tiotepa, altretamina, melfalán, Trastuzumab, Lerozole, fulvestrant, exemestano, ifosfamida, Rituximab, C225 y Campath, 5-fluorouracilo y leucovorina, con o sin un inhibidor del receptor 5-HT3 (por ejemplo, dolansetron, granisetrón, ondansetrón) con o sin dexametasona.
[0023] Sin embargo, otra realización de la descripción es un método de tratamiento de la diabetes en un sujeto (por ejemplo, un humano) en en necesidad del mismo mediante la administración al sujeto de una cantidad eficaz del compuesto o la formulación farmacéutica de la presente invención.
[0024] Sin embargo, otra realización de la descripción es un método de tratamiento de la obesidad o sobrepeso en un sujeto (por ejemplo, un humano) en necesidad del mismo mediante la administración al sujeto de una cantidad eficaz del compuesto o la formulación farmacéutica de la presente invención.
[0025] Sin embargo, otra realización de la descripción es un método de tratamiento de leiomiomas uterinos en un sujeto (por ejemplo, un humano) en necesidad del mismo mediante la administración al sujeto de una cantidad eficaz del compuesto o la formulación farmacéutica de la presente invención.
[0026] Sin embargo, otra realización de la descripción es un método de tratamiento de infecciones microbianas en un sujeto (por ejemplo, un humano) en necesidad del mismo mediante la administración al sujeto de una cantidad eficaz del compuesto o la formulación farmacéutica de la presente invención.
[0027] Sin embargo, otra realización de la descripción es un método de tratamiento de infecciones virales, incluyendo pero no limitado a infecciones causadas por HCMV, virus de influenza A, Hepatis de virus C, CVB3, virus de picorna, EBC y el virus dengue en un sujeto (por ejemplo, un ser humano) en necesidad del mismo mediante la administración al sujeto de una cantidad eficaz del compuesto o la formulación farmacéutica de la presente invención.
[0028] Si se formula como una dosis fija, tales productos de combinación emplean los compuestos de esta invención dentro del intervalo de dosis descrito en el presente documento (o como es conocido por los expertos en la técnica) y el otro agente farmacéuticamente activo o tratamiento dentro de su intervalo de dosificación. Por ejemplo, se ha encontrado el inhibidor de olomucina de CDC2 actúa sinérgicamente con agentes citotóxicos conocidos en la inducción de apoptosis (J. Cell Sci., (1995) 108, 2897). Los compuestos de la divulgación también pueden ser administrados secuencialmente con agentes anticáncer conocidos o citotóxicos cuando una formulación de combinación es inapropiada. En cualquier tratamiento de combinación, la invención no está limitada en la secuencia de administración; compuestos de las Fórmulas pueden administrarse ya sea antes o después de la administración
del agente anticanceroso o citotóxico conocido. Por ejemplo, la actividad citotóxica de el inhibidor de quinasa dependiente de ciclina flavopiridol se ve afectado por la secuencia de administración con agentes anticancerosos. Cancer Research, (1997) 57, 3375. Tales técnicas están dentro de las habilidades de personas con habilidad en la técnica, así como los médicos tratantes.
[0029] Cualquiera de los métodos antes mencionados puede ser aumentado por la administración de fluidos (tales como agua), diuréticos de bucle, uno o más de un agente quimioterapéutico o antineoplásico, como leucovorina y fluorouracilo, y un agente quimioterapéutico adjuntivo (tales como filgrastim y eritropoyetina), o cualquier combinación de los anteriores.
[0030] También se describe aquí un método para administrar un compuesto de la presente invención a un sujeto (por ejemplo, un humano) en necesidad del mismo mediante la administración al sujeto la formulación farmacéutica de la presente invención.
[0031] Aún otra realización es un método de preparación de una formulación farmacéutica de la presente invención al mezclar al menos un compuesto farmacéuticamente aceptable de la presente invención, y, opcionalmente, aditivos o uno o más excipientes farmacéuticamente aceptables.
[0032] Para preparar composiciones farmacéuticas de los compuestos descritos por esta invención, los vehículos aceptables farmacéuticamente inertes, pueden ser sólidos o líquidos. Las preparaciones en forma sólida incluyen polvos, comprimidos, gránulos dispersables, cápsulas, sellos y supositorios. Los polvos y comprimidos pueden comprender ingrediente activo de aproximadamente 5 a aproximadamente 95 porciento. Los vehículos sólidos adecuados son conocidos en la técnica, por ejemplo, carbonil de magnesio, estearato de magnesio, talco, azúcar o lactosa. Los comprimidos, polvos, sellos y cápsulas pueden usarse como formas de dosificación sólidas adecuadas para administración oral. Los ejemplos de vehículos farmacéuticamente aceptables y métodos de fabricación para diversas composiciones pueden encontrar en A. Gennaro (ed.), Remington Pharmaceutical Sciences, 18a Edición, (1990), Mack Publishing Co., Easton, Pa.
[0033] Las preparaciones en forma líquida incluyen soluciones, suspensiones y emulsiones. Como ejemplo se puede mencionar agua o soluciones de glicol de agua-propileno para inyección parenteral o adición de edulcorantes y opacificantes para soluciones orales, suspensiones y emulsiones. Las preparaciones en forma líquida pueden incluir también soluciones para administración intranasal.
[0034] Las preparaciones en aerosol adecuadas para la inhalación pueden incluir soluciones y sólidos en forma de polvo, que pueden estar en combinación con un vehículo farmacéuticamente aceptable, tal como un gas comprimido inerte, por ejemplo nitrógeno.
[0035] También se incluyen preparaciones en forma sólida que están destinadas a ser convertidas, poco antes del uso, a preparaciones de forma líquida para administración oral o parenteral. Tales formas líquidas incluyen soluciones, suspensiones y emulsiones.
[0036] Los compuestos de la invención también pueden administrarse por vía transdérmica. Las composiciones transdérmicas pueden tomar la forma de cremas, lociones, aerosoles y/o emulsiones y pueden incluirse en un parche transdérmico del tipo matriz o de depósito como son convencionales en la técnica para este propósito.
[0037] Los compuestos de esta invención también se pueden administrar por vía subcutánea.
[0038] Preferiblemente, el compuesto se administra por vía oral o por vía intravenosa.
[0039] Preferiblemente, la preparación farmacéutica está en una forma de dosificación unitaria. En tal forma, la preparación se subdivide en dosis unitarias de tamaño adecuado que contienen cantidades apropiadas del componente activo, por ejemplo, una cantidad eficaz para lograr el propósito deseado.
[0040] La cantidad de compuesto activo en una dosis unitaria de preparación puede variarse o ajustarse desde aproximadamente 1 mg a aproximadamente 1000 mg, preferiblemente de aproximadamente 1 mg a aproximadamente 500 mg, más preferiblemente de aproximadamente 1 mg a aproximadamente 250 mg, aún más preferiblemente de aproximadamente 1 mg a aproximadamente 25 mg, según la aplicación particular.
[0041] La dosificación real empleada puede variarse dependiendo de los requerimientos del paciente y la severidad de la afección a tratar. La determinación del régimen de dosificación apropiado para una situación particular está dentro de la experiencia de la técnica. Por conveniencia, la dosificación diaria total puede ser dividida y administrada en porciones durante el día según se requiera.
[0042] La cantidad y frecuencia de administración de los compuestos de la invención y/o las sales farmacéuticamente aceptables de los mismos se regularán de acuerdo al juicio del asistente clínico considerando tales factores como edad, condición y tamaño del paciente así como la gravedad de los síntomas que están siendo
tratados. Un régimen de dosificación diaria típica recomendada para la administración oral puede variar de aproximadamente 1 mg/día a aproximadamente 500 mg/día, preferiblemente 1 mg/día a 200 mg/día, en dos a cuatro dosis divididas.
Definiciones
[0043] Tal como se usa anteriormente, y en toda esta descripción, los siguientes términos, a menos que se indique otra cosa, se entenderá que tienen los siguientes significados. Si una definición no se encuentra, controla definición de la convención como es conocido para un experto en la técnica.
[0044] "Paciente" incluye tanto seres humanos como animales.
[0045] "Mamífero" significa seres humanos y otros animales mamíferos.
[0046] El término "FASN" se refiere todas las clases, tipos, subtipos, isotipos, segmentos, variantes y formas mutantes de la sintasa de ácido graso.
[0047] El término "inhibidor" se refiere a una molécula tal como un compuesto, un fármaco, un activador enzimático o una hormona que bloquea o de otro modo interfiere con una actividad biológica particular.
[0048] Los términos "cantidad eficaz" o "cantidad terapéuticamente eficaz" se refieren a una cantidad suficiente del agente para proporcionar el resultado biológico deseado. Ese resultado puede ser la reducción y/o alivio de los signos, síntomas, o causa de una enfermedad, o cualquier otra alteración deseada de un sistema biológico. Por ejemplo, una "cantidad eficaz" para uso terapéutico es la cantidad de la composición que comprende un compuesto como se describe en la presente memoria requerida para proporcionar una disminución significativa clínicamente en una enfermedad. Una cantidad "eficaz" apropiada en cualquier caso individual puede ser determinada por alguien de habilidad normal en la técnica usando experimentación de rutina. Por lo tanto, la "cantidad eficaz" de expresión generalmente se refiere a la cantidad para la que la sustancia activa tiene efectos terapéuticos.
[0049] Tal como se utiliza aquí, los términos "tratar" o "tratamiento" son sinónimos con el término "prevenir" y se entiende para indicar un aplazamiento del desarrollo de las enfermedades, la prevención del desarrollo de las enfermedades, y/o reducir la severidad de tales síntomas que se desarrollarán o que se espera que se desarrollarán. Por lo tanto, estos términos incluyen mejorar los síntomas de la enfermedad existentes, prevenir los síntomas adicionales, mejorar o prevenir las causas metabólicas subyacentes de los síntomas, la inhibición del trastorno o enfermedad, por ejemplo, detener el desarrollo del trastorno o enfermedad, aliviar el trastorno o enfermedad, causar regresión del trastorno o enfermedad, el alivio de una condición causada por la enfermedad o trastorno, o la detención o aliviar los síntomas de la enfermedad o trastorno.
[0050] Por "farmacéuticamente aceptable" o "farmacológicamente aceptable" se entiende un material que no es indeseable biológicamente o de otra manera - el material puede administrarse a un individuo sin causar efectos biológicos indeseables o interactuar de manera perjudicial con cualquiera de los componentes de la composición en el que está contenido.
[0051] "Materiales de portador" o lo que también se hace referencia como "excipientes" incluyen cualquiera de los excipientes utilizados habitualmente en farmacia y deberían ser seleccionados sobre la base de la compatibilidad y las propiedades del perfil de liberación de la forma de dosificación deseada. Materiales de soporte de ejemplo incluyen, por ejemplo, aglutinantes, agentes de suspensión, agentes de desintegración, agentes de relleno, agentes tensioactivos, solubilizantes, estabilizantes, lubricantes, agentes humectantes, diluyentes y similares. "Materiales portadores farmacéuticamente compatibles" pueden comprender, por ejemplo, acacia, gelatina, dióxido de silicio coloidal, glicerofosfato de calcio, lactato de calcio, maltodextrina, glicerina, silicato de magnesio, caseinato de sodio, lecitina de soja, cloruro sódico, fosfato tricálcico, fosfato dipotásico, estearoil lactilato de sodio, carragenina, monoglicérido, diglicérido, almidón pregelatinizado, y similares. Ver, p.ej. Hoover, John E., Remington’s Pharmaceutical Sciences, Mack Publishing Co., Easton, Pa. 1975.
[0052] Como se usa en el presente documento, el término "sujeto" incluye mamíferos y no mamíferos. Ejemplos de mamíferos incluyen, pero no se limitan a, cualquier miembro de la clase de mamíferos: seres humanos, primates no humanos tales como chimpancés, y otras especies de simios y monos; animales de granja tales como ganado vacuno, caballos, ovejas, Cabras, cerdos; animales domésticos tales como conejos, perros y gatos; animales de laboratorio incluyendo roedores, tales como ratas, ratones y cobayas, y similares. Ejemplos de no mamíferos incluyen, pero no se limitan a, aves, peces y similares. En una realización de la presente invención, el mamífero es un humano.
[0053] Como se usa en el presente documento, "alquilo" significa una cadena lineal o cadena saturada ramificada que tiene de 1 a 10 átomos de carbono. Grupos alquilo saturados representativos incluyen, pero no se limitan a, metilo, etilo, n-propilo, isopropilo, 2-metil-1 -propilo, 2-metil-2-propilo, 2-metil-1 -butilo, 3-metil-1 -butilo, 2-metil-3-butilo, 2,2-dimetil-1 -propilo, 2-metil-1 -pentilo, 3-metil-1 -pentilo, 4-metil-1 -pentilo, 2-metil-2-pentilo, 3-metil-2-pentilo, 4-metil2-pentilo, 2,2-dimetil-1 -butilo, 3, 3-dimetil-1 -butilo, 2-etil-1 -butilo, butilo, isobutilo, t-butilo, n-pentilo, isopentilo, neopentilo, n-hexilo y similares, y grupos alquilo más largos, tales como heptilo, y octilo y similares. Un grupo alquilo puede estar insustituido o sustituido. Los grupos alquilo que contienen tres o más átomos de carbono pueden ser lineales, ramificados o ciclados. Como se usa en el presente documento, "alquilo inferior" significa un alquilo que tiene de 1 a 6 átomos de carbono.
[0054] Como se usa en este documento, un "alquenilo" incluye una cadena de hidrocarburo no ramificada o ramificada que tiene uno o más dobles enlaces en el mismo. El doble enlace de un grupo alquenilo puede ser conjugado o sin conjugar a otro grupo. Grupos alquenilo ilustrativos insaturados incluyen, pero no se limitan a grupos alquenilo (C2-C8), tales como etilenilo, vinilo, alilo, butenilo, pentenilo, hexenilo, butadienilo, pentadienilo, hexadienilo, 2-etilhexenil, 2-propil-2-butenilo, 4-(2-metil-3-buteno) pentenilo y similares. Un grupo alquenilo puede estar no sustituido o sustituido.
[0055] Como se usa en el presente documento, "alquinilo" incluye una cadena de hidrocarburo no ramificada o ramificada que tiene uno o más triplebonds en el mismo. El enlace triple de un grupo alquinilo puede ser conjugado o sin conjugar a otro grupo. Grupos alquinilo adecuados insaturados incluyen, pero no se limitan a, grupos alquinilo(C2-C6), tales como etinilo, propinilo, butinilo, pentinilo, hexinilo, metilopropinilo, 4-metil-1 -butinilo, 4-propil-2-pentinilo, 4-butil-2-hexinilo y similares. Un grupo alquinilo puede ser no sustituido o sustituido.
[0056] Los términos "trifluorometilo", "sulfonilo", y "carboxilo" incluyen CF3 , SO2, y CO2 H, respectivamente.
[0057] El término "hidroxilo" significa un grupo OH;
[0058] El término hidroxilo alquilo o hidroxialquilo significa un grupo alquilo como se define anteriormente, en donde el grupo alquilo tiene un grupo OH dispuesto sobre el mismo.
[0059] El término "alcoxi" como se usa en este documento incluye -O-(alquilo), donde alquilo se define anteriormente.
[0060] El término "aminoalquilo", como se usa en este documento significa un grupo que tiene uno o más átomos de nitrógeno y uno o más grupos alquilo como se definió anteriormente en el nitrógeno.
[0061] "Aralquilo" o "arilalquilo" significa un grupo arilalquilo en donde se describen como anteriormente el arilo y alquilo. Alquilos preferidos comprenden un grupo alquilo inferior. Los ejemplos no limitantes de grupos aralquilo adecuados incluyen bencilo, 2-fenetilo y naftalenilmetilo. El enlace con el resto parental es a través del alquilo.
[0062] "Heteroarilalquilo" significa un resto heteroarilo como se define aquí unido a través de un resto alquilo (definido anteriormente) a un núcleo parenteral. Los ejemplos no limitantes de heteroarilos adecuados incluyen 2-piridinilmetil, quinolinilmetilo y similares.
[0063] "Heterociclilalquilo" significa un resto heterociclilo, ya definido antes unido a través de un resto alquilo (definido anteriormente) a un núcleo parenteral. Los ejemplos no limitantes de heterociclilalquilos adecuados incluyen piperidinilmetilo, piperazinlmetilo y similares.
[0064] También debe observarse que cualquier carbono así como heteroátomo con valencias no satisfechas en el texto, esquemas, ejemplos y Tablas en este documento se asume que tiene el número suficiente de átomo(s) de hidrógeno para satisfacer las valencias.
[0065] Cuando cualquier variable (por ejemplo, arilo, heterociclo, R2, etc.) aparece más de una vez en cualquier constituyente o en las Fórmulas, su definición en cada ocasión es independiente de su definición en cualquier otra aparición.
[0066] Tal como se utiliza aquí, el término "composición" pretende abarcar un producto que comprende los ingredientes especificados sin las cantidades especificadas, así como cualquier producto que resulte, directa o indirectamente, de la combinación de los ingredientes especificados en las cantidades especificadas.
[0067] El término "deuterio" como se usa en este documento significa un isótopo estable del hidrógeno con un número impar de protones y neutrones.
[0068] El término "halo" como se usa en este documento significa un sustituyente que tiene al menos un halógeno seleccionado de flúor, cloro, bromo, y yodo.
[0069] El término "ciano", como se usa en este documento significa un sustituyente que tiene un átomo de carbono unido a un átomo de nitrógeno por un triple enlace.
[0070] El término "amino" como se usa en este documento significa un sustituyente que contiene al menos un átomo
de nitrógeno.
[0071] El término "(amino)alcoxi" como se usa en este documento significa un sustituyente que tiene al menos un grupo amino y al menos un grupo alcoxi.
[0072] El término "ariloxi" como se usa en este documento significa un sustituyente de la forma Ar-O- en donde Ar es un grupo arilo como se ha definido aquí.
[0073] El término "metilendioxi", como se usa en este documento significa un grupo funcional con la fórmula estructural -O-CH2-O- que está conectado a la molécula mediante dos enlaces químicos a través de los oxígenos.
[0074] Como se usa en este documento, "alcoxialquilo" se refiere a -(alquil)-O-(alquilo), en donde cada "alquilo" es independientemente un grupo alquilo definido anteriormente.
[0075] El término "(alcoxialquilo)amino" como se usa en este documento significa un sustituyente que tiene al menos un grupo alcoxialquilo tal como se define anteriormente y al menos un grupo amino como se define anteriormente.
[0076] Tal como se utiliza aquí, el término "arilo" se refiere a un anillo monocíclico o policíclico condensado, carbociclo aromático (estructura de anillo que tiene átomos en el anillo que son todos de carbono) que tiene de 3 a 24 átomos de anillo por anillo. Los ejemplos ilustrativos de grupos arilo incluyen, pero no se limitan a los siguientes restos:
y similares.
[0077] Arilos sustituidos ilustrativos incluyen:
y similares.
[0078] Tal como se utiliza aquí, el término "heteroarilo" se refiere a un anillo monocíclico o policíclico condensado, heterociclo aromático (estructura de anillo que tiene átomos de anillo seleccionados entre átomos de carbono, así como nitrógeno, oxígeno y azufre) heteroátomos que tienen de 3 a 24 átomos de anillo por anillo. Los ejemplos ilustrativos de grupos heteroarilo y heteroarilo sustituidos incluyen, pero no se limitan a los siguientes restos:
y similares.
[0079] Tal como se utiliza aquí, el término "cicloalquilo" se refiere a un carbociclo saturado o parcialmente saturado, monocíclico o condensado o espiropolicíclico, que tiene de 3 a 24 átomos de anillo por anillo. Los ejemplos ilustrativos de grupos cicloalquilo incluyen, pero no se limitan a, los siguientes restos:
y similares.
[0080] Tal como se utiliza aquí, el término "heterocicloalquilo" se refiere a un anillo monocíclico, o fusionado o espiro, policíclicos, estructura de anillo está saturada o parcialmente saturada y tiene de 3 a 24 átomos de anillo por anillo seleccionados de átomos de C y heteroátomos N, O, y S. Los ejemplos ilustrativos de heterocicloalquilo y grupos heterocicloalquilo sustituidos se incluyen, pero no se limitan a:
y similares.
[0081] Los intervalos numéricos, como se usan en el presente documento, pretenden incluir números enteros secuenciales. Por ejemplo, un intervalo expresado "de 0 a 4" incluiría 0, 1,2, 3 y 4.
[0082] Tal como se usa en el presente documento, los términos "arilo, heteroarilo, cicloalquilo, o heterocicloalquilo monocíclico, bicíclico, o tricíclico," significan que cualquier anillo de una estructura bicíclica o tricíclica puede estar independientemente arilo, heteroarilo, cicloalquilo, o heterocicloalquilo en un sistema fusionado orto o orto y peri.
[0083] Tal como se utiliza aquí, el término "sustituido" significa que el grupo o resto porta uno o más sustituyentes especificados en donde los sustituyentes pueden conectarse al grupo o resto especificado en una o más posiciones. Por ejemplo, un arilo sustituido con un cicloalquilo puede indicar que el cicloalquilo se conecta a un átomo del arilo con un enlace o mediante la fusión con el arilo y compartiendo dos o más átomos de comunes.
[0084] Tal como se utiliza aquí, el término "no sustituido" significa que el grupo especificado no lleva sustituyentes.
[0085] Tal como se utiliza aquí, el término "opcionalmente sustituido" significa que el grupo especificado está sin sustituir o sustituido por uno o más sustituyentes.
[0086] Cuando se muestra un resto multifuncional, el punto de unión al núcleo puede ser identificado por una línea. P.ej. (cicloalquiloxi)alquilo- se refiere a que alquilo es el punto de unión al núcleo, mientras que cicloalquilo está unido a alquilo por medio del grupo oxi. En ausencia de una línea, puede ser asumida la unión en cualquier posición.
[0087] La expresión "agente quimioterapéutico adyuvante" se refiere generalmente a agentes que tratan, alivian, mitigan o mejoran los efectos secundarios de los agentes quimioterapéuticos. Tales agentes incluyen los que modifican el crecimiento de las células sanguíneas y maduración. Ejemplos de agentes quimioterapéuticos adyuvantes incluyen, pero no se limitan a, filgrastim y eritropoyetina. Otros de tales agentes quimioterapéuticos adyuvantes incluyen los que inhiben las náuseas asociadas con administración de los agentes quimioterapéuticos, tales como inhibidor del receptor 5-HT3 (por ejemplo, dolansetrón, granisetrón, ondansetrón o), con o sin dexametasona.
[0088] Los términos "agente quimioterapéutico" y "agente antineoplásico" generalmente se refieren a agentes que tratan, previenen, curan, sanan, alivian, mitigan, alteran, remedian, mejoran, mejoran, o afectan malignidades y sus metástasis. Ejemplos de tales agentes (también conocidos como "agentes antineoplásicos") incluyen, pero no se limitan a, prednisona, fluorouracilo (por ejemplo, 5-fluorouracilo (5-FU)), anastrozol, bicalutamida, carboplatino, cisplatino, clorambucilo, cisplatino, carboplatino, docetaxel, doxorubicina, flutamida, interferón-alfa, letrozol, leuprolida, megestrol, mitomicina, oxaliplatino, paclitaxel, plicamicina (Mithracin™), tamoxifeno, tiotepa, topotecan, valrubicina, vinblastina, vincristina, y cualquier combinación de cualquiera de lo expuesto. Adicionalmente tales agentes se describen más adelante.
[0089] Hay que señalar que, tal como se utiliza en la especificación y las reivindicaciones adjuntas, las formas singulares "un", "una", "el" y “ella” incluyen referentes plurales a menos que el contexto indique claramente lo contrario.
[0090] Cuando se utiliza como un agente terapéutico los inhibidores de la FASN (FASN) descritos en el presente documento pueden ser administrados con uno o más excipientes fisiológicamente aceptables. Un vehículo o excipiente fisiológicamente aceptable es una formulación a la que el compuesto se puede añadir para que se disuelva o de otra manera facilitar su administración.
[0091] Las formas de dosificación de la presente invención pueden contener una mezcla de uno o más compuestos de esta invención, y pueden incluir materiales adicionales conocidos por los expertos en la técnica como excipientes farmacéuticos. Aditivos estabilizantes pueden incorporarse en la solución de agente de entrega. Con algunas drogas, la presencia de tales aditivos promueve la estabilidad y dispersabilidad del agente en solución. Los aditivos estabilizantes se pueden emplear a una concentración desde alrededor de 0,1 a 5% (P/V), preferiblemente de aproximadamente 0,5% (P/V). Adecuados, pero no limitativos, los ejemplos de aditivos estabilizantes incluyen goma arábiga, gelatina, metilcelulosa, polietilenglicol, ácidos carboxílicos y sales de los mismos, y polilisina. Los aditivos estabilizantes son goma arábiga, gelatina y metilcelulosa.
[0092] Agentes acidificantes (ácido acético, ácido acético glacial, ácido cítrico, ácido fumárico, ácido clorhídrico, ácido clorhídrico diluido, ácido málico, ácido nítrico, ácido fosfórico, ácido fosfórico diluido, ácido sulfúrico, ácido tartárico); propelentes de aerosoles (butano, diclorodifluorometano, diclorotetrafluoroetano, isobutano, propano, tricloromonofluorometano); desplazamientos de aire (dióxido de carbono, nitrógeno); desnaturalizantes de alcohol (benzoato de denatonio, metil isobutil cetona, sucrose octacetato de sacarosa); agentes alcalinizantes (solución de amoniaco fuerte, carbonil de amonio, dietanolamina, diisopropanolamina, hidróxido de potasio, bicarbonato de sodio, borato de sodio, carbonil de sodio, hidróxido de sodio, trolamina); antiaglomerantes (ver deslizante); agentes antiespumantes (dimeticona, simeticona); conservantes antimicrobianos (cloruro de benzalconio, solución de cloruro de benzalconio, cloruro de benceltonio, ácido benzoico, alcohol bencílico, butilparabeno, cetilpiridiniocloruro, clorobutanol, clorocresol, cresol, ácido deshidroacético, etilparabeno, metilparabeno, metilparabeno de sodio, fenol, alcohol feniletílico, acetato fenilmercúrico, nitrato fenilmercúrico, benzoato de potasio, sorbato de potasio, propilparabeno, propilparabeno sódico, benzoato sódico, dehidroacetato de sodio, propionato de sodio, ácido sórbico, timerosal, el timol); antioxidantes (ácido ascórbico, palmitato de ascorbilo, hidroxianisol butilado, hidroxitolueno butilado, ácido hipofosforoso, monotioglicerol, galato de propilo, formaldehído sulfoxilato de sodio, metabisulfito de sodio, tiosulfato de sodio, dióxido de azufre, tocoferol, excipiente de tocoferoles); los agentes tampón (ácido acético, carbonil de amonio, fosfato de amonio, ácido bórico, ácido cítrico, ácido láctico, ácido fosfórico, citrato de potasio, metafosfato de potasio, fosfato de potasio monobásico, acetato de sodio, citrato de sodio, solución de lactato de sodio, fosfato de sodio dibásico, sodio monobásico fosfato); lubricantes cápsula (ver tabletas y lubricante de cápsulas); Los agentes quelantes (edetato disódico, ácido etilendiaminotetraacético y sales, ácido edético); los agentes de recubrimiento (carboximetilcelulosa de sodio, acetato de celulosa, ftalato de acetato de celulosa, etilcelulosa, gelatina, esmalte farmacéutico, hidroxipropilcelulosa, hidroxipropilmetilcelulosa, ftalato de hidroxipropilmetilcelulosa, copolímero de ácido metacrílico, metilcelulosa, polietilenglicol, acetato ftalato de polivinilo, goma laca, sacarosa, dióxido de titanio, cera de carnauba, cera microcristalina, zeína); colorantes (caramelo, rojo, amarillo, negro o mezclas, óxido férrico); agentes complejantes (ácido etilendiaminotetraacético y sales (EDTA), ácido etilendiaminotetraacético y sales, ácido edético, ácido gentísico, etanolmaide, sulfato de oxiquinolina); los desecantes (cloruro de calcio, sulfato de calcio, dióxido de silicio); los agentes emulsionantes y/o solubilizantes
(acacia, colesterol, dietanolamina (adyuvantes), monoestearato de glicerilo, alcoholes de lanolina, lecitina, mono y diglicéridos, monoetanolamina (adyuvantes) ácido oleico (adyuvantes) alcohol oleilo (estabilizante), poloxámero, estearato de polioxietileno 50, aceite de ricino de polioxilo 40, polisorbato 20, polisorbato 40, polisorbato 60, polisorbato 80, diacetato de propilenglicol, monoestearato de propilglicol, sulfato de laurilo sódico, estearato sódico, monolaurato de sorbitán, monooleato de sorbitán, monopalmitato de sorbitán, monoestearato de sorbitán, ácido esteárico, trolamina, cera emulsionante); ayudas de filtrado (celulosa en polvo, tierra silícea purificada); sabores y perfumes (anetol, benzaldehído, etil vainillina, mentol, salicilato de metilo, glutamato monosódico, aceite de flor de naranja, menta, aceite de menta, alcohol de menta, aceite de rosa, agua de rosas más fuerte, timol, tintura tolu bálsamo, vainilla, tintura de vainilla, vainillina); los deslizantes y agentes/antiaglomerantes (silicato de calcio, silicato de magnesio, dióxido de silicio coloidal, talco); los humectantes (glicerina, hexilenglicol, propilenglicol, sorbitol); plastificantes (aceite de ricino, monoglicéridos diacetilados, ftalato de dietilo, glicerina, mono y diglicéridos diacetilados, polietilenglicol, propilenglicol, triacetina, citrato de trietilo); polímeros (por ejemplo, acetato de celulosa, celulosas de alquilo, hidroxialquilocelulosas, polímeros acrílicos y copolímeros); los disolventes (acetona, alcohol, alcohol diluido, hidrato de amileno, benzoato de bencilo, alcohol butílico, tetracloruro de carbono, cloroformo, aceite de maíz, aceite de semilla de algodón, acetato de etilo, glicerina, hexilenglicol, alcohol isopropílico, alcohol metílico, cloruro de metileno, metil isobutil cetona, aceite mineral, aceite de cacahuete, polietilenglicol, carbonil de propileno, propilenglicol, aceite de sésamo, agua para inyección, agua estéril para inyección, agua estéril para irrigación, agua purificada); sorbentes (polvo de celulosa, carbón de leña, tierras silíceas purificadas); sorbentes dióxido de carbono (cal hidróxido de bario, de sosa y cal); agentes de refuerzo (aceite de ricino hidrogenado, ceto estearil alcohol, alcohol cetílico, cera de ésteres de cetilo, grasa dura, parafina, excipiente polietileno, alcohol estearílico, cera emulsionante, cera blanca, cera amarilla); suspensión y/o agentes que incrementan la viscosidad (acacia, agar, ácido algínico, monoestearato de aluminio, bentonita, bentonita purificada, bentonita magma, carbómero 934P, carboximetilcelulosa de calcio, carboximetilcelulosa de sodio, carboximetilcelulosa de sodio 12, carragenina, microcristalina y carboximetilcelulosa de sodio de celulosa, dextrina, gelatina, goma guar, hidroxietil celulosa, hidroxipropil celulosa, hidroxipropil metilcelulosa, silicato de aluminio y magnesio, metilcelulosa, pectina, óxido de polietileno, alcohol polivinílico, povidona, glicolalginato de propileno, dióxido de silicio, dióxido de silicio coloidal, alginato de sodio, goma de tragacanto, goma de xantano); los agentes edulcorantes (aspartamo, dextratos, dextrosa, dextrosa excipiente, fructosa, manitol, sacarina, sacarina de calcio, sacarina de sodio, sorbitol, solución de sorbitol, sacarosa, azúcar compresible, azúcar de confitería, jarabe); aglutinantes de comprimidos (acacia, ácido algínico, carboximetilcelulosa de sodio, microcristalinacelulosa, dextrina, etilcelulosa, gelatina, glucosa líquida, goma guar, hidroxipropil metilcelulosa, metilcelulosa, óxido de polietileno, povidona, almidón pregelatinizado, jarabe); diluyentes comprimidos y/o de cápsula (carbonil de calcio, fosfato de calcio dibásico, fosfato de calcio tribásico, sulfato de calcio, microcristalinacelulosa, celulosa en polvo, dextratos, dextrina, excipiente de dextrosa, fructosa, caolín, lactosa, manitol, sorbitol, almidón, almidón pregelatinizado, sacarosa, azúcar compresible, azúcar de pastelería); disgregantes de comprimidos (ácido algínico, microcristalinacelulosa, croscarmelosa de sodio, corspovidona, polacrilina de potasio, glicolato de almidón sódico, almidón, almidón pregelatinizado); lubricantes en tableta y/o cápsula (estearato de calcio, behenato de glicerilo, estearato de magnesio, aceite mineral ligero, polietilenglicol, estearil fumarato de sodio, ácido esteárico, ácido esteárico purificado, talco, aceite hidrogenado vegetal, estearato de zinc); agente de tonicidad (dextrosa, glicerina, manitol, cloruro de potasio, cloruro de sodio); vehículo: sabor y/o azucarada (elixir aromático, compuesto elixir benzaldehído, elixir iso-alcohólico, agua de menta, sorbitolsolution, jarabe, jarabe de bálsamo de Tolú); Vehículo: oleaginosa (aceite de almendras, aceite de maíz, aceite de algodón, oleato de etilo, miristato de isopropilo, palmitato de isopropilo, aceite mineral, aceite mineral ligero, alcohol de miristilo, octildodecanol, aceite de oliva, aceite de cacahuete, persicoil, aceite de sésamo, aceite de soja, escualeno); vehículo: vehículo sólido (esferas de azúcar); vehículo: estéril (agua bacteriostática para inyección, inyección de cloruro de sodio bacteriostático); aumento de viscosidad (ver agente de suspensión); agente repelente al agua (ciclometicona, dimeticona, simeticona); y agente humectante y/o solubilizante (cloruro de benzalconio, cloruro de benzetonio, cloruro de cetilpiridinio, sodio de docusato, nonoxinol 9, nonoxinol 10, octoxinol 9, poloxámero, aceite de ricino de polioxil 35, de polioxilo 40, aceite de ricino hidrogenado, polioxil 50 estearato, polioxil 10 oleil éter, polioxil 20, cetoesteariléter, estearato de polioxilo 40, polisorbato 20, polisorbato 40, polisorbato 60, polisorbato 80, lauril sulfato de sodio, monolaurato de sorbitán, monooleato de sorbitán, monopalmitato de sorbitán, monoestearato de sorbitán, tiloxapol) pueden ser usedos como excipientes. Esta lista no pretende ser exclusiva, pero en su lugar meramente representativa de las clases de excipientes y los excipientes particulares que se pueden usar en formas de dosificación de la presente invención.
[0093] Los compuestos de Fórmulas I, I-A, I-B, I-C y I-D se pueden formar sales que también están dentro del alcance de esta invención. La referencia a un compuesto de la Fórmula en el presente documento se entiende que incluye referencia a sales del mismo, unlessotherwise indicado. El término "sal (es)", como se emplea aquí, denota sales ácidas formadas con ácidos inorgánicos y/o organicacids, así como sales básicas formadas con inorgánica y/o bases orgánicas. Además, cuando un compuesto de la Fórmula contiene tanto un resto básico, tales como, pero sin limitación, una piridina o imidazol, como un resto ácido, tal como, pero no limitado a un ácido carboxílico, zwitteriones ("sales internas") pueden ser y se incluyen dentro del término "sal(es)" como se utiliza aquí. Se prefieren sales farmacéuticamente aceptables (es decir, no tóxicas, fisiológicamente aceptables), aunque otras sales también son útiles. Las sales de los compuestos de la fórmula pueden estar formadas, por ejemplo, por reacción de un compuesto de Fórmula con una cantidad de ácido o base, tal como una cantidad equivalente, en un medio tal como uno en donde la sal se precipita o en un medio acuoso seguido de liofilización.
[0094] Sales de adición de ácido ejemplares incluyen acetatos, ascorbatos, benzoatos, bencenosulfonatos, bisulfatos, boratos, butiratos, citratos, canforatos, canforsulfonatos, fumaratos, hidrocloruros, hidrobromuros, hidroyoduros, lactatos, maleatos, metanosulfonatos, naftalenosulfonatos, nitratos, oxalatos, fosfatos, propionatos, salicilatos, succinatos, sulfatos, tartratos, tiocianatos, toluenosulfonatos (también conocidos como tosilatos) y similares. Además, ácidos que se consideran generalmente adecuados para la formación de sales farmacéuticamente útiles de compuestos farmacéuticamente básicos, por ejemplo, por P. Stahl et al, Camille G. (eds.) Handbook of Pharmaceutical Salts. Properties, Selection and Use. (2002) Zurich: Wiley-VCH; S. Berge et al, Journal of Pharmaceutical Sciences (1977) 66 (1) 1-19; P. Gould, J. International J. of Pharmaceutics (1986) 33201 -217; Anderson et al, The Practice of Medicinal Chemistry (1996), Academic Press, Nueva York; y en The Orange Book (Food & Drug Administration, Washington, DC, y en su web). Estas descripciones se incorporan en este documento por referencia.
[0095] Las sales básicas ejemplares incluyen sales de amonio, sales de metales alcalinos tales como sodio, litio, y sales de potasio, sales de metales alcalinotérreos tales como sales de calcio y magnesio, sales con bases orgánicas (por ejemplo, aminas orgánicas) tales como diciclohexilaminas, t-butil aminas, y sales con aminoácidos tales como arginina, lisina y similares. Grupos que contienen nitrógeno básico pueden cuaternizarse con agentes tales como haluros de alquilo inferior (por ejemplo metilo, etilo y butilcloruros, bromuros y yoduros), sulfatos de dialquilo (por ejemplo sulfatos de dimetilo, dietilo, y dibutilo), haluros de cadena larga (p.ej. decilo, laurilo, y cloruros de estearilo, bromuros y yoduros), haluros de aralquilo (por ejemplo bromuros de bencilo y fenetilo), y otros.
[0096] Todas las sales de ácidos y sales de bases pretenden ser sales farmacéuticamente aceptables dentro del alcance de la invención y todas las sales ácidas y básicas se consideran equivalentes a las formas libres de los correspondientes compuestos para los propósitos de la invención.
[0097] Los compuestos de las diversas fórmulas, y sales, solvatos y ésteres de los mismos, pueden existir en su forma tautomérica (por ejemplo, como una amida o imino éter). Todas estas formas tautoméricas se contemplan en el presente documento como parte de la presente invención.
[0098] Los compuestos de las diversas fórmulas pueden contener centros asimétricos o quirales, y, por lo tanto, existir formas estereoisoméricas indiferente. Se pretende que todas las formas estereoisoméricas de los compuestos de las diversas fórmulas así como mezclas de los mismos, incluyendo mezclas racémicas, forman parte de la presente invención. Además, la presente invención abarca todos los isómeros geométricos y posicionales. Por ejemplo, si un compuesto de las diversas fórmulas incorporan un doble enlace o un anillo condensado, tanto las formas cis y trans, así como mezclas, están abarcadas dentro del alcance de la invención. Cada compuesto desvelado en este documento incluye todos los enantiómeros que se ajustan a la estructura general del compuesto. Los compuestos pueden estar en una forma racémica o enantioméricamente pura, o cualquier otra forma en términos de estereoquímica.
[0099] Las mezclas diastereoméricas pueden separarse en sus diastereómeros individuales sobre la base de sus diferencias fisicoquímicas por métodos bien conocidos por los expertos en la técnica, tales como, por ejemplo, por cromatografía y/o cristalización fraccional. Los enantiómeros pueden separarse convirtiendo la mezcla enantiomérica en una mezcla diastereomérica por reacción con un compuesto ópticamente activo apropiado (por ejemplo, auxiliar quiral tal como un alcohol quiral cloruro de ácido de Mosher), separando los diastereómeros y convirtiendo (por ejemplo, hidrolizando) los diastereómeros a los correspondientes enantiómeros puros. Además, algunos de los compuestos de las diversas fórmulas pueden ser atropisómeros (por ejemplo, biarilos sustituidos) y se consideran como parte de esta invención. Los enantiómeros también pueden separarse mediante el uso de una columna quiral de HPLC.
[0100] También es posible que los compuestos de las diversas fórmulas pueden existir en diferentes formas tautoméricas, y tales formas están abarcadas dentro del alcance de la invención. También, por ejemplo, todas las formas ceto-enol e imina-enamina de los compuestos se incluyen en la invención.
[0101] Todos los estereoisómeros (por ejemplo, isómeros geométricos, isómeros ópticos y similares) de los presentes compuestos (incluyendo los de las sales, solvatos, ésteres y profármacos de los compuestos así como las sales, solvatos y ésteres de los profármacos), tales como los que pueden existir debido a carbonos asimétricos en diversos sustituyentes, incluyendo formas enantioméricas (que pueden existir incluso en ausencia de carbonos asimétricos), formas rotaméricas, atropisómeros y formas diastereoméricas, se contemplan dentro del alcance de esta invención, como lo son los isómeros posicionales (tal como, por ejemplo, 4-piridilo y 3-piridilo). (Por ejemplo, si un compuesto de las diversas fórmulas incorpora un doble enlace o un anillo condensado, tanto las formas cis como trans, así como mezclas, están abarcadas dentro del alcance de la invención. También, por ejemplo, todas las formas ceto-enol e imina-enamina de los compuestos se incluyen en la invención.) Los estereoisómeros individuales de los compuestos de la invención pueden, por ejemplo, estar sustancialmente libres de otros isómeros, o pueden estar mezclados, por ejemplo, como racematos o con todos los demás, u otros estereoisómeros seleccionados. Los centros quirales de la presente invención pueden tener la configuración S o R como se define por las IUPAC 1974 Recommendations. El uso de los términos "sal", "solvato", "éster", y similares, pretende aplicarse igualmente a la sal, solvato y éster de enantiómeros, estereoisómeros, rotámeros, tautómeros, isómeros posicionales o racematos de los
compuestos de la invención.
[0102] La presente invención también abarca compuestos marcados isotópicamente de la presente invención que son idénticos a los citados en el presente documento, pero por el hecho de que uno o más átomos se reemplazan por un átomo que tiene el número de una masa atómica o masa diferente de la masa atómica o número másico usualmente encontrado en la naturaleza. Ejemplos de isótopos que pueden ser incorporados en los compuestos de la invención incluyen isótopos de hidrógeno, carbono, nitrógeno, oxígeno, fósforo, flúor y cloro, tales como 2H, 3H, 13C, 14C, 15N, 18O, 17O, 31P, 32P, 35S, 18F, y 36Cl, respectivamente.
[0103] Ciertos compuestos marcados isotópicamente de las diversas fórmulas (por ejemplo, los marcados con 3H y 14C) son útiles en ensayos de compuesto y/o de distribución en tejidos sustrato. Los isótopos tritiados (es decir, 3H) y carbono-14 (es decir, 14C) los isótopos son particularmente preferidos por su facilidad de preparación y detectabilidad. Además, la sustitución con isótopos más pesados tales como deuterio (es decir, 2H) puede proporcionar ciertas ventajas terapéuticas resultantes de una mayor estabilidad metabólica (por ejemplo, aumento en vida media in vivo o menores requisitos de dosificación) y por lo tanto puede preferirse en algunas circunstancias. Compuestos etiquetadas isotópicamente de las diversas fórmulas se pueden preparar generalmente siguiendo procedimientos análogos a los descritos en los Esquemas y/o en los Ejemplos más adelante, sustituyendo un reactivo apropiado marcado isotópicamente por un reactivo no marcado isotópicamente.
[0104] Las formas polimórficas de los compuestos de las diversas fórmulas y de las sales, solvatos y ésteres de los compuestos de las diversas fórmulas, están destinadas a ser incluidas en la presente invención.
[0105] Ventajas de la presente invención incluyen la administración oral de una cantidad óptima de un inhibidor de FASN.
[0106] Ventajas de la presente invención incluyen la administración intravenosa de una cantidad óptima de un inhibidor de FASN.
[0107] Ventajas de la presente invención incluyen la administración intraperitoneal de una cantidad óptima de un inhibidor de FASN.
[0108] Ventajas de la presente invención incluyen la administración intramural de una cantidad óptima de un inhibidor de FASN.
[0109] Ventajas de la presente invención incluyen la administración intramuscular de una cantidad óptima de un inhibidor de FASN.
[0110] Ventajas de la presente invención incluyen la administración subcutánea de una cantidad óptima de un inhibidor de FASN.
[0111] Ventajas de la presente invención incluyen la administración intra-tumor de una cantidad óptima de un inhibidor de FASN.
[0112] Ventajas de la presente invención incluyen la administración intratecal de una cantidad óptima de un inhibidor de FASN.
[0113] Ventajas de la presente invención incluyen la administración subdural de una cantidad óptima de un inhibidor de FASN.
[0114] Ventajas de la presente invención incluyen la administración periorbital de una cantidad óptima de un inhibidor de FASN.
[0115] Basándose en estos resultados, la presente invención tiene implicaciones importantes para el diseño de nuevas estrategias de tratamiento para los pacientes con cáncer, incluyendo leucemias y tumores sólidos, enfermedades inflamatorias, infecciones virales, osteoporosis, aterosclerosis; síndrome del intestino irritable o inflamatorio; diabetes, la obesidad y otras condiciones descritas aquí o que son conocidas por los expertos en la técnica.
Descripción de las realizaciones preferidas
[0116] Un aspecto de la presente invención se refiere a compuestos descritos en este documento.
[0117] Un aspecto de la presente invención se refiere a compuestos que son o pueden ser inhibidores de FASN.
[0118] Un aspecto de la presente descripción se refiere al uso de un inhibidor de FASN para la preparación de un medicamento usado en el tratamiento, prevención, inhibición o eliminación de tumores.
[0119] Un aspecto de la presente descripción se refiere al uso de un inhibidor de FASN para la preparación de un medicamento usado en el tratamiento, prevención, inhibición o eliminación del cáncer.
[0120] Un aspecto de la presente descripción se refiere al uso de un inhibidor de FASN para la preparación de un medicamento usado en el tratamiento, prevención, inhibición o eliminación de cáncer, donde el cáncer se selecciona de leucemia, linfoma, cáncer de ovario, cáncer de mama, cáncer de útero, cáncer de colon, cáncer de cuello uterino, cáncer de pulmón, cáncer de próstata, cáncer de piel, cáncer del SNC, cáncer de vejiga, cáncer de páncreas y enfermedad de Hodgkin.
[0121] Un aspecto de la presente descripción se refiere al uso de un inhibidor de FASN para la preparación de un medicamento usado en el tratamiento, prevención, inhibición o eliminación de la diabetes.
[0122] Un aspecto de la presente descripción se refiere al uso de un inhibidor de FASN para la preparación de un medicamento usado en el tratamiento, prevención, inhibición o eliminación de las enfermedades infecciosas virales.
[0123] Un aspecto de la presente descripción se refiere al uso de un inhibidor de FASN para la preparación de un medicamento usado en el tratamiento, prevención, inhibición o eliminación de sobrepeso u obesidad.
[0124] Un aspecto de la presente descripción se refiere al uso de un inhibidor de FASN para la preparación de un medicamento usado en el tratamiento, prevención, inhibición o eliminación de los leiomiomas uterinos.
[0125] La presente invención también describe uno o más métodos de síntesis de los compuestos de la presente invención.
[0126] La descripción también describe uno o más usos de los compuestos de la presente invención.
[0127] La descripción también describe uno o más usos de los compuestos de la presente invención con un agente adjunto tales como el uso con TNF, G-SF, u otros agentes quimioterapéuticos.
[0128] La descripción también describe uno o más usos de las composiciones farmacéuticas de la presente invención.
[0129] Un aspecto de la presente descripción se refiere al uso como un inhibidor de FASN para la preparación de un medicamento usado en el tratamiento de enfermedades inflamatorias.
[0130] Un aspecto de la presente descripción se refiere al uso como un inhibidor de FASN para la preparación de un medicamento usado en el tratamiento de enfermedades inflamatorias, tales como síndrome de intestino irritable o la enfermedad inflamatoria intestinal.
[0131] Un aspecto de la presente descripción se refiere al uso como un inhibidor de FASN para la preparación de un medicamento usado en el tratamiento de la enfermedad ósea tal como osteoporosis.
[0132] Un aspecto de la presente descripción se refiere al uso como un inhibidor de FASN para la preparación de un medicamento usado en el tratamiento de enfermedad del sistema cardiovascular, tales como la aterosclerosis.
[0133] Un aspecto de la presente descripción se refiere al uso como un inhibidor de FASN para la preparación de un medicamento usado en el tratamiento de una enfermedad o una condición causada por un nivel elevado de FASN.
[0134] Dicha enfermedad o afección es una o más seleccionadas del grupo que consiste en cáncer, cáncer de ovario, cáncer de mama, cáncer de útero, cáncer de colon, cáncer cervical, cáncer de pulmón, cáncer de próstata, cáncer de piel, cáncer de vejiga, cáncer pancreático, leucemia, linfoma, enfermedad de Hodgkin, infecciones virales, virus de inmunodeficiencia humana, virus de la hepatitis, virus del herpes, herpes simplex, trastornos inflamatorios, síndrome del intestino irritable, enfermedad inflamatoria intestinal, artritis reumatoide, asma, enfermedad pulmonar obstructiva crónica, osteoartritis, osteoporosis, dermatitis, dermatitis atóptica, psoriasis, lupus eritematoso sistémico, esclerosis múltiple, artritis psoriásica, espondilitis anquilosante, enfermedad de injerto contra huésped, accidente cerebrovascular, aterosclerosis, diabetes, glomerulonephiritis, síndrome metabólico, cáncer de pulmón de células no pequeñas, cáncer de pulmón de células, mieloma múltiple, linfomas, cánceres de células escamosas, cáncer de riñón, cáncer uretral y de la vejiga, cánceres de cabeza y cuello, cáncer de cerebro y sistema nervioso central (SNC).
[0135] Los compuestos de la invención pueden ser útiles en la terapia de enfermedades proliferativas tales como cáncer, enfermedades autoinmunes, enfermedades virales, enfermedades fúngicas, trastornos neurológicos/neurodegenerativos, artritis, inflamación, anti-proliferativa (por ejemplo, retinopatía ocular), neuronal, alopecia y enfermedad cardiovascular. Muchas de estas enfermedades y trastornos son enumerados en la Patente de los Estados Unidos. No. 6,413,974.
[0136] Más específicamente, los compuestos pueden ser útiles en el tratamiento de una variedad de cánceres, incluyendo (pero no limitado a) los siguientes: carcinoma, incluyendo el de vejiga, mama, colon, riñón, hígado, pulmón, incluyendo cáncer de pulmón de las células pequeñas, cáncer de pulmón de las células no pequeñas, cabeza y cuello, esófago, vesícula biliar, ovario, páncreas, estómago, cuello del útero, tiroides, próstata y piel, incluyendo carcinoma de células escamosas; tumores hematopoyéticos de linaje linfoide, incluyendo leucemia, leucemia linfocítica aguda, leucemia linfoblástica aguda, linfoma de células B, linfoma de células T, linfoma de Hodgkins, linfoma no Hodgkin, linfoma de células pilosas, linfoma de células del manto, mieloma y linfoma de Burkett; tumores hematopoyéticos de linaje mieloide, incluyendo leucemias mielógenas agudas y crónicas, síndrome mielodisplásico y leucemia promielocítica; tumores de origen mesenquimal.
[0137] Los compuestos de la invención pueden inducir o inhibir la apoptosis.
[0138] Los compuestos de la invención también pueden ser útiles en la quimioprevención del cáncer. La quimioprevención se define como inhibir el desarrollo de cáncer invasivo bloqueando el evento mutagénico iniciador o bloqueando la progresión de las células pre-malignas que ya han sufrido una recidiva tumoral insulto o inhibidora.
[0139] Un aspecto adicional de la descripción es un método de inhibición de FASN en un animal, dicho método comprende administrar a dicho animal una cantidad farmacéuticamente aceptable de un compuesto de la invención a un animal en necesidad del mismo.
[0140] Un aspecto adicional de la invención es una formulación farmacéutica que comprende un compuesto de la invención.
[0141] Otra realización de la invención comprende una formulación farmacéutica de la invención, en donde la formulación farmacéutica, tras la administración a un ser humano, da como resultado una disminución de la carga tumoral.
[0142] Todavía otra realización de la invención es una formulación farmacéutica, que comprende además uno o más de un agente antineoplásico, un agente quimioterapéutico, o un agente quimioterapéutico adyuvante.
[0143] Las formulaciones farmacéuticas de la invención pueden comprender además una cantidad terapéutica eficaz de un agente quimioterapéutico adyuvante.
[0144] El agente quimioterapéutico adyuvante puede ser un agente que modifica el crecimiento de células de la sangre y maturation. Ejemplos no limitantes de agente quimioterapéutico adyuvante son filgrastim, pegfilgrastim y la eritropoyetina.
[0145] La descripción también está dirigida a un método de tratamiento o prevención de un trastorno asociado con la tasa de crecimiento excesiva de células en un mamífero que comprende administrar al mamífero una cantidad eficaz de la formulación farmacéutica de la invención. Los ejemplos no limitantes de trastornos incluyen el cáncer o metástasis de tumores malignos.
[0146] Otro aspecto de la descripción es un método de inhibición de crecimiento de células tumorales y la tasa de división en un mamífero con cáncer, u otro trastorno asociado con células anormalmente divisorias que comprende administrar al mamífero una cantidad efectiva de la formulación farmacéutica de esta invención.
[0147] Otra realización de la descripción es un método para tratar el dolor de huesos debido a un crecimiento excesivo de un tumor o metástasis al hueso en un mamífero en necesidad del mismo que comprende administrar al mamífero una cantidad eficaz de la formulación farmacéutica de esta invención.
[0148] Todavía otra realización de la invención es un método para la administración de una compoundto un mamífero en necesidad del mismo que comprende la administración al mamífero de la formulación farmacéutica de la invención. En una realización que contiene inhibidor de FASN, el mamífero es un humano.
[0149] Una realización adicional de la invención es un método de preparación de una formulación farmacéutica que comprende el compuesto mixingat menos un vehículo farmacéuticamente aceptable de la presente invención, y, opcionalmente, uno o más excipientes o aditivos farmacéuticamente aceptables.
[0150] La invención también se dirige a métodos para sintetizar compuestos de la presente invención.
Compuestos de la Invención
[0151] La presente invención se refiere a moléculas particulares y sales farmacéuticamente aceptables o isómeros de las sales. La invención se refiere además a moléculas que son útiles en la inhibición de la sintasa de ácido graso de la enzima (FASN) y sales farmacéuticamente aceptables o isómeros de las mismas.
[0152] La invención se refiere a compuestos como se describe en este documento y sales farmacéuticamente aceptables o isómeros de las mismas, y composiciones farmacéuticas que comprenden uno o más compuestos como se describe aquí y sales farmacéuticamente aceptables o isómeros de las mismas. Un aspecto de esta invención es la provisión de compuestos, composiciones, y kits para inhibición de FASN que comprende un compuesto de fórmula I:
en donde
R1 es
L es un alquilo monocíclico o bicíclico de 5-10 miembros o heteroalquilo en donde (i) los miembros del anillo heteroátomo del heteroalquilo monocíclico o bicíclico de 5-10 miembros se seleccionan independientemente de O, S, o N, y (ii) cada uno del alquilo monocíclico o bicíclico de 5-10 miembros o heteroalquilo es o bien sustituido u opcionalmente no sustituido con sustituyentes seleccionados del grupo que consiste de deuterio y -Rb;
A y B son independientemente O o S;
Ar1 es un anillo monocíclico de 4-10 miembros o arilo bicíclico, heteroarilo o heterocicloalquilo, en donde (i) dicho heteroarilo o heterocicloalquilo monocíclico o bicíclico de 4-10 miembros tienen 1, 2, 3 ó 4 heteroátomos que son independientemente seleccionados de N, S u O, y (ii) cada uno de dichos arilo, heteroarilo, o heterocicloalquilo monocíclico o bicíclico de 4-10 miembros es o bien sin sustituir u opcionalmente sustituido independientemente con 1 o más sustituyentes que pueden ser el mismo o diferente y se seleccionan independientemente del grupo que consiste de deuterio, halo, alquilo, - CHzF3-z, ciano, hidroxilo, hidroxialquilo, amino, aminoalquilo, (amino)alcoxi, - CONH2 , -C(O)NH(alquilo), -C(O)N(alquilo)2, -C(O)NH(arilo), -C(O)N(arilo)2, - OCHzF3-z, -alquilo, -alquenilo, alquinilo, alcoxi o (alcoxialquilo)amino-, -N(Rc)-(O)alquilo, -N(Rc)-C(O)arilo, cicloalquilo, heterocicloalquilo, arilo, y - heteroarilo, con la condición de que no hay dos heteroátomos de anillo adyacente adyacentes son ambos S o ambos O;
R2 es H o un arilo, heteroarilo, cicloalquilo, o heterocicloalquilo monocíclico, bicíclico, o tricíclico de 4-15 miembros, (i) heterocicloalquilo o heteroarilo monocíclico, bicíclico o tricíclico de 4-15 miembros tiene 1, 2, 3, 4, 5, 6, 7, o 8 heteroatomos que se seleccionan independientemente de N, S u O, y (ii) en donde cada uno de dicho arilo, heteroarilo, cicloalquilo, y heterocicloalquilo o bien no sustituido o sustituido opcionalmente con 1 o más sustituyentes que pueden ser iguales o diferentes y se seleccionan independientemente del grupo que consiste de deuterio, halo, ciano, hidroxilo, hidroxilalquilo-, hidroxilcicloalquilo-, hidroxilo-heterocicloalquilo, hidroxilo-aril-, hidroxilo-heteroarilo, amino, aminoalquilo, (amino)alcoxi, - CONH2 , -C(O)NH(alquilo), -C(O)N(alquilo)2 , -C(O)NH(arilo), -C(O)N(arilo)2 , - CHzF3-z, -OCHzF3-z, -alquilo, alcoxi, alquenilo, alquinilo, ariloxi, (alcoxialquilo)amino-, cicloalquilo, heterocicloalquilo, (heterocicloalquil)alquilo, - arilo, heteroarilo, -O(alquilo), -O(cicloalquilo), -O(heterocicloalquilo), -O(arilo), -O(heteroarilo), ONH2 , -C(O)NH(alquilo), -C(O)N(arilo)2 , -C(O)NH(cicloalquilo), -NH(CO)cicloalquilo, -NH(SO2), -NH(SO2)alquilo, -NH(SO2)arilo,
NH(SO2)heteroarilo, -N(SO2)cicloalquilo, -C(O)N(alquilo)2, (aril)alquilo, heteroarilo, (heteroaril)alquilo, -S(O)2alquilo, -S(O)2-arilo, -S(O)2cicloalquilo, -C(O)N(alquilo)2, -C(O)alquilo, -NH-(O)alquilo, -NH-C(O)-cicloalquilo, NH-C(O)heterocicloalquilo, NH-C(O)heterocicloalquilo-Rd, -NH-C(O)-Rd-(O)alquilo, -NH-C(O)-arilo, -NH-C(O)-NH-alquilo, NH-C(O)-NH-cicloalquilo, NH2 (CO)-alquilo, NH-C(O)-NH-arilo, -NH-C(O)-O-alquilo, NH-C(O)-NH-cicloalquilo, -NH-C(O)-O cicloalquilo, -NH(Rd)-(O)-alquilo, -NH(Rd)-(O)-arilo, -NH(Rd)-SO2)cicloalquilo, -S(O2)NH2 , - SO2)NH(alquilo), -S(O2)N(Rd)cicloalquilo, -S(O2)N(alquilo)2 , -C(O)N(H)(alquilo), -C(O)N(Rd)(cicloalquilo), metilendioxi, -CHzF3-z, -OCHzF3-z, y alcoxi;
Rb es H, halo, C1-C4 alquilo, C1-C3 hidroxilo-alquilo, o C3-C4 cicloalquilo;
Rc es H, halo, C1-C4 alquilo, o C3-C4 cicloalquilo;
Rd es H, halo, C1-C4 alquilo, o C3-C4 cicloalquilo;
y z es 0, 1 ó 2;
y las sales farmacéuticamente aceptables de los mismos;
además en donde:
R2 no es una forma sustituida o sin sustituir de
en donde X es N o CH
cuando Ar1 es
contectado a
en la posición 1, y X1 y X2 son independientemente N o C-Rz, y Ry y Rz son cualquier sustituyente, entonces Rx no incluye alquinilo, alquenilo, arilo, heterocíclico de 5-14 miembros, heteroaromático de 5-14 miembros o carbocíclico de 4-9 miembros;
cuando Ar1 es una forma sustituida o no sustituida de un heteroarilo de 5 miembros, An es una forma sustituida o no sustituida de
y cuando R2 es
Ari no es una forma sustituida o no sustituida
de o
[0153] En otra realización, el compuesto de Fórmula I está representado por el compuesto de Fórmula I-A:
en donde:
R1 es
o
Ar1 es un anillo monocíclico de 4-10 miembros o arilo bicíclico, heteroarilo o heterocicloalquilo, en donde (i) dicho heteroarilo monocíclico o bicíclico de 4-10 miembros o heterocicloalquilo tienen 1, 2, 3 ó 4 heteroátomos que son independientemente seleccionados de N, S u O, y (ii) cada uno de dichos arilo, heteroarilo, o heterocicloalquilo monocíclico o bicíclico de 4-10 miembros es o bien sin sustituir u opcionalmente sustituido independientemente con 1 o más sustituyentes que pueden ser el mismo o diferente y se seleccionan independientemente del grupo que consiste de deuterio, halo, alquilo, - CHzF3-z, ciano, hidroxilo, hidroxialquilo, amino, aminoalquilo, (amino)alcoxi, - CONH2 , -C(O)NH(alquilo), -C(O)N(alquilo)2, -C(O)NH(arilo), -C(O)N(arilo)2 , - OCHzF3-z, -alquilo, -alquenilo, alquinilo, alcoxi o (alcoxialquilo)amino-, -N(Rc)-(O)alquilo, -N(Rc)-C(O)arilo, cicloalquilo, heterocicloalquilo, arilo, y - heteroarilo, con la condición de que no hay dos heteroátomos de anillo adyacente adyacentes son ambos S o ambos O;
R2 es H o un arilo, heteroarilo, cicloalquilo, o heterocicloalquilo monocíclico, bicíclico, o tricíclico de 4-15 miembros, (i) heterocicloalquilo o heteroarilo monocíclico, bicíclico o tricíclico de 4-15 miembros tiene 1, 2, 3, 4, 5, 6, 7, o 8 heteroátomos que se seleccionan independientemente de N, S u O, y (ii) en donde cada uno de
dichos arilo, heteroarilo, cicloalquilo, y heterocicloalquilo es no sustituido o sustituido opcionalmente con 1 o más sustituyentes que pueden ser los mismos o diferentes y se seleccionan independientemente del grupo que consiste de deuterio, halo, ciano, hidroxilo, hidroxilalquil, hidroxilcicloalquilo-, hidroxilo-heterocicloalquilo, hidroxilo-aril-, hidroxilo-heteroaril, amino, aminoalquilo, (amino)alcoxi, - CONH2 , -C(O)NH(alquilo), -C(O)N(alquilo)2 , -C(O)NH(arilo), -C(O)N(arilo)2 , - CHzF3-z, -OCHzF3-z, -alquilo, alcoxi, alquenilo, alquinilo, ariloxi, (alcoxialquilo)amino-, cicloalquilo, heterocicloalquilo, (heterocicloalquil)alquilo, - arilo, heteroarilo, -O(alquilo), -O(cicloalquilo), -O(heterocicloalquilo), -O(arilo), -O(heteroarilo), ONH2 , -C(O)NH(alquilo), -C(O)N(arilo)2 , -C(O)NH(cicloalquilo), -NH(CO)cicloalquilo, -NH(SO2), -NH(SO2)alquilo, -NH(SO2)arilo, -NH(SO2)heteroarilo, -N(SO2)cicloalquilo, -C(O)N(alquilo)2 , (aril)alquilo, heteroarilo, (heteroaril)alquilo, -S(O)2alquilo, -S(O)2-arilo, -S(O)2cicloalquilo, -C(O)N(alquilo)2 , -C(O)alquilo, -NH-(O)alquilo, -NH-C(O)-cicloalquilo, NH-C(O)heterocicloalquilo, NH-C(O)heterocicloalquilo-Rd, -NH-C(O)-Rd-(O)alquilo, -NH-C(O)-arilo, -NH-C(O)-NH-alquilo, NH-C(O)-NH-cicloalquilo, NH2(CO)-alquilo, NH-C(O)-NH-arilo, -NH-C(O)-O-alquilo, NH-C(O)-NH-cicloalquilo, -NH-C(O)-O cicloalquilo, -NH(Rd)-(O)-alquilo, -NH(Rd)-(O)-arilo, -NH(Rd)-SO2)cicloalquilo, -S(O2)NH2 , - SO2)NH(alquilo), -S(O2)N(Rd)cicloalquilo, -S(O2)N(alquilo)2, -C(O)N(H)(alquilo), -C(O)N(Rd)(cicloalquilo), metilendioxi, -CHzF3-z, -OCHzF3-z, y alcoxi;
Rc es H, halo, C1-C4 alquilo, o C3-C4 cicloalquilo;
Rd es H, halo, C1-C4 alquilo, o C3-C4 cicloalquilo;
y z es 0, 1 ó 2;
y las sales farmacéuticamente aceptables de los mismos.
[0154] En otra realización, el compuesto de Fórmula I está representado por el compuesto de Fórmula I-B:
En donde:
Ar1 es un arilo, heteroarilo o heterocicloalquilo monocíclico o bicíclico de 4-10 miembros, en donde (i) dicho heteroarilo monocíclico o bicíclico de 4-10 miembros o heterocicloalquilo tienen 1, 2, 3 ó 4 heteroátomos que son independientemente seleccionados de N, S u O, y (ii) cada uno de dichos arilo, heteroarilo, o heterocicloalquilo monocíclico o bicíclico de 4-10 miembros es o bien sin sustituir u opcionalmente sustituido independientemente con 1 o más sustituyentes que pueden ser el mismo o diferente y se seleccionan independientemente del grupo que consiste de deuterio, halo, alquilo, - CHzF3-z, ciano, hidroxilo, hidroxialquilo, amino, aminoalquilo, (amino)alcoxi, - CONH2 , -C(O)NH(alquilo), -C(O)N(alquilo)2 , -C(O)NH(arilo), -C(O)N(arilo)2 , - OCHzF3-z, -alquilo, -alquenilo, alquinilo, alcoxi o (alcoxialquilo)amino-, -N(Rc)-(O)alquilo, -N(Rc)-C(O)arilo, cicloalquilo, heterocicloalquilo, arilo, y - heteroarilo, con la condición de que no hay dos heteroátomos de anillo adyacente adyacentes son ambos S o ambos O;
R2 es H o un arilo, heteroarilo, cicloalquilo, o heterocicloalquilo monocíclico, bicíclico, o tricíclico de 4-15 miembros, (i) heterocicloalquilo o heteroarilo monocíclico, bicíclico o tricíclico de 4-15 miembros tiene 1, 2, 3, 4, 5, 6, 7, u 8 heteroátomos que se seleccionan independientemente de N, S u O, y (ii) en donde cada uno de dichos arilo, heteroarilo, cicloalquilo, y heterocicloalquilo es no sustituido o sustituido opcionalmente con 1 o más sustituyentes que pueden ser iguales o diferentes y se seleccionan independientemente del grupo que consiste en deuterio, halo, ciano, hidroxilo, hidroxilalquil, hidroxilcicloalquilo-, hidroxilo-heterocicloalquilo, hidroxilo-aril-, hidroxilo-heteroaril, amino, aminoalquilo, (amino)alcoxi, - CONH2 , -C(O)NH(alquilo), -C(O)N(alquilo)2 , -C(O)NH(arilo), -C(O)N(arilo)2 , - CHzF3-z, -OCHzF3-z, -alquilo, alcoxi, alquenilo, alquinilo, ariloxi, (alcoxialquilo)amino-, cicloalquilo, heterocicloalquilo, (heterocicloalquil)alquilo, - arilo, heteroarilo, -O(alquilo), -O(cicloalquilo), -O(heterocicloalquilo), -O(arilo), -O(heteroarilo), ONH2 , -C(O)NH(alquilo), -C(O)N(arilo)2 , -C(O)NH(cicloalquilo), -NH(CO)cicloalquilo, -NH(SO2), -NH(SO2)alquilo, -NH(SO2)arilo, -NH(SO2)heteroarilo, -N(SO2)cicloalquilo, -C(O)N(alquilo)2 , (aril)alquilo, heteroarilo, (heteroaril)alquilo, -S(O)2alquilo, -S(O)2-arilo, -S(O)2cicloalquilo, -C(O)N(alquilo)2 , -C(O)alquilo, -NH-(O)alquilo, -NH-C(O)-cicloalquilo, NH-C(O)heterocicloalquilo, NH-C(O)heterocicloalquilo-Rd, -NH-C(O)-Rd-(O)alquilo, -NH-C(O)-arilo, -NH-C(O)-NH-alquilo, NH-C(O)-NH-cicloalquilo, NH2(CO)-alquilo, NH-C(O)-NH-arilo, -NH-C(O)-O-alquilo, NH-C(O)-NH-cicloalquilo, -NH-C(O)-O cicloalquilo, -NH(Rd)-(O)-alquilo, -NH(Rd)-(O)-arilo, -NH(Rd)-SO2)cicloalquilo, -S(O2)NH2 , -SO2)NH(alquilo), -S(O2)N(Rd)cicloalquilo, -S(O2)N(alquilo)2 , -C(O)N(H)(alquilo), -C(O)N(Rd)(cicloalquilo), metilendioxi, -CHzF3-z, -OCHzF3-z, y alcoxi;
Rc es H, halo, C1-C4 alquilo, o C3-C4 cicloalquilo;
Rd es H, halo, C1-C4 alquilo, o C3-C4 cicloalquilo; y z es 0, 1 ó 2; y las sales farmacéuticamente aceptables de
los mismos.
[0155] En otra realización, el compuesto de Fórmula I está representado por el compuesto de Fórmula I-C:
en donde:
R1 es
R2 es H o un arilo, heteroarilo, cicloalquilo, o heterocicloalquilo monocíclico, bicíclico, o tricíclico de 4-15 miembros, (i) heterocicloalquilo o heteroarilo monocíclico, bicíclico o tricíclico de 4-15 miembros tiene 1, 2, 3, 4, 5, 6, 7, o 8 heteroátomos que se seleccionan independientemente de N, S u O, y (ii) en donde cada uno de dichos arilo, heteroarilo, cicloalquilo, y heterocicloalquilo es no sustituido o sustituido opcionalmente con 1 o más sustituyentes que pueden ser los mismos o diferentes y se seleccionan independientemente del grupo que consiste de deuterio, halo, ciano, hidroxilo, hidroxilalquil, hidroxilcicloalquilo-, hidroxilo-heterocicloalquilo, hidroxilo-aril-, hidroxilo-heteroaril, amino, aminoalquilo, (amino)alcoxi, - CONH2 , -C(O)NH(alquilo), -C(O)N(alquilo)2 , -C(O)NH(arilo), -C(O)N(arilo)2 , - CHzF3-z, -OCHzF3-z, -alquilo, alcoxi, alquenilo, alquinilo, ariloxi, (alcoxialquilo)amino-, cicloalquilo, heterocicloalquilo, (heterocicloalquil)alquilo, - arilo, heteroarilo, -O(alquilo), -O(cicloalquilo), -O(heterocicloalquilo), -O(arilo), -O(heteroarilo), ONH2 , -C(O)NH(alquilo), -C(O)N(arilo)2 , -C(O)NH(cicloalquilo), -NH(CO)cicloalquilo, -NH(SO2), -NH(SO2)alquilo, -NH(SO2)arilo, -NH(SO2)heteroarilo, -N(SO2)cicloalquilo, -C(O)N(alquilo)2 , (aril)alquilo, heteroarilo, (heteroaril)alquilo, -S(O)2alquilo, -S(O)2-arilo, -S(O)2cicloalquilo, -C(O)N(alquilo)2 , -C(O)alquilo, -NH-(O)alquilo, -NH-(O)cicloalquilo, C-NH(O)heterocicloalquilo, NH-C(O)heterocicloalquilo-Rd, -NH-C(O)-Rd-(O)alquilo, -NH-C(O)-arilo, -NH-C(O)-NH-alquilo, NH-C(O)-NH-cicloalquilo, NH2 (CO)-alquilo, NH-C(O)-NH-arilo, -NH-C(O)-O-alquilo, NH-C(O)-NH-cicloalquilo, -NH-C(O)-O cicloalquilo, -NH(Rd)-(O)-alquilo, -NH(Rd)-(O)-arilo, -NH(Rd)-SO2)cicloalquilo, -S(O2)NH2 , - SO2)NH(alquilo), -S(O2)N(Rd)cicloalquilo, -S(O2)N(alquilo)2 , -C(O)N(H)(alquilo), -C(O)N(Rd)(cicloalquilo), metilendioxi, -CHzF3-z, -OCHzF3-z, y alcoxi;
Rd es H, halo, C1-C4 alquilo, o C3-C4 cicloalquilo;
Rq es H, halo, C1-C4 alquilo, o C3-C4 cicloalquilo;
y z es 0, 1 ó 2;
y las sales farmacéuticamente aceptables de los mismos.
[0156] En otra realización, el compuesto de Fórmula I está representado por el compuesto de Fórmula I-D:
en donde:
Ri' es OH o NH2 ;
R2 es H o un arilo, heteroarilo, cicloalquilo, o heterocicloalquilo monocíclico, bicíclico, o tricíclico de 4-15 miembros, (i) heterocicloalquilo o heteroarilo monocíclico, bicíclico o tricíclico de 4-15 miembros tiene 1, 2, 3, 4, 5, 6, 7, o 8 heteroátomos que se seleccionan independientemente de N, S u O, y (ii) en donde cada uno de dichos arilo, heteroarilo, cicloalquilo, y heterocicloalquilo es no sustituido o sustituido opcionalmente con 1 o más sustituyentes que pueden ser los mismos o diferentes y se seleccionan independientemente del grupo que consiste de deuterio, halo, ciano, hidroxilo, hidroxilalquil, hidroxilcicloalquilo-, hidroxilo-heterocicloalquilo, hidroxilo-aril-, hidroxilo-heteroaril, amino, aminoalquilo, (amino)alcoxi, - CONH2 , -C(O)NH(alquilo), -C(O)N(alquilo)2, -C(O)NH(arilo), -C(O)N(arilo)2, - CHzF3-z, -OCHzF3-z, alquilo, alcoxi, alquenilo, alquinilo, ariloxi, (alcoxialquilo)amino-, cicloalquilo, heterocicloalquilo, (heterocicloalquil)alquilo, - arilo, heteroarilo, -O(alquilo), -O(cicloalquilo), -O(heterocicloalquilo), -O(arilo), -O(heteroarilo), ONH2 , -C(O)NH(alquilo), -C(O)N(arilo)2 , -C(O)NH(cicloalquilo), -NH(CO)cicloalquilo, -NH(SO2), -NH(SO2)alquilo, -NH(SO2)arilo, -NH(SO2)heteroarilo, -N(SO2)cicloalquilo, -C(O)N(alquilo)2, (aril)alquilo, heteroarilo, (heteroaril)alquilo, -S(O)2alquilo, -S(O)2-arilo, -S(O)2cicloalquilo, -C(O)N(alquilo)2 , -C(O)alquilo, -NH-(O)alquilo, -NH-C(O)-cicloalquilo, NH-C(O)heterocicloalquilo, NH-C(O)heterocicloalquilo-Rd, -NH-C(O)-Rd-(O)alquilo, -NH-C(O)-arilo, -NH-C(O)-NH-alquilo, NH-C(O)-NH-cicloalquilo, NH2 (CO)-alquilo, NH-C(O)-NH-arilo, -NH-C(O)-O-alquilo, NH-C(O)-NH-cicloalquilo, -NH-C(O)-O cicloalquilo, -NH(Rd)-(O)-alquilo, -NH(Rd)-(O)-arilo, -NH(Rd)-SO2)cicloalquilo, -S(O2)NH2 , - SO2)NH(alquilo), -S(O2)N(Rd)cicloalquilo, -S(O2)N(alquilo)2 , -C(O)N(H)(alquilo), -C(O)N(Rd)(cicloalquilo), metilendioxi, -CHzF3-z, -OCHzF3-z, y alcoxi;
Rd es H, halo, C1-C4 alquilo, o C3-C4 cicloalquilo;
y z es 0, 1 O2 ;
y sales farmacéuticamente aceptables, solvatos, ésteres, profármacos e isómeros de las mismas.
[0157] En los compuestos de las Fórmulas I, I-A, I-B, I-C y I-D, los diversos restos se seleccionan independientemente.
[0158] Las siguientes realizaciones están dirigidas a las Fórmulas I, I-A, I-B, I-C y I-D, según corresponda. Para cualesquiera restos que no están definidos específicamente, el anterior control de definiciones. Además, los restos arilo, heteroarilo, y heterocicloalquilo en estas realizaciones pueden ser independientemente no sustituidos o sustituidos opcionalmente o fusionados opcionalmente como se ha escrito anteriormente.
[0159] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, R1 es
y A, B, L, Ar1, R2, Rp, Rp1, Ra, Ra1 , Rb, Rc, Rd, Rq y z son como se definen.
[0160] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, R1 es
y A, B, L, Ari, R2, Rp, Rpi, Ra, Raí, Rb, Rc, Rre, Rq y z son como se definen.
[0161] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, A y B son O, y R1 , L, Ar1 , R2 , Rp, Rp1, Ra, Ra1, Rb, Rc, Rd, Rq y z son como se definen.
[0162] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, A y B son S, y R1, L, Ar1, R2 , Rp, Rp1, Ra, Ra1 , Rb, Rc, Rd, Rq y z son como se definen.
[0163] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, ya sea A o B es O, el otro es S, y R1, L, Ar1, R2 , Rp, Rp1 , Ra, Ra1, Rq y z son como se definen.
[0164] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, L es un alquilo monocíclico de 5-10 miembros, y A, B, R1, Ar1, R2 , Rp, Rp1 ,
Ra, Ra1, Rb, Rc, Rd, Rq y z son como se definen.
[0165] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, L es un alquilo bicíclico de 5-10 miembros, y A, B, R1, Ar1, R2, Rp, Rp1, Ra,
Ra1, Rb, Rc, Rd, Rq y z son como se definen.
[0166] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, L es un heteroalquilo monocíclico de 5-10 miembros, y A, B, R1, An, R2 , Rp,
Rp1, Ra, Ra1, Rb, Rc, Rd, Rq y Z son como se definen.
[0167] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, L es un heteroalquilo bicíclico de 5-10 miembros, y A, B, R1, Ar1, R2 , Rp,
Rp1, Ra, Ra1, Rb, Rc, Rd, Rq y Z son como se definen.
[0168] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, L es
m es 1,2, o 3, n es 0, 1,2, o 3, y A, B, R1, Ar1, R2 , Rp, Rp1, Ra, Ra1, Rb, Rc, Rd, Rq y z son como se definen.
[0169] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, L es
y A, B, R1, Ar1, R2 , Rp, Rp1, Ra, Ra1, Rb, Rc, Rd, Rq y z son como se definen.
[0170] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, L es
[0171] Una realización de la invención es la provisión de un compuesto, en donde los diversos restos son seleccionan independientemente, Ar1 es un grupo arilo, y A, B, R1, L, R2, Rp, Rp1, Ra, Ra1, Rb, Rc, Rd, Rq y z son como se definen.
[0172] Una realización de la invención es la provisión de un compuesto, en donde los diversos restos son seleccionan independientemente, Ar1 es un heteroarilo, y A, B, R1, L, R2, Rp, Rp1 , Ra, Ra1, Rb, Rc, Rd, Rq y z son como se definen.
[0173] Una realización de la invención es la provisión de un compuesto, en donde los diversos restos son seleccionan independientemente, Ar1 es un arilo monocíclico de 5-10 miembros, y A, B, R1, L, R2 , Rp, Rp1 , Ra, Ra1, Rb, Rc, Rd, Rq y z son como se definen.
[0174] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, An es un arilo bicíclico de 5-10 miembros, y A, B, R1, L, R2 , Rp, Rp1, Ra, Ra1, Rb, Rc, Rd, Rq y z son como se definen.
[0175] Una realización de la invención es la provisión de un compuesto, en donde los diversos restos se seleccionan independientemente, Ar1 es un heteroarilo monocíclico de 5-10 miembros, y A, B, R1, L, R2 , Rp, Rp1 , Ra, Ra1, Rb, Rc, Rd, Rq y z son como se definen.
[0176] Una realización de la invención es la provisión de un compuesto, en donde los diversos restos son seleccionan independientemente, An es un miembros heteroarilo bicíclico de 5-10, y A, B, R1, L, R2 , Rp, Rp1, Ra, Ra1, Rb, Rc, Rd, Rq y Z son tal como se definen.
[0177] Una realización de la invención es la provisión de un compuesto, en donde los diversos restos se seleccionan independientemente, An es un arilo monocíclico sustituido o no sustituido de 5 miembros o heteroarilo y dicho heteroarilo tiene 1 o 2 heteroátomos que son independientemente S o N, y A, B, R1, L, R2 , Rp, Rp1, Ra, Ra1, Rb, Rc, Rd, Rq y z son como se definen.
[0178] Una realización de la invención es la provisión de un compuesto, en donde los diversos restos se seleccionan independientemente, Ar1 es una forma sustituida o no sustituida de
y A, B, R1, L, R2 , Rp, Rp1, Ra, Ra1, Rb, Rc, Rd, Rq y z son como se definen.
[0179] Una realización de la invención es la provisión de un compuesto, en donde los diversos restos se seleccionan independientemente, An es un arilo monocíclico sustituido o no sustituido de 6 miembros o heteroarilo y dicho heteroarilo tiene 1 o 2 heteroatomos que son N, y A, B, R1, L, R2 , Rp, Rp1, Ra, Ra1, Rb, Rc, Rd, Rq y z son como se definen.
[0180] Una realización de la invención es la provisión de un compuesto, en donde los diversos restos se seleccionan independientemente, Ar1 es una forma sustituida o no sustituida de
Phi es fenilo, piridinilo, pirazinilo o pirimidinilo, Re es H, halo, o L, R2 , Rp, Rc, Rd, Rq y z son como se definen.
[0181] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, An es una forma sustituida o no sustituida de
[0182] Una realización de la invención es la provisión de un compuesto, en donde los diversos restos se seleccionan independientemente, Ari es un arilo monocíclico sustituido o no sustituido de 6 miembros, y A, B, Ri, L, R2 , Rp, Rpi,
Ra, Rai, Rb, Rc, Rd, Rq y z son como se definen.
[0183] Una realización de la invención es la provisión de un compuesto, en donde los diversos restos se seleccionan independientemente, Ari es
Re es H, halo, o Ci-C3 alquilo, y A, B, Ri, L, R2 Rai, Rb, Rc, Rd, Rq y z son co [0184] Una realización de la invención es la provisión de un compuesto, en donde los diversos restos se seleccionan independientemente, Ari es
y A, B, Ri, L, R2 , Rp, Rpi, Ra, Raí, Rb, Rc, Rd, Rq y z son como se definen.
[0185] Una realización de la invención es la provisión de un compuesto, en donde los diversos restos se seleccionan independientemente, An es heteroarilo 6,5-bicíclico sustituido o no sustituido de 9 miembros y dicho heteroarilo tiene 1, 2, o 3 heteroátomos que son independientemente O, S o N, y A, B, R1, L, R2, Rp, Rp1, Ra, Ra1, Rb, Rc, Rd, Rq y z son como se definen.
[0186] Una realización de la invención es la provisión de un compuesto, en donde los diversos restos se seleccionan independientemente, Ar1 es una forma sustituida o sin sustituir de
un dicho heteroarilo tiene 1, 2, o 3 heteroátomos que son independientemente S o N, y A, B, R1, L, R2, Rp, Rp1, Ra, Ra1, Rb, Rc, Rd, Rq y z son como se definen.
[0187] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, R2 es un arilo sustituido o no sustituido, y A, B, R1, L, Ar1, Rp, Rp1 , Ra, Ra1, Rb, Rc, Rd, Rq y z son como se definen.
[0188] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan
independientemente los diversos restos, R2 es un heteroarilo sustituido o no sustituido, y A, B, Ri, L, Ari, Rp, Rpi, Ra,
Rai, Rb, Rc, Rd, Rq y z son como se definen.
[0189] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, R2 es un cicloalquilo sustituido o no sustituido, y A, B, R1, L, Ar1, Rp, Rp1 , Ra,
Ra1, Rb, Rc, Rd, Rq y z son como se definen.
[0190] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, R2 es un heterocicloalquilo sustituido o no sustituido, y A, B, R1, L, Ar1, Rp,
Rp1, Ra, Ra1, Rb, Rc, Rd, Rq y z son como se definen.
[0191] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, R2 es un arilo monocíclico o bicíclico sustituido o no sustituido de 5-10 miembros, o heteroarilo, y A, B, R1, L, Ar1, Rp, Rp1 , Ra, Ra1, Rb, Rc, Rd, Rq y z son como se def
[0192] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, R2 es un arilo monocíclico no sustituido o sustituido de 6 miembros, y A, B,
R1, L, Ar1, Rp, Rp1, Ra, Ra1, Rb, Rc, Rd, Rq y z son como se definen.
[0193] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, R2 es
o
y A, B, Ri, L, Ari, Rp, Rpi, Ra, Raí, Rb, Rc, Rd, Rq y z son como se definen.
[0194] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, R2 es un arilo sustituido o no sustituido bicíclico de 8-10 miembros o heteroarilo de 8-10 miembros, y A, B, R1, L, Ar1, Rp, Rp1 , Ra, Ra1, Rb, Rc, Rd, Rq y z son como se def [0195] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, R2 es un heteroarilo 5,5 bicíclico sustituido o no sustituido de 8 miembros y
dicho heteroarilo tiene 1,2, 3, o 4 heteroátomos y dichos hetroátomos son independientemente O, S, o N, y A, B, R1,
L, Ar1, Rp, Rp1 , Ra, Ra1, Rb, Rc, Rd, Rq y z son como se definen.
[0196] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, R2 es una forma sustituida o no sustituida de
y A, B, R1, L, Ar1, Rp, Rp1, Ra, Ra1, Rb, Rc, Rd, Rq y z son como se definen.
[0197] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, R2 es un heteroarilo 6,5 bicíclico sustituido o no sustituido de 9 miembros y
dicho heteroarilo tiene 1, 2, 3, o 4 heteroátomos y dichos heteroátomos son independientemente O, S, o N, y A, B,
R1, L, Ar1, Rp, Rp1, Ra, Ra1, Rb, Rc, Rd, Rq y z son como se definen.
[0198] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, R2 es una forma sustituida o no sustituida de
Rc, Rd y z son como se definen.
[0199] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, R2 es un arilo 6,6 bicíclico sustituido o no sustituido de 10 miembros o heteroarilo y dicho heteroarilo tiene 1, 2, 3, o 4 heteroátomos y dichos heteroátomos son O, S, o N, y A, B, R1 , L,
Ar1, Rp, Rp1 , Ra, Ra1, Rb, Rc, Rd, Rq y z son como se definen.
[0200] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, R2 es una forma sustituida o no sustituida de
y A, B, R1, L, Ar1, Rp, Rp1 , Ra, Ra1, Rb, Rc, Rd, Rq y z son como se definen.
[0201] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, Rp es H, y A, B, R1, L, Ar1, R2 , Rp1, Ra, Ra1, Rb, Rc, Rd, definen.
[0202] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, Rp es halo, y A, B, R1, L, Ar1, R2 , Rp1, Ra, Ra1, Rb, Rc, Rd, definen.
[0203] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, Rp es C1-C4 alquilo, y A, B, R1, L, Ar1, R2 , Rp1, Ra, Ra1, Rb, Rc, Rd, Rq y z son
como se definen.
[0204] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, Rp es C3-C4 cicloalquilo, y A, B, R1, L, Ar1, R2 , Rp1, Ra, Ra1, Rb, Rc, Rd, Rq y z son como se definen.
[0205] Una realización de la invención es la provisión de un compuesto, en donde los diversos restos se seleccionan independientemente, Rp1 es H, y A, B, R1, L, Ar1, R2, Rp, Ra, Ra1, Rb, Rc, Rd, Rq y z son como se definen.
[0206] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, Rp1 es halo, y A, B, R1, L, Ar1, R2 , Rp, Ra, Ra1, Rb, Rc, Rd, Rq y z son como se definen.
[0207] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, Rp1 es C1-C4 alquilo, y A, B, R1, L, Ar1, R2 , Rp, Ra, Ra1, Rb, como se definen.
[0208] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, Rp1 es C3-C4 cicloalquilo, y A, B, R1, L, Ar1, R2 , Rp, Ra, Ra1, Rb, Rc, Rd, Rq y z son como se definen.
[0209] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, Ra es H, y A, B, R1, L, Ar1, R2 , Rp, Rp1 , Ra1, Rb, Rc, definen.
[0210] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, Ra es halo, y A, B, R1, L, An, R2 , Rp, Rp1, Ra1, Rb, Rc, Rd, Rq y z son como se definen.
[0211] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, Ra es C1-C4 alquilo, y A, B, R1, L, Ar1, R2 , Rp, Rp1, Ra1, Rb, Rc, como se definen.
[0212] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, Ra es C3-C4 cicloalquilo, y A, B, R1, L, An, R2 , Rp, Rp1 , Ra1, Rb, Rc, Rd, Rq y z son como se definen.
[0213] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, Ra1 es H, y A, B, R1, L, An, R2, Rp, Rp1, Ra, Rb, Rc, Rd, Rq y z son como se definen.
[0214] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, Ra1 es halo, y A, B, R1, L, An, R2 , Rp, Rp1, Ra, Rb, Rc, definen.
[0215] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, Ra1 es C1-C4 alquilo, y A, B, R1, L, An, R2 , Rp, Rp1, Ra, Rb, Rc, Rd, Rq y z son como se definen.
[0216] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, Ra1 es C3-C4 cicloalquilo, y A, B, R1, L, An, R2 , Rp, Rp1, Ra, Rb, son como se definen.
[0217] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, Rb es H, y A, B, R1, L, An, R2, Rp, Rp1, Ra, Ra1, Rc, Rd, Rq y z son como se definen.
[0218] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, Rb es halo, y A, B, R1, L, An, R2 , Rp, Rp1, Ra, Ra1, Rc, Rd, Rq y z son como se definen.
[0219] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, Rb es C1-C4 alquilo, y A, B, R1, L, An, R2, Rp, Rp1, Ra, Ra1, Rc, Rd, Rq y z son como se definen.
[0220] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan
independientemente los diversos restos, Rb es C1-C3 hidroxilo-alquilo, y A, B, Ri, L, 2 , Rp, Rpi, Rq y z son como se definen.
[0221] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, Rb es C3-C4 cicloalquilo, y A, B, Ri, L, Ari, R2 , Rp, Rpi, Ra, Raí, Rc, Rd, Rq y z son como se definen.
[0222] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, Rc es H, y A, B, Ri, L, Ari, R2 , Rp, Rpi, Ra, Rai, Rb, Rd, Rq y z son como se definen.
[0223] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, Rc es halo, y A, B, Ri, L, Ari, R2 , Rp, Rpi, Ra, Rai, Rb, Rd, Rq y z son como se definen.
[0224] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, Rc es Ci-C4 alquilo, y A, B, Ri, L, Ari, R2, Rp, Rpi, Ra, Rai, como se definen.
[0225] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, Rc es C3-C4 cicloalquilo, y A, B, Ri, L, Ari, R2 , Rp, Rpi, Ra, Rai, Rb, Rd, Rq y z son como se definen.
[0226] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, Rd es H, y A, B, Ri, L, Ari, R2 , Rp, Rpi, Ra, Rai, Rb, Rc, Rq y z son como se definen.
[0227] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, Rd es halo, y A, B, Ri, L, An, R2 , Rp, Rpi, Ra, Rai, Rb, Rc, Rq y definen.
[0228] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, Rd es Ci-C4 alquilo, y A, B, Ri, L, Ari, R2 , Rp, Rpi, Ra, Rai, Rb, como se definen.
[0229] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, Rd es C3-C4 cicloalquilo, y A, B, Ri, L, Ari, R2 , Rp, Rpi, Ra, Rai, Rb, Rc, Rq y z son como se definen.
[0230] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, Rq es H, y A, B, Ri, L, Ari, R2 , Rp, Rpi, Ra, Rai, Rb, definen.
[0231] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, Rq es halo, y A, B, Ri, L, Ari, R2 , Rp, Rpi, Ra, Rai, Rb, definen.
[0232] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, Rq es Ci-C4 alquilo, y A, B, Ri, L, Ari, R2 , Rp, Rpi, Ra, Rai, Rb, como se definen.
[0233] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, Rq es C3-C4 cicloalquilo, y A, B, Ri, L, Ari, R2 , Rp, Rpi, Ra, Rai, Rb, son como se definen.
[0234] Una realización de la invención es la provisión de un compuesto, en donde los diversos restos se seleccionan independientemente, z es 0, y A, B, Ri, L, Ari, R2, Rp, Rpi, Ra, Rai, Rb, Rc, Rd y Rq son como se definen.
[0235] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, z es i y A, B, Ri, L, Ari, R2 , Rp, Rpi, Ra, Rai, Rb, Rc, Rd definen.
[0236] Una realización de la invención es la provisión de un compuesto, en donde se seleccionan independientemente los diversos restos, z es 2 y A, B, Ri, L, Ari, R2 , Rp, Rpi, Ra, Rai, Rb, Rc, Rd definen.
[0237] Una realización de la invención es la provisión de un compuesto como se ha descrito en las Fórmulas I, I-A, I B, I-C o I-D, en donde R2 no es una forma sustituida o sin sustituir de
X es N o CH.
[0238] Una realización de la invención es la provisión de un compuesto como se ha descrito en las Fórmulas I, I-A, I B, I-C o I-D en donde cuando Ar1 es
conectado a
en la posición 1, y X1 y X2 son independientemente N o C-Rz y Ry y Rz son cualquier sustituyente, entonces Rx no incluye alquinilo, alquenilo, arilo, heterocíclico de 5-14 miembros, heteroaromático de 5-14 miembros o carbocíclico de 4-9 miembros.
[0239] Una realización de la invención es la provisión de un compuesto como se ha descrito en las Fórmulas I, I-A, I B, I-C o I-D o en donde cuando R2 es
Ar1 no es una forma sustituida o no sustituida de
[0240] Una realización de la invención es la provisión de un compuesto como se ha descrito en las Fórmulas I, I-A, I B, I-C o I-D o en donde cuando Ar1 es una forma sustituida o no sustituida de un heteroarilo de 5 miembros, An es
[0241] En otra realización, la invención se ilustra adicionalmente por un compuesto seleccionado de:
1 -[(4-{[2-fluoro-4-(1 -metil-1 H-indol-5-il)fenil]carbonil}piperazin-1 -il}carbonil)ciclopropan-1 -ol;
1 -[(4-{[4-(isoquinolin-6-il)fenil]carbonil}piperazin-1 -il}carbonil)ciclopropan-1 -ol;
1 -[(4-{[3-cloro-4-(quinolin-3-il)fenil]carbonil}piperazin-1 -il}carbonil)ciclopropan-1 -ol;
5-[2-cloro-4-({4-[(1-hidroxiciclopropil}carbonil)piperazin-1-il}carbonil)fenil]-1 H-indol-3-carbonitril;
1-[(4-{[4-(quinolin-2-il)fenil]carbonil}piperazin-1-il}carbonil)ciclopropan-1-ol;
1 -{4-[2-fluoro-4-(1 -metil-1 H-1,3-benzodiazol-5-il)benzoil] piperazina-1 -carbonil}ciclopropan-1 -ol;
1 -[(4-{[3-cloro-4-(1 -metil-1 H-indol-5-il)fenil]carbonil}piperazin-1 -il}carbonil)ciclopropan-1 -ol;
1 -[(4-{[2-cloro-4-(1 -metil-1 H-indol-5-il)fenil]carbonil}piperazin-1 -il}carbonil)ciclopropan-1 -ol;
1 -[(4-{[4-(1 H-indol-4-il)fenil]carbonil}piperazin-1 -il}carbonil)ciclopropan-1 -ol; y
1 -[(4-{[3-metil-4-(1 -metil-1 H-indol-5-il)fenil]carbonil}piperazin-1 -il}carbonil)ciclopropan-1 -ol.
[0242] Se describen además los compuestos en Tabla 1, que enumera los nombres de la IUPAC y las estructuras de los compuestos.
Tabla 1.
Ejemplos
[0243] Los siguientes son ilustrativos, pero no limitativos, ejemplos de ciertas realizaciones de la presente invención. Los esquemas sintéticos se presentan para la síntesis de ciertos compuestos en el presente documento se da a conocer. También se describen el proceso y los resultados para los ensayos que prueban la inhibición de FASN y los efectos sobre la proliferación de línea celular de cáncer.
Definiciones utilizadas en los siguientes Esquemas y en otras partes en el presente documento son:
[0244]
Ar-B(OH)2 aril ácido borónico
Ar-B(OR))2 aril éster borónico
Ar-X haluro de arilo
Atm atmósfera
BOP 4-(3-(piridin-3-Imetilo)ureido)bencenosulfinato de amonio
8 desplazamiento químico (ppm)
CbzCl cloroformato de bencilo
DCM diclorometano o cloruro de metileno
DDQ 2,3-dicloro-5,6-diciano-p-benzoquinona
DIEA N,N-diisopropiletiloamina
DMA N,N-dimetiloacetamida
DMF N,N-dimetiloformamida
DMSO dimetilosulfóxido
EDC clorhidrato de N1-((etilimino)metileno)-N3,N3-dimetilpropano-1,3-diamina
ES electrospray
Et3N tritilamina
EtOAc acetato de etilo
EtOH etanol
EtN(i-Pr)2 amina de diisopropiletilo
equiv equivalentes
FCC cromatografía de columna flash
GF/F filtro de microfibra de vidrio
1HRMN resonancia magnética nuclear de protones
HCl cloruro de hidrógeno
HOAc ácido acético
HATU 2-(3H-[1,2,3]triazolo[4,5-b]piridin-3-il)-1,1,3,3-tetrametilisouronio hexafluorofosfato HBTU O-(benzotriazol-1 -il)-N,N,N’,N’-hexafluorofosfato de tetrametiluronio
HOBt 1 H-benzo[d][1,2,3]triazol-1 -ol hidrato
HPLC cromatografía líquida de alta presión
i-PrOH isopropanol
(i-PR2)NEt N,N-Diisopropiletiloamina
LC-MS cromatografía líquida/espectrometría de masas
LiOH hidróxido de masa
(M+1) masa 1
m/z relación de masa a carga
MS espectrometría de masa o tamices moleculares
N2 nitrógeno
NaH hidruro de sodio
nm nanómetro
NaOH hidróxido de sodio
NaHCO3 bicarbonato de sodio
Mel yoduro de metilo
MeOH metanol
MeSO3H ácido sulfónico de metano
MgSO4 sulfato de magnesio
mmol milimoles
ponda microondas
Pd(PPh3)4 Tetrakis(trifenilfosfina)paladio
Pd2(dba)3 tris(dibencilidenacetona)dipaladio
Pd(dppf)Cl2 [1,1 ’-bis(difenilfosfino)ferroceno]dicloropaladio(M)
PTLC cromatografía de capa fina preparativa
RCO2H ácido 1 -hidroxiciclopropanocarboxílico
rt o RT temperatura ambiente
SOCÍ2 cloruro de tionilo
TEA trietiloamina
TFA ácido trifluoroacético
THF tetrahidrofurano
TLC cromatografía de capa fina
UV ultravioleta
X-Phos 2-diciclohexilfosfino-2',4',6'-triisopropil-bifenil
Materiales
[0245] A menos que se indique lo contrario, todos los materiales se obtuvieron de proveedores comerciales y se usaron sin purificación adicional. Los disolventes anhidros se obtuvieron de Sigma-Aldrich (Milwaukee, WI) y se usaron directamente. Todas las reacciones con reactivos sensibles al aire o a la humedad se realizaron bajo una atmósfera de nitrógeno. Datos espectrales de masa de pureza y baja resolución fueron medidos utilizando: (1) Sistema de cromatografía líquida de rendimiento ultra Waters Acquity (UPLC) (Waters Acquity UPLC con el organizador de muestras y Waters Micromass ZQ Mass Spectrometer) con detección de UV a 220 nm y un modo de iones positivos baja de electrospray de baja resonancia (ESI) (columna: Acquity UPLC BEH Ci81,7|um 2,1 X 50 mm; gradiente: 5-100% de disolvente B (95/5/0,09%: acetonitrilo/agua/ácido fórmico) en el disolvente A (95/5/0,1%: 10 mM formato de amonio/acetonitrilo/ácido fórmico) para 2,2 min entonces 100-5% disolvente B en disolvente A durante 0,01 min, luego mantenga a 5% disolvente B en disolvente A durante 0,29 min) o el (2) sistema de cromatografía líquida de alta resolución Waters HT2790 Alliance (HPLC) (Waters 996 PDA y Waters ZQ Single Quad Mass Spectrometer) con detección de UV a 220 nm y 254 nm y un modo de ionización electrospray de baja resonancia (positivo/negativo) (ESI) (columna: fenil XBridge o C18, 5|um 4,6x50 mm; gradiente: 5-95% de disolvente B (95% de metanol/5% de agua con 0,1% de ácido fórmico) en el disolvente A (95% de agua/5% de metanol con 0,1% de ácido fórmico) durante 2,5 minutos a continuación, mantenga al 95% de Disolvente B en disolvente a durante 1 min).
Métodos generales para la síntesis de compuestos:
[0246]
Método 1
(etapa 2)
(etapa 3] D M F
Etapa 1 terc-butilo 4-(4-bromobenzoil)piperazina-1-carboxilato (Intermedio 1)
[0247] N,N-diisopropiletilamina (28,6 ml, 164 mmol) se añadió a una solución a 0°C de terc-butilo piperazina-1-carboxilato de metilo (10,18 g, 54,7 mmol) y cloruro de 4-bromobenzoílo (12,0 g, 54,7 mmol) en DMF (80 ml), y la mezcla de reacción se agitó a ta durante 6 h. Se añadió agua y la mezcla resultante se agitó durante la noche y luego se filtró y driedto proporcionar terc-butílico del ácido 4-(4-bromobenzoil)piperazina-1-carboxilato de metilo (19,388 g, 52,5 mmol, 96% de rendimiento) como un solid.MS blancuzcos (. ESI, ión pos) m/z: 369, 371 (m 1). Etapa 2. terc-butilo 4- cloro-2'-fluorobifenil}carbonil)piperazina-1-carboxilato
[0248] Se añadió tetraquis(trifenilfosfina)paladio(0) (1,565 g, 1,354 mmol) a una mezcla de terc-butilo 4-(4-bromobenzoil)piperazina-1-carboxilato (5,00 g, 13,54 mmol), 4-cloro-2-ácido fluorofenilborónico (2,95 g, 16,93 mmol), y carbonil de sodio (5,74 g, 54,2 mmol) en 1,4-dioxano (50 ml) y agua (10 ml). La mezcla se agitó a 70°C
durante 5 h. La mezcla de reacción se filtró a través de Celite y se concentró para dar un aceite naranja. Este material era cromatografía en columna purifiedvia sobre gel de sílice (columna Biotage de 100 g, gradiente de elución con 0-50% acetato de etilo-hexano) para producir terc-butilo 4-(4’-cloro-2'-fluorobifenil}carbonil)piperazina-1-carboxilato de etilo (5,508 g, 13,15 mmol, 97% de rendimiento) como un sólido marrón. MS (. ESI, ión pos.) m/z: 419 (M 1).
Etapa 3. (4’-cloro-2’-fluorobifenil-4-il)(piperazin-1-il)metanona 2,2,2-trifluoroacetato
[0249] Se añadió ácido trifluoroacético (20,0 ml, 260 mmol) a una solución de terc-butilo 4-(4’-cloro-2'-fluorobifenil}carbonil)piperazina-1-carboxilato de metilo (11,35 g, 27,1 mmol) en diclorometano (100 ml) y la solución se agitó a ta durante 1,5 h. La mezcla de reacción se concentró y el residuo se trituró con éter dietílico para proporcionar (4’-cloro-2'-fluorobifenil-4-il)(piperazin-1-il)metanona 2,2,2-trifluoroacetato (12,02 g, 27,8 mmol, 100% de rendimiento) como un sólido de color tostado. MS (ESI, ión pos) m/z: 319 (M 1).
Etapa 4. (4’-cloro-2'-fluorobifenil-4-il)(4-(1-hidroxiciclopropanocarbonil)piperazin-1-il)metanona
[0250] N,N-Diisopropiletilamina (9,12 ml, 52,2 mmol) se añadió a una solución de (4’-cloro-2’-fluorobifenil-4-il)(piperazin-1-il)metanona 2,2,2-trifluoroacetato (5,647 g, 13,05 mmol), ácido 1-hidroxiciclopropanocarboxílico (1,332g, 13,05 mmol), y hexafluorofosfato de O-(benzotriazol-1-il)-N,N,N’,N’-tetrametiluronio (7,42 g, 19,57 mmol) en DMF (50,0 ml), y la mezcla de reacción se agitó a ta durante 18 h. La mezcla de reacción se repartió entre acetato de etilo y agua. La fase orgánica se lavó con agua y salmuera, se secó sobre sulfato de sodio anhidro, se filtró, y se concentró para proporcionar un aceite de color amarillo. Este material se purificó por cromatografía en columna sobre gel de sílice (Biotage 100 gcolumn, mmol, 30% de rendimiento) como un sólido blanco. MS (ESI, ión pos) m/z: 403 (M 1).
Método 2.
Etapa 1. (4-bromofenil) (piperazin-1-il)metanona 2,2,2-trifluoroacetato
[0251] Se añadió ácido trifluoroacético (5,0 ml, 64,9 mmol) a una solución de terc-butilo 4-(4-bromobenzoil)piperazina-1-carboxilato (2,00 g, 5,42 mmol) en diclorometano (25,0 ml), y la solución se agitó a ta durante 2 h. La mezcla de reacción se concentró y el residuo se trituró con éter dietílico para producir (4-bromofenil)(piperazin-1-il)metanona 2,2,2-trifluoroacetato. (1,992 g, 5,20 mmol, 96% de rendimiento) como un sólido blanco. MS (ESI, ión pos) m/z: 269, 271 (M 1).
Etapa 2. (4-(4-bromobenzoil)piperazin-1-il)(1-hidroxiciclopropil)metanona
[0252] N,N-diisopropiletilamina (0,46 ml, 2,6 mmol) se añadió a una solución de (4-bromofenil)(piperazin-1-il)metanona 2,2,2-trifluoroacetato (0,250 g, 0,652 mmol), ácido 1-hidroxiciclopropanocarboxílico (0,067 g, 0,652 mmol), y hexafluorofosfato de O-(benzotriazol-1-il)-N,N,N’,N’-tetrametiluronio (0,371 g, 0,979 mmol) en DMF (5,0 ml), y la mezcla de reacción se agitó a ta durante 18 h. La mezcla de reacción se repartió entre acetato de etilo y agua. La fase orgánica se lavó con salmuera, se secó sobre sulfato de sodio anhidro, se filtró y se concentró para proporcionar anorange aceite. Este material se purificó por cromatografía en columna sobre gel de sílice (columna Biotage de 25 g, elución con gradiente 0-5% de metanol-diclorometano) para proporcionar (4-(4-bromobenzoil)piperazin-1-il)(1-hidroxiciclopropil)metanona (0,195 g, 0,552 mmol, 85% de rendimiento) como un sólido de color naranja claro. MS (ESI, ión pos) m/z: 353, 355 (M 1).
Etapa 3. (4-(4-(benzo[d]tiazol-5-il)benzoil)piperazin-1-il)(1-hidroxiciclopropil)metanona
[0253] Se añadió tetraquis(trifenilfosfina)paladio(0) se añadió (0,016 g, 0,014 mmol) a una mezcla de (4-(4-bromobenzoil)piperazin-1-il)(1-hidroxiciclopropil)metanona (0,050 g, 0,142 mmol), 5-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)benzo[d]tiazol (0,055 g, 0,212 mmol), y carbonil de sodio (0,060 g, 0,566 mmol) en dioxano (1,5 ml) y agua (0,30 ml). La mezcla se agitó en el microondas a 50°C durante 1 h. La mezcla de reacción se filtró a través de Celite y se concentró para proporcionar un aceite de color amarillo. Este material se purificó por cromatografía en columna sobre gel de sílice (columna Biotage 25 g, gradiente de elución con 0-5% de metanol-acetato de etilo) para proporcionar (4-(4-(benzo[d]tiazol-5-il)piperazin-1-il)(1-hidroxiciclopropil)metanona (0,020 g, 0,049 mmol, 35% de rendimiento) como un sólido de color blanquecino. MS (ESI, ión pos) m/z: 408 (M 1).
Método 3.
Etapa 1. terc-butilo 4-(4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)benzoil)piperazina-1-carboxilato
[0254] Una mezcla de 4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)ácido benzoico (15 g, 60,5 mmol), terc-butilo piperazina-1-carboxilato (11,26 g, 60,5 mmol), 1H-benzo[d][1,2,3]triazol-1-ol hidrato (4,63 g, 30,2 mmol), NI-{[etilimino)metileno)-N3,N3-dimetilpropano-1,3-hidrocloruro de diamina (12,75 g, 66,5 mmol), y trietilamina (33,7 ml, 242 mmol) en diclorometano (180 ml) se agitó a temperatura ambiente durante la noche. La mezcla de reacción se lavó con solución de bicarbonato de sodio saturatedaqueous (75 ml), solución HCl 0,5 M (75 ml), y de nuevo con solución de bicarbonato de sodio acuoso saturado (75 ml). Las fases orgánicas combinadas se concentraron y el sólido resultante se suspendió en una solución de 1:1 metil terc-butilo éter/hexano (200 ml). El material se filtró y se secó para proporcionar terc-butilo 4-(4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)benzoil)piperazina-1-carboxilato (20,03 g, 48,1 mmol, 80%). MS (ESI, ión pos) m/z: 417 (M 1).
Etapa 2 (Pd(PPh3)4). terc-butilo 4-(4-(1H-benzo[d]imidazol-2-il)benzoil)piperazina-1-carboxilato
[0255] Se añadió tetraquis(trifenilfosfina)paladio(0) (0,028 g, 0,024 mmol) a una mezcla de terc-butil4-(4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)benzoil)piperazina-1-carboxilato (0,050 g, 0,120 mmol), 2-bromo-1H-benzo[d]imidazol (0,035 g, 0,180 mmol), y carbonil de sodio (0,051 g, 0,480 mmol) en dioxano (1,5 ml) y se agua (0,30 ml). La mezcla se agitó en el microondas a 50°C durante 3 h. La mezcla de reacción se filtró a través de Celite y se concentró. El residuo se purificó por cromatografía en columna sobre gel de sílice (columna de 10 g Biotage, gradiente de elución con 0-50% acetato de etilo-hexano) para proporcionar terc-butilo 4-(4-(1H-benzo[d]imidazol-2-il)benzoil)piperazina-1-carboxilato (0,027 g, 0,066 mmol, 55% de rendimiento) como un sólido de color blanquecino. MS (ESI, ión pos) m/z: 407 (M 1).
Etapa 2 (X-Phos). terc-butilo 4-(4-(pirazolo[1,5-a]piridin-2-il)benzoil)piperazina-1-carboxilato
[0256] Una mezcla de terc-butilo 4-(4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)benzoil)piperazina-1-carboxilato (0,100 g, 0,240 mmol), 2-cloropirazolo[1,5-a]piridina (0,046 g, 0,300 mmol), tris(dibencilidenacetona)dipaladio (0,011 g, 0,012 mmol), 2-diciclohexilfosfino-2’,4’,6'-triisopropil-bifenil (X-Phos, 0,011 g, 0,024 mmol), y carbonil de cesio (0,235 g, 0,721 mmol) en dioxano (2,5 ml) y agua (0,50 ml) se agitó en el microondas a 80°C durante 1 h. La mezcla de reacción se filtró a través de Celite y se concentró para proporcionar un aceite de color amarillo-marrón. Este material se purificó por cromatografía en columna sobre gel de sílice (columna Biotage de 25 g, gradiente de elución con 0-50-100% acetato-hexano etilo) para proporcionar terc-butilo 4-(4-(pirazolo[1,5-a]piridin-2-il)benzoil)piperazina-1-carboxilato (0,056 g, 0,138 mmol, 57% de rendimiento) como un sólido de color blanquecino. MS (ESI, ión pos.)
m/z: 407 (M 1).
Etapa 3. (4-(1H-benzo[d]imidazol-2-il)fenil)(piperazin-1-il)metanona 2,2,2-trifluoroacetato (Intermedio 2)
[0257] Se añadió ácido trifluoroacético (1,0 ml, 12,98 mmol) a una solución de terc-butilo 4-(4-(1H-benzo[d]imidazol-2-il)benzoil)piperazina-1-carboxilato (0,027 g, 0,066 mmol) en diclorometano (3,0 ml), y la solución se agitó a ta foR1,5 h. La mezcla de reacción se concentró y el residuo se trituró con éter dietílico y se filtró para proporcionar (4-(1H-benzo[d]imidazol-2-il)fenil)(piperazin-1-il)metanona 2,2,2-trifluoroacetato (0,028 g, 0,067 mmol, 100% de rendimiento) como una película marrón. MS (ESI, ión pos) m/z: 307 (M 1).
Etapa 4. (4-(4-(1H-benzo[d]imidazol-2-il)benzoil)piperazin-1-il)(1-hidroxiciclopropil)metanona
[0258] DIEA (0,047 ml, 0,266 mmol) se añadió a una solución de (4-(1H-benzo[d]imidazol-2-il)fenil)(piperazin-1-il)metanona 2,2,2-trifluoroacetato (0,028 g, 0,067 mmol), ácido 1-hidroxiciclopropanocarboxílico (7,14 mg, 0,070mmol) y O-(benzotriazol-1-il)-N,N,N’,N’-tetrametiluronio (0,038 g, 0,100 mmol) en Dm F (1,0 ml), y la mezcla de reacción se agitó a ta durante 20 h. Se añadió agua y la mezcla se repartió entre acetato de etilo y agua. La fase acuosa se separó y se extrajo con diclorometano. Las fases orgánicas combinadas se lavaron con salmuera, se secó sobre sulfato de sodio anhidro, y se filtró para proporcionar un aceite marrón. Este material se purificó a través de cromatografía en columna sobre gel de sílice (columna de 10 g Biotage, gradiente de elución con 0-5% de metanol-acetato de etilo) para proporcionar (4-(4-(1H-benzo[d]imidazol-2-il)benzoil) (1-hidroxiciclopropil)metanona piperazin-1 -il)(0,004 g, 10,24pmol, 15% de rendimiento) como un sólido blanco. MS (ESI, ión pos) m/z: 391 (M 1).
Método 4.
Etapa 1.4-(benzo[d]oxazol-2-il)benzoato de metilo
[0259] Se añadió cloruro de tionilo (10 ml, 137 mmol) a tereftalato de mono-metilo (5,00 g, 27,8 mmol). Se añadió una gota de DMF, y la mezcla se calentó a 80°C durante 2 h. El exceso de cloruro de tionilo se eliminó, y los residuewas trató con 2-aminofenol (3,03 g, 27,8 mmol) y dioxano (60 ml). Se añadió ácido metanosulfónico (5,59 ml, 86 mmol) y la mezcla de reacción se calentó a reflujo durante 18 h. La solución se concentró y el residuo waspartitioned entre diclorometano y solución sat. ac. solución de bicarbonato de sodio. La fase acuosa se lavó separatedand con diclorometano y las fases orgánicas combinadas se lavaron con salmuera, se filtró, y concentratedto proporcionar un sólido marrón. Este material se trituró con metanol, se filtró, y se secó para
proporcionar 4-(benzo[d]oxazol-2-il)benzoato de metilo (4,827 g, 19,06 mmol, rendimiento del 69%) como un sólido de color blanquecino. MS (ESI, ión pos) m/z: 254 (M 1).
Etapa 2 (LiOH). 4-(benzo[d]oxazol-2-il)ácido benzoico
[0260] Se añadió hidróxido de litio (0,894 g, 37,3 mmol) a una solución de 4-(benzo[d]oxazol-2-il)benzoato de metilo (4,728 g, 18,67 mmol) en THF (25 ml), metanol (25 ml), se y agua (25 ml), y la mezcla se agitó a ta durante 18 h. La mezcla de reacción se concentró y la solución acuosa se acidificó a pH = 5-6 con solución 1 N HCl ac. Theresulting precipitado blanquecino se filtró y se secó para proporcionar 4-(benzo[d]oxazol-2-il)ácido benzoico (3,846 g, 16,08 mmol, 86% de rendimiento) como un sólido de color blanquecino. MS (ESI, ión pos) m/z: 240 (M 1).
Etapa 2 (NaOH).4-(5-cianobenzo[d]oxazol-2-il)ácido benzoico
[0261] Se añadió hidróxido de sodio (0,067 g, 1,675 mmol) a una solución de 4-(5-cianobenzo[d]oxazol-2-il)benzoato de metilo (0,233 g, 0,837 mmol) en THF (4,0 ml) y agua (2,00 ml), y la mezcla se agitó a ta durante 18 h. La mezcla de reacción se concentró y la solución acuosa se acidificó a pH = 5-6 con solución 1 N HCl ac. El apagado resultante precipitado blanco se filtró y se secó para proporcionar 4-(5-cianobenzo[d]oxazol-2-il)ácido benzoico (0,176 g, 0,666 mmol, 80% de rendimiento) como un sólido de color blanquecino. MS (ESI, ión pos) m/z: 265 (M 1).
Etapa 3. terc-butilo 4-(4-(benzo[d]oxazol-2-il)benzoil)piperazina-1-carboxilato
[0262] se añadió cloruro de tionilo (25,0 ml, 343 mmol) a 4-(benzo[d]oxazol-2-il)ácido benzoico (3,5 g, 14,63 mmol). Se añadió una gota de DMF y la mezcla se calentó a 80°C durante 1 h. El exceso de cloruro de tionilo se eliminó y DMF se añadió (40 ml). Se añadieron terc-butilo piperazina-1-carboxilato (2,72 g, 14,63 mmol) y N,N-diisopropiletilamina (7,67mL, 43,9 mmol), y la mezcla de reacción se agitó a ta durante 1,5 h. Se añadió agua y la mezcla resultante se agitó y después se filtró y se secó para proporcionar terc-butilo 4-(4-(benzo[d]oxazol-2-il)benzoil)piperazina-1-carboxilato (5,006 g, 12,29 mmol, 84% de rendimiento) como un sólido de color tostado claro. MS (ESI, ión pos) m/z: 408 (M 1).
Etapa 4. (4-(benzo[d]oxazol-2-il)fenil)(piperazin-1-il)metanona 2,2,2-trifluoroacetato
[0263] Se añadió ácido trifluoroacético (10,0 ml, 130 mmol) a una solución de terc-butilo 4-(4-(benzo[d]oxazol-2-il)benzoil)piperazina-1 -carboxilato (5,006 g, 12,29 mmol) en diclorometano (50 ml), y la solución se agitó a ta durante 5 h. La mezcla de reacción se concentró y el residuo se trituró con éter dietílico y se filtró para proporcionar (4-(benzo[d]oxazol-2-il)fenil)(piperazin-1-il)metanona 2,2,2-trifluoroacetato (5,501 g, 13,06 mmol, 100% de rendimiento) como un sólido blanquecino. MS (ESI, ión pos) m/z: 308 (M 1).
Etapa 5 (acoplamiento de cloruro de ácido). (4-(4-(benzo[d]oxazol-2-il)benzoil)piperazin-1-il)(1-hidroxiciclopropil)metanona
[0264] Se añadió cloruro de tionilo (2,0 ml, 27,4 mmol) a ácido 1-hidroxiciclopropanocarboxílico (0,115 g, 1,123mmol). Se añadió una gota de DMF y la mezcla se calentó a 80°C durante 1 h. El exceso de cloruro de tionilo fue retirado para proporcionar un aceite marrón. Este material se añadió a una solución de (4-(benzo[d]oxazol-2-il)fenil)(piperazin-1-il)metanona 2,2,2-trifluoroacetato (0,338 g, 0,802 mmol) y N,N-diisopropiletilamina (0,70 ml, 4,01 mmol) en diclorometano (3,0 ml). La mezcla de reacción se agitó a ta durante 2 h. La mezcla se concentró y el residuo se purificó a través de en columna sobre gel de sílice (columna Biotage de 25 g, gradiente de elución con 0-5% de metanol-acetato de etilo) para proporcionar (4-(4-(benzo[d]oxazol-2-il)benzoil)piperazin-1-il)(1-hidroxiciclopropil)-metanona (0,208 g, 0,531 mmol, 66% de rendimiento) como un sólido rosa. MS (ESI, ión pos) m/z: 392 (M 1).
Etapa 5 (acoplamiento HBTU). (4-(4-(5-clorobenzo[d]oxazol-2-il)benzoil)piperazin-1-il)(1-hidroxiciclopropil)metanona
[0265] N,N-diisopropiletilamina (0,376 ml, 2,150 mmol) se añadió a una solución de (4-(5-clorobenzo[d]oxazol-2-il)fenil)(piperazin-1-il)metanona 2,2,2 trifluoroacetato (0,245 g, 0,537 mmol), ácido 1-hidroxiciclopropanocarboxílico (0,058 g, 0,564 mmol), y hexafluorofosfato de O-(benzotriazol-1-il)-N,N,N’,N’-tetrametiluronio (HBTU, 0,306 g, 0,806 mmol) en DMF (5,0 ml), y la mezcla de reacción se agitó a ta durante 20 h. Se añadió agua y el precitipado resultante se filtró y se secó. Este material se purificó por cromatografía en columna sobre gel de sílice (Columna Biotage 50 g, elución de gradiente con 0-5% metanol-acetato de etilo) para proporcionar (4-(4-(5-clorobenzo[d]oxazol-2-il)benzoil)piperazin-1-il)(1-hidroxiciclopropil)metanona (0,136 g, 0,319 mmol, 59% de rendimiento) como un sólido de color blanquecino. MS (ESI, ión pos) m/z: 426 (M 1).
Método 5.
Preparación de (4-(2-cloro-4-(quinolin-6-il)benzoil)piperazin-1-il)(1-hidroxiciclopropil)metanona
[0266] 4-Bromo-2-ácido clorobenzoico (0,2 m en 1,4-dioxano, 180 pL, 0,036 mmol) se añadió a una solución de terc-butilpiperazina-1-carboxilato de etilo (solución 0,2 m en 1,4-dioxano con 5% de N,N-diisopropiletilamina, 150 pL, 0,03 mmol). (Benzotriazol-1-iloxi) tris(dimetilamino) fosfonio hexafluorofosfato (BOP, solución 0,5 m en 1,2-dicloroetano, 72 pL, 0,036 mmol) se añadió, y la mezcla resultante se puso en un agitador a temperatura ambiente durante 2 horas. Quinolin-6-ácido ilborónico (solución 0,2 M en 1,4-dioxano, 225 pL, 0,045 mmol) y fosfato de potasio (1 M acuoso, 150 pL, 0,15 mmol) se añadieron. Una solución Tetrakis(trifenilfosfina)paladio(0) (0,02 M tolueno, 75 pL, 1,5 pmol) se añadió entonces bajo una atmósfera de nitrógeno, y la mezcla resultante se puso en un agitador en una caja de guantes bajo atmósfera de nitrógeno y calentado a 80°C durante la noche. Después de enfriar a Ta, la mezcla se diluyó con salmuera (0,30 ml) y acetato de etilo (0,5 ml). La capa orgánica se separó y la capa acuosa se extrajo de nuevo con acetato de etilo (0,6 ml). Las capas orgánicas reunidas se secaron y el residuo se volvió a disolver en metanol (400 pL). Solución de HCl (4 N en 1,4-dioxano, 75 pL, 0,2 mmol), se añadió y la mezcla se calentó en un agitador a 50°C durante 1 hora. La mezcla de reacción se secó en vacío y el residuo se volvió a disolver en una solución de 10% N,N-diisopropiletilamina en dimetilacetamida (200 pL). Ácido 1-hidroxiciclopropanocarboxílico (0,2 m en 1,4-dioxano, 225 pL, 0,045 mmol) se añadió seguido por la solución BOP (0,5 m en 1,2-DCE, 90 pL, 0,045 mmol). La mezcla se puso en un agitador a temperatura ambiente durante 2 horas. A continuación, la mezcla de reacción se diluyó con solución de hidróxido de sodio (1 N en salmuera, 0,45 ml) y acetato de etilo (0,5 ml). La capa orgánica se separó y la capa acuosa se extrajo con acetato de etilo (0,6 ml). Las capas se combinaron orgánicamente y se concentraron y el residuo se purificó por cromatografía líquida de alto rendimiento (recogida de fracciones de preparación HPLC dirigida por Waters Autopurification MS con las siguientes condiciones: Columna: Waters XBridge OBD C18, 5pm, 19x50mm; velocidad de flujo 20 ml/min; fase móvil, agua con hidróxido de amonio 0,1% (A) y metanol con hidróxido de amonio al 0,1% (B) que se ejecuta el siguiente gradiente de 0 a 2 minutos (15% B), de 2 a 6 minutos (15-100% B); Detector ZQ Mass Detector en el modo de ionización por electrospray) para proporcionar (4-(2-cloro-4-(quinolin-6-il)benzoil)metanona piperazin-1 -il)(1 -hidroxiciclopropil) (5,9 mg, 14pM 11, 45% de rendimiento). MS (ESI, ión pos) m/z: 436 (M 1).
Método 6.
E tapa 1. terc-butilo 4-(4-(benzo[d]tiazol-2-il)benzoil)piperazina-1-carboxilato
[0267] Se añadió tetraquis(trifenilfosfina)paladio(0) se añadió (0,313 g, 0,271 mmol) a una mezcla de terc-butilo 4-(4-bromobenzoil)piperazina-1-carboxilato (1,00 g, 2,71 mmol), 2-(tributilestannil)benzo[d]tiazol (1,00 ml, 2,84 mmol), cloruro de litio (0,230 g, 5,42 mmol), y cobre (I) yoduro (0,026 g, 0,135 mmol) en dMF (25 ml). La mezcla stirredat 80°C durante 2 h y después a 90°C durante 8 h. La mezcla de reacción se filtró a través de Celite y el filtrado se particionó entre diclorometano y agua. La fase orgánica se separó y se lavó con salmuera, se secó sobre sulfato de sodio anhidro, se filtró y se concentró para proporcionar un aceite naranja. Este material se purificó por cromatografía de columna en gel de sílice (columna Biotage 50 g, gradiente de elución con 0-50% acetato de etilohexano) para proporcionar terc-butilo 4-(4-(benzo[d]tiazol-2-il)benzoil)piperazina-1-carboxilato (0,586 g, 1,384 mmol, 51% de rendimiento) como un sólido marrón. MS (ESI, ión pos) m/z: 424 (M 1).
E tapa 2. (4-(benzo[d]tiazol-2-il)fenil)(piperazin-1-il)metanona 2,2,2-trifluoroacetato
[0268] Se añadió ácido trifluoroacético (1,00 ml, 13,0 mmol) a una solución de terc-butilo 4-(4-(benzo[d]tiazol-2-il)benzoil)piperazina-1-carboxilato (0,586 g, 1,38 mmol) en diclorometano (5,0 ml), y la solución se agitó a ta durante 3 h. La mezcla de reacción se concentró y el residuo se trituró con éter dietílico y se filtró para proporcionar (4-(benzo[d]tiazol-2-il)fenilo)(piperazin-1-il)metanona 2,2,2-trifluoroacetato (0,542 g, 1,239 mmol, 90% de rendimiento) como un sólido marrón. MS (ESI, ión pos) m/z: 324 (M 1).
Etapa 3. (4-(4-(benzo[d]tiazol-2-il)benzoil)piperazin-1-il)(1-hidroxiciclopropil)metanona
[0269] N,N-diisopropiletilamina (0,87 ml, 5,0 mmol) se añadió a una solución de (4-(benzo[d]tiazol-2-il)fenil)(piperazin-1-il)metanona 2,2,2-trifluoroacetato (0,542 g, 1,239 mmol), ácido 1-hidroxiciclopropanocarboxílico (0,133 g, 1,301 mmol), y hexafluorofosfato de O-(benzotriazol-1-il)-N,N,N’,N’-tetrametiluronio (0,705 g, 1,859 mmol) inDMF (5,0 ml), y la mezcla de reacción se agitó a ta durante 16 h. Se añadió agua y el precipitado resultante se secó y se filtró. Este material se purificó por cromatografía en columna sobre gel de sílice (columna Biotage de 50 g, elución con gradiente 0-5% de metanol-acetato de etilo) para proporcionar (4-(4-(benzo[d]tiazol-2-il)benzoil)piperazin-1-il)(1-hidroxiciclopropil)metanona (0,235 g, 0,577 mmol, 47% de rendimiento) como un sólido de color blanquecino. MS (ESI, ión pos) m/z: 408 (M 1).
Método 7.
Preparación de 5-(4-(4-(1-hidroxiciclopropanocarbonil}piperazina-1-carbonil)fenil)-1H-indol-3-carbonitril:
[0270] A una solución de terc-butilo 4-(4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)benzoil)piperazina-1-carboxilato (0,2 m en 1,4-dioxano, 100 pL, 0,02 mmol), se añadió 5-bromo-1 H-indol-3-carbonitril (0,2 m en 1,4-dioxano, 100 pL, 0,02 mmol) y una solución de fosfato de potasio (1 M acuoso, 100 pL, 0,1 mmol). La mezcla se burbujeó con nitrógeno y tetrakis(trifenilfosfina)paladio(0) (0,02 M en tolueno, 50 pL, 1 pmol) se añadió). La mezcla resultante se metió en un agitador en una caja de guantes bajo atmósfera de nitrógeno y se calentó a 80°C durante la noche. Después de enfriarse a ta, La mezcla se diluyó con 0,35 ml de salmuera y 0,5 ml de acetato de etilo. La capa orgánica se separó y la capa acuosa se extrajo de nuevo con acetato de etilo (0,6 ml). Las capas orgánicas combinadas se concentraron y el residuewas disuelven en 200 pL de metanol. solución de HCl (50 pL, 4 N en 1,4-dioxano, 0,2 mmol) se añadió. La mezcla se introdujo en un agitador a 50°C durante 1 hora. La mezcla de reacción se concentró al vacío y el residuo se disolvió en una solución de 10% N,N-diisopropiletilamina en dimetilacetamida (200 pL). Ácido 1-hidroxiciclopropanocarboxílico (0,2 M en 1,4-dioxano, 120 pL se añadió, 0,024 mmol), seguido por solución de BOP (0,5 M en 1,2-dicloroetano, 48 pL, 0,024 mmol). La mezcla se puso en un agitador a temperatura ambiente durante 2 horas. La mezcla de reacción se diluyó con 0,45 ml de IN NaOH en salmuera y 0,5 ml de acetato de etilo. La capa orgánica se separó y la capa acuosa se extrajo de nuevo con acetato de etilo (0,6 ml). Las capas orgánicas combinadas se concentraron y el residuo se purificó por recogida de fracción preparativa HPLC dirigida por Water Autopurification MS con las siguientes condiciones de columna, Waters XBridge OBD C18, 5pm, 19x50mm; caudal de flujo 20 ml/min; fase móvil, agua con hidróxido de amonio 0,1% (A) y metanol con 0,1% hidróxido de amonio (B) que se ejecuta el siguiente gradiente de 0 a 2 minutos (15% B), 2 a 6 minutos (15-100% B); Detector ZQ Mass Detector en modo de ionización por electrospray. 5-(4-(4-(1-Hidroxiciclopropanocarbonil}piperazina-1-carbonil)fenil)-1H-indol-3-carbonitril (3,5 mg, 8,4pmol, rendimiento 42%). MS (ESI, ión pos) m/z: 415 (m 1).
Método de referencia 8.
1-(4-(bifenil)carbonil) paiperazin-1-il)-2-metoxi-2-metilpropan-1-ona
[0271] Se añadió hidruro de sodio (9,08 mg, 0,227 mmol) a una solución de 1-(4-(bifenil}carbonil)piperazin-1-il)-2-hidroxi-2-metilpropan-1-ona (32 mg, 0,091 mmol) en DMF (4 ml). Después de agitarse a ta durante 30 min, yoduro de metilo (0,028mL, 0,454 mmol) se añadió. La mezcla se agitó a ta durante una noche. La mezcla se concentró y el
residuewas purificó por medio de HPLC en fase inversa preparativa (20 ml/min, gradiente de 10 min 15%- 85% CH3CN, 0,01% HCO2H onan XTerra Prep MS C18 Ob D 5pm, columna de 19x100 mm) para dar 1-(4-(bifenil}carbonil)piperazin-1-il)-2-metoxi-2-metilpropan-1-ona (12,2 mg, 37%). MS (ESI, ión pos) m/z: 367 (M 1).
Método 9.
Preparación de (4-(2-cloro-4-(quinolin-6-il)benzoil)piperazin-1-il)(1-hidroxiciclopropil)metanona
[0272] A una solución de ferc-butilo piperazina-1-carboxilato (0,2 m de 1,4-dioxano con 5% W,W-diisopropiletilamina, 150 pL, 0,03 mmol), se añadió ácido 4-fenoxibenzoico (0,2 M de 1,4-dioxano, 150 pL, 0,03 mmol), seguido de solución (benzotriazol-1-iloxi) tris(dimetilamino) fosfonio hexafluorofosfato (BOP, 0,5 M en 1,2-dicloroetano, 66 pL, 0,033 mmol). La mezcla resultante se puso en un agitador a temperatura ambiente durante 2 horas. Solución de ácido clorhídrico (4 N en 1,4-dioxano, 75 gL) se añadió y la mezcla se puso en un agitador a 50°C durante 1 hora. Después de enfriarse a temperatura ambiente, la mezcla se concentró, y el residuo se volvió a disolver en una solución de 10% diisopropiletil amina en dimetilacetamida (200 pL). Ácido 1-Hidroxiciclopropanocarboxílico (0,2 M de 1,4-dioxano, 180 pL, 0,036 mmol) se añadió a la mezcla, seguido de una solución BOP (0,5 M en 1,2-dicloroetano, 72 pL, 0,036 mmol). La mezcla se agitó un agitador a temperatura ambiente durante 2 horas. Después, la mezcla de reacción se diluyó con solución de hidróxido de sodio (1 N en salmuera, 0,45 ml) y acetato de etilo (0,5 ml). La capa orgánica se separó y la capa acuosa se extrae con acetato de etilo (0,6 ml). Las capas orgánicas combinadas se concentraron y el residuo se purificó por cromatografía líquida de alta resolución (recogida de fracción preparativa HPLC dirigida por Water Autopurification MS con las siguientes condiciones: Columna: Waters XBridge OBD C18, 5pm, 19x50mm; velocidad de flujo 20 ml/min; fase móvil, agua con hidróxido de amonio 0,1% (A) y metanol con hidróxido de amonio al 0,1% (B) que se ejecuta el siguiente gradiente de 0 a 2 minutos (15% B), de 2 a 6 minutos (15-100% B); Detector ZQ detector de masas en modo de ionización por electrospray) para proporcionar (4-(2-cloro-4-(quinolin-6-il)benzoil)piperazin-1-il)(1-hidroxiciclopropil)metanona (4,1 mg, 11pmol, 37% de rendimiento). MS (ESI, pos.ion) m/z: 367 (M 1).
Método 10.
Etapa 1. terc-Butilo 4-(3-cloro-4-(1H-indol-5-il)benzoil)piperazina-1-carboxilato
[0273] A una solución de terc-butilo 4-(4-bromo-3-clorobenzoil)piperazina-1-carboxilato (505 mg, 1,25 mmol) en 1,4-dioxano (9 ml) se añadió 5-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1 H-indol (365 mg, 1,5 mmol), fosfato de potasio (1,06 g, 5 mmol) y agua (3 ml). La mezcla se burbujeó con (0) se añadió nitrógeno y tetrakis (trifenilfosfina)paladio (72,2 mg, 0,063 mmol). La mezcla se selló y se calentó a 80°C durante la noche. Después de enfriarse a rt, la mezcla se diluyó con agua (10 ml) y acetato de etilo (20 ml). La capa orgánica se separó y la capa
acuosa se extrajo con acetato de etilo (20 ml). Las capas orgánicas combinadas se concentraron para producir terc-butilo 4-(3-cloro-4-(1 H-indol-5-il)benzoil)piperazina-1-carboxilato (578 mg, 1,31 mmol, 100% de rendimiento). El producto en bruto se utilizó sin purificación adicional. MS (ESI, ión pos) m/z: 440 (M 1).
E tapa 2. (4-(3-cloro-4-(1-isopropil-1H-indol-5-il)benzoil)piperazin-1-il)(1-hidroxiciclopropil)metanona
[0274] A un vial cargado con hidruro de sodio (60% en aceite mineral, 1,6 mg, 0,040 mmol) y DMF (0,1 ml), se añadió terc-butilo 4-(3-cloro-4-(1H-indol-5-il)benzoil)piperazina-1-carboxilato (0,2 M en DMF, 0,1 ml, 0,02 mmol), seguido por 2-yodopropano (0,2 M en DMF, 0,2 ml, 0,04 mmol). La mezcla resultante se puso en un agitador durante 30 min. a temperatura ambiente. Después, la mezcla se diluyó con agua y acetato de etilo. La capa orgánica se separó y la capa acuosa se extrajo con acetato de etilo. Las capas orgánicas combinadas se concentraron a vacío. El residuo se disolvió en metanol (0,3 ml) y una solución de HCl (4 N 1,4-dioxano, 50 pL) se añadió. La mezcla se puso en un agitador a 50°C durante 1 hora. Después de enfriarse a temperatura ambiente, se concentró la mezcla. El residuo se disolvió en una solución de 5% N,N-diisopropiletilamina en dimetilacetamida (0,2 ml) y ácido 1-hidroxiciclopropanocarboxílico (0,2 m de 1,4-dioxano, 120 pL, 0,024 mmol) se añadió, seguido por solución de BOP (0,5 M en 1,2-dicloroetano, 48 pL, 0,024 mmol). La mezcla se puso en un agitador a temperatura ambiente durante 2 horas. La mezcla de reacción se diluye con solución de hidróxido sódico (1 N en salmuera, 0,45 ml) y acetato de etilo (0,5 ml). La capa orgánica se separó y la capa acuosa se extrajo con acetato de etilo (0,6 ml). Las capas orgánicas combinadas se concentraron y el residuo se purificó por cromatografía líquida de alto rendimiento (recogida de fracción preparativa HPLC dirigida por Water Autopurification MS con las siguientes condiciones: Columna: Waters XBridge OBD C18, 5pm, 19x50mm; velocidad de flujo 20 ml/min; mobilephase, agua con hidróxido de amonio 0,1% (A) y metanol con hidróxido de amonio al 0,1% (B) que ejecuta el followinggradient 0 a 2 minutos (15% B), de 2 a 6 minutos (15-100% B); Detector de masas ZQ Detector en modo de ionización por electrospray) toafford (4-(3-cloro-4-(1-isopropil-1H-indol-5-il)benzoil)piperazin-1-il)(1-hidroxiciclopropil)metanona (2,2 mg, 4,7 pmol, 24% de rendimiento). Ms (ESI, ión pos) m/z: 466 (M 1).
Método 11.
Etapa 1. te rc -B u tilo 4-(3’-amino-[1,1 -bifenil]-4-carbonil)piperazina-1-carboxilato
[0275] A una solución de terc-butilo piperazina-1-carboxilato (745 mg, 4 mmol) en DMF (20 ml) se añadió N,N-diisopropiletilamina (1,43 ml, 8 mmol), seguido de 3’-aminobifenil-4-ácido carboxílico (853 mg, 4 mmol) y (benzotriazol-1-iloxi)tris(dimetilamino)fosfonio hexafluorofosfato (BOP, 2,12 g, 4. 8 mmol). La mezcla resultante se agitó a temperatura ambiente durante 1 hora. Después, la mezcla se vertió en hielo-agua (40 ml) con agitación. El precipitado se filtró, se lavó con agua y se secó al aire para dar terc-butilo 4-(3’-aminobifenil}carbonil)piperazina-1-carboxilato (1,2 g, 3,15 mmol, 79% de rendimiento). El producto se usó para la siguiente etapa sin purificación adicional. MS (ESI, ión pos) m/z: 382 (M 1).
Etapa 2. W-(4'-(4-(1-Hidroxiciclopropanocarbonil}piperazina-1-carbonil)-[1,1'-bifenil]-3-il)bencenosulfonamida o etilo (4'-(4-(1-hidroxiciclopropano-1-carbonil)piperazina-1-carbonil)-[1,1’-bifenil]-3-il)carbamato
[0276] A una solución de terc-Butilo 4-(3’-aminobifenil}carbonil)piperazina-1-carboxilato (0,2 M de 1,4-dioxano, 150 pL, 0,03 mmol) se añadió piridina (9,7 pL, 0,12 mmol) seguido de cloruro de bencenosulfonilo (0,2 M en 1,4-dioxano,
300 pL, 0,06 mmol) o clorocarbonil de etilo (0,2 M in1,4-dioxano, 300 pL, 0,06 mmol). La mezcla resultante se puso en un agitador a 80°C durante la noche. La mezcla de reacción se diluyó con solución de hidróxido de sodio (1 N en salmuera, 0,45 ml) y acetato de etilo (0,6 ml). La capa orgánica se separó y la capa acuosa se extrajo con acetato de etilo (0,6 ml). Las capas orgánicas combinadas se concentraron. El residuo se disolvió en metanol (200 pL) y solución HCl (4 N en 1,4-dioxano, 75 pL) se añadió. La mezcla se puso en un agitador a 50°C durante 1 hora. La mezcla de reacción se concentró al vacío y el residuo se disolvió en una solución de dimetilacetamida con 10%N, Ndiisopropiletilamina (200 pL). ácido 1-Hidroxiciclopropanocarboxílico (0,2 M en 1,4-dioxano, 180 pL, 0,036 mmol) se añadió seguido por solución BOP (0,5 M en 1,2-dicloroetano, 72 pL, 0,036 mmol). La mezcla se puso en un rt shakerat durante 2 horas. Después, la mezcla de reacción se diluyó con solución de hidróxido de sodio (1 N en salmuera, 0,45 ml) y acetato de etilo (0,5 ml). La capa orgánica se separó y la capa acuosa se extrajo con acetato de etilo (0,6 ml).Las capas orgánicas combinadas se concentraron y el residuo se purificó por cromatografía líquida de alto rendimiento (dirigida-MS Aguas autopurificación HPLC recogida de fracciones de preparación con las siguientes condiciones: columna: Waters XBridgeOBD C18, 5pm, 19x50mm; velocidad de flujo 20 ml/min; fase móvil, agua con hidróxido de amonio 0,1% (A) y metanol con hidróxido de amonio al 0,1% (B) que se ejecuta el siguiente gradiente de 0 a 2 minutos (15% B), de 2 a 6 minutos (15-100% B); Detector de masas Detector Zq en el modo de ionización por electrospray) para proporcionar N-(4'-(4-(1-hidroxiciclopropanocarbonil}piperazina-1-carbonil)bifenil-3-il)bencenosulfonamida (7,8 mg, 15pmol, 51% de rendimiento). MS (ESI, ión pos) m/z: 506 (M 1).
Método 12.
Preparación de N-(4'-(4-(1-hidroxiciclopropanocarbonil}piperazina-1-carbonil)bifenil-3-il)oxetano-3-carboxamida
[0277] (3’-aminobifenil-4-il)(4-(1-hidroxiciclopropanocarbonil}piperazin-1-il)metanona (0,168 g, 0,460 mmol), N,N-diisopropiletilamina (0,241 ml, 1,379 mmol) y oxetano-3-ácido carboxílico (0,055 g, 0,506 mmol) se combinaron en DMF (5 ml). O-(benzotriazol-1-il)-N,N,N’,N’-tetrametiluronio (0,244 g, 0,644 mmol) se añadió para dar una solución de color amarillo claro. Esto se agitó durante 18 h. N,N-diisopropiletilamina (0,120 ml, 0,687 mmol), O-(benzotriazol-1-il)-N,N,N’,N’-tetrametiluronio (0,18 g, 0,474 mmol), y oxetano-3-ácido carboxílico (0,025 g, 0,244 mmol) se añadieron. Se continuó agitando durante 5 h. La reacción se diluyó con 10 ml de agua y agitación. Se añadieron otros 15 ml de agua y la emulsión acuosa se extrajo con 50 ml de diclorometano y luego 20 ml de diclorometano. Las capas orgánicas combinadas se levaron con 20 mL de agua y luego con 20 mL de salmuera, secada sobre MgSO4 y concentrada. El material se purificó por cromatografía en columna sobre gel de sílice (columna Biotage de 25 g, gradiente de elución con 0-6% metanol/diclorometano). El material obtenido se volvió a purificar en columna de gel de sílice segundo ona (columna Biotage de 25 g, 4-6,5% de metanol/diclorometano). La concentración de la fracciones proporcionó una película amarilla. Este material se recogió en 40 ml de diclorometano y se lavó dos veces con 5 ml de NaHCO3 diluido y una vez con 5ml de salmuera. La solución se secó sobre MgSO4 y se concentró para proporcionar un aceite amarillo. Este aceite se recogió en diclorometano y se trituró con hexanos. La filtración proporcionó N-(4'-(4-(1 -hidroxiciclopropano-carbonil}piperazina-1 -carbonil)bifenil-3-il)oxetano-3-carboxamida (0,036 g, 0,076 mmol, 17%) como un sólido amarillo. MS (ESI, ión pos) m/z: 450 (M 1).
Método 13.
l t í apa 1] (Etapa 2)
Etapa 1.6-fluorobenzo[d]oxazol-2(3H)tiona
[0278] En un matraz de fondo redondo de 250 ml, se colocó 2-amino-5-fluorofenol (8 g, 62,93 mmol, 1,00 equiv), etoxi (potasiosulfanil)metanotiona (11,1 g, 69,25 mmol, 1,10 equiv), etanol (150 ml). La solución resultante se calentó a reflujo durante la noche en un baño de aceite. La mezcla de reacción se enfrió a temperatura ambiente con un baño de agua y después se concentró a vacío. La suspensión resultante se diluyó con 150 ml de agua y su valor pH se ajustó a 5 con ácido acético y se formó precipitación. Los sólidos se recogieron por filtración y se secaron en un horno. Esto dio lugar a 9,2 g (86%) del compuesto del título como un sólido gris. LC-MS (ES, m/z) 170 [M+H]+ Etapa 2. 2-cloro-6-fluorobenzo[d]oxazol
[0279] En un matraz de fondo redondo de 500 ml, se colocó 6-fluoro-2,3-dihidro-1,3-benzoxazol-2-tiona (9,2 g, 54,38mmol, 1,00 equiv), cloruro de tionilo (200 ml) y DMF (0,5 ml). La solución resultante se agitó durante 6 h a 80°C en un baño de aceite. Después de la reacción, el exceso de SOCl2 se eliminó a vacío. El residuo se aplicó sobre una columna de gel de sílice con etilo acetato/petróleo éter (0/100 ~ 7/93). Las fracciones se recogieron y se concentraron al vacío. Esto dio lugar a 3,5 g (38%) del compuesto del título como un aceite marrón. LC-MS (ES, m /z) 172 [M+H]+
Etapa 3. Cloruro de 4-bromo-2-fluorobenzoilo
[0280] En un matraz de fondo redondo de 250 ml, se colocó 4-bromo-2-ácido fluorobenzoico (10 g, 45,66 mmol), cloruro de tionilo (50 ml) y N,N-dimetilformamida (0,1 ml). La mezcla resultante se agitó durante 2 h a 80°C. Después de enfriarse a temperatura ambiente, la solución se concentró a vacío. Esto dio lugar a 10 g (92%) del compuesto del título como aceite amarillo claro. El producto se usó en la siguiente etapa directamente sin purificación adicional.
Etapa 4. terc-butilo 4-(4-bromo-2-fluorobenzoilo)piperazina-1-carboxilato
[0281] En un matraz de fondo redondo de 250 ml, se colocó una solución de cloruro de 4-bromo-2-fluorobenzoilo (10 g, 42,11 mmol, 1,00 equiv) en N,N-dimetilformamida (100 ml). Esto fue seguido por la adición de terc-butilo piperazina-1-carboxilato (7,88 g, 42,31 mmol, 1,00 equiv) en varias porciones. Después, DIEA (16,25 g, 125,74 mmol, 2,99 equiv) se añadió. La solución resultante se agitó durante la noche a temperatura ambiente. El producto se precipitó por la adición de 400 ml de H2O. Los sólidos se recogieron por filtración y se secaron en un horno. Esto dio lugar a 14 g (86%) del compuesto del título como un sólido blanco. lC-MS (ES,m /z) 387, 389 [M+H]+
Paso 5. terc-butilo 4-(2-fluoro-4-(4,4,5,5-tetramet¡l-1,3,2-d¡oxaborolan-2-¡l)benzo¡l)p¡peraz¡na-1-carbox¡lato (Intermedio 3)
[0282] En un matraz de fondo redondo de 2000 ml purgado y mantenido con una atmósfera inerte de nitrógeno, se colocó una solución de terc-butilo 4-[(4-bromo-2-fluorofenil}carbonil)piperazina-1-carboxilato (57 g, 147,19 mmol, 1.00 equiv) en N,N-dimetilformamida (800 ml), 4,4,5,5-tetrametil-2-(tetrametil-1,3,2-dioxaborolan-2-il)-1,3,2-dioxaborolano (76,2 g, 300,07 mmol, 2,01 equiv), PdCl2 (Dppf) (11 g, 15,03 mmol, 0,10 equiv), KOAc (44,1 g, 449,36 mmol, 3,00 equiv). La mezcla resultante se agitó durante la noche a 70°C. Después de enfriarse a temperatura ambiente, la mezcla se vertió en 3 L de H2O. Los sólidos se recogieron por filtración, se purificaron adicionalmente mediante una columna de gel de sílice con etilo acetato/petróleo éter (3: 7). Las fracciones recogidas se combinaron y se concentraron bajo vacío. Esto dio lugar a 30 g (47%) del compuesto del titulo como un sólido de color marrón claro. LC-MS (ES, m /z) 435 [M+H]+
Paso 6. terc-but¡lo 4-(2-fluoro-4-(6-fluorobenzo[d]oxazol-2-¡l)benzo¡l)p¡peraz¡na-1-carbox¡lato
[0283] En un matraz de fondo redondo de 100 ml purgado y mantenido con una atmósfera inerte de nitrógeno, se colocó una solución de terc-butilo 4-[(2-fluoro-4-(tetrametil-1,3,2-dioxaborolan-2-il)fenil]carbonil]piperazina-1-carboxilato (1,26 g, 2,90 mmol, 1,00 equiv) en tolueno (24 ml), 2-cloro-6-fluoro-1,3-benzoxazol (500 mg, 2,91 mmol, 1.00 equiv), Pd(PPh3)4 (336 mg, 0,29 mmol, 0,10 equiv), carbonil sódico (12 ml, 2 M), etanol (3,3 ml). La mezcla resultante se agitó durante la noche a 95°C. Después de enfriarse a temperatura ambiente, la solución resultante se diluyó con 30 ml de agua y se extrajo con 2x30 ml de acetato de etilo. Las capas orgánicas se combinaron y secaron sobre sulfato y sodio anhidro y se concentró bajo vacío. El residuo se aplicó sobre una columna de gel de sílice con EA/DCM (3/10). Este resultado en 1,1 g (86%) del compuesto del título como un sólido gris. LC-MS (ES,m/z) 444 [M+H]+
Paso 7. (2-fluoro-4-(6-fluorobenzo[d]oxazol-2-¡l)fen¡l)(p¡peraz¡n-1-¡l)metanona
[0284] En un matraz de fondo redondo de 250 ml, se colocó una solución de terc-butilo 4-[(2-fluoro-4-(6-fluoro-1,3-benzoxazol-2-il)fenil]carbonil]piperazina-1-carboxilato de (1,1 g, 2,48 mmol, 1,00 equiv) en diclorometano (100 ml). A lo anterior se introdujo el gas de cloruro de hidrógeno. La solución resultante se agitó durante 1 h a temperatura ambiente. Los sólidos se recogieron por filtración y después se disolvieron en agua, luego se ajustaron a pH 6~7 con bicarbonato de sodio. Entonces el los sólidos fueron recogidos por filtración y se secaron en horno. Esto dio lugar a 700 mg (82%) del compuesto del título como un sólido gris. LCMS (ES,m /z) 344 [M+H]+
Paso 8. (4-(2-fluoro-4-(6-fluorobenzo[d]oxazol-2-¡l)benzo¡l)p¡peraz¡n-1-¡l)(1-h¡drox¡c¡cloprop¡l)metanona
[0285] En un matraz de fondo redondo de 50 ml, se colocó una solución de 6-fluoro-2-[3-fluoro-4-[(piperazin-1-il}carbonil)fenil]-1,3-benzoxazol (538 mg, 1,57 mmol, 1,00 equiv) en N,N-dimetilformamida (15 ml), 1-hidroxiciclopropano-1-ácido carboxílico (160 mg, 1,57 mmol, 1,00 equiv), HBTU (891 mg, 2,35 mmol, 1,50 equiv), DIEA (809 mg, 6,26 mmol, 4,00 equiv). La solución resultante se agitó durante la noche a temperatura ambiente. La mezcla de reacción se diluye con 30 ml de agua. La solución resultante se extrajo con 2x20 ml de diclorometano y las capas orgánicas combinads y se secaron sobre sulfato de sodio anhidro y se concentraron a vacío. El residuo se aplicó sobre una columna de gel de sílice con etilo acetato/petróleo éter (7: 1). se recogió y se concentró la fracción. Este producto se recristalizó a partir de EA/PE en la relación de 10/1. Esto dio lugar a 206,7 mg (30%) del compuesto del título en forma de un sólido blanco. LC-MS (ES,m/z) 428 [M+H]+
Método 14.
Etapa 1. terc-butilo 4-(4-(1-met¡l-1H-benzo[d]¡m¡dazol-5-¡l)benzo¡l)p¡peraz¡na-1-carbox¡lato
[0286] En un matraz de fondo redondo de 100 ml, se colocó terc-butilo 4-[(4-(tetrametil-1,3,2-dioxaborolan-2-il)fenil]carbonil]piperazina-1-carboxilato (832 mg, 2,00 mmol, 1,00 equiv), 5-bromo-1-metil-1H-1,3-benzodiazol (422 mg, 2,00 mmol, 1,00 equiv), Pd(PPh3)4 (232 mg, 0,20 mmol, 0,10 equiv), carbonil sódico (2 N, 5 ml), tolueno (10 ml), etanol (3 ml). La mezcla resultante se agitó durante la noche a 95°C en un baño de aceite. Después de enfriarse a temperatura ambiente, la solución resultante se diluyó con 10 ml de agua, se extrajo con 3x20 ml de acetato de etilo. Las capas orgánicas se combinaron, se secaron sobre sulfato de sodio anhidro y se concentraron bajo vacío. El residuo se aplicó a una columna de gel de sílice con etilo acetato/petróleo éter (0/100 ~ 100/0). Las fracciones recogidas se combinaron y se concentraron bajo vacío. Esto dio lugar a 800 mg (95%) del compuesto del título como un sólido de color amarillo claro. LC-MS (ES, m /z): 421 [M+H]+
Etapa 2. (4-(1-met¡l-1H-benzo[d]¡m¡dazol-5-¡l)fen¡l)(p¡peraz¡n-1-¡l)metanona
[0287] En un matraz de fondo redondo de 100 ml, se colocó terc-butilo 4-[(4-(1-metil-1H-1,3-benzodiazol-5-il)fenil]carbonil]piperazina-1-carboxilato (800 mg, 1,90 mmol, 1,00 equiv), diclorometano (20 ml). A continuación, se introdujo en gas HCl. La solución resultante se agitó durante 1,5 h a temperatura ambiente. Los sólidos se recogieron por filtración y se secó bajo vacío. Esto dio lugar a 580 mg (95%) del compuesto del título como un sólido de color blanquecino. LC-MS (ES, m /z): 321 [M+H]+
Etapa 3. terc-but¡lo (1-(4-(4-(1-met¡l-1H-benzo[d]¡m¡dazol-5-¡l)benzo¡l)p¡peraz¡na-1-carbon¡l)c¡cloprop¡l)carbamato
[0288] En un matraz de fondo redondo de 50 ml, se colocó 1-metil-5-[4-[(piperazin-1-il}carbonil)fenil]-1H-1,3-benzodiazol hidrocloruro (580 mg, 1,63 mmol, 1,00 equiv), 1-[((terc-butoxi}carbonil)amino]ciclopropano-1-ácido carboxílico (360 mg, 1,79 mmol, 1,10 equiv), HBTU (927 mg, 2,44 mmol, 1,50 equiv), DIEA (841 mg, 6,51 mmol, 4,00 equiv), N,N-dimetilformamida (10 ml). La mezcla se agitó durante la noche a temperatura ambiente durante toda la noche. Los solución resultantes se diluyó con 60 ml de agua, se extrajo con 3x60 ml de diclorometano. Las capas orgánicas se combinaron, se secaron sobre sulfato de sodio anhidro y se concentraron bajo vacío. El residuo se aplicó sobre una columna de gel de sílice con diclorometano/metanol (80/20). Las fracciones recogidas se combinaron y se concentraron bajo vacío. Esto dio lugar a 800 mg (cuantitativo) del compuesto del título como un aceite incoloro. LC-MS (ES, m/z): 504 [M+H]+
Etapa 4. (4-(1-am¡noc¡clopropano-1-carbon¡l)p¡peraz¡n-1-¡l)(4-(1-met¡l-1H-benzo[d]¡m¡dazol-5-¡l)fen¡l)metanona [0289] En un matraz de fondo redondo de 100 ml, se colocó terc-butilo N-[1-[(4-[(4-(1-metil-1H-1,3-benzodiazol-5-il)fenil]carbonil]piperazin-1-il}carbonil)ciclopropil]carbamato (800 mg, 1,59 mmol, 1,00 equiv), diclorometano (50 mL).
A continuación el gas HCl se burbujeó durante 1,5 h a temperatura ambiente. Los sólidos se recogieron por filtración y se lavaron con DCM (50 ml). A continuación, los sólidos se disolvieron en 5 ml de agua. El valor pH de la solución se ajustó a 8 carbonil con potasio (2 M). La mezcla resultante se extrajo con 2x50 ml de diclorometano y las capas orgánicas se combinaron y se concentraron a vacío. El producto en bruto se purificó por prep-HPLC con las siguientes condiciones (Waters III): Columna, Xbridge RP18 19*150; fase móvil, agua (0,05% NH4HCO3) y MeCN (15% CH3CN hasta el 75% en 10 min); Detector, UV 220 y 254 nm. Esto dio lugar a 93,1 mg (15%) del compuesto del título como un sólido blanco. LC-MS (ES, m/z) 404 [M+H]+.
Método 15.
Etapa 1.4-bromo-2-cloruro de fluorobenzoilo
[0290] En un matraz de fondo redondo de 250 ml, se colocó 4-bromo-2-ácido fluorobenzoico (10 g, 45,66 mmol, 1,00 equiv), cloruro de tionilo (50 ml), N,N-dimetilformamida (0,1 ml). La solución resultante se agitó durante 2 h a 80°C. después de enfriarse a temperatura ambiente, la mezcla resultante se concentró bajo vacío. Esto dio lugar a 10 g (92%) del compuesto del titulo como aceite amarillo claro. El producto se usó en la siguiente etapa directamente sin purificación adicional.
Etapa 2. terc-butilo 4-(4-bromo-2-fluorobenzoilo)piperazina-1-carboxilato
[0291] En un matraz de fondo redondo de 250 ml, se colocó una solución de cloruro de 4-bromo-2-fluorobenzoilo (10 g, 42,11 mmol, 1,00 equiv) en N,N-dimetilformamida (100 ml). Esto fue seguido por la adición de terc-butilo piperazina-1-carboxilato (7,88 g, 42,31 mmol, 1,00 equiv) en varias porciones. DIEA Entonces a esto se añadió (16,25 g, 125,74 mmol, 2,99 equiv). La mezcla resultante se agitó durante la noche a temperatura ambiente. La mezcla se vertió en 300 ml de agua. Los sólidos se recogieron por filtración y se secaron a vacío. Esto dio lugar a 14 g (86%) del compuesto del título como un sólido blanco. LC-MS (ES,m/z): 387, 389 [M+H]+
[0292] En un matraz de fondo redondo de 100 ml purgado y mantenido con una atmósfera inerte de nitrógeno, se colocó una solución de terc-butilo 4-(4-bromo-2-fluorobenzoilo)piperazina-1-carboxilato (1 g, 2,58 mmol, 1,00 equiv) en tolueno (10 ml), (4-cloro-2-fluorofenil)ácido borónico (540 mg, 3,10 mmol, 1,20 equiv), Pd(PPh3)4 (358 mg, 0,31 mmol, 0,12 equiv), carbonil de sodio (2 M en agua, 5 ml), etanol (1,4 ml). La mezcla resultante se agitó durante la noche a 105°C. Después de enfriarse a temperatura ambiente, la solución resultante se diluyó con 20 ml de H2O y se extrajo con 3x20 ml de acetato de etilo. Las capas orgánicas se combinaron, se lavaron con 3x20 ml de salmuera, se secó sobre sulfato de sodio anhidro y se concentra bajo vacío. El residuo se aplicó sobre una columna de gel de sílice con etilo acetato/petróleo éter (3: 7). Se recogieron las fracciones y se combinaron y se concentraron a vacío. Esto dio lugar a 1 g (89%) del compuesto de título como un sólido de color amarillo claro. LC-MS (ES,m/z): 437 [M+H]+
Etapa 4. cloro-2',3-difluoro-[1,1 ’-bifenil]-4-il)(piperazin-1-il)hidrocloruro de metanona
[0293] En un matraz de fondo redondo de 100 ml, se colocó terc-butilo 4-(4’-cloro-2', 3-difluoro-[1,1’-bifenil]-4-carbonil)piperazina-1-carboxilato de (1 g, 2,28 mmol, 1,00 equiv), ácido clorhídrico en 1,4-dioxano (4 M, 30 ml). La solución resultante se agitó durante 30 min a temperatura ambiente. La mezcla resultante se concentró bajo vacío. Esto dio lugar a 600 mg (78%) del compuesto del título como un sólido de color blanquecino. LC-MS (ES,m/z): 337 [M+H]+
Paso 5. (4- cloro-2’,3-difluoro-[1,1 ’-b¡fen¡l]-4-carbon¡l)p¡peraz¡n-1-¡l)(1-hidrox¡c¡cloprop¡l)metanona [0294] En un matraz de fondo redondo de 100 ml, se colocó una solución de (4’-cloro-2’,3-difluoro-[1,1’-bifenil]-4-il)(piperazin-1-il)metanona (500 mg, 1,48 mmol, 1,00 equiv), N,N-dimetilformamida (20 ml), 1-hidroxiciclopropano-1-ácido carboxílico (166 mg, 1,63 mmol, 1,10 equiv), HBTU (841 mg, 2,22 mmol, 1,49 equiv), DIEA (764 mg, 5,91 mmol, 3,98 equiv). La solución resultante se agitó durante la noche a temperatura ambiente. La mezcla se vertió into80 ml de agua y se formó precipitación. Los sólidos se recogieron por filtración y se aplicaron sobre un gel de sílice columnwith acetato de etilo/hexano (3: 2). Las fracciones recogidas se combinaron y se concentraron bajo vacío. Esto resultó en 260 mg (42%) del compuesto del título como un sólido de color blanquecino. LC-MS (ES,m/z): 421 [M+H]+
Método 16.
Etapa 1.5-bromo-N-met¡l-2H-benzo[d][1,2,3]tr¡azol
[0295] En un matraz de fondo redondo de 100 ml, se colocó una solución de 6-bromo-1H-1,2,3-benzotriazol (600 mg, 3,03 mmol, 1,00 equiv) en N,N-dimetilformamida (10 ml). Esto fue seguido por la adición de hidruro de sodio (60% en aceite, 303 mg, 7,58 mmol, 2,50 equiv) en porciones a 0°C. Después de agitarse durante 30 min a 0°C, CH3 I (650 mg, 4,58 mmol, 1,50 equiv) se añadió gota a gota en. La solución resultante se dejó reaccionar, con agitación, durante un adicional de 18 h a 20°C. a continuación La mezcla de reacción se diluyó con 10 ml de hielo/agua, se extrajo con 3x20 ml de acetato de etilo. Las capas orgánicas se combinaron, se secaron sobre sulfato de sodio anhidro y se concentraron a vacío. El residuo se aplicó sobre una columna de gel de sílice con PE: EA (200: 1~3: 1). Esto dio lugar a 700 mg (bruto) de una mezcla de los compuestos del título como un aceite amarillo. LC-MS (ES, m/z): 212, 214 [M+H]+
Etapa 2. terc-but¡lo 4-(4-(N-met¡l-2H-benzo[d][1,2,3]tr¡azol-5-¡l)benzo¡l)p¡peraz¡na-1-carbox¡lato
[0296] En un matraz de fondo redondo de 100 ml purgado y mantenido con una atmósfera inerte de nitrógeno, se colocó terc-butilo del ácido 4-[(4-(tetrametil-1,3,2-dioxaborolan-2-il)fenil]carbonil]piperazin-1-carboxilato (1,51 g, 3,63 mmol, 1,10equiv), la mezcla de 5-bromo-N-metil-2H-benzo[d][1,2,3]triazoles (700 mg, 3,30 mmol, 1,00 equiv), Pd(Ppha)4 (382 mg, 0,33 mmol, 0 , 10 equiv) y tolueno/EtOH (30/4,5 ml), carbonil sódico (15 ml, 2 M). La mezcla resultante se agitó durante 18 horas a 90°C. Después de enfriarse a temperatura ambiente, la mezcla de reacción se diluyó con 50 ml de agua, se extrajo con 3x30 ml de acetato de etilo. Las capas orgánicas se combinaron, se secaron sobre sulfato de sodio anhidro y el vacío se concentró bajo vacío. El residuo se aplicó sobre una columna de gel de sílice con diclorometano/metanol (200/1 ~ 20/1). Esto resultó en 1,2 g (crudo) de una mezcla de los compuestos del título como un sólido de color amarillo claro. LC-MS (ES, m/z): 422 [M+H]+
Etapa 3. (4-(N-met¡l-2H-benzo[d][1,2,3]tr¡azol-5-¡l)fen¡l)(p¡peraz¡n-1-¡l)metanona
[0297] En un matraz de fondo redondo de 100 ml, se colocó la mezcla de terc-butilo 4-(4-(N-metil-2H-benzo[d][1,2,3]triazol-5-il)benzoil)piperazina-1-carboxilato de etilo (1,2 g, 2,85 mmol, 1,00 equiv) y diclorometano (50 ml). Entonces, el cloruro de hidrógeno (gas) se introdujo. La solución resultante se agitó durante 30 min a 20°C. Los sólidos resultantes se recogieron por filtración y se secaron bajo presión reducida. Esto dio lugar a 800 mg (79%) de una mezcla de los compuestos del título como sólido amarillo claro. LC-MS (ES, m/z): 322 [M+H]+
Etapa 4. (4-(1 -h¡drox¡c¡clopropano-1 -carbon¡l)p¡peraz¡n-1 -¡l)(4-(2-met¡l-2H-benzo[d][1,2,3]tr¡azol-5-¡l)fen¡l)metanona
[0298] En un matraz de fondo redondo de 100 ml, se colocó una solución de 1-hidroxiciclopropano-1-ácido carboxílico (240 mg, 2,35 mmol, 1,10 equiv) en N,N-dimetilformamida (10 ml), la mezcla de (4-(N-metil-2H-benzo[d][1,2,3]triazol-5-il)fenil)(piperazin-1-il)metanona (766 mg, 2,14 mmol, 1,00 equiv, 98%), HBTU (1,22 g, 3,22 mmol, 1,50 equiv), DIEA (1,11 g, 8,59 mmol, 4,00 equiv). La solución resultante se agitó durante 18 h a 20°C. La mezcla de reacción se diluyó con 20 ml de agua, se extrajo con 3x20 ml de acetato de etilo. Las capas orgánicas se combinaron, se secaron sobre sulfato de sodio anhidro y se concentraron bajo vacío. El residuo se purificó por prep-HPLC con las siguientes condiciones (Waters III): Columna, XBridge Prep C18 OBD Columna, 5 um, 19 * 150 mm; fase móvil, con 0,03 agua% NH3H2O y MeCN (16% de MeCN hasta un 34% en 8 min); Detector, 254 y 220 nm. Esto dio lugar a 90 mg (10%) del compuesto del titulo como un sólido de color amarillo claro. LC-MS (ES, m/z) 406 [M+H]+ Método 17.
[Intermedio 3) I E t i c a I !
apa Eta
pa 1. (4-(4-(terc-butox¡carbon¡l}p¡peraz¡na-1-carbon¡l)fen¡l)ác¡do borón¡co
[0299] En un matraz de 1 L de fondo redondo se colocó Intermed¡o 3 (12,5 g, 30,03 mmol, 1,00 equiv) una solución de peryodato de sodio (32,1 g, 150,00 mmol, 5,00 equiv) en acetona (300 ml), acetato de amonio (150 ml, 5,00 equiv, 1 M). La solución resultante se agitó durante 18 h a ta. La solución resultante se diluyó con 300 ml de agua y se extrajo con 3 x 100 ml de acetato de etilo. Las capas orgánicas se combinaron y se secaron sobre sulfato de sodio. Los sólidos se filtraron y la solución se concentró a vacío. Esto proporcionó el compuesto de título (10,1 g, 96%) como un sólido amarillo claro. LC-MS (ES, m/z) 335 [M+H]+
Etapa 2. terc-but¡lo 4-(4-(2-met¡l-1H-benzo[d]¡m¡dazol-1-¡l)benzo¡l)p¡peraz¡na-1-carbox¡lato
[0300] En un matraz de fondo redondo de 250 ml, se colocó una solución de (4-(4-(terc-butoxicarbonil}piperazina-1-carbonil)fenil)ácido borónico (3,34 g, 9,05 mmol, 2,00 equiv) en diclorometano (50 ml), 2-metil-1H-benzo[d]imidazol (660 mg, 4,99 mmol, 1,00 equiv), Cu (OAc)2 (1,23 mg, 1,50 equiv), piridina (790 mg, 9,99 mmol, 2,00 equiv), 4a
molecularsieves (3 g). La mezcla resultante se agitó durante 18 h a 20°C. Los sólidos se separaron por filtración. El filtrado fue concentrado bajo vacío. El residuo se aplicó sobre una columna de gel de sílice con DCM/MeOH (200/1 ~20/1). Esto dio lugar a 1 g (27%) del compuesto del título como aceite amarillo. LC-MS (ES, m/z): 421 [M+H]+ Etapa 3. (4-(2-met¡l-1H-benzo[d]¡m¡dazol-1-¡l)fen¡l)(p¡peraz¡n-1-¡l)metanona
[0301] En un matraz de fondo redondo de 100 ml, se colocó terc-butilo 4-(4-(2-metil-1H-benzo[d]imidazol-1-il)benzoil)piperazina-1-carboxilato (960 mg, 2,28 mmol, 1,00 equiv), DCM (30 ml), THF (30 ml). Entonces se introdujo cloruro de hidrógeno (gas). La solución resultante se agitó durante 30 min a 20°C. Los sólidos se recogieron por filtración y se secaron bajo vacío. Esto dio lugar a 600 mg del compuesto del título como un sólido de color amarillo claro. LC-MS (ES, m/z): 321 [M+H]+
Etapa 4. (4-(1-h¡drox¡c¡clopropano-1-carbon¡l)p¡peraz¡n-1-¡l)(4-(2-met¡l-1H-benzo[d]¡m¡dazol-1-¡l)fen¡l)metanona
[0302] En un matraz de fondo redondo de 100 ml, se colocó 1-hidroxiciclopropano-1-ácido carboxílico (190 mg, 1,86 mmol, 1,10 equiv), (4-(2-metil-1H-benzo[d]imidazol-1-il)fenil)(piperazin-1-il)metanona (600 mg, 1,68 mmol, 1,00 equiv), HBTU (955 mg, 2,52 mmol, 1,50 equiv), N,N-dimetilformamida (10 ml), DIEA (867 mg, 6,71 mmol, 4,00 equivalentes). La solución resultante se agitó durante 18 h a 20°C. La mezcla de reacción se diluyó con 20 ml de agua, se extrajo con 3x20 ml de acetato de etilo. Todas las capas orgánicas se combinaron, se secaron sobre sulfato de sodio anhidro y se concentraron bajo vacío. El residuo se purificó por prep-HPLC con las siguientes condiciones (Waters I): Columna, Xbridge Prep C18 OBD, 5 um, 19 * 150 mm; fase móvil, Agua (0,05% NH4HCO3) y CH3CN (16% CH3CN hasta 34% en 10 min); Detector, UV 220 y 254 nm. Esto dio lugar a 130 mg (19%) del compuesto del título como un sólido blanco. LC-MS (ES, m/z): 405 [M+H]+
Método 18.
t i d ’ C , O u r i n l t ! . j r . í ¡ T f
ptátw i]
| l n t e r m e c l i o 4 i (Etapa 3)
Etapa 1. terc-but¡lo 4-(4-(2-met¡l-1H-¡ndol-1-¡l)benzo¡l)p¡peraz¡na-1-carbox¡lato
[0303] En un matraz de fondo redondo de 250 ml purgado y mantenido con una atmósfera inerte de nitrógeno, se colocó una solución de terc-butilo 4-[(4-bromofenil}carbonil)piperazina-1-carboxilato (Intermed¡o 1 (X=H), 1,69 g, 4,58 mmol, 1,00 equiv) en tolueno (50 ml), 2-metil-1 H-indol (600 mg, 4,57 mmol, 1,00 equiv), Cul (87 mg, 0,46 mmol, 0,10 equiv), carbonil de potasio (1,9 g, 13,75 mmol, 3,00 equiv), (1R, 2R)-1-N, 2-N-dimetilciclohexano-1,2-diamina (130 mg, 0,91 mmol, 0,20 equiv). La mezcla resultante se agitó durante la noche a 120°C. Después de enfriarse a temperatura ambiente, la mezcla de reacción se diluyó con 50 ml de H2O, se extrajo con 3x50 ml de acetato de etilo. Las capas orgánicas se combinaron, se secaron sobre sulfato de sodio anhidro y se concentró bajo vacío. El residuo se aplicó sobre una columna de gel de sílice con etilo acetato/petróleo éter (1: 1). Las fracciones recogidas se combinaron y se concentraron bajo vacío. Esto resultó en 1,4 g (73%) del compuesto del título como un sólido rojo. LC-MS (ES, m/z): 420 [M+H]+
Etapa 2. (4-(2-met¡l-1H-¡ndol-1-¡l)fen¡l)(p¡peraz¡n-1-¡l)metanona (Intermed¡o 4)
[0304] En un matraz de fondo redondo de 100 ml, se colocó una solución de terc-butilo 4-(4-(2-metil-1 H-indol-1 -il)benzoil)piperazina-1-carboxilato (1,4 g, 3,34 mmol) en diclorometano (30 ml). A lo anterior se introdujo el gas HCl anteriormente. La solución resultante se agitó durante 30 min a temperatura ambiente. La mezcla resultante se concentró a vacío. Esto resultó en 1,4 g (59%) del compuesto del título como un sólido rojo. LC-MS (ES, m/z): 320 [M+H]+
Etapa 3. (4-(1-h¡drox¡c¡clopropano-1-carbon¡l)p¡peraz¡n-1-¡l)(4-(2-met¡l-1H-¡ndol-1-¡l)fen¡l)metanona
[0305] En un matraz de fondo redondo de 100 ml, se colocó una solución de (4-(2-metil-1 H-indol-1 -M)fenil)(piperazin-1-il)metanona (658 mg, 1,85 mmol, 1,00 equiv) en N,N-dimetilformamida (20 ml), 1-hidroxiciclopropano-1-ácido carboxílico (189 mg, 1,85 mmol, 1,00 equiv), HbTU (1,05 g, 2,77 mmol, 1,50 equiv), DiEA (955 mg, 7,39 mmol, 4,00 equiv). La solución resultante se agitó durante la noche a temperatura ambiente. La mezcla de reacción se diluye con 30 ml de agua y se extrajo con 3x30 ml de acetato de etilo. Las capas orgánicas se combinaron, se secaron sobre sulfato de sodio anhidro y se concentraron a vacío. El residuo se aplicó sobre una columna de gel de sílice con diclorometano/metanol (10: 1). Las fracciones recogidas se combinaron y se concentraron bajo vacío. Esto resultó en 112,3mg (15%) del compuesto del título como un sólido de color marrón claro. LC-MS (ES, m/z): 404 [M+H]+
Método 19.
Etapa 1. terc-butilo 4-(4-(indolin-1-il)benzoil)piperazina-1-carboxilato
[0306] En un matraz de fondo redondo de 100 ml purgado y mantenido con una atmósfera inerte de nitrógeno, se colocó 2,3-dihidro-1 H-indol (390 mg, 3,27 mmol, 1,00 equiv), terc-butilo 4-[(4-bromofenil}carbonil)piperazina-1-carboxilato (Intermedio 1 (R = H), 1,5 g, 3,60 mmol, 1,10 equiv), Cs2CO3 (3,74 g, 11,48 mmol, 3,51 equiv), tolueno (50 ml), se RuPhos paladio (ii) mesilato bifenil-2-amina (276 mg). La mezcla resultante se agitó durante la noche a 85°C. Después de enfriarse la temperatura ambiente, la mezcla resultante se concentró a vacío y se re-disolvió con 200 ml de EA. La mezcla resultante se lavó con 3x50 ml de salmuera, se secó sobre sulfato de sodio anhidro y se concentró bajo vacío. El residuo se aplicó sobre una columna de gel de sílice con éter/acetato de etilo de petróleo (50:50). Esto dio como resultado en 1 g (75%) del compuesto del título como un sólido amarillo. LC-MS (ES, m/z): 408 [M+H]+
Etapa 2. (4-(indolin-1-il)fenil)(piperazin-1-il)hidrocloruro de metanona
[0307] En un matraz de fondo redondo de 100 ml, se colocó terc-butilo 4-(4-(indolin-1-il)benzoil)piperazina-1-carboxilato (1 g, 2,45 mmol, 1,00 equiv), una solución de cloruro de hidrógeno en 1,4-dioxano (4 M, 20 ml). La solución resultante se agita durante 1 h a temperatura ambiente. Los sólidos se recogieron por filtración y se secaron bajo vacío. Esto dio lugar a 800 mg (95%) del compuesto del título como un sólido amarillo. LC-MS (ES, m /z): 308 [M+H]+
Etapa 3. (4-(1-hidroxiciclopropano-1-carbonil)piperazin-1-il)(4-(indolin-1-il)fenil)metanona
[0308] En un matraz de fondo redondo de 100 ml, se colocó (4-(indolin-1-il)fenil)(piperazin-1-il)metanona (540 mg, 1,57 mmol, 1,00 equiv), 1-hidroxiciclopropano-1-ácido carboxílico (160 mg, 1,57 mmol, 1,00 equiv), N,N-dimetilformamida (20 ml), HBTU (892 mg, 2,35 mmol, 1,50 equiv), DIEA (810 mg, 6,27 mmol, 3,99 equiv). La solución resultante se agitó durante la noche a temperatura ambiente. La mezcla de reacción se diluyó con 50 ml de EA, se lavó con 3x30 ml de salmuera, se secó sobre sulfato de sodio anhidro y se concentró a vacío. El residuo se purificó por Prep-HPLC con las siguientes condiciones (Waters I): Columna, SunFire Prep C18, 5 um, 19 * 100 mm; fase móvil, Agua (0,05% NH4HCO3) y CH3CN (50% CH3CN hasta el 100% en 10 min); Detector, UV 220 y 254 nm. Esto resultó en 63,8mg (10%) del compuesto del título como un sólido de color blanquecino. LC-MS (ES, m/z): 392 [M+H]+
Método 20.
intermedio i) tEtipi 1]
Etapa 1. terc-butilo 4-(4-(3,4-dihidroquinolin-1(2H)-il)benzoil)piperazina-1-carboxilato
[0309] En un matraz de fondo redondo de 100 ml purgado y mantenido con una atmósfera inerte de nitrógeno, se colocó Pd2(Dba)4 (305 mg), DavePhos (627 mg), tolueno (50 ml). La mezcla se agitó a temperatura ambiente durante 30 min. A continuación 1,2,3,4-tetrahidroquinolina (700 mg, 5,26 mmol, 1,00 equiv), terc-butilo 4-[(4-bromofenil}carbonil)piperazina-1-carboxilato(Intermedio 1, 1,94 g, 5,25 mmol, 1,00 equiv), t-BuOK (1,18 g, 10,52 mmol, 2,00 equiv) se añadieron sistema util se evacuó y se volvió a llenar con N2 para 5 veces. La mezcla resultante se agitó durante 18 h a 120°C en un baño de aceite. Después de enfriarse a temperatura ambiente, la mezcla resultante se concentró bajo vacío. El residuo se aplicó en una columna de gel de sílice con etilo acetato/petróleo éter (0/100~45/55). Las fracciones recogidas se combinaron y se concentraron bajo vacío. Esto dio lugar a 540 mg (24%) del compuesto del título como un sólido amarillo. LC-MS (ES, m /z): 422 [M+H]+
Etapa 2. (4-(3,4-dihidroquinolin-1(2H)-il)fenil)(piperazin-1-il)metanona
[0310] En un matraz de fondo redondo de 100 ml, se colocó terc-butilo 4-(4-(3,4-dihidroquinolin-1 (2H)-il)benzoil)piperazina-1-carboxilato (540 mg, 1,28 mmol, 1,00 equiv), diclorometano (40 ml). Entonces se burbujeó gas cloruro de hidrógeno. La solución resultante util se agitó durante 2 h a temperatura ambiente. La mezcla resultante se concentró a vacío. Esto resultó en 635 mg (cuantitativo) del compuesto del título como un sólido amarillo. LC-MS (ES, m /z): 322 [M+H]+
Etapa 3. (4-(4-(3,4-dihidroquinolin-1(2H)-il)benzoil)piperazin-1-il)(1-hidroxiciclopropil)metanona
[0311] En un matraz de fondo redondo de 100 ml, se colocó 1-hidroxiciclopropano-1-ácido carboxílico (635 mg, 6,22 mmol, 1,00 equiv), (4-(3,4-dihidroquinolin-1(2H)-il)fenil)(piperazin-1-il)metanona (181 mg, 0,51 mmol, 0,08equiv), HBTU (1,34 g, 3,53 mmol, 0,57 equiv), N,N-dimetilformamida (15 ml), DIEA (457 mg, 3,54 mmol, 0,57 equiv). La solución resultante se agitó durante la noche a temperatura ambiente. La mezcla de reacción se diluyó con 60 ml de EA, se lavó con 4x20 ml de agua y 1x20 ml de salmuera. La fase orgánica se secó sobre sulfato de sodio anhidro y se concentra bajo vacío. El residuo se aplicó sobre una columna de gel de sílice con etilo acetato/petróleo éter (0/100 ~ 100/0). El producto bruto resultante se purificó adicionalmente por prep-HPLC con las siguientes condiciones (Waters III): Columna, Xbridge RP18 19 * 150; fase móvil, agua (0,05% NH4HCO3) y MeCN (15% CH3CN hasta el 75% en 10 min); Detector, UV 220 y 254 nm. Esto dio lugar a 66,3 mg (3%) del compuesto del título como un sólido púrpura. LC-MS (ES, m /z): 406 [M+H]+
Método 21.
Etapa 1. terc-butilo 4-(4-(1-(2-((terc-butildimetilsilil)oxi)etil)-1H-benzo[d]imidazol-5 y 6-il)benzoil)piperazina-1-carboxilato
[0312] En un matraz de fondo redondo de 250 ml, se colocó terc-butilo 4-(4-(1H-benzo[d]imidazol-5-il)benzoil)p¡peraz¡na-1-carbox¡lato (1 g, 2,46 mmol, 1,00 equiv), (2-bromoetoxi) (terc-butil) dimetilsilano (883 mg, 3,69 mmol, 1,50 equiv), N,N-dimetilformamida (50 ml), CS2CO3 (2,41 g, 7,40 mmol, 3,01 equiv). La mezcla resultante se agitó durante la nocha a 70°C. Después de enfriarse a temperatura ambiente, la mezcla de reacción se diluyó con 100 ml de EA, se lavó con 3x50 mL de agua y 50 ml de salmuera. La fase orgánica se secó sobre sulfato de sodio anhidro y bajo vacío concentrado. El residuo se purificó por prep-HPLC con las siguientes condiciones (Waters I): Columna, SunFire Prep C18,5um, 19 * 100 mm; fase móvil, Agua (0,05% NH4HCO3) y CH3CN (55% CH3CN hasta el 75% en 7 min); Detector, UV220 y 254 nm. Esto dio lugar a 380 mg (27%) de terc-butilo 4-(4-(1-(2-((tercbutildimetilsilil)oxi)etil)-1H-benzo[d]imidazol-5-il)benzoil)piperazina-1-carboxilato como un sólido amarillo y 390 mg (28%) de terc-butilo 4-(4-(1 -(2-((terc-butildimetilsilil)oxi)etil)-1 H-benzo[d]imidazol-6-il)benzoil)piperazina-1 -carboxilato como un sólido amarillo. LC-MS (ES, m/z): 565 [M+H]+
Etapa 2. (4-(1-(2-hidroxietil)-1H-benzo[d]imidazol-6-il)fenil)(piperazin-1-il)metanona
[0313] En un matraz de fondo redondo de 100 ml, se colocó terc-butilo 4-(4-(1-(2-((terc-butildimetilsilil)oxi)etil)-1H-benzo[d]imidazol-6-il)benzoil)piperazina-1-carboxilato (380 mg, 0,67 mmol, 1,00 equiv) y dioxano (40 ml). Entonces el gas HCl se introdujo. La solución resultante se agitó durante 1 h a temperatura ambiente. La mezcla resultante se concentró bajo vacío. Esto dio lugar a 250 mg (96%) del compuesto del título como un sólido amarillo. LC-MS (ES, m/z): 351 [M+H]+
Etapa 3. (4-(1-hidroxiciclopropano-1-carbonil)piperazin-1-il)(4-(1-(2-hidroxietil)-1H-benzo[d]imidazol-5-il)fenil)metanona
[0314] En un matraz de fondo redondo de 100 ml, se colocó (4-(1-(2-hidroxietil)-1H-benzo[d]imidazol-6-il)fenil)(piperazin-1-il)metanona (250 mg, 0,65 mmol, 1,00 equiv), 1-hidroxiciclopropano-1-ácido carboxílico (66 mg, 0,65 mmol, 1,00 equiv), N,N-dimetilformamida (20 ml), HBTU ( 3 67 mg, 0,97 mmol, 1,50 equiv), DIEA (333 mg, 2,58 mmol, 3,99 equiv). La solución resultante se agitó durante la noche a temperatura ambiente. La mezcla de reacción se lavó con agua, se secó sobre Na2SO4 y se concentró a vacío. El residuo se purificó por prep-HPLC con las siguientes condiciones (Waters I): Columna, SunFire Prep C18, 5 um, 19 * 100 mm; fase móvil, Agua (0,05% NH4HCO3) y CH3CN (55% CH3CN hasta el 75% en 7min); Detector, UV 220 y 254 nm. Esto dio lugar a 75 mg (27%) del compuesto del título como un sólido blanquecino. LC-MS (ES, m/z): 435 [M+H]+
Método 22.
Etapa 1. terc-butilo (3-(3-bromofenil)¡soxazol-5-¡l)carbamato
[0315] En un matraz de fondo redondo de 250 ml, se colocó una solución de 3-(3-bromofenil)-1,2-oxazol-5-amina (1 g, 4,18 mmol, 1,00 equiv) en diclorometano (40 ml), Boc2O (1,83 g, 8,38 mmol, 2,00 equiv), trietilamina (1,27 g, 12,55mmol, 3,00 equiv), 4-dimetilaminopiridina (51,24 mg, 0,42 mmol, 0,10 equiv). La solución resultante se agitó durante 1 hora a temperatura ambiente. La mezcla resultante se lavó con 2x20 ml de ácido clorhídrico (0,5 M), se secó sobre sulfato de sodio anhidro, se concentró a vacío. Esto dio lugar a 1,42 g (bruto) del compuesto del título como un sólido de color blanquecino. LC-MS (ES, m/z): 339 [M+H]+
Etapa 2. bencilo 4-(4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)benzoil)piperazina-1-carboxilato (Intermedio 5)
[0316] En un matraz de 1 L de fondo redondo se colocó bencil piperazina-1-carboxilato (15 g, 68,10 mmol, 1,00 equiv), 4-(tetrametil-1,3,2-dioxaborolan-2-il)ácido benzoico (16,9 g, 68,12 mmol, 1,00 equiv), EDC (14,4 g, 75,12 mmol, 1,10equiv), HOBt (5,8 g, 42,92 mmol, 0,50 equiv) y trietilamina (27,6 g 272,75 mmol, 4,00 equiv) en diclorometano (300 ml). La solución resultante se agitó durante 18 h a ta. Después, la mezcla se lavó con 0,5 M de carbonil de sodio (acuoso, 75 ml). Después, la mezcla resultante se lavó con 0,5 m HCl (aq, 75 ml) seguido de 0,5 M de carbonil de sodio (acuoso, 75 ml). La solución se concentró en vacío y el producto bruto se recristalizó en TBME/hexano (1: 1). Esto proporcionó el compuesto del título (26 g, 84%) como un sólido blanco. LC-MS (ES, m/z): 451 [M+H]+
Etapa 3. bencil 4-(3'-(5-((terc-butox¡carbon¡l)am¡no)¡soxazol-3-¡l)-[1,1 ’-b¡fen¡l]-4-carbon¡l)p¡peraz¡na-1-carboxilato
[0317] En un matraz de fondo redondo de 250 ml purgado y mantenido con una atmósfera inerte de nitrógeno, se colocó una solución de terc-butilo (3-(3-bromofenil)isoxazol-5-il)carbamato de metilo (1,42 g, 4,19 mmol, 1,00 equiv) en 1,4-dioxano (30 ml), bencilo 4-(4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)benzoil)piperazina-1-carboxilato (1,89 g, 4,20 mmol, 1,00equiv), Pd(dppf)Cl2 -CH2Cl2 (410 mg, 0,50 mmol, 0,12 equiv), Cs2CO3 (4,11 g, 12,61 mmol, 3,01 equiv), agua (10 ml). La solución resultante se agitó durante la noche a 60°C. Después de enfriarse a temperatura ambiente, se diluyó la mezcla de reacción con 30 ml de H2O, se extrajo con 3x30 ml de acetato de etilo. Las capas orgánicas se combinaron, se lavaron con 30 ml de salmuera, se secaron sobre sulfato de sodio anhidro y se concentraron a vacío. El residuo se aplicó sobre una columna de gel de sílice con etilo acetato/petróleo éter (1: 1). Las fracciones recogidas se combinaron y se concentraron a vacío. Esto dio lugar a 780 mg (32%) del compuesto del título como un sólido de color blanquecino. LC-MS (ES, m/z): 583 [M+H]+
Etapa 4. terc-butilo (3-(4'-(p¡peraz¡na-1-carbon¡l)-[1,1’-b¡fen¡l]-3-¡l)¡soxazol-5-¡l)carbamato
[0318] En un matraz de fondo redondo de 100 ml, se colocó bencil 4-(3'-(5-((terc-butoxicarbonil)amino)isoxazol-3-il)-[1,1’-bifenil]-4-carbonil)piperazina-1-carboxilato (1,8 g, 3,09 mmol, 1,00 equiv), metanol (40 ml) y catalizador de Lindlar (1,8 g). El matraz se evacuó y back-lleno de hidrógeno durante 6 veces. La solución resultante se agitó temperatura ambiente durante la nocha a. Los sólidos se separaron por filtración. El filtrado se concentró bajo vacío. El residuo fue appliedonto una columna de gel de sílice con diclorometano/metanol (90:10). Las fracciones recogidas se combinaron y se concentraron a vacío. Esto dio lugar a 850 mg (61%) del compuesto del título como un sólido de color amarillo claro. LC-MS (ES, m/z): 449 [M+H]+
Etapa 5. terc-but¡lo (3-(4'-(4-(1 -h¡drox¡c¡clopropano-1 -carbon¡l)p¡peraz¡na-1 -carbon¡l)-[1, 1 ’-b¡fen¡l]-3-¡l)¡soxazol-5-¡l)carbamato
[0319] En un matraz de fondo redondo de 100 ml, se colocó una solución de terc-butilo (3-(4'-(piperazina-1-carbonil)-[1,1’-bifenil]-3-il)isoxazol-5-il)carbamato de metilo (850 mg, 1,90 mmol, 1,00 equiv) en N,N-dimetilformamida (20 ml), 1-hidroxiciclopropano-1-ácido carboxílico (194 mg, 1,90 mmol, 1,00 equiv), HBTU (1,08 g, 2,85 mmol, 1,50 equiv), DIEA (980 mg, 7,58mmol, 4,00 equiv). La solución resultante se agitó durante la noche a temperatura ambiente. La mezcla de reacción se diluye con 30 ml de EA, se lavó con 3x30 ml de salmuera, se secó sobre sulfato de sodio anhidro y se concentró a vacío. El residuo se aplicó sobre una columna de gel de sílice con diclorometano/metanol (90:10). Las fracciones recogidas se combinaron y se concentraron a vacío. Esto dio lugar a 600 mg (59%) del compuesto del título como un sólido marrón. LCMS (ES, m/z): 533 [M+H]+
Etapa 6. (4-(3'-(3-¡l-5-am¡no¡soxazol)-[1,1 ’-b¡fen¡l]-4-carbon¡l)p¡peraz¡n-1-¡l)(1-h¡drox¡c¡cloprop¡l)metanona [0320] En un matraz de fondo redondo de 100 ml, se colocó terc-butilo (3-(4'-(4-(1-hidroxiciclopropano-1-carbonil)piperazina-1-carbonil)-[1,1’-bifenil]-3-il)isoxazol-5-il)carbamato (600 mg, 1,13 mmol, 1,00 equiv), diclorometano (30 ml). A lo anterior se introdujo el gas de HCl anteriormente. La solución resultante se agitó durante 1 h a temperatura ambiente. La mezcla se concentró y se disolvió en 5ml de metanol. El valor pH de la solución se ajustó a 8 con solución de bicarbonato de sodio saturado. La solución resultante se extrajo con 2x30 ml de diclorometano. Las capas orgánicas se combinaron, se secaron sobre sulfato de sodio anhidro y se concentraron a vacío. El residuo se purificó por PrepHPLC con las siguientes condiciones (Waters I): Columna, Xbridge Prep C18 OBD columna, 5 um, 19*150 mm; fase móvil, Agua (0,05% NH4HCO3) y CH3CN (30% CH3CN hasta el 70% en 9 min); Detector, UV 220 y 254 nm. Esto resultó en 107,4 mg (22%) del compuesto del título como un sólido blanco. LC-MS (ES, m/z): 433 [M+H]+
Método 23.
[E ta p a 2) I Etapa 1
Etapa 4]
Etapa 1.4-(1-met¡l-1H-benzo[d]¡m¡dazol-5-¡l)ác¡do benzo¡co
[0321] En un matraz de fondo redondo de 250 ml purgado y mantenido con una atmósfera inerte de nitrógeno, se colocó una solución de 4-(tetrametil-1,3,2-dioxaborolan-2-il)ácido benzoico (2,35 g, 9,47 mmol, 1,00 equiv) en CH3CN/tolueno (70/12 ml), 5-bromo-1-metil-1H-benzo[d]imidazol (2 g, 9,48 mmol, 1,00 equiv), Pd(PPh3)4 (548 mg, 0,47 mmol, 0,05 equiv), carbonil sódico (0,4 M, 50 ml, 2,00 equiv). La solución resultante se agitó durante 18 h a 90°C. Después de enfriarse a temperatura ambiente, la mezcla de reacción se vertió en 50 ml de agua. La mezcla se lavó con 2x100 ml de acetato de etilo y se recogió la capa acuosa. El valor pH de la solución se ajustó a 4 con ácido clorhídrico (1 N). Los sólidos se recogieron por filtración y se secaron bajo vacío. Esto dio lugar a 2 g (84%) del compuesto del título como un sólido blanco, que se secó al vacío. LC-MS (ES, m/z): 253 [M+H]+
Etapa 2. terc-butilo (R)-2-metil-4-(4-(1-metil-1H-benzo[d]imidazol-5-il)benzoil)piperazina-1-carboxilato
[0322] En un matraz de fondo redondo de 50 ml, se colocó una solución de 4-(1-metil-1H-benzo[d]imidazol-5-il)ácido benzoico (600 mg, 2,38 mmol, 1,00 equiv) en N,N-dimetilformamida (15 ml), terc-butilo (2R)-2-metilpiperazina-1-carboxilato (476 mg, 2,38 mmol, 1,00 equiv), HBTU (1,35 g, 3,56 mmol, 1,50 equiv), DIEA (1,22 g, 9,44 mmol, 4,00 equiv). La solución resultante se agitó durante la noche a temperatura ambiente. La mezcla de reacción se vertió en 100 ml de agua, se extrajo con 3x100 ml de diclorometano. Las capas orgánicas se combinaron, se secaron sobre sulfato de sodio anhidro y se concentró bajo vacío. El residuo se aplicó sobre una columna de gel de sílice con éter/acetato de etilo de petróleo (1/15). Esto dio lugar a 650 mg (63%) del compuesto del título como un aceite rojo. LC-MS (ES, m/z): 435 [M+H]+
Etapa 3. (fí)-(4-(1-metil-1H-benzo[d]imidazol-5-il)fenil)metanona (3-metilpiperazin-1-il)
[0323] En un matraz de fondo redondo de 50 ml, se colocó una solución de terc-butilo (R)-2-metil-4-(4-(1-metil-1H-benzo[d]imidazol-5-il)benzoil)piperazina-1-carboxilato (650 mg, 1,50 mmol, 1,00 equiv) en diclorometano (20 ml). Al cloruro de abovehidrogen (gas) se introdujo en. La solución resultante se agitó durante 0,5 h a temperatura ambiente. La mezcla resultante se concentró a vacío. El residuo se trituró con 2x100 ml de éter. Los sólidos se collectedby filtración y se secaron bajo vacío. Esto dio lugar a 500 mg (90%) del compuesto del título como un sólido rojo. LC-MS (ES, m/z): 335 [M+H]+
Etapa 4. (fí)-(4-(1-hidroxiciclopropano-1-carbonil)-3-metilpiperazin-1-il)(4-(1-metil-1H-benzo[d]imidazol-5-il)fenil)metanona
[0324] En un matraz de fondo redondo de 50 ml, se colocó una solución de (R)-(4-(1-metil-1H-benzo[d]imidazol-5-il)fenil)(3-metilpiperazin-1-il)metanona (500 mg, 1,35 mmol, 1,00 equiv) en N,N-dimetilformamida (15 ml), 1-hidroxiciclopropano-1-ácido carboxílico (137 mg, 1,34 mmol, 1,00 equiv), HBTU (766 mg, 2,02 mmol, 1,50 equiv), DIE (695 mg, 5,38 mmol, 4,00 equiv). La solución resultante se agitó durante la noche a temperatura ambiente. La mezcla de reacción se vertió en 100 ml de agua, se extrajo con 3x50 ml de diclorometano. Las capas orgánicas se combinaron, se secaron sobre sulfato de sodio anhidro y se concentraron bajo vacío. El residuo se purificó por prep-HPLC con las siguientes condiciones (IntelFlash-1): Columna, C18 gel de sílice; fase móvil, C^CN/agua con 0,05% de NH4HCO3 = 20% aumentando a CHaCN/agua con 0,05% de NH4HCO3 = 60% dentro de 30 min; Detector, UV 254 y 220 nm. Esto resultó en 200,3 mg (36%) del compuesto del título como un sólido blanco. LC-MS (ES, m /z): 419 [M+H]+
Método 24.
Etapa 1.7-bencilo 4-(terc-butil) 4,7-diazaespiro[2,5]octano-4,7-dicarboxilato
[0325] En un matraz de fondo redondo de 100 ml, se colocó una solución de terc-butilo 4, 7-diaza-espiro[2,5]octano-4-carboxilato de metilo (3 g, 14,13 mmol, 1,00 equiv) y TEA (4,25 g, 42,00 mmol, 2,97 equiv) en diclorometano (30 ml). Esto se siguió por la adición de CbzCl (2,88 g, 16,88 mmol, 1,19 equiv) gota a gota con agitación a 0°C. La solución resultante se agita durante 3 h a 25°C. La mezcla de reacción se diluyó con 50 ml de agua, se extrajo con 3x50 ml de diclorometano. Las capas orgánicas se combinaron, se lavaron con 2x100 ml de solución de carbonil de sodio (2M), se secaron sobre Na2SO4, y se concentraron bajo vacío. Esto dio lugar a 4 g (82%) del compuesto del título como aceite amarillo. LC-MS (ES, m/z) 347 [M+H]+
Etapa 2. bencilo 4,7-diaza-espiro[2,5]octano-7-clorhidrato de carboxilato
[0326] En un matraz de fondo redondo de 100 ml, se colocó una solución de 7-bencilo 4-terc-butilo 4, 7-diazaespiro[2,5]octano-4,7-dicarboxilato (4 g, 11,55 mmol, 1,00 equiv) en diclorometano/tetrahidrofurano (20/20 ml). A la solución anterior, se introdujo cloruro de hidrógeno (gas). La solución resultante se agitó durante 3 h a 25°C. Los sólidos fueron recogidos por filtración. Esto dio lugar a 3 g (bruto) del compuesto del título como un aceite amarillo. LC-MS (ES, m /z) 247 [M+H]+
Etapa 3. bencilo 4-(4-(6-fluorobenzo[d]oxazol-2-il)benzoil)-4,7-diazaespiro[2,5]octano-7-carboxilato [0327] En un matraz de fondo redondo de 100 ml, se colocó HATU (1,55 g, 4,08 mmol, 1,00 equiv), 4-(6-fluoro-1,3-benzoxazol-2-il)ácido benzoico (951 mg, 3,70 mmol, 0,91 equiv), bencilo 4,7-diazaespiro[2,5]octano-7-hidrógeno de carboxilato sal de cloruro (1 g, 4,06 mmol, 1,00 equiv), DiEA (955 mg, 7,39 mmol, 1,82 equiv) y N,N-dimetilformamida (30 ml). La solución resultante se agitó durante 18 h a 25°C. Después, la mezcla se diluyó con 50 ml de EA, se lavó con 2x50 ml de agua, se secó sobre Na2SO4 y se concentró a vacío. El residuo se aplicó sobre una columna de gel de sílice con etilo acetato/petróleo éter (10%-90%). Esto dio lugar a 1,2 g (bruto) del compuesto del título como un aceite amarillo. LC-MS (ES, m/z): 486 [M+H]+
Etapa 4. (4-(6-fluorobenzo[d]oxazol-2-il)fenil)(4,7-diazaespiro[2,5]octan-4-il)metanona
[0328] En un matraz de fondo redondo de 100 ml, se colocó bencilo 4-[(4-(6-fluoro-1,3-benzoxazol-2-il)fenil]carbonil]-4,7-diazaespiro[2,5]octano-7-carboxilato (Intermedio 2, 1,2 g, 2,47 mmol, 1,00 equiv), paladio sobre carbón activo (1,2 g) y metanol (30 ml). A continuación, el matraz se evacuó y se rellenó con hidrógeno durante tres veces. La solución resultante se agitó durante 3 h a 25°C. Los sólidos se separaron por filtración. El filtrado se concentró bajo vacío. Esto resultó en 700 mg (en bruto) del compuesto del título como un sólido de color amarillo claro. LC-MS (ES, m/z): 352 [M+H]+
Etapa 5. (4-(4-(6-fluorobenzo[d]oxazol-2-¡l)benzoil)-4,7-d¡azaesp¡ro[2,5]octan-7-¡l)(1-hidroxiciclopropil)metanona
[0329] En un matraz de fondo redondo de 100 ml, se colocó HATU (658 mg, 1,73 mmol, 1,00 equiv), 1-hidroxiciclopropano-1-ácido carboxílico (160 mg, 1,57 mmol, 0,91 equiv), 2-[4-[(4,7-diazaespiro[2,5]octan-4-il]carbonil)fenil]-6-fluoro-1,3-benzoxazol (608 mg, 1,73 mmol, 1,00 equiv), DIeA (406 mg, 3,14 mmol, 1,82 equiv) y N,N-dimetilformamida (15 ml). La solución resultante se agitó durante 18 h a 25°C. La mezcla resultante se concentró bajo vacío. El residuo se aplicó sobre una columna de gel de sílice con etilo acetato/petróleo éter (10%-90%). El producto en bruto se purificó por Prep-HPLC con las siguientes condiciones (Waters I): Columna, Xbridge Prep C18 OBD columna, 5 um, 19*150 mm; fase móvil, Agua (0,05% NH4HCO3) y CH3CN (10% CH3CN hasta el 40% en 9 min); Detector, UV 220 y 254 nm. Esto resultó en 171,6 mg (23%) del compuesto del título como un sólido blanco. LC-MS (ES, m/z): 436 [M+H]+
Método 25.
Etapa 1. bencilo 4-(3'-(5-((terc-butox¡carbon¡l)am¡no)-1H-pirazol-3-¡l)-[1,1’-b¡fen¡l]-4-carbon¡l)p¡peraz¡na-1-carbox¡lato
[0330] En un matraz de fondo redondo de 100 ml purgado y mantenido con una atmósfera inerte de nitrógeno, se colocó una solución de bencilo 4-[(4-(tetrametil-1,3,2-dioxaborolan-2-il)fenil]carbonil]piperazina-1-carboxilato (Intermedio 5, 710 mg, 1,58 mmol, 1,00 equiv) en 1,4-dioxano (20 ml), terc-butilo N-[3-(3-bromofenil)-1 H-pirazol-5-il]carbamato (533,2 mg, 1,58 mmol, 1,00 equiv), Pd(dppf)Cl2 (115,5 mg, 0,16 mmol, 0,10 equiv), carbonil sódico (2 M, 5 ml). La mezcla resultante se agitó durante la noche a 85°C. Después de enfriarse a temperatura ambiente, la mezcla de reacción se diluyó con 30 ml de agua, se extrajo con 2x100 ml de acetato de etilo. Las capas orgánicas se combinaron, se secaron sobre sulfato de sodrio anhidro y se concentró a vacío. El residuo se aplicó sobre una columna de gel de sílice con etilo acetato/petróleo éter (4/1). Esto dio lugar a 300 mg (33%) del compuesto del título como un sólido amarillo. LC-MS (ES, m/z): 582 [M+H]+
Etapa 2. terc-butilo (3-(4'-(piperazina-1-carbonil)-[1,1 ’-bifenil]-3-¡l)-1 H-pirazol-5-il)carbamato
[0331] En un matraz de fondo redondo de 50 ml, se colocó una solución de 4-(3'-(5-((terc-butoxicarbonil)amino)-1Hpirazol-3-il)-[1,1’-bifenil]-4-carbonil)piperazina-1-carboxilato (670 mg, 1,15 mmol, 1,00 equiv) en metanol (20 ml). Esto fue seguido por la adición de carbono de paladio (670 mg). A lo anterior se introdujo el hidrógeno. La solución resultante se agitó durante 5 h a temperatura ambiente. Los sólidos se separaron por filtración. El filtrado se concentró a vacío. Esto resultó en 515,7 mg (100%) del compuesto del título como un sólido naranja. LC-MS (ES, m/z): 448 [M+H]+
Etapa 3. terc-butilo (3-(4'-(4-(1-h¡drox¡c¡clopropano-1-carbon¡l)p¡peraz¡na-1-carbon¡l)-[1,1’-b¡fen¡l]-3-¡l)-1 Hp¡razol-5-¡l)carbamato
[0332] En un matraz de fondo redondo de 250 ml, se colocó una solución de terc-butilo (3-(4'-(piperazina-1-carbonil)-[1,1’-bifenil]-3-il)-1H-pirazol-5-il)carbamato de metilo (515,7 mg, 1,15 mmol, 1,00 equiv) en N,N-dimetilformamida (50 ml), 1-hidroxiciclopropano-1-ácido carboxílico (117 mg, 1,15 mmol, 1,00 equiv), HBTU (654 mg, 1,72 mmol, 1,50 equiv), DIEA (445,5mg, 3,45 mmol, 3,00 equiv). La solución resultante se agitó durante la noche a temperatura ambiente. A continuación, la mezcla de reacción se diluyó con 50 ml de agua, se extrajo con 2x150 ml de diclorometano. Las capas orgánicas se combinaron, se secaron sobre sulfato de sodio anhidro y se concentraron a vacío. El residuo se aplicó en una columna de con etilo de etilo/petróleo éter gel de sílice (2/1). Esto dio lugar a 400 mg (65%) del compuesto del título como un sólido marrón. LC-MS (ES, m/z): 532 [M+H]+
Etapa 4. (4-(3'-(5-am¡no-1H-p¡razol-3-¡l)-[1,1’-b¡fen¡l]-4-carbon¡l)p¡peraz¡n-1-¡l)(1-h¡drox¡c¡cloprop¡l)metanona [0333] En un matraz de fondo redondo de 100 ml, se colocó una solución de terc-butilo (3-(4'-(4-(1-hidroxiciclopropano-1-carbonil)piperazina-1-carbonil)-[1,1'-bifenil]-3-il)-1H-pirazol-5-il)carbamato de metilo (400 mg, 0,75 mmol, 1,00 equiv) en diclorometano (30 ml). A lo anterior se introdujo el gas de HCl. La solución resultante se agitó durante 1 h en la sala de sólidos temperatura ambiente.El se recogieron por filtración y se disolvió en 10 ml de agua. El valor de pH se ajustó a 6~7 con solución saturada de bicarbonato de sodio. Los sólidos se recogieron por filtración. El residuo se purificó por Flash-Prep-HPLC con las siguientes condiciones (IntelFlash-1): Columna, C18 gel de sílice; fase móvil, C^CN/agua con 0,1% NH4HCO3 = 1/5 aumentando a CH3CN/agua con 0,1% NH4HCO3 = 3/2 dentro de 20 min; Detector, UV 254 y 220 nm. Esto resultó en 102,9mg (32%) del compuesto del título como un sólido blanco. LC-MS (ES, m/z): 432 [M+H]+
Método 26.
Etapa 1. N-(4-bromofen¡l)-3-met¡l-4,5,6,7-tetrah¡dro-1 y 2H-¡ndazol
[0334] En un matraz de fondo redondo de 250 ml (1 atm) purgado y mantenido con una atmósfera inerte de nitrógeno, se colocó 2-acetilciclohexan-1-ona (4,08 g, 29,11 mmol, 1,00 equiv), (4-bromofenil) hidrazina (6,5 g, 29,08 mmol, 1,00 equiv), TsOH (500 mg, 2,90 mmol, 0,10 equiv), etano-1,2-diol (100 ml). La solución resultante se agitó durante 2 días a 105°C en un baño de aceite. La mezcla resultante se concentró bajo vacío. El producto en bruto (4 g) se purificó por Flash-Prep-HPLC con las siguientes condiciones (IntelFlash-1): Columna, C18 gel de sílice; fase móvil, solución de NH4HCO3 0,05%, MeCN = 95/5 aumentando a 0,05% de solución NH4HCO3, MeCW = 0/100 dentro de 60 min; Detector, UV 254 nm. Se obtuvo 1,5 g de producto. Esto dio lugar a 1,5 g (18%) de 2-(4-bromofenil)-3-metil-4,5,6,7-tetrahidro-2H-indazol en forma de un sólido de color amarillo claro y 0,8 g (9%) de 1-(4-bromofenil)-3-metil-4,5,6,7-tetrahidro-2H-indazol en forma de sólido de color amarillo fuego. LC-MS (ES, m/z): 292 [M+H]+
Etapa 2. 1-(4-bromofenil)-3-met¡l-1H-¡ndazol
[0335] En un matraz de fondo redondo de 250 ml purgado y mantenido con una atmósfera inerte de nitrógeno, se colocó 1-(4-bromofenil)-3-metil-4,5,6,7-tetrahidro-1H-indazol (3,5 g, 12,02 mmol, 1,00 equiv), benceno (100 ml), DDQ (10,9 g, 48,02 mmol, 3,99 equiv). La solución resultante se agitó durante 22 h a 85°C en un baño de aceite. Después de enfriarse a temperatura ambiente, la mezcla resultante se concentró bajo vacío y se diluyó con 200 ml de EA y se lavó con 1x250 ml de agua y 3x100 ml de salmuera. La fase orgánica se secó sobre sulfato de sodio anhidro y se concentró bajo vacío. El residuo se aplicó sobre una columna de gel de sílice con etilo acetato/petróleo éter (0/100~10/90). Esto resultó en 800 mg (23%) del compuesto del título como un sólido blanco. LC-MS (ES, m/z) 287, 289 [M+H]+
Etapa 3. terc-butilo 4-(4-(3-metil-1H-indazol-1-il)benzoil)piperazina-1-carboxilato
[0336] En un tanque de presión de 250 ml, se colocó 1-(4-bromofenil)-3-metil-1H-indazol (800 mg, 2,79 mmol, 1,00 equiv), terc-butilo piperazina-1-carboxilato (770 mg, 4,13 mmol, 1,48 equiv), Pd(dppf)Cl2 CH2Cl2 (113 mg, 0,14 mmol, 0,05 equiv), tolueno (120 ml), trietilamina (837 mg, 8,27 mmol, 2,97 equiv). Luego se evacuó el reactor y se rellenó con CO durante tres veces. La mezcla resultante se agitó durante 24 h a 130°C bajo presión de CO de 20 atm. Después de enfriarse a temperatura ambiente, la mezcla resultante se concentró bajo vacío. El residuo se aplicó sobre una columna de gel de sílice con etilo acetato/petróleo éter (0/100~25/75). Esto dio lugar a 1,0 g (85%) del título compoundas un sólido de color amarillo claro. LC-MS (ES, m/z) 421 [M+H]+
Etapa 4. (4-(3-met¡l-1H-¡ndazol-1-¡l)fen¡l)(p¡peraz¡n-1-¡l)metanona
[0337] En un matraz de fondo redondo de 250 ml, se colocó terc-butilo 4-(4-(3-metil-1H-indazol-1-il)benzoil)piperazina-1-carboxilato (1 g, 2,38 mmol, 1,00 equiv), diclorometano (100 ml). Entonces se introdujo cloruro de hidrógeno (gas) solución resultante util se agitó durante 2 h a temperatura ambiente. Los sólidos se recogieron por filtración. Esto resultó en 930 mg (en bruto) del compuesto del título como un sólido de color amarillo claro. LC-MS (ES, m/z) 321 [M+H]+
Etapa 5. (4-(1-h¡drox¡c¡clopropano-1-carbon¡l)p¡peraz¡n-1-¡l)(4-(3-met¡l-1H-¡ndazol-1-¡l)fen¡l)metanona [0338] En un matraz de fondo redondo de 100 ml, se colocó 1-hidroxiciclopropano-1-ácido carboxílico (265 mg, 2,60 mmol, 1,00 equiv), HBTU (1,086 g, 2,86 mmol, 1,10 equiv), N,N-dimetilformamida (20 ml), (4-(3-metil-1H-indazol-1-il)fenil)(piperazin-1-il)metanona (930 mg, 2,61 mmol, 1,00 equiv), DIEA (1,68 g, 13,00 mmol, 5,01 equiv). La solución resultante se agitó durante la noche a temperatura ambiente. La solución resultante se diluyó con 100 ml de EA, se lavó con 3x20 ml de agua y 1x20 ml de salmuera. La fase orgánica se secó sobre sulfato de sodio anhidro y concentrado al vacío. El residuo se aplicó sobre una columna de gel de sílice con etilo acetato/petróleo éter (0/100~100/0). Las fracciones recogidas se combinaron y se concentraron bajo vacío. El sólido resultante se agitó en 2x20 ml de MeCN, se recogió por filtración y se secó a presión reducida. Esto dio lugar a 228,5 mg (22%) del titulo compuesto como un sólido de color blanquecino. LC-MS (ES, m/z) 405 [M+H]+
Método 27.
Etapa 1. (S)-(4-(4-(terc-butox¡carbon¡l)-3-met¡lp¡peraz¡na-1-carbon¡l)-3-fluorofen¡l)ác¡do borónico
[0339] En un 250 ml de flash de fondo redondo se colocó una solución de 4-(dihidroxiboranil)-2-ácido fluorobenzoico (1,84 g, 10,00 mmol, 1,00 equiv) en DMF (30 ml). HBTU (15,16 g, 39,97 mmol, 4,00 equiv) seguido por DIEA (1,94 g, 15,01 mmol, 1,50 equiv). La solución resultante se agitó durante 10 min. a ta, a continuación, una solución de terc
butilo (2R)-2-metilpiperazina-1-carboxilato (2 g, 9,99 mmol, 1,00 equiv) en DMF (5 ml) se añadió. La solución resultante se permitió agitar durante la noche. Después, la solución se diluyó con EtOAc (50 ml) y se lavó con salmuera (3 x 50 ml). Se secó la capa orgánica sobre sulfato de sodio, se filtró y se concentró a vacío. El residuo se purificó por elución FCC con diclorometano/metanol (90:10). Esto proporcionó el compuesto del título (3,5 g, 96%) como un sólido marrón. LC-MS (ES, m/z) 367 [M+H]+
Etapa 2. terc-butilo (S)-4-(2-fluoro-4-(1-metil-1H-benzo[d]imidazol-5-il)benzoil)-2-metilpiperazina-1-carboxilato [0340] En un matraz de fondo redondo de 100 ml purgado y mantenido con una atmósfera inerte de nitrógeno, se colocó una solución de (S)-(4-(4-(terc-butoxicarbonil)-3-metilpiperazina-1-carbonil)-3-fluorofenil)ácido borónico (837 mg, 2,29 mmol, 1,00 equiv) en tolueno (20 ml), se 5-bromo-1-metil-1H-1,3-benzodiazol (400 mg, 1,90 mmol, 0,83 equiv), Pd(PPh3)4 (264 mg, 0,23 mmol, 0,10 equiv), carbonil sódico (2 M, 10 ml), etanol (2,8 ml). La mezcla resultante se agitó durante la noche a 95°C. Después de enfriarse a temperatura ambiente, la solución resultante se diluyó con 20 ml de H2O, se extrae con 3x30 ml de acetato de etilo. Las capas orgánicas se combinaron, se secaron sobre sulfato de sodio anhidro y se concentró bajo vacío. El residuo se aplicó sobre una columna de gel de sílice con diclorometano/metanol (90:10). Las fracciones recogidas se combinaron y se concentraron a vacío. Esto dio lugar a 800 mg (77%) del compuesto del título como un sólido marrón. LC-MS (ES, m/z) 453 [M+H]+
Etapa 3. (S)-(2-fluoro-4-(1-metil-1H-benzo[d]imidazol-5-il)fenil)(3-metilpiperazin-1-il)metanona
[0341] En un matraz de fondo redondo de 100 ml, se colocó una solución de terc-butilo (S)-4-(2-fluoro-4-(1-metil-1H-benzo[d]imidazol-5-il)benzoil)-2-metilpiperazina-1-carboxilato (800 mg, 1,77 mmol, 1,00 equiv) en diclorometano (30 ml). A lo anterior se introdujo HCl (gas). La solución resultante se agitó durante 2 h a temperatura ambiente. Los sólidos se recogieron por filtración. Esto dio lugar a 650 mg (95%) del compuesto del título como un sólido marrón. LC-MS (ES, m /z) 353 [M+H]+
Etapa 4. (S)-(4-(2-fluoro-4-(1-metil-1H-benzo[d]imidazol-5-il)benzoil)-2-metilpiperazin-1-il)(1-hidroxiciclopropil)metanona
[0342] En un matraz de fondo redondo de 100 ml, se colocó una solución de (S)-(2-fluoro-4-(1-metil-1H-benzo[d]imidazol-5-il)fenil)(3-metilopiperazin-1-il)metanona (650 mg, 1,67 mmol, 1,00 equiv) en N,N-dimetilformamida (20 ml), 1-hidroxiciclopropano-1-ácido carboxílico (180 mg, 1,76 mmol, 1,05 equiv), HBTU (734 mg, 1,94 mmol, 1,16equiv), DIEA (908 mg, 7,03 mmol, 4,20 equiv). La solución resultante se agitó durante la noche a temperatura ambiente. La mezcla de reacción se diluyó con 30 ml de EA, se lavó con 3x30 ml de agua y 30 ml de salmuera. La fase orgánica se secó sobre sulfato de sodio anhidro y se concentró a vacío. El residuo se aplicó sobre una columna de gel de sílice con diclorometano/metanol (90:10). El producto en bruto se purificó adicionalmente por prep-HPLC con las siguientes condiciones (Waters III): Columna, Xbridge RP18 5 um, 19*150; fase móvil, agua (0,05% NH4HCO3) y MeCN (10% CH3 CN hasta el 70% en 9 min); Detector, UV 220 y 254 nm. Esto dio lugar a 203,1 mg (28%) del compuesto del título como un sólido blanco. LC-MS (ES, m /z) 437 [M+H]+
Método 28.
Etapa 1. terc-butilo (S)-(1-(4-(4-(6-fluorobenzo[d]oxazol-2-il)benzoil)-2-metilpiperazina-1-carbonil)ciclopropil)carbamato
[0343] En un matraz de fondo redondo de 100 ml, se colocó 1-[(terc-butoxi}carbonil) aminociclopropano-1-ácido carboxílico (Intermedio 2, 400 mg, 1,99 mmol, 0,90 equiv), HbTU (830 mg, 2,19 mmol, 1,0 equiv), N,N-dimetilformamida (30 ml), (S)-(4-(6-fluorobenzo[d]oxazol-2-il)fenil)(3-metilpiperazin-1-il)metanona (750 mg, 2,21 mmol, 1,00equiv) y DIEA (514 mg, 3,98 mmol, 1,80 equiv). La solución resultante se agitó durante 18 h a 25°C. La solución resultante se diluyó con 50 ml de EA y se lavó con 2x50 ml de agua. La capa orgánica se secó sobre Na2SO4 y se concentró bajo vacío. Esto dio lugar a 800 mg (en bruto) del compuesto del título como un sólido amarillo. LC-MS (ES, m/z): 523 [M+H]+
Etapa 2. (S)-(4-(1-aminociclopropano-1-carbonil)-3-metilpiperazin-1-il)(4-(6-fluorobenzo[d]oxazol-2-il)fenil)metanona
[0344] En un matraz de fondo redondo de 100 ml, se colocó terc-butilo (S)-(1-(4-(4-(6-fluorobenzo[d]oxazol-2-il)benzoil)-2-metil-piperazin-1-carbonil)ciclopropil)carbamato (800 mg, 1,53 mmol, 1,00 equiv), diclorometano (20 ml), tetrahidrofurano (20 ml). Entonces se burbujeó cloruro de hidrógeno (gas) en la mezcla. La solución resultante se
agitó durante 3 h a 25°C. La mezcla resultante se concentró bajo vacío y se disolvió en 10 ml de agua. El valor pH del solución se ajustó a 8 con solución saturada de carbonil sódico. Los sólidos se recogieron por filtración. El producto crudo se purificó por prep-HPLC con las siguientes condiciones (Waters I): Columna, Xbridge Prep C18 OBDcolumn, 5 um, 19*150 mm; fase móvil, Agua (0,05% NH4HCO3) y CH3CN (7% CH3CN hasta 35% en 10 min); Detector, UV 220 y 254 nm. Esto dio lugar a 163,6 mg (25%) del compuesto del título como un sólido blanco. LC-MS (ES, m/z): 423 [M+H]+
Método 29.
Etapa 1. terc-butilo 4-(4-(3-aminobenzo[d]isoxazol-6-il)benzoil)piperazina-1-carboxilato
[0345] En un matraz de fondo redondo de 250 ml purgado y mantenido con una atmósfera inerte de nitrógeno, se colocó una solución de terc-butilo 4-[(4-(tetrametil-1,3,2-dioxaborolan-2-il)fenil]carbonil]piperazina-1-carboxilato (Intermedio 3, 1,9 g, 4,56 mmol, 1,00 equiv) en dioxano (100 ml), 6-bromo-1,2-benzoxazol-3-amina (1 g, 4,69 mmol, 1,00 equiv), Pd(dppf)Cl2 (344 mg, 0,47 mmol, 0,10 equiv), carbonil sódico (20 ml, 2 M). La solución resultante se agitó durante la nocha a 80°C. Después de enfriarse a temperatura ambiente, la mezcla resultante se diluyó con DCM, se lavó con agua y se concentró a vacío. El residuo se aplicó sobre una columna de gel de sílice con diclorometano/metanol (10/1). Esto resultó en 1,6 g (83%) del compuesto del título como un sólido gris. LC-MS (ES, m/z) 423 [M+H]+
Etapa 2. terc-butilo 4-(4-(3-(ciclopropanocarboxamido)benzo[d]isoxazol-6-il)benzoil)piperazina-1-carboxilato [0346] En un matraz de fondo redondo de 100 ml, se colocó una solución de terc-butilo 4-[(4-(3-amino-1,2-benzoxazol-6-il)fenil]carbonil]piperazina-1-carboxilato (800 mg, 1,89 mmol, 1,00 equiv) en piridina (20 ml), cloruro de ciclopropanocarbonil (199 mg, 1,90 mmol, 1,00 equiv). La solución resultante se agitó durante 2 h a 70°C. Después de enfriarse a temperatura ambiente, la mezcla de reacción se diluyó con EtOAc, se lavó con agua y se concentró a vacío. El residuo se aplicó en una columna de gel de sílice con etilo acetato/petróleo éter (1/1). Esto dio lugar a 535 mg (58%) del compuesto del titulo como un sólido blanco. LC-MS (ES, m/z): 491 [M+H]+
Etapa 3. N-(6-(4-(piperazin-1-carbonil)fenil)benzo[d]isoxazol-3-il)ciclopropanocarboxamida
[0347] En un matraz de fondo redondo de 100 ml, se colocó una solución de terc-butilo 4-[(4-(3-ciclopropanoamido-1,2-benzoxazol-6-il)fenil]carbonil]piperazina-1-carboxilato (535 mg, 1,09 mmol, 1,00 equiv) en diclorometano (30 ml). A lo anterior se introdujo cloruro de hidrógeno (g). La solución resultante se agitó durante 1 h a temperatura ambiente. La mezcla resultante se concentró a vacío. Esto dio lugar a 466 mg (cuantitativo) del compuesto del título como un sólido blanco. LC-MS (ES, m/z): 391 [M+H]+
Etapa 4. N-(6-(4-(4-(1-hidroxiciclopropano-1-carbonil)piperazina-1-carbonil)fenil)benzo[d]isoxazol-3-il)ciclopropanocarboxamida
[0348] En un matraz de fondo redondo de 50 ml, se colocó una solución de 1-hidroxiciclopropano-1-ácido carboxílico (111 mg, 1,09 mmol, 1,00 equiv) en N,N-dimetilformamida (20 ml), HBTU (620 mg, 1,63 mmol, 1,50 equiv), DIEA (563 mg, 4,36mmol, 4,00 equiv). La mezcla anterior se agitó durante 1 h a temperatura ambiente. A esto se añadió N-(6-[4-[(piperazin-1-il}carbonil)fenil]-1,2-benzoxazol-3-il)ciclopropanocarboxamida (466 mg, 1,09 mmol, 1,00 equiv). La resultante mezcla se agitó durante la noche a temperatura ambiente. La mezcla de reacción se diluyó con DCM, se lavó con agua y se concentró bajo vacío. El residuo se aplicó sobre una columna de gel de sílice con diclorometano/metanol (10/1), y se purificó adicionalmente por prep-HPLC con las siguientes condiciones (IntelFlash-1): Columna, C18 gel de sílice; fase móvil, CH3CN/agua con 0,05% de NH4HCO3 = 40% aumentando a CHaCN/agua con 0,05% de NH4HCO3 = 60% dentro de 15 minutos; Detector, UV 254 y 220 nm. Esto dio lugar a
123,9 mg (24%) del compuesto del título como un sólido blanco. LC-MS (ES, m/z): 475 [M+H]+
Método 30.
Etapa 1. terc-butilo 4-(3’-am¡no-[1,1’-b¡fen¡l]-4-carbon¡l)p¡peraz¡na-1-carbox¡lato
[0349] Se añadió a un matraz RB de 100 ml de terc-butilo piperazina-1-carboxilato (1,310 g, 7,03 mmol), 3’-aminobifenil-4-ácido carboxílico (1,5 g, 7,03 mmol) y DIEA (2,457 ml, 14,07 mmol) en DMF (25 ml) seguido de HBTU (3,20 g, 8,44mmol) para dar una suspensión marrón. Esto se agitó a ta durante 8 h. Se añadió agua (50 ml) y la reacción se extrajo dos veces con cloruro de metileno (2 x 100 ml). Las capas orgánicas se combinaron y se lavaron con agua (25 ml) y salmuera (25 ml). Se secó la capa orgánica sobre sulfato de magnesio, se filtró y se concentró a vacío. El residuo bruto se purificó por FCC (0-4% de MeOH/CH2Cl2 ) proporcionando el compuesto del título (1,70 g, 63%) como un sólido amarillo. LC-MS (ES, m/z): 382 [M+H]+
Etapa 2 (RCOCl). terc-but¡lo 4-(3'-(c¡clopentanocarboxam¡do)-[1,1’-b¡fen¡l]-4-carbon¡l)p¡peraz¡na-1-carbox¡lato
[0350] En un vial de centelleo de 20 ml se le añadió terc-butilo 4-(3’-aminobifenil}carbonil)piperazina-1-carboxilato (150 mg, 0,393 mmol), piridina (0,095 ml, 1,180 mmol), y cloruro de ciclopentanocarbonil (0,057 ml, 0,472 mmol) en THF (9 ml) para dar una suspensión de color amarillo claro. Esto se agitó a ta durante 2 horas. La reacción se recogió en 75 ml de cloruro de metileno. La solución orgánica se lavó dos veces con solución diluida de bicarbonato de sodio (acuoso, 35 ml) y una vez con salmuera (15 ml). Después, la capa orgánica se secó sobre sulfato de magnesio, se filtró y se concentró a vacío. El producto bruto se purificó por FCC (EtOAc al 0-60%/hexanos) proporcionando el compuesto del título (116 mg, 62%). LC-MS (ES, m/z): 478 [M+H]+
Etapa 2 (RCO2H). terc-But¡lo 4-(3'-(3,3-d¡fluoroc¡clobutanocarboxam¡do)b¡fen¡lcarbon¡l)p¡peraz¡na-1-carbox¡lato
[0351] En un vial de centelleo de 20 ml se le añadió terc-butilo 4-(3’-aminobifenil}carbonil)piperazina-1-carboxilato (200 mg, 0,524 mmol), ácido 3,3-difluorociclobutanocarboxílico (86 mg, 0,629 mmol) y Base de Hunig (0,275 ml, 1,573 mmol) en DMF (5 ml) seguido de HBTU (239 mg, 0,629 mmol) para dar una suspensión marrón. Esto se agitó a TA durante la noche y después la reacción se diluyó con agua (20 ml). Después, la mezcla de reacción se extrajo con cloruro de metileno (2 x 40 ml). Las capas orgánicas combinadas se lavaron con agua (20 ml) y salmuera (20 ml). La capa orgánica se secó sobre sulfato de magnesio, se filtró y se concentró a vacío. El producto en bruto se purificó por FCC (EtOAc al 0-60%/hexanos) proporcionando el compuesto del título como un vidrio espumoso. LC-MS (ES, m/z): 500 [M+H]+
Etapa 3. N-(4'-(p¡peraz¡na-1-carbon¡l)-[1,1-b¡fen¡l]-3-¡l)c¡clopentanocarboxam¡da 2,2,2-tr¡fluoroacetato
[0352] En un matraz de 100 ml de fondo redondo se añadió terc-butilo 4-(3'-(ciclopentanocarboxamido)bifenil}carbonil)piperazina-1-carboxilato (114 mg, 0,239 mmol) en cloruro de metileno (15 ml) para dar una suspensión amarilla. Se añadió ácido trifluoroacético (0,552 ml, 7,16 mmol) poco a poco con una jeringa. La solución se agitó a ta durante 2,5 horas. La solución se concentró y el producto bruto se trituró con éter y luego se decantó. El sólido resultante se secó en vacío dando el compuesto del título (117 mg, 100%) como un sólido espumoso. LC-MS (ES, m/z): 378 [M+H]+
Etapa 4. N-(4'-(4-(1-h¡drox¡c¡clopropano-1-carbon¡l)p¡peraz¡na-1-carbon¡l)-[1,1’-b¡fen¡l]-3-¡l)c¡clopentanocarboxam¡da
[0353] En un matraz de fondo redondo de 100 ml se añadió N-(4'-(piperazina-1-carbonil)bifenil-3-il)ciclopentanocarboxamida 2,2,2-trifluoroacetato (118 mg, 0,24 mmol), ácido 1-hidroxiciclopropanocarboxílico (19,60 mg, 0,192 mmol) y piridina (0,058 ml, 0,720 mmol) en DMF (5 ml) seguido de HBTU (127 mg, 0,336 mmol) para dar una suspension amarilla. Esto se agitó a TA durante 4,5 horas. se añadió base de Hunig (0,021 ml, 0,12 mmoles) y la agitación se continuó. Después de 18 horas se añadió base de Hunig adicional (0,063 ml, 0,36 mmoles) y la solución de reacción se agitó durante la noche. La reacción se diluyó con agua (20 ml) y se extrajo con cloruro de metileno (2 x 50 ml). Las capas orgánicas se combinaron y se lavaron con agua (10 ml) y salmuera (10 ml). El disolvente se secó sobre sulfato de magnesio, se filtró y se concentró a vacío. El producto crudo se purificó por FCC (0-7% MeOH/CH2Cl2) proporcionando el compuesto del título (35,5 mg, 29%) como un sólido de color blanquecino. LC-MS (ES, m/z): 462 [M+H]+
Método 31.
Etapa 1. ferc-Butilo 4-(4'-bromo-[1,1’-bifenil]-4-carbonil)piperazina-1-carboxilato
[0354] A una suspensión de 4'-bromo-[1,1’-bifenil]-4-ácido carboxílico (1,5 g, 5,4 mmol) en DMF (35 ml) se añadió TEA (1,21 ml, 8,6 mmol), seguido de terc-butilo piperazina-1-carboxilato (1,11 g, 6,0 mmol) y HATU (2,6 g, 6,8 mmol). La mezcla de reacción se agitó a temperatura ambiente durante la noche y después se diluyó con agua y se extrajo con EtOAc. La fase orgánica se lavó con agua, ácido acético al 5%, NaHC03 saturado, salmuera, se secó sobre Na2SO4 y se concentró a presión reducida. El material bruto se cromatografió en una columna de gel de sílice eluyendo con un gradiente de EtOAc en CH2Cl2 para proporcionar 2,0 g (83% de rendimiento) del compuesto del título.
Etapa 2. ferc-Butilo 4-(4'-(1H-p¡razol-4-¡l)-[1,1’-b¡fen¡l]-4-carbon¡l)p¡peraz¡na-1-carboxilato
[0355] Tere-Butilo 4-(4'-bromo-[1,1'-bifenilo]-4-carbonilo)piperazina-1-carboxilato (1,0 g, 2,3 mmol), (1H-pirazol-4-il)ácido borónico (sal como HCl, 0,67 g, 4,5 mmol) y 2M K3 PO4 (ac) (4,5 ml, 9,0 mmol) se mezclaron con 30 ml de DMF en un tubo de microondas. La mezcla resultante se aspiró varias veces y se volvió a llenar con argón antes de añadir Pd(PPh3)4 (0,39 g, 0,3 mmol). La mezcla de reacción se sometió a microondas durante 35 min a 150°C. Después de enfriarse a temparature ambiente, La mezcla de reacción se diluyó con agua y se saturó NaHCO3 y se extrajo con la mezcla de disolventes MeOH/CHCl3. La fase orgánica se secó sobre Na2SO4 y se concentró a presión reducida. El producto bruto se purificó dos veces mediante ISCO (columna de gel de sílice 24 g) eluyendo con un gradiente de 0,7 N NH3/MeOH en CHCl3 para dar 160 mg (-rendimiento del 17%) del producto deseado.
Etapa 3. (4'-(1H-p¡razol-4-¡l)-[1,1’-b¡fen¡l]-4-¡l)(p¡peraz¡n-1-il)metanona, sal de HCl
[0356] fere-Butilo 4-(4'-(1H-pirazol-4-il)-[1,1’-bifenil]-4-carbonil)piperazina-1-carboxilato (160 mg, 0,37 mmol) se disolvió en 18 ml de MeOH anhidro saturado con HCl (gas) a 0°C y se agitó a temperatura ambiente durante ~3h. La solución resultante se concentró a sequedad bajo presión reducida. El residuo se trituró con 2% MeOH en Et2 O seguido de Et2O y pentano para proporcionar 150 mg (cuant. rendimiento) del compuesto del título como la sal de hidrocloruro que se usó en la siguiente etapa sin purificación adicional.
Etapa 4. (4-(4'-(1H-p¡razol-4-¡l)-[1,1’-b¡fen¡l]-4-carbon¡l)p¡peraz¡n-1-¡l)(1-h¡drox¡c¡cloprop¡l)metanona
[0357] A una solución de (4'-(1H-pirazol-4-il)-[1,1’-bifenil]-4-il)(piperazin-1-il)metanona, sa1HCl (150 mg, 0,37mol) y 1-hidroxiciclopropano-1-ácido carboxílico (69 se añadió mg, 0,56 mmol) en 3ml de DMF HBTU (230 mg, 0,6 mmol), seguido de la adición de DIEA (0,33 ml, 1,8 mmol). La solución resultante se agitó durante la noche a temperatura ambiente. La mezcla de reacción se diluyó con agua y NaHCO3 saturado y se extrajo varias veces con con EtOAc/MeOH y la mezcla MeOH/CHCh de disolventes. Las capas orgánicas se combinaron, se lavaron con agua, salmuera, se secaron sobre Na2SO4 y se concentraron bajo presión reducida. El crudo se purificó mediante ISCO dos veces (columna de oro de gel de sílice 24 g) eluyendo con un gradiente de 0,7 N NH3/MeOH en EtOAc y 0,7 N
NH3/MeOH en CHCI3. El producto obtenido después de cromatografía se trituró en Et2O, para dar 110 mg (71% de rendimiento) del compuesto diana puro. LC-MS (ES, m/z): 417 [M+H]+
Método 32.
Etapa 1. terc-Butilo 4-(4-bromo-2,6-difluorobenzoil)piperazina-1-carboxilato
[0358] A una solución de 4-bromo-2,6-difluoro-ácido benzoico (1,00 g, 4,22 mmol), terc-butilo piperazina-1-carboxilato (0,786g, 4,22 mmol), y HBTU (1,925 g, 5,06 mmol) en DMF (10,0 ml) se añadió DIEA (2,95 ml, 16,88 mmol). La reacción se agitó a temperatura ambiente durante la noche. Se añadió bicarbonato sódico saturado (acuoso, 10 ml) seguido por agua (10 ml). Después, la solución de reacción se extrajo varias veces con EtOAc (3 x 20 ml). Los extractos orgánicos se agruparon y se lavaron con agua (2 x 20 ml) y salmuera (20 ml). La capa orgánica se secó sobre sulfato de sodio, se filtró y se concentró a vacío proporcionando el producto bruto como un aceite naranja. El producto bruto se sometió a FCC (Biotage SNAP 25; eluyente: 15%- 25% de EtOAc en hexanos durante 10 CV). Esto proporcionó el compuesto del título (1,44 g, 86%) como un sólido de color blanquecino. LC-MS (ES, m/z): 405 [M+H]+
Etapa 2. terc-butilo 4-(2,6-difluoro-4-(1-metil-1H-indazol-6-il)benzoil)piperazina-1-carboxilato
[0359] terc-Butilo 4-(4-bromo-2,6-difluorobenzoil)piperazina-1-carboxilato (383,2mg, 0,946 mmol), 1 -metil-1 H-indazol-6-ácido ilborónico (166 mg, 0,946 mmol) y fosfato de potasio (1,00 g, 4,73 mmol) se suspendieron en una solución de nitrógeno purgada de dioxano (6,0 ml) y agua (1,2 ml). La mezcla de reacción se purgó adicionalmente con nitrógeno durante 5 minutos. Se añadió paladio tetrakis (109 mg, 0,095 mmol) y la solución de reacción se purgó con nitrógeno durante 5 minutos más. La mezcla se sometió a irradiación de microondas a 130°C durante 30 minutos dando como resultado una solución bifásica amarilla. Se eliminó la capa orgánica (parte superior), se filtró a través de celite y se concentró al vacío para proporcionar el producto en bruto como un polvo de color rojo claro. El producto bruto se sometió a FCC (Biotage SNAp 25; gradiente de eluyente: 0 - 20% de MeOH en EtOAc con 0,5% de trietilamina sobre 15 CV). Esto proporcionó el compuesto del título (327 mg, 76%) como un polvo beige claro. LC-MS (ES, m/z): 421 [M+H]+
Etapa 3. (2,6-difluoro-4-(1-metil-1H-indazol-6-il)fenil)(piperazin-1-il)metanona
[0360] HCl (4 N en 1,4-dioxano) (0,106 ml, 3,51 mmol) se añadió a una solución de terc-butilo 4-(2,6-difluoro-4-(1-metil-1H-indazol-6-il)benzoil)piperazina-1-carboxilato (320,0mg, 0,701 mmol) en dioxano (4,0 ml). La solución de reacción se agitó a temperatura ambiente durante 2 horas dando como resultado la formación de un precipitado blanco. Éter (10 ml) se añadió a la reacción y después el precipitado se recogió por filtración. El precipitado se lavó adicionalmente con éter (10 ml), se recogió y se secó a vacío proporcionando el compuesto del título (275 mg, 100%) como un polvo blanco. lC-MS (ES, m/z): 356 [M+H]+
Etapa 4. (4-(2,6-difluoro-4-(1-metil-1H-indazol-6-il)benzoil)piperazin-1-il)(1-hidroxiciclopropil)metanona [0361] A una solución de (2,6-difluoro-4-(1-metil-1H-indazol-6-il)fenil)(piperazin-1-il)metanona (218,3mg, 0,556 mmol), ácido 1-hidroxiciclopropanocarboxílico (56,7 mg, 0,556 mmol), y HBTU (254 mg, 0,667 mmol) en DMF (4,0 ml) se añadió DIEA (0,388 ml, 2,223 mmol). La reacción se agitó a temperatura ambiente durante la noche. Bicarbonato de sodio saturado (acuoso, 10 ml) seguido por agua (10 ml). La solución de reacción luego se extrajo varias veces con EtOAc (3 x 20 ml). Los extractos orgánicos se combinaron y se lavaron con agua (2 x 20 ml) y salmuera (20 ml). La capa orgánica se secó sobre sulfato de sodio, se filtró y se concentró a vacío proporcionando el producto crudo como un aceite naranja. El producto bruto se sometió a FCC (Biotage SNAP 25; eluyente: 20 - 10% hexanesin EtOAc durante 10 CV). A continuación, el producto se sometió a una purificación adicional a través de FCC (Biotage SNAP 25; eluyente gradiente: 5-15% MeOH en cloruro de metileno). Esto proporcionó el compuesto del título (105,2 mg, 43%) como un polvo blanco. LCMS (ES, m/z): 441 [M+H]+
Método 33.
Etapa 1. terc-butilo 4-(3’-nitrobifenil}carbonil)piperazina-1-carboxilato
[0362] A una solución de terc-butilo 4-(4-bromobenzoil)piperazina-1-carboxilato (1,00 g, 2,71 mmol), ácido 3-nitrofenilborónico (0,452 g, 2,71 mmol) y fosfato de potasio (2,87 g, 13,54 mmol) en dioxano burbujeado por nitrógeno (10,0 ml) y agua burbujeada por nitrógeno (2,0 ml) se añadió paladio tetrakis (0,313 g, 0,271 mmol). La solución de reacción se burbujeó adicionalmente con una corriente de nitrógeno durante 15 minutos. Después, la reacción se realizó durante la noche a 80°C. La reacción se enfrió a temperatura ambiente dando como resultado un precipitado amarillo. El precipitado se recogió por filtración. El precipitado después se lavó con metanol (20 ml) y éter (10 ml). Esto proporcionó el compuesto del título (1,0 g, 92%) como un polvo amarillo claro. LC-MS (ES, m/z): 412 [M+H]+
Etapa 2. terc-Butilo 4-(3’-aminobifenil}carbonil)piperazina-1-carboxilato
[0363] Una mezcla de terc-butilo 4-(3’-nitrobifenil}carbonil)piperazina-1-carboxilato (1,00 g, 2,430 mmol) y paladio hidróxido sobre carbono activado (0,341 g, 2,430 mmol) se suspendió en MeOH (30 ml). La bomba se colocó en un Parr Shaker y se cargó con gas de hidrógeno a 30 psi. La reacción se dejó agitar durante 3 horas. La reacción se ventiló con nitrógeno, se filtró a través de celite y se concentró a vacío proporcionando el compuesto del título (924 mg, 100%) como un sólido marrón claro. LC-MS (ES, m/z): 382 [M+H]+
Etapa 3. terc-Butilo 4-(3'-(ciclobutanosulfonamido)bifenil}carbonil)piperazina-1-carboxilato
[0364] A una solución de terc-butilo 4-(3’-aminobifenil}carbonil)piperazina-1-carboxilato (500,0mg, 1,311 mmol) en piridina anhidra (6,5 ml) se añadió cloruro de ciclobutanosulfonilo (203 mg, 1,311 mmol) a 40°C. La solución de reacción (color rojo) se agitó a 40°C durante 2 días. La solución de reacción se enfrió a temperatura ambiente y se diluyó con agua (10 ml). Después, la solución se extrajo varias veces con EtOAc (3 x 20 ml). Los extractos orgánicos se combinaron se lavaron con ácido cítrico 1M (acuoso, 20 ml), agua (20 ml) y salmuera (20 ml). La capa orgánica se secó sobre sulfato sódico, se filtró y se concentró al vacío. El producto bruto se sometió a FCC (Biotage SNAP 50; eluyente en gradiente: 40 - 50% de EtOAc en hexanos durante 15 CV). Esto proporcionó el compuesto del título (173 mg, 26,3%) como un polvo blanco. LC-MS (ES, m/z): 500 [M+H]+
Etapa 4. N-(4'-(piperazina-1-carbonil)bifenil-3-il)ciclobutanosulfonamida
[0365] Se añadió cloruro de hidrógeno (4,0 N en 1,4-dioxano) (0,438 ml, 1,751 mmol) a una solución de terc-butilo 4-(3'-(ciclobutanosulfonamido)bifenil}carbonil)piperazina-1-carboxilato (175,0mg, 0,350 mmol) en dioxano (2,0 ml). La solución de reacción se agitó a temperatura ambiente durante 3 horas dando como resultado la formación de un precipitado de color blanco apagado. Éter (10 ml) se añadió a la reacción y después el precipitado se recogió por filtración. El precipitado se lavó adicionalmente (10 ml), se recogió y se secó a vacío proporcionando el compuesto del título (153 mg, 100%) como un polvo de color blanquecino. LC-MS (ES, m/z): 400 [M+H]+
Etapa 5. N-(4'-(4-(1-hidroxiciclopropanocarbonil}piperazina-1-carbonil)bifenil-3-il)ciclobutanosulfonamida [0366] A una solución de N-(4'-(piperazina-1-carbonil)bifenil-3-il)ciclobutanosulfonamida (164,5mg, 0,377 mmol), ácido 1-hidroxiciclopropanocarboxílico (38,5 mg, 0,377 mmol), y HBTU (172 mg, se añadió 0,453 mmol) en DMF (2,0 ml) DIEA (0,264 ml, 1,509 mmol). La reacción se agitó a temperatura ambiente durante la noche. Se añadió bicarbonato de sodio saturado (acuoso, 10 ml) seguido por agua (10 ml). La solución de reacción fue entonces extraida varias veces con EtOAc (3 x 20 ml). Los extractos orgánicos se combinaron y se lavaron con agua (2 x 20 ml) y salmuera (20 ml). La capa orgánica se secó sobre sulfato de sodio, se filtró y se concentró a vacío proporcionando el producto crudo como un aceite naranja. El producto bruto se sometió a FCC (Biotage SNAP 25; eluyente: 100% EtOAc durante 10 CV) seguido por una purificación adicional FCC (Biotage SNAP 25; eluyente en gradiente: 0 - 5% de MeOH en cloruro de metileno). Esto proporcionó el compuesto del título (55 mg, 30,3%) como un sólido transparente vítreo. LC-MS (ES, m/z): 484 [M+H]+
Método
Etapa 1. ferc-Butilo 4-(3'-(ciclobutilmetilosulfonamido)-[1,1 -bifenil]-4-carbonil)piperazina-1-carboxilato [0367] A una solución enfriada con hielo de terc-butilo 4-(3’-amino-(1,1’-bifenil]-4-carbonil)piperazina-1-carboxilato (300 mg, 0,79 mmol) en piridina (4 ml) cloruro de ciclobutilmetanosulfonil se añadió gota a gota (200 mg, 1,2 mmol). La mezcla resultante se dejó calentar hasta temperatura ambiente durante 4 h y después se concentró y se mantuvo en una línea de alto vacío durante la noche. El residuo se disolvió en EtOAc, se lavó con agua, ácido acético al 5%, NaHCO3 saturado, salmuera, se secó sobre Na2SO4 y se concentró bajo presión reducida. El material bruto se cromatografió en una columna de gel de sílice eluyendo con gradiente de EtOAc en CH2Cl2 para obtener 295 mg (73% de rendimiento) del compuesto del título.
Etapa 2 (HCl). 1-ciclobutil-N-(4'-(piperazina-1-carbonil)-[1,1’-bifenil]-3-il)metanosulfonamida cloruro de hidrógeno
[0368] terc-Butilo 4-(3'-(ciclobutilmetilosulfonamido)-[1,1’-bifenil]-4-carbonil)piperazina-1-carboxilato (295 mg, 0,57 mmol) se disolvió en 18 ml de MeOH anhidro saturado con HCl (gas) y se agitó a temperatura ambiente durante ~ 3h. La solución resultante se concentró a sequedad bajo presión reducida. El residuo se trituró con 2% de MeOH en Et2O seguido de trituración con Et2 O y se secó para proporcionar 200 mg (rendimiento 78%) del compuesto del título como la sal de hidrocloruro que se usó para la siguiente etapa sin purificación adicional.
Etapa 2 (TFA). W-(4'-(piperazina-1-carbonil)-[1,1 ’-bifenil]-3-il)tetrahidro-2H-piran-4-sulfonamida trifluoroacetato
[0369] A una solución de ferc-butilo 4-(3'-(tetrahidro-2H-piran-4-sulfonamido)-[1,1’-bifenil]-4-carbonil)-piperazina-1-carboxilato (70 mg, 0,13 mmol) en DCM (3 ml) se añadió TFA (0,5 ml). La mezcla se agitó a la temperatura ambiente durante 2 horas. Después de la eliminación de los disolventes a presión reducida, se utilizó el compuesto del título
bruto (69 mg, 100%) directamente en la siguiente etapa sin purificación adicional.
Etapa 3. 1 -ciclobutil-N-(4'-(4-(1 -hidroxiciclopropanocarbonil}piperazina-1 -carbonil)-[1,1 ’-bifenil]-3-il)metanosulfonamida
[0370] A una solución de 1-ciclobutil-N-(4'-(piperazina-1-carbonil)-[1,1’-bifenil]-3-il)metanosulfonamida cloruro de hidrógeno (295 mg, 0,45 mol) y 1-hidroxiciclopropano-1-ácido carboxílico (77 mg, 0,76 mmol) en 3ml de DMF se añadió HBTU (300 mg, 0,81 mmol) seguido de una adición de DIEA (0,42 ml, 2,4 mmol). La solución resultante se agitó a temperatura ambiente durante la noche. La mezcla de reacción se diluyó con agua y satu. NaHCO3 y se extrajo varias veces con mezcla de disolventes CH2Cl2 y MeOH/CHCh. Las capas orgánicas se combinaron, se lavaron con agua, salmuera, se secaron sobre Na2SO4 y se concentraron bajo presión reducida. El material bruto se purificó dos veces mediante ISCO (columna de oro de gel de sílice 40 g) eluyendo con un gradiente de MeOH en CH2Cl2 y después se trituró en 2-3% de MeOH en Et2 O proporcionan 129 mg (58% de rendimiento) del compuesto del título. LC-MS (ES, m/z): 498 [M+H]+
Etapa 1. terc-butilo (1-(4-(2-fluoro-4-(2-metil-1H-indol-1-il)benzoil)piperazina-1-carbonil)ciclopropil)carbamato [0371] En un matraz de fondo redondo de 100 ml se colocó 1-[3-fluoro-4-[(piperazin-1-il}carbonil)fenil]-2-metil-1H-indol (Intermedio 4, 600 mg, 1,60 mmol, 1,00 equiv), 1-[((terc-butoxi}carbonil)amino]ciclopropano-1-ácido carboxílico (322 mg, 1,60 mmol, 1,00 equiv), N,N-dimetilformamida (40 ml), HBTU (729 mg, 1,92 mmol, 1,20equiv), DIEA (828 mg, 6,41 mmol, 3,99 equiv). La solución resultante se agitó durante la noche a temperatura ambiente. La mezcla de reacción se diluyó con 50 ml de EA, se lavó con 3x50 ml de agua y 50 ml de salmuera. La fase orgánica se concentró a vacío. El residuo se aplicó sobre una columna de gel de sílice con etilo acetato/petróleo éter (70:30). Esto dio lugar a 300 mg (36%) del compuesto del título como un sólido amarillo. LC-MS (ES, m/z): 521 [M+H]+ Etapa 2. (4-(1-aminociclopropano-1-carbonil)piperazin-1-il)(2-fluoro-4-(2-metil-1H-indol-1-il)fenil)metanona [0372] En un matraz de fondo redondo de 100 ml, se colocó terc-butilo N-[1-[(4-[(2-fluoro-4-(2-metil-1H-indol-1-il)fenil]carbonil]piperazin-1-il}carbonil)ciclopropil]carbamato (300 mg, 0,58 mmol, 1,00 equiv), diclorometano (20 ml), ácido trifluoroacético (5 ml). La solución resultante se agitó durante la noche a temperatura ambiente. La mezcla resultante se concentró bajo vacío. El residuo se purificó por prep-HPLC con las siguientes condiciones (Waters I): Columna, SunFire Prep C18, 5 um, 19*100 mm; fase móvil, Agua (0,05% NH4HCO3) y CH3CN (65% CH3CN hasta el 85% en 7min); Detector, UV 220 y 254 nm. Esto dio lugar a 73,3 mg (30%) del compuesto del título como un sólido blanco. LC-MS (ES, m/z): 421 [M+H]+
Método 36.
Etapa 1. terc-butilo 4-(6-hidroxi-naftalen-2-il)-3,6-dihidropiridin-1(2H)-carboxilato
[0373] En un 250 ml de flash de fondo redondo se colocó 6-bromonaftalen-2-ol (2 g, 8,97 mmol, 1,00 equiv), tercbutil 4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-3,6-dihidropiridin-1(2H)-carboxilato de (2,7 g, 8,70 mmol, 1,00 equiv), carbonil de potasio (3,6 g, 26,05 mmol, 3,00 equiv), y Pd(dppf)Cl2 (100 mg, 0,14 mmol, 0,01 equiv) en 1,4-dioxano (30 ml) y agua (10 ml). La solución resultante se agitó durante la noche a 110°C en un baño de aceite. La mezcla de reacción se enfrió, se diluyó con EtOAc (120 ml) y se lavó con salmuera (2 x 100 ml). La capa orgánica se secó sobre sulfato sódico, se filtró y se concentró al vacío. El producto bruto se purificó por cromatografía en gel de sílice eluyendo con diclorometano/metanol (50: 1). Esto dio lugar a 1,9 g (65%) del compuesto del título como un sólido amarillo. LC-MS (ES, m/z): 326 [M+H]+
Etapa 2. terc-butilo 4-(6-hidroxi-naftalen-2-il)piperidina-1-carboxilato
[0374] En un matraz de fondo redondo de 250 ml se colocó terc-butilo 4-(6-hidroxi-naftalen-2-il)-3,6-dihidropiridin-1(2H)-carboxilato (1,9 g, 5,84 mmol, 1,00 equiv), etanol (50 ml) y paladio al 10% sobre carbono (0,5 g). Esta suspensión fue cargada en gas hidrógeno. La solución resultante se agitó durante 2 horas a temperatura ambiente, Los sólidos se filtraron y la solución se concentró a vacío proporcionando el compuesto del título (1,9 g, 99%) como un sólido amarillo claro. LC-MS (ES, m/z): 328 [M+H]+
Etapa 3. terc-butilo 4-(6-(((trifluorometil)sulfonil)oxi)naftalen-2-il)piperidina-1-carboxilato
[0375] En un matraz de fondo redondo de 100 ml se colocó terc-butilo 4-(6-hidroxi-naftalen-2-il)piperidina-1-carboxilato (1,9 g, 5,79 mmol, 1,00 equiv), diclorometano (20 ml), 2,6-lutidina (3,4 ml, 3,00 equiv) y anhídrido tríflico (1,5 ml, 1,50 equiv). La solución resultante se agitó a -40°C durante 10 minutos y después se calentó lentamente a ta durante 2 horas. La reacción se inactivó mediante la adición de agua (100 ml). Después, la capa orgánica se lavó con salmuera (2 x 100 ml) y ácido clorhídrico al 5% (2 x 50 ml). La capa orgánica se secó sobre sulfato de sodio, se filtró y se concentró in vacuo. El producto en bruto se purificó por cromatografía en gel de sílice eluyendo con EtOAc/petróleo éter (1: 5). Esto resultó en 2,1 g (79%) del compuesto del título como un sólido blanco. LC-MS (ES, m/z): 461 [M+H]+
Etapa 4. terc-butilo 4-(6-cianonaphthalen-2-il)piperidina-1-carboxilato
[0376] En un vial de 30 ml se colocó terc-butilo 4-(6-(((trifluorometil)sulfonil)oxi)naftalen-2-il)piperidina-1-carboxilato (1,5 g, 3,26 mmol, 1,00 equiv), cianuro de zinc (840 mg, 7,15 mmol, 2,20 equiv), y Pd(dppf)Cl2 (100 mg, 0,14 mmol, 0,04 equiv) en DMF (10 ml). La solución resultante se sometió a irradiación de microondas a 160°C durante 15 minutos. La reacción se enfrió, se diluyó con 100 ml de EtOAc y se lavó con agua (2 x 100 ml) y salmuera (2 x 50 ml). La capa orgánica se secó sobre sulfato sódico, se filtró y se concentró a vacío. El producto bruto se purificó por cromatografía en gel de sílice eluyendo con EtOAc/petróleo éter (1:10). Esto dio lugar a 1,0 g (91%) del compuesto del título como awhite sólido. LC-Ms (ES, m/z): 337 [M+H]+
Etapa 5. 6-(piperidin-4-il)-2-hidrocloruro de naftonitrilo
[0377] En un matraz de fondo redondo de 100 ml se colocó terc-butilo 4-(6-cianonaftalen-2-il)piperidina-1-carboxilato (1,0 g, 2,97 mmol, 1,00 equiv) en diclorometano (20 ml). HCl (g) se hizo burbujear en la solución de reacción y se agitó durante 30 minutos a temperatura ambiente resultando en un precipitado. Se recogió el sólido y se secó a vacío proporcionando el compuesto del título (0,7 g, 100%) como un sólido blanco. LC-MS (ES, m/z): 237 [M+H]+
Etapa 6. terc-butilo 4-(4-(6-cianonaftalen-2-il)piperidina-1-carbonil)piperazina-1-carboxilato
[0378] En un matraz de 100 ml de fondo redondo se colocó 6-(piperidin-4-il)-2-naftonitrilo, trifosgeno (1,0 g, 3,37 mmol, 1,10 equiv), Et3N (1,8 ml, 4,80 equiv) en diclorometano (20 ml). La reacción se agitó durante 2 horas y luego piridina (0,35 ml, 1,50 equiv) y terc-butilo piperazina-1-carboxilato (700 mg, 3,76 mmol, 1,20 equiv) se añadieron. La solución resultante se agitó durante la noche a ta la mezcla de reacción se lavó a continuación con agua (2 x 100 ml) y salmuera (2 x 50 ml). La capa orgánica se secó sobre sulfato de sodio, se filtró y se concentró a vacío proporcionando el compuesto del titulo (0,8 g, 60%) como un sólido amarillo. LC-MS (ES, m/z): 449 [M+H]+
Paso 7.6-(1-(piperazina-1-carbonil)piperidin-4-il)-2-hidrocloruro de naftonitrilo
[0379] En un matraz de fondo redondo de 100 ml se colocó terc-butilo 4-(4-(6-cianonaftalen-2-il)piperidina-1-carbonil)piperazina-1-carboxilato (800 mg, 1,78 mmol, 1,00 equiv) en diclorometano (15 ml). HCl (g) se hizo burbujear en la solución de reacción y se agitó durante 2 horas a temperatura ambiente la solución de reacción se concentró a vacío proporcionando el compuesto del título (0,6 g, 97%) como un sólido blanco. LC-MS (ES, m/z): 349 [M+H]+
Paso 8.6-(1-(4-(1-hidroxiciclopropano-1-carbonil)piperazina-1-carbonil)piperidin-4-il)-2-naftonitrilo
[0380] En un matraz de fondo redondo de 100 ml se colocó 1-hidroxiciclopropano-1-ácido carboxílico (180 mg, 1,76 mmol, 1,00 equiv), HBTU (900 mg, 2,37 mmol, 2,30 equiv), y 6-(1-(piperazina-1-carbonil)piperidin-4-il)-2- hidrocloruro de naftonitrilo (600 mg, 1,72 mmol, 1,00 equiv) en dMf (15 ml). Se añadió DIEA (0,8 ml, 5,00 equiv) y la solución resultante se agitó durante la noche a ta La solución de reacción se diluyó con 100 ml de EtOAc y se lavó con agua (2 x 100 ml) y salmuera (2 x 50 ml). Se secó la capa orgánica sobre sulfato de sodio, se filtró y se concentró in vacuo. El producto en bruto se purificó por cromatografía en gel de sílice eluyendo con diclorometano/metanol (20: 1) y luego se sometió a Prep-HPLC con las siguientes condiciones (Waters I): columna, la columna Xbridge Prep C18 OBD, 5 um, 19*150 mm; fase móvil, Agua (0,05% NH4HCO3) y CH3CN (33% CH3CN hasta el 38% en 12 min). Este resultó en 106,9 mg (14%) del compuesto del título como un sólido blanco. LC-MS (ES, m/z): 433 [M+H]+
Intermedios
[0381]
terc-Butilo 4-(4-(2-oxo-1,2-dihidroquinolin-3-il)benzoil)piperazina-1-carboxilato
[0382] Se añadió tetraquis(trifenilfosfina)paladio(0) (0,078 g, 0,068 mmol) a una mezcla de terc-butilo 4-(4-bromobenzoil)piperazina-1-carboxilato (0,250 g, 0,677 mmol), 2-fluoroquinolin-3-ácido ilborónico (0,129 g, 0,677 mmol), y carbonil de sodio (0,287 g, 2,71 mmol) en dioxano (5,0 ml) y agua (1,0 ml). La mezcla se agitó en el microondas a 60°C durante 1,5 h. La mezcla de reacción se filtró y se concentró para proporcionar un aceite de color amarillo. Este material era cromatografía en columna purificada via sobre gel de sílice (columna Biotage de 25 g, gradiente de elución con 50-100% de acetato de etilo-hexano) para proporcionar terc-butilo 4-(4-(2-oxo-1,2-dihidroquinolin-3-il)benzoil)piperazina-1-carboxilato (0,228 g, 0,526 mmol, 78% de rendimiento) como un sólido
blanco. MS (ESI, ión pos) m/z: 434 (M 1).
Cloruro de 5-bromopicolinoil
[0383] Se añadió cloruro de tionilo (10 ml, 137 mmol) a ácido 5-bromopicolínico (5,00 g, 24,75 mmol). Se añadió una gota de DMF, y la mezcla se calentó a 80°C durante 2 h. El exceso de cloruro de tionilo se eliminó para proporcionar cloruro de 5-bromopicolinoil (5,413 g, 24,55 mmol, 99% de rendimiento) como un sólido amarillo pálido. Una parte alícuota se inactivó con metanol toafford metil 5-bromopicolinate. MS (ESI, ión pos) m/z: 216, 218 (M 1).
5-bromo-1 H-indol-2-carbonitril
Etapa 1.5-bromo-1H-indol-2-carboxamida
[0384] Se añadió 5-bromo-1H-indol-2-ácido carboxílico (0,75 g, 3,12 mmol) a diclorometano (10 ml) para dar una suspensión. se añadió cloruro de tionilo (0,616 ml, 8,44 mmol) poco a poco con una jeringa. Se añadió una gota de DMF y la suspensión se calentó a reflujo durante 2,5 h. La mezcla se enfrió a temperatura ambiente y después se vertió con agitación en 5 N de hidróxido de amonio (20 ml, 100 mmol) en 18 ml de hielo. El precipitado se agitó durante 2 h. La emulsión acuosa se diluyó y después se extrajo dos veces con acetato de etilo. El secado sobre MgSO4 y la concentración produjo un sólido crudo amarillo. Esto se trituró con hexanos, se filtró, se lavó con hexanos, y se secó para proporcionar 5-bromo-1H-indol-2-carboxamida (0,81 g, 3,15 mmol, 93% de rendimiento) como un sólido de color tostado. MS (ESI, ión pos) m/z: 239, 241 (M 1)
Etapa 2. 5-bromo-1H-indol-2-carbonitril
[0385] Se añadió 5-bromo-1 H-indol-2-carboxamida (0,68 mg, 2,84 mmol) a tolueno (20 ml) para dar una suspensión. El oxicloruro de fósforo (1,326 ml, 14,22 mmol) se añadió poco a poco con una jeringa. La suspensión se calentó a reflujo durante 1,5 h. La reacción se vertió en NaHCO3 saturado y se dejó apagar. Las capas se extrajeron dos veces con 50 ml de diclorometano. Las capas combinadas se lavaron con 20 ml de salmuera, se secaron sobre MgSO4 y se concentró para dar el producto bruto. Este material se purificó por cromatografía en columna sobre gel de sílice (columna Biotage de 25 g, gradiente de elución con 0-5% de acetato de etilo/diclorometano) para proporcionar 5-bromo-1H-indol-2-carbonitril (0,408 g, 1,85 mmol, 65%) como un sólido de color tostado. MS (ESI, ion neg.) M/z 219/221
terc-butilo 4-(5-bromopiridina-2-carbonil)piperazin-1-carboxilato
Etapa 1.5-bromopiridina-2-cloruro de carbonil
[0386] Se añadió cloruro de tionilo (3,96 ml, 54,2 mmol) a 5-bromopiridina-2-ácido carboxílico (2,0 g, 9,85 mmol). Se añadió una gota de DMF, y la mezcla se calentó a 80°C durante 2 horas. El exceso de cloruro de tionilo se eliminó en vacío proporcionando cloruro de 5-bromopiridina-2-carbonilo como un sólido amarillo pálido. El material se usó sin purificationin el siguiente paso.
Etapa 2. terc-butilo 4-(5-bromopiridina-2-carbonil)piperazina-1-carboxilato
[0387] 5-Bromopirimidina-2-cloruro de carbonilo (2,181 g, 9,85 mmol) y N,N-diisopropiletilamina (5,16 ml, 29,6mmol) se recogieron en solución en DMF (30 ml). Se añadió terc-butilo piperazina-1-carboxilato y la mezcla de reacción se agitó durante 1,25 h. Se añadió agua (100 ml) y la mezcla se agitó. Después, la mezcla acuosa se extrajo dos veces con 100 ml de acetato de etilo. El segundo fue una emulsión pero saturar con NaCl separó las fases. Las fases orgánicas combinadas se lavaron una vez con salmuera, se secaron sobre MgSO4 y se concentraron. El producto bruto se cromatografía en columna purificada sobre gel de sílice (Biotage, gradiente de elución con metanol al 0-10%/diclorometano) para proporcionar terc-butilo 4-(5-bromopiridina-2-carbonil)piperazina-1-carboxilato (3,1 g, 7,93 mmol, 81 %) como un sólido de color tostado claro. Ms (ESI, ión pos) m/z: 371/373 (M 1)
2-cloro-4-(5-(ciclopropanosulfonamido)piridin-3-il)ácido benzoico
Etapa 1. N-(5-bromopiridin-3-il)ciclopropanosulfonamida
[0388] 5-Bromopiridin-3-amina (0,304 ml, 3,0 mmol) y piridina (0,534 ml, 1,1 mmol) se combinaron en diclorometano (15 ml) para dar una solución marrón. Cloruro de ciclopropanosulfonilo (0,973 ml, 9,00 mmol) se añadió paulatinamente por jeringa. Esto se agitó a ta durante 1 día. Se añadieron piridina adicional (3,0 mmol) y 1 equivalente de ciclopropanosulfonilocloruro (3,00 mmol). Después de 1 día adicional la reacción se había completado. La reacción se diluyó con 75 ml de diclorometano y se lavó con 40 ml de NaHCO3 saturado. La capa acuosa se extrajo con 10 ml de diclorometano y las fases orgánicas combinadas se lavaron con 20 ml de salmuera. Después, el disolvente se secó con MgSO4 y se concentró. El producto bruto se purificó por cromatografía en columna sobre gel de sílice (columna Biotage de 100 g, gradiente de elución con acetato de etilo al 0-50%/hexanos) para proporcionar N-(5-bromopiridin-3-il)ciclopropanosulfonamida (0,81mgs, 2,92 mmol, 73 %) como un sólido de color melocotón. MS (ESI, ión pos) m/z: 277, 279 (M 1).
Etapa 2. 2-cloro-4-(5-(ciclopropanosulfonamido)piridin-3-il)ácido benzoico
[0389] N-(5-bromopiridin-3-il)ciclopropanosulfonamida (0,810 g, 2,92 mmol), carbonil de sodio (1,24 g, 11,69 mmol) y 2-cloro-4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)ácido benzoico (0,991 g, 3,51 mmol) se combinaron en 1,4 dioxano (32 ml) y agua (6,4 ml) seguido de tetraquis(trifenilfosfina)paladio(0) (0,34 g, 0,292 mmol) para dar una suspensión de color amarillo claro. La suspensión se colocó en nitrógeno y se calentó durante 16 h a 80°C. La reacción se filtró a través de Celite y los sólidos se lavaron con 1,4-dioxano seguido de acetato de etilo. Concentrar los disolventes obtuvo un sólido amarillo pegajoso pálido. Esto se suspendió en 50 ml de agua y se basificó con solución de 1 N NaOH hasta que el pH era 12. La capa básica se lavó una vez con 25 ml de acetato de etilo. Después de un retro-extracción de la fase orgánica 20 ml de agua a pH = 12, las fases básicas combinadas se acidificaron con 1 N HCl hasta que se alcanzó pH = 5. Después de mantenerse durante la noche se recogió el precipitado y se secó para proporcionar 2-cloro-4-(5-(ciclopropanosulfonamido)piridin-3-il)ácido benzoico (0,438 g, 1,24 mmol, 35%) como un sólido de color blanquecino. MS (ESI, ión pos) m/z: 353, 355 (M 1).
N-(3-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)fenil)ciclobutanocarboxamida
[0390] 3-(4,4,5,5-Tetrametil-1,3,2-dioxaborolan-2-il)anilina (0,50 g, 2,28 mmol) y N,N-diisopropiletilamina (1,20 ml, 6,85 mmol), se combinaron en diclorometano (5 ml) para dar una solución de color amarillo claro. Cloruro de ciclobutancarbonil (0,260 ml, 2,282 mmol) se añadió gradualmente mediante una jeringa. La mezcla se agitó durante 2,5 h. La reacción se diluyó con 70 ml de diclorometano y después se lavó dos veces con 20 ml de agua. La capa orgánica se lavó con 20 ml de salmuera y se secó sobre MgSO4. Concentrar dio un sólido blanco que se purificó a través de en columna sobre gel de sílice (columna Biotage de 50 g, gradiente de elución con acetato de etilo al 0-40%/hexanos) para proporcionar N-(4'-(4-(1 -hidroxiciclopropanocarbonil}piperazina-1 -carbonil)bifenil-3-il)oxetano-3-carboxamida como un sólido blanco ceroso. MS (ESI, pos. Ion) m/z 302 (M 1).
1 N-(5-bromopiridin-3-il)ciclopropanocarboxamida
[0391] 5-Bromopiridin-3-amina (0,292 ml, 2,89 mmol) y N,N-diisopropiletilamina (0,757 ml, 4,33 mmol) se combinaron en diclorometano (15 ml) para dar una solución de color amarillo claro. Cloruro de ciclopropanocarbonil (0,263 ml, 2,89 mmol) se añadió gradualmente mediante una jeringa. La reacción se agitó a ta durante 1,5 h. La reacción se diluyó con 50 ml de diclorometano y se lavó con 25 ml de NaHCO3 saturado. Después de extraer la capa acuosa con 20 ml de diclorometano las fases orgánicas combinadas se lavaron con 20 ml de NaHCO3 , 20 ml de salmuera, y se secaron sobre MgSO4. El disolvente se concentró dejando un semisólido marrón. El residuo se purificó por cromatografía en columna sobre gel de sílice (columna Biotage 50 g, gradiente de elución con metanol al 0-4%/diclorometano) para proporcionar N-(5-bromopiridin-3-il)ciclopropanocarboxamida (0,603 g, 2,50 mmol, 87%) como un sólido castaño claro. MS (ESI, ión pos) m/z: 241,243 (M 1).
N-(3-bromofenil)etanosulfonamida
[0392] 3-bromoanilina (0,158 ml, 1,453 mmol), y piridina (0,118 ml, 1,453 mmoles) se combinaron en agua (10 ml) para dar una solución y cloruro de etanosulfonilo (0,138 ml, 1,453 mmol) se añadió poco a poco con una jeringa. Después de 1 h de cloruro adicional de etanosulfonilo (0,138 ml, 1,453 mmol) se añadió y la agitación se continuó otra 1 h. La reacción se extrajo con dos veces con 15 ml de acetato de etilo y las capas orgánicas combinadas se lavaron con 10 mL de salmuera y se secaron sobre MgSO4. El disolvente se concentró para proporcionar un aceite rojo pálido. Este material se purificó mediante columna de cromatografía sobre gel de sílice (columna Biotage de 25 g, gradiente de elución con acetato de etilo al 0-30%/hexanos) para proporcionar N-(3-bromofenil)etanosulfonamida (0,345 g, 1,24 mmol, 85%) como una película viscosa incolora que solidificó parcialmente. MS (ESI ion neg.) M/z 262,264 (M-1).
(3’-aminobifenil-4-il)(4-(1-hidroxiciclopropanocarbonil}piperazin-1-il)metanona
[0393] (4-(1-Hidroxiciclopropanocarbonil}piperazin-1-il)(3’-nitrobifenil-4-il)metanona (0,263 g, 0,665 mmol, preparado de acuerdo con el Procedimiento General B) se suspendió en etanol (6 ml) y agua (2 ml). Se añadieron polvo de hierro (0,371 g, 6,65 mmol) y cloruro de amonio (8,89 mg, 0,166 mmol) y la suspensión se calentó a 80°C durante 2 h. La suspensión se diluyó con metanol y se filtró a través de Celite. El filtrado se concentró y se añadió 50 ml de cloroformo. La solución se lavó con 30 ml de NaHCO3 saturado y la fase acuosa se separó y se lavó con 20 ml de cloroformo. Las capas orgánicas combinadas se lavaron con 20 ml de salmuera y se secó sobre MgSO4. La mezcla se concentró y el residuo se purificó por cromatografía en columna sobre gel de sílice (columna 25 g Biotage, gradiente de elución con 0-6% de metanol/cloroformo) para proporcionar una película de color ámbar. Este se
recogió en diclorometano y se trituró con hexanos para proporcionar (3’-aminobifenil-4-il)(4-(1-hidroxiciclopropanocarbonil)-piperazin-1-il)metanona (0,152 g, 0,345 mmol, 52%) como un sólido espumoso. MS (ESI, pos. Ion) m/z 366 (M 1).
terc-butilo 4-(2-cloro-4-(5-(ciclopropanosulfonamido)piridin-3-il)benzoil)piperazina-1-carboxilato
[0394] terc-Butilo piperazina-1-carboxilato (0,139 g, 0,748 mmol), 2-cloro-4-(5-(ciclopropanosulfonamido)-piridin-3-il)ácido benzoico (0,240 g, 0,680 mmol) y N,N-diisopropiletilamina (0,131 ml, 0,748 mmol) se combinaron en DMF (5 ml), y hexafluorofosfato de O-(benzotriazol-1-il)-N,N,N’,N’-tetrametiluronio (0,387 g, 1,020 mmol) se añadió para dar una solución de color pardo. Esto se agitó durante 1 d.
[0395] La reacción se diluyó con 30 ml de agua y se agitó. La mezcla se extrajo con 60 ml de diclorometano y luego con 15 ml de diclorometano. Las capas orgánicas combinadas se lavaron con 20 ml de agua y 20 ml de salmuera y se concentró. El residuo se purificó por cromatografía en columna sobre gel de sílice (columna Biotage 50 g, elución de gradiente con metanol al 0-4%/diclorometano) para proporcionar terc-butilo 4-(2-cloro-4-(5-(ciclopropanosulfonamido)piridin-3-il)benzoil)piperazina-1-carboxilato (0,252 g, 71% de rendimiento) como una película vítrea de color ámbar. MS (ESI, ión pos) m/z: 521/523.
terc-butilo 4-(2-cloro-4-(5-(ciclopropanocarboxamido)piridin-3-il)benzoil)piperazina-1-carboxilato
[0396] terc-Butilo piperazina-1-carboxilato (0,137 g, 0,736 mmol), 2-cloro-4-(5-(ciclopropanocarboxamido)-piridin-3-il)ácido benzoico (0,212 g, 0,669 mmol), y N,N-diisopropiletilamina (0,129 ml, 0,736 mmol) se combinaron en DMF (5 ml) seguido de O-(benzotriazol-1 -il)-N,N,N’,N’-tetrametiluronio (0,381 mg, 1,004 mmol) para dar una solución marrón. Esto se agitó durante 1 d. Se añadió agua (10 ml) y la reacción se agitó. La suspension se diluyó con 60 ml de diclorometano y 20 ml de agua. La fase acuosa se separó y se extrajo con 15 ml de diclorometano. Las capas orgánicas combinadas se lavaron con 20 ml de agua y 20 ml de salmuera, se secaron sobre sulfato de magnesio anhidro, se filtró y se concentró. El producto bruto se purificó por cromatografía en columna sobre gel de sílice (columna Biotage de 50 g, gradiente de elución con metanol al 0-4%/diclorometano) para proporcionar terc-butilo 4-(2-cloro-4-(5-(ciclopropanocarboxamido)-piridin-3-il)benzoil)piperazina-1 -carboxilato (0,454 g, 140%) como un amberglass. MS (ESI, ión pos) m/z: 485/487.
Boc
terc-butilo 5-bromo-3-metil-1H-pirazolo[3,4-b]piridina-1-carboxilato
[0397] En un matraz de fondo redondo de 100 ml, se colocó 5-bromo-3-metil-1H-pirazolo[3,4-b] piridina (800 mg, 3,77mmol, 1,00 equiv), Boc2O (1,22 g, 5,59 mmol, 1,50 equiv), 4-dimetilaminopiridina (55 mg, 0,45 mmol, 0,12 equiv), TEA (756 mg, 7,47 mmol, 2,00 equiv) y tetrahidrofurano (20 ml). La solución resultante se agitó durante 18 h a 20°C. La solución resultante se diluyó con 50 ml de H2O, se extrajo con 3x20 ml de acetato de etilo. Las capas orgánicas se combinaron, se secaron sobre sulfato de sodio anhidro y se concentraron bajo vacío. Esto dio lugar a 1,18 g (95%) del compuesto del titulo como un sólido blanco. LC-MS (Es , m/z): 312, 314 [M+H]+
terc-butilo 5-bromo-2-(((terc-butox¡carbon¡l)ox¡)metil)-1H-benzo[d]¡m¡dazol-1-carbox¡lato
[0398] En un matraz de fondo redondo de 50 ml, se colocó (5-bromo-1H-1,3-benzodiazol-2-il)metanol (600 mg, 2,64 mmol, 1,00 equiv), diclorometano (20 ml), Boc2 O (1 g, 4,58 mmol, 1,73 equiv), TEA (800 mg, 7,91 mmol, 2,99 equiv), 4-dimetilaminopiridina (32 mg, 0,26 mmol, 0,10 equiv). La solución resultante se agitó durante 4 h a 25°C. La mezcla se diluyó con 20 ml de diclorometano, se lavó con 3*30 ml de agua y 30 ml de salmuera. La fase orgánica se secó sobre sulfato de sodio anhidro y se concentró a vacío. Esto dio lugar a 600 mg (en bruto) del compuesto del titulo como un aceite amarillo. LC-MS (ES, m/z) 429427 [M+H]+
terc-but¡lo (3-(3-bromofen¡l)-1 H-p¡razol-5-¡l)carbamato
[0399] En un matraz de fondo redondo de 50 ml, se colocó una solución de 3-(3-bromofenil)-1H-pirazol-5-amina (500 mg, 2,10 mmol, 1,00 equiv) en diclorometano (20 ml), (Boc)2O (916 mg, 4,20 mmol, 2,00 equiv), 4-dimetilaminopiridina (25,6 mg, 0,21 mmol, 0,10 equiv), TEA (636,5 mg, 6,29 mmol, 3,00 equiv). La solución resultante se agitó durante 1 h temperatura ambiente. La mezcla de reacción se vertió entonces en 100 ml de agua, se extrajo con 2x100 ml de diclorometano. Las capas orgánicas se combinaron, se secaron sobre sulfato de sodio anhidro y se concentró bajo vacío. Esto resultó en 710 mg (100%) de terc-butilo N-[3-(3-bromofenil)-1H-pirazol-5-il]carbamato de bencilo como un aceite marrón. LC-MS (ES, m/z): 338 [M+H]+
terc-but¡lo 3-bromo-7-fluoro-1 H-¡ndazol-1 -carbox¡lato
[0400] En un matraz de fondo redondo de 50 ml, se colocó 3-bromo-7-fluoro-1H-indazol (700 mg, 3,26 mmol, 1,00 equiv), diclorometano (20 ml), Boc2O (1,5 g, 6,87 mmol, 2,11 equiv), TEA (1 g, 9,88 mmol, 3,04 equiv), 4-dimetilaminopiridina (40 mg, 0,33 mmol, 0,10 equiv). La solución resultante se agitó durante 4 h a 25°C. La mezcla resultante se vertió en 50 ml de agua, se extrajo y se concentró a vacío. Esto dio lugar a 1 g (bruto) del título de compuesto como aceite rojo. LC-MS (ES, m/z): 315, 317 [M+H]+
terc-but¡lo (5-bromobenzo[d]¡soxazol-3-¡l)carbamato
[0401] En un matraz de fondo redondo de 50 ml, se colocó 5-bromo-1,2-benzoxazol-3-amina (1 g, 4,69 mmol, 1,00 equiv), diclorometano (20 ml), Boc2O (2,1 g, 9,62 mmol, 2,05 equiv), 4-dimetilaminopiridina (57 mg, 0,47 mmol, 0,10equiv), TEA (1,4 g, 13,84 mmol, 2,95 equiv). La mezcla de reacción se agitó durante 3 h a 25°C. La mezcla resultante se lavó con 30 ml de agua, 3x30 ml de salmuera, se secó sobre sulfato de sodio anhidro y se concentró a vacío. Esto resultó en 650 mg (en bruto) del compuesto del título como un aceite amarillo. LC-MS (ES, m/z): 313, 315 [M+H]+
2-cloro-6-fluoroqu¡nazol¡na
[0402] En un matraz de fondo redondo de 100 ml purgado y mantenido con una atmósfera inerte de nitrógeno, se colocó 2,4-dicloro-6-fluoroquinazolina (1 g, 4,61 mmol, 1,00 equiv), salmuera (23 ml), diclorometano (25 ml), hidrato de amoniaco (2 ml), Zn (0,9 g, 13,8 mmol, 3,0 equiv). La mezcla resultante se agitó durante la noche a 50°C en un baño de aceite. La mezcla de reacción se enfrió a temperatura ambiente y se diluyó con 50 ml de H2O, se extrajo con 2x100 ml de diclorometano. Las capas orgánicas se combinaron y se concentraron a vacío. El residuo se purificó por Combi-Flash con las siguientes condiciones (IntelFlash-1): columna, gel de sílice; fase móvil, EA: PE = 100% aumentando a EA: PE = 60% con 40 min; Detector, UV 254 nm. Esto dio lugar a 0,35 g (35%) del compuesto del título como un sólido amarillo. LC-MS (ES, m/z) 183 [M+H]+
6-bromo-1-metil-1H-indazol-3-ol
[0403] En un tubo sellado de 5 ml, se colocó metilo 4-bromo-2-fluorobenzoato (300 mg, 1,29 mmol, 1,00 equiv), metilhidrazina (71,4 mg, 1,55 mmol, 1,20 equiv), DMA (2 ml). La solución resultante se agitó durante la noche a 150°C en un baño de asand. Después de enfriarse a temperatura ambiente, la mezcla de reacción se diluyó con 10 ml de acetato de etilo, se lavó con 3x10 ml de H2O y 1x20 ml de salmuera. La fase orgánica se concentró a vacío. Esto dio lugar a 225 mg (77%) de 6-bromo-1-metil-1H-indazol-3-ol como un sólido blanquecino. LC-MS (ES, m/z): 227, 229 [M+H]+
6-bromo-1-(metilsulfonil)-1H-indol
[0404] A una solución de 6-bromoindol (2,94 g, 15 mmol, 1 eq.) en DMF anhidro (45 ml) se enfrió en un baño de agua helada se añadió NaH (0,72 g, 18 mmol, 1,2 eq.) en porciones en atmósfera de N2. La mezcla se agitó durante 20 min. y MeSO2 Cl (1,4 ml, 18 mmol, 1,2 eq.) se añadió después gota a gota. Se dejó que la mezcla de reacción se calentara a temperatura ambiente y se agitó durante 1 hora antes de inactivar con hielo y se diluyó con EtOAc. La capa orgánica se lavó con agua (2 x) y salmuera (2 x), se secó sobre Na2SO4 y se concentró al vacío. El residuo bruto se purificó por cromatografía flash (gel de sílice) eluyendo con EtOAc/hexanos (0~20%) para dar el compuesto del título como un sólido blanco (0,94 g, 23%).
Ensayo enzimático para los inhibidores de FASN
[0405] Los ensayos se realizaron en una placa de color negro de 384 pocillos para medir la inhibición de las actividades de FASN por compuestos individuales descritos en este documento. Una parte alícuota de 250 nL de compuesto se incubó con 10 pL de enzima de FASN de 40 nM en ensayo de tampón (50 mM HEPES pH = 7,3, EDTA 0,5 mM, ascorbato 1 mM, NaCl 100 mM y 0,04% de Triton X-100) en cada pocillo a 25°C durante 60 minutos. Después de que la placa se centrifugó brevemente, 10 pL de mezcla de sustrato (20pm acetil-CoA, 60pm Malonyl-CoA, y 100pm NADPH en tampón de ensayo) se añadió a cada pocillo. La reacción se mantuvo a 25°C durante 90 minutos. Después, la reacción se inactivó mediante la adición de 10 pL de 90 pm 7-dietilamino-3-(4'-Maleimidilfenil)-4-metil-coumarina en 50/50 solución etanol/H2O. La placa de ensayo se incubó a 25°C durante 15 minutos, y se lee en un lector de una placa con excitación y longitud de onda de emisión a 360 nm y 530 nm, respectivamente. El CI50 de un compuesto dado se calculó mediante el ajuste de la curva de respuesta a la dosis con una ecuación logística de cuatro parámetros.
Resultados
[0406] La Tabla 2-1 enumera los compuestos que tienen un CI 50 <0,5 pM.
Tabla 2-2 enumera los compuestos que tienen un CI50 e 0,5 pm y <5,0 pM.
Tabla 2-3 enumera los compuestos que tienen un CI 50 e 5,0 pM.
[0407] Además, el peso molecular, resultados de espectrometría de iones de masas, tiempo de retención de HPLC, y el Método utilizado para sintetizar el compuesto también se enumeran.
Tabla 2-1
(continuado)
(continuado)
(continuado)
(continuado)
(continuado)
(continuado)
(continuado)
(continuado)
(continuado)
(continuado)
(continuado)
(continuado)
(continuado)
(continuado)
(continuado)
Tabla 2-2
(continuado)
(continuado)
Tabla 2-3
(continuado)
Ensayos de proliferación celular de los inhibidores de FASN
[0408] Los efectos de los inhibidores de FASN en la proliferación de células de cáncer cultivadas eran estudios con ensayos de proliferación de células. PC3 de células se mantuvieron a medio de cultivo estándar (medio F12K suplementado con suero bovino fetal al 10%, ácido amino 1X MEM no esencial y 1X penicilina/estreptomicina).
2000-3000cells/100 pL/pocillo se sembró en una placa de cultivo transparente de 96 pocillos. Las células se incubaron durante la noche en 5% de CO2 a 37°C para la fijación. Los medios celulares se eliminaron y se reemplazaron con medios F12K que contienen 10% de suero reducido por lípidos y compuesto. La concentración final de DMSO es 0,1%. Las células se mantuvieron en 5% de CO2 a 37°C durante 4 días. La viabilidad de las células se determinó mediante ensayos de MTT. El CI50 de un compuesto dado se calculó mediante el ajuste de la curva de respuesta a la dosis con una ecuación logística de cuatro parámetros.
Resultados
[0409] Tabla 3-1 enumera los compuestos que tienen un CI50 <0,5 pM.
Tabla 3-2 enumera los compuestos que tienen un CI50 >0,5 pM.
[0410] Además, el peso molecular, los resultados de espectrometría de masas de iones, tiempo de retención de HPLC, y el Método utilizado para sintetizar el compuesto también se enumeran.
Tabla 3-1
(continuado)
(continuado)
(continuado)
(continuado)
Tabla 3-2
[0411] Aunque la presente invención ha sido descrita conjuntamente con las realizaciones específicas expuestas anteriormente, muchas alternativas, modificaciones y otras variaciones de las mismas serán evidentes para los expertos normales en la técnica.
Claims (46)
1. Un com puesto de fórmula I:
en donde:
R1 es
L es un anillo monocíclico de 5-10 miembros o alquilo bicíclico o heteroalquilo en donde (i) los miembros del anillo de heteroátomos del heteroalquilo monocíclico o bicíclico de 5-10 miembros se seleccionan independientemente de O, S, o N, y (ii) cada uno del alquilo o heteroalquilo monocíclico o bicíclico de 5-10 miembros o no se sustituye o se sustituye opcionalmente con sustituyentes seleccionados del grupo que consiste de deuterio y -Rb;
A y B son independientemente O o S;
An es
arilo, heteroarilo o heterocicloalquilo monocíclico o bicíclico de 4-10 miembros, en donde (i) dicho heteroarilo o heterocicloalquilo monocíclico o bicíclico de 4-10 miembros tienen 1, 2, 3, o 4 heteroátomos que se seleccionan independientemente de N, S u O, y (ii) cada uno de dichos arilo, heteroarilo o heterocicloalquilo monocíclico o bicíclico de 4-10 miembros, está o bien no sustituido u opcionalmente sustituido independientemente con 1 o más sustituyentes que pueden ser el mismo o diferentes y se seleccionan independientemente del grupo que consiste de deuterio, halo, alquilo, -CHzF3-z, ciano, hidroxilo, hidroxialquilo, amino, aminoalquilo, (amino)alcoxi, -CONH2 , -C(O)NH(alquilo), -C(O)N(alquilo)2 , -C(O)NH(arilo), -C(O)N(arilo)2, -OCHzF3-z, -alquilo, -alquenilo, alquinilo, alcoxi o (alcoxialquilo)amino -, -N(Rc)-(O)-alquilo, -N(Rc)-C(O)arilo, cicloalquilo, heterocicloalquilo, arilo, y heteroarilo, con la condición de que no hay dos heteroátomos adyacentes en el anillo son ambos S o ambos O;
R2 es H o un anillo de arilo, heteroarilo, cicloalquilo, o heterocicloalquilo monocíclico, bicíclico o tricíclico de 4-15 miembros (i) el heteroarilo o heterocicloalquilo monocíclico, bicíclico o tricíclico de 4-15 miembros tiene 1, 2, 3, 4, 5, 6, 7, o 8 heteroátomos que se seleccionan independientemente entre N, S u O, y (ii) en donde cada uno de dicho arilo, heteroarilo, cicloalquilo, y heterocicloalquilo o bien no sustituido o sustituido opcionalmente con 1 o más sustituyentes que pueden ser los mismos o diferentes y se seleccionan independientemente del grupo que consiste en deuterio, halo, ciano, hidroxilo, hidroxilo-alquilo-, hidroxilcicloalquilo-, hidroxilo-heterocicloalquil, aminoalquilo hidroxilo-aril-, hidroxilheteroarilo-, amino, (amino)alcoxi, - CONH2 , -C(O)NH(alquilo), -C(O)N(alquilo)2 , -C(O)NH(arilo), -C(O)N(arilo)2 , -CHzF3-z, -OCHzF3-z, -alquilo, alcoxi, alquenilo, alquinilo, ariloxi, (alcoxialquilo)amino-, cicloalquilo, heterocicloalquilo, (heterocicloalquil)alquilo-, - arilo, heteroarilo, -O(alquilo), -O(cicloalquilo), -O(heterocicloalquilo), -O(arilo), -O(heteroarilo), ONH2, -C(O)NH(alquilo), -C(O)N(arilo)2 , -C(O)NH(cicloalquilo), -NH(CO)cicloalquilo, -NH(SO2), -NH(SO2)alquilo, -NH(SO2)arilo, -NH(SO2)heteroarilo, -N(SO2)cicloalquilo, -C(O)N(alquilo)2 , (aril)alquilo-, - heteroarilo, (heteroaril)alquilo, -S(O)2alquilo, -S(O)2-arilo, -S(O)2cicloalquilo, -C(O)N(alquilo)2 , -(O)alquilo, -NH-C(O)-alquilo, -NH-C(O)-cicloalquilo, NH-(O)heterocicloalquilo, NH-(O)heterocicloalquilo-Rd, -NH-C(O)-Rd-(O)alquilo, -NH-C(O)-arilo, -NH-C(O)-NH-alquilo, NH-C(O)-NH-cicloalquilo, NH2 (CO)-alquilo,
NH-C(O)-NH-arilo, -NH-C(O)-O-alquilo, NH-C(O)-NH-cicloalquilo, -NH-C(O)-O-c¡cloalquilo, -NH(Rd)-(O)-alquilo, -NH(Rd)-(O)-arilo, -NH(Rd)-SO2)cicloalquilo, -SO2)NH2 , -SO2)NH(alquilo), -SO2)N(Rd)cicloalquilo,
-SO2)N(alquilo)2 , -C(O)N(H)(alquilo), -C(O)N(Rd)(cicloalquilo), metilendioxi, -CHzF3-z, -OCHzF3-z, y alcoxi; Rb es H, halo, C1-C4 alquilo, C1-C3 hidroxilo-alquilo, o C3-C4 cicloalquilo;
Rc es H, halo, C1-C4 alquilo, o C3-C4 cicloalquilo;
Rd es H, halo, C1-C4 alquilo, o C3-C4 cicloalquilo;
y z es 0, 1 ó 2;
y las sales farmacéuticamente aceptables de los mismos
adicionalmente en donde:
R2 no es una forma sustituida o sin sustituir de
en donde X es N o CH;
cuando Ar1 es
conectado a
en la posición 1, y X1 y X2 son independientemente N o C-Rz y Ry y Rz son cualquier sustituyente, entonces Rx no incluye alquinilo, alquenilo, arilo, heterocíclico de 5-14 miembros, heteroaromático de 5-14 miembros o carbocíclico de 4-9 miembros;
cuando Ar1 es una forma sustituida o no sustituida de un heteroarilo de 5 miembros, Ar1 es una forma sustituida o no sustituida de
y cuando R2 es
Ai no es una forma sustituida o no sustituida de
3. El compuesto de la reivindicación 1, en donde A y B son O.
7. El compuesto de la reivindicación 1 en donde Ar1 es un arilo o heteroarilo monocíclico sustituido o no sustituido de 5-6 miembros.
9. El compuesto de la reivindicación 7, en donde Ar1 es un arilo o heteroarilo monocíclico sustituido o no sustituido de 6 miembros y dicho heteroarilo tiene 1 o 2 heteroátomos que son N.
14. El compuesto de la reivindicación 1, en donde Ar1 es un heteroarilo 6,5-bicíclico sustituido o no sustituido de 9 miembros y dicho heteroarilo tiene 1,2, o 3 heteroátomos que son independientemente O, S o N.
16. El compuesto de la reivindicación 1, en donde R2 es un arilo o heteroarilo monocíclico o bicíclico sustituido o no sustituido de 5-10 miembros.
17. El compuesto de la reivindicación 16, en donde R2 es un arilo monocíclico de sustituido o no sustituido de 6 miembros.
19. El compuesto de la reivindicación 16, en donde R2 es un arilo bicíclico de 8-10 miembros sustituido o no sustituido o heteroarilo de 8-10 miembros.
20. El compuesto de la reivindicación 17, en donde R2 es un heteroarilo 5,5 bicíclico sustituido o no sustituido de 8 miembros y dicho heteroarilo tiene 1,2, 3, o 4 heteroátomos y dichos heteroátomos son independientemente O, S, o N.
22. El compuesto de la reivindicación 16, en donde R2 es un heteroarilo 6,5 bicíclico sustituido o no sustituido de 9 miembros y dicho heteroarilo tiene 1,2, 3, o 4 heteroátomos y dichos heteroátomos son independientemente O, S, o N.
24. El compuesto de la reivindicación 16, en donde R2 es un arilo o heteroarilo 6,6 biciclico sustituido o no sustituido de 10 miembros y dicho heteroarilo tiene 1,2, 3, o 4 heteroátomos y dichos heteroátomos son O, S, o N.
26. El compuesto de la reivindicación 1, en donde el compuesto es un compuestode Fórmula I-A:
en donde:
Ri es
Ari es un arilo bicíclico, heteroarilo, o heterocicloalquilo monocíclico de 4-10 miembros en donde (i) dicho heteroarilo bicíclico, o heterocicloalquilo monocíclico de 4-10 miembros tiene 1, 2, 3, o 4 heteroátomos que se seleccionan independientemente entre N, S u O, y (ii) cada uno de dichos arilo o heteroarilo monocíclico o bicíclico de 4-10 miembros está no sustituido u opcionalmente sustituido independientemente con 1 o más sustituyentes que pueden ser el mismo o diferente y se seleccionan independientemente del grupo que consiste de deuterio, halo, alquilo, -CHzF3-z, ciano, hidroxilo, hidroxialquilo, amino, aminoalquilo, (amino)alcoxi, -CONH2 , -C(O)NH(alquilo), -C(O)N(alquilo)2 , -C(O)NH(arilo), -C(O)N(arilo)2 , -OCHzF3-z, -alquilo, -alquenilo, alquinilo, alcoxi o (alcoxialquilo)amino -, -N(Rc)-(O)-alquilo, -N(Rc)-C(O)arilo, cicloalquilo, heterocicloalquilo, arilo, y heteroarilo, con la condición de dos heteroátomos de anillo adyacentes son ambos S o ambos O;
R2 es H o un arilo, heteroarilo, cicloalquilo, o heterocicloalquilo monocíclico, bicíclico o tricíclico de 4-15 miembros, (i) el heteroarilo o heterocicloalquilo monocíclico, bicíclico o tricíclico de 4-15 miembros tiene 1, 2, 3, 4, 5, 6, 7, o 8 heteroátomos que se seleccionan independientemente entre N, S u O, y (ii) en donde cada uno de dicho arilo, heteroarilo, cicloalquilo, y heterocicloalquilo o bien no sustituido o sustituido opcionalmente con 1 o más sustituyentes pueden ser los mismos o diferentes y se seleccionan independientemente del grupo que consiste en deuterio, halo, ciano, hidroxilo, hidroxilo-alquilo-, hidroxilcicloalquilo-, hidroxilo-heterocicloalquil, aminoalquilo hidroxilo-aril-, hidroxilheteroarilo-, amino, (amino)alcoxi, - CONH2 , -C(O)NH(alquilo), -C(O)N(alquilo)2 , -C(O)NH(arilo), -C(O)N(arilo)2 , -CHzF3-z, -OCHzF3-z, -alquilo, alcoxi, alquenilo, alquinilo, ariloxi, (alcoxialquilo)amino-, cicloalquilo, heterocicloalquilo, (heterocicloalquil)alquilo-, - arilo, heteroarilo, -O(alquilo), -O(cicloalquilo), -O(heterocicloalquilo), -O(arilo), -O(heteroarilo), ONH2 , -C(O)NH(alquilo), -C(O)N(arilo)2 , -C(O)NH(cicloalquilo), -NH(CO)cicloalquilo, -NH(SO2), -NH(SO2)alquilo, -NH(SO2)arilo, -NH(SO2)heteroarilo, -N(SO2)cicloalquilo, -C(O)N(alquilo)2 , (aril)alquilo-, - heteroarilo, (heteroaril)alquilo, -S(O)2alquilo, -S(O)2-arilo, -S(O)2cicloalquilo, -C(O)N(alquilo)2, -(O)alquilo, -NH C(O)-alquilo, -NH-C(O)-cicloalquilo, NH-(O)heterocicloalquilo, Nh-(O)-heterocicloalquilalquilo, Rd, -NH-C(O)-Rd-(O)alquilo, -NH-C(O)-arilo, -NH-C(O)-NH-alquilo, NH-C(O)-NH-cicloalquilo, NH2 (CO)-alquilo, NH-C(O)-NH-arilo, -NH-C(O)-O-alquilo,
NH-C(O)-NH-cicloalquilo, -NH-C(O)-O-cicloalquilo, -NH(Rd)-(O)alquilo, -S(O2)N(Rd)cicloalquilo, -NH(Rd)-(O)-arilo, -NH(Rd)-SO2)cicloalquilo, -SO2)NH2 , -SO2)NH(alquilo), -SO2)N(alquilo)2 , -C(O)N(H)(alquilo), -C(O)N(Rd)(cicloalquilo), metilendioxi, -CHzF3-z, -OCHzF3-z, y alcoxi;
Rc es H, halo, C1-C4 alquilo, o C3-C4 cicloalquilo;
Rd es H, halo, C1-C4 alquilo, o C3-C4 cicloalquilo; y
z es 0 , 1 ó 2 ;
o una sal farmacéuticamente aceptable del mismo.
27. El compuesto de la reivindicación 1, en donde el compuesto es un compuesto de fórmula I-B:
en donde:
Ari es un arilo, heteroarilo, o heterocicloalquilo monocíclico o bicíclico de 4-10 miembros, en donde (i) dicho heteroarilo o heterocicloalquilo monocíclico o bicíclico de 4-10 miembros o tiene 1, 2, 3, o 4 heteroátomos que se seleccionan independientemente a partir de N, S, u O, y (ii) cada uno de dichos arilo o heteroarilo monocíclico o bicíclico de 4-10 miembros o está o bien no sustituido u opcionalmente sustituido independientemente con 1 o más sustituyentes que pueden ser el mismo o diferente y se seleccionan independientemente del grupo que consiste de deuterio, halo, alquilo, -CHzF3-z, ciano, hidroxilo, hidroxialquilo, amino, aminoalquilo, (amino)alcoxi-, - CONH2 , -C(O)NH(alquilo), -C(O)N(alquilo)2 , -C(O)NH(arilo), -C(O)N(arilo)2, - OCHzF3-z, -alquilo, -alquenilo, alquinilo, alcoxi o (alcoxialquilo)amino-, -N(Rc)-(O)-alquilo, -N(Rc)-C(O)arilo, cicloalquilo, heterocicloalquilo, arilo, y heteroarilo, con la condición de que dos heteroátomos de anillo adyacentes no son ambos S o ambos O;
R2 es H o un arilo, heteroarilo, cicloalquilo, o heterocicloalquilo, monocíclico, bicíclico o tricíclico de 4-15 miembros, (i) el heteroarilo o heterocicloalquilo monocíclico, bicíclico, tricíclico de 4-15 miembros tiene 1, 2, 3, 4, 5, 6, 7, o 8 heteroátomos que se seleccionan independientemente entre N, S, u O, y (ii) en donde cada uno de dichos arilo, heteroarilo, cicloalquilo, y heterocicloalquilo es o bien no sustituido o sustituido opcionalmente con 1 o más sustituyentes que pueden ser los mismos o diferentes y se seleccionan independientemente del grupo que consiste de deuterio, halo, ciano, hidroxilo, hidroxilo-alquilo-, hidroxilcicloalquilo-, hidroxilo-heterocicloalquilo, hidroxilo-aril-, hidroxilheteroarilo-, amino, aminoalquilo, (amino)alcoxi, -CONH2 , -C(O)NH(alquilo), -C(O)N(alquilo)2 , -C(O)NH(arilo), -C(O)N(arilo)2 , -CHzF3-z, -OCHzF3-z, -alquilo, alcoxi, alquenilo, alquinilo, ariloxi, (alcoxialquilo)amino-, cicloalquilo, heterocicloalquilo, (heterocicloalquil)alquilo-, - arilo, heteroarilo, -O(alquilo), -O(cicloalquilo), -O(heterocicloalquilo), -O(arilo), -O(heteroarilo), ONH2, -C(O)NH(alquilo), -C(O)N(arilo)2 , -C(O)NH(cicloalquilo), -NH(CO)cicloalquilo, -NH(SO2), -NH(SO2)alquilo, -NH(SO2)arilo, -NH(SO2)heteroarilo, -N(SO2)cicloalquilo, -C(O)N(alquilo)2 , (aril)alquilo-, - heteroarilo, (heteroaril)alquilo, -S(O)2alquilo, -S(O)2-arilo, -S(O)2cicloalquilo, -C(O)N(alquilo)2, -(O)alquilo, -NH-C(O)-alquilo, -NH-C(O)-cicloalquilo, NH-(O)heterocicloalquilo, Nh -(O)-heterocicloalquilalquilo, Rd, -NH-C(O)-Rd-(O)alquilo, -NH-C(O)-arilo, -NH-C(O)-NH-alquilo, NH-C(O)-NH-cicloalquilo, NH2 (CO)-alquilo, NH-C(O)-NH-arilo, -NH-C(O)-O-alquilo, NH-C(O)-NH-cicloalquilo, -NH-C(O)-O-cicloalquilo, -NH(Rd)-(O)-alquilo, -NH(Rd)-(O)-arilo, -NH(Rd)-SO2)cicloalquilo, -SO2)NH2 , -SO2)NH(alquilo), -SO2)N(Rd)cicloalquilo, -SO2)N(alquilo)2 , -C(O)N(H)(alquilo), -C(O)N(Rd)(cicloalquilo), metilendioxi, -CHzF3-z, -OCHzF3-z, y alcoxi;
Rc es H, halo, C1-C4 alquilo, o C3-C4 cicloalquilo;
Rd es H, halo, C1-C4 alquilo, o C3-C4 cicloalquilo;
y z es 0, 1 ó 2;
o una sal farmacéuticamente aceptable del mismo.
28. El compuesto de la reivindicación 1, en donde el compuesto es un compuesto de fórmula I-C:
en donde:
Ri es
R2 es H o un arilo, heteroarilo, cicloalquilo, o heterocicloalquilo monocíclico, bicíclico o tricíclico de 4-15 miembros, (i) el heteroarilo o heterocicloalquilo monocíclico, bicíclico o tricíclico de 4-15 miembros tiene 1, 2, 3, 4, 5, 6, 7, o 8 heteroátomos que se seleccionan independientemente entre N, S u O, y (ii) en donde cada uno de dicho arilo, heteroarilo, cicloalquilo, y heterocicloalquilo o bien no sustituido o sustituido opcionalmente con 1 o más sustituyentes que pueden ser los mismos o diferentes y se seleccionan independientemente del grupo que consiste en deuterio, halo, ciano, hidroxilo, hidroxilo-alquilo-, hidroxilcicloalquilo-, hidroxilo-heterocicloalquil, aminoalquilo hidroxilo-aril-, hidroxilheteroarilo-, amino, (amino)alcoxi, - CONH2 , -C(O)NH(alquilo), -C(O)N(alquilo)2 , -C(O)NH(arilo), -C(O)N(arilo)2 , -CHzF3-z, -OCHzF3-z, -alquilo, alcoxi, alquenilo, alquinilo, ariloxi, (alcoxialquilo)amino-, cicloalquilo, heterocicloalquilo, (heterocicloalquil)alquilo-, - arilo, heteroarilo, -O(alquilo), -O(cicloalquilo), -O(heterocicloalquilo), -O(arilo), -O(heteroarilo), ONH2 , -C(O)NH(alquilo), -C(O)N(arilo)2 , -C(O)NH(cicloalquilo), NH2 (CO)cicloalquilo-, -NH(CO)cicloalquilo, -NH(SO2), -NH(SO2)alquilo, -NH(SO2)arilo, -NH(SO2)heteroarilo, -N(SO2)cicloalquilo, -C(O)N(alquilo)2 , (aril)alquilo, heteroarilo, (heteroaril)alquilo, -S(O)2alquilo, -S(O)2-arilo, -S(O)2cicloalquilo, -C(O)N(alquilo)2 , -(O)alquilo, -NH-(O)alquilo, -NH-(O)cicloalquilo, NH-(O)heterocicloalquilo, NH-(O)R -heterocicloalquilalquilo-Rd, -NH-C(O)-Rd-(O)alquilo, -NH-C(O)-arilo, -NH-C(O)-NH-alquilo, NH-C(O)-NH-cicloalquilo, NH-C(O)-NH, arilo, -NH-C(O)-O-alquilo, NH-C(O)-NH-cicloalquilo, -NH-C(O)-O-cicloalquilo, -NH(Rd)-(O)alquilo, -S(O2)N(Rd) CY, -NH(Rd)-(O)-arilo, -NH(Rd)-SO2)cicloalquilo, -SO2)NH2 , -SO2)NH(alquilo), cicloalquilo, -S(O2)N(alquilo)2 , -C(O)N(H)(alquilo), -C(O)N(Rd)(cicloalquilo), metilendioxi, -CHzF3-z, -OCHzF3-z, y alcoxi;
Rd es H, halo, C1-C4 alquilo, o C3-C4 cicloalquilo;
Rq es H, halo, C1-C4 alquilo, o C3-C4 cicloalquilo;
y z es 0, 1 ó 2;
y las sales farmacéuticamente aceptables de los mismos.
29. El compuesto de la reivindicación 1, en donde el compuesto es un compuesto de fórmula I-D:
en donde:
R1 ' es OH o NH2 ;
R2 es H o un arilo, heteroarilo, cicloalquilo, o heterocicloalquilo monocíclico, bicíclico o tricíclico de 4-15 miembros, (i) el heteroarilo o heterocicloalquilo monocíclico, bicíclico o tricíclico de 4-15 miembros tiene 1, 2, 3, 4, 5, 6, 7, o 8 heteroátomos que se seleccionan independientemente entre N, S u O, y (ii) en donde cada uno de dicho arilo, heteroarilo, cicloalquilo, y heterocicloalquilo o bien no sustituido o sustituido opcionalmente con 1 o más sustituyentes que pueden ser los mismos o diferentes y se seleccionan independientemente del grupo que consiste en deuterio, halo, ciano, hidroxilo, hidroxilo-alquilo-, hidroxilcicloalquilo-, hidroxilo-heterocicloalquil, aminoalquilo hidroxilo-aril-, hidroxilheteroarilo-, amino, (amino)alcoxi, - CONH2 , -C(O)NH(alquilo), -C(O)N(alquilo)2 , -C(O)NH(arilo), -C(O)N(arilo)2 , -CHzF3-z, -OCHzF3-z, -alquilo, alcoxi, alquenilo, alquinilo, ariloxi, (alcoxialquilo)amino-, cicloalquilo, heterocicloalquilo, (heterocicloalquil)alquilo-, - arilo, heteroarilo, -O(alquilo), -O(cicloalquilo), -O(heterocicloalquilo), -O(arilo),
O(heteroarilo), ONH2 , -C(O)NH(alquilo), -C(O)N(arilo)2 , -C(O)NH(cicloalquilo), NH2(CO)cicloalquilo-, -NH(CO)cicloalquilo, -NH(SO2), -NH(SO2)alquilo, -NH(SO2)arilo, -NH(SO2)heteroarilo, -N(SO2)cicloalquilo, -C(O)N(alquilo)2 , (aril)alquilo, heteroarilo, (heteroaril)alquilo, -S(O)2alquilo, -S(O)2-arilo, -S(O)2cicloalquilo, -C(O)N(alquilo)2 , -(O)alquilo, -NH-(O)alquilo, -NH-(O)cicloalquilo, NH-(O)heterocicloalquilo, NH-(O)R -heterocicloalquilalquilo-Rd, -NH-C(O)-Rd-(O)alquilo, -NH-C(O)-arilo, -NH-C(O)-NH-alquilo, NH-C(O)-NH-cicloalquilo, NH-C(O)-NH-arilo, -NH-C(O)-O-alquilo, NH-C(O)-NH-cicloalquilo, -NH-C(O)-O-cicloalquilo, -NH(Rd)-(O)alquilo, -S(O2)N(Rd)cicloalquilo, -S(O2)N(alquilo)2 , -C(O)N(H)(alquilo), -C(O)N(Rd)(cicloalquilo), metilendioxi, -CHzF3-z, -OCHzF3-z, y alcoxi;
Rd es H, halo, C1-C4 alquilo, o C3-C4 cicloalquilo;
Rq es H, halo, C1-C4 alquilo, o C3-C4 cicloalquilo;
y z es 0, 1 ó 2;
y las sales farmacéuticamente aceptables de los mismos.
30. Los compuestos de la reivindicación 29, en donde R2 es un:
arilo de 6 miembros sin sustituir o sustituido opcionalmente con 1 o más sustituyentes que pueden ser los mismos o diferentes y se seleccionan independientemente del grupo que consiste de deuterio, halo, ciano, alquilo, arilo, -S(O)2alquilo, -S(O)2-arilo, -S(O)2cicloalquilo, - -NH-C(O)alquilo, -NH-C(O)cicloalquilo, NH-C(O)heterocicloalquilo, NH-C(O)R -heterocicloalquilalquilo-Rd, -NH-C(O)-Rd-(O)alquilo, -NH-C(O)-arilo, -NH-C(O)-NH-alquilo, NH-C(O)-NH-cicloalquilo, NH2 (CO)-alquilo, NH-C(O)-NH-arilo, -NH-C(O)-O-alquilo, NH-C(O)-NH-cicloalquilo, -NH-C(O)-O-cicloalquilo, -NH(Rd)-(O)-alquilo, -NH(Rd)-(O)-arilo, -NH(Rd)-SO2)cicloalquilo, -S(O2)NH2 , -SO2)NH(alquilo), -S(O2)N(Rd)cicloalquilo, -S(O2)N(alquilo)2 , -C(O)N(H)(alquilo), y -C(O)N(Rd)(cicloalquilo); o
heteroarilo bicíclico de 9 miembros que tiene 1, 2, o 3 o 4 heteroátomos que se seleccionan independientemente entre N, S u O, y en donde cada uno de dicho heteroarilo, o bien no sustituido o sustituido opcionalmente con 1 o más sustituyentes que pueden ser los mismos o diferentes y son seleccionados independientemente del grupo que consiste de deuterio, halo, ciano, alquilo, arilo, -S(O)2alquilo, -S(O)2-arilo, -S(O)2cicloalquilo, -NH-C(O)alquilo, -NH-C(O)cicloalquilo, NH-C(O)heterocicloalquilo, NH-C(O)heterocicloalquilo-Rd, -NH-C(O)-Rd-(O)alquilo, -NH-C(O)-arilo, -NH-C(O)-NH-alquilo, NH-C(O)-NH-cicloalquilo, NH2 (CO)-alquilo, NH-C(O)-NH-arilo, -NH-C(O)-O-alquilo, NH-C(O)-NH-cicloalquilo, -NH-C(O)-O-cicloalquilo, -NH(Rd)-(O)-alquilo, -NH(Rd)-(O)-arilo, -NH(Rd)-SO2)cicloalquilo, -S(O2)NH2 , -SO2)NH(alquilo), -S(O2)N(Rd)cicloalquilo, -S(O2)N(alquilo)2 , -C(O)N(H)(alquilo), y-(O)N(Rd)(cicloalquil).
31. Un compuesto de la reivindicación 1 seleccionado de:
1 -[(4-{[2-fluoro-4-(1 -metil-1 H-indol-5-il)fenil]carbonil}piperazin-1 -il)carbonil]ciclopropan-1 -ol;
1 -[(4-{[4-(isoquinolin-6-il)fenil]carbonil}piperazin-1 -il)carbonil]ciclopropan-1 -ol;
1 -[(4-{[3-cloro-4-(quinolin-3-il)fenil]carbonil}piperazin-1 -il)carbonil]ciclopropan-1 -ol;
5-[2-cloro-4-({4-[(1 -hidroxiciclopropil)carbonil]piperazin-1 -il}carbonil)fenil]-1 H-indole-3 -carbonitril;
1 -[(4-{[4-(quinolin-2-il)fenil]carbonil}piperazin-1 -il)carbonil]ciclopropan-1 -ol;
1 -{4-[2-fluoro-4-(1 -metil-1 H-1,3-benzodiazol-5-il)benzoil]piperazin-1 -carbonil}ciclopropan-1 -ol;
1 -[(4-{[3-cloro-4-(1 -metil-1 H-indol-5-il)fenil]carbonil}piperazin-1 -il)carbonil]ciclopropan-1 -ol;
1 -[(4-{[2-cloro-4-(1 -metil-1 H-indol-5-il)fenil]carbonil}piperazin-1 -il)carbonil]ciclopropan-1 -ol;
1-[(4-{[4-(1 H-indol-4-il)fenil]carbonil}piperazin-1 -il}carbonil)ciclopropan-1-ol; y
1 -[(4-{[3-metil-4-(1 -metil-1 H-indol-5-il)fenil]carbonil}piperazin-1-il}carbonil)ciclopropan-1-ol.
32. Un compuesto de la reivindicación 31, en donde el compuesto es 1-[(4-{[2-fluoro-4-(1-metil-1H-indol-5-il)fenil]carbonil}piperazin-1 -il}carbonil)ciclopropan-1 -ol.
33. Un compuesto de la reivindicación 31, en donde el compuesto es 1-[(4-{[4-(isoquinolin-6-il)fenil]carbonil}piperazin-1 -il}carbonil)ciclopropan-1 -ol.
34. Un compuesto de la reivindicación 31, en donde el compuesto es 1-[(4-{[3-cloro-4-(quinolin-3-il)fenil]carbonil}piperazin-1 -il}carbonil)ciclopropan-1 -ol.
35. Un compuesto de la reivindicación 31, donde el compuesto es 5-[2-cloro-4-({4-[(1-hidroxiciclopropil}carbonil)piperazin-1-il}carbonil)fenil]-1 H-indol-3-carbonitril.
36. Un compuesto de la reivindicación 31, en donde el compuesto es 1-[(4-{[4-(quinolin-2-il)fenil]carbonil}piperazin-1-il}carbonil)ciclopropan-1 -ol.
37. Un compuesto de la reivindicación 31, donde el compuesto es 1-{4-[2-fluoro-4-(1-metil-1H-1,3-benzodiazol-5-il)benzoil]piperazina-1 -carbonil}ciclopropan-1 -ol.
38. Un compuesto de la reivindicación 31, en donde el compuesto es 1-[(4-{[3-cloro-4-(1-metil-1H-indol-5-il)fenil]carbonil}piperazin-1 -il}carbonil)ciclopropan-1 -ol.
39. Un compuesto de la reivindicación 31, en donde el compuesto es 1-[(4-{[2-cloro-4-(1-metil-1H-indol-5-il)fenil]carbonil}piperazin-1 -il}carbonil)ciclopropan-1 -ol.
40. Un compuesto de la reivindicación 31, en donde el compuesto es 1-[(4-{[4-(1H-indol-4-il)fenil]carbonil}piperazin-1 -il}carbonil)ciclopropan-1 -ol.
41. Un compuesto de la reivindicación 31, donde el compuesto 1 -[(4-{[3-metil-4-(1 -metil-1 H-indol-5-il)fenil]carbonil}piperazin-1 -il}carbonil)ciclopropan-1 -ol.
42. Una composición farmacéutica que comprende cantidades terapéuticamente eficaces de al menos un compuesto de cualquiera de las reivindicaciones 1 a 41, o una sal farmacéuticamente aceptable del mismo, y al menos un vehículo farmacéuticamente aceptable.
43. Al menos un compuesto de una cualquiera de las reivindicaciones 1 a 41, o una sal farmacéuticamente aceptable del mismo, para su uso en un método de inhibir la sintasa de ácido graso ("FASN") en un paciente mediante la administración de cantidades terapéuticamente eficaces de dicho al menos un compuesto, o una sus sales farmacéuticamente aceptables.
44. Una composición farmacéutica de la reivindicación 42 para uso en un método de inhibición de FASN en un paciente mediante la administración de cantidades terapéuticamente eficaces de dicha composición farmacéutica.
45. La composición farmacéutica de la reivindicación 42, que comprende además cantidades terapéuticamente eficaces de uno o más agentes terapéuticos adicionales.
46. La composición farmacéutica de la reivindicación 45, en donde dicho uno o más agentes terapéuticos adicionales son seleccionados de grupo que consiste en agente citotóxico, cisplatino, doxorrubicina, taxotere, taxol, etopósido, irinotecan, camptostar, topotecan, paclitaxel, docetaxel, las epotilonas, tamoxifeno, 5-fluorouracilo, metotrexato, temozolomida, ciclofosfamida, SCH66336, tipifarnib (Zarnestra®), R115777, L778,123, BMS 214662, Iressa®, Tarceva®, C225, GLEEVEC®, Intron®, Peg-Intron®, combinaciones de aromatasa, ara-C, adriamicina, Cytoxan, gemcitabina, mostaza de uracilo, clormetina, ifosfamida, melfalán, clorambucilo, pipobromán, trietilenmelamina, trietilentiofosforamina, busulfán, carmustina, lomustina, estreptozocina, dacarbazina, floxuridina, citarabina, 6-mercaptopurina, 6-tioguanina, fosfato de fludarabina, leucovirina, oxaliplatino (ELOXATIN®), pentostatina, vinblastina, vincristina, vindesina, bleomicina, dactinomicina, daunorubicina, epirubicina, idarubicina, Mitramycin™, desoxicoformicina, mitomicina-C-, L-asparaginasa, tenipósido 17a-Etinilestradiol, dietilestilbestrol, testosterona, prednisona, fluoximesterona, propionato de dromostanolona, testolactona, acetato de megestrol, metilprednisolona, metiltestosterona, prednisolona, triamcinolona, clorotrianiseno, hidroxiprogesterona, aminoglutetimida, estramustina, acetato de medroxiprogesterona, leuprolida, flutamida, toremifeno, goserelina, carboplatino, hidroxiurea, amsacrina, procarbazina, mitotano, mitoxantrona, levamisol, navelbeno, anastrazol, Letrazol, capecitabina, Reloxafina, Droloxafina, Hexametilmelamina, Avastin, Herceptin, Bexxar, Velcade, Zevalin, Trisenox, Xeloda, vinorelbina, Porfimer, Erbitux, liposomal, tiotepa, altretamina, melfalán, Trastuzumab, Lerozole, fulvestrant, exemestano, Rituximab, C225, Campath, leucovorina, dexametasona, bicalutamida, carboplatino, clorambucilo, cisplatino, letrozol, y megestrol,valrubicin.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201361779962P | 2013-03-13 | 2013-03-13 | |
| US201361779908P | 2013-03-13 | 2013-03-13 | |
| PCT/US2014/023388 WO2014164749A1 (en) | 2013-03-13 | 2014-03-11 | Novel compounds and compositions for inhibition of fasn |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2753386T3 true ES2753386T3 (es) | 2020-04-08 |
Family
ID=51658962
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES19188403T Active ES2861180T3 (es) | 2013-03-13 | 2014-03-11 | Derivados de 2-hidroxi-1-{4-[(4-fenil)fenil]carbonil}piperazin-1-il}etan-1-ona y compuestos relacionados como inhibidores de sintasa de ácido graso (FASN) para el tratamiento del cáncer |
| ES14779048T Active ES2753386T3 (es) | 2013-03-13 | 2014-03-11 | Derivados de 2-hidroxi-1-{4-[(4-fenil)fenil]carbonil}piperazin-1-il}etano-1-ona y compuestos relacionados como inhibidores de sintasa de ácido graso (FASN) para el tratamiento del cáncer |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES19188403T Active ES2861180T3 (es) | 2013-03-13 | 2014-03-11 | Derivados de 2-hidroxi-1-{4-[(4-fenil)fenil]carbonil}piperazin-1-il}etan-1-ona y compuestos relacionados como inhibidores de sintasa de ácido graso (FASN) para el tratamiento del cáncer |
Country Status (37)
| Country | Link |
|---|---|
| US (8) | US20160002188A1 (es) |
| EP (2) | EP3587406B1 (es) |
| JP (2) | JP2016517412A (es) |
| KR (1) | KR102194745B1 (es) |
| CN (2) | CN105492008B (es) |
| AU (3) | AU2014249003A1 (es) |
| BR (1) | BR112015023279B1 (es) |
| CA (1) | CA2905751A1 (es) |
| CL (1) | CL2015002698A1 (es) |
| CR (1) | CR20150541A (es) |
| CU (1) | CU24341B1 (es) |
| CY (1) | CY1122244T1 (es) |
| DK (1) | DK2968316T3 (es) |
| EC (1) | ECSP15043280A (es) |
| ES (2) | ES2861180T3 (es) |
| HK (1) | HK1220409A1 (es) |
| HR (1) | HRP20191860T1 (es) |
| HU (1) | HUE045701T2 (es) |
| IL (1) | IL241699B (es) |
| LT (1) | LT2968316T (es) |
| ME (1) | ME03564B (es) |
| MX (1) | MX364895B (es) |
| MY (1) | MY191366A (es) |
| NI (1) | NI201500141A (es) |
| NO (1) | NO20151329A1 (es) |
| PE (1) | PE20160122A1 (es) |
| PH (1) | PH12015502097A1 (es) |
| PL (1) | PL2968316T3 (es) |
| PT (1) | PT2968316T (es) |
| RS (1) | RS59411B1 (es) |
| RU (2) | RU2686323C2 (es) |
| SA (1) | SA515361086B1 (es) |
| SG (2) | SG10201707409PA (es) |
| SI (1) | SI2968316T1 (es) |
| TN (1) | TN2015000420A1 (es) |
| WO (2) | WO2014164749A1 (es) |
| ZA (1) | ZA201506922B (es) |
Families Citing this family (19)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN105492008B (zh) | 2013-03-13 | 2020-11-27 | 福马治疗股份有限公司 | 用于抑制fasn的化合物及组合物 |
| WO2014146747A1 (en) * | 2013-03-21 | 2014-09-25 | Merck Patent Gmbh | Piperazine derivatives as fasn inhibitors |
| JP6899323B2 (ja) * | 2014-10-14 | 2021-07-07 | ラ ホーヤ インスティテュート オブ アレルギー アンド イミュノロジー | 低分子量タンパク質チロシンホスファターゼの阻害剤、及びその使用 |
| EP3220901B1 (en) | 2014-11-20 | 2020-02-19 | VIB vzw | Means and methods for treatment of early-onset parkinson's disease |
| CN107847765B (zh) | 2015-06-18 | 2021-05-04 | 89生物有限公司 | 1,4-取代的哌啶衍生物 |
| JP6986972B2 (ja) | 2015-06-18 | 2021-12-22 | エイティナイン バイオ リミテッド | 置換4−ベンジル及び4−ベンゾイルピペリジン誘導体 |
| DK3458448T3 (da) * | 2016-04-25 | 2021-08-23 | Forma Therapeutics Inc | Fasn-inhibitorer til anvendelse til behandling af non-alkoholisk steatohepatitis |
| CN106806371A (zh) * | 2017-01-19 | 2017-06-09 | 伊希珍 | 一种化合物在制备治疗发作性睡病药物中的应用 |
| CN107056695A (zh) * | 2017-01-26 | 2017-08-18 | 青岛辰达生物科技有限公司 | 一种治疗胃癌药物阿帕替尼的合成方法 |
| EP3619210A4 (en) | 2017-05-01 | 2020-12-02 | Sanford Burnham Prebys Medical Discovery Institute | LOW MOLECULAR PROTEIN TYROSINE PHOSPHATASE (LMPTP) INHIBITORS AND USES THEREOF |
| US20210252011A1 (en) * | 2017-10-25 | 2021-08-19 | Forma Therapeutics, Inc. | Treatment of glioblastoma with fasn inhibitors |
| TWI767148B (zh) * | 2018-10-10 | 2022-06-11 | 美商弗瑪治療公司 | 抑制脂肪酸合成酶(fasn) |
| WO2020077071A1 (en) * | 2018-10-10 | 2020-04-16 | Forma Therapeutics, Inc. | Inhibiting fatty acid synthase (fasn) |
| US10793554B2 (en) | 2018-10-29 | 2020-10-06 | Forma Therapeutics, Inc. | Solid forms of 4-(2-fluoro-4-(1-methyl-1H-benzo[d]imidazol-5-yl)benzoyl)piperazin-1-yl)(1-hydroxycyclopropyl)methanone |
| WO2020092376A1 (en) * | 2018-10-29 | 2020-05-07 | Forma Therapeutics, Inc. | Treating non-alcoholic steatohepatitis (nash) |
| AU2019395201A1 (en) | 2018-12-06 | 2021-05-20 | Daiichi Sankyo Company, Limited | Cycloalkane-1,3-diamine derivative |
| WO2020191356A1 (en) * | 2019-03-21 | 2020-09-24 | Goncalves Marcus | Anti-fructose therapy for colorectal and small intestine cancers |
| CA3135502C (en) * | 2019-12-20 | 2024-01-09 | Josep Bassaganya-Riera | Lanthionine c-like protein 2 ligands, cells prepared therewith, and therapies using same |
| CN117203211A (zh) * | 2021-11-29 | 2023-12-08 | 中国海洋大学 | 咪唑并噻唑衍生物及其制备方法与应用 |
Family Cites Families (206)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5759837A (en) | 1989-01-17 | 1998-06-02 | John Hopkins University | Chemotherapy for cancer by inhibiting the fatty acid biosynthetic pathway |
| EP0385043A1 (en) * | 1989-02-28 | 1990-09-05 | Fabrica Espanola De Productos Quimicos Y Farmaceuticos, S.A. (Faes) | New derivatives of 4-substituted piperazines |
| HU209678B (en) | 1992-06-09 | 1994-10-28 | Richter Gedeon Vegyeszet | Process for producing biologically active eburnamenin-14-carbonyl-amino derivatives and pharmaceutical compositions containing them |
| US5376664A (en) | 1992-07-27 | 1994-12-27 | The Du Pont Merck Pharmaceutical Company | Unsymmetrical mono-3-nitro bis-naphthalimides as anticancer agents |
| CA2077252C (en) * | 1992-08-31 | 2001-04-10 | Khashayar Karimian | Methods of making ureas and guanidines, and intermediates therefor |
| US6083903A (en) | 1994-10-28 | 2000-07-04 | Leukosite, Inc. | Boronic ester and acid compounds, synthesis and uses |
| US5856326A (en) | 1995-03-29 | 1999-01-05 | Merck & Co., Inc. | Inhibitors of farnesyl-protein transferase |
| IL117580A0 (en) | 1995-03-29 | 1996-07-23 | Merck & Co Inc | Inhibitors of farnesyl-protein transferase and pharmaceutical compositions containing them |
| EP0869784B1 (en) | 1995-11-17 | 2005-08-31 | The Johns Hopkins University | Inhibition of fatty acid synthase as a means to reduce adipocyte mass |
| EP0922099B1 (en) | 1996-07-19 | 2004-09-08 | Takeda Chemical Industries, Ltd. | Fas ligand-like protein, its production and use |
| DE19743435A1 (de) * | 1997-10-01 | 1999-04-08 | Merck Patent Gmbh | Benzamidinderivate |
| US6413974B1 (en) | 1998-02-26 | 2002-07-02 | Aventis Pharmaceuticals Inc. | 6,9,-disubstituted 2-[trans-(4-aminocyclohexyl) amino] purines |
| AU769917B2 (en) | 1998-04-23 | 2004-02-12 | Duke University | Method of predicting the ability of compounds to modulate the biological activity of receptors |
| EP1589029B1 (en) | 1998-06-11 | 2010-03-17 | Ortho-McNeil Pharmaceuticals, Inc. | Pyrazinone protease inhibitors |
| JP2002523448A (ja) | 1998-08-28 | 2002-07-30 | サイオス インコーポレイテッド | p38−αキナーゼのインヒビター |
| WO2000022909A2 (en) | 1998-10-19 | 2000-04-27 | Biotech Australia Pty. Limited | Systems for oral delivery |
| CO5180605A1 (es) | 1999-06-23 | 2002-07-30 | Smithkline Beecham Corp | Compuestos de indol |
| CO5190665A1 (es) | 1999-06-23 | 2002-08-29 | Smithkline Beecham Corp | Compuestos de indol |
| CN1217932C (zh) | 1999-08-10 | 2005-09-07 | 英国生物技术药物有限公司 | 抗菌剂 |
| EP1206464A4 (en) | 1999-08-23 | 2002-12-18 | Smithkline Beecham Corp | FATTY ACID SYNTHASE INHIBITORS |
| WO2001014362A1 (en) | 1999-08-23 | 2001-03-01 | Smithkline Beecham Corporation | Fatty acid synthase inhibitors |
| AR029001A1 (es) | 1999-08-23 | 2003-06-04 | Smithkline Beecham Corp | Derivados de bencil-3,4-metilendioxicinamico y el uso de los mismos para la manufactura de un medicamento |
| US6541477B2 (en) * | 1999-08-27 | 2003-04-01 | Scios, Inc. | Inhibitors of p38-a kinase |
| AU6715200A (en) | 1999-09-04 | 2001-04-10 | Astrazeneca Ab | Amides as inhibitors for pyruvate dehydrogenase |
| US6486211B1 (en) | 1999-10-22 | 2002-11-26 | Smithkline Beecham Corporation | Indole compounds |
| EP1242075A4 (en) | 1999-10-22 | 2002-12-04 | Smithkline Beecham Corp | indole compounds |
| CA2391534A1 (en) | 1999-11-15 | 2001-05-25 | Drug Innovation & Design, Inc. | Selective cellular targeting: multifunctional delivery vehicles |
| EP1255567A1 (en) | 1999-11-15 | 2002-11-13 | Drug Innovation & Design, Inc. | Selective cellular targeting: multifunctional delivery vehicles |
| AU1607501A (en) | 1999-11-15 | 2001-05-30 | Drug Innovation & Design, Inc. | Selective cellular targeting: multifunctional delivery vehicles |
| EP1299376A1 (en) | 2000-05-24 | 2003-04-09 | Smithkline Beecham | Fatty acid synthase inhibitors |
| EP1164374A1 (en) | 2000-06-16 | 2001-12-19 | Max-Planck-Gesellschaft zur Förderung der Wissenschaften e.V. | Method for identifying apoptosis-modified proteins |
| US20040022779A1 (en) | 2000-06-16 | 2004-02-05 | Thomas Rudel | Method for identifying apoptosis-modified proteins |
| AU2001270200A1 (en) | 2000-06-27 | 2002-01-08 | Smith Kline Beecham Corporation | Fatty acid synthase inhibitors |
| AU2001271531A1 (en) | 2000-06-27 | 2002-01-08 | Smith Kline Beecham Corporation | Fatty acid synthase inhibitors |
| WO2002002119A1 (en) | 2000-06-29 | 2002-01-10 | Smithkline Beecham Corporation | Fatty acid synthase inhibitors |
| WO2002009688A1 (en) | 2000-08-02 | 2002-02-07 | Smithkline Beecham Corporation | Fatty acid synthase inhibitors |
| WO2002009651A2 (en) | 2000-08-02 | 2002-02-07 | Smithkline Beecham Corporation | Fatty acid synthase inhibitors |
| JP2004513887A (ja) | 2000-09-22 | 2004-05-13 | スミスクライン・ビーチャム・コーポレイション | 脂肪酸合成酵素阻害剤 |
| JPWO2002026745A1 (ja) | 2000-09-29 | 2004-02-05 | 日本曹達株式会社 | チエノピリミジン化合物とその塩並びに製造方法 |
| AU2001294824A1 (en) * | 2000-09-29 | 2002-04-08 | Millennium Pharmaceuticals, Inc. | Piperazine based inhibitors of factor xa |
| US20070208087A1 (en) * | 2001-11-02 | 2007-09-06 | Sanders Virginia J | Compounds, compositions and methods for the treatment of inflammatory diseases |
| WO2002055661A2 (en) | 2000-11-17 | 2002-07-18 | Smithkline Beecham Corporation | Fatty acid synthase inhibitors |
| EP1401469A2 (en) | 2001-04-09 | 2004-03-31 | Lorantis Limited | Therapeutic use and identification of modulators of a hedgehog signalling pathway or one of its target pathways |
| WO2002095007A2 (en) | 2001-05-23 | 2002-11-28 | Dendreon San Diego Llc | Conjugates activated by cell surface proteases and therapeutic uses thereof |
| GB0115109D0 (en) | 2001-06-21 | 2001-08-15 | Aventis Pharma Ltd | Chemical compounds |
| FR2829766A1 (fr) | 2001-09-14 | 2003-03-21 | Lipha | Derives d'oxamates comportant un heterocycle azote diversement substitue |
| US7309788B2 (en) | 2001-09-21 | 2007-12-18 | Boryung Pharmaceutical Co., Ltd. | Method for preparing pyrimidinone compound and pharmaceutically acceptable salts thereof |
| WO2003053366A2 (en) | 2001-12-20 | 2003-07-03 | Osi Pharmaceuticals, Inc. | Pyrimidine a2b selective antagonist compounds, their synthesis and use |
| US20030170244A1 (en) | 2001-12-21 | 2003-09-11 | Pluenneke John D. | Inhibition of Fas signaling |
| US20050119251A1 (en) | 2001-12-21 | 2005-06-02 | Jian-Min Fu | Nicotinamide derivatives and their use as therapeutic agents |
| US20030232863A1 (en) | 2002-03-05 | 2003-12-18 | Bayly Christopher I. | Cathepsin cysteine protease inhibitors |
| US7728153B2 (en) | 2002-04-17 | 2010-06-01 | The Burnham Institute For Medical Research | Method for the asymmetric synthesis of beta-lactone compounds |
| AU2003226370A1 (en) | 2002-04-17 | 2003-11-03 | The Burnham Institute | Inhibition of fatty acid synthase by beta-lactones and other compounds for inhibition of cellular proliferation |
| BR0309475A (pt) | 2002-04-23 | 2005-03-01 | Shionogi & Co | Derivados de pirazolo-[1,5-a]-pirimidina e inibidores de nad(p)h oxidase que contêm os mesmos |
| US20040001801A1 (en) | 2002-05-23 | 2004-01-01 | Corvas International, Inc. | Conjugates activated by cell surface proteases and therapeutic uses thereof |
| EP1539730A4 (en) | 2002-07-09 | 2007-03-28 | Fasgen Inc | NEW COMPOUNDS, PHARMACEUTICAL COMPOSITIONS CONTAINING THEM AND METHOD FOR THEIR APPLICATION |
| AU2003253925A1 (en) | 2002-07-18 | 2004-02-09 | Banyu Pharmaceutical Co., Ltd. | Combination therapy for the treatment of obesity |
| US20040132726A1 (en) | 2002-08-09 | 2004-07-08 | Astrazeneca Ab And Nps Pharmaceuticals, Inc. | New compounds |
| JP2006505531A (ja) | 2002-09-11 | 2006-02-16 | メルク エンド カムパニー インコーポレーテッド | メラノコルチン−4受容体作働薬としてのピペラジン尿素誘導体 |
| WO2004030637A2 (en) | 2002-10-01 | 2004-04-15 | Merck & Co., Inc. | Treatment of obesity and other disorders associated with excessive food intake |
| EP1554260A1 (en) | 2002-10-22 | 2005-07-20 | Glaxo Group Limited | Aryloxyalkylamine derivatives as h3 receptor ligands |
| CA2508487A1 (en) | 2002-12-04 | 2004-06-17 | Merck & Co., Inc. | Phenylalanine derivatives as dipeptidyl peptidase inhibitors for the treatment or prevention of diabetes |
| US20040122033A1 (en) | 2002-12-10 | 2004-06-24 | Nargund Ravi P. | Combination therapy for the treatment of obesity |
| WO2004110375A2 (en) | 2003-06-06 | 2004-12-23 | Merck & Co., Inc. | Combination therapy for the treatment of diabetes |
| WO2004110368A2 (en) | 2003-06-06 | 2004-12-23 | Merck & Co., Inc. | Combination therapy for the treatment of hypertension |
| US20060148721A1 (en) | 2003-06-06 | 2006-07-06 | Erondu Ngozi E | Combination therapy for the treatment of dyslipidemia |
| EP1648457A2 (en) | 2003-07-22 | 2006-04-26 | Merck & Co., Inc. | Piperidine derivatives as melanocortin-4 receptor agonists |
| US20050043300A1 (en) * | 2003-08-14 | 2005-02-24 | Pfizer Inc. | Piperazine derivatives |
| EP1663234A1 (en) | 2003-08-14 | 2006-06-07 | Pfizer Limited | Piperazine derivatives for the treatment of hiv infections |
| WO2005035534A1 (ja) | 2003-10-08 | 2005-04-21 | Ono Pharmaceutical Co., Ltd. | 複素ビシクロ環および複素トリシクロ環化合物およびその医薬 |
| GB0326029D0 (en) * | 2003-11-07 | 2003-12-10 | Astrazeneca Ab | Chemical compounds |
| WO2005073186A1 (ja) * | 2004-01-29 | 2005-08-11 | Ono Pharmaceutical Co., Ltd. | ピロリジン誘導体 |
| TW200528101A (en) * | 2004-02-03 | 2005-09-01 | Astrazeneca Ab | Chemical compounds |
| PL1751131T3 (pl) | 2004-03-10 | 2009-04-30 | Janssen Pharmaceutica Nv | Arylopiperydyny lub -piperazyny podstawione 5-członowymi heterocyklilami jako inhibitory MTP |
| PE20060285A1 (es) * | 2004-03-30 | 2006-05-08 | Aventis Pharma Inc | Piridonas sustituidas como inhibidores de pol(adp-ribosa)-polimerasa (parp) |
| DE602005018758D1 (de) | 2004-04-01 | 2010-02-25 | Lilly Co Eli | Am histamin-h3-rezeptor wirksame mittel, herstellung und therapeutische anwendungen |
| US8008301B2 (en) | 2004-04-01 | 2011-08-30 | Eli Lilly And Company | Histamine H3 receptor agents, preparation and therapeutic uses |
| CA2562130C (en) | 2004-04-12 | 2011-06-07 | Torrent Pharmaceuticals Ltd. | 2-propene-1-ones as hsp 70 inducers |
| CA2565599C (en) * | 2004-05-18 | 2012-07-31 | Schering Corporation | Substituted 2-quinolyl-oxazoles useful as pde4 inhibitors |
| US20050261292A1 (en) | 2004-05-19 | 2005-11-24 | Solvay Pharmaceuticals Gmbh | Pharmaceutical composition containing N-sulfamoyl-N'-arylpiperazines for the treatment or inhibition of obesity and related conditions |
| JP2007538054A (ja) | 2004-05-19 | 2007-12-27 | ゾルファイ ファーマスーティカルズ ゲゼルシャフト ミット ベシュレンクテル ハフツング | 肥満および関係する病気の予防または治療のためのn−スルファモイル−n′−アリールピペラジンを含有する薬剤 |
| WO2005116006A1 (ja) | 2004-05-28 | 2005-12-08 | Riken | フラーレン誘導体の製造方法 |
| CA2577191A1 (en) | 2004-08-26 | 2006-03-02 | Kudos Pharmaceuticals Limited | 4-heteroarylmethyl substituted phthalazinone derivatives |
| JP5149009B2 (ja) | 2004-09-20 | 2013-02-20 | ゼノン・ファーマシューティカルズ・インコーポレイテッド | ヒトステアロイル−CoAデサチュラーゼを阻害するためのピリダジン誘導体 |
| BRPI0516958A (pt) | 2004-09-20 | 2008-03-25 | 4Sc Ag | inibidores da nf-capab heterocìclicos |
| CA2577821A1 (en) | 2004-09-24 | 2006-04-06 | Merck & Co., Inc. | Combination therapy for the treatment of obesity |
| EP1799684B1 (en) | 2004-10-04 | 2014-12-03 | Millennium Pharmaceuticals, Inc. | Lactam compounds useful as protein kinase inhibitors |
| US20080200376A1 (en) | 2004-10-29 | 2008-08-21 | Maccoss Malcolm | Compositions and Methods For the Treatment Of Obesity and Sexual Dysfunction |
| FR2877667B1 (fr) | 2004-11-05 | 2007-03-23 | Sod Conseils Rech Applic | Derives de 4,7-dioxobenzothiazole-2-carboxamides, leur preparation et leurs applications therapeutiques |
| JP5254620B2 (ja) | 2004-12-03 | 2013-08-07 | メルク・シャープ・アンド・ドーム・コーポレーション | Cb1アンタゴニストとしての置換ピペラジン |
| FR2879598B1 (fr) | 2004-12-17 | 2007-03-30 | Sod Conseils Rech Applic | Inhibiteurs de phosphatases cdc25 |
| EP1884513A4 (en) | 2005-05-23 | 2010-04-28 | Japan Tobacco Inc | PYRAZOLE COMPOUND AND THERAPEUTIC AGENT FOR DIABETES COMPRISING THE SAME |
| US20060270650A1 (en) | 2005-05-26 | 2006-11-30 | Macneil Tanya | Combination therapy for the treatment of obesity |
| ES2337728T3 (es) | 2005-06-20 | 2010-04-28 | Schering Corporation | Piperidinas sustituidas unidas a carbono y sus derivados utiles como antagonistas de histamina h3. |
| GB0518237D0 (en) | 2005-09-07 | 2005-10-19 | Angeletti P Ist Richerche Bio | Therapeutic compounds |
| US7473688B2 (en) | 2005-09-13 | 2009-01-06 | Bristol-Myers Squibb Company | Indolobenzazepine HCV NS5B inhibitors |
| CN101272685A (zh) | 2005-09-27 | 2008-09-24 | Irm责任有限公司 | 包含二芳基胺的化合物和组合物以及它们作为c-kit受体调节剂的用途 |
| CN101346357B (zh) | 2005-10-25 | 2014-04-02 | 盐野义制药株式会社 | 氨基二氢噻嗪衍生物 |
| EP1948636A2 (en) | 2005-11-14 | 2008-07-30 | Irm Llc | Compounds and compositions as lxr modulators |
| ATE449776T1 (de) | 2005-12-15 | 2009-12-15 | Hoffmann La Roche | Pyrroloä2,3-cüpyridinderivate |
| ATE467632T1 (de) | 2005-12-16 | 2010-05-15 | Hoffmann La Roche | Pyrroloä2,3-büpyridinderivate als modulatoren des h3-rezeptors |
| KR20080080201A (ko) | 2005-12-21 | 2008-09-02 | 쉐링 코포레이션 | 히스타민 h3 길항제로서 유용한 치환된 아닐린 유도체 |
| CN101426777A (zh) | 2005-12-21 | 2009-05-06 | 先灵公司 | 用作组胺h3拮抗剂的苯氧基哌啶及其类似物 |
| US20070203236A1 (en) | 2006-01-11 | 2007-08-30 | Smith Jeffrey W | Novel antagonists of the human fatty acid synthase thioesterase |
| US8008354B2 (en) | 2006-01-11 | 2011-08-30 | Burnham Institute For Medical Research | Death receptor sensitizing compounds and methods of use therefor |
| BRPI0707916A2 (pt) | 2006-01-13 | 2011-05-17 | Hoffmann La Roche | compostos, processo para a sua manufatura, composições farmacêuticas que os compreendem e uso destes compostos |
| CA2637717A1 (en) | 2006-01-20 | 2007-08-02 | Schering Corporation | Heterocycles as nicotinic acid receptor agonists for the treatment of dyyslipidemia |
| JP5031771B2 (ja) | 2006-01-23 | 2012-09-26 | エフ.ホフマン−ラ ロシュ アーゲー | H3受容体活性を有するシクロヘキシルスルホンアミド誘導体 |
| US20090048276A1 (en) | 2006-01-30 | 2009-02-19 | Goulet Mark T | Inhibitors of Fatty Acid Synthase (Fas) |
| US7807671B2 (en) | 2006-04-25 | 2010-10-05 | Bristol-Myers Squibb Company | Diketo-piperazine and piperidine derivatives as antiviral agents |
| US7601716B2 (en) | 2006-05-01 | 2009-10-13 | Cephalon, Inc. | Pyridopyrazines and derivatives thereof as ALK and c-Met inhibitors |
| JP2009538859A (ja) | 2006-05-30 | 2009-11-12 | エフ.ホフマン−ラ ロシュ アーゲー | ピペリジニルピリミジン誘導体 |
| GB0610680D0 (en) | 2006-05-31 | 2006-07-12 | Istituto Di Ricerche D Biolog | Therapeutic compounds |
| AU2007266840B2 (en) | 2006-05-31 | 2012-09-20 | Istituto Di Ricerche Di Biologia Molecolare P. Angeletti Spa | Pyrrolo[1,2-A]pyrazin-1(2H)-one and pyrrolo[1,2-D][1,2,4]triazin-1(2H)-one derivatives as inhibitors of poly(ADP-ribose)polymerase(PARP) |
| US8088923B2 (en) | 2006-07-07 | 2012-01-03 | The Texas A&M University System | Cyclic-fused beta-lactones and their synthesis |
| EP2051977A2 (en) * | 2006-07-20 | 2009-04-29 | Amgen Inc. | SUBSTITUTED AZOLE AROMATIC HETEROCYCLES AS INHIBITORS OF LLbeta-HSD-1 |
| JPWO2008023720A1 (ja) * | 2006-08-23 | 2010-01-14 | アステラス製薬株式会社 | ウレア化合物又はその塩 |
| CA2662337A1 (en) | 2006-09-05 | 2008-03-13 | Bipar Sciences, Inc. | Inhibition of fatty acid synthesis by parp inhibitors and methods of treatment thereof |
| CA2664113C (en) | 2006-09-22 | 2013-05-28 | Merck & Co., Inc. | Use of platencin and platensimycin as fatty acid synthesis inhibitors to treat obesity, diabetes and cancer |
| JO2653B1 (en) | 2006-10-24 | 2012-06-17 | شركة جانسين فارماسوتيكا ان. في | Tetrahydroflavin 1-carboxylic acid substituted with pyridine or pyrazine inhibit MTB |
| RU2009120679A (ru) | 2006-11-02 | 2010-12-10 | Санофи-Авентис Дойчланд Гмбх (De) | Новый дифенилазетидинон, замещенный пиперазин-1-сульфокислотой, обладающий улучшенными фармакологическими свойствами |
| WO2008059214A1 (en) | 2006-11-13 | 2008-05-22 | Astrazeneca Ab | Bisamlde derivatives and use thereof as fatty acid synthase inhibitors |
| CN101190894A (zh) | 2006-11-23 | 2008-06-04 | 中国人民解放军军事医学科学院毒物药物研究所 | 脂肪酸合成酶抑制剂及其制药用途 |
| WO2008066789A2 (en) | 2006-11-27 | 2008-06-05 | H. Lundbeck A/S | Heteroaryl amide derivatives |
| CN101679297B (zh) | 2006-12-08 | 2012-01-11 | 埃克塞利希斯股份有限公司 | Lxr和fxr调节剂 |
| TW200833663A (en) | 2006-12-21 | 2008-08-16 | Astrazeneca Ab | Therapeutic agents |
| WO2008075077A1 (en) | 2006-12-21 | 2008-06-26 | Astrazeneca Ab | Piperidine derivatives for the treatment of obesity |
| TW200831092A (en) | 2006-12-21 | 2008-08-01 | Astrazeneca Ab | Therapeutic agents |
| US8466150B2 (en) | 2006-12-28 | 2013-06-18 | Abbott Laboratories | Inhibitors of poly(ADP-ribose)polymerase |
| DE102007007751A1 (de) | 2007-02-16 | 2008-08-21 | Boehringer Ingelheim Pharma Gmbh & Co. Kg | Neue substituierte Arylsulfonylglycine, deren Herstellung und deren Verwendung als Arzneimittel |
| ES2369440T3 (es) | 2007-02-28 | 2011-11-30 | Conatus Pharmaceuticals, Inc. | Método para el tratamiento de la hepatitis viral de tipo c crónica usando ro 113-0830. |
| PL2144604T3 (pl) | 2007-02-28 | 2012-02-29 | Conatus Pharmaceuticals Inc | Sposoby leczenia przewlekłego zapalenia wątroby typu C z zastosowaniem RO 113-0830 |
| WO2008106167A1 (en) | 2007-02-28 | 2008-09-04 | Conatus Pharmaceuticals, Inc. | Combination therapy comprising matrix metalloproteinase inhibitors and caspase inhibitors for the treatment of liver diseases |
| JP2010520291A (ja) | 2007-03-07 | 2010-06-10 | コンサート ファーマシューティカルズ インコーポレイテッド | 抗狭心症化合物としての重水素化ピペラジン誘導体 |
| BRPI0809680A2 (pt) | 2007-03-30 | 2014-10-07 | Hoffmann La Roche | Compostos, processo para a sua manufatura, composições farmacêuticas que os compreendem, método para o tratamento terapêutico e/ou profilático de enfermidades que são moduladas por agonistas de lxr alfa e/ou lxr beta e uso dos compostos. |
| US7682857B2 (en) | 2007-04-16 | 2010-03-23 | Mitsubishi Electric Corporation | Method for manufacturing semiconductor optical device |
| EP2151435A4 (en) | 2007-04-24 | 2011-09-14 | Shionogi & Co | PHARMACEUTICAL COMPOSITION FOR THE TREATMENT OF ALZHEIMER'S DISEASE |
| JP2010525062A (ja) | 2007-04-25 | 2010-07-22 | エグゼリクシス, インコーポレイテッド | Pimモジュレーターとしてのピリミジノン類 |
| KR20100047190A (ko) | 2007-06-13 | 2010-05-07 | 오스펙스 파마슈티칼스, 인코포레이티드 | 치환 피페라진 |
| NZ582760A (en) * | 2007-06-21 | 2011-12-22 | Cara Therapeutics Inc | Substituted imidazoheterocycles |
| EP2019091A1 (en) | 2007-06-25 | 2009-01-28 | Fundació Privada Institut d'Investigació Biomédica de Girona - Dr. Josep Trueta | Novel polyhydroxylated compounds as Fatty Acid Synthase (FASN) inhibitors |
| US20090023727A1 (en) | 2007-07-05 | 2009-01-22 | Muhammad Hashim Javaid | Phthalazinone derivatives |
| US8314091B2 (en) | 2007-08-20 | 2012-11-20 | Msd Oss B.V. | N-benzyl,N'-arylcarbonylpiperazine derivatives |
| MX2010003868A (es) * | 2007-10-09 | 2010-04-27 | Hoffmann La Roche | Cis-imidazolinas quirales. |
| JP2011503620A (ja) | 2007-11-13 | 2011-01-27 | ファスゲン ダイアグノスティクス,リミティド ライアビリティ カンパニー | リン酸化脂肪酸シンターゼ及び癌 |
| AU2008345225A1 (en) | 2007-12-21 | 2009-07-09 | University Of Rochester | Method for altering the lifespan of eukaryotic organisms |
| EP2247600A4 (en) * | 2008-02-06 | 2011-09-14 | Biomarin Pharm Inc | BENZOXAZOLEBOXYLIC ACID AMIDE AS INHIBITORS OF POLY (ADP-RIBOSE) POLYMERASE (PARP) |
| WO2009098282A1 (en) * | 2008-02-06 | 2009-08-13 | Novasaid Ab | Low molecular weight 2,5-disubstituted thiophene derivatives and use thereof in therapy |
| US8129398B2 (en) | 2008-03-19 | 2012-03-06 | Bristol-Myers Squibb Company | HIV integrase inhibitors |
| US8871753B2 (en) | 2008-04-24 | 2014-10-28 | Incyte Corporation | Macrocyclic compounds and their use as kinase inhibitors |
| TW201006816A (en) | 2008-05-15 | 2010-02-16 | Organon Nv | Hexafluoroisopropanol derivatives |
| WO2009143404A1 (en) | 2008-05-23 | 2009-11-26 | Wyeth | Piperazine metabotropic glutamate receptor 5 (mglur5) negative allosteric modulators for anxiety/depression |
| WO2009151910A2 (en) | 2008-05-25 | 2009-12-17 | Wyeth | Combination product of receptor tyrosine kinase inhibitor and fatty acid synthase inhibitor for treating cancer |
| PT2326650E (pt) * | 2008-08-06 | 2014-05-06 | Biomarin Pharm Inc | Inibidores de di-hidropiridoftalazinona de poli(adpribose) polimerase (parp) |
| TW201022230A (en) | 2008-08-28 | 2010-06-16 | Organon Nv | 1-(4-ureidobenzoyl)piperazine derivatives |
| AU2009314629B2 (en) | 2008-11-14 | 2014-09-25 | The Scripps Research Institute | Methods and compositions related to targeting monoacylglycerol lipase |
| EP2414348B1 (en) | 2009-04-03 | 2013-11-20 | Merck Sharp & Dohme Corp. | Bicyclic piperidine and piperazine derivatives as gpcr modulators for the treatment of obesity, diabetes and other metabolic disorders |
| CA2759098A1 (en) | 2009-04-14 | 2010-10-21 | Smith Holdings, Llc | Methods and compositions for the treatment of medical conditions involving cellular programming |
| AU2010254161A1 (en) | 2009-05-27 | 2011-11-10 | F. Hoffmann-La Roche Ag | Bicyclic pyrimidine PI3K inhibitor compounds selective for p110 delta, and methods of use |
| CA2764526A1 (en) | 2009-06-24 | 2010-12-29 | Christine Kritikou | The use of spinosyns and spinosyn compositions against diseases caused by protozoans, viral infections and cancer |
| WO2011035018A2 (en) | 2009-09-18 | 2011-03-24 | Fate Therapeutics, Inc. | Suicide ready cells |
| WO2011037793A1 (en) | 2009-09-25 | 2011-03-31 | Merck Sharp & Dohme Corp. | Substituted aminopiperidines as dipeptidyl peptidase-iv inhibitors for the treatment of diabetes |
| BR112012006802A2 (pt) | 2009-09-28 | 2020-08-18 | F.Hoffmann-La Roche Ag | composto, composição farmacêutica, método para tratar câncer, usos de um composto, kit e invenção |
| EP2485728B1 (en) | 2009-10-07 | 2013-07-10 | Siena Biotech S.p.a. | Wnt pathway antagonists |
| US20120208827A1 (en) | 2009-10-27 | 2012-08-16 | Glaxosmithkline Llc | Benzimidazoles as fatty acid synthase inhibitors |
| WO2011053821A1 (en) | 2009-10-30 | 2011-05-05 | Tranzyme Pharma, Inc. | Macrocyclic ghrelin receptor antagonists and inverse agonists and methods of using the same |
| EP2503890A4 (en) | 2009-11-24 | 2013-05-15 | Glaxosmithkline Llc | AZABENZIMIDAZOLE AS A FATTY ACID SYNTHESIS HEMMER |
| MX2012009720A (es) | 2010-02-22 | 2012-10-09 | Glaxosmithkline Llc | Triazolonas como inhibidores de acido graso sintasa. |
| WO2011140296A1 (en) | 2010-05-05 | 2011-11-10 | Infinity Pharmaceuticals | Triazoles as inhibitors of fatty acid synthase |
| EP2566853B1 (en) | 2010-05-05 | 2017-01-25 | Infinity Pharmaceuticals, Inc. | Tetrazolones as inhibitors of fatty acid synthase |
| JP5925770B2 (ja) | 2010-06-24 | 2016-05-25 | トラスティーズ オブ タフツ カレッジ | ナイアシン模倣体、およびその使用方法 |
| CN103096895B (zh) | 2010-06-24 | 2016-06-01 | 塔夫茨大学信托人 | 烟酸模拟物及其使用的方法 |
| SG186850A1 (en) | 2010-07-29 | 2013-02-28 | Rigel Pharmaceuticals Inc | Ampk-activating heterocyclic compounds and methods for using the same |
| CN102372698A (zh) | 2010-08-10 | 2012-03-14 | 江苏恒瑞医药股份有限公司 | 酞嗪酮类衍生物、其制备方法及其在医药上的应用 |
| US20130172384A1 (en) | 2010-09-17 | 2013-07-04 | Glaxosmithkline Intellectual Property Development Limited | Fatty acid synthase inhibitors |
| EP2615918A4 (en) | 2010-09-17 | 2014-01-29 | Glaxosmithkline Ip Dev Ltd | INHIBITORS OF ACID GRAS SYNTHASE |
| US20130237535A1 (en) | 2010-11-08 | 2013-09-12 | Nicholas D. Adams | Fatty acid synthase inhibitors |
| WO2012064632A1 (en) * | 2010-11-12 | 2012-05-18 | Wake Forest University Health Sciences | Methods of treating cancer and other disorders |
| SG10201602857UA (en) | 2010-11-15 | 2016-05-30 | Abbvie Inc | NAMPT And Rock Inhibitors |
| US20140243401A1 (en) | 2010-11-24 | 2014-08-28 | The Johns Hopkins University | Methods of screening compounds that are cytotoxic to tumor cells and methods of treating tumor cells using such compound |
| TWI549947B (zh) | 2010-12-29 | 2016-09-21 | 阿吉歐斯製藥公司 | 治療化合物及組成物 |
| JP2014515345A (ja) | 2011-01-10 | 2014-06-30 | グラクソスミスクライン・リミテッド・ライアビリティ・カンパニー | 脂肪酸シンターゼ阻害剤としてのピリミジノン誘導体 |
| WO2012101013A1 (en) | 2011-01-28 | 2012-08-02 | Boehringer Ingelheim International Gmbh | Substituted pyridinyl-pyrimidines and their use as medicaments |
| AR086837A1 (es) | 2011-03-08 | 2014-01-29 | 3 V Biosciences Inc | Moduladores heterociclicos de sintesis lipidica |
| KR101930106B1 (ko) | 2011-03-08 | 2018-12-17 | 3-브이 바이오사이언시스, 인코포레이티드 | 지질 합성의 헤테로사이클릭 조절자 |
| EP2686305B1 (en) | 2011-03-14 | 2020-09-16 | Impact Therapeutics, Inc. | Quinazolinediones and their use |
| TWI527800B (zh) | 2011-04-01 | 2016-04-01 | 南京英派藥業有限公司 | 作為聚(二磷酸腺苷酸-核醣)聚合酶(parp)之抑制劑之1-(芳基甲基)喹唑啉-2,4(1h,3h)-二酮及其應用 |
| CN103608016A (zh) | 2011-05-03 | 2014-02-26 | 安吉奥斯医药品有限公司 | 丙酮酸激酶激活剂在治疗中的用途 |
| FI3406251T3 (fi) | 2011-05-03 | 2024-02-21 | Agios Pharmaceuticals Inc | Pyruvaattikinaasin aktivaattoreita terapeuttista käyttöä varten |
| WO2013028445A1 (en) * | 2011-08-19 | 2013-02-28 | Glaxosmithkline Llc | Fatty acid synthase inhibitors |
| WO2013028495A1 (en) * | 2011-08-19 | 2013-02-28 | Biomarin Pharmaceutical Inc. | Dihydropyridophthalazinone inhibitors of poly (adp-ribose) polymerase (parp) for the treatment of multiple myeloma |
| BR112014004845A2 (pt) * | 2011-08-30 | 2017-04-04 | Chdi Foundation Inc | pelo menos uma entidade química; pelo menos um composto; composição farmacêutica; uso de uma quantidade terapeuticamente eficaz de pelo menos uma entidade química; composição farmacêutica embalada |
| EP2760862B1 (en) | 2011-09-27 | 2015-10-21 | Sanofi | 6-(4-hydroxy-phenyl)-3-alkyl-1h-pyrazolo[3,4-b]pyridine-4-carboxylic acid amide derivatives as kinase inhibitors |
| WO2013060636A1 (en) | 2011-10-25 | 2013-05-02 | Sanofi | 6-(4-hydroxy-phenyl)-1h-pyrazolo[3,4-b]pyridine-4-carboxylic acid amide derivatives as kinase inhibitors |
| WO2013064083A1 (en) | 2011-11-01 | 2013-05-10 | Impact Therapeutics, Inc. | 1-(arylmethyl)-5,6,7,8-tetrahydroquinazoline-2,4-diones and analogs and the use thereof |
| CN103130723B (zh) | 2011-11-30 | 2015-01-14 | 成都地奥制药集团有限公司 | 一种多聚(adp-核糖)聚合酶抑制剂 |
| CN102627610B (zh) * | 2012-04-11 | 2014-06-25 | 江苏先声药物研究有限公司 | 一类苯并咪唑类衍生物及其应用 |
| US9096579B2 (en) | 2012-04-20 | 2015-08-04 | Boehringer Ingelheim International Gmbh | Amino-indolyl-substituted imidazolyl-pyrimidines and their use as medicaments |
| CN103420890B (zh) | 2012-05-15 | 2015-06-24 | 天津药物研究院 | 3-吡咯甲酸衍生物及其制备方法和用途 |
| AR092211A1 (es) * | 2012-09-24 | 2015-04-08 | Merck Patent Ges Mit Beschränkter Haftung | Derivados de hidropirrolopirrol |
| CN105492008B (zh) | 2013-03-13 | 2020-11-27 | 福马治疗股份有限公司 | 用于抑制fasn的化合物及组合物 |
| WO2014146747A1 (en) | 2013-03-21 | 2014-09-25 | Merck Patent Gmbh | Piperazine derivatives as fasn inhibitors |
| CN105392785B (zh) | 2013-07-29 | 2017-12-22 | 默克专利股份公司 | 1,3‑二取代的环戊烷衍生物 |
| JP6986972B2 (ja) | 2015-06-18 | 2021-12-22 | エイティナイン バイオ リミテッド | 置換4−ベンジル及び4−ベンゾイルピペリジン誘導体 |
| CN107847765B (zh) | 2015-06-18 | 2021-05-04 | 89生物有限公司 | 1,4-取代的哌啶衍生物 |
| DK3458448T3 (da) | 2016-04-25 | 2021-08-23 | Forma Therapeutics Inc | Fasn-inhibitorer til anvendelse til behandling af non-alkoholisk steatohepatitis |
-
2014
- 2014-03-11 CN CN201480028031.6A patent/CN105492008B/zh not_active Expired - Fee Related
- 2014-03-11 ME MEP-2019-282A patent/ME03564B/me unknown
- 2014-03-11 CU CUP2015000120A patent/CU24341B1/es unknown
- 2014-03-11 SG SG10201707409PA patent/SG10201707409PA/en unknown
- 2014-03-11 SG SG11201507486SA patent/SG11201507486SA/en unknown
- 2014-03-11 MX MX2015012470A patent/MX364895B/es active IP Right Grant
- 2014-03-11 SI SI201431348T patent/SI2968316T1/sl unknown
- 2014-03-11 ES ES19188403T patent/ES2861180T3/es active Active
- 2014-03-11 PE PE2015001983A patent/PE20160122A1/es not_active Application Discontinuation
- 2014-03-11 PT PT147790489T patent/PT2968316T/pt unknown
- 2014-03-11 CA CA2905751A patent/CA2905751A1/en not_active Abandoned
- 2014-03-11 LT LT14779048T patent/LT2968316T/lt unknown
- 2014-03-11 CN CN202011251734.9A patent/CN112521369A/zh active Pending
- 2014-03-11 WO PCT/US2014/023388 patent/WO2014164749A1/en active Application Filing
- 2014-03-11 HU HUE14779048A patent/HUE045701T2/hu unknown
- 2014-03-11 DK DK14779048.9T patent/DK2968316T3/da active
- 2014-03-11 RU RU2015141772A patent/RU2686323C2/ru active
- 2014-03-11 EP EP19188403.0A patent/EP3587406B1/en active Active
- 2014-03-11 WO PCT/US2014/023420 patent/WO2014164767A1/en active Application Filing
- 2014-03-11 BR BR112015023279-5A patent/BR112015023279B1/pt not_active IP Right Cessation
- 2014-03-11 RS RSP20191323 patent/RS59411B1/sr unknown
- 2014-03-11 AU AU2014249003A patent/AU2014249003A1/en not_active Abandoned
- 2014-03-11 KR KR1020157028847A patent/KR102194745B1/ko active IP Right Grant
- 2014-03-11 PL PL14779048T patent/PL2968316T3/pl unknown
- 2014-03-11 RU RU2019111684A patent/RU2737434C2/ru active
- 2014-03-11 ES ES14779048T patent/ES2753386T3/es active Active
- 2014-03-11 EP EP14779048.9A patent/EP2968316B1/en active Active
- 2014-03-11 JP JP2016501223A patent/JP2016517412A/ja not_active Withdrawn
- 2014-03-11 MY MYPI2015002324A patent/MY191366A/en unknown
- 2014-03-11 US US14/775,877 patent/US20160002188A1/en not_active Abandoned
-
2015
- 2015-09-13 SA SA515361086A patent/SA515361086B1/ar unknown
- 2015-09-14 TN TN2015000420A patent/TN2015000420A1/en unknown
- 2015-09-14 CL CL2015002698A patent/CL2015002698A1/es unknown
- 2015-09-14 PH PH12015502097A patent/PH12015502097A1/en unknown
- 2015-09-16 IL IL241699A patent/IL241699B/en unknown
- 2015-09-16 NI NI201500141A patent/NI201500141A/es unknown
- 2015-09-17 ZA ZA2015/06922A patent/ZA201506922B/en unknown
- 2015-10-06 NO NO20151329A patent/NO20151329A1/en not_active Application Discontinuation
- 2015-10-13 EC ECIEPI201543280A patent/ECSP15043280A/es unknown
- 2015-10-13 CR CR20150541A patent/CR20150541A/es unknown
-
2016
- 2016-07-20 HK HK16108629.4A patent/HK1220409A1/zh unknown
-
2017
- 2017-10-17 US US15/786,539 patent/US10457655B2/en not_active Expired - Fee Related
- 2017-11-28 AU AU2017268536A patent/AU2017268536B2/en not_active Ceased
-
2018
- 2018-08-31 US US16/119,962 patent/US10399951B2/en not_active Expired - Fee Related
- 2018-10-29 JP JP2018203058A patent/JP6790040B2/ja active Active
-
2019
- 2019-04-12 US US16/383,296 patent/US10472342B2/en not_active Expired - Fee Related
- 2019-04-19 US US16/389,286 patent/US10450286B2/en not_active Expired - Fee Related
- 2019-09-10 US US16/566,119 patent/US10800750B2/en active Active
- 2019-10-08 AU AU2019246753A patent/AU2019246753B2/en not_active Ceased
- 2019-10-14 HR HRP20191860TT patent/HRP20191860T1/hr unknown
- 2019-11-05 CY CY20191101150T patent/CY1122244T1/el unknown
-
2020
- 2020-05-20 US US15/929,751 patent/US10995078B2/en active Active
-
2021
- 2021-02-26 US US17/187,061 patent/US20210214323A1/en active Pending
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2753386T3 (es) | Derivados de 2-hidroxi-1-{4-[(4-fenil)fenil]carbonil}piperazin-1-il}etano-1-ona y compuestos relacionados como inhibidores de sintasa de ácido graso (FASN) para el tratamiento del cáncer | |
| ES2742409T3 (es) | Inhibidores de quinasa de pirazolilquinoxalina | |
| ES2739348T3 (es) | Pteridinas como inhibidores del FGFR | |
| ES2731216T3 (es) | Nuevos compuestos | |
| EP2855459B1 (en) | Aminoquinazoline and pyridopyrimidine derivatives | |
| JP2019518059A (ja) | PI3Kβ阻害剤としてのアザベンゾイミダゾール誘導体 | |
| EA034235B1 (ru) | Новые композиции, их использование и способы получения | |
| JP2022547294A (ja) | キナーゼ阻害剤としての3,5-ジ置換ピラゾール化合物およびその応用 | |
| WO2020231739A2 (en) | Compounds and methods for treating cancer | |
| JP2018087173A (ja) | 悪性脳腫瘍治療薬 | |
| BR112019020309A2 (pt) | derivados de quinoxalina e piridopirazina como inibidores de pi3k-beta |