CN108966638B - 用于形成保护性涂层的植物提取物组合物 - Google Patents
用于形成保护性涂层的植物提取物组合物 Download PDFInfo
- Publication number
- CN108966638B CN108966638B CN201680079439.5A CN201680079439A CN108966638B CN 108966638 B CN108966638 B CN 108966638B CN 201680079439 A CN201680079439 A CN 201680079439A CN 108966638 B CN108966638 B CN 108966638B
- Authority
- CN
- China
- Prior art keywords
- cutin
- alkyl
- alkenyl
- alkynyl
- mixture
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 239000000203 mixture Substances 0.000 title claims description 265
- 239000000419 plant extract Substances 0.000 title description 34
- 239000011253 protective coating Substances 0.000 title description 25
- 229920000832 Cutin Polymers 0.000 claims abstract description 168
- 239000000178 monomer Substances 0.000 claims abstract description 162
- 239000002904 solvent Substances 0.000 claims abstract description 162
- 238000000034 method Methods 0.000 claims abstract description 160
- 239000000463 material Substances 0.000 claims abstract description 32
- 238000010438 heat treatment Methods 0.000 claims abstract description 30
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 claims description 137
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 claims description 87
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 claims description 70
- 102000011782 Keratins Human genes 0.000 claims description 68
- 108010076876 Keratins Proteins 0.000 claims description 68
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims description 63
- 239000000126 substance Substances 0.000 claims description 58
- 125000003118 aryl group Chemical group 0.000 claims description 57
- 125000001072 heteroaryl group Chemical group 0.000 claims description 52
- 229910052736 halogen Inorganic materials 0.000 claims description 42
- 235000021122 unsaturated fatty acids Nutrition 0.000 claims description 42
- 125000000304 alkynyl group Chemical group 0.000 claims description 36
- 239000012298 atmosphere Substances 0.000 claims description 33
- 229920006395 saturated elastomer Polymers 0.000 claims description 31
- 239000002253 acid Substances 0.000 claims description 30
- -1 unsaturated fatty acid esters Chemical class 0.000 claims description 29
- 125000000217 alkyl group Chemical group 0.000 claims description 26
- 239000007788 liquid Substances 0.000 claims description 25
- 125000000753 cycloalkyl group Chemical group 0.000 claims description 24
- 238000006467 substitution reaction Methods 0.000 claims description 24
- 238000009835 boiling Methods 0.000 claims description 22
- 150000002367 halogens Chemical group 0.000 claims description 21
- 150000004670 unsaturated fatty acids Chemical class 0.000 claims description 21
- 125000003342 alkenyl group Chemical group 0.000 claims description 17
- 150000004671 saturated fatty acids Chemical class 0.000 claims description 15
- 238000004519 manufacturing process Methods 0.000 claims description 14
- 150000001721 carbon Chemical group 0.000 claims description 12
- 229910052799 carbon Inorganic materials 0.000 claims description 12
- 125000004367 cycloalkylaryl group Chemical group 0.000 claims description 12
- 125000000623 heterocyclic group Chemical group 0.000 claims description 12
- 239000007791 liquid phase Substances 0.000 claims description 9
- 235000003441 saturated fatty acids Nutrition 0.000 claims description 9
- 238000012691 depolymerization reaction Methods 0.000 claims description 7
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 claims description 3
- 230000008569 process Effects 0.000 abstract description 75
- 230000002378 acidificating effect Effects 0.000 abstract description 2
- IMNFDUFMRHMDMM-UHFFFAOYSA-N N-Heptane Chemical compound CCCCCCC IMNFDUFMRHMDMM-UHFFFAOYSA-N 0.000 description 166
- 239000000047 product Substances 0.000 description 154
- 150000001875 compounds Chemical class 0.000 description 129
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 126
- 241000196324 Embryophyta Species 0.000 description 102
- 239000006227 byproduct Substances 0.000 description 70
- 150000002148 esters Chemical class 0.000 description 57
- 239000006228 supernatant Substances 0.000 description 38
- 238000000944 Soxhlet extraction Methods 0.000 description 37
- 238000000576 coating method Methods 0.000 description 37
- 235000007688 Lycopersicon esculentum Nutrition 0.000 description 28
- 240000003768 Solanum lycopersicum Species 0.000 description 28
- 239000011248 coating agent Substances 0.000 description 28
- VJZBXAQGWLMYMS-UHFFFAOYSA-N 10,16-Dihydroxyhexadecanoic acid Chemical compound OCCCCCCC(O)CCCCCCCCC(O)=O VJZBXAQGWLMYMS-UHFFFAOYSA-N 0.000 description 27
- 239000002244 precipitate Substances 0.000 description 27
- 125000004494 ethyl ester group Chemical group 0.000 description 25
- 238000001816 cooling Methods 0.000 description 23
- 125000005908 glyceryl ester group Chemical group 0.000 description 22
- 238000000605 extraction Methods 0.000 description 21
- 238000004704 ultra performance liquid chromatography Methods 0.000 description 21
- 244000025272 Persea americana Species 0.000 description 20
- 235000008673 Persea americana Nutrition 0.000 description 20
- 239000000284 extract Substances 0.000 description 20
- 238000006243 chemical reaction Methods 0.000 description 19
- 239000000758 substrate Substances 0.000 description 19
- 239000006184 cosolvent Substances 0.000 description 18
- 235000011187 glycerol Nutrition 0.000 description 17
- 239000012535 impurity Substances 0.000 description 15
- 150000004702 methyl esters Chemical class 0.000 description 15
- 235000021588 free fatty acids Nutrition 0.000 description 14
- 238000004949 mass spectrometry Methods 0.000 description 14
- 238000002390 rotary evaporation Methods 0.000 description 13
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 12
- 239000000287 crude extract Substances 0.000 description 12
- 238000000354 decomposition reaction Methods 0.000 description 12
- 235000014113 dietary fatty acids Nutrition 0.000 description 12
- 239000000194 fatty acid Substances 0.000 description 12
- 229930195729 fatty acid Natural products 0.000 description 12
- YFRDEHYAUAROBO-UHFFFAOYSA-N 10,18-dihydroxyoctadecanoic acid Chemical compound OCCCCCCCCC(O)CCCCCCCCC(O)=O YFRDEHYAUAROBO-UHFFFAOYSA-N 0.000 description 10
- 235000013399 edible fruits Nutrition 0.000 description 10
- 238000010932 ethanolysis reaction Methods 0.000 description 10
- 238000001914 filtration Methods 0.000 description 10
- IPCSVZSSVZVIGE-UHFFFAOYSA-N hexadecanoic acid Chemical compound CCCCCCCCCCCCCCCC(O)=O IPCSVZSSVZVIGE-UHFFFAOYSA-N 0.000 description 10
- 239000007787 solid Substances 0.000 description 10
- MEHUJCGAYMDLEL-UHFFFAOYSA-N Aleuretic Acid Chemical compound OCCCCCCC(O)C(O)CCCCCCCC(O)=O MEHUJCGAYMDLEL-UHFFFAOYSA-N 0.000 description 9
- 238000005481 NMR spectroscopy Methods 0.000 description 9
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 9
- 229910002092 carbon dioxide Inorganic materials 0.000 description 9
- 238000012512 characterization method Methods 0.000 description 9
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 9
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 8
- 239000007789 gas Substances 0.000 description 8
- 230000003647 oxidation Effects 0.000 description 8
- 238000007254 oxidation reaction Methods 0.000 description 8
- 210000000434 stratum corneum Anatomy 0.000 description 8
- 239000000654 additive Substances 0.000 description 7
- 239000012043 crude product Substances 0.000 description 7
- 150000004665 fatty acids Chemical class 0.000 description 7
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 6
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 6
- 230000015556 catabolic process Effects 0.000 description 6
- 239000010410 layer Substances 0.000 description 6
- 229910052757 nitrogen Inorganic materials 0.000 description 6
- 210000000056 organ Anatomy 0.000 description 6
- 239000007858 starting material Substances 0.000 description 6
- 239000001993 wax Substances 0.000 description 6
- 241000894006 Bacteria Species 0.000 description 5
- 239000002028 Biomass Substances 0.000 description 5
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 5
- 241000233866 Fungi Species 0.000 description 5
- 235000021314 Palmitic acid Nutrition 0.000 description 5
- 238000000668 atmospheric pressure chemical ionisation mass spectrometry Methods 0.000 description 5
- 230000008901 benefit Effects 0.000 description 5
- 230000006378 damage Effects 0.000 description 5
- 238000006731 degradation reaction Methods 0.000 description 5
- 230000007613 environmental effect Effects 0.000 description 5
- FBBCRDRITUULHX-UHFFFAOYSA-N ethyl 10,16-dihydroxyhexadecanoate Chemical compound CCOC(=O)CCCCCCCCC(O)CCCCCCO FBBCRDRITUULHX-UHFFFAOYSA-N 0.000 description 5
- 238000002474 experimental method Methods 0.000 description 5
- 150000004676 glycans Chemical class 0.000 description 5
- 238000001027 hydrothermal synthesis Methods 0.000 description 5
- WQEPLUUGTLDZJY-UHFFFAOYSA-N n-Pentadecanoic acid Natural products CCCCCCCCCCCCCCC(O)=O WQEPLUUGTLDZJY-UHFFFAOYSA-N 0.000 description 5
- 238000005457 optimization Methods 0.000 description 5
- 239000012071 phase Substances 0.000 description 5
- 229920001282 polysaccharide Polymers 0.000 description 5
- 239000005017 polysaccharide Substances 0.000 description 5
- UGAGPNKCDRTDHP-UHFFFAOYSA-N 16-hydroxyhexadecanoic acid Chemical compound OCCCCCCCCCCCCCCCC(O)=O UGAGPNKCDRTDHP-UHFFFAOYSA-N 0.000 description 4
- 238000005160 1H NMR spectroscopy Methods 0.000 description 4
- XWQVQSXLXAXOPJ-QNGMFEMESA-N 4-[[[6-[5-chloro-2-[[4-[[(2r)-1-methoxypropan-2-yl]amino]cyclohexyl]amino]pyridin-4-yl]pyridin-2-yl]amino]methyl]oxane-4-carbonitrile Chemical compound C1CC(N[C@H](C)COC)CCC1NC1=CC(C=2N=C(NCC3(CCOCC3)C#N)C=CC=2)=C(Cl)C=N1 XWQVQSXLXAXOPJ-QNGMFEMESA-N 0.000 description 4
- OISFHODBOQNZAG-UHFFFAOYSA-N 9,10,18-trihydroxyoctadecanoic acid Chemical compound OCCCCCCCCC(O)C(O)CCCCCCCC(O)=O OISFHODBOQNZAG-UHFFFAOYSA-N 0.000 description 4
- XSIHTLJPWOWWPE-UHFFFAOYSA-N 9,16-dihydroxy-palmitic acid Chemical compound OCCCCCCCC(O)CCCCCCCC(O)=O XSIHTLJPWOWWPE-UHFFFAOYSA-N 0.000 description 4
- BTDPBXZCKBVWTJ-UHFFFAOYSA-N 9,18-dihydroxyoctadecanoic acid Chemical compound OCCCCCCCCCC(O)CCCCCCCC(O)=O BTDPBXZCKBVWTJ-UHFFFAOYSA-N 0.000 description 4
- 102000004190 Enzymes Human genes 0.000 description 4
- 108090000790 Enzymes Proteins 0.000 description 4
- 239000005909 Kieselgur Substances 0.000 description 4
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 4
- 239000006057 Non-nutritive feed additive Substances 0.000 description 4
- 241000700605 Viruses Species 0.000 description 4
- QTBSBXVTEAMEQO-UHFFFAOYSA-N acetic acid Substances CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 4
- 230000000996 additive effect Effects 0.000 description 4
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 4
- 239000001913 cellulose Substances 0.000 description 4
- 229920002678 cellulose Polymers 0.000 description 4
- 239000012065 filter cake Substances 0.000 description 4
- 235000013305 food Nutrition 0.000 description 4
- 239000011491 glass wool Substances 0.000 description 4
- 238000005984 hydrogenation reaction Methods 0.000 description 4
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 4
- 230000000269 nucleophilic effect Effects 0.000 description 4
- 239000001301 oxygen Substances 0.000 description 4
- 229910052760 oxygen Inorganic materials 0.000 description 4
- 102000004169 proteins and genes Human genes 0.000 description 4
- 108090000623 proteins and genes Proteins 0.000 description 4
- 230000035484 reaction time Effects 0.000 description 4
- LMBFAGIMSUYTBN-MPZNNTNKSA-N teixobactin Chemical compound C([C@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CO)C(=O)N[C@H](CCC(N)=O)C(=O)N[C@H]([C@@H](C)CC)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CO)C(=O)N[C@H]1C(N[C@@H](C)C(=O)N[C@@H](C[C@@H]2NC(=N)NC2)C(=O)N[C@H](C(=O)O[C@H]1C)[C@@H](C)CC)=O)NC)C1=CC=CC=C1 LMBFAGIMSUYTBN-MPZNNTNKSA-N 0.000 description 4
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 3
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 3
- RBNPOMFGQQGHHO-UWTATZPHSA-N D-glyceric acid Chemical compound OC[C@@H](O)C(O)=O RBNPOMFGQQGHHO-UWTATZPHSA-N 0.000 description 3
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 3
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 description 3
- 150000007513 acids Chemical class 0.000 description 3
- 150000001335 aliphatic alkanes Chemical class 0.000 description 3
- 229930013930 alkaloid Natural products 0.000 description 3
- 150000001450 anions Chemical class 0.000 description 3
- 230000004888 barrier function Effects 0.000 description 3
- 235000021466 carotenoid Nutrition 0.000 description 3
- 150000001747 carotenoids Chemical class 0.000 description 3
- 239000003054 catalyst Substances 0.000 description 3
- 150000001768 cations Chemical class 0.000 description 3
- 239000000571 coke Substances 0.000 description 3
- 230000007423 decrease Effects 0.000 description 3
- 230000003247 decreasing effect Effects 0.000 description 3
- 238000000151 deposition Methods 0.000 description 3
- 239000000539 dimer Substances 0.000 description 3
- 238000001035 drying Methods 0.000 description 3
- 230000000694 effects Effects 0.000 description 3
- 230000008030 elimination Effects 0.000 description 3
- 238000003379 elimination reaction Methods 0.000 description 3
- 230000032050 esterification Effects 0.000 description 3
- 238000005886 esterification reaction Methods 0.000 description 3
- 238000001704 evaporation Methods 0.000 description 3
- 229930003935 flavonoid Natural products 0.000 description 3
- 150000002215 flavonoids Chemical class 0.000 description 3
- 235000017173 flavonoids Nutrition 0.000 description 3
- 125000002485 formyl group Chemical class [H]C(*)=O 0.000 description 3
- 230000008014 freezing Effects 0.000 description 3
- 238000007710 freezing Methods 0.000 description 3
- 230000012010 growth Effects 0.000 description 3
- 229930013686 lignan Natural products 0.000 description 3
- 150000005692 lignans Chemical class 0.000 description 3
- 235000009408 lignans Nutrition 0.000 description 3
- OKKJLVBELUTLKV-VMNATFBRSA-N methanol-d1 Chemical compound [2H]OC OKKJLVBELUTLKV-VMNATFBRSA-N 0.000 description 3
- 230000004048 modification Effects 0.000 description 3
- 238000012986 modification Methods 0.000 description 3
- 238000004806 packaging method and process Methods 0.000 description 3
- 238000010587 phase diagram Methods 0.000 description 3
- 150000002989 phenols Chemical class 0.000 description 3
- 238000012545 processing Methods 0.000 description 3
- 238000005086 pumping Methods 0.000 description 3
- 238000000746 purification Methods 0.000 description 3
- DCBSHORRWZKAKO-UHFFFAOYSA-N rac-1-monomyristoylglycerol Chemical compound CCCCCCCCCCCCCC(=O)OCC(O)CO DCBSHORRWZKAKO-UHFFFAOYSA-N 0.000 description 3
- 238000011084 recovery Methods 0.000 description 3
- 238000005057 refrigeration Methods 0.000 description 3
- 239000007921 spray Substances 0.000 description 3
- 150000003505 terpenes Chemical class 0.000 description 3
- 230000007704 transition Effects 0.000 description 3
- RBNPOMFGQQGHHO-UHFFFAOYSA-N -2,3-Dihydroxypropanoic acid Natural products OCC(O)C(O)=O RBNPOMFGQQGHHO-UHFFFAOYSA-N 0.000 description 2
- HHDSNPUMYBUKJJ-UHFFFAOYSA-N 10-hydroxyhexadec-15-enoic acid Chemical compound OC(CCCCCCCCC(=O)O)CCCCC=C HHDSNPUMYBUKJJ-UHFFFAOYSA-N 0.000 description 2
- BBNYCLAREVXOSG-UHFFFAOYSA-N 2-palmitoylglycerol Chemical compound CCCCCCCCCCCCCCCC(=O)OC(CO)CO BBNYCLAREVXOSG-UHFFFAOYSA-N 0.000 description 2
- OISFHODBOQNZAG-DLBZAZTESA-N 9,10,18-Trihydroxyoctadecanoic acid Natural products OCCCCCCCC[C@H](O)[C@H](O)CCCCCCCC(O)=O OISFHODBOQNZAG-DLBZAZTESA-N 0.000 description 2
- 238000007309 Fischer-Speier esterification reaction Methods 0.000 description 2
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 2
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N Phenol Chemical compound OC1=CC=CC=C1 ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 description 2
- HEDRZPFGACZZDS-MICDWDOJSA-N Trichloro(2H)methane Chemical compound [2H]C(Cl)(Cl)Cl HEDRZPFGACZZDS-MICDWDOJSA-N 0.000 description 2
- 240000001717 Vaccinium macrocarpon Species 0.000 description 2
- 241000607479 Yersinia pestis Species 0.000 description 2
- 150000001298 alcohols Chemical class 0.000 description 2
- 239000012736 aqueous medium Substances 0.000 description 2
- 159000000032 aromatic acids Chemical class 0.000 description 2
- 230000015572 biosynthetic process Effects 0.000 description 2
- 239000001569 carbon dioxide Substances 0.000 description 2
- 230000008859 change Effects 0.000 description 2
- 229920006037 cross link polymer Polymers 0.000 description 2
- 230000008020 evaporation Effects 0.000 description 2
- 239000012530 fluid Substances 0.000 description 2
- 238000009472 formulation Methods 0.000 description 2
- 230000002538 fungal effect Effects 0.000 description 2
- 125000005456 glyceride group Chemical group 0.000 description 2
- 230000003301 hydrolyzing effect Effects 0.000 description 2
- 229910052943 magnesium sulfate Inorganic materials 0.000 description 2
- 235000019341 magnesium sulphate Nutrition 0.000 description 2
- 230000035800 maturation Effects 0.000 description 2
- OWNLLILEAVFEFO-UHFFFAOYSA-N methyl 10,16-dihydroxyhexadecanoate Chemical compound COC(=O)CCCCCCCCC(O)CCCCCCO OWNLLILEAVFEFO-UHFFFAOYSA-N 0.000 description 2
- 235000014571 nuts Nutrition 0.000 description 2
- 230000009965 odorless effect Effects 0.000 description 2
- 239000003921 oil Substances 0.000 description 2
- 235000019198 oils Nutrition 0.000 description 2
- 239000012044 organic layer Substances 0.000 description 2
- 239000012074 organic phase Substances 0.000 description 2
- 239000003002 pH adjusting agent Substances 0.000 description 2
- 230000035699 permeability Effects 0.000 description 2
- 238000001782 photodegradation Methods 0.000 description 2
- 229920000728 polyester Polymers 0.000 description 2
- 239000000843 powder Substances 0.000 description 2
- 230000001681 protective effect Effects 0.000 description 2
- 230000002829 reductive effect Effects 0.000 description 2
- 238000000926 separation method Methods 0.000 description 2
- 210000003491 skin Anatomy 0.000 description 2
- CDBYLPFSWZWCQE-UHFFFAOYSA-L sodium carbonate Substances [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 2
- 229910000029 sodium carbonate Inorganic materials 0.000 description 2
- 239000011343 solid material Substances 0.000 description 2
- 239000008247 solid mixture Substances 0.000 description 2
- 238000005507 spraying Methods 0.000 description 2
- 239000012134 supernatant fraction Substances 0.000 description 2
- 239000013638 trimer Substances 0.000 description 2
- 235000013311 vegetables Nutrition 0.000 description 2
- 238000005406 washing Methods 0.000 description 2
- RPQJFAIEPUKQHK-IWQZZHSRSA-N (9Z)-16-hydroxyhexadec-9-enoic acid Chemical compound OCCCCCC\C=C/CCCCCCCC(O)=O RPQJFAIEPUKQHK-IWQZZHSRSA-N 0.000 description 1
- DLTAWNZQSGEZLQ-HWKANZROSA-N (E)-16-hydroxyhexadec-10-enoic acid Chemical compound OCCCCC/C=C/CCCCCCCCC(=O)O DLTAWNZQSGEZLQ-HWKANZROSA-N 0.000 description 1
- DLTAWNZQSGEZLQ-HYXAFXHYSA-N (Z)-16-hydroxyhexadec-10-enoic acid Chemical compound OCCCCC\C=C/CCCCCCCCC(=O)O DLTAWNZQSGEZLQ-HYXAFXHYSA-N 0.000 description 1
- YFRMOIMZVUXHCF-HNQUOIGGSA-N 1,3-dihydroxypropan-2-yl (E)-16-hydroxyhexadec-9-enoate Chemical compound OCCCCCC/C=C/CCCCCCCC(=O)OC(CO)CO YFRMOIMZVUXHCF-HNQUOIGGSA-N 0.000 description 1
- YFRMOIMZVUXHCF-IWQZZHSRSA-N 1,3-dihydroxypropan-2-yl (Z)-16-hydroxyhexadec-9-enoate Chemical compound OCCCCCC\C=C/CCCCCCCC(=O)OC(CO)CO YFRMOIMZVUXHCF-IWQZZHSRSA-N 0.000 description 1
- CPMLBHCSPPPITL-UHFFFAOYSA-N 1,3-dihydroxypropan-2-yl 10,16-dihydroxyhexadecanoate Chemical compound OCCCCCCC(O)CCCCCCCCC(=O)OC(CO)CO CPMLBHCSPPPITL-UHFFFAOYSA-N 0.000 description 1
- CADWAGFKCYLGQI-UHFFFAOYSA-N 1,3-dihydroxypropan-2-yl 10,18-dihydroxyoctadecanoate Chemical compound OC(CCCCCCCCC(=O)OC(CO)CO)CCCCCCCCO CADWAGFKCYLGQI-UHFFFAOYSA-N 0.000 description 1
- LDVVTQMJQSCDMK-UHFFFAOYSA-N 1,3-dihydroxypropan-2-yl formate Chemical compound OCC(CO)OC=O LDVVTQMJQSCDMK-UHFFFAOYSA-N 0.000 description 1
- KSGFJKSNZLTEDI-UHFFFAOYSA-N 1-[benzyl(methyl)amino]-3-[3-(trifluoromethyl)phenoxy]propan-2-ol Chemical compound C=1C=CC=CC=1CN(C)CC(O)COC1=CC=CC(C(F)(F)F)=C1 KSGFJKSNZLTEDI-UHFFFAOYSA-N 0.000 description 1
- VJZBXAQGWLMYMS-UHFFFAOYSA-M 10,16-dihydroxyhexadecanoate Chemical compound OCCCCCCC(O)CCCCCCCCC([O-])=O VJZBXAQGWLMYMS-UHFFFAOYSA-M 0.000 description 1
- RPQJFAIEPUKQHK-HNQUOIGGSA-N 16-hydroxy-9E-hexadecenoic acid Chemical compound OCCCCCC\C=C\CCCCCCCC(O)=O RPQJFAIEPUKQHK-HNQUOIGGSA-N 0.000 description 1
- HAFGDDFWCDLGEW-UHFFFAOYSA-N 2,2-dihydroxyhexadecanoic acid Chemical compound CCCCCCCCCCCCCCC(O)(O)C(O)=O HAFGDDFWCDLGEW-UHFFFAOYSA-N 0.000 description 1
- PUTHBBXPAQTOMK-HNQUOIGGSA-N 2,3-dihydroxypropyl (E)-16-hydroxyhexadec-9-enoate Chemical compound OCCCCCC/C=C/CCCCCCCC(=O)OCC(CO)O PUTHBBXPAQTOMK-HNQUOIGGSA-N 0.000 description 1
- PUTHBBXPAQTOMK-IWQZZHSRSA-N 2,3-dihydroxypropyl (Z)-16-hydroxyhexadec-9-enoate Chemical compound OCCCCCC\C=C/CCCCCCCC(=O)OCC(CO)O PUTHBBXPAQTOMK-IWQZZHSRSA-N 0.000 description 1
- ZCSPMSRILJREOV-UHFFFAOYSA-N 2,3-dihydroxypropyl 10,16-dihydroxyhexadecanoate Chemical compound OCCCCCCC(O)CCCCCCCCC(=O)OCC(O)CO ZCSPMSRILJREOV-UHFFFAOYSA-N 0.000 description 1
- FCHDDNHFKIKCIJ-UHFFFAOYSA-N 2,3-dihydroxypropyl 10,18-dihydroxyoctadecanoate Chemical compound OC(CCCCCCCCC(=O)OCC(CO)O)CCCCCCCCO FCHDDNHFKIKCIJ-UHFFFAOYSA-N 0.000 description 1
- RHSNZPVMORXINW-UHFFFAOYSA-N 2,3-dihydroxypropyl 10-hydroxyhexadec-15-enoate Chemical compound OC(CCCCCCCCC(=O)OCC(CO)O)CCCCC=C RHSNZPVMORXINW-UHFFFAOYSA-N 0.000 description 1
- IUUBODMNDCMSEU-UHFFFAOYSA-N 3-[6-amino-3-(3-hydroxypropyl)-2,4,5,9-tetrahydropurin-2-yl]propan-1-ol Chemical compound NC1=NC(CCCO)N(CCCO)C2N=CNC12 IUUBODMNDCMSEU-UHFFFAOYSA-N 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical group [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- 235000005979 Citrus limon Nutrition 0.000 description 1
- 244000131522 Citrus pyriformis Species 0.000 description 1
- 240000003133 Elaeis guineensis Species 0.000 description 1
- 235000001950 Elaeis guineensis Nutrition 0.000 description 1
- 240000009088 Fragaria x ananassa Species 0.000 description 1
- 241000238631 Hexapoda Species 0.000 description 1
- 240000008790 Musa x paradisiaca Species 0.000 description 1
- LOBOQEVQRNKDQD-GQCTYLIASA-N OCCCCC/C=C/CCCCCCCCC(=O)OC Chemical compound OCCCCC/C=C/CCCCCCCCC(=O)OC LOBOQEVQRNKDQD-GQCTYLIASA-N 0.000 description 1
- JRBLQTRVXDWLIZ-HWKANZROSA-N OCCCCC/C=C/CCCCCCCCC(=O)OC(CO)CO Chemical compound OCCCCC/C=C/CCCCCCCCC(=O)OC(CO)CO JRBLQTRVXDWLIZ-HWKANZROSA-N 0.000 description 1
- JIZWEWFMGMKLQC-FNORWQNLSA-N OCCCCC/C=C/CCCCCCCCC(=O)OCC Chemical compound OCCCCC/C=C/CCCCCCCCC(=O)OCC JIZWEWFMGMKLQC-FNORWQNLSA-N 0.000 description 1
- XZUWSCKOEICART-HWKANZROSA-N OCCCCC/C=C/CCCCCCCCC(=O)OCC(CO)O Chemical compound OCCCCC/C=C/CCCCCCCCC(=O)OCC(CO)O XZUWSCKOEICART-HWKANZROSA-N 0.000 description 1
- LOBOQEVQRNKDQD-XQRVVYSFSA-N OCCCCC\C=C/CCCCCCCCC(=O)OC Chemical compound OCCCCC\C=C/CCCCCCCCC(=O)OC LOBOQEVQRNKDQD-XQRVVYSFSA-N 0.000 description 1
- JRBLQTRVXDWLIZ-HYXAFXHYSA-N OCCCCC\C=C/CCCCCCCCC(=O)OC(CO)CO Chemical compound OCCCCC\C=C/CCCCCCCCC(=O)OC(CO)CO JRBLQTRVXDWLIZ-HYXAFXHYSA-N 0.000 description 1
- JIZWEWFMGMKLQC-ALCCZGGFSA-N OCCCCC\C=C/CCCCCCCCC(=O)OCC Chemical compound OCCCCC\C=C/CCCCCCCCC(=O)OCC JIZWEWFMGMKLQC-ALCCZGGFSA-N 0.000 description 1
- XZUWSCKOEICART-HYXAFXHYSA-N OCCCCC\C=C/CCCCCCCCC(=O)OCC(CO)O Chemical compound OCCCCC\C=C/CCCCCCCCC(=O)OCC(CO)O XZUWSCKOEICART-HYXAFXHYSA-N 0.000 description 1
- 235000019482 Palm oil Nutrition 0.000 description 1
- 235000021355 Stearic acid Nutrition 0.000 description 1
- 235000012545 Vaccinium macrocarpon Nutrition 0.000 description 1
- 235000002118 Vaccinium oxycoccus Nutrition 0.000 description 1
- 238000005299 abrasion Methods 0.000 description 1
- 230000002411 adverse Effects 0.000 description 1
- LFVVNPBBFUSSHL-UHFFFAOYSA-N alexidine Chemical compound CCCCC(CC)CNC(=N)NC(=N)NCCCCCCNC(=N)NC(=N)NCC(CC)CCCC LFVVNPBBFUSSHL-UHFFFAOYSA-N 0.000 description 1
- 150000003797 alkaloid derivatives Chemical class 0.000 description 1
- 230000004075 alteration Effects 0.000 description 1
- VBIXEXWLHSRNKB-UHFFFAOYSA-N ammonium oxalate Chemical compound [NH4+].[NH4+].[O-]C(=O)C([O-])=O VBIXEXWLHSRNKB-UHFFFAOYSA-N 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 235000021015 bananas Nutrition 0.000 description 1
- 235000015278 beef Nutrition 0.000 description 1
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 1
- 230000001413 cellular effect Effects 0.000 description 1
- 238000007385 chemical modification Methods 0.000 description 1
- 239000007795 chemical reaction product Substances 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- 239000008199 coating composition Substances 0.000 description 1
- 235000009508 confectionery Nutrition 0.000 description 1
- 238000005112 continuous flow technique Methods 0.000 description 1
- 238000010411 cooking Methods 0.000 description 1
- 235000021019 cranberries Nutrition 0.000 description 1
- 235000004634 cranberry Nutrition 0.000 description 1
- 230000008021 deposition Effects 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- 238000007865 diluting Methods 0.000 description 1
- 238000003618 dip coating Methods 0.000 description 1
- 238000007598 dipping method Methods 0.000 description 1
- 238000009826 distribution Methods 0.000 description 1
- 235000013601 eggs Nutrition 0.000 description 1
- 238000005265 energy consumption Methods 0.000 description 1
- STICMCJKHUAQPR-HWKANZROSA-N ethyl (E)-16-hydroxyhexadec-9-enoate Chemical compound OCCCCCC/C=C/CCCCCCCC(=O)OCC STICMCJKHUAQPR-HWKANZROSA-N 0.000 description 1
- STICMCJKHUAQPR-HYXAFXHYSA-N ethyl (Z)-16-hydroxyhexadec-9-enoate Chemical compound OCCCCCC\C=C/CCCCCCCC(=O)OCC STICMCJKHUAQPR-HYXAFXHYSA-N 0.000 description 1
- QZDLRJYWXXLKPI-UHFFFAOYSA-N ethyl 10,18-dihydroxyoctadecanoate Chemical compound OC(CCCCCCCCC(=O)OCC)CCCCCCCCO QZDLRJYWXXLKPI-UHFFFAOYSA-N 0.000 description 1
- BGFYFLBWVQKPIG-UHFFFAOYSA-N ethyl 10-hydroxyhexadec-15-enoate Chemical compound OC(CCCCCCCCC(=O)OCC)CCCCC=C BGFYFLBWVQKPIG-UHFFFAOYSA-N 0.000 description 1
- 238000003810 ethyl acetate extraction Methods 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 235000011389 fruit/vegetable juice Nutrition 0.000 description 1
- 230000007062 hydrolysis Effects 0.000 description 1
- 238000006460 hydrolysis reaction Methods 0.000 description 1
- 230000000640 hydroxylating effect Effects 0.000 description 1
- 150000002576 ketones Chemical class 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 150000002632 lipids Chemical class 0.000 description 1
- 230000008018 melting Effects 0.000 description 1
- 238000002844 melting Methods 0.000 description 1
- 229910000000 metal hydroxide Inorganic materials 0.000 description 1
- 150000004692 metal hydroxides Chemical class 0.000 description 1
- CTADAIAFJLTGMU-DUXPYHPUSA-N methyl (E)-16-hydroxyhexadec-9-enoate Chemical compound OCCCCCC/C=C/CCCCCCCC(=O)OC CTADAIAFJLTGMU-DUXPYHPUSA-N 0.000 description 1
- CTADAIAFJLTGMU-RQOWECAXSA-N methyl (Z)-16-hydroxyhexadec-9-enoate Chemical compound OCCCCCC\C=C/CCCCCCCC(=O)OC CTADAIAFJLTGMU-RQOWECAXSA-N 0.000 description 1
- DBTSJZUVIGCMRU-UHFFFAOYSA-N methyl 10,18-dihydroxyoctadecanoate Chemical compound OC(CCCCCCCCC(=O)OC)CCCCCCCCO DBTSJZUVIGCMRU-UHFFFAOYSA-N 0.000 description 1
- AFPYFUCRDKPVSZ-UHFFFAOYSA-N methyl 10-hydroxyhexadec-15-enoate Chemical compound OC(CCCCCCCCC(=O)OC)CCCCC=C AFPYFUCRDKPVSZ-UHFFFAOYSA-N 0.000 description 1
- 239000003595 mist Substances 0.000 description 1
- 239000003607 modifier Substances 0.000 description 1
- 230000007935 neutral effect Effects 0.000 description 1
- 229910052759 nickel Inorganic materials 0.000 description 1
- 231100000252 nontoxic Toxicity 0.000 description 1
- 230000003000 nontoxic effect Effects 0.000 description 1
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical class CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 1
- 239000003960 organic solvent Substances 0.000 description 1
- 229910000489 osmium tetroxide Inorganic materials 0.000 description 1
- 239000012285 osmium tetroxide Substances 0.000 description 1
- 235000006408 oxalic acid Nutrition 0.000 description 1
- 230000020477 pH reduction Effects 0.000 description 1
- 239000005022 packaging material Substances 0.000 description 1
- 229910052763 palladium Inorganic materials 0.000 description 1
- 239000002540 palm oil Substances 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 239000003208 petroleum Substances 0.000 description 1
- 230000005501 phase interface Effects 0.000 description 1
- 230000008832 photodamage Effects 0.000 description 1
- 238000006116 polymerization reaction Methods 0.000 description 1
- 239000011148 porous material Substances 0.000 description 1
- 244000144977 poultry Species 0.000 description 1
- 235000013594 poultry meat Nutrition 0.000 description 1
- 238000001556 precipitation Methods 0.000 description 1
- 150000003138 primary alcohols Chemical class 0.000 description 1
- 238000004886 process control Methods 0.000 description 1
- 238000011403 purification operation Methods 0.000 description 1
- 239000002994 raw material Substances 0.000 description 1
- 230000009257 reactivity Effects 0.000 description 1
- 238000010992 reflux Methods 0.000 description 1
- 235000014102 seafood Nutrition 0.000 description 1
- 238000007789 sealing Methods 0.000 description 1
- 150000003333 secondary alcohols Chemical class 0.000 description 1
- 239000002002 slurry Substances 0.000 description 1
- 238000000527 sonication Methods 0.000 description 1
- 235000021012 strawberries Nutrition 0.000 description 1
- 238000012360 testing method Methods 0.000 description 1
- 238000009283 thermal hydrolysis Methods 0.000 description 1
- 239000011782 vitamin Substances 0.000 description 1
- 229940088594 vitamin Drugs 0.000 description 1
- 229930003231 vitamin Natural products 0.000 description 1
- 235000013343 vitamin Nutrition 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N25/00—Biocides, pest repellants or attractants, or plant growth regulators, characterised by their forms, or by their non-active ingredients or by their methods of application, e.g. seed treatment or sequential application; Substances for reducing the noxious effect of the active ingredients to organisms other than pests
- A01N25/32—Ingredients for reducing the noxious effect of the active substances to organisms other than pests, e.g. toxicity reducing compositions, self-destructing compositions
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N25/00—Biocides, pest repellants or attractants, or plant growth regulators, characterised by their forms, or by their non-active ingredients or by their methods of application, e.g. seed treatment or sequential application; Substances for reducing the noxious effect of the active ingredients to organisms other than pests
- A01N25/34—Shaped forms, e.g. sheets, not provided for in any other sub-group of this main group
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N37/00—Biocides, pest repellants or attractants, or plant growth regulators containing organic compounds containing a carbon atom having three bonds to hetero atoms with at the most two bonds to halogen, e.g. carboxylic acids
- A01N37/06—Unsaturated carboxylic acids or thio analogues thereof; Derivatives thereof
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N37/00—Biocides, pest repellants or attractants, or plant growth regulators containing organic compounds containing a carbon atom having three bonds to hetero atoms with at the most two bonds to halogen, e.g. carboxylic acids
- A01N37/36—Biocides, pest repellants or attractants, or plant growth regulators containing organic compounds containing a carbon atom having three bonds to hetero atoms with at the most two bonds to halogen, e.g. carboxylic acids containing at least one carboxylic group or a thio analogue, or a derivative thereof, and a singly bound oxygen or sulfur atom attached to the same carbon skeleton, this oxygen or sulfur atom not being a member of a carboxylic group or of a thio analogue, or of a derivative thereof, e.g. hydroxy-carboxylic acids
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D11/00—Solvent extraction
- B01D11/02—Solvent extraction of solids
- B01D11/028—Flow sheets
- B01D11/0284—Multistage extraction
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D11/00—Solvent extraction
- B01D11/02—Solvent extraction of solids
- B01D11/0288—Applications, solvents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C29/00—Preparation of compounds having hydroxy or O-metal groups bound to a carbon atom not belonging to a six-membered aromatic ring
- C07C29/132—Preparation of compounds having hydroxy or O-metal groups bound to a carbon atom not belonging to a six-membered aromatic ring by reduction of an oxygen containing functional group
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C29/00—Preparation of compounds having hydroxy or O-metal groups bound to a carbon atom not belonging to a six-membered aromatic ring
- C07C29/17—Preparation of compounds having hydroxy or O-metal groups bound to a carbon atom not belonging to a six-membered aromatic ring by hydrogenation of carbon-to-carbon double or triple bonds
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C51/00—Preparation of carboxylic acids or their salts, halides or anhydrides
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C51/00—Preparation of carboxylic acids or their salts, halides or anhydrides
- C07C51/09—Preparation of carboxylic acids or their salts, halides or anhydrides from carboxylic acid esters or lactones
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C51/00—Preparation of carboxylic acids or their salts, halides or anhydrides
- C07C51/347—Preparation of carboxylic acids or their salts, halides or anhydrides by reactions not involving formation of carboxyl groups
- C07C51/36—Preparation of carboxylic acids or their salts, halides or anhydrides by reactions not involving formation of carboxyl groups by hydrogenation of carbon-to-carbon unsaturated bonds
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C51/00—Preparation of carboxylic acids or their salts, halides or anhydrides
- C07C51/347—Preparation of carboxylic acids or their salts, halides or anhydrides by reactions not involving formation of carboxyl groups
- C07C51/367—Preparation of carboxylic acids or their salts, halides or anhydrides by reactions not involving formation of carboxyl groups by introduction of functional groups containing oxygen only in singly bound form
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C51/00—Preparation of carboxylic acids or their salts, halides or anhydrides
- C07C51/347—Preparation of carboxylic acids or their salts, halides or anhydrides by reactions not involving formation of carboxyl groups
- C07C51/377—Preparation of carboxylic acids or their salts, halides or anhydrides by reactions not involving formation of carboxyl groups by splitting-off hydrogen or functional groups; by hydrogenolysis of functional groups
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C53/00—Saturated compounds having only one carboxyl group bound to an acyclic carbon atom or hydrogen
- C07C53/126—Acids containing more than four carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C57/00—Unsaturated compounds having carboxyl groups bound to acyclic carbon atoms
- C07C57/02—Unsaturated compounds having carboxyl groups bound to acyclic carbon atoms with only carbon-to-carbon double bonds as unsaturation
- C07C57/03—Monocarboxylic acids
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C57/00—Unsaturated compounds having carboxyl groups bound to acyclic carbon atoms
- C07C57/02—Unsaturated compounds having carboxyl groups bound to acyclic carbon atoms with only carbon-to-carbon double bonds as unsaturation
- C07C57/03—Monocarboxylic acids
- C07C57/12—Straight chain carboxylic acids containing eighteen carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C59/00—Compounds having carboxyl groups bound to acyclic carbon atoms and containing any of the groups OH, O—metal, —CHO, keto, ether, groups, groups, or groups
- C07C59/01—Saturated compounds having only one carboxyl group and containing hydroxy or O-metal groups
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C59/00—Compounds having carboxyl groups bound to acyclic carbon atoms and containing any of the groups OH, O—metal, —CHO, keto, ether, groups, groups, or groups
- C07C59/01—Saturated compounds having only one carboxyl group and containing hydroxy or O-metal groups
- C07C59/10—Polyhydroxy carboxylic acids
- C07C59/105—Polyhydroxy carboxylic acids having five or more carbon atoms, e.g. aldonic acids
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C59/00—Compounds having carboxyl groups bound to acyclic carbon atoms and containing any of the groups OH, O—metal, —CHO, keto, ether, groups, groups, or groups
- C07C59/40—Unsaturated compounds
- C07C59/42—Unsaturated compounds containing hydroxy or O-metal groups
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C63/00—Compounds having carboxyl groups bound to a carbon atoms of six-membered aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C67/00—Preparation of carboxylic acid esters
- C07C67/03—Preparation of carboxylic acid esters by reacting an ester group with a hydroxy group
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C67/00—Preparation of carboxylic acid esters
- C07C67/08—Preparation of carboxylic acid esters by reacting carboxylic acids or symmetrical anhydrides with the hydroxy or O-metal group of organic compounds
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C67/00—Preparation of carboxylic acid esters
- C07C67/475—Preparation of carboxylic acid esters by splitting of carbon-to-carbon bonds and redistribution, e.g. disproportionation or migration of groups between different molecules
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C69/00—Esters of carboxylic acids; Esters of carbonic or haloformic acids
- C07C69/02—Esters of acyclic saturated monocarboxylic acids having the carboxyl group bound to an acyclic carbon atom or to hydrogen
- C07C69/22—Esters of acyclic saturated monocarboxylic acids having the carboxyl group bound to an acyclic carbon atom or to hydrogen having three or more carbon atoms in the acid moiety
- C07C69/24—Esters of acyclic saturated monocarboxylic acids having the carboxyl group bound to an acyclic carbon atom or to hydrogen having three or more carbon atoms in the acid moiety esterified with monohydroxylic compounds
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C69/00—Esters of carboxylic acids; Esters of carbonic or haloformic acids
- C07C69/52—Esters of acyclic unsaturated carboxylic acids having the esterified carboxyl group bound to an acyclic carbon atom
- C07C69/533—Monocarboxylic acid esters having only one carbon-to-carbon double bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C69/00—Esters of carboxylic acids; Esters of carbonic or haloformic acids
- C07C69/52—Esters of acyclic unsaturated carboxylic acids having the esterified carboxyl group bound to an acyclic carbon atom
- C07C69/533—Monocarboxylic acid esters having only one carbon-to-carbon double bond
- C07C69/58—Esters of straight chain acids with eighteen carbon atoms in the acid moiety
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C69/00—Esters of carboxylic acids; Esters of carbonic or haloformic acids
- C07C69/52—Esters of acyclic unsaturated carboxylic acids having the esterified carboxyl group bound to an acyclic carbon atom
- C07C69/587—Monocarboxylic acid esters having at least two carbon-to-carbon double bonds
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C69/00—Esters of carboxylic acids; Esters of carbonic or haloformic acids
- C07C69/66—Esters of carboxylic acids having esterified carboxylic groups bound to acyclic carbon atoms and having any of the groups OH, O—metal, —CHO, keto, ether, acyloxy, groups, groups, or in the acid moiety
- C07C69/67—Esters of carboxylic acids having esterified carboxylic groups bound to acyclic carbon atoms and having any of the groups OH, O—metal, —CHO, keto, ether, acyloxy, groups, groups, or in the acid moiety of saturated acids
- C07C69/675—Esters of carboxylic acids having esterified carboxylic groups bound to acyclic carbon atoms and having any of the groups OH, O—metal, —CHO, keto, ether, acyloxy, groups, groups, or in the acid moiety of saturated acids of saturated hydroxy-carboxylic acids
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C69/00—Esters of carboxylic acids; Esters of carbonic or haloformic acids
- C07C69/66—Esters of carboxylic acids having esterified carboxylic groups bound to acyclic carbon atoms and having any of the groups OH, O—metal, —CHO, keto, ether, acyloxy, groups, groups, or in the acid moiety
- C07C69/73—Esters of carboxylic acids having esterified carboxylic groups bound to acyclic carbon atoms and having any of the groups OH, O—metal, —CHO, keto, ether, acyloxy, groups, groups, or in the acid moiety of unsaturated acids
- C07C69/732—Esters of carboxylic acids having esterified carboxylic groups bound to acyclic carbon atoms and having any of the groups OH, O—metal, —CHO, keto, ether, acyloxy, groups, groups, or in the acid moiety of unsaturated acids of unsaturated hydroxy carboxylic acids
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D303/00—Compounds containing three-membered rings having one oxygen atom as the only ring hetero atom
- C07D303/02—Compounds containing oxirane rings
- C07D303/38—Compounds containing oxirane rings with hydrocarbon radicals, substituted by carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G63/00—Macromolecular compounds obtained by reactions forming a carboxylic ester link in the main chain of the macromolecule
- C08G63/02—Polyesters derived from hydroxycarboxylic acids or from polycarboxylic acids and polyhydroxy compounds
- C08G63/06—Polyesters derived from hydroxycarboxylic acids or from polycarboxylic acids and polyhydroxy compounds derived from hydroxycarboxylic acids
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08J—WORKING-UP; GENERAL PROCESSES OF COMPOUNDING; AFTER-TREATMENT NOT COVERED BY SUBCLASSES C08B, C08C, C08F, C08G or C08H
- C08J11/00—Recovery or working-up of waste materials
- C08J11/04—Recovery or working-up of waste materials of polymers
- C08J11/10—Recovery or working-up of waste materials of polymers by chemically breaking down the molecular chains of polymers or breaking of crosslinks, e.g. devulcanisation
- C08J11/14—Recovery or working-up of waste materials of polymers by chemically breaking down the molecular chains of polymers or breaking of crosslinks, e.g. devulcanisation by treatment with steam or water
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08J—WORKING-UP; GENERAL PROCESSES OF COMPOUNDING; AFTER-TREATMENT NOT COVERED BY SUBCLASSES C08B, C08C, C08F, C08G or C08H
- C08J11/00—Recovery or working-up of waste materials
- C08J11/04—Recovery or working-up of waste materials of polymers
- C08J11/10—Recovery or working-up of waste materials of polymers by chemically breaking down the molecular chains of polymers or breaking of crosslinks, e.g. devulcanisation
- C08J11/18—Recovery or working-up of waste materials of polymers by chemically breaking down the molecular chains of polymers or breaking of crosslinks, e.g. devulcanisation by treatment with organic material
- C08J11/22—Recovery or working-up of waste materials of polymers by chemically breaking down the molecular chains of polymers or breaking of crosslinks, e.g. devulcanisation by treatment with organic material by treatment with organic oxygen-containing compounds
- C08J11/24—Recovery or working-up of waste materials of polymers by chemically breaking down the molecular chains of polymers or breaking of crosslinks, e.g. devulcanisation by treatment with organic material by treatment with organic oxygen-containing compounds containing hydroxyl groups
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09D—COATING COMPOSITIONS, e.g. PAINTS, VARNISHES OR LACQUERS; FILLING PASTES; CHEMICAL PAINT OR INK REMOVERS; INKS; CORRECTING FLUIDS; WOODSTAINS; PASTES OR SOLIDS FOR COLOURING OR PRINTING; USE OF MATERIALS THEREFOR
- C09D167/00—Coating compositions based on polyesters obtained by reactions forming a carboxylic ester link in the main chain; Coating compositions based on derivatives of such polymers
- C09D167/04—Polyesters derived from hydroxycarboxylic acids, e.g. lactones
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23B—PRESERVING, e.g. BY CANNING, MEAT, FISH, EGGS, FRUIT, VEGETABLES, EDIBLE SEEDS; CHEMICAL RIPENING OF FRUIT OR VEGETABLES; THE PRESERVED, RIPENED, OR CANNED PRODUCTS
- A23B7/00—Preservation or chemical ripening of fruit or vegetables
- A23B7/16—Coating with a protective layer; Compositions or apparatus therefor
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS, OR NON-ALCOHOLIC BEVERAGES, NOT COVERED BY SUBCLASSES A21D OR A23B-A23J; THEIR PREPARATION OR TREATMENT, e.g. COOKING, MODIFICATION OF NUTRITIVE QUALITIES, PHYSICAL TREATMENT; PRESERVATION OF FOODS OR FOODSTUFFS, IN GENERAL
- A23L3/00—Preservation of foods or foodstuffs, in general, e.g. pasteurising, sterilising, specially adapted for foods or foodstuffs
- A23L3/34—Preservation of foods or foodstuffs, in general, e.g. pasteurising, sterilising, specially adapted for foods or foodstuffs by treatment with chemicals
- A23L3/3454—Preservation of foods or foodstuffs, in general, e.g. pasteurising, sterilising, specially adapted for foods or foodstuffs by treatment with chemicals in the form of liquids or solids
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23V—INDEXING SCHEME RELATING TO FOODS, FOODSTUFFS OR NON-ALCOHOLIC BEVERAGES AND LACTIC OR PROPIONIC ACID BACTERIA USED IN FOODSTUFFS OR FOOD PREPARATION
- A23V2002/00—Food compositions, function of food ingredients or processes for food or foodstuffs
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G63/00—Macromolecular compounds obtained by reactions forming a carboxylic ester link in the main chain of the macromolecule
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08J—WORKING-UP; GENERAL PROCESSES OF COMPOUNDING; AFTER-TREATMENT NOT COVERED BY SUBCLASSES C08B, C08C, C08F, C08G or C08H
- C08J2391/00—Characterised by the use of oils, fats or waxes; Derivatives thereof
- C08J2391/06—Waxes
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09D—COATING COMPOSITIONS, e.g. PAINTS, VARNISHES OR LACQUERS; FILLING PASTES; CHEMICAL PAINT OR INK REMOVERS; INKS; CORRECTING FLUIDS; WOODSTAINS; PASTES OR SOLIDS FOR COLOURING OR PRINTING; USE OF MATERIALS THEREFOR
- C09D167/00—Coating compositions based on polyesters obtained by reactions forming a carboxylic ester link in the main chain; Coating compositions based on derivatives of such polymers
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09D—COATING COMPOSITIONS, e.g. PAINTS, VARNISHES OR LACQUERS; FILLING PASTES; CHEMICAL PAINT OR INK REMOVERS; INKS; CORRECTING FLUIDS; WOODSTAINS; PASTES OR SOLIDS FOR COLOURING OR PRINTING; USE OF MATERIALS THEREFOR
- C09D5/00—Coating compositions, e.g. paints, varnishes or lacquers, characterised by their physical nature or the effects produced; Filling pastes
Abstract
本文描述了从含角质的植物物质制备角质‑衍生的单体、寡聚体或它们的组合的方法。所述方法可以包括在升高的温度和压强在溶剂中加热角质‑衍生的植物物质。在某些优选的实施方案中,所述方法可以在不使用另外的酸性或碱性物质的情况下进行。
Description
相关申请的交叉引用
本申请要求2015年12月10日提交的美国临时专利申请系列号62/265,726的优先权的权益。
技术领域
本公开内容涉及用于用在农业涂布制剂中的植物提取物组合物和分离植物衍生的单体、寡聚体、及其混合物的方法。
背景
普通农业产品当暴露于环境时易于降解和分解(即,酸败)。这样的农业产品可以包括例如卵、水果、蔬菜、农产品(produce)、种子、坚果、花卉和/或整个植株(包括其加工和半加工形式)。非农业产品(例如,维生素、糖果等)当暴露于周围环境时也易于降解。农业产品的降解可以作为以下因素的结果经由非生物方式发生:从农业产品的外表面向大气的蒸发性水分损失,和/或从环境扩散进农业产品中的氧的氧化,和/或对表面的机械损伤,和/或光诱导的降解(即,光降解)。此外,生物应激源例如细菌、真菌、病毒和/或害虫也可以侵染和分解农业产品。
防止降解、保持品质和增加农业产品寿命的常规方案包括冷藏和/或特殊包装。冷藏需要资金密集型设备,要求持续的能量消耗,如果不小心地控制的话可以造成对所述产品的损伤或品质损失,必须进行主动管理,并且在控温供给链中断后其益处丧失。特殊包装也可能需要昂贵的设备,消耗包装材料,增加运输成本,和需要主动管理。尽管冷藏和特殊包装可以提供益处,但是农业产品的处理和运输可能造成表面磨损或擦伤,其对消费者来说是美学上令人不快的并且充当细菌和真菌的进入点。此外,与这样的方案有关的费用可能增加农业产品的成本。
形成多数植物(诸如高等植物)的空气表面的细胞包括外包膜或角质层,其提供不同程度的针对水损失、氧化、机械损伤、光降解和/或生物应激源的保护,取决于植物种和植物器官(例如,果实、种子、树皮、花、叶、茎等)。角质(其为从细胞脂质衍生出的生物聚酯)形成角质层的主要结构组分,并且用于给植物提供免于环境应激源(非生物的和生物的)的保护。角质的厚度、密度以及组成(即,形成角质的单体的不同类型及其相对比例)可以随以下因素变化:植物种、在相同或不同植物种内的植物器官、和植物成熟的阶段。植物的含角质部分还可以含有另外的化合物(例如,上角质层蜡、酚、抗氧化剂、有色的化合物、蛋白质、多糖等)。植物种和/或植物器官和/或处于不同成熟阶段的给定植物之间的角质组成以及角质层的厚度和密度的这种变化可以导致在植物种或植物器官之间不同程度的对环境应激源(即,水损失、氧化、机械损伤和光)和/或生物应激源(例如,真菌、细菌、病毒、昆虫等)的攻击的抵抗。
发明内容
本文描述了从含角质的植物物质制备角质-衍生的单体、寡聚体或它们的组合的方法。所述方法可以包括在升高的温度和压强在溶剂中加热所述含角质的植物物质。
因此,在一个方面,本公开内容提供了一种从含角质的植物物质制备角质-衍生的单体、寡聚体或它们的组合的方法,所述方法包括:
从所述含角质的植物物质得到角质;
将所述角质加入溶剂以形成第一混合物,所述溶剂具有在1个大气压的压强下在第一温度的沸点;和
将所述第一混合物加热至第二温度和第二压强,所述第二温度高于所述第一温度且所述第二压强高于1个大气压,以形成包含所述角质-衍生的单体、寡聚体或它们的组合的第二混合物。
在另一个方面,本公开内容提供了一种形成植物提取物组合物的方法,所述方法包括:
从含角质的植物物质得到角质;
将所述角质加入第一溶剂以形成第一混合物,所述第一溶剂具有在1个大气压的压强下在第一温度的第一沸点;
将所述第一混合物加热至第二温度和第二压强,所述第二温度高于所述第一温度且所述第二压强高于1个大气压,以形成包含角质-衍生的单体、寡聚体或它们的组合的第二混合物;
将所述第一溶剂与所述第二混合物中的角质-衍生的单体、寡聚体或它们的组合分离;和
将所述角质-衍生的单体、寡聚体或它们的组合溶解在第二溶剂中。
在另一个方面,本公开内容提供了一种形成植物提取物组合物的方法,所述方法包括:
从含角质的植物物质得到角质;
将所述角质加入第一溶剂以形成第一混合物,所述第一溶剂具有在第一温度和第一压强的沸点;和
将所述第一混合物加热至第二温度,所述第二温度高于所述第一温度,以形成包含角质-衍生的单体、寡聚体或它们的组合的第二混合物,其中所述第二混合物中角质-衍生的单体或寡聚体的至少一部分是不饱和的。
在另一个方面,本公开内容提供了一种从含角质的植物物质制备角质-衍生的单体、寡聚体或它们的组合的方法,所述方法包括:
从所述含角质的植物物质得到角质;
将所述角质加入溶剂以形成第一混合物,所述溶剂具有在1个大气压的压强下在第一温度的沸点;
将所述第一混合物加热至第二温度和第二压强,所述第二温度高于所述第一温度且所述第二压强高于1个大气压,以形成包含第一组式I的化合物的第二混合物:
其中:
R1、R2、R3、R4、R5、R6、R7、R8、R9和R10各自独立地是-H、-OR13、-NR13R14、-SR13、卤素、-C1-C6烷基、-C1-C6烯基、-C1-C6炔基、-C3-C7环烷基、芳基或5--10-元环杂芳基,其中每个烷基、烯基、炔基、环烷基、芳基或杂芳基任选地被-OR13、-NR13R14、-SR13或卤素取代;
R13和R14各自独立地是-H、-C1-C6烷基、-C1-C6烯基或-C1-C6炔基;
R11是-H、-甘油基、-C1-C6烷基、-C1-C6烯基、-C1-C6炔基、-C3-C7环烷基、芳基或5-10元环杂芳基,其中每个烷基、烯基、炔基、环烷基、芳基或杂芳基任选地被-OR13、-NR13R14、-SR13或卤素取代;
R12是-OH、-H、-C1-C6烷基、-C1-C6烯基、-C1-C6炔基、-C3-C7环烷基、芳基或5-10元环杂芳基,其中每个烷基、烯基、炔基、环烷基、芳基或杂芳基任选地被-OR13、-NR13R14、-SR13、卤素、-COOH或-COOR11取代;且
m、n和o各自独立地是在0-30的范围内的整数,且0≤m+n+o≤30。
在另一个方面,本公开内容提供了一种制备组合物的方法,所述组合物包含角质-衍生的脂肪酸的酯。所述方法包括:从含角质的植物物质得到角质,和将所述角质加入溶剂以形成混合物,所述溶剂具有在1个大气压的压强下在第一温度的沸点。所述方法还包括将所述混合物加热至第二温度和第二压强,所述第二温度高于所述第一温度且所述第二压强高于1个大气压,由此形成包含所述酯的组合物。
在另一个方面,本公开内容提供了一种制备组合物的方法,所述组合物包含角质-衍生的游离脂肪酸单体、寡聚体或它们的组合。所述方法包括:从含角质的植物物质得到角质,将所述角质加入水以形成混合物。所述方法还包括将所述混合物从第一温度和第一压强加热至第二温度和第二压强,所述第二温度高于水在1个大气压下的沸点且所述第二压强高于1个大气压,由此形成包含角质-衍生的游离脂肪酸单体、寡聚体或它们的组合的组合物。
在另一个方面,本公开内容提供了一种形成保护性涂层的方法。所述方法包括:从第一植物种的角质层提取组合物,所述组合物包括多种角质-衍生的单体、寡聚体或它们的组合,和将所述组合物布置(dispose)在第二植物种上,所述第二植物种与所述第一植物种相同或不同以在所述第二植物种上面形成所述保护性涂层。
在另一个方面,本公开内容提供了一种形成保护性涂层的方法。所述方法包括:从第一植物的植物物质的角质层提取组合物,所述组合物包括多种角质-衍生的游离脂肪酸单体或寡聚体、脂肪酸酯或它们的组合,和将所述组合物布置在不同于所述第一植物的第二植物的植物物质上,由此在所述第二植物的植物物质上面形成所述保护性涂层。
在另一个方面,本公开内容提供了一种从含角质的植物物质制备角质-衍生的单体、寡聚体或它们的组合的方法,所述方法包括:
从所述含角质的植物物质得到角质;
将所述角质加入溶剂以形成第一混合物,所述溶剂具有在1个大气压的压强下在第一温度的沸点;
将所述第一混合物加热至第二温度和第二压强,所述第二温度高于所述第一温度且所述第二压强高于1个大气压,以形成包含第一组式II的化合物的第二混合物:
其中:
R1、R2、R4和R5各自独立地是-H、-OR11、-NR11R12、-SR11、卤素、-C1-C6烷基、-C1-C6烯基、-C1-C6炔基、-C3-C7环烷基、芳基或5-10元环杂芳基,其中每个烷基、烯基、炔基、环烷基、芳基或杂芳基任选地被-OR11、-NR11R12、-SR11或卤素取代;
R11和R12各自独立地是-H、-C1-C6烷基、-C1-C6烯基或-C1-C6炔基;
n是在0-11的范围内的整数;
m是在0-25的范围内的整数;且
0≤m+n≤25。
在另一个方面,本公开内容提供了一种从含角质的植物物质制备角质-衍生的单体、寡聚体或它们的组合的方法,所述方法包括:
从所述含角质的植物物质得到角质;
将所述角质加入溶剂以形成第一混合物,所述溶剂具有在1个大气压的压强下在第一温度的沸点;
将所述第一混合物加热至第二温度和第二压强,所述第二温度高于所述第一温度且所述第二压强高于1个大气压,以形成包含第一组式III的化合物的第二混合物:
其中:
R1、R2、R5、R6、R9、R10、R11、R12和R13在每次出现时各自独立地是-H、-OR14、-NR14R15、-SR14、卤素、-C1-C6烷基、-C2-C6烯基、-C2-C6炔基、-C3-C7环烷基、芳基或杂芳基,其中每个烷基、烯基、炔基、环烷基、芳基或杂芳基任选地被一个或多个-OR14、-NR14R15、-SR14或卤素取代;
R3、R4、R7和R8在每次出现时各自独立地是-H、-OR14、-NR14R15、-SR14、卤素、-C1-C6烷基、-C2-C6烯基、-C2-C6烯基、-C2-C6炔基、-C3-C7环烷基、芳基或杂芳基,其中每个烷基、炔基、环烷基、芳基或杂芳基任选地被一个或多个-OR14、-NR14R15、-SR14或卤素取代;或
R3和R4可以与它们所连接的碳原子组合以形成C3-C6环烷基、C4-C6环烯基或3-6元环杂环;和/或
R7和R8可以与它们所连接的碳原子组合以形成C3-C6环烷基、C4-C6环烯基或3-6元环杂环;
R14和R15在每次出现时各自独立地是-H、-C1-C6烷基、-C2-C6烯基或-C2-C6炔基;
n是0、1、2、3、4、5、6、7或8;
m是0、1、2或3;
q是0、1、2、3、4或5;且
r是0、1、2、3、4、5、6、7或8;且
R选自-H、-C1-C6烷基、-C2-C6烯基、-C2-C6炔基、-C3-C7环烷基、芳基、1-甘油、2-甘油或杂芳基。
本文描述的方法和制剂可以各自包括下述步骤或特征中的一个或多个,无论单独地还是彼此组合。可以将所述第二混合物冷却至第三温度,所述第三温度低于所述第二温度。冷却所述第二混合物的步骤可以进一步包括将所述第二压强降低至第三压强,所述第三压强低于所述第二压强。所述第三温度可以低于所述第一温度。所述第三压强可以与所述第一压强基本上相同。所述第三压强可以是约1个大气压。所述方法可以进一步包括将所述溶剂与所述第二混合物分离以分离所述角质-衍生的单体、寡聚体或它们的组合。所述第二温度可以比所述第一温度高至少5%。所述第二压强可以足够高以将液相中的所述溶剂的至少一部分维持在所述第二温度。所述第二压强可以高于所述第一压强。在将所述角质加入所述溶剂之前,可以将所述角质与所述植物物质的不含角质部分(non-cutincontaining portion)至少部分地分离。
所述形成第二混合物的方法可以进一步导致不饱和脂肪酸的产生。所述形成第二混合物的方法可以导致饱和的和不饱和的脂肪酸的产生。所述不饱和脂肪酸的产生可以是与脂肪酸链结合的羟基基团的消除的结果。饱和脂肪酸的浓度可以实质上高于所述第二混合物中不饱和脂肪酸的浓度。所述形成第二混合物的方法可以进一步导致不饱和脂肪酸的产生。所述形成第二混合物的方法可以导致饱和的和不饱和的脂肪酸酯的产生。所述不饱和脂肪酸酯的产生可以是与脂肪酸链结合的羟基基团的消除的结果。饱和脂肪酸酯的浓度可以实质上高于所述第二混合物中不饱和脂肪酸酯的浓度。
当所述第一混合物是在容器中时,可以执行所述第一混合物的加热,且所述方法可以进一步包括在加热所述第一混合物的过程中将气体或液体注入所述容器。在所述第二温度的解聚反应可以产生不带电荷的角质-衍生的单体、寡聚体或它们的组合。可以选择所述溶剂,使得当将所述溶剂保持在所述第二温度时,分散在其中的反应性阴离子和反应性阳离子的浓度足以至少部分地解聚所述角质和产生不带电荷的角质-衍生的单体、寡聚体或它们的组合。在所述第二温度和所述第二压强时所述溶剂中所述角质的解聚速率可以是在所述第一温度在1个大气压的压强下的至少100倍。所述第二混合物中的角质-衍生的单体、寡聚体或它们的组合可以在约298K基本上可溶于所述溶剂。所述第二温度可以大于约393K。所述第二温度可以是至少约498K。所述溶剂可以选自水、甘油、甲醇、乙醇、液体CO2和超临界CO2或它们的组合。所述溶剂可以是亲核溶剂。所述溶剂可以是水。所述第一混合物还可以包括共溶剂(co-solvent)。所述共溶剂可以包含CO2。所述溶剂可以基本上不含有加入的酸或碱。
所述第二温度可以是至少约498K,且所述第二压强可以是至少约360psi,并且可以将所述第一混合物在所述第二温度和第二压强保持至少约8小时。所述第二温度可以是至少约523K,且所述第二压强可以是至少约575psi,并且可以将所述第一混合物在所述第二温度和第二压强保持至少约2小时。所述第一混合物还可以包括反应性添加剂。所述反应性添加剂可以是酶、NaOH、Na2CO3、乙酸、pH调节剂或它们的组合。
在将所述角质加入所述第一溶剂之前,可以将所述角质与所述植物物质的不含角质部分至少部分地分离。可以将所述第二混合物中的角质-衍生的单体、寡聚体或它们的组合从未解聚的残余物中过滤并与所述第一溶剂分离。所述角质-衍生的单体、寡聚体或它们的组合的至少一部分可以是不饱和脂肪酸。所述方法可以进一步包括将所述不饱和脂肪酸氢化,然后将它们加入所述第二溶剂。可以将所述不饱和脂肪酸不经氢化溶解在所述第二溶剂中。所述角质-衍生的单体、寡聚体或它们的组合的至少一部分可以是不饱和脂肪酸酯。所述方法可以进一步包括将所述不饱和脂肪酸酯氢化,然后将它们加入所述第二溶剂。可以将所述不饱和脂肪酸酯不经氢化溶解在所述第二溶剂中。
所述方法可以进一步包括:将所述第一溶剂与所述第二混合物中的角质-衍生的单体、寡聚体或它们的组合分离,并将所述不饱和的角质-衍生的单体和寡聚体氢化以形成包含角质-衍生的单体、寡聚体或它们的组合的第三混合物,其中所述第三混合物中基本上所有的角质-衍生的单体或寡聚体是饱和的。所述第二混合物中不饱和的角质-衍生的单体和寡聚体可以在氢化之前与所述第二混合物中的饱和的角质-衍生的单体和寡聚体分离。在某些实施方案中,所述第二混合物中的不饱和的角质-衍生的单体和寡聚体在氢化之前没有与所述第二混合物中的饱和的角质-衍生的单体和寡聚体分离。所述第二混合物中的约10%至98%的角质-衍生的单体和寡聚体可以是不饱和的。所述第二混合物中的0.5%至30%、大于0%但是小于40%、小于10%、约1%至98%、1%至99%或基本上所有的角质-衍生的单体和寡聚体可以是不饱和的。所述方法可以进一步包括将所述第三混合物溶解在第二溶剂中。
所述方法可以进一步产生式II的化合物:
其中:
R1、R2、R4和R5各自独立地是-H、-OR11、-NR11R12、-SR11、卤素、-C1-C6烷基、-C1-C6烯基、-C1-C6炔基、-C3-C7环烷基、芳基或5-10元环杂芳基,其中每个烷基、烯基、炔基、环烷基、芳基或杂芳基任选地被-OR11、-NR11R12、-SR11或卤素取代;
R11和R12各自独立地是-H、-C1-C6烷基、-C1-C6烯基或-C1-C6炔基;
n是在0-11的范围内的整数;
m是在0-25的范围内的整数;且
0≤m+n≤25。
所述方法可以进一步产生第二组式I的化合物,所述第二组式I的化合物不同于所述第一组式I的化合物。所述方法可以产生式II的化合物,然后可以将其转化成式I的化合物,例如通过常规合成转化,其中由此形成的式I的化合物可以不同于通过热解聚直接产生的式I的化合物。例如,通过本文所述的水热解聚方法形成的酸可以随后转化成酯。所述保护性涂层的形成可以包括造成所述角质-衍生的单体、寡聚体或它们的组合的至少一些在所述第二植物种上交联。所述方法还可以包括,在将所述组合物布置在所述第二植物种上之前,化学修饰所述角质-衍生的单体、寡聚体或它们的组合。化学修饰所述角质-衍生的单体、寡聚体或它们的组合可以包括将所述角质-衍生的单体、寡聚体或它们的组合甘油酸酯化(例如,形成对应的脂肪酸或酯的甘油酯)。所述保护性涂层的化学组成可以不同于所述第二植物种的角质层的化学组成。从所述第一植物种的角质层提取所述组合物可以包括:从所述第一植物种的角质层得到角质,将所述角质加入溶剂以形成第一混合物,所述溶剂具有在1个大气压的压强下在第一温度的沸点,和将所述第一混合物加热至第二温度和第二压强,所述第二温度高于所述第一温度且所述第二压强高于1个大气压,以形成包含所述角质-衍生的单体、寡聚体或它们的组合的第二混合物。所述方法可以进一步包括修饰式II的化合物以形成式I的化合物,其中式II和式I如前面所述。所述方法可以进一步包括修饰式III的化合物以形成式I的化合物,其中式III和式I如前面所述。
向其中加入角质的溶剂可以包含乙醇,且得到的组合物的酯可以包含乙基酯。向其中加入角质的溶剂可以包含甲醇,且得到的组合物的酯可以包含甲基酯。向其中加入角质的溶剂可以包含甘油,且得到的组合物的酯可以包含甘油基酯。
本文中使用的术语“底物(substrate)”表示在其上面形成涂层或沉积物质的任何物体或材料。在特定实现中,所述底物是人类可食用的,且所述涂层是可食用的涂层。可食用的底物的例子包括农业产品和食品诸如水果、蔬菜、农产品(produce)、种子、坚果、牛肉、家禽和海味。尽管可以在底物的整个外表面上形成涂层,但是在某些实现中,所述涂层可以覆盖所述底物的外部分的表面。所述涂层还可以包括小孔或多孔区域,其暴露所述底物的部分的外表面。
本文中使用的“植物物质”表示植物的任何部分,例如,果实(在植物学意义上,包括果皮和汁囊)、叶、茎、皮、种子、花或植物的任意其它部分。
附图说明
图1是H2O的相图。
图2A、2B、2C、2D、2E和2F分别显示了10,16-二羟基十六烷酸、10,18-二羟基十八烷酸、9,16-二羟基十六烷酸、9,18-二羟基十八烷酸、9,10,16-三羟基十六烷酸、9,10,18-三羟基十八烷酸的化学结构。
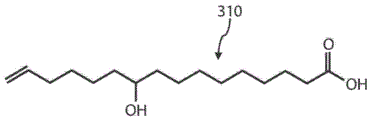
图3A、3B、3C、3D、3E、3F、3G、3H和3I是在热解聚过程中可以从10,16-二羟基十六烷酸单体和/或寡聚体的分解产生的副产物。
图4A和4B是直接解聚产物和不饱和间接副产物的相对浓度随着时间而变化的定性图,其源自当将水用作溶剂时角质的热解聚。
图5A、5B和5C是可以从角质的热解聚的不饱和间接副产物形成的分子的化学组成。
图6A和6B是通过溶剂(其包括乙醇)中角质的热解聚可以形成的酯。
图6C和6D是通过溶剂(其包括甲醇)中角质的热解聚可以形成的酯。
图6E、6F、6G和6H是通过溶剂(其包括甘油)中角质的热解聚可以形成的酯。
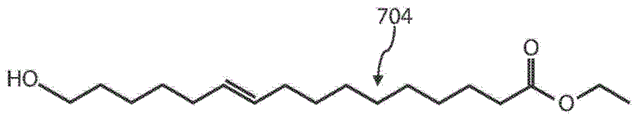
图7A、7B、7C、7D、7E、7F、7G、7H和7I是通过溶剂(其包括乙醇)中角质的热解聚可以形成的酯。
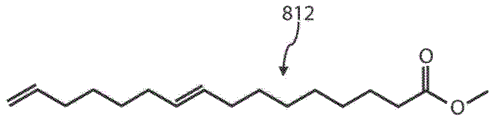
图8A、8B、8C、8D、8E、8F、8G、8H和8I是通过溶剂(其包括甲醇)中角质的热解聚可以形成的酯。
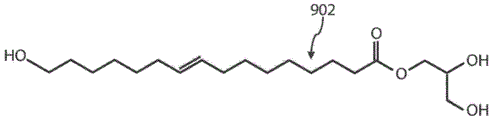
图9A、9B、9C、9D、9E、9F、9G、9H和9I是通过溶剂(其包括甘油)中角质的热解聚可以形成的酯。
图10A、10B、10C、10D、10E、10F、10G、10H和10I是通过溶剂(其包括甘油)中角质的热解聚可以形成的酯。
图11解释了一种用于形成保护性涂层的方法。
图12A解释了对于不同的温度和反应持续时间,通过角质在水中的热解聚回收的粗制角质单体和/或寡聚体的量的图。
图12B解释了对于不同的温度和停留时间,在索克斯累特(soxhlet)萃取以后从庚烷沉淀物中的粗制角质单体和/或寡聚体分离的产物(饱和产物和/或不饱和副产物)的量的图。
图12C是对于不同的温度和停留时间,在索克斯累特萃取以后从庚烷上清液中的粗制角质单体和/或寡聚体分离的不饱和副产物的量的图。
图12D解释了对于不同的温度和停留时间,在索克斯累特萃取以后从乙酸乙酯上清液中的粗制角质单体和/或寡聚体分离的饱和产物的量的图。
图13的表示出了在不同的温度和反应持续时间在水中热水解以后,使用庚烷和乙酸乙酯在索克斯累特萃取以后分离的产物的性质。
图14A是对于不同的温度和停留时间通过角质在乙醇中的热解聚回收的粗产物的百分比的图。
图14B是对于不同的温度和停留时间,在角质在乙醇中的热解聚过程中从庚烷沉淀物回收的产物的百分比的图。
图14C是对于不同的温度和停留时间,在角质在乙醇中的热解聚过程中从庚烷上清液回收的产物的百分比的图。
图15的表示出了对于角质在乙醇中的热解聚,在不同的解聚温度和停留时间从庚烷沉淀物和从庚烷上清液回收哪些产物。
图16是用通过本文描述的方法形成的组合物涂布的鳄梨的质量损失速率的图。
图17显示了在548K水热解聚1小时以后回收的粗产物的UPLC迹线。
图18显示了在提取前在548K水热解聚1小时以后回收的10,16-二羟基十六烷酸的UPLC迹线(traces)和质谱法分析。
图19显示了在提取前在548K水热解聚1小时以后回收的不饱和脂肪酸的UPLC迹线和质谱法分析。
图20显示了在548K水热解聚1小时和使用庚烷的索克斯累特萃取后从庚烷沉淀物回收的10,16-二羟基十六烷酸的UPLC迹线和质谱法分析。
图21显示了在548K水热解聚1小时和使用庚烷的索克斯累特萃取后从庚烷上清液回收的不饱和脂肪酸的UPLC迹线和质谱法分析。
图22显示了在548K水热解聚1小时和使用乙酸乙酯的索克斯累特萃取后从乙酸乙酯上清液回收的10,16-二羟基十六烷酸的UPLC迹线和质谱法分析。
图23显示了在548K乙醇分解解聚4小时后回收的粗产物的UPLC迹线。
图24显示了在548K乙醇分解解聚4小时和使用庚烷的索克斯累特萃取后从庚烷上清液回收的10,16-二羟基十六酸乙酯的UPLC迹线和质谱法分析。
图25显示了在548K乙醇分解解聚4小时和使用庚烷的索克斯累特萃取后从庚烷上清液回收的不饱和脂肪酸乙酯的UPLC迹线和质谱法分析。
在各附图中的相同引用符号表示相同元素。
详细描述
生物聚酯角质形成角质层的主要结构组分,其组成大多数陆生植物的空气表面并在给植物提供针对非生物和生物应激源的保护屏障中发挥显著作用。角质的厚度、密度以及组成(即,形成角质的单体的不同类型及其相对比例)可以随以下因素变化:植物种,在相同或不同植物种内的植物器官,和植物成熟阶段。这些变化可以定义由角质层向植物或植物器官提供的针对环境和/或生物应激源的保护的量、程度或品质(和可塑性程度)。角质由聚合的单羟基和/或多羟基脂肪酸以及包埋的角质蜡的混合物形成。角质层的羟基脂肪酸形成具有高交联密度的紧密结合的网络,由此作为水分损失和氧化的屏障起作用,以及提供针对其它环境应激源的保护。
本文描述了从植物物质制备和形成植物提取物组合物的方法。所述植物提取物组合物从角质或其它交联的聚合物(例如,聚酯)的分解(例如,解聚)形成,且包括在角质层或其它交联的聚合物网络中发现的羟基脂肪酸和羟基脂肪酸酯(以及它们的寡聚体及其混合物)。随后可以将植物提取物组合物应用于其它植物或农业产品,以便在所述产品上面形成保护性涂层,或增强或改变在所述产品的外表面上的既有涂层(天然存在的或沉积的涂层)。应用的涂层可以例如起作用以保护所述产品免于生物应激源诸如细菌、真菌、病毒和/或害虫。应用的涂层还可以(或可替代地)起作用以在不经冷冻的情况下增加产品(produce)的贮存期限和/或控制产品(produce)的成熟速率。形成植物提取物组合物的方法可以导致所述组合物基本上不含有其它伴随的植物衍生的化合物(例如,蛋白、多糖、酚、木酚素、芳族酸、萜类化合物、类黄酮、类胡萝卜素、生物碱、醇、烷烃和醛),由此改善随后形成的保护性涂层的效力。
如上所述,所述植物提取物组合物的单体和/或寡聚体单元可以由在植物物质中发现的角质获得。植物物质通常包括含有角质和/或具有高密度角质的一些部分(例如,果皮、叶、嫩枝等),以及不含有角质或具有低密度角质的其它部分(例如,果肉、种子等)。含角质部分可以用于生产包含角质-衍生的单体和/或寡聚体的植物提取物组合物,且也可以包括其它组分诸如蛋白、多糖、酚、木酚素、芳族酸、萜类化合物、类黄酮、类胡萝卜素、生物碱、醇、烷烃和醛。低角质密度或不含角质的部分可以经常缺乏单体和/或寡聚体单元,或者要不然包括低得多的单体和/或寡聚体单元与其它组分的比率(相对于含有较高密度角质的部分)。
本文描述的用于形成植物提取物组合物的方法可以包括:首先将植物物质的含角质部分与不含角质部分分离(或至少部分地分离),和从所述含角质部分得到角质(例如,当所述含角质部分是果皮时,将所述果皮与果实本体(fruit body)分离,和/或将所述角质与所述果皮分离)。然后使用热过程(在下面详细描述)将角质或含角质的果皮解聚(或至少部分地解聚),以便得到包括多种脂肪酸或酯化的角质-衍生的单体、寡聚体或它们的组合的混合物。解聚的热过程造成所述混合物的大多数或基本上所有的(例如,至少95%的)得到的单体和/或寡聚体被质子化或赋予中性(即,不带电荷),不需要任何另外的过程(例如,酸化)。换而言之,本文描述的解聚过程可以在没有加入的碱或酸存在下进行。这导致所述单体和/或寡聚体处于这样的状态:使得它们可以随后被化学修饰以提供化合物,其性质可以为特定应用定制。例如,通过化学修饰所述单体和/或寡聚体可以控制随后形成的涂层的氧和水屏障性质,并且这样的修饰可能要求首先将所述单体和/或寡聚体质子化或赋予中性。此外,可以定制单体和/或寡聚体的化学修饰以改变提取物组合物的溶解度,从而允许用于扩大的涂布沉积选项。最后,将包括游离脂肪酸和/或游离脂肪酸酯单体和/或寡聚体单元的混合物溶解在另一种溶剂中以形成溶液,由此产生适合用于涂布应用(例如,农业涂布应用)的植物提取物组合物。任选地,在形成植物提取物组合物之前,将所述混合物的游离脂肪酸和/或游离脂肪酸酯单体和/或寡聚体单元活化或修饰(例如,甘油酸酯化),例如以形成1-单酰甘油酯和/或2-单酰甘油酯的混合物,并将经修饰的单体和/或寡聚体单元(例如,1-单酰甘油酯和/或2-单酰甘油酯)的混合物溶解在溶剂中以形成溶液,由此产生植物提取物组合物。
如上所述,为了形成适合用于涂布应用的角质-衍生的植物提取物组合物,首先将植物物质的含角质部分与不含角质部分分离(或至少部分地分离)。这可以通过许多方法实现,无论单独地还是彼此组合地。例如,可以热和/或机械和/或酶促和/或化学地处理所述植物物质以将含角质部分与不含角质部分至少部分地分离。或者,可以使所述植物物质在水性介质中经受升高的温度和/或压强(例如,如在加压蒸煮中)以将植物物质的含角质部分与不含角质部分部分地分离。可替换地,可以使所述植物物质经受较低的温度(例如,如在冷冻中)以将植物物质的含角质部分与不含角质部分部分地分离。还可以对所述植物物质进行在水性介质中的声处理以将植物物质的含角质部分与不含角质部分部分地分离。任选地,可以在草酸铵和草酸的混合物中加热含角质部分以辅助角质与不含角质部分(即,角质层的剩余物和不希望的植物物质)的分离。任选地,该分离可以使用能够水解酯键的酶和/或可替换地使用能够分解多糖(其构成植物的不含角质部分)的酶来酶促地实现(或辅助)。可以任选地将含角质部分在至少一种有机溶剂(诸如氯仿和/或甲醇)中回流以从角质除去残余的蜡和/或任何剩余的可溶性组分。可替换地,使用液体或超临界CO2可以实现残余的蜡和剩余的可溶性组分的除去。
将植物物质的含角质部分与不含角质部分分离(或至少部分地分离)以后,然后将从植物物质得到的角质(或含角质组分)加入溶剂中以形成第一混合物。所述溶剂可以例如是亲核溶剂诸如水、甲醇、乙醇、甘油或它们的组合。所述第一混合物可以任选地包括共溶剂诸如水、甲醇、乙醇、甘油、液体CO2或超临界CO2。所述共溶剂还可以是亲核的(例如,当所述共溶剂是水、甲醇、甘油或乙醇时),或可替换地所述共溶剂可以不是亲核的(例如,当所述共溶剂是液体CO2或超临界CO2时)。任选地,所述溶剂可以充当反应改性剂。任选地,所述共溶剂可以充当催化剂以解聚含角质的部分,且所述溶剂可以用于将中间解聚产物转酯化。任选地,所述溶剂还可以包括反应性添加剂或加工助剂诸如酶、NaOH、Na2CO3、乙酸、另一种pH调节剂或它们的组合。如果包括反应性添加剂或加工助剂,所述反应性添加剂或加工助剂的浓度可以足够低,使得角质的实质解聚在没有下述热条件存在下不会发生。可替换地,可以包括足够高浓度的反应性添加剂或加工助剂以催化所述解聚过程,且可以执行热过程来进一步增强或增加所述解聚过程的反应速率。
然后使包括在溶剂(和任选地共溶剂和/或反应性添加剂或加工助剂)中的含角质组分的第一混合物经受升高的温度和压强(即,热过程)足够长的时间以允许所述角质(或含角质组分)至少部分地解聚成角质-衍生的单体、寡聚体、其酯或它们的组合,由此形成包含角质-衍生的单体、寡聚体、其酯或它们的组合的第二混合物。例如,可以将所述第一混合物放在容器中,使得大约50-100%的容器体积被所述第一混合物填充,且然后可以将所述容器和装入的第一混合物密封并加热至大于所述溶剂在大气压下的沸点(即,如果将所述溶剂维持在1个大气压它已经沸腾的温度)的温度。例如,可以将所述容器和装入的第一混合物加热到特定温度以上,所述特定温度比所述溶剂在大气压下(即,在1个大气压)的沸点大至少5%、至少10%、至少15%、至少20%、至少25%、至少30%、至少40%、至少45%、至少50%、至少55%、至少60%、至少65%、至少70%、至少75%、至少80%、至少85%、至少90%或至少100%。在某些实现中,所述溶剂是水,并将混合物加热至至少393K、至少423K、至少453K、至少473K、至少498K或至少523K的温度。在某些实现中,将所述混合物维持在1000K的温度以下。
由于混合物(和在密封容器中的任何空气或其它气体或流体)的热膨胀以及溶剂的蒸发,所述容器内的压强在升高的温度增加,且可以例如是大于1atm、大于5atm、大于10atm或大于100atm。在某些实现中,所述压强自我调节至这样的值:其在或接近所述溶剂在升高的温度的液体-气体转变点的值,如下面进一步描述的。所述压强可以任选地在所述容器内进一步增加,例如通过将氮气泵入所述容器中,或通过将溶剂泵入所述容器中,并通过返流或压强调节器来维持压强。可以将第一混合物保持在升高的温度和压强预定量的时间,其足以造成第一混合物中的含角质组分解聚成角质-衍生的单体、寡聚体、酯或它们的组合,由此形成所述第二混合物。在将所述第一混合物保持在升高的温度和压强预定量的时间以形成第二混合物以后,将所述第二混合物冷却并释放压力。
这里使用的缩写包括DHPA[10,16-二羟基十六烷酸]、MEHPA[(E/Z)-16-羟基十六碳-9-烯酸]、EtDHPA[10.16-二羟基十六烷酸乙酯]和EtMEHPA[(E/Z)-16-羟基十六碳-9-烯酸乙酯]。
本文中使用的术语“温度”表示绝对温度,如以开耳文温度(K)的单位测量的。因此,如果第一温度比第二温度大X%,所述第一温度(以K为单位测量)是所述第二温度(以K为单位测量)的至少(1+X/100)倍。例如,就在1个大气压具有373.15K的沸点的水而言,在1个大气压比水的沸点大至少5%的温度对应于大于391.81K(即,大于1.05×373.15K)的温度。
在某些实现中,由热解聚过程产生的角质-衍生的单体、寡聚体、酯或它们的组合在以下温度可溶于所述溶剂中:进行所述热过程时的升高的温度,以及还有随后将第二混合物冷却至的温度(通常室温)。当所述溶剂是例如乙醇或甲醇时,可以是这种情况。在其它实现中,由热解聚过程产生的角质-衍生的单体、寡聚体、酯或它们的组合在以下温度不溶于所述溶剂中:进行所述热过程时的升高的温度,以及还有随后将第二混合物冷却至的温度。在其它实现中,由热解聚过程产生的角质-衍生的单体、寡聚体、酯或它们的组合在进行所述热过程时的升高的温度可溶于所述溶剂,但是在随后将第二混合物冷却至的温度(例如,室温或约300K)是不溶性的。在该情况下,在升高的温度溶解的单体、寡聚体、酯或它们的组合随着将第二混合物冷却至室温而沉淀,从而导致所述单体、寡聚体、酯或它们的组合悬浮于所述溶剂中,且例如与作为固体焦炭的其它非角质植物物质混合。当将水用作溶剂时,例如,角质-衍生的单体、寡聚体、酯或它们的组合通常在室温可以是不溶性的,但是在升高的温度和压强可以是或不是可溶性的,取决于所述角质源自的具体植物。
如前面描述的,当将第一混合物加热至升高的温度并将它保持在该温度时,可以增加所述容器内的压强,以确保至少50%的所述溶剂维持在液相中。例如,考虑图1中所示的水(H2O)的相图100。当将在1个大气压具有约373K的沸点的水用作第一混合物中的溶剂时,可以将所述第一混合物加热至大于373K的第二温度(例如,图1中的温度104)并基本上维持在液相(如果也将压强增加至第二压强,其大于或约等于在该特定温度的液-气相界面处的压强)。例如,当将所述第一混合物加热至温度104时,所述压强可以增加,使得所述混合物中的水是在图1的相图100中的点102。
如前面描述的,可以实现在升高的温度将至少50%的溶剂维持在液相所需的增加的压强,例如,通过密封所述容器,使得所述容器中的压强随着温度升高而增加,这归因于混合物的热膨胀、溶剂的一些部分的蒸发和/或密封容器中的任何空气或其它气体或流体的热膨胀。得到的所述容器中的压强可以自我调节,使得它大约是在液体-气体转变点。例如,所述压强可以调节至在升高的温度在液体-气体转变点的1%内、2%内或5%内的值。得到的压强的确切值至少部分地取决于用所述混合物填充的容器的体积百分比。但是,如果填充比过大,例如,如果填充比接近1,压强可能变得对于所述容器而言过高,而不能机械地支持。因此,在某些实现中,超过50%但是小于99%的容器体积被混合物填充。例如,60%至95%或70%至95%的容器体积可以被混合物填充。此外,在某些实现中,在升高的温度在所述容器中的压强足以将至少60%、至少70%、至少80%、至少90%或基本上所有的溶剂维持在液相。
另外,通过将另外的气体或液体(例如氮气)泵入所述容器中,可以进一步增加在所述容器内的压强。这可以允许借助于压强调节器或返流阻止器(backflow preventer)而直接控制在所述容器内的压强以便更好地优化解聚过程,这在下面进一步描述。此外,如果液体含有要处理的另外的材料,可以实现流过反应(flow through reaction)。
可以选择在其中解聚含角质部分的溶剂,使得含角质部分在室温(例如,在300K)基本上不解聚,和/或在1个大气压在低于沸点的温度基本上不解聚或具有非常低的解聚速率。因而,在许多情况下,解聚速率仅对于在将温度升高至实质上高于所述溶剂的大气压沸点(例如,在大气压沸点以上至少5%或至少10%)时发生实质解聚而言是足够高的。这样,为了将溶剂维持在液相从而使得解聚可以发生,因此升高所述容器中的压强,如前面描述的。
可替换地,通过酸化或碱化所述溶剂,例如通过将金属氢氧化物加入所述溶剂,可以在室温或在低于所述溶剂的大气压沸点的温度实现含角质部分的实质解聚。但是,上述的热解聚过程可以提供胜过这样的过程的某些优点。例如,热解聚过程可以在所述溶剂中自我产生反应性阴离子和阳离子,由此将所述角质解聚成单体/寡聚体单元。解聚产物是固有地不带电荷的,这对于随后修饰(例如,酯化或甘油酸酯化)所述单体/寡聚体单元而言和/或对于从所述单体/寡聚体单元形成保护性涂层而言可能是必要的或合乎需要的。相反,在强碱中的解聚通常不会产生不带电荷的解聚过程的单体和/或寡聚体产物。这样,可能需要在其中中和单体/寡聚体产物的额外步骤,以便从所述单体/寡聚体单元形成具有合乎需要的性质的保护性涂层。另外,从解聚过程省略强酸和/或碱的使用,可以导致所述过程被认为是完全有机的。
可以选择进行热解聚过程的具体温度、以及所述溶剂的组成,使得当将所述溶剂保持在升高的温度(和对应的升高的压强)时,所述溶剂中的反应性阴离子和反应性阳离子的浓度足以解聚所述角质。可以进一步选择温度,使得在升高的温度(和对应的升高的压强)所述溶剂中所述角质的解聚速率是在标准温度和压强时的至少100倍。例如,当将H2O用作热解聚过程的溶剂时,所述温度可以大于393K,例如至少413K、至少433K、至少453K、至少473K、大于483K、大于498K、大于513K、大于523K、在473K和523K之间或在493K和533K之间。在某些实现中,使用超临界H2O作为溶剂并任选地使用超临界CO2作为共溶剂进行热解聚过程,在该情况下,升高的温度大于647K且压强大于218个大气压(例如,在218-1000个大气压之间)。在某些实现中,使用超临界乙醇作为溶剂并任选地使用超临界CO2作为共溶剂进行热解聚过程,在该情况下,升高的温度可以大于514K且压强可以大于60.6个大气压(例如,在60.6和1000个大气压之间)。
图2A显示了10,16-二羟基十六烷酸(图2A中的200)的化学组成,图2B显示了10,18-二羟基十八烷酸(图2B中的202)的化学组成,它们二者是用水作为溶剂进行的角质热解聚过程的典型直接单体产物,并形成角质的主要构建单元。从用水作为溶剂进行的角质热解聚过程可以产生的其它直接单体产物显示在图2C、2D、2E和2F中,其中图2C显示了9,16-二羟基十六烷酸(图2C中的204)的化学组成,图2D显示了9,18-二羟基十八烷酸(图2D中的206)的化学组成,图2E显示了9,10,16-三羟基十六烷酸(图2E中的208)的化学组成,和图2F显示了9,10,18-三羟基十八烷酸(图2F中的210)的化学组成。从热解聚过程直接产生的确切产物取决于角质的特定植物来源和在其中进行热解聚过程的溶剂。例如,来自番茄的角质倾向于具有高比例的C16酸(例如,具有16的碳链长度的脂肪酸)诸如图2A、2C、2E和2G的酸,而来自酸果蔓的角质倾向于具有高比例的C18酸诸如图2B、2D和2F的酸。在某些实现中,所述热解聚过程产生式I的化合物:
其中R1、R2、R3、R4、R5、R6、R7、R8、R9、R10、R11、R12、m、n和o如前面关于式I所定义。在某些实施方案中,在式I中的R1、R2、R3、R4、R5、R6、R7、R8、R9、R10、R11、R12是H。
除了式I的化合物、以及分别在图2A-2F中的分子200、202、204、206、208和210的单体和/或寡聚体以外,在水中进行热解聚过程期间也可能形成其它产物,通过其它方法对角质的解聚不形成所述其它产物。例如,在水中进行热解聚过程期间可以形成分别在图3A-3I中的不饱和产物302、304、306、308、310、312、314、316和/或318。在这里,图3A解释了(E)-16-羟基十六碳-9-烯酸(302),图3B解释了(E)-16-羟基十六碳-10-烯酸(304),图3C解释了(Z)-16-羟基十六碳-9-烯酸(306),图3D解释了(Z)-16-羟基十六碳-10-烯酸(308),图3E解释了10-羟基十六碳-15-烯酸(310),图3F解释了(E)-十六碳-9,15-二烯酸(312),图3G解释了(E)-十六碳-10,15-二烯酸(314),图3H解释了(Z)-十六碳-9,15-二烯酸(316),和图3I解释了(Z)-十六碳-10,15-二烯酸(318)。一般而言,本文描述的热解聚方法可以产生式II的化合物:
其中R1、R2、R3、R3’、R4、R5、R6、R6’、m和n如前面关于式II所定义。在某些实施方案中,在式II中的R1、R2、R3、R3’、R4、R5、R6、R6’是H。
在某些实施方案中,本文描述的热解聚方法可以产生式III的化合物:
其中:
R1、R2、R5、R6、R9、R10、R11、R12和R13在每次出现时各自独立地是-H、-OR14、-NR14R15、-SR14、卤素、-C1-C6烷基、-C2-C6烯基、-C2-C6炔基、-C3-C7环烷基、芳基或杂芳基,其中每个烷基、烯基、炔基、环烷基、芳基或杂芳基任选地被一个或多个-OR14、-NR14R15、-SR14或卤素取代;
R3、R4、R7和R8在每次出现时各自独立地是-H、-OR14、-NR14R15、-SR14、卤素、-C1-C6烷基、-C2-C6烯基、-C2-C6烯基、-C2-C6炔基、-C3-C7环烷基、芳基或杂芳基,其中每个烷基、炔基、环烷基、芳基或杂芳基任选地被一个或多个-OR14、-NR14R15、-SR14或卤素取代;或
R3和R4可以与它们所连接的碳原子组合以形成C3-C6环烷基、C4-C6环烯基或3-6元环杂环;和/或
R7和R8可以与它们所连接的碳原子组合以形成C3-C6环烷基、C4-C6环烯基或3-6元环杂环;
R14和R15在每次出现时各自独立地是-H、-C1-C6烷基、-C2-C6烯基或-C2-C6炔基;
n是0、1、2、3、4、5、6、7或8;
m是0、1、2或3;
q是0、1、2、3、4或5;且
r是0、1、2、3、4、5、6、7或8;且
R选自-H、-C1-C6烷基、-C2-C6烯基、-C2-C6炔基、-C3-C7环烷基、芳基、1-甘油、2-甘油或杂芳基。
在某些实施方案中,R可以是-H、-CH3或-CH2CH3。
在某些实施方案中,本文描述的热解聚方法可以产生式III-A的化合物:
其中:
每个Ra独立地是-H或-C1-C6烷基;
每个Rb独立地选自-H、-C1-C6烷基或-OH;
R1、R2、R5、R6、R9、R10、R11、R12和R13在每次出现时各自独立地是-H、-OR14、-NR14R15、-SR14、卤素、-C1-C6烷基、-C2-C6烯基、-C2-C6炔基、-C3-C7环烷基、芳基或杂芳基,其中每个烷基、烯基、炔基、环烷基、芳基或杂芳基任选地被一个或多个-OR14、-NR14R15、-SR14或卤素取代;
R3、R4、R7和R8在每次出现时各自独立地是-H、-OR14、-NR14R15、-SR14、卤素、-C1-C6烷基、-C2-C6烯基、-C2-C6炔基、-C3-C7环烷基、芳基或杂芳基,其中每个烷基、炔基、环烷基、芳基或杂芳基任选地被一个或多个-OR14、-NR14R15、-SR14或卤素取代;或
R3和R4可以与它们所连接的碳原子组合以形成C3-C6环烷基、C4-C6环烯基或3-6元环杂环;和/或
R7和R8可以与它们所连接的碳原子组合以形成C3-C6环烷基、C4-C6环烯基或3-6元环杂环;
R14和R15在每次出现时各自独立地是-H、-C1-C6烷基、-C2-C6烯基或-C2-C6炔基;
n是0、1、2、3、4、5、6、7或8;
m是0、1、2或3;
q是0、1、2、3、4或5;且
r是0、1、2、3、4、5、6、7或8。
在某些实施方案中,本文描述的热解聚方法可以产生式III-B的化合物:
其中:
每个Ra独立地是-H或-C1-C6烷基;
每个Rb独立地选自-H、-C1-C6烷基或-OH;
R1、R2、R5、R6、R9、R10、R11、R12和R13在每次出现时各自独立地是-H、-OR14、-NR14R15、-SR14、卤素、-C1-C6烷基、-C2-C6烯基、-C2-C6炔基、-C3-C7环烷基、芳基或杂芳基,其中每个烷基、烯基、炔基、环烷基、芳基或杂芳基任选地被一个或多个-OR14、-NR14R15、-SR14或卤素取代;
R3、R4、R7和R8在每次出现时各自独立地是-H、-OR14、-NR14R15、-SR14、卤素、-C1-C6烷基、-C2-C6烯基、-C2-C6炔基、-C3-C7环烷基、芳基或杂芳基,其中每个烷基、烯基、炔基、环烷基、芳基或杂芳基任选地被一个或多个-OR14、-NR14R15、-SR14或卤素取代;或
R3和R4可以与它们所连接的碳原子组合以形成C3-C6环烷基、C4-C6环烯基或3-6元环杂环;和/或
R7和R8可以与它们所连接的碳原子组合以形成C3-C6环烷基、C4-C6环烯基或3-6元环杂环;
R14和R15在每次出现时各自独立地是-H、-C1-C6烷基、-C2-C6烯基或-C2-C6炔基;
n是0、1、2、3、4、5、6、7或8;
m是0、1、2或3;
q是0、1、2、3、4或5;且
r是0、1、2、3、4、5、6、7或8。
在某些实施方案中,本文描述的热解聚方法可以产生下述脂肪酸化合物中的一种或多种:
在某些实施方案中,本文描述的热解聚方法可以产生下述甲基酯化合物中的一种或多种:
在某些实施方案中,本文描述的热解聚方法可以产生下述乙基酯化合物中的一种或多种:
在某些实施方案中,本文描述的热解聚方法可以产生下述2-甘油酯化合物中的一种或多种:
在某些实施方案中,本文描述的热解聚方法可以产生下述1-甘油酯化合物中的一种或多种:
在某些实施方案中,本文所述化合物(例如,式I、II或III的化合物)中的任一种可以交联产生二聚体、三聚体或寡聚体。例如,二聚体可以具有下述结构:
本领域技术人员会理解,根据本公开内容可以制备其它交联的二聚体、三聚体或寡聚体。另外,本领域技术人员会理解,在本文描述的用于解聚角质的温度和压强,可以发生伯醇或仲醇的氧化。例如,当在有氧(例如,空气)存在下进行时,可能将醇部分氧化成对应的酮。
不希望受理论的约束,据信,饱和产物(例如,200、202、204、206、208和/或210)在角质层内交联,且由此通过解聚反应直接分离成单体和/或寡聚体单元,而不饱和产物(例如,302、304、306、308、310、312、314、316、318和/或式II的产物)是通过直接产物(例如,200、202、204、206、208和/或210)的分解形成的间接副产物。所述分解可以发生,例如,如果在热解聚过程中将高温和/或高压条件维持过长的时间段,其中产生不饱和副产物所需的时间长度随温度升高而缩短。但是,不饱和产物(例如,302、304、306、308、310、312、314、316、318和/或式II的产物)也可能存在于角质层中且由此在通过本文描述的热解聚方法形成所述组合物时变成提取物组合物的组分,但是当使用其它方法(例如,酸性或碱性解聚)进行角质解聚时,这些产物的产生受到遏制或抑制。或者,不饱和产物可以作为热解聚过程的部分而产生。
在某些实现中,优选的是角质解聚的直接产物(例如,200、202、204、206、208和/或210)存在于第二混合物中,而不是从所述直接产物的分解(例如,消除)产生的间接不饱和副产物(例如,302、304、306、308、310、312、314、316、318和/或式II的产物)。例如,当得到的第二混合物随后用于形成保护性涂层时,在许多情况下,当第二混合物包括大比例的饱和解聚产物(例如,200、202、204、206、208和/或210)同时具有尽可能小的不饱和间接副产物(例如,302、304、306、308、310、312、314、316、318和/或式II的产物)浓度时,所述涂层可以具有合乎需要的性质(例如,更高的交联密度、更低的水和/或氧渗透性)。这样,可以调节热解聚过程的条件(例如,溶剂组合物、温度、压强、所述混合物在高温和压强的停留时间、以及加热和冷却所述混合物的时间),使得所述混合物在解聚以后包括大比例的直接产物,诸如单体200、202、204、206、208和/或210(和任选地其形成的寡聚体)。
在某些实现中,使用本文描述的解聚过程的角质向角质-衍生的单体和/或寡聚体单元或酯(直接产物和间接副产物)的转化率(按质量)可以是至少5%、至少10%、至少20%、至少30%、至少40%、至少50%、至少60%、至少70%、至少80%、至少90%或至少95%。此外,在得到的单体和/或寡聚体和/或酯解聚产物(直接产物和间接副产物)中,至少50%、至少60%、至少70%、至少80%、至少90%或至少95%可以是直接产物诸如单体200和/或202(和/或其形成的寡聚体)。可以将所述解聚产物进一步纯化,例如通过选择性过滤,以形成适合用于涂布应用的植物提取物组合物,其为直接解聚产物诸如单体200、202、204、206、208和/或210(和/或其形成的寡聚体)或由所述直接解聚产物形成的酯化或甘油酸酯化化合物的基本上纯的组合物。
在热解聚过程中将所述混合物保持在升高的温度和压强的持续时间可以至少部分地取决于升高的温度和压强的具体值、以及加热和冷却所述混合物所需的时间。通常,较低的温度和/或压强需要较长的停留时间以实现角质向单体和/或寡聚体单元的高转化率。因而可能优选的是使用较高的温度和/或压强以便减小处理时间。但是,过高的温度可以造成直接单体/寡聚体(例如,图2A-2F各自的单体200、202、204、206、208或210)分解成其它副产物,如前面所述(例如,在图3中),其在许多情况下可以不利地影响随后从植物提取物组合物形成的涂层的性质。例如,在520K长于1小时的停留时间(residence time)可以导致显著量的不饱和产物,且所述分解在甚至更高的温度进一步加速。
图4A和4B是当将水用作溶剂时对于不同的热解聚条件随着时间而变化的在所述混合物中的直接解聚产物(例如,200、202、204、206、208和/或210)和不饱和间接副产物(例如,302、304、306、308、310、312、314、316和/或318)的相对浓度的定性图。图4A对应于498K的温度和约22.1个大气压(约325psi)的压强,而图4B对应于523K的温度和约37.4个大气压(约550psi)的压强。在两种情况下,所述角质得自番茄皮。402和404代表在热解聚过程中在不同时间在所述混合物中的直接解聚单体产物(例如,200、202、204、206、208和/或210的单体)的相对浓度,而406和408代表在热解聚过程中在不同时间在所述混合物中的间接不饱和副产物(例如,302、304、306、308、310、312、314、316和/或318)的相对浓度。
如在图4A和4B中所见,在两种条件下,在时间t=0(在热解聚过程开始时),在所述混合物中不存在实质浓度的直接或间接解聚产物。现在参考图4A,在498K,直接解聚单体产物的浓度随时间稳定升高,直到所述浓度在几乎8小时以后饱和(参见402)。但是,如果将升高的温度维持超过约8小时,直接解聚单体产物的浓度开始下降,这对应于直接解聚单体产物向不饱和副产物的分解。因此,在498K,不饱和副产物的浓度保持较低直到约8小时,在此时,它随着直接解聚单体产物开始分解而开始升高(参见406)。
现在参考图4B,在523K,直接解聚单体产物的浓度稳定地升高,并然后在约1小时以后达到饱和(参见404)。不久以后,随着直接解聚单体产物开始分解成不饱和副产物,直接解聚单体产物的浓度开始下降。相应地,在523K,不饱和副产物的浓度保持较低直到接近约1小时,在此时,它随着直接解聚单体产物开始分解而开始升高(参见408)。对于在523K大于约2小时的时间,不饱和副产物的浓度增加至大于直接解聚单体产物的浓度的值。这样,在498K和22.1个大气压在水中,从番茄皮衍生出的角质向单体的实质转化在约8小时的过程中发生,但是在523K和37.4个大气压,所述转化需要小于1小时。
在图4A中还定性地解释了随着时间而变化的具有1<n<10的寡聚体(n-聚体)的浓度(410)。如看到的,最初,寡聚体浓度以比单体浓度快得多的速率升高。但是,在远远小于8小时的时间以后,寡聚体浓度饱和,并然后下降至远远小于单体浓度的值。不希望受理论的约束,据信,在498K和22.1个大气压在水中,所述角质最初主要分解成寡聚体单元(n-聚体,1<n<10),且所述寡聚体单元随后分解成单体单元。
在较高温度和/或压强直接单体/寡聚体产物(例如,分别在图2A-2F中的200、202、204、206、208或210)向不饱和副产物(诸如图3A-3I的那些)的分解的速率进一步受加热至升高的温度和/或从升高的温度冷却的速率影响。在某些实施方案中,在特定的升高的温度和压强,对于给定的停留时间,较长的加热和/或冷却时间可以导致较高的单体/寡聚体分解成不饱和副产物的速率。这样,为了阻止或遏制该分解,尽可能快速地加热和冷却所述混合物可以是优选的。例如,在某些实现中,大于10℃/min、大于20℃/min或大于40℃/min的加热和冷却速率是优选的,更快的速率是更优选的。
同样可以使用用于使所述混合物经受升高的温度和/或压强的其它方法。具体地,使温度升高和下降时间最小化的方法可以是优选的,因为它们可以降低单体/寡聚体在较高温度和/或压强的分解速率,并允许更好的过程控制。例如,可以使用浆进料或连续流过程,其中使所述混合物穿过一系列阀门(所述混合物可以穿过它们流动)连续地流入并然后流出所述容器,并同时允许控制所述容器内的温度和压强。或者,也可以使用电介质加热来加热所述混合物。
在某些实现中,可能优选的是,某些百分比(例如,大于20%、大于40%、大于60%、大于70%、大于80%或大于90%)的直接解聚产物(例如,分别图2A-2F的单体200、202、204、206、208和/或210)分解成通常不会得自角质(或含角质组分)的解聚的其它单体/寡聚体副产物(例如,图3A-3I各自的不饱和副产物302、304、306、308、310、312、314、316和318)。具体地,可以将图3A-3I各自的不饱和副产物302、304、306、308、310、312、314、316和318以及式II的化合物各自分离和进一步加工以形成其它饱和分子诸如在图5A、5B和5C中所示的那些,其中图5A解释了9,10,16-三羟基十六烷酸(502),图5B解释了16-羟基十六烷酸(504),且图5C解释了棕榈酸(506)。类似地,可以将不饱和的酯副产物(诸如在图7A-7I、8A-8I、9A-9I和10A-10I中所示并在下面更详细地描述的那些)各自分离和进一步加工以形成其它饱和分子诸如在图6A-6H中所示的那些(其也在下面更详细地描述)。例如,参考图4B,可以驱动将饱和单体转化成不饱和副产物的反应至结束,例如通过在523K和37.4个大气压在水中进行热解聚过程大于2小时的时间。然后可以将不饱和副产物用催化剂(例如Ni或Pd)氢化以形成棕榈酸506或16-羟基十六烷酸504。因此,在这样的过程中,可以从非棕榈来源形成棕榈酸。从油棕生产棕榈油具有大的环境影响,包括滥伐和生境损失,以及社会学影响,因为在发展中世界中土著人经常被转移以给大量种植腾出空间。因为这些原因,可以合乎需要的是从非棕榈来源得到棕榈酸。
可替换地,在驱动将饱和单体转化成不饱和副产物的反应至结束以后,可以将所述不饱和副产物用催化剂(例如,四氧化锇或另一种羟基化试剂)羟基化以形成,例如,9,10,16-三羟基十六烷酸(502)或式I的其它化合物,其中式I如前面所定义。
用于形成保护性涂层的植物提取物组合物随后可以从图2A、2B、2C、2D、2E、2F、5A、5B和5C各自的分子200、202、204、206、208、210、502、504或506中的任一种以及任意其它直接解聚产物(例如,式I的化合物)形成。所述涂层可以各自主要由这些类型的分子之一形成,或可替换地由这些分子的组合形成。可替换地,可以首先将所述分子酯化(例如,甘油酸酯化以形成1-单酰甘油酯和/或2-单酰甘油酯),所述植物提取物组合物可以由所述酯或甘油酸酯化分子形成,且所述涂层可以由植物提取物组合物中的所述酯或甘油酸酯化分子形成。从由分子502或分子504形成的植物提取物组合物、或者从分子200、202、204、206、208、210、502、504和506的组合、或者从由其形成的酯或甘油酸酯化分子形成涂层,可以允许对提取物组合物和涂层的性质进一步控制。例如,分子502、504和506(和由其形成的酯或甘油酸酯化分子)在不同溶剂中的溶解度不同于分子200、202、204、206、208和210(和由其形成的酯或甘油酸酯化分子)的溶解度。这样,与可以用于仅包括大量角质解聚的直接副产物(例如,分子200、202、204、206、208和/或210、或由其形成的酯或甘油酸酯化分子)的植物提取物组合物相比,更宽种类的溶剂可用于从分子502、504或506(或由其形成的酯或甘油酸酯化分子)、或从分子200、202、204、206、208、210、502、504和506(或由其形成的酯或甘油酸酯化分子)的组合形成植物提取物组合物。此外,可以为使用分子502、504和506(和/或由其形成的酯或甘油酸酯化分子)(单独地或与分子200、202、204、206、208、210组合和/或彼此组合)的特定应用进一步定制从植物提取物形成的涂层的性质。例如,得到的保护膜的交联密度可以随植物提取物组合物中的分子200、202、204、206、208、210、502、504和506(和/或由其形成的酯或甘油酸酯化分子)中的每一种的质量百分比而变化,其可以允许为在其中使用所述膜的特定应用特别定制膜性质诸如密度和渗透性。此外,可以化学修饰这些分子以便定制它们的性质,例如,溶解度、稳定性和膜形成性质。
如前面描述的,在某些实现中,从解聚(例如,化合物200、202、204、206、208或210)直接地或通过后续加工步骤(例如,化合物502、504或506)间接地得到的分子/化合物被甘油酸酯化以形成1-单酰甘油酯和/或2-单酰甘油酯单体、其形成的寡聚体、或组合。在该情况下,随后从其形成保护性涂层的植物提取物组合物包括任选地溶解在溶剂中的1-单酰甘油酯和/或2-单酰甘油酯。1-单酰甘油酯和2-单酰甘油酯之间的差异是甘油酯基的连接点。本公开内容的发明人已经在许多情况下发现,从包括2-单酰甘油酯和1-单酰甘油酯的组合(或任选地,替代1-单酰甘油酯的不同添加剂)的制剂在底物(诸如水果)上形成的保护性涂层在阻止水损失和氧化中表现出优异性能,而不会改变所述底物的物理外观。
尽管在本文描述的热解聚过程以后可以经由酯化(例如,Fischer酯化)形成直接解聚产物200或202的酯(例如,甘油基酯),但是可替换地可以通过合适的溶剂选择在热解聚过程中直接形成酯。例如,当在水中进行角质的热解聚时,得到的直接解聚产物可以是游离脂肪酸(例如,图2A-2F的化合物200、202、204、206、208或210)。但是,角质在其它溶剂(例如,乙醇、甲醇或甘油)中的热解聚可以直接导致酯的产生。
例如,图6A和6B分别显示了10,16-二羟基十六酸乙酯600和10,18-二羟基十八烷酸乙酯602的化学结构,它们分别是化合物10,16-二羟基十六烷酸(图2A中的200)和10,18-二羟基十八烷酸(图2B中的202)的乙酯。通过在乙醇中进行角质的热解聚,或可替换地通过在包括乙醇的溶剂(例如含有作为共溶剂加入的乙醇的水)中进行热解聚过程,可以直接地生产化合物600和/或602。
作为另一个实施例,图6C和6D分别显示了10,16-二羟基十六烷酸甲酯610和10,18-二羟基十八烷酸甲酯612的化学结构,它们分别是化合物10,16-二羟基十六烷酸(图2A中的200)和10,18-二羟基十八烷酸(图2B中的202)的甲酯。通过在甲醇中进行角质的热解聚,或可替换地通过在包括甲醇的溶剂中(例如在含有作为共溶剂加入的甲醇的水中)进行热解聚过程,可以直接地生产化合物610和/或612。
作为另一个实施例,图6E、6F、6G和6H分别显示了10,16-二羟基十六烷酸2,3-二羟基丙酯620、10,16-二羟基十六烷酸1,3-二羟基丙-2-基酯630、10,18-二羟基十八烷酸2,3-二羟基丙酯622和10,18-二羟基十八烷酸1,3-二羟基丙-2-基酯632的化学结构。化合物620和630是10,16-二羟基十六烷酸(图2A中的200)的甘油基酯,且化合物622和632是10,18-二羟基十八烷酸(图2B中的202)的甘油基酯。通过在甘油中进行角质的热解聚,或可替换地通过在包括甘油的溶剂中(例如在含有作为共溶剂加入的甘油的水中)进行热解聚过程,可以直接生产化合物620、630、622和/或632。
还可以在本文描述的热解聚过程以后经由酯化(例如,Fischer酯化)形成不饱和副产物(例如,图3A-3I中的化合物302、304、306、308、310、312、314、316和318)的酯。例如,参考图4B,可以驱动将饱和单体转化成不饱和副产物(302、304、306、308、310、312、314、316和/或318)的热过程至结束,例如通过在水中在523K和37.4个大气压进行角质的热解聚大于2小时的时间,然后可以将不饱和副产物酯化。可替换地,类似于上面关于酯600、602、610、612、620、622、630和632的直接形成所述的过程,可以通过合适的溶剂选择在热解聚过程中直接形成不饱和副产物的酯。具体地,当在水中进行角质的热解聚时,得到的不饱和副产物可以是不饱和脂肪酸(例如,化合物302、304、306、308、310、312、314、316和/或318)。但是,角质在其它溶剂(例如,乙醇、甲醇或甘油)中的热解聚可以直接导致不饱和脂肪酸酯的产生。
例如,图7A显示了(E)-16-羟基十六碳-9-烯酸乙酯702的化学结构,图7B显示了(E)-16-羟基十六碳-10-烯酸乙酯704的化学结构,图7C显示了(Z)-16-羟基十六碳-9-烯酸乙酯706的化学结构,图7D显示了(Z)-16-羟基十六碳-10-烯酸乙酯708的化学结构,图7E显示了10-羟基十六碳-15-烯酸乙酯710的化学结构,图7F显示了(E)-十六碳-9,15-二烯酸乙酯712的化学结构,图7G显示了(E)-十六碳-10,15-二烯酸乙酯714的化学结构,图7H显示了(Z)-十六碳-9,15-二烯酸乙酯716的化学结构,以及图7I显示了(Z)-十六碳-10,15-二烯酸乙酯718的化学结构。化合物702是化合物302的乙酯,化合物704是化合物304的乙酯,化合物706是化合物306的乙酯,化合物708是化合物308的乙酯,化合物710是化合物310的乙酯,化合物712是化合物312的乙酯,化合物714是化合物314的乙酯,化合物716是化合物316的乙酯,以及化合物718是化合物318的乙酯。通过在足够高的温度在乙醇中进行角质的热解聚足够长的时间,或可替换地通过在包括乙醇的溶剂(例如含有作为共溶剂加入的乙醇的水)中进行热解聚过程,可以直接生产化合物702、704、706、708、710、712、714、716和/或718。
作为另一个实例,图8A显示了(E)-16-羟基十六碳-9-烯酸甲酯802的化学结构,图8B显示了(E)-16-羟基十六碳-10-烯酸甲酯804的化学结构,图8C显示了(Z)-16-羟基十六碳-9-烯酸甲酯806的化学结构,图8D显示了(Z)-16-羟基十六碳-10-烯酸甲酯808的化学结构,图8E显示了10-羟基十六碳-15-烯酸甲酯810的化学结构,图8F显示了(E)-十六碳-9,15-二烯酸甲酯812的化学结构,图8G显示了(E)-十六碳-10,15-二烯酸甲酯814的化学结构,图8H显示了(Z)-十六碳-9,15-二烯酸甲酯816的化学结构,以及图8I显示了(Z)-十六碳-10,15-二烯酸甲酯818的化学结构。化合物802是化合物302的甲酯,化合物804是化合物304的甲酯,化合物806是化合物306的甲酯,化合物808是化合物308的甲酯,化合物810是化合物310的甲酯,化合物812是化合物312的甲酯,化合物814是化合物314的甲酯,化合物816是化合物316的甲酯,以及化合物818是化合物318的甲酯。通过在足够高的温度在甲醇中进行角质的热解聚足够长的时间,或可替换地通过在包括甲醇的溶剂(例如含有作为共溶剂加入的甲醇的水)中进行热解聚过程,可以直接生产化合物802、804、806、808、810、812、814、816和/或818。
作为另一个实施例,图9A显示了(E)-16-羟基十六碳-9-烯酸2,3-二羟基丙酯902的化学结构,图9B显示了(E)-16-羟基十六碳-10-烯酸2,3-二羟基丙酯904的化学结构,图9C显示了(Z)-16-羟基十六碳-9-烯酸2,3-二羟基丙酯906的化学结构,图9D显示了(Z)-16-羟基十六碳-10-烯酸2,3-二羟基丙酯908的化学结构,图9E显示了10-羟基十六碳-15-烯酸2,3-二羟基丙酯910的化学结构,图9F显示了(E)-十六碳-9,15-二烯酸2,3-二羟基丙酯912的化学结构,图9G显示了(E)-十六碳-10,15-二烯酸2,3-二羟基丙酯914的化学结构,图9H显示了(Z)-十六碳-9,15-二烯酸2,3-二羟基丙酯916的化学结构,以及图9I显示了(Z)-十六碳-10,15-二烯酸2,3-二羟基丙酯918的化学结构。化合物902是化合物302的甘油基酯,化合物904是化合物304的甘油基酯,化合物906是化合物306的甘油基酯,化合物908是化合物308的甘油基酯,化合物910是化合物310的甘油基酯,化合物912是化合物312的甘油基酯,化合物914是化合物314的甘油基酯,化合物916是化合物316的甘油基酯,以及化合物918是化合物318的甘油基酯。
作为再一个实例,图10A显示了(E)-16-羟基十六碳-9-烯酸1,3-二羟基丙烷-2-基酯1002的化学结构,图10B显示了(E)-16-羟基十六碳-10-烯酸1,3-二羟基丙烷-2-基酯1004的化学结构,图10C显示了(Z)-16-羟基十六碳-9-烯酸1,3-二羟基丙烷-2-基酯1006的化学结构,图10D显示了(Z)-16-羟基十六碳-10-烯酸1,3-二羟基丙烷-2-基酯1008的化学结构,图10E显示了10-羟基十六碳-15-烯酸1,3-二羟基丙烷-2-基酯1010的化学结构,图10F显示了(E)-十六碳-9,15-二烯酸1,3-二羟基丙烷-2-基酯1012的化学结构,图10G显示了(E)-十六碳-10,15-二烯酸1,3-二羟基丙烷-2-基酯1014的化学结构,图10H显示了(Z)-十六碳-9,15-二烯酸1,3-二羟基丙烷-2-基酯1016的化学结构,以及图10I显示了(Z)-十六碳-10,15-二烯酸1,3-二羟基丙烷-2-基酯1018的化学结构。化合物1002是化合物302的甘油基酯,化合物1004是化合物304的甘油基酯,化合物1006是化合物306的甘油基酯,化合物1008是化合物308的甘油基酯,化合物1010是化合物310的甘油基酯,化合物1012是化合物312的甘油基酯,化合物1014是化合物314的甘油基酯,化合物1016是化合物316的甘油基酯,以及化合物1018是化合物318的甘油基酯。通过在足够高的温度在甘油中进行角质的热解聚足够长的时间,或可替换地通过在包括甲醇的溶剂(例如含有作为共溶剂加入的甲醇的水)中进行热解聚过程,可以直接生产化合物902、904、906、908、910、912、914、916、918、1002、1004、1006、1008、1010、1012、1014、1016和/或1018。
在某些实现中,混合物的溶剂(即,在其中进行所述热解聚过程的溶剂)在标准温度和压强(即,约273K和约1个大气压)下是液体,但是当达到升高的温度和压强时至少部分地经历相变化。例如,在所述溶剂是水(H2O)的情况下,如果使混合物的温度升高到647K以上且使压强升高到218个大气压以上,H2O变成超临界的,并在超临界H2O中进行所述热解聚过程。或者,在所述溶剂是乙醇的情况下,如果使混合物的温度升高到513.9K以上且使压强升高到60.6个大气压以上,乙醇变成超临界的,并在超临界乙醇中进行所述热解聚过程。
因为得自含角质部分的角质通常与前述的许多其它组分混合,得自热解聚过程的提取物可能具有比在农业涂布应用中可耐受的水平更高的杂质组分水平。这样,通过选择性地除去或滤出杂质组分,可以纯化角质。选择性过滤可以在解聚过程之前或之后发生,或者在解聚之前和之后发生。选择性过滤可以包括下述过程中的一种或多种:
(a)在解聚或部分地解聚角质之前,在选择性溶剂中洗涤和/或加热角质,杂质组分在所述选择性溶剂中的溶解度高于所述角质的溶解度。在该情况下,杂质溶解在选择性溶剂中,由此导致在解聚以后的随即第一中间提取物中的更少杂质。这样的溶剂的例子可以包括氯仿、乙醚、二氯甲烷、己烷、石油醚、乙酸乙酯、丙酮、异丙醇、乙醇、甲醇、超临界二氧化碳、超临界水、水、及其混合物。
(b)在解聚或部分地解聚角质以得到包含第一中间提取物(其包括在溶剂中的解聚产物)的第二混合物以后,在选择性溶剂(例如,庚烷、乙酸乙酯、乙腈等)中洗涤和/或加热所述第一中间提取物,杂质组分在所述选择性溶剂中的溶解度低于所述单体和/或寡聚体的溶解度。在该情况下,单体和/或寡聚体被溶解在选择性溶剂中,而杂质不会。然后可以将杂质滤出,从而产生溶解在选择性溶剂中的第二中间提取物,其中所述第二中间提取物具有比所述第一中间提取物更高的纯度。随后可以将所述第二中间提取物固化,例如,通过蒸发所述选择性溶剂。
(c)在解聚或部分地解聚角质以得到包含第一中间提取物(其包括在溶剂中的解聚产物)的第二混合物以后,在选择性溶剂(例如,氯仿或己烷)中洗涤和/或加热所述第一中间提取物,杂质组分在所述选择性溶剂中的溶解度高于所述单体和/或寡聚体的溶解度。在该情况下,杂质被溶解在选择性溶剂中,由此从所述提取物除去杂质,并得到具有比所述第一中间提取物更高的纯度的第二中间提取物。
(d)从植物物质的含角质部分得到包含角质的化合物之后和在解聚或部分地解聚所述角质之前,将所述化合物暴露于超临界二氧化碳以选择性地降低蛋白、多糖、酚、木酚素、芳族酸、萜类化合物、类黄酮、类胡萝卜素、生物碱、醇、烷烃、醛、蜡、未表征的有色杂质或未列出的任意其它杂质中的至少一种的浓度。
(e)在解聚或部分地解聚角质以得到包含第一中间提取物(其包括在溶剂中的解聚产物)的第二混合物以后,将第二溶剂加入所述混合物,其中所述第一溶剂和第二溶剂是不可混溶的,所述第二溶剂具有这样的性质:相对于所述第一溶剂,杂质或单体/寡聚体(但不是二者都)选择性地分离到所述第二溶剂中。
(f)在解聚或部分地解聚角质以得到包含第一中间提取物(其包括溶解在溶剂中的解聚产物)的第二混合物以后,造成单体/寡聚体结晶并将它们从混合物中过滤,或可替换地造成杂质结晶并将它们从混合物中过滤。
使用在图11中图解的方法1100,可以从上述的植物提取物组合物形成保护性涂层。首先,将单体和/或寡聚体单元的固体混合物溶解在溶剂(例如,水、乙醇或它们的组合)中以形成植物提取物组合物(步骤1102)。所述溶剂中的固体混合物的浓度可以例如是在约0.1-100mg/mL的范围内。接着,将包括单体和/或寡聚体单元的溶液施加于要涂布的底物的表面上(步骤1104),例如通过喷雾涂布底物或通过将底物浸入溶液中。在喷雾涂布的情况下,可以例如将溶液放在产生细雾喷雾的喷雾瓶中。然后可以将喷雾瓶头保持在离底物大约6-12英寸,然后将底物喷雾。在浸渍涂布的情况下,可以例如将底物放在袋中,将含有所述组合物的溶液倒入袋中,并然后将所述袋密封和轻轻搅动,直到底物的整个表面是湿的。将所述溶液施加于底物以后,允许所述底物干燥直到所有的溶剂已经蒸发,由此允许由单体和/或寡聚体单元组成的涂层在底物的表面上形成(步骤1106)。
本文描述的涂层和方法会提供许多胜过目前的保持农业产品和食品的新鲜度的方法的独特特征和优点。例如,所述涂层可以阻止水损失和保护农业产品免于威胁诸如细菌、真菌、病毒等。所述涂层还可以保护例如植物和食物产品免于物理损伤(例如,擦伤)、水损失、氧化和光损伤。因此,可以使用所述组合物、溶液和涂层来帮助储存农业产品延长的时间段而不腐坏。在某些情况下,所述组合物和涂层允许食品在没有冷冻存在下保持新鲜。本文描述的组合物和涂层还可以是可食用的(即,所述涂层可以对于人消费而言是无毒的)。用于形成本文描述的涂层的方法可以是完全有机的。在某些实现中,所述涂层是无味的、无色和/或无臭的。所述涂层可以由在植物角质层中发现的天然的相同化学原料(例如,羟基和/或二羟基棕榈酸,和/或羟基油酸和硬脂酸)制成,且因而可以是有机的和全天然的。
在某些实现中,从提取自第一植物种的角质(例如,利用前面描述的热解聚过程)的角质衍生的单体和/或寡聚体和/或其酯形成植物提取物组合物,然后将所述组合物布置在相同植物种的植物物质上面,使得提取的单体和/或寡聚体和/或酯在第一植物种的植物物质上面形成保护性涂层。这样的涂层可以例如增强在所述植物物质上面天然存在的角质层。在其它实现中,从提取自第一植物种的角质(例如,利用前面描述的热解聚过程)的角质衍生的单体和/或寡聚体和/或酯形成植物提取物组合物,然后将所述组合物布置在不同于(尽管在某些情况下,可以相同)所述第一植物种的第二植物种的植物物质上面,使得提取的单体和/或寡聚体和/或酯在所述第二植物的植物物质种上面形成保护性涂层。例如,可以从提取自角质(其得自番茄或蔓越莓皮)的单体和/或寡聚体和/或酯形成植物提取物组合物,然后施加于草莓、香蕉、指橙(finger limes)、柠檬或不同于所述角质的来源植物种的其它植物种上面,以便形成保护性涂层。这样,从植物提取物组合物的单体和/或寡聚体和/或酯形成的保护性涂层可以提供对抗生物和非生物应激源的保护形式(其为第二植物种的天然角质层固有地不能提供)。例如,与天然角质层可以固有地提供的效果相比,沉积在所述底物上的保护性涂层可以提供对抗水损失和氧化的优良保护。或者,可以将植物提取物组合物配制成抑制真菌生长或提供对抗真菌生长的保护(其为天然角质层几乎不会提供或根本不会提供的保护)。在某些实现中,在将所述组合物布置在植物物质上面以形成涂层之前,将角质衍生的单体和/或寡聚体甘油酸酯化以形成单酰甘油酯。这可以例如增加单体和/或寡聚体的反应性并允许它们在布置于植物物质上面以后交联。
在某些实施方案中,可以将解聚反应的饱和产物(例如,图2中的游离脂肪酸化合物200和202)与本文描述的解聚反应的不饱和产物(或副产物)(例如,图3A-3I中的不饱和脂肪酸化合物)分离或至少部分地分离。在某些实施方案中,分离或至少部分地分离不同类型的反应产物的能力可以用于纯化例如饱和产物(即,其中羟基基团已经被消除的化合物)。换而言之,提取本文所述的水热解聚反应的粗产物根据使用的溶剂可以用于纯化或富集给定产物的百分比。
如在下面实施例(例如,实施例2、3和7)中所述,就在水中热解聚角质以产生游离脂肪酸而言,首先使用索克斯累特(soxhlet)设备和庚烷萃取来自解聚反应的粗制分离物。过夜萃取并冷却得到的庚烷以后,发现萃取的产物的部分从庚烷相沉淀。发现所述沉淀物含有饱和产物(例如,化合物200和202)、不饱和产物(例如,化合物302和304)、或饱和及不饱和产物的混合物。但是,发现庚烷上清液含有富集(例如,超过90%、超过95%、超过96%、超过97%、超过98%或超过99%)不饱和脂肪酸(例如,属于图3中所示的类型)的解聚产物。
在使用庚烷的索克斯累特萃取以后,使用索克斯累特设备和乙酸乙酯再次萃取粗制分离物。发现得到的乙酸乙酯相含有富集(例如,超过90%、超过95%、超过96%、超过97%、超过98%或超过99%)饱和脂肪酸的产物,例如化合物诸如200和202。
图12A显示了使用15g番茄渣作为起始原料在不同温度和反应时间在水中热解聚以后回收的粗制分离物的图。回收率作为原始15g投入的百分比给出。如在图12A中所示,在更长的反应时间(例如,约4小时)以后和在相对更高的温度(例如,约250℃或更高)回收通常更多的粗制分离物(即,角质-衍生的单体和寡聚体)。
使用索克斯累特萃取器使用庚烷和乙酸乙酯萃取来自图12A的粗制分离物。图12B显示了相对于最初的15g番茄渣在使用庚烷的第一次索克斯累特萃取以后回收的分离物的量。具体地,图12B显示了在索克斯累特萃取以后从庚烷沉淀的分离物的量。相反,图12C显示了在索克斯累特萃取以后保持溶解在庚烷上清液中的分离物的量(相对于用作起始原料的15g番茄渣)。不希望受理论的约束,发现己烷萃取的上清液主要含有(例如,超过90%或基本上所有的)本文描述的水热反应的不饱和游离脂肪酸副产物(例如,化合物诸如来自图3的3A-3I)。
图12D显示了在使用乙酸乙酯作为溶剂的索克斯累特萃取以后从庚烷萃取的粗制分离物回收的分离物的量。相对于用作起始原料的15g番茄渣给出所述量。不希望受理论的约束,发现使用乙酸乙酯萃取的物质主要含有(例如,超过90%或基本上所有的)本文描述的水热反应的饱和游离脂肪酸产物(例如,化合物诸如来自图2的200和202)。
图13给出的表格概括了分别使用庚烷和乙酸乙酯对从水热解聚回收的粗制分离物的两次索克斯累特萃取以后,从庚烷沉淀物、庚烷上清液和乙酸乙酯上清液分离的产物。左侧列给出了用于解聚角质以产生粗制角质分离物的水热反应条件。
图17显示了在548K水热解聚1小时以后回收的粗产物的UPLC迹线(UPLC traces)。图18显示了在提取以前在548K水热解聚1小时以后回收的10,16-二羟基十六烷酸的UPLC迹线和质谱法分析。图19显示了在提取以前在548K水热解聚1小时以后回收的不饱和脂肪酸的UPLC迹线和质谱法分析。图20显示了在548K水热解聚1小时和使用庚烷的索克斯累特萃取以后从庚烷沉淀物回收的10,16-二羟基十六烷酸的UPLC迹线和质谱法分析。图21显示了在548K水热解聚1小时和使用庚烷的索克斯累特萃取以后从庚烷上清液回收的不饱和脂肪酸的UPLC迹线和质谱法分析。图22显示了在548K水热解聚1小时和使用乙酸乙酯的索克斯累特萃取以后从乙酸乙酯上清液回收的10,16-二羟基十六烷酸的UPLC迹线和质谱法分析。
除了水热解聚的产物以外,可以使用选择性的或至少部分地选择性的萃取(例如,索克斯累特萃取)和不同的溶剂(例如,不同极性的溶剂)类似地分离或至少部分地分离乙醇分解的产物(即,乙酯)。
例如,如在下面实施例(例如,实施例4、5和8)中所述,可以使用庚烷对分离自乙醇分解的粗产物进行索克斯累特萃取。在某些实施方案中,从乙醇分解分离的乙酯可以具有比通过水解分离的游离脂肪酸更低的极性。如在下面实施例中所述,使用庚烷进行粗制乙醇分解物质的过夜索克斯累特萃取并随后冷却以后,发现从庚烷萃取物形成沉淀物。发现所述庚烷沉淀物含有富集(例如,超过90%、超过95%、超过96%、超过97%、超过98%或超过99%)饱和乙酯的产物(例如,羟基化产物诸如化合物600或化合物602)。相反,发现上清液含有富集(例如,超过90%、超过95%、超过96%、超过97%、超过98%或超过99%)不饱和乙酯的溶解的产物,例如化合物诸如在图7A-图7I中所示的那些。在某些实施方案中,没有针对庚烷萃取的乙醇分解分离物进行乙酸乙酯萃取。例如,在某些实施方案中,一旦冷却,来自庚烷萃取的饱和的(例如,羟基化的)产物的选择性沉淀足以实现羟基化产物的纯化(例如,通过过滤)。
图14A显示了使用15g番茄渣作为起始原料在不同温度和反应时间在乙醇中热解聚以后回收的粗制分离物的图。回收率作为原始15g投入的百分比给出。如在图14A中所示,在更长的反应时间(例如,约4小时)以后和在相对更高的温度(例如,约523K或更高)回收通常更多的粗制分离物(即,角质-衍生的单体和寡聚体)。
使用索克斯累特萃取器使用庚烷萃取来自图14A的粗制分离物。图14B显示了相对于最初的15g番茄渣使用庚烷进行索克斯累特萃取以后回收的分离物的量。具体地,图14B显示了在索克斯累特萃取和冷却以后从庚烷沉淀的分离物的量。相反,图14C显示了在索克斯累特萃取以后保持溶解在庚烷上清液中的分离物的量(相对于用作起始原料的15g番茄渣)。不希望受理论的约束,发现己烷萃取的上清液主要含有(例如,超过90%或基本上所有的)本文描述的水热反应的不饱和乙酯副产物(例如,化合物诸如来自图7的7A-7I)(即,保持溶解在庚烷上清液中的不饱和乙酯)。
不希望受理论的约束,发现在萃取以后从庚烷沉淀的物质(其可以通过过滤分离)主要含有(例如,超过90%或基本上所有的)本文描述的水热反应的饱和乙酯产物(例如,化合物诸如来自图6的600和602)。
图15给出的表格概括了在索克斯累特萃取从乙醇分解解聚回收的粗制分离物以后从庚烷沉淀物和庚烷上清液分离的产物。左侧列给出了用于解聚角质以产生粗制角质分离物的乙醇分解反应条件。
图23显示了在548K乙醇分解解聚4小时以后回收的粗产物的UPLC迹线。图24显示了在548K乙醇分解解聚4小时和使用庚烷的索克斯累特萃取以后从庚烷上清液回收的10,16-二羟基十六酸乙酯的UPLC迹线和质谱法分析。图25显示了在548K乙醇分解解聚4小时和使用庚烷的索克斯累特萃取以后从庚烷上清液回收的不饱和脂肪酸乙酯的UPLC迹线和质谱法分析。
实施例
下述实施例和合成实施例进一步解释了本公开内容,它们不应当解释为将本公开内容的范围或精神限制为本文描述的具体操作。应当理解,提供了实施例来解释某些实施方案,并不意图限制本公开内容的范围。进一步应当理解,可以包括本领域技术人员可能显而易见的各种其它的实施方案,修改及其等同方案,而不背离本公开内容的精神和/或所附权利要求书的范围。所有溶剂和其它化学试剂得自商业来源(例如,Sigma-Aldrich(St.Louis,MO)),并不经进一步纯化地使用,除非另有指出。
已经进行下述步骤来执行本文描述的热解聚过程中的一种或多种,其中将角质层物质热处理成游离脂肪酸。对于实施例2-5中的每一个,进行完整过程多次以便收集统计上显著的数据。在适用时,在这些实施例中,将呈现的数据给出为不同重复的平均值,以及从所述平均值的统计偏差。
实施例1:在解聚之前制备番茄渣的方法
将得自市售番茄加工设施的番茄渣在粉碎机中切碎,并过筛以得到不同的粒度分布(例如>500μm、250-500μm、125-250μm等)。与250-500μm对应的级分依次经历氯仿(CHCl3)过夜和甲醇过夜的索克斯累特萃取以除去表面蜡和其它可溶性组分,随后在真空下(<1托)干燥。然后将经洗涤的渣低压冻干(<0.02托)过夜以除去水,然后储存在干燥器中备用。
实施例2:在498K在水中解聚角质
将15g 250-500μm经萃取的番茄渣(来自实施例1)加入具有600mL的内部体积的Parr 4563B反应器。向其中加入375mL水,此后将系统密封并将反应器固定至系统,随后加热至约498K的目标温度(target temperature)。从环境室温(通常约298K)至目标温度的加热时间是约45分钟。然后将所述混合物在498K保持约8小时,此后将它通过内部冷却环快速冷却至25℃和40℃之间的温度。
冷却后,将反应器去压、拆卸和去密封。将反应器的内部组件和壁用乙酸乙酯冲洗,直到所有物质从壁松解,并将得到的固体/液体混合物透过中孔隙率过滤器玻璃料(medium porosity filter frit)过滤。将反应器主体用第二部分的乙酸乙酯洗涤,并将其透过滤饼过滤。将固体饼(其产生‘焦炭’或残余物质)用另外部分的乙酸乙酯洗涤。乙酸乙酯洗液的典型总体积是约350mL。将过滤收集的水/乙酸乙酯混合物在1L分液漏斗中分离。分离各相,并将有机层收集和通过加入硫酸镁干燥,然后透过多孔玻璃料过滤。然后将乙酸乙酯通过旋转蒸发从有机相除去并在高真空下(P<0.1托)进一步干燥。得到的粗提取组合物(其包括饱和的和不饱和的脂肪酸)的总质量是平均2.86g[平均]±0.23g(n=3)。
收集粗提取组合物以后进行纯化。首先,将粗提取物溶解在甲醇中,此后加入3倍质量的硅藻土545。通过旋转蒸发除去甲醇,从而使所述物质沉积在硅藻土上。将该混合物转移至纤维素萃取套筒(thimble),并将玻璃绒放在所述混合物的顶部。将所述套筒置于索克斯累特萃取器中,用氮气冲洗,并用500mL庚烷萃取过夜。
冷却后,一些单体产物(例如,图2A中的200)或不饱和副产物(例如,图3A-3D各自的302、306和/或308)沉淀出溶液。将设备拆卸,并将萃取套筒放在一边。然后分离圆底中的庚烷(被称作庚烷上清液),并通过旋转蒸发除去庚烷。将沉淀物和上清液级分保持分离,沉淀物称重为0.594g[平均]±0.18g(n=3),且庚烷上清液(仅含有不饱和副产物,例如,302、304)称重为0.500g[平均]±0.06g(n=3)。按照与前述庚烷索克斯累特萃取相同的操作,对萃取套筒进行使用乙酸乙酯的索克斯累特萃取。冷却后,将设备拆卸,并通过旋转蒸发除去圆底中的乙酸乙酯。在高真空下干燥以后,回收具有1.20g[平均]±0.21g(n=3)的质量的粘稠油。表征表明,所述产物主要包含化合物200(图2A)。不希望受理论的约束,发现不同的索克斯累特萃取基于用于所述萃取的溶剂选择性地分离单体产物或不饱和副产物。不饱和副产物选择性地分离在庚烷索克斯累特萃取上清液中,而单体产物选择性地分离在乙酸乙酯索克斯累特萃取上清液中。
通过比重测定、超高效液相色谱法-电喷雾或大气压强化学电离质谱法和核磁共振实验进行生物质的转化和产物表征。在下面给出了回收的产物的1HNMR数据。
10,16-二羟基棕榈酸:1H NMR(600MHz,甲醇-d4)δ3.53(td,J=6.8,2.8Hz,2H),3.49(dq,J=7.4,3.7Hz,1H),2.26(t,J=7.4Hz,3H),1.60(q,J=7.2Hz,4H),1.52(q,J=6.9Hz,4H),1.43(tt,J=9.1,4.7Hz,6H),1.39-1.22(m,23H)。
(E/Z)-16-羟基十六碳-9-烯酸:1H NMR(600MHz,甲醇-d4)δ5.44-5.29(m,2H),3.53(td,J=6.7,2.3Hz,2H),2.26(t,J=7.5Hz,3H),2.03(dd,J=8.3,4.8Hz,1H),1.97(p,J=5.8Hz,3H),1.59(p,J=7.2Hz,3H),1.56-1.48(m,3H),1.43(dt,J=11.2,4.2Hz,1H),1.40-1.27(m,20H)。
实施例3:在523K在水中解聚角质
将15g 250-500μm经萃取的番茄渣(来自实施例1)加入具有600mL的内部体积的Parr 4563B反应器。向其中加入375mL水,此后将系统密封并将反应器固定至系统,随后加热至约523K的目标温度。从环境室温(通常约298K)至目标温度的加热时间是约45分钟。然后将所述混合物在523K保持约2小时,此后将它通过内部冷却环快速冷却至25℃和40℃之间的温度。
冷却后,将反应器去压、拆卸和去密封。将反应器的内部组件和壁用乙酸乙酯冲洗,直到所有物质从壁松解,并将得到的固体/液体混合物透过中孔隙率过滤器玻璃料过滤。将反应器主体用第二部分的乙酸乙酯洗涤,并将其透过滤饼过滤。将固体饼(其产生‘焦炭’或残余物质)用另外部分的乙酸乙酯洗涤。乙酸乙酯洗液的典型总体积是约350mL。将过滤收集的水/乙酸乙酯混合物在1L分液漏斗中分离。分离各相,并将有机层收集和通过加入硫酸镁干燥,然后透过多孔玻璃料过滤。然后将乙酸乙酯通过旋转蒸发从有机相除去并在高真空下(P<0.1托)进一步干燥。得到的粗提取组合物(其包括饱和的和不饱和的脂肪酸)的总质量是3.30g[平均]±0.08g(n=3)。
收集粗提取组合物以后进行纯化。首先,将粗提取物溶解在甲醇中,此后加入3倍质量的硅藻土545(Celite 545)。通过旋转蒸发除去甲醇,从而使所述物质沉积在硅藻土上。将该混合物转移至纤维素萃取套筒,并将玻璃绒放在所述混合物的顶部。将所述套筒置于索克斯累特萃取器中,用氮气冲洗,并用500mL庚烷萃取过夜。
冷却后,一些单体产物(例如,图2A中的200)或不饱和副产物(例如,图3A-3D各自的302、304、306和/或308)沉淀出溶液。将设备拆卸,并将萃取套筒放在一边。然后分离圆底中的庚烷(被称作庚烷上清液),并通过旋转蒸发除去庚烷。将沉淀物和上清液级分保持分离,沉淀物称重为0.800g,且庚烷上清液(含有不饱和副产物(例如,302、304))称重为0.530g。按照与前述庚烷索克斯累特萃取相同的操作,对萃取套筒进行使用乙酸乙酯的索克斯累特萃取。冷却后,将设备拆卸,并通过旋转蒸发除去圆底中的乙酸乙酯。在高真空下干燥以后,回收具有1.35g[平均]±0.15g(n=3)的质量的粘稠油。不希望受理论的约束,表征表明,所述产物主要包含化合物200(参见图2A)。通过比重测定、超高效液相色谱法-电喷雾或大气压强化学电离质谱法和核磁共振实验进行生物质的转化和产物表征。
实施例4:在498K在乙醇中解聚角质
将15g 250-500μm经萃取的番茄渣(来自实施例1)加入具有600mL的内部体积的Parr 4563B反应器。向其中加入170mL乙醇,此后将系统密封并将反应器固定至系统,随后加热至约498K的目标温度。从环境室温(通常约298K)至目标温度的加热时间是约45分钟。密封的Parr 4563B反应器系统中的压强是约667psi(约45.4个大气压)。然后将所述混合物在498K保持约16小时,此后将它通过内部冷却环快速冷却至25℃和40℃之间的温度。
冷却后,将反应器去压、拆卸和去密封。将固体/液体混合物透过中孔隙率过滤器玻璃料过滤,并将反应器主体和滤饼用另外的乙醇洗涤,直到洗液是澄清的。洗液的典型总体积是约350mL。通过旋转蒸发从液体部分除去乙醇,此后所述物质经受高真空(P<0.1托)。得到的粗提取组合物(其包括饱和的和不饱和的脂肪酸乙酯)的总质量是6.79g[平均]±0.14g(n=3)。
然后如下将不饱和脂肪酸乙酯与粗提取组合物分离。将得到的混合物(包括饱和的和不饱和的脂肪酸乙酯)溶解在乙酸乙酯中,并加入3倍质量的硅藻土545粉末。通过旋转蒸发除去乙酸乙酯,从而允许物质沉积在所述硅藻土上。将该混合物转移至纤维素萃取套筒,并将玻璃绒放在所述混合物的顶部。将所述套筒置于索克斯累特萃取器中,用氮气冲洗,并用500mL庚烷萃取过夜。冷却至室温以后,将系统拆卸,并使圆底烧瓶在室温结晶过夜。然后将固体透过布氏漏斗和滤纸过滤分离。该固体材料(其包含饱和脂肪酸乙酯,但是不包含不饱和脂肪酸乙酯)是2.28g[平均]±0.25g(n=3)。通过比重测定、超高效液相色谱法-电喷雾或大气压强化学电离质谱法和核磁共振实验进行生物质的转化和产物表征。
在下面给出了回收的产物的1HNMR数据。
10,16-二羟基十六烷酸乙酯:1H NMR(600MHz,氯仿-d)δ4.11(q,J=7.1Hz,2H),3.63(t,J=6.8Hz,2H),3.57(s,1H),2.27(t,J=7.6Hz,2H),1.66-1.51(m,6H),1.49-1.25(m,21H),1.24(t,J=7.1Hz,3H)。
(E/Z)-16-羟基十六碳-9-烯酸乙酯:1H NMR(600MHz,氯仿-d)δ5.45-5.27(m,2H),4.11(q,J=7.1Hz,2H),3.63(t,J=6.7Hz,2H),2.27(t,J=7.6Hz,2H),2.05-1.89(m,4H),1.64-1.51(m,5H),1.38-1.22(m,22H)。
实施例5:在548K在乙醇中解聚角质
将15g 250-500μm经萃取的番茄渣(来自实施例1)加入具有600mL的内部体积的Parr 4563B反应器。向其中加入170mL乙醇,此后将系统密封并将反应器固定至系统,随后加热至约548K的目标温度。从环境室温(通常约298K)至目标温度的加热时间是约60分钟。密封的Parr 4563B反应器系统中的压强是约1348psi(约91.7个大气压)。然后将所述混合物在548K保持约2小时,此后将它通过内部冷却环快速冷却至25℃和40℃之间的温度。
冷却后,将反应器去压、拆卸和去密封。将固体/液体混合物透过中孔隙率过滤器玻璃料过滤,并将反应器主体和滤饼用另外的乙醇洗涤,直到洗液是澄清的。洗液的典型总体积是约350mL。通过旋转蒸发从液体部分除去乙醇,此后所述物质经受高真空(P<0.1托)。得到的粗提取组合物(其包括饱和的和不饱和的脂肪酸乙酯)的总质量是7.95g[平均]±0.25g(n=3)。
然后如下将不饱和脂肪酸乙酯与粗提取组合物分离。将得到的混合物(包括饱和的和不饱和的脂肪酸乙酯)溶解在乙酸乙酯中,并加入3倍质量的硅藻土545粉末。通过旋转蒸发除去乙酸乙酯,从而允许物质沉积在所述硅藻土上。将该混合物转移至纤维素萃取套筒,并将玻璃绒放在所述混合物的顶部。将所述套筒置于索克斯累特萃取器中,用氮气冲洗,并用500mL庚烷萃取过夜。冷却至室温以后,将系统拆卸,并使圆底烧瓶在室温结晶过夜。然后将固体通过滤过布氏漏斗和滤纸分离。不希望受理论的约束,该固体材料(其包含饱和脂肪酸乙酯,但是不包含不饱和脂肪酸乙酯)是2.03g[平均]±0.25g(n=3)。
将庚烷上清液使用旋转蒸发器蒸发至干,然后置于高真空(P<0.1托)。该油状物质(其包含不饱和脂肪酸)是2.89g[平均]±0.09g(n=3)。通过比重测定、超高效液相色谱法-电喷雾或大气压强化学电离质谱法和核磁共振实验进行生物质的转化和产物表征。
实施例6:在573K在甘油中解聚角质
将15g 250-500μm经萃取的番茄渣(来自实施例1)加入具有600mL的内部体积的Parr 4563B反应器。向其中加入190mL甘油和10mL H2O,此后将系统密封并将反应器固定至系统,随后加热至约573K的目标温度。从环境室温(通常约298K)至目标温度的加热时间是约60分钟。密封的Parr4563B反应器系统中的压强是约290psi(约19.7个大气压)。然后将混合物在573K保持约4小时,此后将它通过内部冷却环快速冷却至25℃和40℃之间的温度。
冷却后,将反应器去压、拆卸和去密封。通过用300mL水稀释所述混合物,萃取保留在所述混合物的液体和固体部分中的提取物组合物的组分。然后用400mL乙酸乙酯萃取期望的产物。将残余的甘油通过用1L水洗涤它而从乙酸乙酯混合物除去。通过旋转蒸发除去乙酸乙酯。一旦将液体蒸发至完全干燥,就记录最终的质量。不希望受理论的约束,得到的粗制组合物(发现其富含不饱和脂肪酸甘油酯(例如,图9A-9D各自的化合物902、904、906和908))的总质量是8.01g。通过比重测定、超高效液相色谱法-电喷雾或大气压强化学电离质谱法和核磁共振实验进行生物质的转化和产物表征。横跨使用上面的过程的多个解聚的回收产物的典型1HNMR数据在下面给出。
1H NMR(600MHz,甲醇-d4)δ5.41-5.31(m,2H),4.14(dd,J=11.4,4.3Hz,1H),4.05(dd,J=11.3,6.3Hz,1H),3.81(p,J=5.6Hz,1H),3.65(dtd,J=16.8,11.6,5.2Hz,2H),2.34(t,J=7.4Hz,4H),2.03(t,2H),1.97(d,J=7.2Hz,3H),1.60(s,3H),1.54-1.49(m,3H),1.30(m,28H)。
实施例7:提取条件的优化和角质在水中的解聚
还进行了在以上实施例2-3中描述的步骤的各种另外优化。例如,除了在实施例2-3(在水中的热解聚)中描述的温度和停留时间以外,还如下通过本文所述的方法进行角质在水中的解聚:在225℃(498K)进行1小时、2小时、4小时和8小时;在250℃(523K)进行1小时、2小时和4小时;和在275℃(548K)进行1小时、2小时和4小时。在每个温度和时间点确定回收的饱和的和不饱和的脂肪酸的百分比(相对于最初加入反应器中的15g番茄渣),并描绘在图12A中。如在图12A中所见,回收的粗提取物的百分比在更高的温度和更长的停留时间增加。
在索克斯累特纯化以后,确定直接单体产物(例如,图2A中的200)和不饱和副产物(例如,图3A-3D各自的302、304、306和308)的量。如前面描述的以及在下面参考图13所示的,在庚烷沉淀物中收集直接单体产物、直接单体和不饱和副产物的混合物、或不饱和副产物,其中每种在庚烷沉淀物中的相对量取决于温度和停留时间。不希望受理论的约束,据信,沉淀物组成的该变化可以是由于溶剂洗液的高温,从而导致所述物质的熔化和随后流出索克斯累特萃取器(一个非选择性的过程),而不是溶解在溶剂中和作为溶液除去(一个更具选择性的过程)。这可以如下克服:改变设备设计(例如,冷却的接收器),或使用压强来调节溶剂的沸点并由此调节冷凝的溶剂的温度。图12B描绘了从庚烷沉淀物回收的量(作为相对于最初的15g番茄渣的百分比)。如前面描述的,将不饱和副产物选择性地分离在庚烷上清液中,其回收的量(作为相对于最初的15g番茄渣的百分比)显示在图12C中。想到乙酸乙酯上清液选择性地分离直接单体产物,其回收的量(作为相对于最初的15g番茄渣的百分比)显示在图12D中。一般而言,更长的停留时间和更高的温度导致增加的向副产物的转化。
如上所述,索克斯累特萃取可以选择性地分离直接单体产物或不饱和副产物。此外,调节时间和温度可以至少部分地确定生成哪种脂肪酸产物(直接单体产物或不饱和副产物)。图13的表示出了在试验的不同解聚温度和停留时间从庚烷沉淀物、从庚烷上清液和从乙酸乙酯上清液回收了哪些产物。在图13中,‘Sat’表示直接单体产物(包括,例如,图2A中的200),且‘Unsat’表示不饱和副产物(包括,例如,图3A-3D各自的化合物302、304、306和308中的任一种)。首先参考庚烷沉淀物产物,在较低的解聚温度(例如,在498K),直到8小时的所有停留时间仅回收直接单体产物(且在1小时停留时间没有回收任何种类的实质产物)。在中间解聚温度(523K),1小时停留时间仅回收直接单体产物,而更长的停留时间(2小时和4小时)回收直接单体产物和不饱和副产物的混合物。在更高的解聚温度(548K),更短的停留时间(1小时和2小时)回收直接单体产物和不饱和副产物的混合物,而更长的(4小时)停留时间仅回收不饱和副产物。
图17-22显示了在548K在水中解聚番茄渣1h的UPLC表征数据。现在参考庚烷上清液产物,在其中选择性地分离不饱和副产物,在4小时或更小的停留时间在低解聚温度(498K)没有观察到不饱和副产物,但是对于8小时停留时间的情况在498K观察到了不饱和副产物。在中间和更高的解聚温度(分别523K和548K),所有停留时间(1小时、2小时和4小时)观察到了不饱和副产物。
现在参考乙酸乙酯上清液产物,在其中选择性地分离直接单体产物,在2小时或更小的停留时间在低解聚温度(498K)没有观察到直接单体产物,但是对于4小时和8小时停留时间的情况在498K观察到了。在中间解聚温度(523K),所有停留时间(1小时、2小时和4小时)观察到直接单体产物。在更高的解聚温度(548K),1小时和2小时停留时间观察到直接单体产物,但是在4小时停留时间的情况下没有观察到。
实施例8:提取条件的优化和角质在乙醇中的解聚
除了在上面实施例7中描述的实施例2-3(在水中的热解聚)中的步骤的优化以外,还进行了在上面实施例4-5(在乙醇中的热解聚)中描述的步骤的另外优化。例如,除了在实施例4-5中描述的温度和停留时间以外,还如下通过本文所述的方法进行了角质在乙醇中的解聚:在225℃(498K)进行2小时和6小时;在250℃(523K)进行1小时、2小时和4小时;在275℃(548K)进行1小时和4小时;和在300℃进行1小时、2小时和4小时。在每个温度和时间点确定回收的饱和的和不饱和的脂肪酸的百分比(相对于最初加入反应器中的15g番茄渣),并描绘在图14A中。如在图14A中所见,在更高的温度和更长的停留时间回收的粗提取物的百分比增加。
在庚烷索克斯累特纯化操作以后,确定直接单体乙酯产物(例如,图6A中的600)和不饱和乙酯副产物(例如,图7A-7D各自中的702、704、706和708)的各自量。如前面描述的,在庚烷沉淀物中收集直接单体产物,由此将直接单体产物与不饱和副产物分离。图14B描绘了从庚烷沉淀物回收的量(作为相对于最初的15g番茄渣的百分比)。如前面描述的,不饱和副产物被选择性地分离在庚烷上清液中,其回收量(作为相对于最初的15g番茄渣的百分比)显示在图14C中。一般而言,较长的停留时间和较高的温度导致增加的向期望产物的转化率。
如上所述,索克斯累特萃取可以选择性地分离直接单体酯产物或不饱和的酯副产物。此外,调节时间和温度可以至少部分地决定产生哪种脂肪酸酯产物(直接单体酯产物或不饱和的酯副产物)。图15的表示出了在试验的不同解聚温度和停留时间从庚烷沉淀物和从庚烷上清液回收哪些产物。在图15中,‘Sat’表示直接单体酯产物(例如,图6A中的600),且‘Unsat’表示不饱和的酯副产物(包括,例如,图7A-7D各自中的化合物702、704、706和708中的任一种)。首先参考庚烷沉淀物产物,在较低的解聚温度(例如,在498K),至少6小时的停留时间仅回收直接单体产物(且在2小时停留时间没有回收任何种类的实质产物)。在较高的解聚温度(523K和573K),1小时、2小时和4小时的停留时间回收直接单体产物。在548K的解聚温度,1小时、2小时、4小时和8小时的停留时间回收直接单体产物。
现在参考庚烷上清液产物,在其中选择性地分离不饱和副产物,在2小时、4小时或16小时的停留时间在低解聚温度(498K)没有观察到不饱和副产物。在中间解聚温度(523K),在2小时或更小的停留时间没有观察到不饱和副产物,但是对于4小时停留时间的情况在523K观察到了不饱和副产物。在更高的解聚温度(548K和573K),所有停留时间(1小时、2小时和4小时)观察到不饱和副产物。
图23-25给出了在乙醇中在548K解聚番茄渣4小时以后的UPLC表征数据。
实施例9:在鳄梨上形成的保护性涂层
如下在鳄梨上形成保护性涂层:通过本文描述的方法(角质的热解聚)提取化合物,并将化合物沉积在(未剥皮的)鳄梨的外表面上。然后测量鳄梨的质量损失速率,并与未涂布的鳄梨的值进行对比。如下形成所有涂层:将鳄梨浸入溶液中,所述溶液包含以10mg/mL的浓度溶解在基本上纯的乙醇中的有关化合物,将鳄梨放在干燥架上,并允许鳄梨在环境房间条件下在约23℃-27℃范围内的温度和约40%-55%范围内的湿度干燥。在试验它们的整个持续时间中,将鳄梨保持在这些相同温度和湿度条件。
质量损失速率显示在图16中,对于未处理的(例如,未涂布的)鳄梨,在条1602中,对于用10,16-二羟基十六酸乙酯(被称作“EtDHPA”)涂布的鳄梨,在条1604中,和对于用EtDHPA和十六烷酸1,3-二羟基丙烷-2-基酯的混合物(被称作“PA-2G”)涂布的鳄梨,在条1606中,其中对于条1606,以30:70的质量比混合EtDHPA和PA-2G。对于条1604和1606,通过如本文中所述的角质在乙醇中的热解聚形成EtDHPA,而通过利用棕榈酸作为起始原料的多步骤过程形成PA-2G,其中所述过程详细地描述在名称为“PRECURSOR COMPOUNDS FORMOLECULAR COATINGS”的美国专利申请号15/530,403中。图中的每个条代表30个鳄梨的组。所有鳄梨得自相同来源,在大约同时采摘,并处于类似的成熟阶段。
如在图16中所见,未涂布的鳄梨的质量(条1602)以每天约1.21%的平均速率减小,用EtDHPA涂布的鳄梨的质量(条1604)以每天约1.06%的平均速率减小,且用EtDHPA/PA-2G混合物涂布的鳄梨的质量(条1606)以每天约0.94%的平均速率减小。这样,用EtDHPA涂布的鳄梨的平均质量损失速率(条1604)与未涂布的鳄梨(条1602)相比减小了超过12%,且用EtDHPA/PA-2G混合物涂布的鳄梨的平均质量损失速率(条1606)与未涂布的鳄梨(条1602)相比减小了超过22%。
在上面已经描述了所述组合物和方法的不同实现方式。但是,应当理解,它们仅仅作为示例呈现,而不是用来限制。在上述的方法和步骤指示以某种顺序发生某些事件的情况下,受教于本公开内容的本领域普通技术人员会认识到,可以改变某些步骤的顺序,且这样的改变是属于根据本公开内容的变化。已经具体地显示和描述了实现方式,但是应该理解,可以做出形式和细节的多种变化。因此,其它实现方式是在下述权利要求的范围内。
Claims (21)
1.一种从含角质的植物物质制备角质-衍生的单体、寡聚体或它们的组合的方法,所述方法包括:
从所述含角质的植物物质得到角质;
将所述角质加入基本上不含有加入的酸或碱的溶剂以形成第一混合物,所述溶剂具有在1个大气压的压强下在第一温度的沸点,其中所述溶剂选自甘油、甲醇、乙醇、液体CO2和超临界CO2;
将所述第一混合物加热至第二温度和第二压强,所述第二温度高于所述第一温度且所述第二压强高于1个大气压,以形成包含所述角质-衍生的单体、寡聚体或它们的组合的第二混合物;和
其中所述第二压强足够高以将液相中的所述溶剂的至少一部分维持在所述第二温度。
2.根据权利要求1所述的方法,所述方法还包括:
将所述溶剂与所述第二混合物中的角质-衍生的单体、寡聚体或它们的组合分离从而分离出角质-衍生的单体、寡聚体或它们的组合。
3.根据权利要求2所述的方法,所述方法还包括将分离出的角质-衍生的单体、寡聚体或它们的组合溶解在第二溶剂中。
4.根据权利要求1所述的方法,其中所述第二混合物中角质-衍生的单体、寡聚体或它们的组合的至少一部分是不饱和的。
5.根据权利要求4所述的方法,所述方法还包括将所述不饱和的角质-衍生的单体、寡聚体或它们的组合氢化。
6.根据权利要求1所述的方法,其中在所述第二温度和所述第二压强时所述溶剂中所述角质的解聚速率是在所述第一温度在1个大气压下的至少100倍。
7.根据权利要求1所述的方法,其中所述第二温度是至少393K。
8.根据权利要求7所述的方法,其中所述第二压强是大于5atm。
9.根据权利要求1所述的方法,其中所述形成第二混合物的过程导致饱和的和不饱和的脂肪酸的产生。
10.根据权利要求9所述的方法,其中饱和脂肪酸的浓度高于不饱和脂肪酸的浓度。
11.根据权利要求1所述的方法,其中所述形成第二混合物的过程导致饱和的和不饱和的脂肪酸酯的产生。
12.根据权利要求11所述的方法,其中饱和脂肪酸酯的浓度高于不饱和脂肪酸酯的浓度。
13.根据权利要求1所述的方法,其中在所述第二温度的解聚反应产生第二混合物中不带电荷的角质-衍生的单体、寡聚体或它们的组合。
14.一种从含角质的植物物质制备角质-衍生的单体、寡聚体或它们的组合的方法,所述方法包括:
从所述含角质的植物物质得到角质;
将所述角质加入基本上不含有加入的酸或碱的溶剂以形成第一混合物,所述溶剂具有在1个大气压的压强下在第一温度的沸点,其中所述溶剂选自水、甘油、甲醇、乙醇、液体CO2和超临界CO2;
将所述第一混合物加热至第二温度和第二压强,所述第二温度高于所述第一温度且所述第二压强高于1个大气压,以形成包含第一组式I角质-衍生的单体的第二混合物:
其中:
R1、R2、R3、R4、R5、R6、R7、R8、R9和R10各自独立地是-H、-OR13、-NR13R14、-SR13、卤素、-C1-C6烷基、-C1-C6烯基、-C1-C6炔基、-C3-C7环烷基、芳基或5-10元环杂芳基,其中每个烷基、烯基、炔基、环烷基、芳基或杂芳基任选地被-OR13、-NR13R14、-SR13或卤素取代;
R13和R14各自独立地是-H、-C1-C6烷基、-C1-C6烯基或-C1-C6炔基;
R11是-H、-甘油基、-C1-C6烷基、-C1-C6烯基、-C1-C6炔基、-C3-C7环烷基、芳基或5-10元环杂芳基,其中每个烷基、烯基、炔基、环烷基、芳基或杂芳基任选地被-OR13、-NR13R14、-SR13或卤素取代;
R12是-OH、-H、-C1-C6烷基、-C1-C6烯基、-C1-C6炔基、-C3-C7环烷基、芳基或5-10元环杂芳基,其中每个烷基、烯基、炔基、环烷基、芳基或杂芳基任选地被-OR13、-NR13R14、-SR13、卤素、-COOH或-COOR11取代;且
m、n和o各自独立地是在0-30的范围内的整数,且0≤m+n+o≤30;和
其中所述第二压强足够高以将液相中的所述溶剂的至少一部分维持在所述第二温度。
15.根据权利要求14所述的方法,第二混合物还包括式II角质-衍生的单体:
其中:
R1、R2、R4和R5各自独立地是-H、-OR11、-NR11R12、-SR11、卤素、-C1-C6烷基、-C1-C6烯基、-C1-C6炔基、-C3-C7环烷基、芳基或5-10元环杂芳基,其中每个烷基、烯基、炔基、环烷基、芳基或杂芳基任选地被-OR11、-NR11R12、-SR11或卤素取代;
R11和R12各自独立地是-H、-C1-C6烷基、-C1-C6烯基或-C1-C6炔基;
当R6和R6’之间的是单键时,R6是-OH且R6’选自-H、-C1-C6烷基、-C1-C6烯基、-C1-C6炔基、-C3-C7环烷基和-C6-C10芳基,以及当R6和R6’之间的代表双键时,R6和R6’不存在;
n是在0-11的范围内的整数;
m是在0-25的范围内的整数;且
0≤m+n≤25。
16.根据权利要求15所述的方法,所述方法还包括修饰式II角质-衍生的单体中的至少一些以形成第二组式I角质-衍生的单体。
17.根据权利要求14所述的方法,其中第二混合物还包括式III角质-衍生的单体:
其中:
R1、R2、R5、R6、R9、R10、R11、R12和R13在每次出现时各自独立地是-H、-OR14、-NR14R15、-SR14、卤素、-C1-C6烷基、-C2-C6烯基、-C2-C6炔基、-C3-C7环烷基、芳基或杂芳基,其中每个烷基、烯基、炔基、环烷基、芳基或杂芳基任选地被一个或多个-OR14、-NR14R15、-SR14或卤素取代;
R3、R4、R7和R8在每次出现时各自独立地是-H、-OR14、-NR14R15、-SR14、卤素、-C1-C6烷基、-C2-C6烯基、-C2-C6烯基、-C2-C6炔基、-C3-C7环烷基、芳基或杂芳基,其中每个烷基、炔基、环烷基、芳基或杂芳基任选地被一个或多个-OR14、-NR14R15、-SR14或卤素取代;或
R3和R4可以与它们所连接的碳原子结合以形成C3-C6环烷基、C4-C6环烯基或3-6元环杂环;和/或
R7和R8可以与它们所连接的碳原子结合以形成C3-C6环烷基、C4-C6环烯基或3-6元环杂环;
R14和R15在每次出现时各自独立地是-H、-C1-C6烷基、-C2-C6烯基或-C2-C6炔基;
n是0、1、2、3、4、5、6、7或8;
m是0、1、2或3;
q是0、1、2、3、4或5;且
r是0、1、2、3、4、5、6、7或8;且
R选自-H、-C1-C6烷基、-C2-C6烯基、-C2-C6炔基、-C3-C7环烷基、芳基、1-甘油、2-甘油或杂芳基。
18.根据权利要求17所述的方法,所述方法还包括修饰式III角质-衍生的单体中的至少一些以形成第二组式I角质-衍生的单体。
19.一种从含角质的植物物质制备角质-衍生的单体、寡聚体或它们的组合的方法,所述方法包括:
从所述含角质的植物物质得到角质;
将所述角质加入基本上不含有加入的酸或碱的溶剂以形成第一混合物,所述溶剂具有在1个大气压的压强下在第一温度的沸点,其中所述溶剂选自水、甘油、甲醇、乙醇、液体CO2和超临界CO2;和
将所述第一混合物加热至第二温度和第二压强,所述第二温度高于所述第一温度且所述第二压强高于1个大气压,以形成包含式III角质-衍生的单体的第二混合物:
其中:
R1、R2、R5、R6、R9、R10、R11、R12和R13在每次出现时各自独立地是-H、-OR14、-NR14R15、-SR14、卤素、-C1-C6烷基、-C2-C6烯基、-C2-C6炔基、-C3-C7环烷基、芳基或杂芳基,其中每个烷基、烯基、炔基、环烷基、芳基或杂芳基任选地被一个或多个-OR14、-NR14R15、-SR14或卤素取代;
R3、R4、R7和R8在每次出现时各自独立地是-H、-OR14、-NR14R15、-SR14、卤素、-C1-C6烷基、-C2-C6烯基、-C2-C6烯基、-C2-C6炔基、-C3-C7环烷基、芳基或杂芳基,其中每个烷基、炔基、环烷基、芳基或杂芳基任选地被一个或多个-OR14、-NR14R15、-SR14或卤素取代;或
R3和R4可以与它们所连接的碳原子结合以形成C3-C6环烷基、C4-C6环烯基或3-6元环杂环;和/或
R7和R8可以与它们所连接的碳原子结合以形成C3-C6环烷基、C4-C6环烯基或3-6元环杂环;
R14和R15在每次出现时各自独立地是-H、-C1-C6烷基、-C2-C6烯基或-C2-C6炔基;
n是0、1、2、3、4、5、6、7或8;
m是0、1、2或3;
q是0、1、2、3、4或5;且
r是0、1、2、3、4、5、6、7或8;且
R选自-H、-C1-C6烷基、-C2-C6烯基、-C2-C6炔基、-C3-C7环烷基、芳基、1-甘油、2-甘油或杂芳基;和
其中所述第二压强足够高以将液相中的所述溶剂的至少一部分维持在所述第二温度。
20.根据权利要求19所述的方法,所述方法还包括修饰式III单体中的至少一些以形成式I单体:
其中:
R1、R2、R3、R4、R5、R6、R7、R8、R9和R10各自独立地是-H、-OR13、-NR13R14、-SR13、卤素、-C1-C6烷基、-C1-C6烯基、-C1-C6炔基、-C3-C7环烷基、芳基或5-10元环杂芳基,其中每个烷基、烯基、炔基、环烷基、芳基或杂芳基任选地被-OR13、-NR13R14、-SR13或卤素取代;
R13和R14各自独立地是-H、-C1-C6烷基、-C1-C6烯基或-C1-C6炔基;
R11是-H、-甘油基、-C1-C6烷基、-C1-C6烯基、-C1-C6炔基、-C3-C7环烷基、芳基或5-10元环杂芳基,其中每个烷基、烯基、炔基、环烷基、芳基或杂芳基任选地被-OR13、-NR13R14、-SR13或卤素取代;
R12是-OH、-H、-C1-C6烷基、-C1-C6烯基、-C1-C6炔基、-C3-C7环烷基、芳基或5-10元环杂芳基,其中每个烷基、烯基、炔基、环烷基、芳基或杂芳基任选地被-OR13、-NR13R14、-SR13、卤素、-COOH或-COOR11取代;且
m、n和o各自独立地是在0-30的范围内的整数,且0≤m+n+o≤30。
21.一种从含角质的植物物质制备角质-衍生的单体、寡聚体或它们的组合的方法,所述方法包括:
从含角质的植物物质得到角质;
将角质加入基本上不含有加入的酸或碱的溶剂以形成第一混合物,其中所述溶剂选自甘油、甲醇、乙醇、液体CO2和超临界CO2;和
将所述第一混合物加热至至少498K的温度和至少360psi的压强,由此形成包含角质-衍生的单体、寡聚体或它们的组合的第二混合物。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN202110066463.8A CN112841185A (zh) | 2015-12-10 | 2016-12-09 | 用于形成保护性涂层的植物提取物组合物 |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201562265726P | 2015-12-10 | 2015-12-10 | |
| US62/265,726 | 2015-12-10 | ||
| PCT/US2016/065917 WO2017100636A1 (en) | 2015-12-10 | 2016-12-09 | Plant extract compositions for forming protective coatings |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN202110066463.8A Division CN112841185A (zh) | 2015-12-10 | 2016-12-09 | 用于形成保护性涂层的植物提取物组合物 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN108966638A CN108966638A (zh) | 2018-12-07 |
| CN108966638B true CN108966638B (zh) | 2021-01-26 |
Family
ID=57708794
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN202110066463.8A Pending CN112841185A (zh) | 2015-12-10 | 2016-12-09 | 用于形成保护性涂层的植物提取物组合物 |
| CN201680079439.5A Active CN108966638B (zh) | 2015-12-10 | 2016-12-09 | 用于形成保护性涂层的植物提取物组合物 |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN202110066463.8A Pending CN112841185A (zh) | 2015-12-10 | 2016-12-09 | 用于形成保护性涂层的植物提取物组合物 |
Country Status (7)
| Country | Link |
|---|---|
| US (5) | US9957215B2 (zh) |
| EP (2) | EP3649860B1 (zh) |
| JP (1) | JP6549326B2 (zh) |
| CN (2) | CN112841185A (zh) |
| ES (2) | ES2939007T3 (zh) |
| IL (2) | IL259820B (zh) |
| WO (1) | WO2017100636A1 (zh) |
Families Citing this family (19)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9744542B2 (en) | 2013-07-29 | 2017-08-29 | Apeel Technology, Inc. | Agricultural skin grafting |
| WO2016168319A1 (en) * | 2015-04-13 | 2016-10-20 | University Of South Florida | Cutin-like materials with advanced functionalities and methods of manufacture |
| EP3673738B1 (en) | 2015-05-20 | 2024-02-28 | Apeel Technology, Inc. | Plant extract compositions and methods of preparation thereof |
| ES2935595T3 (es) | 2015-09-16 | 2023-03-08 | Apeel Tech Inc | Método de formación de un recubrimiento protector aplicando compuestos de glicéridos de ácidos grasos a una superficie |
| ES2939007T3 (es) | 2015-12-10 | 2023-04-18 | Apeel Tech Inc | Composiciones de extractos de plantas para formar recubrimientos protectores |
| EP3407713A1 (en) | 2016-01-26 | 2018-12-05 | Apeel Technology, Inc. | Method for preparing and preserving sanitized products |
| EP3541192A4 (en) | 2016-11-17 | 2020-07-01 | Apeel Technology, Inc. | COMPOSITIONS MOLDED FROM PLANT EXTRACTS AND METHOD FOR THE PRODUCTION THEREOF |
| JP2021536457A (ja) * | 2018-09-05 | 2021-12-27 | アピール テクノロジー,インコーポレイテッド | 保護コーティング用の化合物および配合物 |
| JP2023516406A (ja) | 2020-03-04 | 2023-04-19 | アピール テクノロジー,インコーポレイテッド | 被覆された農産物及び対応する方法 |
| WO2021252369A1 (en) | 2020-06-07 | 2021-12-16 | Comestaag Llc | Selectively treating plant items |
| WO2021252403A1 (en) | 2020-06-07 | 2021-12-16 | Comestaag Llc | Barrier coating compositions for perishables and methods, kits and coated items relating thereto |
| MX2023000749A (es) | 2020-08-04 | 2023-02-13 | Apeel Tech Inc | Metodos de control de la maduracion de productos agricolas. |
| CN116457332A (zh) * | 2020-10-30 | 2023-07-18 | 阿比尔技术公司 | 组合物及其制备方法 |
| CN112322156A (zh) * | 2020-11-25 | 2021-02-05 | 上海源育节能环保科技有限公司 | 一种天然清香环保涂料及其制备方法 |
| IT202100017945A1 (it) | 2021-07-07 | 2023-01-07 | Tomapaint S R L | Metodo di estrazione di cutina da scarti di lavorazione del pomodoro |
| WO2023150072A1 (en) * | 2022-02-01 | 2023-08-10 | Sinclair David A | Compositions and methods for the preservation of plant matter |
| WO2023187159A1 (en) * | 2022-04-01 | 2023-10-05 | Lamberti Spa | Method for coating a paper substrate by using a modified cutin extract |
| ES2954422B2 (es) * | 2022-04-13 | 2024-04-09 | Univ Alicante | Procedimiento para la obtencion de cutina a partir de residuos vegetales y cutina obtenida |
| ES2954532B2 (es) * | 2022-04-13 | 2024-04-15 | Univ Alicante | Metodo para la obtencion de cutina a partir de residuos vegetales y cutina obtenida |
Family Cites Families (211)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US1016761A (en) | 1909-04-16 | 1912-02-06 | Charles C Moore | Process of producing starch and glucose. |
| US1040737A (en) | 1911-01-18 | 1912-10-08 | Jeremiah L Mahoney | Apparatus for producing rubber bulbs for atomizers, syringes, &c. |
| US1026670A (en) | 1911-03-23 | 1912-05-21 | Russell J Goodnow | Fruit and nut squeezer. |
| US1051731A (en) | 1912-02-24 | 1913-01-28 | Michael Greenfeld | Belt-buckle. |
| US1056115A (en) | 1912-04-29 | 1913-03-18 | Arthur G Mumford | Valve-gear for fluid-pressure engines. |
| US1084399A (en) | 1913-08-05 | 1914-01-13 | Charles E Collins | Unbuttoning implement. |
| US1943468A (en) | 1932-11-22 | 1934-01-16 | Wilbur White Chemical Company | Wax emulsion coating, and coating process |
| US2363232A (en) | 1934-09-13 | 1944-11-21 | Brogdex Co | Processes of and compositions for protectively coating fresh fruits or vegetables |
| US2222000A (en) | 1937-06-02 | 1940-11-19 | Schmidt Erich Kurt Julius | Process for the preservation of eggs and fresh fruit |
| US2213557A (en) | 1937-08-26 | 1940-09-03 | Du Pont | Produce coating compositions |
| US2275659A (en) | 1939-02-25 | 1942-03-10 | Johnson & Son Inc S C | Water removable wax coating |
| US2324448A (en) | 1939-03-08 | 1943-07-13 | Wehrli Gottlieb | Method and product for producing a cleansing and preserving coating on fruits and vegetables |
| US2342063A (en) | 1940-07-31 | 1944-02-15 | Fmc Corp | Method for treating fruit |
| US2333887A (en) | 1941-07-26 | 1943-11-09 | Lorenz M Redlinger | Protective coating and process of manufacture therefor |
| GB587532A (en) | 1943-03-20 | 1947-04-29 | Colgate Palmolive Peet Co | Improvements in or relating to alcoholysis of fatty glycerides |
| GB647174A (en) | 1948-07-23 | 1950-12-06 | Nopco Chem Co | Improvements relating to the production of alkyl esters of fatty acids |
| BE500510A (zh) | 1950-01-11 | |||
| US2840606A (en) | 1955-04-15 | 1958-06-24 | Du Pont | Nylon hydrolysis |
| US2857282A (en) | 1957-09-27 | 1958-10-21 | Eugene F Jansen | Inhibition of enzymes in plant tissue |
| US3189467A (en) | 1959-12-14 | 1965-06-15 | Fmc Corp | Preservation of perishable products |
| US3232765A (en) | 1962-12-17 | 1966-02-01 | Grace W R & Co | Water-in-oil chocolate emulsion |
| US3471303A (en) | 1966-03-07 | 1969-10-07 | Archer Daniels Midland Co | Edible coating compositions and method for coating food |
| US3715024A (en) | 1971-04-23 | 1973-02-06 | Fmc Corp | Fruit orienting apparatus |
| US3821421A (en) | 1971-07-06 | 1974-06-28 | Lever Brothers Ltd | Process for the flavouring of foods |
| US4002775A (en) | 1973-07-09 | 1977-01-11 | Kabara Jon J | Fatty acids and derivatives of antimicrobial agents |
| DE2505428C3 (de) | 1975-02-08 | 1981-04-09 | Müller's Mühle Müller GmbH & Co KG, 4650 Gelsenkirchen | Verwendung einer Emulsion zur Erzeugung eines Glasurüberzuges auf geschälten Erbsen |
| US3997674A (en) | 1975-02-25 | 1976-12-14 | Tsukihoshi Kasei Kabushiki Kaisha | Preservation of agricultural products |
| AU531759B2 (en) | 1978-04-17 | 1983-09-08 | Ici Ltd. | Electrostatic spraying |
| IL59407A (en) | 1979-03-06 | 1983-12-30 | Sanofi Sa | Di-n-propylacetic acid diesters of glycerol,their preparation and pharmaceutical compositions containing them |
| US4654370A (en) | 1979-03-12 | 1987-03-31 | Abbott Laboratories | Glyceryl valproates |
| US4353962A (en) | 1980-05-15 | 1982-10-12 | Environmental Chemicals, Inc. | In-flight encapsulation of particles |
| JPS5889140A (ja) | 1981-11-24 | 1983-05-27 | Koutou Kk | 青果物の被膜剤組成物 |
| GB2119399A (en) | 1982-05-06 | 1983-11-16 | Hop Dev Ltd | Extraction of plant material by using carbon dioxide |
| US4421775A (en) | 1982-06-04 | 1983-12-20 | The United States Of America As Represented By The Secretary Of Agriculture | Method for removing the outer waxy cutin-containing layer from papaya |
| EP0104043A3 (en) | 1982-09-20 | 1984-06-06 | Ajinomoto Co., Inc. | Foodstuffs and pharmaceuticals |
| US4726898A (en) | 1982-09-30 | 1988-02-23 | Pennwalt Corporation | Apparatus for spinning fruit for sorting thereof |
| US5051448A (en) | 1984-07-24 | 1991-09-24 | The Mclean Hospital Corporation | GABA esters and GABA analog esters |
| FI77441C (fi) * | 1985-03-04 | 1989-03-10 | Kemira Oy | Foerfarande foer omvandling av vaextmaterial till kemikalier. |
| US4661359A (en) | 1985-06-03 | 1987-04-28 | General Mills, Inc. | Compositions and methods for preparing an edible film of lower water vapor permeability |
| US4820533A (en) | 1985-10-16 | 1989-04-11 | General Mills, Inc. | Edible barrier for composite food articles |
| US4710228A (en) | 1985-10-16 | 1987-12-01 | General Mills, Inc. | Edible coating composition and method of preparation |
| JPH0724544B2 (ja) | 1985-11-26 | 1995-03-22 | 三栄源エフ・エフ・アイ株式会社 | 生野菜の大腸菌殺菌と鮮度保持 |
| US4874618A (en) | 1985-12-27 | 1989-10-17 | General Mills, Inc. | Package containing a moisture resistant edible internal barrier |
| DE3622191A1 (de) | 1986-07-02 | 1988-01-07 | Ni I Sadovodstva Necernozemnoj | Gemisch zur obst- und gemuesefrischhaltung |
| GB8617527D0 (en) | 1986-07-17 | 1986-08-28 | Ici Plc | Spraying process |
| US4959232A (en) | 1989-04-26 | 1990-09-25 | Red Arrow Products Company, Inc. | Process for making liquid smoke compositions and resin treated liquid smoke compositions |
| US5126153A (en) | 1988-05-13 | 1992-06-30 | Basic American Foods, Inc. | Compositions and methods for inhibiting browning of processed produce |
| DE3825248A1 (de) | 1988-07-25 | 1990-02-01 | Peter Siegfried | Verfahren zur herstellung von reinen monoglyceriden und reinen diglyceriden aus einem gemisch, das mono-, di- und triglyceride enthaelt |
| US4960600A (en) | 1988-12-21 | 1990-10-02 | The Procter & Gamble Co. | Polyol polyesters as a protective moisture barrier for foods |
| US5019403A (en) | 1989-12-13 | 1991-05-28 | The United States Of America As Represented By The Secretary Of Agriculture | Coatings for substrates including high moisture edible substrates |
| JPH0416173A (ja) | 1990-05-09 | 1992-01-21 | Nippon Oil & Fats Co Ltd | 野菜類、果実類の鮮度保持剤 |
| US5137743A (en) | 1990-09-07 | 1992-08-11 | Opta Food Ingredients, Inc. | Foods having an oil phase thickened with an oil soluble polyester |
| US5198254A (en) | 1991-04-03 | 1993-03-30 | The United States Of America As Represented By The Secretary Of Agriculture | Composition and method of increasing stability of fruits, vegetables or fungi |
| US5366995A (en) | 1991-05-01 | 1994-11-22 | Mycogen Corporation | Fatty acid based compositions for the control of established plant infections |
| JP2969234B2 (ja) | 1991-07-19 | 1999-11-02 | 株式会社アドバンス | Acat阻害剤 |
| WO1993006735A1 (en) | 1991-10-10 | 1993-04-15 | Vioryl S.A. | Post-harvest fruit protection using components of natural essential oils in combination with coating waxes |
| USH1591H (en) | 1992-10-09 | 1996-09-03 | Fulcher; John | Preparation of flavor-enhanced reduced calorie fried foods |
| AU682864B2 (en) | 1993-05-13 | 1997-10-23 | Loders Croklaan B.V. | Process for production of human milk fat replacers |
| JPH0778098A (ja) | 1993-09-08 | 1995-03-20 | Fujitsu Ltd | ファイル管理システム |
| US5435633A (en) | 1994-01-03 | 1995-07-25 | Hayes Wheels International, Inc. | Aluminum full face vehicle wheel |
| US5483871A (en) | 1994-02-24 | 1996-01-16 | Sunkist Growers, Inc. | Apparatus for spray washing fruit in a brush bed |
| JPH0856564A (ja) | 1994-08-25 | 1996-03-05 | Mitsubishi Chem Corp | 青果物の果皮障害防止方法及びそのための剤 |
| SE518619C2 (sv) | 1994-12-09 | 2002-10-29 | Gs Dev Ab | Komposition för reglerad frisättning innehållande monokaproin |
| US5741505A (en) | 1995-01-20 | 1998-04-21 | Mars, Incorporated | Edible products having inorganic coatings |
| US20050233039A1 (en) | 1995-07-11 | 2005-10-20 | Wolfe Steven K | Method for cleaning, packing, and transporting vegetables |
| US5827553A (en) | 1995-11-06 | 1998-10-27 | Mantrose-Haeuser Co., Inc. | Edible adhesive |
| ATE210706T1 (de) | 1996-03-26 | 2001-12-15 | Minnesota Mining & Mfg | Kationisch polymerisierbare zusmmensetzungen, die zur beschichtung in einem elektrostatischen verfahren verwendet werden können |
| JP3689983B2 (ja) | 1996-06-24 | 2005-08-31 | 凸版印刷株式会社 | 抗菌性高分子及び抗菌性を有する包装材料 |
| DE19706023A1 (de) | 1997-02-17 | 1998-08-20 | Bayer Ag | Abbau von biologisch abbaubaren Polymeren mit Enzymen |
| US6066316A (en) * | 1997-03-21 | 2000-05-23 | Shiseido Co., Ltd. | Fine dispersion composition of wax, hair cosmetic preparation and glazing agent |
| KR20010013377A (ko) | 1997-06-04 | 2001-02-26 | 데이비드 엠 모이어 | 마일드한 잔류성 항균 조성물 |
| US5939117A (en) | 1997-08-11 | 1999-08-17 | Mantrose-Haeuser Co., Inc. | Methods for preserving fresh fruit and product thereof |
| MY129120A (en) | 1997-08-19 | 2007-03-30 | Global Palm Products Sdn Bhd | Process for the production of monoglyceride based on the glycerolysis of methyl ester |
| US6241971B1 (en) | 1997-09-25 | 2001-06-05 | The Procter & Gamble Company | Hair styling compositions comprising mineral salt, lipophilic material, and low levels of surfactant |
| US5925395A (en) | 1998-01-09 | 1999-07-20 | Mantrose-Haeuser Co., Inc. | Methods for preserving fresh vegetables |
| US6033705A (en) | 1998-07-08 | 2000-03-07 | Isaacs; Charles E. | Method for treating foodstuffs to reduce or prevent microbial activity |
| US8424243B1 (en) | 1998-10-27 | 2013-04-23 | The United States Of America As Represented By Secretary Of Agriculture | Use of coated protective agent to protect horticultural crops from disease |
| NL1010673C2 (nl) | 1998-11-27 | 2000-05-30 | Stork Pmt | Toevoegen van additief aan een vleesprodukt. |
| US6165529A (en) | 1999-01-13 | 2000-12-26 | Planet Polymer Technologies, Inc. | Process for preventing fresh produce and coating composition therefor |
| IL133827A (en) | 1999-01-13 | 2004-02-08 | Agway Inc | Process for preserving fresh produce and coating composition therefor |
| ES1041955Y (es) | 1999-02-01 | 2000-01-16 | Fernandez Ruben Benigno Lopez | Limpiadora automatica de frutos carnosos. |
| US6162475A (en) | 1999-03-30 | 2000-12-19 | The United States Of America As Represented By The Secretary Of Agriculture | Edible food coatings containing polyvinyl acetate |
| WO2001001980A1 (en) | 1999-07-06 | 2001-01-11 | The Regents Of The University Of California | Methods for the amelioration of neuropsychiatric disorders by inhibiting the inactivating transport of endogenous cannabinoid substances |
| US6392070B1 (en) | 1999-08-10 | 2002-05-21 | Regents Of The University Of Minnesota | Birch bark processing and the isolation of natural products from birch bark |
| US6254645B1 (en) | 1999-08-20 | 2001-07-03 | Genencor International, Inc. | Enzymatic modification of the surface of a polyester fiber or article |
| AU2001229462A1 (en) | 2000-01-14 | 2001-07-24 | The Procter And Gamble Company | Vase-added compositions for controlling plant and flower moisture transpiration rates |
| US6348217B1 (en) | 2000-08-04 | 2002-02-19 | Mantrose-Haeuser Co. Inc. | Method for preparing stable bleached shellac |
| WO2002035553A2 (en) | 2000-10-23 | 2002-05-02 | Simon Fraser University | Method and apparatus for producing a discrete particle |
| GB0104268D0 (en) | 2001-02-21 | 2001-04-11 | Unilever Plc | Antiperspirant or deodorant compositions |
| US6500974B2 (en) | 2001-02-28 | 2002-12-31 | Council Of Scientific And Industrial Research | Process for the preparation of a monoglyceride |
| JP3583380B2 (ja) | 2001-04-26 | 2004-11-04 | 高砂香料工業株式会社 | コーティング剤およびコーティング粉末 |
| BR0210964A (pt) | 2001-07-12 | 2004-10-13 | Advanced Food Technologies Inc | Tipo de produto alimentìcio cozido, método de preparar um alimento cozido de conveniência/refeição leve, produto, e, método de preparar um produto alimentìcio |
| EP1785130A3 (en) | 2001-07-18 | 2007-11-28 | Unilever PLC | Hair and/or scalp treatment compositions |
| FR2828487B1 (fr) | 2001-08-09 | 2005-05-27 | Genfit S A | Nouveaux composes derives d'acides gras, preparation et utilisations |
| US7013232B2 (en) | 2001-08-15 | 2006-03-14 | National Insurance Corporation | Network-based system for configuring a measurement system using configuration information generated based on a user specification |
| US20030194445A1 (en) | 2001-11-12 | 2003-10-16 | Kuhner Carla H. | Compositions and methods of use of peptides in combination with biocides and/or germicides |
| US20040071845A1 (en) | 2002-06-07 | 2004-04-15 | Hekal Ihab M. | Methods for preserving fresh produce |
| US20040220283A1 (en) | 2002-07-29 | 2004-11-04 | Transform Pharmaceuticals, Inc. | Aqueous 2,6-diisopropylphenol pharmaceutical compositions |
| US7935375B2 (en) | 2002-08-02 | 2011-05-03 | Basf Corporation | Process and coating composition for extending the shelf life of post harvest produce |
| US20100210745A1 (en) | 2002-09-09 | 2010-08-19 | Reactive Surfaces, Ltd. | Molecular Healing of Polymeric Materials, Coatings, Plastics, Elastomers, Composites, Laminates, Adhesives, and Sealants by Active Enzymes |
| US20110240064A1 (en) | 2002-09-09 | 2011-10-06 | Reactive Surfaces, Ltd. | Polymeric Coatings Incorporating Bioactive Enzymes for Cleaning a Surface |
| AU2003282921B2 (en) | 2002-10-03 | 2009-06-25 | Agroshield, Llc | Polymers for protecting materials from damage |
| US7776926B1 (en) | 2002-12-11 | 2010-08-17 | Advanced Cardiovascular Systems, Inc. | Biocompatible coating for implantable medical devices |
| US8367047B2 (en) | 2002-12-20 | 2013-02-05 | L'oreal | Hair compositions |
| CA2424200C (en) | 2003-03-31 | 2009-08-04 | The Sunblush Technologies Corporation | Compound and method for preserving cut apples |
| JP4179034B2 (ja) | 2003-04-18 | 2008-11-12 | ソニー株式会社 | 通信システム、通信装置、通信方法及びプログラム |
| US6822105B1 (en) | 2003-08-12 | 2004-11-23 | Stepan Company | Method of making alkyl esters using glycerin |
| US8101221B2 (en) | 2003-08-28 | 2012-01-24 | Mantrose-Haeuser Co., Inc. | Methods for preserving fresh produce |
| US20050053593A1 (en) | 2003-09-09 | 2005-03-10 | 3M Innovative Properties Company | Antimicrobial compositions and methods |
| JP2005097437A (ja) | 2003-09-25 | 2005-04-14 | Fuji Photo Film Co Ltd | 静電インクジェット用インク組成物およびインクジェット記録方法 |
| ES2229948B1 (es) | 2003-10-14 | 2006-07-01 | Universidad Politecnica De Valencia | Preparacion de monoesteres de acidos grasos. |
| US7357957B2 (en) | 2004-05-07 | 2008-04-15 | Fractec Research & Development Inc. | Spreadable food product |
| FR2872068B1 (fr) | 2004-06-28 | 2006-10-27 | Centre Nat Rech Scient Cnrse | Procede et dispositif pour le depot de couches minces par pulverisation electrohydrodynamique, notamment en post-decharge |
| JP2006008968A (ja) * | 2004-06-29 | 2006-01-12 | Ono Yoshio | グミ植物種子成分抽出方法 |
| MXPA06014986A (es) | 2004-07-02 | 2007-09-14 | Basf Corp | Proceso para conservar productos frescos y composiciones de revestimiento para el mismo. |
| FR2874424B1 (fr) | 2004-08-17 | 2007-05-11 | Materiel Arboriculture | Dispositif d'analyse optique de produits tels que des fruits a eclairage indirect |
| DE102004043824A1 (de) | 2004-09-10 | 2006-03-16 | Cognis Ip Management Gmbh | Emulsionen mit ungesättigten Fettsäuren und deren Estern |
| DE102004049107A1 (de) | 2004-10-07 | 2006-04-13 | Behr Gmbh & Co. Kg | Beschichtungsverfahren |
| KR101282098B1 (ko) | 2005-02-04 | 2013-07-04 | 안칭 중창 바이오테크놀로지 컴파니 리미티드 | 지방산 제조 방법 |
| EP1693436A1 (en) | 2005-02-21 | 2006-08-23 | Cargill Inc. | Hardened vegetable oils and derivatives thereof |
| FI120684B (fi) | 2005-10-21 | 2010-01-29 | Valtion Teknillinen | Menetelmä oligo-/polyestereiden valmistamiseksi suberiinin ja/tai kutiinin karboksyylihapposeoksesta |
| US8247609B2 (en) | 2005-10-25 | 2012-08-21 | Pharamleads | Aminoacid derivatives containing a disulfanyl group in the form of mixed disulfanyl and aminopeptidase N inhibitors |
| FR2893628B1 (fr) | 2005-11-18 | 2008-05-16 | Expanscience Laboratoires Sa | Procede d'obtention d'une huile d'avocat raffinee riche en triglycerides et huile susceptible d'etre obtenue par un tel procede |
| GB0524979D0 (en) | 2005-12-07 | 2006-01-18 | Queen Mary & Westfield College | An electrospray device and a method of electrospraying |
| US7897651B2 (en) | 2005-12-09 | 2011-03-01 | Kazutoshi Ikenaga | Method for depolymerizing polyester and unsaturated polyester, and method for recovering polyester monomer using the depolymerization |
| CA2641117C (en) | 2006-01-31 | 2018-01-02 | Nanocopoeia, Inc. | Nanoparticle coating of surfaces |
| EP1991624A2 (en) | 2006-02-23 | 2008-11-19 | E.I. Du Pont De Nemours And Company | Removable antimicrobial coating compositions and methods of use |
| CA2649704A1 (en) | 2006-04-18 | 2007-10-25 | Regents Of The University Of Minnesota | Depolymerization extraction of compounds from birch bark |
| US7550617B2 (en) | 2006-10-02 | 2009-06-23 | Medical College Of Georgia Research Institute | Compositions and methods for the treatment of renal and cardiovascular disease |
| US7732470B2 (en) | 2006-10-02 | 2010-06-08 | Medical College Of Georgia Research Institute | Compositions and methods for the treatment of renal and cardiovascular disease |
| AU2008211160B2 (en) | 2007-01-31 | 2013-07-25 | Valent Biosciences Coporation | Use of adjuvants to improve abscisic acid performance |
| EP2144985A2 (en) | 2007-03-30 | 2010-01-20 | Reliance Life Sciences Pvt., Ltd. | An integrated process for the preparation of fatty acid methyl ester (biodiesel) |
| US20100278784A1 (en) | 2007-05-15 | 2010-11-04 | Puretech Ventures | Methods and compositions for treating skin conditions |
| US7997026B2 (en) | 2007-06-15 | 2011-08-16 | State of Oregon, by and through the State Board of Higher Education on behalf of Oregon State University | Perishable-fruit-bearing cut-limb preservation and distribution method, coating and shipping container therefor |
| FI120835B (fi) | 2007-07-10 | 2010-03-31 | Valtion Teknillinen | Uusia esteraaseja ja niiden käyttö |
| US7879384B2 (en) | 2007-11-08 | 2011-02-01 | Kraft Foods Global Brands Llc | Structured glycerol esters useful as edible moisture barriers |
| US20090142453A1 (en) | 2007-11-30 | 2009-06-04 | Lobisser George F | Nutraceutical Coatings fo Fruits and Vegetables |
| CA2709649A1 (en) | 2007-12-20 | 2009-07-02 | Novozymes A/S | Cutinase for detoxification of feed products |
| WO2009087632A2 (en) | 2008-01-08 | 2009-07-16 | M.D. Lederman Consulting Ltd. | Emulsified wax compositions and uses thereof |
| US20090181114A1 (en) | 2008-01-11 | 2009-07-16 | U.S. Nutraceuticals, Llc D/B/A Valensa International | Chia seed beverage and related method |
| BRPI0908879B1 (pt) | 2008-02-29 | 2019-07-09 | University Of Central Florida Research Foundation, Inc. | Método de degradação de planta, coquetel de degradação de plantas, material de planta homogeneizado e coquetel de enzimas |
| TW200939956A (en) | 2008-03-26 | 2009-10-01 | Riken | Agent for controlling post-harvest disease and method for controlling post-harvest disease |
| US20110244095A1 (en) | 2008-09-22 | 2011-10-06 | Xeda International | Method for Coating Food Products |
| US8501445B2 (en) | 2008-10-27 | 2013-08-06 | Toyo Seikan Kaisha, Ltd. | Method for producing oligomer and/or monomer by degrading biodegradable resin |
| US20100186674A1 (en) | 2009-01-26 | 2010-07-29 | E. I. Du Pont De Nemours And Company | Methods and compositions for treating fertilized avian eggs |
| SE534010C2 (sv) | 2009-02-13 | 2011-03-29 | Stfi Packforsk Ab | Förfarande för omvandling av suberin- och/eller cutin-innehållande växtdelar till en blandning innehållande en suberinmonomer |
| WO2010124131A1 (en) | 2009-04-23 | 2010-10-28 | State Of Oregon Acting By And Through The State Board Of Higher Education On Behalf Of Oregaon State University | Flexible films and methods of making and using flexible films |
| US8252354B2 (en) | 2009-06-08 | 2012-08-28 | Mas Marketing Holding Company, Llc | Manufacture of seed derivative compositions |
| DE102009031053A1 (de) | 2009-06-30 | 2011-01-13 | Clariant International Ltd. | Kontinuierliches Verfahren zur Herstellung von Estern aliphatischer Carbonsäuren |
| CA2767935A1 (en) | 2009-07-31 | 2011-02-03 | Ecology Coatings, Inc. | Coated substrates and methods of preparing the same |
| ES2705211T3 (es) | 2009-08-26 | 2019-03-22 | Mantrose Haeuser Company Inc | Película flexible impresa para envasado de alimentos |
| JP2013514066A (ja) | 2009-12-16 | 2013-04-25 | ビーエーエスエフ ソシエタス・ヨーロピア | 生鮮食品のための、キトサン、界面活性剤、およびポリエチレングリコールを含有するコーティング組成物 |
| US20130095141A1 (en) | 2010-03-08 | 2013-04-18 | Beverly A. Schad | Food grade dry film coating composition and methods of making and using the same |
| US9492395B2 (en) | 2010-05-11 | 2016-11-15 | Sensient Colors Llc | Film coating composition and methods of making and using the same |
| IL212563A0 (en) | 2010-05-25 | 2011-07-31 | Rohm & Haas | Waxy coatings on plant parts |
| US8586807B2 (en) * | 2010-06-24 | 2013-11-19 | Old Dominion University Research Foundation | Process for the selective production of hydrocarbon based fuels from plants containing aliphatic biopolymers utilizing water at subcritical conditions |
| US20120003356A1 (en) | 2010-06-30 | 2012-01-05 | Athula Ekanayake | Process for Producing Cassava Flour |
| US20120015093A1 (en) | 2010-07-16 | 2012-01-19 | Finney John M | Whole seed processing and controlled viscosity products |
| MX348348B (es) | 2010-08-09 | 2017-04-24 | Inst Tecnologico Estudios Superiores Monterrey | Extracto de aguacate enriquecido en compuestos bioactivos con actividad antimicrobiana, antibacteriana e inhibidora de la germinacion de esporas bacterianas. |
| US8263751B2 (en) | 2010-11-19 | 2012-09-11 | Daedalus Innovations Llc | Method for removing a protein from a metal chelate resin |
| WO2012095486A1 (en) | 2011-01-12 | 2012-07-19 | Dsm Ip Assets B.V. | Reduction of weight loss of fruits |
| FI123867B (fi) | 2011-04-06 | 2013-11-29 | Teknologian Tutkimuskeskus Vtt | Uusia kutinaaseja, niiden tuottaminen ja käytöt |
| MX2011003856A (es) | 2011-04-11 | 2012-10-24 | Univ Mexico Nacional Autonoma | Composicion de nanoparticulas lipidicas solidas para la conservacion prolongada por recubrimiento de frutas, verduras, semillas, cereales y/o alimentos frescos. |
| AU2012279209A1 (en) | 2011-07-01 | 2014-01-23 | Synedgen, Inc. | Methods and compositions of reducing and preventing bacterial growth and the formation of biofilm on a surface utilizing chitosan-derivative compounds |
| US20130209617A1 (en) | 2011-08-10 | 2013-08-15 | Pace International, Llc | Compositions and methods for use in promoting produce health |
| EP2581340B1 (de) | 2011-10-14 | 2017-02-22 | Evonik Degussa GmbH | Verbessertes Verfahren zur Behandlung von Wasser mit Chlordioxid |
| CN102335142B (zh) | 2011-10-25 | 2014-03-26 | 上海理工大学 | 一种能够原位自组装成难溶药物的纳米脂质体的复合微球及其制备方法 |
| US8708575B2 (en) | 2011-11-11 | 2014-04-29 | Sae Magnetics (H.K.) Ltd. | Active optical connector using audio port |
| JP5944303B2 (ja) | 2011-12-08 | 2016-07-05 | 花王株式会社 | 脂肪酸モノグリセライド含有混合物の製造方法。 |
| US9648890B2 (en) | 2012-03-29 | 2017-05-16 | Yissum Research Development Company Of The Hebrew University Of Jerusalem Ltd. | Edible coating for plant matter |
| EA029545B1 (ru) | 2012-04-06 | 2018-04-30 | Эйч А Ди Корпорейшн | Применение высоких скоростей сдвига при обработке масел |
| US20140033926A1 (en) | 2012-08-03 | 2014-02-06 | Robert Scott Fassel | Filtration System |
| US9095152B2 (en) | 2012-09-12 | 2015-08-04 | Munger Bros., LLC | Method for disinfecting, sanitizing, and packaging ready-to-eat produce |
| US9388098B2 (en) | 2012-10-09 | 2016-07-12 | Elevance Renewable Sciences, Inc. | Methods of making high-weight esters, acids, and derivatives thereof |
| US20140199449A1 (en) | 2013-01-14 | 2014-07-17 | Andy Hernandez | Methods for extending the shelf life of processed cucurbita pepo vegetables |
| US10400128B2 (en) | 2013-03-14 | 2019-09-03 | Oregon State University | Nano-cellulose edible coatings and uses thereof |
| WO2014162238A2 (en) | 2013-03-31 | 2014-10-09 | Jain Pranay | A process for recycling a metalized polyester film |
| DK2789681T3 (en) | 2013-04-11 | 2017-10-02 | Purac Biochem Bv | PREPARATION OF LACTYLATES DIRECT FROM OIL |
| EP2993993A2 (en) | 2013-04-26 | 2016-03-16 | Solazyme, Inc. | Low polyunsaturated fatty acid oils and uses thereof |
| WO2014190113A1 (en) | 2013-05-23 | 2014-11-27 | Nature Seal, Inc. | Antimicrobial wash |
| CN103283830B (zh) | 2013-05-24 | 2014-11-05 | 南京林业大学 | 银杏果复合保鲜剂及保鲜方法 |
| BR112015032346A2 (pt) | 2013-06-24 | 2017-07-25 | Merial Inc | compostos de isotiazolina para o combate de pragas de invertebrados |
| US9744542B2 (en) | 2013-07-29 | 2017-08-29 | Apeel Technology, Inc. | Agricultural skin grafting |
| ITPR20130066A1 (it) * | 2013-08-26 | 2015-02-27 | Chiesa Virginio | Metodo di estrazione di un polimero poliestere o cutina dagli scarti di pomodoro e polimero poliestere cosi' estratto. |
| WO2015031663A1 (en) | 2013-08-28 | 2015-03-05 | Sensient Colors Llc | Edible coating compositions, edible coatings, and methods for making and using the same |
| FR3011467B1 (fr) | 2013-10-08 | 2016-02-12 | Centre Nat Rech Scient | Composes et compositions comprenant de tels composes pour la prevention ou le traitement des dyslipidemies |
| EP3071043A4 (en) | 2013-11-22 | 2017-05-31 | Agri-Néo Inc. | A novel composition and method of use to control pathogens and prevent diseases in seeds |
| CN103719261B (zh) | 2013-12-18 | 2015-10-28 | 广西科技大学 | 一种芒果保水杀菌涂膜液及其制备方法 |
| WO2015176020A1 (en) | 2014-05-16 | 2015-11-19 | Provivi, Inc. | Synthesis of olefinic alcohols via enzymatic terminal hydroxylation |
| EP3253380A1 (en) | 2015-02-05 | 2017-12-13 | Nanomedex, LLC | Emulsion containing two oils and stabilizers |
| CA2976722C (en) | 2015-03-30 | 2021-06-08 | Dentsply Detrey Gmbh | Dental composition |
| WO2016168319A1 (en) * | 2015-04-13 | 2016-10-20 | University Of South Florida | Cutin-like materials with advanced functionalities and methods of manufacture |
| US20160324172A1 (en) | 2015-05-04 | 2016-11-10 | Jones-Hamilton Co. | Post-Harvest Coating for Fresh Produce |
| EP3673738B1 (en) | 2015-05-20 | 2024-02-28 | Apeel Technology, Inc. | Plant extract compositions and methods of preparation thereof |
| US9475643B1 (en) | 2015-06-12 | 2016-10-25 | Djt Investments, Llc. | Roller system for sorting produce |
| WO2017043972A1 (en) | 2015-09-09 | 2017-03-16 | Arec Crop Protection B.V. | An antifungal composition comprising natamycin and c4-c22 fatty acids, monoglycerides of these fatty acids and/or derivatives of these fatty acids |
| ES2935595T3 (es) | 2015-09-16 | 2023-03-08 | Apeel Tech Inc | Método de formación de un recubrimiento protector aplicando compuestos de glicéridos de ácidos grasos a una superficie |
| ES2939007T3 (es) | 2015-12-10 | 2023-04-18 | Apeel Tech Inc | Composiciones de extractos de plantas para formar recubrimientos protectores |
| EP3195731A1 (en) | 2016-01-19 | 2017-07-26 | Liquidseal Holding B.V. | Coating for fruit |
| EP3407713A1 (en) | 2016-01-26 | 2018-12-05 | Apeel Technology, Inc. | Method for preparing and preserving sanitized products |
| CN109561674B (zh) | 2016-04-01 | 2022-05-31 | 阿比尔技术公司 | 在贮藏和运输期间降低收获产品中的腐败的方法 |
| CN109561702B (zh) | 2016-07-08 | 2024-01-30 | 阿比尔技术公司 | 控制收获产品成熟速率的方法 |
| WO2018042435A1 (en) | 2016-08-31 | 2018-03-08 | Nontoxico Ltd | A pest control composition and method thereof |
| EP3541192A4 (en) | 2016-11-17 | 2020-07-01 | Apeel Technology, Inc. | COMPOSITIONS MOLDED FROM PLANT EXTRACTS AND METHOD FOR THE PRODUCTION THEREOF |
| CN107794114A (zh) | 2017-11-20 | 2018-03-13 | 重庆汇达柠檬科技集团有限公司 | 一种冷榨制备脱苦柠檬籽油的加工工艺 |
| CN107828560B (zh) | 2017-12-04 | 2019-11-22 | 奇德喜 | 一种皂米的制作方法 |
| US20200068912A1 (en) | 2018-09-05 | 2020-03-05 | Apeel Technology, Inc. | Compounds and formulations for protective coatings |
| CN110255947B (zh) | 2019-05-22 | 2022-03-04 | 湖南昌迪环境科技有限公司 | 一种助磨剂及其应用 |
| JP2022537536A (ja) | 2019-06-21 | 2022-08-26 | アピール テクノロジー,インコーポレイテッド | 植物質から取り出された化合物及びその調製方法 |
| CN116457332A (zh) | 2020-10-30 | 2023-07-18 | 阿比尔技术公司 | 组合物及其制备方法 |
| CN112898630B (zh) | 2021-01-26 | 2022-06-17 | 佛山科学技术学院 | 一种聚酯类塑料的机械化学绿色降解方法 |
-
2016
- 2016-12-09 ES ES19214825T patent/ES2939007T3/es active Active
- 2016-12-09 CN CN202110066463.8A patent/CN112841185A/zh active Pending
- 2016-12-09 EP EP19214825.2A patent/EP3649860B1/en active Active
- 2016-12-09 ES ES16820459T patent/ES2797697T3/es active Active
- 2016-12-09 EP EP16820459.2A patent/EP3386303B1/en active Active
- 2016-12-09 WO PCT/US2016/065917 patent/WO2017100636A1/en active Application Filing
- 2016-12-09 JP JP2018530034A patent/JP6549326B2/ja active Active
- 2016-12-09 CN CN201680079439.5A patent/CN108966638B/zh active Active
-
2017
- 2017-08-18 US US15/680,541 patent/US9957215B2/en active Active
-
2018
- 2018-04-02 US US15/943,553 patent/US10561155B2/en active Active
- 2018-06-05 IL IL259820A patent/IL259820B/en active IP Right Grant
- 2018-10-03 US US16/151,268 patent/US10407377B2/en active Active
-
2019
- 2019-11-22 US US16/692,807 patent/US11028030B2/en active Active
-
2020
- 2020-01-16 IL IL272083A patent/IL272083B/en unknown
-
2021
- 2021-06-07 US US17/340,952 patent/US11767278B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| US10561155B2 (en) | 2020-02-18 |
| US11028030B2 (en) | 2021-06-08 |
| CN108966638A (zh) | 2018-12-07 |
| IL272083B (en) | 2021-07-29 |
| EP3649860A1 (en) | 2020-05-13 |
| US9957215B2 (en) | 2018-05-01 |
| IL259820A (en) | 2018-07-31 |
| ES2797697T3 (es) | 2020-12-03 |
| WO2017100636A1 (en) | 2017-06-15 |
| EP3386303A1 (en) | 2018-10-17 |
| EP3649860B1 (en) | 2023-02-01 |
| IL259820B (en) | 2020-02-27 |
| ES2939007T3 (es) | 2023-04-18 |
| US20210291074A1 (en) | 2021-09-23 |
| US20190031590A1 (en) | 2019-01-31 |
| EP3386303B1 (en) | 2020-03-11 |
| JP6549326B2 (ja) | 2019-07-24 |
| JP2019501154A (ja) | 2019-01-17 |
| US10407377B2 (en) | 2019-09-10 |
| CN112841185A (zh) | 2021-05-28 |
| US11767278B2 (en) | 2023-09-26 |
| IL272083A (en) | 2020-03-31 |
| US20180222835A1 (en) | 2018-08-09 |
| US20180044276A1 (en) | 2018-02-15 |
| US20200100514A1 (en) | 2020-04-02 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN108966638B (zh) | 用于形成保护性涂层的植物提取物组合物 | |
| JP7194678B2 (ja) | 植物抽出物から形成される組成物及びその調製方法 | |
| US20240081358A1 (en) | Plant extract compositions and methods of preparation thereof | |
| EP0989181B1 (en) | Process for producing essential oils via treatment with supercritical water and essential oils obtained by treatment with supercritical water | |
| EP1144561B1 (en) | A process of obtaining natural antioxidants from plants |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| GR01 | Patent grant | ||
| GR01 | Patent grant |