WO2009131189A1 - ケトオキシムエステル系化合物及びその利用 - Google Patents
ケトオキシムエステル系化合物及びその利用 Download PDFInfo
- Publication number
- WO2009131189A1 WO2009131189A1 PCT/JP2009/058096 JP2009058096W WO2009131189A1 WO 2009131189 A1 WO2009131189 A1 WO 2009131189A1 JP 2009058096 W JP2009058096 W JP 2009058096W WO 2009131189 A1 WO2009131189 A1 WO 2009131189A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- group
- carbon atoms
- general formula
- compound
- acid
- Prior art date
Links
- LCSAOPVSVLGDLE-UHFFFAOYSA-N C(C1OC1)Oc1ccc(C2(c3ccccc3-c3ccccc23)c(cc2)ccc2OCC2OC2)cc1 Chemical compound C(C1OC1)Oc1ccc(C2(c3ccccc3-c3ccccc23)c(cc2)ccc2OCC2OC2)cc1 LCSAOPVSVLGDLE-UHFFFAOYSA-N 0.000 description 1
- FLQPMQLWYJZKNM-UHFFFAOYSA-N CC(C1)C(C(CCCC(OC)=O)=O)=CC=C1F Chemical compound CC(C1)C(C(CCCC(OC)=O)=O)=CC=C1F FLQPMQLWYJZKNM-UHFFFAOYSA-N 0.000 description 1
- LOCXTTRLSIDGPS-AZPGRJICSA-N CCCCCC/C(/C(c(cc1)ccc1Sc1ccccc1)=O)=N\OC(c1ccccc1)=O Chemical compound CCCCCC/C(/C(c(cc1)ccc1Sc1ccccc1)=O)=N\OC(c1ccccc1)=O LOCXTTRLSIDGPS-AZPGRJICSA-N 0.000 description 1
- GTJXQUNBEWGMLS-UHFFFAOYSA-N CCCCOC(CC/C(/C(c(cc1)ccc1Sc1ccccc1)=O)=[I]\OC(C)=O)=O Chemical compound CCCCOC(CC/C(/C(c(cc1)ccc1Sc1ccccc1)=O)=[I]\OC(C)=O)=O GTJXQUNBEWGMLS-UHFFFAOYSA-N 0.000 description 1
- NEFJYOIBBHASIW-BSYVCWPDSA-N COC(CC/C(/C(c(cc1)ccc1Sc1cc2ccccc2cc1)=O)=N\O)=O Chemical compound COC(CC/C(/C(c(cc1)ccc1Sc1cc2ccccc2cc1)=O)=N\O)=O NEFJYOIBBHASIW-BSYVCWPDSA-N 0.000 description 1
- VSOGBIJHAUEXPN-UHFFFAOYSA-N COC(CCCC(c(cc1)ccc1Sc1ccc(cccc2)c2c1)=O)=O Chemical compound COC(CCCC(c(cc1)ccc1Sc1ccc(cccc2)c2c1)=O)=O VSOGBIJHAUEXPN-UHFFFAOYSA-N 0.000 description 1
- JLJQMYBHTDPEDU-UHFFFAOYSA-N COC(CCCC(c(cc1)ccc1Sc1ccc(cccc2)c2c1)O)=O Chemical compound COC(CCCC(c(cc1)ccc1Sc1ccc(cccc2)c2c1)O)=O JLJQMYBHTDPEDU-UHFFFAOYSA-N 0.000 description 1
- QGMMAQOHPBFUPD-UHFFFAOYSA-N COC(CCCC(c(cc1)ccc1Sc1ccccc1)=O)=O Chemical compound COC(CCCC(c(cc1)ccc1Sc1ccccc1)=O)=O QGMMAQOHPBFUPD-UHFFFAOYSA-N 0.000 description 1
- 0 Cc1c(*)c(-c2c(*)c(*)c(*)c(*)c2*2*)c2c(*)c1* Chemical compound Cc1c(*)c(-c2c(*)c(*)c(*)c(*)c2*2*)c2c(*)c1* 0.000 description 1
- RFCQDOVPMUSZMN-UHFFFAOYSA-N Sc1cc2ccccc2cc1 Chemical compound Sc1cc2ccccc2cc1 RFCQDOVPMUSZMN-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C323/00—Thiols, sulfides, hydropolysulfides or polysulfides substituted by halogen, oxygen or nitrogen atoms, or by sulfur atoms not being part of thio groups
- C07C323/23—Thiols, sulfides, hydropolysulfides or polysulfides substituted by halogen, oxygen or nitrogen atoms, or by sulfur atoms not being part of thio groups containing thio groups and nitrogen atoms, not being part of nitro or nitroso groups, bound to the same carbon skeleton
- C07C323/46—Thiols, sulfides, hydropolysulfides or polysulfides substituted by halogen, oxygen or nitrogen atoms, or by sulfur atoms not being part of thio groups containing thio groups and nitrogen atoms, not being part of nitro or nitroso groups, bound to the same carbon skeleton having at least one of the nitrogen atoms, not being part of nitro or nitroso groups, further bound to other hetero atoms
- C07C323/47—Thiols, sulfides, hydropolysulfides or polysulfides substituted by halogen, oxygen or nitrogen atoms, or by sulfur atoms not being part of thio groups containing thio groups and nitrogen atoms, not being part of nitro or nitroso groups, bound to the same carbon skeleton having at least one of the nitrogen atoms, not being part of nitro or nitroso groups, further bound to other hetero atoms to oxygen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C323/00—Thiols, sulfides, hydropolysulfides or polysulfides substituted by halogen, oxygen or nitrogen atoms, or by sulfur atoms not being part of thio groups
- C07C323/50—Thiols, sulfides, hydropolysulfides or polysulfides substituted by halogen, oxygen or nitrogen atoms, or by sulfur atoms not being part of thio groups containing thio groups and carboxyl groups bound to the same carbon skeleton
- C07C323/62—Thiols, sulfides, hydropolysulfides or polysulfides substituted by halogen, oxygen or nitrogen atoms, or by sulfur atoms not being part of thio groups containing thio groups and carboxyl groups bound to the same carbon skeleton having the sulfur atom of at least one of the thio groups bound to a carbon atom of a six-membered aromatic ring of the carbon skeleton
- C07C323/63—Thiols, sulfides, hydropolysulfides or polysulfides substituted by halogen, oxygen or nitrogen atoms, or by sulfur atoms not being part of thio groups containing thio groups and carboxyl groups bound to the same carbon skeleton having the sulfur atom of at least one of the thio groups bound to a carbon atom of a six-membered aromatic ring of the carbon skeleton the carbon skeleton being further substituted by nitrogen atoms, not being part of nitro or nitroso groups
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D209/00—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D209/56—Ring systems containing three or more rings
- C07D209/80—[b, c]- or [b, d]-condensed
- C07D209/82—Carbazoles; Hydrogenated carbazoles
- C07D209/86—Carbazoles; Hydrogenated carbazoles with only hydrogen atoms, hydrocarbon or substituted hydrocarbon radicals, directly attached to carbon atoms of the ring system
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/0005—Production of optical devices or components in so far as characterised by the lithographic processes or materials used therefor
- G03F7/0007—Filters, e.g. additive colour filters; Components for display devices
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/004—Photosensitive materials
- G03F7/0045—Photosensitive materials with organic non-macromolecular light-sensitive compounds not otherwise provided for, e.g. dissolution inhibitors
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/004—Photosensitive materials
- G03F7/027—Non-macromolecular photopolymerisable compounds having carbon-to-carbon double bonds, e.g. ethylenic compounds
- G03F7/028—Non-macromolecular photopolymerisable compounds having carbon-to-carbon double bonds, e.g. ethylenic compounds with photosensitivity-increasing substances, e.g. photoinitiators
- G03F7/031—Organic compounds not covered by group G03F7/029
Definitions
- the present invention relates to a ketoxime ester compound useful as a photopolymerization initiator, a photopolymerization initiator comprising the compound, and a photopolymerizable composition containing the photopolymerization initiator. More specifically, for example, insulating coating layers, solder resist films, cover layers of various electronic components in liquid crystal display elements, plasma displays, printed wiring boards, large-scale integrated circuits, thin transistors, semiconductor packages, color filters, organic electroluminescence, and the like.
- the present invention relates to a photopolymerizable composition useful for forming a film or the like.
- ketoxime ester compound of the present invention can be used as a highly sensitive photopolymerization initiator, it can be used in the production of optical color filters used in color televisions, liquid crystal display elements, solid-state image sensors, cameras, and the like.
- a photopolymerizable composition containing a coloring material used for pixels hereinafter sometimes referred to as “RGB”), black matrix (hereinafter sometimes referred to as “BM”), and the like; It can be used for transparent photopolymerizable compositions for coatings, ribs (liquid crystal alignment control protrusions), photo spacers, and the like, and its application technical fields are wide.
- an interlayer insulating film for protecting the TFT array element is formed between the TFT array element and the transparent conductive film forming the pixel electrode.
- a contact hole for connecting the drain electrode of the TFT array and the wiring formed by the transparent conductive film is usually formed in the interlayer insulating film.
- a photosensitive thermosetting composition is generally used as a material for the interlayer insulating film.
- thermosetting composition used for such applications, a positive photosensitive composition comprising an alkali-soluble resin and a 1,2-quinonediazide compound is known (for example, see Patent Document 1). Moreover, a photopolymerizable composition is known as a negative thermosetting composition (see, for example, Patent Document 2).
- a negative photosensitive composition containing a color material is applied on a transparent substrate, and each color pixel is formed by repeating image exposure, development, and curing as necessary.
- the pigment dispersion method is widely adopted because it has high accuracy such as pixel position and film thickness, is excellent in durability such as light resistance and heat resistance, and has few defects such as pinholes.
- the photosensitive composition for forming a pixel of a color filter it is required to exhibit high sensitivity and high resolution under the condition of high color density, and for the photosensitive composition for forming BM, a thin film is required. Therefore, it is required to exhibit high sensitivity and high resolution under conditions of high light shielding properties.
- a photosensitive composition having a certain light transmittance such as a general photosensitive composition or a colored photosensitive composition for a color filter (for pixel formation or BM formation) has sensitivity and resolution.
- a photosensitive composition for a color filter containing an initiator composed of a pigment, a binder resin, a polyfunctional acrylic monomer, and a triazine compound is known (see Patent Documents 3 to 6).
- the initiator is bisimidazole in a similar composition (see Patent Documents 7 to 8).
- the photopolymerization initiator for example, bisimidazole or triazine compound
- the photopolymerization initiator used in the conventional pixel or resin BM is simply replaced with the oxime ester compound.
- the image characteristics required for the resin BM that is, sensitivity and resolution cannot be sufficiently improved.
- highly sensitive negative photosensitive compositions are widely required for photospacer compositions, rib compositions, and the like, and this is a technical problem. The point was mainly in the selection of the photopolymerization initiator.
- an object of the present invention is to provide a ketoxime ester compound that can be used as a novel and highly sensitive photopolymerization initiator. Furthermore, an object of the present invention is to provide a photopolymerizable composition useful for use with an interlayer insulating film having high sensitivity and high transmittance. Still another object of the present invention is to provide a photopolymerizable composition useful for color filter applications.
- the present inventors have found a structure of a ketoxime ester compound having a higher photopolymerization efficiency as a photopolymerization initiator, and using the ketoxime ester compound as a photopolymerization initiator.
- the present inventors have found that the above problems can be solved. Furthermore, it has been found that such a specific ketoxime ester compound is itself a novel compound and is effective as an excellent photopolymerization initiator regardless of the presence or absence of a coloring material, and has led to the completion of the present invention. It was.
- X represents a direct bond or an alkylene group having 1 to 20 carbon atoms, each of which may have a substituent, — (CH ⁇ CH) ⁇ —, — (C ⁇ C) ⁇ -Or a combination thereof ( ⁇ represents an integer of 1 to 5), a divalent organic group
- R 1 represents a monovalent organic group which may have a substituent, including an aromatic ring or a heteroaromatic ring
- R 2 is an optionally substituted alkylthio group having 1 to 12 carbon atoms, an alkoxycarbonyl group having 2 to 12 carbon atoms, an alkenyloxycarbonyl group having 3 to 12 carbon atoms, or an alkylthio group having 3 to 12 carbon atoms.
- R 30 and R 31 each independently represents an alkyl group having 1 to 12 carbon atoms or an aryl group having 6 to 20 carbon atoms, each of which may have a substituent
- R 3 represents an optionally substituted alkanoyl group having 2 to 12 carbon atoms, an alkenoyl group having 3 to 25 carbon atoms, a cycloalkanoyl group having 4 to 8 carbon atoms, and an aryloyl group having 7 to 20 carbon atoms.
- a heteroaryloyl group having 3 to 20 carbon atoms, an alkoxycarbonyl group having 2 to 10 carbon atoms, an aryloxycarbonyl group having 7 to 20 carbon atoms, a heteroaryl group having 2 to 20 carbon atoms, or an alkyl having 2 to 20 carbon atoms Represents an aminocarbonyl group.
- X is an alkylene group having 1 to 20 carbon atoms which may have a substituent, and R 2 may have 2 to carbon atoms each having a substituent. 12.
- R 1 is represented by the following general formula (III).
- R 4 to R 8 are each independently a hydrogen atom, a halogen atom, a hydroxyl group, an alkyl group having 1 to 12 carbon atoms which may have a substituent, or 5 to 5 carbon atoms.
- R 9 is a hydrogen atom, an alkyl group having 1 to 12 carbon atoms which may have a substituent, an alkanoyl group having 2 to 8 carbon atoms, an alkenyl group having 3 to 12 carbon atoms, or 6 to 6 carbon atoms.
- R 10 and R 11 are each independently a hydrogen atom, an optionally substituted alkyl group having 1 to 12 carbon atoms, a hydroxyl alkyl group having 2 to 4 carbon atoms, or an alkenyl group having 3 to 5 carbon atoms.
- R 4 to R 8 may be bonded to each other to form a ring structure.
- R 4, R 5, R 7 and R 8 have the same meanings as R 4, R 5, R 7 and R 8 in the general formula (III).
- R 9 is a hydrogen atom, an alkyl group having 1 to 12 carbon atoms that may have a substituent, an alkanoyl group having 2 to 8 carbon atoms, an alkenyl group having 3 to 12 carbon atoms, or an alkyl group having 6 to 20 carbon atoms. Represents an aryl group or a trialkylsilyl group having 3 to 15 carbon atoms; ) [6] A photopolymerization initiator comprising the ketoxime ester compound according to any one of [1] to [5] above.
- the keto according to any one of [1] to [5], comprising (A) an ethylenically unsaturated group-containing compound and (B) a photopolymerization initiator, wherein (B) the photopolymerization initiator is A photopolymerizable composition comprising an oxime ester compound.
- a liquid crystal display device comprising an interlayer insulating film formed of the photopolymerizable composition according to [7].
- a color filter comprising a black matrix formed of the photopolymerizable composition according to [8] or [9].
- a color filter comprising a pixel formed of the photopolymerizable composition according to [8] or [9].
- the ketoxime ester compound of the present invention can be used as a novel and highly sensitive photopolymerization initiator.
- a photopolymerizable composition having high sensitivity and high transmittance and useful particularly for interlayer insulating film applications can be constituted.
- a photopolymerizable composition useful for color filter applications can be constituted by further combining with a color material.
- a photopolymerizable composition using this ketoxime ester compound in combination with a black pigment as a photopolymerization initiator has excellent light sensitivity and resolution while being highly light-shielding in a thin film.
- the resin BM can be formed.
- the photopolymerizable composition using the ketoxime ester compound of the present invention as a photopolymerization initiator in combination with pigments of each color such as red, green, and blue is excellent in adhesion to the substrate and electrical characteristics, and is suitable for applying pixels. There is little outbreak.
- a color filter in which a resin BM or a pixel is formed using the photopolymerizable composition of the present invention is excellent in accuracy, flatness, and durability, the display quality of a liquid crystal display element can be improved.
- the manufacturing process and the color filter itself do not contain harmful substances, the danger to the human body is reduced and the environmental safety is improved.
- the photopolymerization initiator and the photopolymerizable composition of the present invention are not limited to those for interlayer insulating films, color filter pixels, and BM, but for overcoats, ribs (liquid crystal alignment control protrusions), and photospacers. It can also be used for transparent photopolymerizable compositions such as for applications, and its applied technical field is extremely wide.
- (meth) acryl means “acryl and / or methacryl”, and the same applies to “(meth) acryloyl”.
- (Poly) hydroxy means “hydroxy and / or polyhydroxy”.
- ketoxime ester compounds The ketoxime ester compound of the present invention is represented by the following general formula (I).
- X represents a direct bond or an alkylene group having 1 to 20 carbon atoms, each of which may have a substituent, — (CH ⁇ CH) ⁇ —, — (C ⁇ C) ⁇ -Or a combination thereof ( ⁇ represents an integer of 1 to 5), a divalent organic group
- R 1 represents a monovalent organic group which may have a substituent, including an aromatic ring or a heteroaromatic ring
- R 2 is an optionally substituted alkylthio group having 1 to 12 carbon atoms, an alkoxycarbonyl group having 2 to 12 carbon atoms, an alkenyloxycarbonyl group having 3 to 12 carbon atoms, or an alkylthio group having 3 to 12 carbon atoms.
- R 30 and R 31 each independently represents an alkyl group having 1 to 12 carbon atoms or an aryl group having 6 to 20 carbon atoms, each of which may have a substituent
- R 3 represents an optionally substituted alkanoyl group having 2 to 12 carbon atoms, an alkenoyl group having 3 to 25 carbon atoms, a cycloalkanoyl group having 4 to 8 carbon atoms, and an aryloyl group having 7 to 20 carbon atoms.
- a heteroaryloyl group having 3 to 20 carbon atoms, an alkoxycarbonyl group having 2 to 10 carbon atoms, an aryloxycarbonyl group having 7 to 20 carbon atoms, a heteroaryl group having 2 to 20 carbon atoms, or an alkyl having 2 to 20 carbon atoms Represents an aminocarbonyl group.
- X represents a direct bond or an alkylene group having 1 to 20 carbon atoms, each of which may have a substituent, — (CH ⁇ CH) ⁇ - [alkenylene group], — (C ⁇ C) A divalent organic group consisting of ⁇ - [alkynylene group] or a combination thereof ( ⁇ represents an integer of 1 to 5).
- ⁇ is preferably 1 to 3 from the viewpoint of ease of production.
- alkylene group of X examples include a methylene group, an ethylene group, a trimethylene group, a tetramethylene group, an octamethylene group, a decamethylene group, and a group represented by the following structural formula.
- Me represents a methyl group. The same applies hereinafter.
- Examples of the alkenylene group of X include an ethynylene group and a group represented by the following structural formula.
- examples of the alkynylene group of X include groups represented by the following structural formula in addition to the acetylene group.
- an alkylene group or alkenylene group having 1 to 20 carbon atoms which may have a substituent is preferably used. Most preferred is an alkylene group which may have a substituent.
- the number of carbon atoms of the alkylene group is preferably 2 or more. Moreover, Preferably it is 15 or less, More preferably, it is 10 or less.
- R 1 represents a monovalent organic group which may have a substituent, including an aromatic ring or a heteroaromatic ring.
- R 1 is derived from a phenyl group and a condensed ring composed of an aromatic hydrocarbon ring such as a naphthalene ring, anthracene ring, chrysene ring, phenanthrene ring, azulene ring, fluorene ring, acenaphthylene ring, and indene ring.
- an aromatic hydrocarbon ring such as a naphthalene ring, anthracene ring, chrysene ring, phenanthrene ring, azulene ring, fluorene ring, acenaphthylene ring, and indene ring.
- Groups groups derived from heterocyclic rings such as pyridine ring, pyrimidine ring, imidazole ring, triazine ring; acridine ring, phenanthridine ring, xanthene ring, carbazole ring, phenazine ring, phenothiazine ring, phenoxazine ring, benzothiazole ring, etc. Examples thereof include a group derived from a condensed ring composed of an aromatic hydrocarbon ring and an aromatic heterocycle.
- R 1 is particularly preferably a group represented by the following general formula (III).
- R 4 to R 8 are each independently a hydrogen atom, a halogen atom, a hydroxyl group, an alkyl group having 1 to 12 carbon atoms which may have a substituent, or 5 to 5 carbon atoms.
- R 9 is a hydrogen atom, an alkyl group having 1 to 12 carbon atoms which may have a substituent, an alkanoyl group having 2 to 8 carbon atoms, an alkenyl group having 3 to 12 carbon atoms, or 6 to 6 carbon atoms.
- R 10 and R 11 are each independently a hydrogen atom, an optionally substituted alkyl group having 1 to 12 carbon atoms, a hydroxyl alkyl group having 2 to 4 carbon atoms, or an alkenyl group having 3 to 5 carbon atoms.
- R 4 to R 8 may be bonded to each other to form a ring structure.
- R 4 to R 8 include a hydrogen atom; a halogen atom such as F, Cl and Br; a hydroxyl group; An alkyl group having 1 to 12 carbon atoms such as a methyl group, an ethyl group or a butyl group; A cycloalkyl group having 5 to 8 carbon atoms such as a cyclohexyl group and a cyclopentyl group; Aryl groups having 6 to 20 carbon atoms such as phenyl group, toluyl group and naphthyl group; Arylalkyl groups having 7 to 20 carbon atoms such as benzyl group and phenylpropyl group; Aryloyl groups having 7 to 20 carbon atoms such as benzoyl group, toluoyl group, naphthoyl group; An alkanoyl group having 2 to 12 carbon atoms such as an acetyl group and a propylcarbonyl group; A heteroaryloyl group
- R 4 , R 5 , R 6 , R 7 and R 8 is —SR 9 or —NR 10 R 11 .
- R 4 to R 8 may combine with each other to form a ring structure.
- R 6 is a group represented by —NR 10 R 11
- R 10 or R 11 is bonded to R 5 or R 7 to form a carbazole ring represented by the general formula (IV) described later. May be.
- R 4 , R 5 , R 7 and R 8 in the formula (III) are independently a hydrogen atom, an alkyl group, an alkoxy group, or the like, and R 6 Is preferably —SR 9 or —NR 10 R 11 .
- R 9 examples include a methyl group, a phenyl group, and a naphthyl group, and an aryl group such as a phenyl group and a naphthyl group is preferable.
- R 10 and R 11 include a methyl group and an ethyl group
- NR 10 R 11 is preferably a dialkylamino group such as a morpholino group, a dimethylamino group, or a diethylamino group.
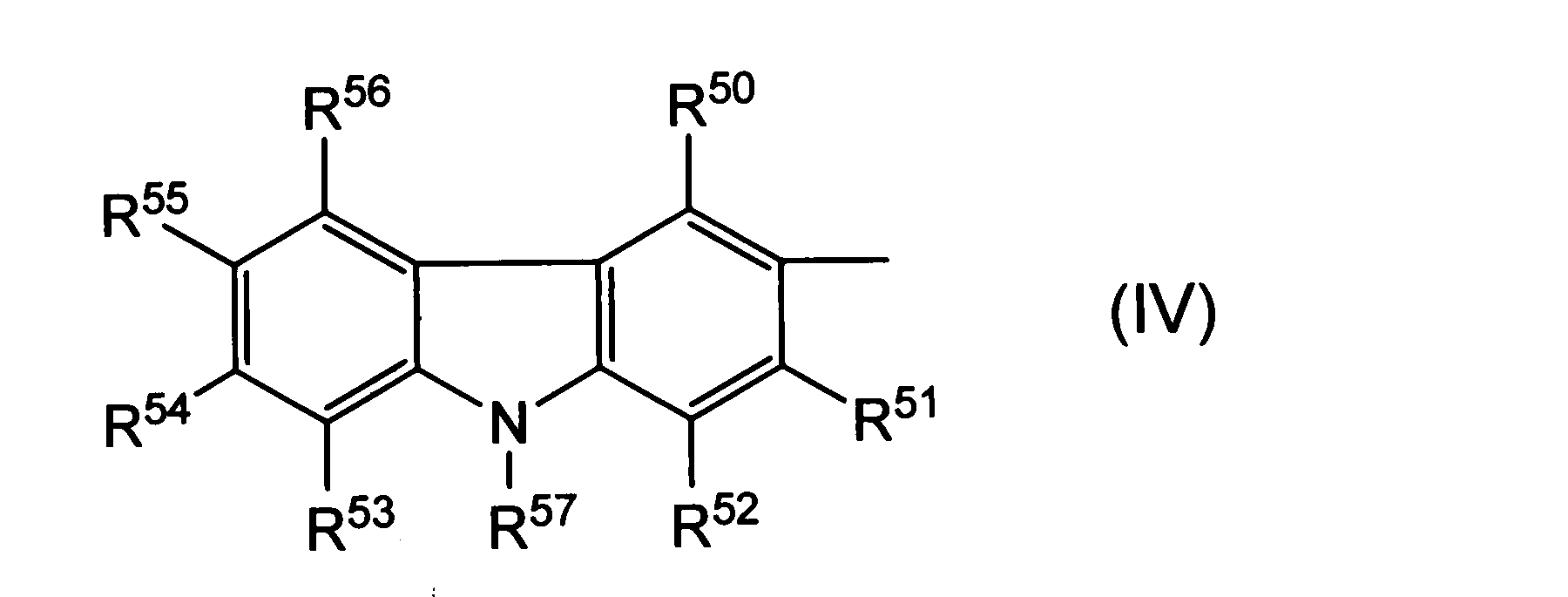
- R 1 is an optionally substituted carbazole ring represented by the following general formula (IV).
- R 50 to R 56 have the same meanings as R 4 to R 8 in the general formula (III), and R 57 represents R 10 or R 11 in the general formula (III). Synonymous.
- R 50 to R 56 have the same meanings as R 4 to R 8 in the general formula (III), and preferred examples thereof are the same as R 4 to R 8 . More preferred is an aryloyl group.
- R 55 is preferably an aryloyl group because of its large absorption in the ultraviolet region and high sensitivity.
- R 57 has the same meaning as R 10 or R 11 in the general formula (III). Among these, preferred are the same as R 10 or R 11 , but more preferably an alkyl group.
- R 1 is a benzene ring represented by the following general formula (V), in which the p-position of the bonding position of the carbonyl group is substituted with a sulfur atom, and may further have another substituent. It is also preferable.
- R 4, R 5, R 7 and R 8 have the same meanings as R 4, R 5, R 7 and R 8 in the general formula (III).
- R 9 is A hydrogen atom, an optionally substituted alkyl group having 1 to 12 carbon atoms, an alkanoyl group having 2 to 8 carbon atoms, an alkenyl group having 3 to 12 carbon atoms, an aryl group having 6 to 20 carbon atoms, or Represents a trialkylsilyl group having 3 to 15 carbon atoms.
- R 4, R 5, R 7 and R 8 has the same meaning as R 4, R 5, R 7 and R 8 in the general formula (III), the preferred among these Is the same, particularly preferably a hydrogen atom.
- R 9 are also the same as those described as R 9 in the general formula (III), but may be an alkyl group or an aryl group particularly from the viewpoint of the stability of the raw material. preferable.
- R 2 is specifically the following groups each optionally having a substituent.
- Alkylthio groups having 1 to 12 carbon atoms such as methylthio group, ethylthio group, n-propylthio group, isopropylthio group, n-butylthio group, n-hexylthio group, n-octylthio group, n-dodecylthio group; Methoxycarbonyl group, ethoxycarbonyl group, n-propoxycarbonyl group, isopropoxycarbonyl group, n-butoxycarbonyl group, t-butoxycarbonyl group, n-pentyloxycarbonyl group, t-amyloxycarbonyl group, n-hexyloxycarbonyl An alkoxycarbonyl group having 2 to 12 carbon atoms such as a group, n-octyloxycarbonyl group, n-
- R 2 is a group containing a hetero atom such as an oxygen atom, a nitrogen atom, or a sulfur atom.
- R 2 is a group containing a hetero atom such as an oxygen atom, a nitrogen atom, or a sulfur atom.
- An image (pattern) formed from a photopolymerizable composition having excellent adhesion and internal curability is, for example, easily formed into a forward taper (trapezoidal) shape, hardly eroded by a developer, etc. Excellent properties such as difficulty. Therefore, if a photopolymerizable composition containing the ketoxime ester compound of the present invention as a photopolymerization initiator is used, a fine image can be stably formed.
- R 2 is preferably an alkylthio group, an alkoxycarbonyl group, an aryloxycarbonyl group, a heteroaryloxycarbonyl group, a heteroarylthiocarbonyl group or an alkylthioalkoxy group, particularly preferably an alkylthio group or an alkoxycarbonyl group.
- the carbon number of each of the above groups is as follows: the alkylthio group has 1 to 2 carbon atoms, the alkoxycarbonyl group has 2 to 4 carbon atoms, the aryloxycarbonyl group has 7 to 9 carbon atoms, and the heteroaryloxycarbonyl group has carbon atoms.
- the heteroarylthiocarbonyl group preferably has 3 to 7 carbon atoms
- the alkylthioalkoxy group preferably has 2 to 4 carbon atoms. Since each of these groups has a strong interaction (hydrogen bonding force) with a resin or the like in the composition, the effect of the compound of the present invention such as the above-described adhesion and internal curability is particularly strong. Since it is obtained, it is preferable.
- R 1 is a group represented by the general formula (IV) or a group represented by the general formula (V), it is easy to handle due to the crystallinity of an intermediate during the production process.
- R 2 is preferably an alkoxycarbonyl group having 1 to 4 carbon atoms.
- X is an optionally substituted alkylene group having 1 to 20 carbon atoms
- R 2 is an alkoxycarbonyl group having 2 to 12 carbon atoms or an alkylthio group having 1 to 12 carbon atoms. It is preferable that The preferable range of carbon number of each group is as described above.
- R 3 each may have a substituent, an alkanoyl group having 2 to 12 carbon atoms, an alkenoyl group having 3 to 25 carbon atoms, a cycloalkanoyl group having 4 to 8 carbon atoms, An aryloyl group having 7 to 20 carbon atoms, a heteroaryloyl group having 3 to 20 carbon atoms, an alkoxycarbonyl group having 2 to 10 carbon atoms, an aryloxycarbonyl group having 7 to 20 carbon atoms, and a heteroaryl group having 2 to 20 carbon atoms Or an alkylaminocarbonyl group having 2 to 20 carbon atoms.
- Examples of the alkanoyl group having 2 to 12 carbon atoms of R 3 include an acetyl group, a propanoyl group, and a butanoyl group, and an acetyl group is preferable.
- the carbon number is preferably 2 to 10, more preferably 2 to 7.
- Examples of the alkenoyl group having 3 to 25 carbon atoms of R 3 include a crotonoyl group and an acryloyl group, and a crotonoyl group is preferable.
- the carbon number is preferably 3 to 12, more preferably 3 to 7.
- Examples of the cycloalkanoyl group having 4 to 8 carbon atoms of R 3 include a cyclohexylcarbonyl group, a methylcyclohexylcarbonyl group, and a cyclopentylcarbonyl group, and a cyclohexylcarbonyl group is preferable.
- the carbon number is preferably 4-7.
- Examples of the aryloyl group having 7 to 20 carbon atoms of R 3 include a benzoyl group, a methylbenzoyl group, and a naphthoyl group, and a benzoyl group is preferable.
- the carbon number is preferably 7 to 12, more preferably 7 to 10.
- Examples of the alkoxycarbonyl group having 2 to 10 carbon atoms of R 3 include a methoxycarbonyl group, an ethoxycarbonyl group, and a propoxycarbonyl group, and a methoxycarbonyl group is preferable.
- the number of carbon atoms is preferably 2-8.
- Examples of the aryloxycarbonyl group having 7 to 20 carbon atoms of R 3 include a phenoxycarbonyl group, a p-methylphenoxycarbonyl group, and a naphthoxycarbonyl group, and a phenoxycarbonyl group is preferable.
- the carbon number is preferably 7 to 15, more preferably 7 to 10.
- heteroaryl group having 2 to 20 carbon atoms of R 3 examples include a thienyl group, a pyrrolyl group, a pyridyl group, and the like, and a thienyl group is preferable.
- the carbon number is preferably 2 to 12, more preferably 2 to 7.
- heteroaryloyl group having 3 to 20 carbon atoms of R 3 examples include a thiophenecarbonyl group, a pyrrolylcarbonyl group, a pyridinecarbonyl group, and the like, and preferably a thiophenecarbonyl group.
- the carbon number is preferably 5 to 15, more preferably 7 to 10.
- Examples of the alkylaminocarbonyl group having 2 to 20 carbon atoms of R 3 include a morpholinocarbonyl group, a dimethylaminocarbonyl group, and a methylaminocarbonyl group, and a dimethylaminocarbonyl group is preferable.
- the carbon number is preferably 2 to 12, more preferably 2 to 10.
- R 3 is preferably an alkanoyl group, a cycloalkanoyl group , or an aryloyl group, and more preferably an alkanoyl group or an aryloyl group.
- ⁇ Substituent group Z examples thereof include halogen atoms such as fluorine atom, chlorine atom, bromine atom and iodine atom, hydroxyl group, nitro group, cyano group, and any organic group.
- halogen atoms such as fluorine atom, chlorine atom, bromine atom and iodine atom, hydroxyl group, nitro group, cyano group, and any organic group.
- R 12 to R 23 each represents a hydrogen atom, an alkyl group, an alkanoyl group, an alkylcarbonyloxy group, an alkenyl group, an aryl group or an aralkyl group.
- the positional relationship of each substituent selected from the above substituent group Z is not particularly limited, and when it has a plurality of substituents, it may be the same or different.
- each substituent selected from the substituent group Z a plurality of substituents may be bonded to each other to form a ring, and the formed ring is a saturated or unsaturated aromatic hydrocarbon ring or aromatic It may be a heterocyclic ring, and may each further have a substituent on the ring, and the substituent may further form a ring.
- ketoxime ester compounds of the present invention are shown in Tables 1 to 7 as combinations of R 1 , R 2 , R 3 and X in the following general formula (I) as follows.
- the ketoxime ester compound is not limited to the following. In the following table, Me represents a methyl group, Et represents an ethyl group, Pr represents a propyl group, and Bu represents a butyl group.
- ketoxime ester compound of the present invention ⁇ Method for producing ketoxime ester compound of the present invention> The specific method for producing the ketoxime ester compound of the present invention will be described in detail in the examples described later.
- an aromatic ring compound or heteroaromatic ring compound that can constitute R 1 in the general formula (I) Into the alkanoyl group having X and R 2 in the general formula (I) is introduced by Friedel-Crafts reaction or the like. A ketoxime group is formed on the obtained compound by the method described in Organic Reaction (1953), 7, 327, etc., and this is further subjected to an esterification reaction with a compound capable of constituting R 3 in the general formula (I). It can synthesize
- the ketoxime ester compound of the present invention can be suitably used as a photopolymerization initiator. Details thereof will be described later.
- the photopolymerization initiator of the present invention comprises the ketoxime ester compound of the present invention.
- the photopolymerization initiator of the present invention is usually used as one component of a photopolymerizable composition described later, and has a function of polymerizing an ethylenically unsaturated group of an ethylenically unsaturated group-containing compound.
- photopolymerizable composition Next, the photopolymerizable composition of the present invention (hereinafter sometimes referred to as “resist”) will be described.
- the photopolymerizable composition of the present invention is a photopolymerizable composition containing (A) an ethylenically unsaturated group-containing compound and (B) a photopolymerization initiator, wherein (B) the photopolymerization initiator is the above-mentioned photopolymerization composition. It contains the ketoxime ester compound of the invention.
- (C) an alkali-soluble resin, (D) a surfactant, (E) a solvent, (F) a coloring material, (G) other components, and the like can be appropriately combined.
- each of these compounding components will be described.
- composition ingredients > (A) Ethylenically unsaturated group-containing compound
- a compound having one or more ethylenically unsaturated groups is used as the ethylenically unsaturated group-containing compound used in the composition of the present invention.
- ester of aliphatic (poly) hydroxy compound and unsaturated carboxylic acid ester of aromatic (poly) hydroxy compound and unsaturated carboxylic acid, unsaturated carboxylic acid, polyvalent carboxylic acid and aliphatic poly Esters obtained from hydroxy compounds, ethylene oxide of aromatic polyhydroxy compounds, esterification reaction products of propylene oxide adducts and unsaturated carboxylic acids, ethylene oxides of aliphatic polyhydroxy compounds, caprolactone-modified polyhydric alcohols and unsaturated carboxylic acids Esters, polyhydric alcohols, polyisocyanates and unsaturated carboxylic acids, styryl-terminated compounds, phosphoric acid unsaturated compounds, polyepoxy and unsaturated carboxylic acid adducts, and the like.
- ester of an aliphatic polyhydroxy compound and an unsaturated carboxylic acid include ethylene glycol diacrylate, triethylene glycol diacrylate, neopentyl glycol diacrylate, hexanediol diacrylate, trimethylol propane tri Acrylate esters such as acrylate, trimethylolethane triacrylate, pentaerythritol diacrylate, pentaerythritol triacrylate, pentaerythritol tetraacrylate, dipentaerythritol tetraacrylate, dipentaerythritol pentaacrylate, dipentaerythritol hexaacrylate, glycerol acrylate, etc.
- esters of aromatic polyhydroxy compounds and unsaturated carboxylic acids include unsaturated carboxylic acids and aromatics such as hydroquinone, resorcin, pyrogallol, bisphenol F, bisphenol A, and bis-1,1- (4-hydroxyphenyl) fluorene.
- Group polyhydroxy compounds, or their reactants with ethylene oxide adducts include bisphenol A di (meth) acrylate, bisphenol A bis [oxyethylene (meth) acrylate], bisphenol A bis [glycidyl ether (meth) acrylate], and the like.
- esters obtained by reacting unsaturated carboxylic acids with polyvalent carboxylic acids and polyvalent hydroxy compounds include condensates of (meth) acrylic acid, phthalic acid and ethylene glycol, (meth) acrylic Examples include condensates of acid, maleic acid and diethylene glycol, condensates of (meth) acrylic acid, terephthalic acid and pentaerythritol, condensates of (meth) acrylic acid, adipic acid, butanediol and glycerin. These are not necessarily a single substance, but may be a mixture of compounds having a plurality of similar structures.
- ethylenically unsaturated group-containing compound used in the present invention examples include acrylamides such as ethylene bisacrylamide; allyl esters such as diallyl phthalate; vinyl group-containing compounds such as divinyl phthalate.
- ethylenically unsaturated group-containing compounds preferred are those having a (meth) acryloyl group, more preferably an acryloyl group.
- examples of such compounds include trimethylolpropane triacrylate, trimethylolethane triacrylate, pentaerythritol diacrylate, pentaerythritol triacrylate, pentaerythritol tetraacrylate, dipentaerythritol tetraacrylate, dipentaerythritol pentaacrylate, dipentaerythritol hexaacrylate, etc. Is mentioned.
- ethylenically unsaturated group-containing compounds may be used alone or in combination of two or more.
- compositions for a transparent protective film such as an interlayer insulating film
- it may contain an ester of an aromatic polyhydroxy compound and an unsaturated carboxylic acid in order to make the film after thermosetting have a sufficient hardness.
- an ester of an aliphatic polyhydroxy compound and an unsaturated carboxylic acid from the viewpoint of curability.
- the content of the (A) ethylenically unsaturated group-containing compound in the photopolymerizable composition of the present invention is usually 10% by mass or more, preferably 20% by mass or more, based on the total solid content. Usually, it is 70 mass% or less, Preferably it is 60 mass% or less. If the amount of the compound having an ethylenically unsaturated group is excessively small, the sensitivity and the development dissolution rate may be decreased, and if excessively large, the reproducibility of the cross-sectional shape of the image is decreased. It may be easy to invite film slippage.
- (B) Photopolymerization initiator The photopolymerizable composition of the present invention is characterized in that (B) the photopolymerization initiator contains the ketoxime ester compound of the present invention.
- the photopolymerization initiator (B) used in the photopolymerizable composition of the present invention only one kind of the ketoxime ester compound of the present invention represented by the general formula (I) may be used. Two or more kinds may be used in combination.
- ketoxime ester compound of the present invention may be used in combination with other components such as other photopolymerization initiators and sensitizing dyes. Further high sensitivity can be expected by using a suitable combination depending on the application.
- the other photopolymerization initiator used in the present invention is not particularly limited as long as it is a compound that polymerizes an ethylenically unsaturated group with actinic rays, and a known photopolymerization initiator can be used.
- Examples of other photopolymerization initiator compounds that can be used in combination with the ketoxime ester compound of the present invention include the following compounds.
- 2- (4-methoxyphenyl) -4,6-bis (trichloromethyl) -s-triazine 2- (4-methoxynaphthyl) -4,6-bis (trichloromethyl) -s-triazine
- 2- Halomethylated triazine derivatives such as (4-ethoxynaphthyl) -4,6-bis (trichloromethyl) -s-triazine, 2- (4-ethoxycarbonylnaphthyl) -4,6-bis (trichloromethyl) -s-triazine 2-trichloromethyl-5- (2′-benzofuryl) -1,3,4-oxadiazole, 2-trichloromethyl-5- [ ⁇ - (2′-benzofuryl) vinyl] -1,3,4- Oxadiazole, 2-trichlor
- Benzophenone derivatives 2,2-dimethoxy-2-phenylacetophenone, 2,2-diethoxyacetophenone, 1-hydroxycyclohexyl phenyl ketone, ⁇ -hydroxy-2-methylphenylpropanone, 1-hydroxy-1-methylethyl- ( p-isopropylphenyl) ketone, 1-hydroxy-1- (p-dodecylphenyl) ketone, 2-methyl- (4 ′-(methylthio) phenyl) -2-morpholino-1- Acetophenone derivatives such as ropanone and 1,1,1-trichloromethyl- (p-butylphenyl) ketone, thioxanthone, 2-ethylthioxanthone, 2-isopropylthioxanthone, 2-chlorothioxanthone, 2,4-dimethylthioxanthone, 2,4 Thioxanthone derivatives such as diethylthioxanthone and 2,4
- the content of the initiator of the present invention in the photopolymerizable composition of the present invention is preferably 0.1 parts by mass or more and usually 50 parts by mass or less with respect to 100 parts by mass of the total solid content. Preferably it is 30 mass parts or less. If the amount of the photopolymerization initiator is excessively small, sensitivity may not be obtained, and if it is excessively large, the resolution tends to be lowered.
- the content of the agent is usually 0.1 parts by mass or more, preferably 0.3 parts by mass or more, and usually 30 parts by mass or less, preferably 20 parts by mass or less with respect to 100 parts by mass of the total solid content.
- the total content of the photopolymerization initiator is usually 0.2 parts by mass or more, preferably 100 parts by mass of the total solid content. Is 0.5 parts by mass or more, usually 40 parts by mass or less, preferably 30 parts by mass or less. If the amount of the photopolymerization initiator is too small, the effect of the present invention of high sensitivity tends to be small, and if it is too large, background staining (deterioration of development solubility) tends to occur.
- a sensitizing dye can also be added to the photopolymerizable composition of the present invention.
- a sensitizing dye in order to cause a photopolymerization reaction in a highly light-shielding resin composition such as a BM composition, it is preferable to add a sensitizing dye.
- Examples of such a sensitizing dye include coumarin compounds having a heterocyclic ring described in JP-A-3-239703 and JP-A-5-289335, and 3-ketocoumarin described in JP-A-63-221110.
- Sensitizing dyes, diaminobenzene compounds described in JP-A-11-326624, and the likeOf these sensitizing dyes, amino group-containing sensitizing dyes and xanthene dyes are particularly prefer
- the content of the sensitizing dye in the photopolymerizable composition of the present invention is preferably 0.5% by mass or more and usually 30% by mass with respect to the total solid content. Hereinafter, it is preferably 20% by mass or less.
- the blending ratio of the sensitizing dye to the photopolymerization initiator (B) is usually 300 parts by mass or less, preferably 200 parts by mass or less, preferably 10 parts by mass or more with respect to 100 parts by mass of the component (B). is there.
- the photopolymerizable composition of the present invention may contain an alkali-soluble resin.
- the alkali-soluble resin used in the photopolymerizable composition of the present invention is not particularly limited as long as it is a resin that is soluble in an alkaline solvent, but is preferably a resin containing a carboxyl group or a hydroxyl group.
- epoxy resin (a) As such an alkali-soluble resin, ⁇ , ⁇ -unsaturated monocarboxylic acid and / or ⁇ , ⁇ -unsaturated monocarboxylic acid ester (b) having a carboxyl group in the ester moiety is added to epoxy resin (a).
- a carboxyl group-containing epoxy acrylate resin synthesized by reacting the polybasic acid anhydride (c); unsaturated carboxylic acid such as (meth) acrylic acid and maleic acid, or (meth) acrylic acid ester Hydroxyl group- or carboxyl group-containing vinyl resin obtained by polymerizing a compound having a hydroxyl group or carboxyl group bonded thereto and another vinyl compound; and polyamide, polyester, polyether, polyurethane, polyvinyl butyral, polyvinyl alcohol, polyvinyl Pyrrolidone, acetylcellulose, etc. It is. These may be used alone or in combination of two or more.
- carboxyl group-containing epoxy acrylate resins and carboxyl group-containing vinyl resins are preferred from the viewpoints of alkali developability and image formability.
- a carboxyl group-containing vinyl resin that does not contain an unsaturated group is preferably used among carboxyl group-containing vinyl resins from the viewpoint of peelability after exposure and development.
- a carboxyl group-containing vinyl resin containing an unsaturated group is preferable.
- a carboxyl group-containing epoxy acrylate resin is preferably used for BM use.
- epoxy acrylate resin is an ⁇ , ⁇ -unsaturated monocarboxylic acid having an ⁇ , ⁇ -unsaturated monocarboxylic acid and / or ester moiety in the epoxy resin (a). It is synthesized by adding a carboxylic acid ester (b) and further reacting with a polybasic acid anhydride (c). Such a reaction product has substantially no epoxy group in terms of chemical structure and is not limited to “acrylate”, but epoxy resin is a raw material, and “acrylate” is a representative example. It is named like this according to common usage.
- R 24 and R 25 each independently represents an alkyl group or a halogen atom.
- R 26 and R 27 each independently represents an alkylene group.
- m and n each independently represents an integer of 0 or more.
- a novolak type epoxy resin or an epoxy resin represented by the general formula (a-1) is preferable, and in particular, the unsaturated bond concentration is high from the viewpoint of the balance between alkali developer resistance and developability,
- a resin having a suitable carboxylic acid concentration and a solid core is preferable, and an epoxy resin represented by the general formula (a-1) is particularly preferable.
- the alkyl group represented by R 24 and R 25 is preferably an alkyl group having 1 to 10 carbon atoms, and the halogen atom includes Cl, Br, F, and the like.
- R 24 and R 25 are particularly preferably each independently an alkyl group having 1 to 5 carbon atoms.
- R 24 and R 25 The details of the mechanism of action of the alkyl groups and halogen atoms of R 24 and R 25 are not clear, but they affect the three-dimensional structure of the polymer molecule and control its solubility in the developer. It is guessed. Therefore, from the above viewpoint, p and q in the general formula (a-1) each independently represent an integer of 0 to 4, preferably 1 or 2.
- the bonding position of R 24 and R 25 to the benzene ring is not particularly limited,
- R 24 and R 25 may be the same group or different groups, but are preferably the same group from the viewpoint of production cost.
- R 26 and R 27 examples include an alkylene group having 1 to 10 carbon atoms, and it is particularly preferable that they are each independently an ethylene group or a propylene group.
- R 26 and R 27 may be the same group or different groups, but are preferably the same group from the viewpoint of production cost.
- M and n each independently represents an integer of 0 or more, but is usually about 0 to 6, preferably about 0 to 3.
- M and n each independently represents an integer of 0 or more, but is usually about 0 to 6, preferably about 0 to 3.
- the sensitivity may be lowered.
- the molecular weight of these epoxy resins (a) is usually in the range of 200 to 200,000, preferably 300 to 100,000, as the weight average molecular weight in terms of polystyrene by gel permeation chromatography (GPC) measurement. If the molecular weight is less than the above range, there are many problems in film formation, and conversely, resins exceeding the above range are prone to gelation during the addition reaction of ⁇ , ⁇ -unsaturated monocarboxylic acid and difficult to produce. There is a risk of becoming.
- GPC gel permeation chromatography
- Examples of the ⁇ , ⁇ -unsaturated monocarboxylic acid include itaconic acid, crotonic acid, cinnamic acid, acrylic acid, methacrylic acid and the like, preferably acrylic acid and methacrylic acid, and particularly acrylic acid is highly reactive. Therefore, it is preferable.
- Examples of the ⁇ , ⁇ -unsaturated monocarboxylic acid ester having a carboxyl group in the ester moiety include 2-succinoyloxyethyl acrylate, 2-malenoyloxyethyl acrylate, 2-phthaloyloxyethyl acrylate, Acrylic acid-2-hexahydrophthaloyloxyethyl, methacrylic acid-2-succinoyloxyethyl, methacrylic acid-2-malenoyloxyethyl, methacrylic acid-2-phthaloyloxyethyl, methacrylic acid-2-hexahydrophthalo Yloxyethyl, crotonic acid-2-succinoyloxyethyl, and the like.
- Preferred are 2-maleoyloxyethyl acrylate and 2-phthaloyloxyethyl acrylate, and in particular, 2-maleic acrylate. Noyloxyethyl is preferred.
- ⁇ , ⁇ -unsaturated monocarboxylic acid and / or its ester (b) and the epoxy resin (a) a known method can be used.
- the ⁇ , ⁇ -unsaturated monocarboxylic acid and / or its ester (b) and the epoxy resin (a) can be reacted at a temperature of 50 to 150 ° C. in the presence of an esterification catalyst.
- esterification catalyst used here tertiary amines such as triethylamine, trimethylamine, benzyldimethylamine, and benzyldiethylamine, quaternary ammonium salts such as tetramethylammonium chloride, tetraethylammonium chloride, dodecyltrimethylammonium chloride, and the like can be used. .
- the epoxy resin (a), the ⁇ , ⁇ -unsaturated monocarboxylic acid and / or the ⁇ , ⁇ -unsaturated monocarboxylic acid ester (b) having a carboxyl group in the ester moiety, and the esterification catalyst are all one kind. May be used alone, or two or more may be mixed and used.
- the amount of ⁇ , ⁇ -unsaturated monocarboxylic acid and / or its ester (b) used is preferably in the range of 0.5 to 1.2 equivalents, more preferably 1 equivalent of the epoxy group of the raw material epoxy resin (a). Is in the range of 0.7 to 1.1 equivalents. If the amount of ⁇ , ⁇ -unsaturated monocarboxylic acid and / or ester (b) used is small, the amount of unsaturated groups introduced is insufficient and the subsequent reaction with polybasic acid anhydride (c) becomes insufficient. . Also, it is not advantageous that a large amount of epoxy groups remain. On the other hand, if the amount used is large, ⁇ , ⁇ -unsaturated monocarboxylic acid and / or ester thereof remains as an unreacted product. In either case, there is a tendency for the curing properties to deteriorate.
- the polybasic acid anhydride (c) to be further added to the epoxy resin (a) to which the ⁇ , ⁇ -unsaturated carboxylic acid and / or its ester (b) is added includes maleic anhydride, succinic anhydride, itaconic anhydride.
- a known method can also be used for the addition reaction of polybasic acid anhydride (c), which is the same as the addition reaction of ⁇ , ⁇ -unsaturated carboxylic acid and / or its ester (b) to epoxy resin (a). Can be obtained by continuing the reaction under various conditions.
- the addition amount of the polybasic acid anhydride (c) is preferably such that the acid value of the resulting epoxy acrylate resin is in the range of 10 to 150 mg-KOH / g, more preferably 20 to 140 mg-KOH / g. Is particularly preferred. When the resin acid value is less than the above range, alkali developability is poor, and when it exceeds the above range, a tendency to be inferior in curing performance is recognized.
- the weight average molecular weight in terms of polystyrene measured by gel permeation chromatography (GPC) of an epoxy acrylate resin having a carboxyl group used as an alkali-soluble resin is usually 1,000 or more, preferably 1,500 or more. Usually, it is 30,000 or less, preferably 20,000 or less, more preferably 10,000 or less, and particularly preferably 8,000 or less. If the molecular weight is too large, the developability may be deteriorated. On the other hand, if the molecular weight is too small, the alkali resistance may be inferior.
- the carboxyl group-containing vinyl resin include a copolymer of an unsaturated carboxylic acid and a vinyl compound.
- the unsaturated carboxylic acid include (meth) acrylic acid, crotonic acid, isocrotonic acid, maleic acid, maleic anhydride, itaconic acid, citraconic acid and the like. These may be used alone or in combination of two or more.
- vinyl compounds include styrene, ⁇ -methylstyrene, hydroxystyrene, methyl (meth) acrylate, ethyl (meth) acrylate, propyl (meth) acrylate, butyl (meth) acrylate, pentyl (meth) acrylate, hexyl (meta ) Acrylate, dodecyl (meth) acrylate, 2-ethylhexyl (meth) acrylate, hydroxymethyl (meth) acrylate, hydroxyethyl (meth) acrylate, glycidyl (meth) acrylate, isobornyl (meth) acrylate, dicyclopentanyl (meth) Acrylate, benzyl (meth) acrylate, N, N-dimethylaminoethyl (meth) acrylate, N- (meth) acryloylmorpholine, (meth) acrylonitrile
- dicyclopentanyl (meth) acrylate is preferable in that it provides a wide latitude for development time and developer deterioration.
- dicyclopentanyl (meth) acrylate include compounds described in JP-A-2001-89533, such as dicyclopentadiene skeleton, dicyclopentanyl skeleton, dicyclopentenyl skeleton, dicyclopentenyloxy.
- examples include (meth) acrylate having an alkyl skeleton.
- a styrene- (meth) acrylate- (meth) acrylic acid copolymer is preferable from the viewpoint of image shape, sensitivity, and cured film strength, and styrene 3 to More preferably, the copolymer comprises 60 mol%, (meth) acrylate 10 to 70 mol%, (meth) acrylic acid 10 to 60 mol%, styrene 5 to 50 mol%, (meth) acrylate 20 to 60 mol%, A copolymer comprising 15 to 55 mol% of (meth) acrylic acid is particularly preferred.
- the acid value of these carboxyl group-containing vinyl resins is usually 30 to 250 mg-KOH / g, preferably 50 to 200 mg-KOH / g, and more preferably 70 to 150 mg-KOH / g.
- the molecular weight of these carboxyl group-containing vinyl resins is usually 1,000 or more, preferably 1,500 or more, more preferably 2,000 or more, and usually 100, as the weight average molecular weight in terms of polystyrene by GPC measurement. 000 or less, preferably 50,000 or less, more preferably 30,000 or less, particularly preferably 20,000 or less.
- carboxyl group-containing vinyl resin in the above range it is preferable because the peelability after development is good.
- the carboxyl group-containing vinyl resin is preferably one having an ethylenically unsaturated bond in the side chain.
- a carboxyl group-containing polymer having an aliphatic epoxy group-containing unsaturated compounds such as monoalkyl monog
- Examples thereof include a reaction product obtained by copolymerization such that the ratio of the compound having a saturated group to the whole is 10 to 90 mol%, preferably about 30 to 80 mol%.
- the alkali-soluble resin when the photopolymerizable composition of the present invention is used for a pixel those described in JP-A-2008-304766 can be used in addition to those described above.
- the content of the alkali-soluble resin is usually 30% by mass or more, preferably 40% by mass or more, based on the total solid content. Yes, usually 70% by mass or less, preferably 60% by mass or less. If the amount of the alkali-soluble resin is excessively small, the reproducibility of the image cross-sectional shape may be deteriorated and the heat resistance may be decreased. If the amount is excessively large, the sensitivity may be decreased and the development dissolution rate may be decreased.
- the photopolymerizable composition of the present invention is nonionic, anionic, for the purpose of improving the coating property of the composition as a coating liquid and the developability of the photopolymerizable composition layer. It may contain a cationic or amphoteric surfactant, or a fluorine or silicone surfactant.
- nonionic surfactant examples include polyoxyethylene alkyl ethers, polyoxyethylene polyoxypropylene alkyl ethers, polyoxyethylene alkylphenyl ethers, polyoxyethylene alkyl esters, polyoxyethylene fatty acid esters, Glycerin fatty acid esters, polyoxyethylene glycerin fatty acid esters, pentaerythritol fatty acid esters, polyoxyethylene pentaerythritol fatty acid esters, sorbitan fatty acid esters, polyoxyethylene sorbitan fatty acid esters, sorbit fatty acid esters, polyoxy And ethylene sorbite fatty acid esters.
- examples of these commercially available products include polyoxyethylene surfactants such as “Emulgen 104P” and “Emulgen A60” manufactured by Kao Corporation.
- anionic surfactant examples include alkyl sulfonates, alkyl benzene sulfonates, alkyl naphthalene sulfonates, polyoxyethylene alkyl ether sulfonates, alkyl sulfates, alkyl sulfate esters, and higher alcohol sulfates.
- anionic surfactants such as “Emar 10” manufactured by Kao Co., Ltd. for alkyl sulfates, and “Perex NB-L” manufactured by Kao Co., Ltd. for alkyl naphthalene sulfonates.
- anionic surfactants such as “Emar 10” manufactured by Kao Co., Ltd. for alkyl sulfates, and “Perex NB-L” manufactured by Kao Co., Ltd. for alkyl naphthalene sulfonates.
- special polymer surfactants include “Homogenol L-18” and “Homogenol L-100” manufactured by Kao Corporation.
- the cationic surfactants include quaternary ammonium salts, imidazoline derivatives, amine salts, and the like
- the amphoteric surfactants include betaine-type compounds, imidazolium salts, imidazolines, amino acids, and the like. Is mentioned. Of these, quaternary ammonium salts are preferred, and stearyltrimethylammonium salts are more preferred. Examples of commercially available products include “Acetamine 24” manufactured by Kao Corporation for alkylamine salts, and “Cotamine 24P” and “Cotamin 86W” manufactured by Kao Corporation for quaternary ammonium salts.
- a compound having a fluoroalkyl or fluoroalkylene group in at least one of the terminal, main chain and side chain is suitable.
- 1,1,2,2-tetrafluorooctyl (1,1,2,2-tetrafluoropropyl) ether
- 1,1,2,2-tetrafluorooctyl hexyl ether 1,1,2,2-tetrafluoropropyl ether
- 1,1,2,2-tetrafluorooctyl hexyl ether 1,1,2,2-tetrafluorobutyl) ether
- hexaethylene glycol di (1,1,2,2,3,3-hexafluoropentyl) ether 1,1,2,2-tetrafluorobutyl
- octapropylene glycol di 1,1,2, 2-tetrafluorobutyl
- hexapropylene glycol di (1,1,2,2,3,3-hexafluoropentyl) ether sodium perfluorododecylsulfonate
- 1,1,2,2,8,8, Examples include 9,9,10,10-decafluorododecane and
- BM-1000 and “BM-1100” manufactured by BM Chemie, “Megafuck F142D”, “Megafuck F172”, “Megafuck F173”, and “Megafuck F183” manufactured by Dainippon Ink, Inc. ”,“ Megafuck F470 ”,“ Megafuck F475 ”,“ FC430 ”manufactured by Sumitomo 3M,“ DFX-18 ”manufactured by Neos, and the like.
- silicone-based surfactant examples include “Toray Silicone DC3PA”, “Short SH7PA”, “Same DC11PA”, “Short SH21PA”, “Short SH28PA”, “Short SH29PA”, “Short SH30PA” manufactured by Torre Silicone Co., Ltd. "SH8400”, “TSF-4440”, “TSF-4300”, “TSF-4445”, “TSF-444 (4) (5) (6) (7) 6", “TSF” manufactured by Toshiba Silicone Co., Ltd.
- Commercially available products such as “-4460”, “TSF-4442”, “KP341” manufactured by Silicone, “BYK323”, “BYK330” manufactured by BYK Chemie.
- a fluorine-based surfactant and a silicone-based surfactant are preferable from the viewpoint of coating film thickness uniformity.
- Two or more kinds of surfactants may be combined.
- Silicone surfactant / fluorine surfactant, silicone surfactant / special polymer surfactant, fluorine surfactant / special polymer surfactant Examples include combinations of agents. Of these, silicone surfactants / fluorine surfactants are preferred.
- silicone surfactant / fluorine surfactant combination for example, “TSF4460” manufactured by Toshiba Silicone, “DFX-18” manufactured by Neos, “BYK-300” or “BYK-330” manufactured by BYK Chemie “S-393” manufactured by Seimi Chemical Co., “KP340” manufactured by Shin-Etsu Silicone Co., Ltd. “F-478” or “F-475” manufactured by Dainippon Ink Co., Ltd. “SH7PA” manufactured by Toray Silicone Co., Ltd., “DS-401 manufactured by Daikin Co., Ltd. “L-77” manufactured by Nihon Unicar Co., Ltd., “FC4430” manufactured by Sumitomo 3M Co., Ltd., and the like.
- the content of the surfactant in the photopolymerizable composition is preferably 10% by mass or less based on the total solid content. More preferably, the content is 1 to 5% by mass.
- the photopolymerizable composition of the present invention is usually (A) an ethylenically unsaturated group-containing compound, (B) a photopolymerization initiator, and (C) an alkali-soluble resin that is blended as necessary. (D) A surfactant, (F) a coloring material and other optional components described below are used in a state where they are dissolved or dispersed in (E) a solvent.
- a solvent that can dissolve or disperse each component constituting the composition and has a boiling point in the range of 100 to 200 ° C. More preferably, it has a boiling point of 120 to 170 ° C.
- Examples of such a solvent include ethylene glycol monomethyl ether, ethylene glycol monoethyl ether, ethylene glycol monopropyl ether, ethylene glycol monobutyl ether, ethylene glycol monobutyl ether, propylene glycol monomethyl ether, propylene glycol-t-butyl ether, diethylene glycol monomethyl.
- Glycol mono such as ether, diethylene glycol monoethyl ether, methoxymethyl pentanol, propylene glycol monoethyl ether, dipropylene glycol monoethyl ether, dipropylene glycol monomethyl ether, 3-methyl-3-methoxybutanol, tripropylene glycol methyl ether Alkyl ethers; ethylene Glycol dialkyl ethers such as coal dimethyl ether, ethylene glycol diethyl ether, diethylene glycol dimethyl ether, diethylene glycol diethyl ether, diethylene glycol dipropyl ether, diethylene glycol dibutyl ether; ethylene glycol monomethyl ether acetate, ethylene glycol monoethyl ether acetate, propylene glycol monomethyl ether acetate, Glycols such as propylene glycol monoethyl ether acetate, propylene glycol monopropyl ether acetate, methoxybutyl
- Solvents corresponding to the above include mineral spirits, Valsol # 2, Apco # 18 solvent, Apco thinner, Soal Solvent No. 1 and no. 2, commercially available products with trade names such as Solvesso # 150, Shell TS28 Solvent, Carbitol, Ethyl Carbitol, Butyl Carbitol, Methyl Cellosolve, Ethyl Cellosolve, Ethyl Cellosolve Acetate, Diglyme.
- propylene glycol monomethyl ether propylene glycol monoethyl ether, propylene glycol monomethyl ether acetate, propylene glycol monoethyl ether acetate, propylene glycol mono Propyl ether acetate, methoxybutyl acetate, 3-methyl-3-methoxybutyl acetate, methyl isopropyl ketone, methyl isoamyl ketone, diisobutyl ketone, methyl isobutyl ketone, cyclohexanone, butyl acetate, propyl acetate, amyl acetate, ethylene glycol acetate, ethyl pro Pionate, propylpropionate, butyl butyrate, isobutyl butyrate, methyl isobutyrate, ethyl caprylate, buty Stearate, ethy
- the coloring material is not an essential component in the photopolymerizable composition of the present invention, but is used in combination in many applications such as pixels and BM.
- the colorant refers to a component that colors the photopolymerizable composition.
- dyed pigments can be used, but pigments are preferred from the viewpoint of heat resistance and light resistance.
- various color pigments such as a blue pigment, a green pigment, a red pigment, a yellow pigment, a purple pigment, an orange pigment, a brown pigment, and a black pigment can be used.
- organic pigments such as azo, phthalocyanine, quinacridone, benzimidazolone, isoindolinone, dioxazine, indanthrene, and perylene
- various inorganic pigments can be used. It is.
- black pigment a single black pigment or a black pigment obtained by mixing red, green, blue and the like can be used.
- These black pigments can be appropriately selected from inorganic or organic pigments and dyes, and can be used alone or in combination.
- Examples of the single black pigment include carbon black, acetylene black, lamp black, bone black, graphite, iron black, aniline black, cyanine black, and titanium black.
- carbon black and titanium black are particularly preferable from the viewpoints of light shielding rate and image characteristics.
- Carbon black may be used in combination with other black or colored inorganic or organic pigments.
- Other pigments naturally have a light shielding property or image characteristic lower than that of carbon black, so the mixing ratio is naturally limited.
- Titanium black can be produced by heating a mixture of titanium dioxide and titanium metal in a reducing atmosphere for reduction (Japanese Patent Laid-Open No. 49-5432), or ultrafine dioxide obtained by high-temperature hydrolysis of titanium tetrachloride.
- a method of reducing titanium in a reducing atmosphere containing hydrogen Japanese Patent Laid-Open No. 57-205322
- a method of reducing titanium dioxide or titanium hydroxide at high temperature in the presence of ammonia Japanese Patent Laid-Open No. 60-65069, Japanese Patent Laid-Open No. Sho 61-201610
- a method of attaching a vanadium compound to titanium dioxide or titanium hydroxide and reducing it at a high temperature in the presence of ammonia JP-A 61-201610), etc. is not.
- the photopolymerizable composition of the present invention can be used for various applications, but its high sensitivity to irradiation light and excellent image forming properties were used for forming a black matrix for a color filter. It is particularly effective when.
- (F) Use the black pigments such as carbon black and titanium black described above as the color material, or mix multiple types of pigments other than black and adjust the color to black. That's fine.
- the photopolymerizable composition of the present invention is also effective when used for the formation of a pixel for a color filter because it has high electrical properties, high adhesion to the substrate, and little occurrence of overhang.
- a pigment suitable for the color of a desired pixel may be appropriately selected, combined, adjusted, and used.
- composition of the present invention contains a pigment or the like as the color material (F), the color material is finely dispersed and the dispersion state is stabilized. Is important for quality stability, it is desirable to add a pigment dispersant.
- the pigment dispersant has affinity for both (F) a colorant such as a pigment and (C) an alkali-soluble resin, and examples thereof include surfactants such as nonions, cations and anions, and polymer dispersants. .
- polymer dispersants are preferable, and polymer dispersants having basic functional groups such as primary, secondary, or tertiary amino groups, and nitrogen-containing heterocycles such as pyridine, pyrimidine, and pyrazine are particularly advantageously used. Is done.
- polymer dispersants having basic functional groups include, for example, polyisocyanate compounds, compounds having one or two hydroxyl groups in the molecule, and active hydrogen in the same molecule.
- examples thereof include resins obtained by reacting a compound having a tertiary amino group. This resin is particularly preferred when a black pigment such as titanium black or carbon black is used as the color material (F), and most preferred when carbon black is used.
- polyisocyanate compounds examples include paraphenylene diisocyanate, 2,4-tolylene diisocyanate, 2,6-tolylene diisocyanate, 4,4′-diphenylmethane diisocyanate, naphthalene-1,5-diisocyanate, and tolidine diisocyanate.
- the polyisocyanate may be converted into an isocyanate group using an appropriate trimerization catalyst such as tertiary amines, phosphines, alkoxides, metal oxides, carboxylates and the like. And the trimerization is stopped by adding a catalyst poison, and then the unreacted polyisocyanate is removed by solvent extraction and thin-film distillation to obtain the desired isocyanurate group-containing polyisocyanate.
- an appropriate trimerization catalyst such as tertiary amines, phosphines, alkoxides, metal oxides, carboxylates and the like.
- Examples of compounds having one or two hydroxyl groups in the same molecule include polyether glycol, polyester glycol, polycarbonate glycol, polyolefin glycol, etc., and one terminal hydroxyl group of these compounds is alkoxylated with an alkyl group having 1 to 25 carbon atoms. And the like. Moreover, these 2 or more types of mixtures are also mentioned.
- Polyether glycols include polyether diols, polyether ester diols, and mixtures of two or more of these.
- polyether diols are those obtained by homopolymerizing or copolymerizing alkylene oxides, such as polyethylene glycol, polypropylene glycol, polyethylene-propylene glycol, polyoxytetramethylene glycol, polyoxyhexamethylene glycol, polyoxyoctamethylene glycol, and the like. The mixture of 2 or more types of those is mentioned.
- Polyether ester diols include those obtained by reacting a mixture of ether group-containing diols or other glycols with dicarboxylic acids or their anhydrides or reacting polyester glycols with alkylene oxides, such as poly (poly And oxytetramethylene) adipate.
- the most preferable polyether glycol is polyethylene glycol, polypropylene glycol, polyoxytetramethylene glycol or a compound in which one terminal hydroxyl group of these compounds is alkoxylated with an alkyl group having 1 to 25 carbon atoms.
- Polyester glycol includes dicarboxylic acid (succinic acid, glutaric acid, adipic acid, sebacic acid, fumaric acid, maleic acid, phthalic acid, etc.) or anhydrides thereof and glycol (ethylene glycol, diethylene glycol, triethylene glycol, propylene glycol, Dipropylene glycol, tripropylene glycol, 1,2-butanediol, 1,3-butanediol, 1,4-butanediol, 2,3-butanediol, 3-methyl-1,5-pentanediol, neopentyl glycol 2-methyl-1,3-propanediol, 2-methyl-2-propyl-1,3-propanediol, 2-butyl-2-ethyl-1,3-propanediol, 1,5-pentanediol, , 6-hexanediol, 2-methyl-2,4 Pentanediol, 2,2,
- Polycarbonate glycols include poly (1,6-hexylene) carbonate and poly (3-methyl-1,5-pentylene) carbonate.
- Polyolefin glycols include polybutadiene glycol, hydrogenated polybutadiene glycol, and hydrogenated poly. Examples include isoprene glycol.
- the number average molecular weight of a compound having one or two hydroxyl groups in the same molecule is 300 to 10,000, preferably 500 to 6,000, more preferably 1,000 to 4,000.
- the compound having an active hydrogen and a tertiary amino group in the same molecule used in the present invention will be described.
- the active hydrogen that is, a hydrogen atom directly bonded to an oxygen atom, a nitrogen atom or a sulfur atom
- a hydrogen atom in a functional group such as a hydroxyl group, an amino group, and a thiol group.
- a hydrogen atom of an amino group is preferred.
- the tertiary amino group is not particularly limited, and examples thereof include an amino group having an alkyl group having 1 to 4 carbon atoms, or a heterocyclic structure, more specifically, an imidazole ring or a triazole ring.
- Examples of such compounds having an active hydrogen and a tertiary amino group in the same molecule include N, N-dimethyl-1,3-propanediamine, N, N-diethyl-1,3-propanediamine, N, N-dipropyl-1,3-propanediamine, N, N-dibutyl-1,3-propanediamine, N, N-dimethylethylenediamine, N, N-diethylethylenediamine, N, N-dipropylethylenediamine, N, N-dibutylethylenediamine, N, N-dimethyl-1,4-butanediamine, N, N-diethyl-1,4-butanediamine, N, N-dipropyl-1,4-butanediamine, N, N-dibutyl- Examples include 1,4-butanediamine.
- the tertiary amino group is a nitrogen-containing heterocycle, such as pyrazole ring, imidazole ring, triazole ring, tetrazole ring, indole ring, carbazole ring, indazole ring, benzimidazole ring, benzotriazole ring, benzoxazole ring, benzo
- nitrogen-containing hetero 5-membered rings such as thiazole ring and benzothiadiazole ring
- nitrogen-containing hetero 6-membered rings such as pyridine ring, pyridazine ring, pyrimidine ring, triazine ring, quinoline ring, acridine ring and isoquinoline ring.
- Preferred as these nitrogen-containing heterocycles are an imidazole ring or a triazole ring.
- these compounds having an imidazole ring and an amino group include 1- (3-aminopropyl) imidazole, histidine, 2-aminoimidazole, 1- (2-aminoethyl) imidazole and the like.
- specific examples of the compound having a triazole ring and an amino group include 3-amino-1,2,4-triazole, 5- (2-amino-5-chlorophenyl) -3-phenyl-1H-1 , 2,4-triazole, 4-amino-4H-1,2,4-triazole-3,5-diol, 3-amino-5-phenyl-1H-1,3,4-triazole, 5-amino-1 , 4-diphenyl-1,2,3-triazole, 3-amino-1-benzyl-1H-2,4-triazole and the like.
- N, N-dimethyl-1,3-propanediamine, N, N-diethyl-1,3-propanediamine, 1- (3-aminopropyl) imidazole, 3-amino-1,2,4-triazole is preferred.
- a preferable blending ratio of the dispersant raw material is 10 to 200 parts by mass, preferably 20 to 200 parts by mass of a compound having a number average molecular weight of 300 to 10,000 having one or two hydroxyl groups in the same molecule with respect to 100 parts by mass of the polyisocyanate compound.
- 190 parts by mass, more preferably 30 to 180 parts by mass, and the compound having an active hydrogen and a tertiary amino group in the same molecule is 0.2 to 25 parts by mass, preferably 0.3 to 24 parts by mass.
- the weight average molecular weight in terms of polystyrene measured by gel permeation chromatography (GPC) of the polymer dispersant having a basic functional group is usually 1,000 to 200,000, preferably 2,000 to 100,000. More preferably, it is in the range of 3,000 to 50,000.
- GPC gel permeation chromatography
- the polymer dispersant is produced according to a known method for producing a polyurethane resin.
- ketones such as acetone, methyl ethyl ketone, methyl isobutyl ketone, cyclopentanone, cyclohexanone, isophorone, ethyl acetate, butyl acetate, cellosolve acetate, etc.
- Esters hydrocarbons such as benzene, toluene, xylene, hexane, diacetone alcohol, isopropanol, sec-butanol, tert-butanol and some other alcohols, chlorides such as methylene chloride and chloroform, tetrahydrofuran, diethyl ether And aprotic polar solvents such as dimethylformamide, N-methylpyrrolidone, and dimethyl sulfoxide.
- hydrocarbons such as benzene, toluene, xylene, hexane, diacetone alcohol, isopropanol, sec-butanol, tert-butanol and some other alcohols
- chlorides such as methylene chloride and chloroform, tetrahydrofuran, diethyl ether
- aprotic polar solvents such as dimethylformamide, N-methylpyrrolidone, and dimethyl sulfoxide.
- a urethanization reaction catalyst is usually used.
- the urethanization reaction catalyst include tin-based compounds such as dibutyltin dilaurate, dioctyltin dilaurate, dibutyltin dioctoate, stannous octoate, iron-based compounds such as iron acetylacetonate and ferric chloride, triethylamine, and triethylenediamine. And tertiary amines.
- the amount of the compound having an active hydrogen and a tertiary amino group in the same molecule is preferably controlled in the range of 1 to 100 mg-KOH / g in terms of amine value after reaction (in terms of effective solid content). More preferably, it is in the range of 5 to 95 mg-KOH / g.
- the amine value is a value obtained by neutralizing and titrating a basic amino group with an acid, and representing the acid value in mg of KOH. When the amine value is less than the above range, the dispersing ability tends to decrease, and when it exceeds the above range, the developability tends to decrease.
- thermosetting a thermal crosslinking agent for the purpose of improving the heat resistance and chemical resistance of the film after thermosetting. Also good. Any known thermal crosslinking agent can be used as long as it undergoes a crosslinking reaction by hard baking after image formation by exposure and development. Specific examples include the following, and these may be used alone or in combination of two or more.
- (G-2-1) Compound having epoxy group in molecule
- a monohydroxy compound or polyhydroxy compound and epichlorohydrin are reacted.
- compounds ranging from low molecules to macromolecules for example, a monohydroxy compound or polyhydroxy compound and epichlorohydrin.
- polyglycidyl ether compound examples include diglycidyl ether type epoxy of polyethylene glycol, diglycidyl ether type epoxy of bis (4-hydroxyphenyl), bis (3,5 Diglycidyl ether type epoxy of -dimethyl-4-hydroxyphenyl), diglycidyl ether type epoxy of bisphenol F, diglycidyl ether type epoxy of bisphenol A, diglycidyl ether type epoxy of tetramethylbisphenol A, diglycidyl ether type epoxy of ethylene oxide Glycidyl ether type epoxy, dihydroxyoxyfluorene type epoxy, dihydroxyalkyleneoxylfluorene type epoxy, bisphenol A / aldehyde novolak type epoxy Poxy, phenol novolac type epoxy, and cresol novolac type epoxy are exemplified.
- the polyglycidyl ether compound includes polyglycidyl ether resin.
- Polyglycidyl ether resins include bisphenol S epoxy resin, phenol novolac epoxy resin, cresol novolac epoxy resin, trisphenol epoxy resin, phenol and dicyclopentadiene polymerized epoxy resin, phenol and naphthalene polymerized epoxy resin, etc.
- a type epoxy resin is mentioned.
- These (poly) glycidyl ether compounds may be those obtained by reacting a remaining hydroxyl group with an acid anhydride, a divalent acid compound, or the like to introduce a carboxyl group.
- polyglycidyl ester compound examples include diglycidyl ester type epoxy of hexahydrophthalic acid, diglycidyl ester type epoxy of phthalic acid, and the like.
- polyglycidylamine compound examples include diglycidylamine type epoxy of bis (4-aminophenyl) methane and triglycidylamine type epoxy of isocyanuric acid, respectively. It is done.
- (G-2-1-4) Others include glycidyl (meth) acrylate, glycidyl ⁇ -ethyl acrylate, glycidyl ⁇ -n-propyl acrylate, glycidyl ⁇ -n-butyl acrylate. , (Meth) acrylic acid-3,4-epoxybutyl, (meth) acrylic acid-4,5-epoxypentyl, (meth) acrylic acid-6,7-epoxyheptyl, ⁇ -ethylacrylic acid-6,7- Examples thereof include polymers obtained by reacting (meth) acrylate having an epoxy group such as epoxyheptyl alone or in combination of two or more. Alternatively, there may be mentioned polymers in which (meth) acrylate structural units having an epoxy group contain other copolymerization monomers in an amount of usually 10 to 70 mol%, preferably 15 to 60 mol%.
- Examples of the monomer for copolymerization include (meth) acrylic acid, methyl (meth) acrylate, ethyl (meth) acrylate, butyl (meth) acrylate, 2-ethylhexyl (meth) acrylate, (meth ) Esters of (meth) acrylic acid such as phenyl acrylate, cyclohexyl (meth) acrylate, dicyclopentanyl (meth) acrylate, dicyclopentanyloxyethyl (meth) acrylate, isobornyl (meth) acrylate, And vinyl aromatic compounds such as styrene, ⁇ -methylstyrene, p-methylstyrene, and vinylnaphthalene.
- Preferred examples of the (meth) acrylate having an epoxy group include glycidyl (meth) acrylate.
- Preferred examples of the monomer for copolymerization include dicyclopentanyl (meth) acrylate and ⁇ -styrene.
- the preferred molecular weight is not particularly limited as long as the photopolymerizable composition of the present invention can be uniformly applied in a solution state. First, it is appropriately selected according to the thickness of the coating film to be formed, coating conditions, purpose, and the like.
- the molecular weight is usually preferably in the range of 2,000 to 300,000, preferably 3,000 to 100,000, more preferably 4,000 to 50,000.
- the epoxy group used in the epoxy compound or epoxy resin used in the photopolymerizable composition of the present invention is usually a 1,2-epoxy group, but it can improve stability over time or provide flexibility.
- 1,3-epoxy group (oxetane), 4,3-epoxycyclohexyl group may be used.
- an epoxy compound which concerns on this Embodiment it is what does not contain an aromatic ring, or it is unsubstituted or contains the phenyl group which has a substituent in p (para) position by heat processing of a protective film. This is preferable because discoloration (red coloring) can be suppressed.
- examples of such an epoxy compound include a bisphenol A type epoxy compound and an epoxy resin, an epoxy compound and an epoxy resin having a fluorene skeleton which may have a substituent, and a copolymer of glycidyl (meth) acrylate. be able to.
- the photopolymerizable composition of the present invention contains (G-2) a compound having an epoxy group in the molecule as a thermal cross-linking agent
- the photopolymerizable composition contains a compound having an epoxy group in the molecule.
- the amount is usually 60% by mass or less, preferably 50% by mass or less, more preferably 30% by mass or less, and usually 1% by mass or more, based on the total solid content.
- the content of the compound having an epoxy group in the molecule is excessively large, the storage stability of the photopolymerizable composition solution is lowered, and the peelability after exposure / development is easily lowered.
- Nitrogen-containing thermally crosslinkable compound examples include compounds in which formalin is allowed to act on melamine, benzoguanamine, glycoluril, or urea, or alkyl-modified compounds thereof. .
- Cymel (registered trademark) 300, 301, 303, 350, 736, 738, 370, 771 manufactured by Cytec Industries, 325, 327, 703, 701, 266, 267, 285, 232, 235, 238, 1141, 272, 254, 202, 1156, 1158, “Nikarak” (registered trademark) E-2151, Sanwa Chemical Co., MW -100LM, MX-750LM, etc.
- Cymel (registered trademarks) 1123, 1125, 1128, and the like can be given as examples of a compound obtained by allowing formalin to act on benzoguanamine or an alkyl modified product thereof.
- Examples of compounds obtained by allowing formalin to act on glycoluril or alkyl-modified products thereof include “Cymel” (registered trademark) 1170, 1171, 1174, 1172, “Nicarak” (registered trademark) MX-270, and the like. Can do.
- Examples of compounds in which formalin is reacted with urea or alkyl-modified products thereof include “UFR” (registered trademark) 65 and 300, “Nicarak” (registered trademark) MX-290 manufactured by Cytec Industries, and the like. be able to.
- (G-2) thermal crosslinking agent in the present invention a compound having —N (CH 2 OR) 2 group (wherein R represents an alkyl group or a hydrogen atom) in the molecule is preferable.
- a compound obtained by allowing formalin to act on urea or melamine or an alkyl-modified product thereof is particularly preferable.
- the photopolymerizable composition of the present invention contains (G-2) a nitrogen-containing thermally crosslinkable compound as a thermal crosslinking agent
- the content of the nitrogen-containing thermally crosslinkable compound in the composition is as follows: On the other hand, it is usually 40% by mass or less, preferably 30% by mass or less, and more preferably 20% by mass or less. If the amount of the nitrogen-containing thermally crosslinkable compound is excessively large, the remaining film ratio during development and the resolution are liable to be reduced.
- Adhesion aid An adhesive aid can be blended with the photopolymerizable composition of the present invention for the purpose of improving the adhesion to the substrate.
- the adhesion assistant include a silane coupling agent. More specifically, for example, trimethoxysilylbenzoic acid, ⁇ -methacryloxypropyltrimethoxysilane, vinyltriacetoxysilane, vinyltrimethoxysilane, ⁇ -glycidoxypropyltrimethoxysilane, ⁇ -isocyanatopropyltriethoxy Examples thereof include silane and ⁇ - (3,4-epoxycyclohexyl) ethyltrimethoxysilane. These silane coupling agents may be used alone or in combination of two or more.
- the silane coupling agent has not only a function as an adhesion assistant but also a function of imparting appropriate heat melting (thermal fluidity) to the protective film in heat treatment to improve flatness.
- blended for such a purpose the silane coupling agent which has an epoxy group is mentioned, for example. More specifically, examples include ⁇ -gridoxypropylmethoxysilane, ⁇ - (3,4-epoxycyclohexyl) ethyltrimethoxysilane, and the like.
- the amount of the adhesion assistant is usually 0.1% by mass or more, usually 20% by mass or less, preferably 10% with respect to the total solid content of the photopolymerizable composition. It is below mass%.
- the photopolymerizable composition of the present invention contains a thermal crosslinking agent (G-2), it further contains a curing agent for shortening the time under curing conditions or changing the set temperature, Different curing conditions can be appropriately selected depending on the manufacturing process of the element.
- Such a curing agent is not particularly limited as long as it does not impair the required function.
- it contains a benzoic acid compound, a polyvalent carboxylic acid (anhydride), and a polyvalent carboxylic acid (anhydride).
- examples include polymers, thermal acid generators, amine compounds, polyamine compounds, and block carboxylic acids.
- the epoxy group-containing compound is contained as a thermal crosslinking agent, it is preferable to use a thermosetting agent.
- (G-4-1) Benzoic acid compound
- a hydroxyl group, a halogen atom, an alkyl group, an acyl group, an acyloxyl group are located at positions 2 to 6 on the benzene ring of benzoic acid or benzoic acid.
- those having a substituent such as an alkoxyl group, an aryl group, and an allyl group.
- those having a hydroxyl group having high curing ability for epoxy as a substituent are preferable, and those having two or more hydroxyl groups are particularly preferable.
- benzoic acid compounds include 3,4,5-trihydroxybenzoic acid, 2,5-dihydroxybenzoic acid, 2,6-dihydroxybenzoic acid, 3,4-dihydroxybenzoic acid, 2,4 , 6-trihydroxybenzoic acid and the like.
- polyvalent carboxylic acid examples include alicyclic polyvalent carboxylic acids such as methyl hymic anhydride, hexahydrophthalic anhydride, tetrahydrophthalic anhydride, trialkyltetrahydrophthalic anhydride, and methylcyclohexene dicarboxylic acid anhydride.
- aromatic polycarboxylic acid anhydrides such as phthalic anhydride, trimellitic anhydride, pyromellitic anhydride, benzophenone tricarboxylic anhydride, benzophenone tetracarboxylic anhydride; succinic acid, trimellitic acid, Examples thereof include alicyclic acid anhydrides such as maleic acid and cyclopentanetetracarboxylic acid; hydrolysates of aromatic acid anhydrides and the like.
- trimellitic acid (anhydride) and phthalic anhydride are preferable.
- the polymer containing polyvalent carboxylic acid (anhydride) includes (anhydrous) polyvalent carboxylic acid such as (anhydrous) maleic acid. And a polymer with a compound having at least one ethylenically unsaturated bond in the molecule, a partial half ester modified polymer of a polyvalent carboxylic acid (anhydride) portion in such a polymer, and the like. .
- Examples of the compound having one or more ethylenically unsaturated bonds in the molecule include (meth) acrylic acid and alkyl esters thereof, (meth) acrylonitrile, (meth) acrylamide, styrene, (poly) alkyleneoxy groups or alkyls. And alkylene having a locating group such as a group.
- polymers containing polyvalent carboxylic acid (anhydride), maleic anhydride and alkylene having a quenching group such as a (poly) alkyleneoxy group or an alkyl group are particularly preferred from the viewpoints of light transmittance and cured film strength. And a copolymer are preferred.
- thermal acid generator examples include various aromatic diazonium salts, diaryliodonium salts, monophenylsulfonium salts, triallylsulfonium salts, triallyl selenium salts, and the like. Examples include onium salt compounds, sulfonic acid esters, and halogen compounds. Specific examples include aromatic diazonium salts such as chlorobenzenediazonium hexafluorophosphate, dimethylaminobenzenediazonium hexafluoroantimonate, naphthyldiazonium hexafluorophosphate, dimethylaminonaphthyldiazonium tetrafluoroborate.
- aromatic diazonium salts such as chlorobenzenediazonium hexafluorophosphate, dimethylaminobenzenediazonium hexafluoroantimonate, naphthyldiazonium hexafluorophosphate, dimethylaminonaphth
- diaryl iodonium salt examples include diphenyl iodonium tetrafluoroborate, diphenyl iodonium hexafluoroantimonate, diphenyl iodonium hexafluorophosphate, diphenyl iodonium triflate, 4,4′-di-t-butyl-diphenyl iodonium triflate, 4 4,4′-di-t-butyl-diphenyliodonium tetrafluoroborate, 4,4′-di-t-butyl-diphenyliodonium hexafluorophosphate, and the like.
- monophenylsulfonium salts include benzyl-p-hydroxyphenylmethylsulfonium hexafluorophosphate, p-hydroxyphenyldimethylsulfonium hexafluoroantimonate, p-acetoxyphenyldimethylsulfonium hexafluoroantimony.
- benzyl-p-hydroxyphenylmethylsulfonium hexafluoroantimonate monophenylsulfonium salt types such as compounds represented by the following general formula, and benzylphenylsulfonium salt types.
- triallylsulfonium salt triphenylsulfonium tetrafluoroborate, triphenylsulfonium hexafluorophosphate, triphenylsulfonium hexafluoroantimonate, tri (p-chlorophenyl) sulfonium tetrafluoroborate And tri (p-chlorophenyl) sulfonium hexafluorophosphate, tri (p-chlorophenyl) sulfonium hexafluoroantimonate, 4-t-butyltriphenylsulfonium hexafluorophosphate, and the like.
- Triaryl selenium salts include triallyl selenium tetrafluoroborate, triallyl selenium hexafluorophosphate, triallyl selenium hexafluoroantimonate, di (chlorophenyl) phenyl selenium tetrafluoroborate, di (chlorophenyl) phenyl selenium hexafluorophosphate , Di (chlorophenyl) phenyl selenium hexafluoroantimonate and the like.
- sulfonate esters examples include benzoin tosylate, p-nitrobenzyl-9,10-ethoxyanthracene-2-sulfonate, 2-nitrobenzyl tosylate, 2,6-dinitrobenzyl tosylate, and 2,4-dinitrobenzyl. And tosylate.
- halogen compounds include 2-chloro-2-phenylacetophenone, 2,2 ′, 4′-trichloroacetophenone, 2,4,6-tris (trichloromethyl) -s-triazine, 2- (p-methoxystyryl)- 4,6-bis (trichloromethyl) -s-triazine, 2-phenyl-4,6-bis (trichloromethyl) -s-triazine, 2- (p-methoxyphenyl) -4,6-bis (trichloromethyl) -S-triazine, 2- (4'-methoxy-1'-naphthyl) -4,6-bis (trichloromethyl) -s-triazine, bis-2- (4-chlorophenyl) -1,1,1-trichloroethane Bis-1- (4-chlorophenyl) -2,2,2-trichloroethanol, bis-2- (4-methoxyphenyl) -1,1,1
- the monophenylsulfonium salt type or the benzylphenylsulfonium salt type is preferable from the viewpoints of light transmittance and cured film strength.
- (G-4-5) Amine compound examples include ethylediamine, 1,3-diaminopropane, 1,4-diaminobutane, hexamethylenediamine, 2,5-dimethylhexamethylenediamine, piperidine, pyrrolidine, Ethylenediamine, trimethylhexamethylenediamine, dimethylcyclohexylamine, tetramethylguanidine, triethanolamine, N, N′-dimethylpiperazine, dicyanamide, or derivatives thereof; DBU (1,8-diazabiscyclo (5,4,0) undecene-1 ), Aliphatic amines such as DBU-based tetraphenylborate salts (first, second, third); metaphenylenediamine, diaminodiphenylmethane, diaminodiphenylsulfone, diaminodiethyldiphenylmethane, benzyldimethyl Min, dimethyl
- dicyanamide and DBU-based tetraphenylborate salts are preferable from the viewpoint of cured film strength.
- polyamine compound examples include triethyltetramine, tetraethylenepentamine, pentaethylenehexamine, dimethylaminopropylamine, diethylaminopropylamine, N-aminoethylpiperazine, mensendiamine, and isofluorodiamine.
- Aliphatic polyamines such as bis (4-amino-3-methylcyclohexyl) methane, diaminodicyclohexylamine, N, N-dimethylcyclohexylamine, m-xylenediamine, xylylenediamine, xylylenediamine derivatives, xylylenediamine trimer And aromatic polyamines such as body.
- N, N-dimethylcyclohexylamine is preferable.
- block carboxylic acid examples include, for example, the above (polyvalent) carboxylic acids and carboxylic acids of polymers containing them, and JP-A-4-218561 and JP-A-2003-66223. And block carboxylic acids to which vinyl ether is added by the methods described in JP-A No. 2004-339332, JP-A No. 2004-339333, and the like.
- polymers containing polyvalent carboxylic acids (anhydrides), onium salt compounds, block carboxylic acid compounds, and benzoic acid compounds have good curing reaction activity and high hardness and support ( It is preferable in that adhesion to a substrate) is obtained.
- curing agents may be used alone or in combination of two or more.
- the curing agent among them, the polyvalent carboxylic acid copolymer and the benzoic acid compound are excellent in improving the adhesion to the support, and the monosulfonium salt is excellent in improving the hardness.
- benzoic acid compounds are preferable because they are excellent in thermosetting, have high light transmittance, and are less affected by color change due to heat.
- the content of the curing agent in the photopolymerizable composition is usually 0.05% by mass or more, preferably 0.1%, based on the total solid content. It is 20 mass% or less normally, Preferably it is 10 mass% or less. If the amount of the curing agent is excessively small, adhesion to the support (substrate) and hardness are liable to decrease, and conversely if excessively large, decrease in thermal weight is likely to increase.
- the photopolymerizable composition of the present invention includes, for example, o-hydroxybenzophenone, hydroquinone, p-methoxyphenol, 2,6-di-t which may have a substituent.
- a thermal polymerization inhibitor such as -butyl-p-cresol can be blended.
- the compounding ratio of these compounds is usually 10% by mass or less, preferably 2% by mass or less, based on the total solid content.
- a plasticizer such as dioctyl phthalate, didodecyl phthalate, or tricresyl phosphate is 40% by mass or less, preferably 20%, based on the total solid content. You may contain in the ratio of the mass% or less.
- a polymerization accelerator can be added to the photopolymerizable composition of the present invention, if necessary.
- the polymerization accelerator include, for example, esters of amino acids such as N-phenylglycine or dipolar ionic compounds thereof, 2-mercaptobenzothiazole, 2-mercaptobenzimidazole, 2-mercaptobenzoxazole, 3-mercapto-1, Contains mercapto groups such as 2,4-triazole, 2-mercapto-4 (3H) -quinazoline, ⁇ -mercaptonaphthalene, ethylene glycol dithiopropionate, trimethylolpropane tristhiopropionate, pentaerythritol tetrakisthiopropionate Compounds, polyfunctional thiol compounds such as hexanedithiol, trimethylolpropane tristhioglyconate, pentaerythritol tetrakisthiopropionate
- the content is preferably 20% by mass or less, and preferably 1 to 10% by mass with respect to the total solid content. Further preferred.
- an ultraviolet absorber can be added to the photopolymerizable composition of the present invention as necessary.
- the UV absorber controls the photocuring rate when the film of the photopolymerizable composition of the present invention formed on the substrate is exposed by absorbing a specific wavelength of the light source used for exposure by the UV absorber. It is added for the purpose.
- an ultraviolet absorber it is possible to improve the pattern shape after exposure / development and to eliminate residues remaining in the non-exposed areas after development.
- the ultraviolet absorber for example, a compound having an absorption maximum between 250 nm and 400 nm can be used. More specifically, for example, Sumisorb 130 (manufactured by Sumitomo Chemical Co., Ltd.), EVERSORB10, EVERSORB11, EVERSORB12 (manufactured by Yongkou Chemical Industry Co., Ltd.), Tomissorb 800 (manufactured by API Corporation), SESORB100, SESORB101, SEESORB101S, SEESORB102, SEESORB102, SEESORB102 Benzophenone compounds such as SESORB105, SEESORB106, SEESORB107, SEESORB151 (manufactured by Sipro Kasei Co., Ltd.); Johoku Chemical Industry Co., Ltd.), TINUVIN PS, TINUVIN99-2 TINUVIN109, TINUVIN384-2, TINUVIN900, TINUVIN928, TINUVIN1130 (manufactured by
- the blending ratio is usually 0.01% by mass or more and 15% by mass or less, preferably 0.05% by mass or more and 10% by mass with respect to the total solid content of the photopolymerizable composition. % Or less. If the blending ratio of the UV absorber is less than this range, effects such as improvement of the pattern shape and / or removal of the residue tend to be difficult to obtain, and if it is large, the sensitivity and / or the remaining film ratio are decreased. Tend.
- the photopolymerizable composition of the present invention is produced according to a conventional method known per se.
- a photopolymerizable composition containing a color material (F) such as a pixel or BM composition is produced will be described as an example.
- a photopolymerizable composition used for an application that does not include a color material such as an interlayer insulating film, a photospacer, or a rib (liquid crystal alignment control protrusion)
- A an ethylenically unsaturated group-containing compound
- B A photopolymerization initiator
- C an alkali-soluble resin
- E a solvent
- G other components as necessary may be mixed to obtain a uniform dispersion solution.
- a coloring material (E) a solvent, and if necessary, (G-1) a pigment dispersant are weighed in predetermined amounts, and in the dispersion treatment step, the coloring material is dispersed to obtain a pigment dispersion (ink-like liquid). Liquid).
- a paint conditioner, a sand grinder, a ball mill, a roll mill, a stone mill, a jet mill, a homogenizer, or the like can be used.
- the color material is made into fine particles, so that the coating characteristics of the photopolymerizable composition are improved, and the transmittance of the product color filter substrate is improved.
- the above (C) alkali-soluble resin may be used in combination.
- the dispersion treatment is performed using a paint conditioner or the like, it is preferable to use glass beads or zirconia beads having a diameter of 0.1 to several mm.
- the temperature during the dispersion treatment is usually set in the range of 0 ° C. to 100 ° C., preferably in the range of room temperature to 80 ° C.
- the dispersion time varies depending on the composition of the pigment dispersion (coloring material, solvent, pigment dispersant), the size of the apparatus, and the like, and thus needs to be adjusted as appropriate.
- a black pigment dispersion (so that the 20-degree specular gloss in JIS Z8741 is in the range of 100 to 200)
- Control of the gloss of the ink-like liquid) is a measure of dispersion.
- the gloss of the black pigment dispersion is low, the dispersion treatment is not sufficient and coarse pigment particles often remain, which is often insufficient in terms of developability, adhesion, resolution, and the like. Further, when the dispersion treatment is carried out until the gloss value exceeds the above range, a large number of ultrafine particles are produced, so that the dispersion stability tends to be impaired.
- the photopolymerizable composition of the present invention is suitably used for, for example, an image forming application for producing various members such as a liquid crystal display device.
- an image forming application for producing various members such as a liquid crystal display device.
- ⁇ Method for forming interlayer insulating film> A method for forming an interlayer insulating film using the photopolymerizable composition of the present invention will be described. ⁇ 1 ⁇ Coating process First, the photopolymerizable composition of the present embodiment described above is applied onto a substrate using an application device such as a spinner, a wire bar, a flow coater, a die coater, a roll coater, or a spray.
- the coating thickness of the photopolymerizable composition is usually 0.5 to 5 ⁇ m.
- ⁇ 2 ⁇ Drying Step A volatile component is removed (dried) from the coating film to form a dry coating film.
- drying vacuum drying, hot plate, IR oven, convection oven or the like can be used.
- Preferred drying conditions are a temperature of 40 to 150 ° C. and a drying time of 10 seconds to 60 minutes.
- a photomask is placed on the dry coating film of the photopolymerizable composition layer, and image exposure is performed through the photomask. After the exposure, an unexposed uncured portion is removed by development to form an image.
- post-exposure baking may be performed after exposure for the purpose of improving sensitivity before development.
- a hot plate, an IR oven, a convection oven, or the like can be used.
- Post-exposure bake conditions are usually in the range of 40 to 150 ° C. and drying time of 10 seconds to 60 minutes.
- an image obtained after development is required to have a fine line reproducibility of 10 ⁇ m width.
- higher fine line reproducibility tends to be required.
- a rectangular shape with a clear contrast between the non-image and the image area as the cross-sectional shape of the fine line image after development is developed such as development time, developer aging, development shower physical stimulation, etc. A wide margin is preferable.
- Examples of the light source used in the exposure process of the dried coating film include xenon lamps, halogen lamps, tungsten lamps, high-pressure mercury lamps, ultra-high pressure mercury lamps, metal halide lamps, medium-pressure mercury lamps, low-pressure mercury lamps, and other light sources, argon ion lasers, and YAG lasers. And laser light sources such as excimer laser and nitrogen laser. When only light of a specific wavelength is used, an optical filter can be used.
- the solvent used for the development treatment is not particularly limited as long as it is a solvent capable of dissolving the coating film of the uncured portion, but as mentioned above, points such as environmental pollution, harm to the human body, fire risk, etc. Therefore, it is preferable to use an alkali developer instead of an organic solvent.
- alkali developer examples include inorganic alkali compounds such as sodium carbonate, sodium hydrogen carbonate, potassium carbonate, potassium hydrogen carbonate, sodium silicate, potassium silicate, sodium hydroxide, potassium hydroxide, or diethanolamine, triethylamine, An aqueous solution containing an organic alkali compound such as ethanolamine or tetramethylammonium hydroxide can be mentioned.
- the alkaline developer may contain a surfactant, a water-soluble organic solvent, a wetting agent, a low molecular compound having a hydroxyl group or a carboxylic acid group, etc., if necessary.
- a surfactant since many surfactants have an improving effect on developability, resolution, residue and the like.
- the surfactant used in the developer examples include an anionic surfactant having a sodium naphthalenesulfonate group, a sodium benzenesulfonate group, a nonionic surfactant having a polyalkyleneoxy group, and a tetraalkylammonium group. And cationic surfactants.
- the development processing method it is usually carried out by a method such as immersion development, paddle development, spray development, brush development, ultrasonic development at a development temperature of 10 to 50 ° C., preferably 15 to 45 ° C. Is called.
- ⁇ 4 ⁇ Heat treatment step The photopolymerizable composition film image-formed by the exposure / development step is then subjected to a heat treatment (hard baking) step to become a cured product (thermosetting film).
- a heat treatment hard baking
- the entire surface exposure may be performed for the purpose of suppressing the generation of outgas during the hard baking before the hard baking.
- ultraviolet light or visible light is used as the light source.
- a laser light source such as an argon ion laser, a YAG laser, an excimer laser, and a nitrogen laser.
- a hot plate, IR oven, convection oven, etc. can be used for hard baking.
- the hard baking conditions are usually in the range of 100 to 250 ° C. and drying time of 30 seconds to 90 minutes.
- the manufacturing method of the color filter using the photopolymerizable composition of this invention is demonstrated.
- the photopolymerizable composition of this invention is not only the pixel and black matrix in a color filter, but the photo spacer and rib ( It can also be used to form liquid crystal alignment control projections).
- the photopolymerizable composition of the present invention is applied and dried, then a photomask is placed on the coating film, and exposure is performed through the photomask.
- the resin BM is formed by development and, if necessary, thermosetting or photocuring. Further, the same operation is repeated for each of the three RGB colors to form pixels and form a color filter.
- the transparent substrate used here is a transparent substrate for a color filter, and its material is not particularly limited.
- polyester such as polyethylene terephthalate, polypropylene, polyolefin such as polyethylene, polycarbonate, etc.
- thermoplastic plastic sheets such as polymethyl methacrylate and polysulfone, thermosetting plastic sheets such as epoxy resin, polyester resin and poly (meth) acrylic resin, and various glass plates.
- a glass plate and a heat-resistant plastic sheet are preferably used from the viewpoint of heat resistance.
- such a transparent substrate can be previously subjected to corona discharge treatment, ozone treatment, thin film treatment of various polymers such as silane coupling agents and urethane polymers, and the like.
- the coating method of the photopolymerizable composition on the transparent substrate is not particularly limited, but is usually performed using a coating device such as a spinner, a wire bar, a flow coater, a die coater, a roll coater, or a spray. Is called.
- a coating device such as a spinner, a wire bar, a flow coater, a die coater, a roll coater, or a spray.
- a hot plate, IR oven, convection oven or the like can be used.
- Preferred drying conditions are 40 to 150 ° C., and drying time is in the range of 10 seconds to 60 minutes.
- the film thickness of the resin BM after coating and drying is 0.1 to 2 ⁇ m, preferably 0.1 to 1.5 ⁇ m, more preferably 0.1 to 1 ⁇ m.
- the resin BM formed from the photopolymerizable composition of the present invention preferably has an optical density of 3.0 or more at a film thickness of 1 ⁇ m from the viewpoint of light shielding properties. Further, it is advantageous that the 20 degree gloss value of BM is 100 to 200 as an indicator of the dispersion state of solid components such as pigments.
- the light source used for the exposure is, for example, a xenon lamp, a halogen lamp, a tungsten lamp, a high-pressure mercury lamp, an ultra-high pressure mercury lamp, a metal halide lamp, a medium-pressure mercury lamp, a low-pressure mercury lamp, or an argon ion laser, YAG Laser light sources such as lasers, excimer lasers, nitrogen lasers, etc.
- an optical filter can also be used.
- the solvent used for the development treatment is not particularly limited as long as it is a solvent capable of dissolving the resist film in the unexposed area.
- organic solvents such as acetone, methylene chloride, trichlene, and cyclohexanone can be used.
- organic solvents since many organic solvents have environmental pollution, harmfulness to human body, fire risk, etc., it is preferable to use an alkaline developer without such danger.
- alkali developer examples include inorganic alkali agents such as sodium carbonate, potassium carbonate, sodium silicate, potassium silicate, sodium hydroxide, potassium hydroxide, or diethanolamine, triethanolamine, tetraalkylammonium hydroxide salt, etc. And an aqueous solution containing an organic alkali agent.
- the alkali developer may contain a surfactant, a water-soluble organic solvent, a low molecular compound having a hydroxyl group or a carboxyl group, etc., if necessary.
- a surfactant it is preferable to add a surfactant since many surfactants have an improving effect on developability, resolution, and background stains.
- a surfactant for a developer an anionic surfactant having a sodium naphthalenesulfonate group, a sodium benzenesulfonate group, a nonionic surfactant having a polyalkyleneoxy group, a cation having a tetraalkylammonium groupcan be mentioned.
- the development processing method is not particularly limited, but is usually carried out at a development temperature of 10 to 50 ° C., preferably 15 to 45 ° C., by a method such as immersion development, spray development, brush development, ultrasonic development and the like.
- a method such as immersion development, spray development, brush development, ultrasonic development and the like.
- application, drying, exposure, and development of the photopolymerizable composition are repeated for each of the BM and RGB three colors to produce a color filter.
- the photopolymerizable composition of the present invention can be used for BM formation and RGB three-color pixel formation.
- the photopolymerizable composition of the present invention can be used to form a photo spacer, a rib (liquid crystal alignment control protrusion), and the like in addition to the interlayer insulating film, the color filter BM, and RGB three-color pixels as described above.
- a rib liquid crystal alignment control protrusion
- the photospacer is formed by applying the photopolymerizable composition of the present invention to a substrate, drying, exposing, developing, and thermosetting.
- the photopolymerizable composition of the present invention is applied to a substrate.
- a coating method a conventionally known method such as a spinner method, a wire bar method, a flow coating method, a die coating method, a roll coating method, or a spray coating method can be used.
- the die coating method greatly reduces the amount of coating solution (photopolymerizable composition) used, and has no influence from mist or the like that adheres during spin coating. It is preferable from a comprehensive viewpoint.
- the coating amount is adjusted so that the dry film thickness is usually in the range of 0.5 to 10 ⁇ m, preferably 1 to 8 ⁇ m, particularly preferably 1 to 5 ⁇ m.
- the photopolymerizable composition of the present invention may be supplied in a pattern on a substrate by an inkjet method or a printing method.
- the drying of the photopolymerizable composition after application is preferably performed by a hot plate, IR oven, convection oven or the like. Moreover, you may combine the reduced pressure drying method of drying in a reduced pressure chamber, without raising temperature. Drying conditions can be appropriately selected according to the type of solvent component, the performance of the dryer used, and the like. The drying conditions are usually selected in the range of 40 to 100 ° C. for 15 seconds to 5 minutes, preferably 50 to 90 ° C., depending on the type of solvent component and the performance of the dryer used. It is selected in the range of 30 seconds to 3 minutes.
- the exposure is carried out by overlaying a negative mask pattern on the photopolymerizable composition coating film and irradiating an ultraviolet or visible light source through the mask pattern.
- the composition may be cured in a pattern by a scanning exposure method using laser light.
- the light source used for said exposure is not specifically limited.
- laser light sources such as excimer laser, nitrogen laser, helium cadmium laser, blue-violet semiconductor laser, and near infrared semiconductor laser.
- An optical filter can also be used when used by irradiating light of a specific wavelength.
- an image pattern can be formed on the substrate by development using an aqueous solution containing an alkaline compound and a surfactant or an organic solvent.
- This aqueous solution may further contain an organic solvent, a buffering agent, a complexing agent, a dye or a pigment.
- Alkaline compounds include sodium hydroxide, potassium hydroxide, lithium hydroxide, sodium carbonate, potassium carbonate, sodium bicarbonate, potassium bicarbonate, sodium silicate, potassium silicate, sodium metasilicate, sodium phosphate, potassium phosphate
- Inorganic alkaline compounds such as sodium hydrogen phosphate, potassium hydrogen phosphate, sodium dihydrogen phosphate, potassium dihydrogen phosphate, ammonium hydroxide, mono-di- or triethanolamine, mono-di- or trimethylamine , Mono-di- or triethylamine, mono- or diisopropylamine, n-butylamine, mono-di- or triisopropanolamine, ethyleneimine, ethylenediimine, tetramethylammonium hydroxide (TMAH), choline, etc.
- Machine alkaline compounds These alkaline compounds may be a mixture of two or more.
- surfactant examples include nonionic surfactants such as polyoxyethylene alkyl ethers, polyoxyethylene alkyl aryl ethers, polyoxyethylene alkyl esters, sorbitan alkyl esters, monoglyceride alkyl esters, and alkylbenzene sulfonic acids.
- nonionic surfactants such as polyoxyethylene alkyl ethers, polyoxyethylene alkyl aryl ethers, polyoxyethylene alkyl esters, sorbitan alkyl esters, monoglyceride alkyl esters, and alkylbenzene sulfonic acids.
- anionic surfactants such as salts, alkylnaphthalene sulfonates, alkyl sulfates, alkyl sulfonates, and sulfosuccinate esters
- amphoteric surfactants such as alkylbetaines and amino acids.
- the organic solvent examples include isopropyl alcohol, benzyl alcohol, ethyl cellosolve, butyl cellosolve, phenyl cellosolve, propylene glycol, diacetone alcohol and the like.
- the organic solvent can be used alone or in combination with an aqueous solution.
- the substrate after development is preferably subjected to a thermosetting treatment.
- the thermosetting treatment conditions at this time are selected such that the temperature is in the range of 100 to 280 ° C., preferably in the range of 150 to 250 ° C., and the time is in the range of 5 to 60 minutes.
- a rib is a protrusion formed on a transparent electrode in order to improve the viewing angle of a liquid crystal display device.
- the liquid crystal is aligned in multiple directions.
- the photopolymerizable composition of the present invention is formed on a transparent substrate usually having a thickness of 0.1 to 2 mm obtained by depositing ITO on a color filter. It is applied using an application device such as a spinner, wire bar, flow coater, die coater, roll coater or spray.
- the coating thickness of the composition is usually 0.5 to 5 ⁇ m.
- the cross-sectional shape of the fine line image after development is preferably a rectangular shape in which the contrast between the non-image area and the image area is clear.
- the rectangular shape is preferable because a development margin such as development time, developer aging, and physical stimulation of a development shower is widened.
- an image after development usually has a cross-sectional shape close to a rectangular shape.
- the temperature of the heat treatment is usually 150 ° C. or higher, preferably 180 ° C. or higher, more preferably 200 ° C. or higher, usually 400 ° C. or lower, preferably 300 ° C. or lower, more preferably 280 ° C. or lower.
- the time for the heat treatment is usually 10 minutes or longer, preferably 15 minutes or longer, more preferably 20 minutes or longer, usually 120 minutes or shorter, preferably 60 minutes or shorter, more preferably 40 minutes or shorter.
- the range of deformation during heating can be adjusted by appropriately adjusting the composition of the photopolymerizable composition and heating conditions.
- W1 / W2 is usually 1.2 or more, preferably 1.3 or more, more preferably 1.5 or more, usually 10 or less, preferably 8 or less.
- the higher the heating temperature or the longer the heating time the higher the deformation rate.
- the lower the heating temperature or the shorter the heating time the lower the deformation rate.
- the photopolymerizable composition of this invention can be used also for the method (collective formation method) which forms simultaneously the hardened
- Examples of the cured product include subphotospacers (photospacers having a pattern height slightly lower than ordinary photospacers), overcoats (protective films), and the like in addition to the photospacers and ribs. .
- Examples of combinations of cured products having different heights and shapes include, for example, photo spacers and sub-photo spacers, photo spacers and ribs, photo spacers and overcoats, and the photopolymerizable composition of the present invention simultaneously combines them. It can also be used in the batch forming method.
- the methods such as coating, drying, exposure, development, and thermosetting used in the batch forming method are the same as those described in the method for forming the photospacer and rib, but a plurality of light transmission amounts are used in the exposure step. It is preferable to use a halftone mask or the like having a plurality of openings adjusted to the type. By adjusting the exposure amount suitable for each cured product using a halftone mask, cured products having different heights and shapes can be formed simultaneously. Moreover, it is possible to collectively form cured products having different heights and shapes by curing the composition in a pattern by a scanning exposure method using laser light.
- the photopolymerizable composition of the present invention containing the ketoxime ester compound of the present invention is capable of forming a step (difference in height) with high sensitivity, and having a cured product when a halftone mask is used. Good uniformity in height, good adhesion even at low exposure due to the halftone mask, good shape of the cured product such as photo spacers and ribs formed, etc. This is also suitable for the batch forming method.
- Ketoxime (1.2 g, 2.70 mmol) and acetyl chloride (0.64 g, 8.10 mmol) were dissolved in 50 g of dichloromethane and ice-cooled, and triethylamine (0.82 g, 8.10 mmol) was added dropwise.
- the reaction was performed at room temperature for 4 hours.
- water was added to separate the organic layer, washed twice with a saturated NH 4 Cl aqueous solution, three times with a 5% Na 2 CO 3 aqueous solution, and then twice with a saturated saline solution. And dried over sodium sulfate and evaporated.
- the NMR shift value of the compound was as follows. 1 H-NMR ⁇ [ppm] 1.50 (t, 3H), 1.55 (s, 3H), 2.30 (s, 3H), 2.37 (t, 2H), 3.78 (s, 2H), 4.45 (q , 2H), 7.3-7.6 (m, 6H), 8.18 (dd, 1H), 8.37 (dd, 1H), 8.60 (d, 1H), 8.90 (d, 1H)
- the reaction formula is as follows.
- Example 2 (Production of ketoxime ester compound I-2) ⁇ Production of diketone body> A white solid was obtained in the same manner as in Example 1 from the monoketone body of Example 1 (10 g, 31.91 mmol), ethylglutaryl chloride (5.84 g, 32.71 mmol), and aluminum chloride (13.62 g, 102.11 mmol). 12.4 g was obtained.
- the reaction formula is as follows.
- ketoxime ester In the same manner as in Example 1, 1.6 g of white crystals were obtained from ketoxime (5.0 g, 10.32 mmol), acetyl chloride (1.62 g, 20.64 mmol) and triethylamine (2.09 g, 20.64 mmol). A ketoxime ester compound I-2 was obtained.
- the NMR shift value of the compound was as follows. 1 H-NMR ⁇ [ppm] 1.17 (t, 3H), 1.45 (t, 3H), 2.30 (s, 3H), 2.37 (s, 3H), 2.75 (t, 2H), 3.15 (t , 2H), 4.15 (q, 2H), 4.38 (q, 2H), 7.3-7.5 (m, 6H), 8.18 (dd, 1H), 8.37 (dd, 1H), 8.60 (d, 1H), 8.82 (d, 1H)
- the reaction formula is as follows.
- ketoxime ester compound I-8 was produced in the same manner as in the production of the diketone product in Example 2, except that ethylglutaryl chloride was changed to methylglutaryl chloride.
- the NMR shift value of the obtained compound was as follows.
- the organic layer was washed successively with water, 5% aqueous sodium carbonate solution and saturated aqueous sodium chloride solution, and dried by adding magnesium sulfate. Magnesium sulfate was filtered and the solvent was concentrated by an evaporator to obtain 11.33 g (yield 77%) of the desired product. This was used in the next reaction without purification.
- the reaction formula is as follows.
- the organic layer was washed sequentially with a saturated aqueous sodium hydrogen carbonate solution and a saturated aqueous sodium chloride solution, and dried by adding magnesium sulfate. After filtering the magnesium sulfate and concentrating the solvent with an evaporator, purification was performed by silica gel column chromatography to obtain 1.80 g (yield 78%) of the following ketoxime ester compound I-9.
- the NMR shift value of the obtained compound was as follows. 1 H-NMR ⁇ [ppm] 1.15 (t, 3H), 1.49 (t, 3H), 2.27 (s, 3H), 2.72 (t, 2H), 3.12 (t, 2H), 3.58 (s) , 3H), 4.43 (q, 2H), 7.3 to 7.5 (m, 6H), 8.06 (dd, 1H), 8.29 (dd, 1H), 8.59 (d, 1H), 8.83 (dd, 1H)
- the reaction formula is as follows.
- ketoxime ester compound I-10 was produced in the same manner as in the production of the diketone product in Example 4 except that ethylglutaryl chloride was changed to methylglutaryl chloride.
- the NMR shift value of the obtained compound was as follows.
- Example 6 (Production of ketoxime ester compound I-11) In the production of the diketone body in Example 2, except that ethyl glutaryl chloride was changed to methyl glutaryl chloride and acetyl chloride was changed to benzoyl chloride in the production of ketoxime ester, A ketoxime ester compound I-11 was produced.
- the NMR shift value of the obtained compound was as follows.
- Example 7 (Production of ketoxime ester compound I-12) ⁇ Production of diketone body> Under a nitrogen atmosphere, a ketone body 14.2 g (35 mmol), methylglutaryl chloride 6.4 g (39 mmol), and methylene chloride 120 ml were added to a 500 ml four-necked flask. After cooling the reaction solution to 5 ° C., 15.6 g (117 mmol) of aluminum chloride was slowly added over 25 minutes. After completion of the addition, the mixture was further stirred at 3 ° C. for 2 hours, and the reaction solution was added little by little to 600 ml of ice water.
- the organic layer was washed successively with water, 5% aqueous sodium carbonate solution and saturated aqueous sodium chloride solution, and dried by adding magnesium sulfate. Magnesium sulfate was filtered, and the solvent was concentrated by an evaporator to obtain 10.5 g of a light brown solid. Recrystallization from a methylene chloride / hexane solvent gave 9.2 g (yield 49%) of the yellow target product.
- the reaction formula is as follows.
- the organic layer was washed in turn with a 10% aqueous potassium carbonate solution and a saturated aqueous sodium chloride solution, dried over magnesium sulfate. After filtering the magnesium sulfate and concentrating the solvent with an evaporator, purification was performed by silica gel column chromatography to obtain 5.1 g (yield 54%) of the desired product.
- the reaction formula is as follows.
- ketoxime ester A 50 ml four-necked flask was charged with 2.6 g (4.7 mmol) of the ketoxime obtained above, 16 ml of tetrahydrofuran, and 0.95 g (9.4 mmol) of triethylamine, and the system was replaced with nitrogen. After the reaction solution was cooled to 5 ° C., 0.49 g (6.3 mmol) of acetyl chloride was added. After completion of the addition, the mixture was further stirred at 5 ° C. for 4 hours, and 10 ml of a saturated aqueous sodium hydrogen carbonate solution was added.
- the NMR shift value of the obtained compound was as follows. 1 H-NMR ⁇ [ppm] 1.46 (3H, t), 2.24 (3H, s), 2.70 (2H, t), 3.10 (2H, t), 3.55 (3H, s) 4.38 (2H, q), 7.26-7.46 (7H, m), 7.82 (2H, d), 8.11 (2H, d), 8.27 (1 H, d), 8.61 (2H, s), 8.71 (1H, s)
- the reaction formula is as follows.
- Example 8 (Production of ketoxime ester compound I-13) The following ketoxime ester compound I-13 was produced in the same manner as in the production of the ketoxime ester in Example 7 except that acetyl chloride was changed to benzoyl chloride.
- the NMR shift value of the obtained compound was as follows. 1 H-NMR ⁇ [ppm] 1.47 (3H, t), 2.77 (2H, t), 3.23 (2H, t), 3.54 (3H, s), 4.39 (2H, q), 7.26-7.69 (10H, m), 7.80 (2H, d), 8.11 (4H, dd), 8.38 (1H, d), 8.60 (2H, s), 8.80 (1H, s)
- ketoxime ester A 50 ml three-necked flask was charged with 1.09 g (3.17 mmol) of the ketoxime obtained above, 10 ml of tetrahydrofuran and 0.66 g (6.52 mmol) of triethylamine, and the system was replaced with nitrogen. After the reaction solution was cooled to 0 ° C., 0.363 g (3.59 mmol) of acetyl chloride was added. After completion of the addition, the mixture was further stirred at room temperature for 1.5 hours, and 2 ml of a saturated aqueous sodium hydrogen carbonate solution was added.
- ketoxime ester A 50 ml three-necked flask was charged with 1.42 g (4.43 mmol) of the ketoxime obtained above, 20 ml of tetrahydrofuran and 0.897 g (8.86 mmol) of triethylamine, and the system was replaced with nitrogen. After the reaction solution was cooled to 0 ° C., 0.382 g (4.87 mmol) of acetyl chloride was added. After completion of the addition, the mixture was further stirred at room temperature for 2.5 hours, and 2 ml of a saturated aqueous sodium hydrogen carbonate solution was added.
- the organic layer was washed sequentially with a saturated aqueous sodium hydrogen carbonate solution and a saturated aqueous sodium chloride solution, and dried by adding magnesium sulfate. Magnesium sulfate was filtered and the solvent was concentrated by an evaporator to obtain 14.5 g (yield 89%) of the desired product. This was used in the next reaction without purification.
- the reaction formula is as follows.
- the organic layer was washed sequentially with a saturated aqueous sodium hydrogen carbonate solution and a saturated aqueous sodium chloride solution, and dried by adding magnesium sulfate. Magnesium sulfate was filtered and the solvent was concentrated by an evaporator to obtain 10.3 g (yield 72%) of the desired product as a white solid. This was used in the next reaction without purification.
- the reaction formula is as follows.
- Example 13 (Production of ketoxime ester compound I-19) ⁇ Manufacture of ketone bodies> Under a nitrogen atmosphere, 10.0 g (54 mmol) of diphenyl sulfide and 170 ml of methylene chloride were added to a 300 ml three-necked flask and cooled to 3 ° C. To this was added 6.2 g (54 mmol) of glutaric anhydride, and then 16 g (123 mmol) of aluminum chloride was slowly added over 1 hour. After completion of the addition, the mixture was further stirred at 3 ° C. for 5 hours, and the reaction solution was poured little by little into 100 ml of ice water.
- ketoxime ester A 50 ml three-necked flask was charged with 1.4 g (4 mmol) of the ketoxime obtained above, 12 ml of tetrahydrofuran, and 0.7 g (7 mmol) of triethylamine, and the system was replaced with nitrogen. After the reaction solution was cooled to 3 ° C., 0.4 g (5 mmol) of acetyl chloride was added. After completion of the addition, the mixture was further stirred at 3 ° C. for 2 hours, and 10 ml of a saturated aqueous sodium hydrogen carbonate solution was added.
- the mixture was extracted with ethyl acetate, washed successively with a saturated aqueous sodium bicarbonate solution and a saturated aqueous sodium chloride solution, and dried by adding sodium sulfate. After filtering sodium sulfate and concentrating the solvent with an evaporator, purification was performed by silica gel column chromatography to obtain 0.40 g (yield 91%) of the following ketoxime ester compound I-15.
- the NMR shift value of the obtained compound was as follows. 1 H-NMR ⁇ [ppm] 0.86 (3H, t), 1.25-1.32 (4H, m), 1.35-1.43 (2H, m), 1.48 (3H, t), 1.56-1. 65 (2H, m), 2.28 (3H, s), 2.35 (3H, s), 2.84 (2H, t), 4.43 (2H, q), 7.25-7.49 (6H, m), 8.05 (1H, dd), 8.29 (1H, dd), 8.61 (1H, d), 8.83 (1H, d)
- the reaction formula is as follows.
- Photopolymerizable compositions were prepared at the blending ratios shown in Table 8. The obtained photopolymerizable composition was applied on a glass substrate (Asahi Glass Co., Ltd. color filter glass plate “AN100”), dried on a hot plate at 90 ° C. for 90 seconds, and a coating film having a dry film thickness of 4 ⁇ m. Got. Thereafter, exposure was performed from the coating film side using a 3 kW high pressure mercury lamp through a mask having a fine line pattern having a line width of 5 to 50 ⁇ m.
- the image plane illuminance measured with an illuminometer with a wavelength of 365 nm was 30 mW / cm 2 , and the exposure amount was the optimum exposure amount described later.
- development was performed by immersing the substrate in the developer at 25 ° C. for 110 seconds, followed by rinsing with pure water to form an exposed film. Obtained.
- the obtained exposure film was heated at 220 ° C. for 1 hour in a convection oven to obtain a thermosetting film.
- Various evaluations were performed on the photopolymerizable composition, the exposure film, and the thermosetting film (interlayer insulating film). The results are also shown in Table 8.
- the alkali-soluble resin was measured according to JIS-K0070 (acid test value, saponification value, ester value, iodine value, hydroxyl value, and unsaponified test method for chemical products).
- ⁇ Evaluation method of photopolymerizable composition> (sensitivity)
- the photopolymerizable composition was applied on a glass substrate so that the dry film thickness was about 4 ⁇ m, and baked on a hot plate at 90 ° C. for 90 seconds. Then, it exposed with the illumination intensity of 30 mW / cm ⁇ 2 > with the high pressure mercury lamp. As exposure conditions, the exposure energy amount was set in the range of 4 mJ / cm 2 to 64 mJ / cm 2 and the exposure energy amount was set at intervals of 2.5 times. After the exposure, the film was immersed in a 0.4 mass% tetramethylammonium hydroxide aqueous solution at 25 ° C.
- the film thickness of the obtained exposure film is plotted against the exposure amount, and the minimum exposure amount at which the difference in film thickness of the exposure film between a certain exposure amount and 2.5 times the exposure amount is within 10% is determined. , And defined as sensitivity (mJ / cm 2 ). (Residual film rate) The ratio of the film thickness of the thermosetting film obtained by the procedure for forming the interlayer insulating film to the film thickness before exposure was defined as the remaining film ratio (%).
- thermosetting film obtained by the procedure for forming the interlayer insulating film was measured with a spectrophotometer, and the transmittance (%) per 3 ⁇ m film thickness at a wavelength of 400 nm was determined.
- Resolution The image of the thermosetting film obtained by the procedure for forming the interlayer insulating film was observed with an optical microscope, and the minimum line width ( ⁇ m) resolved was defined as the resolving power.
- Pattern shape The cross-sectional shape of the 10 ⁇ m line and space of the thermosetting film obtained by the procedure for forming the interlayer insulating film (in which images and spaces having a line width of 10 ⁇ m were alternately formed) was observed with a scanning electron microscope.
- thermosetting film used for the measurement of the transmittance was immersed in 20% by mass hydrochloric acid at 40 ° C. for 20 minutes, and then the light transmittance of the film was measured with a spectrophotometer, and the transmission per 3 ⁇ m thickness at a wavelength of 400 nm. The rate (%) was determined, and the change in transmittance before and after immersion in hydrochloric acid was calculated according to the following equation.
- [Chemical resistance] [Transmittance before immersion in hydrochloric acid]-[Transmittance after immersion in hydrochloric acid]
- Ethylenically unsaturated group-containing compound M-1 “Epoxy ester 3000A” manufactured by Kyoei Chemical Co., Ltd.
- P-2 Styrene / methyl methacrylate / n-butyl methacrylate / methacrylic acid quaternary copolymer (molar ratio: 45/30/5/20) Acid value: 110 mg-KOH / g, Mw: 7,000
- P-3 benzyl methacrylate / dicyclopentanyl methacrylate / methacrylic acid terpolymer (molar ratio: 40/20/40) Acid value: 138 mg-KOH / g, Mw: 10,000
- P-7 Styrene / methyl methacrylate / methacrylic acid terpolymer (molar ratio: 45/25/30) Acid value: 126 mg-KOH / g, Mw: 9,300
- D Surfactant D-1: Fluorosurfactant “FC4432” manufactured by Sumitomo 3M Limited
- E Organic solvent
- E-1 Propylene glycol monomethyl ether acetate (PGMEA)
- G-2-i Thermal crosslinking agent
- NC-3000 manufactured by Nippon Kayaku Co., Ltd. (epoxy equivalent: 277 g / eq, softening point: 56.5 ° C.)
- the amine value of the solution containing the polymer dispersant thus obtained was determined by neutralization titration to be 14 mg-KOH / g. Further, the resin content was found to be 40% by mass when determined by the dry-up method (at 150 ° C. for 30 minutes, the solvent was removed on a hot plate and the resin concentration was calculated from the weight change).
- ⁇ Evaluation of black resist> The black resist was applied to a glass substrate (“7059” manufactured by Corning) with a spin coater, and dried on a hot plate at 80 ° C. for 1 minute. The thickness of the resist film after drying was measured with a stylus-type film thickness meter (“ ⁇ -Step” manufactured by Tencor Corporation) and found to be 1 ⁇ m. Next, this sample was exposed by changing the exposure amount with a high-pressure mercury lamp through a photomask. A resist pattern was obtained by spray development using a sodium carbonate aqueous solution at a temperature of 25 ° C. and a concentration of 0.8 mass% at a pressure of 0.1 MPa. Sensitivity, alkali resistance, light-shielding properties and film unevenness were evaluated according to the following criteria, and are also shown in Table 9.
- sensitivity It displayed with the appropriate exposure amount (mJ / cm ⁇ 2 >) which can form a mask pattern of 20 micrometers according to the dimension. That is, a resist with a small exposure amount has high sensitivity because an image can be formed with a low exposure amount.
- Resolving power alkali resistance
- the minimum resist pattern size that can be resolved when the development time is 80 seconds at the exposure amount that faithfully reproduces the 20 ⁇ m mask pattern determined as described above was obtained by microscopic observation at a magnification of 200 times. A smaller minimum pattern dimension indicates a higher resolution.
- Light shielding The optical density (OD) of the image area was measured with a Macbeth reflection densitometer (“TR927” manufactured by Kolmorgun).
- the OD value is a numerical value indicating the light shielding ability, and the larger the numerical value, the higher the light shielding property.
- the coated surface was visually observed and evaluated. Uniform without any unevenness : ⁇ Some unevenness is visible, but there is no problem: ⁇ (Linearity)
- the development time was 80 seconds, and five resist patterns having a width of 20 ⁇ m and a length of 100 ⁇ m were observed with a microscope at a magnification of 200 times. The number of occurrences of unevenness of 2 ⁇ m or more on the side having a desired length of 100 ⁇ m was counted.
- the obtained alkali-soluble resin P-5 had a weight average molecular weight of 8,000 and an acid value of 175 mgKOH / g.
- the thus obtained alkali-soluble resin P-6 had a mass average molecular weight Mw measured by GPC of about 8,400 and an acid value of 80 mgKOH / g.
- This mill base was subjected to a dispersion treatment using 600 parts by mass of 0.5 mm ⁇ zirconia beads in a bead mill apparatus at a peripheral speed of 10 m / s and a residence time of 3 hours to obtain a dispersion of P.B. 15: 6.
- a blue resist was coated on a glass substrate on which chromium was vapor-deposited with a spin coater, and pre-baked for 3 minutes on a hot plate at 80 ° C. to form a dry coating film.
- a linear mask pattern with a width of 1 ⁇ m with a width of 1 ⁇ m to 25 ⁇ m is set with a 150 ⁇ m gap using a high pressure mercury lamp, and through this, a dry coating film of blue resist is exposed at 60 mJ / cm 2 using a 2 kW high pressure mercury lamp.
- 0.04 mass% aqueous potassium hydroxide solution was used, and spray development was performed at a developer temperature of 23 ° C.
- the development time was set to twice the dissolution time of the blue resist measured in advance.
- the dissolution time was the same as described above, after applying and drying a blue resist on a glass substrate (“AN-100” manufactured by Asahi Glass Co., Ltd.), using a 0.04 mass% potassium hydroxide aqueous solution, a developer temperature of 23 ° C., a pressure
- the time when the uncolored blue colored resist was completely dissolved in the developer and the substrate was exposed was defined as the dissolution time of the blue resist.
- the substrate was rinsed with sufficient water and then dried with clean air. Thereafter, post-baking was performed in an oven at 230 ° C. for 30 minutes. The film thickness after drying was about 2.5 ⁇ m.
- a blue resist was applied on a glass substrate (“AN-100” manufactured by Asahi Glass Co., Ltd.) using a spin coater, and then dried at 80 ° C. for a period of time. Subsequently, the whole surface exposure process was performed at 60 mJ / cm 2 using a 2 kW high-pressure mercury lamp. Thereafter, development and washing treatment were performed in the same manner as in the production of the pattern (pixel), and post-baking was performed in a 230 ° C. oven for 30 minutes to prepare a colored plate. The film thickness after drying was about 2.5 ⁇ m. With respect to the colored plate thus obtained, a transmission spectrum was measured with a spectrophotometer (“U-3310” manufactured by Hitachi, Ltd.), and chromaticity was calculated with a C light source.
- VHR voltage holding ratio
- the blue resists of the examples and comparative examples were applied by spin coating, heated on a hot plate at 80 ° C. for 3 minutes, and the entire surface was exposed at 100 mJ / cm 2 . Thereafter, spray development was performed for 30 seconds at a water pressure of 0.3 MPa with a 0.1 mass% sodium carbonate aqueous solution at 23 ° C. Then, baking was performed at 230 ° C. for 30 minutes in a hot air circulating furnace. The application conditions were adjusted so that the film thickness after firing was 1.7 ⁇ m.
- the liquid crystal cell was annealed (heated at 105 ° C. for 2.5 hours in a hot air circulating furnace), and then a pulse voltage was applied to the electrode substrates A and B under the conditions of an applied voltage of 5 V and a pulse frequency of 60 Hz, and the voltage holding ratio was measured.
- the ketoxime ester compound of the present invention can be used as a novel and highly sensitive photopolymerization initiator.
- a photopolymerizable composition having high sensitivity and high transmittance and useful particularly for interlayer insulating film applications can be constituted.
- a photopolymerizable composition useful for color filter applications can be formed by further combining with a color material.
- a photopolymerizable composition using this ketoxime ester compound in combination with a black pigment as a photopolymerization initiator has excellent light sensitivity and resolution while being highly light-shielding in a thin film.
- the resin BM can be formed.
- the color filter in which the resin BM is formed using the photopolymerizable composition of the present invention is excellent in accuracy, flatness, and durability, the display quality of the liquid crystal display element can be improved. In addition, since the manufacturing process and the color filter itself do not contain harmful substances, the danger to the human body is reduced and the environmental safety is improved.
- the photopolymerization initiator and the photopolymerizable composition of the present invention are not limited to those for interlayer insulating films, color filter pixels, and BM, but for overcoats, ribs (liquid crystal alignment control protrusions), and photospacers. It can also be used for transparent photopolymerizable compositions such as for applications, and its applied technical field is extremely wide.
Abstract
Description
更に、かかる特定のケトオキシムエステル系化合物は、それ自体新規な化合物であり、かつ優れた光重合開始剤として色材の存在有無にかかわらず有効であることを見出し、本発明を完成するに至った。
[1] 下記一般式(I)で表されることを特徴とするケトオキシムエステル系化合物。
R1は、芳香環又はヘテロ芳香環を含む、置換基を有していてもよい1価の有機基を表し、
R2は、それぞれ置換基を有していてもよい炭素数1~12のアルキルチオ基、炭素数2~12のアルコキシカルボニル基、炭素数3~12のアルケニルオキシカルボニル基、炭素数3~12のアルキニルオキシカルボニル基、炭素数7~12のアリールオキシカルボニル基、炭素数3~12のヘテロアリールオキシカルボニル基、炭素数2~12のアルキルチオカルボニル基、炭素数3~12のアルケニルチオカルボニル基、炭素数3~12のアルキニルチオカルボニル基、炭素数7~12のアリールチオカルボニル基、炭素数3~12のヘテロアリールチオカルボニル基、炭素数2~12のアルキルチオアルコキシ基、-O-N=CR30R31、-N(OR30)-OCO-R31又は下記一般式(II)で表される基
R3は、それぞれ置換基を有していてもよい炭素数2~12のアルカノイル基、炭素数3~25のアルケノイル基、炭素数4~8のシクロアルカノイル基、炭素数7~20のアリーロイル基、炭素数3~20のヘテロアリーロイル基、炭素数2~10のアルコキシカルボニル基、炭素数7~20のアリールオキシカルボニル基、炭素数2~20のヘテロアリール基又は炭素数2~20のアルキルアミノカルボニル基を表す。)
[2] 前記一般式(I)において、Xが置換基を有していてもよい炭素数1~20のアルキレン基であり、R2がそれぞれ置換基を有していてもよい炭素数2~12のアルコキシカルボニル基又は炭素数1~12のアルキルチオ基であることを特徴とする上記[1]に記載のケトオキシムエステル系化合物。
[3] 前記一般式(I)において、R1が、下記一般式(III)で表されることを特徴とする上記[1]または[2]に記載のケトオキシムエステル系化合物。
ただし、R9 は、水素原子、それぞれ置換基を有していてもよい炭素数1~12のアルキル基、炭素数2~8のアルカノイル基、炭素数3~12のアルケニル基、炭素数6~20のアリール基又は炭素数3~15のトリアルキルシリル基を表し、
R10及びR11は、互いに独立して水素原子、それぞれ置換基を有していてもよい炭素数1~12のアルキル基、炭素数2~4のヒドロキシルアルキル基、炭素数3~5のアルケニル基又は炭素数6~20のアリール基を表す。
R4~R8は、互いに結合して環構造を形成してもよい。)
[4] 前記一般式(III)が、下記一般式(IV)で表されることを特徴とする上記[3]に記載のケトオキシムエステル系化合物。
[5] 前記一般式(III)が、下記一般式(V)で表されることを特徴とする上記[3]に記載のケトオキシムエステル系化合物。
R9 は、水素原子、それぞれ置換基を有していてもよい炭素数1~12のアルキル基、炭素数2~8のアルカノイル基、炭素数3~12のアルケニル基、炭素数6~20のアリール基又は炭素数3~15のトリアルキルシリル基を表す。)
[6] 上記[1]~[5]のいずれか一項に記載のケトオキシムエステル系化合物からなることを特徴とする光重合開始剤。
[7] (A)エチレン性不飽和基含有化合物及び(B)光重合開始剤を含有し、(B)光重合開始剤が上記[1]~[5]のいずれか一項に記載のケトオキシムエステル系化合物を含有することを特徴とする光重合性組成物。
[8] 更に(F)色材を含有することを特徴とする上記[7]に記載の光重合性組成物。
[9] 更に(G-1)顔料分散剤を含有することを特徴とする上記[8]に記載の光重合性組成物。
[10] 上記[7]に記載の光重合性組成物により形成された層間絶縁膜を備えることを特徴とする液晶表示装置。
[11] 上記[8]又は[9]に記載の光重合性組成物により形成されたブラックマトリックスを備えることを特徴とするカラーフィルター。
[12] 上記[8]又は[9]に記載の光重合性組成物により形成された画素を備えることを特徴とするカラーフィルター。
本発明のケトオキシムエステル系化合物は、下記一般式(I)で表されることを特徴とする。
R1は、芳香環又はヘテロ芳香環を含む、置換基を有していてもよい1価の有機基を表し、
R2は、それぞれ置換基を有していてもよい炭素数1~12のアルキルチオ基、炭素数2~12のアルコキシカルボニル基、炭素数3~12のアルケニルオキシカルボニル基、炭素数3~12のアルキニルオキシカルボニル基、炭素数7~12のアリールオキシカルボニル基、炭素数3~12のヘテロアリールオキシカルボニル基、炭素数2~12のアルキルチオカルボニル基、炭素数3~12のアルケニルチオカルボニル基、炭素数3~12のアルキニルチオカルボニル基、炭素数7~12のアリールチオカルボニル基、炭素数3~12のヘテロアリールチオカルボニル基、炭素数2~12のアルキルチオアルコキシ基、-O-N=CR30R31、-N(OR30)-OCO-R31又は下記一般式(II)で表される基
R3は、それぞれ置換基を有していてもよい炭素数2~12のアルカノイル基、炭素数3~25のアルケノイル基、炭素数4~8のシクロアルカノイル基、炭素数7~20のアリーロイル基、炭素数3~20のヘテロアリーロイル基、炭素数2~10のアルコキシカルボニル基、炭素数7~20のアリールオキシカルボニル基、炭素数2~20のヘテロアリール基又は炭素数2~20のアルキルアミノカルボニル基を表す。)
上記一般式(I)において、Xは、直接結合又はそれぞれ置換基を有していてもよい炭素数1~20のアルキレン基、-(CH=CH)α-[アルケニレン基]、-(C≡C)α-[アルキニレン基]又はそれらの組み合わせ(αは1~5の整数を表す。)からなる2価の有機基である。αは、製造の簡便さの点から、好ましくは1~3である。
最も好ましいのは置換基を有していてもよいアルキレン基である。アルキレン基の炭素数は、好ましくは2以上である。また、好ましくは15以下、より好ましくは10以下である。
前記一般式(I)において、R1は、芳香環又はヘテロ芳香環を含む、置換基を有していてもよい1価の有機基を表す。
ただし、R9は、水素原子、それぞれ置換基を有していてもよい炭素数1~12のアルキル基、炭素数2~8のアルカノイル基、炭素数3~12のアルケニル基、炭素数6~20のアリール基又は炭素数3~15のトリアルキルシリル基を表し、
R10及びR11は、互いに独立して水素原子、それぞれ置換基を有していてもよい炭素数1~12のアルキル基、炭素数2~4のヒドロキシルアルキル基、炭素数3~5のアルケニル基又は炭素数6~20のアリール基を表す。
R4~R8は、互いに結合して環構造を形成してもよい。)
メチル基、エチル基、ブチル基等の炭素数1~12のアルキル基;
シクロヘキシル基、シクロペンチル基等の炭素数5~8のシクロアルキル基;
フェニル基、トルイル基、ナフチル基等の炭素数6~20のアリール基;
ベンジル基、フェニルプロピル基等の炭素数7~20のアリールアルキル基;
ベンゾイル基、トルオイル基、ナフトイル基等の炭素数7~20のアリーロイル基;
アセチル基、プロピルカルボニル基等の炭素数2~12のアルカノイル基;
チオフェンカルボニル基、ピリジンカルボニル基等の炭素数3~20のヘテロアリーロイル基;
メトキシカルボニルエチルカルボニル基、エトキシカルボニルエチルカルボニル基等の炭素数3~20のアルコキシカルボニルアルカノイル基;
フェノキシカルボニルエチルカルボニル基等の炭素数8~20のアリールオキシカルボニルアルカノイル基;
チオフェンオキシカルボニルエチルカルボニル基等の炭素数5~20のヘテロアリールオキシカルボニルアルカノイル基;
メトキシカルボニル、エトキシカルボニル等の炭素数2~12のアルコキシカルボニル基;
フェノキシカルボニル基等の炭素数7~20のアリールオキシカルボニル基;
メチルチオ基、エチルチオ基等の-SR9;
メチルスルホキシ基等の-SOR9;
メチルジスルホキシ基等の-SO2R9;
又は、ジメチルアミノ基、モルホリノ基等の-NR10R11
等が挙げられ、かつ、R4、R5、R6、R7及びR8の少なくとも一つは、-SR9又は-NR10R11である。
なお、R4~R8は互いに結合して環構造を形成してもよい。例えば、R6が-NR10R11で表される基の場合、R10又はR11がR5又はR7と結合し、後述する一般式(IV)で表されるようなカルバゾール環を形成してもよい。
前記一般式(I)において、R2は、具体的には、それぞれ置換基を有していてもよい以下の各基である。
メチルチオ基、エチルチオ基、n-プロピルチオ基、イソプロピルチオ基、n-ブチルチオ基、n-ヘキシルチオ基、n-オクチルチオ基、n-ドデシルチオ基などの炭素数1~12のアルキルチオ基;
メトキシカルボニル基、エトキシカルボニル基、n-プロポキシカルボニル基、イソプロポキシカルボニル基、n-ブトキシカルボニル基、t-ブトキシカルボニル基、n-ペンチルオキシカルボニル基、t-アミルオキシカルボニル基、n-ヘキシルオキシカルボニル基、n-オクチルオキシカルボニル基、n-デカニルオキシカルボニル基、n-ドデカニルオキシカルボニル基などの炭素数2~12のアルコキシカルボニル基;
ビニルオキシカルボニル基、アリルオキシカルボニル基などの炭素数3~12のアルケニルオキシカルボニル基;
プロパルギルオキシカルボニル基などの炭素数3~12のアルキニルオキシカルボニル基;
フェニルオキシカルボニル基、1-ナフチルオキシカルボニル基、2-ナフチルオキシカルボニル基などの炭素数7~12のアリールオキシカルボニル基;
2-フラニルオキシカルボニル基、3-フラニルオキシカルボニル基、2-ピリジルオキシカルボニル基、3-ピリジルオキシカルボニル基、4-ピリジルオキシカルボニル基、2-ベンゾチアゾリルオキシカルボニル基などの炭素数3~12のヘテロアリールオキシカルボニル基;
メチルチオカルボニル基、エチルチオカルボニル基、n-プロピルチオカルボニル基、イソプロピルチオカルボニル基、n-ブチルチオカルボニル基、n-ヘキシルチオカルボニル基、n-オクチルチオカルボニル基、n-ドデシルチオカルボニル基などの炭素数2~12のアルキルチオカルボニル基;
ビニルチオカルボニル基、アリルチオカルボニル基などの炭素数3~12のアルケニルチオカルボニル基;
プロパギルチオカルボニル基などの炭素数3~12のアルキニルチオカルボニル基;
フェニルチオカルボニル基、1-ナフチルチオカルボニル基、2-ナフチルチオカルボニル基などの炭素数7~12のアリールチオカルボニル基;
2-フラニルチオカルボニル基、3-フラニルチオカルボニル基、4-ピリジルチオカルボニル基、2-ベンゾオキサゾリルチオカルボニル基、2-ベンゾチオアゾリルカルボニル基などの炭素数3~12のヘテロアリールチオカルボニル基;
メチルチオメトキシ基、メチルチオエトキシ基、エチルチオメトキシ基、エチルチオエトキシ基、メチルチオプロポキシ基、エチルチオプロポキシ基などの炭素数2~12のアルキルチオアルコキシ基;
-O-N=CR30R31、-N(OR30)-OCO-R31又は下記一般式(II)で表される基であって、R30およびR31が、置換基を有していてもよい炭素数1~12のアルキル基あるいは置換基を有していてもよい炭素数6~20のアリール基である基。
密着性や内部硬化性に優れた光重合性組成物により形成された画像(パターン)は、例えば、順テーパー(台形)状に形成されやすい、現像液等に侵食されにくい、剥離やかけが起こりにくい等の優れた性質を有する。従って、本発明のケトオキシムエステル系化合物を光重合開始剤として含有する光重合性組成物を用いれば、微細な画像を安定的に形成することができる。
また、上述した各基の炭素数は、それぞれ、アルキルチオ基は炭素数1~2、アルコキシカルボニル基は炭素数2~4、アリールオキシカルボニル基は炭素数7~9、ヘテロアリールオキシカルボニル基は炭素数3~7、ヘテロアリールチオカルボニル基は炭素数3~7、アルキルチオアルコキシ基は炭素数2~4であることが好ましい。
これらの各基は、組成物中の樹脂等との相互作用(水素結合力)が強いこと等から、前記したような、密着性や内部硬化性が高いという本発明の化合物の効果が特に強く得られるため好ましい。
本発明の化合物においては、Xが置換基を有していてもよい炭素数1~20のアルキレン基であり、R2が炭素数2~12のアルコキシカルボニル基又は炭素数1~12のアルキルチオ基であることが好ましい。それぞれの基の炭素数の好ましい範囲は、前記のとおりである。
前記一般式(I)において、R3は、それぞれ置換基を有していてもよい炭素数2~12のアルカノイル基、炭素数3~25のアルケノイル基、炭素数4~8のシクロアルカノイル基、炭素数7~20のアリーロイル基、炭素数3~20のヘテロアリーロイル基、炭素数2~10のアルコキシカルボニル基、炭素数7~20のアリールオキシカルボニル基、炭素数2~20のヘテロアリール基又は炭素数2~20のアルキルアミノカルボニル基である。
フッ素原子、塩素原子、臭素原子、ヨウ素原子などのハロゲン原子、水酸基、ニトロ基、シアノ基、任意の有機基などを挙げることができる。任意の有機基としては、例えば、以下のもの等が挙げられる。
メチル基、エチル基、n-プロピル基、イソプロピル基、n-ブチル基、イソブチル基、t-ブチル基、アミル基、t-アミル基、n-ヘキシル基、n-ヘプチル基、n-オクチル基、t-オクチル基等の炭素数1~18の直鎖又は分岐のアルキル基;
シクロプロピル基、シクロブチル基、シクロペンチル基、シクロヘキシル基、アダマンチル基等の炭素数3~18のシクロアルキル基;
ビニル基、プロペニル基、ヘキセニル基等の炭素数2~18の直鎖又は分岐のアルケニル基;
シクロペンテニル基、シクロヘキセニル基等の炭素数3~18のシクロアルケニル基;
メトキシ基、エトキシ基、n-プロポキシ基、イソプロポキシ基、n-ブトキシ基、s-ブトキシ基、t-ブトキシ基、n-アミルオキシ基、t-アミルオキシ基、n-ヘキシルオキシ基、n-ヘプチルオキシ基、n-オクチルオキシ基、t-オクチルオキシ基等の炭素数1~18の直鎖又は分岐のアルコキシ基;
メチルチオ基、エチルチオ基、n-プロピルチオ基、イソプロピルチオ基、n-ブチルチオ基、s-ブチルチオ基、t-ブチルチオ基、n-アミルチオ基、t-アミルチオ基、n-ヘキシルチオ基、n-ヘプチルチオ基、n-オクチルチオ基、t-オクチルチオ基等の炭素数1~18の直鎖又は分岐のアルキルチオ基;
フェニル基、トリル基、キシリル基、メシチル基等の、アルキル基で置換されていてもよい炭素数6~18のアリール基;
ベンジル基、フェネチル基等の炭素数7~18のアラルキル基;
ビニルオキシ基、プロペニルオキシ基、ヘキセニルオキシ基等の炭素数2~18の直鎖又は分岐のアルケニルオキシ基;
ビニルチオ基、プロペニルチオ基、ヘキセニルチオ基等の炭素数2~18の直鎖又は分岐のアルケニルチオ基;
-COR12で表されるアシル基;
カルボキシル基;
-OCOR13で表されるアシルオキシ基;
-NR14R15で表されるアミノ基;
-NHCOR16で表されるアシルアミノ基;
-NHCOOR17で表されるカーバメート基;
-CONR18R19で表されるカルバモイル基;
-COOR20で表されるカルボン酸エステル基;
-SO3NR21R22で表されるスルファモイル基;
-SO3R23で表されるスルホン酸エステル基;
2-チエニル基、2-ピリジル基、フリル基、オキサゾリル基、ベンゾキサゾリル基、チアゾリル基、ベンゾチアゾリル基、モルホリノ基、ピロリジニル基、テトラヒドロチオフェンジオキサイド基等の飽和もしくは不飽和の芳香族複素環基;
トリメチルシリル基などのトリアルキルシリル基。
上記置換基群Zから選ばれる各置換基の位置関係は特に限定されず、複数の置換基を有する場合、同種でも異なっていてもよい。
本発明のケトオキシムエステル系化合物の具体的な製造方法については、後述する実施例において詳細を述べるが、例えば、前記一般式(I)におけるR1を構成し得る芳香環化合物あるいはヘテロ芳香環化合物に、フリーデルクラフツ反応などで前記一般式(I)におけるX及びR2を有するアルカノイル基を導入する。得られた化合物に、Organic Reaction(1953), 7, 327に記載の方法などによりケトオキシム基を形成し、さらにこれを前記一般式(I)におけるR3を構成し得る化合物とのエステル化反応に供することにより、合成することができる。
本発明のケトオキシムエステル系化合物は、光重合開始剤として好適に使用することができる。その詳細については後述する。
本発明の光重合開始剤は、前記本発明のケトオキシムエステル系化合物からなることを特徴とする。
本発明の光重合開始剤は、通常、後述する光重合性組成物の一成分として用いられ、エチレン性不飽和基含有化合物のエチレン性不飽和基を重合させる働きを有する。
次に、本発明の光重合性組成物(以下、「レジスト」と称することがある。)について説明する。
また、その他に(C)アルカリ可溶性樹脂、(D)界面活性剤、(E)溶剤、(F)色材、(G)その他成分等を適宜組み合わせて含有させることができる。
以下、これらの各配合成分について説明する。
(A)エチレン性不飽和基含有化合物
本発明の組成物で用いられるエチレン性不飽和基含有化合物としては、エチレン性不飽和基を一個以上有する化合物が使用される。具体的には、脂肪族(ポリ)ヒドロキシ化合物と不飽和カルボン酸とのエステル、芳香族(ポリ)ヒドロキシ化合物と不飽和カルボン酸とのエステル、不飽和カルボン酸と多価カルボン酸と脂肪族ポリヒドロキシ化合物により得られるエステル、芳香族ポリヒドロキシ化合物のエチレンオキシド、プロピレンオキシド付加物と不飽和カルボン酸とのエステル化反応物、脂肪族ポリヒドロキシ化合物のエチレンオキシド、カプロラクトン変性多価アルコールと不飽和カルボン酸とのエステル、多価アルコールと多価イソシアナートと不飽和カルボン酸との反応物、スチリル末端化合物、含リン酸不飽和化合物、ポリエポキシと不飽和カルボン酸との付加物等が挙げられる。
また、例えば、BM用やカラーフィルターの画素形成用の組成物として用いる場合には、硬化性の点から、脂肪族ポリヒドロキシ化合物と不飽和カルボン酸とのエステルを用いることが好ましい。
本発明の光重合性組成物は、(B)光重合開始剤が前記本発明のケトオキシムエステル系化合物を含有することを特徴とする。
本発明の光重合性組成物において用いられる(B)光重合開始剤としては、前記一般式(I)で表される本発明のケトオキシムエステル系化合物の1種のみを使用してもよく、2種以上を併用してもよい。
例えば、2-(4-メトキシフェニル)-4,6-ビス(トリクロロメチル)-s-トリアジン、2-(4-メトキシナフチル)-4,6-ビス(トリクロロメチル)-s-トリアジン、2-(4-エトキシナフチル)-4,6-ビス(トリクロロメチル)-s-トリアジン、2-(4-エトキシカルボニルナフチル)-4,6-ビス(トリクロロメチル)-s-トリアジン等のハロメチル化トリアジン誘導体、2-トリクロロメチル-5-(2’-ベンゾフリル)-1,3,4-オキサジアゾール、2-トリクロロメチル-5-〔β-(2’-ベンゾフリル)ビニル〕-1,3,4-オキサジアゾール、2-トリクロロメチル-5-〔β-(2’-(6”-ベンゾフリル)ビニル)〕-1,3,4-オキサジアゾール、2-トリクロロメチル-5-フリル-1,3,4-オキサジアゾール等のハロメチル化オキサジアゾール誘導体、2-(2’-クロロフェニル)-4,5-ジフェニルイミダゾール2量体、2-(2’-クロロフェニル)-4,5-ビス(3’-メトキシフェニル)イミダゾール2量体、2-(2’-フルオロフェニル)-4,5-ジフェニルイミダゾール2量体、2-(2’-メトキシフェニル)-4,5-ジフェニルイミダゾール2量体、(4’-メトキシフェニル)-4,5-ジフェニルイミダゾール2量体等のイミダゾール誘導体、ベンゾインメチルエーテル、ベンゾインフェニルエーテル、ベンゾインイソブチルエーテル、ベンゾインイソプロピルエーテル等のベンゾインアルキルエーテル類、2-メチルアントラキノン、2-エチルアントラキノン、2-t-ブチルアントラキノン、1-クロロアントラキノン等のアントラキノン誘導体、ベンズアンスロン誘導体、ベンゾフェノン、ミヒラーケトン、2-メチルベンゾフェノン、3-メチルベンゾフェノン、4-メチルベンゾフェノン、2-クロロベンゾフェノン、4-ブロモベンゾフェノン、2-カルボキシベンゾフェノン等のベンゾフェノン誘導体、2,2-ジメトキシ-2-フェニルアセトフェノン、2,2-ジエトキシアセトフェノン、1-ヒドロキシシクロヘキシルフェニルケトン、α-ヒドロキシ-2-メチルフェニルプロパノン、1-ヒドロキシ-1-メチルエチル-(p-イソプロピルフェニル)ケトン、1-ヒドロキシ-1-(p-ドデシルフェニル)ケトン、2-メチル-(4’-(メチルチオ)フェニル)-2-モルホリノ-1-プロパノン、1,1,1-トリクロロメチル-(p-ブチルフェニル)ケトン等のアセトフェノン誘導体、チオキサントン、2-エチルチオキサントン、2-イソプロピルチオキサントン、2-クロロチオキサントン、2,4-ジメチルチオキサントン、2,4-ジエチルチオキサントン、2,4-ジイソプロピルチオキサントン等のチオキサントン誘導体、p-ジメチルアミノ安息香酸エチル、p-ジエチルアミノ安息香酸エチル等の安息香酸エステル誘導体、9-フェニルアクリジン、9-(p-メトキシフェニル)アクリジン等のアクリジン誘導体、9,10-ジメチルベンズフェナジン等のフェナジン誘導体、ビス-シクロペンタジエニル-Ti-ジクロライド、ビス-シクロペンタジエニル-Ti-ビス-フェニル、ビス-シクロペンタジエニル-Ti-ビス-(2,3,4,5,6-ペンタフルオロフェニ-1-イル)、ビス-シクロペンタジエニル-Ti-ビス-(2,3,5,6-テトラフルオロフェニ-1-イル)、ビス-シクロペンタジエニル-Ti-ビス-(2,4,6-トリフルオロフェニ-1-イル)、ビス-シクロペンタジエニル-Ti-2,6-ジ-フルオロフェニ-1-イル、ビス-シクロペンタジエニル-Ti-2,4-ジ-フルオロフェニ-1-イル、ビス-メチルシクロペンタジエニル-Ti-ビス-(2,3,4,5,6-ペンタフルオロフェニ-1-イル)、ビス-メチルシクロペンタジエニル-Ti-ビス-(2,6-ジ-フルオロフェニ-1-イル)、ビス-シクロペンタジエニル-Ti-2,6-ジ-フルオロ-3-(ピル-1-イル)-フェニ-1-イル等のチタノセン誘導体等が挙げられる。
更には、特開2000-80068号公報、特表平2004-534797に記載されているオキシム系開始剤も特に好適に使用できる。
本発明の光重合性組成物は、アルカリ可溶性樹脂を含有していてもよい。本発明の光重合性組成物において使用されるアルカリ可溶性樹脂としては、アルカリ性の溶媒に可溶な樹脂であれば特に限定されないが、カルボキシル基又は水酸基を含む樹脂であることが好適である。
上記エポキシアクリレート樹脂は、エポキシ樹脂(a)に、α,β-不飽和モノカルボン酸及び/又はエステル部分にカルボキシル基を有するα,β-不飽和モノカルボン酸エステル(b)を付加させ、さらに、多塩基酸無水物(c)を反応させることにより合成される。かかる反応生成物は化学構造上、実質的にエポキシ基を有さず、かつ「アクリレート」に限定されるものではないが、エポキシ樹脂が原料であり、かつ「アクリレート」が代表例であるので、慣用に従いこのように命名したものである。
カルボキシル基含有ビニル系樹脂としては、例えば、不飽和カルボン酸とビニル化合物との共重合体等が挙げられる。不飽和カルボン酸としては、例えば(メタ)アクリル酸、クロトン酸、イソクロトン酸、マレイン酸、無水マレイン酸、イタコン酸、シトラコン酸等が挙げられる。これらは1種を単独で用いてもよく、2種以上を混合して用いてもよい。
本発明の光重合性組成物は、該組成物の塗布液としての塗布性、及び光重合性組成物層の現像性の向上等を目的として、ノニオン性、アニオン性、カチオン性、両性界面活性剤、或いは、フッ素系やシリコーン系等の界面活性剤を含有していてもよい。
本発明の光重合性組成物は、通常、(A)エチレン性不飽和基含有化合物、(B)光重合開始剤と、必要に応じて配合される(C)アルカリ可溶性樹脂、(D)界面活性剤や後述する(F)色材及びその他の任意成分を(E)溶剤に溶解又は分散した状態で使用される。
本発明の光重合性組成物において色材は必須の成分ではないが、画素及びBM用途等の多くの用途において色材を組合わせて利用する。ここで、色材とは、光重合性組成物を着色する成分をいう。
(G-1)顔料分散剤
本発明の組成物において(F)色材として顔料等を含有する場合、色材を微細に分散し、且つ、その分散状態を安定化させることが品質安定上重要なため顔料分散剤を配合するのが望ましい。
本発明の光重合性組成物を層間絶縁膜として用いる場合、熱硬化後の膜の耐熱性及び耐薬品性を向上させる目的で、熱架橋剤を含有していてもよい。熱架橋剤としては、露光・現像による画像形成後のハードベークにより、架橋反応をするものであれば、公知のものを用いることができる。具体的には、下記のものが挙げられ、これらは1種を単独で用いてもよく、2種以上を混合して用いてもよい。
本実施の形態に使用される、分子内にエポキシ基を有する化合物としては、例えば、モノヒドロキシ化合物あるいはポリヒドロキシ化合物とエピクロルヒドリンとを反応させて得られる(ポリ)グリシジルエーテル化合物、(ポリ)カルボン酸化合物とエピクロルヒドリンとを反応させて得られるポリグリシジルエステル化合物、及び(ポリ)アミン化合物とエピクロルヒドリンを反応させて得られる(ポリ)グリシジルアミン化合物等の、低分子から高分子にわたる化合物が挙げられる。
ポリグリシジルエーテル化合物としては、例えば、ポリエチレングリコールのジグリシジルエーテル型エポキシ、ビス(4-ヒドロキシフェニル)のジグリシジルエーテル型エポキシ、ビス(3,5-ジメチル-4-ヒドロキシフェニル)のジグリシジルエーテル型エポキシ、ビスフェノールFのジグリシジルエーテル型エポキシ、ビスフェノールAのジグリシジルエーテル型エポキシ、テトラメチルビスフェノールAのジグリシジルエーテル型エポキシ、エチレンオキシド付加ビスフェノールAのジグリシジルエーテル型エポキシ、ジハイドロオキシルフルオレン型エポキシ、ジハイドロオキシルアルキレンオキシルフルオレン型エポキシ、ビスフェノールA/アルデヒドノボラック型エポキシ、フェノールノボラック型エポキシ、クレゾールノボラック型エポキシが挙げられる。
ポリグリシジルエステル化合物としては、例えば、ヘキサヒドロフタル酸のジグリシジルエステル型エポキシ、フタル酸のジグリシジルエステル型エポキシ等が挙げられる。
ポリグリシジルアミン化合物としては、例えば、ビス(4-アミノフェニル)メタンのジグリシジルアミン型エポキシ、イソシアヌル酸のトリグリシジルアミン型エポキシ等が、それぞれ挙げられる。
また、その他の例として、例えば、(メタ)アクリル酸グリシジル、α-エチルアクリル酸グリシジル、α-n-プロピルアクリル酸グリシジル、α-n-ブチルアクリル酸グリシジル、(メタ)アクリル酸-3,4-エポキシブチル、(メタ)アクリル酸-4,5-エポキシペンチル、(メタ)アクリル酸-6,7-エポキシヘプチル、α-エチルアクリル酸-6,7-エポキシヘプチル等のエポキシ基を有する(メタ)アクリレート等を1種単独又は2種以上の組み合わせで反応させた重合体が挙げられる。あるいは、エポキシ基を有する(メタ)アクリレート構成単位に他の共重合用単量体を通常10~70モル%、好ましくは15~60モル%含有させた重合体が挙げられる。
含窒素熱架橋性化合物としては、メラミン、ベンゾグアナミン、グリコールウリル、若しくは尿素にホルマリンを作用させた化合物、又はそれらのアルキル変性化合物を挙げることができる。
本発明の光重合性組成物には、基板との密着性を向上させる目的で、接着助剤を配合することができる。接着助剤としては、例えば、シランカップリング剤を挙げることができる。より具体的には、例えば、トリメトキシシリル安息香酸、γ-メタクリロキシプロピルトリメトキシシラン、ビニルトリアセトキシシラン、ビニルトリメトキシシラン、γ-グシリドキシプロピルトリメトキシシラン、γ-イソシアナトプロピルトリエトキシシラン、β-(3,4-エポキシシクロヘキシル)エチルトリメトキシシランなどが挙げられる。これらのシランカップリング剤は、1種単独でも2種以上混合して用いてもよい。
本発明の光重合性組成物が熱架橋剤(G-2)を含有する場合、硬化条件における時間の短縮や設定温度の変更のためさらに硬化剤を含有し、各々の素子の製造プロセスにより異なる硬化条件を適正に選択することができる。
安息香酸系化合物としては、安息香酸、安息香酸のベンゼン環上の2位から6位の位置に水酸基、ハロゲン原子、アルキル基、アシル基、アシルオキシル基、アルコキシル基、アリール基、アリル基等の置換基を有するものを挙げることができる。中でも、エポキシに対する硬化能力の高い水酸基を置換基として有するものが好ましく、特には水酸基を2つ以上有するものが好ましい。このような安息香酸系化合物としては、例えば、3,4,5-トリヒドロキシ安息香酸、2,5-ジヒドロキシ安息香酸、2,6-ジヒドロキシ安息香酸、3,4-ジヒドロキシ安息香酸、2,4,6-トリヒドロキシ安息香酸等が挙げられる。
多価カルボン酸(無水物)としては、例えば、無水メチルハイミック酸、ヘキサヒドロ無水フタル酸、テトラヒドロ無水フタル酸、トリアルキルテトラヒドロ無水フタル酸、メチルシクロヘキセンジカルボン酸無水物等の脂環式多価カルボン酸(無水物);無水フタル酸、無水トリメリット酸、無水ピロメリット酸、ベンゾフェノントリカルボン酸無水物、ベンゾフェノンテトラカルボン酸無水物等の芳香族多価カルボン酸無水物;コハク酸、トリメリット酸、マレイン酸、シクロペンタンテトラカルボン酸等の脂環式酸無水物;芳香族酸無水物の加水分解物等が挙げられる。これらの中でも、トリメリット酸(無水物)、無水フタル酸が好ましい。
多価カルボン酸(無水物)を含有する重合体としては、(無水)マレイン酸等の(無水)多価カルボン酸と、エチレン性不飽和結合を分子内に1個以上有する化合物との重合体や、そのような重合体中の多価カルボン酸(無水物)部分の部分ハーフエステル変成重合体、等が挙げられる。
熱酸発生剤としては、例えば、芳香族ジアゾニウム塩、ジアリールヨードニウム塩、モノフェニルスルフォニウム塩、トリアリルスルフォニウム塩、トリアリルセレニウム塩等の各種オニウム塩系化合物、スルフォン酸エステル、ハロゲン化合物等が挙げられる。具体例として、クロロベンゼンジアゾニウムヘキサフルオロフォスフェイト、ジメチルアミノベンゼンジアゾニウムヘキサフルオロアンチモネート、ナフチルジアゾニウムヘキサフルオロフォスフェイト、ジメチルアミノナフチルジアゾニウムテトラフルオロボレート等の芳香族ジアゾニウム塩が挙げられる。
アミン化合物としては、例えば、エチレジアミン、1,3-ジアミノプロパン、1,4-ジアミノブタン、ヘキサメチレンジアミン、2,5-ジメチルヘキサメチレンジアミン、ピペリジン、ピロリジン、トリエチレンジアミン、トリメチルヘキサメチレンジアミン、ジメチルシクロヘキシルアミン、テトラメチルグアニジン、トリエタノールアミン、N,N’-ジメチルピペラジン、ジシアンアミド、又はその誘導体;DBU(1,8-ジアザビスシクロ(5,4,0)ウンデセン-1),DBU系テトラフェニルボレート塩等の脂肪族アミン(第1、第2、第3);メタフェニレンジアミン、ジアミノジフェニルメタン、ジアミノジフェニルスルホン、ジアミノジエチルジフェニルメタン、ベンジルジメチルアミン、ジメチルアミノ-p-クレゾール、2-(ジメチルアミノメチル)フェノール、2,4,6-トリス(ジメチルアミノメチル)フェノール、ピリジン、ピコリン、DBU(1,8-ジアザビスシクロ(5,4,0)ウンデセン-1)、2,4,6-トリス(ジメチルアミノメチル)フェノールのトリ-2-エチルヘキシル酸塩等の芳香族アミン(第1、第2、第3);2-メチルイミダゾール、2-エチル-4-メチルイミダゾール、2-エチル-4-メチルイミダゾール、2-ウンデシルイミダゾール、2-ヘプタデシルイミダゾール、2-フェニルイミダゾール、1-ベンジル-2-メチルイミダゾール、1-シアノエチル-2-メチルイミダゾール、1-シアノエチル-2-エチル-4-メチルイミダゾール、1-シアノエチル-2-ウンデシルイミダゾール、1-シアノエチル-2-ウンデシルイミダゾリウム・トリメリテート、2-メチルイミダゾリウム・イソシアヌレート、2-フェニルイミダゾリウム・イソシアヌレート、2,4-ジアミノ-6-[2-メチルイミダゾリル-(1)]-エチル-S-トリアジン、2,4-ジアミノ-6-[2-エチルイミダゾリル-(1)]-エチル-S-トリアジン、2,4-ジアミノ-6-[2-ウンデシルイミダゾリル-(1)]-エチル-S-トリアジン、2-フェニル-4,5-ジヒドキシメチルイミダゾール、2-フェニル-4-メチル-5-ヒドロキシメチルイミダゾール、1-シアノエチル-2-フェニル-4,5-ジ(シアノエトキシメチル)イミダゾール等のイミダゾール化合物;ジエチレントリアミン、イミノビスプロピルアミン、ビス(ヘキサメチレン)トリアミン等が挙げられる。
ポリアミン化合物としては、例えば、トリエチルテトラミン、テトラエチレンペンタミン、ペンタエチレンヘキサミン、ジメチルアミノプロピルアミン、ジエチルアミノプロピルアミン、N-アミノエチルピペラジン、メンセンジアミン、イソフルオロジアミン、ビス(4-アミノ-3-メチルシクロヘキシル)メタン、ジアミノジシクロヘキシルアミン、N,N-ジメチルシクロヘキシルアミン等の脂肪族ポリアミン、m-キシレンジアミン、キシリレンジアミン、キシリレンジアミン誘導体、キシリレンジアミン三量体等の芳香族ポリアミンが挙げられる。これらの中でも、N,N-ジメチルシクロヘキシルアミンが好ましい。
ブロックカルボン酸としては、例えば、前記(多価)カルボン酸及びそれらを含有する重合体のカルボン酸に、特開平4-218561号公報、特開2003-66223号公報、特開2004-339332号公報、特開2004-339333号公報などに記載の方法によりビニルエーテルを付加させたブロックカルボン酸等が挙げられる。
本発明の光重合性組成物には、例えば、置換基を有していてもよいo-ハイドロキシベンゾフェノン、ハイドロキノン、p-メトキシフェノール、2,6-ジ-t-ブチル-p-クレゾール等の熱重合防止剤を配合することができる。これら化合物の配合割合としては、全固形分に対して、通常10質量%以下、好ましくは2質量%以下である。
本発明の光重合性組成物には、ジオクチルフタレート、ジドデシルフタレート、トリクレジルホスフェート等の可塑剤を、全固形分に対して、40質量%以下、好ましくは20質量%以下の割合で含有していてもよい。
更に、本発明の光重合性組成物には、必要に応じて、重合加速剤を添加することもできる。重合加速剤として具体的には、例えば、N-フェニルグリシンなどのアミノ酸のエステル又はその双極イオン化合物、2-メルカプトベンゾチアゾール、2-メルカプトベンゾイミダゾール、2-メルカプトベンゾオキサゾール、3-メルカプト-1,2,4-トリアゾール、2-メルカプト-4(3H)-キナゾリン、β-メルカプトナフタレン、エチレングリコールジチオプロピオネート、トリメチロールプロパントリスチオプロピオネート、ペンタエリスリトールテトラキスチオプロピオネート等のメルカプト基含有化合物類、ヘキサンジチオール、トリメチロールプロパントリスチオグリコネート、ペンタエリスリトールテトラキスチオプロピオネート等の多官能チオール化合物類、N,N-ジアルキルアミノ安息香酸エステル、N-フェニルグリシン又はそのアンモニウム塩やナトリウム塩等の誘導体、フェニルアラニン、又はそのアンモニウムやナトリウム塩等の塩、エステル等の誘導体等の芳香族環を有するアミノ酸又はその誘導体類等が挙げられる。
更に、本発明の光重合性組成物には、必要に応じて、紫外線吸収剤を添加することもできる。紫外線吸収剤は、露光に用いられる光源の特定の波長を該紫外線吸収剤によって吸収させることにより、基板上に形成した本発明の光重合性組成物の膜を露光したときの光硬化速度を制御する目的で添加されるものである。紫外線吸収剤の添加により、露光・現像後のパターン形状を改善したり、現像後に非露光部に残る残渣をなくしたりするなどの効果が得られる。
本発明の光重合性組成物は、それ自体公知の常法に従って製造される。以下に、画素又はBM用組成物のように(F)色材を含有する光重合性組成物を製造する場合を例に挙げて説明する。なお、層間絶縁膜、フォトスペーサー、リブ(液晶配向制御突起)等の色材を含まない用途に用いられる光重合性組成物を製造する場合には、(A)エチレン性不飽和基含有化合物、(B)光重合開始剤、(C)アルカリ可溶性樹脂、(E)溶剤、必要に応じて前記(G)他の成分などを混合し、均一な分散溶液とすればよい。
まず、(F)色材、(E)溶剤と、必要に応じて(G-1)顔料分散剤とを各所定量秤量し、分散処理工程において、色材を分散させて顔料分散液(インク状液体)とする。この分散処理工程では、ペイントコンディショナー、サンドグラインダー、ボールミル、ロールミル、ストーンミル、ジェットミル、ホモジナイザーなどを使用することができる。この分散処理を行うことによって色材が微粒子化されるため、光重合性組成物の塗布特性が向上し、製品のカラーフィルター基板の透過率が向上する。
本発明の光重合性組成物は、例えば、液晶表示装置等の各種部材を製造するための画像形成用途等に好適に用いられる。以下、これらについてさらに具体的に説明する。
本発明の光重合性組成物を用いた層間絶縁膜の形成方法について説明する。
{1}塗工工程
まず、基板上に、上述した本実施の形態の光重合性組成物をスピナー、ワイヤーバー、フローコーター、ダイコーター、ロールコーター、スプレー等の塗布装置を用いて塗布する。光重合性組成物の塗布膜厚は通常0.5~5μmである。
上記塗布膜から揮発成分を除去(乾燥)して乾燥塗膜を形成する。乾燥には、真空乾燥、ホットプレート、IRオーブン、コンベクションオーブン等を用いることができる。好ましい乾燥条件は温度40~150℃、乾燥時間10秒~60分の範囲である。
次いで、光重合性組成物層の乾燥塗膜上にフォトマスクを置き、該フォトマスクを介して画像露光する。露光後、未露光の未硬化部分を現像にて除去することにより、画像を形成する。なお、露光後、現像前に感度向上の目的でポスト・エクスポージャ・ベークを行う場合もある。この場合のベークには、ホットプレート、IRオーブン、コンベクションオーブン等を用いることができる。ポスト・エクスポージャ・ベーク条件は通常、40~150℃、乾燥時間10秒~60分の範囲である。
露光・現像工程により画像形成された光重合性組成物膜は、次いで、熱処理(ハードベーク)工程を経て硬化物(熱硬化膜)となる。なお、現像後、ハードベーク前にハードベーク時のアウトガスの発生を抑制する目的で、全面露光を行う場合もある。
次に、本発明の光重合性組成物を用いたカラーフィルターの製造方法について説明する。なお、以下には画素及びブラックマトリックスの形成に用いられる場合を例に挙げるが、本発明の光重合性組成物はカラーフィルターにおける画素及びブラックマトリックスのみならず、液晶表示装置におけるフォトスペーサーやリブ(液晶配向制御突起)等の形成に使用することもできる。
ここで用いる透明基板は、カラーフィルター用の透明基板であり、その材質は特に限定されるものではないが、例えば、ポリエチレンテレフタレート等のポリエステルやポリプロピレン、ポリエチレン等のポリオレフィン等、ポリカーボネート、ポリメチルメタクリレート、ポリスルホン等の熱可塑性プラスチックシート、エポキシ樹脂、ポリエステル樹脂、ポリ(メタ)アクリル樹脂等の熱硬化性プラスチックシート、或いは各種ガラス板等を挙げることができる。特に、耐熱性の点からガラス板、耐熱性プラスチックシートが好ましく用いられる。このような透明基板には、表面の接着性等の物性を改良するために、予め、コロナ放電処理、オゾン処理、シランカップリング剤やウレタンポリマー等の各種ポリマーの薄膜処理等を行うこともできる。
透明基板への光重合性組成物の塗布方法は特に限定されないが、通常、スピナー、ワイヤーバー、フローコーター、ダイコーター、ロールコーター、スプレー等の塗布装置を用いて行われる。塗布後の乾燥においてはホットプレート、IRオーブン、コンベクションオーブン等を用いることができ、好ましい乾燥条件は40~150℃、乾燥時間は10秒~60分の範囲である。塗布、乾燥後の樹脂BMの膜厚は、0.1~2μm、好ましくは0.1~1.5μm、さらに好ましくは0.1~1μmの範囲とするのがよい。なお、本発明の光重合性組成物により形成される樹脂BMは、遮光性の点から膜厚1μmにおいて、光学濃度が3.0以上であるのが好ましい。また、顔料等の固型分の分散状態の指標として、BMの20度光沢値が100~200であるのが有利である。
露光に用いる光源は、例えば、キセノンランプ、ハロゲンランプ、タングステンランプ、高圧水銀灯、超高圧水銀灯、メタルハライドランプ、中圧水銀灯、低圧水銀灯等のランプ光源やアルゴンイオンレーザー、YAGレーザー、エキシマーレーザー、窒素レーザー等のレーザー光源等が挙げられる。特定の照射光の波長のみを使用する場合には光学フィルターを利用することもできる。
上記のとおり光重合性組成物の塗布、乾燥、露光、現像をBM及びRGB3色について各々繰り返して行って、カラーフィルターを作製する。本発明の光重合性組成物はこのようにBMの形成にもRGB3色の画素形成にも用いることができる。
本発明の光重合性組成物は、上述のような層間絶縁膜、カラーフィルターのBMやRGB3色の画素以外に、フォトスペーサーやリブ(液晶配向制御突起)等の形成にも用いることができる。以下、この使用形態について説明する。
フォトスペーサーは、本発明の光重合性組成物を基板に塗布、乾燥、露光、現像、熱硬化処理することにより形成される。フォトスペーサーの形成にあたり、本発明の光重合性組成物は、基板に塗布される。塗布方法としては、従来公知の方法、例えば、スピナー法、ワイヤーバー法、フローコート法、ダイコート法、ロールコート法、スプレーコート法などによって行うことができる。中でも、ダイコート法によれば、塗布液(光重合性組成物)の使用量が大幅に削減され、かつ、スピンコート法による塗布の際に付着するミストなどの影響が全くない、異物発生が抑制されるなど、総合的な観点から好ましい。
なお、上述以外の塗布方法としては、例えば、インクジェット法や印刷法などにより、本発明の光重合性組成物を基板上にパターン状に供給してもよい。
リブ(液晶配向制御突起)とは、液晶表示装置の視野角を改善するために、透明電極上に形成する突起をいい、前記突起のスロープを利用して液晶を局所的に傾け、一画素内で液晶を多方向に配向させるものである。
本発明の光重合性組成物によりリブを形成するには、まず、カラーフィルター上にITOを蒸着してなる通常0.1~2mm厚の透明基板上に、本発明の光重合性組成物をスピナー、ワイヤーバー、フローコーター、ダイコーター、ロールコーター、スプレー等の塗布装置を用いて塗布する。組成物の塗布膜厚は通常0.5~5μmである。該組成物からなる塗布膜を乾燥した後、乾燥塗膜上にフォトマスクを置き、該フォトマスクを介して画像露光する。露光後、未露光(未硬化)部分を現像にて除去することにより、画像を形成する。通常、現像後得られる画像は、5~20μmの巾の細線再現性が求められ、高画質のディスプレイの要求からより高精細な細線再現性が要求される傾向にある。高精細な細線を安定し再現する上で、現像後の細線画像の断面形状は、非画像部と画像部のコントラストが明瞭な矩形型が好ましい。矩形型にすることにより、現像時間、現像液経時、現像シャワーの物理刺激などの現像マージンが広くなるため好ましい。
また、本発明の光重合性組成物は、高さや形状の異なる硬化物を同一材料で同時に形成する方法(一括形成法)にも用いることができる。
<モノケトン体の製造>
エチルカルバゾール(5g、25.61mmol)とo-ナフトイルクロリド(5.13g、26.89mmol)を30mlのジクロロメタンに溶解し、氷水バスにて2℃に冷却して攪拌し、塩化アルミニウム(3.41g、25.61mmol)を添加した。さらに室温にて3時間攪拌した。反応液を氷水200mlにあけ、ジクロロメタン200mlを添加し有機層を分液した。回収した有機層を硫酸マグネシウムで乾燥後、エバポレートし、白色固体(10g)を得た。反応式は下記の通りである。
モノケトン体(7.05g、22.34mmol)と3-メチルチオプロピオン酸クロリド(3.77g、21.06mmol)を100mlのジクロロメタンに溶解し、氷水バスにて2℃に冷却して攪拌し、塩化アルミニウム(6.30g、40.21mmol)を添加した。さらに室温にて3.5時間攪拌した。反応液を氷水500mlにあけ、ジクロロメタン200mlを添加し有機層を分液した。回収した有機層を硫酸マグネシウムで乾燥後、エバポレートし濃縮した。得られたオイルを酢酸エチル/n-ヘキサン(重量比1/1)で再結晶し、白色固体9.8gを得た。反応式は下記の通りである。
ジケトン体(5.80g、13.96mmol)を50mlのジクロロメタンに溶解し、-5℃に冷却して攪拌し、亜硝酸イソアミル(2.13g、18.14mmol)を添加した。さらに-13℃に冷却し、トリメチルシリルクロリド(1.97g、18.14mmol)を滴下した。滴下終了後、室温まで1時間かけて昇温した。反応液をエバポレートし濃縮した。残渣を酢酸エチル/n-ヘキサン=2/1(重量比)の混合溶媒を使用してカラムで精製して淡黄色結晶2.3gを得た。反応式は下記の通りである。
ケトオキシム体(1.2g、2.70mmol)とアセチルクロリド(0.64g、8.10mmol)をジクロロメタン50gに溶解して氷冷し、トリエチルアミン(0.82g、8.10mmol)を滴下して、さらに室温で4時間反応した。薄層クロマトグラフィーにより原料の消失を確認した後、水を入れて有機層を分液し、飽和NH4Cl水溶液で2回、5%Na2CO3水溶液で3回洗浄後、飽和食塩水で2回洗浄し、硫酸ナトリウムで乾燥し、エバポレートした。残渣を酢酸エチル/n-ヘキサン=2/1(重量比)の混合溶媒を使用してカラムで精製して1.0gの白色結晶として下記ケトオキシムエステル系化合物I-1を得た。
1H-NMR δ[ppm]
1.50(t,3H),1.55(s,3H),2.30(s,3H),2.37(t,2H),3.78(s,2H),4.45(q,2H),7.3-7.6(m,6H),8.18(dd,1H),8.37(dd,1H),8.60(d,1H),8.90(d,1H)
また、反応式は下記の通りである。
<ジケトン体の製造>
上記実施例1のモノケトン体(10g、31.91mmol)とエチルグルタリルクロリド(5.84g、32.71mmol)、塩化アルミニウム(13.62g、102.11mmol)から実施例1と同様にして白色固体12.4gを得た。反応式は下記の通りである。
ジケトン体(3.82g、8.61mmol)、亜硝酸イソアミル(1.36g、11.62mmol)、トリメチルシリルクロリド(3.12g、27.72mmol)から実施例1と同様にして淡黄色結晶2.0gを得た。反応式は下記の通りである。
ケトオキシム体(5.0g、10.32mmol)、アセチルクロリド(1.62g、20.64mmol)、トリエチルアミン(2.09g、20.64mmol)から実施例1と同様にして1.6gの白色結晶として下記ケトオキシムエステル系化合物I-2を得た。
1H-NMR δ[ppm]
1.17(t,3H),1.45(t,3H),2.30(s,3H),2.37(s,3H),2.75(t,2H),3.15(t,2H),4.15(q,2H),4.38(q,2H),7.3-7.5(m,6H),8.18(dd,1H),8.37(dd,1H),8.60(d,1H),8.82(d,1H)
また、反応式は下記の通りである。
前記実施例2おけるジケトン体の製造において、エチルグルタリルクロリドをメチルグルタリルクロリドに変更した以外は同様にして、下記のケトオキシムエステル系化合物I-8を製造した。得られた化合物のNMRシフト値は次の通りであった。
1H-NMR δ[ppm]
1.49(t,3H),2.29(s,3H),2.36(s,3H),2.73(t,2H),3.14(t,2H),3.60(s,3H),4.43(q,2H),7.3~r7.5(m,6H),8.06(dd,1H),8.29(dd,1H),8.59(d,1H),8.83(dd,1H)
<ジケトン体の製造>
窒素雰囲気下、1L四つ口フラスコにケトン体 10.48g(30.0mmol)、エチルグルタリルクロリド 5.35g(30.0mmol)、塩化メチレン400mlを加えた。反応溶液を0℃に冷却した後、塩化アルミニウム 12.0g(90.0mmol)を30分かけてゆっくり添加した。
添加終了後、更に3℃で2時間攪拌し、反応溶液を氷水600mlに少しずつ投入した。有機層を水、5%炭酸ナトリウム水溶液、飽和塩化ナトリウム水溶液で順に洗浄し、硫酸マグネシウムを加えて乾燥した。硫酸マグネシウムをろ過してエバポレーターにより溶媒を濃縮し、目的物11.33g(収率77%)を得た。これを精製せずにそのまま次の反応に用いた。なお、反応式は下記のとおりである。
窒素雰囲気下、100ml四つ口フラスコに上記で得られたジケトン体4.99g(10.2mmol)と塩化メチレン50mlを入れ、4℃に冷却した。これに亜硝酸n-ペンチル1.55g(13.2mmol)とクロロトリメチルシラン2.88g(26.5mmol)を順に添加した。
添加終了後、更に10℃で3時間攪拌した。エバポレーターにより溶媒を濃縮した後、酢酸エチルで抽出し、飽和炭酸水素ナトリウム水溶液、飽和塩化ナトリウム水溶液で順に洗浄し、硫酸マグネシウムを加えて乾燥した。硫酸マグネシウムをろ過してエバポレーターにより溶媒を濃縮した後、シリカゲルカラムクロマトグラフィーにより精製を行い3.94g(収率74%)の目的物を得た。なお、反応式は下記のとおりである。
50ml四つ口フラスコに上記で得られたケトオキシム体2.13g(4.40mmol)、塩化メチレン20ml、トリエチルアミン0.89g(8.80mmmol)を入れ、系中を窒素で置換した。反応溶液を4℃に冷却した後、塩化アセチル0.414g(5.28mmol)を添加した。
添加終了後、更に室温で2時間攪拌し、飽和炭酸水素ナトリウム水溶液5mlを添加した。有機層を飽和炭酸水素ナトリウム水溶液、飽和塩化ナトリウム水溶液で順に洗浄し、硫酸マグネシウムを加えて乾燥した。硫酸マグネシウムをろ過してエバポレーターにより溶媒を濃縮した後、シリカゲルカラムクロマトグラフィーにより精製を行い1.80g(収率78%)の下記ケトオキシムエステル系化合物I-9を得た。
1H-NMR δ[ppm]
1.15(t,3H)、1.49(t,3H),2.27(s,3H),2.72(t,2H),3.12(t,2H),3.58(s,3H),4.43(q,2H),7.3~7.5(m,6H),8.06(dd,1H),8.29(dd,1H),8.59(d,1H),8.83(dd,1H)
なお、反応式は下記のとおりである。
上記実施例4におけるジケトン体の製造において、エチルグルタリルクロリドをメチルグルタリルクロリドに変更した以外は同様にして、下記のケトオキシムエステル系化合物I-10を製造した。得られた化合物のNMRシフト値は次の通りであった。
1H-NMR δ[ppm]
1.49(t,3H),2.27(s,3H),2.72(t,2H),3.12(t,2H),3.58(s,3H),4.43(q,2H),7.2~7.6(m,5H),7.64(d,1H),7.95(d,1H),8.05(t,2H),8.11(dd,1H),8.29(dd,1H),8.67(d,1H),8.78(dd,1H)
前記実施例2おけるジケトン体の製造において、エチルグルタリルクロリドをメチルグルタリルクロリドに変更したことと、ケトオキシムエステル体の製造においてアセチルクロリドをベンゾイルクロリドに変更したこと以外は同様にして、下記のケトオキシムエステル系化合物I-11を製造した。得られた化合物のNMRシフト値は次の通りであった。
1H-NMR δ[ppm]
1.48(3H,t)、2.35(3H,s)、2.80(2H,t)、3.27(2H,t)、3.59(3H,s)、4.42(2H、q)、7.29-7.66(9H,m)、8.08(1H,dd)、8.14(2H,dd)、8.37(1H,dd)、8.60(1H,d)、8.93(1H,d)
<ジケトン体の製造>
窒素雰囲気下、500ml四つ口フラスコにケトン体 14.2g(35mmol)、メチルグルタリルクロリド 6.4g(39mmol)、塩化メチレン120mlを加えた。反応溶液を5℃に冷却した後、塩化アルミニウム 15.6g(117mmol)を25分かけてゆっくり添加した。
添加終了後、更に3℃で2時間攪拌し、反応溶液を氷水600mlに少しずつ投入した。有機層を水、5%炭酸ナトリウム水溶液、飽和塩化ナトリウム水溶液で順に洗浄し、硫酸マグネシウムを加えて乾燥した。硫酸マグネシウムをろ過してエバポレーターにより溶媒を濃縮し、10.5gの淡褐色固体を得た。塩化メチレン/ヘキサン溶媒で再結晶して、黄色の目的物9.2g(収率49%)を得た。
反応式は下記のとおりである。
窒素雰囲気下、200ml四つ口フラスコに上記で得られたジケトン体9.0g(17mmol)と塩化メチレン68mlを入れ、3℃に冷却した。これに1N塩化水素/ジエチルエーテル溶液 34mlと亜硝酸n-ペンチル2.6g(22mmol)を順に添加した。
添加終了後、更に10℃で6時間攪拌し、そのまま冷蔵庫に2日間放置した。10%炭酸カリウム水溶液50mlを添加し、塩化メチレンで抽出した。有機層を10%炭酸カリウム水溶液、飽和塩化ナトリウム水溶液で順に洗浄し、硫酸マグネシウムを加えて乾燥した。硫酸マグネシウムをろ過してエバポレーターにより溶媒を濃縮した後、シリカゲルカラムクロマトグラフィーにより精製を行い5.1g(収率54%)の目的物を得た。
反応式は下記のとおりである。
50ml四つ口フラスコに上記で得られたケトオキシム体2.6g(4.7mmol)、テトラヒドロフラン16ml、トリエチルアミン0.95g(9.4mmmol)を入れ、系中を窒素で置換した。反応溶液を5℃に冷却した後、塩化アセチル0.49g(6.3mmol)を添加した。
添加終了後、更に5℃で4時間攪拌し、飽和炭酸水素ナトリウム水溶液10mlを添加した。次に酢酸エチルで抽出し、飽和炭酸水素ナトリウム水溶液、飽和塩化ナトリウム水溶液で順に洗浄し、硫酸マグネシウムを加えて乾燥した。硫酸マグネシウムをろ過してエバポレーターにより溶媒を濃縮した後、シリカゲルカラムクロマトグラフィーにより精製を行い1.0g(収率36%)の下記ケトオキシムエステル系化合物I-12を得た。
1H-NMR δ[ppm]
1.46(3H,t)、2.24(3H,s)、2.70(2H,t)、3.10(2H,t)、
3.55(3H,s)4.38(2H,q)、7.26-7.46(7H,m)、
7.82(2H,d)、8.11(2H,d)、8.27(1H,d)、8.61(2H,s)、
8.71(1H,s)
反応式は下記のとおりである。
上記実施例7おけるケトオキシムエステル体の製造において、アセチルクロリドをベンゾイルクロリドに変更したこと以外は同様にして、下記のケトオキシムエステル系化合物I-13を製造した。得られた化合物のNMRシフト値は次の通りであった。
1H-NMR δ[ppm]
1.47(3H,t)、2.77(2H,t)、3.23(2H,t)、3.54(3H,s)、
4.39(2H,q)、7.26-7.69(10H,m)、7.80(2H,d)、
8.11(4H,dd)、8.38(1H,d)、8.60(2H、s)、
8.80(1H、s)
<ケトン体の製造>
100ml三つ口フラスコにジフェニルスルフィド5.00g(26.8mmol)、メチルグルタリルクロリド4.41g(26.8mmol)、塩化メチレン50mlを加え、系中を窒素で置換した。反応溶液を0℃に冷却した後、塩化アルミニウム7.14g(53.6mmol)を1時間かけてゆっくり添加した。
添加終了後、更に室温で2時間攪拌し、反応溶液を水100ml中に注ぎ、酢酸エチルで抽出した。酢酸エチル層を飽和炭酸水素ナトリウム水溶液、飽和塩化ナトリウム水溶液で順に洗浄し、硫酸ナトリウムを加えて乾燥した。硫酸ナトリウムをろ過してエバポレーターにより溶媒を濃縮し、7.83g(収率93%)の目的物を得た。反応式は下記の通りである。
50ml三口フラスコに、上記で得られたケトン体1.00g(3.18mmol)、塩化メチレン6ml、1N塩化水素/ジエチルエーテル溶液6.4mlを入れ、系中を窒素で置換した。反応溶液を10℃に冷却した後、亜硝酸n-ペンチル0.484g(4.13mmol)を添加した。
添加終了後、更に10℃で4時間攪拌し、飽和炭酸水素ナトリウム水溶液2mlを添加した。その後、酢酸エチルで抽出し、飽和炭酸水素ナトリウム水溶液、飽和塩化ナトリウム水溶液で順に洗浄し、硫酸ナトリウムを加えて乾燥した。硫酸ナトリウムをろ過してエバポレーターにより溶媒を濃縮し、1.09g(収率100%)の目的物を得た。反応式は下記の通りである。
50ml三口フラスコに上記で得られたケトオキシム体1.09g(3.17mmol)、テトラヒドロフラン10ml、トリエチルアミン0.66g(6.52mmmol)を入れ、系中を窒素で置換した。反応溶液を0℃に冷却した後、塩化アセチル0.363g(3.59mmol)を添加した。
添加終了後、更に室温で1.5時間攪拌し、飽和炭酸水素ナトリウム水溶液2mlを添加した。エバポレーターで濃縮した後、酢酸エチルで抽出し、飽和炭酸水素ナトリウム水溶液、飽和塩化ナトリウム水溶液で順に洗浄し、硫酸ナトリウムを加えて乾燥した。硫酸ナトリウムをろ過してエバポレーターにより溶媒を濃縮した後、シリカゲルカラムクロマトグラフィーにより精製を行い1.08g(収率86%)の下記ケトオキシムエステル系化合物I-14を得た。
1H-NMR δ[ppm]
2.25(3H,s)、2.66(2H,t)、3.04(2H,t)、3.60(3H,s)、7.16(2H、d)、7.41(3H,m)、7.51(2H,m)、7.94(2H,m)
また、反応式は下記の通りである。
<ケトン体の製造>
100ml三つ口フラスコにフルオロベンゼン 2.92g(30.4mmol)、メチルグルタリルクロリド 5.00g(30.4mmol)、塩化メチレン50mlを加え、系中を窒素で置換した。反応溶液を0℃に冷却した後、塩化アルミニウム 8.11g(60.8mmol)を1時間かけてゆっくり添加した。
添加終了後、更に室温で2時間攪拌し、反応溶液を水100ml中に注ぎ、酢酸エチルで抽出した。酢酸エチル層を飽和炭酸水素ナトリウム水溶液、飽和塩化ナトリウム水溶液で順に洗浄し、硫酸ナトリウムを加えて乾燥した。硫酸ナトリウムをろ過してエバポレーターにより溶媒を濃縮し、5.63g(収率83%)の目的物を得た。
反応式は下記のとおりである。
冷却後、反応溶液を水50ml中に注ぎ、酢酸エチルで抽出した。酢酸エチル層を飽和炭酸水素ナトリウム水溶液、飽和塩化ナトリウム水溶液で順に洗浄し、硫酸ナトリウムを加えて乾燥した。硫酸ナトリウムをろ過してエバポレーターにより溶媒を濃縮し、4.00g(収率55%)の目的物を得た。
反応式は下記のとおりである。
50ml三口フラスコに上記で得られたケトン体2.00g(6.86mmol)、塩化メチレン14ml、1N塩化水素/ジエチルエーテル溶液 12mlを入れ、系中を窒素で置換した。反応溶液を10℃に冷却した後、亜硝酸n-ペンチル1.04g(8.92mmol)を添加した。
添加終了後、更に10℃で7時間攪拌し、飽和炭酸水素ナトリウム水溶液2mlを添加した。その後、酢酸エチルで抽出し、飽和炭酸水素ナトリウム水溶液、飽和塩化ナトリウム水溶液で順に洗浄し、硫酸ナトリウムを加えて乾燥した。硫酸ナトリウムをろ過してエバポレーターにより溶媒を濃縮した後、シリカゲルカラムクロマトグラフィーにより精製を行い1.42g(収率65%)の目的物を得た。
反応式は下記のとおりである。
50ml三口フラスコに上記で得られたケトオキシム体1.42g(4.43mmol)、テトラヒドロフラン20ml、トリエチルアミン0.897g(8.86mmmol)を入れ、系中を窒素で置換した。反応溶液を0℃に冷却した後、塩化アセチル0.382g(4.87mmol)を添加した。
添加終了後、更に室温で2.5時間攪拌し、飽和炭酸水素ナトリウム水溶液2mlを添加した。エバポレーターで濃縮した後、酢酸エチルで抽出し、飽和炭酸水素ナトリウム水溶液、飽和塩化ナトリウム水溶液で順に洗浄し、硫酸ナトリウムを加えて乾燥した。硫酸ナトリウムをろ過してエバポレーターにより溶媒を濃縮した後、シリカゲルカラムクロマトグラフィーにより精製を行い1.20g(収率75%)の下記ケトオキシムエステル系化合物I-16を得た。
1H-NMR δ[ppm]
2.26(3H,s)、2.66(2H,t)、3.06(2H,t)、3.35(4H,m)、3.61(3H,s)、3.84(4H,m)、6.86(2H、d)、8.04(2H,d)
反応式は下記のとおりである。
<ケトン体の製造>
100ml三つ口フラスコにフルオロベンゼン 7.0g(73mmol)、メチルグルタリルクロリド 12.2g(73mmol)、塩化メチレン40mlを加え、系中を窒素で置換した。反応溶液を6℃に冷却した後、塩化アルミニウム 22.3g(168mmol)を1時間かけてゆっくり添加した。
添加終了後、3℃で5.5時間攪拌し、反応溶液を氷水200mlに少量ずつ投入した。有機層を飽和炭酸水素ナトリウム水溶液、飽和塩化ナトリウム水溶液で順に洗浄し、硫酸マグネシウムを加えて乾燥した。硫酸マグネシウムをろ過してエバポレーターにより溶媒を濃縮し、14.5g(収率89%)の目的物を得た。これを精製せずに次の反応に用いた。
反応式は下記のとおりである。
冷却後、反応溶液を飽和塩化ナトリウム水溶液50ml中に注ぎ、トルエンで抽出した。有機層を過塩素酸ナトリウム水溶液、飽和塩化ナトリウム水溶液で順に洗浄し、硫酸マグネシウムを加えて乾燥した。硫酸マグネシウムをろ過してエバポレーターにより溶媒を濃縮し、褐色固体を得た。これを酢酸エチルで再結晶し、13.0g(収率55%)の目的物を得た。
反応式は下記のとおりである。
窒素雰囲気下、200ml三口フラスコに上記で得られたケトン体7.3g(20mmol)と塩化メチレン80mlを入れ、3℃に冷却した。これに1N塩化水素/ジエチルエーテル溶液 40mlと亜硝酸n-ペンチル3.0g(26mmol)を順に添加した。
添加終了後、更に3℃で7時間攪拌し、飽和炭酸水素ナトリウム水溶液50mlを添加した。その後、塩化メチレンで抽出し、飽和炭酸水素ナトリウム水溶液、飽和塩化ナトリウム水溶液で順に洗浄し、硫酸マグネシウムを加えて乾燥した。硫酸マグネシウムをろ過してエバポレーターにより溶媒を濃縮した後、シリカゲルカラムクロマトグラフィーにより精製を行い6.0g(収率76%)の目的物を得た。
反応式は下記のとおりである。
100ml三口フラスコに上記で得られたケトオキシム体3.9g(10mmol)、テトラヒドロフラン33ml、トリエチルアミン2.0g(20mmmol)を入れ、系中を窒素で置換した。反応溶液を3℃に冷却した後、塩化アセチル1.0g(13mmol)を添加した。
添加終了後、更に3℃で2時間攪拌し、飽和炭酸水素ナトリウム水溶液10mlを添加した。その後、酢酸エチルで抽出し、飽和炭酸水素ナトリウム水溶液、飽和塩化ナトリウム水溶液で順に洗浄し、硫酸マグネシウムを加えて乾燥した。硫酸マグネシウムをろ過してエバポレーターにより溶媒を濃縮した後、シリカゲルカラムクロマトグラフィーにより精製を行い3.1g(収率74%)の下記ケトオキシムエステル系化合物I-17を得た。
1H-NMR(CDCl3) δ[ppm]
2.26(3H,s)、2.70(2H,t)、3.05(2H,t)、3.62(3H,s)、7.25(2H,d)、7.56(3H、m)、7.90(5H,m)、8.10(1H,s)
反応式は下記のとおりである。
<ジケトン体の製造>
200ml三つ口フラスコにジフェニルスルフィド 6.0g(32mmol)、メチルグルタリルクロリド 10.8g(64mmol)、塩化メチレン80mlを加え、系中を窒素で置換した。反応溶液を3℃に冷却した後、塩化アルミニウム 19.8g(148mmol)を1時間かけてゆっくり添加した。
添加終了後、更に3℃で5時間攪拌し、反応溶液を氷水200mlに少しずつ投入した。有機層を飽和炭酸水素ナトリウム水溶液、飽和塩化ナトリウム水溶液で順に洗浄し、硫酸マグネシウムを加えて乾燥した。硫酸マグネシウムをろ過してエバポレーターにより溶媒を濃縮し、10.3g(収率72%)の白色固体の目的物を得た。これを精製せずに次の反応に用いた。
反応式は下記のとおりである。
窒素雰囲気下、200ml三口フラスコに上記で得られたケトン体4.4g(10mmol)と塩化メチレン40mlを入れ、3℃に冷却した。これに1N塩化水素/ジエチルエーテル溶液 40mlと亜硝酸n-ペンチル3.0g(26mmol)を順に添加した。
添加終了後、更に3℃で6時間攪拌し、10%炭酸カリウム水溶液20mlを添加した。その後、塩化メチレンで抽出し、10%炭酸カリウム水溶液、飽和塩化ナトリウム水溶液で順に洗浄し、硫酸マグネシウムを加えて乾燥した。硫酸マグネシウムをろ過してエバポレーターにより溶媒を濃縮した後、シリカゲルカラムクロマトグラフィーにより精製を行い3.8g(収率76%)の目的物を得た。
反応式は下記のとおりである。
50ml三口フラスコに上記で得られたケトオキシム体3.8g(7.6mmol)、テトラヒドロフラン25ml、トリエチルアミン3.1g(30mmmol)を入れ、系中を窒素で置換した。反応溶液を3℃に冷却した後、塩化アセチル1.6g(20mmol)を添加した。
添加終了後、更に3℃で2時間攪拌し、飽和炭酸水素ナトリウム水溶液10mlを添加した。次に酢酸エチルで抽出し、飽和炭酸水素ナトリウム水溶液、飽和塩化ナトリウム水溶液で順に洗浄し、硫酸マグネシウムを加えて乾燥した。硫酸マグネシウムをろ過してエバポレーターにより溶媒を濃縮した後、シリカゲルカラムクロマトグラフィーにより精製を行い2.6g(収率59%)の下記ケトオキシムエステル系化合物I-18を得た。
1H-NMR δ[ppm]
2.29(6H,s)、2.73(4H,t)、3.08(4H,t)、3.64(6H,s)、7.44(4H、d)、8.05(4H,d)
反応式は下記のとおりである。
<ケトン体の製造>
窒素雰囲気下、300ml三つ口フラスコにジフェニルスルフィド 10.0g(54mmol)と塩化メチレン170mlを加え3℃に冷却した。これに無水グルタル酸 6.2g(54mmol)を添加した後、塩化アルミニウム 16g(123mmol)を1時間かけてゆっくり添加した。
添加終了後、更に3℃で5時間攪拌し、反応溶液を氷水100mlに少しずつ投入した。塩化ナトリウム40gを加えて水層を飽和させ、塩化メチレンを加えて抽出した。有機層を飽和塩化ナトリウム水溶液で洗浄し、硫酸マグネシウムを加えて乾燥した。硫酸マグネシウムをろ過してエバポレーターにより溶媒を濃縮し、得られた固体を酢酸エチルで再結晶を行い、10g(収率65%)の目的物を得た。
反応式は下記のとおりである。
その後、酢酸エチルで抽出し、飽和炭酸水素ナトリウム水溶液、飽和塩化ナトリウム水溶液で順に洗浄し、硫酸マグネシウムを加えて乾燥した。硫酸マグネシウムをろ過してエバポレーターにより溶媒を濃縮した後、2.4g(収率68%)の目的物を得た。
反応式は下記のとおりである。
窒素雰囲気下、50ml三口フラスコに上記で得られたケトン体3.0g(7mmol)と塩化メチレン27mlを入れ、3℃に冷却した。これに1N塩化水素/ジエチルエーテル溶液 14mlと亜硝酸n-ペンチル1.0g(9mmol)を順に添加した。
添加終了後、更に3~10℃で7時間攪拌し、10%炭酸カリウム水溶液40mlを添加した。その後、塩化メチレンで抽出し、10%炭酸カリウム水溶液、飽和塩化ナトリウム水溶液で順に洗浄し、硫酸マグネシウムを加えて乾燥した。硫酸マグネシウムをろ過してエバポレーターにより溶媒を濃縮した後、シリカゲルカラムクロマトグラフィーにより精製を行い1.4g(収率53%)の目的物を得た。
反応式は下記のとおりである。
50ml三口フラスコに上記で得られたケトオキシム体1.4g(4mmol)、テトラヒドロフラン12ml、トリエチルアミン0.7g(7mmmol)を入れ、系中を窒素で置換した。反応溶液を3℃に冷却した後、塩化アセチル0.4g(5mmol)を添加した。
添加終了後、更に3℃で2時間攪拌し、飽和炭酸水素ナトリウム水溶液10mlを添加した。次に酢酸エチルで抽出し、飽和炭酸水素ナトリウム水溶液、飽和塩化ナトリウム水溶液で順に洗浄し、硫酸マグネシウムを加えて乾燥した。硫酸マグネシウムをろ過してエバポレーターにより溶媒を濃縮した後、シリカゲルカラムクロマトグラフィーにより精製を行い1.28g(収率83%)のケトオキシムエステル系化合物I-19を得た。
1H-NMR δ[ppm]
0.90(3H,t)、1.32(2H,m)、1.54(2H,m)、2.67(2H,t)、3.06(2H,t)、4.02(2H,t)、7.19(2H、d)、7.50(5H,m)、7.96(2H,d)
反応式は下記のとおりである。
<ジケトン体の製造>
50ml三つ口フラスコに前記実施例1におけると同様に合成したモノケトン体 5.00g(16.0mmol)、n-オクタノイルクロリド 2.85g(17.5mmol)、塩化メチレン50mlを加え、系中を窒素で置換した。反応溶液を0℃に冷却した後、塩化アルミニウム 4.76g(35.7mmol)をゆっくり添加した。
添加終了後、更に室温で2時間攪拌し、反応溶液を水100ml中に注ぎ、酢酸エチルで抽出した。酢酸エチル層を飽和炭酸水素ナトリウム水溶液、飽和塩化ナトリウム水溶液で順に洗浄し、硫酸ナトリウムを加えて乾燥した。硫酸ナトリウムをろ過してエバポレーターにより溶媒を濃縮し、7.00gの粘調なオイルを得た。これに酢酸エチル/n-ヘキサン溶液を加えて固体を析出させ、ろ過して6.00(収率85%)の目的物を得た。
反応式は下記の通りである。
50ml三口フラスコにナトリウムメトキシド0.48g(8.87mmol)とメタノール6mlを入れ、系中を窒素で置換した。この中に亜硝酸イソアミル1.04g(8.87mmol)を添加し、引き続き上記で合成したジケトン体3.00g(6.82mmol)をTHF8.4mlに溶解させて添加した。
添加終了後、室温で36時間攪拌した。反応液に酢酸1.6g/水20ml溶液を添加した後、酢酸エチルで抽出し、飽和炭酸水素ナトリウム水溶液、飽和塩化ナトリウム水溶液で順に洗浄し、硫酸ナトリウムを加えて乾燥した。硫酸ナトリウムをろ過してエバポレーターにより溶媒を濃縮した後、シリカゲルカラムクロマトグラフィーにより精製を行い0.40g(収率13%)の目的物を得た。
反応式は下記の通りである。
50ml三口フラスコに上記で得られたケトオキシム体0.40g(0.85mmol)、塩化メチレン 5ml、トリエチルアミン0.19g(1.88mmmol)を入れ、系中を窒素で置換した。反応溶液を0℃に冷却した後、塩化アセチル0.15g(1.88mmol)を添加した。
添加終了後、更に室温で2時間攪拌し、飽和炭酸水素ナトリウム水溶液2mlを添加した。酢酸エチルで抽出し、飽和炭酸水素ナトリウム水溶液、飽和塩化ナトリウム水溶液で順に洗浄し、硫酸ナトリウムを加えて乾燥した。硫酸ナトリウムをろ過してエバポレーターにより溶媒を濃縮した後、シリカゲルカラムクロマトグラフィーにより精製を行い0.40g(収率91%)の下記ケトオキシムエステル系化合物I-15を得た。
1H-NMR δ[ppm]
0.86(3H,t)、1.25-1.32(4H,m)、1.35-1.43(2H,m)、1.48(3H,t)、1.56-1.65(2H,m)、2.28(3H,s)、2.35(3H,s)、2.84(2H,t)、4.43(2H,q)、7.25-7.49(6H,m)、8.05(1H,dd)、8.29(1H,dd)、8.61(1H,d)、8.83(1H,d)
また、反応式は下記の通りである。
表8に示す配合割合にて光重合性組成物を調製した。
得られた光重合性組成物を、ガラス基板(旭硝子社製カラーフィルター用ガラス板「AN100」)上に塗布し、ホットプレート上で90℃にて90秒間乾燥し、乾燥膜厚4μmの塗布膜を得た。その後、塗布膜側から線幅5~50μmの細線パターンを有するマスクを介して3kW高圧水銀灯を用いて露光した。露光条件としては、波長365nmの照度計で測定した像面照度が30mW/cm2で、後述の最適露光量となる露光量とした。
次に0.4質量%のテトラメチルアンモニウムヒドロキシド水溶液を現像液として用い、25℃で110秒間、現像液に基板を浸漬することにより現像を施し、更に純水にてリンスして露光膜を得た。得られた露光膜をコンベクションオーブンで220℃、1時間加熱することにより、熱硬化膜を得た。
上記光重合性組成物、露光膜、及び熱硬化膜(層間絶縁膜)について、各種評価を行なった。結果を表8に併記した。
(酸価)
アルカリ可溶性樹脂につき、JIS-K0070(化学製品の酸価、けん化価、エステル価、よう素価、水酸基価及び不けん化物の試験方法)に準拠して測定した。
(感度)
光重合性組成物をガラス基板上に、乾燥膜厚がほぼ4μmとなるように塗布し、ホットプレート上で90℃、90秒間の条件でベークした。その後、高圧水銀灯により30mW/cm2の照度で露光した。露光条件としては、露光エネルギー量として4mJ/cm2から64mJ/cm2までの範囲で、2.5倍毎の間隔で露光エネルギー量を設定して露光した。露光後、25℃の0.4質量%テトラメチルアンモニウムヒドロキシド水溶液に110秒間浸漬し、純水でリンスし、残存する硬化膜(露光膜)の膜厚を測定した。得られた露光膜の膜厚を、露光量に対してプロットし、ある露光量と、その2.5倍の露光量とにおける露光膜の膜厚差が、10%以内となる最小露光量を、感度(mJ/cm2)と定義した。
(残膜率)
前記層間絶縁膜の形成手順にて得られた熱硬化膜の膜厚と露光前の膜厚の比を残膜率(%)とした。
(透過率)
前記層間絶縁膜の形成手順にて得られた熱硬化膜の光透過率を分光光度計で測定し、波長400nmにおける膜厚3μm当りの透過率(%)を求めた。
(解像力)
前記層間絶縁膜の形成手順にて得られた熱硬化膜の画像を光学顕微鏡により観察し、解像している最小の線幅(μm)を解像力とした。
(パターン形状)
前記層間絶縁膜の形成手順にて得られた熱硬化膜の10μmライン・アンド・スペース(線幅10μmの画像と空間を交互に形成したもの)の断面形状を走査電子顕微鏡により観察した。
(耐薬品性)
前記透過率の測定に用いた熱硬化膜を、20質量%塩酸に40℃で20分間浸漬した後、該膜の光透過率を分光光度計で測定し、波長400nmにおける膜厚3μm当りの透過率(%)を求め、塩酸浸漬前後の透過率変化を下式により算出した。
[耐薬品性]=[塩酸浸漬前の透過率]-[塩酸浸漬後の透過率]
M-1:共栄化学社製「エポキシエステル3000A」
I-1:実施例1参照
I-2:実施例2参照
I-14:実施例9参照
I-15:参考例1参照
I-18:実施例12参照
I-19:実施例13参照
P-1:スチレン/α-メチルスチレン/アクリル酸3元共重合体(モル比:70/10/20)
酸価:108mg-KOH/g、Mw:4,600
酸価:110mg-KOH/g、Mw:7,000
酸価:138mg-KOH/g、Mw:10,000
酸価:126mg-KOH/g、Mw:9,300
D-1:住友スリーエム社製 フッ素系界面活性剤「FC4432」
(E)有機溶剤
E-1:プロピレングリコールモノメチルエーテルアセテート(PGMEA)
(G-2)熱架橋剤
G-2-i:日本化薬社製「NC-3000」(エポキシ等量:277g/eq、軟化点:56.5℃)
500mL四つ口フラスコ中に、下記式(a-2)で表されるビスフェノールフルオレン型エポキシ樹脂235g(エポキシ当量235)とテトラメチルアンモニウムクロライド110mg、2,6-ジ-t-ブチル-4-メチルフェノール100mg及びアクリル酸72.0gと、プロピレングリコールモノメチルエーテルアセテート300gを仕込み、これに25mL/分の速度で空気を吹き込みながら90~100℃で加熱溶解した。
次に、溶液が白濁した状態のまま徐々に昇温し、120℃に加熱して完全溶解させた。ここで溶液は次第に透明粘稠になったがそのまま撹拌を継続した。この間、酸価を測定し、1.0mg-KOH/g未満になるまで加熱撹拌を続けた。酸価が目標に達するまで12時間を要した。そして室温まで冷却し、ビスフェノールフルオレン型エポキシアクリレートを得た。
次いで、このようにして得られた上記のビスフェノールフルオレン型エポキシアクリレート617.0gにプロピレングリコールモノメチルエーテルアセテート300gを加えて溶解した後、ビフェニル-3,3',4,4'-テトラカルボン酸二酸無水物73.5g及び臭化テトラエチルアンモニウム1gを混合し、徐々に昇温して110~115℃で4時間反応させた。
酸無水物基の消失を確認した後、1,2,3,6-テトラヒドロ無水フタル酸38.0gを混合し、90℃で6時間反応させ、酸価100mg-KOH/g、分子量(ゲルパーミュエーションクロマトグラフィー(GPC)測定によるポリスチレン換算の重量平均分子量、以下同様)3,900のアルカリ可溶性樹脂P-4を得た。
トリレンジイソシアネートの三量体(三菱化学社製「マイテックGP750A」、樹脂固形分50質量%、酢酸ブチル溶液)32gと触媒としてジブチルチンジラウレート0.02gをプロピレングリコールモノメチルエーテルアセテート(PGMEA)47gで希釈溶解した。
攪拌下に、これに、片末端がメトキシ基となっている数平均分子量1,000のポリエチレングリコール(日本油脂社製「ユニオックスM-1000」)14.4gと数平均分子量1,000のポリプロピレングリコール(三洋化成工業社製「サンニックスPP-1000」)9.6gとの混合物を滴下した後、70℃でさらに3時間反応させた。 次に、N,N-ジメチルアミノ-1,3-プロパンジアミン1gを加え、40℃でさらに1時間反応させた。このようにして得られた高分子分散剤を含有する溶液のアミン価を中和滴定により求めたところ14mg-KOH/gであった。また、樹脂含有量をドライアップ法(150℃で30分間、ホットプレート上で溶剤を除去し重量変化量により樹脂濃度を算出)により求めたところ40質量%であった。
<カーボンブラックの分散液の調製>
カラーフィルター用カーボンブラック(三菱化学社製、MA-220)50質量部に、参考例3で調製した高分子分散剤G-1-iを、固形分として5質量部加え、さらに固形分濃度が50質量%となるように、PGMEAを加えて混合し、分散液を得た。分散液の全質量は50gであった。これを攪拌機によりよく攪拌しプレミキシングを行った。
次に、ペイントシェーカーにより25~45℃の範囲で6時間分散処理を行った。ビーズは0.5mmφのジルコニアビーズを用い、分散液と同じ重量を加えた。分散終了後、フィルターによりビーズと分散液を分離した。
上述したカーボンブラックの分散液を用いて、固形分として下記表9の配合割合となるように各成分を加え、スターラーにより攪拌、溶解させ、ブラックレジストを調製した。
ブラックレジストをスピンコーターにてガラス基板(コーニング社製「7059」)に塗布し、ホットプレートで80℃、1分間乾燥した。乾燥後のレジストの膜厚を触針式膜厚計(テンコール社製「α-ステップ」)で測定したところ1μmであった。次に、このサンプルに対し、フォトマスクを通して高圧水銀灯で露光量を変えて露光した。温度25℃、濃度0.8質量%炭酸ナトリウム水溶液を用いて圧力0.1MPaでスプレー現像することによりレジストパターンを得た。
感度、耐アルカリ性、遮光性及び膜ムラを下記の基準で評価し、表9に併記した。
20μmのマスクパターンを寸法通り形成できる適正露光量(mJ/cm2)をもって表示した。すなわち、露光量の少ないレジストは低露光量で画像形成が可能であるため高感度であることを示す。
(解像力(耐アルカリ性))
上記のとおり決定した20μmのマスクパターンを忠実に再現する露光量において、現像時間を80秒とした場合に解像可能なレジスト最小パターン寸法を200倍の倍率で顕微鏡観察することにより求めた。最小パターン寸法が小さいものほど、解像力が高いことを示す。
(遮光性)
画線部の光学濃度(OD)をマクベス反射濃度計(コルモルグン社製「TR927」)で測定した。なお、OD値は遮光能力を示す数値であり数値が大きい程高遮光性であることを示す。
(膜ムラ)
目視により塗布表面を観察し評価した。
全くムラが見えず均一 :◎
若干ムラが見えるが問題ない :○
(直線性)
上記のとおり決定した20μmのマスクパターンを忠実に再現する露光量において、現像時間を80秒とし、幅20μm、長さ100μmのレジストパターン5本を200倍の倍率で顕微鏡観察し、凹凸なく直線であるべき長さ100μmの辺において2μm以上の凹凸の発生個数を数えた。
(B)光重合開始剤
I-9:実施例4参照
I-10:実施例5参照
(C)アルカリ可溶性樹脂
P-4:参考例2参照
(D)界面活性剤
D-2:住友スリーエム社製 フッ素系界面活性剤「FC-430」
(E)有機溶剤
E-2:メトキシブチルアセテートとジエチレングリコールモノブチルエーテルアセテートの80/20(重量比)混合物
(F)色剤(黒色顔料)
F-1:三菱化学社製 カーボンブラック「MA-220」
(G-1)顔料分散剤
G-1-i:参考例3参照
プロピレングリコールモノメチルエーテルアセテート114.0gを500mlの4つ口フラスコに入れ、窒素バブリングを行いながら85℃まで昇温した。これにベンジルメタクリレート96.8g(0.55mol)、メタクリル酸33.3g(0.45mol)、2,2’-アゾビス(イソブチロニトリル) 9.85g(0.06mol)をプロピレングリコールモノメチルエーテルアセテート96.45gに溶解し、4時間かけて滴下した。滴下後反応液を85℃に保ったままさらに2時間攪拌し、その後窒素バブリングを止めて100℃に昇温し1時間攪拌した。得られたアルカリ可溶性樹脂P-5の重量平均分子量は8000、酸価175mgKOH/gであった。
プロピレングリコールモノメチルエーテルアセテート145質量部を窒素置換しながら攪拌し、120℃に昇温した。ここにスチレン10質量部、グリシジルメタクリレート85.2質量部及びトリシクロデカン骨格を有するモノアクリレート(日立化成社製「FA-513M」)66質量部、及び2,2’-アゾビス-2-メチルブチロニトリル8.47質量部を3時間かけて滴下し、更に90℃で2時間攪拌し続けた。次に反応容器内を空気置換に変え、アクリル酸43.2質量部にトリスジメチルアミノメチルフェノール0.7質量部及びハイドロキノン0.12質量部を投入し、100℃で12時間反応を続けた。その後、テトラヒドロ無水フタル酸(THPA)56.2質量部、トリエチルアミン0.7質量部を加え、100℃、3.5時間反応させた。こうして得られたアルカリ可溶性樹脂P-6のGPCにより測定した質量平均分子量Mwは約8,400、酸価は80mgKOH/gであった。
<青色顔料分散液の調製>
プロピレングリコールモノメチルエーテルアセテート78.4質量部、青色顔料C.I.ピグメントブルー(P.B.)15:6を12.0質量部、アクリル系分散剤(ビッグケミー社製「DB2000」)3.6質量部、上記参考例4で合成したアルカリ可溶性樹脂P-5を4.0質量部混合し、攪拌機で3時間攪拌して固形分濃度が20質量%のミルベースを調製した。このミルベースを600質量部の0.5mmφのジルコニアビーズを用いビーズミル装置にて周速10m/s、滞留時間3時間で分散処理を施しP.B. 15:6の分散液を得た。
以上のようにして得られた分散液に、下記表10に示す配合比になるように上記参考例5で合成したアルカリ可溶性樹脂P-6、エチレン性不飽和基含有化合物、光重合開始剤、界面活性剤を混合攪拌し、最終的な固形分濃度が20質量%になるように溶媒(プロピレングリコールモノメチルエーテルアセテート)を加えて、青色画素用の青色レジストを得た。
クロムが蒸着されたガラス基板に、青色レジストをそれぞれスピンコーターにて塗布し、80℃のホットプレートにて3分間プリベークを行い、乾燥塗布膜を形成した。
次に、高圧水銀灯により幅1μmから25μmの1μm刻みの直線状マスクパターンを、150μmギャップで設置し、これを通して、青色レジストの乾燥塗布膜を2kW高圧水銀灯を用いて60mJ/cm2で露光した後、0.04質量%水酸化カリウム水溶液を使用し、現像液温度23℃で0.25MPa圧でスプレー現像した。現像した時間は、あらかじめ測定した青色レジストの溶解時間の2倍とした。
溶解時間は、上記同様にガラス基板(旭硝子社製「AN-100」)上に青色レジストを塗布・乾燥した後、0.04質量%水酸化カリウム水溶液を用いて、現像液温度23℃、圧力0.25MPaで現像したときに、未露光部の青色着色レジストが現像液へ完全に溶解し、基板が露出した時間を、その青色レジストの溶解時間とした。基板は現像後、十分な水でリンスした後、クリーンエアで乾燥した。その後、230℃のオーブンにて30分間ポストベークを行った。乾燥後膜厚は2.5μm程度であった。
ガラス基板(旭硝子社製「AN-100」)上に青色レジストをスピンコーターで塗布した後、80℃分間乾燥した。次いで2kW高圧水銀灯を用いて60mJ/cm2で全面露光処理を行った。その後パターン(画素)の製造と同様に現像、水洗処理を行い、230℃オーブンにて30分間ポストベークを行い、着色板を作製した。乾燥後膜厚は2.5μm程度であった。こうして得られた着色板について、分光光度計(日立製作所社製「U-3310」)により透過スペクトルを測定し、C光源にて色度を算出した。
上記手順で得られた幅25μmの直線状マスクを用いて得られたパターンを光学顕微鏡で観測し、その線幅を測定した。線幅の太いものほど高感度である。
上記<パターン(画素)の製造>にて得られた直線状パターンのうち、基板に残った最小幅パターンを密着性とした。
前記のパターン(画素)の製造方法と同様に、高圧水銀灯により幅50μm、長さ3mmの直線状マスクパターンを通してサンプルを80mJ/cm2で露光した後、0.04質量%水酸化カリウム水溶液を使用し、現像液温度を23℃に保ち、0.25MPa圧で溶解時間の4倍の時間でスプレー現像した。
このようにして得られたパターン10本を、光学顕微鏡を用いて10倍の倍率で観察し、線の縁の窪みをかけの数として数えた。再現性を確認するため、これを2回繰り返して平均をとった。
かけの数が少ないものほど、密着性や内部硬化性に優れることを示す。
2.5cm角の無アルカリガラス基板(旭硝子社製「AN-100」)の片全面にITO膜を形成した電極基板Aと、2.5cm角の同ガラス基板の片面中央部に、2mm幅の取り出し電極がつながった1cm角のITO膜を形成した電極基板Bを用意した。
電極基板AおよびB上に、スピンコート法により、配向膜剤(日産化学社製「サンエバー7492」)を塗布し、ホットプレート上で110℃で1分間乾燥させた後、熱風循環炉内で200℃1時間加熱して、膜厚70nmの塗膜を形成した。
配向膜剤を塗布した電極基板A上に、各実施例及び比較例の青色レジストをスピンコート法により塗布し、ホットプレート上で80℃3分間加熱して、全面を100mJ/cm2で露光した後、23℃の0.1質量%炭酸ナトリウム水溶液にて0.3MPaの水圧で30秒間スプレー現像した。その後、熱風循環炉内で230℃30分間の焼成を行った。なお、焼成後の膜厚が1.7μmとなるように塗布条件を調整した。
こうして得られた空セルに、液晶(メルクジャパン社製「MLC-6846-000」)を注入し、周辺部をUV硬化型シール剤によって封止して、電圧保持率測定用液晶セルを完成した。
電圧保持率が高いものほど、硬化物の安定性が高いことを示す。
(B)光重合開始剤
I-5:2,4-ジエチルチオキサントン
P-5:参考例4参照
P-6:参考例5参照
(D)界面活性剤
D-3:大日本インキ化学工業社製 フッ素系界面活性剤「F-475」
(F)色剤(青色顔料)
F-2:青色顔料C.I.ピグメントブルー(P.B.)15:6
(G-2)顔料分散剤
G-2-ii:ビッグケミー社製 アクリル系分散剤「DB2000」
また、さらに色材と組み合わせることによりカラーフィルター用途に有用な光重合性組成物を構成することができる。特に、このケトオキシムエステル系化合物を光重合開始剤として黒色顔料と組み合わせて用いた光重合性組成物は、薄膜において高遮光性でありながら感度、解像性に優れるため、低コストで高品質の樹脂BMを形成することができる。
本発明の光重合性組成物を用いて樹脂BMを形成したカラーフィルターは、精度、平坦性、耐久性において優れるため、液晶表示素子の表示品位を向上させることができる。また、製造工程およびカラーフィルター自体にも有害な物質を含まないため、人体に対する危険性を低減し環境安全性が向上する。
本発明の光重合開始剤及び光重合性組成物は、層間絶縁膜用、カラーフィルターの画素用及びBM用に限定されることなく、オーバーコート用、リブ(液晶配向制御突起)用及びフォトスペーサー用などの透明な光重合性組成物にも利用可能であり、その応用技術分野は極めて広範である。
Claims (12)
- 下記一般式(I)で表されることを特徴とするケトオキシムエステル系化合物。
R1は、芳香環又はヘテロ芳香環を含む、置換基を有していてもよい1価の有機基を表し、
R2は、それぞれ置換基を有していてもよい炭素数1~12のアルキルチオ基、炭素数2~12のアルコキシカルボニル基、炭素数3~12のアルケニルオキシカルボニル基、炭素数3~12のアルキニルオキシカルボニル基、炭素数7~12のアリールオキシカルボニル基、炭素数3~12のヘテロアリールオキシカルボニル基、炭素数2~12のアルキルチオカルボニル基、炭素数3~12のアルケニルチオカルボニル基、炭素数3~12のアルキニルチオカルボニル基、炭素数7~12のアリールチオカルボニル基、炭素数3~12のヘテロアリールチオカルボニル基、炭素数2~12のアルキルチオアルコキシ基、-O-N=CR30R31、-N(OR30)-OCO-R31又は下記一般式(II)で表される基
R3は、それぞれ置換基を有していてもよい炭素数2~12のアルカノイル基、炭素数3~25のアルケノイル基、炭素数4~8のシクロアルカノイル基、炭素数7~20のアリーロイル基、炭素数3~20のヘテロアリーロイル基、炭素数2~10のアルコキシカルボニル基、炭素数7~20のアリールオキシカルボニル基、炭素数2~20のヘテロアリール基又は炭素数2~20のアルキルアミノカルボニル基を表す。) - 前記一般式(I)において、Xが置換基を有していてもよい炭素数1~20のアルキレン基であり、R2がそれぞれ置換基を有していてもよい炭素数2~12のアルコキシカルボニル基又は炭素数1~12のアルキルチオ基であることを特徴とする請求項1に記載のケトオキシムエステル系化合物。
- 前記一般式(I)において、R1が、下記一般式(III)で表されることを特徴とする請求項1または2に記載のケトオキシムエステル系化合物。
ただし、R9 は、水素原子、それぞれ置換基を有していてもよい炭素数1~12のアルキル基、炭素数2~8のアルカノイル基、炭素数3~12のアルケニル基、炭素数6~20のアリール基又は炭素数3~15のトリアルキルシリル基を表し、
R10及びR11は、互いに独立して水素原子、それぞれ置換基を有していてもよい炭素数1~12のアルキル基、炭素数2~4のヒドロキシルアルキル基、炭素数3~5のアルケニル基又は炭素数6~20のアリール基を表す。
R4~R8は、互いに結合して環構造を形成してもよい。) - 前記請求項1~5のいずれか一項に記載のケトオキシムエステル系化合物からなることを特徴とする光重合開始剤。
- (A)エチレン性不飽和基含有化合物及び(B)光重合開始剤を含有し、(B)光重合開始剤が請求項1~5のいずれか一項に記載のケトオキシムエステル系化合物を含有することを特徴とする光重合性組成物。
- 更に(F)色材を含有することを特徴とする請求項7に記載の光重合性組成物。
- 更に(G-1)顔料分散剤を含有することを特徴とする請求項8に記載の光重合性組成物。
- 請求項7に記載の光重合性組成物により形成された層間絶縁膜を備えることを特徴とする液晶表示装置。
- 請求項8又は9に記載の光重合性組成物により形成されたブラックマトリックスを備えることを特徴とするカラーフィルター。
- 請求項8又は9に記載の光重合性組成物により形成された画素を備えることを特徴とするカラーフィルター。
Priority Applications (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN200980114528.9A CN102015633B (zh) | 2008-04-25 | 2009-04-23 | 酮肟酯类化合物及其应用 |
| JP2010509224A JP5494479B2 (ja) | 2008-04-25 | 2009-04-23 | ケトオキシムエステル系化合物及びその利用 |
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008-114943 | 2008-04-25 | ||
| JP2008114943 | 2008-04-25 | ||
| JP2009023348 | 2009-02-04 | ||
| JP2009-023348 | 2009-02-04 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2009131189A1 true WO2009131189A1 (ja) | 2009-10-29 |
Family
ID=41216917
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2009/058096 WO2009131189A1 (ja) | 2008-04-25 | 2009-04-23 | ケトオキシムエステル系化合物及びその利用 |
Country Status (5)
| Country | Link |
|---|---|
| JP (1) | JP5494479B2 (ja) |
| KR (1) | KR101632081B1 (ja) |
| CN (1) | CN102015633B (ja) |
| TW (1) | TWI443086B (ja) |
| WO (1) | WO2009131189A1 (ja) |
Cited By (50)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2010008713A (ja) * | 2008-06-26 | 2010-01-14 | Mitsubishi Chemicals Corp | ホログラム記録層形成用組成物、並びにそれを用いたホログラム記録材料及びホログラム光記録媒体 |
| JP2010032940A (ja) * | 2008-07-31 | 2010-02-12 | Tokyo Ohka Kogyo Co Ltd | 着色感光性樹脂組成物、カラーフィルター、及び液晶表示ディスプレイ |
| JP2010128344A (ja) * | 2008-11-28 | 2010-06-10 | Fujifilm Corp | 着色硬化性組成物、カラーフィルタ、および液晶表示装置 |
| JP2010164964A (ja) * | 2008-12-19 | 2010-07-29 | Fujifilm Corp | 感光性組成物、カラーフィルタ、および液晶表示装置 |
| WO2011062198A1 (ja) | 2009-11-20 | 2011-05-26 | 富士フイルム株式会社 | 分散組成物及び感光性樹脂組成物、並びに固体撮像素子 |
| JP2011132215A (ja) * | 2009-11-27 | 2011-07-07 | Adeka Corp | オキシムエステル化合物及び該化合物を含有する光重合開始剤 |
| WO2011093479A1 (en) * | 2010-01-29 | 2011-08-04 | Fujifilm Corporation | Polymerizable composition, color filter, method of producing color filter and solid-state image sensor |
| JP2011227295A (ja) * | 2010-04-20 | 2011-11-10 | Fujifilm Corp | 重合性組成物、硬化膜、カラーフィルタ、カラーフィルタの製造方法、固体撮像素子、および新規化合物 |
| JP2012058728A (ja) * | 2010-08-10 | 2012-03-22 | Sumitomo Chemical Co Ltd | 感光性樹脂組成物 |
| EP2472330A1 (en) | 2010-12-28 | 2012-07-04 | Fujifilm Corporation | Titanium black dispersion composition for forming light blocking film and method of producing the same, black radiation-sensitive composition, black cured film, solid-state imaging element, and method of producing black cured film |
| WO2012176816A1 (ja) * | 2011-06-21 | 2012-12-27 | 旭硝子株式会社 | ネガ型感光性樹脂組成物、隔壁、ブラックマトリックス、カラーフィルタおよび液晶表示素子 |
| WO2013038974A1 (en) | 2011-09-14 | 2013-03-21 | Fujifilm Corporation | Colored radiation-sensitive composition for color filter, pattern forming method, color filter and method of producing the same, and solid-state image sensor |
| JP2013101337A (ja) * | 2011-10-20 | 2013-05-23 | Mitsubishi Chemicals Corp | 着色樹脂組成物、カラーフィルタ、液晶表示装置及び有機el表示装置 |
| WO2013099948A1 (ja) | 2011-12-28 | 2013-07-04 | 富士フイルム株式会社 | 光学部材セット及びこれを用いた固体撮像素子 |
| WO2013099945A1 (ja) | 2011-12-28 | 2013-07-04 | 富士フイルム株式会社 | 光学部材セット及びこれを用いた固体撮像素子 |
| CN103204960A (zh) * | 2012-12-28 | 2013-07-17 | 南通缔威化工有限公司 | 新型三级胺类酮肟酯类光引发剂及其制备方法 |
| JP2013167786A (ja) * | 2012-02-16 | 2013-08-29 | Mitsubishi Chemicals Corp | 有機絶縁膜用硬化性樹脂組成物、硬化物、tftアクティブマトリックス基板及び液晶表示装置 |
| WO2013140979A1 (ja) | 2012-03-21 | 2013-09-26 | 富士フイルム株式会社 | 着色感放射線性組成物、着色硬化膜、カラーフィルタ、パターン形成方法、カラーフィルタの製造方法、固体撮像素子、及び画像表示装置 |
| WO2013141156A1 (ja) | 2012-03-19 | 2013-09-26 | 富士フイルム株式会社 | 着色感放射線性組成物、着色硬化膜、カラーフィルタ、着色パターン形成方法、カラーフィルタの製造方法、固体撮像素子、及び画像表示装置 |
| WO2014034814A1 (ja) | 2012-08-31 | 2014-03-06 | 富士フイルム株式会社 | 分散組成物、これを用いた硬化性組成物、透明膜、マイクロレンズ、及び固体撮像素子 |
| WO2014034815A1 (ja) | 2012-08-31 | 2014-03-06 | 富士フイルム株式会社 | 分散組成物、これを用いた硬化性組成物、透明膜、マイクロレンズ、及び固体撮像素子 |
| WO2014104137A1 (ja) | 2012-12-28 | 2014-07-03 | 富士フイルム株式会社 | 硬化性樹脂組成物、赤外線カットフィルタ及びこれを用いた固体撮像素子 |
| WO2014104136A1 (ja) | 2012-12-28 | 2014-07-03 | 富士フイルム株式会社 | 赤外線反射膜形成用の硬化性樹脂組成物、赤外線反射膜及びその製造方法、並びに赤外線カットフィルタ及びこれを用いた固体撮像素子 |
| WO2014103628A1 (ja) | 2012-12-27 | 2014-07-03 | 富士フイルム株式会社 | カラーフィルタ用組成物、赤外線透過フィルタ及びその製造方法、並びに赤外線センサー |
| WO2014168217A1 (ja) | 2013-04-12 | 2014-10-16 | 富士フイルム株式会社 | 遠赤外線遮光層形成用組成物 |
| WO2015033814A1 (ja) | 2013-09-06 | 2015-03-12 | 富士フイルム株式会社 | 着色組成物、硬化膜、カラーフィルタ、カラーフィルタの製造方法、固体撮像素子、画像表示装置、ポリマー、キサンテン色素 |
| JP2016053185A (ja) * | 2015-12-24 | 2016-04-14 | 東京応化工業株式会社 | ブラックカラムスペーサ用感光性樹脂組成物、ブラックカラムスペーサ、表示装置、及びブラックカラムスペーサの形成方法 |
| JP2016167030A (ja) * | 2015-03-10 | 2016-09-15 | 三菱化学株式会社 | 感光性着色組成物、硬化物、着色スペーサー、及び画像表示装置 |
| JP2017512886A (ja) * | 2014-03-18 | 2017-05-25 | 常州強力先端電子材料有限公司Cahngzhou Tronly Advanced Electronic Materials Co.,Ltd. | ビスオキシムエステル系光重合開始剤及びその製造方法と応用 |
| WO2017110982A1 (ja) | 2015-12-25 | 2017-06-29 | 富士フイルム株式会社 | 樹脂、組成物、硬化膜、硬化膜の製造方法および半導体デバイス |
| JP2017523465A (ja) * | 2014-07-15 | 2017-08-17 | 常州強力電子新材料股▲ふん▼有限公司Cahngzhou Tronly New Electronic Materials Co.,Ltd. | オキシムエステル類光開始剤含有感光性組成物及びその使用 |
| WO2017158914A1 (ja) | 2016-03-14 | 2017-09-21 | 富士フイルム株式会社 | 組成物、膜、硬化膜、光学センサおよび膜の製造方法 |
| JP2017181976A (ja) * | 2016-03-31 | 2017-10-05 | 新日鉄住金化学株式会社 | 遮光膜用感光性樹脂組成物、これを硬化させた遮光膜を備えたディスプレイ用基板、及びディスプレイ用基板の製造方法 |
| WO2018052024A1 (ja) * | 2016-09-16 | 2018-03-22 | 三菱ケミカル株式会社 | 感光性樹脂組成物、硬化物及び画像表示装置 |
| WO2018105532A1 (ja) * | 2016-12-05 | 2018-06-14 | 旭化成株式会社 | 感光性樹脂組成物、感光性樹脂積層体、樹脂パターンの製造方法及び硬化膜パターン製造方法 |
| JP2019500637A (ja) * | 2015-12-03 | 2019-01-10 | ローム・アンド・ハース・エレクトロニック・マテリアルズ・コリア・リミテッド | 感光性樹脂組成物及びそれから調製された有機絶縁膜 |
| JP2019147789A (ja) * | 2019-02-21 | 2019-09-05 | 三菱ケミカル株式会社 | カルバゾール化合物 |
| WO2019176409A1 (ja) | 2018-03-13 | 2019-09-19 | 富士フイルム株式会社 | 硬化膜の製造方法、固体撮像素子の製造方法 |
| WO2020049930A1 (ja) | 2018-09-07 | 2020-03-12 | 富士フイルム株式会社 | 車両用ヘッドライトユニット、ヘッドライト用の遮光膜、ヘッドライト用の遮光膜の製造方法 |
| WO2020152120A1 (en) | 2019-01-23 | 2020-07-30 | Basf Se | Oxime ester photoinitiators having a special aroyl chromophore |
| WO2020203277A1 (ja) | 2019-03-29 | 2020-10-08 | 富士フイルム株式会社 | 感光性樹脂組成物、硬化膜、インダクタ、アンテナ |
| WO2021039253A1 (ja) | 2019-08-30 | 2021-03-04 | 富士フイルム株式会社 | 組成物、膜、光学フィルタ及びその製造方法、固体撮像素子、赤外線センサ、並びに、センサモジュール |
| WO2021039205A1 (ja) | 2019-08-29 | 2021-03-04 | 富士フイルム株式会社 | 組成物、膜、近赤外線カットフィルタ、パターン形成方法、積層体、固体撮像素子、赤外線センサ、画像表示装置、カメラモジュール、及び、化合物 |
| WO2021175855A1 (en) | 2020-03-04 | 2021-09-10 | Basf Se | Oxime ester photoinitiators |
| WO2022059706A1 (ja) | 2020-09-18 | 2022-03-24 | 富士フイルム株式会社 | 組成物、磁性粒子含有膜、及び、電子部品 |
| WO2022065183A1 (ja) | 2020-09-24 | 2022-03-31 | 富士フイルム株式会社 | 組成物、磁性粒子含有硬化物、磁性粒子導入基板、電子材料 |
| WO2022070593A1 (ja) | 2020-09-30 | 2022-04-07 | 富士フイルム株式会社 | インクセット、積層体、及び、積層体の製造方法 |
| WO2022202394A1 (ja) | 2021-03-22 | 2022-09-29 | 富士フイルム株式会社 | 組成物、磁性粒子含有硬化物、磁性粒子導入基板、電子材料 |
| WO2023054565A1 (ja) | 2021-09-30 | 2023-04-06 | 富士フイルム株式会社 | 磁性粒子含有組成物の製造方法、磁性粒子含有組成物、磁性粒子含有硬化物、磁性粒子導入基板、電子材料 |
| JP7433385B2 (ja) | 2018-11-02 | 2024-02-19 | artience株式会社 | 感光性着色組成物、ブラックマトリックス、およびシリコン基板 |
Families Citing this family (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP5760374B2 (ja) * | 2009-10-23 | 2015-08-12 | 三菱化学株式会社 | ケトオキシムエステル系化合物及びその利用 |
| TWI568763B (zh) * | 2012-03-19 | 2017-02-01 | 奇美實業股份有限公司 | 感光性樹脂組成物、彩色濾光片及其液晶顯示元件 |
| TWI550643B (zh) * | 2012-03-30 | 2016-09-21 | Taiyo Holdings Co Ltd | Conductive paste and conductive circuit |
| TWI479264B (zh) * | 2012-12-20 | 2015-04-01 | Chi Mei Corp | 感光性樹脂組成物、彩色濾光片及其液晶顯示元件 |
| JP6095104B2 (ja) * | 2012-12-26 | 2017-03-15 | 日本化薬株式会社 | 活性エネルギー線硬化型樹脂組成物、表示素子用着色スペーサー及びブラックマトリックス |
| JP6602062B2 (ja) * | 2015-06-17 | 2019-11-06 | 東京応化工業株式会社 | 硬化性組成物、硬化物の製造方法、及びハードコート材 |
| CN109666088A (zh) | 2017-10-16 | 2019-04-23 | 北京英力科技发展有限公司 | 一种双酮肟酯化合物及其制造方法与应用 |
| KR102335614B1 (ko) * | 2018-03-21 | 2021-12-03 | 동우 화인켐 주식회사 | 착색 감광성 수지 조성물, 이를 포함하는 컬러필터 및 화상표시장치 |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2000080068A (ja) * | 1998-06-26 | 2000-03-21 | Ciba Specialty Chem Holding Inc | 新規o―アシルオキシム光開始剤 |
| JP2004300367A (ja) * | 2003-04-01 | 2004-10-28 | Toyo Ink Mfg Co Ltd | 光重合開始剤組成物 |
| JP2004300108A (ja) * | 2003-04-01 | 2004-10-28 | Toyo Ink Mfg Co Ltd | オキシムスルホニウム錯体 |
| JP2006232968A (ja) * | 2005-02-24 | 2006-09-07 | Konica Minolta Medical & Graphic Inc | 活性光線硬化型インクとそれを用いた画像形成方法及びインクジェット方式記録装置 |
| JP2007119686A (ja) * | 2005-10-31 | 2007-05-17 | Toyo Ink Mfg Co Ltd | 光重合性組成物 |
Family Cites Families (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2505746B2 (ja) * | 1986-05-20 | 1996-06-12 | 旭化成工業株式会社 | 感光性組成物 |
| JPS62286961A (ja) * | 1986-06-05 | 1987-12-12 | Asahi Chem Ind Co Ltd | 新規なオキシムエステル化合物及びその製造方法 |
| JPS6327833A (ja) * | 1986-07-22 | 1988-02-05 | Asahi Chem Ind Co Ltd | 耐熱性を有する画像の形成方法 |
| JPH087282B2 (ja) | 1988-04-05 | 1996-01-29 | 松下電器産業株式会社 | カラーフィルタ |
| JPH0695211B2 (ja) | 1987-12-09 | 1994-11-24 | 松下電器産業株式会社 | カラーフィルタ |
| JPH02153353A (ja) | 1988-07-25 | 1990-06-13 | Matsushita Electric Ind Co Ltd | 着色光重合組成物およびカラーフィルタ |
| JPH0675373A (ja) | 1992-08-28 | 1994-03-18 | Toppan Printing Co Ltd | 感光性着色組成物およびカラーフィルターの製造方法およびカラーフィルター |
| JPH0675372A (ja) | 1992-08-28 | 1994-03-18 | Toppan Printing Co Ltd | 感光性着色組成物およびカラーフィルターの製造方法およびカラーフィルター |
| JP4651800B2 (ja) | 2000-10-24 | 2011-03-16 | 富士フイルム株式会社 | 層間絶縁膜用ネガ型感光性熱硬化性転写材料、層間絶縁膜の形成方法、ハイアパーチャー型液晶表示装置及びその製造方法 |
| JP2002323762A (ja) | 2001-04-25 | 2002-11-08 | Nippon Kayaku Co Ltd | ネガ型着色感光性組成物 |
| EP1395615B1 (en) | 2001-06-11 | 2009-10-21 | Basf Se | Oxime ester photoinitiators having a combined structure |
| JP4283582B2 (ja) | 2002-04-15 | 2009-06-24 | シャープ株式会社 | 感放射線性樹脂組成物、パターン状絶縁性被膜の形成方法、アクティブマトリクス基板およびそれを備えた平面表示装置、並びに平面表示装置の製造方法 |
| JP4830310B2 (ja) | 2004-02-23 | 2011-12-07 | 三菱化学株式会社 | オキシムエステル系化合物、光重合性組成物及びこれを用いたカラーフィルター |
| JP2007187875A (ja) | 2006-01-13 | 2007-07-26 | Toyo Ink Mfg Co Ltd | 重合性組成物およびそれを用いたネガ型レジストおよびそれを用いた画像パターン形成方法。 |
| JP5354863B2 (ja) | 2006-02-24 | 2013-11-27 | 富士フイルム株式会社 | オキシム誘導体、光重合性組成物、カラーフィルタおよびその製造方法 |
| JP4792367B2 (ja) * | 2006-09-29 | 2011-10-12 | 富士フイルム株式会社 | 平版印刷版原版および平版印刷版の作製方法 |
-
2009
- 2009-04-23 KR KR1020107016825A patent/KR101632081B1/ko active IP Right Grant
- 2009-04-23 WO PCT/JP2009/058096 patent/WO2009131189A1/ja active Application Filing
- 2009-04-23 CN CN200980114528.9A patent/CN102015633B/zh active Active
- 2009-04-23 JP JP2010509224A patent/JP5494479B2/ja active Active
- 2009-04-24 TW TW98113609A patent/TWI443086B/zh active
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2000080068A (ja) * | 1998-06-26 | 2000-03-21 | Ciba Specialty Chem Holding Inc | 新規o―アシルオキシム光開始剤 |
| JP2004300367A (ja) * | 2003-04-01 | 2004-10-28 | Toyo Ink Mfg Co Ltd | 光重合開始剤組成物 |
| JP2004300108A (ja) * | 2003-04-01 | 2004-10-28 | Toyo Ink Mfg Co Ltd | オキシムスルホニウム錯体 |
| JP2006232968A (ja) * | 2005-02-24 | 2006-09-07 | Konica Minolta Medical & Graphic Inc | 活性光線硬化型インクとそれを用いた画像形成方法及びインクジェット方式記録装置 |
| JP2007119686A (ja) * | 2005-10-31 | 2007-05-17 | Toyo Ink Mfg Co Ltd | 光重合性組成物 |
Cited By (59)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2010008713A (ja) * | 2008-06-26 | 2010-01-14 | Mitsubishi Chemicals Corp | ホログラム記録層形成用組成物、並びにそれを用いたホログラム記録材料及びホログラム光記録媒体 |
| JP2010032940A (ja) * | 2008-07-31 | 2010-02-12 | Tokyo Ohka Kogyo Co Ltd | 着色感光性樹脂組成物、カラーフィルター、及び液晶表示ディスプレイ |
| JP2010128344A (ja) * | 2008-11-28 | 2010-06-10 | Fujifilm Corp | 着色硬化性組成物、カラーフィルタ、および液晶表示装置 |
| JP2010164964A (ja) * | 2008-12-19 | 2010-07-29 | Fujifilm Corp | 感光性組成物、カラーフィルタ、および液晶表示装置 |
| WO2011062198A1 (ja) | 2009-11-20 | 2011-05-26 | 富士フイルム株式会社 | 分散組成物及び感光性樹脂組成物、並びに固体撮像素子 |
| US8148045B2 (en) | 2009-11-27 | 2012-04-03 | Adeka Corporation | Oxime ester compound and photopolymerization initiator containing the same |
| JP2011132215A (ja) * | 2009-11-27 | 2011-07-07 | Adeka Corp | オキシムエステル化合物及び該化合物を含有する光重合開始剤 |
| WO2011093479A1 (en) * | 2010-01-29 | 2011-08-04 | Fujifilm Corporation | Polymerizable composition, color filter, method of producing color filter and solid-state image sensor |
| JP2011158655A (ja) * | 2010-01-29 | 2011-08-18 | Fujifilm Corp | 重合性組成物、カラーフィルタ、カラーフィルタの製造方法、固体撮像素子 |
| US8835081B2 (en) | 2010-01-29 | 2014-09-16 | Fujifilm Corporation | Polymerizable composition, color filter, method of producing color filter and solid-state image sensor |
| JP2011227295A (ja) * | 2010-04-20 | 2011-11-10 | Fujifilm Corp | 重合性組成物、硬化膜、カラーフィルタ、カラーフィルタの製造方法、固体撮像素子、および新規化合物 |
| JP2012058728A (ja) * | 2010-08-10 | 2012-03-22 | Sumitomo Chemical Co Ltd | 感光性樹脂組成物 |
| EP2472330A1 (en) | 2010-12-28 | 2012-07-04 | Fujifilm Corporation | Titanium black dispersion composition for forming light blocking film and method of producing the same, black radiation-sensitive composition, black cured film, solid-state imaging element, and method of producing black cured film |
| WO2012176816A1 (ja) * | 2011-06-21 | 2012-12-27 | 旭硝子株式会社 | ネガ型感光性樹脂組成物、隔壁、ブラックマトリックス、カラーフィルタおよび液晶表示素子 |
| WO2013038974A1 (en) | 2011-09-14 | 2013-03-21 | Fujifilm Corporation | Colored radiation-sensitive composition for color filter, pattern forming method, color filter and method of producing the same, and solid-state image sensor |
| JP2013101337A (ja) * | 2011-10-20 | 2013-05-23 | Mitsubishi Chemicals Corp | 着色樹脂組成物、カラーフィルタ、液晶表示装置及び有機el表示装置 |
| WO2013099945A1 (ja) | 2011-12-28 | 2013-07-04 | 富士フイルム株式会社 | 光学部材セット及びこれを用いた固体撮像素子 |
| WO2013099948A1 (ja) | 2011-12-28 | 2013-07-04 | 富士フイルム株式会社 | 光学部材セット及びこれを用いた固体撮像素子 |
| JP2013167786A (ja) * | 2012-02-16 | 2013-08-29 | Mitsubishi Chemicals Corp | 有機絶縁膜用硬化性樹脂組成物、硬化物、tftアクティブマトリックス基板及び液晶表示装置 |
| WO2013141156A1 (ja) | 2012-03-19 | 2013-09-26 | 富士フイルム株式会社 | 着色感放射線性組成物、着色硬化膜、カラーフィルタ、着色パターン形成方法、カラーフィルタの製造方法、固体撮像素子、及び画像表示装置 |
| WO2013140979A1 (ja) | 2012-03-21 | 2013-09-26 | 富士フイルム株式会社 | 着色感放射線性組成物、着色硬化膜、カラーフィルタ、パターン形成方法、カラーフィルタの製造方法、固体撮像素子、及び画像表示装置 |
| WO2014034815A1 (ja) | 2012-08-31 | 2014-03-06 | 富士フイルム株式会社 | 分散組成物、これを用いた硬化性組成物、透明膜、マイクロレンズ、及び固体撮像素子 |
| WO2014034814A1 (ja) | 2012-08-31 | 2014-03-06 | 富士フイルム株式会社 | 分散組成物、これを用いた硬化性組成物、透明膜、マイクロレンズ、及び固体撮像素子 |
| EP3124548A1 (en) | 2012-08-31 | 2017-02-01 | FUJIFILM Corporation | Dispersion composition, curable composition using the same, transparent film, microlens, and solid-state imaging device |
| EP3135733A1 (en) | 2012-08-31 | 2017-03-01 | FUJIFILM Corporation | Dispersion composition, and curable composition, transparent film, microlens and solid-state imaging element using same |
| WO2014103628A1 (ja) | 2012-12-27 | 2014-07-03 | 富士フイルム株式会社 | カラーフィルタ用組成物、赤外線透過フィルタ及びその製造方法、並びに赤外線センサー |
| WO2014104137A1 (ja) | 2012-12-28 | 2014-07-03 | 富士フイルム株式会社 | 硬化性樹脂組成物、赤外線カットフィルタ及びこれを用いた固体撮像素子 |
| WO2014104136A1 (ja) | 2012-12-28 | 2014-07-03 | 富士フイルム株式会社 | 赤外線反射膜形成用の硬化性樹脂組成物、赤外線反射膜及びその製造方法、並びに赤外線カットフィルタ及びこれを用いた固体撮像素子 |
| CN103204960A (zh) * | 2012-12-28 | 2013-07-17 | 南通缔威化工有限公司 | 新型三级胺类酮肟酯类光引发剂及其制备方法 |
| WO2014168217A1 (ja) | 2013-04-12 | 2014-10-16 | 富士フイルム株式会社 | 遠赤外線遮光層形成用組成物 |
| WO2015033814A1 (ja) | 2013-09-06 | 2015-03-12 | 富士フイルム株式会社 | 着色組成物、硬化膜、カラーフィルタ、カラーフィルタの製造方法、固体撮像素子、画像表示装置、ポリマー、キサンテン色素 |
| JP2017512886A (ja) * | 2014-03-18 | 2017-05-25 | 常州強力先端電子材料有限公司Cahngzhou Tronly Advanced Electronic Materials Co.,Ltd. | ビスオキシムエステル系光重合開始剤及びその製造方法と応用 |
| JP2017523465A (ja) * | 2014-07-15 | 2017-08-17 | 常州強力電子新材料股▲ふん▼有限公司Cahngzhou Tronly New Electronic Materials Co.,Ltd. | オキシムエステル類光開始剤含有感光性組成物及びその使用 |
| US10392462B2 (en) | 2014-07-15 | 2019-08-27 | Changzhou Tronly Advanced Electronic Materials Co., Ltd. | Photosensitive composition containing oxime-ester photoinitiator and application thereof |
| JP2016167030A (ja) * | 2015-03-10 | 2016-09-15 | 三菱化学株式会社 | 感光性着色組成物、硬化物、着色スペーサー、及び画像表示装置 |
| JP2019500637A (ja) * | 2015-12-03 | 2019-01-10 | ローム・アンド・ハース・エレクトロニック・マテリアルズ・コリア・リミテッド | 感光性樹脂組成物及びそれから調製された有機絶縁膜 |
| JP2016053185A (ja) * | 2015-12-24 | 2016-04-14 | 東京応化工業株式会社 | ブラックカラムスペーサ用感光性樹脂組成物、ブラックカラムスペーサ、表示装置、及びブラックカラムスペーサの形成方法 |
| WO2017110982A1 (ja) | 2015-12-25 | 2017-06-29 | 富士フイルム株式会社 | 樹脂、組成物、硬化膜、硬化膜の製造方法および半導体デバイス |
| WO2017158914A1 (ja) | 2016-03-14 | 2017-09-21 | 富士フイルム株式会社 | 組成物、膜、硬化膜、光学センサおよび膜の製造方法 |
| JP2017181976A (ja) * | 2016-03-31 | 2017-10-05 | 新日鉄住金化学株式会社 | 遮光膜用感光性樹脂組成物、これを硬化させた遮光膜を備えたディスプレイ用基板、及びディスプレイ用基板の製造方法 |
| JP2018156093A (ja) * | 2016-09-16 | 2018-10-04 | 三菱ケミカル株式会社 | 感光性樹脂組成物、硬化物及び画像表示装置 |
| JP6341351B1 (ja) * | 2016-09-16 | 2018-06-13 | 三菱ケミカル株式会社 | 感光性樹脂組成物、硬化物及び画像表示装置 |
| WO2018052024A1 (ja) * | 2016-09-16 | 2018-03-22 | 三菱ケミカル株式会社 | 感光性樹脂組成物、硬化物及び画像表示装置 |
| WO2018105532A1 (ja) * | 2016-12-05 | 2018-06-14 | 旭化成株式会社 | 感光性樹脂組成物、感光性樹脂積層体、樹脂パターンの製造方法及び硬化膜パターン製造方法 |
| JPWO2018105532A1 (ja) * | 2016-12-05 | 2019-10-24 | 旭化成株式会社 | 感光性樹脂組成物、感光性樹脂積層体、樹脂パターンの製造方法及び硬化膜パターン製造方法 |
| WO2019176409A1 (ja) | 2018-03-13 | 2019-09-19 | 富士フイルム株式会社 | 硬化膜の製造方法、固体撮像素子の製造方法 |
| WO2020049930A1 (ja) | 2018-09-07 | 2020-03-12 | 富士フイルム株式会社 | 車両用ヘッドライトユニット、ヘッドライト用の遮光膜、ヘッドライト用の遮光膜の製造方法 |
| JP7433385B2 (ja) | 2018-11-02 | 2024-02-19 | artience株式会社 | 感光性着色組成物、ブラックマトリックス、およびシリコン基板 |
| WO2020152120A1 (en) | 2019-01-23 | 2020-07-30 | Basf Se | Oxime ester photoinitiators having a special aroyl chromophore |
| JP2019147789A (ja) * | 2019-02-21 | 2019-09-05 | 三菱ケミカル株式会社 | カルバゾール化合物 |
| WO2020203277A1 (ja) | 2019-03-29 | 2020-10-08 | 富士フイルム株式会社 | 感光性樹脂組成物、硬化膜、インダクタ、アンテナ |
| WO2021039205A1 (ja) | 2019-08-29 | 2021-03-04 | 富士フイルム株式会社 | 組成物、膜、近赤外線カットフィルタ、パターン形成方法、積層体、固体撮像素子、赤外線センサ、画像表示装置、カメラモジュール、及び、化合物 |
| WO2021039253A1 (ja) | 2019-08-30 | 2021-03-04 | 富士フイルム株式会社 | 組成物、膜、光学フィルタ及びその製造方法、固体撮像素子、赤外線センサ、並びに、センサモジュール |
| WO2021175855A1 (en) | 2020-03-04 | 2021-09-10 | Basf Se | Oxime ester photoinitiators |
| WO2022059706A1 (ja) | 2020-09-18 | 2022-03-24 | 富士フイルム株式会社 | 組成物、磁性粒子含有膜、及び、電子部品 |
| WO2022065183A1 (ja) | 2020-09-24 | 2022-03-31 | 富士フイルム株式会社 | 組成物、磁性粒子含有硬化物、磁性粒子導入基板、電子材料 |
| WO2022070593A1 (ja) | 2020-09-30 | 2022-04-07 | 富士フイルム株式会社 | インクセット、積層体、及び、積層体の製造方法 |
| WO2022202394A1 (ja) | 2021-03-22 | 2022-09-29 | 富士フイルム株式会社 | 組成物、磁性粒子含有硬化物、磁性粒子導入基板、電子材料 |
| WO2023054565A1 (ja) | 2021-09-30 | 2023-04-06 | 富士フイルム株式会社 | 磁性粒子含有組成物の製造方法、磁性粒子含有組成物、磁性粒子含有硬化物、磁性粒子導入基板、電子材料 |
Also Published As
| Publication number | Publication date |
|---|---|
| KR20110005233A (ko) | 2011-01-17 |
| JPWO2009131189A1 (ja) | 2011-08-25 |
| KR101632081B1 (ko) | 2016-06-20 |
| JP5494479B2 (ja) | 2014-05-14 |
| CN102015633B (zh) | 2014-08-06 |
| CN102015633A (zh) | 2011-04-13 |
| TW201000448A (en) | 2010-01-01 |
| TWI443086B (zh) | 2014-07-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5494479B2 (ja) | ケトオキシムエステル系化合物及びその利用 | |
| JP5760374B2 (ja) | ケトオキシムエステル系化合物及びその利用 | |
| JP6361838B2 (ja) | 感光性着色組成物、硬化物、ブラックマトリクス、着色スペーサー及び画像表示装置 | |
| JP4830310B2 (ja) | オキシムエステル系化合物、光重合性組成物及びこれを用いたカラーフィルター | |
| JP5652510B2 (ja) | 着色樹脂組成物、カラーフィルタ、液晶表示装置及び有機elディスプレイ | |
| TWI448453B (zh) | 肟酯系化合物、光聚合引發劑、光聚合性組成物、彩色濾光片以及液晶顯示裝置 | |
| JP2006016545A (ja) | 着色樹脂組成物、カラーフィルタ及び液晶表示装置 | |
| CN110618583A (zh) | 着色树脂组合物、滤色片、以及图像显示装置 | |
| JP2011232735A (ja) | 着色組成物、カラーフィルタ及びカラー液晶表示素子 | |
| WO2016002911A1 (ja) | 樹脂、感光性樹脂組成物、硬化物、カラーフィルタ及び画像表示装置 | |
| JP2022078139A (ja) | 感光性着色組成物、硬化物、着色スペーサー、画像表示装置 | |
| JP6853493B2 (ja) | 光重合性組成物、硬化物、画像表示装置及びオキシムエステル系化合物 | |
| JP6344108B2 (ja) | 感光性樹脂組成物、これを硬化させてなる硬化物、ブラックマトリックス及び画像表示装置 | |
| TW201906875A (zh) | 感光性樹脂組合物、硬化物、黑色矩陣及圖像顯示裝置 | |
| JP6607054B2 (ja) | 感光性樹脂組成物、硬化物、ブラックマトリックス及び画像表示装置 | |
| JP2018159930A (ja) | 感光性樹脂組成物、これを硬化させてなる硬化物、ブラックマトリックス及び画像表示装置 | |
| JP2019015966A (ja) | 感光性着色組成物、硬化物、着色スペーサー、及び画像表示装置 | |
| JP6874805B2 (ja) | 感光性樹脂組成物、これを硬化させてなる硬化物、ブラックマトリックス及び画像表示装置 | |
| JP2019014884A (ja) | 光重合性組成物、硬化物、画像表示装置及びオキシムエステル系化合物 | |
| JP2017214338A (ja) | 光重合開始剤、感光性樹脂組成物、硬化物、カラーフィルタ及び画像表示装置 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| WWE | Wipo information: entry into national phase |
Ref document number: 200980114528.9 Country of ref document: CN |
|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 09734786 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 20107016825 Country of ref document: KR Kind code of ref document: A |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2010509224 Country of ref document: JP |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| 122 | Ep: pct application non-entry in european phase |
Ref document number: 09734786 Country of ref document: EP Kind code of ref document: A1 |