DE69911235T2 - Neuartige ester abgeleitet von substituierten phenyl-cyclohexyl-verbindungen - Google Patents
Neuartige ester abgeleitet von substituierten phenyl-cyclohexyl-verbindungen Download PDFInfo
- Publication number
- DE69911235T2 DE69911235T2 DE69911235T DE69911235T DE69911235T2 DE 69911235 T2 DE69911235 T2 DE 69911235T2 DE 69911235 T DE69911235 T DE 69911235T DE 69911235 T DE69911235 T DE 69911235T DE 69911235 T2 DE69911235 T2 DE 69911235T2
- Authority
- DE
- Germany
- Prior art keywords
- phenyl
- dimethylaminomethyl
- compound
- cyclohexyl
- optionally substituted
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C219/00—Compounds containing amino and esterified hydroxy groups bound to the same carbon skeleton
- C07C219/26—Compounds containing amino and esterified hydroxy groups bound to the same carbon skeleton having esterified hydroxy groups bound to carbon atoms of at least one six-membered aromatic ring and amino groups bound to acyclic carbon atoms or to carbon atoms of rings other than six-membered aromatic rings of the same carbon skeleton
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C271/00—Derivatives of carbamic acids, i.e. compounds containing any of the groups, the nitrogen atom not being part of nitro or nitroso groups
- C07C271/06—Esters of carbamic acids
- C07C271/40—Esters of carbamic acids having oxygen atoms of carbamate groups bound to carbon atoms of six-membered aromatic rings
- C07C271/42—Esters of carbamic acids having oxygen atoms of carbamate groups bound to carbon atoms of six-membered aromatic rings with the nitrogen atoms of the carbamate groups bound to hydrogen atoms or to acyclic carbon atoms
- C07C271/44—Esters of carbamic acids having oxygen atoms of carbamate groups bound to carbon atoms of six-membered aromatic rings with the nitrogen atoms of the carbamate groups bound to hydrogen atoms or to acyclic carbon atoms to hydrogen atoms or to carbon atoms of unsubstituted hydrocarbon radicals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/04—Centrally acting analgesics, e.g. opioids
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C219/00—Compounds containing amino and esterified hydroxy groups bound to the same carbon skeleton
- C07C219/26—Compounds containing amino and esterified hydroxy groups bound to the same carbon skeleton having esterified hydroxy groups bound to carbon atoms of at least one six-membered aromatic ring and amino groups bound to acyclic carbon atoms or to carbon atoms of rings other than six-membered aromatic rings of the same carbon skeleton
- C07C219/28—Compounds containing amino and esterified hydroxy groups bound to the same carbon skeleton having esterified hydroxy groups bound to carbon atoms of at least one six-membered aromatic ring and amino groups bound to acyclic carbon atoms or to carbon atoms of rings other than six-membered aromatic rings of the same carbon skeleton having amino groups bound to acyclic carbon atoms of the carbon skeleton
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C219/00—Compounds containing amino and esterified hydroxy groups bound to the same carbon skeleton
- C07C219/26—Compounds containing amino and esterified hydroxy groups bound to the same carbon skeleton having esterified hydroxy groups bound to carbon atoms of at least one six-membered aromatic ring and amino groups bound to acyclic carbon atoms or to carbon atoms of rings other than six-membered aromatic rings of the same carbon skeleton
- C07C219/28—Compounds containing amino and esterified hydroxy groups bound to the same carbon skeleton having esterified hydroxy groups bound to carbon atoms of at least one six-membered aromatic ring and amino groups bound to acyclic carbon atoms or to carbon atoms of rings other than six-membered aromatic rings of the same carbon skeleton having amino groups bound to acyclic carbon atoms of the carbon skeleton
- C07C219/30—Compounds containing amino and esterified hydroxy groups bound to the same carbon skeleton having esterified hydroxy groups bound to carbon atoms of at least one six-membered aromatic ring and amino groups bound to acyclic carbon atoms or to carbon atoms of rings other than six-membered aromatic rings of the same carbon skeleton having amino groups bound to acyclic carbon atoms of the carbon skeleton with amino groups linked to the six-membered aromatic ring, or to the condensed ring system containing that ring, by carbon chains further substituted by singly-bound oxygen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains two hetero rings
- C07D487/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07B—GENERAL METHODS OF ORGANIC CHEMISTRY; APPARATUS THEREFOR
- C07B2200/00—Indexing scheme relating to specific properties of organic compounds
- C07B2200/07—Optical isomers
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2601/00—Systems containing only non-condensed rings
- C07C2601/12—Systems containing only non-condensed rings with a six-membered ring
- C07C2601/14—The ring being saturated
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2601/00—Systems containing only non-condensed rings
- C07C2601/12—Systems containing only non-condensed rings with a six-membered ring
- C07C2601/16—Systems containing only non-condensed rings with a six-membered ring the ring being unsaturated
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Neurology (AREA)
- Neurosurgery (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Biomedical Technology (AREA)
- Public Health (AREA)
- Pain & Pain Management (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
Description
- Gebiet der Erfindung
- Die vorliegende Erfindung betrifft neue Ester, die von aus Tramadol hergeleiteten substituierten Phenyl-Cyclohexyl-Verbindungen abgeleitet sind. Die erzielten Verbindungen weisen eine große analgetische Wirksamkeit, eine geringere Toxizität und eine längere Wirkzeit als Tramadol auf.
- Hintergrund der Erfindung
- Die Behandlung von Schmerz ist auf dem Gebiet der Medizin von großer Bedeutung. Die pharmakologischen Wirkstoffe, die gegenwärtig zur Behandlung von Schmerz verwendet werden, können einfach in zwei große Gruppen eingeteilt werden: Opioid-Verbindungen und nicht-steroidale antiinflammatorische Mittel (non-steroidal anti-inflammatories = NSAIs). Die NSAIs sind lediglich im Falle von leichtem oder mittelschwerem Schmerz von Nutzen; schwerer Schmerz wurde traditionell mit Opiaten bzw. Opioid-Verbindungen behandelt. Jedoch weisen diese Opioid-Verbindungen mehrere unerwünschte Wirkungen auf, wie beispielsweise Verstopfung, Atemdepression, Toleranzbildung und Suchtgefahr.
- US-Patent Nr. 3 652 589 beschreibt einen Typ analgetischer Verbindungen mit einer Struktur substituierter Cycloalkanolphenolether mit einer basischen Amino-Gruppe im Cycloalkylring. Unter diesen wird die (1R, 2R oder 1S, 2S)-2-[(dimethylamino)methyl]-1-(3-methoxyphenyl) cyclohexanol-Verbindung, die im allgemeinen als Tramadol bekannt ist, speziell erwähnt und in diesem Patent speziell beansprucht.
-
- Dieses Patent beschreibt ebenfalls Produkte, die von solchen des US-Patents abgeleitet sind, bei denen die Methoxyl-Gruppe in der 3-Position des Phenylrings demethyliert wurde. D. h., Produkte folgender Struktur:
- O-demethyltramadol ist in solchen Produkten enthalten, die im Patent NL 661 10 022 beschrieben sind, wobei das Produkt als eines der Metabolisierungsprodukte von Tramadol beschrieben wurde (von W. Lintz et al. Arzneim. Forsch (Drug Res) 31(II): 1932–43 (1981)). Die analgetische Wirksamkeit von Tramadol wird seinem (+) Isomer zugeschrieben (Lars Poulsen et al. Clin. Pharmacol. Ther (St. Louis) 1996, 60 (6), 636–644). Es existieren jedoch keine Daten bzgl. der klinischen Verwendung des O-demethyltramadol-Metaboliten.
- Kürzlich wurden im Patent
EP 753 506 - Tramadol weist eine Opioid-Agonisten-Wirkung auf. Jedoch zeigt die klinische Erfahrung mit Tramadol, dass es trotzdem einige der Nebenwirkungen nicht zeigt, die für Opioid-Agonisten typisch sind, wie beispielsweise Atemdepression (W. Vogel et al. Arzneim. Forsch (Drug Res) 28 (I), 1983 (1978)), Verstopfung (I. Arend et al. Arzneim. Forsch (Drug Res) 28 (I), 199 (1978), Toleranz (L. Flohe et al., Arzneim. Forsch (Drug Res) 28 (I), 213 (1978)) und Mißbrauchsmöglichkeit (T. Yenagila et al. Arzneim. Forsch (Drug Res) 28 (I), 158 (1978)). Es wurden einige für Tramadol spezifische Nebenwirkungen gefunden, die verursacht werden, wenn es intravenös (i. v.) und rasch injiziert wird, wie beispielsweise Hitzewallungen und Schwitzen.
- Weitere der mit Tramadol verbundenen Nachteile sind eine kurze Wirkdauer (T. Matthiesen, T. Wohrmann, T. P. Coogan, H. Uragg, „The experimental toxicology of tamadol: an overview", Toxicology Letters 95, 63–71, (1998)).
- Das Patent US-A-5 733 936 offenbart einige Ester von 6-Dimethylaminomethyl-1-phenylcyclohexan in der allgemeinen Formel des Abschnitts Beschreibung mit einer analgetischen Aktivität und einer geringen Toxizität.
- Die Aufgabe des Patents US-A-5 733 936 besteht darin, Ester, Phosphonate, Ether, Phenole, Karbonate, Karbamate etc. aus Derivaten von 6-Dimethylaminomethyl-1-phenyl-cyclohexan zu gewinnen, wobei diese Derivate in der 5-Position von Cyclohexyl substituiert sein können (gemäß der Bedeutung von R2 und R3 in den Ansprüchen, ebenso wie von ihren dehydroxylierten, chlorierten, fluorierten Analog-Verbindungen).
- Darüber hinaus betrifft, obwohl das Patent US-A-5 733 936 einige Ester von 6-Dimethylaminomethyl-1-phenyl-cyclohexan offenbart, keines der Beispiele von US A-5 733 936 einen Ester von O-demethyltramadol. Eines dieser Beispiele schließt Verbindungen ein, die das tertiäre OH aufweisen, das für O-demethyltramadol charakteristisch ist. Insbesondere offenbart Beispiel 13, das der Anmeldung am nächsten ist, einen Ester eines Analogs von Odemethyltramadol mit Acetylsalicylsäure und nicht einen Ester von O-demethyltramadol. Deswegen offenbart das Patent US-A-5 733 936 keinen Ester von O-demethyltramadol mit der charakteristischen Hydroxyl-Gruppe in der 1-Position. Das Patent US-A-5 733 936 offenbart keine Arbeitsbeispiele für einen Ester von O-demethyltramadol. Den drei anderen beispielhaft aufgeführten Estern (Beispiele 14, 15, 16) fehlt ebenfalls die tertiäre Hydroxyl-Gruppe.
- Deswegen konnten Stabilitäts-, Wirksamkeits- und Nebenwirkungsdaten nicht vorhergesehen noch nahegelegt worden sein. Gemäß der vorliegenden Anmeldung wird ein überraschender Effekt mit den Verbindungen der Formel I erzielt.
- Auf Grundlage des obigen Hintergrunds der Erfindung sind Verbindungen mit einer analgetischen Aktivität, die derjenigen von Tramadol ähnlich oder höher als diese ist und die eine geringere Toxizität und eine längere Wirkdauer aufweisen, nach wie vor von Interesse.
- Beschreibung der Erfindung
- Die vorliegende Erfindung betrifft Ester von O-demethyltramadol oder dessen 1,2-dehydratisiertem bzw. dehydriertem Derivat.
- Die analgetische Aktivität dieser Verbindungen hat sich höher als diejenige von Tramadol herausgestellt, mit einer geringeren Toxizität und einer längeren Wirkdauer, wenn sie oral verabreicht wird (siehe
1 ). - Die vorliegende Erfindung beschreibt insbesondere und beansprucht solche Produkte der allgemeinen Formel (I), deren Salze und optische Isomere ebenso wie das Verfahren diese zu gewinnen.
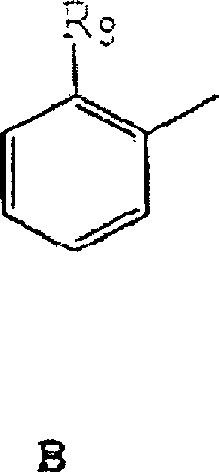
- Die Produkte der vorliegenden Erfindung werden durch die nachfolgende allgemeine Formel (I) repräsentiert: die die Möglichkeit asymmetrischer Kohlenstoffatome zeigt, wobei R1 folgendes ist: R2: OH ist;
R3: H ist;
oder R2 und R3 zusammen eine Doppelbindung bilden;
R8OH, -O-CO-N(CH3)2 oder NH-R11 ist;
R11: Phenyl; Phenyl, das wahlweise durch ein oder mehrere der nachfolgenden Substituenten substituiert ist: Cl, Br, I, NO2, C1-C6 Alkyl, C2-C6 Alkenyl, OH oder NH2;
wenn R1 B ist, ist R8 vorzugsweise OH oder -O-CO-N(CH3)2. - Insbesondere ist, wenn B R1 ist, das Produkt folgendes:
- – 3-(2-Dimethylaminomethyl-1-hydroxy-cyclohexyl)-phenyl-2-hydroxybenzoat
- – 3-(2-Dimethylaminomethyl-cyclohex-1-enyl)-phenyl-2-hydroxybenzoat
- – 3-(2-Dimethylaminomethyl-1-hydroxy-cyclohexyl)
- –phenyl-2-dimethylcarbamoyloxybenzoat
- – 3-(2-Dimethylaminomethyl-1-cyclohex-1-enyl)-phenyl-2-dimethylcarbamoyloxybenzoat.
- Beschreibung der Verfahren
- Die Verbindungen der allgemeinen Formel (I) der vorliegenden Erfindung können durch ein allgemeines Verfahren gewonnen werden, das durch Umsetzen einer Verbindung der allgemeinen Formel (II) mit der entsprechenden Säure oder Säurederivat der allgemeinen Formel (III) charakterisiert ist. wobei R1, R2, R3 die oben definierte Bedeutung aufweisen, und
X OH, Halogen, R15, O-R14 oder -CO- ist
R14 = C1-6 Alkyl, Phenyl, optional substituiertes Phenyl, und
R15 = Alkyl, ein Phenyl-Ring, der optional durch einen oder mehrere Substituenten substituiert ist oder ein heterozyklischer Ring, der optional durch ein oder mehrere Substituenten substituiert ist. - Vorzugsweise ist X OH oder Halogen.
- Die Reaktion wird in einem inerten Lösungsmittel, vorzugsweise Dichlormethan, Tetrahydrofuran etc. in einem Temperaturbereich von –20° bis 120°C, vorzugsweise einem Bereich von 0–35°C und vorzugsweise in Gegenwart eines die Kondensation fördernden Mittels wie beispielsweise Carbonyldiimidazol, Dicyclohexylcarbodiimid etc. durchgeführt.
- Die Verbindungen der Formel (II) werden gemäß der in der Literatur offenbarten Verfahren gewonnen (NL 6610022 oder Flick et al. Arneim. Forsch/Drug Res. (1978), 28 (I), 107–113).
- Beschreibung der pharmakologischen Prozesse
- Analgetische Wirksamkeitstests
- Die pharmakologische Wirksamkeit bzw. Aktivität der Produkte der vorliegenden Erfindung wurde in vivo in mehreren experimentellen Modellen getestet, von denen bekannt ist, dass sie den Schmerz bei Tieren evaluieren.
- a) Heissplatten-Verfahren
- Das wie von Eddy N. B. und Leimbach D. (J. Pharm. Exp. Ther. 107: 385–393, 1953) beschriebene Verfahren wurde verwendet. Die analgetische Wirkung der Produkte wurde durch Untersuchen des Verhaltens der Tiere auf einer heißen Oberfläche bei 55°C ± 1°C evaluiert.
- Männliche Swiss-Mäuse mit einem Gewicht von 20–25 g wurden verwendet. Die Verbindungen die getestet wurden, wurden oral oder intraperitoneal 1 Stunde oder 30 Minuten vor Beginn des Testes jeweils verabreicht.
- Der Prozess bestand aus der Anordnung der Tiere auf der Platte und aus dem Halten von diesen in einem Plexiglaszylinder, der 25 cm hoch und 21 cm hoch war. Die Zeit die benötigt wurde, bis die Tiere von der heißen Oberfläche hochsprangen, wurde bestimmt. Die Tiere wurden vor Beginn des Testes so ausgewählt, dass solche, die länger als 10 Sekunden zum Springen brauchten, nicht in die Gruppe eingeschlossen wurden, die eine Behandlung empfangen würden.
- 30 Minuten nach Verabreichung des zu testenden Produktes wurde der Test wiederholt und die maximale Zeit, die benötigt wurde, damit die Tiere sprangen, wurde aufgezeichnet. Solche Tiere, die nach 60 Sekunden nicht sprangen, wurden von der Platte entfernt, um irgendwelche Verletzungen zu vermeiden und wurden als 100% Schutz aufgezeichnet.
- Die Ergebnisse sind als % der Sprungzeitzunahme ausgedrückt, die wie folgt berechnet wurden:
- Um die Dauer der analgetischen Wirkung der oral verabreichten Produkte zu bestimmen, wurde die analgetische Wirkung auf der heißen Platte 1, 3, 6, 8 und 24 Stunden nach Verabreichung des Produktes ebenso wie bei der Kontrollgruppe evaluiert, die lediglich eine Behandlung mit dem Trägerstoff erhielt. Die Basis-Reaktionen wurden bei 30 und 5 Minuten vor Verabreichung der Produkte evaluiert.
- b) Bestimmung der DL50 der Produkte
- (EUDRA/S/87/011, Single Dose Toxicity, Europäische Richtlinie 75/318/EEC) (ICH S4, Toxicity Studies, single dose and repeated dose, CPMP Band III, Februar 87, Single dose toxicity).
- Männliche Swiss-Mäuse derselben Gruppe, die 20–25 g wogen, wurden verwendet um die akute Toxizität der Produkte einzuschätzen.
- Vor Verabreichung der Produkte ließ man die Tiere 12 Stunden ohne Einnahme von Nahrungsmittel, jedoch mit freiem Zugang zu Wasser, fasten. Mehrere Untergruppen von 10 Tieren wurden zufallsbedingt ausgewählt und diesen wurden zunehmende Dosen des Produktes in einfacher bzw. in einer einzelnen Verabreichung oral verabreicht, wonach sie für eine Zeitspanne von 14 Tagen mit freiem Zugang zu Wasser und Nahrungsmitteln unter Beobachtung verblieben. Zuletzt wurde die Anzahl toter Tiere in jeder Sub-Gruppe quantifiziert und der Wert der DL50 wurde berechnet (1–2).
- Beschreibung der Figur
-
1 zeigt die analgetische Wirkung des Heissplatten-Testes bei Mäusen bzgl. der Zeit, ausgedrückt als Prozent der zugenommenen Reaktionszeit bzgl. der Zeit (in Stunden), die seit der Verabreichung des Produktes verstrich. Sie ist in grau für Tramadol, gestreift für die Verbindung (I) von Beispiel 1 dargestellt. - Einer Lösung von 7,3 g (29,3 mmol) (RR-SS)-3-(2-dimethylaminomethyl-1-hydroxycyclohexyl)-phenol und 2,6 g (32,5 mmol) Pyridin in 50 ml CH2Cl2 wurde eine 5,8 g (29,3 mmol) Lösung von Acetylsalicyloylchlorid in 50 ml CH2Cl2 tropfenweise bei 0°C zugesetzt. Das Gemisch wurde für 10 Stunden bei 0°C gehalten, 100 ml Methanol und 100 ml HCl 1 N wurden zugesetzt und es wurde für 4 Tage bei 25°C gehalten. Nach Abdampfen des Methanols und Alkalisieren auf einen pH von 8,5 mit Na2CO3 wurde es mit EtOAc (3 × 50 ml) extrahiert. Die kombinierten organischen Extrakte wurden getrocknet (MgSO4) und abgedampft und der Rückstand wurde durch Silikagel-Chromatographie durch Eluieren mit CH2Cl2/MeOH/NH4OH 1000 : 30 : 3 aufgereinigt, so dass sich 1,7 g (16%) der Titelverbindung als gelbes Öl ergaben.
1H-NMR (CDCl3): 1,20–2,25 (m, 16H) einschließlich 2,11 (s, 6H); 2,45 (dd, 1H); 6,90–7,15 (m, 3H); 7,30–7,48 (m, 3H); 7,48–7,62 (m, 1H): 8,08 (dd, 1H); 10,55 (s, 1H, Austausch mit D2O) - Ausgehend von 3-(2-Dimethylaminomethyl-cyclohex-1-enyl)-phenol und folgend dem im Beispiel 1 beschriebenen Verfahren wurde die Titelverbindung als gelbes Öl erzielt.
1H-NMR (CDCl3): 1,60–1,80 (m, 4H), 2,10 (s, 6H); 2,15–2,35 (m, 4H); 2,75 (s, 2H); 6,90–7,10 (m, 5H); 7,40 (t, 1H): 7,55 (t, 1H); 8,10 (d, 1H); 10,50 (sa, 1H, Austausch durch D2O) - Einer Lösung von 1,82 g (8,0 nmol) von 2-Dimethylcarbamoyloxybenzoylchlorid in 25 ml CH2Cl2 wurde tropfenweise eine Lösung von 1,9 g (7,7 nmol) von (RR-SS)-3-(2-Dimethylaminomethyl-1-hydroxycyclohexyl)-phenol und 0,73 g (9,2 nmol) Pyridin in 50 ml CH2Cl2 zugesetzt. Das Gemisch wurde für 10 Stunden bei 0°C gehalten und über gefrorenes Wasser gegossen, die Phasen wurden getrennt und die wäßrige Phase wurde mit 100 ml CH2Cl2 extrahiert. Die organische Phase wurde getrocknet (MgSO4) und abgedampft. Der Rückstand wurde auf Silikagel durch Eluieren mit CH2Cl2/Aceton 80 : 20 chromatographiert. 570 mg (48%) der Titelverbindung wurden als oranges Öl gewonnen.
1H-NMR (CDCl3): 1,30–1,90 (m, 9H), 2,05 (m, 1H); 2,10 (s, 6H); 2,45 (dd, 1H); 2,95 (s, 3H); 3,05 (s, 3H): 7,00–7,10 (m, 1H); 7,20 (d, 1H); 7,30–7,40 (m, 4H); 7,60 (t, 1H); 8,15 (d, 1H). - Ausgehend von 925 mg (4,0 mmol) 3-(2-Dimethylaminomethyl-cyclohex-1-enyl)-phenol und folgend dem in Beispiel 8 beschriebenen Verfahren wurden 190 mg (32%) der Titelverbindung als gelbes Öl gewonnen.
1H-NMR (CDCl3): 1,70 (m, 4H), 2,07 (s, 6H); 2,10–2,30 (m, 4H); 2,75 (s, 2H); 2,95 (s, 3H); 3,10 (s, 2H): 6,90 (s, 1H); 6,95 (d, 1H); 7,05 (d, 1H); 7,20 (d, 1H); 7,30–7,45 (m, 2H); 7,65 (t, 1H); 8,20 (d, 1H). - Beispiele für pharmakologische Ergebnisse
- Tabelle 1 nachstehend zeigt die Ergebnisse der pharmakologischen Wirksamkeit mehrerer Beispiele des erfindungsgemäßen Produktes ebenso wie von Tramadol. Die Ergebnisse sind als Prozentsatz der erhöhten Reaktionszeit auf dem Heissplatten-Test ausgedrückt.
- Tabelle 2 zeigt die akuten Toxizitätszahlen für Tramadol und von Beispielen des erfindungsgemäßen Produktes, wobei die geringere Toxizität des letzteren zu beobachten ist.
Claims (8)
- Verbindung der allgemeinen Formel (I): wobei R1 bedeutet: R2 ist: OH; R3 ist : H oder R2 und R3 zusammen eine Zweifachbindung bilden; R8 ist : OH, -O-CO-N(CH3)2 oder NH-R11; R11 ist: Phenyl; ein wahlweise durch einen oder mehrere der folgenden Substituenten substituiertes Phenyl: Cl, Br, I, NO2, C1-C6-Alkyl , C2-C6-Alkenyl , OH oder NH2.
- Verbindung nach Anspruch 1, dadurch gekennzeichnet , dass R8 OH oder -O-CO-N(CH3)2 ist .
- Verbindung nach Anspruch 2, dadurch gekennzeichnet, dass sie aus einer der nachfolgenden Verbindungen ausgewählt ist: 3-(2-Dimethylaminomethyl-1-hydroxy-cyclohexyl)-phenyl-2-hydroxybenzoat; 3-(2-Dimethylaminomethyl-cyclohex-1-enyl)-phenyl-2-hydroxybenzoat; 3-(2-Dimethylaminomethyl-1-hydroxy-cyclohexyl)-phenyl-2-dimethylcarbamoyloxybenzoat; 3-(2-Dimethylaminomethyl-cyclohex-1-enyl)-phenyl-2-dimethylcarbamoyloxybenzoat.
- Verfahren zur Herstellung einer Verbindung nach Anspruch 1, dadurch gekennzeichnet, dass eine Verbindung der Formel (II) mit einer Verbindung der Formel (III) umgesetzt wird: wobei: R2 = OH R3 = H oder R2 und R3 zusammen eine Zweifachbindung bilden; X = OH, Halogen, O-R14 oder -CO-R15, R14 = C1/6-Alkyl, Phenyl, wahlweise ein substituiertes Phenyl, und R15 = Alkyl, ein Phenylring, wahlweise substituiert mit einem oder mehreren Substituenten oder ein heterozyklischer Ring, wahlweise substituiert durch einen oder mehrere Substituenten; R1: wobei R8 bedeutet : OH, -O-CO-N(CH3)2 oder NH-R11; R11 bedeutet: Phenyl, Phenyl, das wahlweise mit 1 oder mehreren der folgenden Substituenten substituiert ist: Cl, Br, I, NO2, C1-C6-Alkyl, C2-C6-Alkenyl, OH oder NH2; in einem inerten Lösungsmittel in einem Temperaturbereich von –20° bis 120°C in der Gegenwart oder Abwesenheit eines Kondensationsunterstützenden Mittels.
- Verbindung nach Anspruch 4, dadurch gekennzeichnet, dass das inerte Lösungsmittel Dichlormethan oder Tetrahydrofuran ist.
- Verbindung nach Anspruch 4, dadurch gekennzeichnet, dass das Kondensations-unterstützende Mittel Carbonyldiimidazol oder Dicyclohexylcarbodiimid ist.
- Verbindung nach Anspruch 4, dadurch gekennzeichnet, dass der Temperaturbereich von 0° bis 35°C reicht.
- Verwendung einer Verbindung der allgemeinen Formel (I) nach einem der Ansprüche 1 bis 7 zur Herstellung eines Arzneimittels zur Behandlung von Schmerz.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| ES9802329 | 1998-11-06 | ||
| ES009802329A ES2141688B1 (es) | 1998-11-06 | 1998-11-06 | Nuevos esteres derivados de compuestos fenil-ciclohexil sustituidos. |
| PCT/ES1999/000352 WO2000027799A1 (es) | 1998-11-06 | 1999-11-04 | Nuevos esteres derivados de compuestos fenil-ciclohexil sustituidos |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| DE69911235D1 DE69911235D1 (de) | 2003-10-16 |
| DE69911235T2 true DE69911235T2 (de) | 2004-07-01 |
Family
ID=8305698
Family Applications (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| DE69911235T Expired - Fee Related DE69911235T2 (de) | 1998-11-06 | 1999-11-04 | Neuartige ester abgeleitet von substituierten phenyl-cyclohexyl-verbindungen |
| DE69914229T Expired - Fee Related DE69914229T2 (de) | 1998-11-06 | 1999-11-04 | Neuartige Ester abgeleitet von substituierten Phenyl-Zyklohexyl-Verbindungen |
| DE69914231T Expired - Fee Related DE69914231T2 (de) | 1998-11-06 | 1999-11-04 | Neuartige Ester abgeleitet von substituierten Phenyl-Zyklohexyl-Verbindungen |
Family Applications After (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| DE69914229T Expired - Fee Related DE69914229T2 (de) | 1998-11-06 | 1999-11-04 | Neuartige Ester abgeleitet von substituierten Phenyl-Zyklohexyl-Verbindungen |
| DE69914231T Expired - Fee Related DE69914231T2 (de) | 1998-11-06 | 1999-11-04 | Neuartige Ester abgeleitet von substituierten Phenyl-Zyklohexyl-Verbindungen |
Country Status (39)
| Country | Link |
|---|---|
| US (1) | US6455585B1 (de) |
| EP (3) | EP1219623B1 (de) |
| JP (1) | JP2002529442A (de) |
| KR (1) | KR100453613B1 (de) |
| CN (1) | CN1176902C (de) |
| AP (1) | AP1222A (de) |
| AT (3) | ATE257817T1 (de) |
| AU (1) | AU755681B2 (de) |
| BG (1) | BG105556A (de) |
| BR (1) | BR9915727A (de) |
| CA (1) | CA2349245A1 (de) |
| CR (1) | CR6368A (de) |
| CU (1) | CU23006A3 (de) |
| CZ (1) | CZ20011500A3 (de) |
| DE (3) | DE69911235T2 (de) |
| DK (3) | DK1219623T3 (de) |
| EA (1) | EA003742B1 (de) |
| EE (1) | EE200100246A (de) |
| ES (4) | ES2141688B1 (de) |
| GE (1) | GEP20033116B (de) |
| HR (1) | HRP20010412B1 (de) |
| HU (1) | HUP0104218A3 (de) |
| ID (1) | ID29017A (de) |
| IL (1) | IL142592A0 (de) |
| IS (1) | IS5934A (de) |
| MA (1) | MA26765A1 (de) |
| MX (1) | MXPA01004432A (de) |
| NO (1) | NO20012234L (de) |
| NZ (1) | NZ511739A (de) |
| OA (1) | OA11672A (de) |
| PL (1) | PL347492A1 (de) |
| PT (3) | PT1219623E (de) |
| SI (3) | SI1127871T1 (de) |
| SK (1) | SK284068B6 (de) |
| TR (3) | TR200200416T2 (de) |
| UA (1) | UA59477C2 (de) |
| WO (1) | WO2000027799A1 (de) |
| YU (1) | YU29601A (de) |
| ZA (1) | ZA200104026B (de) |
Families Citing this family (39)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ES2160534B1 (es) * | 1999-12-30 | 2002-04-16 | Vita Invest Sa | Nuevos esteres derivados de (rr,ss)-2-hidroxibenzoato de 3-(2-dimetilaminometil-1-hidroxiciclohexil) fenilo. |
| DE10049483A1 (de) * | 2000-09-29 | 2002-05-02 | Gruenenthal Gmbh | Substituierte 1-Aminobutan-3-ol-Derivate |
| US7776314B2 (en) | 2002-06-17 | 2010-08-17 | Grunenthal Gmbh | Abuse-proofed dosage system |
| WO2004026291A1 (fr) * | 2002-08-28 | 2004-04-01 | Shuyi Zhang | Formulations orales d'ibuprofene et de tramadol, methodes de preparation de ces dernieres |
| ATE391498T1 (de) * | 2002-11-22 | 2008-04-15 | Gruenenthal Gmbh | Verwendung von (1rs,3rs,6rs)-6- dimethylaminomethyl-1-(3-methoxy-phenyl)- cyclohexan-1,3-diol zur behandlung von entzündungsschmerz |
| US20040248979A1 (en) * | 2003-06-03 | 2004-12-09 | Dynogen Pharmaceuticals, Inc. | Method of treating lower urinary tract disorders |
| DE10336400A1 (de) | 2003-08-06 | 2005-03-24 | Grünenthal GmbH | Gegen Missbrauch gesicherte Darreichungsform |
| DE10361596A1 (de) | 2003-12-24 | 2005-09-29 | Grünenthal GmbH | Verfahren zur Herstellung einer gegen Missbrauch gesicherten Darreichungsform |
| US8075872B2 (en) | 2003-08-06 | 2011-12-13 | Gruenenthal Gmbh | Abuse-proofed dosage form |
| US20070048228A1 (en) | 2003-08-06 | 2007-03-01 | Elisabeth Arkenau-Maric | Abuse-proofed dosage form |
| DE102005005446A1 (de) | 2005-02-04 | 2006-08-10 | Grünenthal GmbH | Bruchfeste Darreichungsformen mit retardierter Freisetzung |
| DE102004032051A1 (de) | 2004-07-01 | 2006-01-19 | Grünenthal GmbH | Verfahren zur Herstellung einer gegen Missbrauch gesicherten, festen Darreichungsform |
| DE102004032049A1 (de) | 2004-07-01 | 2006-01-19 | Grünenthal GmbH | Gegen Missbrauch gesicherte, orale Darreichungsform |
| DE102004034619A1 (de) * | 2004-07-16 | 2006-02-23 | Grünenthal GmbH | Substituierte Aminoverbindungen als 5-HT/NA Uptakehemmer |
| DE102005005449A1 (de) | 2005-02-04 | 2006-08-10 | Grünenthal GmbH | Verfahren zur Herstellung einer gegen Missbrauch gesicherten Darreichungsform |
| DE102007011485A1 (de) | 2007-03-07 | 2008-09-11 | Grünenthal GmbH | Darreichungsform mit erschwertem Missbrauch |
| KR101616246B1 (ko) | 2008-01-25 | 2016-05-02 | 그뤼넨탈 게엠베하 | 약제학적 투여형 |
| PL2273983T3 (pl) | 2008-05-09 | 2017-01-31 | Grünenthal GmbH | Sposób wytwarzania pośredniego preparatu proszkowego i końcowej stałej postaci dawkowania z zastosowaniem etapu zestalania rozpyłowego |
| JP5667183B2 (ja) | 2009-07-22 | 2015-02-12 | グリュネンタール・ゲゼルシャフト・ミト・ベシュレンクテル・ハフツング | 加熱溶融押出成型した制御放出性投与剤型 |
| WO2011009604A1 (en) | 2009-07-22 | 2011-01-27 | Grünenthal GmbH | Oxidation-stabilized tamper-resistant dosage form |
| EP2383255A1 (de) * | 2010-04-28 | 2011-11-02 | Lacer, S.A. | Neue Verbindungen, deren Synthese und Verwendung bei der Schmerzbehandlung |
| ES2487244T3 (es) | 2010-09-02 | 2014-08-20 | Grünenthal GmbH | Forma de dosificación resistente a la manipulación que comprende un polímero aniónico |
| BR112013005194A2 (pt) | 2010-09-02 | 2016-05-03 | Gruenenthal Gmbh | forma de dosagem resistente à violação compreendendo sal inorgânico |
| WO2012100423A1 (en) * | 2011-01-27 | 2012-08-02 | Eli Lilly And Company | Analgesic compounds, methods, and formulations |
| EP2530072A1 (de) | 2011-06-03 | 2012-12-05 | Lacer, S.A. | Neue Verbindungen, deren Synthese und Verwendung bei der Schmerzbehandlung |
| US10702485B2 (en) | 2011-07-09 | 2020-07-07 | Syntrix Biosystems Inc. | Compositions and methods for overcoming resistance to tramadol |
| MX348491B (es) | 2011-07-29 | 2017-06-15 | Gruenenthal Gmbh | Tableta a prueba de manipulacion que proporciona liberacion inmediata de fármaco. |
| MX348054B (es) | 2011-07-29 | 2017-05-25 | Gruenenthal Gmbh | Tableta a prueba de alteracion que proporciona liberacion inmediata del farmaco. |
| BR112014019988A8 (pt) | 2012-02-28 | 2017-07-11 | Gruenenthal Gmbh | Forma de dosagem resistente a socamento compreendendo um composto farmacologicamente ativo e um polímero aniônico |
| TR201815502T4 (tr) | 2012-04-18 | 2018-11-21 | Gruenenthal Gmbh | Kurcalama veya dirençli ve doz boşalımına dirençli farmasötik dozaj formu. |
| US9339484B2 (en) * | 2012-05-10 | 2016-05-17 | Cellix Bio Private Limited | Compositions and methods for the treatment of restless leg syndrome and fibromyalgia |
| US10064945B2 (en) | 2012-05-11 | 2018-09-04 | Gruenenthal Gmbh | Thermoformed, tamper-resistant pharmaceutical dosage form containing zinc |
| US10154966B2 (en) | 2013-05-29 | 2018-12-18 | Grünenthal GmbH | Tamper-resistant dosage form containing one or more particles |
| JP6466417B2 (ja) | 2013-05-29 | 2019-02-06 | グリュネンタール・ゲゼルシャフト・ミト・ベシュレンクテル・ハフツング | 二峰性放出プロファイルを有する改変防止(tamper−resistant)剤形 |
| EA032465B1 (ru) | 2013-07-12 | 2019-05-31 | Грюненталь Гмбх | Защищенная от применения не по назначению пероральная фармацевтическая лекарственная форма, содержащая этиленвинилацетатный полимер, и способ ее изготовления |
| WO2015078891A1 (en) | 2013-11-26 | 2015-06-04 | Farmaceutici Formenti S.P.A. | Preparation of a powdery pharmaceutical composition by means of cryo-milling |
| CA2947786A1 (en) | 2014-05-12 | 2015-11-19 | Grunenthal Gmbh | Tamper resistant immediate release capsule formulation comprising tapentadol |
| JP2018517676A (ja) | 2015-04-24 | 2018-07-05 | グリュネンタール・ゲゼルシャフト・ミト・ベシュレンクテル・ハフツング | 即時放出および溶媒抽出に対する耐性を有する改変防止製剤 |
| EP3346991A1 (de) | 2015-09-10 | 2018-07-18 | Grünenthal GmbH | Schutz vor oraler überdosierung mit missbrauchssicheren formulierungen mit sofortiger freisetzung |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE1199764B (de) * | 1963-04-02 | 1965-09-02 | Gruenenthal Chemie | Verfahren zur Herstellung von basisch substituierten Phenolaethern |
| US3652589A (en) * | 1967-07-27 | 1972-03-28 | Gruenenthal Chemie | 1-(m-substituted phenyl)-2-aminomethyl cyclohexanols |
| DE19525137C2 (de) * | 1995-07-11 | 2003-02-27 | Gruenenthal Gmbh | 6-Dimethylaminomethyl-1-phenyl-cyclohexanverbin -dungen als Zwischenprodukte zur Herstellung pharmazeutischer Wirkstoffe |
| DE19609847A1 (de) * | 1996-03-13 | 1997-09-18 | Gruenenthal Gmbh | Dimethyl-(3-aryl-but-3-enyl)-aminverbindungen als pharmazeutische Wirkstoffe |
-
1998
- 1998-11-06 ES ES009802329A patent/ES2141688B1/es not_active Expired - Fee Related
-
1999
- 1999-04-11 UA UA2001063799A patent/UA59477C2/uk unknown
- 1999-11-04 DE DE69911235T patent/DE69911235T2/de not_active Expired - Fee Related
- 1999-11-04 DK DK02075837T patent/DK1219623T3/da active
- 1999-11-04 CZ CZ20011500A patent/CZ20011500A3/cs unknown
- 1999-11-04 SI SI9930450T patent/SI1127871T1/xx unknown
- 1999-11-04 CA CA002349245A patent/CA2349245A1/en not_active Abandoned
- 1999-11-04 ES ES02075838T patent/ES2213732T3/es not_active Expired - Lifetime
- 1999-11-04 TR TR2002/00416T patent/TR200200416T2/xx unknown
- 1999-11-04 AU AU10473/00A patent/AU755681B2/en not_active Ceased
- 1999-11-04 EP EP02075837A patent/EP1219623B1/de not_active Expired - Lifetime
- 1999-11-04 AT AT02075838T patent/ATE257817T1/de not_active IP Right Cessation
- 1999-11-04 EP EP99953994A patent/EP1127871B1/de not_active Expired - Lifetime
- 1999-11-04 AP APAP/P/2001/002161A patent/AP1222A/en active
- 1999-11-04 OA OA1200100111A patent/OA11672A/en unknown
- 1999-11-04 US US09/831,177 patent/US6455585B1/en not_active Expired - Fee Related
- 1999-11-04 ID IDW00200101215A patent/ID29017A/id unknown
- 1999-11-04 DK DK02075838T patent/DK1219594T3/da active
- 1999-11-04 AT AT02075837T patent/ATE257837T1/de not_active IP Right Cessation
- 1999-11-04 CN CNB998129259A patent/CN1176902C/zh not_active Expired - Fee Related
- 1999-11-04 EA EA200100476A patent/EA003742B1/ru not_active IP Right Cessation
- 1999-11-04 MX MXPA01004432A patent/MXPA01004432A/es unknown
- 1999-11-04 DE DE69914229T patent/DE69914229T2/de not_active Expired - Fee Related
- 1999-11-04 YU YU29601A patent/YU29601A/sh unknown
- 1999-11-04 SK SK584-2001A patent/SK284068B6/sk unknown
- 1999-11-04 TR TR2001/01160T patent/TR200101160T2/xx unknown
- 1999-11-04 PL PL99347492A patent/PL347492A1/xx unknown
- 1999-11-04 AT AT99953994T patent/ATE249418T1/de not_active IP Right Cessation
- 1999-11-04 TR TR2002/00415T patent/TR200200415T2/xx unknown
- 1999-11-04 WO PCT/ES1999/000352 patent/WO2000027799A1/es not_active Application Discontinuation
- 1999-11-04 EP EP02075838A patent/EP1219594B1/de not_active Expired - Lifetime
- 1999-11-04 GE GEAP19995930A patent/GEP20033116B/en unknown
- 1999-11-04 PT PT02075837T patent/PT1219623E/pt unknown
- 1999-11-04 DK DK99953994T patent/DK1127871T3/da active
- 1999-11-04 SI SI9930540T patent/SI1219594T1/xx unknown
- 1999-11-04 EE EEP200100246A patent/EE200100246A/xx unknown
- 1999-11-04 KR KR10-2001-7005667A patent/KR100453613B1/ko not_active IP Right Cessation
- 1999-11-04 DE DE69914231T patent/DE69914231T2/de not_active Expired - Fee Related
- 1999-11-04 ES ES02075837T patent/ES2213731T3/es not_active Expired - Lifetime
- 1999-11-04 ES ES99953994T patent/ES2207298T3/es not_active Expired - Lifetime
- 1999-11-04 PT PT02075838T patent/PT1219594E/pt unknown
- 1999-11-04 SI SI9930541T patent/SI1219623T1/xx unknown
- 1999-11-04 NZ NZ511739A patent/NZ511739A/xx unknown
- 1999-11-04 IL IL14259299A patent/IL142592A0/xx unknown
- 1999-11-04 HU HU0104218A patent/HUP0104218A3/hu unknown
- 1999-11-04 PT PT99953994T patent/PT1127871E/pt unknown
- 1999-11-04 JP JP2000580979A patent/JP2002529442A/ja active Pending
- 1999-11-04 BR BR9915727-6A patent/BR9915727A/pt not_active IP Right Cessation
-
2001
- 2001-05-03 IS IS5934A patent/IS5934A/is unknown
- 2001-05-04 NO NO20012234A patent/NO20012234L/no unknown
- 2001-05-07 CU CU2001010920010109A patent/CU23006A3/es unknown
- 2001-05-16 CR CR6368A patent/CR6368A/es not_active Application Discontinuation
- 2001-05-17 ZA ZA200104026A patent/ZA200104026B/en unknown
- 2001-05-23 MA MA26211A patent/MA26765A1/fr unknown
- 2001-05-29 HR HR20010412A patent/HRP20010412B1/xx not_active IP Right Cessation
- 2001-06-01 BG BG105556A patent/BG105556A/xx unknown
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| DE69911235T2 (de) | Neuartige ester abgeleitet von substituierten phenyl-cyclohexyl-verbindungen | |
| EP0753506B1 (de) | 6-Dimethylaminomethyl-1-phenyl-cyclo-hexanverbindungen als pharmazeutische Wirkstoffe | |
| DE1568621C3 (de) | Diurethane, Verfahren zur Herstellung dieser Verbindungen sowie diese enthaltende herbizide Mittel | |
| DE69535315T2 (de) | 1-aminoindanderivate und zusammensetzungen hiervon | |
| EP1251120B1 (de) | Ester abgeleitet vom (rr,ss)-2-hydroxybenzoat des 3-(2-dimethylaminomethyl-1-hydroxycyclohexl)phenyl | |
| EP1758860B1 (de) | Gesättigte und ungesättigte 3-pyridyl-benzocycloalkylmethyl-amine zur behandlung von schmerzen, depressionen und angstzuständen | |
| EP1694318B1 (de) | (s)-2-n-propylamino-5-hydroxytetralin als d3-agonistisches therapeutikum | |
| EP0693475A1 (de) | 1-Phenyl-3-dimethylamino-propanverbindungen mit pharmakologischer Wirkung | |
| DD202001A5 (de) | Verfahren zur herstellung von aminoaethanolen | |
| EP0983995A2 (de) | Dimethyl-(3-aryl-but-3-enyl)-aminverbindungen als pharmazeutische Wirkstoffe | |
| DE60315973T2 (de) | Hydroxy-tetrahydro-naphthalinylharnstoff-derivate | |
| DD145265A5 (de) | Verfahren zur herstellung von phenethanolaminen | |
| EP0521422B1 (de) | Benzomorphane und ihre Verwendung als Arzneimittel | |
| DE3320394A1 (de) | Optisch aktive n-arylierte oxazolidinon-(2)-derivate, deren verwendung als spezifische und reversible inhibitoren von monoaminooxydase des b-typs sowie verfahren zu deren herstellung | |
| DE10048715A1 (de) | Verwendung von Aminosäure zur Behandlung von Schmerz | |
| DE69819922T2 (de) | 2-Amino-6-methyl-7-acetyl-tetralin und pharmazeutische Zusammensetzungen zur Vorbeugung und therapeutischen Behandlung von entzündlichen und/oder Autoimmunkrankheiten | |
| DE2458908C2 (de) | Alkanolaminderivate und sie enthaltende pharmazeutische Zusammensetzungen | |
| DE69725467T2 (de) | Phenylethylamin-derivate | |
| DE2632118A1 (de) | Apovincaminolester und verfahren zu deren herstellung | |
| DE60127182T2 (de) | Prodrugs von exzitatorischen aminosäuren | |
| DE602004009041T2 (de) | Hydroxytetrahydronaphthalenylharnstoffderivate | |
| DE102005009217A1 (de) | Phosphatsalze der 6-Dimethylaminomethyl-1-(3-methoxyphenyl)-1,3-dihydroxy-cyclohexanverbindungen | |
| DD144764A5 (de) | Verfahren zur herstellung von r-n-(2-phenyl-2-hydroxyethyl)-3-phenylpropylaminen | |
| CH643536A5 (de) | Alkanolaminderivate. | |
| CH334848A (de) | Verfahren zur Herstellung von 3-Alkoxyphenoxy-2-oxy-propyl-carbaminsäureestern |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 8364 | No opposition during term of opposition | ||
| 8339 | Ceased/non-payment of the annual fee |