CN1668331A - 半抗原-载体偶联物及其用途 - Google Patents
半抗原-载体偶联物及其用途 Download PDFInfo
- Publication number
- CN1668331A CN1668331A CNA038167484A CN03816748A CN1668331A CN 1668331 A CN1668331 A CN 1668331A CN A038167484 A CNA038167484 A CN A038167484A CN 03816748 A CN03816748 A CN 03816748A CN 1668331 A CN1668331 A CN 1668331A
- Authority
- CN
- China
- Prior art keywords
- conjugate
- nicotine
- phage
- virus
- hapten
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/0013—Therapeutic immunisation against small organic molecules, e.g. cocaine, nicotine
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K17/00—Carrier-bound or immobilised peptides; Preparation thereof
- C07K17/02—Peptides being immobilised on, or in, an organic carrier
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/005—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from viruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/12—Viral antigens
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/385—Haptens or antigens, bound to carriers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/69—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit
- A61K47/6901—Conjugates being cells, cell fragments, viruses, ghosts, red blood cells or viral vectors
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/30—Drugs for disorders of the nervous system for treating abuse or dependence
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/30—Drugs for disorders of the nervous system for treating abuse or dependence
- A61P25/34—Tobacco-abuse
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/51—Medicinal preparations containing antigens or antibodies comprising whole cells, viruses or DNA/RNA
- A61K2039/525—Virus
- A61K2039/5258—Virus-like particles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/555—Medicinal preparations containing antigens or antibodies characterised by a specific combination antigen/adjuvant
- A61K2039/55505—Inorganic adjuvants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/60—Medicinal preparations containing antigens or antibodies characteristics by the carrier linked to the antigen
- A61K2039/6031—Proteins
- A61K2039/6075—Viral proteins
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2730/00—Reverse transcribing DNA viruses
- C12N2730/00011—Details
- C12N2730/10011—Hepadnaviridae
- C12N2730/10111—Orthohepadnavirus, e.g. hepatitis B virus
- C12N2730/10122—New viral proteins or individual genes, new structural or functional aspects of known viral proteins or genes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2795/00—Bacteriophages
- C12N2795/00011—Details
- C12N2795/18011—Details ssRNA Bacteriophages positive-sense
- C12N2795/18111—Leviviridae
- C12N2795/18123—Virus like particles [VLP]
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Organic Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Epidemiology (AREA)
- Immunology (AREA)
- Virology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Mycology (AREA)
- Microbiology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Molecular Biology (AREA)
- Genetics & Genomics (AREA)
- Biophysics (AREA)
- Biochemistry (AREA)
- Gastroenterology & Hepatology (AREA)
- Addiction (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Neurosurgery (AREA)
- Hematology (AREA)
- Cell Biology (AREA)
- Neurology (AREA)
- Biomedical Technology (AREA)
- Psychiatry (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Peptides Or Proteins (AREA)
- Medicinal Preparation (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
Abstract
本发明提供含有一种半抗原与一种载体以有序、重复阵列形式的偶联物的组合物,以及制备这种组合物的方法。本发明的偶联物和组合物可以含有来源于真核生物病毒或噬菌体的病毒样颗粒作为载体,它们与多种半抗原偶联,包括激素、毒素和药物,特别是成瘾性药物,如尼古丁。本发明的组合物和偶联物可用来诱导针对半抗原的免疫应答,它们可能用于多种治疗、预防和诊断方案。在某些实施方案中,使用本发明的偶联物、组合物和方法产生的免疫应答可以用来预防或治疗滥用药物成瘾和与药物成瘾有关的疾病。
Description
发明背景
发明领域
本发明属于医学、公共卫生、免疫学、分子生物学和病毒学领域。
相关技术
成瘾性药物滥用疾病有许多特殊的、公认的后遗症,会导致社会与经济后果。其中包括死亡、疾病、暴力、犯罪、失业、生产力降低、关系与家庭破裂、HIV和其它性传播疾病扩散。1992年,即可以获得可靠数据的最后一年,美国社会由于药物滥用(不包括烟草)造成的经济代价估计为980亿美元(“美国酒精及药物滥用的经济代价-1992年”,国家药物滥用研究所(NIDA))。这些费用包括犯罪(591亿美元)、早产儿死亡(146亿美元)、生产力损失/工伤事故(142亿美元)、福利(104亿美元)、卫生保健(55亿美元)和机动车事故。这些费用主要由政府(46%)、药物滥用者及其家庭(44%)负担。已经公认,药物滥用仍然是社会的一个严重问题。在1992年的研究之后三年,在1995年,NIDA估计社会的药物滥用费用为1100亿美元。
滥用药物本身即对使用者具有毒害作用。然而,已经认识到这些药物的成瘾性既是与使用这些药物有关问题的关键,也是不能治疗成瘾个体及减少社会上药物成瘾流行的根源。
世界上最广泛使用的成瘾性药物是烟草。尼古丁是来源于烟叶的一种生物碱,是烟草的主要成瘾性成分。1999年,美国有4650万成年人是吸烟者。在美国,吸烟是可预防性死亡的唯一主要原因。据疾病预防控制中心(CDC)称,美国每年有430,000例死亡可归因于吸烟。肺癌、冠心病、慢性肺病和中风是死亡的主要原因。吸烟不仅对于个体是危险的,而且产生惊人的社会费用。1993年由吸烟引起的医疗费用估计超过500亿美元,与吸烟有关的失能造成的生产力损失和收入减少费用估计每年为470亿美元。因此,与尼古丁成瘾有关的总经济费用超过其它所有类型的成瘾性药物的费用总和。
尽管最近在行为治疗和药物治疗方面取得了进展,但是大多数试图戒烟的吸烟者都不会成功(综述见Fiore等人(2000)Treatingtobacoo use and dependence,clinical practice guideline,US Departmentof Health and Human Services,Public Health Service)。尼古丁替代治疗是当前使用的一种治疗方法,形式为尼古丁胶、吸入剂、喷鼻剂或透皮贴剂。单独的透皮尼古丁贴剂的效能在安慰剂作为对照的双盲临床试验中遭到质疑(Joseph等人,N.Engl.J.Med.(1999),340:1157-1158;Jorenby等人,N.Engl J.Med.(1999)340:685-691)。此外,对于尼古丁贴剂也观察到尼古丁胶的不良作用,如口腔刺激、颌肌疼痛、消化不良、恶心、呃逆、感觉异常、搔痒、红斑、睡眠障碍、胃肠问题、嗜眠、神经过敏、头晕和出汗。使用抗抑郁剂氨非他酮治疗能够使12个月的戒瘾率提高约30%(Jorenby等人,同上)。
显然需要治疗及预防尼古丁和其它药物成瘾的新方法。自1974年以来,改变药物的行为影响的免疫策略已经是研究的主题。在恒河猴中,使用吗啡-6-半琥珀酸-BSA的主动免疫和使用产生的抗体的被动免疫都可减少了海洛因的自我使用(Bonese等人,Nature252:708-710(1974);Killian等人,Pharmacol.Biochem.Behav.9:347-352(1978))。也已经证明免疫对尼古丁成瘾有效。在大鼠中,主动免疫减少了随后的尼古丁施用的影响(Carrera等人,Nature379:727-730(1995)),证明主动和被动免疫都能消除自我使用尼古丁(Fox等人,Nature Med 2:1129-1132(1996))。最近,在可卡因成瘾的大鼠中,用GNC-KLH偶联物免疫消除了药物的自我使用(Carrera等人Proc.Nat.Acad Sci USA 97:6202-6206 1992(2000)),用GOND-KLH偶联物免疫或者转移抗可卡因单克隆抗体都可阻断可卡因的作用(Carrera等人Proc.Nat.Acad Sci USA,98:1988-1992(2001))。
已经产生了抗苯环利定(PCP)抗体,它在减少脑中PCP水平、减少行为影响方面显示有效,并且显示类似于阻断PCP类似物的生理学效应的能力(Hardin等人.J Pharmacol Exp Ther 285:1113-1122(1998);Proksch等人.J.Pharmacol Exp Ther.292:831-837(2000))。也已经在大鼠中成功产生了抗甲基苯丙胺抗体(Byrnes-Blake等人,IntImmunopharmacol 1:329-338(2001))。美国专利号5,256,409公开了一种疫苗,其含有一种载体蛋白,该载体蛋白与来自地昔帕明/米帕明类药物的一个半抗原和来自去甲替林/阿米替林类药物的另外一个半抗原结合。
因此,能够产生针对药物的免疫应答,抗体能够阻断药物的作用,动物模型已经证明,接种作为一种治疗药物滥用和成瘾的一般方法是有效的。据信免疫应答通过阻止药物进入中枢神经系统来阻断药物的作用(Carrera等人Nature 379:727-730(1995))。通过减少与药物使用有关的后果,成瘾的个体不再有使用药物的动力。
由于药物的成瘾作用是由它们在脑中的作用引起的,因此血清中的抗体应当能够减少药物向脑中的输送。Cerny(WO 92/03163)描述了用于对抗滥用药物的一种疫苗和免疫血清。该疫苗包含与一种载体蛋白结合的一种半抗原。该文献也公开了针对药物的抗体的产生,这些抗体在服用药物的个体的解毒中的用途。
尼古丁、可卡因、海洛因和大多数滥用药物都是半抗原,它们没有免疫原性。半抗原与蛋白质载体的偶联一般提高它们的免疫原性。
已经描述了几种不同的尼古丁半抗原、载体和偶联方法。Matsushita等人(Biochem.Biophys.Res.Comm.(1974)57,1006-1010)和Castro等人(Eur.J.Biochem.(1980)104,331-340)制备了在尼古丁的6位通过一个接头与牛血清白蛋白(BSA)偶联的尼古丁半抗原。另外,Castro等人(Biochem.Biophys.Res.Commun.(1975)67,583-589)也公开了两种尼古丁白蛋白偶联物:N-琥珀酰-6-氨基-(+/-)-尼古丁-BSA和6-(σ-氨基癸酰氨基)-(+/-)-尼古丁-BSA。Noguchi等人(Biochem.Biophys.Res.Comm.(1975)83,83-86)制备了与尼古丁在尼古丁的1位处偶联的一种尼古丁-BSA偶联物。Langone等人(Biochemistry(1973)12,5025-5030和Meth.Enzymol.(1982)84,628-635)制备了半抗原衍生物O-琥珀酰-3′-羟甲基-尼古丁,并将其与牛血清白蛋白和匙孔戚血蓝蛋白偶联。按照Langone等人(同上)的方法,Abad等人(Anal.Chem.(1993)65,3227-3231)合成了尼古丁半抗原3′-(羟甲基)-尼古丁半琥珀酸酯,并将其与牛血清白蛋白偶联,用于免疫小鼠,产生抗尼古丁单克隆抗体。Isomura等人(J.Org.Chem.(2001)66,4115-4121)提供了合成与尼古丁的1’位连接的尼古丁偶联物的方法,它与匙孔戚血蓝蛋白(KLH)和BSA偶联。使用与KLH的偶联物免疫小鼠,产生抗尼古丁的单克隆抗体。Svensson等人(WO 99/61054)公开了通过吡啶环偶联的尼古丁半抗原,并且进一步公开了与KLH偶联的一种尼古丁半抗原,以及使用这些偶联物诱导尼古丁特异性IgG抗体。当在弗氏完全佐剂存在下施用时,测定尼古丁特异的ELISA滴度为1∶3000-1∶15500,而在不存在弗氏佐剂的情况下,检测到滴度为1∶500-1∶3000。Ennifar等人(美国专利号6,232,082)公开了通过吡咯烷环偶联的尼古丁半抗原,并且公开了与重组铜绿假单胞菌(Psuedomonas aeruginosa)外毒素A(rEPA)偶联的一种尼古丁半抗原,以及当偶联物在弗氏完全佐剂存在下施用时,尼古丁特异性IgG抗体的诱导。Swain等人(美国专利号5,876,727)公开了一种尼古丁半抗原与BSA的偶联,以及当偶联物与弗氏完全佐剂混合施用时,小鼠中尼古丁特异性IgG抗体的诱导。
已经基本证明了针对尼古丁接种的可行性(Hieda等人,J.Pharm.Exp.Ther.(1997)288,1076-1081;Hieda等人,Psychopharm.(1999),143,150-157;Hieda等人,Int.J.Immunopharm.(2000)22,809-819;Pentel等人,Pharm.Biochem.Behav.(2000),65,191-198,Malin等人,Pharm.Biochem.Behav.(2001),68,87-92)。制备了尼古丁与KLH或rEPA的共价偶联物,在弗氏完全佐剂存在下注射小鼠或大鼠,诱导了尼古丁特异性IgG抗体。疫苗的效能通过几种不同的方法被证实。用尼古丁攻击后,与单独用载体免疫的对照组相比,在尼古丁-KLH或尼古丁-rEPA免疫的大鼠组中,血清中有更多的尼古丁保持结合,脑中的尼古丁浓度较低。免疫也降低了与尼古丁有关的精神药理学活性,因为免疫的动物对于尼古丁的运动影响、多巴胺释放(Svensson等人,WO 99/61054)和缓解尼古丁戒断症状的敏感性也较低。
上述文献证明了含有弗氏完全佐剂的疫苗组合物诱导针对尼古丁的免疫应答的效能。弗氏完全佐剂是可以使用的最有效的佐剂之一,然而由于它的副作用,它未被批准用于人。因此,需要不使用弗氏完全佐剂即能够诱导针对尼古丁的强免疫应答的疫苗组合物。此外,尽管BSA已经在动物模型中成功用作载体,但是由于不良反应的危险,如传播朊病毒病(变异型克罗伊茨费尔特-雅各布病)的危险,它可能不适合在人类疫苗组合物中使用。研制针对尼古丁的有效疫苗的另外一个挑战是需要能够快速减少可被脑吸收的尼古丁的免疫应答。来源于香烟的尼古丁被粘膜表面(特别是口和肺中)吸收,通过血液转运到脑中。如果尼古丁特异性抗体成功减少尼古丁向脑的输送,则必须克服在吸入数秒内呈递给大脑的极高的动脉尼古丁浓度(Hieda等人,1999,同上)。因此,血液中需要有高浓度的尼古丁特异性抗体,主要是IgG亚型。在粘膜表面,IgA抗体是主要的亚型。因此,除了血液中的抗体之外,肺中IgA亚型的尼古丁特异性抗体将有利于在开始在血液中循环之前中和吸烟过程中吸入的尼古丁。
霍乱毒素是本领域已知的一种载体蛋白,能够诱导IgA抗体,特别是在鼻内施用之后。霍乱毒素也能够作为一种佐剂,从而在疫苗组合物中不需要弗氏完全佐剂。然而,当霍乱毒素作为一种粘膜佐剂施用时,它主要刺激TH2型免疫应答,白介素-4水平升高,总的及特异性IgE抗体水平相应升高(Yamamoto等人,(1997)Proc.Natl.Acad.SciUSA 94,5267-5272)。在霍乱毒素存在下经鼻免疫后,在小鼠肺内发展与IgE相关的炎症反应(Simecka等人,(2000)Infect.Immunol.68,672-679,Hodge等人,(2001)Infect.Immunol.,69,2328-2338)。尽管在霍乱毒素存在下的鼻内免疫大有希望,但是也存在发生特征在于肺呼吸道炎症的不利免疫病理学反应的可能性(Hodge等人,(2001)Infect.Immunol.,69,2328-2338)。
因此,仍然需要这样的载体系统:它能够刺激针对半抗原的免疫应答,而不需要使用毒性佐剂,不需要使用耐受性较差的载体蛋白,在某些情况下,不刺激潜在病理性TH2免疫应答。满足这些要求的新型载体系统能够用来形成适于治疗成瘾性的新型偶联物和组合物,与其它疾病相比,这是当前急需的。
发明概述
我们发现,与核心颗粒连接产生高度有序、重复的半抗原阵列的半抗原在诱导针对半抗原的免疫应答,特别是诱导抗体方面出人意料地有效。含有第一附着位点的核心颗粒和含有第二附着位点的半抗原通过该第一和第二附着位点连接,形成有序、重复的半抗原阵列。第一与第二位点之间的相互作用可以是直接的,或者可能涉及至少一个其它分子,例如接头。
在一个实施方案中,第一附着位点在核心颗粒中天然存在。或者,也可以通过化学偶联或重组技术添加第一附着位点。优选的第一附着位点包括氨基、羧基或巯基。包含第一附着位点的优选氨基酸选自:赖氨酸、精氨酸、半胱氨酸、天冬氨酸、谷氨酸、酪氨酸和组氨酸。特别优选的是赖氨酸残基。
半抗原上适当的第二附着位点有胺、酰胺、羧基和巯基。已经研制了多种化合物,用于通过与核心颗粒蛋白质分子的反应性基团形成共价键,使得肽/蛋白质能够交联,或者蛋白质与衍生化分子能够偶联。
本发明包含第一附着位点的核心颗粒包括适于形成有序、重复阵列的任何颗粒。在一些实施方案中,这类核心颗粒包括病毒样颗粒(VLP)、噬菌体、噬菌体病毒样颗粒、菌毛等。在某些实施方案中,核心颗粒包括HBcAg VLP、噬菌体VLP和I型菌毛。本发明也提供仍然能够形成有序、重复结构的核心颗粒的变体形式。变体形式包括核心颗粒的重组及天然形式和突变形式。在某些实施方案中,核心颗粒的突变形式包括第一附着位点的类型或数量与亲本不同的形式。核心颗粒上赖氨酸残基数量的改变是特别优选的。
在某些实施方案中,本发明的偶联物包含适于诱导针对各种分子的免疫应答的半抗原,包括但不限于毒素、激素和药物。更优选的是药物,更优选的是滥用性药物或成瘾性药物。本发明的半抗原含有第二附着位点,用于与核心颗粒的第一附着位点直接连接或者通过至少一个连接分子连接。在一个实施方案中,该半抗原适于诱导针对可卡因(例如琥珀酰化去甲可卡因)的免疫应答。
本发明优选的实施方案是尼古丁半抗原偶联物。适合本发明偶联物的尼古丁半抗原可以含有与尼古丁的吡啶或吡咯烷环上的任一位点键合的至少一个、优选地一个侧链。本领域技术人员知道如何生产适当的尼古丁半抗原衍生物。例如,尼古丁可以在3’位化学衍生,产生一个羟基残基,该残基适合与琥珀酸酐等试剂反应,形成O-琥珀酰-3′-羟甲基-尼古丁。可以使用活化试剂EDC,将该尼古丁衍生物与核心颗粒的氨基酸(如赖氨酸)偶联。在一个进一步优选的实施方案中,O-琥珀酰-3′-羟甲基-尼古丁可以用EDC活化,产生的活化的羧基用N-羟基琥珀酰亚胺稳定。在其它一些实施方案中,在两个当量的二异丙基乙胺的存在下,通过在二氯甲烷中用琥珀酸酐酰化降烟碱,产生半抗原。然后使用活化试剂如HATU,使这种尼古丁半抗原与本发明的核心颗粒偶联。还提供了合成适合本发明偶联物和组合物的半抗原的其它一些方法。
本发明提供包含核心颗粒和半抗原的、适于诱导免疫应答的组合物。本发明的组合物包括疫苗组合物,其中含有或不含其它药学上可接受的赋形剂或佐剂。提供了免疫方法。更优选的是鼻内免疫。
本发明的组合物诱导免疫应答,包括抗体的产生。因此,在另外一个实施方案中,本发明提供生产针对这些半抗原的抗体的方法。本发明的这些抗体可用于疾病的治疗或预防,以及半抗原的检测,例如诊断与动物组织或循环中存在一种或多种半抗原有关的疾病的方法。
在一个相关实施方案中,本发明可用于疾病、紊乱或病症的预防或治疗,包括但不限于:毒素中毒、激素水平紊乱(disregulation)、药物中毒或药物成瘾等。用本发明的半抗原-载体偶联物免疫产生针对该半抗原的免疫应答,致使免疫分子、特别是抗体与该半抗原结合。被动给予抗体也可以用于疾病的治疗和预防。成瘾性的治疗在与成瘾有关的其它疾病和病症的治疗中也是有用的。
我们发现,与病毒样颗粒连接的尼古丁-半抗原偶联物诱导高尼古丁特异性IgG抗体。因此本发明提供用于尼古丁成瘾的一种治疗剂,它是以一种有序、重复的VLP-尼古丁偶联物为基础的。这种治疗剂在接种的动物中能够诱导高滴度的抗尼古丁抗体。甚至在不使用佐剂时也能够诱导高滴度抗体,不仅包括IgG亚型,而且包括IgA亚型。而且,令人吃惊的是,这种治疗剂与潜在病理性免疫应答(如炎症)的诱导无关。本发明的治疗组合物包含至少一个尼古丁半抗原分子和VLP,或者至少一个尼古丁半抗原和其他核心颗粒,如HBcAg或菌毛。
因此,本发明包括治疗和预防方法,包括使用本发明的偶联物和组合物。这些方法可用于与药物、激素和毒素有关的疾病、紊乱和病症的治疗和预防。
在本发明的另外一个实施方案中,提供了一种药物组合物,其用于治疗尼古丁成瘾、缓解尼古丁戒断症状、帮助戒烟或者防止复吸,该组合物含有本发明的疫苗组合物与另一种药物的治疗有效的组合。在一个实施方案中,这另一种药物选自:抗抑郁剂;尼古丁受体调节剂;大麻素受体拮抗剂;阿片受体拮抗剂;单胺氧化酶抑制剂;抗焦虑剂,或这些药物的任意组合。
本发明的其它实施方案包括使用本发明的偶联物、组合物和方法的适合诊断和筛查的试剂盒。根据本领域所知、下列附图和发明描述以及权利要求书,技术人员将会明了本发明的其它实施方案。
附图简述
图1显示Nic-Qβ偶联物的SDS-PAGE和Westernblot分析。尼古丁衍生物Suc-Nic以不同的浓度(1x、5x、50x、100x和500x摩尔过量)与Qβ偶联。将反应溶液等份加样到16%SDS-PAGE凝胶上,用考马斯蓝染色(A)。将蛋白质从平行电泳的凝胶上转移到硝酸纤维素上,用一种抗尼古丁-霍乱毒素的抗血清检测,随后进行HRPO-偶联的山羊抗小鼠IgG和ECL检测(B)。左侧空白处是分子量标准。
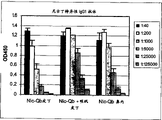
图2显示尼古丁特异性IgG抗体和IgG滴度。通过ELISA检测来自接种小鼠的血清对与BSA偶联的尼古丁的反应性。显示了每个血清稀释度获得的450nm的光密度(A)。根据获得半数最大光密度时的稀释度计算滴度(B)。显示了每组三只小鼠的平均值。
图3显示尼古丁特异的IgG亚型。通过ELISA检测来自接种小鼠的血清对与BSA偶联的尼古丁的反应性,并用IgG亚型IgGI(A)、IgG2a(B)、IgG2b(C)和IgG3(D)特异的第二抗体检测。显示了每个血清稀释度获得的450nm的光密度。显示了每组三只小鼠的平均值。
图4显示尼古丁特异的IgE抗体。通过ELISA检测来自接种小鼠的血清对与BSA偶联的尼古丁的反应性,并用IgE亚型特异的第二抗体检测。显示了每个血清稀释度获得的450nm的光密度。显示了每组三只小鼠的平均值。
图5显示尼古丁特异的IgA抗体。通过ELISA检测来自接种小鼠的血清对与BSA偶联的尼古丁的反应性,并用IgA亚型特异的第二抗体检测。显示了每个血清稀释度获得的450nm的光密度。显示了每组三只小鼠的平均值。
图6显示尼古丁-VLP接种的效能。用尼古丁-VLP免疫小鼠,在注射3H-尼古丁后测定血清和脑中的尼古丁浓度。显示每组4或5只小鼠的平均值。
发明详述
应当理解,以上概述和以下详述只是举例说明,旨在进一步说明要求保护的本发明。
定义
下列定义是相关领域技术人员通常理解的概念的概括,是为了理解本发明,而并非意在限制本发明。
佐剂:如此处所用的术语“佐剂”指免疫应答的非特异性刺激剂,或者可以在宿主中产生储存的物质,当分别与本发明的疫苗和药物组合物混合时,可以引起更强的免疫应答。可以使用多种佐剂。例子包括:弗氏完全及不完全佐剂、氢氧化铝和修饰的胞壁酰二肽。其它佐剂包括:无机凝胶如氢氧化铝,表面活性物质如溶血卵磷脂,pluronic多聚醇,聚阴离子,肽,油状乳剂,匙孔戚血蓝蛋白,二硝基酚,以及潜在可用于人的佐剂,如BCG(卡介苗)和小棒杆菌(Corynebacteriumparvum)。这些佐剂在本领域公知。能够与本发明的组合物一起施用的其它佐剂包括但不限于:单磷酸脂免疫调节剂、AdjuVax 100a、QS-21、QS-18、CRL1005、铝盐(明矾)、MF-59、OM-174、OM-197、OM-294和病毒体佐剂技术。佐剂也可包括这些物质的混合物。
本领域已知来源于南美树木Quillaja Saponaria Molina树皮的、具有佐剂活性的免疫活性皂苷级分。例如,QS21,也被称为QA21,是一种HPLC纯化的来自Quillaja Saponaria Molina树的级分,在美国专利号5,057,540中公开(作为QA21)了其生产方法。Scott等人,Int.Archs.Allergy Appl.Immun.,1985,77,409也公开了作为佐剂的Quillaja皂苷。单磷酸脂A及其衍生物在本领域公知。一种优选的衍生物是3-脱氧酰化单磷酰脂A。进一步优选的佐剂在WO00/00462中描述,其公开内容在此引用作为参考。
然而,本发明的一个有利的特征是本发明组合物的高免疫原性。如此处已经概述的,或者随着本说明书的继续将要理解的,在另外一个或优选的实施方案中,提供了不含佐剂的疫苗和药物组合物,产生用于治疗药物成瘾,优选地治疗尼古丁成瘾的疫苗和药物组合物,其不含佐剂,因而具有出色的安全性,因为佐剂可引起副作用。如此处所用的术语“不含”在治疗药物成瘾、优选地治疗尼古丁成瘾的疫苗和药物组合物中指在无佐剂的情况下使用疫苗和药物组合物。
动物:如此处所用的术语“动物”包括,例如:人、绵羊、麋鹿、鹿、黑尾鹿、水貂、哺乳动物、猴、马、牛、猪、山羊、狗、猫、大鼠、小鼠、鸟类、鸡、爬行动物、鱼、昆虫和蜘蛛类动物。
抗体:如此处所用的术语“抗体”是指能够结合表位或抗原决定簇的分子。该术语包括整个抗体及其抗原结合性片段,包括单链抗体。最优选地,这些抗体是人抗原结合性抗体片段,包括但不限于:Fab、Fab’和F(ab’)2、Fd、单链Fvs(scFv)、单链抗体、二硫键连接的Fvs(sdFv),以及包含VL或VH域的片段。这些抗体可以来自任何动物来源,包括鸟类和哺乳动物。优选地,这些抗体是人、鼠、兔、山羊、豚鼠、骆驼、马等哺乳动物或其它合适的动物如鸡的抗体。如此处所用的“人”抗体包括含有人免疫球蛋白氨基酸序列的抗体,包括分离自人免疫球蛋白文库、或者来自表达一种或多种人免疫球蛋白且不表达内源性免疫球蛋白的转基因动物的抗体,如美国专利号5,939,598所述,其公开内容在此全文引用作为参考。
主动免疫:如此处所用的术语“主动免疫”是指通过施用免疫原、疫苗、抗原或半抗原-载体偶联物,在个体、一般是在动物中引起的免疫应答的诱导。相反,被动免疫是指通过向个体内转移免疫分子或细胞使该个体具有免疫力。
甲病毒:如此处所用的术语“甲病毒”是指甲病毒属包括的所有RNA病毒。Strauss和Strauss,Microbiol.Rev.,58:491-562(1994)描述了该属的成员。甲病毒的例子包括:奥拉病毒、毕巴鲁病毒、卡巴苏病毒、屈曲病毒、东方马脑炎病毒、摩根堡病毒、盖塔病毒、克孜勒阿加什病毒、马亚罗病毒、米德尔堡病毒、穆茨布病毒、恩杜姆病毒、皮克孙纳病毒、托纳特病毒、特里尼蒂病毒、乌纳病毒、西方马脑炎病毒、沃达罗河病毒、辛德毕斯病毒(SIN)、塞姆利基森林病毒(SFV)、委内瑞拉马脑炎病毒(VEE)和罗斯河病毒。
抗原:如此处所用的术语“抗原”是指如果被MHC分子呈递时能够被抗体或T细胞受体(TCR)结合的分子。抗原还能够被免疫系统识别和/或能够诱导体液免疫应答和/或细胞免疫应答,导致B和/或T淋巴细胞激活。然而,至少在某些情况下,这可能需要抗原含有或连接于Th细胞表位,并且包含于佐剂中。抗原可能包含一个或多个表位(B和T表位)。上述特异性反应是指抗原优先、通常以高选择性方式与其相应抗体或TCR反应,而不与可能由其它抗原诱导的许多其它抗体或TCR反应。如此处所用的抗原也可以是几种不同抗原的混合物。
抗原决定簇:如此处所用的术语“抗原决定簇”是指可被B或T淋巴细胞特异识别的抗原部分。B淋巴细胞响应抗原决定簇产生抗体,而T淋巴细胞通过增殖和建立对于细胞和/或体液免疫的介导至关重要的效应功能,响应抗原决定簇。
连接(association):如此处所用的术语“连接”当用于第一和第二附着位点时,是指第一与第二附着位点优选地通过至少一个非肽键结合。连接的性质可能是共价、离子、疏水、极性的或其任意组合,优选地,连接的性质是共价的。
第一附着位点:如此处所用的短语“第一附着位点”是指核心颗粒的元件,位于抗原或抗原决定簇上的第二附着位点可与之连接。第一附着位点可以是蛋白质、多肽、氨基酸、肽、糖、多核苷酸、天然或合成的聚合物、次级代谢物或化合物(生物素、荧光素、视黄醇、洋地黄毒苷、金属离子、苯甲基磺酰氟)或其组合,或者是其化学反应性基团。非天然分子支架的表面上以重复方式存在着多个第一附着位点。
第二附着位点:如此处所用的短语“第二附着位点”是指与半抗原相关的元件,位于非天然分子支架表面上的第一附着位点可与之连接。半抗原的第二附着位点包含任何化学基团,优选地是胺、酰胺、羧基、巯基、羟基、醛、酰卤、肼、重氮基或酰肼,或者是能够与第一附着位点特异反应的其它化学基团。而且,第二附着位点可能包括多肽、肽、糖、多核苷酸、天然或合成的聚合物、次级代谢物或化合物(生物素、荧光素、视黄醇、洋地黄毒苷、金属离子、苯甲基磺酰氟)、其组合或其化学反应性基团。半抗原上存在至少一个第二附着位点。因此,术语含有至少一个第二附着位点的“半抗原”是指至少含有半抗原和第二附着位点的半抗原构建体。然而,特别是对于半抗原内非天然存在的第二附着位点,这些半抗原含有一个将半抗原与第二附着位点相结合的接头,或者更优选地,该接头已经包含或者含有第二附着位点。
结合(bound):如此处所用的术语“结合”是指结合或附着,它们可以是共价的,例如通过化学偶联,或者是非共价的,例如离子相互作用、疏水相互作用、氢键等。共价键可以是,例如:酯、醚、磷酯、酰胺、肽、酰亚胺、碳-硫键、碳-磷键等。术语“结合”比术语如“偶联”、“融合”和“附着”范围更广,并且包括后者。
核心颗粒:如此处所用的术语“核心颗粒”是指具有固有重复组织的刚性结构,它为第一附着位点的附着提供基础。如此处使用的核心颗粒可以是一种合成方法的产物或一种生物学方法的产物。
外壳蛋白:如此处所用的术语“外壳蛋白”是指噬菌体或RNA噬菌体的蛋白质,它能够掺入噬菌体或RNA噬菌体的衣壳装配体内。然而,当指RNA噬菌体的外壳蛋白基因的具体基因产物时,使用术语“CP”。例如,RNA噬菌体Qβ的外壳蛋白基因的具体基因产物被称为“QβCP”,而噬菌体Qβ的“外壳蛋白”包括“QβCP”以及辅助A1蛋白。噬菌体Qβ的衣壳主要由QβCP组成,含有少量A1蛋白。同样,VLP Qβ外壳蛋白主要含有QβCP,以及少量A1蛋白。
偶联物:如此处所用的名词“偶联物”是指一个或多个(a)核心颗粒如VLP与一个或多个(b)如此处所述的有机分子、半抗原、抗原或抗原决定簇偶联的产物,其中组分(a)和(b)彼此结合。
组合物:如此处所用的术语“组合物”是指混合或组合不同组分或成分的产物。
疾病、紊乱、病症:如此处所用的术语“疾病”或“紊乱”是指个体的任何不利病症,包括肿瘤、癌症、变态反应、成瘾、自身免疫、中毒或最佳精神或身体机能的损害。如此处所用的“病症”包括疾病和紊乱,而且也指生理状态。例如,生育力是一种生理状态,而不是一种疾病或紊乱。因此,适合通过降低生育力防止妊娠的本发明的组合物作为一种病症(生育力)的治疗,而不是一种紊乱或疾病的治疗。本领域技术人员知道其它一些病症。
有效量:如此处所用的术语“有效量”是指足以达到希望的生物学效应的量或必需的量。组合物的有效量是能够达到所选结果的量,此含量可由本领域技术人员常规确定。例如,治疗免疫系统缺陷的有效量是引起免疫系统激活、在接触抗原后产生抗原特异性免疫应答所必需的量。该术语也与“足量”同义。
用于任何一种具体用途,有效量可能根据如下因素而变化:所治疗的疾病或病症、施用的具体组合物、患者体重和/或疾病的严重程度。本领域技术人员能够根据经验确定本发明的具体组合物的有效量,而不需要过多的实验。
表位:如此处所用的术语“表位”是指被个体抗体或T细胞受体识别的基本元件或最小单位,因而是指该抗体或T细胞受体能够结合的特定结构域、区或分子结构。一个抗原可以包含多个表位,而一个半抗原一般可能含有极少的表位。
融合:如此处所用的术语“融合”是指不同来源的氨基酸序列通过其编码核苷酸序列的框内组合在一条多肽链中组合。除了与末端之一融合外,术语“融合”还包括内部融合,即不同来源的序列插入一条多肽链内。
半抗原:如此处所用的术语“半抗原”是指一种低分子量有机化合物,它本身不能引发免疫应答,但是在与一种载体分子连接后能引发免疫应答。本发明的偶联物、组合物和方法中使用的说明性半抗原包括药物、激素和毒素,但是不限于这些具体的半抗原。
异源序列:如此处所用的术语“异源序列”是指核酸或蛋白质的第二种序列,它不是该核酸或蛋白质正常所见序列,通常是人工添加到该序列中,以提供特定的性质。在一个实施例中,为了蛋白质的纯化或者作为第一附着位点,可以向重组衣壳蛋白中添加异源氨基酸。
分离的:如此处所用的术语“分离的”当用于一种分子时,该术语的含义是,该分子已经从其天然环境中分离。例如,活动物中自然存在的多核苷酸或多肽不是“分离的”,但是与天然状态的共存物质分开的相同多核苷酸或多肽是“分离的”。此外,对于本发明而言,载体中所含的重组DNA分子被认为是分离的。分离的RNA分子包括DNA和RNA分子的体内或体外RNA复制产物。分离的核酸分子还包括通过合成生产的分子。另外,重组宿主细胞中所含的载体分子也是分离的。因此,不是所有“分离的”分子都必须是“纯化的”。
免疫应答:如此处所用的术语“免疫应答”是指导致B和/或T淋巴细胞和/或抗原呈递细胞激活或增殖的体液免疫应答和/或细胞免疫应答。然而,在某些情况下,免疫应答可能是低强度的,只有在使用至少一种本发明的物质时才能检测到。“免疫原性的”是指一种试剂,它用来刺激活生物的免疫系统,使得免疫系统的一种或多种功能增强,并且针对该免疫原性试剂。“免疫原性多肽”是一种多肽,无论它是单独的还是与载体相连接,使用还是不使用佐剂,它都能引发细胞和/或体液免疫应答。优选地,抗原呈递细胞可以被激活。
“增强”免疫应答的物质是指这样一种物质:与不添加该物质时测得的相同的免疫应答相比,添加该物质时观察到更高或增强或偏离的免疫应答。例如利用51Cr释放试验,能够测定在免疫中使用及不使用该物质获得的样品中细胞毒性T细胞的裂解活性。与不使用该物质时的CTL裂解活性相比,CTL裂解活性提高时的物质的量被认为是足以增强动物对该抗原的免疫应答的量。在一个优选实施方案中,免疫应答至少以约2倍、更优选地约3倍或更多的方式增强。分泌的细胞因子的量或类型也可能改变。或者,诱导的抗体或其亚类的量也可能改变。
免疫:如此处所用的术语“免疫”或相关术语是指提供产生针对靶抗原或表位的实质性免疫应答(包括抗体和/或细胞免疫,如效应CTL)的能力。这些术语不要求产生完全免疫,而是产生实质性高于基线的免疫应答。例如,如果在使用本发明的方法后哺乳动物产生针对靶抗原的细胞和/或体液免疫应答,则可认为该动物针对该靶抗原进行了免疫。
免疫治疗剂:如此处所用的术语“免疫治疗剂”是一种用于治疗疾病、紊乱或病症的组合物。更具体而言,该术语是指一种治疗方法,其中通过接种或者通过给予免疫分子,产生一种有利的免疫应答。
免疫有效量:如此处所用的术语“免疫有效量”是指当导入个体时足以在该个体中诱导免疫应答的组合物的量。对于主动免疫,该术语与“免疫原性有效的量”同义。达到免疫有效所需的组合物的量根据多种因素而不同,包括组合物、组合物中其它成分(例如佐剂)的存在、抗原、免疫途径、个体、在先免疫或生理状态等。
个体:如此处所用的术语“个体”是指多细胞生物,包括植物和动物。优选的多细胞生物是动物,更优选的是脊椎动物,更加优选的是哺乳动物,最优选的是人。
低或不可检测的:如此处所用的短语“低或不可检测的”当用于基因表达水平时,是指表达水平显著低于基因最大诱导时所见(例如至少低5倍),或者用下文实施例部分所述方法不易检测到。
凝集素:在此使用时,指特别是从豆科植物的种子,以及从其它多种植物和动物来源获得的蛋白质,它们具有特定单糖或寡糖的结合位点。例子包括伴刀豆球蛋白A和麦胚凝集素,它们在糖蛋白研究中广泛用作分析性和制备性试剂。
天然来源:如此处所用的术语“天然来源”是指其全部或部分不是合成的,而是自然存在或产生的。
非天然的:如此处所用的该术语通常是指并非来源于自然,更具体而言,该术语是指来自人工。
非天然来源:如此处所用的术语“非天然来源”通常是指合成的或者并非来自天然;更具体而言,该术语是指来自人工。
非天然分子支架:如此处所用的短语“非天然分子支架”是指用来提供第一附着位点的刚性、重复阵列的人工制成的任何产物。理想地但不是必须地,这些第一附着位点为几何顺序。非天然分子支架的部分或全部可以是有机或无机的,可以化学合成或者通过生物学方法合成。非天然分子支架包括:(a)一种天然或非天然来源的核心颗粒;(b)至少一个第一附着位点,它通过至少一个共价键与核心颗粒连接。在一个具体实施方案中,非天然分子支架可以是一种病毒、病毒样颗粒、细菌菌毛、病毒衣壳颗粒、噬菌体、其重组形式或合成颗粒。
尼古丁半抗原:如本发明使用的术语“尼古丁半抗原”是指其对映体纯的(S)-或(R)-形式的尼古丁或其混合物,它可以衍生化含有至少一个第二附着位点,于是能够与载体的第一附着位点直接结合或者通过一种接头结合。优选地,将尼古丁半抗原衍生化,使其只含一个第二附着位点。这种衍生化进一步提高了尼古丁半抗原-载体偶联物的顺序和重复性,并确保尼古丁半抗原与载体的定向、控制的偶联。
有序、重复的抗原或抗原决定簇阵列:如此处所用的术语“有序、重复的抗原或抗原决定簇阵列”通常是指抗原或抗原决定簇的一种重复模式,其特征在于抗原或抗原决定簇相对于非天然分子支架均匀空间排列。在本发明的一个实施方案中,这种重复模式可以是一种几何模式。合适的有序、重复抗原或抗原决定簇阵列的典型和优选实例是具有严格重复的抗原或抗原决定簇类结晶排列的阵列,优选地间隔0.5-30纳米,优选地5-15纳米。
被动免疫:如此处所用的术语“被动免疫”是指通过任何途径向动物体内施以外部产生的免疫分子(例如抗体)或细胞(例如T细胞)产生免疫。被动免疫不同于“主动”免疫,后者是通过向个体内导入免疫原、疫苗、抗原或半抗原-载体偶联物,引发免疫应答而获得免疫。
菌毛:如此处所用的术语“菌毛”是指细菌细胞的胞外结构,它由蛋白质单体(例如菌毛单体)组成,这些单体组成有序、重复的模式。此外,菌毛也是与多种过程有关的结构,如细菌细胞与宿主细胞表面受体的附着、细胞间基因交换和细胞-细胞识别。菌毛的例子包括1型菌毛、P-菌毛、F1C菌毛、S-菌毛和987P-菌毛。菌毛的其它例子在此处其它部分描述。
菌毛样结构:如此处所用的短语“菌毛样结构”是指具有类似于菌毛的特征、由蛋白质单体组成的结构。“菌毛样结构”的一个例子是由细菌细胞形成的一种结构,该细胞表达修饰的菌毛蛋白,该菌毛蛋白不形成与天然菌毛基本相同的有序、重复的阵列。
多肽:如此处所用的术语“多肽”是指由单体(氨基酸)通过酰胺键(也被称为肽键)线性连接而成的分子。它是指氨基酸分子链,不是指特定长度的产物。因此,多肽的定义内包括肽、二肽、三肽、寡肽和蛋白质。该术语也指多肽的表达后修饰,例如糖基化、乙酰化、磷酸化等。重组或衍生的多肽不一定由指定的核酸序列翻译而来。也可以用任何一种方法生产,包括化学合成。
蛋白质:如此处所用的术语蛋白质是指大小通常超过约5个或更多、10个或更多、20个或更多、25个或更多、50个或更多、75个或更多、100个或更多、200个或更多、500个或更多、1000个或更多、2000个或更多氨基酸的多肽。蛋白质通常具有确定的三维结构,尽管它们不一定必须是折叠的,但通常指折叠的,不同于通常不具有确定三维结构的肽和多肽,后者能够采取许多不同的构象,被称为非折叠的。然而,肽也可以采取三维结构。对于由第二附着位点介导、特别是使用一种化学交联剂通过第一与第二附着位点之间的化学交联介导的核心颗粒与蛋白质的结合,蛋白质的确定的三维结构是特别重要的。在本发明的某些方面,氨基酸接头也与蛋白质的结构特征密切相关。
纯化的:如此处所用的术语“纯化的”当用于分子时,是指相对于在其自然环境或其产生、发现或合成的环境中与之相伴的分子,纯化分子的浓度提高。自然相伴的分子包括蛋白质、核酸、脂类和糖,通常不包括水、缓冲液和为了保持纯化分子的完整性或便于纯化而添加的试剂。例如,即使在oligo dT柱层析过程中用水溶剂稀释mRNA,如果自然相伴的核酸和其它生物分子不与该柱结合,并且与所述mRNA分子分开,则通过这种层析纯化了该mRNA分子。根据此定义,相对于污染物,一种物质的纯度可能是5%或以上、10%或以上、20%或以上、30%或以上、40%或以上、50%或以上、60%或以上、70%或以上、80%或以上、90%或以上、95%或以上、98%或以上、99%或以上或100%。
受体:如此处所用的术语“受体”是指能够与被称为配体的另外一种分子相互作用的蛋白质或糖蛋白或其片段。配体可能属于任何类别的生物化学或化学化合物。受体不一定必须是膜结合蛋白。可溶性蛋白质,例如麦芽糖结合蛋白或视黄醇结合蛋白,也是受体。
残基:如此处所用的术语“残基”是指多肽骨架或侧链内的具体氨基酸。
重组宿主细胞:如此处所用的术语“重组宿主细胞”是指已经导入一种或多种本发明的核酸分子的宿主细胞。
重组病毒:如此处所用的短语“重组病毒”是指人工基因修饰的病毒。该短语包括本领域所知的任何病毒。更具体而言,该短语是指一种人工基因修饰的甲病毒,最具体来说,该短语是指人工基因修饰的辛德毕斯病毒。
RNA-噬菌体:如此处所用的术语“RNA-噬菌体”或其缩写是指感染细菌的RNA病毒,优选地是指感染细菌的单链正义RNA病毒。
自身抗原:如此处所用的术语“自身抗原”是指由宿主DNA编码的蛋白质,宿主DNA编码的蛋白质或RNA产生的产物被定义为自身的。另外,由两种或几种自身分子组合产生的蛋白质,或者作为自身分子和蛋白质一部分的蛋白质,以及与如上所述两种自身分子具有高度同源性(>95%,优选地>97%,更优选地>99%)的蛋白质,也可以认为是自身的。
疫苗:如此处所用的术语“疫苗”是指一种制剂,其含有本发明的组合物,并且其形式能够对动物施用。一般而言,疫苗包含常用的盐水或缓冲水溶液介质,本发明的组合物悬浮或溶解于其中。以这种形式,本发明的组合物能够方便地用来预防、改善或治疗一种疾病。在导入宿主后,疫苗能够引起免疫应答,包括但不限于抗体、细胞因子的产生和/或细胞毒性T细胞、抗原呈递细胞、辅助T细胞、树状细胞的激活和/或其它细胞应答。任选地,本发明的疫苗还包含一种佐剂,与本发明的化合物相比,这种佐剂可能占一小部分或大部分。
载体:如此处所用的术语“载体”是指用来向宿主细胞内传递遗传物质的制剂(例如质粒或病毒)。载体可能由DNA或RNA组成。
病毒样颗粒(VLP):如此处所用的术语“病毒样颗粒”是指一种类似于病毒颗粒的结构。而且,根据本发明的病毒样颗粒是非复制性和非传染性的,因为它缺乏病毒基因组的全部或一部分,特别是病毒基因组的复制和传染成分。根据本发明的病毒样颗粒可能含有不同于其基因组的核酸。
噬菌体的病毒样颗粒:如此处所用的术语“噬菌体的病毒样颗粒”是指一种病毒样颗粒,它类似于噬菌体的结构,是非复制性和非传染性的,至少缺乏编码噬菌体复制机制的基因,一般也缺乏编码负责病毒附着或进入宿主的蛋白质的基因。根据本发明的病毒样颗粒缺乏病毒基因组的全部或一部分,特别是病毒基因组的复制和传染成分。根据本发明的病毒样颗粒可能含有不同于其基因组的核酸。本发明病毒样颗粒的一个典型的优选实施方案是一种病毒衣壳,如相应病毒、噬菌体或RNA噬菌体的病毒衣壳。术语“病毒衣壳”或“衣壳”在此可以互换使用,是指由病毒蛋白质亚单位组成的大分子装配体。一般且优选地,病毒蛋白质亚单位分别装配为病毒衣壳和衣壳,其结构具有固有的重复组织,其中这种结构一般是球形或管状。例如,RNA噬菌体或HBcAg的衣壳是二十面体对称的球形。如此处所用的术语“衣壳样结构”是指由病毒蛋白质亚单位组成的大分子装配体,它类似于上述衣壳形态,但是与典型的对称装配体不同,而保持足够程度的顺序和重复性。
噬菌体的病毒样颗粒:如此处所用的术语“噬菌体的病毒样颗粒”是指一种病毒样颗粒,它类似于噬菌体的结构,是非复制性和非传染性的,至少缺乏编码噬菌体复制机制的基因,一般也缺乏编码负责病毒附着或进入宿主的蛋白质的基因。然而,该定义也包括如下噬菌体的病毒样颗粒,其中上述基因仍然存在但是无活性,于是也产生非复制性和非传染性的噬菌体病毒样颗粒。
RNA噬菌体外壳蛋白的VLP:由RNA噬菌体外壳蛋白的180个亚单位自装配而成、任选地含有宿主RNA的衣壳结构被称为“RNA噬菌体外壳蛋白的VLP”。一个具体例子是Qβ外壳蛋白的VLP。在此具体情况下,Qβ外壳蛋白的VLP可能仅仅由Qβ CP亚单位(通过QβCP基因的表达产生,该基因含有例如一个TAA终止密码子,通过抑制阻止任何更长A1蛋白的表达,参见Kozlovska,T.M.等人,Intervirology 39:9-15(1996))装配而成,或者在衣壳装配体中还含有A1蛋白亚单位。
病毒颗粒:如此处所用的术语“病毒颗粒”是指病毒的形态学形状。某些病毒类型含有由蛋白质衣壳围绕的基因组;其它一些具有附加结构(例如包膜、尾等)。
一种(个):术语“一种(个)”在本公开内容中使用时,除非另外说明,是指“至少一种(个)”或“一种(个)或一种(个)以上”。
在此使用时,当涉及任何数值时,术语“大约”是指所述数值±10%(例如,“约50℃”包括45℃-55℃的温度;同样,“约100mM”包括90mM-110mM的浓度)。
概述
一方面,本发明提供一个或多个半抗原与一种载体的有序、重复的半抗原-载体偶联物,以及制备这种偶联物的方法。本发明也提供包含至少一种本发明的偶联物和至少一种其它成分(合适的是至少一种赋形剂或载体,特别是至少一种药学上可接受的赋形剂或载体)的偶联物。适于在本发明的偶联物和组合物中使用的半抗原包括但不限于激素、毒素和药物,特别是成瘾性药物,如尼古丁。本发明的偶联物和组合物可用于诱导针对半抗原的免疫应答。这种免疫应答能够用来产生抗体,可以用于治疗、预防和诊断目的。免疫应答能够用来预防或治疗滥用药物成瘾和所产生的与药物成瘾有关的疾病。
本发明的偶联物包含高度有序、重复的半抗原阵列。根据本发明该方面的偶联物阵列包含(a)核心颗粒,其包含第一附着位点,(b)半抗原,其包含第二附着位点,其中成分(a)和(b)通过第一和第二附着位点连接,形成有序、重复的半抗原阵列。
适于在本发明的偶联物和组合物中使用的核心颗粒可以是天然的或是非天然的。本发明的天然核心颗粒包括病毒颗粒、病毒样颗粒和菌毛。这些天然核心颗粒的蛋白质可以是天然的或是重组的。核心颗粒上的第一附着位点可以是自然存在的,或者可以通过化学或重组方法导入。本发明的半抗原适于诱导针对多种分子的免疫应答,包括但不限于毒素、激素和药物,特别是滥用药物和/或成瘾性药物。半抗原上的第二附着位点可以自然存在的或导入的。第一与第二附着位点之间的相互作用可能是直接的,或者可能涉及至少一种其它分子,例如接头。接头包括交联分子。
本发明的偶联物和组合物在诱导针对半抗原的免疫应答、特别是诱导抗体方面特别有效。因此,它们可以在适于免疫动物的组合物中使用,用于治疗或预防与不同药物、激素或毒素有关的疾病、紊乱或病症。用本发明的偶联物和组合物免疫产生的抗体也可用于治疗和预防目的。
在其它实施方案中,本发明提供使用本发明的偶联物和组合物治疗和预防疾病的方法。在另外一个实施方案中,本发明提供适于诊断和筛选的试剂盒。
有序、重复的抗原或抗原决定簇阵列的组合物及其制备方法
本发明提供偶联物和偶联物的组合物,其包含有序、重复的半抗原阵列。此外,本发明也使技术人员能够方便地构建有序、重复的半抗原阵列,用于不同目的,优选地诱导针对有机分子的免疫应答。
本发明的偶联物基本包含或者由下列两种成分组成:(1)非天然分子支架;和(2)半抗原,其含有至少一个第二附着位点,能够通过至少一个键与所述第一附着位点连接。
非天然分子支架包含或者由下列成分组成:(a)一种核心颗粒,其选自(1)非天然来源的核心颗粒,和(2)天然来源的核心颗粒;(b)至少一个第一附着位点,它通过至少一个共价键与该核心颗粒连接。在本发明的偶联物、组合物和方法中使用的核心颗粒包括无机分子、病毒颗粒、病毒样颗粒和细菌菌毛。在本发明的偶联物、组合物和方法中使用的半抗原含有至少一个第二附着位点,其选自:(a)该半抗原内非自然存在的附着位点;和(b)该抗原或抗原决定簇内自然存在的附着位点。
本发明提供一种有序、重复的半抗原阵列,它是由第二附着位点与第一附着位点通过至少一个键结合而成的。因此,通过第一附着位点与第二附着位点的这种连接,半抗原与非天然分子支架结合在一起,形成一种有序、重复的抗原阵列。
技术人员可以具体地设计半抗原和第二附着位点,使得与非天然分子支架(或者在某些实施方案中,与核心颗粒)结合的所有半抗原均一排列。例如,可以将单一第二附着位点置于半抗原上,从而通过设计确保与非天然分子支架附着的所有半抗原均一排列。因此,本发明提供一种便利的方法,用来将任何半抗原以确定的顺序和可形成一种重复模式的方式置于非天然分子支架上。
本领域技术人员应当清楚,本发明的某些实施方案涉及重组核酸技术的使用,如克隆、聚合酶链反应、DNA和RNA的纯化、重组蛋白在原核和真核细胞中的表达等。这些方法是本领域技术人员公知的,在出版的实验室方法手册中常见(例如,Sambrook,J.等人编著,《分子克隆:实验室手册》,第二版,Cold Spring Harbor LaboratoryPress,Cold Spring Habor,N.Y.(1989);Ausubel,F.等人编著,《现代分子生物学方法》,John H.Wiley & Sons,Inc.(1997))。应用组织培养细胞系进行的基本实验室技术(Celis,J.编著,《细胞生物学》,Academic Press,第二版,(1988))和基于抗体的技术(Harlow,E.和Lane,D.,《抗体:实验室手册》,Cold Spring Harbor Laboratory,Cold SpringHabor,N.Y.(1988);Deutscher,M.P.,“蛋白质纯化指南”,Meth.Enzymol.128,Academic Press San Diego(1990);Scopes,R.K.,《蛋白质纯化原理与实践》,第三版,Springer-Verlag,New York(1994))在文献中也有大量描述,全部文献在此引用作为参考。
此外,本领域技术人员也公知有机分子与氨基酸偶联的技术,和制备如实施本发明所必需的含有适当第二附着位点的半抗原衍生物的方法。这些方法可以在化学教科书和公开文献中找到,例子包括如下文献,在此引用作为参考:美国专利号5,876,727;WO 99/61054;Isomura,S.等人,J.Org.Chem.66:4115-4121(2001);Matsushita,H.等人,Biochem.Biophys.Res.Comm.57:1006-1010(1974);Langone,J.L.和Van Vunakis,H.,Methods Enzymol.84:628-640(1982);Wong,《蛋白质偶联和交联的化学》CRC Press,Inc.,Boca Raton,Fla(1991)。
核心颗粒与非天然分子支架
在一个实施方案中,本发明提供形成有序、重复的半抗原阵列的方法。根据本发明,其制备方法是通过第一和第二附着位点核心颗粒与一个或多个半抗原的连接。
因此,本发明的某些偶联物和组合物中的一种元件是非天然分子支架,其包含或者由核心颗粒和第一附着位点组成。更具体而言,非天然分子支架包含或者由下列成分组成:(a)一种天然或非天然来源的核心颗粒,(b)至少一个第一附着位点,其通过至少一个共价键与核心颗粒连接。
核心颗粒 在本发明的一个实施方案中,核心颗粒是一种合成聚合物、脂微囊或金属。这类核心颗粒是本领域中公知的,其提供建立本发明的新型非天然分子支架的基础。例如,美国专利号5,770,380和美国专利号5,334,394公开了合成聚合物或金属核心颗粒,在此全文引用作为参考。合适的金属包括但不限于:铬、铷、铁、锌、硒、镍、金、银、铂。合适的陶瓷材料包括但不限于:二氧化硅、二氧化钛、氧化铝、氧化钌和氧化锡。该实施方案的核心颗粒可以由有机材料制成,包括但不限于碳和适当的聚合物,包括聚苯乙烯、尼龙和硝酸纤维素。对于纳米晶体颗粒,由氧化锡、二氧化钛或碳(钻石)制成的颗粒是有用的。用于本发明的脂微囊通过本领域公知的任何方法制备,例如,Baiselle和Millar(Biophys.Chem.4:355-361(1975))或Corti等人(Chem.Phys.Lipids 38:197-214(1981))或Lopez等人(FEBS Lett.426:314-318(1998))或Topchieva和Karezin(J.Colloid Interface Sci.213:29-35(1999))或Morein等人(Nature 308:457-460(1984)),在此全文引用作为参考。
在本发明的一个实施方案中,核心颗粒通过一种生物学方法生产,它们可以是天然的或非天然的。例如,病毒和细菌菌毛或菌毛样结构由可组织为有序、重复结构的蛋白质构成。因此,本发明包括包含有用的核心颗粒的偶联物、组合物和方法,这些核心颗粒包括但不限于:病毒、病毒样颗粒、细菌菌毛、噬菌体、病毒衣壳颗粒或其片段。在某些这样的实施方案中,蛋白质可以是重组的。
在某些实施方案中,非天然分子支架的核心颗粒包括病毒、细菌菌毛、细菌菌毛蛋白形成的结构、噬菌体、病毒样颗粒、病毒衣壳颗粒或其重组形式。可以选择本领域公知的具有有序、重复外壳和/或核心蛋白结构的任何病毒,在本发明的方法、偶联物和组合物中作为非天然分子支架。合适的病毒例子包括但不限于:辛德毕斯病毒和其它甲病毒,弹状病毒(例如水泡性口炎病毒),小RNA病毒(例如人鼻病毒、Aichi病毒),披膜病毒(例如风疹病毒),正粘病毒(例如索戈托病毒、贝特肯病毒、家禽瘟疫病毒),多瘤病毒(例如多瘤病毒BK、多瘤病毒JC、禽多瘤病毒BFDV),细小病毒,轮状病毒,噬菌体Qβ,噬菌体R17,噬菌体M11,噬菌体MX1,噬菌体NL95,噬菌体fr,噬菌体GA,噬菌体SP,噬菌体MS2,噬菌体f2,噬菌体PP7,噬菌体AP205,诺瓦克病毒,口蹄疫病毒,逆转录病毒,乙型肝炎病毒,烟草花叶病毒,禽兽棚病毒,和人乳头瘤病毒(例如,参见Bachman,M.F.和Zinkernagel,R.M.,Immunol.Today 17:553-558(1996)中的表1)。在本发明的一个更具体的实施方案中,核心颗粒可包含或者由下列成分组成:重组轮状病毒蛋白,重组诺瓦克病毒蛋白,重组甲病毒蛋白,可形成细菌菌毛或菌毛样结构的重组蛋白,重组口蹄疫病毒蛋白,重组逆转录病毒蛋白,重组乙型肝炎病毒蛋白(例如HBcAg),重组烟草花叶病毒蛋白,重组禽兽棚病毒蛋白,和重组人乳头瘤病毒蛋白。
在本发明的偶联物、组合物和方法中使用的核心颗粒还可包含或者由下列成分组成:这些蛋白质的一种或多种片段,以及这些蛋白质的变体,它们仍保留彼此结合形成有序、重复抗原或抗原决定簇阵列的能力。例如,如WO 02/056905所述,核心颗粒可以由人HBcAg的变体形式构成,这种变体在氨基酸序列同一性和相似性和序列长度方面与野生型颗粒显著不同。例如,感染雪鹅和鸭的乙型肝炎病毒HBcAg的氨基酸序列与感染哺乳动物的病毒的HbcAg显著不同,难以进行蛋白质比对。然而,这两种病毒都保留形成核心结构的能力,适于形成有序、重复的抗原阵列。类似地,在除去N端前导序列,进一步对序列进行缺失、置换或添加之后,HBcAg可能保留形成多聚颗粒(通常是病毒颗粒)的能力。能够用来确定蛋白质是否形成这种结构的方法包括凝胶过滤、琼脂糖凝胶电泳、蔗糖梯度离心和电子显微镜检查(例如,Koschel,M.等人,J.Virol.73:2153-2160(1999))。
第一附着位点 无论是天然的还是非天然的,在本发明的偶联物、组合物和方法中使用的核心颗粒通常含有一种成分,该成分包含第一附着位点,其通过至少一个共价键与天然或非天然核心颗粒连接。包含第一附着位点的元件以非随机方式与核心颗粒结合,为产生有序、重复的阵列提供了核化位点。理想地但不是必须地,该元件与核心颗粒以几何顺序结合。第一附着位点可能是核心颗粒的天然部分,如适合与第二附着位点偶联的表面暴露的氨基酸残基。例如,赖氨酸和半胱氨酸可通过氨基酸上的反应性基团形成非肽键。或者,也可以通过化学偶联或者通过设计重组分子,将含有第一附着位点的元件导入核心颗粒内。第一附着位点可以是通过至少一个共价键与核心颗粒结合的任何元件,或者存在于该元件中。
包含或者由第一附着位点组成的元件可以是蛋白质、多肽、肽、氨基酸(即蛋白质、多肽或肽的残基)、糖、多核苷酸、天然或合成的聚合物、次级代谢物或化合物(生物素、荧光素、视黄醇、洋地黄毒苷、金属离子、苯甲基磺酰氟)或其组合,或其化学反应性基团。在一个更具体的实施方案中,第一附着位点包括抗原、抗体或抗体片段、生物素、抗生物素蛋白、链霉抗生物素、受体、受体配体、配体、配体结合蛋白、相互作用性亮氨酸拉链多肽、氨基、氨基反应性化学基团;羧基,羧基反应性化学基团,巯基,巯基反应性化学基团,或其组合。
在一个实施方案中,本发明通过一种病毒的遗传工程改造,产生有序、重复的病毒包膜蛋白与包含第一附着位点的元件的融合体,该元件包括异源蛋白质、肽、抗原决定簇或选择的反应性氨基酸残基。非天然分子支架的构建可以使用本领域公知的其它遗传操作;例如,可能希望通过基因突变限制重组病毒的复制能力。为了与含有第一附着位点的蛋白质融合而选择的病毒蛋白应当具有有序、重复的结构。这种有序、重复的结构包括类晶体结构,在病毒表面上其间距为0.5-30nm,优选地5-15nm。这类融合蛋白的产生将在病毒表面产生多个有序、重复的第一附着位点。因此,由此产生的第一附着位点的有序、重复的组织反映了天然病毒蛋白的正常组织结构。
本领域技术人员理解,第一附着位点可以是任何合适的蛋白质、多肽、糖、多核苷酸、肽(氨基酸)、天然或合成聚合物、次级代谢物或其组合,或是它们的一部分,它们可用来使选择的抗原或抗原决定簇与非天然分子支架特异连接。在一个实施方案中,附着位点是一种可选自本领域所知类型的蛋白质或肽。例如,第一附着位点可以是配体、受体、凝集素、抗生物素蛋白、链霉抗生物素、生物素、表位如HA或T7标签、Myc、Max、免疫球蛋白域和本领域公知可以用作第一附着位点的其它任何氨基酸序列。
本领域技术人员进一步理解,在本发明的另外一个实施方案中,可以在产生携带第一附着位点(即蛋白质或多肽)的用于构建与衣壳蛋白的框内融合体的元件后产生第一附着位点。例如,一种蛋白质可以用来与包膜蛋白融合,其含有已知以特定方式糖基化的氨基酸序列,添加的糖部分然后可以通过与作为抗原的第二附着位点的凝集素结合,作为病毒支架的第一附着位点。或者,一种序列也可以在体内被生物素化,生物素部分可以作为本发明的第一附着位点,或者该序列可以在体外进行不同氨基酸残基的化学修饰,这种修饰作为第一附着位点。
在本发明的一个具体实施方案中,第一附着位点是与乙型肝炎衣壳(核心)蛋白(HBcAg)框内融合的JUN-FOS亮氨酸拉链蛋白结构域。然而,本领域技术人员理解,在融合蛋白构建体中也可以使用其它病毒衣壳蛋白,用于定位本发明非天然分子支架中的第一附着位点。例如,在本发明的另外一些实施方案中,选择与HBcAg框内融合的赖氨酸或半胱氨酸残基作为第一附着位点。本领域技术人员也理解,在融合蛋白构建体中也可以使用其它病毒衣壳或病毒样颗粒,用于定位本发明非天然分子支架中的第一附着位点。
病毒颗粒 在本发明的一个实施方案中,核心颗粒是一种重组甲病毒,更具体而言,是一种重组辛德毕斯病毒。甲病毒科的几个成员,辛德毕斯病毒(Xiong,C.等人,Science 243:1188-1191(1989);Schlesinger,S.,Trends Biotechnol.11:18-22(1993))、西门利启森林病毒(SFV)(Liljestrm,P.& Garoff,H.,Bio/Technology 9:1356-1361(1991))及其它病毒(Davis,N.L.等人,Virology 171:189-204(1989)),在作为许多不同蛋白质的基于病毒的表达载体(Lundstrom,K.,Curr.Opin.Biotechnol.8:578-582(1997);Liljestrm,P.,Curr.Opin.Biotechnol.5:495-500(1994))以及作为疫苗研制的候选物方面已经受到极大关注。甲病毒在异源蛋白质表达和疫苗研制中的用途已经公开(参见美国专利号5,766,602;5,792,462;5,739,026;5,789,245;5,814,482),其公开内容在此全文引用作为参考。本发明的甲病毒支架的构建可以用重组DNA技术领域公知的方法进行,如上述文章所述,在此引用作为参考。可以使用多种不同的重组宿主细胞生产基于病毒的核心颗粒,用于抗原或抗原决定簇的附着。
包装的RNA序列也可以用来感染宿主细胞。这些包装的RNA序列可以通过添加到培养基中而导入宿主细胞内。例如,在大量资料中描述了非传染性甲病毒颗粒的制备,包括“辛德毕斯表达系统”,C版(Invitrogen Corporation,Carlsbad CA;目录号K750-1)。
当使用哺乳动物细胞作为重组宿主细胞生产基于病毒的核心颗粒时,这些细胞通常在组织培养基中培养。在培养基中培养细胞的方法在本领域中公知(参见,例如:Celis,J.编著,《细胞生物学》,AcademicPress,第二版,(1998);Sambrook,J.等人编著,《分子克隆:实验室手册》,第二版,Cold Spring Harbor Laboratory Press,Cold Spring Habor,N.Y.(1989);Ausubel,F.等人编著,《现代分子生物学方法》,John H.Wiley & Sons,Inc.(1997);Freshney,R.,《动物细胞培养》,Alan R.Liss,Inc.(1983))。
因此本发明包括基于病毒的核心颗粒,其包含或者由下列成分组成:病毒、病毒样颗粒、噬菌体、病毒衣壳颗粒或其重组形式。熟练技术人员知道如何生产这些核心颗粒以及与第一附着位点连接。WO00/32227的实施例17-22公开了生产乙型肝炎病毒样颗粒(特别是由HBcAg装配或自装配的)和麻疹病毒衣壳颗粒作为核心颗粒,该文献在此明确引用作为参考。在这些实施方案中,可以用JUN亮氨酸拉链蛋白结构域或FOS亮氨酸拉链蛋白结构域作为本发明的非天然分子支架的第一附着位点。本领域技术人员知道构建如下乙型肝炎核心颗粒的方法,该颗粒携带含反应性赖氨酸残基的框内融合肽,以及携带基因融合的半胱氨酸残基的抗原,分别作为第一和第二附着位点。
在另外一些实施方案中,在本发明的组合物中使用的核心颗粒由乙型肝炎衣壳(核心)蛋白(HBcAg)、HBcAg的片段或能够形成病毒样颗粒的其它蛋白质或肽组成,它们是有序的阵列,已经修饰除去了游离半胱氨酸残基或者减少了其数量。Zhou等人(J.Virol.66:5393-5398(1992))证实,修饰后除去自然存在的半胱氨酸残基的HBcAg保留结合并形成多聚体结构的能力。因此,适于在本发明的组合物中使用的核心颗粒包括包含修饰HBcAg或其片段的核心颗粒,其中一个或多个自然存在的半胱氨酸残基已经删除或被置换为另外一种氨基酸残基(例如丝氨酸残基)。在一个优选实施方案中,HBcAg含有如SEQ IDNO:1所示的氨基酸序列,或者与SEQ ID NO:1的序列至少约80%、至少约85%、至少约90%、至少约95%、更优选地至少约99%或100%相同的序列。在本发明的一个实施方案中,利用含有SEQ ID NO:1所示氨基酸序列的修饰HBcAg或其亚部分制备非天然分子支架。具体而言,适用于实施本发明的修饰HBcAg包含如下蛋白质:其中在对应于具有SEQ ID NO:1所示氨基酸序列的蛋白质的位点48、61、107、185的位点处,一个或多个半胱氨酸残基已经被删除或者被置换为其它氨基酸残基(例如丝氨酸残基)。本领域技术人员知道,在含有不同于SEQ ID NO:1所示的氨基酸序列的HBcAg变体中,位于类似位点处的半胱氨酸残基也可能被删除或者被置换为其它氨基酸残基。然后可以用修饰的HBcAg变体制备本发明的疫苗组合物。
在某些情况下(例如,当使用异双功能交联剂连接抗原或抗原决定簇与非天然分子支架时),认为HBcAg中存在游离半胱氨酸残基使得毒性成分与核心颗粒共价偶联,以及单体交联,形成不确定的物质。
另外,在许多情况下,对本发明的组合物进行测定可能无法检测到这些毒性成分。这是因为毒性成分与非天然分子支架的共价偶联将形成一群不同的物质,其中毒性成分与HBcAg的不同半胱氨酸残基连接,或者在某些情况下,不与半胱氨酸残基连接。换句话说,不是每个HBcAg的每个游离半胱氨酸残基将与毒性成分共价连接。在许多情况下,特定HBcAg的半胱氨酸残基均不与毒性成分连接。因此,这些毒性成分的存在可能难以检测,因为它们以混合分子群的形式存在。然而,对个体施用包含毒性成分的HBcAg可能导致严重的不良作用。
本领域公知,游离半胱氨酸残基能够参与大量化学副反应。这些副反应包括二硫键交换、与例如在与其它物质联合治疗中注射或形成的化学物质或代谢物反应、或暴露于紫外线后的直接氧化以及与核苷酸的反应。因而能够产生毒性加合物,特别是考虑到HBcAg具有结合核酸的强烈倾向这一事实。使用以含有游离半胱氨酸的HBcAg和异双功能交联剂制备的衣壳,难以检测抗原-衣壳偶联物中的这些毒性产物,因为将产生大范围分子量产物的分布。毒性加合物分布于多个种,它们单个均以低浓度存在,但在一起存在时达到毒性水平。
如上所述,在疫苗组合物中使用修饰后除去自然存在的半胱氨酸残基的HBcAg的一个优点是,当抗原或抗原决定簇与非天然分子支架连接时,毒性物质能够结合的位点数量减少或者完全消失。此外,也可以用高浓度的交联剂生产高度修饰的颗粒,而没有产生HBcAg单体的大量不确定交联种类(即交联的单体HBcAg的不同混合物)的缺点。
适于在实施本发明中使用的一些天然存在的HBcAg变体已经被鉴定。例如,Yuan等人(J.Virol.73:10122-10128(1999))描述了在对应于SEQ ID NO:1中位点97的位点处异亮氨酸残基被置换为亮氨酸残基或苯丙氨酸残基的变体。一些HBcAg变体以及几种乙型肝炎核心抗原前体变体的氨基酸序列在下列GenBank报告中公开:AAF121240、AF121239、X85297、X02496、X85305、X85303、AF151735、X85259、X85286、X85260、X85317、X85298、AF043593、M20706、X85295、X80925、X85284、X85275、X72702、X85291、X65258、X85302、M32138、X85293、X85315、U95551、X85256、X85316、X85296、AB033559、X59795、X8529、X85307、X65257、X85311、X85301、X85314、X85287、X85272、X85319、AB010289、X85285、AB010289、AF121242、M90520、P03153、AFll0999和M95589,其公开内容均在此引用作为参考。这些HBcAg变体在多个位点处的氨基酸序列不同,包括对应于SEQ ID NO:1中位点12、13、21、22、24、29、32、33、35、38、40、42、44、45、49、51、57、58、59、64、66、67、69、74、77、80、81、87、92、93、97、98、100、103、105、106、109、113、116、121、126、130、133、135、141、147、149、157、176、178、182和183处的氨基酸残基。
在WO 00/198333、WO 00/177158和WO 00/214478中描述了适于在本发明的组合物中使用、并且可以根据本说明书公开内容进一步修饰的其它一些HBcAg变体,这些文献在此全文引用作为参考。
适于本发明使用的HBcAg可以来源于任何生物,只要它们能够结合形成有序、重复的抗原阵列。在本发明的疫苗组合物中将使用一般加工的(即缺乏前导序列的)HBcAg。本发明包括如下疫苗组合物以及应用这些组合物的方法,它们使用上述变异HBcAg制备非天然分子支架。本发明的范围内还包括能够结合形成二聚体或多聚体结构的其它HBcAg变体。因此,本发明还包括包含HBcAg多肽的疫苗组合物,该多肽包含或者由如下氨基酸序列组成:这些序列与上述序列(包括SEQ ID NO:1)所示的任何一种氨基酸序列至少约80%、约85%、约90%、约95%、约97%或约99%相同,以及必要时加工除去N端前导序列的这些蛋白质的形式。
一种多肽的氨基酸序列是否具有与上述氨基酸序列之一或其亚部分至少80%、85%、90%、95%、97%或99%相同的氨基酸序列,可以利用公知的计算机程序如Bestfit程序常规测定。当利用Bestfit或其它任何序列比对程序确定一种具体序列与根据本发明的参照氨基酸序列是否例如约95%相同时,参数设置为在参照氨基酸序列的全长上计算百分同一性,并且使同源性缺口可达参照序列中氨基酸残基总数的5%。这样,可以对SEQ ID NO:1的HBcAg序列与其它HBcAg进行比较。当比较相对类似的蛋白质时,HBcAg变体中位于对应于SEQ ID NO:1中特定位点处的氨基酸残基,是指在SEQ ID NO:1所示氨基酸序列中该位点处存在的氨基酸残基。在感染哺乳动物的乙型肝炎病毒之间,这些HBcAg变体之间的同源性在很大程度上足够高,因此本领域技术人员不难检查分别如SEQ ID NO:1所示的氨基酸序列以及一种具体HBcAg变体的氨基酸序列,并鉴定“相应的”氨基酸残基。例如,通过比较SEQ ID NO:1与来源于感染土拨鼠的一种病毒的HBcAg的氨基酸序列,显然在该序列中,在SEQ ID NO:1的氨基酸残基155与156之间存在3个氨基酸残基的插入部分。
然而,当难以比对时,本领域技术人员可以认识到序列中特定氨基酸残基或基序的重要性。例如,来自人病毒的HBcAg的氨基酸序列不同于鸭病毒,因此难以比对,本领域技术人员可以认识到,在包含于本发明的疫苗组合物中之前,保守半胱氨酸残基可以被置换为另外一种氨基酸残基或者删除。
在一个实施方案中,具有SEQ ID NO:1所示氨基酸序列的蛋白质的位点48和107处的半胱氨酸残基被删除或者被置换为另外一种氨基酸残基,而位点61处的半胱氨酸仍然保留。然后用修饰的多肽制备本发明的疫苗组合物。
可以用于本发明的乙型肝炎病毒样颗粒的制备已在下列专利中公开,例如:WO 00/32227,具体见实施例17-19和21-24,以及WO01/85208,具体见实施例17-19、21-24、31-41,和WO 02/056905。最后一个申请具体参见实施例23、24、31和51。这三篇文献全部在此均引用作为参考。
如WO 02/056905的实施例31所述,例如通过定点诱变可以除去溶剂可及的位点48和107处的半胱氨酸残基。此外,本发明人也发现,如WO 02/056905(在此全文引用作为参考)所述构建的Cys-48-Ser、Cys-107-Ser HBcAg双突变体能够在大肠杆菌中表达。
如上所述,除去游离半胱氨酸残基可减少毒性成分能够结合HBcAg的位点数量,也除去了相同或相邻HBcAg分子的赖氨酸和半胱氨酸残基能够发生交联的位点。位点61处的半胱氨酸参与二聚体的形成并且与另外一个HBcAg的位点61处的半胱氨酸形成二硫键,为了本发明的HBcAg二聚体和多聚体的稳定性,通常保留该半胱氨酸。用(1)含有游离半胱氨酸残基的HBcAg和(2)用碘乙酰胺使其游离半胱氨酸残基无反应性的HBcAg进行的交联实验表明,HBcAg的游离半胱氨酸残基通过异双功能交联剂衍化的赖氨酸侧链与游离半胱氨酸残基之间的反应,引起HBcAg之间的交联。也发现,HBcAg亚单位的交联导致大小不确定的高分子量种的形成,它们不能用SDS-聚丙烯酰胺凝胶电泳分析。
当抗原或抗原决定簇与非天然分子支架通过赖氨酸残基连接时,置换或者删除位于对应于SEQ ID NO:1位点7和96的位点处的自然存在的赖氨酸残基之一或全部以及HBcAg变体中存在的其它赖氨酸残基是有利的。除去这些赖氨酸残基就除去了可能破坏有序阵列的与抗原或抗原决定簇的结合位点,提高了终疫苗组合物的质量和均一性。
在许多情况中,当对应于SEQ ID NO:1位点7和96的位点处自然存在的两个赖氨酸残基均被删除时,向HBcAg中引入另外一个赖氨酸作为抗原或抗原决定簇的附着位点。插入这种赖氨酸残基的方法如WO 02/056905的实施例23所述,在此全文引用作为参考。例如,当对应于SEQ ID NO:1位点7和96的位点处自然存在的两个赖氨酸残基均被改变,并且试图利用一种异双功能交联剂连接抗原或抗原决定簇与非天然分子支架时,向HBcAg内引入一个赖氨酸残基通常是有利的。
已经证明HBcAg的C端引导该蛋白质的核定位(Eckhardt等人,J.Virol.65:575-582(1991))。而且也认为该蛋白质的这一区域使HBcAg具有结合核酸的能力。
在一些实施方案中,本发明的疫苗组合物含有具有核酸结合活性的HBcAg(例如含有自然存在的HBcAg核酸结合域)。含有一个或多个核酸结合域的HBcAg可用于制备显示T细胞刺激活性提高的疫苗组合物。因此,本发明的疫苗组合物包括含有具有核酸结合活性的HBcAg的组合物。另外还包括这样的疫苗组合物以及这些组合物在接种方案中的用途,其中HBcAg与核酸结合。这些HBcAg在对个体施用之前可以与核酸结合,或者可以在施用后与核酸结合。
适于在本发明的实施中使用的其它HBcAg包括N端和C端截短突变体,以及其氨基酸序列包含或者由下列氨基酸序列组成的突变蛋白:这些序列与上述截短突变体至少约80%、约85%、约90%、约95%、约97%或约99%相同。
如上所述,在本发明的某些实施方案中,向构成非天然分子支架的多肽内引入赖氨酸残基作为第一附着位点。在优选实施方案中,使用一种HBcAg制备本发明的疫苗组合物,该HBcAg包含或者由下列氨基酸组成:SEQ ID NO:1的氨基酸1-144或氨基酸1-149或氨基酸1-185,其经过修饰,使得对应于位点79和80的氨基酸被替换为具有氨基酸序列Gly-Gly-Lys-Gly-Gly(SEQ ID NO:11)的肽,位点48和107处的半胱氨酸残基被删除或者被置换为另外一种氨基酸残基,而位点61处的半胱氨酸仍然保留。
本发明还包括包含HBcAg片段的疫苗组合物,该片段包含或者由与SEQ ID NO:1所示不同的氨基酸序列组成,该序列中删除了在SEQ ID NO:1相应位点处不存在的半胱氨酸残基。
本发明的疫苗组合物可能包含不同HBcAg的混合物。因此,这些疫苗组合物可能由氨基酸序列不同的HBcAg组成。例如,可以制备包含“野生型”HBcAg和修饰HBcAg的疫苗组合物,在修饰HBcAg中一个或多个氨基酸残基已经改变(例如删除、插入或置换)。本发明还包括使用与另外一种蛋白质融合的HBcAg制备非天然分子支架的疫苗组合物。如上所述,这种融合蛋白的一个例子是HBcAg/FOS融合蛋白。适于在本发明的疫苗组合物中使用的HBcAg融合蛋白的其它例子包括已经添加了一种有助于形成和/或稳定HBcAg二聚体和多聚体的氨基酸序列的融合蛋白。这种添加的氨基酸序列可与HBcAg的C端融合。这种融合蛋白的一个例子是HBcAg与酿酒酵母GCN4螺旋区的融合蛋白,它通过非共价相互作用形成同型二聚体,能够用来制备并稳定HBcAg二聚体和多聚体。
在一个实施方案中,本发明提供使用HBcAg融合蛋白制备的疫苗组合物,该融合蛋白包含一种HBcAg或其片段,以及与C端融合的一种GCN4多肽(PAALKRARNEAARRSRARKLQRMKQLEDKVEELLSKNYHLENEVARLKK(SEQ ID NO:12))。该GCN4多肽也可以与HBcAg的N端融合。
HBcAg/src homology 3(SH3)域融合蛋白也可以用来制备本发明的疫苗组合物。SH3域是在大量蛋白质中可见的相对较小的结构域,它提供与蛋白质结合配偶体中特定富含脯氨酸序列相互作用的能力(参见McPherson,Cell Signal 11:229-238(1999))。HBcAg/SH3融合蛋白可以以几种方式使用。首先,SH3域能够形成第一附着位点,该位点可与抗原或抗原决定簇的第二附着位点相互作用。同样,可以向HBcAg中添加富含脯氨酸的氨基酸序列,并且作为对于抗原或抗原决定簇的SH3域第二附着位点的第一附着位点。其次,SH3域能够与引入HBcAg内的富含脯氨酸区结合。因此,SH3域和富含脯氨酸的SH3相互作用位点可以插入相同或不同的HBcAg内,用来形成并稳定本发明的二聚体和多聚体。
上述实例所证实,本领域技术人员知道如何由HBcAg和HBcAg衍生突变蛋白构建包含核心颗粒和第一附着位点的分子支架。应用本领域公知的技术和常规实验,本领域技术人员知道如何类似地利用其它病毒构建分子支架。
如此处其它部分所述,病毒衣壳可以用于(1)半抗原的呈递,(2)本发明的疫苗组合物的制备。具体而言,在本发明的实施中有用的是病毒衣壳蛋白,在此也被称为“外壳蛋白”,它在表达后形成衣壳或衣壳样结构。因此,这些衣壳蛋白能够形成核心颗粒和非天然分子支架。这些衣壳或衣壳样结构通常形成有序、重复的阵列,该阵列能够用于呈递半抗原决定簇和制备本发明的疫苗组合物。
可以利用任何方法将一个或多个(例如1、2、3、4、5个等)半抗原与一个或多个(例如1、2、3、4、5个等)蛋白质连接,形成衣壳或衣壳样结构(例如噬菌体外壳蛋白)以及其它蛋白质。例如,可以利用第一和第二附着位点连接半抗原与核心颗粒。此外,也可以利用一个或多个(例如1、2、3、4、5个等)异双功能交联剂分子连接半抗原与一个或多个蛋白质,形成病毒衣壳或衣壳样结构。
例如,可以使用病毒衣壳蛋白或其片段制备核心颗粒和本发明的疫苗组合物。例如,噬菌体Qβ外壳蛋白可以在大肠杆菌中重组表达。进而,这些蛋白质在表达后自发形成衣壳,它们是病毒样颗粒。另外,这些衣壳也形成有序、重复的抗原阵列,这些阵列能够用于半抗原呈递和疫苗组合物的制备。如以下实施例1所述,能够利用噬菌体Qβ外壳蛋白制备可以引发对半抗原的免疫应答的疫苗组合物。
在一个优选实施方案中,病毒样颗粒包含、基本由或者由RNA-噬菌体的重组蛋白或其片段组成。优选地,RNA-噬菌体选自:a)噬菌体Qβ;b)噬菌体R17;c)噬菌体fr;d)噬菌体GA;e)噬菌体SP;f)噬菌体MS2;g)噬菌体M11;h)噬菌体MX1;i)噬菌体NL95;k)噬菌体f2;1)噬菌体PP7;m)噬菌体AP205。
在本发明的另外一个优选实施方案中,病毒样颗粒包含或者基本由或者由RNA-噬菌体Qβ或RNA-噬菌体fr或RNA-噬菌体AP205的重组蛋白或其片段组成。
在本发明的一个进一步优选的实施方案中,重组蛋白包含或者基本由或者由RNA噬菌体的外壳蛋白组成。
可以用来制备本发明的组合物的噬菌体外壳蛋白的具体实例包括如下RNA噬菌体的外壳蛋白:噬菌体Qβ(SEQ ID NO:3;PIR数据库,登录号VCBPQβ,指QβCP;和SEQ ID NO:4,登录号AAA16663,指QβA1蛋白),噬菌体R17(SEQ ID NO:24;PIR登录号VCBPR7),噬菌体fr(SEQ ID NO:25;PIR登录号VCBPFR),噬菌体GA(SEQ IDNO:26;GenBank登录号NP-040754),噬菌体SP(SEQ ID NO:27;GenBank登录号CAA30374,指SP CP;和SEQ ID NO:28,登录号NP 695026,指SP A1蛋白),噬菌体MS2(SEQ ID NO:29;PIR登录号VCBPM2),噬菌体M11(SEQ ID NO:30;GenBank登录号AAC06250),噬菌体MX1(SEQ ID NO:31;GenBank登录号AAC14699),噬菌体NL95(SEQ ID NO:32;GenBank登录号AAC14704),噬菌体f2(SEQ ID NO:33;GenBank登录号P03611),噬菌体PP7(SEQ ID NO:13),噬菌体AP205(SEQ ID NO:14)。本领域技术人员知道,形成衣壳或衣壳样结构的任何蛋白质都可以用于制备本发明的疫苗组合物。此外,噬菌体Qβ的A1蛋白(Genbank登录号AAA16663(SEQ ID NO:4))或C端丢失多达约100个、约150个或约180个氨基酸的C端截短形式可能掺入Qβ外壳蛋白的衣壳装配体中。A1蛋白也可以与含有第一附着位点的元件融合,用来与含有第二附着位点的半抗原连接。通常,为了确保衣壳形成,通常限制衣壳装配体中A1蛋白相对于QβCP的百分比。
也发现Qβ外壳蛋白当在大肠杆菌中表达时自装配为衣壳(Kozlovska TM.等人,GENE 137:133-137(1993))。获得的衣壳或病毒样颗粒显示一种二十面体噬菌体样衣壳结构,其直径为25nm,T=3准对称。此外,噬菌体Qβ的晶体结构已经被解析。该衣壳含有180个拷贝的外壳蛋白,它们通过二硫键连接为共价五聚体和六聚体(Golmohammadi R.等人,Structure 4:543-5554(1996))。也证实其它一些RNA噬菌体外壳蛋白在细菌宿主中表达后自装配(Kastelein,RA等人,Gene 23:245-254(1983),Kozlovskaya,TM.等人,Dokl.Akad.Nauk SSSR 287:452-455(1986),Adhin,MR.等人,Virology170:238-242(1989),Ni,CZ.等人,Protein Sci.5:2485-2493(1996),Priano,C.等人,J.Mol.Biol.249:283-297(1995))。Qβ噬菌体衣壳除了外壳蛋白外还含有所谓的通读蛋白A1和成熟蛋白A2。A1通过在UGA终止密码子处抑制而产生,长度为329个氨基酸。本发明中使用的噬菌体Qβ重组外壳蛋白的衣壳都缺乏A2裂解蛋白,而含有来自宿主的RNA。RNA噬菌体的外壳蛋白是一种RNA结合蛋白,与复制酶基因的核糖体结合位点的茎环相互作用,作为病毒生命周期中的一种翻译抑制物。这种相互作用的序列和结构组件已知(Witherell,GW.& Uhlenbeck,OC.Biochemistry 28:71-76(1989);Lim F.等人,J.Biol.Chem.271:31839-31845(1996))。已知这种茎环和RNA通常参与病毒装配(Golmohammadi,R.等人,Structure 4:543-5554(1996))。
我们通过如Stoll,E.等人,J.Biol.Chem.252:990-993(1977)所述的N端Edman测序发现,在大肠杆菌中表达后,Qβ外壳蛋白的N端甲硫氨酸通常被删除。本发明的范围内也包括由这样的Qβ外壳蛋白组成的VLP,其中N端甲硫氨酸尚未删除,或者含有Qβ外壳蛋白混合物的VLP,其中N端甲硫氨酸被切除或得仍然存在。
WO 02/056905公开了本发明的RNA噬菌体、特别是Qβ的进一步优选的病毒样颗粒,其公开内容在此全文引用作为参考。
也已经证实,另外一些RNA噬菌体外壳蛋白在细菌宿主中表达后自装配(Kastelein,RA等人,Gene 23:245-254(1983),Kozlovskaya,TM.等人,Dokl.Akad.Nauk SSSR 287:452-455(1986),Adhin,MR.等人,Virology 170:238-242(1989),Ni,CZ.等人,Protein Sci.5:2485-2493(1996),Priano,C.等人,J.Mol.Biol.249:283-297(1995))。Qβ噬菌体衣壳除了外壳蛋白外还含有所谓的通读蛋白A1和成熟蛋白A2。A1通过在UGA终止密码子处抑制而产生,长度为329个氨基酸。本发明中使用的噬菌体Qβ重组外壳蛋白的衣壳都缺乏A2裂解蛋白,而含有来自宿主的RNA。RNA噬菌体的外壳蛋白是一种RNA结合蛋白,与复制酶基因的核糖体结合位点的茎环相互作用,作为病毒生命周期中的一种翻译抑制物。这种相互作用的序列和结构组件已知(Witherell,GW.& Uhlenbeck,OC.Biochemistry 28:71-76(1989);Lim F.等人,J.Biol.Chem.271:31839-31845(1996))。已知这种茎环和RNA通常参与病毒装配(Golmohammadi,R.等人,Structure 4:543-5554(1996))。
在本发明的一个进一步优选的实施方案中,病毒样颗粒包含或者基本由或者由RNA噬菌体的重组蛋白或其片段组成,其中该重组蛋白包含、基本由或者由RNA噬菌体的突变外壳蛋白组成。在另外一个优选实施方案中,突变外壳蛋白已经通过置换除去至少一个赖氨酸残基、更优选地至少两个赖氨酸残基,或者通过置换添加至少一个赖氨酸残基而被修饰。此外,这些突变外壳蛋白也可以是通过删除至少一个赖氨酸残基、更优选地至少两个赖氨酸残基,或者通过插入添加至少一个赖氨酸残基、更优选地至少两个赖氨酸残基而被修饰。
在另外一个优选实施方案中,病毒样颗粒包含、基本由或者由RNA噬菌体Qβ的重组蛋白或其片段组成,其中该重组蛋白包含、基本由或者由下列成分组成:具有SEQ ID NO:3的氨基酸序列的外壳蛋白,或具有SEQ ID NO:3和SEQ ID NO:4的氨基酸序列的外壳蛋白的混合物,或SEQ ID NO:4的突变体,其中N端甲硫氨酸优选地被切除。
在本发明的一个进一步优选的实施方案中,病毒样颗粒包含、基本由或者由Qβ的重组蛋白或其片段组成,其中该重组蛋白包含、基本由或者由突变Qβ外壳蛋白组成。在另外一个优选实施方案中,这些突变外壳蛋白已经通过置换去除至少一个赖氨酸残基或者通过置换添加至少一个赖氨酸残基而被修饰。此外,这些突变外壳蛋白也可以是通过删除至少一个赖氨酸残基或者通过插入添加至少一个赖氨酸残基而被修饰。
有4个赖氨酸残基暴露于Qβ外壳蛋白的衣壳表面。本发明也可以使用以精氨酸替换暴露赖氨酸残基的Qβ突变体。因此在本发明的实施中可以使用下列Qβ外壳蛋白突变体和突变QβVLP:“Qβ-240”(Lys13-Arg;SEQ ID NO:6),“Qβ-243”(Asn 10-Lys;SEQ IDNO:7),“Qβ-250”(Lys 2-Arg,Lys13-Arg;SEQ ID NO:8),“Qβ-251”(SEQID NO:9)和“Qβ-259”(Lys 2-Arg,Lys16-Arg;SEQ ID NO:10)。因此,在本发明的进一步优选的实施方案中,病毒样颗粒包含、基本由或者由突变Qβ外壳蛋白的重组蛋白组成,其包含具有选自下列的氨基酸序列的蛋白质:a)SEQ ID NO:6的氨基酸序列;b)SEQ ID NO:7的氨基酸序列;c)SEQ ID NO:8的氨基酸序列;d)SEQ ID NO:9的氨基酸序列;e)SEQ ID NO:10的氨基酸序列。上述Qβ外壳蛋白、突变Qβ外壳蛋白VLP和衣壳的构建、表达和纯化分别在WO 02/056905中有描述。具体参照上述申请的实施例18。
在本发明的一个进一步优选的实施方案中,病毒样颗粒包含、基本由或者由Qβ的重组蛋白或其片段组成,其中该重组蛋白包含、基本由或者由上述Qβ突变体之一和相应A1蛋白的混合物组成。
在本发明的一个进一步优选的实施方案中,病毒样颗粒包含或者基本由或者由RNA噬菌体AP205的重组蛋白或其片段组成。
AP205基因组包含一个成熟蛋白质、一个外壳蛋白、一个复制酶和相关噬菌体中不存在的两个开放阅读框、一个裂解基因和一个在成熟基因的翻译中起作用的开放阅读框(Klovins,J.等人,J.Gen.Virol.83:1523-33(2002))。AP205外壳蛋白可以由质粒pAP283-58(SEQ IDNO:15)表达,该质粒是pQb10的衍生物(Kozlovska,T.M.等人,Gene137:133-37(1993)),其含有一个AP205核糖体结合位点。此外,AP205外壳蛋白也可以克隆到pQb185内,位于载体中存在的核糖体结合位点的下游。这两种方法都导致蛋白质的表达和衣壳的形成,如实施例10所述。载体pQb10和pQb185是由pGEM载体衍生的载体,这些载体中克隆基因的表达受trp启动子控制(Kozlovska,T.M.等人,Gene137:133-37(1993))。质粒pAP283-58(SEQ ID NO:15)在下列序列中含有一个推断的AP205核糖体结合位点,它位于AP205外壳蛋白的XbaI位点下游和ATG起始密码子的直接上游:tctagaATTTTCTGCGCACCCATCCCGGGTGGCGCCCAAAGT
GAGG AAAATCACatg(SEO ID NO:16)。载体pQb185在XbaI位点下游和起始密码子上游含有一个SD序列(tctagaTTAACCCAACGCGT
AGGAGTCAGGCCatg,(SEQ ID NO:17),SD序列以下划线标出)。
在本发明的一个进一步优选的实施方案中,病毒样颗粒包含或者基本由或者由RNA噬菌体AP205的重组外壳蛋白或其片段组成。
本发明的这一优选实施方案因此包含可构成衣壳的AP205外壳蛋白。这些蛋白质重组表达或从天然来源中制备。电子显微镜检查(EM)和免疫扩散证实,细菌产生的AP205外壳蛋白自发形成衣壳。由EM可见,AP205外壳蛋白(SEQ ID NO:14)形成的衣壳与AP205RNA噬菌体外壳蛋白形成的衣壳的结构特征几乎无法辨别。AP205VLP具有高度免疫原性,能够与抗原和/或抗原决定簇连接,产生展示以重复方式定向的抗原和/或抗原决定簇的疫苗构建体。能够产生针对这样展示的抗原的高滴度抗体,表明结合的抗原和/或抗原决定簇能够与抗体分子相互作用,并且具有免疫原性。
在本发明的一个进一步优选的实施方案中,病毒样颗粒包含或者基本由或者由RNA噬菌体AP205的重组突变外壳蛋白或其片段组成。
AP205 VLP的可装配突变形式,包括氨基酸5处的脯氨酸被置换为苏氨酸的AP205外壳蛋白(SEQ ID NO:18),也可以在本发明的实施中使用,产生本发明的一个进一步优选的实施方案。这些VLP、来自天然来源的AP205 VLP或AP205病毒颗粒可以与抗原结合,产生本发明的有序、重复的抗原阵列。
AP205 P5-T突变外壳蛋白可以由质粒pAP281-32(SEQ ID NO:19)表达,该质粒由pQb185直接衍生,其含有突变AP205外壳蛋白基因代替Qβ外壳蛋白基因。为了表达AP205外壳蛋白,用表达AP205外壳蛋白的载体转染大肠杆菌。
实施例9和10中描述了分别表达外壳蛋白和突变外壳蛋白、使其自装配为VLP的方法。合适的大肠杆菌株包括但不限于:大肠杆菌K802、JM 109、RR1。合适的载体和菌株及其组合可以按照如下鉴定:通过SDS-PAGE分别检测外壳蛋白和突变外壳蛋白的表达,任选地首先通过凝胶过滤纯化衣壳,随后用免疫扩散试验(Ouchterlony试验)或电子显微镜检查(Kozlovska,T.M.等人,Gene 137:133-137(1993))检测衣壳的形成和装配。
由载体pAP283-58和pAP281-32表达的AP205外壳蛋白由于在大肠杆菌细胞质中加工,可能缺乏初始甲硫氨酸。AP205 VLP的切割、未切割形式或其混合物是本发明的进一步优选的实施方案。
在本发明的一个进一步优选的实施方案中,病毒样颗粒包含或者基本由或者由RNA噬菌体AP205的重组外壳蛋白或其片段和RNA噬菌体AP205的重组突变外壳蛋白或其片段的混合物组成。
在本发明的一个进一步优选的实施方案中,病毒样颗粒包含或者基本由或者由RNA噬菌体AP205的重组外壳蛋白或重组突变外壳蛋白的片段组成。
能够分别装配为VLP和衣壳的重组AP205外壳蛋白片段在本发明的实施中也是有用的。可以通过内部删除或者分别在外壳蛋白和突变外壳蛋白的末端删除产生这些片段。与VLP装配相容的向外壳蛋白和突变外壳蛋白序列中插入、或者抗原序列与外壳蛋白和突变外壳蛋白序列融合是本发明的其它实施方案,分别产生嵌合AP205外壳蛋白和颗粒。插入、缺失以及与外壳蛋白序列融合的结果,以及是否与VLP装配相容,可以通过电子显微镜检查确定。
由上述AP205外壳蛋白、外壳蛋白片段和嵌合外壳蛋白形成的颗粒可以分离为纯化形式,分离方法是组合使用通过沉淀的分级分离步骤和通过凝胶过滤的纯化步骤,例如使用Sepharose CL-4B、SepharoseCL-2B、Sepharose CL-6B柱及其组合。分离病毒样颗粒的其它一些方法在本领域公知,可以用来分离噬菌体AP205的病毒样颗粒(VLP)。例如,美国专利号4,918,166描述了超速离心分离酵母逆转录转座子Ty的VLP的用途,在此全文引用作为参考。
根据本发明,一个或多个半抗原可以与RNA噬菌体外壳蛋白衣壳的一个亚单位连接。RNA噬菌体外壳蛋白的衣壳、特别是Qβ衣壳的每个亚单位偶联几个半抗原的能力可以产生密集的半抗原阵列。其它一些病毒衣壳可以通过化学交联共价连接半抗原,例如在主要免疫显性区中有赖氨酸残基修饰的HBcAg(MIR;WO 00/32227)。HBcAg刺突之间的距离(对应于MIR)是50埃(Wynne,SA.等人,Mol.Cell3:771-780(1999)),因此不能产生间距小于50A的半抗原阵列。
Qβ外壳蛋白的衣壳在其表面展示确定数量的赖氨酸残基,其具有明确的拓扑学,有3个赖氨酸残基指向衣壳内部,并且与RNA相互作用,另外4个赖氨酸残基暴露于衣壳外面。这些明确的特征有利于半抗原与颗粒外部连接,而不与颗粒内部连接,在内部赖氨酸残基与RNA相互作用。其它RNA噬菌体外壳蛋白的衣壳在其表面也有确定数量的赖氨酸残基,这些赖氨酸残基有明确的拓扑学。来源于RNA噬菌体的衣壳的另一个优点是它们在细菌中的高表达量,这允许以较低的成本大量生产材料。
Qβ外壳蛋白的衣壳的另外一个特征是其稳定性。Qβ亚单位通过二硫键彼此结合,共价连接亚单位。Qβ衣壳蛋白也显示对有机溶剂和变性剂有异常抗性。我们惊奇地发现,可以使用高达约30%的DMSO和乙腈浓度和高至约1M的胍盐浓度,而不影响衣壳的稳定性和形成半抗原阵列的能力。因此,可以利用这些有机溶剂偶联疏水分子,如激素、药物和毒素。特别是对于免疫和接种哺乳动物和人的用途而言,Qβ外壳蛋白的衣壳的高稳定性是一个重要特征。衣壳对有机溶剂的抗性使得在水性缓冲液中不可溶的半抗原能够偶联。
美国专利号5,698,424描述了向RNA噬菌体MS-2外壳蛋白的N端β发夹中的插入半胱氨酸残基,在此全文引用作为参考。然而我们注意到,衣壳中存在暴露的游离半胱氨酸残基可使衣壳通过形成二硫键寡聚化。上述美国专利中所述的其它连接涉及抗原与Qβ颗粒之间二硫键的形成。这些连接对含有巯基的分子不稳定。
Qβ上的半胱氨酸残基最初形成的二硫键与含有游离巯基残基的抗原之间的反应释放含巯基的分子,而不是半抗原。这些新形成的含巯基分子能够与颗粒上存在的其它二硫键再次反应,从而建立平衡。一旦与颗粒上形成的二硫键反应,半抗原即可与颗粒的半胱氨酸残基、或者与在颗粒上最初形成二硫键的离去基团分子的半胱氨酸残基形成二硫键。而且,通过使用一侧与Qβ颗粒上的半胱氨酸反应、另一侧与抗原上的赖氨酸残基反应的异双功能交联剂,另一连接方法可使抗原在颗粒上随机定向。
我们进一步注意到,与Qβ和Fr外壳蛋白的衣壳不同,美国专利号5,698,424所述的重组MS-2基本不含核酸,而在上述两种衣壳内包装有RNA。
我们描述了允许形成具有可变半抗原密度的强半抗原阵列的新颖而有创造性的组合物。我们证实,半抗原与VLP附着可以获得极高的表位密度。此外,改变含有适当第一附着位点的残基数量和类型也能够改变半抗原的密度和间距。例如,WO 02/056905公开了一种含有额外赖氨酸残基的Qβ突变外壳蛋白,它适于获得比野生型Qβ外壳蛋白密度更高的阵列。此外,上述申请也公开了适于以适当间距同时展示几种半抗原的偶联物,和以适当和希望的方式添加辅助分子以提高溶解度或修饰衣壳的组合物。在WO 02/056905中公开了一些其它形成的衣壳(病毒样颗粒)的Qβ外壳蛋白突变体,适于生产本发明的组合物。具体而言,当半抗原和Qβ-半抗原抗原阵列的可溶性限制了能够与Qβ病毒样颗粒连接的半抗原残基的数量时,可以使用赖氨酸残基已经被置换为精氨酸(它没有与赖氨酸残基相同的反应性)的突变体。在制备这些组合物时,可以使用高浓度的半抗原或修饰后含有第二附着位点的半抗原与突变Qβ病毒样颗粒上的赖氨酸残基完全反应,而不会象使用野生型Qβ病毒样颗粒时那样,产生可能不溶的含有更多附着半抗原的颗粒。
几种RNA噬菌体的晶体结构已经被测定(Golmohammadi,R.等人,Structure 4:543-554(1996))。利用这些信息,本领域技术人员可以容易地鉴定表面暴露的残基,并修饰噬菌体外壳蛋白,使得能够插入一个或多个反应性氨基酸残基。因此,本领域技术人员可以容易地产生并鉴定能够在本发明的实施中使用的噬菌体外壳蛋白的修饰形式。因此,也可以利用形成衣壳或衣壳样结构的蛋白质变体(例如噬菌体Qβ、噬菌体R17、噬菌体fr、噬菌体GA、噬菌体SP、噬菌体MS2的外壳蛋白)制备本发明的疫苗组合物。
尽管上述变异蛋白质的序列与其野生型对应物不同,但是这些变异蛋白质通常保留形成衣壳或衣壳样结构的能力。因此,本发明还包括:含有可形成衣壳或衣壳样结构的蛋白质变体的疫苗组合物,以及制备这些疫苗组合物的方法,用来制备这些疫苗组合物的各种蛋白质亚单位。因此,本发明的范围内包括野生型蛋白质的变体,它们可形成有序、重复的半抗原阵列(例如形成衣壳或衣壳样结构的蛋白质的变体),并且保留结合并形成衣壳或衣壳样结构的能力。C端和N端截短变体通常保留形成病毒样颗粒的能力。因此,包括缺失、添加或置换在内的变异形式、嵌合形式和自然存在的变体,都是本发明的适当成分。
细菌菌毛和菌毛蛋白 在另外一个实施方案中,本发明的核心颗粒包含、优选地由细菌菌毛或菌毛样颗粒组成。菌毛颗粒包含由包括下列生物产生的菌毛蛋白的蛋白质、突变蛋白质或片段:大肠杆菌、流感嗜血菌(Haemophilus influenzae)、脑膜炎奈瑟氏球菌(Neisseriameningitidis)、淋病奈瑟氏球菌(Neisseria gonorrhoeae)、新月柄杆菌(Caulobacter crescentus)、施氏假单胞菌(Pseudomonas stutzeri)和铜绿假单胞菌(Pseudomonas aeruginosa);沙门氏菌属(Salmonella)的种;和霍乱弧菌(Vibrio cholera)。在一个优选实施方案中,菌毛蛋白或其片段选自:a)1型菌毛蛋白;和b)P-菌毛蛋白。在另外一个实施方案中,菌毛蛋白是重组蛋白,或者菌毛或菌毛样颗粒含有重组和非重组蛋白的混合物。在另外一个实施方案中,菌毛或菌毛样颗粒含有I型菌毛蛋白或其片段。在另外一个实施方案中,菌毛蛋白是突变蛋白,优选地是如下修饰的蛋白质:通过置换除去至少一个赖氨酸残基,通过置换添加至少一个赖氨酸残基,删除至少一个赖氨酸残基,或者通过插入添加至少一个赖氨酸残基。在一个优选实施方案中,I型菌毛蛋白含具有如SEQ ID NO:2所示的氨基酸序列。在另外一个方面,本发明提供合有本发明的偶联物和药学上可接受的载体的组合物,其中核心颗粒包含、优选地由细菌菌毛或菌毛样颗粒组成。
在其它一些实施方案中,利用细菌菌毛蛋白、细菌菌毛蛋白的亚部分或含有细菌菌毛蛋白或其亚部分的融合蛋白制备本发明的疫苗组合物。菌毛蛋白的例子包括大肠杆菌、流感嗜血菌(Haemophilusinfluenzae)、脑膜炎奈瑟氏球菌(Neisseria meningitidis)、淋病奈瑟氏球菌(Neisseria gonorrhoeae)、新月柄杆菌(Caulobacter crescentus)、施氏假单胞菌(Pseudomonas stutzeri)和铜绿假单胞菌(Pseudomonasaeruginosa)产生的菌毛蛋白。适用于本发明的菌毛蛋白的氨基酸序列包括GenBank报告AJ000636、AJ132364、AF229646、AF051814、AF051815和X00981所述的序列,其完整公开内容在此引用作为参考。
细菌菌毛蛋白在输入细菌周质之前,通常被加工,除去N端前导序列。此外,本领域技术人员可以认识到,用来制备本发明疫苗组合物的细菌菌毛蛋白通常不含天然存在的前导序列。
适用于本发明的菌毛蛋白的一个具体例子是大肠杆菌的P-菌毛蛋白(GenBank报告AF237482)。适用于本发明的1型大肠杆菌菌毛蛋白的一个例子是含有GenBank报告P04128所述氨基酸序列(SEQ IDNO:2)的菌毛蛋白,它由具有GenBank报告M27603所示核苷酸序列的核酸编码。这些GenBank报告的完整公开内容在此引用作为参考。另外,通常也用上述蛋白质的成熟形式制备本发明的疫苗组合物。
适于在本发明的实施中使用的细菌菌毛蛋白或菌毛蛋白亚部分通常能够结合形成非天然分子支架。在体外制备菌毛和菌毛样结构的方法在本领域公知。例如,Bullitt等人,Proc.Natl.Acad.Sci.USA93:12890-12895(1996)描述了大肠杆菌P-菌毛亚单位的体外重建。此外,Eshdat等人(J.Bacteriol.148:308-314(1981))也描述了适于裂解大肠杆菌1型菌毛和菌毛重建的方法。简言之,这些方法如下:通过在饱和盐酸胍中37℃孵育裂解菌毛。然后通过层析纯化菌毛蛋白,之后对5mM盐酸三(羟甲基)氨基甲烷(pH 8.0)透析,形成菌毛蛋白二聚体。Eshdat等人也发现,在对含有5mM MgCl2的5mM三(羟甲基)氨基甲烷(pH 8.0)透析后,菌毛蛋白二聚体重装配形成菌毛。
另外,例如使用常规基因工程和蛋白质修饰方法,也可以修饰菌毛蛋白,使之含有第一附着位点,半抗原通过第二附着位点与此第一附着位点连接。此外,半抗原也可以通过第二附着位点与这些蛋白质中自然存在的氨基酸残基直接连接。这些修饰的菌毛蛋白然后可以在本发明的免疫组合物中使用。
用来制备本发明的组合物的细菌菌毛蛋白可以用类似于此处对于HBcAg所述的方法修饰。例如,可以将半胱氨酸和赖氨酸残基删除或者置换为其它氨基酸残基,并且可以向这些蛋白质中添加第一附着位点。此外,菌毛蛋白也可以以修饰的形式表达,或者可以在表达后化学修饰。类似地,也可以从细菌中收获完整的菌毛,然后化学修饰。
在另外一个实施方案中,从细菌(例如大肠杆菌)中收获菌毛或菌毛样结构,用来形成本发明的疫苗组合物。适于制备疫苗组合物的一个例子是大肠杆菌1型菌毛,它由含有SEQ ID NO:2所示氨基酸序列的菌毛蛋白单体构成。
本领域公知一些收获细菌菌毛的方法。例如,Bullitt和Makowski(Biophys.J.74:623-632(1998))描述了一种从大肠杆菌中收获P-菌毛的菌毛纯化方法。根据该方法,从含有P-菌毛质粒的多菌毛大肠杆菌上剪切菌毛,通过溶解和MgCl2(1.0M)沉淀的循环纯化。WO02/056905公开了从自然产生菌毛或者已经导入编码负责菌毛产生的fim操纵子之载体的细菌中收获和纯化I型菌毛。
收获后,菌毛或菌毛样结构可以用多种方法修饰。例如,可以向菌毛中添加第一附着位点,半抗原可以通过第二附着位点与之连接。换句话说,可以收获并修饰细菌菌毛或菌毛样结构,形成非天然分子支架。
也可以在没有非天然第一附着位点的条件下通过半抗原的连接修饰菌毛或菌毛样结构。例如,抗原或抗原决定簇能够与自然存在的半胱氨酸残基或赖氨酸残基连接。在这些情况下,自然存在的氨基酸残基的高度有序和重复性将指导抗原或抗原决定簇与菌毛或菌毛样结构偶联。例如,使用一种异双功能交联剂,菌毛或菌毛样结构能够与半抗原的第二附着位点连接。
当利用生物自然合成的结构(例如菌毛)制备本发明的疫苗组合物时,遗传工程改造这些生物使它们产生具有希望的特征的结构通常是有利的。例如,当使用大肠杆菌1型菌毛时,可以修饰从中收获菌毛的大肠杆菌,使之产生具有特定特征的结构。可能的菌毛蛋白修饰的例子包括一个或多个赖氨酸残基的插入,一个或多个自然存在的赖氨酸残基的缺失或置换,一个或多个自然存在的半胱氨酸残基的缺失或置换(例如SEQ ID NO:2中位点44和84处的半胱氨酸残基)。
另外也可以对菌毛蛋白基因进行其它修饰,产生含有并非赖氨酸残基的第一附着位点的表达产物(例如FOS或JUN域)。当然,合适的第一附着位点通常仅限于不妨碍菌毛蛋白形成适于在本发明的疫苗组合物中使用的菌毛或菌毛样结构的位点。重组菌毛蛋白形成菌毛的能力可以用包括电子显微镜检查在内的多种方法测定。
可以在体内修饰(例如通过同源重组)细菌细胞中自然存在的菌毛蛋白基因,或者可以将具有特定特征的菌毛蛋白基因插入这些细胞内。例如,可以将菌毛蛋白基因导入细菌细胞中,作为复制型克隆载体或插入细菌染色体内的载体的一种成分。插入的菌毛蛋白基因也可以与表达调节控制序列(例如lac操纵基因)连接。
在大多数情况下,在本发明的疫苗组合物中使用的菌毛或菌毛样结构由一种类型的菌毛蛋白亚单位构成。然而,本发明的组合物也包括包含由不同菌毛蛋白亚单位构成的菌毛或菌毛样结构的疫苗。通常使用由相同亚单位组成的菌毛或菌毛样结构,因为它们预期能够形成表现高度有序、重复抗原阵列的结构。
第二附着位点 本发明提供了显示有序、重复阵列的分子支架的制备,包括具有高表位密度的RNA噬菌体外壳蛋白的衣壳的组合物。本领域技术人员可以理解,半抗原的性质、半抗原上第二附着位点的性质和位置是可能影响构建本发明的偶联物的方法和这些偶联物诱导免疫应答的效果的重要因素。
设计第二附着位点的一个前提条件是融合、插入或基因改造或连接位点的选择。熟练技术人员知道如何找到选择第二附着位点的位置的指南,可以考虑与这种决定有关的多种因素。半抗原的化学和/或晶体结构可以提供关于适于偶联的分子结构域或基团的信息。反应性基团或结构域的溶剂可及性可能是与第一附着位点化学偶联的化学物的动力学限制因素。适于偶联的基团必须是可以利用的,如巯基残基。如果用半抗原免疫旨在抑制该半抗原(也可以是一种自身抗原)与其天然配体(如受体)的相互作用,则通常添加第二附着位点,以便产生针对与天然配体相互作用位点的抗体。因此选择第二附着位点的位置,以避免第二附着位点或含有它的任何接头或氨基酸接头的空间位阻。在其它一些实施方案中,希望针对半抗原(也可以是一种自身抗原)与其天然配体相互作用位点以外之位点的抗体应答。在这些实施方案中,可以选择第二附着位点,防止产生针对该半抗原与其天然配体的相互作用位点的抗体。考虑的其它因素包括半抗原的性质、其生物化学性质如pI、电荷分布、进一步的修饰。柔性接头通常是优选的。
选择第二附着位点位置的其它标准包括:半抗原的寡聚状态、寡聚位点、辅因子的存在、半抗原的化学反应性、以及揭示半抗原结构和序列中相关位点的实验证据的有无:即该位点处半抗原的修饰与半抗原功能的一致性或者与适于产生可识别该半抗原、优选地阻断半抗原功能的抗体的一致性。
含有多肽接头的半抗原与VLP、特别是与RNA噬菌体外壳蛋白的衣壳的一个特别优选的连接方法是RNA噬菌体外壳蛋白衣壳表面的赖氨酸残基与多肽接头上的巯基残基(如半胱氨酸残基中所见)连接。类似地,半抗原上的游离巯基也可能是有效的附着位点。为了作为第二附着位点,氧化的巯基必须是被还原的状态,此时可以用例如DTT、TCEP或β-巯基乙醇进行还原。
在本发明的一个优选实施方案中,合成半抗原,使其含有一个第二附着位点,该位点能够与RNA噬菌体外壳蛋白衣壳表面上的赖氨酸残基反应。
根据本发明,通过选择交联剂和其它反应条件可以调节RNA噬菌体外壳蛋白衣壳上的表位密度。例如,交联剂Sulfo-GMBS和SMPH能够获得高表位密度。高浓度反应物正向影响衍生化,可以利用操作反应条件控制与RNA噬菌体衣壳蛋白偶联的、特别是与Qβ衣壳蛋白偶联的抗原数量。另外,核心颗粒上第一附着位点的数量是影响半抗原阵列密度的另外一个因素。在本发明的一个实施方案中,我们提供了一种Qβ突变外壳蛋白,它含有额外的赖氨酸残基,适于获得更高密度的阵列。
交联 本领域技术人员公知连接半抗原与核心颗粒的方法,有大量参考文献可帮助技术人员(例如,Sambrook,J.等人编著,《分子克隆:实验室手册》,第二版,Cold Spring Harbor Laboratory Press,ColdSpring Habor,N.Y.(1989);Ausubel,F.等人编著,《现代分子生物学方法》,John H.Wiley & Sons,Inc.(1997);Celis,J.编著,《细胞生物学》,Academic Press,第二版,(1988);Harlow,E.和Lane,D.,《抗体:实验室手册》,Cold Spring Harbor Laboratory,Cold Spring Habor,N.Y.(1988),这些文献全部在此全文引用作为参考。
本发明公开了使核心颗粒与半抗原结合的不同方法,并在WO02/056905中有进一步描述。方法包括,JUN和FOS亮氨酸拉链蛋白域分别用作本发明的第一和第二附着位点。
本发明的优选实施方案包括非天然分子支架与半抗原通过化学交联偶联。已经研制了大量化合物,用来促进蛋白质/肽的交联或蛋白质与衍化分子(例如半抗原)的偶联。包括但不限于本领域技术人员公知的羧酸衍化的活性酯(活化的化合物)、混合酸酐、酰卤、酰叠氮、烷基卤、N-马来酰亚胺、亚氨基酯、异氰酸酯和异硫氰酸酯。它们能够与蛋白质分子的反应性基团形成共价键。根据活化基团的不同,反应性基团是蛋白质分子上的赖氨酸残基的氨基,或载体蛋白或修饰载体蛋白分子中的硫醇基,它们在反应时导致酰胺、胺、硫醚、脒或硫脲键的形成。本领域技术人员可以确定其它合适的活化基团,例如,见普通参考文献,如《蛋白质偶联和交联的化学》(Wong(1991)CRCPress,Inc.,Boca Raton,Fla.)。大多数试剂优先与赖氨酸侧链基团反应。
在一些实施方案中,使用一种异双功能交联剂,使抗原通过化学交联与核心颗粒连接。有几种异双功能交联剂在本领域公知。在一个实施方案中,异双功能交联剂含有一个能够与核心颗粒赖氨酸残基的侧链氨基反应的官能团,和另外一个能够与半抗原上存在的半胱氨酸残基或巯基反应的官能团,这些基团通过还原可用于该反应,或者在半抗原上构建或连接并任选地通过还原用于该反应。该方法的第一步,称为衍生化,是核心颗粒与交联剂反应。反应产物是活化的核心颗粒,也被称为活化的载体。第二步,用常用方法如凝胶过滤或透析除去未反应的交联剂。第三步,抗原与活化核心颗粒反应,该步骤被称为偶联步骤。未反应的抗原任选地可在第四步除去。
在另一个实施方案中,用适于交联第一附着位点的活性物质衍生化半抗原,产生活化的半抗原。这种衍生化可以在分离的半抗原上发生或者通过化学合成发生。活化的半抗原然后与核心颗粒反应,从而发生偶联。
有几种异双功能交联剂在本领域公知。包括交联剂SMPH(Pierce)、Sulfo-MBS、Sulfo-EMCS、Sulfo-GMBS、Sulfo-SIAB、Sulfo-SMPB、Sulfo-SMCC、SVSB、SIA和可以获得的其它一些交联剂,例如可从Pierce Chemical Company(Rockford,IL,USA)获得,其含有一个氨基反应性官能团和一个SH残基反应性官能团。上述交联剂均能导致硫醚键的形成。适于在本发明的实施中使用的另一类交联剂,其特征在于偶联后在半抗原与核心颗粒之间引入一个二硫键。属于这一类的交联剂包括,例如SPDP和Sulfo-LC-SPDP(Pierce)。根据有机化学领域的反应理论众所周知,用交联剂衍生化核心颗粒的程度可能受不同实验条件影响,如反应双方各自的浓度、一种试剂相对于另一种的过量、pH、温度和离子强度。偶联度,即每个载体上半抗原的数量,可通过改变上述实验条件来调节,以满足疫苗的要求。半抗原的可溶性可以限制能够在每个亚单位上偶联的抗原的数量,当获得的疫苗不可溶时,减少每个亚单位上抗原的数量是有利的。
在一个具体实施方案中,化学试剂是异双功能交联剂ε-马来酰亚胺基己酸N-羟基琥珀酰亚胺酯(Tanimori等人,J.Pharm.Dyn.4:812(1981);Fujiwara等人,J.Immunol.Meth.45:195(1981)),其含有(1)氨基反应性琥珀酰亚胺基,和(2)SH基反应性马来酰亚胺基。可以改造第一附着位点的异源蛋白质或多肽,使之含有一个或多个赖氨酸残基,作为异双功能交联剂的琥珀酰亚胺部分的反应性基团。一旦与异源蛋白质的赖氨酸残基化学偶联,异双功能交联剂的马来酰亚胺基即可与抗原或抗原决定簇上半胱氨酸残基的SH基反应。在此情况下,抗原或抗原决定簇的制备可能需要构建一个巯基作为第二附着位点,使其可与交联剂上的游离马来酰亚胺官能团反应,而该交联剂与非天然分子支架的第一附着位点结合。因此,在这种情况下,异双功能交联剂与非天然分子支架的第一附着位点结合,并且将该支架与抗原或抗原决定簇的第二结合位点连接。
半抗原与核心颗粒的其它偶联方法包括半抗原与核心颗粒利用碳二亚胺化合物交联的方法。这包括碳二亚胺EDC(1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸),任选地在反应中也可以使用N-羟基-琥珀酰亚胺NHS。在一种方法中,EDC与含有游离羧酸的半抗原混合,然后添加到蛋白质载体上。在另外一些方法中,使用同型双功能交联剂,如戊二醛、DSG、BM[PEO]4、BS3(Pierce Chemical Company,Rockford,IL,USA)或其它已知的同型双功能交联剂(其含有对核心颗粒的胺基或羧基具有反应性的官能团),使该半抗原与核心颗粒连接。
适于分别连接半抗原与核心颗粒和病毒样颗粒的其它交联方法和交联剂,以及进行偶联反应和使用化学交联剂和化学交联方法的指南,可见Hermanson,G.T.《生物偶联技术》,Academic Press Inc.,SanDiego,CA,USA。
结合核心颗粒与半抗原的其它方法包括核心颗粒被生物素化、半抗原与链霉抗生物素融合的方法,或半抗原和核心颗粒均被生物素化的方法。在这种情况下,首先使半抗原与链霉抗生物素或抗生物素蛋白结合,通过调节半抗原与链霉抗生物素的比例,使得仍有自由结合位点可以与下一步添加的核心颗粒结合。或者,也可以在“一锅”反应中混合所有成分。受体和配体的可溶形式都存在时,能够与核心颗粒或半抗原交联的其它配体-受体对也可以作为结合半抗原与核心颗粒的结合剂。
半抗原 本发明的一个实施方案提供适于对半抗原免疫的有序、重复的半抗原阵列。优选的半抗原是激素、药物和毒性化合物。更优选的是药物,特别是成瘾性药物。针对这些药物、激素和毒性化合物的免疫应答可以用来保护处于暴露于所述化合物的危险中的个体,以治疗这样暴露的个体,或者用来预防或治疗成瘾性。
代表性激素包括但不限于:孕酮、睾酮、雌激素、黑色素刺激激素、可的松、促卵泡激素、肾上腺素和去甲肾上腺素。针对这些激素的免疫应答可以用于治疗黑素瘤;生殖器官癌症,如乳腺癌、卵巢癌、子宫癌、睾丸癌和子宫颈癌;以及用于希望改变激素水平的情况,如用于避孕。
代表性毒性化合物包括但不限于:毒性植物、动物和微生物的天然产物;包括但不限于黄曲霉毒素、鱼肉毒素(ciguautera toxin)和河豚毒素。人工生产的或者代谢产生的代表性毒性化合物包括抗生素(例如万古霉素等)、抗癌化合物(例如长春碱等)和化学战剂(例如肉毒毒素、沙林、塔崩、梭曼、VX等)。本发明的一个方面包括针对常用药物的毒性代谢物的抗体的产生,使得个体可以继续接受药物的有利作用,而没有与毒性代谢物有关的副作用
治疗相关疾病的医学领域的技术人员知道如何选择抗原或抗原决定簇,用于治疗药物成瘾、特别是寻乐性药物成瘾的组合物和方法。这些抗原或抗原决定簇的代表性实例包括,例如:阿片类和吗啡衍生物,如可待因、芬太尼、海洛因、吗啡和鸦片;弛缓剂,如安定;兴奋剂,如安非他明、可卡因、MDMA(亚甲二氧基甲基苯丙胺)、甲基苯丙胺、哌甲酯和尼古丁;致幻剂,如PCP、LSD、麦斯卡林和西洛西宾;大麻素类,如大麻和印度大麻;以及地昔帕明/米帕明类药物,以及去甲替林/阿米替林类药物。对尼古丁成瘾的治疗也可以针对尼古丁代谢物,包括降烟碱和可替宁,这两者比尼古丁有更长的半衰期,具有类似于尼古丁的药理学和神经药理学作用,可能成瘾。
在上述实施方案中,免疫半抗原不必包含整个激素、药物或毒素分子。针对目的药物、激素或毒素的适当免疫应答可以利用药物、激素或毒素的片段或相关化学结构产生。
本发明包括半抗原与载体的不同连接位点和连接方法,并且在本发明的前面已经说明,参考实施例。优选的连接位点和方法可以根据现有的经验、理论并通过常规实验确定。
尼古丁和尼古丁代谢物 适合尼古丁的免疫应答可以用通过吡啶或吡咯烷环与核心颗粒偶联的半抗原产生。在一个实施方案中,由6-氨基-(±)-尼古丁合成6-(羧甲基脲基)-(±)-尼古丁(CMUNic)偶联物,它与异氰基乙酸乙酯反应,形成6-(羧乙基脲基)-(±)-尼古丁,然后用氢氧化锂水解,形成CMUNic,如(Hieda等人Int J Pharmacol 22:809-819(2000))所述,该文献在此全文引用作为参考。半抗原通过末端羧基与核心颗粒偶联,末端羧基例如可以用1-乙基-3-(3-二甲基氨丙基)碳二亚胺HCl活化。在另外一个实施方案中,如WO 99/61054所述,6-氨基-(±)-尼古丁与载体蛋白偶联,该文献在此全文引用作为参考。
在本发明的另外一个实施方案中,如Cushman和Castignoli(J OrgChem 37:1268-1271(1972))所述,由反式-3′-羟甲基尼古丁醇通过甲苯磺酸酯制备反式-3′-氨甲基尼古丁偶联物,该文献在此全文引用作为参考。半抗原通过一个琥珀酸接头与核心颗粒偶联,利用1-乙基-3-(3-二甲基氨基丙基)碳二亚胺HCl(EDAC)活化接头的羧酸基团。
在一个有关实施方案中,与尼古丁半抗原的3′-连接如下进行:首先产生反式-3′-羟甲基尼古丁,它与琥珀酸酐反应,产生琥珀酰化的羟甲基尼古丁(O-琥珀酰-3′-羟甲基-尼古丁)。该产物然后与EDAC和核心颗粒混合,用于碳二亚胺活化的偶联,如Langone和Van Vunakis(Methods Enzymol.84:629-641(1982))所述,该文献在此全文引用作为参考。在另外一个实施方案中,反式-4′-羧基可替宁类似地用EDAC活化,用于与一种蛋白质载体偶联。
在一个实施方案中,尼古丁半抗原通过转化为氨乙基吡啶鎓衍生物S-1-(b-氨乙基)氯化尼古丁鎓二盐酸,经由1位氮偶联,后者在1-环己基-3-(2-吗啉代乙基)-碳二亚胺metho-对甲苯磺酸盐存在下与核心颗粒偶联,如Noguchi等人(Biochenl Biophys Res Comm.83:83-86(1978))所述,该文献在此全文引用作为参考。在一个相关实施方案中,利用相同的常用方法,通过形成S-1-(b-氨乙基)氯化可替宁盐酸,将可替宁与核心颗粒偶联。
在一个实施方案中,如Isomura等人(J Org Chem 66:4115-4121(2001)所述(在此全文引用作为参考),通过形成N-[1-氧代-6-[(2S)-2-(3-吡啶基)-1-吡咯烷基]己基]-β-丙氨酸,尼古丁半抗原通过1′-位偶联。这种活化的半抗原然后与一种蛋白质载体偶联。在另外三个实施方案中,在蛋白质核心颗粒上的第一附着位点与可替宁半抗原4-氧代-4-[[6-[(5S)-2-氧代-5-(3-吡啶基)-1-吡咯烷基]]己基]氨基]-丁酸或尼古丁半抗原(2S)-2-(3-吡啶基)-1-吡咯烷丁酸苯甲酯或(2R)-2-(3-吡啶基)-1-吡咯烷丁酸苯甲酯之间形成偶联物。
在一个实施方案中,可替宁4′-羧酸与载体在赖氨酸处共价结合,如Bjerke等人(J.Immunol.Methods,96,239-246(1987))所述,该文献在此全文引用作为参考。
尼古丁半抗原可以通过一个接头在尼古丁的6位处与载体蛋白偶联。根据这些方法,在本发明的实施方案中使用下列半抗原:N-琥珀酰-6-氨基-(.+-.)-尼古丁;6-(σ.-氨基癸酰胺基)-(.+-.)-尼古丁和6-(.σ.-氨基癸酰胺基)-(.+-.)-尼古丁,如(Castro等人.Eur.J.Biochem.,104,331-340(1980);Castro等人.Biochem.Biophys.Res.Commun.67,583-589(1975);Castro等人.Res.Commun Chem.Path.Pharm.51,393-404(1986))所述,这些文献在此全文引用作为参考。
在本发明的其它一些实施方案中,尼古丁半抗原通过氨甲基尼古丁的琥珀酰化由3′、4′或5′位偶联,用EDC活化,随后与载体混合,如美国专利号6,232,082所述,该文献在此全文引用作为参考。在其它一些实施方案中,氨甲基尼古丁通过聚谷氨酸-ADH与核心颗粒偶联。在其它一些实施方案中,由3′、4′或5′位衍化的乙酰尼古丁和醛尼古丁形成偶联物。
在其它一些实施方案中,半抗原载体偶联物含有尼古丁的5-位和6-位连接,包括5-(1-甲基-2-吡咯烷基)-2-或3-吡啶基-偶联物和5-(N-甲基-2-吡咯烷基)-2-或3-吡啶基-偶联物。用于这些偶联物的半抗原的构建在WO 99/61054中有描述,后者在此全文引用作为参考。在其它一些实施方案中,使用5-和6-氨基尼古丁作为初始材料,它在氨基处进一步衍生化,一般添加以适当的反应性基团(包括胺和羧酸)为末端的碳链。这些半抗原因此适合与本发明的核心颗粒偶联。在其它一些实施方案中,使用5-或6-溴尼古丁作为与炔反应的适当起始物,导致在不饱和碳基团中加入以适用于偶联的基团(包括胺和羧酸)为末端的链,从而与核心颗粒偶联。
本发明的其它实施方案包括含有在尼古丁的1、2、4、5、6或1′位偶联的尼古丁半抗原的偶联物,如Swain等人(WO 98/14216)所述,在此全文引用作为参考。
本发明的其它实施方案包括含有如Janda等人(WO02/058635)所述的尼古丁半抗原的偶联物。
其它实施方案包括构象约束的尼古丁半抗原,如Meijler等人.(J.Am.Chem.Soc,2003,125,7164-7165)所述。
可卡因与相关药物 本发明提供包含与核心颗粒偶联的可卡因的偶联物、组合物和方法。在一类实施方案中,苯甲酰可卡因和苯甲酰芽子碱(ecognine)的重氮盐与载体蛋白偶联。在其它一些实施方案中,可卡因和去甲可卡因的对亚氨酯衍生物与核心颗粒偶联。美国专利号3,88,866、4,123,431和4,197,237描述了适合这些实施方案的半抗原,在此全文引用作为参考。利用不同可卡因衍生物的苯环的对位,由于引入一个酰胺键,可卡因的偶联物显示水解稳定性提高。
本发明的其它实施方案包括如美国专利号5,876,727所述的可卡因半抗原,在此全文引用作为参考。
在一个实施方案中,通过在两个当量的二异丙基乙胺存在下,在DMF中用溴乙酰溴酰化芽子碱甲酯,合成本发明的偶联物的前体。产物然后与硫醇化载体蛋白的巯基偶联获得偶联物。
在另外一个实施方案中,通过在两个当量的三乙胺存在下,在DMF中用琥珀酸酐琥珀酰化芽子碱甲酯,合成本发明的偶联物的前体。产物然后与一种载体蛋白的赖氨酸残基的氨基偶联获得偶联物。在一个实施方案中,通过在两个当量的三乙胺存在下,去甲可卡因与琥珀酸酐在二氯甲烷中反应,合成本发明的偶联物的前体。在其它一些实施方案中,通过去甲可卡因、单活化的琥珀酸和三乙胺的溶液反应,形成琥珀酰化的去甲可卡因,合成本发明的偶联物的前体。在每种情况下,产生的琥珀酰去甲可卡因由至少两种异构体的混合物组成,即琥珀酰基的exo和endo形式。在这些实施方案中,然后利用EDC,使琥珀酰去甲可卡因与一种载体蛋白的赖氨酸的ε-氨基偶联,产生偶联物。在一个替代实施方案中,使用一种预先活化的琥珀酰化去甲可卡因衍生物进行该偶联反应。即,可以分离并鉴定中间体。通过在二环己基碳二亚胺(DCC)和DMF存在下,4-羟基-3-硝基苯磺酸钠盐与琥珀酰化的去甲可卡因反应,合成这种预先活化的琥珀酰化去甲可卡因衍生物。该产物与一种载体蛋白的赖氨酸残基的氨基偶联,产生偶联物。
在另一个实施方案中,通过在氯甲酸乙酯、N-甲基吗啉(NMM)和DMF存在下,琥珀酰化去甲可卡因与N-羟基琥珀酰亚胺反应,合成本发明的化合物。该产物然后与一种载体蛋白的赖氨酸残基的氨基偶联,产生偶联物。
在一个实施方案中,通过亚硫酰氯与琥珀酰化的去甲可卡因反应,合成本发明的化合物。该产物然后与一种载体蛋白偶联,产生偶联物。在另外一个实施方案中,如Carpino((1993)J.Am.Chem.Soc.115:4397-4398)所述(在此全文引用作为参考),通过琥珀酰化的去甲可卡因与HATU在DMF和二异丙基乙胺中反应,合成本发明的化合物。将该产物加入含有载体蛋白的水溶液中,产生偶联物。
在另外一个实施方案中,通过在DMF和二异丙基乙胺中,琥珀酰化的去甲可卡因与PyBroP反应,合成本发明的化合物。将该产物加入含有载体蛋白的水溶液中,产生偶联物。在一个相关实施方案中,载体蛋白在硼酸缓冲液中用琥珀酸酐琥珀酰化。然后在EDC存在下使该产物与去甲可卡因偶联,产生偶联物。
在另外一个实施方案中,用硼烷-二甲亚砜复合物实现苯甲酰芽子碱中的可卡因游离酸还原为相应的伯醇。该醇与琥珀酸酐在DMF中反应,其产物然后在EDC存在下与一种载体蛋白的游离氨基酸基团偶联,产生偶联物。
在另外一个实施方案中,通过在EDC存在下使苯甲酰芽子碱与一种载体蛋白的赖氨酸残基的氨基偶联,合成本发明的化合物。
在一个实施方案中,通过在两个当量的二异丙基乙胺存在下,在二氯甲烷中用琥珀酸酐酰化外消旋的尼古丁,合成该偶联物的前体。然后利用HATU,使该反应的产物与一种载体蛋白的赖氨酸残基偶联,产生偶联物。在另外一个实施方案中,在无水甲醇中用3-溴丁酸乙酯、5-溴戊酸、6-溴己酸或8-溴辛酸选择性烷基化(S)-(-)-尼古丁中的吡啶氮,产生适合利用HATU与载体蛋白偶联的产物。
组合物、疫苗及其施用以及治疗方法
如上所述,本发明提供可用于预防和/或治疗疾病或病症的组合物。本发明还提供用来预防和/或治疗个体的疾病或病症的接种方法。在一个优选实施方案中,该组合物刺激免疫应答,产生可与有机分子结合的免疫分子,包括抗体。本发明还提供用来预防和/或治疗个体的疾病或病症的接种方法。
免疫应答的性质或类型不是本公开内容的限制因素。根据本领域公知的原则,根据疾病的不同,治疗或预防性免疫应答所希望的结果可能不同。例如,一种针对吸入药物(例如尼古丁、可卡因)的疫苗可以用来诱导高滴度的血清IgG,以及在呼吸道上皮中诱导分泌型sIgA抗体,从而结合呼吸道及血流中的尼古丁。而当靶向一种注射的滥用药物(例如海洛因)时,sIgA抗体的滴度可能不太相关。然而,针对注射的滥用药物的接种方法若产生高血清滴度以及sIgA,也将是有效的,只要血清滴度足够即可。
本发明包括足以治疗或预防一种疾病或病症或成瘾的疫苗。本发明还包括降低症状的数量、严重程度或持续时间的疫苗,和可以有效减少患此症状的人群中的个体数量的疫苗组合物。本发明包括作用于免疫系统的组合物,它可以帮助治疗一种疾病,作为对一种疾病的全面治疗干预的一个方面。由于成瘾具有明显复杂的性质,本发明包括帮助治疗药物成瘾的组合物,但是还伴有精神、行为、社会和法律的干预。
此外,根据本领域公知的原则,根据疾病不同,希望刺激不同类型的免疫应答。例如,众所周知,某些免疫应答比其它免疫应答更适于特定抗原。某些免疫应答实际上是不适当的,能够引起病理,如病理性炎症。
抗原性质、导入体内的途径、剂量、剂量方案、抗原的重复性、宿主背景和免疫系统的信号传导因子可能影响免疫应答的性质。这些知识在本领域公知。因此,利用本领域公知的理论和常规实验可以调节免疫应答。
此外,本发明还包括在对药物接种过程中使用不同的核心颗粒。对核心颗粒如菌毛产生强烈免疫应答的个体,可以用包含相同半抗原但核心颗粒不同的组合物免疫。
不希望局限于理论或者本发明操作的任何具体机制说明,本发明的偶联物作为产生免疫应答的药物组合物的成分,特别是作为疫苗,具有新的不同寻常的优点。本领域公知的其它一些载体,包括BSA、匙孔戚血蓝蛋白、破伤风类毒素、细菌外膜蛋白、霍乱毒素和铜绿假单胞菌外毒素A,对个体可能不适用,特别是对于人。上述载体可诱导变态反应、或刺激病理性免疫应答(例如霍乱毒素、KLH、BSA)。上述载体可能需要使用佐剂,如现在认为不适于人用的弗氏完全佐剂。有一些载体可能是现有疫苗的成分(例如,破伤风类毒素、霍乱毒素、外毒素A)。因此,个体可能预先具有对这些载体的高水平免疫,因此用抗原-载体偶联物免疫将诱导对该载体相对更强(相对新抗原而言)的免疫应答。由于这些原因之一或全部,本发明的偶联物和组合物与上述载体蛋白相比具有有益的进步。本发明证明了尼古丁-QβVLP偶联物组合物刺激针对尼古丁的免疫应答的应用,它不需要使用弗氏完全佐剂,也没有病理性免疫应答的证据。
在本发明实施方案的应用中,与核心颗粒偶联的半抗原能够被抗原呈递细胞摄取,从而刺激T辅助细胞诱导免疫应答。T辅助细胞应答可分为1型(TH1)和2型(TH2)T辅助细胞应答(Romagnani,Immunol.Today 18:263-266(1997))。TH1细胞分泌干扰素-γ和其它细胞因子,引发B细胞产生IgG1-3抗体。相反,TH2细胞产生的一种关键细胞因子是IL-4,它使B细胞产生IgG4和IgE。在许多实验系统中,TH1和TH2应答的发展互相排斥,因为TH1细胞抑制TH2细胞的诱导,反之亦然。因此,引发强烈TH1应答的抗原同时抑制TH2应答的发展,因此抑制IgE抗体的产生。有趣的是,实际上所有病毒都在宿主中诱导TH1应答,但不能触发IgE抗体的产生(Coutelier等人,J.Exp.Med.165:64-69(1987))。IgE同型抗体是变态反应的重要成分。肥大细胞在其表面结合IgE抗体,并且在特异抗原与结合在肥大细胞表面的IgE分子结合后,释放组胺和变态反应的其它介质。TH1应答典型的同型模式不限于活病毒,对灭活或重组病毒颗粒也可观察到(Lo-Man等人,Eur.J.Immunol.28:1401-1407(1998))。因此,利用本发明的方法(例如甲疫苗技术),病毒颗粒能够装载不同的半抗原用于免疫。由于所产生半抗原的“病毒结构”,将引发TH1应答,产生“保护性”IgG1-3抗体,并且阻止产生引起变态反应的IgE抗体。因此,本发明包括能够诱导优选的免疫应答(特别是TH1型应答)的组合物。此外,本发明还包括本发明的组合物对抗由针对目的半抗原的其他疫苗诱导的变态反应的用途。
本发明的另外一个有利特征是,半抗原可以在颗粒上以有序、重复的阵列存在,无论是否有T细胞辅助,均能够诱导有效的免疫应答。本发明的这一特征特别有利。
与分离的蛋白质不同,在不用任何佐剂、有及没有T细胞辅助的情况下,病毒均诱导快速、有效的免疫应答(Bachmann和Zinkernagel,Ann.Rev.Immunol.15:235-270(1997))。尽管病毒通常极少含蛋白质,但是它们比分离的成分能引发更强的免疫应答。对于B细胞应答,已知病毒免疫原性的一个关键因素是表面表位的重复性和顺序。许多病毒展示一种准晶体表面,其表面显示规则的表位阵列,可有效交联B细胞上表位特异的免疫球蛋白(Bachmann和Zinkernagel,Immunol.Today 17:553-558(1996))。B细胞上表面免疫球蛋白的这种交联是一种强激活信号,可直接诱导细胞周期的进展和IgM抗体的产生。进而,这些触发的B细胞能够激活T辅助细胞,随后诱导B细胞由产生IgM抗体向产生IgG抗体转换,并产生长期B细胞记忆—这是所有接种的目标(Bachmann和Zinkernagel,Ann.Rev.Immunol.15:235-270(1997))。本发明提供一种提高接种效力的方法,该方法是通过半抗原与核心颗粒结合,提高用于免疫的半抗原的重复程度。如前所述,本发明提供含有如下核心颗粒的组合物,这些核心颗粒经过修饰改变了第一附着位点的数量和/或排列。
本领域普通技术人员可以理解,当对个体施用本发明的偶联物时,该偶联物可以存在于一种组合物中,其中含有希望用来提高偶联物效能的盐、缓冲剂、佐剂或其它物质、赋形剂或载体。大量资料中提供了适合于或满足制备药物组合物的材料的例子,包括Remington’s Pharmaceutical Sciences(Osol,A,ed.,Mack PublishingCo.,(1990))。
如果接受个体能够耐受本发明的组合物的施用,则称该组合物是“药理学可接受的”。此外,本发明的组合物将以“治疗有效量”(即产生希望的生理学效应的量)施用。
本发明的组合物可以通过本领域公知的多种方法施用,但是通常通过注射、输液、吸入、口服或其它适当的物理方法施用。这些组合物也可以肌肉内、静脉内、透粘膜、透皮或皮下施用。用于施用的组合物成分包括无菌水性(例如生理盐水)或非水性溶液和悬液。非水溶剂的例子包括丙二醇、聚乙二醇、植物油如橄榄油、和注射用有机酯如油酸乙酯。可以利用载体或封闭性包衣提高皮肤通透性并提高抗原吸收。
在一个具体实施方案中,尼古丁成瘾者(人)用5-500μg、优选地25-200μg、更优选地50-100μg、最优选地100μg Nic-Qβ偶联物免疫,在第3周和第6周时加强,更优选地在第4周和第8周时加强。免疫途径可能包括肌肉内、皮下、皮内、透皮或静脉内注射。免疫两周后,使用如此处其它部分所述的试剂盒监测免疫应答。产生的免疫应答是尼古丁特异的,包括高血清IgG,足以抑制脑的尼古丁摄取。产生的免疫应答持续时间长,因此个体不能体会到尼古丁的愉悦效果,而停止使用尼古丁。本领域技术人员根据测定的免疫应答将会知道是否需要进一步的免疫来维持尼古丁特异的IgG水平。在本发明的一个替代实施方案中,通过鼻内接种施用本发明的尼古丁半抗原载体偶联物。这种施用产生高抗体滴度,包括IgA,如实施例所述。
在本发明的另外一个实施方案中,提供了药物组合物用于治疗尼古丁成瘾、缓解尼古丁戒断症状、帮助戒烟或防止复吸,该组合物含有本发明的疫苗组合物与另外的药物的治疗有效的组合。在一个实施方案中,该另外的药物选自:抗抑郁剂;尼古丁受体调节剂;大麻素受体拮抗剂;阿片受体拮抗剂;单胺氧化酶抑制剂;抗焦虑剂,或这些药物的任意组合。优选地,该另外的药物是抗抑郁剂,其选自:丁氨苯丙酮、多塞平、地昔帕明、氯米帕明、米帕明、去甲替林、阿米替林、普罗替林、曲米帕明、氟西汀、氟伏沙明、帕罗西汀、舍曲林、苯乙肼、反苯环丙胺、阿莫沙平、马普替林、曲唑酮、文拉法辛、米氮平、它们的药物活性盐以及它们的旋光异构体。在一个非常优选的实施方案中,抗抑郁剂是丁氨苯丙酮或其药学上可接受的盐,或者是去甲替林或其药学上可接受的盐。
在另一个实施方案中,该另外的药物是尼古丁受体调节剂,其选自:美卡拉明、SSR591813、金刚烷胺、潘必啶、二氢-β-刺桐碱、六甲双铵、刺桐定碱、松达氯铵、樟磺咪芬、氯筒箭毒碱、d-筒箭毒碱、varenicline、它们的药学上可接受的盐以及它们的旋光异构体。在一个非常优选的实施方案中,该尼古丁受体调节剂是美卡拉明或其药学上可接受的盐。在另外一个优选实施方案中,该尼古丁受体调节剂是varenicline或其药学上可接受的盐。
在一个实施方案中,本发明包括一种治疗烟草成瘾或尼古丁成瘾、缓解尼古丁戒断症状、防止复吸或者帮助戒烟的方法,包括对患者施用本发明的疫苗组合物和另外的药物的步骤。在一个优选实施方案中,该疫苗组合物经鼻内、经口、皮下、透皮、肌肉内或静脉内施用,其中该另外的药物口服施用或者通过透皮贴剂施用。在一个更优选的实施方案中,本发明的疫苗组合物含有与Qβ病毒样颗粒偶联的O-琥珀酰-3′-羟甲基-尼古丁。
抗抑郁剂、尼古丁受体激动剂和拮抗剂、大麻素和阿片受体拮抗剂、单胺氧化酶抑制剂和抗焦虑剂能够缓解戒烟过程中的某些症状,如退隐、渴望,抑郁、易怒、无力、缺乏动力(amotivation)、食欲改变、恶心和睡眠过度。它们主要直接作用于脑中的受体。此外,戒烟后的体重增加也是许多人的一个主要顾虑。接种抑制脑的尼古丁摄取,从而抑制它的奖赏效应(rewarding effect)。它不抑制戒断症状,而是抑制吸烟后尼古丁成瘾的增强。因此,接种与使用抗抑郁剂、尼古丁受体拮抗剂、大麻素受体拮抗剂、单胺氧化酶抑制剂和抗焦虑剂以及抑制体重增加的其它药物相组合,有利于帮助戒烟和防止复吸。
抗抑郁剂用来治疗尼古丁戒断症状、帮助戒烟。一种这样的抗抑郁剂是丁氨苯丙酮,商品名为Zyban的一种丁氨苯丙酮HCl缓释制剂作为一种戒烟助药在市场上销售。推测丁氨苯丙酮的作用机制包括抑制多巴胺和/或去甲肾上腺素的神经再摄取。由于多巴胺与成瘾性物质如尼古丁的奖赏效应有关,预计抑制去甲肾上腺素摄取可诱导戒断症状减少。美国专利号3′819′706和3′885′046公开了生产丁氨苯丙酮及其药学上可接受的盐的方法。生产光学纯(+)-丁氨苯丙酮和纯(-)-丁氨苯丙酮的方法已经公开(Castaldi G等人,J.Org.Chem.,1987,52:3018,Musso等人,1993,Chirality 5:495-500)。
本发明的一个优选实施方案涉及通过用尼古丁-VLP偶联物、优选地用尼古丁-Qβ偶联物接种,并且施用丁氨苯丙酮、优选地盐酸丁氨苯丙酮,对患者进行联合治疗,以帮助戒烟或防止复吸。配制将要施用的丁氨苯丙酮,使其提供每天约150mg共6天的初始剂量,随后是每天300mg的剂量。
去甲替林用来治疗抑郁症,也证明在帮助戒烟中有作用(da Costa等人,2002,Chest,122,403-408)。本领域技术人员已知生产去甲替林的方法。本发明的一个优选实施方案涉及通过用尼古丁-VLP偶联物、优选地用尼古丁-Qβ偶联物接种,并且施用去甲替林,对患者进行联合治疗,以帮助戒烟或防止复吸。去甲替林以每天10-150mg、最优选每天75mg的剂量施用。
用来与接种组合的其它抗抑郁剂包括:多塞平、氟西汀、地昔帕明、氯米帕明、米帕明、阿米替林、曲米帕明、氟伏沙明、proxetine、舍曲林、苯乙肼、反苯环丙胺、阿莫沙平、马普替林、曲唑酮、文拉法辛、mirtazapine、它们的药物活性的盐或其旋光异构体。
尼古丁受体激动剂和拮抗剂通过阻断受体减弱使用烟草所致的奖赏效果。
酒石酸Varenicline是另外一种选择性烟碱受体调节剂。酒石酸Varenicline(7,8,9,10-四氢-6,10-亚甲基-6H-吡嗪并[2,3-h][3]苯并氮杂(2R,3R)-2,3-二羟基丁二酮酸盐)降低了尼古丁戒断症状的严重程度。它的合成在WO 01/62736中有描述。本发明的一个优选实施方案涉及通过用尼古丁-VLP偶联物、优选地用尼古丁-Qβ偶联物接种,并且施用varenicline、优选地酒石酸varenicline,对患者进行联合治疗,以帮助戒烟或防止复吸。施用酒石酸varenicline的剂量为1mg,每天两次。
(5aS,8S,10aR)-5a,6,9,10-四氢-7H,11H-8,10a-亚甲基吡啶并[2′,3′:5,6]吡喃并-[2,3-d]氮杂(SSR591813)是可与α4β2烟碱乙酰胆碱受体(nAChR)亚型高亲和力结合的一种化合物。其衍生物的合成在US6538003中有描述。本发明的一个优选实施方案涉及通过用尼古丁-VLP偶联物、优选地用尼古丁-Qβ偶联物接种,并且施用SSR591813,对患者进行联合治疗,以帮助戒烟或防止复吸。SSR591813的剂量配制为每天1mg-500mg。
在本发明的一个优选实施方案中,对患者施用尼古丁受体拮抗剂盐酸美加明或其药学上可接受的盐,并联合使用尼古丁-VLP偶联物、优选地尼古丁-Qβ偶联物接种,以帮助戒烟或者防止复吸。盐酸美加明已经证明可阻断尼古丁的许多生理、行为和强化效应。盐酸美加明配制为每天约1mg-约25mg的剂量。
其它具体的尼古丁拮抗剂包括:金刚烷胺、潘必啶、二氢-β-刺桐定、六甲双铵、刺桐定碱、松达氯铵、樟磺咪芬、氯筒箭毒碱、d-筒箭毒碱、它们的药学上可接受的盐或者它们的旋光异构体。
中枢大麻素受体拮抗剂也被用来帮助戒烟。这种大麻素拮抗剂是N-哌啶子基-5-(4-氯-苯基)-1-(2,4-二氯苯基)-4-甲基吡唑-3-甲酰胺,在下文中被称为利莫那班。它的合成和含有它的药物组合物在专利申请EP-576′357、EP-656′354、WO 96/02248和WO 03/040105中公开。Cohen等人(Behav Pharmacol.2002,13,451-63)已经描述了利莫那班的效能。
本发明的一个优选实施方案涉及通过用尼古丁-VLP偶联物、优选地用尼古丁-Qβ偶联物接种,并且施用利莫那班,对患者进行联合治疗,以帮助戒烟或防止复吸。施用的利莫那班的剂量配制为5-40mg/天,优选地20mg/天的剂量。
在另外一个实施方案中,阿片拮抗剂如纳曲酮可以与针对尼古丁的接种联合使用。美国专利申请6′004′970描述了纳曲酮和有关化合物在戒烟中的用途。剂量一般为12.5mg-150mg。
抗焦虑剂也被用来治疗尼古丁脱瘾。抗焦虑剂对抗在戒烟治疗或者酒精中毒和其它滥用物质治疗过程中出现的轻度焦虑症状。抗焦虑剂异戊酰胺已经被推荐用于戒烟(Baladrin等人,WO94/28888)。其它抗焦虑剂包括丁螺环酮、羟嗪和甲丙氨酯。丁螺环酮以每天约5mg-60mg的剂量施用。
已经描述了单胺氧化酶抑制剂用于治疗药物戒断症状(WO92/21333和WO01/12176)。单胺氧化酶A的可逆选择性抑制剂、单胺氧化酶B的可逆选择性抑制剂或单胺氧化酶A和B的可逆混合抑制剂可能具有减少戒断症状的活性。在可逆单胺氧化酶A抑制剂中,可以提到贝氟沙通、吗氯贝胺、溴法罗明、phenoxathine、乙磺普隆、befol、RS 8359(Sankyo)、T794(Tanabe)、KP 9(Krenitsky USA)、E 2011(Eisei)、托洛沙酮、吡吲哚、amiflavine、sercloremine和巴嗪普令。这些化合物是已知的,它们的制备在本领域中已有描述。在单胺氧化酶B的可逆选择性抑制剂中,可以提到拉扎贝胺、米拉醋胺、卡罗沙酮、IFO、司来吉兰(deprenyl)、AGN-1135、MDL72145和J-508。贝氟沙通或3-[4-(4,4,4-三氟-3R-羟基丁氧基)苯基]5(R)-甲氧基甲基-2-噁唑烷酮在治疗肥胖症中的用途在WO 01/12176中已经描述。司来吉兰(deprenyl)异构体司来吉兰(selegeline)的用途在WO92/21333中已有描述。
在戒烟中有用的另外一种化合物是可乐定(Gourlay等人,Cochrane Library 2003,2)。本发明的一个优选实施方案涉及通过用尼古丁-VLP偶联物、优选地用尼古丁-Qβ偶联物接种,并且施用可乐定、优选地盐酸可乐定,对患者进行联合治疗,以帮助戒烟或防止复吸。
在戒烟中有用的另外一种化合物是西布曲明。FDA已经批准西布曲明用于帮助人们减肥,它抑制5-羟色胺和去甲肾上腺素的再摄取。优选地,西布曲明以盐酸盐一水合物的形式施用。施用剂量配制为每天1-20mg,优选地每天10-15mg。本发明的一个优选实施方案涉及通过用尼古丁-VLP偶联物、优选地用尼古丁-Qβ偶联物接种,并且施用西布曲明、优选地盐酸西布曲明,对患者进行联合治疗,以帮助戒烟或防止复吸。
上述所有药物都可以作为片剂或者胶囊口服给药、或者作为透皮贴剂给药。片剂、胶囊和透皮贴剂制剂在本领域中有描述。
也已经用抗抑郁剂和抗焦虑剂的组合(Glazer,美国专利号4′788′189)或尼古丁受体拮抗剂与抗抑郁剂或抗焦虑药物的组合(Cary,WO99/17803)治疗戒烟。
本发明的另外一些实施方案包括用本发明的组合物免疫产生的免疫分子。免疫分子包括抗体和T细胞受体。这些免疫分子可以在接种的个体中用于结合靶半抗原。当向未用本发明的组合物免疫的另外一个个体转移时,免疫分子也可能是有用的,从而“被动”转移免疫力。在一个实施方案中,免疫分子是一种抗体。可以向个体中转移适合与毒素、激素或药物结合的单克隆抗体,以实现治疗或预防。抗尼古丁和其它成瘾性药物的抗体可以临时减轻成瘾行为。在其它一些实施方案中,可以对处于中毒危险的个体或者已经严重暴露于毒剂的个体施用抗体。
在另外一个实施方案中,将抗体转移给免疫缺陷个体,如使用环孢菌素或其它免疫抑制药物的情况,或免疫缺陷疾病患者,例如HIV感染患者。HIV感染通常与滥用药物特别是注射用药物的成瘾同时发生,成瘾可能是产生增加个体感染HIV危险的行为的原因(例如共用针头、卖淫)。因此,治疗成瘾行为有助于防止HIV向人群中未感染个体的传播。
在采用被动免疫的实施方案中,根据经验确定,利用最佳免疫方案、用本发明的偶联物免疫一组人类供者。在不同时间通过穿刺从供者采血,通过ELISA测定抗可卡因抗体的滴度。收集来自多名供者的超免疫血浆,通过冷乙醇分级分离IgG级分。根据人用超免疫抗体制剂的需要,将抗体制剂缓冲、稳定、防腐并标准化。通过ELISA或其它基于抗体的测定试验将抗半抗原抗体的水平标准化。
对患者肌肉内、皮下或静脉内施用适当剂量的纯化抗体。在一个实施方案中,为了引发主动免疫,将抗体与偶联物疫苗一起在不同解剖部位施用。通过在注射超免疫抗体制剂后24小时或其它适当时间点,利用ELISA或其它基于抗体的测定法测定受试患者群体中受体的血清水平,和/或测定不同的剂量抑制半抗原效果的有效性,确定适当的剂量。
被动转移的免疫球蛋白在患者中抑制激素、毒素或药物作用。使用人供者、多克隆抗体和供者库中的大量供者等因素限制了患者对转移的抗体产生免疫应答的机会。
本发明的其它实施方案包括生产本发明的组合物的方法和使用该组合物进行医学治疗的方法。治疗成瘾的各同方法适合作为防止复发(复吸)的共同治疗,包括精神、社会和法律校正。在成瘾的共同治疗中有用的药物包括地昔帕明、丁丙诺啡、纳洛酮、氟哌啶醇、氯丙嗪、溴隐亭、伊波加因、氯苯咪吲哚、抗抑郁药和本领域技术人员将会认识到的其它药物。
试剂盒
本发明还包括用试剂盒中本发明组合物免疫产生的抗体在通过免疫测定法(例如ELISA)检测半抗原的用途。在一个有关实施方案中,重复、有序的半抗原阵列可以用来通过结合测定法检测抗半抗原的抗体。
在一些具体实施方案中,可以将本发明的组合物组装为试剂盒,用于检测试验或工业场合、诊断或检测疾病、病症或紊乱。这些本发明的试剂盒可以含有至少一个容器,其中含有一种或多种上述偶联物或组合物,包括半抗原-核心颗粒偶联物和针对这些偶联物的免疫分子。本发明的另一种试剂盒可以含有一种或多种本发明的抗体,这些抗体是通过本发明的方法或者通过本领域技术人员熟知的免疫方法利用本发明的偶联物和组合物产生的。本发明的试剂盒任选地还可以含有至少另外一个容器,其中可以含有例如一种或多种抗原、一种或多种半抗原、一种或多种核心颗粒、一种或多种本发明的偶联物/组合物、一种或多种药学上可接受的载体或赋形剂、一种或多种缓冲液、一种或多种蛋白质、一种或多种核酸分子等。
本发明提供能够在上述方法中使用的试剂盒。在一个实施方案中,试剂盒在一个或多个容器中含有通过本发明的方法产生的抗体,优选地一种纯化的抗体。在一个具体实施方案中,本发明的试剂盒含有一种基本分离的半抗原,它对于试剂盒中所含的抗体具有特异免疫反应性。优选地,本发明的试剂盒还含有一种不与目的半抗原反应的对照抗体。在另外一个具体实施方案中,本发明的试剂盒含有检测抗体与目的半抗原结合的工具(例如,抗体可以与下列成分偶联:一种可检测物质如荧光化合物、酶底物、放射性化合物或发光化合物,或者可以识别第一抗体的第二抗体可以与一种可检测物质偶联)。
在本发明的另一个具体实施方案中,试剂盒是一种诊断试剂盒,用于筛选含有抗尼古丁特异性抗体的血清。这种试剂盒含有抗尼古丁的IgA、IgE、IgG和IgG亚类抗体,这些抗体是通过用本发明的尼古丁-QβVLP偶联物免疫人体获得的。这种试剂盒包含一种不与尼古丁反应的对照抗体,和基本分离的尼古丁、可替宁和降烟碱半抗原,和不含半抗原的纯化的核心颗粒。此外,这种试剂盒还含有检测该抗体与尼古丁半抗原结合的工具(例如,抗体可以与下列成分偶联:一种荧光化合物如能够通过流式细胞术检测的荧光素或罗丹明,或用于ELISA的HRP)。在一个具体实施方案中,该试剂盒可含有与固体支持体连接的尼古丁。本发明包括这种试剂盒的用途,其中通过ELISA测定不同免疫球蛋白类别和亚类的滴度。该试剂盒提供的抗尼古丁IgA、IgE和IgG抗体用作测定患者血清中抗体相对滴度的对照。在血清和试剂盒中的抗体与尼古丁半抗原结合,并且通过洗涤除去未结合的血清成分后,抗体与免疫球蛋白亚型特异的抗体反应,后者与报道分子偶联。在另外一个洗涤步骤除去未结合的标记抗体后,在适当荧光、发光或比色底物(Sigma,St.Louis,MO)的存在下,测定与固相结合的报道分子的量。
因此,利用上述试剂盒,本发明提供了一种监测尼古丁免疫进展的方法。在免疫过程中监测被免疫者的抗尼古丁IgG和IgA抗体,以及缺乏标志变态反应发生的抗尼古丁IgE抗体。如果免疫应答主要针对核心颗粒而不是半抗原,则使用另一种尼古丁偶联物,其含有一种不同的核心颗粒,在一个实施方案中,含有一种不同的半抗原。
在一个实施方案中,试剂盒含有一种固体支持物,尼古丁-核心颗粒偶联物与之连接。在该实施方案中,通过报道分子-标记抗体的结合能够检测到个体血清中的抗体与呈递在核心颗粒上的抗原的结合。
上述测定试验中的固体表面试剂用公知的连接蛋白质材料与固体支持材料(如聚合物珠、测量尺、96孔板或过滤材料)的技术制备。这些连接方法通常包括支持体非特异性吸附蛋白质,或者蛋白质与固体支持体上的化学反应性基团(如活化的羧基、羟基或醛基)的共价连接,这一般是通过游离胺基连接。此外,链霉抗生物素蛋白包被的平板也可以与生物素化的抗原联合使用。
因此,本发明提供了用于实施诊断方法的一种测定系统或试剂盒。该试剂盒通常含有结合的重组抗原和一种报道分子标记的抗体,用于检测结合的抗-抗原抗体。本领域技术人员理解本发明的其它合适的试剂盒。
本领域技术人员可以理解,对此处所述的方法和应用的其它适当修改是明显的,可以在不背离本发明的范围或其任何实施方案的情况下进行这种改变。现在已经详细描述了本发明,通过下列实施例将能更清楚地理解,这些实施例只是用于说明并非意在限制本发明。
实施例
实施例1
尼古丁-Qβ偶联物的偶联方法
根据Langone等人(1982,同上)所述合成一种适合与VLP偶联的尼古丁衍生物。反式-4′-羧基可替宁可从商业途径获得。反式-4′-羧基可替宁的甲酯通过反式-4′-羧基可替宁与甲醇硫酸反应产生。该溶液用碳酸氢钠中和,用氯仿萃取,在旋转蒸发器上浓缩,从乙醚-丙酮中重结晶。用氢化铝锂在乙醚中还原甲酯产生反式-3′-羟甲基尼古丁。然后通过在苯中加入琥珀酸酐产生O′-琥珀酰-羟甲基尼古丁。将该溶液在旋转蒸发器上浓缩。随后通过加入EDC(1-乙基-3-(3-二甲氨基丙基)-碳二亚胺)和N-羟基琥珀酰亚胺(NHS),产生O′-琥珀酰-羟甲基尼古丁的N-羟基琥珀酰亚胺酯(在下文中缩写为“Suc-Nic”),实现羧基的活化。
将QβCP VLP(SEQ ID NO:3)对Hepes-缓冲盐溶液HBS(50mMHepes,150mM NaCl,pH 8.0)透析。尼古丁衍生物Suc-Nic以121mM的浓度溶解于HBS中。将其以1x、5x、50x、100x和500x摩尔过量加入QβCP VLP溶液(0.14mM)中,在室温下在摇床上孵育2小时。反应溶液然后对HBS,pH 8.0透析(截止值10000Da),在液氮中骤冻,贮存于-80℃下。在酰胺键形成条件下,将尼古丁衍生物suc-nic与Qβ表面的赖氨酸反应。产生的共价偶联物在此被命名为“Nic-Qβ”。
SDS-PAGE分析显示,随着Suc-Nic摩尔过量的增加,Qβ单体带向较高分子量转移(图1A)。使用一种抗尼古丁抗血清,通过westernblot证实偶联产物中尼古丁的存在。未偶联的Qβ对照和以1x和5x过量与尼古丁偶联的Qβ不显示抗尼古丁反应带,而以50x、100x和500x偶联的带清楚地证实尼古丁与Qβ共价偶联(图1B)。这一点通过ELISA证实,使用包被在孔上的尼古丁-BSA,并用一种抗尼古丁抗血清检测。当使用与500倍过量的尼古丁偶联的Qβ时,与50倍过量产生的疫苗相比,获得了更高的吸光度。
实施例2
用Nic-Qβ对小鼠的免疫,以及抗尼古丁抗体滴度的测定
A.小鼠的免疫
对10周龄雌性Balb/c小鼠用由500倍过量的Suc-Nic偶联产生的30μg尼古丁-Qβ(Nic-Qβ)接种两次。疫苗在无菌PBS中稀释,在添加或不添加明矾(Imject,Pierce)的情况下,鼻内施用或者皮下注射。在第一次免疫14天后,对小鼠进行加强接种(表1)。在第29天,通过ELISA检测血清中尼古丁特异的抗体滴度。
表I:小鼠的免疫方案:
| 第0天 | 第14天 | 第29天 | ||
| 动物数 | 疫苗 | 含量(μg) | 含量(μg) | 采血 |
| 3 | Nic-Qβ皮下 | 30 | 30 | 采血 |
| 3 | Nic-Qβ皮下+明矾 | 30 | 30 | 采血 |
| 3 | Nic-Qβ鼻内 | 30 | 30 | 采血 |
B.ELISA
血清用尼古丁特异的ELISA分析:微量滴定板(Maxisorp,Nunc)用包被缓冲液(pH 9.6)中的5μg/ml与BSA(NAB03)偶联的尼古丁包被过夜。在用溶于PBS的2%BSA洗涤并封闭后,加入用2%BSA/1%FCS/PBS以不同稀释度稀释的血清。在室温下孵育2小时后,洗板(0.05%Tween 20/PBS),加入HRPO标记的小鼠抗体亚类特异的抗体。孵育1小时后,洗板,加入溶于柠檬酸缓冲液的显色底物OPD。5分钟后,用5%H2SO4终止显色反应。
用ELISA读板仪(Benchmark,Becton Dickinson)读取450nm处的光密度。为了检测IgE,在加到ELISA板上之前,血清在Eppendorf管中与蛋白G珠(Pierce)在摇床上预孵育30分钟。
Nic-Qβ疫苗诱导了尼古丁特异的IgG抗体(图3A)。对于总IgG反应计算ELISA滴度(图3B,表II)。ELISA滴度被定义为在ELISA中获得半数最大光密度信号(OD 50%)的血清稀释度。对于使用明矾的皮下途径,用Nic-Qβ获得的平均IgG滴度为13228。对于鼻内途径,尼古丁-Qβ滴度为38052。
也通过ELISA测定了IgG亚型和IgE,并测定滴度(图3,图4,表II)。在所有试验条件下,均未检测到明显高于背景(免疫前血清)的IgE反应。IgG2a与IgG1抗体滴度之比代表Th1介导的免疫应答。对于在不使用明矾的情况下用Nic-Qβ皮下免疫的小鼠,检测到2.1的比值,当鼻内施用时,甚至提高到2.6。正如所料,明矾使免疫应答趋于更多的Th2型应答,得到0.4的比值。值得注意的是,Nic-Qβ疫苗也诱导高IgG2b和IgG3滴度。在血清中能够发现大量的抗尼古丁IgA抗体(图5),提示粘膜表面存在IgA。
鼻内免疫后的高尼古丁滴度是特别值得注意的。
表II:接种的小鼠中尼古丁特异的抗体滴度
滴度计算为在ELISA中获得半数最大光密度的血清稀释度。显示每组3只小鼠的平均滴度。
| 疫苗 | IgG滴度 | IgG1滴度 | IgG2a滴度 | IgG2b滴度 | IgG3滴度 |
| Nic-Qβ,皮下 | 13228 | 672 | 1386 | 515 | 2030 |
| Nic-Qβ明矾,皮下 | 93762 | 9642 | 10016 | 14977 | 19701 |
| Nic-Qβ,鼻内 | 38052 | 2845 | 7493 | 3617 | 6107 |
实施例3
大鼠血浆和脑中尼古丁分布的评价
各大鼠组用尼古丁-VLP疫苗免疫,在第21天加强。一组在第35天接受第二次加强。最后一次加强7-10天后,麻醉大鼠,将导管置于股动脉和静脉中用于采样,另一条腿的颈静脉中的导管用于施用尼古丁。通过颈静脉在10秒内以1ml/kg 0.9%盐水输注含有3μCi3H-(-)-尼古丁的0.03mg/kg尼古丁。加入放射标记物,以便能够由极小体积的血液估计尼古丁浓度。这是可能的,因为在对大鼠施用尼古丁后前90秒钟内,尼古丁向可替宁的代谢可以忽略。每15秒至90秒从股动脉和静脉导管中采集血液(0.3ml),立即离心,分离血清进行测定。在3分钟时通过斩首杀死大鼠,迅速取出大脑,用水漂洗,贮存于-20℃下,直到测定。为了测定血清中的3H-尼古丁浓度,将100μl血清与液体闪烁液混合。脑标本用5倍体积的NaOH消化,之后提取,并在加入闪烁液后分析。
接种诱导的尼古丁特异性抗体能够结合血清中的3H-尼古丁,抑制或降低它向脑中的扩散。因此,测定到脑尼古丁浓度的降低和血浆尼古丁浓度的升高。
实施例4
尼古丁半抗原与HBcAg-Lys的化学偶联
如实施例1所述制备O-琥珀酰-羟甲基尼古丁,与EDC和NHS一起孵育,产生活化的N-羟基琥珀酰胺酯(Suc-Nic)。如共同未决的美国专利申请号10/050,902所述制备纯化的HbcAg-Lys VLP。向纯度为95%的HBcAg-Lys颗粒溶液(2mg/ml)中加入1x、5x、50x、100x和500x摩尔过量的Suc-Nic在HBS中的溶液,在室温下孵育2小时。反应完成后,将混合物对HBS,pH8.0透析过夜,在液氮中骤冻,贮存于-80℃下。通过SDS-PAGE分析和使用抗尼古丁抗血清的western blot分析来监测反应。向啮齿动物注射尼古丁装饰的颗粒,以诱导针对尼古丁的免疫应答。
实施例5
尼古丁半抗原与大肠杆菌1型菌毛的化学偶联
I型菌毛由载体pFIMAICDFGK转化的大肠杆菌W3110株制备,通过超速离心纯化,如2002年1月18日提交的同一申请人拥有的共同未决的美国专利申请号10/050,902所述,其公开内容在此全文引用作为参考。溶于HBS的活化的半抗原以1x、5x、50x、100x和500x摩尔过量加入纯度为95%的I型菌毛颗粒溶液(2mg/ml)中,在室温下孵育2小时。在反应完成后,将混合物对HBS,pH 8.0透析,在液氮中骤冻,贮存于-80℃下。通过SDS-PAGE分析和使用抗尼古丁抗血清的western blot分析来监测反应。向啮齿动物中注射尼古丁装饰的颗粒,以诱导针对尼古丁的免疫应答。
实施例6
适合治疗尼古丁成瘾的多半抗原疫苗的合成
制备一种针对尼古丁成瘾的疫苗,它用来针对尼古丁的多个表位以及药学活性的代谢物可替宁和降烟碱。制备6-(羧甲基脲基)-(±)-尼古丁(CMUNic)、反式-3′-氨甲基尼古丁琥珀酸盐、O-琥珀酰-3′-羟甲基-尼古丁、反式-4′-羧基可替宁、N-[1-氧代-6-[(25)-2-(3-吡啶基)-1-吡咯烷基]己基]-β-丙氨酸、4-氧代-4-[[6-[(5S)-2-氧代-5-(3-吡啶基)-1-吡咯烷基]]己基]氨基]-丁酸、(2S)-2-(3-吡啶基)-1-吡咯烷丁酸苯甲酯、(2R)-2-(3-吡啶基)-1-吡咯烷丁酸苯甲酯、可替宁4’-羧酸、N-琥珀酰-6-氨基-(.+-.)-尼古丁;6-(σ-氨基癸酰胺基)-(.+-.)-尼古丁-偶联物和6-(σ-氨基癸酰胺基)-(.+-.)-尼古丁-偶联物;琥珀酰化的3’、4’和5’氨甲基尼古丁,5和6氨基尼古丁和乙酰尼古丁的3’、4’、5’乙酰衍生物在HBS中的各120mM溶液。如其它部分所述,将这些溶液与EDC和NHS混合,形成活化的形式,它们在不同的反应中以10-100倍摩尔过量加入QβVLP中。
使用1-环己基-3-(2-吗啉代乙基)-碳二亚胺metho-对甲苯磺酸盐,使S-1-(b-氨乙基)氯化尼古丁鎓二盐酸盐和S-1-(b-氨乙基)氯化可替宁鎓盐酸盐的溶液与QβVLP偶联。
通过这种偶联物的选择,然后混合8种尼古丁半抗原QβVLP偶联物、一种可替宁QβVLP偶联物和一种降烟碱偶联物QβVLP,形成一种疫苗组合物,它用来接种个体。在2次给药后,用与HBc-LysVLP偶联物偶联的平行半抗原加强个体3次。
实施例7
可卡因VLP-半抗原偶联物的合成
如美国专利5,876,727所述,盐酸去甲可卡因(1g,3.07mmol)、三乙胺(0.86ml,6.14mmol)在二氯甲烷(20ml)中的溶液用琥珀酸酐(614mg,6.14mmol)处理,将混合物在45℃下加热过夜。减压除去溶剂,利用硅胶快速层析法纯化残余物(2∶1氯仿∶甲醇作为洗脱剂)。这产生琥珀酰化的去甲可卡因(1.0g,84%),是一种粘稠糖浆(3β-(苯甲酸基)-8-琥珀酰-8-氮杂二环[3.2.1]辛烷-2β-羧酸甲酯)。在0℃下,向该酸(14mg,0.036mmol)在蒸馏水(1ml)中的溶液中加入EDC(10.4mg,0.055mmol)。5分钟后,逐滴加入QβVLP在PBS(1ml)中的溶液,将混合物加温至室温过夜。该偶联物通过对PBS透析纯化,偶联度用质谱分析法分析。利用获得的偶联物免疫个体。
为了便于清楚地理解,在此已经通过举例说明和实施例全面详细地描述了本发明,本领域技术人员可以理解,在不影响本发明或其任何具体实施方案的范围的情况下,能够在条件、制剂和其它参数的大量等同物范围内修饰或改变本发明,这些修饰或改变包括于所附权利要求书的范围之内。
本说明书中提到的所有出版物、专利和专利申请都代表本发明所属领域中技术人员的水平,均在此引用作为参考,等同于每个出版物、专利或专利申请具体、单独地引用作为参考。
实施例8
小鼠血浆和脑中尼古丁分布的评价
各组4-5只小鼠用如实施例1所述制备的60μg尼古丁-VLP疫苗免疫,在第35天和第63天用等量疫苗加强。最后一次加强14天后,给小鼠尾根静脉内注射含有750ng(-)-酒石酸氢尼古丁和5μCi3H-(-)-尼古丁的溶液。尼古丁的量相当于0.03mg/kg,相当于吸烟者吸2支烟摄入的尼古丁量。加入放射标记物,以便能够由极小体积的血液估计尼古丁浓度。5分钟后用CO2杀死小鼠。穿刺心脏取血,制备血清。立即切下大脑,清除粘附的血液,称重。为了测定血清中的3H-尼古丁浓度,将50μl血清与液体闪烁液混合。将脑标本完全溶解于2ml组织溶解剂(Tissue Solubilizer,Serva)中,在加入闪烁液后分析。根据放射性计算血清和脑中的尼古丁浓度(图7)。
接种诱导的尼古丁特异性抗体能够结合血清中的3H-尼古丁,并且抑制或降低它向脑中的扩散。因此,测定到脑尼古丁浓度的降低和血浆尼古丁浓度的升高。在不含明矾的情况下,尼古丁-VLP疫苗56%抑制脑摄取尼古丁,在明矾存在下,68%抑制(图7)。
其它的免疫程序,如在第0天免疫、第14天加强,也产生能够显著减少脑摄取尼古丁的抗体水平。高抗尼古丁抗体滴度通常与较高的接种效率有关。
实施例9
AP205外壳蛋白基因的克隆
AP205外壳蛋白(CP)的cDNA(SEQ ID NO:90)由两个cDNA片段装配而成,这两个片段是利用反转录PCR技术由噬菌体AP205 RNA产生的,并且克隆到商品质粒pCR 4-TOPO内进行测序。反转录技术为相关领域技术人员所周知。质粒p205-246中所含的第一个片段含有位于CP序列上游的269个核苷酸和编码CP前24个N端氨基酸的74个核苷酸。质粒p205-262中所含的第二个片段含有编码CP的氨基酸12-131的364个核苷酸和位于CP序列下游的另外162个核苷酸。p205-246和p205-262均由J.Klovins惠赠。
质粒283.-58由两步PCR设计,是为了将来自质粒p205-246和p205-262的两个CP片段融合于一个全长CP序列内。
使用上游引物p1.44(为了向质粒pQb185内克隆其含有NcoI位点)或者p1.45(为了向质粒pQb10内克隆其含有XbaI位点)和含有HindIII限制位点的下游引物p1.46(限制性内切酶识别序列用下划线标出):
p1.44 5′-NN
CC ATG GCA AAT AAG CCA ATG CAA CCG-3′(SEQ ID NO:5)
p1.45 5′-NN
TCTAGAATTTTCTGCGCACCCATCCCGG-3′(SEQID NO:20)
p1.46 5′NN
AAGC TTA AGC AGT AGT ATC AGA CGA TACG-3′(SEQ ID NO:21)
另外两条引物,与p205-262所含片段的5′端退火的p1.47和与质粒p205-246所含片段的3′端退火的p1.48,用来在第一个PCR中扩增这些片段。引物p1.47和p1.48彼此互补。
p1.47:
5′-GAGTGATCCAACTCGTTTATCAACTACATTTTCAGCAAGTCTG-3′(SEQ ID NO:22)
p1.48:
5′-CAGACTTGCTGAAAATGTAGTTGATAAACGAGTTGGATCACTC-3′(SEQ ID NO:23)
前两个PCR反应产生了两个片段。第一个片段用引物p1.45和p1.48和模板p205-246产生。第二个片段用引物p1.47和p1.46和模板p205-262产生。这两个片段都作为模板用于第二个PCR反应,即一种剪接重叠延伸,其中使用引物组合p1.45和p1.46或p1.44和p1.46。这两个第二步PCR反应的产物分别用XbaI或NcoI和HindIII消化,利用相同的限制酶切位点将其分别克隆到pQb10或pQb185内,这是pGEM衍生的两种表达载体,处于大肠杆菌色氨酸操纵子启动子的控制之下。
获得两种质粒,pAP283-58(SEQ ID NO:15)和pAP281-32(SEQ IDNO:19),前者在pQb10中含有编码野生型AP205 CP的基因(SEQ IDNO:14),后者在pQb185中含有突变Pro5→Thr(SEQ ID NO:18)。外壳蛋白序列通过DNA测序证实。pAP283-58含有位于CP的ATG起始密码子上游和XbaI位点下游的49个核苷酸,并且含有推断的外壳蛋白mRNA的原始核糖体结合位点。
实施例10
重组AP205 VLP的表达与纯化
A.重组AP205 VLP的表达
大肠杆菌JM109用质粒pAP283-58转化。在5ml含有20μg/ml氨苄青霉素的LB液体培养基中接种单菌落,不加振摇在37℃下孵育16-24小时。
制备的接种物用100-300ml含有20μg/ml氨苄青霉素的LB培养基1∶100稀释,不加振摇在37℃下孵育过夜。获得的第二种接种物用含有0.2%葡萄糖和磷酸盐进行缓冲的2TY培养基1∶50稀释,并且在摇床上37℃孵育过夜。离心收集细胞,冻存于-80℃。
B.重组AP205 VLP的纯化
溶液与缓冲液:
1.裂解缓冲液
50mM Tris-HCl pH 8.0,含5mM EDTA,0.1%tritonX100和5微克/毫升PMSF。
2.S
AS
饱和硫酸铵水溶液。
3.缓冲液
NET
20mM Tris-HCl,pH 7.8,含5mM EDTA和150mM NaCl。
4.
PEG
40%(w/v)聚乙二醇6000,溶于NET
裂解:
将冷冻细胞以2ml/g细胞的浓度重悬浮于裂解缓冲液中。该混合物以22kH超声处理5次各15秒,间隔1分钟,在冰上冷却该溶液。然后用F34-6-38转子(Ependorf)以12000rpm离心裂解液20分钟。除非另外说明,以下所述的离心步骤全都使用相同的转子进行。将上清液贮存于4℃,而细胞碎片用裂解缓冲液洗涤2次。离心后合并裂解液上清液和洗涤级分。
可以进一步利用硫酸铵沉淀纯化AP205 VLP。第一步,选择AP205 VLP不会沉淀的硫酸铵浓度。弃去获得的沉淀。第二步,选择AP205 VLP定量沉淀的硫酸铵浓度,通过离心(14000rpm,20分钟)从该沉淀步骤的沉淀中分离AP205 VLP。将获得的沉淀溶解于NET缓冲液中。
层析:
将来自合并上清液的衣壳蛋白上样到Sepharose 4B柱(2.8×70cm)上,用NET缓冲液以4ml/小时/级分的速度洗脱。收集级分28-40,用60%饱和的硫酸铵沉淀。这些级分在沉淀之前通过SDS-PAGE和使用AP205特异抗血清的Western Blot分析。将离心分离的沉淀重新溶解于NET缓冲液中,上样到Sepharose 2B柱(2.3×65cm)上,以3ml/h/级分的流速洗脱。这些级分通过SDS-PAGE分析,收集级分44-50,合并,用60%饱和的硫酸铵沉淀。将离心分离的沉淀重新溶解于NET缓冲液中,用Sepharose 6B柱(2.5×47cm)纯化,以3ml/h/级分的流速洗脱。这些级分通过SDS-PAGE分析。收集级分23-27,将盐浓度调节为0.5M,用PEG 6000沉淀,加入40%贮存水溶液,至终浓度为13.3%。将离心分离的沉淀重新溶解于NET缓冲液中,上样到与以上相同的Sepharose 2B柱上,以相同的方式洗脱。收集级分43-53,用60%饱和的硫酸铵沉淀。将离心分离的沉淀重新溶解于水中,获得的蛋白质溶液对水充分透析。从每克细胞能够分离到约10mg纯化的蛋白质。用电子显微镜检查病毒样颗粒显示,它们与噬菌体颗粒相同。
序列表
<110>赛托斯生物技术公司
马丁·F·巴克曼
帕特里克·毛雷尔
<120>半抗原-载体偶联物及其用途
<130>PA031wo
<150>US 60/396,575
<151>2002-07-18
<160>33
<170>PatentIn version 3.2
<210>1
<211>185
<212>PRT
<213>乙型肝炎病毒
<400>1
Met Asp Ile Asp Pro Tyr Lys Glu Phe Gly Ala Thr Val Glu Leu Leu
1 5 10 15
Ser Phe Leu Pro Ser Asp Phe Phe Pro Ser Val Arg Asp Leu Leu Asp
20 25 30
Thr Ala Ser Ala Leu Tyr Arg Glu Ala Leu Glu Ser Pro Glu His Cys
35 40 45
Ser Pro His His Thr Ala Leu Arg Gln Ala Ile Leu Cys Trp Gly Glu
50 55 60
Leu Met Thr Leu Ala Thr Trp Val Gly Asn Asn Leu Glu Asp Pro Ala
65 70 75 80
Ser Arg Asp Leu Val Val Asn Tyr Val Asn Thr Asn Met Gly Leu Lys
85 90 95
Ile Arg Gln Leu Leu Trp Phe His Ile Ser Cys Leu Thr Phe Gly Arg
100 105 110
Glu Thr Val Leu Glu Tyr Leu Val Ser Phe Gly Val Trp Ile Arg Thr
115 120 125
Pro Pro Ala Tyr Arg Pro Pro Asn Ala Pro Ile Leu Ser Thr Leu Pro
130 135 140
Glu Thr Thr Val Val Arg Arg Arg Asp Arg Gly Arg Ser Pro Arg Arg
145 150 155 160
Arg Thr Pro Ser Pro Arg Arg Arg Arg Ser Gln Ser Pro Arg Arg Arg
165 170 175
Arg Ser Gln Ser Arg Glu Ser Gln Cys
<210>2
<211>182
<212>PRT
<213>大肠杆菌
<400>2
Met Lys Ile Lys Thr Leu Ala Ile Val Val Leu Ser Ala Leu Ser Leu
1 5 10 15
Ser Ser Thr Thr Ala Leu Ala Ala Ala Thr Thr Val Asn Gly Gly Thr
20 25 30
Val His Phe Lys Gly Glu Val Val Asn Ala Ala Cys Ala Val Asp Ala
35 40 45
Gly Ser Val Asp Gln Thr Val Gln Leu Gly Gln Val Arg Thr Ala Ser
50 55 60
Leu Ala Gln Glu Gly Ala Thr Ser Ser Ala Val Gly Phe Asn Ile Gln
65 70 75 80
Leu Asn Asp Cys Asp Thr Asn Val Ala Ser Lys Ala Ala Val Ala Phe
85 90 95
Leu Gly Thr Ala Ile Asp Ala Gly His Thr Asn Val Leu Ala Leu Gln
100 105 110
Ser Ser Ala Ala Gly Ser Ala Thr Asn Val Gly Val Gln Ile Leu Asp
115 120 125
Arg Thr Gly Ala Ala Leu Thr Leu Asp Gly Ala Thr Phe Ser Ser Glu
130 135 140
Thr Thr Leu Asn Asn Gly Thr Asn Thr Ile Pro Phe Gln Ala Arg Tyr
145 150 155 160
Phe Ala Thr Gly Ala Ala Thr Pro Gly Ala Ala Asn Ala Asp Ala Thr
165 170 175
Phe Lys Val Gln Tyr Gln
180
<210>3
<211>132
<212>PRT
<213>噬菌体Qβ
<400>3
Ala Lys Leu Glu Thr Val Thr Leu Gly Asn Ile Gly Lys Asp Gly Lys
1 5 10 15
Gln Thr Leu Val Leu Asn Pro Arg Gly Val Asn Pro Thr Asn Gly Val
20 25 30
Ala Ser Leu Ser Gln Ala Gly Ala Val Pro Ala Leu Glu Lys Arg Val
35 40 45
Thr Val Ser Val Ser Gln Pro Ser Arg Asn Arg Lys Asn Tyr Lys Val
50 55 60
Gln Val Lys Ile Gln Asn Pro Thr Ala Cys Thr Ala Asn Gly Ser Cys
65 70 75 80
Asp Pro Ser Val Thr Arg Gln Ala Tyr Ala Asp Val Thr Phe Ser Phe
85 90 95
Thr Gln Tyr Ser Thr Asp Glu Glu Arg Ala Phe Val Arg Thr Glu Leu
100 105 110
Ala Ala Leu Leu Ala Ser Pro Leu Leu Ile Asp Ala Ile Asp Gln Leu
115 120 125
Asn Pro Ala Tyr
130
<210>4
<211>329
<212>PRT
<213>噬菌体Qβ
<400>4
Met Ala Lys Leu Glu Thr Val Thr Leu Gly Asn Ile Gly Lys Asp Gly
1 5 10 15
Lys Gln Thr Leu Val Leu Asn Pro Arg Gly Val Asn Pro Thr Asn Gly
20 25 30
Val Ala Ser Leu Ser Gln Ala Gly Ala Val Pro Ala Leu Glu Lys Arg
35 40 45
Val Thr Val Ser Val Ser Gln Pro Ser Arg Asn Arg Lys Asn Tyr Lys
50 55 60
Val Gln Val Lys Ile Gln Asn Pro Thr Ala Cys Thr Ala Asn Gly Ser
65 70 75 80
Cys Asp Pro Ser Val Thr Arg Gln Ala Tyr Ala Asp Val Thr Phe Ser
85 90 95
Phe Thr Gln Tyr Ser Thr Asp Glu Glu Arg Ala Phe Val Arg Thr Glu
100 105 110
Leu Ala Ala Leu Leu Ala Ser Pro Leu Leu Ile Asp Ala Ile Asp Gln
115 120 125
Leu Asn Pro Ala Tyr Trp Thr Leu Leu Ile Ala Gly Gly Gly Ser Gly
130 135 140
Ser Lys Pro Asp Pro Val Ile Pro Asp Pro Pro Ile Asp Pro Pro Pro
145 150 155 160
Gly Thr Gly Lys Tyr Thr Cys Pro Phe Ala Ile Trp Ser Leu Glu Glu
165 170 175
Val Tyr Glu Pro Pro Thr Lys Asn Arg Pro Trp Pro Ile Tyr Asn Ala
180 185 190
Val Glu Leu Gln Pro Arg Glu Phe Asp Val Ala Leu Lys Asp Leu Leu
195 200 205
Gly Asn Thr Lys Trp Arg Asp Trp Asp Ser Arg Leu Ser Tyr Thr Thr
210 215 220
Phe Arg Gly Cys Arg Gly Asn Gly Tyr Ile Asp Leu Asp Ala Thr Tyr
225 230 235 240
Leu Ala Thr Asp Gln Ala Met Arg Asp Gln Lys Tyr Asp Ile Arg Glu
245 250 255
Gly Lys Lys Pro Gly Ala Phe Gly Asn Ile Glu Arg Phe Ile Tyr Leu
260 265 270
Lys Ser Ile Asn Ala Tyr Cys Ser Leu Ser Asp Ile Ala Ala Tyr His
275 280 285
Ala Asp Gly Val Ile Val Gly Phe Trp Arg Asp Pro Ser Ser Gly Gly
290 295 300
Ala Ile Pro Phe Asp Phe Thr Lys Phe Asp Lys Thr Lys Cys Pro Ile
305 310 315 320
Gln Ala Val Ile Val Val Pro Arg Ala
325
<210>5
<211>28
<212>DNA
<213>人工序列
<220>
<223>p1.44引物
<220>
<221>misc_特征
<222>(1)..(2)
<223>n可以是任何核苷酸,优选a
<400>5
nnccatggca aataagccaa tgcaaccg
<210>6
<211>132
<212>PRT
<213>人工序列
<220>
<223>噬菌体Qβ240突变体
<400>6
Ala Lys Leu Glu Thr Val Thr Leu Gly Asn Ile Gly Arg Asp Gly Lys
1 5 10 15
Gln Thr Leu Val Leu Asn Pro Arg Gly Val Asn Pro Thr Asn Gly Val
20 25 30
Ala Ser Leu Ser Gln Ala Gly Ala Val Pro Ala Leu Glu Lys Arg Val
35 40 45
Thr Val Ser Val Ser Gln Pro Ser Arg Asn Arg Lys Asn Tyr Lys Val
50 55 60
Gln Val Lys Ile Gln Asn Pro Thr Ala Cys Thr Ala Asn Gly Ser Cys
65 70 75 80
Asp Pro Ser Val Thr Arg Gln Lys Tyr Ala Asp Val Thr Phe Ser Phe
85 90 95
Thr Gln Tyr Ser Thr Asp Glu Glu Arg Ala Phe Val Arg Thr Glu Leu
100 105 110
Ala Ala Leu Leu Ala Ser Pro Leu Leu Ile Asp Ala Ile Asp Gln Leu
115 120 125
Asn Pro Ala Tyr
130
<210>7
<211>132
<212>PRT
<213>人工序列
<220>
<223>噬菌体Qβ243突变体
<400>7
Ala Lys Leu Glu Thr Val Thr Leu Gly Lys Ile Gly Lys Asp Gly Lys
1 5 10 15
Gln Thr Leu Val Leu Asn Pro Arg Gly Val Asn Pro Thr Asn Gly Val
20 25 30
Ala Ser Leu Ser Gln Ala Gly Ala Val Pro Ala Leu Glu Lys Arg Val
35 40 45
Thr Val Ser Val Ser Gln Pro Ser Arg Asn Arg Lys Asn Tyr Lys Val
50 55 60
Gln Val Lys Ile Gln Asn Pro Thr Ala Cys Thr Ala Asn Gly Ser Cys
65 70 75 80
Asp Pro Ser Val Thr Arg Gln Lys Tyr Ala Asp Val Thr Phe Ser Phe
85 90 95
Thr Gln TVr Ser Thr Asp Glu Glu Arg Ala Phe Val Arg Thr Glu Leu
100 105 110
Ala Ala Leu Leu Ala Ser Pro Leu Leu Ile Asp Ala Ile Asp Gln Leu
115 120 125
Asn Pro Ala Tyr
130
<210>8
<211>132
<212>PRT
<213>人工序列
<220>
<223>噬菌体Qβ250突变体
<400>8
Ala Arg Leu Glu Thr Val Thr Leu Gly Asn Ile Gly Arg Asp Gly Lys
1 5 10 15
Gln Thr Leu Val Leu Asn Pro Arg Gly Val Asn Pro Thr Asn Gly Val
20 25 30
Ala Ser Leu Ser Gln Ala Gly Ala Val Pro Ala Leu Glu Lys Arg Val
35 40 45
Thr Val Ser Val Ser Gln Pro Ser Arg Asn Arg Lys Asn Tyr Lys Val
50 55 60
Gln Val Lys Ile Gln Asn Pro Thr Ala Cys Thr Ala Asn Gly Ser Cys
65 70 75 80
Asp Pro Ser Val Thr Arg Gln Lys Tyr Ala Asp Val Thr Phe Ser Phe
85 90 95
Thr Gln Tyr Ser Thr Asp Glu Glu Arg Ala Phe Val Arg Thr Glu Leu
100 105 110
Ala Ala Leu Leu Ala Ser Pro Leu Leu Ile Asp Ala Ile Asp Gln Leu
115 120 125
Asn Pro Ala Tyr
130
<210>9
<211>132
<212>PRT
<213>人工序列
<220>
<223>噬菌体Qβ251突变体
<400>9
Ala Lys Leu Glu Thr Val Thr Leu Gly Asn Ile Gly Lys Asp Gly Arg
1 5 10 15
Gln Thr Leu Val Leu Asn Pro Arg Gly Val Asn Pro Thr Asn Gly Val
20 25 30
Ala Ser Leu Ser Gln Ala Gly Ala Val Pro Ala Leu Glu Lys Arg Val
35 40 45
Thr Val Ser Val Ser Gln Pro Ser Arg Asn Arg Lys Asn Tyr Lys Val
50 55 60
Gln Val Lys Ile Gln Asn Pro Thr Ala Cys Thr Ala Asn Gly Ser Cys
65 70 75 80
Asp Pro Ser Val Thr Arg Gln Lys Tyr Ala Asp Val Thr Phe Ser Phe
85 90 95
Thr Gln Tyr Ser Thr Asp Glu Glu Arg Ala Phe Val Arg Thr Glu Leu
100 105 110
Ala Ala Leu Leu Ala Ser Pro Leu Leu Ile Asp Ala Ile Asp Gln Leu
115 120 125
Asn Pro Ala Tyr
130
<210>10
<211>132
<212>PRT
<213>人工序列
<220>
<223>噬菌体Qβ259突变体
<400>10
Ala Arg Leu Glu Thr Val Thr Leu Gly Asn Ile Gly Lys Asp Gly Arg
1 5 10 15
Gln Thr Leu Val Leu Asn Pro Arg Gly Val Asn Pro Thr Asn Gly Val
20 25 30
Ala Ser Leu Ser Gln Ala Gly Ala Val Pro Ala Leu Glu Lys Arg Val
35 40 45
Thr Val Ser Val Ser Gln Pro Ser Arg Asn Arg Lys Asn Tyr Lys Val
50 55 60
Gln Val Lys Ile Gln Asn Pro Thr Ala Cys Thr Ala Asn Gly Ser Cys
65 70 75 80
Asp Pro Ser Val Thr Arg Gln Lys Tyr Ala Asp Val Thr Phe Ser Phe
85 90 95
Thr Gln Tyr Ser Thr Asp Glu Glu Arg Ala Phe Val Arg Thr Glu Leu
100 105 110
Ala Ala Leu Leu Ala Ser Pro Leu Leu Ile Asp Ala Ile Asp Gln Leu
115 120 125
Asn Pro Ala Tyr
130
<210>11
<211>5
<212>PRT
<213>人工序列
<220>
<223>接头
<400>11
Gly Gly Lys Gly Gly
1 5
<210>12
<211>49
<212>PRT
<213>人工序列
<220>
<223>GCN4
<400>12
Pro Ala Ala Leu Lys Arg Ala Arg Asn Glu Ala Ala Arg Arg Ser Arg
1 5 10 15
Ala Arg Lys Leu Gln Arg Met Lys Gln Leu Glu Asp Lys Val Glu Glu
20 25 30
Leu Leu Ser Lys Asn Tyr His Leu Glu Asn Glu Val Ala Arg Leu Lys
35 40 45
Lys
<210>13
<211>128
<212>PRT
<213>噬菌体PP7
<400>13
Met Ser Lys Thr Ile Val Leu Ser Val Gly Glu Ala Thr Arg Thr Leu
1 5 10 15
Thr Glu Ile Gln Ser Thr Ala Asp Arg Gln Ile Phe Glu Glu Lys Val
20 25 30
Gly Pro Leu Val Gly Arg Leu Arg Leu Thr Ala Ser Leu Arg Gln Asn
35 40 45
Gly Ala Lys Thr Ala Tyr Arg Val Asn Leu Lys Leu Asp Gln Ala Asp
50 55 60
Val Val Asp Cys Ser Thr Ser Val Cys Gly Glu Leu Pro Lys Val Arg
65 70 75 80
Tyr Thr Gln Val Trp Ser His Asp Val Thr Ile Val Ala Asn Ser Thr
85 90 95
Glu Ala Ser Arg Lys Ser Leu Tyr Asp Leu Thr Lys Ser Leu Val Ala
100 105 110
Thr Ser Gln Val Glu Asp Leu Val Val Asn Leu Val Pro Leu Gly Arg
115 120 125
<210>14
<211>131
<212>PRT
<213>噬菌体AP205
<400>14
Met Ala Asn Lys Pro Met Gln Pro Ile Thr Ser Thr Ala Asn Lys Ile
1 5 10 15
Val Trp Ser Asp Pro Thr Arg Leu Ser Thr Thr Phe Ser Ala Ser Leu
20 25 30
Leu Arg Gln Arg Val Lys Val Gly Ile Ala Glu Leu Asn Asn Val Ser
35 40 45
Gly Gln Tyr Val Ser Val Tyr Lys Arg Pro Ala Pro Lys Pro Glu Gly
50 55 60
Cys Ala Asp Ala Cys Val Ile Met Pro Asn Glu Asn Gln Ser Ile Arg
65 70 75 80
Thr Val Ile Ser Gly Ser Ala Glu Asn Leu Ala Thr Leu Lys Ala Glu
85 90 95
Trp Glu Thr His Lys Arg Asn Val Asp Thr Leu Phe Ala Ser Gly Asn
100 105 110
Ala Gly Leu Gly Phe Leu Asp Pro Thr Ala Ala Ile Val Ser Ser Asp
115 120 125
Thr Thr Ala
130
<210>15
<211>3635
<212>DNA
<213>人工序列
<220>
<223>质粒pAP283-58,编码RNA噬菌体AP205外壳蛋白
<400>15
cgagctcgcc cctggcttat cgaaattaat acgactcact atagggagac cggaattcga 60
gctcgcccgg ggatcctcta gaattttctg cgcacccatc ccgggtggcg cccaaagtga 120
ggaaaatcac atggcaaata agccaatgca accgatcaca tctacagcaa ataaaattgt 180
gtggtcggat ccaactcgtt tatcaactac attttcagca agtctgttac gccaacgtgt 240
taaagttggt atagccgaac tgaataatgt ttcaggtcaa tatgtatctg tttataagcg 300
tcctgcacct aaaccggaag gttgtgcaga tgcctgtgtc attatgccga atgaaaacca 360
atccattcgc acagtgattt cagggtcagc cgaaaacttg gctaccttaa aagcagaatg 420
ggaaactcac aaacgtaacg ttgacacact cttcgcgagc ggcaacgccg gtttgggttt 480
ccttgaccct actgcggcta tcgtatcgtc tgatactact gcttaagctt gtattctata 540
gtgtcaccta aatcgtatgt gtatgataca taaggttatg tattaattgt agccgcgttc 600
taacgacaat atgtacaagc ctaattgtgt agcatctggc ttactgaagc agaccctatc 660
atctctctcg taaactgccg tcagagtcgg tttggttgga cgaaccttct gagtttctgg 720
taacgccgtt ccgcaccccg gaaatggtca ccgaaccaat cagcagggtc atcgctagcc 780
agatcctcta cgccggacgc atcgtggccg gcatcaccgg cgccacaggt gcggttgctg 840
gcgcctatat cgccgacatc accgatgggg aagatcgggc tcgccacttc gggctcatga 900
gcgcttgttt cggcgtgggt atggtggcag gccccgtggc cgggggactg ttgggcgcca 960
tctccttgca tgcaccattc cttgcggcgg cggtgctcaa cggcctcaac ctactactgg 1020
gctgcttcct aatgcaggag tcgcataagg gagagcgtcg atatggtgca ctctcagtac 1080
aatctgctct gatgccgcat agttaagcca actccgctat cgctacgtga ctgggtcatg 1140
gctgcgcccc gacacccgcc aacacccgct gacgcgccct gacgggcttg tctgctcccg 1200
gcatccgctt acagacaagc tgtgaccgtc tccgggagct gcatgtgtca gaggttttca 1260
ccgtcatcac cgaaacgcgc gaggcagctt gaagacgaaa gggcctcgtg atacgcctat 1320
ttttataggt taatgtcatg ataataatgg tttcttagac gtcaggtggc acttttcggg 1380
gaaatgtgcg cggaacccct atttgtttat ttttctaaat acattcaaat atgtatccgc 1440
tcatgagaca ataaccctga taaatgcttc aataatattg aaaaaggaag agtatgagta 1500
ttcaacattt ccgtgtcgcc cttattccct tttttgcggc attttgcctt cctgtttttg 1560
ctcacccaga aacgctggtg aaagtaaaag atgctgaaga tcagttgggt gcacgagtgg 1620
gttacatcga actggatctc aacagcggta agatccttga gagttttcgc cccgaagaac 1680
gttttccaat gatgagcact tttaaagttc tgctatgtgg cgcggtatta tcccgtattg 1740
acgccgggca agagcaactc ggtcgccgca tacactattc tcagaatgac ttggttgagt 1800
actcaccagt cacagaaaag catcttacgg atggcatgac agtaagagaa ttatgcagtg 1860
ctgccataac catgagtgat aacactgcgg ccaacttact tctgacaacg atcggaggac 1920
cgaaggagct aaccgctttt ttgcacaaca tgggggatca tgtaactcgc cttgatcgtt 1980
gggaaccgga gctgaatgaa gccataccaa acgacgagcg tgacaccacg atgcctgtag 2040
caatggcaac aacgttgcgc aaactattaa ctggcgaact acttactcta gcttcccggc 2100
aacaattaat agactggatg gaggcggata aagttgcagg accacttctg cgctcggccc 2160
ttccggctgg ctggtttatt gctgataaat ctggagccgg tgagcgtggg tctcgcggta 2220
tcattgcagc actggggcca gatggtaagc cctcccgtat cgtagttatc tacacgacgg 2280
ggagtcaggc aactatggat gaacgaaata gacagatcgc tgagataggt gcctcactga 2340
ttaagcattg gtaactgtca gaccaagttt actcatatat actttagatt gatttaaaac 2400
ttcattttta atttaaaagg atctaggtga agatcctttt tgataatctc atgaccaaaa 2460
tcccttaacg tgagttttcg ttccactgag cgtcagaccc cgtagaaaag atcaaaggat 2520
cttcttgaga tccttttttt ctgcgcgtaa tctgctgctt gcaaacaaaa aaaccaccgc 2580
taccagcggt ggtttgtttg ccggatcaag agctaccaac tctttttccg aaggtaactg 2640
gcttcagcag agcgcagata ccaaatactg tccttctagt gtagccgtag ttaggccacc 2700
acttcaagaa ctctgtagca ccgcctacat acctcgctct gctaatcctg ttaccagtgg 2760
ctgctgccag tggcgataag tcgtgtctta ccgggttgga ctcaagacga tagttaccgg 2820
ataaggcgca gcggtcgggc tgaacggggg gttcgtgcac acagcccagc ttggagcgaa 2880
cgacctacac cgaactgaga tacctacagc gcgagcattg agaaagcgcc acgcttcccg 2940
aagggagaaa ggcggacagg tatccggtaa gcggcagggt cggaacagga gagcgcacga 3000
gggagcttcc agggggaaac gcctggtatc tttatagtcc tgtcgggttt cgccacctct 3060
gacttgagcg tcgatttttg tgatgctcgt caggggggcg gagcctatgg aaaaacgcca 3120
gcaacgcggc ctttttacgg ttcctggcct tttgctggcc ttttgctcac atgttctttc 3180
ctgcgttatc ccctgattct gtggataacc gtattaccgc ctttgagtga gctgataccg 3240
ctcgccgcag ccgaacgacc gagcgcagcg agtcagtgag cgaggaagcg gaagagcgcc 3300
caatacgcaa accgcctctc cccgcgcgtt ggccgattca ttaatgcagc tgtggtgtca 3360
tggtcggtga tcgccagggt gccgacgcgc atctcgactg catggtgcac caatgcttct 3420
ggcgtcaggc agccatcgga agctgtggta tggccgtgca ggtcgtaaat cactgcataa 3480
ttcgtgtcgc tcaaggcgca ctcccgttct ggataatgtt ttttgcgccg acatcataac 3540
ggttctggca aatattctga aatgagctgt tgacaattaa tcatcgaact agttaactag 3600
tacgcaagtt cacgtaaaaa gggtatcgcg gaatt 3635
<210>16
<211>57
<212>DNA
<213>人工序列
<220>
<223>质粒pAP283-58的推定的AP205核糖体结合位点
<400>16
tctagaattt tctgcgcacc catcccgggt ggcgcccaaa gtgaggaaaa tcacatg 57
<210>17
<211>35
<212>DNA
<213>人工序列
<220>
<223>载体pQb185的SD序列
<400>17
tctagattaa cccaacgcgt aggagtcagg ccatg 35
<210>18
<211>131
<212>PRT
<213>人工序列
<220>
<223>噬菌体AP205突变体
<400>18
Met Ala Asn Lys Thr Met Gln Pro Ile Thr Ser Thr Ala Asn Lys Ile
1 5 10 15
Val Trp Ser Asp Pro Thr Arg Leu Ser Thr Thr Phe Ser Ala Ser Leu
20 25 30
Leu Arg Gln Arg Val Lys Val Gly Ile Ala Glu Leu Asn Asn Val Ser
35 40 45
Gly Gln Tyr Val Ser Val Tyr Lys Arg Pro Ala Pro Lys Pro Glu Gly
50 55 60
Cys Ala Asp Ala Cys Val Ile Met Pro Asn Glu Asn Gln Ser Ile Arg
65 70 75 80
Thr Val Ile Ser Gly Ser Ala Glu Asn Leu Ala Thr Leu Lys Ala Glu
85 90 95
Trp Glu Thr His Lys Arg Asn Val Asp Thr Leu Phe Ala Ser Gly Asn
100 105 110
Ala Gly Leu Gly Phe Leu Asp Pro Thr Ala Ala Ile Val Ser Ser Asp
115 120 125
Thr Thr Ala
130
<210>19
<211>3613
<212>DNA
<213>人工序列
<220>
<223>质粒pAP281-32,编码RNA噬菌体AP205外壳蛋白
<400>19
cgagctcgcc cctggcttat cgaaattaat acgactcact atagggagac cggaattcga 60
gctcgcccgg ggatcctcta gattaaccca acgcgtagga gtcaggccat ggcaaataag 120
acaatgcaac cgatcacatc tacagcaaat aaaattgtgt ggtcggatcc aactcgttta 180
tcaactacat tttcagcaag tctgttacgc caacgtgtta aagttggtat agccgaactg 240
aataatgttt caggtcaata tgtatctgtt tataagcgtc ctgcacctaa accggaaggt 300
tgtgcagatg cctgtgtcat tatgccgaat gaaaaccaat ccattcgcac agtgatttca 360
gggtcagccg aaaacttggc taccttaaaa gcagaatggg aaactcacaa acgtaacgtt 420
gacacactct tcgcgagcgg caacgccggt ttgggtttcc ttgaccctac tgcggctatc 480
gtatcgtctg atactactgc ttaagcttgt attctatagt gtcacctaaa tcgtatgtgt 540
atgatacata aggttatgta ttaattgtag ccgcgttcta acgacaatat gtacaagcct 600
aattgtgtag catctggctt actgaagcag accctatcat ctctctcgta aactgccgtc 660
agagtcggtt tggttggacg aaccttctga gtttctggta acgccgttcc gcaccccgga 720
aatggtcacc gaaccaatca gcagggtcat cgctagccag atcctctacg ccggacgcat 780
cgtggccggc atcaccggcg ccacaggtgc ggttgctggc gcctatatcg ccgacatcac 840
cgatggggaa gatcgggctc gccacttcgg gctcatgagc gcttgtttcg gcgtgggtat 900
ggtggcaggc cccgtggccg ggggactgtt gggcgccatc tccttgcatg caccattcct 960
tgcggcggcg gtgctcaacg gcctcaacct actactgggc tgcttcctaa tgcaggagtc 1020
gcataaggga gagcgtcgat atggtgcact ctcagtacaa tctgctctga tgccgcatag 1080
ttaagccaac tccgctatcg ctacgtgact gggtcatggc tgcgccccga cacccgccaa 1140
cacccgctga cgcgccctga cgggcttgtc tgctcccggc atccgcttac agacaagctg 1200
tgaccgtctc cgggagctgc atgtgtcaga ggttttcacc gtcatcaccg aaacgcgcga 1260
ggcagcttga agacgaaagg gcctcgtgat acgcctattt ttataggtta atgtcatgat 1320
aataatggtt tcttagacgt caggtggcac ttttcgggga aatgtgcgcg gaacccctat 1380
ttgtttattt ttctaaatac attcaaatat gtatccgctc atgagacaat aaccctgata 1440
aatgcttcaa taatattgaa aaaggaagag tatgagtatt caacatttcc gtgtcgccct 1500
tattcccttt tttgcggcat tttgccttcc tgtttttgct cacccagaaa cgctggtgaa 1560
agtaaaagat gctgaagatc agttgggtgc acgagtgggt tacatcgaac tggatctcaa 1620
cagcggtaag atccttgaga gttttcgccc cgaagaacgt tttccaatga tgagcacttt 1680
taaagttctg ctatgtggcg cggtattatc ccgtattgac gccgggcaag agcaactcgg 1740
tcgccgcata cactattctc agaatgactt ggttgagtac tcaccagtca cagaaaagca 1800
tcttacggat ggcatgacag taagagaatt atgcagtgct gccataacca tgagtgataa 1860
cactgcggcc aacttacttc tgacaacgat cggaggaccg aaggagctaa ccgctttttt 1920
gcacaacatg ggggatcatg taactcgcct tgatcgttgg gaaccggagc tgaatgaagc 1980
cataccaaac gacgagcgtg acaccacgat gcctgtagca atggcaacaa cgttgcgcaa 2040
actattaact ggcgaactac ttactctagc ttcccggcaa caattaatag actggatgga 2100
ggcggataaa gttgcaggac cacttctgcg ctcggccctt ccggctggct ggtttattgc 2160
tgataaatct ggagccggtg agcgtgggtc tcgcggtatc attgcagcac tggggccaga 2220
tggtaagccc tcccgtatcg tagttatcta cacgacgggg agtcaggcaa ctatggatga 2280
acgaaataga cagatcgctg agataggtgc ctcactgatt aagcattggt aactgtcaga 2340
ccaagtttac tcatatatac tttagattga tttaaaactt catttttaat ttaaaaggat 2400
ctaggtgaag atcctttttg ataatctcat gaccaaaatc ccttaacgtg agttttcgtt 2460
ccactgagcg tcagaccccg tagaaaagat caaaggatct tcttgagatc ctttttttct 2520
gcgcgtaatc tgctgcttgc aaacaaaaaa accaccgcta ccagcggtgg tttgtttgcc 2580
ggatcaagag ctaccaactc tttttccgaa ggtaactggc ttcagcagag cgcagatacc 2640
aaatactgtc cttctagtgt agccgtagtt aggccaccac ttcaagaact ctgtagcacc 2700
gcctacatac ctcgctctgc taatcctgtt accagtggct gctgccagtg gcgataagtc 2760
gtgtcttacc gggttggact caagacgata gttaccggat aaggcgcagc ggtcgggctg 2820
aacggggggt tcgtgcacac agcccagctt ggagcgaacg acctacaccg aactgagata 2880
cctacagcgc gagcattgag aaagcgccac gcttcccgaa gggagaaagg cggacaggta 2940
tccggtaagc ggcagggtcg gaacaggaga gcgcacgagg gagcttccag ggggaaacgc 3000
ctggtatctt tatagtcctg tcgggtttcg ccacctctga cttgagcgtc gatttttgtg 3060
atgctcgtca ggggggcgga gcctatggaa aaacgccagc aacgcggcct ttttacggtt 3120
cctggccttt tgctggcctt ttgctcacat gttctttcct gcgttatccc ctgattctgt 3180
ggataaccgt attaccgcct ttgagtgagc tgataccgct cgccgcagcc gaacgaccga 3240
gcgcagcgag tcagtgagcg aggaagcgga agagcgccca atacgcaaac cgcctctccc 3300
cgcgcgttgg ccgattcatt aatgcagctg tggtgtcatg gtcggtgatc gccagggtgc 3360
cgacgcgcat ctcgactgca tggtgcacca atgcttctgg cgtcaggcag ccatcggaag 3420
ctgtggtatg gccgtgcagg tcgtaaatca ctgcataatt cgtgtcgctc aaggcgcact 3480
cccgttctgg ataatgtttt ttgcgccgac atcataacgg ttctggcaaa tattctgaaa 3540
tgagctgttg acaattaatc atcgaactag ttaactagta cgcaagttca cgtaaaaagg 3600
gtatcgcgga att 3613
<210>20
<211>30
<212>DNA
<213>人工序列
<220>
<223>p1.45引物
<220>
<221>misc_特征
<222>(1)..(2)
<223>n可以是任何核苷酸,优选a
<400>20
nntctagaat tttctgcgca cccatcccgg 30
<210>21
<211>31
<212>DNA
<213>人工序列
<220>
<223>p1.46引物
<220>
<221>misc_特征
<222>(1)..(2)
<223>n可以是任何核苷酸,优选a
<400>21
nnaagcttaa gcagtagtat cagacgatac g 31
<210>22
<211>43
<212>DNA
<213>人工序列
<220>
<223>p1.47引物
<400>22
gagtgatcca actcgtttat caactacatt ttcagcaagt ctg 43
<210>23
<211>43
<212>DNA
<213>人工序列
<220>
<223>p1.48引物
<400>23
cagacttgct gaaaatgtag ttgataaacg agttggatca ctc 43
<210>24
<211>129
<212>PRT
<213>噬菌体R17
<400>24
Ala Ser Asn Phe Thr Gln Phe Val Leu Val Asn Asp Gly Gly Thr Gly
1 5 10 15
Asn Val Thr Val Ala Pro Ser Asn Phe Ala Asn Gly Val Ala Glu Trp
20 25 30
Ile Ser Ser Asn Ser Arg Ser Gln Ala Tyr Lys Val Thr Cys Ser Val
35 40 45
Arg Gln Ser Ser Ala Gln Asn Arg Lys Tyr Thr Ile Lys Val Glu Val
50 55 60
Pro Lys Val Ala Thr Gln Thr Val Gly Gly Val Glu Leu Pro Val Ala
65 70 75 80
Ala Trp Arg Ser Tyr Leu Asn Met Glu Leu Thr Ile Pro Ile Phe Ala
85 90 95
Thr Asn Ser Asp Cys Glu Leu Ile Val Lys Ala Met Gln Gly Leu Leu
100 105 110
Lys Asp Gly Asn Pro Ile Pro Ser Ala Ile Ala Ala Asn Ser Gly Ile
115 120 125
Tyr
<210>25
<211>130
<212>PRT
<213>噬菌体fr
<400>25
Met Ala Ser Asn Phe Glu Glu Phe Val Leu Val Asp Asn Gly Gly Thr
1 5 10 15
Gly Asp Val Lys Val Ala Pro Ser Asn Phe Ala Asn Gly Val Ala Glu
20 25 30
Trp Ile Ser Ser Asn Ser Arg Ser Gln Ala Tyr Lys Val Thr Cys Ser
35 40 45
Val Arg Gln Ser Ser Ala Asn Asn Arg Lys Tyr Thr Val Lys Val Glu
50 55 60
Val Pro Lys Val Ala Thr Gln Val Gln Gly Gly Val Glu Leu Pro Val
65 70 75 80
Ala Ala Trp Arg Ser Tyr Met Asn Met Glu Leu Thr Ile Pro Val Phe
85 90 95
Ala Thr Asn Asp Asp Cys Ala Leu Ile Val Lys Ala Leu Gln Gly Thr
100 105 110
Phe Lys Thr Gly Asn Pro Ile Ala Thr Ala Ile Ala Ala Asn Ser Gly
115 120 125
Ile Tyr
130
<210>26
<211>130
<212>PRT
<213>噬菌体GA
<400>26
Met Ala Thr Leu Arg Ser Phe Val Leu Val Asp Asn Gly Gly Thr Gly
1 5 10 15
Asn Val Thr Val Val Pro Val Ser Asn Ala Asn Gly Val Ala Glu Trp
20 25 30
Leu Ser Asn Asn Ser Arg Ser Gln Ala Tyr Arg Val Thr Ala Ser Tyr
35 40 45
Arg Ala Ser Gly Ala Asp Lys Arg Lys Tyr Ala Ile Lys Leu Glu Val
50 55 60
Pro Lys Ile Val Thr Gln Val Val Asn Gly Val Glu Leu Pro Gly Ser
65 70 75 80
Ala Trp Lys Ala Tyr Ala Ser Ile Asp Leu Thr Ile Pro Ile Phe Ala
85 90 95
Ala Thr Asp Asp Val Thr Val Ile Ser Lys Ser Leu Ala Gly Leu Phe
100 105 110
Lys Val Gly Asn Pro Ile Ala Glu Ala Ile Ser Ser Gln Ser Gly Phe
115 120 125
Tyr Ala
130
<210>27
<211>132
<212>PRT
<213>噬菌体SP
<400>27
Met Ala Lys Leu Asn Gln Val Thr Leu Ser Lys Ile Gly Lys Asn Gly
1 5 10 15
Asp Gln Thr Leu Thr Leu Thr Pro Arg Gly Val Asn Pro Thr Asn Gly
20 25 30
Val Ala Ser Leu Ser Glu Ala Gly Ala Val Pro Ala Leu Glu Lys Arg
35 40 45
Val Thr Val Ser Val Ala Gln Pro Ser Arg Asn Arg Lys Asn Phe Lys
50 55 60
Val Gln Ile Lys Leu Gln Asn Pro Thr Ala Cys Thr Arg Asp Ala Cys
65 70 75 80
Asp Pro Ser Val Thr Arg Ser Ala Phe Ala Asp Val Thr Leu Ser Phe
85 90 95
Thr Ser Tyr Ser Thr Asp Glu Glu Arg Ala Leu Ile Arg Thr Glu Leu
100 105 110
Ala Ala Leu Leu Ala Asp Pro Leu Ile Val Asp Ala Ile Asp Asn Leu
115 120 125
Asn Pro Ala Tyr
130
<210>28
<211>329
<212>PRT
<213>噬菌体SP
<400>28
Ala Lys Leu Asn Gln Val Thr Leu Ser Lys Ile Gly Lys Asn Gly Asp
1 5 10 15
Gln Thr Leu Thr Leu Thr Pro Arg Gly Val Asn Pro Thr Asn Gly Val
20 25 30
Ala Ser Leu Ser Glu Ala Gly Ala Val Pro Ala Leu Glu Lys Arg Val
35 40 45
Thr Val Ser Val Ala Gln Pro Ser Arg Asn Arg Lys Asn Phe Lys Val
50 55 60
Gln Ile Lys Leu Gln Asn Pro Thr Ala Cys Thr Arg Asp Ala Cys Asp
65 70 75 80
Pro Ser Val Thr Arg Ser Ala Phe Ala Asp Val Thr Leu Ser Phe Thr
85 90 95
Ser Tyr Ser Thr Asp Glu Glu Arg Ala Leu Ile Arg Thr Glu Leu Ala
100 105 110
Ala Leu Leu Ala Asp Pro Leu Ile Val Asp Ala Ile Asp Asn Leu Asn
115 120 125
Pro Ala Tyr Trp Ala Ala Leu Leu Val Ala Ser Ser Gly Gly Gly Asp
130 135 140
Asn Pro Ser Asp Pro Asp Val Pro Val Val Pro Asp Val Lys Pro Pro
145 150 155 160
Asp Gly Thr Gly Arg Tyr Lys Cys Pro Phe Ala Cys Tyr Arg Leu Gly
165 170 175
Ser Ile Tyr Glu Val Gly Lys Glu Gly Ser Pro Asp Ile Tyr Glu Arg
180 185 190
Gly Asp Glu Val Ser Val Thr Phe Asp Tyr Ala Leu Glu Asp Phe Leu
195 200 205
Gly Asn Thr Asn Trp Arg Asn Trp Asp Gln Arg Leu Ser Asp Tyr Asp
210 215 220
Ile Ala Asn Arg Arg Arg Cys Arg Gly Asn Gly Tyr Ile Asp Leu Asp
225 230 235 240
Ala Thr Ala Met Gln Ser Asp Asp Phe Val Leu Ser Gly Arg Tyr Gly
245 250 255
Val Arg Lys Val Lys Phe Pro Gly Ala Phe Gly Ser Ile Lys Tyr Leu
260 265 270
Leu Asn Ile Gln Gly Asp Ala Trp Leu Asp Leu Ser Glu Val Thr Ala
275 280 285
Tyr Arg Ser Tyr Gly Met Val Ile Gly Phe Trp Thr Asp Ser Lys Ser
290 295 300
Pro Gln Leu Pro Thr Asp Phe Thr Gln Phe Asn Ser Ala Asn Cys Pro
305 310 315 320
Val Gln Thr Val Ile Ile Ile Pro Ser
325
<210>29
<211>130
<212>PRT
<213>噬菌体MS2
<400>29
Met Ala Ser Asn Phe Thr Gln Phe Val Leu Val Asp Asn Gly Gly Thr
1 5 10 15
Gly Asp Val Thr Val Ala Pro Ser Asn Phe Ala Asn Gly Val Ala Glu
20 25 30
Trp Ile Ser Ser Asn Ser Arg Ser Gln Ala Tyr Lys Val Thr Cys Ser
35 40 45
Val Arg Gln Ser Ser Ala Gln Asn Arg Lys Tyr Thr Ile Lys Val Glu
50 55 60
Val Pro Lys Val Ala Thr Gln Thr Val Gly Gly Val Glu Leu Pro Val
65 70 75 80
Ala Ala Trp Arg Ser Tyr Leu Asn Met Glu Leu Thr Ile Pro Ile Phe
85 90 95
Ala Thr Asn Ser Asp Cys Glu Leu Ile Val Lys Ala Met Gln Gly Leu
100 105 110
Leu Lys Asp Gly Asn Pro Ile Pro Ser Ala Ile Ala Ala Asn Ser Gly
115 120 125
Ile Tyr
130
<210>30
<211>133
<212>PRT
<213>噬菌体M11
<400>30
Met Ala Lys Leu Gln Ala Ile Thr Leu Ser Gly Ile Gly Lys Lys Gly
1 5 10 15
Asp Val Thr Leu Asp Leu Asn Pro Arg Gly Val Asn Pro Thr Asn Gly
20 25 30
Val Ala Ala Leu Ser Glu Ala Gly Ala Val Pro Ala Leu Glu Lys Arg
35 40 45
Val Thr Ile Ser Val Ser Gln Pro Ser Arg Asn Arg Lys Asn Tyr Lys
50 55 60
Val Gln Val Lys Ile Gln Asn Pro Thr Ser Cys Thr Ala Ser Gly Thr
65 70 75 80
Cys Asp Pro Ser Val Thr Arg Ser Ala Tyr Ser Asp Val Thr Phe Ser
85 90 95
Phe Thr Gln Tyr Ser Thr Val Glu Glu Arg Ala Leu Val Arg Thr Glu
100 105 110
Leu Gln Ala Leu Leu Ala Asp Pro Met Leu Val Asn Ala Ile Asp Asn
115 120 125
Leu Asn Pro Ala Tyr
130
<210>31
<211>133
<212>PRT
<213>噬菌体MX1
<400>31
Met Ala Lys Leu Gln Ala Ile Thr Leu Ser Gly Ile Gly Lys Asn Gly
1 5 10 15
Asp Val Thr Leu Asn Leu Asn Pro Arg Gly Val Asn Pro Thr Asn Gly
20 25 30
Val Ala Ala Leu Ser Glu Ala Gly Ala Val Pro Ala Leu Glu Lys Arg
35 40 45
Val Thr Ile Ser Val Ser Gln Pro Ser Arg Asn Arg Lys Asn Tyr Lys
50 55 60
Val Gln Val Lys Ile Gln Asn Pro Thr Ser Cys Thr Ala Ser Gly Thr
65 70 75 80
Cys Asp Pro Ser Val Thr Arg Ser Ala Tyr Ala Asp Val Thr Phe Ser
85 90 95
Phe Thr Gln Tyr Ser Thr Asp Glu Glu Arg Ala Leu Val Arg Thr Glu
100 105 110
Leu Lys Ala Leu Leu Ala Asp Pro Met Leu Ile Asp Ala Ile Asp Asn
115 120 125
Leu Asn Pro Ala Tyr
130
<210>32
<211>330
<212>PRT
<213>噬菌体NL95
<400>32
Met Ala Lys Leu Asn Lys Val Thr Leu Thr Gly Ile Gly Lys Ala Gly
1 5 10 15
Asn Gln Thr Leu Thr Leu Thr Pro Arg Gly Val Asn Pro Thr Asn Gly
20 25 30
Val Ala Ser Leu Ser Glu Ala Gly Ala Val Pro Ala Leu Glu Lys Arg
35 40 45
Val Thr Val Ser Val Ala Gln Pro Ser Arg Asn Arg Lys Asn Tyr Lys
50 55 60
Val Gln Ile Lys Leu Gln Asn Pro Thr Ala Cys Thr Lys Asp Ala Cys
65 70 75 80
Asp Pro Ser Val Thr Arg Ser Gly Ser Arg Asp Val Thr Leu Ser Phe
85 90 95
Thr Ser Tyr Ser Thr Glu Arg Glu Arg Ala Leu Ile Arg Thr Glu Leu
100 105 110
Ala Ala Leu Leu Lys Asp Asp Leu Ile Val Asp Ala Ile Asp Asn Leu
115 120 125
Asn Pro Ala Tyr Trp Ala Ala Leu Leu Ala Ala Ser Pro Gly Gly Gly
130 135 140
Asn Asn Pro Tyr Pro Gly Val Pro Asp Ser Pro Asn Val Lys Pro Pro
145 150 155 160
Gly Gly Thr Gly Thr Tyr Arg Cys Pro Phe Ala Cys Tyr Arg Arg Gly
165 170 175
Glu Leu Ile Thr Glu Ala Lys Asp Gly Ala Cys Ala Leu Tyr Ala Cys
180 185 190
Gly Ser Glu Ala Leu Val Glu Phe Glu Tyr Ala Leu Glu Asp Phe Leu
195 200 205
Gly Asn Glu Phe Trp Arg Asn Trp Asp Gly Arg Leu Ser Lys Tyr Asp
210 215 220
Ile Glu Thr His Arg Arg Cys Arg Gly Asn Gly Tyr Val Asp Leu Asp
225 230 235 240
Ala Ser Val Met Gln Ser Asp Glu Tyr Val Leu Ser Gly Ala Tyr Asp
245 250 255
Val Val Lys Met Gln Pro Pro Gly Thr Phe Asp Ser Pro Arg Tyr Tyr
260 265 270
Leu His Leu Met Asp Gly Ile Tyr Val Asp Leu Ala Glu Val Thr Ala
275 280 285
Tyr Arg Ser Tyr Gly Met Val Ile Gly Phe Trp Thr Asp Ser Lys Ser
290 295 300
Pro Gln Leu Pro Thr Asp Phe Thr Arg Phe Asn Arg His Asn Cys Pro
305 310 315 320
Val Gln Thr Val Ile Val Ile Pro Ser Leu
325 330
<210>33
<211>129
<212>PRT
<213>噬菌体f2
<400>33
Ala Ser Asn Phe Thr Gln Phe Val Leu Val Asn Asp Gly Gly Thr Gly
1 5 10 15
Asn Val Thr Val Ala Pro Ser Asn Phe Ala Asn Gly Val Ala Glu Trp
20 25 30
Ile Ser Ser Asn Ser Arg Ser Gln Ala Tyr Lys Val Thr Cys Ser Val
35 40 45
Arg Gln Ser Ser Ala Gln Asn Arg Lys Tyr Thr Ile Lys Val Glu Val
50 55 60
Pro Lys Val Ala Thr Gln Thr Val Gly Gly Val Glu Leu Pro Val Ala
65 70 75 80
Ala Trp Arg Ser Tyr Leu Asn Leu Glu Leu Thr Ile Pro Ile Phe Ala
85 90 95
Thr Asn Ser Asp Cys Glu Leu Ile Val Lys Ala Met Gln Gly Leu Leu
100 105 110
Lys Asp Gly Asn Pro Ile Pro Ser Ala Ile Ala Ala Asn Ser Gly Ile
115 120 125
Tyr
Claims (115)
1.一种半抗原-载体偶联物,其包含:
(a)含有至少一个第一附着位点的载体;和
(b)含有至少一个第二附着位点的至少一个半抗原,
其中所述载体包含、优选地是一种核心颗粒;
其中所述第二附着位点能够通过至少一个共价键与所述第一附着位点连接,形成一种有序、重复的半抗原-载体偶联物。
2.权利要求1的偶联物,其中所述核心颗粒选自:
i)病毒;
ii)病毒样颗粒;
iii)噬菌体;
iv)RNA噬菌体的病毒样颗粒;
v)细菌菌毛;
vi)病毒衣壳颗粒;和
vii)(i)、(ii)、(iii)、(iv)、(v)或(vi)的重组形式。
3.权利要求1的偶联物,其中所述核心颗粒包含、优选地是病毒样颗粒,其中优选地该病毒样颗粒是一种重组病毒样颗粒。
4.权利要求2或3的偶联物,其中所述病毒样颗粒包含选自下列的一种或多种重组蛋白或其片段:
(a)重组乙型肝炎病毒蛋白;
(b)重组麻疹病毒蛋白;
(c)重组辛德毕斯病毒蛋白;
(d)重组轮状病毒蛋白;
(e)重组口蹄疫病毒蛋白;
(f)重组逆转录病毒蛋白;
(g)重组诺瓦克病毒蛋白;
(h)重组甲病毒蛋白;
(i)重组人乳头瘤病毒蛋白;
(j)重组多瘤病毒蛋白;
(k)重组噬菌体蛋白;
(l)重组RNA噬菌体蛋白;
(m)重组Ty蛋白;
(n)重组Qβ-噬菌体蛋白;
(o)重组GA-噬菌体蛋白;
(p)重组fr-噬菌体蛋白;
(q)重组AP205噬菌体蛋白;和
(r)(a)-(q)中任何一种重组蛋白的片段。
5.权利要求2或3的偶联物,其中所述病毒样颗粒包含一种乙型肝炎病毒衣壳蛋白。
6.权利要求5的偶联物,其中乙型肝炎病毒衣壳蛋白的氨基酸序列与SEQ ID No:1的序列至少约80%相同。
7.权利要求5的偶联物,其中所述外壳蛋白已经通过删除至少一个赖氨酸残基、通过插入添加至少一个赖氨酸残基或者通过置换至少一个赖氨酸残基而被修饰。
8.权利要求2或3的偶联物,其中所述病毒样颗粒包含或者由RNA噬菌体的重组蛋白或其片段组成。
9.权利要求8的偶联物,其中所述RNA噬菌体选自:
(a)噬菌体Qβ;
(b)噬菌体R17;
(c)噬菌体fr;
(d)噬菌体GA;
(e)噬菌体SP;
(f)噬菌体MS2;
(g)噬菌体M11;
(h)噬菌体MX1;
(i)噬菌体NL95;
(j)噬菌体f2;
(k)噬菌体AP205;和
(l)噬菌体PP7。
10.权利要求2或3的偶联物,其中所述病毒样颗粒包含或者由RNA噬菌体Qβ的重组蛋白或其片段组成。
11.权利要求2或3的偶联物,其中所述病毒样颗粒包含或者由RNA噬菌体fr的重组蛋白或其片段组成。
12.权利要求2或3的偶联物,其中所述病毒样颗粒包含或者由RNA噬菌体AP205的重组蛋白或其片段组成。
13.权利要求3-12中任何一项的偶联物,其中所述重组蛋白包含或者基本由或者由RNA噬菌体的外壳蛋白组成。
14.权利要求13的偶联物,其中RNA噬菌体的外壳蛋白具有选自下列的氨基酸序列:
(a)SEQ ID NO:3;
(b)SEQ ID NO:3和SEQ ID NO:4的混合物;
(c)SEQ ID NO:24;
(d)SEQ ID NO:25;
(e)SEQ ID NO:26;
(f)SEQ ID NO:27;
(g)SEQ ID NO:27和SEQ ID NO:28的混合物;
(h)SEQ ID NO:29;
(i)SEQ ID NO:30;
(j)SEQ ID NO:31;
(k)SEQ ID NO:32;
(l)SEQ ID NO:33;
(m)SEQ ID NO:13;和
(n)SEQ ID NO:14。
15.权利要求3-11中任何一项的偶联物,其中所述RNA噬菌体的重组蛋白包含或者基本由或者由RNA噬菌体的一种或多种突变外壳蛋白组成。
16.权利要求15的偶联物,其中所述RNA噬菌体选自:
(a)噬菌体Qβ;
(b)噬菌体R17;
(c)噬菌体fr;
(d)噬菌体GA;
(e)噬菌体SP;
(f)噬菌体MS2;
(g)噬菌体M11;
(h)噬菌体MX1;
(i)噬菌体NL95;
(k)噬菌体f2;
(l)噬菌体PP7;和
(m)噬菌体AP205。
17.权利要求16的偶联物,其中所述RNA噬菌体的突变外壳蛋白已经通过置换除去至少一个赖氨酸残基而被修饰。
18.权利要求16或17的偶联物,其中所述RNA噬菌体的突变外壳蛋白已经通过置换添加至少一个赖氨酸残基而被修饰。
19.权利要求16或17的偶联物,其中所述RNA噬菌体的突变外壳蛋白已经通过删除至少一个赖氨酸残基而被修饰。
20.权利要求16或17的偶联物,其中所述RNA噬菌体的突变外壳蛋白已经通过插入添加至少一个赖氨酸残基而被修饰。
21.权利要求8的偶联物,其中所述重组蛋白包含具有SEQ IDNO:3所示氨基酸序列的外壳蛋白、或具有SEQ ID NO:4的氨基酸序列的外壳蛋白或其突变体与具有SEQ ID NO:3的氨基酸序列的外壳蛋白或其突变体的混合物。
22.权利要求8的偶联物,其中所述病毒样颗粒基本由具有SEQID NO:3所示氨基酸序列的外壳蛋白组成,或者基本由具有SEQ IDNO:4的氨基酸序列的外壳蛋白或其突变体与具有SEQ ID NO:3的氨基酸序列的外壳蛋白或其突变体的混合物组成。
23.权利要求10的偶联物,其中所述重组蛋白包含突变Qβ外壳蛋白。
24.权利要求23的偶联物,其中所述突变Qβ外壳蛋白已经通过置换除去至少一个赖氨酸残基或者通过置换添加至少一个赖氨酸残基而被修饰。
25.权利要求23的偶联物,其中所述突变Qβ外壳蛋白已经通过删除至少一个赖氨酸残基或者通过插入添加至少一个赖氨酸残基而被修饰。
26.权利要求23的偶联物,其中所述突变Qβ外壳蛋白含有具有选自下列的氨基酸序列的蛋白:
(a)SEQ ID NO:6的氨基酸序列;
(b)SEQ ID NO:7的氨基酸序列;
(c)SEQ ID NO:8的氨基酸序列;
(d)SEQ ID NO:9的氨基酸序列;和
(e)SEQ ID NO:10的氨基酸序列。
27.权利要求2的偶联物,其中所述病毒样颗粒基本由具有选自下列的氨基酸序列的突变Qβ外壳蛋白组成:
(a)SEQ ID NO:6的氨基酸序列;
(b)SEQ ID NO:7的氨基酸序列;
(c)SEQ ID NO:8的氨基酸序列;
(d)SEQ ID NO:9的氨基酸序列;
(e)SEQ ID NO:10的氨基酸序列。
28.前述权利要求中任一项的偶联物,其中所述第一附着位点含有:
(a)氨基;
(b)羧基;
(c)巯基;
(d)羟基;
(e)胍基;或
(f)组氨酸残基。
29.前述权利要求中任一项的偶联物,其中所述至少一个第一附着位点选自:赖氨酸残基、精氨酸残基、半胱氨酸残基、天冬氨酸残基、谷氨酸残基、丝氨酸残基、苏氨酸残基、组氨酸残基和酪氨酸残基。
30.前述权利要求中任一项的偶联物,其中所述至少一个第一附着位点是赖氨酸残基。
31.前述权利要求中任一项的偶联物,其中所述第二附着位点能够通过至少一个非肽键与第一附着位点连接。
32.前述权利要求中任一项的偶联物,其中所述半抗原是适合诱导针对药物、激素或毒素的免疫应答的有机分子。
33.前述权利要求中任一项的半抗原-载体偶联物,其中所述半抗原适合引发针对药物的免疫应答。
34.权利要求33的偶联物,其中所述药物是成瘾性药物或滥用性药物。
35.权利要求33或34的偶联物,其中所述药物选自:
(a)可待因;
(b)芬太尼;
(c)海洛因;
(d)吗啡;
(e)安非他明;
(f)可卡因;
(g)亚甲二氧基甲基苯丙胺;
(h)甲基苯丙胺;
(i)哌甲酯;
(j)尼古丁;
(k)可替宁;
(l)降烟碱;
(m)PCP;
(n)LSD;
(o)麦斯卡林;
(p)西洛西宾;
(q)四氢大麻酚;
(r)安定;
(s)地昔帕明;
(t)米帕明;
(u)去甲替林;
(v)阿米替林类药物。
36.权利要求33或34的偶联物,其中所述药物是尼古丁、可替宁或降烟碱。
37.权利要求33或34的偶联物,其中所述药物是尼古丁。
38.权利要求36的偶联物,其中所述偶联物由选自下列的起始材料形成:
(a)6-(羧甲基脲基)-(±)-尼古丁(CMUNic);
(b)反式-3′-氨基甲基尼古丁琥珀酸盐;
(c)O-琥珀酰-3′-羟甲基-尼古丁;
(d)反式-4′-羧基可替宁;
(e)N-[1-氧代-6-[(25)-2-(3-吡啶基)-1-吡咯烷基]己基]-β-丙氨酸;
(f)4-氧代-4-[[6-[(5S)-2-氧代-5-(3-吡啶基)-1-吡咯烷基]]己基]氨基]-丁酸;
(g)(2S)-2-(3-吡啶基)-1-吡咯烷丁酸苯甲酯;
(h)(2R)-2-(3-吡啶基)-1-吡咯烷丁酸苯甲酯;
(i)可替宁4’-羧酸,N-琥珀酰-6-氨基-(±)-尼古丁;
(j)6-(σ-氨基癸酰胺基)-(±)-尼古丁;
(k)6-(σ-氨基癸酰胺基)-(±)-尼古丁;
(l)3’氨甲基尼古丁;
(m)4’氨甲基尼古丁;
(n)5’氨甲基尼古丁;
(o)5氨基尼古丁;
(p)6氨基尼古丁;
(q)S-1-(b-氨乙基)氯化尼古丁鎓;和
(r)S-1-(b-氨乙基)氯化可替宁鎓。
39.权利要求36的偶联物,其中所述半抗原含有起始材料O-琥珀酰-3′-羟甲基-尼古丁。
40.权利要求36的偶联物,其中所述偶联物含有与Qβ病毒样颗粒偶联的O-琥珀酰-3′-羟甲基-尼古丁。
41.权利要求36的偶联物,其中所述半抗原由起始材料O-琥珀酰-3′-羟甲基-尼古丁形成。
42.前述权利要求中任一项的偶联物,其中第二附着位点含有、优选地是选自下列的活性基团:
(a)胺;
(b)酰胺;
(c)羧基;
(d)巯基;
(e)羟基;
(f)醛;
(g)重氮基;
(h)酰卤;
(i)肼;
(j)乙烯基;
(k)马来酰亚胺;
(l)琥珀酰亚胺;和
(m)酰肼。
43.前述权利要求中任一项的偶联物,其中所述第二附着位点由O-琥珀酰-3′-羟甲基-尼古丁的O-琥珀酰部分与第一附着位点反应形成。
44.前述权利要求中任一项的偶联物,其中第二附着位点含有、优选地是一种酰胺。
45.前述权利要求中任一项的偶联物,其中所述第二附着位点由O-琥珀酰-3′-羟甲基-尼古丁的O-琥珀酰部分与作为第一附着位点的赖氨酸残基反应形成。
46.前述权利要求中任一项的偶联物,其中所述偶联物含有O-琥珀酰-3′-羟甲基-尼古丁,后者与RNA噬菌体的病毒样颗粒偶联、优选地与Qβ病毒样颗粒偶联,优选地与包含或者优选地由RNA噬菌体Qβ外壳蛋白组成的Qβ病毒样颗粒偶联。
47.前述权利要求中任一项的偶联物,其中第二附着位点含有选自下列的活性基团:
(a)胺;
(b)酰胺;
(c)羧基;
(d)巯基;
(e)羟基;
(f)醛;
(g)重氮基;
(h)酰卤;
(i)肼;
(j)乙烯基;
(k)马来酰亚胺;
(l)琥珀酰亚胺;和
(m)酰肼。
48.权利要求33的偶联物,其中成瘾性药物或滥用药物是可卡因。
49.权利要求48的偶联物,其中所述偶联物由选自下列的起始材料形成:
(a)苯甲酰可卡因的重氮盐;
(b)苯甲酰芽子碱的重氮盐;
(c)酰化的芽子碱甲酯;
(d)琥珀酰化的芽子碱甲酯;
(e)琥珀酰化的去甲可卡因;
(f)去甲可卡因;和
(g)苯甲酰芽子碱。
50.权利要求48或49的偶联物,其中第二附着位点含有选自下列的活性基团:
(a)胺;
(b)酰胺;
(c)羧基;
(d)巯基;
(e)羟基;
(f)醛;
(g)重氮基;
(h)酰卤;
(i)肼;
(j)乙烯基;
(k)马来酰亚胺;
(l)琥珀酰亚胺;和
(m)酰肼。
51.一种适合治疗或预防药物成瘾性的组合物,其包含前述权利要求中任一项的偶联物和药学上可接受的赋形剂。
52.权利要求51的组合物,其还含有佐剂。
53.一种治疗或预防药物成瘾性的方法,该方法包括对个体施用前述权利要求中任一项的偶联物。
54.一种治疗或预防药物成瘾性的方法,该方法包括对个体施用针对前述权利要求中任一项的偶联物的抗体。
55.权利要求1-32中任一项的偶联物,其中所述半抗原是一种激素。
56.权利要求55的组合物,其中所述激素选自:
(a)孕酮;
(b)雌激素;
(c)睾酮;
(d)促卵泡激素;
(e)黑色素刺激激素;
(f)肾上腺素;
(g)去甲肾上腺素;和
(h)(a)-(e)中任一项的片段。
57.权利要求55或56的组合物,其中第二附着位点含有选自下列的活性基团:
(a)胺;
(b)酰胺;
(c)羧基;
(d)巯基;
(e)羟基;
(f)醛;
(g)重氮基;
(h)酰卤;
(i)肼;
(j)乙烯基;
(k)马来酰亚胺;
(l)琥珀酰亚胺;和
(m)酰肼。
58.权利要求1-32中任一项的偶联物,其中所述半抗原是一种毒素。
59.权利要求58的偶联物,其中所述毒素选自:
(a)黄曲霉毒素;
(b)鱼肉毒素;
(c)河豚毒素;
(d)抗生素;和
(e)抗癌剂。
60.权利要求58或59的偶联物,其中所述毒素是动物体产生的一种代谢物。
61.权利要求60的偶联物,其中所述代谢物是一种药物的代谢物。
62.权利要求58的偶联物,其中所述毒素是一种化学战剂。
63.一种药物组合物,其含有前述权利要求中任一项的偶联物和药学上可接受的载体。
64.权利要求63的药物组合物,它还含有佐剂。
65.权利要求63的药物组合物,其中所述组合物不含佐剂。
66.一种疫苗组合物,其含有权利要求1-62中任一项的偶联物。
67.权利要求66的疫苗组合物,其还含有佐剂。
68.权利要求66的疫苗组合物,其中该疫苗组合物不含佐剂。
69.一种在动物中诱导对药物的免疫应答的方法,该方法包括对动物施用免疫有效量的前述权利要求中任一项的偶联物,使该动物产生针对该药物的免疫应答。
70.权利要求69的方法,其中通过选自下列的途径对所述动物施用所述偶联物:鼻内、口服、皮下、透皮、肌肉内或静脉内。
71.权利要求70的方法,其中所述途径是鼻内。
72.权利要求70的方法,它包括一次以上的免疫。
73.权利要求72的方法,其中各次免疫是通过相同或者不同的途径。
74.权利要求69-73中任一项的方法,其中所述药物选自:
(a)可待因;
(b)芬太尼;
(c)海洛因;
(d)吗啡;
(e)安非他明;
(f)可卡因;
(g)亚甲二氧基甲基苯丙胺;
(h)甲基苯丙胺;
(i)哌甲酯;
(j)尼古丁;
(k)可替宁;
(l)降烟碱;
(m)PCP;
(n)LSD;
(o)麦斯卡林;
(p)西洛西宾;
(q)四氢大麻酚;
(r)安定;
(s)地昔帕明;
(t)米帕明;
(u)去甲替林;和
(v)阿米替林类药物。
75.一种识别半抗原的抗体,该抗体是通过用权利要求63的组合物免疫动物产生的。
76.一种组合物,其含有针对一种半抗原的抗体或Fab片段,所述抗体或Fab片段是通过用半抗原-载体偶联物免疫动物产生的,该偶联物含有:
(a)含有至少一个第一附着位点的载体,和
(b)含有至少一个第二附着位点的至少一个半抗原;
其中该载体是一种核心颗粒;和
其中所述第二附着位点能够通过至少一个共价键与所述第一附着位点连接,形成一种有序、重复的半抗原-载体偶联物。
77.权利要求76的抗体组合物,其中所述抗体是单克隆抗体。
78.权利要求76的抗体或Fab片段,它是人源化的。
79.一种用权利要求76的抗体或Fab片段检测半抗原的方法。
80.权利要求79的方法,其中该方法是ELISA、放射免疫测定、Western blot或FACS。
81.一种治疗个体成瘾性的方法,包括对该个体施用权利要求76的抗体或Fab片段。
82.一种预防成瘾的方法,包括对个体施用权利要求76的抗体或Fab片段。
83.权利要求76的方法,其中该个体是免疫缺陷的。
84.一种预防或治疗与成瘾有关的疾病的方法,包括对动物施用权利要求76的抗体或Fab片段。
85.一种预防或治疗与成瘾有关的疾病的方法,包括对动物施用权利要求63-65中任一项的组合物。
86.一种检测尼古丁的试剂盒,该试剂盒包含一种抗尼古丁抗体或Fab片段,所述抗体或Fab片段是通过用半抗原-载体偶联物免疫动物产生的,该偶联物含有:
(a)含有至少一个第一附着位点的载体,和
(b)含有至少一个第二附着位点的至少一个尼古丁半抗原;
其中该载体是一种病毒样颗粒;和
其中所述第二附着位点能够通过至少一个共价键与所述第一附着位点连接,形成一种有序、重复的尼古丁半抗原-载体偶联物。
87.一种治疗或预防动物尼古丁成瘾的方法,所述方法包括对动物施用免疫有效量的尼古丁半抗原-载体偶联物,该偶联物含有:
(a)含有至少一个第一附着位点的病毒样颗粒载体,和
(b)含有至少一个第二附着位点的至少一个尼古丁半抗原;
其中所述第二附着位点能够通过至少一个共价键与所述第一附着位点连接,形成一种有序、重复的尼古丁半抗原-载体偶联物。
88.权利要求87的方法,其中对所述动物鼻内、口服、皮下、透皮、肌肉内或静脉内施用所述组合物。
89.权利要求81的方法,其中所述动物是人。
90.作为药物的前述权利要求中任一项的一种偶联物或组合物。
91.前述权利要求中任一项的偶联物或组合物在制备治疗药物成瘾及相关疾病的药物中的用途。
92.一种用于治疗尼古丁成瘾、缓解尼古丁戒断症状、帮助戒烟或防止复吸的药物组合物,其含有权利要求1-68中任一项的疫苗组合物与另外药物的治疗有效的组合。
93.权利要求92的组合物,其中所述另外的药物选自:
(a)抗抑郁剂;
(b)尼古丁受体调节剂;
(c)大麻素受体拮抗剂;
(d)阿片受体拮抗剂;
(e)单胺氧化酶抑制剂;
(f)抗焦虑剂。
94.权利要求92的组合物,其中所述另外的药物是抗抑郁剂,其选自:丁氨苯丙酮、多塞平、地昔帕明、氯米帕明、米帕明、去甲替林、阿米替林、普罗替林、曲米帕明、氟西汀、氟伏沙明、帕罗西汀、舍曲林、苯乙肼、反苯环丙胺、阿莫沙平、马普替林、曲唑酮、文拉法辛、米氮平、它们的药学活性盐以及它们的旋光异构体。
95.权利要求94的组合物,其中所述抗抑郁剂是丁氨苯丙酮或其药学上可接受的盐,或者是去甲替林或其药学上可接受的盐。
96.权利要求92的组合物,其中所述另外的药物是一种尼古丁受体调节剂,其选自:美卡拉明、SSR591813、金刚烷胺、潘必啶、二氢-β-刺桐碱、六甲双铵、刺桐定碱、松达氯铵、樟磺咪芬、氯筒箭毒碱、d-筒箭毒碱、varenicline、它们的药学上可接受的盐以及它们的旋光异构体。
97.权利要求96的组合物,其中所述尼古丁受体调节剂是美卡拉明或其药学上可接受的盐。
98.权利要求96的组合物,其中所述尼古丁受体调节剂是酒石酸varenicline。
99.权利要求92的组合物,其中所述另外的药物是一种大麻素受体拮抗剂,所述大麻素受体拮抗剂是利莫那班。
100.权利要求92的组合物,其中所述另外的药物是一种抗焦虑剂,其选自:羟嗪、甲丙氨酯、丁螺环酮、它们的药学上可接受的盐以及它们的旋光异构体。
101.权利要求92的组合物,其中所述另外的药物是可乐定。
102.权利要求92的组合物,其中所述另外的药物是西布曲明。
103.一种治疗烟草成瘾或尼古丁成瘾、缓解尼古丁戒断症状、防止复吸或者帮助戒烟的方法,包括对患者施用权利要求66-68中任一项的疫苗组合物和另外的药物的步骤。
104.权利要求103的方法,其中所述疫苗组合物通过鼻内、口服、皮下、透皮、肌肉内或静脉内施用,其中所述另外的药物经口服施用或者通过透皮贴剂施用。
105.权利要求103或104的方法,其中所述疫苗组合物含有与Q3病毒样颗粒偶联的O-琥珀酰-3′-羟甲基-尼古丁。
106.权利要求103的方法,其中所述另外的药物选自:
(a)抗抑郁剂;
(b)尼古丁受体调节剂;
(c)大麻素受体拮抗剂;
(d)阿片受体拮抗剂;
(e)单胺氧化酶抑制剂;和
(f)抗焦虑剂。
107.权利要求103的方法,其中所述另外的药物是一种抗抑郁剂,其选自:丁氨苯丙酮、多塞平、地昔帕明、氯米帕明、米帕明、去甲替林、阿米替林、普罗替林、曲米帕明、氟西汀、氟伏沙明、帕罗西汀、舍曲林、苯乙肼、反苯环丙胺、阿莫沙平、马普替林、曲唑酮、文拉法辛、米氮平、它们的药学活性盐以及它们的旋光异构体。
108.权利要求103的方法,其中所述抗抑郁剂是丁氨苯丙酮或其药学上可接受的盐,或者是去甲替林或其药学上可接受的盐。
109.权利要求103的方法,其中所述另外的药物是一种尼古丁受体调节剂,其选自:美卡拉明、SSR591813、金刚烷胺、潘必啶、二氢-β-刺桐碱、六甲双铵、刺桐定碱、松达氯铵、樟磺咪芬、氯筒箭毒碱、d-筒箭毒碱、varenicline、它们的药学上可接受的盐以及它们的旋光异构体。
110.权利要求109的方法,其中所述尼古丁受体调节剂是美卡拉明或其药学上可接受的盐。
111.权利要求109的方法,其中所述尼古丁受体调节剂是酒石酸varenicline。
112.权利要求103的方法,其中所述另外的药物是一种大麻素受体拮抗剂,该大麻素受体拮抗剂是利莫那班。
113.权利要求103的方法,其中所述另外的药物是一种抗焦虑剂,其选自:羟嗪、甲丙氨酯、丁螺环酮、它们的药学上可接受的盐以及它们的旋光异构体。
114.权利要求103的方法,其中所述另外的药物是可乐定。
115.权利要求103的方法,其中所述另外的药物是西布曲明。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US39657502P | 2002-07-18 | 2002-07-18 | |
| US60/396,575 | 2002-07-18 |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN2009101392979A Division CN101574518B (zh) | 2002-07-18 | 2003-07-18 | 半抗原-载体偶联物及其用途 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN1668331A true CN1668331A (zh) | 2005-09-14 |
| CN100518823C CN100518823C (zh) | 2009-07-29 |
Family
ID=30770921
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN2009101392979A Expired - Fee Related CN101574518B (zh) | 2002-07-18 | 2003-07-18 | 半抗原-载体偶联物及其用途 |
| CNB038167484A Expired - Fee Related CN100518823C (zh) | 2002-07-18 | 2003-07-18 | 半抗原-载体偶联物及其用途 |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN2009101392979A Expired - Fee Related CN101574518B (zh) | 2002-07-18 | 2003-07-18 | 半抗原-载体偶联物及其用途 |
Country Status (16)
| Country | Link |
|---|---|
| US (4) | US6932971B2 (zh) |
| EP (2) | EP1523334A2 (zh) |
| JP (1) | JP5084103B2 (zh) |
| KR (2) | KR20120041739A (zh) |
| CN (2) | CN101574518B (zh) |
| AU (1) | AU2003250106B2 (zh) |
| BR (1) | BR0312297A (zh) |
| CA (1) | CA2487849A1 (zh) |
| IL (1) | IL165249A0 (zh) |
| IN (1) | IN2008CN05409A (zh) |
| MX (1) | MXPA04012010A (zh) |
| NZ (1) | NZ537003A (zh) |
| PL (1) | PL375598A1 (zh) |
| RU (2) | RU2326693C2 (zh) |
| WO (1) | WO2004009116A2 (zh) |
| ZA (1) | ZA200409389B (zh) |
Cited By (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN102119155A (zh) * | 2008-08-08 | 2011-07-06 | 诺瓦提斯公司 | 制备基于烟碱的半抗原的方法 |
| CN102245200A (zh) * | 2008-10-12 | 2011-11-16 | 麻省理工学院 | 尼古丁免疫纳米疗法 |
| CN101443038B (zh) * | 2006-05-12 | 2012-07-04 | 希托斯生物技术股份公司 | 尼古丁-载体疫苗制剂 |
| CN101413946B (zh) * | 2008-10-31 | 2012-08-08 | 江南大学 | 一种盐酸西布曲明的酶联免疫检测方法 |
| CN103230590A (zh) * | 2005-09-28 | 2013-08-07 | 赛托斯生物技术公司 | 白介素-1偶联物及其用途 |
| CN104080479A (zh) * | 2011-11-07 | 2014-10-01 | 诺华股份有限公司 | 包括spr0096和spr2021抗原的运载体分子 |
| CN104411336A (zh) * | 2012-06-28 | 2015-03-11 | 辉瑞公司 | 抗托法替尼抗体及其用于药物监测的用途 |
| CN106905434A (zh) * | 2017-02-28 | 2017-06-30 | 国药中生生物技术研究院有限公司 | 一种包含蹄蝠肝炎病毒核心蛋白的重组融合蛋白及其制备方法和应用 |
| CN108884127A (zh) * | 2016-01-21 | 2018-11-23 | 斯克利普斯研究院 | 合成的阿片类疫苗 |
| CN111363011A (zh) * | 2020-03-13 | 2020-07-03 | 北京大学 | 一种甲基苯丙胺疫苗及其制备方法与应用 |
| CN112924665A (zh) * | 2021-02-19 | 2021-06-08 | 山东莱博生物科技有限公司 | 一种抗体辣根过氧化物酶标记物及其制备与应用 |
| CN114907255A (zh) * | 2022-04-25 | 2022-08-16 | 杭州同舟生物技术有限公司 | 一种利他林人工半抗原、人工抗原及其制备方法和应用 |
| CN116283885A (zh) * | 2022-12-01 | 2023-06-23 | 杭州奥泰生物技术股份有限公司 | 一种帕罗西汀半抗原和人工抗原及其制备方法与应用 |
Families Citing this family (99)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20020032316A1 (en) * | 1995-03-31 | 2002-03-14 | Cantab Pharmaceuticals Research Limited | Hapten-carrier conjugates for use in drug-abuse therapy and methods for preparation of same |
| WO2001085208A2 (en) * | 2000-05-05 | 2001-11-15 | Cytos Biotechnology Ag | Molecular antigen arrays and vaccines |
| US7094409B2 (en) * | 2001-01-19 | 2006-08-22 | Cytos Biotechnology Ag | Antigen arrays for treatment of allergic eosinophilic diseases |
| US7264810B2 (en) * | 2001-01-19 | 2007-09-04 | Cytos Biotechnology Ag | Molecular antigen array |
| US7128911B2 (en) | 2001-01-19 | 2006-10-31 | Cytos Biotechnology Ag | Antigen arrays for treatment of bone disease |
| SE521512C2 (sv) * | 2001-06-25 | 2003-11-11 | Niconovum Ab | Anordning för administrering av en substans till främre delen av en individs munhåla |
| US7115266B2 (en) | 2001-10-05 | 2006-10-03 | Cytos Biotechnology Ag | Angiotensin peptide-carrier conjugates and uses thereof |
| JP4598519B2 (ja) * | 2002-06-20 | 2010-12-15 | サイトス バイオテクノロジー アーゲー | アジュバントとして使用するためのパッケージ化されたウィルス様粒子:調製法及び使用法 |
| BR0312935A (pt) * | 2002-07-17 | 2005-06-21 | Cytos Biotechnology Ag | Partìcula semelhante a vìrus, muteìna, vetores para produzir a referida partìcula e proteìna recombinante, composição, processo para produção de fileira ordena e repetitva de antìgeno, molécula de ácido nucléico, célula hospedeira, método para produção da referida partìcula e uso da composição de vacina |
| BR0312297A (pt) * | 2002-07-18 | 2005-04-12 | Cytos Biotechnology Ag | Conjugados veìculos de hapteno e seu uso |
| NZ537688A (en) * | 2002-07-19 | 2007-01-26 | Cytos Biotechnology Ag | Vaccine compositions containing amyloid beta1-6 antigen arrays for treating and/or attenuating Alzheimer's disease |
| JP4708795B2 (ja) * | 2002-12-20 | 2011-06-22 | ニコノヴァム エービー | 物理的および化学的に安定なニコチン−含有粒状物質 |
| WO2005030798A2 (en) * | 2003-09-24 | 2005-04-07 | Government Of The United States Of America, Represented By The Secretary, Department Of Health And Human Services | TNFαCONVERTING ENZYME INHIBITORY AGENTS AND STIMULATORY AGENTS- |
| US7923109B2 (en) | 2004-01-05 | 2011-04-12 | Board Of Regents, The University Of Texas System | Inorganic nanowires |
| GB0419199D0 (en) * | 2004-08-27 | 2004-09-29 | Curidium Ltd | Methods of diagnosis |
| AU2005291231B2 (en) * | 2004-10-05 | 2010-12-23 | Cytos Biotechnology Ag | VLP-antigen conjugates and their uses as vaccines |
| ZA200701792B (en) * | 2004-10-25 | 2008-12-31 | Cytos Biotechnology Ag | Gastric inhibitory polypeptide (GIP) antigen arrays and uses thereof |
| US9492400B2 (en) | 2004-11-04 | 2016-11-15 | Massachusetts Institute Of Technology | Coated controlled release polymer particles as efficient oral delivery vehicles for biopharmaceuticals |
| GB0424563D0 (en) | 2004-11-05 | 2004-12-08 | Novartis Ag | Organic compounds |
| US20060111271A1 (en) * | 2004-11-24 | 2006-05-25 | Cerny Erich H | Active and passive immunization against pharmacologically active hapten molecules using a synthetic carrier compound composed of similar elements |
| US20060154259A1 (en) * | 2005-01-07 | 2006-07-13 | Huan-Cheng Chang | Diamond crystallites for biotechnological applications |
| NZ561375A (en) | 2005-06-27 | 2011-06-30 | Biovail Lab Int Srl | Bupropion hydrobromide, and crystalline forms, compositions, and uses of this compound |
| US20070020620A1 (en) * | 2005-07-14 | 2007-01-25 | Finn M G | Compositions and methods for coupling a plurality of compounds to a scaffold |
| US20110086086A1 (en) * | 2005-07-26 | 2011-04-14 | Pfizer Inc | Transdermal system for varenicline |
| WO2007070682A2 (en) | 2005-12-15 | 2007-06-21 | Massachusetts Institute Of Technology | System for screening particles |
| CA2646942C (en) | 2006-03-16 | 2014-07-29 | Niconovum Ab | Improved snuff composition |
| JP2009534309A (ja) * | 2006-03-31 | 2009-09-24 | マサチューセッツ インスティテュート オブ テクノロジー | 治療剤の標的化送達のためのシステム |
| US20080044462A1 (en) * | 2006-04-06 | 2008-02-21 | Collegium Pharmaceutical, Inc. Delaware | Stabilized transdermal bupropion preparations |
| EP1849780A1 (en) | 2006-04-21 | 2007-10-31 | De Staat der Nederlanden, vert. door de minister van VWS | Vaccine against nicotine addiction |
| JP5630998B2 (ja) | 2006-05-15 | 2014-11-26 | マサチューセッツ インスティテュート オブ テクノロジー | 機能的粒子のためのポリマー |
| US20110052697A1 (en) * | 2006-05-17 | 2011-03-03 | Gwangju Institute Of Science & Technology | Aptamer-Directed Drug Delivery |
| WO2007150030A2 (en) | 2006-06-23 | 2007-12-27 | Massachusetts Institute Of Technology | Microfluidic synthesis of organic nanoparticles |
| WO2008019142A2 (en) * | 2006-08-04 | 2008-02-14 | Massachusetts Institute Of Technology | Oligonucleotide systems for targeted intracellular delivery |
| US20080087279A1 (en) * | 2006-10-11 | 2008-04-17 | Tieck Catharine Laureen Johnso | Metered dose inhaler |
| AU2007319951A1 (en) * | 2006-11-09 | 2008-05-22 | Pfizer Products Inc. | Polymorphs of nicotinic intermediates |
| WO2008079324A1 (en) * | 2006-12-21 | 2008-07-03 | Boston Biomedical Research Institute | Immunological modulation of insulin-like growth factor 1 for cancer prevention/treatment and prolonging longevity |
| WO2008098165A2 (en) * | 2007-02-09 | 2008-08-14 | Massachusetts Institute Of Technology | Oscillating cell culture bioreactor |
| WO2008124632A1 (en) | 2007-04-04 | 2008-10-16 | Massachusetts Institute Of Technology | Amphiphilic compound assisted nanoparticles for targeted delivery |
| WO2008124634A1 (en) * | 2007-04-04 | 2008-10-16 | Massachusetts Institute Of Technology | Polymer-encapsulated reverse micelles |
| EP1982729A1 (en) * | 2007-04-20 | 2008-10-22 | Cytos Biotechnology AG | Vaccination Regimen for B-Cell Vaccines |
| AU2008257419B2 (en) * | 2007-05-23 | 2013-10-24 | The Trustees Of The University Of Pennsylvania | Targeted carriers for intracellular drug delivery |
| AU2008314647B2 (en) | 2007-10-12 | 2013-03-21 | Massachusetts Institute Of Technology | Vaccine nanotechnology |
| WO2009070533A1 (en) * | 2007-11-29 | 2009-06-04 | Complegen, Inc. | Methods of inhibiting steroyl coa desaturase |
| US8710069B2 (en) * | 2008-03-27 | 2014-04-29 | University Of Kentucky Research Foundation | Opioid-nornicotine codrugs combinations for pain management |
| US20090270264A1 (en) * | 2008-04-09 | 2009-10-29 | United States Army As Represenfed By The Secretary Of The Army, On Behalf Of Usacidc | System and method for the deconvolution of mixed dna profiles using a proportionately shared allele approach |
| US20110086063A1 (en) * | 2008-06-04 | 2011-04-14 | Cornell University | Vaccines for prevention and treatment of addiction |
| US20110182918A1 (en) | 2008-06-13 | 2011-07-28 | Nabi Biopharmaceuticals | Personalized drug treatment and smoking cessation kit and method |
| US20100009389A1 (en) * | 2008-07-14 | 2010-01-14 | Masood Unnabi Khan | Method of Making and Using Versatile Positive Controls and Antibody Detection Assays |
| WO2010042743A2 (en) * | 2008-10-08 | 2010-04-15 | Chimeros Inc. | Chimeric multiplexes, compositions, and methods for using same |
| US8343498B2 (en) * | 2008-10-12 | 2013-01-01 | Massachusetts Institute Of Technology | Adjuvant incorporation in immunonanotherapeutics |
| US8277812B2 (en) | 2008-10-12 | 2012-10-02 | Massachusetts Institute Of Technology | Immunonanotherapeutics that provide IgG humoral response without T-cell antigen |
| US8343497B2 (en) * | 2008-10-12 | 2013-01-01 | The Brigham And Women's Hospital, Inc. | Targeting of antigen presenting cells with immunonanotherapeutics |
| US8151804B2 (en) * | 2008-12-23 | 2012-04-10 | Williams Jonnie R | Tobacco curing method |
| PL222496B1 (pl) * | 2009-04-10 | 2016-08-31 | Inst Biochemii I Biofizyki Pan | Wektorowa cząsteczka wirusopodobna, sposób jej wytwarzania oraz kompozycja farmaceutyczna zawierająca wektorową cząsteczkę wirusopodobną |
| EP2421561A2 (en) * | 2009-04-21 | 2012-02-29 | Selecta Biosciences, Inc. | Immunonanotherapeutics providing a th1-biased response |
| US8629151B2 (en) | 2009-05-27 | 2014-01-14 | Selecta Biosciences, Inc. | Immunomodulatory agent-polymeric compounds |
| JP2013500988A (ja) | 2009-07-31 | 2013-01-10 | ナビ バイオファーマシューティカルズ | ニコチン中毒を処置するための方法およびキット |
| WO2011041483A2 (en) * | 2009-09-30 | 2011-04-07 | Toxcure, Inc. | Use of botulinum neurotoxin to treat substance addictions |
| WO2011050158A1 (en) | 2009-10-22 | 2011-04-28 | The Trustees Of Columbia University In The City Of New York | Anti-drug vaccines |
| US9682133B2 (en) | 2010-03-17 | 2017-06-20 | Cornell University | Disrupted adenovirus-based vaccine against drugs of abuse |
| US9801927B2 (en) | 2010-03-29 | 2017-10-31 | Centre National De La Recherche Scientifique-Cnrs | Pharmaceutical compositions comprising a polypeptide comprising at least one CXXC motif and heterologous antigens and uses thereof |
| GB201006324D0 (en) | 2010-04-15 | 2010-06-02 | Glaxosmithkline Biolog Sa | Vaccine |
| EP2575773A4 (en) | 2010-05-26 | 2014-06-25 | Selecta Biosciences Inc | SYNTHETIC NANOTRÄGERKOMBINATIONSIMPFSTOFFE |
| EP2611788B1 (en) | 2010-09-03 | 2017-04-12 | University of Florida Research Foundation, Incorporated | Nicotine compounds and analogs thereof, synthetic methods of making compounds, and methods of use |
| US20120321694A1 (en) * | 2010-10-27 | 2012-12-20 | Daniel Larocque | Compositions and uses |
| EA201390660A1 (ru) | 2010-11-05 | 2013-11-29 | Селекта Байосайенсиз, Инк. | Модифицированные никотиновые соединения и связанные способы |
| MX356426B (es) | 2011-04-04 | 2018-05-29 | Univ Iowa Res Found | Metodos para mejorar inmunogenicidad de vacuna. |
| TWI488865B (zh) * | 2011-06-16 | 2015-06-21 | Nat Univ Chung Hsing | 經改造之油體鈣蛋白(caleosins)及其用於半抗原之抗體製造 |
| CN103702687A (zh) | 2011-07-29 | 2014-04-02 | 西莱克塔生物科技公司 | 产生体液和细胞毒性t淋巴细胞(ctl)免疫应答的合成纳米载体 |
| WO2013096866A2 (en) * | 2011-12-21 | 2013-06-27 | Apse, Llc | Processes using vlps with capsids resistant to hydrolases |
| BR112014013035A2 (pt) | 2011-12-22 | 2018-10-09 | Hoffmann La Roche | métodos de seleção de células, conjuntos de expressão bicistrônica, células eucarióticas, vetores lentivirais, uso de vetor lentiviral, bibliotecas de ventores lentivirais e de células eucarióticas, métodos de seleção de células, fluxos de trabalho e uso de célula |
| US10093947B2 (en) | 2012-02-28 | 2018-10-09 | Cornell University | AAV-directed persistent expression of an anti-nicotine antibody gene for smoking cessation |
| US10004811B2 (en) | 2012-04-13 | 2018-06-26 | Cornell University | Development of a highly efficient second generation nicotine-conjugate vaccine to treat nicotine addiction |
| CN107973856B (zh) | 2012-07-04 | 2021-11-23 | 弗·哈夫曼-拉罗切有限公司 | 共价连接的抗原-抗体缀合物 |
| US9457096B2 (en) | 2012-07-06 | 2016-10-04 | Consejo Nacional De Investigaciones Cientificas Y Tecnicas (Concet) | Protozoan variant-specific surface proteins (VSP) as carriers for oral drug delivery |
| CA2912131C (en) | 2013-06-19 | 2020-07-07 | Apse, Llc | Oligonucleotides comprising capsid specific packaging sequences and methods of manufacture thereof |
| EA032441B1 (ru) * | 2013-09-05 | 2019-05-31 | Иммьюн Дизайн Корп. | Вакцинные композиции против никотиновой зависимости |
| PL3089996T3 (pl) | 2014-01-03 | 2021-12-13 | F. Hoffmann-La Roche Ag | Dwuswoiste przeciwciała przeciw haptenowi/przeciw receptorowi występującemu w barierze krew-mózg, ich kompleksy i ich zastosowanie jako przenośniki wahadłowe występujące w barierze krew-mózg |
| EP3089759B1 (en) | 2014-01-03 | 2018-12-05 | F. Hoffmann-La Roche AG | Covalently linked polypeptide toxin-antibody conjugates |
| RU2694981C2 (ru) | 2014-01-03 | 2019-07-18 | Ф. Хоффманн-Ля Рош Аг | Ковалентно связанные конъюгаты хеликар-антитело против хеликара и их применения |
| US10780054B2 (en) | 2015-04-17 | 2020-09-22 | Curevac Real Estate Gmbh | Lyophilization of RNA |
| CN107921237A (zh) | 2015-04-27 | 2018-04-17 | 反射医学公司 | 交感神经心肺神经调节系统和方法 |
| US10729654B2 (en) | 2015-05-20 | 2020-08-04 | Curevac Ag | Dry powder composition comprising long-chain RNA |
| CN104897864B (zh) * | 2015-06-18 | 2016-08-31 | 北京勤邦生物技术有限公司 | 检测金刚烷胺的酶联免疫试剂盒及其应用 |
| WO2017139487A1 (en) | 2016-02-09 | 2017-08-17 | Northwind Medical, Inc. | Methods, agents, and devices for local neuromodulation of autonomic nerves |
| AU2017290353B2 (en) | 2016-06-29 | 2023-05-18 | Tulavi Therapeutics, Inc. | Treatment of sepsis and related inflammatory conditions by local neuromodulation of the autonomic nervous system |
| EP4070815A1 (en) * | 2016-10-03 | 2022-10-12 | The U.S.A. as represented by the Secretary, Department of Health and Human Services | Hiv-1 env fusion peptide immunogens and their use |
| CN107501409A (zh) * | 2017-09-06 | 2017-12-22 | 杨蕾 | 一种尿酸人工抗原的制备方法 |
| GB2571696B (en) | 2017-10-09 | 2020-05-27 | Compass Pathways Ltd | Large scale method for the preparation of Psilocybin and formulations of Psilocybin so produced |
| CN107982517B (zh) * | 2017-12-15 | 2020-03-06 | 苏州科技城医院 | 治疗心肌缺血型慢性心力衰竭的西药复方组合物 |
| CN117598837A (zh) | 2018-07-02 | 2024-02-27 | 图拉维治疗股份有限公司 | 原位形成神经帽的方法和装置 |
| US20210315587A1 (en) | 2018-07-02 | 2021-10-14 | Tulavi Therapeutics, Inc. | Methods and devices for in situ formed nerve cap with rapid release |
| CN109884021A (zh) * | 2019-03-29 | 2019-06-14 | 铁道警察学院 | 一种量子点标记的thc包被抗原、其制备方法及利用其检测食品中大麻含量的方法 |
| KR20220009954A (ko) | 2019-04-17 | 2022-01-25 | 컴퍼스 패쓰파인더 리미티드 | 신경인지 장애, 만성 통증을 치료하고 염증을 감소시키는 방법 |
| WO2021178257A1 (en) * | 2020-03-02 | 2021-09-10 | Unm Rainforest Innovations | Virus-like particle vaccines for opioid drugs |
| EP4141110A1 (en) | 2020-04-24 | 2023-03-01 | Obshchestvo S Ogranichennoy Otvetstvennost'yu "Ingenik" | Method for producing particles of bacteriophages of the genus levivirus |
| KR20240096817A (ko) | 2020-05-19 | 2024-06-26 | 사이빈 아이알엘 리미티드 | 중수소화된 트립타민 유도체 및 사용 방법 |
| EP4157348A4 (en) * | 2020-05-27 | 2024-06-19 | Behnam, Babak | COMPOSITIONS AND METHODS FOR THE TREATMENT OF MORPHINE, HEROIN AND ALCOHOL DEPENDENCE |
| CN114344288B (zh) * | 2022-01-25 | 2023-07-04 | 深圳技术大学 | 盐酸多塞平在制备抗病毒药物中的应用 |
Family Cites Families (93)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US81295A (en) * | 1868-08-18 | bob in son | ||
| US64529A (en) * | 1867-05-07 | hellen | ||
| US388866A (en) | 1888-09-04 | O o o o o o oop o o q o o q q | ||
| US175290A (en) * | 1876-03-28 | Improvement in rotary postmarking and canceling presses | ||
| US175711A (en) * | 1876-04-04 | Improvement in bale-ties | ||
| US64533A (en) * | 1867-05-07 | William s | ||
| US157479A (en) * | 1874-12-08 | Improvement in fire-proof shutters | ||
| US3885046A (en) | 1969-12-04 | 1975-05-20 | Burroughs Wellcome Co | Meta chloro or fluoro substituted alpha-T-butylaminopropionphenones in the treatment of depression |
| BE759838A (fr) | 1969-12-04 | 1971-06-03 | Wellcome Found | Cetones a activite biologique |
| US4045420A (en) | 1973-05-29 | 1977-08-30 | Syva Company | Non-oxo-carbonyl containing benzoyl ecgonine and cocaine compounds polypeptide and derivatives thereof |
| US4197237A (en) * | 1973-06-01 | 1980-04-08 | Syva Company | Antibodies to nitrogen derivatives of benzoyl ecgonine antigenic conjugates thereof |
| US3888866A (en) * | 1973-06-01 | 1975-06-10 | Syva Co | Nitrogen derivatives of benzoyl ecgonine |
| US4722840A (en) * | 1984-09-12 | 1988-02-02 | Chiron Corporation | Hybrid particle immunogens |
| CA1319101C (en) | 1986-09-03 | 1993-06-15 | Marta Iris Sabara | Rotavirus nucleocapsid protein with or without binding peptides as immunologic carriers for macromolecules |
| US5374426A (en) * | 1986-09-03 | 1994-12-20 | University Of Saskatchewan | Rotavirus nucleocapsid protein VP6 in vaccine compositions |
| WO1988001873A1 (en) | 1986-09-22 | 1988-03-24 | Emory University | Vaccine and method of preparation |
| US5143726A (en) * | 1986-12-09 | 1992-09-01 | The Scripps Research Institute | T cell epitopes of the hepatitis B virus nucleocapsid protein |
| US4918166A (en) * | 1987-04-10 | 1990-04-17 | Oxford Gene Systems Limited | Particulate hybrid HIV antigens |
| US5057540A (en) | 1987-05-29 | 1991-10-15 | Cambridge Biotech Corporation | Saponin adjuvant |
| US4788189A (en) | 1988-02-29 | 1988-11-29 | Glazer Howard I | Method to treat smoking withdrawal symptoms by potentiated central noradrenergic blocking |
| JPH0656106B2 (ja) | 1988-10-29 | 1994-07-27 | マツダ株式会社 | 過給機付エンジンの吸気装置 |
| CA2005726A1 (en) * | 1988-12-21 | 1990-06-21 | Haruo Tomita | Thermoplastic resin composition |
| GB8903313D0 (en) | 1989-02-14 | 1989-04-05 | Wellcome Found | Conjugates |
| US5703055A (en) * | 1989-03-21 | 1997-12-30 | Wisconsin Alumni Research Foundation | Generation of antibodies through lipid mediated DNA delivery |
| DE69018926T2 (de) | 1989-09-04 | 1995-08-24 | Wellcome Found | Vakzine gegen Bordetella. |
| DE69120146T2 (de) * | 1990-01-12 | 1996-12-12 | Cell Genesys Inc | Erzeugung xenogener antikörper |
| GB9001694D0 (en) | 1990-01-25 | 1990-03-28 | Therapeutic Antibodies Inc | Immunogenic compositions |
| US5334394A (en) | 1990-06-22 | 1994-08-02 | The Regents Of The University Of California | Human immunodeficiency virus decoy |
| US5178882A (en) | 1990-06-22 | 1993-01-12 | The Regents Of The University Of California | Viral decoy vaccine |
| US6699474B1 (en) * | 1990-08-20 | 2004-03-02 | Erich Hugo Cerny | Vaccine and immunserum against drugs of abuse |
| CH678394A5 (zh) | 1990-08-22 | 1991-09-13 | Cerny Erich H | |
| SE9003978D0 (sv) * | 1990-12-13 | 1990-12-13 | Henrik Garoff | Dna expressionssystem baserade paa ett virus replikon |
| EP0563091A1 (en) | 1990-12-20 | 1993-10-06 | SMITHKLINE BEECHAM BIOLOGICALS s.a. | Vaccines based on hepatitis b surface antigen |
| GB9101550D0 (en) * | 1991-01-24 | 1991-03-06 | Mastico Robert A | Antigen-presenting chimaeric protein |
| AU1992592A (en) | 1991-05-24 | 1993-01-08 | Pharmavene, Inc. | Treatment of drug withdrawal symptoms and drug craving with type b monoamine oxidase inhibitors |
| GB9114003D0 (en) | 1991-06-28 | 1991-08-14 | Mastico Robert A | Chimaeric protein |
| US5232082A (en) * | 1992-01-28 | 1993-08-03 | Philip Morris Incorporated | Pinless belt feeder |
| FR2713225B1 (fr) | 1993-12-02 | 1996-03-01 | Sanofi Sa | N-pipéridino-3-pyrazolecarboxamide substitué. |
| FR2692575B1 (fr) | 1992-06-23 | 1995-06-30 | Sanofi Elf | Nouveaux derives du pyrazole, procede pour leur preparation et compositions pharmaceutiques les contenant. |
| US6004763A (en) * | 1992-09-11 | 1999-12-21 | Institut Pasteur | Antigen-carrying microparticles and their use in the induction of humoral or cellular responses |
| FR2695563B1 (fr) | 1992-09-11 | 1994-12-02 | Pasteur Institut | Microparticules portant des antigènes et leur utilisation pour l'induction de réponses humorales ou cellulaires. |
| DK0678034T3 (da) * | 1993-01-11 | 1999-11-08 | Dana Farber Cancer Inst Inc | Induktion af cytotoksiske T-lymfocytreaktioner |
| US6210677B1 (en) * | 1993-01-29 | 2001-04-03 | Robert C. Bohannon | Method to reduce the physiologic effects of drugs on mammals |
| WO1994017813A1 (en) | 1993-02-08 | 1994-08-18 | Paravax, Inc. | Defective sindbis virus vectors that express toxoplasma gondii p30 antigens |
| US5506268A (en) | 1993-06-11 | 1996-04-09 | Nps Pharmaceuticals, Inc. | Use of isovaleramide as a mild anxiolytic and sedative agent |
| US6015686A (en) | 1993-09-15 | 2000-01-18 | Chiron Viagene, Inc. | Eukaryotic layered vector initiation systems |
| US5596106A (en) | 1994-07-15 | 1997-01-21 | Eli Lilly And Company | Cannabinoid receptor antagonists |
| AT402898B (de) | 1994-08-08 | 1997-09-25 | Int Centre Genetic Eng & Bio | Molekulares präsentiersystem |
| US5876727A (en) | 1995-03-31 | 1999-03-02 | Immulogic Pharmaceutical Corporation | Hapten-carrier conjugates for use in drug-abuse therapy and methods for preparation of same |
| DE69637089T2 (de) * | 1995-03-31 | 2008-01-17 | Xenova Research Ltd., Slough | Hapten-Träger-Konjugate zur Anwendung in der Drogen-Missbrauchs-Therapie |
| CN1185811A (zh) | 1995-03-31 | 1998-06-24 | H·沃尔夫 | 依赖于逆转录病毒样颗粒的抗原呈递系统 |
| US5792462A (en) | 1995-05-23 | 1998-08-11 | University Of North Carolina At Chapel Hill | Alphavirus RNA replicon systems |
| RU2193413C2 (ru) | 1996-03-01 | 2002-11-27 | Новартис Аг | Пептидные иммуногены для вакцинации и лечения аллергии |
| EP0828489A4 (en) | 1996-03-13 | 2001-04-04 | Univ Yale | Smoking cessation treatment using naltrexone and related compounds |
| US5770380A (en) | 1996-09-13 | 1998-06-23 | University Of Pittsburgh | Synthetic antibody mimics--multiple peptide loops attached to a molecular scaffold |
| GB9621091D0 (en) | 1996-10-09 | 1996-11-27 | Fondation Pour Le Perfectionem | Attenuated microorganisms strains and their uses |
| CA2297786C (en) | 1997-08-05 | 2011-06-14 | Vlaams Interuniversitair Instituut Voor Biotechnologie | New immunoprotective influenza antigen and its use in vaccination |
| US6169175B1 (en) | 1997-08-06 | 2001-01-02 | Centers For Disease Control And Prevention | Preparation and use of recombinant influenza A virus M2 construct vaccines |
| US6054312A (en) * | 1997-08-29 | 2000-04-25 | Selective Genetics, Inc. | Receptor-mediated gene delivery using bacteriophage vectors |
| AU750808B2 (en) | 1997-10-03 | 2002-07-25 | Cary Medical Corporation | Compositon for the treatment of nicotine addiction containing a nicotine receptor antagonist and an anti-depressant or anti-anxiety drug |
| US6605610B1 (en) | 1997-12-31 | 2003-08-12 | Pfizer Inc | Aryl fused azapolycyclic compounds |
| TR200002338T2 (tr) | 1998-02-12 | 2002-06-21 | Immune Complex Corporation | Stratejik olarak yenilenmiş hepatit B çekirdek proteinler. |
| US5990085A (en) | 1998-05-04 | 1999-11-23 | Michigan State University | Inhibin-HBc fusion protein |
| SE9801923D0 (sv) * | 1998-05-29 | 1998-05-29 | Independent Pharmaceutical Ab | Nicotine vaccine |
| TWI227241B (en) | 1998-06-20 | 2005-02-01 | United Biomedical Inc | IgE-CH3 domain antigen peptide, peptide conjugate containing the same, and pharmaceutical composition for treating allergies containing the peptide conjugate |
| US6231964B1 (en) * | 1998-06-30 | 2001-05-15 | Ncr Corporation | Thermal transfer ribbons with large size wax or resin particles |
| AU761396B2 (en) | 1998-06-30 | 2003-06-05 | Om Pharma | Novel acyl pseudodipeptides, preparation method and pharmaceutical compositions containing same |
| ATE314095T1 (de) | 1998-10-21 | 2006-01-15 | Us Health | Virusähnliche partikel zur induktion von autoantikörpern |
| US6380364B1 (en) * | 1998-11-23 | 2002-04-30 | Loyola University Of Chicago | Chimeric biotin-binding papillomavirus protein |
| NZ512456A (en) | 1998-11-30 | 2003-10-31 | Cytos Biotechnology Ag | Ordered molecular presentation of antigens |
| US6232082B1 (en) * | 1998-12-01 | 2001-05-15 | Nabi | Hapten-carrier conjugates for treating and preventing nicotine addiction |
| CZ20011907A3 (cs) | 1998-12-04 | 2002-01-16 | Biogen, Inc. | Částice jádra HBV s imunogenními sloľkami navázanými prostřednictvím peptidových ligandů |
| NZ513680A (en) | 1999-02-25 | 2001-09-28 | Peptide Therapeutics Ltd | Epitodes or mimotopes derived from the c-epsilon-3 or c-epsilon-4 domains of IgE, antagonists thereof, and their therapeutic uses |
| FR2790474B1 (fr) | 1999-03-05 | 2001-04-06 | Synthelabo | Derives de pyridopyranoazepines, leur preparation et leur application en therapeutique |
| JP2002541156A (ja) | 1999-04-07 | 2002-12-03 | トーマス・ジェファーソン・ユニバーシティー | ケモカイン由来合成ペプチド |
| EP1078632A1 (en) | 1999-08-16 | 2001-02-28 | Sanofi-Synthelabo | Use of monoamine oxydase inhibitors for the manufacture of drugs intended for the treatment of obesity |
| BR0108566A (pt) | 2000-02-21 | 2002-11-19 | Pharmexa As | Método para a regulação negativa in vivo de proteìna amilóide em um animal, incluindo um ser humano e para o tratamento e/ou prevenção e/ou melhora da doença de alzheimer ou outras doenças e condições cartacterizadas por depósitos de amilóide, análogo de um polipeptìdeo amiloidogênico,composição imunogênica, fragmento de ácido nucleico, vetor, célula transformada, composição para induzir a produção de anticorpos contra um polipeptìdeo amiloidogênico, linhagem celular estável, métodos para a preparação de uma célula, para a identificação de um polipeptìdeo amiloidogênico modificado, e para preparação de uma composição imunogênica, uso de um polipeptìdeo amiloidogênico ou de uma subsequência do mesmo, e, uso de um análogo de um polipeptìdeo amiloidogênico |
| KR100808313B1 (ko) | 2000-04-07 | 2008-02-27 | 유니버시티 오브 리즈 이노베이션즈 리미티드 | 비형 간염 코어 항원 융합 단백질 |
| WO2001085208A2 (en) | 2000-05-05 | 2001-11-15 | Cytos Biotechnology Ag | Molecular antigen arrays and vaccines |
| JP2004500868A (ja) | 2000-06-22 | 2004-01-15 | セルテック ファーマスーティカルズ リミテッド | B型肝炎コア抗原の修飾 |
| US20030138769A1 (en) | 2000-08-16 | 2003-07-24 | Birkett Ashley J. | Immunogenic HBc chimer particles having enhanced stability |
| US7128911B2 (en) | 2001-01-19 | 2006-10-31 | Cytos Biotechnology Ag | Antigen arrays for treatment of bone disease |
| US7264810B2 (en) | 2001-01-19 | 2007-09-04 | Cytos Biotechnology Ag | Molecular antigen array |
| US7094409B2 (en) | 2001-01-19 | 2006-08-22 | Cytos Biotechnology Ag | Antigen arrays for treatment of allergic eosinophilic diseases |
| WO2002058635A2 (en) | 2001-01-26 | 2002-08-01 | The Scripps Research Institute | Nicotine immunogens and antibodies and uses thereof |
| US7115266B2 (en) * | 2001-10-05 | 2006-10-03 | Cytos Biotechnology Ag | Angiotensin peptide-carrier conjugates and uses thereof |
| FR2831883B1 (fr) | 2001-11-08 | 2004-07-23 | Sanofi Synthelabo | Forme polymorphe du rimonabant, son procede de preparation et les compositions pharmaceutiques en contenant |
| US20030219459A1 (en) | 2002-01-18 | 2003-11-27 | Cytos Biotechnology Ag | Prion protein carrier-conjugates |
| US20050089524A1 (en) * | 2002-03-01 | 2005-04-28 | Sanderson Sam D. | Compositions and compounds for use as molecular adjuvant for a nicotine vaccine |
| BR0312935A (pt) * | 2002-07-17 | 2005-06-21 | Cytos Biotechnology Ag | Partìcula semelhante a vìrus, muteìna, vetores para produzir a referida partìcula e proteìna recombinante, composição, processo para produção de fileira ordena e repetitva de antìgeno, molécula de ácido nucléico, célula hospedeira, método para produção da referida partìcula e uso da composição de vacina |
| BR0312297A (pt) * | 2002-07-18 | 2005-04-12 | Cytos Biotechnology Ag | Conjugados veìculos de hapteno e seu uso |
| NZ537688A (en) | 2002-07-19 | 2007-01-26 | Cytos Biotechnology Ag | Vaccine compositions containing amyloid beta1-6 antigen arrays for treating and/or attenuating Alzheimer's disease |
| JP2006504653A (ja) | 2002-07-19 | 2006-02-09 | サイトス バイオテクノロジー アーゲー | グレリン−担体複合体 |
-
2003
- 2003-07-18 BR BR0312297-2A patent/BR0312297A/pt not_active IP Right Cessation
- 2003-07-18 CN CN2009101392979A patent/CN101574518B/zh not_active Expired - Fee Related
- 2003-07-18 EP EP03765047A patent/EP1523334A2/en not_active Withdrawn
- 2003-07-18 EP EP11004588A patent/EP2392345A3/en not_active Withdrawn
- 2003-07-18 IL IL16524903A patent/IL165249A0/xx unknown
- 2003-07-18 MX MXPA04012010A patent/MXPA04012010A/es active IP Right Grant
- 2003-07-18 KR KR1020127002278A patent/KR20120041739A/ko not_active Application Discontinuation
- 2003-07-18 CA CA002487849A patent/CA2487849A1/en not_active Abandoned
- 2003-07-18 AU AU2003250106A patent/AU2003250106B2/en not_active Ceased
- 2003-07-18 IN IN5409CHN2008 patent/IN2008CN05409A/en unknown
- 2003-07-18 US US10/622,064 patent/US6932971B2/en not_active Expired - Fee Related
- 2003-07-18 CN CNB038167484A patent/CN100518823C/zh not_active Expired - Fee Related
- 2003-07-18 KR KR1020047020001A patent/KR101228376B1/ko not_active IP Right Cessation
- 2003-07-18 RU RU2005104430/15A patent/RU2326693C2/ru not_active IP Right Cessation
- 2003-07-18 WO PCT/EP2003/007850 patent/WO2004009116A2/en active Application Filing
- 2003-07-18 NZ NZ537003A patent/NZ537003A/en not_active IP Right Cessation
- 2003-07-18 PL PL03375598A patent/PL375598A1/xx not_active Application Discontinuation
- 2003-07-18 JP JP2004522508A patent/JP5084103B2/ja not_active Expired - Fee Related
-
2004
- 2004-11-22 ZA ZA200409389A patent/ZA200409389B/en unknown
-
2005
- 2005-05-10 US US11/125,402 patent/US7452541B2/en not_active Expired - Fee Related
-
2008
- 2008-01-18 RU RU2008101922/13A patent/RU2008101922A/ru not_active Application Discontinuation
- 2008-10-08 US US12/285,576 patent/US8187607B2/en not_active Expired - Fee Related
-
2012
- 2012-05-21 US US13/476,685 patent/US20130142821A1/en not_active Abandoned
Cited By (15)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN103230590A (zh) * | 2005-09-28 | 2013-08-07 | 赛托斯生物技术公司 | 白介素-1偶联物及其用途 |
| CN101443038B (zh) * | 2006-05-12 | 2012-07-04 | 希托斯生物技术股份公司 | 尼古丁-载体疫苗制剂 |
| CN102119155A (zh) * | 2008-08-08 | 2011-07-06 | 诺瓦提斯公司 | 制备基于烟碱的半抗原的方法 |
| CN102245200A (zh) * | 2008-10-12 | 2011-11-16 | 麻省理工学院 | 尼古丁免疫纳米疗法 |
| CN101413946B (zh) * | 2008-10-31 | 2012-08-08 | 江南大学 | 一种盐酸西布曲明的酶联免疫检测方法 |
| CN104080479A (zh) * | 2011-11-07 | 2014-10-01 | 诺华股份有限公司 | 包括spr0096和spr2021抗原的运载体分子 |
| CN104411336A (zh) * | 2012-06-28 | 2015-03-11 | 辉瑞公司 | 抗托法替尼抗体及其用于药物监测的用途 |
| CN108884127A (zh) * | 2016-01-21 | 2018-11-23 | 斯克利普斯研究院 | 合成的阿片类疫苗 |
| CN106905434A (zh) * | 2017-02-28 | 2017-06-30 | 国药中生生物技术研究院有限公司 | 一种包含蹄蝠肝炎病毒核心蛋白的重组融合蛋白及其制备方法和应用 |
| CN106905434B (zh) * | 2017-02-28 | 2021-01-26 | 国药中生生物技术研究院有限公司 | 一种包含蹄蝠肝炎病毒核心蛋白的重组融合蛋白及其制备方法和应用 |
| CN111363011A (zh) * | 2020-03-13 | 2020-07-03 | 北京大学 | 一种甲基苯丙胺疫苗及其制备方法与应用 |
| CN112924665A (zh) * | 2021-02-19 | 2021-06-08 | 山东莱博生物科技有限公司 | 一种抗体辣根过氧化物酶标记物及其制备与应用 |
| CN112924665B (zh) * | 2021-02-19 | 2023-10-03 | 山东莱博生物科技有限公司 | 一种抗体辣根过氧化物酶标记物及其制备与应用 |
| CN114907255A (zh) * | 2022-04-25 | 2022-08-16 | 杭州同舟生物技术有限公司 | 一种利他林人工半抗原、人工抗原及其制备方法和应用 |
| CN116283885A (zh) * | 2022-12-01 | 2023-06-23 | 杭州奥泰生物技术股份有限公司 | 一种帕罗西汀半抗原和人工抗原及其制备方法与应用 |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN101574518B (zh) | 半抗原-载体偶联物及其用途 | |
| CA2489410C (en) | Molecular antigen arrays | |
| CN1301132C (zh) | 分子抗原阵列 | |
| CA2462857C (en) | Angiotensin peptide-carrier conjugates and uses thereof | |
| CN1321695C (zh) | 用于治疗变应性嗜酸细胞性疾病的展示il-5、il-3或嗜酸细胞活化趋化因子的抗原阵列 | |
| CN1662253A (zh) | 用作佐剂的包装的病毒样颗粒:制备方法与用途 | |
| US20030157479A1 (en) | Antigen arrays for treatment of allergic eosinophilic diseases | |
| CN1665565A (zh) | Ghrelin-载体偶联物 | |
| CN1599623A (zh) | 免疫刺激物向病毒样颗粒内的包装:制备方法与用途 | |
| CN1764719A (zh) | Melan-a肽类似物-病毒样颗粒偶联物 | |
| JP2008513035A (ja) | Ap205のコートタンパク質と抗原性ポリペプチドとの融合タンパク質を含んでなるウイルス粒子 | |
| CN101076352A (zh) | Il-15抗原阵列及其用途 | |
| CN1905903A (zh) | 生长素释放肽-载体偶联物 | |
| CN101023103A (zh) | 包含ap205外壳蛋白和抗原性多肽的融合蛋白的病毒样颗粒 | |
| US20030219459A1 (en) | Prion protein carrier-conjugates | |
| CN1582164A (zh) | 用于治疗骨病的抗原阵列 | |
| US8088392B2 (en) | Capsid proteins and uses therefore | |
| CN101193654A (zh) | 抗原偶联物及其用途 | |
| KR101015508B1 (ko) | 안지오텐신 펩티드-캐리어-컨쥬게이트 및 그의 용도 | |
| CN101049502A (zh) | 用于治疗变应性嗜酸细胞性疾病的展示il-5、il-3或嗜酸细胞活化趋化因子的抗原阵列 | |
| CN100589842C (zh) | 分子抗原阵列 | |
| KR20070057921A (ko) | Ap205의 외피 단백질 및 항원 폴리펩타이드의 융합단백질을 포함하는 바이러스 유사 입자 | |
| KR20050020790A (ko) | 애주번트로서 사용하기 위한 패킹된 바이러스-양 입자,제조 방법 및 용도 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| C14 | Grant of patent or utility model | ||
| GR01 | Patent grant | ||
| C17 | Cessation of patent right | ||
| CF01 | Termination of patent right due to non-payment of annual fee |
Granted publication date: 20090729 Termination date: 20130718 |