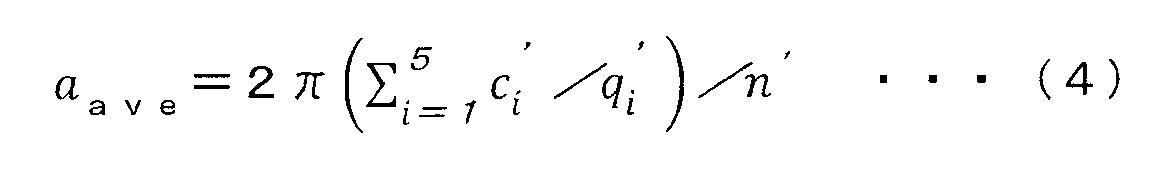WO2019135348A1 - 固体電解質材料、および、電池 - Google Patents
固体電解質材料、および、電池 Download PDFInfo
- Publication number
- WO2019135348A1 WO2019135348A1 PCT/JP2018/046264 JP2018046264W WO2019135348A1 WO 2019135348 A1 WO2019135348 A1 WO 2019135348A1 JP 2018046264 W JP2018046264 W JP 2018046264W WO 2019135348 A1 WO2019135348 A1 WO 2019135348A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- range
- peak
- solid electrolyte
- value
- electrolyte material
- Prior art date
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01G—COMPOUNDS CONTAINING METALS NOT COVERED BY SUBCLASSES C01D OR C01F
- C01G25/00—Compounds of zirconium
- C01G25/006—Compounds containing, besides zirconium, two or more other elements, with the exception of oxygen or hydrogen
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01F—COMPOUNDS OF THE METALS BERYLLIUM, MAGNESIUM, ALUMINIUM, CALCIUM, STRONTIUM, BARIUM, RADIUM, THORIUM, OR OF THE RARE-EARTH METALS
- C01F17/00—Compounds of rare earth metals
- C01F17/30—Compounds containing rare earth metals and at least one element other than a rare earth metal, oxygen or hydrogen, e.g. La4S3Br6
- C01F17/36—Compounds containing rare earth metals and at least one element other than a rare earth metal, oxygen or hydrogen, e.g. La4S3Br6 halogen being the only anion, e.g. NaYF4
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01G—COMPOUNDS CONTAINING METALS NOT COVERED BY SUBCLASSES C01D OR C01F
- C01G29/00—Compounds of bismuth
- C01G29/006—Compounds containing, besides bismuth, two or more other elements, with the exception of oxygen or hydrogen
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01G—COMPOUNDS CONTAINING METALS NOT COVERED BY SUBCLASSES C01D OR C01F
- C01G33/00—Compounds of niobium
- C01G33/006—Compounds containing, besides niobium, two or more other elements, with the exception of oxygen or hydrogen
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01G—COMPOUNDS CONTAINING METALS NOT COVERED BY SUBCLASSES C01D OR C01F
- C01G35/00—Compounds of tantalum
- C01G35/006—Compounds containing, besides tantalum, two or more other elements, with the exception of oxygen or hydrogen
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01G—COMPOUNDS CONTAINING METALS NOT COVERED BY SUBCLASSES C01D OR C01F
- C01G9/00—Compounds of zinc
- C01G9/006—Compounds containing, besides zinc, two ore more other elements, with the exception of oxygen or hydrogen
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01B—CABLES; CONDUCTORS; INSULATORS; SELECTION OF MATERIALS FOR THEIR CONDUCTIVE, INSULATING OR DIELECTRIC PROPERTIES
- H01B1/00—Conductors or conductive bodies characterised by the conductive materials; Selection of materials as conductors
- H01B1/06—Conductors or conductive bodies characterised by the conductive materials; Selection of materials as conductors mainly consisting of other non-metallic substances
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/052—Li-accumulators
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/052—Li-accumulators
- H01M10/0525—Rocking-chair batteries, i.e. batteries with lithium insertion or intercalation in both electrodes; Lithium-ion batteries
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/056—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes
- H01M10/0561—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes the electrolyte being constituted of inorganic materials only
- H01M10/0562—Solid materials
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/62—Selection of inactive substances as ingredients for active masses, e.g. binders, fillers
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2002/00—Crystal-structural characteristics
- C01P2002/70—Crystal-structural characteristics defined by measured X-ray, neutron or electron diffraction data
- C01P2002/72—Crystal-structural characteristics defined by measured X-ray, neutron or electron diffraction data by d-values or two theta-values, e.g. as X-ray diagram
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2002/00—Crystal-structural characteristics
- C01P2002/70—Crystal-structural characteristics defined by measured X-ray, neutron or electron diffraction data
- C01P2002/74—Crystal-structural characteristics defined by measured X-ray, neutron or electron diffraction data by peak-intensities or a ratio thereof only
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2004/00—Particle morphology
- C01P2004/60—Particles characterised by their size
- C01P2004/61—Micrometer sized, i.e. from 1-100 micrometer
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2006/00—Physical properties of inorganic compounds
- C01P2006/40—Electric properties
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M2300/00—Electrolytes
- H01M2300/0017—Non-aqueous electrolytes
- H01M2300/0065—Solid electrolytes
- H01M2300/0068—Solid electrolytes inorganic
- H01M2300/008—Halides
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/10—Energy storage using batteries
Definitions
- the present disclosure relates to solid electrolyte materials and batteries.
- Patent Document 1 discloses an all-solid-state battery using a sulfide solid electrolyte.
- Non-Patent Document 1 discloses Li 3 YCl 6 .
- Non-Patent Document 2 discloses Li 3 YBr 6 .
- the solid electrolyte material in one aspect of the present disclosure is composed of Li, M and X.
- the M is at least one selected from metal elements
- the X is at least one selected from the group consisting of Cl, Br, and I.
- the plurality of sublattices of the atoms of X have a close-packed structure.
- the average value of the distance between two adjacent X atoms among the plurality of X atoms is the distance between two adjacent X atoms in a rock salt structure consisting of only Li and X. In comparison, it is longer than 1.8%.
- a solid electrolyte material having high lithium ion conductivity can be realized.
- FIG. 1 is a cross-sectional view showing a schematic configuration of a battery in the third embodiment.
- FIG. 2 is a schematic view showing a method of evaluating the ion conductivity.
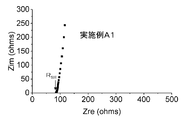
- FIG. 3 is a graph showing evaluation results of ion conductivity by AC impedance measurement.
- FIG. 4A is a graph showing an XRD pattern in Example A1-A11.
- FIG. 4B is a graph showing an XRD pattern in Example A1-A11.
- FIG. 5 is a graph showing initial discharge characteristics.
- FIG. 6A is a graph showing an XRD pattern in Example B1-B13.
- FIG. 6B is a graph showing an XRD pattern in Example B1-B13.
- FIG. 7A is a graph showing an XRD pattern in Comparative Example 1-3.
- FIG. 7B is a graph showing an XRD pattern in Comparative Example 1-3.
- FIG. 8 is a graph showing the relationship between the lithium ion conductivity and a ave / a LiX in Examples A1-A11 and B1-B13 and Comparative Example 1-3.
- the solid electrolyte material in the first embodiment is a material composed of Li and M which are cations and X which is an anion.
- M is at least one selected from metal elements.
- X is at least one selected from the group consisting of Cl, Br, and I.
- the plurality of sublattices of the atoms of X contained in the solid electrolyte material in Embodiment 1 have a close-packed structure.
- the average value of the distance between two adjacent atoms of X among the plurality of atoms of X is adjacent to each other in a rock salt structure formed only of Li and X 1.8% or more longer than the distance between the two X atoms.
- halide solid electrolytic material which is a solid electrolyte material having high lithium ion conductivity.
- the solid electrolyte material of Embodiment 1 it is possible to realize an all-solid secondary battery not containing sulfur. That is, the solid electrolyte material of Embodiment 1 is not a configuration that generates hydrogen sulfide when exposed to the air (for example, the configuration of Patent Document 1). Therefore, it is possible to realize an all-solid secondary battery excellent in safety without generating hydrogen sulfide.
- the first conversion pattern obtained by converting the X-ray diffraction pattern of the solid electrolyte material in Embodiment 1 so that the horizontal axis changes from the diffraction angle 2 ⁇ to q has a value of q of 2. to 11 ⁇ -1 or higher 2.31A -1 within at which the range or less, including the reference peak.
- q 4 ⁇ sin ⁇ / ⁇ , where ⁇ is the wavelength of the X-ray.
- the second conversion pattern obtained by converting the X-ray diffraction pattern so that the horizontal axis is a diffraction angle 2 ⁇ to q / q 2 has a value of q / q 2 of 0.50 or more and 0. 0. 0.
- a first range of 52 or less in a second range in which the value of q / q 2 is 1.28 or more and 1.30 or less, and in a range of 1.51 or more and 1.54 or less of the value of q / q 2
- the peak is included in at least one selected from the group consisting of a third range.
- q 2 is the value of q corresponding to the reference peak in the first conversion pattern.
- the solid electrolyte material in the first embodiment is May be satisfied.
- q 1 is the value of the q of the peak included in the first range.
- q 2 is the value of q 2 described above.
- q 3 is the value of the q of the peaks included in the second range.
- q 4 is the value of the q of the peak included in the third range.
- a LiX in the formula (1) is It is.
- the solid electrolyte material in the first embodiment may include the first crystal phase.
- the first crystal phase include crystal phases from which the above-described characteristic diffraction pattern can be obtained.
- the solid electrolyte material in Embodiment 1 may contain the first crystal phase.
- the first crystal phase from which the above-mentioned characteristic diffraction pattern is obtained is a structure in which the anion sublattice has a hexagonal close-packed structure or an atomic arrangement in which the hexagonal close-packed structure is distorted, and Li and halogen
- the average distance between anions is extended by 1.8% or more compared to crystals of rock salt structure consisting of Usually, it was thought that high ion conduction did not occur when the anion exhibited a close-packed structure (Nature Materials 14, 1026-1031 (2015)).
- the first crystal phase from which the above-mentioned characteristic diffraction pattern is obtained is not limited to a specific crystal structure, but includes, for example, the crystal structures as follows.
- LEC Li 3 ErCl 6
- LYC Li 3 YbCl 6 having a crystal structure belonging to the structural or space group Pnma
- ICSD inorganic crystal structure database
- the solid electrolyte material in the first embodiment may include a heterogeneous crystal phase having a crystal structure different from that of the first crystal phase.
- a weighted average of equivalent peaks may be taken when virtually higher-order symmetry is considered.
- the LYC structure described above is a cuboidal crystal structure, but focusing on only the arrangement of the anions, it is considered that the hexagonal close-packed structure is distorted as described above.
- the (401) plane and the (231) plane of the LYC structure are all approximately equivalent to the (101) plane in the hexagonal close-packed structure. Therefore, when diffraction peaks from the (401) plane and the (231) plane can be separated, the value of q x may be obtained from a weighted average weighted by both peak intensities.
- the number of moles of cations may be smaller than the number of moles of anions. Thereby, empty sites for lithium ion conduction are formed, and the ion conductivity is improved.
- the solid electrolyte material in the second embodiment further includes the following configuration in addition to the configuration of the solid electrolyte material in the first embodiment described above.
- the first conversion pattern obtained by converting the X-ray diffraction pattern of the solid electrolyte material according to the second embodiment so that the horizontal axis is the diffraction angle 2 ⁇ to q has a value of q of 1.76 ⁇ ⁇ .
- the reference peak is included in the range of 1 or more and 2.18 ⁇ ⁇ 1 or less.
- q 4 ⁇ sin ⁇ / ⁇ , where ⁇ is the wavelength of the X-ray.
- the second conversion pattern obtained by converting the X-ray diffraction pattern so that the horizontal axis is a diffraction angle 2 ⁇ to q / q 1 ′ has a value of q / q 1 ′ of 1.14 or more Within the first range of 1.17 or less, within the second range of the value of q / q 1 ′ of from 1.62 to 1.65, the value of q / q 1 ′ of from 1.88 to 1.
- the peak is included in at least one selected from the group consisting of the third range of 94 or less and the fourth range of the q / q 1 ′ value of 1.9 or more and 2.1 or less.
- q 1 ′ is the value of q corresponding to the reference peak in the first conversion pattern.
- halide solid electrolytic material which is a solid electrolyte material having high lithium ion conductivity.
- the solid electrolyte material in the second embodiment is May be satisfied.
- q 1 ' is the value of q 1 ' described above.
- q 2 ′ is a value of the q of the peak included in the first range.
- q 3 ′ is a value of the q of the peak included in the second range.
- q 4 ′ is a value of the q of the peak included in the third range.
- q 5 ′ is the value of q of the peak included in the fourth range.
- c 5 ′ ⁇ 12 when the peak is included in the fourth range
- c 5 0 when the peak is not included in the fourth range.
- a LiX is the formula (3) described in Embodiment 1 above.
- the solid electrolyte material in the second embodiment may include the second crystal phase.
- the second crystal phase include crystal phases from which the above-mentioned characteristic diffraction pattern can be obtained.
- the solid electrolyte material in Embodiment 2 may include the second crystal phase.
- the second crystal phase from which the above-mentioned characteristic diffraction pattern is obtained is a structure in which the anion sublattice has a cubic close-packed structure or an atomic arrangement in which the cubic close-packed structure is distorted, and from Li and halogen
- the lattice constant corresponding to the rock salt structure is extended to 1.8% or more, as compared with the crystals of the rock salt structure.
- high ion conduction did not occur when the anion exhibited a close-packed structure (Nature Materials 14, 1026-1031 (2015)).
- the first crystal phase from which the above-mentioned characteristic diffraction pattern is obtained is not limited to a specific crystal structure, but includes, for example, the crystal structures as follows.
- one includes a structure of Li 3 ErBr 6 (hereinafter also referred to as LEB) having a crystal structure belonging to the space group C2 / m.
- LEB Li 3 ErBr 6
- the detailed atomic arrangement is listed in Inorganic Crystal Structure Database (ICSD) (ICSD No. 50182).
- Other examples also include spinel structures belonging to the space groups Fd-3m or Imma, etc. and inverse spinel structures.
- the solid electrolyte material in the second embodiment may contain a heterocrystal phase having a crystal structure different from that of the second crystal phase.
- q 1 ′ (q 11 ′ I 11 ′ + q 12 ′ I 12 ') / (I 11' + I 12 ') as q 1' may define.
- a weighted average of equivalent peaks may be taken when virtually higher-order symmetry is considered.
- the LYB structure described above is a monoclinic crystal structure, but focusing on only the arrangement of anions, it is considered that the cubic close-packed structure is distorted as described above.
- the (20-2) plane and the (131) plane of the LYB structure are both approximately equivalent to the (200) plane in the rock salt structure. Therefore, when the diffraction peaks from the (20-2) plane and the (131) plane can be separated, the value of q x ′ may be obtained from a weighted average weighted by both peak intensities.
- the number of moles of cations may be smaller than the number of moles of anions. Thereby, empty sites for lithium ion conduction are formed, and the ion conductivity is improved.
- the shape of the solid electrolyte material in Embodiment 1 or 2 is not specifically limited, For example, needle shape, spherical shape, elliptical spherical shape, etc. may be sufficient.
- the solid electrolyte material in Embodiment 1 or 2 may be particles. After laminating a plurality of particles, they may be formed into pellets or plates by pressure.
- the median diameter may be 0.1 ⁇ m or more and 100 ⁇ m or less.
- the median diameter may be 0.5 ⁇ m or more and 10 ⁇ m or less.
- the ion conductivity can be further enhanced.
- a better dispersion state of the solid electrolyte material, the active material, and the like in Embodiment 1 or 2 can be formed.
- the solid electrolyte material may be smaller than the median diameter of the active material.
- the expression “a range in which the predetermined value A is the value B to the value C” means “the range in which B ⁇ A ⁇ C”.
- the solid electrolyte material in Embodiment 1 or 2 can be produced, for example, by the following method.
- a raw material powder of binary halide is prepared so as to obtain a target constituent element.
- a target constituent element For example, in the case of preparing a solid electrolyte material having a composition of Li 2.5 Y 0.5 Zr 0.5 Cl 6 , the ratio of LiCl, YCl 3 and ZrCl 4 to 2.5: 0.5: 0.5 Prepare in molar ratio.
- the composition of the anion can be determined by selecting the type of the raw material powder. After the raw material powders are thoroughly mixed, the raw material powders are mixed, pulverized and reacted using a method of mechanochemical milling. Thereafter, it may be fired in vacuum or in an inert atmosphere. Alternatively, the raw material powders may be well mixed and then fired in vacuum or in an inert atmosphere.
- the baking conditions may be, for example, baking within a range of 100 ° C. to 650 ° C. for one hour or more.
- composition of the crystal phase in the solid material, the crystal structure, the X-ray diffraction pattern using Cu-K ⁇ as a radiation source, and the position of each peak in the conversion pattern are the adjustment of the raw material ratio and the reaction of the raw material powders It can be determined by adjusting the method and reaction conditions.
- Embodiment 1 or 2 The description overlapping with the above-described Embodiment 1 or 2 is omitted as appropriate.
- the battery in the third embodiment is configured using the solid electrolyte material described in the first or second embodiment described above.
- the battery according to Embodiment 3 includes a solid electrolyte material, a positive electrode, a negative electrode, and an electrolyte layer.
- the electrolyte layer is a layer provided between the positive electrode and the negative electrode.
- At least one of the positive electrode, the electrolyte layer, and the negative electrode contains the solid electrolyte material according to Embodiment 1 or 2.
- the charge and discharge characteristics of the battery can be improved.
- FIG. 1 is a cross-sectional view showing a schematic configuration of a battery 1000 in the third embodiment.
- Battery 1000 in the third embodiment includes positive electrode 201, negative electrode 203, and electrolyte layer 202.
- the positive electrode 201 includes positive electrode active material particles 204 and solid electrolyte particles 100.
- the electrolyte layer 202 is disposed between the positive electrode 201 and the negative electrode 203.
- the electrolyte layer 202 includes an electrolyte material (eg, a solid electrolyte material).
- an electrolyte material eg, a solid electrolyte material
- the negative electrode 203 includes negative electrode active material particles 205 and solid electrolyte particles 100.
- Solid electrolyte particle 100 is a particle made of the solid electrolyte material in Embodiment 1 or 2, or a particle containing the solid electrolyte material in Embodiment 1 or 2 as a main component.
- the positive electrode 201 includes a material having a property of absorbing and releasing metal ions (for example, lithium ions).
- the positive electrode 201 includes, for example, a positive electrode active material (for example, positive electrode active material particles 204).
- positive electrode active materials include lithium-containing transition metal oxides (eg, Li (NiCoAl) O 2 , LiCoO 2 , etc.), transition metal fluorides, polyanions and fluorinated polyanion materials, and transition metal sulfides, transitions Metal oxyfluorides, transition metal oxysulfides, transition metal oxynitrides, etc. may be used.
- the median diameter of the positive electrode active material particles 204 may be 0.1 ⁇ m or more and 100 ⁇ m or less. If the median diameter of the positive electrode active material particles 204 is smaller than 0.1 ⁇ m, there is a possibility that the positive electrode active material particles 204 and the halide solid electrolyte material can not form a good dispersed state at the positive electrode. As a result, the charge and discharge characteristics of the battery are degraded. In addition, when the median diameter of the positive electrode active material particles 204 is larger than 100 ⁇ m, lithium diffusion in the positive electrode active material particles 204 becomes slow. For this reason, the operation at high power of the battery may be difficult.
- the median diameter of the positive electrode active material particles 204 may be larger than the median diameter of the halide solid electrolyte material. Thereby, a good dispersed state of the positive electrode active material particles 204 and the halide solid electrolyte material can be formed.
- the volume ratio “v: 100 ⁇ v” of the positive electrode active material particles 204 and the halide solid electrolyte material contained in the positive electrode 201 may be 30 ⁇ v ⁇ 95.
- v ⁇ 30 it may be difficult to secure sufficient energy density of the battery.
- v> 95 operation at high output may be difficult.
- the thickness of the positive electrode 201 may be 10 ⁇ m or more and 500 ⁇ m or less. When the thickness of the positive electrode 201 is smaller than 10 ⁇ m, it may be difficult to secure sufficient energy density of the battery. When the thickness of the positive electrode 201 is greater than 500 ⁇ m, operation at high output may be difficult.
- the electrolyte layer 202 is a layer containing an electrolyte material.
- the electrolyte material is, for example, a solid electrolyte material. That is, the electrolyte layer 202 may be a solid electrolyte layer.
- the solid electrolyte layer may contain, as a main component, the solid electrolyte material in the above-described Embodiment 1 or 2. That is, the solid electrolyte layer may contain, for example, 50% or more (50% by weight or more) of the solid electrolyte material in the above-described Embodiment 1 or 2 in a weight ratio to the entire solid electrolyte layer.
- the charge and discharge characteristics of the battery can be further improved.
- the solid electrolyte layer may contain, for example, 70% or more (70% by weight or more) of the solid electrolyte material in the above-described Embodiment 1 or 2 in a weight ratio to the entire solid electrolyte layer.
- the charge and discharge characteristics of the battery can be further improved.
- solid electrolyte layer contains the solid electrolyte material as a main component in Embodiment 1 or 2 described above, starting materials used when synthesizing unavoidable impurities or the above-mentioned solid electrolyte material and By-products and decomposition products may be included.
- the solid electrolyte layer may include, for example, 100% (100% by weight) of the solid electrolyte material in Embodiment 1 or 2 in terms of the weight ratio to the entire solid electrolyte layer except impurities which are inevitably mixed. Good.
- the charge and discharge characteristics of the battery can be further improved.
- the solid electrolyte layer may be composed of only the solid electrolyte material in Embodiment 1 or 2.
- it may be composed of only a solid electrolyte material different from the solid electrolyte material in the first or second embodiment.
- a solid electrolyte material different from the solid electrolyte material in Embodiment 1 or 2 for example, Li 2 MgX 4 , Li 2 FeX 4 , Li (Al, Ga, In) X 4 , Li 3 (Al, Ga, In) X 6 , LiI, etc. (X: F, Cl, Br, I) may be used.
- the solid electrolyte layer may simultaneously contain the solid electrolyte material in Embodiment 1 or 2 and a solid electrolyte material different from the solid electrolyte material in Embodiment 1 or 2 described above. At this time, both may be dispersed uniformly.
- the layer made of the solid electrolyte material in Embodiment 1 or 2 and the layer made of a solid electrolyte material different from the solid electrolyte material in Embodiment 1 or 2 described above are arranged in order with respect to the stacking direction of the battery. It may be
- the thickness of the solid electrolyte layer may be 1 ⁇ m or more and 1000 ⁇ m or less.
- the thickness of the solid electrolyte layer is smaller than 1 ⁇ m, the possibility of short circuit between the positive electrode 201 and the negative electrode 203 is increased.
- the thickness of the solid electrolyte layer is thicker than 1000 ⁇ m, operation at high output may be difficult.
- the negative electrode 203 includes a material having a property of inserting and extracting metal ions (eg, lithium ions).
- the negative electrode 203 includes, for example, a negative electrode active material (for example, negative electrode active material particles 205).
- metal materials, carbon materials, oxides, nitrides, tin compounds, silicon compounds, etc. may be used.
- the metal material may be a single metal.
- the metal material may be an alloy.
- metal materials include lithium metal, lithium alloy, and the like.
- carbon materials include natural graphite, coke, graphitized carbon, carbon fibers, spherical carbon, artificial graphite, amorphous carbon and the like. From the viewpoint of capacity density, silicon (Si), tin (Sn), a silicon compound, and a tin compound can be suitably used.
- a negative electrode active material having a low average reaction voltage is used, the effect of suppressing the electrolysis by the solid electrolyte material in Embodiment 1 or 2 is better exhibited.
- the median diameter of the negative electrode active material particles 205 may be 0.1 ⁇ m or more and 100 ⁇ m or less. If the median diameter of the negative electrode active material particles 205 is smaller than 0.1 ⁇ m, there is a possibility that the negative electrode active material particles 205 and the solid electrolyte particles 100 can not form a good dispersed state in the negative electrode. This degrades the charge and discharge characteristics of the battery. In addition, when the median diameter of the negative electrode active material particles 205 is larger than 100 ⁇ m, the lithium diffusion in the negative electrode active material particles 205 becomes slow. For this reason, the operation at high power of the battery may be difficult.
- the median diameter of the negative electrode active material particles 205 may be larger than the median diameter of the solid electrolyte particles 100. Thereby, a favorable dispersed state of the negative electrode active material particles 205 and the halide solid electrolyte material can be formed.
- the volume ratio “v: 100 ⁇ v” of the negative electrode active material particles 205 to the solid electrolyte particles 100 contained in the negative electrode 203 may be 30 ⁇ v ⁇ 95.
- v ⁇ 30 it may be difficult to secure sufficient energy density of the battery.
- v> 95 operation at high output may be difficult.
- the thickness of the negative electrode 203 may be 10 ⁇ m or more and 500 ⁇ m or less. If the thickness of the negative electrode is smaller than 10 ⁇ m, it may be difficult to secure sufficient energy density of the battery. In addition, when the thickness of the negative electrode is greater than 500 ⁇ m, operation at high output may be difficult.
- At least one of the positive electrode 201, the electrolyte layer 202, and the negative electrode 203 contains a sulfide solid electrolyte or an oxide solid electrolyte for the purpose of enhancing ion conductivity or chemical stability / electrochemical stability.
- a sulfide solid electrolyte Li 2 S-P 2 S 5 , Li 2 S-SiS 2 , Li 2 S-B 2 S 3 , Li 2 S-GeS 2 , Li 3.25 Ge 0.25 P 0.75 S 4 , Li 10 GeP 2 S 12 , etc. may be used.
- a NASICON-type solid electrolyte represented by LiTi 2 (PO 4 ) 3 and its element substitution product, (LaLi) TiO 3 -based perovskite-type solid electrolyte, Li 14 ZnGe 4 O 16 , Li 4 SiO 4 LISICON type solid electrolyte represented by LiGeO 4 and its element substituted body, Garnet type solid electrolyte represented by Li 7 La 3 Zr 2 O 12 and its element substituted body, Li 3 N and its H substituted body, Li 3 PO 4 and its N-substituted, etc. can be used.
- An organic polymer solid electrolyte may be included in at least one of the positive electrode 201, the electrolyte layer 202, and the negative electrode 203 for the purpose of enhancing the ion conductivity.
- the organic polymer solid electrolyte for example, a compound of a polymer compound and a lithium salt can be used.
- the polymer compound may have an ethylene oxide structure. By having an ethylene oxide structure, a large amount of lithium salt can be contained, and the ionic conductivity can be further enhanced.
- the lithium salt LiPF 6, LiBF 4, LiSbF 6, LiAsF 6, LiSO 3 CF 3, LiN (SO 2 CF 3) 2, LiN (SO 2 C 2 F 5) 2, LiN (SO 2 CF 3) ( SO 2 C 4 F 9), LiC (SO 2 CF 3) 3, etc., may be used.
- a lithium salt one lithium salt selected therefrom can be used alone. Alternatively, a mixture of two or more lithium salts selected therefrom may be used as the lithium salt.
- At least one of the positive electrode 201, the electrolyte layer 202, and the negative electrode 203 contains a non-aqueous electrolyte solution, a gel electrolyte, and an ionic liquid in order to facilitate lithium ion transfer and improve the output characteristics of the battery. May be
- the non-aqueous electrolyte contains a non-aqueous solvent and a lithium salt dissolved in the non-aqueous solvent.
- a non-aqueous solvent cyclic carbonate solvents, chain carbonate solvents, cyclic ether solvents, chain ether solvents, cyclic ester solvents, chain ester solvents, fluorine solvents, and the like may be used.
- cyclic carbonate solvents include ethylene carbonate, propylene carbonate, butylene carbonate, and the like.
- chain carbonate solvents include dimethyl carbonate, ethyl methyl carbonate, diethyl carbonate, and the like.
- cyclic ether solvents examples include tetrahydrofuran, 1,4-dioxane, 1,3-dioxolane, and the like.
- the chain ether solvents include 1,2-dimethoxyethane, 1,2-diethoxyethane, and the like.
- cyclic ester solvents examples include ⁇ -butyrolactone and the like.
- linear ester solvents include methyl acetate and the like.
- fluorine solvents include fluoroethylene carbonate, methyl fluoropropionate, fluorobenzene, fluoroethyl methyl carbonate, fluorodimethylene carbonate, and the like.
- non-aqueous solvent one non-aqueous solvent selected therefrom can be used alone.
- the non-aqueous electrolytic solution may contain at least one fluorine solvent selected from the group consisting of fluoroethylene carbonate, methyl fluoropropionate, fluorobenzene, fluoroethyl methyl carbonate and fluorodimethylene carbonate.
- the lithium salt LiPF 6, LiBF 4, LiSbF 6, LiAsF 6, LiSO 3 CF 3, LiN (SO 2 CF 3) 2, LiN (SO 2 C 2 F 5) 2, LiN (SO 2 CF 3) ( SO 2 C 4 F 9), LiC (SO 2 CF 3) 3, etc., may be used.
- lithium salt one lithium salt selected therefrom can be used alone. Alternatively, a mixture of two or more lithium salts selected therefrom may be used as the lithium salt.
- concentration of lithium salt is, for example, in the range of 0.5 to 2 mol / liter.
- the gel electrolyte one in which a non-aqueous electrolyte is contained in a polymer material can be used.
- a polymer material polyethylene oxide, polyacrylonitrile, polyvinylidene fluoride, polymethyl methacrylate, a polymer having an ethylene oxide bond, and the like may be used.
- the cations constituting the ionic liquid are aliphatic chain quaternary salts such as tetraalkylammonium and tetraalkylphosphonium, pyrrolidiniums, morpholiniums, imidazoliniums, tetrahydropyrimidiniums, piperaziniums, piperidiniums and the like And nitrogen-containing heterocyclic aromatic cations such as cyclic ammonium, pyridiniums, and imidazoliums.
- aliphatic chain quaternary salts such as tetraalkylammonium and tetraalkylphosphonium, pyrrolidiniums, morpholiniums, imidazoliniums, tetrahydropyrimidiniums, piperaziniums, piperidiniums and the like
- nitrogen-containing heterocyclic aromatic cations such as cyclic ammonium, pyridiniums, and imidazoliums.
- Anions constituting the ionic liquid are PF 6 ⁇ , BF 4 ⁇ , SbF 6 ⁇ ⁇ , AsF 6 ⁇ , SO 3 CF 3 ⁇ , N (SO 2 CF 3 ) 2 ⁇ , N (SO 2 C 2 F 5 ) 2 ⁇ , N (SO 2 CF 3 ) (SO 2 C 4 F 9 ) ⁇ , C (SO 2 CF 3 ) 3 ⁇ or the like.
- the ionic liquid may also contain a lithium salt.
- a binder may be contained in at least one of the positive electrode 201, the electrolyte layer 202, and the negative electrode 203 for the purpose of improving the adhesion between the particles.
- the binder is used to improve the binding properties of the material constituting the electrode.
- the binder polyvinylidene fluoride, polytetrafluoroethylene, polyethylene, polypropylene, aramid resin, polyamide, polyimide, polyamideimide, polyacrylonitrile, polyacrylic acid, polyacrylic acid methyl ester, polyacrylic acid ethyl ester, poly Acrylic acid hexyl ester, polymethacrylic acid, polymethacrylic acid methyl ester, polymethacrylic acid ethyl ester, polymethacrylic acid hexyl ester, polyvinyl acetate, polyvinyl pyrrolidone, polyether, polyether sulfone, hexafluoropolypropylene, styrene buta
- tetrafluoroethylene, hexafluoroethylene, hexafluoropropylene, perfluoroalkyl vinyl ether, vinylidene fluoride, chlorotrifluoroethylene, ethylene, propylene, pentafluoropropylene, fluoromethyl vinyl ether, acrylic acid, hexadiene Copolymers of two or more selected materials can be used. Moreover, 2 or more types selected from these may be mixed and it may be used as a binding agent.
- At least one of the positive electrode 201 and the negative electrode 203 may contain a conductive aid, if necessary.
- the conductive aid is used to reduce the electrode resistance.
- Conductive aids include graphites of natural graphite or artificial graphite, carbon blacks such as acetylene black and ketjen black, conductive fibers such as carbon fibers or metal fibers, metal powders such as fluorinated carbon and aluminum, Examples thereof include conductive whiskers such as zinc oxide or potassium titanate, conductive metal oxides such as titanium oxide, and conductive polymer compounds such as polyaniline, polypyrrole and polythiophene.
- cost reduction can be achieved by using a carbon conductive support as the conductive support.
- the battery in the second embodiment can be configured as a battery of various shapes such as coin type, cylindrical type, square type, sheet type, button type, flat type, and laminated type.
- Example A1 [Preparation of solid electrolyte material]
- FIG. 2 is a schematic view showing a method of evaluating lithium ion conductivity.
- the pressure forming die 300 is composed of an electrically insulating polycarbonate frame 301 and an electron conductive stainless steel punch upper portion 303 and a punch lower portion 302.
- the ion conductivity was evaluated by the following method using the configuration shown in FIG.
- the powder of the solid electrolyte material of Example A1 was filled in a pressure forming die 300 in a dry atmosphere with a dew point of ⁇ 30 ° C. or less, uniaxially pressurized at 400 MPa, and a conductivity measurement cell of Example A1 was produced.
- the ionic conductivity was calculated from the following equation using the resistance value of the electrolyte.
- ⁇ (R SE ⁇ S / t) ⁇ 1
- ⁇ is the ion conductivity
- S is the electrolyte area (in FIG. 2, the inner diameter of the frame 301)
- R SE is the resistance value of the solid electrolyte in the above impedance measurement
- t is the thickness of the electrolyte (in FIG. Of the solid electrolyte particle 100).
- the ion conductivity of the solid electrolyte material of Example A1 measured at 22 ° C. was 1.2 ⁇ 10 ⁇ 3 S / cm.
- FIG. 4A is a graph showing an XRD pattern.
- an X-ray diffraction pattern was measured in a dry environment with a dew point of ⁇ 45 ° C. or less using an X-ray diffractometer (MiniFlex 600 manufactured by RIGAKU Co., Ltd.).
- X-ray diffractometer MiniFlex 600 manufactured by RIGAKU Co., Ltd.
- Cu-K ⁇ ray was used for the X-ray source.
- the solid electrolyte material of Example A1 for 700 ⁇ m thickness equivalent, 8.5 mg of the above-mentioned mixture and 16.5 mg of Al powder were laminated in this order.
- the first electrode and the solid electrolyte layer were obtained by pressure-molding this at a pressure of 300 MPa.
- metal In 200 micrometers in thickness
- pressure-molding this at a pressure of 80 MPa a laminate composed of the first electrode, the solid electrolyte layer, and the second electrode was produced.
- the secondary battery of Example A1 was placed in a thermostat of 25 ° C.
- Constant current charging was performed at a current value at which a rate of 0.05 C (20-hour rate) with respect to the theoretical capacity of the battery was reached, and charging was terminated at a voltage of 3.6 V.
- the battery was discharged at a current value of 0.05 C rate, and the discharge was finished at a voltage of 1.9 V.
- the initial discharge capacity of the secondary battery of Example A1 was 0.467 mAh.
- the ion conductivity was measured in the same manner as in Example A1 except for the above.
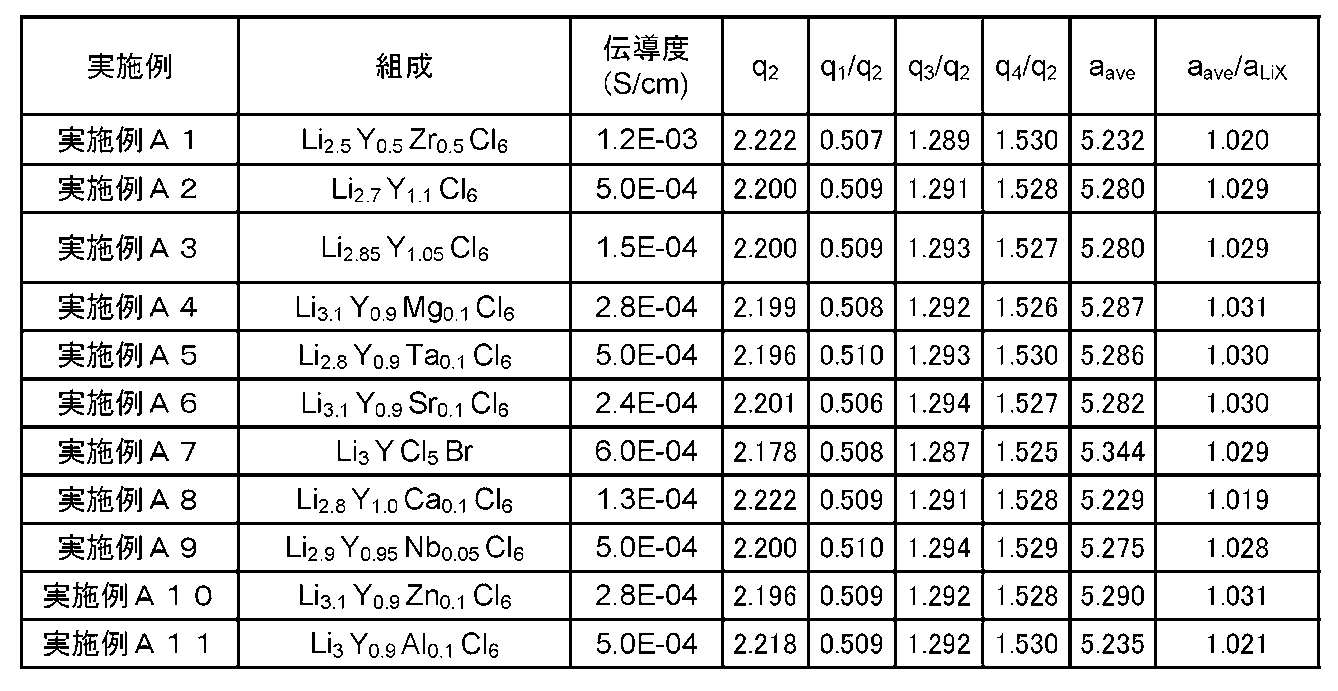
- the value of q / q 2 is, in the range of 0.50 to 0.52,1.28 from 1.30,1.51 1.54, peaks were observed, respectively. These peaks of q / q 2 values, and the value of q 2 are shown in Table 1 below.
- the value of aave was calculated using these values and Formula (2), and the value of aave / aLiX was calculated using Formula (3). The calculated results are shown in Table 1 below.
- the secondary batteries of Examples A2 to A11 were produced in the same manner as in Example A1 except for the above.
- Example A2 The charge / discharge test of each of the secondary batteries of Examples A2 to A11 was conducted in the same manner as in Example A1 described above.
- the initial discharge characteristics of Examples A2 to A11 showed the same characteristics as Example A1, and good discharge characteristics were obtained.
- the initial discharge characteristics in Example A2 are shown in FIG.
- the discharge capacity of Example A2 was 0.657 mAh.
- the composition is Li a Y b M c Br d
- LiBr: YBr 3: MBr m a: b: mixing weighed in a ratio of c.
- M is a metal element
- m is a valence of M.
- milling was performed at 600 rpm for 12 hours using a planetary ball mill.
- a heat treatment was then performed at 300 ° C. for 5 hours.
- the ion conductivity was measured in the same manner as in Example A1 except for the above.
- the secondary batteries of Examples B1 to B13 were produced in the same manner as in Example A1 except for the above.
- the ion conductivity was measured in the same manner as in Example A1 except for the above.
- a secondary battery of Comparative Example 2 was produced in the same manner as in Example A1 except for the above.
- Examples A1 to A11 and B1 to B13 show high ion conductivity of 1 ⁇ 10 -4 S / cm or more at around room temperature as compared with Comparative Examples 1 to 3.
- Examples A1 to A11 peaks were observed in the range of 0.50 to 0.52, 1.28 to 1.30, 1.51 to 1.54, and the value of q / q 2 was a halogen ion.
- the sublattices of the present invention show characteristic peaks observed when the hexagonal subpacked structure is a hexagonal close-packed structure or a hexagonal close-packed structure is a distorted structure.
- the range of q / q ′ is in the range of 1.14-1.17, 1.625-1.645, 1.88-1.94, 1.90-2.10.
- Comparative Example 3 has a structure in which the value of a ave / a LiX exceeds 1.018 as in Example A1. The ion conductivity is greatly improved compared to
- Examples A1 to A11 and B1 to B13 the charge and discharge operation of the battery was shown at room temperature. On the other hand, in Comparative Example 2, the discharge capacity was hardly obtained, and the battery operation could not be confirmed. Furthermore, since the materials of Examples A1 to A1 and B1 to B13 do not contain sulfur as a constituent element, there is no generation of hydrogen sulfide.
- the solid electrolyte material does not generate
- the battery of the present disclosure can be utilized, for example, as an all solid lithium secondary battery.
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Inorganic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Electrochemistry (AREA)
- Manufacturing & Machinery (AREA)
- Physics & Mathematics (AREA)
- Condensed Matter Physics & Semiconductors (AREA)
- General Physics & Mathematics (AREA)
- Geology (AREA)
- Life Sciences & Earth Sciences (AREA)
- Materials Engineering (AREA)
- Secondary Cells (AREA)
- Conductive Materials (AREA)
- Inorganic Compounds Of Heavy Metals (AREA)
- Battery Electrode And Active Subsutance (AREA)
- Compounds Of Alkaline-Earth Elements, Aluminum Or Rare-Earth Metals (AREA)
Abstract
本開示の一態様に係る固体電解質材料は、LiとMとXとからなる。前記Mは、金属元素から選択される少なくとも1種であり、前記Xは、Cl、Br、及びIからなる群より選択される少なくとも1種である。複数の前記Xの原子の副格子が最密充填構造を有する。前記複数の前記Xの原子のうち、互いに隣接する2つの前記Xの原子間の距離の平均値は、Liと前記Xのみからなる岩塩構造における互いに隣接する2つの前記Xの原子間の距離に比べて、1.8%以上、長い。
Description
本開示は、固体電解質材料、および、電池に関する。
特許文献1には、硫化物固体電解質を用いた全固体電池が開示されている。
非特許文献1には、Li3YCl6が開示されている。
非特許文献2には、Li3YBr6が開示されている。
Z.Anorg.Allg.Chem.623(1997)、1067-1073.
Z.Anorg.Allg.Chem.623(1997)、1352-1356.
従来技術においては、高いリチウムイオン伝導度を有する固体電解質材料の実現が望まれる。
本開示の一様態における固体電解質材料は、LiとMとXとからなる。前記Mは、金属元素から選択される少なくとも1種であり、前記Xは、Cl、Br、及びIからなる群より選択される少なくとも1種である。複数の前記Xの原子の副格子が最密充填構造を有する。前記複数の前記Xの原子のうち、互いに隣接する2つの前記Xの原子間の距離の平均値は、Liと前記Xのみからなる岩塩構造における互いに隣接する2つの前記Xの原子間の距離に比べて、1.8%以上、長い。
本開示によれば、高いリチウムイオン伝導度を有する固体電解質材料を実現できる。
以下、本開示の実施の形態が、図面を参照しながら説明される。
(実施の形態1)
実施の形態1における固体電解質材料は、カチオンであるLi及びMと、アニオンであるXとからなる材料である。
実施の形態1における固体電解質材料は、カチオンであるLi及びMと、アニオンであるXとからなる材料である。
Mは、金属元素から選択される少なくとも1種である。
Xは、Cl、Br、及びIからなる群より選択される少なくとも1種である。
実施の形態1における固体電解質材料に含まれる、複数の前記Xの原子の副格子が最密充填構造である。
実施の形態1における固体電解質材料において、前記複数の前記Xの原子のうち、互いに隣接する2つの前記Xの原子間の距離の平均値は、LiとXのみからなる岩塩構造における互いに隣接する2つの前記Xの原子間の距離に比べて、1.8%以上、長い。
以上の構成によれば、高いリチウムイオン伝導度を有する固体電解質材料であるハロゲン化物固体電解材料を実現できる。
また、以上の構成によれば、実施の形態1の固体電解質材料を用いることで、充放電特性に優れた全固体二次電池を実現することができる。
また、実施の形態1の固体電解質材料を用いることで、硫黄を含まない全固体二次電池を実現することができる。すなわち、実施の形態1の固体電解質材料は、大気に曝露された際に硫化水素が発生する構成(例えば、特許文献1の構成)ではない。このため、硫化水素の発生が無く、安全性に優れた全固体二次電池を実現することができる。
なお、実施の形態1における固体電解質材料のX線回折パターンを、横軸が回折角2θからqとなるように変換することにより得られる、第1の変換パターンが、前記qの値が2.11Å-1以上2.31Å-1以下である範囲内に、基準ピークを含む。
ここで、q=4πsinθ/λであり、λはX線の波長である。
前記X線回折パターンを、横軸が回折角2θからq/q2となるように変換することにより得られる、第2の変換パターンが、前記q/q2の値が0.50以上0.52以下である第1範囲内、前記q/q2の値が1.28以上1.30以下である第2範囲内、及び前記q/q2の値が1.51以上1.54以下である第3範囲内からなる群から選択される少なくとも1つにおいて、ピークを含む。
ここで、q2は、前記第1の変換パターンにおける前記基準ピークに対応する前記qの値である。
以上の構成によれば、高いリチウムイオン伝導度を有する固体電解質材料を実現できる。
以上の構成によれば、高いリチウムイオン伝導度を有する固体電解質材料を実現できる。
q1は、前記第1範囲内に含まれる前記ピークの前記qの値である。
q2は前述のq2の値である。
q3は、前記第2範囲内に含まれる前記ピークの前記qの値である。
q4は、前記第3範囲内に含まれる前記ピークの前記qの値である。
c1=2/3、c2=√(41/24)、c3=√(17/6)、c4=2である。但し、十分な回折強度が得られずに、第2の変換パターンにおいて、q1からq4のうちqiに対応するピークが上述の範囲内に含まれない場合には、ci=0とする。
すなわち、前記第1範囲内に前記ピークが含まれる場合にはc1=2/3であり、前記第1範囲内に前記ピークが含まれない場合にはc1=0、である。
また、c2=√(41/24)、である。
また、前記第2範囲内に前記ピークが含まれる場合にはc3=√(17/6)であり、前記第2範囲内に前記ピークが含まれない場合には、c3=0、である。
また、前記第3範囲内に前記ピークが含まれる場合にはc4=2であり、前記第3範囲内に前記ピークが含まれない場合には、c4=0、である。
nは、ci≠0のciの数である。例えば、ciが全てci≠0の場合は、n=4である。
実施の形態1における固体電解質材料の前記Xに含まれるCl、Br、及びIのモル比を、Cl:Br:I=xCl:xBr:xI(ただし、xCl+xBr+xI=1)とする。
また、aLiCl=5.130Å(=LiClの格子定数)、aLiBr=5.500Å(=LiBrの格子定数)、aLiI=6.0257Å(=LiIの格子定数)とする。
なお、実施の形態1における固体電解質材料は、第1結晶相を含んでもよい。当該第1結晶相としては、上述の特徴的な回折パターンが得られる結晶相が挙げられる。
すなわち、実施の形態1における固体電解質材料は、第1結晶相を含んでもよい。
上述の特徴的な回折図形が得られる第1結晶相は、アニオンの副格子が六方最密充填構造、もしくは、六方最密充填構造が歪んだ原子配列となる構造であり、かつ、Liとハロゲンからなる岩塩構造の結晶に比べ、アニオン間の平均距離が1.8%以上に広がった構造であることを示す。通常、アニオンが最密充填構造を示す場合には、高いイオン伝導が発現しないと考えられていた(Nature Materials 14, 1026-1031(2015))。一方、発明者らが検討した結果、アニオンが六方最密充填構造で、前述の式(1)を満たす場合に、1×10-4S/cm以上の高いリチウムイオン伝導を得られることを見出した。これは、格子の広がりにより、イオン伝導の律速過程となる八面体サイトから準安定な四面体サイトへの移動が促進されるためであると考えられる。
以上の構成によれば、より高いリチウムイオン伝導度を有する固体電解質材料を実現できる。
上述の特徴的な回折図形が得られる第1結晶相は、特定の結晶構造に限定されないが、例えば、下記のような結晶構造が挙げられる。
例えば、空間群P-3m1に属する結晶構造を有するLi3ErCl6(以下、LECとも表記される)構造または空間群Pnmaに属する結晶構造を有するLi3YbCl6(以下、LYCとも表記される)構造が挙げられる。その詳細な原子配列は、無機結晶構造データベース(ICSD)に掲載されている(LEC構造:ICSD No.50151、LYC構造:ICSD No.50152)。
なお、実施の形態1における固体電解質材料は、第1結晶相とは異なる結晶構造を有する異種結晶相を含んでもよい。
なお、上述のq1からq4を定める際に、近接する高強度のピークが存在する場合には、近接ピークのピーク位置とピーク強度との加重平均をとってq1からq4を定めてもよい。具体例を示すと、近接するq11とq12の位置に強度がI11とI12のピークが存在する場合に、q1=(q11I11+q12I12)/(I11+I12)としてq1を定めてもよい。
その際に、結晶構造の対称性を考慮して、仮想的に高次の対称性を考慮した際に等価なピーク同士の加重平均をとってもよい。具体例を示すと、前述のLYC構造は直方晶系の結晶構造であるが、アニオンの配列のみに着目すると、前述のとおり六方最密充填構造が歪んだ構造と考えられる。近似的にLYC構造を六方最密充填構造と考えると、LYC構造の(401)面と(231)面は、いずれも六方最密充填構造における(101)面と近似的には等価である。従って、(401)面と(231)面からの回折ピークが分離可能な場合に、双方のピーク強度によって重みづけされた加重平均からqxの値を求めてもよい。
第一結晶相においては、構成元素のうち、カチオンのモル数がアニオンのモル数より少なくてもよい。それにより、リチウムイオンが伝導するための空のサイトが形成され、イオン伝導度が向上する。
(実施の形態2)
以下、実施の形態2が説明される。上述の実施の形態1と重複する説明は、適宜、省略される。
以下、実施の形態2が説明される。上述の実施の形態1と重複する説明は、適宜、省略される。
実施の形態2における固体電解質材料は、上述の実施の形態1における固体電解質材料の構成に加えて、下記の構成をさらに備える。
実施の形態2における固体電解質材料のX線回折パターンを、横軸が回折角2θからqとなるように変換することにより得られる、第1の変換パターンが、前記qの値が1.76Å-1以上2.18Å-1以下である範囲内に、基準ピークを含む。
ここで、q=4πsinθ/λであり、λはX線の波長である。
前記X線回折パターンを、横軸が回折角2θからq/q1’となるように変換することにより得られる、第2の変換パターンが、前記q/q1’の値が1.14以上1.17以下である第1範囲内、前記q/q1’の値が1.62以上1.65以下である第2範囲内、前記q/q1’の値が1.88以上1.94以下である第3範囲内、及び前記q/q1’の値が1.9以上2.1以下である第4範囲内からなる群から選択される少なくとも1つにおいて、ピークを含む。
ここで、q1’は、前記第1の変換パターンにおける前記基準ピークに対応する前記qの値である。
以上の構成によれば、高いリチウムイオン伝導度を有する固体電解質材料であるハロゲン化物固体電解材料を実現できる。
また、以上の構成によれば、実施の形態2の固体電解質材料を用いることで、充放電特性に優れた全固体二次電池を実現することができる。
以上の構成によれば、高いリチウムイオン伝導度を有する固体電解質材料を実現できる。
q1’は前述のq1’の値である。
q2’は、前記第1範囲内に含まれる前記ピークの前記qの値である。
q3’は、前記第2範囲内に含まれる前記ピークの前記qの値である。
q4’は、前記第3範囲内に含まれる前記ピークの前記qの値である。
q5’は、前記第4範囲内に含まれる前記ピークの前記qの値である。
c1’=√3、c2’=2、c3’=2√2、c4’=√11、c5’=√12、である。但し、十分な回折強度が得られずに、q1’からq5’のうちのあるqi’に対応するピークが上述の範囲内に含まれない場合には、ci’=0とする。
すなわち、c1’=√3、である。
また、前記第1範囲内に前記ピークが含まれる場合にはc2’=2であり、前記第1範囲内に前記ピークが含まれない場合にはc2’=0、である。
また、前記第2範囲内に前記ピークが含まれる場合にはc3’=2√2であり、前記第2範囲内に前記ピークが含まれない場合にはc3’=0、である。
また、前記第3範囲内に前記ピークが含まれる場合にはc4’=√11であり、前記第3範囲内に前記ピークが含まれない場合にはc4’=0、である。
また、前記第4範囲内に前記ピークが含まれる場合にはc5’=√12であり、前記第4範囲内に前記ピークが含まれない場合にはc5’=0、である。
n’は、ci’≠0であるci’の数である。例えば、ci’が全てci’≠0の場合は、n=5である。
aLiXは、上述の実施の形態1で記載した式(3)である。
なお、実施の形態2における固体電解質材料は、第2結晶相を含んでもよい。当該第2結晶相としては、上述の特徴的な回折パターンが得られる結晶相が挙げられる。
すなわち、実施の形態2における固体電解質材料は、第2結晶相を含んでもよい。
上述の特徴的な回折図形が得られる第2結晶相は、アニオンの副格子が立方最密充填構造、もしくは立方最密充填構造が歪んだ原子配列となる構造であり、かつ、Liとハロゲンからなる岩塩構造の結晶に比べ、岩塩構造に相当する格子定数が1.8%以上に広がった構造であることを示す。通常、アニオンが最密充填構造を示す場合には、高いイオン伝導が発現しないと考えられていた(Nature Materials 14, 1026-1031(2015))。一方、発明者らが検討した結果、アニオンが立方最密充填構造で、前述の式(1)を満たす場合に、1×10-4S/cm以上の高いリチウムイオン伝導を得られることを見出した。これは、格子の広がりにより、イオン伝導の律速過程となる八面体サイトから準安定な四面体サイトへの移動が促進されるためであると考えられる。
上述の特徴的な回折図形が得られる第1結晶相は、特定の結晶構造に限定されないが、例えば、下記のような結晶構造が挙げられる。
例えば、一つは、空間群C2/mに属する結晶構造を有するLi3ErBr6(以下、LEBとも表記される)構造が挙げられる。その詳細な原子配列は、無機結晶構造データベース(ICSD)に掲載されている(ICSD No.50182)。他の例として、空間群Fd-3mまたはImmaなどに属するスピネル構造、及び、逆スピネル構造も挙げられる。
なお、実施の形態2における固体電解質材料は、第2結晶相とは異なる結晶構造を有する異種結晶相を含んでもよい。
以上の構成によれば、より高いリチウムイオン伝導度を有する固体電解質材料を実現できる。
なお、上述のq1’からq5’を定める際に、近接する高強度のピークが存在する場合には、近接ピークのピーク位置とピーク強度との加重平均をとってq1’からq5’を定めてもよい。具体例を示すと、近接するq11’とq12’の位置に強度がI11’とI12’のピークが存在する場合に、q1’=(q11’I11’+q12’I12’)/(I11’+I12’)としてq1’を定めてもよい。
その際に、結晶構造の対称性を考慮して、仮想的に高次の対称性を考慮した際に等価なピーク同士の加重平均をとってもよい。具体例を示すと、前述のLYB構造は単斜晶系の結晶構造であるが、アニオンの配列のみに着目すると、前述のとおり立方最密充填構造が歪んだ構造と考えられる。近似的にLYB構造を岩塩構造と考えると、LYB構造の(20-2)面と(131)面は、いずれも岩塩構造における(200)面と近似的には等価である。従って、(20-2)面と(131)面からの回折ピークが分離可能な場合に、双方のピーク強度によって重みづけされた加重平均からqx’の値を求めてもよい。
第一結晶相においては、構成元素のうち、カチオンのモル数がアニオンのモル数より少なくてもよい。それにより、リチウムイオンが伝導するための空のサイトが形成され、イオン伝導度が向上する。
なお、実施の形態1または2における固体電解質材料の形状は、特に限定されるものではなく、例えば、針状、球状、楕円球状など、であってもよい。例えば、実施の形態1または2における固体電解質材料は、粒子であってもよい。複数の粒子を積層した後、加圧によりペレット状もしくは板状に成形してもよい。
例えば、実施の形態1または2における固体電解質材料の形状が粒子状(例えば、球状)の場合、メジアン径は、0.1μm以上かつ100μm以下であってもよい。
また、実施の形態1または2においては、メジアン径は0.5μm以上かつ10μm以下であってもよい。
以上の構成によれば、イオン伝導性をより高めることができる。また、実施の形態1または2における固体電解質材料と活物質などとのより良好な分散状態を形成できる。
また、実施の形態1または2においては、固体電解質材料は、活物質のメジアン径より小さくてもよい。
以上の構成によれば、実施の形態1または2における固体電解質材料と活物質などとのより良好な分散状態を形成できる。
なお、本開示において、「所定の値Aが、値Bから値Cである範囲」との表記は、「B≦A≦Cである範囲」を意味する。
<固体電解質材料の製造方法>
実施の形態1または2における固体電解質材料は、例えば、下記の方法により、製造されうる。
実施の形態1または2における固体電解質材料は、例えば、下記の方法により、製造されうる。
目的とする構成元素が得られるよう、二元系ハロゲン化物の原料粉を用意する。例えば、Li2.5Y0.5Zr0.5Cl6の組成の固体電解質材料を作製する場合には、LiClとYCl3とZrCl4とを2.5:0.5:0.5のモル比で用意する。このとき、原料粉の種類を選択することで、アニオンの組成を決定することができる。原料粉をよく混合した後、メカノケミカルミリングの方法を用いて原料粉同士を混合・粉砕・反応させる。その後、真空中または不活性雰囲気中で焼成してもよい。もしくは、原料粉をよく混合した後、真空中または不活性雰囲気中で焼成してもよい。焼成条件は、例えば、100℃から650℃の範囲内で、1時間以上の焼成を行ってもよい。
これにより、前述したような組成を含む固体電解質材料が得られる。
なお、固体質材料における結晶相の構成、結晶構造、および、Cu-Kαを線源として用いたX線回折パターンおよび、変換パターンにおける各ピークの位置は、原料比率の調整および原料粉どうしの反応方法および反応条件の調整により、決定することができる。
(実施の形態3)
以下、実施の形態3が説明される。上述の実施の形態1または2と重複する説明は、適宜、省略される。
以下、実施の形態3が説明される。上述の実施の形態1または2と重複する説明は、適宜、省略される。
実施の形態3における電池は、上述の実施の形態1または2で説明された固体電解質材料を用いて構成される。
実施の形態3における電池は、固体電解質材料と、正極と、負極と、電解質層と、を備える。
電解質層は、正極と負極との間に設けられる層である。
正極と電解質層と負極とのうちの少なくとも1つは、実施の形態1または2における固体電解質材料を含む。
以上の構成によれば、電池の充放電特性を向上させることができる。
以下に、実施の形態3における電池の具体例が、説明される。
図1は、実施の形態3における電池1000の概略構成を示す断面図である。
実施の形態3における電池1000は、正極201と、負極203と、電解質層202とを備える。
正極201は、正極活物質粒子204と固体電解質粒子100とを含む。
電解質層202は、正極201と負極203との間に配置される。
電解質層202は、電解質材料(例えば、固体電解質材料)を含む。
負極203は、負極活物質粒子205と固体電解質粒子100とを含む。
固体電解質粒子100は、実施の形態1または2における固体電解質材料からなる粒子、または、実施の形態1または2における固体電解質材料を主たる成分として含む粒子である。
正極201は、金属イオン(例えば、リチウムイオン)を吸蔵・放出する特性を有する材料を含む。正極201は、例えば、正極活物質(例えば、正極活物質粒子204)を含む。
正極活物質には、例えば、リチウム含有遷移金属酸化物(例えば、Li(NiCoAl)O2、LiCoO2、など)、遷移金属フッ化物、ポリアニオンおよびフッ素化ポリアニオン材料、および、遷移金属硫化物、遷移金属オキシフッ化物、遷移金属オキシ硫化物、遷移金属オキシ窒化物、など、が用いられうる。
正極活物質粒子204のメジアン径は、0.1μm以上かつ100μm以下であってもよい。正極活物質粒子204のメジアン径が0.1μmより小さいと、正極において、正極活物質粒子204とハロゲン化物固体電解質材料とが、良好な分散状態を形成できない可能性が生じる。この結果、電池の充放電特性が低下する。また、正極活物質粒子204のメジアン径が100μmより大きいと、正極活物質粒子204内のリチウム拡散が遅くなる。このため、電池の高出力での動作が困難となる場合がある。
正極活物質粒子204のメジアン径は、ハロゲン化物固体電解質材料のメジアン径よりも、大きくてもよい。これにより、正極活物質粒子204とハロゲン化物固体電解質材料との良好な分散状態を形成できる。
正極201に含まれる、正極活物質粒子204とハロゲン化物固体電解質材料の体積比率「v:100-v」について、30≦v≦95であってもよい。v<30では、十分な電池のエネルギー密度確保が困難となる可能性がある。また、v>95では、高出力での動作が困難となる可能性がある。
正極201の厚みは、10μm以上かつ500μm以下であってもよい。なお、正極201の厚みが10μmより薄い場合には、十分な電池のエネルギー密度の確保が困難となる可能性がある。なお、正極201の厚みが500μmより厚い場合には、高出力での動作が困難となる可能性がある。
電解質層202は、電解質材料を含む層である。当該電解質材料は、例えば、固体電解質材料である。すなわち、電解質層202は、固体電解質層であってもよい。
なお、固体電解質層は、上述の実施の形態1または2における固体電解質材料を、主成分として、含んでもよい。すなわち、固体電解質層は、上述の実施の形態1または2における固体電解質材料を、例えば、固体電解質層の全体に対する重量割合で50%以上(50重量%以上)、含んでもよい。
以上の構成によれば、電池の充放電特性を、より向上させることができる。
また、固体電解質層は、上述の実施の形態1または2における固体電解質材料を、例えば、固体電解質層の全体に対する重量割合で70%以上(70重量%以上)、含んでもよい。
以上の構成によれば、電池の充放電特性を、より向上させることができる。
なお、固体電解質層は、上述の実施の形態1または2における固体電解質材料を主成分として含みながら、さらに、不可避的な不純物、または、上述の固体電解質材料を合成する際に用いられる出発原料および副生成物および分解生成物など、を含んでいてもよい。
また、固体電解質層は、実施の形態1または2における固体電解質材料を、例えば、混入が不可避的な不純物を除いて、固体電解質層の全体に対する重量割合で100%(100重量%)、含んでもよい。
以上の構成によれば、電池の充放電特性を、より向上させることができる。
以上のように、固体電解質層は、実施の形態1または2における固体電解質材料のみから構成されていてもよい。
もしくは、実施の形態1または2における固体電解質材料とは異なる固体電解質材料のみから構成されていてもよい。実施の形態1または2における固体電解質材料とは異なる固体電解質材料として、例えば、Li2MgX4、Li2FeX4、Li(Al,Ga,In)X4、Li3(Al,Ga,In)X6、LiI、など(X:F,Cl,Br,I)、が用いられうる。
固体電解質層は、実施の形態1または2における固体電解質材料と、上述の実施の形態1または2における固体電解質材料とは異なる固体電解質材料とを、同時に含んでもよい。このとき、両者が均一に分散していてもよい。実施の形態1または2における固体電解質材料からなる層と、上述の実施の形態1または2における固体電解質材料とは異なる固体電解質材料からなる層とが、電池の積層方向に対して、順に配置されていてもよい。
固体電解質層の厚みは、1μm以上かつ1000μm以下であってもよい。固体電解質層の厚みが1μmより薄い場合には、正極201と負極203とが短絡する可能性が高まる。また、固体電解質層の厚みが1000μmより厚い場合には、高出力での動作が困難となる可能性がある。
負極203は、金属イオン(例えば、リチウムイオン)を吸蔵・放出する特性を有する材料を含む。負極203は、例えば、負極活物質(例えば、負極活物質粒子205)を含む。
負極活物質には、金属材料、炭素材料、酸化物、窒化物、錫化合物、珪素化合物、など、が使用されうる。金属材料は、単体の金属であってもよい。もしくは、金属材料は、合金であってもよい。金属材料の例として、リチウム金属、リチウム合金、など、が挙げられる。炭素材料の例として、天然黒鉛、コークス、黒鉛化途上炭素、炭素繊維、球状炭素、人造黒鉛、非晶質炭素、など、が挙げられる。容量密度の観点から、珪素(Si)、錫(Sn)、珪素化合物、錫化合物、を好適に使用できる。平均反応電圧が低い負極活物質を用いた場合に、実施の形態1または2における固体電解質材料による電気分解抑制の効果が、より良く発揮される。
負極活物質粒子205のメジアン径は、0.1μm以上かつ100μm以下であってもよい。負極活物質粒子205のメジアン径が0.1μmより小さいと、負極において、負極活物質粒子205と固体電解質粒子100とが、良好な分散状態を形成できない可能性が生じる。これにより、電池の充放電特性が低下する。また、負極活物質粒子205のメジアン径が100μmより大きいと、負極活物質粒子205内のリチウム拡散が遅くなる。このため、電池の高出力での動作が困難となる場合がある。
負極活物質粒子205のメジアン径は、固体電解質粒子100のメジアン径よりも、大きくてもよい。これにより、負極活物質粒子205とハロゲン化物固体電解質材料との良好な分散状態を形成できる。
負極203に含まれる、負極活物質粒子205と固体電解質粒子100の体積比率「v:100-v」について、30≦v≦95であってもよい。v<30では、十分な電池のエネルギー密度確保が困難となる可能性がある。また、v>95では、高出力での動作が困難となる可能性がある。
負極203の厚みは、10μm以上かつ500μm以下であってもよい。負極の厚みが10μmより薄い場合には、十分な電池のエネルギー密度の確保が困難となる可能性がある。また、負極の厚みが500μmより厚い場合には、高出力での動作が困難となる可能性がある。
正極201と電解質層202と負極203とのうちの少なくとも1つには、イオン伝導性または化学的安定性・電気化学的安定性を高める目的で、硫化物固体電解質または酸化物固体電解質が含まれてもよい。硫化物固体電解質として、Li2S-P2S5、Li2S-SiS2、Li2S-B2S3、Li2S-GeS2、Li3.25Ge0.25P0.75S4、Li10GeP2S12、など、が用いられうる。酸化物固体電解質として、LiTi2(PO4)3およびその元素置換体を代表とするNASICON型固体電解質、(LaLi)TiO3系のペロブスカイト型固体電解質、Li14ZnGe4O16、Li4SiO4、LiGeO4およびその元素置換体を代表とするLISICON型固体電解質、Li7La3Zr2O12およびその元素置換体を代表とするガーネット型固体電解質、Li3NおよびそのH置換体、Li3PO4およびそのN置換体、など、が用いられうる。
正極201と電解質層202と負極203とのうちの少なくとも1つには、イオン伝導性を高める目的で、有機ポリマー固体電解質が含まれてもよい。有機ポリマー固体電解質として、例えば高分子化合物と、リチウム塩との化合物が用いられうる。高分子化合物はエチレンオキシド構造を有していてもよい。エチレンオキシド構造を有することで、リチウム塩を多く含有することができ、イオン導電率をより高めることができる。リチウム塩としては、LiPF6、LiBF4、LiSbF6、LiAsF6、LiSO3CF3、LiN(SO2CF3)2、LiN(SO2C2F5)2、LiN(SO2CF3)(SO2C4F9)、LiC(SO2CF3)3、など、が使用されうる。リチウム塩として、これらから選択される1種のリチウム塩が、単独で、使用されうる。もしくは、リチウム塩として、これらから選択される2種以上のリチウム塩の混合物が、使用されうる。
正極201と電解質層202と負極203とのうちの少なくとも1つには、リチウムイオンの授受を容易にし、電池の出力特性を向上する目的で、非水電解質液、ゲル電解質、イオン液体が含まれてもよい。
非水電解液は、非水溶媒と、非水溶媒に溶けたリチウム塩と、を含む。非水溶媒としては、環状炭酸エステル溶媒、鎖状炭酸エステル溶媒、環状エーテル溶媒、鎖状エーテル溶媒、環状エステル溶媒、鎖状エステル溶媒、フッ素溶媒、など、が使用されうる。環状炭酸エステル溶媒の例としては、エチレンカーボネート、プロピレンカーボネート、ブチレンカーボネート、など、が挙げられる。鎖状炭酸エステル溶媒の例としては、ジメチルカーボネート、エチルメチルカーボネート、ジエチルカーボネート、など、が挙げられる。環状エーテル溶媒の例としては、テトラヒドロフラン、1,4-ジオキサン、1,3-ジオキソラン、など、が挙げられる。鎖状エーテル溶媒としては、1,2-ジメトキシエタン、1,2-ジエトキシエタン、など、が挙げられる。環状エステル溶媒の例としては、γ-ブチロラクトン、など、が挙げられる。鎖状エステル溶媒の例としては、酢酸メチル、など、が挙げられる。フッ素溶媒の例としては、フルオロエチレンカーボネート、フルオロプロピオン酸メチル、フルオロベンゼン、フルオロエチルメチルカーボネート、フルオロジメチレンカーボネート、など、が挙げられる。非水溶媒として、これらから選択される1種の非水溶媒が、単独で、使用されうる。もしくは、非水溶媒として、これらから選択される2種以上の非水溶媒の組み合わせが、使用されうる。非水電解液には、フルオロエチレンカーボネート、フルオロプロピオン酸メチル、フルオロベンゼン、フルオロエチルメチルカーボネート、フルオロジメチレンカーボネートからなる群より選択される少なくとも1種のフッ素溶媒が含まれていてもよい。リチウム塩としては、LiPF6、LiBF4、LiSbF6、LiAsF6、LiSO3CF3、LiN(SO2CF3)2、LiN(SO2C2F5)2、LiN(SO2CF3)(SO2C4F9)、LiC(SO2CF3)3、など、が使用されうる。リチウム塩として、これらから選択される1種のリチウム塩が、単独で、使用されうる。もしくは、リチウム塩として、これらから選択される2種以上のリチウム塩の混合物が、使用されうる。リチウム塩の濃度は、例えば、0.5から2mol/リットルの範囲にある。
ゲル電解質は、ポリマー材料に非水電解液を含ませたものを用いることができる。ポリマー材料として、ポリエチレンオキシド、ポリアクリルニトリル、ポリフッ化ビニリデン、ポリメチルメタクリレート、エチレンオキシド結合を有するポリマー、など、が用いられてもよい。
イオン液体を構成するカチオンは、テトラアルキルアンモニウム、テトラアルキルホスホニウムなどの脂肪族鎖状4級塩類、ピロリジニウム類、モルホリニウム類、イミダゾリニウム類、テトラヒドロピリミジニウム類、ピペラジニウム類、ピペリジニウム類などの脂肪族環状アンモニウム、ピリジニウム類、イミダゾリウム類などの含窒ヘテロ環芳香族カチオンなどであってもよい。イオン液体を構成するアニオンは、PF6
-、BF4
-、SbF6-
-、AsF6
-、SO3CF3
-、N(SO2CF3)2
-、N(SO2C2F5)2
-、N(SO2CF3)(SO2C4F9)-、C(SO2CF3)3
-などであってもよい。また、イオン液体はリチウム塩を含有してもよい。
正極201と電解質層202と負極203とのうちの少なくとも1つには、粒子同士の密着性を向上する目的で、結着剤が含まれてもよい。結着剤は、電極を構成する材料の結着性を向上するために、用いられる。結着剤としては、ポリフッ化ビニリデン、ポリテトラフルオロエチレン、ポリエチレン、ポリプロピレン、アラミド樹脂、ポリアミド、ポリイミド、ポリアミドイミド、ポリアクリルニトリル、ポリアクリル酸、ポリアクリル酸メチルエステル、ポリアクリル酸エチルエステル、ポリアクリル酸ヘキシルエステル、ポリメタクリル酸、ポリメタクリル酸メチルエステル、ポリメタクリル酸エチルエステル、ポリメタクリル酸ヘキシルエステル、ポリ酢酸ビニル、ポリビニルピロリドン、ポリエーテル、ポリエーテルサルフォン、ヘキサフルオロポリプロピレン、スチレンブタジエンゴム、カルボキシメチルセルロース、など、が挙げられる。また、結着剤としては、テトラフルオロエチレン、ヘキサフルオロエチレン、ヘキサフルオロプロピレン、パーフルオロアルキルビニルエーテル、フッ化ビニリデン、クロロトリフルオロエチレン、エチレン、プロピレン、ペンタフルオロプロピレン、フルオロメチルビニルエーテル、アクリル酸、ヘキサジエンより選択された2種以上の材料の共重合体が用いられうる。また、これらのうちから選択された2種以上が混合されて、結着剤として用いられてもよい。
また、正極201および負極203のうちの少なくとも一方は、必要に応じて、導電助剤を含んでもよい。
導電助剤は、電極抵抗を低減するために、用いられる。導電助剤としては、天然黒鉛または人造黒鉛のグラファイト類、アセチレンブラック、ケッチェンブラックなどのカーボンブラック類、炭素繊維または金属繊維などの導電性繊維類、フッ化カーボン、アルミニウムなどの金属粉末類、酸化亜鉛またはチタン酸カリウムなどの導電性ウィスカー類、酸化チタンなどの導電性金属酸化物、ポリアニリン、ポリピロール、ポリチオフェンなどの導電性高分子化合物、など、が挙げられる。なお、導電助剤として、炭素導電助剤を用いることで、低コスト化が図れる。
なお、実施の形態2における電池は、コイン型、円筒型、角型、シート型、ボタン型、扁平型、積層型、など、種々の形状の電池として、構成されうる。
以下、実施例および比較例を用いて、本開示の詳細が説明される。
≪実施例A1≫
[固体電解質材料の作製]
露点-60℃以下のアルゴン雰囲気で、原料粉LiClとYCl3とZrCl4とを、モル比でLiCl:YCl3:ZrCl4=2.5:0.5:0.5となるように、秤量した。その後、遊星型ボールミルを用い、12時間、600rpmでミリング処理した。
[固体電解質材料の作製]
露点-60℃以下のアルゴン雰囲気で、原料粉LiClとYCl3とZrCl4とを、モル比でLiCl:YCl3:ZrCl4=2.5:0.5:0.5となるように、秤量した。その後、遊星型ボールミルを用い、12時間、600rpmでミリング処理した。
[リチウムイオン伝導度の評価]
図2は、リチウムイオン伝導度の評価方法を示す模式図である。
図2は、リチウムイオン伝導度の評価方法を示す模式図である。
加圧成形用ダイス300は、電子的に絶縁性のポリカーボネート製の枠型301と、電子伝導性のステンレス製のパンチ上部303およびパンチ下部302とから構成される。
図2に示す構成を用いて、下記の方法にて、イオン伝導度の評価を行った。
露点-30℃以下のドライ雰囲気で、実施例A1の固体電解質材料の粉末を加圧成形用ダイス300に充填し、400MPaで一軸加圧し、実施例A1の伝導度測定セルを作製した。
加圧状態のまま、パンチ上部303とパンチ下部302のそれぞれから導線を取り回し、周波数応答アナライザを搭載したポテンショスタット(Princeton Applied Research社 VersaSTAT4)に接続し、電気化学的インピーダンス測定法により、室温におけるイオン伝導度の測定を行った。
インピーダンス測定結果のCole-Cole線図を図3に示す。
図3において、複素インピーダンスの位相の絶対値が最も小さい測定点(図3中の矢印)のインピーダンスの実数値を実施例A1の固体電解質のイオン伝導に対する抵抗値とみなした。
電解質の抵抗値を用いて、下記式より、イオン伝導度を算出した。
σ=(RSE×S/t)-1
ここで、σはイオン伝導度、Sは電解質面積(図2中、枠型301の内径)、RSEは上記のインピーダンス測定における固体電解質の抵抗値、tは電解質の厚み(図2中、複数の固体電解質粒子100の圧縮体の厚み)である。
σ=(RSE×S/t)-1
ここで、σはイオン伝導度、Sは電解質面積(図2中、枠型301の内径)、RSEは上記のインピーダンス測定における固体電解質の抵抗値、tは電解質の厚み(図2中、複数の固体電解質粒子100の圧縮体の厚み)である。
22℃で測定された、実施例A1の固体電解質材料のイオン伝導度は、1.2×10-3S/cmであった。
[結晶構造の解析]
図4Aは、XRDパターンを示すグラフである。
図4Aは、XRDパターンを示すグラフである。
図4Aに示される結果は、下記の方法により、測定された。
すなわち、固体電解質の結晶構造の解析には、X線回折装置(RIGAKU社MiniFlex600)を用いて、露点-45℃以下のドライ環境でX線回折パターンを測定した。X線源については、Cu-Kα線を用いた。
図4Bは、上述のXRDパターンの横軸2θをq=4πsin(θ)/λで変換し、更に、前述のピーク位置2θ=31.64°におけるq値、q2=2.222Å―1で規格化したq/q2の値を横軸にとった場合の回折図形である。図4Bにおいては、q/q2=0.507、1.289、1.530の位置にピークを観測した。これらのピークのq値をq1/q2=0.507、q3/q2=1.289、q4/q2=1.530とし、式(2)を用いてaaveの値を算出すると、5.232Åであった。式(3)においてxCl=1,xBr=0,xI=0を用いてaLiXを算出し、aave/aLiXの値を算出すると、aave/aLiX=1.020であった。
[二次電池の作製]
アルゴングローブボックス内で、実施例A1の固体電解質材料と、活物質であるLiCoO2を、70:30の体積比率で秤量した。これらをメノウ乳鉢で混合することで、合剤を作製した。
アルゴングローブボックス内で、実施例A1の固体電解質材料と、活物質であるLiCoO2を、70:30の体積比率で秤量した。これらをメノウ乳鉢で混合することで、合剤を作製した。
絶縁性外筒の中で、実施例A1の固体電解質材料を700μm厚相当分、上述の合剤を8.5mg、Al粉末を16.5mgの順に積層した。これを300MPaの圧力で加圧成型することで、第1電極と固体電解質層を得た。
次に、固体電解質層の第1電極と接する側とは反対側に、金属In(厚さ200μm)を積層した。これを80MPaの圧力で加圧成型することで、第1電極、固体電解質層、第2電極からなる積層体を作製した。
次に、積層体の上下にステンレス鋼集電体を配置し、集電体に集電リードを付設した。
最後に、絶縁性フェルールを用いて、絶縁性外筒内部を外気雰囲気から遮断・密閉した。
以上により、実施例A1の二次電池を作製した。
[充放電試験]
実施例A1の二次電池の充放電試験を下記の方法で行った。
実施例A1の二次電池の充放電試験を下記の方法で行った。
実施例A1の二次電池を、25℃の恒温槽に、配置した。
電池の理論容量に対して0.05Cレート(20時間率)となる電流値で、定電流充電し、電圧3.6Vで充電を終了した。
次に、同じく0.05Cレートとなる電流値で、放電し、電圧1.9Vで放電を終了した。
以上の測定の結果、実施例A1の二次電池の初期放電容量は、0.467mAhであった。
≪実施例A2からA11≫
以下、実施例A2からA11の合成および評価方法について説明する。
以下、実施例A2からA11の合成および評価方法について説明する。
[固体電解質材料の作製]
実施例A2からA11においては、露点-60℃以下、酸素値5ppm以下のドライ・低酸素雰囲気で保たれるグローブボックス内で、所定の組成となるよう原料粉を秤量した。実施例A2からA11のそれぞれにおいて作製した固体電解質の組成は、後述の表1に示される。例えば、組成がLiaYbMcCldの場合、LiCl:YCl3:MClm=a:b:cの比で秤量し混合した。ここで、Mは金属元素で、mはMの価数である。その後、遊星型ボールミルを用い、12時間、600rpmでミリング処理した。実施例A3、A8においては、それぞれ500℃、300℃で5時間の熱処理を行った。
実施例A2からA11においては、露点-60℃以下、酸素値5ppm以下のドライ・低酸素雰囲気で保たれるグローブボックス内で、所定の組成となるよう原料粉を秤量した。実施例A2からA11のそれぞれにおいて作製した固体電解質の組成は、後述の表1に示される。例えば、組成がLiaYbMcCldの場合、LiCl:YCl3:MClm=a:b:cの比で秤量し混合した。ここで、Mは金属元素で、mはMの価数である。その後、遊星型ボールミルを用い、12時間、600rpmでミリング処理した。実施例A3、A8においては、それぞれ500℃、300℃で5時間の熱処理を行った。
[イオン伝導度の評価]
露点-90℃以下、酸素値5ppm以下のドライ・低酸素雰囲気で保たれるグローブボックス内で、上記の実施例A1と同様の方法で、実施例A2からA11のそれぞれの伝導度測定セルを作製した。
露点-90℃以下、酸素値5ppm以下のドライ・低酸素雰囲気で保たれるグローブボックス内で、上記の実施例A1と同様の方法で、実施例A2からA11のそれぞれの伝導度測定セルを作製した。
これ以外は、上記の実施例A1と同様の方法で、イオン伝導度の測定を行った。
上述の実施例A2からA11におけるイオン伝導度は、後述の表1に示される。
[結晶構造の解析]
上記の実施例A1と同様の方法で、実施例A2からA11のそれぞれの固体電解質材料の結晶構造の測定を行った。
上記の実施例A1と同様の方法で、実施例A2からA11のそれぞれの固体電解質材料の結晶構造の測定を行った。
実施例A1からA11のX線回折図形は、図4Aに示される。
実施例A1と同様に、図4Aに示されるX線回折図形の横軸2θをq=4πsin(θ)/λで変換し、更に、q=2.11Å-1から2.31Å-1の範囲内の強度の高いピークのq値をq2とした際に、q2で規格化したq/q2の値を横軸にとった場合の回折図形は図4Bに示される。
q/q2の値が、0.50から0.52、1.28から1.30、1.51から1.54の範囲内に、それぞれピークが観測された。これらのピークのq/q2の値、及び、q2の値は後述の表1に示される。これらの値と式(2)を用いてaaveの値を算出し、式(3)を用いてaave/aLiXの値を算出した。算出した結果は後述の表1に示される。
ただし、実施例A3については、q1,q2,q3,q4のいずれを求める際に、近接するピーク同士の強度によって重みづけされた加重平均より求めた。具体的には、q1の算出にはq=1.117と1.122のピークの加重平均、q2の算出にはq=2.195と2.202のピークの加重平均、q3の算出にはq=2.838と2.844のピークの加重平均、q4の算出にはq=3.355と3.369のピークの加重平均の値を用いた。
[二次電池の作製]
露点-90℃以下、酸素値5ppm以下のドライ・低酸素雰囲気で保たれるグローブボックス内で、実施例A2からA11のそれぞれの固体電解質材料と、正極活物質であるLiCoO2を、30:70の体積比率で秤量した。これらをメノウ乳鉢で混合することで、実施例A2からA11のそれぞれの正極合剤を作製した。
露点-90℃以下、酸素値5ppm以下のドライ・低酸素雰囲気で保たれるグローブボックス内で、実施例A2からA11のそれぞれの固体電解質材料と、正極活物質であるLiCoO2を、30:70の体積比率で秤量した。これらをメノウ乳鉢で混合することで、実施例A2からA11のそれぞれの正極合剤を作製した。
これら以外は、上記の実施例A1と同様の方法で、実施例A2からA11のそれぞれの二次電池を作製した。
[充放電試験]
上記の実施例A1と同様の方法で、実施例A2からA11のそれぞれの二次電池の充放電試験を行った。実施例A2からA11の初期放電特性は、実施例A1と同様の特性を示し、良好な放電特性を得た。実施例A2における初期放電特性を図5に示す。実施例A2の放電容量は0.657mAhであった。
上記の実施例A1と同様の方法で、実施例A2からA11のそれぞれの二次電池の充放電試験を行った。実施例A2からA11の初期放電特性は、実施例A1と同様の特性を示し、良好な放電特性を得た。実施例A2における初期放電特性を図5に示す。実施例A2の放電容量は0.657mAhであった。
≪実施例B1からB13≫
以下、実施例B1からB13の合成および評価方法について説明する。
以下、実施例B1からB13の合成および評価方法について説明する。
[固体電解質材料の作製]
実施例B1からB13においては、露点-60℃以下、酸素値5ppm以下のドライ・低酸素雰囲気で保たれるグローブボックス内で、原料粉を秤量した。実施例B1からB13のそれぞれにおいて作製した固体電解質の組成は、後述の表2に示される。
実施例B1からB13においては、露点-60℃以下、酸素値5ppm以下のドライ・低酸素雰囲気で保たれるグローブボックス内で、原料粉を秤量した。実施例B1からB13のそれぞれにおいて作製した固体電解質の組成は、後述の表2に示される。
例えば、組成がLiaYbMcBrdの場合、LiBr:YBr3:MBrm=a:b:cの比で秤量し混合した。ここで、Mは金属元素で、mはMの価数である。その後、遊星型ボールミルを用い、12時間、600rpmでミリング処理した。実施例B8においては、その後300℃で5時間の熱処理を行った。
これら以外は、上記の実施例A1と同様の方法で、実施例B1からB13のそれぞれの固体電解質材料を作製した。
[結晶構造の解析]
上記の実施例A1と同様の方法で、実施例B1からB13のそれぞれの固体電解質材料の結晶構造の測定を行った。
上記の実施例A1と同様の方法で、実施例B1からB13のそれぞれの固体電解質材料の結晶構造の測定を行った。
実施例B1からB13のX線回折図形は、図6Aに示される。
図6Aに示されるX線回折図形の横軸2θをq=4πsin(θ)/λで変換し、更に、q=1.76Å-1~2.18Å-1の範囲内の強度の高いピークのq値をq1’とした際に、q1’で規格化したq/q1’の値を横軸にとった場合の回折図形は図6Bに示される。
q/q1’の値が、1.14から1.17、1.62から1.65、1.88から1.94、1.9から2.1の範囲内に、それぞれピークが観測された。これらのピークのq/q1’の値、及び、q1’の値は後述の表2に示される。これらの値と式(4)を用いてaaveの値を算出し、式(3)を用いてaave/aLiXの値を算出した。算出した結果は後述の表2に示される。
[イオン伝導度の評価]
露点-90℃以下、酸素値5ppm以下のドライ・低酸素雰囲気で保たれるグローブボックス内で、上記の実施例A1と同様の方法で、実施例B1からB13のそれぞれの伝導度測定セルを作製した。
露点-90℃以下、酸素値5ppm以下のドライ・低酸素雰囲気で保たれるグローブボックス内で、上記の実施例A1と同様の方法で、実施例B1からB13のそれぞれの伝導度測定セルを作製した。
これ以外は、上記の実施例A1と同様の方法で、イオン伝導度の測定を行った。
上述の実施例B1からB13におけるイオン伝導度は、後述の表2に示される。
[二次電池の作製]
露点-90℃以下、酸素値5ppm以下のドライ・低酸素雰囲気で保たれるグローブボックス内で、実施例B1からB13のそれぞれの固体電解質材料と、正極活物質であるLiCoO2を、30:70の体積比率で秤量した。これらをメノウ乳鉢で混合することで、実施例B1からB13のそれぞれの正極合剤を作製した。
露点-90℃以下、酸素値5ppm以下のドライ・低酸素雰囲気で保たれるグローブボックス内で、実施例B1からB13のそれぞれの固体電解質材料と、正極活物質であるLiCoO2を、30:70の体積比率で秤量した。これらをメノウ乳鉢で混合することで、実施例B1からB13のそれぞれの正極合剤を作製した。
これら以外は、上記の実施例A1と同様の方法で、実施例B1からB13のそれぞれの二次電池を作製した。
[充放電試験]
上記の実施例A1と同様の方法で、実施例B1からB13のそれぞれの二次電池の充放電試験を行った。実施例B1からB13の初期放電特性は、実施例A1と同様の特性を示し、良好な充放電特性を得た。
上記の実施例A1と同様の方法で、実施例B1からB13のそれぞれの二次電池の充放電試験を行った。実施例B1からB13の初期放電特性は、実施例A1と同様の特性を示し、良好な充放電特性を得た。
≪比較例1から3≫
以下、比較例1から3の合成および評価方法について説明する。
以下、比較例1から3の合成および評価方法について説明する。
[固体電解質材料の作製]
比較例1から3においては、露点-60℃以下、酸素値5ppm以下のドライ・低酸素雰囲気で保たれるグローブボックス内で、原料粉を秤量した。比較例1から3のそれぞれにおいて作製した固体電解質の組成は、後述の表3に示される。比較例3においては、その後200℃で1時間の熱処理を行った。
比較例1から3においては、露点-60℃以下、酸素値5ppm以下のドライ・低酸素雰囲気で保たれるグローブボックス内で、原料粉を秤量した。比較例1から3のそれぞれにおいて作製した固体電解質の組成は、後述の表3に示される。比較例3においては、その後200℃で1時間の熱処理を行った。
これら以外は、上記の実施例A1と同様の方法で、比較例1から3のそれぞれの固体電解質材料を作製した。
[結晶構造の解析]
上記の実施例A1と同様の方法で、比較例1から3のそれぞれの固体電解質材料の結晶構造の測定を行った。
上記の実施例A1と同様の方法で、比較例1から3のそれぞれの固体電解質材料の結晶構造の測定を行った。
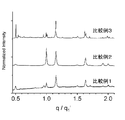
比較例1から3のX線回折図形は、図7Aに示される。
実施例B1と同様に、図7Aに示されるX線回折図形の横軸2θをq=4πsin(θ)/λで変換し、更に、q=1.76Å-1から2.18Å-1の範囲内の強度の高いピークのq値をq1’とした際に、q1’で規格化したq/q1’の値を横軸にとった場合の回折図形は図7Bに示される。
q/q1’の値が、1.14から1.17、1.62から1.65、1.88から1.94、1.9から2.1の範囲内に、それぞれピークが観測された。これらのピークのq/q1’の値、及び、q1’の値は後述の表2に示される。これらの値と式(4)を用いてaaveの値を算出し、式(3)を用いてaave/aLiXの値を算出した。算出した結果は後述の表3に示される。
ただし、比較例3については、q1’とq3’を求める際に、近接するピーク同士の強度によって重みづけされた加重平均より求めた。具体的には、q1’の算出にはq=2.078と2.109のピークの加重平均、q3’の算出にはq=3.389と3.429のピークの加重平均の値を用いた。
[イオン伝導度の評価]
露点-90℃以下、酸素値5ppm以下のドライ・低酸素雰囲気で保たれるグローブボックス内で、上記の実施例A1と同様の方法で、比較例1から3のそれぞれの伝導度測定セルを作製した。
露点-90℃以下、酸素値5ppm以下のドライ・低酸素雰囲気で保たれるグローブボックス内で、上記の実施例A1と同様の方法で、比較例1から3のそれぞれの伝導度測定セルを作製した。
これ以外は、上記の実施例A1と同様の方法で、イオン伝導度の測定を行った。
上述の比較例1から3におけるイオン伝導度は、後述の表3に示される。
[二次電池の作製]
露点-90℃以下、酸素値5ppm以下のドライ・低酸素雰囲気で保たれるグローブボックス内で、比較例2のそれぞれの固体電解質材料と、正極活物質であるLiCoO2を、30:70の体積比率で秤量した。これらをメノウ乳鉢で混合することで、比較例2の正極合剤を作製した。
露点-90℃以下、酸素値5ppm以下のドライ・低酸素雰囲気で保たれるグローブボックス内で、比較例2のそれぞれの固体電解質材料と、正極活物質であるLiCoO2を、30:70の体積比率で秤量した。これらをメノウ乳鉢で混合することで、比較例2の正極合剤を作製した。
これら以外は、上記の実施例A1と同様の方法で、比較例2の二次電池を作製した。
[充放電試験]
上記の実施例A1と同様の方法で、比較例2の二次電池の充放電試験を行った。比較例2の初期放電特性は、ほとんど放電せず、電池動作を示さなかった。
上記の実施例A1と同様の方法で、比較例2の二次電池の充放電試験を行った。比較例2の初期放電特性は、ほとんど放電せず、電池動作を示さなかった。
上述の実施例A1からA11,B1からB13および比較例1から3における各組成と評価結果とが、表1から3に示される。
≪考察≫
実施例A1からA11,B1からB13は、比較例1から3と比較して、室温近傍において、1×10-4S/cm以上の高いイオン伝導性を示すことがわかる。
実施例A1からA11,B1からB13は、比較例1から3と比較して、室温近傍において、1×10-4S/cm以上の高いイオン伝導性を示すことがわかる。
又、実施例A1からA11は、q/q2の値が、0.50から0.52、1.28から1.30、1.51から1.54の範囲にピークが観測され、ハロゲンイオンからなる副格子が六方最密充填構造、もしくは、六方最密充填構造が歪んだ構造である場合に観察される特徴的なピークを示した。実施例B1からB13においては、q/q’の範囲が、1.14-1.17、1.625-1.645、1.88-1.94、1.90-2.10の範囲にピークが観測され、ハロゲンイオンからなる副格子が立方最密充填構造、もしくは、立方最密充填構造が歪んだ構造である場合に観察される特徴的なピークを示した。実施例A1からA11、および、B1からB13は、aave/aLiXの値が1.018以上であった。このことは、実施例A1からA11,B1からB13のそれぞれの組成と同等のハロゲン比率を有するリチウムとハロゲンのみから成る結晶構造に比べ約1.8%以上の格子の広がりを有することに相当する。一方、比較例1から3においては、aave/aLiXの値が1.018未満であった。本発明において得られたイオン伝導度とaave/aLiXとの関係を図8に示す。明らかに、aave/aLiXが1.018以上の領域において、室温にてイオン伝導度が1×10-4S/cm以上の良好な特性が得られることを見出した。
特に、実施例A1と比較例3とを比べると、構成元素は同じであるものの、実施例A1のようにaave/aLiXの値が1.018を超える構造とすることで、比較例3に比べてイオン伝導度が大きく向上した。
また、実施例A1からA11,B1からB13においては、いずれも室温において電池の充放電動作を示した。一方で、比較例2においては、放電容量がほとんど取れず、電池動作の確認ができなかった。さらに、実施例A1からA1,B1からB13の材料は、構成元素に硫黄を含まないため、硫化水素の発生がない。
以上により、本開示による固体電解質材料は、硫化水素の発生が無く、かつ、高いリチウムイオン伝導度を示し、良好な充放電動作をすることができる電解質材料であることが示される。
本開示の電池は、例えば、全固体リチウム二次電池などとして、利用されうる。
100 固体電解質粒子
201 正極
202 電解質層
203 負極
204 正極活物質粒子
205 負極活物質粒子
300 加圧成形用ダイス
301 枠型
302 パンチ下部
303 パンチ上部
1000 電池
201 正極
202 電解質層
203 負極
204 正極活物質粒子
205 負極活物質粒子
300 加圧成形用ダイス
301 枠型
302 パンチ下部
303 パンチ上部
1000 電池
Claims (9)
- LiとMとXとからなり、
前記Mは、金属元素から選択される少なくとも1種であり、
前記Xは、Cl、Br、及びIからなる群より選択される少なくとも1種であり、
複数の前記Xの原子の副格子が最密充填構造を有し、
前記複数の前記Xの原子のうち、互いに隣接する2つの前記Xの原子間の距離の平均値は、Liと前記Xのみからなる岩塩構造における互いに隣接する2つの前記Xの原子間の距離に比べて、1.8%以上、長い、
固体電解質材料。 - 前記固体電解質材料のX線回折パターンを、横軸が回折角2θからqとなるように変換することにより得られる、第1の変換パターンが、
前記qの値が2.11Å-1以上2.31Å-1以下である範囲内に、基準ピークを含み、
ここで、q=4πsinθ/λであり、λはX線の波長であり、
前記X線回折パターンを、横軸が回折角2θからq/q2となるように変換することにより得られる、第2の変換パターンが、
前記q/q2の値が0.50以上0.52以下である第1範囲内、前記q/q2の値が1.28以上1.30以下である第2範囲内、及び前記q/q2の値が1.51以上1.54以下である第3範囲内からなる群から選択される少なくとも1つにおいて、ピークを含み、
ここで、q2は、前記第1の変換パターンにおける前記基準ピークに対応する前記qの値である、
請求項1に記載の固体電解質材料。 - 前記第2の変換パターンにおいて、
前記第1範囲内に前記ピークが含まれる場合にはc1=2/3、前記第1範囲内に前記ピークが含まれない場合にはc1=0とし、
c2=√(41/24)とし、
前記第2範囲内に前記ピークが含まれる場合にはc3=√(17/6)、前記第2範囲内に前記ピークが含まれない場合にはc3=0とし、
前記第3範囲内に前記ピークが含まれる場合にはc4=2、前記第3範囲内に前記ピークが含まれない場合にはc4=0とし、
前記第1範囲内に含まれる前記ピークの前記qの値をq1とし、
前記第2範囲内に含まれる前記ピークの前記qの値をq3とし、
前記第3範囲内に含まれる前記ピークの前記qの値をq4とし、
ここで、nはci≠0を満たすciの数であり、
前記Xに含まれるCl、Br、及びIのモル比を、Cl:Br:I=xCl:xBr:xI
とし、
ここで、xCl+xBr+xI=1であり、
aLiCl=5.130Å、aLiBr=5.500Å、aLiI=6.0257Å
とし、
請求項2に記載の固体電解質材料。 - 前記固体電解質材料のX線回折パターンを、横軸が回折角2θからqとなるように変換することにより得られる、第1の変換パターンが、
前記qの値が1.76Å-1以上2.18Å-1以下である範囲内に、基準ピークを含み、
ここで、q=4πsinθ/λであり、λはX線の波長であり、
前記X線回折パターンを、横軸が回折角2θからq/q1’となるように変換することにより得られる、第2の変換パターンが、
前記q/q1’の値が1.14以上1.17以下である第1範囲内、前記q/q1’の値が1.62以上1.65以下である第2範囲内、前記q/q1’の値が1.88以上1.94以下である第3範囲内、及び前記q/q1’の値が1.9以上2.1以下である第4範囲内からなる群から選択される少なくとも1つにおいて、ピークを含み、
ここで、q1’は、前記第1の変換パターンにおける前記基準ピークに対応する前記qの値である、
請求項1に記載の固体電解質材料。 - 前記第2の変換パターンにおいて、
c1’=√3とし、
前記第1範囲内に前記ピークが含まれる場合にはc2’=2、前記第1範囲内に前記ピークが含まれない場合にはc2’=0とし、
前記第2範囲内に前記ピークが含まれる場合にはc3’=2√2、前記第2範囲内に前記ピークが含まれない場合にはc3’=0とし、
前記第3範囲内に前記ピークが含まれる場合にはc4’=√11、前記第3範囲内に前記ピークが含まれない場合にはc4’=0とし、
前記第4範囲内に前記ピークが含まれる場合にはc5’=√12、前記第4範囲内に前記ピークが含まれない場合にはc5’=0とし、
前記第1範囲内に含まれる前記ピークの前記qの値をq2’とし、
前記第2範囲内に含まれる前記ピークの前記qの値をq3’とし、
前記第2範囲内に含まれる前記ピークの前記qの値をq4’とし、
前記第4範囲内に含まれる前記ピークの前記qの値をq5’とし、
ここで、n’はci’≠0を満たすci’の数であり、
前記Xに含まれるCl、Br、及びIのモル比を、Cl:Br:I=xCl:xBr:xI
とし、
ここで、xCl+xBr+xI=1であり、
aLiCl=5.130Å、aLiBr=5.500Å、aLiI=6.0257Å
とし、
請求項4に記載の固体電解質材料。 - 前記Mは、Yを含む、
請求項1から5のいずれかに記載の固体電解質材料。 - 前記Mは、Mg、Ca、Sr、Ba、Zn、Sc、La、Al、Sm、Bi、Zr、Hf、Nb、及びTaからなる群より選択される少なくとも1つ1種を含む、
請求項6に記載の固体電解質材料。 - 組成式Lia1Ma2Xa3で表され、
(a1+a2)/a3<0.7、を満たす、
請求項1から7のいずれかに記載の固体電解質材料。 - 正極と、
負極と、
前記正極と前記負極との間に設けられる電解質層と、
を備え、
前記正極、前記負極、及び前記電解質層からなる群から選択される少なくとも1つは、請求項1から8のいずれかに記載の固体電解質材料を含む、
電池。
Priority Applications (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP18898873.7A EP3736833A4 (en) | 2018-01-05 | 2018-12-17 | SOLID ELECTROLYTE MATERIAL AND BATTERY |
| JP2019563958A JPWO2019135348A1 (ja) | 2018-01-05 | 2018-12-17 | 固体電解質材料、および、電池 |
| CN201880070646.3A CN111279432B (zh) | 2018-01-05 | 2018-12-17 | 固体电解质材料和电池 |
| US16/915,424 US11560320B2 (en) | 2018-01-05 | 2020-06-29 | Solid electrolyte material and battery |
| JP2023201322A JP2024019241A (ja) | 2018-01-05 | 2023-11-29 | 固体電解質材料、および、電池 |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2018-000435 | 2018-01-05 | ||
| JP2018000435 | 2018-01-05 |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| US16/915,424 Continuation US11560320B2 (en) | 2018-01-05 | 2020-06-29 | Solid electrolyte material and battery |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2019135348A1 true WO2019135348A1 (ja) | 2019-07-11 |
Family
ID=67143742
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2018/046264 WO2019135348A1 (ja) | 2018-01-05 | 2018-12-17 | 固体電解質材料、および、電池 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US11560320B2 (ja) |
| EP (1) | EP3736833A4 (ja) |
| JP (2) | JPWO2019135348A1 (ja) |
| CN (1) | CN111279432B (ja) |
| WO (1) | WO2019135348A1 (ja) |
Cited By (18)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN111725560A (zh) * | 2020-05-31 | 2020-09-29 | 国联汽车动力电池研究院有限责任公司 | 化合物晶体及其制备方法和固体电解质材料、固态锂电池 |
| JPWO2019135341A1 (ja) * | 2018-01-05 | 2020-12-17 | パナソニックIpマネジメント株式会社 | 固体電解質材料、および、電池 |
| JPWO2019135342A1 (ja) * | 2018-01-05 | 2020-12-24 | パナソニックIpマネジメント株式会社 | 固体電解質材料、および、電池 |
| WO2021024876A1 (ja) * | 2019-08-07 | 2021-02-11 | Tdk株式会社 | 固体電解質、固体電解質層及び固体電解質電池 |
| WO2021075243A1 (ja) * | 2019-10-17 | 2021-04-22 | パナソニックIpマネジメント株式会社 | 固体電解質材料およびそれを用いた電池 |
| WO2021209380A1 (en) * | 2020-04-14 | 2021-10-21 | Solvay Sa | New lithium rare-earth halides |
| WO2021241172A1 (ja) * | 2020-05-28 | 2021-12-02 | パナソニックIpマネジメント株式会社 | 固体電解質材料およびそれを用いた電池 |
| WO2021260592A1 (en) * | 2020-06-23 | 2021-12-30 | Toyota Jidosha Kabushiki Kaisha | Metal lithium chloride derivatives in the space group of p21/c as li super-ionic conductor, solid electrolyte, and coating layer for li metal battery and li-ion battery |
| WO2021260584A1 (en) * | 2020-06-23 | 2021-12-30 | Toyota Jidosha Kabushiki Kaisha | Li zn cl4 derivatives in the space group of pmn2_1 as li super-ionic conductor, solid electrolyte, and coating layer for li metal battery and li-ion battery |
| KR20220139218A (ko) * | 2021-04-07 | 2022-10-14 | 연세대학교 산학협력단 | 리튬할라이드계 고체전해질, 이의 제조방법 및 상기 리튬할라이드계 고체전해질을 포함하는 전고체 전지 |
| US11522217B2 (en) | 2020-04-14 | 2022-12-06 | Saint-Gobain Ceramics & Plastics, Inc. | Electrolyte material and methods of forming |
| US11532816B2 (en) | 2020-04-23 | 2022-12-20 | Saint-Gobain Ceramics & Plastics, Inc. | Ion conductive layer including binder material |
| US11637315B2 (en) | 2020-08-07 | 2023-04-25 | Saint-Gobain Ceramics & Plastics, Inc. | Electrolyte material and methods of forming |
| US11664531B2 (en) | 2020-04-14 | 2023-05-30 | Saint-Gobain Ceramics & Plastics, Inc. | Ion conductive material including complex metal halide, electrolyte including the same, and methods of forming the same |
| KR20230092885A (ko) * | 2021-05-17 | 2023-06-26 | 세인트-고바인 세라믹스 앤드 플라스틱스, 인크. | 전해질 물질 및 형성 방법 |
| US11735765B2 (en) | 2021-01-08 | 2023-08-22 | Samsung Electronics Co., Ltd. | Solid ion conductor, solid electrolyte including the solid ion conductor, electrochemical device including the solid electrolyte, and method of preparing the solid ion conductor |
| US11757099B2 (en) | 2020-04-23 | 2023-09-12 | Saint-Gobain Ceramics & Plastics, Inc. | Ion conductive layer and methods of forming |
| US11961962B2 (en) | 2020-07-02 | 2024-04-16 | Samsung Electronics Co., Ltd. | Solid ion conductor compound, solid electrolyte including the same, electrochemical cell including the same, and preparation method thereof |
Families Citing this family (19)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP7253707B2 (ja) | 2018-01-05 | 2023-04-07 | パナソニックIpマネジメント株式会社 | 固体電解質材料、および、電池 |
| CN111492524B (zh) | 2018-01-05 | 2024-07-12 | 松下知识产权经营株式会社 | 固体电解质材料和电池 |
| EP3736822A4 (en) | 2018-01-05 | 2021-03-10 | Panasonic Intellectual Property Management Co., Ltd. | SOLID ELECTROLYTE AND BATTERY |
| EP3736829A4 (en) | 2018-01-05 | 2021-03-10 | Panasonic Intellectual Property Management Co., Ltd. | SOLID ELECTROLYTE MATERIAL AND BATTERY |
| CN111295789B (zh) | 2018-01-05 | 2024-07-19 | 松下知识产权经营株式会社 | 固体电解质材料和电池 |
| WO2019135346A1 (ja) | 2018-01-05 | 2019-07-11 | パナソニックIpマネジメント株式会社 | 正極材料、および、電池 |
| EP3736834A4 (en) | 2018-01-05 | 2021-03-10 | Panasonic Intellectual Property Management Co., Ltd. | SOLID ELECTROLYTE MATERIAL, AND BATTERY |
| CN111279431B (zh) | 2018-01-05 | 2022-03-25 | 松下知识产权经营株式会社 | 固体电解质材料和电池 |
| CN111480258B (zh) | 2018-01-05 | 2024-05-24 | 松下知识产权经营株式会社 | 电池 |
| CN111587508A (zh) | 2018-01-26 | 2020-08-25 | 松下知识产权经营株式会社 | 电池 |
| EP3745508A4 (en) | 2018-01-26 | 2021-03-17 | Panasonic Intellectual Property Management Co., Ltd. | POSITIVE ELECTRODE MATERIAL AND BATTERY USING IT |
| EP3745503A4 (en) | 2018-01-26 | 2021-03-10 | Panasonic Intellectual Property Management Co., Ltd. | POSITIVE ELECTRODE MATERIAL AND USING BATTERY |
| WO2020110479A1 (ja) | 2018-11-29 | 2020-06-04 | パナソニックIpマネジメント株式会社 | 負極材料、および、電池 |
| JP7429870B2 (ja) | 2018-11-29 | 2024-02-09 | パナソニックIpマネジメント株式会社 | 負極材料、および電池 |
| CN112840412B (zh) * | 2018-12-26 | 2023-12-08 | 松下知识产权经营株式会社 | 固体电解质和使用它的电池 |
| WO2020136951A1 (ja) | 2018-12-26 | 2020-07-02 | パナソニックIpマネジメント株式会社 | ハロゲン化物の製造方法 |
| WO2020137392A1 (ja) | 2018-12-26 | 2020-07-02 | パナソニックIpマネジメント株式会社 | 固体電解質材料およびそれを用いた電池 |
| US11928472B2 (en) | 2020-09-26 | 2024-03-12 | Intel Corporation | Branch prefetch mechanisms for mitigating frontend branch resteers |
| CN112397779B (zh) * | 2020-11-17 | 2022-09-27 | 郑州新世纪材料基因组工程研究院有限公司 | 一种卤族快离子导体 |
Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2006244734A (ja) * | 2005-02-28 | 2006-09-14 | National Univ Corp Shizuoka Univ | 全固体型リチウム二次電池 |
| JP2011129312A (ja) | 2009-12-16 | 2011-06-30 | Toyota Motor Corp | 硫化物固体電解質材料の製造方法、硫化物固体電解質材料およびリチウム電池 |
| JP2012246196A (ja) * | 2011-05-30 | 2012-12-13 | Ohara Inc | リチウムイオン伝導性無機物質 |
| JP2017518622A (ja) * | 2014-03-28 | 2017-07-06 | ビーワイディー カンパニー リミテッドByd Company Limited | リチウムイオン電池、固体電解質及びその作製方法 |
| WO2017154766A1 (ja) * | 2016-03-10 | 2017-09-14 | セイコーエプソン株式会社 | 固体電解質およびリチウムイオン電池 |
| WO2018025582A1 (ja) * | 2016-08-04 | 2018-02-08 | パナソニックIpマネジメント株式会社 | 固体電解質材料、および、電池 |
Family Cites Families (61)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4352869A (en) | 1980-12-24 | 1982-10-05 | Union Carbide Corporation | Solid state electrolytes |
| EP0055135B1 (en) | 1980-12-24 | 1985-06-19 | Union Carbide Corporation | Composition for use as solid state electrolyte and solid state cell employing same |
| US5714279A (en) * | 1989-10-24 | 1998-02-03 | The United States Of America As Represented By The Secretary Of The Navy | Non-aqueous lithium cells |
| JP3151925B2 (ja) | 1992-05-07 | 2001-04-03 | 松下電器産業株式会社 | 非晶質リチウムイオン伝導性固体電解質並びにその合成法 |
| US5506073A (en) * | 1992-06-22 | 1996-04-09 | Arizona State University (Arizona Board Of Regents, A Body Corporate Acting On Behalf Of Arizona State University) | Lithium ion conducting electrolytes |
| JPH08171938A (ja) | 1994-12-15 | 1996-07-02 | Mitsubishi Cable Ind Ltd | Li二次電池及びその正極 |
| JPH09293516A (ja) | 1996-04-25 | 1997-11-11 | Matsushita Electric Ind Co Ltd | 全固体リチウム電池 |
| JPH11238528A (ja) | 1998-02-20 | 1999-08-31 | Ngk Insulators Ltd | リチウム二次電池 |
| JP2001052733A (ja) | 1999-08-05 | 2001-02-23 | Matsushita Electric Ind Co Ltd | 全固体リチウム二次電池 |
| KR100513726B1 (ko) | 2003-01-30 | 2005-09-08 | 삼성전자주식회사 | 고체 전해질, 이를 채용한 전지 및 그 고체 전해질의 제조방법 |
| JP5076134B2 (ja) | 2004-06-08 | 2012-11-21 | 国立大学法人東京工業大学 | リチウム電池素子 |
| JP4945182B2 (ja) | 2006-07-13 | 2012-06-06 | シャープ株式会社 | リチウム二次電池及びその製造方法 |
| JP5448038B2 (ja) | 2009-02-27 | 2014-03-19 | 公立大学法人大阪府立大学 | 硫化物固体電解質材料 |
| JP2011065982A (ja) | 2009-08-18 | 2011-03-31 | Seiko Epson Corp | リチウム電池用電極体及びリチウム電池 |
| WO2012001773A1 (ja) | 2010-06-29 | 2012-01-05 | トヨタ自動車株式会社 | 硫化物固体電解質材料の製造方法、リチウム固体電池の製造方法 |
| US20130295464A1 (en) | 2011-01-27 | 2013-11-07 | Idemitsu Kosan Co., Ltd. | Composite material of alkaline metal sulfide and conducting agent |
| JP2013073791A (ja) | 2011-09-28 | 2013-04-22 | Panasonic Corp | 非水電解質二次電池 |
| WO2014010043A1 (ja) | 2012-07-11 | 2014-01-16 | トヨタ自動車株式会社 | 全固体電池及びその製造方法 |
| FR3004467B1 (fr) * | 2013-04-12 | 2016-05-27 | Saint-Gobain Cristaux Et Detecteurs | Fabrication d'une elpasolite stoechiometrique |
| FR3005207B1 (fr) | 2013-04-24 | 2016-06-24 | Batscap Sa | Electrode positive pour batterie lithium |
| JP6003831B2 (ja) | 2013-06-28 | 2016-10-05 | トヨタ自動車株式会社 | 硫化物固体電解質材料、硫化物ガラス、リチウム固体電池、および、硫化物固体電解質材料の製造方法 |
| WO2015011937A1 (ja) | 2013-07-25 | 2015-01-29 | 三井金属鉱業株式会社 | リチウムイオン電池用硫化物系固体電解質 |
| JP2015032529A (ja) | 2013-08-06 | 2015-02-16 | トヨタ自動車株式会社 | 硫化物系固体電解質 |
| WO2015030052A1 (ja) | 2013-09-02 | 2015-03-05 | 三菱瓦斯化学株式会社 | 全固体電池 |
| JP6187069B2 (ja) | 2013-09-13 | 2017-08-30 | 富士通株式会社 | リチウム電池 |
| WO2015049986A1 (ja) | 2013-10-04 | 2015-04-09 | 独立行政法人産業技術総合研究所 | 非晶質性の(リチウム)ニオブ硫化物又は(リチウム)チタンニオブ硫化物 |
| JP5873533B2 (ja) | 2014-07-16 | 2016-03-01 | 三井金属鉱業株式会社 | リチウムイオン電池用硫化物系固体電解質 |
| US9608288B2 (en) | 2014-07-17 | 2017-03-28 | Samsung Electronics Co., Ltd. | Positive electrode for lithium ion secondary battery and lithium ion secondary battery including the same |
| EP3220393B1 (en) | 2014-11-10 | 2021-06-30 | Murata Manufacturing Co., Ltd. | Glass ceramic, lithium-ion conductor, cell, electronic device, and method for manufacturing electrode |
| JP6222134B2 (ja) | 2015-02-25 | 2017-11-01 | トヨタ自動車株式会社 | 硫化物固体電解質材料、電池および硫化物固体電解質材料の製造方法 |
| JP6672848B2 (ja) | 2015-03-10 | 2020-03-25 | Tdk株式会社 | ガーネット型又はガーネット型類似の結晶構造を有するリチウムイオン伝導性酸化物セラミックス材料 |
| US10218032B2 (en) | 2015-03-10 | 2019-02-26 | Tdk Corporation | Li-ion conductive oxide ceramic material including garnet-type or similar crystal structure |
| US10446872B2 (en) | 2015-08-04 | 2019-10-15 | Samsung Electronics Co., Ltd. | Solid electrolyte and lithium battery including the same |
| JP2017059342A (ja) | 2015-09-15 | 2017-03-23 | トヨタ自動車株式会社 | 全固体電池の製造方法 |
| JP2017091953A (ja) | 2015-11-16 | 2017-05-25 | 旭化成株式会社 | リチウムイオン伝導体及びこれを用いたリチウムイオン電池 |
| JP2017091955A (ja) | 2015-11-16 | 2017-05-25 | 旭化成株式会社 | リチウムイオン伝導体及びこれを用いたリチウムイオン電池 |
| CN105254184A (zh) | 2015-11-27 | 2016-01-20 | 宁波大学 | 一种稀土离子掺杂的Li3YCl6微晶玻璃及其制备方法 |
| CN108292780B (zh) | 2015-12-22 | 2021-03-12 | 丰田自动车欧洲公司 | 用于固体电解质的材料 |
| US11245131B2 (en) * | 2015-12-25 | 2022-02-08 | Samsung Electronics Co., Ltd. | Solid electrolyte and lithium battery including the same |
| JP6881892B2 (ja) | 2015-12-25 | 2021-06-02 | 三星電子株式会社Samsung Electronics Co.,Ltd. | 固体電解質、全固体電池及び固体電解質の製造方法 |
| JP6748344B2 (ja) | 2016-02-26 | 2020-09-02 | 富士通株式会社 | 全固体電池 |
| JPWO2017154922A1 (ja) | 2016-03-08 | 2018-11-22 | 株式会社村田製作所 | 固体電解質、全固体電池、固体電解質の製造方法及び全固体電池の製造方法 |
| CN105680048B (zh) | 2016-04-05 | 2019-05-17 | 惠州亿纬锂能股份有限公司 | 一种包含氮掺杂石墨烯的正极、其制备方法及采用该正极的锂电池 |
| WO2017176936A1 (en) | 2016-04-05 | 2017-10-12 | Massachusetts Institute Of Technology | Lithium metal electrodes and batteries thereof |
| JP2017224474A (ja) | 2016-06-15 | 2017-12-21 | 出光興産株式会社 | 正極合材 |
| CN108258358B (zh) | 2016-12-28 | 2022-11-11 | 松下知识产权经营株式会社 | 电池 |
| CN111480258B (zh) | 2018-01-05 | 2024-05-24 | 松下知识产权经营株式会社 | 电池 |
| EP3736822A4 (en) | 2018-01-05 | 2021-03-10 | Panasonic Intellectual Property Management Co., Ltd. | SOLID ELECTROLYTE AND BATTERY |
| CN111492524B (zh) | 2018-01-05 | 2024-07-12 | 松下知识产权经营株式会社 | 固体电解质材料和电池 |
| CN111295719B (zh) * | 2018-01-05 | 2022-03-29 | 松下知识产权经营株式会社 | 固体电解质材料和电池 |
| CN111316378B (zh) | 2018-01-05 | 2021-09-28 | 松下知识产权经营株式会社 | 固体电解质材料和电池 |
| WO2019135346A1 (ja) | 2018-01-05 | 2019-07-11 | パナソニックIpマネジメント株式会社 | 正極材料、および、電池 |
| EP3736834A4 (en) | 2018-01-05 | 2021-03-10 | Panasonic Intellectual Property Management Co., Ltd. | SOLID ELECTROLYTE MATERIAL, AND BATTERY |
| CN111557058B (zh) | 2018-01-05 | 2023-09-01 | 松下知识产权经营株式会社 | 固体电解质材料和电池 |
| CN111295789B (zh) | 2018-01-05 | 2024-07-19 | 松下知识产权经营株式会社 | 固体电解质材料和电池 |
| EP3736829A4 (en) | 2018-01-05 | 2021-03-10 | Panasonic Intellectual Property Management Co., Ltd. | SOLID ELECTROLYTE MATERIAL AND BATTERY |
| CN111279431B (zh) | 2018-01-05 | 2022-03-25 | 松下知识产权经营株式会社 | 固体电解质材料和电池 |
| JP7253707B2 (ja) | 2018-01-05 | 2023-04-07 | パナソニックIpマネジメント株式会社 | 固体電解質材料、および、電池 |
| CN111566757B (zh) | 2018-01-26 | 2022-08-12 | 松下知识产权经营株式会社 | 固体电解质材料和电池 |
| EP3745422A4 (en) | 2018-01-26 | 2021-03-10 | Panasonic Intellectual Property Management Co., Ltd. | SOLID ELECTROLYTE AND BATTERY |
| EP3745518B1 (en) | 2018-01-26 | 2022-04-13 | Panasonic Intellectual Property Management Co., Ltd. | Battery |
-
2018
- 2018-12-17 WO PCT/JP2018/046264 patent/WO2019135348A1/ja unknown
- 2018-12-17 JP JP2019563958A patent/JPWO2019135348A1/ja active Pending
- 2018-12-17 CN CN201880070646.3A patent/CN111279432B/zh active Active
- 2018-12-17 EP EP18898873.7A patent/EP3736833A4/en active Pending
-
2020
- 2020-06-29 US US16/915,424 patent/US11560320B2/en active Active
-
2023
- 2023-11-29 JP JP2023201322A patent/JP2024019241A/ja active Pending
Patent Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2006244734A (ja) * | 2005-02-28 | 2006-09-14 | National Univ Corp Shizuoka Univ | 全固体型リチウム二次電池 |
| JP2011129312A (ja) | 2009-12-16 | 2011-06-30 | Toyota Motor Corp | 硫化物固体電解質材料の製造方法、硫化物固体電解質材料およびリチウム電池 |
| JP2012246196A (ja) * | 2011-05-30 | 2012-12-13 | Ohara Inc | リチウムイオン伝導性無機物質 |
| JP2017518622A (ja) * | 2014-03-28 | 2017-07-06 | ビーワイディー カンパニー リミテッドByd Company Limited | リチウムイオン電池、固体電解質及びその作製方法 |
| WO2017154766A1 (ja) * | 2016-03-10 | 2017-09-14 | セイコーエプソン株式会社 | 固体電解質およびリチウムイオン電池 |
| WO2018025582A1 (ja) * | 2016-08-04 | 2018-02-08 | パナソニックIpマネジメント株式会社 | 固体電解質材料、および、電池 |
Non-Patent Citations (5)
| Title |
|---|
| BOHNSACK, ANDREAS ET AL.: "Ternary Halides of the A3 MX 6 Type. VI. Ternary Chlorides of the Rare- Earth Elements with Lithium, Li3 MC 16(M=Tb-Lu, Y, Sc):Synthesis, Crystal Structures, and Ionic Motion", JOURNAL OF INORGANIC AND GENERAL CHEMISTRY, vol. 623, 1997, pages 1067 - 1073, XP055600040, DOI: doi:10.1002/chin.199739018 * |
| BOHNSACK, ANDREAS ET AL.: "Ternary Halides of the A3 MX 6Type. VII. The Bromides Li3MBr6 (M=Sm-Lu, Y): Synthesis, Crystal Structure, and Ionic Mobility", JOURNAL OF INORGANIC AND GENERAL CHEMISTRY, vol. 623, 1997, pages 1352 - 1356, XP055600030, DOI: doi:10.1002/zaac.19976230905 * |
| NATURE MATERIALS, vol. 14, 2015, pages 1026 - 1031 |
| See also references of EP3736833A4 |
| Z. ANORG. ALLG. CHEM., vol. 623, 1997, pages 1352 - 1356 |
Cited By (34)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP7165899B2 (ja) | 2018-01-05 | 2022-11-07 | パナソニックIpマネジメント株式会社 | 固体電解質材料、および、電池 |
| JPWO2019135341A1 (ja) * | 2018-01-05 | 2020-12-17 | パナソニックIpマネジメント株式会社 | 固体電解質材料、および、電池 |
| JPWO2019135342A1 (ja) * | 2018-01-05 | 2020-12-24 | パナソニックIpマネジメント株式会社 | 固体電解質材料、および、電池 |
| JP7165898B2 (ja) | 2018-01-05 | 2022-11-07 | パナソニックIpマネジメント株式会社 | 固体電解質材料、および、電池 |
| CN114207897A (zh) * | 2019-08-07 | 2022-03-18 | Tdk株式会社 | 固体电解质、固体电解质层和固体电解质电池 |
| CN114207897B (zh) * | 2019-08-07 | 2024-04-02 | Tdk株式会社 | 固体电解质、固体电解质层和固体电解质电池 |
| WO2021024876A1 (ja) * | 2019-08-07 | 2021-02-11 | Tdk株式会社 | 固体電解質、固体電解質層及び固体電解質電池 |
| JP7565544B2 (ja) | 2019-10-17 | 2024-10-11 | パナソニックIpマネジメント株式会社 | 固体電解質材料およびそれを用いた電池 |
| WO2021075243A1 (ja) * | 2019-10-17 | 2021-04-22 | パナソニックIpマネジメント株式会社 | 固体電解質材料およびそれを用いた電池 |
| EP4046971A4 (en) * | 2019-10-17 | 2022-11-23 | Panasonic Intellectual Property Management Co., Ltd. | SOLID ELECTROLYTE MATERIAL AND BATTERY WITH USE THEREOF |
| WO2021209380A1 (en) * | 2020-04-14 | 2021-10-21 | Solvay Sa | New lithium rare-earth halides |
| US11973186B2 (en) | 2020-04-14 | 2024-04-30 | Saint-Gobain Ceramics & Plastics, Inc. | Ion conductive material including halide material, electrolyte including the same, and methods of forming the same |
| US11978847B2 (en) | 2020-04-14 | 2024-05-07 | Saint-Gobain Ceramics & Plastics, Inc. | Ion conductive material, electrolyte including ion conductive material, and methods of forming |
| US11664531B2 (en) | 2020-04-14 | 2023-05-30 | Saint-Gobain Ceramics & Plastics, Inc. | Ion conductive material including complex metal halide, electrolyte including the same, and methods of forming the same |
| US11522217B2 (en) | 2020-04-14 | 2022-12-06 | Saint-Gobain Ceramics & Plastics, Inc. | Electrolyte material and methods of forming |
| US12095089B2 (en) | 2020-04-23 | 2024-09-17 | Saint-Gobain Ceramics & Plastics, Inc. | Ion conductive layer and methods of forming |
| US11532816B2 (en) | 2020-04-23 | 2022-12-20 | Saint-Gobain Ceramics & Plastics, Inc. | Ion conductive layer including binder material |
| US11984598B2 (en) | 2020-04-23 | 2024-05-14 | Saint-Gobain Ceramics & Plastics, Inc. | Ion conductive layer and methods of forming |
| US11735732B2 (en) | 2020-04-23 | 2023-08-22 | Saint-Gobain Ceramics & Plastics, Inc. | Ion conductive layer and methods of forming |
| US11757099B2 (en) | 2020-04-23 | 2023-09-12 | Saint-Gobain Ceramics & Plastics, Inc. | Ion conductive layer and methods of forming |
| EP4160746A4 (en) * | 2020-05-28 | 2024-07-10 | Panasonic Ip Man Co Ltd | SOLID ELECTROLYTE MATERIAL AND BATTERY IN WHICH IT IS USED |
| WO2021241172A1 (ja) * | 2020-05-28 | 2021-12-02 | パナソニックIpマネジメント株式会社 | 固体電解質材料およびそれを用いた電池 |
| CN111725560A (zh) * | 2020-05-31 | 2020-09-29 | 国联汽车动力电池研究院有限责任公司 | 化合物晶体及其制备方法和固体电解质材料、固态锂电池 |
| WO2021260584A1 (en) * | 2020-06-23 | 2021-12-30 | Toyota Jidosha Kabushiki Kaisha | Li zn cl4 derivatives in the space group of pmn2_1 as li super-ionic conductor, solid electrolyte, and coating layer for li metal battery and li-ion battery |
| WO2021260592A1 (en) * | 2020-06-23 | 2021-12-30 | Toyota Jidosha Kabushiki Kaisha | Metal lithium chloride derivatives in the space group of p21/c as li super-ionic conductor, solid electrolyte, and coating layer for li metal battery and li-ion battery |
| US11961962B2 (en) | 2020-07-02 | 2024-04-16 | Samsung Electronics Co., Ltd. | Solid ion conductor compound, solid electrolyte including the same, electrochemical cell including the same, and preparation method thereof |
| US11978849B2 (en) | 2020-08-07 | 2024-05-07 | Saint-Gobain Ceramics & Plastics, Inc. | Electrolyte material and methods of forming |
| US11637315B2 (en) | 2020-08-07 | 2023-04-25 | Saint-Gobain Ceramics & Plastics, Inc. | Electrolyte material and methods of forming |
| US11735765B2 (en) | 2021-01-08 | 2023-08-22 | Samsung Electronics Co., Ltd. | Solid ion conductor, solid electrolyte including the solid ion conductor, electrochemical device including the solid electrolyte, and method of preparing the solid ion conductor |
| KR102657399B1 (ko) * | 2021-04-07 | 2024-04-16 | 연세대학교 산학협력단 | 리튬할라이드계 고체전해질, 이의 제조방법 및 상기 리튬할라이드계 고체전해질을 포함하는 전고체 전지 |
| KR20220139218A (ko) * | 2021-04-07 | 2022-10-14 | 연세대학교 산학협력단 | 리튬할라이드계 고체전해질, 이의 제조방법 및 상기 리튬할라이드계 고체전해질을 포함하는 전고체 전지 |
| KR102637203B1 (ko) | 2021-05-17 | 2024-02-19 | 세인트-고바인 세라믹스 앤드 플라스틱스, 인크. | 전해질 물질 및 형성 방법 |
| US11848414B2 (en) | 2021-05-17 | 2023-12-19 | Saint-Gobain Ceramics & Plastics, Inc. | Electrolyte material and methods of forming |
| KR20230092885A (ko) * | 2021-05-17 | 2023-06-26 | 세인트-고바인 세라믹스 앤드 플라스틱스, 인크. | 전해질 물질 및 형성 방법 |
Also Published As
| Publication number | Publication date |
|---|---|
| US11560320B2 (en) | 2023-01-24 |
| US20200335817A1 (en) | 2020-10-22 |
| CN111279432B (zh) | 2022-09-09 |
| CN111279432A (zh) | 2020-06-12 |
| JP2024019241A (ja) | 2024-02-08 |
| EP3736833A4 (en) | 2021-03-10 |
| EP3736833A1 (en) | 2020-11-11 |
| JPWO2019135348A1 (ja) | 2021-01-14 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| WO2019135348A1 (ja) | 固体電解質材料、および、電池 | |
| US11498849B2 (en) | Solid electrolyte material and battery | |
| CN111295720B (zh) | 固体电解质材料及电池 | |
| JP6934626B2 (ja) | 固体電解質材料、および、電池 | |
| CN111492443B (zh) | 固体电解质材料和电池 | |
| WO2019146218A1 (ja) | 固体電解質材料、および、電池 | |
| WO2019135347A1 (ja) | 固体電解質材料、および、電池 | |
| WO2019135317A1 (ja) | 固体電解質材料、および、電池 | |
| WO2019135344A1 (ja) | 固体電解質材料、および、電池 | |
| WO2019135320A1 (ja) | 固体電解質材料、および、電池 | |
| WO2019135316A1 (ja) | 固体電解質材料、および、電池 | |
| US11485646B2 (en) | Solid electrolyte material and battery | |
| WO2019135336A1 (ja) | 固体電解質材料、および、電池 | |
| CN111295721B (zh) | 固体电解质材料及电池 | |
| CN113039616A (zh) | 固体电解质材料和使用该材料的电池 | |
| WO2022180964A1 (ja) | 固体電解質材料およびそれを用いた電池 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 18898873 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 2019563958 Country of ref document: JP Kind code of ref document: A |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| ENP | Entry into the national phase |
Ref document number: 2018898873 Country of ref document: EP Effective date: 20200805 |