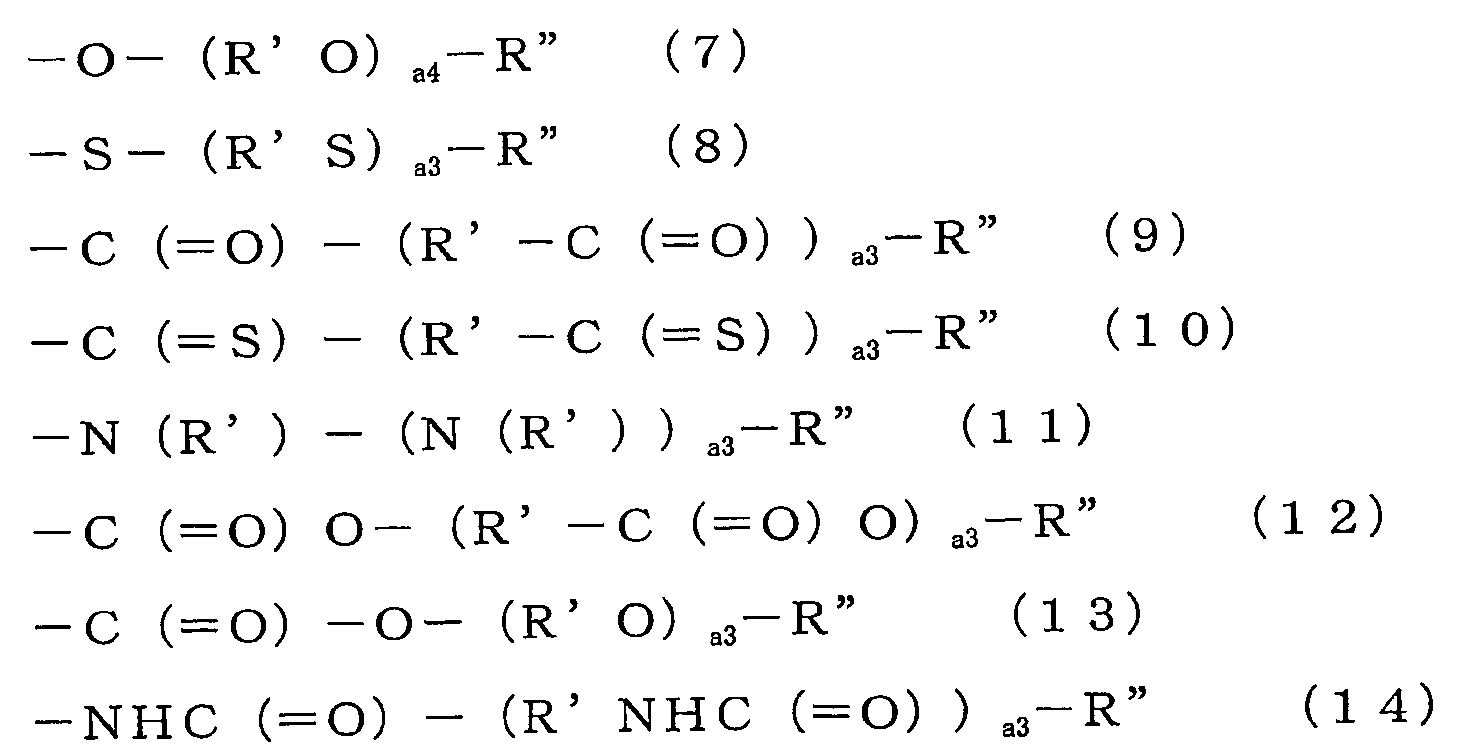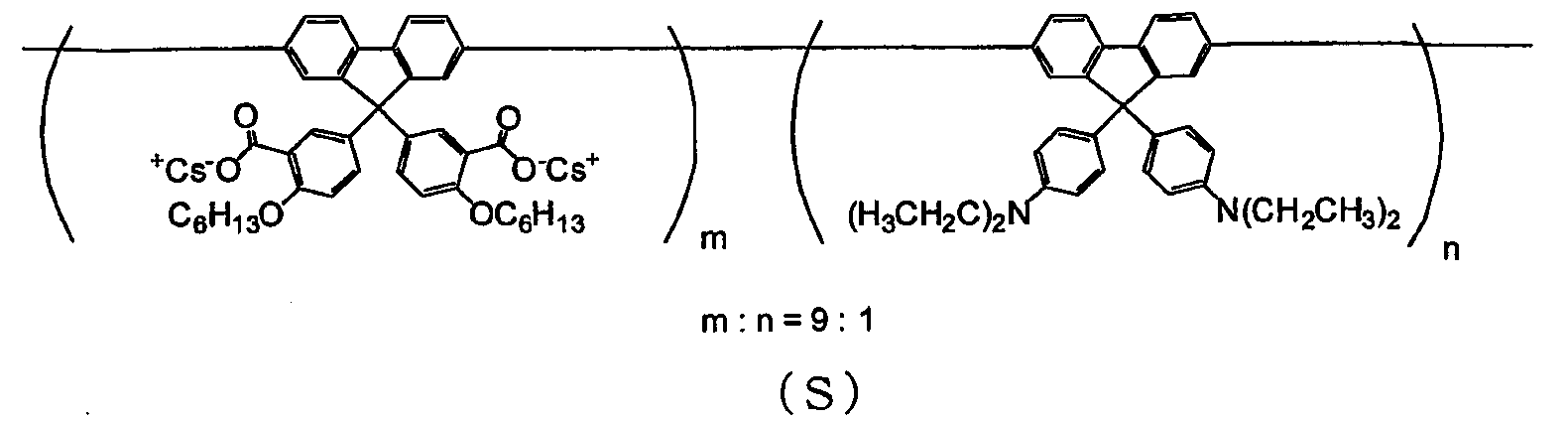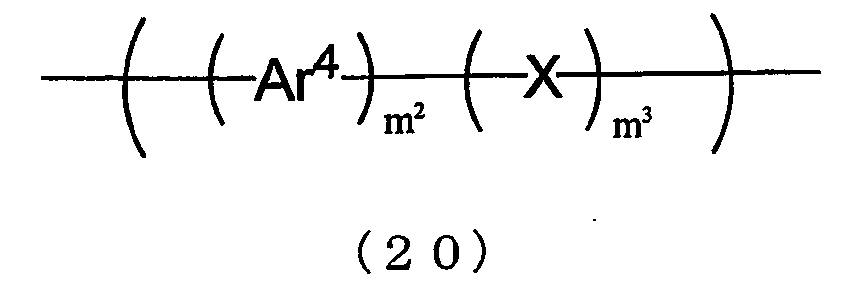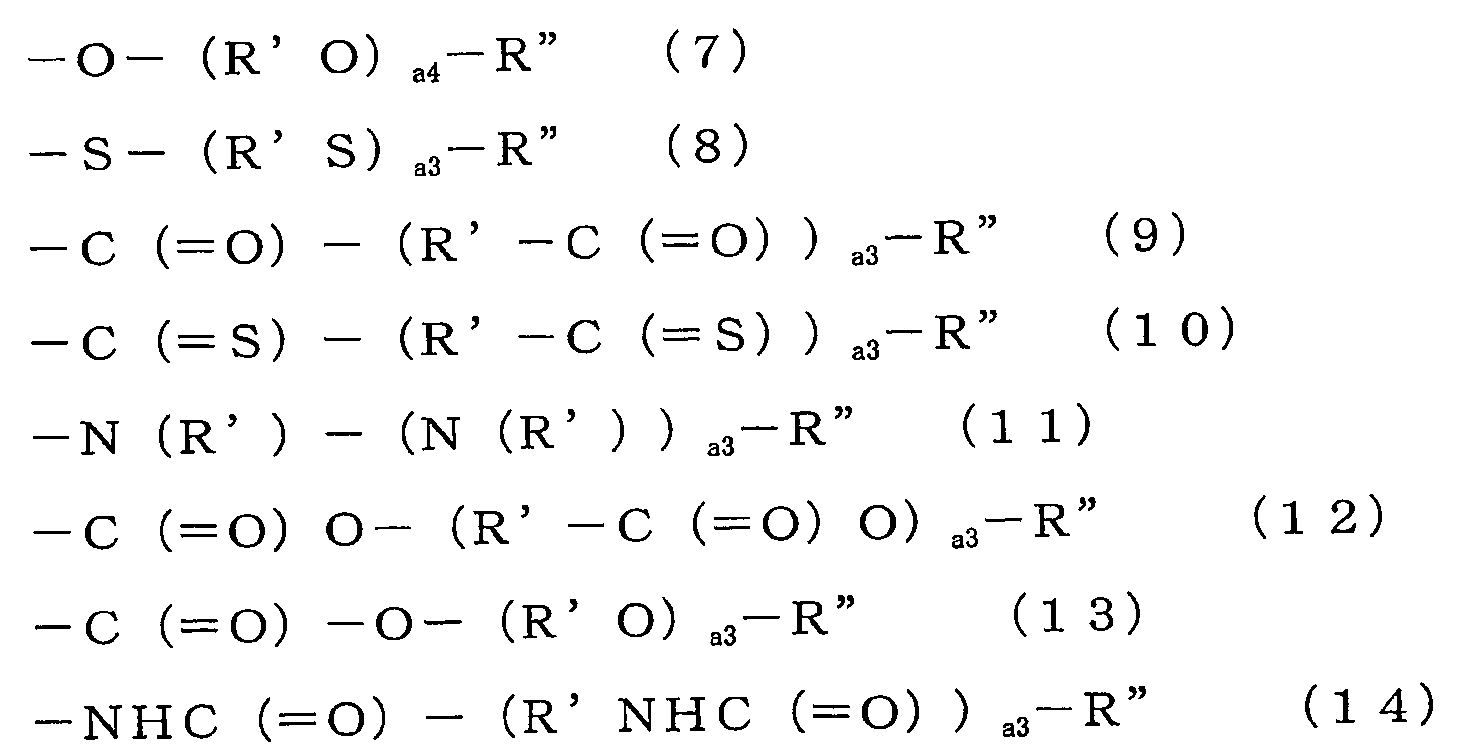KR20110000731A - 적층 구조체 - Google Patents
적층 구조체 Download PDFInfo
- Publication number
- KR20110000731A KR20110000731A KR1020107021391A KR20107021391A KR20110000731A KR 20110000731 A KR20110000731 A KR 20110000731A KR 1020107021391 A KR1020107021391 A KR 1020107021391A KR 20107021391 A KR20107021391 A KR 20107021391A KR 20110000731 A KR20110000731 A KR 20110000731A
- Authority
- KR
- South Korea
- Prior art keywords
- group
- formula
- substituent
- represented
- layer
- Prior art date
Links
- 0 C(C1)C2C1C*C2 Chemical compound C(C1)C2C1C*C2 0.000 description 5
Classifications
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G61/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
- C08G61/02—Macromolecular compounds containing only carbon atoms in the main chain of the macromolecule, e.g. polyxylylenes
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G61/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
- C08G61/12—Macromolecular compounds containing atoms other than carbon in the main chain of the macromolecule
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G61/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
- C08G61/12—Macromolecular compounds containing atoms other than carbon in the main chain of the macromolecule
- C08G61/122—Macromolecular compounds containing atoms other than carbon in the main chain of the macromolecule derived from five- or six-membered heterocyclic compounds, other than imides
-
- H—ELECTRICITY
- H05—ELECTRIC TECHNIQUES NOT OTHERWISE PROVIDED FOR
- H05B—ELECTRIC HEATING; ELECTRIC LIGHT SOURCES NOT OTHERWISE PROVIDED FOR; CIRCUIT ARRANGEMENTS FOR ELECTRIC LIGHT SOURCES, IN GENERAL
- H05B33/00—Electroluminescent light sources
- H05B33/12—Light sources with substantially two-dimensional radiating surfaces
- H05B33/20—Light sources with substantially two-dimensional radiating surfaces characterised by the chemical or physical composition or the arrangement of the material in which the electroluminescent material is embedded
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/14—Carrier transporting layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/10—Organic polymers or oligomers
- H10K85/111—Organic polymers or oligomers comprising aromatic, heteroaromatic, or aryl chains, e.g. polyaniline, polyphenylene or polyphenylene vinylene
- H10K85/115—Polyfluorene; Derivatives thereof
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G2261/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
- C08G2261/10—Definition of the polymer structure
- C08G2261/12—Copolymers
- C08G2261/124—Copolymers alternating
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G2261/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
- C08G2261/10—Definition of the polymer structure
- C08G2261/14—Side-groups
- C08G2261/142—Side-chains containing oxygen
- C08G2261/1426—Side-chains containing oxygen containing carboxy groups (COOH) and/or -C(=O)O-moieties
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G2261/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
- C08G2261/30—Monomer units or repeat units incorporating structural elements in the main chain
- C08G2261/31—Monomer units or repeat units incorporating structural elements in the main chain incorporating aromatic structural elements in the main chain
- C08G2261/314—Condensed aromatic systems, e.g. perylene, anthracene or pyrene
- C08G2261/3142—Condensed aromatic systems, e.g. perylene, anthracene or pyrene fluorene-based, e.g. fluorene, indenofluorene, or spirobifluorene
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G2261/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
- C08G2261/30—Monomer units or repeat units incorporating structural elements in the main chain
- C08G2261/31—Monomer units or repeat units incorporating structural elements in the main chain incorporating aromatic structural elements in the main chain
- C08G2261/316—Monomer units or repeat units incorporating structural elements in the main chain incorporating aromatic structural elements in the main chain bridged by heteroatoms, e.g. N, P, Si or B
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G2261/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
- C08G2261/30—Monomer units or repeat units incorporating structural elements in the main chain
- C08G2261/32—Monomer units or repeat units incorporating structural elements in the main chain incorporating heteroaromatic structural elements in the main chain
- C08G2261/322—Monomer units or repeat units incorporating structural elements in the main chain incorporating heteroaromatic structural elements in the main chain non-condensed
- C08G2261/3221—Monomer units or repeat units incorporating structural elements in the main chain incorporating heteroaromatic structural elements in the main chain non-condensed containing one or more nitrogen atoms as the only heteroatom, e.g. pyrrole, pyridine or triazole
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G2261/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
- C08G2261/50—Physical properties
- C08G2261/52—Luminescence
- C08G2261/522—Luminescence fluorescent
- C08G2261/5222—Luminescence fluorescent electrofluorescent
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G2261/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
- C08G2261/70—Post-treatment
- C08G2261/80—Functional group cleavage, e.g. removal of side-chains or protective groups
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E10/00—Energy generation through renewable energy sources
- Y02E10/50—Photovoltaic [PV] energy
- Y02E10/549—Organic PV cells
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10S—TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10S428/00—Stock material or miscellaneous articles
- Y10S428/917—Electroluminescent
Landscapes
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Organic Chemistry (AREA)
- Materials Engineering (AREA)
- Engineering & Computer Science (AREA)
- Optics & Photonics (AREA)
- Physics & Mathematics (AREA)
- Electroluminescent Light Sources (AREA)
- Polyoxymethylene Polymers And Polymers With Carbon-To-Carbon Bonds (AREA)
- Photovoltaic Devices (AREA)
Abstract
제 1 전극 및 제 2 전극과, 그 제 1 전극과 그 제 2 전극과의 사이에 발광층 혹은 전하 분리층을 가지며, 그 발광층 혹은 전하 분리층과 그 제 1 전극과의 사이에 공액 고분자 화합물을 포함하는 층을 가지며, 그 공액 고분자 화합물이 식 (1) 로 나타내지는 반복 단위 등으로 이루어지는 군에서 선택되는 반복 단위를 갖는 적층 구조체.
(식 중, Ar1 은 2 가의 방향족기를 나타내고, R1 은 식 (2) 로 나타내지는 기를 포함하는 치환기를 나타내고, 그 Ar1 은 R1 이외의 치환기를 가지고 있어도 된다. n1 은 1 이상의 정수를 나타낸다.)
(식 중, R2 는 치환기를 가지고 있어도 되는 2 가의 방향족기를 나타내고, Q1 은 치환기를 가지고 있어도 되는 2 가의 유기기를 나타내고, Y1 은 카르보 카티온, 암모늄 카티온, 포스포닐 카티온 또는 술포닐 카티온을 나타내고, M1 은 F-, Cl-, Br-, I-, OH-, RaSO3 -, RaCOO-, ClO-, ClO2 -, ClO3 -, ClO4 -, SCN-, CN-, NO3 -, SO4 2 -, HSO4 -, PO4 3 -, HPO4 2 -, H2PO4 -, BF4 - 또는 PF6 - 을 나타내고, Z1 은 금속 이온 또는 치환기를 가지고 있어도 되는 암모늄 이온을 나타내고, c1 은 0 또는 1 을 나타내고, n2 는 0 이상의 정수를 나타낸다. 단, c1 이 0 인 경우, n2 는 0 이다. a1 은 1 이상의 정수를 나타내고, b1 은 0 이상의 정수를 나타낸다. a1 및 b1 은, 식 (2) 로 나타내지는 치환기의 전하가 0 이 되도록 선택된다. Ra 는 치환기를 가지고 있어도 되는 탄소수 1 ∼ 30 의 알킬기 또는 치환기를 가지고 있어도 되는 탄소수 6 ∼ 50 의 아릴기를 나타낸다.
(식 중, Ar1 은 2 가의 방향족기를 나타내고, R1 은 식 (2) 로 나타내지는 기를 포함하는 치환기를 나타내고, 그 Ar1 은 R1 이외의 치환기를 가지고 있어도 된다. n1 은 1 이상의 정수를 나타낸다.)
(식 중, R2 는 치환기를 가지고 있어도 되는 2 가의 방향족기를 나타내고, Q1 은 치환기를 가지고 있어도 되는 2 가의 유기기를 나타내고, Y1 은 카르보 카티온, 암모늄 카티온, 포스포닐 카티온 또는 술포닐 카티온을 나타내고, M1 은 F-, Cl-, Br-, I-, OH-, RaSO3 -, RaCOO-, ClO-, ClO2 -, ClO3 -, ClO4 -, SCN-, CN-, NO3 -, SO4 2 -, HSO4 -, PO4 3 -, HPO4 2 -, H2PO4 -, BF4 - 또는 PF6 - 을 나타내고, Z1 은 금속 이온 또는 치환기를 가지고 있어도 되는 암모늄 이온을 나타내고, c1 은 0 또는 1 을 나타내고, n2 는 0 이상의 정수를 나타낸다. 단, c1 이 0 인 경우, n2 는 0 이다. a1 은 1 이상의 정수를 나타내고, b1 은 0 이상의 정수를 나타낸다. a1 및 b1 은, 식 (2) 로 나타내지는 치환기의 전하가 0 이 되도록 선택된다. Ra 는 치환기를 가지고 있어도 되는 탄소수 1 ∼ 30 의 알킬기 또는 치환기를 가지고 있어도 되는 탄소수 6 ∼ 50 의 아릴기를 나타낸다.
Description
본 발명은 적층 구조체에 관한 것이다.
적층 구조체를 포함하는 전계 발광 소자 혹은 광전 변환 소자의 특성을 향상시키기 위해서, 전계 발광 소자의 발광층과 전극 사이 혹은 광전 변환 소자의 전하 분리층과 전극 사이에 다양한 층을 삽입하는 검토가 이루어지고 있다. 예를 들어, 발광층과 전극 사이에, 카티온과 헤테로 원자를 2 개를 갖는 치환기를 포함하는 비공액 고분자 화합물로 이루어지는 층을 갖는 전계 발광 소자가 알려져 있다 (일본 공표특허공보 2003-530676호).
그러나, 상기 전계 발광 소자의 휘도는 아직 충분한 것은 아니었다.
본 발명의 목적은 고휘도로 발광하는 전계 발광 소자를 부여할 수 있는 적층 구조체를 제공하는 것에 있다.
즉 본 발명은 첫 번째로, 제 1 전극 및 제 2 전극과, 그 제 1 전극과 그 제 2 전극과의 사이에 발광층 혹은 전하 분리층을 가지며, 그 발광층 혹은 전하 분리층과 그 제 1 전극과의 사이에 공액 고분자 화합물을 포함하는 층을 가지며, 그 공액 고분자 화합물이 식 (1) 로 나타내지는 반복 단위, 식 (3) 으로 나타내지는 반복 단위 및 식 (5) 로 나타내지는 반복 단위로 이루어지는 군에서 선택되는 1 종 이상의 반복 단위를 갖는 적층 구조체를 제공한다.
(식 중, R1 은 식 (2) 로 나타내지는 기를 포함하고, Ar1 은 2 가의 방향족기를 나타내고, R1 은 식 (2) 로 나타내지는 기를 포함하는 치환기를 나타내고, 그 Ar1 은 R1 이외의 치환기를 가지고 있어도 된다. n1 은 1 이상의 정수를 나타낸다. R1 이 복수 개 있는 경우, 그들은 동일하여도 되고 상이하여도 된다.)
(식 중, R2 는 치환기를 가지고 있어도 되는 2 가의 방향족기를 나타내고, Q1 은 치환기를 가지고 있어도 되는 2 가의 유기기를 나타내고, Y1 은 카르보 카티온, 암모늄 카티온, 포스포닐 카티온 또는 술포닐 카티온을 나타내고, M1 은 F-, Cl-, Br-, I-, OH-, RaSO3 -, RaCOO-, ClO-, ClO2 -, ClO3 -, ClO4 -, SCN-, CN-, NO3 -, SO4 2-, HSO4 -, PO4 3-, HPO4 2-, H2PO4 -, BF4 - 또는 PF6 - 을 나타내고, Z1 은 금속 이온 또는 치환기를 가지고 있어도 되는 암모늄 이온을 나타내고, c1 은 0 또는 1 을 나타내고, n2 는 0 이상의 정수를 나타내고, c1 이 0 일 때는 n2 는 0 을 나타낸다. a1 은 1 이상의 정수를 나타내고, b1 은 0 이상의 정수를 나타낸다. a1 및 b1 은, 식 (2) 로 나타내지는 치환기의 전하가 0 이 되도록 선택된다. Ra 는 치환기를 가지고 있어도 되는 탄소수 1 ∼ 30 의 알킬기 또는 치환기를 가지고 있어도 되는 탄소수 6 ∼ 50 의 아릴기를 나타낸다. Q1 이 복수 개 있는 경우, 그들은 동일하여도 되고 상이하여도 된다. M1 이 복수 개 있는 경우, 그들은 동일하여도 되고 상이하여도 된다. Z1 이 복수 개 있는 경우, 그들은 동일하여도 되고 상이하여도 된다.)
(식 중, Ar2 는 2 가의 방향족기를 나타내고, R3 은 식 (4) 로 나타내지는 기를 포함하는 치환기를 나타내고, 그 Ar2 는 R3 이외의 치환기를 가지고 있어도 된다. n3 은 1 이상의 정수를 나타낸다. R3 이 복수 개 있는 경우, 그들은 동일하여도 되고 상이하여도 된다.)
(식 중, R4 는 치환기를 가지고 있어도 되는 2 가의 방향족기를 나타내고, Q2 는 치환기를 가지고 있어도 되는 2 가의 유기기를 나타내고, Y2 는 -CO2 -, -SO3 -, -SO2 -, 또는 -PO3 2 - 를 나타내고, M2 는 금속 카티온 또는 치환기를 가지고 있어도 되는 암모늄 카티온을 나타내고, Z2 는 F-, Cl-, Br-, I-, OH-, RbSO3 -, RbCOO-, ClO-, ClO2 -, ClO3 -, ClO4 -, SCN-, CN-, NO3 -, SO4 2-, HSO4 -, PO4 3-, HPO4 2-, H2PO4 -, BF4 - 또는 PF6 - 을 나타내고, c2 는 0 또는 1 을 나타내고, n4 는 0 이상의 정수를 나타낸다. 단, Y2 가 SO3 - 인 경우, n4 는 0 이다. a2 는 1 이상의 정수를 나타내고, b2 는 0 이상의 정수를 나타낸다. a2 및 b2 는, 식 (4) 로 나타내지는 치환기의 전하가 0 이 되도록 선택된다. Rb 는 치환기를 가지고 있어도 되는 탄소수 1 ∼ 30 의 알킬기 또는 치환기를 가지고 있어도 되는 탄소수 6 ∼ 50 의 아릴기를 나타낸다. Q2 가 복수 개 있는 경우, 그들은 동일하여도 되고 상이하여도 된다. M2 가 복수 개 있는 경우, 그들은 동일하여도 되고 상이하여도 된다. Z2 가 복수 개 있는 경우, 그들은 동일하여도 되고 상이하여도 된다.
(식 중, Ar3 은 2 가의 방향족기를 나타내고, R5 는 식 (6) 으로 나타내지는 기를 포함하는 치환기를 나타내고, 그 Ar3 은 R5 이외의 치환기를 가지고 있어도 된다. n5 는 1 이상의 정수를 나타낸다. 복수 개 있는 R5 는, 동일하여도 되고 상이하여도 된다.)
(식 중, R6 은 1 가의 방향족기를 나타내고, n6 은 0 이상의 정수를 나타내고, m1 은 1 이상의 정수를 나타낸다. Y3 은 -CN 또는 식 (7) ∼ (14) 로 나타내지는 기를 나타낸다. Y3 이 복수 개 있는 경우, 그들은 동일하여도 되고 상이하여도 된다. n6 이 복수 개 있는 경우, 그들은 동일하여도 되고 상이하여도 된다. 식 (6) 중, 헤테로 원자가 4 개 이상 포함된다.
(식 (7) ∼ (14) 중, R' 는 치환기를 가지고 있어도 되는 2 가의 탄화 수소기를 나타내고, R" 는 수소 원자, 치환기를 가지고 있어도 되는 1 가의 탄화 수소기, -COOH, -SO3H, -OH, -SH, -NRc 2, -CN 또는 -C(=O)NRc 2 를 나타내고, a3 은 0 이상의 정수를 나타내고, a4 는 3 ∼ 20 의 정수를 나타낸다. Rc 는 치환기를 가지고 있어도 되는 탄소수 1 ∼ 30 의 알킬기 또는 치환기를 가지고 있어도 되는 탄소수 6 ∼ 50 의 아릴기를 나타낸다. R'가 복수 개 있는 경우, 그들은 동일하여도 되고 상이하여도 된다.)
본 발명은 두 번째로, 제 1 전극이 음극인 상기 적층 구조체를 제공한다.
본 발명은 세 번째로, 제 1 전극 및 제 2 전극과, 그 제 1 전극과 그 제 2 전극과의 사이에 발광층 혹은 전하 분리층을 가지며, 그 발광층 혹은 전하 분리층과 그 제 1 전극과의 사이에 용해도 파라미터가 9.3 미만인 용매에 대해 불용인 공액 고분자 화합물을 포함하는 층을 갖는 적층 구조체를 제공한다.
본 발명은 네 번째로, 상기 적층 구조체를 포함하는 전계 발광 소자를 제공한다.
본 발명은 다섯 번째로, 상기 적층 구조체를 포함하는 광전 변환 소자를 제공한다.
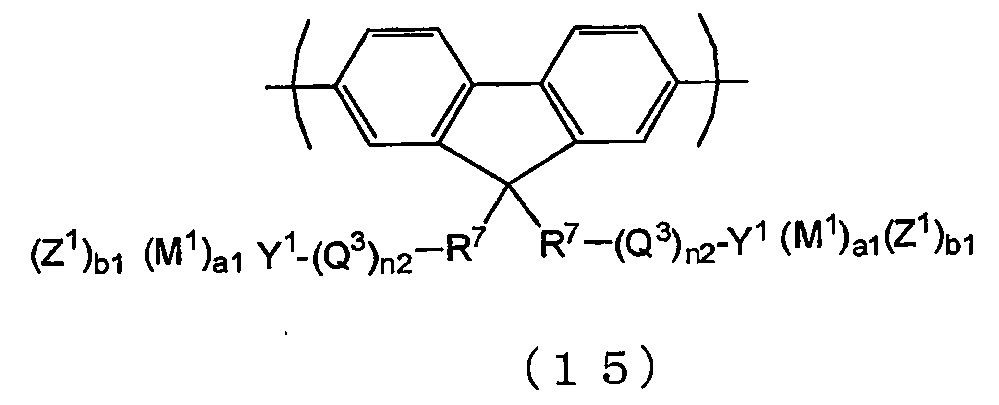
본 발명은 여섯 번째로, 식 (15) 로 나타내지는 반복 단위를 포함하는 공액 고분자 화합물을 제공한다.
(식 중, R7 은 치환기를 가지고 있어도 되는 2 가의 방향족기를 나타낸다. Q3 은 치환기를 가지고 있어도 되는 알킬렌기 또는 치환기를 가지고 있어도 되는 옥시알킬렌기를 나타내고, Y1 은 카르보 카티온, 암모늄 카티온, 포스포닐 카티온 또는 술포닐 카티온을 나타내고, M1 은 F-, Cl-, Br-, I-, OH-, RaSO3 -, RaCOO-, ClO-, ClO2 -, ClO3 -, ClO4 -, SCN-, CN-, NO3 -, SO4 2 -, HSO4 -, PO4 3 -, HPO4 2 -, H2PO4 -, BF4 - 또는 PF6 - 을 나타내고, Z1 은 금속 이온 또는 치환기를 가지고 있어도 되는 암모늄 이온을 나타내고, n2 는 0 이상의 정수를 나타낸다. a1 은 1 이상의 정수를 나타내고, b1 은 0 이상의 정수를 나타낸다. a1 및 b1 은 식 (15) 로 나타내지는 반복 단위의 전하가 0 이 되도록 선택된다. Ra 는 치환기를 가지고 있어도 되는 탄소수 1 ∼ 30 의 알킬기 또는 치환기를 가지고 있어도 되는 탄소수 6 ∼ 50 의 아릴기를 나타낸다. 복수 개 있는 R7, Y1, M1, a1, b1, n2 는 동일하여도 되고 상이하여도 된다. Z1 이 복수 개 있는 경우, 그들은 동일하여도 되고 상이하여도 된다. Q3 이 복수 개 있는 경우, 그들은 동일하여도 되고 상이하여도 된다.)
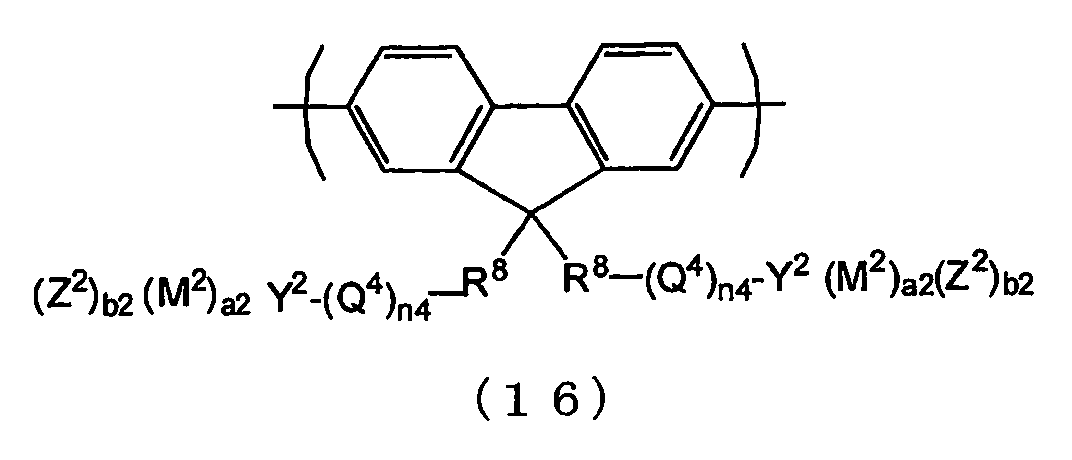
본 발명은 일곱 번째로, 식 (16) 으로 나타내지는 반복 단위를 포함하는 공액 고분자 화합물을 제공한다.
(식 중, R8 은 치환기를 가지고 있어도 되는 2 가의 방향족기를 나타낸다. Q4 는 치환기를 가지고 있어도 되는 알킬렌기 또는 치환기를 가지고 있어도 되는 옥시알킬렌기를 나타내고, Y2 는 -CO2 -, -SO3 -, -SO2 - 또는 -PO3 - 을 나타내고, M2 는 금속 카티온 또는 치환기를 가지고 있어도 되는 암모늄 카티온을 나타내고, Z2 는 F-, Cl-, Br-, I-, OH-, RbSO3 -, RbCOO-, ClO-, ClO2 -, ClO3 -, ClO4 -, SCN-, CN-, NO3 -, SO4 2-, HSO4 -, PO4 3-, HPO4 2-, H2PO4 -, BF4 - 또는 PF6 - 을 나타내고, n4 는 0 이상의 정수를 나타낸다. 단, Y2 가 SO3 -인 경우, n4 는 0 이다. a2 는 1 이상의 정수를 나타내고, b2 는 0 이상의 정수를 나타낸다. a2 및 b2 는 식 (16) 으로 나타내지는 반복 단위의 전하가 0 이 되도록 선택된다. Rb 는 치환기를 가지고 있어도 되는 탄소수 1 ∼ 30 의 알킬기 또는 치환기를 가지고 있어도 되는 탄소수 6 ∼ 50 의 아릴기를 나타낸다. 복수 개 있는 R8, Y2, M2, a2, b2, n4 는 동일하여도 되고 상이하여도 된다. Z2 가 복수 개 있는 경우, 그들은 동일하여도 되고 상이하여도 된다. Q4 가 복수 개 있는 경우, 그들은 동일하여도 되고 상이하여도 된다.)
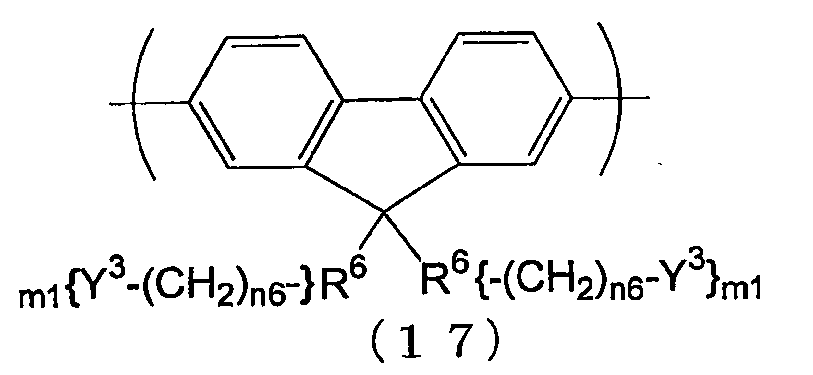
본 발명은 여덟 번째로, 식 (17) 로 나타내지는 반복 단위를 포함하는 공액 고분자 화합물을 제공한다.
(식 중, R6 은 1 가의 방향족기를 나타내고, n6 는 0 이상의 정수를 나타내고, m1 은 1 이상의 정수를 나타낸다. Y3 은 -CN 또는 식 (7) ∼ (14) 로 나타내지는 기를 나타낸다. 복수 개 있는 R6, m1, n6, Y3 은, 동일하여도 되고 상이하여도 된다.
(식 (7) ∼ (14) 중, R' 는 치환기를 가지고 있어도 되는 2 가의 탄화 수소기를 나타내고, R" 는 수소 원자, 치환기를 가지고 있어도 되는 1 가의 탄화 수소기, -COOH, -SO3H, -OH, -SH, -NRc 2, -CN 또는 -C(=O)NRc 2 를 나타내고, a3 은 0 이상의 정수를 나타내고, a4 는 3 ∼ 20 의 정수를 나타낸다. Rc 는 치환기를 가지고 있어도 되는 탄소수 1 ∼ 30 의 알킬기 또는 치환기를 가지고 있어도 되는 탄소수 6 ∼ 50 의 아릴기를 나타낸다. R'가 복수 개 있는 경우, 그들은 동일하여도 되고 상이하여도 된다.)
이하, 본 발명을 상세하게 설명한다.
본 발명에 사용되는 공액 고분자 화합물은, 식 (1) 로 나타내지는 반복 단위, 식 (3) 으로 나타내지는 반복 단위 및 식 (5) 로 나타내지는 반복 단위로 이루어지는 군에서 선택되는 1 종 이상의 반복 단위를 가지고 있다. 그 공액 고분자 화합물로서는, 식 (1) 로 나타내지는 반복 단위만을 갖는 공액 고분자 화합물, 식 (3) 으로 나타내지는 반복 단위만을 갖는 공액 고분자 화합물, 식 (5) 로 나타내지는 반복 단위만을 갖는 공액 고분자 화합물, 식 (1) 로 나타내지는 반복 단위 및 식 (3) 으로 나타내지는 반복 단위를 갖는 공액 고분자 화합물, 식 (1) 로 나타내지는 반복 단위 및 식 (5) 로 나타내지는 반복 단위를 갖는 공액 고분자 화합물, 식 (3) 으로 나타내지는 반복 단위 및 식 (5) 로 나타내지는 반복 단위를 갖는 공액 고분자 화합물, 식 (1) 로 나타내지는 반복 단위, 식 (3) 으로 나타내지는 반복 단위 및 식 (5) 로 나타내지는 반복 단위를 갖는 공액 고분자 화합물 등을 들 수 있다.
상기 공액 고분자 화합물은, 식 (1) 로 나타내지는 반복 단위를 2 종류 이상 포함하고 있어도 되고, 식 (3) 으로 나타내지는 반복 단위를 2 종류 이상 포함하고 있어도 되고, 식 (5) 로 나타내지는 반복 단위를 2 종류 이상 포함하고 있어도 된다.
식 (1) 로 나타내지는 반복 단위에 있어서, Ar1 은 2 가의 방향족기를 나타내고, R1 은 식 (2) 로 나타내지는 기를 포함하는 치환기를 나타내고, 그 Ar1 은 R1 이외의 치환기를 가지고 있어도 된다. n1 은 1 이상의 정수를 나타낸다. 식 (2) 로 나타내지는 기는, Ar1 에 직접 결합되어 있어도 되고, 치환기를 가지고 있어도 되는 메틸렌기, 에틸렌기, 프로필렌기, 부틸렌기, 펜틸렌기, 헥실렌기, 노닐렌기, 도데실렌기, 시클로프로필렌기, 시클로부틸렌기, 시클로펜틸렌기, 시클로헥실렌기, 시클로노닐렌기, 시클로도데실렌기, 노르보닐렌기, 아다만틸렌기 등의 탄소 원자수 1 ∼ 50 정도의 2 가의 알킬렌기, 치환기를 가지고 있어도 되는 옥시메틸렌기, 옥시에틸렌기, 옥시프로필렌기, 옥시부틸렌기, 옥시펜틸렌기, 옥시헥실렌기, 옥시노닐렌기, 옥시도데실렌기, 시클로프로필렌옥시기, 시클로부틸렌옥시기, 시클로펜틸렌옥시기, 시클로헥실렌옥시기, 시클로노닐렌옥시기, 시클로도데실렌옥시기, 노르보닐렌옥시기, 아다만틸렌옥시기 등의 탄소 원자수 1 ∼ 50 정도의 옥시알킬렌기, 치환기를 가지고 있어도 되는 이미노기, 치환기를 가지고 있어도 되는 실릴렌기, 치환기를 가지고 있어도 되는 에테닐렌기 또는 에티닐렌기, 치환기를 가지고 있어도 되는 메탄트리일기, 산소 원자, 질소 원자, 황 원자 등의 헤테로 원자를 개재하여 Ar1 에 결합되어 있어도 된다.
하나의 양태로서, R1 은 식 (2) 로 나타내지는 기이다.
식 (1) 중의 Ar1 로 나타내지는 2 가의 방향족기로서는, 2 가의 방향족 탄화 수소기, 2 가의 방향족 복소 고리기를 들 수 있으며, 탄소 원자, 수소 원자, 질소 원자 및 산소 원자로 이루어지는 군에서 선택되는 하나 이상의 원자로 이루어지는 2 가의 방향족기가 바람직하다. 그 2 가의 방향족기의 예로서는, 벤젠 고리, 피리딘 고리, 1,2-디아진 고리, 1,3-디아진 고리, 1,4-디아진 고리, 1,3,5-트리아진 고리, 푸란 고리, 피롤 고리, 피라졸 고리, 이미다졸 고리, 옥사졸 고리, 옥사디아졸 고리, 아자디아졸 고리 등의 단고리형 방향 고리로부터 수소 원자를 2 개 제외한 2 가의 기, 그 단고리형 방향 고리로부터 선택한 2 개 이상의 고리가 축합된 축합 다고리형 방향 고리로부터 수소 원자를 2 개 제외한 2 가의 기, 2 개 이상의 방향 고리를, 단결합, 에테닐렌기 또는 에티닐렌기로 연결한 다고리로부터 수소 원자를 2 개 제외한 2 가의 기, 2 개의 방향 고리를 메틸렌기, 에틸렌기, 카르보닐기 등의 2 가의 기로 가교된 구조를 갖는 가교된 다고리형 방향 고리로부터 수소 원자를 2 개 제외한 2 가의 기 등을 들 수 있다.
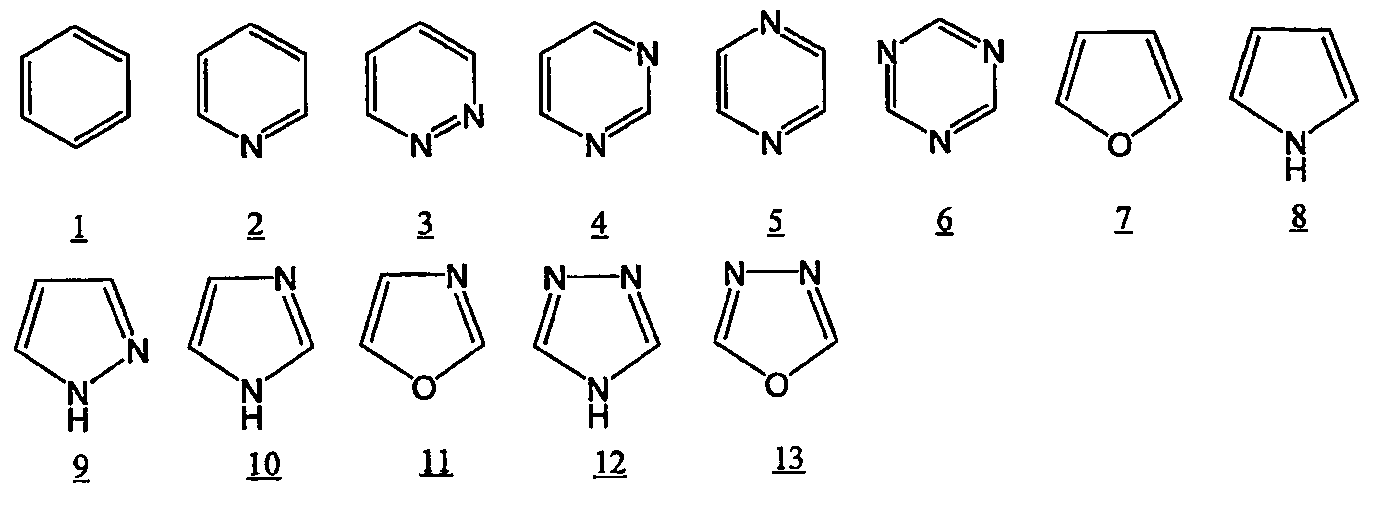
단고리형 방향 고리로서는, 예를 들어, 이하의 고리를 들 수 있다.
축합 다고리형 방향 고리로서는, 예를 들어, 이하의 고리를 들 수 있다.
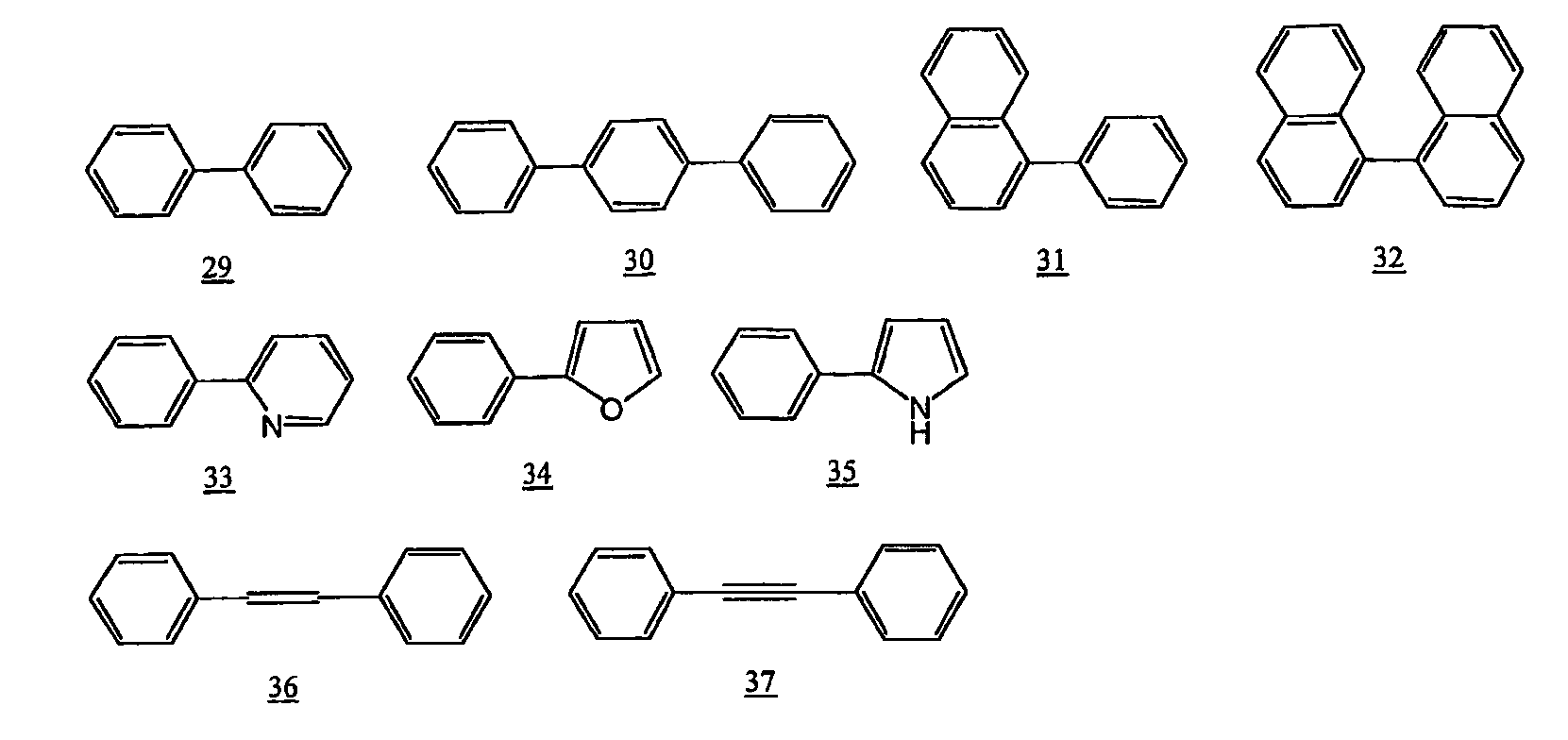
2 개 이상의 방향 고리를, 단결합, 에테닐렌기 또는 에티닐렌기로 연결한 다고리로서는, 예를 들어, 이하의 고리를 들 수 있다.
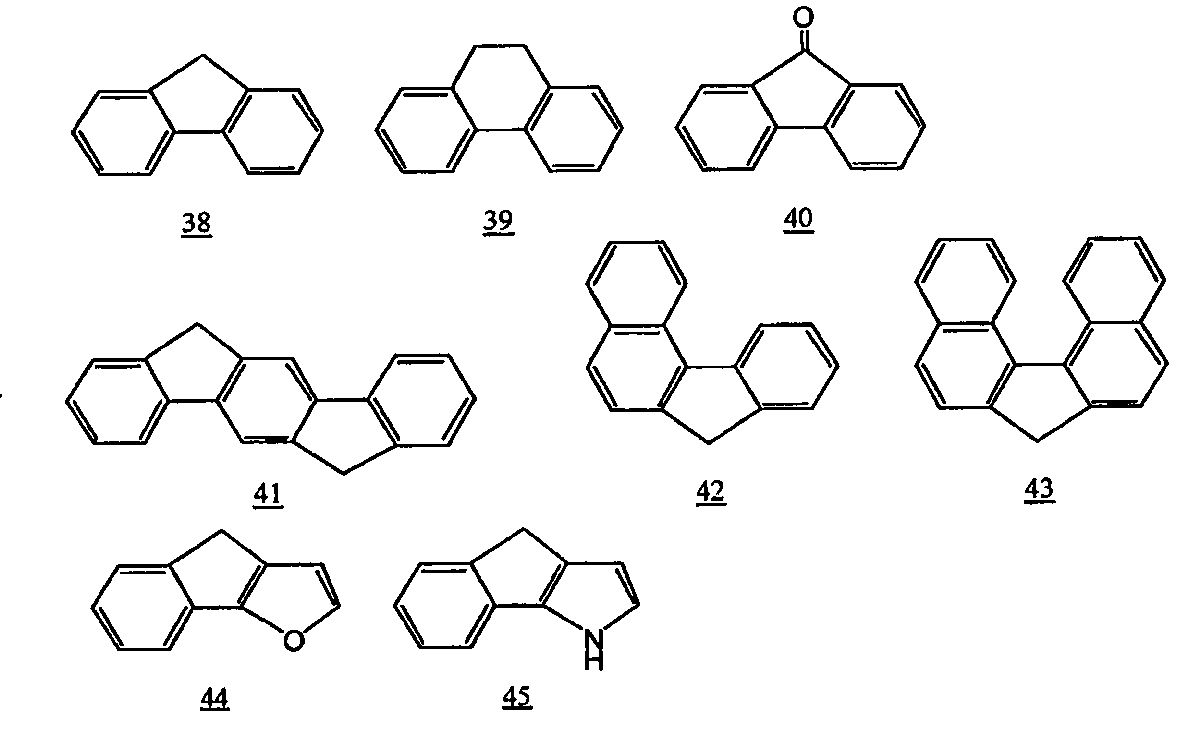
유교 다고리형 방향 고리로서는, 예를 들어, 이하의 고리를 들 수 있다.
상기 2 가의 방향족기로서는, 원료 모노머 합성의 용이함의 관점에서, 식 1 ∼ 15, 식 27 ∼ 30, 식 38 ∼ 40 또는 식 42 로 나타내지는 고리로부터 수소 원자를 2 개 제거한 기가 바람직하고, 식 1 ∼ 6, 식 8, 식 14, 식 27, 식 28, 식 38 또는 식 42 로 나타내지는 고리로부터 수소 원자를 2 개 제거한 기가 보다 바람직하고, 식 1, 식 38 또는 식 42 로 나타내지는 고리로부터 수소 원자를 2 개 제거한 기가 더욱 바람직하다.
상기 2 가의 방향족기는, R1 로 나타내지는 치환기를 1 개 이상 가지며, R1 로 나타내지는 치환기 이외의 치환기를 가지고 있어도 된다. 당해 치환기의 예로서는, 알킬기, 알콕시기, 알킬티오기, 아릴기, 아릴옥시기, 아릴티오기, 아릴알킬기, 아릴알콕시기, 아릴알킬티오기, 아릴알케닐기, 아릴알키닐기, 아미노기, 치환 아미노기, 실릴기, 치환 실릴기, 할로겐 원자, 아실기, 아실옥시기, 이민 잔기, 아미드기, 산이미드기, 1 가의 복소 고리기, 하이드록시기, 카르복실기, 치환 옥시카르보닐기, 시아노기 또는 니트로기 등을 들 수 있으며, 상기 치환기가 복수 개 존재하는 경우에는, 그들은 동일하여도 되고 상이하여도 된다.
알킬기는, 직사슬형이거나 분기형이어도 되고, 시클로알킬기여도 된다. 알킬기의 탄소수는 통상 1 ∼ 20 정도이며, 1 ∼ 10 이 바람직하다. 알킬기의 예로서는, 메틸기, 에틸기, 프로필기, 이소프로필기, 부틸기, 이소부틸기, s-부틸기, t-부틸기, 펜틸기, 헥실기, 시클로헥실기, 헵틸기, 옥틸기, 노닐기, 데실기, 라우릴기 등을 들 수 있다. 상기 알킬기 중의 수소 원자는 불소 원자로 치환되어 있어도 된다. 불소 원자로 치환된 알킬기의 예로서는, 트리플루오로메틸기, 펜타플루오로에틸기, 퍼플루오로부틸기, 퍼플루오로헥실기, 퍼플루오로옥틸기 등을 들 수 있다.
알콕시기는, 직사슬형이거나 분기사슬형이어도 되고, 시클로알킬옥시기이어도 되고, 치환기를 가지고 있어도 된다. 알콕시기의 탄소수는 통상 1 ∼ 20 정도이며, 1 ∼ 10 이 바람직하다. 알콕시기의 예로서는, 메톡시기, 에톡시기, 프로필옥시기, 이소프로필옥시기, 부톡시기, 이소부톡시기, s-부톡시기, t-부톡시기, 펜틸옥시기, 헥실옥시기, 시클로헥실옥시기, 헵틸옥시기, 옥틸옥시기, 노닐옥시기, 데실옥시기, 라우릴옥시기 등을 들 수 있다. 알콕시기에는 메톡시메틸옥시기, 2-메톡시에틸옥시기도 포함된다.
상기 알콕시기 중의 수소 원자는 불소 원자로 치환되어 있어도 된다. 불소 원자로 치환된 알콕시기의 예로서는, 트리플루오로메톡시기, 펜타플루오로에톡시기, 퍼플루오로부톡시기, 퍼플루오로헥실옥시기, 퍼플루오로옥틸옥시기 등을 들 수 있다.
알킬티오기는, 직사슬형이거나 분기사슬형이어도 되고, 시클로알킬티오기여도 되고, 치환기를 가지고 있어도 된다. 알킬티오기의 탄소수는 통상 1 ∼ 20 정도이며, 1 ∼ 10 이 바람직하다. 알킬티오기의 예로서는, 메틸티오기, 에틸티오기, 프로필티오기, 이소프로필티오기, 부틸티오기, 이소부틸티오기, s-부틸티오기, t-부틸티오기, 펜틸티오기, 헥실티오기, 시클로헥실티오기, 헵틸티오기, 옥틸티오기, 노닐티오기, 데실티오기, 라우릴티오기 등을 들 수 있다. 상기 알킬티오기 중의 수소 원자는 불소 원자로 치환되어 있어도 된다. 불소 원자로 치환된 알콕시기의 예로서는, 트리플루오로메틸티오기 등을 들 수 있다.
아릴기는, 방향족 탄화수소로부터 수소 원자 1 개를 제외한 원자단으로, 벤젠 고리를 갖는 것, 축합 고리를 갖는 것, 독립된 벤젠 고리 또는 축합 고리 2 개 이상이 직접 혹은 비닐렌 등의 2 가의 기를 개재하여 결합된 것도 포함된다. 아릴기는, 탄소수가 통상 6 ∼ 60 정도이며, 7 ∼ 48 이 바람직하다. 아릴기의 예로서는, 페닐기, C1 ∼ C12 알콕시페닐기 (C1 ∼ C12 는, 탄소수 1 ∼ 12 인 것을 나타낸다. 이하도 동일하다.), C1 ∼ C12 알킬페닐기, 1-나프틸기, 2-나프틸기, 1-안트라세닐기, 2-안트라세닐기, 9-안트라세닐기 등을 들 수 있다. 상기 아릴기 중의 수소 원자는 불소 원자로 치환되어 있어도 된다. 불소 원자로 치환된 아릴기의 예로서는, 펜타플루오로페닐기 등을 들 수 있다. 아릴기 중에서는, C1 ∼ C12 알콕시페닐기, C1 ∼ C12 알킬페닐기가 바람직하다.
C1 ∼ C12 알콕시페닐기의 예로서는, 메톡시페닐기, 에톡시페닐기, 프로필옥시페닐기, 이소프로필옥시페닐기, 부톡시페닐기, 이소부톡시페닐기, s-부톡시페닐기, t-부톡시페닐기, 펜틸옥시페닐기, 헥실옥시페닐기, 시클로헥실옥시페닐기, 헵틸옥시페닐기, 옥틸옥시페닐기, 2-에틸헥실옥시페닐기, 노닐옥시페닐기, 데실옥시페닐기, 3,7-디메틸옥틸옥시페닐기, 라우릴옥시페닐기 등을 들 수 있다.
C1 ∼ C12 알킬페닐기의 예로서는, 메틸페닐기, 에틸페닐기, 디메틸페닐기, 프로필페닐기, 메시틸기, 메틸에틸페닐기, 이소프로필페닐기, 부틸페닐기, 이소부틸페닐기, t-부틸페닐기, 펜틸페닐기, 이소아밀페닐기, 헥실페닐기, 헵틸페닐기, 옥틸페닐기, 노닐페닐기, 데실페닐기, 도데실페닐기 등을 들 수 있다.
아릴옥시기는, 탄소수가 통상 6 ∼ 60 정도이며, 7 ∼ 48 이 바람직하다. 아릴옥시기의 예로서는, 페녹시기, C1 ∼ C12 알콕시페녹시기, C1 ∼ C12 알킬페녹시기, 1-나프틸옥시기, 2-나프틸옥시기, 펜타플루오로페닐옥시기 등을 들 수 있다. 아릴옥시기 중에서는, C1 ∼ C12 알콕시페녹시기 및 C1 ∼ C12 알킬페녹시기가 바람직하다.
C1 ∼ C12 알콕시페녹시기의 예로서는, 메톡시페녹시기, 에톡시페녹시기, 프로필옥시페녹시기, 이소프로필옥시페녹시기, 부톡시페녹시기, 이소부톡시페녹시기, s-부톡시페녹시기, t-부톡시페녹시기, 펜틸옥시페녹시기, 헥실옥시페녹시기, 시클로헥실옥시페녹시기, 헵틸옥시페녹시기, 옥틸옥시페녹시기, 2-에틸헥실옥시페녹시기, 노닐옥시페녹시기, 데실옥시페녹시기, 3,7-디메틸옥틸옥시페녹시기, 라우릴옥시페녹시기 등을 들 수 있다.
C1 ∼ C12 알킬페녹시기의 예로서는, 메틸페녹시기, 에틸페녹시기, 디메틸페녹시기, 프로필페녹시기, 1,3,5-트리메틸페녹시기, 메틸에틸페녹시기, 이소프로필페녹시기, 부틸페녹시기, 이소부틸페녹시기, s-부틸페녹시기, t-부틸페녹시기, 펜틸페녹시기, 이소아밀페녹시기, 헥실페녹시기, 헵틸페녹시기, 옥틸페녹시기, 노닐페녹시기, 데실페녹시기, 도데실페녹시기 등을 들 수 있다.
아릴티오기는, 전술한 아릴기에 황 원소가 결합된 기이고, 상기 아릴기의 방향 고리 상에 치환기를 가지고 있어도 된다. 아릴티오기는, 탄소수가 통상 6 ∼ 60 정도이며, 6 ∼ 30 이 바람직하다. 아릴티오기의 예로서는, 페닐티오기, C1 ∼ C12 알콕시페닐티오기, C1 ∼ C12 알킬페닐티오기, 1-나프틸티오기, 2-나프틸티오기, 펜타플루오로페닐티오기 등을 들 수 있다.
아릴알킬기는, 전술한 아릴기에 전술한 알킬기가 결합된 기이고, 치환기를 가지고 있어도 된다. 아릴알킬기는, 탄소수가 통상 7 ∼ 60 정도이며, 7 ∼ 30 이 바람직하다. 아릴알킬기의 예로서는, 페닐-C1 ∼ C12 알킬기, C1 ∼ C12 알콕시페닐-C1 ∼ C12 알킬기, C1 ∼ C12 알킬페닐-C1 ∼ C12 알킬기, 1-나프틸-C1 ∼ C12 알킬기, 2-나프틸-C1 ∼ C12 알킬기 등을 들 수 있다.
아릴알콕시기는, 전술한 아릴기에 전술한 알콕시기가 결합된 기이고, 치환기를 가지고 있어도 된다. 아릴알콕시기는, 탄소수가 통상 7 ∼ 60 정도이며, 7 ∼ 30 이 바람직하다. 아릴알콕시기의 예로서는, 페닐-C1 ∼ C12 알콕시기, C1 ∼ C12 알콕시페닐-C1 ∼ C12 알콕시기, C1 ∼ C12 알킬페닐-C1 ∼ C12 알콕시기, 1-나프틸-C1 ∼ C12 알콕시기, 2-나프틸-C1 ∼ C12 알콕시기 등을 들 수 있다.
아릴알킬티오기는, 전술한 아릴기에 전술한 알킬티오기가 결합된 기이고, 치환기를 가지고 있어도 된다. 아릴알킬티오기는, 탄소수가 통상 7 ∼ 60 이며, 7 ∼ 30 이 바람직하다. 아릴알킬티오기의 예로서는, 페닐-C1 ∼ C12 알킬티오기, C1 ∼ C12 알콕시페닐-C1 ∼ C12 알킬티오기, C1 ∼ C12 알킬페닐-C1 ∼ C12 알킬티오기, 1-나프틸-C1 ∼ C12 알킬티오기, 2-나프틸-C1 ∼ C12 알킬티오기 등을 들 수 있다.
아릴알케닐기는, 전술한 아릴기에 알케닐기가 결합된 기이다. 아릴알케닐기는, 탄소수가 통상 8 ∼ 60 정도이며, 8 ∼ 30 이 바람직하다. 아릴알케닐기의 예로서는, 페닐-C2 ∼ C12 알케닐기, C1 ∼ C12 알콕시페닐-C2 ∼ C12 알케닐기, C1 ∼ C12 알킬페닐-C2 ∼ C12 알케닐기, 1-나프틸-C2 ∼ C12 알케닐기, 2-나프틸-C2 ∼ C12 알케닐기 등을 들 수 있으며, C1 ∼ C12 알콕시페닐-C2 ∼ C12 알케닐기, C2 ∼ C12 알킬페닐-C2 ∼ C12 알케닐기가 바람직하다.
아릴알키닐기는, 전술한 아릴기에 알키닐기가 결합된 기이다. 아릴알키닐기는, 탄소수가 통상 8 ∼ 60 정도이며, 8 ∼ 30 이 바람직하다. 아릴알키닐기의 예로서는, 페닐-C2 ∼ C12 알키닐기, C1 ∼ C12 알콕시페닐-C2 ∼ C12 알키닐기, C1 ∼ C12 알킬페닐-C2 ∼ C12 알키닐기, 1-나프틸-C2 ∼ C12 알키닐기, 2-나프틸-C2 ∼ C12 알키닐기 등을 들 수 있으며, C1 ∼ C12 알콕시페닐-C2 ∼ C12 알키닐기, C1 ∼ C12 알킬페닐-C2 ∼ C12 알키닐기가 바람직하다.
치환 아미노기로서는, 알킬기, 아릴기, 아릴알킬기 및 1 가의 복소 고리기로 이루어지는 군에서 선택되는 1 또는 2 개의 기에 의해 치환된 아미노기가 바람직하다. 그 알킬기, 아릴기, 아릴알킬기 또는 1 가의 복소 고리기는 치환기를 가지고 있어도 된다. 치환 아미노기의 탄소수는, 그 치환기의 탄소수를 포함하지 않고 통상 1 ∼ 60 정도이며, 2 ∼ 48 이 바람직하다. 치환 아미노기의 예로서는, 메틸아미노기, 디메틸아미노기, 에틸아미노기, 디에틸아미노기, 프로필아미노기, 디프로필아미노기, 이소프로필아미노기, 디이소프로필아미노기, 부틸아미노기, 이소부틸아미노기, s-부틸아미노기, t-부틸아미노기, 펜틸아미노기, 헥실아미노기, 시클로헥실아미노기, 헵틸아미노기, 옥틸아미노기, 2-에틸헥실아미노기, 노닐아미노기, 데실아미노기, 3,7-디메틸옥틸아미노기, 라우릴아미노기, 시클로펜틸아미노기, 디시클로펜틸아미노기, 시클로헥실아미노기, 디시클로헥실아미노기, 피롤리딜기, 피페리딜기, 디트리플루오로메틸아미노기, 페닐아미노기, 디페닐아미노기, C1 ∼ C12 알콕시페닐아미노기, 디(C1 ∼ C12 알콕시페닐)아미노기, 디(C1 ∼ C12 알킬페닐)아미노기, 1-나프틸아미노기, 2-나프틸아미노기, 펜타플루오로페닐아미노기, 피리딜아미노기, 피리다지닐아미노기, 피리미딜아미노기, 피라질아미노기, 트리아질아미노기, 페닐-C1 ∼ C12 알킬아미노기, C1 ∼ C12 알콕시페닐-C1 ∼ C12 알킬아미노기, C1 ∼ C12 알킬페닐-C1 ∼ C12 알킬아미노기, 디(C1 ∼ C12 알콕시페닐-C1 ∼ C12 알킬)아미노기, 디(C1 ∼ C12 알킬페닐-C1 ∼ C12 알킬)아미노기, 1-나프틸-C1 ∼ C12 알킬아미노기, 2-나프틸-C1 ∼ C12 알킬아미노기 등을 들 수 있다.
치환 실릴기로서는, 알킬기, 아릴기, 아릴알킬기 및 1 가의 복소 고리기로 이루어지는 군에서 선택되는 1 ∼ 3 개의 기에 의해 치환된 실릴기가 바람직하다. 치환 실릴기는, 탄소수가 통상 1 ∼ 60 정도이며, 3 ∼ 48 이 바람직하다. 치환 실릴기 중의 그 알킬기, 아릴기, 아릴알킬기 또는 1 가의 복소 고리기는 치환기를 가지고 있어도 된다. 치환 실릴기의 예로서는, 트리메틸실릴기, 트리에틸실릴기, 트리프로필실릴기, 트리-이소프로필실릴기, 디메틸-이소프로필실릴기, 디에틸-이소프로필실릴기, t-부틸디메틸실릴기, 펜틸디메틸실릴기, 헥실디메틸실릴기, 헵틸디메틸실릴기, 옥틸디메틸실릴기, 2-에틸헥실-디메틸실릴기, 노닐디메틸실릴기, 데실디메틸실릴기, 3,7-디메틸옥틸-디메틸실릴기, 라우릴디메틸실릴기, 페닐-C1 ∼ C12 알킬실릴기, C1 ∼ C12 알콕시페닐-C1 ∼ C12 알킬실릴기, C1 ∼ C12 알킬페닐-C1 ∼ C12 알킬실릴기, 1-나프틸-C1 ∼ C12 알킬실릴기, 2-나프틸-C1 ∼ C12 알킬실릴기, 페닐-C1 ∼ C12 알킬디메틸실릴기, 트리페닐실릴기, 트리-p-자일릴실릴기, 트리벤질실릴기, 디페닐메틸실릴기, t-부틸디페닐실릴기, 디메틸페닐실릴기 등을 들 수 있다.
할로겐 원자의 예로서는, 불소 원자, 염소 원자, 브롬 원자 및 요오드 원자를 들 수 있다.
아실기는, 탄소수가 통상 2 ∼ 20 정도이며, 2 ∼ 18 이 바람직하다. 아실기의 예로서는, 아세틸기, 프로피오닐기, 부티릴기, 이소부티릴기, 피발로일기, 벤조일기, 트리플루오로아세틸기, 펜타플루오로벤조일기 등을 들 수 있다.
아실옥시기는, 탄소수가 통상 2 ∼ 20 정도이며, 2 ∼ 18 이 바람직하다. 아실옥시기의 예로서는, 아세톡시기, 프로피오닐옥시기, 부티릴옥시기, 이소부티릴옥시기, 피발로일옥시기, 벤조일옥시기, 트리플루오로아세틸옥시기, 펜타플루오로벤조일옥시기 등을 들 수 있다.
이민 잔기는, 이민 화합물 (분자 내에 식 : -N=C- 로 나타내지는 기를 갖는 유기 화합물을 가리키며, 예를 들어, 알디민, 케티민 및 이들의 N 상의 수소 원자가 알킬기 등으로 치환된 화합물을 들 수 있다.) 로부터 수소 원자 1 개를 제외한 잔기로, 그 탄소수가 통상 2 ∼ 20 정도이며, 2 ∼ 18 이 바람직하다. 이민 잔기로서는, 예를 들어 이하의 기를 들 수 있다.
아미드기는, 탄소수가 통상 2 ∼ 20 정도이며, 2 ∼ 18 이 바람직하다. 아미드기의 예로서는, 포름아미드기, 아세트아미드기, 프로피오아미드기, 부티로아미드기, 벤즈아미드기, 트리플루오로아세트아미드기, 펜타플루오로벤즈아미드기, 디포름아미드기, 디아세트아미드기, 디프로피오아미드기, 디부티로아미드기, 디벤즈아미드기, 디트리플루오로아세트아미드기, 디펜타플루오로벤즈아미드기 등을 들 수 있다.
산이미드기로서는, 산이미드로부터 질소 원자에 결합된 수소 원자를 제외하고 얻어지는 잔기를 들 수 있으며, 그 탄소수가 통상 4 ∼ 20 정도이며, 4 ∼ 18 이 바람직하다. 산이미드기로서는, 예를 들어 이하의 기를 들 수 있다.
1 가의 복소 고리기란, 복소 고리 화합물로부터 수소 원자 1 개를 제외한 나머지 원자단을 가리킨다. 1 가의 복소 고리기는, 그 탄소수가 통상 4 ∼ 60 정도이며, 4 ∼ 20 이 바람직하다. 1 가의 복소 고리기의 탄소수에는, 치환기의 탄소수는 포함하지 않는다. 복소 고리 화합물이란, 고리형 구조를 갖는 유기 화합물 중, 고리를 구성하는 원소가 탄소 원자뿐만 아니라, 산소, 황, 질소, 인, 붕소 등의 헤테로 원자를 고리 내에 포함하는 것을 가리킨다. 이와 같은 1 가의 복소 고리기로서는, 예를 들어, 티에닐기, C1 ∼ C12 알킬티에닐기, 피롤릴기, 푸릴기, 피리딜기, C1 ∼ C12 알킬피리딜기, 피페리딜기, 퀴놀릴기, 이소퀴놀릴기 등을 들 수 있으며, 그 중에서도, 티에닐기, C1 ∼ C12 알킬티에닐기, 피리딜기 및 C1 ∼ C12 알킬피리딜기가 보다 바람직하다.
치환 옥시카르보닐기는, 알킬기, 아릴기, 아릴알킬기 또는 1 가의 복소 고리기로 치환된 옥시카르보닐기, 즉,
-C(=O)OR (R 은 알킬기, 아릴기, 아릴알킬기 또는 1 가의 복소 고리기) 로 나타내지는 기이다.
치환 옥시카르보닐기는, 탄소수가 통상 2 ∼ 60 정도이며, 2 ∼ 48 이 바람직하다. 상기 알킬기, 아릴기, 아릴알킬기 또는 1 가의 복소 고리기는, 치환기를 가지고 있어도 된다. 상기 탄소수에는, 상기 치환기의 탄소수는 포함하지 않는 것으로 한다. 치환 옥시카르보닐기의 예로서는, 메톡시카르보닐기, 에톡시카르보닐기, 프로폭시카르보닐기, 이소프로폭시카르보닐기, 부톡시카르보닐기, 이소부톡시카르보닐기, s-부톡시카르보닐기, t-부톡시카르보닐기, 펜틸옥시카르보닐기, 헥실옥시카르보닐기, 시클로헥실옥시카르보닐기, 헵틸옥시카르보닐기, 옥틸옥시카르보닐기, 2-에틸헥실옥시카르보닐기, 노닐옥시카르보닐기, 데실옥시카르보닐기, 3,7-디메틸옥틸옥시카르보닐기, 도데실옥시카르보닐기, 트리플루오로메톡시카르보닐기, 펜타플루오로에톡시카르보닐기, 퍼플루오로부톡시카르보닐기, 퍼플루오로헥실옥시카르보닐기, 퍼플루오로옥틸옥시카르보닐기, 페녹시카르보닐기, 나프톡시카르보닐기, 피리딜옥시카르보닐기 등을 들 수 있다.
Ar1 이 R1 이외의 치환기를 갖는 경우, 그 치환기 중에서는, 공액 고분자 화합물의 원료가 되는 모노머 합성의 용이함의 관점에서, 알킬기, 알콕시기, 아릴기, 아릴옥시기, 카르복실기 또는 치환 옥시카르보닐기가 바람직하다.
식 (1) 중, n1 은 1 이상의 정수를 나타내고, 바람직하게는 1 에서 4 이며, 보다 바람직하게는 1 에서 3 이다.
본 발명에 있어서 공액이란, 다중 결합이 하나의 단결합 또는 질소 원자를 사이에 두고 이어져, 서로 상호 작용하는 상태를 나타낸다.
하나의 양태로서, R1 은 식 (2) 로 나타내진다.
(식 중, R2 는 치환기를 가지고 있어도 되는 2 가의 방향족기를 나타내고, Q1 은 치환기를 가지고 있어도 되는 2 가의 유기기를 나타내고, Y1 은 카르보 카티온, 암모늄 카티온, 포스포닐 카티온 또는 술포닐 카티온을 나타내고, M1 은 F-, Cl-, Br-, I-, OH-, RaSO3 -, RaCOO-, ClO-, ClO2 -, ClO3 -, ClO4 -, SCN-, CN-, NO3 -, SO4 2-, HSO4 -, PO4 3 -, HPO4 2 -, H2PO4 -, BF4 - 또는 PF6 - 을 나타내고, Z1 은 금속 이온 또는 치환기를 가지고 있어도 되는 암모늄 이온을 나타내고, c1 은 0 또는 1 을 나타내고, n2 는 0 이상의 정수를 나타낸다. 단, c1 이 0 인 경우, n2 는 0 이다. a1 은 1 이상의 정수를 나타내고, b1 은 0 이상의 정수를 나타낸다. a1 및 b1 은, 식 (2) 로 나타내지는 치환기의 전하가 0 이 되도록 선택된다. Ra 는 치환기를 가지고 있어도 되는 탄소수 1 ∼ 30 의 알킬기 또는 치환기를 가지고 있어도 되는 탄소수 6 ∼ 50 의 아릴기를 나타낸다.)
식 (2) 중, R2 로 나타내지는 2 가의 방향족기의 예로서는, 1,4-페닐렌기, 1,3-페닐렌기, 1,4-나프틸렌기, 1,5-나프틸렌기, 2,6-나프틸렌기, 2,6-안트라세닐렌기, 9,10-안트라세닐렌기, 비페닐-4,4'-디일기 등을 들 수 있으며, 원료 모노머 합성의 용이함의 관점에서는, 1,4-페닐렌기, 1,3-페닐렌기가 바람직하다.
상기 2 가의 방향족기가 가지고 있어도 되는 치환기로서는, 전술한 Ar1 이 가지고 있어도 되는 R1 이외의 치환기와 동일한 치환기를 들 수 있으며, 상기 공액 고분자 화합물을 열적으로 안정화하는 관점에서는, 치환기를 가지고 있는 것이 바람직하다. 치환기가 복수 개 존재하는 경우에는, 그들은 동일하여도 되고 상이하여도 된다.
식 (2) 중, Q1 로 나타내지는 2 가의 유기기의 예로서는, 치환기를 가지고 있어도 되는 메틸렌기, 에틸렌기, 프로필렌기, 부틸렌기, 펜틸렌기, 헥실렌기, 노닐렌기, 도데실렌기, 시클로프로필렌기, 시클로부틸렌기, 시클로펜틸렌기, 시클로헥실렌기, 시클로노닐렌기, 시클로도데실렌기, 노르보닐렌기, 아다만틸렌기 등의 탄소 원자수 1 ∼ 50 정도의 2 가의 알킬렌기, 치환기를 가지고 있어도 되는 옥시메틸렌기, 옥시에틸렌기, 옥시프로필렌기, 옥시부틸렌기, 옥시펜틸렌기, 옥시헥실렌기, 옥시노닐렌기, 옥시도데실렌기, 시클로프로필렌옥시기, 시클로부틸렌옥시기, 시클로펜틸렌옥시기, 시클로헥실렌옥시기, 시클로노닐렌옥시기, 시클로도데실렌옥시기, 노르보닐렌옥시기, 아다만틸렌옥시기 등의 탄소 원자수 1 ∼ 50 정도의 옥시알킬렌기, 치환기를 가지고 있어도 되는 이미노기, 치환기를 가지고 있어도 되는 실릴렌기, 치환기를 가지고 있어도 되는 에테닐렌기 또는 에티닐렌기를 들 수 있으며, 원료인 모노머 합성의 용이함의 관점에서는, 알킬렌기, 옥시알킬렌기가 바람직하다.
식 (2) 중, Y1 은 카르보 카티온, 암모늄 카티온, 포스포닐 카티온 또는 술포닐 카티온을 나타낸다.
카르보 카티온으로서는, 예를 들어,
(여기에 R 은, 동일 또는 상이하며, 알킬기, 아릴기를 나타낸다.) 로 나타내지는 기를 들 수 있다.
암모늄 카티온으로서는, 예를 들어,
(여기에 R 은, 동일 또는 상이하며, 알킬기, 아릴기를 나타낸다.) 으로 나타내지는 기를 들 수 있다.
포스포닐 카티온으로서는, 예를 들어,
(여기에 R 은, 동일 또는 상이하며, 알킬기, 아릴기를 나타낸다.) 으로 나타내지는 기를 들 수 있다.
술포닐 카티온으로서는, 예를 들어,
(여기에 R 은, 동일 또는 상이하며, 알킬기, 아릴기를 나타낸다.) 로 나타내지는 기를 들 수 있다.
식 (2) 중, Y1 로서는, 원료 모노머 합성의 용이함 및 원료 모노머 및 공액 고분자 화합물의 공기, 습기 또는 열에 대한 안정성의 관점에서는, 암모늄 카티온이 바람직하다.
식 (2) 중, Z1 은 금속 이온 또는 치환기를 가지고 있어도 되는 암모늄 이온을 나타낸다. 금속 이온으로서는, 1 가, 2 가 또는 3 가의 이온이 바람직하고, Li, Na, K, Cs, Be, Mg, Ca, Ba, Ag, Al, Bi, Cu, Fe, Ga, Mn, Pb, Sn, Ti, V, W, Y, Yb, Zn, Zr 의 이온을 들 수 있다. 암모늄 이온이 가지고 있어도 되는 치환기로서는, 메틸기, 에틸기, 프로필기, 이소프로필기, n-부틸기, 이소부틸기, t-부틸기 등의 탄소 원자수 1 ∼ 10 정도의 알킬기를 들 수 있다.
식 (2) 중, c1 은 공액 고분자 화합물의 안정성의 관점에서는, 1 이 바람직하다.
식 (2) 중, n2 는 0 이상의 정수를 나타내고, 바람직하게는 0 에서 6 이며, 보다 바람직하게는 0 이다.
식 (2) 중, a1 은 1 이상의 정수를 나타내고, 바람직하게는 1 에서 3 이며, 보다 바람직하게는 1 에서 2 이다. b1 은, 0 이상의 정수를 나타내고, 바람직하게는 0 에서 2 이며, 보다 바람직하게는 0 에서 1 이다.
a1 및 b1 은, 식 (2) 로 나타내지는 치환기의 전하가 0 이 되도록 선택된다. 식 (2) 로 나타내지는 기 중,
-(R2)c1-(Q1)n2-Y1
로 나타내지는 부분의 전하는, 통상 +1 이므로, 이 경우의 a1 과 b1 의 관계에 대해, 이하에 설명한다.
a) M1 이 1 가의 아니온인 경우 (즉, M1 이 F-, Cl-, Br-, I-, OH-, RaSO3 -, RaCOO-, ClO-, ClO2 -, ClO3 -, ClO4 -, SCN-, CN-, NO3 -, HSO4 -, H2PO4 -, BF4 - 또는 PF6 - 인 경우)
a-1) Z1 이 1 가의 금속 이온 또는 치환기를 가지고 있어도 되는 암모늄 이온일 때,
a1=b1+1
a-2) Z1 이 2 가의 금속 이온일 때,
a1=2×b1+1
a-3) Z1 이 3 가의 금속 이온일 때,
a1=3×b1+1 이다.
b) M1 이 2 가의 아니온인 경우 (즉, M1 이 SO4 2 -, HPO4 2 - 인 경우)
b-1) Z1 이 1 가의 금속 이온 또는 치환기를 가지고 있어도 되는 암모늄 이온일 때,
b1=2×a1-1
b-2) Z1 이 2 가의 금속 이온일 때,
2×a1=2×b1+1 의 관계를 만족하고,
b-3) Z1 이 3 가의 금속 이온일 때,
2×a1=3×b1+1
Ra 는 치환기를 가지고 있어도 되는 탄소수 1 ∼ 30 의 알킬기 또는 치환기를 가지고 있어도 되는 탄소수 6 ∼ 50 의 아릴기를 나타낸다. 이들 기가 가지고 있어도 되는 치환기로서는, 전술한 Ar1 이 가지고 있어도 되는 R1 이외의 치환기와 동일한 치환기를 들 수 있다. 치환기가 복수 개 존재하는 경우에는, 그들은 동일하여도 되고 상이하여도 된다. Ra 의 예로서는, 메틸기, 에틸기, 프로필기, 이소프로필기, 부틸기, 이소부틸기, s-부틸기, t-부틸기, 펜틸기, 헥실기, 시클로헥실기, 헵틸기, 옥틸기, 노닐기, 데실기, 라우릴기 등의 탄소수 1 ∼ 20 의 알킬기, 페닐기, 1-나프틸기, 2-나프틸기, 1-안트라세닐기, 2-안트라세닐기, 9-안트라세닐기 등의 탄소수 6 ∼ 30 의 아릴기를 들 수 있다.
식 (1) 로 나타내지는 반복 단위 중에서는, Ar1 이 식 38 로 나타내지는 고리로부터 수소 원자를 2 개 제거한 기인 반복 단위가 바람직하고, 하기 식
(식 중, Ry 는 식 (2) 로 나타내지는 기를 포함하는 치환기를 나타내고, R* 는 Ry, 수소 원자, 알킬기 또는 아릴기를 나타낸다.)
로 나타내지는 반복 단위가, 보다 바람직하다.
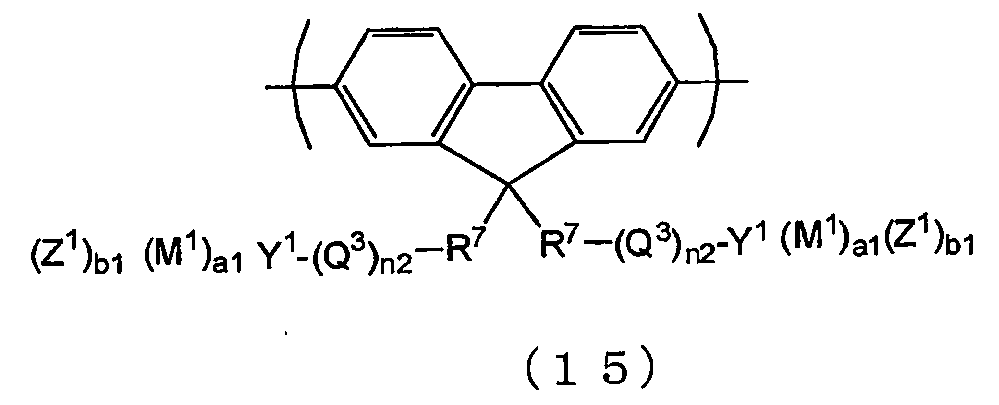
식 (1) 로 나타내지는 반복 단위 중에서는, 전자 수송성의 관점에서는, 식 (15) 로 나타내지는 반복 단위가 바람직하다.
(식 중, R7 은 치환기를 가지고 있어도 되는 2 가의 방향족기를 나타내고, Q3 은 치환기를 가지고 있어도 되는 알킬렌기 또는 치환기를 가지고 있어도 되는 옥시알킬렌기를 나타내고, n2, Y1, M1, Z1, a1 및 b1 은 전술한 바와 같은 의미를 나타낸다. 복수 개 있는 n2, R7, Y1, M1, a1 및 b1 은 동일하여도 되고 상이하여도 된다. Q3 이 복수 개 있는 경우, 그들은 동일하여도 되고 상이하여도 된다. Z1 이 복수 개 있는 경우, 그들은 동일하여도 되고 상이하여도 된다.
식 (15) 중, R7 로 나타내지는 2 가의 방향족기의 예로서는, 1,4-페닐렌기, 1,3-페닐렌기, 1,4-나프틸렌기, 1,5-나프틸렌기, 2,6-나프틸렌기, 2,6-안트라세닐렌기, 9,10-안트라세닐렌기, 비페닐-4,4'-디일기 등을 들 수 있으며, 원료 모노머 합성의 용이함의 관점에서는, 1,4-페닐렌기, 1,3-페닐렌기가 바람직하다.
R7 로 나타내지는 2 가의 방향족기가 가지고 있어도 되는 치환기로서는, 전술한 Ar1 이 가지고 있어도 되는 R1 이외의 치환기와 동일한 치환기를 들 수 있으며, 상기 공액 고분자 화합물을 열적으로 안정화하는 관점에서는, 치환기를 가지고 있는 것이 바람직하다. 치환기가 복수 개 존재하는 경우에는, 그들은 동일하여도 되고 상이하여도 된다.
식 (15) 로 나타내지는 반복 단위 중에서는, 공액 고분자 화합물의 흡습성의 관점에서는, 식 (18) 로 나타내지는 반복 단위가 바람직하다.
(식 중, R7, n2, Y1, M1, Z1, a1 및 b1 은 전술한 바와 같은 의미를 나타낸다.)
식 (18) 로 나타내지는 반복 단위의 예로서는, 이하의 반복 단위를 들 수 있다.
식 (3) 으로 나타내지는 반복 단위에 있어서, Ar2 는 2 가의 방향족기를 나타내고, R3 은 식 (4) 로 나타내지는 기를 포함하는 치환기를 나타내고, 그 Ar2 는 R3 이외의 치환기를 가지고 있어도 된다. n3 은 1 이상의 정수를 나타낸다. 식 (4) 로 나타내지는 기는, Ar2 에 직접 결합되어 있어도 되고, 치환기를 가지고 있어도 되는 메틸렌기, 에틸렌기, 프로필렌기, 부틸렌기, 펜틸렌기, 헥실렌기, 노닐렌기, 도데실렌기, 시클로프로필렌기, 시클로부틸렌기, 시클로펜틸렌기, 시클로헥실렌기, 시클로노닐렌기, 시클로도데실렌기, 노르보닐렌기, 아다만틸렌기 등의 탄소 원자수 1 ∼ 50 정도의 2 가의 알킬렌기, 치환기를 가지고 있어도 되는 옥시메틸렌기, 옥시에틸렌기, 옥시프로필렌기, 옥시부틸렌기, 옥시펜틸렌기, 옥시헥실렌기, 옥시노닐렌기, 옥시도데실렌, 시클로프로필렌옥시기, 시클로부틸렌옥시기, 시클로펜틸렌옥시기, 시클로헥실렌옥시기, 시클로노닐렌옥시기, 시클로도데실렌옥시기, 노르보닐렌옥시기, 아다만틸렌옥시기 등의 탄소 원자수 1 ∼ 50 정도의 옥시알킬렌기, 치환기를 가지고 있어도 되는 이미노기, 치환기를 가지고 있어도 되는 실릴렌기, 치환기를 가지고 있어도 되는 에테닐렌기 또는 에티닐렌기, 치환기를 가지고 있어도 되는 메탄트리일기, 산소 원자, 질소 원자, 황 원자 등의 헤테로 원자를 개재하여 Ar2 에 결합되어 있어도 된다. 하나의 양태로서, R3 은 식 (4) 로 나타내지는 기이다.
Ar2 로 나타내지는 2 가의 방향족기로서는, 원료 모노머 합성의 용이함의 관점에서, 식 1 ∼ 15, 식 27 ∼ 30, 식 38 ∼ 40 또는 식 42 로 나타내지는 고리로부터 수소 원자를 2 개 제거한 기가 바람직하고, 식 1 ∼ 6, 식 8, 식 14, 식 27, 식 28, 식 38 또는 식 42 로 나타내지는 고리로부터 수소 원자를 2 개 제거한 기가 보다 바람직하고, 식 1, 식 38 또는 식 42 로 나타내지는 고리로부터 수소 원자를 2 개 제거한 기가 더욱 바람직하다.
식 (4) 중, R4 는 치환기를 가지고 있어도 되는 2 가의 방향족기를 나타내고, Q2 는 치환기를 가지고 있어도 되는 2 가의 유기기를 나타내고, Y2 는 -CO2 -, -SO3 -, -SO2 - 또는 -PO3 - 을 나타내고, 공액 고분자 화합물의 산성도의 관점에서는 -CO2 -, -SO2 - 또는 -PO3 - 가 바람직하고, -CO2 - 가 보다 바람직하다. M2 는 금속 카티온 또는 치환기를 가지고 있어도 되는 암모늄 카티온을 나타내고, Z2 는 F-, Cl-, Br-, I-, OH-, RbSO3 -, RbCOO-, ClO-, ClO2 -, ClO3 -, ClO4 -, SCN-, CN-, NO3 -, SO4 2-, HSO4 -, PO4 3-, HPO4 2-, H2PO4 -, BF4 - 또는 PF6 - 을 나타내고, c2 는 0 또는 1 을 나타내고, n4 는 0 이상의 정수를 나타낸다. 단, Y2 가 SO3 - 인 경우, n4 는 0 이다. a2 는 1 이상의 정수를 나타내고, b2 는 0 이상의 정수를 나타낸다. a2 및 b2 는, 식 (4) 로 나타내지는 치환기의 전하가 0 이 되도록 선택된다. Rb 는 치환기를 가지고 있어도 되는 탄소수 1 ∼ 30 의 알킬기 또는 치환기를 가지고 있어도 되는 탄소수 6 ∼ 50 의 아릴기를 나타낸다. Q2 가 복수 개 있는 경우, 그들은 동일하여도 되고 상이하여도 된다. M2 가 복수 개 있는 경우, 그들은 동일하여도 되고 상이하여도 된다. Z2 가 복수 개 있는 경우, 그들은 동일하여도 되고 상이하여도 된다.
식 (4) 중, R4 로 나타내지는 치환기를 가지고 있어도 되는 2 가의 방향족기로서는, 예를 들어, 1,3-페닐렌기, 1,4-페닐렌기, 1,4-나프틸렌기, 1,5-나프틸렌기, 2,6-나프틸렌기, 비페닐-4,4'-디일기 등의 탄소 원자수 6 ∼ 50 정도의 아릴렌기를 들 수 있다.
상기 2 가의 방향족기가 가지고 있어도 되는 치환기로서는, 전술한 Ar1 이 가지고 있어도 되는 R1 이외의 치환기와 동일한 치환기를 들 수 있으며, 상기 공액 고분자 화합물을 열적으로 안정화하는 관점에서는, 치환기를 가지고 있는 것이 바람직하다. 치환기가 복수 개 존재하는 경우에는, 그들은 동일하여도 되고 상이하여도 된다.
식 (4) 중, Q2 로 나타내지는 2 가의 유기기로서는, 전술한 Q1 로 나타내지는 2 가의 유기기와 동일한 기를 들 수 있으며, 원료인 모노머 합성의 용이함의 관점에서는, 알킬렌기, 옥시알킬렌기가 바람직하다.
상기 2 가의 유기기가 가지고 있어도 되는 치환기로서는, 전술한 Ar1 이 가지고 있어도 되는 R1 이외의 치환기와 동일한 치환기를 들 수 있다. 치환기가 복수 개 존재하는 경우에는, 그들은 동일하여도 되고 상이하여도 된다.
식 (4) 중, M2 는 금속 카티온 또는 치환기를 가지고 있어도 되는 암모늄 카티온을 나타낸다. 금속 카티온으로서는, 1 가, 2 가 또는 3 가의 이온이 바람직하고, Li, Na, K, Cs, Be, Mg, Ca, Ba, Ag, Al, Bi, Cu, Fe, Ga, Mn, Pb, Sn, Ti, V, W, Y, Yb, Zn, Zr 등의 이온을 들 수 있다. 암모늄 이온이 가지고 있어도 되는 치환기로서는, 메틸기, 에틸기, 프로필기, 이소프로필기, n-부틸기, i-부틸기, t-부틸기 등의 탄소 원자수 1 ∼ 10 정도의 알킬기를 들 수 있다.
식 (4) 중, n4 는 0 이상의 정수를 나타낸다. 원료인 모노머 합성의 관점에서, 바람직하게는 0 에서 8 이며, 보다 바람직하게는 0 이다. 단, Y2 가 SO3 - 인 경우, n4 는 0 이다.
식 (4) 중, a2 는 1 이상의 정수를 나타낸다. 바람직하게는 1 에서 5 이며, 보다 바람직하게는 1 에서 2 이다. b2 는 0 이상의 정수를 나타낸다. 바람직하게는 0 에서 4 이며, 보다 바람직하게는 0 에서 2 이다.
a2 및 b2 는, 식 (4) 로 나타내지는 치환기의 전하가 0 이 되도록 선택된다. 예를 들어, Y2 가 -CO2 -, -SO3 -, -SO2 - 또는 -PO3 - 이며, M2 가 1 가의 금속 카티온 또는 치환기를 가지고 있어도 되는 암모늄 카티온이며, Z2 가 F-, Cl-, Br-, I-, OH-, RbSO3 -, RbCOO-, ClO-, ClO2 -, ClO3 -, ClO4 -, SCN-, CN-, NO3 -, HSO4 -, H2PO4 -, BF4 - 또는 PF6 - 인 경우는, a2=b2+1 이다. Y2 가 -CO2 -, -SO3 -, -SO2 -, 또는 -PO3 - 이며, M2 가 2 가의 금속 카티온이며, Z2 가 F-, Cl-, Br-, I-, OH-, RbSO3 -, RbCOO-, ClO-, ClO2 -, ClO3 -, ClO4 -, SCN-, CN-, NO3 -, HSO4 -, H2PO4 -, BF4 - 또는 PF6 - 인 경우는, b2=2×a2-1 이다. Y2 가 -CO2 -, -SO3 -, -SO2 -, 또는 -PO3 - 이며, M2 가 3 가의 금속 카티온이며, Z2 가 F-, Cl-, Br-, I-, OH-, RbSO3 -, RbCOO-, ClO-, ClO2 -, ClO3 -, ClO4 -, SCN-, CN-, NO3 -, HSO4 -, H2PO4 -, BF4 -, 또는 PF6 - 인 경우는, b2=3×a2-1 이다. Y2 가 -CO2 -, -SO3 -, -SO2 - 또는 -PO3 - 이며, M2 가 1 가의 금속 카티온 또는 치환기를 가지고 있어도 되는 암모늄 카티온이며, Z2 가 SO4 2- 또는 HPO4 2- 인 경우에는, a2=2×b2+1 이다.
Rb 는 치환기를 가지고 있어도 되는 탄소수 1 ∼ 30 의 알킬기, 치환기를 가지고 있어도 되는 탄소수 6 ∼ 50 의 아릴기를 나타내지만, 이들 기가 가지고 있어도 되는 치환기로서는, 전술한 Ar1 이 가지고 있어도 되는 R1 이외의 치환기와 동일한 치환기를 들 수 있다. 치환기가 복수 개 존재하는 경우에는, 그들은 동일하여도 되고 상이하여도 된다. Rb 의 예로서는, 메틸기, 에틸기, 프로필기, 이소프로필기, 부틸기, 이소부틸기, s-부틸기, t-부틸기, 펜틸기, 헥실기, 시클로헥실기, 헵틸기, 옥틸기, 노닐기, 데실기, 라우릴기 등의 탄소수 1 ∼ 20 의 알킬기, 페닐기, 1-나프틸기, 2-나프틸기, 1-안트라세닐기, 2-안트라세닐기, 9-안트라세닐기 등의 탄소수 6 ∼ 30 의 아릴기를 들 수 있다.
식 (3) 으로 나타내지는 반복 단위 중에서는, Ar2 가 식 38 로 나타내지는 고리로부터 수소 원자를 2 개 제거한 기인 반복 단위가 바람직하고, 하기 식
(식 중, Ry' 는 식 (4) 로 나타내지는 기를 포함하는 치환기를 나타내고, R** 는 Ry', 수소 원자, 알킬기 또는 아릴기를 나타낸다.)
으로 나타내지는 반복 단위가, 보다 바람직하다.
식 (3) 으로 나타내지는 반복 단위로서는, 전자 수송성의 관점에서는, 식 (16) 으로 나타내지는 반복 단위가 바람직하다.
(식 중, R8 은 치환기를 가지고 있어도 되는 2 가의 방향족기를 나타내고, Q4 는 치환기를 가지고 있어도 되는 알킬렌기 또는 치환기를 가지고 있어도 되는 옥시알킬렌기를 나타내고, n4, Y2, M2, Z2, a2 및 b2 는 전술한 바와 같은 의미를 나타낸다. 복수 개 있는 n4, R8, Y2, M2, a2 및 b2 는 동일하여도 되고 상이하여도 된다. Q4 가 복수 개 있는 경우, 그들은 동일하여도 되고 상이하여도 된다. Z2 가 복수 개 있는 경우, 그들은 동일하여도 되고 상이하여도 된다.)
식 (16) 중, R8 로 나타내지는 2 가의 방향족기로서는, 1,4-페닐렌기, 1,3-페닐렌기, 1,4-나프틸렌기, 1,5-나프틸렌기, 2,6-나프틸렌기, 2,6-안트라세닐렌기, 9,10-안트라세닐렌기, 비페닐-4,4'-디일기 등을 들 수 있다.
R8 에 있어서의 2 가의 방향족기로서는, 원료가 되는 모노머 합성의 용이함의 관점에서는, 1,4-페닐렌기, 1,3-페닐렌기가 바람직하다.
R8 로 나타내지는 2 가의 방향족기가 가지고 있어도 되는 치환기로서는, 전술한 Ar1 이 가지고 있어도 되는 R1 이외의 치환기와 동일한 치환기를 들 수 있으며, 상기 공액 고분자 화합물을 열적으로 안정화하는 관점에서는, 치환기를 가지고 있는 것이 바람직하다. 치환기가 복수 개 존재하는 경우에는, 그들은 동일하여도 되고 상이하여도 된다. 치환기의 종류는, 상기 공액 고분자 화합물의 용해성의 관점에서, 알킬기, 알콕시기, 하이드록시기가 바람직하다.
M2 는 상기 공액 고분자 화합물의 합성의 관점에서는, Li 카티온, Na 카티온, K 카티온, Cs 카티온 또는 테트라메틸암모늄 카티온이 바람직하다.
식 (15) 로 나타내지는 반복 단위로서는, 공액 고분자 화합물의 내수성의 관점에서는, 식 (19) 로 나타내지는 반복 단위가 바람직하다.
(식 중, R8, n4, Y2, M2, Z2, a2 및 b2 는 전술한 바와 같은 의미를 나타낸다.)
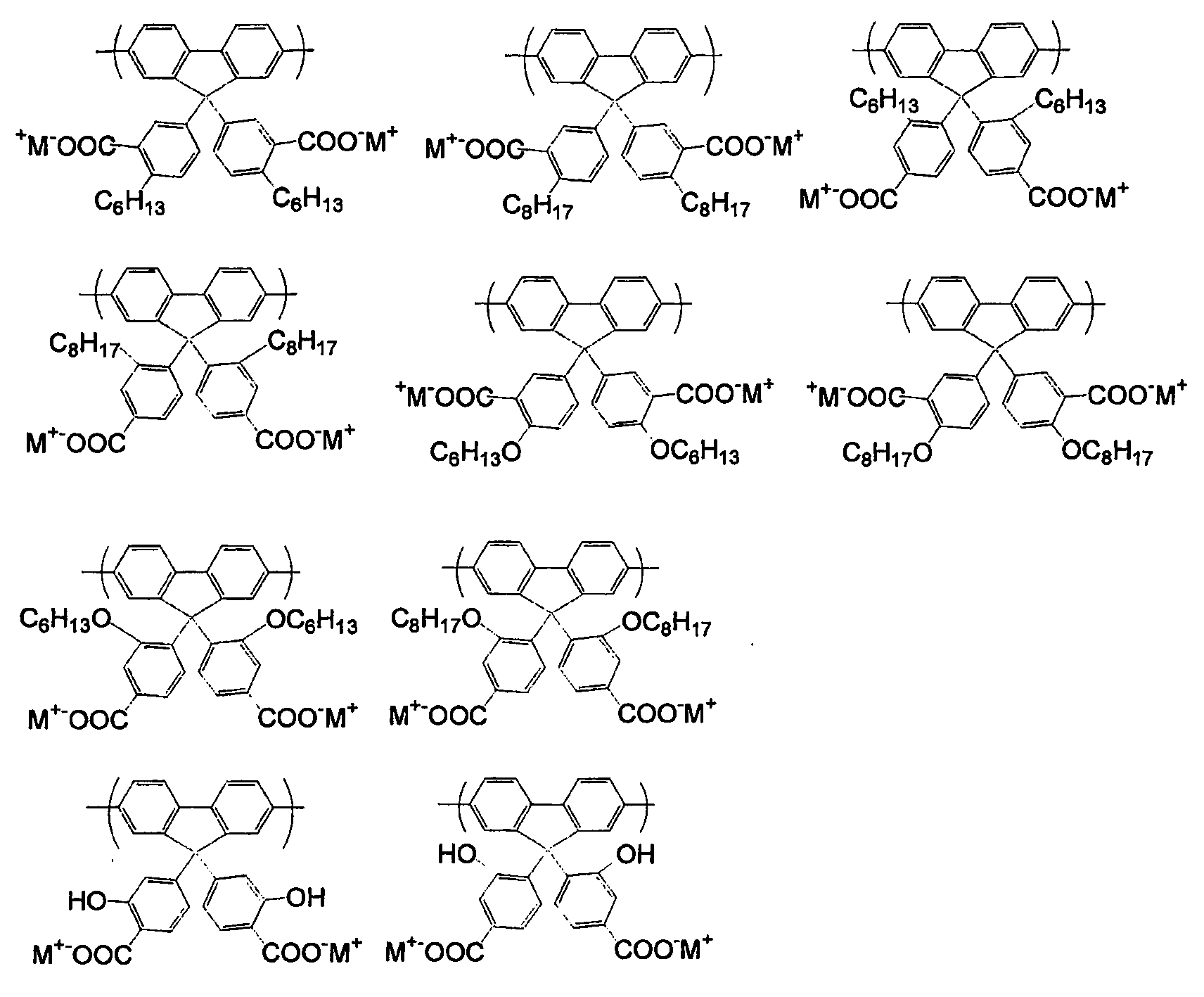
식 (19) 로 나타내지는 반복 단위의 예로서는, 이하의 반복 단위를 들 수 있다.
(식 중, M 은 Li, Na, K, Cs 또는 NMe4 를 나타낸다.)
식 (5) 로 나타내지는 반복 단위에 있어서, Ar3 은 2 가의 방향족기를 나타내고, R5 는 식 (6) 으로 나타내지는 기를 포함하는 치환기를 나타내고, 그 Ar3 은 R5 이외의 치환기를 가지고 있어도 된다. n5 는 1 이상의 정수를 나타낸다. R5 는 헤테로 원자를 4 개 이상 포함한다. 식 (6) 으로 나타내지는 기는, Ar3 에 직접 결합되어 있어도 되고, 치환기를 가지고 있어도 되는 메틸렌기, 에틸렌기, 프로필렌기, 부틸렌기, 펜틸렌기, 헥실렌기, 노닐렌기, 도데실렌기, 시클로프로필렌기, 시클로부틸렌기, 시클로펜틸렌기, 시클로헥실렌기, 시클로노닐렌기, 시클로도데실렌기, 노르보닐렌기, 아다만틸렌기 등의 탄소 원자수 1 ∼ 50 정도의 2 가의 알킬렌기, 치환기를 가지고 있어도 되는 옥시메틸렌기, 옥시에틸렌기, 옥시프로필렌기, 옥시부틸렌기, 옥시펜틸렌기, 옥시헥실렌기, 옥시노닐렌기, 옥시도데실렌기, 시클로프로필렌옥시기, 시클로부틸렌옥시기, 시클로펜틸렌옥시기, 시클로헥실렌옥시기, 시클로노닐렌옥시기, 시클로도데실렌옥시기, 노르보닐렌옥시기, 아다만틸렌옥시기 등의 탄소 원자수 1 ∼ 50 정도의 옥시알킬렌기, 치환기를 가지고 있어도 되는 이미노기, 치환기를 가지고 있어도 되는 실릴렌기, 치환기를 가지고 있어도 되는 에테닐렌기 또는 에티닐렌기, 치환기를 가지고 있어도 되는 메탄트리일기, 산소 원자, 질소 원자, 황 원자 등의 헤테로 원자를 개재하여 Ar3 에 결합되어 있어도 된다. 하나의 양태로서, R5 는 식 (6) 으로 나타내지는 기이다.
R5 에 포함되는 헤테로 원자로서는, 산소, 황, 셀렌, 텔루르, 질소, 인, 안티몬, 비소, 붕소 등을 들 수 있다. R5 는, 같은 종류의 헤테로 원자를 2 개 이상 가지고 있어도 되고, 2 종류 이상의 헤테로 원자를 가지고 있어도 된다. 원료가 되는 모노머 합성의 용이함의 관점에서는, 헤테로 원자가 산소, 황, 질소, 인, 붕소인 것이 바람직하다. 헤테로 원자의 수는, 공액 고분자 화합물의 용해성의 관점에서는, 4 ∼ 30 이 바람직하고, 6 ∼ 20 이 보다 바람직하다.
n5 는 1 이상의 정수를 나타낸다. 공액 고분자 화합물의 용해성의 관점에서는, 바람직하게는 2 에서 4 이며, 보다 바람직하게는 2 에서 3 이다.
Ar3 은 R5 이외의 치환기를 가지고 있어도 된다.
Ar3 으로 나타내지는 2 가의 방향족기로서는, 원료 모노머 합성의 용이함의 관점에서, 식 1 ∼ 15, 식 27 ∼ 30, 식 38 ∼ 40 또는 식 42 로 나타내지는 고리로부터 수소 원자를 2 개 제거한 기가 바람직하고, 식 1 ∼ 6, 식 8, 식 14, 식 27, 식 28, 식 38 또는 식 42 로 나타내지는 고리로부터 수소 원자를 2 개 제거한 기가 보다 바람직하고, 식 1, 식 38 또는 식 42 로 나타내지는 고리로부터 수소 원자를 2 개 제거한 기가 더욱 바람직하다.
Ar3 으로 나타내지는 2 가의 방향족기가 가지고 있어도 되는 R5 이외의 치환기로서는, 전술한 Ar1 이 가지고 있어도 되는 R1 이외의 치환기와 동일한 치환기를 들 수 있다. 치환기가 복수 개 존재하는 경우에는, 그들은 동일하여도 되고 상이하여도 된다.
R5 는, 식 (6) 으로 나타내지는 기를 포함하는 치환기이다.
(식 중, R6 은 1 가의 방향족기를 나타내고, n6 은 0 이상의 정수를 나타내고, m1 은 1 이상의 정수를 나타낸다. Y3 은 -CN 또는 식 (7) ∼ (14) 로 나타내지는 기를 나타낸다. Y3 이 복수 개 있는 경우, 그들은 동일하여도 되고 상이하여도 된다. n6 이 복수 개 있는 경우, 그들은 동일하여도 되고 상이하여도 된다. 식 (6) 으로 나타내지는 기는, 헤테로 원자를 4 개 이상 포함한다.
(식 (7) ∼ (14) 중, R' 는 치환기를 가지고 있어도 되는 2 가의 탄화 수소기를 나타내고, R" 는 수소 원자, 치환기를 가지고 있어도 되는 1 가의 탄화 수소기, -COOH, -SO3H, -OH, -SH, -NRc 2, -CN 또는 -C(=O)NRc 2 를 나타내고, a3 은 0 이상의 정수를 나타내고, a4 는 3 ∼ 20 의 정수를 나타낸다. Rc 는 치환기를 가지고 있어도 되는 탄소수 1 ∼ 30 의 알킬기 또는 치환기를 가지고 있어도 되는 탄소수 6 ∼ 50 의 아릴기를 나타낸다. R'가 복수 개 있는 경우, 그들은 동일하여도 되고 상이하여도 된다.) 하나의 양태로서, R6 은 식 (6) 으로 나타내지는 기이다.
식 (6) 중, n6 은 0 이상의 정수를 나타낸다. 바람직하게는 0 에서 20 이며, 보다 바람직하게는 0 에서 8 이다.
식 (6) 중, m1 은 공액 고분자 화합물의 용해성의 관점에서는, 1 에서 4 인 것이 바람직하고, 1 에서 3 인 것이 보다 바람직하다.
식 (6) 에 있어서, R6 은{-(CH2)n6-Y3}으로 나타내지는 치환기를 m1 개 갖는 1 가의 방향족기를 나타낸다. R6 으로 나타내지는 1 가의 방향족기로서는, 단고리형 방향 고리로부터 수소 원자를 1 개 제거한 기, 축합 다고리형 방향 고리로부터 수소 원자를 1 개 제외한 1 가 의 기, 2 개 이상의 방향 고리를, 단결합, 에테닐렌기 또는 에티닐렌기로 연결한 다고리로부터 수소 원자를 1 개 제거한 기, 유교 다고리형 방향 고리로부터 수소 원자를 1 개 제거한 기 등을 들 수 있다. 단고리형 방향 고리, 축합 다고리형 방향 고리, 에테닐렌기 또는 에티닐렌기로 연결한 다고리 및 유교 다고리형 방향 고리의 예로서는, 전술한 Ar1 의 설명에 사용한 단고리형 방향 고리, 축합 다고리형 방향 고리, 에테닐렌기 또는 에티닐렌기로 연결한 다고리 및 유교 다고리형 방향 고리의 예와 동일한 화합물을 들 수 있으며, 원료인 모노머 합성의 관점에서, 페닐기, 피리딜기, 피리다질기, 피리미디닐기, 피라질기, 트리아질기, 나프틸기, 안트라세닐기, 퀴놀릴기, 이소퀴놀릴기, 퀴녹살리닐기, 비페닐기가 바람직하다.
R6 은,{-(CH2)n6-Y3}으로 나타내지는 치환기 이외의 치환기를 가지고 있어도 된다. 그 치환기의 예로서는, 전술한 Ar1 이 가지고 있어도 되는 R1 이외의 치환기와 동일한 치환기를 들 수 있다. 그 치환기가 복수 개 존재하는 경우에는, 그들은 동일하여도 되고 상이하여도 된다.
식 (7) ∼ (14) 중, R' 로 나타내지는 2 가의 탄화 수소기로서는, 메틸렌기, 에틸렌기, 1,2-프로필렌기, 1,3-프로필렌기, 1,2-부틸렌기, 1,3-부틸렌기, 1,4-부틸렌기, 1,5-펜틸렌기, 1,6-헥실렌기, 1,9-노닐렌기, 1,12-도데실렌기 등의 탄소수 1 ∼ 50 정도의 2 가의 포화 탄화 수소기, 에테닐렌기, 프로페닐렌기, 3-부테닐렌기, 2-펜테닐렌기, 2-헥세닐렌기, 2-노네닐렌기, 2-도데세닐렌기 등의 탄소수 2 ∼ 50 정도의 2 가의 불포화 탄화 수소기, 시클로프로필렌기, 시클로부틸렌기, 시클로펜틸렌기, 시클로헥실렌기, 시클로노닐렌기, 시클로도데실렌기, 노르보닐렌기, 아다만틸렌기 등의 탄소 원자수 3 ∼ 50 정도의 2 가의 고리형 포화 탄화 수소기, 에테닐렌기, 프로페닐렌기, 3-부테닐렌기, 2-부테닐렌기, 2-펜테닐렌기, 2-헥세닐렌기, 2-노네닐렌기, 2-도데세닐렌기 등의 탄소 원자수 2 ∼ 50 정도의 알케닐렌기, 1,3-페닐렌기, 1,4-페닐렌, 1,4-나프틸렌기, 1,5-나프틸렌기, 2,6-나프틸렌기, 비페닐-4,4'-디일기 등의 탄소 원자수 6 ∼ 50 정도의 아릴렌기, 메틸렌옥시기, 에틸렌옥시기, 프로필렌옥시기, 부틸렌옥시기, 펜틸렌옥시기, 헥실렌옥시기 등의 탄소 원자수 1 ∼ 50 정도의 알킬렌옥시기 등을 들 수 있다.
R' 는 치환기를 가지고 있어도 되고, 그 치환기로서는, 전술한 Ar1 이 가지고 있어도 되는 R1 이외의 치환기와 동일한 치환기를 들 수 있다. 치환기가 복수 개 존재하는 경우에는, 그들은 동일하여도 되고 상이하여도 된다.
식 (7) ∼ (14) 중, R" 로 나타내지는 1 가의 탄화 수소기로서는, 메틸기, 에틸기, 프로필기, 이소프로필기, 부틸기, 이소부틸기, s-부틸기, t-부틸기, 펜틸기, 헥실기, 시클로헥실기, 헵틸기, 옥틸기, 노닐기, 데실기, 라우릴기 등의 탄소수 1 ∼ 20 의 알킬기, 페닐기, 1-나프틸기, 2-나프틸기, 1-안트라세닐기, 2-안트라세닐기, 9-안트라세닐기 등의 탄소수 6 ∼ 30 의 아릴기 등을 들 수 있다. 용해성의 관점에서는, 메틸기, 에틸기, 페닐기, 1-나프틸기, 2-나프틸기가 바람직하다. R" 는 치환기를 가지고 있어도 되고, 그 치환기로서는, 전술한 Ar1 이 가지고 있어도 되는 R1 이외의 치환기와 동일한 치환기를 들 수 있다. 치환기가 복수 개 존재하는 경우에는, 그들은 동일하여도 되고 상이하여도 된다.
식 (7) ∼ (14) 중, Rc 는 공액 고분자 화합물의 용해성의 관점에서는, 메틸기, 에틸기, 페닐기, 1-나프틸기, 2-나프틸기가 바람직하다.
식 (7) 중, a4 는 3 ∼ 20 의 정수를 나타내고, 3 ∼ 10 이 바람직하다. 식 (8) ∼ (14) 중, a3 은 0 이상의 정수를 나타낸다. 식 (8) 에 있어서는, 0 ∼ 30 이 바람직하고, 3 ∼ 20 이 보다 바람직하다. 식 (9) ∼ (12) 에 있어서는, 0 ∼ 10 이 바람직하고, 0 ∼ 5 가 보다 바람직하다. 식 (13) 에 있어서는, 0 ∼ 20 이 바람직하고, 3 ∼ 20 이 보다 바람직하다. 식 (14) 에 있어서는, 0 ∼ 20 이 바람직하고, 0 ∼ 10 이 보다 바람직하다.
Y3 으로서는, 원료가 되는 모노머 합성의 용이함의 관점에서는, -CN, 식 (7) 로 나타내지는 기, 식 (8) 로 나타내지는 기, 식 (12) 로 나타내지는 기, 식 (13) 으로 나타내지는 기가 바람직하고, 식 (7) 로 나타내지는 기, 식 (8) 로 나타내지는 기, 식 (13) 으로 나타내지는 기가 보다 바람직하다. 더욱 바람직하게는, 이하의 기를 들 수 있다.
식 (5) 로 나타내지는 반복 단위 중에서는, Ar2 가 식 38 로 나타내지는 고리로부터 수소 원자를 2 개 제거한 기인 반복 단위가 바람직하고, 하기 식
(식 중, Ry " 는 식 (4) 로 나타내지는 기를 포함하는 치환기를 나타내고, R*** 는 Ry ", 수소 원자, 알킬기 또는 아릴기를 나타낸다.)
으로 나타내지는 반복 단위가 보다 바람직하다.
식 (5) 로 나타내지는 반복 단위로서는, 전자 수송성의 관점에서는, 식 (17) 로 나타내지는 반복 단위가 바람직하다.
(식 중, n6, m1, R6, Y3 은 전술한 바와 같은 의미를 나타낸다. 복수 개 있는 n6, m1, R6 및 Y3 은, 동일하여도 되고 상이하여도 된다.)
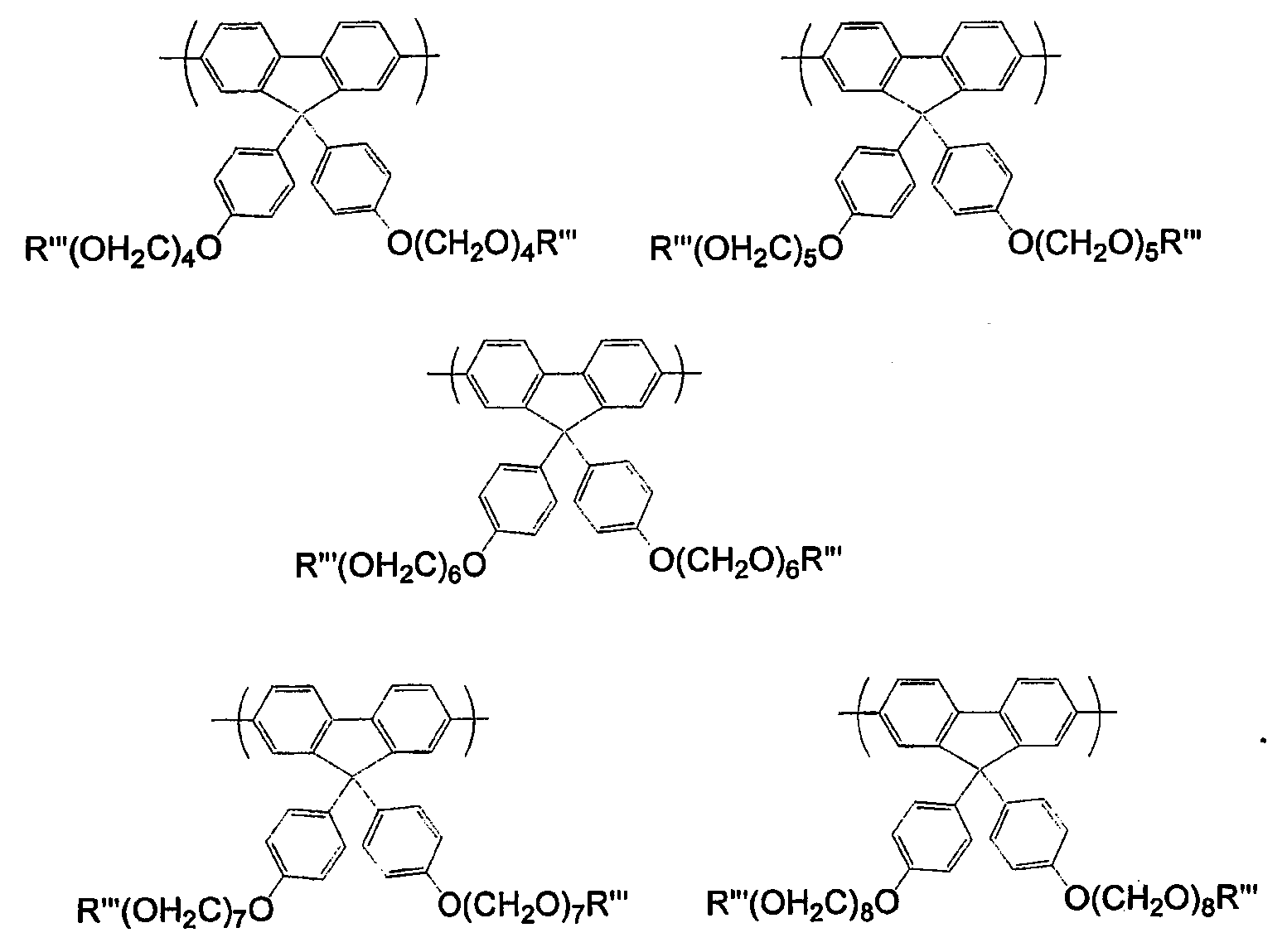
식 (17) 로 나타내지는 반복 단위의 예로서는, 이하의 반복 단위를 들 수 있다.
(식 중 R''' 은 수소 원자 또는 메틸기를 나타낸다.)
본 발명에 사용되는 공액 고분자 화합물은, 추가로 식 (20) 으로 나타내지는 반복 단위를 가지고 있어도 된다.
(식 중, Ar4 는 치환기를 가지고 있어도 되는 2 가의 방향족기 또는 치환기를 가지고 있어도 되는 2 가의 방향족 아민 잔기를 나타낸다. X 는 치환기를 가지고 있어도 되는 이미노기, 치환기를 가지고 있어도 되는 실릴렌기, 치환기를 가지고 있어도 되는 에테닐렌기 또는 에티닐렌기를 나타내고, m2 및 m3 은 각각 독립적으로 0 또는 1 을 나타내고, m2 및 m3 의 적어도 1 개는 1 이다.)
식 (20) 중의 Ar4 로 나타내지는 2 가의 방향족기로서는, 2 가의 방향족 탄화 수소기, 2 가의 방향족 복소 고리기를 들 수 있다. 그 2 가의 방향족기로서는, 벤젠 고리, 피리딘 고리, 1,2-디아진 고리, 1,3-디아진 고리, 1,4-디아진 고리, 1,3,5-트리아진 고리, 푸란 고리, 피롤 고리, 티오펜 고리, 피라졸 고리, 이미다졸 고리, 옥사졸 고리, 옥사디아졸 고리, 아자디아졸 고리 등의 단고리형 방향 고리로부터 수소 원자를 2 개 제외한 2 가의 기, 그 단고리형 방향 고리 중에서 서로 독립적으로 선택한 2 개 이상이 축합된 축합 다고리형 방향 고리로부터 수소 원자를 2 개 제외한 2 가의 기, 2 개 이상의 방향 고리를, 단결합, 에테닐렌기 또는 에티닐렌기로 연결한 다고리로부터 수소 원자를 2 개 제외한 2 가의 기, 2 개의 방향 고리를 메틸렌기, 에틸렌기, 카르보닐기, 이미노기 등의 2 가의 기로 가교한 구조를 갖는 유교 다고리형 방향 고리로부터 수소 원자를 2 개 제외한 2 가의 기 등을 들 수 있다.
상기 축합 다고리형 방향 고리에 있어서, 축합하는 단고리형 방향 고리의 수는, 공액 고분자 화합물의 용해성의 관점에서는, 2 ∼ 4 가 바람직하고, 2 ∼ 3 이 보다 바람직하고, 2 가 더욱 바람직하다. 상기 2 개 이상의 방향 고리를, 단결합, 에테닐렌기 또는 에티닐렌기로 연결한 다고리에 있어서, 연결되는 방향 고리의 수로서, 용해성의 관점에서는, 2 ∼ 4 가 바람직하고, 2 ∼ 3 이 보다 바람직하고, 2 가 더욱 바람직하다. 상기 유교 다고리형 방향 고리에 있어서, 가교되는 방향 고리의 수로서, 공액 고분자 화합물의 용해성의 관점에서는, 2 ∼ 4 가 바람직하고, 2 ∼ 3 이 보다 바람직하고, 2 가 더욱 바람직하다.
상기 단고리형 방향 고리로서는, 예를 들어, 이하의 고리를 들 수 있다.
상기 축합 다고리형 방향 고리로서는, 예를 들어, 이하의 고리를 들 수 있다.
상기 2 개 이상의 방향 고리를, 단결합, 에테닐렌기 또는 에티닐렌기로 연결한 다고리로서는, 예를 들어, 이하의 고리를 들 수 있다.
상기 유교 다고리형 방향 고리로서는, 예를 들어, 이하의 고리를 들 수 있다.
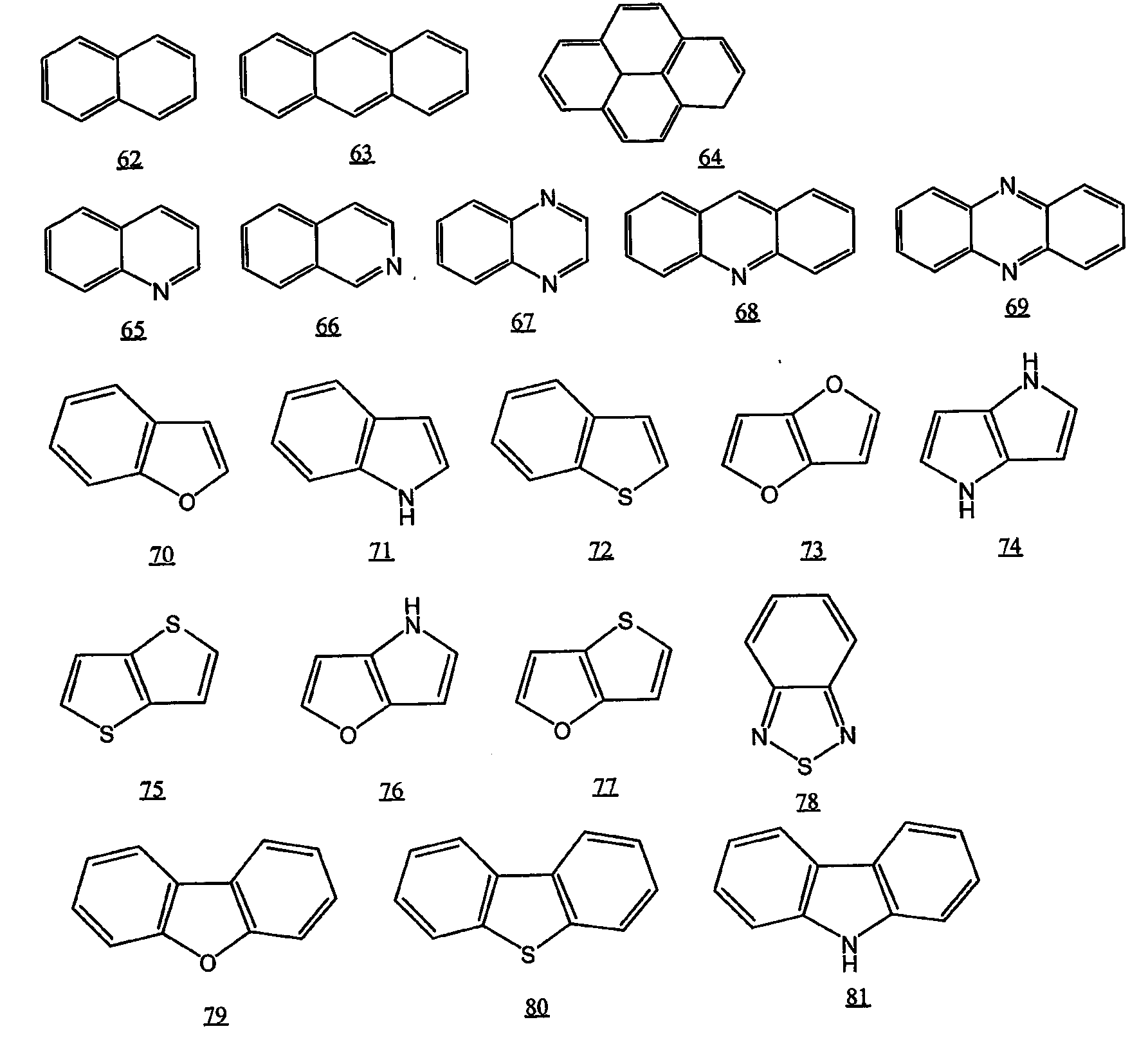
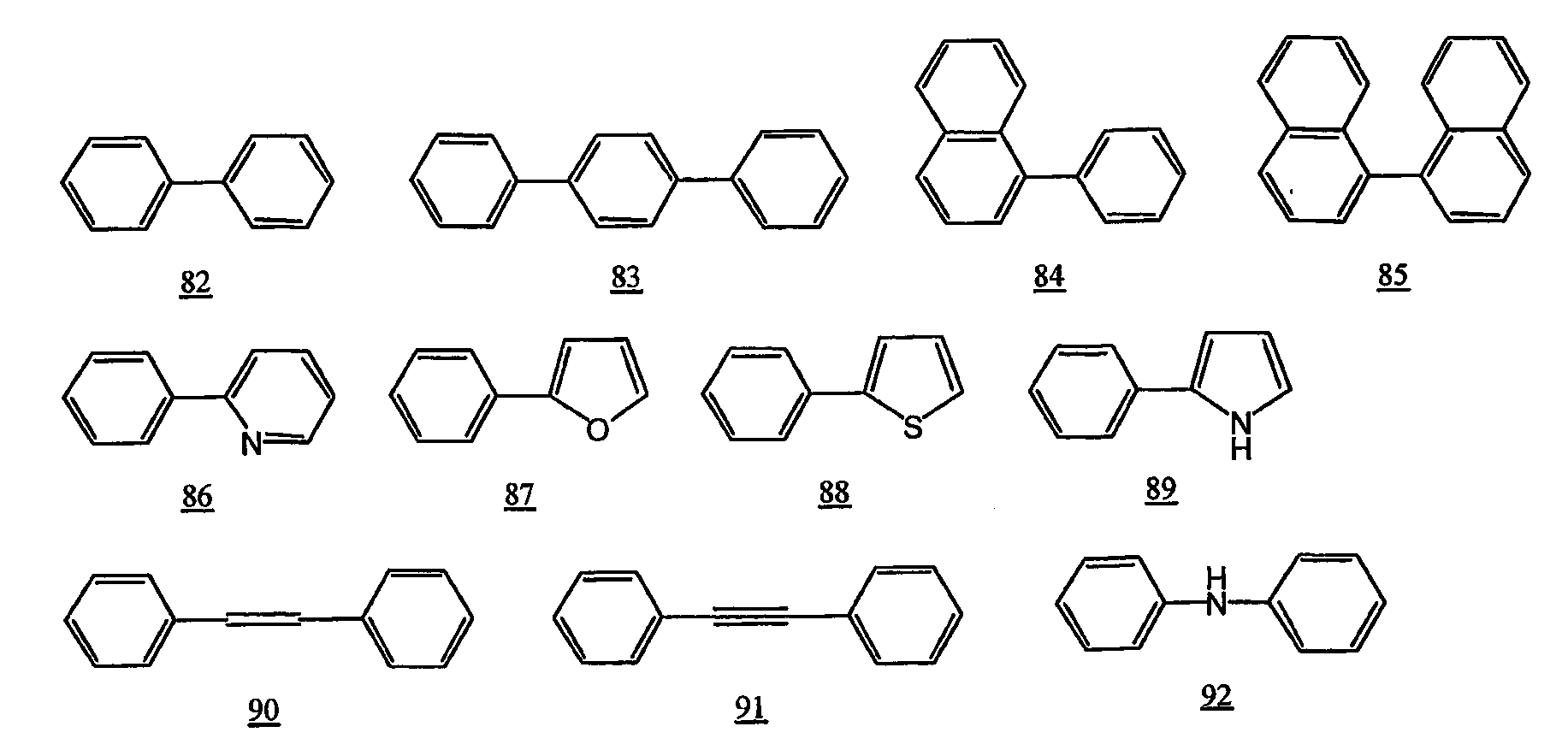
상기 공액 고분자 화합물의 전자 및/또는 홀 수용성의 관점에서는, Ar4 로 나타내지는 2 가의 방향족기는 식 46 ∼ 61, 식 62 ∼ 72, 식 78 ∼ 81, 식 92, 식 93, 식 94, 식 97 로 나타내지는 고리로부터 수소 원자를 2 개 제외한 2 가의 기가 바람직하고, 식 46 ∼ 51, 식 60, 식 61, 식 78, 식 81, 식 92, 식 93, 식 97 로 나타내지는 고리로부터 수소 원자를 2 개 제외한 2 가의 기가 보다 바람직하다.
상기 2 가의 방향족기는, R1, R2, R3 으로 나타내지는 치환기 이외의 치환기를 가지고 있어도 된다. 당해 치환기로서는, 전술한 Ar1 이 가지고 있어도 되는 R1 이외의 치환기와 동일한 치환기를 들 수 있다.
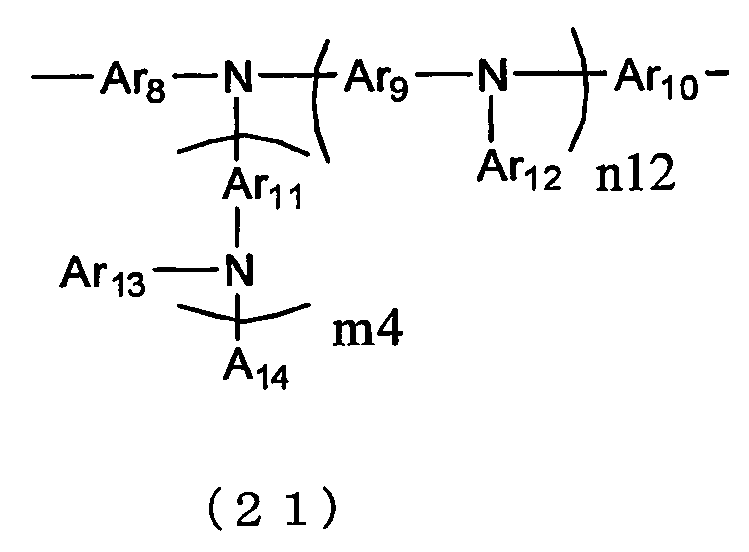
식 (20) 중의 Ar4 로 나타내지는 2 가의 방향족기 아민 잔기로서는, 식 (21) 로 나타내지는 기를 들 수 있다.
식 중, Ar8, Ar9, Ar10 및 Ar11 은 각각 독립적으로, 치환기를 가지고 있어도 되는 아릴렌기 또는 치환기를 가지고 있어도 되는 2 가의 복소 고리기를 나타내고, Ar12, Ar13 및 Ar14 는 치환기를 가지고 있어도 되는 아릴기 또는 치환기를 가지고 있어도 되는 1 가의 복소 고리기를 나타내고, n12 및 m4 는, 각각 독립적으로, 0 또는 1 을 나타낸다.
상기 아릴렌기, 아릴기, 2 가의 복소 고리기, 1 가의 복소 고리기가 가지고 있어도 되는 치환기로서는, 할로겐 원자, 알킬기, 알킬옥시기, 알킬티오기, 아릴기, 아릴옥시기, 아릴티오기, 아릴알킬기, 아릴알킬옥시기, 아릴알킬티오기, 알케닐기, 알키닐기, 아릴알케닐기, 아릴알키닐기, 아실기, 아실옥시기, 아미드기, 산이미드기, 이민 잔기, 치환 아미노기, 치환 실릴기, 치환 실릴옥시기, 치환 실릴티오기, 치환 실릴아미노기, 시아노기, 니트로기, 1 가의 복소 고리기, 헤테로아릴옥시기, 헤테로아릴티오기, 알킬옥시카르보닐기, 아릴옥시카르보닐기, 아릴알킬옥시카르보닐기, 헤테로아릴옥시카르보닐기 및 카르복실기 등을 들 수 있다. 그 치환기는, 비닐기, 아세틸렌기, 부테닐기, 아크릴기, 아크릴레이트기, 아크릴아미드기, 메타크릴기, 메타크릴레이트기, 메타크릴아미드기, 비닐에테르기, 비닐아미노기, 실란올기, 소원자 고리 (예를 들어 시클로프로필기, 시클로부틸기, 에폭시기, 옥세탄기, 디케텐기, 에피설파이드 등) 를 갖는 기, 락톤기, 락탐기, 또는 실록산 유도체의 구조를 함유하는 기 등의 가교기이어도 된다.
n12 가 0 인 경우, Ar8 중의 탄소 원자와 Ar10 중의 탄소 원자가 직접 결합되어도 되고, -O-, -S- 등의 2 가의 기를 개재하여 결합되어 있어도 된다. 상기 결합을 형성할 수 있는 아릴렌기로서는, 페닐렌기 등을 들 수 있으며, 2 가의 복소 고리기로서는, 피리딘디일기 등을 들 수 있다.
반복 단위로서 2 가의 방향족 아민 잔기를 포함하는 공액 고분자 화합물은, 추가로 다른 반복 단위를 가지고 있어도 된다. 다른 반복 단위로서는, 페닐렌기, 플루오렌디일기 등의 아릴렌기 등을 들 수 있다. 이들의 공액 고분자 화합물 중에서는, 가교기를 포함하고 있는 것이 보다 바람직하다.
식 (21) 로 나타내지는 2 가의 방향족 아민 잔기의 예로서는, 예를 들어, 하기 일반식 102 ∼ 111 로 나타내지는 방향족 아민으로부터 수소 원자를 2 개 제거한 기를 들 수 있다.
식 102 ∼ 111 로 나타내지는 방향족 아민은 치환기를 가지고 있어도 되고, 그 치환기로서는, 전술한 Ar1 이 가지고 있어도 되는 R1 이외의 치환기와 동일한 치환기를 들 수 있으며, 치환기가 복수 개 존재하는 경우에는, 그들은 동일하여도 되고 상이하여도 된다.
식 (20) 중, X 는 치환기를 가지고 있어도 되는 이미노기, 치환기를 가지고 있어도 되는 실릴렌기, 치환기를 가지고 있어도 되는 에테닐렌기 또는 에티닐렌기를 나타낸다. 이미노기, 실릴기 혹은 에테닐렌기가 가지고 있어도 되는 치환기로서는 메틸기, 에틸기, 프로필기, 이소프로필기, 부틸기, 이소부틸기, s-부틸기, t-부틸기, 펜틸기, 헥실기, 시클로헥실기, 헵틸기, 옥틸기, 2-에틸헥실기, 노닐기, 데실기, 3,7-디메틸옥틸기, 라우릴기 등의 탄소수 1 ∼ 20 의 알킬기, 페닐기, 1-나프틸기, 2-나프틸기, 1-안트라세닐기, 2-안트라세닐기, 9-안트라세닐기 등의 탄소수 6 ∼ 30 의 아릴기 등을 들 수 있으며, 치환기를 복수 개 갖는 경우에는, 그들은 동일하여도 되고 상이하여도 된다.
상기 공액 고분자 화합물의 공기, 습기 또는 열에 대한 안정성의 관점에서는, X 는 이미노기, 에테닐렌기, 에티닐렌기가 바람직하다.
상기 공액 고분자 화합물의 전자 및/또는 홀 수용성의 관점에서는, m2 가 1 이며, m3 이 0 인 것이 바람직하다.
식 (20) 으로 나타내지는 반복 단위로서는, 상기 공액 고분자 화합물의 전자 수용성의 관점에서는, 식 (22) 로 나타내지는 반복 단위가 바람직하다.
(식 중, Ar5 는 치환기를 가지고 있어도 되는 피리딘디일기, 치환기를 가지고 있어도 되는 피라진디일기, 치환기를 가지고 있어도 되는 피리미딘디일기, 치환기를 가지고 있어도 되는 피리다진디일기 또는 치환기를 가지고 있어도 되는 트리아진디일기를 나타낸다.)
피리딘디일기가 가지고 있어도 되는 치환기로서는, 전술한 Ar4 가 가지고 있어도 되는 치환기와 동일한 치환기를 들 수 있다. 치환기가 복수 개 존재하는 경우에는, 그들은 동일하여도 되고 상이하여도 된다. 피라진디일기가 가지고 있어도 되는 치환기로서는, 전술한 Ar4 가 가지고 있어도 되는 치환기와 동일한 치환기를 들 수 있다. 치환기가 복수 개 존재하는 경우에는, 그들은 동일하여도 되고 상이하여도 된다. 피리미딘디일기가 가지고 있어도 되는 치환기로서는, 전술한 Ar4 가 가지고 있어도 되는 치환기와 동일한 치환기를 들 수 있다. 치환기가 복수 개 존재하는 경우에는, 그들은 동일하여도 되고 상이하여도 된다. 피리다진디일기가 가지고 있어도 되는 치환기로서는, 전술한 Ar4 가 가지고 있어도 되는 치환기와 동일한 치환기를 들 수 있다. 치환기가 복수 개 존재하는 경우에는, 그들은 동일하여도 되고 상이하여도 된다. 트리아진디일기가 가지고 있어도 되는 치환기로서는, 전술한 Ar4 가 가지고 있어도 되는 치환기와 동일한 치환기를 들 수 있다. 치환기가 복수 개 존재하는 경우에는, 그들은 동일하여도 되고 상이하여도 된다.
전계 발광 소자의 효율의 관점에서는, 식 (1) 로 나타내지는 반복 단위만을 갖는 공액 고분자 화합물, 식 (3) 으로 나타내지는 반복 단위만을 갖는 공액 고분자 화합물, 식 (1) 로 나타내지는 반복 단위 및 식 (5) 로 나타내지는 반복 단위를 갖는 공액 고분자 화합물, 식 (3) 으로 나타내지는 반복 단위 및 식 (5) 로 나타내지는 반복 단위를 갖는 공액 고분자 화합물이 바람직하고, 식 (1) 로 나타내지는 반복 단위만을 갖는 공액 고분자 화합물, 식 (3) 으로 나타내지는 반복 단위만을 갖는 공액 고분자 화합물, 식 (3) 으로 나타내지는 반복 단위 및 식 (5) 로 나타내지는 반복 단위를 갖는 공액 고분자 화합물이 보다 바람직하다.
본 발명에 사용되는 공액 고분자 화합물 중에 포함되는 식 (1) 로 나타내지는 반복 단위, 식 (3) 으로 나타내지는 반복 단위 및 식 (5) 로 나타내지는 반복 단위의 수의 합계는, 그 공액 고분자 화합물이 갖는 전체 반복 단위의 수의 합계를 100 몰로 한 경우, 15 ∼ 100 몰인 것이 바람직하고, 전계 발광 소자의 효율의 관점에서는 50 ∼ 100 몰인 것이 보다 바람직하다.
공액 고분자 화합물의 도포에 의한 막 형성성의 관점에서, 본 발명에 사용되는 공액 고분자 화합물의 폴리스티렌 환산의 수 평균 분자량이 5×103 ∼ 1×108 인 것이 바람직하고, 5×103 ∼ 1×107 인 것이 보다 바람직하고, 1×104 ∼ 1×107 인 것이 더욱 바람직하다. 또, 폴리스티렌 환산의 중량 평균 분자량이 5×103 ∼ 1×108 인 것이 바람직하고, 5×103 ∼ 1×107 인 것이 보다 바람직하다.
본 발명에 사용되는 공액 고분자 화합물의 폴리스티렌 환산의 수 평균 분자량 및 중량 평균 분자량은, 예를 들어, 겔 퍼미에이션 크로마토그래피 (GPC) 를 이용하여 구할 수 있다.
공액 고분자 화합물의 전자 및/또는 홀의 수용성을 향상시키는 관점에서는, 본 발명에 사용되는 공액 고분자 화합물의 최저 비점유 분자 궤도 (LUMO) 의 궤도 에너지가, -5.0 eV 이상 -2.0 eV 이하인 것이 바람직하고, -4.5 eV ∼ -2.0 eV 이하가 보다 바람직하다. 또, 최고 점유 분자 궤도 (HOMO) 의 궤도 에너지가, -6.0 eV 이상 -3.0 eV 이하인 것이 바람직하고, -5.5 eV 이상 -3.0 eV 이하가 보다 바람직하다.
본 발명의 다른 실시형태로서, 용해도 파라미터가 9.3 미만인 용매에 대해 불용인 공액 고분자 화합물을 사용한 적층 구조체를 들 수 있으며, 용해도 파라미터가 9.3 미만인 용매 및 물에 대해 불용인 공액 고분자 화합물을 사용한 적층 구조체가 바람직하다.
용해도 파라미터의 값으로서는, 아사하라 쇼조 저 「용제 핸드북」 (14 판, 코단샤, 1996 년 발행) 에 기재된 값을 사용한다.
「공액 고분자 화합물이 용매에 불용」 이란, 공액 고분자 화합물 10 ㎎ 과 용매 1 ㎖ 를 혼합하여 20 ℃ 에서 교반한 후에, 5 ㎎ 이상의 공액 고분자 화합물이 용해되지 않고 잔존하고 있는 것을 가리킨다.
용해도 파라미터가 9.3 미만인 용매에 가용인 공액 고분자 화합물은, 도포할 때에 그 용매가 그 공액 고분자 화합물을 포함하는 층과 접촉하는 유기층을 녹이는 경우가 있다. 물에 가용인 경우에는, 그 공액 고분자 화합물을 포함하는 층의 흡습성이 높아지는 경향이 있다.
용해도 파라미터가 9.3 미만인 용매 (각 괄호 내의 값은, 각 용매의 용해도 파라미터의 값을 나타낸다) 로서는, 이소펜틸알코올 (9.2), 클로로포름 (9.1), 시클로헥산 (8.2), 헥산 (7.3), 디에틸에테르 (7.4), 이소옥탄 (7.0), 사염화탄소 (8.6), 테트라하이드로푸란 (9.1), 톨루엔 (8.9) 또는 혼합 용매를 들 수 있다. 용매는 단독이더라도, 혼합한 경우이더라도, 용해도 파라미터가 9.3 이상 20 미만이면 사용할 수 있다. 용매 1 과 용매 2 를 혼합한 경우에는 용해도 파라미터 (δm) 는, δm=δ1×φ1+δ2×φ2 에 의해 구한다 (δ1 은 용매 1 의 용해도 파라미터, φ1 은 용매 1 의 체적 분율, δ2 는 용매 2 의 용해도 파라미터, φ2 는 용매 2 의 체적 분율을 나타낸다.).
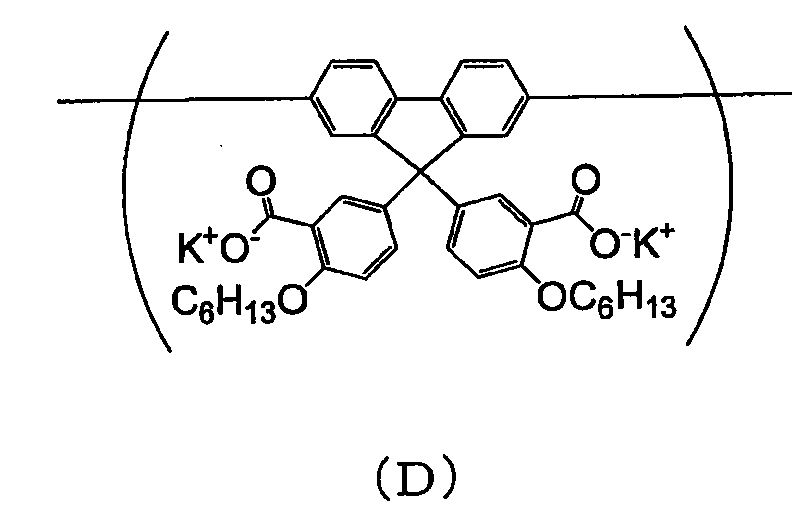
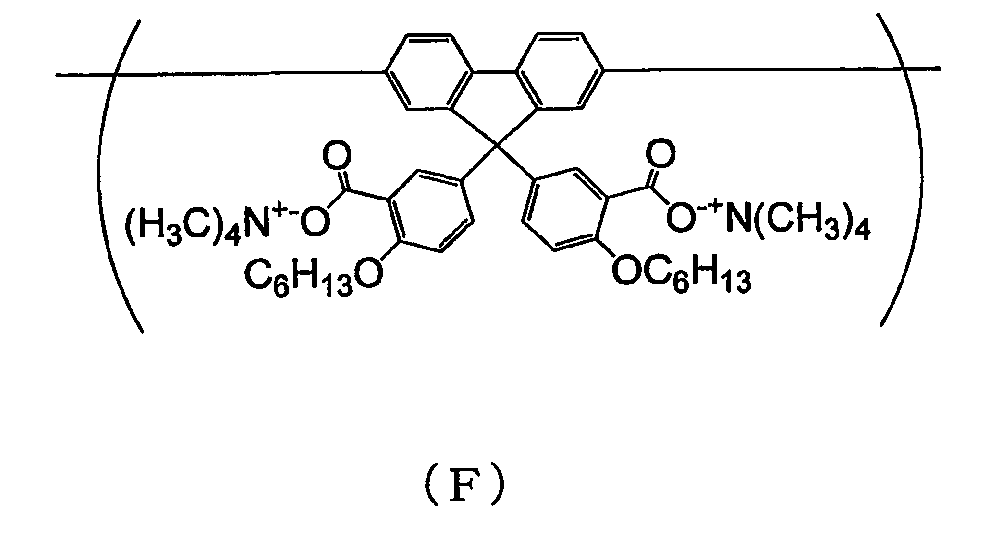
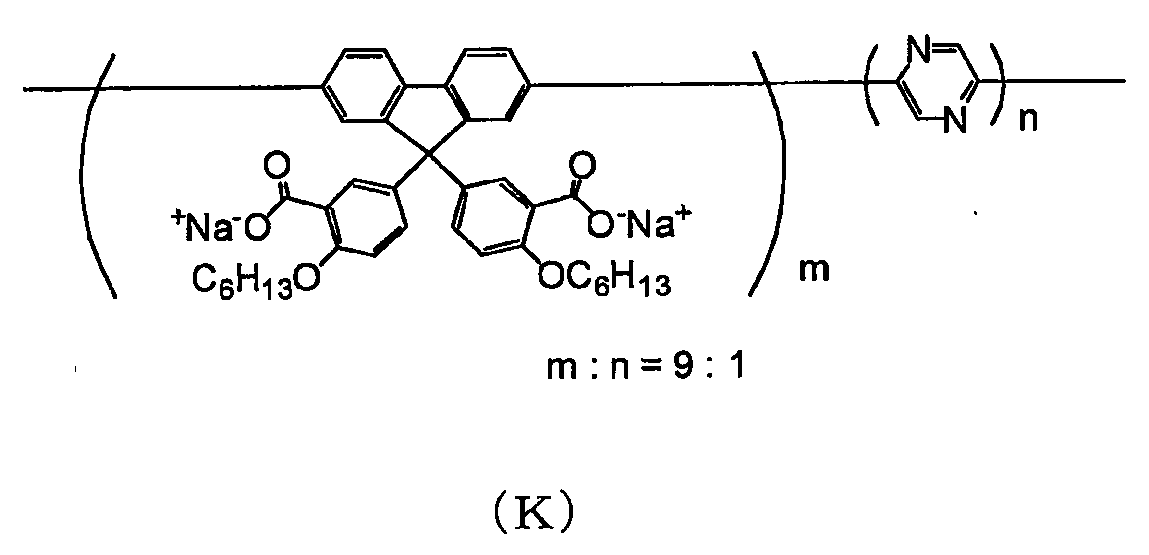
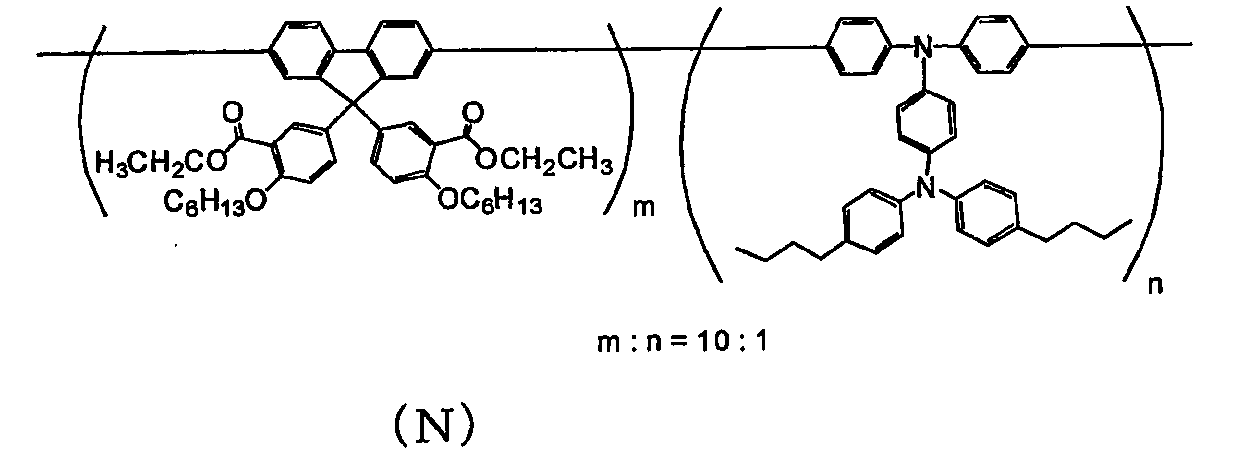
용해도 파라미터가 9.3 미만인 용매에 불용인 공액 고분자 화합물로서는, 예를 들어 이하의 공액 고분자 화합물을 들 수 있다.
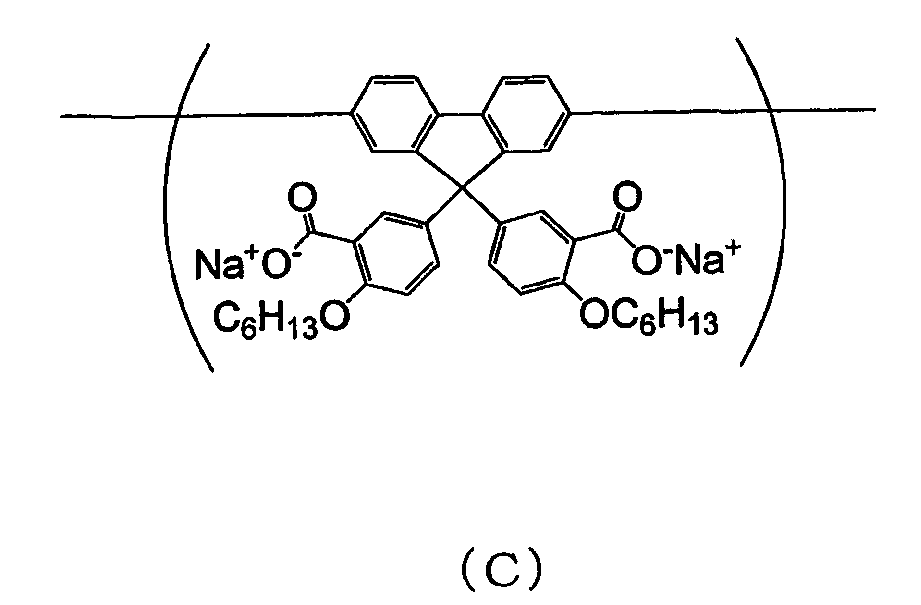
본 발명에 사용되는 공액 고분자 화합물의 바람직한 하나의 양태는, 식 (30) 으로 나타내지는 반복 단위를 갖는 공액 고분자 화합물이다.
(식 중, Rx 는 알칼리 금속을 나타내고, RY 는 알킬기 또는 알콕시기를 나타낸다.)
식 (30) 으로 나타내지는 반복 단위로서는, 식 (31) 로 나타내지는 반복 단위가 바람직하다.
(식 중, Rx, RY 는 전술한 바와 같은 의미를 나타낸다.)
본 발명에 사용되는 공액 고분자 화합물의 바람직한 다른 양태는, 식 (30) 으로 나타내지는 반복 단위와 아릴렌기인 반복 단위를 갖는 공액 고분자 화합물이다. 아릴렌기로서는, 페닐렌기, 플루오렌디일기가 바람직하다.
다음으로, 본 발명에 사용되는 공액 고분자 화합물을 제조하는 방법에 대해 설명한다. 본 발명에 사용되는 공액 고분자 화합물을 제조하기 위한 바람직한 방법으로서는, 예를 들어, 하기 일반식 (23) 으로 나타내지는 화합물을 원료의 하나로서 적절히 선택하여 이용하고, 그 중에서도, 상기 일반식 (23) 중의 -Aa- 가 식 (1), (3), (5), (15) ∼ (19) 로 나타내지는 반복 단위인 화합물을 각각 필수 성분으로 함유시켜, 이것을 축합 중합시키는 방법을 들 수 있다.
Y4-Aa-Y5 (23)
(식 중 Y4 및 Y5 는 각각 독립적으로 축합 중합에 관여하는 기를 나타낸다.)
본 발명에 사용되는 공액 고분자 화합물 중에 상기 식 (23) 중의 -Aa- 로 나타내지는 반복 단위와 함께, 상기 -Aa- 이외의 다른 반복 단위를 함유시키는 경우에는, 상기 -Aa- 이외의 다른 반복 단위가 되는, 2 개의 축합 중합에 관여하는 치환기를 갖는 화합물을 이용하고, 이것을 상기 식 (23) 으로 나타내지는 화합물과 함께 공존시켜 축합 중합시키면 된다.
이와 같은 다른 반복 단위를 함유시키기 위해서 사용되는 2 개의 축합 중합에 관여하는 기를 갖는 화합물로서는, 식 (24) 로 나타내지는 화합물이 예시된다. 이와 같이 하여, 상기 Y4-Aa-Y5 로 나타내지는 화합물에 추가하여, 식 (24) 로 나타내지는 화합물을 축합 중합시킴으로써, -Ab- 로 나타내지는 반복 단위를 추가로 갖는 본 발명에 관련된 공액 고분자 화합물을 제조할 수 있다.
(식 중, Ab 는 상기 일반식 (20) 으로 나타내지는 반복 단위 또는 일반식 (22) 로 나타내지는 반복 단위로, Y9 및 Y10 은 각각 독립적으로, 축합 중합에 관여하는 기를 나타낸다.)
이와 같은 축합 중합에 관여하는 기 (Y4, Y5, Y9 및 Y10) 로서는, 할로겐 원자, 알킬술포네이트기, 아릴술포네이트기, 아릴알킬술포네이트기, 붕산에스테르 잔기, 술포늄메틸기, 포스포늄메틸기, 포스포네이트메틸기, 모노할로겐화메틸기, -B(OH)2, 포르밀기, 시아노기 또는 비닐기 등을 들 수 있다.
이와 같은 축합 중합에 관여하는 기로서 선택될 수 있는 할로겐 원자로서는, 불소 원자, 염소 원자, 브롬 원자 또는 요오드 원자를 들 수 있다.
상기 축합 중합에 관여하는 기로서 선택될 수 있는 알킬술포네이트기로서는, 메탄술포네이트기, 에탄술포네이트기, 트리플루오로메탄술포네이트기 등이 예시되고, 아릴술포네이트기로서는, 벤젠술포네이트기, p-톨루엔술포네이트기 등이 예시되고, 아릴술포네이트기로서는, 벤질술포네이트기 등이 예시된다.
또, 상기 축합 중합에 관여하는 기로서 선택될 수 있는 붕산에스테르 잔기로서는, 하기 식으로 나타내지는 기가 예시된다.
또한, 상기 축합 중합에 관여하는 기로서 선택될 수 있는 술포늄메틸기로서는, 하기 식 :
(E 는 할로겐 원자를 나타내고, Ph 는 페닐기를 나타낸다.)
로 나타내지는 기가 예시된다.
상기 축합 중합에 관여하는 기로서 선택될 수 있는 포스포늄메틸기로서는, 하기 식 :
(E 는 할로겐 원자를 나타낸다.)
로 나타내지는 기가 예시된다.
상기 축합 중합에 관여하는 기로서 선택될 수 있는 포스포네이트메틸기로서는, 하기 식 :
(R' 는 알킬기, 아릴기, 아릴알킬기를 나타낸다.)
로 나타내지는 기가 예시된다.
또한, 상기 축합 중합에 관여하는 기로서 선택될 수 있는 모노할로겐화메틸기로서는, 불화메틸기, 염화메틸기, 브롬화메틸기 또는 요오드화메틸기가 예시된다.
또한, 축합 중합에 관여하는 기로서 바람직한 기로서는, 중합 반응의 종류에 따라 상이한 것으로 일률적으로는 말할 수 없지만, 예를 들어, 야마모토 커플링 반응 등 0 가 니켈 착물을 사용하는 경우에는, 할로겐 원자, 알킬술포네이트기, 아릴술포네이트기 또는 아릴알킬술포네이트기를 들 수 있다. 스즈키 커플링 반응 등 니켈 촉매 또는 팔라듐 촉매를 사용하는 경우에는, 알킬술포네이트기, 할로겐 원자, 붕산에스테르 잔기, -B(OH)2 등을 들 수 있으며, 산화제 또는 전기 화학적으로 산화 중합하는 경우에는 수소 원자를 들 수 있다.
본 발명에 사용되는 공액 고분자 화합물을 제조할 때에는, 예를 들어, 축합 중합에 관여하는 기를 복수 갖는 상기 일반식 (23) 또는 (24) 로 나타내지는 화합물 (모노머) 을, 필요에 따라 유기 용매에 용해시키고, 알칼리나 적당한 촉매를 적절히 이용하여, 유기 용매의 융점 이상 비점 이하의 온도에서 반응시키는 중합 방법을 채용하여도 된다. 이와 같은 중합 방법으로서는, 예를 들어, "올가닉 리액션즈 (Organic Reactions)", 제 14 권, 270-490 페이지, 죤 와일리 앤드 선즈, (John Wiley & Sons, Inc.), 1965 년, "올가닉 신세시스 (Organic Syntheses)", 콜렉티브 제 6 권 (Collective Volume VI), 407-411 페이지, 죤 와일리 앤드 선즈 (John Wiley & Sons, Inc.), 1988 년, 케미컬 리뷰 (Chem. Rev.), 제 95 권, 2457 페이지 (1995 년), 저널 오브 올가노메탈릭 케미스트리 (J. Organomet. Chem.), 제 576 권, 147 페이지 (1999 년), 마크로모레큘러 케미스트리 마크로모레큘러 신포지움 (Macromol. Chem., Macromol. Symp.), 제 12 권, 229 페이지 (1987 년) 등에 기재된 공지된 방법을 적절히 채용할 수 있다.
본 발명에 사용되는 공액 고분자 화합물을 제조할 때에는, 축합 중합에 관여하는 기에 따라, 이미 알려진 축합 중합 반응을 적절히 채용하여도 된다. 이와 같은 중합 방법으로서는, 예를 들어 해당하는 모노머를, 스즈키 커플링 반응에 의해 중합하는 방법, 그리냐르 반응에 의해 중합하는 방법, Ni (0) 착물에 의해 중합하는 방법, FeCl3 등의 산화제에 의해 중합하는 방법, 전기 화학적으로 산화 중합하는 방법, 또는 적당한 탈리기를 갖는 중간체 고분자의 분해에 의한 방법 등을 들 수 있다. 이와 같은 중합 반응 중에서도, 스즈키 커플링 반응에 의해 중합하는 방법, 그리냐르 반응에 의해 중합하는 방법, 및 니켈 제로가 (價) 착물에 의해 중합하는 방법이, 얻어지는 고분자 화합물의 구조를 제어하기 쉽기 때문에 바람직하다.
본 발명에 사용되는 공액 고분자 화합물의 바람직한 제조 방법의 하나의 양태는, 축합 중합에 관여하는 기 (Y4, Y5, Y9 및 Y10) 가 각각 독립적으로 할로겐 원자, 알킬술포네이트기, 아릴술포네이트기 또는 아릴알킬술포네이트기에서 선택되고, 또한 니켈 제로가 착물 존재하에서 축합 중합하여 고분자 화합물을 제조하는 방법을 들 수 있다. 이와 같은 방법에 사용하는 원료 화합물로서는, 예를 들어, 디할로겐화 화합물, 비스(알킬술포네이트) 화합물, 비스(아릴술포네이트) 화합물, 비스(아릴알킬술포네이트) 화합물, 할로겐-알킬술포네이트 화합물, 할로겐-아릴술포네이트 화합물, 할로겐-아릴알킬술포네이트 화합물, 알킬술포네이트-아릴술포네이트 화합물, 알킬술포네이트-아릴알킬술포네이트 화합물 및 아릴술포네이트-아릴알킬술포네이트 화합물 등을 들 수 있다.
상기 공액 고분자 화합물의 바람직한 제조 방법의 다른 양태는, 축합 중합에 관여하는 기 (Y4, Y5, Y9, Y10) 가 각각 독립적으로, 할로겐 원자, 알킬술포네이트기, 아릴술포네이트기, 아릴알킬술포네이트기, 붕산기, 또는 붕산에스테르 잔기로부터 선택되고, 전체 원료 화합물이 갖는, 할로겐 원자, 알킬술포네이트기, 아릴술포네이트기 및 아릴알킬술포네이트기의 몰수의 합계 (J) 와, 붕산기 (-B(OH)2) 및 붕산에스테르 잔기의 몰수의 합계 (K) 의 비가 실질적으로 1 (통상 K/J 는 0.7 ∼ 1.2 의 범위) 이며, 또한 니켈 촉매 또는 팔라듐 촉매를 이용하여 축합 중합하여 공액계 폴리머를 제조하는 방법을 들 수 있다.
이와 같은 공액 고분자 화합물의 제조 방법을 채용하는 경우에 있어서의 구체적인 원료 화합물의 조합으로서는, 디할로겐화 화합물만의 조합, 비스(알킬술포네이트) 화합물만의 조합, 비스(아릴술포네이트) 화합물과 비스(아릴알킬술포네이트) 화합물의 어느 하나와 디붕산 화합물 또는 디붕산에스테르 화합물의 어느 하나와의 조합 등을 들 수 있다. 시퀀스를 제어한 공액계 폴리머를 제조하는 관점에서는, 할로겐-붕산 화합물, 할로겐-붕산에스테르 화합물, 알킬술포네이트-붕산 화합물, 알킬술포네이트-붕산에스테르 화합물, 아릴술포네이트-붕산 화합물, 아릴술포네이트-붕산에스테르 화합물, 아릴알킬술포네이트-붕산 화합물, 아릴알킬술포네이트-붕산에스테르 화합물을 사용하는 것이 바람직하다.
상기 유기 용매로서는, 사용하는 화합물이나 반응에 따라 상이하기도 하지만, 일반적으로 부반응을 억제하기 위해서 충분히 탈산소 처리를 실시한 것을 사용하는 것이 바람직하고, 고분자 화합물을 제조할 때에는, 이와 같은 유기 용매를 이용하여 불활성 분위기하에서 반응을 진행시키는 것이 바람직하다. 상기 유기 용매에 있어서는, 상기 탈산소 처리와 마찬가지로 탈수 처리를 실시하는 것이 바람직하다. 단, 스즈키 커플링 반응과 같은 물과의 2 상 계에서의 반응인 경우에는 예외로 한다.
이와 같은 유기 용매로서는, 펜탄, 헥산, 헵탄, 옥탄, 시클로헥산 등의 포화 탄화수소, 벤젠, 톨루엔, 에틸벤젠, 자일렌 등의 불포화 탄화수소, 사염화탄소, 클로로포름, 디클로로메탄, 클로로부탄, 브로모부탄, 클로로펜탄, 브로모펜탄, 클로로헥산, 브로모헥산, 클로로시클로헥산, 브로모시클로헥산 등의 할로겐화 포화 탄화수소, 클로로벤젠, 디클로로벤젠, 트리클로로벤젠 등의 할로겐화 불포화 탄화수소, 메탄올, 에탄올, 프로판올, 이소프로판올, 부탄올, t-부틸알코올 등의 알코올류, 포름산, 아세트산, 프로피온산 등의 카르복실산류, 디메틸에테르, 디에틸에테르, 메틸-t-부틸에테르, 테트라하이드로푸란, 테트라하이드로피란, 디옥산 등의 에테르류, 트리메틸아민, 트리에틸아민, N,N,N',N'-테트라메틸에틸렌디아민, 피리딘 등의 아민류, N,N-디메틸포름아미드, N,N-디메틸아세트아미드, N,N-디에틸아세트아미드, N-메틸모르폴린옥사이드 등의 아미드류 등이 예시된다. 이들의 유기 용매는 1 종을 단독으로, 또는 2 종 이상을 혼합하여 사용하여도 된다. 또, 이와 같은 유기 용매 중에서도, 반응성의 관점에서는 에테르류가 보다 바람직하고, 테트라하이드로푸란, 디에틸에테르가 더욱 바람직하다. 또, 반응 속도의 관점에서는 톨루엔, 자일렌이 바람직하다.
상기 공액 고분자 화합물을 제조할 때에는, 원료 화합물을 반응시키기 위해서 적절히 알칼리나 적당한 촉매를 첨가하는 것이 바람직하다. 이와 같은 알칼리 또는 촉매는, 채용하는 중합 방법 등에 따라 선택하면 된다. 이와 같은 알칼리 또는 촉매로서는, 반응에 사용하는 용매에 충분히 용해되는 것이 바람직하다. 상기 알칼리 또는 촉매를 혼합하는 방법으로서는, 반응액을 아르곤이나 질소 등의 불활성 분위기하에서 교반하면서 천천히 알칼리 또는 촉매의 용액을 첨가하거나, 반대로 알칼리 또는 촉매의 용액에 반응액을 천천히 첨가하는 방법이 예시된다.
본 발명에 관련된 공액 고분자 화합물에 있어서는, 말단기에 중합 활성기가 그대로 남아 있으면 본 발명의 고분자 발광 소자의 발광 특성이나 수명 특성이 저하될 가능성이 있기 때문에, 말단기가 안정된 기로 보호되어 있어도 된다. 이와 같이 안정된 기로 말단기가 보호되어 있는 경우에는, 주사슬의 공액 구조와 연속된 공액 결합을 가지고 있는 것이 바람직하고, 그 구조로서는, 예를 들어, 탄소-탄소 결합을 개재하여 아릴기 또는 복소 고리기와 결합되어 있는 구조를 들 수 있다. 이와 같은 말단기를 보호하는 안정된 기로서는, 예를 들어, 일본 공개특허공보 평9-45478호에 있어서 화 10 의 구조식으로 나타내지는 1 가의 방향족 화합물기 등의 치환기를 들 수 있다.
식 (1) 로 나타내지는 반복 단위를 포함하는 공액 고분자 화합물을 제조하는 다른 바람직한 방법으로서는, 제 1 공정에서 이온을 갖지 않는 공액 고분자 화합물을 중합하고, 제 2 공정에서 그 공액 고분자 화합물로부터 이온을 함유하는 공액 고분자 화합물을 제조하는 방법을 들 수 있다. 제 1 공정의 이온을 갖지 않는 공액 고분자 화합물을 중합하는 방법으로서는, 전술한 축합 중합 반응을 들 수 있다. 제 2 공정의 반응으로서는, 할로겐화알킬을 사용한 아민의 4 급 암모늄 염화 반응, SbF5 에 의한 할로겐 추출 반응 등을 들 수 있다.
식 (3) 으로 나타내지는 반복 단위를 포함하는 공액 고분자 화합물을 제조하는 다른 바람직한 방법으로서는, 제 1 공정에서 카티온을 갖지 않는 공액 고분자 화합물을 중합하고, 제 2 공정에서 그 공액 고분자 화합물로부터 카티온을 함유하는 공액 고분자 화합물을 제조하는 방법을 들 수 있다. 제 1 공정의 카티온을 갖지 않는 공액 고분자 화합물을 중합하는 방법으로서는, 전술한 축합 중합 반응을 들 수 있다. 제 2 공정의 반응으로서는, 금속 수산화물, 알킬암모늄하이드록시 등에 의한 가수 분해 반응 등을 들 수 있다.
<적층 구조체>
다음으로, 본 발명에 관련된 적층 구조체에 대해 설명한다.
본 발명의 적층 구조체는, 제 1 전극 및 제 2 전극과, 그 제 1 전극과 그 제 2 전극과의 사이에 발광층 혹은 전하 분리층을 가지며, 그 발광층 혹은 전하 분리층과 그 제 1 전극과의 사이에 공액 고분자 화합물을 포함하는 층을 가지며, 그 공액 고분자 화합물이 식 (1) 로 나타내지는 반복 단위, 식 (3) 으로 나타내지는 반복 단위 및 식 (5) 로 나타내지는 반복 단위로 이루어지는 군에서 선택되는 1 종 이상의 반복 단위를 갖는다.
본 발명의 적층 구조체는, 전계 발광 소자, 광전 변환 소자 등에 사용할 수 있다. 적층 구조체를 전계 발광 소자에 사용하는 경우에는, 적층 구조체 중에 발광층을 가지고 있다. 적층 구조체를 광전 변환 소자에 사용하는 경우에는, 적층 구조체 중에 전하 분리층을 가지고 있다.
본 발명에 사용되는 공액 고분자 화합물은 전하의 주입성이나 수송성이 우수하기 때문에, 그 공액 고분자 화합물을 포함하는 층을 전계 발광 소자에 사용한 경우, 고휘도로 발광하는 소자가 얻어진다. 그 공액 고분자 화합물을 포함하는 층을 광전 변환 소자에 사용한 경우, 변환 효율이 높은 소자가 얻어진다.
<전계 발광 소자>
본 발명의 적층 구조체를 사용한 전계 발광 소자는, 음극, 양극, 및 상기 음극과 양극 사이에 발광층을 갖는다. 본 발명의 전계 발광 소자는, 통상 임의의 구성 요소로서 기판을 추가로 가질 수 있으며, 이러한 기판의 면 상에 상기 음극, 양극, 발광층 및 본 발명의 공액 고분자 화합물을 포함하는 층, 그리고 필요에 따라 그 밖의 임의의 구성 요소를 형성한 구성으로 할 수 있다.
본 발명의 전계 발광 소자의 하나의 양태로서는, 기판 상에 양극이 형성되고, 그 상층에 발광층이 적층되고, 다시 그 상층에 음극이 적층된다. 다른 하나의 양태로서는, 음극을 기판 상에 형성하고, 양극을 발광층의 상층에 형성하여도 된다. 다른 양태로서는, 기판측으로부터 채광하는 소위 보텀 이미션 타입, 기판과 반대측으로부터 채광하는 소위 탑 이미션 타입, 또는 양면 채광형 중 어느 타입의 전계 발광 소자이어도 된다. 또 다른 양태로서는, 임의의 보호막, 버퍼막, 반사층 등의 다른 기능을 갖는 층을 형성하여도 된다. 전계 발광 소자의 구성에 대해서는, 하기에서 별도로 상세하게 서술한다. 전계 발광 소자는 또한 밀봉막, 혹은 밀봉 기판이 덮어씌워져 전계 발광 소자가 외기와 차단된 발광 장치가 형성된다.
본 발명에 사용되는 공액 고분자 화합물을 포함하는 층은, 전계 발광 소자에 있어서의 음극과 발광층 사이의 층 또는 양극과 발광층 사이의 층 등으로서 사용할 수 있으며, 전하 주입층 또는 전하 수송층 등으로서 사용된다.
공액 고분자 화합물을 포함하는 층을 형성하는 방법으로서는, 예를 들어, 공액 고분자 화합물을 함유하는 용액을 이용하여 막 형성하는 방법을 들 수 있다.
이와 같은 용액으로부터의 막 형성에 사용하는 용매로서는, 물을 제외한 용해도 파라미터가 9.3 이상인 용매가 바람직하다. 그 용매의 예 (각 괄호 내의 값은, 각 용매의 용해도 파라미터의 값을 나타낸다) 로서는, 메탄올 (12.9), 에탄올 (11.2), 2-프로판올 (11.5), 1-부탄올 (9.9), t-부틸알코올 (10.5), 아세토니트릴 (11.8), 1,2-에탄디올 (14.7), N,N-디메틸포름아미드 (11.5), 디메틸술폭사이드 (12.8), 아세트산 (12.4), 니트로벤젠 (11.1), 니트로메탄 (11.0), 1,2-디클로로에탄 (9.7), 디클로로메탄 (9.6), 클로로벤젠 (9.6), 브로모벤젠 (9.9), 디옥산 (9.8), 탄산프로필렌 (13.3), 피리딘 (10.4), 2 황화탄소 (10.0), 또는 이들의 용매의 혼합 용매 등을 들 수 있다. 용매 1 과 용매 2 의 혼합 용매의 경우에는 용해도 파라미터 (δm) 는, δm=δ1×φ1+δ2×φ2 에 의해 구하는 것으로 한다 (δ1 은 용매 1 의 용해도 파라미터, φ1 은 용매 1 의 체적 분율, δ2 는 용매 2 의 용해도 파라미터, φ2 는 용매 2 의 체적 분율이다.).
용액으로부터의 막 형성 방법으로서는, 예를 들어, 스핀 코트법, 캐스팅법, 마이크로 그라비아 코트법, 그라비아 코트법, 바 코트법, 롤 코트법, 와이어 바 코트법, 딥 코트법, 슬릿 코트법, 캡 코트법, 스프레이 코트법, 스크린 인쇄법, 플렉소 인쇄법, 오프셋 인쇄법, 잉크젯 프린트법, 노즐 코트법 등의 도포법을 들 수 있다.
공액 고분자 화합물을 포함하는 층의 막두께로서는, 사용하는 공액 고분자 화합물에 따라 최적치가 상이하기 때문에, 구동 전압과 발광 효율이 알맞은 값이 되도록 적절히 선택하면 되고, 적어도 핀홀이 발생하지 않는 두께인 것이 바람직하다. 소자의 구동 전압을 낮게 하는 관점에서는, 1 ㎚ ∼ 1 ㎛ 인 것이 바람직하고, 2 ㎚ ∼ 500 ㎚ 인 것이 보다 바람직하고, 2 ㎚ ∼ 200 ㎚ 인 것이 더욱 바람직하다.
전계 발광 소자는 음극 및 양극을 가지며, 음극과 양극 사이에 발광층을 갖는데, 이들과 더불어, 추가로 구성 요소를 구비한다.
예를 들어, 양극과 발광층 사이에는 정공 주입층, 인터레이어, 정공 수송층 중 1 층 이상을 가질 수 있다. 정공 주입층이 존재하는 경우에는, 발광층과 정공 주입층 사이에 인터레이어, 정공 수송층 중 1 층 이상을 가질 수 있다.
한편, 음극과 유기 발광층 사이에는 전자 주입층, 전자 수송층, 정공 블록층 중 1 층 이상을 가질 수 있다. 전자 주입층이 존재하는 경우에는, 유기 발광층과 전자 주입층 사이에 전자 수송층, 정공 블록층 중 1 층 이상을 가질 수 있다.
본 발명에 사용되는 공액 고분자 화합물을 포함하는 층은, 정공 주입층, 정공 수송층, 인터레이어, 전자 주입층, 전자 수송층, 정공 블록층 등에 사용할 수 있다. 공액 고분자 화합물을 포함하는 층을 정공 주입층, 정공 수송층, 인터레이어로서 사용하는 경우, 제 1 전극은 양극이 되고, 제 2 전극은 음극이 된다. 공액 고분자 화합물을 포함하는 층을 전자 주입층, 전자 수송층, 정공 블록층으로서 사용하는 경우, 제 1 전극은 음극이 되고, 제 2 전극은 양극이 된다.
양극은 정공 주입층, 정공 수송층, 인터레이어, 발광층 등에 정공을 공급하는 것이며, 음극은 전자 주입층, 전자 수송층, 정공 블록층, 발광층 등에 전자를 공급하는 것이다.
발광층이란, 전계를 인가했을 때에, 양극측에 인접하는 층으로부터 정공을 수취하고, 음극측에 인접하는 층으로부터 전자를 수취하는 기능, 수취한 전하 (전자와 정공) 를 전계의 힘으로 이동시키는 기능, 전자와 정공의 재결합의 장소를 제공하여, 이것을 발광으로 연결하는 기능을 갖는 층을 가리킨다.
전자 주입층 및 전자 수송층이란, 음극으로부터 전자를 수취하는 기능, 전자를 수송하는 기능, 양극으로부터 주입된 정공을 차단하는 기능 중 어느 기능을 갖는 층을 가리킨다. 정공 블록층이란, 주로 양극으로부터 주입된 정공을 장벽치는 기능을 가지며, 추가로 필요에 따라 음극으로부터 전자를 수취하는 기능, 전자를 수송하는 기능 중 어느 기능을 갖는 층을 가리킨다.
정공 주입층 및 정공 수송층이란, 양극으로부터 정공을 수취하는 기능, 정공을 수송하는 기능, 발광층에 정공을 공급하는 기능, 음극으로부터 주입된 전자를 장벽치는 기능 중 어느 기능을 갖는 층을 가리킨다. 인터레이어층이란, 양극으로부터 정공을 수취하는 기능, 정공을 수송하는 기능, 발광층에 정공을 공급하는 기능, 음극으로부터 주입된 전자를 장벽치는 기능 중 적어도 하나 이상을 가지며, 통상, 발광층에 인접하여 배치되어, 발광층과 양극, 또는 발광층과 정공 주입층 혹은 정공 수송층을 격리시키는 역할을 한다.
전자 수송층과 정공 수송층을 총칭하여 전하 수송층이라고 부른다. 전자 주입층과 정공 주입층을 총칭하여 전하 주입층이라고 부른다.
즉, 본 발명의 전계 발광 소자는 하기의 층 구성 (a) 를 가질 수 있거나, 또는, 층 구성 (a) 로부터, 정공 주입층, 정공 수송층, 인터레이어, 정공 블록층, 전자 수송층, 전자 주입층의 1 층 이상을 생략한 층 구성을 가질 수도 있다. 층 구성 (a) 에 있어서, 본 발명에 사용되는 공액 고분자 화합물을 포함하는 층은, 정공 주입층, 정공 수송층, 인터레이어, 전자 주입층, 전자 수송층 및 정공 블록층으로 이루어지는 군에서 선택되는 하나 이상의 층으로서 사용할 수 있다.
(a) 양극-정공 주입층-(정공 수송층 및/또는 인터레이어)-발광층-(정공 블록층 및/또는 전자 수송층)-전자 주입층-음극
부호 「-」 는 각층이 인접하여 적층되어 있는 것을 나타낸다.
「(정공 수송층 및/또는 인터레이어)」 는, 정공 수송층만으로 이루어지는 층, 인터레이어만으로 이루어지는 층, 정공 수송층-인터레이어의 층 구성, 인터레이어-정공 수송층의 층 구성, 또는 그 밖의, 정공 수송층 및 인터레이어를 각각 1 층 이상 포함하는 임의의 층 구성을 나타낸다.
「(정공 블록층 및/또는 전자 수송층)」 은, 정공 블록층만으로 이루어지는 층, 전자 수송층만으로 이루어지는 층, 정공 블록층-전자 수송층의 층 구성, 전자 수송층-정공 블록층의 층 구성, 또는 그 밖의, 정공 블록층 및 전자 수송층을 각각 1 층 이상 포함하는 임의의 층 구성을 나타낸다. 이하의 층 구성의 설명에서도 동일하다.
또한, 본 발명의 전계 발광 소자는, 하나의 적층 구조 중에 2 층의 발광층을 가질 수 있다. 이 경우, 전계 발광 소자는 하기의 층 구성 (b) 를 가질 수 있거나, 또는, 층 구성 (b) 로부터, 정공 주입층, 정공 수송층, 인터레이어, 정공 블록층, 전자 수송층, 전자 주입층, 전극의 1 층 이상을 생략한 층 구성을 가질 수도 있다. 층 구성 (b) 에 있어서, 공액 고분자 화합물을 포함하는 층은, 양극과 양극에 가장 가까운 발광층과의 사이에 존재하는 층으로서 사용되거나, 음극과 음극에 가장 가까운 발광층과의 사이에 존재하는 층으로서 사용된다.
(b) 양극-정공 주입층-(정공 수송층 및/또는 인터레이어)-발광층-(정공 블록층 및/또는 전자 수송층)-전자 주입층-전극-정공 주입층-(정공 수송층 및/또는 인터레이어)-발광층-(정공 블록층 및/또는 전자 수송층)-전자 주입층-음극
또한, 본 발명의 전계 발광 소자는, 하나의 적층 구조 중에 3 층 이상의 발광층을 가질 수 있다. 이 경우, 전계 발광 소자는 하기의 층 구성 (c) 를 가질 수 있거나, 또는, 층 구성 (c) 로부터, 정공 주입층, 정공 수송층, 인터레이어, 정공 블록층, 전자 수송층, 전자 주입층, 전극의 1 층 이상을 생략한 층 구성을 가질 수도 있다. 층 구성 (c) 에 있어서, 공액 고분자 화합물을 포함하는 층은, 양극과 양극에 가장 가까운 발광층과의 사이에 존재하는 층으로서 사용되거나, 음극과 음극에 가장 가까운 발광층과의 사이에 존재하는 층으로서 사용된다.
(c) 양극-정공 주입층-(정공 수송층 및/또는 인터레이어)-발광층-(정공 블록층 및/또는 전자 수송층)-전자 주입층-반복 단위 A-반복 단위 A…-음극
「반복 단위 A」 는, 전극-정공 주입층-(정공 수송층 및/또는 인터레이어)-발광층-(정공 블록층 및/또는 전자 수송층)-전자 주입층의 층 구성의 단위를 나타낸다.
본 발명의 전계 발광 소자의 층 구성의 바람직한 예로서는, 하기의 것을 들 수 있다. 하기 층 구성에 있어서, 본 발명에 사용되는 공액 고분자 화합물을 포함하는 층은, 정공 주입층, 정공 수송층, 인터레이어, 전자 주입층, 전자 수송층 및 정공 블록층으로 이루어지는 군에서 선택되는 하나 이상의 층으로서 사용할 수 있다.
(d) 양극-정공 수송층-발광층-음극
(e) 양극-발광층-전자 수송층-음극
(f) 양극-정공 수송층-발광층-전자 수송층-음극
이들 구조의 각 하나에 대해, 발광층과 양극 사이에, 발광층에 인접하여 인터레이어층을 형성하는 구조도 예시된다. 즉, 이하의 (d') ∼ (g') 의 구조가 예시된다.
(d') 양극-인터레이어층-발광층-음극
(e') 양극-정공 수송층-인터레이어층-발광층-음극
(f') 양극-인터레이어층-발광층-전자 수송층-음극
(g') 양극-정공 수송층-인터레이어층-발광층-전자 수송층-음극
본 발명에 있어서, 전하 주입층 (전자 주입층, 정공 주입층) 을 형성한 전계 발광 소자의 예로서는, 음극에 인접하여 전하 주입층을 형성한 전계 발광 소자, 양극에 인접하여 전하 주입층을 형성한 전계 발광 소자를 들 수 있다. 그 구체예로는, 예를 들어, 이하의 (h) ∼ (s) 의 구조를 들 수 있다.
(h) 양극-전하 주입층-발광층-음극
(i) 양극-발광층-전하 주입층-음극
(j) 양극-전하 주입층-발광층-전하 주입층-음극
(k) 양극-전하 주입층-정공 수송층-발광층-음극
(l) 양극-정공 수송층-발광층-전하 주입층-음극
(m) 양극-전하 주입층-정공 수송층-발광층-전하 주입층-음극
(n) 양극-전하 주입층-발광층-전자 수송층-음극
(o) 양극-발광층-전자 수송층-전하 주입층-음극
(p) 양극-전하 주입층-발광층-전자 수송층-전하 주입층-음극
(q) 양극-전하 주입층-정공 수송층-발광층-전자 수송층-음극
(r) 양극-정공 수송층-발광층-전자 수송층-전하 주입층-음극
(s) 양극-전하 주입층-정공 수송층-발광층-전자 수송층-전하 주입층-음극
(d') ∼ (g') 와 유사하게, 이들 구조의 각 하나에 대해, 발광층과 양극 사이에, 발광층에 인접하여 인터레이어층을 형성하는 구조도 예시된다. 이 경우, 인터레이어층이 정공 주입층 및/또는 정공 수송층을 겸하여도 된다.
본 발명에 사용되는 공액 고분자 화합물을 포함하는 층은, 전자 주입층 또는 전자 수송층인 것이 바람직하다. 공액 고분자 화합물을 포함하는 층이, 전자 주입층 또는 전자 수송층인 경우, 제 1 전극은 통상 음극이다.
본 발명의 전계 발광 소자는, 추가로 전극과의 밀착성 향상이나 전극으로부터의 전하 (즉 정공 또는 전자) 주입의 개선을 위해서, 전극에 인접하여 절연층을 형성하여도 되고, 또, 계면의 밀착성 향상이나 혼합의 방지 등을 위해서 전하 수송층 (즉 정공 수송층 또는 전자 수송층) 또는 발광층의 계면에 얇은 버퍼층을 삽입하여도 된다. 적층하는 층의 순서나 수, 및 각층의 두께에 대해서는, 발광 효율이나 소자 수명을 감안하여 적절히 사용할 수 있다.
다음으로, 본 발명의 전계 발광 소자를 구성하는 각 층의 재료 및 형성 방법에 대해, 보다 구체적으로 설명한다.
<기판>
본 발명의 전계 발광 소자를 구성하는 기판은, 전극을 형성하고, 유기물 층을 형성할 때에 변화하지 않는 것이면 되고, 예를 들어 유리, 플라스틱, 고분자 필름, 금속 필름, 실리콘 기판, 이들을 적층한 것 등이 사용된다. 상기 기판으로서는, 시판되는 것을 입수할 수 있거나, 또는 공지된 방법에 의해 제조할 수 있다.
본 발명의 전계 발광 소자가 디스플레이 장치의 화소를 구성할 때에는, 당해 기판 상에 화소 구동용 회로가 형성되어 있어도 되고, 당해 구동 회로 상에 평탄화막이 형성되어 있어도 된다. 평탄화막이 형성되는 경우에는, 그 평탄화막의 중심선 평균 거침도 (Ra) 가 Ra<10 ㎚ 를 만족하는 것이 바람직하다.
Ra 는 일본 공업 규격 JIS 의 JIS-B0601-2001 에 기초하여, JIS-B0651 에서 JIS-B0656 및 JIS-B0671-1 등을 참고로 계측할 수 있다.
<양극>
본 발명의 전계 발광 소자를 구성하는 양극은, 정공 주입층, 정공 수송층, 인터레이어, 발광층 등에서 사용되는 유기 반도체 재료에 대한 정공 공급성의 관점에서, 이러한 양극의 발광층측 표면의 일 함수가 4.0 eV 이상인 것이 바람직하다.
양극의 재료에는, 금속, 합금, 금속 산화물, 금속 황화물 등의 전기 전도성 화합물, 또는 이들의 혼합물 등을 사용할 수 있다. 양극의 재료의 예로서는, 산화주석, 산화아연, 산화인듐, 산화인듐주석 (ITO), 산화인듐아연 (IZO), 산화몰리브덴 등의 도전성 금속 산화물, 또는, 금, 은, 크롬, 니켈 등의 금속, 또한 이들의 도전성 금속 산화물과 금속과의 혼합물 등을 들 수 있다.
상기 양극은, 이들 재료의 1 종 또는 2 종 이상으로 이루어지는 단층 구조이어도 되고, 동일 조성 또는 이종 조성의 복수 층으로 이루어지는 다층 구조이어도 된다. 다층 구조인 경우는, 일 함수가 4.0 eV 이상인 재료를 발광층측의 최표면층에 사용하는 것이 보다 바람직하다.
양극의 제작 방법으로서는, 특별히 한정되지 않고 공지된 방법을 이용할 수 있으며, 진공 증착법, 스퍼터링법, 이온 플레이팅법, 도금법 등을 들 수 있다.
양극의 막두께는, 통상 10 ㎚ ∼ 10 ㎛ 이며, 바람직하게는 50 ㎚ ∼ 500 ㎚ 이다.
단락 등의 전기적 접속의 불량을 방지하는 관점에서, 양극의 발광층측 표면의 중심선 평균 거침도 (Ra) 는 Ra<10 ㎚ 를 만족하는 것이 바람직하고, 보다 바람직하게는 Ra<5 ㎚ 이다.
또한, 그 양극은 상기 방법으로 제작된 후에, UV 오존, 실란 커플링제, 2,3,5,6-테트라플루오로-7,7,8,8-테트라시아노퀴노디메탄 등의 전자 수용성 화합물을 포함하는 용액 등으로 표면 처리가 실시되는 경우가 있다. 표면 처리에 의해 그 양극에 접하는 유기층과의 전기적 접속이 개선된다.
본 발명의 전계 발광 소자에 있어서 양극을 광 반사 전극으로서 사용하는 경우에는, 이러한 양극이, 고 광반사성 금속으로 이루어지는 광 반사층과 4.0 eV 이상의 일 함수를 갖는 재료를 포함하는 고 일함수 재료층을 조합한 다층 구조가 바람직하다.
이와 같은 양극의 구성예로서는,
(i) Ag-MoO3
(ii) (Ag-Pd-Cu 합금)-(ITO 및/또는 IZO)
(iii) (Al-Nd 합금)-(ITO 및/또는 IZO)
(iV) (Mo-Cr 합금)-(ITO 및/또는 IZO)
(V) (Ag-Pd-Cu 합금)-(ITO 및/또는 IZO)-MoO3
등이 예시된다. 충분한 광 반사율을 얻기 위해, Al, Ag, Al 합금, Ag 합금, Cr 합금 등의 고광 반사성 금속층의 막두께는 50 ㎚ 이상인 것이 바람직하고, 보다 바람직하게는 80 ㎚ 이상이다. ITO, IZO, MoO3 등의 고일 함수 재료층의 막두께는 통상, 5 ㎚ ∼ 500 ㎚ 의 범위이다.
<정공 주입층>
본 발명의 전계 발광 소자에 있어서, 본 발명에 사용되는 공액 고분자 화합물 이외의 정공 주입층을 형성하는 재료로서는, 카르바졸 유도체, 트리아졸 유도체, 옥사졸 유도체, 옥사디아졸 유도체, 이미다졸 유도체, 폴리아릴알칸 유도체, 피라졸린 유도체, 피라졸론 유도체, 페닐렌디아민 유도체, 아릴아민 유도체, 스타버스트형 아민, 프탈로시아닌 유도체, 아미노 치환 칼콘 유도체, 스티릴안트라센 유도체, 플루오레논 유도체, 히드라존 유도체, 스틸벤 유도체, 실라잔 유도체, 방향족 제 3 급 아민 화합물, 스티릴아민 화합물, 방향족 디메틸리딘계 화합물, 포르피린계 화합물, 폴리실란계 화합물, 폴리(N-비닐카르바졸) 유도체, 유기 실란 유도체, 및 이들을 포함하는 중합체를 들 수 있다. 산화바나듐, 산화탄탈, 산화텅스텐, 산화몰리브덴, 산화루테늄, 산화알류미늄 등의 도전성 금속 산화물, 폴리아닐린, 아닐린계 공중합체, 티오펜 올리고머, 폴리티오펜 등의 도전성 고분자 및 올리고머, 폴리(3,4-에틸렌디옥시티오펜)·폴리스티렌술폰산, 폴리피롤 등의 유기 도전성 재료 및 이들을 포함하는 중합체, 아모르퍼스 카본을 들 수 있다. 또한, 테트라시아노퀴노디메탄 유도체 (예를 들어 2,3,5,6-테트라플루오로-7,7,8,8-테트라시아노퀴노디메탄), 1,4-나프토퀴논 유도체, 디페노퀴논 유도체, 폴리니트로 화합물 등의 억셉터성 유기 화합물, 옥타데실트리메톡시실란 등의 실란 커플링제 등도 바람직하게 사용할 수 있다.
상기 재료는 단일 성분으로 사용하거나 복수의 성분으로 이루어지는 조성물로서 사용하여도 된다. 상기 정공 주입층은, 상기 재료의 1 종 또는 2 종 이상으로 이루어지는 단층 구조이어도 되고, 동일 조성 또는 이종 조성의 복수 층으로 이루어지는 다층 구조이어도 된다. 정공 수송층 혹은 인터레이어에서 사용할 수 있는 재료로서 열기하는 재료도 정공 주입층에서 사용할 수 있다.
정공 주입층의 제작 방법으로서는, 공지된 여러 가지의 방법을 이용할 수 있다. 무기 화합물 재료의 경우에는, 진공 증착법, 스퍼터링법, 이온 플레이팅법 등을 들 수 있으며, 저분자 유기 재료의 경우에는, 진공 증착법, 레이저 전사나 열 전사 등의 전사법, 용액으로부터의 막 형성에 의한 방법 (고분자 바인더와의 혼합 용액을 사용하여도 된다) 등을 들 수 있다. 고분자 유기 재료에서는, 용액으로부터의 막 형성에 의한 방법이 예시된다.
정공 주입 재료가, 피라졸린 유도체, 아릴아민 유도체, 스틸벤 유도체, 트리페닐디아민 유도체 등의 저분자 화합물인 경우에는, 진공 증착법을 이용하여 정공 주입층을 형성할 수 있다.
고분자 화합물 바인더와 상기 저분자 정공 주입 재료를 분산시킨 혼합 용액을 이용하여 정공 주입층을 막 형성할 수도 있다. 혼합하는 고분자 화합물 바인더로서는, 전하 수송을 극도로 저해하지 않는 것이 바람직하고, 가시광에 대한 흡수가 강하지 않은 것이 바람직하게 사용되며, 그 예로서는, 폴리(N-비닐카르바졸), 폴리아닐린 혹은 그 유도체, 폴리티오펜 혹은 그 유도체, 폴리(p-페닐렌비닐렌) 혹은 그 유도체, 폴리(2,5-티에닐렌비닐렌) 혹은 그 유도체, 폴리카보네이트, 폴리아크릴레이트, 폴리메틸아크릴레이트, 폴리메틸메타크릴레이트, 폴리스티렌, 폴리염화비닐, 폴리실록산 등을 들 수 있다.
용액으로부터의 막 형성에 사용하는 용매로서는, 정공 주입 재료를 용해시키는 것이면 특별히 제한은 없다. 그 용매로서 물, 클로로포름, 염화메틸렌, 디클로로에탄 등의 함염소 용매, 테트라하이드로푸란 등의 에테르 용매, 톨루엔, 자일렌 등의 방향족 탄화수소 용매, 아세톤, 메틸에틸케톤 등의 케톤 용매, 아세트산에틸, 아세트산부틸, 에틸셀로솔브아세테이트 등의 에스테르 용매 등이 예시된다.
용액으로부터의 막 형성 방법으로서는, 용액으로부터의 스핀 코트법, 캐스팅법, 마이크로 그라비아 코트법, 그라비아 코트법, 바 코트법, 롤 코트법, 와이어 바 코트법, 딥 코트법, 슬릿 코트법, 캐필러리 코트법, 스프레이 코트법, 노즐 코트법 등의 코트법, 그라비아 인쇄법, 스크린 인쇄법, 플렉소 인쇄법, 오프셋 인쇄법, 반전 인쇄법, 잉크젯 프린트법 등의 인쇄법 등의 도포법을 사용할 수 있다. 패턴 형성이 용이하다는 점에서, 그라비아 인쇄법, 스크린 인쇄법, 플렉소 인쇄법, 오프셋 인쇄법, 반전 인쇄법, 잉크젯 프린트법 등의 인쇄법이나 노즐 코트법이 바람직하다.
정공 주입층에 이어서, 정공 수송층, 인터레이어, 발광층 등의 유기 화합물층을 형성하는 경우, 특히, 양방의 층을 도포법에 의해 형성하는 경우에는, 먼저 도포한 층이 나중에 도포하는 층의 용액에 함유되는 용매에 용해되어 적층 구조를 제작할 수 없게 되는 경우가 있다. 이 경우에는, 하층을 용매 불용으로 하는 방법을 사용할 수 있다. 용매 불용으로 하는 방법으로서는, 고분자 화합물에 가교기를 걸고, 가교시켜 불용화하는 방법, 방향족 비스아지드로 대표되는 방향 고리를 갖는 가교기를 가진 저분자 화합물을 가교제로서 혼합하고, 가교시켜 불용화하는 방법, 아크릴레이트기로 대표되는 방향 고리를 갖지 않는 가교기를 가진 저분자 화합물을 가교제로서 혼합하고, 가교시켜 불용화하는 방법, 하층을 자외광에 감광시키고 가교시켜, 상층의 제조에 사용하는 유기 용매에 대해 불용화하는 방법, 하층을 가열하고 가교시켜, 상층의 제조에 사용하는 유기 용매에 대해 불용화하는 방법 등을 들 수 있다. 하층을 가열하는 경우의 가열 온도는 통상 100 ℃ ∼ 300 ℃ 정도이며, 시간은 통상 1 분 ∼ 1 시간 정도이다.
가교 이외에 하층을 용해시키지 않고 적층하는 그 밖의 방법으로서, 서로 이웃한 층의 제조에 상이한 극성의 용액을 사용하는 방법이 있으며, 예를 들어, 하층에 수용성 고분자 화합물을 이용하고, 상층에 유용성 고분자 화합물을 이용하여, 도포하여도 하층이 용해되지 않도록 하는 방법 등이 있다.
정공 주입층의 막두께로서는, 사용하는 재료에 따라 최적치가 상이하여, 구동 전압과 발광 효율이 알맞은 값이 되도록 선택하면 되는데, 적어도 핀홀이 발생하지 않는 두께가 필요하며, 너무 두꺼우면 소자의 구동 전압이 높아져 바람직하지 않다. 따라서, 그 정공 주입층의 막두께로서는, 예를 들어 1 ㎚ ∼ 1 ㎛ 이며, 바람직하게는 2 ㎚ ∼ 500 ㎚ 이며, 더욱 바람직하게는 10 ㎚ ∼ 100 ㎚ 이다.
<정공 수송층 및 인터레이어>
본 발명의 전계 발광 소자에 있어서, 본 발명에 사용되는 공액 고분자 화합물 이외의 정공 수송층 및 인터레이어를 구성하는 재료로서는, 예를 들어, 카르바졸 유도체, 트리아졸 유도체, 옥사졸 유도체, 옥사디아졸 유도체, 이미다졸 유도체, 폴리아릴알칸 유도체, 피라졸린 유도체, 피라졸론 유도체, 페닐렌디아민 유도체, 아릴아민 유도체, 아미노 치환 칼콘 유도체, 스티릴안트라센 유도체, 플루오레논 유도체, 히드라존 유도체, 스틸벤 유도체, 실라잔 유도체, 방향족 제 3 급 아민 화합물, 스티릴아민 화합물, 방향족 디메틸리딘계 화합물, 포르피린계 화합물, 폴리실란계 화합물, 폴리(N-비닐카르바졸) 유도체, 유기 실란 유도체, 및 이들의 구조를 포함하는 중합체를 들 수 있다. 아닐린계 공중합체, 티오펜 올리고머, 폴리티오펜 등의 도전성 고분자 및 올리고머, 폴리피롤 등의 유기 도전성 재료도 들 수 있다.
상기 재료는 단일 성분이거나 혹은 복수의 성분으로 이루어지는 조성물이어도 된다. 상기 정공 수송층 및 인터레이어는, 상기 재료의 1 종 또는 2 종 이상으로 이루어지는 단층 구조이어도 되고, 동일 조성 또는 이종 조성의 복수 층으로 이루어지는 다층 구조이어도 된다. 정공 주입층에서 사용할 수 있는 재료로서 열기하는 재료도 정공 수송층에서 사용할 수 있다.
정공 수송층 및 인터레이어를 구성하는 재료의 예로서는, 일본 공개특허공보 소63-70257, 일본 공개특허공보 소63-175860, 일본 공개특허공보 평2-135359, 일본 공개특허공보 평2-135361, 일본 공개특허공보 평2-209988, 일본 공개특허공보 평3-37992, 일본 공개특허공보 평3-152184, 일본 공개특허공보 평5-263073, 일본 공개특허공보 평6-1972, WO2005/52027, 일본 공개특허공보2006-295203 등에 개시되는 화합물을 들 수 있다. 그 중에서도, 반복 단위로서 2 가의 방향족 아민 잔기를 포함하는 중합체가 바람직하게 사용된다.
2 가의 방향족 아민 잔기로서는, 식 (21) 로 나타내지는 기를 들 수 있다.
정공 수송층 및 인터레이어의 막 형성 방법으로서는, 정공 주입층의 막 형성과 동일한 방법을 들 수 있다. 용액으로부터의 막 형성 방법으로서는, 상기한 스핀 코트법, 캐스팅법, 바 코트법, 슬릿 코트법, 스프레이 코트법, 노즐 코트법, 그라비아 인쇄법, 스크린 인쇄법, 플렉소 인쇄법, 잉크젯 프린트법 등의 도포법 및 인쇄법을 들 수 있으며, 승화성 화합물 재료를 사용하는 경우에는, 진공 증착법, 전사법 등을 들 수 있다. 용액으로부터의 막 형성에 사용하는 용매의 예로서는, 정공 주입층의 막 형성 방법에서 열기한 용매를 들 수 있다.
정공 수송층 및 인터레이어에 이어서, 발광층 등의 유기 화합물층을 도포법으로 형성할 때에, 하층이 나중에 도포하는 층의 용액에 함유되는 용매에 용해되는 경우에는, 정공 주입층의 막 형성 방법에서의 예시와 동일한 방법으로 하층을 용매 불용으로 할 수 있다.
정공 수송층 및 인터레이어의 막두께는, 사용하는 재료에 따라 최적치가 상이하여, 구동 전압과 발광 효율이 알맞은 값이 되도록 선택하면 되는데, 적어도 핀홀이 발생하지 않는 두께가 필요하며, 너무 두꺼우면 소자의 구동 전압이 높아져 바람직하지 않다. 따라서, 그 정공 수송층 및 인터레이어의 막두께로서는, 예를 들어 1 ㎚ ∼ 1 ㎛ 이며, 바람직하게는 2 ㎚ ∼ 500 ㎚ 이며, 더욱 바람직하게는 5 ㎚ ∼ 100 ㎚ 이다.
<발광층>
본 발명의 전계 발광 소자에 있어서, 발광층이 고분자 화합물을 포함하는 경우, 고분자 화합물로서는, 폴리플루오렌 유도체, 폴리파라페닐렌비닐렌 유도체, 폴리페닐렌 유도체, 폴리파라페닐렌 유도체, 폴리티오펜 유도체, 폴리디알킬플루오렌, 폴리플루오렌벤조티아디아졸, 폴리알킬티오펜 등의 공액 고분자 화합물을 바람직하게 사용할 수 있다.
이들 고분자 화합물을 포함하는 발광층은, 페릴렌계 색소, 쿠마린계 색소, 로다민계 색소 등의 고분자계 색소 화합물이나, 루브렌, 페릴렌, 9,10-디페닐안트라센, 테트라페닐부타디엔, 나일레드, 쿠마린 6, 퀴나크리돈 등의 저분자 색소 화합물을 함유하여도 된다. 나프탈렌 유도체, 안트라센 혹은 그 유도체, 페릴렌 혹은 그 유도체, 폴리메틴계, 잔텐계, 쿠마린계, 시아닌계 등의 색소류, 8-하이드록시퀴놀린 혹은 그 유도체의 금속 착물, 방향족 아민, 테트라페닐시클로펜타디엔 혹은 그 유도체, 또는 테트라페닐부타디엔 혹은 그 유도체, 트리스(2-페닐피리딘)이리듐 등의 인광을 발광하는 금속 착물을 함유하여도 된다.
본 발명의 전계 발광 소자가 갖는 발광층은, 비공액 고분자 화합물과 상기 유기 색소나 상기 금속 착물 등의 발광성 유기 화합물과의 조성물로 구성되어도 된다. 비공액 고분자 화합물로서는, 폴리에틸렌, 폴리염화비닐, 폴리카보네이트, 폴리스티렌, 폴리메틸메타크릴레이트, 폴리부틸메타크릴레이트, 폴리에스테르, 폴리술폰, 폴리페닐렌옥사이드, 폴리부타디엔, 폴리(N-비닐카르바졸), 탄화수소 수지, 케톤 수지, 페녹시 수지, 폴리아미드, 에틸셀룰로오스, 아세트산비닐, ABS 수지, 폴리우레탄, 멜라민 수지, 불포화 폴리에스테르 수지, 알키드 수지, 에폭시 수지, 실리콘 수지를 들 수 있다. 상기의 비공액 고분자 화합물은 측사슬에 카르바졸 유도체, 트리아졸 유도체, 옥사졸 유도체, 옥사디아졸 유도체, 이미다졸 유도체, 폴리아릴알칸 유도체, 피라졸린 유도체, 피라졸론 유도체, 페닐렌디아민 유도체, 아릴아민 유도체, 아미노 치환 칼콘 유도체, 스티릴안트라센 유도체, 플루오레논 유도체, 히드라존 유도체, 스틸벤 유도체, 실라잔 유도체, 방향족 제 3 급 아민 화합물, 스티릴아민 화합물, 방향족 디메틸리딘 화합물, 포르피린 화합물, 및 유기 실란 유도체로 이루어지는 군에서 선택되는 하나 이상의 유도체 혹은 화합물로 나타내지는 구조를 가지고 있어도 된다.
발광층이 저분자 화합물을 포함하는 경우, 그 저분자 화합물로서는, 루브렌, 페릴렌, 9,10-디페닐안트라센, 테트라페닐부타디엔, 나일레드, 쿠마린 6, 카르바졸, 퀴나크리돈 등의 저분자 색소 화합물, 나프탈렌 유도체, 안트라센 혹은 그 유도체, 페릴렌 혹은 그 유도체, 폴리메틴계, 잔텐계, 쿠마린계, 시아닌계, 인디고계 등의 색소류, 8-하이드록시퀴놀린 혹은 그 유도체의 금속 착물, 프탈로시아닌 혹은 그 유도체의 금속 착물, 방향족 아민, 테트라페닐시클로펜타디엔 혹은 그 유도체, 또는 테트라페닐부타디엔 혹은 그 유도체 등을 들 수 있다.
발광층이 인광을 발광하는 금속 착물을 포함하는 경우, 그 금속 착물로서는, 트리스(2-페닐피리딘)이리듐, 티에닐피리딘 배위자 함유 이리듐 착물, 페닐퀴놀린 배위자 함유 이리듐 착물, 트리아자시클로노난 골격 함유 테르븀 착물 등을 들 수 있다.
발광층에 사용되는 고분자 화합물의 예로서는, WO97/09394, WO98/27136, WO99/54385, WO00/22027, WO01/19834, GB2340304A, GB2348316, US573636, US5741921, US5777070, EP0707020, 일본 공개특허공보 평9-111233, 일본 공개특허공보 평10-324870, 일본 공개특허공보 평2000-80167, 일본 공개특허공보2001-123156, 일본 공개특허공보2004-168999, 일본 공개특허공보2007-162009, 「유기 EL 소자의 개발과 구성 재료」 (씨엠씨 출판, 2006 년 발행) 등에 개시되어 있는 폴리플루오렌, 그 유도체 및 공중합체, 폴리아릴렌, 그 유도체 및 공중합체, 폴리아릴렌비닐렌, 그 유도체 및 공중합체, 방향족 아민 및 그 유도체의 (공) 중합체 등을 들 수 있다.
저분자 화합물의 예로서는, 예를 들어, 일본 공개특허공보 소57-51781, 「유기 박막 일 함수 데이터집 [제 2 판]」 (씨엠씨 출판, 2006 년 발행), 「유기 EL 소자의 개발과 구성 재료」 (씨엠씨 출판, 2006 년 발행) 등에 기재되어 있는 화합물을 들 수 있다.
상기 재료는 단일 성분이거나 혹은 복수의 성분으로 이루어지는 조성물이어도 된다. 상기 발광층은, 상기 재료의 1 종 또는 2 종 이상으로 이루어지는 단층 구조이어도 되고, 동일 조성 또는 이종 조성의 복수 층으로 이루어지는 다층 구조이어도 된다.
발광층의 막 형성 방법의 예로서는, 정공 주입층의 막 형성과 동일한 방법을 들 수 있다. 용액으로부터의 막 형성 방법의 예로서는, 스핀 코트법, 캐스팅법, 바 코트법, 슬릿 코트법, 스프레이 코트법, 노즐 코트법, 그라비아 인쇄법, 스크린 인쇄법, 플렉소 인쇄법, 잉크젯 프린트법 등의 상기 도포법 및 인쇄법을 들 수 있으며, 승화성 화합물 재료를 사용하는 경우에는, 진공 증착법, 전사법 등을 들 수 있다.
용액으로부터의 막 형성에 사용하는 용매의 예로서는, 정공 주입층의 막 형성 방법에서 열기한 용매를 들 수 있다.
발광층에 이어서, 전자 수송층 등의 유기 화합물층을 도포법으로 형성할 때에, 하층이 나중에 도포하는 층의 용액에 함유되는 용매에 용해되는 경우에는, 정공 주입층의 막 형성 방법에서의 예시와 동일한 방법으로 하층을 용매 불용으로 할 수 있다.
발광층의 막두께로서는, 사용하는 재료에 따라 최적치가 상이하여, 구동 전압과 발광 효율이 알맞은 값이 되도록 선택하면 되는데, 적어도 핀홀이 발생하지 않는 두께가 필요하며, 너무 두꺼우면 소자의 구동 전압이 높아져 바람직하지 않다. 따라서, 발광층의 막두께로서는, 예를 들어 5 ㎚ ∼ 1 ㎛ 이며, 바람직하게는 10 ㎚ ∼ 500 ㎚ 이며, 더욱 바람직하게는 30 ㎚ ∼ 200 ㎚ 이다.
<전자 수송층 및 정공 블록층>
본 발명의 전계 발광 소자에 있어서, 본 발명에 사용되는 공액 고분자 화합물 이외의 전자 수송층 및 정공 블록층을 구성하는 재료로서는, 공지된 것을 사용할 수 있으며, 트리아졸 유도체, 옥사졸 유도체, 옥사디아졸 유도체, 이미다졸 유도체, 플루오레논 유도체, 벤조퀴논 혹은 그 유도체, 나프토퀴논 혹은 그 유도체, 안트라퀴논 혹은 그 유도체, 테트라시아노안트라퀴노디메탄 혹은 그 유도체, 플루오레논 유도체, 디페닐디시아노에틸렌 혹은 그 유도체, 디페노퀴논 유도체, 안트라퀴노디메탄 유도체, 안트론 유도체, 티오피란디옥사이드 유도체, 카르보디이미드 유도체, 플루오레닐리덴메탄 유도체, 디스티릴피라진 유도체, 나프탈렌, 페릴렌 등의 방향 고리 테트라카르복실산 무수물, 프탈로시아닌 유도체, 8-퀴놀리놀 유도체의 금속 착물이나 메탈프탈로시아닌, 벤조옥사졸이나 벤조티아졸을 배위자로 하는 금속 착물로 대표되는 각종 금속 착물, 유기 실란 유도체, 8-하이드록시퀴놀린 혹은 그 유도체의 금속 착물, 폴리퀴놀린 혹은 그 유도체, 폴리퀴녹살린 혹은 그 유도체, 폴리플루오렌 혹은 그 유도체 등을 들 수 있다. 이들 중, 트리아졸 유도체, 옥사디아졸 유도체, 벤조퀴논 혹은 그 유도체, 안트라퀴논 혹은 그 유도체, 또는 8-하이드록시퀴놀린 혹은 그 유도체의 금속 착물, 폴리퀴놀린 혹은 그 유도체, 폴리퀴녹살린 혹은 그 유도체, 폴리플루오렌 혹은 그 유도체가 바람직하다.
상기 재료는 단일 성분이거나 혹은 복수의 성분으로 이루어지는 조성물이어도 된다. 상기 전자 수송층 및 정공 블록층은, 상기 재료의 1 종 또는 2 종 이상으로 이루어지는 단층 구조이어도 되고, 동일 조성 또는 이종 조성의 복수 층으로 이루어지는 다층 구조이어도 된다. 또, 전자 주입층에서 사용할 수 있는 재료로서 열기하는 재료도 전자 수송층 및 정공 블록층에서 사용할 수 있다.
전자 수송층 및 정공 블록층의 막 형성 방법으로서는, 정공 주입층의 막 형성과 동일한 방법을 들 수 있다. 용액으로부터의 막 형성 방법으로서는, 스핀 코트법, 캐스팅법, 바 코트법, 슬릿 코트법, 스프레이 코트법, 노즐 코트법, 그라비아 인쇄법, 스크린 인쇄법, 플렉소 인쇄법, 잉크젯 프린트법 등의 상기 도포법 및 인쇄법을 들 수 있으며, 승화성 화합물 재료를 사용하는 경우에는, 진공 증착법, 전사법 등을 들 수 있다.
용액으로부터의 막 형성에 사용하는 용매의 예로서는, 정공 주입층의 막 형성 방법에서 열기한 용매를 들 수 있다.
전자 수송층 및 정공 블록층에 이어서, 전자 주입층 등의 유기 화합물층을 도포법으로 형성할 때에, 하층이 나중에 도포하는 층의 용액에 함유되는 용매에 용해되는 경우에는, 정공 주입층의 막 형성 방법에서의 예시와 동일한 방법으로 하층을 용매 불용으로 할 수 있다.
전자 수송층 및 정공 블록층의 막두께로서는, 사용하는 재료에 따라 최적치가 상이하여, 구동 전압과 발광 효율이 알맞은 값이 되도록 선택하면 되는데, 적어도 핀홀이 발생하지 않는 두께가 필요하며, 너무 두꺼우면 소자의 구동 전압이 높아져 바람직하지 않다. 따라서, 그 전자 수송층 및 정공 블록층의 막두께로서는, 예를 들어 1 ㎚ ∼ 1 ㎛ 이며, 바람직하게는 2 ㎚ ∼ 500 ㎚ 이며, 더욱 바람직하게는 5 ㎚ ∼ 100 ㎚ 이다.
<전자 주입층>
본 발명의 전계 발광 소자에 있어서, 본 발명에 사용되는 공액 고분자 화합물 이외의 전자 주입층을 구성하는 재료로서는, 공지된 것을 사용할 수 있으며, 트리아졸 유도체, 옥사졸 유도체, 옥사디아졸 유도체, 이미다졸 유도체, 플루오레논 유도체, 벤조퀴논 혹은 그 유도체, 나프토퀴논 혹은 그 유도체, 안트라퀴논 혹은 그 유도체, 테트라시아노안트라퀴노디메탄 혹은 그 유도체, 플루오레논 유도체, 디페닐디시아노에틸렌 혹은 그 유도체, 디페노퀴논 유도체, 안트라퀴노디메탄 유도체, 안트론 유도체, 티오피란디옥사이드 유도체, 카르보디이미드 유도체, 플루오레닐리덴메탄 유도체, 디스티릴피라진 유도체, 나프탈렌, 페릴렌 등의 방향 고리 테트라카르복실산 무수물, 프탈로시아닌 유도체, 8-퀴놀리놀 유도체의 금속 착물이나 메탈프탈로시아닌, 벤조옥사졸이나 벤조티아졸을 배위자로 하는 금속 착물로 대표되는 각종 금속 착물, 유기 실란 유도체 등을 들 수 있다.
상기 재료는 단일 성분이거나 혹은 복수의 성분으로 이루어지는 조성물이어도 된다. 상기 전자 주입층은, 상기 재료의 1 종 또는 2 종 이상으로 이루어지는 단층 구조이어도 되고, 동일 조성 또는 이종 조성의 복수 층으로 이루어지는 다층 구조이어도 된다. 전자 수송층 및 정공 블록층에서 사용할 수 있는 재료로서 열기하는 재료도 전자 주입층에서 사용할 수 있다.
전자 주입층의 막 형성 방법에 제한은 없고, 정공 주입층의 막 형성과 동일한 방법을 들 수 있다. 용액으로부터의 막 형성 방법으로서는, 스핀 코트법, 캐스팅법, 바 코트법, 슬릿 코트법, 스프레이 코트법, 노즐 코트법, 그라비아 인쇄법, 스크린 인쇄법, 플렉소 인쇄법, 잉크젯 프린트법 등의 상기 도포법 및 인쇄법을 들 수 있으며, 승화성 화합물 재료를 사용하는 경우에는, 진공 증착법, 전사법 등을 들 수 있다.
용액으로부터의 막 형성에 사용하는 용매의 예로서는, 정공 주입층의 막 형성 방법에서 열기한 용매를 들 수 있다.
전자 주입층의 막두께로서는, 사용하는 재료에 따라 최적치가 상이하여, 구동 전압과 발광 효율이 알맞은 값이 되도록 선택하면 되는데, 적어도 핀홀이 발생하지 않는 두께가 필요하며, 너무 두꺼우면 소자의 구동 전압이 높아져 바람직하지 않다. 따라서, 그 전자 주입층의 막두께로서는, 예를 들어 1 ㎚ ∼ 1 ㎛ 이며, 바람직하게는 2 ㎚ ∼ 500 ㎚ 이며, 더욱 바람직하게는 5 ㎚ ∼ 100 ㎚ 이다.
<음극>
본 발명의 전계 발광 소자에 있어서, 음극은, 발광층, 전자 수송층, 정공 블록층, 전자 주입층 등에 인접하여, 이들 층에 전자를 공급하는 기능을 갖는 것이다. 그 음극은, 단일 재료 또는 복수 재료로 이루어지는 단층 구조이어도 되고, 복수 층으로 이루어지는 다층 구조이어도 된다. 다층 구조인 경우, 제 1 음극층과 커버 음극층의 2 층 구조 혹은 제 1 음극층, 제 2 음극층 및 커버 음극층의 3 층 구조가 바람직하다. 제 1 음극층은, 음극 중에서 가장 발광층측에 있는 층을 가리키며, 커버 음극층은 2 층 구조의 경우에는 제 1 음극층을, 3 층 구조의 경우에는 제 1 음극층과 제 2 음극층을 덮는 층을 가리킨다. 전자 공급능의 관점에서는, 제 1 음극층의 재료의 일 함수가 3.5 eV 이하인 것이 바람직하다. 일 함수가 3.5 eV 이하인 금속의 산화물, 불화물, 탄산화물, 복합 산화물 등도 제 1 음극층 재료로서 바람직하게 사용된다. 커버 음극층의 재료에는, 저항률이 낮고, 수분에 대한 내부식성이 높은 금속, 금속 산화물 등이 바람직하게 사용된다.
제 1 음극층 재료의 예로서는, 알칼리 금속이나 알칼리 토금속, 상기 금속을 1 종류 이상 포함하는 합금, 상기 금속의 산화물, 할로겐화물, 탄산화물, 복합 산화물, 및 이들의 혼합물로 이루어지는 군에서 선택되는 하나 이상의 재료 등을 들 수 있다. 알칼리 금속 또는 그 산화물, 할로겐화물, 탄산화물, 복합 산화물의 예로서는, 리튬, 나트륨, 칼륨, 루비듐, 세슘, 산화리튬, 산화나트륨, 산화칼륨, 산화루비듐, 산화세슘, 불화리튬, 불화나트륨, 불화칼륨, 불화루비듐, 불화세슘, 탄산리튬, 탄산나트륨, 탄산칼륨, 탄산루비듐, 탄산세슘, 몰리브덴산칼륨, 티탄산칼륨, 텅스텐산칼륨, 몰리브덴산세슘 등을 들 수 있다. 알칼리 토금속 또는 그 산화물, 할로겐화물, 탄산화물, 복합 산화물의 예로서는, 마그네슘, 칼슘, 스트론튬, 바륨, 산화마그네슘, 산화칼슘, 산화스트론튬, 산화바륨, 불화마그네슘, 불화칼슘, 불화스트론튬, 불화바륨, 탄산마그네슘, 탄산칼슘, 탄산스트론튬, 탄산화바륨, 몰리브덴산바륨, 텅스텐산바륨 등을 들 수 있다. 알칼리 금속 또는 알칼리 토금속을 1 종류 이상 포함하는 합금의 예로서는, Li-Al 합금, Mg-Ag 합금, Al-Ba 합금, Mg-Ba 합금, Ba-Ag 합금, Ca-Bi-Pb-Sn 합금 등을 들 수 있다. 제 1 음극층 재료로서 열기한 재료와 전자 주입층을 구성하는 재료로서 열기한 재료와의 조성물도 제 1 음극층에 사용할 수 있다. 제 2 음극층의 재료의 예로서는, 제 1 음극층의 재료와 동일한 재료가 예시된다.
커버 음극층 재료의 예로서는, 금, 은, 구리, 알루미늄, 크롬, 주석, 납, 니켈, 티탄 등의 저저항 금속 및 이들을 포함하는 합금, 산화주석, 산화아연, 산화인듐, 산화인듐주석 (ITO), 산화인듐아연 (IZO), 산화몰리브덴 등의 도전성 금속 산화물, 또한 이들의 도전성 금속 산화물과 금속과의 혼합물 등을 들 수 있다.
음극이 다층 구조인 경우의 구조의 예로서는, Mg/Al, Ca/Al, Ba/Al, NaF/Al, KF/Al, RbF/Al, CsF/Al, Na2CO3/Al, K2CO3/Al, Cs2CO3/Al 등의 제 1 음극층과 커버 음극층의 2 층 구조, LiF/Ca/Al, NaF/Ca/Al, KF/Ca/Al, RbF/Ca/Al, CsF/Ca/Al, Ba/Al/Ag, KF/Al/Ag, KF/Ca/Ag, K2CO3/Ca/Ag 등의 제 1 음극층, 제 2 음극층 및 커버 음극층의 3 층 구조를 들 수 있다 (부호 「/」 는 각 층이 인접하고 있는 것을 나타낸다). 제 2 음극층의 재료가 제 1 음극층의 재료에 대해 환원 작용을 갖는 것이 바람직하다. 재료간의 환원 작용의 유무·정도는, 예를 들어, 화합물간의 결합 해리 에너지 (ΔrHо) 로부터 추측할 수 있다. 즉, 제 2 음극층을 구성하는 재료에 의한, 제 1 음극층을 구성하는 재료에 대한 환원 반응에 있어서, 결합 해리 에너지가 플러스인 조합인 경우, 제 2 음극층의 재료가 제 1 음극층의 재료에 대해 환원 작용을 갖는다고 할 수 있다. 결합 해리 에너지는, 예를 들어 「전기 화학 편람 제 5 판」 (마루젠, 2000 년 발행), 「열역학 데이터베이스 MALT」 (과학 기술사, 1992 년 발행) 등에서 참조할 수 있다.
음극의 제작 방법은 공지된 여러 가지의 방법을 이용할 수 있으며, 진공 증착법, 스퍼터링법, 이온 플레이팅법 등이 예시된다. 금속, 금속의 산화물, 불화물, 탄산화물을 사용하는 경우에는 진공 증착법이 다용되고, 고비등점의 금속 산화물, 금속 복합 산화물이나 산화인듐주석 (ITO) 등의 도전성 금속 산화물을 사용하는 경우에는, 스퍼터링법, 이온 플레이팅법이 다용된다. 이종 재료와의 조성물을 막 형성하는 경우에는, 공증착법, 스퍼터링법, 이온 플레이팅법 등이 사용된다. 특히, 저분자 유기물과 금속 또는 금속의 산화물, 불화물, 탄산화물과의 조성물을 막 형성하는 경우에는 공증착법이 적합하다.
음극의 막두께는 사용하는 재료, 층 구조에 따라 최적치가 상이하여, 구동 전압, 발광 효율, 소자 수명이 알맞은 값이 되도록 선택하면 된다. 통상, 제 1 음극층의 막두께는 0.5 ㎚ ∼ 20 ㎚ 의 범위이며, 커버 음극층의 막두께는 10 ㎚ ∼ 1 ㎛ 의 범위이다. 예를 들어, 제 1 음극층에 Ba 또는 Ca, 커버 음극층에 Al 을 사용하는 경우, Ba 또는 Ca 의 막두께는 2 ㎚ ∼ 10 ㎚, Al 의 막두께는 10 ㎚ ∼ 500 ㎚ 인 것이 바람직하고, 제 1 음극층에 NaF 또는 KF, 커버 음극층에 Al 을 사용하는 경우, NaF 또는 KF 의 막두께는 1 ㎚ ∼ 8 ㎚, Al 의 막두께는 10 ㎚ ∼ 500 ㎚ 인 것이 바람직하다.
본 발명의 전계 발광 소자에 있어서 음극을 광 투과성 전극으로서 사용하는 경우에는, 커버 음극층의 가시광 투과율이 40 % 이상, 바람직하게는 50 % 이상인 것이 바람직하다. 이와 같은 가시광 투과율은, 커버 음극층 재료로서 산화인듐주석 (ITO), 산화인듐아연 (IZO), 산화몰리브덴 등의 투명 도전성 금속 산화물을 사용하거나, 혹은, 금, 은, 구리, 알루미늄, 크롬, 주석, 납 등의 저저항 금속 및 이들을 포함하는 합금을 사용한 커버 음극층의 막두께를 30 ㎚ 이하로 함으로써 달성된다. 예를 들어, 제 1 음극층에 Ba 를 5 ㎚, 제 2 음극층에 Al 을 1 ㎚, 커버 음극층에 Ag 를 15 ㎚ 로 한 음극 구조의 경우, 음극의 가시광 투과율은 50 % 가 된다.
음극측으로부터의 광 투과율을 향상시키는 것을 목적으로 하여, 음극의 커버 음극층 상에 반사 방지층을 형성할 수도 있다. 반사 방지층에 사용되는 재료로서는, 굴절률이 1.8 ∼ 3.0 정도인 것이 바람직하고, 예를 들어, ZnS, ZnSe, WO3 등을 들 수 있다. 반사 방지층의 막두께는 재료의 조합에 따라 상이한데, 통상 10 ㎚ ∼ 150 ㎚ 의 범위이다. 예를 들어, 음극으로서, 제 1 음극층으로서 Ba 를 5 ㎚, 제 2 음극층으로서 Al 을 1 ㎚, 커버 음극층으로서 Ag 를 15 ㎚ 적층시킨 경우, 커버 음극층에 접하여 반사 방지층으로서 WO3 을 21 ㎚ 적층시키면, 발광층측으로부터의 광 투과율은 10 % 정도 향상된다.
<절연층>
본 발명의 전계 발광 소자가 임의로 가질 수 있는 막두께 5 ㎚ 이하의 절연층은, 전극과의 밀착성 향상, 전극으로부터의 전하 (즉 정공 또는 전자) 주입 개선, 인접층과의 혼합 방지 등의 기능을 갖는 것이다. 상기 절연층의 재료로서는, 금속 불화물, 금속 산화물, 유기 절연 재료 (폴리메틸메타크릴레이트 등) 등을 들 수 있다. 막두께 5 ㎚ 이하의 절연층을 형성한 전계 발광 소자로서는, 음극에 인접하여 막두께 5 ㎚ 이하의 절연층을 형성한 것, 양극에 인접하여 막두께 5 ㎚ 이하의 절연층을 형성한 것을 들 수 있다.
본 발명의 전계 발광 소자는, 예를 들어, 기판 상에 각 층을 순차 적층함으로써 제조할 수 있다. 구체적으로는, 기판 상에 양극을 형성하고, 그 위에 정공 주입층, 정공 수송층, 인터레이어 등의 층을 필요에 따라 형성하고, 그 위에 발광층을 형성하고, 그 위에 전자 수송층, 전자 주입층 등의 층을 필요에 따라 형성하고, 다시 그 위에 음극을 적층함으로써 제조할 수 있다.
본 발명의 전계 발광 소자를 이용하여 디스플레이 장치를 제조할 수 있다. 그 디스플레이 장치는, 전계 발광 소자를 1 화소 단위로서 구비한다. 화소 단위의 배열 양태는, 특별히 한정되지 않고, 텔레비전 등의 디스플레이 장치에서 통상 채용되는 배열로 할 수 있으며, 다수의 화소가 공통의 기판 상에 배열된 양태로 할 수 있다. 본 발명의 장치에 있어서, 기판 상에 배열되는 화소는, 필요에 따라, 뱅크에서 규정되는 화소 영역 내에 형성할 수 있다.
상기 장치는, 추가로 필요에 따라, 발광층 등을 사이에 두고 기판과 반대측에 밀봉 부재를 가질 수 있다. 또한, 필요에 따라, 컬러 필터 또는 형광 변환 필터 등의 필터, 화소의 구동에 필요한 회로 및 배선 등의, 디스플레이 장치를 구성하기 위한 임의의 구성 요소를 가질 수 있다.
<광전 변환 소자>
다음으로, 본 발명의 적층 구조체를 이용하여 제조할 수 있는 광전 변환 소자에 대해 설명한다.
본 발명의 광전 변환 소자는, 음극 및 양극과, 음극과 양극과의 사이에 전하 분리층을 가지며, 전하 분리층과 음극 및/또는 전하 분리층과 음극과의 사이에 본 발명에 사용되는 공액 고분자 화합물을 포함하는 층을 갖는다. 양극과 전하 분리층 사이에 공액 고분자 화합물을 포함하는 층을 갖는 경우, 제 1 전극은 양극이며, 제 2 전극이 음극이며, 공액 고분자 화합물을 포함하는 층은 정공 수송층 등으로서 사용된다. 음극과 전하 분리층 사이에 공액 고분자 화합물을 포함하는 층을 갖는 경우, 제 1 전극은 음극이며, 제 2 전극이 양극이며, 공액 고분자 화합물을 포함하는 층은 전자 수송층 등으로서 사용된다.
본 발명의 광전 변환 소자의 전하 분리층은, 통상 전자 공여성 화합물과 전자 수용성 화합물을 포함한다. 전자 공여성 화합물로서는, 공액 고분자 화합물을 들 수 있으며, 그 예로서는, 티오펜디일기를 포함하는 고분자 화합물, 플루오로디일기를 포함하는 고분자 화합물 등을 들 수 있다. 전자 수용성 화합물의 예로서는, 플러렌 및 플러렌 유도체 등을 들 수 있다.
본 발명의 광전 변환 소자는, 통상은 지지 기판 상에 형성된다. 지지 기판으로서는 유기 광전 변환 소자로서의 특성을 저해하지 않으면 재질은 특별히 제한되지 않지만, 유리 기판이나 플렉시블한 필름 기판이나 플라스틱 기판도 사용할 수 있다.
본 발명의 광전 변환 소자는, 공지된 방법, 예를 들어, Synth. Met., 102, 982 (1999) 에 기재된 방법이나 Science, 270, 1789 (1995) 에 기재된 방법에 의해 제조할 수 있다.
실시예
이하 실시예 및 비교예에 기초하여 본 발명을 보다 구체적으로 설명하지만, 본 발명은 이하의 실시예에 한정되는 것은 아니다.
중합체의 중량 평균 분자량 (Mw), 수 평균 분자량 (Mn) 은, 겔 퍼미에이션 크로마토그래피 (GPC) (토소 주식회사 제조 : HLC-8220 GPC) 를 이용하여, 폴리스티렌 환산의 수 평균 분자량 및 중량 평균 분자량으로서 구하였다. 측정하는 시료는, 약 0.5 wt% 의 농도가 되도록 테트라하이드로푸란에 용해시켜, GPC 에 50 ㎕ 주입한다. 또한, GPC 의 이동상으로서는 테트라하이드로푸란을 이용하고, 0.5 ㎖/min 의 유속으로 흐르게 하였다. 중합체의 구조 분석은 Varian 사 제조 300 MHz NMR 스펙트로미터를 사용한, 1H-NMR 해석에 의해 실시하였다. 측정은, 20 ㎎/㎖ 의 농도가 되도록 시료를 가용인 중용매에 용해시켜 실시하였다. 중합체의 최고 점유 분자 궤도 (HOMO) 의 궤도 에너지는 중합체의 이온화 포텐셜로부터 구하고, 최저 비점유 분자 궤도 (LUMO) 의 궤도 에너지는 이온화 포텐셜 및 HOMO 와 LUMO 의 에너지 차로부터 구하였다. 이온화 포텐셜의 측정에는 광 전자 분광 장치 (리켄 계기 주식회사 제조 : AC-2) 를 사용하였다. HOMO 와 LUMO 의 에너지 차는 자외·가시·근적외 분광 광도계 (Varian 사 제조 : Cary5E) 를 이용하여 중합체의 흡수 스펙트럼을 측정하고, 그 흡수 말단으로부터 구하였다.
참고예 1
2,7-디브로모-9,9-비스(4-헥실옥시-3-에톡시카르보닐페닐)-플루오렌 (BSAFBr2) 의 합성
2,7-디브로모-9-플루오레논 (20.3 g), 살리실산에틸 (59.8 g), 메르캅토아세트산 (0.55 g) 을 300 ㎖ 플라스크에 넣고, 질소 치환하였다. 메탄술폰산 (250 ㎖) 을 첨가하여, 혼합물을 75 ℃ 에서 철야 교반하였다. 혼합물을 방랭시키고, 빙수에 첨가하여 1 시간 교반하였다. 생긴 고체를 여과 분리하고, 따뜻한 아세토니트릴로 세정하였다. 혼합물을 아세톤으로부터 재결정함으로써, 고체를 얻었다. 이 고체 (3.3 g), 1-브로모헥산 (2.5 g), 탄산칼륨 (3.5 g), 18-크라운-6 (0.4 g) 을 N,N-디메틸포름아미드 (DMF) (35 ㎖) 에 용해시키고, 용액을 플라스크에 옮겨 105 ℃ 에서 철야 교반하였다. 혼합물을 실온까지 방랭시키고, 빙수에 첨가하여 1 시간 교반하였다. 생긴 고체를 회수하여, 에탄올로부터 재결정함으로써, 2,7-디브로모-9,9-비스(4-헥실옥시-3-에톡시카르보닐페닐)-플루오렌 (BSAFBr2) 을 얻었다.
참고예 2
폴리(9,9-비스(4-헥실옥시-3-에톡시카르보닐페닐)-플루오렌) (BSAFP) 의 합성
BSAFBr2 (2.0 g) 를 200 ㎖ 플라스크에 넣고, 질소 치환하였다. 탈수 테트라하이드로푸란 (75 ㎖) 을 시린지에 의해 첨가하고, 혼합물을 55 ℃ 로 승온시켰다. 거기에, 2,2'-비피리딘 (0.68 g), 비스(1,5-시클로옥타디엔)니켈 (1.2 g) 을 첨가하여, 55 ℃ 에서 5 시간 교반하였다. 혼합물을 실온까지 냉각시킨 후, 반응 용액을 메탄올 (200 ㎖), 물 (200 ㎖), 15 % 암모니아수 (50 ㎖) 의 혼합액에 적하하였다. 생긴 침전물을 여과에 의해 수집하여, 감압 건조시킨 후, 톨루엔에 재용해시켰다. 용액을 셀라이트를 이용하여 여과한 후, 여과액을 알루미나 칼럼에 통액시켜, 칼럼 처리액을 감압 농축하였다. 농축한 용액에 메탄올을 적하하고, 생긴 침전물을 여과에 의해 수집한 후 감압 건조시킴으로써, 식 (A) 로 나타내지는 반복 단위로 이루어지는 백색의 BSAFP (752 ㎎) 를 얻었다. BSAFP 의 수 평균 분자량 (Mn) 은 398000 이며, 중량 평균 분자량 (Mw) 은 729000 이며, 분산 (Mw/Mn) 은 1.83 이었다.
실시예 1
BSAFP 리튬염 (BSAFLi) 의 합성
BSAFP (160 ㎎) 를 100 ㎖ 플라스크에 넣고, 질소 치환하였다. 테트라하이드로푸란 (20 ㎖), 에탄올 (20 ㎖) 을 첨가하고, 혼합물을 55 ℃ 로 승온시켰다. 거기에, 수산화리튬 (100 ㎎) 을 물 (2 ㎖) 에 녹인 수용액을 첨가하여, 55 ℃ 에서 1 시간 교반하였다. 반응계 중에 고체가 석출된 후, 추가로 메탄올 (40 ㎖) 을 첨가하여 다시 2 시간 교반하였다. 혼합물을 실온까지 냉각시킨 후, 반응 용매를 감압 증류 제거하였다. 생긴 고체를 물로 세정하고, 감압 건조시킴으로써 옅은 황색의 고체 (150 ㎎) 를 얻었다. NMR 스펙트럼에 의해, BSAFP 내의 에틸에스테르 부위의 에틸기 유래의 시그널이 완전히 소실되고 있음을 확인하였다. 얻어진 BSAFP 의 리튬염을 공액 고분자 화합물 1 로 부른다. 공액 고분자 화합물 1 은 식 (B) 로 나타내지는 반복 단위로 이루어진다. 공액 고분자 화합물 1 의 HOMO 의 궤도 에너지는 -5.78 eV, LUMO 의 궤도 에너지는 -3.14 eV 였다.
실시예 2
BSAFP 나트륨염 (BSAFNa) 의 합성
BSAFP (200 ㎎) 를 100 ㎖ 플라스크에 넣고, 질소 치환하였다. 테트라하이드로푸란 (20 ㎖), 에탄올 (20 ㎖) 을 첨가하고, 혼합물을 55 ℃ 로 승온시켰다. 거기에, 수산화나트륨 (200 ㎎) 을 물 (2 ㎖) 에 녹인 수용액을 첨가하여, 55 ℃ 에서 3 시간 교반하였다. 혼합물을 실온까지 냉각시킨 후, 반응 용매를 감압 증류 제거하였다. 생긴 고체를 물로 세정하고, 감압 건조시킴으로써 옅은 황색의 고체 (180 ㎎) 를 얻었다. NMR 스펙트럼에 의해, BSAFP 내의 에틸에스테르 부위의 에틸기 유래의 시그널이 완전히 소실되고 있음을 확인하였다. 얻어진 BSAFP 의 나트륨염을 공액 고분자 화합물 2 로 부른다. 공액 고분자 화합물 2 는 식 (C) 로 나타내지는 반복 단위로 이루어진다. 공액 고분자 화합물 2 의 HOMO 의 궤도 에너지는 -5.67 eV, LUMO 의 궤도 에너지는 -3.04 eV 였다.
실시예 3
BSAFP 칼륨염 (BSAFK) 의 합성
BSAFP (150 ㎎) 를 100 ㎖ 플라스크에 넣고, 질소 치환하였다. 테트라하이드로푸란 (20 ㎖), 에탄올 (20 ㎖) 을 첨가하고, 혼합물을 55 ℃ 로 승온시켰다. 거기에, 수산화칼륨 (200 ㎎) 을 물 (2 ㎖) 에 녹인 수용액을 첨가하여, 55 ℃ 에서 3 시간 교반하였다. 혼합물을 실온까지 냉각시킨 후, 반응 용매를 감압 증류 제거하였다. 생긴 고체를 물로 세정하고, 감압 건조시킴으로써 옅은 황색의 고체 (130 ㎎) 를 얻었다. NMR 스펙트럼에 의해, BSAFP 내의 에틸에스테르 부위의 에틸기 유래의 시그널이 완전히 소실되고 있음을 확인하였다. 얻어진 BSAFP 의 칼륨염을 공액 고분자 화합물 3 으로 부른다. 공액 고분자 화합물 3 은 식 (D) 로 나타내지는 반복 단위로 이루어진다. 공액 고분자 화합물 3 의 HOMO 의 궤도 에너지는 -5.65 eV, LUMO 의 궤도 에너지는 -3.02 eV 였다.
실시예 4
BSAFP 세슘염 (BSAFCs) 의 합성
BSAFP (100 ㎎) 를 100 ㎖ 플라스크에 넣고, 질소 치환하였다. 테트라하이드로푸란 (20 ㎖), 에탄올 (20 ㎖) 을 첨가하고, 혼합물을 55 ℃ 로 승온시켰다. 거기에, 수산화세슘 (200 ㎎) 을 물 (2 ㎖) 에 녹인 수용액을 첨가하고, 55 ℃ 에서 3 시간 교반하였다. 혼합물을 실온까지 냉각시킨 후, 반응 용매를 감압 증류 제거하였다. 생긴 고체를 물로 세정하고, 감압 건조시킴으로써 옅은 황색의 고체 (90 ㎎) 를 얻었다. NMR 스펙트럼에 의해, BSAFP 내의 에틸에스테르 부위의 에틸기 유래의 시그널이 완전히 소실되고 있음을 확인하였다. 얻어진 BSAFP 의 세슘염을 공액 고분자 화합물 4 로 부른다. 공액 고분자 화합물 4 는 식 (E) 로 나타내지는 반복 단위로 이루어진다. 공액 고분자 화합물 4 의 HOMO 의 궤도 에너지는 -5.65 eV, LUMO 의 궤도 에너지는 -3.11 eV 였다.
실시예 5
BSAFP 테트라메틸암모늄염 (BSAFNMe4) 의 합성
BSAFP (100 ㎎) 를 100 ㎖ 플라스크에 넣고, 질소 치환하였다. 테트라하이드로푸란 (20 ㎖), 에탄올 (20 ㎖) 을 첨가하고, 혼합물을 55 ℃ 로 승온시켰다. 거기에, 테트라메틸암모늄하이드록사이드 (27.3 ㎎) 를 물 (2 ㎖) 에 녹인 수용액을 첨가하여, 55 ℃ 에서 3 시간 교반하였다. 혼합물을 실온까지 냉각시킨 후, 반응 용매를 감압 증류 제거하였다. 생긴 고체를 물로 세정하고, 감압 건조시킴으로써 옅은 황색의 고체 (90 ㎎) 를 얻었다. NMR 스펙트럼에 의해, BSAFP 내의 에틸에스테르 부위의 에틸기 유래의 시그널이 완전히 소실되고, 대신에 테트라메틸암모늄 이온의 시그널이 나타나고 있음을 확인하였다. 얻어진 BSAFP 의 암모늄염을 공액 고분자 화합물 5 로 부른다. 공액 고분자 화합물 5 는 식 (F) 로 나타내지는 반복 단위로 이루어진다. 공액 고분자 화합물 5 의 HOMO 의 궤도 에너지는 -5.75 eV, LUMO 의 궤도 에너지는 -2.89 eV 였다.
실시예 6
에틸렌글리콜 사슬 함유 BSAFP (BSAF-EG) 의 합성
BSAFP (100 ㎎) 를 100 ㎖ 플라스크에 넣고, 질소 치환하였다. 트리에틸렌글리콜모노메틸에스테르 (20 ㎖), 트리에틸렌글리콜디메틸에스테르 (20 ㎖), 농황산 (1 ㎖) 을 첨가하고, 혼합물을 150 ℃ 로 승온 2 일간 교반하였다. 혼합물을 실온까지 냉각시킨 후, 물 (100 ㎖), 메탄올 (100 ㎖) 의 혼합액에 적하하였다. 생긴 침전물을 여과에 의해 수집하여, 감압 건조시킴으로써 옅은 황색의 고체 (90 ㎎) 를 얻었다. NMR 스펙트럼에 의해, BSAFP 내의 에틸에스테르 부위의 에틸기 유래의 시그널이 완전히 소실되고, 대신에 트리에틸렌글리콜메틸에스테르의 시그널이 나타나고 있음을 확인하였다. 얻어진 에틸렌글리콜 사슬 함유 BSAFP 를 공액 고분자 화합물 6 으로 부른다. 공액 고분자 화합물 6 은 식 (G) 로 나타내지는 반복 단위로 이루어진다. 공액 고분자 화합물 6 의 HOMO 의 궤도 에너지는 -5.84 eV, LUMO 의 궤도 에너지는 -3.18 eV 였다.
참고예 3
2,7-비스(4,4,5,5-테트라메틸-1,3,2-디옥사보롤란-2-일)-9,9-비스(4-헥실옥시-3-에톡시카르보닐페닐)-플루오렌 (BSAFBE) 의 합성
질소 분위기하, BSAFBr2 (100 g), 비스(피나콜레이트)디보론 (68.08 g), [1,1'-비스(디페닐포스피노)페로센]디클로로팔라듐 (II) 디클로로메탄 착물 (5.97 g), 1,1'-비스(디페닐포스피노)페로센 (4.05 g), 아세트산칼륨 (71.75 g), 디옥산 (1300 ㎖) 을 혼합하고, 110 ℃ 로 가열하여, 10 시간 가열 환류시켰다. 방랭 후, 반응 용액을 여과하여, 여과액을 감압 농축하였다. 반응 혼합물을 톨루엔에 용해시키고, 아세토니트릴에 첨가하여 재침전시켜, 생긴 침전물을 회수하였다. 침전물을 톨루엔에 용해시키고, 용액에 활성탄을 첨가하여 교반한 후 여과를 실시하여, 여과액을 감압 농축하였다. 또한, 아세토니트릴 및 물을 첨가하여 교반한 후 여과를 실시하고, 여과 분리한 고체를 톨루엔에 용해시켜 아세토니트릴로부터 재침전을 실시함으로써, 2,7-비스(4,4,5,5-테트라메틸-1,3,2-디옥사보롤란-2-일)-9,9-비스(4-헥실옥시-3-에톡시카르보닐페닐)-플루오렌 (BSAFBE) (78.6 g) 을 얻었다.
참고예 4
페닐기 공중합체 (중합체 A (BSAF-Ph)) 의 합성
불활성 분위기하, 1,4-디브로모벤젠 (0.21 g), BSAFBE (0.80 g), 트리페닐포스핀팔라듐 (0.01 g), 메틸트리옥틸암모늄 클로라이드 (알드리치 제조, 상품명 Aliquat336 (등록 상표)) (0.20 g), 톨루엔 (10 ㎖) 을 혼합하여, 105 ℃ 로 가열하였다. 이 반응 용액에 2 M 탄산나트륨 (Na2CO3) 수용액 (5 ㎖) 을 적하하여, 10 시간 환류시켰다. 반응 후, 이 반응액을 실온까지 냉각시키고, 메탄올 120 ㎖ 중에 적하하여 1 시간 교반한 후, 석출된 침전을 여과하여 2 시간 감압 건조시켜, 테트라하이드로푸란 20 ㎖ 에 용해시켰다. 이 용액을 메탄올 120 ㎖, 물 50 ㎖ 의 혼합 용매 중에 적하하여 1 시간 교반한 후, 석출된 침전을 여과하여 2 시간 감압 건조시켜, 테트라하이드로푸란 20 ㎖ 에 용해시켰다. 이 용액을 아세톤 120 ㎖ 에 적하하여 30 분 교반한 후, 석출된 침전을 여과하여 20 시간 감압 건조시켰다. 얻어진 페닐기 공중합체 (중합체 A (BSAF-Ph)) 의 수량은 400 ㎎ 이었다.
중합체 A (BSAF-Ph) 의 폴리스티렌 환산의 수 평균 분자량은, 1.2×104 였다. 주입으로부터 추정되는 BSAF-Ph 에 포함되는 반복 단위는, 식 (H) 로 나타내지는 반복 단위이다.
실시예 7
중합체 A (BSAF-Ph) 의 세슘염 (BSAFCs-Ph) 의 합성
중합체 A (BSAF-Ph) (200 ㎎) 를 100 ㎖ 플라스크에 넣고, 질소 치환하였다. 테트라하이드로푸란 (20 ㎖), 에탄올 (5 ㎖) 을 첨가하고, 혼합물을 55 ℃ 로 승온시켰다. 거기에, 수산화세슘 (200 ㎎) 을 물 (1 ㎖) 에 녹인 수용액을 첨가하여, 55 ℃ 에서 3 시간 교반하였다. 혼합물을 실온까지 냉각시킨 후, 반응 용매를 감압 증류 제거하였다. 생긴 고체를 물로 세정하고, 감압 건조시킴으로써 옅은 황색의 고체 (190 ㎎) 를 얻었다. NMR 스펙트럼에 의해, 중합체 A (BSAF-Ph) 의 에틸에스테르 부위의 에틸기 유래의 시그널이 완전히 소실되고 있음을 확인하였다. 얻어진 중합체 A (BSAF-Ph) 의 세슘염을 공액 고분자 화합물 7 로 부른다. 공액 고분자 화합물 7 은 식 (I) 로 나타내지는 반복 단위로 이루어진다. 공액 고분자 화합물 7 의 HOMO 의 궤도 에너지는 -5.78 eV, LUMO 의 궤도 에너지는 -3.19 eV 였다.
참고예 5
피라진 공중합체 (9 : 1) (중합체 B (BSAF-pyrazine (9 : 1))) 의 합성
불활성 분위기하, BSAFBr2 (0.35 g), BSAFBE (0.5 g), 2,5-디브로모피라진 (0.03 g) 트리페닐포스핀팔라듐 (0.002 g), 메틸트리옥틸암모늄 클로라이드 (알드리치 제조, 상품명 Aliquat336 (등록 상표)) (0.20 g), 톨루엔 (10 ㎖) 을 혼합하여, 105 ℃ 로 가열하였다. 이 반응 용액에 2 M Na2CO3 수용액 (5 ㎖) 을 적하하여, 5 시간 환류시켰다. 반응 후, 이 반응액을 실온까지 냉각시키고, 메탄올 120 ㎖ 중에 적하하여 1 시간 교반한 후, 석출된 침전을 여과하여 2 시간 감압 건조시켜, 테트라하이드로푸란 20 ㎖ 에 용해시켰다. 이 용액을 메탄올 120 ㎖, 물 50 ㎖ 의 혼합 용매 중에 적하하여 1 시간 교반한 후, 석출된 침전을 여과하여 2 시간 감압 건조시켜, 테트라하이드로푸란 20 ㎖ 에 용해시켰다. 이 용액을 아세톤 120 ㎖ 에 적하하여 30 분 교반한 후, 석출된 침전을 여과하여 20 시간 감압 건조시켰다. 피라진 중합체 (9 : 1) (중합체 B (BSAF-pyrazine (9 : 1))) 의 수량은 550 ㎎ 이었다.
중합체 B (BSAF-pyrazine (9 : 1)) 의 폴리스티렌 환산의 수 평균 분자량은, 4.5×104 였다. 중합체 B (BSAF-pyrazine (9 : 1)) 는 식 (J) 로 나타내진다. 식 (J) 중, m : n 은 반복 단위의 몰비를 나타낸다.
실시예 8
중합체 B (BSAF-pyrazine (9 : 1)) 의 나트륨염 (BSAFNa-pyrazine (9 : 1)) 의 합성
중합체 B (BSAF-pyrazine (9 : 1)) (200 ㎎) 를 100 ㎖ 플라스크에 넣고, 질소 치환하였다. 테트라하이드로푸란 (20 ㎖), 에탄올 (5 ㎖) 을 첨가하고, 혼합물을 55 ℃ 로 승온시켰다. 거기에, 수산화나트륨 (120 ㎎) 을 물 (1 ㎖) 에 녹인 수용액을 첨가하여, 55 ℃ 에서 3 시간 교반하였다. 혼합물을 실온까지 냉각시킨 후, 반응 용매를 감압 증류제거하였다. 생긴 고체를 물로 세정하고, 감압 건조시킴으로써 옅은 황색의 고체 (120 ㎎) 를 얻었다. NMR 스펙트럼에 의해, 중합체 B (BSAF-pyrazine (9 : 1)) 의 에틸에스테르 부위의 에틸기 유래의 시그널이 완전히 소실되고 있음을 확인하였다. 얻어진 중합체 B (BSAF-pyrazine (9 : 1)) 의 나트륨염을 공액 고분자 화합물 8 로 부른다. 공액 고분자 화합물 8 은 식 (K) 로 나타내진다. 식 (K) 중, m : n 은 반복 단위의 몰비를 나타낸다. 공액 고분자 화합물 8 의 HOMO 의 궤도 에너지는 -5.65 eV, LUMO 의 궤도 에너지는 -3.14 eV 였다.
참고예 6
피라진 공중합체 (99 : 1) (중합체 C (BSAF-pyrazine (99 : 1))) 의 합성
불활성 분위기하, BSAFBr2 (0.43 g), BSAFBE (0.5 g), 2,5-디브로모피라진 (0.003 g) 트리페닐포스핀팔라듐 (0.002 g), 메틸트리옥틸암모늄 클로라이드 (알드리치 제조, 상품명 Aliquat336 (등록 상표)) (0.20 g), 톨루엔 (10 ㎖) 을 혼합하여, 105 ℃ 로 가열하였다. 이 반응 용액에 2 M Na2CO3 수용액 (5 ㎖) 을 적하하여, 5 시간 환류시켰다. 반응 후, 이 반응액을 실온까지 냉각시키고, 메탄올 120 ㎖ 중에 적하하여 1 시간 교반한 후, 석출된 침전을 여과하여 2 시간 감압 건조시켜, 테트라하이드로푸란 20 ㎖ 에 용해시켰다. 이 용액을 메탄올 120 ㎖, 물 50 ㎖ 의 혼합 용매 중에 적하하여 1 시간 교반한 후, 석출된 침전을 여과하여 2 시간 감압 건조시켜, 테트라하이드로푸란 20 ㎖ 에 용해시켰다. 이 용액을 아세톤 120 ㎖ 에 적하하여 30 분 교반한 후, 석출된 침전을 여과하여 20 시간 감압 건조시켰다. 피라진 공중합체 (99 : 1) (중합체 C (BSAF-pyrazine (99 : 1))) 의 수량은 530 ㎎ 이었다.
중합체 C (BSAF-pyrazine (99 : 1)) 의 폴리스티렌 환산의 수 평균 분자량은, 6.8×104 였다. 중합체 C (BSAF-pyrazine (99 : 1)) 는 식 (L) 로 나타내진다. 식 (L) 중, m : n 은 반복 단위의 몰비를 나타낸다.
실시예 9
중합체 C (BSAF-pyrazine (99 : 1)) 의 나트륨염 (BSAFNa-pyrazine (99 : 1)) 의 합성
중합체 C (BSAF-pyrazine (99 : 1)) (200 ㎎) 를 100 ㎖ 플라스크에 넣고, 질소 치환하였다. 테트라하이드로푸란 (20 ㎖), 에탄올 (5 ㎖) 을 첨가하고, 혼합물을 55 ℃ 로 승온시켰다. 거기에, 수산화나트륨(120 ㎎) 을 물 (1 ㎖) 에 녹인 수용액을 첨가하여, 55 ℃ 에서 3 시간 교반하였다. 혼합물을 실온까지 냉각시킨 후, 반응 용매를 감압 증류 제거하였다. 생긴 고체를 물로 세정하고, 감압 건조시킴으로써 옅은 황색의 고체 (150 ㎎) 를 얻었다. NMR 스펙트럼에 의해, 중합체 C (BSAF-pyrazine (99 : 1)) 의 에틸에스테르 부위의 에틸기 유래의 시그널이 완전히 소실되고 있음을 확인하였다. 얻어진 중합체 C (BSAF-pyrazine (99 : 1)) 의 나트륨염을 공액 고분자 화합물 9 로 부른다. 공액 고분자 화합물 9 는 식 (M) 으로 나타내진다. 식 (M) 중, m : n 은 반복 단위의 몰비를 나타낸다. 공액 고분자 화합물 9 의 HOMO 의 궤도 에너지는 -5.58 eV, LUMO 의 궤도 에너지는 -2.99 eV 였다.
참고예 7
N,N-비스(4-브로모페닐)-N',N'-비스(4-부틸페닐)-1,4-페닐렌디아민 (방향족 아민 A) 의 합성
불활성 분위기하, 300 ㎖ 3 구 플라스크에 트리스(디벤질리덴아세톤)디팔라듐 0.24 g (0.27 m㏖), 디페닐포스피노페로센 0.22 g (0.4 m㏖), 나트륨t-부톡사이드 2.56 g (26.7 m㏖), 및 톨루엔 125 ㎖ 를 넣고, 실온에서 10 분간 교반하였다. 계속해서, 트리스(4-브로모페닐)아민 12.9 g (26.7 m㏖) 을 넣고, 다시 실온에서 10 분간 교반하였다. 그 후, 비스(4-부틸페닐)아민 5 g (17.8 m㏖) 을 넣고, 125 ℃ 까지 승온, 9 시간 환류시켰다. 반응 종료 후, 반응액을 여과하여 불용물을 제거 후, 실리카 겔의 쇼트 칼럼을 통과시키고, 다시 시클로헥산을 전개 용매로 하는 실리카 겔 칼럼으로 정제함으로써, N,N-비스(4-브로모페닐)-N',N'-비스(4-부틸페닐)-1,4-페닐렌디아민 (방향족 아민 A) (2.96 g, 수율 24 %) 을 얻었다.
참고예 8
방향족 아민 A 공중합체 (중합체 D (BSAF-방향족 아민 A)) 의 합성
방향족 아민 A (0.21 g), BSAFBr2 0.38 g 및 2,2'-비피리딜 390 ㎎ 을 탈수한 테트라하이드로푸란 28 ㎖ 에 용해시킨 후, 질소 분위기하에서, 이 용액에, 비스(1,5-시클로옥타디엔)니켈 (0) 690 ㎎ 을 첨가하고, 60 ℃ 까지 승온시켜, 3 시간 반응시켰다. 반응 후, 이 반응액을 실온까지 냉각시키고, 25 % 암모니아수 10 ㎖/메탄올 120 ㎖/이온 교환수 50 ㎖ 혼합 용액 중에 적하하여 1 시간 교반한 후, 석출된 침전을 여과하여 2 시간 감압 건조시켜, 톨루엔 50 ㎖ 에 용해시켰다. 이 용액에 1 N 의 염산 30 ㎖ 를 첨가하여 실온에서 3 시간 교반하여, 수층을 제거 후, 4 % 암모니아수 30 ㎖ 를 첨가하여 실온에서 3 시간 교반, 수층을 제거하였다. 남은 톨루엔 용액을 메탄올 150 ㎖ 로 기화시킴으로써 재침전시켜, 불용물을 여과하여 제거하였다. 그 후, 다시 톨루엔에 녹여 알루미나 칼럼 (활성 알루미나 10 g) 을 통과시켜 정제를 실시하고, 회수한 톨루엔 용액을 메탄올 200 ㎖ 에 적하하여 30 분간 교반하고, 석출된 침전을 여과하여 2 시간 감압 건조시켰다. 얻어진 방향족 아민 A 공중합체 (중합체 D (BSAF-방향족 아민 A)) 의 수량은 300 ㎎ 이었다.
중합체 D (BSAF-방향족 아민 A) 의 폴리스티렌 환산의 수 평균 분자량은, 4.8×104 였다. 중합체 D (BSAF-방향족 아민 A) 는 식 (N) 으로 나타내진다. 식 (N) 중, m : n 은 반복 단위의 몰비를 나타낸다.
실시예 10
중합체 D (BSAF-방향족 아민 A) 의 세슘염 (BSAFCs-방향족 아민 A) 의 합성
중합체 D (BSAF-방향족 아민 A) (200 ㎎) 를 100 ㎖ 플라스크에 넣고, 질소 치환하였다. 테트라하이드로푸란 (20 ㎖), 에탄올 (10 ㎖) 을 첨가하고, 혼합물을 55 ℃ 로 승온시켰다. 거기에, 수산화세슘 (200 ㎎) 을 물 (2 ㎖) 에 녹인 수용액을 첨가하여, 55 ℃ 에서 3 시간 교반하였다. 혼합물을 실온까지 냉각시킨 후, 반응 용매를 감압 증류 제거하였다. 생긴 고체를 물로 세정하고, 감압 건조시킴으로써 옅은 황색의 고체 (190 ㎎) 를 얻었다. NMR 스펙트럼에 의해, 중합체 D (BSAF-방향족 아민 A) 의 에틸에스테르 부위의 에틸기 유래의 시그널이 완전히 소실되고 있음을 확인하였다. 얻어진 중합체 D (BSAF-방향족 아민 A) 의 세슘염을 공액 고분자 화합물 10 으로 부른다. 공액 고분자 화합물 10 은 식 (O) 로 나타내진다. 식 (O) 중, m : n 은 반복 단위의 몰비를 나타낸다. 공액 고분자 화합물 10 의 HOMO 의 궤도 에너지는 -5.63 eV, LUMO 의 궤도 에너지는 -3.02 eV 였다.
참고예 9
방향족 아민 B 공중합체 (중합체 E (BSAF-방향족 아민 B)) 의 합성
불활성 분위기하, BSAFBr2 (0.41 g), BSAFBE (0.5 g), N,N'-비스(4-브로모페닐)-N,N'-비스(4-t-부틸-2,6-디메틸페닐)1,4-페닐렌디아민 (0.11 g) 트리페닐포스핀팔라듐 (0.002 g), 메틸트리옥틸암모늄 클로라이드 (알드리치 제조, 상품명 Aliquat336 (등록 상표)) (0.20 g), 톨루엔 (10 ㎖) 을 혼합하여, 105 ℃ 로 가열하였다. 이 반응 용액에 2 M Na2CO3 수용액 (5 ㎖) 을 적하하여, 8 시간 환류시켰다. 반응 후, 이 반응액을 실온까지 냉각시키고, 메탄올 120 ㎖ 중에 적하하여 1 시간 교반한 후, 석출된 침전을 여과하여 2 시간 감압 건조시켜, 테트라하이드로푸란 20 ㎖ 에 용해시켰다. 이 용액을 메탄올 120 ㎖, 물 50 ㎖ 의 혼합 용매 중에 적하하여 1 시간 교반한 후, 석출된 침전을 여과하여 2 시간 감압 건조시켜, 테트라하이드로푸란 20 ㎖ 에 용해시켰다. 이 용액을 아세톤 120 ㎖ 에 적하하여 30 분 교반한 후, 석출된 침전을 여과하여 20 시간 감압 건조시켰다. 얻어진 방향족 아민 B 공중합체 (중합체 E (BSAF-방향족 아민 B)) 의 수량은 400 ㎎ 이었다.
중합체 E (BSAF-방향족 아민 B) 의 폴리스티렌 환산의 수 평균 분자량은, 3.6×105 였다. 중합체 E (BSAF-방향족 아민 B) 는 식 (P) 로 나타내진다. 식 (P) 중, m : n 은 반복 단위의 몰비를 나타낸다.
N,N'-비스(4-브로모페닐)-N,N'-비스(4-t-부틸-2,6-디메틸페닐)1,4-페닐렌디아민은, 예를 들어, 일본 공개특허공보 2008-74917호의 합성예 1 에 기재되어 있는 방법으로 합성할 수 있다.
실시예 11
중합체 E (BSAF-방향족 아민 B) 의 세슘염 (BSAFCs-방향족 아민 B) 의 합성
중합체 E (BSAF-방향족 아민 B) (200 ㎎) 를 100 ㎖ 플라스크에 넣고, 질소 치환하였다. 테트라하이드로푸란 (20 ㎖), 에탄올 (5 ㎖) 을 첨가하고, 혼합물을 55 ℃ 로 승온시켰다. 거기에, 수산화세슘 (200 ㎎) 을 물 (1 ㎖) 에 녹인 수용액을 첨가하여, 55 ℃ 에서 3 시간 교반하였다. 혼합물을 실온까지 냉각시킨 후, 반응 용매를 감압 증류 제거하였다. 생긴 고체를 물로 세정하고, 감압 건조시킴으로써 옅은 황색의 고체 (160 ㎎) 를 얻었다. NMR 스펙트럼에 의해, 중합체 E (BSAF-방향족 아민 B) 의 에틸에스테르 부위의 에틸기 유래의 시그널이 완전히 소실되고 있음을 확인하였다. 얻어진 중합체 E (BSAF-방향족 아민 B) 의 세슘염을 공액 고분자 화합물 11 로 부른다. 공액 고분자 화합물 11 은 식 (Q) 로 나타내진다. 식 (Q) 중, m : n 은 반복 단위의 몰비를 나타낸다. 공액 고분자 화합물 11 의 HOMO 의 궤도 에너지는 -5.21 eV, LUMO 의 궤도 에너지는 -2.62 eV 였다.
참고예 10
아미노기 함유 플루오렌 폴리머 (중합체 F (BSAF-FN)) 의 합성
불활성 분위기하, BSAFBr2 (0.41 g), BSAFBE (0.5 g), 2,7-디브로모-9,9-비스(4-N,N-디에틸아미노페닐)-플루오렌 (0.08 g), 트리페닐포스핀팔라듐 (0.002 g), 메틸트리옥틸암모늄 클로라이드 (알드리치 제조, 상품명 Aliquat336 (등록 상표)) (0.20 g), 톨루엔 (10 ㎖) 을 혼합하여, 105 ℃ 로 가열하였다. 이 반응 용액에 2 M Na2CO3 수용액 (5 ㎖) 을 적하하여, 7 시간 환류시켰다. 반응 후, 이 반응액을 실온까지 냉각시키고, 메탄올 120 ㎖ 중에 적하하여 1 시간 교반한 후, 석출된 침전을 여과하여 2 시간 감압 건조시켜, 테트라하이드로푸란 20 ㎖ 에 용해시켰다. 이 용액을 메탄올 120 ㎖, 물 50 ㎖ 의 혼합 용매 중에 적하하여 1 시간 교반한 후, 석출된 침전을 여과하여 2 시간 감압 건조시켜, 테트라하이드로푸란 20 ㎖ 에 용해시켰다. 이 용액을 아세톤 120 ㎖ 에 적하하여 30 분 교반한 후, 석출된 침전을 여과하여 20 시간 감압 건조시켰다. 얻어진 아미노기 함유 플루오렌 폴리머 (중합체 F (BSAF-FN)) 의 수량은 430 ㎎ 이었다. 중합체 F (BSAF-FN) 의 폴리스티렌 환산의 수 평균 분자량은, 1.2×104 였다. 중합체 F (BSAF-FN) 는 식 (R) 로 나타내진다. 식 (R) 중, m : n 은 반복 단위의 몰비를 나타낸다.
2,7-디브로모-9,9-비스(4-N,N-디에틸아미노페닐)-플루오렌은 예를 들어, 폴리머 (Polymer) 제 49 권, 218 페이지 (2008 년) 에 기재되어 있는 방법으로 합성할 수 있다.
실시예 12
중합체 F (BSAF-FN) 의 세슘염 (BSAFCs-FN) 의 합성
중합체 F (BSAF-FN) (200 ㎎) 를 100 ㎖ 플라스크에 넣고, 질소 치환하였다. 테트라하이드로푸란 (20 ㎖), 에탄올 (5 ㎖) 을 첨가하고, 혼합물을 55 ℃ 로 승온시켰다. 거기에, 수산화세슘 (200 ㎎) 을 물 (1 ㎖) 에 녹인 수용액을 첨가하여, 55 ℃ 에서 3 시간 교반하였다. 혼합물을 실온까지 냉각시킨 후, 반응 용매를 감압 증류 제거하였다. 생긴 고체를 물로 세정하고, 감압 건조시킴으로써 옅은 황색의 고체 (180 ㎎) 를 얻었다. NMR 스펙트럼에 의해, 중합체 F (BSAF-FN) 의 에틸에스테르 부위의 에틸기 유래의 시그널이 완전히 소실되고 있음을 확인하였다. 얻어진 중합체 F (BSAF-FN) 의 세슘염을 공액 고분자 화합물 12 로 부른다. 공액 고분자 화합물 12 는 식 (S) 로 나타내진다. 식 (S) 중, m : n 은 반복 단위의 몰비를 나타낸다. 공액 고분자 화합물 12 의 HOMO 의 궤도 에너지는 -5.53 eV, LUMO 의 궤도 에너지는 -2.76 eV 였다.
참고예 11
2,7-디브로모-9,9-비스[3,4-비스[2-[2-(2-메톡시에톡시)에톡시]에톡시]페닐]플루오렌 (FEGBr2) 의 합성
불활성 분위기하, 2,7-디브로모플루오렌 (50 g) 및 카테콜 (345 g) 을 혼합하여, 130 도로 승온시켰다. 3-메르캅토프로피온산 (1.96 g) 및 황산 (7 g) 을 첨가하여, 130 도에서 1.5 시간 반응시켰다. 방랭 후, 물 (2 L) 에 투입하고, 석출된 결정을 여과에 의해 회수하였다. 결정을 에탄올에 용해시켜, 여과를 한 후, 여과액을 농축하고, 농축액을 물에 첨가하여 재침전을 실시하였다. 생긴 고체를 여과에 의해 회수하고, 톨루엔에 용해시켜, 여과를 한 후, 에탄올을 첨가하고, 용액을 헥산에 적하하여, 5 ℃ 로 냉각시켰다. 생긴 고체를 여과에 의해 회수하여, 감압 건조시킴으로써 백색 고체를 얻었다. 불활성 분위기하, 백색 고체 20 g, 트리에틸렌글리콜모노메틸에스테르토실레이트 (72 g), 무수 탄산칼륨 (52 g), 아세토니트릴 (500 ㎖) 을 혼합하여, 가열 환류하, 4 시간 교반시켰다. 방랭 후, 반응 용액을 여과하고, 여과액을 감압 농축하였다. 반응 혼합물을 아세트산에틸을 전개 용매로 하는 실리카 겔 크로마토그래피, 또한 THF 및 아세트산에틸의 혼합 용매를 전개 용매로 하는 실리카 겔 크로마토그래피에 의해 정제함으로써, 2,7-디브로모-9,9-비스[3,4-비스[2-[2-(2-메톡시에톡시)에톡시]에톡시]페닐]플루오렌 (FEGBr2) (18 g, 수율 43.2 %) 을 얻었다.
참고예 12
에틸렌글리콜 사슬 함유 플루오렌 공중합체 (중합체 G (BSAF-FEG))
불활성 분위기하, FEGBr2 (0.80 g), BSAFBE (0.98 g), 트리페닐포스핀팔라듐 (0.01 g), 메틸트리옥틸암모늄 클로라이드 (알드리치 제조, 상품명 Aliquat336 (등록 상표)) (0.20 g), 톨루엔 (10 ㎖) 을 혼합하여, 105 ℃ 로 가열하였다. 이 반응 용액에 2 M Na2CO3 수용액 (5 ㎖) 을 적하하여, 10 시간 환류시켰다. 반응 후, 이 반응액을 실온까지 냉각시키고, 메탄올 120 ㎖ 중에 적하하여 1 시간 교반한 후, 석출된 침전을 여과하여 2 시간 감압 건조시켜, 테트라하이드로푸란 20 ㎖ 에 용해시켰다. 이 용액을 메탄올 120 ㎖, 물 50 ㎖ 의 혼합 용매 중에 적하하여 1 시간 교반한 후, 석출된 침전을 여과하여 2 시간 감압 건조시켜, 테트라하이드로푸란 20 ㎖ 에 용해시켰다. 이 용액을 아세톤 120 ㎖ 에 적하하여 30 분 교반한 후, 석출된 침전을 여과하여 20 시간 감압 건조시켰다. 얻어진 에틸렌글리콜 사슬 함유 플루오렌 공중합체 (중합체 G (BSAF-FEG)) 의 수량은 920 ㎎ 이었다.
BSAF-FEG 의 폴리스티렌 환산의 수 평균 분자량은, 1.2×104 였다. 중합체 G (BSAF-FEG) 는 식 (T) 로 나타내지는 반복 단위로 이루어진다.
실시예 13
중합체 G (BSAF-FEG) 의 세슘염 (BSAFCs-FEG) 의 합성
중합체 G (BSAFCs-FEG) (200 ㎎) 를 100 ㎖ 플라스크에 넣고, 질소 치환하였다. 테트라하이드로푸란 (20 ㎖), 에탄올 (5 ㎖) 을 첨가하고, 혼합물을 55 ℃ 로 승온시켰다. 거기에, 수산화세슘 (200 ㎎) 을 물 (1 ㎖) 에 녹인 수용액을 첨가하여, 55 ℃ 에서 3 시간 교반하였다. 혼합물을 실온까지 냉각시킨 후, 반응 용매를 감압 증류 제거하였다. 생긴 고체를 물로 세정하고, 감압 건조시킴으로써 옅은 황색의 고체 (170 ㎎) 를 얻었다. NMR 스펙트럼에 의해, 중합체 G (BSAFCs-FEG) 의 에틸에스테르 부위의 에틸기 유래의 시그널이 완전히 소실되고 있음을 확인하였다. 얻어진 중합체 G (BSAFCs-FEG) 의 세슘염을 공액 고분자 화합물 13 으로 부른다. 공액 고분자 화합물 13 은 식 (U) 로 나타내지는 반복 단위로 이루어진다. 공액 고분자 화합물 13 의 HOMO 의 궤도 에너지는 -5.52 eV, LUMO 의 궤도 에너지는 -2.91 eV 였다.
참고예 13
(2,7-디브로모)-9H-플루오렌-9,9-디프로피온산디부틸에스테르 (F2COOBuBr2) 의 합성
2,7-디브로모플루오렌 (8.02 g) 및 벤질트리에틸암모늄 클로라이드 (0.56 g) 를 30 ㎖ 의 벤젠에 용해시킨 후, 질소 분위기하에서 50 % 수산화나트륨 수용액 8 ㎖ 를 적하하여, 15 분 교반하였다. N-부틸아크릴레이트 (12.65 g) 를 적하하여, 실온에서 5 시간 반응시켰다. 반응 용액을 아세트산에틸 200 ㎖ 에 희석시켜, 물로 3 회, 염수로 1 회 세정하고, 유기층을 황산 마그네슘에 의해 건조시켰다. 용액을 여과하여, 용매 증류 제거한 후, 디클로로메탄을 전개 용매로 하는 실리카 겔 칼럼 크로마토그래피에 의해 정제하고, 다시 헥산으로부터 재결정을 실시함으로써 (2,7-디브로모)-9H-플루오렌-9,9-디프로피온산 (F2COOBuBr2) (7.87 g, 55 %) 을 얻었다.
참고예 14
카르복실산기 함유 플루오렌 폴리머 (중합체 H (F8-F2COOBu)) 의 합성
불활성 분위기하, 2,7-비스(1,3,2-디옥사보롤란-2-일)-9,9-디옥틸플루오렌 (1.00 g), F2COOBuBr2 (1.09 g), 트리페닐포스핀팔라듐 (0.03 g), 메틸트리옥틸암모늄 클로라이드 (알드리치 제조, 상품명 Aliquat336 (등록 상표)) (0.20 g, 알드리치 제조), 톨루엔 (20 ㎖) 을 혼합하여, 105 ℃ 로 가열하였다. 이 반응 용액에 2 M Na2CO3 수용액 (5 ㎖) 을 적하하여, 4 시간 환류시켰다. 반응 후, 이 반응액을 실온까지 냉각시키고, 메탄올 120 ㎖ 중에 적하하여 1 시간 교반한 후, 석출된 침전을 여과하여 2 시간 감압 건조시켜, 테트라하이드로푸란 20 ㎖ 에 용해시켰다. 이 용액을 메탄올 120 ㎖, 물 50 ㎖ 의 혼합 용매 중에 적하하여 1 시간 교반한 후, 석출된 침전을 여과하여 2 시간 감압 건조시켜, 테트라하이드로푸란 20 ㎖ 에 용해시켰다. 이 용액을 아세톤 120 ㎖ 에 적하하여 30 분 교반한 후, 석출된 침전을 여과하여 20 시간 감압 건조시켰다. 얻어진 카르복실산기 함유 플루오렌 폴리머 (중합체 H (F8-F2COOBu)) 의 수량은 300 ㎎ 이었다.
중합체 H (F8-F2COOBu) 의 폴리스티렌 환산의 수 평균 분자량은, 3.5×104 였다. 중합체 H (F8-F2COOBu) 는 식 (V) 로 나타내지는 반복 단위로 이루어진다.
실시예 14
카르복실산기 함유 플루오렌 폴리머 나트륨염 (F8-F2COONa) 의 합성
중합체 H (F8-F2COOBu) (200 ㎎) 를 100 ㎖ 플라스크에 넣고, 질소 치환하였다. 테트라하이드로푸란 (20 ㎖), 에탄올 (5 ㎖) 을 첨가하고, 혼합물을 55 ℃ 로 승온시켰다. 거기에, 수산화나트륨(120 ㎎) 을 물 (1 ㎖) 에 녹인 수용액을 첨가하여, 55 ℃ 에서 3 시간 교반하였다. 혼합물을 실온까지 냉각시킨 후, 반응 용매를 감압 증류 제거하였다. 생긴 고체를 물로 세정하고, 감압 건조시킴으로써 옅은 황색의 고체 (120 ㎎) 를 얻었다. NMR 스펙트럼에 의해, 중합체 H (F8-F2COOBu) 의 부틸에스테르 부위의 부틸기 유래의 시그널이 완전히 소실되고 있음을 확인하였다. 얻어진 중합체 H (F8-F2COOBu) 의 나트륨염을 공액 고분자 화합물 14 로 부른다. 공액 고분자 화합물 14 는 식 (W) 로 나타내지는 반복 단위로 이루어진다. 공액 고분자 화합물 14 의 HOMO 의 궤도 에너지는 -5.56 eV, LUMO 의 궤도 에너지는 -2.75 eV 였다.
참고예 15
카르복실산기 함유 페닐렌 폴리머 (중합체 I (F8-PhCOOMe)) 의 합성
불활성 분위기하, 2,7-비스(1,3,2-디옥사보롤란-2-일)-9,9-디옥틸플루오렌 (1.00 g), 2,5-디브로모벤조산메틸 (알드리치 제조) (0.52 g), 트리스(디벤질리덴아세톤)디팔라듐 (0.01 g), 메틸트리옥틸암모늄 클로라이드 (알드리치 제조, 상품명 Aliquat336 (등록 상표)) (0.20 g, 알드리치 제조), 톨루엔 (20 ㎖) 을 혼합하여, 105 ℃ 로 가열하였다. 이 반응 용액에 2 M Na2CO3 수용액 (5 ㎖) 을 적하하여, 4 시간 환류시켰다. 반응 후, 이 반응액을 실온까지 냉각시키고, 메탄올 120 ㎖ 중에 적하하여 1 시간 교반한 후, 석출된 침전을 여과하여 2 시간 감압 건조시켜, 테트라하이드로푸란 20 ㎖ 에 용해시켰다. 이 용액을 메탄올 120 ㎖, 물 50 ㎖ 의 혼합 용매 중에 적하하여 1 시간 교반한 후, 석출된 침전을 여과하여 2 시간 감압 건조시켜, 테트라하이드로푸란 20 ㎖ 에 용해시켰다. 이 용액을 아세톤 120 ㎖ 에 적하하여 30 분 교반한 후, 석출된 침전을 여과하여 20 시간 감압 건조시켰다. 얻어진 카르복실산기 함유 페닐렌 폴리머 (중합체 I (F8-PhCOOMe)) 의 수량은 300 ㎎ 이었다.
중합체 I (F8-PhCOOMe) 의 폴리스티렌 환산의 수 평균 분자량은, 3.5×104 이였다.
중합체 I (F8-PhCOOMe) 는 식 (X) 로 나타내지는 반복 단위로 이루어진다.
실시예 15
카르복실산기 함유 페닐렌 폴리머 세슘염 (F8-PhCOOCs) 의 합성
중합체 I (F8-PhCOOMe) (160 ㎎) 을 100 ㎖ 플라스크에 넣고, 질소 치환하였다. 테트라하이드로푸란 (20 ㎖), 에탄올 (5 ㎖) 을 첨가하고, 혼합물을 55 ℃ 로 승온시켰다. 거기에, 수산화세슘 (120 ㎎) 을 물 (1 ㎖) 에 녹인 수용액을 첨가하여, 55 ℃ 에서 3 시간 교반하였다. 혼합물을 실온까지 냉각시킨 후, 반응 용매를 감압 증류 제거하였다. 생긴 고체를 물로 세정하고, 감압 건조시킴으로써 옅은 황색의 고체 (110 ㎎) 를 얻었다. NMR 스펙트럼에 의해, 중합체 I (F8-PhCOOMe) 의 메틸에스테르 부위의 메틸기 유래의 시그널이 완전히 소실되고 있음을 확인하였다. 얻어진 중합체 I (F8-PhCOOMe) 의 나트륨염을 공액 고분자 화합물 15 로 부른다. 공액 고분자 화합물 15 는 식 (Y) 로 나타내지는 반복 단위로 이루어진다. 공액 고분자 화합물 15 의 HOMO 의 궤도 에너지는 -5.72 eV, LUMO 의 궤도 에너지는 -2.93 eV 였다.
참고예 16
폴리우레탄나트륨염 (비공액 이온-Na) 의 합성
1,3-부탄디올 (1.0 g), 디부틸주석디라우레이트 (7.5 ㎎), 디메틸올프로피온산 (0.5 g) 을 100 ㎖ 플라스크에 넣고, DMF (50 ㎖) 를 첨가하여, 90 ℃ 에서 30 분간 교반하였다. 이소포론디이소시아네이트 (3.3 g) 를 첨가하여, 90 ℃ 에서 3 시간 가열하였다. 60 ℃ 까지 온도를 내리고, 1 M 수산화나트륨 수용액을 첨가하여 중화하였다. 60 ℃ 에서 다시 1 시간 교반한 후, 용매를 증류 제거함으로써 백색의 고체 (2.0 g) 를 얻었다. 얻어진 폴리우레탄나트륨염을 비공액 고분자 화합물 1 로 부른다. 비공액 고분자 화합물 1 은 식 (Z) 로 나타내지는 반복 단위로 이루어진다.
실시예 16
<전계 발광 소자>
양극으로서 ITO 가 막 형성 패터닝된 유리 기판의 ITO 양극 상에, 정공 주입 재료 용액을 도포하여, 스핀 코트법에 의해 막두께가 60 ㎚ 가 되도록 정공 주입층을 막 형성하였다.
막 형성된 유리 기판을 공기 중에서, 200 ℃ 에서 10 분 가열하여 정공 주입층을 불용화시키고, 기판을 실온까지 자연 냉각시켜, 정공 주입층을 얻었다.
정공 주입 재료 용액에는, 스탈크 V 테크 (주) 제조 PEDOT : PSS 용액 (폴리(3,4에틸렌디옥시티오펜)·폴리스티렌술폰산,「제품명 : Baytron」) 을 사용하였다.
다음으로, 정공 수송성 고분자 재료와 자일렌을 혼합하여, 정공 수송성 고분자 재료가 0.7 중량% 인 정공 수송층 형성용 조성물을 얻었다. 정공 수송 고분자 재료로서는, 이하의 방법으로 합성한 것을 사용하였다.
환류 냉각기 및 오버헤드 스터러를 장비한 1 리터의 3 구 환저 플라스크에, 2,7-비스(1,3,2-디옥시보롤)-9,9-디(1-옥틸)플루오렌 (3.863 g, 7.283 m㏖), N,N-디(p-브로모페닐)-N-(4-(부탄-2-일)페닐)아민 (3.177 g, 6.919 m㏖) 및 디(4-브로모페닐)벤조시클로부탄아민 (156.3 ㎎, 0.364 m㏖) 을 첨가하였다. 이어서, 메틸트리옥틸암모늄 클로라이드 (알드리치 제조, 상품명 Aliquat336 (등록 상표)) (2.29 g), 계속해서 톨루엔 50 ㎖ 를 첨가하였다. PdCl2(PPh3)2 촉매 (4.9 ㎎) 를 첨가한 후, 혼합물을, 105 ℃ 의 오일욕 중에서 15 분간 교반하였다. 탄산나트륨 수용액 (2.0 M, 14 ㎖) 을 첨가하여, 반응물을 105 ℃ 의 오일욕 중, 16.5 시간 교반하였다. 이어서, 페닐보론산 (0.5 g) 을 첨가하여, 반응물을 7 시간 교반하였다. 수층을 제거하고, 유기층을 물 50 ㎖ 로 세정하였다. 유기층을 반응 플라스크로 돌려보내고, 디에틸디티오카르바민산나트륨 0.75 g 및 물 50 ㎖ 를 첨가하였다. 반응물을 85 ℃ 의 오일욕 중, 16 시간 교반하였다. 수층을 제거하고, 유기층을 100 ㎖ 의 물로 3 회 세정하고, 이어서 실리카 겔 및 염기성 알루미나의 칼럼에 통과시켰다. 이어서, 폴리머를 포함하는 톨루엔 용액을 메탄올에 침전시키는 조작을 2 회 반복하고, 폴리머를 60 ℃ 에서 진공 건조시켜, 정공 수송성 고분자 4.2 g 을 얻었다. 정공 수송성 고분자 재료의 폴리스티렌 환산의 중량 평균 분자량은 124,000 이며, 분산 (Mw/Mn) 은 2.8 이었다.
상기에서 얻은 정공 주입층 형성을 마친 기판의 정공 주입층 상에, 정공 수송층 형성용 조성물을 스핀 코트법에 의해 도포하여, 막두께 20 ㎚ 의 도포막을 얻었다.
이 도포막을 형성한 기판을 불활성 (질소) 분위기하에서, 190 ℃ 에서 20 분간 가열하여, 도포막을 불용화시킨 후, 실온까지 자연 냉각시켜, 정공 수송층을 얻었다.
다음으로, 발광 고분자 재료 (서메이션 (주) 제조 「BP361」) 와 자일렌을 혼합하여, 발광 고분자 재료가 1.4 중량% 인 발광층 형성용 조성물을 얻었다.
상기에서 얻은 정공 수송층 형성을 마친 기판의 정공 수송층 상에, 발광층 형성용 조성물을 스핀 코트법에 의해 도포하여, 막두께 80 ㎚ 의 도포막을 얻었다.
이 도포막을 형성한 기판을 불활성 (질소) 분위기하에서, 130 ℃ 에서 20 분간 가열하여, 용매를 증발시킨 후, 실온까지 자연 냉각시켜, 발광층을 얻었다.
메탄올과 테트라하이드로푸란을 체적비 9 : 1 로 혼합한 용매 (용해도 파라미터 12.5) 와 공액 고분자 화합물 1 을 혼합하여, 공액 고분자 화합물 1 이 0.2 중량% 인 조성물을 얻었다.
상기에서 얻은 발광층 형성을 마친 기판의 발광층 상에, 상기 조성물을 스핀 코트법에 의해 도포하여, 막두께 10 ㎚ 의 도포막을 얻었다.
이 도포막을 형성한 기판을 불활성 (질소) 분위기하에서, 100 ℃ 에서 10 분간 가열하여, 용매를 증발시킨 후, 실온까지 자연 냉각시켜, 공액 고분자 화합물 2 를 포함하는 층을 얻었다.
상기에서 얻은 공액 고분자 화합물 1 을 포함하는 층을 형성한 기판을 진공 장치 내에 삽입하고, 진공 증착법에 의해 Al 을 80 ㎚ 막 형성하고, 음극을 형성하여, 적층 구조체 1 을 제조하였다.
상기에서 얻은 음극 형성을 마친 기판을 진공 장치로부터 꺼내어, 불활성 (질소) 분위기하에서, 밀봉 유리와 2 액 혼합형 에폭시 수지로 밀봉하여, 전계 발광 소자 1 로 하였다.
실시예 16
공액 고분자 화합물 1 대신에, 공액 고분자 화합물 2 를 사용한 것 이외에는, 실시예 15 와 마찬가지로 조작하여, 전계 발광 소자 2 를 얻었다.
실시예 17
공액 고분자 화합물 1 대신에, 공액 고분자 화합물 3 을 사용한 것 이외에는, 실시예 15 와 마찬가지로 조작하여, 전계 발광 소자 3 을 얻었다.
실시예 18
공액 고분자 화합물 1 대신에, 공액 고분자 화합물 4 를 사용한 것 이외에는, 실시예 15 와 마찬가지로 조작하여, 전계 발광 소자 4 를 얻었다.
실시예 19
공액 고분자 화합물 1 대신에, 공액 고분자 화합물 5 를 사용한 것 이외에는, 실시예 15 와 마찬가지로 조작하여, 전계 발광 소자 5 를 얻었다.
실시예 20
공액 고분자 화합물을 포함하는 층의 형성 이외에는, 실시예 15 와 마찬가지로 조작하여, 전계 발광 소자 6 을 얻었다. 공액 고분자 화합물을 포함하는 층은, 메탄올과 테트라하이드로푸란을 체적비 1 : 1 로 혼합한 용매 (용해도 파라미터 11.0) 와 공액 고분자 화합물 6 을 혼합하여, 공액 고분자 화합물 6 이 0.2 중량% 인 조성물을 얻고, 발광층 형성한 기판의 발광층 상에, 그 조성물을 스핀 코트법에 의해 도포함으로써, 막두께 10 ㎚ 의 층을 형성하였다.
실시예 21
공액 고분자 화합물 1 대신에, 공액 고분자 화합물 7 을 사용한 것 이외에는, 실시예 15 와 마찬가지로 조작하여, 전계 발광 소자 7 을 얻었다.
실시예 22
공액 고분자 화합물 1 대신에, 공액 고분자 화합물 8 을 사용한 것 이외에는, 실시예 15 와 마찬가지로 조작하여, 전계 발광 소자 8 을 얻었다.
실시예 23
공액 고분자 화합물 1 대신에, 공액 고분자 화합물 9 를 사용한 것 이외에는, 실시예 15 와 마찬가지로 조작하여, 전계 발광 소자 9 를 얻었다.
실시예 24
공액 고분자 화합물 1 대신에, 공액 고분자 화합물 10 을 사용한 것 이외에는, 실시예 15 와 마찬가지로 조작하여, 전계 발광 소자 10 을 얻었다.
실시예 25
공액 고분자 화합물 1 대신에, 공액 고분자 화합물 11 을 사용한 것 이외에는, 실시예 15 와 마찬가지로 조작하여, 전계 발광 소자 11 을 얻었다.
실시예 26
공액 고분자 화합물 1 대신에, 공액 고분자 화합물 12 를 사용한 것 이외에는, 실시예 15 와 마찬가지로 조작하여, 전계 발광 소자 12 를 얻었다.
실시예 27
공액 고분자 화합물 1 대신에, 공액 고분자 화합물 13 을 사용한 것 이외에는, 실시예 15 와 마찬가지로 조작하여, 전계 발광 소자 13 을 얻었다.
실시예 28
공액 고분자 화합물 1 대신에, 공액 고분자 화합물 14 를 사용한 것 이외에는, 실시예 15 와 마찬가지로 조작하여, 전계 발광 소자 14 를 얻었다.
실시예 29
공액 고분자 화합물 1 대신에, 공액 고분자 화합물 15 를 사용한 것 이외에는, 실시예 15 와 마찬가지로 조작하여, 전계 발광 소자 15 를 얻었다.
비교예 1
공액 고분자 화합물 1 을 포함하는 층을 형성하지 않은 것 이외에는, 실시예 7 과 마찬가지로 조작하여, 전계 발광 소자 16 을 얻었다.
비교예 2
공액 고분자 화합물 1 대신에, 비공액 고분자 화합물 1 을 사용한 것 이외에는, 실시예 7 과 마찬가지로 조작하여, 전계 발광 소자 17 을 얻었다.
상기에서 얻어진 전계 발광 소자 1 ∼ 17 에, 10 V 의 순방향 전압을 인가하여, 발광 휘도와 발광 효율을 측정하였다. 결과를 표 1 에 나타낸다.
표 1 에서 분명한 바와 같이, 본 발명의 적층 구조체를 포함하는 전계 발광 소자는, 상기 적층 구조체를 포함하지 않는 전계 발광 소자에 비해, 발광 휘도가 현저하게 우수하다.
산업상 이용가능성
본 발명의 적층 구조체를 사용하면, 휘도가 높은 전계 발광 소자를 제조할 수 있으므로, 본 발명은 공업적으로 매우 유용하다.
Claims (29)
- 제 1 전극 및 제 2 전극과, 그 제 1 전극과 그 제 2 전극과의 사이에 발광층 혹은 전하 분리층을 가지며, 그 발광층 혹은 전하 분리층과 그 제 1 전극과의 사이에 공액 고분자 화합물을 포함하는 층을 가지며, 그 공액 고분자 화합물이 식 (1) 로 나타내지는 반복 단위, 식 (3) 으로 나타내지는 반복 단위 및 식 (5) 로 나타내지는 반복 단위로 이루어지는 군에서 선택되는 1 종 이상의 반복 단위를 갖는 적층 구조체.
(식 중, Ar1 은 2 가의 방향족기를 나타내고, R1 은 식 (2) 로 나타내지는 기를 포함하는 치환기를 나타내고, 그 Ar1 은 R1 이외의 치환기를 가지고 있어도 된다. n1 은 1 이상의 정수를 나타낸다. R1 이 복수 개 있는 경우, 그들은 동일하여도 되고 상이하여도 된다.)
(식 중, R2 는 치환기를 가지고 있어도 되는 2 가의 방향족기를 나타내고, Q1 은 치환기를 가지고 있어도 되는 2 가의 유기기를 나타내고, Y1 은 카르보 카티온, 암모늄 카티온, 포스포닐 카티온 또는 술포닐 카티온을 나타내고, M1 은 F-, Cl-, Br-, I-, OH-, RaSO3 -, RaCOO-, ClO-, ClO2 -, ClO3 -, ClO4 -, SCN-, CN-, NO3 -, SO4 2 -, HSO4 -, PO4 3 -, HPO4 2 -, H2PO4 -, BF4 - 또는 PF6 - 을 나타내고, Z1 은 금속 이온 또는 치환기를 가지고 있어도 되는 암모늄 이온을 나타내고, c1 은 0 또는 1 을 나타내고, n2 는 0 이상의 정수를 나타낸다. 단, c1 이 0 인 경우, n2 는 0 이다. a1 은 1 이상의 정수를 나타내고, b1 은 0 이상의 정수를 나타낸다. a1 및 b1 은, 식 (2) 로 나타내지는 치환기의 전하가 0 이 되도록 선택된다. Ra 는 치환기를 가지고 있어도 되는 탄소수 1 ∼ 30 의 알킬기 또는 치환기를 가지고 있어도 되는 탄소수 6 ∼ 50 의 아릴기를 나타낸다. Q1 이 복수 개 있는 경우, 그들은 동일하여도 되고 상이하여도 된다. M1 이 복수 개 있는 경우, 그들은 동일하여도 되고 상이하여도 된다. Z1 이 복수 개 있는 경우, 그들은 동일하여도 되고 상이하여도 된다.)
(식 중, Ar2 는 2 가의 방향족기를 나타내고, R3 은 식 (4) 로 나타내지는 기를 포함하는 치환기를 나타내고, 그 Ar2 는 R3 이외의 치환기를 가지고 있어도 된다. n3 은 1 이상의 정수를 나타낸다. R3 이 복수 개 있는 경우, 그들은 동일하여도 되고 상이하여도 된다.)
(식 중, R4 는 치환기를 가지고 있어도 되는 2 가의 방향족기를 나타내고, Q2 는 치환기를 가지고 있어도 되는 2 가의 유기기를 나타내고, Y2 는, -CO2 -, -SO3 -, -SO2 -, 또는 -PO3 2- 를 나타내고, M2 는 금속 카티온 또는 치환기를 가지고 있어도 되는 암모늄 카티온을 나타내고, Z2 는 F-, Cl-, Br-, I-, OH-, RbSO3 -, RbCOO-, ClO-, ClO2 -, ClO3 -, ClO4 -, SCN-, CN-, NO3 -, SO4 2-, HSO4 -, PO4 3-, HPO4 2-, H2PO4 -, BF4 - 또는 PF6 - 을 나타내고, c2 는 0 또는 1 을 나타내고, n4 는 0 이상의 정수를 나타낸다. 단, Y2 가 SO3 - 인 경우, n4 는 0 이다. a2 는 1 이상의 정수를 나타내고, b2 는 0 이상의 정수를 나타낸다. a2 및 b2 는, 식 (4) 로 나타내지는 치환기의 전하가 0 이 되도록 선택된다. Rb 는 치환기를 가지고 있어도 되는 탄소수 1 ∼ 30 의 알킬기 또는 치환기를 가지고 있어도 되는 탄소수 6 ∼ 50 의 아릴기를 나타낸다. Q2 가 복수 개 있는 경우, 그들은 동일하여도 되고 상이하여도 된다. M2 가 복수 개 있는 경우, 그들은 동일하여도 되고 상이하여도 된다. Z2 가 복수 개 있는 경우, 그들은 동일하여도 되고 상이하여도 된다.
(식 중, Ar3 은 2 가의 방향족기를 나타내고, R5 는 식 (6) 으로 나타내지는 기를 포함하는 치환기를 나타내고, 그 Ar3 은 R5 이외의 치환기를 가지고 있어도 된다. n5 는 1 이상의 정수를 나타낸다. R5 가 복수 개 있는 경우, 그들은 동일하여도 되고 상이하여도 된다.)
(식 중, R6 은 1 가의 방향족기를 나타내고, n6 은 0 이상의 정수를 나타내고, m1 은 1 이상의 정수를 나타낸다. Y3 은 -CN 또는 식 (7) ∼ (14) 로 나타내지는 기를 나타낸다. Y3 이 복수 개 있는 경우, 그들은 동일하여도 되고 상이하여도 된다. n6 이 복수 개 있는 경우, 그들은 동일하여도 되고 상이하여도 된다. 식 (6) 으로 나타내지는 기는, 헤테로 원자를 4 개 이상 포함한다.
(식 (7) ∼ (14) 중, R' 는 치환기를 가지고 있어도 되는 2 가의 탄화 수소기를 나타내고, R" 는 수소 원자, 치환기를 가지고 있어도 되는 1 가의 탄화 수소기, -COOH, -SO3H, -OH, -SH, -NRc 2, -CN 또는 -C(=O)NRc 2 를 나타내고, a3 은 0 이상의 정수를 나타내고, a4 는 3 ∼ 20 의 정수를 나타낸다. Rc 는 치환기를 가지고 있어도 되는 탄소수 1 ∼ 30 의 알킬기 또는 치환기를 가지고 있어도 되는 탄소수 6 ∼ 50 의 아릴기를 나타낸다. R'가 복수 개 있는 경우, 그들은 동일하여도 되고 상이하여도 된다.) - 제 2 항에 있어서,
Ar1 로 나타내지는 2 가의 방향족기가, 식 1, 식 38 또는 식 42 로 나타내지는 고리로부터 수소 원자를 2 개 제거한 기인 적층 구조체. - 제 4 항에 있어서,
Ar2 로 나타내지는 2 가의 방향족기가, 식 1, 식 38 또는 식 42 로 나타내지는 고리로부터 수소 원자를 2 개 제거한 기인 적층 구조체. - 제 6 항에 있어서,
Ar3 으로 나타내지는 2 가의 방향족기가, 식 1, 식 38 또는 식 42 로 나타내지는 고리로부터 수소 원자를 2 개 제거한 기인 적층 구조체. - 제 3 항에 있어서,
식 (1) 로 나타내지는 반복 단위가 식 (15) 로 나타내지는 반복 단위인 적층 구조체.
(식 중, R7 은 치환기를 가지고 있어도 되는 2 가의 방향족기를 나타내고, Q3 은 치환기를 가지고 있어도 되는 알킬렌기 또는 치환기를 가지고 있어도 되는 옥시알킬렌기를 나타내고, n2, Y1, M1, Z1, a1 및 b1 은 전술한 바와 같은 의미를 나타낸다. 복수 개 있는 n2, R7, Y1, M1, a1 및 b1 은 동일하여도 되고 상이하여도 된다. Z1 이 복수 개 있는 경우, 그들은 동일하여도 되고 상이하여도 된다. Q3 이 복수 개 있는 경우, 그들은 동일하여도 되고 상이하여도 된다.) - 제 5 항에 있어서,
식 (3) 으로 나타내지는 반복 단위가 식 (16) 으로 나타내지는 반복 단위인 적층 구조체.
(식 중, R8 은 치환기를 가지고 있어도 되는 2 가의 방향족기를 나타내고, Q4 는 치환기를 가지고 있어도 되는 알킬렌기 또는 치환기를 가지고 있어도 되는 옥시알킬렌기이며, n4, Y2, M2, Z2, a2 및 b2 는 전술한 바와 같은 의미를 나타낸다. 복수 개 있는 n4, R8, Y2, M2, a2 및 b2 는 동일하여도 되고 상이하여도 된다. Z2 가 복수 개 있는 경우, 그들은 동일하여도 되고 상이하여도 된다. Q4 가 복수 개 있는 경우, 그들은 동일하여도 되고 상이하여도 된다.) - 제 1 항 내지 제 10 항 중 어느 한 항에 있어서,
공액 고분자 화합물이 추가로 식 (20) 으로 나타내지는 반복 단위를 갖는 공액 고분자 화합물인 적층 구조체.
(식 중, Ar4 는 치환기를 가지고 있어도 되는 2 가의 방향족기 또는 치환기를 가지고 있어도 되는 2 가의 방향족 아민 잔기를 나타낸다. X 는 치환기를 가지고 있어도 되는 이미노기, 치환기를 가지고 있어도 되는 실릴렌기, 치환기를 가지고 있어도 되는 에테닐렌기 또는 에티닐렌기를 나타내고, m2 및 m3 은 각각 독립적으로, 0 또는 1 을 나타내고, m2 와 m3 의 적어도 하나는 1 이다.) - 제 1 항 내지 제 11 항 중 어느 한 항에 있어서,
공액 고분자 화합물 중의 식 (1) 로 나타내지는 반복 단위, 식 (3) 으로 나타내지는 반복 단위 및 식 (5) 로 나타내지는 반복 단위의 수의 합계가, 그 공액 고분자 화합물이 갖는 전체 반복 단위의 수의 합계를 100 몰로 한 경우, 15 ∼ 100 몰인 적층 구조체. - 제 1 항 내지 제 12 항 중 어느 한 항에 있어서,
공액 고분자 화합물의 수 평균 분자량이 5×103 이상 5×106 이하인 적층 구조체. - 제 1 항 내지 제 13 항 중 어느 한 항에 있어서,
공액 고분자 화합물의 최저 비점유 분자 궤도 (LUMO) 의 궤도 에너지가, -5.0 eV 이상 -2.0 eV 이하인 적층 구조체. - 제 1 항 내지 제 14 항 중 어느 한 항에 있어서,
공액 고분자 화합물의 최고 점유 분자 궤도 (HOMO) 의 궤도 에너지가, -6.0 eV 이상 -3.0 eV 이하인 적층 구조체. - 제 1 항 내지 제 15 항 중 어느 한 항에 있어서,
제 1 전극이 음극인 적층 구조체. - 제 1 전극 및 제 2 전극과, 그 제 1 전극과 그 제 2 전극과의 사이에 발광층 혹은 전하 분리층을 가지며, 그 발광층 혹은 전하 분리층과 그 제 1 전극과의 사이에 용해도 파라미터가 9.3 미만인 용매에 대해 불용인 공액 고분자 화합물을 포함하는 층을 갖는 적층 구조체.
- 제 1 항 내지 제 17 항 중 어느 한 항에 기재된 적층 구조체를 포함하는 전계 발광 소자.
- 제 1 항 내지 제 17 항 중 어느 한 항에 기재된 적층 구조체를 포함하는 광전 변환 소자.
- 식 (15) 로 나타내지는 반복 단위를 포함하는 공액 고분자 화합물.
(식 중, R7 은 치환기를 가지고 있어도 되는 2 가의 방향족기를 나타낸다. Q3 은 치환기를 가지고 있어도 되는 알킬렌기 또는 치환기를 가지고 있어도 되는 옥시알킬렌기를 나타내고, Y1 은 카르보 카티온, 암모늄 카티온, 포스포닐 카티온 또는 술포닐 카티온을 나타내고, M1 은 F-, Cl-, Br-, I-, OH-, RaSO3 -, RaCOO-, ClO-, ClO2 -, ClO3 -, ClO4 -, SCN-, CN-, NO3 -, SO4 2 -, HSO4 -, PO4 3 -, HPO4 2 -, H2PO4 -, BF4 - 또는 PF6 - 을 나타내고, Z1 은 금속 이온 또는 치환기를 가지고 있어도 되는 암모늄 이온을 나타내고, n2 는 0 이상의 정수를 나타낸다. a1 은 1 이상의 정수를 나타내고, b1 은 0 이상의 정수를 나타낸다. a1 및 b1 은 식 (15) 로 나타내지는 반복 단위의 전하가 0 이 되도록 선택된다. Ra 는 치환기를 가지고 있어도 되는 탄소수 1 ∼ 30 의 알킬기 또는 치환기를 가지고 있어도 되는 탄소수 6 ∼ 50 의 아릴기를 나타낸다. 복수 개 있는 R7, Y1, M1, a1, b1, n2 는 동일하여도 되고 상이하여도 된다. Z1 이 복수 개 있는 경우, 그들은 동일하여도 되고 상이하여도 된다. Q3 이 복수 개 있는 경우, 그들은 동일하여도 되고 상이하여도 된다.) - 식 (16) 으로 나타내지는 반복 단위를 포함하는 공액 고분자 화합물.
(식 중, R8 은 치환기를 가지고 있어도 되는 2 가의 방향족기를 나타낸다. Q4 는 치환기를 가지고 있어도 되는 알킬렌기 또는 치환기를 가지고 있어도 되는 옥시알킬렌기를 나타내고, Y2 는 -CO2 -, -SO3 -, -SO2 - 또는 -PO3 - 을 나타내고, M2 는 금속 카티온 또는 치환기를 가지고 있어도 되는 암모늄 카티온을 나타내고, Z2 는 F-, Cl-, Br-, I-, OH-, RbSO3 -, RbCOO-, ClO-, ClO2 -, ClO3 -, ClO4 -, SCN-, CN-, NO3 -, SO4 2 -, HSO4 -, PO4 3 -, HPO4 2 -, H2PO4 -, BF4 - 또는 PF6 - 을 나타내고, n4 는 0 이상의 정수를 나타낸다. 단, Y2 가 SO3-인 경우, n4 는 0 이다. a2 는 1 이상의 정수를 나타내고, b2 는 0 이상의 정수를 나타낸다. a2 및 b2 는 식 (16) 으로 나타내지는 반복 단위의 전하가 0 이 되도록 선택된다. Rb 는 치환기를 가지고 있어도 되는 탄소수 1 ∼ 30 의 알킬기 또는 치환기를 가지고 있어도 되는 탄소수 6 ∼ 50 의 아릴기를 나타낸다. 복수 개 있는 R8, Y2, M2, a2, b2, n4 는 동일하여도 되고 상이하여도 된다. Z2 가 복수 개 있는 경우, 그들은 동일하여도 되고 상이하여도 된다. Q4 가 복수 개 있는 경우, 그들은 동일하여도 되고 상이하여도 된다.) - 식 (17) 로 나타내지는 반복 단위를 포함하는 공액 고분자 화합물.
(식 중, R6 은 1 가의 방향족기를 나타내고, n6 은 0 이상의 정수를 나타내고, m1 은 1 이상의 정수를 나타낸다. Y3 은 -CN 또는 식 (7) ∼ (14) 로 나타내지는 기를 나타낸다. 복수 개 있는 R6, m1, n6, Y3 은 동일하여도 되고 상이하여도 된다.
(식 (7) ∼ (14) 중, R' 는 치환기를 가지고 있어도 되는 2 가의 탄화 수소기를 나타내고, R" 는 수소 원자, 치환기를 가지고 있어도 되는 1 가의 탄화 수소기, -COOH, -SO3H, -OH, -SH, -NRc 2, -CN 또는 -C(=O)NRc 2 를 나타내고, a3 은 0 이상의 정수를 나타내고, a4 는 3 ∼ 20 의 정수를 나타낸다. Rc 는 치환기를 가지고 있어도 되는 탄소수 1 ∼ 30 의 알킬기 또는 치환기를 가지고 있어도 되는 탄소수 6 ∼ 50 의 아릴기를 나타낸다. R'가 복수 개 있는 경우, 그들은 동일하여도 되고 상이하여도 된다.) - 제 20 항 또는 제 23 항에 있어서
공액 고분자 화합물 중의 식 (15) 로 나타내지는 반복 단위의 수의 합계가, 그 공액 고분자 화합물이 갖는 전체 반복 단위의 수의 합계를 100 몰로 한 경우, 15 ∼ 100 몰인 공액 고분자 화합물. - 제 21 항 또는 제 23 항에 있어서
공액 고분자 화합물 중의 식 (16) 으로 나타내지는 반복 단위의 수의 합계가, 그 공액 고분자 화합물이 갖는 전체 반복 단위의 수의 합계를 100 몰로 한 경우, 15 ∼ 100 몰인 공액 고분자 화합물. - 제 22 항 또는 제 23 항에 있어서
공액 고분자 화합물 중의 식 (17) 로 나타내지는 반복 단위의 수의 합계가, 그 공액 고분자 화합물이 갖는 전체 반복 단위의 수의 합계를 100 몰로 한 경우, 15 ∼ 100 몰인 공액 고분자 화합물. - 제 20 항 내지 제 26 항 중 어느 한 항에 있어서,
수 평균 분자량이 5×103 이상 1×108 이하인 공액 고분자 화합물. - 제 20 항 내지 제 27 항 중 어느 한 항에 있어서,
최저 비점유 분자 궤도 (LUMO) 의 궤도 에너지가, -5.0 eV 이상 -2.0 eV 이하인 공액 고분자 화합물. - 제 20 항 내지 제 28 항 중 어느 한 항에 있어서,
최고 점유 분자 궤도 (HOMO) 의 궤도 에너지가, -6.0 eV 이상 -3.0 eV 이하인 공액 고분자 화합물.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008057570 | 2008-03-07 | ||
| JPJP-P-2008-057570 | 2008-03-07 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20110000731A true KR20110000731A (ko) | 2011-01-05 |
| KR101626994B1 KR101626994B1 (ko) | 2016-06-03 |
Family
ID=41056186
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020107021391A KR101626994B1 (ko) | 2008-03-07 | 2009-03-05 | 적층 구조체 |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US8951646B2 (ko) |
| EP (2) | EP2846374B1 (ko) |
| JP (2) | JP5514458B2 (ko) |
| KR (1) | KR101626994B1 (ko) |
| CN (1) | CN102017219B (ko) |
| TW (1) | TWI496689B (ko) |
| WO (1) | WO2009110642A1 (ko) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20140012976A (ko) * | 2011-02-21 | 2014-02-04 | 스미또모 가가꾸 가부시키가이샤 | 유기 전계 발광 소자의 제조 방법 |
Families Citing this family (62)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR101626994B1 (ko) * | 2008-03-07 | 2016-06-03 | 스미또모 가가꾸 가부시끼가이샤 | 적층 구조체 |
| WO2011040388A1 (ja) * | 2009-09-30 | 2011-04-07 | 住友化学株式会社 | 積層構造体、重合体、電界発光素子及び光電変換素子 |
| CN102576804A (zh) * | 2009-10-29 | 2012-07-11 | 住友化学株式会社 | 有机光电转换元件及其制造方法 |
| EP2518111B1 (en) | 2009-12-25 | 2019-03-13 | Sumitomo Chemical Company, Limited | Composition and luminescent element obtained using same |
| CZ309346B6 (cs) | 2010-11-01 | 2022-09-14 | Varroc Lighting Systems, s.r.o. | Světlovodný modul se seřiditelným osvětlením povrchu obrysu |
| JP5876239B2 (ja) * | 2010-06-29 | 2016-03-02 | 住友化学株式会社 | 発光素子、その製造方法及び光電変換素子 |
| TW201220574A (en) * | 2010-07-21 | 2012-05-16 | Sumitomo Chemical Co | Method for manufacturing organic electroluminescence display device and organic electroluminescence display device |
| US8963422B2 (en) * | 2010-07-21 | 2015-02-24 | Sumitomo Chemical Company, Limited | Method for manufacturing organic light-emitting device and organic light-emitting device |
| EP2597934A4 (en) * | 2010-07-21 | 2014-07-16 | Sumitomo Chemical Co | METHOD OF MANUFACTURING AN ORGANIC EL-ELEMENT |
| WO2012011471A1 (ja) * | 2010-07-21 | 2012-01-26 | 住友化学株式会社 | 有機エレクトロルミネッセンスディスプレイ装置の製造方法及び有機エレクトロルミネッセンスディスプレイ装置 |
| EP2597696A4 (en) * | 2010-07-21 | 2018-01-10 | Sumitomo Chemical Company Limited | Organic el element |
| EP2597933B1 (en) * | 2010-07-21 | 2019-06-12 | Sumitomo Chemical Company, Limited | Manufacturing method for organic electroluminescence element |
| JP5653122B2 (ja) * | 2010-08-10 | 2015-01-14 | 住友化学株式会社 | 有機エレクトロルミネッセンス素子およびその製造方法 |
| JP5750247B2 (ja) * | 2010-08-31 | 2015-07-15 | 住友化学株式会社 | 有機薄膜トランジスタ及びその製造方法 |
| JP5875820B2 (ja) * | 2010-10-08 | 2016-03-02 | 住友化学株式会社 | 発光素子及び光電変換素子、並びにこれらの製造方法 |
| JP2012084306A (ja) * | 2010-10-08 | 2012-04-26 | Sumitomo Chemical Co Ltd | 有機el装置 |
| WO2012053444A1 (ja) * | 2010-10-22 | 2012-04-26 | 住友化学株式会社 | 環状構造を有する有機化合物 |
| JP2012114188A (ja) * | 2010-11-24 | 2012-06-14 | Sumitomo Chemical Co Ltd | 発光装置 |
| GB2486203A (en) | 2010-12-06 | 2012-06-13 | Cambridge Display Tech Ltd | Transition metal oxide doped interface by deposition and drying of precursor |
| GB2486202A (en) | 2010-12-06 | 2012-06-13 | Cambridge Display Tech Ltd | Adhesion layer for solution-processed transition metal oxides on inert metal contacts of organic thin film transistors. |
| GB2487207B (en) * | 2011-01-12 | 2013-07-31 | Cambridge Display Tech Ltd | Electroluminescence |
| JP5899635B2 (ja) * | 2011-03-23 | 2016-04-06 | 住友化学株式会社 | 有機el素子 |
| WO2012133229A1 (ja) * | 2011-03-28 | 2012-10-04 | 住友化学株式会社 | 電子デバイス及び高分子化合物 |
| WO2012133462A1 (ja) * | 2011-03-28 | 2012-10-04 | 住友化学株式会社 | 電子デバイス、高分子化合物 |
| EP2692796B1 (en) | 2011-03-28 | 2019-07-10 | Sumitomo Chemical Co., Ltd | Composition |
| CN103460428B (zh) * | 2011-03-28 | 2016-09-07 | 住友化学株式会社 | 电子设备、高分子化合物、有机化合物及高分子化合物的制备方法 |
| JP2012216815A (ja) * | 2011-03-28 | 2012-11-08 | Sumitomo Chemical Co Ltd | 電子デバイス、高分子化合物 |
| WO2012133165A1 (ja) * | 2011-03-28 | 2012-10-04 | 住友化学株式会社 | 発光素子及びその製造方法 |
| GB201110770D0 (en) | 2011-06-24 | 2011-08-10 | Cambridge Display Tech Ltd | Process for controlling the acceptor strength of solution-processed transition metal oxides for OLED applications |
| US9520569B2 (en) | 2011-10-17 | 2016-12-13 | Sumitomo Chemical Company, Limited | Aryl compounds for application in a highly polar solvent |
| KR102093793B1 (ko) * | 2011-10-31 | 2020-03-27 | 삼성전자주식회사 | 광 다이오드 |
| WO2013079676A1 (en) | 2011-11-30 | 2013-06-06 | Novaled Ag | Organic electronic device |
| JP5939423B2 (ja) * | 2012-03-01 | 2016-06-22 | 日立化成株式会社 | ポリマー又はオリゴマー、及びこれを用いた有機エレクトロニクス素子 |
| EP2832761B1 (en) | 2012-03-27 | 2020-11-18 | Sumitomo Chemical Company, Limited | Polymer compound and light emitting element using same |
| KR101950836B1 (ko) * | 2012-05-22 | 2019-02-22 | 엘지디스플레이 주식회사 | 유기 발광 소자 및 그의 제조 방법 |
| JP6065909B2 (ja) * | 2012-07-11 | 2017-01-25 | コニカミノルタ株式会社 | タッチパネル用透明電極、タッチパネル、および表示装置 |
| GB2505893A (en) | 2012-09-13 | 2014-03-19 | Cambridge Display Tech Ltd | Compounds for use in organic optoelectronic devices |
| JP6167549B2 (ja) * | 2013-02-18 | 2017-07-26 | 住友化学株式会社 | 電極形成用の組成物 |
| GB2513378A (en) * | 2013-04-25 | 2014-10-29 | Cambridge Display Tech Ltd | Device |
| US10103384B2 (en) | 2013-07-09 | 2018-10-16 | Evonik Degussa Gmbh | Electroactive polymers, manufacturing process thereof, electrode and use thereof |
| DE102014003300A1 (de) | 2014-03-07 | 2015-09-10 | Evonik Degussa Gmbh | Neue Tetracyanoanthrachinondimethanpolymere und deren Verwendung |
| DE102014004760A1 (de) | 2014-03-28 | 2015-10-01 | Evonik Degussa Gmbh | Neue 9,10-Bis(1,3-dithiol-2-yliden)-9,10-dihydroanthracenpolymere und deren Verwendung |
| WO2015159932A1 (ja) * | 2014-04-18 | 2015-10-22 | 住友化学株式会社 | 発光素子およびそれに用いる高分子化合物 |
| GB2539404A (en) * | 2015-06-15 | 2016-12-21 | Cambridge Display Tech Ltd | Organic diode |
| GB2545499A (en) * | 2015-12-18 | 2017-06-21 | Cambridge Display Tech Ltd | Dopant, charge transfer salt and organic electronic device |
| EP3262094B1 (de) | 2015-08-26 | 2018-12-26 | Evonik Degussa GmbH | Verwendung bestimmter polymere als ladungsspeicher |
| WO2017032583A1 (de) | 2015-08-26 | 2017-03-02 | Evonik Degussa Gmbh | Verwendung bestimmter polymere als ladungsspeicher |
| CN108292709B (zh) | 2015-12-07 | 2020-10-30 | 住友化学株式会社 | 发光元件 |
| KR102345329B1 (ko) | 2016-01-29 | 2022-01-03 | 스미또모 가가꾸 가부시키가이샤 | 조성물, 인광 발광성 화합물 및 발광 소자 |
| KR102146324B1 (ko) | 2016-06-02 | 2020-08-21 | 에보니크 오퍼레이션즈 게엠베하 | 전극 물질을 제조하는 방법 |
| TWI686415B (zh) | 2016-08-05 | 2020-03-01 | 德商贏創運營有限公司 | 含有噻嗯之聚合物作為電荷儲存裝置之用途 |
| WO2018046387A1 (de) | 2016-09-06 | 2018-03-15 | Evonik Degussa Gmbh | Verfahren zur verbesserten oxidation sekundärer amingruppen |
| JP6836908B2 (ja) | 2017-01-10 | 2021-03-03 | 住友化学株式会社 | 有機デバイスの製造方法 |
| CN110235266B (zh) | 2017-01-27 | 2021-04-02 | 住友化学株式会社 | 组合物和使用该组合物得到的发光元件 |
| EP3576175B1 (en) | 2017-01-27 | 2021-06-16 | Sumitomo Chemical Company Limited | Composition, film using said composition, and method for producing light emitting element |
| KR20190141210A (ko) | 2017-04-27 | 2019-12-23 | 스미또모 가가꾸 가부시키가이샤 | 발광 소자 |
| CN107204400A (zh) * | 2017-05-24 | 2017-09-26 | 京东方科技集团股份有限公司 | 显示基板及其制作方法以及显示装置 |
| JPWO2019082771A1 (ja) | 2017-10-27 | 2020-11-26 | 住友化学株式会社 | 発光素子 |
| US20200266378A1 (en) | 2017-10-27 | 2020-08-20 | Sumitomo Chemical Company, Limited | Light-emitting element |
| WO2020071276A1 (ja) * | 2018-10-01 | 2020-04-09 | コニカミノルタ株式会社 | 有機エレクトロルミネッセンス素子用の混合組成物 |
| JP7216754B2 (ja) | 2020-03-31 | 2023-02-01 | 住友化学株式会社 | 組成物及びそれを含有する発光素子 |
| GB2605405B (en) * | 2021-03-30 | 2024-04-03 | Sumitomo Chemical Co | Polymer |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2007058368A1 (ja) * | 2005-11-18 | 2007-05-24 | Sumitomo Chemical Company, Limited | 高分子化合物およびそれを用いた高分子発光素子 |
| US20080015269A1 (en) * | 2006-04-17 | 2008-01-17 | Bazan Guillermo C | Hybrid polymer light-emitting devices |
| US20080020208A1 (en) * | 2006-06-07 | 2008-01-24 | Lee Tae-Woo | Conducting polymer composition, conductive film formed using the conducting polymer composition, and electronic device including the conductive film |
| JP2008047610A (ja) * | 2006-08-11 | 2008-02-28 | Seiko Epson Corp | 有機エレクトロルミネッセンス装置、有機エレクトロルミネッセンス装置の製造方法並びに電子機器 |
Family Cites Families (53)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US573636A (en) | 1896-12-22 | Car-truck | ||
| US4356429A (en) | 1980-07-17 | 1982-10-26 | Eastman Kodak Company | Organic electroluminescent cell |
| JPS6370257A (ja) | 1986-09-12 | 1988-03-30 | Fuji Xerox Co Ltd | 電子写真用電荷輸送材料 |
| JPS63175860A (ja) | 1987-01-16 | 1988-07-20 | Fuji Xerox Co Ltd | 電子写真感光体 |
| JP2651237B2 (ja) | 1989-02-10 | 1997-09-10 | 出光興産株式会社 | 薄膜エレクトロルミネッセンス素子 |
| JPH02135359A (ja) | 1988-11-16 | 1990-05-24 | Fuji Xerox Co Ltd | 電子写真感光体 |
| JPH02135361A (ja) | 1988-11-16 | 1990-05-24 | Fuji Xerox Co Ltd | 電子写真感光体 |
| JPH0337992A (ja) | 1989-07-04 | 1991-02-19 | Idemitsu Kosan Co Ltd | 有機エレクトロルミネッセンス素子の製造方法 |
| JPH03152184A (ja) | 1989-11-08 | 1991-06-28 | Nec Corp | 有機薄膜el素子 |
| JPH07110940B2 (ja) | 1991-06-05 | 1995-11-29 | 住友化学工業株式会社 | 有機エレクトロルミネッセンス素子 |
| JPH05263073A (ja) | 1992-03-17 | 1993-10-12 | Sumitomo Chem Co Ltd | 有機エレクトロルミネッセンス素子 |
| DE4436773A1 (de) | 1994-10-14 | 1996-04-18 | Hoechst Ag | Konjugierte Polymere mit Spirozentren und ihre Verwendung als Elektrolumineszenzmaterialien |
| DE4442052A1 (de) | 1994-11-25 | 1996-05-30 | Hoechst Ag | Konjugierte Polymere mit Hetero-Spiroatomen und ihre Verwendung als Elektrolumineszenzmaterialien |
| JP3367064B2 (ja) | 1995-02-01 | 2003-01-14 | 住友化学工業株式会社 | 高分子蛍光体とその製造方法および有機エレクトロルミネッセンス素子 |
| EP0848739A1 (de) | 1995-09-04 | 1998-06-24 | Hoechst Research & Technology Deutschland GmbH & Co. KG | Polymere mit triarylamin-einheiten als elektrolumineszenzmaterialien |
| JP3760491B2 (ja) | 1995-10-16 | 2006-03-29 | 住友化学株式会社 | 高分子蛍光体、その製造方法及び有機エレクトロルミネッセンス素子 |
| EP0885461B1 (en) * | 1996-03-04 | 2003-08-13 | DuPont Displays, Inc. | Polyfluorenes as materials for photoluminescence and electroluminescence |
| DE19652261A1 (de) | 1996-12-16 | 1998-06-18 | Hoechst Ag | Arylsubstituierte Poly(p-arylenvinylene), Verfahren zur Herstellung und deren Verwendung in Elektroluminszenzbauelementen |
| US6309763B1 (en) | 1997-05-21 | 2001-10-30 | The Dow Chemical Company | Fluorene-containing polymers and electroluminescent devices therefrom |
| JPH10324870A (ja) | 1997-05-23 | 1998-12-08 | Sumitomo Chem Co Ltd | 高分子蛍光体および有機エレクトロルミネッセンス素子 |
| JP4366727B2 (ja) | 1997-07-22 | 2009-11-18 | 住友化学株式会社 | 正孔輸送性高分子とその製造方法および有機エレクトロルミネッセンス素子 |
| KR100243089B1 (ko) | 1997-07-29 | 2000-02-01 | 정선종 | 이오노머를전하수송층으로하는고분자/유기물전기발광소자의구조및그제조방법 |
| US5777070A (en) | 1997-10-23 | 1998-07-07 | The Dow Chemical Company | Process for preparing conjugated polymers |
| GB9805476D0 (en) | 1998-03-13 | 1998-05-13 | Cambridge Display Tech Ltd | Electroluminescent devices |
| GB2340304A (en) | 1998-08-21 | 2000-02-16 | Cambridge Display Tech Ltd | Organic light emitters |
| DE19846768A1 (de) | 1998-10-10 | 2000-04-20 | Aventis Res & Tech Gmbh & Co | Konjugierte Polymere enthaltend 2,7-Fluorenyleinheiten mit verbesserten Eigenschaften |
| GB2348316A (en) | 1999-03-26 | 2000-09-27 | Cambridge Display Tech Ltd | Organic opto-electronic device |
| TW484341B (en) | 1999-08-03 | 2002-04-21 | Sumitomo Chemical Co | Polymeric fluorescent substance and polymer light emitting device |
| AU7432400A (en) | 1999-09-16 | 2001-04-17 | Cambridge Display Technology Limited | Preparation of benzenediboronic acid via a disilylated aryl-intermediate |
| KR100337021B1 (ko) | 1999-10-18 | 2002-05-16 | 윤덕용 | 이오노머형 발광 고분자 및 이를 이용한 전기 발광 소자 |
| KR20010095429A (ko) | 2000-03-30 | 2001-11-07 | 윤덕용 | 단일 이온 전도체를 전자 혹은 정공 주입층으로 이용하는유기/고분자 전기 발광 소자 |
| GB0111549D0 (en) * | 2001-05-11 | 2001-07-04 | Cambridge Display Tech Ltd | Polymers, their preparation and uses |
| JP2003077673A (ja) | 2001-06-19 | 2003-03-14 | Honda Motor Co Ltd | 有機エレクトロルミネッセンス素子 |
| KR100946005B1 (ko) * | 2002-05-10 | 2010-03-09 | 캠브리지 디스플레이 테크놀로지 리미티드 | 중합체, 그의 제조 및 용도 |
| JP4461762B2 (ja) | 2002-10-30 | 2010-05-12 | 住友化学株式会社 | 高分子化合物およびそれを用いた高分子発光素子 |
| TWI365218B (en) | 2003-11-17 | 2012-06-01 | Sumitomo Chemical Co | Conjugated oligomers or polymers based on crosslinkable arylamine compounds |
| CN100490206C (zh) | 2003-12-25 | 2009-05-20 | 华南理工大学 | 有机/高分子发光二极管 |
| EP1709140A4 (en) | 2004-01-30 | 2012-06-27 | Sk Innovation Co Ltd | ORGANIC ELECTROLUMINESCENCE POLYMER WITH 9,9-DI (FLUORENYL) -2,7-FLUORENYL UNIT AND ORGANIC ELECTROLUMINESCENZING DEVICE PREPARED THEREWITH |
| KR101170168B1 (ko) | 2004-01-30 | 2012-07-31 | 에스케이이노베이션 주식회사 | 9,9-디(플루오레닐)-2,7-플루오레닐 단위를 함유하는 유기전기발광고분자 및 이를 이용한 전기발광소자 |
| WO2005121203A1 (ja) | 2004-04-14 | 2005-12-22 | Kanazawa University Technology Licensing Organization Ltd. | 高い蛍光量子収率を示す共役系高分子と金属塩とのハイブリッド体、その製造方法及びそれを用いた蛍光発光材料 |
| JP5588096B2 (ja) * | 2004-10-11 | 2014-09-10 | ケンブリッジ ディスプレイ テクノロジー リミテッド | 極性半導体正孔輸送材料 |
| CN101061089B (zh) | 2004-12-03 | 2011-07-27 | 住友化学株式会社 | 水杨酸酯取代的共轭聚合物及器件 |
| CN100440572C (zh) | 2005-05-31 | 2008-12-03 | 华南理工大学 | 一种有机小分子或高分子顶发射发光器件 |
| GB0514476D0 (en) * | 2005-07-14 | 2005-08-17 | Cambridge Display Tech Ltd | Conductive polymer compositions in opto-electrical devices |
| US20100176377A1 (en) * | 2005-11-18 | 2010-07-15 | Sumitomo Chemical Company, Limited | Polymeric compound and polymeric electroluminescence element using the same |
| JP5217153B2 (ja) | 2005-11-18 | 2013-06-19 | 住友化学株式会社 | 高分子化合物およびそれを用いた高分子発光素子 |
| KR101243919B1 (ko) * | 2006-01-27 | 2013-03-14 | 삼성디스플레이 주식회사 | 전도성 고분자 조성물 및 이를 채용한 유기 광전 소자 |
| WO2008016091A1 (fr) * | 2006-07-31 | 2008-02-07 | Sumitomo Chemical Company, Limited | Composé polymère et dispositif luminescent polymère l'utilisant |
| JP2008056910A (ja) * | 2006-07-31 | 2008-03-13 | Sumitomo Chemical Co Ltd | 高分子化合物及びそれを用いた高分子発光素子 |
| JP5162868B2 (ja) | 2006-09-20 | 2013-03-13 | 住友化学株式会社 | 高分子発光素子及び有機トランジスタ並びにそれらに有用な組成物 |
| JP5144938B2 (ja) | 2007-02-02 | 2013-02-13 | 住友化学株式会社 | 高分子発光素子、高分子化合物、組成物、液状組成物及び導電性薄膜 |
| KR101626994B1 (ko) * | 2008-03-07 | 2016-06-03 | 스미또모 가가꾸 가부시끼가이샤 | 적층 구조체 |
| JP5428034B2 (ja) | 2009-01-23 | 2014-02-26 | 住友化学株式会社 | 電子素子およびそれに有用なビピリジニウム骨格を有する高分子化合物 |
-
2009
- 2009-03-05 KR KR1020107021391A patent/KR101626994B1/ko active IP Right Grant
- 2009-03-05 CN CN2009801162956A patent/CN102017219B/zh not_active Expired - Fee Related
- 2009-03-05 US US12/921,108 patent/US8951646B2/en not_active Expired - Fee Related
- 2009-03-05 TW TW098107085A patent/TWI496689B/zh not_active IP Right Cessation
- 2009-03-05 EP EP14186012.2A patent/EP2846374B1/en active Active
- 2009-03-05 WO PCT/JP2009/054708 patent/WO2009110642A1/ja active Application Filing
- 2009-03-05 EP EP09717451.0A patent/EP2249411A4/en not_active Withdrawn
- 2009-03-09 JP JP2009054593A patent/JP5514458B2/ja active Active
-
2014
- 2014-03-28 JP JP2014067946A patent/JP5790819B2/ja active Active
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2007058368A1 (ja) * | 2005-11-18 | 2007-05-24 | Sumitomo Chemical Company, Limited | 高分子化合物およびそれを用いた高分子発光素子 |
| US20080015269A1 (en) * | 2006-04-17 | 2008-01-17 | Bazan Guillermo C | Hybrid polymer light-emitting devices |
| US20080020208A1 (en) * | 2006-06-07 | 2008-01-24 | Lee Tae-Woo | Conducting polymer composition, conductive film formed using the conducting polymer composition, and electronic device including the conductive film |
| JP2008047610A (ja) * | 2006-08-11 | 2008-02-28 | Seiko Epson Corp | 有機エレクトロルミネッセンス装置、有機エレクトロルミネッセンス装置の製造方法並びに電子機器 |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20140012976A (ko) * | 2011-02-21 | 2014-02-04 | 스미또모 가가꾸 가부시키가이샤 | 유기 전계 발광 소자의 제조 방법 |
Also Published As
| Publication number | Publication date |
|---|---|
| EP2846374B1 (en) | 2019-11-06 |
| EP2249411A1 (en) | 2010-11-10 |
| WO2009110642A1 (ja) | 2009-09-11 |
| JP2014194017A (ja) | 2014-10-09 |
| US20110006294A1 (en) | 2011-01-13 |
| CN102017219A (zh) | 2011-04-13 |
| US8951646B2 (en) | 2015-02-10 |
| JP5790819B2 (ja) | 2015-10-07 |
| KR101626994B1 (ko) | 2016-06-03 |
| JP5514458B2 (ja) | 2014-06-04 |
| TWI496689B (zh) | 2015-08-21 |
| JP2009239279A (ja) | 2009-10-15 |
| CN102017219B (zh) | 2013-03-27 |
| TW200946340A (en) | 2009-11-16 |
| EP2846374A1 (en) | 2015-03-11 |
| EP2249411A4 (en) | 2014-03-26 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5790819B2 (ja) | 共役高分子化合物 | |
| KR101704090B1 (ko) | 적층 구조체, 중합체, 전계 발광 소자 및 광전 변환 소자 | |
| JP6046361B2 (ja) | 電子デバイス、高分子化合物 | |
| KR101320711B1 (ko) | 고분자 재료 및 고분자 발광 소자 | |
| US9306170B2 (en) | Electronic device and polymer compound | |
| JP2012216811A (ja) | 電子デバイス及び高分子化合物 | |
| KR20110041463A (ko) | 공중합체 및 그것을 이용한 고분자 발광 소자 | |
| JP2004002703A (ja) | 高分子化合物およびそれを用いた高分子発光素子 | |
| WO2012133462A1 (ja) | 電子デバイス、高分子化合物 | |
| EP2692796B1 (en) | Composition | |
| KR20080036631A (ko) | 고분자 화합물 및 이것을 사용한 고분자 발광 소자 | |
| KR101278894B1 (ko) | 블록 공중합체 및 고분자 발광소자 | |
| JP5428034B2 (ja) | 電子素子およびそれに有用なビピリジニウム骨格を有する高分子化合物 | |
| WO2012128334A1 (ja) | 有機el素子 | |
| KR20140012976A (ko) | 유기 전계 발광 소자의 제조 방법 | |
| JP2009013413A (ja) | 高分子化合物およびそれを用いた高分子発光素子 | |
| JP2004162011A (ja) | 高分子化合物およびそれを用いた高分子発光素子 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A201 | Request for examination | ||
| E902 | Notification of reason for refusal | ||
| E902 | Notification of reason for refusal | ||
| E701 | Decision to grant or registration of patent right | ||
| FPAY | Annual fee payment |
Payment date: 20190516 Year of fee payment: 4 |