WO2014065176A1 - 重合性化合物、重合性組成物、高分子、及び光学異方体 - Google Patents
重合性化合物、重合性組成物、高分子、及び光学異方体 Download PDFInfo
- Publication number
- WO2014065176A1 WO2014065176A1 PCT/JP2013/078103 JP2013078103W WO2014065176A1 WO 2014065176 A1 WO2014065176 A1 WO 2014065176A1 JP 2013078103 W JP2013078103 W JP 2013078103W WO 2014065176 A1 WO2014065176 A1 WO 2014065176A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- group
- carbon atoms
- substituent
- polymerizable compound
- formula
- Prior art date
Links
- 0 C[*@](*)C(*)=NN(*)* Chemical compound C[*@](*)C(*)=NN(*)* 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D277/00—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings
- C07D277/02—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings
- C07D277/20—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D277/00—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings
- C07D277/02—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings
- C07D277/20—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members
- C07D277/32—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D277/38—Nitrogen atoms
- C07D277/50—Nitrogen atoms bound to hetero atoms
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F222/00—Copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and at least one being terminated by a carboxyl radical and containing at least one other carboxyl radical in the molecule; Salts, anhydrides, esters, amides, imides, or nitriles thereof
- C08F222/10—Esters
- C08F222/1006—Esters of polyhydric alcohols or polyhydric phenols
- C08F222/104—Esters of polyhydric alcohols or polyhydric phenols of tetraalcohols, e.g. pentaerythritol tetra(meth)acrylate
- C08F222/1045—Esters of polyhydric alcohols or polyhydric phenols of tetraalcohols, e.g. pentaerythritol tetra(meth)acrylate of aromatic tetraalcohols
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F222/00—Copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and at least one being terminated by a carboxyl radical and containing at least one other carboxyl radical in the molecule; Salts, anhydrides, esters, amides, imides, or nitriles thereof
- C08F222/10—Esters
- C08F222/12—Esters of phenols or saturated alcohols
- C08F222/24—Esters containing sulfur
- C08F222/245—Esters containing sulfur the ester chains containing seven or more carbon atoms
-
- G—PHYSICS
- G02—OPTICS
- G02B—OPTICAL ELEMENTS, SYSTEMS OR APPARATUS
- G02B1/00—Optical elements characterised by the material of which they are made; Optical coatings for optical elements
- G02B1/04—Optical elements characterised by the material of which they are made; Optical coatings for optical elements made of organic materials, e.g. plastics
-
- G—PHYSICS
- G02—OPTICS
- G02B—OPTICAL ELEMENTS, SYSTEMS OR APPARATUS
- G02B5/00—Optical elements other than lenses
- G02B5/30—Polarising elements
- G02B5/3016—Polarising elements involving passive liquid crystal elements
-
- G—PHYSICS
- G02—OPTICS
- G02B—OPTICAL ELEMENTS, SYSTEMS OR APPARATUS
- G02B1/00—Optical elements characterised by the material of which they are made; Optical coatings for optical elements
- G02B1/08—Optical elements characterised by the material of which they are made; Optical coatings for optical elements made of polarising materials
-
- G—PHYSICS
- G02—OPTICS
- G02F—OPTICAL DEVICES OR ARRANGEMENTS FOR THE CONTROL OF LIGHT BY MODIFICATION OF THE OPTICAL PROPERTIES OF THE MEDIA OF THE ELEMENTS INVOLVED THEREIN; NON-LINEAR OPTICS; FREQUENCY-CHANGING OF LIGHT; OPTICAL LOGIC ELEMENTS; OPTICAL ANALOGUE/DIGITAL CONVERTERS
- G02F1/00—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics
- G02F1/01—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics for the control of the intensity, phase, polarisation or colour
- G02F1/13—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics for the control of the intensity, phase, polarisation or colour based on liquid crystals, e.g. single liquid crystal display cells
- G02F1/133—Constructional arrangements; Operation of liquid crystal cells; Circuit arrangements
- G02F1/1333—Constructional arrangements; Manufacturing methods
- G02F1/1335—Structural association of cells with optical devices, e.g. polarisers or reflectors
- G02F1/13363—Birefringent elements, e.g. for optical compensation
- G02F1/133633—Birefringent elements, e.g. for optical compensation using mesogenic materials
Definitions
- the present invention relates to a polymerizable compound, a polymerizable composition, a polymer, and an optical anisotropic body, which can produce an optical film capable of uniform polarization conversion in a wide wavelength range.
- FPDs Flat panel display devices
- optical films such as polarizing plates and retardation plates.
- the retardation plate examples include a 1 ⁇ 4 wavelength plate that converts linearly polarized light into circularly polarized light, and a 1 ⁇ 2 wavelength plate that converts the polarization vibration plane of linearly polarized light by 90 degrees. These retardation plates can accurately convert a specific monochromatic light into a phase difference of 1 ⁇ 4 ⁇ or 1 ⁇ 2 ⁇ of the light wavelength.
- the conventional retardation plate has a problem that polarized light output through the retardation plate is converted into colored polarized light. This is because the material constituting the retardation plate has wavelength dispersion with respect to the retardation, and distribution occurs in the polarization state for each wavelength with respect to white light that is a composite wave in which light rays in the visible light range are mixed.
- the low molecular weight polymerizable compounds or polymerizable compositions described in these documents have insufficient reverse wavelength dispersion or high melting points that are not suitable for processing in industrial processes. It has many problems in terms of performance, such as difficult to apply to film, extremely narrow temperature range showing liquid crystallinity, and low solubility in solvents commonly used in industrial processes. ing. Further, these low molecular weight polymerizable compounds and the like have a problem in terms of cost because they are synthesized in multiple stages by making full use of a synthesis method using a very expensive reagent.
- Japanese Patent Laid-Open No. 10-68816 Japanese Patent Laid-Open No. 10-90521 Japanese Patent Laid-Open No. 11-52131 JP 2000-284126 A (US20020159005A1) JP 2001-4837 A International Publication No. 2000/026705 JP 2002-267838 A JP 2003-160540 A (US20030102458A1) JP 2005-208414 A JP 2005-208415 A JP 2005-208416 A Japanese Patent Laying-Open No.
- the present invention has been made in view of the above-described prior art, has a practically low melting point, excellent solubility in general-purpose solvents, can be produced at low cost, and is uniform in a wide wavelength range. It is an object to provide a polymerizable compound, a polymerizable composition, a polymer, and an optical anisotropic body capable of obtaining an optical film capable of polarization conversion.
- an optical anisotropic body comprising a polymerizable compound represented by the following formula (I) or a polymer obtained by polymerizing a polymerizable composition containing the polymerizable compound and a polymerization initiator as a constituent material is obtained.
- a polymerizable compound represented by the following formula (I) or a polymer obtained by polymerizing a polymerizable composition containing the polymerizable compound and a polymerization initiator as a constituent material is obtained.
- the polymerizable compounds (1) to (7), the polymerizable compositions (8) and (9), the polymers (10) and (11), and the optical compound (12) A cuboid is provided.
- Y 1 to Y 8 are each independently a chemical single bond, —O—, —S—, —O—C ( ⁇ O) —, —C ( ⁇ O) —O—, — OC ( ⁇ O) —O—, —NR 1 —C ( ⁇ O) —, —C ( ⁇ O) —NR 1 —, —O—C ( ⁇ O) —NR 1 —, —NR 1 — C ( ⁇ O) —O—, —NR 1 —C ( ⁇ O) —NR 1 —, or —NR 1 —O— is represented.
- R 1 represents a hydrogen atom or an alkyl group having 1 to 6 carbon atoms.
- G 1 and G 2 each independently represents a divalent aliphatic group having 1 to 20 carbon atoms which may have a substituent [the aliphatic group includes —O—, —S—, —O—C ( ⁇ O) —, —C ( ⁇ O) —O—, —O—C ( ⁇ O) —O—, —NR 2 —C ( ⁇ O) —, —C ( ⁇ O) — NR 2 —, —NR 2 —, or —C ( ⁇ O) — may be present. However, the case where two or more of —O— or —S— are adjacent to each other is excluded.
- R 2 represents a hydrogen atom or an alkyl group having 1 to 6 carbon atoms.
- Z 1 and Z 2 each independently represents an alkenyl group having 2 to 10 carbon atoms which may be substituted with a halogen atom.
- a x represents the following formula (II)
- X represents a nitrogen atom or a carbon atom.
- R a and R b each independently represent a hydrogen atom, an alkyl group having 1 to 20 carbon atoms which may have a substituent, or a substituent.
- a y may have a hydrogen atom, an alkyl group having 1 to 20 carbon atoms which may have a substituent, an alkenyl group having 2 to 20 carbon atoms which may have a substituent, or a substituent.
- a good cycloalkyl group having 3 to 12 carbon atoms or a group represented by the formula (II) is shown.
- a 1 represents a trivalent aromatic group which may have a substituent.
- a 2 and A 3 each independently represents a C 3-30 divalent alicyclic hydrocarbon group which may have a substituent.
- a 4 and A 5 each independently represents a C 4-30 divalent aromatic group which may have a substituent.
- Q 1 represents a hydrogen atom or an alkyl group having 1 to 6 carbon atoms which may have a substituent.
- m and n each independently represents 0 or 1. ] The polymerizable compound shown by this.
- R a and R b may each independently have a hydrogen atom, a C 1-20 alkyl group which may have a substituent, or a substituent.
- [X a represents a nitrogen atom or a carbon atom.
- R X represents a hydrogen atom, a halogen atom, an alkyl group having 1 to 6 carbon atoms, a cyano group, a nitro group, an alkylsulfinyl group having 1 to 6 carbon atoms, an alkylsulfonyl group having 1 to 6 carbon atoms, or 1 to 6 carbon atoms.
- Fluoroalkyl groups alkoxy groups having 1 to 6 carbon atoms, alkylthio groups having 1 to 6 carbon atoms, mono-substituted amino groups, disubstituted amino groups, alkylsulfamoyl groups having 1 to 6 carbon atoms, or 2 to 12 carbon atoms
- R 6 represents a hydrogen atom or an alkyl group having 1 to 6 carbon atoms.
- R X may be all the same or different, and the C—R x bond may be replaced with a nitrogen atom.
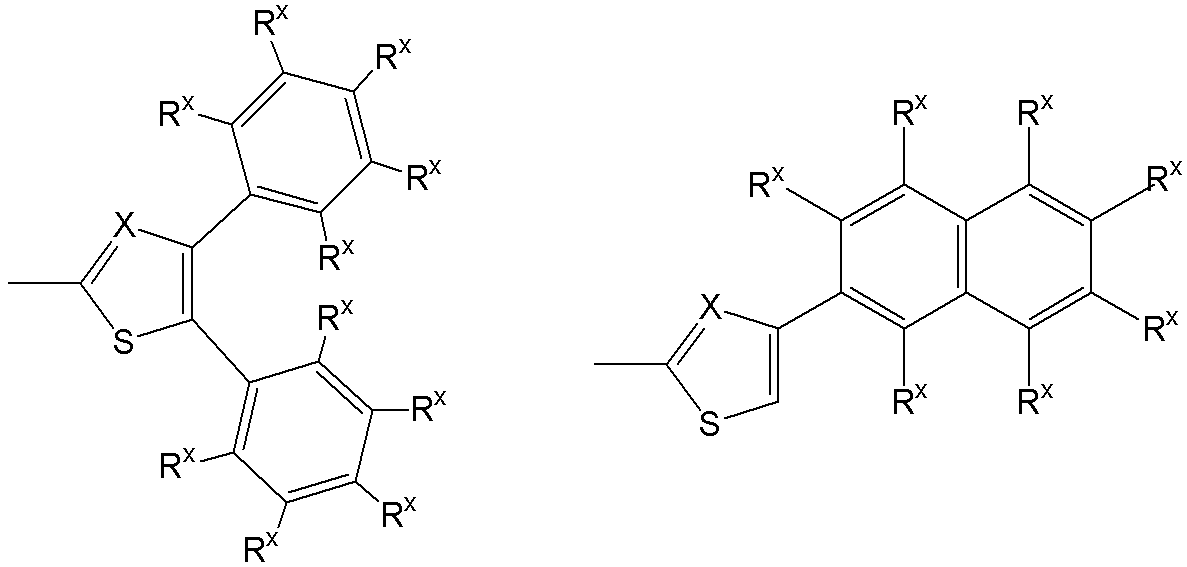
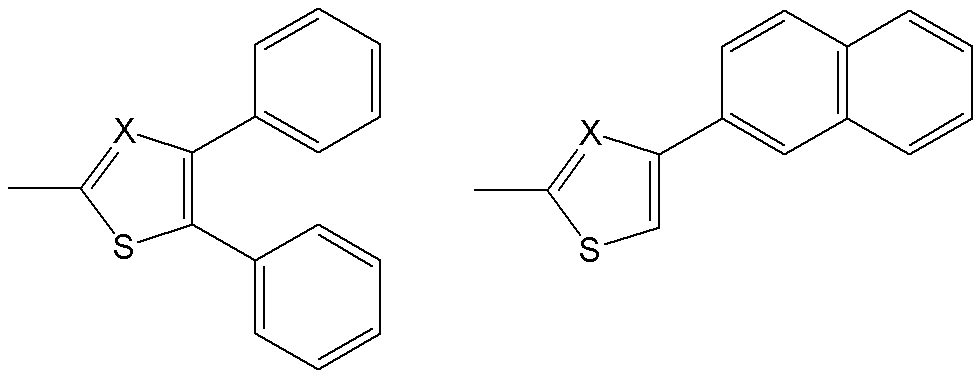
- a 1 is an optionally substituted trivalent benzene ring group or trivalent naphthalene ring group, and A 4 and A 5 each independently have a substituent.
- the polymerizable compound according to (1) which may be a phenylene group or a naphthylene group.
- Y 1 to Y 8 are each independently a chemical single bond, —O—, —O—C ( ⁇ O) —, —C ( ⁇ O) —O—, or —O—.
- the polymerizable compound according to (1) which is C ( ⁇ O) —O—.
- (10) A polymer obtained by polymerizing the polymerizable compound according to any one of (1) to (7) or the polymerizable composition according to (8) or (9).
- (11) The polymer as described in (10), which is a liquid crystalline polymer.
- (12) An optical anisotropic body comprising the polymer according to (11) as a constituent material.
- the polymerizable compound, the polymerizable composition, and the polymer of the present invention it is possible to obtain an optically anisotropic body that is capable of uniform polarization conversion in a wide wavelength range and that is satisfactory in terms of performance at low cost. it can. Since the optical anisotropic body of the present invention is composed of the polymer of the present invention, it is obtained at a low cost and is capable of uniform polarization conversion in a wide wavelength range and is satisfactory in terms of performance.
- an antireflection film can be produced by combining the film-like optical anisotropic body of the present invention with a polarizing plate. This can be suitably used industrially, for example, for preventing reflection of a touch panel or an organic electroluminescent element.
- the polymerizable compound of the present invention is a compound represented by the formula (I) (compound (I)).
- Y 1 to Y 8 are each independently a chemical single bond, —O—, —S—, —O—C ( ⁇ O) —, —C ( ⁇ O) —O—, —O.
- R 1 represents a hydrogen atom or an alkyl group having 1 to 6 carbon atoms.
- alkyl group having 1 to 6 carbon atoms of R 1 include methyl group, ethyl group, n-propyl group, isopropyl group, n-butyl group, sec-butyl group, t-butyl group, n-pentyl group, n- A hexyl group etc. are mentioned.
- R 1 is preferably a hydrogen atom or an alkyl group having 1 to 4 carbon atoms.
- Y 1 to Y 8 are each independently a chemical single bond, —O—, —O—C ( ⁇ O) —, —C ( ⁇ O) —O—, or —O.
- G 1 and G 2 each independently represent a divalent aliphatic group having 1 to 20 carbon atoms which may have a substituent.
- Examples of the divalent aliphatic group having 1 to 20 carbon atoms include divalent aliphatic groups having a chain structure; fats such as saturated cyclic hydrocarbon (cycloalkane) structures and unsaturated cyclic hydrocarbon (cycloalkene) structures A divalent aliphatic group having a cyclic structure; and the like.
- Examples of the substituent for the divalent aliphatic group of G 1 and G 2 include halogen atoms such as fluorine atom, chlorine atom, bromine atom and iodine atom; methoxy group, ethoxy group, n-propoxy group and isopropoxy group
- halogen atoms such as fluorine atom, chlorine atom, bromine atom and iodine atom
- An alkoxy group having 1 to 6 carbon atoms such as an n-butoxy group, a sec-butoxy group, a t-butoxy group, an n-pentyloxy group, and an n-hexyloxy group.
- a fluorine atom, a methoxy group, and an ethoxy group are preferable.
- the aliphatic group includes —O—, —S—, —O—C ( ⁇ O) —, —C ( ⁇ O) —O—, —O—C ( ⁇ O) —O—, — NR 2 —C ( ⁇ O) —, —C ( ⁇ O) —NR 2 —, —NR 2 —, or —C ( ⁇ O) — may be present (provided that —O— or — Excluding the case where two or more S-s are adjacent to each other.)
- R 2 represents the same hydrogen atom or alkyl group having 1 to 6 carbon atoms as R 1, and is preferably a hydrogen atom or a methyl group.
- the group intervening in the aliphatic group is preferably —O—, —O—C ( ⁇ O) —, —C ( ⁇ O) —O—, —C ( ⁇ O) —.
- G 1 and G 2 are each independently an alkylene group having 1 to 20 carbon atoms, an alkenylene group having 2 to 20 carbon atoms, or the like, from the viewpoint of better expressing the desired effect of the present invention.
- a divalent aliphatic group having a chain structure is preferable and has 1 to 12 carbon atoms such as a methylene group, an ethylene group, a trimethylene group, a propylene group, a tetramethylene group, a pentamethylene group, a hexamethylene group, and an octamethylene group.
- An alkylene group is more preferable, and a tetramethylene group [— (CH 2 ) 4 —] and a hexamethylene group [— (CH 2 ) 6 —] are particularly preferable.
- Z 1 and Z 2 each independently represents an alkenyl group having 2 to 10 carbon atoms which may be substituted with a halogen atom.
- the alkenyl group preferably has 2 to 6 carbon atoms.
- Examples of the halogen atom that is a substituent of the alkenyl group of Z 1 and Z 2 include a fluorine atom, a chlorine atom, a bromine atom, and the like, and a chlorine atom is preferable.
- alkenyl group having 2 to 10 carbon atoms of Z 1 and Z 2 include CH 2 ⁇ CH—, CH 2 ⁇ C (CH 3 ) —, CH 2 ⁇ CH—CH 2 —, CH 3 —CH ⁇ .
- Z 1 and Z 2 are each independently CH 2 ⁇ CH 2 —, CH 2 ⁇ C (CH 3 ) —, CH 2 ⁇ C (Cl) —, CH 2 ⁇ CH—CH 2 —, CH 2 ⁇ C (CH 3 ) —CH 2 —, or CH 2 ⁇ C (CH 3 ) —CH 2 —CH 2 —.
- CH 2 ⁇ CH 2 —, CH 2 ⁇ C (CH 3 ) —, or CH 2 ⁇ C (Cl) — is more preferable, and CH 2 ⁇ CH 2 — is particularly preferable.
- a x represents a group represented by the formula (II).
- X represents a nitrogen atom or a carbon atom, and a nitrogen atom is preferable.
- R a and R b are each independently a hydrogen atom, an optionally substituted alkyl group having 1 to 20 carbon atoms, or an optionally substituted carbon number 2
- alkyl group having 1 to 20 carbon atoms which may have a substituent of R a and R b include a methyl group, an ethyl group, an n-propyl group, an isopropyl group, n-butyl group, sec-butyl group, t-butyl group, n-pentyl group, isopentyl group, neopentyl group, n-hexyl group, isohexyl group, n-heptyl group, n-octyl group, n-nonyl group, n-decyl group, n-undecyl group, n-dodecyl group, n-tridecyl group, n-tetradecyl group, n-pentadecyl group, n-hexadecyl group, n-heptadecyl group, n-octadecyl group, n
- Examples of the substituent of the alkyl group having 1 to 20 carbon atoms which may have a substituent include halogen atoms such as fluorine atom and chlorine atom; cyano group; substituted amino group such as dimethylamino group; methoxy group, ethoxy group
- An alkoxy group having 1 to 6 carbon atoms such as an isopropoxy group; an alkoxy group having 1 to 6 carbon atoms substituted with an alkoxy group having 1 to 6 carbon atoms such as a methoxymethoxy group or a methoxyethoxy group; a nitro group;
- alkenyl group having 2 to 20 carbon atoms which may have a substituent in R a and R b include a vinyl group, a propenyl group, an isopropenyl group, a butenyl group, and a pentenyl group.
- the carbon number of the alkenyl group having 2 to 20 carbon atoms which may have a substituent is preferably 2 to 12.
- the cycloalkyl group having 3 to 18 carbon atoms of the cycloalkyl group having 3 to 18 carbon atoms which may have a substituent for R a and R b includes a cyclopropyl group, a cyclobutyl group, a cyclopentyl group, and a cyclohexyl group. , Cycloheptyl group, cyclooctyl group, cyclodecyl group, cyclododecyl group and the like. And a cycloalkyl group having 3 to 18 carbon atoms.
- Examples of the substituent of the alkenyl group having 2 to 20 carbon atoms which may have a substituent and the cycloalkyl group having 3 to 18 carbon atoms which may have a substituent include a fluorine atom and a chlorine atom.
- Halogen atom cyano group; substituted amino group such as dimethylamino group; alkoxy group having 1 to 6 carbon atoms such as methoxy group, ethoxy group and isopropoxy group; nitro group; aryl group such as phenyl group and naphthyl group; A cycloalkyl group having 3 to 8 carbon atoms such as a group, a cyclopentyl group, and a cyclohexyl group; —C ( ⁇ O) —R 4 ; —C ( ⁇ O) —OR 4 ; —SO 2 R 4 ; It is done.
- R 4 represents the same meaning as described above.
- Examples of the aromatic hydrocarbon ring group having 1 to 20 carbon atoms which may have a substituent include a benzene ring group, a naphthalene ring group, and an anthracene ring group.
- Examples of the aromatic heterocyclic group having 1 to 20 carbon atoms that may have a substituent include a pyrrole ring group, a furan ring group, a thiophene ring group, a pyridine ring group, a pyridazine ring group, and a pyrimidine.
- Monocyclic aromatic heterocyclic groups such as ring groups, pyrazine ring groups, pyrazole ring groups, imidazole ring groups, oxazole ring groups, thiazole ring groups; benzothiazole ring groups, benzoxazole ring groups, quinoline ring groups, phthalazine ring groups , Benzimidazole ring group, benzopyrazole ring group, benzofuran ring group, benzothiophene ring group and other condensed aromatic heterocyclic groups;
- Examples of the substituent of the aromatic hydrocarbon ring group and aromatic heterocyclic group include halogen atoms such as fluorine atom and chlorine atom; cyano group; alkyl group having 1 to 6 carbon atoms such as methyl group, ethyl group and propyl group An alkenyl group having 2 to 6 carbon atoms such as a vinyl group or an allyl group; a halogenated alkyl group having 1 to 6 carbon atoms such as a trifluoromethyl group; a substituted amino group such as a dimethylamino group; a methoxy group, an ethoxy group, an iso An alkoxy group having 1 to 6 carbon atoms such as a propoxy group; a nitro group; an aryl group such as a phenyl group or a naphthyl group; —C ( ⁇ O) —R 4 ; —C ( ⁇ O) —OR 4 ; —SO 2 R 4 ; etc.
- R 4 represents
- the aromatic hydrocarbon group having 1 to 20 carbon atoms which may have a substituent and the aromatic heterocyclic group having 1 to 20 carbon atoms which may have a substituent include Groups represented by formulas (II-1) to (II-5) are preferred.
- Xa represents a nitrogen atom or a carbon atom.
- R X represents a hydrogen atom; a halogen atom such as a fluorine atom, a chlorine atom or a bromine atom; an alkyl group having 1 to 6 carbon atoms such as a methyl group or an ethyl group; a cyano group; a nitro group; a methylsulfinyl group or an ethylsulfinyl group An alkylsulfinyl group having 1 to 6 carbon atoms; an alkylsulfonyl group having 1 to 6 carbon atoms such as a methylsulfonyl group or an ethylsulfonyl group; a fluoroalkyl group having 1 to 6 carbon atoms such as a trifluoromethyl group or a pentafluoromethyl group An alkoxy group having 1 to 6 carbon atom
- the plurality of R X may be all the same or different, and 1 to 3 C—R x bonds may be replaced with a nitrogen atom. All of R X are preferably hydrogen atoms.
- the groups represented by the formulas (II-1) to (II-5) are used from the viewpoint of better expressing the desired effect of the present invention. Are preferred. Examples of the group represented by the formula (II-3) include the following formula
- R x ′ represents the same meaning as R x described above, provided that the CR x ′ bond is not replaced by a nitrogen atom.
- the group etc. which are represented by these are mentioned. Examples of the group represented by the formula (II-4) include the following formula
- R a and R b are a hydrogen atom
- R a is a group represented by the above formulas (II-1) to (II-5)
- R a , R b Preferably, each b is independently a group represented by the above formulas (II-1) to (II-5), R b is a hydrogen atom, and R a is represented by the above formula (II-4).
- R a and R b are each independently a group represented by the formula (II-3) are more preferable.
- a x is preferably a group represented by the following formula:
- a y has a hydrogen atom, an optionally substituted alkyl group having 1 to 20 carbon atoms, an optionally substituted alkenyl group having 2 to 20 carbon atoms, and a substituent.
- cycloalkyl group which may having 3 to 12 carbon atoms, or the same as a x, a group represented by the formula (II).
- Ay an alkyl group having 1 to 20 carbon atoms which may have a substituent, an alkenyl group having 2 to 20 carbon atoms which may have a substituent, and an optionally substituted carbon
- the alkyl group having 3 to 12 carbon atoms the alkyl group having 1 to 20 carbon atoms which may have a substituent for the above R a and R b , and 2 to 20 carbon atoms which may have a substituent.
- Ay is preferably a hydrogen atom.
- a 1 represents a trivalent aromatic group which may have a substituent.
- the trivalent aromatic group may be a trivalent carbocyclic aromatic group or a trivalent heterocyclic aromatic group. From the viewpoint of better expressing the desired effect of the present invention, a trivalent carbocyclic aromatic group is preferable, a trivalent benzene ring group or a trivalent naphthalene ring group is more preferable, and a trivalent represented by the following formula: The benzene ring group or trivalent naphthalene ring group is more preferable.
- the substituents Y 1 and Y 2 are described for convenience in order to clarify the bonding state (Y 1 and Y 2 represent the same meaning as described above, and the same applies hereinafter). .
- a 1 groups represented by the following formulas (A11) to (A25) are more preferable.
- A13 groups represented by the following formulas (A11), (A13), (A15), (A19), and (A23) are particularly preferred.
- a 1 as a trivalent substituent which may be possessed by the aromatic group, the same ones as exemplified as the substituents of the aromatic groups of the A X and the like.
- a 1 preferably has no substituent.
- a 2 and A 3 each independently represents a C 3-30 divalent alicyclic hydrocarbon group which may have a substituent.
- Examples of the divalent alicyclic hydrocarbon group having 3 to 30 carbon atoms include a cycloalkanediyl group having 3 to 30 carbon atoms and a divalent alicyclic condensed ring group having 10 to 30 carbon atoms.
- Examples of the cycloalkanediyl group having 3 to 30 carbon atoms include cyclopropanediyl group; cyclobutanediyl group such as cyclobutane-1,2-diyl group and cyclobutane-1,3-diyl group; cyclopentane-1,2-diyl group Cyclopentanediyl groups such as cyclopentane-1,3-diyl group; cyclohexanediyl groups such as cyclohexane-1,2-diyl group, cyclohexane-1,3-diyl group, cyclohexane-1,4-diyl group; Cycloheptanediyl groups such as cycloheptane-1,2-diyl group, cycloheptane-1,3-diyl group, cycloheptane-1,4-diyl group; cyclooc
- Examples of the divalent alicyclic condensed ring group having 10 to 30 carbon atoms include decalin-2,5-diyl group, decalin-2,7-diyl group, etc .; adamantane-1,2-diyl group, adamantane Adamantanediyl group such as -1,3-diyl group; bicyclo [2.2.1] heptane-2,3-diyl group, bicyclo [2.2.1] heptane-2,5-diyl group, bicyclo And bicyclo [2.2.1] heptanediyl groups such as [2.2.1] heptane-2,6-diyl group.
- These divalent alicyclic hydrocarbon groups may have a substituent at any position.
- substituents the same ones as exemplified as the substituents of the aromatic groups of the A X and the like.
- a 2 and A 3 a divalent alicyclic hydrocarbon group having 3 to 12 carbon atoms is preferable, a cycloalkanediyl group having 3 to 12 carbon atoms is more preferable, and the following formula (A31) to (A34)
- the divalent alicyclic hydrocarbon group having 3 to 30 carbon atoms is a cis type or a trans type based on a difference in configuration of carbon atoms bonded to Y 1 , Y 3 (or Y 2 , Y 4 ).
- Stereoisomers can exist.
- a cis-type isomer (A32a) and a trans-type isomer (A32b) may exist.
- it may be a cis type, a trans type, or a mixture of cis and trans isomers.
- a trans type Preferably, there is a trans type.
- a 4 and A 5 each independently represents a divalent aromatic group having 4 to 30 carbon atoms, which may have a substituent.
- the aromatic groups of A 4 and A 5 may be monocyclic or polycyclic. Specific examples of A 4 and A 5 include, but are not limited to, the following.
- the aromatic groups mentioned as specific examples of A 4 and A 5 may have a substituent at any position.
- the substituent include a halogen atom, a cyano group, a hydroxyl group, an alkyl group having 1 to 6 carbon atoms, an alkoxy group having 1 to 6 carbon atoms, a nitro group, and a —C ( ⁇ O) —OR group.
- R represents an alkyl group having 1 to 6 carbon atoms.
- a halogen atom, an alkyl group having 1 to 6 carbon atoms, and an alkoxy group are preferable.
- the halogen atom is preferably a fluorine atom
- the alkyl group having 1 to 6 carbon atoms is preferably a methyl group, an ethyl group or a propyl group
- the alkoxy group is more preferably a methoxy group or an ethoxy group.
- a 4 and A 5 are each independently preferably a phenylene group or a naphthylene group which may have a substituent.
- the group represented by the following formulas (A41), (A42) and (A43) which may have a group is more preferable, and the group represented by the formula (A41) which may have a substituent is Particularly preferred.
- Q 1 represents a hydrogen atom or an alkyl group having 1 to 6 carbon atoms which may have a substituent.
- the alkyl group which has 1 carbon atoms which may be ⁇ 6 have a substituent, the same ones as exemplified in the A X and the like.
- Q 1 is preferably a hydrogen atom or an alkyl group having 1 to 6 carbon atoms, more preferably a hydrogen atom or a methyl group.
- M and n each independently represent 0 or 1, and both are preferably 0.
- stereoisomers based on a carbon-nitrogen double bond may exist, but these are all included in the present invention.
- the polymerizable compound of the present invention can be produced, for example, by the reaction shown below.
- Y 1 to Y 8 , G 1 , G 2 , Z 1 , Z 2 , A x , A 1 to A 5 , Q 1 , R a , R b , m and n have the same meaning as described above.
- L 2 representing the a y not hydrogen atoms of the a y each independently represent a leaving group such as a halogen atom, a methanesulfonyloxy group, p- toluenesulfonyloxy group .
- an equimolar amount of thiosemicarbazide hydrochloride (1) is added to the carbonyl compound (carbonyl compound (4)) represented by the formula (4) and reacted (reaction 1), and then the equimolar formula (4).
- the target polymerizable compound represented by the formula (Ia) of the present invention can be produced by adding and reacting the compound represented by 2) (compound (2)) (reaction 2).
- the solvent used in this reaction is not particularly limited as long as it is inert to the reaction.
- alcohol solvents such as methyl alcohol, ethyl alcohol, n-propyl alcohol, isopropyl alcohol, n-butyl alcohol, isobutyl alcohol, sec-butyl alcohol, t-butyl alcohol; diethyl ether, tetrahydrofuran, 1,2-dimethoxyethane Ether solvents such as 1,4-dioxane and cyclopentyl methyl ether; ester solvents such as ethyl acetate, propyl acetate and methyl propionate; aromatic hydrocarbon solvents such as benzene, toluene and xylene; n-pentane, n Aliphatic hydrocarbon solvents such as hexane and n-heptane; amide solvents such as N, N-dimethylformamide, N-methylpyrrolidone and hexamethylphosphoric tri
- the amount of the solvent used is not particularly limited and can be appropriately determined in consideration of the type of compound used, reaction scale, etc., but is usually 1 to 100 g with respect to 1 g of the carbonyl compound (4).
- Reaction 1 and reaction 2 proceed smoothly in a temperature range from ⁇ 10 ° C. to the boiling point of the solvent used.
- the reaction time for each reaction is usually from several minutes to several hours depending on the reaction scale.
- a hydrazine compound (hydrazine compound (5)) represented by formula (5) is converted into a carbonyl compound (carbonyl compound (4)) represented by formula (4) and [hydrazine compound (5): carbonyl compound ( 4)] at a molar ratio of 1: 2 to 2: 1, preferably 1: 1.5 to 1.5: 1.
- the polymerizable compound represented by the formula (I) can be produced.
- the reaction can be carried out by adding an acid catalyst such as an organic acid such as ( ⁇ ) -10-camphorsulfonic acid and paratoluenesulfonic acid; an inorganic acid such as hydrochloric acid and sulfuric acid;
- an acid catalyst By adding an acid catalyst, the reaction time may be shortened and the yield may be improved.
- the addition amount of the acid catalyst is usually 0.001 to 1 mol with respect to 1 mol of the carbonyl compound (4). Further, the acid catalyst may be added as it is, or may be added as a solution dissolved in an appropriate solution.
- the solvent used in this reaction is not particularly limited as long as it is inert to the reaction.
- alcohol solvents such as methyl alcohol, ethyl alcohol, n-propyl alcohol, isopropyl alcohol, n-butyl alcohol, isobutyl alcohol, sec-butyl alcohol, t-butyl alcohol; diethyl ether, tetrahydrofuran, 1,2-dimethoxyethane Ether solvents such as 1,4-dioxane and cyclopentyl methyl ether; ester solvents such as ethyl acetate, propyl acetate and methyl propionate; aromatic hydrocarbon solvents such as benzene, toluene and xylene; n-pentane, n -Aliphatic hydrocarbon solvents such as hexane and n-heptane; Amides solvents such as N, N-dimethylformamide, N-methylpyrrolidone and hexamethyl
- the amount of the solvent used is not particularly limited and can be appropriately determined in consideration of the type of compound used, reaction scale, etc., but is usually 1 to 100 g with respect to 1 g of the hydrazine compound (3).
- the reaction proceeds smoothly in the temperature range from ⁇ 10 ° C. to the boiling point of the solvent used.
- the reaction time for each reaction is usually from several minutes to several hours depending on the reaction scale.
- the hydrazine compound (5) can be produced as follows.
- a x and A y represent the same meaning as described above.
- X represents a leaving group such as a halogen atom, amino group, methylthio group, methanesulfonyloxy group, p-toluenesulfonyloxy group, etc.
- the compound represented by the formula (7a) and hydrazine (6) are mixed in an appropriate solvent at a molar ratio of (compound (7a): hydrazine (6)) of 1: 1 to 1:20, preferably 1 : 2 to 1:10 to obtain the corresponding hydrazine compound (5a). Furthermore, by reacting the hydrazine compound (5a) with the compound represented by the formula (7b), the hydrazine compound ( 5) can be obtained.
- hydrazine (6) a monohydrate is usually used.
- hydrazine (6) a commercially available product can be used as it is.
- the solvent used in this reaction is not particularly limited as long as it is inert to the reaction.
- alcohol solvents such as methyl alcohol, ethyl alcohol, n-propyl alcohol, isopropyl alcohol, n-butyl alcohol, isobutyl alcohol, sec-butyl alcohol, t-butyl alcohol; diethyl ether, tetrahydrofuran, 1,2-dimethoxyethane Ether solvents such as 1,4-dioxane and cyclopentyl methyl ether
- aromatic hydrocarbon solvents such as benzene, toluene and xylene
- aliphatic hydrocarbon solvents such as n-pentane, n-hexane and n-heptane
- amide solvents such as N, N-dimethylformamide, N-
- the amount of the solvent to be used is not particularly limited and can be appropriately determined in consideration of the type of compound used, reaction scale, etc., but is usually 1 to 100 g with respect to 1 g of hydrazine.
- the reaction proceeds smoothly in a temperature range from ⁇ 10 ° C. to the boiling point of the solvent used.
- the reaction time for each reaction is usually from several minutes to several hours depending on the reaction scale.
- the hydrazine compound (5) can be produced by reducing the diazonium salt (8) using a conventionally known method as follows.
- X ⁇ represents an anion which is a counter ion for diazonium.
- examples of X ⁇ include inorganic anions such as hexafluorophosphate ion, borofluoride ion, chloride ion, sulfate ion; polyfluoroalkylcarboxylate ion, polyfluoroalkylsulfonate ion, tetraphenylborate ion And organic anions such as aromatic carboxylate ions and aromatic sulfonate ions.
- a metal salt reducing agent is mentioned as a reducing agent used for the said reaction.
- a metal salt reducing agent is generally a compound containing a low-valent metal or a compound comprising a metal ion and a hydride source (“Organic Synthesis Experiment Handbook”, 1990, published by Maruzen Co., Ltd., edited by the Society of Synthetic Organic Chemistry, Japan). See).
- R is an alkyl group having 1 to 6 carbon atoms. LiAlH 4 , iBu 2 AlH, LiBH 4 , NaBH 4 , SnCl 2 , CrCl 2 , TiCl 3 and the like.
- the diazonium salt (8) can be produced from a compound such as aniline by a conventional method.
- the carbonyl compound (4) typically has an ether bond (—O—), an ester bond (—C ( ⁇ O) —O—, —O—C ( ⁇ O) —), a carbonate bond (—O—).
- Formation of an ether bond can be performed as follows.
- D1-hal hal represents a halogen atom; the same shall apply hereinafter
- D2-OMet Metal represents an alkali metal (mainly sodium). The same) is mixed and condensed (Williamson synthesis).
- D1 and D2 represent arbitrary organic groups (the same applies hereinafter).
- a compound represented by the formula: D1-hal and a compound represented by the formula: D2-OH are mixed and condensed in the presence of a base such as sodium hydroxide or potassium hydroxide.
- a compound represented by the formula: D1-J J represents an epoxy group
- a compound represented by the formula: D2-OH are mixed in the presence of a base such as sodium hydroxide or potassium hydroxide.
- a base such as sodium hydroxide or potassium hydroxide.
- D1-OFN OFN represents a group having an unsaturated bond
- D2-OMet are mixed with a base such as sodium hydroxide or potassium hydroxide. In the presence, they are mixed and subjected to an addition reaction.
- a compound represented by the formula: D1-hal and a compound represented by the formula: D2-OMet are mixed and condensed in the presence of copper or cuprous chloride (Ullman condensation).
- Formation of an ester bond and an amide bond can be performed as follows.
- a compound represented by the formula: D1-COOH and a compound represented by the formula: D2-OH or D2-NH 2 are dehydrated in the presence of a dehydration condensing agent (N, N-dicyclohexylcarbodiimide or the like). Allow to condense.
- a dehydration condensing agent N, N-dicyclohexylcarbodiimide or the like. Allow to condense.
- a compound represented by the formula: D1-CO-hal is obtained by allowing a halogenating agent to act on the compound represented by the formula: D1-COOH, which is combined with the formula: D2-OH or D2-NH. The compound represented by 2 is reacted in the presence of a base.
- a group represented by the formula: Z 2 —Y 6 —G 2 —Y 4 —A 3 —Y 2 — in the formula (4) is represented by the formula: Z 1 —Y 5 —G 1 —Y 3 —A 2 —Y 1 — is the same as the group represented by — 1 and Y 1 is a group represented by Y 11 —C ( ⁇ O) —O—.
- Compound (4 ′) can be produced by the reaction shown below.
- Y 1 represents a group to be a Y 1 is representative of the same meaning as above, a hydroxyl group, a halogen atom, a methanesulfonyloxy group, a leaving group such as p- toluenesulfonyloxy group Represents.
- the compound (10) is a compound having a hydroxyl group in formula (10) (carboxylic acid), dehydration condensation of 1-ethyl-3- (3-dimethylaminopropyl) carbodiimide hydrochloride, dicyclohexylcarbodiimide, etc.
- the target product can be obtained by reacting in the presence of the agent.
- the amount of the dehydrating condensing agent to be used is generally 1 to 3 mol per 1 mol of compound (10).
- the desired product can be obtained by reacting in the presence of a base.
- a base examples include organic bases such as triethylamine and pyridine; and inorganic bases such as sodium hydroxide, sodium carbonate and sodium hydrogen carbonate.
- the amount of the base to be used is generally 1 to 3 mol per 1 mol of compound (10).
- the compound (10) is a compound (mixed acid anhydride) in which L is a methanesulfonyloxy group or a p-toluenesulfonyloxy group in the formula (10) is the same as in the case of a halogen atom.
- solvent used in the above reaction examples include chlorine solvents such as chloroform and methylene chloride; amide solvents such as N-methylpyrrolidone, N, N-dimethylformamide, N, N-dimethylacetamide, and hexamethylphosphoric triamide.
- Solvents such as 1,4-dioxane, cyclopentylmethyl ether, tetrahydrofuran, tetrahydropyran, 1,3-dioxolane; sulfur-containing solvents such as dimethyl sulfoxide and sulfolane; aromatic hydrocarbons such as benzene, toluene and xylene Solvents; aliphatic hydrocarbon solvents such as n-pentane, n-hexane and n-octane; alicyclic hydrocarbon solvents such as cyclopentane and cyclohexane; and mixed solvents composed of two or more of these solvents; etc. Is mentioned.
- the amount of the solvent to be used is not particularly limited and can be appropriately determined in consideration of the type of compound used, reaction scale, etc., but is usually 1 to 50 g with respect to 1 g of dihydroxy compound (9).
- the compound (9) is a known substance, and can be produced and obtained by a known method.
- a compound in which A 1 is a trivalent benzene ring group and Q 1 is a hydrogen atom is obtained by adding 1,4-dimethoxybenzene to N, N, N ′, N′-tetramethyl.
- alkyllithium such as n-butyllithium
- a base such as ethylenediamine
- N, N-dimethylformamide is added and the whole volume is stirred to obtain a formyl form.
- boron bromide to act, the desired product which is a demethylated product can be obtained.
- what is marketed as a compound (9) can also be refine
- Many of the compounds (10) are known compounds, and include an ether bond (—O—), an ester bond (—C ( ⁇ O) —O—, —O—C ( ⁇ O) —), a carbonate bond (—O—).
- any reaction after the completion of the reaction, the usual post-treatment operation in organic synthetic chemistry is performed, and if desired, by applying known separation / purification means such as column chromatography, recrystallization method, distillation method, etc. Product can be isolated.
- separation / purification means such as column chromatography, recrystallization method, distillation method, etc.
- the structure of the target compound can be identified by measurement of NMR spectrum, IR spectrum, mass spectrum, etc., elemental analysis or the like.
- the second of the present invention is a polymerizable composition containing the polymerizable compound of the present invention and a polymerization initiator.
- a polymerization initiator is mix
- the polymerization initiator to be used an appropriate one may be selected and used according to the type of polymerizable group possessed by the polymerizable compound. For example, a radical polymerization initiator is used if the polymerizable group is radically polymerizable, an anionic polymerization initiator is used if it is an anionically polymerizable group, and a cationic polymerization initiator is used if it is a cationically polymerizable group. Good.
- a thermal radical generator which is a compound that generates an active species capable of initiating polymerization of a polymerizable compound by heating; and visible light, ultraviolet light (i-line, etc.), far ultraviolet light, electron
- photoradical generators which are compounds that generate active species capable of initiating polymerization of polymerizable compounds upon exposure to exposure light such as X-rays and X-rays, can be used, but photoradical generators are used. Is preferred.
- Photoradical generators include acetophenone compounds, biimidazole compounds, triazine compounds, O-acyloxime compounds, onium salt compounds, benzoin compounds, benzophenone compounds, ⁇ -diketone compounds, polynuclear quinone compounds , Xanthone compounds, diazo compounds, imide sulfonate compounds, and the like. These compounds are components that generate active radicals or active acids, or both active radicals and active acids upon exposure.
- a radical photogenerator can be used individually by 1 type or in combination of 2 or more types.
- acetophenone compounds include 2-hydroxy-2-methyl-1-phenylpropan-1-one, 2-methyl-1- [4- (methylthio) phenyl] -2-morpholinopropan-1-one 2-benzyl-2-dimethylamino-1- (4-morpholinophenyl) butan-1-one, 1-hydroxycyclohexyl phenyl ketone, 2,2-dimethoxy-1,2-diphenylethane-1-one, Examples thereof include 1,2-octanedione, 2-benzyl-2-dimethylamino-4′-morpholinobutyrophenone, and the like.
- biimidazole compound examples include 2,2′-bis (2-chlorophenyl) -4,4 ′, 5,5′-tetrakis (4-ethoxycarbonylphenyl) -1,2′-biimidazole, 2 , 2'-bis (2-bromophenyl) -4,4 ', 5,5'-tetrakis (4-ethoxycarbonylphenyl) -1,2'-biimidazole, 2,2'-bis (2-chlorophenyl) -4,4 ', 5,5'-tetraphenyl-1,2'-biimidazole, 2,2'-bis (2,4-dichlorophenyl) -4,4', 5,5'-tetraphenyl-1 , 2′-biimidazole, 2,2′-bis (2,4,6-trichlorophenyl) -4,4 ′, 5,5′-tetraphenyl-1,2′-biimi
- a hydrogen donor in combination because sensitivity can be further improved.
- the “hydrogen donor” means a compound that can donate a hydrogen atom to a radical generated from a biimidazole compound by exposure.
- the hydrogen donor mercaptan compounds, amine compounds and the like defined below are preferable.
- Examples of mercaptan compounds include 2-mercaptobenzothiazole, 2-mercaptobenzoxazole, 2-mercaptobenzimidazole, 2,5-dimercapto-1,3,4-thiadiazole, 2-mercapto-2,5-dimethylaminopyridine and the like. Can be mentioned.
- Examples of amine compounds include 4,4′-bis (dimethylamino) benzophenone, 4,4′-bis (diethylamino) benzophenone, 4-diethylaminoacetophenone, 4-dimethylaminopropiophenone, ethyl-4-dimethylaminobenzoate, Examples include 4-dimethylaminobenzoic acid and 4-dimethylaminobenzonitrile.
- triazine compounds examples include 2,4,6-tris (trichloromethyl) -s-triazine, 2-methyl-4,6-bis (trichloromethyl) -s-triazine, 2- [2- (5-methylfuran -2-yl) ethenyl] -4,6-bis (trichloromethyl) -s-triazine, 2- [2- (furan-2-yl) ethenyl] -4,6-bis (trichloromethyl) -s-triazine 2- [2- (4-diethylamino-2-methylphenyl) ethenyl] -4,6-bis (trichloromethyl) -s-triazine, 2- [2- (3,4-dimethoxyphenyl) ethenyl] -4 , 6-Bis (trichloromethyl) -s-triazine, 2- (4-methoxyphenyl) -4,6-bis (trichloromethyl) -s-tri
- O-acyloxime compounds include 1- [4- (phenylthio) phenyl] -heptane-1,2-dione 2- (O-benzoyloxime), 1- [4- (phenylthio) phenyl]- Octane-1,2-dione 2- (O-benzoyloxime), 1- [4- (benzoyl) phenyl] -octane-1,2-dione 2- (O-benzoyloxime), 1- [9-ethyl- 6- (2-Methylbenzoyl) -9H-carbazol-3-yl] -ethanone 1- (O-acetyloxime), 1- [9-ethyl-6- (3-methylbenzoyl) -9H-carbazole-3- Yl] -ethanone 1- (O-acetyloxime), 1- (9-ethyl-6-benzoyl-9H-carbazol-3-yl) -ethanone 1- (O-acetyl)
- anionic polymerization initiator examples include alkyl lithium compounds; monolithium salts or monosodium salts such as biphenyl, naphthalene, and pyrene; polyfunctional initiators such as dilithium salt and trilithium salt; and the like.
- the cationic polymerization initiator examples include proton acids such as sulfuric acid, phosphoric acid, perchloric acid and trifluoromethanesulfonic acid; Lewis acids such as boron trifluoride, aluminum chloride, titanium tetrachloride and tin tetrachloride; A combined system of a group onium salt or an aromatic onium salt and a reducing agent.
- proton acids such as sulfuric acid, phosphoric acid, perchloric acid and trifluoromethanesulfonic acid
- Lewis acids such as boron trifluoride, aluminum chloride, titanium tetrachloride and tin tetrachloride
- a combined system of a group onium salt or an aromatic onium salt and a reducing agent can be used singly or in combination of two or more.
- the blending ratio of the polymerization initiator is usually 0.1 to 30 parts by weight, preferably 0.5 to 10 parts by weight with respect to 100 parts by weight of the polymerizable
- a surfactant is added to the polymerizable composition of the present invention in order to adjust the surface tension.
- the surfactant is not particularly limited, but a nonionic surfactant is usually preferable.
- a commercially available product may be used as the nonionic surfactant, and examples thereof include a nonionic surfactant that is an oligomer having a molecular weight of about several thousand, such as KH-40 manufactured by Seimi Chemical Co., Ltd.
- the blending ratio of the surfactant is usually 0.01 to 10 parts by weight, preferably 0.1 to 2 parts by weight with respect to 100 parts by weight of the polymerizable compound.
- the polymerizable composition of the present invention further includes other copolymerizable monomers, metals, metal complexes, dyes, pigments, fluorescent materials, phosphorescent materials, leveling agents, thixotropic agents, and gelling agents described later.
- Other additives such as polysaccharides, ultraviolet absorbers, infrared absorbers, antioxidants, ion exchange resins, and metal oxides such as titanium oxide may be blended.
- the blending ratio of other additives is usually 0.1 to 20 parts by weight per 100 parts by weight of the polymerizable compound.
- the polymerizable composition of the present invention can be usually prepared by mixing and dissolving a predetermined amount of the polymerizable compound of the present invention, a polymerization initiator, and optionally other additives in an appropriate organic solvent. .
- Organic solvents to be used include ketones such as cyclopentanone, cyclohexanone and methyl ethyl ketone; acetate esters such as butyl acetate and amyl acetate; halogenated hydrocarbons such as chloroform, dichloromethane and dichloroethane; 1,4-dioxane, cyclopentylmethyl And ethers such as ether, tetrahydrofuran, tetrahydropyran, and 1,3-dioxolane;
- ketones such as cyclopentanone, cyclohexanone and methyl ethyl ketone
- acetate esters such as butyl acetate and amyl acetate
- halogenated hydrocarbons such as chloroform, dichloromethane and dichloroethane
- 1,4-dioxane 1,4-dioxane
- cyclopentylmethyl And ethers such as
- the polymerizable composition obtained as described above is useful as a raw material for producing the polymer and optical anisotropic body of the present invention, as will be described later.
- the third of the present invention is (1) a polymer obtained by polymerizing the polymerizable compound of the present invention, or (2) a polymer obtained by polymerizing the polymerizable composition of the present invention. is there.
- polymerization means a chemical reaction in a broad sense including a crosslinking reaction in addition to a normal polymerization reaction.
- Polymer obtained by polymerizing the polymerizable compound of the present invention includes a homopolymer of the polymerizable compound of the present invention and the polymerizability of the present invention. Examples thereof include a copolymer composed of two or more kinds of compounds, or a copolymer of the polymerizable compound of the present invention and another copolymerizable monomer.
- the other copolymerizable monomer is not particularly limited, and examples thereof include 4- (2-methacryloyloxyethyloxy) benzoic acid-4′-methoxyphenyl and 4- (6-methacryloyloxyhexyl).
- LC-242 manufactured by BASF
- the compounds disclosed in the above can also be used.
- polyfunctional monomers having a plurality of polymerizable unsaturated groups such as acryloyl group, methacryloyl group, vinyl group and allyl group can be used.
- polyfunctional monomers include 1,2-butanediol diacrylate, 1,3-butanediol diacrylate, 1,4-butanediol diacrylate, neopentanediol diacrylate, and 1,6-hexanediol.
- Alkanediol diacrylates such as diacrylate; 1,2-butanediol dimethacrylate, 1,3-butanediol dimethacrylate, 1,4-butanediol dimethacrylate, neopentanediol dimethacrylate, 1,6-hexanediol di
- Alkanediol dimethacrylates such as metalylate; polyethylene glycols such as ethylene glycol diacrylate, diethylene glycol diacrylate, triethylene glycol diacrylate, tetraethylene glycol diacrylate Acrylates; polypropylene glycol diacrylates such as propylene glycol diacrylate, dipropylene glycol diacrylate, tripropylene glycol diacrylate, tetrapropylene glycol diacrylate; ethylene glycol dimethacrylate, diethylene glycol dimethacrylate, triethylene glycol dimethacrylate, tetraethylene Polyethylene glycol dimethacrylates
- (Co) polymerization of the polymerizable compound of the present invention and other copolymerizable monomers used as necessary can be carried out in the presence of a suitable polymerization initiator.
- the proportion of the polymerization initiator used may be the same as the proportion of the polymerizable compound in the polymerizable composition.
- the content of the polymerizable compound unit of the present invention is particularly limited. However, it is preferably 50% by weight or more, more preferably 70% by weight or more based on the total structural units. If it exists in this range, since the glass transition temperature (Tg) of a polymer is high and high film
- Tg glass transition temperature
- the polymer of (1) includes (A) the polymerizable compound in the presence of a suitable polymerization initiator, and other copolymerizable monomers used as necessary. (Co) polymerization in a suitable organic solvent, the target polymer is isolated, and the resulting polymer is dissolved in a suitable organic solvent to prepare a solution.
- a solution prepared by dissolving, for example, a polymerization initiator together with a polymerization initiator on a substrate by a known coating method, then removing the solvent, and then heating or irradiating active energy rays to perform a polymerization reaction is preferable.
- the polymerization initiator to be used include those exemplified as the components of the polymerizable composition.
- the organic solvent used in the polymerization reaction (A) is not particularly limited as long as it is inert.
- aromatic hydrocarbons such as toluene, xylene and mesitylene
- ketones such as cyclohexanone, cyclopentanone and methyl ethyl ketone
- acetate esters such as butyl acetate and amyl acetate
- halogenated hydrocarbons such as chloroform, dichloromethane and dichloroethane
- ethers such as cyclopentyl methyl ether, tetrahydrofuran and tetrahydropyran;
- those having a boiling point of 60 to 250 ° C. are preferred, and those having a temperature of 60 to 150 ° C. are more preferred, from the viewpoint of excellent handleability.
- Examples of the organic solvent for dissolving the polymer in the method (A) and the organic solvent used in the method (B) include ketone solvents such as acetone, methyl ethyl ketone, methyl isobutyl ketone, cyclopentanone, and cyclohexanone; Ester solvents such as butyl acetate and amyl acetate; halogenated hydrocarbon solvents such as dichloromethane, chloroform and dichloroethane; tetrahydrofuran, tetrahydropyran, 1,2-dimethoxyethane, 1,4-dioxane, cyclopentylmethyl ether, 1,3 -Ether solvents such as dioxolane; aprotic polar solvents such as N, N-dimethylformamide, N, N-dimethylacetamide, dimethyl sulfoxide, ⁇ -butyrolactone, N-methylpyrrolidone; and the like.
- a substrate to be used a known and usual material can be used regardless of organic or inorganic.
- organic materials include polycycloolefins (for example, ZEONEX, ZEONOR (registered trademark; manufactured by ZEON CORPORATION), ARTON (registered trademark; manufactured by JSR), and APPEL (registered trademark; manufactured by Mitsui Chemicals)), polyethylene terephthalate.
- inorganic materials include silicon, glass, calcite, etc. Of these, organic materials are preferred.
- the substrate used may be a single layer or a laminate. As the substrate, an organic material is preferable, and a resin film using the organic material as a film is more preferable.
- a known method can be used, for example, a curtain coating method.
- polymer obtained by polymerizing the polymerizable composition of the present invention The polymer of the present invention can be easily obtained by polymerizing the polymerizable composition of the present invention.
- a polymerizable composition containing a polymerization initiator as described above, particularly a photopolymerization initiator it is preferable to use a polymerizable composition containing a polymerization initiator as described above, particularly a photopolymerization initiator.
- the polymer of the present invention by applying the method (B), that is, the polymerizable composition of the present invention onto a substrate and polymerizing the same.
- the substrate to be used include a substrate used for producing an optical anisotropic body described later.
- Examples of the method for applying the polymerizable composition of the present invention on a substrate include known and commonly used coating methods such as bar coating, spin coating, roll coating, gravure coating, spray coating, die coating, cap coating, and dipping. .
- a known and commonly used organic solvent may be added to the polymerizable composition of the present invention. In this case, it is preferable to remove the organic solvent by natural drying, heat drying, reduced pressure drying, reduced pressure heat drying or the like after applying the polymerizable composition of the present invention on the substrate.
- Examples of the method for polymerizing the polymerizable compound or the polymerizable composition of the present invention include a method of irradiating active energy rays, a thermal polymerization method, etc., but it is active because the reaction proceeds at room temperature without requiring heating.
- a method of irradiating energy rays is preferable.
- a method of irradiating light such as ultraviolet rays is preferable because the operation is simple.
- the temperature during irradiation is preferably 30 ° C. or lower.
- the light irradiation intensity is usually in the range of 1 W / m 2 to 10 kW / m 2 , preferably in the range of 5 W / m 2 to 2 kW / m 2 .
- the polymer obtained by polymerizing the polymerizable compound or polymerizable composition of the present invention can be used as a single substance by peeling from the substrate, or it can be used as it is as an organic material for an optical film without peeling from the substrate. You can also.
- the number average molecular weight of the polymer of the present invention obtained as described above is preferably 500 to 500,000, more preferably 5,000 to 300,000. If the number average molecular weight is within such a range, a high film hardness can be obtained and handleability is excellent, which is desirable.
- the number average molecular weight of the polymer can be measured by gel permeation chromatography (GPC) using monodispersed polystyrene as a standard sample and tetrahydrofuran as an eluent.
- the polymer of the present invention is presumed that the cross-linking points exist uniformly in the molecule, has high cross-linking efficiency, and is excellent in hardness. According to the polymer of the present invention, an optical film that can perform uniform polarization conversion in a wide wavelength range and is satisfactory in terms of performance can be obtained at low cost.
- optical anisotropic body of the present invention comprises the polymer of the present invention as a constituent material.
- the optical anisotropic body of the present invention can be obtained, for example, by forming an alignment film on a substrate and further forming a liquid crystal layer made of the polymer of the present invention on the alignment film.
- the alignment film is formed on the surface of the substrate in order to regulate the alignment of the organic semiconductor compound in one direction in the plane.
- the alignment film is formed by applying a solution (composition for alignment film) containing a polymer such as polyimide, polyvinyl alcohol, polyester, polyarylate, polyamideimide, or polyetherimide onto the substrate in a film shape, drying, and unidirectional It can be obtained by rubbing.
- the thickness of the alignment film is preferably 0.001 to 5 ⁇ m, and more preferably 0.001 to 1 ⁇ m.
- the alignment film or the substrate can be rubbed.
- the rubbing treatment method is not particularly limited, and examples thereof include a method of rubbing the alignment film in a certain direction with a roll made of a synthetic fiber such as nylon or a natural fiber such as cotton or a felt.
- a function of regulating the alignment in one direction within the plane can also be provided by a method of irradiating the surface of the alignment film with polarized ultraviolet rays.
- the method for forming the liquid crystal layer comprising the polymer of the present invention on the alignment film includes the same method as described in the section of the polymer of the present invention.
- the optical anisotropic body of the present invention is composed of the polymer of the present invention, the optical anisotropic body can be manufactured at low cost and can perform uniform polarization conversion in a wide wavelength range, and has excellent performance. is there.
- the optical anisotropic body of the present invention include a retardation plate, an alignment film for liquid crystal display elements, a polarizing plate, a viewing angle widening plate, a color filter, a low-pass filter, a light polarizing prism, and various optical filters.
- the structure of the target product was identified by 1 H-NMR.
- a three-necked reactor equipped with a thermometer was charged with 2.00 g (2.92 mmol) of the intermediate A synthesized in Step 1 and 20 ml of tetrahydrofuran (THF) in a nitrogen stream to obtain a uniform solution.
- THF tetrahydrofuran
- 60 ml of ethanol and 0.38 g (2.92 mmol) of thiosemicarbazide hydrochloride were added, and the whole volume was stirred at 25 ° C. for 1.5 hours. Thereafter, 0.72 g (2.92 mmol) of 2-bromoacetylnaphthalene was added, and the mixture was further stirred at the same temperature for 2 hours.
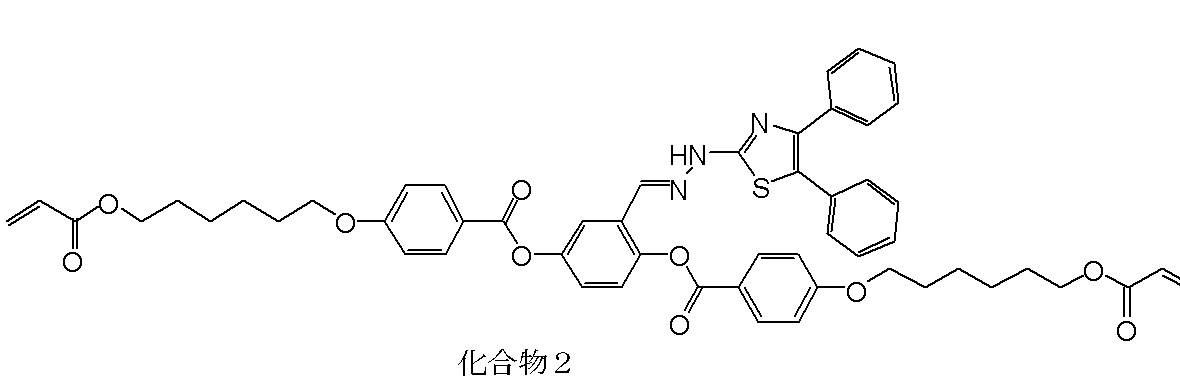
- Step 2 Synthesis of Compound 2> A three-necked reactor equipped with a thermometer was charged with 3.75 g (5.45 mmol) of Intermediate A synthesized in Step 1 of Example 1 and 30 ml of THF in a nitrogen stream to obtain a uniform solution. To this solution, 90 ml of ethanol and 0.7 g (5.45 mmol) of thiosemicarbazide hydrochloride were added, and the whole volume was stirred at 25 ° C. for 2 hours. Thereafter, 1.25 g (5.45 mmol) of 2-chloro-2-phenylacetophenone was added, and the mixture was further stirred at 60 ° C. for 3 hours.
- Step 2 Synthesis of Compound A>
- 10.5 g (15.3 mmol) of the intermediate A synthesized in Step 1 of Synthesis Example 1 above 3.0 g of 2-hydrazinobenzothiazole (18 .3 mmol) and 80 ml of tetrahydrofuran (THF) were added to obtain a uniform solution.
- 18 mg (0.08 mmol) of ( ⁇ ) -10-camphorsulfonic acid was added, and the whole volume was stirred at 25 ° C. for 3 hours.
- the reaction solution was poured into 800 ml of 10% sodium bicarbonate water and extracted twice with 100 ml of ethyl acetate.
- the ethyl acetate layer was collected and dried over anhydrous sodium sulfate, and sodium sulfate was filtered off.
- Ethyl acetate was distilled off from the filtrate under reduced pressure using a rotary evaporator to obtain a pale yellow solid.
- the structure of the target product was identified by 1 H-NMR and mass spectrum.
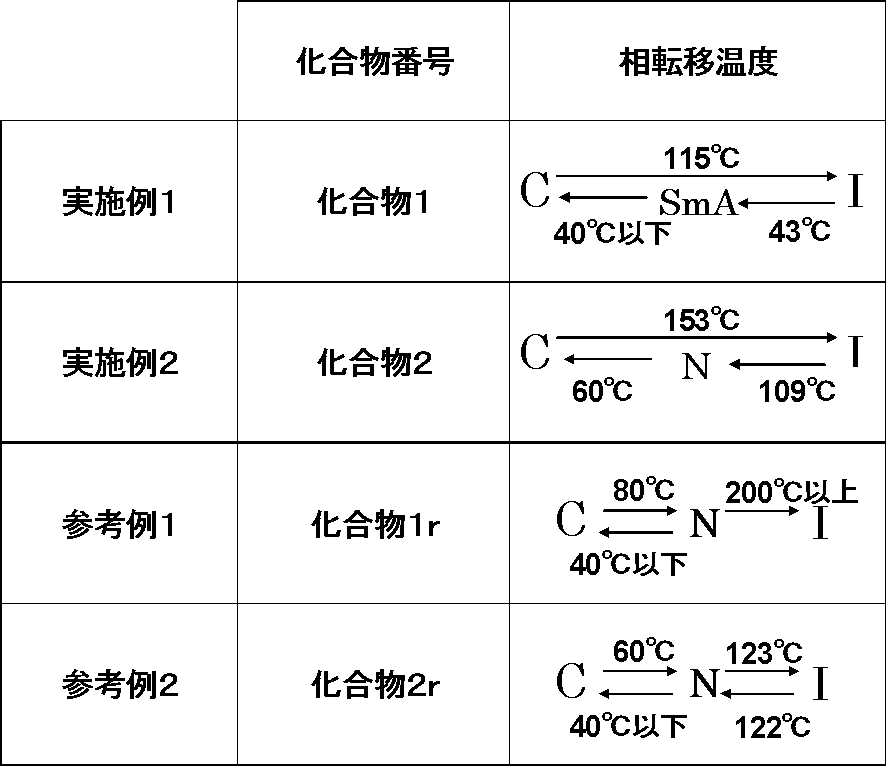
- phase transition temperature 10 mg of each of the compounds 1, 2, 1r and 2r was weighed and kept in a solid state, and a glass substrate with a polyimide alignment film subjected to rubbing treatment (trade name: orientation-treated glass substrate; EHC Co., Ltd.). , Ltd.) between two sheets. This substrate was placed on a hot plate, heated from 40 ° C. to 200 ° C., and then cooled again to 40 ° C. Changes in the structure of the structure when the temperature was raised or lowered were observed with a polarizing optical microscope (Nikon Corporation, ECLIPSE LV100POL type). The measured phase transition temperatures are shown in Table 1 below.
- C represents Crystal
- N represents Nematic
- I represents Isotropic
- SmA represents Smatic A
- Crystal means that the test compound is in the solid phase
- Nematic means that the test compound is in the nematic liquid crystal phase
- Isotropic means that the test compound is in the isotropic liquid phase. Indicates that the test compound is in the smectic A phase.
- Example 3 0.5 g of the compound 1 obtained in Example 1, 0.5 g of the compound A obtained in Synthesis Example 2, and Adekaoptomer N-1919 (manufactured by ADEKA, the same applies hereinafter) as a photopolymerization initiator.
- 30 mg and 100 mg of a 1% cyclopentanone solution of KH-40 (manufactured by AGC Seimi Chemical Co., the same below) as a surfactant was dissolved in 2.2 g of cyclopentanone. This solution was filtered through a disposable filter having a pore diameter of 0.45 ⁇ m to obtain a polymerizable composition 1.
- Example 4 0.5 g of the compound 2 obtained in Example 2, 0.5 g of the compound A obtained in Synthesis Example 2, 30 mg of Adekaoptomer N-1919 as a photopolymerization initiator, and KH— as a surfactant 40 mg of a 1% cyclopentanone solution was dissolved in 2.2 g of cyclopentanone. This solution was filtered through a disposable filter having a pore diameter of 0.45 ⁇ m to obtain a polymerizable composition 2.
- ⁇ In the case of ideal wavelength dispersion exhibiting broadband characteristics, that is, reverse wavelength dispersion, ⁇ is smaller than 1 and ⁇ is larger than 1. In the case of flat chromatic dispersion, ⁇ and ⁇ have the same value. If it has a general normal variance, ⁇ will be greater than 1 and ⁇ will be less than 1. That is, flat wavelength dispersibility in which ⁇ and ⁇ are approximately the same is preferable, and reverse wavelength dispersibility in which ⁇ is smaller than 1 and ⁇ is larger than 1 is particularly preferable.
- the polymers obtained in Examples 1 and 2 according to the present invention are optically anisotropic.
- the ⁇ and ⁇ values of the obtained optical anisotropic body are approximately the same, and the ⁇ value is larger than ⁇ , which has a preferable reverse wavelength dispersion.
Abstract
Description
しかしながら、従来の位相差板には、位相差板を通過して出力される偏光が有色の偏光に変換されてしまうという問題があった。これは、位相差板を構成する材料が位相差について波長分散性を有し、可視光域の光線が混在する合成波である白色光に対して各波長ごとの偏光状態に分布が生じることから、全ての波長領域において正確な1/4λ又は1/2λの位相差に調整することが不可能であることに起因する。
このような問題を解決するため、広い波長域の光に対して均一な位相差を与え得る広帯域位相差板、いわゆる逆波長分散性を有する位相差板が種々検討されている(特許文献1~6)。
薄層化の方法としては、フィルム基材に低分子重合性化合物を含有する重合性組成物を塗布することにより位相差板を作成する方法が、近年では最も有効な方法とされている。優れた波長分散性を有する低分子重合性化合物又はそれを用いた重合性組成物の開発が多く行われている(特許文献7~24)。
(1)下記式(I)
G1、G2はそれぞれ独立して、置換基を有していてもよい炭素数1~20の2価の脂肪族基を表す〔該脂肪族基には、-O-、-S-、-O-C(=O)-、-C(=O)-O-、-O-C(=O)-O-、-NR2-C(=O)-、-C(=O)-NR2-、-NR2-、又は、-C(=O)-が介在していてもよい。ただし、-O-又は-S-がそれぞれ2以上隣接して介在する場合を除く。ここで、R2は、水素原子又は炭素数1~6のアルキル基を表す。〕。
Z1、Z2はそれぞれ独立して、ハロゲン原子で置換されていてもよい炭素数2~10のアルケニル基を表す。
Axは下記式(II)
Ayは水素原子、置換基を有していてもよい炭素数1~20のアルキル基、置換基を有していてもよい炭素数2~20のアルケニル基、置換基を有していてもよい炭素数3~12のシクロアルキル基、又は、前記式(II)で表される基を示す。
A1は、置換基を有していてもよい三価の芳香族基を表す。
A2、A3はそれぞれ独立して、置換基を有していてもよい炭素数3~30の二価の脂環式炭化水素基を表す。
A4、A5はそれぞれ独立して、置換基を有していてもよい炭素数4~30の二価の芳香族基を表す。
Q1は、水素原子、又は、置換基を有していてもよい炭素数1~6のアルキル基を表す。m、nはそれぞれ独立して、0又は1を表す。〕で示される重合性化合物。
(4)前記Y1~Y8がそれぞれ独立して、化学的な単結合、-O-、-O-C(=O)-、-C(=O)-O-、又は、-O-C(=O)-O-である(1)に記載の重合性化合物。
(5)前記Z1、Z2がそれぞれ独立して、CH2=CH-、CH2=C(CH3)-、又は、CH2=C(Cl)-である(1)に記載の重合性化合物。
(6)前記G1、G2がそれぞれ独立して、置換基を有していてもよい炭素数1~12の2価の脂肪族基〔該脂肪族基には、-O-、-O-C(=O)-、-C(=O)-O-又は-C(=O)-が介在していてもよい。ただし、-O-が2以上隣接して介在する場合を除く。〕である(1)に記載の重合性化合物。
(8)前記(1)~(7)のいずれかに記載の重合性化合物を少なくとも1種類含有する重合性組成物。
(9)前記(1)~(7)のいずれかに記載の重合性化合物、及び重合開始剤を含有する重合性組成物。
(11)液晶性高分子である(10)に記載の高分子。
(12)前記(11)に記載の高分子を構成材料とする光学異方体。
本発明の光学異方体は、本発明の高分子を構成材料とするため、低コストで得られ、広い波長域において一様の偏光変換が可能な、性能面で満足のいくものである。
その具体的な実用例としては、本発明のフィルム状の光学異方体を偏光板と組み合わせることで反射防止フィルムを作製することができる。このものは、産業上例えばタッチパネルや有機電界発光素子の反射防止に好適に使用することができる。
本発明の重合性化合物は、前記式(I)で表される化合物(化合物(I))である。
式中、Y1~Y8はそれぞれ独立して、化学的な単結合、-O-、-S-、-O-C(=O)-、-C(=O)-O-、-O-C(=O)-O-、-NR1-C(=O)-、-C(=O)-NR1-、-O-C(=O)-NR1-、-NR1-C(=O)-O-、-NR1-C(=O)-NR1-、-O-NR1-、又は、-NR1-O-を表す。
R1の炭素数1~6のアルキル基としては、メチル基、エチル基、n-プロピル基、イソプロピル基、n-ブチル基、sec-ブチル基、t-ブチル基、n-ペンチル基、n-へキシル基等が挙げられる。
R1としては、水素原子又は炭素数1~4のアルキル基が好ましい。
炭素数1~20の2価の脂肪族基としては、鎖状構造を有する2価の脂肪族基;飽和環状炭化水素(シクロアルカン)構造、不飽和環状炭化水素(シクロアルケン)構造等の脂環式構造を有する2価の脂肪族基;等が挙げられる。
前記脂肪族基に介在する基としては、-O-、-O-C(=O)-、-C(=O)-O-、-C(=O)-が好ましい。
該アルケニル基の炭素数としては、2~6が好ましい。Z1及びZ2のアルケニル基の置換基であるハロゲン原子としては、フッ素原子、塩素原子、臭素原子等が挙げられ、塩素原子が好ましい。
式(II)中、Xは窒素原子又は炭素原子を表し、窒素原子が好ましい。
式(II)中、Ra、Rbはそれぞれ独立して、水素原子、置換基を有していてもよい炭素数1~20のアルキル基、置換基を有していてもよい炭素数2~20のアルケニル基、置換基を有していてもよい炭素数3~18のシクロアルキル基、置換基を有していてもよい炭素数1~20の芳香族炭化水素環基、置換基を有していてもよい炭素数1~20の芳香族複素環基を表す。
Ra、Rbの、置換基を有していてもよい炭素数1~20のアルキル基の炭素数1~20のアルキル基としては、メチル基、エチル基、n-プロピル基、イソプロピル基、n-ブチル基、sec-ブチル基、t-ブチル基、n-ペンチル基、イソペンチル基、ネオペンチル基、n-へキシル基、イソヘキシル基、n-ヘプチル基、n-オクチル基、n-ノニル基、n-デシル基、n-ウンデシル基、n-ドデシル基、n-トリデシル基、n-テトラデシル基、n-ペンタデシル基、n-ヘキサデシル基、n-ヘプタデシル基、n-オクタデシル基、n-ノナデシル基、n-イコシル基等が挙げられる。置換基を有してもよい炭素数1~20のアルキル基の炭素数は、1~12であることが好ましく、1~6であることが更に好ましい。
置換基を有していてもよい炭素数1~20の芳香族複素環基の芳香族複素環基としては、ピロール環基、フラン環基、チオフェン環基、ピリジン環基、ピリダジン環基、ピリミジン環基、ピラジン環基、ピラゾール環基、イミダゾール環基、オキサゾール環基、チアゾール環基等の単環の芳香族複素環基;ベンゾチアゾール環基、ベンゾオキサゾール環基、キノリン環基、フタラジン環基、ベンゾイミダゾール環基、ベンゾピラゾール環基、ベンゾフラン環基、ベンゾチオフェン環基等の縮合環の芳香族複素環基;等が挙げられる。
RXは、水素原子;フッ素原子、塩素原子、臭素原子等のハロゲン原子;メチル基、エチル基等の炭素数1~6のアルキル基;シアノ基;ニトロ基;メチルスルフィニル基、エチルスルフィニル基等の炭素数1~6のアルキルスルフィニル基;メチルスルホニル基、エチルスルホニル基等の炭素数1~6のアルキルスルホニル基;トリフルオロメチル基、ペンタフルオロメチル基等の炭素数1~6のフルオロアルキル基;メトキシ基、エトキシ基等の炭素数1~6のアルコキシ基;メチルチオ基、エチルチオ基等の炭素数1~6のアルキルチオ基;メチルアミノ基、エチルアミノ基等のモノ置換アミノ基;ジメチルアミノ基、ジエチルアミノ基等のジ置換アミノ基;メチルスルファモイル基等の炭素数1~6のアルキルスルファモイル基;ジメチルスルファモイル基等の炭素数2~12のジアルキルスルファモイル基;又は、-C(=O)-O-R6を表す。ここで、R6は、水素原子又は炭素数1~6のアルキル基を表す。
RXはすべて水素原子であるのが好ましい。
式(II-1)~(II-5)で表される基の中でも、本発明の所望の効果をより良好に発現させる観点から、式(II-3)、(II-4)で表される基が好ましい。
式(II-3)で表される基としては、例えば、下記式
で表される基等が挙げられる。
式(II-4)で表される基としては、例えば、下記式
で表される基等が挙げられる。
Axとしては、下記式で表される基が好ましく、
下記式で表される基がより好ましく、
下記式で表される基が特に好ましい。
これらの中でも、Ayとしては、水素原子であるのが好ましい。
なお、下記式においては、結合状態をより明確にすべく、置換基Y1、Y2を便宜上記載している(Y1、Y2は、前記と同じ意味を表す。以下にて同じ。)。
炭素数3~30の二価の脂環式炭化水素基としては、炭素数3~30のシクロアルカンジイル基、炭素数10~30の二価の脂環式縮合環基等が挙げられる。
前記炭素数3~30の二価の脂環式炭化水素基は、Y1、Y3(又はY2、Y4)と結合する炭素原子の立体配置の相違に基づく、シス型、トランス型の立体異性体が存在し得る。例えば、シクロヘキサン-1,4-ジイル基の場合には、下記に示すように、シス型の異性体(A32a)とトランス型の異性体(A32b)が存在し得る。
A4、A5の芳香族基は単環のものであっても、多環のものであってもよい。
A4、A5の具体例としては、下記のものが挙げられるが、これらに限定されない。
置換基を有していてもよい炭素数1~6のアルキル基としては、前記AXで例示したのと同様のものが挙げられる。
これらの中でも、Q1は、水素原子又は炭素数1~6のアルキル基が好ましく、水素原子又はメチル基がより好ましい。
また、m、nはそれぞれ独立して、0又は1を表し、双方が0であることが好ましい。
なお、本発明化合物には、炭素-窒素二重結合に基づく立体異性体が存在し得るが、これらはすべて本発明に含まれる。
(1)製造方法1
本発明の重合性化合物のうち、Ayが水素原子で、AxのXが窒素原子である化合物である化合物である、下記式(Ia)で表される化合物は、次のようにして製造することができる。
すなわち、先ず、式(4)で表されるカルボニル化合物(カルボニル化合物(4))に、当モルのチオセミカルバジド塩酸塩(1)を加えて反応させ(反応1)、次いで、当モルの式(2)で表される化合物(化合物(2))を加えて反応させること(反応2)により、目的とする本発明の式(Ia)で示される重合性化合物を製造することができる。
これらの中でも、アルコール系溶媒、エーテル系溶媒、及びアルコール系溶媒とエーテル系溶媒の混合溶媒が好ましい。
本発明の重合性化合物(I)は、下記に示す反応によっても製造することができる。
すなわち、式(5)で表されるヒドラジン化合物(ヒドラジン化合物(5))を、式(4)で表されるカルボニル化合物(カルボニル化合物(4))と、〔ヒドラジン化合物(5):カルボニル化合物(4)〕のモル比で、1:2~2:1、好ましくは1:1.5~1.5:1の割合で反応させることにより、高選択的かつ高収率で目的とする本発明の式(I)で示される重合性化合物を製造することができる。
これらの中でも、アルコール系溶媒、エーテル系溶媒、及びアルコール系溶媒とエーテル系溶媒の混合溶媒が好ましい。
この反応に用いる溶媒としては、反応に不活性なものであれば特に限定されない。例えば、メチルアルコール、エチルアルコール、n-プロピルアルコール、イソプロピルアルコール、n-ブチルアルコール、イソブチルアルコール、sec-ブチルアルコール、t-ブチルアルコール等のアルコール系溶媒;ジエチルエーテル、テトラヒドロフラン、1,2-ジメトキシエタン、1,4-ジオキサン、シクロペンチルメチルエーテル等のエーテル系溶媒;ベンゼン、トルエン、キシレン等の芳香族炭化水素系溶媒;n-ペンタン、n-ヘキサン、n-ヘプタン等の脂肪族炭化水素系溶媒;N,N-ジメチルホルムアミド、N-メチルピロリドン、ヘキサメチルリン酸トリアミド等のアミド系溶媒;ジメチルスルホキシド、スルホラン等の含硫黄系溶媒;及びこれらの2種以上からなる混合溶媒;等が挙げられる。
これらの中でも、アルコール系溶媒、エーテル系溶媒、及びアルコール系溶媒とエーテル系溶媒の混合溶媒が好ましい。
反応は、-10℃から用いる溶媒の沸点までの温度範囲で円滑に進行する。各反応の反応時間は、反応規模にもよるが、通常、数分から数時間である。
金属塩還元剤とは、一般に低原子価金属を含む化合物、もしくは金属イオンとヒドリド源からなる化合物である(「有機合成実験法ハンドブック」1990年社団法人有機合成化学協会編 丸善株式会社発行810ページを参照)。
金属塩還元剤としては、NaAlH4、NaAlHp(Or)q(p、qはそれぞれ独立して1~3の整数を表し、p+q=4である。rは炭素数1~6のアルキル基を表す。)、LiAlH4、iBu2AlH、LiBH4、NaBH4、SnCl2、CrCl2、TiCl3等が挙げられる。
また、ジアゾニウム塩(8)は、アニリン等の化合物から常法により製造することができる。
(i)式:D1-hal(halはハロゲン原子を表す。以下にて同じ。)で表される化合物と、式:D2-OMet(Metはアルカリ金属(主にナトリウム)を表す。以下にて同じ。)で表される化合物とを混合して縮合させる(ウイリアムソン合成)。なお、式中、D1及びD2は任意の有機基を表す(以下にて同じ。)
(ii)式:D1-halで表される化合物と、式:D2-OHで表される化合物とを水酸化ナトリウム、水酸化カリウム等の塩基存在下、混合して縮合させる。
(iii)式:D1-J(Jはエポキシ基を表す。)で表される化合物と、式:D2-OHで表される化合物とを水酸化ナトリウム、水酸化カリウム等の塩基存在下、混合して縮合させる。
(iv)式:D1-OFN(OFNは不飽和結合を有する基を表す。)で表される化合物と、式:D2-OMetで表される化合物を、水酸化ナトリウム、水酸化カリウム等の塩基存在下、混合して付加反応させる。
(v)式:D1-halで表される化合物と、式:D2-OMetで表される化合物とを、銅又は塩化第一銅存在下、混合して縮合させる(ウルマン縮合)。
(vi)式:D1-COOHで表される化合物と、式:D2-OH又はD2-NH2で表される化合物とを、脱水縮合剤(N,N-ジシクロヘキシルカルボジイミド等)の存在下に脱水縮合させる。
(vii)式:D1-COOHで表される化合物にハロゲン化剤を作用させることにより、式:D1-CO-halで表される化合物を得、このものと式:D2-OH又はD2-NH2で表される化合物とを、塩基の存在下に反応させる。
(viii)式:D1-COOHで表される化合物に酸無水物を作用させることにより、混合酸無水物を得た後、このものに、式:D2-OH又はD2-NH2で表される化合物を反応させる。
(ix)式:D1-COOHで表される化合物と、式:D2-OH又はD2-NH2で表される化合物とを、酸触媒又は塩基触媒の存在下に脱水縮合させる。
脱水縮合剤の使用量は、化合物(10)1モルに対し、通常1~3モルである。
用いる塩基としては、トリエチルアミン、ピリジン等の有機塩基;水酸化ナトリウム、炭酸ナトリウム、炭酸水素ナトリウム等の無機塩基が挙げられる。
塩基の使用量は、化合物(10)1モルに対し、通常1~3モルである。
化合物(10)が、式(10)中、Lがメタンスルホニルオキシ基、又はp-トルエンスルホニルオキシ基の化合物(混合酸無水物)である場合もハロゲン原子の場合と同様である。
溶媒の使用量は、特に限定されず、用いる化合物の種類や反応規模等を考慮して適宜定めることができるが、ジヒドロキシ化合物(9)1gに対し、通常1~50gである。
本発明の第2は、本発明の重合性化合物、及び重合開始剤を含有する重合性組成物である。重合開始剤は本発明の重合性化合物の重合反応をより効率的に行う観点から配合される。
「水素供与体」とは、露光によりビイミダゾール系化合物から発生したラジカルに対して、水素原子を供与することができる化合物を意味する。水素供与体としては、下記で定義するメルカプタン系化合物、アミン系化合物等が好ましい。
これらの重合開始剤は一種単独で、又は二種以上を組み合わせて用いることができる。
本発明の重合性組成物において、重合開始剤の配合割合は、重合性化合物100重量部に対し、通常、0.1~30重量部、好ましくは0.5~10重量部である。
本発明の第3は、(1)本発明の重合性化合物を重合して得られる高分子、又は、(2)本発明の重合性組成物を重合して得られる高分子である。
ここで、「重合」とは、通常の重合反応のほか、架橋反応を含む広い意味での化学反応を意味するものとする。
本発明の重合性化合物を重合して得られる高分子としては、本発明の重合性化合物の単独重合体、本発明の重合性化合物の2種以上からなる共重合体、又は、本発明の重合性化合物と他の共重合可能な単量体との共重合体が挙げられる。
市販品としては、LC-242(BASF社製)等を用いることができる。また、特開2007-002208号公報、特開2009-173893号公報、特開2009-274984号公報、特開2010-030979号公報、特開2010-031223号公報、特開2011-006360号公報等に開示されている化合物等も用いることができる。
このような多官能単量体としては、1,2-ブタンジオールジアクリレート、1,3-ブタンジオールジアクリレート、1,4-ブタンジオールジアクリレート、ネオペンタンジオールジアクリレート、1,6-ヘキサンジオールジアクリレート等のアルカンジオールジアクリレート類;1,2-ブタンジオールジメタクリレート、1,3-ブタンジオールジメタクリレート、1,4-ブタンジオールジメタクリレート、ネオペンタンジオールジメタクリレート、1,6-ヘキサンジオールジメタリレート等のアルカンジオールジメタクリレート類;エチレングリコールジアクリレート、ジエチレングリコールジアクリレート、トリエチレングリコールジアクリレート、テトラエチレングリコールジアクリレート等のポリエチレングリコールジアクリレート類;プロピレングリコールジアクリレート、ジプロピレングリコールジアクリレート、トリプロピレングリコールジアクリレート、テトラプロピレングリコールジアクリレート等のポリプロピレングリコールジアクリレート類;エチレングリコールジメタクリレート、ジエチレングリコールジメタクリレート、トリエチレングリコールジメタクリレート、テトラエチレングリコールジメタクリレート等のポリエチレングリコールジメタクリレート類;プロピレングリコールジメタクリレート、ジプロピレングリコールジメタクリレート、トリプロピレングリコールジメタクリレート、テトラプロピレングリコールジメタクリレート等のポリプロピレングリコールジメタクリレート類;エチレングリコールジビニルエーテル、ジエチレングリコールジビニルエーテル、トリエチレングリコールジビニルエーテル、テトラエチレングリコールジビニルエーテル等のポリエチレングリコールジビニルエーテル類;エチレングリコールジアリルエーテル、ジエチレングリコールジアリルエーテル、トリエチレングリコールジアリルエーテル、テトラエチレングリコールジアリルエーテル等のポリエチレングリコールジアリルエーテル類;ビスフェノールFエトキシレートジアクリレート;ビスフェノールFエトキシレートジメタクリレート;ビスフェノールAエトキシレートジアクリレート;ビスフェノールAエトキシレートジメタクリレート;トリメチロールプロパントリアクリレート;トリメチロールプロパントリメタクリレート;トリメチロールプロパンエトキシレートトリアクリレート;トリメチロールプロパンエトキシレートトリメタクリレート;トリメチロールプロパンプロポキシレートトリアクリレート;トリメチロールプロパンプロポキシレートトリメタクリレート;イソシアヌル酸エトキシレートトリアクリレート;グリセロールエトキシレートトリアクリレート;グリセロールプロポキシレートトリアクリレート;ペンタエリスリトールエトキシレートテトラアクリレート;ジトリメチロールプロパンエトキリレートテトラアクリレート;ジペンタエリスリトールエトキシレートヘキサアクリレート等が挙げられる。
用いる重合開始剤としては、前記重合性組成物の成分として例示したのと同様のものが挙げられる。
また、用いる基板は、単層のものであっても、積層体であってもよい。
基板としては、有機材料が好ましく、この有機材料をフィルムとした樹脂フィルムが更に好ましい。
本発明の重合性組成物を重合することにより、本発明の高分子を容易に得ることができる。本発明においては、重合反応をより効率的に行う観点から、前記したような重合開始剤、特に光重合開始剤を含む重合性組成物を用いるのが好ましい。
本発明の高分子によれば、広い波長域において一様の偏光変換が可能な、性能面で満足のいく光学フィルムを低コストで得ることができる。
本発明の光学異方体は、本発明の高分子を構成材料とする。
本発明の光学異方体は、例えば、基板上に配向膜を形成し、該配向膜上に、さらに、本発明の高分子からなる液晶層を形成することによって、得ることができる。
配向膜は、ポリイミド、ポリビニルアルコール、ポリエステル、ポリアリレート、ポリアミドイミド、ポリエーテルイミド等のポリマーを含有する溶液(配向膜用組成物)を基板上に膜状に塗布し、乾燥させ、そして一方向にラビング処理等することで、得ることができる。
配向膜の厚さは0.001~5μmであることが好ましく、0.001~1μmであることがさらに好ましい。
また、ラビング処理する方法以外に、配向膜の表面に偏光紫外線を照射する方法によっても、面内で一方向に配向規制する機能を持たせることができる。
本発明の光学異方体としては、位相差板、液晶表示素子用配向膜、偏光板、視野角拡大板、カラーフィルター、ローパスフィルター、光偏光プリズム、各種光フィルター等が挙げられる。
目的物の構造は1H-NMRで同定した。
目的物の構造は1H-NMRで同定した。
温度計を備えた3つ口反応器に、窒素気流中、実施例1のステップ1で合成した中間体A 3.75g(5.45mmol)とTHF30mlを入れ、均一な溶液とした。この溶液に、エタノール90mlとチオセミカルバジド塩酸塩 0.7g(5.45mmol)を加え、全容を25℃で2時間攪拌した。その後、2-クロロ-2-フェニルアセトフェノン 1.25g(5.45mmol)を加え、60℃でさらに3時間攪拌した。反応終了後、反応液に、蒸留水200mlと飽和食塩水70mlを加え、酢酸エチル300mlで2回抽出した。有機層を集め、無水硫酸ナトリウムで乾燥し、硫酸ナトリウムをろ別した。ロータリーエバポレーターにてろ液を減圧濃縮し、残留物をシリカゲルカラムクロマトグラフィー(クロロホルム:THF=97:3)により精製し、淡黄色固体として化合物2を1.15g得た(収率:22%)。
目的物の構造は1H-NMRで同定した。
温度計を備えた4つ口反応器に、窒素気流中、先の合成例1のステップ1で合成した中間体A 10.5g(15.3mmol)、2-ヒドラジノベンゾチアゾール 3.0g(18.3mmol)、及びテトラヒドロフラン(THF)80mlを入れ、均一な溶液とした。この溶液に、(±)-10-カンファースルホン酸18mg(0.08mmol)を加え、全容を25℃にて3時間撹拌した。反応終了後、反応液を10%重曹水800mlに投入し、酢酸エチル100mlで2回抽出した。酢酸エチル層を集め、無水硫酸ナトリウムで乾燥し、硫酸ナトリウムをろ別した。ロータリーエバポレーターにてろ液から酢酸エチルを減圧留去して、淡黄色固体を得た。この淡黄色固体をシリカゲルカラムクロマトグラフィー(トルエン:酢酸エチル=8:2(体積比))により精製し、淡黄色固体として化合物Aを8.0g得た(収率:62.7%)。
目的物の構造は1H-NMR、マススペクトルで同定した。
化合物1、2、1r及び2rを、それぞれ10mg計量し、固体状態のままで、ラビング処理を施したポリイミド配向膜付きのガラス基板(商品名:配向処理ガラス基板;E.H.C.Co.,Ltd.製)2枚に挟んだ。この基板をホットプレート上に載せ、40℃から200℃まで昇温した後、再び40℃まで降温した。昇温、降温する際の組織構造の変化を偏光光学顕微鏡(ニコン社製、ECLIPSE LV100POL型)で観察した。測定した相転移温度を下記表1に示す。
実施例1で得られた化合物1 0.5g、合成例2で得られた化合物A 0.5g、光重合開始剤として、アデカオプトマーN-1919(ADEKA社製、以下にて同じ。)を30mg、及び、界面活性剤として、KH-40(AGCセイミケミカル社製、以下にて同じ。)の1%シクロペンタノン溶液100mgを、シクロペンタノン2.2gに溶解させた。この溶液を0.45μmの細孔径を有するディスポーサブルフィルターでろ過し、重合性組成物1を得た。
実施例2で得られた化合物2 0.5g、合成例2で得られた化合物A 0.5g、光重合開始剤として、アデカオプトマーN-1919を30mg、及び、界面活性剤として、KH-40の1%シクロペンタノン溶液100mgを、シクロペンタノン2.2gに溶解させた。この溶液を0.45μmの細孔径を有するディスポーサブルフィルターでろ過し、重合性組成物2を得た。
参考例1の化合物1r、及び参考例2の化合物2rのそれぞれを1g、光重合開始剤として、アデカオプトマーN-1919を30mg、及び、界面活性剤として、KH-40の1%シクロペンタノン溶液100mgを、シクロペンタノン2.3gに溶解させた。この溶液を0.45μmの細孔径を有するディスポーサブルフィルターでろ過し、重合性組成物1r及び2rをそれぞれ得た。
(i)重合性組成物による液晶層の形成
ラビング処理されたポリイミド配向膜の付与された透明ガラス基板(商品名:配向処理ガラス基板;E.H.C.Co.,Ltd.製)に、重合性組成物1、2、1r、2rのそれぞれを、♯4のワイヤーバーを使用して塗布した。塗膜を、下記表2に示す温度で30秒間乾燥した後、表2に示す温度で1分間配向処理し、液晶層を形成した。その後、液晶層の塗布面側から2000mJ/cm2の紫外線を照射して重合させ、波長分散測定用の試料とした。
得られた試料につき、400nmから800nm間の位相差を、エリプソメーター(J.A.Woollam社製 M2000U型)を用いて測定した。
測定した位相差を用いて以下のように算出されるα、β値から波長分散を評価した。
即ち、αとβが同程度の値となるフラットな波長分散性が好ましく、αが1より小となり、βが1より大となる逆波長分散性が特に好ましい。
Claims (12)
- 下記式(I)
G1、G2はそれぞれ独立して、置換基を有していてもよい炭素数1~20の2価の脂肪族基を表す〔該脂肪族基には、-O-、-S-、-O-C(=O)-、-C(=O)-O-、-O-C(=O)-O-、-NR2-C(=O)-、-C(=O)-NR2-、-NR2-、又は、-C(=O)-が介在していてもよい。ただし、-O-又は-S-がそれぞれ2以上隣接して介在する場合を除く。ここで、R2は、水素原子又は炭素数1~6のアルキル基を表す。〕。
Z1、Z2はそれぞれ独立して、ハロゲン原子で置換されていてもよい炭素数2~10のアルケニル基を表す。
AXは下記式(II)
Ayは、水素原子、置換基を有していてもよい炭素数1~20のアルキル基、置換基を有していてもよい炭素数2~20のアルケニル基、置換基を有していてもよい炭素数3~12のシクロアルキル基、又は、前記式(II)で表される基を示す。
A1は、置換基を有していてもよい三価の芳香族基を表す。
A2、A3はそれぞれ独立して、置換基を有していてもよい炭素数3~30の二価の脂環式炭化水素基を表す。
A4、A5はそれぞれ独立して、置換基を有していてもよい炭素数4~30の二価の芳香族基を表す。
Q1は、水素原子、又は、置換基を有していてもよい炭素数1~6のアルキル基を表す。m、nはそれぞれ独立して、0又は1を表す。}
で示される重合性化合物。 - 前記式(II)中、Ra、Rbがそれぞれ独立して、水素原子、置換基を有していてもよい炭素数1~20のアルキル基、置換基を有していてもよい炭素数2~20のアルケニル基、置換基を有していてもよい炭素数3~18のシクロアルキル基、又は、下記式(II-1)~(II-5)
- 前記A1が、置換基を有していてもよい、三価のベンゼン環基又は三価のナフタレン環基であり、A4、A5が、それぞれ独立して、置換基を有していてもよい、フェニレン基又はナフチレン基である請求項1に記載の重合性化合物。
- 前記Y1~Y8が、それぞれ独立して、化学的な単結合、-O-、-O-C(=O)-、-C(=O)-O-、又は、-O-C(=O)-O-である請求項1に記載の重合性化合物。
- 前記Z1、Z2が、それぞれ独立して、CH2=CH-、CH2=C(CH3)-、又は、CH2=C(Cl)-である請求項1に記載の重合性化合物。
- 前記G1、G2がそれぞれ独立して、置換基を有していてもよい炭素数1~12の2価の脂肪族基〔該脂肪族基には、-O-、-O-C(=O)-、-C(=O)-O-又は-C(=O)-が介在していてもよい。ただし、-O-が2以上隣接して介在する場合を除く。〕である請求項1に記載の重合性化合物。
- 前記G1、G2がそれぞれ独立して、炭素数1~12の2価のアルキレン基である請求項1に記載の重合性化合物。
- 請求項1~7のいずれかに記載の重合性化合物を少なくとも1種類含有する重合性組成物。
- 請求項1~7のいずれかに記載の重合性化合物、及び重合開始剤を含有する重合性組成物。
- 請求項1~7のいずれかに記載の重合性化合物、又は、請求項8若しくは請求項9に記載の重合性組成物を重合して得られる高分子。
- 液晶性高分子である請求項10に記載の高分子。
- 請求項11に記載の高分子を構成材料とする光学異方体。
Priority Applications (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP13848209.6A EP2913349B1 (en) | 2012-10-23 | 2013-10-16 | Polymerizable compound, polymerizable composition, polymer, and optical anistropic body |
| JP2014543251A JP6206414B2 (ja) | 2012-10-23 | 2013-10-16 | 重合性化合物、重合性組成物、高分子、及び光学異方体 |
| US14/437,748 US9777096B2 (en) | 2012-10-23 | 2013-10-16 | Polymerizable compound, polymerizable composition, polymer, and optical anisotropic body |
| KR1020157008225A KR102111538B1 (ko) | 2012-10-23 | 2013-10-16 | 중합성 화합물, 중합성 조성물, 고분자, 및 광학 이방체 |
| CN201380055206.8A CN104755513B (zh) | 2012-10-23 | 2013-10-16 | 聚合性化合物、聚合性组合物、高分子以及光学各向异性体 |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2012-233672 | 2012-10-23 | ||
| JP2012233672 | 2012-10-23 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2014065176A1 true WO2014065176A1 (ja) | 2014-05-01 |
Family
ID=50544556
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2013/078103 WO2014065176A1 (ja) | 2012-10-23 | 2013-10-16 | 重合性化合物、重合性組成物、高分子、及び光学異方体 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US9777096B2 (ja) |
| EP (1) | EP2913349B1 (ja) |
| JP (2) | JP6206414B2 (ja) |
| KR (1) | KR102111538B1 (ja) |
| CN (1) | CN104755513B (ja) |
| WO (1) | WO2014065176A1 (ja) |
Cited By (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2015064698A1 (ja) * | 2013-10-31 | 2015-05-07 | 日本ゼオン株式会社 | 重合性化合物、重合性組成物、高分子、及び光学異方体 |
| WO2016088749A1 (ja) * | 2014-12-04 | 2016-06-09 | Dic株式会社 | 重合性化合物、組成物、重合体、光学異方体、液晶表示素子及び有機el素子 |
| WO2016114348A1 (ja) * | 2015-01-16 | 2016-07-21 | Dic株式会社 | 重合性組成物及び光学異方体 |
| WO2016114066A1 (ja) * | 2015-01-16 | 2016-07-21 | Dic株式会社 | 重合性組成物及びそれを用いた光学異方体 |
| WO2016136533A1 (ja) * | 2015-02-24 | 2016-09-01 | Dic株式会社 | 重合性化合物及び光学異方体 |
| WO2017090418A1 (ja) * | 2015-11-25 | 2017-06-01 | Dic株式会社 | 重合性組成物及びそれを用いた光学異方体 |
| WO2018096938A1 (ja) | 2016-11-22 | 2018-05-31 | 日本ゼオン株式会社 | 重合性化合物、重合性組成物、高分子、光学フィルム、光学異方体、偏光板、フラットパネル表示装置、有機エレクトロルミネッセンス表示装置、反射防止フィルム、および化合物 |
| WO2018123586A1 (ja) | 2016-12-27 | 2018-07-05 | 日本ゼオン株式会社 | 重合性化合物、重合性液晶混合物、高分子、光学フィルム、光学異方体、偏光板、表示装置、反射防止フィルム、および化合物 |
| WO2018168778A1 (ja) | 2017-03-17 | 2018-09-20 | 日本ゼオン株式会社 | 重合性化合物、重合性液晶混合物、高分子、光学フィルム、光学異方体、偏光板、表示装置、反射防止フィルム、および化合物 |
| WO2018173954A1 (ja) | 2017-03-23 | 2018-09-27 | 日本ゼオン株式会社 | 重合性化合物およびその製造方法、重合性組成物、高分子、光学フィルム、光学異方体、偏光板、表示装置、反射防止フィルム、並びに、化合物およびその使用方法 |
| WO2019039165A1 (ja) | 2017-08-23 | 2019-02-28 | 日本ゼオン株式会社 | 重合性液晶材料、重合性液晶組成物、高分子、光学フィルム、光学異方体、偏光板、反射防止フィルム、表示装置、並びに、重合性液晶組成物の製造方法 |
| US10723952B2 (en) | 2014-10-09 | 2020-07-28 | Dic Corporation | Polymerizable compound and optically anisotropic body |
| JP2020173460A (ja) * | 2015-06-03 | 2020-10-22 | 富士フイルム株式会社 | 光学フィルム、偏光板および画像表示装置 |
| US11046889B2 (en) | 2015-12-08 | 2021-06-29 | Dic Corporation | Polymerizable compound and optically anisotropic body |
| US11186669B2 (en) | 2015-01-16 | 2021-11-30 | Dic Corporation | Polymerizable composition and optically anisotropic body using same |
| US11261378B2 (en) | 2014-12-25 | 2022-03-01 | Dic Corporation | Polymerizable compound and optically anisotropic object |
| US11697695B2 (en) | 2015-01-16 | 2023-07-11 | Dic Corporation | Polymerizable composition and optically anisotropic body using same |
Families Citing this family (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN107253935B (zh) | 2012-07-09 | 2020-10-09 | 日本瑞翁株式会社 | 肼化合物、聚合性化合物的制备方法及将肼化合物作为聚合性化合物的制造原料使用的方法 |
| US20180275329A1 (en) * | 2015-09-30 | 2018-09-27 | Zeon Corporation | Optical film and method for producing same |
| US20200115482A1 (en) * | 2016-12-26 | 2020-04-16 | Zeon Corporation | Mixture, polymer, optical film, optically anisotropic product, polarizing plate, display device, antireflection film, and production method for mixture |
| JP7363887B2 (ja) * | 2019-03-01 | 2023-10-18 | 三菱ケミカル株式会社 | 異方性色素膜形成用組成物、異方性色素膜、および光学素子 |
| US20220315613A1 (en) * | 2019-04-26 | 2022-10-06 | National University Corporation Hokkaido University | Rare earth complex, rare earth complex solution, luminescent molded article, method for producing luminescent product, luminescent sheet, and vinyl greenhouse for agriculture |
| CN112480027B (zh) * | 2019-09-12 | 2023-08-29 | 石家庄诚志永华显示材料有限公司 | 聚合性化合物、聚合性组合物、聚合物、光学各向异性体、液晶显示器件 |
| JPWO2021085300A1 (ja) * | 2019-10-28 | 2021-05-06 |
Citations (36)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5567349A (en) | 1994-03-30 | 1996-10-22 | Hoffmann-La Roche Inc. | Photo cross-linkable liquid crystals |
| JPH1068816A (ja) | 1996-08-29 | 1998-03-10 | Sharp Corp | 位相差板及び円偏光板 |
| JPH1090521A (ja) | 1996-07-24 | 1998-04-10 | Sumitomo Chem Co Ltd | 偏光軸回転積層位相差板およびこれを用いた投射型液晶表示装置 |
| JPH1152131A (ja) | 1997-08-01 | 1999-02-26 | Sumitomo Bakelite Co Ltd | 位相差板及びそれを用いた偏光素子 |
| WO2000026705A1 (fr) | 1998-10-30 | 2000-05-11 | Teijin Limited | Film a differences de phase et dispositif optique dans lequel il est utilise |
| JP2000284126A (ja) | 1999-01-27 | 2000-10-13 | Fuji Photo Film Co Ltd | 位相差板、円偏光板および反射型液晶表示装置 |
| US6139771A (en) | 1997-04-04 | 2000-10-31 | Displaytech, Inc. | Mesogenic materials with anomalous birefringence dispersion and high second order susceptibility (X.sup.(2)). |
| JP2001004837A (ja) | 1999-06-22 | 2001-01-12 | Fuji Photo Film Co Ltd | 位相差板および円偏光板 |
| US6203724B1 (en) | 1998-12-03 | 2001-03-20 | Merck Patent Gesellschaft Mit Beschrankter Haftung | Crosslinked cyclohexane derivatives, and liquid-crystalline medium |
| JP2002267838A (ja) | 2001-03-06 | 2002-09-18 | Fuji Photo Film Co Ltd | 位相差膜 |
| US20020159005A1 (en) | 1998-11-06 | 2002-10-31 | Kohei Arakawa | Quarter wave plate comprising two optically anisotropic layers |
| JP2003160540A (ja) | 2001-09-17 | 2003-06-03 | Fuji Photo Film Co Ltd | 四員環化合物、それを用いた複屈折媒体および光学部材 |
| JP2005208414A (ja) | 2004-01-23 | 2005-08-04 | Nitto Denko Corp | 逆波長分散位相差フィルム、それを用いた偏光板及びディスプレイ装置 |
| JP2005208415A (ja) | 2004-01-23 | 2005-08-04 | Nitto Denko Corp | 逆波長分散位相差フィルム、それを用いた偏光板及びディスプレイ装置 |
| JP2005208416A (ja) | 2004-01-23 | 2005-08-04 | Nitto Denko Corp | 逆波長分散位相差フィルム、それを用いた偏光板及びディスプレイ装置 |
| JP2005289980A (ja) | 2004-03-08 | 2005-10-20 | Fuji Photo Film Co Ltd | 液晶化合物、液晶組成物、重合体、位相差板、及び楕円偏光板 |
| JP2005336103A (ja) | 2004-05-27 | 2005-12-08 | Fuji Photo Film Co Ltd | フェニルヒドラジン類の製造方法 |
| WO2006052001A1 (ja) | 2004-11-11 | 2006-05-18 | Sumitomo Chemical Company, Limited | 光学フィルム |
| JP2006330710A (ja) | 2005-04-28 | 2006-12-07 | Sumitomo Chemical Co Ltd | フィルム及びその製造方法 |
| JP2007002208A (ja) | 2004-11-11 | 2007-01-11 | Sumitomo Chemical Co Ltd | 光学フィルム |
| JP2008291218A (ja) * | 2007-04-24 | 2008-12-04 | Nippon Zeon Co Ltd | 重合性液晶化合物、重合性液晶組成物、液晶性高分子および光学異方体 |
| US20090072194A1 (en) | 2005-04-28 | 2009-03-19 | Motohiro Yamahara | Films and Processes for Producing the Same |
| JP2009149754A (ja) * | 2007-12-20 | 2009-07-09 | Sumitomo Chemical Co Ltd | 重合性化合物および該重合性化合物を重合してなる光学フィルム |
| US20090189120A1 (en) | 2008-01-29 | 2009-07-30 | Fujifilm Corporation | Compound, liquid crystal composition, and anisotropic material |
| JP2009173893A (ja) | 2007-12-28 | 2009-08-06 | Sumitomo Chemical Co Ltd | 化合物、光学フィルムおよび光学フィルムの製造方法 |
| JP2009274984A (ja) | 2008-05-14 | 2009-11-26 | Sumitomo Chemical Co Ltd | 化合物、光学フィルムおよび光学フィルムの製造方法 |
| JP2010031223A (ja) | 2007-12-28 | 2010-02-12 | Sumitomo Chemical Co Ltd | 化合物、光学フィルム及び光学フィルムの製造方法 |
| US20100201920A1 (en) | 2007-09-03 | 2010-08-12 | Merck Patent Gesellschaft | Calamitic Mesogenic Compounds |
| US20100301271A1 (en) | 2007-09-03 | 2010-12-02 | Merck Patent Gesellschaft Mit Beschrankter Haftung | Fluorene derivatives |
| JP2011006361A (ja) | 2009-06-26 | 2011-01-13 | Sumitomo Chemical Co Ltd | 化合物、光学フィルム及び光学フィルムの製造方法 |
| JP2011006360A (ja) | 2009-06-26 | 2011-01-13 | Sumitomo Chemical Co Ltd | 化合物、光学フィルム及び光学フィルムの製造方法 |
| JP2011042606A (ja) | 2009-08-20 | 2011-03-03 | Sumitomo Chemical Co Ltd | 化合物、光学フィルム及び光学フィルムの製造方法 |
| WO2012141245A1 (ja) * | 2011-04-15 | 2012-10-18 | 日本ゼオン株式会社 | 重合性化合物、重合性組成物、高分子、及び光学異方体 |
| WO2012147904A1 (ja) * | 2011-04-27 | 2012-11-01 | 日本ゼオン株式会社 | 重合性化合物、重合性組成物、高分子、及び光学異方体 |
| WO2013018526A1 (ja) * | 2011-07-29 | 2013-02-07 | 日本ゼオン株式会社 | 光学異方体の波長分散調整方法及び重合性組成物 |
| WO2013046781A1 (ja) * | 2011-09-27 | 2013-04-04 | 日本ゼオン株式会社 | 重合性化合物の製造中間体及びその製造方法 |
Family Cites Families (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB2359809B (en) * | 1999-12-24 | 2004-01-14 | Sumitomo Chemical Co | Phenylacetylene compound liquid crystal composition, polymer optically anisotropic product, and liquid crystal or optical element |
| US6958797B2 (en) * | 2002-07-23 | 2005-10-25 | Nitto Denko Corporation | Optical film having low chromaticity variation and quarter wavelength plate, and liquid crystal display using the same |
| CN101361011A (zh) * | 2005-11-05 | 2009-02-04 | 3M创新有限公司 | 包括高折射率涂层和抗反射涂层的光学薄膜 |
| CN101687778B (zh) | 2007-04-24 | 2013-09-25 | 日本瑞翁株式会社 | 聚合性液晶化合物、聚合性液晶组合物、液晶高分子及光学各向异性体 |
| CN101452090A (zh) * | 2007-12-05 | 2009-06-10 | 住友化学株式会社 | 组合物、由该组合物得到的共聚物和光学膜以及该光学膜的制造方法 |
| JP2010116528A (ja) * | 2007-12-21 | 2010-05-27 | Sumitomo Chemical Co Ltd | 光学フィルム及び該光学フィルムの製造方法 |
| TW200938587A (en) * | 2008-01-23 | 2009-09-16 | Sumitomo Chemical Co | Optical film and method for manufacturing the same |
| JP5510321B2 (ja) * | 2008-06-30 | 2014-06-04 | 日本ゼオン株式会社 | 重合性液晶化合物、重合性液晶組成物、液晶性高分子及び光学異方体 |
-
2013
- 2013-10-16 JP JP2014543251A patent/JP6206414B2/ja active Active
- 2013-10-16 CN CN201380055206.8A patent/CN104755513B/zh active Active
- 2013-10-16 WO PCT/JP2013/078103 patent/WO2014065176A1/ja active Application Filing
- 2013-10-16 KR KR1020157008225A patent/KR102111538B1/ko active IP Right Grant
- 2013-10-16 EP EP13848209.6A patent/EP2913349B1/en active Active
- 2013-10-16 US US14/437,748 patent/US9777096B2/en active Active
-
2017
- 2017-09-05 JP JP2017170590A patent/JP6544400B2/ja active Active
Patent Citations (43)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5567349A (en) | 1994-03-30 | 1996-10-22 | Hoffmann-La Roche Inc. | Photo cross-linkable liquid crystals |
| JPH1090521A (ja) | 1996-07-24 | 1998-04-10 | Sumitomo Chem Co Ltd | 偏光軸回転積層位相差板およびこれを用いた投射型液晶表示装置 |
| JPH1068816A (ja) | 1996-08-29 | 1998-03-10 | Sharp Corp | 位相差板及び円偏光板 |
| US6139771A (en) | 1997-04-04 | 2000-10-31 | Displaytech, Inc. | Mesogenic materials with anomalous birefringence dispersion and high second order susceptibility (X.sup.(2)). |
| JPH1152131A (ja) | 1997-08-01 | 1999-02-26 | Sumitomo Bakelite Co Ltd | 位相差板及びそれを用いた偏光素子 |
| WO2000026705A1 (fr) | 1998-10-30 | 2000-05-11 | Teijin Limited | Film a differences de phase et dispositif optique dans lequel il est utilise |
| US20020159005A1 (en) | 1998-11-06 | 2002-10-31 | Kohei Arakawa | Quarter wave plate comprising two optically anisotropic layers |
| US6203724B1 (en) | 1998-12-03 | 2001-03-20 | Merck Patent Gesellschaft Mit Beschrankter Haftung | Crosslinked cyclohexane derivatives, and liquid-crystalline medium |
| JP2000284126A (ja) | 1999-01-27 | 2000-10-13 | Fuji Photo Film Co Ltd | 位相差板、円偏光板および反射型液晶表示装置 |
| JP2001004837A (ja) | 1999-06-22 | 2001-01-12 | Fuji Photo Film Co Ltd | 位相差板および円偏光板 |
| JP2002267838A (ja) | 2001-03-06 | 2002-09-18 | Fuji Photo Film Co Ltd | 位相差膜 |
| JP2003160540A (ja) | 2001-09-17 | 2003-06-03 | Fuji Photo Film Co Ltd | 四員環化合物、それを用いた複屈折媒体および光学部材 |
| US20030102458A1 (en) | 2001-09-17 | 2003-06-05 | Naoyuki Nishikawa | 4-Membered ring compound and optical phase optical retardation plate using the same |
| JP2005208414A (ja) | 2004-01-23 | 2005-08-04 | Nitto Denko Corp | 逆波長分散位相差フィルム、それを用いた偏光板及びディスプレイ装置 |
| JP2005208415A (ja) | 2004-01-23 | 2005-08-04 | Nitto Denko Corp | 逆波長分散位相差フィルム、それを用いた偏光板及びディスプレイ装置 |
| JP2005208416A (ja) | 2004-01-23 | 2005-08-04 | Nitto Denko Corp | 逆波長分散位相差フィルム、それを用いた偏光板及びディスプレイ装置 |
| JP2005289980A (ja) | 2004-03-08 | 2005-10-20 | Fuji Photo Film Co Ltd | 液晶化合物、液晶組成物、重合体、位相差板、及び楕円偏光板 |
| US20070176145A1 (en) | 2004-03-08 | 2007-08-02 | Fuji Photo Film Co., Ltd. | Liquid crystal compound comprising two condensed and substituted rings |
| JP2005336103A (ja) | 2004-05-27 | 2005-12-08 | Fuji Photo Film Co Ltd | フェニルヒドラジン類の製造方法 |
| JP2007002208A (ja) | 2004-11-11 | 2007-01-11 | Sumitomo Chemical Co Ltd | 光学フィルム |
| WO2006052001A1 (ja) | 2004-11-11 | 2006-05-18 | Sumitomo Chemical Company, Limited | 光学フィルム |
| US20070298191A1 (en) | 2004-11-11 | 2007-12-27 | Motohiro Yamahara | Optical Film |
| US20090072194A1 (en) | 2005-04-28 | 2009-03-19 | Motohiro Yamahara | Films and Processes for Producing the Same |
| JP2006330710A (ja) | 2005-04-28 | 2006-12-07 | Sumitomo Chemical Co Ltd | フィルム及びその製造方法 |
| JP2008291218A (ja) * | 2007-04-24 | 2008-12-04 | Nippon Zeon Co Ltd | 重合性液晶化合物、重合性液晶組成物、液晶性高分子および光学異方体 |
| US20100201920A1 (en) | 2007-09-03 | 2010-08-12 | Merck Patent Gesellschaft | Calamitic Mesogenic Compounds |
| JP2010537955A (ja) | 2007-09-03 | 2010-12-09 | メルク パテント ゲゼルシャフト ミット ベシュレンクテル ハフツング | フルオレン誘導体 |
| JP2010537954A (ja) | 2007-09-03 | 2010-12-09 | メルク パテント ゲゼルシャフト ミット ベシュレンクテル ハフツング | カラミチックメソゲン化合物 |
| US20100301271A1 (en) | 2007-09-03 | 2010-12-02 | Merck Patent Gesellschaft Mit Beschrankter Haftung | Fluorene derivatives |
| JP2009149754A (ja) * | 2007-12-20 | 2009-07-09 | Sumitomo Chemical Co Ltd | 重合性化合物および該重合性化合物を重合してなる光学フィルム |
| JP2010031223A (ja) | 2007-12-28 | 2010-02-12 | Sumitomo Chemical Co Ltd | 化合物、光学フィルム及び光学フィルムの製造方法 |
| JP2010030979A (ja) | 2007-12-28 | 2010-02-12 | Sumitomo Chemical Co Ltd | 化合物、光学フィルム及び光学フィルムの製造方法 |
| JP2009173893A (ja) | 2007-12-28 | 2009-08-06 | Sumitomo Chemical Co Ltd | 化合物、光学フィルムおよび光学フィルムの製造方法 |
| JP2009179563A (ja) | 2008-01-29 | 2009-08-13 | Fujifilm Corp | 化合物、液晶組成物及び異方性材料 |
| US20090189120A1 (en) | 2008-01-29 | 2009-07-30 | Fujifilm Corporation | Compound, liquid crystal composition, and anisotropic material |
| JP2009274984A (ja) | 2008-05-14 | 2009-11-26 | Sumitomo Chemical Co Ltd | 化合物、光学フィルムおよび光学フィルムの製造方法 |
| JP2011006361A (ja) | 2009-06-26 | 2011-01-13 | Sumitomo Chemical Co Ltd | 化合物、光学フィルム及び光学フィルムの製造方法 |
| JP2011006360A (ja) | 2009-06-26 | 2011-01-13 | Sumitomo Chemical Co Ltd | 化合物、光学フィルム及び光学フィルムの製造方法 |
| JP2011042606A (ja) | 2009-08-20 | 2011-03-03 | Sumitomo Chemical Co Ltd | 化合物、光学フィルム及び光学フィルムの製造方法 |
| WO2012141245A1 (ja) * | 2011-04-15 | 2012-10-18 | 日本ゼオン株式会社 | 重合性化合物、重合性組成物、高分子、及び光学異方体 |
| WO2012147904A1 (ja) * | 2011-04-27 | 2012-11-01 | 日本ゼオン株式会社 | 重合性化合物、重合性組成物、高分子、及び光学異方体 |
| WO2013018526A1 (ja) * | 2011-07-29 | 2013-02-07 | 日本ゼオン株式会社 | 光学異方体の波長分散調整方法及び重合性組成物 |
| WO2013046781A1 (ja) * | 2011-09-27 | 2013-04-04 | 日本ゼオン株式会社 | 重合性化合物の製造中間体及びその製造方法 |
Non-Patent Citations (3)
| Title |
|---|
| "Jikken Kagaku Koza", vol. 20, 1992, MARUZEN CO., LTD. |
| "Shin-Jikken Kagaku Koza", vol. 14, 1978, MARUZEN CO., LTD. |
| "Yuki Gosei Jikkenhou Handbook", 1990, MARUZEN CO., LTD., pages: 810 |
Cited By (35)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPWO2015064698A1 (ja) * | 2013-10-31 | 2017-03-09 | 日本ゼオン株式会社 | 重合性化合物、重合性組成物、高分子、及び光学異方体 |
| WO2015064698A1 (ja) * | 2013-10-31 | 2015-05-07 | 日本ゼオン株式会社 | 重合性化合物、重合性組成物、高分子、及び光学異方体 |
| US10723952B2 (en) | 2014-10-09 | 2020-07-28 | Dic Corporation | Polymerizable compound and optically anisotropic body |
| CN111548324A (zh) * | 2014-12-04 | 2020-08-18 | Dic株式会社 | 聚合性化合物、组合物、聚合物、光学各向异性体、液晶显示元件和有机el元件 |
| CN107001242B (zh) * | 2014-12-04 | 2020-11-17 | Dic株式会社 | 聚合性化合物、组合物、聚合物、光学各向异性体、液晶显示元件和有机el元件 |
| KR102624959B1 (ko) * | 2014-12-04 | 2024-01-16 | 디아이씨 가부시끼가이샤 | 중합성 화합물, 조성물, 중합체, 광학 이방체, 액정 표시 소자 및 유기 el 소자 |
| WO2016088749A1 (ja) * | 2014-12-04 | 2016-06-09 | Dic株式会社 | 重合性化合物、組成物、重合体、光学異方体、液晶表示素子及び有機el素子 |
| JPWO2016088749A1 (ja) * | 2014-12-04 | 2017-04-27 | Dic株式会社 | 重合性化合物、組成物、重合体、光学異方体、液晶表示素子及び有機el素子 |
| US10633353B2 (en) | 2014-12-04 | 2020-04-28 | Dic Corporation | Polymerizable compound, composition, polymer, optically anisotropic body, liquid crystal display element, and organic EL display |
| KR20170086047A (ko) * | 2014-12-04 | 2017-07-25 | 디아이씨 가부시끼가이샤 | 중합성 화합물, 조성물, 중합체, 광학 이방체, 액정 표시 소자 및 유기 el 소자 |
| CN107001242A (zh) * | 2014-12-04 | 2017-08-01 | Dic株式会社 | 聚合性化合物、组合物、聚合物、光学各向异性体、液晶显示元件和有机el元件 |
| US11261378B2 (en) | 2014-12-25 | 2022-03-01 | Dic Corporation | Polymerizable compound and optically anisotropic object |
| JPWO2016114066A1 (ja) * | 2015-01-16 | 2017-04-27 | Dic株式会社 | 重合性組成物及びそれを用いた光学異方体 |
| JP2017203168A (ja) * | 2015-01-16 | 2017-11-16 | Dic株式会社 | 重合性組成物及びそれを用いた光学異方体 |
| WO2016114348A1 (ja) * | 2015-01-16 | 2016-07-21 | Dic株式会社 | 重合性組成物及び光学異方体 |
| US11186669B2 (en) | 2015-01-16 | 2021-11-30 | Dic Corporation | Polymerizable composition and optically anisotropic body using same |
| US11697695B2 (en) | 2015-01-16 | 2023-07-11 | Dic Corporation | Polymerizable composition and optically anisotropic body using same |
| JPWO2016114348A1 (ja) * | 2015-01-16 | 2017-04-27 | Dic株式会社 | 重合性組成物及び光学異方体 |
| WO2016114066A1 (ja) * | 2015-01-16 | 2016-07-21 | Dic株式会社 | 重合性組成物及びそれを用いた光学異方体 |
| CN107207419A (zh) * | 2015-02-24 | 2017-09-26 | Dic株式会社 | 聚合性化合物和光学各向异性体 |
| WO2016136533A1 (ja) * | 2015-02-24 | 2016-09-01 | Dic株式会社 | 重合性化合物及び光学異方体 |
| US10597371B2 (en) | 2015-02-24 | 2020-03-24 | Dic Corporation | Polymerizable compound and optical isomer |
| CN107207419B (zh) * | 2015-02-24 | 2021-03-09 | Dic株式会社 | 聚合性化合物和光学各向异性体 |
| JP2020173460A (ja) * | 2015-06-03 | 2020-10-22 | 富士フイルム株式会社 | 光学フィルム、偏光板および画像表示装置 |
| US11208596B2 (en) | 2015-06-03 | 2021-12-28 | Fujifilm Corporation | Optical film, polarizing plate, and image display device |
| WO2017090418A1 (ja) * | 2015-11-25 | 2017-06-01 | Dic株式会社 | 重合性組成物及びそれを用いた光学異方体 |
| JPWO2017090418A1 (ja) * | 2015-11-25 | 2018-03-29 | Dic株式会社 | 重合性組成物及びそれを用いた光学異方体 |
| US11046889B2 (en) | 2015-12-08 | 2021-06-29 | Dic Corporation | Polymerizable compound and optically anisotropic body |
| JPWO2018096938A1 (ja) * | 2016-11-22 | 2019-10-17 | 日本ゼオン株式会社 | 重合性化合物、重合性組成物、高分子、光学フィルム、光学異方体、偏光板、フラットパネル表示装置、有機エレクトロルミネッセンス表示装置、反射防止フィルム、および化合物 |
| WO2018096938A1 (ja) | 2016-11-22 | 2018-05-31 | 日本ゼオン株式会社 | 重合性化合物、重合性組成物、高分子、光学フィルム、光学異方体、偏光板、フラットパネル表示装置、有機エレクトロルミネッセンス表示装置、反射防止フィルム、および化合物 |
| WO2018123586A1 (ja) | 2016-12-27 | 2018-07-05 | 日本ゼオン株式会社 | 重合性化合物、重合性液晶混合物、高分子、光学フィルム、光学異方体、偏光板、表示装置、反射防止フィルム、および化合物 |
| WO2018168778A1 (ja) | 2017-03-17 | 2018-09-20 | 日本ゼオン株式会社 | 重合性化合物、重合性液晶混合物、高分子、光学フィルム、光学異方体、偏光板、表示装置、反射防止フィルム、および化合物 |
| WO2018173954A1 (ja) | 2017-03-23 | 2018-09-27 | 日本ゼオン株式会社 | 重合性化合物およびその製造方法、重合性組成物、高分子、光学フィルム、光学異方体、偏光板、表示装置、反射防止フィルム、並びに、化合物およびその使用方法 |
| US11492552B2 (en) | 2017-08-23 | 2022-11-08 | Zeon Corporation | Polymerizable liquid crystal material, polymerizable liquid crystal composition, polymer, optical film, optically anisotropic body, polarizing plate, anti-reflection film, display device, and method of producing polymerizable liquid crystal composition |
| WO2019039165A1 (ja) | 2017-08-23 | 2019-02-28 | 日本ゼオン株式会社 | 重合性液晶材料、重合性液晶組成物、高分子、光学フィルム、光学異方体、偏光板、反射防止フィルム、表示装置、並びに、重合性液晶組成物の製造方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| CN104755513B (zh) | 2016-05-18 |
| CN104755513A (zh) | 2015-07-01 |
| JP2018048315A (ja) | 2018-03-29 |
| JPWO2014065176A1 (ja) | 2016-09-08 |
| EP2913349A4 (en) | 2016-04-06 |
| JP6206414B2 (ja) | 2017-10-04 |
| KR102111538B1 (ko) | 2020-05-15 |
| KR20150079579A (ko) | 2015-07-08 |
| EP2913349A1 (en) | 2015-09-02 |
| EP2913349B1 (en) | 2019-06-19 |
| JP6544400B2 (ja) | 2019-07-17 |
| US20150274872A1 (en) | 2015-10-01 |
| US9777096B2 (en) | 2017-10-03 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6206414B2 (ja) | 重合性化合物、重合性組成物、高分子、及び光学異方体 | |
| JP6183514B2 (ja) | 光学フィルム | |
| JP6439825B2 (ja) | 重合性化合物、重合性組成物、高分子、光学フィルム、光学異方体、フラットパネル表示装置および反射防止フィルム | |
| JP6206481B2 (ja) | 重合性化合物、重合性組成物、高分子、及び光学異方体 | |
| JP6544399B2 (ja) | 化合物 | |
| JP6485354B2 (ja) | 重合性化合物、重合性組成物、高分子、及び光学異方体 | |
| JP6428637B2 (ja) | 重合性化合物、重合性組成物、高分子、及び光学異方体 | |
| JP6222085B2 (ja) | 重合性化合物、重合性組成物、高分子、及び光学異方体 | |
| JP6575360B2 (ja) | 重合性化合物、重合性組成物、高分子、及び光学異方体 | |
| WO2012169424A1 (ja) | 重合性化合物、重合性組成物、高分子、及び光学異方体 | |
| WO2012141245A1 (ja) | 重合性化合物、重合性組成物、高分子、及び光学異方体 | |
| WO2012176679A1 (ja) | 重合性化合物、重合性組成物、高分子、及び光学異方体 | |
| WO2015122384A1 (ja) | 重合性化合物、重合性組成物、高分子、及び光学異方体 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 13848209 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 2014543251 Country of ref document: JP Kind code of ref document: A |
|
| ENP | Entry into the national phase |
Ref document number: 20157008225 Country of ref document: KR Kind code of ref document: A |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2013848209 Country of ref document: EP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 14437748 Country of ref document: US |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |