JPWO2012144201A1 - 非水電解質二次電池 - Google Patents
非水電解質二次電池 Download PDFInfo
- Publication number
- JPWO2012144201A1 JPWO2012144201A1 JP2013510884A JP2013510884A JPWO2012144201A1 JP WO2012144201 A1 JPWO2012144201 A1 JP WO2012144201A1 JP 2013510884 A JP2013510884 A JP 2013510884A JP 2013510884 A JP2013510884 A JP 2013510884A JP WO2012144201 A1 JPWO2012144201 A1 JP WO2012144201A1
- Authority
- JP
- Japan
- Prior art keywords
- lithium
- active material
- negative electrode
- secondary battery
- positive electrode
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
- 239000011255 nonaqueous electrolyte Substances 0.000 title claims abstract description 66
- 239000010936 titanium Substances 0.000 claims abstract description 162
- 239000007773 negative electrode material Substances 0.000 claims abstract description 76
- 229910052744 lithium Inorganic materials 0.000 claims abstract description 72
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 claims abstract description 70
- 239000007774 positive electrode material Substances 0.000 claims abstract description 53
- 239000013078 crystal Substances 0.000 claims abstract description 46
- 230000002427 irreversible effect Effects 0.000 claims abstract description 40
- GWEVSGVZZGPLCZ-UHFFFAOYSA-N Titan oxide Chemical compound O=[Ti]=O GWEVSGVZZGPLCZ-UHFFFAOYSA-N 0.000 claims abstract description 33
- OGIDPMRJRNCKJF-UHFFFAOYSA-N titanium oxide Inorganic materials [Ti]=O OGIDPMRJRNCKJF-UHFFFAOYSA-N 0.000 claims abstract description 32
- 229910000314 transition metal oxide Inorganic materials 0.000 claims abstract description 28
- 229910052596 spinel Inorganic materials 0.000 claims abstract description 27
- 239000011029 spinel Substances 0.000 claims abstract description 27
- 230000033228 biological regulation Effects 0.000 claims abstract description 12
- 150000001875 compounds Chemical class 0.000 claims description 53
- 239000011149 active material Substances 0.000 claims description 19
- 229910052782 aluminium Inorganic materials 0.000 claims description 6
- 229910013716 LiNi Inorganic materials 0.000 claims description 5
- 229910014422 LiNi1/3Mn1/3Co1/3O2 Inorganic materials 0.000 claims description 5
- 229910012851 LiCoO 2 Inorganic materials 0.000 claims description 4
- 229910052748 manganese Inorganic materials 0.000 claims description 4
- 229910052719 titanium Inorganic materials 0.000 claims description 4
- 229910052791 calcium Inorganic materials 0.000 claims description 3
- 229910052749 magnesium Inorganic materials 0.000 claims description 3
- 229910052726 zirconium Inorganic materials 0.000 claims description 3
- 230000014759 maintenance of location Effects 0.000 abstract description 36
- 238000007600 charging Methods 0.000 description 54
- 238000007599 discharging Methods 0.000 description 53
- 229910052751 metal Inorganic materials 0.000 description 43
- 239000002184 metal Substances 0.000 description 43
- XEEYBQQBJWHFJM-UHFFFAOYSA-N iron Substances [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 description 37
- 230000000052 comparative effect Effects 0.000 description 23
- 239000000463 material Substances 0.000 description 18
- 238000011156 evaluation Methods 0.000 description 15
- 229910001416 lithium ion Inorganic materials 0.000 description 12
- HBBGRARXTFLTSG-UHFFFAOYSA-N Lithium ion Chemical compound [Li+] HBBGRARXTFLTSG-UHFFFAOYSA-N 0.000 description 11
- 230000002829 reductive effect Effects 0.000 description 11
- 238000004090 dissolution Methods 0.000 description 9
- 238000001556 precipitation Methods 0.000 description 9
- 230000001105 regulatory effect Effects 0.000 description 9
- PXHVJJICTQNCMI-UHFFFAOYSA-N nickel Substances [Ni] PXHVJJICTQNCMI-UHFFFAOYSA-N 0.000 description 8
- 239000004743 Polypropylene Substances 0.000 description 7
- 238000006243 chemical reaction Methods 0.000 description 7
- 229920001155 polypropylene Polymers 0.000 description 7
- 238000012360 testing method Methods 0.000 description 7
- KMTRUDSVKNLOMY-UHFFFAOYSA-N Ethylene carbonate Chemical compound O=C1OCCO1 KMTRUDSVKNLOMY-UHFFFAOYSA-N 0.000 description 5
- 239000004698 Polyethylene Substances 0.000 description 5
- JBTWLSYIZRCDFO-UHFFFAOYSA-N ethyl methyl carbonate Chemical compound CCOC(=O)OC JBTWLSYIZRCDFO-UHFFFAOYSA-N 0.000 description 5
- 229920000573 polyethylene Polymers 0.000 description 5
- 238000007789 sealing Methods 0.000 description 5
- 238000006467 substitution reaction Methods 0.000 description 5
- 239000002131 composite material Substances 0.000 description 4
- 230000007423 decrease Effects 0.000 description 4
- 230000003993 interaction Effects 0.000 description 4
- -1 lithium titanate compound Chemical class 0.000 description 4
- 239000004745 nonwoven fabric Substances 0.000 description 4
- 230000036961 partial effect Effects 0.000 description 4
- 239000000126 substance Substances 0.000 description 4
- 229910013870 LiPF 6 Inorganic materials 0.000 description 3
- 229910045601 alloy Inorganic materials 0.000 description 3
- 239000000956 alloy Substances 0.000 description 3
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 3
- 230000003247 decreasing effect Effects 0.000 description 3
- 239000008151 electrolyte solution Substances 0.000 description 3
- SWAIALBIBWIKKQ-UHFFFAOYSA-N lithium titanium Chemical compound [Li].[Ti] SWAIALBIBWIKKQ-UHFFFAOYSA-N 0.000 description 3
- 238000000034 method Methods 0.000 description 3
- 239000004570 mortar (masonry) Substances 0.000 description 3
- 230000033116 oxidation-reduction process Effects 0.000 description 3
- 239000002994 raw material Substances 0.000 description 3
- WMFOQBRAJBCJND-UHFFFAOYSA-M Lithium hydroxide Chemical compound [Li+].[OH-] WMFOQBRAJBCJND-UHFFFAOYSA-M 0.000 description 2
- 229910010413 TiO 2 Inorganic materials 0.000 description 2
- 238000002441 X-ray diffraction Methods 0.000 description 2
- 239000000654 additive Substances 0.000 description 2
- 230000000996 additive effect Effects 0.000 description 2
- 239000011230 binding agent Substances 0.000 description 2
- 239000004020 conductor Substances 0.000 description 2
- 230000001351 cycling effect Effects 0.000 description 2
- 230000006866 deterioration Effects 0.000 description 2
- 239000003792 electrolyte Substances 0.000 description 2
- 238000010304 firing Methods 0.000 description 2
- 238000009413 insulation Methods 0.000 description 2
- 229910052742 iron Inorganic materials 0.000 description 2
- 238000012423 maintenance Methods 0.000 description 2
- 238000004519 manufacturing process Methods 0.000 description 2
- 238000005259 measurement Methods 0.000 description 2
- 239000012982 microporous membrane Substances 0.000 description 2
- 238000002156 mixing Methods 0.000 description 2
- 239000000203 mixture Substances 0.000 description 2
- 229910052759 nickel Inorganic materials 0.000 description 2
- 239000003960 organic solvent Substances 0.000 description 2
- 229920001343 polytetrafluoroethylene Polymers 0.000 description 2
- 239000004810 polytetrafluoroethylene Substances 0.000 description 2
- 239000000843 powder Substances 0.000 description 2
- 238000002360 preparation method Methods 0.000 description 2
- 239000002904 solvent Substances 0.000 description 2
- ZZXUZKXVROWEIF-UHFFFAOYSA-N 1,2-butylene carbonate Chemical compound CCC1COC(=O)O1 ZZXUZKXVROWEIF-UHFFFAOYSA-N 0.000 description 1
- VAYTZRYEBVHVLE-UHFFFAOYSA-N 1,3-dioxol-2-one Chemical compound O=C1OC=CO1 VAYTZRYEBVHVLE-UHFFFAOYSA-N 0.000 description 1
- 229910018072 Al 2 O 3 Inorganic materials 0.000 description 1
- 229910018131 Al-Mn Inorganic materials 0.000 description 1
- 229910018461 Al—Mn Inorganic materials 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- VYZAMTAEIAYCRO-UHFFFAOYSA-N Chromium Chemical compound [Cr] VYZAMTAEIAYCRO-UHFFFAOYSA-N 0.000 description 1
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 1
- OIFBSDVPJOWBCH-UHFFFAOYSA-N Diethyl carbonate Chemical compound CCOC(=O)OCC OIFBSDVPJOWBCH-UHFFFAOYSA-N 0.000 description 1
- YCKRFDGAMUMZLT-UHFFFAOYSA-N Fluorine atom Chemical compound [F] YCKRFDGAMUMZLT-UHFFFAOYSA-N 0.000 description 1
- 229910010199 LiAl Inorganic materials 0.000 description 1
- 229910013063 LiBF 4 Inorganic materials 0.000 description 1
- 229910013733 LiCo Inorganic materials 0.000 description 1
- 229910012820 LiCoO Inorganic materials 0.000 description 1
- 229910015634 LiNi0.81 Inorganic materials 0.000 description 1
- 229910012465 LiTi Inorganic materials 0.000 description 1
- ZOKXTWBITQBERF-UHFFFAOYSA-N Molybdenum Chemical compound [Mo] ZOKXTWBITQBERF-UHFFFAOYSA-N 0.000 description 1
- 241000283068 Tapiridae Species 0.000 description 1
- RTAQQCXQSZGOHL-UHFFFAOYSA-N Titanium Chemical compound [Ti] RTAQQCXQSZGOHL-UHFFFAOYSA-N 0.000 description 1
- 239000006230 acetylene black Substances 0.000 description 1
- 239000006183 anode active material Substances 0.000 description 1
- 229910052796 boron Inorganic materials 0.000 description 1
- 239000003575 carbonaceous material Substances 0.000 description 1
- 229920002678 cellulose Polymers 0.000 description 1
- 239000001913 cellulose Substances 0.000 description 1
- 150000005678 chain carbonates Chemical class 0.000 description 1
- 229910052804 chromium Inorganic materials 0.000 description 1
- 239000011651 chromium Substances 0.000 description 1
- 238000010280 constant potential charging Methods 0.000 description 1
- 238000010277 constant-current charging Methods 0.000 description 1
- 229910052802 copper Inorganic materials 0.000 description 1
- 239000010949 copper Substances 0.000 description 1
- 150000005676 cyclic carbonates Chemical class 0.000 description 1
- 125000004122 cyclic group Chemical group 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- IEJIGPNLZYLLBP-UHFFFAOYSA-N dimethyl carbonate Chemical compound COC(=O)OC IEJIGPNLZYLLBP-UHFFFAOYSA-N 0.000 description 1
- VUPKGFBOKBGHFZ-UHFFFAOYSA-N dipropyl carbonate Chemical compound CCCOC(=O)OCCC VUPKGFBOKBGHFZ-UHFFFAOYSA-N 0.000 description 1
- 230000000694 effects Effects 0.000 description 1
- 229920006351 engineering plastic Polymers 0.000 description 1
- 239000011737 fluorine Substances 0.000 description 1
- 229910052731 fluorine Inorganic materials 0.000 description 1
- 239000002608 ionic liquid Substances 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 229910003002 lithium salt Inorganic materials 0.000 description 1
- 159000000002 lithium salts Chemical class 0.000 description 1
- 239000012046 mixed solvent Substances 0.000 description 1
- 229910052750 molybdenum Inorganic materials 0.000 description 1
- 239000011733 molybdenum Substances 0.000 description 1
- 239000005486 organic electrolyte Substances 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 230000002093 peripheral effect Effects 0.000 description 1
- 229920000728 polyester Polymers 0.000 description 1
- 229920000098 polyolefin Polymers 0.000 description 1
- 230000002265 prevention Effects 0.000 description 1
- RUOJZAUFBMNUDX-UHFFFAOYSA-N propylene carbonate Chemical compound CC1COC(=O)O1 RUOJZAUFBMNUDX-UHFFFAOYSA-N 0.000 description 1
- 229920006395 saturated elastomer Polymers 0.000 description 1
- 229930195734 saturated hydrocarbon Natural products 0.000 description 1
- 239000011343 solid material Substances 0.000 description 1
- 238000003746 solid phase reaction Methods 0.000 description 1
- 239000000243 solution Substances 0.000 description 1
- 239000010935 stainless steel Substances 0.000 description 1
- 229910001220 stainless steel Inorganic materials 0.000 description 1
- 229910052720 vanadium Inorganic materials 0.000 description 1
Images
Classifications
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/48—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides
- H01M4/485—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides of mixed oxides or hydroxides for inserting or intercalating light metals, e.g. LiTi2O4 or LiTi2OxFy
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/052—Li-accumulators
- H01M10/0525—Rocking-chair batteries, i.e. batteries with lithium insertion or intercalation in both electrodes; Lithium-ion batteries
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/13—Electrodes for accumulators with non-aqueous electrolyte, e.g. for lithium-accumulators; Processes of manufacture thereof
- H01M4/131—Electrodes based on mixed oxides or hydroxides, or on mixtures of oxides or hydroxides, e.g. LiCoOx
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/48—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides
- H01M4/50—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides of manganese
- H01M4/505—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides of manganese of mixed oxides or hydroxides containing manganese for inserting or intercalating light metals, e.g. LiMn2O4 or LiMn2OxFy
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/48—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides
- H01M4/52—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides of nickel, cobalt or iron
- H01M4/525—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides of nickel, cobalt or iron of mixed oxides or hydroxides containing iron, cobalt or nickel for inserting or intercalating light metals, e.g. LiNiO2, LiCoO2 or LiCoOxFy
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M2004/026—Electrodes composed of, or comprising, active material characterised by the polarity
- H01M2004/027—Negative electrodes
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/42—Methods or arrangements for servicing or maintenance of secondary cells or secondary half-cells
- H01M2010/4292—Aspects relating to capacity ratio of electrodes/electrolyte or anode/cathode
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/10—Energy storage using batteries
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02T—CLIMATE CHANGE MITIGATION TECHNOLOGIES RELATED TO TRANSPORTATION
- Y02T10/00—Road transport of goods or passengers
- Y02T10/60—Other road transportation technologies with climate change mitigation effect
- Y02T10/70—Energy storage systems for electromobility, e.g. batteries
Landscapes
- Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Electrochemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Inorganic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Manufacturing & Machinery (AREA)
- Battery Electrode And Active Subsutance (AREA)
- Secondary Cells (AREA)
- Compounds Of Iron (AREA)
- Inorganic Compounds Of Heavy Metals (AREA)
Abstract
本発明の目的の1つは、サイクル特性に優れた非水電解質二次電池を提供することである。本発明の非水電解質二次電池は、リチウムの吸蔵放出が可能な正極3cであって、層状結晶構造を有するリチウム含有遷移金属酸化物からなる正極活物質を含む正極3cと、リチウムの吸蔵放出が可能な負極3aであって、スピネル結晶構造を有するリチウム含有チタン酸化物のTi元素の一部をTiとは異なる1種以上の元素で置換したリチウム含有遷移金属酸化物からなる負極活物質を含む負極3aとを備え、前記負極のリテンションを前記正極のリテンションより大きく設定し、前記負極の不可逆容量率を前記正極の不可逆容量率より大きく設定し、負極規制によって放電が終止するものである。
Description
本願は、リチウム含有チタン酸化物を含む負極活物質および層状構造を有する正極活物質を備えた非水電解質二次電池、特にリチウムイオン二次電池に関する。
近年、種々の非水電解質二次電池が開発されている。非水電解質二次電池の代表的なものとして、リチウムイオン二次電池がある。リチウムイオン二次電池の負極活物質として、従来、炭素材料が主に用いられていたが、新たにリチウムチタン複合酸化物材料が開発され、注目されている。例えば、負極活物質にLi4Ti5O12を用いたリチウムイオン二次電池が既に実用化されている。
Li4Ti5O12は、スピネル型の結晶構造を持つ材料であり、Liの吸蔵または放出が繰り返し可能であるため、リチウムイオン二次電池の活物質として用いることができる。Li4Ti5O12は、リチウムの標準酸化還元電位(Li/Li+)を基準として約1.5Vの電位でLiの吸蔵または放出を行う。このため、Li4Ti5O12を負極活物質としてリチウムイオン二次電池に用いた場合、急速充電などで反応過電圧が生じても、負極でリチウム金属が析出しにくく、安全性の高いリチウムイオン二次電池が実現すると考えられる。また、充放電に伴う格子膨張が非常に少ないという特徴を備える。
一方で、リチウムイオン二次電池の正極活物質としては、層状もしくはスピネル型の結晶構造を有する酸化物材料が一般的に用いられている。特に、層状の結晶構造を有する酸化物材料は高容量を実現できるため、注目されている。代表的な例としては、LiCoO 2、LiNi0.81Co0.15Al0.04O2、LiNi1/3Mn1/3Co1/3O2などが挙げられる。
したがって、層状構造を有する複合酸化物およびLi4Ti5O12をそれぞれ正極活物質および負極活物質として用いるリチウムイオン電池の開発が進められている。例えば、特許文献1は、一般式LiaTi3-aO4(式中aは0<a<3の数を示す)で表されるチタン酸リチウム化合物を負極に用い、一般式LiCobNi1-bO2(0≦b≦1)、LiAlcCodNia-c-dO2(0≦c≦1、0≦d≦1、0≦c+d≦1)で表される化合物を正極に用いたリチウムイオン二次電池を提案している。
上述した正極および負極を備える従来の非水電解質二次電池において、負極の初回充放電時の不可逆容量率(リテンション)は、正極よりも小さい。そのため、放電時に負極の電位が上昇するよりも前に正極の電位が降下することにより、電池のカット電圧(終止電圧)に達する。このように、正極電位の降下によって、電池電圧がカット電圧に達することを正極規制と呼ぶ。また、逆に、正極の電位が降下する前に負極の電位が上昇することにより、電池電圧がカット電圧に達することを負極規制と呼ぶ。
しかしながら、上記従来技術の非水電解質二次電池では、放電時に正極の電位が降下するため、正極活物質の劣化が進行し、サイクル特性が悪化するという問題がある。
本願の限定的ではない例示的なある実施形態は、サイクル特性に優れた非水電解質二次電池を提供する。
本願に開示された非水電解質二次電池は、リチウムの吸蔵放出が可能な正極であって、層状結晶構造を有するリチウム含有遷移金属酸化物からなる正極活物質を含む正極と、リチウムの吸蔵放出が可能な負極であって、スピネル結晶構造を有するリチウム含有チタン酸化物のTi元素の一部をTiとは異なる1種以上の元素で置換したリチウム含有遷移金属酸化物からなる負極活物質を含む負極とを備え、負極規制によって放電が終止する。
本発明の一態様にかかる非水電解質二次電池によれば、負極活物質は、リチウム含有チタン酸化物のTi元素の一部がTiとは異なる1種以上の元素で置換された化合物によって構成されるため、リチウム含有チタン酸化物よりも大きな不可逆容量率を有することができる。これにより、負極規制とすることで、サイクル特性に優れた非水電解質二次電池を実現することができる。
本発明の一態様の概要は以下の通りである。
本発明の一態様である非水電解質二次電池は、リチウムの吸蔵放出が可能な正極であって、層状結晶構造を有するリチウム含有遷移金属酸化物からなる正極活物質を含む正極と、リチウムの吸蔵放出が可能な負極であって、スピネル結晶構造を有するリチウム含有チタン酸化物のTi元素の一部をTiとは異なる1種以上の元素で置換したリチウム含有遷移金属酸化物からなる負極活物質を含む負極とを備え、負極規制によって放電が終止する。
前記負極活物質は前記正極活物質より大きい不可逆容量率を有する。
前記リチウム含有チタン酸化物はLi4Ti5O12である。
前記スピネル結晶構造を有するリチウム含有チタン酸化物のTi元素の一部をTiとは異なる1種以上の元素で置換したリチウム含有遷移金属酸化物は、Li4Ti5-wMnwO1 2(0<w≦0.3)で表される化合物を含む。
前記スピネル結晶構造を有するリチウム含有チタン酸化物のTi元素の一部をTiとは異なる1種以上の元素で置換したリチウム含有遷移金属酸化物は、Li4Ti5-xFexO1 2(0<x≦0.3)で表される化合物を含む。
前記スピネル結晶構造を有するリチウム含有チタン酸化物のTi元素の一部をTiとは異なる1種以上の元素で置換したリチウム含有遷移金属酸化物は、Li4Ti5-yVyO12(0<y≦0.05)で表される化合物を含む。
前記スピネル結晶構造を有するリチウム含有チタン酸化物のTi元素の一部をTiとは異なる1種以上の元素で置換したリチウム含有遷移金属酸化物は、Li4Ti5-zBzO12(0<z≦0.3)で表される化合物を含む。
前記スピネル結晶構造を有するリチウム含有チタン酸化物のTi元素の一部をTiとは異なる1種以上の元素で置換したリチウム含有遷移金属酸化物は、Li4Ti5-w-yMnwVyO12(0<w≦0.3、0<y≦0.05)で表される化合物を含む。
前記スピネル結晶構造を有するリチウム含有チタン酸化物のTi元素の一部をTiとは異なる1種以上の元素で置換したリチウム含有遷移金属酸化物は、Li4Ti5-w-zMnwBzO12(0<w≦0.3、0<z≦0.3)で表される化合物を含む。
前記スピネル結晶構造を有するリチウム含有チタン酸化物のTi元素の一部をTiとは異なる1種以上の元素で置換したリチウム含有遷移金属酸化物は、Li4Ti5-x-yFexVyO12(0<x≦0.3、0<y≦0.05)で表される化合物を含む。
前記スピネル結晶構造を有するリチウム含有チタン酸化物のTi元素の一部をTiとは異なる1種以上の元素で置換したリチウム含有遷移金属酸化物は、Li4Ti5-x-zFexBzO12(0<x≦0.3、0<z≦0.3)で表される化合物を含む。
前記正極活物質は、LiaNi1-b-cCobMcO2(0.95≦a≦1.12、0≦b≦1、0≦c≦0.50、0≦b+c≦1、MはAl、Mn、Ti、Mg、Mo、Y、ZrおよびCaからなる群より選ばれる少なくとも1種以上の元素である)で表される化合物の少なくとも1種を含んでいる。
前記正極活物質は、LiCoO2で表される化合物、LiNi1/3Mn1/3Co1/3O2で表される化合物およびLiNi0.81Co0.15Al0.04O2で表される化合物からなる群から選ばれる少なくとも1種を含んでいる。
以下、図面を参照しながら、本発明による非水電解質二次電池の実施形態を説明する。
図1Aは、本発明による非水電解質二次電池の一実施形態である、円筒形の非水電解質二次電池の断面を模式的に示している。円筒形以外に角形電池やスタック電池など様々な形状で本発明の非水電解質二次電池を実施することができる。
図1Aに示す非水電解質二次電池は、渦巻状に巻回された電極群3を備える。電極群3は、図1Bに示すように、負極3aと、正極3cと、負極3aおよび正極3cの間に配置されたセパレータ3bとを含む。本実施形態では、電極群3が巻回されることによって負極3aと正極3cとが接触しないように、正極3cのセパレータ3bが設けられた面と反対の面に配置されたセパレータ3dをさらに含む。円筒形以外の形態を実施する場合には、セパレータ3dは無くてもよい。
負極3aおよび正極3cは、それぞれリチウムの吸蔵放出が可能な負極活物質および正極活物質を含んでいる。セパレータ3b、3dは、正極3cおよび負極3aの間に配置され、これらの電極間を絶縁し、かつ所定の間隔で保持している。
電極群3は、電池ケース6内に収納されている。正極3cからは正極リード1が引き出されて封口板7に接続され、負極3aからは負極リード2が引き出されて電池ケース6の底部に接続されている。電池ケース6や正極リード1、負極リード2には、耐有機電解液性の電子伝導性をもつ金属や合金を用いることができる。例えば、鉄、ニッケル、チタン、クロム、モリブデン、銅、アルミニウムなどの金属またはそれらの合金を用いることができる。例えば、電池ケース6には、ステンレス鋼板またはAl−Mn合金板を加工したものを用いてもよい。また、正極リード1にはアルミニウムを用いてもよい。負極リード2はニッケルあるいはアルミニウムを用いてもよい。また、電池ケース6には、軽量化を図るため各種エンジニアリングプラスチックスおよびこれと金属の併用したものを用いることも可能である。電極群3の上部および下部にはそれぞれ絶縁板4および5が設けられている。
以下において詳細に説明するように本実施形態の非水電解質二次電池において、正極活物質は、層状結晶構造を有するリチウム含有遷移金属酸化物からなる。また、負極活物質は、スピネル結晶構造を有するリチウム含有チタン酸化物のTi元素の一部をTiとは異なる1種以上の元素で置換したリチウム含有遷移金属酸化物からなる。
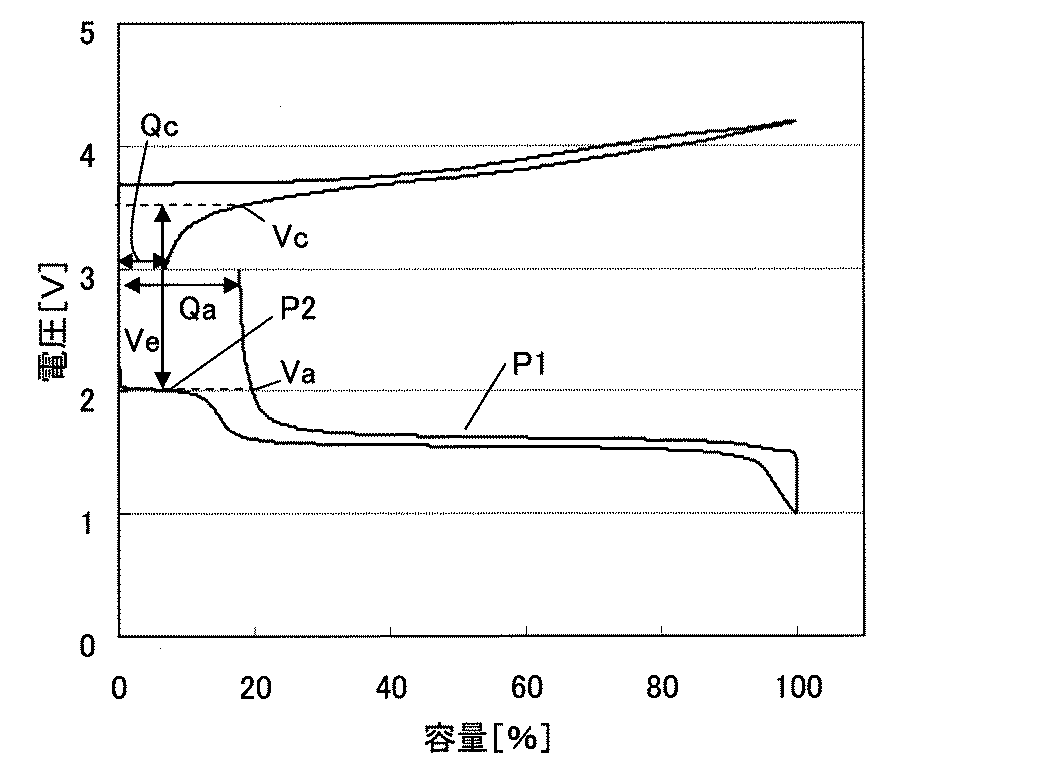
図1Cは、本実施形態の非水電解質二次電池における正極および負極の充放電曲線の一例を示している。図1Cは、負極活物質として、Li4Ti4.7Mn0.3O12を用い、正極活物質として、LiNi0.81Co0.15Al0.04O2を用いた場合の例を示している。QaとQcは、それぞれ負極と正極の不可逆容量率(リテンションとも言う)を示す。不可逆容量率Qa、Qcは、以下に示すように、初回充放電において、充電容量のうち放電できない容量の、充電容量に対する割合(%)で定義される。本実施形態の非水電解質二次電池において、正極活物質および負極活物質の充填容量(初期容量)は互いに等しい。また、正極および負極の予備充電等は行っていない。
図1Cに示すように、本実施形態の非水電解質二次電池において、負極の不可逆容量率Qaは、正極の不可逆容量率Qcよりも大きい。このため、本実施形態の非水電解質二次電池を放電させる場合、正極の電位が低下する前に、負極の電位が大幅に上昇し、電池電圧が急激に低下することによって、非水電解質二次電池の電圧が放電終止電圧Veに達する。このような構成により、負極規制となる非水電解質二次電池、とりわけ、リチウムイオン二次電池を実現することができる。その結果、放電時に正極の電位降下を防ぎ、正極活物質の層状正極の劣化を抑制し、サイクル特性を向上することができる。なお、放電終止時において、負極の電位はVaである。このとき、負極では、放出可能なLiはほとんど残っていない。一方、放電終止時における正極の電位はVcである。このとき、正極はまだLiを吸蔵することが可能である。
本実施形態の非水電解質二次電池に用いる負極活物質は、スピネル結晶構造を有する。このことは、X線回折などにより容易に確認することができる。負極活物質は、リチウム含有チタン酸化物のTi元素の一部をTiとは異なる1種以上の元素で置換したリチウム含有遷移金属酸化物からなる。リチウム含有チタン酸化物のTi元素の一部をTiとは異なる1種以上の元素で置換することにより、リチウム含有チタン酸化物よりも大きな不可逆容量率を有し、負極規制の非水電解質二次電池を実現することができる。
スピネル結晶構造を有するリチウム含有チタン酸化物として、例えば、Li4Ti5O12が挙げられる。この他、スピネル結晶構造を有していれば、LiTi2O4等、他の組成比を有するリチウム含有チタン酸化物であってもよい。
本実施形態で用いる負極活物質は、このようなリチウム含有チタン酸化物のTi元素の一部をTiとは異なる1種以上の元素で置換したリチウム含有遷移金属酸化物からなる。負極活物質の具体的な例としては、Li4Ti5-wMnwO12(0<w≦0.3)で表される化合物、Li4Ti5-xFexO12(0<x≦0.3)で表される化合物、Li4Ti5-yVyO12(0<y≦0.05)で表される化合物、Li4Ti5-zBzO12(0<z≦0.3)で表される化合物、Li4Ti5-w-yMnwVyO12(0<w≦0.3、0<y≦0.05)で表される化合物、Li4Ti5-w-zMnwBzO12(0<w≦0.3、0<z≦0.3)で表される化合物、Li4Ti5-x-yFexVyO12(0<x≦0.3、0<y≦0.05)で表される化合物、Li4Ti5-x-zFexBzO12(0<x≦0.3、0<z≦0.3)で表される化合物などが挙げられる。
Li4Ti5-wMnwO12(0<w≦0.3)で表される化合物は、Li4Ti5O12のTi元素の一部をMn元素で置換することにより、Li4Ti5O12よりも大きな不可逆容量率が得られる。この原因としては、(1)Ti元素の一部を置換しているMn元素は3価もしくは4価で存在していると考えられるが、初回充電時に還元されやすく、放電時にはほとんど酸化されないこと、(2)Mn元素で部分的に置換されていることにより、構造に歪が生じ、初回充電時に還元されたTi元素の一部が放電時に酸化されにくい状態をとること、などが可能性として考えられる。実際に、Li4Ti5-wMnwO12(0<w≦0.3)で表される化合物を活物質として充放電評価を行うと、図1Cに示すように、初回の充電曲線は、Li4Ti5O12に特徴的に見られる1.55V(金属Liの溶解析出電位基準)付近にプラトー(P1)を有するだけでなく、約2.0〜2.1V付近にもプラトー(P2)を有する。したがって、この約2.0〜2.1V付近のプラトー(P2)は、Mn元素の還元によるものだと考えられる。また、図1Cに示すように、放電曲線は、約2.0〜2.1V付近にプラトーを有しておらず、初回充電時におけるプラトー(P2)の電位(約2.0〜2.1V)で放電が生じないことがわかる。したがって、Li4Ti5 -wMnwO12(0<w≦0.3)で表される化合物に含まれるMn元素は還元された後、酸化されないまま存在すると考えられ、このことが不可逆容量率増大の主な原因となっていると思われる。
Li4Ti5-xFexO12(0<x≦0.3)で表される化合物は、Li4Ti5O12のTi元素の一部をFe元素で置換することにより、Li4Ti5O12よりも大きな不可逆容量率が得られる。この原因としては、(1)Ti元素の一部を置換しているFe元素は3価で存在していると考えられるが、初回充電時に還元されやすく、放電時には酸化されにくいこと、(2)Fe元素で部分的に置換されていることにより、構造に歪が生じ、初回充電時に還元されたTi元素の一部が放電時に酸化されにくい状態をとること、などが可能性として考えられる。実際に、Li4Ti5-xFexO12(0<x≦0.3)で表される化合物を活物質として充放電評価を行うと、初回充放電曲線は、Li4Ti5O12に特徴的に見られる1.55V(金属Liの溶解析出電位基準)付近にプラトーを有するだけでなく、約2.0〜2.3V付近にもプラトーを有する。したがって、この約2.0〜2.3V付近のプラトーは、Fe元素の酸化還元によるものだと考えられる。また、充放電曲線のこの約2.0〜2.3V付近のプラトーにおける容量変化は、充電容量>放電容量となっている。したがって、Li4Ti5-xFexO12(0<x≦0.3)で表される化合物に含まれるFe元素は還元されたのち部分的に安定となり一部が酸化されないまま存在すると考えられ、このことが不可逆容量率増大の主な原因となっていると思われる。
Li4Ti5-yVyO12(0<y≦0.05)で表される化合物は、Li4Ti5O12のTi元素の一部をV元素で置換することにより、Li4Ti5O12よりも大きな不可逆容量率が得られる。この原因としては、(1)Ti元素の一部を置換しているV元素は5価で存在していると考えられるが、初回充電時に還元されやすく、放電時には酸化されにくいこと、(2)V元素で部分的に置換されていることにより、構造に歪が生じ、初回充電時に還元されたTi元素の一部が放電時に酸化されにくい状態をとること、などが可能性として考えられる。実際に、Li4Ti5-yVyO12(0<y≦0.05)で表される化合物を活物質として充放電評価を行うと、初回充電曲線は、Li4Ti5O12に特徴的に見られる1.55V(金属Liの溶解析出電位基準)付近にプラトーを有するだけでなく、約1.8〜2.0V付近にもプラトーを有する。したがって、この約1.8〜2.0V付近のプラトーは、V元素の還元によるものだと考えられる。また、放電曲線は、約1.8〜2.0V付近にプラトーを有しておらず、初回充電時におけるプラトーの電位(約2.0〜2.1V)で放電が生じないことがわかる。したがって、Li4Ti5-yVyO12(0<y≦0.05)で表される化合物に含まれるV元素は還元された後酸化されないまま存在すると考えられ、このことが不可逆容量率増大の主な原因となっていると思われる。
Li4Ti5-zBzO12(0<z≦0.3)で表される化合物は、Li4Ti5O12のTi元素の一部をB元素で置換することにより、Li4Ti5O12よりも大きな不可逆容量率が得られる。この原因としては、B元素で部分的に置換されていることにより、構造に歪が生じ、初回充電時に還元されたTi元素の一部が放電時に酸化されにくい状態をとることが可能性として考えられる。実際に、Li4Ti5-zBzO12(0<z≦0.3)で表され化合物を活物質として充放電評価を行うと、初回充放電時に見られるプラトーは、Li4Ti5O12に特徴的に見られる1.55V(金属Liの溶解析出電位基準)付近のみである。このことは、B元素が酸化還元されないことを示唆している。B元素の置換量zを増やしていくと充電容量および放電容量ともに減少するが、放電容量の減少率の方が若干大きいため、不可逆容量率がLi4Ti5O12よりも若干大きくなる。また、不可逆容量率の大きさはB元素の添加量にはあまり依存しない。このことからも、B元素が酸化還元していないことが示唆される。
Li4Ti5-w-yMnwVyO12(0<w≦0.3、0<y≦0.05)で表される化合物は、上記のLi4Ti5-wMnwO12(0<w≦0.3)で表される化合物と同様の理由で、Ti元素の一部をMn元素で置換することにより、不可逆容量率が増大していると考えられる。さらに、Li4Ti5-yVyO12(0<y≦0.05)で表される化合物と同様の理由で、Ti元素の一部をV元素で置換することにより、不可逆容量率が増大していると考えられる。実際に、Li4Ti5-w-yMnwVyO12(0<w≦0.3、0<y≦0.05)で表される化合物を活物質として充放電評価を行うと、初回充電曲線は、Li4Ti5O 12に特徴的に見られる1.55V(金属Liの溶解析出電位基準)付近にプラトーを有するだけでなく、約1.8〜2.0V付近にもプラトーを有する。したがって、この約1.8〜2.0V付近のプラトーは、Mn元素およびV元素の還元によるものだと考えられる。Mn元素のみで置換した場合の電位が約2.0〜2.1Vであるのに比べ、若干低い電位が得られた。この原因としては、Mn元素とV元素の電子的なあるいは結晶構造の歪による相互作用によるものと考えられる。
Li4Ti5-w-zMnwBzO12(0<w≦0.3、0<z≦0.3)で表される化合物は、上記のLi4Ti5-wMnwO12(0<w≦0.3)で表される化合物と同様の理由で、Ti元素の一部をMn元素で置換することにより、不可逆容量率が増大していると考えられる。さらに、Li4Ti5-zBzO12(0<z≦0.3)で表される化合物と同様の理由で、Ti元素の一部をB元素で置換することにより、不可逆容量率が増大していると考えられる。実際に、Li4Ti5-w-zMnwBzO12(0<w≦0.3、0<z≦0.3)で表される化合物を活物質として充放電評価を行うと、初回充電曲線は、Li4Ti5O12に特徴的に見られる1.55V(金属Liの溶解析出電位基準)付近にプラトーを有するだけでなく、約1.8〜2.0V付近にもプラトーを有する。したがって、この約1.8〜2.0V付近のプラトーは、Mn元素の還元によるものだと考えられる。Mn元素のみで置換した場合の電位が約2.0〜2.1Vであるのに比べ、若干低い電位が得られた。この原因としては、Mn元素とB元素の電子的なあるいは結晶構造の歪による相互作用によるものと考えられる。
Li4Ti5-x-yFexVyO12(0<x≦0.3、0<y≦0.05)で表される化合物は、上記のLi4Ti5-xFexO12(0<x≦0.3)で表される化合物と同様の理由で、Ti元素の一部をFe元素で置換することにより、不可逆容量率が増大していると考えられる。さらに、Li4Ti5-yVyO12(0<y≦0.05)で表される化合物と同様の理由で、Ti元素の一部をV元素で置換することにより、不可逆容量率が増大していると考えられる。実際に、Li4Ti5-x-yFexVyO12(0<x≦0.3、0<y≦0.05)で表される化合物を活物質として充放電評価を行うと、初回充電曲線は、Li4Ti5O 12に特徴的に見られる1.55V(金属Liの溶解析出電位基準)付近にプラトーを有するだけでなく、約2.0〜2.3V付近および約1.8〜2.0V付近にもプラトーを有する。この約2.0〜2.3V付近のプラトーは、Fe元素の還元によるものだと考えられる。また約1.8〜2.0V付近のプラトーは、その容量から、Fe元素およびV元素の両方の還元によるものだと考えられる。Fe元素のみで置換した場合の電位が約2.0〜2.3Vのみであるのに比べ、若干低い電位にもFe元素の還元によるプラトーが得られた。この原因としては、Fe元素とV元素の電子的なあるいは結晶構造の歪による相互作用によるものと考えられる。
Li4Ti5-x-zFexBzO12(0<x≦0.3、0<z≦0.3)で表される化合物は上記のLi4Ti5-xFexO12(0<x≦0.3)で表される化合物と同様の理由で、Ti元素の一部をFe元素で置換することにより、不可逆容量率が増大していると考えられる。さらに、Li4Ti5-zBzO12(0<z≦0.3)で表される化合物と同様の理由で、Ti元素の一部をB元素で置換することにより、不可逆容量率が増大していると考えられる。実際に、Li4Ti5-x-zFexBzO12(0<x≦0.3、0<z≦0.3)で表される化合物を活物質として充放電評価を行うと、初回充電曲線は、Li4Ti5O12に特徴的に見られる1.55V(金属Liの溶解析出電位基準)付近にプラトーを有するだけでなく、約2.0〜2.3V付近および約1.8〜2.0V付近にもプラトーを有する。この、約2.0〜2.3V付近および約1.8〜2.0V付近のプラトーは、Fe元素の還元によるものだと考えられる。Fe元素のみで置換した場合の電位が約2.0〜2.3Vのみであるのに比べ、若干低い電位にもFe元素の還元によるプラトーが得られた。この原因としては、Fe元素とB元素の電子的なあるいは結晶構造の歪による相互作用によるものと考えられる。
本実施形態の非水電解質二次電池に含まれる正極活物質は、層状の結晶構造を有する。このことは、X線回折などにより容易に確認することができる。正極活物質は、化学式がLiaNi1-b-cCobMcO2(0.95≦a≦1.12、0≦b≦1、0≦c≦0.50、0≦b+c≦1、MはAl、Mn、Ti、Mg、Mo、Y、ZrおよびCaからなる群より選ばれる少なくとも1種以上の元素である)で表される化合物の少なくとも1種を含んでいる。特に、化学式がLiCoO2で表される化合物、化学式LiNi1/3Mn1/3Co1/3O2で表される化合物、化学式がLiNi0.81Co0.15Al0.04O2で表される化合物の少なくとも1種を含んでいることが、容量やサイクル特性などの面からより好ましい。なお、正極活物質は、これらに限定されるものではなく、層状の結晶構造を有する活物質であれば他の活物質を用いてもよい。
非水電解質二次電池は、さらに、非水電解質を備える。非水電解質は、電極群3が収納された電池ケース6内に充填さることによって、セパレータ内や負極および正極の周囲に配置される。非水電解質を注入した後、周縁部にガスケット8を装着した封口板7により電池ケース6の開口部を密封する。このとき、安全弁を封口板に設けることができる。安全弁の他、従来から知られている種々の安全素子を備えつけてもよい。例えば、過電流防止素子として、ヒューズ、バイメタル、PTC素子などが用いられる。また、安全弁のほかに電池ケースの内圧上昇の対策として、内圧が異常に上昇したとき正極リードと封口板の端子部との間の電気的接続部分を切り離すようにするなど公知の手段を用いることができる。
本実施形態における非水電解質二次電池の非水電解質としては、Liイオン伝導性を有する有機溶媒、イオン液体、ゲル状物質、固体物質、あるいはその組合せを用いることができる。有機溶媒の具体例としては、エチレンカーボネ−ト、プロピレンカーボネート、ブチレンカーボネート、ビニレンカーボネートなどの環状カーボネート類、ジメチルカーボネート、ジエチルカーボネート、エチルメチルカーボネート、ジプロピルカーボネートなどの鎖状カーボネート類、フッ素含有環状飽和炭化水素類、あるいはその混合溶媒等にLiPF6やLiBF4などのリチウム塩を溶解させたものを挙げることができる。
本実施形態における非水電解質二次電池のセパレータとしては、ポリオレフィンの微多孔膜や不織布などが使用できる。不織布はポリエステルやセルロースなどの材料でもよい。
なお、本実施形態および以下の実施例では、非水電解質二次電池における、正極活物質および負極活物質の充填容量(初期容量)は互いに等しい。しかし、本発明による非水電解質二次電池はこのような構成に限られない。上述したように、本実施形態の非水電解質二次電池に用いる負極活物質は、従来に比べて大きな不可逆容量率を有しているため、放電時に正極の電位が降下し、正極活物質の劣化が進行することを抑制し得る。したがって、通常の使用状態において、負極規制によって放電が終止する限り、非水電解質二次電池における正極活物質および負極活物質の充填容量が異なっていてもよい。また、必要に応じて、正極および負極の少なくとも一方に予備充電が施されていてもよい。このような非水電解質二次電池も本発明の実施形態あるいは実施例として好適に実現し得る。
以下、本実施形態の非水電解質二次電池に用いる種々の負極活物質の不可逆容量率(以下、第1リテンションと呼ぶ)および正極活物質の不可逆容量率(以下、第2リテンションと呼ぶ)に関する評価結果を示す。
第1リテンションおよび第2リテンション測定時の参照電極としては、非水電解質二次電池の活物質の特性評価において一般的に用いられる金属Liを用いた。金属Liの溶解析出電位は充放電においてほぼ一定を保つことが知られており、それにより、充放電における正極及び負極活物質の反応電位、不可逆容量率を適正に評価することができる。
1.活物質材料の準備
実施例1〜29の負極活物質には、Li4Ti5-wMnwO12、Li4Ti5-xFexO12、Li4Ti5-yVyO12、Li4Ti5-zBzO12、Li4Ti5-w-yMnwVyO12、Li4Ti5 -w-zMnwBzO12、Li4Ti5-x-yFexVyO12あるいはLi4Ti5-x-zFexBzO12で表される、スピネル型の結晶構造を有するリチウムチタン複合酸化物を用いた。一方、比較例1の負極活物質には、Li4Ti5O12を用いた。各実施例および比較例1におけるMn、Fe、V、Bの添加量w、x、y、zを表1にまとめて示す。
実施例1〜29の負極活物質には、Li4Ti5-wMnwO12、Li4Ti5-xFexO12、Li4Ti5-yVyO12、Li4Ti5-zBzO12、Li4Ti5-w-yMnwVyO12、Li4Ti5 -w-zMnwBzO12、Li4Ti5-x-yFexVyO12あるいはLi4Ti5-x-zFexBzO12で表される、スピネル型の結晶構造を有するリチウムチタン複合酸化物を用いた。一方、比較例1の負極活物質には、Li4Ti5O12を用いた。各実施例および比較例1におけるMn、Fe、V、Bの添加量w、x、y、zを表1にまとめて示す。
実施例1〜29および比較例1の負極活物質は、固相反応法により合成した。LiOH・H2O、TiO2、MnO2、Fe2O3、V2O5、HBO3の原料粉末を、Li/Ti/Mn/Fe/V/Bのモル混合比が4/(5−w−x−y−z)/w/x/y/z(各実施例および比較例において、w、x、y、zは表1に示す値)となるように秤量し、これらを乳鉢に入れ混合した。原料のTiO2には、アナターゼ型の結晶構造を有し、平均粒径が約0.3μmのものを用いた。混合後の原料粉末をAl2O3製のるつぼに入れ、大気雰囲気の電気炉内で焼成した。焼成温度は850℃、焼成温度の保持時間は12時間とした。焼成後の材料をるつぼから取り出し、乳鉢にて粉砕し、目的のリチウムチタン複合酸化物を得た。
実施例30の正極活物質には、層状の結晶構造を有するLiCoO2を用いた。実施例31の正極活物質には、層状の結晶構造を有するLiNi1/3Mn1/3Co1/3O2を用いた。実施例32の正極活物質には、層状の結晶構造を有するLiNi0.81Co0.15Al0.04O2を用いた。
2.電極の作製
実施例1〜29および比較例1の負極活物質、実施例30〜32の正極活物質をそれぞれ用いて、電極を作製した。活物質/導電材/バインダーを85/10/5の重量比になるよう秤量し、乳鉢で混合した。導電材にはアセチレンブラック、バインダーにはポリテトラフルオロエチレン(PTFE)を用いた。混合後、ローラーで圧延し、打ち抜いてペレット状の電極にした。
実施例1〜29および比較例1の負極活物質、実施例30〜32の正極活物質をそれぞれ用いて、電極を作製した。活物質/導電材/バインダーを85/10/5の重量比になるよう秤量し、乳鉢で混合した。導電材にはアセチレンブラック、バインダーにはポリテトラフルオロエチレン(PTFE)を用いた。混合後、ローラーで圧延し、打ち抜いてペレット状の電極にした。
3.電池の作製(リテンション評価用)
コイン形の電池を作製した。実施例1〜32および比較例1を用いて作製した上記電極と、電解液を含浸させたセパレータ、金属Li板の順に重ね、コイン形のケースに入れ、封止して、電池とした。セパレータは旭化成イーマテリアルズ社製のPE微多孔膜と、タピルス社製のPP不織布を、PP/PE/PPの順で3枚重ねて使用した。電解液には、EC/EMC=1/3となるように混合した溶媒に、1mol/LのLiPF6を溶解させたものを用いた。
コイン形の電池を作製した。実施例1〜32および比較例1を用いて作製した上記電極と、電解液を含浸させたセパレータ、金属Li板の順に重ね、コイン形のケースに入れ、封止して、電池とした。セパレータは旭化成イーマテリアルズ社製のPE微多孔膜と、タピルス社製のPP不織布を、PP/PE/PPの順で3枚重ねて使用した。電解液には、EC/EMC=1/3となるように混合した溶媒に、1mol/LのLiPF6を溶解させたものを用いた。
4.第1リテンションの評価
負極活物質の第1リテンションを測定するために、作製した実施例1〜29および比較例1の電池を、一度充電させた後に放電させた。第1リテンションとは、第1カット電圧における不可逆容量率である。第1カット電圧とは、充放電曲線において放電末期に保持容量はほとんど変化しないが急激に電位が変化する領域における電極電位を言う。評価対象の活物質は負極に用いる活物質であるから、本試験では、充電とは負極活物質の電位を下げる方向、すなわち対極をLiとする二次電池としての電圧が低下する反応である。放電はその逆の方向の反応である。充放電試験には、ナガノ社製の充放電システムを使用した。充放電の電圧範囲は1V〜3V、すなわち、第1カット電圧が3Vとなるようにした。電流レートは、0.02Cレートとなるようにした。ここで、1Cレートは1時間放電率を表す電流値と定義され、0.02Cレートは、1Cレートの0.02倍の電流値、すなわち50時間放電率を表す電流値である。
負極活物質の第1リテンションを測定するために、作製した実施例1〜29および比較例1の電池を、一度充電させた後に放電させた。第1リテンションとは、第1カット電圧における不可逆容量率である。第1カット電圧とは、充放電曲線において放電末期に保持容量はほとんど変化しないが急激に電位が変化する領域における電極電位を言う。評価対象の活物質は負極に用いる活物質であるから、本試験では、充電とは負極活物質の電位を下げる方向、すなわち対極をLiとする二次電池としての電圧が低下する反応である。放電はその逆の方向の反応である。充放電試験には、ナガノ社製の充放電システムを使用した。充放電の電圧範囲は1V〜3V、すなわち、第1カット電圧が3Vとなるようにした。電流レートは、0.02Cレートとなるようにした。ここで、1Cレートは1時間放電率を表す電流値と定義され、0.02Cレートは、1Cレートの0.02倍の電流値、すなわち50時間放電率を表す電流値である。
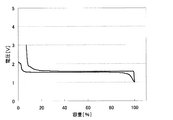
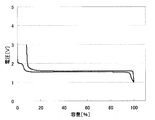
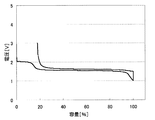
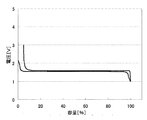
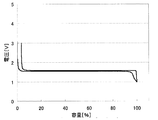
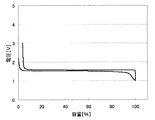
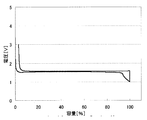
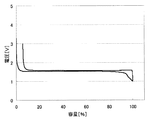
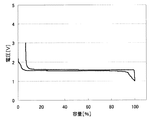
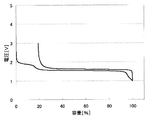
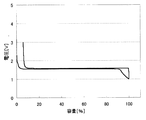
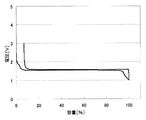
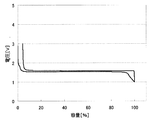
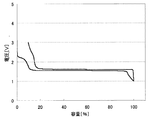
上記のようにして測定した、各負極活物質における初回の充放電における充放電曲線を、図2〜31に示す。わかりやすくするため、初回充放電における満充電時の容量を100%としたときの容量の割合を横軸にとっている。また、放電カーブは、100%より折り返した形で図に示している。縦軸は、リチウムの標準酸化還元電位を基準とした電池の電圧を示している。
この初回充放電における不可逆容量率、すなわち第1リテンションは、以下の式により算出される。
第1リテンション(%)=100−放電容量(mAh)÷充電容量(mAh)×100
第1リテンション(%)=100−放電容量(mAh)÷充電容量(mAh)×100
上記方法で調べた実施例1〜29および比較例1の負極活物質の第1リテンションを表2に示す。
実施例1〜29および比較例1に対応した充放電曲線を図2〜31に示す。これらより、実施例1〜29の負極活物質の充放電曲線は比較例1のLi4Ti5O12を負極活物質とする場合の充放電曲線と異なっていることがわかる。実施の形態にて述べたような、それぞれの材料の組成に対応した充放電曲線が得られた。
表2のとおり、実施例1〜29の負極活物質の第1リテンションは比較例1の第1リテンションよりも大きい。比較例1の第1リテンションの値が1.7%と非常に小さい値であるのに対し、実施例1〜29の第1リテンションは2.8〜19.2%と増大している。これは添加元素による効果であると考えられる。添加元素の量が多いほど、第1リテンションの値は大きい傾向にあることがわかる。
5.第2リテンションの評価
正極活物質の第2リテンションを測定するために、作製した実施例30〜32の電池を、一度充電させた後に、放電させた。第2リテンションとは、第2カット電圧における不可逆容量率である。第2カット電圧とは、充放電曲線において放電末期に保持容量はほとんど変化しないが急激に電位が変化する領域における電極電位を言う。評価対象の活物質は正極に用いる活物質であるから、本試験では充電とは正極活物質の電位を下げる方向、すなわち対極をLiとする二次電池としての電圧が上昇する反応である。放電はその逆の方向の反応である。充放電試験には、ナガノ社製の充放電システムを使用した。充放電の電圧範囲は、その材料が一般的に充放電で用いられる範囲とするため、実施例30は3V〜4.3V、実施例31および実施例32は3V〜4.2Vとした。すなわち、実施例31〜33の第2カット電圧は3Vとした。電流レートは、0.02Cレートとなるようにした。ここで、1Cレートは1時間放電率を表す電流値と定義され、0.02Cレートは、1Cレートの0.02倍の電流値、すなわち50時間放電率を表す電流値である。
正極活物質の第2リテンションを測定するために、作製した実施例30〜32の電池を、一度充電させた後に、放電させた。第2リテンションとは、第2カット電圧における不可逆容量率である。第2カット電圧とは、充放電曲線において放電末期に保持容量はほとんど変化しないが急激に電位が変化する領域における電極電位を言う。評価対象の活物質は正極に用いる活物質であるから、本試験では充電とは正極活物質の電位を下げる方向、すなわち対極をLiとする二次電池としての電圧が上昇する反応である。放電はその逆の方向の反応である。充放電試験には、ナガノ社製の充放電システムを使用した。充放電の電圧範囲は、その材料が一般的に充放電で用いられる範囲とするため、実施例30は3V〜4.3V、実施例31および実施例32は3V〜4.2Vとした。すなわち、実施例31〜33の第2カット電圧は3Vとした。電流レートは、0.02Cレートとなるようにした。ここで、1Cレートは1時間放電率を表す電流値と定義され、0.02Cレートは、1Cレートの0.02倍の電流値、すなわち50時間放電率を表す電流値である。
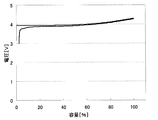
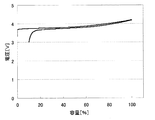
上記のようにして測定した、各負極活物質における初回の充放電における充放電曲線を、図32〜34に示す。わかりやすくするため、満充電時の容量を100%としたときの容量の割合を横軸にとっている。また、放電カーブは、100%より折り返した形で図に示している。
この初回充放電における不可逆容量率、すなわち第2リテンションは、以下の式により算出される。
第2リテンション(%)=100−放電容量(mAh)÷充電容量(mAh)×100
第2リテンション(%)=100−放電容量(mAh)÷充電容量(mAh)×100
上記方法で調べた実施例31〜33の正極活物質の第2リテンションを表3に示す。
表3のとおり、実施例30〜32の正極活物質は、2.3%〜10.1%の第2リテンションの値が得られた。
6.電池の作製(サイクル特性評価用)
コイン形の電池を作製した。実施例8の負極活物質を用いて作製した電極を負極とし、実施例32の正極活物質を用いて作製した電極を正極とした。正極の上に、電解液を含浸させたセパレータ、負極の順に重ね、コイン形のケースに入れ、封止して、電池とした。セパレータは旭化成イーマテリアルズ社製のポリエチレン(PE)製微多孔膜と、タピルス社製のポリプロピレン(PP)製不織布を、PP/PE/PPの順で3枚重ねて使用した。電解液には、エチレンカーボネート(EC)およびエチルメチルカーボネート(EMC)をEC/EMC=1/3の割合で混合した溶媒に、1mol/LのLiPF6を溶解させたものを用いた。作成した電池を実施例のサイクル特性評価用電池呼ぶ。
コイン形の電池を作製した。実施例8の負極活物質を用いて作製した電極を負極とし、実施例32の正極活物質を用いて作製した電極を正極とした。正極の上に、電解液を含浸させたセパレータ、負極の順に重ね、コイン形のケースに入れ、封止して、電池とした。セパレータは旭化成イーマテリアルズ社製のポリエチレン(PE)製微多孔膜と、タピルス社製のポリプロピレン(PP)製不織布を、PP/PE/PPの順で3枚重ねて使用した。電解液には、エチレンカーボネート(EC)およびエチルメチルカーボネート(EMC)をEC/EMC=1/3の割合で混合した溶媒に、1mol/LのLiPF6を溶解させたものを用いた。作成した電池を実施例のサイクル特性評価用電池呼ぶ。
比較のために、比較例1の負極活物質を用いて作製した電極を負極とし、実施例32の正極活物質を用いて作製した電極を正極として用いた電池を作製した。これを比較例のサイクル特性評価用電池と呼ぶ。
7.サイクル特性の評価
作製した実施例および比較例のサイクル特性評価用電池を用いてサイクル特性を評価した。0.05Cの電流値で2サイクル以上充放電させた後に、サイクル試験を行った。充放電時の電圧範囲は1〜3Vとした。サイクル試験において充電は、1Cの電流値で定電流充電した後に0.05Cの電流値になるまで定電圧充電を行った。放電は、1Cの電流値で低電流充電した。上記条件での充放電を200サイクル繰り返し、サイクル試験の第1回目の放電の容量を100%として各サイクルの放電容量の維持率を計算した。
作製した実施例および比較例のサイクル特性評価用電池を用いてサイクル特性を評価した。0.05Cの電流値で2サイクル以上充放電させた後に、サイクル試験を行った。充放電時の電圧範囲は1〜3Vとした。サイクル試験において充電は、1Cの電流値で定電流充電した後に0.05Cの電流値になるまで定電圧充電を行った。放電は、1Cの電流値で低電流充電した。上記条件での充放電を200サイクル繰り返し、サイクル試験の第1回目の放電の容量を100%として各サイクルの放電容量の維持率を計算した。
容量維持率の結果を図35に示す。図35からわかるように、実施例のサイクル特性評価用電池は、200サイクル後でも90%以上の容量を維持しており、比較例のサイクル特性評価用電池に比べて10%以上容量の維持率が高い。
8.考察
表2および表3の結果より、比較例1の負極活物質の第1リテンションは、実施例30〜31の正極活物質の第2リテンションよりも小さい。したがって、負極活物質に比較例1の材料を用い、正極活物質に実施例31〜33のいずれの材料を用いて電池を作製したとしても、正極規制の電池となってしまうことがわかる。例えば、比較例1の負極活物質および実施例32の正極活物質を用いて非水電解質二次電池を作製した場合、図36に示すような充放電曲線を有する電池が得られる。図36からわかるように、放電時において、負極の電圧が上昇する前に、正極の電圧が低下するため、正極規制によって二次電池の放電が終止する。つまり、正極規制の二次電池となる。このため、正極活物質が深く放電されるため、充放電を繰り返すうちに正極活物質の結晶構造が変化し、サイクル特性が低下し易いと考えられる。
表2および表3の結果より、比較例1の負極活物質の第1リテンションは、実施例30〜31の正極活物質の第2リテンションよりも小さい。したがって、負極活物質に比較例1の材料を用い、正極活物質に実施例31〜33のいずれの材料を用いて電池を作製したとしても、正極規制の電池となってしまうことがわかる。例えば、比較例1の負極活物質および実施例32の正極活物質を用いて非水電解質二次電池を作製した場合、図36に示すような充放電曲線を有する電池が得られる。図36からわかるように、放電時において、負極の電圧が上昇する前に、正極の電圧が低下するため、正極規制によって二次電池の放電が終止する。つまり、正極規制の二次電池となる。このため、正極活物質が深く放電されるため、充放電を繰り返すうちに正極活物質の結晶構造が変化し、サイクル特性が低下し易いと考えられる。
これに対して、実施例1〜29の負極活物質の第1リテンションは、実施例30の第2リテンションよりも大きい。したがって、負極活物質に実施例1〜29の材料を用い、正極活物質に実施例30の材料を用いて電池を作製した場合、負極規制の電池を作製することができる。上述したように図1Cは、実施例4の負極活物質および実施例32の正極活物質を用いて非水電解質二次電池を作製した場合における充放電曲線を示している。図1Cからわかるように、正極の不可逆容量率Qcよりも負極の不可逆容量率Qaのほうが大きい。言い換えれば、第1カット電圧における第1リテンションのほうが第2カット電圧における第2リテンションより大きい。したがって、非水電解質二次電池の放電時において、正極の電圧が低下する前に、負極におけるリチウムイオンの放出が飽和することによって負極の電圧が上昇し、負極規制によって二次電池の放電が終止する。つまり、負極規制の二次電池となる。このため、正極活物質が深く放電されるのが抑制され、充放電を繰り返しても正極活物質の結晶構造の変化が抑制される。このため、実施例の非水電解質二次電池は優れたサイクル特性を示すと考えられる。
上述したように、図35は、実施例のサイクル特性評価用電池のサイクル特性が比較例に比べて向上していることを示している。これは、本実施例のサイクル特性評価用電池では、負極規制によって放電が終止することにより、正極活物質が深く放電されるのが抑制される結果、放電が繰り返されても、正極活物質の結晶構造が変化し、正極の容量が低下するのが抑制されることにより、高い放電容量を維持しているからであるからと考えられる。
また、実施例31および実施例32の正極活物質の第2リテンションは10.1%および6.9%と大きいが、より大きな第1リテンションを有する負極活物質と組み合わせることで、負極規制の電池を作製することができる。すなわち、負極活物質に実施例2〜4、8、16、19、23、24、26、28、29のいずれかの材料を用い、正極活物質に実施例31の材料を用いて電池を作製した場合、負極規制の電池を作製することができる。また、負極活物質に実施例4、16、19、23、24、29の材料を用い、正極活物質に実施例32の材料を用いて電池を作製した場合、負極規制の電池を作製することができる。
なお、上記実施例1〜29の負極において、充放電曲線に第2プラトーが見られる場合、これらの負極を含む非水電解質二次電池の放電終止時における負極の電位は、負極の初充電時における第2プラトーの電圧値に設定することが好ましい。例えば図3(実施例2)や図4(実施例3)に示される充放電曲線からわかるように、第2プラトーの電位を超えて放電が進むと急激に負極の電位は上昇する。このため、放電終止時における負極の電位を第2プラトーの電圧値に設定することによって、確実に負極規制、つまり、負極の電位が急激に上昇することによって、非水電解質二次電池の電池電圧が放電終止電圧に達し、放電を終了させることができるからである。
なお、本実施例では、第1カット電圧と第2カット電圧が等しい例を示したが、異なっていても良い。
上記実施例で示したように、負極の不可逆容量率を正極の不可逆容量率より大きく設定することができ、負極規制とすることで正極活物質の劣化を抑制し、サイクル特性に優れた非水電解質二次電池を実現することができる。
本願に開示された非水電解質二次電池は、放電時に負極規制となるためサイクル特性に優れ、モバイル用の非水電解質二次電池として有用である。また大型電池や電気自動車等の用途にも応用できる。
1 正極リード
2 負極リード
3 電極群
4 絶縁板
5 絶縁板
6 電池ケース
7 封口板
8 ガスケット
2 負極リード
3 電極群
4 絶縁板
5 絶縁板
6 電池ケース
7 封口板
8 ガスケット
Claims (13)
- リチウムの吸蔵放出が可能な正極であって、層状結晶構造を有するリチウム含有遷移金属酸化物からなる正極活物質を含む正極と、
リチウムの吸蔵放出が可能な負極であって、スピネル結晶構造を有するリチウム含有チタン酸化物のTi元素の一部をTiとは異なる1種以上の元素で置換したリチウム含有遷移金属酸化物からなる負極活物質を含む負極と
を備え、
負極規制によって放電が終止する非水電解質二次電池。 - 前記負極活物質は前記正極活物質より大きい不可逆容量率を有する、請求項1に記載の非水電解質二次電池。
- 前記リチウム含有チタン酸化物はLi4Ti5O12である請求項1または2に記載の非水電解質二次電池。
- 前記スピネル結晶構造を有するリチウム含有チタン酸化物のTi元素の一部をTiとは異なる1種以上の元素で置換したリチウム含有遷移金属酸化物は、Li4Ti5-wMnwO1 2(0<w≦0.3)で表される化合物を含む請求項1または2に記載の非水電解質二次電池。
- 前記スピネル結晶構造を有するリチウム含有チタン酸化物のTi元素の一部をTiとは異なる1種以上の元素で置換したリチウム含有遷移金属酸化物は、Li4Ti5-xFexO1 2(0<x≦0.3)で表される化合物を含む請求項1または2に記載の非水電解質二次電池。
- 前記スピネル結晶構造を有するリチウム含有チタン酸化物のTi元素の一部をTiとは異なる1種以上の元素で置換したリチウム含有遷移金属酸化物は、Li4Ti5-yVyO12(0<y≦0.05)で表される化合物を含む請求項1または2に記載の非水電解質二次電池。
- 前記スピネル結晶構造を有するリチウム含有チタン酸化物のTi元素の一部をTiとは異なる1種以上の元素で置換したリチウム含有遷移金属酸化物は、Li4Ti5-zBzO12(0<z≦0.3)で表される化合物を含む請求項1または2に記載の非水電解質二次電池。
- 前記スピネル結晶構造を有するリチウム含有チタン酸化物のTi元素の一部をTiとは異なる1種以上の元素で置換したリチウム含有遷移金属酸化物は、Li4Ti5-w-yMnwVyO12(0<w≦0.3、0<y≦0.05)で表される化合物を含む請求項1または2に記載の非水電解質二次電池。
- 前記スピネル結晶構造を有するリチウム含有チタン酸化物のTi元素の一部をTiとは異なる1種以上の元素で置換したリチウム含有遷移金属酸化物は、Li4Ti5-w-zMnwBzO12(0<w≦0.3、0<z≦0.3)で表される化合物を含む請求項1または2に記載の非水電解質二次電池。
- 前記スピネル結晶構造を有するリチウム含有チタン酸化物のTi元素の一部をTiとは異なる1種以上の元素で置換したリチウム含有遷移金属酸化物は、Li4Ti5-x-yFexVyO12(0<x≦0.3、0<y≦0.05)で表される化合物を含む請求項1または2に記載の非水電解質二次電池。
- 前記スピネル結晶構造を有するリチウム含有チタン酸化物のTi元素の一部をTiとは異なる1種以上の元素で置換したリチウム含有遷移金属酸化物は、Li4Ti5-x-zFexBzO12(0<x≦0.3、0<z≦0.3)で表される化合物を含む請求項1または2に記載の非水電解質二次電池。
- 前記正極活物質は、LiaNi1-b-cCobMcO2(0.95≦a≦1.12、0≦b≦1、0≦c≦0.50、0≦b+c≦1、MはAl、Mn、Ti、Mg、Mo、Y、ZrおよびCaからなる群より選ばれる少なくとも1種以上の元素である)で表される化合物の少なくとも1種を含んでいる、請求項1から11のいずれかに記載の非水電解質二次電池。
- 前記正極活物質は、
LiCoO2で表される化合物、
LiNi1/3Mn1/3Co1/3O2で表される化合物および
LiNi0.81Co0.15Al0.04O2で表される化合物
からなる群から選ばれる少なくとも1種を含んでいる、請求項1から11のいずれかに記載の非水電解質二次電池。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201161477501P | 2011-04-20 | 2011-04-20 | |
| US61/477,501 | 2011-04-20 | ||
| PCT/JP2012/002664 WO2012144201A1 (ja) | 2011-04-20 | 2012-04-18 | 非水電解質二次電池 |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2014027626A Division JP2014132582A (ja) | 2011-04-20 | 2014-02-17 | 非水電解質二次電池 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP5490315B2 JP5490315B2 (ja) | 2014-05-14 |
| JPWO2012144201A1 true JPWO2012144201A1 (ja) | 2014-07-28 |
Family
ID=47021580
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2013510884A Active JP5490315B2 (ja) | 2011-04-20 | 2012-04-18 | 非水電解質二次電池 |
| JP2014027626A Pending JP2014132582A (ja) | 2011-04-20 | 2014-02-17 | 非水電解質二次電池 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2014027626A Pending JP2014132582A (ja) | 2011-04-20 | 2014-02-17 | 非水電解質二次電池 |
Country Status (5)
| Country | Link |
|---|---|
| US (3) | US8920976B2 (ja) |
| EP (1) | EP2701231A4 (ja) |
| JP (2) | JP5490315B2 (ja) |
| CN (1) | CN103503218B (ja) |
| WO (1) | WO2012144201A1 (ja) |
Families Citing this family (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2013118220A1 (ja) * | 2012-02-10 | 2013-08-15 | パナソニック株式会社 | リチウムイオン二次電池用負極活物質材料およびその製造方法 |
| JP2014056747A (ja) * | 2012-09-13 | 2014-03-27 | Dainippon Screen Mfg Co Ltd | 電池用電極製造方法 |
| JP6162414B2 (ja) * | 2013-01-30 | 2017-07-12 | 株式会社東芝 | 組電池装置 |
| JP6109603B2 (ja) * | 2013-02-28 | 2017-04-05 | 株式会社東芝 | 電池 |
| JP6305112B2 (ja) * | 2013-03-14 | 2018-04-04 | 株式会社東芝 | 非水電解質電池及び電池パック |
| JP2015011930A (ja) * | 2013-07-01 | 2015-01-19 | トヨタ自動車株式会社 | 非水電解質二次電池 |
| WO2015079629A1 (ja) * | 2013-11-29 | 2015-06-04 | 三洋電機株式会社 | 非水電解質二次電池 |
| JP6597599B2 (ja) * | 2014-04-03 | 2019-10-30 | 株式会社村田製作所 | 二次電池、電池パック、電子機器、電動車両、蓄電装置および電力システム |
| CA2941308C (en) * | 2014-04-03 | 2020-09-22 | Sony Corporation | Positive and negative electrode configuration of a secondary battery, battery pack, electronic device, electrically driven vehicle, storage device, and power system |
| KR20170090196A (ko) * | 2016-01-28 | 2017-08-07 | 주식회사 엘지화학 | 전기화학 성능이 우수한 양극활물질 및 이를 포함하는 리튬 이차 전지 |
| CN105958018A (zh) * | 2016-05-10 | 2016-09-21 | 内蒙古科技大学 | 一种掺杂钒的钛酸锂负极材料的制备方法 |
| JP2019003798A (ja) * | 2017-06-14 | 2019-01-10 | 株式会社Gsユアサ | 蓄電素子及び蓄電素子の製造方法 |
| CN107282048B (zh) * | 2017-06-26 | 2019-05-10 | 厦门大学 | 一种通过原子置换制备高稳定性纳米催化剂的方法 |
| JP7282482B2 (ja) * | 2017-10-27 | 2023-05-29 | 株式会社東芝 | バッテリーシステム |
| CN113422038B (zh) * | 2021-06-11 | 2023-03-17 | 青岛多元锂业有限公司 | 一种锂电池5v复合材料的制备方法 |
| WO2024096028A1 (ja) * | 2022-11-01 | 2024-05-10 | 三井金属鉱業株式会社 | 活物質、電極合剤、塗布用組成物、電極、電池及び活物質の製造方法 |
Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH07335261A (ja) * | 1994-06-09 | 1995-12-22 | Matsushita Electric Ind Co Ltd | リチウム二次電池 |
| JPH10144351A (ja) * | 1996-09-13 | 1998-05-29 | Matsushita Electric Ind Co Ltd | 全固体リチウム二次電池と集合電池およびその充電方法 |
| JP2001126728A (ja) * | 1999-10-26 | 2001-05-11 | Toyota Motor Corp | リチウムイオン2次電池用負極 |
| JP2001196061A (ja) * | 2000-01-11 | 2001-07-19 | Yuasa Corp | 非水電解質リチウム二次電池 |
| JP2005135775A (ja) * | 2003-10-30 | 2005-05-26 | Yuasa Corp | リチウムイオン二次電池 |
| JP2006128119A (ja) * | 2004-10-28 | 2006-05-18 | Samsung Sdi Co Ltd | リチウム二次電池用導電剤/正極活物質複合体,リチウム二次電池用導電剤/正極活物質複合体の製造方法,リチウム二次電池用正極,およびリチウム二次電池 |
| JP2006216305A (ja) * | 2005-02-02 | 2006-08-17 | Nissan Motor Co Ltd | 二次電池 |
Family Cites Families (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6022640A (en) | 1996-09-13 | 2000-02-08 | Matsushita Electric Industrial Co., Ltd. | Solid state rechargeable lithium battery, stacking battery, and charging method of the same |
| US6458487B1 (en) * | 1997-07-25 | 2002-10-01 | Kabushiki Kaisha Toshiba | Positive active material and non-aqueous secondary cell made by using the same |
| JP4623786B2 (ja) | 1999-11-10 | 2011-02-02 | 住友電気工業株式会社 | 非水二次電池 |
| JP3827545B2 (ja) * | 2001-09-13 | 2006-09-27 | 松下電器産業株式会社 | 正極活物質、その製造方法および非水電解質二次電池 |
| US6706445B2 (en) * | 2001-10-02 | 2004-03-16 | Valence Technology, Inc. | Synthesis of lithiated transition metal titanates for lithium cells |
| JP2003297433A (ja) * | 2002-03-28 | 2003-10-17 | Hitachi Maxell Ltd | 電気化学素子 |
| JP2004235144A (ja) | 2003-01-10 | 2004-08-19 | Nichia Chem Ind Ltd | 非水電解質二次電池用負極活物質および非水電解質二次電池 |
| US7927742B2 (en) | 2004-10-29 | 2011-04-19 | Medtronic, Inc. | Negative-limited lithium-ion battery |
| JP4625744B2 (ja) * | 2005-09-29 | 2011-02-02 | 株式会社東芝 | 非水電解質電池および電池パック |
| JP5066831B2 (ja) | 2006-05-12 | 2012-11-07 | 株式会社Gsユアサ | 非水電解質二次電池 |
| US7879493B2 (en) | 2006-06-05 | 2011-02-01 | A123 Systems, Inc. | Alkali metal titanates and methods for their synthesis |
| JP5217281B2 (ja) | 2006-08-01 | 2013-06-19 | 株式会社Gsユアサ | 非水電解質二次電池 |
| JP4284348B2 (ja) | 2006-09-27 | 2009-06-24 | 株式会社東芝 | 非水電解質電池、電池パック及び自動車 |
| JP5095179B2 (ja) * | 2006-11-10 | 2012-12-12 | 株式会社東芝 | 非水電解質電池、リチウムチタン複合酸化物および電池パック |
| CN101373829B (zh) * | 2008-10-07 | 2011-05-11 | 深圳市贝特瑞新能源材料股份有限公司 | 钛系负极活性物质及其制备方法、钛系锂离子动力电池 |
| CN102246333A (zh) * | 2009-09-18 | 2011-11-16 | 松下电器产业株式会社 | 非水电解质二次电池用电极及其制造方法以及非水电解质二次电池 |
| US20120045696A1 (en) | 2010-08-23 | 2012-02-23 | Herle P Subramanya | Negative electrode materials for non-aqueous electrolyte secondary battery |
-
2012
- 2012-04-18 US US13/450,155 patent/US8920976B2/en active Active
- 2012-04-18 WO PCT/JP2012/002664 patent/WO2012144201A1/ja active Application Filing
- 2012-04-18 EP EP12774775.6A patent/EP2701231A4/en not_active Withdrawn
- 2012-04-18 JP JP2013510884A patent/JP5490315B2/ja active Active
- 2012-04-18 CN CN201280018739.4A patent/CN103503218B/zh active Active
-
2014
- 2014-02-17 JP JP2014027626A patent/JP2014132582A/ja active Pending
- 2014-10-23 US US14/522,575 patent/US20150099177A1/en not_active Abandoned
-
2016
- 2016-11-03 US US15/342,899 patent/US10103382B2/en active Active
Patent Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH07335261A (ja) * | 1994-06-09 | 1995-12-22 | Matsushita Electric Ind Co Ltd | リチウム二次電池 |
| JPH10144351A (ja) * | 1996-09-13 | 1998-05-29 | Matsushita Electric Ind Co Ltd | 全固体リチウム二次電池と集合電池およびその充電方法 |
| JP2001126728A (ja) * | 1999-10-26 | 2001-05-11 | Toyota Motor Corp | リチウムイオン2次電池用負極 |
| JP2001196061A (ja) * | 2000-01-11 | 2001-07-19 | Yuasa Corp | 非水電解質リチウム二次電池 |
| JP2005135775A (ja) * | 2003-10-30 | 2005-05-26 | Yuasa Corp | リチウムイオン二次電池 |
| JP2006128119A (ja) * | 2004-10-28 | 2006-05-18 | Samsung Sdi Co Ltd | リチウム二次電池用導電剤/正極活物質複合体,リチウム二次電池用導電剤/正極活物質複合体の製造方法,リチウム二次電池用正極,およびリチウム二次電池 |
| JP2006216305A (ja) * | 2005-02-02 | 2006-08-17 | Nissan Motor Co Ltd | 二次電池 |
Non-Patent Citations (1)
| Title |
|---|
| PIERRE KUBIAK ET AL.: "Phase transition in the spinel Li4Ti5O12 induced by lithium insertion Influence of the substitutions", JOURNAL OF POWER SOURCES, vol. Vol.119-121, JPN6012020479, 2003, pages 626 - 630, ISSN: 0002733206 * |
Also Published As
| Publication number | Publication date |
|---|---|
| US20150099177A1 (en) | 2015-04-09 |
| EP2701231A1 (en) | 2014-02-26 |
| US20120270105A1 (en) | 2012-10-25 |
| JP2014132582A (ja) | 2014-07-17 |
| CN103503218A (zh) | 2014-01-08 |
| US20170054150A1 (en) | 2017-02-23 |
| WO2012144201A1 (ja) | 2012-10-26 |
| US10103382B2 (en) | 2018-10-16 |
| EP2701231A4 (en) | 2014-11-19 |
| US8920976B2 (en) | 2014-12-30 |
| CN103503218B (zh) | 2016-02-03 |
| JP5490315B2 (ja) | 2014-05-14 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5490315B2 (ja) | 非水電解質二次電池 | |
| US7927506B2 (en) | Cathode active material and lithium battery using the same | |
| US7935270B2 (en) | Cathode active material and lithium battery using the same | |
| JP5095098B2 (ja) | 非水電解質二次電池 | |
| CN101150189B (zh) | 正极活性材料和使用其的锂电池 | |
| KR100612089B1 (ko) | 과방전 시 양극 종료전압을 조절하는 방법 및 리튬 이차전지용 양극활물질 | |
| JP4518865B2 (ja) | 非水電解質二次電池およびその製造方法 | |
| US11005099B2 (en) | Nonaqueous electrolyte secondary battery | |
| KR100823816B1 (ko) | 비수전해질 이차전지 | |
| JP5781386B2 (ja) | 非水電解液及び非水電解液電池 | |
| JP5485065B2 (ja) | 非水電解質二次電池 | |
| WO2015125444A1 (ja) | 非水電解質二次電池用正極活物質 | |
| US10340521B2 (en) | Non-aqueous electrolyte secondary battery | |
| JP2004342500A (ja) | 非水電解質二次電池および電池充放電システム | |
| US20190173085A1 (en) | Nonaqueous electrolyte secondary battery | |
| JP2002319398A (ja) | 非水電解質二次電池 | |
| US10553856B2 (en) | Nonaqueous electrolyte secondary battery | |
| JP6633049B2 (ja) | 非水電解質二次電池 | |
| JPWO2015059778A1 (ja) | リチウムイオン二次電池用正極活物質およびリチウムイオン二次電池 | |
| JP2014167873A (ja) | リチウムイオン二次電池用負極活物質、その製造方法及びリチウムイオン二次電池 | |
| JP4746846B2 (ja) | リチウムイオン電池用負極活物質、その製造方法およびリチウムイオン電池 | |
| JP2010287526A (ja) | 非水電解質二次電池用負極活物質、それを用いた非水電解質二次電池用負極および非水電解質二次電池 | |
| JP2016058334A (ja) | リチウム二次電池用正極材料 | |
| WO2014155708A1 (ja) | リチウムイオン二次電池用正極材料、リチウムイオン二次電池用正極、及びリチウムイオン二次電池 | |
| JP2016062788A (ja) | リチウム二次電池用正極材料 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20140128 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20140225 |
|
| R151 | Written notification of patent or utility model registration |
Ref document number: 5490315 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R151 |