JP2012507553A - 単一ドメイン抗原結合分子の製剤 - Google Patents
単一ドメイン抗原結合分子の製剤 Download PDFInfo
- Publication number
- JP2012507553A JP2012507553A JP2011534779A JP2011534779A JP2012507553A JP 2012507553 A JP2012507553 A JP 2012507553A JP 2011534779 A JP2011534779 A JP 2011534779A JP 2011534779 A JP2011534779 A JP 2011534779A JP 2012507553 A JP2012507553 A JP 2012507553A
- Authority
- JP
- Japan
- Prior art keywords
- formulation
- tnf
- concentration
- molecule
- binding
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
- A61K39/39591—Stabilisation, fragmentation
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/08—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing oxygen, e.g. ethers, acetals, ketones, quinones, aldehydes, peroxides
- A61K47/10—Alcohols; Phenols; Salts thereof, e.g. glycerol; Polyethylene glycols [PEG]; Poloxamers; PEG/POE alkyl ethers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/26—Carbohydrates, e.g. sugar alcohols, amino sugars, nucleic acids, mono-, di- or oligo-saccharides; Derivatives thereof, e.g. polysorbates, sorbitan fatty acid esters or glycyrrhizin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/16—Agglomerates; Granulates; Microbeadlets ; Microspheres; Pellets; Solid products obtained by spray drying, spray freeze drying, spray congealing,(multiple) emulsion solvent evaporation or extraction
- A61K9/1605—Excipients; Inactive ingredients
- A61K9/1617—Organic compounds, e.g. phospholipids, fats
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/16—Agglomerates; Granulates; Microbeadlets ; Microspheres; Pellets; Solid products obtained by spray drying, spray freeze drying, spray congealing,(multiple) emulsion solvent evaporation or extraction
- A61K9/1605—Excipients; Inactive ingredients
- A61K9/1617—Organic compounds, e.g. phospholipids, fats
- A61K9/1623—Sugars or sugar alcohols, e.g. lactose; Derivatives thereof; Homeopathic globules
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/16—Agglomerates; Granulates; Microbeadlets ; Microspheres; Pellets; Solid products obtained by spray drying, spray freeze drying, spray congealing,(multiple) emulsion solvent evaporation or extraction
- A61K9/1605—Excipients; Inactive ingredients
- A61K9/1629—Organic macromolecular compounds
- A61K9/1641—Organic macromolecular compounds obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyethylene glycol, poloxamers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/19—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles lyophilised, i.e. freeze-dried, solutions or dispersions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/04—Drugs for disorders of the alimentary tract or the digestive system for ulcers, gastritis or reflux esophagitis, e.g. antacids, inhibitors of acid secretion, mucosal protectants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/06—Antipsoriatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/08—Drugs for skeletal disorders for bone diseases, e.g. rachitism, Paget's disease
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P21/00—Drugs for disorders of the muscular or neuromuscular system
- A61P21/04—Drugs for disorders of the muscular or neuromuscular system for myasthenia gravis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/06—Immunosuppressants, e.g. drugs for graft rejection
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/08—Antiallergic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P5/00—Drugs for disorders of the endocrine system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/24—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against cytokines, lymphokines or interferons
- C07K16/241—Tumor Necrosis Factors
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/15—Medicinal preparations ; Physical properties thereof, e.g. dissolubility
-
- G—PHYSICS
- G06—COMPUTING; CALCULATING OR COUNTING
- G06Q—INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR ADMINISTRATIVE, COMMERCIAL, FINANCIAL, MANAGERIAL OR SUPERVISORY PURPOSES; SYSTEMS OR METHODS SPECIALLY ADAPTED FOR ADMINISTRATIVE, COMMERCIAL, FINANCIAL, MANAGERIAL OR SUPERVISORY PURPOSES, NOT OTHERWISE PROVIDED FOR
- G06Q99/00—Subject matter not provided for in other groups of this subclass
-
- G—PHYSICS
- G16—INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR SPECIFIC APPLICATION FIELDS
- G16Z—INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR SPECIFIC APPLICATION FIELDS, NOT OTHERWISE PROVIDED FOR
- G16Z99/00—Subject matter not provided for in other main groups of this subclass
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
- A61K2039/507—Comprising a combination of two or more separate antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/22—Immunoglobulins specific features characterized by taxonomic origin from camelids, e.g. camel, llama or dromedary
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/24—Immunoglobulins specific features characterized by taxonomic origin containing regions, domains or residues from different species, e.g. chimeric, humanized or veneered
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
- C07K2317/565—Complementarity determining region [CDR]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
- C07K2317/569—Single domain, e.g. dAb, sdAb, VHH, VNAR or nanobody®
Abstract
Description
本出願は、その内容の全体が本明細書中に参照により組み込まれている、2008年10月29日に出願の米国特許出願第61/109,474号の優先権を主張するものである。
本出願は、EFS−Webにより提出されており、その全体が本明細書中に参照により組み込まれている配列表を含有する。2009年10月27日に作成された前記のASCIIコピーは、名称がW22373WO.txtであり、大きさが8,343バイトである。
10mMのヒスチジン=10mM
5%のスクロースは約146mMに相当する
5%=5g/100mL=50g/L→(50g/L)/(342.3g/mol)=0.146mol/L=146mM
0.01%のポリソルベート80は本質的に0モル濃度を及ぼし、無視することができる。
100mg/mLのタンパク質:実験により、100mg/mLの抗TNFナノボディタンパク質は約48mMに相当する浸透圧を及ぼすことが決定された。
10mM+146mM+48mM=204mM
であり、標的モル濃度が310mMである場合は、標的の残りを構成するための対応するモル濃度の量は、
310mM−204mM=106mM
である。
10mMのヒスチジン+146mMのスクロース+48mMのタンパク質+100mMのグリシン=304mMであり、
製剤の実験による浸透圧値=305mOsm
である。
単一ドメイン抗原結合(SDAB)分子には、その相補性決定領域が単一ドメインポリペプチドの一部である分子が含まれる。例には、それだけには限定されないが、重鎖可変ドメイン、軽鎖を天然に欠く結合分子、慣用の4本鎖抗体に由来する単一ドメイン、操作したドメインおよび抗体に由来するもの以外の単一ドメイン足場が含まれる。SDAB分子は、当技術分野の任意のもの、または任意の将来の単一ドメイン分子であり得る。SDAB分子は、それだけには限定されないが、マウス、ヒト、ラクダ、ラマ、サカナ、サメ、ヤギ、ウサギ、およびウシを含めた任意の種に由来するものであり得る。また、この用語には、ラクダ科(Camelidae)およびサメ以外の種に由来する天然に存在する単一ドメイン抗体分子も含まれる。
腫瘍壊死因子アルファは、当技術分野において関節リウマチ、クローン病、潰瘍性大腸炎および多発性硬化症などの炎症性障害に関連していることで知られている。TNFaならびに受容体(CD120aおよびCD120b)はどちらも非常に詳細に研究されている。生物活性型のTNFaは三量体である。抗TNFa抗体を用いてTNFaの作用と拮抗するいくつかの戦略が開発されており、Remicade(登録商標)およびHumira(登録商標)などが現在市販されている。TNFaに対する抗体分子が知られている。TNFa結合単一ドメイン抗原結合分子(たとえばナノボディ)の数々の例は、そのすべての内容がその全体で本明細書中に参照により組み込まれている、WO2004/041862号、WO2004/041865号、WO2006/122786号に開示されている。単一ドメイン抗原結合分子のさらなる例は、そのすべての内容がその全体で本明細書中に参照により組み込まれている、US2006/286066号、US2008/0260757号、WO06/003388号、US05/0271663号、US06/0106203号に開示されている。他の実施形態では、TNFaおよび血清タンパク質、たとえばHSAに対する単一、二重、三重および他の多特異的な単一ドメイン抗体が、これらの参考文献中に開示されている。
SDAB分子は、組換えの、CDR移植した、ヒト化した、ラクダ化した、脱免疫化した、および/またはin vitroで作製した(たとえばファージディスプレイによって選択した)、1つまたは複数の単一ドメイン分子(たとえばナノボディ)からなり得る。抗体およびSDAB分子を作製する技法、ならびに組換えによってそれらを改変する技法は当技術分野で知られており、以下に詳述する。
本発明の製剤は、フレームワーク領域のうちの1つ中の少なくとも1つのアミノ酸位置が、天然に存在するドメイン、たとえばVHドメインのアミノ酸配列と異なるアミノ酸配列を有する、少なくとも1つのSDAB分子、たとえばナノボディ分子を含有し得る。
SDAB分子、たとえばナノボディ分子の製剤には、SDAB分子、凍結保護剤として役割を果たすことができる化合物、および緩衝液が含まれる。製剤のpHは、一般にpH5.5〜7.0である。一部の実施形態では、製剤は液体として貯蔵する。他の実施形態では、製剤は液体として調製し、その後、貯蔵の前に、たとえば、凍結乾燥または噴霧乾燥によって乾燥させる。乾燥製剤は、乾燥化合物、たとえばエアロゾルもしくは粉末として使用するか、または、その元のもしくは別の濃度まで、たとえば、水、緩衝液、もしくは他の適切な液体を用いて再構成することができる。
本明細書中に記載の製剤のpHは、一般に、pH約5.0〜約7.0、たとえばpH約5.5〜約6.5、pH約5.5〜約6.0、pH約6.0〜約6.5、pH5.5、pH6.0、またはpH6.5である。一般に、溶液をpH5.5〜6.5に維持することができる緩衝液、たとえば約6.0のpKAを有する緩衝液を用いて製剤を調製する。適切な緩衝液には、それだけには限定されないが、ヒスチジン緩衝液、トリス、2−(N−モルホリノ)エタンスルホン酸(MES)、カコジレート、ホスフェート、アセテート、スクシネート、およびシトレートが含まれる。緩衝液の濃度は約4mM〜約60mM、たとえば約5mM〜約25mMであり、たとえば、ヒスチジンは一般に60mMの濃度で使用する。一部の場合では、ヒスチジン緩衝液は約5mM、約10mMまたは約20mMの濃度で使用する。他の場合では、アセテートまたはスクシネート緩衝液は約5mMまたは約10mMの濃度で使用する。
特定の実施形態では、界面活性剤を製剤中に含める。界面活性剤の例には、それだけには限定されないが、ポリソルベート(たとえば、ポリソルベート20、ポリソルベート40、ポリソルベート60、ポリソルベート65、ポリソルベート80、またはポリソルベート85)などの非イオン性界面活性剤、Triton(商標)、ドデシル硫酸ナトリウム(SDS)、ラウレル(laurel)硫酸ナトリウム、オクチルグリコシドナトリウム、ラウリル−スルホベタイン、ミリスチル−スルホベタイン、リノレイル−スルホベタイン、ステアリル−スルホベタイン、ラウリル−サルコシン、ミリスチル−サルコシン、リノレイル−サルコシン、ステアリル−サルコシン、リノレイル−ベタイン、ミリスチル−ベタイン、セチル−ベタイン、ラウロアミドプロピル−ベタイン、コカミドプロピル−ベタイン、リノレアミドプロピル−ベタイン、ミリスタミドプロピル−ベタイン、パルミドプロピル−ベタイン、イソステアラミドプロピル−ベタイン(たとえばラウロアミドプロピル)、ミリスタルニドプロピル(myristarnidopropyl)−、パルミドプロピル−、またはイソステアラミドプロピル−ジメチルアミン、メチルココイルタウリン酸ナトリウム、またはメチルオフェイル(ofeyl)タウリン酸二ナトリウム、ならびにMonaquat(商標)シリーズ(Mona Industries,Inc.、Paterson、N.J.)、ポリエチルグリコール、ポリプロピルグリコール、およびエチレンとプロピレングリコールとのコポリマー、たとえばポロキサマー(たとえばポロキサマー188)が含まれる。
製剤は、無菌溶液または無菌凍結乾燥物として貯蔵する。また、製剤中の微生物作用の防止は、少なくとも1つの抗菌剤および/または抗真菌剤、たとえば、パラベン、クロロブタノール、フェノール、アスコルビン酸、チメロサールなどを製剤中に含めることによっても達成することができる。一部の場合では、凍結乾燥物を静菌水(たとえば0.9%のベンジルアルコールを含有する水)で再構成する。保存料を製剤中に包含させる際の考慮事項は当技術分野で知られており、特定の製剤および送達方法に適合する保存料を特定する方法も知られている(たとえばGuptaら(2003)、AAPS Pharm.Sci.、5:論文8、ページ1〜9を参照)。
凍結
一部の場合では、抗体を含有する製剤を貯蔵のために凍結する。したがって、製剤は、凍結解凍サイクル下を含めたそのような条件下で比較的安定であることが望ましい。製剤の適切性を判定する1つの方法は、試料製剤を、少なくとも2回、たとえば、3回、4回、5回、8回、10回、またはそれ以上のサイクルの凍結(たとえば−20℃または−80℃で)および解凍(たとえば、37℃の水浴中の急速解凍または2℃〜8℃の緩徐解凍による)に供し、凍結解凍サイクル後に蓄積されるLMW種および/またはHMW種の量を決定し、凍結解凍手順の前に試料中に存在するLMW種またはHMW種の量と比較することである。LMWまたはHMW種の増加が安定性の減少を示す。
製剤は凍結乾燥後に貯蔵することができる。したがって、凍結乾燥後の製剤のタンパク質構成成分の安定性について製剤を試験することは、製剤の適切性の判定に有用である。この方法は、凍結について上述したものと同様であるが、試料製剤を凍結する代わりに凍結乾燥し、その元の体積まで再構成し、LMW種および/またはHMW種の存在について試験する。凍結乾燥した試料製剤を凍結乾燥しなかった対応する試料製剤と比較する。対応する試料と比較した凍結乾燥試料中のLMWまたはHMW種の増加が、凍結乾燥した試料の安定性の減少を示す。
一部の場合では、製剤を噴霧乾燥し、その後に貯蔵する。噴霧乾燥は当技術分野で知られている方法を用いて実施し、液体または凍結の噴霧乾燥を使用するように改変することができる(たとえば、Niro Inc.(Madison、WI)、Upperton Particle Technologies(Nottingham、英国)、もしくはBuchi(Brinkman Instruments Inc.、Westbury、NY)、または米国特許公開第20030072718号および第20030082276号などの方法を用いる)。
LMW種およびHMW種の蓄積は、抗体安定性の有用な測定である。製剤中のLMWまたはHMWのいずれかの蓄積は、製剤の一部として貯蔵されるタンパク質の不安定性の指標である。HPLCを伴ったサイズ排除クロマトグラフィーを用いてLMWおよびHMW種の存在を決定することができる。そのような測定のための適切な系は当技術分野で知られており、たとえばHPLC系(Waters、Milford,MA)である。当技術分野で知られている他の系、たとえば、SDS−PAGE(HMWおよびLMW種を監視するため)、抗体活性のバイオアッセイ、酵素結合免疫吸着アッセイ、精製した標的タンパク質(たとえばTNFα)と結合する能力、ならびに陽イオン交換−HPLC(CEX−HPLC、変異体を検出し、表面荷電を監視するため)を用いて、製剤中の抗体の完全性を評価することができる。一例では、バイオアッセイは、生物活性を実証するためにTNFα依存性の活性の阻害を様々な濃度の製剤化したナノボディ分子の存在下で検査する、細胞に基づくアッセイである。
また、本出願は、本明細書中に記載の製剤が含まれる製品も提供し、製剤の使用説明書を提供する。
本発明の製剤は、対象(たとえばヒト対象)に、単独でまたは第2の薬剤、たとえば第2の治療上もしくは薬理学的に活性な薬剤と組合せて、TNFα関連障害、たとえば炎症性または自己免疫性障害を治療または予防する(たとえばそれに関連する1つまたは複数の症状を低下または寛解させる)ために投与される。用語「処置する」とは、治療剤を、統計的に有意な度合までまたは当業者が検出可能な度合まで、障害に関連する状態、症状、もしくはパラメータを改善させる、または障害の進行を妨げるために有効な量、様式、および/またはモードで、投与することをいう。有効な量、様式、またはモードは対象に応じて変動する場合があり、対象に合わせ得る。
ATN−103の高濃度の凍結乾燥製剤の安定性(6カ月期間)
たとえば治療的用途のために使用する抗体を貯蔵する一方法は、凍結乾燥によって調製した乾燥粉末としての方法である。したがって、凍結乾燥TNF結合製剤の長期安定性を研究した。
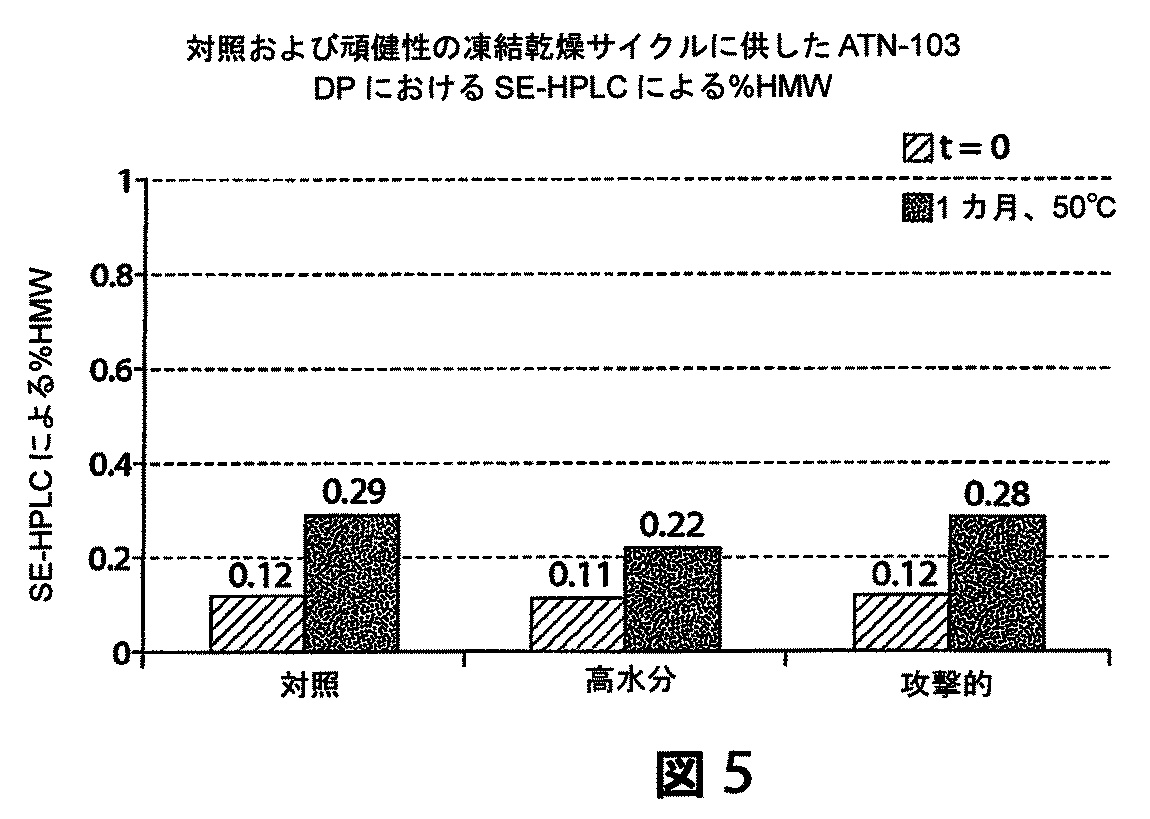
凍結乾燥に対するTNF結合ナノボディ製剤の頑健性
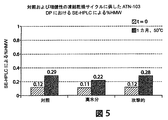
標的凍結乾燥サイクルを適用することによって凍結乾燥製剤に加えて(実施例1)、2つの追加の「頑健性」凍結乾燥サイクルを同じ製剤に適用することによって、2つの追加の薬物製品のロットを調製した。2つの「頑健性」凍結乾燥サイクルは、製造の設定において起こり得る顕著なプロセスの逸脱を模倣する。標的(対照)凍結乾燥サイクル研究と同じ薬物製品の製剤を頑健性研究で使用した:10mMのヒスチジン、5%のスクロース、0.01%のポリソルベート80、50mg/mLのTNF結合ナノボディ、pH6.0。再構成した後(凍結乾燥前の充填された生成物の約半分の体積の再構成希釈剤を使用)、ATN−103製剤は以下の通りであった:20mMのヒスチジン、10%のスクロース、0.02%のポリソルベート80、100mg/mLのTNF結合ナノボディ、pH6.0。
すべての実行において、凍結乾燥機内の放射を最小限にするために、扉の前のアルミニウム箔遮蔽および63mmの棚の高さを使用した。すべての実行において、凍結乾燥機に対して一定の負荷を維持するために1つのトレイを完全に満たした。すべてのタンパク質バイアルについて栓をオートクレーブし、乾燥させた。タンパク質試料のすべてのバイアルを脱イオン水ですすぎ、発熱物質を除去した。トレイの残りの部分を埋めるために使用したバイアルおよび栓は未処理であった。
mDSC用のすべての試料は、0.5℃の振幅および100秒間の期間の変調モードで実行した。凍結乾燥後の粉末には、試料を2℃/分で150℃まで加熱した。すべての粉末試料は窒素をパージしたグローブボックスを用いて調製した。液体試料には、すべての温度勾配を0.5℃/分で行い、温度を凍結乾燥サイクルで利用したものと一致させた。最終加熱勾配は2℃/分で行ってガラス転移を拡大した。液体試料は実験室ベンチ上で調製した。
カールフィッシャー滴定を用いて凍結乾燥した試料中の水分をアッセイした。凍結乾燥した試料は3mlのメタノールで再構成した。
FTIRにより、乾燥粉末状態の抗体の二次構造を測定した。300mgのKBr中に分散させた約1mgの製剤化した乾燥タンパク質を含有するペレットを圧延し、200回走査した。データ収集後、分析はスクロースプラセボのスペクトル減算、ベースライン補正、補整、二次導関数、および面積の正規化を含む。
製剤中の凍結乾燥した抗体の安定性を貯蔵時間および温度の関数として評価した。凍結乾燥したTNF結合ナノボディの試料を、凍結乾燥後、2℃〜8℃で4週間の貯蔵後、ならびに50℃で2週間および4週間の貯蔵後にアッセイした。冷蔵試料はウォークイン型の冷蔵した冷室中で貯蔵した。高温試料は50℃に設定したLab Line Imperial Incubator中で貯蔵した。適切な時点で、試料を貯蔵から取り出し、アッセイ前に室温まで加温または冷却した。
凍結乾燥後分析および貯蔵安定性分析のどちらからの凍結乾燥製剤のバイアルも、1.3mlの滅菌注射用水で再構成する前、その間、およびその後に視覚的に検査した。バイアルを、ライトボックス中で黒および白色の背景の両方に対して、再構成前のケーク色、完全性、水分、粒子、および欠陥について検査した。凍結乾燥したケークを視覚検査した後、クリンプ除去装置(de−crimper)を使用して蓋およびクリンプシールをバイアルから取り外した。栓を取り外し、適切なピペットを用いて滅菌注射用水をバイアル内にゆっくりと分注した。ケークを完全に湿らせることを確実にするために回旋動作を用いて希釈剤を分注した。希釈剤を完全に分注した後、標準の実験室タイマーを用いて再構成の測時を開始し、バイアルに再度栓をした。最後の固体片が溶けた際に再構成が完了した。バイアルを手の間で回転させることで再構成が促進された。凍結乾燥したケークが再構成の過程にある間、透明度、気泡発生、および発泡などの、溶解中の溶液の状態に関する観察を記録した。再構成が完了した後、再構成時間を記録し、生じた溶液が定着し、再構成中に形成された気泡の大部分が散逸されることを可能にするために、バイアルをベンチ上に数分間静置した。その後、再構成した溶液を、ライトボックス中で黒および白色の背景の両方に対して、色、透明度、および粒子について検査した。
2マイクロリットルのTNF結合ナノボディ製剤のニートな試料を、保護カラムを備えたG3000swxlカラム上に注入した(TosoHaas部品番号08541および08543)。移動相は、250mMの塩化ナトリウムを加えたリン酸緩衝液(PBS)であった。流速は0.75ml/分であり、実行時間は30分間であった。紫外線吸光度を280nmの波長で監視した。Waters Empower(商標)ソフトウェアを用いて、主なTNF結合ナノボディピークを高および低分子量種から分離するためにクロマトグラムを積分した。
100mg/mlの濃度の抗体を有する製剤の試料を、10μlの試料をそれぞれ1990μlおよび3990μlの10mMのヒスチジン、5%のスクロース、pH6.0に加えることによって約0.5mg/mLおよび0.25mg/mLまで希釈した。200マイクロリットルの生じた溶液を、96ウェルマイクロプレート中の個々のウェル中に緩衝液ブランクと共に入れた。プレートを、Spectramax(登録商標)Plusプレートリーダーで280nmおよび320nmの波長の紫外線吸光度について読み取った。320nmの吸光度を280nmの吸光度から減算し、消光係数(1.405mL/mg−cm)×経路長(1cm)によって除算することで、それぞれのウェル中の溶液のタンパク質濃度が決定された。適切な希釈係数を適用し、平均タンパク質濃度を決定した。
200マイクロリットルの分析するそれぞれのTNF結合ナノボディ試料を、96ウェルマイクロプレート上の個々のウェル内に一定分量で入れた。緩衝液ブランクが対照として役割を果たした。プレートを、Spectramax Plusプレートリーダーで420nmの波長の可視吸光度について読み取った。
一連の連続的なステップ(以下に記載)を使用して凍結乾燥サイクルを開発した。
TNF結合ナノボディの生成物臨界温度は変調示差走査熱量(mDSC)によって特定した。この方法は、凍結した生成物のガラス転移温度を特定するために使用する(mDSC)。一次乾燥中に生成物をこの温度未満に維持する凍結乾燥サイクルにより、インタクトなケーク構造が得られるはずである。最低温度の適切な温度は−25℃であると推定され、したがって、この温度は、一般に、本明細書中に記載の抗体の製剤およびその凍結乾燥方法を開発する際に条件および製剤を試験するために設計された手順に含まれる。
上述した研究の結果に基づいて、3つの異なる凍結乾燥サイクルを行って、貯蔵に適した凍結乾燥製剤を調製するための適切な凍結乾燥手順または他の手順を開発における、3つの目的のパラメータを検査した。検査した第1のパラメータは対照サイクルであり、以前の安定性研究からのサイクルを繰り返す。すべての以前の開発上の安定性サイクルでこのサイクルを利用したため、これがこの分析の出発点として役割を果たした。
TNF結合ナノボディ製剤に対する選択した凍結乾燥サイクルの評価は、2つの側面、すなわち、凍結乾燥後に行った試験に基づく即時比較、および加速条件下でインキュベーションした後に引き起こされる潜在的な長期的影響に分割して行った。
TNF結合ナノボディ製剤生成物は、ほぼ50%のタンパク質を含有していた。したがって、タンパク質が凍結および凍結乾燥した状態の物理特性を支配すると予測された。凍結乾燥前に、周囲以下の変調示差走査熱量(mDSC)により、製剤の凍結濃縮した非晶質相のガラス転移温度を検索した。攻撃的凍結乾燥開発サイクルのデータに基づいて、−12℃の生成物温度が、凍結乾燥中にそれ未満に保つ臨界温度として選択された。
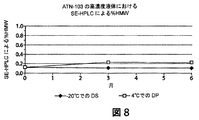
TNF結合ナノボディの高濃度液体製剤の安定性(6カ月期間)
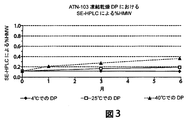
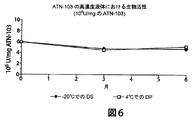
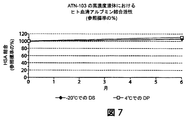
一部の場合では、TNF結合ナノボディ製剤を液体様式で貯蔵することが望ましい。したがって、比較的高濃度のTNF結合ナノボディを含有する液体TNF結合製剤の長期安定性を研究した。手短に述べると、ヒト化TNF結合ナノボディ(約80mg/mL)、10mMのヒスチジン、5%のスクロース、0.01%のポリソルベート80、pH6.0を含有する製剤を、製剤を発熱物質除去したステンレス鋼製容器中で滅菌濾過することによって貯蔵用に調製した。製剤を−20℃または4℃で約3カ月および6カ月間貯蔵した。高濃度液体の安定性は、生物活性、ヒト血清アルブミン(HSA)結合、SE−HPLCによるHMWのパーセンテージおよびLMWのパーセンテージ、SDS−CEによるATN−103のパーセンテージおよび生成物ではない不純物のパーセンテージ、ならびに相対的保持時間のCEX−HPLC評価および溶出プロファイルとTNF結合ナノボディ参照標準との比較性によって評価した。
液体の充填済みシリンジ中のTNF結合ナノボディの高濃度液体製剤の安定性(12カ月期間)
10mMのヒスチジン、5%のスクロース、0.01%のポリソルベート80、約80mg/mLのTNF結合ナノボディ、pH6.0の製剤で充填済みシリンジ内に満たしたTNF結合ナノボディの高濃度液体の安定性を、SE−HPLCによるHMWのパーセンテージおよびLMWのパーセンテージ、CEX−HPLCによる酸性および塩基性種のパーセンテージ、ならびに相対的保持時間の評価および溶出プロファイルとTNF結合ナノボディ参照標準との比較性によって評価した。製剤を4℃で12カ月、25℃で3カ月、および40℃で2カ月間貯蔵した。
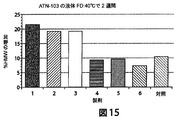
ATN−103の高濃度液体−他の製剤の安定性(他の安定化および不安定化賦形剤の特定)
TNF結合ナノボディ液体製剤の可能な賦形剤をスクリーニングするために、他の高濃度のTNF結合ナノボディ液体製剤の安定性を検査した。さらなる安定性を提供し、製剤を等張(ヒト対象への注射に適切)にするために、様々な賦形剤を用いた補足研究を行った。TNF結合ナノボディの濃度は88mg/mL〜100mg/mLの範囲であった。
1.10mMのヒスチジン、5%のスクロース、0.01%のポリソルベート80、100mMのアルギニン(塩基)、pH5.8
2.10mMのヒスチジン、5%のスクロース、0.01%のポリソルベート80、55mMのNaCl、pH6.1
3.10mMのヒスチジン、5%のスクロース、0.01%のポリソルベート80、55mMのアルギニンHCl、pH6.1
4.10mMのヒスチジン、5%のスクロース、0.01%のポリソルベート80、100mMのグリシン、pH6.0
5.10mMのヒスチジン、5%のスクロース、0.01%のポリソルベート80、100mMのメチオニン、pH6.0
6.10mMのヒスチジン、8%のスクロース、0.01%のポリソルベート80、pH6.0
対照:10mMのヒスチジン、5%のスクロース、0.01%のポリソルベート80、pH6.0
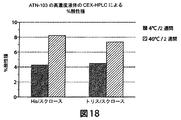
高濃度液体製剤TNF結合ナノボディ、短期間(2週間の期間)、ヒスチジンおよびトリス緩衝液の安定性
液体としてのTNF結合ナノボディの安定性を以下の図16〜19に例示する。2つの製剤、すなわち、20mMのヒスチジン、5%のスクロース、pH6.0中の118mg/mLのATN−103、および20mMのトリス、5%のスクロース、pH7.2中の117mg/mLのATN−103を検査した。製剤の安定性を、SE−HPLCによるHMWのパーセンテージおよびLMWのパーセンテージ、ならびにCEX−HPLCによる酸性のパーセンテージおよび塩基性種のパーセンテージによって評価した。データは、分解生成物の限定的な変化を4℃での貯蔵時間の関数として示す。分解生成物の一部の注目すべき変化が、液体のストレス条件である40℃で観察された。データは、ヒスチジンおよびトリス緩衝液中のTNF結合ナノボディの安定性がこれらの製剤化条件下で本質的に同様であることを示し、ヒスチジンがわずかにより有利な性能を有する(わずかに少ないLMW)。後に、製剤化前の活性により上昇したpH(7以上)がより高度のLMW形成をもたらすことが決定され、このことが以下で観察される利点を説明している。
TNF結合ナノボディの高濃度液体製剤の安定性:界面ストレス(凍結/解凍)の評価
図20〜23は、10mMのヒスチジン、5%のスクロース、0.01%のポリソルベート80、pH6.0中の約80mg/mLの液体TNF結合ナノボディ製剤の安定性を実証している。評価は−80℃および37℃の複数の凍結解凍サイクル後のサイズ排除−HPLC、濁度、および濃度の評価に基づく。
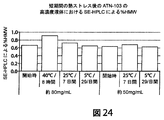
TNF結合ナノボディの高濃度液体製剤の安定性:製造プロセスにおいて潜在的に遭遇する短期間の熱ストレスの評価
図24は、液体TNF結合ナノボディが原薬および薬物製品の製造プロセス中に潜在的に遭遇し得る短期間の熱ストレスに対して頑健であることを実証する。高濃度液体を、10mMのヒスチジン、5%のスクロース、0.01%のポリソルベート80、pH6.0中、約80mg/mLおよび50mg/mLで研究した。評価は、40℃で8時間、25℃で7日間、および5℃で29日間曝露させた後の、サイズ排除HPLCによるHMWのパーセンテージおよびLMWのパーセンテージに基づく。データは、凝集体の限定的な変化を5℃および25℃での貯蔵時間の関数として示す。凝集体の一部の変化が、液体のストレス条件である40℃で観察された。
ATN−103の低濃度液体製剤の安定性:最適pHおよび製剤化の評価
図25〜28は、pH5.5、6.0、6.5、および7.0で緩衝した、低濃度(約1mg/mL)の液体TNF結合ナノボディ製剤の安定性を実証する。低濃度液体TNF結合ナノボディの安定性を、40℃の温度への曝露などのストレス(図25および26)、振盪(図28)、ならびに凍結/解凍に応答した、製剤化およびpHの関数として検査した。3つの以下の製剤、すなわち、10mMのヒスチジン、5%のスクロース、0.01%のTween−80、10mMのヒスチジン、5%のスクロース、0.01%のTween−80、150mMのアルギニンHCl、および10mMのヒスチジン、5%のスクロース、0.01%のTween−80、75mMの塩化ナトリウムのそれぞれについて、4つのpHを評価した。このデータ組では、Tween−80をポリソルベート80の別名として使用している。研究試料はSE−HPLCおよびUVを用いて評価した(濃度および濁度−A455によって測定)。
HST:10mMのヒスチジン、5%のスクロース、0.01%のTween−80
HSTA:10mMのヒスチジン、5%のスクロース、0.01%のTween−80、150mMのアルギニンHCl
HSTS:10mMのヒスチジン、5%のスクロース、0.01%のTween−80、75mMの塩化ナトリウム
低濃度TNF結合ナノボディ液体:pHおよび製剤化の関数としての振盪の効果の評価
また、TNF結合ナノボディがこのpH範囲にわたって300rpmで4時間(15℃)の振盪に感受性があることを示すデータも提示する(図28)。塩化ナトリウムおよびアルギニンを含有する製剤が振盪に対して特に感受性がある。ヒスチジン、スクロース、tween−80の製剤が、それぞれのpH群内で最も少ない高分子量分解を示した。pH6.0および7.0のヒスチジン、スクロース、tween−80の製剤が最も少ないHMW分解を示した。
高濃度液体製剤のTNF結合ナノボディの安定性、短期間(2週間の期間)、等張性調整剤の検査
液体としてのTNF結合ナノボディの安定性を以下に例示する。
低濃度および高濃度の液体製剤でのTNF結合ナノボディの安定性、標的製剤の確認、ならびに一次包装容器の検査
液体としてのTNF結合ナノボディの安定性を以下に例示する。
(a)10mg/mLのTNF結合ナノボディ、20mMのヒスチジン、7.5%のスクロース、0.01%のポリソルベート80、
(b)50mg/mLのTNF結合ナノボディ、20mMのヒスチジン、7.5%のスクロース、0.01%のポリソルベート80、
(c)100mg/mLのTNF結合ナノボディ、20mMのヒスチジン、7.5%のスクロース、0.01%のポリソルベート80。
(a)1つの販売業者からの事前充填可能なI型医薬グレードのガラス製シリンジおよびWest 4432のシリコン処理した灰色のゴム製プランジャー
(b)第2の販売業者からの事前充填可能なガラス製のI型医薬グレードのシリンジおよびWest 4432のシリコン処理した灰色のゴム製プランジャー
(c)事前充填可能な環状オレフィンコポリマーおよびWest 4432のシリコン処理した灰色のゴム製プランジャー。
本明細書中で言及したすべての参考文献は、それぞれの個々の出版物または特許もしくは特許出願が、その全体がすべての目的ために参照により組み込まれていると明確にかつ個別に示されている場合と同じ程度に、すべての目的のためにその全体が参照により本明細書中に組み込まれている。
Claims (30)
- (a)約10mg/mL〜約250mg/mLの濃度のTNF結合ナノボディ分子、
(b)約5%〜約10%の濃度の、スクロース、ソルビトール、またはトレハロースから選択される凍結乾燥保護剤、
(c)約0.01%〜0.6%の濃度の、ポリソルベート80またはポロキサマー188から選択される界面活性剤、および
(d)製剤のpHが約5.0〜7.5となるような、約10〜約20mMの濃度のヒスチジン緩衝液または約20mMの濃度のトリス緩衝液から選択される緩衝液、
を含み、製剤中のTNF結合ナノボディ分子が、4℃で少なくとも3カ月間貯蔵した後にその結合活性の少なくとも約70%を保持している製剤。 - (i)4℃で少なくとも12カ月間貯蔵した後に5%未満の高分子量(HMW)種、
(ii)4℃で少なくとも12カ月間貯蔵した後に5%未満の低分子量(LMW)種、
(iii)4℃で少なくとも12カ月間貯蔵した後に10%未満の酸性種、および/または
(iv)4℃で少なくとも12カ月間貯蔵した後に5%未満の塩基性種
を有する、請求項1に記載の製剤。 - 液体形態、凍結乾燥形態、再構成した凍結乾燥形態、または凍結した大量貯蔵形態である、請求項1または2に記載の製剤。
- (a)約10mg/mL〜約130mg/mLの濃度のTNF結合ナノボディ分子、
(b)約5%〜約10%の濃度のスクロース、
(c)約0.01%〜0.02%の濃度のポリソルベート80、および
(d)製剤のpHが約5.0〜7.5となるような、約10〜約20mMの濃度のヒスチジン緩衝液からなる群から選択される緩衝液、
を含む液体製剤または凍結乾燥製剤である、請求項1から3のいずれかに記載の製剤。 - (a)約80mg/mL〜約280mg/mLの濃度のTNF結合ナノボディ分子、
(b)約5%〜約10%の濃度のスクロース、
(c)約0.01%〜0.02%の濃度のポリソルベート80、および
(d)製剤のpHが約5.0〜7.5となるような、約10〜約20mMの濃度のヒスチジン緩衝液からなる群から選択される緩衝液、
を含む大量貯蔵製剤であり、少なくとも100リットルの製剤が凍結条件で貯蔵される、請求項1から3のいずれかに記載の製剤。 - 製剤のpHが、5、5.5、5.8〜6.1、6.0、6.1、6.5および7からなる群から選択される、請求項1から5のいずれかに記載の製剤。
- スクロース、ソルビトールまたはトレハロースの濃度が、約5%、約7.5%、または約10%である、請求項1から6のいずれかに記載の製剤。
- TNF結合ナノボディ分子が、1つまたは複数の単一ドメイン分子で構成される単鎖ポリペプチドである、請求項1から7のいずれかに記載の製剤。
- TNF結合ナノボディ分子が一価または多価である、請求項8に記載の製剤。
- TNF結合ナノボディ分子が単一特異性または多特異性である、請求項8に記載の製剤。
- 1つまたは複数の単一ドメイン分子が、CDR移植した、ヒト化した、ラクダ化した、脱免疫化した、またはファージディスプレイによって選択したものである、請求項8に記載の製剤。
- TNF結合ナノボディ分子が、腫瘍壊死因子α(TNFα)と結合する1つまたは複数の単一ドメイン分子と、ヒト血清アルブミン(HSA)タンパク質と結合する1つの単一ドメイン分子とを含む単鎖融合ポリペプチドである、請求項8に記載の製剤。
- TNF結合ナノボディ分子が、図30に示すアミノ酸配列(配列番号1)、またはそれに少なくとも90%同一のアミノ酸配列を含む、請求項1から7のいずれかに記載の製剤。
- TNF結合ナノボディ分子の単一ドメイン分子のうちの少なくとも1つが、DYWMY(配列番号2)(CDR1)、EINTNGLITKYPDSVKG(配列番号3)(CDR2)およびSPSGFN(配列番号4)(CDR3)のアミノ配列を有する、または前記CDRのうちの1つと1個の保存的アミノ酸置換によって異なるCDRを有する3個のCDRを含む、請求項1から7のいずれかに記載の製剤。
- TNF結合ナノボディ分子の単一ドメイン分子のうちの少なくとも1つが、図30(配列番号1)のアミノ酸約1〜115のアミノ酸配列を有する可変領域、または前記可変領域と10個までのアミノ酸が異なる可変領域を含む、請求項1から7のいずれかに記載の製剤。
- TNF結合ナノボディ分子が、HSAと結合する少なくとも1つの単一ドメイン分子をさらに含み、SFGMS(配列番号5)(CDR1)、SISGSGSDTLYADSVKG(配列番号6)(CDR2)およびGGSLSR(配列番号7)(CDR3)のアミノ配列を有する、または前記CDRのうちの1つと1個の保存的アミノ酸置換によって異なるCDRを有する3個のCDRを含む、請求項1から7のいずれかに記載の製剤。
- TNF結合ナノボディ分子の単一ドメイン分子のうちの少なくとも1つが、HSAと結合し、図30(配列番号1)のアミノ酸約125〜239のアミノ酸配列を有する可変領域、または前記可変領域と10個までのアミノ酸が異なる可変領域を含む、請求項1から7のいずれかに記載の製剤。
- TNF結合ナノボディを細胞培養物中で発現させることと、
TNF結合ナノボディを、クロマトグラフィー精製ステップ、または限外濾過/ダイアフィルトレーションステップのうちの少なくとも1つに通すことによって、TNF結合ナノボディを精製することと、
約5%〜約10%の濃度のスクロース、約0.01%、0.02%の濃度のポリソルベート80、および、製剤のpHが約5〜7.5となるような、約10〜約20mMの濃度のヒスチジン緩衝液または約20mMの濃度のトリス緩衝液を含有する製剤中で、TNF結合ナノボディの濃度を約10〜250mg/mLに調整することと
を含む、TNF結合ナノボディの製剤を調製する方法またはプロセス。 - TNF結合ナノボディ分子と凍結乾燥保護剤、界面活性剤、および緩衝液との混合物を凍結乾燥することによって、凍結乾燥した混合物を形成することと、
凍結乾燥した混合物を希釈剤中で再構成することによって、(a)約10mg/mL〜約130mg/mLの濃度のTNF結合ナノボディ分子、(b)約5%〜約10%の濃度の、スクロースまたはトレハロースからなる群から選択される凍結乾燥保護剤、(c)約0.01%〜0.02%の濃度の、界面活性剤としてのポリソルベート80、および(d)製剤のpHが約5.0〜7.5となるような、約10〜約20mMの濃度のヒスチジン緩衝液または約20mMの濃度のトリス緩衝液を含む、再構成した製剤を調製することと
を含む、TNF結合ナノボディ分子を含有する再構成した製剤を調製する方法。 - 請求項1から17のいずれかに記載の製剤と使用説明書とを含有する容器を含む、キットまたは製品。
- 製剤がバイアルまたは注射用シリンジ中に存在する、請求項20に記載のキットまたは製品。
- 製剤が充填済み注射用シリンジ中に存在する、請求項20に記載のキットまたは製品。
- シリンジまたはバイアルが、ガラス、プラスチック、または環状オレフィンポリマーもしくはコポリマーから選択されるポリマー材料でできている、請求項21に記載のキットまたは製品。
- 対象に、請求項1から17のいずれかに記載の製剤を含む医薬組成物を投与することによって、TNF関連障害に関連する1つまたは複数の症状を低下させることを含む、TNF関連障害を治療または予防する方法。
- TNF関連障害が炎症性または自己免疫性障害である、請求項24に記載の方法。
- TNF関連障害が、関節リウマチ(RA)、関節炎状態(たとえば、乾癬性関節炎、多関節若年性特発性関節炎(JIA)、強直性脊椎炎(AS)、乾癬、潰瘍性大腸炎、クローン病、炎症性腸疾患、または多発性硬化症から選択される、請求項24に記載の方法。
- 請求項1から17のいずれかに記載の製剤の試料を提供することと、
色、透明度、粘度、または1つもしくは複数のHMW、LMW、酸性もしくは塩基性種の量から選択される製剤のパラメータを評価することと、
パラメータが事前に選択された基準を満たすかどうかを判定することによって、プロセスを分析することと
を含む、製造プロセスを分析する方法。 - バッチ間の変動を監視もしくは制御する方法または試料を参照標準と比較する方法において2つ以上の試料製剤を比較することをさらに含む、請求項27に記載の方法。
- 前記比較に基づいて、製剤を分類、選択、受入もしくは廃棄、出荷もしくは保留、薬物製品へと加工、輸送、異なる場所に移動、製剤化、ラベル貼付、包装することをさらに含む、請求項28に記載の方法。
- 製剤の評価したパラメータに関するデータが含まれ、製剤のバッチの識別情報が任意選択により含まれる記録を提供することと、前記記録を決定者に提出することと、任意選択で、前記決定者から通信を受信することと、任意選択で、決定者からの通信に基づいて製剤のバッチを出荷または市場取引するかどうかを判定することとをさらに含む、請求項29に記載の方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US10947408P | 2008-10-29 | 2008-10-29 | |
| US61/109,474 | 2008-10-29 | ||
| PCT/US2009/062611 WO2010077422A2 (en) | 2008-10-29 | 2009-10-29 | Formulations of single domain antigen binding molecules |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2014262998A Division JP6421031B2 (ja) | 2008-10-29 | 2014-12-25 | 単一ドメイン抗原結合分子の製剤 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2012507553A true JP2012507553A (ja) | 2012-03-29 |
| JP2012507553A5 JP2012507553A5 (ja) | 2012-11-29 |
| JP5823867B2 JP5823867B2 (ja) | 2015-11-25 |
Family
ID=41467056
Family Applications (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011534779A Active JP5823867B2 (ja) | 2008-10-29 | 2009-10-29 | 単一ドメイン抗原結合分子の製剤 |
| JP2014262998A Active JP6421031B2 (ja) | 2008-10-29 | 2014-12-25 | 単一ドメイン抗原結合分子の製剤 |
| JP2017017004A Pending JP2017105807A (ja) | 2008-10-29 | 2017-02-01 | 単一ドメイン抗原結合分子の製剤 |
Family Applications After (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2014262998A Active JP6421031B2 (ja) | 2008-10-29 | 2014-12-25 | 単一ドメイン抗原結合分子の製剤 |
| JP2017017004A Pending JP2017105807A (ja) | 2008-10-29 | 2017-02-01 | 単一ドメイン抗原結合分子の製剤 |
Country Status (14)
| Country | Link |
|---|---|
| US (4) | US9393304B2 (ja) |
| EP (3) | EP2362767B1 (ja) |
| JP (3) | JP5823867B2 (ja) |
| KR (2) | KR101581986B1 (ja) |
| CN (2) | CN104740631B (ja) |
| AR (1) | AR073997A1 (ja) |
| AU (1) | AU2009333791B2 (ja) |
| BR (2) | BRPI0919979A2 (ja) |
| CA (1) | CA2738243C (ja) |
| HK (2) | HK1210431A1 (ja) |
| IL (2) | IL211932A (ja) |
| MX (1) | MX345226B (ja) |
| RU (2) | RU2481824C2 (ja) |
| WO (1) | WO2010077422A2 (ja) |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2015166885A1 (ja) * | 2014-04-28 | 2015-11-05 | エーザイ・アール・アンド・ディー・マネジメント株式会社 | Hgf凍結乾燥製剤 |
| JP2017516848A (ja) * | 2014-05-23 | 2017-06-22 | アレス トレーディング ソシエテ アノニム | 液体医薬組成物 |
| JP2019524719A (ja) * | 2016-07-11 | 2019-09-05 | クレッシェンド、バイオロジックス、リミテッドCrescendo Biologics Limited | 障害の治療のための組成物 |
| US11548926B2 (en) | 2016-03-17 | 2023-01-10 | Eisai R&D Management Co., Ltd. | Method for producing an active hepatocyte growth factor (HGF) |
Families Citing this family (57)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| MX339524B (es) | 2001-10-11 | 2016-05-30 | Wyeth Corp | Composiciones inmunogenicas novedosas para la prevencion y tratamiento de enfermedad meningococica. |
| JP2008543839A (ja) | 2005-06-14 | 2008-12-04 | アムジェン インコーポレーテッド | 自己緩衝タンパク質製剤 |
| MX2011004558A (es) | 2008-10-29 | 2011-06-01 | Wyeth Llc | Procedimientos para la purificacion de moleculas de union a antigeno de un unico dominio. |
| MX345226B (es) | 2008-10-29 | 2017-01-20 | Ablynx Nv | Formulaciones de moleculas de union a antigeno de dominio sencillo. |
| US10005830B2 (en) | 2009-03-05 | 2018-06-26 | Ablynx N.V. | Antigen binding dimer-complexes, methods of making/avoiding and uses thereof |
| US9265834B2 (en) * | 2009-03-05 | 2016-02-23 | Ablynx N.V. | Stable formulations of polypeptides and uses thereof |
| US9884117B2 (en) * | 2009-09-03 | 2018-02-06 | Ablynx N.V. | Stable formulations of polypeptides and uses thereof |
| EP2533814A2 (en) * | 2010-02-11 | 2012-12-19 | Ablynx N.V. | Delivery of immunoglobulin variable domains and constructs thereof |
| WO2011141926A2 (en) | 2010-05-10 | 2011-11-17 | Intas Biopharmaceuticals Limited | Liquid formulation of polypeptides containing an fc domain of an immunoglobulin |
| WO2012007880A2 (en) * | 2010-07-16 | 2012-01-19 | Ablynx Nv | Modified single domain antigen binding molecules and uses thereof |
| PL3246044T3 (pl) * | 2010-08-23 | 2021-08-23 | Wyeth Llc | Stabilne preparaty antygenów rLP2086 Neisseria meningitidis |
| ES2728282T3 (es) | 2010-09-10 | 2019-10-23 | Wyeth Llc | Variantes no lipidadas de antígenos ORF2086 de Neisseria meningitidis |
| JP6130350B2 (ja) * | 2011-03-30 | 2017-05-17 | アブリンクス エン.ヴェー. | TNFαに対する単一ドメイン抗体で免疫障害を処置する方法 |
| KR102289394B1 (ko) * | 2011-03-31 | 2021-08-13 | 머크 샤프 앤드 돔 코포레이션 | 인간 프로그램화된 사멸 수용체 pd-1에 대한 항체의 안정한 제제 및 관련된 치료 |
| JOP20200043A1 (ar) * | 2011-05-10 | 2017-06-16 | Amgen Inc | طرق معالجة أو منع الاضطرابات المختصة بالكوليسترول |
| GB201112429D0 (en) * | 2011-07-19 | 2011-08-31 | Glaxo Group Ltd | Antigen-binding proteins with increased FcRn binding |
| KR102143506B1 (ko) | 2011-08-17 | 2020-08-12 | 글락소 그룹 리미티드 | 변형된 단백질 및 펩티드 |
| WO2013043071A1 (en) * | 2011-09-23 | 2013-03-28 | Technophage, Investigação E Desenvolvimento Em Biotecnologia, Sa | Modified albumin-binding domains and uses thereof to improve pharmacokinetics |
| EP2758434A2 (en) | 2011-09-23 | 2014-07-30 | Technophage, Investigação E Desenvolvimento Em Biotecnologia, SA | Anti-tumor necrosis factor-alpha agents and uses thereof |
| CN102512384B (zh) * | 2011-12-29 | 2014-11-26 | 嘉和生物药业有限公司 | 一种冻干剂型蛋白组合物及其制备方法 |
| SG11201405475UA (en) | 2012-03-07 | 2014-10-30 | Cadila Healthcare Ltd | Pharmaceutical formulations of tnf-alpha antibodies |
| SA115360586B1 (ar) | 2012-03-09 | 2017-04-12 | فايزر انك | تركيبات لعلاج الالتهاب السحائي البكتيري وطرق لتحضيرها |
| EP3485906A1 (en) | 2012-03-09 | 2019-05-22 | Pfizer Inc | Neisseria meningitidis compositions and methods thereof |
| NL1040254C2 (en) | 2013-05-17 | 2014-11-24 | Ablynx Nv | Stable formulations of immunoglobulin single variable domains and uses thereof. |
| KR20210002757A (ko) | 2013-09-08 | 2021-01-08 | 화이자 인코포레이티드 | 나이세리아 메닌지티디스 조성물 및 그의 방법 |
| CN106170298B (zh) | 2013-10-16 | 2024-01-09 | 前瞻疗法公司 | 用于提高抗体稳定性的缓冲液制剂 |
| CN105012949A (zh) * | 2014-04-28 | 2015-11-04 | 上海药明康德新药开发有限公司 | 重组人抗人TNFα单克隆抗体的制剂 |
| KR102385802B1 (ko) * | 2014-05-07 | 2022-04-13 | 다케다 야쿠힝 고교 가부시키가이샤 | Gm-csf 중화 화합물을 포함하는 액체 제제 |
| PL2946765T3 (pl) | 2014-05-23 | 2017-08-31 | Ares Trading S.A. | Ciekła kompozycja farmaceutyczna |
| EP2946766B1 (en) | 2014-05-23 | 2016-03-02 | Ares Trading S.A. | Liquid pharmaceutical composition |
| CN105267960A (zh) * | 2014-06-13 | 2016-01-27 | 亚宝药业太原制药有限公司 | 一种重组腺病毒疫苗制剂及其制备方法 |
| NL2013007B1 (en) | 2014-06-16 | 2016-07-05 | Ablynx Nv | Methods of treating TTP with immunoglobulin single variable domains and uses thereof. |
| WO2016118707A1 (en) | 2015-01-21 | 2016-07-28 | Oncobiologics, Inc. | Modulation of charge variants in a monoclonal antibody composition |
| MX2017010705A (es) | 2015-02-19 | 2017-12-04 | Pfizer | Composiciones de neisseria meningitidis y metodos de la misma. |
| BR112017020275A8 (pt) | 2015-03-31 | 2023-01-31 | Sorriso Pharmaceuticals Inc | Polipeptídeos |
| AR104847A1 (es) | 2015-06-17 | 2017-08-16 | Lilly Co Eli | Formulación de anticuerpo anti-cgrp |
| US20170059561A1 (en) * | 2015-08-28 | 2017-03-02 | The Florida International University Board Of Trustees | Thermally Stable Electrochemical Sensor With Long Shelf-Life |
| EP3411401A1 (en) | 2016-02-03 | 2018-12-12 | Oncobiologics, Inc. | Buffer formulations for enhanced antibody stability |
| CA3019482A1 (en) | 2016-03-31 | 2017-10-05 | Vhsquared Limited | Compositions |
| CN106265480A (zh) * | 2016-09-03 | 2017-01-04 | 山西纳安生物科技有限公司 | 纳米抗体阴道给药系统及制备方法和应用 |
| CN106267191A (zh) * | 2016-09-03 | 2017-01-04 | 山西纳安生物科技有限公司 | 纳米抗体生物药透皮给药制剂系统及制备方法和应用 |
| EP3519438A1 (en) | 2016-09-30 | 2019-08-07 | VHsquared Limited | Compositions |
| MX2019004580A (es) * | 2016-10-21 | 2019-08-12 | Amgen Inc | Formulaciones farmaceuticas y metodos para prepararlas. |
| KR102471458B1 (ko) * | 2016-12-28 | 2022-11-25 | 제이씨알 파마 가부시키가이샤 | 동결건조 제제 |
| CN107674122A (zh) * | 2016-12-28 | 2018-02-09 | 天津天锐生物科技有限公司 | 一种识别人血清白蛋白的单域抗体 |
| IL303108B1 (en) | 2017-01-31 | 2024-03-01 | Pfizer | NEISSERIA MENINGITIDIS preparations and methods therefor |
| JOP20190260A1 (ar) | 2017-05-02 | 2019-10-31 | Merck Sharp & Dohme | صيغ ثابتة لأجسام مضادة لمستقبل الموت المبرمج 1 (pd-1) وطرق استخدامها |
| SG11201909955XA (en) | 2017-05-02 | 2019-11-28 | Merck Sharp & Dohme | Formulations of anti-lag3 antibodies and co-formulations of anti-lag3 antibodies and anti-pd-1 antibodies |
| MX2020008294A (es) | 2018-02-06 | 2020-11-18 | Ablynx Nv | Metodos de tratamiento de episodio inicial de ttp con dominios variables simples de inmunoglobulina. |
| WO2020060183A1 (ko) * | 2018-09-18 | 2020-03-26 | 삼성바이오에피스 주식회사 | 트라스투주맙 항체 안정화 액체 제제 |
| CN111228225B (zh) * | 2018-11-28 | 2022-08-26 | 鲁南制药集团股份有限公司 | 一种重组人肿瘤坏死因子受体-Fc融合蛋白冻干制剂 |
| MX2021015763A (es) | 2019-06-21 | 2022-04-18 | Sorriso Pharmaceuticals Inc | Polipeptidos. |
| CN114466864A (zh) | 2019-06-21 | 2022-05-10 | 索瑞索制药公司 | 多肽 |
| CN111349159A (zh) * | 2020-03-17 | 2020-06-30 | 暨南大学 | 一种抗人血清白蛋白的纳米抗体及其应用 |
| WO2023186174A1 (en) * | 2022-04-01 | 2023-10-05 | Zai Lab (Shanghai) Co., Ltd. | Topical formulation comprising an il-17a binding molecule and uses thereof |
| CN114957467B (zh) * | 2022-06-21 | 2023-04-18 | 天津大学 | 特异性结合TNF-α的纳米抗体及其用途 |
| WO2024038112A1 (en) * | 2022-08-17 | 2024-02-22 | Institut National de la Santé et de la Recherche Médicale | Improved anti-albumin nanobodies and their uses |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH11510170A (ja) * | 1995-07-27 | 1999-09-07 | ジェネンテック インコーポレーテッド | タンパク質の処方 |
| JP2003516361A (ja) * | 1999-12-02 | 2003-05-13 | カイロン コーポレイション | 凍結乾燥の際に生物学的分子を安定化するための組成物および方法 |
| JP2006249084A (ja) * | 2005-03-08 | 2006-09-21 | Pharmacia & Upjohn Co Llc | 抗MadCAM抗体組成物 |
| WO2006122786A2 (en) * | 2005-05-18 | 2006-11-23 | Ablynx Nv | Improved nanobodies™ against tumor necrosis factor-alpha |
| WO2007014073A2 (en) * | 2005-07-22 | 2007-02-01 | Amgen Inc. | Concentrated protein lyophilates, methods, and uses |
Family Cites Families (163)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2073403A (en) | 1935-11-23 | 1937-03-09 | Abraham G Goldberg | Display device |
| SE307996B (ja) | 1965-11-30 | 1969-01-27 | Asea Ab | |
| US3773919A (en) | 1969-10-23 | 1973-11-20 | Du Pont | Polylactide-drug mixtures |
| CU22545A1 (es) | 1994-11-18 | 1999-03-31 | Centro Inmunologia Molecular | Obtención de un anticuerpo quimérico y humanizado contra el receptor del factor de crecimiento epidérmico para uso diagnóstico y terapéutico |
| IE52535B1 (en) | 1981-02-16 | 1987-12-09 | Ici Plc | Continuous release pharmaceutical compositions |
| US4475196A (en) | 1981-03-06 | 1984-10-02 | Zor Clair G | Instrument for locating faults in aircraft passenger reading light and attendant call control system |
| US4447233A (en) | 1981-04-10 | 1984-05-08 | Parker-Hannifin Corporation | Medication infusion pump |
| US4714681A (en) | 1981-07-01 | 1987-12-22 | The Board Of Reagents, The University Of Texas System Cancer Center | Quadroma cells and trioma cells and methods for the production of same |
| US4474893A (en) | 1981-07-01 | 1984-10-02 | The University of Texas System Cancer Center | Recombinant monoclonal antibodies |
| US4439196A (en) | 1982-03-18 | 1984-03-27 | Merck & Co., Inc. | Osmotic drug delivery system |
| US4447224A (en) | 1982-09-20 | 1984-05-08 | Infusaid Corporation | Variable flow implantable infusion apparatus |
| US4487603A (en) | 1982-11-26 | 1984-12-11 | Cordis Corporation | Implantable microinfusion pump system |
| GB8308235D0 (en) | 1983-03-25 | 1983-05-05 | Celltech Ltd | Polypeptides |
| US4816567A (en) | 1983-04-08 | 1989-03-28 | Genentech, Inc. | Recombinant immunoglobin preparations |
| US4486194A (en) | 1983-06-08 | 1984-12-04 | James Ferrara | Therapeutic device for administering medicaments through the skin |
| JPS6147500A (ja) | 1984-08-15 | 1986-03-07 | Res Dev Corp Of Japan | キメラモノクロ−ナル抗体及びその製造法 |
| EP0173494A3 (en) | 1984-08-27 | 1987-11-25 | The Board Of Trustees Of The Leland Stanford Junior University | Chimeric receptors by dna splicing and expression |
| GB8422238D0 (en) | 1984-09-03 | 1984-10-10 | Neuberger M S | Chimeric proteins |
| US4596556A (en) | 1985-03-25 | 1986-06-24 | Bioject, Inc. | Hypodermic injection apparatus |
| US5225539A (en) | 1986-03-27 | 1993-07-06 | Medical Research Council | Recombinant altered antibodies and methods of making altered antibodies |
| GB8607679D0 (en) | 1986-03-27 | 1986-04-30 | Winter G P | Recombinant dna product |
| US4790824A (en) | 1987-06-19 | 1988-12-13 | Bioject, Inc. | Non-invasive hypodermic injection device |
| US4941880A (en) | 1987-06-19 | 1990-07-17 | Bioject, Inc. | Pre-filled ampule and non-invasive hypodermic injection device assembly |
| US5770198A (en) | 1988-05-18 | 1998-06-23 | The Research Foundation Of The State Of New York | Platelet-specific chimeric 7E3 immunoglobulin |
| US4925648A (en) | 1988-07-29 | 1990-05-15 | Immunomedics, Inc. | Detection and treatment of infectious and inflammatory lesions |
| US5601819A (en) | 1988-08-11 | 1997-02-11 | The General Hospital Corporation | Bispecific antibodies for selective immune regulation and for selective immune cell binding |
| US5223409A (en) | 1988-09-02 | 1993-06-29 | Protein Engineering Corp. | Directed evolution of novel binding proteins |
| IL91501A (en) | 1988-09-02 | 1998-03-10 | Dyax Corp | Generation of a variegated library of mutant potential binding proteins and screening of said library for proteins with a desired binding activity |
| JP2919890B2 (ja) | 1988-11-11 | 1999-07-19 | メディカル リサーチ カウンスル | 単一ドメインリガンド、そのリガンドからなる受容体、その製造方法、ならびにそのリガンドおよび受容体の使用 |
| US5530101A (en) | 1988-12-28 | 1996-06-25 | Protein Design Labs, Inc. | Humanized immunoglobulins |
| GB8905400D0 (en) | 1989-03-09 | 1989-04-19 | Jonker Margreet | Medicaments |
| EP0739904A1 (en) | 1989-06-29 | 1996-10-30 | Medarex, Inc. | Bispecific reagents for aids therapy |
| SE509359C2 (sv) | 1989-08-01 | 1999-01-18 | Cemu Bioteknik Ab | Användning av stabiliserade protein- eller peptidkonjugat för framställning av ett läkemedel |
| AU640400B2 (en) | 1989-08-07 | 1993-08-26 | Peptide Technology Ltd. | Tumour necrosis factor binding ligands |
| US5064413A (en) | 1989-11-09 | 1991-11-12 | Bioject, Inc. | Needleless hypodermic injection device |
| US5312335A (en) | 1989-11-09 | 1994-05-17 | Bioject Inc. | Needleless hypodermic injection device |
| US5859205A (en) | 1989-12-21 | 1999-01-12 | Celltech Limited | Humanised antibodies |
| US5427908A (en) | 1990-05-01 | 1995-06-27 | Affymax Technologies N.V. | Recombinant library screening methods |
| GB9015198D0 (en) | 1990-07-10 | 1990-08-29 | Brien Caroline J O | Binding substance |
| ATE185601T1 (de) | 1990-07-10 | 1999-10-15 | Cambridge Antibody Tech | Verfahren zur herstellung von spezifischen bindungspaargliedern |
| GB9016299D0 (en) | 1990-07-25 | 1990-09-12 | Brien Caroline J O | Binding substances |
| US5612034A (en) | 1990-10-03 | 1997-03-18 | Redcell, Inc. | Super-globuling for in vivo extended lifetimes |
| US5843440A (en) | 1990-10-03 | 1998-12-01 | Redcell Canada, Inc. | Cellular and serum protein anchors for modulating pharmacokinetics |
| JP3583420B2 (ja) | 1990-10-05 | 2004-11-04 | メダレツクス・インコーポレーテツド | 二特異的試薬を用いた標的免疫化 |
| GB9021679D0 (en) | 1990-10-05 | 1990-11-21 | Gorman Scott David | Antibody preparation |
| AU8727291A (en) | 1990-10-29 | 1992-06-11 | Cetus Oncology Corporation | Bispecific antibodies, method of production, and uses thereof |
| WO1992009690A2 (en) | 1990-12-03 | 1992-06-11 | Genentech, Inc. | Enrichment method for variant proteins with altered binding properties |
| DE69233697T2 (de) | 1991-03-01 | 2008-01-24 | Dyax Corp., Cambridge | Verfahren zur Entwicklung von bindenden Mikroproteinen |
| ATE192302T1 (de) | 1991-03-21 | 2000-05-15 | Masimo Corp | Rauscharmer optischer wandler |
| DK1471142T3 (da) | 1991-04-10 | 2009-03-09 | Scripps Research Inst | Heterodimere receptor-biblioteker under anvendelse af fagemider |
| ES2093778T3 (es) | 1991-04-26 | 1997-01-01 | Surface Active Ltd | Nuevos anticuerpos y metodos para su uso. |
| DE122004000008I1 (de) | 1991-06-14 | 2005-06-09 | Genentech Inc | Humanisierter Heregulin Antikörper. |
| DE4122599C2 (de) | 1991-07-08 | 1993-11-11 | Deutsches Krebsforsch | Phagemid zum Screenen von Antikörpern |
| US5728536A (en) | 1993-07-29 | 1998-03-17 | St. Jude Children's Research Hospital | Jak kinases and regulation of Cytokine signal transduction |
| DK0627940T3 (da) | 1992-03-05 | 2003-09-01 | Univ Texas | Anvendelse af immunokonjugater til diagnose og/eller terapi af vaskulariserede tumorer |
| US5383851A (en) | 1992-07-24 | 1995-01-24 | Bioject Inc. | Needleless hypodermic injection device |
| EP0584421A1 (en) | 1992-08-21 | 1994-03-02 | Cécile Casterman | Immunoglobulins devoid of light chains |
| PT1498427E (pt) | 1992-08-21 | 2010-03-22 | Univ Bruxelles | Imunoglobulinas desprovidas de cadeias leves |
| ATE264388T1 (de) | 1992-09-24 | 2004-04-15 | Tanox Biosystems Inc | Umgestaltete monoklonale antikörper gegen ein immunglobulinisotyp |
| ATE236655T1 (de) | 1993-01-06 | 2003-04-15 | Kinerton Ltd | Ionische molekularkonjugate von bioabbaubaren polyestern und bioaktiven polypeptiden |
| GB9403857D0 (en) | 1994-03-01 | 1994-04-20 | Scotia Holdings Plc | Fatty acid derivatives |
| CN1073119C (zh) | 1994-05-18 | 2001-10-17 | 吸入治疗系统公司 | 干扰素干粉配方的方法及组合物 |
| US5731168A (en) | 1995-03-01 | 1998-03-24 | Genentech, Inc. | Method for making heteromultimeric polypeptides |
| EP0739981A1 (en) | 1995-04-25 | 1996-10-30 | Vrije Universiteit Brussel | Variable fragments of immunoglobulins - use for therapeutic or veterinary purposes |
| EP0822830B1 (en) | 1995-04-27 | 2008-04-02 | Amgen Fremont Inc. | Human anti-IL-8 antibodies, derived from immunized xenomice |
| AU2466895A (en) | 1995-04-28 | 1996-11-18 | Abgenix, Inc. | Human antibodies derived from immunized xenomice |
| GB2302024B (en) | 1995-06-09 | 1998-10-07 | Malix Polymer Engineering Limi | Obstetric vacuum extractor |
| ZA966075B (en) * | 1995-07-27 | 1998-01-19 | Genentech Inc | Protein formulation. |
| US5697151A (en) | 1995-08-07 | 1997-12-16 | General Electric Company | Method for repairing partitions of a turbine diaphragm |
| AU725609C (en) | 1995-08-18 | 2002-01-03 | Morphosys Ag | Protein/(poly)peptide libraries |
| US7368111B2 (en) | 1995-10-06 | 2008-05-06 | Cambridge Antibody Technology Limited | Human antibodies specific for TGFβ2 |
| WO1997029131A1 (en) | 1996-02-09 | 1997-08-14 | Basf Aktiengesellschaft | HUMAN ANTIBODIES THAT BIND HUMAN TNF$g(a) |
| US6417337B1 (en) | 1996-10-31 | 2002-07-09 | The Dow Chemical Company | High affinity humanized anti-CEA monoclonal antibodies |
| CA2722378C (en) | 1996-12-03 | 2015-02-03 | Amgen Fremont Inc. | Human antibodies that bind tnf.alpha. |
| EP0983303B1 (en) | 1997-05-21 | 2006-03-08 | Biovation Limited | Method for the production of non-immunogenic proteins |
| US5994511A (en) | 1997-07-02 | 1999-11-30 | Genentech, Inc. | Anti-IgE antibodies and methods of improving polypeptides |
| EP1015480A2 (en) | 1997-08-18 | 2000-07-05 | Innogenetics N.V. | Interferon-gamma-binding molecules for treating septic shock, cachexia, immune diseases and skin disorders |
| ATE461282T1 (de) | 1997-10-27 | 2010-04-15 | Bac Ip Bv | Multivalente antigenbindende proteine |
| EP0954978B1 (en) | 1998-03-12 | 2011-11-30 | VHsquared Limited | New products comprising inactivated yeasts or moulds provided with active antibodies |
| HUP9900956A2 (hu) | 1998-04-09 | 2002-04-29 | Aventis Pharma Deutschland Gmbh. | Egyláncú, több antigéntkötőhely kialakítására képes molekulák, előállításuk és alkalmazásuk |
| WO1999064069A1 (en) | 1998-06-10 | 1999-12-16 | Ophidian Pharmaceuticals, Inc. | Antibodies to cytokines in the prevention and treatment of inflammatory bowel disease |
| EP1002861A1 (en) | 1998-10-26 | 2000-05-24 | Unilever Plc | Antigen-binding proteins comprising a linker which confers restricted conformational flexibility |
| IL127127A0 (en) | 1998-11-18 | 1999-09-22 | Peptor Ltd | Small functional units of antibody heavy chain variable regions |
| ATE352559T1 (de) | 1998-12-08 | 2007-02-15 | Biovation Ltd | Verfahren zur verminderung der immunogenität von proteinen |
| US6897044B1 (en) | 1999-01-28 | 2005-05-24 | Biogen Idec, Inc. | Production of tetravalent antibodies |
| US6419934B1 (en) | 1999-02-24 | 2002-07-16 | Edward L. Tobinick | TNF modulators for treating neurological disorders associated with viral infection |
| TR200503572T2 (tr) | 1999-03-25 | 2006-04-21 | Knoll Gmbh & Co. Kg. | Beşeri IL-12'yi bağlayan beşeri antikorlar ve bunları üretmek için yöntemler. |
| EP1118669A3 (en) | 1999-12-17 | 2001-08-29 | Unilever Plc | Production of camelid antibodies in plants |
| CA2390691C (en) | 1999-12-24 | 2016-05-10 | Genentech, Inc. | Methods and compositions for prolonging elimination half-times of bioactive compounds |
| EP2338515A3 (en) | 2000-02-10 | 2011-11-16 | Abbott Laboratories | Antibodies that bind human interleukin-18 and methods of making and using |
| US7097840B2 (en) | 2000-03-16 | 2006-08-29 | Genentech, Inc. | Methods of treatment using anti-ErbB antibody-maytansinoid conjugates |
| US7943129B2 (en) | 2000-05-26 | 2011-05-17 | National Research Council Of Canada | Single-domain brain-targeting antibody fragments derived from llama antibodies |
| SE0002898L (sv) | 2000-08-14 | 2002-02-15 | Telia Ab | Kommunikationstjänst |
| US6699473B2 (en) | 2000-10-13 | 2004-03-02 | Uab Research Foundation | Human anti-epidermal growth factor receptor single-chain antibodies |
| WO2002039121A2 (en) | 2000-11-03 | 2002-05-16 | Board Of Regents, The University Of Texas System | Methods for detecting the efficacy of anticancer treatments |
| WO2002048193A2 (en) | 2000-12-13 | 2002-06-20 | Unilever N.V. | Camelidae antibody arrays |
| GB0031448D0 (en) | 2000-12-22 | 2001-02-07 | Leuven K U Res & Dev | Inhibition of the vWF-collagen interaction by anti-human vWF monoclonal antibody (82D6A3) results in abolition of in vivo arterial platelet thrombus formation |
| WO2002096948A2 (en) | 2001-01-29 | 2002-12-05 | Idec Pharmaceuticals Corporation | Engineered tetravalent antibodies and methods of use |
| MXPA03008102A (es) | 2001-03-07 | 2003-12-12 | Procter & Gamble | Composicion topica que comprende un agente cosmetico enlazante con base de sal de diazonio. |
| DE60234759D1 (de) | 2001-03-28 | 2010-01-28 | Heska Corp | Nachweisverfahren für eine frühe nierenkrankheit in tieren |
| US20060073141A1 (en) | 2001-06-28 | 2006-04-06 | Domantis Limited | Compositions and methods for treating inflammatory disorders |
| AU2002319402B2 (en) | 2001-06-28 | 2008-09-11 | Domantis Limited | Dual-specific ligand and its use |
| US20050271663A1 (en) | 2001-06-28 | 2005-12-08 | Domantis Limited | Compositions and methods for treating inflammatory disorders |
| US20030020733A1 (en) | 2001-07-24 | 2003-01-30 | Yin Memphis Zhihong | Computer display having selective area magnification |
| CA2457636C (en) | 2001-08-10 | 2012-01-03 | Aberdeen University | Antigen binding domains |
| US7041812B2 (en) | 2001-08-29 | 2006-05-09 | Amersham Biosciences Corp | Labeled nucleoside polyphosphates |
| US7084257B2 (en) | 2001-10-05 | 2006-08-01 | Amgen Inc. | Fully human antibody Fab fragments with human interferon-gamma neutralizing activity |
| US6723359B2 (en) | 2001-10-18 | 2004-04-20 | Firmenich Sa | Spray-dried compositions and method for their preparation |
| JP2005289809A (ja) | 2001-10-24 | 2005-10-20 | Vlaams Interuniversitair Inst Voor Biotechnologie Vzw (Vib Vzw) | 突然変異重鎖抗体 |
| US8420353B2 (en) | 2002-03-22 | 2013-04-16 | Aprogen, Inc. | Humanized antibody and process for preparing same |
| JP2006512895A (ja) | 2002-06-28 | 2006-04-20 | ドマンティス リミテッド | リガンド |
| JP5138867B2 (ja) | 2002-08-01 | 2013-02-06 | イミューノメディクス、インコーポレイテッド | α−フェトタンパク質Immu31抗体および融合タンパク質ならびにその使用方法 |
| US20060228355A1 (en) | 2003-11-07 | 2006-10-12 | Toon Laeremans | Camelidae single domain antibodies vhh directed against epidermal growth factor receptor and uses therefor |
| US20100003253A1 (en) | 2002-11-08 | 2010-01-07 | Ablynx N.V. | Single domain antibodies directed against epidermal growth factor receptor and uses therefor |
| CN102584997A (zh) | 2002-11-08 | 2012-07-18 | 埃博灵克斯股份有限公司 | 针对肿瘤坏死因子-α的单结构域抗体及其用途 |
| EP1900753B1 (en) | 2002-11-08 | 2017-08-09 | Ablynx N.V. | Method of administering therapeutic polypeptides, and polypeptides therefor |
| US20060034833A1 (en) | 2002-11-08 | 2006-02-16 | Els Beirnaert | Single domain antibodies directed against interferron-gamma and uses therefor |
| US20060034845A1 (en) | 2002-11-08 | 2006-02-16 | Karen Silence | Single domain antibodies directed against tumor necrosis factor alpha and uses therefor |
| EP2267032A3 (en) | 2002-11-08 | 2011-11-09 | Ablynx N.V. | Method of administering therapeutic polypeptides, and polypeptides therefor |
| US8003117B2 (en) | 2002-11-20 | 2011-08-23 | Nof Corporation | Polyalkylene glycol derivative and modified bio-related substance |
| MXPA05007163A (es) | 2002-12-31 | 2005-09-21 | Nektar Therapeutics Al Corp | Derivados polimericos de acido maleamico y sus bioconjugados. |
| CA2509153C (en) | 2002-12-31 | 2013-04-16 | Nektar Therapeutics Al, Corporation | Hydrolytically stable maleimide-terminated polymers |
| JP4869064B2 (ja) * | 2003-04-04 | 2012-02-01 | ジェネンテック, インコーポレイテッド | 高濃度抗体及びタンパク質製剤 |
| PL1639011T3 (pl) | 2003-06-30 | 2009-05-29 | Domantis Ltd | Pegilowane przeciwciała jednodomenowe (dAb) |
| US7026432B2 (en) | 2003-08-12 | 2006-04-11 | General Electric Company | Electrically conductive compositions and method of manufacture thereof |
| US7605120B2 (en) | 2003-10-22 | 2009-10-20 | Amgen Inc. | Antagonists of the brandykinin B1 receptor |
| CN102276717B (zh) | 2003-10-27 | 2015-09-09 | 惠氏公司 | 使用羟磷灰石层析除去高分子量聚集体 |
| US7785903B2 (en) | 2004-04-09 | 2010-08-31 | Genentech, Inc. | Variable domain library and uses |
| US8921528B2 (en) | 2004-06-01 | 2014-12-30 | Domantis Limited | Bispecific fusion antibodies with enhanced serum half-life |
| US7632924B2 (en) | 2004-06-18 | 2009-12-15 | Ambrx, Inc. | Antigen-binding polypeptides and their uses |
| EP1814917A2 (en) | 2004-10-13 | 2007-08-08 | Ablynx N.V. | Single domain camelide anti-amyloid beta antibodies and polypeptides comprising the same for the treatment and diagnosis of degenerative neural diseases such as alzheimer's disease |
| JP2008521870A (ja) | 2004-12-02 | 2008-06-26 | ドマンティス リミテッド | 抗il−1r1単一ドメイン抗体および治療使用 |
| WO2006099308A2 (en) | 2005-03-11 | 2006-09-21 | Wyeth | A method of weak partitioning chromatography |
| DE102005023617A1 (de) * | 2005-05-21 | 2006-11-23 | Aspre Ag | Verfahren zum Mischen von Farben in einem Display |
| WO2006138553A2 (en) | 2005-06-17 | 2006-12-28 | Wyeth | Methods of purifying fc region containing proteins |
| MX2007016032A (es) * | 2005-06-21 | 2008-03-10 | Xoma Technology Ltd | Anticuerpos de enlace a il-1-beta y fragmentos de los mismos. |
| US9017662B2 (en) * | 2005-08-30 | 2015-04-28 | Actogenix N.V. | Anti-TNF alpha producing lactic acid bacteria for the treatment of chronic enterocolitis |
| EA200870264A1 (ru) * | 2006-02-15 | 2009-02-27 | Имклоун Системз Инкорпорейтед | Композиция антител |
| WO2007100535A2 (en) | 2006-02-22 | 2007-09-07 | Merck & Co., Inc. | Oxyntomodulin derivatives |
| EP2004690A2 (en) | 2006-03-13 | 2008-12-24 | Ablynx N.V. | Amino acid sequences directed against il-6 and polypeptides comprising the same for the treatment of diseases and disorders associated with il-6-mediated signalling |
| AU2007280929B2 (en) | 2006-07-26 | 2012-03-22 | Abbott Rapid Diagnostics International Unlimited Company | Analysis device for biological sample |
| EP2094729A1 (en) | 2006-12-11 | 2009-09-02 | F.Hoffmann-La Roche Ag | Abeta antibody parenteral formulation |
| WO2008075356A2 (en) | 2006-12-19 | 2008-06-26 | Shay Bushinsky | Interactive broadcast system and method |
| EP2101801A1 (en) * | 2006-12-20 | 2009-09-23 | Ablynx N.V. | Oral delivery of polypeptides |
| EP3124045A3 (en) * | 2006-12-20 | 2017-05-03 | Xoma (Us) Llc | Treatment of il-1 beta related diseases |
| AU2007338791B2 (en) * | 2006-12-21 | 2014-03-13 | Amgen Inc | Stable buffered formulations containing polypeptides |
| EP2097451A2 (en) | 2006-12-22 | 2009-09-09 | Ablynx N.V. | Anti-chemokine (ccl2, ccl3, ccl5, cxcl11, cxcl12) single-domain antibodies |
| US7691980B2 (en) | 2007-01-09 | 2010-04-06 | Bio-Rad Laboratories, Inc. | Enhanced capacity and purification of antibodies by mixed mode chromatography in the presence of aqueous-soluble nonionic organic polymers |
| EA200970880A1 (ru) * | 2007-03-22 | 2010-02-26 | Имклоун Элэлси | Стабильные композиции на основе антител |
| US8359965B2 (en) | 2007-09-17 | 2013-01-29 | Oxford J Craig | Apparatus and method for broad spectrum radiation attenuation |
| JP2011504740A (ja) | 2007-11-27 | 2011-02-17 | アブリンクス エン.ヴェー. | ヘテロ二量体サイトカイン及び/又はこれらの受容体に指向性を有するアミノ酸配列、並びにこれを含むポリペプチド |
| WO2009095235A1 (en) | 2008-01-29 | 2009-08-06 | Ablynx N.V. | Methods to stabilize proteins and polypeptides |
| CA2721947C (en) | 2008-04-29 | 2016-03-08 | Ascendis Pharma As | Pegylated recombinant human growth hormone compounds |
| MX2011004558A (es) | 2008-10-29 | 2011-06-01 | Wyeth Llc | Procedimientos para la purificacion de moleculas de union a antigeno de un unico dominio. |
| MX345226B (es) | 2008-10-29 | 2017-01-20 | Ablynx Nv | Formulaciones de moleculas de union a antigeno de dominio sencillo. |
| JP5593488B2 (ja) | 2008-11-17 | 2014-09-24 | 独立行政法人国立がん研究センター | 癌間質の構成因子に対して特異的結合能を有する物質と抗腫瘍性化合物との複合体による新規の癌ターゲティング治療 |
| WO2010060212A1 (en) | 2008-11-26 | 2010-06-03 | National Research Council Of Canada | Single-domain antibody targeted formulations with superparamagnetic nanoparticles |
| US20110097302A1 (en) | 2009-07-16 | 2011-04-28 | Ta Tung Yuan | Il-1ra-polymer conjugates |
| US9884117B2 (en) | 2009-09-03 | 2018-02-06 | Ablynx N.V. | Stable formulations of polypeptides and uses thereof |
| WO2012007880A2 (en) | 2010-07-16 | 2012-01-19 | Ablynx Nv | Modified single domain antigen binding molecules and uses thereof |
| CN102786590A (zh) | 2011-05-19 | 2012-11-21 | 江苏豪森药业股份有限公司 | 分枝型peg修饰的glp-1类似物及其可药用盐 |
| EP4019272B1 (en) | 2014-01-24 | 2024-04-24 | Ceraloc Innovation AB | Method of forming a decorative layer of a building panel |
| KR102578824B1 (ko) | 2016-11-30 | 2023-09-15 | 삼성전자주식회사 | 3차원 정보를 제공하는 차량용 레이더 장치 |
-
2009
- 2009-10-29 MX MX2011004557A patent/MX345226B/es active IP Right Grant
- 2009-10-29 AR ARP090104169A patent/AR073997A1/es not_active Application Discontinuation
- 2009-10-29 EP EP09748625.2A patent/EP2362767B1/en active Active
- 2009-10-29 KR KR1020117009665A patent/KR101581986B1/ko active IP Right Grant
- 2009-10-29 CN CN201510098158.1A patent/CN104740631B/zh active Active
- 2009-10-29 BR BRPI0919979A patent/BRPI0919979A2/pt not_active Application Discontinuation
- 2009-10-29 WO PCT/US2009/062611 patent/WO2010077422A2/en active Application Filing
- 2009-10-29 CA CA2738243A patent/CA2738243C/en active Active
- 2009-10-29 CN CN200980153163.0A patent/CN102271707B/zh active Active
- 2009-10-29 KR KR1020137022657A patent/KR101593285B1/ko active IP Right Grant
- 2009-10-29 RU RU2011113438/10A patent/RU2481824C2/ru not_active IP Right Cessation
- 2009-10-29 EP EP22174073.1A patent/EP4104821A1/en active Pending
- 2009-10-29 EP EP15189934.1A patent/EP3011953A1/en not_active Ceased
- 2009-10-29 BR BR122018013284-1A patent/BR122018013284B1/pt active IP Right Grant
- 2009-10-29 AU AU2009333791A patent/AU2009333791B2/en not_active Ceased
- 2009-10-29 JP JP2011534779A patent/JP5823867B2/ja active Active
- 2009-10-29 US US12/608,553 patent/US9393304B2/en not_active Expired - Fee Related
-
2011
- 2011-03-24 IL IL211932A patent/IL211932A/en not_active IP Right Cessation
- 2011-12-19 HK HK15111290.7A patent/HK1210431A1/xx unknown
- 2011-12-19 HK HK11113681.4A patent/HK1160376A1/xx unknown
-
2013
- 2013-02-01 RU RU2013104181A patent/RU2683861C2/ru active
-
2014
- 2014-12-25 JP JP2014262998A patent/JP6421031B2/ja active Active
-
2015
- 2015-07-16 IL IL239992A patent/IL239992B/en active IP Right Grant
-
2016
- 2016-02-11 US US15/041,690 patent/US9993552B2/en active Active
-
2017
- 2017-02-01 JP JP2017017004A patent/JP2017105807A/ja active Pending
-
2018
- 2018-05-03 US US15/969,896 patent/US20180353604A1/en not_active Abandoned
-
2021
- 2021-11-22 US US17/531,916 patent/US20220175923A1/en active Pending
Patent Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH11510170A (ja) * | 1995-07-27 | 1999-09-07 | ジェネンテック インコーポレーテッド | タンパク質の処方 |
| JP2003516361A (ja) * | 1999-12-02 | 2003-05-13 | カイロン コーポレイション | 凍結乾燥の際に生物学的分子を安定化するための組成物および方法 |
| JP2006249084A (ja) * | 2005-03-08 | 2006-09-21 | Pharmacia & Upjohn Co Llc | 抗MadCAM抗体組成物 |
| JP2006249083A (ja) * | 2005-03-08 | 2006-09-21 | Pharmacia & Upjohn Co Llc | 抗m−csf抗体組成物 |
| JP2006249081A (ja) * | 2005-03-08 | 2006-09-21 | Pharmacia & Upjohn Co Llc | 抗ctla−4抗体組成物 |
| WO2006122786A2 (en) * | 2005-05-18 | 2006-11-23 | Ablynx Nv | Improved nanobodies™ against tumor necrosis factor-alpha |
| WO2007014073A2 (en) * | 2005-07-22 | 2007-02-01 | Amgen Inc. | Concentrated protein lyophilates, methods, and uses |
Cited By (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2015166885A1 (ja) * | 2014-04-28 | 2015-11-05 | エーザイ・アール・アンド・ディー・マネジメント株式会社 | Hgf凍結乾燥製剤 |
| JPWO2015166885A1 (ja) * | 2014-04-28 | 2017-04-20 | エーザイ・アール・アンド・ディー・マネジメント株式会社 | Hgf凍結乾燥製剤 |
| RU2693472C2 (ru) * | 2014-04-28 | 2019-07-03 | Эйсай Ар Энд Ди Менеджмент Ко., Лтд. | Лиофилизированный состав на основе hgf |
| AU2015254307B2 (en) * | 2014-04-28 | 2019-11-07 | Eisai R&D Management Co., Ltd. | Lyophilized formulation of HGF |
| US11547743B2 (en) | 2014-04-28 | 2023-01-10 | Eisai R&D Management Co., Ltd. | Lyophilized formulation of HGF |
| JP2017516848A (ja) * | 2014-05-23 | 2017-06-22 | アレス トレーディング ソシエテ アノニム | 液体医薬組成物 |
| JP2021107399A (ja) * | 2014-05-23 | 2021-07-29 | フレゼニウス カビ ドイチュラント ゲゼルシャフト ミット ベシュレンクテル ハフツング | 液体医薬組成物 |
| US11548926B2 (en) | 2016-03-17 | 2023-01-10 | Eisai R&D Management Co., Ltd. | Method for producing an active hepatocyte growth factor (HGF) |
| JP2019524719A (ja) * | 2016-07-11 | 2019-09-05 | クレッシェンド、バイオロジックス、リミテッドCrescendo Biologics Limited | 障害の治療のための組成物 |
| JP7178985B2 (ja) | 2016-07-11 | 2022-11-28 | クレッシェンド、バイオロジックス、リミテッド | 障害の治療のための組成物 |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US20220175923A1 (en) | Formulations of single domain antigen binding molecules | |
| US10758621B2 (en) | Liquid formulation comprising GM-CSF neutralizing compound | |
| JP6769879B2 (ja) | Gm−csf中和化合物を含む液体製剤 | |
| JP6339578B2 (ja) | Gm−csf中和化合物を含む凍結乾燥製剤 | |
| AU2013202856B2 (en) | Formulations of single domain antigen binding molecules |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A711 | Notification of change in applicant |
Free format text: JAPANESE INTERMEDIATE CODE: A711 Effective date: 20120123 |
|
| RD03 | Notification of appointment of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7423 Effective date: 20120127 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20120130 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20120130 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20120123 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20121011 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20121011 |
|
| RD03 | Notification of appointment of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7423 Effective date: 20130621 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20131203 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20140206 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20140214 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20140602 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20140603 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20140902 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20141225 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20150218 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20150306 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20150324 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20150526 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20150824 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20150929 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20151008 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5823867 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |