ES2864286T3 - Agente para el control de plagas que contiene un derivado de amida y uso del agente para el control de plagas - Google Patents
Agente para el control de plagas que contiene un derivado de amida y uso del agente para el control de plagas Download PDFInfo
- Publication number
- ES2864286T3 ES2864286T3 ES16166952T ES16166952T ES2864286T3 ES 2864286 T3 ES2864286 T3 ES 2864286T3 ES 16166952 T ES16166952 T ES 16166952T ES 16166952 T ES16166952 T ES 16166952T ES 2864286 T3 ES2864286 T3 ES 2864286T3
- Authority
- ES
- Spain
- Prior art keywords
- group
- substituent
- phenyl
- formula
- atom
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 0 **c1c(*)c(N(*)C(c2c(*)[s]c(C(*)*C(O*)=O)n2)=O)c(*)c(*)c1*I Chemical compound **c1c(*)c(N(*)C(c2c(*)[s]c(C(*)*C(O*)=O)n2)=O)c(*)c(*)c1*I 0.000 description 6
- HEGCANXMLSQJLC-UHFFFAOYSA-N CNc(cccc1C(Nc(c(C(F)(F)F)cc(C(C(F)(F)F)(C(F)(F)F)F)c2)c2Br)=O)c1F Chemical compound CNc(cccc1C(Nc(c(C(F)(F)F)cc(C(C(F)(F)F)(C(F)(F)F)F)c2)c2Br)=O)c1F HEGCANXMLSQJLC-UHFFFAOYSA-N 0.000 description 1
- ZJCXDRHVMCTZKN-UHFFFAOYSA-N Nc(c(I)cc(C(C(F)(F)F)(C(F)(F)F)F)c1)c1I Chemical compound Nc(c(I)cc(C(C(F)(F)F)(C(F)(F)F)F)c1)c1I ZJCXDRHVMCTZKN-UHFFFAOYSA-N 0.000 description 1
- AEXXAWIGFPEZCE-UHFFFAOYSA-N Nc1ccc(C(C(C(F)(F)F)(F)F)(C(F)(F)F)F)cc1 Chemical compound Nc1ccc(C(C(C(F)(F)F)(F)F)(C(F)(F)F)F)cc1 AEXXAWIGFPEZCE-UHFFFAOYSA-N 0.000 description 1
- PWDDQCRAKBGDTI-UHFFFAOYSA-N Nc1ccc(C(C(F)(F)F)(C(F)(F)F)F)cc1 Chemical compound Nc1ccc(C(C(F)(F)F)(C(F)(F)F)F)cc1 PWDDQCRAKBGDTI-UHFFFAOYSA-N 0.000 description 1
- JIVCMYVTZXFMQF-UHFFFAOYSA-N [O-][N+](c(cccc1C(Nc(c(C(F)(F)F)cc(C(C(C(F)(F)F)(F)F)(C(F)(F)F)F)c2)c2I)=O)c1F)=O Chemical compound [O-][N+](c(cccc1C(Nc(c(C(F)(F)F)cc(C(C(C(F)(F)F)(F)F)(C(F)(F)F)F)c2)c2I)=O)c1F)=O JIVCMYVTZXFMQF-UHFFFAOYSA-N 0.000 description 1
- USGQPAJWWQUUCU-UHFFFAOYSA-N [O-][N+](c(cccc1C(Nc(c(C(F)(F)F)cc(C(C(F)(F)F)(C(F)(F)F)F)c2)c2I)=O)c1Cl)=O Chemical compound [O-][N+](c(cccc1C(Nc(c(C(F)(F)F)cc(C(C(F)(F)F)(C(F)(F)F)F)c2)c2I)=O)c1Cl)=O USGQPAJWWQUUCU-UHFFFAOYSA-N 0.000 description 1
- PRIGHYHJLGBCAE-UHFFFAOYSA-N [O-][N+](c(cccc1C(Nc(c(OC(F)(F)F)cc(C(C(F)(F)F)(C(F)(F)F)F)c2)c2Br)=O)c1F)=O Chemical compound [O-][N+](c(cccc1C(Nc(c(OC(F)(F)F)cc(C(C(F)(F)F)(C(F)(F)F)F)c2)c2Br)=O)c1F)=O PRIGHYHJLGBCAE-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C237/00—Carboxylic acid amides, the carbon skeleton of the acid part being further substituted by amino groups
- C07C237/28—Carboxylic acid amides, the carbon skeleton of the acid part being further substituted by amino groups having the carbon atom of at least one of the carboxamide groups bound to a carbon atom of a non-condensed six-membered aromatic ring of the carbon skeleton
- C07C237/42—Carboxylic acid amides, the carbon skeleton of the acid part being further substituted by amino groups having the carbon atom of at least one of the carboxamide groups bound to a carbon atom of a non-condensed six-membered aromatic ring of the carbon skeleton having nitrogen atoms of amino groups bound to the carbon skeleton of the acid part, further acylated
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N37/00—Biocides, pest repellants or attractants, or plant growth regulators containing organic compounds containing a carbon atom having three bonds to hetero atoms with at the most two bonds to halogen, e.g. carboxylic acids
- A01N37/18—Biocides, pest repellants or attractants, or plant growth regulators containing organic compounds containing a carbon atom having three bonds to hetero atoms with at the most two bonds to halogen, e.g. carboxylic acids containing the group —CO—N<, e.g. carboxylic acid amides or imides; Thio analogues thereof
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N37/00—Biocides, pest repellants or attractants, or plant growth regulators containing organic compounds containing a carbon atom having three bonds to hetero atoms with at the most two bonds to halogen, e.g. carboxylic acids
- A01N37/44—Biocides, pest repellants or attractants, or plant growth regulators containing organic compounds containing a carbon atom having three bonds to hetero atoms with at the most two bonds to halogen, e.g. carboxylic acids containing at least one carboxylic group or a thio analogue, or a derivative thereof, and a nitrogen atom attached to the same carbon skeleton by a single or double bond, this nitrogen atom not being a member of a derivative or of a thio analogue of a carboxylic group, e.g. amino-carboxylic acids
- A01N37/46—N-acyl derivatives
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/34—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with one nitrogen atom as the only ring hetero atom
- A01N43/40—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with one nitrogen atom as the only ring hetero atom six-membered rings
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/72—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with nitrogen atoms and oxygen or sulfur atoms as ring hetero atoms
- A01N43/74—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with nitrogen atoms and oxygen or sulfur atoms as ring hetero atoms five-membered rings with one nitrogen atom and either one oxygen atom or one sulfur atom in positions 1,3
- A01N43/78—1,3-Thiazoles; Hydrogenated 1,3-thiazoles
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N47/00—Biocides, pest repellants or attractants, or plant growth regulators containing organic compounds containing a carbon atom not being member of a ring and having no bond to a carbon or hydrogen atom, e.g. derivatives of carbonic acid
- A01N47/08—Biocides, pest repellants or attractants, or plant growth regulators containing organic compounds containing a carbon atom not being member of a ring and having no bond to a carbon or hydrogen atom, e.g. derivatives of carbonic acid the carbon atom having one or more single bonds to nitrogen atoms
- A01N47/10—Carbamic acid derivatives, i.e. containing the group —O—CO—N<; Thio analogues thereof
- A01N47/20—N-Aryl derivatives thereof
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C233/00—Carboxylic acid amides
- C07C233/64—Carboxylic acid amides having carbon atoms of carboxamide groups bound to carbon atoms of six-membered aromatic rings
- C07C233/66—Carboxylic acid amides having carbon atoms of carboxamide groups bound to carbon atoms of six-membered aromatic rings having the nitrogen atom of at least one of the carboxamide groups bound to a carbon atom of a hydrocarbon radical substituted by halogen atoms or by nitro or nitroso groups
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C233/00—Carboxylic acid amides
- C07C233/64—Carboxylic acid amides having carbon atoms of carboxamide groups bound to carbon atoms of six-membered aromatic rings
- C07C233/81—Carboxylic acid amides having carbon atoms of carboxamide groups bound to carbon atoms of six-membered aromatic rings having the nitrogen atom of at least one of the carboxamide groups bound to a carbon atom of a hydrocarbon radical substituted by carboxyl groups
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C237/00—Carboxylic acid amides, the carbon skeleton of the acid part being further substituted by amino groups
- C07C237/28—Carboxylic acid amides, the carbon skeleton of the acid part being further substituted by amino groups having the carbon atom of at least one of the carboxamide groups bound to a carbon atom of a non-condensed six-membered aromatic ring of the carbon skeleton
- C07C237/40—Carboxylic acid amides, the carbon skeleton of the acid part being further substituted by amino groups having the carbon atom of at least one of the carboxamide groups bound to a carbon atom of a non-condensed six-membered aromatic ring of the carbon skeleton having the nitrogen atom of the carboxamide group bound to a carbon atom of a six-membered aromatic ring
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C255/00—Carboxylic acid nitriles
- C07C255/49—Carboxylic acid nitriles having cyano groups bound to carbon atoms of six-membered aromatic rings of a carbon skeleton
- C07C255/57—Carboxylic acid nitriles having cyano groups bound to carbon atoms of six-membered aromatic rings of a carbon skeleton containing cyano groups and carboxyl groups, other than cyano groups, bound to the carbon skeleton
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C255/00—Carboxylic acid nitriles
- C07C255/49—Carboxylic acid nitriles having cyano groups bound to carbon atoms of six-membered aromatic rings of a carbon skeleton
- C07C255/58—Carboxylic acid nitriles having cyano groups bound to carbon atoms of six-membered aromatic rings of a carbon skeleton containing cyano groups and singly-bound nitrogen atoms, not being further bound to other hetero atoms, bound to the carbon skeleton
- C07C255/60—Carboxylic acid nitriles having cyano groups bound to carbon atoms of six-membered aromatic rings of a carbon skeleton containing cyano groups and singly-bound nitrogen atoms, not being further bound to other hetero atoms, bound to the carbon skeleton at least one of the singly-bound nitrogen atoms being acylated
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C271/00—Derivatives of carbamic acids, i.e. compounds containing any of the groups, the nitrogen atom not being part of nitro or nitroso groups
- C07C271/06—Esters of carbamic acids
- C07C271/08—Esters of carbamic acids having oxygen atoms of carbamate groups bound to acyclic carbon atoms
- C07C271/26—Esters of carbamic acids having oxygen atoms of carbamate groups bound to acyclic carbon atoms with the nitrogen atom of at least one of the carbamate groups bound to a carbon atom of a six-membered aromatic ring
- C07C271/28—Esters of carbamic acids having oxygen atoms of carbamate groups bound to acyclic carbon atoms with the nitrogen atom of at least one of the carbamate groups bound to a carbon atom of a six-membered aromatic ring to a carbon atom of a non-condensed six-membered aromatic ring
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D213/00—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members
- C07D213/02—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members
- C07D213/04—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D213/60—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D213/78—Carbon atoms having three bonds to hetero atoms, with at the most one bond to halogen, e.g. ester or nitrile radicals
- C07D213/81—Amides; Imides
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D213/00—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members
- C07D213/02—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members
- C07D213/04—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D213/60—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D213/78—Carbon atoms having three bonds to hetero atoms, with at the most one bond to halogen, e.g. ester or nitrile radicals
- C07D213/81—Amides; Imides
- C07D213/82—Amides; Imides in position 3
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D277/00—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings
- C07D277/02—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings
- C07D277/20—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D277/00—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings
- C07D277/02—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings
- C07D277/20—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members
- C07D277/32—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D277/56—Carbon atoms having three bonds to hetero atoms with at the most one bond to halogen
Landscapes
- Organic Chemistry (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Health & Medical Sciences (AREA)
- Environmental Sciences (AREA)
- Engineering & Computer Science (AREA)
- Dentistry (AREA)
- General Health & Medical Sciences (AREA)
- Wood Science & Technology (AREA)
- Zoology (AREA)
- Plant Pathology (AREA)
- Pest Control & Pesticides (AREA)
- Agronomy & Crop Science (AREA)
- Agricultural Chemicals And Associated Chemicals (AREA)
- Pyridine Compounds (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Plural Heterocyclic Compounds (AREA)
- Thiazole And Isothizaole Compounds (AREA)
- Hydrogenated Pyridines (AREA)
Abstract
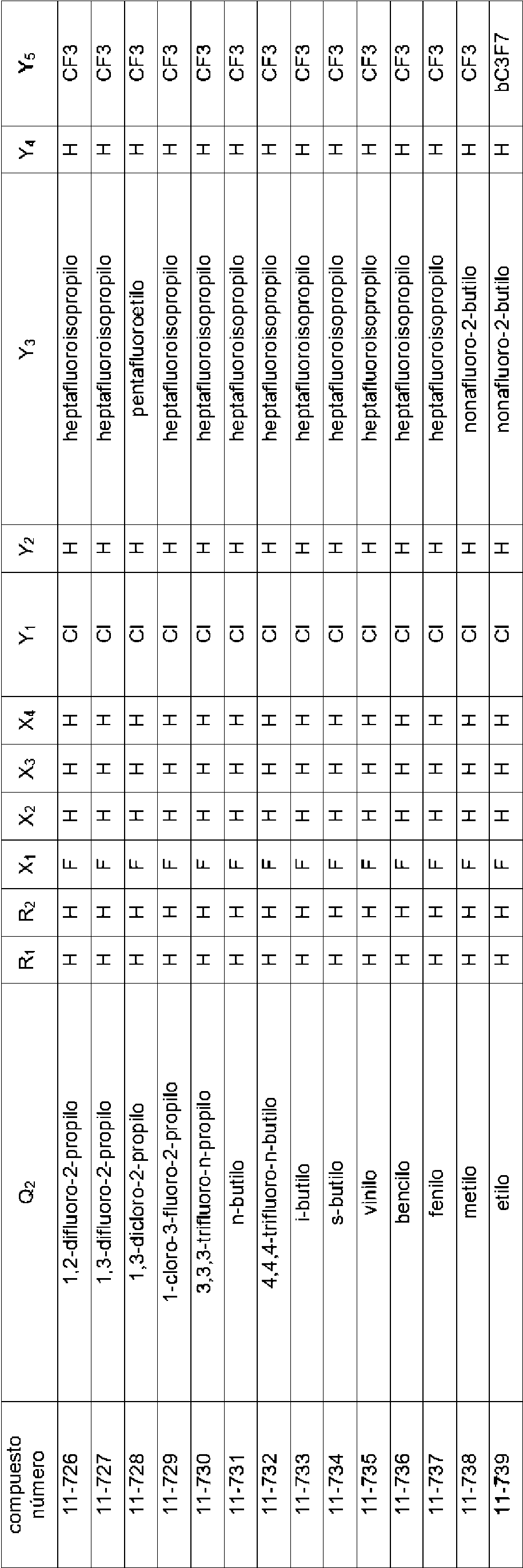
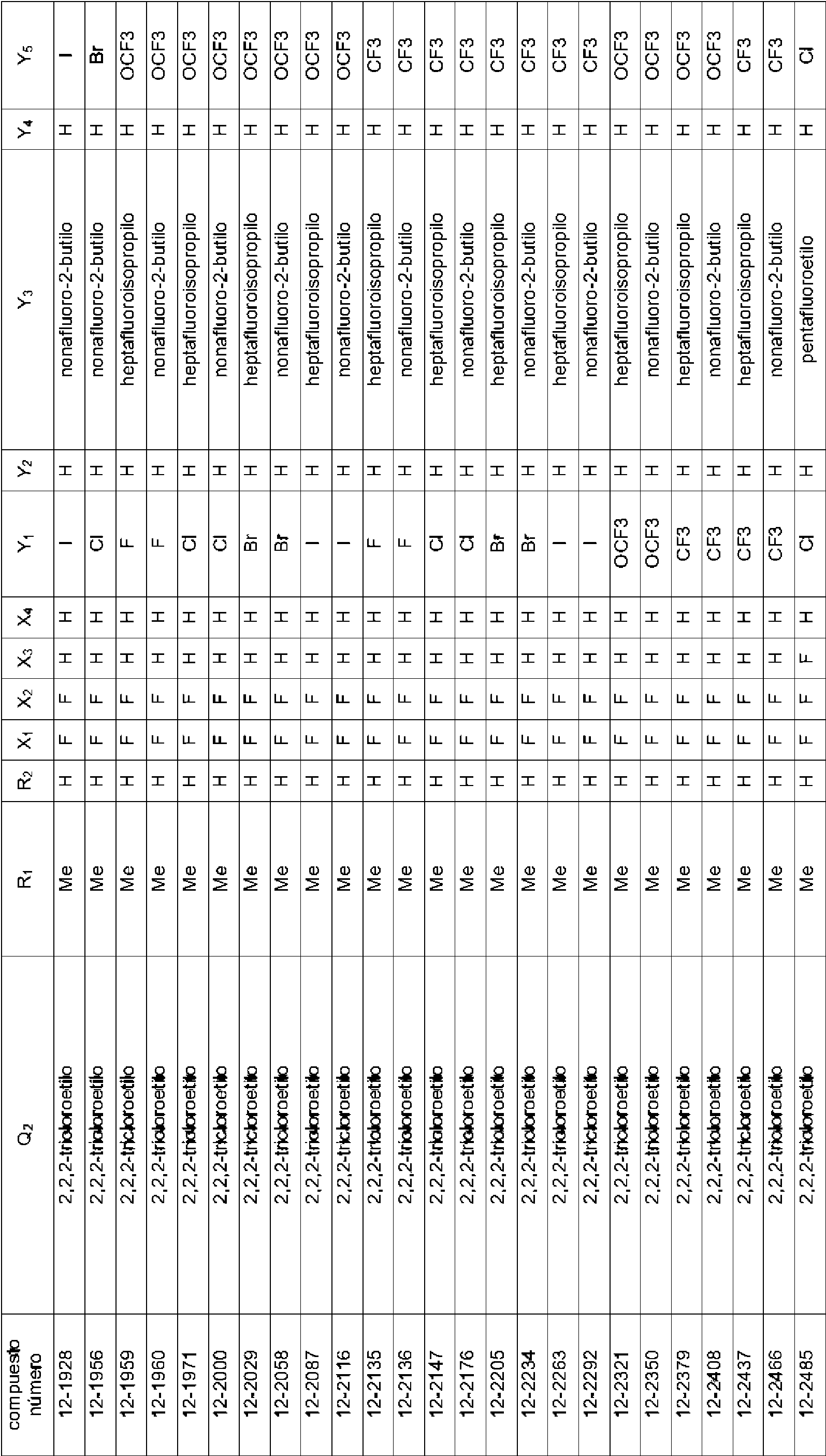
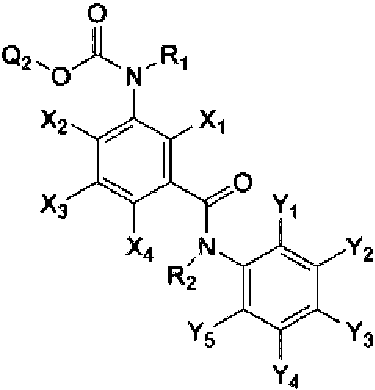
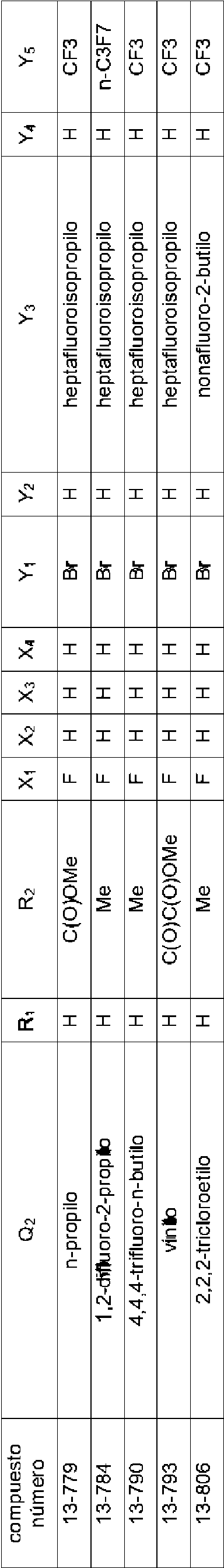
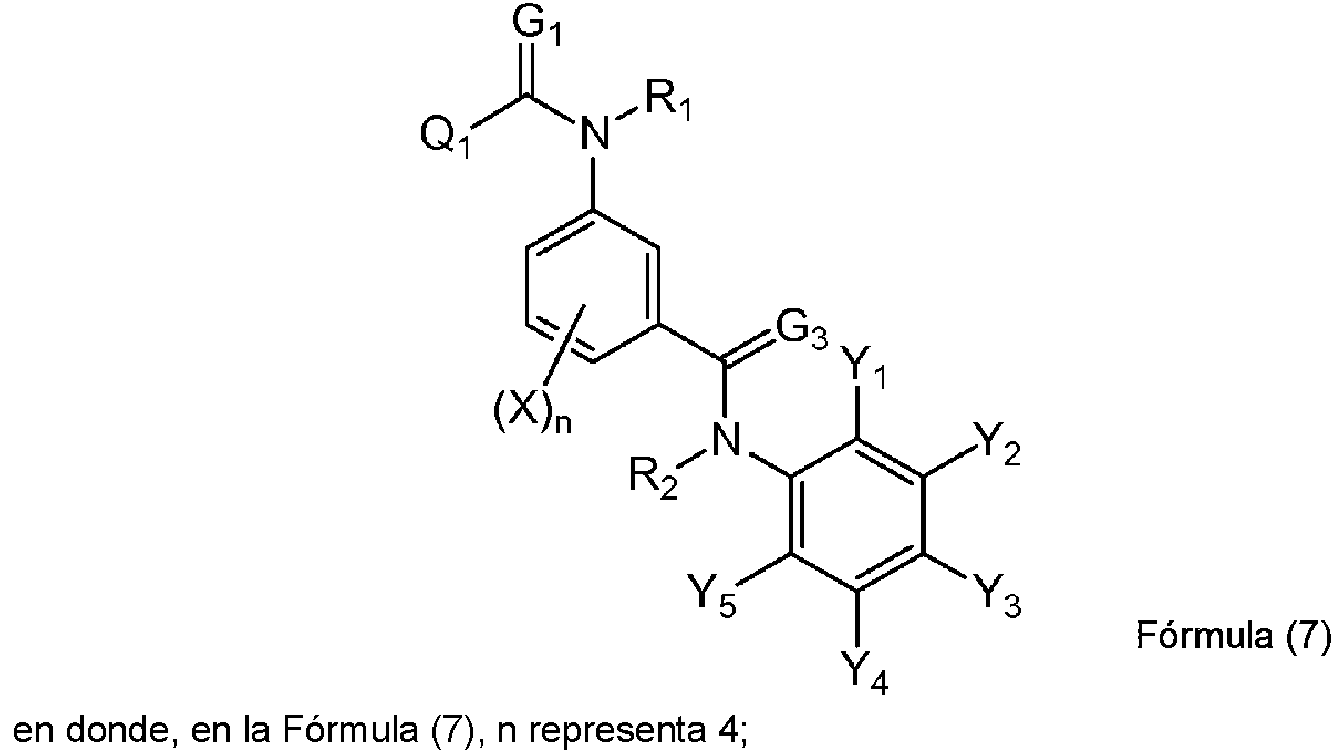
Un agente para el control de plagas que comprende al menos un derivado de amida seleccionado entre el grupo que consiste en las siguientes Fórmula (1), Fórmula (7), Fórmula (8) y Fórmula (9) como principio activo: **(Ver fórmula)** en donde, en la Fórmula (1): A representa un átomo de carbono, un átomo de oxígeno, un átomo de nitrógeno, un átomo de nitrógeno oxidado o un átomo de azufre; K representa un grupo de átomo no metálico necesario para formar un grupo de unión cíclico derivado de piridina, N-óxido de piridina, pirrol, tiazol, furano o tiofeno, junto con A y dos átomos de carbono a los que se une A; X representa un átomo de hidrógeno, un átomo de halógeno, un grupo alquilo C1-C6, un grupo haloalquilo C1-C6, un grupo cicloalquilo C3-C9, un grupo halocicloalquilo C3-C9, un grupo alquenilo C2-C6, un grupo haloalquenilo C2-C6, un grupo alquinilo C2-C6, un grupo haloalquinilo C2-C6, un grupo alcoxi C1-C6, un grupo haloalcoxi C1- C6, un grupo alqueniloxi C2-C6, un grupo haloalqueniloxi C2-C6, un grupo alquiniloxi C2-C6, un grupo haloalquiniloxi C2-C6, un grupo cicloalcoxi C3-C9, un grupo halocicloalcoxi C3-C9, un grupo alquiltio C1-C6, un grupo haloalquiltio C1-C6, un grupo alquilsulfinilo C1-C6, un grupo haloalquilsulfinilo C1-C6, un grupo alquilsulfonilo C1-C6, un grupo haloalquilsulfonilo C1-C6, un grupo alquilsulfoniloxi C1-C6, un grupo haloalquilsulfoniloxi C1-C6, un grupo alquilcarbonilo C2-C7, un grupo haloalquilcarbonilo C2-C7, un grupo alquenilcarbonilo C3-C7, un grupo haloalquenilcarbonilo C3-C7, un grupo alquinilcarbonilo C3-C7, un grupo haloalquinilcarbonilo C3-C7, un grupo cicloalquilcarbonilo C4-C10, un grupo halocicloalquilcarbonilo C4-C10, un grupo alquilcarboniloxi C2-C7, un grupo haloalquilcarboniloxi C2-C7, un grupo arilcarboniloxi, un grupo alcoxicarbonilo C2-C7, un grupo haloalcoxicarbonilo C2-C7, un grupo alqueniloxicarbonilo C3-C7, un grupo haloalqueniloxicarbonilo C3-C7, un grupo alquiniloxicarbonilo C3-C7, un grupo haloalquiniloxicarbonilo C3-C7, un grupo cicloalquiloxicarbonilo C4-C10, un grupo halocicloalquiloxicarbonilo C4-C10, un grupo alquilcarbonilamino C2-C7, un grupo haloalquilcarbonilamino C2-C7, un grupo alcoxicarbonilamino C2-C7, un grupo haloalcoxicarbonilamino C2-C7, un grupo alcoxicarboniloxi C2-C7, un grupo haloalcoxicarboniloxi C2-C7, un grupo arilcarbonilamino, un grupo amino, un grupo carbamoílo, un grupo ciano, un grupo hidroxi, un grupo pentafluorosulfanilo, un grupo alquilamino C1-C6, un grupo haloalquilamino C1-C6, un grupo alquenilamino C2-C6, un grupo haloalquenilamino C2-C6, un grupo alquinilamino C2-C6, un grupo haloalquinilamino C2-C6, un grupo cicloalquilamino C3-C9, un grupo halocicloalquilamino C3-C9, un grupo alquilaminocarbonilo C2-C7, un grupo haloalquilaminocarbonilo C2-C7, un grupo alquenilaminocarbonilo C3-C7, un grupo haloalquenilaminocarbonilo C3-C7, un grupo alquinilaminocarbonilo C3-C7, un grupo haloalquinilaminocarbonilo C3-C7, un grupo cicloalquilaminocarbonilo C4-C10, un grupo halocicloalquilaminocarbonilo C4-C10, un grupo fenilo o un grupo heterocíclico, y cuando hay varios X, cada X puede ser igual o diferente entre sí; n representa un número entero de 0 a 4; T representa -C(=G1)-Q1 o -C(=G1)-G2Q2; cada uno de G1 y G2 representa independientemente un átomo de oxígeno o un átomo de azufre; cada uno de Q1 y Q2 representa: un átomo de hidrógeno, un grupo alquilo C1-C6, un grupo haloalquilo C1-C6, un grupo alquenilo C2-C6, un grupo haloalquenilo C2-C6, un grupo alquinilo C2-C6, un grupo haloalquinilo C2-C6, un grupo cicloalquilo C3- C9, un grupo halocicloalquilo C3-C9, un grupo bencilo, un grupo fenilo que puede tener un sustituyente, un grupo naftilo o un grupo heterocíclico que puede tener un sustituyente; Y1 e Y5 representan un átomo de halógeno o un grupo haloalquilo C1-C3 e Y1 o Y5 representan un grupo haloalquilo C1-C3; Y2 e Y4 representan un átomo de hidrógeno; Y3 representa un grupo perfluoroalquilo C2-C4; en donde, en Q1 y Q2, el sustituyente de un grupo fenilo que puede tener un sustituyente y un grupo heterocíclico que puede tener un sustituyente representan uno o más sustituyentes seleccionados entre un grupo que consiste en: un átomo de halógeno, un grupo alquilo C1-C6, un grupo haloalquilo C1-C6, un grupo cicloalquilo C3-C9, un grupo halocicloalquilo C3-C9, un grupo alquenilo C2-C6, un grupo haloalquenilo C2-C6, un grupo alquinilo C2-C6, un grupo haloalquinilo C2-C6, un grupo alcoxi C1-C6, un grupo haloalcoxi C1-C6, un grupo alqueniloxi C2-C6, un grupo haloalqueniloxi C2-C6, un grupo alquiniloxi C2-C6, un grupo haloalquiniloxi C2- C6, un grupo cicloalcoxi C3-C9, un grupo halocicloalcoxi C3-C9, un grupo alquiltio C1-C6, un grupo haloalquiltio C1-C6, un grupo alquilsulfinilo C1-C6, un grupo haloalquilsulfinilo C1-C6, un grupo alquilsulfonilo C1-C6, un grupo haloalquilsulfonilo C1-C6, un grupo alquilcarbonilo C2-C7, un grupo haloalquilcarbonilo C2-C7, un grupo alquenilcarbonilo C3-C7, un grupo haloalquenilcarbonilo C3-C7, un grupo alquinilcarbonilo C3-C7, un grupo haloalquinilcarbonilo C3-C7, un grupo cicloalquilcarbonilo C4-C10, un grupo halocicloalquilcarbonilo C4-C10, un grupo alquilcarboniloxi C2-C7, un grupo haloalquilcarboniloxi C2-C7, un grupo alquilsulfoniloxi C1-C6, un grupo haloalquilsulfoniloxi C1-C6, un grupo alcoxicarbonilo C2- C7, un grupo haloalcoxicarbonilo C2-C7, un grupo alqueniloxicarbonilo C3-C7, un grupo haloalqueniloxicarbonilo C3-C7, un grupo alquiniloxicarbonilo C3-C7, un grupo haloalquiniloxicarbonilo C3- C7, un grupo cicloalquiloxicarbonilo C4-C10, un grupo halocicloalquiloxicarbonilo C4-C10, un grupo alquilcarbonilamino C2-C7, un grupo haloalquilcarbonilamino C2-C7, un grupo alcoxicarbonilamino C2-C7, un grupo haloalcoxicarbonilamino C2-C7, un grupo alquilamino C1-C6, un grupo haloalquilamino C1-C6, un grupo alquenilamino C2-C6, un grupo haloalquenilamino C2-C6, un grupo alquinilamino C2-C6, un grupo haloalquinilamino C2-C6, un grupo cicloalquilamino C3-C9, un grupo halocicloalquilamino C3-C9, un grupo alquilaminocarbonilo C2-C7, un grupo haloalquilaminocarbonilo C2-C7, un grupo alquenilaminocarbonilo C3-C7, un grupo haloalquenilaminocarbonilo C3-C7, un grupo alquinilaminocarbonilo C3-C7, un grupo haloalquinilaminocarbonilo C3-C7, un grupo cicloalquilaminocarbonilo C4-C10, un grupo halocicloalquilaminocarbonilo C4-C10, un grupo amino, un grupo carbamoílo, un grupo ciano, un grupo nitro, un grupo hidroxi, un grupo pentafluorosulfanilo, un grupo fenilo que puede tener un sustituyente y un grupo heterocíclico que puede tener un sustituyente, y cuando hay dos o más sustituyentes, los sustituyentes pueden ser iguales o diferentes entre sí; en donde, el grupo heterocíclico en X, Q1, y Q2 representan un grupo piridilo, un grupo N-óxido de piridina, un grupo pirimidinilo, un grupo pirazinilo, un grupo piridazilo, un grupo furilo, un grupo tienilo, un grupo oxazolilo, un grupo isoxazolilo, un grupo oxadiazolilo, un grupo tiazolilo, un grupo isotiazolilo, un grupo tiadiazolilo, un grupo pirrolilo, un grupo imidazolilo, un grupo triazolilo, un grupo pirazolilo o un grupo tetrazolilo; G3 representa un átomo de oxígeno o un átomo de azufre; y cada uno de R1 y R2 representa independientemente un átomo de hidrógeno, un átomo de oxígeno, un átomo de halógeno, un grupo hidroxi, un grupo nitro, un grupo nitroso, un grupo trimetilsililo, un grupo t- butildimetilsililo, un grupo ciano, un grupo amino, un grupo alquilo C1-C6 que puede tener un sustituyente, un grupo haloalquilo C1-C6 que puede tener un sustituyente, un grupo alquilcarbonilo C2-C7, un grupo haloalquilcarbonilo C2-C7, un grupo alquenilo C2-C6 que puede tener un sustituyente, un grupo haloalquenilo C2-C6 que puede tener un sustituyente, un grupo alquinilo C2-C6 que puede tener un sustituyente, un grupo haloalquinilo C2-C6 que puede tener un sustituyente, un grupo alcoxicarbonilo C2- C7, un grupo haloalcoxicarbonilo C2-C7, un grupo alqueniloxicarbonilo C3-C7, un grupo haloalqueniloxicarbonilo C3-C7, un grupo alquiniloxicarbonilo C3-C7, un grupo haloalquiniloxicarbonilo C3- C7, un grupo fenoxicarbonilo, un grupo alquilaminocarbonilo C2-C7, un grupo haloalquilaminocarbonilo C2- C7, un grupo alquilcarboniloxi C2-C7, un grupo haloalquilcarboniloxi C2-C7, un grupo benzoílo, un grupo alcoxi C1-C6, un grupo haloalcoxi C1-C6, un grupo alquiltio C1-C6, un grupo haloalquiltio C1-C6, un grupo alquilsulfinilo C1-C6, un grupo haloalquilsulfinilo C1-C6, un grupo alquilsulfonilo C1-C6, un grupo haloalquilsulfonilo C1-C6, un grupo bencenosulfonilo, un grupo bencilsulfonilo, un grupo bencilo o - C(=O)C(=O)R7, en donde R7 representa un grupo alquilo C1-C6, un grupo haloalquilo C1-C6, un grupo alcoxi C1-C6 o un grupo haloalcoxi C1-C6; **(Ver fórmula)** en donde, en la Fórmula (7), n representa 4; cada X representa independientemente un átomo de hidrógeno, un átomo de halógeno o un grupo ciano; Y3 representa un grupo perfluoroalquilo C2-C4; Y2 e Y4 representan un átomo de hidrógeno; Y1 e Y5 representan un átomo de halógeno o un grupo haloalquilo C1-C3 e Y1 o Y5 representan un grupo haloalquilo C1-C3; cada uno de G1 y G3 representa independientemente un átomo de oxígeno o un átomo de azufre; Q1 representa un átomo de hidrógeno, un grupo alquilo C1-C6, un grupo haloalquilo C1-C6, un grupo alquenilo C2- C6, un grupo haloalquenilo C2-C6, un grupo alquinilo C2-C6, un grupo haloalquinilo C2-C6, un grupo cicloalquilo C3-C9, un grupo halocicloalquilo C3-C9, un grupo bencilo, un grupo fenilo que puede tener un sustituyente, un grupo naftilo o un grupo heterocíclico que puede tener un sustituyente; en donde, en Q1, el sustituyente de un grupo fenilo que puede tener un sustituyente y un sustituyente de grupo heterocíclico que puede tener un sustituyente representan uno o más sustituyentes seleccionados entre un grupo que consiste en: un átomo de halógeno, un grupo alquilo C1-C6, un grupo haloalquilo C1-C6, un grupo cicloalquilo C3-C9, un grupo halocicloalquilo C3-C9, un grupo alquenilo C2-C6, un grupo haloalquenilo C2-C6, un grupo alquinilo C2-C6, un grupo haloalquinilo C2-C6, un grupo alcoxi C1-C6, un grupo haloalcoxi C1-C6, un grupo alqueniloxi C2-C6, un grupo haloalqueniloxi C2-C6, un grupo alquiniloxi C2-C6, un grupo haloalquiniloxi C2-C6, un grupo cicloalcoxi C3- C9, un grupo halocicloalcoxi C3-C9, un grupo alquiltio C1-C6, un grupo haloalquiltio C1-C6, un grupo alquilsulfinilo C1-C6, un grupo haloalquilsulfinilo C1-C6, un grupo alquilsulfonilo C1-C6, un grupo haloalquilsulfonilo C1-C6, un grupo alquilcarbonilo C2-C7, un grupo haloalquilcarbonilo C2-C7, un grupo alquenilcarbonilo C3-C7, un grupo haloalquenilcarbonilo C3-C7, un grupo alquinilcarbonilo C3-C7, un grupo haloalquinilcarbonilo C3-C7, un grupo cicloalquilcarbonilo C4-C10, un grupo halocicloalquilcarbonilo C4-C10, un grupo alquilcarboniloxi C2-C7, un grupo haloalquilcarboniloxi C2-C7, un grupo alquilsulfoniloxi C1-C6, un grupo haloalquilsulfoniloxi C1-C6, un grupo alcoxicarbonilo C2-C7, un grupo haloalcoxicarbonilo C2-C7, un grupo alqueniloxicarbonilo C3-C7, un grupo haloalqueniloxicarbonilo C3-C7, un grupo alquiniloxicarbonilo C3-C7, un grupo haloalquiniloxicarbonilo C3-C7, un grupo cicloalquiloxicarbonilo C4-C10, un grupo halocicloalquiloxicarbonilo C4-C10, un grupo alquilcarbonilamino C2-C7, un grupo haloalquilcarbonilamino C2-C7, un grupo alcoxicarbonilamino C2-C7, un grupo haloalcoxicarbonilamino C2-C7, un grupo alquilamino C1-C6, un grupo haloalquilamino C1-C6, un grupo alquenilamino C2-C6, un grupo haloalquenilamino C2-C6, un grupo alquinilamino C2-C6, un grupo haloalquinilamino C2-C6, un grupo cicloalquilamino C3-C9, un grupo halocicloalquilamino C3-C9, un grupo alquilaminocarbonilo C2-C7, un grupo haloalquilaminocarbonilo C2-C7, un grupo alquenilaminocarbonilo C3-C7, un grupo haloalquenilaminocarbonilo C3-C7, un grupo alquinilaminocarbonilo C3-C7, un grupo haloalquinilaminocarbonilo C3-C7, un grupo cicloalquilaminocarbonilo C4-C10, un grupo halocicloalquilaminocarbonilo C4-C10, un grupo amino, un grupo carbamoílo, un grupo ciano, un grupo nitro, un grupo hidroxi, un grupo pentafluorosulfanilo, un grupo fenilo que puede tener un sustituyente y un grupo heterocíclico que puede tener un sustituyente, y cuando hay dos o más sustituyentes, los sustituyentes pueden ser iguales o diferentes entre sí; en donde, el grupo heterocíclico en Q1 representa un grupo piridilo, un grupo N-óxido de piridina, un grupo pirimidinilo, un grupo pirazinilo, un grupo piridazilo, un grupo furilo, un grupo tienilo, un grupo oxazolilo, un grupo isoxazolilo, un grupo oxadiazolilo, un grupo tiazolilo, un grupo isotiazolilo, un grupo tiadiazolilo, un grupo pirrolilo, un grupo imidazolilo, un grupo triazolilo, un grupo pirazolilo o un grupo tetrazolilo; cada uno de R1 y R2 representa independientemente un átomo de hidrógeno, un átomo de oxígeno, un átomo de halógeno, un grupo hidroxi, un grupo nitro, un grupo nitroso, un grupo trimetilsililo, un grupo t-butildimetilsililo, un grupo ciano, un grupo amino, un grupo alquilo C1-C6 que puede tener un sustituyente, un grupo haloalquilo C1- C6 que puede tener un sustituyente, un grupo alquilcarbonilo C2-C7, un grupo haloalquilcarbonilo C2-C7, un grupo alquenilo C2-C6 que puede tener un sustituyente, un grupo haloalquenilo C2-C6 que puede tener un sustituyente, un grupo alquinilo C2-C6 que puede tener un sustituyente, un grupo haloalquinilo C2-C6 que puede tener un sustituyente, un grupo alcoxicarbonilo C2-C7, un grupo haloalcoxicarbonilo C2-C7, un grupo alqueniloxicarbonilo C3-C7, un grupo haloalqueniloxicarbonilo C3-C7, un grupo alquiniloxicarbonilo C3-C7, un grupo haloalquiniloxicarbonilo C3-C7, un grupo fenoxicarbonilo, un grupo alquilaminocarbonilo C2-C7, un grupo haloalquilaminocarbonilo C2-C7, un grupo alquilcarboniloxi C2-C7, un grupo haloalquilcarboniloxi C2-C7, un grupo benzoílo, un grupo alcoxi C1-C6, un grupo haloalcoxi C1-C6, un grupo alquiltio C1-C6, un grupo haloalquiltio C1- C6, un grupo alquilsulfinilo C1-C6, un grupo haloalquilsulfinilo C1-C6, un grupo alquilsulfonilo C1-C6, un grupo haloalquilsulfonilo C1-C6, un grupo bencenosulfonilo, un grupo bencilsulfonilo, un grupo bencilo o -C(=O)C(=O)R7, en donde R7 representa un grupo alquilo C1-C6, un grupo haloalquilo C1-C6, un grupo alcoxi C1-C6 o un grupo haloalcoxi C1-C6; **(Ver fórmula)** en donde, en la Fórmula (8), Q1 representa un grupo fenilo o un grupo piridilo que pueden tener un sustituyente seleccionado entre un grupo que consiste en: un átomo de halógeno, un grupo haloalquilo C1, un grupo nitro y un grupo ciano, en un caso donde Q1 tiene el sustituyente, el número de los sustituyentes es 1 o 2; cada uno de X1 y X2 representa independientemente un átomo de hidrógeno o un átomo de flúor y X3 y X4 representan un átomo de hidrógeno; cada uno de R1 y R2 representa independientemente un átomo de hidrógeno o un grupo metilo; cada uno de Y1 e Y5 representa independientemente un átomo de cloro, un átomo de bromo, un átomo de yodo, un grupo trifluorometoxi, un grupo trifluorometilo o un grupo pentafluoroetilo; Y2 e Y4 representan un átomo de hidrógeno; e Y3 representa un grupo perfluoroalquilo C3-C4; en un caso donde Y1 e Y5 representan átomos de halógeno simultáneamente, al menos uno de X1 o X2 representa un átomo de flúor; y **(Ver fórmula)** en un caso donde Y1 o Y5 representan un grupo trifluorometoxi, X2 representa un átomo de flúor; en donde, en la Fórmula (9), n representa 4; cada uno de los cuatro X representa independientemente un átomo de hidrógeno, un átomo de halógeno o un grupo ciano; Y3 representa un grupo perfluoroalquilo C2-C4; Y2 e Y4 representan un átomo de hidrógeno; cada Y1 e Y5 representa independientemente un átomo de halógeno o un grupo haloalquilo C1-C3, e Y1 o Y5 representan un grupo haloalquilo C1-C3; cada uno de G1, G2 y G3 representa independientemente un átomo de oxígeno o un átomo de azufre; Q2 representa un átomo de hidrógeno, un grupo alquilo C1-C6, un grupo haloalquilo C1-C6, un grupo alquenilo C2- C6, un grupo haloalquenilo C2-C6, un grupo alquinilo C2-C6, un grupo haloalquinilo C2-C6, un grupo cicloalquilo C3-C9, un grupo halocicloalquilo C3-C9, un grupo bencilo, un grupo fenilo que puede tener un sustituyente, un grupo naftilo o un grupo heterocíclico que puede tener un sustituyente; en donde, en Q2, el sustituyente de un grupo fenilo que puede tener un sustituyente y un grupo heterocíclico que puede tener un sustituyente representan uno o más sustituyentes seleccionados entre un grupo que consiste en: un átomo de halógeno, un grupo alquilo C1-C6, un grupo haloalquilo C1-C6, un grupo cicloalquilo C3-C9, un grupo halocicloalquilo C3-C9, un grupo alquenilo C2-C6, un grupo haloalquenilo C2-C6, un grupo alquinilo C2- C6, un grupo haloalquinilo C2-C6, un grupo alcoxi C1-C6, un grupo haloalcoxi C1-C6, un grupo alqueniloxi C2- C6, un grupo haloalqueniloxi C2-C6, un grupo alquiniloxi C2-C6, un grupo haloalquiniloxi C2-C6, un grupo cicloalcoxi C3-C9, un grupo halocicloalcoxi C3-C9, un grupo alquiltio C1-C6, un grupo haloalquiltio C1-C6, un grupo alquilsulfinilo C1-C6, un grupo haloalquilsulfinilo C1-C6, un grupo alquilsulfonilo C1-C6, un grupo haloalquilsulfonilo C1-C6, un grupo alquilcarbonilo C2-C7, un grupo haloalquilcarbonilo C2-C7, un grupo alquenilcarbonilo C3-C7, un grupo haloalquenilcarbonilo C3-C7, un grupo alquinilcarbonilo C3-C7, un grupo haloalquinilcarbonilo C3-C7, un grupo cicloalquilcarbonilo C4-C10, un grupo halocicloalquilcarbonilo C4-C10, un grupo alquilcarboniloxi C2-C7, un grupo haloalquilcarboniloxi C2-C7, un grupo alquilsulfoniloxi C1-C6, un grupo haloalquilsulfoniloxi C1-C6, un grupo alcoxicarbonilo C2-C7, un grupo haloalcoxicarbonilo C2-C7, un grupo alqueniloxicarbonilo C3-C7, un grupo haloalqueniloxicarbonilo C3-C7, un grupo alquiniloxicarbonilo C3- C7, un grupo haloalquiniloxicarbonilo C3-C7, un grupo cicloalquiloxicarbonilo C4-C10, un grupo halocicloalquiloxicarbonilo C4-C10, un grupo alquilcarbonilamino C2-C7, un grupo haloalquilcarbonilamino C2- C7, un grupo alcoxicarbonilamino C2-C7, un grupo haloalcoxicarbonilamino C2-C7, un grupo alquilamino C1- C6, un grupo haloalquilamino C1-C6, un grupo alquenilamino C2-C6, un grupo haloalquenilamino C2-C6, un grupo alquinilamino C2-C6, un grupo haloalquinilamino C2-C6, un grupo cicloalquilamino C3-C9, un grupo halocicloalquilamino C3-C9, un grupo alquilaminocarbonilo C2-C7, un grupo haloalquilaminocarbonilo C2-C7, un grupo alquenilaminocarbonilo C3-C7, un grupo haloalquenilaminocarbonilo C3-C7, un grupo alquinilaminocarbonilo C3-C7, un grupo haloalquinilaminocarbonilo C3-C7, un grupo cicloalquilaminocarbonilo C4-C10, un grupo halocicloalquilaminocarbonilo C4-C10, un grupo amino, un grupo carbamoílo, un grupo ciano, un grupo nitro, un grupo hidroxi, un grupo pentafluorosulfanilo, un grupo fenilo que puede tener un sustituyente, y un grupo heterocíclico que puede tener un sustituyente, y cuando hay dos o más sustituyentes, los sustituyentes pueden ser iguales o diferentes entre sí; en donde, el grupo heterocíclico en Q2 representa un grupo piridilo, un grupo N-óxido de piridina, un grupo pirimidinilo, un grupo pirazinilo, un grupo piridazilo, un grupo furilo, un grupo tienilo, un grupo oxazolilo, un grupo isoxazolilo, un grupo oxadiazolilo, un grupo tiazolilo, un grupo isotiazolilo, un grupo tiadiazolilo, un grupo pirrolilo, un grupo imidazolilo, un grupo triazolilo, un grupo pirazolilo o un grupo tetrazolilo; cada uno de R1 y R2 representa independientemente un átomo de hidrógeno, un átomo de oxígeno, un átomo de halógeno, un grupo hidroxi, un grupo nitro, un grupo nitroso, un grupo trimetilsililo, un grupo t-butildimetilsililo, un grupo ciano, un grupo amino, un grupo alquilo C1-C6 que puede tener un sustituyente, un grupo haloalquilo C1-C6 que puede tener un sustituyente, un grupo alquilcarbonilo C2-C7, un grupo haloalquilcarbonilo C2-C7, un grupo alquenilo C2-C6 que puede tener un sustituyente, un grupo haloalquenilo C2-C6 que puede tener un sustituyente, un grupo alquinilo C2-C6 que puede tener un sustituyente, un grupo haloalquinilo C2-C6 que puede tener un sustituyente, un grupo alcoxicarbonilo C2-C7, un grupo haloalcoxicarbonilo C2-C7, un grupo alqueniloxicarbonilo C3-C7, un grupo haloalqueniloxicarbonilo C3-C7, un grupo alquiniloxicarbonilo C3-C7, un grupo haloalquiniloxicarbonilo C3-C7, un grupo fenoxicarbonilo, un grupo alquilaminocarbonilo C2-C7, un grupo haloalquilaminocarbonilo C2-C7, un grupo alquilcarboniloxi C2-C7, un grupo haloalquilcarboniloxi C2-C7, un grupo benzoílo, un grupo alcoxi C1-C6, un grupo haloalcoxi C1-C6, un grupo alquiltio C1-C6, un grupo haloalquiltio C1-C6, un grupo alquilsulfinilo C1-C6, un grupo haloalquilsulfinilo C1-C6, un grupo alquilsulfonilo C1-C6, un grupo haloalquilsulfonilo C1-C6, un grupo bencenosulfonilo, un grupo bencilsulfonilo, un grupo bencilo o -C(=O)C(=O)R7, en donde R7 representa un grupo alquilo C1-C6, un grupo haloalquilo C1-C6, un grupo alcoxi C1-C6 o un grupo haloalcoxi C1-C6, en donde la plaga se selecciona entre el grupo que consiste en: Insectos Siphonaptera tales como Ctenocephalides felis, Ctenocephalides canis, Echidnophaga gallinacea, Pulex irritans, y Xenopsylla cheopis; insectos Mallophaga tales como Menacanthus stramineus, y Bovicola bovis; insectos Anoplura tales como Haematopinus eurysternus, Haematopinus suis, Linognathus vituli, y Soleno- potes capillatus; Ixodidae tales como Boophilus microplus, Rhipicephalus sanguineus, Haemaphysalis longicornis, Haema- physalis flava, Haemaphysalis campanulata, Ixodes ovatus, Ixodes persulcatus, Amblyomma spp., y Dermacentor spp.; Cheyletidae tales como Cheyletiella yasguri, y Cheyletiella blakei; Demodicidae tales como Demodex canis, Demodex cati; Psoroptidae tales como Psoroptes ovis; y Sarcoptidae tales como Sarcoptes scabiei, Notoedres cati y Knemidocoptes spp.
Description
DESCRIPCIÓN
Agente para el control de plagas que contiene un derivado de amida y uso del agente para el control de plagas Campo técnico
La presente invención se refiere a un agente para el control de plagas, con un derivado de amida contenido en el agente para el control de plagas.
Técnica antecedente
Se describen diversos derivados de amida en el texto de la Publicación Internacional WO 2005/21488, la Publicación Internacional WO 2005/73165, la Publicación Internacional WO 2006/137376, y la Publicación Internacional WO 2006/137395.
Divulgación de la invención
Problemas a resolver por la invención
En la producción de, por ejemplo, cultivos agrícolas y hortícolas, debido a causas tales como el daño a gran escala debido a plagas o similares que se produce en la actualidad y a la propagación de plagas que tienen resistencia a los agentes químicos existentes, existe demanda de un nuevo agente para el control de plagas agrícolas/hortícolas. Un objetivo de la presente invención es proporcionar un agente para el control de plagas que contiene un derivado de amida como principio activo que muestre un efecto plaguicida contra una gran variedad de plagas agrícolas/hortícolas y un método para el control de plagas.
Medios para resolver los nuevos problemas
Los presentes inventores han llevado a cabo estudios intensivos para desarrollar un nuevo agente para el control de plagas, y como resultado, han descubierto que el derivado aromático de carboxamida representado por la fórmula (1) de la presente invención es un nuevo compuesto desconocido en la bibliografía, y también es un agente para el control de plagas, en particular, un agente para el control de plagas agrícolas/hortícolas, que muestra una eficacia particularmente elevada, y por lo tanto han completado la presente invención.
Además, también han descubierto un nuevo método de preparación y un intermedio útil para la preparación del compuesto de la presente invención. Como resultado, han completado la presente invención.
Es decir, la presente invención es como se indica a continuación.
1. Un agente para el control de plagas que comprende al menos un derivado de amida seleccionado entre el grupo que consiste en la siguiente Fórmula (1), Fórmula (7), Fórmula (8) y Fórmula (9) como principio activo:
en el que, en la Fórmula (1), A representa un átomo de carbono, un átomo de oxígeno, un átomo de nitrógeno, un átomo de nitrógeno oxidado o un átomo de azufre; K representa un grupo de átomo no metálico necesario para formar un grupo de unión cíclico derivado de piridina, N-óxido de piridina, pirrol, tiazol, furano o tiofeno, junto con A y dos átomos de carbono a los que se une A;
X representa un átomo de hidrógeno, un átomo de halógeno, un grupo alquilo C1-C6, un grupo haloalquilo C1-C6, un grupo cicloalquilo C3-C9, un grupo halocicloalquilo C3-C9, un grupo alquenilo C2-C6, un grupo haloalquenilo C2-C6 un grupo alquinilo C2-C6, un grupo haloalquinilo C2-C6, un grupo alcoxi C1-C6, un grupo haloalcoxi C1-C6, un grupo alqueniloxi C2-C6, un grupo haloalqueniloxi C2-C6, un grupo alquiniloxi C2-C6, un grupo haloalquiniloxi C2-C6, un grupo cicloalcoxi C3-C9, un grupo halocicloalcoxi C3-C9, un grupo alquiltio C1-C6, un grupo haloalquiltio C1-C6, un grupo alquilsulfinilo C1-C6, un grupo haloalquilsulfinilo C1-C6, un grupo alquilsulfonilo C1-C6, un grupo haloalquilsulfonilo C1-C6, un grupo alquilsulfoniloxi C1-C6, un grupo haloalquilsulfoniloxi C1-C6, un grupo alquilcarbonilo C2-C7, un grupo haloalquilcarbonilo C2-C7, un grupo alquenilcarbonilo C3-C7, un grupo haloalquenilcarbonilo C3-C7, un grupo alquinilcarbonilo C3-C7, un grupo haloalquinilcarbonilo C3-C7, un grupo cicloalquilcarbonilo C4-C10, un grupo halocicloalquilcarbonilo C4-C10 un grupo alquilcarboniloxi C2-C7, un grupo haloalquilcarboniloxi C2-C7, un grupo arilcarboniloxi, un grupo alcoxicarbonilo C2-C7, un grupo haloalcoxicarbonilo C2-C7, un grupo alqueniloxicarbonilo C3-C7, un grupo haloalqueniloxicarbonilo C3-C7, un grupo alquiniloxicarbonilo C3-C7, un grupo haloalquiniloxicarbonilo C3-C7, un grupo cicloalquiloxicarbonilo C4-C10, un grupo halocicloalquiloxicarbonilo C4-C10, un grupo alquilcarbonilamino C2-C7, un grupo haloalquilcarbonilamino C2-C7, un grupo alcoxicarbonilamino C2-C7, un grupo haloalcoxicarbonilamino C2-C7, un grupo alcoxicarboniloxi C2-C7, un grupo haloalcoxicarboniloxi C2-C7, un grupo arilcarbonilamino, un grupo amino, un grupo carbamoílo, un grupo ciano, un grupo hidroxi, un grupo pentafluorosulfanilo, un grupo alquilamino C1-C6, un grupo haloalquilamino C1-C6, un grupo alquenilamino C2-C6, un grupo haloalquenilamino C2-C6, un grupo alquinilamino C2-C6, un grupo haloalquinilamino C2-C6, un grupo cicloalquilamino C3-C9, un grupo halocicloalquilamino C3-C9, un grupo alquilaminocarbonilo C2-C7, un grupo haloalquilaminocarbonilo C2-C7, un grupo alquenilaminocarbonilo C3-C7, un grupo haloalquenilaminocarbonilo C3-C7, un grupo alquinilaminocarbonilo C3-C7, un grupo haloalquinilaminocarbonilo C3-C7, un grupo cicloalquilaminocarbonilo C4-C10, un grupo halocicloalquilaminocarbonilo C4-C10, un grupo fenilo o un grupo heterocíclico, y cuando hay varios X, cada X puede ser igual o diferente entre sí;
n representa un número entero de 0 a 4;
T representa -C(=G-i)-Q1 o -C(=G-i)-G2Q2;
cada uno de G1 y G2 representa independientemente un átomo de oxígeno o un átomo de azufre;
cada uno de Q1 y Q2 representa un átomo de hidrógeno, un grupo alquilo C1-C6, un grupo haloalquilo C1-C6, un grupo alquenilo C2-C6, un grupo haloalquenilo C2-C6 un grupo alquinilo C2-C6, un grupo haloalquinilo C2-C6, un grupo cicloalquilo C3-C9, un grupo halocicloalquilo C3-C9, un grupo bencilo, un grupo fenilo que puede tener un sustituyente, un grupo naftilo o un grupo heterocíclico que puede tener un sustituyente:
Y1 e Y5 representan un átomo de halógeno o un grupo haloalquilo C1-C3, e Y1 o Y5 representa un grupo haloalquilo C1-C3; Y2 e Y4 representan un átomo de hidrógeno; Y3 representa un grupo perfluoroalquilo C2-C4; en el que, en Q1 y Q2, el sustituyente de un grupo fenilo que puede tener un sustituyente y un grupo heterocíclico que puede tener un sustituyente representa uno o más sustituyentes seleccionados entre un grupo que consiste en un átomo de halógeno, un grupo alquilo C1-C6, un grupo haloalquilo C1-C6, un grupo cicloalquilo C3-C9, un grupo halocicloalquilo C3-C9, un grupo alquenilo C2-C6, un grupo haloalquenilo C2-C6 un grupo alquinilo C2-C6, un grupo haloalquinilo C2-C6, un grupo alcoxi C1-C6, un grupo haloalcoxi C1-C6, un grupo alqueniloxi C2-C6, un grupo haloalqueniloxi C2-C6, un grupo alquiniloxi C2-C6, un grupo haloalquiniloxi C2-C6, un grupo cicloalcoxi C3-C9, un grupo halocicloalcoxi C3-C9, un grupo alquiltio C1-C6, un grupo haloalquiltio C1-C6, un grupo alquilsulfinilo C1-C6, un grupo haloalquilsulfinilo C1-C6, un grupo alquilsulfonilo C1-C6, un grupo haloalquilsulfonilo C1-C6, un grupo alquilcarbonilo C2-C7, un grupo haloalquilcarbonilo C2-C7, un grupo alquenilcarbonilo C3-C7, un grupo haloalquenilcarbonilo C3-C7, un grupo alquinilcarbonilo C3-C7, un grupo haloalquinilcarbonilo C3-C7, un grupo cicloalquilcarbonilo C4-C10, un grupo halocicloalquilcarbonilo C4-C10 un grupo alquilcarboniloxi C2-C7, un grupo haloalquilcarboniloxi C2-C7, un grupo alquilsulfoniloxi C1-C6, un grupo haloalquilsulfoniloxi C1-C6, un grupo alcoxicarbonilo C2-C7, un grupo haloalcoxicarbonilo C2-C7, un grupo alqueniloxicarbonilo C3-C7, un grupo haloalqueniloxicarbonilo C3-C7, un grupo alquiniloxicarbonilo C3-C7, un grupo haloalquiniloxicarbonilo C3-C7, un grupo cicloalquiloxicarbonilo C4-C10, un grupo halocicloalquiloxicarbonilo C4-C10, un grupo alquilcarbonilamino C2-C7, un grupo haloalquilcarbonilamino C2-C7, un grupo alcoxicarbonilamino C2-C7, un grupo haloalcoxicarbonilamino C2-C7, un grupo alquilamino C1-C6, un grupo haloalquilamino C1-C6, un grupo alquenilamino C2-C6, un grupo haloalquenilamino C2-C6, un grupo alquinilamino C2-C6, un grupo haloalquinilamino C2-C6, un grupo cicloalquilamino C3-C9, un grupo halocicloalquilamino C3-C9, un grupo alquilaminocarbonilo C2-C7, un grupo haloalquilaminocarbonilo C2-C7, un grupo alquenilaminocarbonilo C3-C7, un grupo haloalquenilaminocarbonilo C3-C7, un grupo alquinilaminocarbonilo C3-C7, un grupo haloalquinilaminocarbonilo C3-C7, un grupo cicloalquilaminocarbonilo C4-C10, un grupo halocicloalquilaminocarbonilo C4-C10, un grupo amino, un grupo carbamoílo, un grupo ciano, un grupo nitro, un grupo hidroxi, un grupo pentafluorosulfanilo, un grupo fenilo que puede tener un sustituyente, y un grupo heterocíclico que puede tener un sustituyente, y cuando hay dos o más sustituyentes, los sustituyentes pueden ser iguales o diferentes entre sí; en el que, el grupo heterocíclico en X, Q1 y Q2 representan un grupo piridilo, un grupo N-óxido de piridina, un grupo pirimidinilo, un grupo pirazinilo, un grupo piridazilo, un grupo furilo, un grupo tienilo, un grupo oxazolilo, un grupo isoxazolilo, un grupo oxadiazolilo, un grupo tiazolilo, un grupo isotiazolilo, un grupo tiadiazolilo, un grupo pirrolilo, un grupo imidazolilo, un grupo triazolilo, un grupo pirazolilo o un grupo tetrazolilo;
G3 representa un átomo de oxígeno o un átomo de azufre y
Cada uno de R1 y R2 representa independientemente un átomo de hidrógeno, un átomo de oxígeno, un átomo
de halógeno, un grupo hidroxi, un grupo nitro, un grupo nitroso, un grupo trimetilsililo, un grupo t-butildimetilsilMo, un grupo ciano, un grupo amino, un grupo alquilo C1-C6 que puede tener un sustituyente, un grupo haloalquilo C1-C6 que puede tener un sustituyente, un grupo alquilcarbonilo C2-C7, un grupo haloalquilcarbonilo C2-C7, un grupo alquenilo C2-C6 que puede tener un sustituyente, un grupo haloalquenilo C2-C6 que puede tener un sustituyente, un grupo alquinilo C2-C6 que puede tener un sustituyente, un grupo haloalquinilo C2-C6 que puede tener un sustituyente, un grupo alcoxicarbonilo C2-C7, un grupo haloalcoxicarbonilo C2-C7, un grupo alqueniloxicarbonilo C3-C7, un grupo haloalqueniloxicarbonilo C3-C7, un grupo alquiniloxicarbonilo C3-C7, un grupo haloalquiniloxicarbonilo C3-C7, un grupo fenoxicarbonilo, un grupo alquilaminocarbonilo C2-C7, un grupo haloalquilaminocarbonilo C2-C7, un grupo alquilcarboniloxi C2-C7, un grupo haloalquilcarboniloxi C2-C7, un grupo benzoílo, un grupo alcoxi C1-C6, un grupo haloalcoxi C1-C6, un grupo alquiltio C1-C6, un grupo haloalquiltio C1-C6, un grupo alquilsulfinilo C1-C6, un grupo haloalquilsulfinilo C1-C6, un grupo alquilsulfonilo C1-C6, un grupo haloalquilsulfonilo C1-C6, un grupo bencenosulfonilo, un grupo bencilsulfonilo, un grupo bencilo o -C(=O)C(=O)R7, en el que R7 representa un grupo alquilo C1-C6, un grupo haloalquilo C1-C6, un grupo alcoxi C1-C6 o un grupo haloalcoxi C1-C6;
en el que, en la Fórmula (7), n representa 4;
cada X representa independientemente un átomo de hidrógeno, un átomo de halógeno o grupo ciano;
Y3 representa un grupo perfluoroalquilo C2-C4; Y2 e Y4 representan un átomo de hidrógeno;
Y1 e Y5 representan un átomo de halógeno o un grupo haloalquilo C1-C3, e Y1 o Y5 representa un grupo haloalquilo C1-C3;
Cada uno de G1 y G3 representa independientemente un átomo de oxígeno o un átomo de azufre.
Q1 representa un átomo de hidrógeno, un grupo alquilo C1-C6, un grupo haloalquilo C1-C6, un grupo alquenilo C2-C6, un grupo haloalquenilo C2-C6 un grupo alquinilo C2-C6, un grupo haloalquinilo C2-C6, un grupo cicloalquilo C3-C9, un grupo halocicloalquilo C3-C9, un grupo bencilo, un grupo fenilo que puede tener un sustituyente, un grupo naftilo o un grupo heterocíclico que puede tener un sustituyente;
en el que, en Q1, el sustituyente de un grupo fenilo que puede tener un sustituyente y un sustituyente grupo heterocíclico que puede tener un sustituyente representa uno o más sustituyentes seleccionados entre un grupo que consiste en un átomo de halógeno, un grupo alquilo C1-C6, un grupo haloalquilo C1-C6, un grupo cicloalquilo C3-C9, un grupo halocicloalquilo C3-C9, un grupo alquenilo C2-C6, un grupo haloalquenilo C2-C6 un grupo alquinilo C2-C6, un grupo haloalquinilo C2-C6, un grupo alcoxi C1-C6, un grupo haloalcoxi C1-C6, un grupo alqueniloxi C2-C6, un grupo haloalqueniloxi C2-C6, un grupo alquiniloxi C2-C6, un grupo haloalquiniloxi C2-C6, un grupo cicloalcoxi C3-C9, un grupo halocicloalcoxi C3-C9, un grupo alquiltio C1-C6, un grupo haloalquiltio C1-C6, un grupo alquilsulfinilo C1-C6, un grupo haloalquilsulfinilo C1-C6, un grupo alquilsulfonilo C1-C6, un grupo haloalquilsulfonilo C1-C6, un grupo alquilcarbonilo C2-C7, un grupo haloalquilcarbonilo C2-C7, un grupo alquenilcarbonilo C3-C7, un grupo haloalquenilcarbonilo C3-C7, un grupo alquinilcarbonilo C3-C7, un grupo haloalquinilcarbonilo C3-C7, un grupo cicloalquilcarbonilo C4-C10, un grupo halocicloalquilcarbonilo C4-C10 un grupo alquilcarboniloxi C2-C7, un grupo haloalquilcarboniloxi C2-C7, un grupo alquilsulfoniloxi C1-C6, un grupo haloalquilsulfoniloxi C1-C6, un grupo alcoxicarbonilo C2-C7, un grupo haloalcoxicarbonilo C2-C7, un grupo alqueniloxicarbonilo C3-C7, un grupo haloalqueniloxicarbonilo C3-C7, un grupo alquiniloxicarbonilo C3-C7, un grupo haloalquiniloxicarbonilo C3-C7, un grupo cicloalquiloxicarbonilo C4-C10, un grupo halocicloalquiloxicarbonilo C4-C10, un grupo alquilcarbonilamino C2-C7, un grupo haloalquilcarbonilamino C2-C7, un grupo alcoxicarbonilamino C2-C7, un grupo haloalcoxicarbonilamino C2-C7, un grupo alquilamino C1-C6, un grupo haloalquilamino C1-C6, un grupo alquenilamino C2-C6, un grupo haloalquenilamino C2-C6, un grupo alquinilamino C2-C6, un grupo haloalquinilamino C2-C6, un grupo cicloalquilamino C3-C9, un grupo halocicloalquilamino C3-C9, un grupo alquilaminocarbonilo C2-C7, un grupo
haloalquilaminocarbonilo C2-C7, un grupo alquenilaminocarbonilo C3-C7, un grupo haloalquenilaminocarbonilo C3-C7, un grupo alquinilaminocarbonilo C3-C7, un grupo haloalquinilaminocarbonilo C3-C7, un grupo cicloalquilaminocarbonilo C4-C10, un grupo halocicloalquilaminocarbonilo C4-C10, un grupo amino, un grupo carbamoílo, un grupo ciano, un grupo nitro, un grupo hidroxi, un grupo pentafluorosulfanilo, un grupo fenilo que puede tener un sustituyente, y un grupo heterocíclico que puede tener un sustituyente, y cuando hay dos o más sustituyentes, los sustituyentes pueden ser iguales o diferentes entre sí; en el que, el grupo heterocíclico en Q1 representa un grupo piridilo, un grupo N-óxido de piridina, un grupo pirimidinilo, un grupo pirazinilo, un grupo piridazilo, un grupo furilo, un grupo tienilo, un grupo oxazolilo, un grupo isoxazolilo, un grupo oxadiazolilo, un grupo tiazolilo, un grupo isotiazolilo, un grupo tiadiazolilo, un grupo pirrolilo, un grupo imidazolilo, un grupo triazolilo, un grupo pirazolilo o un grupo tetrazolilo;
Cada uno de R1 y R2 representa independientemente un átomo de hidrógeno, un átomo de oxígeno, un átomo de halógeno, un grupo hidroxi, un grupo nitro, un grupo nitroso, un grupo trimetilsililo, un grupo t-butildimetilsililo, un grupo ciano, un grupo amino, un grupo alquilo C1-C6 que puede tener un sustituyente, un grupo haloalquilo C1-C6 que puede tener un sustituyente, un grupo alquilcarbonilo C2-C7, un grupo haloalquilcarbonilo C2-C7, un grupo alquenilo C2-C6 que puede tener un sustituyente, un grupo haloalquenilo C2-C6 que puede tener un sustituyente, un grupo alquinilo C2-C6 que puede tener un sustituyente, un grupo haloalquinilo C2-C6 que puede tener un sustituyente, un grupo alcoxicarbonilo C2-C7, un grupo haloalcoxicarbonilo C2-C7, un grupo alqueniloxicarbonilo C3-C7, un grupo haloalqueniloxicarbonilo C3-C7, un grupo alquiniloxicarbonilo C3-C7, un grupo haloalquiniloxicarbonilo, un grupo fenoxicarbonilo, un grupo alquilaminocarbonilo C2-C7, un grupo haloalquilaminocarbonilo C2-C7, un grupo alquilcarboniloxi C2-C7, un grupo haloalquilcarboniloxi C2-C7, un grupo benzoílo, un grupo alcoxi C1-C6, un grupo haloalcoxi C1-C6, un grupo alquiltio C1-C6, un grupo haloalquiltio C1-C6, un grupo alquilsulfinilo C1-C6, un grupo haloalquilsulfinilo C1-C6, un grupo alquilsulfonilo C1-C6, un grupo haloalquilsulfonilo C1-C6, un grupo bencenosulfonilo, un grupo bencilsulfonilo, un grupo bencilo o -C(=O)C(=O)R7, en el que R7 representa un grupo alquilo C1-C6, un grupo haloalquilo C1-C6, un grupo alcoxi C1-C6 o un grupo haloalcoxi C1-C6;
en el que, en la Fórmula (8), Q1 representa un grupo fenilo o un grupo piridilo que puede tener un sustituyente seleccionado entre un grupo que consiste en: un átomo de halógeno, un grupo haloalquilo C1, un sustituyente grupo nitro, y un grupo ciano, en un caso donde Q1 tiene el sustituyente sustituyentes, el número de sustituyentes es 1 o 2 ;
Cada uno de X1 y X2 representa independientemente un átomo de hidrógeno o un átomo de flúor, y X3 y X4 representan un átomo de hidrógeno;
Cada uno de R1 y R2 representa independientemente un átomo de hidrógeno o un grupo metilo;
Cada uno de Y1 e Y5 representa independientemente un átomo de cloro, un átomo de bromo, un átomo de yodo, un grupo trifluorometoxi, un grupo trifluorometilo o un grupo pentafluoroetilo;
Y2 e Y4 representan un átomo de hidrógeno; e Y3 representa un grupo perfluoroalquilo C3-C4; en un caso donde Y1 e Y5 representan átomos de halógeno simultáneamente, al menos uno de X1 o X2 representa un átomo de flúor; y en un caso donde Y1 o Y5 representan un grupo trifluorometoxi, X2 representa un átomo de flúor;
en el que, en la Fórmula (9), n representa 4;
cada uno de los cuatro X representa independientemente un átomo de hidrógeno, un átomo de halógeno o grupo ciano.
Y3 representa un grupo perfluoroalquilo C2-C4; Y2 e Y4 representan un átomo de hidrógeno; cada Y1 e Y5 representa independientemente un átomo de halógeno o un grupo haloalquilo C1-C3, e Y1 o Y5 representa un grupo haloalquilo C1-C3;
G1, G2 y G3 representan cada uno independientemente un átomo de oxígeno o un átomo de azufre.
Q2 representa un átomo de hidrógeno, un grupo alquilo C1-C6, un grupo haloalquilo C1-C6, un grupo alquenilo C2-C6, un grupo haloalquenilo C2-C6 un grupo alquinilo C2-C6, un grupo haloalquinilo C2-C6, un grupo cicloalquilo C3-C9, un grupo halocicloalquilo C3-C9, un grupo bencilo, un grupo fenilo que puede tener un sustituyente, un grupo naftilo o un grupo heterocíclico que puede tener un sustituyente;
en el que, en Q2, el sustituyente de un grupo fenilo que puede tener un sustituyente y un grupo heterocíclico que puede tener un sustituyente representa uno o más sustituyentes seleccionados entre un grupo que consiste en un átomo de halógeno, un grupo alquilo C1-C6, un grupo haloalquilo C1-C6, un grupo cicloalquilo C3-C9, un grupo halocicloalquilo C3-C9, un grupo alquenilo C2-C6, un grupo haloalquenilo C2-C6 un grupo alquinilo C2-C6, un grupo haloalquinilo C2-C6, un grupo alcoxi C1-C6, un grupo haloalcoxi C1-C6, un grupo alqueniloxi C2-C6, un grupo haloalqueniloxi C2-C6, un grupo alquiniloxi C2-C6, un grupo haloalquiniloxi C2-C6, un grupo cicloalcoxi C3-C9, un grupo halocicloalcoxi C3-C9, un grupo alquiltio C1-C6, un grupo haloalquiltio C1-C6, un grupo alquilsulfinilo C1-C6, un grupo haloalquilsulfinilo C1-C6, un grupo alquilsulfonilo C1-C6, un grupo haloalquilsulfonilo C1-C6, un grupo alquilcarbonilo C2-C7, un grupo haloalquilcarbonilo C2-C7, un grupo alquenilcarbonilo C3-C7, un grupo haloalquenilcarbonilo C3-C7, un grupo alquinilcarbonilo C3-C7, un grupo haloalquinilcarbonilo C3-C7, un grupo cicloalquilcarbonilo C4-C10, un grupo halocicloalquilcarbonilo C4-C10 un grupo alquilcarboniloxi C2-C7, un grupo haloalquilcarboniloxi C2-C7, un grupo alquilsulfoniloxi C1-C6, un grupo haloalquilsulfoniloxi C1-C6, un grupo alcoxicarbonilo C2-C7, un grupo haloalcoxicarbonilo C2-C7, un grupo alqueniloxicarbonilo C3-C7, un grupo haloalqueniloxicarbonilo C3-C7, un grupo alquiniloxicarbonilo C3-C7, un grupo haloalquiniloxicarbonilo C3-C7, un grupo cicloalquiloxicarbonilo C4-C10, un grupo halocicloalquiloxicarbonilo C4-C10, un grupo alquilcarbonilamino C2-C7, un grupo haloalquilcarbonilamino C2-C7, un grupo alcoxicarbonilamino C2-C7, un grupo haloalcoxicarbonilamino C2-C7, un grupo alquilamino C1-C6, un grupo haloalquilamino C1-C6, un grupo alquenilamino C2-C6, un grupo haloalquenilamino C2-C6, un grupo alquinilamino C2-C6, un grupo haloalquinilamino C2-C6, un grupo cicloalquilamino C3-C9, un grupo halocicloalquilamino C3-C9, un grupo alquilaminocarbonilo C2-C7, un grupo haloalquilaminocarbonilo C2-C7, un grupo alquenilaminocarbonilo C3-C7, un grupo haloalquenilaminocarbonilo C3-C7, un grupo alquinilaminocarbonilo C3-C7, un grupo haloalquinilaminocarbonilo C3-C7, un grupo cicloalquilaminocarbonilo C4-C10, un grupo halocicloalquilaminocarbonilo C4-C10, un grupo amino, un grupo carbamoílo, un grupo ciano, un grupo nitro, un grupo hidroxi, un grupo pentafluorosulfanilo, un grupo fenilo que puede tener un sustituyente, y un grupo heterocíclico que puede tener un sustituyente, y cuando hay dos o más sustituyentes, los sustituyentes pueden ser iguales o diferentes entre sí; en el que, el grupo heterocíclico en Q2 representa un grupo piridilo, un grupo N-óxido de piridina, un grupo pirimidinilo, un grupo pirazinilo, un grupo piridazilo, un grupo furilo, un grupo tienilo, un grupo oxazolilo, un grupo isoxazolilo, un grupo oxadiazolilo, un grupo tiazolilo, un grupo isotiazolilo, un grupo tiadiazolilo, un grupo pirrolilo, un grupo imidazolilo, un grupo triazolilo, un grupo pirazolilo o un grupo tetrazolilo;
Cada uno de R1 y R2 representa independientemente un átomo de hidrógeno, un átomo de oxígeno, un átomo de halógeno, un grupo hidroxi, un grupo nitro, un grupo nitroso, un grupo trimetilsililo, un grupo t-butildimetilsililo, un grupo ciano, un grupo amino, un grupo alquilo C1-C6 que puede tener un sustituyente, un grupo haloalquilo C1-C6 que puede tener un sustituyente, un grupo alquilcarbonilo C2-C7, un grupo haloalquilcarbonilo C2-C7, un grupo alquenilo C2-C6 que puede tener un sustituyente, un grupo haloalquenilo C2-C6 que puede tener un
sustituyente, un grupo alquinilo C2-C6 que puede tener un sustituyente, un grupo haloalquinilo C2-C6 que puede tener un sustituyente, un grupo alcoxicarbonilo C2-C7, un grupo haloalcoxicarbonilo C2-C7, un grupo alqueniloxicarbonilo C3-C7, un grupo haloalqueniloxicarbonilo C3-C7, un grupo alquiniloxicarbonilo C3-C7, un grupo haloalquiniloxicarbonilo, un grupo fenoxicarbonilo, un grupo alquilaminocarbonilo C2-C7, un grupo haloalquilaminocarbonilo C2-C7, un grupo alquilcarboniloxi C2-C7, un grupo haloalquilcarboniloxi C2-C7, un grupo benzoílo, un grupo alcoxi C1-C6, un grupo haloalcoxi C1-C6, un grupo alquiltio C1-C6, un grupo haloalquiltio C1-C6, un grupo alquilsulfinilo C1-C6, un grupo haloalquilsulfinilo C1-C6, un grupo alquilsulfonilo C1-C6, un grupo haloalquilsulfonilo C1-C6, un grupo bencenosulfonilo, un grupo bencilsulfonilo, un grupo bencilo o -C(=O)C(=O)R7, en el que R7 representa un grupo alquilo C1-C6, un grupo haloalquilo C1-C6, un grupo alcoxi C1-C6 o un grupo haloalcoxi C1-C6, en el que la plaga se selecciona entre el grupo que consiste en:
Insectos Siphonaptera tales como Ctenocephalides felis, Ctenocephalides canis, Echidnophaga gallinácea, Pulex irritans, y Xenopsylla cheopis;
insectos Mallophaga tales como Menacanthus stramineus, y Bovicola bovis;
insectos Anoplura tales como Haematopinus eurysternus, Haematopinus suis, Linognathus vituli, y Solenopotes capillatus;
ixodidae tales como Boophilus microplus, Rhipicephalus sanguineus, Haemaphysalis longicornis, Haemaphysalis flava, Haemaphysalis campanulata, Ixodes ovatus, Ixodes persulcatus, Amblyomma spp., y Dermacentor spp.;
cheyletidae tales como Cheyletiella yasguri, y Cheyletiella blakei;
demodicidae tales como Demodex canis, Demodex cati;
psoroptidae tales como Psoroptes ovis; y sarcoptidae tales como Sarcoptes scabiei, Notoedres cati, y Knemidocoptes spp.
2. Una composición que comprende un agente para el control de plagas que comprende al menos un derivado de amida de acuerdo con la Fórmula (1), Fórmula (7), Fórmula (8) o Fórmula (9), como se define en 1.
3. Un método de control de plagas que comprende aplicar el agente para el control de plagas según 1, o la composición como se define en 2 a una plaga como se define en 1, en el que el método no es un método de tratamiento.
4. Un agente para el control de plagas que comprende al menos un derivado de amida de acuerdo con la Fórmula (1), Fórmula (7), Fórmula (8) y Fórmula (9), como se define en 1, o una composición como se define en 2, para su uso en un método de tratamiento del cuerpo humano o animal.
5. Un agente para el control de plagas que comprende al menos un derivado de amida de acuerdo con la Fórmula (1), Fórmula (7), Fórmula (8) y Fórmula (9), como se define en 1, o una composición como se define en 2, para su uso en un método de tratamiento del cuerpo humano o animal,
en el que el método es para exterminar una plaga seleccionada del grupo que consiste en:
Insectos Siphonaptera tales como Ctenocephalides felis, Ctenocephalides canis, Echidnophaga gallinacea, Pulex irritans, y Xenopsylla cheopis;
insectos Mallophaga tales como Menacanthus stramineus, y Bovicola bovis;
insectos Anoplura tales como Haematopinus eurysternus, Haematopinus suis, Linognathus vituli, y Solenopotes capillatus;
ixodidae tales como Boophilus microplus, Rhipicephalus sanguineus, Haemaphysalis longicornis, Haemaphysalis flava, Haemaphysalis campanulata, Ixodes ovatus, Ixodes persulcatus, Amblyomma spp., y Dermacentor spp.;
cheyletidae tales como Cheyletiella yasguri, y Cheyletiella blakei;
demodicidae tales como Demodex canis, Demodex cati;
psoroptidae tales como Psoroptes ovis; y
sarcoptidae tales como Sarcoptes scabiei, Notoedres cati, y Knemidocoptes spp.
6. Uso de un agente para el control de plagas que comprende al menos un derivado de amida de acuerdo con la Fórmula (1), Fórmula (7), Fórmula (8) y Fórmula (9), como se define en 1, o una composición como se define en 2, como un agente para el control de plagas, en el que el uso no es un método de tratamiento del cuerpo humano o animal.
7. El uso de acuerdo con 6, en el que el uso es para el control de una plaga seleccionada del grupo que consiste en:
Insectos Siphonaptera tales como Ctenocephalides felis, Ctenocephalides canis, Echidnophaga gallinacea, Pulex irritans, y Xenopsylla cheopis;
insectos Mallophaga tales como Menacanthus stramineus, y Bovicola bovis;
insectos Anoplura tales como Haematopinus eurysternus, Haematopinus suis, Linognathus vituli, y Solenopotes capillatus;
ixodidae tales como Boophilus microplus, Rhipicephalus sanguineus, Haemaphysalis longicornis, Haemaphysalis flava, Haemaphysalis campanulata, Ixodes ovatus, Ixodes persulcatus, Amblyomma spp., y Dermacentor spp.;
cheyletidae tales como Cheyletiella yasguri, y Cheyletiella blakei;
demodicidae tales como Demodex canis, Demodex cati;
psoroptidae tales como Psoroptes ovis; y
sarcoptidae tales como Sarcoptes scabiei, Notoedres cati, y Knemidocoptes spp.
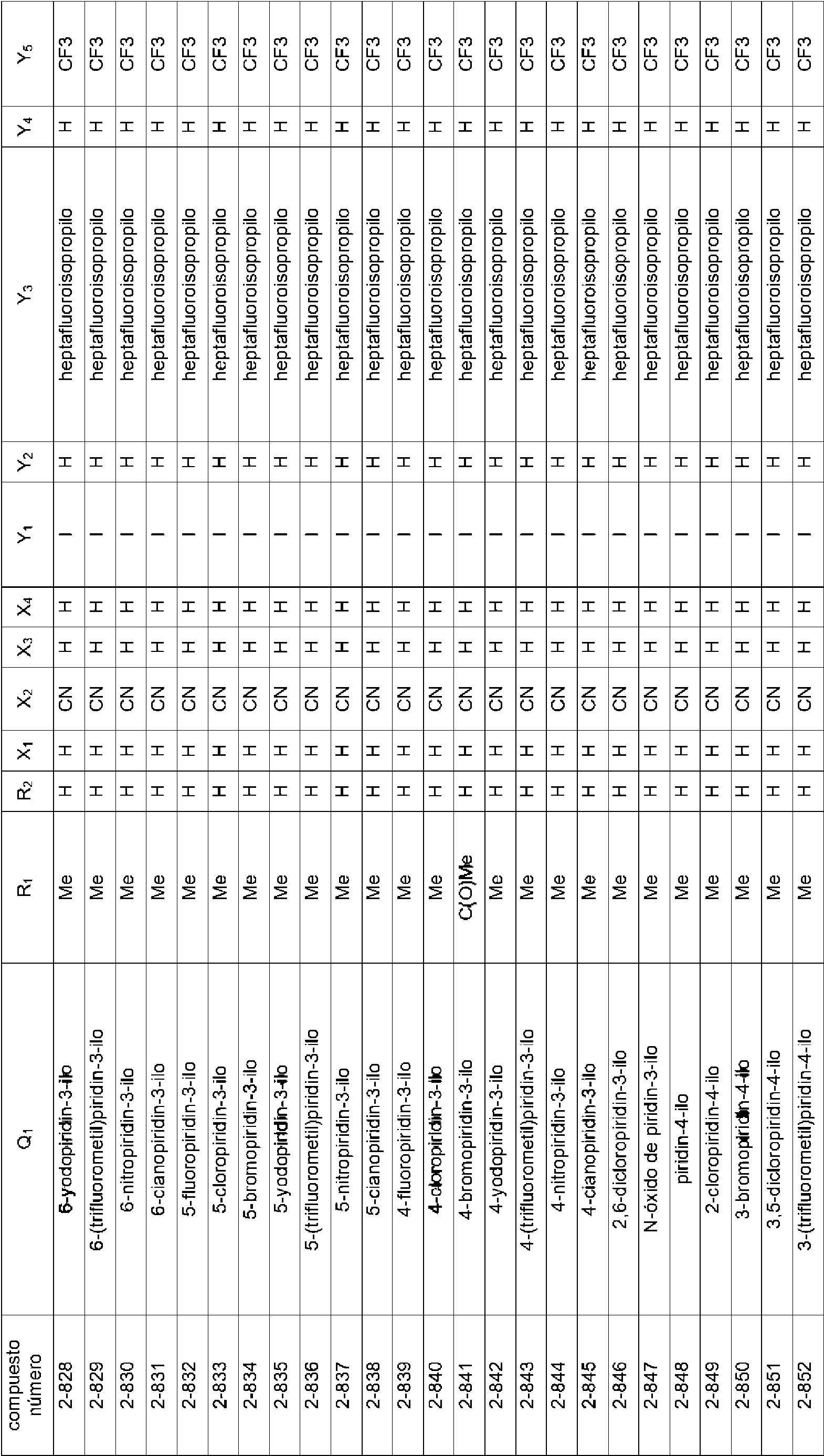
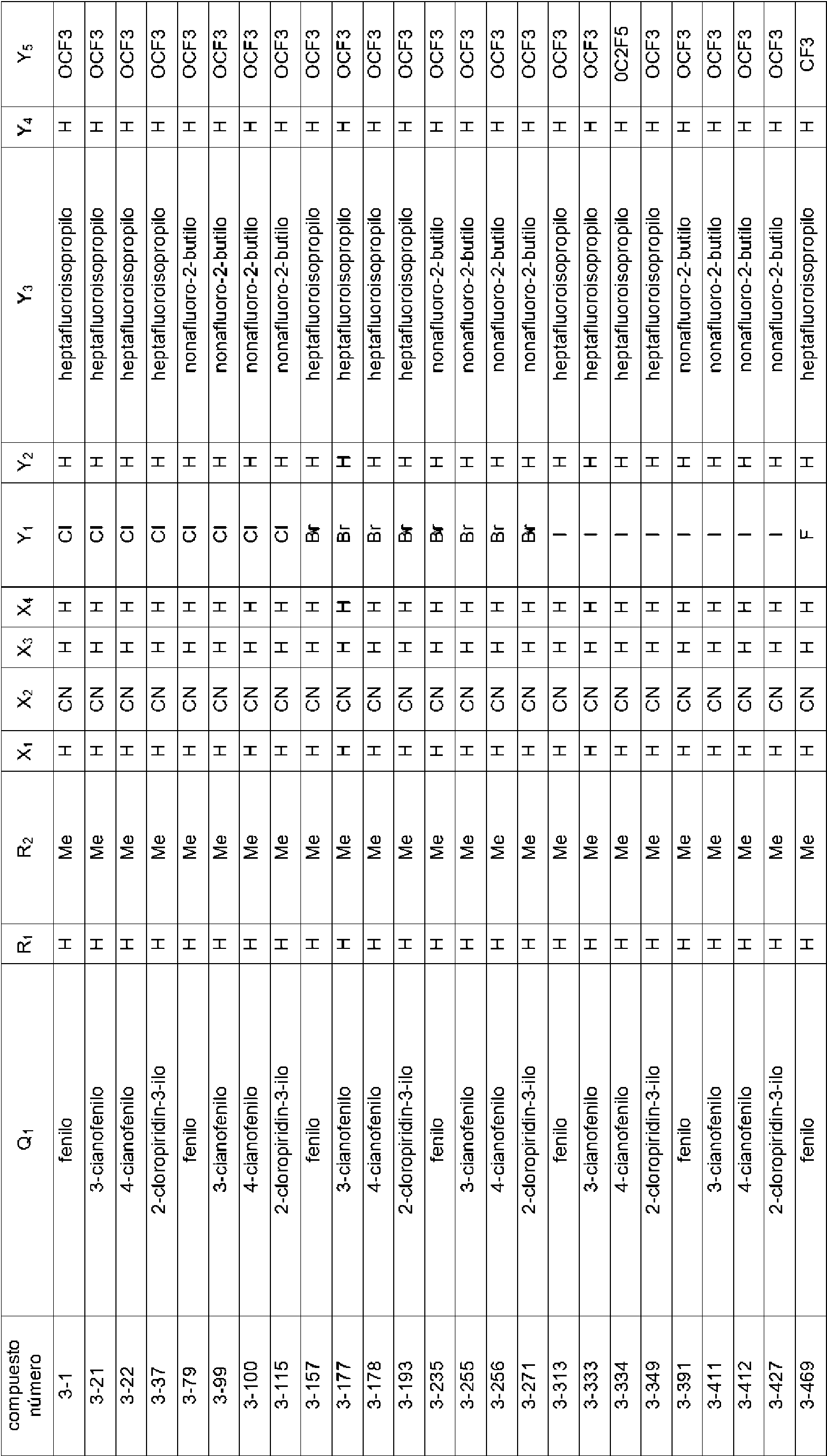
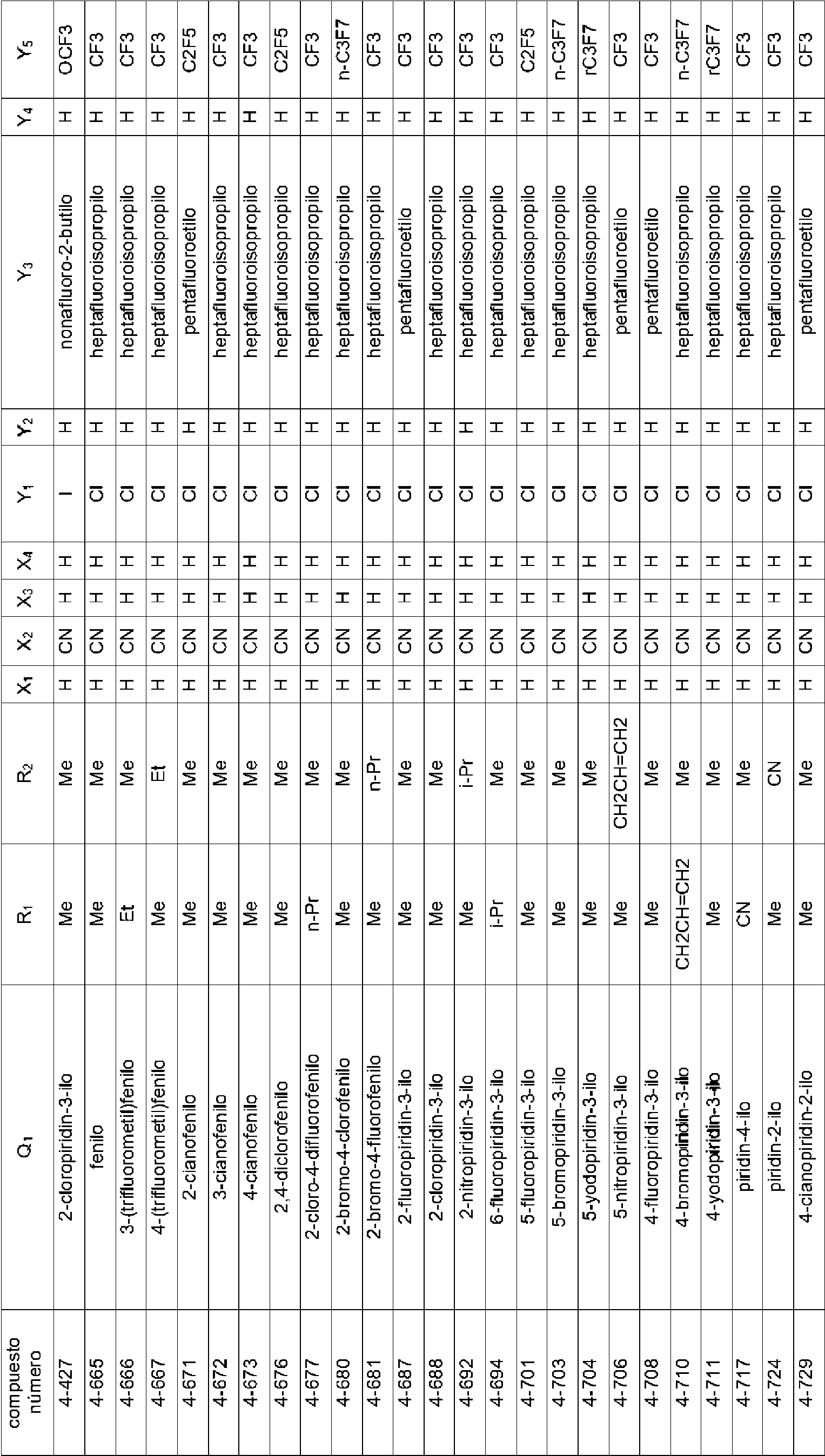
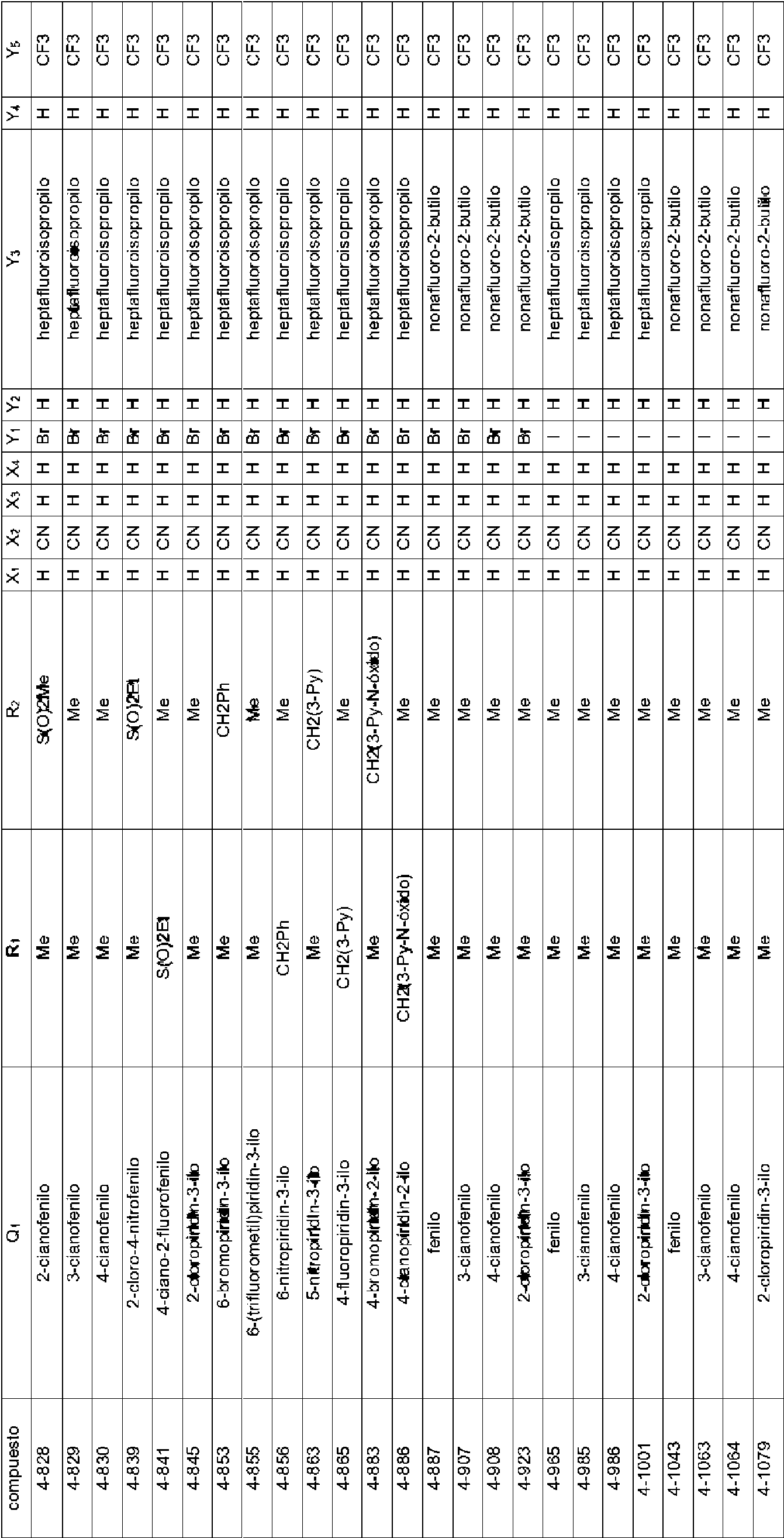
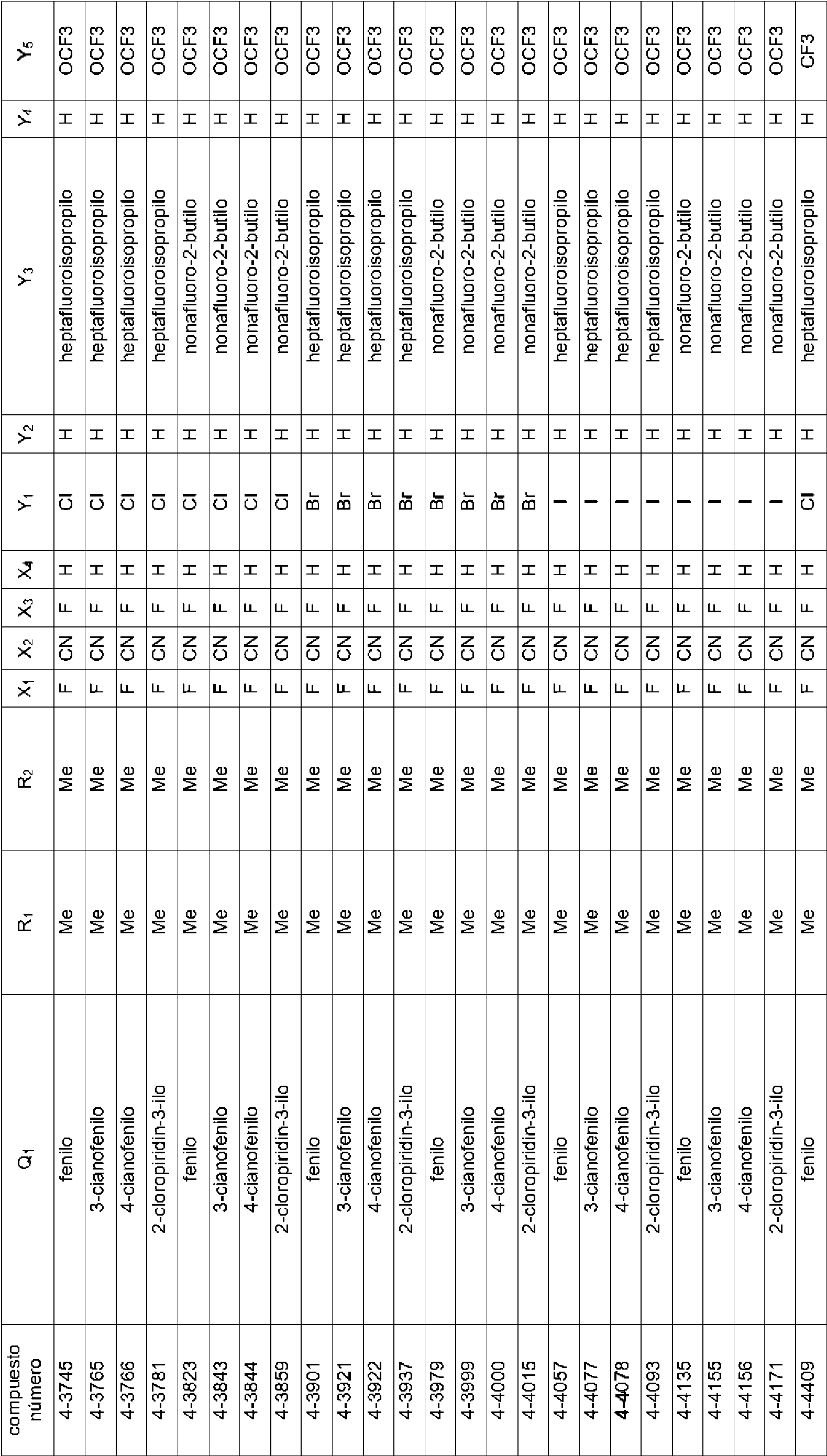
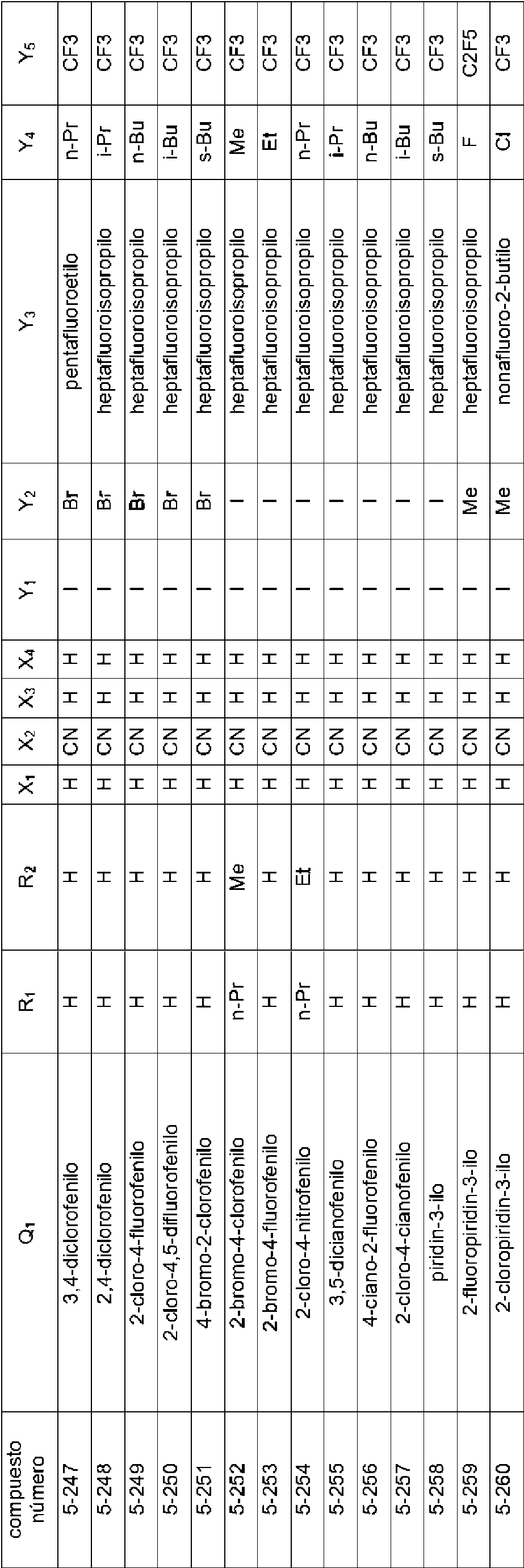
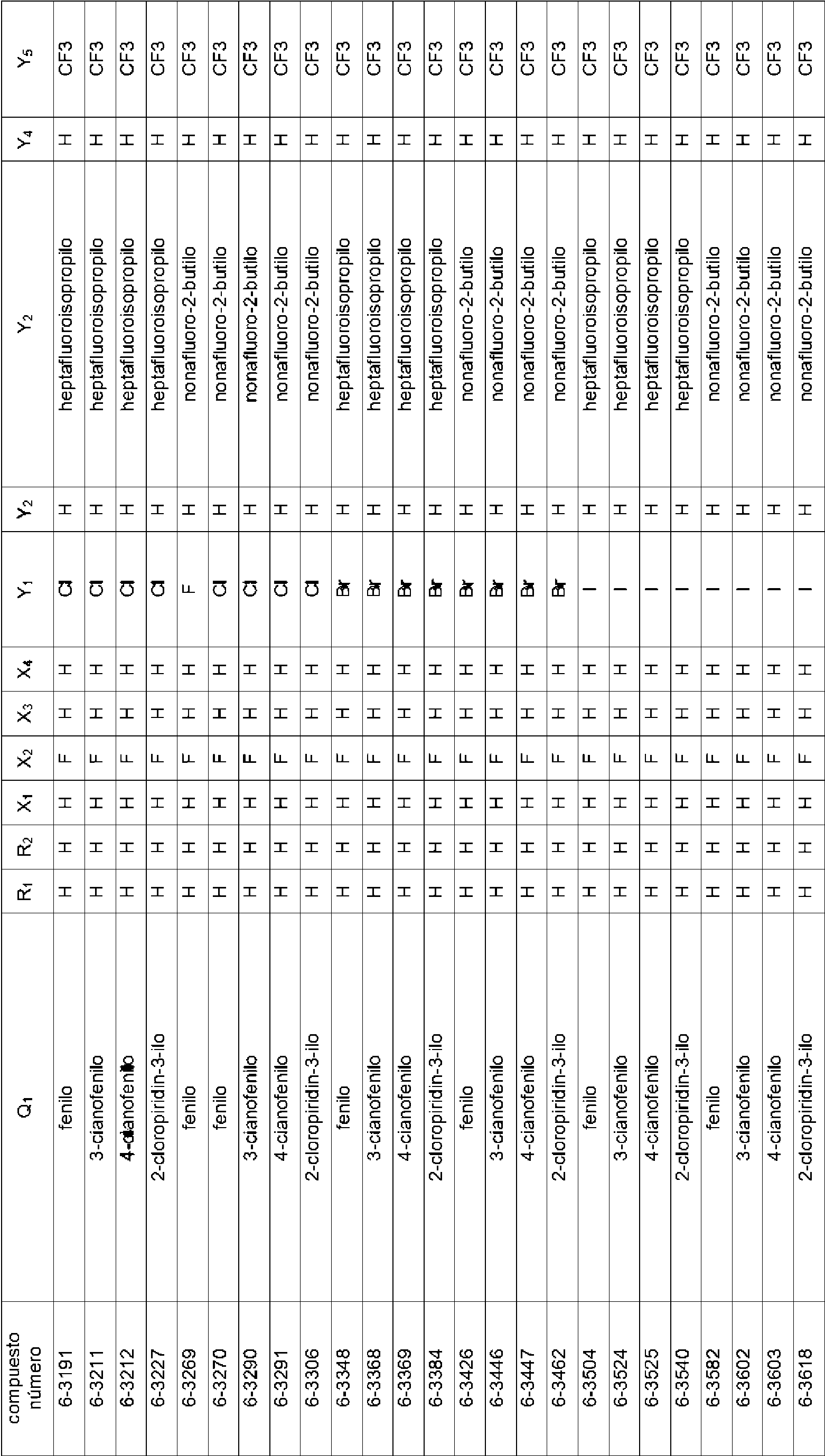
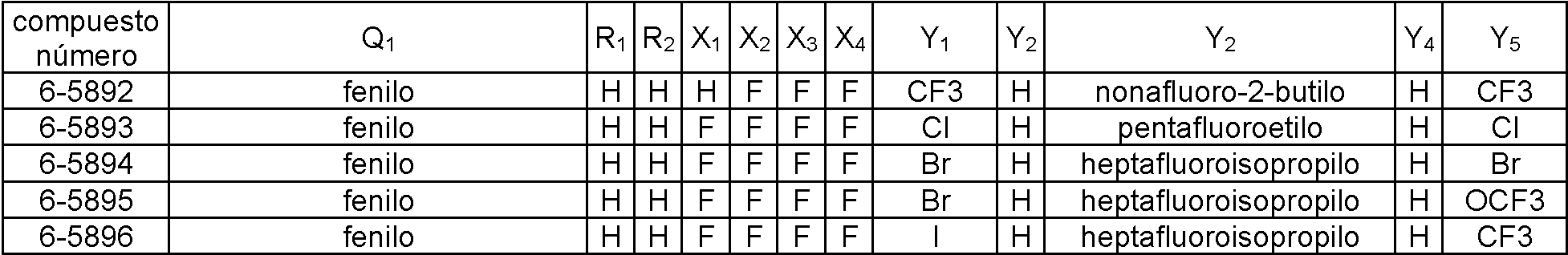
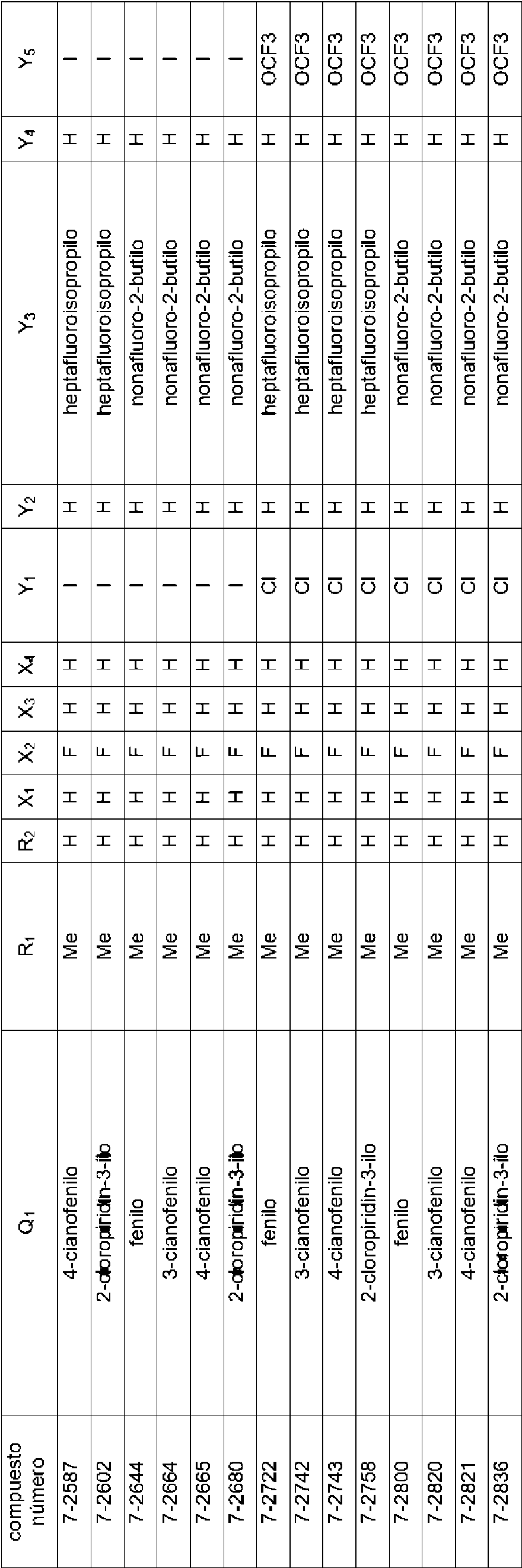
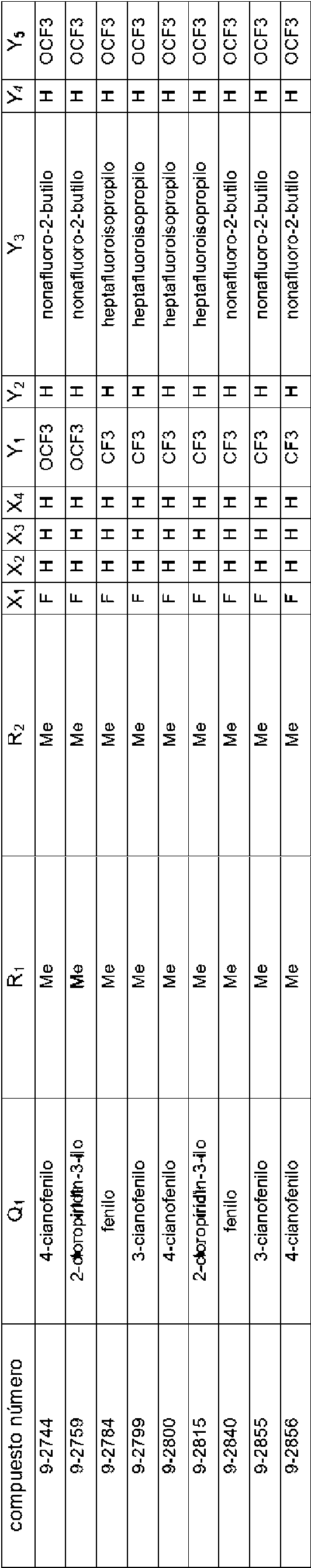
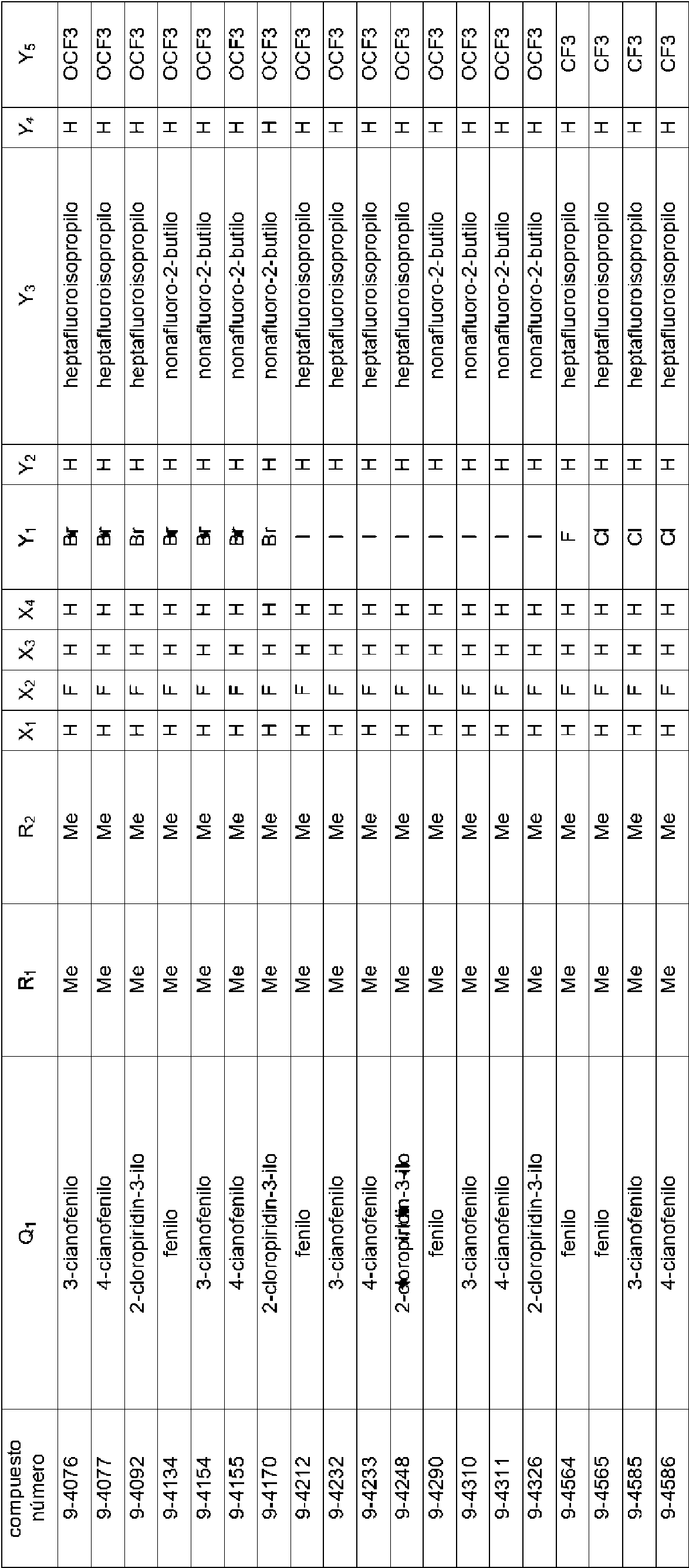
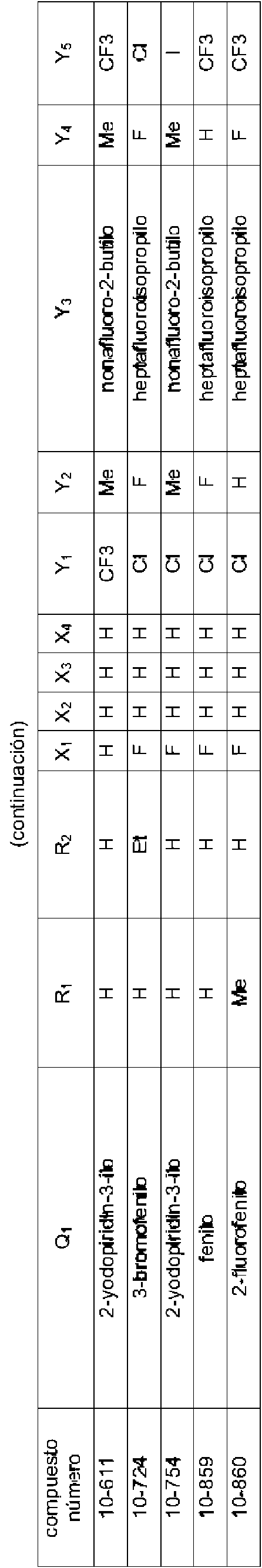
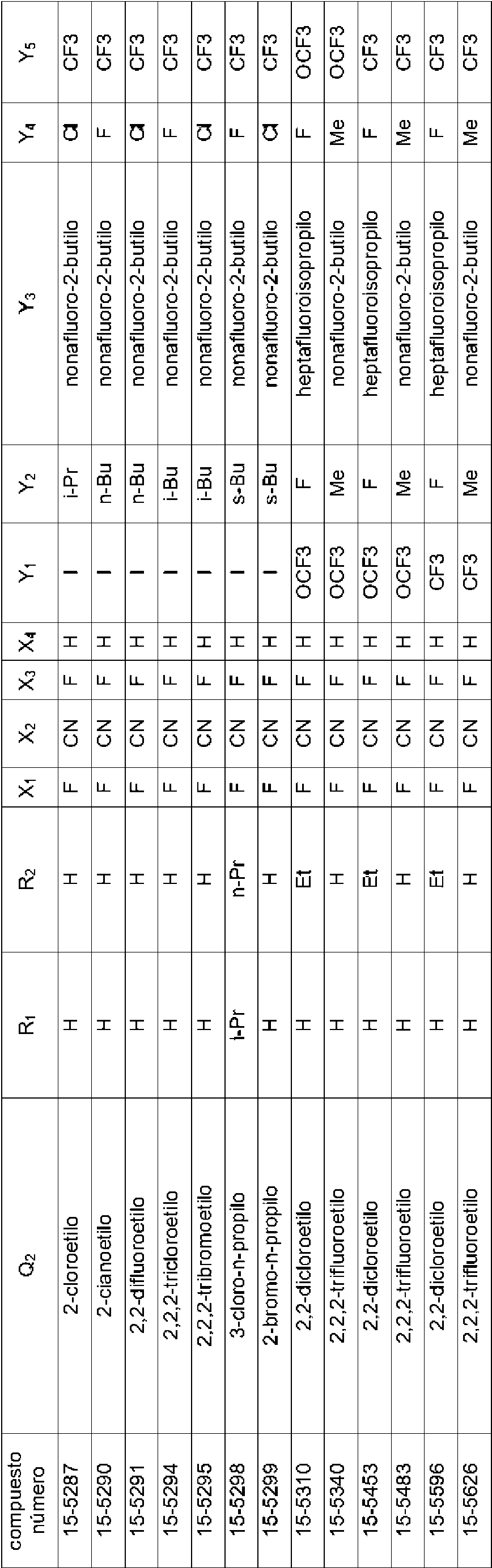
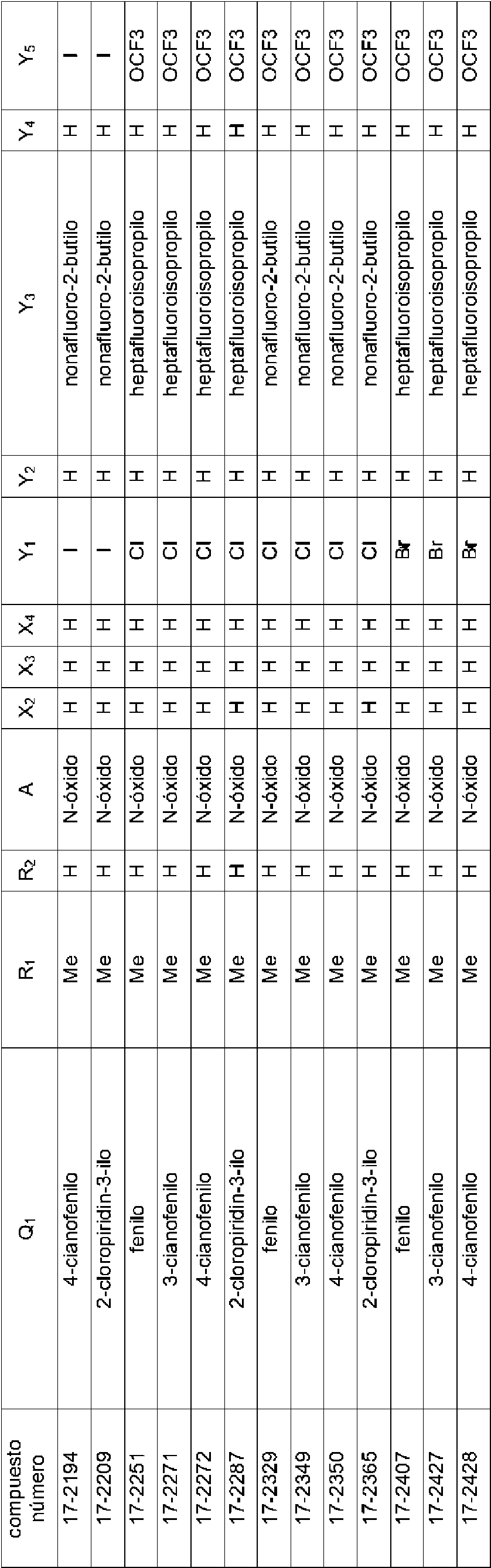
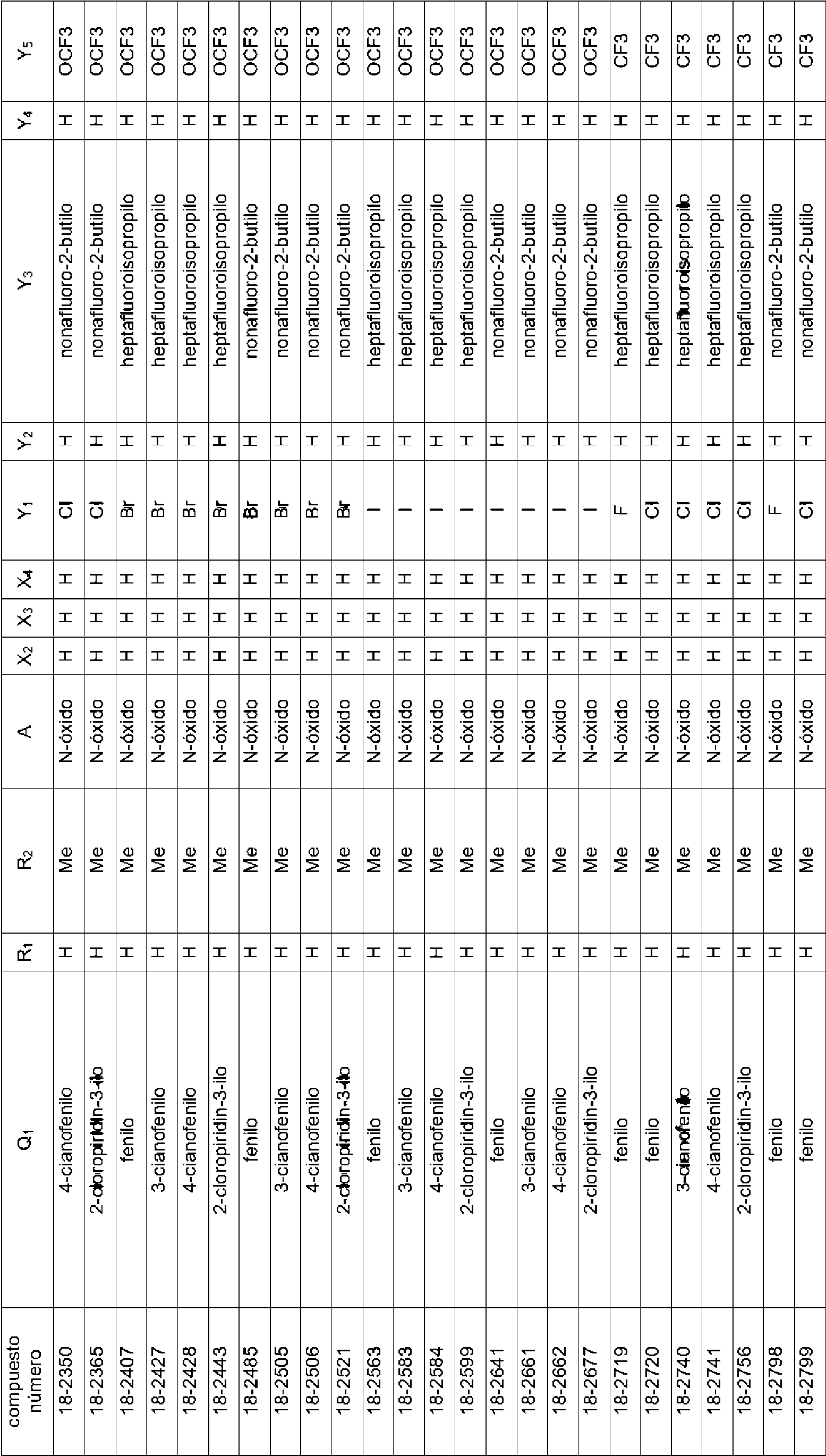
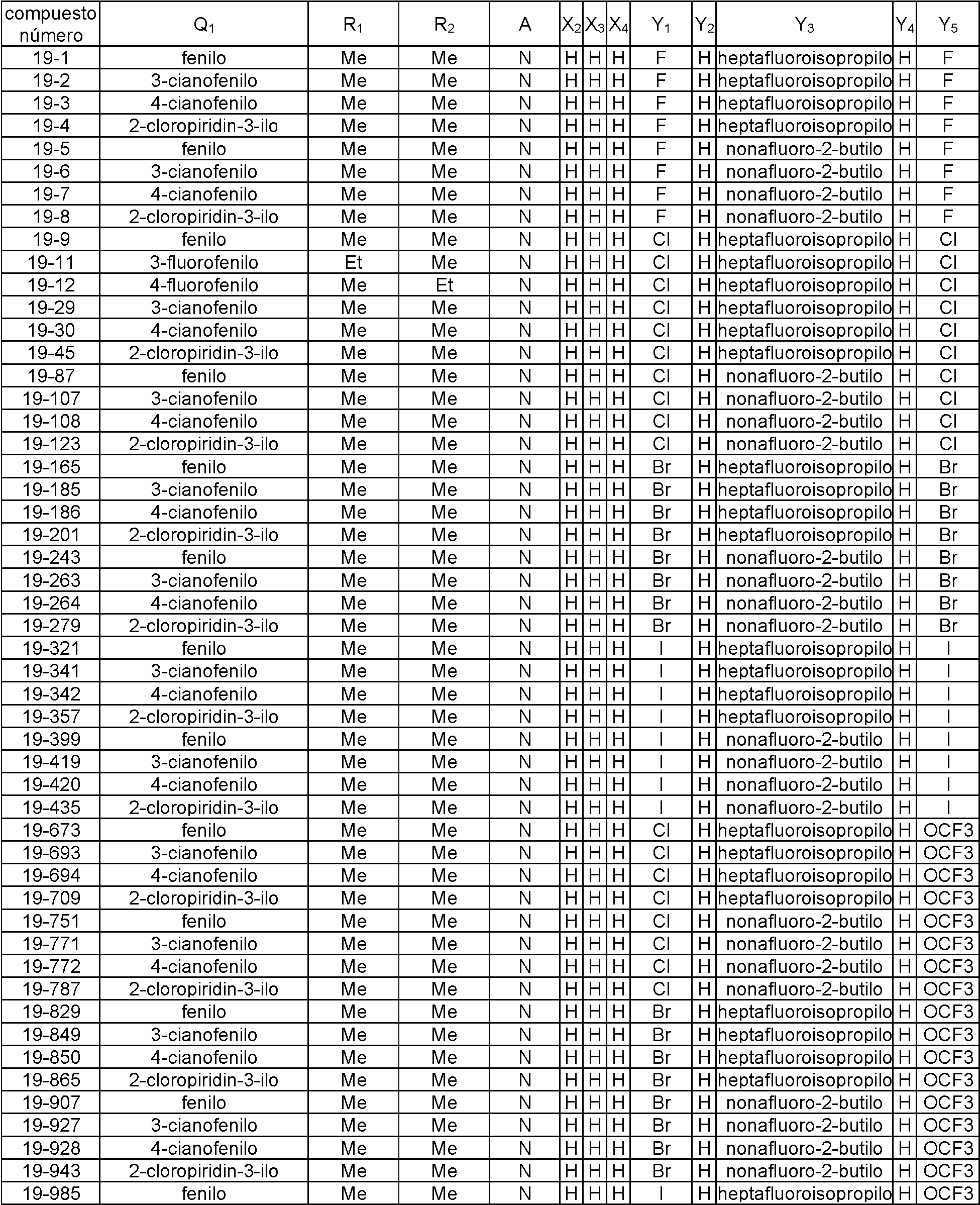
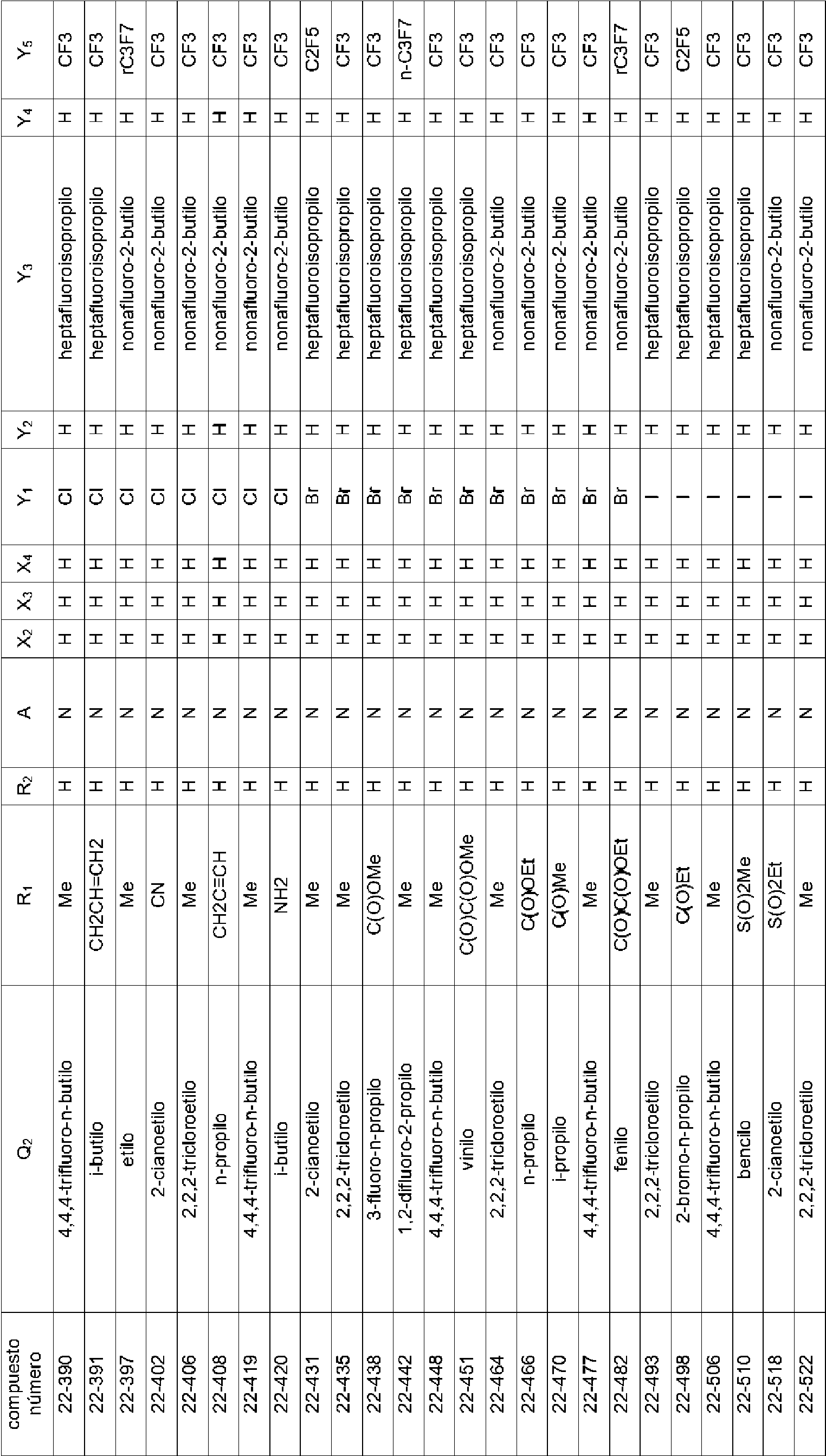
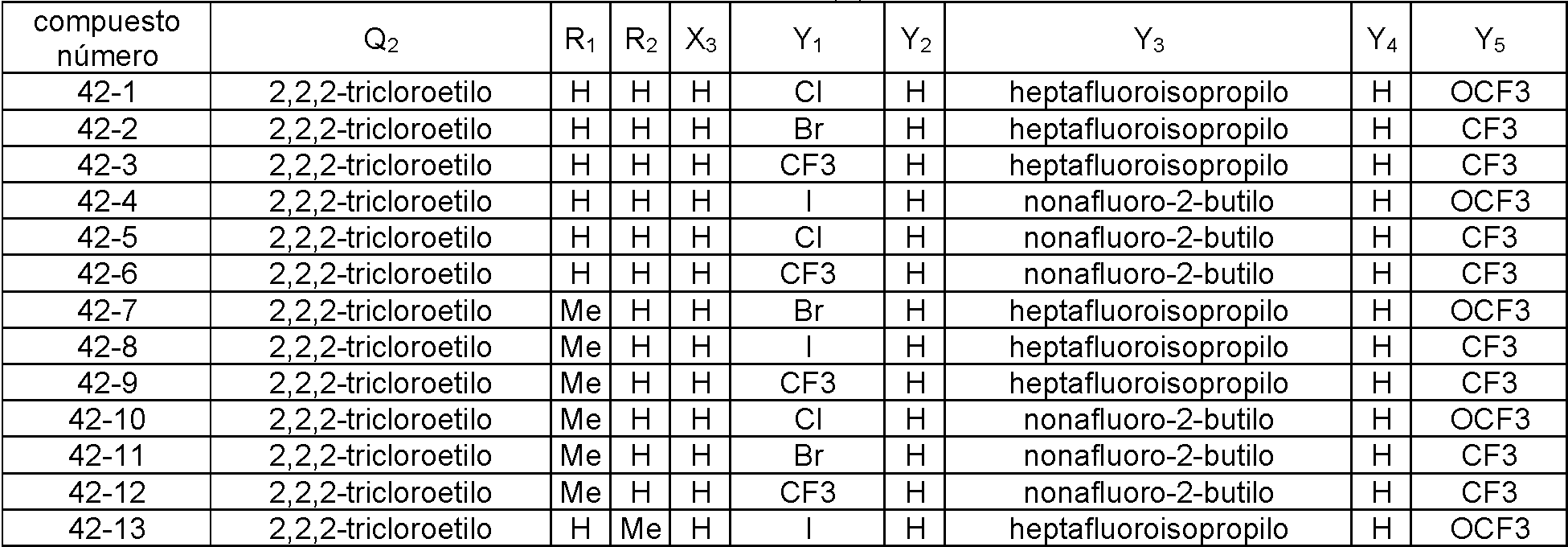
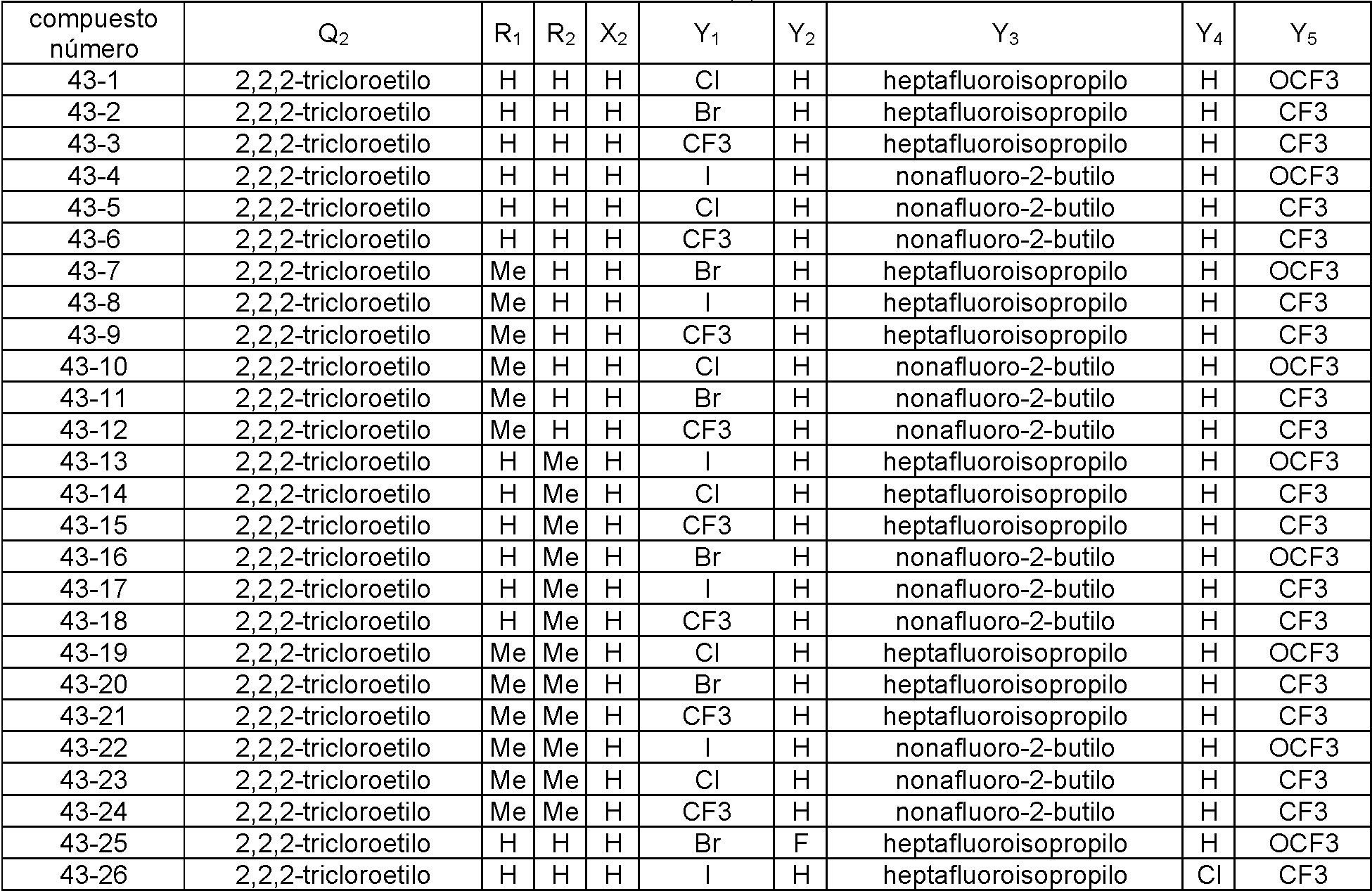
En la Fórmula (8), Qi puede representar un grupo fenilo, un grupo 2-fluorofenilo, un grupo 3-fluorofenilo, un grupo 4-fluorofenilo, un grupo 2-clorofenilo, un grupo 3-clorofenilo, un grupo 4-clorofenilo, un grupo 2-bromofenilo, un grupo 3-bromofenilo, un grupo 4-bromofenilo, un grupo 2-yodofenilo, un grupo 3-yodofenilo, un grupo 4-yodofenilo, un grupo (2-trifluorometil)fenilo, un grupo (3-trifluorometil)fenilo, un grupo (4-trifluorometil)fenilo, un grupo 2-nitrofenilo, un grupo 3-nitrofenilo, un grupo 4-nitrofenilo, un grupo 2-cianofenilo, un grupo 3-cianofenilo, un grupo 4-cianofenilo, un grupo 2,6-difluorofenilo, un grupo 3,4-diclorofenilo, un grupo 2,4-diclorofenilo, un grupo 2-cloro-4-fluorofenilo, un grupo 4-bromo-2-clorofenilo, un grupo 2-bromo-4-clorofenilo, un grupo 2-bromo-4-fluorofenilo, un grupo 2-cloro-4-nitrofenilo, un grupo 3,5-dicianofenilo, un grupo 4-ciano-2-fluorofenilo, un grupo 2-cloro-4-cianofenilo, un grupo piridin-3-ilo, un grupo 2-fluoropiridin-3-ilo, un grupo 2-cloropiridin-3-ilo, un grupo 2-bromopiridin-3-ilo, un grupo 2-yodopyodin-3-ilo, un grupo 2-(trifluorometil)piridin-3-ilo, un grupo 2-nitropiridin-3-ilo, un grupo 2-cianopiridin-3-ilo, un grupo 6-fluoropiridin-3-ilo, un grupo 6-cloropiridin-3-ilo, un grupo 6-bromopiridin-3-ilo, un grupo 6-yodopiridin-3-ilo, un grupo 6-(trifluorometil)piridin-3-ilo, un grupo 6-nitoropiridin-3-ilo, un grupo 6-cianopiridin-3-ilo, un grupo 5-fluoropiridin-3-ilo, un grupo 5-cloropiridin-3-ilo, un grupo 5-bromopiridin-3-ilo, un grupo 5-yodopiridin-3-ilo, un grupo 5-(trifluorometil)piridin-3-ilo, un grupo 5-nitropiridin-3-ilo, un grupo 5-cianopiridin-3-ilo, un grupo 4-fluoropiridin-3-ilo, un grupo 4-cloropiridin-3-ilo, un grupo 4-bromopiridin-3-ilo, un grupo 4-yodopiridin-3-ilo, un grupo 4-(trifluorometil)piridin-3-ilo, un grupo 4-nitropiridin-3-ilo, un grupo 4-cianopiridin-3-ilo, un grupo 2,6-dicloropiridin-3-ilo, un grupo piridin-4-ilo, un grupo 2-cloropiridin-4-ilo, un grupo 3-bromopiridin-4-ilo, un grupo 3,5-dicloropiridin-4-ilo, un grupo 3-(trifluorometil)piridina4-ilo, un grupo 2,6-dicianopiridin-4-ilo, un grupo piridin-2-ilo, un grupo 3-cloropiridin-2-ilo, un grupo 4-bromopiridin-2-ilo, un grupo 5-yodopiridin-2-ilo, un grupo 6-cloropiridin-2-ilo o un grupo 4-cianopiridin-2-ilo.
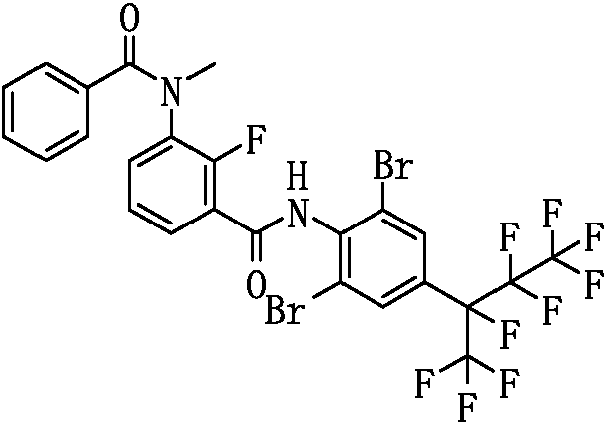
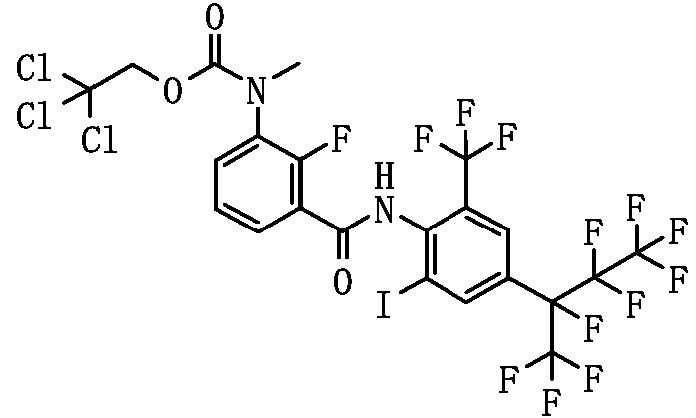
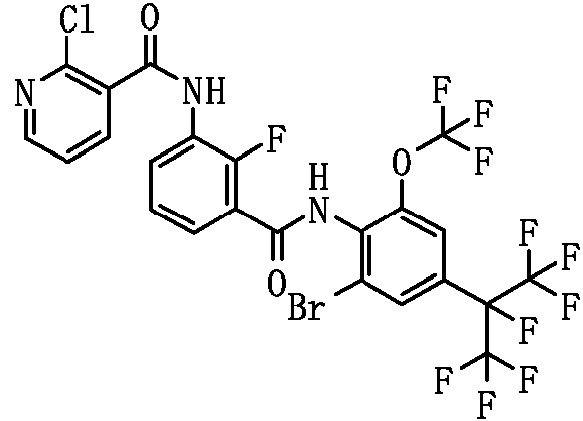
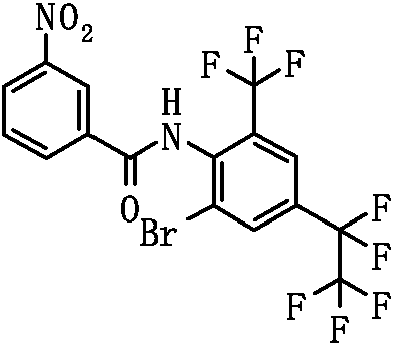
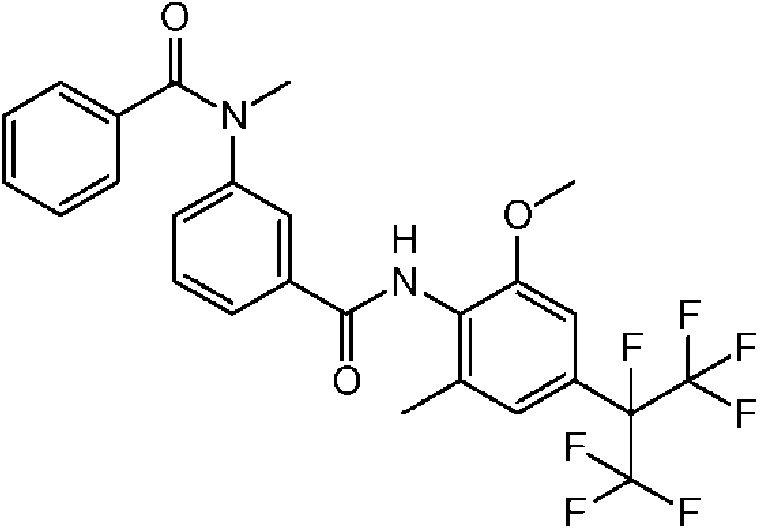
El compuesto representado por la Fórmula (8) puede ser 3-benzamido-N-(2-bromo-6-cloro-4-(perfluoropropan-2-il)fenil)-2-fluorobenzamida, 2-cloro-N-(3-(2,6-dibromo-4-(perfluoropropan-2-il)fenilcarbamoil)-2-fluorofenil)nicotinamida, 3-(4-ciano-N-metilbenzamido)-N-(2,6-dibromo-4-(perfluoropropan-2-il)fenil)-2-fluorobenzamida, 2-cloro-N-(3-(2,6-dibromo-4-(perfluoropropan-2-il)fenilcarbamoil)-2-fluorofenil)-N-metilnicotinamida, 3-benzamido-N-(2,6-diyodo-4-(perfluoropropan-2-il)fenil)-2-fluorobenzamida, 3-benzamido-N-(2,6-dibromo-4-(perfluoropropan-2-il)fenil)-2-fluorobenzamida, N-(2,6-dibromo-4-(perfluoropropan-2-il)fenil)-2-fluoro-3-(N-metilbenzamido)benzamida, 6-cloro-N-(3-(2,6-dibromo-4-(perfluoropropan-2-il)fenilcarbamoil)-2-fluorofenil)-N-metilnicotinamida, 3-(3-ciano-N-metilbenzamido)-N-(2,6-dibromo-4-(perfluoropropan-2-il)fenil)-2-fluorobenzamida, N-(2,6-dicloro-4-(perfluoropropan-2-il)fenil)-2-fluoro-3-(N-metilbenzamido)benzamida, 3-(4-ciano-N-metilbenzamido)-N-(2,6-dicloro-4-(perfluoropropan-2-il)fenil)-2-fluorobenzamida, 2-cloro-N-(3-(2,6-dicloro-4-(perfluoropropan-2-il)fenilcarbamoil)-2-fluorofenil)-N-metilnicotinamida, N-(2,6-diyodo-4-(perfluoropropan-2-il)fenil)-2-fluoro-3-(N-metilbenzamido)benzamida, 3-(4-ciano-N-metilbenzamido)-N-(2,6-diyodo-4-(perfluoropropan-2-il)fenil)-2-fluorobenzamida, 3- benzamido-N-(2,6-dibromo-4-(perfluorobutan-2-il)fenil)-2-fluorobenzamida, N-(2,6-diyodo-4-(perfluoropropan-2-il)fenil)-2-fluoro-3-(2-fluorobenzamido)benzamida, N-(2,6-diyodo-4-(perfluoropropan-2-il)fenil)-2-fluoro-3-(4-fluorobenzamido)benzamida, 3-(2,6-difluorobenzamido)-N-(2,6-diyodo-4-(perfluoropropan-2-il)fenil)-2-fluorobenzamida, N-(2-bromo-6-yodo-4-(perfluoropropan-2-il)fenil)-2-fluoro-3-(N-metilbenzamido)benzamida, N-(3-(2-bromo-6-yodo-4-(perfluoropropan-2-il)fenilcarbamoil)-2-fluorofenil)-2-cloro-N-metilnicotinamida, 3-(4-cianobenzamido)-N-(2,6-dibromo-4-(perfluorobutan-2-il)fenil)-2-fluorobenzamida, 3-(3-cianobenzamido)-N-(2,6-dibromo-4-(perfluorobutan-2-il)fenil)-2-fluorobenzamida, N-(2,6-dibromo-4-(perfluorobutan-2-il)fenil)-2-fluoro-3-(N-metilbenzamido)benzamida, 3-(4-ciano-N-metilbenzamido)-N-(2,6-dibromo-4-(perfluorobutan-2-il)fenil)-2-fluorobenzamida, 3-(3-ciano-N-metilbenzamido)-N-(2,6-dibromo-4-(perfluorobutan-2-il)fenil)-2-fluorobenzamida, 6-cloro-N-(3-(2,6-dibromo-4-(perfluorobutan-2-il)fenilcarbamoil)-2-fluorofenil)-N-metilnicotinamida, 3-benzamido-N-(2,6-diyodo-4- (perfluorobutan-2-il)fenil)-2-fluorobenzamida, 3-(3-cianobenzamido)-N-(2,6-diyodo-4-(perfluorobutan-2-il)fenil)-2-fluorobenzamida, 3-(4-cianobenzamido)-N-(2,6-diyodo-4-(perfluorobutan-2-il)fenil)-2-fluorobenzamida, N-(2,6-diyodo-4-(perfluorobutan-2-il)fenil)-2-fluoro-3-(N-metilbenzamido)benzamida, 3-(3-ciano-N-metilbenzamido)-N-(2,6-diyodo-4-(perfluorobutan-2-il)fenil)-2-fluorobenzamida, 3-(4-ciano-N-metilbenzamido)-N-(2,6-diyodo-4-(perfluorobutan-2-il)fenil)-2-fluorobenzamida, 3-benzamido-N-(2,6-diyodo-4-(perfluorobutan-2-il)fenil)benzamida, 2-cloro-N-(3-(2,6-diyodo-4-(perfluorobutan-2-il)fenilcarbamoil)fenil)nicotinamida, 6-cloro-N-(3-(2,6-diyodo-4-(perfluorobutan-2-il)fenilcarbamoil)fenil)nicotinamida, 3-ciano-N-(3-(2,6-diyodo-4-(perfluorobutan-2-il)fenilcarbamoil)fenil)benzamida, 3-(4-cianobenzamido)-N-(2,6-diyodo-4-(perfluorobutan-2-il)fenil)benzamida, N-(3-(2,6-diyodo-4-(perfluorobutan-2-il)fenilcarbamoil)fenil)-2-fluorobenzamida, N-(2,6-diyodo-4-(perfluorobutan-2-il)fenil)-3-(3-fluorobenzamido)benzamida, N-(2,6-diyodo-4-(perfluorobutan-2-il)fenil)-3-(4-fluorobenzamido)benzamida, N-(3-(2,6-diyodo-4-(perfluorobutan-2-il)fenilcarbamoil)fenil)-2,6-difluorobenzamida, N-(3-(2,6-diyodo-4-(perfluorobutan-2-il)fenilcarbamoil)fenil)-N-metilbenzamida, 2-cloro-N-(3-(2,6-diyodo-4-(perfluorobutan-2-il)fenilcarbamoil)fenil)-N-metilnicotinamida, 6-cloro-N-(3-(2,6-diyodo-4-(perfluorobutan-2-il)fenilcarbamoil)fenil)-N-metilnicotinamida, 3-ciano-N-(3-(2,6-diyodo-4-(perfluorobutan-2-il)fenilcarbamoil)fenil)-N-metilbenzamida, 4-ciano-N-(3-(2,6-diyodo-4-(perfluorobutan-2-il)fenilcarbamoil)fenil)-N-metilbenzamida, N-(3-(2,6-diyodo-4-(perfluorobutan-2-il)fenilcarbamoil)fenil)-2-fluoro-N-metilbenzamida, N-(3-(2,6-diyodo-4-(perfborobutan-2-il)fenilcarbamoil)fenil)-3-fluoro-N-metilbenzamida, N-(3-(2,6-diyodo-4-(perfluorobutan-2-il)fenilcarbamoil)fenil)-4-fluoro-N-metilbenzamida, N-(3-(2,6-diyodo-4-(perfluorobutan-2-il)fenilcarbamoil)fenil)-2,6-difluoro-N-metilbenzamida, 2-cloro-N-(3-(2,6-diyodo-4-(perfluorobutan-2-il)fenilcarbamoil)-2-fluorofenil)nicotinamida, 6-cloro-N-(3-(2,6-diyodo-4-(perfluorobutan-2-il)fenilcarbamoil)-2-fluorofenil)nicotinamida, N-(2,6-diyodo-4-(perfluorobutan-2-il)fenil)-2-fluoro-3-(2-fluorobenzamido)benzamida, N-(2,6-diyodo-4-(perfluorobutan-2-il)fenil)-2-fboro-3-(3
fluorobenzamido)benzamida, N-(2,6-diyodo-4-(perfluorobutan-2-il)fenil)-2-fluoro-3-(4-fluorobenzamido)benzamida, 3-(2,6-difluorobenzamido)-N-(2,6-diyodo-4-(perfluorobutan-2-il)fenil)-2-fluorobenzamida, 3-benzamido-N-(2,6-dibromo-4-(perfluorobutan-2-il)fenil)benzamida, 6-doro-N-(3-(2,6-dibromo-4-(perfborobutan-2-il)fenilcarbamoil)fenil)nicotinamida, N-(3-(2,6-dibromo-4-(perfluorobutan-2-il)fenilcarbamoil)fenil)-2-fluorobenzamida, 2-doro-N-(3-(2,6-dibromo-4-(perfluorobutan-2-il)fenilcarbamoil)fenil)nicotinamida, N-(2,6-dibromo-4-(perfluorobutan-2-il)fenil)-3-(3-fluorobenzamido)benzamida, N-(2,6-dibromo-4-(perfluorobutan-2-il)fenil)-3-(4-fluorobenzamido)benzamida, N-(3-(2,6-dibromo-4-(perfluorobutan-2-il)fenilcarbamoil)fenil)-2,6-difluorobenzamida, 3-ciano-N-(3-(2,6-dibromo-4-(perfluorobutan-2-il)fenilcarbamoil)fenil)benzamida, 3-(4-danobenzamido)-N-(2,6-dibromo-4-(perfluorobutan-2-il)fenil)benzamida, 2-doro-N-(3-(2,6-diyodo-4-(perfborobutan-2-il)fenilcarbamoil)-2-fluorofenil)-N-metilnicotinamida, 6-doro-N-(3-(2,6-diyodo-4-(perfluorobutan-2-il)fenilcarbamoil)-2-fluorofenil)-N-metilnicotinamida, N-(3-(2,6-diyodo-4-(perfborobutan-2-il)fenilcarbamoil)-2-fluorofenil)-2-fluoro-N-metilbenzamida, N-(2,6-diyodo-4-(perfluorobutan-2-il)fenil)-2-fluoro-3-(3-fluoro-N-metilbenzamido)benzamida, N-(2,6-diyodo-4-(perfluorobutan-2-il)fenil)-2-fluoro-3-(4-fluoro-N-metilbenzamido)benzamida, N-(3-(2,6-diyodo-4-(perfluorobutan-2-il)fenilcarbamoil)-2-fluorofenil)-2,6-difluoro-N-metilbenzamida, N-(3-(2,6-dibromo-4-(perfluorobutan-2-il)fenilcarbamoil)fenil)-N-iTietilbenzamida, 2-doro-N-(3-(2,6-dibromo-4-(perfluorobutan-2-il)fenilcarbamoil)fenil)-N-metilnicotinamida, 6-cloro-N-(3-(2,6-dibromo-4-(perfluorobutan-2-il)fenilcarbamoil)fenil)-N-metilnicotinamida, 3-dano-N-(3-(2,6-dibromo-4-(perfborobutan-2-il)fenilcarbamoil)fenil)-N-metilbenzamida, 4-dano-N-(3-(2,6-dibromo-4-(perfluorobutan-2-il)fenilcarbamoil)fenil)-N-metilbenzamida, N-(3-(2,6-dibromo-4-(perfluorobutan-2-il)fenilcarbamoil)fenil)-2-fluoro-N-iTietilbenzamida, N-(3-(2,6-dibromo-4-(perfluorobutan-2-il)fenilcarbamoil)fenil)-3-fluoro-N-metilbenzamida, N-(3-(2,6-dibromo-4-(perfluorobutan-2-il)fenilcarbamoil)fenil)-4-fluoro-N-metilbenzamida, N-(3-(2,6-dibromo-4-(perfluorobutan-2-il)fenilcarbamoil)fenil)-2,6-difluoro-N-metilbenzamida, 2-doro-N-(3-(2,6-dibromo-4-(perfluorobutan-2-il)fenilcarbamoil)-2-fluorofenil)nicotinamida, 6-doro-N-(3-(2,6-dibromo-4-(perfluorobutan-2-il)fenilcarbamoil)-2-fluorofenil)nicotinamida, N-(2,6-dibromo-4-(perfluorobutan-2-il)fenil)-2-fluoro-3-(2-fluorobenzamido)benzamida, N-(2,6-dibromo-4-(perfluorobutan-2-il)fenil)-2-fluoro-3-(3-fluorobenzamido)benzamida, N-(2,6-dibromo-4-(perfluorobutan-2-il)fenil)-2-fluoro-3-(4-fluorobenzamido)benzamida, N-(2,6-dibromo-4-(perfluorobutan-2-il)fenil)-3-(2,6-difluorobenzamido)-2-fluorobenzamida, 2-doro-N-(3-(2,6-diyodo-4-(perfluoropropan-2-il)fenilcarbamoil)-2-fluorofenil)nicotinamida, 6-cloro-N-(3-(2,6-diyodo-4-(perfluoropropan-2-il)fenilcarbamoil)-2-fluorofenil)nicotinamida, 3-(3-cianobenzamido)-N-(2,6-diyodo-4-(perfluoropropan-2-il)fenil)-2-fluorobenzamida, 3-(4-cianobenzamido)-N-(2,6-diyodo-4-(perfluoropropan-2-il)fenil)-2-fluorobenzamida, N-(2,6-diyodo-4-(perfluoropropan-2-il)fenil)-2-fluoro-3-(3-fluorobenzamido)benzamida, 2-doro-N-(3-(2,6-dibromo-4-(perfluorobutan-2-il)fenilcarbamoil)-2-fluorofenil)-N-iTietilnicotinamida, N-(3-(2,6-dibromo-4-(perfluorobutan-2-il)fenilcarbamoil)-2-fluorofenil)-2-fluoro-N-metilbenzamida, N-(2,6-dibromo-4-(perfluorobutan-2-il)fenil)-2-fluoro-3-(3-fluoro-N-metilbenzamido)benzamida, N-(2,6-dibromo-4-(perfluorobutan-2-il)fenil)-2-fluoro-3-(4-fluoro-N-metilbenzaiTiido)benzaiTiida, N-(3-(2,6-dibromo-4-(perfluorobutan-2-il)fenilcarbamoil)-2-fluorofenil)-2,6-difluoro-N-metilbenzamida, 3-(3-dano-N-metilbenzamido)-N-(2,6-diyodo-4-(perfluoropropan-2-il)fenil)-2-fluorobenzamida, N-(3-(2,6-diyodo-4-(perfluoropropan-2-il)fenilcarbamoil)-2-fluorofenil)-2-fluoro-N-metilbenzamida, N-(2,6-diyodo-4-(perfluoropropan-2-il)fenil)-2-fluoro-3-(3-fluoro-N-metilbenzamido)benzamida, 6-doro-N-(3-(2,6-diyodo-4-(perfluoropropan-2-il)fenilcarbamoil)-2-fluorofenil)-N-iTietilnicotinamida, N-(2,6-diyodo-4-(perfluoropropan-2-il)fenil)-2-fluoro-3-(4-fluoro-N-metilbenzamido)benzamida, N-(3-(2,6-diyodo-4-(perfluoropropan-2-il)fenilcarbamoil)-2-fluorofenil)-2,6-difluoro-N-metilbenzamida, N-(2,6-dibromo-4-(perfluoropropan-2-il)fenil)-2-fluoro-3-(2-fluorobenzamido)benzamida, N-(2,6-dibromo-4-(perfluoropropan-2-il)fenil)-2-fluoro-3-(3-fluorobenzamido)benzamida, N-(2,6-dibromo-4-(perfluoropropan-2-il)fenil)-2-fluoro-3-(4-fluorobenzamido)benzamida, N-(2,6-dibromo-4-(perfluoropropan-2-il)fenil)-3-(2,6-difluorobenzamido)-2-fluorobenzamida, 6-cloro-N-(3-(2,6-dibromo-4-(perfluoropropan-2-il)fenilcarbamoil)-2-fluorofenil)nicotinamida, 3-(3-cianobenzamido)-N-(2,6-dibromo-4-(perfluoropropan-2-il)fenil)-2-fluorobenzamida, 3-(4-cianobenzamido)-N-(2,6-dibromo-4-(perfluoropropan-2-il)fenil)-2-fluorobenzamida, 2-doro-N-(3-(2,6-diyodo-4-(perfluoropropan-2-il)fenilcarbamoil)-2-fluorofenil)-N-metilnicotinamida, N-(3-(2,6-dibromo-4-(perfluoropropan-2-il)fenilcarbamoil)-2-fluorofenil)-2-fluoro-N-metilbenzamida, N-(2,6-dibromo-4-(perfluoropropan-2-il)fenil)-2-fluoro-3-(3-fluoro-N-metilbenzamido)benzamida, N-(2,6-dibromo-4-(perfluoropropan-2-il)fenil)-2-fluoro-3-(4-fluoro-N-metilbenzamido)benzamida, N-(3-(2,6-dibromo-4-(perfluoropropan-2-il)fenilcarbamoil)-2-fluorofenil)-2,6-difluoro-N-metilbenzamida, 3-benzamido-N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometoxi)fenil)-2-fluorobenzamida, N-(3-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometoxi)fenilcarbamoil)-2-fluorofenil)-2-cloronicotinamida, N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometoxi)fenil)-3-(4-cianobenzamido)-2-fluorobenzamida, 3-benzamido-N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)benzamida, N-(3-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-2-cloronicotinamida, N-(3-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluoromethil)fenilcarbamoil)fenil)-N-metilbenzamida, N-(3-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-2-cloro-N-metilnicotinamida, 3-benzamido-N-(2-cloro-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)benzamida, 2-cloro-N-(3-(2-cloro-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)nicotinamida, N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-3-(3-cianobenzamido)benzamida.
N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-3-(4-cianobenzamido)benzamida, N-(3-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-3-ciano-N-metilbenzamida, N-(3-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-4-ciano-N-metilbenzamida, N-(3-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-2-fluoro-N-metilnicotinamida, N-(3-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-N-metil-4-nitrobenzamida, N-(3-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-6-cloro-N-metilnicotinamida, N-(3-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-6-ciano-N-metilnicotinamida, N-(3-(2-bromo-3-(perfluoropropan-2-il)-6(trifluorometil)fenilcarbamoil)fenil)-N-metil-4-nitrobenzamida, N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-N-metil-3-(N-metilbenzamido)benzamida, N-(3-((2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)(metil)carbamoil)fenil)-2-doro-N-metilnicotinamida, 2-bromo-N-(3-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)nicotinamida, 2-doro-N-(3-(2-doro-4-(perfluoropropan-2-N)-6-(trifluorometil)fenilcarbamoil)fenil)-N-metilnicotinamida, N-(3-(2-doro-4-(perfluoropropan-2-N)-6-(trifluorometN)fenN-carbamoil)fenil)-4-ciano-N-metilbenzamida, 3-benzamido-N-(2-bromo-4-(perfluoropropan-2-N)-6-(trifluorometN)fenN)-4-fluorobenzamida, N-(5-(2-bromo-4-(perfluoropropan-2-N)-6-(trifluorometN)fenNcarbamoN)-2-fluorofenN)-2-doronicotinamida, N-(3-((2-bromo-4-(perfluoropropan-2-N)-6-(trifluorometN)fenNXmetN)carbamoN)fenN)-2-doronicotinamida, N-(2-bromo-4-(perfluoropropan-2-N)-6-(trifluorometN)fenN)-4-fluoro-3-(N-metN-benzamido)benzamida, N-(2-bromo-4-(perfluoropropan-2-N)-6-(trifluorometN)fenN)-3-(4-dano-N-metNbenzamido)-4-fluorobenzamida, N-(5-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)-2-fluorofenil)-2-cloro-N-metilnicotinamida, 3-benzamido-N-(4-(perfluoropropan-2-il)-2,6-bis(trifluorometil)fenil)benzamida, 2-cloro-N-(3-(4-(perfluoropropan-2-il)-2,6-bis(trifluorometil)fenilcarbamoil)fenil)nicotinamida, N-metil-N-(3-(4-(perfluoropropan-2-il)-2,6-bis(trifluorometil)fenilcarbamoil)fenil)benzamida, 2-doro-N-metN-N-(3-(4-(perfluoropropan-2-il)-2,6-bis(trifluorometil)fenilcarbamoil)fenil)nicotinamida, 3-benzamido-N-(2-bromo-4-(perfluoropropan-2-N)-6-(trifluorometil)fenil)-N-metilbenzamida, N-(2-bromo-4-(perfluoropropan-2-N)-6-(trifluorometN)fenN)-3-(3-cianobenzamido)-N-metilbenzamida, N-(2-bromo-4-(perfluoropropan-2-N)-6-(trifluorometN)fenN)-3-(4-cianobenzamido)-N-metilbenzamida, N-(2-bromo-4-(perfluoropropan-2-N)-6-(trifluorometN)fenN)-3-(3-dano-N-metN-benzamido)-N-metilbenzamida, N-(2-bromo-4-(perfluoropropan-2-N)-6-(trifluorometN)fenN)-3-(4-dano-N-metN-benzamido)-N-metilbenzamida, 2-bromo-N-(3-(2-bromo-4-(perfluoropropan-2-N)-6-(trifluorometN)fenNcarbamoN)fenN)-N-metilnicotinamida, 3-benzamido-N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-2-fluorobenzamida, 2-bromo-N-(3-((2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)(metil)carbamoil)fenil)nicotinamida, N-(3-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)-2-fluorofenil)-2-cloronicotinamida, 3-benzamido-N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)benzamida, 2-doro-N-(3-(2-bromo-4-(perfboropropan-2-N)-6-(trifluorometil)fenilcarbamoil)fenil)nicotinamida, N-(3-(2-bromo-4-(perfluoropropan-2-N)-6-(trifluorometN)fenN-carbamoil)fenil)-4-ciano-2-fluoro-N-metilbenzamida, N-(3-(2-bromo-4-(perfluoropropan-2-N)-6-(trifluorometN)fenN-carbamoil)fenil)-4-ciano-2-fluorobenzamida, 3-dano-N-(3-(4-(perfluoropropan-2-N)-2,6-bis(trifluorometN)fenN-carbamoil)fenil)benzamida, 3-(4-cianobenzamido)-N-(4-(perfluoropropan-2-il)-2,6-bis(trifluorometil)fenil)benzamida, 3-ciano-N-metil-N-(3-(4-(perfluoropropan-2-il)-2,6-bis(trifluorometil)fenilcarbamoil)fenil)benzamida, 4-ciano-N-metil-N-(3-(4-(perfluoropropan-2-il)-2,6-bis(trifluorometil)fenilcarbamoil)fenil)benzamida, N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-3-(4-cianobenzamido)-2-fluorobenzamida, N-(3-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)-2-fluorofenil)-2-cloro-N-metilnicotinamida, N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-3-(4-ciano-N-metilbenzamido)-2-fluorobenzamida, N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-2-fluoro-3-(N-metilbenzamido)benzamida, N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-3-(3-ciano-N-metilbenzamido)-2-fluorobenzamida, N-(3-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-2-cloro-4-ciano-N-metilbenzamida, 3-benzamido-N-metil-N-(4-(perfluoropropan-2-il)-2,6-bis(trifluorometil)fenil)benzamida, 2-doro-N-(3-(metil(4-(perfluoropropan-2-N)-2,6-bis(trifluorometil)fenil)carbamoil)fenil)nicotinamida, 3-(3-danobenzamido)-N-metil-N-(4-(perfluoropropan-2-N)-2,6-bis(trifluorometil)fenil)benzamida, 2-bromo-N-(3-(metil(4-(perfluoropropan-2-il)-2,6-bis(trifluorometil)fenil)carbamoil)fenil)nicotinamida, 2-bromo-N-(3-(4-(perfluoropropan-2-N)-2,6-bis(trifluorometN)fenN-carbamoil)fenil)nicotinamida, 2-bromo-N-metN-N-(3-(4-(perfluoropropan-2-N)-2,6-bis(trifluorometN)fenN-carbamoil)fenil)nicotinamida, 3-(4-danobenzamido)-N-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)benzamida, 3-dano-N-(3-(2-yodo-4-(perfluoropropan-2-N)-6-(trifluorometN)fenN-carbamoil)fenil)benzamida, 2-bromo-N-(3-(2-yodo-4-(perfluoropropan-2-N)-6-(trifluorometN)fenN-carbamoil)fenil)nicotinamida, 4-dano-N-(3-(2-yodo-4-(perfluoropropan-2-N)-6-(trifluorometN)fenNcarbamoN)fenN)-N-metilbenzamida, 2-doro-N-(3-(2-yodo-4-(perfluoropropan-2-N)-6-(trifluorometN)fenNcarbamoN)fenN)-N-metN-nicotinamida, N-(3-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-2-yodonicotinamida, N-(3-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)-2-fluorofenil)-N-metilnicotinamida, N-(3-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)-2-fluorofenil)-6-fluoro-N-metilnicotinamida, N-(3-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)-2-fluorofenil)-4-ciano-2-fluoro-N- metilbenzamida, N-(3-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)-2-fluorofenil)-6-cloro-N-metilnicotinamida, N-(3-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)-2-fluorofenil)-3,5-diciano-N-metilbenzamida, 3-benzamido-2-fluoro-N-(4-(perfluoropropan-2-il)-2,6-bis(trifluorometil)fenil)benzamida, N-(3-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-3,5-diciano-N-metilbenzamida, 3-benzamido-2-fluoro-N-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)benzamida, 2-cloro-N-(2-fluoro-3-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)nicotinamida, 3-benzamido-N-(2-bromo-6-(perfluoroetil)-4-(perfluoropropan-2-il)fenil)-2-fluorobenzamida, 3-benzamido-N-(2-bromo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenil)-2-fluorobenzamida, N-(3-(2-bromo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenilcarbamoil)-2-fluorofenil)-2-cloronicotinamida, N-(2-bromo-6-(perfluoroetil)-4-(perfluoropropan-2-il)fenil)-3-(4-cianobenzamido)-2-fluorobenzamida, N-(2-bromo-4-(perfluorobutan-2- il)-6-(trifluorometil)fenil)-2-fluoro-3-(N-metilbenzamido)benzamida, N-(2-bromo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenil)-3-(3-ciano-N-metilbenzamido)-2-fluorobenzamida, N-(2-bromo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenil)-3-(4-ciano-N-metilbenzamido)-2-fluorobenzamida, 2-fluoro-N-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-3-(N-metilbenzamido)benzamida, 3-(4-ciano-N-metilbenzamido)-2-fluoro-N-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)benzamida, N-(3-(2-bromo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-N-metilbenzamida, 3-benzamido-N-(2-bromo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenil)benzamida, 3- benzamido-2-fluoro-N-(2-yodo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenil)benzamida, 2-fluoro-N-(2-yodo-4(perfluorobutan-2-il)-6-(trifluorometil)fenil)-3-(N-metilbenzamido)benzamida, 3-(4-ciano-N-metilbenzamido)-2-fluoro-N-(2-yodo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenil)benzamida, 3-(3-ciano-N-metilbenzamido)-2-fluoro-N-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)benzamida, 2-fluoro-N-(2-fluoro-3-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-N-metilbenzamida, 2-fluoro-3-(3-fluoro-N-metilbenzamido)-N-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)benzamida, 2-fluoro-3-(4-fluoro-N-metilbenzamido)-N-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)benzamida, 2,6-difluoro-N-(2-fluoro-3-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluoroiTietil)femlcarbamoil)fenil)-N-metilbenzamida, 6-doro-N-(2-fluoro-3-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)femlcarbamoil)fenil)nicotinamida, 3-(3-cianobenzamido)-2-fluoro-N-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)benzamida , 3-(4-cianobenzamido)-2-fluoro-N-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)benzamida , 2-fluoro-3-(2-fluorobenzamido)-N-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)benzamida , 2-fluoro-3-(3-fluorobenzamido)-N-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)benzamida , N-(3-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)femlcarbamoil)-2-fluorofeml)-2-fluoro-N-metilbenzamida, N-(3-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)femlcarbaiTioil)-2-fluorofeml)-2,6-difluoro-N-metilbenzamida, N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-2-fluoro-3-(3-fluoro-N-iTietilbenzamido)benzamida, N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-2-fluoro-3-(4-fluoro-N-iTietilbenzamido)benzamida, N-(3-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)femlcarbamoil)-2-fluorofeml)-2-cloronicotinamida, N-(3-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)femlcarbaiTioil)-2-fluorofeml)-6-cloronicotinamida, N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-3-(3-cianobenzaiTiido)-2-fluorobenzamida, N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-2-fluoro-3-(2-fluorobenzaiTiido)benzaiTiida, N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-2-fluoro-3-(3-fluorobenzamido)benzamida, N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-2-fluoro-3-(4-fluorobenzamido)benzamida, N-(3-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)-2-fluorofenil)-N-metilnicotinamida, 2-cloro-N-(2-fluoro-3-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-N-metilnicotinamida, 2-fluoro-3-(4-fluorobenzamido)-N-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)benzamida, 3-(2,6-difluorobenzamido)-2-fluoro-N-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)benzamida, 6-cloro-N-(2-fluoro-3-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-N-metilnicotinamida, N-(3-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)femlcarbamoil)fenil)-6-cloronicotinamida, N-(3-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)femlcarbaiTioil)feml)-2-fluorobenzamida, N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-3-(3-fluorobenzamido)benzamida, N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-3-(4-fluorobenzamido)benzamida, N-(3-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-2,6-difluorobenzamida, N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-3-(2,6-difluorobenzamido)-2-fluorobenzamida, 3-fluoro-N-(3-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)benzamida, 3-(4-fluorobenzamido)-N-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)benzamida, 2-fluoro-N-(3-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)femlcarbamoil)fenil)benzamida, 2,6-difluoro-N-(3-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)femlcarbamoil)fenil)benzamida, 6-doro-N-(3-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)femlcarbamoil)fenil)nicotinamida, 6-doro-N-(3-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)femlcarbaiTioil)feml)-N-metilnicotinamida, 3-dano-N-(3-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)femlcarbaiTioil)feml)-N-iTietilbenzamida, 2-fluoro-N-(3-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-N-metilbenzamida, 3-fluoro-N-(3-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-N-metilbenzamida, 4-fluoro-N-(3-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-N-metilbenzamida, N-(3-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-2-fluoro-N-metilbenzamida, N-(3-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-3-fluoro-N-metilbenzamida, N-(3-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-4-fluoro-N-metilbenzamida, N-(3-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-2,6-difluoro-N-metilbenzamida, 2,4-didoro-N-(3-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)benzamida, 3-(2,4-didorobenzamido)-2-fluoro-N-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)benzamida, 2,6-difluoro-N-(3-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)femlcarbaiTioil)feml)-N-metilbenzamida, 3-(2-doro-4-fluorobenzamido)-2-fluoro-N-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)benzamida, N-(3-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-N-metilbenzamida, 3-benzamido-N-(2-yodo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenil)benzamida, 2-cloro-N-(3-(2-yodo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)nicotinamida, 6-doro-N-(3-(2-yodo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)nicotinamida, 3-dano-N-(3-(2-yodo-4-(perfluorobutan-2-il)-6-(trifluorometil)femlcarbamoil)fenil)benzamida, 3-(4-cianobenzamido)-N-(2-yodo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenil)benzamida, 2-fluoro-N-(3-(2-yodo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)benzamida, 3-fluoro-N-(3-(2-yodo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)benzamida, 3-(4-fluorobenzamido)-N-(2-yodo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenil)benzamida, 2,6-difluoro-N-(3-(2-yodo-4-(perfluorobutan-2-il)-6-(trifluorometil)femlcarbamoil)fenil)benzamida, N-(3-(2-yodo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-N-metilbenzamida, 2-cloro-N-(3-(2-yodo-4-(perfborobutan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-N-metilnicotinamida, 3-ciano-N-(3-(2-yodo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-N-metilbenzamida, 4-ciano-N-(3-(2-yodo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-N-metilbenzamida, 3-fluoro-N-(3-(2-yodo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-N-metilbenzamida, 4-fluoro-N-(3-(2-yodo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-N-metilbenzamida, N-(3-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)-2-fluorofenil)-N-metilisonicotinamida, 1-óxido de 3-((3-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)-2-fluorofenil)(metil)carbamoil)piridina, 1-óxido de 4-((3-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)-2-fluorofenil)(metil)carbamoil)piridina, 2-cloro-4-fluoro-N-(3-(2-yodo-4-(perfluoropropan-2-il)-6-(trifborometil)fenilcarbamoil)fenil)benzamida, N-(3-(2-bromo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-2-cloronicotinamida, N-(2-bromo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenil)-3-(3cianobenzamido)benzamida, N-(3-(2-bromo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-2-fluorobenzamida, N-(2-bromo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenil)-3-(3-fluorobenzamido)benzamida, N-(3-(2-bromo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-6-doronicotinamida, N-(2-bromo-4-(perfluorobutan-2- il)-6-(trifluorometil)fenil)-3-(4-cianobenzamido)benzamida, N-(2-bromo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenil)-3- (4-fluorobenzamido)benzamida, N-(3-(2-bromo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-2,6-difluorobenzamida, N-(3-(2-bromo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-2-cloro-N-metilnicotinamida, N-(3-(2-bromo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-3-ciano-N-metilbenzamida, N-(3-(2-bromo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-2-fluoro-N-metilbenzamida, N-(3-(2-bromo-4- (perfluorobutan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-3-fluoro-N-metilbenzamida, N-(3-(2-bromo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-6-cloro-N-metilnicotinamida, N-(3-(2-bromo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-4-ciano-N-metilbenzamida, N-(3-(2-bromo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-4-fluoro-N-metilbenzamida, N-(3-(2-bromo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-2,6-difluoro-N-metilbenzamida, 6-cloro-N-(2-fluoro-3-(2-yodo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)nicotinamida, 3-(3-cianobenzamido)-2-fluoro-N-(2-yodo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenil)benzamida, 3-(4-cianobenzamido)-2-fluoro-N-(2-yodo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenil)benzamida, 2-fluoro-3-(2-fluorobenzamido)-N-(2-yodo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenil)benzamida, 2-fluoro-3-(3-fluorobenzamido)-N-(2-yodo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenil)benzamida, 2-fluoro-3-(4-fluorobenzamido)-N-(2-yodo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenil)benzamida, 3-(2,6-difluorobenzamido)-2-fluoro-N-(2-yodo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenil)benzamida, N-(3-(2-bromo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenilcarbamoil)-2-fluorofenil)-6-cloronicotinamida, N-(2-bromo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenil)-3-(3-cianobenzamido)-2-fluorobenzamida, N-(2-bromo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenil)-3-(4-cianobenzamido)-2-fluorobenzamida, N-(2-bromo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenil)-2-fluoro-3-(2-fluorobenzamido)benzamida, N-(2-bromo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenil)-2-fluoro-3-(3-fluorobenzamido)benzamida, N-(2-bromo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenil)-2-fluoro-3-(4-fluorobenzamido)benzamida, N-(2-bromo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenil)-3-(2,6-difluorobenzamido)-2-fluorobenzamida, 2-cloro-N-(2-fluoro-3-(2-yodo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-N-metilnicotinamida, 6-cloro-N-(2-fluoro-3-(2-yodo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-N-metilnicotinamida, 3-(3-ciano-N-metilbenzamido)-2-fluoro-N-(2-yodo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenil)benzamida, 2-fluoro-N-(2-fluoro-3-(2-yodo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-N-metilbenzamida, 2-fluoro-3-(3-fluoro-N-metilbenzamido)-N-(2-yodo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenil)benzamida, 2-fluoro-3-(4-fluoro-N-metilbenzamido)-N-(2-yodo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenil)benzamida, 2-cloro-4,5-difluoro-N-(3-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)benzamida, 2-cloro-4-fluoro-N-(3-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-N-metilbenzamida, N-(3-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-2-cloro-4-fluorobenzamida, 2-cloro-N-(3-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)benzamida, 3-(2-clorobenzamido)-2-fluoro-N-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)benzamida, 2-cloro-N-(3-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-N-metilbenzamida, N-(3-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-2-clorobenzamida, 2-cloro-N-(3-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-4-nitrobenzamida, N-(2-fluoro-3-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)-N-metilnicotinamida, 1-óxido de 3-((2-fluoro-3-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)(metil)carbamoil)piridina, 4-bromo-2-cloro-N-(3-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)benzamida, 2-bromo-4-cloro-N-(3-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)benzamida, 2-bromo-4-fluoro-N-(3-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)benzamida, 2-fluoro-3-(3-tluoro-N-metilbenzamido)-N-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-N-metilbenzamida, N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-2-fluoro-N-metil-3-(N-metilbenzamido)benzamida o N-(2-cloro-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-2-fluoro-3-(N-metilbenzamido)benzamida.
En la Fórmula (1), K puede representar un grupo de átomo no metálico necesario para formar un grupo de unión cíclico derivado de piridina, en combinación con A y dos átomos de carbono a los que se une A.
En la Fórmula (1), K puede representar un grupo de átomo no metálico necesario para formar un grupo de unión cíclico derivado de piridina, N-óxido de piridina o tiazol, en combinación con A y dos átomos de carbono a los que se une A.
En la fórmula (7), G1 y G3 pueden representar átomos de oxígeno. <33> En la Fórmula (9), G1, G2, y G3 pueden representar átomos de oxígeno. <34> En la Fórmula (1), G1, G2, y G3 pueden representar átomos de oxígeno.
Efectos de la invención
De acuerdo con la presente invención, se proporcionan un agente para el control de plagas que contiene un derivado de amida como principio activo que muestra un efecto pesticida frente a una amplia diversidad de plagas agrícolas/hortícolas y un método de control de plagas. Realización del mejor modo para realizar la invención representada
Un compuesto de amida para uso en el agente para el control de plagas de acuerdo con la presente invención está representado por la siguiente Fórmula (1).
<Las definiciones para los grupos X, n, K, A, de Y1 a Y5, T, G3, R1 y R2 en el compuesto de fórmula (1) se han proporcionado anteriormente.>
Las definiciones para los grupos X, n, de Y1 a Y5, Q1, G1, G3, R1 y R2 en el compuesto de Fórmula (7) se han proporcionado anteriormente.
Un compuesto de amida adicional para uso en el agente para el control de plagas se representa por la Fórmula (8):
Las definiciones para los grupos X1 a X4, de Y1 a Y5, Q1, R1 y R2 en el compuesto de Fórmula (8) se han proporcionado anteriormente.
Otro compuesto de amida para uso en el agente para el control de plagas está representado por la Fórmula (9):
Las definiciones para los grupos X, n, de Y1 a Y5, Q2, G1, G2, G3, R1 y R2 en el compuesto de Fórmula (9) se han proporcionado anteriormente.
Los términos usados en las fórmulas, incluyendo la Fórmula (1) y similares de acuerdo con la presente invención, tienen los mismos significados que se describen a continuación en las definiciones.
El "átomo de halógeno" representa un átomo de flúor, un átomo de cloro, un átomo de bromo o un átomo de yodo.
La expresión "Ca-Cb (en la que a y b representan un número entero de 1 o más)", por ejemplo, "C1-C3" significa el número de carbono de 1 a 3, el "C2-C6" significa el número de átomos de carbono de 2 a 6, y el "C1-C4" significa el número de átomos de carbono de 1 a 4.
"n-" significa normal, "i-" significa iso, "s-" significa secundario, y "t-" significa terciario.
El "grupo alquilo C1-C3" en la presente invención representa, por ejemplo, un grupo alquilo lineal o ramificado que tiene de 1 a 3 átomos de carbono, tal como metilo, etilo, n-propilo, i-propilo, y similares.
El "grupo haloalquilo C1-C3" representa, por ejemplo, un grupo alquilo lineal o ramificado que tiene de 1 a 3 átomos de carbono, este está sustituido con uno o más átomos de halógeno que pueden ser iguales o diferentes entre sí, tales como trifluorometilo, pentafluoroetilo, heptafluoro-n-propilo, heptafluoro-i-propilo, 2,2-difluoroetilo, 2,2-dicloroetilo, 2,2,2-trifluoroetilo, 2-fluoroetilo, 2-cloroetilo, 2-bromoetilo, 2-yodoetilo, 2,2,2-tricloroetilo, 2,2,2-tribromoetilo, 1,3-difluoro-2-propilo, 1,3-dicloro-2-propilo, 1-cloro-3-fluoro-2-propilo, 1,1,1-trifluoro-2-propilo, 2,3,3,3-trifluoro-n-propilo, 1.1.1.3.3.3- hexafluoro-2-propilo, 1,1,1,3,3,3-hexafluoro-2-cloro-2-propilo, 1,1,1,3,3,3-hexafluoro-2-bromo-2-propilo, 1.1.2.3.3.3- hexafluoro-2-cloro-n-propilo, 1,1,2,3,3,3-hexafluoro-2-bromo-n-propilo, 1,1,2,3,3,3-hexafluoro-1-bromo-2-propilo, 2,2,3,3,3-pentafluoro-n-propilo, 3-fluoro-n-propilo, 3-cloro-n-propilo, 3-bromo-n-propilo, y similares.
El "grupo alquilo C1-C4" representa, por ejemplo, un grupo alquilo lineal o ramificado que tiene de 1 a 4 átomos de carbono, tal como metilo, etilo, n-propilo, i-propilo, n-butilo, s-butilo, t-butilo, y similares.
El "grupo haloalcoxi C1-C3" representa, por ejemplo, un grupo alcoxi lineal o ramificado que tiene de 1 a 3 átomos de carbono, este está sustituido con uno o más átomos de halógeno que pueden ser iguales o diferentes entre sí, tales como trifluorometoxi, pentafluoroetoxi, heptafluoro-n-propiloxi, heptafluoro-i-propiloxi, 2,2-difluoroetoxi, 2,2-dicloroetoxi, 2,2,2-trifluoroetoxi, 2-fluoroetoxi, 2-cloroetoxi, 2-bromoetoxi, 2-yodoetoxi, 2,2,2-tricloroetoxi, 2,2,2-tribromoetoxi, 1,3-difluoro-2-propiloxi, 1,3-dicloro-2-propiloxi, 1-cloro-3-fluoro-2-propiloxi, 1,1,1-trifluoro-2-propiloxi, 2.3.3.3- trifluoro-n-propiloxi, 1,1,1,3,3,3-hexafluoro-2-propiloxi, 1,1,1,3,3,3-hexafluoro-2-cloro-2-propiloxi, 1,1,1,3,3,3-hexafluoro-2-bromo-2-propiloxi, 1,1,2,3,3,3-hexafluoro-2-cloro-n-propiloxi, 1,1,2,3,3,3-hexafluoro-2-bromo-n-propiloxi, 1.1.2.3.3.3- hexafluoro-1-bromo-2-propiloxi, 2,2,3,3,3-pentafluoro-n-propiloxi, 3-fluoro-n-propiloxi, 3-cloro-n-propiloxi, 3-bromo-n-propiloxi, y similares.
El "grupo perfluoroalquilo C3-C4" representa, por ejemplo, un grupo alquilo lineal o ramificado que tiene de 3 a 4 átomos de carbono, todos esos átomos de hidrógeno están sustituidos con átomos de flúor, tales como perfluoro-npropilo, perfluoro-i-propilo, perfluoro-n-butilo, perfluoro-i-butilo, perfluoro-s-butilo, perfluoro-t-butilo, y similares.
El "grupo haloalquilo C1" representa, por ejemplo, un grupo metilo que está sustituido con uno o más átomos de
halógeno que pueden ser iguales o diferentes entre sí, tales como trifluorometilo, 1,1-difluoro-1-bromometilo, y similares.
El "grupo alquilo C1-C6" en la presente invención representa, por ejemplo, un grupo alquilo lineal o ramificado que tiene de 1 a 6 átomos de carbono, tal como metilo, etilo, n-propilo, i-propilo, n-butilo, s-butilo, t-butilo, n-pentilo, 2-pentilo, neopentilo, 4-metil-2-pentilo, n-hexilo, 3-metil-n-pentilo, y similares.
El "grupo haloalquilo C1-C6" representa, por ejemplo, un grupo alquilo lineal o ramificado que tiene de 1 a 6 átomos de carbono, este está sustituido con uno o más átomos de halógeno que pueden ser iguales o diferentes entre sí, tales como trifluorometilo, pentafluoroetilo, heptafluoro-n-propilo, heptafluoro-i-propilo, 2,2-difluoroetilo, 2,2-dicloroetilo, 2,2,2-trifluoroetilo, 2-fluoroetilo, 2-cloroetilo, 2-bromoetilo, 2-yodoetilo, 2,2,2-tricloroetilo, 2,2,2-tribromoetilo, 1,3-difluoro-2-propilo, 1,3-dicloro-2-propilo, 1-cloro-3-fluoro-2-propilo, 1,1,1-trifluoro-2-propilo, 2,3,3,3-trifluoro-n-propilo, 4,4,4-trifluoro-n-butilo, 1,1,1,3,3,3-hexafluoro-2-propilo, 1,1,1,3,3,3-hexafluoro-2-cloro-2-propilo, 1,1,1,3,3,3-hexafluoro-2-bromo-2-propilo, 1,1,2,3,3,3-hexafluoro-2-cloro-n-propilo, 1,1,2,3,3,3-hexafluoro-2-bromo-n-propilo, 1,1,2,3,3,3-hexafluoro-1-bromo-2-propilo, 2,2,3,3,3-pentafluoro-n-propilo, 3-fluoro-n-propilo, 3-cloro-n-propilo, 3-bromo-n-propilo, 3,3,4,4,4-pentafluoro-2-butilo, nonafluoro-n-butilo, nonafluoro-2-butilo, 5,5,5-trifluoro-n-pentilo, 4,4,5,5,5-pentafluoro-2-pentilo, 3-cloro-n-pentilo, 4-bromo-2-pentilo, y similares.
El "grupo cicloalquilo C3-C9" representa, por ejemplo, un grupo cicloalquilo que tiene de 3 a 9 átomos de carbono, que tiene una estructura cíclica, tal como ciclopropilo, ciclobutilo, ciclopentilo, 2-metilciclopentilo, 3-metilciclopentilo, ciclohexilo, 2-metilciclohexilo, 3-metilciclohexilo, 4-metilciclohexilo, y similares.
El "grupo halocicloalquilo C3-C9" representa, por ejemplo, un grupo cicloalquilo que tiene de 3 a 9 átomos de carbono, que está sustituido con uno o más átomos de halógeno que pueden ser iguales o diferentes entre sí y tiene una estructura cíclica, tal como, 2,2,3,3-tetrafluorociclobutilo, 2-clorociclohexilo, 4-clorociclohexilo, y similares.
El "grupo alquenilo C2-C6" representa, por ejemplo, un grupo alquenilo que tiene de 2 a 6 átomos de carbono, que tiene un doble enlace en la cadena de carbono, tal como vinilo, alilo, 2-butenilo, 3-butenilo, y similares.
El "grupo haloalquenilo C2-C6" representa, por ejemplo, un grupo alquenilo lineal o ramificado que tiene de 2 a 6 átomos de carbono, que está sustituido con uno o más átomos de halógeno que pueden ser iguales o diferentes entre sí y tiene un doble enlace en la cadena de carbono, tal como 3,3-difluoro-2-propenilo, 3,3-dicloro-2-propenilo, 3,3-dibromo-2-propenilo, 2,3-dibromo-2-propenilo, 4,4-difluoro-3-butenilo, 3,4,4-tribromo-3-butenilo, y similares.
El "grupo alquinilo C2-C6" representa, por ejemplo, un grupo alquinilo que tiene de 2 a 6 átomos de carbono, que tiene un triple enlace en la cadena de carbono, tal como propargilo, 1 -butin-3-ilo, 1-butin-3-metil-3-ilo, y similares.
El "grupo haloalquinilo C2-C6" representa, por ejemplo, un grupo alquinilo lineal o ramificado que tiene de 2 a 6 átomos de carbono, que está sustituido con uno o más átomos de halógeno que pueden ser iguales o diferentes entre sí y tiene un triple enlace en la cadena de carbono, tal como fluoroetinilo, cloroetinilo, bromoetinilo, 3,3,3-trifluoro-1-propinilo, 3,3,3-tricloro-1-propinilo, 3,3,3-tribromo-1-propinilo, 4,4,4-trifluoro-1-butinilo, 4,4,4-tricloro-1 -butinilo, 4,4,4-tribromo-1-butinilo, y similares.
El "grupo alcoxi C1-C6" representa, por ejemplo, un grupo alcoxi lineal, ramificado o cíclico que tiene de 1 a 6 átomos de carbono, tal como metoxi, etoxi, n-propiloxi, i-propiloxi, ciclopropoxi, n-butoxi, s-butoxi, i-butoxi, t-butoxi, n-pentiloxi, i-pentiloxi, n-hexiloxi, ciclohexiloxi, y similares.
El "grupo haloalcoxi C1-C6" representa, por ejemplo, un grupo alcoxi lineal, ramificado o cíclico que tiene de 1 a 6 átomos de carbono, este está sustituido con uno o más átomos de halógeno que pueden ser iguales o diferentes entre sí, tales como trifluorometoxi, pentafluoroetoxi, 2-cloroetoxi, 2,2,2-trifluoroetoxi, heptafluoro-n-propoxi, heptafluoro-ipropoxi, 1,1,1,3,3,3-hexafluoro-2-propoxi, 3-fluoro-n-propoxi, 1-clorociclopropoxi, 2-bromociclopropoxi, 3,3,4,4,4-pentafluoro-2-butoxi, nonafluoro-n-butoxi, nonafluoro-2-butoxi, 5,5,5-trifluoro-n-pentiloxi, 4,4,5,5,5-pentafluoro-2-pentiloxi, 3-cloro-n-pentiloxi, 4-bromo-2-pentiloxi, 4-clorobutiloxi, 2-yodo-n-propiloxi, y similares.
El "grupo alquiltio C1-C6" representa, por ejemplo, un grupo alquiltio lineal, ramificado o cíclico que tiene de 1 a 6 átomos de carbono, tal como metiltio, etiltio, n-propiltio, i-propiltio, ciclopropiltio, n-butiltio, s-butiltio, i-butiltio, t-butiltio, n-pentiltio, i-pentiltio, n-hexiltio, ciclohexiltio y similares.
El "grupo haloalquiltio C1-C6" representa, por ejemplo, un grupo alquiltio lineal, ramificado o cíclico que tiene de 1 a 6 átomos de carbono, este está sustituido con uno o más átomos de halógeno que pueden ser iguales o diferentes entre sí, tal como trifluorometiltio, pentafluoroetiltio, 2-cloroetiltio, 2,2,2-trifluoroetiltio, heptafluoro-n-propiltio, heptafluoro-ipropiltio, 1,1,1,3,3,3-hexafluoro-2-propiltio, 3-fluoro-n-propiltio, 1-clorociclopropiltio, 2-bromociclopropiltio, 3,3,4,4,4-pentafluoro-2-butiltio, nonafluoro-n-butiltio, nonafluoro-2-butiltio, 5,5,5-trifluoro-n-pentiltio, 4,4,5,5,5-pentafluoro-2-pentiltio, 3-cloro-n-pentiltio, 4-bromo-2-pentiltio, 4-clorobutiltio, 2-yodo-n-propiltio, y similares.
El "grupo alquilsulfinilo C1-C6" representa, por ejemplo, un grupo alquilsulfinilo lineal, ramificado o cíclico que tiene de
1 a 6 átomos de carbono, tal como metilsulfinilo, etilsulfinilo, n-propilsulfinilo, i-propilsulfinilo, ciclopropilsulfinilo, nbutilsulfinilo, s-butilsulfinilo, i-butilsulfinilo, t-butilsulfinilo, n-pentilsulfinilo, i-pentilsulfinilo, n-hexilsulfinilo, ciclohexilsulfinilo y similares.
El "grupo haloalquilsulfinilo C1-C6" representa, por ejemplo, un grupo alquilsulfinilo lineal, ramificado o cíclico que tiene de 1 a 6 átomos de carbono, este está sustituido con uno o más átomos de halógeno que pueden ser iguales o diferentes entre sí, tal como trifluorometilsulfinilo, pentafluoroetilsulfinilo, 2-cloroetilsulfinilo, 2,2,2-trifluoroetilsulfinilo, heptafluoro-n-propilsulfinilo, heptafluoro-i-propilsulfinilo, 1,1,1,3,3,3-hexafluoro-2-propilsulfinilo, 3-fluoro-npropilsulfinilo, 1-clorociclopropilsulfinilo, 2-bromociclopropilsulfinilo, 3,3,4,4,4-pentafluoro-2-butilsulfinilo, nonafluoro-nbutilsulfinilo, nonafluoro-2-butilsulfinilo, 5,5,5-trifluoro-n-pentilsulfinilo, 4,4,5,5,5-pentafluoro-2-pentilsulfinilo, 3-cloro-npentilsulfinilo, 4-bromo-2-pentilsulfinilo, 4-clorobutilsulfinilo, 2-yodo-n-propilsulfinilo, y similares.
El "grupo alquilsulfonilo C1-C6" representa, por ejemplo, un grupo alquilsulfonilo lineal, ramificado o cíclico que tiene de 1 a 6 átomos de carbono, tal como metilsulfonilo, etilsulfonilo, n-propilsulfonilo, i-propilsulfonilo, ciclopropilsulfonilo, n-butilsulfonilo, s-butilsulfonilo, i-butilsulfonilo, t-butilsulfonilo, n-pentilsulfonilo, i-pentilsulfonilo, n-hexilsulfonilo, ciclohexilsulfonilo y similares.
El "grupo haloalquilsulfonilo C1-C6" representa, por ejemplo, un grupo alquilsulfonilo lineal, ramificado o cíclico que tiene de 1 a 6 átomos de carbono, este está sustituido con uno o más átomos de halógeno que pueden ser iguales o diferentes entre sí, tal como trifluorometilsulfonilo, pentafluoroetilsulfonilo, 2-cloroetilsulfonilo, 2,2,2-trifluoroetilsulfonilo, heptafluoro-n-propilsulfonilo, heptafluoro-i-propilsulfonilo, 1,1,1,3,3,3-hexafluoro-2-propilsulfonilo, 3-fluoro-npropilsulfonilo, 1-clorociclopropilsulfonilo, 2-bromociclopropilsulfonilo, 3,3,4,4,4-pentafluoro-2-butilsulfonilo, nonafluoro-n-butilsulfonilo, nonafluoro-2-butilsulfonilo, 5,5,5-trifluoro-n-pentilsulfonilo, 4,4,5,5,5-pentafluoro-2-pentilsulfonilo, 3-cloro-n-pentilsulfonilo, 4-bromo-2-pentilsulfonilo, 4-clorobutilsulfonilo, 2-yodo-n-propilsulfonilo, y similares.
El "grupo alquilsulfoniloxi C1-C6" representa, por ejemplo, un grupo alquilsulfoniloxi lineal, ramificado o cíclico que tiene de 1 a 6 átomos de carbono, tal como metanosulfoniloxi, etanosulfoniloxi, n-propanosulfoniloxi, ipropanosulfoniloxi, ciclopropanosulfoniloxi, n-butanosulfoniloxi, s-butanosulfoniloxi, i-butanosulfoniloxi, tbutanosulfoniloxi, n-pentanosulfoniloxi, i-pentanosulfoniloxi, n-hexanosulfoniloxi, ciclohexanosulfoniloxi y similares.
El "grupo haloalquilsulfoniloxi C1-C6" representa, por ejemplo, un grupo alquilsulfoniloxi lineal, ramificado o cíclico que tiene de 1 a 6 átomos de carbono, este está sustituido con uno o más átomos de halógeno que pueden ser iguales o diferentes entre sí, tal como trifluorometanosulfoniloxi, pentafluoropropanosulfoniloxi, 2-cloropropanosulfoniloxi, 2,2,2-trifluoropropanosulfoniloxi, heptafluoro-n-propanosulfoniloxi, heptafluoro-i-propanosulfoniloxi, 1,1,1,3,3,3-hexafluoro-2-propanosulfoniloxi, 3-fluoro-n-propanosulfoniloxi, 1-clorociclopropanosulfoniloxi, 2-bromociclopropanosulfoniloxi, 3,3,4,4,4-pentafluoro-2-butanosulfoniloxi, nonafluoro-n-butanosulfoniloxi, nonafluoro-2-butanosulfoniloxi, 5,5,5-trifluoro-n-pentanosulfoniloxi, 4,4,5,5,5-pentafluoro-2-pentanosulfoniloxi, 3-cloro-n-pentanosulfoniloxi, 4-bromo-2-pentanosulfoniloxi, 4-clorobutanosulfoniloxi, 2-yodo-n-propanosulfoniloxi, y similares.
El "grupo alquilcarbonilo C2-C7" representa, por ejemplo, un grupo alquilcarbonilo lineal, ramificado o cíclico que tiene de 1 a 7 átomos de carbono, tal como acetilo, propionilo, i-propilcarbonilo, ciclopropilcarbonilo, n-butilcarbonilo, sbutilcarbonilo, t-butilcarbonilo, n-pentilcarbonilo, 2-pentilcarbonilo, neopentilcarbonilo, ciclopentilcarbonilo, y similares.
El "grupo haloalquilcarbonilo C2-C7" representa, por ejemplo, un grupo alquilcarbonilo lineal, ramificado o cíclico que tiene de 1 a 7 átomos de carbono, este está sustituido con uno o más átomos de halógeno que pueden ser iguales o diferentes entre sí, tal como trifluoroacetilo, pentafluoropropionilo, 2-cloropropionilo, 2,2,2-trifluoropropionilo, heptafluoro-n-propilcarbonilo, heptafluoro-i-propilcarbonilo, 1,1,1,3,3,3-hexafluoro-2-propilcarbonilo, 3-fluoro-npropilcarbonilo, 1-clorociclopropilcarbonilo, 2-bromociclopropilcarbonilo, 3,3,4,4,4-pentafluoro-2-butilcarbonilo, nonafluoro-n-butilcarbonilo, nonafluoro-2-butilcarbonilo, 5,5,5-trifluoro-n-pentilcarbonilo, 4,4,5,5,5-pentafluoro-2-pentilcarbonilo, 3-cloro-n-pentilcarbonilo, 4-bromo-2-pentilcarbonilo, 4-clorobutilcarbonilo, 2-yodo-n-propilcarbonilo, y similares.
El "grupo alquilcarboniloxi C2-C7" representa, por ejemplo, un grupo alquilcarboniloxi lineal, ramificado o cíclico que tiene de 1 a 7 átomos de carbono, tal como acetiloxi, propioniloxi, i-propilcarboniloxi, ciclopropilcarboniloxi, nbutilcarboniloxi, s-butilcarboniloxi, t-butilcarboniloxi, n-pentilcarboniloxi, 2-pentilcarboniloxi, neopentilcarboniloxi, ciclopentilcarboniloxi, y similares.
El "grupo haloalquilcarboniloxi C2-C7" representa, por ejemplo, un grupo alquilcarboniloxi lineal, ramificado o cíclico que tiene de 1 a 7 átomos de carbono, que está sustituido con uno o más átomos de halógeno que pueden ser iguales o diferentes entre sí, tales como trifluoroacetiloxi, pentafluoropropioniloxi, 2-cloropropioniloxi, 2,2,2-trifluoropropioniloxi, heptafluoro-n-propilcarboniloxi, heptafluoro-i-propilcarboniloxi, 1,1,1,3,3,3-hexafluoro-2-propilcarboniloxi, 3-fluoro-npropilcarboniloxi, 1-clorociclopropilcarboniloxi, 2-bromociclopropilcarboniloxi, 3,3,4,4,4-pentafluoro-2-butilcarboniloxi, nonafluoro-n-butilcarboniloxi, nonafluoro-2-butilcarboniloxi, 5,5,5-trifluoro-n-pentilcarboniloxi, 4,4,5,5,5-pentafluoro-2-pentilcarboniloxi, 3-cloro-n-pentilcarboniloxi, 4-bromo-2-pentilcarboniloxi, 4-clorobutilcarboniloxi, 2-yodo-npropilcarboniloxi, y similares.
El "grupo alcoxicarbonilo C2-C7" representa, por ejemplo, un grupo alcoxicarbonilo lineal, ramificado o cíclico que tiene de 1 a 7 átomos de carbono, tal como metoxicarbonilo, etoxicarbonilo, isopropoxicarbonilo, ciclopropoxicarbonilo, nbutoxicarbonilo, s-butoxicarbonilo, t-butoxicarbonilo, n-pentiloxicarbonilo, 2-pentiloxicarbonilo, neopentiloxicarbonilo, ciclopentiloxicarbonilo y similares.
El "grupo haloalcoxicarbonilo C2-C7" representa, por ejemplo, un grupo alcoxicarbonilo lineal, ramificado o cíclico que tiene de 1 a 7 átomos de carbono, este está sustituido con uno o más átomos de halógeno que pueden ser iguales o diferentes entre sí, tal como trifluorometoxicarbonilo, pentafluoroetoxicarbonilo, 2-cloroetoxicarbonilo, 2,2,2-trifluoroetoxicarbonilo, heptafluoro-n-propoxicarbonilo, heptafluoro-i-propoxicarbonilo, 1,1,1,3,3,3-hexafluoro-2-propoxicarbonilo, 3-fluoro-n-propoxicarbonilo, 1-clorociclopropoxicarbonilo, 2-bromociclopropoxicarbonilo, 3,3,4,4,4-pentafluoro-2-butoxicarbonilo, nonafluoro-n-butoxicarbonilo, nonafluoro-2-butoxicarbonilo, 5,5,5-trifluoro-npentiloxicarbonilo, 4,4,5,5,5-pentafluoro-2-pentiloxicarbonilo, 3-cloro-n-pentiloxicarbonilo, 4-bromo-2-pentiloxicarbonilo, 4-clorobutiloxicarbonilo, 2-yodo-n-propiloxicarbonilo, y similares.
El "grupo alquilcarbonilamino C2-C7" representa, por ejemplo, un grupo alquilcarbonilamino lineal, ramificado o cíclico que tiene de 1 a 7 átomos de carbono, tal como acetilamino, propionilamino, n-propilcarbonilamino, ipropilcarbonilamino, ciclopropilcarbonilamino, n-butilcarbonilamino, s-butilcarbonilamino, i-butilcarbonilamino, tbutilcarbonilamino, n-pentilcarbonilamino, i-pentilcarbonilamino, n-hexilcarbonilamino, ciclohexilcarbonilamino y similares.
El "grupo haloalquilcarbonilamino C2-C7" representa, por ejemplo, un grupo alquilcarbonilamino lineal, ramificado o cíclico que tiene de 1 a 7 átomos de carbono, este está sustituido con uno o más átomos de halógeno que pueden ser iguales o diferentes entre sí, tal como trifluoroacetilamino, pentafluoropropionilamino, 2-cloropropionilamino, 2,2,2-trifluoropropionilamino, heptafluoro-n-propilcarbonilamino, heptafluoro-i-propilcarbonilamino, 1,1,1,3,3,3-hexafluoro-2-propilcarbonilamino, 3-fluoro-n-propilcarbonilamino, 1-clorociclopropilcarbonilamino, 2-bromociclopropilcarbonilamino, 3.3.4.4.4- pentafluoro-2-butilcarbonilamino, nonafluoro-n-butilcarbonilamino, nonafluoro-2-butilcarbonilamino, 5,5,5-trifluoro-n-pentilcarbonilamino, 4,4,5,5,5-pentafluoro-2-pentilcarbonilamino, 3-cloro-n-pentilcarbonilamino, 4-bromo-2-pentilcarbonilamino, 4-clorobutilcarbonilamino, 2-yodo-n-propilcarbonilamino, y similares.
El "grupo alcoxicarbonilamino C2-C7" representa, por ejemplo, un grupo alcoxicarbonilamino lineal, ramificado o cíclico que tiene de 1 a 7 átomos de carbono, tal como metoxicarbonilamino, etoxicarbonilamino, n-propiloxicarbonilamino, ipropiloxicarbonilamino, ciclopropoxicarbonilamino, n-butoxicarbonilamino, s-butoxicarbonilamino, ibutoxicarbonilamino, t-butoxicarbonilamino, n-pentiloxicarbonilamino, i-pentiloxicarbonilamino, nhexiloxicarbonilamino, ciclohexiloxicarbonilamino, y similares.
El "grupo haloalcoxicarbonilamino C2-C7" representa, por ejemplo, un grupo alcoxicarbonilamino lineal, ramificado o cíclico que tiene de 1 a 7 átomos de carbono, este está sustituido con uno o más átomos de halógeno que pueden ser iguales o diferentes entre sí, tal como trifluorometoxicarbonilamino, pentafluoroetoxicarbonilamino, 2-cloroetoxicarbonilamino, 2,2,2-trifluoroetoxicarbonilamino, heptafluoro-n-propoxicarbonilamino, heptafluoro-ipropoxicarbonilamino, 1,1,1,3,3,3-hexafluoro-2-propoxicarbonilamino, 3-fluoro-n-propoxicarbonilamino, 1-clorociclopropoxicarbonilamino, 2-bromociclopropoxicarbonilamino, 3,3,4,4,4-pentafluoro-2-butoxicarbonilamino, nonafluoro-n-butoxicarbonilamino, nonafluoro-2-butoxicarbonilamino, 5,5,5-trifluoro-n-pentiloxicarbonilamino, 4.4.5.5.5- pentafluoro-2-pentiloxicarbonilamino, 3-cloro-n-pentiloxicarbonilamino, 4-bromo-2-pentiloxicarbonilamino, 4-clorobutiloxicarbonilamino, 2-yodo-n-propiloxicarbonilamino, y similares.
El "grupo alcoxicarboniloxi C2-C7" representa, por ejemplo, un grupo alcoxicarboniloxi lineal, ramificado o cíclico que tiene de 1 a 7 átomos de carbono, tal como metoxicarboniloxi, etoxicarboniloxi, n-propiloxicarboniloxi, ipropiloxicarboniloxi, ciclopropoxicarboniloxi, n-butoxicarboniloxi, s-butoxicarboniloxi, i-butoxicarboniloxi, tbutoxicarboniloxi, n-pentiloxicarboniloxi, i-pentiloxicarboniloxi, n-hexiloxicarboniloxi, ciclohexiloxicarboniloxi y similares.
El "grupo haloalcoxicarboniloxi C2-C7" representa, por ejemplo, un grupo alcoxicarboniloxi lineal, ramificado o cíclico que tiene de 1 a 7 átomos de carbono, este está sustituido con uno o más átomos de halógeno que pueden ser iguales o diferentes entre sí, tal como trifluorometoxicarboniloxi, pentafluoroetoxicarboniloxi, 2-cloroetoxicarboniloxi, 2,2,2-trifluoroetoxicarboniloxi, heptafluoro-n-propoxicarboniloxi, heptafluoro-i-propoxicarboniloxi, 1,1,1,3,3,3-hexafluoro-2-propoxicarboniloxi, 3-fluoro-n-propoxicarboniloxi, 1-clorociclopropoxicarboniloxi, 2-bromociclopropoxicarboniloxi, 3,3,4,4,4-pentafluoro-2-butoxicarboniloxi, nonafluoro-n-butoxicarboniloxi, nonafluoro-2-butoxicarboniloxi, 5,5,5-trifluoro-n-pentiloxicarboniloxi, 4,4,5,5,5-pentafluoro-2-pentiloxicarboniloxi, 3-cloro-n-pentiloxicarboniloxi, 4-bromo-2-pentiloxicarboniloxi, 4-clorobutiloxicarboniloxi, 2-yodo-n-propiloxi-carboniloxi, y similares.
El "grupo alquilamino C1-C6" representa, por ejemplo, un grupo alquilamino lineal, ramificado o cíclico que tiene de 1 a 6 átomos de carbono, tal como metilamino, dimetilamino, etilamino, dietilamino, n-propilamino, i-propilamino, ciclopropilamino, n-butilamino, s-butilamino, i-butilamino, t-butilamino, n-pentilamino, i-pentilamino, n-hexilamino, ciclohexilamino, y similares.
El "grupo haloalquilamino C1-C6" representa, por ejemplo, un grupo alquilamino lineal, ramificado o cíclico que tiene de 1 a 6 átomos de carbono sustituido con uno o más átomos de halógeno que pueden ser iguales o diferentes entre sí, tal como trifluorometilamino, ditrifluorometilamino, pentafluoroetilamino, dipentafluoroetilamino, 2-cloroetilamino, 2,2,2-trifluoroetilamino, heptafluoro-n-propilamino, heptafluoro-i-propilamino, 1,1,1,3,3,3-hexafluoro-2-propilamino, 3-fluoro-n-propilamino, 1-clorociclopropilamino, 2-bromociclopropilamino, 3,3,4,4,4-pentafluoro-2-butilamino, nonafluoro-n-butilamino, nonafluoro-2-butilamino, 5,5,5-trifluoro-n-pentilamino, 4,4,5,5,5-pentafluoro-2-pentilamino, 3-cloro-n-pentilamino, 4-bromo-2-pentilamino, 4-clorobutilamino, 2-yodo-n-propilamino, y similares.
El "grupo alqueniloxi C2-C6" representa, por ejemplo, un grupo alqueniloxi que tiene de 2 a 6 átomos de carbono, que tiene un doble enlace en la cadena de carbono, tal como viniloxi, aliloxi, 2-buteniloxi, 3-buteniloxi, y similares.
El "grupo haloalqueniloxi C2-C6" representa, por ejemplo, un grupo alqueniloxi lineal o ramificado que tiene de 2 a 6 átomos de carbono, que está sustituido con uno o más átomos de halógeno que pueden ser iguales o diferentes entre sí y tiene un doble enlace en la cadena de carbono, tal como 3,3-difluoro-2-propeniloxi, 3,3-dicloro-2-propeniloxi, 3,3-dibromo-2-propeniloxi, 2,3-dibromo-2-propeniloxi, 4,4-difluoro-3-buteniloxi, 3,4,4-tribromo-3-buteniloxi, y similares.
El "grupo alquiniloxi C2-C6" representa, por ejemplo, un grupo alquiniloxi que tiene de 2 a 6 átomos de carbono, que tiene un triple enlace en la cadena de carbono, tal como propargiloxi, 1 -butin-3-iloxi, 1-butin-3-metil-3-iloxi, y similares.
El "grupo haloalquiniloxi C2-C6" representa, por ejemplo, un grupo alquiniloxi lineal o ramificado que tiene de 2 a 6 átomos de carbono, que está sustituido con uno o más átomos de halógeno que pueden ser iguales o diferentes entre sí y tiene un triple enlace en la cadena de carbono, tal como fluoroetiniloxi, cloroetiniloxi, bromoetiniloxi, 3,3,3-trifluoro-1-propiniloxi, 3,3,3-tricloro-1-propiniloxi, 3,3,3-tribromo-1-propiniloxi, 4,4,4-trifluoro-1 -butiniloxi, 4,4,4-tricloro-1-butiniloxi, 4,4,4-tribromo-1-butiniloxi, y similares.
El "grupo cicloalcoxi C3-C9" representa, por ejemplo, un grupo cicloalquiloxi que tiene de 3 a 9 átomos de carbono, que tiene una estructura cíclica, tal como ciclopropiloxi, ciclobutiloxi, ciclopentiloxi, 2-metilciclopentiloxi, 3-metilciclopentiloxi, ciclohexiloxi, 2-metilciclohexiloxi, 3-metilciclohexiloxi, 4-metilciclohexiloxi, y similares.
El "grupo halocicloalcoxi C3-C9" representa, por ejemplo, un grupo cicloalquiloxi que tiene de 3 a 9 átomos de carbono, que está sustituido con uno o más átomos de halógeno que pueden ser iguales o diferentes entre sí y tiene una estructura cíclica, tal como 2,2,3,3-tetrafluorociclobutiloxi, 2-clorociclohexiloxi, 4-clorociclohexiloxi, y similares.
El "grupo alquenilcarbonilo C3-C7" representa, por ejemplo, un grupo alquenilcarbonilo que tiene de 3 a 7 átomos de carbono, que tiene un doble enlace en la cadena de carbono, tal como vinilcarbonilo, alilcarbonilo, 2-butenilcarbonilo, 3-butenilcarbonilo, y similares.
El "grupo haloalquenilcarbonilo C3-C7" representa un grupo alquenilcarbonilo que tiene de 3 a 7 átomos de carbono, que está sustituido con uno o más átomos de halógeno que pueden ser iguales o diferentes entre sí y tiene un doble enlace en la cadena de carbono, tal como 3,3-difluoro-2-propenilcarbonilo, 3,3-dicloro-2-propenilcarbonilo, 3,3-dibromo-2-propenilcarbonilo, 2,3-dibromo-2-propenilcarbonilo, 4,4-difluoro-3-butenilcarbonilo, 3,4,4-tribromo-3-butenilcarbonilo, y similares.
El "grupo alquinilcarbonilo C3-C7" representa un grupo alquinilcarbonilo que tiene de 3 a 7 átomos de carbono y tiene un triple enlace en la cadena de carbono, tal como propargilcarbonilo, 1 -butin-3-ilcarbonilo, 1-butin-3-metil-3-ilcarbonilo, y similares.
El "grupo haloalquinilcarbonilo C3-C7" representa, por ejemplo, un grupo alquinilcarbonilo lineal o ramificado que tiene de 3 a 7 átomos de carbono, que está sustituido con uno o más átomos de halógeno que pueden ser iguales o diferentes entre sí y tiene un triple enlace en la cadena de carbono, tal como fluoroetinilcarbonilo, cloroetinilcarbonilo, bromoetinilcarbonilo, 3,3,3-trifluoro-1 -propinilcarbonilo, 3,3,3-tricloro-1 -propinilcarbonilo, 3,3,3-tribromo-1-propinilcarbonilo, 4,4,4-trifluoro-1 -butinilcarbonilo, 4,4,4-tricloro-1 -butinilcarbonilo, 4,4,4-tribromo-1-butinilcarbonilo, y similares.
El "grupo cicloalquilcarbonilo C4-C10" representa, por ejemplo, un grupo cicloalquilcarbonilo que tiene de 4 a 10 átomos de carbono, que tiene una estructura cíclica, tal como ciclopropilcarbonilo, ciclobutilcarbonilo, ciclopentilcarbonilo, 2-metilciclopentilcarbonilo, 3-metilciclopentilcarbonilo, ciclohexilcarbonilo, 2-metilciclohexilcarbonilo, 3-metilciclohexilcarbonilo, 4-metilciclohexilcarbonilo, y similares.
El "grupo halocicloalquilcarbonilo C4-C10" representa, por ejemplo, un grupo cicloalquilcarbonilo que tiene de 4 a 10 átomos de carbono, que está sustituido con uno o más átomos de halógeno que pueden ser iguales o diferentes entre sí y tiene una estructura cíclica, tal como 2,2,3,3-tetrafluorociclobutilcarbonilo, 2-clorociclohexilcarbonilo, 4-clorociclohexilcarbonilo, y similares.
El "grupo alqueniloxicarbonilo C3-C7" representa un grupo alqueniloxicarbonilo que tiene de 3 a 7 átomos de carbono, que tiene un doble enlace en la cadena de carbono, tal como viniloxicarbonilo, aliloxicarbonilo, 2-buteniloxicarbonilo,
3- buteniloxicarbonilo, y similares.
El "grupo haloalqueniloxicarbonilo C3-C7" representa, por ejemplo, un grupo alqueniloxicarbonilo lineal o ramificado que tiene de 3 a 7 átomos de carbono, que está sustituido con uno o más átomos de halógeno que pueden ser iguales o diferentes entre sí y tiene un doble enlace en la cadena de carbono, tal como 3,3-difluoro-2-propeniloxicarbonilo, 3.3- dicloro-2-propeniloxicarbonilo, 3,3-dibromo-2-propeniloxicarbonilo, 2,3-dibromo-2-propeniloxicarbonilo, 4,4-difluoro-3-buteniloxicarbonilo, 3,4,4-tribromo-3-buteniloxicarbonilo, y similares.
El "grupo alquiniloxicarbonilo C3-C7" representa, por ejemplo, un grupo alquiniloxicarbonilo que tiene de 3 a 7 átomos de carbono, que tiene un triple enlace en la cadena de carbono, tal como propargiloxicarbonilo, 1 -butin-3-iloxicarbonilo, 1-butin-3-metil-3-iloxicarbonilo, y similares.
El "grupo haloalquiniloxicarbonilo C3-C7" representa, por ejemplo, un grupo alquiniloxicarbonilo lineal o ramificado que tiene de 3 a 7 átomos de carbono, que está sustituido con uno o más átomos de halógeno que pueden ser iguales o diferentes entre sí y tiene un triple enlace en la cadena de carbono, tal como fluoroetiniloxicarbonilo, cloroetiniloxicarbonilo, bromoetiniloxicarbonilo, 3,3,3-trifluoro-1 -propiniloxicarbonilo, 3,3,3-tricloro-1-propiniloxicarbonilo, 3,3,3-tribromo-1-propiniloxicarbonilo, 4,4,4-trifluoro-1 -butiniloxicarbonilo, 4,4,4-tricloro-1-butiniloxicarbonilo, 4,4,4-tribromo-1-butiniloxicarbonilo, y similares.
El "grupo cicloalquiloxicarbonilo C4-C10" representa, por ejemplo, un grupo cicloalquiloxicarbonilo que tiene de 4 a 10 átomos de carbono, que tiene una estructura cíclica, tal como ciclopropiloxicarbonilo, ciclobutiloxicarbonilo, ciclopentiloxicarbonilo, 2-metilciclopentiloxicarbonilo, 3-metilciclopentiloxicarbonilo, ciclohexiloxicarbonilo, 2-metilciclohexiloxicarbonilo, 3-metilciclohexiloxicarbonilo, 4-metilciclohexiloxicarbonilo, y similares.
El "grupo halocicloalquiloxicarbonilo C4-C10" representa, por ejemplo, un grupo cicloalquiloxicarbonilo que tiene de 4 a 10 átomos de carbono, que está sustituido con uno o más átomos de halógeno que pueden ser iguales o diferentes entre sí y tiene una estructura cíclica, tal como 2,2,3,3-tetrafluorociclobutiloxicarbonilo, 2-clorociclohexiloxicarbonilo, 4- clorociclohexiloxicarbonilo, y similares.
El "grupo alquenilamino C2-C6" representa, por ejemplo, un grupo alquenilamino que tiene de 2 a 6 átomos de carbono, que tiene un doble enlace en la cadena de carbono, tal como vinilamino, alilamino, 2-butenilamino, 3-butenilamino, y similares.
El "grupo haloalquenilamino C2-C6" representa un grupo alquenilamino lineal o ramificado que tienen de 2 a 6 átomos de carbono, que está sustituido con uno o más átomos de halógeno que pueden ser iguales o diferentes entre sí y tiene un doble enlace en la cadena de carbono, tal como 3,3-difluoro-2-propenilamino, 3,3-dicloro-2-propenilamino, 3.3- dibromo-2-propenilamino, 2,3-dibromo-2-propenilamino, 4,4-difluoro-3-butenilamino, 3,4,4-tribromo-3-butenilamino, y similares.
El "grupo alquinilamino C2-C6" representa, por ejemplo, un grupo alquinilamino que tiene de 2 a 6 átomos de carbono, que tiene un triple enlace en la cadena de carbono, tal como propargilamino, 1-butin-3-ilamino, 1-butin-3-metil-3-ilamino, y similares.
El "grupo haloalquinilamino C2-C6" representa, por ejemplo, un grupo alquinilamino lineal o ramificado que tiene de 2 a 6 átomos de carbono, que está sustituido con uno o más átomos de halógeno que pueden ser iguales o diferentes entre sí y tiene un triple enlace en la cadena de carbono, tal como fluoroetinilamino, cloroetinilamino, bromoetinilamino, 3.3.3- trifluoro-1-propinilamino, 3,3,3-tricloro-1-propinilamino, 3,3,3-tribromo-1-propinilamino, 4,4,4-trifluoro-1-butinilamino, 4,4,4-tricloro-1-butinilamino, 4,4,4-tribromo-1-butinilamino, y similares.
El "grupo cicloalquilamino C3-C9" representa, por ejemplo, un grupo cicloalquilamino que tiene de 3 a 9 átomos de carbono, que tiene una estructura cíclica, tal como ciclopropilamino, ciclobutilamino, ciclopentilamino, 2-metilciclopentilamino, 3-metilciclopentilamino, ciclohexilamino, 2-metilciclohexilamino, 3-metilciclohexilamino, 4-metilciclohexilamino, y similares.
El "grupo halocicloalquilamino C3-C9" representa, por ejemplo, un grupo cicloalquilamino que tiene de 3 a 9 átomos de carbono, que está sustituido con uno o más átomos de halógeno que pueden ser iguales o diferentes entre sí y tiene una estructura cíclica, tal como 2,2,3,3-tetrafluorociclobutilamino, 2-clorociclohexilamino, 4-clorociclohexilamino, y similares.
El "grupo alquilaminocarbonilo C2-C7" representa, por ejemplo, un grupo alquilaminocarbonilo lineal o ramificado que tiene de 2 a 7 átomos de carbono, tal como metilaminocarbonilo, etilaminocarbonilo, n-propilaminocarbonilo, ipropilaminocarbonilo, n-butilaminocarbonilo, s-butilaminocarbonilo, t-butilaminocarbonilo, n-pentilaminocarbonilo, 2-pentilaminocarbonilo, neopentilaminocarbonilo, 4-metil-2-pentilaminocarbonilo, n-hexilaminocarbonilo, 3-metil-npentilaminocarbonilo, y similares.
El "grupo haloalquilaminocarbonilo C2-C7" representa, por ejemplo, un grupo alquilaminocarbonilo lineal o ramificado
que tiene de 2 a 7 átomos de carbono, este está sustituido con uno o más átomos de halógeno que pueden ser iguales o diferentes entre sí, tal como trifluorometilaminocarbonilo, pentafluoroetilaminocarbonilo, heptafluoro-npropilaminocarbonilo, heptafluoro-i-propilaminocarbonilo, 2,2-difluoroetilaminocarbonilo, 2,2-dicloroetilaminocarbonilo, 2,2,2-trifluoroetilaminocarbonilo, 2-fluoroetilaminocarbonilo, 2-cloroetilaminocarbonilo, 2-bromoetilaminocarbonilo, 2-yodoetilaminocarbonilo, 2,2,2-tricloroetilaminocarbonilo, 2,2,2-tribromoetilaminocarbonilo, 1,3-difluoro-2-propilaminocarbonilo, 1,3-dicloro-2-propilaminocarbonilo, 1-cloro-3-fluoro-2-propilaminocarbonilo, 1,1,1 -trifluoro-2-propilaminocarbonilo, 2,3,3,3-trifluoro-n-propilaminocarbonilo, 4,4,4-trifluoro-n-butilaminocarbonilo, 1,1,1,3,3,3-hexafluoro-2-propilaminocarbonilo, 1,1,1,3,3,3-hexafluoro-2-cloro-2-propilaminocarbonilo, 1,1,1,3,3,3-hexafluoro-2-bromo-2-propilaminocarbonilo, 1,1,2,3,3,3-hexafluoro-2-cloro-n-propilaminocarbonilo, 1,1,2,3,3,3-hexafluoro-2-bromon-propilaminocarbonilo, 1,1,2,3,3,3-hexafluoro-1-bromo-2-propilaminocarbonilo, 2,2,3,3,3-pentafluoro-npropilaminocarbonilo, 3-fluoro-n-propilaminocarbonilo, 3-cloro-n-propilaminocarbonilo, 3-bromo-npropilaminocarbonilo, 3,3,4,4,4-pentafluoro-2-butilaminocarbonilo, nonafluoro-n-butilaminocarbonilo, nonafluoro-2-butilaminocarbonilo, 5,5,5-trifluoro-n-pentilaminocarbonilo, 4,4,5,5,5-pentafluoro-2-pentilaminocarbonilo, 3-cloro-npentilaminocarbonilo, 4-bromo-2-pentilaminocarbonilo, y similares.
El "grupo alquenilaminocarbonilo C3-C7" representa, por ejemplo, un grupo alquenilaminocarbonilo que tiene de 3 a 7 átomos de carbono, que tiene un doble enlace en la cadena de carbono, tal como vinilaminocarbonilo, alilaminocarbonilo, 2-butenilaminocarbonilo, 3-butenilaminocarbonilo, y similares.
El "grupo haloalquenilaminocarbonilo C3-C7" representa, por ejemplo, un grupo alquenilaminocarbonilo lineal o ramificado que tiene de 3 a 7 átomos de carbono, que está sustituido con uno o más átomos de halógeno que pueden ser iguales o diferentes entre sí y tiene un doble enlace en la cadena de carbono, tal como 3,3-difluoro-2-propenilaminocarbonilo, 3,3-dicloro-2-propenilaminocarbonilo, 3,3-dibromo-2-propenilaminocarbonilo, 2,3-dibromo-2-propenilaminocarbonilo, 4,4-difluoro-3-butenilaminocarbonilo, 3,4,4-tribromo-3-butenilaminocarbonilo, y similares.
El "grupo alquinilaminocarbonilo C3-C7" representa, por ejemplo, un grupo alquinilaminocarbonilo que tiene de 3 a 7 átomos de carbono, que tiene un triple enlace en la cadena de carbono, tal como propargilaminocarbonilo, 1 -butin-3-ilaminocarbonilo, 1-butin-3-metil-3-ilaminocarbonilo, y similares.
El "grupo haloalquinilaminocarbonilo C3-C7" representa, por ejemplo, un grupo alquinilaminocarbonilo lineal o ramificado que tiene de 3 a 7 átomos de carbono, que está sustituido con uno o más átomos de halógeno que pueden ser iguales o diferentes entre sí y tiene un triple enlace en la cadena de carbono, tal como fluoroetinilaminocarbonilo, cloroetinilaminocarbonilo, bromoetinilaminocarbonilo, 3,3,3-trifluoro-1-propinilaminocarbonilo, 3,3,3-tricloro-1-propinilaminocarbonilo, 3,3,3-tribromo-1-propinilaminocarbonilo, 4,4,4-trifluoro-1-butinilaminocarbonilo, 4,4,4-tricloro-1-butinilaminocarbonilo, 4,4,4-tribromo-1-butinilaminocarbonilo, y similares.
El "grupo cicloalquilaminocarbonilo C4-C10" representa, por ejemplo, un grupo cicloalquilaminocarbonilo que tiene de 4 a 10 átomos de carbono, que tiene una estructura cíclica, tal como ciclopropilaminocarbonilo, ciclobutilaminocarbonilo, ciclopentilaminocarbonilo, 2-metilciclopentilaminocarbonilo, 3-metilciclopentilaminocarbonilo, ciclohexilaminocarbonilo, 2-metilciclohexilaminocarbonilo, 3-metilciclohexilaminocarbonilo, 4-metilciclohexilaminocarbonilo, y similares.
El "grupo halocicloalquilaminocarbonilo C4-C10" representa, por ejemplo, un grupo cicloalquilaminocarbonilo que tiene de 4 a 10 átomos de carbono que está sustituido con uno o más átomos de halógeno que pueden ser iguales o diferentes entre sí, y tiene una estructura cíclica, tal como 2,3,3-tetrafluorociclobutilaminocarbonilo, 2-clorociclohexilaminocarbonilo, 4-clorociclohexilaminocarbonilo, y similares.
El "grupo arilo" representa, por ejemplo, un hidrocarburo aromático monocíclico y policíclico, tal como un grupo fenilo, grupo naftilo, y similares.
El "grupo arilcarboniloxi" representa, por ejemplo, un grupo arilcarboniloxi, tal como un grupo fenilcarboniloxi, un grupo naftilcarboniloxi, y similares.
El "grupo arilcarbonilamino" representa, por ejemplo, un grupo arilcarbonilamino, tal como un grupo fenilcarbonilamino, un grupo naftilcarbonilamino, y similares.
El "grupo alquilo C1-C6 que puede tener un sustituyente" en R1 y R2 representa un grupo alquilo no sustituido, lineal, ramificado o cíclico que tiene de 1 a 6 átomos de carbono o un grupo alquilo lineal, ramificado o cíclico que tiene de 1 a 6 átomos de carbono, que está sustituido únicamente con al menos uno de un grupo nitro, un grupo fenilo que puede tener un sustituyente, y un grupo heterocíclico insaturado que puede tener un sustituyente. Además, cuando hay dos o más sustituyentes, estos sustituyentes son iguales o diferentes entre sí.
El "grupo haloalquilo C1-C6 que puede tener un sustituyente" en R1 y R2 representa un grupo alquilo lineal, ramificado o cíclico que tiene de 1 a 6 átomos de carbono, que está sustituido con uno o más átomos de halógeno o un grupo alquilo lineal, ramificado o cíclico que tiene de 1 a 6 átomos de carbono, que está sustituido con al menos uno de un grupo nitro, un grupo fenilo que puede tener un sustituyente, y un grupo heterocíclico insaturado que puede tener un
sustituyente, además de uno o más átomos de halógeno.
El "grupo alquenilo C2-C6 que puede tener un sustituyente" en Ri y R2 representa un grupo alquenilo no sustituido lineal, ramificado o cíclico que tiene de 2 a 6 átomos de carbono o un grupo alquenilo lineal, ramificado o cíclico que tiene de 2 a 6 átomos de carbono, que está sustituido con al menos uno de un grupo nitro, un grupo fenilo que puede tener un sustituyente, y un grupo heterocíclico insaturado que puede tener un sustituyente. Además, cuando hay dos o más sustituyentes, estos sustituyentes son iguales o diferentes entre sí.
El "grupo haloalquenilo C2-C6 que puede tener un sustituyente" en R1 y R2 representa un grupo alquenilo lineal, ramificado o cíclico que tiene de 2 a 6 átomos de carbono, que está sustituido únicamente con uno o más átomos de halógeno o un grupo alquenilo lineal, ramificado o cíclico que tiene de 2 a 6 átomos de carbono, que está sustituido con al menos uno de un grupo nitro, un grupo fenilo que puede tener un sustituyente, y un grupo heterocíclico insaturado que puede tener un sustituyente, además de uno o más átomos de halógeno.
El "grupo alquinilo C2-C6 que puede tener un sustituyente" en R1 y R2 representa un grupo alquinilo no sustituido, lineal, ramificado o cíclico que tiene de 2 a 6 átomos de carbono o un grupo alquinilo lineal, ramificado o cíclico que tiene de 2 a 6 átomos de carbono, que está sustituido con al menos uno de un grupo nitro, un grupo fenilo que puede tener un sustituyente, y un grupo heterocíclico insaturado que puede tener un sustituyente. Además, cuando hay dos o más sustituyentes, estos sustituyentes son iguales o diferentes entre sí.
El "grupo haloalquinilo C2-C6 que puede tener un sustituyente" en R1 y R2 representa un grupo alquinilo lineal, ramificado o cíclico que tiene de 2 a 6 átomos de carbono, que está sustituido únicamente con uno o más átomos de halógeno o un grupo alquinilo lineal, ramificado o cíclico que tiene de 2 a 6 átomos de carbono, que está sustituido con al menos uno de un grupo nitro, un grupo fenilo que puede tener un sustituyente, y un grupo heterocíclico insaturado que puede tener un sustituyente, además de uno o más átomos de halógeno.
Además, cada uno de los sustituyentes en la presente invención puede tener adicionalmente un sustituyente, y los ejemplos del sustituyente incluyen los siguientes:
uno o más sustituyentes seleccionados entre un grupo que consiste en un átomo de halógeno, un grupo alquilo C1-C6, un grupo haloalquilo C1-C6, un grupo cicloalquilo C3-C9, un grupo halocicloalquilo C3-C9, un grupo alquenilo C2-C6, un grupo haloalquenilo C2-C6 un grupo alquinilo C2-C6, un grupo haloalquinilo C2-C6, un grupo alcoxi C1-C6, un grupo haloalcoxi C1-C6, un grupo alquiltio C1-C6, un grupo haloalquiltio C1-C6, un grupo alquilsulfinilo C1-C6, un grupo haloalquilsulfinilo C1-C6, un grupo alquilsulfonilo C1-C6, un grupo haloalquilsulfonilo C1-C6, un grupo alquilcarbonilo C2-C7, un grupo haloalquilcarbonilo C2-C7, un grupo alquilcarboniloxi C2-C7, un grupo haloalquilcarboniloxi C2-C7, un grupo alquilsulfoniloxi C1-C6, un grupo haloalquilsulfoniloxi C1-C6, un grupo alcoxicarbonilo C2-C7, un grupo haloalcoxicarbonilo C2-C7, un grupo alquilcarbonilamino C2-C7, un grupo haloalquilcarbonilamino C2-C7, un grupo alcoxicarbonilamino C2-C7, un grupo haloalcoxicarbonilamino C2-C7, un grupo alquilaminocarbonilo C2-C7, un grupo haloalquilaminocarbonilo C2-C7, un grupo alquilamino C1-C6, un grupo haloalquilamino C1-C6, un grupo alquenilamino C2-C6, un grupo haloalquenilamino C2-C6, un grupo alquinilamino C2-C6, un grupo haloalquinilamino C2-C6, un grupo cicloalquilamino C3-C9, un grupo halocicloalquilamino C3-C9, un grupo alquenilaminocarbonilo C3-C7, un grupo haloalquenilaminocarbonilo C3-C7, un grupo alquinilaminocarbonilo C3-C7, un grupo haloalquinilaminocarbonilo C3-C7, un grupo cicloalquilaminocarbonilo C4-C10, un grupo halocicloalquilaminocarbonilo C4-C10, un grupo amino, un grupo carbamoílo, un grupo sulfamoílo, un grupo ciano, un grupo nitro, un grupo hidroxilo, un grupo carboxílico, un grupo pentatluorosulfanilo, un grupo fenilo que puede tener un sustituyente, un grupo heterocíclico que puede tener un sustituyente, un grupo bencilo que puede tener un sustituyente, un grupo fenilcarbonilo que puede tener un sustituyente, y un grupo fenilamino que puede tener un sustituyente, y cuando hay dos o más sustituyentes, cada sustituyente puede ser igual o diferente entre sí. Fórmula (9)
Los compuestos representados por la Fórmula (1), Formula (7), Formula (8), y para uso en el agente para el control de plagas de la presente invención pueden incluir uno o varios átomos de carbono quirales o centros quirales en sus Fórmulas estructurales, y por tanto pueden existir dos o más isómeros ópticos. Sin embargo, la presente invención incluye cada uno de los isómeros ópticos y una mezcla de los mismos en cualquier proporción. Además, los compuestos representados por la Fórmula (1), Formula (7), Formula (8), y la Fórmula (9) para uso en el agente para el control de plagas de la presente invención pueden incluir dos o más clases de isómeros geométricos derivados de dobles enlaces carbono-carbono en las Fórmulas estructurales. Sin embargo, la presente invención incluye cada uno de los isómeros geométricos y una mezcla de los mismos en cualquier proporción.
Las combinaciones de los sustituyentes o átomos preferidos como los sustituyentes o similares pare el derivado de amida representado por la Fórmula (1) para uso en el agente para el control de plagas de la presente invención son como se indican a continuación. T es preferentemente -C(=G1)-Q1, G1 es preferentemente un átomo de oxígeno, Q1 es preferentemente un grupo fenilo que puede tener un sustituyente o un grupo piridilo que puede tener un sustituyente, y Q1 es más preferentemente un grupo fenilo o un grupo piridilo que tiene uno o más sustituyentes seleccionados entre un grupo que consiste en un átomo de halógeno, un grupo haloalquilo C1, un grupo nitro, y un grupo ciano, y cuando hay dos o más sustituyentes, cada sustituyente puede ser igual o diferente entre sí.
G3 es preferentemente un átomo de oxígeno.
Ri es preferentemente un átomo de hidrógeno o un grupo alquilo C1-C3.
R2 es preferentemente un átomo de hidrógeno.
X es preferentemente un átomo de hidrógeno, un átomo de halógeno o un grupo ciano, y más preferentemente un átomo de hidrógeno, un átomo de flúor o un grupo ciano.
Cuando X es un sustituyente distinto de un átomo de hidrógeno, n es preferentemente 0, 1o 2.
Y5 es preferentemente un grupo haloalquilo C1-C3.
Además, las combinaciones del sustituyente o átomo preferidas como el sustituyente y similares para el derivado de amida representado por la Fórmula (8) son como se indican a continuación.
Los métodos representativos para producir el compuesto para uso en el agente para el control de plagas de la presente invención se muestran a continuación, y el método para producir el derivado de amida de la presente invención no está limitado a los métodos de preparación siguientes.
En la Fórmula mostrada en el siguiente método de preparación, A, K, X, n, R1, R2, T, G3, Y1, Y2, Y3, Y4, e Y5 representan las mismas definiciones que A, K, X, n, R1, R2, T, G3, Y1, Y2, Y3, Y4, e Y5, respectivamente, en la Fórmula (1). LG representa un grupo funcional que tiene una capacidad saliente, tal como un átomo de halógeno, un grupo hidroxi o similar, Hal representa un átomo de cloro o un átomo de bromo, y Xa, Xb, y Xc representan átomos de cloro, átomos de bromo o átomos de yodo. Los métodos también son adecuados para la preparación de compuestos de las Fórmulas (7), (8) y (9).
<Método de preparación 1>
Fórmula (21) Fórmula (22) ^ Formula (28)
Un derivado nitro de carboxamida aromática representado por la Fórmula (23) o la Fórmula (28) puede prepararse haciendo reaccionar un derivado nitro de ácido carboxílico aromático que tiene un grupo saliente representado por la Fórmula (21) con un derivado de amina aromática representado por la Fórmula (22) en un disolvente adecuado o sin ningún disolvente. En la presente etapa, puede usarse una base adecuada.
El disolvente puede ser cualquiera de aquellos que no inhiban significativamente la presente reacción. Los ejemplos de los mismos pueden incluir agua e hidrocarburos aromáticos, tales como benceno, tolueno, xileno, y similares, hidrocarburos halogenados, tales como diclorometano, cloroformo, tetracloruro de carbono, y similares, éteres de cadena o cíclicos, tales como éter dietílico, dioxano, tetrahidrofurano, 1 ,2-dimetoxietano, y similares, ésteres, tales como acetato de etilo, acetato de butilo, y similares, alcoholes, tales como metanol, etanol, y similares, cetonas, tales como acetona, metil isobutil cetona, ciclohexanona, y similares, amidas, tales como dimetilformamida, dimetilacetamida, y similares, nitrilos, tales como acetonitrilo y similares, y disolventes inertes, tales como 1,3-dimetil-2-imidazolidinona y similares. Estos disolventes pueden usarse solos o como una mezcla de dos o más clases de los mismos.
Adicionalmente, los ejemplos de la base pueden incluir bases orgánicas, tales como trietilamina, tri-n-butilamina, piridina, 4-dimetilaminopiridina, y similares, hidróxidos de metal alcalino, tales como hidróxido sódico, hidróxido potásico, y similares, carbonatos, tales como hidrogenocarbonato sódico, carbonato potásico, y similares, fosfatos, tales como monohidrogenofosfato dipotásico, fosfato trisódico, y similares, sales de hidruro de metal alcalino, tales como hidruro sódico y similares, alcóxidos de metal alcalino, tales como metóxido sódico, etóxido sódico, y similares, y amidas de litio, tales como diisopropilamida de litio, y similares.
Estas bases pueden usarse adecuadamente en una cantidad en el intervalo de 0,01 veces equivalentes molares a 5 veces equivalentes molares con respecto al compuesto representado por la Fórmula (21).
La temperatura de reacción puede seleccionarse adecuadamente de -20 ° a la temperatura de reflujo del disolvente utilizado. Además, el tiempo de reacción puede seleccionarse adecuadamente dentro del intervalo de varios minutos a 96 horas.
Entre los compuestos representados por la Fórmula (21), el derivado de haluro de carbonilo aromático puede prepararse fácilmente mediante un método general usando un agente de halogenación a partir de un ácido carboxílico aromático. Los ejemplos del agente de halogenación incluyen cloruro de tionilo, bromuro de tionilo, oxicloruro de fósforo, cloruro de oxalilo, tricloruro de fósforo, y similares.
Mientras tanto, es posible preparar el compuesto representado por la Fórmula (23) o la Fórmula (28) a partir del derivado nitro de ácido carboxílico aromático y el compuesto representado por la Fórmula (22) si usar un agente de halogenación. Los ejemplos del método pueden incluir un método descrito en, por ejemplo, Chem. Ber. p. 788 (1970), en el que se usa adecuadamente un agente de condensación, tal como N,N'-diciclohexilcarbodiimida y similares, adecuadamente con el uso de un aditivo, tal como 1-hidroxibenzotriazol y similares. Otros agentes de condensación que pueden usarse en este caso pueden incluir 1-etil-3-(3-dimetilaminopropil)carbodiimida, 1,1'-carbonilbis-1H-imidazol, y similares.
Adicionalmente, los ejemplos de otros métodos para producir el compuesto representado por la Fórmula (23) o la Fórmula (28) pueden incluir un método de anhídrido mixto usando ésteres de ácido clorofórmico, y los ejemplos de los mismos incluyen un método descrito en J. Am. Chem. Soc., p. 5012 (1967), mediante el cual puede prepararse el compuesto representado por la Fórmula (23) o la Fórmula (28). Los ejemplos de los ésteres de ácido clorofórmico usados en este caso pueden incluir cloroformiato de isobutilo, cloroformiato de isopropilo y similares. Además de ésteres de ácido clorofórmico, también pueden incluirse cloruro de dietilacetilo, cloruro de trimetilacetilo y similares.
Tanto el método que usa un agente de condensación como el método de anhídrido mixto no están limitados por el disolvente, la temperatura reacción, ni el tiempo de reacción de acuerdo con la literatura anterior. Puede usarse un disolvente inerte que no inhiba significativamente el avance de la reacción adecuado, y la temperatura de reacción y el tiempo de reacción también pueden seleccionarse adecuadamente de acuerdo con avance de la reacción.
1-(ii): Fórmula (23) ^ Fórmula (24)
Fórmula (28) ^ Fórmula (29)
Un derivado de carboxamida aromático que tiene un grupo amino representado por la Fórmula (24) o la Fórmula (29) puede obtenerse a partir del derivado de carboxamida aromático que tiene un grupo nitro representado por la Fórmula (23) o la Fórmula (28) por medio de una reacción de reducción. Los ejemplos de tal reducción incluyen un método que usa una reacción de hidrogenación y un método que usa un compuesto metálico (por ejemplo, cloruro estanoso (anhídrido), polvo de hierro, polvo de cinc, y similares).
La reacción del método anterior puede realizarse en un disolvente adecuado en presencia de un catalizador a una presión normal o a una presión más alta en una atmósfera de hidrógeno. Los ejemplos del catalizador pueden incluir catalizadores de paladio, tales como paladio-carbono y similares, catalizadores de níquel, tales como níquel Raney y similares, catalizadores de cobalto, catalizadores de rutenio, catalizadores de rodio, catalizadores de platino, y similares, y los ejemplos del disolvente pueden incluir agua; alcoholes, tales como metanol, etanol, y similares; hidrocarburos aromáticos, tales como benceno, tolueno, y similares; éteres de cadena o cíclicos, tales como éter, dioxano, tetrahidrofurano, y similares; y ésteres, tales como acetato de etilo y similares. La presión puede seleccionarse adecuadamente dentro de un intervalo de 0,1 MPa a 10MPa, la temperatura de reacción puede seleccionarse adecuadamente dentro de un intervalo de -20 °C a la temperatura de reflujo del disolvente utilizado, y el tiempo de reacción puede seleccionarse adecuadamente dentro de un intervalo desde varios minutos hasta 96 horas, mediante el cual puede prepararse eficazmente el compuesto de Fórmula (24) o Fórmula (29).
Los ejemplos del último método incluyen un método que usa cloruro estanoso (anhídrido) como un compuesto metálico en las condiciones descritas en "Organic Syntheses" Coll. Vol. III, P. 453.
1-(iii): Fórmula (24) Fórmula (26) ^ Fórmula (25)
Un derivado de carbamato o carboxamida aromática representado por la Fórmula (25) puede prepararse haciendo reaccionar el derivado de amina aromática representado por la Fórmula (24) con el derivado de ácido carboxílico o el derivado de éster de carbonato que tiene un grupo saliente representado por la Fórmula (26) en un disolvente adecuado. En la presente etapa, puede usarse un disolvente o base adecuada, y como la base o disolvente, pueden usarse los ilustrados en 1-(i). Los ejemplos de la temperatura de reacción, el tiempo de reacción, y similares pueden incluir los ilustrados en 1-(i).
En la Fórmula (26), el derivado de cloruro de carbonilo puede prepararse fácilmente a partir de un derivado de ácido carboxílico por un método general usando un agente de halogenación. El agente de halogenación puede incluir los ilustrados en 1-(i).
Puede haber un método para producir un compuesto representado por la Fórmula (25) a partir del derivado de ácido carboxílico (26) y el compuesto representado por la Fórmula (24) sin el uso de un agente de halogenación, y la preparación puede realizarse de acuerdo con el método ilustrado en 1-(i).
1-(iv): Fórmula (25) Fórmula (27) ^ Fórmula (1)
El compuesto representado por la Fórmula (1) de la presente invención puede prepararse haciendo reaccionar el compuesto de amida representado por la Fórmula (25) con el compuesto que tiene un grupo saliente, tal como halógeno y similares, representado por la Fórmula (27) en un disolvente sin ningún disolvente. Los compuestos de Fórmula (7), (8) y (9) también pueden prepararse de esta manera. En la presente etapa, puede usarse un disolvente 0 base adecuada, y como la base o disolvente, pueden usarse los ilustrados en 1-(i). Los ejemplos de la temperatura de reacción, el tiempo de reacción, y similares pueden incluir los ilustrados en 1-(i).
1-(v): Fórmula (28) Fórmula (30) ^ Fórmula (23)
El compuesto representado por la Fórmula (23) puede prepararse haciendo reaccionar el compuesto de amida representado por la Fórmula (28) con el compuesto que tiene un grupo saliente, tal como halógeno y similares, representado por la Fórmula (30) en un disolvente sin ningún disolvente. En la presente etapa, puede usarse un disolvente o base adecuada, y como la base o disolvente, pueden usarse los ilustrados en 1-(i). Los ejemplos de la temperatura de reacción, el tiempo de reacción, y similares pueden incluir los ilustrados en 1-(i).
1 -(vi): Fórmula (29) ^ Fórmula (31)
(Método A)
Un compuesto representado por la Fórmula (31) puede prepararse haciendo reaccionar el compuesto representado por la Fórmula (29) con un aldehido o una cetona en un disolvente, y haciéndolos reaccionar en una atmósfera de hidrógeno con la adición de un catalizador.
El disolvente puede ser cualquiera de aquellos que no inhiban significativamente el avance de la reacción, y los ejemplos de los mismos pueden incluir hidrocarburos alifáticos, tales como hexano, ciclohexano, metilciclohexano, y similares, hidrocarburos aromáticos, tales como benceno, xileno, tolueno, y similares, hidrocarburos halogenados, tales como diclorometano, cloroformo, tetracloruro de carbono, 1,2-dicloroetano, y similares, éteres, tales como éter dietílico, dioxano, tetrahidrofurano, 1,2-dimetoxietano, y similares, amidas, tales como dimetilformamida, dimetilacetamida, y similares, nitrilos, tales como acetonitrilo, propionitrilo, y similares, cetonas, tales como acetona, metil isobutil cetona, ciclohexanona, metil etil cetona, y similares, ésteres, tales como acetato de etilo, acetato de butilo, y similares, alcoholes, tales como 1,3-dimetil-2-imidazolidinona, sulfolano, dimetilsulfóxido, metanol, etanol, y similares, y agua. Estos disolventes pueden usarse solos o como una mezcla de dos o más clases de los mismos.
Los ejemplos del catalizador pueden incluir catalizadores de paladio, tales como paladio-carbono, hidróxido de paladiocarbono, y similares, catalizadores de níquel, tales como níquel Raney y similares, catalizadores de cobalto, catalizadores de platino, catalizadores de rutenio, catalizadores de rodio, y similares.
Los ejemplos de los aldehídos pueden incluir formaldehído, acetaldehído, propionaldehído, trifluoroacetaldehído, difluoroacetaldehído, fluoroacetaldehído, cloroacetaldehído, dicloroacetaldehído, tricloroacetaldehído, bromoacetaldehído, y similares.
Los ejemplos de las cetonas pueden incluir acetona, perfluoroacetona, metil etil cetona, y similares.
La presión de reacción puede seleccionarse adecuadamente dentro del intervalo de 1 atm a 100 atm. La temperatura de reacción puede seleccionarse adecuadamente dentro del intervalo de -20 °C a la temperatura de reflujo del disolvente utilizado. Además, el tiempo de reacción puede seleccionarse adecuadamente dentro del intervalo de varios minutos a 96 horas.
(Método B)
Un compuesto representado por la Fórmula (31) puede prepararse haciendo reaccionar el compuesto representado por la Fórmula (29) con un aldehído o una cetona en un disolvente, y tratando el producto con un agente reductor.
El disolvente puede ser cualquiera de aquellos que no inhiban significativamente el avance de la reacción, y los ejemplos de los mismos pueden incluir hidrocarburos alifáticos, tales como hexano, ciclohexano, metilciclohexano, y similares, hidrocarburos aromáticos, tales como benceno, xileno, tolueno, y similares, hidrocarburos halogenados, tales como diclorometano, cloroformo, tetracloruro de carbono, 1,2-dicloroetano, y similares, éteres, tales como éter dietílico, dioxano, tetrahidrofurano, 1,2-dimetoxietano, y similares, amidas, tales como dimetilformamida, dimetilacetamida, y similares, nitrilos, tales como acetonitrilo, propionitrilo, y similares, cetonas, tales como acetona, metil isobutil cetona, ciclohexanona, metil etil cetona, y similares, ésteres, tales como acetato de etilo, acetato de butilo, y similares, alcoholes, tales como 1,3-dimetil-2-imidazolidinona, sulfolano, dimetilsulfóxido, metanol, etanol, y similares, agua, y similares. Estos disolventes pueden usarse solos o como una mezcla de dos o más clases de los mismos.
Los ejemplos del agente de reducción pueden incluir, por ejemplo, borohidruros, tales como borohidruro sódico, cianoborohidruro sódico, triacetato borohidruro sódico, y similares.
Los ejemplos de los aldehídos pueden incluir formaldehído, acetaldehído, propionaldehído, trifluoroacetaldehído, difluoroacetaldehído, fluoroacetaldehído, cloroacetaldehído, dicloroacetaldehído, tricloroacetaldehído, bromoacetaldehído, y similares.
Los ejemplos de las cetonas pueden incluir acetona, perfluoroacetona, metil etil cetona, y similares.
La temperatura de reacción puede seleccionarse adecuadamente dentro del intervalo de -20 °C a la temperatura de reflujo del disolvente utilizado. Además, el tiempo de reacción puede seleccionarse adecuadamente dentro del intervalo de varios minutos a 96 horas.
(Método C)
Un compuesto de Fórmula (31) puede prepararse haciendo reaccionar el compuesto representado por la Fórmula (29) con un aldehído en un disolvente o sin ningún disolvente.
El disolvente puede ser cualquiera de aquellos que no inhiban significativamente el avance de la reacción, y los ejemplos de los mismos pueden incluir hidrocarburos alifáticos, tales como hexano, ciclohexano, metilciclohexano, y similares, hidrocarburos aromáticos, tales como benceno, xileno, tolueno, y similares, hidrocarburos halogenados, tales como diclorometano, cloroformo, tetracloruro de carbono, 1,2-dicloroetano, y similares, éteres, tales como éter dietílico, dioxano, tetrahidrofurano, 1,2-dimetoxietano, y similares, amidas, tales como dimetilformamida, dimetilacetamida, y similares, nitrilos, tales como acetonitrilo, propionitrilo, y similares, cetonas, tales como acetona, metil isobutil cetona, ciclohexanona, metil etil cetona, y similares, ésteres, tales como acetato de etilo, acetato de butilo, y similares, alcoholes, tales como 1,3-dimetil-2-imidazolidinona, sulfolano, dimetilsulfóxido, metanol, etanol, y similares, ácidos inorgánicos, tales como ácido sulfúrico, ácido clorhídrico, y similares, ácidos orgánicos, tales como ácido fórmico, ácido acético, y similares, agua, y similares. Estos disolventes pueden usarse solos o como una mezcla de dos o más clases de los mismos.
Los ejemplos de los aldehídos pueden incluir formaldehído, acetaldehído, propionaldehído, y similares.
La temperatura de reacción puede seleccionarse adecuadamente dentro del intervalo de -20 °C a la temperatura de reflujo del disolvente utilizado. y el tiempo de reacción puede seleccionarse adecuadamente dentro del intervalo de varios minutos a 96 horas.
1-(vii): Fórmula (31) Fórmula (26) ^ Fórmula General (32)
Un derivado de carbamato o carboxamida aromática representado por la Fórmula (32) puede prepararse haciendo reaccionar el derivado de amina aromática representado por la Fórmula (31) con el derivado de ácido carboxílico o el derivado de éster de carbonato que tiene un grupo saliente representado por la Fórmula (26) en un disolvente adecuado. En la presente etapa, puede usarse un disolvente o base adecuada, y como la base o disolvente, pueden usarse los ilustrados en 1-(i). Los ejemplos de la temperatura de reacción, el tiempo de reacción, y similares pueden incluir los ilustrados en 1-(i).
En la Fórmula (26), el derivado de cloruro de carbonilo puede prepararse fácilmente a partir de un derivado de ácido carboxílico por un método general usando un agente de halogenación. El agente de halogenación puede incluir los ilustrados en 1-(i).
Puede ilustrarse un método para producir un compuesto representado por la Fórmula (32) a partir del derivado de ácido carboxílico (26) y el compuesto representado por la Fórmula (31) sin el uso de un agente de halogenación, y la
preparación puede realizarse de acuerdo con el método ilustrado en 1-(i).
1 -(viii): Fórmula (32) Fórmula (30) ^ Fórmula (1)
El compuesto representado por la Fórmula (1) de la presente invención puede prepararse haciendo reaccionar el compuesto de amida representado por la Fórmula (32) con el compuesto que tiene un grupo saliente, tal como halógeno y similares, representado por la Fórmula (30) en un disolvente o sin ningún disolvente. Los compuestos de Fórmula (7), (8) y (9) también pueden prepararse de esta manera. En la presente etapa, puede usarse un disolvente o base adecuada, y como la base o disolvente, pueden usarse los ilustrados en 1-(i). Los ejemplos de la temperatura de reacción, el tiempo de reacción, y similares pueden incluir los ilustrados en 1-(i).
<Método de preparación 2>
Un compuesto representado por la Fórmula (34) puede prepararse haciendo reaccionar el compuesto representado por la Fórmula (33) con un compuesto representado por la Fórmula (22) en las condiciones descritas en 1-(i).
2-(ii): Fórmula (34) ^ Fórmula (36)
Un compuesto representado por la Fórmula (36) puede prepararse realizando una reacción de aminación usando un agente de aminación, tal como amoniaco y similares de acuerdo con las condiciones descritas, por ejemplo, en J. Org. Chem. p. 280 (1958). Sin embargo, las condiciones, tales como un disolvente de reacción y similares, no están restringidas a las descritas en la bibliografía, y puede usarse un disolvente inerte que no inhiba significativamente el avance adecuado de la reacción. La temperatura de reacción y el tiempo de reacción pueden seleccionarse adecuadamente según tenga lugar la reacción. Además, los ejemplos del agente de aminación incluyen metilamina, etilamina o similares, además de amoniaco.
2-(iii): Fórmula (36) Fórmula (26) ^ Fórmula (1)
El compuesto representado por la Fórmula (1) puede prepararse haciendo reaccionar el compuesto representado por la Fórmula (36) con un compuesto representado por la Fórmula (26) de acuerdo con las condiciones descritas en 1-(i).
<Método de preparación 3>
Un derivado de carbamato o carboxamida aromática representado por la Fórmula (35) puede prepararse haciendo reaccionar el derivado de amina aromática representado por la Fórmula (29) con el derivado de ácido carboxílico o el derivado de éster de carbonato que tiene un grupo saliente representado por la Fórmula (26) en un disolvente
adecuado. En la presente etapa, puede usarse un disolvente o base adecuada, y como la base o disolvente, pueden usarse los ilustrados en 1-(i). Los ejemplos de la temperatura de reacción, el tiempo de reacción, y similares pueden incluir los ilustrados en 1-(i).
En la Fórmula (26), el derivado de cloruro de carbonilo puede prepararse fácilmente a partir de un derivado de ácido carboxílico por un método general usando un agente de halogenación. El agente de halogenación puede incluir los ilustrados en 1-(i).
Puede ilustrarse un método para producir un compuesto representado por la Fórmula (35) a partir del derivado de ácido carboxílico (26) y el compuesto representado por la Fórmula (29) sin el uso de un agente de halogenación, y la preparación puede realizarse de acuerdo con el método ilustrado en 1-(i).
3-(ii): Fórmula (35) Fórmula (27) ^ Fórmula (1a)
El compuesto representado por la Fórmula (1a) de la presente invención puede prepararse haciendo reaccionar el compuesto de amida representado por la Fórmula (35) con el compuesto que tiene un grupo saliente, tal como halógeno y similares, representado por la Fórmula (27) en un disolvente sin ningún disolvente. En la presente etapa, puede usarse un disolvente o base adecuada, y como la base o disolvente, pueden usarse los ilustrados en 1-(i). Los ejemplos de la temperatura de reacción, el tiempo de reacción, y similares pueden incluir los ilustrados en 1-(i). <Método de preparación 4>
4-(i): Fórmula (24) ^ Fórmula (36)
Un compuesto representado por la Fórmula (36) puede prepararse haciendo reaccionar el compuesto representado por la Fórmula (24) como un material de partida de acuerdo con las condiciones del (Método A), (Método B) o (Método C) descritos en 1 -(vi).
4-(i'): Fórmula (24) Fórmula (27) ^ Fórmula (36)
Un derivado de carboxamida aromática representado por la Fórmula (36) puede prepararse haciendo reaccionar el derivado de amina aromática representado por la Fórmula (24) con el derivado de ácido carboxílico o el derivado de éster de carbonato que tiene un grupo saliente representado por la Fórmula (27) en un disolvente adecuado. En la presente etapa, puede usarse un disolvente o base adecuada, y como la base o disolvente, pueden usarse los ilustrados en 1-(i). Los ejemplos de la temperatura de reacción, el tiempo de reacción, y similares pueden incluir los ilustrados en 1-(i).
En la Fórmula (27), el derivado de cloruro de carbonilo puede prepararse fácilmente a partir de un derivado de ácido carboxílico por un método general usando un agente de halogenación. El agente de halogenación puede incluir los ilustrados en 1-(i).
Puede ilustrarse un método para producir un compuesto representado por la Fórmula (36) a partir del derivado de ácido carboxílico (27) y el compuesto representado por la Fórmula (24) sin el uso de un agente de halogenación, y la preparación puede realizarse de acuerdo con el método ilustrado en 1-(i).
4-(ii): Fórmula (36) Fórmula (26) Fórmula (1)
Un compuesto representado por la Fórmula (1) puede prepararse haciendo reaccionar el compuesto representado por la Fórmula (36) y el compuesto representado por la Fórmula (26) como materiales de partida de acuerdo con las condiciones descritas en 1-(i).
<Método de preparación 5>
Los compuestos de Fórmula (7), (8) y (9) también pueden prepararse de esta manera.
5-(i): Fórmula (37) Fórmula (22) ^ Fórmula (38)
Un compuesto representado por la Fórmula (38) puede prepararse haciendo reaccionar el compuesto representado por la Fórmula (37) y el compuesto representado por la Fórmula (22) de acuerdo con las condiciones descritas en 1-(i).
5-(ii): Fórmula (38) ^ Fórmula (39)
Un compuesto representado por la Fórmula (39) puede prepararse haciendo reaccionar el derivado nitro de carboxamida aromática representado por la Fórmula (38) con un agente de fluoración adecuado en un disolvente adecuado o sin ningún disolvente.
El disolvente puede ser cualquiera de aquellos que no inhiban significativamente el avance de la reacción, y los ejemplos de los mismos pueden incluir hidrocarburos alifáticos, tales como hexano, ciclohexano, metilciclohexano, y similares, hidrocarburos aromáticos, tales como benceno, tolueno, xileno, y similares, hidrocarburos halogenados, tales como diclorometano, cloroformo, tetracloruro de carbono, 1,2-dicloroetano, y similares, éteres de cadena o cíclicos, tales como éter dietílico, dioxano, tetrahidrofurano, 1,2-dimetoxietano, y similares, ésteres, tales como acetato de etilo, acetato de butilo, y similares, cetonas, tales como acetona, metil isobutil cetona, ciclohexanona, metil etil cetona, y similares, nitrilos, tales como acetonitrilo, propionitrilo, y similares, y disolventes apróticos polares, tales como 1,3-dimetil-2-imidazolidinona, sulfolano, dimetilsulfóxido, N,N-dimetilformamida, N-metilpirrolidona, N,N-dimetilacetamida, y similares. Estos disolventes pueden usarse solos o como una mezcla de dos o más clases de los mismos.
Los ejemplos del agente de fluoración pueden incluir 1,1,2,2-tetrafluoroetildietilamina, 2-cloro-1,1,2-trifluoroetil dietilamina, trifluorodifenilfosfolano, difluorotrifenilfosfolano, ésteres de ácido fluorofórmico, tetrafluoruro de azufre, fluoruro potásico, hidrogenofluoruro potásico, fluoruro de cesio, fluoruro de rubidio, fluoruro sódico, fluoruro de litio, fluoruro de antimonio (III), fluoruro de antimonio (V), fluoruro de cinc, fluoruro de cobalto, fluoruro de plomo, fluoruro de cobre, fluoruro de mercurio (II), fluoruro de plata, fluoroborato de plata, fluoruro de talio (I), fluoruro de molibdeno (VI), fluoruro de arsénico (III), fluoruro de bromo, tetrafluoruro de selenio, difluorotrimetilsilicato de tris(dimetilamino)sulfonio, hexafluorosilicato de sodio, fluoruros de amonio cuaternario, (2-cloroetil)dietilamina, trifluoruro de dietilaminoazufre, trifluoruro de morfolinoazufre, tetrafluoruro de silicio, fluoruro de hidrógeno, ácido fluorhídrico, complejo de fluoruro de hidrógeno-piridina, complejo de fluoruro de hidrógeno-trietilamina, sales de fluoruro de hidrógeno, trifluoruro de bis(2-metoxietil)aminoazufre, 2,2-difluoro-1,3-dimetil-2-imidazolidinona, pentafluoruro de yodo, 2,2,3,3,4,4-hexafluorociclobutaniluro de tris(dietilamino)fosfonio, hexafluorociclobutaniluro de trietilamonio, hexafluoropropeno, y similares. Estos agentes de fluoración pueden usarse solos o como una mezcla de dos o más clases de los mismos.
El agente de fluoración puede seleccionarse adecuadamente y usarse como un disolvente, en el intervalo de 1 vez equivalente molar a 10 veces equivalentes molares con respecto al derivado nitro de carboxamida aromática representado por la Fórmula
(38).
Pueden usarse aditivos, y los ejemplos de los mismos pueden éteres corona, tales como 18-corona-6 y similares, catalizadores de transferencia de fases, tales como una sal de tetrafenilfosfonio y similares, sales inorgánicas, tales como fluoruro de calcio, cloruro de calcio, y similares, óxidos metálicos, tales como óxido de mercurio y similares, resinas de intercambio iónico, y similares. Estos aditivos pueden añadirse no solo al sistema de reacción si no también usarse como un agente de pretratamiento para el agente de fluoración.
La temperatura de reacción puede seleccionarse adecuadamente dentro del intervalo de -80 °C a la temperatura de
reflujo del disolvente utilizado. y el tiempo de reacción puede seleccionarse adecuadamente dentro del intervalo de varios minutos a 96 horas.
<Método de preparación 6>
6-(i): Fórmula (40) Fórmula (22) ^ Fórmula (41)
Un compuesto representado por la Fórmula (41) puede prepararse haciendo reaccionar el compuesto representado por la Fórmula (40) con un compuesto representado por la Fórmula (22) de acuerdo con las condiciones descritas en 1-(i).
6-(ii): Fórmula (41) ^ Fórmula (42)
Un compuesto representado por la Fórmula (42) puede prepararse haciendo reaccionar el derivado halógeno de carboxamida aromática representado por la Fórmula (41) con un agente de cianación adecuado en un disolvente adecuado o sin ningún disolvente.
El disolvente puede ser cualquiera de aquellos que no inhiban significativamente el avance de la presente reacción. Los ejemplos de los mismos pueden incluir hidrocarburos alifáticos, tales como hexano, ciclohexano, metilciclohexano, y similares, hidrocarburos aromáticos, tales como benceno, tolueno, xileno, y similares, hidrocarburos halogenados, tales como diclorometano, cloroformo, tetracloruro de carbono, 1,2-dicloroetano, y similares, éteres de cadena o cíclicos, tales como éter dietílico, dioxano, tetrahidrofurano, 1,2-dimetoxietano, y similares, ésteres, tales como acetato de etilo, acetato de butilo, y similares, cetonas, tales como acetona, metil isobutil cetona, ciclohexanona, metil etil cetona, y similares, nitrilos, tales como acetonitrilo, propionitrilo, y similares, y disolventes apróticos polares, tales como 1,3-dimetil-2-imidazolidinona, sulfolano, dimetilsulfóxido, N,N-dimetilformamida, N-metilpirrolidona, N,N-dimetilacetamida, y similares. Estos disolventes pueden usarse solos o como una mezcla de dos o más clases de los mismos.
Los ejemplos del agente de cianación incluyen sales de cianuro, tales como cianuro sódico, cianuro potásico, cianoborohidruro sódico, y similares, cianuros metálicos, tales como cianuro de cobre, cianuro de plata, cianuro de litio, y similares, cianuro de hidrógeno, cianuro de tetraetilamonio, y similares.
Estos agentes de cianación pueden seleccionarse adecuadamente y usarse en el intervalo de 1 vez equivalente molar a 10 veces equivalentes molares con respecto al derivado halógeno de carboxamida aromática representado por la Fórmula (41).
Pueden usarse aditivos, y los ejemplos de los mismos pueden éteres corona, tales como 18-corona-6 y similares, catalizadores de transferencia de fases, tales como una sal de tetrafenilfosfonio y similares, sales inorgánicas, tales como yoduro sódico y similares.
La temperatura de reacción puede seleccionarse adecuadamente dentro del intervalo de -20 °C a la temperatura de reflujo del disolvente utilizado. Además, el tiempo de reacción puede seleccionarse adecuadamente dentro del intervalo de varios minutos a 96 horas.
<Método de preparación 7>
7-(i): Fórmula (43) ^ Fórmula (44)
Un compuesto representado por la Fórmula (44) puede prepararse haciendo reaccionar el compuesto representado por la Fórmula (43) con un reactivo de Lawesson de acuerdo con las condiciones conocidas descritas en Synthesis p.
463 (1993), Synthesis p.829 (1984) y similares. Las condiciones, tales como un disolvente, temperatura de la reacción y similares no están restringidas a las descritas en la bibliografía.
2-(ii): Fórmula (44) Fórmula (26) ^ Fórmula (45)
Un compuesto representado por la Fórmula (45) puede prepararse haciendo reaccionar el compuesto representado por la Fórmula (44) con un compuesto representado por la Fórmula (26) de acuerdo con las condiciones descritas en 1-(i).
<Método de preparación 8>
8: Fórmula (46) ^ Fórmula (47) Fórmula (48)
Los compuestos representados por la Fórmula (47) y la Fórmula (48) pueden prepararse a partir de un compuesto representado por la Fórmula (46) de acuerdo con las condiciones descritas en 7-(i). Las condiciones, tales como un disolvente, una temperatura de la reacción, y similares no están restringidas a las descritas en la bibliografía. Estos dos compuestos pueden separarse fácilmente y purificarse por una técnica de separación y purificación conocida, tal como cromatografía en columna sobre gel de sílice y similares.
<Método de preparación 9>
Pueden prepararse ácidos carboxílicos que tienen un grupo acilamino representado por la Fórmula (50) haciendo reaccionar un ácido carboxílico que tiene un grupo amino representado por la Fórmula (49) como material de partida con un compuesto representado por la Fórmula (26) de acuerdo con las condiciones descritas en 1-(i).
9-(ii): Fórmula (50) ^ Fórmula (51)
Un compuesto representado por la Fórmula (51) puede prepararse por un método general conocido que incluye hacer reaccionar el compuesto representado por la Fórmula (50) con cloruro de tionilo, cloruro de oxalilo, fosgeno, oxicloruro de fósforo, pentacloruro de fósforo, tricloruro de fósforo, bromuro de tionilo, tribromuro de fósforo, trifluoruro de dietilaminoazufre o similares.
9-(iii): Fórmula (51) Fórmula (22) ^ Fórmula (1)
El compuesto representado por la Fórmula (1) puede prepararse haciendo reaccionar un compuesto representado por la Fórmula (51) con un compuesto representado por la Fórmula (22) de acuerdo con las condiciones descritas en 1-(i). Los compuestos de Fórmula (7), (8) y (9) también pueden prepararse de esta manera.
9-(iv): Fórmula (50) Fórmula (22) ^ Fórmula (1)
El compuesto representado por la Fórmula (1) puede prepararse haciendo reaccionar el compuesto representado por la Fórmula (50) con un compuesto representado por la Fórmula (22) de acuerdo con la condición que usa un agente de condensación o la condición que usa un método de anhídrido mixto de acuerdo con 1-(i). Los compuestos de Fórmula (7), (8) y (9) también pueden prepararse de esta manera.
En todos los métodos de preparación que se han descrito anteriormente, un producto deseado puede aislarse del sistema de reacción después de que se complete la reacción de acuerdo con un método general, pero si se requiere, la purificación puede realizarse mediante operaciones, tales como recristalización, cromatografía en columna, destilación, y similares. Además, el producto deseado también puede proporcionarse para los procesos de reacción posteriores sin separarse del sistema de reacción.
A continuación en el presente documento, se darán ejemplos de los compuestos representativos del derivado de amida representado por la Fórmula (1), Fórmula (7), Fórmula (8) o Fórmula (9) como un principio activo para el agente para el control de plagas de la presente invención en la Tabla 1 a la Tabla 51 siguientes, pero la presente invención no se limita a los mismos.
Además, en las tablas, "n-" representa normal, "i-" representa iso, "s-" representa secundario, "t-" representa terciario, "Me" representa un grupo metilo, "Et" representa un grupo etilo, "n-Pr" representa un grupo propilo normal, "i-Pr" representa un grupo isopropilo, "n-Bu" representa un grupo butilo normal, "i-Bu" representa un grupo isobutilo, "s-Bu" representa un grupo butilo secundario, "t-Bu" representa un grupo butilo terciario, "CF3" representa un grupo trifluorometilo, "C2F5" representa un grupo pentafluoroetilo, "n-C3F7" representa un grupo heptafluoropropilo normal, "i-C3F7" representa un grupo heptafluoroisopropilo, "OCF3" representa un grupo trifluorometoxi, "OC2F5" representa un grupo pentafluoroetoxi, "H" representa un átomo de hidrógeno, "F" representa un átomo de flúor, "Cl" representa un átomo de cloro, "Br" representa un átomo de bromo, "I" representa un átomo de yodo, "O" representa un átomo de oxígeno, "C(O)" representa a grupo carbonilo, "CN" representa un grupo ciano, "Py" representa un grupo piridilo, "Ph" representa un grupo fenilo, y "S(O)2" representa un grupo sulfonilo, respectivamente.
Las Tablas contienen compuestos para uso en los agentes de control de plagas dentro del alcance de las reivindicaciones, y compuestos que son ejemplos de referencia. Estos últimos compuestos se proporcionan para una comprensión útil de la invención. Los compuestos para uso en la invención son compuestos de Fórmula (1), (8) y (9) como se definen en la reivindicación 1.
Los compuestos de Fórmula (1) contienen un grupo de piridina, N-óxido de piridina, pirrol, tiazol, furano o tiofeno, formado a partir de A y K, y dos átomos de carbono a los que se une A. Y1 e Y5 representan un átomo de halógeno o un grupo haloalquilo C1-C3, y Y1 o Y5 representa un grupo haloalquilo C1-C3; Y2 e Y4 representan un átomo de hidrógeno; Y3 representa un grupo perfluoroalquilo C2-C4.
En los compuestos de Fórmula (7), cada X representa independientemente un átomo de hidrógeno, un átomo de halógeno o un grupo ciano; e Y3 representa un grupo perfluoroalquilo C2-C4; Y2 e Y4 representan un átomo de hidrógeno; Y1 e Y5 representan un átomo de halógeno o un grupo haloalquilo C1-C3, y Y1 o Y5 representa un grupo haloalquilo C1-C3.
En los compuestos de Fórmula (8), Q1 representa un grupo fenilo o un grupo piridilo que puede tener un sustituyente seleccionado entre un grupo que consiste en: un átomo de halógeno,
un grupo haloalquilo C1, un grupo nitro, y un grupo ciano, en un caso donde Q1 tiene los sustituyentes, el número de los sustituyentes es 1 o 2; cada uno de X1 y X2 representa independientemente un átomo de hidrógeno o un átomo de flúor, y X3 y X4 representan un átomo de hidrógeno; y cada uno de Y1 e Y5 representa independientemente un átomo de cloro, un átomo de bromo, un átomo de yodo, un grupo trifluorometoxi, un grupo trifluorometilo o un grupo pentafluoroetilo; Y2 e Y4 representan un átomo de hidrógeno; e Y3 representa un grupo perfluoroalquilo C3-C4; en un caso donde Y1 e Y5 representan átomos de halógeno simultáneamente, al menos uno de X1 o X2 representa un átomo de flúor; y en un caso donde Y1 o Y5 representa un grupo trifluorometoxi, X2 representa un átomo de flúor.
En los compuestos de Fórmula (9), cada X representa independientemente un átomo de hidrógeno, un átomo de halógeno o un grupo ciano; Y3 representa un grupo perfluoroalquilo C2-C4; Y2 e Y4 representan un átomo de hidrógeno; cada uno de Y1 e Y5 representa independientemente un átomo de halógeno o un grupo haloalquilo C1-C3, y Y1 o Y5 representa un grupo haloalquilo C1-C3.
Tabla 18
(continuación)
Tabla 112
Tabla 26
(continuación)
Tabla 612
(continuación)
Tabla 614
(continuación)
Tabla 78
(continuación)
Tabla 711
(continuación)
Tabla 713
(continuación)
Tabla 84
(continuación)
Tabla 87
(continuación)
Tabla 88
Tabla 911
Tabla 10 2
continuación
Tabla 11 9
(continuación)
Tabla 16 7
(continuación)
Tabla 17 1
continuación
Tabla 18 1
continuación
Tabla 19 1
continuación
Tabla 26 1
(continuación)
Tabla 26 2
continuación
Tabla 26 3
continuación
Tabla 26 4
continuación
Tabla 26 5
continuación
Tabla 266
continuación
Tabla 26 7
continuación
Tabla 268
continuación
Tabla 26 9
Tabla 27 1
Tabla 27 2
(continuación)
Tabla 27 3
continuación
Tabla 27 4
continuación
Tabla 27 5
(continuación)
Tabla 276
(continuación)
Tabla 27 7
Tabla 28 1
(continuación)
Tabla 28 2
continuación
Tabla 29 3
Tabla 30 1
(continuación)
Tabla 31 1
(continuación)
Tabla 31 2
continuación
Tabla 31 3
continuación
Tabla 31 4
continuación
Tabla 31 5
Tabla 32 1
Tabla 33 1
continuación
Tabla 34 2
Tabla 35 1
(continuación)
Tabla 36 1
continuación
Tabla 37 1
continuación
Tabla 38 1
continuación
Tabla 39 1
Tabla 40 1
Tabla 41 1
Tabla 42 1
continuación
Tabla 43 1
continuación
Tabla 45 1
Tabla 46 1
continuación
Tabla 46 2
continuación
Tabla 47 1
continuación
Tabla 47 2
continuación
Tabla 48 1
continuación
Tabla 48 2
continuación
Tabla 49 1
continuación
Tabla 49 2
Tabla 50 1
continuación
Tabla 50 2
Tabla 51 1
Tabla 51 2
(continuación)
A continuación en el presente documento, la Tabla 52 muestra las propiedades físicas de los compuestos representativos del derivado de amida de la presente invención. Los valores de desplazamiento químico de RMN 1H de los mismos están basados en tetrametilsilano como sustancia de patrón interno a menos que se especifique lo contrario.
Tabla 52 1
(continuación)
Tabla 52 2
(continuación)
Tabla 52 3
(continuación)
Tabla 52 4
(continuación)
Tabla 52 5
Tabla 52 6
Tabla 52 7
Tabla 52 8
Tabla 52 9
Tabla 52 10
Tabla 52 11
Tabla 52 12
Tabla 52 13
Tabla 52 14
Tabla 52 15
Tabla 52 16
Tabla 52 17
Tabla 5218
Tabla 52 19
El agente para el control de plagas que incluye el compuesto como se define en la reivindicación 1 como principio activo puede controlar de manera eficaz, a una baja concentración del mismo, cualquier plaga, tales como insectos, incluyendo diversas plagas agrícolas que dañan los cultivos agrícolas/hortícolas, árboles, y similares, plagas insanas que afectan negativamente al ambiente de los seres humanos, tales como las casas y similares de varios modos, plagas del grano almacenado que dañan al grano y similares almacenadas en un almacén, plagas xilófagas que dañan la madera, tal como edificios y similares, y ácaros, crustáceos, moluscos, y nematodos que se propagan y causan daño de un modo similar al caso de los insectos.
Ejemplos específicos de los insectos, los ácaros, los crustáceos, los moluscos y los nematodos que pueden controlarse usando el compuesto como se define en la reivindicación 1 incluyen insectos lepidópteros, tales como Adoxophyes honmaai, Adoxophyes orana faciata, Archips breviplivanus, Grapholita inopinata, Archips fuscocuperanus, Grapholita molesta, Choristoneura magnanima, Leguminivora glycinivorella, Olethreutes mori, Caloptilia zachrysa, Argyresthia conjugella, Spulerrina astaurota, Matsumuraeses phaseoli, Pandemis heparana, Bucculatrix pyrivorella, Lyonetia clerkella, Carposina niponensis, Lyonetia prunifoliella malinella, Caloptilia theivora, Phyllonorycter ringoniella, Phyllocnistis citrella, Acrolepiopsis sapporensis, Acrolepiopsis suzukiella, Plutella xylostella, Stathmopoda masinissa, Helcystogramma triannulella, Pectinophora gossypiella, Carposina sasakii, Chilo suppressalis, Cnaphalocrocis medinalis, Ephestia elutella, Conogethes punctiferalis, Diaphania indica, Etiella zinckenella, Glyphodes pyloalis, Scirpophaga incertulas, Hellula undalis, Ostrinia furnacalis, Ostrinia scapulalis, Parapediasia teterrella, Parnara guttata, Pieris brassicae, Pieris rapae crucivora, Papilio xuthus, Ascotis selenaria, Pseudoplusia incladens, Euproctis pseudoconspersa, Lymantria dispar, Orgyia thyellina, Hyphantria cunea, Lemyra imparilis, Adris tyrannus, Aedia leucomelas, Agrotis ipsilon, Agrotis segetum, Autographa nigrisigna, Ctenoplusia agnata, Cydla pomonella, Helicoverpa armigera, Helicoverpa assulta, Helicoverpa zea, Heliothis virescens, Ostrinia nubilalis, Mamestra brassicae, Mythimna separata, Sesamia inferens, Naranga aenescens, Spodoptera eridania, Spodoptera exigua, Spodoptera frugiperda, Spodoptera littoralis, Spodoptera litura, Spodoptera depravata, Trichoplusia ni, Endopiza viteana, Manduca quinquemaculata, Manduca sexta, y similares;
insectos hemípteros, tales como Arboridia apicalis, Balclutha saltuella, Epiacanthus stramineus, Empoasca fabae, Empoasca nipponica, Empoasca onukii, Empoasca sakaii, Macrosteles striifrons, Nephotettix cinctinceps, Psuedatomoscelis seriatus, Laodelphax striatella, Nilaparvata lugens, Sogatella furcifera, Diaphorina citri, Psylla pyrisuga, Aleurocanthus spiniferus, Bemisia argentifolii, Bemisia tabaci, Dialeurodes citri, Trialeurodes vaporariorum, Aleurolobus taonabae, Viteus vitifolii, Lipaphis erysimi, Aphis gossypii, Aphis spiraecola, Myzus persicae, Toxoptera aurantii, Drosicha corpulenta, Icerya purchasi, Phenacoccus solani, Pulvinaria aurantii, Planococcus citri, Pseudaonidia duplex, Planococcus kuraunhiae, Pseudococcus comstocki, Comstockaspis perniciosa, Ceroplastes ceriferus, Ceroplastes rubens, Aonidiella aurantii, Fiorinia theae, Pseudaonidia paeoniae, Pseudaulacaspis pentagona, Pseudaulacaspis prunicola, Unaspis euonymi, Unaspis yanonensis, Cimex lectularius, Dolycoris baccarum, Eurydema
rugosum, Eysarcoris aeneus, Eysarcoris lewisi, Eysarcoris ventralis, Glaucas subpunctatus, Halyomorpha halys, Nezara antennata, Nezara viridula, Piezodorus hybneri, Plautia crossota, Scotinophora lurida, Cletus punctiger; Leptocorisa chinensis, Riptortus clavatus, Rhopalus msculatus, Cavelerius saccharivorus, Togo hemipterus, Dysdercus cingulatus, Stephanitis pyrioides, Halticus insularis, Lygus lineolaris, Stenodema sibiricum, Stenotus rubrovittatus, Trigonotylus caelestialium, y similares;
insectos coleópteros, tales como Anomala cuprea, Anomala rufocuprea, Gametis jucunda, Heptophylla picea, Popillia japonica, Lepinotarsa decemlineata, Epilachna varivestis, Melanotus fortnumi, Melanotus tamsuyensis, Lasioderma serricorne, Lyctusbrunneus, Tomicus piniperda, Rhizopertha dominica, Epuraea domina, Epilachna varivestis, Epilachna vigintioctopunctata, Tenebrio molitor; Tribolium castaneum, Anoplophora malasiaca, Monochamus alternatus, Psacothea hilaris, Xylotrechus pyrrhoderus, Callosobruchus chinensis, Aulacophora femoralis, Oulema oryzae, Chaetocnema concinna, Diabrotica undecimpunctata, Diabrotica virgifera, Diabrotica barberi, Phyllotreta striolata, Psylliodes angusticollis, Rhynchites heros, Cylas formicarius, Anthonomus grandis, Echinocnemus squameus, Euscepes postfasciatus, Hypera postica, Lissohoptrus oryzophilus, Otiorhynchus sulcatus, Sitophilus granarius, Sitophilus zeamais, Sphenophorus venatus vestitus, Paederus fiscipes, y similares;
insectos tisanópteros, tales como Frankliniella intonsa, Thrips flavus, Frankliniella occidentalis, Heliothrips haemorrhoidalis, Scirtothrips dorsalis, Thrips palmi, Thrips tabaci, Ponticulothrips diospyrosi, y similares;
insectos dípteros, tales como Asphondylia yushimai, Sitodiplosis mosellana, Bactrocera cucurbitae, Bactrocera dorsalis, Ceratitis capitata, Hydrellia griseola, Drosophila suzukii, Agromyza oryzae, Chromatomyia horticola, Liriomyza bryoniae, Liriomyza chinensis, Liriomyza sativae, Liriomyza trifolii, Delia platura, Delia antique, Pegomya cunicularia, Rhagoletis pomonella, Mayetiola destructor, Musca domestica, Stomoxys calcitrans, Melophagus ovinus, Hypoderma bovis, Hypoderma lineatum, Oestrus ovis, Glossina palpalis, Glossina morsitans, Prosimulium yezoensis, Tabanus trigonus, Telmatoscopus albipunctatus, Leptoconops nipponensis, Culex pipiens pallens, Aedes aegyptii, Aedes albopicutus, Anopheles hyracanus sinesis, y similares;
insectos himenópteros, tales como Apethymus kuri, Athalia rosae, Arge pagana, Neodiprion sertifer; Dryocosmus kuriphilus, Eciton burchelli, Eciton schmitti, Camponotus japonicus, Vespa mandarina, Myrmecia spp., Solenopsis spp., Monomorium pharaonis, y similares;
insectos ortópteros, tales como Teleogryllus emma, Gryllotalpa orientalis, Locusta migratoria, Oxya yezoensis, Schistocerca gregaria, y similares;
insectos colémbolos, tales como Onychiurus folsomi, Onychiurus sibiricus, Bourletiella hortensis, y similares; insectos dictiópteros, tales como Periplaneta fuliginosa, Periplaneta japonica, Blattella germanica, Periplaneta Americana, y similares;
insectos isopteros, tales como Coptotermes formosanus, Reticulitermes speratus, Odontotermes formosanus, y similares; insectos isopteros, tales como Ctenocephalidae felis, Ctenocephalides canis, Echidnophaga gallinacea, Pulex irritans, Xenopsylla cheopis, y similares;
insectos malófagos, tales como Menacanthus stramineus, Bovicola bovis, y similares;
insectos Anoplura, tales como Haematopinus eurysternus, Haematopinus suis, Linognathus vituli, Solenopotes capillataus, y similares;
Tarsonemidae, tales como Phytonemus pallidus, Polyphagotarsonemus latus, Tarsonemus bilobatus, y similares; Eupodidae, tales como Penthaleus erythrocephalus, Penthaleus major, y similares;
tetraníquidos, tales como Oligonychus shinkajii, Panonychus citri, Panonychus mori, Panonychus ulmi, Tetranychus kanzawai, Tetranychus urticae, y similares;
eriófidos, tales como Acaphylla theavagrans, Aceria tulipae, Aculops lycopersici, Aculops pelekassi, Aculus schlechtendali, Eriophyes chibaensis, Phyllocoptruta oleivora, y similares;
ácaros, tales como Rhizoglyphus robini, Tyrophagus putrescentiae, Tyrophagus similis, y similares;
Varroidae, tales como Varroa jacobsoni, y similares;
ixódidos, tales como Boophilus microplus, Rhipicephalus sanguineus, Haemaphysalis longicornis, Haemophysalis flava, Haemophysalis campanulata, Ixodes ovatus, Ixodes persulcatus, Amblyomma spp., Dermacentor spp., y similares; Cheyletidae, tales como Cheyletiella yasguri, Cheyletiella blakei, y similares;
Demodicidae, tales como Demodex canis, Demodex cati, y similares;
Psoroptidae, tales como Psoroptes ovis, y similares;
sarcóptidos, tales como Sarcoptes scabiei, Notoedres cati, Knemidocoptes spp., y similares;
crustáceos, tales como Armadillidium vulgare, y similares;
gastrópodos, tales como Pomacea canalicalata, Achatina fulica, Meghimatium bilineatum, Limax Valentiana, Acusta despecta sieboldiana, Euhadra peliomphala, y similares; y
nematodos, tales como Prathylenchus coffeae, Prathylenchus penetrans, Prathylenchus vulnus, Globodera rostochiensis, Heterodera glycines, Meloidogyne hapla, Meloidogyne incognita, Aphelenchoides besseyi, Bursaphelenchus xylophilus, y similares, pero la presente invención no se limita a los mismos.
El agente para el control de plagas que incluye el compuesto como se define en la reivindicación 1 en forma de ingrediente inactivo tiene un efecto de control significativo contra las plagas dañinas anteriormente descritas que dañan los cultivos de tierras bajas, los cultivos de tierras altas, los árboles frutales, vegetales, y otros cultivos y flores ornamentales, y por lo tanto, puede obtenerse efecto como agente para el control de plagas de la presente invención mediante el tratamiento del agua del campo de arroz, los tallos de la planta y sus hojas o el suelo de los cultivos de tierras bajas, de tierras altas, los árboles frutales, vegetales, y otros cultivos, flores ornamentales, y similares durante las temporadas en las que se espera la aparición de dichas plagas o antes o en el momento en que se observa la aparición de la plaga.
El agente para el control de plagas que incluye el compuesto como se define en la reivindicación 1 como principio activo tiene un efecto de control significativo contra plagas del grano almacenado y similares, generadas durante el almacenamiento de la cosecha. Es decir, el agente para el control de plagas que tiene el compuesto como se define en la reivindicación 1 como principio activo puede emplearse como tratamiento después de la cosecha, tal como mediante rociado, recubrimiento, empapado, revestimiento, fumigación/ahumado, inyección a presión, y similares respecto de la cosecha o el lugar para almacenar la cosecha.
Además, el agente para el control de plagas que incluye el compuesto como se define en la reivindicación 1 como principio activo puede aplicarse a semillas de plantas para prevenir el daño causado por plagas generadas en las plantas después de la siembra. Es decir, el agente para el control de plagas que tiene el compuesto como se define en la reivindicación 1 como principio activo puede emplearse como tratamiento, tal como mediante rociado, empapado, revestimiento, y similares en las semillas en una cantidad eficaz para controlar la plaga tal cual, en forma de una dilución adecuada con agua o similares o en forma de una suspensión para poner en contacto el compuesto como se define en la reivindicación 1 en contacto con las semillas.
Las semillas se refieren a aquellas usadas para su reproducción en la agricultura mediante el almacenamiento de nutrientes para la germinación de la plántula, y los ejemplos de las mismas incluyen semillas tales como maíz, soja, alubia, algodón, arroz, remolacha azucarera, trigo, cebada, girasol, tomate, pepino, berenjena, espinaca, ejotes, calabaza, caña de azúcar, tabaco, pimiento, colza, y similares, tubérculos, tales como taro, patata, batata, konjac, y similares, bulbos, tales como lirios comestibles, tulipanes, y similares, y bolas de semillas, tales como rakkyo y similares.
El agente para el control de plagas que tiene el compuesto como se define en la reivindicación 1 como principio activo tiene un efecto de control significativo contra plagas insanas, tales como plagas de dípteros (Culexpipienspallens, Culexpipiens, Chironomidae, moscas domésticas, flebótomos, tábanos, y similares), plagas de dictiópteros (Blattella germánica, Periplaneta fuliginosa, Periplaneta americana, y similares), y otras plagas.
El agente para el control de plagas que tiene el compuesto como se define en la reivindicación 1 como principio activo tiene un efecto de control significativo contra plagas xilófagas, tales como termitas, Lyctusbrunneus, Rhizopertha dominica, Anobiidae, Cerambycidae, y similares, por lo tanto, las plagas xilófagas anteriormente descritas pueden controlarse mediante el tratamiento de la madera, el suelo, los edificios, y similares con el agente para el control de plagas.
Ya que el compuesto como se define en la reivindicación 1 muestra un efecto de control frente a diversas plagas y también muestra un efecto protector para cultivos útiles y un excelente efecto de control como pesticida o miticida a una baja dosis, tiene el efecto de contribuir a la reducción de su impacto ambiental. Además, el compuesto como se define en la reivindicación 1 también ejerce un excelente efecto de control cuando se usa en combinación con otros plaguicidas, miticidas, nematicidias, fungicidas, herbicidas, reguladores del crecimiento de las plantas, agentes químicos biológicos para agricultura o similares de uso agrícola u hortícola.
Para el uso del compuesto como se define en la reivindicación 1, puede emplearse el compuesto en forma de una preparación en cualquier forma, tal como un concentrado soluble, un concentrado emulsionable, un polvo humectable, un polvo soluble en agua, un gránulo dispersable en agua, un gránulo soluble en agua, una suspensión concentrada, una emulsión concentrada, una suspoemulsión, una microemulsión, un polvo para espolvorear, un gránulo, un comprimido, y un agente emulsionable, normalmente mezclando el compuesto con un vehículo sólido o un vehículo líquido adecuado, además, en caso de que se desee, añadiendo a la mezcla resultante un tensioactivo, un penetrante, un dispersante, un espesante, un agente anticongelante, un aglutinante, un agente antiaglutinante, un disgregante, un agente desespumante, un antiséptico o un estabilizante. Además, desde el punto de vista de ahorro de trabajo y de mejora de la seguridad, el compuesto puede emplearse encapsulando la preparación anterior en cualquier forma en un material de envasado hidrosoluble, tal como una cápsula hidrosoluble y una bolsa de película hidrosoluble.
El vehículo inerte que puede usarse en la presente invención puede ser sólido o líquido, y los ejemplos de los mismos incluyen polvos de soja, polvos de grano, polvo de madera, polvo de corteza, serrín, polvos del tallo del tabaco, polvo de cáscara de nuez, salvados, polvos de celulosa, residuos de la extracción de plantas, polímeros sintéticos, tales como resinas sintéticas pulverizadas, arcillas (por ejemplo, caolín, bentonita, arcilla blanca ácida), talcos (por ejemplo, talco, pirofilita, etc.), sílice (por ejemplo, tierra de diatomeas, arena, mica, carbón blando [polvo de sílice hidratado, silicatos sintéticos de alta dispersidad denominados silicato hidroso, también existen productos que contienen silicato de calcio como componente principal]), carbono activado, polvo de azufre, pumita, polvos de diatomeas calcinados, ladrillos pulverizados, cenizas volantes, arena, polvos minerales inorgánicos, tales como carbonato de calcio, fosfato de calcio, y similares, fertilizantes químicos, tales como sulfato de amonio, fosfato de amonio, nitrato de amonio, urea, cloruro de amonio, y similares, un compost, y otros, que se usan solos o en forma de una mezcla de dos o más tipos de los mismos.
Los materiales que pueden usarse como vehículo líquido inerte se seleccionan entre aquellos que tienen función de disolvente, así como aquellos capaces de dispersar el principio activo con la ayuda de un adyuvante, incluso en el caso de que el vehículo inerte no tenga función de disolvente. Los ejemplos representativos de los mismos incluyen
los vehículos listados a continuación: agua, alcoholes (por ejemplo, metanol, etanol, isopropanol, butanol, etilenglicol, y similares), cetonas (por ejemplo, acetona, metil etil cetona, metil isobutil cetona, diisobutilcetona, ciclohexanona, y similares), éteres (por ejemplo, éter dietílico, dioxano, cellosolve, éter de diisopropilo, tetrahidrofurano, y similares), hidrocarburos alifáticos (por ejemplo, queroseno, aceite mineral, y similares), hidrocarburos aromáticos (por ejemplo, benceno, tolueno, xileno, disolvente de nafta, alquil naftaleno, y similares), hidrocarburos halogenados (por ejemplo, diclorometano, cloroformo, tetraclorocarbono, clorobenceno, y similares), ésteres (por ejemplo, acetato de etilo, acetato de butilo, propionato de etilo, di-isobutilftalato, dibutilftalato, dioctilftalato, y similares), amidas (por ejemplo, dimetil formamida, dietil formamida, dimetil acetamida, y similares), y nitrilos (por ejemplo, acetonitrilo, y similares), que se usan solos o en forma de mezclas de dos o más tipos de los mismos.
Estos vehículos sólidos y líquidos pueden usarse solos o en una combinación de dos o más tipos de los mismos.
Los ejemplos del tensioactivo incluyen tensioactivos no iónicos, tales como éteres alquílicos de polioxietileno, (mono o di)fenil éteres alquílicos de polioxietileno, (mono-, di- o tri-)estiril fenil éteres de polioxietileno, copolímeros de bloque de polioxietileno-polioxipropileno, (mono- o di-)ésteres de ácidos alifáticos de polioxietileno, ésteres de ácidos alifáticos de sorbitano, ésteres de ácidos alifáticos de polioxietileno sorbitano, aductos de aceite ricino-óxido de etileno, acetilenglicol, alcoholes acetilénicos, aductos de acetilenglicol-óxido de etileno, aductos de alcohol acetilénico-óxido de etileno, glucósidos de alquilo, y similares; tensioactivos aniónicos, tales como sales de éster de sulfato de alquilo, sulfonatos de alquilbenceno, sulfonatos de lignina, sulfosuccinatos de alquilo, sulfonatos de naftaleno, sulfonatos de alquilnaftaleno, sales de condensado con formalina de sulfonato de naftaleno, sales de condensado con formalina de sulfonato de alquilnaftaleno, sales de ésteres de sulfato o fosfato de polioxietilenalquiléter, ésteres de sulfato o fosfato de (mono- o di-)alquilfenil éter de polioxietileno, ésteres de sulfato o fosfato de (mono-, di- o tri-)estirilfenil éter de polioxietileno, sales de ácidos policarboxílicos (tales como sales de ácido poliacrílico, sales de ácido polimaleico, copolímeros de ácido maleico-olefina, y similares), sulfonatos de poliestireno, y similares; tensioactivos catiónicos, tales como sales de alquilamina, sales alquílicas de amonio cuaternario, y similares; tensioactivos anfóteros, tales como tensioactivos de tipo aminoácido, tensioactivos de tipo betaína, y similares; tensioactivos basados en silicona; y tensioactivos fluorados.
El contenido de estos tensioactivos no está particularmente limitado, pero se encuentra preferentemente en el intervalo de normalmente 0,05 partes en peso a 20 partes en peso, con respecto a 100 partes en peso de la preparación de la presente invención. Además, estos tensioactivos pueden usarse solos o en combinación con dos o más tipos de los mismos.
Para controlar diversas plagas, puede aplicarse una cantidad eficaz para el control la roya tal cual o en forma de una dilución adecuada con agua o similares o en forma de una suspensión, a los cultivos en los que puede esperarse la aparición de las plagas correspondientes o en sitios donde no es deseable dicha aparición. La cantidad empleada depende de diversos factores, tales como, por ejemplo, el fin, la plaga que va a controlarse, el estado de crecimiento de la planta, las tendencias de aparición de la plaga, el clima, las condiciones ambientales, la formulación, el método de uso, el lugar de uso, el momento del uso, y similares, pero es preferible usar el principio activo a una concentración de 0,0001 ppm a 5000 ppm, y preferentemente de 0,01 ppm a 1000 ppm. La dosis que puede usarse por cada 10 a se encuentra generalmente en el intervalo de 1 g a 300 g del principio activo.
La cantidad del principio activo del compuesto como se define en la reivindicación 1 es normalmente del 0,1 % en peso al 20 % en peso para polvos, del 5 % en peso al 50 % en peso para los concentrados emulsionables, del 3 % en peso al 90 % en peso para los polvos humectables, del 0,1 % en peso al 20 % en peso para los gránulos, del 5 % en peso al 90 % en peso para las formulaciones fluidas o del 3 % en peso al 90 % en peso para los gránulos dispersables en agua. La cantidad del vehículo en cada forma es normalmente del 60 % en peso al 99,9 % en peso para polvos, del 40 % en peso al 95 % en peso para los concentrados emulsionables, del 10 % en peso al 90 % en peso para los polvos humectables, del 80 % en peso al 99,9 % en peso para los gránulos, del 10 % en peso al 95 % en peso para las formulaciones fluidas o del 10 % en peso al 90 % en peso para los gránulos dispersables en agua. Además, la cantidad del adyuvante es normalmente del 0,1 % en peso al 20 % en peso para polvos, del 1 % en peso al 20 % en peso para los concentrados emulsionables, del 0,1 % en peso al 20 % en peso para los polvos humectables, del 0,1 % en peso al 20 % en peso para los gránulos, del 0,1 % en peso al 20 % en peso para las formulaciones fluidas, y del 0,1 % en peso al 20 % en peso para los gránulos dispersables en agua.
Cuando el compuesto como se define en la reivindicación 1 se usa como agente químico agrícola, puede usarse, en caso necesario, como una mezcla con otros herbicidas, diversos plaguicidas, miticidas, nematicidias, fungicidas, reguladores del crecimiento de las plantas, sinérgicos, fertilizantes, acondicionadores del suelo o similares para su aplicación durante la preparación o el espolvoreado.
Ejemplos
Los ejemplos representativos de la presente invención se describirán con referencia a los siguientes Ejemplos, pero la presente invención no se limita a los mismos. En los presentes Ejemplos, DMF significa N,N-dimetilformamida, THF significa tetrahidrofurano, IPE significa éter isopropílico, DMI significa 1,3-dimetil-2-imidazolidinona, y DMSO significa dimetilsulfóxido.
Adicionalmente, el "%" está basado masa a menos que se especifique lo contrario.
<Ejemplo 1>
Preparación de N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-2-fluoro-3-(N-metilbenzamida)benzamida (Compuesto N.° 7-1574).
<1-1>
Preparación de 4-(perfluoropropan-2-il)-2-(trifluorometil)anilina
Se cargaron 100 g (0,608 mol) de 2-(trifluorometil)anilina, 131 g (0,639 mol) de hidrosulfito sódico al 85 % y 20,9 g (0,0608 mol) de hidrogenosulfato de tetrabutilamonio en una solución mixta de 1500 ml de acetato de etilo y 1500 ml de agua, y se le añadieron 53,9 g (0,639 mol) de hidrogenocarbonato sódico. Se le añadieron gota a gota 198 g (0,669 mol) de yoduro de heptafluoroisopropilo a temperatura ambiente, seguido de agitación a temperatura ambiente durante 6 horas. Después de la separación de líquidos, el disolvente de la capa orgánica se evaporó a presión reducida, y se le cargaron 500 ml de acetato de etilo. Se le añadieron gota a gota 160 g (0,608 mol) de una solución 4 M de cloruro de hidrógeno/acetato de etilo, seguido de agitación a temperatura ambiente durante 30 minutos, y después agitando a 5 °C durante 1 hora. Después de la filtración, el filtrado se lavó con agua y una solución acuosa saturada de hidrogenocarbonato sódico en este orden, y después se secó sobre sulfato de magnesio anhidro, y el disolvente se evaporó a presión reducida. El residuo obtenido se purificó por cromatografía en columna sobre gel de sílice (disolvente eluyente; hexano:acetato de etilo = 10:1) para preparar 60,0 g (rendimiento 30 %) de un compuesto diana.
RMN 1H (CDCla, ppm) 84,49 (2H, s ancho), 6,81 (1H, d, J = 8,3 Hz), 7,48 (1H, d, J = 8,3 Hz), 7,64 (1H, s).
<1-2>
Preparación de 2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)anilina
Se cargaron 100 g (0,273 mol) de 4-(perfluoropropan-2-il)-2-(trifluorometil)anilina en 500 ml de DMF, y se le cargaron en porciones separadas 52,1 g (0,287 mol) de N-bromosuccinimida durante 30 minutos. Después de agitar a 60 °C durante 2 horas, y después enfriar a temperatura ambiente, la mezcla se descargó a 2000 ml de agua. La mezcla se extrajo con acetato de etilo, después se lavó con salmuera saturada, y se secó sobre sulfato de magnesio anhidro. El disolvente se evaporó a presión reducida y el residuo obtenido se purificó por cromatografía en columna sobre gel de sílice (disolvente eluyente; hexano:acetato de etilo = 20:1) para preparar 89,0 g (rendimiento 80 %) de un compuesto diana.
RMN 1H (CDCla, ppm) 55,03 (2H, s ancho), 7,61 (1H, s), 7,79 (1H, s).
<1-3>
Preparación de N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-2-doro-3-nitrobenzamida
Se cargaron 3,60 g (8,82 mmol) de 2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)anilina en 20 ml de THF anhidro, y se enfriaron a -70 °C en una atmósfera de nitrógeno. Se le añadieron gota a gota 4,85 ml (9,70 mmol) de a una solución 2,0 M de diisopropilamida de litio en hexano, después se disolvieron 2,34 g (10,7 mmol) de cloruro de ácido, que se preparó a partir de ácido 2-cloro-3-nitrobenzoico y cloruro de tionilo, en 5 ml de THF anhidro, y se le añadió gota a gota, seguido de agitación a -70 °C durante 30 minutos y después agitación a temperatura ambiente durante 30 minutos. La mezcla se descargó a una solución acuosa de cloruro de amonio, después se extrajo con acetato de etilo, y se secó sobre sulfato de magnesio anhidro. El disolvente se evaporó a presión reducida y el residuo obtenido se purificó por cromatografía en columna sobre gel de sílice (disolvente eluyente; hexano:acetato de etilo = 10 :1^8 :2^3 :1 ) para preparar 1,76 g (rendimiento: 34 %) de un compuesto diana.
RMN 1H (CDCla, ppm) 57,61 (1H, t, J = 7,8 Hz), 7,67 (1H, s ancho), 7,93-7,97 (3H, m), 8,18 (1H, s ancho).
<1-4>
Preparación de N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-2-fluoro-3-nitrobenzamida
A una solución de N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-2-cloro-3-nitrobenzamida 4,89 g (8,27 mmol) en 50 ml de DMF anhidra se le añadieron 2,40 g (41,3 mmol) de fluoruro potásico (producto secado por pulverización) en un flujo de nitrógeno, seguido de agitación a 130 °C durante 10 horas. Se realizó separación de líquidos añadiendo acetato de etilo, hexano, y agua a la mezcla de reacción, y después la capa orgánica se lavó con agua y salmuera saturada, y se secó sobre sulfato de magnesio anhidro. El disolvente se evaporó a presión reducida y el residuo obtenido se purificó por cromatografía en columna sobre gel de sílice (disolvente eluyente; hexano: acetato de etilo = 10:1) para preparar 0,940 g (rendimiento 20 %) de un compuesto diana.
RMN 1H (CDCls, ppm) 57,53 (1H, t, J = 7,3 Hz), 7,93 (1H, s ancho), 8,17-8,18 (2H, m), 8,28-8,32 (1H, m), 8,44-8,48 (1H, m).
<1-5>
Preparación de 3-amino-N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-2-fluorobenzamida
Se añadieron 0,940 g (1,63 mmol) de N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-2-fluoro-3-nitrobenzamida y 0,960 g (5,05 mmol) de cloruro estanoso (anhidro) a 10 ml de etanol, y se le añadieron 1,02 ml (9,78 mmol) de ácido clorhídrico concentrado, seguido de agitación a 60 °C durante 4 horas. La mezcla de reacción se ajustó a pH 10 mediante la adición de una solución acuosa de hidróxido sódico, y los materiales insolubles precipitados se retiraron por filtración usando Celite. El filtrado en Celite se lavó con acetato de etilo. El filtrado se extrajo con acetato de etilo, y la capa orgánica se lavó con una solución acuosa al 20 % de hidróxido sódico y salmuera saturada, y después se secó sobre sulfato de magnesio anhidro. El disolvente se evaporó a presión reducida y el residuo obtenido se purificó por cromatografía en columna sobre gel de sílice (disolvente eluyente; hexano:acetato de etilo = 4:1) para preparar 0,930 g (rendimiento 99 %) de un compuesto diana.
RMN 1H (CDCla, ppm) 83,93 (2H, s ancho), 6,99-7,04 (1H, m), 7,11 (1H, t, J = 7,8 Hz), 7,47-7,49 (1H, m), 7,91 (1H, s), 8,14 (1H, s), 8,28 (1H, d, J = 14,6 Hz).
<1-6>
Preparación de N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-2-fluoro-3-(metilamino)benzamida
Se añadieron 0,930 g (1,71 mmol) de 3-amino-N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-2-fluorobenzamida a 5 ml de ácido sulfúrico concentrado y se le cargaron gota a gota 10 ml de una solución acuosa al 37 % de formaldehído a 40 °C. La mezcla de reacción se vertió en agua enfriada con hielo, se ajustó a pH 10 usando una solución acuosa de hidróxido sódico, y se extrajo con la adición de acetato de etilo. La capa orgánica se lavó con una solución acuosa al 20 % de hidróxido sódico y salmuera saturada, y después se secó sobre sulfato de magnesio anhidro. El disolvente se evaporó a presión reducida y el residuo obtenido se purificó por cromatografía en columna sobre gel de sílice (disolvente eluyente; hexano:acetato de etilo = 8:1) para preparar 0,690 g (rendimiento 72 %) de un compuesto diana.
RMN 1H (CDCla, ppm) 82,94 (3H, s), 4,14 (1H, s ancho), 6,88-6,93 (1H, m), 7,18 (1H, t, J = 7,8 Hz), 7,37-7,41 (1H, m), 7,90 (1H, s), 8,13 (1H, s), 8,27 (1H, d, J = 14,6 Hz).
[1-7] Preparación de N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-2-fluoro-3-(N-metilbenzamida)-benzamida (Compuesto N.° 7-1574)
A una solución de 1,54 g (2,75 mmol) de N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-2-fluoro- 3-(metilamino)benzamida y 0,330 g (4,13 mmol) de piridina en 5 ml de THF se le añadieron 0,460 g (3,30 mmol) de cloruro de benzoílo, seguido de agitación a 60 °C durante 5 horas. A la mezcla de reacción se le añadieron agua y
acetato de etilo, y la capa orgánica se lavó con ácido clorhídrico 1 M, una solución acuosa saturada de hidrogenocarbonato sódico, y salmuera saturada, y después se secó sobre sulfato de magnesio anhidro. El disolvente se evaporó a presión reducida y el residuo obtenido se purificó por cromatografía en columna sobre gel de sílice (disolvente eluyente; hexano:acetato de etil = 8:1), y el sólido obtenido se lavó con IPE para preparar 1,45 g (rendimiento 80 %) de un compuesto diana.
RMN 1H (CDCla, ppm) 83,50 (3H, s), 6,99-7,33 (6H, m), 7,43-7,45 (1H, m), 7,90 (1H, s), 7,97-8,06 (2H, m), 8,13 (1H, s).
<Ejemplo 2>
Preparación de 2-cloro-N-(3-(2,6-dibromo-4-(perfluoropropan-2-il)fenilcarbamoil)-2-fluorofenil)nicotinamida (Compuesto N.° 6-1140)
Se cargaron 100 g (1,02 mol) de anilina, 230 g (1,12 mol) de hidrosulfito sódico al 85% y 35,1 g (0,100 mol) de hidrógeno sulfato de tetrabutilamonio a una solución mixta de 1500 ml de t-butil metil éter y 1500 ml de agua, y se le añadieron 94,7 g (1,12 mol) de hidrogenocarbonato sódico. Se le añadieron gota a gota 350 g (1,12 mol) de yoduro de heptafluoroisopropilo a temperatura ambiente, seguido de agitación a temperatura ambiente durante 6 horas. Después de la separación de líquidos, la capa orgánica se lavó con ácido clorhídrico 1 M, agua, y una solución acuosa saturada de hidrogenocarbonato sódico, y después se secó sobre sulfato sódico anhidro. El disolvente se evaporó a presión reducida, y se le cargaron 500 ml de acetato de etilo. Se le añadieron gota a gota 255 g (1,02 mol) de una solución 4 M de cloruro de hidrógeno/acetato de etilo, seguido de agitación a temperatura ambiente durante 30 minutos y a 5 °C durante 1 hora. El sólido precipitado se separó por filtración, y el sólido se cargó en 1000 ml de acetato de etilo, se ajustó a pH de 8 a 9 mediante la adición de 1000 ml de una solución acuosa saturada de hidrogenocarbonato sódico a 20 °C o menos, y se sometió a separación de líquidos. La capa orgánica se secó sobre sulfato sódico anhidro, y después el disolvente se evaporó a presión reducida para preparar 188 g (rendimiento del 71 %) de un compuesto diana.
RMN 1H (CDCla, ppm) 83,92 (2H, s ancho), 6,69-6,74 (2H, m), 7,35 (2H, d, J = 9,3 Hz).
<2-2>
Preparación de 2,6-dibromo-4-(perfluoropropan-2-il)anilina
Se cargaron 216 g (0,802 mol) de 4-(perfluoropropan-2-il)anilina en 863 ml de DMF, seguido de refrigeración a 5 °C. Se le cargaron en porciones separadas 285 g (1,60 mol) de N-bromosuccinimida durante 1 hora. La mezcla se agitó a temperatura ambiente durante 1 hora y después se agitó a 37 °C durante 2 horas. La mezcla se descargó a 2000 ml
de agua, se extrajo con 2000 ml de acetato de etilo, y se lavó con 1000 ml de salmuera saturada. Después de secar sobre sulfato de magnesio anhidro, el disolvente se evaporó a presión reducida. El residuo obtenido se purificó por cromatografía en columna sobre gel de sílice (disolvente eluyente; hexano:acetato de etilo = 20:1) para preparar 304 g (rendimiento 90 %) de un compuesto diana.
RMN 1H (CDCla, ppm) 84,88 (2H, s ancho), 7,59 (2H, s).
<2-3>
Preparación de 2-cloro-N-(2,6-dibromo-4-(perfluoropropan-2-il)fenil)-3-nitrobenzamida
De acuerdo con el método de 1-3 del Ejemplo 1, se preparó un compuesto diana a partir de 2,6-dibromo-4-(perfluoropropan-2-il)anilina.
RMN 1H (CDCla, ppm) 87,58 (1H, t, J = 7,8 Hz), 7,66 (1H, s ancho), 7,90 (2H, s), 7,93 (1H, dd, J = 1,5, 7,8 Hz), 7,98 (1H, d, J = 7,8 Hz).
<2-4>
Preparación de N-(2,6-dibromo-4-(perfluoropropan-2-il)fenil)-2-fluoro-3-nitrobenzamida
De acuerdo con el método de 1-4 del Ejemplo 1, un compuesto diana se preparó a partir de 2-cloro-N-(2,6-dibromo-4-(perfluoropropan-2-il)fenil)-3-nitrobenzamida.
RMN 1H (CDCls, ppm) 87,51-7,55 (1H, m), 7,90 (2H, s), 8,16 (1H, d, J = 11,7 Hz), 8,27-8,31 (1H, m), 8,48 (1H, t, J = 6,3 Hz).
<2-5>
Preparación de 3-amino-N-(2,6-dibromo-4-(perfluoropropan-2-il)fenil)-2-fluorobenzamida
De acuerdo con el método de 1-5 del Ejemplo 1, un compuesto diana se preparó a partir de N-(2,6-dibromo-4-(perfluoropropan-2-il)fenil)-2-fluoro-3-nitrobenzamida.
RMN 1H (CDCls, ppm) 83,93 (2H, s ancho), 6. 99-7,04 (1H, m), 7,11 (1H, t, J = 7,8 Hz), 7,47-7,49 (1H, m), 7,91 (1H, s), 8,14 (1H, s), 8,28 (1H, d, J = 14,6 Hz).
<2-6>
Preparación de 2-doro-N-(3-(2,6-dibromo-4-(perfluoropropan-2-il)fenilcarbamoil)-2-fluorofenil)nicotinamida (Compuesto N.° 6-1140)
De acuerdo con el método de 1-7 del Ejemplo 1, un compuesto diana se preparó a partir de 3-amino-N-(2,6-dibromo-4-(perfluoropropan-2-il)fenil)-2-fluorobenzamida y cloruro del ácido 2-cloronicotínico.
RMN 1H (CDCla, ppm) 87,40-7,49 (2H, m), 7. 89 (2H, s), 7,94-7,96 (1H, m), 8. 13 (1H, d, J = 12,7 Hz), 8,32-8,34 (1H, m), 8,57-8,59 (1H, m), 8,67-8,71 (1H, m), 8,75 (1H, s ancho).
<Ejemplo 3>
Preparación de 3-benzamida-2-fluoro-N-(4-(perfluoropropan-2-il)-2,6-bis(trifluorometil)fenil)benzamida (Compuesto N.° 6-2110)
<3-1>
Preparación de 2,6-diyodo-4-(perfluoropropan-2-il)anilina
A una solución de 5,74 g (22,0 mmol) de 4-(perfluoropropan-2-il)anilina obtenida en 2-1 del Ejemplo 2 en 50 ml de etanol se le añadieron 2,16 g (22,0 mmol) de ácido sulfúrico concentrado a 5 °C. La mezcla de reacción se calentó a temperatura ambiente, y se le añadieron 10,0 g (44,0 mmol) de N-yodosuccinimida, seguido de agitación durante 3 horas. La mezcla de reacción se neutralizó con a una solución saturada de hidrogenocarbonato sódico. Los cristales precipitados se filtraron, se lavaron con agua, y después se secaron para preparar 9,00 g (rendimiento 80 %) de un compuesto diana.
RMN 1H (CDCla, ppm) 84,95 (2H, s ancho), 7,79 (2H, s).
<3-2>
Preparación de 2-cloro-N-(2,6-diyodo-4-(perfluoropropan-2-il)fenil)-3-nitrobenzamida
A una solución de 40,0 g (78,0 mmol) de 2,6-diyodo-4-(perfluoropropan-2-il)anilina en 100 ml de DMI se le añadieron 20,6 g (94,0 mmol) de cloruro de 2-cloro-3-nitrobenzoílo, seguido de agitación a 135 °C durante 3 horas. Después de enfriar a temperatura ambiente, la mezcla de reacción se vertió en 1000 ml de agua. Después de la extracción con la adición de 1000 ml de acetato de etilo, la capa orgánica se lavó con agua y después se secó sobre sulfato de magnesio anhidro. El disolvente se evaporó a presión reducida y el residuo obtenido se lavó con hexano para preparar 56,2 g (rendimiento 99 %) de un compuesto diana.
RMN 1H (CDCla, ppm) 87,58 (1H, t, J = 8,3 Hz), 7,70 (1H, d, J = 3,4 Hz), 7,93 (1H, dd, J = 1,5, 6,3 Hz), 8,08-8,10 (1H, m), 8,13 (2H, s).
<3-3>
Preparación de N-(2,6-diyodo-4-(perfluoropropan-2-il)fenil)-2-fluoro-3-nitrobenzamida
De acuerdo con el método de 1-4 del Ejemplo 1, un compuesto diana se preparó a partir de 2-cloro-N-(2,6-diyodo-4-(perfluoropropan-2-il)fenil)-3-nitrobenzamida.
RMN 1H (CDCla, ppm) 87,52-7,55 (1H, m), 8,12-8,18 (3H, m), 8,29-8,32 (1H, m), 8,48-8,51 (1H, m).
<3-4>
Preparación de 3-amino-N-(2,6-diyodo-4-(perfluoropropan-2-il)fenil)-2-fluorobenzamida
De acuerdo con el método de 1-5 del Ejemplo 1, un compuesto diana se preparó a partir de N-(2,6-diyodo-4-(perfluoropropan-2-il)fenil)-2-fluoro-3-nitrobenzamida.
RMN 1H (CDCls, ppm) 83,93 (2H, s ancho), 6,99-7,04 (1H, m), 7,08 (1H, t, J = 7,8 Hz), 7,39-7,43 (1H, m), 8,10 (2H, s), 8,72 (1H, d, J = 11,2 Hz).
<3-5>
Preparación de 3-benzamida-N-(2,6-diyodo-4-(perfluoropropan-2-il)fenil)-2-fluorobenzamida (Compuesto N.° 6-1260)
De acuerdo con el método de 1-7 del Ejemplo 1, un compuesto diana se preparó a partir de 3-amino-N-(2,6-diyodo-4-(perfluoropropan-2-il)fenil)-2-fluorobenzamida.
RMN 1H (CDCla, ppm) 87,39 (1H, t, J = 7,8 Hz), 7,52-7,57 (4H, m), 7,60-7,63 (2H, m), 7,93-7,94 (4H, m), 8,70 (1H, t, J = 6,3 Hz).
<3-6>
Preparación de 3-benzamida-2-fluoro-N-(4-(perfluoropropan-2-il)-2,6-bis(trifluorometil)fenil)benzamida (Compuesto N.° 6-2110)
Una solución de 1,95 g (2,59 mmol) de 3-benzamida-N-(2,6-diyodo-4-(perfluoropropan-2-il)fenil)-2-fluorobenzamida, 0,10 g (0,520 mmol) de yoduro de cobre, y 1,24 g (6,48 mmol) de difluoroacetato de metil fluorosulfonilo en 50 ml de DMF se agitó a 100 °C durante 6 horas. La mezcla de reacción se enfrió a temperatura ambiente, y después se le añadieron 10 ml de agua y 100 ml de acetato de etilo, seguido de filtración a través de Celite. La capa orgánica del líquido se lavó con agua y una solución saturada de hidrogenocarbonato sódico, y después se secó sobre sulfato de magnesio anhidro. El disolvente se evaporó a presión reducida y el residuo obtenido se purificó por cromatografía en columna sobre gel de sílice (disolvente eluyente; hexano:acetato de etilo = 1:1). El sólido obtenido se lavó con hexano para preparar 0,840 g (rendimiento 51 %) de un compuesto diana.
RMN 1H (CDCla, ppm) 87,36-7,40 (1H, m), 7,53-7,64 (3H, m), 7,84-7,97 (1H, m), 7,92-7,94 (2H, m), 8,04-8,07 (1H, m), 8,08-8,13 (1H, m), 8,20 (2H, s), 8,68-8,72 (1H, m).
<Ejemplo 4>
Preparación de N-(2,6-dibromo-4-(perfluorobutan-2-il)fenil)-2-fluoro-3-(N-metilbenzamida)benzamida (Compuesto N.° 7-1182)
<4-1>
Preparación de 4-(perfluorobutan-2-il)anilina
Se cargaron 4,90 g (52,6 mmol) de anilina, 10,1 g (58,0 mmol) de hidrosulfito sódico al 85 % y 1,90 g (5,77 mmol) de hidrógenosulfato de tetrabutilamonio en una solución mixta de 150 ml de t-butil metil éter y 150 ml de agua usando un recipiente de reacción ligeramente protegido, y se le añadieron 4,84 g (57,6 mmol) de hidrogenocarbonato sódico. Se le añadieron gota a gota 20,0 g (57,8 mmol) de yoduro de nonafluoro-s-butilo a temperatura ambiente, seguido de agitación a temperatura ambiente durante 5 horas. La fase orgánica se recogió mediante separación, se lavó dos veces con 2 mol/l de una solución acuosa de ácido clorhídrico, y después se lavó con salmuera saturada, una solución acuosa de hidrogenocarbonato sódico, y salmuera saturada. La capa orgánica se secó sobre sulfato de magnesio anhidro, y después el disolvente se evaporó a presión reducida para preparar 8,32 g (rendimiento del 51 %) de un compuesto diana.
RMN 1H (CDCla, ppm) 83,92 (2H, s ancho), 6,72 (2H, d, J = 8,8 Hz), 7,34 (2H, d, J = 8,8 Hz).
<4-2>
Preparación de 2,6-dibromo-4-(perfluorobutan-2-il)anilina
De acuerdo con el método de 2-2 del Ejemplo 2, un compuesto diana se preparó a partir de 4-(perfluorobutan-2-il)anilina.
RMN 1H (CDCla, ppm) 84,89 (2H, s ancho), 7,57 (2H, s).
<4-3>
Preparación de 2-cloro-N-(2,6-dibromo-4-(perfluorobutan-2-il)fenil)-3-nitrobenzamida
A 27 ml de DMI se le añadieron 9,90 g (21,1 mmol) de 2,6-dibromo-4-(perfluorobutan-2-il)anilina y 4,60 g (20,9 mmol) de cloruro de 2-cloro-3-nitrobenzoílo, seguido de agitación a 140 °C durante 4 horas. A la solución de reacción se le añadieron agua y acetato de etilo, y la fase orgánica se extrajo, y se lavó con 1 mol/l de una solución acuosa de hidróxido sódico acuoso, salmuera saturada, y se secó sobre sulfato de magnesio anhidro. Después, el disolvente se evaporó a presión reducida. El residuo obtenido se purificó por cromatografía en columna sobre gel de sílice (disolvente eluyente; hexano:acetato de etilo = 20 :1 ^10 :1 ^5 :1 ^3 :1 ) para preparar 5,44 g (rendimiento 40 %) de un compuesto diana.
RMN 1H (CDCls, ppm) 87,52-7,61 (2H, m), 7. 89 (2H, s), 7. 94 (1H, dd, J = 1,5, 8. 3 Hz), 7. 99 (1H, d, J = 7,8 Hz). <4-4>
Preparación de N-(2,6-dibromo-4-(perfluorobutan-2-il)fenil)-2-fluoro-3-nitrobenzamida
A 108 ml de DMSO se le añadieron 5,44 g (8,34 mmol) de 2-cloro-N-(2,6-dibromo-4-(perfluorobutan-2-il)fenil)- 3-nitrobenzamida y 4,90 g (84,3 mmol) de fluoruro potásico (producto secado por pulverización), seguido de agitación a 145 °C durante 2 horas. La solución de reacción se vertió en hielo-agua para precipitar el cristal, y los cristales obtenidos se filtraron y se lavaron con hexano. Los cristales obtenidos se purificaron por cromatografía en columna sobre gel de sílice (disolvente eluyente; hexano:acetato de etilo = 5:1) para preparar 2,42 g (rendimiento 46 %) de un compuesto diana.
RMN 1H (CDCla, ppm) 87,53-7,54 (1H, m), 7,89 (2H, s), 8,17 (1H, d, J = 12,2 Hz), 8,29-8,30 (1H, m), 8,48-8,49 (1H, m).
<4-5>
Preparación de 3-amino-N-(2,6-dibromo-4-(perfluorobutan-2-il)fenil)-2-fluorobenzamida
De acuerdo con el método de 1-5 del Ejemplo 1, un compuesto diana se preparó a partir de N-(2,6-dibromo-4-(perfluorobutan-2-il)fenil)-2-fluoro-3-nitrobenzamida.
RMN 1H (CDCla, ppm) 83,92 (2H, s ancho), 6,99-7,04 (1H, m), 7,11-7,12 (1H, m), 7,48-7,52 (1H, m), 7,86 (2H, s), 8,22 (1H, d, J = 14,1 Hz).
<4-6>
Preparación de N-(2,6-dibromo-4-(perfluorobutan-2-il)fenil)-2-fluoro-3-(metilamino)benzamida
De acuerdo con el método de 1-6 del Ejemplo 1, un compuesto diana se preparó a partir de 3-amino-N-(2,6-dibromo-4-(perfluorobutan-2-il)fenil)-2-fluorobenzamida.
RMN 1H (CDCls, ppm) 82,95 (3H, s), 4,14 (1H, s ancho), 6,91-6,92 (1H, m), 7,17-7,21 (1H, m), 7,39-7,43 (1H, m), 7,85 (2H, s), 8,21 (1H, d, J = 14,1 Hz).
<4-7>
Preparación de N-(2,6-dibromo-4-(perfluorobutan-2-il)fenil)-2-fluoro-3-(N-metilbenzamida)benzamida (Compuesto N.° 7-1182)
De acuerdo con el método de 1-7 del Ejemplo 1, un compuesto diana se preparó a partir de N-(2,6-dibromo-4-(perfluorobutan-2-il)fenil)-2-fluoro-3-(metilamino)benzamida.
RMN 1H (CDCla, ppm) 83,51 (3H, s), 7,22-7,44 (7H, m), 7,85 (2H, s), 8,00-8,03 (2H, m).
<Ejemplo 5>
Preparación de N-(2-bromo-6-(perfluoroetil)-4-(perfluoropropan-2-il)fenil)-3-(4-cianobenzamida)-2-fluorobenzamida (Compuesto N.° 6-5911)
<5-1>
Preparación de 2-(perfluoroetil)-4-(perfluoropropan-2-il)anilina
De acuerdo con el método de 1-1 del Ejemplo 1, un compuesto diana se preparó a partir de 4-(perfluoropropan-2-il)anilina obtenida en el Ejemplo 2-1 y yoduro de 1,1,2,2,2-pentafluoroetilo.
RMN 1H (CDCla, ppm) 84,56 (2H, s ancho), 6,79 (1H, d, J = 8,8 Hz), 7,47 (1H, d, J = 8,8 Hz), 7,53 (1H, s).
<5-2>
Preparación de 2-bromo-6-(perfluoroetil)-4-(perfluoropropan-2-il)anilina
De acuerdo con el método de 1-2 del Ejemplo 1, un compuesto diana se preparó a partir de 2-(perfluoroetil)-4-(perfluoropropan-2-il)anilina.
RMN 1H (CDCla, ppm) 85,14 (2H, s ancho), 7,58 (1H, s), 7,81 (1H, s).
<5-3>
Preparación de N-(2-bromo-6-(perfluoroetil)-4-(perfluoropropan-2-il)fenil)-2-cloro-3-nitrobenzamida
De acuerdo con el método de 4-3 del Ejemplo 4, un compuesto diana se preparó a partir de 2-bromo-6-(perfluoroetil)-4-(perfluoropropan-2-il)anilina.
RMN 1H (CDCla, ppm) 87,56-7,61 (1H, m), 7,73 (1H, s), 7,88 (1H, d, J = 1,5 Hz), 7,92-7,98 (2H, m), 8,21 (1H, s). <5-4>
Preparación de N-(2-bromo-6-(perfluoroetil)-4-(perfluoropropan-2-il)fenil)-2-fluoro-3-nitrobenzamida
De acuerdo con el método de 1-4 del Ejemplo 1, un compuesto diana se preparó a partir de N-(2-bromo-6-(perfluoroetil)-4-(perfluoropropan-2-il)fenil)-2-cloro-3-nitrobenzamida.
APCI-EM m/z (M+1):626
<5-5>
Preparación de 3-amino-N-(2-bromo-6-(perfluoroetil)-4-(perfluoropropan-2-il)fenil)-2-fluorobenzamida
De acuerdo con el método de 1-5 del Ejemplo 1, un compuesto diana se preparó a partir de N-(2-bromo-6-(perfluoroetil)-4-(perfluoropropan-2-il)fenil)-2-fluoro-3-nitrobenzamida.
RMN 1H (CDCla, ppm) 8 3,92 (2H, s ancho), 6,99-7,04 (1H, m), 7,05-7,18 (1H, m), 7,46-7,51 (1H, m), 7,85 (1H, s ancho), 8,17 (1H, s ancho), 8,34 (1H, d, J = 15,1 Hz).
<5-6>
Preparación de N-(2-bromo-6-(perfluoroetil)-4-(perfluoropropan-2-il)fenil)-3-(4-cianobenzamida)-2-fluorobenzamida (Compuesto N.° 6-5911)
De acuerdo con el método de 1-7 del Ejemplo 1, un compuesto diana se preparó a partir de 3-amino-N-(2-bromo-6-(perfluoroetil)-4-(perfluoropropan-2-il)fenil)-2-fluorobenzamida y cloruro de 4-cianobenzoílo.
RMN 1H (CDCla, ppm) 87,41 (1H, t, J = 8,3 Hz), 7,84-7,87 (3H, m), 7,91-7,95 (1H, m), 8,03-8,05 (2H, m), 8,10 (1H, s ancho), 8,17-8,20 (2H, m), 8,63-8,67 (1H, m).
<Ejemplo 6>
Preparación de N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-6-(N-metilbenzamida)picolinamida (Compuesto N.° 17-1103)
<6-1>
Preparación de N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-6-cloropicolinamida
De acuerdo con el método de 1-3 del Ejemplo 1, un compuesto diana se preparó a partir de cloruro del ácido 2-cloropiridin-6-carboxílico preparado a partir de ácido 2-cloropiridin-6-carboxílico y cloruro de tionilo, y 2-bromo-4-(perfluoro-propan-2-il)-6-(trifluorometil)anilina obtenida en 1-2 del Ejemplo 1.
RMN 1H (CDCla, ppm) 87,59 (1H, d, J = 7,3 Hz), 7,90-7,93 (2H, m), 8,14 (1H, s), 8,20-8,24 (1H, m), 9,60 (1H, s). <6-2>
Preparación de N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-6-(metilamino)picolinamida
A una solución de 0,100 g (0,180 mmol) de N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-6
cloropicolinamida en 5 ml de 1,4-dioxano se le añadieron 0,00600 g (0,0360 mmol) de sulfato de cobre y 0,140 g (1,80 mmol) de una solución acuosa al 40 % de metilamina, seguido de agitación a una temperatura de baño de aceite de 80 °C durante 3 horas en una condición cerrada. El líquido de reacción se devolvió a temperatura ambiente y se abrió, y se le añadieron agua y acetato de etilo. La capa orgánica se lavó con agua y salmuera saturada, y se secó sobre sulfato de magnesio anhidro. El disolvente se evaporó a presión reducida y el residuo obtenido se purificó por cromatografía en columna sobre gel de sílice (disolvente eluyente; hexano:acetato de etilo = 2:1) para preparar 0,0700 g (rendimiento 69 %) de un compuesto diana.
RMN 1H (CDCla, ppm) 82,64 (3H, s), 3,79 (1H, s ancho), 7,56-7,60 (1H, m), 7,87-7,93 (2H, m), 8,14-8,15 (1H, m), 8,20-8,23 (1H, m), 9,60 (1H, s).
<6-3>
Preparación de N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-6-(N-metilbenzamida)picolinamida (Compuesto N.° 17-1103)
De acuerdo con el método de 1-7 del Ejemplo 1, un compuesto diana se preparó a partir de N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-6-(metilamino)picolinamida.
RMN 1H (CDCla, ppm) 83,65 (3H, s), 7,28-7,41 (6H, m), 7,77 (1H, t, J = 7,8 Hz), 7,91 (1H, s), 8,00-8,02 (1H, m), 8,14 (1H, s), 9,39 (1H, s).
<Ejemplo 7>
Preparación de N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-2-(2-fluoro-N-metilbenzamida)tiazol- 4-carboxamida (Compuesto N.° 27-628)
<7-1>
Preparación de ácido 2-aminotiazol-4-carboxílico
A 40 ml de una solución acuosa de 4,00 g (23,2 mmol) de 2-aminotiazol-4-carboxilato de etilo se le añadieron 1,86 g (46,5 mmol) de hidróxido sódico, seguido de agitación a temperatura ambiente durante 5 horas. El líquido de reacción se ajustó a pH 1 mediante la adición de ácido clorhídrico concentrado, y los cristales precipitados se recogieron por filtración para preparar 2,84 g (rendimiento del 85 %) de un compuesto diana.
RMN 1H (CDCls, ppm) 87,18 (2H, s ancho), 7,38 (1H, s).
El protón del ácido carboxílico no se detectó.
<7-2>
Preparación de ácido 2-clorotiazol-4-carboxílico
A una solución de 2,84 g (19,7 mmol) de ácido 2-aminotiazol-4-carboxílico en 30 ml de 1,4-dioxano se le añadieron 50 ml de ácido clorhídrico concentrado, seguido de refrigeración a 0 °C, y se le añadieron cargando gota a gota 10 ml de una solución acuosa de 2,04 g (29,6 mmol) de nitrito sódico a de 0 °C a 5 °C. El líquido de reacción se agitó a 0 °C durante 2 horas, y después se le cargaron en porciones separadas 2,93 g (29,6 mmol) de cloruro de cobre. El líquido de reacción se devolvió a temperatura ambiente. seguido de agitación durante 8 horas. Al líquido de reacción se le añadieron agua y acetato de etilo, seguido de la extracción cuatro veces con acetato de etilo. La capa orgánica se lavó con salmuera saturada, y después se secó sobre sulfato de magnesio anhidro. El disolvente se evaporó a presión reducida para preparar 1,77 g (rendimiento 55 %) de un compuesto diana.
RMN 1H (DMSO-da, ppm) 88,41 (1H, s).
El protón del ácido carboxílico no se detectó.
<7-3>
Preparación de N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-2-clorotiazol-4-carboxamida
De acuerdo con el método de 4-3 del Ejemplo 4, un compuesto diana se preparó a partir de cloruro de 2-clorotiazol-4-carbonilo preparado a partir de ácido 2-clorotiazol-4-carboxílico y cloruro de tionilo, y 2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)anilina obtenida en 1-2 del Ejemplo 1.
RMN 1H (CDCla, ppm) 87,91 (1H, s), 8,13 (1H, s), 8,19 (1H, s), 8,82 (1H, s).
<7-4>
Preparación de N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-2-(metilamino)tiazol-4-carboxamida
De acuerdo con el método de 6-2 del Ejemplo 6, un compuesto diana se preparó a partir de N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-2-clorotiazol-4-carboxamida.
RMN 1H (CDCla, ppm) 83,03 (3H, s), 5,11-5,12 (1H, m), 7,50 (1H, s), 7,88 (1H, s), 8,11 (1H, s), 8,99 (1H, s).
<7-5>
Preparación de N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-2-(2-fluoro-N-metilbenzamida)tiazol- 4-carboxamida (Compuesto N.° 27-628)
De acuerdo con el método de 1-7 del Ejemplo 1, un compuesto diana se preparó a partir de N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-2-(metilamino)tiazol-4-carboxamida y cloruro de 2-fluorobenzoílo.
RMN 1H (CDCh, ppm) 83,67 (3H, s), 6,99-7,24 (1H, m), 7,29-7,35 (1H, m), 7,52-7,59 (2H, m), 7,90 (1H, s), 8,06 (1H, s), 8,14 (1H, s), 9,08 (1H, s).
<Ejemplo 8>
Preparación de 2-fluoro-3-(2-yodo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil(metil)carbamato de 2,2,2-tricloroetilo (Compuesto N.° 12-864)
<8-1>
Preparación de 4-(perfluorobutan-2-il)-2-(trifluorometil)anilina
De acuerdo con el método de 1-1 del Ejemplo 1, un compuesto diana se preparó a partir de 2-(trifluorometil)anilina y yoduro de nonafluoro-s-butilo en la condición de reacción de protección ligera.
RMN 1H (CDCl3, ppm) 84,49 (2H, s ancho), 6,81 (1H, d, J = 8,8 Hz), 7,47 (1H, d, J = 8 Hz), 7,61 (1H, s).
<8-2>
Preparación de 2-yodo-4-(perfluorobutan-2-il)-6-(trifluorometil)anilina
A 100 ml de etanol se les añadieron 17,0 g (44,8 mmol) de 4-(perfluorobutan-2-il)-2-(trifluorometil)anilina, y 5,28 g (53,8 mmol) de ácido sulfúrico concentrado y se le añadieron 12,6 g (55,8 mmol) de N-yodosuccinimida en refrigeración con hielo, seguido de agitación a temperatura ambiente durante 1 hora y 30 minutos y a 40 °C durante 4 horas. A la solución de reacción se le añadió una solución acuosa 4 M de hidróxido sódico para neutralizar la solución
de reacción, y después se le añadió acetato de etilo para extraer la fase orgánica. La fase orgánica se lavó con salmuera saturada, y se secó sobre sulfato de magnesio anhidro, y después el disolvente se evaporó a presión reducida. El residuo obtenido se purificó por cromatografía en columna sobre gel de sílice (disolvente eluyente; hexano:acetato de etilo = 10:1) para preparar 14,6 g (rendimiento 65 %) de un compuesto diana.
RMN 1H (CDCla, ppm) 85,04 (2H, s ancho), 7,62 (1H, s), 7,97 (1H, s).
<8-3>
Preparación de 2-cloro-N-(2-yodo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenil)-3-nitrobenzamida
De acuerdo con el método de 4-3 del Ejemplo 4, un compuesto diana se preparó a partir de 2-yodo-4-(perfluorobutan-2-il)-6-(trifluorometil)anilina.
RMN 1H (CDCla, ppm) 87,60-7,61 (1H, m), 7,77 (1H, s), 7,89-7,96 (2H, m), 8,03-8,04 (1H, m), 8,38 (1H, s).
<8-4>
Preparación de 2-fluoro-N-(2-yodo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenil)-3-nitrobenzamida
De acuerdo con el método de 1-4 del Ejemplo 1, un compuesto diana se preparó a partir de 2-cloro-N-(2-yodo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenil)-3-nitrobenzamida.
RMN 1H (CDCh, ppm) 87,53-7,54 (1H, m), 7,95 (1H, s), 8,24-8,32 (2H, m), 8,36 (1H, s), 8,44-8,48 (1H, m).
<8-5>
Preparación de 3-amino-2-fluoro-N-(2-yodo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenil)benzamida
De acuerdo con el método de 1-5 del Ejemplo 1, un compuesto diana se preparó a partir de 2-fluoro-N-(2-yodo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenil)-3-nitrobenzamida.
RMN 1H (CDCh, ppm) 8 3,93 (2H, s ancho), 7,02-7,03 (1H, m), 7,11-7,13 (1H, m), 7,47-7,51 (1H, m), 7,92 (1H, s), 8,31-8,34 (2H, m).
<8-6>
Preparación de 2-fluoro-N-(2-yodo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenil)-3-(metilamino)benzamida
De acuerdo con el método de 1-6 del Ejemplo 1, un compuesto diana se preparó a partir de 3-amino-2-fluoro-N-(2-yodo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenil)benzamida.
RMN 1H (CDCla, ppm) 82,95-2,96 (3H, m), 4,15 (1H, s ancho), 6,91-6,93 (1H, m), 7,19-7,20 (1H, m), 7,38-7,42 (1H, m), 7,92 (1H, s), 8,32 (1H, d, J = 14,1 Hz), 8,34 (1H, s).
<8-7>
Preparación de 2-fluoro-3-(2-yodo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil(metil)carbamato de 2,2,2-tricloroetilo (Compuesto N.° 12-864)
De acuerdo con el método de 1-7 del Ejemplo 1, un compuesto diana se preparó a partir de 2-fluoro-N-(2-yodo-4-(perfluorobutan-2-il)-6-(trifluorometil)fenil)-3-(metilamino)benzamida y cloruro de 2,2,2-tricloroetoxicarbonilo.
RMN 1H (CDCla, ppm) 83,40 (3H, s), 4,74 (2H, s ancho), 7,37 (1H, t, J = 7,8 Hz), 7,52-7,58 (1H, m), 7,93 (1H, s), 8,12 8,15 (1H, m), 8,28-8,34 (2H, m).
<Ejemplo 9>
Preparación de N-(2-cloro-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-4-ciano-3-(4-ciano-N- metilbenzamida)benzamida (Compuesto N.° 2-491)
<9-1>
Preparación de 2-cloro-4-(perfluoropropan-2-il)-6-(trifluorometil)anilina
De acuerdo con el método de 1-2 del Ejemplo 1, un compuesto diana se preparó a partir de 4-(perfluoropropan-2-il)-2-(trifluorometil)anilina obtenida en 1-1 del Ejemplo 1 y N-clorosuccinimida.
RMN 1H (CDCla, ppm) 84,97 (2H, s ancho), 7,57 (1H, s), 7,64 (1H, s).
<9-2>
Preparación de N-(2-cloro-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-4-yodo-3-nitrobenzamida
De acuerdo con el método de 1-3 del Ejemplo 1, un compuesto diana se preparó a partir de cloruro de 4-yodo-3-nitrobenzoílo preparado a partir de ácido 4-yodo-3-nitrobenzoico y cloruro de tionilo, y 2-cloro-4-(perfluoropropan-2-il)-6-(trifluorometil)anilina.
RMN 1H (CDCla, ppm) 87,52-7,81 (2H, m), 7,89 (1H, s), 8,00 (1H, s), 8,25 (1H, d, J = 8,3 Hz), 8,38 (1H, d, J = 1,9 Hz). <9-3>
Preparación de 3-amino-N-(2-cloro-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-4-yodobenzamida
De acuerdo con el método de 1-5 del Ejemplo 1, un compuesto diana se preparó a partir de N-(2-cloro-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-4-yodo-3-nitrobenzamida.
RMN 1H (CDCla, ppm) 84,35 (2H, s), 6,92 (1H, dd, J = 1,9, 8,3 Hz), 7,29 (1H, d, J = 1,9 Hz), 7,60 (1H, s), 7,79 (1H, d, J = 8,3 Hz), 7,86 (1H, s), 7,97 (1H, s).
<9-4>
Preparación de N-(2-cloro-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-4-yodo-3-(metilamino)benzamida
De acuerdo con el método de 1-6 del Ejemplo 1, un compuesto diana se preparó a partir de 3-amino-N-(2-cloro-4
(perfluoropropan-2-il)-6-(trifluorometil)fenil)-4-yodobenzamida.
RMN 1H (CDCla, ppm) 82,97 (3H, s), 4,46 (1H, s ancho), 6,89 (1H, dd, J = 1,9, 8,3 Hz), 7,07 (1H, d, J = 1,9 Hz), 7,65 (1H, s), 7,80 (1H, d, J = 8,3 Hz), 7,86 (1H, s), 7,97 (1H, s).
<9-5>
Preparación de N-(2-doro-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-4-ciano-3-(metilamino)benzamida
A 10 ml de DMF se le añadieron 0,350 g (0,560 mmol) de N-(2-cloro-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-4-yodo-3-(metilamino)benzamida y 0,200 g (2,25 mmol) de cianuro de cobre (I), seguido de agitación a 140 °C durante 1 hora y 30 minutos. Una solución acuosa saturada de tiosulfato sódico se vertió en la solución de reacción para interrumpir la reacción, y la capa orgánica se recogió con acetato de etilo y se lavó con salmuera saturada. La capa orgánica se secó sobre sulfato de magnesio anhidro, y después el disolvente se evaporó a presión reducida. El residuo obtenido se purificó por cromatografía en columna sobre gel de sílice (disolvente eluyente; hexano:acetato de etilo = 5:1 —»3:1) para preparar 0,250 g (rendimiento 86 %) de un compuesto diana.
RMN 1H (CDCla, ppm) 83,01(1/2*3H, s), 3,03 (1/2*3H, s), 4,89 (1/2*1H, s), 4,90 (1/2*1H, s), 7,80 (1H, dd, J = 1,5, 8,3 Hz), 7,21-7,22 (1H, m), 7,54 (1H, d, J = 8,3 Hz), 7,67 (1H, s), 7,88 (1H, s), 7,99 (1H, s).
<9-6>
Preparación de N-(2-cloro-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-4-ciano-3-(4-ciano-N-metilbenzamida)benzamida (Compuesto N.° 2-491)
De acuerdo con el método de 1-7 del Ejemplo 1, un compuesto diana se preparó a partir de N-(2-cloro-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-4-ciano-3-(metilamino)benzamida y cloruro de 4-cianobenzoílo.
RMN 1H (CDCls, ppm) 83,81 (3H, s ancho), 7,52-7,84 (8H, m), 7,89 (1H, s), 8,00 (1H, s).
<Ejemplo 10>
Preparación de N-(3-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)-6-ciano-2-fluorofenil)-6-cloronicotinamida (Compuesto N.° 1-1968)
<10-1>
Preparación de N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-4-ciano-2,3-difluorobenzamida
A una solución de 0,840 g (4,59 mmol) de ácido 4-ciano-2,3-difluorobenzoico en 10 ml de diclorometano se le añadieron una gota de DMF y 0,470 ml (5,51 mmol) de cloruro de oxalilo, seguido de agitación a temperatura ambiente durante 1 hora. El disolvente se evaporó a presión reducida y el cloruro de 4-ciano-2,3-difluorobenzoílo obtenido se añadió a una solución de 1,56 g (3,83 mmol) de 2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)anilina obtenida en 1-2 del Ejemplo 1 en 5 ml de DMI, seguido de agitación a 130 °C durante 5 horas. Al líquido de reacción se le añadieron agua y acetato de etilo, y la capa orgánica se lavó con a una solución saturada de hidrogenocarbonato sódico y salmuera saturada, y después se secó sobre sulfato de magnesio anhidro. El disolvente se evaporó a presión reducida y el residuo obtenido se purificó por cromatografía en columna sobre gel de sílice (disolvente eluyente; hexano:acetato de etilo = 1:0—»10:1) para preparar 0,58 g (rendimiento 27 %) de un compuesto diana.
RMN 1H (CDCla, ppm) 87,52-7,62 (1H, m), 7,92-7,94 (1H, m), 8,02-8,06 (1H, m), 8,13-8,16 (2H, m).
<10-2>
Preparación de 3-amino-N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-4-ciano-2-fluorobenzamida
A una solución de N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-4-ciano-2,3-difluorobenzamida en 5 ml de DMSO se le añadieron 49,0 mg de carbonato de amonio, seguido de agitación a 100 °C durante 5 horas. Al líquido de reacción se le añadieron agua y acetato de etilo, y la capa orgánica se lavó con agua, y después se secó sobre sulfato de magnesio anhidro. El disolvente se evaporó a presión reducida y el residuo obtenido se purificó por cromatografía en columna sobre gel de sílice (disolvente eluyente; hexano:acetato de etilo = 8:1—4:1) para preparar 0,30 g (rendimiento 51 %) de un compuesto diana.
RMN 1H (CDCla, ppm) 84,71 (2H, s ancho), 7,35-7,39 (1H, m), 7,40-7,44 (1H, m), 7,92 (1H, s), 8,12-8,15 (2H, m). <10-3>
Preparación de N-(3-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)-6-ciano-2-fluorofenil)-6-cloronicotinamida (Compuesto N.° 1-1968)
A una solución de 0,0500 g (0,0877 mol) de 3-amino-N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-4-ciano-2-fluorobenzamida en 0,200 ml de DMI se le añadieron 0,0308 g (0,175 mmol) de cloruro de 6-doronicotinoílo, seguido de agitación a 130 °C durante 6 horas. Al líquido de reacción se le añadieron agua y acetato de etilo, y la capa orgánica se lavó con ácido clorhídrico 1 M, una solución acuosa saturada de hidrogenocarbonato sódico, y salmuera saturada, y después se secó sobre sulfato de magnesio anhidro. El disolvente se evaporó a presión reducida y el residuo obtenido se purificó por cromatografía en columna sobre gel de sílice (disolvente eluyente; hexano:acetato de etilo = 2:1) para preparar 0,0100 g (rendimiento 16 %) de un compuesto diana.
RMN 1H (CDCla, ppm) 87,54 (1H, d, J = 8,8 Hz), 7,72 (1H, d, J = 8,8 Hz), 7,93 (1H, s), 8,09 (1H, s), 8,17-8,18 (2H, m), 8,27 (1H, dd, J = 2,4 Hz, 8,8 Hz), 8,38 (1H, d, J = 10,8 Hz), 8,98 (1H, d, J = 2,4 Hz).
<Ejemplo 11>
Preparación de 3-(4-cianobenzamida)-N-(2,6-diyodo-4-(perfluorobutan-2-il)fenil)benzamida (Compuesto N.° 6-79)
<11-1>
Preparación de 2,6-diyodo-4-(perfluorobutan-2-il)anilina
De acuerdo con el método de 3-1 del Ejemplo 3, un compuesto diana se preparó a partir de 4-(perfluorobutan-2-il)anilina obtenida en 4-1 del Ejemplo 4.
RMN 1H (CDCla, ppm) 84,95 (2H, s ancho), 7,78 (2H, s).
<11 -2>
Preparación de N-(2,6-diyodo-4-(perfluorobutan-2-il)fenil)-3-nitrobenzamida
De acuerdo con el método de 4-3 del Ejemplo 4, un compuesto diana se preparó a partir de 2,6-diyodo-4-(perfluorobutan-2-il)anilina y cloruro de 3-nitrobenzoílo.
RMN 1H (CDCla, ppm) 87,74 (1H, t, J = 8,0 Hz), 8,11 (2H, s), 8,42 (1H, d, J = 7,6 Hz), 8,46 (1H, d, J = 8,4 Hz), 8,90 (1H, d, J = 12,4 Hz), 8,92 (1H, s).
<11 -3>
Preparación de 3-amino-N-(2,6-diyodo-4-(perfluorobutan-2-il)fenil)benzamida
De acuerdo con el método de 1-5 del Ejemplo 1, un compuesto diana se preparó a partir de N-(2,6-diyodo-4-(perfluorobutan-2-il)fenil)-3-nitrobenzamida.
RMN 1H (CDCh, ppm) 85,39 (2H, s ancho), 6,89-6,93 (1H, m), 7,29-7,31 (3H, m), 7,68 (1H, s), 8,08 (2H, s).
<11 -4>
Preparación de 3-(4-cianobenzamida)-N-(2,6-diyodo-4-(perfluorobutan-2-il)fenil)benzamida (Compuesto N.° 6-79)
De acuerdo con el método de 1-7 del Ejemplo 1, un compuesto diana se preparó a partir de 3-amino-N-(2,6-diyodo-4-(perfluorobutan-2-il)fenil)benzamida y cloruro de 4-cianobenzoílo.
RMN 1H (CDCla, ppm) 87,58 (1H, t, J = 8,2 Hz), 7,79-7,83 (3H, m), 7,97 (2H, s), 8,01 (2H, d, J = 8,0 Hz), 8,09 (2H, s), 8,18 (1H, s), 8,29 (1H, s).
<Ejemplo 12>
Preparación de N-(3-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometoxi)fenilcarbamoil)-2-fluorofenil)-2-cloronicotinamida (Compuesto N.° 6-5908)
<12-1>
Preparación de 4-(perfluoropropan-2-il)-2-(trifluorometoxi)anilina
De acuerdo con el método de 1-1 del Ejemplo 1, un compuesto diana se preparó a partir de 2-trifluorometoxianilina. RMN 1H (CDCla, ppm) 84,19 (2H, s ancho), 6,86 (1H, d, J = 8,8 Hz), 7,30 (1H, d, J = 8,8 Hz), 7,36 (1H, s).
<12-2>
Preparación de 2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometoxi)anilina
De acuerdo con el método de 1-2 del Ejemplo 1, un compuesto diana se preparó a partir de 4-(perfluoropropan-2-il)-2-(trifluorometoxi)anilina.
RMN 1H (CDCla, ppm) 84,65 (2H, s ancho), 7,33 (1H, s), 7,71 (1H, s).
<12-3>
Preparación de N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometoxi)fenil)-2-cloro-3-nitrobenzamida
De acuerdo con el método de 1-3 del Ejemplo 1, un compuesto diana se preparó a partir de 2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometoxi)anilina.
RMN 1H (CDCla, ppm) 87,49-7,61 (3H, m), 7,80-7,96 (3H, m).
<12-4>
Preparación de N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometoxi)fenil)-2-fluoro-3-nitrobenzamida
De acuerdo con el método de 1-4 del Ejemplo 1, un compuesto diana se preparó a partir de N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometoxi)fenil)-2-doro-3-nitrobenzamida.
RMN 1H (CDCla, ppm) 87,53 (1H, t, J = 7,8 Hz), 7,60 (1H, s ancho), 7,89 (1H, d, J = 1,5 Hz), 8,07 (1H, d ancho, J = 12,7 Hz), 8,29-8,30 (1H, m), 8,43-8,47 (1H, m).
<12-5>
Preparación de 3-amino-N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometoxi)fenil)-2-fluorobenzamida
De acuerdo con el método de 1-5 del Ejemplo 1, un compuesto diana se preparó a partir de N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometoxi)fenil)-2-fluoro-3-nitrobenzamida.
RMN 1H (CDCla, ppm) 83,92 (2H, s ancho), 6,99-7,04 (1H, m), 7,11 (1H, t, J = 7,8 Hz), 7,45-7,49 (1H, m), 7,57 (1H, s ancho), 7,87 (1H, d, J = 2,0 Hz), 8,14 (1H, d, J = 14,2 Hz).
<12-6>
Preparación de N-(3-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometoxi)fenilcarbamoil)-2-fluorofenil)-2-cloronicotinamida (Compuesto N.° 6-5908)
De acuerdo con el método de 1-7 del Ejemplo 1, un compuesto diana se preparó a partir de 3-amino-N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometoxi)fenil)-2-fluorobenzamida y cloruro de 2-cloronicotinoílo.
RMN 1H (CDCla, ppm) 87,39-7,49 (2H, m), 7,59 (1H, s), 7,88-7,94 (2H, m), 8,07 (1H, d, J = 12,2 Hz), 8,31-8,33 (1H, m), 8,57-8,58 (1H, m), 8,60-8,70 (1H, m), 8,74 (1H, s ancho).
<Ejemplo 13>
Preparación de 3-benzamida-N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-4-fluorobenzamida (Compuesto N.° 6-3348)
<13-1>
Preparación de N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-4-fluoro-3-nitrobenzamida
De acuerdo con el método de 1-3 del Ejemplo 1, un compuesto diana se preparó a partir de cloruro de 4-fluoro-3-nitrobenzoílo preparado a partir de ácido 4-fluoro-3-nitrobenzoico y cloruro de tionilo, y 2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)anilina obtenida en 1-2 del Ejemplo 1.
RMN 1H (CDCh, ppm) 87,47-7,50 (1H, m), 7,92 (2H, d, J = 5,9 Hz), 8,16 (1H, s), 8,23-8,28 (1H, m), 8,65-8,67 (1H, m).
<13-2>
Preparación de 3-amino-N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-4-fluorobenzamida
De acuerdo con el método de 1-5 del Ejemplo 1, un compuesto diana se preparó a partir de N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-4-fluoro-3-nitrobenzamida.
APCI-EM m/z (M+1):546
<13-3>
Preparación de 3-benzamida-N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-4-fluorobenzamida (Compuesto N.° 6-3348)
De acuerdo con el método de 1-7 del Ejemplo 1, un compuesto diana se preparó a partir de 3-amino-N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-4-fluorobenzamida.
RMN 1H (CDCla, ppm) 87,29-7,34 (1H, m), 7,53-7,65 (3H, m), 7,80-7,84 (1H, m), 7,90-7,92 (3H, m), 8,14 (1H, s ancho), 8,20 (1H, d, J = 2,9 Hz), 8,25 (1H, s ancho), 9,10 (1H, dd, J = 1,9, 7,3 Hz).
<Ejemplo 14>
Preparación de 2-doro-N-(3-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)nicotinamida (Compuesto N.° 6-460)
<14-1>
Preparación de 2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)anilina
De acuerdo con el método de 8-2 del Ejemplo 8, un compuesto diana se preparó a partir de 4-(perfluoropropan-2-il)-2-(trifluorometil)anilina obtenida en 1-1 del Ejemplo 1 y N-yodosuccinimida.
RMN 1H (CDCla, ppm) 85,04 (2H, s ancho), 7,64 (1H, s), 7,99 (1H, s).
<14-2>
Preparación de N-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-3-nitrobenzamida
De acuerdo con el método de 4-3 del Ejemplo 4, un compuesto diana se preparó a partir de 2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)anilina y cloruro de 3-nitrobenzoílo.
RMN 1H (CDCla, ppm) 87,76-7,80 (2H, m), 7,97 (1H, s), 8,28-8,30 (1H, m), 8,37 (1H, s), 8,49-8,52 (1H, m), 8,78 (1H, s).
<14-3>
Preparación de 3-amino-N-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)benzamida
De acuerdo con el método de 1-5 del Ejemplo 1, un compuesto diana se preparó a partir de N-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-3-nitrobenzamida.
RMN 1H (CDCla, ppm) 83,89 (2H, s ancho), 6,89-6,92 (1H, m), 7,23-7,32 (3H, m), 7,68 (1H, s), 7,93 (1H, s), 8,34-8,36 (1H, m).
<14-4>
Preparación de 2-doro-N-(3-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenilcarbamoil)fenil)nicotinamida (Compuesto N.° 6-460)
De acuerdo con el método de 1-7 del Ejemplo 1, un compuesto diana se preparó a partir de 3-amino-N-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)benzamida y cloruro de 2-cloronicotinoílo.
RMN 1H (CDCla, ppm) 87,43-7,46 (1H, m), 7,58 (1H, t, J = 7,8 Hz), 7,77 (1H, d, J = 7,8 Hz), 7,91-7,95 (2H, m), 8,01 (1H, s), 8,24 (1H, dd, J = 2,0, 7,8 Hz), 8,28 (1H, s), 8,36 (1H, s), 8,41 (1H, s), 8,54-8,56 (1H, m).
<Ejemplo 15>
Preparación de 2-fluoro-3-(4-fluoro-N-metilbenzamida)-N-(2-yodo-4-(perfluoropropan-2-N)-6-(trifluorometN)-fenil)benzamida (Compuesto N.° 7-1733)
<15-1>
Preparación de 2-cloro-N-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-3-nitrobenzamida
De acuerdo con el método de 4-3 del Ejemplo 4, un compuesto diana se preparó a partir de 2-yodo-4-(perfluoropropan
2-il)-6-(trifluorometil)anilina obtenida en 14-1 del Ejemplo 14 y cloruro de 2-cloro-3-nitrobenzoílo.
RMN 1H (CDCla, ppm) 87,60 (1H, t, J = 7,8 Hz), 7,76 (1H, s), 7,94 (1H, dd, J = 1,5, 7,8 Hz), 7,97 (1H, s), 8,03 (1H, dd, J = 1,5, 7,8 Hz), 8,39 (1H, s).
<15-2>
Preparación de 2-fluoro-N-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-3-nitrobenzamida
De acuerdo con el método de 1-4 del Ejemplo 1, un compuesto diana se preparó a partir de 2-cloro-N-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-3-nitrobenzamida.
RMN 1H (CDCla, ppm) 87,51-7,55 (1H, m), 7,97 (1H, s), 8,23 (1H, d, J = 12,2 Hz), 8,28-8,32 (1H, m), 8,37 (1H, s), 8,44-8,48 (1H, m).
<15-3>
Preparación de 3-amino-2-fluoro-N-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)benzamida
De acuerdo con el método de 1-5 del Ejemplo 1, un compuesto diana se preparó a partir de 2-fluoro-N-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-3-nitrobenzamida.
RMN 1H (CDCls, ppm) 83,92 (2H, s ancho), 7,02-7,04 (1H, m), 7,11 (1H, t, J = 7,8 Hz), 7,47-7,52 (1H, m), 7,94 (1H, s), 8,30-8,35 (2H, m).
<15-4>
Preparación de 2-fluoro-N-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-3-(metilamino)benzamida
De acuerdo con el método de 1-6 del Ejemplo 1, un compuesto diana se preparó a partir de 3-amino-2-fluoro-N-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)benzamida.
RMN 1H (CDCls, ppm) 82,95 (3H, s), 4,15 (1H, s ancho), 6,90 (1H, t, J = 8,2 Hz), 7,19 (1H, t, J = 7,8 Hz), 7,40 (1H, t, J = 7,8 Hz), 7,92 (1H, s), 8,30 (1H, s), 8,34 (1H, s).
<15-5>
Preparación de 2-fluoro-3-(4-fluoro-N-metilbenzamida)-N-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)benzamida (Compuesto N.° 7-1733)
De acuerdo con el método de 1-7 del Ejemplo 1, un compuesto diana se preparó a partir de 2-fluoro-N-(2-yodo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-3-(metilamino)benzamida y cloruro de 4-fluorobenzoílo.
RMN 1H (CDCl3, ppm) 83,50 (3H, s), 6,91 (2H, s), 6,93-7,35 (3H, m), 7,46 (1H, t, J = 7,0 Hz), 7,93 (1H, s), 8,01-8,10 (1H, m), 8,13 (1H, s ancho), 8,34 (1H, s).
<Ejemplo 16>
Preparación de N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-2-fluoro-N-metil-3-(N-metilbenzamida)benzamida (Compuesto N.° 9-2164)
A una solución de 0,100 g (0,150 mmol) de N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-2-fluoro-3-(N-metilbenzamida)benzamida obtenida en 1-7 del Ejemplo 1 en 5 ml de d Mf se le añadieron 0,00900 g (0,230 mmol) de hidruro sódico (al 60% en aceite), seguido de agitación a temperatura ambiente durante 40 minutos. Al líquido de reacción se le añadieron 0,0300 g (0,180 mmol) de yoduro de metilo, seguido de agitación a la misma temperatura durante 6 horas. Al líquido de reacción se le añadieron agua y acetato de etilo, y la capa orgánica se lavó con agua y salmuera saturada, y se secó sobre sulfato de magnesio anhidro. El disolvente se evaporó a presión reducida y el residuo obtenido se purificó por cromatografía en columna sobre gel de sílice (disolvente eluyente; hexano:acetato de etilo = 4:1) para preparar 0,106 g de un compuesto diana cuantitativamente.
RMN 1H (CDCla, ppm) 82,18-2,19 (3H, m), 3,48 (3H, s), 7,21-7,25 (4H, m), 7,32-7,40 (4H, m), 7,92 (1H, s), 8,13 (1H, s).
<Ejemplo 17>
Preparación de N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-3-(4-cianobenzamida)-N-metilbenzamida (Compuesto N.° 8-289)
<17-1>
Preparación de N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-3-nitrobenzamida
De acuerdo con el método de 4-3 del Ejemplo 4, un compuesto diana se preparó a partir de 2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)anilina obtenida en 1-2 del Ejemplo 1 y cloruro de 3-nitrobenzoílo.
RMN 1H (CDCla, ppm) 87,75-7,79 (2H, m), 7,94 (1H, s), 8,17 (1H, d, J = 1,0 Hz), 8,28 (1H, dd, J = 1,5, 7,8 Hz), 8,48 8,51 (1H, m), 8,76-8,77 (1H, m).
<17-2>
Preparación de N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-N-metil-3-nitrobenzamida
De acuerdo con el método del Ejemplo 16, un compuesto diana se preparó a partir de N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-3-nitrobenzamida.
RMN 1H (CDCla, ppm) 83,28(1/2*3H, s), 3,44 (1/2*3H, s), 7,41 (1/2*1H, t, J = 7,8 Hz), 7,71-7,76 (2/2*1H, m), 7,84 (1/2*1H, s), 7,93-7,95 (1/2*1H, m), 7,98 (1/2*1H, s), 8,07-8,09 (2/2*1H, m), 8,14-8,16 (1/2*1H, m), 8,19 (1/2*1H, s), 8,39-8,41 (1/2*1H, m), 8,45-8,46 (1/2*1H, m).
<17-3>
Preparación de 3-amino-N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-N-metilbenzamida
De acuerdo con el método de 1-5 del Ejemplo 1, un compuesto diana se preparó a partir de N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-N-metil-3-nitrobenzamida.
RMN 1H (CDCh, ppm) 83,24(3/4*3H, s), 3,37 (1/4*3H, s), 3,80 (2H, s ancho), 6,47 (1/4*1H, d, J = 7,8 Hz), 6,54-6,57 (1/4*1H, m), 6,78-6,84 (5/4*1H, m), 6,86 (3/4*1H, t, J = 2,0 Hz), 6,96 (3/4*1H, d, J = 7,8 Hz), 7,23-7,27 (3/4*1H, m), 7,79 (1/4*1H, s), 7,94 (3/4*1H, s), 8,00 (1/4*1H, s), 8,15 (3/4*1H, s).
<17-4>
Preparación de N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-3-(4-cianobenzamida)-N-metilbenzamida (Compuesto N.° 8-289)
De acuerdo con el método de 1-7 del Ejemplo 1, un compuesto diana se preparó a partir de 3-amino-N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-N-metilbenzamida y cloruro de 4-cianobenzoílo.
RMN 1H (CDCl3, ppm) 83,26 (2/3*3H, s), 3,38 (1/3*3H, s), 7,08-7,09 (1/3*1H, m), 7,12-7,14 (1/3*1H, m), 7,32 (2/3*1H, d, J = 7,8 Hz), 7,45-7,49 (3/3*1H, m), 7,72-7,76 (9/3*1H, m), 7,83 (1/3*1H, s), 7,85-7,89 (4/3*1H, m), 7,95 (2/3*1H, s), 7,98-8,00 (4/3*1H, m), 8,04 (2/3*1H, d, J = 6,3 Hz), 8,16 (2/3*1H, s), 8,57 (2/3*1H, s).
<Ejemplo 18>
Preparación de 3-benzamida-N-(2-bromo-4-(perfluoroetil)-6-(trifluorometil)fenil)benzamida (Compuesto N.° 6-5913)
<18-1>
Preparación de 4-(perfluoroetil)-2-(trifluorometil)anilina
A 40 ml de una solución acuosa de 7,04 g (40,4 mmol) de hidrosulfito sódico al 85 % y 3,40 g (40,4 mmol) de hidrogenocarbonato sódico se le añadieron 13,6 g (33,7 mmol) de 2-(trifluorometil)anilina y 40 ml de DMF. A este líquido de reacción se le añadieron 50 ml de una solución de 11,2 g (45,5 mmol) de yoduro de 1,1,2,2,2-pentafluoroetilo en DMF (DMF se enfrió a -30 °C y se disolvió en el mismo yoduro de 1,1,2,2,2-pentafluoroetilo), y se puso en un autoclave, seguido de agitación a 110 °C durante 9 horas. Después de dejar reposar a temperatura ambiente durante una noche, se añadieron agua y acetato de etilo al líquido de reacción, seguido de la extracción con acetato de etilo. La capa orgánica se lavó con agua, una solución acuosa saturada de hidrogenocarbonato sódico, y salmuera saturada. La capa orgánica se secó sobre sulfato sódico anhidro, después el disolvente se evaporó a presión reducida, y el residuo obtenido se purificó por cromatografía en columna sobre gel de sílice (disolvente eluyente; hexano:acetato de etilo = 10:1 —^ 5:1) para preparar 1,95 g (rendimiento 21 %) de un compuesto diana.
RMN 1H (CDCla, ppm) 84,53 (2H, s ancho), 6,81 (1H, d, J = 8,3 Hz), 7,48 (1H, d, J = 8,3 Hz), 7,63 (1H, s ancho). <18-2>
Preparación de 2-bromo-4-(perfluoroetil)-6-(trifluorometil)anilina
De acuerdo con el método de 1-2 del Ejemplo 1, un compuesto diana se preparó a partir de 4-(perfluoroetil)-2-(trifluorometil)anilina.
RMN 1H (CDCla, ppm) 85,08 (2H, s ancho), 7,62 (1H, s), 7,80 (1H, s).
<18-3>
Preparación de N-(2-bromo-4-(perfluoroetil)-6-(trifluorometil)fenil)-3-nitrobenzamida
A una solución de 2,50 g (6,99 mmol) de 2-bromo-4-(perfluoroetil)-6-(trifluorometil)anilina en 20 ml de piridina se le añadieron 2,72 g (14,7 mmol) de cloruro de 3-nitrobenzoílo, seguido de agitación a 100 °C durante 12 horas. Al líquido de reacción se le añadieron agua y acetato de etilo, seguido de la extracción con acetato de etilo. La capa orgánica se lavó con ácido clorhídrico 1 M, una solución acuosa saturada de hidrogenocarbonato sódico, y salmuera saturada. La capa orgánica se secó sobre sulfato sódico anhidro, y después el disolvente se evaporó a presión reducida. Al residuo obtenido se le añadieron THF y una solución acuosa de hidróxido sódico, seguido de agitación a temperatura ambiente durante 8 horas. El líquido de reacción se extrajo/secó de la misma manera que se ha descrito anteriormente, y el disolvente se evaporó a presión reducida. El residuo obtenido se purificó por cromatografía en columna sobre gel de sílice (disolvente eluyente; hexano:acetato de etilo = 7:1 —^ 5:1) para preparar 0,202 g (rendimiento 6% ) de un compuesto diana.
RMN 1H (CDCla, ppm) 87,75 (1H, s), 7,78 (1H, t, J = 7,8 Hz), 7,94 (1H, s), 8,17 (1H, s), 8,29-8,30 (1H, m), 8,50-8,52 (1H, m), 8,78 (1H, t, J = 2,0 Hz).
<18-4>
Preparación de 3-amino-N-(2-bromo-4-(perfluoroetil)-6-(trifluorometil)fenil)benzamida
De acuerdo con el método de 1-5 del Ejemplo 1, un compuesto diana se preparó a partir de N-(2-bromo-4-(perfluoroetil)-6-(trifluorometil)fenil)-3-nitrobenzamida.
RMN 1H (CDCla, ppm) 83,89 (2H, s ancho), 6,90-6,92 (1H, m), 7,23-7,32 (3H, m), 7,64 (1H, s), 7,90 (1H, s), 8,13 (1H, s).
<18-5>
Preparación de 3-benzamida-N-(2-bromo-4-(perfluoroetil)-6-(trifluorometil)fenil)benzamida (Compuesto N.° 6-5913)
De acuerdo con el método de 1-7 del Ejemplo 1, un compuesto diana se preparó a partir de 3-amino-N-(2-bromo-4-(perfluoroetil)-6-(trifluorometil)fenil)benzamida.
RMN 1H (CDCla, ppm) 87,51-7,62 (4H, m), 7,72 (1H, dd, J = 1,5, 7,8 Hz), 7,89-8,00 (6H, m), 8,14 (1H, s), 8,27 (1H, t, J = 2,0 Hz).
<Ejemplo 19>
Preparación de 3-benzamida-N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-4-cianobenzamida (Compuesto N.° 1-627)
<19-1>
Preparación de N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-4-fluoro-3-nitrobenzamida
De acuerdo con el método de 4-3 del Ejemplo 4, un compuesto diana se preparó a partir de cloruro de 4-fluoro-3-nitrobenzoílo preparado a partir de ácido 4-fluoro-3-nitrobenzoico y cloruro de tionilo, y 2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)anilina obtenida en 1-2 del Ejemplo 1.
RMN 1H (CDCla, ppm) 87,47-7,50 (1H, m), 7,92 (2H, d, J = 5,9 Hz), 8,16 (1H, s), 8,23-8,28 (1H, m), 8,65-8,67 (1H, m). <19-2>
Preparación de N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-4-ciano-3-nitrobenzamida
A una solución de 0,500 g (0,870 mmol) de N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-4-fluoro-3-nitrobenzamida en 5 ml de DMF se le añadieron 0,0639 g (1,31 mmol) de cianuro sódico, seguido de agitación a temperatura ambiente durante 10 horas. Al líquido de reacción se le añadieron agua y acetato de etilo, seguido de la extracción con acetato de etilo. La capa orgánica se lavó con una solución acuosa al 10% de hidróxido sódico y salmuera saturada. La capa orgánica se secó sobre sulfato sódico anhidro, y después el disolvente se evaporó a presión reducida. El residuo obtenido se purificó por cromatografía en columna sobre gel de sílice para preparar 0,0500 g (rendimiento 10 %) de un compuesto diana.
RMN 1H (CDCla, ppm) 87,80 (1H, s), 7,96 (1H, s), 8,12-8,14 (1H, m), 8,18 (1H, s), 8,36 (1H, dd, J = 2,0, 8,3 Hz), 8,84 (1H, d, J = 1,5 Hz).
<19-3>
Preparación de 3-amino-N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-4-cianobenzamida
De acuerdo con el método de 1-5 del Ejemplo 1, un compuesto diana se preparó a partir de N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-4-ciano-3-nitrobenzamida.
RMN 1H (CDCla, ppm) 84,68 (2H, s ancho), 7,18 (1H, dd, J = 1,9, 8,3 Hz), 7,29 (1H, s), 7,52-7,55 (1H, m), 7,68 (1H, s), 7,92 (1H, s), 8,14 (1H, d, J = 1,5 Hz).
<19-4>
Preparación de 3-benzamida-N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-4-cianobenzamida (Compuesto N.° 1-627)
De acuerdo con el método de 1-7 del Ejemplo 1, un compuesto diana se preparó a partir de 3-amino-N-(2-bromo-4-(perfluoropropan-2-il)-6-(trifluorometil)fenil)-4-cianobenzamida.
RMN 1H (CDCh, ppm) 87,56-7,59 (3H, m), 7,64-7,66 (1H, m), 7,80-7,87 (2H, m), 7,94-7,97 (2H, m), 8,16 (1H, s), 8,46 (1H, s), 8,57 (1H, s), 9,16 (1H, s).
A continuación, se mostrarán ejemplos de preparación en los que el compuesto de la presente invención está contenido en forma de principio activo, pero la presente invención no se limita a los mismos. Además, en los ejemplos de preparación, las partes representan partes en peso.
<Ejemplo de preparación 1>
20 partes del compuesto representado por la fórmula (1) de la presente invención, 10 partes de éter de estirilfenilo de polioxietileno, y 70 partes de xileno se mezclaron uniformemente para obtener una emulsión.
<Ejemplo de preparación 2>
10 partes del compuesto representado por la fórmula (1) de la presente invención, 2 partes de lauril sulfato de sodio,
2 partes de sulfosuccinato de dialquilo, 1 parte de una sal sódica de condensado de ácido p-naftaleno sulfónico y formalina, y 85 partes de tierra de diatomeas se agitaron y mezclaron uniformemente para obtener un polvo humectable.
<Ejemplo de preparación 3>
0,3 partes del compuesto representado por la fórmula (1) de la presente invención y 0,3 partes de carbón blanco se mezclaron uniformemente, y 99,2 partes de arcilla y 0,2 partes de DRILESS A (fabricado por Sankyo Agro Co., Ltd.) se añadieron a la misma, seguido de pulverización y mezclado uniforme, obteniendo de este modo polvos.
<Ejemplo de preparación 4>
3 partes del compuesto representado por la fórmula (1) de la presente invención, 1,5 partes de un condensado de polioxietileno/polioxipropileno, 3 partes de carboximetilcelulosa, 64,8 partes de arcilla, y 27,7 partes de talco se pulverizaron y mezclaron uniformemente, y se añadió agua a la misma, seguido de amasado, granulación, y secado, obteniendo de este modo polvos.
<Ejemplo de preparación 5>
10 partes del compuesto representado por la fórmula (1) de la presente invención, 3 partes de una sal sódica de condensado de ácido p-naftaleno sulfónico y formalina, 1 parte de triestirilfenol, 5 partes de propilenglicol, 0,5 partes de un agente desespumante basado en silicio, y 33,5 partes de agua se agitaron suficientemente y se mezclaron, y después se mezclaron con la misma 0,3 partes de goma de xantano y 46,7 partes de agua, seguido de agitación y mezclado nuevamente, obteniendo de este modo una formulación fluida.
<Ejemplo de preparación 6>
20 partes del compuesto representado por la fórmula (1) de la presente invención, 6 partes de una sal metálica de condensado de ácido naftaleno sulfónico y formaldehído, 1 parte de sal metálica de sulfosuccinato de dialquilo, y 73 partes de carbonato de calcio se pulverizaron y mezclaron uniformemente, y se añadió agua a la misma, seguido de amasado, granulación, y secado, obteniendo de este modo un polvo granulado humectable.
Para el uso de las formulaciones obtenidas anteriormente, la formulación se diluyó de 1 vez a 10000 veces con agua o no se diluyó, y después se roció directamente.
A continuación, se describirá la utilidad del compuesto de la presente invención como agente para el control de plagas de manera específica con referencia a los siguientes ejemplos de ensayo, pero la presente invención no se limita a los mismos.
<Ejemplo de ensayo 1>
Prueba plaguicida contra Spodoptera litura
Se sumergió un trozo de hoja de col durante 30 segundos en una solución química en la que se había preparado un compuesto de ensayo a una concentración predeterminada, y se secó al aire, y después se colocó en una copa de polietileno de 7 cm que tenía un papel de filtro dispuesto en la parte inferior de la misma, y se liberaron larvas en estado 2 de Spodoptera litura. Se las dejó en una cámara termostática a 25 °C, y se examinó el número de larvas vivas y las larvas muertas después de 6 días. La prueba se llevó a cabo con cinco larvas por grupo en dos replicados. Además, se usó el siguiente compuesto (A) divulgado en la memoria de la Publicación Internacional WO 2005/073165 como compuesto comparativo.
Compuesto (A)
Como resultados de las pruebas anteriores, las composiciones de los compuestos n.° 1-470, 1-491,1-513, 1-627, 1 1925, 2-491, 6-38, 6-39, 6-45, 6-46, 6-47, 6-57, 6-60, 6-71, 6-72, 6-78, 6-79, 6-80, 6-90, 6-93, 6-111, 6-147, 6-268, 6 269, 6-270, 6-271, 6-272, 6-288, 6-289, 6-290, 6-293, 6-300, 6-304, 6-306, 6-311, 6-346, 6-347, 6-348, 6-349, 6-366, 6-367, 6-368, 6-382, 6-389, 6-424, 6-425, 6-426, 6-427, 6-428, 6-444, 6-445, 6-446, 6-448, 6-449, 6-450, 6-452, 6 453, 6-460, 6-461, 6-467, 6-502, 6-503, 6-504, 6-505, 6-522, 6-523, 6-524, 6-538, 6-545, 6-804, 6-824, 6-825, 6-840, 6- 1104, 6-1105, 6-1106, 6-1107, 6-1124, 6-1125, 6-1126, 6-1140, 6-1147, 6-1182, 6-1183, 6-1184, 6-1185, 6-1202, 6 1203, 6-1204, 6-1218, 6-1225, 6-1260, 6-1261, 6-1262, 6-1263, 6-1280, 6-1281, 6-1282, 6-1296, 6-1303, 6-1338, 6 1339, 6-1340, 6-1341, 6-1358, 6-1359, 6-1360, 6-1374, 6-1381, 6-1574, 6-1575, 6-1576, 6-1577, 6-1594, 6-1595, 6 1596, 6-1610, 6-1617, 6-1652, 6-1653, 6-1654, 6-1655, 6-1672, 6-1673, 6-1674, 6-1688, 6-1695, 6-1730, 6-1731, 6 1732, 6-1733, 6-1734, 6-1750, 6-1751, 6-1752, 6-1754, 6-1755, 6-1766, 6-1773, 6-1808, 6-1809, 6-1810, 6-1811, 6 1828, 6-1829, 6-1830, 6-1851, 6-2110, 6-3348, 6-3384, 6-5902, 6-5903, 6-5904, 6-5905, 6-5906, 6-5907, 6-5908, 6 5909, 6-5910, 6-5911, 6-5912, 7-38, 7-39, 7-45, 7-46, 7-47, 7-57, 7-60, 7-71, 7-72, 7-78, 7-79, 7-80, 7-90, 7-93, 7-132, 7- 147, 7-268, 7-269, 7-270, 7-271, 7-285, 7-286, 7-288, 7-289, 7-290, 7-299, 7-300, 7-301, 7-303, 7-304, 7-305, 7 311, 7-346, 7-347, 7-348, 7-349, 7-366, 7-367, 7-368, 7-382, 7-389, 7-424, 7-425, 7-426, 7-427, 7-428, 7-444, 7-445, 7-446, 7-449, 7-460, 7-467, 7-502, 7-504, 7-505, 7-522, 7-523, 7-538, 7-804, 7-824, 7-825, 7-840, 7-948, 7-969, 7 984, 7-1104, 7-1105, 7-1106, 7-1107, 7-1124, 7-1125, 7-1126, 7-1140, 7-1147, 7-1182, 7-1183, 7-1184, 7-1185, 7 1202, 7-1203, 7-1204, 7-1218, 7-1225, 7-1260, 7-1261, 7-1262, 7-1263, 7-1280, 7-1281, 7-1282, 7-1296, 7-1303, 7 1338, 7-1339, 7-1340, 7-1341, 7-1358, 7-1359, 7-1360, 7-1374, 7-1381, 7-1417, 7-1574, 7-1575, 7-1576, 7-1577, 7 1594, 7-1595, 7-1596, 7-1605, 7-1606, 7-1608, 7-1610, 7-1616, 7-1617, 7-1638, 7-1639, 7-1645, 7-1652, 7-1672, 7 1673, 7-1730, 7-1731, 7-1732, 7-1733, 7-1750, 7-1751, 7-1752, 7-1764, 7-1766, 7-1773, 7-1794, 7-1808, 7-1809, 7 1810, 7-1811, 7-1828, 7-1829, 7-1844, 7-1851, 7-3348, 7-3369, 7-3384, 7-5902, 7-5903, 7-5904, 7-5905, 7-5906, 7 5907, 7-5910, 8-268, 8-288, 8-289, 8-304, 8-804, 8-824, 8-840, 9-270, 9-290, 9-291, 9-306, 9-2164, 9-2322, 11-777, 11-835, 12-777, 12-835, 12-864, 27-627 y 27-663 mostraron cada uno una tasa plaguicida del 70 % o superior a una concentración de 1 ppm.
Además, las composiciones de los compuestos n.° 1-506, 1-1968, 2-513, 2-518, 6-454, 6-5913, 6-5914, 7-316, 7-5911, 7-5912, 7-5908, 7-5909, 17-1103, y 27-628 mostraron cada uno una tasa plaguicida del 70 % o superior a una concentración de 10 ppm.
Mientras tanto, el compuesto (A) tuvo una tasa plaguicida del 50 % o menor a una concentración de 10 ppm.
<Ejemplo de ensayo 2>
Prueba plaguicida contra Plutella xylostella
Se sumergió un trozo de hoja de col durante 30 segundos en una solución química en la que se había preparado un compuesto de ensayo a una concentración predeterminada, y se secó al aire, y después se colocó en una copa de polietileno de 7 cm que tenía un papel de filtro dispuesto en la parte inferior de la misma, y se liberaron larvas en estado 2 de Plutella xylostella. Se las dejó en una cámara termostática a 25 °C, y se examinó el número de larvas vivas y las larvas muertas después de 6 días. La prueba se llevó a cabo con cinco larvas por grupo en dos replicados.
Además, el compuesto (A) anterior se usó como compuesto comparativo.
Como resultados de las pruebas anteriores, las composiciones de los compuestos n.° 1-491, 1-513, 1-627, 1-1925, 1 1968, 2-491,2-513, 6-38, 6-39, 6-45, 6-46, 6-47, 6-57, 6-71,6-72, 6-78, 6-79, 6-80, 6-90, 6-111,6-147, 6-268, 6-270, 6 271,6-272, 6-288, 6-289, 6-290, 6-293, 6-300, 6-304, 6-306, 6-346, 6-347, 6-348, 6-349, 6-366, 6-367, 6-368, 6-382, 6-389, 6-424, 6-425, 6-426, 6-427, 6-428, 6-444, 6-445, 6-446, 6-449, 6-450, 6-453, 6-460, 6-461,6-467, 6-502, 6-503, 6-504, 6-505, 6-522, 6-523, 6-524, 6-538, 6-545, 6-804, 6-824, 6-825, 6-840, 6-1104, 6-1105, 6-1106, 6-1107, 6-1124, 6- 1125, 6-1126, 6-1140, 6-1147, 6-1182, 6-1183, 6-1184, 6-1185, 6-1202, 6-1203, 6-1204, 6-1218, 6-1225, 6-1260, 6 1261, 6-1262, 6-1263, 6-1280, 6-1281, 6-1282, 6-1296, 6-1303, 6-1338, 6-1339, 6-1340, 6-1341, 6-1358, 6-1359, 6 1360, 6-1374, 6-1381, 6-1574, 6-1575, 6-1576, 6-1577, 6-1594, 6-1595, 6-1596, 6-1610, 6-1617, 6-1652, 6-1653, 6 1654, 6-1655, 6-1672, 6-1673, 6-1674, 6-1688, 6-1695, 6-1730, 6-1731, 6-1732, 6-1733, 6-1734, 6-1750, 6-1751, 6 1752, 6-1754, 6-1755, 6-1766, 6-1773, 6-1808, 6-1809, 6-1810, 6-1811, 6-1828, 6-1829, 6-1830, 6-1851, 6-2110, 6 3348, 6-3384, 6-5903, 6-5904, 6-5905, 6-5906, 6-5907, 6-5908, 6-5909, 6-5910, 6-5911, 6-5912, 7-38, 7-39, 7-45, 7 46, 7-47, 7-57, 7-60, 7-71, 7-72, 7-78, 7-79, 7-80, 7-90, 7-93, 7-132, 7-147, 7-268, 7-271, 7-286, 7-288, 7-289, 7-290, 7- 299, 7-300, 7-301, 7-303, 7-304, 7-305, 7-311, 7-346, 7-347, 7-348, 7-349, 7-366, 7-367, 7-368, 7-382, 7-389, 7 424, 7-425, 7-426, 7-427, 7-428, 7-444, 7-445, 7-446, 7-449, 7-460, 7-467, 7-502, 7-504, 7-505, 7-522, 7-523, 7-538, 7-824, 7-840, 7-948, 7-969, 7-984, 7-1104, 7-1105, 7-1106, 7-1107, 7-1124, 7-1125, 7-1126, 7-1140, 7-1147, 7-1182, 7-1183, 7-1184, 7-1185, 7-1202, 7-1203, 7-1204, 7-1218, 7-1225, 7-1260, 7-1261, 7-1262, 7-1263, 7-1280, 7-1281, 7 1282, 7-1296, 7-1303, 7-1338, 7-1339, 7-1340, 7-1341, 7-1358, 7-1359, 7-1360, 7-1374, 7-1381, 7-1417, 7-1574, 7 1575, 7-1576, 7-1577, 7-1594, 7-1595, 7-1596, 7-1605, 7-1606, 7-1608, 7-1610, 7-1616, 7-1617, 7-1638, 7-1639, 7 1645, 7-1652, 7-1672, 7-1673, 7-1730, 7-1731, 7-1732, 7-1733, 7-1750, 7-1751, 7-1752, 7-1764, 7-1766, 7-1773, 7 1794, 7-1808, 7-1809, 7-1810, 7-1811, 7-1828, 7-1829, 7-1844, 7-1851, 7-3348, 7-3369, 7-3384, 7-5902, 7-5903, 7 5904, 7-5905, 7-5906, 7-5907, 7-5909, 7-5910, 8-268, 8-288, 8-289, 8-304, 8-824, 9-270, 9-290, 9-291, 9-306, 9-2164, 9-2322, 11-777, 11-835, 12-777, 12-835, y 12-864 mostraron cada uno una tasa plaguicida del 70 % o superior a una concentración de 1 ppm.
Además, las composiciones de los compuestos n.° 1-470, 1-506, 2-518, 6-60, 6-93, 6-269, 6-311,6-448, 6-452, 6-454, 6-5913, 6-5914, 7-269, 7-270, 7-285, 7-316, 7-804, 7-825, 7-5908, 7-5911, 7-5912, 8-804, 8-840, 17-1103, 27-627, 27-628, y 27-663 mostraron cada uno una tasa plaguicida del 70 % o superior a una concentración de 10 ppm.
Mientras tanto, el compuesto (A) tuvo una tasa plaguicida del 50 % o menor a una concentración de 10 ppm.
<Ejemplo de ensayo 3>
Prueba plaguicida contra Adoxophyes honmai
Se sumergió un alimento artificial finamente cortado durante 30 segundos en una solución química en la que se había preparado un compuesto de ensayo a una concentración predeterminada, y se secó al aire, y después se colocó en una copa de polietileno de 7 cm que tenía un papel de filtro dispuesto en la parte inferior de la misma, y se liberaron larvas en estado 2 de Adoxophyes honmai. Se las dejó en una cámara termostática a 25 °C, y se examinó el número de larvas vivas y las larvas muertas después de 6 días. La prueba se llevó a cabo con cinco larvas por grupo en dos replicados.
Además, el compuesto (A) anterior se usó como compuesto comparativo.
Como resultados de las pruebas anteriores, las composiciones de los compuestos n.° 6-72, 6-80, 6-90, 6-347, 6-348, 6-349, 6-366, 6-382, 6-427, 6-446, 6-449, 6-460, 6-503, 6-504, 6-505, 6-522, 6-524, 6-538, 6-1106, 6-1182, 6-1202, 6 1260, 6-1262, 6-1263, 6-1341, 6-1358, 6-1574, 6-1576, 6-1594, 6-1596, 6-1652, 6-1654, 6-1655, 6-1672, 6-1674, 6 1688, 6-1730, 6-1732, 6-1733, 6-1750, 6-1809, 6-1811, 6-1828, 6-1830, 7-348, 7-366, 7-382, 7-502, 7-505, 7-522, 7 538, 7-1106, 7-1202, 7-1262, 7-1280, 7-1303, 7-1338, 7-1358, 7-1574, 7-1576, 7-1594, 7-1605, 7-1652, 7-1730, 7 1732, 7-1733, 7-1750, 7-1764, 7-1808, 7-1809, 7-1810, y 7-1811 mostraron cada uno una tasa plaguicida del 70 % o superior a una concentración de 1 ppm.
Además, las composiciones de los compuestos n.° 6-271, 6-367, 6-389, 6-426, 6-523, 6-1104, 6-1577, 6-1695, 6-1851, 6-2110, 7-424, 7-444, 7-523, 7-1104, 7-1124, 7-1260, 7-1263, 7-1577, 7-1616, 7-1731, 7-1773, y 7-1851 mostraron cada uno una tasa plaguicida del 70 % o superior a una concentración de 10 ppm.
Mientras tanto, el compuesto (A) tuvo una tasa plaguicida del 50 % o menor a una concentración de 10 ppm.
<Ejemplo de ensayo 4>
Prueba plaguicida contra Choristoneura magnanima
Se sumergió un alimento artificial finamente cortado durante 30 segundos en una solución química en la que se había preparado un compuesto de ensayo a una concentración predeterminada, y se secó al aire, y después se colocó en una copa de polietileno de 7 cm que tenía un papel de filtro dispuesto en la parte inferior de la misma, y se liberaron larvas en estado 2 de Choristoneura magnanima. Se las dejó en una cámara termostática a 25 °C, y se examinó el número de larvas vivas y las larvas muertas después de 6 días. La prueba se llevó a cabo con cinco larvas por grupo en dos replicados.
Además, el compuesto (A) anterior se usó como compuesto comparativo.
Como resultados de las pruebas anteriores, las composiciones de los compuestos n.° 6-72, 6-80, 6-90, 6-271, 6-349, 6-366, 6-367, 6-426, 6-427, 6-1104, 6-1106, 6-1182, 6-1260, 6-1263, 6-1358, 6-1574, 6-1577, 6-1595, 6-1596, 6-1652, 6- 1654, 6-1655, 6-1672, 6-1673, 6-1674, 6-1695, 6-1730, 6-1732, 6-1733, 6-1750, 6-1751,6-1809, 6-1811, 6-1828, 6 1829, 6-1830, 6-1851, 7-90, 7-348, 7-366, 7-382, 7-389, 7-444, 7-502, 7-504, 7-505, 7-523, 7-1104, 7-1106, 7-1107, 7- 1124, 7- 125, 7-1260, 7-1262, 7-1263, 7-1280, 7-1281, 7-1303, 7-1358, 7-1359, 7-1574, 7-1576, 7-1577, 7-1594, 7 1595, 7-1605, 7-1616, 7-1617, 7-1652, 7-1730, 7-1732, 7-1733, 7-1750, 7-1764, 7-1773, 7-1808, 7-1809, 7-1810, 7 1811, 7-1829, y 7-1851 mostraron cada uno una tasa plaguicida del 70 % o superior a una concentración de 1 ppm. Además, las composiciones de los compuestos n.° 6-382, 6-446, 6-460, 6-2110, 7-424, 7-538, y 7-1606 mostraron cada uno una tasa plaguicida del 70 % o superior a una concentración de 10 ppm.
Mientras tanto, el compuesto (A) tuvo una tasa plaguicida del 50 % o menor a una concentración de 10 ppm.
<Ejemplo de ensayo 5>
Prueba plaguicida contra Helicoverpa armigera
Se sumergió un disco foliar de col durante 30 segundos en una solución química en la que se había preparado un compuesto químico a una concentración predeterminada, y se secó al aire. El disco foliar se colocó en una copa de plástico con 6 agujeros que tenía un filtro de papel dispuesto en el fondo de la misma, y se liberaron larvas en estado
2 de Helicoverpa armígera liberándose un insecto por cada agujero. Se las dejó en una cámara termostática a 25 °C, y se examinó el número de larvas vivas y las larvas muertas después de 3 días. La prueba se llevó a cabo con cinco larvas por grupo en dos replicados.
Además, el compuesto (A) anterior se usó como compuesto comparativo.
Como resultados de las pruebas anteriores, las composiciones de los compuestos n.° 6-72, 6-80, 6-90, 6-271, 6-347, 6-348, 6-349, 6-366, 6-367, 6-382, 6-389, 6-426, 6-427, 6-446, 6-449, 6-460, 6-503, 6-504, 6-505, 6-522, 6-523, 6 524, 6-538, 6-1104, 6-1106, 6-1260, 6-1262, 6-1263, 6-1281,6-1341, 6-1358, 6-1359, 6-1574, 6-1576, 6-1577, 6-1594, 6- 1595, 6-1596, 6-1652, 6-1654, 6-1655, 6-1672, 6-1673, 6-1674, 6-1695, 6-1730, 6-1732, 6-1733, 6-1750, 6-1751, 6 1808, 6- 1809, 6-1811,6-1828, 6-1829, 6-1830, 6-1851,6-2110, 7-90, 7-348, 7-366, 7-382, 7-389, 7-424, 7-444, 7-502, 7- 505, 7- 522, 7-523, 7-538, 7-1106, 7-1107, 7-1125, 7-1262, 7-1263, 7-1280, 7-1303, 7-1338, 7-1358, 7-1359, 7-1574, 7-1576, 7-1577, 7-1594, 7-1595, 7-1605, 7-1606, 7-1616, 7-1617, 7-1652, 7-1730, 7-1731, 7-1732, 7-1733, 7-1750, 7 1751, 7-1764, 7-1773, 7-1808, 7-1809, 7-1810, 7-1811,7-1829, y 7-1851 mostraron cada uno una tasa plaguicida del 70 % o superior a una concentración de 1 ppm.
Además, la composición del compuesto n.° 7-1104 mostró una tasa plaguicida del 70 % o más a una concentración de 10 ppm.
Mientras tanto, el compuesto (A) tuvo una tasa plaguicida del 50 % o menor a una concentración de 10 ppm.
<Ejemplo de ensayo 6>
Prueba plaguicida contra Laodelphax striatellus
Se rociaron 2,5 ml de una solución de acetona en la que se había preparado un compuesto de ensayo a una concentración predeterminada sobre plántulas de arroz, se secó al aire, y después se colocaron en un tubo de vidrio que tenía un diámetro de 3 cm y una altura de 13 cm, con agua en su interior, y se liberaron larvas en estado 3 de Laodelphax striatellus y se tapó el tubo. Se las dejó en una cámara termostática a 25 °C, y se examinó el número de larvas vivas y las larvas muertas después de 6 días. La prueba se llevó a cabo con diez larvas por grupo en dos replicados.
Como resultados de las pruebas anteriores, las composiciones de los compuestos n.° 1-491, 1-627, 2-491, 6-39, 6-45, 6-47, 6-57, 6-71,6-72, 6-79, 6-80, 6-90, 6-147, 6-268, 6-269, 6-270, 6-271,6-290, 6-304, 6-306, 6-311,6-346, 6-347, 6 368, 6-382, 6-425, 6-427, 6-444, 6-445, 6-446, 6-460, 6-461,6-503, 6-1104, 6-1106, 6-1107, 6-1124, 6-1126, 6-1140, 6- 1147, 6-1182, 6-1183, 6-1184, 6-1185, 6-1202, 6-1203, 6-1204, 6-1218, 6-1225, 6-1260, 6-1261, 6-1262, 6-1263, 6 1280, 6-1281, 6-1282, 6-1296, 6-1303, 6-1338, 6-1339, 6-1340, 6-1341, 6-1358, 6-1359, 6-1360, 6-1374, 6-1381, 6 1574, 6-1575, 6-1576, 6-1577, 6-1594, 6-1595, 6-1596, 6-1610, 6-1617, 6-1652, 6-1653, 6-1654, 6-1655, 6-1672, 6 1673, 6-1674, 6-1688, 6-1695, 6-1730, 6-1731, 6-1732, 6-1733, 6-1734, 6-1750, 6-1751, 6-1752, 6-1754, 6-1766, 6 1773, 6-1808, 6-1809, 6-1810, 6-1811, 6-1828, 6-1829, 6-1830, 6-1851, 6-2110, 6-3348, 6-3384, 6-5903, 6-5904, 6 5905, 6- 5906, 6-5907, 6-5908, 6-5909, 6-5910, 6-5911, 6-5914, 7-47, 7-57, 7-90, 7-268, 7-285, 7-286, 7-288, 7-289, 7- 301, 7- 303, 7-304, 7-305, 7-311, 7-316, 7-346, 7-348, 7-368, 7-382, 7-389, 7-424, 7-426, 7-427, 7-444, 7-445, 7 446, 7-460, 7-467, 7-538, 7-825, 7-840, 7-948, 7-984, 7-1104, 7-1105, 7-1106, 7-1107, 7-1124, 7-1125, 7-1126, 7 1140, 7-1147, 7-1182, 7-1183, 7-1184, 7-1185, 7-1202, 7-1203, 7-1204, 7-1218, 7-1225, 7-1260, 7-1261, 7-1262, 7 1263, 7-1280, 7-1281, 7-1282, 7-1296, 7-1303, 7-1338, 7-1339, 7-1340, 7-1341, 7-1358, 7-1359, 7-1360, 7-1374, 7 1381, 7-1417, 7-1574, 7-1575, 7-1576, 7-1577, 7-1594, 7-1595, 7-1596, 7-1605, 7-1606, 7-1608, 7-1610, 7-1616, 7 1617, 7-1638, 7-1639, 7-1645, 7-1652, 7-1672, 7-1673, 7-1730, 7-1731, 7-1732, 7-1733, 7-1750, 7-1751, 7-1752, 7 1764, 7-1766, 7-1773, 7-1794, 7-1808, 7-1809, 7-1810, 7-1811, 7-1828, 7-1829, 7-1844, 7-1851, 7-3348, 7-3369, 7 5902, 7-5903, 7-5904, 7-5906, 7-5907, 7-5909, 7-5912, 8-289, 8-304, 8-840, 9-270, 9-290, 9-291, 9-306, 9-2164, 9 2322, 12-835, y 12-864 mostraron cada uno una tasa plaguicida del 70 % o superior a una concentración de 100 ppm.
<Ejemplo de ensayo 7>
Prueba plaguicida contra Musca domestica
Se añadieron gota a gota 1 ml de una solución de acetona en la que se había preparado un compuesto de ensayo a una concentración predeterminada a una placa de Petri que tenía un diámetro de 9 cm, y se secó al aire, y después se liberaron adultos hembra de Musca domestica y se tapó la placa de Petri. Se las dejó en una cámara termostática a 25 °C, y se examinó el número de larvas vivas y las larvas muertas después de 1 día. La prueba se llevó a cabo con cinco larvas por grupo en dos replicados.
Como resultados de las pruebas anteriores, las composiciones de los compue , 6-39, 6-47, 6 72, 6-272, 6-293, 6-346, 6-347, 6-348, 6-366, 6-368, 6-382, 6-389, 6-426, 6-42 6-453, 6-460, 6 503, 6-504, 6-505, 6-522, 6-523, 6-524, 6-538, 6-1105, 6-1107, 6-1124, 6-11 1147, 6-1184, 6-1204, 6 1218, 6-1260, 6-1281, 6-1338, 6-1341, 6-1358, 6-1359, 6-1360, 6-1374, 6-15 1577, 6-1594, 6-1596, 6 1617, 6-1652, 6-1672, 6-1673, 6-1695, 6-1730, 6-1731, 6-1732, 6-1733, 6-17 1751, 6-1752, 6-1773, 6 1808, 6-1809, 6- 1810, 6-1811,6-1828, 6-1829, 6-1830, 6-1851,6-2110, 6-5905, 8, 7-346, 7-348,
7-349, 7-366, 7- 367, 7-368, 7-382, 7-389, 7-424, 7-428, 7-444, 7-446, 7-449, 7-504, 7-522, 7-538, 7-1104, 7-1105, 7 1106, 7-1107, 7-1126, 7-1262, 7-1280, 7-1282, 7-1296, 7-1303, 7-1338, 7-1340, 7-1358, 7-1359, 7-1360, 7-1381, 7 1417, 7-1574, 7-1575, 7-1576, 7-1577, 7-1596, 7-1652, 7-1731, 7-1732, 7-1733, 7-1750, 7-1752, 7-1764, 7-1766, 7 1730, 7-1773, 7-1794, 7-1808, 7-1809, 7-1810, 7-1811, 7-1828, 7-1829, 7-1851, 9-2164, 9-2322, 11-777, 11-835, 12 777, 12-835, 12-864, 17-1103, y 27-627 mostraron cada uno una tasa plaguicida del 70 % o superior a una concentración de 100 ppm.
<Ejemplo de ensayo 8>
Prueba plaguicida contra Blattella germánica
Se añadieron gota a gota 1 ml de una solución de acetona en la que se había preparado un compuesto de ensayo a una concentración predeterminada a una placa de Petri que tenía un diámetro de 9 cm, y se secó al aire, y después se liberaron adultos hembra de Blattella germánica y se tapó la placa de Petri. Se las dejó en una cámara termostática a 25 °C, y se examinó el número de larvas vivas y las larvas muertas después de 1 día. La prueba se llevó a cabo con cinco larvas por grupo en dos replicados.
Como resultados de las pruebas anteriores, las composiciones de los compuestos n.° 1-1925, 6-39, 6-47, 6-346, 6 347, 6-367, 6-368, 6-382, 6-389, 6-426, 6-427, 6-503, 6-538, 6-1105, 6-1106, 6-1107, 6-1124, 6-1125, 6-1126, 6-1147, 6- 1184, 6-1204, 6-1218, 6-1280, 6-1296, 6-1338, 6-1358, 6-1359, 6-1575, 6-1576, 6-1577, 6-1594, 6-1595, 6-1596, 6 1610, 6- 1617, 6-1730, 6-1731,6-1732, 6-1733, 6-1750, 6-1751,6-1752, 6-1773, 6-1811,6-5905, 7-57, 7-268, 7-305, 7 347, 7- 349, 7-367, 7-382, 7-389, 7-424, 7-444, 7-446, 7-502, 7-505, 7-538, 7-1104, 7-1105, 7-1106, 7-1107, 7-1125, 7- 1126, 7-1261, 7-1262, 7-1280, 7-1282, 7-1296, 7-1303, 7-1381, 7-1574, 7-1575, 7-1576, 7-1577, 7-1594, 7-1595, 7 1596, 7-1617, 7-1731,7-1732, 7-1733, 7-1750, 7-1752, 7-1766, 7-1773, y 7-1851 mostraron cada uno una tasa plaguicida del 70 % o superior a una concentración de 100 ppm.
<Ejemplo de ensayo 9>
Agene plaguicida contra Culex pipiens molestus
Se añadieron gota a gota 1 ml de una solución de acetona en la que se había preparado un compuesto de ensayo a una concentración predeterminada a una placa de Petri que tenía un diámetro de 9 cm, y se secó al aire, y después se liberaron adultos hembra de Culex pipiens molestus y se tapó la placa de Petri. Se las dejó en una cámara termostática a 25 °C, y se examinó el número de larvas vivas y las larvas muertas después de 1 día de tratamiento. La prueba se llevó a cabo con cinco larvas por grupo en dos replicados.
Como resultados de las pruebas anteriores, las composiciones de los compuestos n.° 7-424, 7-1574, 7-1577, 7-1730, 7-1732, y 7-1733 mostraron cada uno una tasa plaguicida del 70 % o superior a una concentración de 1000 ppm.
<Ejemplo de ensayo 10>
Prueba plaguicida contra Coptotermes formosanus
Se añadieron gota a gota 20 pl de una solución de acetona en la que se había preparado un compuesto de ensayo a una concentración predeterminada al papel de filtro que tenía un diámetro de 2,6 mm incluido en una copa de polipropileno, y se secó al aire, y después se añadieron 20 pl de agua al mismo. Se liberaron Coptotermes formosanus y se cerró la copa. Se las dejó en una cámara termostática a 28 °C, y se examinó el número de larvas vivas y las larvas muertas después de 5 días de tratamiento. La prueba se llevó a cabo con diez larvas por grupo en dos replicados.
Como resultados de las pruebas anteriores, las composiciones de los compuestos n.° 6-460, 6-1260, 6-1652, 7-268, 7-424, 7-1104, 7-1574, 7-1577, 7-1730, 7-1732, y 7-1733 mostraron cada uno una tasa plaguicida del 70 % o superior a una concentración de 30 ppm.
Aplicabilidad industrial
De acuerdo con la presente invención, es posible proporcionar un nuevo agente para el control de plagas que comprende derivado de amida. El derivado de amida muestra un efecto significativo para una actividad de control de plagas, y tiene una elevada disponibilidad industrial.
Claims (1)
- REIVINDICACIONES1. Un agente para el control de plagas que comprende al menos un derivado de amida seleccionado entre el grupo que consiste en las siguientes Fórmula (1), Fórmula (7), Fórmula (8) y Fórmula (9) como principio activo:en donde, en la Fórmula (1):A representa un átomo de carbono, un átomo de oxígeno, un átomo de nitrógeno, un átomo de nitrógeno oxidado o un átomo de azufre;K representa un grupo de átomo no metálico necesario para formar un grupo de unión cíclico derivado de piridina, N-óxido de piridina, pirrol, tiazol, furano o tiofeno, junto con A y dos átomos de carbono a los que se une A; X representa un átomo de hidrógeno, un átomo de halógeno, un grupo alquilo C1-C6, un grupo haloalquilo C1-C6, un grupo cicloalquilo C3-C9, un grupo halocicloalquilo C3-C9, un grupo alquenilo C2-C6, un grupo haloalquenilo C2-C6, un grupo alquinilo C2-C6, un grupo haloalquinilo C2-C6, un grupo alcoxi C1-C6, un grupo haloalcoxi C1-C6, un grupo alqueniloxi C2-C6, un grupo haloalqueniloxi C2-C6, un grupo alquiniloxi C2-C6, un grupo haloalquiniloxi C2-C6, un grupo cicloalcoxi C3-C9, un grupo halocicloalcoxi C3-C9, un grupo alquiltio C1-C6, un grupo haloalquiltio C1-C6, un grupo alquilsulfinilo C1-C6, un grupo haloalquilsulfinilo C1-C6, un grupo alquilsulfonilo C1-C6, un grupo haloalquilsulfonilo C1-C6, un grupo alquilsulfoniloxi C1-C6, un grupo haloalquilsulfoniloxi C1-C6, un grupo alquilcarbonilo C2-C7, un grupo haloalquilcarbonilo C2-C7, un grupo alquenilcarbonilo C3-C7, un grupo haloalquenilcarbonilo C3-C7, un grupo alquinilcarbonilo C3-C7, un grupo haloalquinilcarbonilo C3-C7, un grupo cicloalquilcarbonilo C4-C10, un grupo halocicloalquilcarbonilo C4-C10, un grupo alquilcarboniloxi C2-C7, un grupo haloalquilcarboniloxi C2-C7, un grupo arilcarboniloxi, un grupo alcoxicarbonilo C2-C7, un grupo haloalcoxicarbonilo C2-C7, un grupo alqueniloxicarbonilo C3-C7, un grupo haloalqueniloxicarbonilo C3-C7, un grupo alquiniloxicarbonilo C3-C7, un grupo haloalquiniloxicarbonilo C3-C7, un grupo cicloalquiloxicarbonilo C4-C10, un grupo halocicloalquiloxicarbonilo C4-C10, un grupo alquilcarbonilamino C2-C7, un grupo haloalquilcarbonilamino C2-C7, un grupo alcoxicarbonilamino C2-C7, un grupo haloalcoxicarbonilamino C2-C7, un grupo alcoxicarboniloxi C2-C7, un grupo haloalcoxicarboniloxi C2-C7, un grupo arilcarbonilamino, un grupo amino, un grupo carbamoílo, un grupo ciano, un grupo hidroxi, un grupo pentafluorosulfanilo, un grupo alquilamino C1-C6, un grupo haloalquilamino C1-C6, un grupo alquenilamino C2-C6, un grupo haloalquenilamino C2-C6, un grupo alquinilamino C2-C6, un grupo haloalquinilamino C2-C6, un grupo cicloalquilamino C3-C9, un grupo halocicloalquilamino C3-C9, un grupo alquilaminocarbonilo C2-C7, un grupo haloalquilaminocarbonilo C2-C7, un grupo alquenilaminocarbonilo C3-C7, un grupo haloalquenilaminocarbonilo C3-C7, un grupo alquinilaminocarbonilo C3-C7, un grupo haloalquinilaminocarbonilo C3-C7, un grupo cicloalquilaminocarbonilo C4-C10, un grupo halocicloalquilaminocarbonilo C4-C10, un grupo fenilo o un grupo heterocíclico, y cuando hay varios X, cada X puede ser igual o diferente entre sí;n representa un número entero de 0 a 4;T representa -C(=G-i)-Q1 o -C(=G-i)-G2Q2;cada uno de G1 y G2 representa independientemente un átomo de oxígeno o un átomo de azufre;cada uno de Q1 y Q2 representa:un átomo de hidrógeno, un grupo alquilo C1-C6, un grupo haloalquilo C1-C6, un grupo alquenilo C2-C6, un grupo haloalquenilo C2-C6, un grupo alquinilo C2-C6, un grupo haloalquinilo C2-C6, un grupo cicloalquilo C3-C9, un grupo halocicloalquilo C3-C9, un grupo bencilo, un grupo fenilo que puede tener un sustituyente, un grupo naftilo o un grupo heterocíclico que puede tener un sustituyente;Y1 e Y5 representan un átomo de halógeno o un grupo haloalquilo C1-C3 e Y1 o Y5 representan un grupo haloalquilo C1-C3;Y2 e Y4 representan un átomo de hidrógeno;Y3 representa un grupo perfluoroalquilo C2-C4;en donde, en Q1 y Q2, el sustituyente de un grupo fenilo que puede tener un sustituyente y un grupo heterocíclico que puede tener un sustituyente representan uno o más sustituyentes seleccionados entre un grupo que consiste en:un átomo de halógeno, un grupo alquilo C1-C6, un grupo haloalquilo C1-C6, un grupo cicloalquilo C3-C9, un grupo halocicloalquilo C3-C9, un grupo alquenilo C2-C6, un grupo haloalquenilo C2-C6, un grupo alquinilo C2-C6, un grupo haloalquinilo C2-C6, un grupo alcoxi C1-C6, un grupo haloalcoxi C1-C6, un grupo alqueniloxi C2-C6, un grupo haloalqueniloxi C2-C6, un grupo alquiniloxi C2-C6, un grupo haloalquiniloxi C2-C6, un grupo cicloalcoxi C3-C9, un grupo halocicloalcoxi C3-C9, un grupo alquiltio C1-C6, un grupo haloalquiltio C1-C6, un grupo alquilsulfinilo C1-C6, un grupo haloalquilsulfinilo C1-C6, un grupo alquilsulfonilo C1-C6, un grupo haloalquilsulfonilo C1-C6, un grupo alquilcarbonilo C2-C7, un grupo haloalquilcarbonilo C2-C7, un grupo alquenilcarbonilo C3-C7, un grupo haloalquenilcarbonilo C3-C7, un grupo alquinilcarbonilo C3-C7, un grupo haloalquinilcarbonilo C3-C7, un grupo cicloalquilcarbonilo C4-C10, un grupo halocicloalquilcarbonilo C4-C10, un grupo alquilcarboniloxi C2-C7, un grupo haloalquilcarboniloxi C2-C7, un grupo alquilsulfoniloxi C1-C6, un grupo haloalquilsulfoniloxi C1-C6, un grupo alcoxicarbonilo C2-C7, un grupo haloalcoxicarbonilo C2-C7, un grupo alqueniloxicarbonilo C3-C7, un grupo haloalqueniloxicarbonilo C3-C7, un grupo alquiniloxicarbonilo C3-C7, un grupo haloalquiniloxicarbonilo C3-C7, un grupo cicloalquiloxicarbonilo C4-C10, un grupo halocicloalquiloxicarbonilo C4-C10, un grupo alquilcarbonilamino C2-C7, un grupo haloalquilcarbonilamino C2-C7, un grupo alcoxicarbonilamino C2-C7, un grupo haloalcoxicarbonilamino C2-C7, un grupo alquilamino C1-C6, un grupo haloalquilamino C1-C6, un grupo alquenilamino C2-C6, un grupo haloalquenilamino C2-C6, un grupo alquinilamino C2-C6, un grupo haloalquinilamino C2-C6, un grupo cicloalquilamino C3-C9, un grupo halocicloalquilamino C3-C9, un grupo alquilaminocarbonilo C2-C7, un grupo haloalquilaminocarbonilo C2-C7, un grupo alquenilaminocarbonilo C3-C7, un grupo haloalquenilaminocarbonilo C3-C7, un grupo alquinilaminocarbonilo C3-C7, un grupo haloalquinilaminocarbonilo C3-C7, un grupo cicloalquilaminocarbonilo C4-C10, un grupo halocicloalquilaminocarbonilo C4-C10, un grupo amino, un grupo carbamoílo, un grupo ciano, un grupo nitro, un grupo hidroxi, un grupo pentafluorosulfanilo, un grupo fenilo que puede tener un sustituyente y un grupo heterocíclico que puede tener un sustituyente, y cuando hay dos o más sustituyentes, los sustituyentes pueden ser iguales o diferentes entre sí;en donde, el grupo heterocíclico en X, Q1, y Q2 representan un grupo piridilo, un grupo N-óxido de piridina, un grupo pirimidinilo, un grupo pirazinilo, un grupo piridazilo, un grupo furilo, un grupo tienilo, un grupo oxazolilo, un grupo isoxazolilo, un grupo oxadiazolilo, un grupo tiazolilo, un grupo isotiazolilo, un grupo tiadiazolilo, un grupo pirrolilo, un grupo imidazolilo, un grupo triazolilo, un grupo pirazolilo o un grupo tetrazolilo;G3 representa un átomo de oxígeno o un átomo de azufre; ycada uno de Ri y R2 representa independientemente un átomo de hidrógeno, un átomo de oxígeno, un átomo de halógeno, un grupo hidroxi, un grupo nitro, un grupo nitroso, un grupo trimetilsililo, un grupo tbutildimetilsililo, un grupo ciano, un grupo amino, un grupo alquilo C1-C6 que puede tener un sustituyente, un grupo haloalquilo C1-C6 que puede tener un sustituyente, un grupo alquilcarbonilo C2-C7, un grupo haloalquilcarbonilo C2-C7, un grupo alquenilo C2-C6 que puede tener un sustituyente, un grupo haloalquenilo C2-C6 que puede tener un sustituyente, un grupo alquinilo C2-C6 que puede tener un sustituyente, un grupo haloalquinilo C2-C6 que puede tener un sustituyente, un grupo alcoxicarbonilo C2-C7, un grupo haloalcoxicarbonilo C2-C7, un grupo alqueniloxicarbonilo C3-C7, un grupo haloalqueniloxicarbonilo C3-C7, un grupo alquiniloxicarbonilo C3-C7, un grupo haloalquiniloxicarbonilo C3-C7, un grupo fenoxicarbonilo, un grupo alquilaminocarbonilo C2-C7, un grupo haloalquilaminocarbonilo C2-C7, un grupo alquilcarboniloxi C2-C7, un grupo haloalquilcarboniloxi C2-C7, un grupo benzoílo, un grupo alcoxi C1-C6, un grupo haloalcoxi C1-C6, un grupo alquiltio C1-C6, un grupo haloalquiltio C1-C6, un grupo alquilsulfinilo C1-C6, un grupo haloalquilsulfinilo C1-C6, un grupo alquilsulfonilo C1-C6, un grupo haloalquilsulfonilo C1-C6, un grupo bencenosulfonilo, un grupo bencilsulfonilo, un grupo bencilo o -C(=O)C(=O)R7, en donde R7 representa un grupo alquilo C1-C6, un grupo haloalquilo C1-C6, un grupo alcoxi C1-C6 o un grupo haloalcoxi C1-C6;cada X representa independientemente un átomo de hidrógeno, un átomo de halógeno o un grupo ciano;Y3 representa un grupo perfluoroalquilo C2-C4;Y2 e Y4 representan un átomo de hidrógeno;Y1 e Y5 representan un átomo de halógeno o un grupo haloalquilo C1-C3 e Y1 o Y5 representan un grupo haloalquilo C1-C3;cada uno de G1 y G3 representa independientemente un átomo de oxígeno o un átomo de azufre;Q1 representa un átomo de hidrógeno, un grupo alquilo C1-C6, un grupo haloalquilo C1-C6, un grupo alquenilo C2-C6, un grupo haloalquenilo C2-C6, un grupo alquinilo C2-C6, un grupo haloalquinilo C2-C6, un grupo cicloalquilo C3-C9, un grupo halocicloalquilo C3-C9, un grupo bencilo, un grupo fenilo que puede tener un sustituyente, un grupo naftilo o un grupo heterocíclico que puede tener un sustituyente;en donde, en Q1, el sustituyente de un grupo fenilo que puede tener un sustituyente y un sustituyente de grupo heterocíclico que puede tener un sustituyente representan uno o más sustituyentes seleccionados entre un grupo que consiste en:un átomo de halógeno, un grupo alquilo C1-C6, un grupo haloalquilo C1-C6, un grupo cicloalquilo C3-C9, un grupo halocicloalquilo C3-C9, un grupo alquenilo C2-C6, un grupo haloalquenilo C2-C6, un grupo alquinilo C2-C6, un grupo haloalquinilo C2-C6, un grupo alcoxi C1-C6, un grupo haloalcoxi C1-C6, un grupo alqueniloxi C2-C6, un grupo haloalqueniloxi C2-C6, un grupo alquiniloxi C2-C6, un grupo haloalquiniloxi C2-C6, un grupo cicloalcoxi C3-C9, un grupo halocicloalcoxi C3-C9, un grupo alquiltio C1-C6, un grupo haloalquiltio C1-C6, un grupo alquilsulfinilo C1-C6, un grupo haloalquilsulfinilo C1-C6, un grupo alquilsulfonilo C1-C6, un grupo haloalquilsulfonilo C1-C6, un grupo alquilcarbonilo C2-C7, un grupo haloalquilcarbonilo C2-C7, un grupo alquenilcarbonilo C3-C7, un grupo haloalquenilcarbonilo C3-C7, un grupo alquinilcarbonilo C3-C7, un grupo haloalquinilcarbonilo C3-C7, un grupo cicloalquilcarbonilo C4-C10, un grupo halocicloalquilcarbonilo C4-C10, un grupo alquilcarboniloxi C2-C7, un grupo haloalquilcarboniloxi C2-C7, un grupo alquilsulfoniloxi C1-C6, un grupo haloalquilsulfoniloxi C1-C6, un grupo alcoxicarbonilo C2-C7, un grupo haloalcoxicarbonilo C2-C7, un grupo alqueniloxicarbonilo C3-C7, un grupo haloalqueniloxicarbonilo C3-C7, un grupo alquiniloxicarbonilo C3-C7, un grupo haloalquiniloxicarbonilo C3-C7, un grupo cicloalquiloxicarbonilo C4-C10, un grupo halocicloalquiloxicarbonilo C4-C10, un grupo alquilcarbonilamino C2-C7, un grupo haloalquilcarbonilamino C2-C7, un grupo alcoxicarbonilamino C2-C7, un grupo haloalcoxicarbonilamino C2-C7, un grupo alquilamino C1-C6, un grupo haloalquilamino C1-C6, un grupo alquenilamino C2-C6, un grupo haloalquenilamino C2-C6, un grupo alquinilamino C2-C6, un grupo haloalquinilamino C2-C6, un grupo cicloalquilamino C3-C9, un grupo halocicloalquilamino C3-C9, un grupo alquilaminocarbonilo C2-C7, un grupo haloalquilaminocarbonilo C2-C7, un grupo alquenilaminocarbonilo C3-C7, un grupo haloalquenilaminocarbonilo C3-C7, un grupo alquinilaminocarbonilo C3-C7, un grupo haloalquinilaminocarbonilo C3-C7, un grupo cicloalquilaminocarbonilo C4-C10, un grupo halocicloalquilaminocarbonilo C4-C10, un grupo amino, un grupo carbamoílo, un grupo ciano, un grupo nitro, un grupo hidroxi, un grupo pentafluorosulfanilo, un grupo fenilo que puede tener un sustituyente y un grupo heterocíclico que puede tener un sustituyente, y cuando hay dos o más sustituyentes, los sustituyentes pueden ser iguales o diferentes entre sí;en donde, el grupo heterocíclico en Q1 representa un grupo piridilo, un grupo N-óxido de piridina, un grupo pirimidinilo, un grupo pirazinilo, un grupo piridazilo, un grupo furilo, un grupo tienilo, un grupo oxazolilo, un grupo isoxazolilo, un grupo oxadiazolilo, un grupo tiazolilo, un grupo isotiazolilo, un grupo tiadiazolilo, un grupo pirrolilo, un grupo imidazolilo, un grupo triazolilo, un grupo pirazolilo o un grupo tetrazolilo;cada uno de R1 y R2 representa independientemente un átomo de hidrógeno, un átomo de oxígeno, un átomo de halógeno, un grupo hidroxi, un grupo nitro, un grupo nitroso, un grupo trimetilsililo, un grupo t-butildimetilsililo, un grupo ciano, un grupo amino, un grupo alquilo C1-C6 que puede tener un sustituyente, un grupo haloalquilo C1-C6 que puede tener un sustituyente, un grupo alquilcarbonilo C2-C7, un grupo haloalquilcarbonilo C2-C7, un grupo alquenilo C2-C6 que puede tener un sustituyente, un grupo haloalquenilo C2-C6 que puede tener un sustituyente, un grupo alquinilo C2-C6 que puede tener un sustituyente, un grupo haloalquinilo C2-C6 que puede tener un sustituyente, un grupo alcoxicarbonilo C2-C7, un grupo haloalcoxicarbonilo C2-C7, un grupo alqueniloxicarbonilo C3-C7, un grupo haloalqueniloxicarbonilo C3-C7, un grupo alquiniloxicarbonilo C3-C7, un grupo haloalquiniloxicarbonilo C3-C7, un grupo fenoxicarbonilo, un grupo alquilaminocarbonilo C2-C7, un grupo haloalquilaminocarbonilo C2-C7, un grupo alquilcarboniloxi C2-C7, un grupo haloalquilcarboniloxi C2-C7, un grupo benzoílo, un grupo alcoxi C1-C6, un grupo haloalcoxi C1-C6, un grupo alquiltio C1-C6, un grupo haloalquiltio C1-C6, un grupo alquilsulfinilo C1-C6, un grupo haloalquilsulfinilo C1-C6, un grupo alquilsulfonilo C1-C6, un grupo haloalquilsulfonilo C1-C6, un grupo bencenosulfonilo, un grupo bencilsulfonilo, un grupo bencilo o -C(=O)C(=O)R7, en donde R7 representa un grupo alquilo C1-C6, un grupo haloalquilo C1-C6, un grupo alcoxi C1-C6 o un grupo haloalcoxi C1-C6;en donde, en la Fórmula (8), Q1 representa un grupo fenilo o un grupo piridilo que pueden tener un sustituyente seleccionado entre un grupo que consiste en: un átomo de halógeno, un grupo haloalquilo C1, un grupo nitro y un grupo ciano, en un caso donde Q1 tiene el sustituyente, el número de los sustituyentes es 1 o 2;cada uno de X 1 y X2 representa independientemente un átomo de hidrógeno o un átomo de flúor y X3 y X4 representan un átomo de hidrógeno;cada uno de R1 y R2 representa independientemente un átomo de hidrógeno o un grupo metilo;cada uno de Y 1 e Y5 representa independientemente un átomo de cloro, un átomo de bromo, un átomo de yodo, un grupo trifluorometoxi, un grupo trifluorometilo o un grupo pentafluoroetilo;Y2 e Y4 representan un átomo de hidrógeno;e Y3 representa un grupo perfluoroalquilo C3-C4;en un caso donde Y 1 e Y5 representan átomos de halógeno simultáneamente, al menos uno de X 1 o X2 representa un átomo de flúor; yen un caso donde Y 1 o Y5 representan un grupo trifluorometoxi, X2 representa un átomo de flúor;en donde, en la Fórmula (9), n representa 4;cada uno de los cuatro X representa independientemente un átomo de hidrógeno, un átomo de halógeno o un grupo ciano;Y3 representa un grupo perfluoroalquilo C2-C4;Y2 e Y4 representan un átomo de hidrógeno;cada Y1 e Y5 representa independientemente un átomo de halógeno o un grupo haloalquilo C1-C3, e Y1 o Y5 representan un grupo haloalquilo C1-C3;cada uno de G1, G2 y G3 representa independientemente un átomo de oxígeno o un átomo de azufre;Q2 representa un átomo de hidrógeno, un grupo alquilo C1-C6, un grupo haloalquilo C1-C6, un grupo alquenilo C2-C6, un grupo haloalquenilo C2-C6, un grupo alquinilo C2-C6, un grupo haloalquinilo C2-C6, un grupo cicloalquilo C3-C9, un grupo halocicloalquilo C3-C9, un grupo bencilo, un grupo fenilo que puede tener un sustituyente, un grupo naftilo o un grupo heterocíclico que puede tener un sustituyente;en donde, en Q2, el sustituyente de un grupo fenilo que puede tener un sustituyente y un grupo heterocíclico que puede tener un sustituyente representan uno o más sustituyentes seleccionados entre un grupo que consiste en:un átomo de halógeno, un grupo alquilo C1-C6, un grupo haloalquilo C1-C6, un grupo cicloalquilo C3-C9, un grupo halocicloalquilo C3-C9, un grupo alquenilo C2-C6, un grupo haloalquenilo C2-C6, un grupo alquinilo C2-C6, un grupo haloalquinilo C2-C6, un grupo alcoxi C1-C6, un grupo haloalcoxi C1-C6, un grupo alqueniloxi C2-C6, un grupo haloalqueniloxi C2-C6, un grupo alquiniloxi C2-C6, un grupo haloalquiniloxi C2-C6, un grupo cicloalcoxi C3-C9, un grupo halocicloalcoxi C3-C9, un grupo alquiltio C1-C6, un grupo haloalquiltio C1-C6, un grupo alquilsulfinilo C1-C6, un grupo haloalquilsulfinilo C1-C6, un grupo alquilsulfonilo C1-C6, un grupo haloalquilsulfonilo C1-C6, un grupo alquilcarbonilo C2-C7, un grupo haloalquilcarbonilo C2-C7, un grupo alquenilcarbonilo C3-C7, un grupo haloalquenilcarbonilo C3-C7, un grupo alquinilcarbonilo C3-C7, un grupo haloalquinilcarbonilo C3-C7, un grupo cicloalquilcarbonilo C4-C10, un grupo halocicloalquilcarbonilo C4-C10, un grupo alquilcarboniloxi C2-C7, un grupo haloalquilcarboniloxi C2-C7, un grupo alquilsulfoniloxi C1-C6, un grupo haloalquilsulfoniloxi C1-C6, un grupo alcoxicarbonilo C2-C7, un grupo haloalcoxicarbonilo C2-C7, un grupo alqueniloxicarbonilo C3-C7, un grupo haloalqueniloxicarbonilo C3-C7, un grupo alquiniloxicarbonilo C3-C7, un grupo haloalquiniloxicarbonilo C3-C7, un grupo cicloalquiloxicarbonilo C4-C10, un grupo halocicloalquiloxicarbonilo C4-C10, un grupo alquilcarbonilamino C2-C7, un grupo haloalquilcarbonilamino C2-C7, un grupo alcoxicarbonilamino C2-C7, un grupo haloalcoxicarbonilamino C2-C7, un grupo alquilamino C1-C6, un grupo haloalquilamino C1-C6, un grupo alquenilamino C2-C6, un grupo haloalquenilamino C2-C6, un grupo alquinilamino C2-C6, un grupo haloalquinilamino C2-C6, un grupo cicloalquilamino C3-C9, un grupo halocicloalquilamino C3-C9, un grupo alquilaminocarbonilo C2-C7, un grupo haloalquilaminocarbonilo C2-C7, un grupo alquenilaminocarbonilo C3-C7, un grupo haloalquenilaminocarbonilo C3-C7, un grupo alquinilaminocarbonilo C3-C7, un grupo haloalquinilaminocarbonilo C3-C7, un grupo cicloalquilaminocarbonilo C4-C10, un grupo halocicloalquilaminocarbonilo C4-C10, un grupo amino, un grupo carbamoílo, un grupo ciano, un grupo nitro, un grupo hidroxi, un grupo pentafluorosulfanilo, un grupo fenilo que puede tener un sustituyente, y un grupo heterocíclico que puede tener un sustituyente, y cuando hay dos o más sustituyentes, los sustituyentes pueden ser iguales o diferentes entre sí;en donde, el grupo heterocíclico en Q2 representa un grupo piridilo, un grupo N-óxido de piridina, un grupo pirimidinilo, un grupo pirazinilo, un grupo piridazilo, un grupo furilo, un grupo tienilo, un grupo oxazolilo, un grupo isoxazolilo, un grupo oxadiazolilo, un grupo tiazolilo, un grupo isotiazolilo, un grupo tiadiazolilo, un grupo pirrolilo, un grupo imidazolilo, un grupo triazolilo, un grupo pirazolilo o un grupo tetrazolilo;cada uno de R1 y R2 representa independientemente un átomo de hidrógeno, un átomo de oxígeno, un átomo de halógeno, un grupo hidroxi, un grupo nitro, un grupo nitroso, un grupo trimetilsililo, un grupo t-butildimetilsililo, un grupo ciano, un grupo amino, un grupo alquilo C1-C6 que puede tener un sustituyente, un grupo haloalquilo C1-C6 que puede tener un sustituyente, un grupo alquilcarbonilo C2-C7, un grupo haloalquilcarbonilo C2-C7, un grupo alquenilo C2-C6 que puede tener un sustituyente, un grupo haloalquenilo C2-C6 que puede tener un sustituyente, un grupo alquinilo C2-C6 que puede tener un sustituyente, un grupo haloalquinilo C2-C6 que puede tener un sustituyente, un grupo alcoxicarbonilo C2-C7, un grupo haloalcoxicarbonilo C2-C7, un grupo alqueniloxicarbonilo C3-C7, un grupo haloalqueniloxicarbonilo C3-C7, un grupo alquiniloxicarbonilo C3-C7, un grupo haloalquiniloxicarbonilo C3-C7, un grupo fenoxicarbonilo, un grupo alquilaminocarbonilo C2-C7, un grupo haloalquilaminocarbonilo C2-C7, un grupo alquilcarboniloxi C2-C7, un grupo haloalquilcarboniloxi C2-C7, un grupo benzoílo, un grupo alcoxi C1-C6, un grupo haloalcoxi C1-C6, un grupo alquiltio C1-C6, un grupo haloalquiltio C1-C6, un grupo alquilsulfinilo C1-C6, un grupo haloalquilsulfinilo C1-C6, un grupo alquilsulfonilo C1-C6, un grupo haloalquilsulfonilo C1-C6, un grupo bencenosulfonilo, un grupo bencilsulfonilo, un grupo bencilo o -C(=O)C(=O)R7, en donde R7 representa un grupo alquilo C1-C6, un grupo haloalquilo C1-C6, un grupo alcoxi C1-C6 o un grupo haloalcoxi C1-C6, en donde la plaga se selecciona entre el grupo que consiste en:Insectos Siphonaptera tales como Ctenocephalides felis, Ctenocephalides canis, Echidnophaga gallinácea, Pulex irritans, y Xenopsylla cheopis;insectos Mallophaga tales como Menacanthus stramineus, y Bovicola bovis;insectos Anoplura tales como Haematopinus eurysternus, Haematopinus suis, Linognathus vituli, y Solenopotes capillatus;Ixodidae tales como Boophilus microplus, Rhipicephalus sanguineus, Haemaphysalis longicornis, Haemaphysalis flava, Haemaphysalis campanulata, Ixodes ovatus, Ixodes persulcatus, Amblyomma spp., y Dermacentor spp.;Cheyletidae tales como Cheyletiella yasguri, y Cheyletiella blakei;Demodicidae tales como Demodex canis, Demodex cati;Psoroptidae tales como Psoroptes ovis; ySarcoptidae tales como Sarcoptes scabiei, Notoedres cati y Knemidocoptes spp.2. Una composición que comprende un agente para el control de plagas que comprende al menos un derivado de amida de acuerdo con la Fórmula (1), la Fórmula (7), la Fórmula (8) o la Fórmula (9), tal como se definen en la reivindicación 1.3. Un método de control de plagas que comprende aplicar el agente para el control de plagas según la reivindicación 1 , o la composición como se define en la reivindicación 2 a una plaga como se define en la reivindicación 1, en donde el método no es un método de tratamiento.4. Un agente para el control de plagas que comprende al menos un derivado de amida de acuerdo con la Fórmula (1), la Fórmula (7), la Fórmula (8) y la Fórmula (9), tal como se definen en la reivindicación 1, o una composición como se define en la reivindicación 2, para su uso en un método de tratamiento del cuerpo humano o animal.5. Un agente para el control de plagas que comprende al menos un derivado de amida de acuerdo con la Fórmula (1), la Fórmula (7), la Fórmula (8) y la Fórmula (9), tal como se definen en la reivindicación 1, o una composición como se define en la reivindicación 2, para su uso en un método de tratamiento del cuerpo humano o animal,en donde el método es para exterminar una plaga seleccionada del grupo que consiste en:Insectos Siphonaptera tales como Ctenocephalides felis, Ctenocephalides canis, Echidnophaga gallinácea, Pulex irritans, y Xenopsylla cheopis;insectos Mallophaga tales como Menacanthus stramineus, y Bovicola bovis;insectos Anoplura tales como Haematopinus eurysternus, Haematopinus suis, Linognathus vituli, y Solenopotes capillatus;Ixodidae tales como Boophilus microplus, Rhipicephalus sanguineus, Haemaphysalis longicornis, Haemaphysalis flava, Haemaphysalis campanulata, Ixodes ovatus, Ixodes persulcatus, Amblyomma spp., y Dermacentor spp.; Cheyletidae tales como Cheyletiella yasguri, y Cheyletiella blakei;Demodicidae tales como Demodex canis, Demodex cati;Psoroptidae tales como Psoroptes ovis; ySarcoptidae tales como Sarcoptes scabiei, Notoedres cati, y Knemidocoptes spp.6. Uso de un agente para el control de plagas que comprende al menos un derivado de amida de acuerdo con la Fórmula (1), la Fórmula (7), la Fórmula (8) y la Fórmula (9), tal como se definen en la reivindicación 1, o una composición tal como se define en la reivindicación 2, como un agente para el control de plagas, en donde el uso no es un método de tratamiento del cuerpo humano o animal.7. El uso de acuerdo con la reivindicación 6, en donde el uso es para el control de una plaga seleccionada del grupo que consiste en:Insectos Siphonaptera tales como Ctenocephalides felis, Ctenocephalides canis, Echidnophaga gallinacea, Pulex irritans, y Xenopsylla cheopis;insectos Mallophaga tales como Menacanthus stramineus, y Bovicola bovis;insectos Anoplura tales como Haematopinus eurysternus, Haematopinus suis, Linognathus vituli, y Solenopotes capillatus;Ixodidae tales como Boophilus microplus, Rhipicephalus sanguineus, Haemaphysalis longicornis, Haemaphysalis flava, Haemaphysalis campanulata, Ixodes ovatus, Ixodes persulcatus, Amblyomma spp., y Dermacentor spp.; Cheyletidae tales como Cheyletiella yasguri, y Cheyletiella blakei;Demodicidae tales como Demodex canis, Demodex cati;Psoroptidae tales como Psoroptes ovis; ySarcoptidae tales como Sarcoptes scabiei, Notoedres cati, y Knemidocoptes spp.
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008208714 | 2008-08-13 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2864286T3 true ES2864286T3 (es) | 2021-10-13 |
Family
ID=41668861
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES16166952T Active ES2864286T3 (es) | 2008-08-13 | 2009-06-30 | Agente para el control de plagas que contiene un derivado de amida y uso del agente para el control de plagas |
| ES09806610.3T Active ES2613053T3 (es) | 2008-08-13 | 2009-06-30 | Derivado de amida, agente para el control de plagas que contiene el derivado de amida y uso del agente para el control de plagas |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES09806610.3T Active ES2613053T3 (es) | 2008-08-13 | 2009-06-30 | Derivado de amida, agente para el control de plagas que contiene el derivado de amida y uso del agente para el control de plagas |
Country Status (19)
| Country | Link |
|---|---|
| EP (2) | EP2319830B1 (es) |
| JP (3) | JP5647895B2 (es) |
| KR (3) | KR101403093B1 (es) |
| CN (2) | CN102119143B (es) |
| AU (1) | AU2009280679B2 (es) |
| BR (1) | BRPI0918021B1 (es) |
| CA (1) | CA2733557C (es) |
| DK (2) | DK3081552T3 (es) |
| ES (2) | ES2864286T3 (es) |
| HR (1) | HRP20210788T1 (es) |
| HU (1) | HUE054543T2 (es) |
| LT (1) | LT3081552T (es) |
| MX (1) | MX2011001536A (es) |
| PL (1) | PL3081552T3 (es) |
| PT (1) | PT3081552T (es) |
| RU (1) | RU2469025C2 (es) |
| SI (1) | SI3081552T1 (es) |
| VN (1) | VN27368A1 (es) |
| WO (1) | WO2010018714A1 (es) |
Families Citing this family (144)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8686044B2 (en) | 2008-08-13 | 2014-04-01 | Mitsui Chemicals Agro, Inc. | Amide derivative, pest control agent containing the amide derivative, and use of the amide derivative |
| MX2011011394A (es) * | 2009-05-06 | 2011-11-18 | Syngenta Participations Ag | Compuestos insecticidas. |
| NZ601203A (en) * | 2010-01-29 | 2015-01-30 | Mitsui Chemicals Agro Inc | Composition for exterminating animal parasite and method for exterminating animal parasite |
| DE102011005091A1 (de) | 2011-03-04 | 2012-09-06 | Siemens Aktiengesellschaft | Supraleitende Synchronmaschine, umfassend einen gegen einen Stator rotierbaren Rotor mit wenigstens einer supraleitenden Wicklung |
| WO2013150988A1 (ja) | 2012-04-03 | 2013-10-10 | 三井化学アグロ株式会社 | アルキル化芳香族アミド誘導体の製造方法 |
| CN104703966B (zh) * | 2012-10-04 | 2018-01-02 | 三井化学Agro株式会社 | 酰亚胺化合物及其制备方法以及作为杀虫剂的应用 |
| BR112015009475A2 (pt) * | 2012-10-31 | 2017-07-04 | Syngenta Participations Ag | compostos inseticidas |
| CN104736148B (zh) | 2012-11-05 | 2018-01-12 | 三井化学Agro株式会社 | 动物寄生虫驱除用组合物及动物寄生虫的驱除方法 |
| CN102936229A (zh) * | 2012-12-03 | 2013-02-20 | 湖南大学 | 具有杀虫活性的4-叔丁基-5-苄基-2-酰氨基噻唑及制备方法 |
| CN102942536A (zh) * | 2012-12-03 | 2013-02-27 | 湖南大学 | 具有杀虫活性的4-叔丁基-5-(1-芳基-2-硝乙基)-2-酰氨基噻唑及制备方法 |
| US9402395B2 (en) | 2013-04-02 | 2016-08-02 | Syngenta Participations Ag | Insecticidal compounds |
| WO2014161849A1 (en) * | 2013-04-02 | 2014-10-09 | Syngenta Participations Ag | Insecticidal compounds |
| JP6352389B2 (ja) * | 2013-04-02 | 2018-07-04 | シンジェンタ パーティシペーションズ アーゲー | パーハロアルキル基を含有するヒンダードアニリンからのアミドの製造方法 |
| CN103204804B (zh) * | 2013-04-10 | 2015-10-28 | 山东省联合农药工业有限公司 | 一种含双苯的烟碱类化合物及其制备方法和用途 |
| BR112015026357A2 (pt) | 2013-04-19 | 2017-07-25 | Basf Se | compostos, composição agrícola ou veterinária, métodos para o combate ou controle das pragas, para a proteção de vegetais, para a proteção do material de propagação e para o tratamento de animais e utilização de um composto |
| CR20160228A (es) | 2013-10-18 | 2016-12-05 | Basf Agrochemical Products Bv | Mezclas activas como insecticidas que comprenden un compuesto de carboxamida |
| BR112016008555A8 (pt) | 2013-10-18 | 2020-03-10 | Basf Agrochemical Products Bv | usos do composto carboxamida ativo pesticida e método de proteção de material de propagação vegetal |
| JP6644679B2 (ja) | 2013-10-18 | 2020-02-12 | ビーエーエスエフ アグロケミカル プロダクツ ビー.ブイ. | カルボキサミド化合物を含む農業用活性混合物 |
| JP6879740B2 (ja) | 2013-12-13 | 2021-06-02 | ダナ−ファーバー キャンサー インスティテュート, インコーポレイテッド | リンパ形質細胞性リンパ腫を処置する方法 |
| AU2014361800B2 (en) * | 2013-12-13 | 2020-05-07 | Dana-Farber Cancer Institute, Inc. | Methods to treat lymphoplasmacytic lymphoma |
| EP3087053B1 (en) | 2013-12-23 | 2019-11-20 | Syngenta Participations AG | Insecticidal compounds |
| JP6571662B2 (ja) | 2013-12-23 | 2019-09-04 | シンジェンタ パーティシペーションズ アーゲー | 殺虫性化合物 |
| RU2016131792A (ru) | 2014-01-03 | 2018-02-06 | Байер Энимэл Хельс ГмбХ | Новые пиразолил-гетероариламиды в качестве средств для борьбы с вредителями |
| RU2017104717A (ru) | 2014-07-15 | 2018-08-15 | Байер Энимэл Хельс ГмбХ | Арилтриазолилпиридины в качестве средств для борьбы с вредителями |
| WO2016055431A1 (en) | 2014-10-06 | 2016-04-14 | Basf Se | Substituted pyrimidinium compounds for combating animal pests |
| BR112017009513A2 (pt) | 2014-11-06 | 2018-02-06 | Basf Se | utilização de um composto heterobicíclico, utilização dos compostos i, compostos, composição agrícola ou veterinária, método para o combate ou controle de pragas, método para a proteção de culturas e sementes |
| CN105685034A (zh) * | 2014-11-26 | 2016-06-22 | 三井化学Agro株式会社 | 有害生物防除混合组合物 |
| AR102942A1 (es) | 2014-12-11 | 2017-04-05 | Bayer Cropscience Ag | Derivados de arilsulfuro y arilsulfóxido de cinco miembros c-n-conectados, como plaguicidas |
| TW201638076A (zh) * | 2014-12-22 | 2016-11-01 | 拜耳作物科學股份有限公司 | 新穎之異噻唑醯胺類,其製備方法及其作為除草劑及/或植物生長調節劑之用途 |
| TW201632507A (zh) * | 2014-12-22 | 2016-09-16 | 拜耳作物科學股份有限公司 | 新穎之異噻唑醯胺、其製法及其作為殺真菌劑之用途 |
| JP6743032B2 (ja) | 2015-02-06 | 2020-08-19 | ビーエーエスエフ ソシエタス・ヨーロピアBasf Se | 硝化抑制剤としてのピラゾール化合物 |
| ES2820320T3 (es) | 2015-02-11 | 2021-04-20 | Basf Se | Mezcla de pesticidas que comprende un compuesto de pirazol, un insecticida y un fungicida |
| WO2016143652A1 (ja) * | 2015-03-06 | 2016-09-15 | 住友化学株式会社 | 3-アミノオキサリルアミノベンズアミド化合物及びその有害節足動物防除用途 |
| WO2016143650A1 (ja) * | 2015-03-06 | 2016-09-15 | 住友化学株式会社 | 3-アミノオキサリルアミノベンズアミド化合物及びその有害節足動物防除用途 |
| BR112017019208B1 (pt) | 2015-03-11 | 2022-06-21 | Basf Agrochemical Products B.V. | Misturas pesticidas, composição de tratamento de sementes, uso de uma mistura, uso de uma composição de tratamento de sementes e métodos para o controle de pragas invertebradas e de nematoides |
| US11219211B2 (en) | 2015-03-11 | 2022-01-11 | Basf Agrochemical Products B.V. | Pesticidal mixture comprising a carboxamide compound and a biopesticide |
| CA2980505A1 (en) | 2015-04-07 | 2016-10-13 | Basf Agrochemical Products B.V. | Use of an insecticidal carboxamide compound against pests on cultivated plants |
| EP3282844A1 (en) | 2015-04-17 | 2018-02-21 | BASF Agrochemical Products B.V. | Method for controlling non-crop pests |
| NZ734931A (en) | 2015-04-17 | 2019-04-26 | Dow Agrosciences Llc | Molecules having pesticidal utility, and intermediates, compositions, and processes, related thereto |
| EP3294690A1 (en) | 2015-05-12 | 2018-03-21 | Basf Se | Thioether compounds as nitrification inhibitors |
| WO2016198611A1 (en) | 2015-06-11 | 2016-12-15 | Basf Se | N-(thio)acylimino heterocyclic compounds |
| WO2016198613A1 (en) | 2015-06-11 | 2016-12-15 | Basf Se | N-(thio)acylimino compounds |
| AU2016287098A1 (en) | 2015-07-02 | 2018-01-25 | BASF Agro B.V. | Pesticidal compositions comprising a triazole compound |
| WO2017016883A1 (en) | 2015-07-24 | 2017-02-02 | Basf Se | Process for preparation of cyclopentene compounds |
| CN108137537B (zh) | 2015-10-02 | 2021-07-23 | 巴斯夫欧洲公司 | 作为有害物防治剂的具有2-氯嘧啶-5-基取代基的亚氨基化合物 |
| CA3003956A1 (en) | 2015-11-30 | 2017-06-08 | Basf Se | Mixtures of cis-jasmone and bacillus amyloliquefaciens |
| KR20180088412A (ko) * | 2015-12-11 | 2018-08-03 | 데이진 화-마 가부시키가이샤 | 아미노아졸 유도체 |
| ES2881621T3 (es) * | 2015-12-18 | 2021-11-30 | Mitsui Chemicals Agro Inc | Método para producir un derivado de amida aromático |
| WO2017122687A1 (ja) * | 2016-01-12 | 2017-07-20 | 三井化学アグロ株式会社 | 吸血性節足動物防除方法および居住空間形成物処理用吸血性節足動物防除組成物 |
| BR112018015328B1 (pt) | 2016-02-19 | 2022-08-16 | Basf Se | Métodos para o controle de pragas em plantas, método para controlar pragas da família de pentatomidae e/ ou miridae e uso de um ou mais compostos de fórmula i |
| US20190077809A1 (en) | 2016-03-09 | 2019-03-14 | Basf Se | Spirocyclic Derivatives |
| CA3015131A1 (en) | 2016-03-11 | 2017-09-14 | Basf Se | Method for controlling pests of plants |
| PL3436457T3 (pl) | 2016-04-01 | 2022-11-28 | Basf Se | Związki bicykliczne |
| US20190276376A1 (en) | 2016-05-18 | 2019-09-12 | Basf Se | Capsules comprising benzylpropargylethers for use as nitrification inhibitors |
| US20200317690A1 (en) * | 2016-06-02 | 2020-10-08 | Bayer Cropscience Aktiengesellschaft | Novel isothiazolopyridones, processes for their preparation and their use as herbicides and/or plant growth regulators |
| CN109476646A (zh) | 2016-07-12 | 2019-03-15 | 拜耳作物科学股份公司 | 作为害虫防治剂的双环化合物 |
| EP3551616A1 (de) | 2016-12-08 | 2019-10-16 | Bayer CropScience Aktiengesellschaft | Verfahren zur herstellung von 5-(1-phenyl-1h-pyrazol-4-yl)-nicotinamid-derivaten und ähnlicher verbindungen ohne isolierung oder aufreinigung der phenylhydrazin-zwischenstufe |
| CN110291072A (zh) | 2016-12-16 | 2019-09-27 | 巴斯夫欧洲公司 | 农药化合物 |
| WO2018162312A1 (en) | 2017-03-10 | 2018-09-13 | Basf Se | Spirocyclic derivatives |
| WO2018166855A1 (en) | 2017-03-16 | 2018-09-20 | Basf Se | Heterobicyclic substituted dihydroisoxazoles |
| ES2950451T3 (es) | 2017-03-28 | 2023-10-10 | Basf Se | Compuestos plaguicidas |
| AU2018241628B2 (en) | 2017-03-31 | 2022-03-17 | Basf Se | Pyrimidinium compounds and their mixtures for combating animal pests |
| BR112019020206A2 (pt) | 2017-03-31 | 2020-04-22 | Mitsui Chemicals Agro Inc | método para controle de pragas que habitam construções e composição para controle de pragas que habitam construções |
| WO2018192793A1 (en) | 2017-04-20 | 2018-10-25 | Basf Se | Substituted rhodanine derivatives |
| CA3058104A1 (en) | 2017-04-26 | 2018-11-01 | Basf Se | Substituted succinimide derivatives as pesticides |
| RS64364B1 (sr) | 2017-04-27 | 2023-08-31 | Ishihara Sangyo Kaisha | Jedinjenje n-(4-piridil) nikotinamida ili njegova so |
| WO2018206479A1 (en) | 2017-05-10 | 2018-11-15 | Basf Se | Bicyclic pesticidal compounds |
| WO2018224455A1 (en) | 2017-06-07 | 2018-12-13 | Basf Se | Substituted cyclopropyl derivatives |
| WO2018229202A1 (en) | 2017-06-16 | 2018-12-20 | Basf Se | Mesoionic imidazolium compounds and derivatives for combating animal pests |
| US11542280B2 (en) | 2017-06-19 | 2023-01-03 | Basf Se | Substituted pyrimidinium compounds and derivatives for combating animal pests |
| WO2018234488A1 (en) | 2017-06-23 | 2018-12-27 | Basf Se | SUBSTITUTED CYCLOPROPYL DERIVATIVES |
| WO2019042932A1 (en) | 2017-08-31 | 2019-03-07 | Basf Se | METHOD FOR CONTROLLING RICE PARASITES IN RICE |
| EP3453706A1 (en) | 2017-09-08 | 2019-03-13 | Basf Se | Pesticidal imidazole compounds |
| CA3076539A1 (en) * | 2017-09-20 | 2019-03-28 | Mitsui Chemicals Agro, Inc. | Prolonged ectoparasite-controlling agent for animal |
| WO2019072906A1 (en) | 2017-10-13 | 2019-04-18 | Basf Se | IMIDAZOLIDINE PYRIMIDINIUM COMPOUNDS FOR CONTROL OF HARMFUL ANIMALS |
| WO2019121143A1 (en) | 2017-12-20 | 2019-06-27 | Basf Se | Substituted cyclopropyl derivatives |
| CN111491925B (zh) | 2017-12-21 | 2023-12-29 | 巴斯夫欧洲公司 | 杀害虫化合物 |
| BR112020013292A2 (pt) | 2018-01-05 | 2020-12-01 | Basf Se | métodos para controlar pragas de plantas de soja, método para controlar pragas das famílias pentatomidae, agromyzidae, noctuidae, pyralidae, e/ ou thripidae e uso de um ou mais compostos de fórmula i |
| US11414438B2 (en) | 2018-01-09 | 2022-08-16 | Basf Se | Silylethynyl hetaryl compounds as nitrification inhibitors |
| WO2019137995A1 (en) | 2018-01-11 | 2019-07-18 | Basf Se | Novel pyridazine compounds for controlling invertebrate pests |
| WO2019158408A1 (en) * | 2018-02-13 | 2019-08-22 | Basf Agrochemical Products B.V. | Crystalline forms of broflanilide |
| CA3089381A1 (en) | 2018-02-28 | 2019-09-06 | Basf Se | Use of pyrazole propargyl ethers as nitrification inhibitors |
| CA3089374A1 (en) | 2018-02-28 | 2019-09-06 | Basf Se | Use of alkoxypyrazoles as nitrification inhibitors |
| IL276745B2 (en) | 2018-02-28 | 2023-10-01 | Basf Se | Use of N-functional alkoxy pyrazole compounds as nitrification inhibitors |
| WO2019175713A1 (en) | 2018-03-14 | 2019-09-19 | Basf Corporation | New catechol molecules and their use as inhibitors to p450 related metabolic pathways |
| WO2019175712A1 (en) | 2018-03-14 | 2019-09-19 | Basf Corporation | New uses for catechol molecules as inhibitors to glutathione s-transferase metabolic pathways |
| WO2019185413A1 (en) | 2018-03-27 | 2019-10-03 | Basf Se | Pesticidal substituted cyclopropyl derivatives |
| WO2019211106A1 (en) | 2018-04-30 | 2019-11-07 | Basf Se | Control of pests of soybean plants with mesoionic compounds |
| CA3099870C (en) | 2018-05-11 | 2023-03-07 | Shenyang University Of Chemical Technology | Benzamide compound and use thereof |
| WO2019219529A1 (en) | 2018-05-15 | 2019-11-21 | Basf Se | Mixtures comprising benzpyrimoxan and oxazosulfyl and uses and methods of applying them |
| WO2019224092A1 (en) | 2018-05-22 | 2019-11-28 | Basf Se | Pesticidally active c15-derivatives of ginkgolides |
| MX2020012524A (es) | 2018-05-24 | 2021-02-16 | Bayer Ag | Proceso para la preparacion de n-arilpirazoles sustituidos. |
| WO2019224143A1 (de) | 2018-05-24 | 2019-11-28 | Bayer Aktiengesellschaft | Wirkstoffkombinationen mit insektiziden, nematiziden und akariziden eigenschaften |
| CN108586279A (zh) * | 2018-06-26 | 2018-09-28 | 上海泰禾国际贸易有限公司 | 一种间二酰胺类化合物及其制备方法和应用 |
| WO2020002472A1 (en) | 2018-06-28 | 2020-01-02 | Basf Se | Use of alkynylthiophenes as nitrification inhibitors |
| CN112424147B (zh) | 2018-07-23 | 2023-06-30 | 巴斯夫欧洲公司 | 取代噻唑烷化合物作为硝化抑制剂的用途 |
| CA3104256A1 (en) | 2018-07-23 | 2020-01-30 | Basf Se | Use of substituted 2-thiazolines as nitrification inhibitors |
| CN113767908B (zh) * | 2018-08-10 | 2022-11-18 | 南通泰禾化工股份有限公司 | 一种含有间二酰胺类化合物的药物组合物及其应用 |
| CN113767907B (zh) * | 2018-08-10 | 2022-11-29 | 南通泰禾化工股份有限公司 | 一种含有间二酰胺类化合物的药物组合物及其应用 |
| WO2020030092A1 (zh) * | 2018-08-10 | 2020-02-13 | 上海泰禾国际贸易有限公司 | 一种含有间二酰胺类化合物的药物组合物及其应用 |
| WO2020030095A1 (zh) * | 2018-08-10 | 2020-02-13 | 上海泰禾国际贸易有限公司 | 一种含有间二酰胺类化合物的药物组合物及其应用 |
| WO2020030094A1 (zh) * | 2018-08-10 | 2020-02-13 | 上海泰禾国际贸易有限公司 | 一种含有间二酰胺类化合物的药物组合物及其应用 |
| CN110810410B (zh) * | 2018-08-10 | 2022-02-11 | 南通泰禾化工股份有限公司 | 一种含有间二酰胺类化合物的药物组合物及其应用 |
| EP3613736A1 (en) | 2018-08-22 | 2020-02-26 | Basf Se | Substituted glutarimide derivatives |
| EP3628158A1 (en) | 2018-09-28 | 2020-04-01 | Basf Se | Pesticidal mixture comprising a mesoionic compound and a biopesticide |
| US20220046925A1 (en) | 2018-09-28 | 2022-02-17 | Basf Se | Method of controlling pests by seed treatment application of a mesoionic compound or mixture thereof |
| EP3628156A1 (en) | 2018-09-28 | 2020-04-01 | Basf Se | Method for controlling pests of sugarcane, citrus, rapeseed, and potato plants |
| EP3628157A1 (en) | 2018-09-28 | 2020-04-01 | Basf Se | Method of controlling insecticide resistant insects and virus transmission to plants |
| EP3643705A1 (en) | 2018-10-24 | 2020-04-29 | Basf Se | Pesticidal compounds |
| CN113166063A (zh) | 2018-11-28 | 2021-07-23 | 巴斯夫欧洲公司 | 杀害虫化合物 |
| BR112021009395A2 (pt) | 2018-12-18 | 2021-08-10 | Basf Se | compostos de pirimidínio substituídos, compostos de fórmula (i), métodos para proteger culturas, para o combate, controle, prevenção ou proteção, método não terapêutico para o tratamento de animais, semente e usos dos compostos de fórmula (i) |
| MX2021007511A (es) | 2018-12-20 | 2021-08-05 | Bayer Ag | Procedimiento para la preparacion de anilinas sustituidas. |
| EP3696177A1 (en) | 2019-02-12 | 2020-08-19 | Basf Se | Heterocyclic compounds for the control of invertebrate pests |
| EP3769623A1 (en) | 2019-07-22 | 2021-01-27 | Basf Se | Mesoionic imidazolium compounds and derivatives for combating animal pests |
| CN113923987B (zh) | 2019-05-29 | 2024-10-01 | 巴斯夫欧洲公司 | 用于防除动物害虫的介离子咪唑鎓化合物和衍生物 |
| CN112142621A (zh) * | 2019-06-27 | 2020-12-29 | 上海泰禾国际贸易有限公司 | 一种间二酰胺类化合物及其制备方法和应用 |
| EP3766879A1 (en) | 2019-07-19 | 2021-01-20 | Basf Se | Pesticidal pyrazole derivatives |
| US20220220073A1 (en) * | 2019-08-26 | 2022-07-14 | Metisa Biotechnology Co., Ltd | Bisamide compound and application thereof |
| CN112707836B (zh) | 2019-10-25 | 2022-10-14 | 南通泰禾化工股份有限公司 | 一种间二酰胺类化合物的制备方法 |
| CN112707841B (zh) * | 2019-10-25 | 2022-08-23 | 南通泰禾化工股份有限公司 | 一种3-n-环丙甲基-2-氟苯甲酰胺类化合物及其制备方法和应用 |
| CN112707835B (zh) | 2019-10-25 | 2022-10-21 | 长沙嘉桥生物科技有限公司 | 一种间二酰胺类化合物的溴化方法 |
| KR102582639B1 (ko) | 2019-11-13 | 2023-09-22 | 한국화학연구원 | 신규한 아마이드 유도체 및 이를 포함하는 진드기 방제용 조성물 |
| KR102267724B1 (ko) * | 2019-12-23 | 2021-06-23 | 한국화학연구원 | 펜타플루오로설파닐 기를 포함하는 화합물 및 이를 함유하는 살충제 조성물 |
| CN113321595B (zh) * | 2020-02-28 | 2023-12-22 | 南通泰禾化工股份有限公司 | 一种间二酰胺类化合物及其应用 |
| WO2022101502A1 (en) * | 2020-11-16 | 2022-05-19 | Virbac | Tablet comprising modoflaner as an active component |
| AU2022216425A1 (en) | 2021-02-02 | 2023-08-17 | Basf Se | Synergistic action of dcd and alkoxypyrazoles as nitrification inhibitors |
| CN115073300B (zh) * | 2021-03-10 | 2024-04-05 | 江西天宇化工有限公司 | 一种4-(全氟丙烷-2-基)-2-三氟甲基苯胺及其制备方法和应用 |
| WO2022200364A1 (en) | 2021-03-25 | 2022-09-29 | Syngenta Crop Protection Ag | Insect, acarina and nematode pest control |
| US20240268386A1 (en) | 2021-05-14 | 2024-08-15 | Syngenta Crop Protection Ag | Seed treatment compositions |
| JP2024516912A (ja) | 2021-05-14 | 2024-04-17 | シンジェンタ クロップ プロテクション アクチェンゲゼルシャフト | 昆虫、ダニ目及び線虫有害生物の防除 |
| CN117355504A (zh) | 2021-05-21 | 2024-01-05 | 巴斯夫欧洲公司 | 乙炔基吡啶化合物作为硝化抑制剂的用途 |
| EP4341248A1 (en) | 2021-05-21 | 2024-03-27 | Basf Se | Use of an n-functionalized alkoxy pyrazole compound as nitrification inhibitor |
| EP3943483A1 (de) | 2021-05-26 | 2022-01-26 | Bayer AG | Verfahren zur herstellung von substituierten anilinen |
| BR112023027004A2 (pt) | 2021-06-21 | 2024-03-12 | Basf Se | Estrutura de metal-orgânica, uso da estrutura de metal-orgânica, composição para uso na redução da nitrificação, mistura agroquímica e métodos de redução da nitrificação, de tratamento de fertilizante ou composição de fertilizante e de preparação de uma estrutura de metal-orgânica |
| WO2022268813A1 (en) | 2021-06-24 | 2022-12-29 | Syngenta Crop Protection Ag | Insect, acarina and nematode pest control |
| WO2022268815A1 (en) | 2021-06-24 | 2022-12-29 | Syngenta Crop Protection Ag | Insect, acarina and nematode pest control |
| WO2023284645A1 (zh) * | 2021-07-12 | 2023-01-19 | 沈阳化工大学 | 一种酰胺类化合物及其用途 |
| WO2023105064A1 (en) | 2021-12-10 | 2023-06-15 | Syngenta Crop Protection Ag | Insect, acarina and nematode pest control |
| WO2023203038A1 (en) | 2022-04-19 | 2023-10-26 | Syngenta Crop Protection Ag | Insect, acarina and nematode pest control |
| WO2023203066A1 (en) | 2022-04-21 | 2023-10-26 | Basf Se | Synergistic action as nitrification inhibitors of dcd oligomers with alkoxypyrazole and its oligomers |
| CN114805294B (zh) * | 2022-06-01 | 2024-05-31 | 海利尔药业集团股份有限公司 | 一种杂芳基取代的间二酰胺类化合物或其作为农药可接受的盐、组合物及其用途 |
| WO2024028243A1 (en) | 2022-08-02 | 2024-02-08 | Basf Se | Pyrazolo pesticidal compounds |
| CN115304510B (zh) * | 2022-09-13 | 2024-01-02 | 海利尔药业集团股份有限公司 | 一种芳基取代的间二酰胺类化合物或其作为农药可接受的盐、组合物及其用途 |
| CN117466813B (zh) * | 2023-05-30 | 2024-09-06 | 湖南化工研究院有限公司 | 间胺基苯甲酸双酰胺类化合物及其中间体 |
Family Cites Families (23)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| MXPA06001500A (es) * | 2003-08-11 | 2006-05-15 | Wyeth Corp | Compuestos de 3-aril-4-hidroxifuranona y composiciones farmaceuticas y veterinarias que los contienen. |
| CN101684079B (zh) | 2003-08-29 | 2013-04-03 | 三井化学株式会社 | 农园艺用杀虫剂的制备中间体及制备方法 |
| KR100857312B1 (ko) * | 2004-01-28 | 2008-09-05 | 미쓰이 가가쿠 가부시키가이샤 | 아미드 유도체 및 그 제조 방법 및 그의 살충제로서의 사용 방법 |
| JP2006306771A (ja) * | 2005-04-28 | 2006-11-09 | Mitsui Chemicals Inc | 農園芸用殺虫剤 |
| US8067638B2 (en) * | 2005-06-21 | 2011-11-29 | Mitsui Chemicals, Inc. | Amide derivative and insecticide containing the same |
| CN101203485A (zh) * | 2005-06-23 | 2008-06-18 | 三井化学株式会社 | 酰胺衍生物、含有该化合物的杀虫剂及其使用方法 |
| AU2006260237A1 (en) * | 2005-06-23 | 2006-12-28 | Mitsui Chemicals, Inc. | Amide derivative, pesticide containing such compound and use thereof |
| JP4580836B2 (ja) * | 2005-07-25 | 2010-11-17 | 三井化学アグロ株式会社 | 殺虫殺菌組成物 |
| CA2616749C (en) * | 2005-07-27 | 2012-01-03 | Mitsui Chemicals, Inc. | Composition for preventing harmful organisms |
| JP2007031395A (ja) * | 2005-07-29 | 2007-02-08 | Bayer Cropscience Ag | 殺虫性3−アシルアミノベンズアニリド類 |
| WO2007083394A1 (ja) * | 2006-01-19 | 2007-07-26 | Mitsui Chemicals, Inc. | ジアミン誘導体を含む有害生物防除組成物 |
| GB0614691D0 (en) * | 2006-07-24 | 2006-08-30 | Syngenta Participations Ag | Insecticidal compounds |
| IL180149A (en) * | 2006-12-18 | 2012-06-28 | David Eduar Sitbon | Method of advertising by using computer multi-monitor monitors |
| JP2010047480A (ja) * | 2006-12-19 | 2010-03-04 | Mitsui Chemicals Inc | 虫害の予防方法 |
| JP2010047479A (ja) * | 2006-12-19 | 2010-03-04 | Mitsui Chemicals Inc | 有害生物防除組成物 |
| JP2010047478A (ja) * | 2006-12-19 | 2010-03-04 | Mitsui Chemicals Inc | 有害生物防除組成物 |
| JP2010047481A (ja) | 2006-12-19 | 2010-03-04 | Mitsui Chemicals Inc | 虫害の予防方法 |
| HUE027503T2 (en) * | 2006-12-21 | 2016-10-28 | Syngenta Participations Ag | Insecticidal compounds |
| GB0704468D0 (en) * | 2007-03-07 | 2007-04-18 | Syngenta Participations Ag | Insecticidal compounds |
| GB0720320D0 (en) * | 2007-10-17 | 2007-11-28 | Syngenta Participations Ag | Insecticidal compounds |
| EP2072501A1 (en) * | 2007-12-21 | 2009-06-24 | Bayer CropScience AG | Aminobenzamide derivatives as useful agents for controlling animal parasites |
| JP5647893B2 (ja) * | 2008-08-01 | 2015-01-07 | 三井化学アグロ株式会社 | アミド誘導体、該アミド誘導体を含有する有害生物防除剤および有害生物の防除方法 |
| JP2010037311A (ja) * | 2008-08-08 | 2010-02-18 | Bayer Cropscience Ag | 新規殺虫性アシルアミノベンズアミド誘導体 |
-
2009
- 2009-06-30 CN CN200980131076.5A patent/CN102119143B/zh active Active
- 2009-06-30 HU HUE16166952A patent/HUE054543T2/hu unknown
- 2009-06-30 PT PT161669528T patent/PT3081552T/pt unknown
- 2009-06-30 LT LTEP16166952.8T patent/LT3081552T/lt unknown
- 2009-06-30 SI SI200932117T patent/SI3081552T1/sl unknown
- 2009-06-30 EP EP09806610.3A patent/EP2319830B1/en active Active
- 2009-06-30 CN CN201510428193.5A patent/CN105061248A/zh active Pending
- 2009-06-30 AU AU2009280679A patent/AU2009280679B2/en active Active
- 2009-06-30 ES ES16166952T patent/ES2864286T3/es active Active
- 2009-06-30 KR KR1020137012685A patent/KR101403093B1/ko active IP Right Grant
- 2009-06-30 EP EP16166952.8A patent/EP3081552B1/en active Active
- 2009-06-30 BR BRPI0918021-4A patent/BRPI0918021B1/pt active IP Right Grant
- 2009-06-30 DK DK16166952.8T patent/DK3081552T3/da active
- 2009-06-30 PL PL16166952T patent/PL3081552T3/pl unknown
- 2009-06-30 VN VN201100622A patent/VN27368A1/vi unknown
- 2009-06-30 ES ES09806610.3T patent/ES2613053T3/es active Active
- 2009-06-30 WO PCT/JP2009/061914 patent/WO2010018714A1/ja active Application Filing
- 2009-06-30 DK DK09806610.3T patent/DK2319830T3/en active
- 2009-06-30 CA CA2733557A patent/CA2733557C/en active Active
- 2009-06-30 MX MX2011001536A patent/MX2011001536A/es active IP Right Grant
- 2009-06-30 JP JP2010524684A patent/JP5647895B2/ja active Active
- 2009-06-30 KR KR1020117004929A patent/KR101409077B1/ko active IP Right Grant
- 2009-08-13 KR KR20117003644A patent/KR101259709B1/ko active IP Right Grant
- 2009-08-13 RU RU2011106925/04A patent/RU2469025C2/ru active
-
2013
- 2013-08-21 JP JP2013171615A patent/JP5728540B2/ja active Active
-
2015
- 2015-02-17 JP JP2015028230A patent/JP2015091901A/ja active Pending
-
2021
- 2021-05-17 HR HRP20210788TT patent/HRP20210788T1/hr unknown
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2864286T3 (es) | Agente para el control de plagas que contiene un derivado de amida y uso del agente para el control de plagas | |
| JP5648083B2 (ja) | アニリン誘導体 | |
| JP5406192B2 (ja) | アミド誘導体の製造方法 | |
| US20110201687A1 (en) | Amide derivative, pest control agent containing the amide derivative, and use of the amide derivative | |
| JP2011157296A (ja) | 有害生物防除組成物 | |
| JP2011157295A (ja) | 植物種子用虫害防除組成物および虫害の予防方法 | |
| JP2011157294A (ja) | 有害生物防除組成物 | |
| JP2011063549A (ja) | アミド誘導体、および該アミド誘導体を含有する有害生物防除剤 |