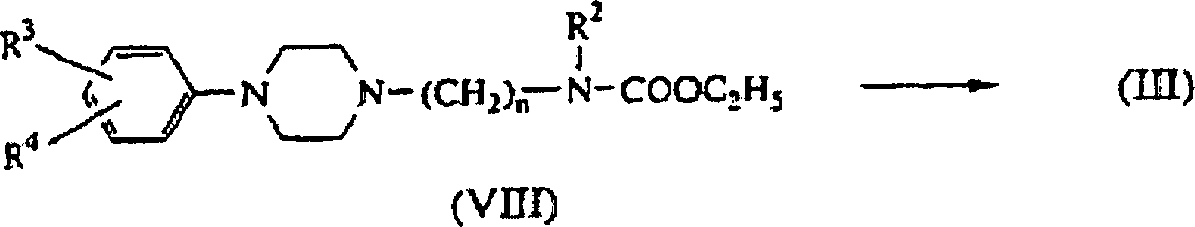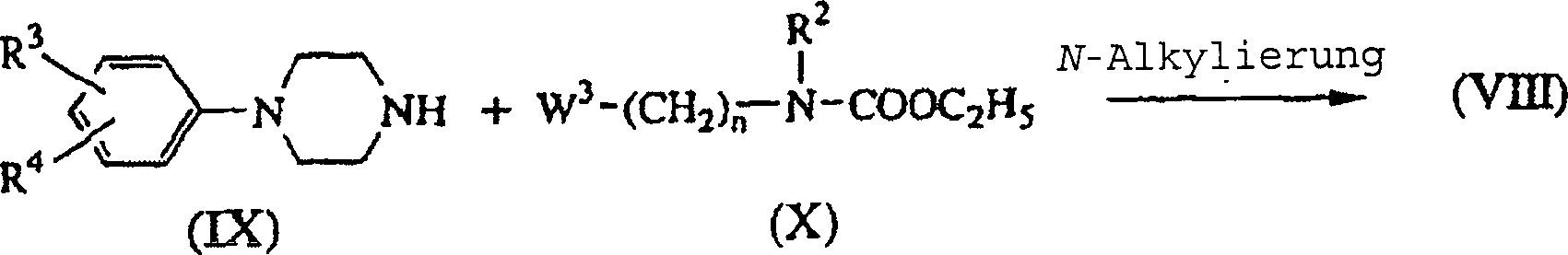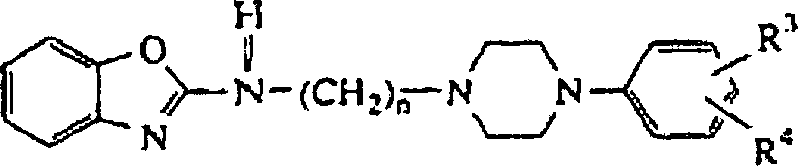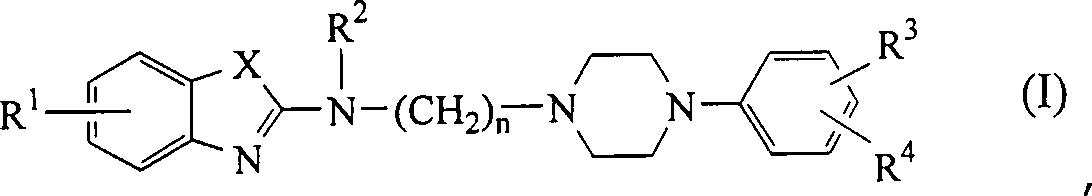DE69737217T2 - Radiomarkierte Alkylamino-benzothiazole und -benzothiazole sowie ihre Verwendung als D4-Liganden - Google Patents
Radiomarkierte Alkylamino-benzothiazole und -benzothiazole sowie ihre Verwendung als D4-Liganden Download PDFInfo
- Publication number
- DE69737217T2 DE69737217T2 DE69737217T DE69737217T DE69737217T2 DE 69737217 T2 DE69737217 T2 DE 69737217T2 DE 69737217 T DE69737217 T DE 69737217T DE 69737217 T DE69737217 T DE 69737217T DE 69737217 T2 DE69737217 T2 DE 69737217T2
- Authority
- DE
- Germany
- Prior art keywords
- formula
- alkyl
- compounds
- hydrogen
- benzothiazolamine
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Lifetime
Links
- IOJUPLGTWVMSFF-UHFFFAOYSA-N benzothiazole Chemical class C1=CC=C2SC=NC2=C1 IOJUPLGTWVMSFF-UHFFFAOYSA-N 0.000 title description 2
- 239000003446 ligand Substances 0.000 title 1
- 150000001875 compounds Chemical class 0.000 claims description 109
- VYFYYTLLBUKUHU-UHFFFAOYSA-N dopamine Chemical compound NCCC1=CC=C(O)C(O)=C1 VYFYYTLLBUKUHU-UHFFFAOYSA-N 0.000 claims description 76
- 229960003638 dopamine Drugs 0.000 claims description 38
- 239000000460 chlorine Substances 0.000 claims description 32
- 125000000217 alkyl group Chemical group 0.000 claims description 28
- 229910052739 hydrogen Inorganic materials 0.000 claims description 23
- 239000001257 hydrogen Substances 0.000 claims description 23
- 238000000034 method Methods 0.000 claims description 21
- 239000002253 acid Substances 0.000 claims description 15
- 150000003839 salts Chemical class 0.000 claims description 15
- 150000002431 hydrogen Chemical class 0.000 claims description 14
- 229910052736 halogen Inorganic materials 0.000 claims description 13
- 150000002367 halogens Chemical class 0.000 claims description 13
- 125000004432 carbon atom Chemical group C* 0.000 claims description 10
- 230000002285 radioactive effect Effects 0.000 claims description 10
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 claims description 9
- 150000001204 N-oxides Chemical group 0.000 claims description 9
- 125000003545 alkoxy group Chemical group 0.000 claims description 7
- 125000004397 aminosulfonyl group Chemical group NS(=O)(=O)* 0.000 claims description 6
- 238000000338 in vitro Methods 0.000 claims description 6
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims description 6
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 claims description 5
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 claims description 5
- 229910052794 bromium Inorganic materials 0.000 claims description 5
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 claims description 4
- YZCKVEUIGOORGS-NJFSPNSNSA-N Tritium Chemical group [3H] YZCKVEUIGOORGS-NJFSPNSNSA-N 0.000 claims description 4
- 239000012620 biological material Substances 0.000 claims description 4
- 239000011737 fluorine Substances 0.000 claims description 4
- 229910052731 fluorine Inorganic materials 0.000 claims description 4
- 238000002372 labelling Methods 0.000 claims description 4
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 claims description 4
- 238000000163 radioactive labelling Methods 0.000 claims description 4
- 229910052722 tritium Inorganic materials 0.000 claims description 4
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 claims description 3
- 125000003236 benzoyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C(*)=O 0.000 claims description 3
- 229910052801 chlorine Inorganic materials 0.000 claims description 3
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 claims description 3
- PNDPGZBMCMUPRI-UHFFFAOYSA-N iodine Chemical compound II PNDPGZBMCMUPRI-UHFFFAOYSA-N 0.000 claims description 3
- 229910052760 oxygen Inorganic materials 0.000 claims description 3
- 229910052717 sulfur Inorganic materials 0.000 claims description 3
- GJLZNEQGOKEFTN-UHFFFAOYSA-N n-[2-(4-phenylpiperazin-1-yl)ethyl]-1,3-benzothiazol-2-amine Chemical compound N=1C2=CC=CC=C2SC=1NCCN(CC1)CCN1C1=CC=CC=C1 GJLZNEQGOKEFTN-UHFFFAOYSA-N 0.000 claims description 2
- KSNPSEKRGHRSPW-UHFFFAOYSA-N n-[2-[4-(4-bromophenyl)piperazin-1-yl]ethyl]-1,3-benzothiazol-2-amine Chemical compound C1=CC(Br)=CC=C1N1CCN(CCNC=2SC3=CC=CC=C3N=2)CC1 KSNPSEKRGHRSPW-UHFFFAOYSA-N 0.000 claims description 2
- 125000001475 halogen functional group Chemical group 0.000 claims 2
- GJSYHSRNGCLVHN-UHFFFAOYSA-N n-[2-[4-(3,4-dichlorophenyl)piperazin-1-yl]ethyl]-1,3-benzothiazol-2-amine Chemical compound C1=C(Cl)C(Cl)=CC=C1N1CCN(CCNC=2SC3=CC=CC=C3N=2)CC1 GJSYHSRNGCLVHN-UHFFFAOYSA-N 0.000 claims 1
- 125000003854 p-chlorophenyl group Chemical group [H]C1=C([H])C(*)=C([H])C([H])=C1Cl 0.000 claims 1
- 239000000203 mixture Substances 0.000 description 51
- 102000005962 receptors Human genes 0.000 description 49
- 108020003175 receptors Proteins 0.000 description 49
- 239000000543 intermediate Substances 0.000 description 48
- 239000002904 solvent Substances 0.000 description 37
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 29
- 239000000243 solution Substances 0.000 description 25
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 22
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 20
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 18
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 16
- 239000003480 eluent Substances 0.000 description 16
- 230000027455 binding Effects 0.000 description 15
- 238000006243 chemical reaction Methods 0.000 description 15
- NLKNQRATVPKPDG-UHFFFAOYSA-M potassium iodide Chemical compound [K+].[I-] NLKNQRATVPKPDG-UHFFFAOYSA-M 0.000 description 15
- 239000011541 reaction mixture Substances 0.000 description 15
- 238000003756 stirring Methods 0.000 description 15
- 239000002244 precipitate Substances 0.000 description 13
- 238000010898 silica gel chromatography Methods 0.000 description 13
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 12
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 12
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 12
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 12
- FYSNRJHAOHDILO-UHFFFAOYSA-N thionyl chloride Chemical compound ClS(Cl)=O FYSNRJHAOHDILO-UHFFFAOYSA-N 0.000 description 12
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 11
- 239000012442 inert solvent Substances 0.000 description 11
- 238000012360 testing method Methods 0.000 description 11
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 11
- 208000035475 disorder Diseases 0.000 description 10
- 230000000694 effects Effects 0.000 description 10
- -1 for example Chemical group 0.000 description 10
- 238000010992 reflux Methods 0.000 description 10
- 239000000706 filtrate Substances 0.000 description 9
- 239000012074 organic phase Substances 0.000 description 8
- 125000005843 halogen group Chemical group 0.000 description 7
- 238000002360 preparation method Methods 0.000 description 7
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 7
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 6
- 238000007126 N-alkylation reaction Methods 0.000 description 6
- KWYUFKZDYYNOTN-UHFFFAOYSA-M Potassium hydroxide Chemical compound [OH-].[K+] KWYUFKZDYYNOTN-UHFFFAOYSA-M 0.000 description 6
- 208000028017 Psychotic disease Diseases 0.000 description 6
- KEAYESYHFKHZAL-UHFFFAOYSA-N Sodium Chemical compound [Na] KEAYESYHFKHZAL-UHFFFAOYSA-N 0.000 description 6
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 6
- 150000007513 acids Chemical class 0.000 description 6
- 230000003042 antagnostic effect Effects 0.000 description 6
- 239000005557 antagonist Substances 0.000 description 6
- 239000002585 base Substances 0.000 description 6
- QZAYGJVTTNCVMB-UHFFFAOYSA-N serotonin Chemical compound C1=C(O)C=C2C(CCN)=CNC2=C1 QZAYGJVTTNCVMB-UHFFFAOYSA-N 0.000 description 6
- 229910000029 sodium carbonate Inorganic materials 0.000 description 6
- 239000012312 sodium hydride Substances 0.000 description 6
- 229910000104 sodium hydride Inorganic materials 0.000 description 6
- 102000015554 Dopamine receptor Human genes 0.000 description 5
- 108050004812 Dopamine receptor Proteins 0.000 description 5
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 5
- 241001465754 Metazoa Species 0.000 description 5
- NTIZESTWPVYFNL-UHFFFAOYSA-N Methyl isobutyl ketone Chemical compound CC(C)CC(C)=O NTIZESTWPVYFNL-UHFFFAOYSA-N 0.000 description 5
- UIHCLUNTQKBZGK-UHFFFAOYSA-N Methyl isobutyl ketone Natural products CCC(C)C(C)=O UIHCLUNTQKBZGK-UHFFFAOYSA-N 0.000 description 5
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 5
- PXFJLKKZSWWVRX-UHFFFAOYSA-N 1-(3,4-dichlorophenyl)piperazine Chemical compound C1=C(Cl)C(Cl)=CC=C1N1CCNCC1 PXFJLKKZSWWVRX-UHFFFAOYSA-N 0.000 description 4
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 4
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 4
- ZAFNJMIOTHYJRJ-UHFFFAOYSA-N Diisopropyl ether Chemical compound CC(C)OC(C)C ZAFNJMIOTHYJRJ-UHFFFAOYSA-N 0.000 description 4
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 4
- 230000000561 anti-psychotic effect Effects 0.000 description 4
- 229910052799 carbon Inorganic materials 0.000 description 4
- 239000003054 catalyst Substances 0.000 description 4
- 230000003197 catalytic effect Effects 0.000 description 4
- JVTAAEKCZFNVCJ-UHFFFAOYSA-N lactic acid Chemical compound CC(O)C(O)=O JVTAAEKCZFNVCJ-UHFFFAOYSA-N 0.000 description 4
- 238000004811 liquid chromatography Methods 0.000 description 4
- LXCFILQKKLGQFO-UHFFFAOYSA-N methylparaben Chemical compound COC(=O)C1=CC=C(O)C=C1 LXCFILQKKLGQFO-UHFFFAOYSA-N 0.000 description 4
- 201000000980 schizophrenia Diseases 0.000 description 4
- HBAQYPYDRFILMT-UHFFFAOYSA-N 8-[3-(1-cyclopropylpyrazol-4-yl)-1H-pyrazolo[4,3-d]pyrimidin-5-yl]-3-methyl-3,8-diazabicyclo[3.2.1]octan-2-one Chemical class C1(CC1)N1N=CC(=C1)C1=NNC2=C1N=C(N=C2)N1C2C(N(CC1CC2)C)=O HBAQYPYDRFILMT-UHFFFAOYSA-N 0.000 description 3
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 3
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 3
- OFOBLEOULBTSOW-UHFFFAOYSA-N Malonic acid Chemical compound OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 description 3
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 3
- 208000019022 Mood disease Diseases 0.000 description 3
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 3
- LRHPLDYGYMQRHN-UHFFFAOYSA-N N-Butanol Chemical compound CCCCO LRHPLDYGYMQRHN-UHFFFAOYSA-N 0.000 description 3
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 3
- FEWJPZIEWOKRBE-UHFFFAOYSA-N Tartaric acid Natural products [H+].[H+].[O-]C(=O)C(O)C(O)C([O-])=O FEWJPZIEWOKRBE-UHFFFAOYSA-N 0.000 description 3
- 239000013543 active substance Substances 0.000 description 3
- 239000000556 agonist Substances 0.000 description 3
- 239000000164 antipsychotic agent Substances 0.000 description 3
- 229940005529 antipsychotics Drugs 0.000 description 3
- 238000009835 boiling Methods 0.000 description 3
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 3
- 239000012458 free base Substances 0.000 description 3
- 238000010438 heat treatment Methods 0.000 description 3
- 238000003384 imaging method Methods 0.000 description 3
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 3
- 150000002825 nitriles Chemical class 0.000 description 3
- 210000000056 organ Anatomy 0.000 description 3
- 150000002978 peroxides Chemical class 0.000 description 3
- 230000000144 pharmacologic effect Effects 0.000 description 3
- 150000004885 piperazines Chemical class 0.000 description 3
- 230000002265 prevention Effects 0.000 description 3
- QELSKZZBTMNZEB-UHFFFAOYSA-N propylparaben Chemical compound CCCOC(=O)C1=CC=C(O)C=C1 QELSKZZBTMNZEB-UHFFFAOYSA-N 0.000 description 3
- 239000000376 reactant Substances 0.000 description 3
- 239000007858 starting material Substances 0.000 description 3
- 239000000126 substance Substances 0.000 description 3
- 238000006467 substitution reaction Methods 0.000 description 3
- 150000000183 1,3-benzoxazoles Chemical class 0.000 description 2
- IBYHHJPAARCAIE-UHFFFAOYSA-N 1-bromo-2-chloroethane Chemical compound ClCCBr IBYHHJPAARCAIE-UHFFFAOYSA-N 0.000 description 2
- BSQLQMLFTHJVKS-UHFFFAOYSA-N 2-chloro-1,3-benzothiazole Chemical compound C1=CC=C2SC(Cl)=NC2=C1 BSQLQMLFTHJVKS-UHFFFAOYSA-N 0.000 description 2
- ZNQVEEAIQZEUHB-UHFFFAOYSA-N 2-ethoxyethanol Chemical compound CCOCCO ZNQVEEAIQZEUHB-UHFFFAOYSA-N 0.000 description 2
- 229940093475 2-ethoxyethanol Drugs 0.000 description 2
- VIQFVCWBQRWTSO-UHFFFAOYSA-N 3-[4-(3,4-dichlorophenyl)piperazin-1-yl]propan-1-amine Chemical compound C1CN(CCCN)CCN1C1=CC=C(Cl)C(Cl)=C1 VIQFVCWBQRWTSO-UHFFFAOYSA-N 0.000 description 2
- RKFLCDRQGFRNHE-UHFFFAOYSA-N 4-[4-(3,4-dichlorophenyl)piperazin-1-yl]butan-1-amine Chemical compound C1CN(CCCCN)CCN1C1=CC=C(Cl)C(Cl)=C1 RKFLCDRQGFRNHE-UHFFFAOYSA-N 0.000 description 2
- 102000040125 5-hydroxytryptamine receptor family Human genes 0.000 description 2
- 108091032151 5-hydroxytryptamine receptor family Proteins 0.000 description 2
- NLHHRLWOUZZQLW-UHFFFAOYSA-N Acrylonitrile Chemical compound C=CC#N NLHHRLWOUZZQLW-UHFFFAOYSA-N 0.000 description 2
- 108060003345 Adrenergic Receptor Proteins 0.000 description 2
- 102000017910 Adrenergic receptor Human genes 0.000 description 2
- VHUUQVKOLVNVRT-UHFFFAOYSA-N Ammonium hydroxide Chemical compound [NH4+].[OH-] VHUUQVKOLVNVRT-UHFFFAOYSA-N 0.000 description 2
- 208000019901 Anxiety disease Diseases 0.000 description 2
- 108010009685 Cholinergic Receptors Proteins 0.000 description 2
- AEMRFAOFKBGASW-UHFFFAOYSA-N Glycolic acid Chemical compound OCC(O)=O AEMRFAOFKBGASW-UHFFFAOYSA-N 0.000 description 2
- 102000000543 Histamine Receptors Human genes 0.000 description 2
- 108010002059 Histamine Receptors Proteins 0.000 description 2
- 241000282412 Homo Species 0.000 description 2
- MHAJPDPJQMAIIY-UHFFFAOYSA-N Hydrogen peroxide Chemical compound OO MHAJPDPJQMAIIY-UHFFFAOYSA-N 0.000 description 2
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 2
- 208000026139 Memory disease Diseases 0.000 description 2
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 2
- FXHOOIRPVKKKFG-UHFFFAOYSA-N N,N-Dimethylacetamide Chemical compound CN(C)C(C)=O FXHOOIRPVKKKFG-UHFFFAOYSA-N 0.000 description 2
- KFSLWBXXFJQRDL-UHFFFAOYSA-N Peracetic acid Chemical compound CC(=O)OO KFSLWBXXFJQRDL-UHFFFAOYSA-N 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- LCTONWCANYUPML-UHFFFAOYSA-N Pyruvic acid Chemical compound CC(=O)C(O)=O LCTONWCANYUPML-UHFFFAOYSA-N 0.000 description 2
- 239000007868 Raney catalyst Substances 0.000 description 2
- NPXOKRUENSOPAO-UHFFFAOYSA-N Raney nickel Chemical compound [Al].[Ni] NPXOKRUENSOPAO-UHFFFAOYSA-N 0.000 description 2
- 229910000564 Raney nickel Inorganic materials 0.000 description 2
- 241000700159 Rattus Species 0.000 description 2
- DBMJMQXJHONAFJ-UHFFFAOYSA-M Sodium laurylsulphate Chemical compound [Na+].CCCCCCCCCCCCOS([O-])(=O)=O DBMJMQXJHONAFJ-UHFFFAOYSA-M 0.000 description 2
- 229920002472 Starch Polymers 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- 206010047700 Vomiting Diseases 0.000 description 2
- 102000034337 acetylcholine receptors Human genes 0.000 description 2
- 230000004913 activation Effects 0.000 description 2
- QGZKDVFQNNGYKY-UHFFFAOYSA-N ammonia Natural products N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 2
- 230000008485 antagonism Effects 0.000 description 2
- 230000002932 anti-schizophrenic effect Effects 0.000 description 2
- 230000036506 anxiety Effects 0.000 description 2
- 230000003542 behavioural effect Effects 0.000 description 2
- 230000009286 beneficial effect Effects 0.000 description 2
- 230000033228 biological regulation Effects 0.000 description 2
- 230000037396 body weight Effects 0.000 description 2
- 239000007795 chemical reaction product Substances 0.000 description 2
- 239000003153 chemical reaction reagent Substances 0.000 description 2
- 125000001309 chloro group Chemical group Cl* 0.000 description 2
- 238000004587 chromatography analysis Methods 0.000 description 2
- 239000011248 coating agent Substances 0.000 description 2
- 238000000576 coating method Methods 0.000 description 2
- XBDQKXXYIPTUBI-UHFFFAOYSA-N dimethylselenoniopropionate Natural products CCC(O)=O XBDQKXXYIPTUBI-UHFFFAOYSA-N 0.000 description 2
- 238000009826 distribution Methods 0.000 description 2
- 229940079593 drug Drugs 0.000 description 2
- 239000003814 drug Substances 0.000 description 2
- 239000006274 endogenous ligand Substances 0.000 description 2
- 238000002474 experimental method Methods 0.000 description 2
- 235000011187 glycerol Nutrition 0.000 description 2
- 230000003993 interaction Effects 0.000 description 2
- 239000004310 lactic acid Substances 0.000 description 2
- 235000014655 lactic acid Nutrition 0.000 description 2
- 239000008101 lactose Substances 0.000 description 2
- XKBGEWXEAPTVCK-UHFFFAOYSA-M methyltrioctylammonium chloride Chemical compound [Cl-].CCCCCCCC[N+](C)(CCCCCCCC)CCCCCCCC XKBGEWXEAPTVCK-UHFFFAOYSA-M 0.000 description 2
- WYBLHBUNVWAKQH-UHFFFAOYSA-N n-[2-[4-(4-chlorophenyl)piperazin-1-yl]ethyl]-6-fluoro-1,3-benzothiazol-2-amine Chemical compound S1C2=CC(F)=CC=C2N=C1NCCN(CC1)CCN1C1=CC=C(Cl)C=C1 WYBLHBUNVWAKQH-UHFFFAOYSA-N 0.000 description 2
- LUABFORHKKFGEL-UHFFFAOYSA-N n-[4-[4-(3,4-dichlorophenyl)piperazin-1-yl]butyl]-6-methyl-1,3-benzothiazol-2-amine Chemical compound S1C2=CC(C)=CC=C2N=C1NCCCCN(CC1)CCN1C1=CC=C(Cl)C(Cl)=C1 LUABFORHKKFGEL-UHFFFAOYSA-N 0.000 description 2
- QDTDFSFRIDFTCF-UHFFFAOYSA-N n-phenyl-1,3-benzothiazol-2-amine Chemical compound N=1C2=CC=CC=C2SC=1NC1=CC=CC=C1 QDTDFSFRIDFTCF-UHFFFAOYSA-N 0.000 description 2
- 230000000955 neuroendocrine Effects 0.000 description 2
- 229910052757 nitrogen Inorganic materials 0.000 description 2
- 239000012044 organic layer Substances 0.000 description 2
- 239000012071 phase Substances 0.000 description 2
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 2
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 2
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 2
- XXQBEVHPUKOQEO-UHFFFAOYSA-N potassium superoxide Chemical compound [K+].[K+].[O-][O-] XXQBEVHPUKOQEO-UHFFFAOYSA-N 0.000 description 2
- YGSDEFSMJLZEOE-UHFFFAOYSA-N salicylic acid Chemical compound OC(=O)C1=CC=CC=C1O YGSDEFSMJLZEOE-UHFFFAOYSA-N 0.000 description 2
- 238000010956 selective crystallization Methods 0.000 description 2
- 239000000741 silica gel Substances 0.000 description 2
- 229910002027 silica gel Inorganic materials 0.000 description 2
- 238000002603 single-photon emission computed tomography Methods 0.000 description 2
- 208000019116 sleep disease Diseases 0.000 description 2
- 235000019333 sodium laurylsulphate Nutrition 0.000 description 2
- 239000012453 solvate Substances 0.000 description 2
- 239000008107 starch Substances 0.000 description 2
- 235000019698 starch Nutrition 0.000 description 2
- 208000024891 symptom Diseases 0.000 description 2
- CIHOLLKRGTVIJN-UHFFFAOYSA-N tert‐butyl hydroperoxide Chemical compound CC(C)(C)OO CIHOLLKRGTVIJN-UHFFFAOYSA-N 0.000 description 2
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 2
- 230000009466 transformation Effects 0.000 description 2
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 description 2
- 230000008673 vomiting Effects 0.000 description 2
- 239000008215 water for injection Substances 0.000 description 2
- UDQTXCHQKHIQMH-KYGLGHNPSA-N (3ar,5s,6s,7r,7ar)-5-(difluoromethyl)-2-(ethylamino)-5,6,7,7a-tetrahydro-3ah-pyrano[3,2-d][1,3]thiazole-6,7-diol Chemical compound S1C(NCC)=N[C@H]2[C@@H]1O[C@H](C(F)F)[C@@H](O)[C@@H]2O UDQTXCHQKHIQMH-KYGLGHNPSA-N 0.000 description 1
- 125000004169 (C1-C6) alkyl group Chemical group 0.000 description 1
- BJEPYKJPYRNKOW-REOHCLBHSA-N (S)-malic acid Chemical compound OC(=O)[C@@H](O)CC(O)=O BJEPYKJPYRNKOW-REOHCLBHSA-N 0.000 description 1
- LGIYMTHBRYKVSV-WLHGVMLRSA-N (e)-but-2-enedioic acid;n-[5-[4-(3,4-dichlorophenyl)piperazin-1-yl]pentyl]-1,3-benzothiazol-2-amine Chemical compound OC(=O)\C=C\C(O)=O.C1=C(Cl)C(Cl)=CC=C1N1CCN(CCCCCNC=2SC3=CC=CC=C3N=2)CC1 LGIYMTHBRYKVSV-WLHGVMLRSA-N 0.000 description 1
- BZTNECSSZCOPQS-UHFFFAOYSA-N 1-(2-chloroethyl)-4-(3,4-dichlorophenyl)piperazine Chemical compound C1CN(CCCl)CCN1C1=CC=C(Cl)C(Cl)=C1 BZTNECSSZCOPQS-UHFFFAOYSA-N 0.000 description 1
- PJHPFAFEJNBIDC-UHFFFAOYSA-N 1-(4-bromophenyl)piperazine Chemical compound C1=CC(Br)=CC=C1N1CCNCC1 PJHPFAFEJNBIDC-UHFFFAOYSA-N 0.000 description 1
- FBQMUBZPJRHSST-UHFFFAOYSA-N 1-(4-phenylpiperazin-1-yl)propan-1-amine Chemical compound C1(=CC=CC=C1)N1CCN(CC1)C(CC)N FBQMUBZPJRHSST-UHFFFAOYSA-N 0.000 description 1
- NCMNOXVMCMQZAE-UHFFFAOYSA-N 1-[2-[4-(3,4-dichlorophenyl)piperazin-1-yl]ethyl]-3-(4-methylphenyl)thiourea Chemical compound C1=CC(C)=CC=C1NC(=S)NCCN1CCN(C=2C=C(Cl)C(Cl)=CC=2)CC1 NCMNOXVMCMQZAE-UHFFFAOYSA-N 0.000 description 1
- NIDSRGCVYOEDFW-UHFFFAOYSA-N 1-bromo-4-chlorobutane Chemical compound ClCCCCBr NIDSRGCVYOEDFW-UHFFFAOYSA-N 0.000 description 1
- QKAOOWJWWKWWOZ-UHFFFAOYSA-N 1-isothiocyanato-2-methoxybenzene Chemical compound COC1=CC=CC=C1N=C=S QKAOOWJWWKWWOZ-UHFFFAOYSA-N 0.000 description 1
- VRPQCVLBOZOYCG-UHFFFAOYSA-N 1-isothiocyanato-4-methoxybenzene Chemical compound COC1=CC=C(N=C=S)C=C1 VRPQCVLBOZOYCG-UHFFFAOYSA-N 0.000 description 1
- ABQKHKWXTUVKGF-UHFFFAOYSA-N 1-isothiocyanato-4-methylbenzene Chemical compound CC1=CC=C(N=C=S)C=C1 ABQKHKWXTUVKGF-UHFFFAOYSA-N 0.000 description 1
- MBPUXARSVLMTGQ-UHFFFAOYSA-N 2-(4-naphthalen-1-ylpiperazin-1-yl)ethanamine Chemical compound C1CN(CCN)CCN1C1=CC=CC2=CC=CC=C12 MBPUXARSVLMTGQ-UHFFFAOYSA-N 0.000 description 1
- ZWEHNKRNPOVVGH-UHFFFAOYSA-N 2-Butanone Chemical compound CCC(C)=O ZWEHNKRNPOVVGH-UHFFFAOYSA-N 0.000 description 1
- FRQMJZZUNJTQCS-UHFFFAOYSA-N 2-[4-(3,4-dichlorophenyl)piperazin-1-yl]ethanamine Chemical compound C1CN(CCN)CCN1C1=CC=C(Cl)C(Cl)=C1 FRQMJZZUNJTQCS-UHFFFAOYSA-N 0.000 description 1
- IVYCDABPAPCTDJ-UHFFFAOYSA-N 2-[4-(4-bromophenyl)piperazin-1-yl]ethanamine Chemical compound C1CN(CCN)CCN1C1=CC=C(Br)C=C1 IVYCDABPAPCTDJ-UHFFFAOYSA-N 0.000 description 1
- UHIQVPRCDRTUKV-UHFFFAOYSA-N 2-[4-(4-chlorophenyl)piperazin-1-yl]ethanamine Chemical compound C1CN(CCN)CCN1C1=CC=C(Cl)C=C1 UHIQVPRCDRTUKV-UHFFFAOYSA-N 0.000 description 1
- YPAYFPSBDMSGPN-UHFFFAOYSA-N 2-[4-(4-iodophenyl)piperazin-1-yl]ethanamine Chemical compound C1CN(CCN)CCN1C1=CC=C(I)C=C1 YPAYFPSBDMSGPN-UHFFFAOYSA-N 0.000 description 1
- YSUIQYOGTINQIN-UZFYAQMZSA-N 2-amino-9-[(1S,6R,8R,9S,10R,15R,17R,18R)-8-(6-aminopurin-9-yl)-9,18-difluoro-3,12-dihydroxy-3,12-bis(sulfanylidene)-2,4,7,11,13,16-hexaoxa-3lambda5,12lambda5-diphosphatricyclo[13.2.1.06,10]octadecan-17-yl]-1H-purin-6-one Chemical compound NC1=NC2=C(N=CN2[C@@H]2O[C@@H]3COP(S)(=O)O[C@@H]4[C@@H](COP(S)(=O)O[C@@H]2[C@@H]3F)O[C@H]([C@H]4F)N2C=NC3=C2N=CN=C3N)C(=O)N1 YSUIQYOGTINQIN-UZFYAQMZSA-N 0.000 description 1
- TVTJUIAKQFIXCE-HUKYDQBMSA-N 2-amino-9-[(2R,3S,4S,5R)-4-fluoro-3-hydroxy-5-(hydroxymethyl)oxolan-2-yl]-7-prop-2-ynyl-1H-purine-6,8-dione Chemical compound NC=1NC(C=2N(C(N(C=2N=1)[C@@H]1O[C@@H]([C@H]([C@H]1O)F)CO)=O)CC#C)=O TVTJUIAKQFIXCE-HUKYDQBMSA-N 0.000 description 1
- FVUFTABOJFRHSU-UHFFFAOYSA-N 2-chloro-6-methoxy-1,3-benzothiazole Chemical compound COC1=CC=C2N=C(Cl)SC2=C1 FVUFTABOJFRHSU-UHFFFAOYSA-N 0.000 description 1
- 125000004493 2-methylbut-1-yl group Chemical group CC(C*)CC 0.000 description 1
- 125000005916 2-methylpentyl group Chemical group 0.000 description 1
- PGNZHTWRCXOGQQ-UHFFFAOYSA-N 3-(4-naphthalen-1-ylpiperazin-1-yl)propan-1-amine Chemical compound C1CN(CCCN)CCN1C1=CC=CC2=CC=CC=C12 PGNZHTWRCXOGQQ-UHFFFAOYSA-N 0.000 description 1
- YNJSNEKCXVFDKW-UHFFFAOYSA-N 3-(5-amino-1h-indol-3-yl)-2-azaniumylpropanoate Chemical compound C1=C(N)C=C2C(CC(N)C(O)=O)=CNC2=C1 YNJSNEKCXVFDKW-UHFFFAOYSA-N 0.000 description 1
- VBIRKPRVXHHCPJ-UHFFFAOYSA-N 3-[4-(3,4-dichlorophenyl)piperazin-1-yl]propanenitrile Chemical compound C1=C(Cl)C(Cl)=CC=C1N1CCN(CCC#N)CC1 VBIRKPRVXHHCPJ-UHFFFAOYSA-N 0.000 description 1
- BTWFACODYSMZPB-UHFFFAOYSA-N 3-[4-(4-bromophenyl)piperazin-1-yl]propan-1-amine Chemical compound C1CN(CCCN)CCN1C1=CC=C(Br)C=C1 BTWFACODYSMZPB-UHFFFAOYSA-N 0.000 description 1
- BMYNFMYTOJXKLE-UHFFFAOYSA-N 3-azaniumyl-2-hydroxypropanoate Chemical compound NCC(O)C(O)=O BMYNFMYTOJXKLE-UHFFFAOYSA-N 0.000 description 1
- NHQDETIJWKXCTC-UHFFFAOYSA-N 3-chloroperbenzoic acid Chemical compound OOC(=O)C1=CC=CC(Cl)=C1 NHQDETIJWKXCTC-UHFFFAOYSA-N 0.000 description 1
- ODMVPIBDMHLJIT-UHFFFAOYSA-N 4-[4-(2,4-dimethylphenyl)piperazin-1-yl]butan-1-amine Chemical compound CC1=CC(C)=CC=C1N1CCN(CCCCN)CC1 ODMVPIBDMHLJIT-UHFFFAOYSA-N 0.000 description 1
- FJPMHRVWHIDPMQ-UHFFFAOYSA-N 4-[4-(4-bromophenyl)piperazin-1-yl]butan-1-amine Chemical compound C1CN(CCCCN)CCN1C1=CC=C(Br)C=C1 FJPMHRVWHIDPMQ-UHFFFAOYSA-N 0.000 description 1
- MPMKMQHJHDHPBE-RUZDIDTESA-N 4-[[(2r)-1-(1-benzothiophene-3-carbonyl)-2-methylazetidine-2-carbonyl]-[(3-chlorophenyl)methyl]amino]butanoic acid Chemical compound O=C([C@@]1(N(CC1)C(=O)C=1C2=CC=CC=C2SC=1)C)N(CCCC(O)=O)CC1=CC=CC(Cl)=C1 MPMKMQHJHDHPBE-RUZDIDTESA-N 0.000 description 1
- QCQCHGYLTSGIGX-GHXANHINSA-N 4-[[(3ar,5ar,5br,7ar,9s,11ar,11br,13as)-5a,5b,8,8,11a-pentamethyl-3a-[(5-methylpyridine-3-carbonyl)amino]-2-oxo-1-propan-2-yl-4,5,6,7,7a,9,10,11,11b,12,13,13a-dodecahydro-3h-cyclopenta[a]chrysen-9-yl]oxy]-2,2-dimethyl-4-oxobutanoic acid Chemical compound N([C@@]12CC[C@@]3(C)[C@]4(C)CC[C@H]5C(C)(C)[C@@H](OC(=O)CC(C)(C)C(O)=O)CC[C@]5(C)[C@H]4CC[C@@H]3C1=C(C(C2)=O)C(C)C)C(=O)C1=CN=CC(C)=C1 QCQCHGYLTSGIGX-GHXANHINSA-N 0.000 description 1
- WUBBRNOQWQTFEX-UHFFFAOYSA-N 4-aminosalicylic acid Chemical compound NC1=CC=C(C(O)=O)C(O)=C1 WUBBRNOQWQTFEX-UHFFFAOYSA-N 0.000 description 1
- 125000004800 4-bromophenyl group Chemical group [H]C1=C([H])C(*)=C([H])C([H])=C1Br 0.000 description 1
- YJWYECKPBYKZSI-UHFFFAOYSA-N 5-(4-naphthalen-1-ylpiperazin-1-yl)pentan-1-amine Chemical compound C1CN(CCCCCN)CCN1C1=CC=CC2=CC=CC=C12 YJWYECKPBYKZSI-UHFFFAOYSA-N 0.000 description 1
- IUJAXFLKTQXMHJ-UHFFFAOYSA-N 5-(methylamino)pentan-1-ol Chemical compound CNCCCCCO IUJAXFLKTQXMHJ-UHFFFAOYSA-N 0.000 description 1
- ZVPAPDJVNWGOGH-UHFFFAOYSA-N 5-[1,3-benzothiazol-2-yl(methyl)amino]pentan-1-ol Chemical compound C1=CC=C2SC(N(CCCCCO)C)=NC2=C1 ZVPAPDJVNWGOGH-UHFFFAOYSA-N 0.000 description 1
- ZTAWOYNDMPXVCF-UHFFFAOYSA-N 5-[4-(2,4-dimethylphenyl)piperazin-1-yl]pentan-1-amine Chemical compound CC1=CC(C)=CC=C1N1CCN(CCCCCN)CC1 ZTAWOYNDMPXVCF-UHFFFAOYSA-N 0.000 description 1
- XZVPQKGPUSWLOS-UHFFFAOYSA-N 5-[4-(3,4-dichlorophenyl)piperazin-1-yl]pentan-1-amine Chemical compound C1CN(CCCCCN)CCN1C1=CC=C(Cl)C(Cl)=C1 XZVPQKGPUSWLOS-UHFFFAOYSA-N 0.000 description 1
- KHBBGXOQJPBHHI-UHFFFAOYSA-N 5-[4-(3,4-dichlorophenyl)piperazin-1-yl]pentanenitrile Chemical compound C1=C(Cl)C(Cl)=CC=C1N1CCN(CCCCC#N)CC1 KHBBGXOQJPBHHI-UHFFFAOYSA-N 0.000 description 1
- JSAWFGSXRPCFSW-UHFFFAOYSA-N 5-chloropentanenitrile Chemical compound ClCCCCC#N JSAWFGSXRPCFSW-UHFFFAOYSA-N 0.000 description 1
- IJRKLHTZAIFUTB-UHFFFAOYSA-N 5-nitro-2-(2-phenylethylamino)benzoic acid Chemical compound OC(=O)C1=CC([N+]([O-])=O)=CC=C1NCCC1=CC=CC=C1 IJRKLHTZAIFUTB-UHFFFAOYSA-N 0.000 description 1
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 1
- 208000017194 Affective disease Diseases 0.000 description 1
- 208000007848 Alcoholism Diseases 0.000 description 1
- 208000035143 Bacterial infection Diseases 0.000 description 1
- 208000020925 Bipolar disease Diseases 0.000 description 1
- 208000027796 Blood pressure disease Diseases 0.000 description 1
- UYDMJSVBZLNEPI-WLHGVMLRSA-N C(\C=C\C(=O)O)(=O)O.ClC1=CC=C(C=C1)N1CCN(CC1)CCNC=1SC2=C(N1)C=CC=C2 Chemical compound C(\C=C\C(=O)O)(=O)O.ClC1=CC=C(C=C1)N1CCN(CC1)CCNC=1SC2=C(N1)C=CC=C2 UYDMJSVBZLNEPI-WLHGVMLRSA-N 0.000 description 1
- UHNRLQRZRNKOKU-UHFFFAOYSA-N CCN(CC1=NC2=C(N1)C1=CC=C(C=C1N=C2N)C1=NNC=C1)C(C)=O Chemical compound CCN(CC1=NC2=C(N1)C1=CC=C(C=C1N=C2N)C1=NNC=C1)C(C)=O UHNRLQRZRNKOKU-UHFFFAOYSA-N 0.000 description 1
- PCBZRNYXXCIELG-WYFCWLEVSA-N COC1=CC=C(C[C@H](NC(=O)OC2CCCC3(C2)OOC2(O3)C3CC4CC(C3)CC2C4)C(=O)N[C@@H]2[C@@H](CO)O[C@H]([C@@H]2O)N2C=NC3=C2N=CN=C3N(C)C)C=C1 Chemical compound COC1=CC=C(C[C@H](NC(=O)OC2CCCC3(C2)OOC2(O3)C3CC4CC(C3)CC2C4)C(=O)N[C@@H]2[C@@H](CO)O[C@H]([C@@H]2O)N2C=NC3=C2N=CN=C3N(C)C)C=C1 PCBZRNYXXCIELG-WYFCWLEVSA-N 0.000 description 1
- PKMUHQIDVVOXHQ-HXUWFJFHSA-N C[C@H](C1=CC(C2=CC=C(CNC3CCCC3)S2)=CC=C1)NC(C1=C(C)C=CC(NC2CNC2)=C1)=O Chemical compound C[C@H](C1=CC(C2=CC=C(CNC3CCCC3)S2)=CC=C1)NC(C1=C(C)C=CC(NC2CNC2)=C1)=O PKMUHQIDVVOXHQ-HXUWFJFHSA-N 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- 206010007559 Cardiac failure congestive Diseases 0.000 description 1
- 241000699802 Cricetulus griseus Species 0.000 description 1
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 1
- 206010012289 Dementia Diseases 0.000 description 1
- 206010012335 Dependence Diseases 0.000 description 1
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 1
- 208000014094 Dystonic disease Diseases 0.000 description 1
- 239000001856 Ethyl cellulose Substances 0.000 description 1
- ZZSNKZQZMQGXPY-UHFFFAOYSA-N Ethyl cellulose Chemical compound CCOCC1OC(OC)C(OCC)C(OCC)C1OC1C(O)C(O)C(OC)C(CO)O1 ZZSNKZQZMQGXPY-UHFFFAOYSA-N 0.000 description 1
- 230000005526 G1 to G0 transition Effects 0.000 description 1
- 208000018522 Gastrointestinal disease Diseases 0.000 description 1
- 201000004311 Gilles de la Tourette syndrome Diseases 0.000 description 1
- 206010019280 Heart failures Diseases 0.000 description 1
- 206010020651 Hyperkinesia Diseases 0.000 description 1
- 206010020751 Hypersensitivity Diseases 0.000 description 1
- 206010020772 Hypertension Diseases 0.000 description 1
- 208000028482 Hypothalamic disease Diseases 0.000 description 1
- 208000025282 Hypothalamo-pituitary disease Diseases 0.000 description 1
- 206010061218 Inflammation Diseases 0.000 description 1
- WTDRDQBEARUVNC-LURJTMIESA-N L-DOPA Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C(O)=C1 WTDRDQBEARUVNC-LURJTMIESA-N 0.000 description 1
- 206010026749 Mania Diseases 0.000 description 1
- 201000009906 Meningitis Diseases 0.000 description 1
- 229920000168 Microcrystalline cellulose Polymers 0.000 description 1
- 208000016285 Movement disease Diseases 0.000 description 1
- WNYVQRNJILIIJI-UHFFFAOYSA-N N-[2-[4-(3,4-dichlorophenyl)piperazin-1-yl]ethyl]-N-phenyl-1,3-benzothiazol-2-amine Chemical compound C1=C(Cl)C(Cl)=CC=C1N1CCN(CCN(C=2SC3=CC=CC=C3N=2)C=2C=CC=CC=2)CC1 WNYVQRNJILIIJI-UHFFFAOYSA-N 0.000 description 1
- 201000005625 Neuroleptic malignant syndrome Diseases 0.000 description 1
- GRYLNZFGIOXLOG-UHFFFAOYSA-N Nitric acid Chemical compound O[N+]([O-])=O GRYLNZFGIOXLOG-UHFFFAOYSA-N 0.000 description 1
- 208000008589 Obesity Diseases 0.000 description 1
- 208000018737 Parkinson disease Diseases 0.000 description 1
- 208000014993 Pituitary disease Diseases 0.000 description 1
- 239000002202 Polyethylene glycol Substances 0.000 description 1
- 241000288906 Primates Species 0.000 description 1
- 235000002357 Ribes grossularia Nutrition 0.000 description 1
- 244000171263 Ribes grossularia Species 0.000 description 1
- 241000283984 Rodentia Species 0.000 description 1
- 240000007651 Rubus glaucus Species 0.000 description 1
- 235000011034 Rubus glaucus Nutrition 0.000 description 1
- 235000009122 Rubus idaeus Nutrition 0.000 description 1
- KDYFGRWQOYBRFD-UHFFFAOYSA-N Succinic acid Natural products OC(=O)CCC(O)=O KDYFGRWQOYBRFD-UHFFFAOYSA-N 0.000 description 1
- 208000000323 Tourette Syndrome Diseases 0.000 description 1
- 208000016620 Tourette disease Diseases 0.000 description 1
- WHMZVJVROTUDFM-UHFFFAOYSA-N [N+](=O)([O-])C1=CC=C(C=C1)N1CCN(CC1)C(CC)N Chemical compound [N+](=O)([O-])C1=CC=C(C=C1)N1CCN(CC1)C(CC)N WHMZVJVROTUDFM-UHFFFAOYSA-N 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 230000008484 agonism Effects 0.000 description 1
- 201000007930 alcohol dependence Diseases 0.000 description 1
- 229910052783 alkali metal Inorganic materials 0.000 description 1
- 150000001340 alkali metals Chemical class 0.000 description 1
- 125000003282 alkyl amino group Chemical group 0.000 description 1
- 239000002168 alkylating agent Substances 0.000 description 1
- 229940100198 alkylating agent Drugs 0.000 description 1
- 230000007815 allergy Effects 0.000 description 1
- BJEPYKJPYRNKOW-UHFFFAOYSA-N alpha-hydroxysuccinic acid Natural products OC(=O)C(O)CC(O)=O BJEPYKJPYRNKOW-UHFFFAOYSA-N 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- 229960004909 aminosalicylic acid Drugs 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- 239000000043 antiallergic agent Substances 0.000 description 1
- 239000000935 antidepressant agent Substances 0.000 description 1
- 229940005513 antidepressants Drugs 0.000 description 1
- 239000000739 antihistaminic agent Substances 0.000 description 1
- 229940125715 antihistaminic agent Drugs 0.000 description 1
- 238000003556 assay Methods 0.000 description 1
- 125000004429 atom Chemical group 0.000 description 1
- 208000022362 bacterial infectious disease Diseases 0.000 description 1
- 230000006399 behavior Effects 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- SRSXLGNVWSONIS-UHFFFAOYSA-N benzenesulfonic acid Chemical compound OS(=O)(=O)C1=CC=CC=C1 SRSXLGNVWSONIS-UHFFFAOYSA-N 0.000 description 1
- 229940092714 benzenesulfonic acid Drugs 0.000 description 1
- PASDCCFISLVPSO-UHFFFAOYSA-N benzoyl chloride Chemical compound ClC(=O)C1=CC=CC=C1 PASDCCFISLVPSO-UHFFFAOYSA-N 0.000 description 1
- KCXMKQUNVWSEMD-UHFFFAOYSA-N benzyl chloride Chemical compound ClCC1=CC=CC=C1 KCXMKQUNVWSEMD-UHFFFAOYSA-N 0.000 description 1
- 230000003851 biochemical process Effects 0.000 description 1
- 210000001124 body fluid Anatomy 0.000 description 1
- 239000010839 body fluid Substances 0.000 description 1
- 210000004556 brain Anatomy 0.000 description 1
- 150000001649 bromium compounds Chemical class 0.000 description 1
- KDYFGRWQOYBRFD-NUQCWPJISA-N butanedioic acid Chemical compound O[14C](=O)CC[14C](O)=O KDYFGRWQOYBRFD-NUQCWPJISA-N 0.000 description 1
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 239000002775 capsule Substances 0.000 description 1
- 238000009903 catalytic hydrogenation reaction Methods 0.000 description 1
- 210000003169 central nervous system Anatomy 0.000 description 1
- 210000003710 cerebral cortex Anatomy 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 210000004978 chinese hamster ovary cell Anatomy 0.000 description 1
- 235000015165 citric acid Nutrition 0.000 description 1
- 239000008119 colloidal silica Substances 0.000 description 1
- 229940125904 compound 1 Drugs 0.000 description 1
- 229940125782 compound 2 Drugs 0.000 description 1
- 229940125851 compound 27 Drugs 0.000 description 1
- 229940125936 compound 42 Drugs 0.000 description 1
- 229940125898 compound 5 Drugs 0.000 description 1
- 229940126545 compound 53 Drugs 0.000 description 1
- 229940126179 compound 72 Drugs 0.000 description 1
- 238000001816 cooling Methods 0.000 description 1
- 239000000625 cyclamic acid and its Na and Ca salt Substances 0.000 description 1
- HCAJEUSONLESMK-UHFFFAOYSA-N cyclohexylsulfamic acid Chemical compound OS(=O)(=O)NC1CCCCC1 HCAJEUSONLESMK-UHFFFAOYSA-N 0.000 description 1
- 229940075894 denatured ethanol Drugs 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 125000001028 difluoromethyl group Chemical group [H]C(F)(F)* 0.000 description 1
- 108010037444 diisopropylglutathione ester Proteins 0.000 description 1
- VAYGXNSJCAHWJZ-UHFFFAOYSA-N dimethyl sulfate Chemical compound COS(=O)(=O)OC VAYGXNSJCAHWJZ-UHFFFAOYSA-N 0.000 description 1
- 201000010099 disease Diseases 0.000 description 1
- 238000006073 displacement reaction Methods 0.000 description 1
- 206010013663 drug dependence Diseases 0.000 description 1
- 230000001544 dysphoric effect Effects 0.000 description 1
- 208000010118 dystonia Diseases 0.000 description 1
- 210000001353 entorhinal cortex Anatomy 0.000 description 1
- CCIVGXIOQKPBKL-UHFFFAOYSA-M ethanesulfonate Chemical compound CCS([O-])(=O)=O CCIVGXIOQKPBKL-UHFFFAOYSA-M 0.000 description 1
- 235000019325 ethyl cellulose Nutrition 0.000 description 1
- 229920001249 ethyl cellulose Polymers 0.000 description 1
- QHSHDVYEJKLXLB-UHFFFAOYSA-N ethyl n-(2-chloroethyl)carbamate Chemical compound CCOC(=O)NCCCl QHSHDVYEJKLXLB-UHFFFAOYSA-N 0.000 description 1
- 208000030533 eye disease Diseases 0.000 description 1
- 230000002349 favourable effect Effects 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 150000002222 fluorine compounds Chemical class 0.000 description 1
- 235000013305 food Nutrition 0.000 description 1
- 239000001530 fumaric acid Substances 0.000 description 1
- 235000011087 fumaric acid Nutrition 0.000 description 1
- 230000006870 function Effects 0.000 description 1
- 239000007903 gelatin capsule Substances 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 229960004275 glycolic acid Drugs 0.000 description 1
- 150000008282 halocarbons Chemical class 0.000 description 1
- 125000004051 hexyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 210000001320 hippocampus Anatomy 0.000 description 1
- 150000004677 hydrates Chemical class 0.000 description 1
- 229930195733 hydrocarbon Natural products 0.000 description 1
- 150000002430 hydrocarbons Chemical class 0.000 description 1
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 1
- 239000008172 hydrogenated vegetable oil Substances 0.000 description 1
- 230000007062 hydrolysis Effects 0.000 description 1
- 238000006460 hydrolysis reaction Methods 0.000 description 1
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 1
- 230000002267 hypothalamic effect Effects 0.000 description 1
- 230000028993 immune response Effects 0.000 description 1
- 230000001771 impaired effect Effects 0.000 description 1
- 238000001727 in vivo Methods 0.000 description 1
- 238000005462 in vivo assay Methods 0.000 description 1
- 238000011065 in-situ storage Methods 0.000 description 1
- 238000011534 incubation Methods 0.000 description 1
- 230000004054 inflammatory process Effects 0.000 description 1
- 230000010365 information processing Effects 0.000 description 1
- 230000005764 inhibitory process Effects 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 150000004694 iodide salts Chemical class 0.000 description 1
- 239000011630 iodine Substances 0.000 description 1
- 229910052740 iodine Inorganic materials 0.000 description 1
- 208000028867 ischemia Diseases 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 150000002576 ketones Chemical class 0.000 description 1
- 208000019423 liver disease Diseases 0.000 description 1
- 235000019359 magnesium stearate Nutrition 0.000 description 1
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 1
- 239000011976 maleic acid Substances 0.000 description 1
- 239000001630 malic acid Substances 0.000 description 1
- 235000011090 malic acid Nutrition 0.000 description 1
- 238000004519 manufacturing process Methods 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 230000001404 mediated effect Effects 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 229940098779 methanesulfonic acid Drugs 0.000 description 1
- 229920000609 methyl cellulose Polymers 0.000 description 1
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 1
- 239000001923 methylcellulose Substances 0.000 description 1
- 235000010981 methylcellulose Nutrition 0.000 description 1
- 235000019813 microcrystalline cellulose Nutrition 0.000 description 1
- 239000008108 microcrystalline cellulose Substances 0.000 description 1
- 229940016286 microcrystalline cellulose Drugs 0.000 description 1
- 150000007522 mineralic acids Chemical class 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 230000007659 motor function Effects 0.000 description 1
- RDTKXZZISRTZAR-UHFFFAOYSA-N n-(4-chlorobutyl)-n-phenyl-1,3-benzothiazol-2-amine Chemical compound N=1C2=CC=CC=C2SC=1N(CCCCCl)C1=CC=CC=C1 RDTKXZZISRTZAR-UHFFFAOYSA-N 0.000 description 1
- HTPMSTGFTOUSSX-UHFFFAOYSA-N n-(5-chloropentyl)-n-methyl-1,3-benzothiazol-2-amine Chemical compound C1=CC=C2SC(N(CCCCCCl)C)=NC2=C1 HTPMSTGFTOUSSX-UHFFFAOYSA-N 0.000 description 1
- NUJVXJQWONGBHO-UHFFFAOYSA-N n-(5-chloropentyl)-n-phenyl-1,3-benzothiazol-2-amine Chemical compound N=1C2=CC=CC=C2SC=1N(CCCCCCl)C1=CC=CC=C1 NUJVXJQWONGBHO-UHFFFAOYSA-N 0.000 description 1
- AEXVFHAEENHHAU-UHFFFAOYSA-N n-[2-[4-(3,4-dichlorophenyl)piperazin-1-yl]ethyl]-6-methyl-1,3-benzothiazol-2-amine Chemical compound S1C2=CC(C)=CC=C2N=C1NCCN(CC1)CCN1C1=CC=C(Cl)C(Cl)=C1 AEXVFHAEENHHAU-UHFFFAOYSA-N 0.000 description 1
- FIKWONMUWBVBJJ-UHFFFAOYSA-N n-[2-[4-(3,4-dichlorophenyl)piperazin-1-yl]ethyl]-n-methyl-1,3-benzothiazol-2-amine Chemical compound N=1C2=CC=CC=C2SC=1N(C)CCN(CC1)CCN1C1=CC=C(Cl)C(Cl)=C1 FIKWONMUWBVBJJ-UHFFFAOYSA-N 0.000 description 1
- FHWYOFCYSFHXDS-UHFFFAOYSA-N n-[2-[4-(4-chlorophenyl)piperazin-1-yl]ethyl]-1,3-benzothiazol-2-amine Chemical compound C1=CC(Cl)=CC=C1N1CCN(CCNC=2SC3=CC=CC=C3N=2)CC1 FHWYOFCYSFHXDS-UHFFFAOYSA-N 0.000 description 1
- SQQQAJILYVEUFG-UHFFFAOYSA-N n-[2-[4-(4-chlorophenyl)piperazin-1-yl]ethyl]-7-methoxy-1,3-benzothiazol-2-amine;hydrochloride Chemical compound Cl.S1C=2C(OC)=CC=CC=2N=C1NCCN(CC1)CCN1C1=CC=C(Cl)C=C1 SQQQAJILYVEUFG-UHFFFAOYSA-N 0.000 description 1
- NHYYKVOAPGFKHL-UHFFFAOYSA-N n-[3-(4-phenylpiperazin-1-yl)propyl]-1,3-benzothiazol-2-amine Chemical compound N=1C2=CC=CC=C2SC=1NCCCN(CC1)CCN1C1=CC=CC=C1 NHYYKVOAPGFKHL-UHFFFAOYSA-N 0.000 description 1
- AJYSDQBKCRYQNF-UHFFFAOYSA-N n-[3-[4-(3,4-dichlorophenyl)piperazin-1-yl]propyl]-6-methoxy-1,3-benzothiazol-2-amine;dihydrochloride Chemical compound Cl.Cl.S1C2=CC(OC)=CC=C2N=C1NCCCN(CC1)CCN1C1=CC=C(Cl)C(Cl)=C1 AJYSDQBKCRYQNF-UHFFFAOYSA-N 0.000 description 1
- ODJJJYLWJQCPDH-UHFFFAOYSA-N n-[3-[4-[3-(trifluoromethyl)phenyl]piperazin-1-yl]propyl]-1,3-benzothiazol-2-amine Chemical compound FC(F)(F)C1=CC=CC(N2CCN(CCCNC=3SC4=CC=CC=C4N=3)CC2)=C1 ODJJJYLWJQCPDH-UHFFFAOYSA-N 0.000 description 1
- QDZCKSIGINHXFC-UHFFFAOYSA-N n-[4-[4-(3,4-dichlorophenyl)piperazin-1-yl]butyl]-6-methoxy-1,3-benzothiazol-2-amine Chemical compound S1C2=CC(OC)=CC=C2N=C1NCCCCN(CC1)CCN1C1=CC=C(Cl)C(Cl)=C1 QDZCKSIGINHXFC-UHFFFAOYSA-N 0.000 description 1
- HVQAGCYLLHLDAE-UHFFFAOYSA-N n-[4-[4-(4-methoxyphenyl)piperazin-1-yl]butyl]-1,3-benzothiazol-2-amine Chemical compound C1=CC(OC)=CC=C1N1CCN(CCCCNC=2SC3=CC=CC=C3N=2)CC1 HVQAGCYLLHLDAE-UHFFFAOYSA-N 0.000 description 1
- AZCNTPSPOFJQJA-UHFFFAOYSA-N n-[5-[4-(3,4-dichlorophenyl)piperazin-1-yl]pentyl]-1,3-benzothiazol-2-amine Chemical compound C1=C(Cl)C(Cl)=CC=C1N1CCN(CCCCCNC=2SC3=CC=CC=C3N=2)CC1 AZCNTPSPOFJQJA-UHFFFAOYSA-N 0.000 description 1
- PTYCWSAKFWICQX-UHFFFAOYSA-N n-benzyl-n-[5-[4-(3,4-dichlorophenyl)piperazin-1-yl]pentyl]-1,3-benzothiazol-2-amine Chemical compound C1=C(Cl)C(Cl)=CC=C1N1CCN(CCCCCN(CC=2C=CC=CC=2)C=2SC3=CC=CC=C3N=2)CC1 PTYCWSAKFWICQX-UHFFFAOYSA-N 0.000 description 1
- 229910017604 nitric acid Inorganic materials 0.000 description 1
- 125000004433 nitrogen atom Chemical group N* 0.000 description 1
- 231100000252 nontoxic Toxicity 0.000 description 1
- 230000003000 nontoxic effect Effects 0.000 description 1
- 208000030212 nutrition disease Diseases 0.000 description 1
- 235000020824 obesity Nutrition 0.000 description 1
- 150000007524 organic acids Chemical class 0.000 description 1
- 235000005985 organic acids Nutrition 0.000 description 1
- 150000001451 organic peroxides Chemical class 0.000 description 1
- 210000001672 ovary Anatomy 0.000 description 1
- 235000006408 oxalic acid Nutrition 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- WLJNZVDCPSBLRP-UHFFFAOYSA-N pamoic acid Chemical compound C1=CC=C2C(CC=3C4=CC=CC=C4C=C(C=3O)C(=O)O)=C(O)C(C(O)=O)=CC2=C1 WLJNZVDCPSBLRP-UHFFFAOYSA-N 0.000 description 1
- FJKROLUGYXJWQN-UHFFFAOYSA-N papa-hydroxy-benzoic acid Natural products OC(=O)C1=CC=C(O)C=C1 FJKROLUGYXJWQN-UHFFFAOYSA-N 0.000 description 1
- 125000001147 pentyl group Chemical group C(CCCC)* 0.000 description 1
- 150000004965 peroxy acids Chemical class 0.000 description 1
- XCRBXWCUXJNEFX-UHFFFAOYSA-N peroxybenzoic acid Chemical class OOC(=O)C1=CC=CC=C1 XCRBXWCUXJNEFX-UHFFFAOYSA-N 0.000 description 1
- 208000022821 personality disease Diseases 0.000 description 1
- 238000000053 physical method Methods 0.000 description 1
- 206010036067 polydipsia Diseases 0.000 description 1
- 229920001223 polyethylene glycol Polymers 0.000 description 1
- 238000002600 positron emission tomography Methods 0.000 description 1
- XAEFZNCEHLXOMS-UHFFFAOYSA-M potassium benzoate Chemical compound [K+].[O-]C(=O)C1=CC=CC=C1 XAEFZNCEHLXOMS-UHFFFAOYSA-M 0.000 description 1
- 159000000001 potassium salts Chemical class 0.000 description 1
- 230000003389 potentiating effect Effects 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 238000003825 pressing Methods 0.000 description 1
- 230000008569 process Effects 0.000 description 1
- 239000000047 product Substances 0.000 description 1
- 235000019260 propionic acid Nutrition 0.000 description 1
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 235000010232 propyl p-hydroxybenzoate Nutrition 0.000 description 1
- 229960003415 propylparaben Drugs 0.000 description 1
- 208000020016 psychiatric disease Diseases 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 239000008213 purified water Substances 0.000 description 1
- 229940107700 pyruvic acid Drugs 0.000 description 1
- 150000003242 quaternary ammonium salts Chemical class 0.000 description 1
- IUVKMZGDUIUOCP-BTNSXGMBSA-N quinbolone Chemical compound O([C@H]1CC[C@H]2[C@H]3[C@@H]([C@]4(C=CC(=O)C=C4CC3)C)CC[C@@]21C)C1=CCCC1 IUVKMZGDUIUOCP-BTNSXGMBSA-N 0.000 description 1
- 239000002287 radioligand Substances 0.000 description 1
- 239000012429 reaction media Substances 0.000 description 1
- 239000002464 receptor antagonist Substances 0.000 description 1
- 229940044551 receptor antagonist Drugs 0.000 description 1
- 230000002787 reinforcement Effects 0.000 description 1
- FDBYIYFVSAHJLY-UHFFFAOYSA-N resmetirom Chemical compound N1C(=O)C(C(C)C)=CC(OC=2C(=CC(=CC=2Cl)N2C(NC(=O)C(C#N)=N2)=O)Cl)=N1 FDBYIYFVSAHJLY-UHFFFAOYSA-N 0.000 description 1
- 229960004889 salicylic acid Drugs 0.000 description 1
- 229920006395 saturated elastomer Polymers 0.000 description 1
- 229930195734 saturated hydrocarbon Natural products 0.000 description 1
- 238000012216 screening Methods 0.000 description 1
- 208000012201 sexual and gender identity disease Diseases 0.000 description 1
- 208000015891 sexual disease Diseases 0.000 description 1
- 230000001568 sexual effect Effects 0.000 description 1
- 230000008054 signal transmission Effects 0.000 description 1
- PFUVRDFDKPNGAV-UHFFFAOYSA-N sodium peroxide Chemical compound [Na+].[Na+].[O-][O-] PFUVRDFDKPNGAV-UHFFFAOYSA-N 0.000 description 1
- ILJOYZVVZZFIKA-UHFFFAOYSA-M sodium;1,1-dioxo-1,2-benzothiazol-3-olate;hydrate Chemical compound O.[Na+].C1=CC=C2C(=O)[N-]S(=O)(=O)C2=C1 ILJOYZVVZZFIKA-UHFFFAOYSA-M 0.000 description 1
- 239000000600 sorbitol Substances 0.000 description 1
- 230000009870 specific binding Effects 0.000 description 1
- 238000001228 spectrum Methods 0.000 description 1
- 229950001675 spiperone Drugs 0.000 description 1
- 230000000707 stereoselective effect Effects 0.000 description 1
- 208000011117 substance-related disease Diseases 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 230000005062 synaptic transmission Effects 0.000 description 1
- 208000011580 syndromic disease Diseases 0.000 description 1
- 239000011975 tartaric acid Substances 0.000 description 1
- 235000002906 tartaric acid Nutrition 0.000 description 1
- 230000001225 therapeutic effect Effects 0.000 description 1
- 238000003325 tomography Methods 0.000 description 1
- 238000000844 transformation Methods 0.000 description 1
- 230000002792 vascular Effects 0.000 description 1
- 208000019553 vascular disease Diseases 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D263/00—Heterocyclic compounds containing 1,3-oxazole or hydrogenated 1,3-oxazole rings
- C07D263/52—Heterocyclic compounds containing 1,3-oxazole or hydrogenated 1,3-oxazole rings condensed with carbocyclic rings or ring systems
- C07D263/54—Benzoxazoles; Hydrogenated benzoxazoles
- C07D263/58—Benzoxazoles; Hydrogenated benzoxazoles with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached in position 2
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/42—Oxazoles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/18—Antipsychotics, i.e. neuroleptics; Drugs for mania or schizophrenia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07B—GENERAL METHODS OF ORGANIC CHEMISTRY; APPARATUS THEREFOR
- C07B59/00—Introduction of isotopes of elements into organic compounds ; Labelled organic compounds per se
- C07B59/002—Heterocyclic compounds
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D277/00—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings
- C07D277/60—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings condensed with carbocyclic rings or ring systems
- C07D277/62—Benzothiazoles
- C07D277/68—Benzothiazoles with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached in position 2
- C07D277/82—Nitrogen atoms
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Medicinal Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Biomedical Technology (AREA)
- Neurology (AREA)
- Neurosurgery (AREA)
- Psychiatry (AREA)
- Epidemiology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Heterocyclic Carbon Compounds Containing A Hetero Ring Having Nitrogen And Oxygen As The Only Ring Hetero Atoms (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Thiazole And Isothizaole Compounds (AREA)
- Nitrogen And Oxygen Or Sulfur-Condensed Heterocyclic Ring Systems (AREA)
Description
- Die vorliegende Anmeldung ist eine Teilanmeldung der am 20. November 1997 als WO 97/43271 veröffentlichen
EP 97923913.4 - Die vorliegende Erfindung betrifft radioaktiv markierte Alkylaminobenzothiazole und -benzoxazole, die ein radioaktives Isotop enthalten, ein Verfahren zur Markierung von Dopamin-D4-Rezeptorstellen und ein Verfahren zur Abbildung eines Organs. Die Verbindungen der vorliegenden Erfindung zeigen einen spezifischen Dopamin-D4-Rezeptorantagonismus. Sie können sich insbesondere für die Untersuchung von psychotischen Erkrankungen wie Schizophrenie eignen.
- Es wird allgemein anerkannt, daß Dopaminrezeptoren bei vielen biochemischen Vorgängen im Tierkörper eine wichtige Rolle spielen. So trägt eine geänderte Funktion dieser Rezeptoren nicht nur zum Entstehen von Psychosen bei, sondern führt auch zu Angstzuständen, Erbrechen, Störungen motorischer Funktionen, Sucht, Schlafstörungen, Ernährungsstörungen, Lernschwierigkeiten, Gedächtnisstörungen, sexuellen Verhaltensstörungen, einer gestörten Steuerung von immunologischen Reaktionen und Blutdruckstörungen. Da Dopaminrezeptoren eine große Zahl pharmakologischer Ereignisse steuern, von denen einige bislang noch unbekannt sind, besteht die Möglichkeit, daß Verbindungen, die eine spezifische Bindungsaffinität für den D4-Rezeptor zeigen, in Menschen ein weites Spektrum therapeutischer Wirkungen haben können.
- In der am 4. Oktober 1989 veröffentlichten EP-A-0,335,586 werden 2-[4-(Diarylmethyl)-1-piperazinyl)alkylamino]-benzothiazole und -benzoxazole beschrieben, die als Antihistaminika und Antiallergika wirken.
- Die radioaktiv markierten Alkylaminobenzothiazole und -benzoxazole der vorliegenden Erfindung zeigen über raschenderweise ein hohes Ausmaß an Bindungsaffinität zum Dopamin-D4-Rezeptor. Außerdem haben die vorliegenden Verbindungen eine gegenüber anderen Dopaminrezeptoren im menschlichen Körper selektive Affinität für den Dopamin-D4-Rezeptor. Die in Rede stehenden Verbindungen zeigen auch eine variable Affinität für andere Rezeptoren wie beispielsweise Serotoninrezeptoren, Histaminrezeptoren, adrenerge Rezeptoren, cholinerge Rezeptoren und die σ-Bindungsstelle.
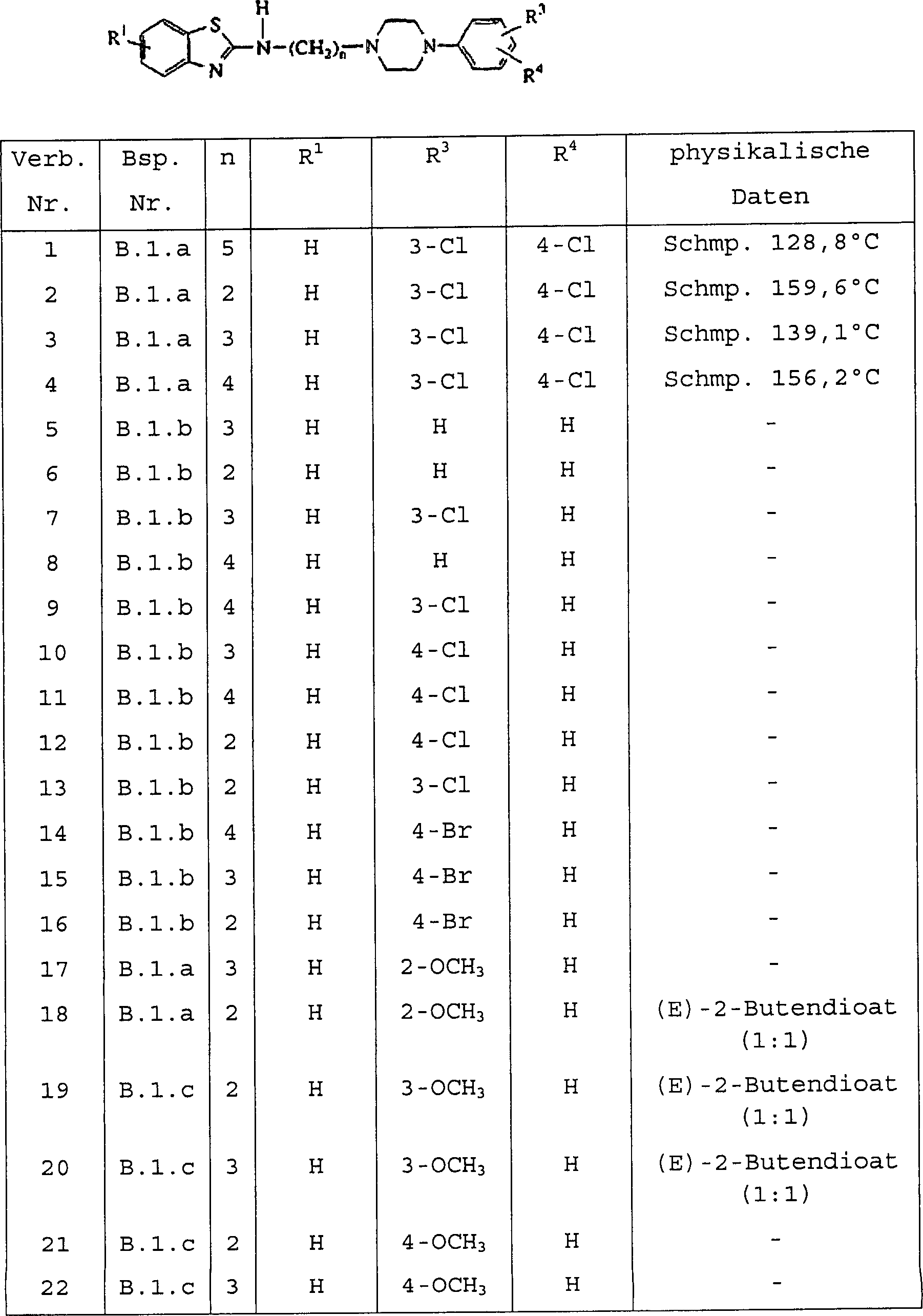
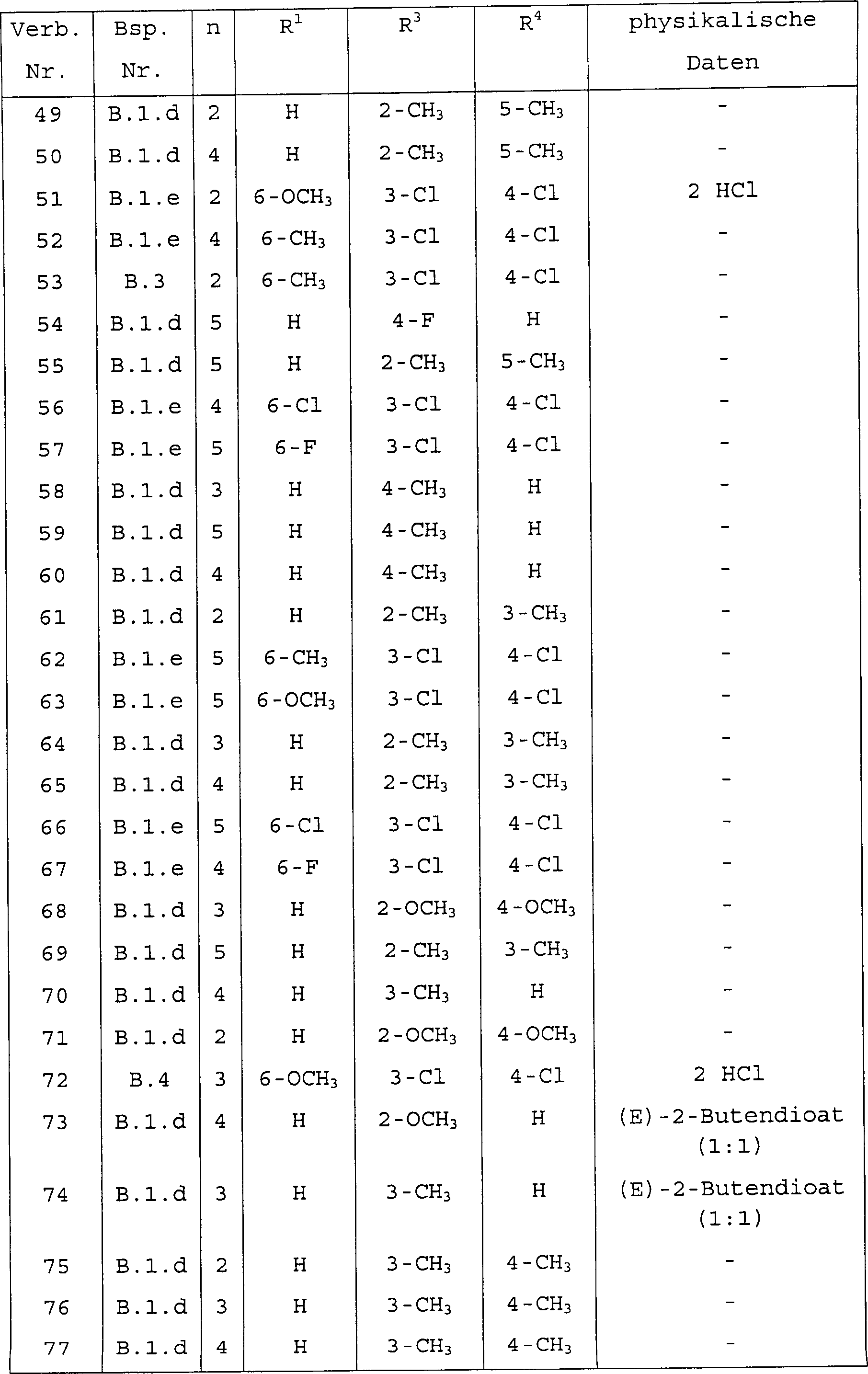
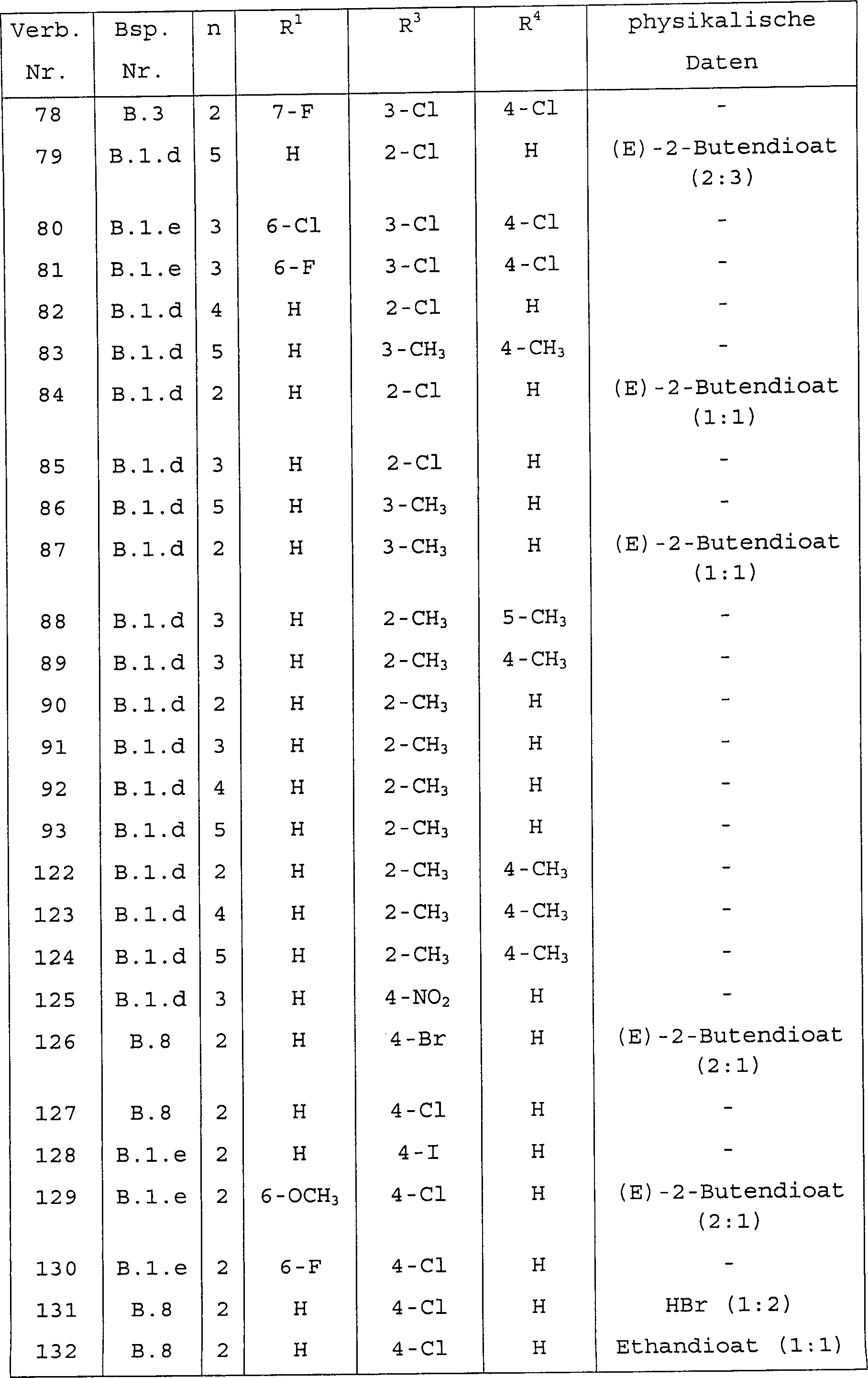
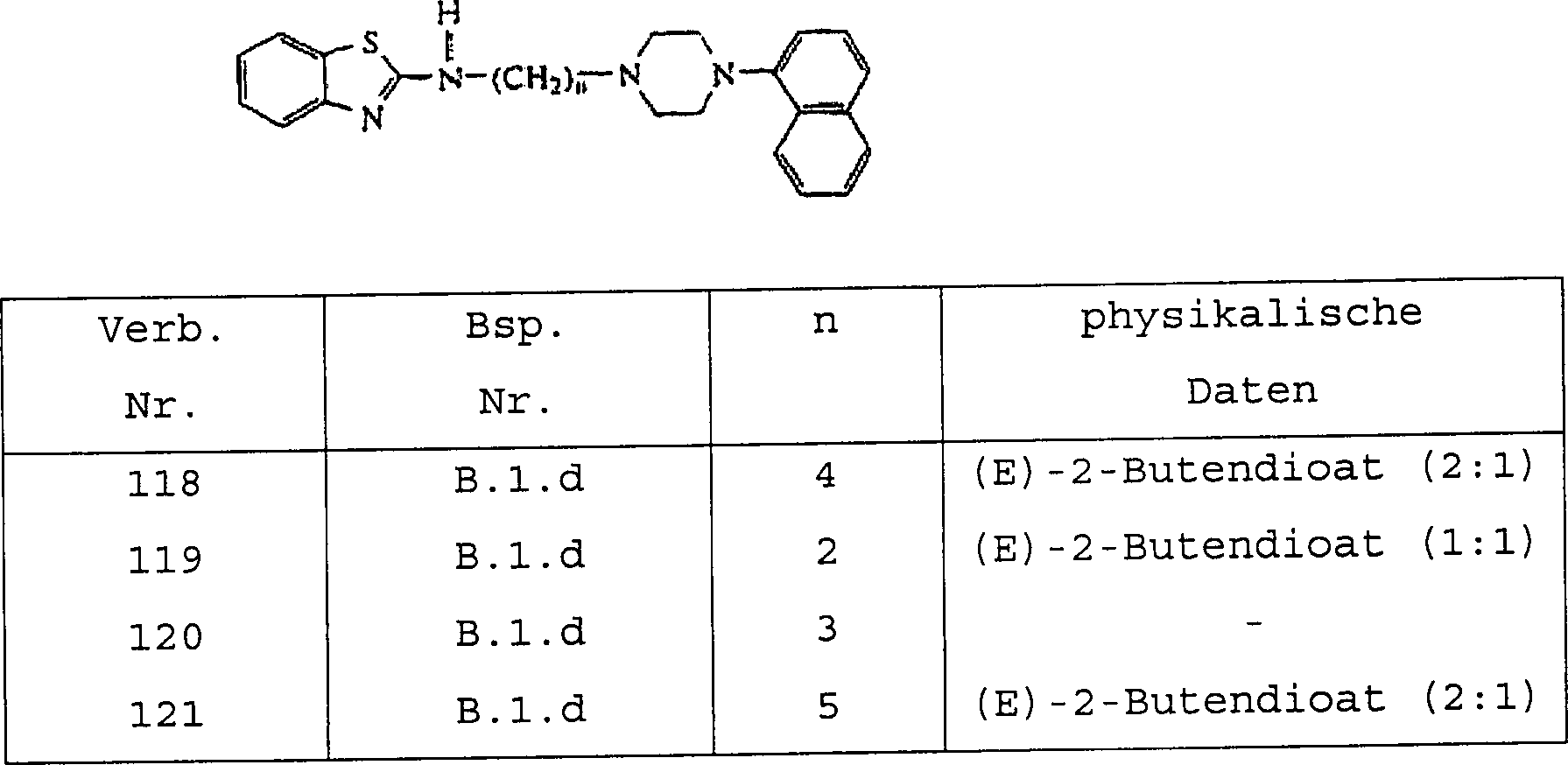
- Die vorliegende Erfindung betrifft radioaktiv markierte Verbindungen der Formel deren N-Oxidformen, pharmazeutisch unbedenkliche Säureadditionssalze und stereochemisch isomere Formen, wobei
X für O oder S steht;
n für 2, 3, 4 oder 5 steht;
R1 für Wasserstoff, C1–6-Alkyl, C1–6-Alkyloxy oder Halogen steht;
R2 für Wasserstoff, C1–6-Alkyl, Phenyl, Phenyl-C1–6-alkyl oder Phenylcarbonyl steht;
R3 und R4 jeweils unabhängig voneinander aus Wasserstoff, Halogen, Nitro, C1–6-Alkyl, C1–6-Alkyloxy, Halogen-C1–6-alkyl, Aminosulfonyl, Mono- oder Di(C1–4-alkyl)aminosulfonyl ausgewählt sind; oder
R3 und R4 auch zusammen einen zweiwertigen Rest der Formel -CH=CH-CH=CH- bilden können, dadurch gekennzeichnet, daß die Verbindungen wenigstens ein Halogen aufweisen, bei dem es sich um ein radioaktives Isotop von Iod, Brom oder Fluor handelt, oder wenigstens ein 11C-Atom oder Tritiumatom aufweisen. - Wie in den vorstehenden Definitionen und im folgenden verwendet, steht Halogen allgemein für Fluor, Chlor, Brom und Iod; C1–4-Alkyl definiert geradkettige und verzweigte gesättigte Kohlenwasserstoffreste mit 1 bis 4 Kohlenstoffatomen wie beispielsweise Methyl, Ethyl, Propyl, Butyl, 1-Methylethyl, 2-Methylpropyl, 2,2-Dimethylethyl und dergleichen; C1–6-Alkyl schließt C1–4-Alkyl und die höheren Homologe davon mit 5 oder 6 Kohlenstoffatomen wie beispielsweise Pentyl, 2-Methylbutyl, Hexyl, 2-Methylpentyl und dergleichen ein; Halogen-C1–6-alkyl ist definiert als polyhalogensubstituiertes C1–6-Alkyl, insbesondere mit 1 bis 6 Halogenatomen substituiertes C1–6-Alkyl, ganz besonders Difluor- oder Trifluormethyl.
- Zu den oben erwähnten pharmazeutisch unbedenklichen Säureadditionssalzen zählen die therapeutisch wirksamen, nicht-toxischen Säureadditionssalzformen, die von den Verbindungen der Formel (I) gebildet werden können. Die Salze lassen sich erhalten, indem man die Basenform der Verbindungen der Formel (I) mit entsprechenden Säuren wie anorganischen Säuren, beispielsweise Halogenwasserstoffsäuren, z.B. Salzsäure oder Bromwasserstoffsäure, Schwefelsäure, Salpetersäure, Phosphorsäure und ähnlichen Säuren, oder organischen Säuren wie beispielsweise Essigsäure, Hydroxyessigsäure, Propionsäure, Milchsäure, Brenztraubensäure, Oxalsäure, Malonsäure, Bernsteinsäure, Maleinsäure, Fumarsäure, Äpfelsäure, Weinsäure, Citronensäure, Methansulfonsäure, Ethansulfonsäure, Benzolsulfonsäure, p-Toluolsulfonsäure, Cyclaminsäure, Salicylsäure, p-Aminosalicylsäure, Pamoasäure und ähnlichen Säuren behandelt.
- Der Ausdruck Additionssalz schließt, wie er oben verwendet wird, auch die Solvate ein, die von den Verbindungen der Formel (I) und deren Salzen gebildet werden können. Solche Solvate sind beispielsweise Hydrate, Alkoholate und dergleichen.
- Zu den N-Oxiden der vorliegenden Verbindungen zählen die Verbindungen der Formel (I), in denen eines oder mehrere Stickstoffatome zu den sogenannten N-Oxiden oxidiert sind.
- Der Ausdruck „stereochemisch isomere Formen" definiert, wie er hier und im folgenden verwendet wird, alle möglichen isomeren Formen, in denen die Verbindungen der Formel (I) vorkommen können. Wenn nicht anders erwähnt oder angegeben wird mit dem chemischen Namen von Verbindungen die Mischung, insbesondere die racemische Mischung, aller möglichen stereochemisch isomeren Formen bezeichnet, wobei die Mischungen alle Diastereomere und Enantiomere der zugrundeliegenden Molekülstruktur enthalten. Die Formel (I) schließt natürlich stereochemisch isomere Formen der Verbindungen der Formel (I) und Mischungen solcher Formen ein.
- Einige der Verbindungen der Formel (I) können auch in ihren tautomeren Formen vorliegen. Diese Formen sollen, auch wenn sie nicht explizit in der obigen Formel angegeben sind, mit in den Schutzbereich der Erfindung fallen. So können beispielsweise Verbindungen der Formel (I), in denen R2 für Wasserstoff steht, in ihrer entsprechenden tautomeren Form vorliegen.
- Eine interessante Gruppe von Verbindungen sind die Verbindungen der Formel (I), in denen X für S steht und R2 für Wasserstoff, C1–6-Alkyl, Phenyl oder Phenyl-C1–6-alkyl steht.
- Eine andere interessante Gruppe von Verbindungen sind die Verbindungen der Formel (I), in denen X für O steht und R2 für Wasserstoff, C1–6-Alkyl oder Phenyl-C1–6-alkyl steht.
- Interessante Verbindungen sind auch die Verbindungen der Formel (I), in denen R3 und R4 aus der aus Wasser stoff, Nitro, Halogen, C1–6-Alkyl, C1–6-Alkyloxy und Trifluormethyl bestehenden Gruppe ausgewählt sind, oder R3 und R4 zusammen einen zweiwertigen Rest der Formel -CH=CH-CH=CH- bilden.
- Besondere Verbindungen sind die interessanten Verbindungen, in denen n für 2, 3 oder 4 steht.
- Bevorzugte Verbindungen sind die Verbindungen der Formel (I), in denen X für S steht, R2 für Wasserstoff, C1–6-Alkyl, Phenyl oder Phenyl-C1–6-alkyl steht und n für 2 steht.
- Andere bevorzugte Verbindungen sind die Verbindungen der Formel (I), in denen R2 und R3 für Wasserstoff stehen und R4 für Chlor steht.
- Die am meisten bevorzugten Verbindungen sind
N-[2-[4-(3, 4-Dichlorphenyl)-1-piperazinyl]ethyl-2-benzothiazolamin;
N-[2-(4-Phenyl-l-piperazinyl)ethyl]-2-benzothiazolamin;
N-[2-[4-(4-Chlorphenyl)-1-piperazinyl]ethyl]-2-benzothiazolamin;
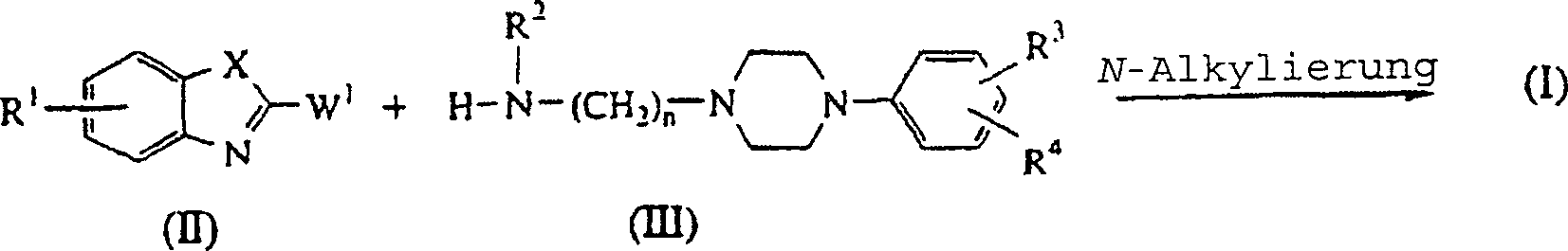
N-[2-[4-(4-Bromphenyl)-1-piperazinyl]ethyl]-2-benzothiazolamin; und deren N-Oxide, deren stereoisomere Formen und deren pharmazeutisch unbedenkliche Säureadditionssalze. - Die nicht radioaktiv markierten Verbindungen der vorliegenden Erfindung lassen sich im allgemeinen darstellen, indem man ein Zwischenprodukt der Formel (III) mit einem Zwischenprodukt der Formel (II), in welchem W1 für eine geeignete reaktive Abgangsgruppe wie beispielsweise ein Halogen steht, N-alkyliert.
- Diese N-Alkylierung kann durch Rühren und Erhitzen der Reaktionspartner in einem reaktionsinerten Lösungsmittel wie Ethanol, 2-Ethoxyethanol, 1-Butanol, Methylisobutylketon oder Toluol, vorzugsweise in Gegenwart einer geeigneten Base wie Natriumcarbonat und gegebenenfalls in Gegenwart eines Katalysators wie beispielsweise Kaliumiodid, durchgeführt werden.
- Bei dieser und den folgenden Zubereitungen können die Reaktionsprodukte aus dem Reaktionsmedium isoliert und, falls erforderlich, weiter nach im Stand der Technik allgemein bekannten Verfahren wie beispielsweise Extrahieren, Kristallisieren, Verreiben und Chromatographieren auf gereinigt werden.
- Durch die Formel (I-a) wiedergegebene Verbindungen der Formel (I), in denen X für S steht, lassen sich darstellen, indem man ein Zwischenprodukt der Formel (III) mit einem Zwischenprodukt der Formel (IV) in einem reaktionsinerten Lösungsmittel wie beispielsweise Tetrahydrofuran umsetzt und anschließend das so gebildete Zwischenprodukt der Formel (V) in einem reaktionsinerten Lösungsmittel wie beispielsweise Chloroform und in Gegenwart eines geeigneten Reagens wie beispielsweise Thionylchlorid cyclisiert. Alternativ dazu kann man Verbindungen der Formel (I-a) darstellen, indem man ein Zwischenprodukt der Formel (III) direkt mit einem Zwischenprodukt der Formel (IV) in einem reaktionsinerten Lösungsmittel wie beispielsweise Chloroform in Gegenwart eines geeigneten Reagens wie beispielsweise Thionylchlorid mischt, wodurch in situ ein Zwischenprodukt der Formel (V) gebildet wird, das während der Reaktion sofort cyclisiert.
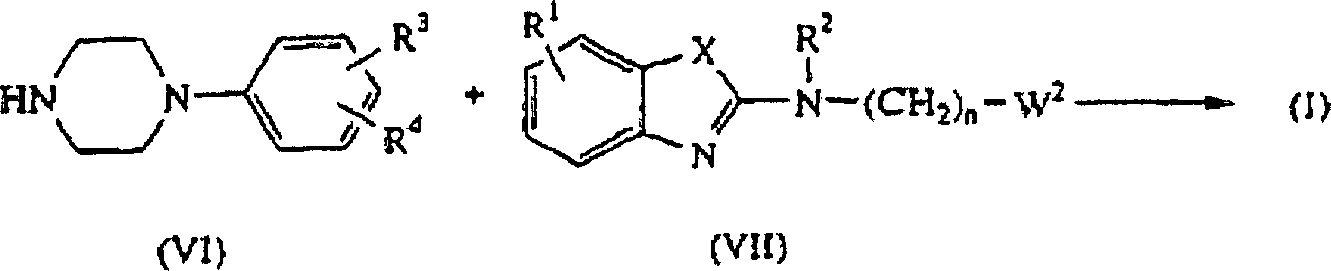
- Die vorliegenden Verbindungen lassen sich auch durch die N-Alkylierung eines Zwischenprodukts der Formel (VI) mit einem Zwischenprodukt der Formel (VII), in dem W2 für eine geeignete Abgangsgruppe wie beispielsweise ein Halogen steht, darstellen, gegebenenfalls in einem reaktionsinerten Lösungsmittel wie beispielsweise Dimethylacetamid.
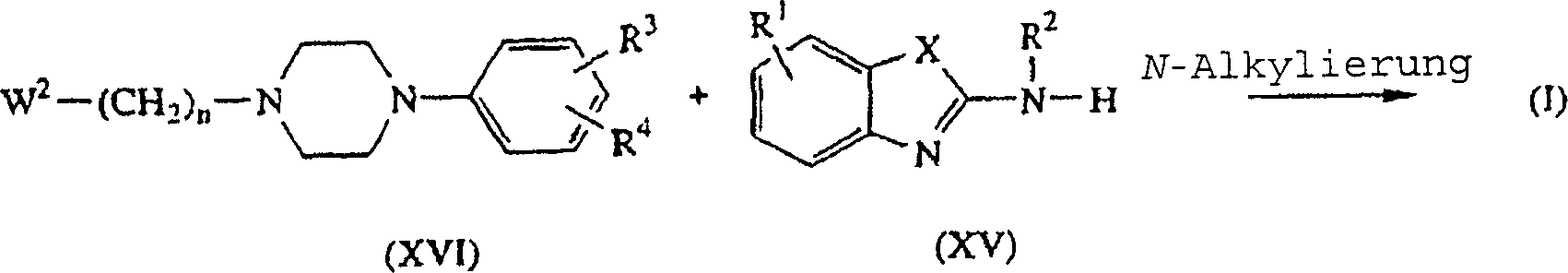
- Alternativ dazu kann man die Verbindungen der Formel (I) darstellen, indem man ein Zwischenprodukt der Formel (XV) mit einem Zwischenprodukt der Formel (XVI), in dem W2 für eine geeignete Abgangsgruppe wie beispielsweise ein Halogen steht, in einem reaktionsinerten Lösungsmittel wie beispielsweise Tetrahydrofuran und in Gegenwart einer geeigneten Base wie beispielsweise Natriumhydrid oder einem funktionellen Äquivalent davon N-alkyliert.
- Die Verbindungen der Formel (I) können auch nach im Stand der Technik bekannten Transformationsreaktionen in andere Verbindungen der Formel (I) umgewandelt werden. Beispielsweise kann man durch die Formel (I-b) wiedergegebene Verbindungen der Formel (I), in denen R2 für Wasserstoff steht, in Verbindungen der Formel (I) umwandeln, in denen R2 nicht für Wasserstoff steht.
- Es ist weiterhin möglich, die Verbindungen der Formel (I) nach im Stand der Technik bekannten Verfahren zur Umwandlung eines trivalenten Stickstoffs in seine N-Oxidform in das entsprechende N-Oxid umzuwandeln. Die N-Oxidationsreaktion läßt sich im allgemeinen durchführen, indem man das Ausgangsmaterial der Formel (I) mit einem geeigneten organischen oder anorganischen Peroxid umsetzt. Geeignete anorganische Peroxide sind beispielsweise Wasserstoffperoxid, Alkali- oder Erdalkaliperoxide, z.B. Natriumperoxid, Kaliumperoxid; als organische Peroxide kommen zum Beispiel Peroxysäuren wie beispielsweise Perbenzoesäure oder halogensubstituierte Perbenzoesäuren, z.B. 3-Chlorperbenzoesäure, Peroxyalkansäuren, z.B. Peressigsäure, Alkylhydroperoxide, z.B. tert.-Butylhydroperoxid, in Frage. Als Lösungsmittel eignen sich beispielsweise Wasser, niedere Alkanole, z.B. Ethanol und dergleichen, Kohlenwasserstoffe, z.B. Toluol, Ketone, z.B. 2-Butanon, halogenierte Kohlenwasserstoffe, z.B. Dichlormethan, und Mischungen solcher Lösungsmittel.
- Die meisten in den obigen Reaktionsvorschriften verwendeten Zwischenprodukte und Ausgangsmaterialien sind bekannte Verbindungen, die im Handel erhältlich sind oder nach im Stand der Technik bekannten Reaktionsvorschriften dargestellt werden können. So lassen sich Zwischenprodukte der Formel (XV) beispielsweise nach der in J. Chem. Soc., 1962, 230 beschriebenen Vorschrift darstellen, und Zwischenprodukte der Formel (XVI) lassen sich nach der in JP-60.202.883. beschriebenen Vorschrift darstellen.
- Die Zwischenprodukte der Formel (III) lassen sich allgemein durch Hydrolyse eines Carbamatesters der Formel (VIII) in einem reaktionsinerten Lösungsmittel wie beispielsweise Isopropanol, und in Gegenwart einer geeigneten Base wie beispielsweise Kaliumhydroxid darstellen. Es kann weiterhin zweckmäßig sein, die Umsetzung bei Rückflußtemperatur durchzuführen.
- Zwischenprodukte der Formel (VIII) lassen sich darstellen, indem man ein Piperazinderivat der Formel (IX) mit einem Carbamatester der Formel (X), in dem W3 für eine geeignete Abgangsgruppe wie beispielsweise ein Halogen steht, N-alkyliert.
- Diese Umsetzung kann durch Rühren und Erhitzen der Reaktionspartner in einem reaktionsinerten Lösungsmittel wie beispielsweise 4-Methyl-2-pentanon in Gegenwart einer geeigneten Base wie Natriumcarbonat und gegebenenfalls in Gegenwart einer katalytischen Menge eines Kaliumsalzes wie beispielsweise Kaliumiodid erfolgen.
- Durch die Formel (III-a) wiedergegebene Zwischenprodukte der Formel (III), in denen R2 für Wasserstoff steht, lassen sich auch durch die katalytische Hydrierung eines Nitrilderivats der Formel (XI) unter Verwendung von Wasserstoff in Gegenwart eines geeigneten Katalysators wie beispielsweise Raney-Nickel darstellen. Es kann zweckmäßig sein, die Umsetzung in einem reaktionsinerten Lösungsmittel wie beispielsweise mit NH3 gesättigtem Methanol oder Tetrahydrofuran durchzuführen.
- Zwischenprodukte der Formel (XI) lassen sich durch N-Alkylierung eines Piperazinderivats der Formel (IX) mit einem Nitrilderivat der Formel (XII), in dem W4 für eine geeignete Abgangsgruppe wie beispielsweise ein Halogen steht, darstellen, analog zu der Darstellung der Zwischenprodukte (VIII) ausgehend von den Zwischenprodukten (IX) und (X).
- Alternativ dazu kann man durch die Formel (XI-a) wiedergegebene Nitrilderivate der Formel (XI), in denen (n-1) für 2 steht, durch N-Alkylierung eines Piperazinderivats der Formel (IX) mit Acrylonitril durch Rühren und Erhitzen der Reaktionspartner in einem reaktionsinerten Lösungsmittel wie beispielsweise 2-Propanol und gegebenenfalls in Gegenwart einer katalytischen Menge eines quaternären Ammoniumsalzes wie beispielsweise N-Methyl-N,N-dioctyloctanaminiumchlorid darstellen.
- Zwischenprodukte der Formel (VII) lassen sich darstellen, indem man zuerst ein Zwischenprodukt der Formel (XIII) mit einem Zwischenprodukt der Formel (II) N-alkyliert und anschließend die Hydroxylgruppe des so erhaltenen Zwischenprodukts der Formel (XIV) durch eine geeignete Abgangsgruppe W4 wie beispielsweise Chlor ersetzt. So kann man beispielsweise Zwischenprodukte der Formel (XIV) unter Bildung eines Zwischenprodukts der Formel (VII), in dem W4 für Chlor steht, mit Thionylchlorid umsetzen.
- Ein alternativer Weg zur Darstellung von Zwischenprodukten der Formel (VII) umfaßt die N-Alkylierung eines Zwischenprodukts der Formel (XV) mit einem Zwischenprodukt der Formel (XVII), in dem LG für eine Abgangsgruppe wie Brom steht und W2 für eine wie bei den Zwischenprodukten der Formel (VII) definierte Abgangsgruppe steht, wobei LG so gewählt ist, daß die Substitutionsreaktion mit dem Zwischenprodukt der Formel (XV) vorzugsweise an dem Kohlenstoffatom stattfindet, das die LG-Gruppe trägt. Diese Umsetzung erfolgt vorzugs weise in einem reaktionsinerten Lösungsmittel in Gegenwart einer geeigneten Base wie beispielsweise Natriumhydrid.
- Auf ähnliche Weise lassen sich Zwischenprodukte der Formel (XVI) durch N-Alkylierung eines Zwischenprodukts der Formel (IX) mit einem Zwischenprodukt der Formel (XVII) darstellen.
- Einige der Verbindungen der Formel (I) und einige der Zwischenprodukte der vorliegenden Erfindung enthalten wenigstens ein asymmetrisches Kohlenstoffatom. Reine stereochemisch isomere Formen dieser Verbindungen und dieser Zwischenprodukte lassen sich unter Anwendung von im Stand der Technik bekannten Vorschriften erhalten. So lassen sich beispielsweise Diastereoisomere durch physikalische Methoden wie selektive Kristallisierung oder chromatographische Verfahren, z.B. Gegenstromverteilung, Flüssigchromatographie und ähnliche Methoden trennen. Enantiomere lassen sich aus racemischen Mischungen erhalten, indem man die racemischen Mischungen zunächst mit geeigneten Mitteln für die Racematspaltung wie beispielsweise chiralen Säuren in Mischungen diastereomerer Salze bzw. Verbindungen umwandelt, dann diese Mischungen diastereomerer Salze bzw. Verbindungen beispielsweise durch selektive Kristallisation oder chromatographische Verfahren, z.B. Flüssigchromatographie und ähnliche Methoden, physikalisch trennt, und schließlich die getrennten diastereomeren Salze bzw. Verbindungen in die entsprechenden Enantiomere umwandelt.
- Bei einem alternativen Verfahren zur Trennung der enantiomeren Formen der Verbindungen der Formel (I) und der Zwischenprodukte bedient man sich der Flüssigchromatographie, insbesondere der Flüssigchromatographie mit einer chiralen stationären Phase.
- Reine stereochemisch isomere Formen der Verbindungen der Formel (I) lassen sich auch aus den reinen stereochemisch isomeren Formen der entsprechenden Zwischenprodukte und Ausgangsmaterialien erhalten, vorausgesetzt, die vorgenommenen Umwandlungen verlaufen stereospezifisch. In den Schutzbereich der vorliegenden Erfindung fallen sowohl die reinen als auch die gemischten stereochemisch isomeren Formen der Verbindungen der Formel (I).
- Die Verbindungen der Formel (I) und deren N-Oxide, pharmazeutisch unbedenkliche Säureadditionssalze und stereochemisch isomere Formen sind wirksame Antagonisten des Dopamin-D4-Rezeptors, d.h. sie zeigen ein hohes Ausmaß an Bindungsaffinität zum Dopamin-D4-Rezeptor, und hemmen somit die Bindung eines endogenen Liganden, insbesondere Dopamin, an den Dopamin-D4-Rezeptor, wie in dem im folgenden beschriebenen pharmakologischen Beispiel gezeigt wird. Die antagonistische Wirkung der Bindung der vorliegenden Verbindungen an den Dopamin-D4-Rezeptor wurde in Assays zur Signalübertragung bestätigt.
- Die vorliegenden Verbindungen zeigen eine interessante Aktivität im sogenannten „differential reinforcement test low rate 72 seconds"-Test (DRL-72), bei dem es sich um einen in-vivo-Test handelt, bei dem die meisten klinisch wirksamen Antidepressiva, in hohen Dosen verabreicht, Wirkung zeigen. In diesem Test können Ratten Futter durch Drücken eines Hebels nur dann erhalten, wenn sie zwischen zwei Hebeldrücken nicht weniger als 72 Sekunden gewartet haben. Die vorliegenden D4-Antagonisten induzieren ein effizienteres Verhalten bei den Ratten, während es unbehandelte Tiere schwierig finden, ihre impulsive Neigung zum Drücken des Hebels zu kontrollieren und einem geeigneten Timing hintanzustellen, um ihre Belohnung zu optimieren. Der Nutzen dieses DRL-72-Tests als Modell für spezifische D4-Antagonisten, wie die vorliegenden Verbindungen, wird weiter durch die Tatsache gestützt, daß (a) Manki et al. (Journal of Affective Disorders 40 (1996), 7–13) gefunden haben, daß es eine signifikante Assoziation zwischen D4-Rezeptorgenpolymorphismus und Gemütskrankheiten gibt, und (b) durch die Tatsache, daß bekannt ist, daß die D4-Rezeptordichte sowohl bei Primaten, Menschen als auch Nagetieren im Hippocampus und im entorhinalen und zerebralen Cortex am größten ist.
- Durch Antagonisieren des Dopamin-D4-Rezeptors werden eine Reihe von Symptomen, die mit durch die Aktivierung, insbesondere die exzessive Aktivierung, dieses Rezeptors induzierten Phänomenen assoziiert sind, unterdrückt bzw. gelindert. Infolgedessen sind die vorliegenden Verbindungen aufgrund ihrer Fähigkeit zur Modulation der durch Dopamin D4 vermittelten Neurotransmission bei der Behandlung und/oder Prävention verschiedener damit assoziierter Krankheiten wie Schlafstörungen, sexuellen Störungen, Denkstörungen, einer gestörten Informationsverarbeitung, Psychose, affektiver Psychose, unorganischer Psychose, Persönlichkeitsstörungen, psychiatrischen Gemütsstörungen, Verhaltens- und Impulsstörungen, Schizophrenie und schizoaffektiven Erkrankungen, Polydipsie, bipolaren Störungen, dysphorischer Manie, Angstzuständen und verwandten Erkrankungen, Erkrankungen des Magen-Darm-Trakts, Obesitas, Erbrechen, bakteriellen Infektionen des ZNS wie Hirnhautentzündung, Lernschwierigkeiten, Gedächtnisstörungen, Parkinson-Krankheit, Depression, extrapyramidalen Nebenwirkungen von Neuroleptika, malignem neuroleptischem Syndrom, Störungen von Hypothalamus/Hypophyse, dekompensierter Herzinsuffizienz, Abhängigkeit von chemischen Substanzen wie Drogen- oder Alkoholabhängigkeit, Gefäß- und Herzkreislaufstörungen, Augenerkrankungen, Dystonie, dystonem Syndrom, Tourette-Syndrom und anderen Hyperkinesen, Demenz, Ischämie, Bewegungsstörungen wie Akathesie, Bluthochdruck und durch ein hyperaktives Immunsystem verursachten Erkrankungen wie Allergien und Entzündungen von potentiellem Nutzen.
- Die Verbindungen der vorliegenden Erfindung zeigen eine deutlich größere Affinität für den Dopamin-D4-Rezeptor als für andere Dopaminrezeptoren wie beispielsweise den Dopamin-D2-Rezeptor. Eine solche Abkopplung von der antagonisierenden Wirkung auf den Dopamin-D4-Rezeptor von der Wirkung auf andere Dopaminrezeptoren kann bei der Behandlung und/oder Prävention der oben erwähnten Störungen von zusätzlichem Nutzen sein. So weisen beispielsweise Van Tol et al. (Nature 1991, 350, 610–614) darauf hin, daß Verbindungen, die selektiv mit dem Dopamin-D4-Rezeptor in Wechselwirkung treten können und eine weniger ausgeprägte Wirkung am Dopamin-D2-Rezeptor haben, eine gleichermaßen nutzbringende antipsychotische Wirkung wie klassische Antipsychotika haben, mit dem zusätzlichen Vorteil, daß sie weniger dazu tendieren, die unerwünschten extrapyramidalen oder neuroendokrinen Nebenwirkungen klassischer Antipsychotika zu entfalten. Aus diesem Grund sind die nicht radioaktiv markierten Verbindungen als Antipsychotika besonders geeignet, vor allem zur Behandlung und/oder Prävention psychotischer Störungen wie Schizophrenie.
- Über ihre antagonistische Wirkung am Dopamin-D4-Rezeptor hinaus zeigen die in Rede stehenden Verbindungen auch eine variable Affinität für andere Rezeptoren wie beispielsweise Serotoninrezeptoren, Histaminrezeptoren, adrenerge Rezeptoren, cholinerge Rezeptoren und die σ-Bindungsstelle. So zeigen einige der vorliegenden Ver bindungen beispielswiese eine günstige Bindungsaffinität für die σ-Bindungsstelle, den 5HT1A-Rezeptor und den α2-Rezeptor.
- Der Ausdruck „eine den Dopamin-D4-Rezeptor antagonisierende Menge" bezieht sich, so wie er hier verwendet wird, auf eine Menge, die ausreicht, die Bindung eines endogenen Liganden, insbesondere Dopamin, an den Dopamin-D4-Rezeptor zu hemmen. Dem Fachmann für die Behandlung der oben erwähnten Störungen sollte es möglich sein, festzustellen, daß eine wirksame, den Dopamin-D4-Rezeptor antagonisierende tägliche Menge von etwa 0,01 mg/kg bis etwa 10 mg/kg Körpergewicht, besonders bevorzugt von etwa 0,04 mg/kg bis etwa 4 mg/kg Körpergewicht, beträgt. Die Verbindungen können während einer Behandlung 1- bis 4-mal pro Tag verabreicht werden.
- Zur Linderung der Symptome psychotischer Erkrankungen wie Schizophrenie, ohne dabei unerwünschte Nebenwirkungen zu verursachen, wird die Dosierungskonzentration der erfindungsgemäßen nicht radioaktiv markierten Verbindung idealerweise so gewählt, daß die verabreichte Dosis eine im wesentlichen vollständige Blockierung des Dopamin-D4-Rezeptors bewirkt und dabei eine günstige Besetzung des Dopamin-D2-Rezeptors zeigt, bei der es zu keinen oder nur geringen unerwünschten extrapyramidalen oder neuroendokrinen Nebenwirkungen kommt.
- Falls gewünscht können die erfindungsgemäßen nicht radioaktiv markierten Verbindungen zusammen mit einem anderen Antipsychotikum, beispielsweise einem, das seine Wirkung über einen oder mehrere der folgenden Mechanismen entfaltet: Dopamin-D2-Rezeptorblockade, 5-HT2-Rezeptorblockade, 5-HT1A-Agonismus und 5-HT3-Antagonismus, verabreicht werden. Man kann sich vorstellen, daß es in solchen Fällen zu einer verstärkten antipsychotischen Wirkung ohne eine entsprechende Zunahme an Nebenwirkungen kommt, wie sie beispielsweise durch eine starke Dopamin-D2-Rezeptorblockade verursacht werden; oder alternativ dazu kann man sich vorstellen, daß es zu einer vergleichbaren antipsychotischen Wirkung mit weniger Nebenwirkungen kommt. Eine solche gemeinsame Verabreichung kann dann wünschenswert sein, wenn sich ein Patient bereits beispielsweise in einer antischizophrenen Behandlung mit herkömmlichen antischizophrenen Medikamenten befindet.
- Aufgrund ihres hohen Grads an Spezifität für den Dopamin-D4-Rezeptor eignen sich die wie oben definierten Verbindungen der Formel (I) zum Markieren bzw. Identifizieren von Rezeptoren, insbesondere Dopamin-D4-Rezeptoren. Für diesen Zweck ist es erforderlich, daß die Verbindungen der vorliegenden Erfindung markiert werden, insbesondere dadurch, daß man ein oder mehrere Atome im Molekül teilweise oder vollständig durch ihre radioaktiven Isotope ersetzt. Radioaktiv markierte Verbindungen, die von Interesse sind, sind beispielsweise die Verbindungen, die wenigstens ein Halogen enthalten, bei dem es sich um ein radioaktives Isotop von Iod, Brom oder Fluor handelt; oder die Verbindungen, die wenigstens ein 11C-Atom oder Tritiumatom enthalten.
- Eine besondere Gruppe besteht aus den Verbindungen der Formel (I), in denen R1 und/oder R3 und/oder R4 für ein radioaktives Halogenatom steht/stehen. Im Prinzip eignen sich alle Verbindungen der Formel (I), die ein Halogenatom enthalten, für eine radioaktive Markierung durch Ersetzen des Halogenatoms durch ein geeignetes Isotop. Für diesen Zweck geeignete Halogen-Radioisotope sind radioaktive Iodide, zum Beispiel 122I, 123I, 125I, 131I; radioaktive Bromide, zum Beispiel 75Br, 76Br, 77Br und 82Br, und radioaktive Fluoride, zum Beispiel 18F. Ein radioaktives Halogenatom läßt sich durch eine geeignete Austauschreaktion einführen, oder durch Anwendung einer der hier oben beschriebenen Vorschriften zur Herstellung von chriften zur Herstellung von Halogenderivaten der Formel (I).
- Bevorzugte radioaktiv markierte Verbindungen sind die Verbindungen der Formel (I), in denen R1 und/oder R3 und/oder R4 für 123I, 125I, 75Br, 76Br, 77Br oder 18F steht/stehen.
- Eine andere interessante Form der radioaktiven Markierung ist durch Substitution eines Kohlenstoffatoms durch ein 11C-Atom, oder die Substitution eines Wasserstoffatoms durch ein Tritiumatom. Ein solches 11C-Atom läßt sich beispielsweise durch die N-Alkylierung einer Verbindung der Formel (I), in welcher R2 für Wasserstoff steht, mit einem 11C-markierten Alkylierungsmittel bewerkstelligen.
- Diese radioaktiv markierten Verbindungen der Formel (I) lassen sich in einem Verfahren zur spezifischen in-vitro-Markierung von Dopamin-D4-Rezeptorstellen in biologischem Material einsetzen. Dieses Verfahren umfaßt die folgenden Schritte: (a) die radioaktive Markierung einer Verbindung der Formel (I), (b) die in-vitro-Verabreichung dieser radioaktiv markierten Verbindung an biologisches Material und anschließend (c) der Nachweis der Emissionen der radioaktiv markierten Verbindung. Der Ausdruck "biologisches Material" soll jegliche Art von Material biologischen Ursprungs umfassen. Ganz insbesondere bezieht sich dieser Ausdruck auf Gewebeproben, Plasma oder Körperflüssigkeiten, jedoch auch auf Teile von Tieren, insbesondere Warmblütern, wie Organe. Die radioaktiv markierten Verbindungen der Formel (I) sind außerdem nützliche Mittel zum in-vitro-Screening darauf, ob eine Testverbindung dazu in der Lage ist, sich an eine Dopamin-D4-Rezeptorstelle zu binden. Das Ausmaß, in dem eine Testverbindung eine Verbindung der Formel (I) von der Dopamin-D4-Rezeptorstelle verdrängt, zeigt die Fähigkeit der Testverbindung entweder als Agonist, als Antagonist oder als gemischter Agonist/Antagonist an chter Agonist/Antagonist an einem Dopamin-D4-Rezeptor zu wirken.
- Bei der Verwendung in in-vivo-Assays werden die radioaktiv markierten Verbindungen in einer entsprechenden Zusammensetzung an ein Tier verabreicht, und die Stellen, an denen sich diese radioaktiv markierten Verbindungen anreichern, werden durch Verfahren zur Bilddarstellung wie beispielsweise der Einzelphotonen-Emissions-Computertomographie (Single Photon Emission Computerized Tomography, SPECT) oder Positronenemissionstomographie (Positron Emission Tomography, PET) und dergleichen nachgewiesen. Auf diese Weise läßt sich die Verteilung von Dopamin-D4-Rezeptorstellen im Körper nachweisen, und Organe, die Dopamin-D4-Rezeptorstellen enthalten, wie beispielsweise das Gehirn, können durch die oben erwähnten Verfahren zur Bilddarstellung sichtbar gemacht werden.
- Die folgenden Beispiele sollen die vorliegende Erfindung näher erläutern, ohne daß dadurch der Umfang der Erfindung eingeschränkt wird.
- Experimenteller Teil
- A. Darstellung der Zwischenprodukte
- Beispiel A.1
-
- a) Eine Mischung aus 1-(4-Bromphenyl)piperazin (0,018 mol) und (2-Chlorethyl)carbaminsäureethylester (0,036 mol) wurde 2 Stunden lang bei 130°C gerührt. Triethylamin (3 ml) wurde zugesetzt, und die Mischung wurde 15 Minuten lang bei 130°C gerührt. Die Reaktionsmischung wurde auf Raumtemperatur abgekühlt und mit CH2Cl2 versetzt, und die so erhaltene Mischung wurde mit Wasser gewaschen. Die organische Phase wurde abgetrennt, getrocknet und filtriert, und das Lösungsmittel wurde abgedampft. Der Rückstand wurde durch Kie selgel-Säulenchromatographie (Laufmittel: CH2Cl2/CH3OH 95/5) aufgereinigt. Die reinen Fraktionen wurden gesammelt und das Lösungsmittel wurde abgedampft, wodurch man 4,3 g (67,2%) [2-[4-(4-Bromphenyl)-1-piperazinyl]ethyl]carbaminsäureethylester (Zwischenprodukt 1) erhielt.
- b) Eine Mischung aus Zwischenprodukt (1) (0,029 mol) und Kaliumhydroxid (0,29 mol) in 2-Propanol (200 ml) wurde unter Rühren 8 Stunden lang auf Rückfluß erhitzt. CH2Cl2 wurde zugesetzt. Zum Lösen der Kaliumsalze wurde Wasser zugetropft. Die organische Phase wurde abgetrennt, getrocknet und filtriert, und das Lösungsmittel wurde abgedampft. Der Rückstand wurde durch Kieselgel-Säulenchromatographie (Laufmittel: CH2Cl2/(CH3OH/NH3) 90/10) aufgereinigt. Die reinen Fraktionen wurden gesammelt und das Lösungsmittel wurde abgedampft, wodurch man 3,8 g (46%) 4-(4-Bromphenyl)-1-piperazinethanamin (Zwischenprodukt 4) erhielt.
- Die folgenden Verbindungen wurden auf ähnliche Weise dargestellt:
4-(4-Iodphenyl)-1-piperazinethanamin (Zwischenprodukt 11);
4-(1-Naphthalinyl)-1-piperazinpentanamin (Zwischenprodukt 12);
4-(1-Naphthalinyl)-1-piperazinethanamin (Zwischenprodukt 13);
4-(1-Naphthalinyl)-1-piperazinpropanamin (Zwischenprodukt 14);
4-(4-Nitrophenyl)-1-piperazinpropanamin (Zwischenprodukt 15) ;
4-(4-Bromphenyl)-1-piperazinbutanamin (Zwischenprodukt 16) ; und
4-(4-Bromphenyl)-1-piperazinpropanamin (Zwischenprodukt 17). - Beispiel A.2
-
- a) Eine Mischung aus 1-(3,4-Dichlorphenyl)piperazin (0,1 mol), 5-Chlorpentannitril (0,13 mol), Natriumcarbonat (10 g) und Kaliumiodid (0,1 g) in 4-Methyl-2-pentanon (280 ml) wurde unter Rühren 10 Stunden lang auf Rückfluß erhitzt. Die Reaktionsmischung wurde abgekühlt und filtriert, und das Filtrat wurde eingedampft. Der Rückstand wurde durch Kieselgel-Säulenchromatographie (Laufmittel: CH2Cl2/CH3OH 95/5) auf gereinigt. Die reinen Fraktionen wurden gesammelt und das Lösungsmittel wurde abgedampft, wodurch man 22,5 g (72%) 4-(3,4-Dichlorphenyl)-1-piperazinpentannitril (Zwischenprodukt 2) erhielt.
- b) Eine Mischung aus Zwischenprodukt (2) (0,072 mol) in Tetrahydrofuran (250 ml) wurde mit Raney-Nickel (2 g) als Katalysator hydriert. Nach Ende der H2-Aufnahme wurde der Katalysator abfiltriert und das Filtrat eingedampft. Der Rückstand wurde in Diisopropylether gerührt und über Dicalite abfiltriert und das Filtrat wurde eingedampft, wodurch man 20 g (88%) 4-(3,4-Dichlorphenyl)-1-piperazinpentanamin (Zwischenprodukt 5) erhielt.
- Die folgenden Verbindungen wurden auf ähnliche Weise dargestellt:
4-(2,4-Dimethylphenyl)-1-piperazinettanamin (Zwischenprodukt 18);
4-(2,4-Dimethylphenyl)-1-piperazinbutanamin (Zwischenprodukt 19);
4-(2,4-Dimethylphenyl)-1-piperazinpentanamin (Zwischenprodukt 20);
4-(3,4-Dichlorphenyl)-1-piperazinpropanamin (Zwischenprodukt 21);
4-(3,4-Dichlorphenyl)-1-piperazinbutanamin (Zwischenprodukt 22); und
4-Phenyl-1-piperazinpropanamin (Zwischenprodukt 23). - Beispiel A.3
- Eine Mischung aus 1-(3,4-Dichlorphenyl)piperazin (0,1 mol), 2-Propennitril (0,15 mol) und N-Methyl-N,N-dioctyloctanaminiumchlorid (1 ml) in 2-Propanol (150 ml) wurde unter Rühren eine Stunde lang auf Rückfluß erhitzt. Das Lösungsmittel wurde abgedampft und der Rückstand wurde durch Kieselgel-Säulenchromatographie (Laufmittel: CH2Cl2/CH3OH 95/5) aufgereinigt. Die reinen Fraktionen wurden gesammelt und das Lösungsmittel wurde abgedampft. Der Rückstand wurde in Diisopropylether/Acetonitril 10/1 gerührt. Das Lösungsmittel wurde abgedampft, wodurch man 28 g (98,5%) 4-(3,4-Dichlorphenyl)-1-piperazinpropannitril (Zwischenprodukt 3) erhielt.
- Beispiel A.4
- Eine Mischung aus 4-(3,4-Dichlorphenyl)-1-piperazinethanamin (0,01 mol) und 4-Methyl-1-isothiocyanatobenzol (0,01 mol) in Tetrahydrofuran (300 ml) wurde 1 Stunde lang bei Raumtemperatur gerührt. Das Lösungsmittel wurde abgedampft. Der Rückstand wurde aus DIPE umkristallisiert. Der Niederschlag wurde abfiltriert und getrocknet. Das Produkt wurde ohne weitere Aufreinigung verwendet, wodurch man 4,2 g N-(4-Methyl-phenyl)-N'-[2-[4-(3,4-dichlorphenyl)-1-piperazinyl]-ethyl]thioharnstoff (Zwischenprodukt 6) erhielt.
- Beispiel A.5
-
- a) Eine Mischung aus 5-(Methylamino)pentanol (0,23 mol), 2-Chlorbenzothiazol (0,3 mol), Natriumcarbonat (0,4 g) und Kaliumiodid (katalytische Menge) in Methylisobutylketon (1000 ml) wurde unter Rühren über Nacht auf Rückfluß erhitzt. Die Reaktionsmischung wurde abgekühlt, mit Wasser gewaschen, getrocknet und filtriert, und das Filtrat wurde eingedampft. Der Rückstand wurde in Wasser gerührt, mit HCl angesäuert, gerührt und mit Diisopropylether gewaschen, und die saure Phase wurde mit NH4OH basisch gestellt. Die Mischung wurde zweimal mit CH2Cl2 extrahiert. Die abgetrennte organische Phase wurde getrocknet und filtriert und das Lösungsmittel wurde abgedampft, wodurch man 56 g N-(5-Hydroxypentyl)-N-methyl-2-benzothiazolamin (Zwischenprodukt 7) erhielt.
- b) Thionylchlorid (60 ml) wurde gerührt in CHCl3 (400 ml). Eine Lösung von Zwischenprodukt (7) (0,22 mol) in CHCl3 (200 ml) wurde tropfenweise zugesetzt. Die Mischung wurde über Nacht bei Raumtemperatur gerührt. Das Lösungsmittel wurde abgedampft und der Rückstand wurde in CH2Cl2 gelöst, mit Wasser gewaschen, getrocknet und filtriert und das Lösungsmittel wurde abgedampft, wodurch man 65 g N-(5-Chlorpentyl)-N-methyl-2-benzothiazolamin (Zwischenprodukt 8) erhielt.
- Beispiel A.6
- Eine Mischung aus 1-(3,4-Dichlorphenyl)piperazin (0,05 mol), 1-Brom-2-chlorethan (0,1 mol) und Triethylamin (0,05 mol) wurde 30 Minuten lang bei 100°C gerührt. Die Mischung wurde abgekühlt und anschließend zwischen CH2Cl2 und Wasser verteilt. Die Phasen wurden getrennt. Die organische Phase wurde über Dicalite filtriert. Das organische Filtrat wurde getrocknet und filtriert, und das Filtrat wurde eingedampft. Der Rückstand wurde durch Kieselgel-Säulenchromatographie (Laufmittel: CH2Cl2/CH3OH 98/2) aufgereinigt. Die reinen Fraktionen wurden gesammelt und das Lösungsmittel wurde abgedampft, wodurch man 5,2 g (35%) 4-(2-Chlorethyl)-1-(3,4-dichlorphenyl)piperazin (Zwischenprodukt 9) erhielt.
- Beispiel A.7
- Natriumhydrid (0,05 mol) wurde portionsweise zu einer Lösung von N-Phenyl-2-benzothiazolamin, dargestellt wie in J. Chem. Soc., 1962, 230 beschrieben, (0,05 mol) in Tetrahydrofuran (200 ml) gegeben. Die Mischung wurde 15 Minuten lang gerührt. Eine Lösung von 1-Brom-4-chlorbutan (0,05 mol) in Tetrahydrofuran (50 ml) wurde zugetropft, und die so erhaltene Reaktionsmischung wurde unter Rühren 48 Stunden lang auf Rückfluß erhitzt. Die Mischung wurde abgekühlt und das Lösungsmittel wurde abgedampft. Der Rückstand wurde zwischen Wasser und CH2Cl2 verteilt. Die organische Phase wurde abgetrennt, getrocknet und filtriert, und das Lösungsmittel wurde abgedampft. Der Rückstand wurde durch Kieselgel-Säulenchromatographie (Laufmittel: CH2Cl2) auf gereinigt. Die gewünschten Fraktionen wurden gesammelt und das Lösungsmittel wurde abgedampft, wodurch man 10,4 g (66%) N-(4-Chlorbutyl)-N-phenyl-2-benzothiazolamin (Zwischenprodukt 10) erhielt.
- N-(5-Chlorpentyl)-N-phenyl-2-benzothiazolamin (Zwischenprodukt 24) wurde auf ähnliche Weise dargestellt.
- B. Darstellung der Endprodukte
- Beispiel B.1
-
- a) Eine Mischung aus Zwischenprodukt (5) (0,015 mol), 2-Chlorbenzothiazol (0,016 mol) und Natriumcarbonat (4 g) in Toluol (150 ml) wurde unter Rühren über Nacht auf Rückfluß erhitzt. Die Reaktionsmischung wurde abgekühlt und filtriert. Das Filtrat wurde abgedampft und der Rückstand wurde durch Kieselgel-Säulenchromatographie (Laufmittel: CH2Cl2/CH3OH 95/5) aufgereinigt. Die gewünschten Fraktionen wurden gesammelt, das Lösungsmittel wurde abgedampft und der Rückstand wurde aus CH3CN kristallisiert. Der Niederschlag wurde abfiltriert und getrocknet, wodurch man 2, 3 g (34%) N-[5-[4-(3,4-Dichlorphenyl)-1-piperazinyl]pentyl]-2-benzothiazolamin (Verbindung 1) erhielt.
- b) N-[3-[4-Phenyl-1-piperazinyl]propyl]-2-benzothiazolamin (Verbindung 5) wurde nach der gleichen Vorschrift wie in Beispiel B.1.a) beschrieben dargestellt, wobei allerdings Ethanol anstelle von Toluol verwendet wurde.
- c) N-[4-[4-(4-Methoxyphenyl)-1-piperazinyl]butyl]-2-benzothiazolamin (Verbindung 26) wurde nach der gleichen Vorschrift wie in Beispiel B.1.a) beschrieben dargestellt, wobei allerdings Methylisobutylketon anstelle von Toluol verwendet wurde.
- d) N-[3-[4-[3-(Trifluormethyl)phenyl]-1-piperazinyl]-propyl]-2-benzothiazolamin (Verbindung 27) wurde nach der gleichen Vorschrift wie in Beispiel B.1.a) beschrieben dargestellt, wobei allerdings 2-Ethoxyethanol anstelle von Toluol verwendet wurde.
- e) N-[4-[4-(3,4-Dichlorphenyl)-1-piperazinyl]butyl]-6-methyl-2-benzothiazolamin (Verbindung 52) wurde nach der gleichen Vorschrift wie in Beispiel B.1.d) beschrieben dargestellt, wobei allerdings der Ausgangsreaktionsmischung eine katalytische Menge Kaliumiodid zugesetzt wurde.
- Beispiel B.2
- 4-(3,4-Dichlorphenyl)-1-piperazinbutanamin (0,0085 mol), dargestellt nach der in Beispiel A.5 beschriebenen Vorschrift, und 2-Chlor-6-methoxybenzothiazol (0,0043 mol) wurden 1 Stunde lang bei 120°C gerührt. Die Mischung wurde auf Raumtemperatur abgekühlt, mit CH2Cl2 verdünnt und mit NH4OH in die freie Base umgewandelt. Die organische Phase wurde abgetrennt, getrocknet (MgSO4) und filtriert, und das Lösungsmittel wurde abgedampft. Der Rückstand wurde durch Kieselgel-Säulenchromatographie (Laufmittel: CH2Cl2/CH3OH 90/10) auf gereinigt. Die reinen Fraktionen wurden gesammelt und das Lösungsmittel wurde abgedampft. Der Rückstand wurde in das (E)-2-Butendisäuresalz (1:1) umgewandelt. Der Niederschlag wurde abfiltriert und getrocknet, wodurch man 1,1 g (44%) N-[4-[4-(3,4-Dichlorphenyl)-1-piperazinyl]butyl]-6-methoxy-2-benzothiazolamin-(E)-2-butendioat (1:1) (Verbindung 42) erhielt.
- Beispiel B.3
- Zwischenprodukt (6) (0,01 mol) wurde in CHCl3 (30 ml) gelöst. Die Mischung wurde auf 0°C abgekühlt. Thionylchlorid (11,5 ml) wurde langsam tropfenweise zugesetzt. Die Mischung wurde langsam auf Raumtemperatur erwärmen gelassen und anschließend 30 Minuten lang gerührt. Das Lösungsmittel wurde abgedampft und der Rückstand wurde mit einer kleinen Menge HCl/2-Propanol in 2-Propanon gewaschen, filtriert, mit 2-Propanon gewaschen und mit einer NH4OH-Lösung in die freie Base umgewandelt. Der Niederschlag wurde abfiltriert und durch Kieselgel-Säulenchromatographie (Laufmittel: CH2Cl2/CH3OH 95/5) aufgereinigt. Die reinen Fraktionen wurden gesammelt und das Lösungsmittel wurde abgedampft, wodurch man 0,7 g (16,7%) N-[2-[4-(3,4-Dichlorphenyl)-1-piperazinyl]-ethyl]-6-methyl-2-benzothiazolamin (Verbindung 53) erhielt.
- Beispiel B.4
- Eine Mischung aus 4-(3,4-Dichlorphenyl)-1-piperazinpropanamin (0,009 mol), dargestellt nach der in Beispiel A.5 beschriebenen Vorschrift, und 1-Isothiocyanato-4-methoxybenzol (0,009 mol) in CHCl3 (100 ml) wurde eine Stunde lang bei Raumtemperatur gerührt und anschließend in einem Eisbad auf 0°C abgekühlt. Thionylchlorid (30 ml) wurde zugetropft, und die so erhaltene Reaktionsmischung wurde langsam auf Raumtemperatur erwärmen gelassen. Die Reaktionsmischung wurde 3 Stunden lang bei 60°C gerührt. Die Mischung wurde auf Raumtemperatur abgekühlt, und der so erhaltene Niederschlag wurde abfiltriert, in kochendem 2-Propanon gerührt, abfiltriert und dann getrocknet. Diese Fraktion wurde durch Zugabe von wäßrigem Ammoniak in die freie Base umgewandelt. Die Mischung wurde mit CH2Cl2 extrahiert. Die abgetrennte organische Phase wurde getrocknet und filtriert, und das Lösungsmittel wurde abgedampft. Der Rückstand wurde aus CH3CN kristallisiert, abfiltriert, in 2-Propanon gelöst und mit HCl/2-Propanol in das Hydrochloridsalz (1:2) überführt. Der Niederschlag wurde abfiltriert und getrocknet, wodurch man 1,6 g (34%) N-[3-[4-(3,4-Dichlorphenyl)-1-piperazinyl]propyl]-6-methoxy-2-benzothiazolamin-dihydrochlorid (Verbindung 72) erhielt.
- Beispiel B.5
- Eine Mischung aus Verbindung (1) (0,01 mol), Chlormethylbenzol (5 ml) und Natriumhydrid (0,015 mol; 60%ige Lösung) in Tetrahydrofuran (200 ml) wurde unter Rühren 8 Stunden lang auf Rückfluß erhitzt. Die Reaktionsmischung wurde abgekühlt und mit einigen Tropfen Wasser versetzt. Das Lösungsmittel wurde abgedampft. Der Rückstand wurde zwischen Wasser und CH2Cl2 verteilt. Die organische Phase wurde abgetrennt, mit Wasser gewaschen, getrocknet und filtriert, und das Lösungsmittel wurde abgedampft. Der Rückstand wurde durch Kieselgel-Säulenchromatographie (Laufmittel: CH2Cl2/Essigsäureethylester 70/30) auf gereinigt. Die reinen Fraktionen wurden gesammelt und das Lösungsmittel wurde abgedampft. Der Rückstand wurde in 2-Propanol gelöst und mit (E)-2-Butendisäure (1 g) in das (E)-2-Butendisäuresalz (1:1) umgewandelt. Die Mischung wurde gekocht und anschließend über Nacht bei Raumtemperatur gerührt. Der Niederschlag wurde abfiltriert und getrocknet, wodurch man 2,70 g (41%) N-[5-[4-(3,4-Dichlorphenyl)-1-piperazinyl]pentyl]-N-phenylmethyl-2-benzothiazolamin-(E)-2-butendioat (1:1) (Verbindung 112) erhielt.
- Beispiel B.6
- Eine Mischung aus Verbindung (3) (0,01 mol), Natriumcarbonat (4 g) und Benzoylchlorid (0,01 mol) in Chloroform (150 ml) und N,N-Dimethylformamid (1 Tropfen) wurde unter Rühren 4 Stunden lang auf Rückfluß erhitzt. Die Mischung wurde warm filtriert und das Filtrat wurde mit Wasser gewaschen. Die organische Phase wurde abgetrennt, getrocknet und filtriert, und das Lösungsmittel wurde abgedampft. Der Rückstand wurde über Kieselgel auf einem Glasfilter (Laufmittel: CH2Cl2/Ethanol 95/5) aufgereinigt. Die reinen Fraktionen wurden gesammelt und das Lösungsmittel wurde abgedampft. Der Rückstand wurde aus CH3CN kristallisiert. Der Niederschlag wurde abfiltriert und getrocknet, wodurch man 4,8 g (92,5%) N-(2-Benzothiazolyl)-N-[3-[4-(3,4-dichlorphenyl)-1-piperazinyl]propyl]benzamid (Verbindung 99) erhielt.
- Beispiel B.7
- Eine Mischung aus 1-(3,4-Dichlorphenyl)piperazin (0,03 mol) und Zwischenprodukt (8) (0,02 mol) in Dimethylacetamid (2 ml) wurde 2 Stunden lang bei 120–130°C gerührt. Die Reaktionsmischung wurde abgekühlt, in CH2Cl2 gelöst, mit wäßrigem Ammoniak gewaschen, getrocknet und filtriert, und das Filtrat wurde eingedampft. Der Rückstand wurde durch Kieselgel-Säulenchromatographie (Laufmittel: CH2Cl2/CH3OH 98/2) aufgereinigt und dann nochmals gereinigt (Laufmittel: CH2Cl2/Essigsäureethylester 50/50). Die reinen Fraktionen wurden gesammelt und das Lösungsmittel wurde abgedampft. Der Rückstand wurde in 2-Propanol gelöst und mit (E)-2-Butendisäure (2 g) in das (E)-2-Butendisäuresalz (1:1) überführt. Die Mischung wurde gekocht und anschließend bei Raumtemperatur gerührt. Der Niederschlag wurde abfiltriert und getrocknet, wodurch man 6,60 g (57%) N-[5-[4-(3,4- Dichlorphenyl)-1-piperazinyl]pentyl]-2-benzothiazolamin-(E)-2-butendioat (1:1) (Verbindung 110) erhielt.
- Beispiel B.8
- Verbindung 12 (0,0058 mol) wurde in warmem Ethanol (75 ml) gelöst. (E)-2-Butendisäure (0,0058 mol) wurde zugesetzt, und die so erhaltene Mischung wurde gerührt, bis alles in Lösung gegangen war. Die Mischung wurde unter Rühren auf Raumtemperatur abkühlen gelassen. Der Niederschlag wurde abfiltriert und getrocknet, wodurch man 2,03 g (80%) N-[2-[4-(4-Chlorphenyl)-1-piperazinyl]ethyl]-2-benzothiazolamin-(E)-2-butendioat (2:1) (Verbindung 127) erhielt.
- Beispiel B.9
- Verbindung 2 (0,015 mol) wurde in Tetrahydrofuran (200 ml) gelöst. Natriumhydrid (0,02 mol) wurde zugesetzt. Die Mischung wurde 15 Minuten lang bei Raumtemperatur gerührt. Dimethylsulfat (0,015 mol) wurde zugegeben, und die so erhaltene Reaktionsmischung wurde 4 Stunden lang bei Raumtemperatur gerührt. Das Lösungsmittel wurde abgedampft und der Rückstand wurde an Kieselgel (Laufmittel: Essigsäureethylester/CH3OH/CH2Cl2 30/0/70, dann 28/2/70) aufgereinigt. Die reinen Fraktionen wurden gesammelt und das Lösungsmittel wurde abgedampft. Der Rückstand wurde in 2-Propanol gelöst und mit (E)-2-Butendisäure (0,8 g) in das (E)-2-Butendisäuresalz (1:1) überführt. Die Mischung wurde gekocht und anschließend über Nacht bei Raumtemperatur gerührt. Der Niederschlag wurde abfiltriert und getrocknet, wodurch man 1,80 g (23%) N-[2-[4-(3,4-Dichlorphenyl)-1-piperazinyl]ethyl]-N-methyl-2-benzothiazolamin-(E)-2-butendioat (1:1) (Verbindung 117) erhielt.
- Beispiel B.10
- Eine Mischung aus 4-(4-Chlorphenyl)-1-piperazinethanamin (0,01 mol) und 1-Isothiocyanato-2-methoxybenzol (0,01 mol) in CCl4 (100 ml) wurde 1 Stunde lang bei Raumtemperatur gerührt. Br2 in CCl4 (0,01 mol in 10 ml) wurde zugesetzt, und die Reaktionsmischung wurde unter Rühren 1 Stunde lang auf Rückfluß erhitzt. Die Reaktionsmischung wurde auf Raumtemperatur abgekühlt, mit CH2Cl2 verdünnt und mit wäßrigem NH3 versetzt. Die organische Phase wurde getrocknet und filtriert, und das Lösungsmittel wurde abgedampft. Der Rückstand wurde durch Kieselgel-Säulenchromatographie (Laufmittel: CH2Cl2/CH3OH 95/5) aufgereinigt. Die reinen Fraktionen wurden gesammelt und das Lösungsmittel wurde abgedampft. Der Rückstand wurde in das Hydrochloridsäuresalz (1:2) umgewandelt. Der Niederschlag wurde abfiltriert und getrocknet, wodurch man 0,4 g (8%) N-[2-[4-(4-Chlorphenyl)-1-piperazinyl]ethyl]-7-methoxy-2-benzothiazolamin-hydrochlorid-(1:2)-hydrat (1:1) (Verbindung 143) erhielt.
- Beispiel B.11
- N-[2-[4-(4-Chlorphenyl)-1-piperazinyl]ethyl]-6-fluor-2-benzothiazolamin (Verbindung 141) wurde nach der in Beispiel B.10 beschriebenen Vorschrift dargestellt, wobei allerdings SOCl2 in CHCl3 anstelle von Br2 in CCl4 verwendet wurde.
- Beispiel B.12
- N-Phenyl-2-benzothiazolamin, dargestellt nach der in J. Chem. Soc., 1962, 230 beschriebenen Vorschrift, (0,03 mol) wurde in Tetrahydrofuran (100 ml) gelöst. Natriumhydrid (0,03 mol) wurde portionsweise zugesetzt. Die Mischung wurde 15 Minuten lang gerührt. Eine Lösung von Zwischenprodukt 9 (0,018 mol) in Tetrahydrofuran (50 ml) wurde zugegeben. Die so erhaltene Reaktionsmischung wurde unter Rühren über Nacht auf Rückfluß erhitzt. Die Reaktionsmischung wurde abgekühlt und das Lösungsmittel wurde abgedampft. Der Rückstand wurde in CH2Cl2 gelöst. Die organische Lösung wurde mit Wasser gewaschen, getrocknet und filtriert, und das Lösungsmittel wurde abgedampft. Der Rückstand wurde durch Kieselgel-Säulenchromatographie (Laufmittel: CH2Cl2/Essigsäureethylester 90/10) aufgereinigt. Die gewünschten Fraktionen wurden gesammelt und das Lösungsmittel wurde abgedampft. Der Rückstand wurde in 2-Propanol gelöst und mit (E)-2-Butendisäure (1,5 g) in das (E)-2-Butendisäuresalz (1:1) überführt. Die Mischung wurde gekocht und anschließend auf Raumtemperatur abkühlen gelassen. Der Niederschlag wurde abfiltriert und getrocknet, wodurch man 3, 66 g (94%) N-[2-[4-(3,4-Dichlorphenyl)-1-piperazinyl]ethyl]-N-phenyl-2-benzothiazolamin-(E)-2-butendioat (1:1) (Verbindung 114) erhielt.
- Die folgenden Verbindungen wurden nach einem der oben beschriebenen Beispiele dargestellt.
- In Tabelle 5 sind sowohl die experimentellen (Spaltenüberschrift "exp.") als auch die thereotischen (Spaltenüberschrift "theor.") Elementaranalysenwerte für Kohlenstoff, Wasserstoff und Stickstoff für die oben im experimentellen Teil dargestellten Verbindungen 10 aufgeführt.
- C. Pharmakologisches Beispiel
- Beispiel C.1.: In-vitro-Bindungsaffinität für den Dopamin-D4-Rezeptor
- Die Wechselwirkung der Verbindungen der Formel (I) mit den Dopamin-D4-Rezeptoren wurde: durch In-vitro-Radioligandenbindungsexperimente untersucht.
- Eine niedrige Konzentration an 3H-Spiperon mit hoher Bindungsaffinität für den Dopamin-D4-Rezeptor wurde mit einer Probe einer Membranzubereitung von transfektierten Zellen aus Eierstöcken chinesischer Hamster (Chinese Hamster Ovary, CHO), die geklonte humane D4-Rezeptoren exprimieren (Receptor Biology, Maryland, USA) in einem gepufferten Medium inkubiert. Nachdem sich ein Bindungsgleichgewicht eingestellt hatte, wurde die rezeptorgebundene Radioaktivität von der nichtgebundenen Radioaktivität abgetrennt, und die rezeptorgebundene Aktivität wurde ausgezählt. Die Wechselwirkung der der Inkubationsmischung in verschiedenen Konzentrationen zugesetzten Testverbindungen mit dem Dopamin-D4-Rezeptor wurde in Verdrängungsbindungsexperimenten wie von Schotte et al. (Psychopharmacology 1996, 124, 57–73) beschrieben, untersucht. Die Verbindungen mit den Nummern 2 bis 4, 6, 8 bis 19, 21, 23, 25, 100, 101, 106, 117 bis 126, 119, 128 bis 130, 134 und 136 bis 147 hatten einen pIC50 größer als oder gleich 7 (der pIC50 ist definiert als der -log IC50, wobei IC50 die Konzentration an Testverbindung ist, die eine 50%ige Inhibierung der Dopamin-D4-Rezeptoren bewirkt). Die übrigen Verbindungen, die im experimentellen Teil zubereitet wurden, wurden entweder nicht getestet oder hatten einen pIC50 kleiner als 7.
- D. Beispiele für Zusammensetzungen
- Der in diesen Beispielen verwendete Begriff „aktive Substanz" (A.S.) bezieht sich auf eine Verbindung der Formel (I), ein pharmazeutisch unbedenkliches Additionssalz oder eine stereochemisch isomere Form davon.
- Beispiel D.1: Kapseln
- 20 Gramm der A.S., 6 Gramm Natriumlaurylsulfat, 56 Gramm Stärke, 56 Gramm Lactose, 0,8 Gramm kolloidales Siliciumdioxid und 1,2 Gramm Magnesiumstearat werden kräftig miteinander verrührt. Die erhaltene Mischung wird anschließend in 1000 geeignete gehärtete Gelatinekapseln gefüllt, die jeweils 20 mg der aktiven Substanz enthielten.
- Beispiel D.2: Lacktabletten
- Herstellung des Tablettenkerns
- Eine Mischung aus A.S. (100 g), Lactose (570 g) und Stärke (200 g) wird gut vermischt und anschließend mit einer Lösung aus Natriumdodecylsulfat (5 g) und Polyvinylpyrrolidon (10 g) in Wasser (200 ml) befeuchtet. Die feuchte Pulvermischung wird gesiebt, getrocknet und nochmals gesiebt. Dann wird mikrokristalline Cellulose (100 g) und hydriertes Pflanzenöl (15 g) zugesetzt. Das Ganze wird gut vermischt und zu Tabletten verpreßt, was 10,000 Tabletten ergibt, die jeweils 10 mg der aktiven Substanz enthalten.
- Überzug
- Eine Lösung von Methylcellulose (10 g) in denaturiertem Ethanol (75 ml) wird mit einer Lösung von Ethylcellulose (5 g) in Dichlormethan (150 ml) versetzt. Anschließend werden Dichlormethan (75 ml) und 1,2,3-Propantriol (2,5 ml) zugesetzt. Polyethylenglykol (10 g) wird geschmolzen und in Dichlormethan (75 ml) gelöst. Nach Zugabe der letztgenannten Lösung zu der erstgenannten werden Magnesiumoctadecanoat (2,5 g), Polyvinylpyrrolidon (5 g) und konzentrierte Farbsuspension (30 ml) zugesetzt, und das Ganze wird homogenisiert. Die Tablettenkerne werden mit der so erhaltenen Mischung in einer Überzugsvorrichtung überzogen.
- Beispiel D.3: Lösung zur oralen Verabreichung
- 9 Gramm 4-Hydroxybenzoesäuremethylester und 1 Gramm 4-Hydroxybenzoesäurepropylester wurden in 4 l kochendem gereinigtem Wasser gelöst. In 3 l dieser Lösung wurden zunächst 10 Gramm 2,3-Dihydroxybutandisäure und anschließend 20 Gramm der A.S. gelöst. Die letztgenannte Lösung wurde mit dem übrigen Teil der ersten Lösung vereinigt und dann mit 12 l 1,2,3-Propantriol und 3 l 70%iger Sorbitlösung versetzt. 40 Gramm Natriumsaccharin wurden in 0,5 l Wasser gelöst und mit 2 ml Himbeeressenz und 2 ml Stachelbeeressenz versetzt. Die letztere Lösung wurde mit der erstgenannten vereinigt und mit q.s. Wasser auf ein Volumen von 20 l aufgefüllt, was eine Lösung zur oralen Verabreichung ergab, die pro Teelöffel voll (5 ml) 5 mg der aktiven Substanz enthielt. Die erhaltene Lösung wurde in geeignete Behälter abgefüllt.
- Beispiel D.4: Injektionslösung
- 1,8 Gramm 4-Hydroxybenzoesäuremethylester und 0,2 Gramm 4-Hydroxybenzoesäurepropylester wurden in etwa 0,5 l kochendem Wasser für Injektionszwecke gelöst. Nach Abkühlen auf ungefähr 50°C wurde die Lösung unter Rühren mit 4 Gramm Milchsäure, 0,05 Gramm Propylenglykol und 4 Gramm der A.S. versetzt. Die Lösung wurde auf Raumtemperatur abgekühlt und mit q.s. Wasser für Injektionszwecke auf ein Volumen von 1 l aufgefüllt, was eine Lösung mit 4 mg A.S. pro ml ergab.
- Die Lösung wurde durch Filtration sterilisiert und in sterile Behälter abgefüllt.
Claims (6)
- Verbindungen der Formel deren N-Oxidformen, deren pharmazeutisch unbedenkliche Säureadditionssalze und deren stereochemisch isomere Formen, wobei X für O oder S steht; n für 2, 3, 4 oder 5 steht; R1 für Wasserstoff, C1–6-Alkyl, C1–6-Alkyloxy oder Halogen steht; R2 für Wasserstoff, C1–6-Alkyl, Phenyl, Phenyl-C1–6-alkyl oder Phenylcarbonyl steht; R3 und R4 jeweils unabhängig voneinander ausgewählt sind aus Wasserstoff, Halogen, Nitro, C1–6-Alkyl, C1–6-Alkyloxy, Halogen-C1–6-Alkyl, Aminosulfonyl, Mono- oder Di-(C1–4-Alkyl) aminosulfonyl; oder R3 und R4 zusammen auch einen zweiwertigen Rest der Formel -CH=CH-CH=CH- bilden können, dadurch gekennzeichnet, daß die Verbindungen wenigstens ein Halogen aufweisen, bei dem es sich um ein radioaktives Isotop von Jod, Brom oder Fluor handelt, oder wenigstens ein 11C-Atom oder Tritiumatom aufweisen.
- Verbindungen nach Anspruch 1, wobei n für 2, 3 oder 4 steht.
- Verbindungen nach Anspruch 1 oder 2, wobei X für S steht und R2 für Wasserstoff, C1–6-Alkyl, Phenyl oder Phenyl-C1–6-Alkyl steht.
- Verbindungen nach Anspruch 1 oder 2, wobei R2 und R3 für Wasserstoff stehen und R4 für Chlor steht.
- Verbindungen nach Anspruch 1, bei denen es sich um N-[2-[4-(3,4-Dichlorphenyl)-1-piperazinyl]ethyl]-2-benzothiazolamin; N-[2-(4-Phenyl-1-piperazinyl)ethyl]-2-benzothiazolamin; N-(2-[4-(4-Chlorphenyl)-1-piperazinyl]ethyl]-2-benzothiazolamin; N-[2-[4-(4-Bromphenyl)-1-piperazinyl]ethyl]-2-benzothiazolamin; ein N-Oxid, eine stereoisomere Form oder ein pharmazeutisch unbedenkliches Säureadditionssalz davon handelt.
- Verfahren zur Markierung eines Dopamin-D4-Rezeptors, bei dem man a) eine Verbindung der Formel (I), eine N-Oxidform, ein pharmazeutisch unbedenkliches Säureadditionssalz oder eine stereochemische isomere Form davon radioaktiv markiert, wobei X für O oder S steht; n für 2, 3, 4 oder 5 steht; R1 für Wasserstoff, C1–6-Alkyl, C1–6-Alkyloxy oder Halogen steht; R2 für Wasserstoff, C1–6-Alkyl, Phenyl, Phenyl-C1–6-alkyl oder Phenylcarbonyl steht; R3 und R4 jeweils unabhängig voneinander ausgewählt sind aus Wasserstoff, Halogen, Nitro, C1–6-Alkyl, C1–6-Alkyloxy, Halogen-C1–6-Alkyl, Aminosulfonyl, Mono- oder Di-(C1–4-Alkyl)aminosulfonyl; oder R3 und R4 zusammen auch einen zweiwertigen Rest der Formel -CH=CH-CH=CH- bilden können; b) diese radioaktiv markierte Verbindung biologischem Material in vitro verabreicht und c) die Emissionen der radioaktiv markierten Verbindung nachweist.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP96201282 | 1996-05-10 | ||
| EP96201282 | 1996-05-10 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| DE69737217D1 DE69737217D1 (de) | 2007-02-15 |
| DE69737217T2 true DE69737217T2 (de) | 2007-11-08 |
Family
ID=8223970
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| DE69730962T Expired - Lifetime DE69730962T2 (de) | 1996-05-10 | 1997-05-02 | Alkylaminobenzothiazole und -benzoxazole derivate |
| DE69737217T Expired - Lifetime DE69737217T2 (de) | 1996-05-10 | 1997-05-02 | Radiomarkierte Alkylamino-benzothiazole und -benzothiazole sowie ihre Verwendung als D4-Liganden |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| DE69730962T Expired - Lifetime DE69730962T2 (de) | 1996-05-10 | 1997-05-02 | Alkylaminobenzothiazole und -benzoxazole derivate |
Country Status (28)
| Country | Link |
|---|---|
| US (2) | US6103725A (de) |
| EP (2) | EP1325917B1 (de) |
| JP (1) | JP3237759B2 (de) |
| KR (1) | KR100330699B1 (de) |
| CN (1) | CN1074766C (de) |
| AR (1) | AR007079A1 (de) |
| AT (2) | ATE350373T1 (de) |
| AU (1) | AU710175B2 (de) |
| BG (1) | BG64097B1 (de) |
| BR (1) | BR9709065A (de) |
| CA (1) | CA2253453C (de) |
| CZ (1) | CZ295639B6 (de) |
| DE (2) | DE69730962T2 (de) |
| EA (1) | EA001360B1 (de) |
| EE (1) | EE03563B1 (de) |
| ES (2) | ES2230605T3 (de) |
| HU (1) | HUP9902993A3 (de) |
| ID (1) | ID16889A (de) |
| IL (1) | IL126968A0 (de) |
| MY (1) | MY117852A (de) |
| NO (1) | NO311027B1 (de) |
| NZ (1) | NZ332309A (de) |
| PL (1) | PL190721B1 (de) |
| SK (1) | SK282919B6 (de) |
| TR (1) | TR199802253T2 (de) |
| TW (1) | TW593290B (de) |
| WO (1) | WO1997043271A1 (de) |
| ZA (1) | ZA974053B (de) |
Families Citing this family (21)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| IT1293804B1 (it) | 1997-08-01 | 1999-03-10 | Recordati Chem Pharm | Diarilalchilpiperazine attive sulle basse vie urinarie |
| US6281216B1 (en) * | 1998-02-09 | 2001-08-28 | Duphar International Research B.V. | 2-aminoquinoline derivatives having d4-agonistic activity |
| EP0982030A3 (de) | 1998-08-17 | 2000-05-10 | Pfizer Products Inc. | 2,7-substituierte Octahydropyrrolo(1,2-a)pyrazinderivate als 5ht 1a Liganden |
| US6284759B1 (en) | 1998-09-30 | 2001-09-04 | Neurogen Corporation | 2-piperazinoalkylaminobenzo-azole derivatives: dopamine receptor subtype specific ligands |
| CN1325397A (zh) * | 1998-09-30 | 2001-12-05 | 纽罗根公司 | 2-哌嗪烷基氨基苯并吡咯衍生物∶多巴胺受体亚型特异配体 |
| US6107313A (en) * | 1998-10-02 | 2000-08-22 | Combichem, Inc. | Dopamine receptor antagonists |
| WO2001000604A1 (fr) * | 1999-06-30 | 2001-01-04 | Santen Pharmaceutical Co., Ltd. | Ligand de liaison avec le recepteur sigma-1 du cerveau |
| US6908929B2 (en) | 2000-03-31 | 2005-06-21 | Ortho-Mcneil Pharmaceutical, Inc. | Phenyl-substituted imidazopyridines |
| WO2001074810A2 (en) * | 2000-03-31 | 2001-10-11 | Ortho Mcneil Pharmaceutical, Inc. | Method for using 2-aryloxyalkylaminobenzoxazoles and 2-aryloxyalkylaminobenzothiazoles as h3 antagonists |
| GB0203299D0 (en) * | 2002-02-12 | 2002-03-27 | Glaxo Group Ltd | Novel compounds |
| WO2004022060A2 (en) * | 2002-09-06 | 2004-03-18 | Janssen Pharmaceutica, N.V. | (1h-benzoimidazol-2-yl)-(piperazinyl)-methanone derivatives and related compounds as histamine h4-receptor antagonists for the treatment of inflammatory and allergic disorders |
| US9017724B2 (en) | 2004-02-24 | 2015-04-28 | The General Hospital Corporation | Catalytic radiofluorination |
| US8257680B1 (en) | 2004-02-24 | 2012-09-04 | The General Hospital Corporation | Catalytic radiofluorination |
| AU2005216949B2 (en) * | 2004-02-24 | 2011-09-22 | The General Hospital Corporation | Catalytic radiofluorination |
| FR2877005A1 (fr) * | 2004-10-22 | 2006-04-28 | Bioprojet Soc Civ Ile | Nouveaux derives d'arylpiperazine |
| US7731940B2 (en) | 2006-01-25 | 2010-06-08 | The Regents Of The University Of California | Compositions and methods related to serotonin 5-HT1A receptors |
| CA2978149C (en) | 2008-03-21 | 2019-02-12 | The General Hospital Corporation | Inositol derivatives for the detection and treatment of alzheimer's disease and related disorders |
| EP3503891A1 (de) * | 2016-08-26 | 2019-07-03 | Bristol-Myers Squibb Company | Inhibitoren der indoleamin-2,3-dioxygenase und verfahren zu deren verwendung |
| PT109740B (pt) | 2016-11-14 | 2020-07-30 | Hovione Farmaciencia Sa | Processo para a preparação de brometo de umeclidínio |
| KR102823891B1 (ko) * | 2020-01-14 | 2025-06-20 | 서울대학교산학협력단 | 혈관생성 저해 효과를 가지는 n-페닐벤조티아졸-2-아민 화합물 및 그를 포함하는 약제학적 조성물 |
| CN116730948A (zh) * | 2022-03-02 | 2023-09-12 | 圣奥化学科技有限公司 | 一种合成n-环己基-2-苯并噻唑的方法 |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4687852A (en) * | 1984-05-22 | 1987-08-18 | Sumitomo Chemical Company, Limited | Radioactive iodospiroperidol |
| AU620327B2 (en) * | 1987-04-08 | 1992-02-20 | Salutar, Inc. | Amyloidosis and alzheimer's disease diagnostic assay and reagents therefor |
| US4929618A (en) * | 1988-03-25 | 1990-05-29 | Ube Industries, Ltd. | Piperdine and piperazine derivatives, and antihistaminic pharmaceutical compositions containing the same |
| FR2656609B1 (fr) * | 1989-12-28 | 1992-03-27 | Synthelabo | Derives de 2-aminopyrimidine-4-carboxamide, leur preparation et leur application en therapeutique. |
| US5731438A (en) * | 1996-08-01 | 1998-03-24 | Isis Pharmaceuticals, Inc. | N-(aminoalkyl)-and/or N-(amidoalkyl)-dinitrogen heterocycles |
-
1997
- 1997-05-01 TW TW086105767A patent/TW593290B/zh not_active IP Right Cessation
- 1997-05-02 DE DE69730962T patent/DE69730962T2/de not_active Expired - Lifetime
- 1997-05-02 PL PL97329849A patent/PL190721B1/pl not_active IP Right Cessation
- 1997-05-02 US US09/180,369 patent/US6103725A/en not_active Expired - Lifetime
- 1997-05-02 EP EP03075959A patent/EP1325917B1/de not_active Expired - Lifetime
- 1997-05-02 AT AT03075959T patent/ATE350373T1/de not_active IP Right Cessation
- 1997-05-02 CZ CZ19983553A patent/CZ295639B6/cs not_active IP Right Cessation
- 1997-05-02 DE DE69737217T patent/DE69737217T2/de not_active Expired - Lifetime
- 1997-05-02 ES ES97923913T patent/ES2230605T3/es not_active Expired - Lifetime
- 1997-05-02 TR TR1998/02253T patent/TR199802253T2/xx unknown
- 1997-05-02 KR KR1019980707914A patent/KR100330699B1/ko not_active Expired - Fee Related
- 1997-05-02 WO PCT/EP1997/002505 patent/WO1997043271A1/en not_active Ceased
- 1997-05-02 HU HU9902993A patent/HUP9902993A3/hu unknown
- 1997-05-02 CA CA002253453A patent/CA2253453C/en not_active Expired - Fee Related
- 1997-05-02 ES ES03075959T patent/ES2279923T3/es not_active Expired - Lifetime
- 1997-05-02 SK SK1532-98A patent/SK282919B6/sk not_active IP Right Cessation
- 1997-05-02 NZ NZ332309A patent/NZ332309A/xx unknown
- 1997-05-02 CN CN97194515A patent/CN1074766C/zh not_active Expired - Lifetime
- 1997-05-02 EP EP97923913A patent/EP0912533B1/de not_active Expired - Lifetime
- 1997-05-02 JP JP54053597A patent/JP3237759B2/ja not_active Expired - Lifetime
- 1997-05-02 EE EE9800378A patent/EE03563B1/xx not_active IP Right Cessation
- 1997-05-02 BR BR9709065A patent/BR9709065A/pt not_active IP Right Cessation
- 1997-05-02 EA EA199801000A patent/EA001360B1/ru not_active IP Right Cessation
- 1997-05-02 AT AT97923913T patent/ATE277917T1/de not_active IP Right Cessation
- 1997-05-02 AU AU29560/97A patent/AU710175B2/en not_active Ceased
- 1997-05-02 IL IL12696897A patent/IL126968A0/xx not_active IP Right Cessation
- 1997-05-07 MY MYPI97002022A patent/MY117852A/en unknown
- 1997-05-09 AR ARP970101955A patent/AR007079A1/es active IP Right Grant
- 1997-05-09 ZA ZA974053A patent/ZA974053B/xx unknown
- 1997-05-09 ID IDP971546A patent/ID16889A/id unknown
-
1998
- 1998-10-07 BG BG102819A patent/BG64097B1/bg unknown
- 1998-11-09 NO NO19985227A patent/NO311027B1/no unknown
-
2000
- 2000-06-27 US US09/604,427 patent/US6224849B1/en not_active Expired - Lifetime
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| DE69737217T2 (de) | Radiomarkierte Alkylamino-benzothiazole und -benzothiazole sowie ihre Verwendung als D4-Liganden | |
| DE69728768T2 (de) | 2,4-diaminopyrimidine derivates als dopamine d4 rezeptorantagonisten | |
| DE60132777T2 (de) | Benzothiazolderivate zur behandlung von alzheimer und parkinson | |
| DE60206652T2 (de) | Benzothiazolderivate als adenosin-rezeptor-liganden | |
| DE69815700T2 (de) | Tetrahydro gamma-carboline | |
| DE69332636T2 (de) | Antidepressiv und gegen die Parkinsonsche Krankheit wirkende Verbindungen | |
| DE69824872T2 (de) | 1,2,3,4-tetrahydro-benzofuro[3,2-c]pyridin derivate | |
| DE69720317T2 (de) | Benzoxazole Derivate als Serotonin 5-HT3 Rezeptor partiell Aktivator | |
| DE60212694T2 (de) | Benzothiazolderivaten | |
| DD283996A5 (de) | Verfahren zur herstellung von aminoderivaten | |
| DE69332366T2 (de) | Arylsubstituierte heterocyclische Verbindungen | |
| DE69329184T2 (de) | Alkylsubstituierte heterocyclische Verbindungen | |
| DE69610104T2 (de) | Kondensierte thiazol-derivate, mit 5-ht-rezeptor affinität | |
| DE602004012388T2 (de) | Benzoxazolderivate und deren verwendung als adenosinrezeptorliganden | |
| DE60309324T2 (de) | Tetracyclische arylcarbonyl indole mit serotoninrezeptoraffinität als arzneimittel, verfahren zu ihrer herstellung und pharmazeutische zubereitungen | |
| DE69918148T2 (de) | Trizyclische delta3-pyridine als arzneimittel | |
| DE69629931T2 (de) | 1-(hetero)aryl-4-(kondensiertes thiazol-2-ylalkyl)-piperazin derivate, deren herstellung und deren verwendung in der behandlung von 5-ht1a-rezeptor vermittelten krankheiten | |
| EP0589903B1 (de) | Aminoalkylsubstituierte 5-mercaptothiazole, ihre herstellung und verwendung | |
| DE602004008447T2 (de) | 7-(ä1,4üdioxan-2-yl)-benzothiazol derivative als adenosin-rezeptoren liganden | |
| DE69320420T2 (de) | Benzyl- und Benzhydryl Alkohole | |
| DE69936219T2 (de) | Benzothieno[3,2-c]pyridine als alpha2-antagonisten | |
| HK1057044B (en) | Radiolabelled alkylamino-benzothiazole and -benzoxazole derivatives and their use as d4 ligands | |
| AT377512B (de) | Verfahren zum herstellen neuer 4-(naphthyloxy)-piperidinderivate und von deren salzen | |
| HK1018457B (en) | Alkylaminobenzothiazole and-benzoxazole derivatives | |
| DE3508947A1 (de) | Mittel zur behandlung des parkinsonismus bzw. der parkinsonschen-erkrankung |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 8381 | Inventor (new situation) |
Inventor name: KENNIS, LUDO E. J., BEERSE, BE Inventor name: MERTENS, JOSEPHUS C., BEERSE, BE Inventor name: PIETERS, SERGE M. A., BEERSE, BE |
|
| 8364 | No opposition during term of opposition |