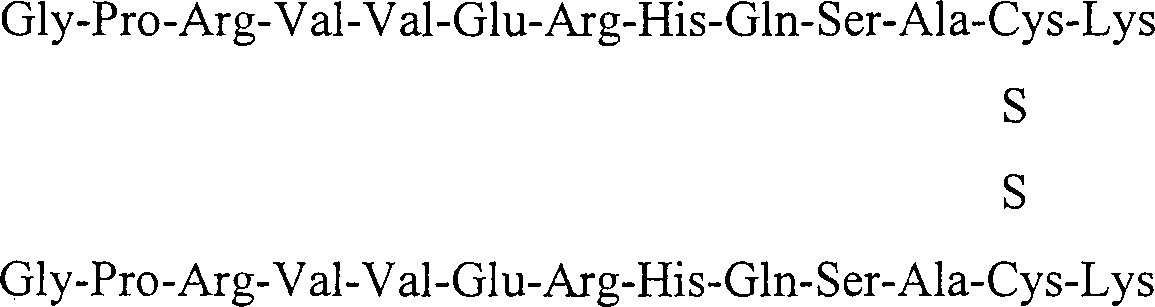DE69736780T2 - Polypeptide mit einzelnem kovalent gebundenen n-terminalen wasserlöslichen polymer - Google Patents
Polypeptide mit einzelnem kovalent gebundenen n-terminalen wasserlöslichen polymer Download PDFInfo
- Publication number
- DE69736780T2 DE69736780T2 DE69736780T DE69736780T DE69736780T2 DE 69736780 T2 DE69736780 T2 DE 69736780T2 DE 69736780 T DE69736780 T DE 69736780T DE 69736780 T DE69736780 T DE 69736780T DE 69736780 T2 DE69736780 T2 DE 69736780T2
- Authority
- DE
- Germany
- Prior art keywords
- polypeptide
- peg
- epo
- terminal
- derivative
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Lifetime
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K1/00—General methods for the preparation of peptides, i.e. processes for the organic chemical preparation of peptides or proteins of any length
- C07K1/107—General methods for the preparation of peptides, i.e. processes for the organic chemical preparation of peptides or proteins of any length by chemical modification of precursor peptides
- C07K1/1072—General methods for the preparation of peptides, i.e. processes for the organic chemical preparation of peptides or proteins of any length by chemical modification of precursor peptides by covalent attachment of residues or functional groups
- C07K1/1077—General methods for the preparation of peptides, i.e. processes for the organic chemical preparation of peptides or proteins of any length by chemical modification of precursor peptides by covalent attachment of residues or functional groups by covalent attachment of residues other than amino acids or peptide residues, e.g. sugars, polyols, fatty acids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/56—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule
- A61K47/59—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyureas or polyurethanes
- A61K47/60—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyureas or polyurethanes the organic macromolecular compound being a polyoxyalkylene oligomer, polymer or dendrimer, e.g. PEG, PPG, PEO or polyglycerol
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/475—Growth factors; Growth regulators
- C07K14/505—Erythropoietin [EPO]
Landscapes
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Genetics & Genomics (AREA)
- Molecular Biology (AREA)
- Biophysics (AREA)
- Biochemistry (AREA)
- Veterinary Medicine (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Pharmacology & Pharmacy (AREA)
- Engineering & Computer Science (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Epidemiology (AREA)
- Analytical Chemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Toxicology (AREA)
- Zoology (AREA)
- Gastroenterology & Hepatology (AREA)
- Peptides Or Proteins (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Other Resins Obtained By Reactions Not Involving Carbon-To-Carbon Unsaturated Bonds (AREA)
- Medicinal Preparation (AREA)
- Addition Polymer Or Copolymer, Post-Treatments, Or Chemical Modifications (AREA)
Description
- Gebiet der Erfindung
- Die vorliegende Erfindung betrifft Polypeptide, an deren N-Termini ein einzelnes wasserlösliches Polymer gebunden ist. Diese Polypeptide haben Eigenschaften, die sie für die Verwendung als Pharmazeutika und Diagnostika vorteilhaft machen. Die Erfindung betrifft außerdem Verfahren zum Herstellen dieser Polypeptide und zugehörige pharmazeutische Zusammensetzungen und Kits.
- Allgemeiner Stand der Technik
- Überall in dieser Anmeldung werden verschiedene Veröffentlichungen zitiert. Die Offenbarung dieser Veröffentlichungen ist hiermit durch Bezugnahme in die Anmeldung aufgenommen, um den Stand der Technik vollständiger zu beschreiben, den diese Erfindung betrifft.
- In der jüngsten Vergangenheit wurden nichtantigene wasserlösliche Polymere, wie Polyethylenglykol („PEG"), für die kovalente Modifikation von Polypeptiden von therapeutischer und diagnostischer Bedeutung verwendet. Zum Beispiel wurde von kovalenter Anlagerung von PEG an therapeutische Polypeptide, wie Interleukine (M.J. Knauf et al., J. Biol. Chem. 1988, 263, 15 064; Y. Tsutsumi et al., J. Controlled Release 1995, 33, 447), Interferone (Y. Kita et al., Drug Des. Delivery 1990, 6, 157) Katalase (A. Abuchowski et al., J. Biol. Chem. 1977, 252, 3 582), Superoxiddismutase (C.O. Beauchamp et al., Anal. Biochem. 1983, 131, 25) und Adenosindeaminase (R. Chen et al., Biochim. Biophy. Acta 1981, 660, 293), berichtet, um ihre Halbwertzeiten in vivo zu verlängern und/oder ihre Immunogenität und Antigenität zu reduzieren.
- Solche Verfahren haben jedoch beträchtliche Nachteile. Speziell werden PEG-Moleküle in den meisten Fällen mittels Aminogruppen unter Verwendung von methoxyliertem PEG („mPEG") mit unterschiedlichen reaktionsfähigen Gruppen an Polypeptiden angelagert. Zu solchen Polymeren zählen mPEG-Succinimidylsuccinat, mPEG-Succinimidylcarbonat, mPEG-Imidat und mPEG-Cyanurchlorid. Die Anlagerung unter Verwendung dieser Polymere war gewöhnlich unspezifisch, d. h. erfolgte auf zufällige Weise an verschiedenen Aminogruppen an den Polypeptiden und nicht ausschließlich an einer bestimmten Aminogruppe. Eine solche unspezifische Anlagerung kann Aminosäurereste an aktiven Orten derart modifizieren, dass die biologische Aktivität der Polypeptide eliminiert wird. Zudem können die resultierenden Konjugate eine heterogene Mischung von modifizierten Polypeptiden enthalten, was für die pharmazeutische Verwendung nicht wünschenswert ist.
- Um diese Probleme zu überwinden, war es wünschenswert, ein Polymer ortsspezifisch an ein Polypeptid anzulagern. Bei dem Polypeptid würde eine solche Vorgehensweise die biologische Aktivität bewahren, die Blutzirkulationszeit verlängern, die Immunogenität reduzieren, die Wasserlöslichkeit erhöhen und die Beständigkeit gegenüber Proteaseverdauung fördern. Ortsspezifische Pegylierung am N-Terminus, an der Seitenkette und am C-Terminus eines potenten Analogons von Somatotropin-releasing-Faktor wurde mittels Festphasensynthese durchgeführt (A.M. Felix et al., Int. J. Peptide Protein Res. 1995, 46, 253). Da die spezifische Pegylierung während der Anordnung des Peptids an einem Harz erzielt wurde, kann das Verfahren nicht auf ein existierendes Peptid angewendet werden.
- Ein weiteres verwendetes Verfahren schloss das Anlagern eines Peptids an Enden von liposomalen, auf die Oberfläche gepfropften PEG-Ketten in einer ortsspezifischen Weise mittels einer reaktionsfähigen Aldehydgruppe am N-Terminus ein, die durch Natriumperiodat-Oxidation von N-terminalem Threonin erzeugt wurde (S. Zalipsky et al., Bioconj. Chem. 1995, 6, 705). Dieses Verfahren ist jedoch auf Polypeptide mit N-terminalen Serin- oder Threoninresten beschränkt.
- Enzymunterstützte Verfahren zum Einführen von aktivierten Gruppen speziell am C-Terminus eines Polypeptids wurden ebenfalls beschrieben (A. Schwarz et al., Methods Enzymol. 1990, 184, 160; K. Rose et al., Bioconjugate Chem. 1991, 2, 154; H.F. Gaertner et al., J. Biol. Chem. 1994, 269, 7 224). In der Regel können diese aktiven Gruppen Hydrazid-, Aldehyd- und aromatische Aminogruppen zur anschließenden Anlagerung von funktionellen Sonden an Polypeptiden sein. Da die Verfahren jedoch auf der Spezifität von Proteasen basieren, bedingen sie äußerste Vorsicht und der Umfang ihrer Anwendung ist begrenzt.
- Ortsspezifische Mutagenese ist ein weiterer Ansatz, der zum Herstellen von Polypeptiden zur ortsspezifischen Anlagerung an Polymeren verwendet wurde. WO 90/12874 beschreibt ortsgerichtete Pegylierung von Proteinen, die durch die Insertion von Cysteinresten oder die Substitution von anderen Resten durch Cysteinreste modifiziert wurden. Diese Veröffentlichung beschreibt außerdem die Herstellung von mPEG-Erythropoetin („mPEG-EPO") durch Umsetzen eines cysteinspezifischen mPEG-Derivats mit einem rekombinant eingeführten Cysteinrest an EPO. In ähnlicher Weise wurde Interleukin-2 an seinem Glykosylierungsort nach einer ortsgerichteten Mutagenese pegyliert (R.J. Goodson et al., Bio/Technology 1990, 8, 343).
- Glykoproteine stellen Kohlenhydrate als zusätzliche Zielorte zur Modifikation bereit. Das Enzym Peroxidase wurde mit PEG-Diamin über seine Kohlenhydratgruppe modifiziert (M. Urrutiogoity et al., Biocatalysis 1989, 2, 145). WO 94/28024 beschreibt die Verfahren zum Herstellen von mPEG-EPO durch periodatoxidiertes Kohlenhydrat. Die involvierte Chemie war Hydrazonbildung durch Umsetzen von mPEG-Hydrazid mit Aldehydgruppen der Kohlenhydratgruppe an EPO. Diese Art von Modifikation erzeugt reaktionsfähige Aldehydgruppen durch einen Oxidationsschritt, die potentiell verschiedene Arten von Zuckerresten in der Kohlenhydratgruppe und einige Aminosäurereste in dem Polypeptid, wie Methionin, oxidieren können. Ein weiterer Nachteil dieses Verfahrens rührt von der Heterogenität der Kohlenhydratgruppen von EPO her. Aus Eierstockzellen des Chinesischen Hamsters exprimiertes EPO weist vier Kohlenhydratketten auf, die drei N-verknüpfte Ketten an den Asparaginen 24, 38 und 83 und eine O-verknüpfte Kette am Serin 126 beinhaltet. Insgesamt 52 unterschiedliche N-verknüpfte und mindestens 6 O-verknüpfte Oligosaccharidstrukturen wurden identifiziert (R.S. Rush et al., Anal. Chem. 1995, 67, 1 442; K.B. Linsley et al., Anal. Biochem. 1994, 219, 207). Dementsprechend ist es schwierig, die Anzahl oder Anlagerungsorte von Polymermolekülen zu kontrollieren, wenn EPO oder ein anderes Protein über seine Kohlenhydratketten modifiziert wird.
- Kurz gesagt, die Verfahren in der Technik zum Anlagern eines wasserlöslichen Polymers an ein Polypeptid leiden unter beträchtlichen Nachteilen. Diese Nachteile beinhalten die folgenden: (a) ein Mangel an Präzision, sowohl stöchiometrisch als auch bezüglich des Anlagerungssitus; (b) das Erfordernis, schwierige und laborintensive Techniken wie ortsspezifische Mutagenese durchzuführen; (c) das Erfordernis, Festphasenpeptidsynthese gleichzeitig mit Polymeranlagerung anzuwenden, anstatt ein Polymer an einem vorher vorhandenen Polypeptid anzulagern; und (d) das unumstößliche Erfordernis, dass die Identität des N-terminalen Aminosäurerests Threonin oder Serin sein muss.
- Seit einiger Zeit hat Bedarf an einem allgemeinen Verfahren zum ortsspezifischen Anlagern eines wasserlöslichen Polymers an dem N-terminalen Aminosäurerest eines Polypeptids bestanden, wobei dieses Verfahren nicht unter den oben identifizierten Nachteilen leidet. Ein solches Verfahren gibt es jedoch nicht.
- Zusammenfassung der Erfindung
- Diese Erfindung stellt zwei Stoffzusammensetzungen bereit. Die erste Stoffzusammensetzung besteht im wesentlichen aus einem Polypeptid und einem wasserlöslichen Polymer, kovalent über eine Hydrazonbindung oder reduzierte Hydrazonbindung an dem N-terminalen α-Kohlenstoffatom des Polypeptids gebunden, unter der Bedingung, dass (a) das Polymer ein Molekulargewicht von 700 bis 20 000 Daltons hat, (b) die natürliche Funktion des Polypeptids bei Entfernung seiner N-terminalen α-Aminogruppe nicht eliminiert wird, und (c) der N-terminale Aminosäurerest des Polypeptids nicht Serin oder Threonin ist.
- Diese Erfindung stellt auch vier Verfahren zum kovalenten Binden eines wasserlöslichen Polymers an das N-terminale α-Kohlenstoffatom eines Polypeptids bereit. Das erste Verfahren, das das Polymer über eine Hydrazonbindung an das Kohlenstoffatom bindet, umfasst die Schritte:
- (a) In-Kontakt-Bringen des Polypeptids mit (i) einem Glyoxylation oder einem Derivat davon in einer Konzentration von 0,1 M bis 2,0 M, (ii) einem Übergangsmetallion in einer Konzentration von 10 μM bis 1 M und (iii) einer Lewis-Base in einer Konzentration von 10 mM bis 10 M, bei einem pH von 5,0 bis 7,0 und einer Temperatur von 0°C bis 100°C, um ein transaminiertes Polypeptid mit einer N-terminalen α-Carbonylgruppe zu bilden; und
- (b) In-Kontakt-Bringen des transaminierten Polypeptids bei einem pH von 3,0 bis 5,0 mit einem wasserlöslichen Polymer, das eine daran kovalent gebundene Gruppe hat, die mit der N-terminalen α-Carbonylgruppe des transaminierten Polypeptids reagiert, um eine Hydrazonbindung zu bilden, wodurch das Polymer über eine Hydrazonbindung an das N-terminale α-Kohlenstoffatom des Polypeptids kovalent gebunden wird, unter der Bedingung, dass das PEG ein Molekulargewicht von 700 bis 20 000 Daltons hat und die natürliche Funktion des Polypeptids bei Entfernen seiner N-terminalen α-Aminogruppe nicht eliminiert wird.
- Diese Erfindung stellt auch eine pharmazeutische Zusammensetzung bereit, die eine wirksame Menge der vorliegenden ersten Zusammensetzung und einen pharmazeutisch akzeptablen Träger umfasst.
- Schließlich stellt diese Erfindung Kits zur Verwendung beim Herstellen der vorliegenden Zusammensetzungen bereit. Das erste Kit zum Herstellen der ersten vorliegenden Zusammensetzung umfasst folgendes:
- (a) ein Glyoxylation oder Derivat davon;
- (b) ein Übergangsmetallion;
- (c) eine Lewis-Base; und
- (d) ein wasserlösliches Polymer mit einem Molekulargewicht von 700 bis 20 000 Daltons und mit einer kovalent angebundenen Gruppe, die mit einer N-terminalen α-Carbonylgruppe des transaminierten Polypeptids reagiert, um eine Hydrazonbindung zu bilden, wodurch das Polymer an das N-terminale α-Kohlenstoffatom des Polypeptids kovalent gebunden wird.
- Kurzbeschreibung der Figuren
-
1 zeigt ein Schema zum Herstellen von N-terminalem modifiziertem EPO. Dabei handelt es sich um eine Reaktion mit zwei Schritten: Transaminierung und Pegylierung. Vier mPEG5000-Derivate (d. h. mPEG mit einem MG von 5 000 Daltons) mit funktionellen Hydrazincarboxylat-(HZC), Hydrazid-(HZ), Semicarbazid-(SCZ) und Oxylamingruppen wurden verwendet. -
2 zeigt das Gelfiltrationschromatogramm von mPEG-EPO mit einer Hydrazonbindung, die unter Verwendung einer Hydrazincarboxylatgruppe (HZC-Gruppe) gebildet wurde, nativem EPO und mPEG5000-Hydrazincarboxylat auf einer TSK-G3000SWXL-Säule (7,5 × 30 mm). Die mobile Phase ist 20 mM Natriumcitrat (pH 7,0), das 100 mM NaCl enthält. -
3 zeigt ein matrixunterstütztes Laserdesorptionslaufzeitmassenspektrum von mPEG5000-Hydrazincarboxylat, nativem EPO und mPEG-EPO mit einer Hydrazonbindung, die unter Verwendung einer Hydrazincarboxylatgruppe (HZC-Gruppe) gebildet wurde. -
4 zeigt die Charakterisierung von mPEG-EPO mittels Elektrophoreseverfahren: (1) 4-15%-ige SDS-PAGE, Coomassie-Färbung; (2) Western-Blot; (3) 4-15%-ige SDS-PAGE, Iodfärbung und (4) isoelektrische Fokussierung (IEF, pH 3-7). Spur 1: MG- oder pI-Markierungen; Spur 2: natives EPO; Spur 3: transaminiertes EPO und Spuren 4 und 5: mPEG-EPO mit Hydrazonbindungen, die unter Verwendung von Hydrazincarboxylatgruppen (HZC-Gruppen) bzw. Hydrazidgruppen (HZ-Gruppen) gebildet wurden. -
5 zeigt einen Graph von Ergebnissen eines ELISA-Assays für mPEG-EPO mit Hydrazonbindungen, die unter Verwendung von Hydrazincarboxylatgruppen (HZC-Gruppen) und Hydrazidgruppen (HZ-Gruppen) gebildet wurden. -
6 zeigt einen Graph der Ergebnisse eines Zellproliferationsassays von nativem EPO, transaminiertem EPO und mPEG-EPO mit Hydrazonbindungen, die unter Verwendung von Hydrazincarboxylatgruppen (HZC-Gruppen) und Hydrazidgruppen (HZ-Gruppen) gebildet wurden. -
7 zeigt einen Graph von Ergebnissen eines Bioassays an exhypoxischen Mäusen für mPEG-EPO mit Hydrazonbindungen, die unter Verwendung von Hydrazincarboxylatgruppen (HZC-Gruppen), Hydrazidgruppen (HZ-Gruppen) und Semicarbazidgruppen (SCZ-Gruppen) gebildet wurden. - Ausführliche Beschreibung der Erfindung
- Diese Erfindung stellt zwei Stoffzusammensetzungen bereit. Die erste Stoffzusammensetzung besteht im wesentlichen aus einem Polypeptid und einem wasserlöslichen Polymer, kovalent über eine Hydrazonbindung oder reduzierte Hydrazonbindung an dem N-terminalen α-Kohlenstoffatom des Polypeptids gebunden, unter der Bedingung, dass (a) das Polymer ein Molekulargewicht von 700 bis 20 000 Daltons hat, (b) die natürliche Funktion des Polypeptids bei Entfernung seiner N-terminalen α-Aminogruppe nicht eliminiert wird, und (c) der N-terminale Aminosäurerest des Polypeptids nicht Serin oder Threonin ist.
- Wie hierin verwendet, beinhaltet „Polypeptid" sowohl Peptide als auch Proteine. „Peptid" steht für ein Polypeptid, das weniger als 10 Aminosäurereste lang ist, und „Protein" steht für ein Polypeptid, das 10 oder mehr Aminosäurereste lang ist. In dieser Erfindung können die Polypeptide natürlich vorkommen oder rekombinant sein (d. h. mittels rekombinanter DNA-Technologie produziert) und können Mutationen (z. B. Punkt-, Insertions- und Deletionsmutationen) als auch andere kovalente Modifikationen (z. B. Glykosylierung und Markierung [über Biotin, Streptavidin, Fluoracin und Radioisotope wie [131]) enthalten. Darüber hinaus kann jede vorliegende Zusammensetzung mehr als ein einzelnes Polypeptid enthalten, d. h. jedes kann ein Monomer (ein an ein Polymer gebundenes Polypeptid) oder ein Multimer (zwei oder mehr an ein Polymer oder aneinander gebundene Polypeptide) sein.
- Zu Polypeptiden zählen beispielsweise monoklonale und polyklonale Antikörper, Cytokine, wie M-CSF und GM-CSF, Lymphokine, IL-2, IL-3, Wachstumsfaktoren, wie PDGF und EGF, Peptidhormone, wie hGH, EPO und Derivate davon, Blutgerinnungsfaktoren, wie Faktor VIII, Immungene, Enzyme, Enzyminhibitoren und andere Liganden. In der bevorzugten Ausführungsform der vorliegenden Zusammensetzungen ist das Polypeptid EPO oder ein Derivat davon. Das EPO kann natürlich vorkommen oder rekombinant sein. Derivate von EPO beinhalten, sind aber nicht darauf beschränkt, die Polypeptide
GGLYLCRFGPVTWDCGYKGG,
GGTYSCHFGPLTWVCKPQGG,
GGDYHCRMGPLTWVCKPLGG,
VGNYMCHFGPITWVCRPGGG,
GGVYACRMGPITWVCSPLGG,
VGNYMAHMGPITWVCRPGG,
GGTYSCHFGPLTWVCKPQ,
GGLYACHMGPMTWVCQPLRG,
TIAQYICYMGPETWECRPSPKA,
YSCHFGPLTWVCK und
YCHFGPLTWVC
sowie die in Tabelle 1 unten aufgeführten Mutationen. Tabelle 1 -
- ++++ = Wildtyp- oder bessere Aktivität
- +++ = ca. 75% der Wildtyp-Aktivität
- ++ = ca. 50% der Wildtyp-Aktivität
- + = ca. 25% der Wildtyp-Aktivität
- +/– = Mutanten-EPO als aktiv angegeben, Daten jedoch nicht vollständig zur Einschätzung der Aktivität in Bezug auf den Wildtyp.
- Zitierte Literaturhinweise
-
- (1) K. Akai, K. Yamaguchi und M. Ueda, Modified forms of
human erythropoietin and DNA sequences encoding genes which can
express them,
EP 0427 189 A1 . - (2) T. Bittorf, R. Jaster und J. Brock (1993), FEBS Letts. 336: 133-136.
- (3) Ergebnisse von H.F. Bunn et al.
- (4) T.E. Byrne und S.G. Elliott, Erythropoietin isoforms,
EP 0 668 351 A1 . - (5) Y. Chern, T. Chung und A.J. Sytkowski (1991), Eur. J. Biochem. 202: 225-229.
- (6) A. Funakoshi, H. Muta, T. Baba und S. Shimizu (1993), Biochem. Biophys. Res. Commun. 195: 717-722.
- (7) G. Okasinski, P.J. Devries, B.S. Mellovitz, J.L. Meuth und V.G. Schaefer, Erythropoietin analog compositions and methods, WO 94/25055.
- (8) J. Grodberg, K.L. Davis und A.J. Sytkowski (1993), Eur. J. Biochem. 218: 597-601.
- (9) Ergebnisse von V. Pulito et al.
- (10) C.B. Shoemaker, Erythropoietin composition,
U.S. 4,835,260 . - Wie hierin verwendet, steht die „natürliche Funktion" eines Polypeptids für seine Funktion vor der kovalenten Modifikation seiner N-terminalen α-Aminogruppe. Zu natürlichen Funktionen zählen beispielsweise enzymatische Aktivität, Rezeptorbindung (z. B. Antikörper), Ligandenbindung und Immunogenität.
- Die unten vollständiger beschriebenen vorliegenden Verfahren bewirken den Verlust der N-terminalen α-Aminogruppe des Polypeptids, das kovalent modifiziert wird. Demgemäß muss das Polypeptid eine derartige primäre Struktur aufweisen, dass seine natürliche Funktion nach der kovalenten Modifikation bewahrt wird und nicht eliminiert werden kann. Die natürliche Funktion des Polypeptids wird durch die Entfernung seiner N-terminalen α-Aminogruppe „eliminiert", wenn eine solche Entfernung die Fähigkeit des Polypeptids, seine natürliche Funktion auszuüben, um mehr als 99% reduziert. In einer Ausführungsform reduziert die Entfernung die Fähigkeit des Polypeptids, seine natürliche Funktion auszuüben, nicht um mehr als 90%. In der bevorzugten Ausführungsform reduziert die Entfernung die Fähigkeit des Polypeptids, seine natürliche Funktion auszuüben, nicht um mehr als 50%.
- Wie hierin verwendet, ist eine „Hydrazonbindung" eine Bindung, die die kovalente Struktur NH-N=C umfasst, und eine „reduzierte Hydrazonbindung" ist eine Bindung, die die kovalente Struktur NH-NH-C umfasst. Hierin sind Verbindungen, die reduzierte Hydrazonbindungen umfassen, bereitgestellt, da diese Bindungen über eine größere chemische Beständigkeit verfügen.
- Wie oben erörtert, sind in der Technik Verfahren zum Binden von wasserlöslichen Polymeren an das N-terminale α-Kohlenstoffatom eines Polypeptids über eine Hydrazonbindung bekannt, solange der N-terminale Aminosäurerest Serin oder Threonin ist. Diese bekannten Verfahren werden nicht mit Polypeptiden mit einem beliebigen anderen N-terminalen Rest funktionieren. Obgleich sich diese bekannten Verfahren grundlegend von den vorliegenden Verfahren unterscheiden, resultieren sie in N-terminalen Serin- und Threonin-Polypeptiden mit einem Polymer, das über eine Hydrazonbindung an das N-terminale α-Kohlenstoffatom gebunden ist. Aus diesem Grund umfasst die vorliegende erste Zusammensetzung nicht ein Polypeptid, das über eine Hydrazonbindung an ein Polymer gebunden ist, wobei der N-terminale Aminosäurerest des Polypeptids Serin oder Threonin ist.
- Zu den in der vorliegenden Erfindung verwendeten wasserlöslichen Polymeren zählen Polyalkylenglykol und Derivate davon, einschließlich PEG, mPEG, PEG-Homopolymere, Polypropylenglykol-Homopolymere, Copolymere von Ethylenglykol mit Propylenglykol, wobei die Homopolymere und Copolymere unsubstituiert oder an einem Ende mit einer Alkylgruppe substituiert sind. Diese Polymere können linear, verzweigt oder sternförmig mit einer großen Auswahl von Molekulargewichten sein. In der bevorzugten Ausführungsform ist das Polymer mPEG.
- Wenn die vorliegenden Zusammensetzungen als Pharmazeutika verwendet werden sollen, ist das Polymer nichttoxisch. Des Weiteren, wenn von einem Polymer gesagt wird, dass es ein gegebenes Molekulargewicht hat, kann dieses Molekulargewicht nur ungefähr sein, wobei es das durchschnittliche Molekulargewicht eines Bestands von Polymermolekülen widerspiegelt, die sich in Bezug auf einander hinsichtlich der Anzahl der in jedem Molekül vorhandenen Untereinheiten unterscheiden.
- In der bevorzugten Ausführungsform hat das PEG oder Derivat davon ein Molekulargewicht von etwa 5 000 Daltons. Außerdem ist das Polypeptid in der bevorzugten Ausführungsform der vorliegenden Zusammensetzungen EPO und das Polymer ist mPEG mit einem Molekulargewicht von etwa 5 000 Daltons.
- Diese Erfindung stellt auch vier Verfahren zum kovalenten Binden eines wasserlöslichen Polymers an das N-terminale α-Kohlenstoffatom eines Polypeptids bereit. Das erste Verfahren, das das Polymer über eine Hydrazonbindung an das Kohlenstoffatom bindet, umfasst die Schritte:
- a) In-Kontakt-Bringen des Polypeptids mit (i) einem Glyoxylation oder einem Derivat davon in einer Konzentration von 0,1 M bis 2,0 M, (ii) einem Übergangsmetallion in einer Konzentration von 10 μM bis 1 M und (iii) einer Lewis-Base in einer Konzentration von 10 mM bis 10 M, bei einem pH von 5,0 bis 7,0 und einer Temperatur von 0°C bis 100°C, um ein transaminiertes Polypeptid mit einer N-terminalen α-Carbonylgruppe zu bilden; und
- b) In-Kontakt-Bringen des transaminierten Polypeptids bei einem pH von 3,0 bis 5,0 mit einem wasserlöslichen Polymer, das eine daran kovalent gebundene Gruppe hat, die mit der N-terminalen α-Carbonylgruppe des transaminierten Polypeptids reagiert, um eine Hydrazonbindung zu bilden, wodurch das Polymer über eine Hydrazonbindung an das N-terminale α-Kohlenstoffatom des Polypeptids kovalent gebunden wird, unter der Bedingung, dass das PEG ein Molekulargewicht von 700 bis 20 000 Daltons hat und die natürliche Funktion des Polypeptids bei Entfernen seiner N-terminalen α-Aminogruppe nicht eliminiert wird.
- Das dritte Verfahren umfasst die Schritte des ersten Verfahrens als auch einen weiteren Schritt des Reduzierens der in Schritt (b) gebildeten Hydrazonbindung. Der Reduzierungsschritt kann gemäß bekannten Verfahren unter Verwendung von beispielsweise Natriumtetrahydridoborat (NaBH4) und Natriumcyanoborhydrid (NaBH3CN) durchgeführt werden.
- Glyoxylationderivate beinhalten, sind aber nicht darauf beschränkt, Glyoxylamid- und Phenylglyoxylionen. Übergangsmetallionen beinhalten, sind aber nicht darauf beschränkt, Kupfer(II)-, Nickel(II)-, Cobalt(II)- und Zink(II)-Ionen. Lewis-Basen beinhalten, sind aber nicht darauf beschränkt, Acetat und Pyridin.
- Gruppen, die mit der N-terminalen α-Carbonylgruppe des transaminierten Polypeptids reagieren, um eine Hydrazonbindung zu bilden, beinhalten, sind aber nicht darauf beschränkt, Hydrazincarboxylat, Hydrazin, Semicarbazid, Hydrazid, Thiosemicarbazid, Kohlensäuredihydrazid, Carbazid, Thiocarbazid und Arylhydrazid. Wasserlösliche Polymere mit diesen Gruppen, die kovalent daran gebunden sind, sind im Handel erhältlich. Darüber hinaus beinhalten Gruppen, die mit der N-terminalen α-Carbonylgruppe des transaminierten Polypeptids reagieren, um eine Oximbindung zu bilden, Oxylamin, sind aber nicht darauf beschränkt. Wasserlösliche Polymere mit Oxylamin (sowie andere oximbildende Gruppen), die kovalent daran gebunden sind, sind im Handel erhältlich.
- In der bevorzugten Ausführungsform der vorliegenden Verfahren ist das Protein EPO oder ein Derivat davon.
- In der bevorzugten Ausführungsform hat das PEG oder das Derivat davon ein Molekulargewicht von etwa 5 000 Daltons.
- In einer Ausführungsform des ersten Verfahrens ist die Gruppe, die an das Polymer gebunden ist, das mit dem transaminierten Polypeptid umgesetzt wird, Hydrazincarboxylat. In der bevorzugten Ausführungsform ist das Polypeptid EPO, das Polymer ist mPEG mit einem Molekulargewicht von etwa 5 000 Daltons und die Gruppe, die kovalent an das Polymer gebunden ist, ist Hydrazincarboxylat.
- In jedem der vorliegenden Verfahren ist die bevorzugte Kontaktzeit für Schritt (a) von 20 Minuten bis 2 Stunden und ist die bevorzugte Kontaktzeit und die bevorzugte Temperatur für Schritt (b) von 10 bis 50 Stunden bzw. von 4°C bis Raumtemperatur.
- Bei bestimmten Polypeptiden ist der N-Terminus eines Polypeptids „vergraben", d. h. nicht Lösemitteln oder Reagenzien darin ausgesetzt, wenn das Polypeptid in seiner nativen Konformation ist. Reagenzien, wie Tetramethylharnstoff oder Harnstoff, können dazu verwendet werden, ein solches Polypeptid zu entfalten, um seinem N-terminalen Rest zu ermöglichen, die erforderlichen Reaktionen der vorliegenden Verfahren einzugehen.
- Diese Erfindung stellt auch eine pharmazeutische Zusammensetzung bereit, die eine wirksame Menge der vorliegenden ersten oder zweiten Zusammensetzung und einen pharmazeutisch akzeptablen Träger umfasst. Die vorliegende pharmazeutische Zusammensetzung kann beispielsweise eine Menge des vorliegenden mPEG-EPO umfassen, die zum Behandeln eines Patienten, der unter Anämie leidet, wirksam ist.
- Pharmazeutisch akzeptable Träger sind dem Fachmann wohl bekannt und beinhalten, sind aber nicht darauf beschränkt, 0,01-0,1 M und vorzugsweise 0,05 M Phosphatpuffer oder 0,8%-ige Kochsalzlösung. Darüber hinaus können solche pharmazeutisch akzeptablen Träger wässrige oder nichtwässrige Lösungen, Suspensionen und Emulsionen sein. Beispiele von nichtwässrigen Lösemitteln sind Propylenglykol, Polyethylenglykol, pflanzliche Öle, wie Olivenöl, und injizierbare organische Ester, wie Ethyloleat. Zu wässrigen Trägern zählen Wasser, alkoholische/wässrige Lösungen, Emulsionen oder Suspensionen, darunter Kochsalzlösung und gepufferte Medien. Zu parenteral verabreichbaren Vehikeln zählen Natriumchloridlösung, Ringer-Dextrose, Dextrose und Natriumchlorid, Ringer-Laktat oder nichtflüssige Öle. Zu intravenös verabreichbaren Vehikeln zählen Mittel zum Wiederauffüllen der Flüssigkeits- und Nährstoffpegel, Mittel zum Wiederauffüllen des Elektrolytpegels, wie die auf Ringer-Dextrose basierten, und dergleichen. Konservierungsstoffe und andere Zusatzstoffe können ebenfalls vorliegen, wie beispielsweise antimikrobielle Mittel, Antioxidantien, Chelatbildner, Inertgase und dergleichen.
- Schließlich stellt diese Erfindung Kits zur Verwendung beim Herstellen der vorliegenden Zusammensetzungen bereit. Das erste Kit zum Herstellen der ersten vorliegenden Zusammensetzung umfasst folgendes:
- (a) ein Glyoxylation oder Derivat davon;
- (b) ein Übergangsmetallion;
- (c) eine Lewis-Base; und
- (d) ein wasserlösliches Polymer mit einem Molekulargewicht von 700 bis 20 000 Daltons und mit einer kovalent angebundenen Gruppe, die mit einer N-terminalen α-Carbonylgruppe des transaminierten Polypeptids reagiert, um eine Hydrazonbindung zu bilden, wodurch das Polymer an das N-terminale α-Kohlenstoffatom des Polypeptids kovalent gebunden wird.
- Die Reagenzien in diesen Kits können in einer vorherbestimmten Quantität verpackt und in separaten Fächern enthalten sein. Alternativ können bestimmte Reagenzien in ein und demselben Fach enthalten sein, so es die Einschränkungen des vorliegenden Verfahrens gestatten. Schließlich können die Kits weiterhin reduzierende Reagenzien zum Erzeugen von reduzierten Hydrazonbindungen gemäß den vorliegenden Verfahren sowie geeignete Puffer und Reaktionsgefäße enthalten.
- Diese Erfindung wird durch Bezugnahme auf die folgenden Versuchsbeispiele besser verstanden werden, der Fachmann wird jedoch bereitwillig zu schätzen wissen, dass die detaillierten spezifischen Versuche die Erfindung lediglich veranschaulichen, wie sie in den Ansprüchen vollständiger beschrieben ist, die danach folgen.
- Versuchsbeispiele
- 1. Herstellung von transaminiertem EPO
- 5 mg EPO in 20 mM Natriumcitrat (pH 6,9) und 100 mM NaCl wurden unter Verwendung von Centricon-10 (Amicon, Beverly, MA, USA) mit 100 mM Natriumacetatpuffer (pH 7,0) ausgetauscht. Die Endkonzentrationen wurden auf 1 mg/ml EPO, 2 M Natriumacetat, 0,4 M Essigsäure, 0,1 M Glyoxylsäure und 10 mM Kupfer(II)-sulfat (pH 5,5) eingestellt (
1 ). Die Reaktion wurde 2 Stunden bei Raumtemperatur laufengelassen und wurde durch Zugabe von 100 ml 0,5 M EDTA gestoppt. Transaminiertes EPO wurde mittels einer Sephadex G-25-Säule (Pharmacia, Piscataway, NJ, USA) unter Verwendung eines 100 mM Natriumacetatpuffers (pH 4,5) gereinigt. - Das Ausmaß der Transaminierung wurde mittels 2,4-Dinitrophenylhydrazin geschätzt, wie in der Literatur beschrieben (R. Fields et al., Biochem. J., 1971, 121, 587). Die Extinktion bei 370 nm wurde nach den ersten paar Minuten und nach einer Stunde gemessen. Die Extinktionsdifferenz ist zur Anzahl der an dem EPO-Molekül vorhandenen Carbonylgruppen proportional. Das transaminierte EPO wurde zudem einer Aminosäureanalyse auf einem ABI 420H-System (Applied Biosystems, Foster City, CA, USA) unter Anwendung von Vorsäulen-PITC-Chemie unterzogen. Die Ergebnisse zeigen, dass Lysinreste, d. h. nicht-N-terminale Reste, nicht transaminiert wurden.
- 2. Herstellung von mPEG-EPO mit mPEG-Hydrazincarboxylat
- Transaminiertes EPO (1 mg) in 100 mM Natriumacetat (pH 4,5) wurde mit 0,5 M Natriumchlorid auf ein Endvolumen von 1 ml eingestellt, zu dem 10 mg mPEG5000-Hydrazincarboxylat (Shearwater Polymers, Hunstville, AL, USA) gegeben wurden. Die Reaktionsmischung wurde 40 Stunden bei Raumtemperatur gerührt und mittels einer Sephacryl s-200-Säule (Pharmacia, Piscataway, NJ, USA) unter Verwendung eines 20 mM Natriumcitratpuffers (7,0), der 100 mM NaCl enthielt, gereinigt. Darüber hinaus kann 0,1%-iges SDS zu der Reaktionsmischung gegeben werden, um die Vereinigungsausbeute zu erhöhen.
- In einer Gelpermeationschromatographie zeigte das mPEG-EPO-Konjugat ein im Vergleich zu denen von EPO und mPEG5000-Hydrazincarboxylat erheblich erhöhtes Molekulargewicht (
2 ). - Matrixunterstützte Laserdesorptionsmassenspektrometrie (Finnigan-MAT LaserMAT 2000, lineare Laufzeit) wurde angewendet, um mPEG-EPO mittels Bestimmung des Molekulargewichts zu charakterisieren (
3 ). mPEG5000-Hydrazincarboxylat zeigt ein Ion bei m/z 5 157,4. EPO zeigt ein zweifach geladenes Monomer (m/z 14 604), ein einfach geladenes Monomer (m/z 28 569), ein Dimer (m/z 57 208) und ein Trimer (m/z 85 284). In ähnlicher Weise zeigt mPEG-EPO ein zweifach geladenes Monomer (m/z 17 092), ein einfach geladenes Monomer (m/z 34 279), ein Dimer (m/z 69 071) und ein Trimer (m/z 102 955). - Ein Zirkulardichroismus-Spektrum (CD-Spektrum) (Jobin-YVON CD6, Dichrograph Spectrometer Instruments, SA, Edison, NJ, USA) von mPEG-EPO zeigte, dass das Protein die in nativem EPO vorliegende α-helikale Bündelstruktur bewahrte (Daten nicht gezeigt). Dieses Ergebnis bedeutet, dass ein PEG-Molekül an dem N-terminalen Ende von EPO seine sekundäre Struktur nicht stört.
- 3. Herstellung von mPEG-EPO mit mPEG-Hydrazid
- Transaminiertes EPO (1 mg) in 100 mM Natriumacetat (pH 4,5) wurde mit 0,5 M Natriumchlorid, 0,1%-igem SDS auf ein Endvolumen von 1 ml eingestellt und 10-20 mg mPEG5000-Hydrazid wurden zugegeben. Die Reaktionsmischung wurde 40 Stunden bei Raumtemperatur gerührt und mittels einer Sephacryl S-200-Säule (Pharmacia, Piscataway, NJ, USA) unter Verwendung eines 20 mM Natriumcitratpuffers (7,0), der 100 mM NaCl enthielt, gereinigt.
- Die mPEG-EPO-Konjugate wurden mittels 4-15%-iger SDS-PAGE (Bio-Rad, Hercules, CA, USA) mit verschiedenen Verfahren analysiert: Coomassie-Färbung (für Proteine spezifisch), Western-Blot (für EPO spezifisch) und Iodfärbung (für PEG spezifisch). Die Migrationsdistanz von mPEG-EPO-Konjugaten mit höherem Molekulargewicht auf SDS-PAGE war geringer als die von nativem EPO. Das isoelektrische Fokussierungsmuster weist darauf hin, dass der isoelektrische Punkt (pI) von EPO bei Modifikation nicht wesentlich verändert wird. Transaminiertes EPO ist jedoch etwas azidischer als natives EPO und mPEG-EPO.
- Da die EPO- und mPEG-EPO-Banden durch SDS-PAGE gut getrennt werden, kann diese Technik zum Überwachen der Effizienz der Konjugationsreaktion verwendet werden. Es wurde beobachtet, dass die Konjugationsreaktion zu > 95% abgeschlossen war, wenn mPEG5000-Hydrazincarboxylat verwendet wurde, wohingegen die Reaktion nur zu etwa 20% abgeschlossen war, wenn mPEG5000-Hydrazid, mPEG5000-Semicarbazid oder mPEG5000-Oxylamin verwendet wurde. Folglich scheint die Hydrazincarboxylatgruppe gegenüber Carbonylgruppen reaktionsfähiger zu sein als die Hydrazid-, Semicarbazid- oder Oxylamingruppe.
- 4. Reaktivität von mPEG-EPO mit Anti-EPO-Antikörper
- Die Antigenität von mPEG-EPO wurde unter Verwendung eines QuantikineTM IVDTM EPO ELISA-Kits (R & D Systems, Minneapolis, MN, USA) untersucht. Das Assay besteht aus einer Mikrotiterplatte, die mit einem monoklonalen Antikörper zu EPO beschichtet ist. EPO oder mPEG-EPO werden mit der beschichteten Platte wechselwirken gelassen. Nach dem Waschen der Platte wird ein Konjugat von polyklonalem Anti-EPO-Antikörper und Meerrettichperoxidase zugegeben. Nach dem Entfernen des überschüssigen Konjugats wird ein Chromogen in die Näpfe gegeben und mittels der Enzymreaktion oxidiert, um einen Komplex von blauer Farbe zu bilden. Die Extinktion dieses Komplexes wird bei 450 nm gemessen.
- Die Ergebnisse des ELISA-Assays für mPEG-EPO mit einer Hydrazonbindung, die aus Hydrazincarboxylat (HZC) und Hydrazid (HZ) gebildet wurde, sind in
5 dargestellt. Die Daten zeigen, dass selbst ein PEG-Molekül, das an den N-Terminus von EPO angelagert ist, die Affinität für monoklonale Antikörperbindung an EPO erheblich verringert, möglicherweise aufgrund sterischer Hinderung. - 5. In-vitro-Aktivität von mPEG-EPO
- Die biologische Aktivität von mPEG-EPO in vitro wurde mit einem Zellproliferationsassay unter Verwendung von FDC-P1/HER-Zellen, einer hämatopoetischen Mauszelllinie, beurteilt. Die Zelllinie exprimiert den EPO-Rezeptor und ist in Bezug auf Wachstum vom EPO abhängig. Nachdem man die Zellen 24 Stunden in Abwesenheit von EPO hat wachsen lassen, wurde den Zellen EPO oder mPEG-EPO zugesetzt. Die Zellen wurden 42 Stunden inkubiert und dann wurde den Zellen tritiiertes Thymidin zugesetzt. Nach 6 Stunden wurde das Zellwachstum durch Beimischung von Thymidin bestimmt.
- Die Ergebnisse des Zellproliferationsassays für transaminiertes EPO und mPEG-EPO mit Hydrazonbindungen, die aus Hydrazincarboxylat (HZC) und Hydrazid (HZ) gebildet wurden, sind in
6 dargestellt. Transaminiertes EPO zeigt volle biologische Aktivität im Vergleich zu nativem EPO, wie durch seinen ED50-Wert bestimmt. Die mPEG-EPO-Proben mit Hydrazonbindungen, die aus Hydrazincarboxylat (HZC) und Hydrazid (HZ) gebildet wurden, bewahren nur 38,5% bzw. 25% Aktivität, wie durch ihre ED50-Werte bestimmt. Die Daten zeigen, dass ein PEG-Molekül, das an den N-Terminus von EPO angelagert ist, die Affinität von EPO für seinen Rezeptor erheblich verringert, möglicherweise aufgrund sterischer Hinderung. - 6. In-vivo-Aktivität von mPEG-EPO
- Die In-vivo-Aktivität von mPEG-EPO wurde mit einem Bioassay an exhypoxischen Mäusen (P.M. Coates et al., Nature, 1961, 191, 1 065) beurteilt. Die Bildung von endogenen Erythrozyten in den Mäusen wurde mittels der Polyzythämie unterdrückt, die durch Einwirkung von vermindertem Druck erzeugt wurde. Das EPO- oder mPEG-EPO-Konjugat wird mit einer Konzentration von 1 Einheit/Maus injiziert. 48 Stunden nach der Injektion von EPO oder mPEG-EPO wurde Eisen-59 verabreicht. Die Eisen-59-Aufnahme, die die Bildung von neuen Erythrozyten anzeigt, wurde 48, 72 und 96 Stunden nach der Verabreichung von EPO oder mPEG-EPO gemessen.
- Die Ergebnisse des Bioassays an exhypoxischen Mäusen für mPEG-EPO mit Hydrazonbindungen, die mit Hydrazincarboxylat (HZC), Hydrazid (HZ) und Semicarbazid (SCZ) gebildet wurden, sind in
7 dargestellt. Die mPEG-EPO-Proben zeigen eine hohe In-vivo-Aktivität sowie eine längere Aktivitätsdauer im Vergleich zu nativem EPO. Die In-vivo-Ergebnisse zeigen, dass mPEG-EPO-Proben eine längere Zirkulationszeit in vivo und eine retardierte Abgabe von EPO während der Zirkulation aufweisen. - 7. Herstellung von mPEG-Fibrin-17-29-Dimer
-
- 2 mg Fibrin-17-29-Dimer wurden in 0,5 ml 2 M Natriumacetat, 0,4 M Essigsäure, 0,1 M Glyoxylsäure und 10 mM Kupfer(II)-sulfat (pH 5,5) gelöst. Die Reaktion wurde 2 Stunden bei Raumtemperatur weiterlaufen gelassen und wurde durch Zugabe von 20 ml 0,5 M EDTA gestoppt. Transaminiertes Fibrin-Dimer wurde mittels einer Sephadex G-10-Säule (Pharmacia, Piscataway, NJ, USA) unter Verwendung eines 100 mM Natriumacetatpuffers (pH 4,5) gereinigt. Transaminiertes Fibrin-Dimer zeigte in der Aminosäureanalyse erheblich reduziertes Gly, was auf die Transaminierung von N-terminalem Gly hindeutet.
- 1 mg transaminiertes Fibrin-Dimer in 0,5 ml 100 mM Natriumacetat (pH 4,5) wurde 10 mg mPEG5000-Hydrazincarboxylat zugesetzt. Die Reaktionsmischung wurde 24 Stunden bei Raumtemperatur gerührt. Das mPEG-Fibrin-Dimer wurde mittels Anionenaustausch-Chromatographie mit einer HEMA IEC BIO CM-Säule (Alltech) gereinigt. Die mobile Phase A war 20 mM Natriumacetat (pH 5,5). Die mobile Phase B war 0,2 M MOPS, 0,05 M einwertiges Kaliumphosphat und 0,25 M zweiwertiges Kaliumphosphat (pH 7,5). Der Gradient war 100% A für 5 Minuten, dann 0 bis 100% B in 25 Minuten. Ein neuer Peak bei 14,5 Minuten, der vor dem unmodifizierten Fibrin-Dimer (18 Minuten) erschien, wurde zur weiteren Analyse gesammelt. Ein Laserdesorptionsmassenspektrum zeigte das Ion bei m/z 8 070,9, was bewies, dass ein PEG-Molekül an dem Fibrin-Dimer angelagert war (m/z 2 986,6).
Claims (12)
- Stoffzusammensetzung, bestehend im wesentlichen aus einem Peptid oder einem Protein und PEG oder einem Derivat davon, kovalent an dem N-terminalen α-Kohlenstoffatom des Polypeptids gebunden, unter der Bedingung, daß (a) das PEG und Polypeptid aneinander über eine Hydrazonbindung oder reduzierte Hydrazonbindung gebunden sind, (b) das PEG ein Molekulargewicht von 700 bis 20 000 Daltons hat, (c) die natürliche Funktion des Polypeptids bei Entfernung seiner N-terminalen Aminogruppe nicht eliminiert wird, und (d) der N-terminale Aminosäurerest des Proteins nicht Serin oder Threonin ist.
- Zusammensetzung nach Anspruch 1, wobei das Protein EPO oder ein Derivat davon ist.
- Zusammensetzung nach Anspruch 1, wobei das PEG oder Derivat davon ein Molekulargewicht von ungefähr 5 000 Daltons hat.
- Zusammensetzung nach Anspruch 1, wobei das Protein EPO ist und das PEG mPEG mit einem Molekulargewicht von ungefähr 5 000 Daltons ist.
- Verfahren zum kovalenten Binden von PEG an das N-terminale α-Kohlenstoffatom eines Polypeptids, das die Schritte umfaßt: a) In-Kontakt-Bringen des Polypeptids mit (i) einem Glyoxylation oder einem Derivat davon in einer Konzentration von 0,1 M bis 2,0 M, (ii) einem Übergangsmetallion in einer Konzentration von 10 μM bis 1 M und (iii) einer Lewis-Base in einer Konzentration von 10 mM bis 10 M, bei einem pH von 5,0 bis 7,0 und einer Temperatur von 0°C bis 100°C, um ein transaminiertes Polypeptid mit einer N-terminalen α-Carbonylgruppe zu bilden; und b) In-Kontakt-Bringen des transaminierten Polypeptids bei einem pH von 3,0 bis 5,0 mit PEG oder einem Derivat davon, das eine daran kovalent gebun dene Gruppe hat, die mit der N-terminalen α-Carbonylgruppe des transaminierten Polypeptids reagiert, um eine Hydrazonbindung zu bilden, wodurch das PEG an das N-terminale α-Kohlenstoffatom des Polypeptids kovalent gebunden wird, unter der Bedingung, daß das PEG ein Molekulargewicht von 700 bis 20 000 Daltons hat und die natürliche Funktion des Polypeptids bei Entfernen seiner N-terminalen α-Aminogruppe nicht eliminiert wird.
- Verfahren nach Anspruch 5, wobei das Protein EPO oder ein Derivat davon ist.
- Verfahren nach Anspruch 5, wobei das PEG oder Derivat davon ein Molekulargewicht von ungefähr 5 000 Daltons hat.
- Verfahren nach Anspruch 5, wobei die Gruppe, die kovalent an das PEG gebunden ist, Hydrazincarboxylat ist.
- Verfahren nach Anspruch 5, wobei das Protein EPO ist, das PEG mPEG mit einem Molekulargewicht von ungefähr 5 000 Daltons ist und die an das PEG kovalent gebundene Gruppe Hydrazincarboxylat ist.
- Verfahren nach Anspruch 5, das weiterhin den Schritt des Reduzierens der in Schritt (b) gebildeten Hydrazonbindung umfaßt, um eine reduzierte Hydrazonbindung zu bilden.
- Pharmazeutische Zusammensetzung, die eine wirksame Menge der Zusammensetzung nach Anspruch 1 und einen pharmazeutisch akzeptablen Träger umfaßt.
- Kit zur Verwendung beim Herstellen der Zusammensetzung nach Anspruch 1, der folgendes umfaßt: (a) ein Glyoxylation oder Derivat davon; (b) ein Übergansmetallion; (c) eine Lewis-Base; und (d) PEG oder ein Derivat davon mit einem Molekulargewicht von 700 bis 20 000 Daltons und mit einer kovalenten angebundenen Gruppe, die mit ei ner N-terminalen α-Carbonylgruppe des transaminierten Polypeptids reagiert, um eine Hydrazonbindung zu bilden, wodurch das PEG an das N-terminale α-Kohlenstoffatom des Polypeptids kovalent gebunden wird.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US2305096P | 1996-08-02 | 1996-08-02 | |
| US23050P | 1996-08-02 | ||
| PCT/US1997/013756 WO1998005363A2 (en) | 1996-08-02 | 1997-08-01 | Polypeptides having a single covalently bound n-terminal water-soluble polymer |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| DE69736780D1 DE69736780D1 (de) | 2006-11-16 |
| DE69736780T2 true DE69736780T2 (de) | 2007-09-06 |
Family
ID=21812842
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| DE69736780T Expired - Lifetime DE69736780T2 (de) | 1996-08-02 | 1997-08-01 | Polypeptide mit einzelnem kovalent gebundenen n-terminalen wasserlöslichen polymer |
Country Status (19)
| Country | Link |
|---|---|
| US (1) | US6077939A (de) |
| EP (2) | EP1731174A3 (de) |
| JP (1) | JP4410852B2 (de) |
| KR (1) | KR20000029673A (de) |
| CN (1) | CN100471521C (de) |
| AT (1) | ATE341344T1 (de) |
| AU (1) | AU3908597A (de) |
| BR (1) | BR9711009A (de) |
| CA (1) | CA2262994A1 (de) |
| DE (1) | DE69736780T2 (de) |
| DK (1) | DK0964702T3 (de) |
| ES (1) | ES2273373T3 (de) |
| IL (2) | IL128229A0 (de) |
| NO (1) | NO990465L (de) |
| NZ (1) | NZ333993A (de) |
| PT (1) | PT964702E (de) |
| RU (1) | RU2199347C2 (de) |
| SI (1) | SI0964702T1 (de) |
| WO (1) | WO1998005363A2 (de) |
Families Citing this family (184)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR100361933B1 (ko) * | 1993-09-08 | 2003-02-14 | 라 졸라 파마슈티칼 컴파니 | 화학적으로정의된비중합성결합가플랫폼분자및그것의콘주게이트 |
| US6458953B1 (en) * | 1998-12-09 | 2002-10-01 | La Jolla Pharmaceutical Company | Valency platform molecules comprising carbamate linkages |
| US7666400B2 (en) * | 2005-04-06 | 2010-02-23 | Ibc Pharmaceuticals, Inc. | PEGylation by the dock and lock (DNL) technique |
| EP2133098A1 (de) | 2000-01-10 | 2009-12-16 | Maxygen Holdings Ltd | G-CSF-Konjugate |
| PL206148B1 (pl) | 2000-02-11 | 2010-07-30 | Bayer HealthCare LLCBayer HealthCare LLC | Koniugat polipeptydowy, polipeptyd, sekwencja nukleotydowa, wektor ekspresyjny, komórka gospodarz, sposób wytwarzania koniugatu polipeptydowego, środek farmaceutyczny i zastosowanie koniugatu polipeptydowego |
| US6586398B1 (en) * | 2000-04-07 | 2003-07-01 | Amgen, Inc. | Chemically modified novel erythropoietin stimulating protein compositions and methods |
| PL219131B1 (pl) | 2000-05-15 | 2015-03-31 | Hoffmann La Roche | Ciekła kompozycja farmaceutyczna, sposób jej wytwarzania oraz jej zastosowanie |
| AU2001268228A1 (en) | 2000-06-08 | 2001-12-17 | La Jolla Pharmaceutical Company | Multivalent platform molecules comprising high molecular weight polyethylene oxide |
| AU2001273387A1 (en) * | 2000-07-12 | 2002-01-21 | Gryphon Therapeutics, Inc. | Polymer-modified bioactive synthetic chemokines, and methods for their manufacture and use |
| US7118737B2 (en) | 2000-09-08 | 2006-10-10 | Amylin Pharmaceuticals, Inc. | Polymer-modified synthetic proteins |
| SK2772003A3 (en) * | 2000-09-08 | 2003-10-07 | Gryphon Therapeutics Inc | Synthetic erythropoiesis stimulating proteins |
| JP5170931B2 (ja) * | 2000-10-16 | 2013-03-27 | 中外製薬株式会社 | Peg修飾エリスロポエチン |
| CA2431964C (en) | 2000-12-20 | 2013-09-10 | F. Hoffmann-La Roche Ag | Conjugates of erythropoietin (pep) with polyethylene glycol (peg) |
| JP2005501801A (ja) | 2001-02-02 | 2005-01-20 | オーソ−マクニール・フアーマシユーチカル・インコーポレーテツド | フラクトピラノーススルファメートとエリスロポイエチンを含んで成る神経学的機能不全治療 |
| WO2002074806A2 (en) | 2001-02-27 | 2002-09-26 | Maxygen Aps | New interferon beta-like molecules |
| US20040077835A1 (en) * | 2001-07-12 | 2004-04-22 | Robin Offord | Chemokine receptor modulators, production and use |
| US7696163B2 (en) | 2001-10-10 | 2010-04-13 | Novo Nordisk A/S | Erythropoietin: remodeling and glycoconjugation of erythropoietin |
| US7795210B2 (en) | 2001-10-10 | 2010-09-14 | Novo Nordisk A/S | Protein remodeling methods and proteins/peptides produced by the methods |
| US7214660B2 (en) | 2001-10-10 | 2007-05-08 | Neose Technologies, Inc. | Erythropoietin: remodeling and glycoconjugation of erythropoietin |
| US7173003B2 (en) | 2001-10-10 | 2007-02-06 | Neose Technologies, Inc. | Granulocyte colony stimulating factor: remodeling and glycoconjugation of G-CSF |
| US6818613B2 (en) | 2001-11-07 | 2004-11-16 | Ortho-Mcneil Pharmaceutical, Inc. | Aqueous sustained-release formulations of proteins |
| US7473680B2 (en) | 2001-11-28 | 2009-01-06 | Neose Technologies, Inc. | Remodeling and glycoconjugation of peptides |
| MXPA04005068A (es) | 2001-11-28 | 2004-08-19 | Ortho Mcneil Pharm Inc | Regimen de dosis de eritropoyetina para el tratamiento de la anemia. |
| US7129267B2 (en) | 2002-03-11 | 2006-10-31 | Janssen Pharmaceutica N.V. | Methods for SHP1 mediated neuroprotection |
| ATE503498T1 (de) | 2002-06-21 | 2011-04-15 | Novo Nordisk Healthcare Ag | Pegylierte glykoformen von faktor vii |
| JP4800614B2 (ja) | 2002-07-19 | 2011-10-26 | ザ ジェネラル ホスピタル コーポレイション | オキシム結合体、およびそれらの形成および使用のための方法 |
| US20040091961A1 (en) * | 2002-11-08 | 2004-05-13 | Evans Glen A. | Enhanced variants of erythropoietin and methods of use |
| US20040136952A1 (en) * | 2002-12-26 | 2004-07-15 | Mountain View Pharmaceuticals, Inc. | Polymer conjugates of cytokines, chemokines, growth factors, polypeptide hormones and antagonists thereof with preserved receptor-binding activity |
| EP1667708B9 (de) * | 2002-12-26 | 2012-10-31 | Mountain View Pharmaceuticals, Inc. | INTERFERON-BETA-1b POLYETHYLENEGLYKOL-KONJUGATE MIT ERHÖHTER IN VITRO BIOLOGISCHER WIRKSAMKEIT |
| WO2004061094A1 (en) | 2002-12-30 | 2004-07-22 | Gryphon Therapeutics, Inc. | Water-soluble thioester and selenoester compounds and methods for making and using the same |
| AU2004221824B2 (en) | 2003-03-14 | 2009-08-27 | Ratiopharm Gmbh | Branched water-soluble polymers and their conjugates |
| WO2004091499A2 (en) | 2003-04-09 | 2004-10-28 | Neose Technologies, Inc. | Intracellular formation of peptide conjugates |
| CA2522345A1 (en) | 2003-04-09 | 2004-11-18 | Neose Technologies, Inc. | Glycopegylation methods and proteins/peptides produced by the methods |
| BRPI0411166A (pt) | 2003-05-12 | 2006-07-18 | Affymax Inc | composto compreendendo uma parcela de peptìdeo, uma parcela espaçadora e uma parcela de polìmero solúvel em água e composição farmacêutica compreendendo tal composto |
| EA010016B1 (ru) | 2003-05-12 | 2008-06-30 | Афимакс, Инк. | Новые модифицированные полиэтиленгликолем соединения и их применение |
| BRPI0411172A (pt) * | 2003-05-12 | 2006-07-18 | Affymax Inc | peptìdeo, dìmero de peptìdeo, seu uso e composição farmacêutica |
| AP2042A (en) * | 2003-05-12 | 2009-09-07 | Affymax Inc | Novel peptides that bind to the erythropoietin receptor |
| US7074755B2 (en) * | 2003-05-17 | 2006-07-11 | Centocor, Inc. | Erythropoietin conjugate compounds with extended half-lives |
| KR20060032140A (ko) * | 2003-05-30 | 2006-04-14 | 센토코 인코포레이티드 | 트랜스글루타미나아제를 이용한 신규 에리트로포이에틴접합체의 형성 |
| WO2005012484A2 (en) | 2003-07-25 | 2005-02-10 | Neose Technologies, Inc. | Antibody-toxin conjugates |
| EP2263684A1 (de) | 2003-10-10 | 2010-12-22 | Novo Nordisk A/S | IL-21 Derivate |
| EP2633866A3 (de) | 2003-10-17 | 2013-12-18 | Novo Nordisk A/S | Kombinationstherapie |
| US20080305992A1 (en) | 2003-11-24 | 2008-12-11 | Neose Technologies, Inc. | Glycopegylated erythropoietin |
| JP4719686B2 (ja) | 2003-11-24 | 2011-07-06 | バイオジェネリックス アーゲー | GlycoPEG化エリスロポエチン |
| US7368169B2 (en) * | 2003-12-01 | 2008-05-06 | Rutgers, The State University Of New Jersey | Hydrazide compounds with angiogenic activity |
| BRPI0506741A (pt) | 2004-01-08 | 2007-05-15 | Neose Technologies Inc | glicosilação de peptìdeos ligados a o |
| EP2368579A1 (de) | 2004-01-21 | 2011-09-28 | Novo Nordisk Health Care AG | Tranglutaminase vermittelte konjugation von peptiden. |
| US20070105770A1 (en) * | 2004-01-21 | 2007-05-10 | Novo Nordisk A/S | Transglutaminase mediated conjugation of peptides |
| BRPI0507169A (pt) | 2004-02-02 | 2007-06-26 | Ambrx Inc | polipeptìdeos do hormÈnio de crescimento humano modificados e seu usos |
| MXPA06014307A (es) * | 2004-06-08 | 2007-03-12 | Alza Corp | Preparacion de conjugados macromoleculares por reaccion de condensacion de cuatro componentes. |
| MXPA06014684A (es) | 2004-06-18 | 2007-02-12 | Ambrx Inc | Novedosos polipeptidos de enlace antigeno y sus usos. |
| EP1771066A2 (de) | 2004-07-13 | 2007-04-11 | Neose Technologies, Inc. | Remodellierung von verzweigtem peg und klykolysierung von glucagonähnlichem peptide-1 glp-1 |
| WO2006091231A2 (en) | 2004-07-21 | 2006-08-31 | Ambrx, Inc. | Biosynthetic polypeptides utilizing non-naturally encoded amino acids |
| US7597884B2 (en) | 2004-08-09 | 2009-10-06 | Alios Biopharma, Inc. | Hyperglycosylated polypeptide variants and methods of use |
| EP1799249A2 (de) | 2004-09-10 | 2007-06-27 | Neose Technologies, Inc. | Glycopegyliertes interferon alpha |
| EP3061461A1 (de) | 2004-10-29 | 2016-08-31 | ratiopharm GmbH | Remodellierung und glykopegylierung von fibroblasten-wachstumsfaktor (fgf) |
| WO2006062685A2 (en) * | 2004-11-11 | 2006-06-15 | Affymax, Inc. | Novel peptides that bind to the erythropoietin receptor |
| AU2005310189A1 (en) * | 2004-11-11 | 2006-06-08 | Affymax, Inc. | Novel peptides that bind to the erythropoietin receptor |
| LT1824988T (lt) * | 2004-11-12 | 2017-10-25 | Bayer Healthcare Llc | Nukreipta į užduotą saitą fviii modifikacija |
| CN103520735B (zh) * | 2004-12-22 | 2015-11-25 | Ambrx公司 | 包含非天然编码的氨基酸的人生长激素配方 |
| MX2007007591A (es) | 2004-12-22 | 2007-07-25 | Ambrx Inc | Metodos para expresion y purificacion de hormona de crecimiento humano recombinante. |
| US7385028B2 (en) | 2004-12-22 | 2008-06-10 | Ambrx, Inc | Derivatization of non-natural amino acids and polypeptides |
| US7736872B2 (en) | 2004-12-22 | 2010-06-15 | Ambrx, Inc. | Compositions of aminoacyl-TRNA synthetase and uses thereof |
| ATE542920T1 (de) | 2004-12-22 | 2012-02-15 | Ambrx Inc | Modifiziertes menschliches wachstumshormon |
| NZ556436A (en) | 2005-01-10 | 2010-11-26 | Biogenerix Ag | Glycopegylated granulocyte colony stimulating factor |
| US7365127B2 (en) * | 2005-02-04 | 2008-04-29 | Enzon Pharmaceuticals, Inc. | Process for the preparation of polymer conjugates |
| US7714114B2 (en) * | 2005-02-16 | 2010-05-11 | Nektar Therapeutics | Conjugates of an EPO moiety and a polymer |
| WO2007010552A2 (en) * | 2005-03-17 | 2007-01-25 | Serum Institute Of India Limited | N- terminal peg conjugate of erythropoietin |
| EP2279756A2 (de) | 2005-04-05 | 2011-02-02 | Instituto di Ricerche di Biologia Molecolare p Angeletti S.P.A. | Verfahren zur Abschirmung von funktionalen Stellen oder Epitopen auf Proteinen |
| US9187546B2 (en) | 2005-04-08 | 2015-11-17 | Novo Nordisk A/S | Compositions and methods for the preparation of protease resistant human growth hormone glycosylation mutants |
| WO2006127910A2 (en) | 2005-05-25 | 2006-11-30 | Neose Technologies, Inc. | Glycopegylated erythropoietin formulations |
| AU2006255122B2 (en) | 2005-06-03 | 2010-10-21 | Ambrx, Inc. | Improved human interferon molecules and their uses |
| US7919461B2 (en) | 2005-06-03 | 2011-04-05 | Affymax, Inc. | Erythropoietin receptor peptide formulations and uses |
| US7550433B2 (en) | 2005-06-03 | 2009-06-23 | Affymax, Inc. | Erythropoietin receptor peptide formulations and uses |
| US8324159B2 (en) * | 2005-06-03 | 2012-12-04 | Affymax, Inc. | Erythropoietin receptor peptide formulations and uses |
| CA2611836A1 (en) * | 2005-06-13 | 2006-12-21 | Nastech Pharmaceutical Company Inc. | Transmucosal delivery of peptide derivatives |
| EP2360170A3 (de) | 2005-06-17 | 2012-03-28 | Novo Nordisk Health Care AG | Selektive Reduktion und Derivatisierung von Proteinen die mindestens ein nicht-natives Cystein enthalten |
| NZ565294A (en) | 2005-08-18 | 2010-06-25 | Ambrx Inc | Compositions of tRNA and uses thereof |
| US20070105755A1 (en) | 2005-10-26 | 2007-05-10 | Neose Technologies, Inc. | One pot desialylation and glycopegylation of therapeutic peptides |
| AU2006286486A1 (en) * | 2005-08-30 | 2007-03-08 | Novo Nordisk Health Care Ag | Liquid formulations of pegylated growth hormone |
| EP1937294A4 (de) * | 2005-10-21 | 2009-11-04 | Synageva Biopharma Corp | Glykolierte und glykosylierte therapeutische proteine von geflügel |
| US20080171696A1 (en) * | 2005-10-21 | 2008-07-17 | Avigenics, Inc. | Pharmacodynamically enhanced therapeutic proteins |
| US20090048440A1 (en) | 2005-11-03 | 2009-02-19 | Neose Technologies, Inc. | Nucleotide Sugar Purification Using Membranes |
| EP2339014B1 (de) | 2005-11-16 | 2015-05-27 | Ambrx, Inc. | Verfahren und Zusammensetzungen mit nichtnatürlichen Aminosäuren |
| CN101062407A (zh) | 2006-04-29 | 2007-10-31 | 中国科学院上海生命科学研究院 | 促红细胞生成素在预防或治疗视网膜损伤中的用途 |
| AU2007254141B2 (en) * | 2006-05-19 | 2012-10-11 | Glycofi, Inc. | Erythropoietin compositions |
| RU2008145084A (ru) | 2006-05-24 | 2010-06-27 | Ново Нордиск Хелс Кеа Аг (Ch) | Аналоги фактора ix, имеющие пролонгированное время полужизни in vivo |
| MX2008016169A (es) * | 2006-07-07 | 2009-01-15 | Novo Nordisk Healthcare Ag | Nuevos conjugados de proteina y metodos para su preparacion. |
| US9187532B2 (en) | 2006-07-21 | 2015-11-17 | Novo Nordisk A/S | Glycosylation of peptides via O-linked glycosylation sequences |
| CN101534847A (zh) * | 2006-08-04 | 2009-09-16 | 普罗龙药品公司 | 修饰型促红细胞生成素 |
| CA2663083A1 (en) | 2006-09-08 | 2008-03-13 | Ambrx, Inc. | Modified human plasma polypeptide or fc scaffolds and their uses |
| CN106190983B (zh) | 2006-09-08 | 2019-05-28 | Ambrx公司 | 用于脊椎动物细胞的杂合抑制tRNA |
| CN101511856B (zh) | 2006-09-08 | 2016-01-20 | Ambrx公司 | 脊椎动物细胞中抑制因子trna的转录 |
| US7985783B2 (en) | 2006-09-21 | 2011-07-26 | The Regents Of The University Of California | Aldehyde tags, uses thereof in site-specific protein modification |
| WO2008057683A2 (en) | 2006-10-03 | 2008-05-15 | Novo Nordisk A/S | Methods for the purification of polypeptide conjugates |
| WO2008094275A1 (en) | 2007-01-30 | 2008-08-07 | New York University | Peptides for treatment of conditions associated with nitric oxide |
| WO2008095004A2 (en) * | 2007-01-31 | 2008-08-07 | Affymax, Inc. | Nitrogen-based linkers for attaching modifying groups to polypeptides and other macromolecules |
| ES2385114T3 (es) | 2007-03-30 | 2012-07-18 | Ambrx, Inc. | Polipéptidos de FGF-21 modificados y sus usos |
| BRPI0809670A8 (pt) | 2007-04-03 | 2018-12-18 | Biogenerix Ag | métodos para aumentar a produção de célula tronco, para aumentar o número de granulócitos em um indivíduo, para prevenir, tratar e aliviar a mielossupressão que resulta de uma terapia contra o câncer, para tratar uma condição em um indivíduo, para tratar neutropenia e trombocitopenia em um mamífero, para expandir células tronco hematopoiéticas em cultura, para aumentar a hematopoiese em um indivíduo, para aumentar o número de célulars progenitoras hematopoiéticas em um indivíduo, e para fornecer enxerto estável da medula óssea, e, forma de dosagem oral. |
| US8114630B2 (en) | 2007-05-02 | 2012-02-14 | Ambrx, Inc. | Modified interferon beta polypeptides and their uses |
| MX2009013259A (es) | 2007-06-12 | 2010-01-25 | Novo Nordisk As | Proceso mejorado para la produccion de azucares de nucleotidos. |
| WO2009003188A2 (en) * | 2007-06-27 | 2008-12-31 | Cedars-Sinai Medical Center | N-terminal specific chemical labeling for proteomics applications |
| KR101656107B1 (ko) | 2007-11-20 | 2016-09-08 | 암브룩스, 인코포레이티드 | 변형된 인슐린 폴리펩티드 및 이의 용도 |
| CN101456911A (zh) * | 2007-12-12 | 2009-06-17 | 江苏豪森药业股份有限公司 | 促红细胞生成素模拟肽衍生物及其可药用盐和其制备方法与用途 |
| CA2707979A1 (en) * | 2007-12-13 | 2009-06-18 | Biovectra Inc. | Polypeptides modified by protein trans-splicing technology |
| MX2010008632A (es) | 2008-02-08 | 2010-08-30 | Ambrx Inc | Leptina-polipeptidos modificados y sus usos. |
| RU2573587C2 (ru) | 2008-02-27 | 2016-01-20 | Ново Нордиск А/С | Конъюгированные молекулы фактора viii |
| EP2318029B1 (de) | 2008-07-23 | 2017-11-01 | Ambrx, Inc. | Modifizierte bovine g-csf-polypeptide und ihre verwendung |
| EP2157432A1 (de) * | 2008-08-15 | 2010-02-24 | Qiagen GmbH | Verfahren zur Analyse einer komplexen Probe durch Massenspektrometrie |
| NZ592249A (en) | 2008-09-26 | 2013-03-28 | Ambrx Inc | Non-natural amino acid replication-dependent microorganisms and vaccines |
| EP2342223B1 (de) | 2008-09-26 | 2017-04-26 | Ambrx, Inc. | Modifizierte tiererythropoietinpolypeptide und anwendungen davon |
| WO2010129248A1 (en) | 2009-05-06 | 2010-11-11 | Centocor Ortho Biotech Inc. | Melanocortin receptor binding conjugates |
| EP3093029A1 (de) * | 2009-07-27 | 2016-11-16 | Baxalta GmbH | Koagulationsproteinkonjugate |
| SG181769A1 (en) | 2009-12-21 | 2012-07-30 | Ambrx Inc | Modified porcine somatotropin polypeptides and their uses |
| CN107674121A (zh) | 2009-12-21 | 2018-02-09 | Ambrx 公司 | 经过修饰的牛促生长素多肽和其用途 |
| WO2011107591A1 (en) | 2010-03-05 | 2011-09-09 | Rigshospitalet | Chimeric inhibitor molecules of complement activation |
| WO2011143274A1 (en) | 2010-05-10 | 2011-11-17 | Perseid Therapeutics | Polypeptide inhibitors of vla4 |
| EP3572091B1 (de) | 2010-08-17 | 2023-12-13 | Ambrx, Inc. | Modifizierte relaxinpolypeptide und deren verwendungen |
| US9567386B2 (en) | 2010-08-17 | 2017-02-14 | Ambrx, Inc. | Therapeutic uses of modified relaxin polypeptides |
| AR083006A1 (es) | 2010-09-23 | 2013-01-23 | Lilly Co Eli | Formulaciones para el factor estimulante de colonias de granulocitos (g-csf) bovino y variantes de las mismas |
| CN102652836A (zh) * | 2011-03-03 | 2012-09-05 | 华中科技大学同济医学院附属协和医院 | 靶向释药的抗癌蛋白质或多肽聚合物前药及其制备方法 |
| CN103930440A (zh) | 2011-07-01 | 2014-07-16 | 拜耳知识产权有限责任公司 | 松弛素融合多肽及其用途 |
| US9150846B2 (en) | 2011-07-05 | 2015-10-06 | Bioasis Technologies, Inc. | P97-antibody conjugates and methods of use |
| CA2875989A1 (en) | 2012-06-08 | 2013-12-12 | Sutro Biopharma, Inc. | Antibodies comprising site-specific non-natural amino acid residues, methods of their preparation and methods of their use |
| US9732161B2 (en) | 2012-06-26 | 2017-08-15 | Sutro Biopharma, Inc. | Modified Fc proteins comprising site-specific non-natural amino acid residues, conjugates of the same, methods of their preparation and methods of their use |
| AU2013296557B2 (en) | 2012-07-31 | 2019-04-18 | Bioasis Technologies Inc. | Dephosphorylated lysosomal storage disease proteins and methods of use thereof |
| US9682934B2 (en) | 2012-08-31 | 2017-06-20 | Sutro Biopharma, Inc. | Modified amino acids |
| AU2013344464A1 (en) | 2012-11-16 | 2015-05-21 | The Regents Of The University Of California | Pictet-Spengler ligation for protein chemical modification |
| US9310374B2 (en) | 2012-11-16 | 2016-04-12 | Redwood Bioscience, Inc. | Hydrazinyl-indole compounds and methods for producing a conjugate |
| CN102935236B (zh) * | 2012-11-21 | 2015-08-26 | 武汉平华生物医药科技有限公司 | 一种具有p-糖蛋白抑制功能的抗肿瘤前药 |
| EP2970433B1 (de) | 2013-03-13 | 2019-09-18 | Bioasis Technologies Inc. | Fragmente von p97 und verwendungen davon |
| EP3019522B1 (de) | 2013-07-10 | 2017-12-13 | Sutro Biopharma, Inc. | Antikörper mit mehreren ortsspezifischen nichtnatürlichen aminosäureresten, verfahren zu deren herstellung und verfahren zu deren verwendung |
| EP3038657A2 (de) | 2013-08-28 | 2016-07-06 | Bioasis Technologies Inc. | Cns-gerichtete konjugate mit modifizierten fc-regionen und verfahren zur verwendung davon |
| EP3055298B1 (de) | 2013-10-11 | 2020-04-29 | Sutro Biopharma, Inc. | Modifizierte aminosäuren mit funktionellen tetrazingruppen, verfahren zur herstellung und verfahren zu deren verwendung |
| NZ758050A (en) | 2013-10-15 | 2024-03-22 | Seagen Inc | Pegylated drug-linkers for improved ligand-drug conjugate pharmacokinetics |
| JP6745218B2 (ja) | 2013-11-27 | 2020-08-26 | レッドウッド バイオサイエンス, インコーポレイテッド | ヒドラジニル−ピロロ化合物及び複合体を生成するための方法 |
| SG11201702824UA (en) | 2014-10-24 | 2017-05-30 | Bristol Myers Squibb Co | Modified fgf-21 polypeptides and uses thereof |
| AU2016354009B2 (en) | 2015-11-09 | 2021-05-20 | R.P. Scherer Technologies, Llc | Anti-CD22 antibody-maytansine conjugates and methods of use thereof |
| ES2919323T3 (es) | 2015-12-04 | 2022-07-26 | Seagen Inc | Conjugados de compuestos de tubulisina cuaternizados |
| US11793880B2 (en) | 2015-12-04 | 2023-10-24 | Seagen Inc. | Conjugates of quaternized tubulysin compounds |
| JP7073266B2 (ja) | 2016-03-25 | 2022-05-23 | シージェン インコーポレイテッド | Peg化薬物リンカー及びその中間体を調製するためのプロセス |
| ES2936226T3 (es) | 2016-04-15 | 2023-03-15 | Beckman Coulter Inc | Macromoléculas fotoactivas y usos de las mismas |
| JP7244987B2 (ja) | 2016-12-14 | 2023-03-23 | シージェン インコーポレイテッド | 多剤抗体薬物コンジュゲート |
| WO2018148419A1 (en) | 2017-02-08 | 2018-08-16 | Bristol-Myers Squibb Company | Modified relaxin polypeptides comprising a pharmacokinetic enhancer and uses thereof |
| KR102648564B1 (ko) | 2017-03-24 | 2024-03-19 | 씨젠 인크. | 글루쿠로니드 약물-링커의 제조 공정 및 그 중간물 |
| CN119286279A (zh) | 2017-12-26 | 2025-01-10 | 贝克顿·迪金森公司 | 深紫外线可激发的水溶剂化聚合物染料 |
| JP2021519841A (ja) | 2018-03-30 | 2021-08-12 | ベクトン・ディキンソン・アンド・カンパニーBecton, Dickinson And Company | ペンダントクロモフォアを有する水溶性ポリマー色素 |
| TW202519270A (zh) | 2018-06-07 | 2025-05-16 | 美商思進公司 | 喜樹鹼結合物 |
| CA3107332A1 (en) | 2018-07-22 | 2020-01-30 | Bioasis Technologies Inc. | Treatment of lymphatic metastases |
| LT3849614T (lt) | 2018-09-11 | 2024-03-25 | Ambrx, Inc. | Interleukino-2 polipeptido konjugatai ir jų panaudojimas |
| AU2019361206A1 (en) | 2018-10-19 | 2021-06-03 | Ambrx, Inc. | Interleukin-10 polypeptide conjugates, dimers thereof, and their uses |
| CN109400695B (zh) * | 2018-10-31 | 2020-06-30 | 中南大学湘雅医院 | 一种多肽的修饰方法及应用 |
| CA3128081A1 (en) | 2019-02-12 | 2020-08-20 | Ambrx, Inc. | Compositions containing, methods and uses of antibody-tlr agonist conjugates |
| JP2022550851A (ja) | 2019-10-04 | 2022-12-05 | シージェン インコーポレイテッド | カンプトテシンペプチドコンジュゲート |
| KR20220151202A (ko) | 2020-03-11 | 2022-11-14 | 암브룩스, 인코포레이티드 | 인터류킨-2 폴리펩타이드 접합체 및 그의 사용 방법 |
| CN115955980A (zh) | 2020-04-10 | 2023-04-11 | 思进公司 | 电荷可变接头 |
| US20210355468A1 (en) | 2020-05-18 | 2021-11-18 | Bioasis Technologies, Inc. | Compositions and methods for treating lewy body dementia |
| US20210393787A1 (en) | 2020-06-17 | 2021-12-23 | Bioasis Technologies, Inc. | Compositions and methods for treating frontotemporal dementia |
| KR20230073200A (ko) | 2020-08-20 | 2023-05-25 | 암브룩스, 인코포레이티드 | 항체-tlr 작용제 접합체, 그 방법 및 용도 |
| TW202246242A (zh) | 2021-01-15 | 2022-12-01 | 美商西健公司 | 免疫調節抗體藥物結合物 |
| CA3206244A1 (en) | 2021-02-03 | 2022-08-11 | Kung-Pern WANG | Immunostimulatory compounds and conjugates |
| US12036286B2 (en) | 2021-03-18 | 2024-07-16 | Seagen Inc. | Selective drug release from internalized conjugates of biologically active compounds |
| AU2022249223A1 (en) | 2021-04-03 | 2023-10-12 | Ambrx, Inc. | Anti-her2 antibody-drug conjugates and uses thereof |
| KR20240015670A (ko) | 2021-05-28 | 2024-02-05 | 씨젠 인크. | 안트라사이클린 항체 접합체 |
| EP4155349A1 (de) | 2021-09-24 | 2023-03-29 | Becton, Dickinson and Company | Wasserlösliche gelbe grünabsorbierende farbstoffe |
| IL312677A (en) | 2021-11-09 | 2024-07-01 | Tubulis Gmbh | Conjugates including phosphorus (V) and a camptothecin component |
| IL312675A (en) | 2021-11-09 | 2024-07-01 | Tubulis Gmbh | Conjugates involving phosphorus (V) and a drug component |
| MX2024011292A (es) | 2022-03-17 | 2024-09-27 | Seagen Inc | Conjugados de camptotecina. |
| CA3252067A1 (en) | 2022-05-06 | 2023-11-09 | Seagen Inc. | Immunomodulatory Antibody-Drug Conjugates |
| AU2023298234A1 (en) | 2022-07-01 | 2025-01-16 | Beckman Coulter, Inc. | Novel fluorescent dyes and polymers from dihydrophenanthrene derivatives |
| AU2023320054A1 (en) | 2022-08-03 | 2025-02-06 | Regents Of The University Of Minnesota | Immunostimulatory anti-pd-l1-drug conjugates |
| EP4321522A1 (de) | 2022-08-12 | 2024-02-14 | Seagen Inc. | Zytotoxische verbindungen und konjugate davon |
| WO2024044327A1 (en) | 2022-08-26 | 2024-02-29 | Beckman Coulter, Inc. | Dhnt monomers and polymer dyes with modified photophysical properties |
| JP2025536308A (ja) | 2022-10-18 | 2025-11-05 | テューブリス ゲーエムベーハー | 新規なNaPi2b抗体を有する新規な抗体-薬物コンジュゲート、治療的方法、ならびにそれらの使用 |
| CN120112312A (zh) | 2022-10-18 | 2025-06-06 | Tubulis 股份有限公司 | 新型抗-tpbg抗体和基于其的抗体-药物偶联物、其治疗方法及用途 |
| CN120417937A (zh) | 2022-11-17 | 2025-08-01 | 赛诺菲 | Ceacam5抗体-药物缀合物及其使用方法 |
| WO2024129756A1 (en) | 2022-12-13 | 2024-06-20 | Seagen Inc. | Site-specific engineered cysteine antibody drug conjugates |
| IL321506A (en) | 2022-12-22 | 2025-08-01 | Tubulis Gmbh | Conjugates comprising a phosphorus(v) moiety and a drug |
| WO2024196805A1 (en) | 2023-03-17 | 2024-09-26 | Beckman Coulter, Inc. | Benzothienopyrrole cyanine dyes |
| TW202506691A (zh) | 2023-04-20 | 2025-02-16 | 美商思進公司 | Sting促效劑化合物及其結合物 |
| WO2025046090A1 (en) | 2023-09-01 | 2025-03-06 | Tubulis Gmbh | Methods of preparing phosphonamidate compounds |
| WO2025064842A1 (en) | 2023-09-21 | 2025-03-27 | Beckman Coulter, Inc. | Dihydrophenanthrene (dhp) bridged dyes for use in flow cytometry |
| WO2025090774A1 (en) | 2023-10-24 | 2025-05-01 | Seagen Inc. | Chemotherapeutic compounds and methods of use |
| WO2025149947A1 (en) | 2024-01-12 | 2025-07-17 | Seagen Inc. | Antibody-drug conjugates |
Family Cites Families (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4835260A (en) * | 1987-03-20 | 1989-05-30 | Genetics Institute, Inc. | Erythropoietin composition |
| US5166322A (en) * | 1989-04-21 | 1992-11-24 | Genetics Institute | Cysteine added variants of interleukin-3 and chemical modifications thereof |
| US5267142A (en) | 1989-04-26 | 1993-11-30 | Fanuc Ltd. | Method for phase-synchronized spindle rotation control |
| KR100221066B1 (ko) * | 1989-10-13 | 1999-10-01 | 스튜어트 엘.왓트 | 에리트로포이에틴 유사체와 그를 포함하는 제약학적 조성물 |
| JPH03151399A (ja) | 1989-11-07 | 1991-06-27 | Snow Brand Milk Prod Co Ltd | 変異ヒトエリスロポエチン |
| CA2101918A1 (en) * | 1991-03-18 | 1992-09-19 | Samuel Zalipsky | Hydrazine containing conjugates of polypeptides and glycopolypeptides with polymers |
| RU2010858C1 (ru) * | 1991-07-03 | 1994-04-15 | Институт биохимии Литовской Академии наук | Способ иммобилизации алкогольоксидазы |
| NZ250375A (en) * | 1992-12-09 | 1995-07-26 | Ortho Pharma Corp | Peg hydrazone and peg oxime linkage forming reagents and protein derivatives |
| EP0744953A4 (de) | 1993-04-29 | 1998-05-06 | Abbott Lab | Zubereitungen und verfahren von erythropoietin-analogen |
| WO1994028024A1 (en) * | 1993-06-01 | 1994-12-08 | Enzon, Inc. | Carbohydrate-modified polymer conjugates with erythropoietic activity |
| ATE171650T1 (de) | 1993-06-03 | 1998-10-15 | Beckman Coulter Inc | Probentraeger |
| US5643575A (en) * | 1993-10-27 | 1997-07-01 | Enzon, Inc. | Non-antigenic branched polymer conjugates |
-
1997
- 1997-08-01 ES ES97936407T patent/ES2273373T3/es not_active Expired - Lifetime
- 1997-08-01 US US08/905,310 patent/US6077939A/en not_active Expired - Lifetime
- 1997-08-01 BR BR9711009A patent/BR9711009A/pt not_active Application Discontinuation
- 1997-08-01 AT AT97936407T patent/ATE341344T1/de active
- 1997-08-01 RU RU99103679/14A patent/RU2199347C2/ru active
- 1997-08-01 DK DK97936407T patent/DK0964702T3/da active
- 1997-08-01 KR KR1019997000751A patent/KR20000029673A/ko not_active Ceased
- 1997-08-01 CN CNB971968292A patent/CN100471521C/zh not_active Expired - Lifetime
- 1997-08-01 EP EP06020565A patent/EP1731174A3/de not_active Withdrawn
- 1997-08-01 WO PCT/US1997/013756 patent/WO1998005363A2/en not_active Ceased
- 1997-08-01 IL IL12822997A patent/IL128229A0/xx active IP Right Grant
- 1997-08-01 PT PT97936407T patent/PT964702E/pt unknown
- 1997-08-01 NZ NZ333993A patent/NZ333993A/xx not_active IP Right Cessation
- 1997-08-01 JP JP50817398A patent/JP4410852B2/ja not_active Expired - Lifetime
- 1997-08-01 EP EP97936407A patent/EP0964702B1/de not_active Expired - Lifetime
- 1997-08-01 CA CA002262994A patent/CA2262994A1/en not_active Abandoned
- 1997-08-01 SI SI9730755T patent/SI0964702T1/sl unknown
- 1997-08-01 DE DE69736780T patent/DE69736780T2/de not_active Expired - Lifetime
- 1997-08-01 AU AU39085/97A patent/AU3908597A/en not_active Abandoned
-
1999
- 1999-01-25 IL IL128229A patent/IL128229A/en not_active IP Right Cessation
- 1999-02-01 NO NO990465A patent/NO990465L/no not_active Application Discontinuation
Also Published As
| Publication number | Publication date |
|---|---|
| WO1998005363A3 (en) | 1998-05-07 |
| AU3908597A (en) | 1998-02-25 |
| CN100471521C (zh) | 2009-03-25 |
| EP1731174A3 (de) | 2007-01-17 |
| NO990465D0 (no) | 1999-02-01 |
| CA2262994A1 (en) | 1998-02-12 |
| IL128229A (en) | 2007-07-04 |
| ES2273373T3 (es) | 2007-05-01 |
| NZ333993A (en) | 2000-01-28 |
| JP4410852B2 (ja) | 2010-02-03 |
| EP0964702A2 (de) | 1999-12-22 |
| BR9711009A (pt) | 1999-08-17 |
| IL128229A0 (en) | 1999-11-30 |
| SI0964702T1 (sl) | 2007-02-28 |
| US6077939A (en) | 2000-06-20 |
| RU2199347C2 (ru) | 2003-02-27 |
| ATE341344T1 (de) | 2006-10-15 |
| NO990465L (no) | 1999-03-23 |
| KR20000029673A (ko) | 2000-05-25 |
| JP2000515553A (ja) | 2000-11-21 |
| PT964702E (pt) | 2006-12-29 |
| DK0964702T3 (da) | 2007-01-08 |
| EP0964702B1 (de) | 2006-10-04 |
| CN1226176A (zh) | 1999-08-18 |
| WO1998005363A2 (en) | 1998-02-12 |
| EP1731174A2 (de) | 2006-12-13 |
| DE69736780D1 (de) | 2006-11-16 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| DE69736780T2 (de) | Polypeptide mit einzelnem kovalent gebundenen n-terminalen wasserlöslichen polymer | |
| DE69935855T2 (de) | Ortsspezifische proteinmodifizierung durch mutagenese | |
| JP5334347B2 (ja) | 化学的に修飾した新規なエリスロポエチン刺激タンパク質組成物および方法 | |
| DE69430251T2 (de) | Verbesserte interferon-polymerkonjugate | |
| DE602004009314T2 (de) | Polysialinsäurederivate | |
| US7074755B2 (en) | Erythropoietin conjugate compounds with extended half-lives | |
| JP4025727B2 (ja) | Peg化およびジグリコシル化されたエリスロポエチン | |
| AU641991B2 (en) | Novel insulin compositions | |
| MXPA97003362A (en) | Conjugates of bdnf and nt-3 with a polymer solubleen a | |
| EP0799890A2 (de) | Rekombinante inaktive Core-Streptavidin Mutanten | |
| AU554929B2 (en) | Polypeptide-toxin hybrid protein | |
| JPWO1990006952A1 (ja) | 化学修飾顆粒球コロニー刺激因子 | |
| EP0305967A2 (de) | Konjugate von Interferon alpha mit Immunglobulinen | |
| DE3026398A1 (de) | Modifiziertes haemoglobin enthaltender blutersatz | |
| DE3876997T2 (de) | Konjugate von superoxiddismutase. | |
| DE4139001A1 (de) | Verfahren zur einschleusung von nukleinsaeuren in zellen | |
| DE69227276T2 (de) | Konjugate von Calcitonin und Polyethylenglycol | |
| AU2009218835B2 (en) | Selenium containing modifying agents and conjugates | |
| DE68917061T2 (de) | O-glycosylierter IGF-1. | |
| DE60313786T2 (de) | Poly(ethylen glykol)-konjugate von insulinähnlichem wachstumfaktor bindenden protein-4 | |
| EP1466614A1 (de) | Polypeptid, dessen konjugat doxorubicin enthält, und auf diesem basierende pharmazeutische zusammensetzung | |
| Ochiai et al. | Better Peptides via Chemical Glycosylation: Somatostatin Analogues Having a Human Complex‐Type N‐Glycan with Improved Drug Properties | |
| DE69612084T2 (de) | Wachstumsfaktor-Analoga | |
| AU778790B2 (en) | Polypeptides having a single covalently bound n-terminal water-soluble polymer | |
| DE19919148A1 (de) | Von Interleukin 12 abgeleitete Peptid-Homodimere und Peptid-Heterodimere |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 8364 | No opposition during term of opposition |