BR112016011052B1 - Instrumento configurado para interagir com um chip de análise em uma estrutura de suporte de chip, chip de análise, método para analisar um espécime, método para sequência de molécula de ácido nucleico alvo, método para sequência de ácido nucleico, aparelho e método para formar um aparelho - Google Patents
Instrumento configurado para interagir com um chip de análise em uma estrutura de suporte de chip, chip de análise, método para analisar um espécime, método para sequência de molécula de ácido nucleico alvo, método para sequência de ácido nucleico, aparelho e método para formar um aparelho Download PDFInfo
- Publication number
- BR112016011052B1 BR112016011052B1 BR112016011052-8A BR112016011052A BR112016011052B1 BR 112016011052 B1 BR112016011052 B1 BR 112016011052B1 BR 112016011052 A BR112016011052 A BR 112016011052A BR 112016011052 B1 BR112016011052 B1 BR 112016011052B1
- Authority
- BR
- Brazil
- Prior art keywords
- sample
- sample well
- chip
- excitation
- sensor
- Prior art date
Links
- 238000004458 analytical method Methods 0.000 title claims abstract description 206
- 238000000034 method Methods 0.000 title claims abstract description 142
- 150000007523 nucleic acids Chemical class 0.000 title claims abstract description 104
- 102000039446 nucleic acids Human genes 0.000 title claims abstract description 97
- 108020004707 nucleic acids Proteins 0.000 title claims abstract description 97
- 108091028043 Nucleic acid sequence Proteins 0.000 title claims description 8
- 230000005284 excitation Effects 0.000 claims abstract description 449
- 230000003287 optical effect Effects 0.000 claims abstract description 100
- 238000012163 sequencing technique Methods 0.000 claims abstract description 16
- 125000003729 nucleotide group Chemical group 0.000 claims description 87
- 239000002773 nucleotide Substances 0.000 claims description 58
- 238000009826 distribution Methods 0.000 claims description 48
- 230000003595 spectral effect Effects 0.000 claims description 33
- 230000002123 temporal effect Effects 0.000 claims description 29
- 102000004190 Enzymes Human genes 0.000 claims description 25
- 108090000790 Enzymes Proteins 0.000 claims description 25
- 238000006243 chemical reaction Methods 0.000 claims description 18
- 230000005291 magnetic effect Effects 0.000 claims description 18
- 238000010348 incorporation Methods 0.000 claims description 17
- 230000000379 polymerizing effect Effects 0.000 claims description 14
- 230000000295 complement effect Effects 0.000 claims description 13
- 238000001914 filtration Methods 0.000 claims description 9
- 230000001419 dependent effect Effects 0.000 claims description 8
- 238000006116 polymerization reaction Methods 0.000 claims description 7
- 230000004044 response Effects 0.000 claims description 6
- 230000004308 accommodation Effects 0.000 claims 1
- 239000000523 sample Substances 0.000 description 719
- 239000010410 layer Substances 0.000 description 314
- 239000000463 material Substances 0.000 description 126
- 230000008569 process Effects 0.000 description 72
- 230000005855 radiation Effects 0.000 description 62
- 230000008878 coupling Effects 0.000 description 40
- 238000010168 coupling process Methods 0.000 description 40
- 238000005859 coupling reaction Methods 0.000 description 40
- 239000004065 semiconductor Substances 0.000 description 39
- 238000012546 transfer Methods 0.000 description 37
- 238000001514 detection method Methods 0.000 description 36
- 239000010409 thin film Substances 0.000 description 35
- 239000010408 film Substances 0.000 description 34
- 239000000758 substrate Substances 0.000 description 34
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 30
- 239000004020 conductor Substances 0.000 description 27
- 238000012545 processing Methods 0.000 description 26
- 239000002096 quantum dot Substances 0.000 description 24
- 239000002245 particle Substances 0.000 description 23
- 238000004088 simulation Methods 0.000 description 22
- 230000001464 adherent effect Effects 0.000 description 19
- 239000006117 anti-reflective coating Substances 0.000 description 19
- 238000000576 coating method Methods 0.000 description 19
- 238000000151 deposition Methods 0.000 description 18
- 238000003860 storage Methods 0.000 description 18
- 210000004027 cell Anatomy 0.000 description 17
- 239000011159 matrix material Substances 0.000 description 17
- 239000002184 metal Substances 0.000 description 16
- 238000004166 bioassay Methods 0.000 description 15
- 230000008021 deposition Effects 0.000 description 15
- 230000015654 memory Effects 0.000 description 15
- 229910052751 metal Inorganic materials 0.000 description 15
- 230000002285 radioactive effect Effects 0.000 description 15
- 238000005070 sampling Methods 0.000 description 15
- 239000003989 dielectric material Substances 0.000 description 14
- 238000005530 etching Methods 0.000 description 14
- 238000002161 passivation Methods 0.000 description 14
- 239000012472 biological sample Substances 0.000 description 13
- 230000000875 corresponding effect Effects 0.000 description 13
- 238000004519 manufacturing process Methods 0.000 description 13
- 230000000873 masking effect Effects 0.000 description 13
- 239000000377 silicon dioxide Substances 0.000 description 13
- 229910019142 PO4 Inorganic materials 0.000 description 12
- 238000010521 absorption reaction Methods 0.000 description 12
- 238000009825 accumulation Methods 0.000 description 12
- 238000000295 emission spectrum Methods 0.000 description 12
- 235000021317 phosphate Nutrition 0.000 description 12
- 229920002477 rna polymer Polymers 0.000 description 12
- 201000009310 astigmatism Diseases 0.000 description 11
- 239000011248 coating agent Substances 0.000 description 11
- 230000000737 periodic effect Effects 0.000 description 11
- 229920001296 polysiloxane Polymers 0.000 description 11
- 108090000623 proteins and genes Proteins 0.000 description 11
- 239000000126 substance Substances 0.000 description 11
- 108020004414 DNA Proteins 0.000 description 10
- 102000053602 DNA Human genes 0.000 description 10
- 239000000853 adhesive Substances 0.000 description 10
- 230000001070 adhesive effect Effects 0.000 description 10
- 230000008033 biological extinction Effects 0.000 description 10
- 238000005137 deposition process Methods 0.000 description 10
- 230000000694 effects Effects 0.000 description 10
- 239000002777 nucleoside Substances 0.000 description 10
- 239000010452 phosphate Substances 0.000 description 10
- 229920002120 photoresistant polymer Polymers 0.000 description 10
- 235000012239 silicon dioxide Nutrition 0.000 description 10
- 239000005547 deoxyribonucleotide Substances 0.000 description 9
- 239000000835 fiber Substances 0.000 description 9
- 238000001459 lithography Methods 0.000 description 9
- 229920000388 Polyphosphate Polymers 0.000 description 8
- 238000004891 communication Methods 0.000 description 8
- 125000002637 deoxyribonucleotide group Chemical group 0.000 description 8
- 230000005672 electromagnetic field Effects 0.000 description 8
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 8
- 238000000206 photolithography Methods 0.000 description 8
- 239000001205 polyphosphate Substances 0.000 description 8
- 235000011176 polyphosphates Nutrition 0.000 description 8
- 102000004169 proteins and genes Human genes 0.000 description 8
- 238000001228 spectrum Methods 0.000 description 8
- 230000009466 transformation Effects 0.000 description 8
- 230000015572 biosynthetic process Effects 0.000 description 7
- 238000004020 luminiscence type Methods 0.000 description 7
- -1 nucleoside monophosphate Chemical class 0.000 description 7
- 239000007787 solid Substances 0.000 description 7
- YBJHBAHKTGYVGT-ZKWXMUAHSA-N (+)-Biotin Chemical compound N1C(=O)N[C@@H]2[C@H](CCCCC(=O)O)SC[C@@H]21 YBJHBAHKTGYVGT-ZKWXMUAHSA-N 0.000 description 6
- IOVCWXUNBOPUCH-UHFFFAOYSA-M Nitrite anion Chemical compound [O-]N=O IOVCWXUNBOPUCH-UHFFFAOYSA-M 0.000 description 6
- ISAKRJDGNUQOIC-UHFFFAOYSA-N Uracil Chemical compound O=C1C=CNC(=O)N1 ISAKRJDGNUQOIC-UHFFFAOYSA-N 0.000 description 6
- 238000000862 absorption spectrum Methods 0.000 description 6
- 229910052782 aluminium Inorganic materials 0.000 description 6
- 239000008280 blood Substances 0.000 description 6
- 210000004369 blood Anatomy 0.000 description 6
- 230000008859 change Effects 0.000 description 6
- OPTASPLRGRRNAP-UHFFFAOYSA-N cytosine Chemical compound NC=1C=CNC(=O)N=1 OPTASPLRGRRNAP-UHFFFAOYSA-N 0.000 description 6
- 238000005516 engineering process Methods 0.000 description 6
- 239000000945 filler Substances 0.000 description 6
- 229910052732 germanium Inorganic materials 0.000 description 6
- GNPVGFCGXDBREM-UHFFFAOYSA-N germanium atom Chemical compound [Ge] GNPVGFCGXDBREM-UHFFFAOYSA-N 0.000 description 6
- 229910052737 gold Inorganic materials 0.000 description 6
- 239000010931 gold Substances 0.000 description 6
- UYTPUPDQBNUYGX-UHFFFAOYSA-N guanine Chemical compound O=C1NC(N)=NC2=C1N=CN2 UYTPUPDQBNUYGX-UHFFFAOYSA-N 0.000 description 6
- 239000003550 marker Substances 0.000 description 6
- 150000003833 nucleoside derivatives Chemical class 0.000 description 6
- 125000002467 phosphate group Chemical group [H]OP(=O)(O[H])O[*] 0.000 description 6
- 125000006850 spacer group Chemical group 0.000 description 6
- RWQNBRDOKXIBIV-UHFFFAOYSA-N thymine Chemical compound CC1=CNC(=O)NC1=O RWQNBRDOKXIBIV-UHFFFAOYSA-N 0.000 description 6
- 108020004635 Complementary DNA Proteins 0.000 description 5
- AHCYMLUZIRLXAA-SHYZEUOFSA-N Deoxyuridine 5'-triphosphate Chemical compound O1[C@H](COP(O)(=O)OP(O)(=O)OP(O)(O)=O)[C@@H](O)C[C@@H]1N1C(=O)NC(=O)C=C1 AHCYMLUZIRLXAA-SHYZEUOFSA-N 0.000 description 5
- 102100034343 Integrase Human genes 0.000 description 5
- 108010092799 RNA-directed DNA polymerase Proteins 0.000 description 5
- 229910045601 alloy Inorganic materials 0.000 description 5
- 239000000956 alloy Substances 0.000 description 5
- 230000003321 amplification Effects 0.000 description 5
- 210000001124 body fluid Anatomy 0.000 description 5
- 238000010804 cDNA synthesis Methods 0.000 description 5
- 238000005229 chemical vapour deposition Methods 0.000 description 5
- 239000002299 complementary DNA Substances 0.000 description 5
- 230000002596 correlated effect Effects 0.000 description 5
- RGWHQCVHVJXOKC-SHYZEUOFSA-N dCTP Chemical compound O=C1N=C(N)C=CN1[C@@H]1O[C@H](CO[P@](O)(=O)O[P@](O)(=O)OP(O)(O)=O)[C@@H](O)C1 RGWHQCVHVJXOKC-SHYZEUOFSA-N 0.000 description 5
- HAAZLUGHYHWQIW-KVQBGUIXSA-N dGTP Chemical compound C1=NC=2C(=O)NC(N)=NC=2N1[C@H]1C[C@H](O)[C@@H](COP(O)(=O)OP(O)(=O)OP(O)(O)=O)O1 HAAZLUGHYHWQIW-KVQBGUIXSA-N 0.000 description 5
- 238000002405 diagnostic procedure Methods 0.000 description 5
- 238000002866 fluorescence resonance energy transfer Methods 0.000 description 5
- 230000006872 improvement Effects 0.000 description 5
- 230000000670 limiting effect Effects 0.000 description 5
- 238000000386 microscopy Methods 0.000 description 5
- 238000003199 nucleic acid amplification method Methods 0.000 description 5
- 238000005289 physical deposition Methods 0.000 description 5
- 238000005554 pickling Methods 0.000 description 5
- 230000010287 polarization Effects 0.000 description 5
- 239000002243 precursor Substances 0.000 description 5
- 108010014303 DNA-directed DNA polymerase Proteins 0.000 description 4
- 102000016928 DNA-directed DNA polymerase Human genes 0.000 description 4
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 4
- 230000008901 benefit Effects 0.000 description 4
- 239000003153 chemical reaction reagent Substances 0.000 description 4
- 210000000349 chromosome Anatomy 0.000 description 4
- 238000010586 diagram Methods 0.000 description 4
- 238000001704 evaporation Methods 0.000 description 4
- 230000008020 evaporation Effects 0.000 description 4
- 230000006870 function Effects 0.000 description 4
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 4
- 229910010272 inorganic material Inorganic materials 0.000 description 4
- 239000011147 inorganic material Substances 0.000 description 4
- 238000003780 insertion Methods 0.000 description 4
- 230000037431 insertion Effects 0.000 description 4
- 150000002500 ions Chemical class 0.000 description 4
- 150000002739 metals Chemical class 0.000 description 4
- 238000000465 moulding Methods 0.000 description 4
- 230000002093 peripheral effect Effects 0.000 description 4
- 102000054765 polymorphisms of proteins Human genes 0.000 description 4
- 229910052709 silver Inorganic materials 0.000 description 4
- 230000002194 synthesizing effect Effects 0.000 description 4
- 210000001519 tissue Anatomy 0.000 description 4
- 229910052719 titanium Inorganic materials 0.000 description 4
- 239000010936 titanium Substances 0.000 description 4
- 239000012780 transparent material Substances 0.000 description 4
- 239000001226 triphosphate Substances 0.000 description 4
- 235000011178 triphosphate Nutrition 0.000 description 4
- 238000001039 wet etching Methods 0.000 description 4
- 108091028664 Ribonucleotide Proteins 0.000 description 3
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical compound [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 description 3
- ATJFFYVFTNAWJD-UHFFFAOYSA-N Tin Chemical compound [Sn] ATJFFYVFTNAWJD-UHFFFAOYSA-N 0.000 description 3
- 239000002250 absorbent Substances 0.000 description 3
- 230000002745 absorbent Effects 0.000 description 3
- 230000009471 action Effects 0.000 description 3
- PNEYBMLMFCGWSK-UHFFFAOYSA-N aluminium oxide Inorganic materials [O-2].[O-2].[O-2].[Al+3].[Al+3] PNEYBMLMFCGWSK-UHFFFAOYSA-N 0.000 description 3
- 150000001413 amino acids Chemical class 0.000 description 3
- 230000003667 anti-reflective effect Effects 0.000 description 3
- 238000003491 array Methods 0.000 description 3
- 238000011953 bioanalysis Methods 0.000 description 3
- 230000005540 biological transmission Effects 0.000 description 3
- 229960002685 biotin Drugs 0.000 description 3
- 235000020958 biotin Nutrition 0.000 description 3
- 239000011616 biotin Substances 0.000 description 3
- 229910052681 coesite Inorganic materials 0.000 description 3
- 239000012141 concentrate Substances 0.000 description 3
- 239000000470 constituent Substances 0.000 description 3
- 229910052802 copper Inorganic materials 0.000 description 3
- 239000010949 copper Substances 0.000 description 3
- 229910052906 cristobalite Inorganic materials 0.000 description 3
- 239000013078 crystal Substances 0.000 description 3
- 229940104302 cytosine Drugs 0.000 description 3
- NHVNXKFIZYSCEB-XLPZGREQSA-N dTTP Chemical compound O=C1NC(=O)C(C)=CN1[C@@H]1O[C@H](COP(O)(=O)OP(O)(=O)OP(O)(O)=O)[C@@H](O)C1 NHVNXKFIZYSCEB-XLPZGREQSA-N 0.000 description 3
- 230000007547 defect Effects 0.000 description 3
- 238000004049 embossing Methods 0.000 description 3
- 238000001900 extreme ultraviolet lithography Methods 0.000 description 3
- 239000012530 fluid Substances 0.000 description 3
- 238000009396 hybridization Methods 0.000 description 3
- 238000002164 ion-beam lithography Methods 0.000 description 3
- 238000005259 measurement Methods 0.000 description 3
- 230000007246 mechanism Effects 0.000 description 3
- 230000005055 memory storage Effects 0.000 description 3
- 229910001092 metal group alloy Inorganic materials 0.000 description 3
- 238000001465 metallisation Methods 0.000 description 3
- 238000001668 nucleic acid synthesis Methods 0.000 description 3
- 238000001020 plasma etching Methods 0.000 description 3
- 239000004033 plastic Substances 0.000 description 3
- 229920003023 plastic Polymers 0.000 description 3
- 238000010791 quenching Methods 0.000 description 3
- 230000000171 quenching effect Effects 0.000 description 3
- 238000002310 reflectometry Methods 0.000 description 3
- 239000002336 ribonucleotide Substances 0.000 description 3
- 125000002652 ribonucleotide group Chemical group 0.000 description 3
- 210000003296 saliva Anatomy 0.000 description 3
- 229910052710 silicon Inorganic materials 0.000 description 3
- 239000010703 silicon Substances 0.000 description 3
- 229910052814 silicon oxide Inorganic materials 0.000 description 3
- 229910052682 stishovite Inorganic materials 0.000 description 3
- 238000003786 synthesis reaction Methods 0.000 description 3
- 229940113082 thymine Drugs 0.000 description 3
- 229910052718 tin Inorganic materials 0.000 description 3
- XOUPWBJVJFQSLK-UHFFFAOYSA-J titanium(4+);tetranitrite Chemical compound [Ti+4].[O-]N=O.[O-]N=O.[O-]N=O.[O-]N=O XOUPWBJVJFQSLK-UHFFFAOYSA-J 0.000 description 3
- 229910052905 tridymite Inorganic materials 0.000 description 3
- 229940035893 uracil Drugs 0.000 description 3
- 210000002700 urine Anatomy 0.000 description 3
- ASJSAQIRZKANQN-CRCLSJGQSA-N 2-deoxy-D-ribose Chemical compound OC[C@@H](O)[C@@H](O)CC=O ASJSAQIRZKANQN-CRCLSJGQSA-N 0.000 description 2
- KDCGOANMDULRCW-UHFFFAOYSA-N 7H-purine Chemical compound N1=CNC2=NC=NC2=C1 KDCGOANMDULRCW-UHFFFAOYSA-N 0.000 description 2
- 229930024421 Adenine Natural products 0.000 description 2
- GFFGJBXGBJISGV-UHFFFAOYSA-N Adenine Chemical compound NC1=NC=NC2=C1N=CN2 GFFGJBXGBJISGV-UHFFFAOYSA-N 0.000 description 2
- 241000713838 Avian myeloblastosis virus Species 0.000 description 2
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 2
- 108010017826 DNA Polymerase I Proteins 0.000 description 2
- 102000004594 DNA Polymerase I Human genes 0.000 description 2
- 102000004163 DNA-directed RNA polymerases Human genes 0.000 description 2
- 108090000626 DNA-directed RNA polymerases Proteins 0.000 description 2
- 239000002202 Polyethylene glycol Substances 0.000 description 2
- 108010019653 Pwo polymerase Proteins 0.000 description 2
- PYMYPHUHKUWMLA-LMVFSUKVSA-N Ribose Natural products OC[C@@H](O)[C@@H](O)[C@@H](O)C=O PYMYPHUHKUWMLA-LMVFSUKVSA-N 0.000 description 2
- 229910052581 Si3N4 Inorganic materials 0.000 description 2
- BQCADISMDOOEFD-UHFFFAOYSA-N Silver Chemical compound [Ag] BQCADISMDOOEFD-UHFFFAOYSA-N 0.000 description 2
- 108010006785 Taq Polymerase Proteins 0.000 description 2
- RTAQQCXQSZGOHL-UHFFFAOYSA-N Titanium Chemical compound [Ti] RTAQQCXQSZGOHL-UHFFFAOYSA-N 0.000 description 2
- 108010001244 Tli polymerase Proteins 0.000 description 2
- 108010020713 Tth polymerase Proteins 0.000 description 2
- NHWNVPNZGGXQQV-UHFFFAOYSA-J [Si+4].[O-]N=O.[O-]N=O.[O-]N=O.[O-]N=O Chemical compound [Si+4].[O-]N=O.[O-]N=O.[O-]N=O.[O-]N=O NHWNVPNZGGXQQV-UHFFFAOYSA-J 0.000 description 2
- 229960000643 adenine Drugs 0.000 description 2
- OIRDTQYFTABQOQ-KQYNXXCUSA-N adenosine group Chemical group [C@@H]1([C@H](O)[C@H](O)[C@@H](CO)O1)N1C=NC=2C(N)=NC=NC12 OIRDTQYFTABQOQ-KQYNXXCUSA-N 0.000 description 2
- 230000002411 adverse Effects 0.000 description 2
- HMFHBZSHGGEWLO-UHFFFAOYSA-N alpha-D-Furanose-Ribose Natural products OCC1OC(O)C(O)C1O HMFHBZSHGGEWLO-UHFFFAOYSA-N 0.000 description 2
- 238000000231 atomic layer deposition Methods 0.000 description 2
- 239000010839 body fluid Substances 0.000 description 2
- 239000000872 buffer Substances 0.000 description 2
- 239000011651 chromium Substances 0.000 description 2
- 239000011247 coating layer Substances 0.000 description 2
- 230000001427 coherent effect Effects 0.000 description 2
- 239000003086 colorant Substances 0.000 description 2
- 238000005056 compaction Methods 0.000 description 2
- 230000001276 controlling effect Effects 0.000 description 2
- 238000007405 data analysis Methods 0.000 description 2
- 230000003247 decreasing effect Effects 0.000 description 2
- 238000012217 deletion Methods 0.000 description 2
- 230000037430 deletion Effects 0.000 description 2
- 238000006073 displacement reaction Methods 0.000 description 2
- 238000001312 dry etching Methods 0.000 description 2
- 230000005684 electric field Effects 0.000 description 2
- 238000000609 electron-beam lithography Methods 0.000 description 2
- 230000005281 excited state Effects 0.000 description 2
- 239000007850 fluorescent dye Substances 0.000 description 2
- 125000000524 functional group Chemical group 0.000 description 2
- 230000002068 genetic effect Effects 0.000 description 2
- 230000036541 health Effects 0.000 description 2
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 2
- 238000003384 imaging method Methods 0.000 description 2
- 239000012212 insulator Substances 0.000 description 2
- 230000001788 irregular Effects 0.000 description 2
- 239000007788 liquid Substances 0.000 description 2
- 230000014759 maintenance of location Effects 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- 229910052755 nonmetal Inorganic materials 0.000 description 2
- 239000013307 optical fiber Substances 0.000 description 2
- 230000037361 pathway Effects 0.000 description 2
- 150000003013 phosphoric acid derivatives Chemical class 0.000 description 2
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Chemical compound [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 description 2
- 238000005498 polishing Methods 0.000 description 2
- 229920001223 polyethylene glycol Polymers 0.000 description 2
- 229920000642 polymer Polymers 0.000 description 2
- 238000003752 polymerase chain reaction Methods 0.000 description 2
- 229920001184 polypeptide Polymers 0.000 description 2
- 102000004196 processed proteins & peptides Human genes 0.000 description 2
- 108090000765 processed proteins & peptides Proteins 0.000 description 2
- 238000004445 quantitative analysis Methods 0.000 description 2
- 230000009467 reduction Effects 0.000 description 2
- 230000002829 reductive effect Effects 0.000 description 2
- PYWVYCXTNDRMGF-UHFFFAOYSA-N rhodamine B Chemical compound [Cl-].C=12C=CC(=[N+](CC)CC)C=C2OC2=CC(N(CC)CC)=CC=C2C=1C1=CC=CC=C1C(O)=O PYWVYCXTNDRMGF-UHFFFAOYSA-N 0.000 description 2
- 238000000926 separation method Methods 0.000 description 2
- 239000004332 silver Substances 0.000 description 2
- 239000010944 silver (metal) Substances 0.000 description 2
- 238000004557 single molecule detection Methods 0.000 description 2
- 241000894007 species Species 0.000 description 2
- 239000007858 starting material Substances 0.000 description 2
- 230000008685 targeting Effects 0.000 description 2
- 239000011135 tin Substances 0.000 description 2
- 238000012549 training Methods 0.000 description 2
- UNXRWKVEANCORM-UHFFFAOYSA-N triphosphoric acid Chemical compound OP(O)(=O)OP(O)(=O)OP(O)(O)=O UNXRWKVEANCORM-UHFFFAOYSA-N 0.000 description 2
- 238000005406 washing Methods 0.000 description 2
- 229910016570 AlCu Inorganic materials 0.000 description 1
- 239000012114 Alexa Fluor 647 Substances 0.000 description 1
- 229910000789 Aluminium-silicon alloy Inorganic materials 0.000 description 1
- 239000002126 C01EB10 - Adenosine Substances 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- VYZAMTAEIAYCRO-UHFFFAOYSA-N Chromium Chemical compound [Cr] VYZAMTAEIAYCRO-UHFFFAOYSA-N 0.000 description 1
- 108091026890 Coding region Proteins 0.000 description 1
- HMFHBZSHGGEWLO-SOOFDHNKSA-N D-ribofuranose Chemical compound OC[C@H]1OC(O)[C@H](O)[C@@H]1O HMFHBZSHGGEWLO-SOOFDHNKSA-N 0.000 description 1
- 108050009160 DNA polymerase 1 Proteins 0.000 description 1
- 238000001712 DNA sequencing Methods 0.000 description 1
- 101150040913 DUT gene Proteins 0.000 description 1
- 102100036254 E3 SUMO-protein ligase PIAS2 Human genes 0.000 description 1
- 241000588724 Escherichia coli Species 0.000 description 1
- XPDWGBQVDMORPB-UHFFFAOYSA-N Fluoroform Chemical compound FC(F)F XPDWGBQVDMORPB-UHFFFAOYSA-N 0.000 description 1
- 229910001218 Gallium arsenide Inorganic materials 0.000 description 1
- 108010078851 HIV Reverse Transcriptase Proteins 0.000 description 1
- 241000725303 Human immunodeficiency virus Species 0.000 description 1
- 102000003960 Ligases Human genes 0.000 description 1
- 108090000364 Ligases Proteins 0.000 description 1
- 241001529936 Murinae Species 0.000 description 1
- 241000699670 Mus sp. Species 0.000 description 1
- 206010028980 Neoplasm Diseases 0.000 description 1
- 108700026244 Open Reading Frames Proteins 0.000 description 1
- 229940123973 Oxygen scavenger Drugs 0.000 description 1
- 108010002747 Pfu DNA polymerase Proteins 0.000 description 1
- 108010010677 Phosphodiesterase I Proteins 0.000 description 1
- ABLZXFCXXLZCGV-UHFFFAOYSA-N Phosphorous acid Chemical compound OP(O)=O ABLZXFCXXLZCGV-UHFFFAOYSA-N 0.000 description 1
- CZPWVGJYEJSRLH-UHFFFAOYSA-N Pyrimidine Chemical compound C1=CN=CN=C1 CZPWVGJYEJSRLH-UHFFFAOYSA-N 0.000 description 1
- 229910000577 Silicon-germanium Inorganic materials 0.000 description 1
- 229910000831 Steel Inorganic materials 0.000 description 1
- 108010017842 Telomerase Proteins 0.000 description 1
- 102100032938 Telomerase reverse transcriptase Human genes 0.000 description 1
- 241000700605 Viruses Species 0.000 description 1
- 238000001015 X-ray lithography Methods 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 150000007513 acids Chemical class 0.000 description 1
- 229960005305 adenosine Drugs 0.000 description 1
- 238000013019 agitation Methods 0.000 description 1
- 125000005600 alkyl phosphonate group Chemical group 0.000 description 1
- 125000003277 amino group Chemical group 0.000 description 1
- 238000003556 assay Methods 0.000 description 1
- 230000006399 behavior Effects 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- 239000011230 binding agent Substances 0.000 description 1
- 239000000090 biomarker Substances 0.000 description 1
- 238000005422 blasting Methods 0.000 description 1
- 238000009534 blood test Methods 0.000 description 1
- 201000011510 cancer Diseases 0.000 description 1
- 229910052799 carbon Inorganic materials 0.000 description 1
- 238000005266 casting Methods 0.000 description 1
- 239000013043 chemical agent Substances 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 229910052804 chromium Inorganic materials 0.000 description 1
- 230000002759 chromosomal effect Effects 0.000 description 1
- 230000000052 comparative effect Effects 0.000 description 1
- 239000002131 composite material Substances 0.000 description 1
- 238000004590 computer program Methods 0.000 description 1
- 230000001268 conjugating effect Effects 0.000 description 1
- 238000011109 contamination Methods 0.000 description 1
- 238000007728 cost analysis Methods 0.000 description 1
- SUYVUBYJARFZHO-RRKCRQDMSA-N dATP Chemical compound C1=NC=2C(N)=NC=NC=2N1[C@H]1C[C@H](O)[C@@H](COP(O)(=O)OP(O)(=O)OP(O)(O)=O)O1 SUYVUBYJARFZHO-RRKCRQDMSA-N 0.000 description 1
- 230000002939 deleterious effect Effects 0.000 description 1
- 230000023077 detection of light stimulus Effects 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 230000004069 differentiation Effects 0.000 description 1
- 239000001177 diphosphate Substances 0.000 description 1
- 235000011180 diphosphates Nutrition 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- 239000000428 dust Substances 0.000 description 1
- 230000005670 electromagnetic radiation Effects 0.000 description 1
- 238000005566 electron beam evaporation Methods 0.000 description 1
- 238000001017 electron-beam sputter deposition Methods 0.000 description 1
- 238000000407 epitaxy Methods 0.000 description 1
- 238000000802 evaporation-induced self-assembly Methods 0.000 description 1
- 230000007717 exclusion Effects 0.000 description 1
- 230000002349 favourable effect Effects 0.000 description 1
- 230000005294 ferromagnetic effect Effects 0.000 description 1
- 239000003269 fluorescent indicator Substances 0.000 description 1
- 102000034287 fluorescent proteins Human genes 0.000 description 1
- 108091006047 fluorescent proteins Proteins 0.000 description 1
- 239000005350 fused silica glass Substances 0.000 description 1
- 239000007789 gas Substances 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 229910021389 graphene Inorganic materials 0.000 description 1
- 125000001188 haloalkyl group Chemical group 0.000 description 1
- 238000007654 immersion Methods 0.000 description 1
- 238000007373 indentation Methods 0.000 description 1
- 239000003999 initiator Substances 0.000 description 1
- 230000003993 interaction Effects 0.000 description 1
- 238000005468 ion implantation Methods 0.000 description 1
- 238000010884 ion-beam technique Methods 0.000 description 1
- 238000002372 labelling Methods 0.000 description 1
- 238000011005 laboratory method Methods 0.000 description 1
- 208000032839 leukemia Diseases 0.000 description 1
- 150000002632 lipids Chemical class 0.000 description 1
- GQYHUHYESMUTHG-UHFFFAOYSA-N lithium niobate Chemical compound [Li+].[O-][Nb](=O)=O GQYHUHYESMUTHG-UHFFFAOYSA-N 0.000 description 1
- 230000004807 localization Effects 0.000 description 1
- 230000001404 mediated effect Effects 0.000 description 1
- 238000003801 milling Methods 0.000 description 1
- 239000000203 mixture Substances 0.000 description 1
- 239000003068 molecular probe Substances 0.000 description 1
- 238000005232 molecular self-assembly Methods 0.000 description 1
- 238000001127 nanoimprint lithography Methods 0.000 description 1
- 239000002086 nanomaterial Substances 0.000 description 1
- 239000002070 nanowire Substances 0.000 description 1
- 150000002843 nonmetals Chemical class 0.000 description 1
- NJPPVKZQTLUDBO-UHFFFAOYSA-N novaluron Chemical compound C1=C(Cl)C(OC(F)(F)C(OC(F)(F)F)F)=CC=C1NC(=O)NC(=O)C1=C(F)C=CC=C1F NJPPVKZQTLUDBO-UHFFFAOYSA-N 0.000 description 1
- 238000003203 nucleic acid sequencing method Methods 0.000 description 1
- 125000003835 nucleoside group Chemical group 0.000 description 1
- 238000005457 optimization Methods 0.000 description 1
- 230000010355 oscillation Effects 0.000 description 1
- 230000003647 oxidation Effects 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- 230000001590 oxidative effect Effects 0.000 description 1
- 230000007170 pathology Effects 0.000 description 1
- 238000000059 patterning Methods 0.000 description 1
- PTMHPRAIXMAOOB-UHFFFAOYSA-L phosphoramidate Chemical compound NP([O-])([O-])=O PTMHPRAIXMAOOB-UHFFFAOYSA-L 0.000 description 1
- 238000000623 plasma-assisted chemical vapour deposition Methods 0.000 description 1
- 238000007747 plating Methods 0.000 description 1
- 229910052697 platinum Inorganic materials 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 238000003825 pressing Methods 0.000 description 1
- 238000003672 processing method Methods 0.000 description 1
- 230000001902 propagating effect Effects 0.000 description 1
- 230000001681 protective effect Effects 0.000 description 1
- 238000011002 quantification Methods 0.000 description 1
- 238000013139 quantization Methods 0.000 description 1
- 239000013079 quasicrystal Substances 0.000 description 1
- 230000000717 retained effect Effects 0.000 description 1
- 238000010839 reverse transcription Methods 0.000 description 1
- 230000002441 reversible effect Effects 0.000 description 1
- 238000012552 review Methods 0.000 description 1
- 125000000548 ribosyl group Chemical group C1([C@H](O)[C@H](O)[C@H](O1)CO)* 0.000 description 1
- 238000007493 shaping process Methods 0.000 description 1
- HQVNEWCFYHHQES-UHFFFAOYSA-N silicon nitride Chemical compound N12[Si]34N5[Si]62N3[Si]51N64 HQVNEWCFYHHQES-UHFFFAOYSA-N 0.000 description 1
- 239000002356 single layer Substances 0.000 description 1
- 239000007779 soft material Substances 0.000 description 1
- 238000004544 sputter deposition Methods 0.000 description 1
- 230000006641 stabilisation Effects 0.000 description 1
- 238000011105 stabilization Methods 0.000 description 1
- 239000010959 steel Substances 0.000 description 1
- 230000001629 suppression Effects 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 230000001360 synchronised effect Effects 0.000 description 1
- 238000001308 synthesis method Methods 0.000 description 1
- 238000012360 testing method Methods 0.000 description 1
- 238000002207 thermal evaporation Methods 0.000 description 1
- 150000007970 thio esters Chemical class 0.000 description 1
- 125000003396 thiol group Chemical group [H]S* 0.000 description 1
- 230000001052 transient effect Effects 0.000 description 1
- 230000005945 translocation Effects 0.000 description 1
- 230000007723 transport mechanism Effects 0.000 description 1
- 238000005019 vapor deposition process Methods 0.000 description 1
- 229920002554 vinyl polymer Polymers 0.000 description 1
- 230000000007 visual effect Effects 0.000 description 1
- 230000036642 wellbeing Effects 0.000 description 1
Images
Classifications
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L3/00—Containers or dishes for laboratory use, e.g. laboratory glassware; Droppers
- B01L3/50—Containers for the purpose of retaining a material to be analysed, e.g. test tubes
- B01L3/508—Containers for the purpose of retaining a material to be analysed, e.g. test tubes rigid containers not provided for above
- B01L3/5085—Containers for the purpose of retaining a material to be analysed, e.g. test tubes rigid containers not provided for above for multiple samples, e.g. microtitration plates
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/62—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light
- G01N21/63—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light optically excited
- G01N21/64—Fluorescence; Phosphorescence
- G01N21/6486—Measuring fluorescence of biological material, e.g. DNA, RNA, cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6869—Methods for sequencing
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6869—Methods for sequencing
- C12Q1/6874—Methods for sequencing involving nucleic acid arrays, e.g. sequencing by hybridisation
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/62—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light
- G01N21/63—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light optically excited
- G01N21/64—Fluorescence; Phosphorescence
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/62—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light
- G01N21/63—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light optically excited
- G01N21/64—Fluorescence; Phosphorescence
- G01N21/645—Specially adapted constructive features of fluorimeters
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/62—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light
- G01N21/63—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light optically excited
- G01N21/64—Fluorescence; Phosphorescence
- G01N21/645—Specially adapted constructive features of fluorimeters
- G01N21/6452—Individual samples arranged in a regular 2D-array, e.g. multiwell plates
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/62—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light
- G01N21/63—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light optically excited
- G01N21/64—Fluorescence; Phosphorescence
- G01N21/645—Specially adapted constructive features of fluorimeters
- G01N21/648—Specially adapted constructive features of fluorimeters using evanescent coupling or surface plasmon coupling for the excitation of fluorescence
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/75—Systems in which material is subjected to a chemical reaction, the progress or the result of the reaction being investigated
- G01N21/77—Systems in which material is subjected to a chemical reaction, the progress or the result of the reaction being investigated by observing the effect on a chemical indicator
- G01N21/7703—Systems in which material is subjected to a chemical reaction, the progress or the result of the reaction being investigated by observing the effect on a chemical indicator using reagent-clad optical fibres or optical waveguides
- G01N21/774—Systems in which material is subjected to a chemical reaction, the progress or the result of the reaction being investigated by observing the effect on a chemical indicator using reagent-clad optical fibres or optical waveguides the reagent being on a grating or periodic structure
- G01N21/7743—Systems in which material is subjected to a chemical reaction, the progress or the result of the reaction being investigated by observing the effect on a chemical indicator using reagent-clad optical fibres or optical waveguides the reagent being on a grating or periodic structure the reagent-coated grating coupling light in or out of the waveguide
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/75—Systems in which material is subjected to a chemical reaction, the progress or the result of the reaction being investigated
- G01N21/77—Systems in which material is subjected to a chemical reaction, the progress or the result of the reaction being investigated by observing the effect on a chemical indicator
- G01N21/7703—Systems in which material is subjected to a chemical reaction, the progress or the result of the reaction being investigated by observing the effect on a chemical indicator using reagent-clad optical fibres or optical waveguides
- G01N21/7746—Systems in which material is subjected to a chemical reaction, the progress or the result of the reaction being investigated by observing the effect on a chemical indicator using reagent-clad optical fibres or optical waveguides the waveguide coupled to a cavity resonator
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2200/00—Solutions for specific problems relating to chemical or physical laboratory apparatus
- B01L2200/12—Specific details about manufacturing devices
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2300/00—Additional constructional details
- B01L2300/08—Geometry, shape and general structure
- B01L2300/0809—Geometry, shape and general structure rectangular shaped
- B01L2300/0829—Multi-well plates; Microtitration plates
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2300/00—Additional constructional details
- B01L2300/08—Geometry, shape and general structure
- B01L2300/0887—Laminated structure
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2300/00—Additional constructional details
- B01L2300/08—Geometry, shape and general structure
- B01L2300/0893—Geometry, shape and general structure having a very large number of wells, microfabricated wells
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2300/00—Additional constructional details
- B01L2300/16—Surface properties and coatings
- B01L2300/168—Specific optical properties, e.g. reflective coatings
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2521/00—Reaction characterised by the enzymatic activity
- C12Q2521/10—Nucleotidyl transfering
- C12Q2521/101—DNA polymerase
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2525/00—Reactions involving modified oligonucleotides, nucleic acids, or nucleotides
- C12Q2525/10—Modifications characterised by
- C12Q2525/101—Modifications characterised by incorporating non-naturally occurring nucleotides, e.g. inosine
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2537/00—Reactions characterised by the reaction format or use of a specific feature
- C12Q2537/10—Reactions characterised by the reaction format or use of a specific feature the purpose or use of
- C12Q2537/157—A reaction step characterised by the number of molecules incorporated or released
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2563/00—Nucleic acid detection characterized by the use of physical, structural and functional properties
- C12Q2563/103—Nucleic acid detection characterized by the use of physical, structural and functional properties luminescence
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2563/00—Nucleic acid detection characterized by the use of physical, structural and functional properties
- C12Q2563/107—Nucleic acid detection characterized by the use of physical, structural and functional properties fluorescence
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2565/00—Nucleic acid analysis characterised by mode or means of detection
- C12Q2565/60—Detection means characterised by use of a special device
- C12Q2565/607—Detection means characterised by use of a special device being a sensor, e.g. electrode
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/62—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light
- G01N21/63—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light optically excited
- G01N21/64—Fluorescence; Phosphorescence
- G01N2021/6417—Spectrofluorimetric devices
- G01N2021/6419—Excitation at two or more wavelengths
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/62—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light
- G01N21/63—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light optically excited
- G01N21/64—Fluorescence; Phosphorescence
- G01N21/6428—Measuring fluorescence of fluorescent products of reactions or of fluorochrome labelled reactive substances, e.g. measuring quenching effects, using measuring "optrodes"
- G01N2021/6439—Measuring fluorescence of fluorescent products of reactions or of fluorochrome labelled reactive substances, e.g. measuring quenching effects, using measuring "optrodes" with indicators, stains, dyes, tags, labels, marks
- G01N2021/6441—Measuring fluorescence of fluorescent products of reactions or of fluorochrome labelled reactive substances, e.g. measuring quenching effects, using measuring "optrodes" with indicators, stains, dyes, tags, labels, marks with two or more labels
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/62—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light
- G01N21/63—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light optically excited
- G01N21/64—Fluorescence; Phosphorescence
- G01N21/645—Specially adapted constructive features of fluorimeters
- G01N2021/6463—Optics
- G01N2021/6478—Special lenses
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/62—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light
- G01N21/63—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light optically excited
- G01N21/64—Fluorescence; Phosphorescence
- G01N21/645—Specially adapted constructive features of fluorimeters
- G01N21/6452—Individual samples arranged in a regular 2D-array, e.g. multiwell plates
- G01N21/6454—Individual samples arranged in a regular 2D-array, e.g. multiwell plates using an integrated detector array
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2201/00—Features of devices classified in G01N21/00
- G01N2201/02—Mechanical
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2201/00—Features of devices classified in G01N21/00
- G01N2201/06—Illumination; Optics
- G01N2201/061—Sources
- G01N2201/06113—Coherent sources; lasers
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2201/00—Features of devices classified in G01N21/00
- G01N2201/06—Illumination; Optics
- G01N2201/061—Sources
- G01N2201/06113—Coherent sources; lasers
- G01N2201/0612—Laser diodes
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2201/00—Features of devices classified in G01N21/00
- G01N2201/06—Illumination; Optics
- G01N2201/062—LED's
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2201/00—Features of devices classified in G01N21/00
- G01N2201/06—Illumination; Optics
- G01N2201/068—Optics, miscellaneous
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2201/00—Features of devices classified in G01N21/00
- G01N2201/12—Circuits of general importance; Signal processing
- G01N2201/125—Digital circuitry
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10T—TECHNICAL SUBJECTS COVERED BY FORMER US CLASSIFICATION
- Y10T29/00—Metal working
- Y10T29/49—Method of mechanical manufacture
- Y10T29/49002—Electrical device making
- Y10T29/49016—Antenna or wave energy "plumbing" making
Landscapes
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Physics & Mathematics (AREA)
- General Health & Medical Sciences (AREA)
- Analytical Chemistry (AREA)
- Immunology (AREA)
- Biochemistry (AREA)
- Engineering & Computer Science (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Organic Chemistry (AREA)
- Pathology (AREA)
- General Physics & Mathematics (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Molecular Biology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Microbiology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Engineering & Computer Science (AREA)
- Genetics & Genomics (AREA)
- Biotechnology (AREA)
- Biophysics (AREA)
- Plasma & Fusion (AREA)
- Biomedical Technology (AREA)
- Clinical Laboratory Science (AREA)
- Hematology (AREA)
- Investigating, Analyzing Materials By Fluorescence Or Luminescence (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Apparatus Associated With Microorganisms And Enzymes (AREA)
- Immobilizing And Processing Of Enzymes And Microorganisms (AREA)
- Optical Measuring Cells (AREA)
- Automatic Analysis And Handling Materials Therefor (AREA)
Abstract
sistema óptico e chip de análise para investigar, detectar e analisar moléculas. aparelho e métodos para analisar molécula única e realizar a sequência de ácido nucleico. um aparelho pode incluir um chip de análise que inclui múltiplos pixels com poços de amostra configurados para receber uma amostra, que, quando excitada, emite energia de emissão; pelo menos um elemento para direcionar a energia de emissão em uma direção particular; e uma passagem de luz pela qual a energia de emissão percorre do poço de amostra em direção a um sensor. o aparelho ainda inclui um instrumento que interage com o chip de análise. o instrumento inclui uma fonte de luz de excitação para excitar a amostra em cada poço de amostra; uma pluralidade de sensores correspondente aos poços de amostra. cada sensor pode detectar a energia de emissão de uma amostra em um respectivo poço de amostra. o instrumento inclui pelo menos um elemento óptico que direciona a energia de emissão de cada poço de amostra em direção a um respectivo sensor da pluralidade de sensores.
Description
[001] Esse pedido reivindica o benefício em 35 U.S.C. §119(e) do Pedido de patente provisório US 61/905,282, intitulado "Dispositivo integrado para Investigar, Detectar e Analisar Moléculas," depositado em 17 de novembro, 2013; Pedido de patente provisório US 61/917,926, intitulado "Dispositivo integrado para Investigar, Detectar e Analisar Moléculas," depositado em 18 dezembro de 2013; Pedido de patente provisório US 61/941,916, intitulado "Dispositivo integrado para Investigar, Detectar e Analisar Moléculas," depositado em 19 de fevereiro de 2014, todos aqui incorporados por referência em sua totalidade.
[002] O presente pedido é direcionado geralmente a dispositivos, métodos e técnicas para a realização rápida massivamente paralela de análise quantitativa de amostras químicas e/ou biológicas, e métodos para fabricar os ditos dispositivos.
[003] Detecção e análise das amostras biológicas podem ser realizadas utilizando ensaio biológico ("bioensaios"). Bioensaios convencionalmente envolvem grandes equipamentos de laboratório caros exigindo cientistas treinados para operar o equipamento e realizar os bioensaios. Além disso, são convencionalmente realizados bioensaios em grandes quantidades de tal modo que uma grande quantidade de um determinado tipo de amostra é necessária para a detecção e quantificação.
[004] Alguns bioensaios são realizados por marcação de amostras com etiqueta luminescente que emitem luz de um determinado comprimento de onda. As etiquetas são iluminadas com uma fonte de luz de excitação para causar luminescência, e a luz luminescente é detectada com um fotodetector para quantificar a quantidade de luz luminescente emitida pelas etiquetas. Bioensaios com etiquetas luminescentes envolvem convencionalmente fontes de luz a laser caras para iluminar amostras e complicadas, ópticas de detecção volumosas e eletrônicos para coletar a luminescência das amostras iluminadas. Sumário
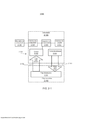
[005] A tecnologia descrita aqui se refere a aparelho e métodos para analisar espécimes rapidamente usando um chip de análise e instrumento. O chip de análise pode estar na forma de um chip descartável ou reciclável que é configurado para receber uma pequena quantidade de um espécime e executar, em paralelo, um grande número de análises de amostras dentro do espécime. O chip de análise e instrumento pode ser usado para detectar a presença de análises específicas químicas ou biológicas em algumas modalidades, para avaliar reações químicas ou biológicas em algumas modalidades e para determinar sequências genéticas em algumas modalidades. De acordo com algumas implementações, o dispositivo integrado pode ser usado para sequência genética de única molécula.
[006] De acordo com algumas implementações, um usuário deposita um espécime em uma câmera no chip de análise e insere o chip de análise em um instrumento receptor. O instrumento, sozinho ou em comunicação com um computador, automaticamente relaciona com o dispositivo integrado, envia e recebe luz do chip de análise, detecta e processa a luz recebida e fornece resultados da análise ao usuário.
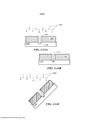
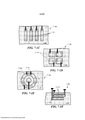
[007] De acordo com algumas modalidades, um chip de análise inclui um poço de amostra configurado para receber uma amostra, que, quando excitado, emite energia de emissão; pelo menos um elemento que direciona a energia de emissão em uma direção particular; e uma passagem de luz pela qual a energia de emissão percorre do poço de amostra em direção a um sensor. Pelo menos um elemento é selecionado do grupo que consiste em um elemento refrativo, um elemento difrativo, um elemento plasmônico e um ressonador.
[008] Em algumas modalidades, o chip de análise é usado em apenas um único ensaio biológico antes de disposição.
[009] Em algumas modalidades, pelo menos um elemento inclui pelo menos uma lente configurada para direcionar a energia de emissão em direção ao sensor.
[0010] Em algumas modalidades, pelo menos uma lente é uma lente refrativa.
[0011] Em algumas modalidades, a passagem de luz inclui pelo menos uma camada antirreflexo configurada para reduzir o reflexo da energia de emissão em uma ou mais interfaces do chip de análise.
[0012] Em algumas modalidades, o chip de análise ainda inclui uma estrutura descartável.
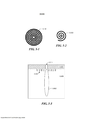
[0013] Em algumas modalidades, pelo menos um elemento inclui uma rede do anel concêntrico.
[0014] Em algumas modalidades, a rede do anel concêntrico é configurada para aumentar a quantidade de luz de excitação de uma fonte de luz de excitação que acopla ao poço de amostra e excita a amostra.
[0015] Em algumas modalidades, a rede do anel concêntrico é ainda configurada para direcionar a energia de emissão em direção ao sensor.
[0016] Em algumas modalidades a rede do anel concêntrico é uma rede do anel concêntrico aperiódico.
[0017] Em algumas modalidades, pelo menos uma lente é uma lente difrativa.
[0018] Em algumas modalidades, pelo menos um elemento compreende uma antena do ressonador dielétrico.
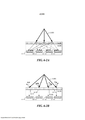
[0019] De acordo com algumas modalidades, um instrumento configurado para interagir com um chip de análise incluindo uma pluralidade de poços de amostra, cada poço de amostra da pluralidade de poços de amostra configurado para receber uma amostra, o instrumento inclui pelo menos uma fonte de luz de excitação configurada para excitar a amostra de pelo menos uma porção da pluralidade de poços de amostra; uma pluralidade de sensores, cada sensor da pluralidade de sensores correspondendo a um poço de amostra da pluralidade de poços de amostra, em que cada sensor da pluralidade de sensores é configurado para detectar energia de emissão da amostra em um respectivo poço de amostra; e pelo menos um elemento óptico configurado para direcionar a energia de emissão de cada poço de amostra da pluralidade de poços de amostra em direção a um respectivo sensor da pluralidade de sensores.
[0020] Em algumas modalidades, o instrumento ainda inclui um espelho policrônico configurado para refletir luz de excitação de pelo menos uma fonte de luz de excitação em direção ao chip de análise e transmitir a energia de emissão da pluralidade de amostras em direção à pluralidade de sensores.
[0021] Em algumas modalidades, pelo menos um elemento óptico compreende uma lente do relé.
[0022] Em algumas modalidades, pelo menos uma fonte de luz de excitação inclui uma pluralidade de fontes de luz, cada fonte de luz da pluralidade de fontes de luz emitindo a luz de excitação em um ou mais de uma pluralidade de comprimentos de onda.
[0023] Em algumas modalidades, o instrumento ainda inclui um combinador de comprimento de onda para espacialmente sobrepor a luz emitida de cada uma da pluralidade de fontes de luz.
[0024] Em algumas modalidades, pelo menos uma fonte de luz de excitação compreende uma fonte de luz pulsada.
[0025] Em algumas modalidades, o instrumento ainda inclui pelo menos um filtro espectral configurado para transmitir a energia de emissão e absorver e/ou refletir a luz de excitação de pelo menos uma fonte de luz de excitação.
[0026] Em algumas modalidades, o instrumento ainda inclui pelo menos um elemento de classificação espectral para espacialmente separar a energia de emissão de um primeiro comprimento de onda de energia de emissão de um segundo comprimento de onda.
[0027] Em algumas modalidades, pelo menos um elemento de classificação espectral compreende um elemento óptico difrativo.
[0028] Em algumas modalidades, o elemento óptico difrativo dispersa cromaticamente a energia de emissão e foca na energia de emissão.
[0029] Em algumas modalidades, o elemento óptico difrativo compreende uma lente Fresnel de compensação.
[0030] Em algumas modalidades, pelo menos um elemento de classificação espectral é um elemento de filtragem de luz.
[0031] Em algumas modalidades, o instrumento ainda inclui um sistema de controle que é programado para (i) direcionar a luz de excitação à dita pluralidade de poços de amostra, (ii) detectar sinais na dita pluralidade de sensores de dita pluralidade de poços, e (iii) utilizar um padrão de distribuição espacial dos ditos sinais para identificar a dita amostra ou subunidade respectiva.
[0032] De acordo com algumas modalidades, um aparelho inclui um chip de análise incluindo uma pluralidade de pixels e um instrumento configurado para interagir com o chip de análise. Cada um da pluralidade de pixels do chip de análise inclui um poço de amostra configurado para receber uma amostra, que, quando excitada, emite energia de emissão; pelo menos um elemento para direcionar a energia de emissão em uma direção particular, em que pelo menos um elemento é selecionado do grupo que consiste em um elemento refrativo, um elemento difrativo, um elemento plasmônico e um ressonador; e uma passagem de luz pela qual a energia de emissão percorre do poço de amostra em direção ao sensor. O instrumento inclui pelo menos uma fonte de luz de excitação configurada para excitar a amostra em cada poço de amostra; uma pluralidade de sensores, cada sensor da pluralidade de sensores correspondendo a um respectivo poço de amostra, em que cada sensor da pluralidade de sensores é configurado para detectar energia de emissão da amostra no respectivo poço de amostra; e pelo menos um elemento óptico configurado para direcionar a energia de emissão de cada poço de amostra em direção ao respectivo sensor da pluralidade de sensores.
[0033] Em algumas modalidades, o chip de análise é configurado para ser conectado e removido do instrumento.
[0034] Em algumas modalidades, quando o chip de análise é conectado ao instrumento, a distância óptica entre um poço de amostra da pluralidade de poços de amostra e o sensor correspondente da pluralidade de sensores é menor que 30 cm.
[0035] Em algumas modalidades, quando o chip de análise é conectado ao instrumento, a distância óptica entre um poço de amostra da pluralidade de poços de amostra e o sensor correspondente da pluralidade de sensores é menor que 5 cm.
[0036] Em algumas modalidades, quando o chip de análise é conectado ao instrumento, a distância óptica entre um poço de amostra da pluralidade de poços de amostra e o sensor correspondente da pluralidade de sensores é menor que 1 cm.
[0037] Em algumas modalidades, o instrumento é portátil.
[0038] Em algumas modalidades, cada amostra inclui uma etiqueta luminescente que emite a energia de emissão dentro de uma faixa de comprimento de onda de uma pluralidade de faixa de comprimento de ondas; e cada sensor da pluralidade de sensores inclui um subssensor configurado para detectar a energia de emissão em cada uma da pluralidade de faixas de comprimento de onda.
[0039] Em algumas modalidades, cada sensor da pluralidade de sensores inclui pelo menos dois subssensores.
[0040] Em algumas modalidades, cada sensor da pluralidade de sensores compreende pelo menos quatro subssensores.
[0041] Em algumas modalidades, o instrumento ainda inclui pelo menos um elemento dependente do comprimento de onda que direciona energia de emissão de um primeiro comprimento de onda em direção a um primeiro subssensor de pelo menos dois subssensores e direciona energia de emissão de um segundo comprimento de onda em direção a um segundo subssensor de pelo menos dois subssensores.
[0042] Em algumas modalidades, pelo menos um elemento dependente do comprimento de onda é um elemento óptico difrativo.
[0043] Em algumas modalidades, pelo menos um elemento dependente do comprimento de onda é um filtro espectral.
[0044] Em algumas modalidades, pelo menos uma fonte de excitação emite luz pulsada.
[0045] Em algumas modalidades, uma primeira etiqueta luminescente associada com uma primeira amostra é excitada por luz de um primeiro comprimento de onda, mas não é excitada por luz de um segundo comprimento de onda; e uma segunda etiqueta luminescente associada com uma segunda amostra é excitada por luz do segundo comprimento de onda, mas não é excitada por luz do primeiro comprimento de onda.
[0046] De acordo com algumas modalidades, um método para analisar um espécime inclui fornecer o espécime na superfície superior de um chip de análise compreendendo uma pluralidade de poços de amostra; alinhar o chip com um instrumento compreendendo pelo menos uma fonte de luz de excitação e pelo menos um sensor; excitar uma amostra do espécime em pelo menos um da pluralidade de poços de amostra com luz de excitação de pelo menos uma fonte de luz de excitação; e detectar, com pelo menos um sensor, energia de emissão gerada pela amostra em pelo menos um poço de amostra em resposta à excitação pela luz de excitação.
[0047] Em algumas modalidades, o método ainda inclui determinar, com base na detecção da energia de emissão, um tipo de molécula que emitiu a energia de emissão.
[0048] Em algumas modalidades, determinar o tipo de molécula inclui medir uma propriedade espectral da energia de emissão.
[0049] Em algumas modalidades, determinar o tipo de molécula ainda inclui determinar o comprimento de onda da luz de excitação que excitou a amostra.
[0050] Em algumas modalidades, pelo menos uma fonte de luz de excitação emite luz de onda contínua.
[0051] Em algumas modalidades, pelo menos uma fonte de luz de excitação emite luz pulsada.
[0052] Em algumas modalidades, pelo menos uma fonte de luz de excitação inclui uma pluralidade de fontes de luz de excitação, cada fonte de luz de excitação da pluralidade de fontes de luz de excitação que emite luz de um comprimento de onda diferente.
[0053] Em algumas modalidades, a amostra inclui pelo menos um nucleotídeo preso a um fluoróforo.
[0054] De acordo com algumas modalidades, um método para sequenciar uma molécula de ácido nucleico alvo inclui: (a) fornecer um chip adjacente a um instrumento que inclui uma fonte de excitação e um sensor, em que o dito chip inclui pelo menos um poço que é acoplado de forma operável à dita fonte de excitação e o dito sensor quando o dito chip está em uma posição de detecção do dito instrumento, e em que o dito poço contém a dita molécula de ácido nucleico alvo, uma enzima de polimerização e uma pluralidade de tipos de nucleotídeos ou análogos de nucleotídeo; (b) com o dito chip na dita posição de detecção, realizar uma reação de extensão em uma localização principal da dita molécula de ácido nucleico alvo na presença da dita enzima de polimerização para sequencialmente incorporar os ditos nucleotídeos ou análogos de nucleotídeo em um filamento crescente que é complementar à dita molécula de ácido nucleico alvo, em que sob incorporação e excitação por energia de excitação da dita fonte de excitação, os ditos nucleotídeos ou análogos de nucleotídeos emitem sinais no dito poço; (c) usar o dito sensor para detectar os padrões de distribuição espacial e/ou temporal dos ditos sinais que são distinguíveis para a dita pluralidade de tipos de nucleotídeos ou análogos de nucleotídeo; e (d) identificar os ditos nucleotídeos ou análogos de nucleotídeo com base nos ditos padrões de distribuição espacial e/ou temporal dos ditos sinais, sequenciando assim a dita molécula de ácido nucleico alvo.
[0055] Em algumas modalidades, os nucleotídeos ou análogos de nucleotídeos incluem etiquetas que emitem os sinais sob incorporação no dito filamento crescente.
[0056] Em algumas modalidades, as etiquetas são etiquetas luminescentes.
[0057] Em algumas modalidades, os nucleotídeos ou análogos de nucleotídeo são identificados subsequentes à detecção dos padrões de distribuição espacial e/ou temporal dos ditos sinais.
[0058] Em algumas modalidades, a pluralidade de tipos de nucleotídeos ou análogos de nucleotídeo incluem quatro diferentes tipos de nucleotídeos ou análogos de nucleotídeo, e em que os padrões de distribuição espacial e/ou temporal dos ditos sinais associados com os ditos quatro diferentes tipos de nucleotídeos ou análogos de nucleotídeo são distinguíveis entre si.
[0059] Em algumas modalidades, os padrões de distribuição espacial e/ou temporal dos sinais associados com os ditos quatro diferentes tipos de nucleotídeos ou análogos de nucleotídeo são detectados separadamente entre si.
[0060] Em algumas modalidades, os padrões de distribuição espacial e/ou temporal dos sinais são distinguíveis entre si com base em uma distribuição de forma e/ou intensidade de cada um dos padrões de distribuição espacial e/ou temporal.
[0061] Em algumas modalidades, a localização principal inclui um iniciador que é complementar à molécula de ácido nucleico alvo.
[0062] Em algumas modalidades, o ato (b) do método inclui realizar uma reação de extensão do iniciador usando o dito iniciador hibridizado na dita molécula de ácido nucleico alvo para produzir o dito filamento crescente.
[0063] Em algumas modalidades, a molécula de ácido nucleico alvo tem duplo filamento.
[0064] Em algumas modalidades, a localização principal é uma fenda ou entalhe na dita molécula de ácido nucleico alvo.
[0065] Em algumas modalidades, a enzima de polimerização é imobilizada no dito poço.
[0066] Em algumas modalidades, enzima de polimerização é imobilizada em uma parte inferior do poço.
[0067] Em algumas modalidades, a enzima de polimerização é imobilizada usando um ligante que é preso a uma superfície do dito poço.
[0068] Em algumas modalidades, a enzima de polimerização exibe a atividade de deslocamento de filamento.
[0069] Em algumas modalidades, o poço está entre uma pluralidade de poços no dito chip.
[0070] Em algumas modalidades, o instrumento inclui uma pluralidade de fontes de excitação acoplada de forma operável à dita pluralidade de poços.
[0071] Em algumas modalidades, antes do ato (c) do método, os padrões de distribuição espacial e/ou temporal dos ditos sinais são gerados dos ditos sinais.
[0072] De acordo com algumas modalidades, um método para sequência de ácido nucleico inclui: (a) fornecer um chip adjacente a um instrumento, em que o dito chip inclui uma pluralidade de poços que é cada um acoplado de forma operável a (i) uma fonte de excitação e (ii) um sensor do dito instrumento quando dito chip está em uma posição de detecção do dito instrumento, e em que um poço individual da dita pluralidade contém a dita molécula de ácido nucleico alvo, uma enzima de polimerização e uma pluralidade de tipos de nucleotídeos ou análogos de nucleotídeo; (b) com o dito chip na dita posição de detecção, submetendo a dita molécula de ácido nucleico alvo a uma reação de polimerização para produzir um filamento crescente que é complementar à dita molécula de ácido nucleico alvo na presença dos ditos nucleotídeos ou análogos de nucleotídeo e da dita enzima de polimerização, em que os ditos nucleotídeos ou análogos de nucleotídeos emitem sinais no dito poço individual sob excitação por energia de excitação da dita fonte de excitação durante a incorporação; (c) que o dito sensor para detectar padrões de distribuição espacial e/ou temporal dos ditos sinais que são distinguíveis para a dita pluralidade de tipos de nucleotídeos ou análogos de nucleotídeo; e (d) identificar uma sequência da dita molécula de ácido nucleico alvo com base nos ditos padrões de distribuição espacial e/ou temporal dos ditos sinais.
[0073] Em algumas modalidades, os nucleotídeos ou análogos de nucleotídeos incluem etiquetas que emitem os ditos sinais sob incorporação no dito filamento crescente.
[0074] Em algumas modalidades, as etiquetas são etiquetas luminescentes.
[0075] Em algumas modalidades, a sequência é identificada subsequente à detecção dos ditos padrões de distribuição espacial e/ou temporal dos ditos sinais
[0076] Em algumas modalidades, a pluralidade de tipos de nucleotídeos ou análogos de nucleotídeo incluem quatro diferentes tipos de nucleotídeos ou análogos de nucleotídeo, e em que os ditos padrões de distribuição espacial e/ou temporal dos ditos sinais associados com os ditos quatro diferentes tipos de nucleotídeos ou análogos de nucleotídeo são distinguíveis entre si.
[0077] Em algumas modalidades, os padrões de distribuição espacial e/ou temporal dos ditos sinais associados com os ditos quatro diferentes tipos de nucleotídeos ou análogos de nucleotídeo são detectados separadamente entre si.
[0078] Em algumas modalidades, o ato (b) do método inclui realizar uma reação de extensão do iniciador usando um iniciador hibridizado na dita molécula de ácido nucleico alvo para produzir o dito filamento crescente.
[0079] Em algumas modalidades, a molécula de ácido nucleico alvo tem filamento único.
[0080] Em algumas modalidades, a enzima de polimerização é imobilizada no dito poço.
[0081] Em algumas modalidades, a fonte de excitação é acoplada de forma operável à dita pluralidade de poços.
[0082] Em algumas modalidades, o ato (c) do método inclui detectar padrões de distribuição espacial e/ou temporal dos ditos sinais.
[0083] Em algumas modalidades, o instrumento inclui uma pluralidade de fontes de excitação que são acopladas de forma operável à dita pluralidade de poços.
[0084] Em algumas modalidades, o instrumento inclui uma pluralidade de sensores que são acoplados de forma operável à dita pluralidade de poços.
[0085] Em algumas modalidades, antes do ato (c) do método, os padrões de distribuição espacial e/ou temporal dos ditos sinais são gerados dos ditos sinais.
[0086] Os aspectos mencionados e outros, além das modalidades e recursos dos presentes ensinamentos podem ser entendidos de forma mais completa a partir da descrição a seguir em conjunto com os desenhos anexos.
[0087] O termo "pixel" pode ser usado na presente revelação para se referir a uma célula unitária de um dispositivo integrado. A célula unitária pode incluir um poço de amostra e um sensor. A célula unitária pode ainda incluir uma fonte de excitação. A célula unitária pode ainda incluir pelo menos uma estrutura óptica de acoplamento de excitação (que pode ser referida como uma "primeira estrutura") que é configurada para melhorar o acoplamento de energia de excitação da fonte de excitação ao poço de amostra. A célula unitária pode ainda incluir pelo menos uma estrutura de acoplamento de emissão que é configurada para melhorar o acoplamento de emissão do poço de amostra ao sensor. A célula unitária pode ainda incluir dispositivos eletrônicos integrados (por exemplo, dispositivos CMOS). Pode haver uma pluralidade de pixels disposta em uma matriz sobre um dispositivo integrado.
[0088] O termo "óptico" pode ser usado na presente revelação para se referir às bandas espectrais infravermelhas de comprimento de onda curto visível próximo de infravermelho.
[0089] O termo "etiqueta" pode ser usado na presente revelação para se referir a uma etiqueta, sonda, marcador ou relator fixado a uma amostra para ser analisada ou fixada a um reagente que pode ser reagido com a amostra.
[0090] A frase "energia de excitação" pode ser usada na presente revelação para se referir a qualquer forma de energia (por exemplo, radioativa ou não radioativa) entregue a uma amostra e/ou etiqueta dentro do poço de amostra. A energia de excitação radioativa pode compreender radiação óptica em um ou mais comprimentos de onda característicos.
[0091] A frase "comprimento de onda característico" pode ser usada na presente revelação para se referir a um comprimento de onda central ou predominante dentro de uma largura de banda de radiação limitada. Em alguns casos, pode se referir a um comprimento de onda máximo de uma largura de banda de radiação. Exemplos de comprimentos de onda característicos de fluoróforos são 563 nm, 595 nm, 662 nm e 687 nm.
[0092] A frase "energia característica" pode ser usada na presente revelação para se referir a uma energia associada com um comprimento de onda característico.
[0093] O termo "emissão" pode ser usado na presente revelação para se referir à emissão de uma etiqueta e/ou amostra. Isso pode incluir emissão radioativa (por exemplo, emissão óptica) ou transferência de energia não radioativa (por exemplo, transferência de energia Dexter ou transferência de energia ressonante Forster). Os resultados da emissão de excitação de uma amostra e/ou etiqueta dentro do poço de amostra.
[0094] A frase "emissão de um poço de amostra" ou "emissão de uma amostra" pode ser usada na presente revelação para se referir à emissão de uma etiqueta e/ou amostra dentro de um poço de amostra.
[0095] O termo "autoalinhado" pode ser usado na presente revelação para se referir a um processo de microfabricação, no qual pelo menos dois elementos distintos (por exemplo, um poço de amostra e uma estrutura de acoplamento de emissão, um poço de amostra e uma fonte de excitação) podem ser fabricados e alinhados uns aos outros sem usar duas etapas de padronização litográfica separada nas quais uma primeira etapa de padronização litográfica (por exemplo, fotolitografia, litografia de feixe de íon, litografia EUV) imprime um padrão de um primeiro elemento e uma segundo etapa de padronização litográfica é alinhada à primeira etapa de padronização litográfica e imprime um padrão do segundo elemento. Um processo autoalinhado pode compreender incluir o padrão do primeiro e do segundo elemento em uma única etapa de padronização litográfica ou pode compreender formar o segundo elemento usando características de um primeiro elemento da estrutura fabricada.
[0096] O termo "sensor" pode ser utilizado na presente revelação para se referir a um ou mais dispositivos de circuito integrado configurado para sentir a emissão do poço de amostra e produzir pelo menos um sinal elétrico representante da emissão sentida.
[0097] O termo "nano-escala" pode ser usado na presente revelação para se referir a uma estrutura tendo pelo menos uma dimensão ou tamanho característico mínimo na ordem de 150 nanômetros (nm) ou menos, mas não maior que aproximadamente 500 nm.
[0098] O termo "microescala" pode ser utilizado na presente revelação para se referir a uma estrutura tendo pelo menos uma dimensão ou tamanho característico mínimo entre aproximadamente 500 nm e aproximadamente 100 microns.
[0099] A frase "melhorar energia de excitação" pode ser utilizada na presente revelação para se referir a aumentar uma intensidade de energia de excitação em uma região de excitação de um poço de amostra. A intensidade pode ser aumentada concentrando e/ou ressoando a energia de excitação incidente no poço de amostra, por exemplo. Em alguns casos, a intensidade pode ser aumentada por revestimentos antirreflexo ou camadas de perda que permitem que a energia de excitação penetre na região de excitação de um poço de amostra. Uma melhoria de energia de excitação pode ser uma referência comparativa a uma modalidade que não inclui estruturas para melhorar a energia de excitação em uma região de excitação de um poço de amostra.
[00100] Os termos "aproximadamente" e "substancialmente" podem ser utilizados na presente revelação para se referir a um valor e pretendem englobar um valor referenciado mais e menor variações aceitáveis. A quantidade de variação poderia ser menor que 5% em algumas modalidades, menor que 10% em algumas modalidades e ainda menor que 20% em algumas modalidades. Em modalidades onde um aparelho pode funcionar apropriadamente sobre uma grande faixa de valores, por exemplo, uma faixa incluindo uma ou mais ordens de magnitude, a quantidade de variação poderia ser um fator de dois. Por exemplo, se um aparelho funciona apropriadamente para um valor variando de 20 a 350, "aproximadamente 80" pode englobar valores entre 40 e 160.
[00101] O termo "adjacente" pode ser utilizado na presente revelação para se referir a dois elementos dispostos dentro da proximidade um do outro (por exemplo, dentro de uma distância que é menor que aproximadamente um quinto de uma dimensão transversa ou dimensão vertical de um pixel). Em alguns casos, pode haver estruturas ou camadas de intervenção entre elementos adjacentes. Em alguns casos, elementos adjacentes podem ser imediatamente adjacentes uns aos outros com nenhuma estrutura ou elemento de intervenção.
[00102] O termo "detectar" pode ser utilizado na presente revelação para se referir à recepção de emissão em um sensor de um poço de amostra e produzindo pelo menos um sinal elétrico representante da ou associada à emissão. O termo "detectar" pode ainda ser utilizado na presente revelação para se referir à determinação da presença de, ou identificar uma propriedade de, uma amostra ou etiqueta específica no poço de amostra baseada na emissão do poço de amostra.
[00103] Os técnicos no assunto entenderão que as figuras, aqui descritas, são para finalidades de ilustração apenas. Deve ser entendido que em alguns casos vários aspectos da invenção podem ser mostrados exagerados ou ampliados para facilitar um entendimento da invenção. Nos desenhos, os caracteres de referência igual geralmente se referem aos recursos, funcionalidade, elementos estruturalmente similares e/ou em todas as várias figuras. Os desenhos não são necessariamente em escala, a ênfase é dada na ilustração dos princípios dos ensinamentos. Os desenhos não são destinados a limitar o escopo dos presentes ensinamentos de qualquer forma.
[00104] A figura 1-1 descreve os espectros do comprimento de onda de emissão, de acordo com algumas modalidades.
[00105] A figura 1-2A descreve espectros do comprimento de onda de absorção, de acordo com algumas modalidades.
[00106] A figura 1-2B descreve espectros do comprimento de onda de emissão, de acordo com algumas modalidades.
[00107] A figura 2-1 é uma representação do diagrama em blocos de um aparelho que pode ser usado para análise rápida móvel de espécimes biológicos e químicos, de acordo com algumas modalidades.
[00108] A figura 2-2 é um diagrama esquemático da relação entre pixels do chip do sensor e pixels do chip de análise, de acordo com algumas modalidades.
[00109] A figura 2-3 descreve componentes associada com um único pixel do chip de análise e um único pixel do chip do sensor, de acordo com algumas modalidades.
[00110] A figura 2-4 descreve uma porção dos componentes do instrumento, de acordo com algumas modalidades.
[00111] A figura 3-1A é uma vista superior do chip de análise e um suporte do chip, de acordo com algumas modalidades.
[00112] A figura 3-1B é uma vista inferior do chip de análise e do suporte do chip, de acordo com algumas modalidades.
[00113] A figura 3-1C descreve o chip de análise e o suporte do chip, de acordo com algumas modalidades.
[00114] A figura 3-2 descreve energia de excitação incidente em um poço de amostra, de acordo com algumas modalidades.
[00115] A figura 3-3 ilustra a atenuação da energia de excitação ao longo de um poço de amostra que é formado como um guia de onda do modo zero, de acordo com algumas modalidades.
[00116] A figura 3-4 descreve um poço de amostra que inclui um entalhe, que aumenta a energia de excitação em uma região de excitação associada com o poço de amostra em algumas modalidades.
[00117] A figura 3-5 compara as intensidades de excitação para poços de amostra com e sem um entalhe, de acordo com uma modalidade.
[00118] A figura 3-6 descreve um poço de amostra e entalhe formados em uma protrusão, de acordo com algumas modalidades.
[00119] A figura 3-7A descreve um poço de amostra tendo paredes laterais afiladas, de acordo com algumas modalidades.
[00120] A figura 3-7B descreve um poço de amostra tendo paredes laterais curvadas e um entalhe com uma dimensão transversal menor, de acordo com algumas modalidades.
[00121] A figura 3-7C e a figura 3-7D representam um poço de amostra formado das estruturas plasmônicas da superfície.
[00122] A figura 3-7E descreve um poço de amostra que inclui uma estrutura de melhoria de energia por excitação formada ao longo das paredes laterais do poço de amostra, de acordo com algumas modalidades.
[00123] A figura 3-7F descreve um poço de amostra formado em uma pilha multicamadas, de acordo com algumas modalidades.
[00124] A figura 3-8 ilustra o revestimento da superfície formado nas superfícies de um poço de amostra, de acordo com algumas modalidades.
[00125] A figura 3-9A à figura 3-9E representam estruturas associadas com um processo de arranque para formar um poço de amostra, de acordo com algumas modalidades.
[00126] A figura 3-9F descreve uma estrutura associada com um processo de arranque alternativo para formar um poço de amostra, de acordo com algumas modalidades.
[00127] A figura 3-10A à figura 3-10D representam estruturas associadas com um processo de decapagem direta para formar um poço de amostra, de acordo com algumas modalidades.
[00128] A figura 3-11 descreve um poço de amostra que pode ser formado em múltiplas camadas usando um processo de arranque ou um processo de decapagem direta, de acordo com algumas modalidades.
[00129] A figura 3-12 descreve uma estrutura associada com um processo de decapagem que pode ser usado para formar um entalhe, de acordo com algumas modalidades.
[00130] A figura 3-13A à figura 3-13C representam estruturas associadas com um processo alternativo para formar um entalhe, de acordo com algumas modalidades.
[00131] A figura 3-14A à figura 3-14D representam estruturas associadas com um processo para depositar um aderente e camadas de passivação, de acordo com algumas modalidades.
[00132] A figura 3-15 descreve uma estrutura associada com um processo para depositar um aderente centralmente dentro de um poço de amostra, de acordo com algumas modalidades.
[00133] A figura 4-1A e a figura 4-1B representam uma estrutura plasmônica da superfície, de acordo com apenas uma modalidade.
[00134] A figura 4-1C descreve uma estrutura plasmônica da superfície formada adjacente a um poço de amostra, de acordo com algumas modalidades.
[00135] A figura 4-1D e a figura 4-1E representam estruturas plasmônicas da superfície formadas em um poço de amostra, de acordo com algumas modalidades.
[00136] A figura 4-2A à figura 4-2C representam exemplos de estruturas plasmônicas da superfície periódicas, de acordo com algumas modalidades.
[00137] A figura 4-2D descreve uma simulação numérica da energia de excitação em um poço de amostra-formado adjacente a uma estrutura plasmônica da superfície periódica, de acordo com algumas modalidades.
[00138] A figura 4-2E à figura 4-2G representam estruturas plasmônicas da superfície periódicas, de acordo com algumas modalidades.
[00139] A figura 4-2H e a figura 4-2I representam uma nanoantena compreendendo estruturas plasmônicas da superfície, de acordo com algumas modalidades.
[00140] A figura 4-3A à figura 4-3E representam estruturas associadas com as etapas do processo para formar uma estrutura plasmônica da superfície, de acordo com algumas modalidades.
[00141] A figura 4-4A à figura 4-4G representam estruturas associadas com etapas do processo para formar uma estrutura plasmônica da superfície e poço de amostra autoalinhado, de acordo com algumas modalidades.
[00142] A figura 4-5A à figura 4-5E representam estruturas associadas com etapas do processo para formar uma estrutura plasmônica da superfície e poço de amostra autoalinhado, de acordo com algumas modalidades.
[00143] A figura 4-6A descreve uma película fina com perdas formada adjacente a um poço de amostra, de acordo com algumas modalidades.
[00144] A figura 4-6B e a figura 4-6C representam resultados de simulações numéricas da energia de excitação na proximidade de um poço de amostra e película fina com perdas, de acordo com algumas modalidades.
[00145] A figura 4-6D descreve uma película fina com perdas espaçada de um poço de amostra, de acordo com algumas modalidades.
[00146] A figura 4-6E descreve uma pilha de película fina com perdas formada adjacente a um poço de amostra, de acordo com algumas modalidades.
[00147] A figura 4-7A ilustra uma pilha reflexiva que pode ser usada para formar uma cavidade ressonante adjacente a um poço de amostra, de acordo com algumas modalidades.
[00148] A figura 4-7B descreve uma estrutura dielétrica que pode ser usada para concentrar a energia de excitação em um poço de amostra, de acordo com algumas modalidades.
[00149] A figura 4-7C e a figura 4-7D representam uma estrutura de banda larga fotônica que pode ser moldada adjacente a um poço de amostra, de acordo com algumas modalidades.
[00150] A figura 4-8A à figura 4-8G representam estruturas associadas com etapas do processo para formar estruturas dielétricas e um poço de amostra autoalinhado, de acordo com algumas modalidades.
[00151] A figura 4-9A e a figura 4-9B representam estruturas para acoplar energia de excitação a uma amostra através de um processo não radioativo, de acordo com algumas modalidades.
[00152] A figura 4-9C descreve uma estrutura para acoplar energia de excitação em uma amostra por múltiplos processos não radioativos, de acordo com algumas modalidades.
[00153] A figura 4-9D descreve uma estrutura que incorpora uma ou mais partículas conversoras de energia para acoplar a energia de excitação em uma amostra através de um processo radioativo ou não radioativo, de acordo com algumas modalidades.
[00154] A figura 4-9E descreve espectros associados com redução de energia de excitação em uma amostra, de acordo com algumas modalidades.
[00155] A figura 4-9F descreve espectros associados com duplicação de energia de excitação em uma amostra, de acordo com algumas modalidades.
[00156] A figura 5-1 descreve uma rede circular plasmônica, concêntrica, de acordo com algumas modalidades.
[00157] A figura 5-2 descreve uma rede plasmônica espiral, de acordo com algumas modalidades.
[00158] A figura 5-3 representam padrões de distribuição espaciais de emissão de uma rede circular plasmônica, concêntrica, de acordo com algumas modalidades.
[00159] A figura 5-4A à figura 5-4B representam nanoantenas plasmônicas, de acordo com algumas modalidades.
[00160] A figura 5-5A à figura 5-5B representam nanoantenas plasmônicas, de acordo com algumas modalidades.
[00161] A figura 5-6A descreve óptica refrativa do chip de análise, de acordo com algumas modalidades.
[00162] A figura 5-6B descreve lentes Fresnel do chip de análise, de acordo com algumas modalidades.
[00163] A figura 6-1 descreve componentes do instrumento microscopia, de acordo com algumas modalidades.
[00164] A figura 6-2A descreve elementos de classificação espectral de campo distante do chip do sensor, de acordo com algumas modalidades.
[00165] A figura 6-2B descreve elementos de filtragem de campo distante do chip do sensor, de acordo com algumas modalidades.
[00166] A figura 6-3A e a figura 6-3B representam películas finas com perdas do chip do sensor, de acordo com algumas modalidades.
[00167] A figura 6-4 descreve o bloco óptico do instrumento, de acordo com algumas modalidades.
[00168] A figura 7-1A descreve, na vista de elevação, um sensor dentro de um pixel de um chip do sensor, de acordo com algumas modalidades.
[00169] A figura 7-1B descreve um sensor de ângulo de desvio tendo duas áreas ativas separadas e concêntricas, de acordo com algumas modalidades.
[00170] A figura 7-1C descreve um sensor de fita tendo quatro áreas ativas separadas, de acordo com algumas modalidades.
[00171] A figura 7-1D descreve um sensor de quadra tendo quatro áreas ativas separadas, de acordo com algumas modalidades.
[00172] A figura 7-1E descreve um sensor de segmento de arco tendo quatro áreas ativas separadas, de acordo com algumas modalidades.
[00173] A figura 7-1F descreve um sensor de segmento empilhado, de acordo com algumas modalidades.
[00174] A figura 7-2A descreve uma distribuição de emissão dos elementos de classificação para a energia emitida em um primeiro comprimento de onda, de acordo com algumas modalidades.
[00175] A figura 7-2B descreve um padrão de radiação recebido por um sensor de ângulo de desvio correspondente à distribuição de emissão representada na figura 7-2A, de acordo com algumas modalidades.
[00176] A figura 7-2C descreve uma distribuição de emissão dos elementos de classificação para a energia emitida em um segundo comprimento de onda, de acordo com algumas modalidades.
[00177] A figura 7-2D descreve um padrão de radiação recebido por um sensor de ângulo de desvio correspondente à distribuição de emissão representada na figura 7-2C, de acordo com algumas modalidades.
[00178] A figura 7-2E representa resultados de uma simulação numérica de detecção de sinal para um sensor de ângulo de desvio tendo duas áreas ativas para um primeiro comprimento de onda de emissão de uma amostra, de acordo com algumas modalidades.
[00179] A figura 7-2F representa os resultados de uma simulação numérica de detecção de sinal para o sensor de ângulo de desvio associado com a figura 7-2E para um segundo comprimento de onda de emissão de uma amostra, de acordo com algumas modalidades.
[00180] A figura 7-2G representa os resultados de uma simulação numérica de detecção de sinal para o sensor de ângulo de desvio associado com a figura 7-2E para um terceiro comprimento de onda de emissão de uma amostra, de acordo com algumas modalidades.
[00181] A figura 7-2H representa os resultados de uma simulação numérica de detecção de sinal para o sensor de ângulo de desvio associado com a figura 7-2E para um quarto comprimento de onda de emissão de uma amostra, de acordo com algumas modalidades.
[00182] A figura 7-2I representa resultados de uma simulação numérica de detecção de sinal para um sensor de ângulo de desvio tendo quatro áreas ativas para um primeiro comprimento de onda de emissão de uma amostra, de acordo com algumas modalidades.
[00183] A figura 7-2J representa resultados de uma simulação numérica de detecção de sinal para o sensor de ângulo de desvio associado com a figura 7-2I para um segundo comprimento de onda de emissão de uma amostra, de acordo com algumas modalidades.
[00184] A figura 7-3A descreve o circuito em um instrumento que pode ser usado para ler sinais de um sensor compreendendo duas áreas ativas, de acordo com algumas modalidades.
[00185] A figura 7-3B descreve um circuito de três transistores que podem ser incluídos em um chip do sensor para acúmulo do sinal e leitura, de acordo com algumas modalidades.
[00186] A figura 7-3C descreve circuito em um instrumento que pode ser usado para ler sinais de um sensor compreendendo quatro áreas ativas, de acordo com algumas modalidades.
[00187] A figura 7-4A descreve características de emissão temporal para dois emissores diferentes que podem ser usados para análise de amostra, de acordo com algumas modalidades.
[00188] A figura 7-4B descreve evolução temporal de uma fonte de excitação e luminescência de uma amostra, de acordo com algumas modalidades.
[00189] A figura 7-4C ilustra amostragem de atraso de tempo, de acordo com algumas modalidades.
[00190] A figura 7-4D descreve características de emissão temporal para dois emissores diferentes, de acordo com algumas modalidades.
[00191] A figura 7-4E descreve dinâmica de tensão em um nó de acúmulo de carga de um sensor, de acordo com algumas modalidades.
[00192] A figura 7-4F descreve uma leitura dupla de um segmento do sensor sem redefinição, de acordo com algumas modalidades.
[00193] A figura 7-4G e a figura 7-4H ilustram o primeiro e o segundo níveis de sinal de leitura associados com dois emissores tendo características de emissão temporalmente distintas, de acordo com algumas modalidades.
[00194] A figura 8-1A e a figura 8-1B representam bandas de excitação espectral das fontes de excitação, de acordo com algumas modalidades.
[00195] A figura 9-1 descreve um método de operação de um aparelho compacto que pode ser usado para análise rápida móvel de espécimes biológicos e químicos, de acordo com algumas modalidades.
[00196] A figura 9-2 descreve um procedimento de calibração, de acordo com algumas modalidades.
[00197] A figura 9-3 descreve um procedimento de análise de dados, de acordo com algumas modalidades.
[00198] A figura 10 descreve um ambiente de computação, de acordo com algumas modalidades.
[00199] Os recursos e vantagens das modalidades do presente pedido se tornarão mais evidentes a partir da descrição detalhada estabelecida abaixo quando em conjunto com os desenhos. Descrição Detalhada Reconhecimento do inventor do problema e solução a ele
[00200] Os inventores reconheceram e observaram que os aparelhos convencionais para realizar bioensaios são grandes, caros e exigem técnicas de laboratório avançadas para serem realizados. Muitos tipos de bioensaios dependem da detecção de molécula única em um espécime. Convencionalmente, a detecção de única molécula pode exigir sistemas grandes a laser volumosos para gerar luz de alta intensidade necessária para excitação de moléculas. Além disso, componentes ópticos volumosos podem ser usados para direcionar a luz de laser ao espécime e componentes ópticos adicionais podem ser usados para direcionar luz luminescente do espécime a um sensor. Esses componentes ópticos convencionais podem exigir alinhamento e estabilização precisos. O equipamento de laboratório convencionais e o treinamento necessário para usar esse equipamento convencional pode resultar em bioensaios caros e complexos.
[00201] Os inventores reconheceram e apreciaram que há uma necessidade por um dispositivo que pode analisar de forma simples e barata os espécimes biológicos e/ou químicos para determinar a identidade de suas partes constituintes. Uma aplicação de tal dispositivo pode ser para sequência de uma biomolécula, como uma molécula de ácido nucleico ou um polipeptídio (por exemplo, proteína) tendo uma pluralidade de aminoácidos. Um aparelho compacto de alta velocidade para realizar a detecção e quantização de molécula únicas ou partículas poderia reduzir o custo para realizar as medições quantitativas das amostras biológicas e/ou químicas e rapidamente avançar a taxa de descobertos tecnológicas bioquímicas. Além disso, um dispositivo custo efetivo que é prontamente transportátil poderia transformar não apenas a forma que os bioensaios são realizados no mundo desenvolvido, mas fornecer pessoas nas regiões em desenvolvimento, pela primeira vez, acesso pronto aos testes diagnósticos essenciais que poderiam melhorar muito sua saúde e bem-estar. Por exemplo, em algumas modalidades, um aparelho para realizar bioensaios é usado para realizar testes diagnósticos de amostras biológicas, como sangue, urina e/ou saliva. O aparelho pode ser usado por pessoas em suas casas, por um médico em uma clínica remota em países em desenvolvimento ou qualquer outra localização, como consultórios rurais. Tais testes diagnósticos podem incluir a detecção de biomoléculas em uma amostra biológica de uma pessoa, como uma molécula de ácido nucleico ou proteína. Em alguns exemplos, testes diagnósticos incluem sequência de uma molécula de ácido nucleico em uma amostra biológica de um sujeito, como sequência de moléculas de ácidos desoxirribonucleicos sem célula ou produtos de expressão em uma amostra biológica do sujeito.
[00202] O termo "ácido nucleico", como aqui usado, geralmente refere-se a uma molécula compreendendo uma ou mais subunidades de ácido nucleico. Um ácido nucleico pode incluir uma ou mais subunidades selecionadas de adenosina (A), citosina (C), guanina (G), timina (T) e uracila (U), ou variantes desses. Em alguns exemplos, um ácido nucleico é um ácido desoxirribonucleico (DNA) ou ácido ribonucleico (RNA), ou derivados desses. Um ácido nucleico pode ser de cadeia única ou dupla. Um ácido nucleico pode ser circular.
[00203] O termo "nucleotídeo", como aqui usado, geralmente se refere a uma subunidade de ácido nucleico, que pode incluir A, C, G, T ou U, ou variantes ou análogos desses. Um nucleotídeo pode incluir qualquer subunidade que pode ser incorporada em um filamento de ácido nucleico em crescimento. Tal subunidade pode ser um A, C, G, T, ou U, ou qualquer outra subunidade que é específica a um ou mais A, C, G, T ou U complementar, ou complementar a uma purina (ou seja, A ou G, ou variante ou análogos desses) ou uma pirimidina (ou seja, C, T ou U, ou variante ou análogos desses). Uma subunidade pode permitir que bases de ácido nucleico individuais ou grupos de bases (por exemplo, AA, TA, AT, GC, CG, CT, TC, GT, TG, AC, CA, ou homólogos de uracil desses) para serem solucionados.
[00204] Um nucleotídeo geralmente inclui um nucleosídeo e pelo menos 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, ou mais grupos de fosfato (PO3). Um nucleotídeo pode incluir uma nucleobase, um açúcar de cinco carbonos (ribose ou desoxirribose) e um ou mais grupos de fosfato. Ribonucleo- tídeos são nucleotídeos nos quais o açúcar é ribose. Desoxirribonucleotí- deos são nucleotídeos nos quais o açúcar é desoxirribose. Um nucleotídeo pode ser um nucleosídeo monofosfato ou um nucleosídeo polifosfato. Um nucleotídeo pode ser um desoxirribonucleotídeo polifosfato, como, por exemplo, um desoxirribonucleotídeo trifosfato, que pode ser selecionado de dseoxiadenosina trifosfato (dATP), desoxicitidina trifosfato (dCTP), desoxiguanosine trifosfato (dGTP), desoxiuridina trifosfato (dUTP) e desoxitimidina trifosfato (dTTP) dNTPs, que incluem etiquetas detectáveis, como etiquetas luminescentes ou marcadores (por exemplo, fluoróforos).
[00205] Um nucleosídeo polifosfato pode ter ‘n’ grupos de fosfato, onde ‘n’ é um número que é maior do que ou igual a 2, 3, 4, 5, 6, 7, 8, 9, ou 10. Exemplos de nucleosídeo polifosfatos incluem nucleosídeo difosfato e nucleosídeo trifosfato. Um nucleotídeo pode ser um terminal fosfato rotulado nucleosídeo, como um terminal fosfato rotulado nucleosídeo polifosfato. Tal rótulo pode de um rótulo luminescente (por exemplo, fluorescente ou quimio-luminescente), um rótulo fluorogênico, um rótulo colorido, um rótulo cromogênico, uma etoieta em massa, um rótulo eletrostático, ou um rótulo eletroquímico. Um rótulo (or marcador) pode ser acoplado a um terminal fosfato através de um ligante. O ligante pode incluir, por exemplo, pelo menos um ou uma pluralidade grupos hidroxilo, grupos sulfidrilo, grupos amino ou grupos haloalquilo que podem ser adequados para formar, por exemplo, um éster fosfato, um tioéster, um fosforamidato ou uma ligação alquil-fosfonato no terminal fosfato de um nucleotídeo natural ou modificado. Um ligante pode ser clivável para separa um rótulo do terminal fosfato, como com o auxílio de uma enzima de polimerização. Exemplos de nucleotídeos e ligantes são fornecidos no Pedido de Patente U.S. No. 7.041,812, que é completamente incorporado aqui por referência.
[00206] O termo "polimerase", como aqui usado, geralmente se refere a qualquer enzima (ou enzima de polimerização) capz de catalisar uma reação de polimerização. Exemplos de polimerases incluem, sem limitação, uma polimerase de ácido nucleico, uma transcriptase ou ligase. Uma polimerase pode ser uma enzima de polimerização.
[00207] O termo "genoma" geralmente se refere a uma totalidade de uma informação de hereditariedade do organismo. Um genoma pode ser codificado em DNA ou em RNA. Um genoma pode compreender codificar as regiões que codificam as proteínas bem como regiões se codificação. Um genoma pode incluir a sequência de todos os cromossomos juntos em um organismo. Por exemplo, o genoma humano tem um total de 46 cromossomos. A sequência de todos esses constituintes juntos forma o genoma humano.
[00208] A presente revelação fornece dispositivos, sistemas e métodos para detectar biomoléculas ou subunidades desses, como moléculas de ácido nucleico. Tal detecção pode incluir a sequência. Uma biomolécula pode ser extraída de uma amostra biológica obtida de um sujeito. A amostra biológica pode ser extraída de fluidos corporais ou tecido do sujeito, como respiração, saliva, urina ou sangue (por exemplo, sangue total ou plasma). O sujeito pode ser suspeito de uma condição de saúde, como uma doença (por exemplo, câncer). Em alguns exemplos, uma ou mais moléculas de ácido nucleico são extraídas dos fluidos corporais ou tecido do sujeito. Um ou mais ácidos nucleicos pode ser extraído de uma ou mais células obtidas do sujeito, como parte de um tecido do sujeito, ou obtido de fluidos corporais sem células do sujeito, como sangue total.
[00209] Uma amostra biológica pode ser processada na preparação para detecção (por exemplo, sequência). Tal processamento pode incluir isolamento e/ou purificação da biomolécula (por exemplo, molécula de ácido nucleico) da amostra biológica e geração de mais cópias da biomolécula. Em alguns exemplos, uma ou mais moléculas de ácido nucleico são isoladas e purificadas formam um fluido corporal ou tecido do sujeito e amplificadas através da amplificação de ácido nucleico, como reação de cadeia de polimerase (PCR). Então, uma ou mais moléculas ou subunidades de ácidos nucleicos dessas podem ser identificadas, como através da sequência.
[00210] A sequência pode incluir a determinação de subunidades individuais de uma biomolécula modelo (por exemplo, molécula de ácido nucleico) pela sintetização de outra biomolécula que é complementar ou análoga ao modelo, como pela sintetização de uma molécula de ácido nucleico que é complementar a uma molécula de ácido nucleico modelo e identificar a incorporação de nucleotídeos com o tempo (ou seja, sequência por síntese). Como uma alternativa, sequência pode incluir a identificação direta de subunidades individuais da biomolécula.
[00211] Durante a sequência, sinais indicativos de subunidades individuais de uma biomolécula podem ser coletados na memória e processados em tempo real ou posteriormente para determinar uma sequência da biomolécula. Tal processamento pode incluir uma comparação dos sinais aos sinais de referência que permitem a identificação das subunidades individuais, que em alguns casos produz leituras. As leituras podem ser sequências de comprimento suficiente (por exemplo, pelo menos aproximadamente 30 pares de base (bp)) que podem ser usadas para identificar uma maior sequência ou região, por exemplo, que pode ser alinhada a uma localização em um cromossomo ou região genômica ou gene.
[00212] As leituras de sequência podem ser usadas para reconstruir uma região mais longa de um genoma de um sujeito (alinhamento). Leituras podem ser usadas para reconstruir as regiões cromossomais, todos os cromossomos, ou todo o genoma. Leituras de sequência ou uma maior sequência gerada dessas leituras pode ser usada para analisar um genoma de um sujeito, como identificar as variantes ou polimorfismos. Exemplos de variantes incluem, entre outros, polimorfismos de único nucleotídeo (SNPs) incluindo SNPs paralelos, exclusões ou inserções de pequena escla multibases, ainda chamadas como indels ou polimorfismos de exclusão e inserção ou DIPs), Polimorfismos Multi-Nucleotídeo (MNPs), Repetições curtas em tandem (STRs), exclusões, incluindo microexclusões, inserções, incluindo microinserções, variações estruturais, incluindo duplicações, inversões, translocalizações, multiplicações, variantes complexas multilocais, variações de número de cópia (CNV). Sequências genômicas podem compreender combinações de variantes. Por exemplo, sequência genômicas podem abranger a combinação de uma ou mais SNPs e um ou mais CNVs.
[00213] Subunidades individuais de biomoléculas podem ser identificadas usando marcadores. Em alguns exemplos, marcadores luminescentes são usados para subunidades individuais de biomoléculas identificadas. Algumas modalidades usam marcadores luminescentes (também aqui chamados de "marcadores"), que podem ser exógenos ou endógenos. Marcadores exógenos podem ser marcadores luminescentes externos usados como um repórter e/ou etiqueta para identificação luminescente. Exemplos de marcadores exógenos podem incluir, entre outros, moléculas fluorescentes, fluoróforos, indicadores fluorescentes, tinturas fluorescentes, indicadores orgânicos, proteínas fluorescentes, espécies que participam em transferência de energia de ressonância de fluorescência (FRET), enzimas, e/ou pontos quânticos. Outros marcadores exógenos são conhecidos na técnica. Tais marcadores exógenos podem ser conjugados a uma sonda ou grupo funcional (por exemplo, molécula, íon e/ou ligante) que especificamente liga a um alvo ou componente particular. Preso à etiqueta exógena ou repórter a uma sonda permite a identificação do alvo através da detecção da presença de etiqueta exógena ou repórter. Exemplos de sondas podem incluir proteínas, ácido nucleico (por exemplo, DNA, RNA) moléculas, lipídeos e sondas de anticorpo. A combinação de um marcador exógeno e um grupo funcional pode formar qualquer sonda adequada, etiquetas, e/ou rótulos usados para detecção, incluindo sondas moleculares, sondas rotuladas, sondas de hibridização, sondas de anticorpo, sondas de proteína (por exemplo, sondas de ligação por biotina), rótulos de enzima, sondas fluorescentes, etiquetas fluorescentes, e/ou repórteres de enzima.
[00214] Embora a presente revelação faz referência aos marcadores luminescentes, outros tipos de marcadores podem ser usados com dispositivos, sistemas e métodos fornecidos aqui. Tais marcadores podem ser etiquetas em massa, etiquetas eletrostáticas ou rótulos eletroquímicos.
[00215] Enquanto algumas modalidades podem ser direcionadas ao teste de diagnóstico pela detecção de moléculas únicas em um espécime, os inventores ainda reconheceram que a detecção de única molécula da presente revelação pode ser usada para realizar sequência polipeptídica (por exemplo, proteína) ou sequência de ácido nucleico (por exemplo, DNA, RNA) de um ou mais segmentos de ácido nucleico de, por exemplo, genes. As tecnologias de sequência de ácido nucleico podem variar nos métodos usados para determinar a sequência de ácido nucleico bem como na taxa, comprimento de leitura e incidência de erros no processo de sequência. Por exemplo, alguns métodos de sequência de ácido nucleico são baseados na sequência por síntese, na qual a identidade de um nucleotídeo é determinada como o nucleotídeo que é incorporado em um filamento recentemente sintetizado de ácido nucleico que é complementar ao ácido nucleico alvo.
[00216] Durante a sequência, uma enzima de polimerização pode acoplar (por exemplo, prender) a uma localização principal de uma molécula de ácido nucleico alvo. A localização principal pode ser um iniciador que é complementar à molécula de ácido nucleico alvo. Como uma alternativa a localização principal é uma fenda ou entalhe que é fornecido dentro de um segmento de duplo filamento da molécula de ácido nucleico alvo. Uma fenda ou entalhe pode ser de 0 a pelo menos 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 20, 30, ou 40 nucleotídeos no comprimento. Um entalhe pode fornecer uma quebra em um filamento de uma sequência de duplo filamento, que pode fornecer uma localização principal para uma enzima de polimerização, como, por exemplo, uma enzima de polimerase de deslocamento de filamento.
[00217] Em alguns casos, um iniciador de sequência pode ser unido a uma molécula de ácido nucleico alvo que pode ou pode não ser imobilizada a um suporte sólido, como um poço de amostra. Em algumas modalidades, um iniciador de sequência pode ser imobilizado em um suporte sólido e hibridização da molécula de ácido nucleico alvo ainda imobiliza a molécula de ácido nucleico alvo ao suporte sólido. Através da ação de uma enzima (por exemplo, uma polimerase) capaz de adicionar ou incorporar um nucleotídeo ao iniciador, nucleotídeos podem ser adicionados ao iniciador em 5’ a 3’, forma de ligação modelo. Tal incorporação de nucleotídeos a um iniciador (por exemplo, através da ação de uma polimerase) pode geralmente ser chamada como uma reação de extensão do iniciador. Cada nucleotídeo pode ser associado com uma etiqueta detectável que pode ser detectada e usada para determinar cada nucleotídeo incorporado ao iniciador e, assim, uma sequência de molécula de ácido nucleico recentemente sintetizada. Através da complementaridade da sequência da molécula de ácido nucleico recentemente sintetizada, a sequência da molécula de ácido nucleico alvo pode ainda ser determinada. Em alguns casos, hibridação de um iniciador de sequência a uma molécula de ácido nucleico alvo e incorporação de nucleotídeos ao iniciador de sequência podem ocorrer em condições de reação similares (por exemplo, a mesma temperatura de reação ou similar) ou em condições de reação diferenciadas (por exemplo, diferentes temperaturas de reação). Além disso, alguns métodos de sequência por síntese podem incluir a presença de uma população de molécula de ácido nucleico alvo (por exemplo, cópias de um ácido nucleico alvo) e/ou uma etapa de amplificação do ácido nucleico alvo para atingir uma população de ácidos nucleicos alvo.
[00218] Modalidades são capazes de sequência de únicas moléculas de ácido nucleico com alta precisão e longos comprimentos de leitura, como uma precisão de pelo menos aproximadamente 50%, 60%, 70%, 75%, 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99%, 99,9%, 99,99%, 99,999%, ou 99,9999% e/ou comprimentos de leitura maiores do que ou iguais a aproximadamente 10 pares de base (bp), 50 bp, 100 bp, 200 bp, 300 bp, 400 bp, 500 bp, 1000 bp, 10.000 bp, 20.000 bp, 30.000 bp, 40.000 bp, 50.000 bp ou 100.000 bp. Em algumas modalidades, a molécula de ácido nucleico alvo usada na sequência de molécula única é um único ácido nucleico alvo entrançado (por exemplo, desoxirriboáci- do nucleico (DNA), derivativos de DNA, riboácido nucleico (RNA), derivativos de RNA) modelo que é adicionado ou imobilizado a um poço de amostra contendo pelo menos um componente adicional de uma reação de sequência (por exemplo, uma polimerase como, um DNA polimerase, um iniciador de sequência) imobilizada ou presa a um suporte sólido como a base do poço de amostra. A molécula de ácido nucleico alvo ou a polimerase pode ser presa a uma parede da amostra, como na base do poço de amostra diretamente ou através de um ligante. O poço de amostra pode ainda conter quaisquer outros reagentes necessários para a síntese de ácido nucleico através da reação de extensão do iniciador, como, por exemplo buffers adequados, cofatores, enzimas (por exemplo, uma polimerase) e polifosfatos de desoxirribonucleotídeos, como por exemplo, trifosfatos de desoxirribo- nucleotídeos, incluindo trifosfato de desoxiadenosina (dATP), trifosfato de desoxicitidina (dCTP), trifosfato de desoxiguanosine (dGTP), trifosfato de desoxiuridina (dUTP) e desoxitimidina trifosfato (dTTP) dNTPs, que incluem etiquetas luminescentes, como fluoróforos. Cada classe de dNTPs (por exemplo dNTPs contendo adenina (por exemplo, dATP), dNTPs contendo citosina (por exemplo, dCTP), dNTPs contendo guanina (por exemplo, dGTP), dNTPs contendo uracila (por exemplo, dUTPs) e dNTPs contendo timina (por exemplo, dTTP)) é conjugada para uma etiqueta luminescente distinta de modo que a detecção de luz emitida da etiqueta indica a identidade do dNTP que foi incorporada a um ácido nucleico recém-sintetizado. A luz emitida da etiqueta luminescente pode ser detectada e atribuída a sua etiqueta luminescente apropriada (e, assim, o dNTP associado) através de qualquer dispositivo e/ou método adequado, incluindo tais dispositivos e métodos para a detecção descrita em outro lugar aqui. A etiqueta luminescente pode ser conjugada ao dNTP em qualquer posição de modo que a presença da etiqueta luminescente não iniba a incorporação do dNTP ao ácido nucleico recém-sintetizado entrançado ou à atividade da polimerase. Em algumas modalidades, a etiqueta luminescente é conjugada ao fosfato terminal (o fosfato gama) do dNTP.
[00219] O modelo de ácido nucleico alvo único entrançado pode ser colocado em contato com um iniciador de sequência, dNTPs, polimerase e outros reagentes necessário para a síntese do ácido nucléico. Em algumas modalidades, todos os dNTPs apropriados podem ser colocados em contato com o modelo de ácido nucleico alvo único entrançado simultaneamente (por exemplo, todos os dNTPs estão simultaneamente presentes) de modo que a incorporação de dNTPs pode ocorrer continuamente. Em outras modalidades, os dNTPs podem ser colocados em contato com o ácido nucleico alvo modelo único entrançado sequencialmente, onde o modelo de ácido nucleico alvo único entrançado é colocado em contato com cada dNTP apropriado separadamente, com etapas de lavagem entre o contato do modelo de ácido nucleico alvo único entrançado com dNTPs divergente. Tal ciclo de contato com o modelo de ácido nucleico alvo único entrançado com cada dNTP separadamente seguido pela lavagem pode ser repetido para cada posição de base sucessiva do modelo de ácido nucleico alvo único entrançado para ser identificado.
[00220] O iniciador de sequência recoze ao modelo de ácido nucleico alvo único entrançado e a polimerase consecutivamente incorpora os dNTPs (ou outro polifosfato de desoxirribonucleotídeo) ao iniciador através do modelo de ácido nucleico alvo único entrançado. A única etiqueta luminescente associada a cada dNTP incorporado pode ser excitada com a luz de excitação apropriada durante ou após a incorporação do dNTP ao iniciador e sua emissão pode ser subsequentemente detectada, usando qualquer dispositivo(s) e/ou método(s) adequado, incluindo dispositivos e métodos para a detecção descrita em outro lugar aqui. A detecção de uma emissão de luz específica pode ser atribuída a um dNTP específico incorporado. A sequência obtida da coleta de etiquetas luminescentes detectadas pode então ser usada para determinar a sequência do modelo de ácido nucleico alvo único entrançado através da complementariedade da sequência.
[00221] Enquanto a presente revelação faz referência aos dNTPs, dispositivos, sistemas e métodos fornecidos aqui podem ser usados com vários tipos de nucleotídeos, como ribonucleotídeos e desoxirribo- nucleotídeos (por exemplo, polifosfatos de desoxirribonucleotídeo com pelo menos 4, 5, 6, 7, 8, 9, ou 10 grupos de fosfato). Tais ribonucleotídeos e desoxirribonucleotídeos podem incluir vários tipos de etiquetas (ou marcadores) e ligantes.
[00222] Sinais emitidos após a incorporação de nucleotídeos pode ser armazenados na memória e processados em um ponto mais tarde no tempo para determinar a sequência do modelo de ácido nucleico alvo. Isso pode incluir comparar os sinais aos sinais de referência para determinar as identidades dos nucleosídeos incorporados como uma função de tempo. Alternativamente ou além disso, o sinal emitida após a incorporação de nucleotídeo pode ser coletado e processado em tempo real (ou seja, após a incorporação de nucleotídeo) para determinar a sequência do modelo de ácido nucleico alvo em tempo real.
[00223] A sequência de ácido nucleico de uma pluralidade de modelos de ácido nucleico alvo únicos entrançado pode ser concluída onde múltiplos poços de amostra são disponíveis, como é o caso no dispositivos descrito em outro lugar aqui. Cada poço de amostra pode ser fornecido com um modelo de ácido nucleico alvo único entrançado e uma reação de sequência pode ser concluída em cada poço de amostra. Cada um dos poços de amostra pode ser colocado em contato com os reagentes apropriados (por exemplo, dNTPs, iniciador de sequências, polimerase, cofatores, buffers apropriados, e etc.) necessários para a síntese de ácido nucleico durante a reação de extensão do iniciador e a reação de sequência pode proceder em cada poço de amostra. Em algumas modalidades, os múltiplos poços de amostra são colocados em contato com todos os dNTPs apropriados simultaneamente. Em outras modalidades, os múltiplos poços de amostra são colocado em contato com cada dNTP apropriado separadamente e cada um é lavado em contato com diferentes dNTPs. Os dNTPs incorporados podem ser detectados em cada poço de amostra e uma sequência determinada para o ácido nucleico alvo único entrançado em cada poço de amostra, como é descrito acima.
[00224] Modalidades direcionadas à sequência de ácido nucleico de molécula única podem usar qualquer polimerase que é capaz de sintetizar um ácido nucleico complementar a uma molécula de ácido nucleico alvo. Exemplos de polimerases incluem, entre outros, um DNA polimerase, um RNA polimerase, uma polimerase termoestável, uma polimerase do tipo selvagem, uma polimerase modificada, E. coli DNA polimerase I, T7 DNA polimerase, bacteriofage T4 DNA polimerase Φ29 (psi29) DNA polimerase, Taq polimerase, Tth polimerase, Tli polimerase, Pfu polimerase, Pwo polimerase, VENT polimerase, PROFUNDOVENT polimerase, EX-Taq polimerase, LA-Taq polimerase, Sso polimerase, Poc polimerase, Pab polimerase, Mth polimerase, ES4 polimerase, Tru polimerase, Tac polimerase, Tne polimerase, Tma polimerase, Tca polimerase, Tih polimerase, Tfi polimerase, Platinum Taq polimerases, Tbr polimerase, Tfl polimerase, Tth polimerase, Pfutubo polimerase, Pyrobest polimerase, Pwo polimerase, KOD polimerase, Bst polimerase, Sac polimerase, fragmento Klenow, polimerase com 3’ a 5’ de atividade de exonuclease e variantes, produtos modificados e derivativos desses. Em algumas modalidades, a polimerase é uma único polimerase de subunidade. Em algumas modalidades, a polimerase é uma polimerase com alta processabi- lidade. A processabilidade da polimerase geralmente se refere à capacidade de uma polimerase de incorporar consecutivamente os dNTPs em um modelo de ácido nucleico sem liberar o modelo de ácido nucléico. Após o pareamento da base entre uma núcleobase de um ácido nucleico alvo e o dNTP complementar, a polimerase incorpora o dNTP ao entrançado de ácido nucleico recém-sintetizado formando uma ligação fósfodiéster entre a extremidade de hidroxila de 3’ da entrançado recém-sintetizado e o alfa fosfato do dNTP. Nos exemplos nos quais a etiqueta luminescente conjugada ao dNTP é um fluoróforo, sua presença é sinalizada pela excitação e um pulso de emissão é detectado durante ou após a etapa de incorporação. Para rótulos de detecção que são conjugados ao fosfato terminal (gama) do dNTP, a incorporação do dNTP em entrançados recém-sintetizados resultou na liberação dos fosfatos beta e gama fosfatos e o rótulo de detecção, que é livre para difundir no poço de amostra, resultando em uma diminuição na emissão detectada do fluoróforo.
[00225] Modalidades direcionadas à sequência de RNA de molécula única pode usar qualquer transcriptase reversa que é capaz de sintetizar DNA complementar (cDNA) de um modelo de RNA. Nessas modalidades, uma transcriptase reversa pode funcionar de maneira similar à polimerase na qual o cDNA pode ser sintetizado de um modelo de RNA através da incorporação de dNTPs a um iniciador de transcipção reversa recozido a um modelo de RNA. O cDNA pode então participar de uma reação de sequência e sua sequência determinada conforme descrito acima. A sequência determinada do cDNA pode então ser usada, através da complementaridade de sequência, para determinar a sequência do modelo de RNA original. Exemplos transcriptases reversas incluem transcriptase reversa do Vírus da Leucemia Moloney Murina (M-MLV), transcriptase reversa do vírus da mieloblastose aviária (AMV), transcriptase reversa do vírus de imunodeficiência humana (HIV-1) e transcriptase reversa de telomerase.
[00226] Tendo reconhecido a necessidade de aparelhos simples, menos complexos, para realizar a detecção de única molécula e/ou sequência de ácido nucleico, os inventores conceberam técnicas para detectar moléculas únicas usando conjuntos de etiquetas luminescentes para identificar diferentes moléculas. Tais moléculas únicas podem ser nucleotídeos ou aminoácidos tendo etiquetas. Etiquetas podem ser detectadas enquanto ligadas às moléculas únicas, na liberação das moléculas únicas, ou enquanto ligadas e na liberação das moléculas únicas. Em alguns exemplos, as etiquetas são etiquetas luminescentes. Cada etiqueta luminescente em um conjunto selecionado é associada com uma respectiva molécula. Por exemplo, um conjunto de quatro etiquetas pode ser usado para "identificar" o nucleobase presente no DNA - cada etiqueta do conjunto sendo associado com uma diferente nucleobase, por exemplo, uma primeira etiqueta sendo associada com adenina (A), uma segunda etiqueta sendo associada com citosina (C), uma terceira etiqueta sendo associada com guanina (G) e uma quarta etiqueta sendo associada com timina (T). Além disso, cada uma das etiquetas luminescentes no conjunto de etiquetas tem diferentes propriedades que podem ser usadas para distinguir uma primeira etiqueta do conjunto de outras etiquetas no conjunto. Dessa forma, cada etiqueta é unicamente identificável usando uma ou mais dessas características distinguíveis. Em forma de exemplo e não limitação, as características das etiquetas que podem ser usadas para distinguir uma etiqueta de outra pode incluir a energia de emissão e/ou comprimento de onda da luz que é emitida pela etiqueta em resposta à energia de excitação e/ou ao comprimento de onda da luz de excitação que é absorvida por uma etiqueta particular para colocar a etiqueta em um estado excitado.
[00227] As modalidades podem utilizar qualquer combinação adequada das características de etiqueta para distinguir uma primeira etiqueta em um conjunto de etiquetas das outras etiquetas no mesmo conjunto. Por exemplo, algumas modalidades podem usar apenas o comprimento de onda da luz de emissão das etiquetas para identificar as etiquetas. Nessas modalidades, cada etiqueta em um conjunto de etiquetas selecionado tem um diferente comprimento de onda de emissão máximo de outras etiquetas no conjunto e as etiquetas luminescentes são todas excitadas por luz de uma única fonte de excitação. A figura 1-1 ilustra os espectros de emissão de quatro etiquetas luminescentes de acordo com uma modalidade onde as quatro etiquetas exibem seu respectivo pico de intensidade em diferentes comprimentos de onda de emissão, aqui chamados de o "comprimento de onda de emissão máximo" da etiqueta. Um primeiro espectro de emissão 1-101 de uma primeira etiqueta luminescente tem um comprimento de onda de emissão máximo a À1, um segundo espectro de emissão 1-102 de uma segunda etiqueta luminescente tem um comprimento de onda de emissão máximo a À2, um terceiro espectro de emissão 1-103 de uma terceira etiqueta luminescente tem um comprimento de onda de emissão máximo a À3 e um quarto espectro de emissão 1-104 de uma quarta etiqueta luminescente tem um comprimento de onda de emissão máximo a À4. Nessa modalidade, os picos de emissão das quatro etiquetas luminescentes podem ter valores adequados que satisfaçam a relação À1 < À2 < À3 < À4. Os quatro espectros de emissão podem ou não se sobrepor. Entretanto, se os espectros de emissão de duas ou mais etiquetas se sobrepõem, é desejável selecionar uma etiqueta luminescente definida de modo que uma etiqueta emita substancialmente mais luz do que qualquer outra etiqueta em cada respectivo comprimento de onda máximo. Nessa modalidade, o comprimento de onda de excitação no qual cada uma das quatro etiquetas absorve no máximo a luz da fonte de excitação é substancialmente o mesmo, mas que não precisa ser o caso. Usando a etiqueta definida acima, quatro diferentes moléculas podem ser identificadas com uma respectiva etiqueta do conjunto de etiqueta, as etiquetas podem ser excitadas usando uma única fonte de excitação e as etiquetas podem ser distinguidas entre si detectando o comprimento de onda de emissão das etiquetas usando um sistema óptico e sensores. Enquanto a figura 1-1 ilustra quatro diferentes etiquetas, deve-se observar que qualquer número adequado de etiquetas pode ser usado.
[00228] Outras modalidades podem usar o comprimento de onda da luz de emissão das etiquetas e o comprimento de onda no qual as etiquetas absorvem a luz de excitação para identificar as etiquetas. Nessas modalidades, cada etiqueta em um conjunto de etiquetas selecionado tem uma diferente combinação de comprimento de onda de emissão e comprimento de onda de excitação das outras etiquetas no conjunto. Assim, algumas etiquetas dentro de um conjunto de etiqueta selecionado podem ter o mesmo comprimento de onda de emissão, mas serem excitadas por luz de diferentes comprimentos de onda. Por outro lado, algumas etiquetas dentro de um conjunto de etiqueta selecionado podem ter o mesmo comprimento de onda de excitação, mas emitem luz em diferentes comprimentos de onda. A figura 1-2A ilustra os espectros de emissão de quatro etiquetas luminescentes de acordo com uma modalidade onde duas das etiquetas têm um primeiro comprimento de onda de emissão máximo e as outras duas etiquetas têm um segundo comprimento de onda de emissão máximo. Um primeiro espectro de emissão 1-105 de uma primeira etiqueta luminescente tem um comprimento de onda de emissão máximo a A1, um segundo espectro de emissão 1-106 de uma segunda etiqueta luminescente ainda tem um comprimento de onda de emissão máximo a A1, um terceiro espectro de emissão 1-107 de uma terceira etiqueta luminescente tem um comprimento de onda de emissão máximo a À2 e um quarto espectro de emissão 1-108 de uma quarta etiqueta luminescente ainda tem um comprimento de onda de emissão máximo a À2. Nessa modalidade, os picos de emissão das quatro etiquetas luminescentes podem ter quaisquer valores adequados que atendam a relação À1 < À2. A figura 1-2B ilustra os espectros de absorção das quatro etiquetas luminescentes, onde duas das etiquetas têm um primeiro comprimento de onda de absorção máximo e as outras duas etiquetas têm um segundo comprimento de onda de absorção máximo. Um primeiro espectro de absorção 1-109 para a primeira etiqueta luminescente tem um comprimento de onda de absorção máximo a À3, um segundo espectro de absorção 1-110 para a segunda etiqueta luminescente tem um comprimento de onda de absorção máximo a À4, um terceiro espectro de absorção 1-111 para a terceira etiqueta luminescente tem um comprimento de onda de absorção máximo a À3 e um quarto espectro de absorção 1-112 para a quarta etiqueta luminescente tem um comprimento de onda de absorção máximo a À4. Observe que as etiquetas que compartilham um comprimento de onda de emissão máximo na figura 1-2A não compartilham um comprimento de onda de absorção máximo na figura 1-2B. Usar tal conjunto de etiqueta permite distinguir entre quatro etiquetas mesmo quando há apenas dois comprimentos de onda de emissão para os quatro indicadores. Isso também é possível usar duas fontes de excitação que emitem em diferentes comprimentos de onda ou uma única fonte de excitação capaz de emitir em múltiplos comprimentos de onda. Se o comprimento de onda da luz de excitação é conhecido para cada evento de emissão detectado, então pode ser determinado qual etiqueta estava presente. A(s) fonte(s) de excitação pode(m) alternar entre um primeiro comprimento de onda de excitação e um segundo comprimento de onda de excitação, que é referido como intercalação. De modo alternativo, dois ou mais pulsos do primeiro comprimento de onda de excitação podem ser usados seguidos por dois ou mais pulsos do segundo comprimento de onda de excitação.
[00229] Enquanto não ilustrado nas figuras, outras modalidades podem determinar a identidade de uma etiqueta luminescente com base na frequência de absorção sozinha. Tais modalidades são possíveis se a luz de excitação pode ser sintonizada a específicos comprimentos de onda que combinam o espectro de absorção das etiquetas em um conjunto de etiqueta. Nessas modalidades, o sistema óptico e o sensor usados para direcionar e detectar a luz emitida de cada etiqueta não precisam ser capazes de detectar o comprimento de onda da luz emitida. Isso pode ser vantajoso em algumas modalidades, pois reduz a complexidade do sistema óptico e sensores, pois detectam o comprimento de onda de emissão que não é necessário nessas modalidades.
[00230] Conforme discutido acima, os inventores reconheceram e apreciaram a necessidade de ser capaz de distinguir as diferentes etiquetas ópticas (por exemplo, luminescente) entre si usando várias características das etiquetas. O tipo de características usado para determinar a identidade de um impacto da etiqueta no dispositivo físico usado para realizar essa análise. O presente pedido revela várias modalidades de um aparelho, dispositivo, instrumento e métodos para realizar essas técnicas diferentes.
[00231] Brevemente, os inventores reconheceram e apreciaram que um dispositivo do sensor de pixel com um número de pixels relativamente grande (por exemplo, centenas, milhares, milhões ou mais) que permitem a detecção de uma pluralidade de moléculas individuais ou partículas paralelamente. Tais moléculas únicas podem ser nucleotídeos ou aminoácidos tendo etiquetas. Etiquetas podem ser detectadas enquanto ligadas a moléculas únicas, na liberação das moléculas únicas, ou enquanto ligada se sob liberação das moléculas únicas. Em alguns exemplos, as etiquetas são etiquetas luminescentes. As moléculas podem ser, em forma de exemplo e não limitação, proteínas e/ou ácidos nucleicos (por exemplo, DNA, RNA). Além disso, um dispositivo de alta velocidade que pode adquirir dados em mais do que centenas estruturas por segundo permite a detecção e análise de processos dinâmicos ou mudanças que ocorrem dentro de uma amostra sendo analisada.
[00232] Os inventores reconheceram e apreciaram que um chip descartável de análise de baixo custo pode ser usado em conexão com um instrumento que inclui uma fonte de luz de excitação, óptica e um sensor de luz para medir um sinal óptico (por exemplo, luz luminescente) emitida de amostras biológicas. Usar um chip de análise de baixo custo reduz o custo de realizar um dado bioensaio. Uma amostra biológica é colocada no chip de análise e, sob conclusão de um único bioensaio, pode ser descartado. Em algumas modalidades, mais do que um tipo de amostra pode ser analisado simultaneamente, paralelamente, colocando múltiplas amostras em diferentes porções do chip de análise ao mesmo tempo. O chip de análise relaciona com o instrumento multiuso mais caro, que pode ser usado repetidamente com muitos diferentes chips de análise descartáveis. Um chip de análise de baixo custo que relaciona com um instrumento compacto portátil pode ser usado em qualquer lugar do mundo, sem a restrição de laboratórios biológicos de alto custo que exigem experiência laboratorial para analisar amostras. Assim, a bioanalítica automatizada pode ser colocada nas regiões do mundo que previamente não poderia realizar análise quantitativa de amostras biológicas. Por exemplo, testes de sangue para crianças podem ser realizados colocando uma amostra de sangue em um chip descartável de análise, colocando o chip descartável de análise no pequeno instrumento portátil para análise e processamento dos resultados por um computador que conecta ao instrumento para revisão imediata por um usuário. Os dados podem ainda ser transmitidos sobre uma rede de dados a uma localização remota para serem analisados, e/ou arquivados para análises clínicas subsequentes. De modo alternativo, o instrumento pode incluir um ou mais processadores para analisar os dados obtidos dos sensores do instrumento. Várias modalidades são descritas em mais detalhes abaixo. Visão geral do aparelho de acordo com algumas modalidades
[00233] Uma visão geral esquemática do aparelho 2-100 é ilustrada na figura 2-1. O sistema compreende um chip de análise 2-110 e um instrumento 2-120 compreendendo uma fonte de excitação 2-121 e pelo menos um sensor 2-122. O chip de análise 2-110 relaciona com o instrumento 2-120 usando qualquer interface de chip de análise adequada. Por exemplo, a interface de chip de análise do instrumento 2-120 pode incluir um soquete (não ilustrado) para receber o chip de análise 2-110 e segurá-lo no alinhamento óptico preciso com a fonte de excitação 2-110 e pelo menos um sensor 2-122. A fonte de excitação externa 2-121 no instrumento 2-120 é configurada para fornecer energia de excitação ao chip de análise 2-110 para a finalidade de excitar uma amostra no poço de amostra 2-111 do chip de análise 2-110. Em algumas modalidades, o chip de análise 2-110 tem múltiplos pixels, o poço de amostra 2-111 de cada pixel configurado para receber uma amostra usada em uma análise independente de outros pixels. Cada pixel do chip de análise 2-110 compreende um poço de amostra 2-211 para receber, reter e analisar uma amostra do espécime sendo analisado. Tais pixels podem ser chamados como "pixels de fonte passiva" visto que os pixels recebem energia de excitação de uma fonte de excitação separada do pixel. Em algumas modalidades, há um pixel no instrumento 2-120 correspondente a cada pixel presente no chip de análise 2-110. Cada pixel do instrumento 2-120 compreende pelo menos um sensor para detectar a energia de emissão emitida pela amostra em resposta à amostra sendo iluminada com energia de excitação da fonte de excitação 2-121. Em algumas modalidades, cada sensor pode incluir múltiplos subssensores, cada subssensor configurado para detectar um diferente comprimento de onda da energia de emissão da amostra. Enquanto mais do que um subssensor pode detectar a energia de emissão de um certo comprimento de onda, cada subssensor pode detectar uma diferente faixa de comprimento de onda da energia de emissão.
[00234] Em algumas modalidades, os elementos ópticos para guiar e acoplar a energia de excitação da fonte de excitação 2-121 ao poço de amostra 2-111 estão localizados no chip de análise 2-110 e no instrumento 2-120, conforme representado pela seta 2-101 na figura 21. Tais elementos fonte-para-poço podem incluir espelhos, lentes, revestimentos dielétricos e combinadores de feixe localizados no o instrumento 2-120 para acoplar a energia de excitação ao chip de análise 2-110 e lentes, elementos plasmônicos e revestimentos dielétricos no chip de análise 1-110 para direcionar a energia de excitação recebida do instrumento 2-120 ao poço de amostra 2-111. Adicionalmente, em algumas modalidades, os elementos ópticos para guiar a energia de emissão do poço de amostra 2-111 ao sensor 2-122 estão localizados no chip de análise 2-110 e no instrumento 2-120, conforme representado pela seta 2-102 na figura 2-1. Tais elementos de poço-para-amostra podem incluir lentes, elementos plasmônicos e revestimentos dielétricos localizados no chip de análise 2-110 para direcionar a energia de emissão do chip de análise 2-110 ao instrumento 2-120 e lentes, espelhos, revestimentos dielétricos, filtros e óptica difrativa no instrumento 1-120 para direcionar a energia de emissão recebida do chip de análise 2-110 ao sensor 2-111. Em algumas modalidades, um único componente pode ter uma função no acoplamento da energia de excitação a um poço de amostra e distribuição de energia de emissão do poço de amostra ao sensor.
[00235] Em algumas modalidades, o chip de análise 2-110 compreende uma pluralidade de pixels, cada pixel associado com seu próprio poço individual de amostra 2-111 e seu próprio sensor 2-122 associado no instrumento 2-120. A pluralidade de pixels pode estar disposta em uma matriz e pode ter qualquer número adequado de pixels. Por exemplo, o chip de análise pode incluir aproximadamente 1.000 pixels, 10.000 pixels, aproximadamente 100.000 pixels, aproximadamente 1.000.000 pixels, aproximadamente 10.000.000 pixels, ou aproximadamente 100.000.000 pixels.
[00236] Em algumas modalidades, o instrumento 2-120 inclui um chip do sensor compreendendo uma pluralidade de sensores 2-122 disposta como uma pluralidade de pixels. Cada pixel do chip do sensor corresponde a um pixel no chip de análise 2-110. A pluralidade de pixels pode ser disposta em uma matriz e pode ter qualquer número adequado de pixels. Em algumas modalidades, o chip do sensor tem o mesmo número de pixels que o chip de análise 2-110. Por exemplo, o chip do sensor pode incluir aproximadamente 10.000 pixels, aproximadamente 100.000 pixels, aproximadamente 1.000.000 pixels, aproximadamente 10.000.000 pixels, ou aproximadamente 100.000.000 pixels.
[00237] O instrumento 2-120 relaciona com o chip de análise 2-110 através de uma interface de chip de análise (não mostrada). A interface de chip de análise pode incluir componentes para posicionar e/ou alinhar o chip de análise 2-110 ao instrumento 2-120 para melhorar o acoplamento da energia de excitação da fonte de excitação 2-121 ao chip de análise 2-110. Em algumas modalidades, a fonte de excitação 2-121 inclui múltiplas fontes de excitação que são combinadas para distribuir energia de excitação ao chip de análise 2-110. As múltiplas fontes de excitação podem ser configuradas para produzir múltiplas energias de excitação, correspondente à luz de diferentes comprimentos de onda.
[00238] O instrumento 2-120 inclui uma interface do usuário 2-125 para controlar a operação do instrumento. A interface do usuário 2-125 é configurada para permitir que um usuário insira informações ao instrumento, como comandos e/ou ajustes usados para controlar o funcionamento do instrumento. Em algumas modalidades, a interface do usuário 2-125 pode incluir botões, interruptores, indicadores e um microfone para comandos por voz. Adicionalmente, a interface do usuário 2-125 pode permitir que um usuário receba feedback sobre o desempenho do instrumento e/ou chip de análise, como alinhamento correto e/ou informações obtidas pelos sinais de leitura dos sensores no chip do sensor. Em algumas modalidades, a interface do usuário 2-125 pode fornecer feedback usando um alto-falante para fornecer feedback sonoro e luzes indicadoras e/ou uma tela para fornecer feedback visual. Em algumas modalidades, o instrumento 2-120 inclui uma interface de computador 2-124 usada para conectar com um dispositivo de computação 2-130. Qualquer interface de computador 2-124 e dispositivo de computação 2-130 adequados podem ser usados. Por exemplo, a interface de computador 2-124 pode ser uma interface USB ou uma interface de firewire. O dispositivo de computação 2-130 pode ser qualquer computador de finalidade geral, como um laptop, desktop, ou tablet, ou um dispositivo móvel como um celular. A interface de computador 2-124 facilita a comunicação das informações entre o instrumento 2-120 e o dispositivo de computação 2-130. As informações de entrada para controlar e/ou configurar o instrumento 2-120 podem ser fornecidas através do dispositivo de computação 2-130 conectado à interface de computador 2-124 do instrumento. Adicionalmente, as informações de saída podem ser recebidas pelo dispositivo de computação 2-130 através da interface de computador 2-124. Tais informações de saída podem incluir feedback sobre desempenho do instrumento 2-120 e informações dos sinais de leitura do sensor 2-122. O instrumento 2-120 pode ainda incluir um dispositivo de processamento 2-123 para analisar dados recebidos do sensor 2-122. Em algumas modalidades, o dispositivo de processamento 2-123 pode ser um processador de finalidade geral (por exemplo, uma unidade de processamento central (CPU), uma matriz de campo de portas programáveis (FPGA) ou um circuito integrado personalizado, como um circuito integrado de aplicação específica (ASIC). Em algumas modalidades, o processamento de dados do sensor 1-122 pode ser realizado pelo dispositivo de processamento 2-123 e pelo dispositivo de computação externo 2-130. Em outras modalidades, o dispositivo de computação 2-130 pode ser omitido e o processamento de dados do sensor 2-122 pode ser realizado apenas pelo dispositivo de processamento 2-123.
[00239] Quando a fonte de excitação 2-121 ilumina o chip de análise 2-110 com energia de excitação, amostras dentro de um ou mais pixels do chip de análise 2-110 podem ser excitadas. Em algumas modalidades, um espécime é rotulado com múltiplos marcadores e os múltiplos marcadores, cada um associado com uma diferente amostra dentro do espécime, são identificáveis pela energia de emissão. A passagem do poço de amostra 2-111 ao sensor 2-122 pode incluir um ou mais componentes que ajudam a identificar os múltiplos marcadores com base na energia de emissão. Componentes podem focar na energia de emissão em direção ao sensor 2-122 e podem, de modo alternativo ou adicional, separar espacialmente as energias de emissão que têm diferentes energias características e, assim, diferentes comprimentos de onda. Em algumas modalidades, o chip de análise 2110 pode incluir componentes que direcionam a energia de emissão em direção ao sensor 2-122 e o instrumento 2-120 pode incluir componentes para espacialmente separar a energia de emissão de diferentes comprimentos de onda. Por exemplo, filtros ópticos ou óptica difrativa podem ser usados para acoplar o comprimento de onda da energia de emissão a um grau de liberdade espacial. O sensor ou região do sensor pode conter múltiplos subssensores configurados para detectar uma distribuição espacial da energia de emissão que depende do padrão de radiação. As etiquetas luminescentes que emitem diferentes energias de emissão e/ou faixas espectrais podem formar diferentes padrões de radiação. O sensor ou região do sensor pode detectar informações sobre a distribuição espacial da energia de emissão que pode ser usada para identificar um marcador entre os múltiplos marcadores.
[00240] A energia de emissão da amostra no poço de amostra 2-110 pode ser detectada pelo sensor 2-122 e convertida em pelo menos um sinal elétrico. Os sinais elétricos podem ser transmitidos ao longo das linhas condutoras no circuito do instrumento 2-120 e processados e/ou analisados pelo dispositivo de processamento 2-123 e/ou dispositivo de computação 2-130.
[00241] A figura 2-2 é uma vista superior do chip de análise 2-110 e a vista superior do chip do sensor 2-260 e ilustra a correspondência entre os pixels dos dois chips. O chip de análise 2-110 compreende uma pluralidade de pixels, cada pixel incluindo um poço de amostra 2-111 formado em um material condutor 2-221. O chip do sensor 2-260 ainda compreende uma pluralidade de pixels, cada pixel incluindo um sensor 2-121 formado em ou sobre um substrato 2-247. As setas nas figura 22 ilustram a correspondência entre dois dos pixels do chip de análise 2110 e dois dos pixels do chip do sensor 2-260. Enquanto não ilustrado para esclarecimento, cada pixel do chip de análise 2-110 é associado com um pixel do chip do sensor 2-260.
[00242] Uma visão geral de alguns componentes associados com um único pixel do chip de análise 2-110 e um único pixel do chip do sensor 2-260 é ilustrada na figura 2-3. O aparelho 2-100 compreende o chip de análise 2-110 e o instrumento 2-120. Em algumas modalidades, o chip de análise 2-110 é um chip descartável desenhado para a análise de um único espécime. O chip de análise 2-110 inclui uma ou mais camadas metálicas 2-221, uma ou mais camadas dielétricas 2-225 e elementos de focagem 2-227. Em algumas modalidades, a camada metálica 2-221 inclui uma pilha de camadas, algumas das quais podem incluir camadas absorventes. O instrumento 2-120 inclui uma ou mais fontes de excitação 2-250, pelo menos um espelho policrônico 2-230 e o chip do sensor 2-260, que pode incluir elementos filtrantes 2-241, elementos de classificação espectral 2-243, elementos de focagem 2245 e pelo menos um sensor 2-122 dentro ou sobre o substrato 2-247. Enquanto a figura 2-3 ilustra apenas um único pixel do chip de análise 2-110 e apenas um único pixel do chip do sensor 2-260, alguns componentes do instrumento 2-120, como a fonte de excitação 2-250, o espelho policrônico 2-230 e os elementos filtrantes 2-241, podem ser comuns a uma pluralidade de pixels. Por exemplo, em algumas modalidades, uma única fonte de excitação 2-250 e espelho policrônico 2-230 podem direcionar a energia de excitação a cada pixel do chip de análise 2-110.
[00243] Em algumas modalidades, o espécime pode incluir fluidos corporais, como sangue, urina ou saliva. O poço de amostra 2-211 dentro da camada metálica 2-221 forma um volume de amostra para uma amostra do espécime entrar. As aberturas na extremidade do poço de amostra 2-211 podem ser chamadas como uma nanoabertura. A nanoabertura pode ter uma largura que é menor que o comprimento de onda da energia de excitação 2-251 emitida pela fonte de excitação 2250. Uma porção do espécime, chamada como uma amostra, pode entrar no volume de amostra definido pelo poço de amostra 2-211. A amostra pode ser qualquer partícula, molécula, proteína, material genético ou qualquer outra amostra presente no espécime.
[00244] A fonte de excitação 2-250 emite a energia de excitação 2251, que é direcionada em direção ao poço de amostra 2-211 para iluminar a amostra. Em algumas modalidades, a fonte de excitação 2251 pode ser uma única fonte de luz que fornece energia de excitação para todo o pixel do chip de análise 2-110. O espelho policrônico 2-230 reflete a luz da fonte de excitação 2-250 e direciona a energia de excitação 2-251 em direção a um ou mais poços de amostra 2-211 do chip de análise 2-110. Assim, em algumas modalidades, pode haver apenas um único espelho policrônico 2-230 que direciona a energia de excitação em direção a todos os poços de amostra, ao invés de cada pixel ser associado com seu próprio espelho policrônico. De forma similar, pode haver uma relação um para muitos entre outros elementos ópticos usados para direcionar a energia de excitação em direção aos poços de amostra 2-211.
[00245] Uma rede circular concêntrica 2-223 pode ser formada adjacente a uma nanoabertura inferior do poço de amostra 2-211. As redes circulares concêntricas 2-223 podem projetar de uma superfície inferior da camada metálica 2-221. O poço de amostra 2-211 pode ser localizado em ou próximo ao centro da rede circular 2-223. Ambas a escala do subcomprimento de onda da nanoabertura do poço de amostra 2-211 e as redes circulares concêntricas 2-223 criam um efeito de melhoria de campo que aumenta a intensidade da energia de excitação no poço de amostra 2-211, resultando no acoplamento elevado da energia de excitação a uma amostra presente no poço de amostra 2-211. Pelo menos algum tempo, a amostra absorve um fóton da energia de excitação e emite um fóton (chamado como "energia de emissão" 2-253) com uma energia menor que a da energia de excitação 2-251. A energia de emissão 2-253 pode ser emitida em uma direção para baixo. As redes circulares 2-223 agem como elementos plasmônicos que podem ser usados para reduzir a dispersão da energia de emissão 2-253 e direcionar a energia de emissão 2-253 em direção a um sensor associado.
[00246] A energia de emissão 2-253 percorre através da camada dielétrica 2-225, que pode ser uma camada espaçadora usada para permitir que a energia de emissão 2-253 propague alguma distância. A camada dielétrica 2-225 pode ainda fornecer resistência estrutural ao chip de análise 2-110. A energia de emissão 2-253 então percorre através de um ou mais elementos de focagem 2-227 usados ainda para direcionar a energia de emissão 2-253 ao sensor 2-122 no pixel do chip do sensor 2-2260 associado dentro do instrumento 2-120.
[00247] O espelho policrônico 2-230 então transmite a energia de emissão 2-253 e reflete uma porção de qualquer energia de excitação 2-251 refletida do chip de análise 2-110. A porção da luz de excitação que não é refletida pelo chip de análise 2-110 é transmitida através do chip de análise ou absorvida pelo chip de análise. Para reduzir mais a quantidade de energia de excitação 2-251 refletida pelo chip de análise 2-110 e não refletida pelo espelho policrônico 2-230, elementos filtrantes 2-241 podem ser dispostos na passagem óptica em direção ao chip do sensor 2-260. Os elementos filtrantes 2-241 podem incluir, em forma de exemplo e não limitação, um filtro de banda larga, um filtro de rejeição ou um filtro de borda, que transmitem energia de emissão 2-253, mas absorvem e/ou refletem energia de excitação 2-251.
[00248] Nas modalidades, para facilitar o uso de propriedades espectrais da energia de emissão 2-253 para determinar a identidade do marcador no poço de amostra 2-211, elementos de classificação espectral 2-243 podem ser incluídos no chip do sensor 2-260 para acoplar o grau de liberdade espectral da energia de emissão 2-253 na direção que a energia de emissão 2-253 está percorrendo. Por exemplo, um elemento óptico difrativo pode ser usado para direcionar energia de emissão 2-253 de um primeiro comprimento de onda em uma primeira direção e energia de emissão 2-253 de um segundo comprimento de onda em uma segunda direção. Um ou mais elementos de focagem 2245 pode ser usado para direcionar a luz classificada espectralmente no sensor 2-122. O sensor 2-122 pode incluir um ou mais subssensores (não mostrados), cada um sendo associado com um diferente comprimento de onda da energia de emissão 2-253 com base na direção da luz de diferentes comprimentos de onda pelo elemento de classificação espectral 2-243.
[00249] A descrição acima da figura 2-3 é uma visão geral de alguns, mas não necessariamente todos, dos componentes do aparelho de acordo com algumas modalidades. Em algumas modalidades, um ou mais elementos da figura 2-3 podem estar ausentes ou em uma diferente localização. Os componentes do chip de análise 2-210 e o instrumento 2-220 são descritos em mais detalhes abaixo.
[00250] O chip de análise 2-110 e o instrumento 2-120 podem ser mecanicamente alinhados, separadamente acoplados e separáveis entre si. O instrumento 2-120 pode incluir um invólucro do instrumento, dentro desse uma placa de montagem 2-405 está disposta. A figura 2-4 ilustra pelo menos alguns dos componentes que podem ser incluídos na placa de montagem 2-405 do instrumento 2-120. A placa de montagem 2-405, que pode incluir uma placa de circuito impresso, pode ter o chip do sensor 2-260 (não visível na figura 2-4), um dissipador de calor 2407 e um invólucro óptico 2-401 montado nele. Os vários componentes do instrumento ópticos 2-120 podem ser dispostos dentro do invólucro óptico 2-401. Em algumas modalidades, o invólucro do instrumento e a placa de montagem podem ter qualquer tamanho adequado. Por exemplo, a placa de montagem pode ser substancialmente circular com um diâmetro de 7-8".
[00251] O chip de análise 2-110 acopla ao invólucro óptico 2-401 para garantir o alinhamento com os componentes ópticos dentro do invólucro óptico 2-401. Um suporte do chip 3-102 pode ser alinhado com uma abertura do invólucro óptico 2-401. Preferivelmente, o chip de análise 2-110 pode ser removivelmente acoplado ao instrumento 2-120. Por exemplo, componentes magnéticos 2-403a à 2-403b de qualquer formato adequado, como cilindros magnéticos, podem ser colocados ao redor de uma abertura do invólucro óptico 3-401 pelo qual a energia de excitação sai do invólucro óptico 2-401. Adicionalmente, os componentes magnéticos 2-403a à 2-403c podem ser calibrados de modo que o suporte do chip 3-102 seja mantido em alinhamento com a abertura. O suporte do chip pode ser posicionado com uma precisão por nível de mícron usando os cilindros de alinhamento. Em algumas modalidades, três cilindros magnéticos 2-403a à 2-403b são usados para criar o alinhamento do suporte do chip. Entretanto, modalidades não são tão limitadas e qualquer número adequado de componente magnético, carregado por mola, pneumático ou outros componentes podem ser usados para segurar o chip no lugar em uma configuração alinhada. Por exemplo, o suporte do chip 3-102 pode ser mantido no lugar co um elemento não magnético, como uma mola, pressão de ar, ou sucção de um vácuo. Opcionalmente, o suporte do chip 3-102 pode ser construído usando qualquer material rígido adequado para posicionar o chip no alinhamento com o bloco óptico.
[00252] De acordo com alguns aspectos do presente pedido, quando o chip é conectado ao sistema, a distância entre os poços de amostra e os sensores pode ser mantida pequena. Em algumas modalidades, a distância óptica entre os poços de amostra e os sensores pode ser menor que 30 cm, menor que 10 cm, menor que 5 cm, ou menor que 1 cm. Chip de análise
[00253] Em algumas modalidades, o chip de análise 2-110 não inclui quaisquer componentes eletrônicos ativos. Ambos a fonte de excitação 2-250 e o sensor 2-122 para cada pixel são localizados fora do chip no instrumento 2-120.
[00254] Em algumas modalidades, o chip de análise 2-110 pode ser alojado em um suporte do chip 3-102 conforme ilustrado na figura 3-1A. O suporte do chip 3-102 pode ser disponível e pode ser disposto junto com o chip de análise 2-110 após um uso único. O chip de análise 2110 pode ser situado na face inferior do suporte do chip 3-102, conforme ilustrado na figura 3-1B. O suporte do chip 3-102 pode compreender qualquer metal ferromagnético adequado, como aço, de modo que os componentes magnéticos 2-403a à 2-403b fixados ao invólucro óptico 2-401 segurem o suporte do chip 3-102 e assim o chip de análise 2-110, no lugar. Em algumas modalidades, o suporte do chip 3-102 pode ser preso à superfície superior do invólucro óptico 2-401 conforme ilustrado na figura 2-4.
[00255] Em outras modalidades, ilustradas na figura 3-1C, o chip de análise pode ser preso a uma superfície superior do suporte do chip 3102. Uma tampa plástica 3-103 envolve o chip de análise 2-110 de modo que a matriz do pixel do chip de análise 2-110 seja exposta através de uma abertura na tampa plástica 3-103. Um usuário do chip de análise 2-110 pode colocar um espécime na abertura da tampa plástica 3-103. Por estar em contato com a superfície superior do chip de análise 2-110, as amostras dentro do espécime podem ser introduzidas a um ou mais da pluralidade de pixels do chip de análise 2-110 para análise. Em algumas modalidades, nenhum canal fluídico ou dispositivo para distribuir porções da amostra aos pixels através do fluxo de fluido forçado é necessário. Camada do poço de amostra
[00256] Conforme ilustrado na figura 2-3 e em mais detalhes na figura 3-2, algumas modalidades incluem um poço de amostra 2-211 formado em um ou mais pixels do chip de análise 2-110. Um poço de amostra pode compreender um pequeno volume ou região formada dentro da camada metálica 2-221 e disposta de modo que amostras possam dispersar dentro e fora do poço de amostra de um espécime depositado na superfície do chip de análise 2-110. Em várias modalidades, um poço de amostra 2-211 pode ser disposto para receber energia de excitação de uma fonte de excitação 2-250. Amostras que difundem ao poço de amostra podem ser retidas, temporariamente ou permanentemente, dentro de uma região de excitação 3-215 do poço de amostra por um aderente 3-211. Na região de excitação, uma amostra pode ser excitada pela energia de excitação (por exemplo, luz de excitação 3-245) e subsequentemente emitir a energia que pode ser observada e avaliada para caracterizar a amostra.
[00257] Em mais detalhes da operação, pelo menos uma amostra 3101 para ser analisada pode ser introduzida a um poço de amostra 2- 211, por exemplo, de um espécime (não mostrado) contendo uma suspensão fluida de amostras. A energia de excitação 3-245 de uma fonte de excitação 2-250 no instrumento 2-120 pode excitar a amostra ou pelo menos uma etiqueta (também chamada como um marcador biológico, relator ou sonda) presa à amostra ou de outra forma associada com a amostra enquanto está dentro de uma região de excitação 3-215 dentro do poço de amostra. De acordo com algumas modalidades, uma etiqueta pode ser uma molécula luminescente (por exemplo, uma etiqueta luminescente ou sonda) ou ponto quântico. Em algumas implementações, pode haver mais do que uma etiqueta que é usada para analisar uma amostra (por exemplo, etiquetas distintas que são usadas para sequenciamento genético de molécula única conforme descrito em "Real-Time DNA Sequencing of Single Polymerase Molecules", por J. Eid, et al., Science 323, p. 133 (2009), que está incorporado por referência). Durante e/ou após a excitação, a amostra ou a etiqueta podem emitir energia de emissão. Quando múltiplas etiquetas são usadas, elas podem emitir em diferentes energias características (e, assim, ter diferentes comprimentos de onda) e/ou emitir com diferentes características temporais. As emissões do poço de amostra 2-211 podem radiar a um sensor 2-122 no instrumento 2120 onde são detectadas e convertidas em sinais elétricos que podem ser usados para caracterizar a amostra.
[00258] De acordo com algumas modalidades, um poço de amostra 2-211 pode ser uma estrutura parcialmente fechada, conforme representado na figura 3-2. Em algumas implementações, um poço de amostra 2-211 compreende um furo com tamanho de submicron ou abertura (caracterizado por pelo menos uma dimensão transversal Dsw) formado em pelo menos uma camada de material 2-221. A dimensão transversal do poço de amostra pode ser entre aproximadamente 20 nanometros e aproximadamente 1 micron, de acordo com algumas modalidades, embora tamanhos menores e maiores possam ser usados em algumas implementações. Um volume do poço de amostra 2-211 pode estar entre sobre 10-21 litros e sobre 10-15 litros, em algumas implementações. um poço de amostra pode ser formado como um guia de onda que pode, ou não pode, suportar um modo de propagação. Em algumas modalidades, um poço de amostra pode ser formado como um guia de onda do modo zero (ZMW) tendo uma forma cilíndrica (ou forma similar) com um diâmetro (ou dimensão transversal maior) Dsw. Um ZMW pode ser formado em uma única camada metálica como um furo de nano-escala que não suporta um modo óptico de propagação através do furo.
[00259] Por causa do poço de amostra 2-211 ter um pequeno volume, a detecção de eventos de única amostra (por exemplo, eventos de molécula única) em cada pixel pode ser possível embora as amostras possam ser concentradas em um espécime examinado em concentrações que são similares às encontradas em ambientes naturais. Por exemplo, as concentrações micromolares da amostra podem estar presentes em um espécime que é colocado em contato com o chip de análise, mas no nível de pixel apenas. Poços de amostra do ensaio 2110 são dimensionados de modo que, estatisticamente, eles tenham nenhuma amostra ou uma amostra, assim essa análise de molécula única pode ser realizada. Por exemplo, em algumas modalidades 3040% dos poços de amostra contém uma única amostra. Entretanto, poços de amostra podem conter mais que uma amostra. Por causa de eventos de molécula única ou amostra única podem ser analisadas em cada pixel, o chip de análise torna possível detectar eventos raros que podem passar despercebidos em medições médias.
[00260] Uma dimensão transversal Dsw de um poço de amostra pode estar entre aproximadamente 500 nanômetros (nm) e aproximadamente um mícron em algumas modalidades, entre aproximadamente 250 nm e aproximadamente 500 nm em algumas modalidades, entre aproximadamente 100 nm e aproximadamente 250 nm em algumas modalidades e ainda entre aproximadamente 20 nm e aproximadamente 100 nm em algumas modalidades. De acordo com algumas implementações, uma dimensão transversal de um poço de amostra está entre aproximadamente 80 nm e aproximadamente 180 nm, ou entre aproximadamente um quarto e um oitavo do comprimento de onda de excitação ou comprimento de onda de emissão. De acordo com outras implementações, uma dimensão transversal de um poço de amostra está entre aproximadamente 120 nm e aproximadamente 170 nm. Em algumas modalidades, a profundidade ou altura do poço de amostra 2-211 podem estar entre aproximadamente 50 nm e aproximadamente 500 nm. Em algumas implementações, a profundidade ou altura do poço de amostra 2-211 pode estar entre aproximadamente 80 nm e aproximadamente 200 nm.
[00261] Um poço de amostra 2-211 tendo um subcomprimento de onda, dimensão transversal pode melhorar a operação de um pixel 2100 de um chip de análise 2-110 em pelo menos duas formas. Por exemplo, a energia de excitação 3-245 incidente no poço de amostra de um lado oposto ao espécime pode acoplar à região de excitação 3-215 com energia exponencialmente decrescente e não propagar através do poço de amostra ao espécime. Como um resultado, a energia de excitação é aumentada na região de excitação onde excita uma amostra de interesse e é reduzida no espécime onde poderia excitar outras amostras que contribuiriam ao ruído de fundo. Ainda, a emissão de uma amostra retida em uma base do poço é preferivelmente direcionada ao sensor no instrumento 2-120, visto que a emissão não pode propagar através do poço de amostra. Ambos esses efeitos podem melhorar o índice de sinal para ruído no pixel. Os inventores reconheceram vários aspectos do poço de amostra que podem ser melhorados para ainda aumentar os níveis de sinal para ruído no pixel. Esses aspectos se referem ao formato do poço e estrutura, além da colocação, com relação às estruturas plasmônicas e ópticas adjacentes (descritas abaixo) que ajudam a acoplar a energia de excitação ao poço de amostra e energia do poço de amostra emitida.
[00262] De acordo com algumas modalidades, um poço de amostra 2-211 pode ser formado como uma nanoabertura de subcorte (SCN), que não suporta um modo de propagação. Por exemplo, o poço de amostra 2-211 pode compreender um furo cilindricamente formado ou furo em uma camada condutora 2-221. O corte transversal de um poço de amostra não precisa ser redondo e pode ser elíptico, quadrado, retangular, ou poligonal em algumas modalidades. A energia de excitação 3-245 (por exemplo, visível ou radiação quase infravermelha) pode entrar no poço de amostra através de uma abertura de entrada 3212 que pode ser definida pelas paredes 3-214 do poço de amostra 2211 em uma primeira extremidade do poço, conforme representado na figura 3-2. Quando formada como um SCN, a energia de excitação 3245 pode decair exponencialmente ao longo do SCN. Em algumas implementações, o guia de onda pode compreender um SCN para energia da amostra emitida, mas pode não ser um SCN para energia de excitação. Por exemplo, a abertura e o guia de onda formados pelo poço de amostra podem ser grandes o suficiente para surpotar um modo de propagação para a energia de excitação, visto que pode ter um comprimento de onda mais curto do que da energia emitida. A emissão, em um comprimento de onda mais longo, pode ser além de um comprimento de onda de corte para um modo de propagação no guia de onda. De acordo com algumas modalidades, o poço de amostra 2-211 pode compreender um SCN para a energia de excitação 3-245, de modo que a maior intensidade de energia de excitação esteja localizada em uma região de excitação 3-215 do poço de amostra em uma entrada ao poço de amostra 2-211 (por exemplo, localizada próxima à interface entre a camada 3-235 e a camada 2-221 conforme representado na figura 3-2). Tal localização da energia de excitação pode aumentar a densidade da energia de emissão da amostra e ainda confinar a energia de excitação próximo à abertura de entrada 3-212, limitando assim a emissão observada a uma única amostra (por exemplo, uma molécula única).
[00263] Um exemplo de localização de excitação próximo a uma entrada de um poço de amostra que compreende um SCN é representado na figura 3-3. Uma simulação numérica foi realizada para determinar a intensidade da energia de excitação dentro e próximo a um poço de amostra 2-211 formado como um SCN. Os resultados mostram que a intensidade da energia de excitação é aproximadamente 70% da energia incidente em uma abertura de entrada do poço de amostra e cai para aproximadamente 20% da intensidade incidente dentro de aproximadamente 100 nm no poço de amostra. Para essa simulação, o comprimento de onda da energia de excitação característico foi 633nm e o diâmetro do poço de amostra 2-211 foi 140 nm. O poço de amostra 2-211 foi formado em uma camada de metal de ouro. Cada divisão horizontal no gráfico é 50 nm. Conforme mostrado pelo gráfico, mais do que uma metade da energia de excitação recebida no poço de amostra está localizada a aproximadamente 50 nm dentro da abertura de entrada 3-212 do poço de amostra 2-211.
[00264] Para melhorar a intensidade da energia de excitação que está localizada no poço de amostra 2-211, outras estruturas do poço de amostra foram desenvolvidas e estudadas pelos inventores. A figura 34 descreve uma modalidade de um poço de amostra que inclui uma cavidade ou entalhe 3-216 em uma extremidade de excitação do poço de amostra 2-211. Como pode ser visto nos resultados de simulação da figura 3-3, uma região de intensidade de excitação mais alta existe apenas antes da abertura de entrada 2-212 do poço de amostra. Adicionar um entalhe 3-216 ao poço de amostra 2-211 permite que uma amostra mova em uma região de intensidade de excitação mais alta, de acordo com algumas modalidades. Em algumas implementações, o formato e a estrutura do entalhe altera o campo de excitação do local (por exemplo, por causa de uma diferença no índice refrativo entre a camada 3-235 e o fluido do espécime no poço de amostra) e pode ainda aumentar a intensidade da energia de excitação no entalhe.
[00265] O entalhe pode ter qualquer formato adequado. O entalhe pode ter uma forma transversal que é substancialmente equivalente a uma forma transversal do poço de amostra, por exemplo, redonda, elíptica, quadrada, retangular, poligonal, etc. Em algumas modalidades, as paredes laterais do entalhe podem ser substancialmente retas e verticais, como as paredes do poço de amostra. Em algumas implementações, as paredes laterais do entalhe podem ser inclinadas e/ou curvas, conforme representado no desenho. A dimensão transversal do entalhe pode ser aproximadamente o mesmo tamanho que a dimensão transversal do poço de amostra em algumas modalidades, pode ser menor do que a dimensão transversal do poço de amostra em algumas modalidades, ou pode ser maior do que a dimensão transversal do poço de amostra em algumas modalidades. O entalhe 3-216 pode estender entre aproximadamente 10 nm e aproximadamente 200 nm além da camada metálica 2-221 do poço de amostra. Em algumas implementações, o entalhe pode estender-se entre aproximadamente 50 nm e aproximadamente 150 nm além da camada metálica 2-221 do poço de amostra. Pela formação do entalhe, a região de excitação 3-215 pode estender-se fora da camada metálica 2-221 do poço de amostra, conforme representado na figura 3-4.
[00266] A figura 3-5 descreve a melhoria da energia de excitação na região de excitação para um poço de amostra contendo um entalhe (mostrado na imagem de simulação esquerda). Para comparação, o campo de excitação é ainda simulado para um poço de amostra sem um entalhe, mostrado à direita. A magnitude do campo foi convertida de uma cor nesses gráficos e a região escura na base do entalhe representa intensidade mais alta do que a região de luz dentro do poço de amostra. As regiões escuras acima do poço de amostra representam a intensidade mais baixa. Como pode ser visto, o entalhe permite que uma amostra 3-101 mova para uma região de intensidade de excitação mais alta e o entalhe ainda aumente a localização da região da intensidade mais alta em uma extremidade de excitação do poço de amostra. Observe que a região da high intensidade é mais distribuída para o poço de amostra sem o entalhe. Em algumas modalidades, o entalhe 3-216 fornece um aumento na energia de excitação na região de excitação por um fator de dois ou mais. Em algumas implementações, um aumento de mais do que um fator de dois pode ser obtido dependendo da forma e profundidade do entalhe. Nessas simulações, o poço de amostra compreende uma camada que tem 100nm de espessura, com um entalhe que tem 50nm de profundidade, com energia de excitação a 635nm de comprimento de onda.
[00267] A figura 3-6 descreve outra modalidade de um poço de amostra 2-211 em que o poço de amostra, incluindo o entalhe, são formados sobre uma protrusão 3-615 em uma superfície de um substrato. Uma estrutura resultante para o poço de amostra pode aumentar a energia de excitação na amostra por mais do que um fator de dois comparado a um poço de amostra mostrado na figura 3-2 e pode direcionar a emissão do poço de amostra em direção ao sensor no instrumento 2-120. De acordo com algumas modalidades, uma protrusão 3-615 é moldada em uma primeira camada 3-610 de material. A protrusão pode ser formada como um pedestal circular ou uma crista com corte transversal retangular em algumas implementações e uma segunda camada 3-620 de material pode ser depositada sobre a primeira camada e a protrusão. Na protrusão, a segunda camada pode formar um formato acima da protrusão que aproxima uma porção cilíndrica 3-625, conforme representado. Em algumas modalidades, uma camada condutora 3-230 (por exemplo, um metal reflexivo) pode ser depositada sobre a segunda camada 3-620 e moldada para formar um poço de amostra 3-210 na camada condutora acima da protrusão. Um entalhe 3-216 pode então ser gravado na segunda camada. O entalhe pode estender-se entre aproximadamente 50 nm e aproximadamente 150 nm abaixo da camada condutora 3-230. De acordo com algumas modalidades, a primeira camada 3-610 e a segunda camada 3-620 podem ser opticamente transparentes e podem ou pode não ser formadas de um mesmo material. Em algumas implementações, a primeira camada 3-610 pode ser formada de um óxido (por exemplo, SiO2) ou um nitrito (por exemplo, Si3N4) e a segunda camada 3-620 pode ser formada de um óxido ou um nitrito.
[00268] De acordo com algumas modalidades, a camada condutora 3-230 acima da protrusão 3-625 é formada aproximadamente como um refletor esférico 3-630. O formato da porção esférica pode ser controlado pela seleção da altura h, diâmetro ou dimensão transversal w da protrusão e uma espessura t da segunda camada 3-620. A localização da região de excitação e posição da amostra pode ser ajustada com relação a um ponto focal óptico do refletor cilíndrico pela seleção da profundidade do entalhe d. Pode ser observado que o refletor esférico 3-630 pode concentrar energia de excitação na região de excitação 3-215 e pode ainda coletar energia emitida de uma amostra e refletir e concentrar a radiação em direção ao sensor 3-260.
[00269] Conforme observado acima, um poço de amostra pode ser formado e, qualquer formato adequado e não é limitado a apenas formas cilíndricas. Em algumas implementações, um poço de amostra pode ser cônico, tetraedro, pentaedro, etc. A figura 3-7A à figura 3-7F ilustram alguns formatos exemplares do poço de amostra e estruturas que podem ser usadas em algumas modalidades. Um poço de amostra 2-211 pode ser formado para ter uma primeira abertura 2-212 que é maior do que uma segunda abertura 2-218 para a energia de excitação, de acordo com algumas modalidades. As paredes laterais do poço de amostra podem ser afiladas ou curvadas. Formar um poço de amostra nessa forma pode admitir mais energia de excitação na região de excitação, ainda atenuar a energia de excitação que percorre em direção ao espécime. Adicionalmente, a emissão radiada por uma amostra pode preferencialmente radiar em direção à extremidade do poço de amostra com a maior abertura, por causa da transferência de energia favorável nessa direção.
[00270] Em algumas modalidades, um entalhe 3-216 pode ter uma dimensão transversal menor do que a base do poço de amostra, conforme representado na figura 3-7B. Um entalhe menor pode ser formado pelo revestimento das paredes laterais do poço de amostra com uma camada sacrificial antes de gravar o entalhe e subsequentemente remover a camada sacrificial. Um entalhe menor pode ser formado para reter uma amostra em uma região que é mais equidistante das paredes condutoras do poço de amostra. Reter uma amostra equidistante das paredes do poço de amostra pode reduzir os efeitos indesejáveis das paredes do poço de amostra na amostra de radiação, por exemplo, têmpera de emissão e/ou alteração das vidas úteis de radiação.
[00271] A figura 3-7C e 3-7D representam outra modalidade de um poço de amostra. De acordo com essa modalidade, um poço de amostra 2-211 pode compreender a estruturas de melhoria de energia por excitação 3-711 e um aderente 3-211 formado adjacente à estruturas de melhoria de energia por excitação. As estruturas de melhoria por energia 3-711 podem compreender plásmon da superfície ou estruturas de nanoantena formadas nos materiais condutores em uma camada opticamente transparente 3-235, de acordo com algumas modalidades. A figura 3-7C descreve uma vista de elevação do poço de amostra 2211 e estrutura próxima e a figura 3-7D descreve uma vista plana. A estruturas de melhoria de energia por excitação 3-711 pode ser formada e disposta para melhorar energia de excitação em uma pequena região localizada. Por exemplo, as estruturas podem incluir condutores indicados tendo ângulos agudos no poço de amostra que aumenta a intensidade da energia de excitação dentro de uma região de excitação 3-215. No exemplo representado, as estruturas de melhoria de energia por excitação 3-711 estão na forma de uma gravata-borboleta. As amostras 3-101 que difundem na região podem ser retidas, temporariamente ou permanentemente, pelo aderente 3-211 e excitadas pela energia de excitação que pode ser distribuída de uma fonte de excitação 2-250 localizada no instrumento 2-120. De acordo com algumas modalidades, a energia de excitação pode acionar as correntes de plásmon da superfície nas estruturas de melhoria por energia 3-711. As correntes de plásmon da superfície resultantes podem produzir campos elétricos altos nas pontas afiadas das estruturas 3-711 e esses campos altos podem excitar uma amostra retida na região de excitação 3-215. Em algumas modalidades, um poço de amostra 2-211 representado na figura 3-7C pode incluir um entalhe 3-216.
[00272] Outra modalidade de um poço de amostra é representada na figura 3-7E e mostra uma estrutura de melhoria de energia por excitação 3-720 formada ao longo das paredes interiores do poço de amostra 2211. A estrutura de melhoria de energia por excitação 3-720 pode compreender um metal ou condutor e pode ser formada usando uma deposição inclinada (ou sombra), direcional onde o substrato no qual o poço de amostra é formado é girado durante a deposição. Durante a deposição, a base do poço de amostra 2-211 é obscura pelas paredes superiores do poço, de modo que o material depositado não acumule na base. A estrutura resultante 3-720 pode formar um ângulo agudo 3722 na base da estrutura e esse ângulo agudo do condutor pode melhorar a energia de excitação dentro do poço de amostra.
[00273] Em uma modalidade conforme representado na figura 3-7E, o material 3-232 no qual o poço de amostra é formado não precisa ser um condutor e pode ser qualquer material adequado como um material dielétrico. De acordo com algumas implementações, o poço de amostra 2-211 e a estrutura de melhoria de energia por excitação 3-720 podem ser formados em um furo cego gravado em uma camada dielétrica 3235 e uma camada separada 3-232 não precisa ser depositada.
[00274] Em algumas implementações, uma evaporação sombra pode ser subsequentemente realizada na estrutura mostrada na figura 3-7E para depositar uma estrutura de melhoria de energia metálica ou condutora, por exemplo, uma estrutura trapezoidal ou cone indicado na base do poço de amostra, conforme representado pela linha tracejada. A estrutura de melhoria de energia pode melhorar a energia de excitação dentro do poço através do plásmon da superfície. Após a evaporação sombra, um processo de planarização (por exemplo, uma etapa de polimento químico-mecânico ou um processo de decapagem de plasma) pode ser realizado parra remover ou gravar o material depositado no topo do poço de amostra, enquanto deixa a estrutura de melhoria de energia dentro do poço.
[00275] Em algumas modalidades, um poço de amostra 2-211 pode ser formado de mais do que uma única camada metálica. A figura 3-7F ilustra um poço de amostra formado em uma estrutura multicamadas, onde diferentes materiais podem ser usados para as diferentes camadas. De acordo com algumas modalidades, um poço de amostra 2-211 pode ser formado em uma primeira camada 3-232 (que pode ser um material semicondutor ou condutor), uma segunda camada 3-234 (que pode ser um isolante ou dielétrico) e uma terceira camada 2-221 (que pode ser um condutor ou semicondutor). Em algumas modalidades, um semicondutor degenerativamente dopado ou grafeno pode ser usado para uma camada do poço de amostra. Em algumas implementações, um poço de amostra pode ser formado em duas camadas e em outras implementações um poço de amostra pode ser formado em quatro ou mais camadas. Em algumas modalidades, materiais multicamadas usados para formar um poço de amostra podem ser selecionados para aumentar a geração de plásmon da superfície em uma base do poço de amostra ou suprimir a radiação do plásmon da superfície em um topo do poço. Em algumas modalidades, materiais multicamadas usados para formar um poço de amostra podem ser selecionados para suprimir a energia de excitação de propagar além do poço de amostra e estrutura multicamadas no espécime a granel.
[00276] Em algumas modalidades, os materiais multicamadas usados para formar um poço de amostra podem ser selecionados para aumentar ou suprimir excitações interfaciais que podem ser geradas pela energia de excitação incidente no poço de amostra. Por exemplo, multi-excitações, como biexcitações e triexitons, podem ser geradas em uma interface entre duas camadas semicondutoras diferentes adjacentes a um poço de amostra. O poço de amostra pode ser formado na camada metálica e na primeira camada semicondutora de modo que a interface entre a primeira camada semicondutora e uma segunda camada semicondutora esteja em uma região de excitação 3-215 do poço de amostra. Excitações interfaciais podem ter vidas úteis mais longas do que as excitações dentro do volume de uma única camada semicondutora, aumentando a probabilidade de as excitações excitarem uma amostra ou etiqueta através de FRET ou DET. Em algumas modalidades, pelo menos um ponto quântico no qual multi- excitações podem ser excitadas, pode ser preso em uma base do poço de amostra (por exemplo, por uma molécula de ligação). Excitações excitadas em um ponto quântico podem ainda ter vidas úteis mais longas do que as excitações dentro do volume de uma única camada semicondutora. Excitações interfaciais ou excitações geradas em um ponto quântico podem aumentar a taxa de FRET ou DET, de acordo com algumas modalidades.
[00277] Vários materiais podem ser usados para formar poços de amostra descritos nas modalidades anteriores. De acordo com algumas modalidades, um poço de amostra 2-211 pode ser formado de pelo menos uma camada de material 2-221, que pode compreender qualquer um ou uma combinação dentre um material condutor, um semicondutor e um isolante. Em algumas modalidades, o poço de amostra 2-211 compreende uma camada metálica altamente condutora, por exemplo, ouro, prata, alumínio, cobre. Em algumas modalidades, a camada 2-221 pode compreender uma pilha multicamadas que inclui qualquer um ou uma combinação dentre ouro, prata, alumínio, cobre, titânio, nitrito de titânio e cromo. Em algumas implementações, outros metais podem ser usados de forma adicional ou alternativa. De acordo com algumas modalidades, um poço de amostra pode compreender uma liga como AlCu ou AlSi.
[00278] Em algumas modalidades, as múltiplas camadas de diferentes metais ou ligas podem ser usadas para formar um poço de amostra. Em algumas implementações, o material no qual o poço de amostra 2-211 é formado pode compreender alternar as camadas de metais e não-metais, por exemplo, alternar as camadas de metal e um ou mais dielétricos. Em algumas modalidades, o não-metal pode incluir um polímero, como ácido fosfônico polivinílico ou um polietileno glicol (PEG) -tiol.
[00279] Uma camada 2-221 na qual um poço de amostra é formado pode ser depositada sobre ou adjacente a pelo menos uma camada opticamente transparente 3-235, de acordo com algumas modalidades, de modo que a energia de excitação (por exemplo, na forma de visível ou radiação quase infravermelha) e energia de emissão (por exemplo, na forma de visível ou radiação quase infravermelha) pode percorrer para e do poço de amostra 2-211 sem atenuação significante. Por exemplo, a energia de excitação de uma fonte de excitação 2-250 pode passar através de pelo menos uma camada opticamente transparente 2-235 à região de excitação 3-215 e emissão da amostra pode passar através da mesma camada ou camadas ao sensor 2-250.
[00280] Em algumas modalidades, pelo menos uma superfície do poço de amostra 2-211 pode ser revestida com uma ou mais camadas 3-211, 3-280 de material que afetam a ação de uma amostra dentro do poço de amostra, conforme representado na figura 3-8. Por exemplo, uma fina camada dielétrica 3-280 (por exemplo, alumina, nitrito de titânio, ou sílica) pode ser depositada como um revestimento de passivação nas paredes laterais do poço de amostra. Tal revestimento pode ser implementado para reduzir a adesão da amostra de uma amostra fora da região de excitação 3-215, ou para reduzir a interação entre uma amostra e o material 2-221 no qual o poço de amostra 2-211 é formado. A espessura de um revestimento de passivação dentro do poço de amostra pode ser entre aproximadamente 5 nm e aproximadamente 50 nm, de acordo com algumas modalidades.
[00281] Em algumas implementações, um material para uma camada de revestimento 3-280 pode ser selecionado com base em uma afinidade de um agente químico para o material, de modo que a camada 3-280 pode ser tratada com uma substância química ou biológica para inibir mais a adesão de uma espécie de amostra à camada. Por exemplo, uma camada de revestimento 3-280 pode compreender alumina, que pode ser passivada com uma camada de passivação de polifosfonato, de acordo com algumas modalidades. Revestimentos adicionais ou alternativos e agentes de passivação podem ser usados em algumas modalidades.
[00282] De acordo com algumas modalidades, pelo menos uma superfície inferior do poço de amostra 2-211 e/ou entalhe 3-216 pode ser tratada com um aderente químico ou biológico 3-211 (por exemplo, biotina) para promover a retenção de uma amostra. A amostra pode ser retida permanentemente ou temporariamente, por exemplo, por pelo menos um período de tempo entre aproximadamente 0,5 milissegundos e aproximadamente 50 milissegundos. Em outra modalidade, o aderente pode promover a retenção temporária de uma amostra 3-101 por períodos mais longos. Qualquer aderente adequado pode ser usado em várias modalidades e não é limitado a biotina.
[00283] De acordo com algumas modalidades, a camada de material 3-235 adjacente ao poço de amostra pode ser selecionada com base em uma finidade de um aderente para o material dessa camada. Em algumas modalidades, a passivação das paredes laterais do poço de amostra podem inibir o revestimento de um aderente nas paredes laterais, de modo que o aderente 3-211 preferencialmente deposite na base do poço de amostra. Em algumas modalidades, um revestimento de aderente pode estender-se até uma porção das paredes laterais do poço de amostra. Em algumas implementações, um aderente pode ser depositado por um processo de deposição física anisotrópica (por exemplo, evaporação, pulverização catódica), de modo que o aderente acumule na base de um poço de amostra ou entalhe e não apreciavelmente forme nas paredes laterais do poço de amostra.
[00284] Várias técnicas de fabricação podem ser empregadas para fabricar poços de amostra 2-211 para um chip de análise. Alguns processos exemplares são descritos abaixo, mas a invenção não é limitada a apenas esses exemplos.
[00285] O poço de amostra 2-211 pode ser formado por qualquer processo adequado de micro- ou nano-fabricação, que pode incluir, but não é limitado a, etapas de processamento associadas com fotolitografia, fotolitografia por ultravioleta profunda, fotolitografia por imersão, fotolitografia de contato óptico de campo próximo, litografia EUV, litografia por nanoimpressão, litografia interferométrica, litografia de passo e flash, litografia de feixe de elétron por escrita direta, litografia por feixe de íons, moagem feixe de íons, processo de arranque, gravura reativa a íon, epitaxia seletiva, automontagem molecular, síntese orgânica, etc. De acordo com algumas modalidades, um poço de amostra 2-211 pode ser formado usando fotolitografia e processo de arranque. Etapas exemplares de fabricação associadas com o processo de arranque de um poço de amostra são representadas na figura 3-9. Embora a fabricação de apenas um único poço de amostra ou estrutura em um pixel seja tipicamente representada nos desenhos, será entendido que um grande número de poços de amostra ou estruturas pode ser fabricado em um substrato (por exemplo, em cada pixel) paralelamente.
[00286] De acordo com algumas modalidades, uma camada 3-235 (por exemplo, uma camada de óxido) em um substrato pode ser coberta com uma camada antirreflexo (ARC) 3-910 e fotorresistiva 3-920, conforme representado na figura 3-9A. A fotoresistência pode ser exposta e moldada usando fotolitografia e desenvolvimento da resistência. A resistência pode ser desenvolvida para remover as porções expostas ou não expostas (dependendo do tipo de resistência), deixando um pilar 3-922 que tem um diâmetro aproximadamente igual a um diâmetro desejado para o poço de amostra, conforme representado na figura 3-9B. A altura do pilar pode ser maior do que uma profundidade desejada do poço de amostra.
[00287] O padrão do pilar 3-922 pode ser transferido à camada ARC 3-910 através da gravação de íon reativo anisotrópica (RIE), por exemplo, conforme mostrado na figura 3-9C. A região pode então ser revestida com pelo menos um material 2-221, por exemplo, um condutor ou metal, que é desejado para formar o poço de amostra. Uma porção do material depositado, ou materiais, forma uma tampa 3-232 sobre o pilar 3-922, conforme representado na figura 3-9D. A resistência e ARC podem então ser removidas do substrato, usando um processo de remoção seletivo (por exemplo, usando um banho químico com ou sem agitação que dissolve pelo menos a resistência e libera ou "remove" a tampa). Se a ARC permanecer, pode ser removida do substrato usando uma gravação seletiva, deixando o poço de amostra 3-210 conforme mostrado na figura 3-9E. De acordo com algumas modalidades, as paredes laterais 3-214 do poço de amostra podem ser inclinadas devido à natureza da deposição de pelo menos um material 2-221.
[00288] Como aqui usado, uma "gravação seletiva" significa um processo de decapagem no qual um líquido seletivamente grava um material que é desejado ser removido ou gravado em uma taxa mais alta (por exemplo, pelo menos duas vezes a taxa) do que o líquido grava outros materiais que não são destinados a serem removidos.
[00289] Por causa da resistência e ARC serem tipicamente à base de polímero, elas são consideradas materiais macios que não podem ser adequados para formar poços de amostra tendo razões altos de aspecto (por exemplo, razões de aspecto maiores do que aproximadamente 2:1 com relação à altura-para-largura). Para poços de amostra tendo razões mais altas, um material rígido pode ser incluído no processo de arranque. Por exemplo, antes de depositar a ARC e a fotoresistência, uma camada de um material rígido (por exemplo, um material inorgânico) pode ser depositada. Em algumas modalidades, uma camada de titânio ou nitrito de silicone pode ser depositada. A camada de material rígido deve exibir gravação preferencial sobre o material, ou materiais, 2-221 no qual o poço de amostra é formado. Após a fotoresistência ser moldada, um padrão do pilar pode ser transferido na ARC e o material rígido subjacente 3-930 produzindo uma estrutura conforme representado na figura 3-9F. A fotoresistência e ARC podem ser então removidas, o material(s) 2-221 depositados e uma etapa de remoção realizada para formar o poço de amostra.
[00290] De acordo com algumas modalidades, um processo de arranque pode ser usado para formar um poço de amostra compreendendo estruturas de melhoria por energia 3-711, conforme representado na figura 3-7C e na figura 3-7D.
[00291] Um processo alternativo para formar um poço de amostra é representado na figura 3-10. Nesse processo, o poço de amostra pode ser diretamente gravado em pelo menos um material 2-211. Por exemplo, pelo menos um material 2-211 no qual um poço de amostra deve ser formado pode ser depositado em um substrato 3-325. A camada pode ser coberta por uma camada de ARC 3-910 e uma fotoresistência 3-920, conforme ilustrado na figura 3-10A. A fotoresistência pode ser moldada para formar um furo tendo um diâmetro aproximadamente igual a um diâmetro desejado do poço de amostra, conforme representado na figura 3-10B. O padrão do furo pode ser transferido à ARC e através da camada 3-230 usando uma gravação por íon reativa anisotrópica, conforme mostrado na figura 3-10C, por exemplo. A resistência e a ARC podem ser removidas, produzindo um poço de amostra conforme representado na figura 3-10D. De acordo com algumas modalidades, as paredes laterais de um poço de amostra formadas por gravação na camada de material 3-230 podem ser mais verticais do que as paredes laterais resultantes de um processo de arranque.
[00292] Em algumas modalidades, a fotoresistência e ARC podem ser usadas para moldar uma máscara rígida (por exemplo, uma camada de nitrito de silicone ou óxido, não mostrada) sobre o material 2-221. O furo moldado pode então ser transferido à máscara rígida, que é então usada para transferir o padrão na camada de material 2-221. Uma máscara rígida pode permitir maior profundidade de gravação na camada de material 2-221, para formar poços de amostra de razão de aspecto mais alta.
[00293] Será observado que os processos de arranque e técnicas de fabricação de gravação direta descritas acima podem ser usados para formar um poço de amostra quando múltiplas camadas de diferentes materiais são usadas para formar uma pilha de material 2-211 na qual o poço de amostra é formado. Uma pilha exemplar é mostrada na figura 2-11. De acordo com algumas modalidades, uma pilha de material pode ser usada para formar um poço de amostra para melhorar o acoplamento de energia de excitação na região de excitação de um poço de amostra, ou para reduzir a transmissão ou radiação de energia de excitação ao espécime a granel. Por exemplo, uma camada absorvente 3-942 pode ser depositada sobre uma primeira camada 3-940. A primeira camada pode compreender um metal ou liga metálica e a camada absorvente pode compreender um material que inibe os plásmons da superfície, por exemplo, silicone amorfo, TaN, TiN, ou Cr. Em algumas implementações, uma superfície camada 3-944 pode ainda ser depositada para passivar a superfície ao redor do poço de amostra (por exemplo, inibir a adesão de moléculas).
[00294] A formação de um poço de amostra incluindo um entalhe 3216 pode ser feita em qualquer forma adequada. Em algumas modalidades, um entalhe pode ser formado pela gravação em uma camada adjacente 3-235, e/ou qualquer camada de intervenção ou camadas, adjacente ao poço de amostra. Por exemplo, após formar um poço de amostra em uma camada de material 2-221, essa camada 2221 pode ser usada como uma máscara de gravação para moldar um entalhe, conforme representado na figura 3-12. Por exemplo, o substrato pode ser submetido a uma gravação de íon reativo anisotrópico seletiva de modo que um entalhe 3-216 possa ser gravado na camada adjacente 3-235. Por exemplo, em uma modalidade onde o material 2-221 é metálico e a camada adjacente 3-235 óxido de silicone, uma gravação por plasma reativo tendo um gás de alimentação compreendendo CHF3 ou CF4 pode ser usada para preferencialmente remover o óxido de silicone exposto abaixo do poço de amostra e formar o entalhe 3-216. Como aqui usado, "óxido de silicone" geralmente se refere à SiOx e pode incluir dióxido de silicone, por exemplo.
[00295] Em algumas modalidades, as condições dentro do plasma (por exemplo, polarização ao substrato e pressão) durante uma gravação podem ser controladas para determinar o perfil da gravação do entalhe 3-216. Por exemplo, em pressão baixa (por exemplo, menor que aproximadamente 100 mTorr) e polarização DC alta (por exemplo, maior do que aproximadamente 20V), a gravação pode ser altamente anisotrópica e formar paredes laterais substancialmente retas e verticais do entalhe, conforme representado no desenho. Em pressões mais altas e polarização mais baixa, a gravação pode ser mais isotrópica produzindo paredes laterais curvadas e/ou afiladas do entalhe. Em algumas implementações, uma gravação úmida pode ser usada para formar o entalhe, que pode ser substancialmente isotrópico e formar um entalhe aproximadamente esférico que pode estender-se lateralmente sob o material 2-221, até ou além das paredes laterais do poço de amostra.
[00296] A figura 3-13A à figura 3-13C representam etapas do procede modo que pode ser usado para formar um entalhe 3-216 tendo uma dimensão transversal menor do que o poço de amostra 2-211 (por exemplo, um entalhe como o representado na figura 3-7B). Em algumas implementações, após formar um poço de amostra, uma camada sacrificial 3-960 conformal pode ser depositada sobre uma região incluindo o poço de amostra. De acordo com algumas modalidades, a camada sacrificial 3-960 pode ser depositada por um processo de deposição por vapor, por exemplo, deposição por vapor químico (CVD), CVD melhorado por plasma, ou deposição de camada atômica (ALD). A camada sacrificial pode então ser gravada novamente usando uma primeira gravação anisotrópica que é seletiva à camada sacrificial 3960, remove a camada das superfícies horizontais, deixa os revestimentos da parede lateral 3-962 nas paredes do poço de amostra, conforme representado na figura 3-13B. A gravação pode ser seletiva e parar no material 2-221 e na camada adjacente 3-235 em algumas modalidades, ou pode ser uma gravação não seletiva temporizada em algumas modalidades.
[00297] Uma segunda gravação anisotrópica que é seletiva à camada adjacente 3-235 pode ser executada para gravar um entalhe 3216 na camada adjacente conforme representado na figura 3-13C. Os revestimentos da parede lateral sacrificial 3-962 podem então ser opcionalmente removidos por uma gravação seletiva úmica ou seca. A remoção dos revestimentos da parede lateral abre ao poço de amostra para ter uma maior dimensão transversal do que o entalhe 3-216.
[00298] De acordo com algumas modalidades, a camada sacrificial 3-960 pode compreender o mesmo material que a camada adjacente 3235. Nessas modalidades, a segunda gravação pode remover pelo menos algum do revestimento da parede lateral 3-962 conforme o entalhe é gravado na camada adjacente 3-235. Essa gravação do revestimento da parede lateral pode formar paredes laterais afiladas do entalhe em algumas modalidades.
[00299] Em algumas implementações, a camada sacrificial 3-960 pode ser formada por, ou incluir uma camada de, um material que é usado para passivar as paredes laterais do poço de amostra (por exemplo, reduzir a adesão de amostras nas paredes laterais do poço de amostra). Pelo menos algumas da camada 3-960 podem então ser deixadas nas paredes do poço de amostra após a formação do entalhe.
[00300] De acordo com algumas modalidades, a formação dos revestimentos da parede lateral 3-962 ocorre após a formação do entalhe. Nessa modalidade a camada 3-960 reveste as paredes laterais do entalhe. Tal processo pode ser usado para passivar as paredes laterais do entalhe e localizar a amostra no centro do entalhe.
[00301] As etapas do processo associadas com a deposição de um aderente 3-211 em uma base de um poço de amostra 2-211 e uma camada de passivação 3-280 são representadas na figura 3-14. De acordo com algumas modalidades, um poço de amostra pode incluir uma primeira camada de passivação 3-280 nas paredes do poço de amostra. A primeira camada de passivação pode ser formada, por exemplo, conforme descrito acima em conexão com a figura 3-13B ou a figura 3-8. Em algumas modalidades, uma primeira camada de passivação 3-280 pode ser formada por qualquer processo de deposição adequado e gravação. Em algumas modalidades, uma primeira camada de passivação pode ser formada por oxidação do material 3-230 no qual o poço de amostra é formado. Por exemplo, o poço de amostra pode ser formado de alumínio, que pode ser oxidado para criar um revestimento de alumina nas paredes laterais do poço de amostra.
[00302] Um aderente 3-980 ou um aderente precursor (por exemplo, um material que preferencialmente liga um aderente) pode ser depositado no substrato usando um processo de deposição física anisotrópica, por exemplo, uma deposição evaporativa, conforme representado na figura 3-14A. O aderente ou aderente precursor pode formar uma camada aderente 3-211 na base do poço de amostra, conforme representado na figura 3-14B e pode revestir uma superfície superior do material 2-221 no qual o poço de amostra é formado. Uma deposição subsequente direcional inclinada representada na figura 314C (às vezes chamada como uma deposição por sombra ou processo de evaporação de sombra) pode ser usada para depositar uma segunda camada de passivação 2-280 sobre uma superfície superior do material 2-221 sem sobrir a camada aderente 3-211. Durante o processo de deposição por sombra, o substrato pode ser girado ao redor de um eixo normal ao substrato, de modo que a segunda camada de passivação 3280 deposite mais uniformemente ao redor de um aro superior do poço de amostra. Uma estrutura resultante é representada na figura 3-14D, de acordo com algumas modalidades. Como uma alternativa à deposição da segunda camada de passivação, uma gravação plana (por exemplo, uma etapa de CMP) pode ser usada para remover o aderente de uma superfície superior do material 3-230.
[00303] De acordo com algumas implementações, uma camada aderente 3-211 pode ser depositada centralmente na base de um poço de amostra afilado, conforme representado na figura 3-15. Por exemplo, um aderente, ou aderente precursor, pode ser depositado direcionalmente, conforme representado na figura 3-14A, em um poço de amostra afilado, formado conforme descrito acima. Paredes do poço de amostra podem ser passivados por um processo de oxidação antes ou após a deposição da camada aderente 3-211. Aderente ou precursor que permanece em uma superfície do material 2-221 pode ser passivado conforme descrito em conexão com a figura 3-14D. Em algumas modalidades, um aderente em uma superfície superior do material 2221 pode ser removido por uma etapa de polimento químico-mecaânico. Por meios da formação de uma camada aderente, ou uma camada aderente precursor, centralmente na base de um poço de amostra, efeitos deletérios na emissão de uma amostra (por exemplo, supressão ou arranque da radiação da amostra das paredes de amostra, distribuição de radiação desfavorável de uma amostra porque não está localizada centralmente com relação às estruturas de acoplamento de energia formadas ao redor de um poço de amostra, efeitos adversos na vida útil luminescente para uma amostra) podem ser reduzidos.
[00304] Em algumas modalidades, os processos de moldagem por elevação, gravação e deposição usados para formar o poço de amostra e entalhe podem ser compatíveis com os processos de CMOS que são usados para formar circuitos CMOS integrados em um chip do sensor. Certamente, o sensor pode ser fabricado usando instalações de CMOS convencionais e técnicas de fabricação, embora instalações de fabricação personalizadas ou especializadas posam ser usadas em algumas implementações.
[00305] As variações das etapas do processo descritas acima podem ser usadas para formar modalidades alternativas de poços de amostra. Por exemplo, um poço de amostra afilado como representada na figura 3-7A ou na figura 3-7B pode ser formado usando um processo de deposição inclinado representado na figura 3-14C. Para o poço de amostra da figura 3-7B, o ângulo de deposição pode ser mudado durante o processo de deposição. Para tais modalidades, um poço de amostra tendo substancialmente paredes laterais retas e verticais pode primeiro ser formado e então material adicional 2-221 depositado por uma deposição inclinada para afilar as paredes laterais do poço de amostra. B. Acoplamento de Energia de Excitação ao Poço de Amostra
[00306] Conforme ilustrado na figura 2-1 e na figura 2-3, a energia de excitação 2-251 da fonte de excitação 2-250 é guiada ao poço de amostra 2-211 usando componentes do instrumento 2-120 e componentes do chip de análise 2-110. Essa seção descreve os componentes do chip de análise 2-110 que podem ajudar no acoplamento de energia de excitação 2-251 ao poço de amostra 2-211.
[00307] O acoplamento de energia de uma fonte de excitação a um poço de amostra pode ser melhorado ou afetado pela formação das estruturas de acoplamento por excitação dentro e/ou adjacente a um poço de amostra. Estruturas de acoplamento por excitação podem compreender estruturas de micro- ou nano-escala fabricadas ao redor de um poço de amostra em algumas modalidades, ou pode compreender estruturas ou partículas formadas em um poço de amostra em algumas modalidades. Estruturas de acoplamento por excitação podem afetar a excitação radiativa de uma amostra em algumas implementações e pode afetar excitação não radiativa de uma amostra em algumas implementações. Em várias modalidades, as estruturas de acoplamento por excitação radiativa podem aumentar uma intensidade de energia de excitação dentro de uma região de excitação de um poço de amostra. Estruturas de acoplamento por excitação não radiativa podem melhorar e/ou alterar as passagens de transferência de energia não radiativa de uma fonte de excitação (que pode ser radiativa ou não-radiativa) a uma amostra. C. Estruturas de Acoplamento por Excitação Radiativa
[00308] Há vários diferentes tipos de estruturas de acoplamento por excitação radiativa que podem ser usadas para afetar o acoplamento de energia de excitação de uma fonte de excitação em uma região de excitação dentro de um poço de amostra. Algumas estruturas de acoplamento radiativas podem ser formadas de um condutor (por exemplo, incluem uma camada metálica) e suportam as oscilações de plásmon da superfície que localmente afetam a energia de excitação (por exemplo, localmente alteram um campo eletromagnético) próximo e/ou dentro do poço de amostra. Em alguns casos, as estruturas plasmônicas da superfície podem melhorar a energia de excitação dentro de uma região de excitação do poço de amostra por um fator de dois ou mais. Algumas estruturas de acoplamento radiativas podem alterar a fase e/ou a amplitude de um campo de excitação para melhorar a energia de excitação dentro de um poço de amostra. Várias modalidades de estruturas de acoplamento por excitação radiativa são descritas nessa seção.
[00309] A figura 4-1A descreve apenas um exemplo de uma estrutura plasmônica da superfície 4-120 que pode ser usado para melhorar o acoplamento de energia de excitação em um poço de amostra. O desenho descreve uma vista plana de uma região ao redor de uma estrutura plasmônica da superfície 4-120 e representa resultados de uma simulação numérica de intensidade de campo elétrico ao redor da estrutura. O desenho descreve uma estrutura plasmônica da superfície compreendendo três recursos retangulares tendo vértices acentuados que são localizados na proximidade a um poço de amostra (não mostrado). De acordo com algumas modalidades, uma estrutura plasmônica da superfície pode compreender um metal ou condutor (por exemplo, um filme fino moldado de qualquer um ou combinação dos seguintes metais ou ligas metálicas: Al, Au, Ag, Ti, TiN). Uma espessura do filme pode estar entre aproximadamente 10 nm e aproximadamente 100 nm em algumas modalidades, embora outras espessuras possam ser usadas em outras modalidades. Uma estrutura plasmônica da superfície, em algumas modalidades, pode incluir recursos acentuados 4-110 localizados na proximidade a um poço de amostra (por exemplo, dentro da aproximadamente 100 nm).
[00310] A figura 4-1B descreve uma vista de elevação transversal da estrutura plasmônica da superfície da figura 4-1A, pela linha tracejada. A simulação mostra uma região de alta intensidade localizada 4-505 da energia de excitação adjacente a um vértice de um triângulo da estrutura plasmônica da superfície. Para essa simulação, a estrutura plasmônica da superfície 4-120 foi localizada em uma camada dielétrica 4-135 (dióxido de silicone). A estrutura plasmônica da superfície utiliza a energia de um campo evanescente do guia de onda e melhora a intensidade no poço de amostra.
[00311] Em algumas modalidades, a melhoria da energia de excitação por uma estrutura plasmônica da superfície pode ser localizada em uma extensão que um profundo poço de amostra 2-211 não é necessário. Por exemplo, se uma região de alta intensidade 4505 é formada tendo um diâmetro de aproximadamente 100 nm com um valor de intensidade máximo maior do que aproximadamente 80% da intensidade fora da região, então um profundo poço de amostra pode não ser necessário. Apenas amostras dentro da região de alta intensidade 4-505 contribuiriam para a emissão apreciável para finalidades de detecção.
[00312] Quando um campo eletromagnético incidente interage com uma estrutura plasmônica da superfície, as correntes da onda da superfície são geradas na estrutura. O formato da estrutura pode afetar a intensidade e a dsitribuição desses plásmons da superfície. Essas correntes localizadas podem interagir e significantemente alterar e intensificar o campo eletromagnético na proximidade imediata da estrutura plasmônica da superfície, por exemplo, conforme representado pela região de alta intensidade 4-505 na figura 4-1B. Em algumas modalidades, um emissor (por exemplo, uma etiqueta fluorescente) que emite energia próximo a uma estrutura plasmônica da superfície pode ter sua emissão alterada pela estrutura, para alterar um padrão de radiação de campo distante do emissor.
[00313] Outra modalidade de uma estrutura plasmônica da superfície 4-122 é representada na vista plana da figura 4-1C. A estrutura de gravata-borboleta ilustrada compreende duas estruturas metálicas triangulares localizadas adjacentes a um poço de amostra 2-211. As estruturas podem ser moldadas abaixo de um poço de amostra, por exemplo, e/ou adjacentes a uma região de excitação do poço de amostra. Pode haver uma fenda 4-127 entre o poço de amostra e recursos acentuados 4-125 da estrutura plasmônica da superfície, em algumas implementações. A fenda 4-127 pode ser entre aproximadamente 10 nm e aproximadamente 200 nm, de acordo com algumas modalidades. Em algumas implementações, a fenda 4-127 pode ser entre aproximadamente 10 nm e aproximadamente 100 nm. Os recursos acentuados 4-125 podem compreender um ponto ou inclinação acentuada em uma borda da estrutura plasmônica da superfície, conforme representado no desenho. Os recursos acentuados podem ter qualquer formato adequado. Em algumas modalidades, um raio de inclinação de um recurso acentuado 4-125 pode ser menor que aproximadamente cinco comprimentos de onda associados com a energia incidente de excitação. Em algumas modalidades, um raio de inclinação de um recurso acentuado 4-125 pode ser menor que aproximadamente dois comprimentos de onda associados com a energia incidente de excitação. Em algumas modalidades, um raio de inclinação de um recurso acentuado 4-125 pode ser menor que aproximadamente cinco comprimentos de onda associados com uma onda do plásmon da superfície que é excitada pela energia incidente de excitação. Em algumas modalidades, um raio de inclinação de um recurso acentuado 4-125 pode ser menor que aproximadamente dois comprimentos de onda associados com uma onda do plásmon da superfície que é excitada pela energia incidente de excitação.
[00314] De acordo com algumas modalidades, estruturas plasmôni- cas da superfície 4-122 podem ser moldadas dentro de um poço de amostra 2-211 conforme ilustrado na vista de elevação da figura 4-1D. Em algumas modalidades, uma estrutura plasmônica da superfície dentro de um poço de amostra pode compreender um ou mais dedos (por exemplo, dedos metálicos) moldados nas paredes laterais do poço de amostra, conforme representado no desenho. A figura 4-1E descreve uma vista plana do poço de amostra 2-211 que mostra as estruturas plasmônicas da superfície 4-122 formadas nas paredes laterais dentro do poço de amostra. Em algumas modalidades, as extremidades inferiores dessas estruturas plasmônicas da superfície 4-122 formam recursos acentuados ou inclinações onde o campo eletromagnético será melhorado. As estruturas plasmônicas da superfície 4-122 podem, ou não, estender-se a uma base do poço de amostra.
[00315] Em algumas modalidades, as estruturas plasmônicas da superfície 4-122 podem estar dispostas para afetar a polarização da energia de excitação e/ou energia emitida do poço de amostra. Por exemplo, um padrão conforme representado na figura 4-1E pode ser usado para afetar uma orientação preferida da polarização de excitação linear ou elíptica e/ou uma orientação linear de polarização linear ou elíptica de um emissor dentro do poço de amostra.
[00316] As estruturas do plásmon da superfície podem ser moldadas nos formatos diferentes dos representados na figura 4-1A à figura 4-1E. Por exemplo, as estruturas plasmônicas da superfície podem ser moldadas como estruturas regulares ou periódicas, conforme representado na figura 4-2A, de acordo com algumas modalidades. Por exemplo, uma estrutura plasmônica da superfície pode ser moldada em uma matriz de recursos projetantes 4-210 em uma superfície inferior de um material 2-221 no qual o poço de amostra 2-211 é formado. Estruturas plasmônicas periódicas da superfície podem ser formadas em uma matriz regular, por exemplo, uma rede, uma grade, uma treliça, uma rede circular, uma rede espiral, uma rede elíptica, ou qualquer outra estrutura adequada. Pode haver um espaçamento a substancialmente uniforme entre as protrusões 4-210 de uma estrutura plasmônica da superfície. Em algumas implementações, o espaçamento s pode ter qualquer valor entre aproximadamente 40 nm e aproximadamente 250 nm. De acordo com algumas modalidades, as protrusões podem ter uma altura h entre aproximadamente 20 nm e aproximadamente 100 nm. Em algumas implementações, o espaçamento s pode ser não- uniforme ou pode ser chiado (tendo um valor decrescente em distâncias radiais maiores). Em algumas modalidades, as protrusões 5-210 de uma estrutura plasmônica da superfície podem ser moldada como uma placa de zona Fresnel. De acordo com algumas modalidades, uma estrutura plasmônica da superfície de 4-210 pode ser formada adjacente a uma camada transparente e/ou camada dielétrica 3-235. Em algumas modalidades, o espaçamento entre as protrusões 4-210 pode ser periódico, enquanto em outras modalidades as protrusões 4-210 podem ser aperiódicas.
[00317] Em algumas implementações, uma estrutura plasmônica da superfície 4-212 pode ser espaçada de um material 2-221 no qual o poço de amostra é formado conforme representado na figura 4-2B. Por exemplo, pode haver uma camada de intervenção dielétrica 4-247 entre a estrutura plasmônica da superfície 4-212 e o material 4-230. De acordo com algumas modalidades, uma estrutura de plásmons da superfície 4-212 pode ser localizada adjacente a um entalhe 3-216 de um poço de amostra, conforme representado no desenho. Por exemplo, uma estrutura plasmônica da superfície 4-212 pode ser localizada adjacente a paredes laterais de um entalhe 3-216, conforme representado na figura 4-2B.
[00318] A figura 4-2C ilustra uma estrutura plasmônica da superfície 4-214 que é formada como uma rede circular concêntrica. A estrutura 4214 pode compreender anéis condutores concêntricos 4-215, de acordo com algumas modalidades. Os anéis podem ser separados por um espaçamento regular s e ter uma altura h, conforme descrito em conexão com a figura 4-2A. De acordo com algumas modalidades, um poço de amostra 4-210 com um entalhe óptico pode ser localizado em um centro dos anéis. A rede circular pode ser moldada adjacente a uma base do poço de amostra.
[00319] Uma periodicidade de uma estrutura plasmônica da superfície pode ser selecionada para formar uma estrutura ressonante de acordo com algumas modalidades. Por exemplo um espaçamento s de uma estrutura plasmônica da superfície pode ser selecionado para ser aproximadamente meio comprimento de onda de uma onda do plásmon da superfície que é gerada na estrutura pela energia de excitação. Quando formada como uma estrutura ressonante, uma estrutura plasmônica da superfície pode acumular e ressonar energia de excitação ao longo da direção da estrutura plasmônica da superfície periódica. Tal comportamento ressonante pode intensificar a energia eletromagnética dentro de um poço de amostra, ou adjacente a um poço de amostra, conforme representado na figura 4-2D. Enquanto o espaçamento da estrutura de plásmon da superfície pode ser periódico em algumas modalidades, em outras modalidades o espaçamento pode ser aperiódico. Usar o espaçamento aperiódico permite que a melhoria do campo seja especificamente desenhada para os comprimentos de onda de energia de excitação e comprimentos de onda de energia de emissão envolvidos. A figura 4-2D representa resultados de campo eletromagnético numericamente simulado na base do poço de amostra e ao redor de uma estrutura plasmônica da superfície periódica. A estrutura plasmônica da superfície 4-216 está localizada adjacente ao material 2-221 no qual o poço de amostra é formado e é adjacente a uma base de um poço de amostra 2-211. A estrutura plasmônica da superfície pode estar na forma de uma rede ou rede circular que repete em intervalos regulares ou irregulares de espaçamento nas regiões distantes do poço de amostra e fora da região simulada. Por exemplo, podem haver entre três e cinquenta protrusões de rede repetidas da estrutura plasmônica da superfície 4-216. Uma região de alta intensidade 4-240 pode ser vista na base do poço de amostra 2-211. A intensidade dentro dessa região foi melhorada por mais do que um fator de 2 sobre a região circundante logo abaixo da estrutura plasmônica da superfície.
[00320] A figura 4-2E descreve, na vista de elevação, uma modalidade alternativa de uma estrutura ressonante plasmônica da superfície 4-218. De acordo com algumas modalidades, uma estrutura plasmônica da superfície pode ser formada como padrões de rede ou grade periódica ou aperiódica e pode ser moldada em múltiplas camadas 4-247. Um poço de amostra 2-211 pode ser moldado através das múltiplas camadas 4-247 e dentro da estrutura ressonante plasmônica da superfície 4-218, de acordo com algumas modalidades. Em algumas implementações, uma estrutura ressonante plasmônica da superfície pode compreender elementos condutores discretos 4-222 representados na vista plana da figura 4-2F. Em algumas implementa-ções, uma estrutura ressonante plasmônica da superfície pode compreender um padrão de treliça contínua 4-250, conforme representado na figura 4-2G. Um filtro dielétrico 4-252 pode ser localizado em vácuos do material condutor 4-250 e um poço de amostra 2-211 pode ser localizado com um vácuo.
[00321] Há uma variedade de diferentes estruturas plasmônicas da superfície que podem ser usadas para melhorar o acoplamento em um poço de amostra ou para afetar a emissão de uma amostra dentro do poço de amostra. A figura 4-2H descreve, em vista plana, ainda uma modalidade alternativa da estrutura plasmônica da superfície. Uma vista de elevação da estrutura é representada na figura 4-2I. De acordo com algumas implementações, uma estrutura plasmônica da superfície pode compreender uma matriz de discos distribuída ao redor de um poço de amostra 2-211. Em algumas implementações, ao invés de usar discos condutores 4-260, uma estrutura plasmônica da superfície pode compreender uma camada condutora pela qual um padrão distribuído de furos é formado. Tal estrutura pode ser chamada como uma "nanoantena".
[00322] Uma variedade de diferentes processos pode ser usada para moldar estruturas plasmônicas da superfície adjacentes a um poço de amostra. A figura 4-3A à figura 4-5E representam estruturas associadas com etapas do processo que pode ser usado para formar estruturas plasmônicas da superfície adjacentes a um poço de amostra, de acordo com algumas modalidades. Agora com referência à figura 4-3A, um processo para formar uma estrutura plasmônica da superfície pode compreender formar uma camada de resistência 4-310 em um revestimento antireflexo (ARC) 4-320 em uma camada de mascara- mento 4-330. As camadas podem estar dispostas em uma camada transparente dielétrica 3-235, de acordo com algumas implementações. A camada de resistência 4-310 pode compreender uma fotoresistência ou uma resistência de deixe por elétron ou íon que pode ser litograficamente moldada. A camada de mascaramento 4-330 pode compreender uma máscara rígida formada por um material inorgânico (por exemplo, silicone ou nitrito de silica, ou qualquer outro material adequado), de acordo com algumas modalidades.
[00323] Em algumas implementações, um processo fotolitográfico pode ser usado para moldar a resistência 4-310 conforme representado na figura 4-3B. O padrão selecionado pode compreender um layout de protrusões ou furos que serão usados para formar uma estrutura plasmônica da superfície desejada. Após desenvolver a resistência 4310, as regiões da ARC serão expostas e o padrão pode ser gravado na camada de ARC 4-320 e então na camada de mascaramento 4-330. A resistência e ARC pode ser removida do substrato e uma estrutura resultante pode aparecer conforme mostrado na figura 4-3C. A camada de mascaramento 4-330 pode então ser usada como uma máscara de gravação, de modo que o padrão possa ser transferido à camada dielétrica subjacente 3-235 através de uma gravura anisotrópica seletiva, conforme representado na figura 4-3D.
[00324] Um material condutor 2-221, ou uma camada de materiais compreendendo um condutor, pode então ser depositado sobre a região, conforme ilustrado na figura 4-3E. Qualquer material adequado condutor pode ser usado para formar uma estrutura de plásmon da superfície, se ou não depositada como uma camada separada do material 2-221. Por exemplo, em alguns casos, um primeiro material condutor pode ser depositado como uma camada de material base 2221 na qual uma estrutura plasmônica da superfície é formada. Exemplos de materiais que podem ser usados para fomar uma estrutura plasmônica da superfície incluem, entre outros, Au, Al, Ti, TiN, Ag, Cu e ligas ou combinação das respectivas camadas.
[00325] O material 2-221, ou camadas de material, pode ser depositado por qualquer processo de deposição adequado, incluindo, entre outros, um processo de deposição físicao ou um processo de deposição química por vapor. Em algumas modalidades, o material 2221 pode ter uma espessura entre aproximadamente 80 nm e aproximadamente 300 nm. Em algumas implementações, o material 2221 pode ser planar (por exemplo, usando um processo de CMP), embora a planarização não seja necessária. Um poço de amostra pode ser formado no material 2-221 usando qualquer processo adequado aqui descrito em conexão com a fabricação de um poço de amostra.
[00326] Os inventores reconheceram que formar uma estrutura plasmônica da superfície de acordo com as etapas mostradas na figura 4-3A à figura 4-3E pode exigir alinhamento preciso do poço de amostra à estrutura plasmônica da superfície. Por exemplo, uma estrutura plasmônica da superfície compreendendo uma rede concêntrica, conforme representado na figura 4-2C, pode exigir alinhamento preciso do poço de amostra 2-211 ao centro da estrutura plasmônica da superfície 4-214. Para evitar dificuldades de fabricação associados com tal alinhamento preciso, os processos de autoalinhamento representados na figura 4-4A à figura 4-5E podem ser usados.
[00327] Agora com referência à figura 4-4A, um processo para formar uma estrutura plasmônica da superfície e poço de amostra que é autoalinhado à estrutura plasmônica da superfície pode compreender formar uma camada de mascaramento 4-410 em uma camada transparente dielétrica 2-235. A camada de mascaramento pode compreender uma máscara rígida formada de um material inorgânico, como nitrito de silicone ou silica, de acordo com algumas modalidades. Uma espessura da camada de mascaramento 4-410 pode ser aproximadamente igual a uma altura desejada de um poço de amostra 2-212. Por exemplo, a espessura da camada de mascaramento pode estar entre aproximadamente 50 nm e aproximadamente 200 nm, de acordo com algumas modalidades, embora outras espessuras possam ser usadas em outras modalidades.
[00328] A camada de mascaramento 4-410 pode ser moldada para criar vácuos 4-430 tendo o padrão desejado de uma estrutura plasmônica da superfície que será moldada na camada dielétrica 2-235. A moldagem da camada de mascaramento 4-410 pode ser feita com qualquer processo de litografia adequado (por exemplo, fotolitografia, litografia de feixe por elétron, litografia de feixe por íon, litografia de EUV, litrografia de raio-X). A estrutura resultante pode parecer conforme mostrado na figura 4-4B. A estrutura pode incluir um pilar central 4-420, que será usado subsequentemente para formar o poço de amostra autoalinhado.
[00329] Uma resistência 4-440 (por exemplo, uma fotoresistência) pode então ser moldada sobre a camada de mascaramento moldada 4410, conforme representado na figura 4-4C. O alinhamento para moldar a resistência 4-440 (por exemplo, máscara para alinhamento de substrato) não precisa ser altamente preciso e apenas exigir a resistência 4-440 para cobrir um pilar central 4-420 e não cobrir vácuos 4-430 que serão usados para formar a estrutura plasmônica da superfície.
[00330] Uma gravação anisotrópica seletiva pode então ser usada para gravar a camada dielétrica 2-235 e transferir o padrão da estrutura plasmônica da superfície à dielétrica, conforme representado na figura 4-4D de acordo com algumas modalidades. Uma gravação isotrópica seletiva pode então ser usada para remover as porções expostas da camada de mascaramento 4-410. A gravação isotrópica pode ser uma gravação úmida, por exemplo, embora uma gravação isotrópica seca possa ser usada em algumas modalidades. Pela resistência 4-440 cobrir o pilar central 4-420, o pilar central não será gravado e permanecerá no substrato, conforme representado na figura 4-4E. A resistência 4-440 pode então ser removida do substrato expondo o pilar 4-420, conforme representado na figura 4-4F.
[00331] De acordo com algumas modalidades, um material condutor metálico 2-221, ou uma pilha de materiais incluindo um material condutor, pode então ser depositado sobre a região conforme ilustrado na figura 4-4G. O pilar central 4-420 e uma tampa de material depositada sobre o pilar pode então ser removida por uma gravação úmida seletiva do pilar, elevando a tampa. A remoção do pilar central deixa um poço de amostra que é autoalinhado com a estrutura plasmônica da superfície 4-450 subjacente.
[00332] Um processo alternativo pode ser usado para formar um poço de amostra que é autoalinhado a uma estrutura plasmônica da superfície e é representado na figura 4-5A à figura 4-5E. De acordo com algumas modalidades, uma ou mais camadas condutoras 4-510, 4-520 podem ser moldadas em uma camada transparente dielétrica 2-235 usando qualquer processo de litografia adequado, conforme representado na figura 4-5A. Em algumas implementações, uma primeira camada 4-510 pode compreender alumínio e uma segunda camada 4-520 pode compreender nitrito de titânio, embora outras combinações do material possam ser usadas em várias modalidades. Uma espessura total de uma ou mais camadas pode ser aproximadamente equivalente a uma altura desejada do poço de amostra, de acordo com algumas modalidades. A moldagem pode formar um poço de amostra 2-211 e vácuos 4-525 adjacentes ao poço de amostra em uma ou mais camadas metálicas. Os vácuos podem estar dispostos no padrão de uma estrutura plasmônica da superfície desejada.
[00333] Em algumas implementações, a camada dielétrica 3-235 pode ser gravada para transferir o padrão da estrutura plasmônica da superfície e poço de amostra 2-211 na camada dielétrica, conforme representado na figura 4-5B. A profundidade da gravação na dielétrica pode ser entre aproximadamente 20 nm e aproximadamente 150 nm, de acordo com algumas modalidades. Uma resistência 4-440 pode ser moldada para cobrir o poço de amostra, conforme representado na figura 4-5C. O alinhamento para moldar a resistência não precisa ser altamente preciso e apenas precisa cobrir o poço de amostra sem cobrir as regiões gravadas adjacentes da camada dielétrica 2-235 que será usada para formar a estrutura plasmônica da superfície.
[00334] Conforme ilustrado na figura 4-5D, um material condutor 4512, ou camadas de materiais incluindo um condutor, pode ser depositado sobre a região usando qualquer processo de deposição adequado. O material 4-512 pode preencher as regiões gravadas da camada dielétrica e pode estender-se acima de uma ou mais camadas 4-510, 4-520. A resistência 4-440 e o material que cobrem a resistência pode então ser removidos de acordo com um processo de arranque. A estrutura resultante, mostrada na figura 4-5E, deixa um poço de amostra que é autoalinhado à estrutura plasmônica da superfície circundante. O poço de amostra inclui um entalhe 3-216.
[00335] Em algumas modalidades, o processo representado na figura 4-5A à figura 4-5E pode ser usado para formar um poço de amostra que não tem um entalhe 3-216. Por exemplo, a resistência 4440 pode ser moldada sobre o poço de amostra 2-211 antes da camada dielétrica 2-235 ser gravado. A camada dielétrica 2-235 pode então ser gravada, que transferirá o padrão da estrutura plasmônica da superfície à camada dielétrica, mas não formará um entalhe. O processo pode então continuar conforme ilustrado na figura 4-5D e na figura 4-5E para criar um poço de amostra autoalinhado tendo nenhum entalhe.
[00336] Outras estruturas, além ou com uma alternativa às estruturas plasmônicas da superfície, podem ser moldadas na proximidade do poço de amostra 2-211 para aumentar a energia de excitação dentro do poço de amostra. Por exemplo algumas estruturas podem alterar a fase e/ou a amplitude do campo de excitação incidente para aumentar a intensidade da energia de excitação dentro do poço de amostra. A figura 4-6A descreve uma película fina com perdas 4-610 que pode ser usada para alterar a fase e a amplitude de energia incidente de excitação e aumentar a intensidade de radiação eletromagnética dentro do poço de amostra.
[00337] De acordo com algumas modalidades, uma película fina com perdas pode criar interferência consecutiva da energia de excitação, resultando na melhoria do campo dentro de uma região de excitação do poço de amostra. A figura 4-6B descreve uma simulação numérica de energia de excitação incidente em um poço de amostra onde uma película fina com perdas 4-610 foi formada logo adjacente ao poço de amostra. Para a simulação, o poço de amostra tem um diâmetro de aproximadamente 80 nm e é formado em uma camada metálica de ouro aproximadamente 200 nm de espessura. O poço de amostra compreende uma SCN e supre a propagação de energia de excitação através do poço de amostra. A película fina com perdas 4-610 tem aproximadamente 10 nm de espessura, é formada de germânio e cobre a dielétrica transparente subjacente compreendendo dióxido de silicone. A película fina com perdas estende-se por uma abertura de entrada do poço de amostra. A simulação mostra que a intensidade da energia de excitação é um valor mais alto na abertura de entrada do poço de amostra. A intensidade da energia de excitação nessa região clara 4620 é mais do que duas vezes o valor da intensidade à esquerda e direita do poço de amostra.
[00338] Uma película fina com perdas pode ser feita de qualquer material adequado. Por exemplo, uma película fina com perdas pode ser feita de um material onde o índice de refração n é aproximadamente a mesma ordem de magnitude que o coeficiente de extinsão k para o material. Em algumas modalidades, uma película fina com perdas pode ser feita por um material onde o índice de refração n está dentro de aproximadamente duas ordens da diferença de magnitude do valor do coeficiente de extinsão k do material. Exemplos não limitativos desses materiais em comprimentos visíveis de onda são germânio e silicone.
[00339] Uma película fina com perdas pode ter qualquer espessura adequada, que pode depender de um comprimento de onda característico, ou comprimentos de onda, associados com a fonte de excitação, ou fontes. Em algumas modalidades, uma película fina com perdas pode estar entre aproximadamente 1 nm e aproximadamente 45 nm de espessura. Em outras modalidades, uma película fina com perdas pode estar entre aproximadamente 15 nm e aproximadamente 45 nm de espessura. Ainda em outras modalidades, uma película fina com perdas pode estar entre aproximadamente 1 nm e aproximadamente 20 nm de espessura.
[00340] Efeitos de uma película fina com perdas na reflexão do material 2-221 no qual um poço de amostra é formado, a perda de energia de excitação dentro da película fina com perdas e perda de energia de excitação dentro do material 2-221 são mostradas no gráfico da figura 4-6C. Uma curva plotada no gráfico representa uma curva de reflexão 4-634 e mostra como a reflexão do material 2-221 e a película fina com perdas 4-610 variam conforme a espessura da película fina com perdas muda de 0 nm a 100 nm. A reflexão atinge um valor mínimo a aproximadamente 25 nm, de acordo com a modalidade simulada. O mínimo de reflexão ocorrerá em diferentes espessuras dependendo de um comprimento de onda característico da energia de excitação e materiais usados paraa película fina com perdas e material 2-221. Em algumas implementações, uma espessura de película fina com perdas é selecionada de modo que a reflexão esteja aproximadamente no seu valor mínimo.
[00341] Em algumas modalidades, uma película fina com perdas 4610 pode ser espaçada de um poço de amostra 2-211 e material 2-221, conforme representado na figura 4-6D. Por exemplo, uma fina camada dielétrica 4-620 (por exemplo, um óxido de silicone SiOx) pode ser formada sobre uma película fina com perdas e um poço de amostra 2211 pode ser formado adjacente à camada dielétrica 4-620. Uma espessura da camada dielétrica 4-620 pode estar entre aproximadamente 10 nm e aproximadamente 150 nm de acordo com algumas modalidades, embora outras espessuras possam ser usadas em algumas modalidades.
[00342] Embora representada como uma única camada, uma película fina com perdas pode compreender múltiplas camadas de dois ou mais materiais. Em algumas implementações, uma pilha multicamadas compreendendo alternar as camadas de uma película fina com perdas 4-610 e uma camada dielétrica 4-620 pode ser formada adjacente a um poço de amostra 2-211, conforme representado na figura 4-6E. Uma espessura de uma película fina com perdas 4-610 em uma pilha de camadas pode estar entre aproximadamente 5 nm e aproximadamente 100 nm e uma espessura de uma camada dielétrica 4-620 dentro da pilha pode estar entre aproximadamente 5 nm e aproximadamente 100 nm, de acordo com algumas modalidades. Em algumas implementações, a pilha multicamadas pode compreender uma camada de dióxido de silicone (4,2 nm de espessura), uma camada de silicone (14,35 nm de espessura) e uma camada de germânio (6,46 nm de espessura), embora outras espessuras possam ser usadas em outras modalidades. Em algumas implementações, a pilha multicama- das pode compreender uma camada de dióxido de silicone (aproximadamente 4,2 nm de espessura), uma camada de silicone (aproximadamente 14,4 nm de espessura) e uma camada de germânio (aproximadamente 6,5 nm de espessura), embora outras espessuras possam ser usadas em outras modalidades.
[00343] Uma película fina com perdas pode ser fabricada de qualquer material adequado que exibe pelo menos alguma perda na radiação incidente. Em algumas modalidades, uma película fina com perdas pode compreender um material semicondutor, por exemplo, silicone e germânio, embora outros materiais possam ser usados. Em algumas implementações, uma película fina com perdas pode compreender material inorgânico ou um metal. Em algumas modalidades, uma película fina com perdas pode compreender uma liga ou semicondutor composto. Por exemplo, uma película fina com perdas pode compreender uma liga incluindo Si (57,4% em peso), Ge (25,8% em peso) e SiO2 (16,8% em peso), embora outras razões e composições possam ser usados em outras modalidades.
[00344] De acordo com algumas modalidades, uma película fina com perdas pode ser formada no substrato usando qualquer processo de deposição de manta adequado, por exemplo, um processo de deposição física, um processo de deposição por vapor químico, um giro no processo, ou uma combinação desses. Em algumas modalidades, uma película fina com perdas pode ser tratada após a deposição, por exemplo, endurecida, recozida e/ou submetida a implantação de íon.
[00345] Outras estruturas de alteração de fase/amplitude podem ser usadas, de modo alternativo ou adicional, para melhorar a energia de excitação dentro do poço de amostra. De acordo com algumas implementações e conforme mostrado na figura 4-7A, uma pilha reflexiva 4-705 pode ser espaçada de um poço de amostra 2-211. Em algumas modalidades, uma pilha reflexiva pode compreender uma pilha dielétrica de materiais tendo índices alternados de refração. Por exemplo uma primeira camada dielétrica 4-710 pode ter um primeiro índice de refração e uma segunda camada dielétrica 4-720 pode ter um segundo índice de refração diferente do primeiro índice de refração. A pilha reflexiva 4-705 pode exibir uma ata reflexidade para energia de excitação em algumas modalidades, e exibir uma balxa reflexidade para emissão radiativa de um emissor dentro do poço de amostra. Por exemplo, uma pilha reflexiva 4-705 pode exibir uma refletividade maior do que aproximadamente 80% para energia de excitação e uma refletividade menor do que aproximadamente 40% para emissão de uma amostra, embora outros valores de refletividade possam ser usados em algumas modalidades. Uma camada dielétrica 4-730 que transmite a energia de excitação pode ser localizada entre a pilha reflexiva e o poço de amostra.
[00346] De acordo com algumas implementações, uma pilha reflexiva 4-705 representada na figura 4-7A pode formar um ressonador com o material 2-221 no qual o poço de amostra 2-211 é formado. Por exemplo, a pilha reflexiva pode ser espaçada do material 2-221 por uma distância que é aproximadamente igual ao meio do comprimento de onda da energia de excitação dentro do material dielétrico 4-730, ou um múltiplo integral desse. Pela formação de um ressonador, a energia de excitação pode passar pela pilha reflexiva, ressoar e criar no espaço entre o material 2-221 e a pilha reflexiva 4-705. Isso pode aumentar a intensidade de excitação dentro do poço de amostra 2-211. Por exemplo, a intensidade pode aumentar dentro da estrutura ressonante por mais do que um fator de 2 em algumas modalidades, e mais do que um fator de 5 em algumas modalidades, e ainda mais do que um fator de 10 em algumas modalidades.
[00347] Estruturas adicionais podem ser adicionadas na proximidade do poço de amostra, conforme representado na figura 4-7B e na figura 4-7C. De acordo com algumas modalidades, um plugue dielétrico 4-740 tendo um primeiro índice de refração que é mais alto do que um segundo índice de refração da camada dielétrica 4-730 pode ser formado adjacente ao poço de amostra 2-211, conforme representado na figura 4-7B. O plugue pode estar no formato de um cilindro tendo um diâmetro aproximadamente igual ao do poço de amostra, embora outros formatos e tamanhos possam ser usados. Por ter o índice refrativo mais alto, o plugue dielétrico 4-740 pode condensar e guiar a energia de excitação em direção ao poço de amostra.
[00348] Uma estrutura dielétrica, como o plugue 4-740, pode ser usada com ou sem uma pilha reflexiva 4-705, de acordo com algumas modalidades. Tal estrutura dielétrica pode ser chamada como uma antena ressonante dielétrica. A antena ressonante dielétrica pode ter qualquer formato adequado, por exemplo, cilíndrico, retangular, quadrado, polígono, trapezoidal, ou pirâmide.
[00349] A figura 4-7C e a figura 4-7D representam uma estrutura de banda larga fotônica (PBG) que pode ser formada na proximidade de um poço de amostra 2-211, de acordo com algumas modalidades. Uma estrutura de banda larga fotônica pode compreender uma matriz regular ou treliça de estruturas de contraste óptico 4-750. As estruturas de contraste óptico pode compreender material dielétrico tendo um índice refrativo que é diferente de um índice refrativo do material circundante dielétrico, de acordo com algumas modalidades. Em algumas implementações, as estruturas de contraste óptico 4-750 podem ter um valor de perda que é diferente do meio circundante. Em algumas implementações, um poço de amostra 2-211 pode ser localizado em um defeito na treliça conforme representado na figura 4-7D. De acordo com várias modalidades, o defeito na treliça fotônica pode confinar fótons dentro da região do defeito pode melhorar a intensidade da energia de excitação no poço de amostra. O confinamento devido à estrutura de banda larga fotônica pode ser substancialmente em duas dimensões transversais a uma superfície do substrato. Quando combinado com a pilha reflexiva 4-705, o confinamento pode estar em três dimensões no poço de amostra. Em algumas modalidades, uma estrutura de banda larga fotônica pode ser usada sem uma pilha reflexiva.
[00350] Vários métodos foram contemplados para fabricar a estrutura de acoplamento por excitação representada na figura 4-6A à figura 4-7D. Estruturas que exigem finos filmes planos (por exemplo, filmes dielétricos de índice refrativo alternado) podem ser formados pelos processos de deposição plana, de acordo com algumas modalidades. Os processos de deposição plana podem compreender deposição física (por exemplo, evaporação de feixe de elétron ou pulverização catódica) ou processo de deposição qu chemical processo de deposição por vapores. Estruturas que exigem dielétricas embutidas diescretas formadas em formatos tridimensionais, como uma antena ressonante dielétrica 4-740 mostrada na figura 4-7B ou as estruturas de contraste óptico 4-750 mostradas na figura 4-7C, podem ser formadas usando moldagem litográfica e processos de decapagem na gravação do molde ao substrato e usando deposição subsequente de uma camada dielétrica e uma planarização do substrato, por exemplo. Ainda contempladas são as técnicas de processamento de autoalinhamento para formar antenas ressonantes dielétricas bem como estruturas de banda larga fotônicas na proximidade do poço de amostra 2-211.
[00351] A figura 4-8A à figura 4-8G representam estruturas associadas com etapas do processo para apenas um processo de autoalinhamento que pode ser usado para formar uma estrutura de banda larga fotônica e um poço de amostra autoalinhado conforme ilustrado na figura 4-7C. De acordo com algumas modalidades, uma pilha reflexiva 4-705 pode ser primeiro formada em um substrato acima de uma camada dielétrica 3-235, conforme ilustrado na figura 4-8A. Uma segunda camada dielétrica 4-730 pode então ser depositada sobre a pilha reflexiva. A espessura da camada dielétrica 4-730 pode ser aproximadamente igual a aproximadamente meio comprimento de onda da energia de excitação no material, ou um múltiplo integral desse. As etapas do processo descritas em conexão com a figura 4-4A à figura 4- 4E podem então ser realizadas para formar um pilar 4-420 acima da camada dielétrica 4-730 e um padrão de recursos gravados 4-810 para a estrutura de banda larga fotônica. Os recursos gravados podem estender-se na camada dielétrica 4-730 e opcionalmente na pilha reflexiva 4-705. A estrutura resultante pode aparecer conforme mostrado na figura 4-8A.
[00352] Uma resistência 4-440 que cobre o pilar 4-420 pode ser removida do substrato e uma deposição conformal realizada para preencher os recursos gravados com um material de enchimento 4-820, conforme representado na figura 4-8B. O material de enchimento 4-820 pode ser o mesmo material que é usado para formar o pilar 4-420, de acordo com algumas modalidades. Por exemplo, o material de enchimento 4-820 e o pilar 4-420 podem ser formados de nitreto de silicone e a camada dielétrica 4-730 pode compreender um óxido, por exemplo, SiO2.
[00353] Uma gravação anisotrópica pode então ser realizar para gravar no material de enchimento 4-820. O material de enchimento pode ser gravado para expor uma superfície da camada dielétrica 4-730, de acordo com algumas modalidades, resultante em uma estrutura conforme representado na figura 4-8C. A gravação pode deixar um pilar 4-830 compreendendo o pilar original 4-420 e paredes laterais 4-822 que permanecem do material de enchimento 4-820.
[00354] Uma resistência 4-440 pode então ser moldada sobre o substrato conforme representado na figura 4-8D. Por exemplo, a resistência pode ser revestida no substrato, um furo moldado na resistência e na resistência desenvolvida para abrir uma região na resistência ao redor do pilar 4-830. O alinhamento do furo ao pilar não precisa ser altamente preciso e apenas precisa expor o pilar 4-830 sem expor as estruturas de banda larga fotônicas subjacentes embutidas na camada dielétrica 4-730.
[00355] Após o pilar 4-830 ser exposto, a gravação isotrópica pode ser usada para reduzir a dimensão transversal do pilar. De acordo com algumas modalidades, o formato do pilar resultante pode aparecer conforme representado na figura 4-8E. A resistência 4-440 pode então ser removida do substrato e um material 2-221, ou camadas de materiais, pode ser depositado sobre a região. Em algumas modalidades, o material 2-221 pode ser gravado usando um processo de CMP para planarizar a região conforme representada na figura 4-8F. Subsequentemente, uma gravação úmida ou seca seletiva pode ser usada para remover a estrutura do pilar remanescente deixando um poço de amostra 2-211, conforme ilustrado na figura 4-8G. Conforme indicado pelos desenhos, o poço de amostra 2-211 é autoalinhado à estrutura de banda larga fotônica moldada na camada dielétrica 4-730.
[00356] Como um processo alternativo, o material de enchimento 4820 pode compreender um diferente material do qual é usado para formar o pilar 4-420. Nesse processo, as etapas associadas com a figura 4-8D e a figura 4-8E podem ser omitidas. Após a deposição de material 2-221 e planarização, conforme representado na figura 4-8F, uma gravação seletiva pode ser realizada para remover o pilar 4-420. Isso pode deixar as paredes laterais do material de enchimento 4-820 alinhando o poço de amostra 2-211.
[00357] D. Estruturas de Acoplamento por Excitação Não Radiativa
[00358] A presente revelação fornece estruturas para acoplamento de energia de excitação não radiativa em uma amostra dentro do poço de amostra. Apenas uma modalidade de uma estrutura de acoplamento não radiativo é representada na figura 4-9A. De acordo com algumas modalidades, uma estrutura de acoplamento não radiativo pode compreender uma camada semicondutora 4-910 formada logo adjacente a um poço de amostra 2-211. A camada semicondutora 4-910 pode ser um semicondutor óptico em algumas modalidades, ou um semicondutor não óptico em algumas modalidades. Em algumas implementações, um entalhe 3-216 pode, ou não, ser formado na camada semicondutora. A camada semicondutora 4-910 pode ter uma espessura entre aproximadamente 5 nm e aproximadamente 100 nm de acordo com algumas modalidades, embora outras espessuras possam ser usadas em algumas modalidades. De acordo com algumas implementações, a energia de excitação ou fótons 4-930 de uma fonte de excitação pode colidir na camada semicondutora 4-910 e produzir excitações 4-920. As excitações podem difundir em uma superfície do poço de amostra onde tpodem não radiativamente recombinar e transferir energia a uma amostra adjacente às paredes do poço de amostra.
[00359] A figura 4-9B descreve outra modalidade na qual uma camada semicondutora 4-912 pode ser usada para transferir não radiativamente a energia de energia de excitação a uma amostra. Em algumas modalidades, uma camada semicondutora 4-912 pode ser formada na base de um poço de amostra ou em um entalhe do poço de amostra 2-211, conforme representado no desenho. A camada semicondutora 4-912 pode ser formada em um poço de amostra usando um processo de deposição direcional conforme descrito aqui em conexão com as etapas do processo para depositar um aderente na base do poço de amostra, de acordo com algumas modalidades. A camada semicondutora 4-912 pode ter uma espessura entre aproximadamente 5 nm e aproximadamente 100 nm de acordo com algumas modalidades, embora outras espessuras possam ser usadas em outras modalidades. A radiação incidente pode gerar excitações dentro da camada semicondutora, que pode então difundir à superfície inferior do poço de amostra 2-211. As excitações podem então transferir não radiativamente a energia a uma amostra dentro do poço de amostra.
[00360] A presente descrição ainda fornece múltiplas passagens não-radiativas para transferir energia de excitação a uma amostra. De acordo com algumas modalidades e conforme representado na figura 49C, uma partícula de transferência de energia 4-940 pode ser depositada dentro de um poço de amostra. A partícula de transferência de energia pode compreender um ponto quântico em algumas modalidades, ou pode compreender uma molécula em algumas modalidades. Em algumas implementações, a partícula de transferência de energia 4-940 pode ser funcionalizada a uma superfície do poço de amostra através de uma molécula de ligação. Uma fina camada semicondutora 4-910 pode ser formada adjacente ao poço de amostra, ou dentro do poço de amostra e excitações podem ser geradas dentro da camada semicondutora da energia de excitação incidente na camada semicondutora, conforme representado no desenho. As excitações podem difundir à superfície do poço de amostra e transferir energia não radiativamente à partícula de transferência de energia 4-940. A partícula de transferência de energia 4-940 pode então transferir não- radiativamente a energia a uma amostra 3-101 dentro do poço de amostra.
[00361] De acordo com algumas implementações, pode haver mais do que uma partícula de transferência de energia 4-940 dentro de um poço de amostra. Por exemplo, uma camada de partículas de transferência de energia 4-942 pode ser depositada dentro de um poço de amostra, como o poço de amostra representado na figura 4-9C.
[00362] Em algumas implementações, as partículas de transferência de energia 4-942, ou uma única partícula de transferência de energia 4940, pode ser depositada em uma base de um poço de amostra, conforme representado na figura 4-9D. A partícula de transferência de energia, ou partículas, pode radiativamente ou não-radiativamente transferir energia de excitação a uma amostra 3-101 dentro do poço. Por exemplo, uma partícula de transferência de energia pode absorver energia incidente para formar um estado excitado da partícula de transferência de energia e então radiativamente ou não-radiativamente transferir energia à amostra 3-101.
[00363] Em algumas implementações, uma partícula de transferência de energia pode absorver energia incidente de excitação e então emitir novamente a energia radiativaa em um comprimento de onda que é diferente do comprimento de onda da energia de excitação absorvida. A energia reemitida pode então ser usada para excitar uma amostra dentro do poço de amostra. A figura 4-9E representa gráficos espectrais associados com uma partícula de transferência de energia de redução. De acordo com algumas modalidades, uma partícula de transferência de energia de redução compreende um ponto quântico que pode absorger radiação de curto comprimento de onda (energia mais alta) e emitir uma ou mais radiações mais longas de comprimento de onda (energia inferior). Uma curva de absorção exemplar 4-952 é representada no gráfico como uma linha tracejada para um ponto quântico tendo um raio entre 6 a 7 nm. O ponto quântico pode emitir uma primeira banda de radiação ilustrada pela curva 4-954, uma segunda banda de radiação ilustrada pela curva 4-956 e uma terceira banda de radiação ilustrada pela curva 4-958.
[00364] Em algumas implementações uma partícula de transferência de energia pode converter energia de uma fonte de excitação. A figura 4-9F descreve espectros associados com a duplicação de uma partícula de transferência de energia. De acordo com algumas modalidades, um ponto quântico pode ser excitado com radiação a aproximadamente 980 nm e então reemitir em uma das três bandas espectrais conforme ilustrado no gráfico. Uma primeira banda pode ser centralizada a aproximadamente 483 nm, uma segunda banda pode ser centralizada a aproximadamente 538 nm e uma terceira banda pode ser centralizada a aproximadamente 642 nm. Os fótons reemitidos do ponto quântico são mais energéticos do que os fótons da radiação usada para excitar o ponto quântico. Certamente, a energia da fonte de excitação é convertida. Uma ou mais das bandas espectrais emitidas podem ser usadas para excitar uma ou mais amostras dentro do poço de amostra. E. Direcionamento da Energia de Emissão em Direção ao Sensor
[00365] O chip de análise 2-110 pode incluir um ou mais componentes por pixel para melhorar a coleta de energia de emissão pelos sensores no instrumento. Tais componentes podem ser desenhados para espacialmente direcionar a energia de emissão em direção aos sensores e aumentar a direcionalidade da energia de emissão do poço de amostra 2-211. A superfície óptica e a óptica de campo distante pode ser usada para direcionar a energia de emissão em direção ao sensor. 1. Superfície Óptica
[00366] Componentes dentro de um pixel do chip de análise 2-110 localizados próximos ao poço de amostra do pixel podem ser configurados para acoplar com a energia de emissão emitida por uma amostra. Tais componentes podem ser formados na interface entre duas camadas do chip de análise. Por exemplo, alguns elementos de acoplamento de energia de emissão podem ser realizados na interface entre uma camada do poço de amostra e a camada adjacente à camada do poço de amostra oposta onde os poços de amostra são formados. Em alguns casos, a camada sob a camada do poço de amostra é uma camada dielétrica e os elementos de acoplamento de energia de emissão podem suportar plásmons da superfície. Em outras modalidades, a camada do poço de amostra pode ser um material condutor adjacente a um material opticamente transparente. Os elementos de acoplamento de energia da superfície podem ser estruturas ópticas da superfície que são excitadas e interagem com a emissão radiativa do poço de amostra.
[00367] Uma dimensão característica de uma estrutura óptica da superfície como um período de concessão, tamanho do recurso ou distância do poço de amostra pode ser selecionado para acoplar ao máximo um componente paralelo de um vetor de impulso da energia de emissão em um vetor de impulso da onda da superfície para um plásmon da superfície. Por exemplo, o componente paralelo do vetor de impulso da energia de emissão pode ser combinado com o vetor de impulso da onda da superfície para um plásmon da superfície suportada pela estrutura, de acordo com algumas modalidades. Em algumas modalidades, uma distância d do poço de amostra a uma borda ou recurso característico de uma estrutura óptica da superfície pode ser selecionada para direcionar a energia de emissão do poço de amostra em uma direção selecionada, como normal à superfície ou inclinada em um ângulo θ de normal à superfície. Por exemplo, a distância, d, pode ser um número integral de comprimentos de onda de plásmon da superfície para direcionar a emissão normal à superfície. Em algumas modalidades, a distância, d, pode ser selecionada para ser um comprimento de onda do plásmon da superfície fracional, ou módulo do comprimento de onda desse.
[00368] De acordo com algumas modalidades, as estruturas ópticas da superfície podem direcionar a energia radiativa de emissão de um poço de amostra em uma direção normal à camada do poço de amostra. A energia acoplada pode ser direcionada na direção normal em um padrão de radiação direcional estreito.
[00369] Um exemplo de uma estrutura óptica da superfície é uma rede concêntrica. Uma estrutura da rede concêntrica que pode ser formada em um pixel do chip de análise para direcionar a energia de emissão em direção a um ou mais sensores do pixel. A estrutura da rede concêntrica pode ser formada ao redor de um poço de amostra. Um exemplo de uma superfície da rede circular concêntrica 5-102 como uma estrutura de plásmon da superfície é representada na figura 5-1. A rede circular pode compreender qualquer número adequado de anéis e o número de anéis (6) mostrado na figura 10-1 é um exemplo não limitador. A rede circular pode compreender anéis projetantes de uma superfície de uma camada condutora. Por exemplo, a rede circular pode ser formada na interface da camada do poço de amostra e uma camada dielétrica formada abaixo d acamada do poço de amostra. A camada do poço de amostra pode ser um material condutor e a rede concêntrica pode ser formada por moldagem da estrutura da rede na interface entre o material condutor e a dielétrica. Os anéis da rede circular podem estar em um espaçamento periódico regular ou podem ter espaçamentos irregulares ou aperiódicos entre os anéis. O poço de amostra pode ser localizado no ou próximo ao centro da rede circular. Em algumas modalidades, o poço de amostra pode ser localizado fora do centro à rede circular e pode ser posicionado a certa distância do centro da rede. Em algumas modalidades, um componente de acoplamento de energia da superfície do tipo rede pode compreender uma rede espiral. Um exemplo de uma rede espiral 5-202 é representado na figura 5-2. A rede espiral 5-202 pode compreender uma abertura espiral em um filme condutor. Qualquer dimensão adequada da rede espiral pode ser usada para formar a rede espiral.
[00370] A figura 5-3 ilustra um padrão de radiação 5-302 para energia de emissão do poço de amostra 2-211. A estrutura da rede concêntrica 2-223 faz com que a energia de emissão tenha maior direcionalidade comparado ao padrão de radiação formado na ausência da estrutura da rede 2-223. Em algumas modalidades, a energia de emissão é direcionada para baixo, normal à camada metálica 2-221.
[00371] Outro exemplo de uma óptica da superfície ou estrutura de plásmon da superfície é uma estrutura da nanoantena. Uma estrutura de nanoantena pode ser desenhada para espacialmente direcionar a energia de emissão do poço de amostra. Em algumas modalidades, a localização do poço de amostra com relação à estrutura de nanoantena é selecionada para direcionar a energia de emissão do poço de amostra em uma direção particular em direção a um ou mais sensores. Nanoantenas podem compreender estruturas de antena dipolo de nanoescala que são desenhadas para produzir um padrão de radiação direcional quando excitada pela energia de emissão. As nanoantenas podem ser distribuídas ao redor de um poço de amostra. O padrão de radiação direcional pode resultar de uma compactação dos campos eletromagnéticos das antenas. Em algumas modalidades, o padrão de radiação direcional pode resultar de uma compactação dos campos eletromagnéticos das antenas com o campo emitido diretamente da amostra. Em algumas implementações, o campo emitido diretamente da amostra pode ser mediado por um plásmon da superfície entre o poço de amostra e a estrutura de nanoantena.
[00372] As dimensões das nanoantenas individuais que formam a estrutura de nanoantena podem ser selecionadas para a capacidade combinada de toda a estrutura de nanoantena para produzir padrões específicos de distribuição. Por exemplo, os diâmetros das nanoantenas individuais podem variar dentro de uma estrutura de nanoantena. Entretanto, em alguns casos, os diâmetros podem ser os mesmos que dentro de um conjunto de nanoantenas. Em outras implementações, alguns diâmetros selecionados podem ser usados por toda a estrutura de nanoantena. Algumas nanoantenas podem ser distribuídas em um círculo de raio R e algumas podem ser deslocadas em uma direção radial do círculo. Algumas nanoantenas podem ser igualmente espaçadas ao redor de um círculo de raio R (por exemplo, centralizadas em incrementos de ângulo polar equivalentes) e algumas podem ser deslocadas em igual espaçamento ao redor do círculo. Em algumas modalidades, as nanoantenas podem estar dispostas em uma configuração espiral ao redor de um poço de amostra. Adicionalmente ou alternativamente, outras configurações de nanoantenas são possíveis, como uma matriz ao redor do poço de amostra, uma distribuição cruzada e distribuições em estrela. Nanoantenas individuais podem ser formadas em outra forma diferente de um círculo, como quadradas, retangulares, cruzadas, triangulares, gravata-borboleta, em anel, pentágono, hexágono, polígonos, etc. Em algumas modalidades, a circunferência de uma abertura ou disco pode ser aproximadamente um número inteiro mútilplo de um comprimento de onda fracional, por exemplo, (N/2)À.
[00373] Uma matriz da nanoantena pode direcionar a energia de emissão de uma amostra em lóbulos de radiação concentrada. Quando uma amostra emite energia, ela pode excitar os plásmons da superfície que propagam do poço de amostra às nanoantenas distribuídas ao redor do poço de amostra. Os plásmons da superfície podem então excitar os modos de radiação ou emissores dipolo nas nanoantenas que emitem radiação perpendicular à superfície da camada do poço de amostra. A fase de um modo excitado dipolo em uma nanoantena dependerá da distância da nanoantena do poço de amostra. Selecionar a distância entre o poço de amostra e uma nanoantena individual controla a fase de radiação emitida da nanoantena. O modo de radiação espacial excitado em uma nanoantena dependerá da geometria e/ou tamanho da nanoantena. Selecionar o tamanho e/ou a geometria de uma nanoantena individual controla o modo de radiação espacial emitido da nanoantena. As contribuições de todas as nanoantenas na matriz e, em alguns casos, o poço de amostra, pode determinar um lóbulo de radiação geral ou lóbulos que formam o padrão de radiação. Como pode ser observado, a fase e o modo de radiação espacial emitida de uma nanoantena individual pode depender do comprimento de onda, de modo que todo o lóbulo ou lóbulos de radiação que formam o padrão de radiação ainda serão dependentes do comprimento de onda. As simulações numéricas dos campos eletromagnéticos podem ser empregadas para determinar todos os padrões do lóbulo de radiação para energias de emissão de diferentes comprimentos de onda característicos.
[00374] A nanoantena pode compreender uma matriz de furos ou aberturas em um filme condutor. Por exemplo, a estrutura de nanoantena pode ser formada na interface entre uma camada condutora do poço de amostra e uma camada dielétrica subjacente. Os furos podem compreender conjuntos de furos distribuídos em círculos concêntricos ao redor de um ponto central. Em algumas modalidades, um poço de amostra é localizado no ponto central da matriz, enquanto em outras modalidades o poço de amostra pode ser fora do centro. Cada conjunto de furos distribuído circularmente pode compreender uma coleta de diferentes diâmetros dispostos do menor ao maior ao redor da distribuição circular. Os diâmetros do furo podem ser diferentes entre os conjuntos (por exemplo, um furo menor em um conjunto pode ser maior do que um furo menor em outro conjunto) e a localização do furo menor pode ser orientado em um diferente ângulo polar para cada conjunto de círculos. Em algumas modalidades, pode haver de um a sete conjuntos de furos circularmente distribuídos em uma nanoantena. Em outras modalidades, pode haver mais do que sete conjuntos. Em algumas modalidades, os furos podem não ser circulares, mas podem ser qualquer formato adequado. Por exemplo, os furos podem ser elipses, triângulos, retângulos, etc. Em outras modalidades, a distribuição de furos pode não ser circular, mas pode criar um formato espiral.
[00375] As figuras 5-4A e 5-4B ilustram uma estrutura de nanoantena exemplar compreendida por furos ou aberturas em uma camada condutora. A figura 5-4A mostra uma vista plana superior da superfície de um chip de análise com um poço de amostra 5-108 envolvido por furos 5-122. Os furos da nanoantena são distribuídos com seus centros sobre ao redor de um círculo de raio R. Nesse exemplo não limitativo, os diâmetros do furo variam aumentando ao redor da circunferência do círculo de furos. A figura 5-4B mostra um esquema de uma vista transversal do chip de análise mostrado na figura 5-4A ao longo da linha B-B’. A camada do poço de amostra 5-116 que inclui poço de amostra 5-108 e aberturas 5-122 que são partes da estrutura de nanoantena. Camada 5-118 do chip de análise fica abaixo da camada do poço de amostra 5-116. A camada 5-118 pode ser um material dielétrico e/ou um material opticamente transparente.
[00376] Em algumas modalidades, a estrutura de nanoantena pode compreender uma pluralidade de discos. Os discos da estrutura de nanoantena podem ser formados como discos condutores que projetam de uma superfície de um material condutor. O material condutor pode ser adjacente a um material opticamente transparente. Em algumas modalidades, as nanoantenas podem ser distribuídas ao redor de um poço de amostra. Em alguns casos, as nanoantenas podem ser distribuídas aproximadamente ao redor de um poço de amostra em um círculo de raio R. Uma matriz da nanoantena pode compreender múltiplos conjuntos de nanoantenas distribuídos aproximadamente em círculos adicionais de diferentes rádios ao redor de um poço de amostra.
[00377] As figuras 5-5A e 5-5B ilustram uma modalidade exemplar de uma estrutura de nanoantena compreendendo discos que projetam de uma camada condutora. A figura 5-5A mostra um esquema de vista plana superior da superfície de um chip de análise com um poço de amostra 5-208 envolvido por discos 5-224. Os discos da nanoantena são distribuídos aproximadamente ao redor de um círculo de raio R. Nesse exemplo não limitativo, dois diâmetros são usados para os discos e os discos alternam entre esses dois diâmetros ao redor da circunferência do círculo de nanoantena. A figura 5-5B mostra um esquema de uma vista transversal do chip de análise mostrado na figura 5-5A ao longo da linha C-C’. A camada do poço de amostra 5-216 que inclui poço de amostra 5-208 e discos 5-224 que são partes da estrutura de nanoantena. Os discos 5-224 projetam da camada do poço de amostra 5-216 por uma certa distância. Em algumas modalidades, a distância que os discos estendem-se da camada do poço de amostra pode variar dentro de uma estrutura de nanoantena. A camada 5-218 do chip de análise fica abaixo da camada do poço de amostra 5-216. A camada 5-18 pode ser um material dielétrico e/ou um material opticamente transparente. A camada do poço de amostra 5-216 e os discos projetantes podem ser um material condutor.
[00378] 2.Óptica de Campo Distante
[00379] Em algumas modalidades, a camada diretamente abaixo da superfície óptica pode ser uma camada espaçadora 2-225 de qualquer espessura adequada e ser feita de qualquer material adequado dielétrico. A camada espaçadora pode ser, por exemplo, 10 μm na espessura e pode ser feita de dióxido de silicone. De modo alternativo, essa camada espaçadora pode ser 48 μm ou 50 μm. Abaido da camada espaçadora pode estar uma ou mais camadas de lente com camadas espaçadoras adicionais. Por exemplo, a figura 5-6A ilustra uma camada de lente superior 5-601 que pode incluir pelo menos uma lente refrativa. Em algumas modalidades, a camada de lente superior pode ser localizada 5 μm abaixo da camada do poço de amostra 2-221. Pode haver uma ou mais lentes associadas com cada poço de amostra. Em algumas modalidades, uma matriz da lente pode ser usada. Em algumas modalidades, cada lente da camada de lente superior 5-601 é centralizada abaixo do poço de amostra 2-211 e pode ter um raio, por exemplo, menor do que 10,5 μm. A camada de lente superior pode ser feita de qualquer material adequado dielétrico como, em forma de exemplo e não limitação, nitrito de silicone.
[00380] A camada diretamente abaixo da camada de lente superior pode ser uma camada estrutural e/ou óptica 5-605 feita de qualquer dielétrica adequada. Essa camada estrutural e/ou óptica 5-605 pode ser feita de dióxido de silicone na forma de sílica fundida. A camada diretamente abaixo da camada estrutural pode ser uma camada de lente inferior 5-603 que pode incluir pelo menos uma lente adicional. Em algumas modalidades, cada lente na camada de lente inferior 5-603 pode ainda ser centralizada abaixo do poço de amostra. A camada de lente inferior 5-603 pode ser feita de qualquer material adequado dielétrico como, em forma de exemplo e não limitação, nitrito de silicone. A distância do topo da camada de lente superior à base da camada de lente inferior pode ser 100-500 μm. A camada diretamente abaixo da camada de lente inferior pode incluir uma camada antirreflexo que passa a energia de excitação e a energia de emissão e reduz a quantidade de luz refletida. A camada diretamente abaixo da camada antirreflexo pode incluir componentes estruturais para permitir que o chip se alinhe com e monte sobre o instrumento. A camada diretamente abaixo da camada de montagem do chip pode incluir uma cobertura protetora para proteger o sistema de danos e contaminação, incluindo poeira.
[00381] Enquanto a figura 5-6A ilustra duas camadas da lente usando lentes refrativas, qualquer lente adequada pode ser usada. Por exemplo, lentes Fresnel, microlentes, pares de lente refrativa e/ou lentes planas podem ser usadas. A figura 5-6B ilustra uma modalidade usando lentes Fresnel em uma camada de lente superior 5-611 e uma camada de lente inferior 5-613, separadas por uma camada estrutural e/ou óptica 5-605.
[00382] Em algumas modalidades, qualquer uma das interfaces entre as camadas descritas acima no chip pode incluir um revestimento antirreflexo ou camada antirreflexo. Ambas a camada de lente superior e a segunda camada de lente podem estar dispostas abaixo do poço de amostra para focar a luminescência emitida da matriz de poços de amostra em uma lente do relé do instrumento. IV. Componentes do Instrumento I. Camada de Microscopia do Instrumento
[00383] Em algumas modalidades, o instrumento pode incluir uma camada de microscopia que pode incluir subcamadas conforme ilustrado na figura 6-1. Em particular, a camada de microscopia pode incluir uma sub-camada que inclui um espelho policrônico 2-230 inclinado em um ângulo θ para direcionar a energia de excitação em direção ao chip de análise. Esse espelho policrônico pode ser substancialmente dielétrico e refletir a energia de excitação enquanto transmite substancialmente a energia de emissão da amostra em um ou mais dos poços de amostra no chip de análise. Opcionalmente, um elemento de compensação de astigmatismo 6-101 que inclui uma camada dielétrica adicional pode ser fornecido abaixo do espelho policrônico e inclinado no mesmo ângulo θ, mas aproximadamente um eixo que é ortogonal à inclinação do espelho policrônico, para fornecer compensação para astigmatismo no espelho policrônico. Na figura 6-1, o elemento de compensação de astigmatismo 6-101 é ilustrado como inclinado no mesmo plano que o filtro superior, mas deve-se observar que a ilustração representa uma inclinação com relação ao filtro superior e não significa limitar a orientação do elemento de compensação de astigmatismo 6-101 em qualquer forma. Esse elemento de compensação de astigmatismo 6-101 pode ainda fornecer filtragem adicional. Por exemplo, o elemento de compensação de astigmatismo 6-101 pode ser outro espelho policrônico que ainda filtras a energia de excitação enquanto transmite a energia de emissão. Uma lente 6-103 pode ser fornecida abaixo do elemento de compensação de astigmatismo 6-101 para ajudar mais a processar a energia de emissão dos poços de amostra. A lente 6-103 pode ser, por exemplo, 25,4 μm em diâmetro, mas qualquer diâmetro adequado pode ser usado. Em algumas modalidades, a lente é uma lente do relé compreendendo uma pluralidade de elementos de lente. Por exemplo, a lente do relé pode incluir seis elementos de lente separados. Em algumas modalidades, a lente do relé pode ser, aproximadamente 17,5 mm no comprimento. Elementos filtrantes adicionais podem ser usados antes ou após a lente 6-103 para ainda rejeitar a energia de excitação para impedir de atingir os sensores. A. Chip do Sensor
[00384] A energia de emissão emitida a partir de uma amostra no poço de amostra pode ser transmitida para o sensor de um pixel em uma variedade de formas, alguns exemplos dos quais são descritos em detalhes abaixo. Algumas modalidades podem utilizar componentes ópticos e/ou plasmônicos para aumentar a probabilidade da luz de um comprimento de onda específico ser direcionada para uma área ou parte do sensor que é dedicado para detectar luz daquele comprimento de onda específico. O sensor pode incluir múltiplos subssensores para simultaneamente detectar a energia de emissão de diferentes comprimentos de onda.
[00385] A figura 6-2A é um diagrama esquemático de um único pixel do chip do sensor de acordo com algumas modalidades onde pelo menos um elemento de classificação 6-127 é utilizado para direcionar a energia de emissão de um comprimento de onda específico para um respectivo subssensor 6-111 a 6-114. A energia de emissão 2-253 viaja de um poço de amostra através do chip de análise e do sistema óptico do instrumento até alcançar um elemento de classificação 6-127 do chip do sensor. O elemento de classificação 6-127 acopla o comprimento de onda da energia de emissão 2-253 a um grau de liberdade espacial, separando assim a energia de emissão em seus componentes de comprimento de onda constituintes, referidos como energia de emissão classificada. A figura 6-2A ilustra esquematicamente a energia de emissão 2-253 sendo dividida em quatro caminhos de energia de emissão classificados através de um material dielétrico 6-129, cada um associado com um subssensor 6-111 a 6-114 do pixel. Dessa forma, cada subssensor é associado com uma parte diferente do espectro, formando um espectrômetro para cada pixel do chip do sensor.
[00386] Qualquer elemento de classificação adequado 6-127 pode ser utilizado para separar os diferentes comprimentos de onda da energia de emissão. As modalidades podem utilizar elementos ópticos ou plasmônicos. Exemplos de elementos de classificação ópticos incluem, mas não estão limitados a, redes holográficas, redes de máscara de fase, redes de máscara de amplitude e lentes Fresnel de compensação. Exemplos de elementos de classificação plasmônicos incluem, mas não estão limitados a matrizes de nanoantena faseadas e plasmônicos quase-cristais.
[00387] A figura 6-2B é um diagrama esquemático de um único pixel do chip do sensor, de acordo com algumas modalidades, onde os elementos de filtração 6-121 a 6-124 são utilizados para direcionar a energia de emissão de um comprimento de onda específico para um respectivo subssensor e prevenir que a energia de emissão de outros comprimentos de onda alcance os outros subssensores. A energia de emissão 2-253 viaja de um poço de amostra através do chip de análise e do sistema óptico do instrumento até alcançar um dos elementos de filtração 6-121 a 6-124. Os elementos de filtração 6-121 a 6-124, cada um associado a um subssensor específico 6-11 a 6-114, são configurados para transmitir a energia de emissão de um respectivo comprimento de onda e rejeitar a energia de emissão de outros comprimentos de onda absorvendo a energia de emissão (não ilustrada na figura 6-1B) e/ou refletindo a energia de emissão. Após passar através de um respectivo elemento de filtração, a energia de emissão filtrada viaja através de um material dielétrico 6-129 e colide com um subssensor correspondente 6-111 a 6-114 do pixel. Dessa forma, cada subssensor é associado a uma parte diferente do espectro, formando um espectrômetro para cada pixel do chip do sensor.
[00388] Quaisquer elementos de filtração adequados podem ser utilizados para separar os diferentes comprimentos de onda da energia de emissão. As modalidades podem utilizar elementos de filtração ópticos ou plasmônicos. Exemplos de elementos de classificação ópticos incluem, mas não estão limitados a, filtros dielétricos ou filtros de absorção de multicamadas refletoras. Exemplos de elementos de classificação plasmônicos incluem, mas não estão limitados a, superfícies seletoras de frequência projetadas para transmitir energia em um comprimento de onda específico e cristais de banda larga fantônica.
[00389] Alternativamente, ou além dos elementos de classificação e dos elementos de filtração mencionados acima, elementos de filtração adicionais podem ser colocados adjacentes a cada subssensor 6-11 a 6-114. Os elementos de filtração adicionais podem incluir um filme um filme com perdas fino configurado para criar interferência construtiva para a energia de emissão de um comprimento de onda específico. O filme com perdas fino pode ser um filme único ou multicamadas. O filme com perdas fino pode ser feito a partir de qualquer material adequado. Por exemplo, o filme com perdas fino pode ser feito a partir de um material onde o índice de refração n que é aproximadamente da mesma ordem de magnitude que o coeficiente de extinção k. Em outras modalidades, o filme com perdas fino pode ser feito a partir de um material onde o índice de refração n está dentro de aproximadamente duas diferenças de ordens de magnitude do valor do coeficiente de extinção k do material. Exemplos não limitativos de tais materiais em comprimentos de onda visíveis são germânio e silicone.
[00390] O filme com perdas fino pode ser de qualquer espessura adequada. Em algumas modalidades, o filme com perdas fino pode ser 1-45 nm de espessura. Em outras modalidades, o filme com perdas fino pode ser 15-45 nm de espessura. Ainda em outras modalidades, o filme com perdas fino pode ser 1-20 nm de espessura. A figura 6-3A ilustra uma modalidade onde os filmes com perdas finos 6-211 a 6-214 tem uma espessura diferente determinada pelo menos em partes pelo comprimento de onda que é associado a cada subssensor 6-11 a 6-114. A espessura do filme determina, pelo menos em partes, um comprimento de onda distinto que passará seletivamente do filme com perdas fino ao subssensor. Como ilustrado na figura 6-211, o filme com perdas fino 6-211 tem uma espessura d1, o filme com perdas fino 6-212 tem uma espessura d2, o filme com perdas fino 6-213 tem uma espessura d3, e o filme com perdas fino 6-214 tem uma espessura d4. A espessura de cada filme com perdas fino subsequente é menor que o filme com perdas fino anterior de modo que d1 > d2 > d3 > d4.
[00391] Adicionalmente, ou alternativamente, os filmes com perdas finos podem ser formados de um material diferente com propriedades diferentes de modo que a energia de emissão de diferentes comprimentos de onda interfira construtivamente em cada respectivo subssensor. Por exemplo, o índice de refração n e/ou o coeficiente de extinção k pode ser selecionado para otimizar a transmissão da energia de emissão de um comprimento de onda específico. A figura 6-3B ilustra os filmes com perdas finos 6-221 a 6-224 com a mesma espessura, mas cada filme com perdas fino é formado a partir de um material diferente. Em algumas modalidades, ambos os materiais dos filmes com perdas finos e a espessura dos filmes com perdas finos podem ser selecionados de modo que a energia de emissão de um comprimento de onda desejado interfira construtivamente e seja transmitido através do filme.
[00392] A figura 6-1 ilustra uma modalidade onde uma combinação de elementos difrativos e lente é utilizada para classificar a energia de emissão pelo comprimento de onda. Uma primeira camada 6-105 do chip do sensor pode incluir uma rede de fase de difração. A rede de difração pode ser marcada, por exemplo, em um ângulo Φ substancialmente igual a 40 graus e o espaçamento de linha da rede de difração (A) pode ser substancialmente igual a 1.25 μm. Um técnico no assunto observaria que diferentes ângulos e periodicidades marcados podem ser utilizados para alcançar a separação de luz de diferentes comprimentos de onda de energia de emissão. Além disso, qualquer elemento óptico difrativo adequado pode ser utilizado para separar os diferentes comprimentos de onda da energia de emissão. Por exemplo, uma máscara de fase, uma máscara de amplitude, uma rede de difração ou uma lente Fresnel de compensação pode ser utilizada.
[00393] Uma segunda camada 6-106 do chip do sensor 2-260 pode incluir uma ou mais lentes Fresnel dispostas abaixo da primeira camada 6-105 para classificar e direcionar a energia de emissão para os sensores 6-107. Além disso, qualquer elemento de lente adequado pode ser utilizado para ainda separar os diferentes comprimentos de onda da energia de emissão. Por exemplo, a lente refrativa pode ser utilizada através de uma lente Fresnel lente.
[00394] Os vários componentes da figura 6-1 podem ser espaçados em quaisquer distâncias adequadas. Por exemplo, a superfície dos sensores pode ser localizada em uma distância de 5 μm abaixo da camada da lente Fresnel 6-106; a distância do centro da lente 6-103 da camada de microscopia para a camada da lente Fresnel 6-106 pode ser de 50,6 mm; a rede de fase de difração 6-105 pode ser localizada em uma distância de aproximadamente 100 μm acima da superfície do sensores. Alternativamente, a distância da parte inferior do chip de análise até a parte superior da rede 6-105 pode ser de aproximadamente 53 mm. A largura da camada do sensor pode ser de aproximadamente 10 mm.
[00395] As várias camadas do chip do instrumento de análise não precisam estar na ordem descrita acima. Em algumas modalidades, os elementos de foco e/ou de classificação e a óptica de imagem do instrumento podem estar em ordem inversa. Por exemplo, a rede de fase de difração 6-105 pode ser colocada após a camada da lente Fresnel 6-106. Alternativamente, os elementos de foco e/ou de classificação e a óptica de imagem podem ser incorporados a um único elemento óptico difrativo (DOE). Além disso, vários componentes do chip e do instrumento de análise podem ser entremeados de modo que, por exemplo, a óptica de imagem possa ocorrer acima e abaixo dos elementos de foco e/ou de classificação.
[00396] Quaisquer das interfaces entre as camadas, incluindo a interface entre ar e uma camada do sistema, descritas acima no sistema podem incluir um revestimento antirreflexo. B. Modalidade do Bloco Óptico do Instrumento
[00397] Em algumas modalidades, o bloco óptico do instrumento 1120 pode incluir alguns ou todos os componentes ópticos descritos acima. O bloco óptico pode fornecer os componentes ópticos como dispostos na figura 6-4. Além disso, para os componentes descritos acima, o bloco óptico pode incluir um primeiro conector de fibra 6-401 onde uma primeira fibra óptica carregando um primeiro comprimento de onda de energia de excitação pode conectar e um segundo conector de fibra 6-402 onde uma segunda fibra óptica carregando um segundo comprimento de onda de energia de excitação pode conectar. Como exemplo e não como limitação, o primeiro comprimento de onda de excitação da energia de excitação pode ser de 630-640nm. Os conectores de fibra óptica podem ser quaisquer conectores convencionais adequados, como um conector FC ou um LC. Se dois diferentes comprimentos de onda forem inseridos, os comprimentos de onda podem ser combinados com um combinador de comprimento de onda 6-403, como um espelho dicroico ou policroico. O segundo comprimento de onda de excitação pode ser de 515-535 nm. A energia de excitação de entrada pode ser de qualquer polarização adequada, como a polarização linear. Em algumas modalidades, a fibra carregando a energia de excitação pode ser uma fibra de preservação de polarização. Opcionalmente, os filtros e polarizadores de excitação, como acopladores de fibra óptica para espaço livre, podem ser utilizados após a inserção de fibra óptica para ainda filtrar ou modificar características da energia de excitação.
[00398] O bloco óptico pode incluir um ou mais alojamentos de metal para manter as lentes e outros componentes ópticos para processamento óptico, como modelagem de feixe. A figura 6-4 ilustra quatro alojamentos de metal 6-405 a 6-408, cada um mantendo uma lente e/ou outros componentes ópticos. Pode haver qualquer número de lentes utilizado para colimar e focar a energia de excitação. Um ou mais espelhos 6-411 e 6-412 são adequados entre alguns dos alojamentos de metal para guiar a energia de excitação em direção ao chip de análise 2-110. Na figura 6-4, o primeiro espelho 6-411direciona a energia de excitação do segundo alojamento 6-406 ao terceiro alojamento 6-407 e o segundo espelho 6-412 reflete a energia de excitação do quarto alojamento 6-408 a um espelho dielétrico policroico 2-230. O espelho dielétrico policroico 2-230 direciona a energia de excitação em direção a um filtro de compensação de astigmatismo 6-601.
[00399] Em algumas modalidades, a luz circularmente polarizada pode ser direcionada ao poço de amostra para fazer com que os marcadores luminescentes emitam luminescência com comprimento similar. Uma placa de um quarto de onda pode ser utilizada para transferir a luz linearmente polarizada para luz circularmente polarizada antes de alcançar o chip de análise. O espelho dielétrico policroico 2230 direciona a energia de excitação para a placa de um quarto de onda 6-415. Como ilustrado na figura 6-4, a placa de um quarto de onda 6415 pode ser disposta entre o filtro de compensação de astigmatismo 6101 e o chip de análise 2-110. A energia de excitação circularmente polarizada é então direcionada à pluralidade de pixels no chip de análise. A energia de excitação que não é direcionada aos pixels pode ser absorvida por um componente de amortecimento de feixe 6-417. A energia de excitação que alcança a amostra dentro de um ou mais poços de amostra fará com que a amostra emita a energia de emissão, que é direcionada ao sensor 2-260. A energia de emissão pode passar através dos componentes ópticos como óptica de polarização, o elemento de compensação de astigmatismo 6-101, o espelho policroico 2-230 e a lente do relé 6-103. O espelho policroico age como um filtro, que pode ser, como exemplo, um filtro de entalhe, um filtro de pico ou um filtro de corte. A lente do relé 6-103 pode espelhar a energia de emissão em direção ao sensor. Uma parte da energia de emissão pode então passar através de um ou mais filtros de emissão 6-421 e 6-422 situados acima do sensor 2-260, que pode ainda filtrar a energia de emissão. Em algumas modalidades, os filtros de emissão podem ser inclinados em um ângulo em relação à direção de propagação de energia de emissão incidente para ajustar as características de transmissão dos filtros e/ou reduzir a interferência causada pelos reflexos. Se o filtro superior 6-421 for inclinado em um ângulo θ, o filtro inferior 6-422 pode ser inclinado no mesmo ângulo θ, mas sobre um eixo que é ortogonal àquele da inclinação do filtro superior, para garantir que nenhum astigmatismo seja introduzido ao caminho do feixe de radiação de emissão. C. Sensores
[00400] A presente revelação fornece várias modalidades de sensores, operação de sensor e métodos de processamento de sinal. De acordo com algumas modalidades, um sensor 2-122 em um pixel do chip do sensor 2-260 pode compreender qualquer sensor adequado capaz de receber a energia de emissão a partir de uma ou mais identificações no poço de amostra e produzindo um ou mais sinais elétricos representantes da energia de emissão recebida. Em algumas modalidades, um sensor pode compreender pelo menos um fotodetector (por exemplo, uma junção p-n formada em um substrato semicondutor). A figura 7-1A e a figura 7-1B retratam uma modalidade de um sensor que pode ser fabricado dentro de um pixel 2-100 de um chip do sensor.
[00401] De acordo com algumas modalidades, um sensor 2-122 pode ser formado em cada pixel 2-100 de um chip do sensor. O sensor pode ser associado a um poço de amostra 2-211 do chip de análise. Pode haver uma ou mais camadas transparentes 7-110 acima do sensor, de modo que a emissão a partir do poço de amostra possa viajar para o sensor sem atenuação significante. O sensor 2-122 pode ser formado em um substrato semicondutor 7-120 em uma base do pixel, de acordo com algumas modalidades, e ser localizado sobre um mesmo lado do poço de amostra como o chip de análise (não mostrado).
[00402] O sensor pode compreender um ou mais segmentos fotodetectores da junção semicondutora. Cada junção semicondutora pode compreender um poço de um primeiro tipo de condutividade. Por exemplo, cada junção semicondutora pode compreender um poço do tipo n formado em um substrato do tipo p, como retratado no desenho. De acordo com algumas modalidades, um sensor 2-122 pode ser disposto como um detector de ângulo de desvio 7-162, como retratado na vista plana da figura 7-1B. Um primeiro fotodetector 7-124 pode estar localizado em um centro do sensor, e um segundo fotodetector anular 7-122 pode rodear o centro do fotodetector. Os contatos elétricos aos poços podem ser feitos através de traços condutores 7-134 formados em um primeiro ou subsequente nível de metalização e através de vias condutoras 7-132. Pode haver uma região de material semicondutor altamente descoberto 7-126 em regiões de contato das vias. Em algumas modalidades, um óxido de campo 7-115 pode ser formado em superfícies entre os fotodetectores e pode cobrir uma parte de cada fotodetector. Em algumas implementações, pode haver diapositivos semicondutores adicionais 7-125 (por exemplo, transistores, amplificadores, e etc.) formados dentro do pixel adjacente ao sensor 2122. Pode haver níveis de metalização adicionais 7-138, 7-136 dentro do pixel.
[00403] Em algumas implementações, os níveis de metalização 7136 podem se estender por uma maioria dos pixel e ter uma abertura centralizada acima do fotodetector 7-124, de modo que a emissão a partir do poço de amostra possa alcançar o sensor. Em alguns casos, um nível de metalização 7-136 pode servir como um potencial de referência ou um plano de superfície e, adicionalmente, serve como um bloco óptico para prevenir pelo menos alguma radiação de fundo (por exemplo, radiação a partir de uma fonte de excitação ou a partir do meio ambiente) de alcançar o sensor 2-260.
[00404] Como retratado na figura 7-1A e na figura 7-1B, um sensor 2-122 pode ser subdividido em uma pluralidade de segmentos fotodetectores 7-122, 7-124 que são espacialmente e eletricamente separados um do outro. Em algumas modalidades, os segmentos de um sensor 2-122 podem compreender regiões do material semicondutor opostamente descoberto. Por exemplo, um primeiro poço de acumulação de carga 7-124 para um primeiro segmento do sensor pode ser formado descobrindo uma primeira região de um substrato para ter um primeiro tipo de condutividade (por exemplo, tipo n) dentro do primeiro poço. O substrato pode ser do tipo p. Um segundo poço de acumulação de carga 7-122 para um segundo segmento do sensor pode ser formado descobrindo uma segunda região do substrato para ter o primeiro tipo de condutividade dentro do segundo poço. O primeiro e o segundo poços podem ser separados por uma região do tipo p do substrato.
[00405] A pluralidade de segmentos do sensor 2-122 pode ser disposta de qualquer forma adequada que não um layout de ângulo de desvio, e pode haver mais de dois segmentos em um sensor. Por exemplo, em algumas modalidades, uma pluralidade de segmentos fotodetectores 7-142 pode ser lateralmente separada entre si para formar um sensor de banda 7-164, como retratado na figura 7-1C. Em algumas modalidades, um sensor de quadra (ou quadrante) 7-166 pode ser formado dispondo os segmentos 7-144 em um padrão de quadra, como mostrado na figura 7-1D. Em algumas implementações, segmentos de arco 7-146 podem ser formados em combinação com o padrão de ângulo de desvio, como retratado na figura 7-1E, para formar um sensor de arcos segmentados 7-168. Outra configuração de sensor pode compreender seções pie-piece, que pode incluir sensores individuais dispostos em seção separada de um círculo. Em alguns casos, os segmentos do sensor podem ser dispostos simetricamente ao redor de um poço de amostra 2-211 ou assimetricamente ao redor de um poço de amostra. A disposição dos segmentos do sensor não é limitada somente às disposições anteriores, e quaisquer distribuições do segmento do sensor adequadas podem ser utilizadas.
[00406] Os inventores descobriram que um sensor quadrante 7-166, sensor pie-sector ou sensor de setor similar pode representar em escala para tamanhos de pixel menores mais favoravelmente que outras configurações de sensor. Os detectores de quadrante de setor podem consumir menos área de pixel para um número de comprimentos de onda detectado e para uma área de sensor ativa.
[00407] Os sensores podem ser dispostos em várias configurações geométricas. Em alguns exemplos, os sensores são dispostos em uma configuração quadrada ou em uma configuração hexagonal.
[00408] Os sensores da presente revelação podem ser independentemente (ou individualmente) endereçáveis. Um individualmente endereçável é capaz de detectar um sinal e fornecer uma saída independente de outros sensores. Um sensor individualmente endereçável pode ser legível individualmente.
[00409] Em algumas modalidades, um sensor empilhado 7-169 pode ser formado fabricando uma pluralidade de segmentos do sensor separados 7-148 em uma pilha vertical, como retratado na figura 7-1F. Por exemplo, os segmentos podem estar localizados um em cima do outro, e pode haver, ou pode não haver, camadas isolantes entre os segmentos empilhados. Cada camada vertical pode ser configurada para absorver a energia de emissão de uma energia específica e passar a emissão em diferentes energias. Por exemplo, um primeiro detector pode absorver e detectar a radiação de comprimento de onda mais curto (por exemplo, radiação de comprimento de onda azul abaixo de aproximadamente 500 nm a partir de uma amostra). O primeiro detector pode passar emissões de comprimento de onda verde e vermelho a partir de uma amostra. Um segundo detector pode absorver e detectar radiação de comprimento de onda verde (por exemplo, entre aproximadamente 500 nm e aproximadamente 600 nm) e passar emissões vermelhas. Um terceiro detector pode absorver e detectar as emissões vermelhas. Os filmes refletores 7-149 podem ser incorporados na pilha, em algumas modalidades, para refletir luz de uma faixa de comprimento de onda selecionado de volta através de um segmento. Por exemplo, um filme pode refletir radiação de comprimento de onda verde que não tenha sido absorvida pelo segundo segmento de volta através do segundo segmento para aumentar sua eficiência de detecção.
[00410] Em algumas modalidades com segmentos do sensor empilhados verticalmente, os componentes de acoplamento de emissão podem não ser incluídos no poço de amostra para produzir padrões de distribuição espaciais distintos da emissão de amostra que são dependentes do comprimento de onda de emissão. O discernimento de emissões espectralmente diferentes pode ser alcançado com um sensor verticalmente empilhado 7-169 analisando a razão de sinais a partir do segmento empilhado, de acordo com algumas modalidades.
[00411] Em algumas modalidades, os segmentos de um sensor 2122 são formados de silicone, embora qualquer semicondutor adequado (por exemplo, Ge, GaAs, SiGe, InP, e etc.) possa ser utilizado. Em algumas modalidades, um segmento do sensor pode compreender um filme fotocondutor orgânico. Em outras modalidades, os fotodetectores de ponto quântico podem ser utilizados para segmentos dos sensores. Os fotodetectores de ponto quântico podem responder a diferentes emissões de energia baseados no tamanho do ponto quântico. Em algumas modalidades, uma pluralidade de pontos quânticos de tamanhos variados pode ser utilizada para discriminar entre diferentes energias de emissões ou comprimentos de onda recebidos a partir do poço de amostra. Por exemplo, um primeiro segmento pode ser formado a partir dos pontos quânticos tendo um primeiro tamanho e um segundo segmento pode ser formado a partir dos pontos quânticos tendo um segundo tamanho. Em várias modalidades, os sensores 2-122 podem ser formados utilizando processos CMOS convencionais CMOS.
[00412] Conforme descrito acima, componentes de acoplamento de emissões podem ser fabricados adjacentes ao poço de amostra em algumas modalidades. Os elementos de classificação 2-243 podem alterar a emissão a partir de uma amostra dentro do poço de amostra 2211 para produzir padrões de distribuição espaciais distintos da emissão de amostra que são dependentes do comprimento de onda de emissão. A figura 7-2A retrata um exemplo de um primeiro padrão de distribuição espacial 7-250 que pode ser produzido a partir de uma primeira amostra em um primeiro comprimento de onda. O primeiro padrão de distribuição espacial 7-250 pode ter um lobo central proeminente direcionado a um segmento central de um sensor de ângulo de desvio 7-162, por exemplo, como mostrado na figura 7-2B. Tal padrão 7-250 pode ser produzido por qualquer elemento difrativo adequado quando a amostra emite em um comprimento de onda de aproximadamente 663 nm. Um padrão projetado 7-252 incidente no sensor pode aparecer como ilustrado na figura 7-2B.
[00413] A figura 7-2C retrata um padrão de distribuição espacial 7260 que pode ser produzido a partir de uma segunda amostra emitindo em um segundo comprimento de onda a partir do mesmo poço de amostra, de acordo com algumas modalidades. O segundo padrão de distribuição espacial 7-260 pode compreender dois lobos de radiação e diferir do primeiro padrão de distribuição espacial 7-250. Um padrão projetado 7-262 do segundo padrão de distribuição espacial 7-260 pode aparecer como retratado na figura 7-2D, de acordo com algumas modalidades. O segundo padrão de distribuição espacial 7-260 pode ser produzido por qualquer elemento difrativo adequado quando a amostra emite em um comprimento de onda de aproximadamente 687 nm.
[00414] Os segmentos de um sensor 2-122 podem ser dispostos para detectar energias de emissão específicas, de acordo com algumas modalidades. Por exemplo, estruturas de acoplamento de emissão adjacentes ao poço de amostra e segmentos de um sensor podem ser projetadas em combinação para aumentar a diferenciação de sinal entre energias de emissão específicas. As energias de emissão podem corresponder às identificações selecionadas que serão utilizadas com o chip do sensor. Como um exemplo, um sensor de ângulo de desvio 7162 poderia ter seus segmentos dimensionados e/ou localizados para combinar melhor com os padrões projetados 7-260, 7-262 a partir de uma amostra, de modo que as regiões de intensidade mais alta cairiam mais centralmente dentro de segmentos do sensor ativo. Alternativa-mente ou adicionalmente, elementos difrativos podem ser projetados para alterar os padrões projetados 7-260, 7-262 de modo que regiões intensas caiam mais centralmente dentro de segmentos do sensor.
[00415] Embora um sensor 2-122 possa compreender dois segmentos, é possível em algumas modalidades discernir mais de duas bandas de emissão espectralmente distintas a partir de uma amostra. Por exemplo, cada banda de emissão pode produzir um padrão projetado distinto nos segmentos do sensor e produzir uma combinação de sinais distintos a partir dos segmentos do sensor. A combinação dos sinais pode ser analizada para discernir e identificar a banda de emissão. As figuras 7-2E a 7-2H representam resultados a partir de simulações numéricas de sinais a partir de um sensor de dois segmentos 2-122 exposto a quatro padrões de emissão distintos. Como pode ser visto, cada combinação de sinais a partir de dois segmentos do sensor é distinta e pode ser utilizada para discriminar emissores nos quatro comprimentos de onda. Para a simulação, visto que o segmento detector externo do sensor de ângulo de desvio 7-162 tem uma área maior, mais sinal foi integrado para aquele detector. Adicionalmente, a luz que colidiu em uma área entre os detectores gerou operadores que podem desviar em direção ao segmento detector e contribuir para sinais a partir de ambos os segmentos.
[00416] Em algumas modalidades, pode haver N segmentos fotodetectores por pixel, onde N pode ser qualquer valor inteiro. Em algumas modalidades, N pode ser maior que ou igual a 1 e menor que ou igual a 10. Em outras modalidades, N pode ser maior que ou igual a 2 e menor que ou igual a 5. O número M de emissões de amostra discernível (por exemplo, comprimentos de onda de emissão distintos a partir de diferentes etiquetas luminescentes) que podem ser detectadas por N detectores pode ser igual a ou maior que N. O discernimento de M emissões de amostra pode ser alcançando avaliando a razão de sinais a partir de cada segmento do sensor, de acordo com algumas modalidades. Em algumas implementações, a razão, soma e/ou amplitudes dos sinais recebidos pode ser medida e analisada para determinar um comprimento de onda de emissão característico a partir do poço de amostra.
[00417] Em algumas modalidades, mais de um emissor pode emitir em diferentes comprimentos de onda característicos em uma dada janela de tempo dentro de um poço de amostra 2-211. Um sensor 2-122 pode simultaneamente detectar sinais a partir de múltiplas emissões em diferentes comprimentos de onda e fornecer o sinal somado para processamento de dados. Em algumas implementações, emissões de múltiplos comprimentos de onda podem ser distinguíveis como outro conjunto de valores de sinal a partir dos segmentos do sensor (por exemplo, valores de sinal diferentes a partir daqueles mostrados na figura 7-2E a 7-2H). Os valores de sinal podem ser analisados para discernir que a emissão de múltiplos comprimentos de onda ocorreu e para identificar uma combinação específica de emissores associados às emissões.
[00418] Os inventores contemplaram e analisaram ainda um sensor de ângulo de desvio tendo quatro segmentos concêntricos. Sinais a partir dos segmentos são traçados na figura 7-2I e na figura 7-2J para as mesmas condições de emissão associadas à figura 7-2G e à figura 7-2H, respectivamente. O sensor de ângulo de desvio de quatro segmentos mostra ainda sinais discerníveis que podem ser analisados para identificar um emissor específico dentro do poço de amostra.
[00419] Quando a filtragem do comprimento de onda é utilizada em cada segmento do sensor, ou a separação espectral é alta, cada segmento de um sensor pode detectar substancialmente somente uma banda de emissão selecionada. Por exemplo, um primeiro comprimento de onda pode ser detectado por um primeiro segmento, um segundo comprimento de onda pode ser detectado por um segundo segmento, e um terceiro comprimento de onda pode ser detectado por um terceiro segmento.
[00420] Referindo-se novamente a figura 7-1A, pode haver um circuito eletrônico adicional 7-125 dentro de um pixel 2-100 que pode ser utilizado para coletar e ler sinais a partir de cada segmento de um sensor 2-122. A figura 7-3A e a figura 7-3D retratam circuitos que podem ser utilizados em combinação com um sensor de multissegmentos, de acordo com algumas modalidades. Como um exemplo, o circuito de coleção de sinal 7-310 pode compreender três transistores para cada segmento do sensor. Uma disposição dos três transistores é retratada na figura 7-3B, de acordo com algumas implementações. Um nível de sinal em um nó de acumulação de carga 7-311 associado a cada segmento pode ser reinicializado por um transistor de reinicialização RST, e um nível de sinal para o segmento (determinado pela quantidade de carga no nó de acúmulo de carga) pode ser lido com um transistor de leitura RD.
[00421] O circuito de pixel pode ainda incluir amplificação e circuito de dupla amostragem correlacionada 7-320, de acordo com algumas modalidades. A amplificação e o circuito de dupla amostragem podem compreender transistores configurados para amplificar o sinal, de acordo com os segmentos do sensor, bem como transistores configurados para reiniciar o nível de tensão no nó de acumulação de carga e para ler, ou "reiniciar", um sinal de fundo no nó quando nenhuma energia de emissão está presente no sensor (por exemplo, antes da aplicação de energia de excitação no poço de amostra) e para ler um sinal de emissão subsequente, por exemplo.
[00422] De acordo com algumas modalidades, a dupla amostragem correlacionada é empregada para reduzir o ruído de fundo subtraindo um nível de sinal de fundo ou de reinicialização a partir do nível de sinal de emissão detectado. O sinal de emissão coletado e o sinal de fundo associado a cada segmento do sensor podem ser lidos nas linhas de coluna 7-330. Em algumas modalidades, um nível de sinal de emissão e o sinal de fundo são de tempo multiplexado em uma linha de coluna comum. Pode haver uma linha de coluna separada para cada segmento do sensor. Os sinais a partir das linhas de coluna podem ser amortecidos e/ou amplificados com o circuito de amplificação 7-340 (que pode ser localizado fora de uma gama de pixels ativos), e fornecidos ainda para processamento e análise. Em algumas modalidades, a subtração dos sinais duplamente amostrados é calculada fora do chio, por exemplo, por um processador de sistema. Em outras modalidades, a subtração pode ser realizada no chip ou em circuitos do instrumento.
[00423] Algumas modalidades de dupla amostragem correlacionada por operar selecionando uma fileira para amostrar, em que os sensores associados à fileira tem cargas de sinal integrada sobre um período de amostragem e contém níveis de sinal. Os níveis de sinal podem ser simultaneamente lidos nas linhas de colunas. Após amostrar os níveis de sinal integrados, todos os pixels na fileira selecionada podem ser reiniciados e imediatamente amostrados. Esse nível de reinicialização pode estar correlacionado ao próximo sinal integrado que começa a acumular após a reinicialização ser liberada e termina integrando um prazo mais tarde quando a mesma fileira é selecionada novamente. Em algumas modalidades, os valores de reinicialização do quadro podem ser armazenados fora do chip de modo que quando os sinais terminaram a integração foram amostrados, os valores de reiniciali- zação correlacionados podem ser subtraídos.
[00424] Em algumas modalidades, um sensor 2-122 com mais de dois segmentos podem exigir circuitos adicionais. A figura 7-3C retrata a correlação de sinal 7-312, a amplificação 7-320 e circuitos de dupla amostragem associados a um sensor de quadra. De acordo com algumas modalidades, sinais a partir de dois ou mais segmentos podem ser de tempo multiplexado em um canal de sinal comum no pixel, como retratado no desenho. Os sinais de tempo multiplexado podem incluir sinais de fundo amostrados para cada segmento para cancelamento de ruído. Adicionalmente, os sinais a partir de dois ou mais segmentos podem ser de tempo multiplexado em uma linha de coluna comum.
[00425] De acordo com algumas modalidades, técnicas de aquisição de sinal temporal podem ser utilizadas para reduzir os níveis de sinal de fundo a partir de uma fonte ou fontes de excitação, e/ou discernir diferentes emissões a partir de diferentes emissores associados a uma amostra. A figura 7-4A retrata a emissão fluorescente e decai de dois emissores diferentes que podem ser utilizados para identificar uma amostra, de acordo com algumas modalidades. Os dois emissores tem características de tempo de extinção consideravelmente diferentes. Uma primeira curva de tempo de extinção 7-410 a partir de um primeiro emissor pode corresponder a uma molécula fluorescente comum, como a rodamina. Uma segunda curva de tempo de extinção 7-420 pode ser característica de um segundo emissor, como um ponto quântico ou um emissor fosforescente. Ambos os emissores exibem uma extinção de emissão traseira que se estende por algum tempo de excitação inicial do emissor. Em algumas modalidades, as técnicas de coleta de sinal aplicadas durante a extinção de emissão traseira podem ser sincronizadas para reduzir um sinal de fundo a partir de uma fonte de excitação, em algumas modalidades, e para distinguir entre os emissores, em algumas modalidades.
[00426] De acordo com algumas implementações, a amostragem de atraso temporal pode ser empregada durante a extinção de emissão traseira para reduzir um sinal de fundo devido à radiação a partir de uma fonte de excitação. A figura 7-4B e a figura 7-4C ilustram uma amostragem de atraso temporal, de acordo com algumas modalidades. A figura 7-4B retrata a evolução temporal de um pulso de excitação 7440 de energia de excitação a partir de uma fonte de excitação, e um subsequente pulso de emissão 7-450 que pode seguir a partir de uma amostra que é excitada dentro do poço de amostra. O pulso de excitação 7-440 pode resultar da condução da fonte de excitação com um sinal de condução 7-442 por um breve período de tempo, como retratado na figura 7-4C. Por exemplo, o sinal de condução pode começar em um primeiro tempo t1 e terminar em um segundo tempo t2. A duração do sinal de condução (t2 - ti) pode estar entre aproximadamente 1 picosegundo e aproximadamente 50 nanosegundos, de acordo com algumas modalidades, embora durações mais curtas possam ser utilizadas em algumas implementações.
[00427] Em um tempo t3 seguindo o término do sinal de condução para a fonte de excitação, um sensor 2-260 (ou segmento do sensor) no pixel pode ser fechado para acumular a carga em um nó de acúmulo de carga 7-311 durante um segundo intervalo de tempo se estendendo de um tempo t3 a um tempo t4. O segundo intervalo de tempo pode estar entre aproximadamente 1 nanosegundo e aproximadamente 50 microsegundos, de acordo com algumas modalidades, embora outras durações possam ser utilizadas em algumas implementações. Como pode ser visto com relação à figura 7-4B, um nó de acúmulo de carga coletará mais cartas de sinal devido à amostra de emissão e então devido à fonte de excitação. Em conformidade, uma razão de sinal para ruído melhorada pode ser obtida.
[00428] Referindo-se novamente à figura 7-4A, devido às diferentes características de emissão temporal dos emissores, sinais correspondentes a um sensor podem ter um pico em momentos diferentes. Em algumas implementações, técnicas de aquisição de sinal aplicadas durante a extinção de emissão traseira podem ser utilizadas para discernir diferentes emissores. Em algumas modalidades, técnicas de detecção temporal podem ser utilizadas juntamente com técnicas espectrais e espaciais (conforme descrito acima juntamente com figura 7-2, por exemplo) para discernir diferentes emissores.
[00429] As figuras 7-4D a 7-4H ilustram como a dupla amostragem em um sensor, ou segmento do sensor, pode ser utilizada para distinguir entre dois emissores tendo diferentes características de emissão temporal. A figura 7-4D retrata curvas de emissão 7-470, 7-475 associadas a um primeiro emissor e a um segundo emissor, respectivamente. Como um exemplo, o primeiro emissor pode ser um fluoróforo comum, como rodamina, e o segundo emissor pode ser um ponto quântico ou emissor fosforescente.
[00430] A figura 7-4E representa níveis de tensão dinâmicos em um nó de acúmulo de carga 7-311 que pode ocorrer em resposta a duas características de emissões diferentes da figura 7-4D. No exemplo, uma primeira curva de tensão 7-472 correspondente ao emissor fluorescente pode mudar mais rapidamente, devido ao período de emissão mais curto, e alcançar seu máximo (ou mínimo, dependendo da polaridade do nó) em um primeiro tempo t1. A segunda curva de tensão 7-477 pode mudar mais devagar devido às características de emissão mais longas do segundo emissor, e alcançar seu máximo (ou mínimo) em um segundo tempo t2.
[00431] Em algumas modalidades, a amostragem do nó de acúmulo de carga pode ser feita em dois tempos t3, t4 após a excitação da amostra, como retratado na figura 7-4F. Por exemplo, um primeiro sinal de leitura 7-481 pode ser aplicado para ler um primeiro valor de tensão a partir do nó de acúmulo de carga em um primeiro tempo t3. Subsequentemente, um segundo sinal de leitura 7-482 pode ser aplicado para ler um segundo valor de tensão a partir do nó de acúmulo de carga em um segundo tempo t4 sem reiniciar o nó de acúmulo de carga entre a primeira leitura e a segunda leitura. Uma análise dos dois valores do sinal amostrado pode então ser utilizada para identificar quais dos dois emissores forneceu os níveis do sinal detectado.
[00432] A figura 7-4G retrata um exemplo de dois sinais a partir da primeira leitura e da segunda leitura que pode ser obtido para o primeiro emissor tendo uma curva de emissão 7-470, como retratado na figura 7-4D. A figura 7-4H retrata um exemplo de dois sinais a partir da primeira leitura e da segunda leitura que pode ser obtido para o segundo emissor tendo uma curva de emissão 7-475, como retratado na figura 7-4D. Por exemplo, a sequência de amostragem mostrada na figura 7-4F para o primeiro emissor amostrará a curva 7-472 e obterá aproximadamente os mesmos valores nos dois momentos de leitura. No caso do segundo emissor, a sequência de amostragem retratada na figura 7-4F amostra dois valores diferentes da curva 7-477 em dois momentos de leitura. Os pares de sinais resultantes a partir dos dois momentos de leitura distinguem entre os dois emissores e podem ser analisados para identificar cada emissor. De acordo com algumas modalidades, a amostragem dupla para subtração de fundo pode ainda ser executada para subtrair um sinal de fundo a partir do primeiro e do segundo sinal de leitura.
[00433] Em operação, os sensores 2-260 de um chip do sensor podem estar sujeitos a um procedimento de calibração de comprimento de onda antes da coleta de dados a partir de um espécime a ser analisado. O procedimento de calibração de comprimento de onda pode incluir sujeitar os sensores a diferentes energias conhecidas tendo comprimentos de onda característicos que podem, ou não, corresponder aos comprimentos de onda fluoróforos que podem ser utilizados como um chip do sensor. As diferentes energias podem ser aplicadas em uma sequência de modo que os sinais de calibração possam ser registrados a partir dos sensores para cada energia. Os sinais de calibração podem então ser armazenados como sinais de referência, que podem ser utilizados para processar a aquisição de dados reais e para determinar qual comprimento de onda ou comprimentos de onda de emissão são detectados pelos sensores. V. Marcadores Luminescentes
[00434] As modalidades podem utilizar quaisquer marcadores luminescentes adequados para rotular amostras (por exemplo, moléculas únicas) no espécime sendo analisado. Em algumas modalidades, fluoróforos comercialmente disponíveis podem ser utilizados. Como exemplo e não como limitação, os seguintes fluoróforos podem ser utilizados: Atto Rho14 ("ATRho14"), Dylight 650 ("D650"), SetaTau 647 ("ST647"), CF 633 ("C633"), CF 647 ("C647"), Alexa fluor 647 ("AF647"), BODIPY 630/650 ("B630"), CF 640R ("C640R") e/ou Atto 647N ("AT647N"). Adicionalmente e/ou opcionalmente, marcadores luminescentes podem ser modificados de qualquer forma adequada para aumentar a velocidade e a precisão do processo de análise de amostra. Por exemplo, um fotoestabilizador pode ser conjugado a um marcador luminescente. Exemplos de fotoestabilizadores incluem, mas não são limitados a, eliminadores de oxigênio ou supressor trigêmeo. Conjugar fotoestabilizadores ao marcador luminescente pode aumentar a taxa de fótons emitidos e pode ainda reduzir um efeito "intermitente" onde o marcador luminescente não emite fótons. Em algumas modalidades, quando um evento biológico ocorre na escala de milissegundos, uma taxa aumentada da emissão de fótons pode aumentar a probabilidade de detecção do evento biológico. Taxas aumentadas de eventos de fótons pode subsequentemente aumentar a razão de sinal para ruído do sinal de luminescência e aumentar a taxa na qual as medições são feitas, levando a uma análise de amostra mais rápida e precisa. Fontes de excitação
[00435] A fonte de excitação 2-250 pode ser qualquer fonte adequada que é disposta para entregar a energia de excitação a pelo menos um poço de amostra 2-111 do chip de análise. Os pixels no chip de análise podem ser pixels de fonte passiva. O termo "pixel de fonte passiva" é utilizado para se referir a um pixel em que a energia de excitação é entregue ao pixel a partir de uma região fora do pixel ou da matriz do pixel do chip de análise, por exemplo, a excitação pode ser no instrumento.
[00436] De acordo com algumas modalidades, uma fonte de excitação pode excitar uma amostra através de um processo radioativo. Por exemplo, uma fonte de excitação pode fornecer radiação visível (por exemplo, radiação tendo um comprimento de onda entre aproximadamente 350 nm e aproximadamente 750 nm), radiação perto do infravermelho (por exemplo, radiação tendo um comprimento de onda entre aproximadamente 0,75 microns e aproximadamente 1,4 microns), e/ou radiação infravermelha de comprimento de onda curto (por exemplo, radiação tendo um comprimento de onda entre aproximadamente 1,4 microns e aproximadamente 3 microns) a pelo menos uma região de excitação 3-215 de pelo menos um poço de amostra do chip de análise. Em algumas modalidades, uma fonte de excitação radioativa pode fornecer energia para excitar um intermediário (por exemplo, a molécula, um ponto quântico ou uma camada do material compreendendo moléculas e/ou pontos quânticos selecionados) que é imediatamente adjacente a uma região de excitação de um poço de amostra. O intermediário pode transferir sua energia para uma amostra através de um processo não radioativo (por exemplo, através de FRET ou DET).
[00437] Em algumas modalidades, uma fonte de excitação pode fornecer mais de uma fonte de energia de excitação. Por exemplo, uma fonte de excitação radioativa pode entregar energias de excitação tendo duas ou mais características espectrais distintas. Como um exemplo, um LED multicolorido pode emitir energias centralizadas em dois ou mais comprimentos de onda e essas energias podem ser entregues a uma região de excitação de um poço de amostra.
[00438] Em uma visão geral e de acordo com algumas modalidades, um instrumento pode incluir pelo menos uma fonte de excitação 2-250 para fornecer energia de excitação a pelo menos uma região de excitação de pelo menos um poço de amostra do chip de análise ou para pelo menos um intermediário que converta ou acople a energia de excitação a pelo menos uma amostra dentro de uma ou mais regiões de excitação. Como retratado na figura 2-3, a energia de excitação de radiação 2-251 a partir de uma fonte de excitação 2-250 pode colidir com uma região ao redor de um poço de amostra 2-211, por exemplo. Em algumas modalidades, pode haver estruturas de acoplamento de excitação 2-223 que ajudam na concentração de energia de excitação incidente dentro de uma região de excitação 2-215 do poço de amostra.
[00439] Uma fonte de excitação pode ser caracterizada por uma ou mais bandas espectrais distintas tendo, cada uma, um comprimento de onda característico. Somente para fins institucionais, um exemplo de emissão espectral a partir de uma fonte de excitação é retratado no gráfico espectral da figura 8-1A. A energia de excitação pode ser substancialmente contida dentro de uma banda de excitação espectral 8-110. Um comprimento de onda máximo 8-120 da banda de excitação espectral pode ser utilizado para caracterizar a energia de excitação. A energia de excitação pode ainda ser caracterizada por uma distribuição espectral, por exemplo, um valor de Largura Total a Meia Intensidade (FWHM) como mostrado no desenho. Uma fonte de excitação produzindo energia, como retratado na figura 8-1A, pode ser caracterizado como entregando energia em um comprimento de onda de aproximadamente 540 nm de radiação e tendo uma largura de banda FWHM de aproximadamente 55 nm.
[00440] A figura 4-1B retrata características espectrais de uma fonte de excitação (ou fontes de excitação) que podem fornecer duas bandas de energia de excitação para um ou mais poços de amostra. De acordo com algumas modalidades, uma primeira banda de excitação 8-112 está em aproximadamente 532 nm e uma segunda banda de excitação 8114 está em aproximadamente 638 nm, como ilustrado no desenho. Em algumas modalidades, uma primeira banda de excitação pode estar em aproximadamente 638 nm e uma segunda banda de excitação pode estar em aproximadamente 650 nm. Em algumas modalidades, uma primeira banda de excitação pode estar em aproximadamente 680 nm e uma segunda banda de excitação pode estar em aproximadamente 690 nm. De acordo com algumas modalidades, os picos das bandas de excitação podem estar dentro de ±5 nm desses valores.
[00441] Em alguns casos, uma fonte de excitação radioativa pode produzir uma banda de excitação ampla, como retratado na figura 8-1A. Uma banda de excitação ampla 8-110 pode ter uma largura de banda maior que aproximadamente 20 nm, de acordo com algumas modalidades. Uma banda de excitação ampla pode ser produzida por um diodo emissor de luz (LED), por exemplo. Em algumas implementações, uma fonte de excitação radioativa pode produzir uma banda de excitação estreita, como retratado na figura 8-1B. Uma banda de excitação estreita pode ser produzida por diodo a laser, por exemplo, ou pode ser produzida filtrando espectralmente uma saída de uma LED.
[00442] Em algumas modalidades, a fonte de excitação pode ser uma fonte de luz. Qualquer fonte de luz adequada pode ser utilizada. Algumas modalidades podem utilizar fontes incoerentes e outras modalidades podem utilizar fontes de luz coerentes. Como exemplo e não como limitação, fontes de luz incoerentes, de acordo com algumas modalidades, podem incluir diferentes tipos diodos emissores de luz (LEDs), como LEDs orgânicos (OLEDs), pontos quânticos (QLEDs), LEDs nanofio e LEDs semicondutores (in)orgânicos. Como exemplo e não como limitação, fontes de luz coerentes, de acordo com algumas modalidades, podem incluir diferentes tipos de lasers, como lasers orgânicos, lasers de pontos quânticos, superfície da cavidade vertical emitindo lasers (VCSELs), bordas emitindo lasers e diodos a laser de reação distribuída (DFB). Adicionalmente ou alternativamente, laser do guia de ondas óptico acoplado à placa (SCOWLs) ou outras estruturas do guia de ondas de modo único assimétrico podem ser utilizados. Adicionalmente ou alternativamente, um laser de estado sólido, como Nd:YAG ou Nd:Glass, diodos ou lanternas pulsados a laser, podem ser utilizados. Adicionalmente ou alternativamente, um laser de fibra pulsado por diodo pode ser utilizado. Em algumas modalidades, a saída de uma fonte de excitação a laser pode ser dobrada em uma frequência até metade do comprimento de onda, em um cristal não linear ou em um Niobato de Lítio Polarizado Periodicamente (PPLN) ou outro cristal não linear polarizado periodicamente. Esse processo de dobramento de sequência pode permitir o uso de lasers eficientes para gerar comprimentos de onda mais adequados para a excitação. Pode haver mais de um tipo de fonte de excitação para uma matriz de pixels. Em algumas modalidades, diferentes tipos de fontes de excitação podem ser combinados. A fonte de excitação pode ser fabricada de acordo com tecnologias convencionais que são utilizadas para fabricar um tipo selecionado de fonte de excitação.
[00443] O comprimento de onda característico de uma fonte de energia de excitação pode ser selecionado baseado em uma escolha de marcadores luminescentes que são utilizados em uma análise de matriz. Em algumas implementações, o comprimento de onda característico de uma fonte energia de excitação é selecionado para excitação direta (por exemplo, excitação de fóton único) de um fluoróforo escolhido. Em algumas implementações, o comprimento de onda característico de uma fonte de energia de excitação é selecionado para excitação indireta (por exemplo, excitação de múltiplos fótons ou conversão harmônica para um comprimento de onda que fornecerá excitação direta). Em algumas modalidades, a energia de excitação pode ser gerada por uma única fonte de luz que é configurada para gerar a energia de excitação em um comprimento de onda específico para aplicação para um poço de amostra. Em algumas modalidades, um comprimento de onda característico da fonte de excitação pode ser menor que um comprimento de onda característico de emissão correspondente a partir de uma amostra. Em algumas implementações, um comprimento de onda característico da fonte de excitação pode ser maior que um comprimento de onda característico de emissão a partir da amostra e a excitação da amostra pode ocorrer através da absorção de múltiplos fótons.
[00444] A fonte de excitação pode incluir uma bateria ou qualquer outra fonte de energia, que pode estar localizada em algum lugar que não o dispositivo de bioanálise integrado. Por exemplo, a fonte de excitação pode estar localizada em um instrumento e a energia pode ser acoplada ao dispositivo de bioanálise integrado através de fios condutores e conectores. Método de Uso, Operação do Instrumento e Interface do Usuário
[00445] O instrumento 2-120 pode ser controlado utilizando software e/ou hardware. Por exemplo, o instrumento pode ser controlado utilizando um dispositivo de processamento 1-123, como um ASIC, um FPGA e/ou um processador para fins gerais executando um software.
[00446] A figura 9-1 ilustra um fluxograma da operação do instrumento 2-120, de acordo com algumas modalidades. Após o usuário ter adquirido um espécime para analisar, o usuário começa uma nova análise no ato 9-101. Isso pode ser feito fornecendo uma indicação para o instrumento 2-120 através da interface do usuário 2-125, por exemplo, pressionando um botão. No ato 9-103, o instrumento 2-120 verifica se o chip de análise 2-110 a partir de uma análise realizada previamente ainda é inserido no instrumento 2-120. Se for determinado que um chip antigo está presente, então a energia para a fonte de excitação pode ser desligada no ato 9-105, o usuário é instruído no ato 9-107 a ejetar o chip anterior utilizando um indicador da interface do usuário 2-125 e o instrumento 2-120 espera que o chip antigo seja ejetado no ato 9-109.
[00447] Quando o chip anterior é ejetado pelo usuário ou se o instrumento 2-120 determinou no ato 9-103 que o chip anterior já foi removido, o usuário é instruído a inserir um novo chip de análise 2-110 para uma nova análise no ato 9-111. O instrumento 2-120 então espera que o novo chip de análise 2-110 seja inserido no ato 9-113. Quando usuário insere o novo chip, o usuário é instruído no ato 9-115 por um indicador da interface do usuário 2-125 a colocar o espécime a ser analisado na superfície superior exposta do chip de análise 2-110 e ainda instruído a fechar a tampa sobre o instrumento 2-120. O instrumento 2120 então espera a tampa ser fechada no ato 9-117. Quando a tampa é fechada pelo usuário, no ato 9-119 a fonte de excitação pode ser conduzida a produzir energia de excitação para excitar as partes da amostra do espécime presente nos poços de amostra do chip de análise 2-110. No ato 9-121, a energia de emissão a partir das amostras é detectada pelo sensor 2-122 e os dados a partir do sensor 2-122 são transmitidos ao dispositivo de processamento 2-123 para análise. Em algumas modalidades, os dados podem ser transmitidos ao dispositivo computacional externo 2-130. No ato 2-123, o instrumento 2-120 verifica se a aquisição de dados está completa. A aquisição de dados pode ser complete após um comprimento de tempo específico, um número de pulsos de excitação específico a partir da fonte de excitação ou um alvo específico foi identificado. Quando a aquisição de dados estiver completa, a análise de dados é finalizada em 9-125.
[00448] A figura 9-2 ilustra um exemplo da rotina de autocalibração, de acordo com algumas modalidades. A rotina de calibração pode ser executada em qualquer momento adequado antes da análise de um espécime. Por exemplo, pode ser feito uma vez pelo fabricante para cada instrumento antes de do envio ao usuário final. Alternativamente, o usuário final pode realizar uma calibração em qualquer momento adequado. Conforme discutido acima, o instrumento 2-120 é capaz de distinguir entre a energia de emissão tendo diferentes comprimentos de onda emitidos a partir de diferentes amostras. O instrumento 2-120 e/ou dispositivo computacional 2-130 pode ser calibrado com a calibração associado a cada cor específica de luz associada a, por exemplo, uma etiqueta luminescente utilizada para rotular moléculas de um espécime sendo analisado. Dessa forma, o sinal de saída preciso associado a uma cor específica pode ser determinado.
[00449] Para calibrar o dispositivo, um espécime de calibração associado a uma única etiqueta luminescente é fornecido ao instrumento 2-120 um de cada vez. A autocalibração começa no ato 9201 quando um usuário coloca um espécime compreendendo etiquetas luminescentes que emitem energia de emissão de um único comprimento de onda e um chip de análise 2-110 e insere o chip de análise 2-110 no instrumento 2-120. Utilizando a interface do usuário 2125, o usuário instruí o instrumento 2-120 a começar a autocalibração. Em resposta, no ato 9-203, o instrumento 2-120 executa a análise de calibração iluminando o chip de análise 2-110 com energia de excitação e medindo o única energia de emissão do comprimento de onda a partir do espécime de calibração. O instrumento 2-120 pode então, no ato 9-205, salvar o padrão de detecção medido na matriz de subssensores do sensor 2-122 para cada pixel da matriz do sensor. O padrão de detecção para cada etiqueta luminescente pode ser considerado uma assinatura de detecção associada à etiqueta luminescente. Dessa forma, as assinaturas podem ser utilizadas como um conjunto de dados de treinamento utilizado para analisar os dados recebidos a partir de amostras desconhecidas analisadas em execuções de análise subsequente.
[00450] A rotina de calibração acima pode então ser executada para cada espécime de calibração associado com uma única etiqueta luminescente. Dessa forma, cada sensor 2-122 da matriz de pixels é associado aos dados de calibração que podem ser utilizados para determinar a etiqueta luminescente presente em um poço de amostra durante uma análise subsequente implementada no ato 9-207 após a conclusão da rotina de calibração.
[00451] A figura 9-3 ainda ilustra como os dados de calibração podem ser adquiridos e utilizados para analisar os dados de acordo com algumas modalidades. No ato 9-301 os dados de calibração são obtidos a partir dos sensores. Isso pode ser feito utilizando a rotina de calibração mencionada anteriormente. No ato 9-303, uma matriz de transformação é gerada baseada nos dados de calibração. A matriz de transformação mapeia os dados do sensor para o comprimento de onda de emissão de uma amostra e é uma matriz m x n, onde m é o número de etiquetas luminescentes com diferentes comprimentos de onda de emissão e n é o número de subssensores utilizados para detectar a energia de emissão por pixel. Assim, cada coluna da matriz de transformação representa os valores de calibração para o sensor. Por exemplo, se houver quatro subssensores por pixel e cinco diferentes etiquetas luminescentes, então a matriz de transformação é uma matriz 4 x 5 (ou seja, quatro fileiras e cinco colunas) e cada coluna está associada a uma diferente etiqueta luminescente, os valores na coluna correspondem aos valores medidos obtidos a partir dos subssensores durante a rotina de autocalibração. Em algumas modalidades, cada pixel pode ter sua própria matriz de transformação. Em outras modalidades, os dados de calibração a partir de pelo menos alguns dos pixels podem ser ponderados e todos os pixels podem então utilizar a mesma matriz de transformação baseados nos dados ponderados.
[00452] No ato 9-305, os dados de análise associados a uma bioanálise são obtidos a partir dos sensores. Isso pode ser feito de quaisquer formas das descritas acima. No ato 9-307, o comprimento de onda da energia de emissão e/ou a identidade da etiqueta luminescente podem ser determinados utilizando a matriz de transformação e os dados de análise. Isso pode ser feito de qualquer forma adequada. Em algumas modalidades, os dados de análise são multiplicados pelo pseudo-inverso da matriz de transformação, resultando em um vetor de m x 1. A etiqueta luminescente associada ao componente do vetor com o valor máximo pode então ser identificada como a etiqueta luminescente presente no poço de amostra. As modalidades não são limitadas a essa técnica. Em algumas modalidades, para prevenir possíveis patologias que possam surgir quando o inverso da matriz com valores pequenos é tomado, uma rotina de otimização limitada, como um método de quadrados mínimos ou uma técnica de máxima probabilidade, pode ser realizada para determinar a etiqueta luminescente presente no poço de amostra.
[00453] O método de utilização dos dados de calibração mencionado acima para analisar dados a partir dos sensores pode ser implementado por qualquer processador adequado. Por exemplo, o dispositivo de processamento 2-123 do instrumento 2-120 pode realizar a análise ou o dispositivo computacional 2-130 pode realizar a análise. IX. Dispositivo Computacional
[00454] A figura 10 ilustra um exemplo de um ambiente de sistema computacional adequado 1000 no qual as modalidades podem ser implementadas. Por exemplo, o dispositivo computacional 2-130 da figura 2-1 pode ser implementado de acordo com o ambiente de sistema computacional 1000. Adicionalmente, o ambiente de sistema computacional 1000 pode agir como um sistema de controle que é programado para controlar o instrumento para realizar uma análise. Por exemplo, o sistema de controle pode controlar a fonte de excitação para emitir e direcionar luz em direção aos poços de amostra do chip de análise; controlar os sensores para permitir a detecção de luz de emissão a partir de uma ou mais amostras nos poços de amostra; e analisar sinais a partir dos sensores para identificar, por exemplo, analisando a distribuição espacial da energia de emissão, a amostra presente em um poço de amostra. O ambiente de sistema computacional 1000 é somente um exemplo de um ambiente computacional adequado e não pretende sugerir qualquer limitação como ao âmbito de uso ou de funcionalidade da invenção. O ambiente computacional 1000 não deve ser interpretado como tendo qualquer dependência ou exigência com relação a qualquer um ou qualquer combinação de componentes ilustrado no ambiente operacional exemplar 1000.
[00455] As modalidades são operacionais com inúmeras outras finalidades gerais ou ambientes ou configurações de sistema computacional de finalidade espacial. Exemplos de sistemas, ambientes e/ou configurações computacionais de poço conhecido que podem ser adequados para o uso com a invenção incluem, mas não estão limitados a, computadores pessoais, computadores de servidores, dispositivos portáteis ou manuais, sistemas de multiprocessadores, sistemas baseados em microprocessadores, descodificadores, eletrônicos de consumo programável, PCs de rede, minicomputadores, computadores mainframe, ambientes computacionais distribuídos que incluem quaisquer dos sistemas ou dispositivos acima, e similares.
[00456] O ambiente computacional pode executar as instruções executáveis por computados, como módulos de programas. Geralmente, módulos de programa incluem rotinas, programas, objetos, componentes, estruturas de dados e etc. que realizam tarefas específicas ou implementam tipos de dados abstratos específicos. A invenção pode ainda ser praticada em ambientes computacionais específicos onde as tarefas são realizadas por dispositivos de processamento remoto que são ligados através de uma rede de comunicações. Em um ambiente computacional distribuído, os módulos de programa podem ser localizados em ambos os meios de armazenamento do computador, local e remoto, incluindo dispositivos de armazenamento de memória.
[00457] Com referência à figura 10, um sistema exemplar para implementar a invenção inclui um dispositivo computacional de finalidade geral na forma de um computador 1010. Os componentes do computador 1010 podem incluir, mas não estão limitados a, uma unidade de processamento 1020, uma memória do sistema 1030 e um barramento do sistema 1021 que acopla vários componentes do sistema, incluindo a memória do sistema, à unidade de processamento 1020. O barramento do sistema 1021 pode ser quaisquer dos vários tipos de estruturas de barramentos incluindo um barramento de memória ou controlador de memória, um barramento periférico e um barramento local utilizando quaisquer de uma variedade de arquiteturas de barramentos. Como exemplo e não como limitação, tais arquiteturas incluem barramento ISA (Industry Standard Architecture), barramento MCA (Micro Channel Architecture), barramento EISA (Enhanced ISA), barramento local VESA (Video Electronics Standards Association) e barramento PCI (Peripheral Component Interconnect) ainda conhecido como barramento Mezzanine.
[00458] O computador 1010 tipicamente inclui uma variedade de meios legíveis por computador. O meio legível por computador pode ser qualquer meio disponível que pode ser acessado por computador 1010 e inclui ambos os meios, volátil e não volátil, meios removíveis e não removíveis. Como exemplo e não como limitação, o meio legível por computador pode compreender um meio de armazenamento do computador e meios de comunicação. O meio de armazenamento por computador inclui ambos os meios volátil e não volátil, removível e não removível implementados em qualquer método ou tecnologia para armazenamento de informações, como instruções legíveis por computador, estruturas de dados, módulos de programa ou outros dados. O meio de armazenamento por computador inclui, mas não é limitado a, RAM, ROM, EEPROM, memória flash ou outra tecnologia de memória, CD-ROM, discos versáteis digitais (DVD) ou outro armazenamento de disco óptico, disquetes magnéticos, fita magnética, armazenamento de disco magnético ou outros dispositivos de armazenamento magnético, ou qualquer outro meio que possa ser utilizado para armazenar a informação desejada e que possa ser acessado por computador 1010. Os meios de comunicação tipicamente englobam instruções legíveis por computador, estruturas de dados, módulos de programa ou outros dados em um sinal de dados modulado, como uma onda portador ou outro mecanismo de transporte e inclui quaisquer informações do meio de entrega. O termo "sinal de dados modulado" significa um sinal que tem uma ou mais dessas características definidas ou alteradas de modo a codificar informações no sinal. Como exemplo e não limitação, o meio de comunicação inclui meios com fio, como uma rede com fio ou conexão direta com fio e meios sem fio, como meio acústico, RF, infravermelho ou outros. Combinações de quaisquer desses devem ainda estar incluídas no âmbito do meio legível por computador.
[00459] A memória do sistema 1030 inclui meio de armazenamento do computador na forma de memória volátil e/ou não volátil, como memória de somente leitura (ROM) 1031 e memória de acesso aleatórios (RAM) 1032. Um sistema básico de entrada/saída 1033 (BIOS), contendo as rotinas básicas que ajudam a transferir informações entre elementos dentro de computador 1010, como durante a inicialização, é tipicamente armazenado em ROM 1031. A RAM 1032 tipicamente contém dados e/ou módulos de programa que são imediatamente acessíveis para e/ou presentemente sendo operados pela unidade de processamento 1020. Como exemplo e não limitação, a figura 10 ilustra sistemas operacionais 1034, programas de aplicação 1035, outros módulos de programas 1036 e dados de programas 1037.
[00460] O computador 1010 pode ainda incluir outo meio de armazenamento de computador removível/não-removível, volátil/não- volátil. Em forma de exemplo apenas a figura 10 ilustra um disco rígido 1041 que lê ou grava no meio magnético não removível e não volátil, uma unidade de disco magnético 1051 que lê ou grava em um disco magnético removível e não volátil 1052 e um unidade de disco óptico 1055 que lê ou grava em um disco óptico removível, não-volátil 1056 como um CD ROM ou outro meio óptico. Outro meio de armazenamento de computador removível/não-removível, volátil/não-volátil que pode ser usado no ambiente operacional exemplar incluir, entre outros, fitas magnéticas, cartões de memória flash, disco digital versátil, fita de vídeo digital, RAM de estado sólido, ROM no estado sólido e semelhantes. O disco rígido 1041 é tipicamente conectado ao barramento do sistema 1021 através de uma interface de memória não removível como interface 1040 e unidade de disco magnético 1051 e disco óptico 1055 são tipicamente conectados ao barramento do sistema 1021 por uma interface de memória removível, como interface 1050.
[00461] As unidades e seu armazenamento de computador associado discutidos acima e ilustrados na figura 10, fornecem instruções legíveis por armazenamento de computador, estruturas de dados, módulos de programa e outros dados para o computador 1010. Na figura 10, por exemplo, o disco rígido 1041 é ilustrado como sistema operacional de armazenamento 1044, programas de aplicativos 1045, outros módulos de programa 1046 e dados de programa 1047. Observe que esses componentes podem ser os mesmos ou diferentes do sistema operacional 1034, programas de aplicativos 1035, outros módulos de programa 1036 e dados de programa 1037. O sistema operacional 1044, programas de aplicativos 1045, outros módulos de programa 1046 e dados de programa 1047 recebem diferentes números aqui para ilustrar que, pelo menos, eles são diferentes cópias. Um usuário pode inserir comandos e informações ao computador 1010 através de dispositivos de entrada como um teclado 1062 e dispositivo indicador 1061, geralmente chamados de mouse, trackball ou touch pad. Outros dispositivos de entrada (não mostrados) podem incluir um microfone, joystick, game pad, satellite dish, scanner ou semelhantes. Esses e outros dispositivos de entrada são geralmente conectados à unidade de processamento 1020 através de uma interface de entrada do usuário 1060 que é acoplada ao barramento do sistema, mas pode ser conectada por outra interface e estruturas de barramento, como uma porta paralela, porta de jogo ou barramento serial universal (USB). Um monitor 1091 ou outro tipo de tela é ainda conectado ao barramento do sistema 1021 através de uma interface, como uma interface de vídeo 1090. Além ao monitor, os computadores podem ainda incluir outros dispositivos de entrada periférica como alto-falantes 1097 e impressora 1096, que pode ser conectado através de uma interface periférica de saída 1095.
[00462] O computador 1010 pode operar em um ambiente de rede usando conexões lógicas a um ou mais computadores remotos, como um computador remoto 1080. O computador remoto 1080 pode ser um computador pessoal, um servidor, um roteador, uma rede de PC, um dispositivo peer ou outro nó de rede comum e tipicamente inclui muitos ou todos os elementos descritos acima com relação ao computador 1010, embora apenas um dispositivo de armazenamento de memória 1081 foi ilustrado na figura 10. As conexões lógicas representadas na figura 10 incluem uma rede de área local (LAN) 1071 e uma rede de área ampla (WAN) 1073, mas pode ainda incluir outras redes. Tais ambientes de rede são comuns em escritórios, redes de computador empresarial, intranets e Internet.
[00463] Quando usado em um ambiente de rede LAN, o computador 1010 é conectado à LAN 1071 através de uma interface de rede ou adaptador 1070. Quando usado em um ambiente de rede WAN, o computador 1010 tipicamente inclui um modem 1072 ou outro meio para estabelecer as comunicações sobre a WAN 1073, como a Internet. O modem 1072, que pode ser interno ou externo, pode ser conectado ao barramento do sistema 1021 através da interface de entrada do usuário 1060, ou outro mecanismo apropriado. Em um ambiente de rede, módulos de programa representados com relação ao computador 1010, ou porções desse, podem ser armazenados no dispositivo de armazenamento de memória remoto. Em forma de exemplo e não limitação, a figura 10 ilustra programas de aplicativos remotos 1085 como residindo no dispositivo de memória 1081. Será observado que as conexões de rede mostradas são exemplares e outros meios para estabelecer um link de comunicações link entre os computadores pode ser usado. VIII. Conclusão
[00464] Tendo então descrito vários aspectos de pelo menos uma modalidade dessa invenção, deve ser observado que várias alterações, modificações e melhorias ocorrerão aos técnicos no assunto.
[00465] Tais alterações, modificações e melhorias pretendem ser parte dessa revelação e estar dentro do âmbito e do escopo da invenção. Ainda, embora as vantagens da presente invenção sejam indicadas, deve-se observar que nem toda modalidade da invenção incluirá cada vantagem descrita. Algumas modalidades podem não implementar quaisquer recursos descritos como vantajosos aqui e em alguns casos. Certamente, a descrição e os desenhos anteriores são em forma de exemplo somente.
[00466] As modalidades da presente invenção descritas acima podem ser implementadas em qualquer de inúmeras formas. Por exemplo, as modalidades podem ser implementadas usando hardware, software ou uma combinação desses. Quando implementadas no software, o código do software pode ser executado em qualquer processador adequado ou coleta de processadores, fornecidos em um único computador ou distribuídas entre múltiplos computadores. Tais processadores podem ser implementados como circuitos integrados, com um ou mais processadores em um componente de circuito integrado, incluindo componentes de circuito integrado disponíveis comercialmente conhecidos na técnica por nomes como chips de CPU, chips de GPU, microprocessador, microcontrolador ou coprocessador. De modo alternativo, um processor pode ser implementado em circuito personalizado, como um ASIC, ou circuito semipersonalizado resultando da configuração de um dispositivo de lógica programável. Ainda como alternativa, um processador pode ser uma porção de um circuito maior ou do dispositivo semicondutor, comercialmente disponível, semipersonalizado ou personalizado. Como um exemplo específico, alguns microprocessadores comercialmente disponíveis têm múltiplas cores de modo que uma ou um subconjunto dessas cores possa constituir um processador. Embora, um processador possa ser implementado usando circuito em qualquer formato adequado.
[00467] Ainda, deve-se observar que um computador pode ser incorporado em qualquer de um número de formas, como um computador montado em rack, um computador de mesa, um computador portátil ou uma tablet. Adicionalmente, um computador pode ser incorporado em um dispositivo geralmente não considerado como um computador, mas com capacidades de processamento adequado, incluindo um Assistente Pessoal Digital (PDA), um smartphone ou qualquer outro dispositivo eletrônico portátil ou fixo adequado.
[00468] Além disso, um computador pode ter um ou mais in dispositivos de entrada e saída. Esses dispositivos podem ser usados, entre outras coisas, para apresentar a interface do usuário. Exemplos de dispositivos de saída que podem ser usados para fornecer uma interface do usuário incluem impressoras ou telas para apresentação visual de saída e alto-falantes ou outros dispositivos de geração de som para apresentação audível de saída. Exemplos de dispositivos de entrada que podem ser usados para uma interface do usuário incluem teclados e dispositivos apontadores, como mouses, touchpads e tablets de digitalização. Como outro exemplo, um computador pode receber informações de entrada através de reconhecimento de voz ou em outro formato audível.
[00469] Tais computadores podem ser interconectados por um ou mais redes em qualquer forma adequada, incluindo como uma rede de área local ou uma rede de área ampla, como uma rede corporativa ou a Internet. Tais redes podem ser baseadas em qualquer tecnologia adequada e podem operar de acordo com qualquer protocolo adequado e podem incluir redes sem fio, redes com fio ou redes de fibra óptica.
[00470] Além disso, os vários métodos ou processos destacados aqui podem ser codificados como software que é executável em um ou mais processadores que empregam qualquer um de uma variedade de sistemas operacionais ou plataformas. Adicionalmente, tais softwares podem ser escritos usando qualquer de um número linguagens de programação e/ou programação adequada ou ferramentas de roteirização e ainda podem ser compilados como código de linguagem executável por máquina ou código intermediário que é executado em um quadro ou uma máquina virtual.
[00471] A esse respeito, a invenção pode ser incorporada como um meio de armazenamento legível por computador (ou múltiplos meios legíveis por computador) (por exemplo, uma memória de computador, um ou mais disquetes, discos compactos (CD), discos ópticos, discos de vídeo digitais (DVD), fitas magnéticas, memórias flash, configurações de circuito em Matrizes de Portas de Campo Programáveis ou outros dispositivos semicondutores, ou outro meio de armazenamento de computador tangível) codificado com um ou mais programas que, quando executados em um ou mais computadores ou outros processadores, realizam métodos que implementam as várias modalidades da invenção discutida acima. Como é aparente dos exemplos mencionados, um meio de armazenamento legível por computador pode reter informações por um tempo suficiente para fornecer instruções legíveis por computador de uma forma não transitória. Tal meio ou meios legíveis por computador podem ser transportáveis, de modo que o programa ou programas ali armazenados podem ser carregados até um ou mais diferentes computadores ou outros processadores para implementar vários aspectos da presente invenção, como discutido acima. Como aqui usado, o termo "meio de armazenamento legível por computador" engloba apenas a meio legível por computador que pode ser considerado como uma manufatura (ou seja, artigo de fabricação) ou uma máquina. De modo alternativo ou adicionalmente, a invenção pode ser incorporada como um meio legível por computador que não um meio de armazenamento legível por computador, como um sinal de propagação.
[00472] Os termos "programa" ou "software" são usados aqui em um senso genérico para se referir a qualquer tipo de código de computador ou instruções de conjunto executáveis em computador que podem ser empregadas para programar um computador ou outro processador para implementar vários aspectos da presente invenção, como discutido acima. Adicionalmente, deve-se observar que de acordo com um aspecto dessa modalidade, um ou mais programas de computador quando executados realizando métodos da presente invenção não precisam residir em um único computador ou processor, mas podem ser distribuídos de uma maneira modular entre um número de diferentes computadores ou processadores para implementar vários aspectos da presente invenção.
[00473] As instruções executáveis em computador podem ser de várias formas, como módulos de programa, executados por um ou mais computadores ou outros dispositivos. Geralmente, os módulos de programa incluem rotinas, programas, objetos, componentes, estruturas de dados e etc. que realizam tarefas específicas ou implementam tipos de dados abstratos específicos. Tipicamente, a funcionalidade dos módulos de programa pode ser combinada ou distribuída conforme em in várias modalidades.
[00474] Ainda, estruturas de dados podem ser armazenadas em um meio legível por computador, de qualquer forma adequada. Para simplicidade de ilustração, as estruturas de dados podem ser mostradas para terem campos que são relacionados através da localização na estrutura de dados. Tais relações podem, dessa forma, ser alcançadas atribuindo armazenamento para os campos com localizações em um meio legível por computador que expressa relação entre os campos. Entretanto, qualquer mecanismo adequado pode ser usado para estabelecer uma relação entre informações em campos de uma estrutura de dados, incluindo através do uso de indicadores, etiquetas ou outros mecanismos que estabeleçam relação entre elementos de dados.
[00475] Vários aspectos da presente invenção podem ser usados sozinhos, em combinação, ou em uma variedade de disposições não especificamente discutidas nas modalidades descritas anteriormente e então não é limitada em seu pedido aos detalhes e disposição de componentes definidos na descrição anterior ou ilustrada nos desenhos. Por exemplo, os aspectos descritos em uma modalidade podem ser combinados em qualquer forma com os aspectos descritos em outras modalidades.
[00476] Ainda, a invenção pode ser incorporada como um método, do qual um exemplo foi fornecido. Os atos realizados como parte do método podem ser organizados de qualquer forma. Certamente, as modalidades podem ser construídas onde os atos são realizados em uma ordem diferente da ilustrada, que pode incluir realizar alguns atos simultaneamente, mesmo embora mostrado como atos sequenciais nas modalidades ilustrativas.
[00477] O uso dos terminais ordinários como "primeiro", "segundo", "terceiro", etc., nas reivindicações para modificar um elemento de reivindicação não conota qualquer prioridade, precedência ou ordem de um elemento de reivindicação sobre outro ou a ordem temporal na qual os atos de um método são realizados, mas são usados meramente como rótulos para distinguir um elemento de reivindicação tendo um certo nome de outro elemento tendo um mesmo nome (mas para uso do termo ordinário) para distinguir os elementos de reivindicação.
[00478] Ainda, a fraseologia e terminologia usadas aqui é para finalidade e descrição e não devem estar relacionadas como limitativas. O use de "incluindo," "compreendendo," ou "tendo," "contendo", "envolvendo", e variações desses aqui, significa abranger os itens listados a seguir e os equivalentes desses bem como itens adicionais.
Claims (26)
1. Instrumento configurado para interagir com um chip de análise em uma estrutura de suporte de chip que permite que um espécime seja colocado em contato com uma superfície do chip de análise, o chip de análise compreendendo uma pluralidade de poços de amostra, cada poço de amostra da pluralidade de poços de amostra configurado para receber uma amostra, o instrumento caracterizado pelo fato de que compreende: uma interface de chip de análise configurada para receber a estrutura de suporte de chip; pelo menos uma fonte de luz de excitação configurada para excitar a amostra de pelo menos uma parte da pluralidade de poços de amostra; uma pluralidade de sensores, um sensor da pluralidade de sensores correspondente a um respectivo poço de amostra e configurado para detectar energia de emissão do respectivo poço de amostra; e pelo menos um elemento óptico configurado para direcionar a energia de emissão, quando a estrutura de suporte de chip é recebida na interface de chip de análise, de um poço de amostra em direção a um respectivo sensor da pluralidade de sensores.
2. Instrumento, de acordo com a reivindicação 1, caracterizado pelo fato de que ainda compreende: um alojamento configurado para acoplar de forma destacável à estrutura de suporte de chip, em que o alojamento tem uma abertura e o chip de análise é configurado para alinhar com a abertura quando a estrutura de suporte de chip é acoplada ao alojamento.
3. Instrumento, de acordo com a reivindicação 2, caracterizado pelo fato de que ainda compreende: pelo menos um componente magnético posicionado próximo da abertura e configurado para posicionar o chip de análise em alinhamento com a abertura quando a estrutura de suporte de chip é acoplada ao alojamento.
4. Instrumento, de acordo com a reivindicação 1, caracterizado pelo fato de que ainda compreende: um espelho policrônico configurado para refletir luz de excitação de pelo menos uma fonte de luz de excitação em direção ao chip de análise e transmitir a energia de emissão a partir da pluralidade de poços de amostras em direção à pluralidade de sensores.
5. Instrumento, de acordo com qualquer uma das reivindicações 1 a 4, caracterizado pelo fato de que pelo menos um elemento óptico compreende uma lente do relé.
6. Instrumento, de acordo com qualquer uma das reivindicações 1 a 5, caracterizado pelo fato de que pelo menos uma fonte de luz de excitação compreende uma pluralidade de fontes de luz, cada fonte de luz da pluralidade de fontes de luz emitindo luz de excitação em um ou mais de uma pluralidade de comprimentos de onda, e o instrumento ainda compreende um combinador de comprimento de onda para espacialmente sobrepor a luz emitida de cada uma da pluralidade de fontes de luz.
7. Instrumento, de acordo com qualquer uma das reivindicações 1 a 6, caracterizado pelo fato de que pelo menos uma fonte de luz de excitação compreende uma fonte de luz pulsada.
8. Instrumento, de acordo com qualquer uma das reivindicações 1 a 7, caracterizado pelo fato de que ainda compreende pelo menos um filtro espectral configurado para transmitir a energia de emissão e absorver e/ou refletir luz de excitação de pelo menos uma fonte de luz de excitação.
9. Instrumento, de acordo com qualquer uma das reivindicações 1 a 8, caracterizado pelo fato de que ainda compreende pelo menos um elemento de classificação espectral para separar espacialmente a energia de emissão de um primeiro comprimento de onda da energia de emissão de um segundo comprimento de onda.
10. Instrumento, de acordo com a reivindicação 9, caracterizado pelo fato de que pelo menos um elemento de classificação espectral compreende um elemento óptico difrativo configurado para dispersar cromaticamente a energia de emissão e o foco da energia de emissão.
11. Instrumento, de acordo com a reivindicação 9, caracterizado pelo fato de que pelo menos um elemento de classificação espectral é um elemento de filtragem de luz.
12. Instrumento, de acordo com qualquer uma das reivindicações 1 a 11, caracterizado pelo fato de que ainda compreende um sistema de controle que é programado para (i) direcionar a luz de excitação para a pluralidade de poços de amostra, (ii) detectar sinais na pluralidade de sensores a partir da pluralidade de poços de amostra, e (iii) usar um padrão de distribuição espacial dos sinais para identificar a amostra e/ou subunidade da amostra.
13. Aparelho caracterizado pelo fato de que compreende: um chip de análise suportado em uma estrutura de suporte de chip que permite que um espécime seja colocado em contato com uma superfície do chip de análise, o chip de análise compreendendo uma pluralidade de pixels, cada da pluralidade de pixels compreendendo: um poço de amostra configurado para receber uma amostra, que, quando excitada, emite energia de emissão; e pelo menos um elemento para direcionar a energia de emissão a partir do poço de amostra em uma direção particular, em que pelo menos um elemento é selecionado do grupo que consiste em um elemento refrativo, um elemento difrativo, um elemento plasmônico e um ressonador; e uma passagem de luz pela qual a energia de emissão percorre do poço de amostra em direção a um sensor; e um instrumento configurado para interagir com o chip de análise, o instrumento compreendendo: uma interface de chip de análise configurada para receber a estrutura de suporte de chip; pelo menos uma fonte de luz de excitação configurada para excitar a amostra; uma pluralidade de sensores, um sensor da pluralidade de sensores correspondente a um respectivo poço de amostra e configurado para detectar a energia de emissão a partir do respectivo poço de amostra; e pelo menos um elemento óptico configurado para direcionar a energia de emissão, quando a estrutura de suporte de chip é recebida na interface de chip de análise, de um poço de amostra em direção a um respectivo sensor da pluralidade de sensores.
14. Aparelho, de acordo com a reivindicação 13, caracterizado pelo fato de que o chip de análise é configurado para ser conectado e removido do instrumento, e quando o chip de análise é conectado ao instrumento, a distância óptica entre um poço de amostra da pluralidade de poços de amostra e o sensor correspondente da pluralidade de sensores é menor que 30 cm.
15. Aparelho, de acordo com a reivindicação 13, caracterizado pelo fato de que: a amostra compreende uma etiqueta luminescente que emite a energia de emissão dentro de uma faixa de comprimento de onda de uma pluralidade de faixas de comprimento de onda; e cada sensor da pluralidade de sensores compreende pelo menos um subsensor configurado para detectar a pluralidade de faixas de comprimento de onda.
16. Aparelho, de acordo com a reivindicação 15, caracterizado pelo fato de que cada sensor da pluralidade de sensores compreende pelo menos dois subsensores.
17. Aparelho, de acordo com a reivindicação 16, caracterizado pelo fato de que o instrumento ainda compreende pelo menos um comprimento de onda dependente do elemento que direciona a energia de emissão de um primeiro comprimento de onda em direção a um primeiro subsensor de pelo menos dois subsensores e direciona a energia de emissão de um segundo comprimento de onda em direção a um segundo subsensor de pelo menos dois subsensores.
18. Aparelho, de acordo com a reivindicação 17, caracterizado pelo fato de que pelo menos um elemento dependente do comprimento de onda inclui pelo menos um dentre um elemento óptico difrativo e um filtro espectral.
19. Aparelho, de acordo com qualquer uma das reivindicações 16 a 18, caracterizado pelo fato de que pelo menos uma fonte de excitação emite a luz pulsada.
20. Aparelho, de acordo com qualquer uma das reivindicações 16 a 18, caracterizado pelo fato de que: uma primeira etiqueta luminescente associada com uma primeira amostra é excitada por luz de um primeiro comprimento de onda, mas não é excitada por luz de um segundo comprimento de onda; e uma segunda etiqueta luminescente associada com uma segunda amostra é excitada por luz do segundo comprimento de onda, mas não é excitada por luz do primeiro comprimento de onda.
21. Chip de análise configurado para ser suportado em uma estrutura de suporte de chip que permite que um espécime seja colocado em contato com uma superfície do chip de análise, o chip de análise caracterizado pelo fato de que compreende: uma amostra de poço configurada para receber uma amostra que, quando excitada, emite energia de emissão; e pelo menos um elemento que direciona a energia de emissão a partir do poço de amostra em uma direção particular, em que pelo menos um elemento é selecionado a partir do grupo que consiste em um elemento refrativo, um elemento difrativo, um elemento plasmônico e um ressonador; e uma passagem de luz pela qual a energia de emissão percorre a partir da amostra de poço em direção a um sensor.
22. Método para analisar um espécime caracterizado pelo fato de que compreende: fornecer o espécime na superfície superior de um chip de análise suportado em uma estrutura de suporte de chip que permite que o espécime seja colocado em contato com uma superfície do chip de análise, o chip de análise compreendendo uma pluralidade de poços de amostra; alinhar o chip de análise com um instrumento compreendendo uma interface de chip de análise configurado para receber a estrutura de suporte de chip, pelo menos uma fonte de luz de excitação e pelo menos um sensor; excitar uma amostra do espécime em pelo menos um da pluralidade de poços de amostra com a luz de excitação de pelo menos uma fonte de luz de excitação; e detectar, com pelo menos um sensor, a energia de emissão a partir do pelo menos um poço de amostra em resposta à excitação pela luz de excitação.
23. Método para sequência de uma molécula de ácido nucleico alvo caracterizado pelo fato de que compreende: fornecer um chip suportado em uma estrutura de suporte de chip que permite que um espécime seja colocado em contato com uma superfície do chip adjacente a um instrumento que inclui uma interface de chip configurada para receber a estrutura de suporte de chip, uma fonte de excitação e um sensor, em que o chip inclui pelo menos um poço que é acoplado de forma operável à fonte de excitação e o sensor quando o chip está em uma posição de detecção do instrumento, e em que o poço contém a molécula de ácido nucleico alvo, uma enzima de polimerização e uma pluralidade de tipos de nucleotídeos ou análogos de nucleotídeo; com o chip na posição de detecção, realizar uma reação de extensão em uma localização principal da molécula de ácido nucleico alvo na presença da enzima de polimerização para sequencialmente incorporar os nucleotídeos ou análogos de nucleotídeo em um filamento crescente que é complementar à molécula de ácido nucleico alvo, em que sob incorporação e excitação pela energia de excitação da fonte de excitação, os nucleotídeos ou análogos de nucleotídeos emitem sinais no poço; usar o sensor para detectar os padrões de distribuição espacial e/ou temporal dos sinais que são distinguíveis para a pluralidade de tipos de nucleotídeos ou análogos de nucleotídeo; e identificar os nucleotídeos ou análogos de nucleotídeo com base nos padrões de distribuição espacial e/ou temporal dos sinais, assim sequenciando a molécula de ácido nucleico alvo.
24. Método para sequência de ácido nucleico caracterizado pelo fato de que compreende: fornecer um chip suportado em uma estrutura de suporte de chip que permite que um espécime seja colocado em contato com uma superfície do chip adjacente a um instrumento que inclui uma interface de chip configurada para receber a estrutura de suporte de chip, em que chip inclui uma pluralidade de poços que são acoplados de forma operável a (i) uma fonte de excitação e (ii) um sensor do dito instrumento quando o chip está em uma posição de detecção do instrumento, e em que um poço individual da pluralidade contém a molécula de ácido nucleico alvo, uma enzima de polimerização e uma pluralidade de tipos de nucleotídeos ou análogos de nucleotídeo; com o chip na posição de detecção, submeter a molécula de ácido nucleico alvo a uma reação de polimerização para produzir um filamento crescente que é complementar à molécula de ácido nucleico alvo na presença dos nucleotídeos ou análogos de nucleotídeo e enzima de polimerização, em que os nucleotídeos ou análogos de nucleotídeos emitem sinais no poço individual sob excitação por energia de excitação da fonte de excitação durante a incorporação; usar o sensor para detectar padrões de distribuição espacial e/ou temporal dos sinais que são distinguíveis para a pluralidade de tipos de nucleotídeos ou análogos de nucleotídeo; e identificar uma sequência da molécula de ácido nucleico alvo com base nos padrões de distribuição espacial e/ou temporal dos sinais.
25. Aparelho caracterizado pelo fato de que compreende: uma matriz de poços de amostra dispostos sobre uma superfície de um chip, em que poços de amostra individuais na matriz são configurados para receber uma amostra; e uma pluralidade de lentes formadas no chip, em que lentes individuais da pluralidade de lentes são configuradas para focar a luz emitida a partir de um poço de amostra na matriz, em que a pluralidade de lentes inclui uma pluralidade de lentes refrativas.
26. Método para formar um aparelho caracterizado pelo fato de que compreende: formar uma matriz de poços de amostra dispostos sobre uma superfície de um chip, em que poços de amostra individuais na matriz são configurados para receber uma amostra; e formar uma pluralidade de lentes no chip, em que lentes individuais da pluralidade de lentes são configuradas para focar a luz emitida a partir de um poço de amostra na matriz, em que a pluralidade de lentes inclui uma pluralidade de lentes refrativas.
Applications Claiming Priority (7)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201361905282P | 2013-11-17 | 2013-11-17 | |
| US61/905,282 | 2013-11-17 | ||
| US201361917926P | 2013-12-18 | 2013-12-18 | |
| US61/917,926 | 2013-12-18 | ||
| US201461941916P | 2014-02-19 | 2014-02-19 | |
| US61/941,916 | 2014-02-19 | ||
| PCT/US2014/066010 WO2015074001A1 (en) | 2013-11-17 | 2014-11-17 | Optical system and assay chip for probing, detecting and analyzing molecules |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| BR112016011052A2 BR112016011052A2 (pt) | 2020-05-19 |
| BR112016011052B1 true BR112016011052B1 (pt) | 2021-09-28 |
Family
ID=52014380
Family Applications (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| BR112016011061-7A BR112016011061B1 (pt) | 2013-11-17 | 2014-11-17 | Dispositivo integrado com fonte de luz externa para sondar, detectar e analisar moléculas, sistema, método para formar um dispositivo integrado, método para analisar um espécime, dispositivo integrado, instrumento e métodos para sequenciar ácido nucleico |
| BR112016011084A BR112016011084B8 (pt) | 2013-11-17 | 2014-11-17 | Dispositivo integrado para analisar uma pluralidade de amostras em paralelo, métodos de análise desta pluralidade de amostras, para a fabricação de uma cavidade de amostra e estrutura ótica alinhada à referida cavidade, de sequenciamento de uma molécula de ácido nucleico e de formação de uma fonte de excitação de escala nano alinhada, e instrumento portátil |
| BR112016011052-8A BR112016011052B1 (pt) | 2013-11-17 | 2014-11-17 | Instrumento configurado para interagir com um chip de análise em uma estrutura de suporte de chip, chip de análise, método para analisar um espécime, método para sequência de molécula de ácido nucleico alvo, método para sequência de ácido nucleico, aparelho e método para formar um aparelho |
Family Applications Before (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| BR112016011061-7A BR112016011061B1 (pt) | 2013-11-17 | 2014-11-17 | Dispositivo integrado com fonte de luz externa para sondar, detectar e analisar moléculas, sistema, método para formar um dispositivo integrado, método para analisar um espécime, dispositivo integrado, instrumento e métodos para sequenciar ácido nucleico |
| BR112016011084A BR112016011084B8 (pt) | 2013-11-17 | 2014-11-17 | Dispositivo integrado para analisar uma pluralidade de amostras em paralelo, métodos de análise desta pluralidade de amostras, para a fabricação de uma cavidade de amostra e estrutura ótica alinhada à referida cavidade, de sequenciamento de uma molécula de ácido nucleico e de formação de uma fonte de excitação de escala nano alinhada, e instrumento portátil |
Country Status (10)
| Country | Link |
|---|---|
| US (11) | US9983135B2 (pt) |
| EP (6) | EP3074531B1 (pt) |
| JP (5) | JP6573899B2 (pt) |
| KR (4) | KR102240166B1 (pt) |
| CN (5) | CN105917003A (pt) |
| AU (4) | AU2014348302B2 (pt) |
| BR (3) | BR112016011061B1 (pt) |
| CA (3) | CA2930834A1 (pt) |
| MX (4) | MX2016006454A (pt) |
| WO (3) | WO2015074005A1 (pt) |
Families Citing this family (166)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US10378053B2 (en) * | 2017-03-17 | 2019-08-13 | Apton Biosystems, Inc. | Sequencing and high resolution imaging |
| US9593371B2 (en) * | 2013-12-27 | 2017-03-14 | Intel Corporation | Integrated photonic electronic sensor arrays for nucleic acid sequencing |
| KR102240166B1 (ko) | 2013-11-17 | 2021-04-14 | 퀀텀-에스아이 인코포레이티드 | 분자들을 프로빙 검출 및 분석하기 위한 외부 광원을 구비한 통합 디바이스 |
| US11287484B2 (en) | 2014-02-03 | 2022-03-29 | Innovaura Corporation | Method and apparatus for triage of electronic items using magnetic field detection |
| US11747407B2 (en) | 2014-02-03 | 2023-09-05 | Innovaura Corporation | System and method for characterizing defects in electronic items using magnetic field detection |
| WO2015117157A1 (en) * | 2014-02-03 | 2015-08-06 | Electromagnetic Landmarks Inc. | Magnetic sensor array and system |
| CN112903638A (zh) | 2014-08-08 | 2021-06-04 | 宽腾矽公司 | 用于对分子进行探测、检测和分析的带外部光源的集成装置 |
| MX2021007934A (es) | 2014-08-08 | 2023-01-17 | Quantum Si Inc | Dispositivo integrado para el depósito temporal de fotones recibidos. |
| US9921157B2 (en) * | 2014-08-08 | 2018-03-20 | Quantum-Si Incorporated | Optical system and assay chip for probing, detecting and analyzing molecules |
| US9721751B2 (en) * | 2014-08-22 | 2017-08-01 | The Board Of Trustees Of The Leland Stanford Junior University | Electron microscopy specimen and method of fabrication |
| US10352899B2 (en) | 2014-10-06 | 2019-07-16 | ALVEO Technologies Inc. | System and method for detection of silver |
| US9921182B2 (en) | 2014-10-06 | 2018-03-20 | ALVEO Technologies Inc. | System and method for detection of mercury |
| US9506908B2 (en) | 2014-10-06 | 2016-11-29 | Alveo Technologies, Inc. | System for detection of analytes |
| US10627358B2 (en) | 2014-10-06 | 2020-04-21 | Alveo Technologies, Inc. | Method for detection of analytes |
| US10196678B2 (en) | 2014-10-06 | 2019-02-05 | ALVEO Technologies Inc. | System and method for detection of nucleic acids |
| US10184892B2 (en) * | 2014-10-29 | 2019-01-22 | Horiba Instruments Incorporated | Determination of water treatment parameters based on absorbance and fluorescence |
| US20180003635A1 (en) | 2015-01-20 | 2018-01-04 | Hyris Limited | Detector for measuring fluorescence in a liquid sample |
| US10018608B2 (en) * | 2015-02-27 | 2018-07-10 | Vitaly Talyansky | System to authenticate and identify items |
| WO2016149397A1 (en) | 2015-03-16 | 2016-09-22 | Pacific Biosciences Of California, Inc. | Integrated devices and systems for free-space optical coupling |
| US11466316B2 (en) | 2015-05-20 | 2022-10-11 | Quantum-Si Incorporated | Pulsed laser and bioanalytic system |
| US10174363B2 (en) | 2015-05-20 | 2019-01-08 | Quantum-Si Incorporated | Methods for nucleic acid sequencing |
| US10605730B2 (en) | 2015-05-20 | 2020-03-31 | Quantum-Si Incorporated | Optical sources for fluorescent lifetime analysis |
| US9874693B2 (en) | 2015-06-10 | 2018-01-23 | The Research Foundation For The State University Of New York | Method and structure for integrating photonics with CMOs |
| EP3308204A4 (en) | 2015-06-12 | 2019-03-13 | Pacific Biosciences of California, Inc. | WAVEGUIDE DEVICES WITH INTEGRATED TARGET AND OPTICAL COUPLING SYSTEMS |
| EP3133386B1 (en) * | 2015-07-27 | 2023-03-15 | Personal Genomics, Inc. | Sensing module and sensing method |
| KR102312555B1 (ko) * | 2015-07-30 | 2021-10-14 | 더 리전트 오브 더 유니버시티 오브 캘리포니아 | 광 공동 pcr |
| US20180252646A1 (en) * | 2015-08-18 | 2018-09-06 | Agency For Scien, Technology And Research | Optical structure and optical light detection system |
| US9733188B2 (en) * | 2015-09-21 | 2017-08-15 | International Business Machines Corporation | Enhancing on-chip fluorescence detection |
| US11320373B2 (en) | 2015-10-22 | 2022-05-03 | Jacob Schneiderman | Systems and methods for identifying and treating biological materials |
| KR101720434B1 (ko) * | 2015-11-10 | 2017-03-28 | 한국과학기술원 | 광 위상배열 안테나 |
| US10248838B2 (en) * | 2015-12-04 | 2019-04-02 | The Regents Of The University Of California | Method and device for single molecule imaging |
| US10352856B2 (en) * | 2015-12-14 | 2019-07-16 | Massachusetts Institute Of Technology | Apparatus and methods for spectroscopy and broadband light emission using two-dimensional plasmon fields |
| US10497682B2 (en) | 2016-01-12 | 2019-12-03 | Apple Inc. | Backplane LED integration and functionalization structures |
| CN109328301B (zh) | 2016-01-28 | 2021-03-12 | 罗斯韦尔生物技术股份有限公司 | 大规模并行dna测序装置 |
| JP7280590B2 (ja) | 2016-01-28 | 2023-05-24 | ロズウェル バイオテクノロジーズ,インコーポレイテッド | 大スケールの分子電子工学センサアレイを使用する被分析物を測定するための方法および装置 |
| JP6854532B2 (ja) | 2016-02-09 | 2021-04-07 | ロズウェル バイオテクノロジーズ,インコーポレイテッド | 電子的、標識フリーのdnaおよびゲノムシークエンシング |
| US10441174B2 (en) | 2016-02-17 | 2019-10-15 | Tesseract Health, Inc. | Sensor and device for lifetime imaging and detection applications |
| US10597767B2 (en) | 2016-02-22 | 2020-03-24 | Roswell Biotechnologies, Inc. | Nanoparticle fabrication |
| EP3433017A4 (en) * | 2016-03-25 | 2020-01-01 | Bioceryx Inc. | DEVICES AND METHODS FOR EVALUATING TARGET SEQUENCES |
| US11579336B2 (en) * | 2016-04-22 | 2023-02-14 | Illumina, Inc. | Photonic structure-based devices and compositions for use in luminescent imaging of multiple sites within a pixel, and methods of using the same |
| US10451518B2 (en) * | 2016-05-10 | 2019-10-22 | Rd2, Llc | All fiber temperature and air density sensor |
| WO2017205868A1 (en) * | 2016-05-27 | 2017-11-30 | Singulex, Inc. | Camera-based single molecule reader |
| US11529213B2 (en) | 2016-05-30 | 2022-12-20 | David Akselrod | Backscatter device-based dental imaging apparatus |
| US11389277B2 (en) | 2016-07-18 | 2022-07-19 | David Akselrod | Material property monitoring using backscatter devices |
| US11226290B2 (en) * | 2016-06-01 | 2022-01-18 | Quantum-Si Incorporated | Photonic structures and integrated device for detecting and analyzing molecules |
| EP3465503B1 (en) * | 2016-06-01 | 2021-09-29 | Quantum-Si Incorporated | Pulse caller and base caller |
| US10758153B2 (en) * | 2016-07-18 | 2020-09-01 | David Akselrod | Material property monitoring and detection using wireless devices |
| US9829456B1 (en) | 2016-07-26 | 2017-11-28 | Roswell Biotechnologies, Inc. | Method of making a multi-electrode structure usable in molecular sensing devices |
| US11386552B2 (en) | 2016-08-01 | 2022-07-12 | Genprime, Inc. | System and method to interpret tests that change color to indicate the presence or non-presence of a compound |
| US10656088B2 (en) * | 2016-08-12 | 2020-05-19 | Silanna UV Technologies Pte Ltd | Ultraviolet biosensor |
| EP3285052A1 (en) | 2016-08-19 | 2018-02-21 | IMEC vzw | Photonic circuit with integrated light coupler |
| CA3037494A1 (en) | 2016-09-23 | 2018-03-29 | Alveo Technologies, Inc. | Methods and compositions for detecting analytes |
| EP4123293A3 (en) * | 2016-11-03 | 2023-04-05 | MGI Tech Co., Ltd. | Biosensor and method of manufacturing the same |
| FR3058521B1 (fr) * | 2016-11-08 | 2021-01-08 | Univ Montpellier | Dispositif et procede de detection de presence de molecules determinees, biocapteur |
| EP3555306B1 (en) * | 2016-12-15 | 2023-01-18 | F. Hoffmann-La Roche AG | Adaptive nanopore signal compression |
| JP2018100959A (ja) * | 2016-12-16 | 2018-06-28 | シャープ株式会社 | 検出器、ならびに、検出器の校正方法、補正方法、検出装置 |
| BR112019012069A2 (pt) | 2016-12-16 | 2019-11-12 | Quantum-Si Incorporated | conjunto de modelagem e direcionamento de feixe compacto |
| CA3047133A1 (en) | 2016-12-16 | 2018-06-21 | Quantum-Si Incorporated | Compact mode-locked laser module |
| BR112019012414A2 (pt) | 2016-12-19 | 2020-02-27 | Quantum-Si Incorporated | Carregamento de moléculas em poços de amostra para análise |
| TWI836905B (zh) | 2016-12-22 | 2024-03-21 | 美商寬騰矽公司 | 具有直接合併像素之整合式光電偵測器 |
| KR102622275B1 (ko) | 2017-01-10 | 2024-01-05 | 로스웰 바이오테크놀로지스 인코포레이티드 | Dna 데이터 저장을 위한 방법들 및 시스템들 |
| WO2018136148A1 (en) | 2017-01-19 | 2018-07-26 | Roswell Biotechnologies, Inc. | Solid state sequencing devices comprising two dimensional layer materials |
| US11419703B2 (en) | 2017-01-27 | 2022-08-23 | David Akselrod | Orthodontic braces and feet orthotics with backscatter based sensors |
| KR101847334B1 (ko) * | 2017-02-02 | 2018-04-10 | 한국기초과학지원연구원 | 형광 이미지 획득 장치 및 방법 |
| GB201701829D0 (en) * | 2017-02-03 | 2017-03-22 | Norwegian Univ Of Science And Tech (Ntnu) | Device |
| US12066434B2 (en) * | 2017-02-08 | 2024-08-20 | Essenlix Corporation | QMAX assays and applications |
| EP3602629B1 (en) * | 2017-03-20 | 2024-07-03 | MGI Tech Co., Ltd. | Biosensors for biological or chemical analysis and methods of manufacturing the same |
| US10508296B2 (en) | 2017-04-25 | 2019-12-17 | Roswell Biotechnologies, Inc. | Enzymatic circuits for molecular sensors |
| KR102692957B1 (ko) | 2017-04-25 | 2024-08-06 | 로스웰 엠이 아이엔씨. | 분자 센서들을 위한 효소 회로들 |
| WO2018204810A1 (en) | 2017-05-05 | 2018-11-08 | Quantum-Si Incorporated | Substrates having modified surface reactivity and antifouling properties in biological reactions |
| EP4023764A3 (en) | 2017-05-09 | 2022-09-21 | Roswell Biotechnologies, Inc. | Binding probe circuits for molecular sensors |
| EP4191236A1 (en) * | 2017-05-23 | 2023-06-07 | Hamamatsu Photonics K.K. | Orientation characteristic measurement method, orientation characteristic measurement program, and orientation characteristic measurement device |
| JP7270254B2 (ja) * | 2017-06-16 | 2023-05-10 | デューク ユニバーシティ | 改善された標識検出、演算、検体感知、および調整可能な乱数生成のための共鳴体ネットワーク |
| CN109103090B (zh) * | 2017-06-21 | 2020-12-04 | 清华大学 | 纳米带的制备方法 |
| KR102083396B1 (ko) * | 2017-06-28 | 2020-03-02 | 주식회사 파나진 | 양자점을 분산광원으로 하는 표적 핵산 검출 방법 |
| CN107390172B (zh) * | 2017-07-17 | 2020-04-28 | 北京大学 | 一种无接触感知定位方法 |
| JP7391828B2 (ja) | 2017-07-24 | 2023-12-05 | クアンタム-エスアイ インコーポレイテッド | 携帯型大規模並列バイオ光電子機器 |
| WO2019023146A1 (en) * | 2017-07-24 | 2019-01-31 | Quantum-Si Incorporated | PHOTONIC STRUCTURES WITH OPTICAL RELEASE |
| CN107402199B (zh) * | 2017-07-31 | 2019-09-10 | 京东方科技集团股份有限公司 | 基因测序芯片及其测序方法以及基因测序装置 |
| WO2019036055A2 (en) | 2017-08-18 | 2019-02-21 | Ignite Biosciences, Inc. | METHODS OF SELECTING BINDING REAGENTS |
| WO2019046589A1 (en) | 2017-08-30 | 2019-03-07 | Roswell Biotechnologies, Inc. | PROCESSIVE ENZYME MOLECULAR ELECTRONIC SENSORS FOR STORING DNA DATA |
| US10784103B2 (en) | 2017-09-19 | 2020-09-22 | Mgi Tech Co., Ltd. | Water level sequencing flow cell fabrication |
| WO2019075100A1 (en) | 2017-10-10 | 2019-04-18 | Roswell Biotechnologies, Inc. | METHODS, APPARATUS AND SYSTEMS FOR STORING DNA DATA WITHOUT AMPLIFICATION |
| EP3501651B1 (en) * | 2017-12-22 | 2024-03-06 | IMEC vzw | Microfluidic routing |
| MX2020007284A (es) * | 2018-01-08 | 2020-09-10 | Quantum Si Inc | Sistema y metodos para la carga electrocinetica de camaras de reaccion a escala submicrometrica. |
| DK3622272T3 (da) * | 2018-01-08 | 2021-11-15 | Illumina Inc | Indretninger til højgennemløbssekventering med halvlederbaseret detektering |
| CN108197052B (zh) * | 2018-01-17 | 2021-02-26 | 上海聚星仪器有限公司 | 一种新型测试测量仪器 |
| BR112020014542A2 (pt) | 2018-01-26 | 2020-12-08 | Quantum-Si Incorporated | Aprendizado de máquina habilitado por aplicação de pulso e de base para dispositivos de sequenciamento |
| IT201800004146A1 (it) * | 2018-03-30 | 2019-09-30 | St Microelectronics Srl | Apparecchio di analisi di molecole tramite rilevamento di segnali fluorescenti e relativo metodo |
| US10965102B2 (en) * | 2018-04-12 | 2021-03-30 | Samsung Electronics Co., Ltd. | Structured light projector and electronic apparatus including the same |
| CN112424587A (zh) | 2018-06-15 | 2021-02-26 | 宽腾矽公司 | 用于具有脉冲光源的先进分析仪器的数据采集控制 |
| EP3581919B1 (en) * | 2018-06-15 | 2022-03-23 | IMEC vzw | An imaging apparatus and a method for imaging an object |
| KR102546320B1 (ko) * | 2018-06-18 | 2023-06-22 | 삼성전자주식회사 | 구조광 프로젝터 및 이를 포함하는 전자 장치 |
| KR20210022688A (ko) | 2018-06-22 | 2021-03-03 | 퀀텀-에스아이 인코포레이티드 | 가변 검출 시간의 전하 저장 빈을 갖는 집적 광검출기 |
| US11619580B2 (en) | 2018-07-23 | 2023-04-04 | The University Of Chicago | Resonator-based ion-selective sensor |
| JP7428701B2 (ja) | 2018-08-29 | 2024-02-06 | クアンタム-エスアイ インコーポレイテッド | サンプルウェル作製技法および集積センサデバイス用の構造 |
| MX2021002414A (es) * | 2018-08-29 | 2021-04-28 | Quantum Si Inc | Sistema y metodos para la deteccion de vida util usando fotodetectores de conteo de fotones. |
| JP6906489B2 (ja) | 2018-09-14 | 2021-07-21 | 株式会社東芝 | ケミカルセンサキット及び分析方法 |
| US11509116B2 (en) * | 2018-10-23 | 2022-11-22 | Analog Photonics LLC | Athermal angular output by combining a laser with a grating based antenna |
| CN111135878B (zh) * | 2018-11-06 | 2021-10-15 | 京东方科技集团股份有限公司 | 微流体通道结构及制作方法、微流体检测装置及使用方法 |
| WO2020094233A1 (de) * | 2018-11-08 | 2020-05-14 | Diamontech Ag | Vorrichtung und verfahren zum analysieren eines stoffs |
| EP3881078A1 (en) | 2018-11-15 | 2021-09-22 | Quantum-Si Incorporated | Methods and compositions for protein sequencing |
| EP3884048A4 (en) | 2018-11-20 | 2022-08-17 | Nautilus Biotechnology, Inc. | DESIGN AND SELECTION OF AFFINITY REAGENTS |
| WO2020142643A1 (en) * | 2019-01-03 | 2020-07-09 | Quantum-Si Incorporated | Optical waveguides and couplers for delivering light to an array of photonic elements |
| TWI687687B (zh) * | 2019-01-11 | 2020-03-11 | 國立中正大學 | 雙光柵感測器、檢測方法及其製備方法 |
| AU2020231492A1 (en) * | 2019-03-05 | 2021-09-16 | Quantum-Si Incorporated | Optical absorption filter for an integrated device |
| KR102306937B1 (ko) * | 2019-03-20 | 2021-09-30 | (주)바이오스퀘어 | 바이오 분석기기 검증용 표준물질 조성물 및 이를 이용한 표준 스트립 |
| WO2020210981A1 (en) | 2019-04-16 | 2020-10-22 | Boe Technology Group Co., Ltd. | Micro-channel device and manufacturing method thereof and micro-fluidic system |
| CN110066723A (zh) * | 2019-05-05 | 2019-07-30 | 京东方科技集团股份有限公司 | 基因测序芯片、设备、制造方法 |
| AU2020294144A1 (en) | 2019-06-14 | 2022-01-27 | Quantum-Si Incorporated | Sliced grating coupler with increased beam alignment sensitivity |
| US11009611B2 (en) | 2019-06-18 | 2021-05-18 | Eagle Technology, Llc | Radiation detection system with surface plasmon resonance detection and related methods |
| US11085878B2 (en) | 2019-06-18 | 2021-08-10 | Eagle Technology, Llc | Radiation detection system with surface plasmon resonance detection and related methods |
| CN110229747A (zh) * | 2019-06-18 | 2019-09-13 | 京东方科技集团股份有限公司 | 基因测序芯片、设备及制备方法 |
| KR20220024702A (ko) | 2019-06-19 | 2022-03-03 | 퀀텀-에스아이 인코포레이티드 | 통합 디바이스를 위한 광학 나노구조 제거기 및 관련 방법들 |
| US11793399B2 (en) | 2019-06-20 | 2023-10-24 | Cilag Gmbh International | Super resolution and color motion artifact correction in a pulsed hyperspectral imaging system |
| US11280737B2 (en) * | 2019-06-20 | 2022-03-22 | Cilag Gmbh International | Super resolution and color motion artifact correction in a pulsed fluorescence imaging system |
| EP3997454A4 (en) * | 2019-07-08 | 2023-07-05 | Illumina, Inc. | WAVEGUIDE INTEGRATION WITH OPTICAL COUPLING STRUCTURES ON A LIGHT DETECTION DEVICE |
| KR20220042449A (ko) | 2019-08-08 | 2022-04-05 | 퀀텀-에스아이 인코포레이티드 | 집적 광학 디바이스들에서의 증가된 방출 수집 효율 |
| US10957731B1 (en) | 2019-10-04 | 2021-03-23 | Visera Technologies Company Limited | Sensor device and method for manufacturing the same |
| US11705472B2 (en) * | 2019-10-10 | 2023-07-18 | Visera Technologies Company Limited | Biosensor and method of distinguishing a light |
| US11630062B2 (en) * | 2019-10-10 | 2023-04-18 | Visera Technologies Company Limited | Biosensor and method of forming the same |
| US11105745B2 (en) * | 2019-10-10 | 2021-08-31 | Visera Technologies Company Limited | Biosensor |
| JP2022551523A (ja) | 2019-10-11 | 2022-12-09 | クアンタム-エスアイ インコーポレイテッド | 気相における表面修飾 |
| KR20220101108A (ko) | 2019-10-29 | 2022-07-19 | 퀀텀-에스아이 인코포레이티드 | 유체의 연동 펌핑 및 연관 방법, 시스템, 및 디바이스 |
| TWI704342B (zh) * | 2019-11-28 | 2020-09-11 | 雷科股份有限公司 | Aoi(自動光學檢測)應用在雷射蝕薄銅線圈的方法及其設備 |
| KR102351249B1 (ko) * | 2020-01-03 | 2022-01-14 | 한국과학기술원 | 분자 다중 이미징 방법 및 장치 |
| US11703454B2 (en) | 2020-01-03 | 2023-07-18 | Korea Advanced Institute Of Science And Technology | Method and apparatus for multiplexed imaging of spectrally-similar fluorophores |
| US11784416B2 (en) * | 2020-01-06 | 2023-10-10 | Raytheon Company | Tunable radio frequency (RF) absorber and thermal heat spreader |
| AU2021208557A1 (en) | 2020-01-14 | 2022-09-01 | Quantum-Si Incorporated | Sensor for lifetime plus spectral characterization |
| WO2021146473A1 (en) | 2020-01-14 | 2021-07-22 | Quantum-Si Incorporated | Integrated sensor for lifetime characterization |
| WO2021150984A1 (en) * | 2020-01-24 | 2021-07-29 | Deepdivebio, Inc. | Optical array qpcr |
| CN111308530B (zh) * | 2020-02-17 | 2021-12-03 | 中国人民解放军战略支援部队信息工程大学 | 一种基于二维波达方向的短波多站和单星协同直接定位方法 |
| EP4111178A1 (en) | 2020-03-02 | 2023-01-04 | Quantum-si Incorporated | Integrated sensor for multi-dimensional signal analysis |
| US20210318238A1 (en) | 2020-04-08 | 2021-10-14 | Quantum-Si Incorporated | Integrated sensor with reduced skew |
| CN111533083B (zh) * | 2020-05-08 | 2023-09-05 | 中北大学 | 一种基于石墨烯的微型分子光镊 |
| EP4143579A2 (en) | 2020-05-20 | 2023-03-08 | Quantum-si Incorporated | Methods and compositions for protein sequencing |
| EP4231174A3 (en) | 2020-06-11 | 2023-11-01 | Nautilus Subsidiary, Inc. | Methods and systems for computational decoding of biological, chemical, and physical entities |
| US20230304932A1 (en) * | 2020-07-23 | 2023-09-28 | Life Technologies Corporation | Compositions, systems and methods for biological analysis involving energy transfer dye conjugates and analytes comprising the same |
| KR102628182B1 (ko) * | 2020-08-28 | 2024-01-24 | 한국과학기술원 | 상호정보량 최소화를 통한 다색 분리 방법 및 장치 |
| EP3961194B1 (en) | 2020-08-25 | 2023-11-08 | Korea Advanced Institute of Science and Technology | Method and apparatus for multiplexed imaging of biomolecules through iterative unmixing of fluorophore signals |
| KR102423723B1 (ko) * | 2020-08-27 | 2022-07-21 | 성균관대학교산학협력단 | 플라즈모닉 우물 기반 핵산 검출장치 및 롤투롤 공정을 이용한 이의 제조방법 |
| GB2599729A (en) * | 2020-10-12 | 2022-04-13 | Sumitomo Chemical Co | Method comprising light emitting marker |
| TWI824273B (zh) * | 2020-12-03 | 2023-12-01 | 仁寶電腦工業股份有限公司 | 天線裝置和配置該天線裝置的方法 |
| CA3203535A1 (en) | 2021-01-21 | 2022-07-28 | Gregory KAPP | Systems and methods for biomolecule preparation |
| CN112837620B (zh) * | 2021-01-22 | 2023-07-04 | 武汉京东方光电科技有限公司 | 柔性显示屏及电子设备 |
| AU2022232933A1 (en) | 2021-03-11 | 2023-09-07 | Nautilus Subsidiary, Inc. | Systems and methods for biomolecule retention |
| DE102021111787A1 (de) * | 2021-05-06 | 2022-11-10 | Gesellschaft für angewandte Mikro- und Optoelektronik mit beschränkter Haftung - AMO GmbH | Verfahren zur Herstellung einer Lochblende, Lochblende sowie Verwendung einer Lochblende in einem optischen Aufbau |
| CN112986206B (zh) * | 2021-05-20 | 2021-07-30 | 北京百奥纳芯生物科技有限公司 | 一种检测基因芯片杂交结果的方法 |
| US11703445B2 (en) * | 2021-05-28 | 2023-07-18 | Visera Technologies Company Limited | Biosensor with grating array |
| WO2023038859A1 (en) | 2021-09-09 | 2023-03-16 | Nautilus Biotechnology, Inc. | Characterization and localization of protein modifications |
| CA3227592A1 (en) | 2021-09-22 | 2023-03-30 | Gregory KAPP | Methods and systems for determining polypeptide interactions |
| EP4416491A1 (en) * | 2021-10-11 | 2024-08-21 | Quantum-Si Incorporated | Light coupling device |
| WO2023081728A1 (en) | 2021-11-03 | 2023-05-11 | Nautilus Biotechnology, Inc. | Systems and methods for surface structuring |
| US20230152211A1 (en) * | 2021-11-11 | 2023-05-18 | California Institute Of Technology | System for Optically Analyzing a Test Sample and Method Therefor |
| US20230184678A1 (en) * | 2021-12-14 | 2023-06-15 | Quantum-Si Incorporated | Methods for loading and data acquisition |
| US11924963B2 (en) | 2022-02-03 | 2024-03-05 | Raytheon Company | Printed-circuit isolation barrier for co-site interference mitigation |
| WO2023164712A2 (en) * | 2022-02-28 | 2023-08-31 | Bio-Rad Laboratories, Inc. | Wide-spectrum analysis system |
| WO2023192162A2 (en) * | 2022-03-29 | 2023-10-05 | Pattern Computer, Inc. | System and method for spectral-based disease detection |
| AU2023241893A1 (en) | 2022-03-29 | 2024-09-26 | Nautilus Subsidiary, Inc. | Integrated arrays for single-analyte processes |
| WO2023250364A1 (en) | 2022-06-21 | 2023-12-28 | Nautilus Subsidiary, Inc. | Method for detecting analytes at sites of optically non-resolvable distances |
| WO2024073599A1 (en) | 2022-09-29 | 2024-04-04 | Nautilus Subsidiary, Inc. | Preparation of array surfaces for single-analyte processes |
| EP4379355A1 (en) * | 2022-11-29 | 2024-06-05 | Gnothis Holding AG | High throughput analysis of single molecule events |
| US20240192202A1 (en) | 2022-12-09 | 2024-06-13 | Nautilus Subsidiary, Inc. | Fluidic media for single-analtye arrays |
| US12109019B2 (en) | 2022-12-15 | 2024-10-08 | Adaptyx Biosciences, Inc. | Systems and methods for analyte detection |
| WO2024130000A1 (en) | 2022-12-15 | 2024-06-20 | Nautilus Subsidiary, Inc. | Inhibition of photon phenomena on single molecule arrays |
| WO2024206122A1 (en) | 2023-03-24 | 2024-10-03 | Nautilus Subsidiary, Inc. | Improved transfer of nanoparticles to array surfaces |
Family Cites Families (197)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5006716A (en) | 1989-02-22 | 1991-04-09 | Research Corporation Technologies, Inc. | Method and system for directional, enhanced fluorescence from molecular layers |
| US5198543A (en) | 1989-03-24 | 1993-03-30 | Consejo Superior Investigaciones Cientificas | PHI29 DNA polymerase |
| US5302509A (en) | 1989-08-14 | 1994-04-12 | Beckman Instruments, Inc. | Method for sequencing polynucleotides |
| CA2044616A1 (en) | 1989-10-26 | 1991-04-27 | Roger Y. Tsien | Dna sequencing |
| JP3018687B2 (ja) * | 1991-12-12 | 2000-03-13 | 松下電器産業株式会社 | 走査型レーザー顕微鏡 |
| US5355215A (en) * | 1992-09-30 | 1994-10-11 | Environmental Research Institute Of Michigan | Method and apparatus for quantitative fluorescence measurements |
| IL108497A0 (en) | 1993-02-01 | 1994-05-30 | Seq Ltd | Methods and apparatus for dna sequencing |
| US5495462A (en) * | 1993-06-18 | 1996-02-27 | Matsushita Electric Industrial Co., Ltd. | Light beam splitting apparatus |
| JP3169742B2 (ja) * | 1993-06-18 | 2001-05-28 | 松下電器産業株式会社 | 光分岐装置および光ディスク装置 |
| JPH07182686A (ja) * | 1993-12-21 | 1995-07-21 | Matsushita Electric Ind Co Ltd | 光モード変換装置および光分岐装置 |
| US5471515A (en) | 1994-01-28 | 1995-11-28 | California Institute Of Technology | Active pixel sensor with intra-pixel charge transfer |
| US6456326B2 (en) | 1994-01-28 | 2002-09-24 | California Institute Of Technology | Single chip camera device having double sampling operation |
| KR970703527A (ko) | 1994-05-27 | 1997-07-03 | 발데그 베르너 | 감쇠 여기되는 발광의 검출법(Process for detecting evanescently excited luminescence) |
| US5912155A (en) | 1994-09-30 | 1999-06-15 | Life Technologies, Inc. | Cloned DNA polymerases from Thermotoga neapolitana |
| US5814565A (en) | 1995-02-23 | 1998-09-29 | University Of Utah Research Foundation | Integrated optic waveguide immunosensor |
| US6261797B1 (en) | 1996-01-29 | 2001-07-17 | Stratagene | Primer-mediated polynucleotide synthesis and manipulation techniques |
| US5990506A (en) | 1996-03-20 | 1999-11-23 | California Institute Of Technology | Active pixel sensors with substantially planarized color filtering elements |
| JP3748571B2 (ja) | 1996-11-18 | 2006-02-22 | ノバルティス アクチエンゲゼルシャフト | 測定装置及びその使用方法 |
| EP1009802B1 (en) | 1997-02-12 | 2004-08-11 | Eugene Y. Chan | Methods for analyzimg polymers |
| EP0983364B1 (en) | 1997-03-12 | 2002-06-12 | PE Corporation (NY) | Dna polymerases having improved labeled nucleotide incorporation properties |
| US6327410B1 (en) | 1997-03-14 | 2001-12-04 | The Trustees Of Tufts College | Target analyte sensors utilizing Microspheres |
| US6825921B1 (en) | 1999-11-10 | 2004-11-30 | Molecular Devices Corporation | Multi-mode light detection system |
| EP0921196A1 (en) | 1997-12-02 | 1999-06-09 | Roche Diagnostics GmbH | Modified DNA-polymerase from carboxydothermus hydrogenoformans and its use for coupled reverse transcription and polymerase chain reaction |
| JPH11173987A (ja) | 1997-12-12 | 1999-07-02 | Hamamatsu Photonics Kk | マイクロタイタビューア |
| DE19810879A1 (de) | 1998-03-13 | 1999-09-16 | Roche Diagnostics Gmbh | Polymerasenchimären |
| CA2325399A1 (en) | 1998-03-23 | 1999-09-30 | Invitrogen Corporation | Modified nucleotides and methods useful for nucleic acid sequencing |
| US7875440B2 (en) | 1998-05-01 | 2011-01-25 | Arizona Board Of Regents | Method of determining the nucleotide sequence of oligonucleotides and DNA molecules |
| JP3813818B2 (ja) | 1998-05-01 | 2006-08-23 | アリゾナ ボード オブ リージェンツ | オリゴヌクレオチドおよびdna分子のヌクレオチド配列の決定方法 |
| GB9810350D0 (en) | 1998-05-14 | 1998-07-15 | Ciba Geigy Ag | Organic compounds |
| JP2000004871A (ja) | 1998-06-29 | 2000-01-11 | Olympus Optical Co Ltd | 培養容器、及び培養容器内の試料を観察する顕微鏡 |
| US6787308B2 (en) | 1998-07-30 | 2004-09-07 | Solexa Ltd. | Arrayed biomolecules and their use in sequencing |
| US6716394B2 (en) | 1998-08-11 | 2004-04-06 | Caliper Technologies Corp. | DNA sequencing using multiple fluorescent labels being distinguishable by their decay times |
| US6210896B1 (en) | 1998-08-13 | 2001-04-03 | Us Genomics | Molecular motors |
| US6280939B1 (en) | 1998-09-01 | 2001-08-28 | Veeco Instruments, Inc. | Method and apparatus for DNA sequencing using a local sensitive force detector |
| US6232075B1 (en) | 1998-12-14 | 2001-05-15 | Li-Cor, Inc. | Heterogeneous assay for pyrophosphate detection |
| US6134002A (en) * | 1999-01-14 | 2000-10-17 | Duke University | Apparatus and method for the rapid spectral resolution of confocal images |
| JP2002537858A (ja) | 1999-03-10 | 2002-11-12 | エーエスエム サイエンティフィック, インコーポレイテッド | 核酸の配列を直接決定するための方法 |
| GB9906929D0 (en) * | 1999-03-26 | 1999-05-19 | Univ Glasgow | Assay system |
| EP1681356B1 (en) | 1999-05-19 | 2011-10-19 | Cornell Research Foundation, Inc. | Method for sequencing nucleic acid molecules |
| US7056661B2 (en) | 1999-05-19 | 2006-06-06 | Cornell Research Foundation, Inc. | Method for sequencing nucleic acid molecules |
| US6137117A (en) | 1999-06-21 | 2000-10-24 | The United States Of America As Represented By The Secretary Of The Navy | Integrating multi-waveguide sensor |
| FR2797053B1 (fr) * | 1999-07-13 | 2001-08-31 | Commissariat Energie Atomique | Support d'analyse a transmission de lumiere de fluorescence |
| US6596483B1 (en) * | 1999-11-12 | 2003-07-22 | Motorola, Inc. | System and method for detecting molecules using an active pixel sensor |
| US6399335B1 (en) | 1999-11-16 | 2002-06-04 | Advanced Research And Technology Institute, Inc. | γ-phosphoester nucleoside triphosphates |
| WO2001043875A1 (de) * | 1999-12-17 | 2001-06-21 | Zeptosens Ag | Flusszellenanordnung und deren verwendung zur multianalytbestimmung |
| JP3978307B2 (ja) * | 2000-02-09 | 2007-09-19 | 株式会社日立製作所 | 紫外レーザ光発生装置並びに欠陥検査装置およびその方法 |
| AU2001249237A1 (en) * | 2000-03-16 | 2001-09-24 | Spectrumedix Corporation | Multi-wavelength array reader for biological assay |
| EP1285290A1 (en) * | 2000-04-28 | 2003-02-26 | Edgelight Biosciences, Inc. | Micro-array evanescent wave fluorescence detection device |
| US6917726B2 (en) * | 2001-09-27 | 2005-07-12 | Cornell Research Foundation, Inc. | Zero-mode clad waveguides for performing spectroscopy with confined effective observation volumes |
| US6936702B2 (en) | 2000-06-07 | 2005-08-30 | Li-Cor, Inc. | Charge-switch nucleotides |
| JP2004516810A (ja) | 2000-06-07 | 2004-06-10 | リ−コール インコーポレーティッド | 電荷スイッチヌクレオチド |
| WO2002001194A1 (en) | 2000-06-25 | 2002-01-03 | Affymetrix, Inc. | Optically active substrates |
| US7277166B2 (en) | 2000-08-02 | 2007-10-02 | Honeywell International Inc. | Cytometer analysis cartridge optical configuration |
| FR2813121A1 (fr) | 2000-08-21 | 2002-02-22 | Claude Weisbuch | Dispositif perfectionne de support d'elements chromophores |
| AU2001286963A1 (en) | 2000-08-30 | 2002-03-13 | University Of Rochester | Method of performing reverse transcription reaction using reverse transcriptase encoded by non-ltr retrotransposable element |
| WO2002023167A1 (en) | 2000-09-11 | 2002-03-21 | The Government Of The United States Of America, As Represented By The Secretary Of The Navy | Fluidics system |
| WO2002034944A1 (en) | 2000-10-23 | 2002-05-02 | Dia Chip Limited | High precision and intellectual biochip arrayer having function of respotting |
| JP3695340B2 (ja) * | 2001-03-30 | 2005-09-14 | 株式会社日立製作所 | Dna検査方法及びその装置並びに蛍光検出方法 |
| US20040259082A1 (en) | 2001-04-24 | 2004-12-23 | Li-Cor, Inc. | Polymerases with charge-switch activity and methods of generating such polymers |
| US7244566B2 (en) | 2001-08-29 | 2007-07-17 | Ge Healthcare Bio-Sciences Corp. | Analyte detection |
| US7223541B2 (en) | 2001-08-29 | 2007-05-29 | Ge Healthcare Bio-Sciences Corp. | Terminal-phosphate-labeled nucleotides and methods of use |
| US7052839B2 (en) | 2001-08-29 | 2006-05-30 | Amersham Biosciences Corp | Terminal-phosphate-labeled nucleotides and methods of use |
| US7033762B2 (en) | 2001-08-29 | 2006-04-25 | Amersham Biosciences Corp | Single nucleotide amplification and detection by polymerase |
| DE60235376D1 (de) | 2001-08-29 | 2010-04-01 | Ge Healthcare Bio Sciences | Markierte nukleosidpolyphosphate |
| US7727722B2 (en) | 2001-08-29 | 2010-06-01 | General Electric Company | Ligation amplification |
| US7256019B2 (en) | 2001-08-29 | 2007-08-14 | Ge Healthcare Bio-Sciences Corp. | Terminal phosphate blocked nucleoside polyphosphates |
| ATE528117T1 (de) * | 2001-08-30 | 2011-10-15 | Bayer Technology Services Gmbh | Verfahren zur herstellung von abformkörpern, insbesondere optischen strukturen, und deren verwendung |
| US20070020622A1 (en) | 2001-09-14 | 2007-01-25 | Invitrogen Corporation | DNA Polymerases and mutants thereof |
| US7057026B2 (en) | 2001-12-04 | 2006-06-06 | Solexa Limited | Labelled nucleotides |
| US7179654B2 (en) | 2002-03-18 | 2007-02-20 | Agilent Technologies, Inc. | Biochemical assay with programmable array detection |
| US6924887B2 (en) | 2002-03-27 | 2005-08-02 | Sarnoff Corporation | Method and apparatus for generating charge from a light pulse |
| US7595883B1 (en) | 2002-09-16 | 2009-09-29 | The Board Of Trustees Of The Leland Stanford Junior University | Biological analysis arrangement and approach therefor |
| EP1592779A4 (en) | 2003-02-05 | 2007-12-12 | Ge Healthcare Bio Sciences | NUCLEOTIDES BRANDED BY TERMINAL PHOSPHATES, HAVING NEW LINKS |
| WO2004092331A2 (en) | 2003-04-08 | 2004-10-28 | Li-Cor, Inc. | Composition and method for nucleic acid sequencing |
| US20040258563A1 (en) * | 2003-06-23 | 2004-12-23 | Applera Corporation | Caps for sample wells and microcards for biological materials |
| WO2005016526A2 (en) * | 2003-08-04 | 2005-02-24 | Irm, Llc | Multi-well container positioning devices and related systems and methods |
| WO2005073407A1 (en) * | 2003-10-07 | 2005-08-11 | Ut-Battelle, Llc | Advanced integrated circuit biochip |
| US7169560B2 (en) | 2003-11-12 | 2007-01-30 | Helicos Biosciences Corporation | Short cycle methods for sequencing polynucleotides |
| US20070281288A1 (en) | 2004-01-27 | 2007-12-06 | Shimshon Belkin | Method and System for Detecting Analytes |
| US7981604B2 (en) | 2004-02-19 | 2011-07-19 | California Institute Of Technology | Methods and kits for analyzing polynucleotide sequences |
| US7462452B2 (en) | 2004-04-30 | 2008-12-09 | Pacific Biosciences Of California, Inc. | Field-switch sequencing |
| US7351538B2 (en) * | 2004-08-23 | 2008-04-01 | U.S. Genomics | Systems and methods for detecting and analyzing polymers |
| WO2006044078A2 (en) | 2004-09-17 | 2006-04-27 | Pacific Biosciences Of California, Inc. | Apparatus and method for analysis of molecules |
| US7170050B2 (en) | 2004-09-17 | 2007-01-30 | Pacific Biosciences Of California, Inc. | Apparatus and methods for optical analysis of molecules |
| US7345764B2 (en) | 2005-02-07 | 2008-03-18 | Vladimir Bulovic | Apparatus and method for a slim format spectrometer |
| US20060223067A1 (en) | 2005-03-31 | 2006-10-05 | Paolo Vatta | Mutant DNA polymerases and methods of use |
| US7738086B2 (en) | 2005-05-09 | 2010-06-15 | The Trustees Of Columbia University In The City Of New York | Active CMOS biosensor chip for fluorescent-based detection |
| CN100401041C (zh) * | 2005-06-09 | 2008-07-09 | 上海交通大学 | 光波导吸收式气体传感器及测量系统 |
| JP2008546424A (ja) | 2005-06-28 | 2008-12-25 | アジェンコート パーソナル ジェノミクス コーポレイション | 修飾ポリヌクレオチドを作製する方法および配列決定する方法 |
| WO2007045998A2 (en) | 2005-07-01 | 2007-04-26 | Dako Denmark A/S | New nucleic acid base pairs |
| US7426322B2 (en) | 2005-07-20 | 2008-09-16 | Searete Llc. | Plasmon photocatalysis |
| EP1913392A4 (en) * | 2005-08-02 | 2010-03-10 | Univ Utah Res Found | BIOSENSORS WITH METALLIC NANOCONITIES |
| US20160355869A1 (en) * | 2005-08-02 | 2016-12-08 | University Of Utah Research Foundation | Biosensors including metallic nanocavities |
| US7453916B2 (en) * | 2005-09-08 | 2008-11-18 | Intel Corporation | High throughput optical micro-array reader capable of variable pitch and spot size array processing for genomics and proteomics |
| US7405281B2 (en) | 2005-09-29 | 2008-07-29 | Pacific Biosciences Of California, Inc. | Fluorescent nucleotide analogs and uses therefor |
| TWI296044B (en) * | 2005-11-03 | 2008-04-21 | Ind Tech Res Inst | Coupled waveguide-surface plasmon resonance biosensor |
| WO2007070572A2 (en) | 2005-12-12 | 2007-06-21 | The Government Of The United States Of America, As Represented By The Secretary Of The Department Of Health And Human Services | Probe for nucleic acid sequencing and methods of use |
| EP3056575B1 (en) | 2005-12-22 | 2017-10-11 | Pacific Biosciences Of California, Inc. | Polymerases for nucleotide analogue incorporation |
| EP1963530B1 (en) | 2005-12-22 | 2011-07-27 | Pacific Biosciences of California, Inc. | Active surface coupled polymerases |
| US7692783B2 (en) | 2006-02-13 | 2010-04-06 | Pacific Biosciences Of California | Methods and systems for simultaneous real-time monitoring of optical signals from multiple sources |
| US7995202B2 (en) | 2006-02-13 | 2011-08-09 | Pacific Biosciences Of California, Inc. | Methods and systems for simultaneous real-time monitoring of optical signals from multiple sources |
| US7715001B2 (en) | 2006-02-13 | 2010-05-11 | Pacific Biosciences Of California, Inc. | Methods and systems for simultaneous real-time monitoring of optical signals from multiple sources |
| US8975216B2 (en) | 2006-03-30 | 2015-03-10 | Pacific Biosciences Of California | Articles having localized molecules disposed thereon and methods of producing same |
| US20080050747A1 (en) | 2006-03-30 | 2008-02-28 | Pacific Biosciences Of California, Inc. | Articles having localized molecules disposed thereon and methods of producing and using same |
| US7750316B2 (en) * | 2006-05-10 | 2010-07-06 | Dublin City University | Polymer biochip for detecting fluorescence |
| DE102006030541B4 (de) | 2006-06-23 | 2010-05-12 | Fraunhofer-Gesellschaft zur Förderung der angewandten Forschung e.V. | Optische Anordnung |
| US8207509B2 (en) | 2006-09-01 | 2012-06-26 | Pacific Biosciences Of California, Inc. | Substrates, systems and methods for analyzing materials |
| AU2007289057C1 (en) | 2006-09-01 | 2014-01-16 | Pacific Biosciences Of California, Inc. | Substrates, systems and methods for analyzing materials |
| AU2007309504B2 (en) | 2006-10-23 | 2012-09-13 | Pacific Biosciences Of California, Inc. | Polymerase enzymes and reagents for enhanced nucleic acid sequencing |
| FR2908888B1 (fr) | 2006-11-21 | 2012-08-03 | Centre Nat Rech Scient | Dispositif pour la detection exaltee de l'emission d'une particule cible |
| WO2008114148A2 (en) | 2007-03-22 | 2008-09-25 | Universite Louis Pasteur | Device for sorting and concentrating electromagnetic energy and apparatus comprising at least one such device |
| US20080241866A1 (en) | 2007-03-30 | 2008-10-02 | Pacific Biosciences Of California, Inc. | Systems and methods for enhancing fluorescent signals |
| JP5222599B2 (ja) * | 2007-07-20 | 2013-06-26 | 株式会社日立ハイテクノロジーズ | 核酸分析デバイス及びそれを用いた核酸分析装置 |
| JP2009022247A (ja) * | 2007-07-23 | 2009-02-05 | Toshiba Corp | 培養容器及び培養組織回収方法 |
| US9410892B2 (en) * | 2007-08-30 | 2016-08-09 | Cornell University | Nanoscale optofluidic devices for molecular detection |
| WO2009038791A1 (en) * | 2007-09-18 | 2009-03-26 | Applied Biosystems Inc. | Methods, systems and apparatus for light concentrating mechanisms |
| US7873085B2 (en) | 2007-10-23 | 2011-01-18 | Andrei Babushkin | Method and device for controlling optical output of laser diode |
| GB0723725D0 (en) | 2007-12-05 | 2008-01-16 | Ge Healthcare Uk Ltd | Apparatus and method for detecting dna damage |
| WO2009082706A1 (en) | 2007-12-21 | 2009-07-02 | The Trustees Of Columbia University In The City Of New York | Active cmos sensor array for electrochemical biomolecular detection |
| US20110165652A1 (en) | 2008-01-14 | 2011-07-07 | Life Technologies Corporation | Compositions, methods and systems for single molecule sequencing |
| AU2009212165A1 (en) | 2008-02-07 | 2009-08-13 | Pacific Biosciences Of California, Inc. | CIS reactive oxygen quenchers integrated into linkers |
| US8652781B2 (en) | 2008-02-12 | 2014-02-18 | Pacific Biosciences Of California, Inc. | Cognate sampling kinetics |
| US8530164B2 (en) | 2008-09-05 | 2013-09-10 | Pacific Biosciences Of California, Inc. | Method for sequencing using branching fraction of incorporatable nucleotides |
| EP2255014A4 (en) | 2008-02-12 | 2011-05-18 | Pacific Biosciences California | COMPOSITIONS AND METHODS FOR USE IN ANALYTICAL REACTIONS |
| US7968702B2 (en) | 2008-03-13 | 2011-06-28 | Pacific Biosciences Of California, Inc. | Labeled reactants and their uses |
| US7973146B2 (en) | 2008-03-26 | 2011-07-05 | Pacific Biosciences Of California, Inc. | Engineered fluorescent dye labeled nucleotide analogs for DNA sequencing |
| CA2991818C (en) | 2008-03-28 | 2022-10-11 | Pacific Biosciences Of California, Inc. | Compositions and methods for nucleic acid sequencing |
| US8143030B2 (en) | 2008-09-24 | 2012-03-27 | Pacific Biosciences Of California, Inc. | Intermittent detection during analytical reactions |
| US8236499B2 (en) | 2008-03-28 | 2012-08-07 | Pacific Biosciences Of California, Inc. | Methods and compositions for nucleic acid sample preparation |
| US8999676B2 (en) | 2008-03-31 | 2015-04-07 | Pacific Biosciences Of California, Inc. | Recombinant polymerases for improved single molecule sequencing |
| WO2009145820A2 (en) | 2008-03-31 | 2009-12-03 | Pacific Biosciences Of California, Inc. | Generation of modified polymerases for improved accuracy in single molecule sequencing |
| US8420366B2 (en) | 2008-03-31 | 2013-04-16 | Pacific Biosciences Of California, Inc. | Generation of modified polymerases for improved accuracy in single molecule sequencing |
| EP2274446B1 (en) | 2008-03-31 | 2015-09-09 | Pacific Biosciences of California, Inc. | Two slow-step polymerase enzyme systems and methods |
| EP2286217B1 (en) | 2008-03-31 | 2015-02-18 | Pacific Biosciences of California, Inc. | Single molecule loading methods and compositions |
| US9127259B2 (en) | 2008-03-31 | 2015-09-08 | Pacific Biosciences Of California, Inc. | Enzymes resistant to photodamage |
| US10114213B2 (en) | 2008-04-04 | 2018-10-30 | Cvi Laser, Llc | Laser systems and optical devices for manipulating laser beams |
| JP5268444B2 (ja) * | 2008-06-23 | 2013-08-21 | 株式会社日立ハイテクノロジーズ | 単分子リアルタイムシーケンス装置,核酸分析装置及び単分子リアルタイムシーケンス方法 |
| EP2148187A1 (de) * | 2008-07-25 | 2010-01-27 | Roche Diagnostics GmbH | Anregungs- und Abbildungsoptik für die Fluoreszenzdetektion |
| US7999454B2 (en) * | 2008-08-14 | 2011-08-16 | Global Oled Technology Llc | OLED device with embedded chip driving |
| FR2936099A1 (fr) * | 2008-09-12 | 2010-03-19 | Thales Sa | Dispositif de detection d'images ameliore pour un imageur multispectral et imageur multispectral comportant ce dispositif |
| AU2009292629B2 (en) | 2008-09-16 | 2014-03-20 | Pacific Biosciences Of California, Inc. | Substrates and optical systems and methods of use thereof |
| US8921046B2 (en) | 2008-09-19 | 2014-12-30 | Pacific Biosciences Of California, Inc. | Nucleic acid sequence analysis |
| US8481264B2 (en) | 2008-09-19 | 2013-07-09 | Pacific Biosciences Of California, Inc. | Immobilized nucleic acid complexes for sequence analysis |
| US9156010B2 (en) | 2008-09-23 | 2015-10-13 | Bio-Rad Laboratories, Inc. | Droplet-based assay system |
| US8383369B2 (en) | 2008-09-24 | 2013-02-26 | Pacific Biosciences Of California, Inc. | Intermittent detection during analytical reactions |
| AU2009300369B2 (en) | 2008-09-30 | 2014-08-14 | Pacific Biosciences Of California, Inc. | Ultra-high multiplex analytical systems and methods |
| EP2182523B1 (en) | 2008-10-31 | 2013-01-09 | CSEM Centre Suisse d'Electronique et de Microtechnique SA -Recherche et Développement | Charge sampling device and method based on a MOS-transmission line |
| KR101045206B1 (ko) * | 2008-10-31 | 2011-06-30 | 삼성전자주식회사 | 여기광 흡수 도파로가 삽입된 집적된 바이오칩 및 그 제조방법 |
| KR101065077B1 (ko) * | 2008-11-05 | 2011-09-15 | 삼성전자주식회사 | 시료 검출용 기판, 이를 채용한 바이오칩, 시료 검출용 기판의 제조방법 및 바이오 물질 검출장치 |
| US8367813B2 (en) | 2008-11-17 | 2013-02-05 | Pacific Biosciences Of California, Inc. | Phospholink nucleotides for sequencing applications |
| CN102482330A (zh) | 2009-01-30 | 2012-05-30 | 牛津纳米孔技术有限公司 | 酶突变体 |
| US8921280B2 (en) * | 2009-02-11 | 2014-12-30 | Samsung Electronics Co., Ltd. | Integrated bio-chip and method of fabricating the integrated bio-chip |
| US8603792B2 (en) | 2009-03-27 | 2013-12-10 | Life Technologies Corporation | Conjugates of biomolecules to nanoparticles |
| WO2010117420A2 (en) | 2009-03-30 | 2010-10-14 | Pacific Biosciences Of California, Inc. | Fret-labeled compounds and uses therefor |
| JP5707030B2 (ja) * | 2009-04-02 | 2015-04-22 | 株式会社日立ハイテクノロジーズ | 核酸分析デバイス、及び核酸分析装置 |
| US8501406B1 (en) | 2009-07-14 | 2013-08-06 | Pacific Biosciences Of California, Inc. | Selectively functionalized arrays |
| JP5462548B2 (ja) * | 2009-08-12 | 2014-04-02 | 株式会社日立ハイテクノロジーズ | 核酸分析素子及びそれを用いた核酸分析装置 |
| WO2011040971A2 (en) | 2009-09-30 | 2011-04-07 | Pacific Biosciences Of California, Inc. | Generation of modified polymerases for improved accuracy in single molecule sequencing |
| US8278728B2 (en) | 2009-10-17 | 2012-10-02 | Florida Institute Of Technology | Array of concentric CMOS photodiodes for detection and de-multiplexing of spatially modulated optical channels |
| US9579402B2 (en) | 2009-12-04 | 2017-02-28 | Biotium, Inc. | Heterocycle-substituted xanthene dyes |
| JP6017107B2 (ja) | 2009-12-28 | 2016-10-26 | ソニー株式会社 | イメージセンサ及びその製造方法、並びにセンサデバイス |
| US20110236983A1 (en) | 2009-12-29 | 2011-09-29 | Joseph Beechem | Single molecule detection and sequencing using fluorescence lifetime imaging |
| US8994946B2 (en) | 2010-02-19 | 2015-03-31 | Pacific Biosciences Of California, Inc. | Integrated analytical system and method |
| EP4378584A2 (en) | 2010-02-19 | 2024-06-05 | Pacific Biosciences Of California, Inc. | Integrated analytical system and method for fluorescence measurement |
| US9482615B2 (en) * | 2010-03-15 | 2016-11-01 | Industrial Technology Research Institute | Single-molecule detection system and methods |
| TWI466278B (zh) | 2010-04-06 | 2014-12-21 | Kingpak Tech Inc | 晶圓級影像感測器構裝結構及其製造方法 |
| US8865077B2 (en) | 2010-06-11 | 2014-10-21 | Industrial Technology Research Institute | Apparatus for single-molecule detection |
| US8865078B2 (en) | 2010-06-11 | 2014-10-21 | Industrial Technology Research Institute | Apparatus for single-molecule detection |
| EP2439512A1 (en) * | 2010-10-01 | 2012-04-11 | Aqsens Oy | A device for holding a sample |
| EP2647060A2 (en) | 2010-11-30 | 2013-10-09 | Tshwane University Of Technology | Cmos based micro-photonic systems |
| EP2646154A2 (en) | 2010-11-30 | 2013-10-09 | Quantumdx Group Limited | The design, fabrication and use of a microfluidics multitemperature flexible reaction device |
| EP2689028B1 (en) | 2011-03-23 | 2017-08-30 | Pacific Biosciences Of California, Inc. | Isolation of polymerase-nucleic acid complexes and loading onto substrates |
| JP2013045857A (ja) | 2011-08-24 | 2013-03-04 | Sony Corp | イメージセンサ及びその製造方法並びに検査装置 |
| FR2982028B1 (fr) * | 2011-10-26 | 2020-02-21 | Aryballe Technologies | Puce microstructuree comprenant des surfaces convexes pour analyse par resonance des plasmons de surface, dispositif d'analyse contenant ladite puce microstructuree et utilisation dudit dispositif |
| AU2012328662B2 (en) | 2011-10-28 | 2015-12-17 | Illumina, Inc. | Microarray fabrication system and method |
| US9606060B2 (en) | 2012-01-13 | 2017-03-28 | California Institute Of Technology | Filterless time-domain detection of one or more fluorophores |
| US8906660B2 (en) | 2012-02-01 | 2014-12-09 | Pacific Biosciences Of California, Inc. | Recombinant polymerases with increased phototolerance |
| WO2013123258A1 (en) | 2012-02-15 | 2013-08-22 | Pacific Biosciences Of California, Inc. | Polymerase enzyme substrates with protein shield |
| CA2867489A1 (en) * | 2012-03-30 | 2013-10-03 | Pacific Biosciences Of California, Inc. | Methods and composition for sequencing modified nucleic acids |
| EP2836821B1 (en) * | 2012-04-10 | 2018-09-26 | The Trustees of Princeton University | Ultra-sensitive sensor |
| WO2013171197A1 (en) * | 2012-05-15 | 2013-11-21 | Ait Austrian Institute Of Technology Gmbh | Compact plasmon-enhanced fluorescence biosensor |
| US9372308B1 (en) * | 2012-06-17 | 2016-06-21 | Pacific Biosciences Of California, Inc. | Arrays of integrated analytical devices and methods for production |
| US8654427B1 (en) | 2012-08-31 | 2014-02-18 | Rosemount Aerospace Inc. | Ruggedized two-axis optical beam steering device |
| EP2936222B1 (en) | 2012-12-18 | 2019-07-03 | Pacific Biosciences Of California, Inc. | An optical analytical device |
| US9624540B2 (en) * | 2013-02-22 | 2017-04-18 | Pacific Biosciences Of California, Inc. | Integrated illumination of optical analytical devices |
| US10933417B2 (en) | 2013-03-15 | 2021-03-02 | Nanobiosym, Inc. | Systems and methods for mobile device analysis of nucleic acids and proteins |
| US9654680B2 (en) * | 2013-10-17 | 2017-05-16 | Canon Kabushiki Kaisha | Image capturing apparatus and control method therefor |
| KR102240166B1 (ko) | 2013-11-17 | 2021-04-14 | 퀀텀-에스아이 인코포레이티드 | 분자들을 프로빙 검출 및 분석하기 위한 외부 광원을 구비한 통합 디바이스 |
| US9765395B2 (en) | 2014-04-28 | 2017-09-19 | Nanomedical Diagnostics, Inc. | System and method for DNA sequencing and blood chemistry analysis |
| CN112903638A (zh) | 2014-08-08 | 2021-06-04 | 宽腾矽公司 | 用于对分子进行探测、检测和分析的带外部光源的集成装置 |
| MX2021007934A (es) | 2014-08-08 | 2023-01-17 | Quantum Si Inc | Dispositivo integrado para el depósito temporal de fotones recibidos. |
| US9921157B2 (en) * | 2014-08-08 | 2018-03-20 | Quantum-Si Incorporated | Optical system and assay chip for probing, detecting and analyzing molecules |
| US9666748B2 (en) | 2015-01-14 | 2017-05-30 | International Business Machines Corporation | Integrated on chip detector and zero waveguide module structure for use in DNA sequencing |
| WO2016149397A1 (en) | 2015-03-16 | 2016-09-22 | Pacific Biosciences Of California, Inc. | Integrated devices and systems for free-space optical coupling |
| US10605730B2 (en) | 2015-05-20 | 2020-03-31 | Quantum-Si Incorporated | Optical sources for fluorescent lifetime analysis |
| US10246742B2 (en) | 2015-05-20 | 2019-04-02 | Quantum-Si Incorporated | Pulsed laser and bioanalytic system |
| JP7391828B2 (ja) | 2017-07-24 | 2023-12-05 | クアンタム-エスアイ インコーポレイテッド | 携帯型大規模並列バイオ光電子機器 |
-
2014
- 2014-11-17 KR KR1020167016350A patent/KR102240166B1/ko active IP Right Grant
- 2014-11-17 CN CN201480073394.1A patent/CN105917003A/zh active Pending
- 2014-11-17 AU AU2014348302A patent/AU2014348302B2/en active Active
- 2014-11-17 EP EP14812050.4A patent/EP3074531B1/en active Active
- 2014-11-17 EP EP14809194.5A patent/EP3068900B1/en active Active
- 2014-11-17 BR BR112016011061-7A patent/BR112016011061B1/pt active IP Right Grant
- 2014-11-17 CA CA2930834A patent/CA2930834A1/en active Pending
- 2014-11-17 EP EP20150539.3A patent/EP3715831A1/en not_active Withdrawn
- 2014-11-17 CN CN201480073505.9A patent/CN105980580B/zh active Active
- 2014-11-17 MX MX2016006454A patent/MX2016006454A/es unknown
- 2014-11-17 KR KR1020167016349A patent/KR102296713B1/ko active IP Right Grant
- 2014-11-17 US US14/543,888 patent/US9983135B2/en active Active
- 2014-11-17 BR BR112016011084A patent/BR112016011084B8/pt active IP Right Grant
- 2014-11-17 WO PCT/US2014/066014 patent/WO2015074005A1/en active Application Filing
- 2014-11-17 JP JP2016554540A patent/JP6573899B2/ja active Active
- 2014-11-17 MX MX2016006455A patent/MX2016006455A/es unknown
- 2014-11-17 JP JP2016554541A patent/JP2016537999A/ja active Pending
- 2014-11-17 US US14/543,865 patent/US10048208B2/en active Active
- 2014-11-17 CN CN201480073365.5A patent/CN106029904A/zh active Pending
- 2014-11-17 CA CA2930832A patent/CA2930832A1/en not_active Abandoned
- 2014-11-17 BR BR112016011052-8A patent/BR112016011052B1/pt active IP Right Grant
- 2014-11-17 EP EP21203429.2A patent/EP3974814A1/en not_active Withdrawn
- 2014-11-17 CN CN202010074109.5A patent/CN111235246B/zh active Active
- 2014-11-17 EP EP14812051.2A patent/EP3068901B1/en active Active
- 2014-11-17 MX MX2016006453A patent/MX2016006453A/es unknown
- 2014-11-17 CN CN201910752352.5A patent/CN110452809B/zh active Active
- 2014-11-17 WO PCT/US2014/066010 patent/WO2015074001A1/en active Application Filing
- 2014-11-17 EP EP20150534.4A patent/EP3709003A1/en not_active Withdrawn
- 2014-11-17 KR KR1020217005386A patent/KR102399962B1/ko active IP Right Grant
- 2014-11-17 KR KR1020167016352A patent/KR102221637B1/ko active IP Right Grant
- 2014-11-17 MX MX2020013247A patent/MX2020013247A/es unknown
- 2014-11-17 JP JP2016554539A patent/JP6673843B2/ja active Active
- 2014-11-17 WO PCT/US2014/066013 patent/WO2015074004A1/en active Application Filing
- 2014-11-17 AU AU2014348306A patent/AU2014348306B2/en active Active
- 2014-11-17 CA CA2930836A patent/CA2930836A1/en active Pending
- 2014-11-17 US US14/543,867 patent/US9863880B2/en active Active
- 2014-11-17 AU AU2014348305A patent/AU2014348305B2/en active Active
-
2017
- 2017-11-10 US US15/808,940 patent/US10533945B2/en active Active
-
2018
- 2018-04-24 US US15/960,751 patent/US10712273B2/en active Active
- 2018-05-09 US US15/974,826 patent/US10712274B2/en active Active
- 2018-07-05 US US16/028,159 patent/US11428635B2/en active Active
-
2019
- 2019-11-19 US US16/689,004 patent/US11287382B2/en active Active
-
2020
- 2020-03-05 JP JP2020037466A patent/JP7015336B2/ja active Active
- 2020-12-11 AU AU2020286308A patent/AU2020286308B2/en active Active
-
2021
- 2021-02-08 JP JP2021018615A patent/JP7242727B2/ja active Active
-
2022
- 2022-02-18 US US17/676,070 patent/US20220170861A1/en active Pending
- 2022-03-25 US US17/704,691 patent/US20220214279A1/en active Pending
- 2022-07-29 US US17/877,837 patent/US20220364996A1/en active Pending
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| AU2020286308B2 (en) | Optical system and assay chip for probing, detecting and analyzing molecules | |
| CN106796175B (zh) | 用于探测、检测和分析分子的光学系统和检测芯片 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| B06U | Preliminary requirement: requests with searches performed by other patent offices: procedure suspended [chapter 6.21 patent gazette] | ||
| B09A | Decision: intention to grant [chapter 9.1 patent gazette] | ||
| B16A | Patent or certificate of addition of invention granted [chapter 16.1 patent gazette] |
Free format text: PRAZO DE VALIDADE: 20 (VINTE) ANOS CONTADOS A PARTIR DE 17/11/2014, OBSERVADAS AS CONDICOES LEGAIS. |