JP2010012331A - ヒト間葉幹細胞分化の系列指向誘導 - Google Patents
ヒト間葉幹細胞分化の系列指向誘導 Download PDFInfo
- Publication number
- JP2010012331A JP2010012331A JP2009242480A JP2009242480A JP2010012331A JP 2010012331 A JP2010012331 A JP 2010012331A JP 2009242480 A JP2009242480 A JP 2009242480A JP 2009242480 A JP2009242480 A JP 2009242480A JP 2010012331 A JP2010012331 A JP 2010012331A
- Authority
- JP
- Japan
- Prior art keywords
- cells
- composition according
- factor
- mesenchymal stem
- mscs
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
- 210000002901 mesenchymal stem cell Anatomy 0.000 title claims abstract description 188
- 241000282414 Homo sapiens Species 0.000 title claims abstract description 48
- 230000006698 induction Effects 0.000 title abstract description 7
- 230000024245 cell differentiation Effects 0.000 title description 5
- 239000000203 mixture Substances 0.000 claims abstract description 58
- 230000004069 differentiation Effects 0.000 claims abstract description 51
- 230000000975 bioactive effect Effects 0.000 claims abstract description 32
- 210000001185 bone marrow Anatomy 0.000 claims description 87
- 210000000988 bone and bone Anatomy 0.000 claims description 42
- 230000015572 biosynthetic process Effects 0.000 claims description 20
- 210000001789 adipocyte Anatomy 0.000 claims description 18
- 210000000845 cartilage Anatomy 0.000 claims description 18
- 230000011164 ossification Effects 0.000 claims description 17
- UREBDLICKHMUKA-CXSFZGCWSA-N dexamethasone Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(F)[C@@H]1[C@@H]1C[C@@H](C)[C@@](C(=O)CO)(O)[C@@]1(C)C[C@@H]2O UREBDLICKHMUKA-CXSFZGCWSA-N 0.000 claims description 15
- 230000002648 chondrogenic effect Effects 0.000 claims description 14
- 229960003957 dexamethasone Drugs 0.000 claims description 14
- 230000009818 osteogenic differentiation Effects 0.000 claims description 9
- 108090000623 proteins and genes Proteins 0.000 claims description 9
- 102000003974 Fibroblast growth factor 2 Human genes 0.000 claims description 8
- 108090000379 Fibroblast growth factor 2 Proteins 0.000 claims description 8
- 230000012010 growth Effects 0.000 claims description 8
- 230000001939 inductive effect Effects 0.000 claims description 8
- 102000004169 proteins and genes Human genes 0.000 claims description 7
- 230000000921 morphogenic effect Effects 0.000 claims description 6
- 108010007726 Bone Morphogenetic Proteins Proteins 0.000 claims description 5
- 102000007350 Bone Morphogenetic Proteins Human genes 0.000 claims description 5
- 102000004125 Interleukin-1alpha Human genes 0.000 claims description 5
- 108010082786 Interleukin-1alpha Proteins 0.000 claims description 5
- 102000004887 Transforming Growth Factor beta Human genes 0.000 claims description 5
- 108090001012 Transforming Growth Factor beta Proteins 0.000 claims description 5
- 229940112869 bone morphogenetic protein Drugs 0.000 claims description 5
- 230000022379 skeletal muscle tissue development Effects 0.000 claims description 5
- 210000002435 tendon Anatomy 0.000 claims description 5
- ZRKFYGHZFMAOKI-QMGMOQQFSA-N tgfbeta Chemical compound C([C@H](NC(=O)[C@H](C(C)C)NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](CC(C)C)NC(=O)CNC(=O)[C@H](C)NC(=O)[C@H](CO)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@@H](NC(=O)[C@H](C)NC(=O)[C@H](C)NC(=O)[C@@H](NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](N)CCSC)C(C)C)[C@@H](C)CC)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](C)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](C)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](C)C(=O)N[C@@H](CC(C)C)C(=O)N1[C@@H](CCC1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(C)C)C(O)=O)C1=CC=C(O)C=C1 ZRKFYGHZFMAOKI-QMGMOQQFSA-N 0.000 claims description 5
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 claims description 4
- 102000008186 Collagen Human genes 0.000 claims description 4
- 108010035532 Collagen Proteins 0.000 claims description 4
- 230000022159 cartilage development Effects 0.000 claims description 4
- 210000003041 ligament Anatomy 0.000 claims description 4
- 102000012422 Collagen Type I Human genes 0.000 claims description 3
- 108010022452 Collagen Type I Proteins 0.000 claims description 3
- 102000015696 Interleukins Human genes 0.000 claims description 3
- 108010063738 Interleukins Proteins 0.000 claims description 3
- SHGAZHPCJJPHSC-YCNIQYBTSA-N all-trans-retinoic acid Chemical compound OC(=O)\C=C(/C)\C=C\C=C(/C)\C=C\C1=C(C)CCCC1(C)C SHGAZHPCJJPHSC-YCNIQYBTSA-N 0.000 claims description 3
- AWUCVROLDVIAJX-UHFFFAOYSA-N alpha-glycerophosphate Natural products OCC(O)COP(O)(O)=O AWUCVROLDVIAJX-UHFFFAOYSA-N 0.000 claims description 3
- 239000003862 glucocorticoid Substances 0.000 claims description 3
- 150000003180 prostaglandins Chemical group 0.000 claims description 3
- 229930002330 retinoic acid Natural products 0.000 claims description 3
- 229960001727 tretinoin Drugs 0.000 claims description 3
- 150000002266 vitamin A derivatives Chemical group 0.000 claims description 3
- GMVPRGQOIOIIMI-UHFFFAOYSA-N (8R,11R,12R,13E,15S)-11,15-Dihydroxy-9-oxo-13-prostenoic acid Natural products CCCCCC(O)C=CC1C(O)CC(=O)C1CCCCCCC(O)=O GMVPRGQOIOIIMI-UHFFFAOYSA-N 0.000 claims description 2
- 108010049931 Bone Morphogenetic Protein 2 Proteins 0.000 claims description 2
- 108010049951 Bone Morphogenetic Protein 3 Proteins 0.000 claims description 2
- 108010049955 Bone Morphogenetic Protein 4 Proteins 0.000 claims description 2
- 102100024506 Bone morphogenetic protein 2 Human genes 0.000 claims description 2
- 102100024504 Bone morphogenetic protein 3 Human genes 0.000 claims description 2
- 102100024505 Bone morphogenetic protein 4 Human genes 0.000 claims description 2
- 108010002350 Interleukin-2 Proteins 0.000 claims description 2
- 229960000711 alprostadil Drugs 0.000 claims description 2
- 229960005070 ascorbic acid Drugs 0.000 claims description 2
- 235000010323 ascorbic acid Nutrition 0.000 claims description 2
- 239000011668 ascorbic acid Substances 0.000 claims description 2
- 108010067471 inhibin A Proteins 0.000 claims description 2
- GMVPRGQOIOIIMI-DWKJAMRDSA-N prostaglandin E1 Chemical compound CCCCC[C@H](O)\C=C\[C@H]1[C@H](O)CC(=O)[C@@H]1CCCCCCC(O)=O GMVPRGQOIOIIMI-DWKJAMRDSA-N 0.000 claims description 2
- XEYBRNLFEZDVAW-UHFFFAOYSA-N prostaglandin E2 Natural products CCCCCC(O)C=CC1C(O)CC(=O)C1CC=CCCCC(O)=O XEYBRNLFEZDVAW-UHFFFAOYSA-N 0.000 claims description 2
- AWUCVROLDVIAJX-GSVOUGTGSA-N sn-glycerol 3-phosphate Chemical compound OC[C@@H](O)COP(O)(O)=O AWUCVROLDVIAJX-GSVOUGTGSA-N 0.000 claims description 2
- 230000004936 stimulating effect Effects 0.000 claims description 2
- 102100026632 Mimecan Human genes 0.000 claims 6
- 101800002327 Osteoinductive factor Proteins 0.000 claims 6
- 230000001131 transforming effect Effects 0.000 claims 3
- 102000018233 Fibroblast Growth Factor Human genes 0.000 claims 2
- 108050007372 Fibroblast Growth Factor Proteins 0.000 claims 2
- 229940126864 fibroblast growth factor Drugs 0.000 claims 2
- 102100020873 Interleukin-2 Human genes 0.000 claims 1
- 239000000411 inducer Substances 0.000 claims 1
- 229940102223 injectable solution Drugs 0.000 claims 1
- 238000000338 in vitro Methods 0.000 abstract description 30
- 238000000034 method Methods 0.000 abstract description 14
- 210000004027 cell Anatomy 0.000 description 195
- 239000002609 medium Substances 0.000 description 76
- NMUSYJAQQFHJEW-KVTDHHQDSA-N 5-azacytidine Chemical group O=C1N=C(N)N=CN1[C@H]1[C@H](O)[C@H](O)[C@@H](CO)O1 NMUSYJAQQFHJEW-KVTDHHQDSA-N 0.000 description 61
- 230000014509 gene expression Effects 0.000 description 59
- 102000004127 Cytokines Human genes 0.000 description 52
- 108090000695 Cytokines Proteins 0.000 description 52
- 241000700159 Rattus Species 0.000 description 48
- 230000001114 myogenic effect Effects 0.000 description 34
- 102000002260 Alkaline Phosphatase Human genes 0.000 description 28
- 108020004774 Alkaline Phosphatase Proteins 0.000 description 28
- 101000958041 Homo sapiens Musculin Proteins 0.000 description 25
- 230000000694 effects Effects 0.000 description 24
- 230000002188 osteogenic effect Effects 0.000 description 24
- 239000013589 supplement Substances 0.000 description 24
- 102000004889 Interleukin-6 Human genes 0.000 description 17
- 108090001005 Interleukin-6 Proteins 0.000 description 17
- 102000004058 Leukemia inhibitory factor Human genes 0.000 description 17
- 108090000581 Leukemia inhibitory factor Proteins 0.000 description 17
- 210000004271 bone marrow stromal cell Anatomy 0.000 description 17
- 229940100601 interleukin-6 Drugs 0.000 description 17
- 108010017213 Granulocyte-Macrophage Colony-Stimulating Factor Proteins 0.000 description 16
- 102100039620 Granulocyte-macrophage colony-stimulating factor Human genes 0.000 description 16
- 210000001519 tissue Anatomy 0.000 description 16
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 15
- 102000004269 Granulocyte Colony-Stimulating Factor Human genes 0.000 description 14
- 108010017080 Granulocyte Colony-Stimulating Factor Proteins 0.000 description 14
- 238000002474 experimental method Methods 0.000 description 14
- 239000012091 fetal bovine serum Substances 0.000 description 13
- 238000001727 in vivo Methods 0.000 description 13
- 102000003815 Interleukin-11 Human genes 0.000 description 12
- 108090000177 Interleukin-11 Proteins 0.000 description 12
- 210000002950 fibroblast Anatomy 0.000 description 12
- 102000046949 human MSC Human genes 0.000 description 12
- 229940074383 interleukin-11 Drugs 0.000 description 12
- 210000003205 muscle Anatomy 0.000 description 12
- 210000005009 osteogenic cell Anatomy 0.000 description 12
- DHCLVCXQIBBOPH-UHFFFAOYSA-N Glycerol 2-phosphate Chemical compound OCC(CO)OP(O)(O)=O DHCLVCXQIBBOPH-UHFFFAOYSA-N 0.000 description 11
- 210000002798 bone marrow cell Anatomy 0.000 description 11
- 210000001612 chondrocyte Anatomy 0.000 description 11
- 210000002808 connective tissue Anatomy 0.000 description 11
- 230000037361 pathway Effects 0.000 description 11
- 238000011160 research Methods 0.000 description 11
- 102000010834 Extracellular Matrix Proteins Human genes 0.000 description 10
- 108010037362 Extracellular Matrix Proteins Proteins 0.000 description 10
- 102000007651 Macrophage Colony-Stimulating Factor Human genes 0.000 description 10
- 108010046938 Macrophage Colony-Stimulating Factor Proteins 0.000 description 10
- 238000003556 assay Methods 0.000 description 10
- 239000000919 ceramic Substances 0.000 description 10
- 210000000963 osteoblast Anatomy 0.000 description 10
- 238000002054 transplantation Methods 0.000 description 10
- 210000002744 extracellular matrix Anatomy 0.000 description 9
- 238000000926 separation method Methods 0.000 description 9
- 102000003505 Myosin Human genes 0.000 description 8
- 108060008487 Myosin Proteins 0.000 description 8
- 102000004142 Trypsin Human genes 0.000 description 8
- 108090000631 Trypsin Proteins 0.000 description 8
- 239000001963 growth medium Substances 0.000 description 8
- 239000000126 substance Substances 0.000 description 8
- 108010002386 Interleukin-3 Proteins 0.000 description 7
- 102000000646 Interleukin-3 Human genes 0.000 description 7
- 210000004408 hybridoma Anatomy 0.000 description 7
- 230000001965 increasing effect Effects 0.000 description 7
- 230000005764 inhibitory process Effects 0.000 description 7
- 229940076264 interleukin-3 Drugs 0.000 description 7
- 210000005088 multinucleated cell Anatomy 0.000 description 7
- 238000002360 preparation method Methods 0.000 description 7
- 238000010186 staining Methods 0.000 description 7
- 210000000130 stem cell Anatomy 0.000 description 7
- 238000012360 testing method Methods 0.000 description 7
- 239000012588 trypsin Substances 0.000 description 7
- XAUDJQYHKZQPEU-KVQBGUIXSA-N 5-aza-2'-deoxycytidine Chemical compound O=C1N=C(N)N=CN1[C@@H]1O[C@H](CO)[C@@H](O)C1 XAUDJQYHKZQPEU-KVQBGUIXSA-N 0.000 description 6
- MIJPAVRNWPDMOR-ZAFYKAAXSA-N L-ascorbic acid 2-phosphate Chemical compound OC[C@H](O)[C@H]1OC(=O)C(OP(O)(O)=O)=C1O MIJPAVRNWPDMOR-ZAFYKAAXSA-N 0.000 description 6
- 102000011117 Transforming Growth Factor beta2 Human genes 0.000 description 6
- 101800000304 Transforming growth factor beta-2 Proteins 0.000 description 6
- 210000003414 extremity Anatomy 0.000 description 6
- 230000001605 fetal effect Effects 0.000 description 6
- 210000003958 hematopoietic stem cell Anatomy 0.000 description 6
- JYGXADMDTFJGBT-VWUMJDOOSA-N hydrocortisone Chemical compound O=C1CC[C@]2(C)[C@H]3[C@@H](O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 JYGXADMDTFJGBT-VWUMJDOOSA-N 0.000 description 6
- 230000000399 orthopedic effect Effects 0.000 description 6
- 230000001105 regulatory effect Effects 0.000 description 6
- 239000000523 sample Substances 0.000 description 6
- 239000006228 supernatant Substances 0.000 description 6
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 5
- JGSARLDLIJGVTE-MBNYWOFBSA-N Penicillin G Chemical compound N([C@H]1[C@H]2SC([C@@H](N2C1=O)C(O)=O)(C)C)C(=O)CC1=CC=CC=C1 JGSARLDLIJGVTE-MBNYWOFBSA-N 0.000 description 5
- 210000001772 blood platelet Anatomy 0.000 description 5
- 210000004556 brain Anatomy 0.000 description 5
- 238000012790 confirmation Methods 0.000 description 5
- 238000010790 dilution Methods 0.000 description 5
- 239000012895 dilution Substances 0.000 description 5
- 210000003743 erythrocyte Anatomy 0.000 description 5
- 210000003098 myoblast Anatomy 0.000 description 5
- 230000008569 process Effects 0.000 description 5
- NMUSYJAQQFHJEW-UHFFFAOYSA-N 5-Azacytidine Natural products O=C1N=C(N)N=CN1C1C(O)C(O)C(CO)O1 NMUSYJAQQFHJEW-UHFFFAOYSA-N 0.000 description 4
- 208000006735 Periostitis Diseases 0.000 description 4
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 4
- 230000009471 action Effects 0.000 description 4
- 238000004458 analytical method Methods 0.000 description 4
- 239000000427 antigen Substances 0.000 description 4
- 102000036639 antigens Human genes 0.000 description 4
- 108091007433 antigens Proteins 0.000 description 4
- 238000013459 approach Methods 0.000 description 4
- 229960002756 azacitidine Drugs 0.000 description 4
- 210000004369 blood Anatomy 0.000 description 4
- 239000008280 blood Substances 0.000 description 4
- 210000002449 bone cell Anatomy 0.000 description 4
- 230000010261 cell growth Effects 0.000 description 4
- 239000003102 growth factor Substances 0.000 description 4
- 238000003306 harvesting Methods 0.000 description 4
- 230000011132 hemopoiesis Effects 0.000 description 4
- 238000002513 implantation Methods 0.000 description 4
- 229910052500 inorganic mineral Inorganic materials 0.000 description 4
- 238000004519 manufacturing process Methods 0.000 description 4
- 239000003550 marker Substances 0.000 description 4
- 239000011159 matrix material Substances 0.000 description 4
- 239000011707 mineral Substances 0.000 description 4
- 235000010755 mineral Nutrition 0.000 description 4
- 210000005087 mononuclear cell Anatomy 0.000 description 4
- 210000003460 periosteum Anatomy 0.000 description 4
- 239000004033 plastic Substances 0.000 description 4
- 210000002966 serum Anatomy 0.000 description 4
- 210000002027 skeletal muscle Anatomy 0.000 description 4
- 210000004872 soft tissue Anatomy 0.000 description 4
- UCSJYZPVAKXKNQ-HZYVHMACSA-N streptomycin Chemical compound CN[C@H]1[C@H](O)[C@@H](O)[C@H](CO)O[C@H]1O[C@@H]1[C@](C=O)(O)[C@H](C)O[C@H]1O[C@@H]1[C@@H](NC(N)=N)[C@H](O)[C@@H](NC(N)=N)[C@H](O)[C@H]1O UCSJYZPVAKXKNQ-HZYVHMACSA-N 0.000 description 4
- 210000005166 vasculature Anatomy 0.000 description 4
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 3
- APKFDSVGJQXUKY-KKGHZKTASA-N Amphotericin-B Natural products O[C@H]1[C@@H](N)[C@H](O)[C@@H](C)O[C@H]1O[C@H]1C=CC=CC=CC=CC=CC=CC=C[C@H](C)[C@@H](O)[C@@H](C)[C@H](C)OC(=O)C[C@H](O)C[C@H](O)CC[C@@H](O)[C@H](O)C[C@H](O)C[C@](O)(C[C@H](O)[C@H]2C(O)=O)O[C@H]2C1 APKFDSVGJQXUKY-KKGHZKTASA-N 0.000 description 3
- 102000000503 Collagen Type II Human genes 0.000 description 3
- 108010041390 Collagen Type II Proteins 0.000 description 3
- 238000002965 ELISA Methods 0.000 description 3
- 102000004190 Enzymes Human genes 0.000 description 3
- 108090000790 Enzymes Proteins 0.000 description 3
- 102000000589 Interleukin-1 Human genes 0.000 description 3
- 108010002352 Interleukin-1 Proteins 0.000 description 3
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 3
- 241000699670 Mus sp. Species 0.000 description 3
- 206010028980 Neoplasm Diseases 0.000 description 3
- OIPILFWXSMYKGL-UHFFFAOYSA-N acetylcholine Chemical compound CC(=O)OCC[N+](C)(C)C OIPILFWXSMYKGL-UHFFFAOYSA-N 0.000 description 3
- 229960004373 acetylcholine Drugs 0.000 description 3
- 230000001464 adherent effect Effects 0.000 description 3
- APKFDSVGJQXUKY-INPOYWNPSA-N amphotericin B Chemical compound O[C@H]1[C@@H](N)[C@H](O)[C@@H](C)O[C@H]1O[C@H]1/C=C/C=C/C=C/C=C/C=C/C=C/C=C/[C@H](C)[C@@H](O)[C@@H](C)[C@H](C)OC(=O)C[C@H](O)C[C@H](O)CC[C@@H](O)[C@H](O)C[C@H](O)C[C@](O)(C[C@H](O)[C@H]2C(O)=O)O[C@H]2C1 APKFDSVGJQXUKY-INPOYWNPSA-N 0.000 description 3
- 229960003942 amphotericin b Drugs 0.000 description 3
- 230000008901 benefit Effects 0.000 description 3
- 239000004068 calcium phosphate ceramic Substances 0.000 description 3
- 230000011712 cell development Effects 0.000 description 3
- 230000036978 cell physiology Effects 0.000 description 3
- 230000008859 change Effects 0.000 description 3
- 238000006243 chemical reaction Methods 0.000 description 3
- 239000003153 chemical reaction reagent Substances 0.000 description 3
- 150000001875 compounds Chemical class 0.000 description 3
- 230000008602 contraction Effects 0.000 description 3
- 239000012228 culture supernatant Substances 0.000 description 3
- 230000007547 defect Effects 0.000 description 3
- 210000004207 dermis Anatomy 0.000 description 3
- 238000001514 detection method Methods 0.000 description 3
- 229940088598 enzyme Drugs 0.000 description 3
- 210000004565 granule cell Anatomy 0.000 description 3
- 229960000890 hydrocortisone Drugs 0.000 description 3
- 210000003559 hypertrophic chondrocyte Anatomy 0.000 description 3
- 238000001000 micrograph Methods 0.000 description 3
- 210000000107 myocyte Anatomy 0.000 description 3
- 230000024121 nodulation Effects 0.000 description 3
- 239000006887 os medium Substances 0.000 description 3
- 230000002138 osteoinductive effect Effects 0.000 description 3
- 239000008188 pellet Substances 0.000 description 3
- 238000007747 plating Methods 0.000 description 3
- 210000001316 polygonal cell Anatomy 0.000 description 3
- 230000004044 response Effects 0.000 description 3
- 239000011780 sodium chloride Substances 0.000 description 3
- 241000894007 species Species 0.000 description 3
- 238000007920 subcutaneous administration Methods 0.000 description 3
- 230000004083 survival effect Effects 0.000 description 3
- 239000003104 tissue culture media Substances 0.000 description 3
- 230000017423 tissue regeneration Effects 0.000 description 3
- 210000000689 upper leg Anatomy 0.000 description 3
- YBJHBAHKTGYVGT-ZKWXMUAHSA-N (+)-Biotin Chemical compound N1C(=O)N[C@@H]2[C@H](CCCCC(=O)O)SC[C@@H]21 YBJHBAHKTGYVGT-ZKWXMUAHSA-N 0.000 description 2
- WDGXQSVUSMTYNG-UHFFFAOYSA-N 2-Methyl-3-(2-methylphenyl)-3,4-dihydroquinazolin-4-one [2-(diphenylmethoxy)ethyl]dimethylamine hydrochloride Chemical compound Cl.C=1C=CC=CC=1C(OCCN(C)C)C1=CC=CC=C1.CC1=CC=CC=C1N1C(=O)C2=CC=CC=C2N=C1C WDGXQSVUSMTYNG-UHFFFAOYSA-N 0.000 description 2
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 2
- 102000018697 Membrane Proteins Human genes 0.000 description 2
- 108010052285 Membrane Proteins Proteins 0.000 description 2
- 241000699666 Mus <mouse, genus> Species 0.000 description 2
- 241000699660 Mus musculus Species 0.000 description 2
- 241000283973 Oryctolagus cuniculus Species 0.000 description 2
- -1 SCF Proteins 0.000 description 2
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 2
- 230000004913 activation Effects 0.000 description 2
- 239000012298 atmosphere Substances 0.000 description 2
- 239000003855 balanced salt solution Substances 0.000 description 2
- 210000002805 bone matrix Anatomy 0.000 description 2
- 238000004113 cell culture Methods 0.000 description 2
- 239000006285 cell suspension Substances 0.000 description 2
- 239000003795 chemical substances by application Substances 0.000 description 2
- 230000009816 chondrogenic differentiation Effects 0.000 description 2
- 239000002131 composite material Substances 0.000 description 2
- 239000003636 conditioned culture medium Substances 0.000 description 2
- 210000001608 connective tissue cell Anatomy 0.000 description 2
- 238000011109 contamination Methods 0.000 description 2
- 230000036461 convulsion Effects 0.000 description 2
- 239000013078 crystal Substances 0.000 description 2
- UHDGCWIWMRVCDJ-ZAKLUEHWSA-N cytidine Chemical class O=C1N=C(N)C=CN1[C@H]1[C@H](O)[C@@H](O)[C@H](CO)O1 UHDGCWIWMRVCDJ-ZAKLUEHWSA-N 0.000 description 2
- 238000009792 diffusion process Methods 0.000 description 2
- 210000002308 embryonic cell Anatomy 0.000 description 2
- 230000002255 enzymatic effect Effects 0.000 description 2
- 239000000835 fiber Substances 0.000 description 2
- 239000008103 glucose Substances 0.000 description 2
- 238000010166 immunofluorescence Methods 0.000 description 2
- 238000003125 immunofluorescent labeling Methods 0.000 description 2
- 238000012744 immunostaining Methods 0.000 description 2
- 238000005462 in vivo assay Methods 0.000 description 2
- 238000011534 incubation Methods 0.000 description 2
- 230000028709 inflammatory response Effects 0.000 description 2
- 238000011081 inoculation Methods 0.000 description 2
- 238000002955 isolation Methods 0.000 description 2
- YWXYYJSYQOXTPL-SLPGGIOYSA-N isosorbide mononitrate Chemical compound [O-][N+](=O)O[C@@H]1CO[C@@H]2[C@@H](O)CO[C@@H]21 YWXYYJSYQOXTPL-SLPGGIOYSA-N 0.000 description 2
- 210000000265 leukocyte Anatomy 0.000 description 2
- 230000007246 mechanism Effects 0.000 description 2
- 210000003593 megakaryocyte Anatomy 0.000 description 2
- 210000004487 mononuclear osteoclast Anatomy 0.000 description 2
- 230000004660 morphological change Effects 0.000 description 2
- 229940126619 mouse monoclonal antibody Drugs 0.000 description 2
- 210000000663 muscle cell Anatomy 0.000 description 2
- 238000011580 nude mouse model Methods 0.000 description 2
- 235000015097 nutrients Nutrition 0.000 description 2
- 210000004663 osteoprogenitor cell Anatomy 0.000 description 2
- 230000001575 pathological effect Effects 0.000 description 2
- 229940056360 penicillin g Drugs 0.000 description 2
- 239000011148 porous material Substances 0.000 description 2
- 239000002243 precursor Substances 0.000 description 2
- 230000007115 recruitment Effects 0.000 description 2
- 230000002829 reductive effect Effects 0.000 description 2
- 238000011069 regeneration method Methods 0.000 description 2
- 230000008439 repair process Effects 0.000 description 2
- 230000028327 secretion Effects 0.000 description 2
- SQGYOTSLMSWVJD-UHFFFAOYSA-N silver(1+) nitrate Chemical compound [Ag+].[O-]N(=O)=O SQGYOTSLMSWVJD-UHFFFAOYSA-N 0.000 description 2
- 230000000638 stimulation Effects 0.000 description 2
- 229960005322 streptomycin Drugs 0.000 description 2
- 210000002536 stromal cell Anatomy 0.000 description 2
- 239000000725 suspension Substances 0.000 description 2
- 238000003786 synthesis reaction Methods 0.000 description 2
- 210000002303 tibia Anatomy 0.000 description 2
- 229940072041 transforming growth factor beta 2 Drugs 0.000 description 2
- 230000003827 upregulation Effects 0.000 description 2
- GEYOCULIXLDCMW-UHFFFAOYSA-N 1,2-phenylenediamine Chemical compound NC1=CC=CC=C1N GEYOCULIXLDCMW-UHFFFAOYSA-N 0.000 description 1
- WEEMDRWIKYCTQM-UHFFFAOYSA-N 2,6-dimethoxybenzenecarbothioamide Chemical compound COC1=CC=CC(OC)=C1C(N)=S WEEMDRWIKYCTQM-UHFFFAOYSA-N 0.000 description 1
- XZKIHKMTEMTJQX-UHFFFAOYSA-N 4-Nitrophenyl Phosphate Chemical compound OP(O)(=O)OC1=CC=C([N+]([O-])=O)C=C1 XZKIHKMTEMTJQX-UHFFFAOYSA-N 0.000 description 1
- 206010003445 Ascites Diseases 0.000 description 1
- 241000271566 Aves Species 0.000 description 1
- 108090001008 Avidin Proteins 0.000 description 1
- 241000283690 Bos taurus Species 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- 241000283707 Capra Species 0.000 description 1
- 102000029816 Collagenase Human genes 0.000 description 1
- 108060005980 Collagenase Proteins 0.000 description 1
- 102000007644 Colony-Stimulating Factors Human genes 0.000 description 1
- 108010071942 Colony-Stimulating Factors Proteins 0.000 description 1
- 108020004414 DNA Proteins 0.000 description 1
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- 102000001554 Hemoglobins Human genes 0.000 description 1
- 108010054147 Hemoglobins Proteins 0.000 description 1
- 108010001336 Horseradish Peroxidase Proteins 0.000 description 1
- 208000026350 Inborn Genetic disease Diseases 0.000 description 1
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 1
- 208000024556 Mendelian disease Diseases 0.000 description 1
- 208000029725 Metabolic bone disease Diseases 0.000 description 1
- 241001465754 Metazoa Species 0.000 description 1
- 208000029027 Musculoskeletal and connective tissue disease Diseases 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- 241001494479 Pecora Species 0.000 description 1
- 229930182555 Penicillin Natural products 0.000 description 1
- 101100385368 Saccharomyces cerevisiae (strain ATCC 204508 / S288c) CSG2 gene Proteins 0.000 description 1
- 241000968352 Scandia <hydrozoan> Species 0.000 description 1
- 206010072610 Skeletal dysplasia Diseases 0.000 description 1
- 238000000692 Student's t-test Methods 0.000 description 1
- YCUVUDODLRLVIC-UHFFFAOYSA-N Sudan black B Chemical compound C1=CC(=C23)NC(C)(C)NC2=CC=CC3=C1N=NC(C1=CC=CC=C11)=CC=C1N=NC1=CC=CC=C1 YCUVUDODLRLVIC-UHFFFAOYSA-N 0.000 description 1
- 102000046299 Transforming Growth Factor beta1 Human genes 0.000 description 1
- 101800002279 Transforming growth factor beta-1 Proteins 0.000 description 1
- 239000007983 Tris buffer Substances 0.000 description 1
- 238000011892 Von Kossa's method Methods 0.000 description 1
- 238000011481 absorbance measurement Methods 0.000 description 1
- 230000003213 activating effect Effects 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 230000000996 additive effect Effects 0.000 description 1
- 239000000853 adhesive Substances 0.000 description 1
- 230000001070 adhesive effect Effects 0.000 description 1
- 238000013019 agitation Methods 0.000 description 1
- 230000019552 anatomical structure morphogenesis Effects 0.000 description 1
- 238000010171 animal model Methods 0.000 description 1
- 239000003242 anti bacterial agent Substances 0.000 description 1
- 229940088710 antibiotic agent Drugs 0.000 description 1
- 239000002543 antimycotic Substances 0.000 description 1
- 238000011882 arthroplasty Methods 0.000 description 1
- 238000002820 assay format Methods 0.000 description 1
- 230000003190 augmentative effect Effects 0.000 description 1
- 210000003651 basophil Anatomy 0.000 description 1
- 238000004166 bioassay Methods 0.000 description 1
- 230000001851 biosynthetic effect Effects 0.000 description 1
- 229960002685 biotin Drugs 0.000 description 1
- 235000020958 biotin Nutrition 0.000 description 1
- 239000011616 biotin Substances 0.000 description 1
- 210000000601 blood cell Anatomy 0.000 description 1
- 230000037396 body weight Effects 0.000 description 1
- 238000010322 bone marrow transplantation Methods 0.000 description 1
- 230000034127 bone morphogenesis Effects 0.000 description 1
- 229940098773 bovine serum albumin Drugs 0.000 description 1
- 239000011575 calcium Substances 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 239000001506 calcium phosphate Substances 0.000 description 1
- 229910000389 calcium phosphate Inorganic materials 0.000 description 1
- 235000011010 calcium phosphates Nutrition 0.000 description 1
- 201000011510 cancer Diseases 0.000 description 1
- OSQPUMRCKZAIOZ-UHFFFAOYSA-N carbon dioxide;ethanol Chemical compound CCO.O=C=O OSQPUMRCKZAIOZ-UHFFFAOYSA-N 0.000 description 1
- 230000007355 cartilage morphogenesis Effects 0.000 description 1
- 230000021164 cell adhesion Effects 0.000 description 1
- 230000005779 cell damage Effects 0.000 description 1
- 208000037887 cell injury Diseases 0.000 description 1
- 230000004663 cell proliferation Effects 0.000 description 1
- 230000001413 cellular effect Effects 0.000 description 1
- 210000004720 cerebrum Anatomy 0.000 description 1
- 238000012512 characterization method Methods 0.000 description 1
- 101150115304 cls-2 gene Proteins 0.000 description 1
- 229920001436 collagen Polymers 0.000 description 1
- 229960002424 collagenase Drugs 0.000 description 1
- 230000001276 controlling effect Effects 0.000 description 1
- 210000004748 cultured cell Anatomy 0.000 description 1
- 210000000805 cytoplasm Anatomy 0.000 description 1
- 230000006378 damage Effects 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 230000008021 deposition Effects 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- 238000010586 diagram Methods 0.000 description 1
- 210000003275 diaphysis Anatomy 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- 238000002224 dissection Methods 0.000 description 1
- 231100000673 dose–response relationship Toxicity 0.000 description 1
- 210000002257 embryonic structure Anatomy 0.000 description 1
- 210000002889 endothelial cell Anatomy 0.000 description 1
- 230000002708 enhancing effect Effects 0.000 description 1
- 230000007613 environmental effect Effects 0.000 description 1
- 210000003979 eosinophil Anatomy 0.000 description 1
- 239000003797 essential amino acid Substances 0.000 description 1
- 235000020776 essential amino acid Nutrition 0.000 description 1
- DEFVIWRASFVYLL-UHFFFAOYSA-N ethylene glycol bis(2-aminoethyl)tetraacetic acid Chemical compound OC(=O)CN(CC(O)=O)CCOCCOCCN(CC(O)=O)CC(O)=O DEFVIWRASFVYLL-UHFFFAOYSA-N 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 230000007717 exclusion Effects 0.000 description 1
- 239000012894 fetal calf serum Substances 0.000 description 1
- 210000003754 fetus Anatomy 0.000 description 1
- 239000012634 fragment Substances 0.000 description 1
- 239000012737 fresh medium Substances 0.000 description 1
- 239000000499 gel Substances 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- 208000016361 genetic disease Diseases 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 238000012787 harvest procedure Methods 0.000 description 1
- 238000011540 hip replacement Methods 0.000 description 1
- 210000003035 hyaline cartilage Anatomy 0.000 description 1
- 230000001969 hypertrophic effect Effects 0.000 description 1
- 230000005965 immune activity Effects 0.000 description 1
- 230000028993 immune response Effects 0.000 description 1
- 238000002649 immunization Methods 0.000 description 1
- 230000003053 immunization Effects 0.000 description 1
- 238000003365 immunocytochemistry Methods 0.000 description 1
- 230000002055 immunohistochemical effect Effects 0.000 description 1
- 238000003364 immunohistochemistry Methods 0.000 description 1
- 230000004941 influx Effects 0.000 description 1
- 238000003780 insertion Methods 0.000 description 1
- 230000037431 insertion Effects 0.000 description 1
- 230000003993 interaction Effects 0.000 description 1
- 229940047122 interleukins Drugs 0.000 description 1
- 238000007912 intraperitoneal administration Methods 0.000 description 1
- 238000013150 knee replacement Methods 0.000 description 1
- 210000002414 leg Anatomy 0.000 description 1
- 208000032839 leukemia Diseases 0.000 description 1
- 210000000982 limb bud Anatomy 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 150000002632 lipids Chemical class 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 210000003141 lower extremity Anatomy 0.000 description 1
- 210000004698 lymphocyte Anatomy 0.000 description 1
- 229920002521 macromolecule Polymers 0.000 description 1
- 239000011777 magnesium Substances 0.000 description 1
- 229910052749 magnesium Inorganic materials 0.000 description 1
- 238000012423 maintenance Methods 0.000 description 1
- 210000001161 mammalian embryo Anatomy 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 230000035800 maturation Effects 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 238000010297 mechanical methods and process Methods 0.000 description 1
- 230000005226 mechanical processes and functions Effects 0.000 description 1
- 230000001404 mediated effect Effects 0.000 description 1
- 210000001704 mesoblast Anatomy 0.000 description 1
- 210000003716 mesoderm Anatomy 0.000 description 1
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 239000003607 modifier Substances 0.000 description 1
- 239000003068 molecular probe Substances 0.000 description 1
- 235000013923 monosodium glutamate Nutrition 0.000 description 1
- 230000000877 morphologic effect Effects 0.000 description 1
- 230000003387 muscular Effects 0.000 description 1
- 210000003887 myelocyte Anatomy 0.000 description 1
- 230000017186 myoblast division Effects 0.000 description 1
- 230000004070 myogenic differentiation Effects 0.000 description 1
- 210000000440 neutrophil Anatomy 0.000 description 1
- 238000010899 nucleation Methods 0.000 description 1
- 230000003287 optical effect Effects 0.000 description 1
- 210000000056 organ Anatomy 0.000 description 1
- 230000008520 organization Effects 0.000 description 1
- 201000008482 osteoarthritis Diseases 0.000 description 1
- 230000004072 osteoblast differentiation Effects 0.000 description 1
- HJGMWXTVGKLUAQ-UHFFFAOYSA-N oxygen(2-);scandium(3+) Chemical compound [O-2].[O-2].[O-2].[Sc+3].[Sc+3] HJGMWXTVGKLUAQ-UHFFFAOYSA-N 0.000 description 1
- 229940094443 oxytocics prostaglandins Drugs 0.000 description 1
- 229940049954 penicillin Drugs 0.000 description 1
- 238000002135 phase contrast microscopy Methods 0.000 description 1
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 1
- 239000010452 phosphate Substances 0.000 description 1
- 235000021317 phosphate Nutrition 0.000 description 1
- 239000008363 phosphate buffer Substances 0.000 description 1
- 238000007781 pre-processing Methods 0.000 description 1
- 238000001556 precipitation Methods 0.000 description 1
- 239000013630 prepared media Substances 0.000 description 1
- 238000002203 pretreatment Methods 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 239000000047 product Substances 0.000 description 1
- 230000001737 promoting effect Effects 0.000 description 1
- 230000001681 protective effect Effects 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 238000011002 quantification Methods 0.000 description 1
- 230000002285 radioactive effect Effects 0.000 description 1
- 230000009257 reactivity Effects 0.000 description 1
- 238000011084 recovery Methods 0.000 description 1
- 230000008929 regeneration Effects 0.000 description 1
- 230000009703 regulation of cell differentiation Effects 0.000 description 1
- 230000031539 regulation of cell division Effects 0.000 description 1
- 238000007634 remodeling Methods 0.000 description 1
- 230000010076 replication Effects 0.000 description 1
- 210000001995 reticulocyte Anatomy 0.000 description 1
- 230000019491 signal transduction Effects 0.000 description 1
- 229910001961 silver nitrate Inorganic materials 0.000 description 1
- 231100001055 skeletal defect Toxicity 0.000 description 1
- 210000003491 skin Anatomy 0.000 description 1
- 210000003625 skull Anatomy 0.000 description 1
- 210000001189 slow twitch fiber Anatomy 0.000 description 1
- 235000017557 sodium bicarbonate Nutrition 0.000 description 1
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 1
- 159000000000 sodium salts Chemical class 0.000 description 1
- 239000000243 solution Substances 0.000 description 1
- 230000002269 spontaneous effect Effects 0.000 description 1
- 238000010561 standard procedure Methods 0.000 description 1
- 229960002385 streptomycin sulfate Drugs 0.000 description 1
- 210000005065 subchondral bone plate Anatomy 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- 230000008093 supporting effect Effects 0.000 description 1
- 238000001356 surgical procedure Methods 0.000 description 1
- 230000009885 systemic effect Effects 0.000 description 1
- 229940037128 systemic glucocorticoids Drugs 0.000 description 1
- 238000012353 t test Methods 0.000 description 1
- UEUXEKPTXMALOB-UHFFFAOYSA-J tetrasodium;2-[2-[bis(carboxylatomethyl)amino]ethyl-(carboxylatomethyl)amino]acetate Chemical compound [Na+].[Na+].[Na+].[Na+].[O-]C(=O)CN(CC([O-])=O)CCN(CC([O-])=O)CC([O-])=O UEUXEKPTXMALOB-UHFFFAOYSA-J 0.000 description 1
- MPLHNVLQVRSVEE-UHFFFAOYSA-N texas red Chemical compound [O-]S(=O)(=O)C1=CC(S(Cl)(=O)=O)=CC=C1C(C1=CC=2CCCN3CCCC(C=23)=C1O1)=C2C1=C(CCC1)C3=[N+]1CCCC3=C2 MPLHNVLQVRSVEE-UHFFFAOYSA-N 0.000 description 1
- 230000001225 therapeutic effect Effects 0.000 description 1
- 238000002560 therapeutic procedure Methods 0.000 description 1
- 230000000451 tissue damage Effects 0.000 description 1
- 231100000827 tissue damage Toxicity 0.000 description 1
- 208000037816 tissue injury Diseases 0.000 description 1
- 229950003937 tolonium Drugs 0.000 description 1
- HNONEKILPDHFOL-UHFFFAOYSA-M tolonium chloride Chemical compound [Cl-].C1=C(C)C(N)=CC2=[S+]C3=CC(N(C)C)=CC=C3N=C21 HNONEKILPDHFOL-UHFFFAOYSA-M 0.000 description 1
- 230000009466 transformation Effects 0.000 description 1
- QORWJWZARLRLPR-UHFFFAOYSA-H tricalcium bis(phosphate) Chemical compound [Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O QORWJWZARLRLPR-UHFFFAOYSA-H 0.000 description 1
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 1
- 230000002792 vascular Effects 0.000 description 1
- 230000003442 weekly effect Effects 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0652—Cells of skeletal and connective tissues; Mesenchyme
- C12N5/0662—Stem cells
- C12N5/0663—Bone marrow mesenchymal stem cells (BM-MSC)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/19—Carboxylic acids, e.g. valproic acid
- A61K31/20—Carboxylic acids, e.g. valproic acid having a carboxyl group bound to a chain of seven or more carbon atoms, e.g. stearic, palmitic, arachidic acids
- A61K31/203—Retinoic acids ; Salts thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/557—Eicosanoids, e.g. leukotrienes or prostaglandins
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/56—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids
- A61K31/57—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids substituted in position 17 beta by a chain of two carbon atoms, e.g. pregnane or progesterone
- A61K31/573—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids substituted in position 17 beta by a chain of two carbon atoms, e.g. pregnane or progesterone substituted in position 21, e.g. cortisone, dexamethasone, prednisone or aldosterone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7042—Compounds having saccharide radicals and heterocyclic rings
- A61K31/7052—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides
- A61K31/706—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides containing six-membered rings with nitrogen as a ring hetero atom
- A61K31/7064—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides containing six-membered rings with nitrogen as a ring hetero atom containing condensed or non-condensed pyrimidines
- A61K31/7068—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides containing six-membered rings with nitrogen as a ring hetero atom containing condensed or non-condensed pyrimidines having oxo groups directly attached to the pyrimidine ring, e.g. cytidine, cytidylic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/12—Materials from mammals; Compositions comprising non-specified tissues or cells; Compositions comprising non-embryonic stem cells; Genetically modified cells
- A61K35/28—Bone marrow; Haematopoietic stem cells; Mesenchymal stem cells of any origin, e.g. adipose-derived stem cells
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/18—Growth factors; Growth regulators
- A61K38/1825—Fibroblast growth factor [FGF]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/18—Growth factors; Growth regulators
- A61K38/1841—Transforming growth factor [TGF]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/18—Growth factors; Growth regulators
- A61K38/1875—Bone morphogenic factor; Osteogenins; Osteogenic factor; Bone-inducing factor
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/19—Cytokines; Lymphokines; Interferons
- A61K38/20—Interleukins [IL]
- A61K38/2006—IL-1
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/19—Cytokines; Lymphokines; Interferons
- A61K38/20—Interleukins [IL]
- A61K38/2013—IL-2
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/22—Hormones
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/39—Connective tissue peptides, e.g. collagen, elastin, laminin, fibronectin, vitronectin, cold insoluble globulin [CIG]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0652—Cells of skeletal and connective tissues; Mesenchyme
- C12N5/0654—Osteocytes, Osteoblasts, Odontocytes; Bones, Teeth
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0652—Cells of skeletal and connective tissues; Mesenchyme
- C12N5/0655—Chondrocytes; Cartilage
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0652—Cells of skeletal and connective tissues; Mesenchyme
- C12N5/0658—Skeletal muscle cells, e.g. myocytes, myotubes, myoblasts
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2500/00—Specific components of cell culture medium
- C12N2500/30—Organic components
- C12N2500/42—Organic phosphate, e.g. beta glycerophosphate
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/06—Anti-neoplasic drugs, anti-retroviral drugs, e.g. azacytidine, cyclophosphamide
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/10—Growth factors
- C12N2501/155—Bone morphogenic proteins [BMP]; Osteogenins; Osteogenic factor; Bone inducing factor
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/20—Cytokines; Chemokines
- C12N2501/23—Interleukins [IL]
- C12N2501/2301—Interleukin-1 (IL-1)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/30—Hormones
- C12N2501/38—Hormones with nuclear receptors
- C12N2501/39—Steroid hormones
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Chemical & Material Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Zoology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Medicinal Chemistry (AREA)
- Biomedical Technology (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Epidemiology (AREA)
- Immunology (AREA)
- Organic Chemistry (AREA)
- Biotechnology (AREA)
- Genetics & Genomics (AREA)
- Wood Science & Technology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Gastroenterology & Hepatology (AREA)
- Cell Biology (AREA)
- Rheumatology (AREA)
- Biochemistry (AREA)
- Developmental Biology & Embryology (AREA)
- Microbiology (AREA)
- General Engineering & Computer Science (AREA)
- Molecular Biology (AREA)
- Hematology (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Biophysics (AREA)
- Virology (AREA)
- Endocrinology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
- Materials For Medical Uses (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Abstract
【解決手段】ヒト間葉幹細胞、および間葉幹細胞の分化を単一特定系列に誘導する生物活性因子あるいは因子の組合せを含むことを特徴とする組成物。
【選択図】図1
Description
ここに記載されたように分離精製されたヒト間葉幹細胞は、例えば骨、骨髄、血液、真皮あるいは骨膜から誘導することができる。骨髄から得られる時には、これは股関節あるいは膝置換手術の間に変形性関節症の患者から得られる大腿骨頭海綿質片の栓子、あるいは将来の骨髄移植に備えて骨髄を収穫された正常なドナーおよび腫瘍患者から得られた吸引骨髄からの栓子を含む数多くの異なった源より得られた骨髄であることができる。収穫された骨髄は次いで細胞培養に備えられる。分離工程は、分化なしで間葉幹細胞成長を可能にするだけでなく培養器のプラスチックあるいはガラス表面への間葉幹細胞のみの直接付着をも可能にする作用薬を含む特別に用意された培地の使用を伴う。非常に微量の間葉組織サンプル内に存在する望ましい間葉幹細胞の選択的付着を可能にする培地を創り出すことにより、次いでもとの間葉細胞に存在する他の細胞(すなわち赤血球、白血球、他の分化間葉細胞、等)から間葉幹細胞を分離することが可能となった。
前に示したように、完全培地は細胞培養分離に収穫骨髄を準備するために当初の収穫過程の特異な型に依存して数多くの異なった分離過程を利用することができる。この点に関して、海綿質骨髄の栓子が利用される場合には、骨髄は完全培地に加えられ、分散を形成するために渦動され、次いで骨片等から骨髄細胞を分離するために遠心分離された。骨髄細胞(主として赤色骨髄および黄色骨髄で、一部微量の間葉幹細胞、等よりなるもの)は次いで一連の16、18、および20ゲージ針を装備した注射器を通じて骨髄細胞を含む完全培地を連続的に通過させることにより単一細胞に解離された。他の酵素分離過程と対比して機械的分離過程の利用を通じて生産される利点は、機械的過程が殆ど細胞の変化をもたらさなかったのに対し、一方酵素過程が培養付着および選択的分離に必要なタンパク質結合部位に対し、およびもしくは前記間葉幹細胞に特異的なモノクローナル抗体の生産に必要なタンパク質部位に対しとりわけ細胞損傷を産み出すこととなったと考えられる。単一細胞懸濁液(約50−100×106有核細胞で形成されたもの)は次いで引き続き懸濁液で見出される残存細胞から間葉幹細胞を選択的に分離しおよびもしくは隔離する目的で100mm皿にプレートされた。
生体内MSCsの誘導骨形成分化
この実施例で記載される実験の目的は、間葉幹細胞(MSCs)が組織培養培地において適切な生物活性因子を提供することにより試験管内で骨形成系列路に沿って指向されたことを示すことであった。この組の実験はMSCsがどのように骨形成系列に向けて指向され得るかについてのただ一つの例を示す。
ヒトMSCsは前に記載の通り骨髄から収穫され分離された。これらの細胞は予備選択された10%の胎児ウシ血清(完全培地)を含むDMEM−LGで培養拡張された。新鮮完全培地は培養が密集近くになるまで3−4日毎にとり替えられ、密集の時点で細胞はトリプシンで平板から遊離され、約40%の密集(100mm皿当り400,000細胞)で新しい皿に再接種された。これらの再平板培養MSCsは一晩付着を許され、その後完全培地はDMEM−LG、10%の胎児ウシ血清、および100nMのデキサメタゾンのみ、あるいは100nMのデキサメタゾンと50μMのアスコルビン酸−2−リン酸塩のいずれか、および10mMのβ−グリセロホスフェート(骨形成補充剤)よりなる培地でとり替えられた。骨形成補充剤は3日毎にとり替えられた。細胞は毎日形態変化を検討された。選択された平板は次いで骨形成系列に入る細胞のマーカーである細胞表面アルカリ性ホスファターゼ(AP)活性を分析された。骨マトリックス合成に引き続き責任があったのはこれらの細胞である。標準酵素組織化学および生化学試薬がこの細胞表面タンパク質の活性を示すために使用された。追加の標本が成熟骨芽細胞母集団の連続した分化および表現型発現に相関するミネラル化細胞外基質小節の存在を評価された。骨小節内でのリン酸カルシウム結晶への硝酸銀沈殿が標準フォン・コッサ染色法を通じて達成された。
公開技術を使用して、MSCsは3人の異なった患者(年齢26−47才)から精製され、培養拡張され(27)、選択されたロットからの10%のFBSを加えたDMEM−LGで20%の密集で48ウエル培養皿に一晩接種された。比較のための基礎培地は、DMEM−LG、BGJb 、αMEMおよびDMEM/F−12(1:1)であった。各検定のための三組の培養が「骨形成補充剤」(OS)(デキサメタゾン100nM、アスコルビン酸−2−リン酸塩50μMおよびβ−グリセロホスフェート10mM(28))の存在あるいは不在下でFBS10%で成長した。培地は3日毎にとり替えられた。各組の培地は細胞数をクリスタル紫検定により、細胞表面アルカリ性ホスファターゼ(AP)を組織化学により、またミネラル化小節形成をフォン・コッサ染色により検定された。AP酵素活性は生体培養をp−ニトロフェニルホスフェート5mMでトリス50mM、NaCl 150mM、pH9.0で保温培養し、サンプルを405nmでエリザ平板リーダーでスキャンニングにより比色反応を定量化することで計数された。AP酵素活性は製品/分/103 細胞のナノモルで発現された。各ウエルにおけるAP正細胞の割合は染色培養から測定され、ミネラル化小節の数はウエル当りで計数された。検定は16日培養期間で4日毎に行われた。対の2個サンプルt−テストが選択されたサンプルで行われた。図4のデータは1人の患者のものを表すが類似の結果はすべての標本から得られた。
ヒト骨形成細胞に対するモノクローナル抗体の生成は生体内胚骨形成および試験管内精製間葉幹細胞の分化を明らかにする
骨髄から誘導される間葉始原細胞が骨芽細胞に分化できることはこれまでに十分確立されている。加えてこれら間葉幹細胞(MSCs)は更に軟骨、腱、靭帯、筋、および他の組織を生み出す。しかしこれら各種の系列に沿ってMSCsの委託および分化に伴う各段階の知識は、骨形成あるいは他の分化路内での各段階と細胞に特異的なプローブの欠除により部分的に制約されてきた。モノクローナル抗体が分化を研究するための有用なプローブであるために、試験管内骨形成系列に誘導するヒト骨髄誘導MSCsの無傷生細胞調製物を用いて我々はマウスを免疫化した。我々は精製MSCsに対するハイブリドーマコロニー、骨形成分化を進行中のMSCs、および長骨が軟骨原基痕跡の周りに発達中である胚ヒト肢の凍結部分を検査した。この検査実験記録は試験管内分化進行中のMSCsおよび生体内ヒト骨形成細胞で反応する抗体の選択を有利にする。このアプローチを用いて、我々はヒト骨髄MSCsから誘導される骨形成細胞についての系列段階特異的表面抗原に対するモノクローナル抗体を生成した。
試験管内MSCsの誘導軟骨形成分化
この実施例で記載される実験の目的は、間葉幹細胞(MSCs)が組織培養培地内で適切な生物活性因子を提供することにより試験管内軟骨形成系列路に向けて指向されるということを示すことであった。この組の実験はMSCsがどのようにして軟骨形成系列に指向できるのかのただ一つの実施例を表す。ヒトMSCsが収穫され、前に記載された通り骨髄から分離された。細胞は予備選択された胎児ウシ血清10%を含むDMEM−LG培地(完全培地)で培養拡張された。培養が密集に近付くまで新鮮培地が3−4日毎にとり替えられ、密集の地点で細胞はトリプシンで平板から遊離され、約50%の密集(100mm皿当り500,000個の細胞)で平板に再接種された。これらの再平板培養MSCsは一晩付着され、その後完全培地は胎児ウシ血清10%およびマーシャル・アール・ユーリスト博士により提供された部分的精製骨形態形成タンパク質(軟骨形成補充剤)5mg/mlとともにDMEM−LGでとり替えられた。この軟骨形成補充剤は3日毎にとり替えられた。細胞は毎日形態形成変化を調べられた。選択された平板は次いで軟骨系列に入った細胞のマーカーであるCSPG−Mを免疫組織化学的に分析された。次いで軟骨のタイプIIコラーゲンマトリックスを合成するため駆動されたのはこれらの細胞である。標準免疫組織化学試薬が細胞外マトリックスタンパク質の存在を示すために使用された。追加の標本が成熟軟骨細胞母集団の連続分化および表現型発現と相関付けるトルイジンブルー染色小節の存在を評価された。肥厚性軟骨細胞のミネラル化小節の存在のためのフォン・コッサ染色は負であった。
実施例4
試験管内MSCsの誘導骨髄ストロマ細胞分化
この実施例に記載される試験の目的はヒト骨髄誘導MSCsが培養培地に適切な生物活性因子を提供することにより試験管内支質形成系列路に沿って指向されることを示すことであった。ヒト骨髄誘導MSCsは骨髄から分離され、前に記載の通り培養で拡張された。ヒトMSCsが骨髄ストロマ細胞系列に誘導される能力を示すために、特異的サイトカイン発現が分化のマーカーとして測定された。MSCsは、予備選択された胎児ウシ血清10%を含むDMEM−LG(完全培地)よりなる培地を用いて分化なしでMSC増殖を有利にする条件、あるいは完全培地プラスインターロイキン−1α(IL−1α)(ストロマ形成補充剤(SS))10U/mlよりなる培地を用いて骨髄ストロマ表現型への発現および分化を有利にする条件の下で成長した。これらの組織培養母集団からの条件付き培養培地は商業的サンドイッチエリザ生物検定(アールアンドディー・システムズ)を用いてサイトカインの存在を分析された。
試験管内MSCsの誘導筋形成分化
この実施例に記載される研究の目的は、5−アザシチジンが筋形成系列に沿って分化するために間葉幹細胞(MSCs)を誘導することを示すことであった。
試験管内ヒト骨髄誘導間葉幹細胞によるサイトカイン発現:IL−1αおよびデキサメタゾンの作用
この研究の目的はサイトカイン発現プロファイルの確認を通じて培養MSCsの表現型特徴を更に確立することであった。我々は各種間葉表現型の細胞分割、分化、あるいは発現の調節に重要であるとして知られているサイトカインの発現水準を確認し測定する商業的エリザを使用した。我々はこれまでに報告した条件の下でMSCサイトカイン発現を確認し、それはMSCが分化なしで有糸分裂で拡張すること(構造的培養拡張培地)を可能にした。加えて、我々はデキサメタゾンあるいはIL−1αで補充された培養培地でMSCsによるサイトカイン発現を検定した。デキサメタゾンは骨始原細胞の骨芽細胞への分化を誘導すると報告されている。対照的に、炎症応答の間に各種の細胞により骨髄徴環境に分泌されるIL−1αは、造血を支持する骨髄ストロマの能力を高めるものと報告されており、かくして骨髄ストロマ繊維芽細胞の分化およびもしくは発現を制御する役割を演じる。
〔MSC分離および培養拡張〕
骨髄は異なった年齢の3人の男性および3人の女性の6人のヒトドナーから得られた(表6)
骨髄誘導MSCsは空気95%およびCO2 5%を含む加湿雰囲気で37℃で完全培地で培養され、培地は3−4日毎にとり替えられた。第1次培養皿が密集近くなると、5分37℃でEDTA、1mM(ジブコ)を含むトリプシン0.25%で分離された。トリプシンの酵素活性はFBS、1/2量の追加で停止した。細胞は計数され、1:3に分割され、7mlの完全培地に再平板培養された。これらの第1継代細胞は、それらが密集近くなるまで4−6日で分割を許された。密集近接第1継代細胞はトリプシン化され、下記に記載される検定形式に再平板培養された。
MSCsによるサイトカイン発現の水準は定量エリザを用いて測定された。下記のサイトカインに対する抗体特異性を持つエリザキット(ミネソタ、ミネアポリス、アールアンドディー・システムズ)が購入された;インターロイキン3(IL−3)、インターロイキン−6(IL−6)、インターロイキン−11(IL−11)、果粒球コロニー刺激因子(G−CSF)、果粒球−マクロファージコロニー刺激因子(GM−CSF)、マクロファージコロニー刺激因子(M−CSF)、幹細胞因子(SCF)、白血病阻害因子(LIF)および形質転換増殖因子−ベータ−2(TGF−β−2)。密集近くになると、第1継代MSCsは平板当り50,000細胞で35mm平板に再平板培養され一晩付着することを許された。培養条件は次いで3個の試験条件の一つに変更された:新鮮完全培地;完全培地と骨形成補充剤;および完全培地と支質形成補充剤がそれである。培養は24時間あるいは48時間で試験培地で保温することを許され、その時点で上澄みが収集され、ドライアイス−エタノールで急速冷凍されすべてのサンプルが一緒に分析を準備されるまでレブコフリーザーで−70℃で貯蔵された。検定は培養上澄み100μlをエリザ平板のウエル上に適用することで実施され、続いて製造業者の指示にもとづき平板を処理することがなされた。標準曲線はキットで供給される標準サイトカインを用いて生成され、適切な濃度に希釈された。ある場合(とりわけIL−6検定)では、上澄みは標準曲線から正確に定量化できる十分に低い吸光測定値を生成するために大幅に希釈されねばならなかった。
結果
〔構造性培養拡張培地条件〕
9個の検定されたサイトカインの6個の検出水準が構造性培養拡張条件に露出24時間後に存在した。(図12A−12Dおよび13A−13Cならびに下記の表7−10を参照のこと)。
骨形成補充剤の完全培地への追加は対照と関連してG−CSF、M−CSFおよびSCFに検出可能な変化を生み出さなかった(図12A−12Dおよび13A−13B;表7−10)。対照的にOS培地は、24時間構造性培養拡張培地条件の下でのこれらサイトカインの発現と関連して、LIF(p<.01)、IL−6(p<.001)およびIL−11(p<.005)の発現を著しく下向き調節した。これらの水準は構造性培養拡張培地条件で48時間のサイトカイン水準よりも統計的に低い段階に留まった(図12A−12Dおよび13A−13C;表7−10)。OS培地媒介阻害の量は3個のサイトカインで変化した。24時間の時点で構造性培養拡張培地条件に関連してOS培地におけるサイトカイン発現の平均水準は以下のようであった;LIF発現、55%±54%,IL−6、16%±9%およびIL−11、1%±3%。LIFパーセント変化における大きな標準偏差は主として1人のドナー(ドナー#4)からの測定に起因し、ここではLIF発現の水準は構造性培養拡張条件に関連してOS培養条件下で事実上高かったためであった(表7)。一定のドナーに対して、あるサイトカインの平均絶対阻害水準に関連してそのサイトカインの阻害パーセントは、平均絶対阻害水準に関連して他の2個の阻害パーセントとは無関係であった(表7−10)。加えて、サイトカインのそれぞれに対して、母集団における6個の個体の間の一定のサイトカインのための阻害パーセントは、構造性培養拡張条件の下での発現の当初の水準とは無関係であった(図12A−12Dおよび13A−13C;表7−10)。
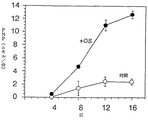
SS培地は濃度依存方法でMSCsによるいくつかのサイトカインの発現を増加した。図14はGM−CFSの発現に関してIL−1αの増加する濃度に対する第2継代MSCsの24時間応答を図解する。0.1−10.0U/mlの間での培養培地でIL−1αの水準が増加するにつれてMSCsによるGM−CSF分泌の水準に線形に近い増加が存在する。培養培地へのIL−1αでの追加のログの増加はGM−CSF発現での追加の増加を殆どもたらさない。これらのデータは下記に記載される実験で培養培地に補充するIL−1αの濃度を確認するために使用された。以下続くすべての検定に対し、IL−1α、10U/mlが培養培地に加えられた。
この研究におけるMSCsについての我々の継続した分析は追加の表現型特性を確認し、MSCsが分化あるいは表現型調整を生じさせる調節分子に露出された時にこの表現型がいかに変化するかを決定することを意図したものである。この研究において、我々は構造性培養拡張条件下で、またOSあるいはSSの存在下でMSCsのサイトカイン発現を特徴付けるためにエリザ検定を使用した。
1.キャプラン,エイ.アイ.:発生生物学協会39回年次シンポジウム,エス.サブテルニーおよびユー.アボット編,3768ページ。ニューヨーク,アラン・アール・リス・インコーポレイテッド,1981年。
2.エルマー他、奇形学、24巻、215−223ページ、1981年。
3.ハウシュカ,エス.ディー.,発生生物学,37巻,345−368ページ、1974年。
4.サラーシュ他、発生生物学、83巻、9−19ページ、1981年。
5.スウォラ他、発生生物学、116巻、31−38ページ、1986年。
6.五島他、臨床整形外科関連研究、269巻、274−283ページ、1991年。
7.アシュトン他、臨床整形外科関連研究、151巻、294−307ページ、1980年。
8.ブルーダー他、骨ミネラル、11巻、141−151ページ、1990年。
9.ベネット他、細胞科学ジャーナル、99巻、131−139ページ、1991年。
10.ベナヤフ他、細胞生理学ジャーナル、140巻、1−7ページ、1989年。
11.中原他、実験細胞研究、195巻,492−503ページ、1991年。
12.デニス他、細胞移植、1巻、2332ページ、1991年。
13.大串他、アクタ・スカンジア.60巻、334−339ページ、1989年。
14.ワン他、増殖因子、9巻、57ページ、1993年。
15.ブキセビッチ他、全米科学アカデミー紀要、86巻、8793ページ、1989年。
16.チェン他、内分泌学、134巻、277ページ、1994年。
17.テネンバウム他、石灰化組織Int.,34巻、76ページ、1982年。
18.ブルーダー他、整形外科研究協会紀要、16巻、58ページ、1991年。
19.レナード他、発生生物学、145巻、99ページ、1991年。
20.チェン他、実験細胞研究、206巻、199ページ、1993年。
21.シフテスタッド他、分化、29巻,230ページ、1985年。
22.チェン他、実験細胞研究、195巻、509ページ、1991年。
23.木村他、生体臨床学研究、5巻、465ページ、1984年。
24.ランギル他、分化、40巻、84ページ、1989年。
25.ラッセル他、実験血液学、20巻、75−79ページ、1992年。
26.ブレンナー他、血液学ブリティッシュジャーナル、77巻、237−244ページ、1991年。
27.ヘインズワース他、骨、13巻、81−88ページ、1992年。
28.グリゴリアディス他、細胞生物学ジャーナル、106巻、2139−2151ページ、1988年。
29.ヘインズワース、他、骨、13巻、69−80ページ、1992年。
30.ブルーダーおよびヘインズワース、準備中。
31.ブルーダーおよびキャプラン、発生生物学、141巻、319−329ページ、1990年。
32.パチフィチ、他、実験細胞研究、195巻、38ページ、1991年。
33.コンスタンチニデス他、ネイチャー、267巻、364−366ページ、1977年。
34.テイラー他、細胞、17巻、771−779ページ、1979年。
35.コニエクスニ他、細胞、38巻、791−800ページ、1984年。
36.ラッサー、細胞、47巻、649−656ページ、1986年。
Claims (33)
- 分離ヒト間葉幹細胞の系列指向分化を単一特定間葉系列に誘導する一つの組成物であって、前記組成物が、ヒト間葉幹細胞と、および間葉幹細胞の分化を単一特定系列に誘導する1個またはそれ以上の生物活性因子とを含むことを特徴とする組成物。
- 請求の範囲第1項記載の組成物であって、ここで前記組成物が、生物活性因子の混合物を含むことを特徴とする組成物。
- 請求の範囲第1項記載の組成物であって、ここで生物活性因子が、骨形成、軟骨形成、腱形成、靭帯形成、筋形成、骨髄ストロマ形成、脂肪細胞形成および皮膚形成の各間葉系列よりなるグループから選択された間葉系列に、分離ヒト間葉幹細胞の分化を誘導することを特徴とする組成物。
- 請求の範囲第1項記載の組成物であって、更に薬理許容担体を含むことを特徴とする組成物。
- 請求の範囲第4項記載の組成物であって、ここで薬理許容担体が、注射可能液であることを特徴とする組成物。
- 請求の範囲第4項記載の組成物であって、ここで薬理許容担体が、硬質多孔性容器であることを特徴とする組成物。
- 請求の範囲第4項記載の組成物であって、ここで薬理許容担体が、ゲルであることを特徴とする組成物。
- 請求の範囲第1項記載の組成物であって、ここで生物活性因子が、ヒト間葉幹細胞の骨形成系列分化を誘導する骨誘導因子であることを特徴とする組成物。
- 請求の範囲第8項記載の組成物であって、ここで骨誘導因子が、骨形態形成タンパク質であることを特徴とする組成物。
- 請求の範囲第9項記載の組成物であって、ここで骨形態形成タンパク質が、BMP−2およびBMP−3よりなるグループから選択されることを特徴とする組成物。
- 請求の範囲第8項記載の組成物であって、ここで骨誘導因子が、繊維芽細胞増殖因子であることを特徴とする組成物。
- 請求の範囲第11項記載の組成物であって、ここで繊維芽細胞増殖因子が、塩基性繊維芽細胞増殖因子であることを特徴とする組成物。
- 請求の範囲第8項記載の組成物であって、ここで骨誘導因子が、グルココルチコイドであることを特徴とする組成物。
- 請求の範囲第13項記載の組成物であって、ここでグルココルチコイドが、デキサメタゾンであることを特徴とする組成物。
- 請求の範囲第8項記載の組成物であって、ここで骨誘導因子が、プロスタグランジンであることを特徴とする組成物。
- 請求の範囲第15項記載の組成物であって、ここでプロスタグランジンが、プロスタグランジンE1であることを特徴とする組成物。
- 請求の範囲第8項記載の組成物であって、更に分離ヒト間葉幹細胞を付随因子と接触させることを含むことを特徴とする組成物。
- 請求の範囲第17項記載の組成物であって、ここで付随因子が、アスコルビン酸およびその類似体ならびにグリセロホスフェートよりなるグループから選択されることを特徴とする組成物。
- 請求の範囲第1項記載の組成物であって、ここで生物活性因子が、ヒト間葉幹細胞の軟骨形成系列分化を誘導する軟骨誘導因子であることを特徴とする組成物。
- 請求の範囲第19項記載の組成物であって、ここで軟骨誘導因子が、形質転換増殖因子−βスーパーファミリーの一員であることを特徴とする組成物。
- 請求の範囲第20項記載の組成物であって、ここで形質転換増殖因子−βスーパーファミリーの一員が、TGF−β1であることを特徴とする組成物。
- 請求の範囲第20項記載の組成物であって、ここで形質転換増殖因子−βスーパーファミリーの一員が、インヒビンAであることを特徴とする組成物。
- 請求の範囲第20項記載の組成物であって、ここで形質転換増殖因子−βスーパーファミリーの一員が、軟骨形成刺激活性因子であることを特徴とする組成物。
- 請求の範囲第20項記載の組成物であって、ここで形質転換増殖因子−βスーパーファミリーの一員が、骨形態形成タンパク質であることを特徴とする組成物。
- 請求の範囲第24項記載の組成物であって、ここで骨形態形成タンパク質が、BMP−4であることを特徴とする組成物。
- 請求の範囲第19項記載の組成物であって、ここで軟骨誘導因子がコラーゲン細胞外マトリックスの成分であることを特徴とする組成物。
- 請求の範囲第26項記載の組成物であって、ここでコラーゲン細胞外マトリックス成分が、コラーゲンIであることを特徴とする組成物。
- 請求の範囲第27項記載の組成物であって、ここでコラーゲンIが、ゲル形態であることを特徴とする組成物。
- 請求の範囲第19項記載の組成物であって、ここで骨誘導因子が、ビタミンA類似体であることを特徴とする組成物。
- 請求の範囲第29項記載の組成物であって、ここでビタミンA類似体が、レチノイン酸であることを特徴とする組成物。
- 請求の範囲第1項記載の組成物であって、生物活性因子が、ヒト間葉幹細胞のストロマ形成系列分化を誘導するストロマ誘導因子であることをと特徴とする組成物。
- 請求の範囲第31項記載の組成物であって、ここでストロマ誘導因子がインターロイキンであることを特徴とする組成物。
- 請求の範囲第32項記載の組成物であって、ここでインターロイキンがインターロイキン1αおよびインターロイキン2よりなるグループから選択されることを特徴とする組成物。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US08/377,461 US5736396A (en) | 1995-01-24 | 1995-01-24 | Lineage-directed induction of human mesenchymal stem cell differentiation |
| US08/377,461 | 1995-01-24 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP52287196A Division JP4454697B2 (ja) | 1995-01-24 | 1996-01-05 | ヒト間葉幹細胞分化の系列指向誘導 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2010012331A true JP2010012331A (ja) | 2010-01-21 |
| JP5173982B2 JP5173982B2 (ja) | 2013-04-03 |
Family
ID=23489200
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP52287196A Expired - Lifetime JP4454697B2 (ja) | 1995-01-24 | 1996-01-05 | ヒト間葉幹細胞分化の系列指向誘導 |
| JP2009242480A Expired - Lifetime JP5173982B2 (ja) | 1995-01-24 | 2009-10-21 | ヒト間葉幹細胞分化の系列指向誘導 |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP52287196A Expired - Lifetime JP4454697B2 (ja) | 1995-01-24 | 1996-01-05 | ヒト間葉幹細胞分化の系列指向誘導 |
Country Status (11)
| Country | Link |
|---|---|
| US (2) | US5736396A (ja) |
| EP (2) | EP0805853B1 (ja) |
| JP (2) | JP4454697B2 (ja) |
| AT (1) | ATE357508T1 (ja) |
| AU (1) | AU719098B2 (ja) |
| CA (1) | CA2211120C (ja) |
| DE (1) | DE69636979T2 (ja) |
| DK (1) | DK0805853T3 (ja) |
| ES (1) | ES2285710T3 (ja) |
| PT (1) | PT805853E (ja) |
| WO (1) | WO1996023059A1 (ja) |
Families Citing this family (338)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5736396A (en) * | 1995-01-24 | 1998-04-07 | Case Western Reserve University | Lineage-directed induction of human mesenchymal stem cell differentiation |
| US6974571B2 (en) * | 1995-03-28 | 2005-12-13 | Thomas Jefferson University | Isolated stromal cells and methods of using the same |
| US6653134B2 (en) * | 1995-03-28 | 2003-11-25 | Cp Hahnemann University | Isolated stromal cells for use in the treatment of diseases of the central nervous system |
| WO1997018299A1 (en) * | 1995-11-16 | 1997-05-22 | Case Western Reserve University | In vitro chondrogenic induction of human mesenchymal stem cells |
| US6787355B1 (en) * | 1996-08-26 | 2004-09-07 | Mcgill University | Multipotent neural stem cells from peripheral tissues and uses thereof |
| US5964805A (en) * | 1997-02-12 | 1999-10-12 | Stone; Kevin R. | Method and paste for articular cartilage transplantation |
| ATE306811T1 (de) * | 1996-12-06 | 2005-11-15 | Osiris Therapeutics Inc | Verbesserte chondrogene differenzierung von menschlichen mesenchym-stammzellen |
| AU731937B2 (en) * | 1996-12-10 | 2001-04-05 | Hadasit Medical Research Services & Development Company Ltd | Serum-derived factor inducing cell differentiation and medical uses thereof |
| CA2284133C (en) * | 1997-03-07 | 2007-05-01 | Chugai Seiyaku Kabushiki Kaisha | Novel cell line and screening method with the use of the same |
| CA2288690A1 (en) * | 1997-05-13 | 1998-11-19 | Osiris Therapeutics, Inc. | Osteoarthritis cartilage regeneration using human mesenchymal stem cells |
| US6110209A (en) * | 1997-08-07 | 2000-08-29 | Stone; Kevin R. | Method and paste for articular cartilage transplantation |
| US6835377B2 (en) | 1998-05-13 | 2004-12-28 | Osiris Therapeutics, Inc. | Osteoarthritis cartilage regeneration |
| ES2292245T3 (es) * | 1998-05-29 | 2008-03-01 | Osiris Therapeutics, Inc. | Celulas madre mesenquimaticas cd45+ y/o fibroblasto+humanas. |
| WO2000005344A1 (en) * | 1998-07-24 | 2000-02-03 | The Carnegie Institution Of Washington | METHOD FOR MAINTENANCE AND PROPAGATION OF GERMLINE STEM CELLS USING MEMBERS OF THE TGF-β FAMILY OF GROWTH FACTORS |
| DE69937888T2 (de) * | 1998-07-31 | 2009-01-02 | Genzyme Corp., Cambridge | Verfahren zur Herstellung mesenchymaler Stammzellen |
| BR9914465A (pt) * | 1998-09-29 | 2001-10-09 | Gamida Cell Ltd | Métodos para controlar a proliferação e a diferenciação de células-tronco e células progenitoras e uma composição farmacêutica para induzir a diferenciação em uma população de células |
| AU1341700A (en) * | 1998-11-13 | 2000-06-05 | Osiris Therapeutics, Inc. | Uses of fibroblasts or supernatants from fibroblasts for the suppression of immune responses in transplantation |
| US7001746B1 (en) | 1999-01-29 | 2006-02-21 | Artecel Sciences, Inc. | Methods and compositions for the differentiation of human preadipocytes into adipocytes |
| US6197061B1 (en) * | 1999-03-01 | 2001-03-06 | Koichi Masuda | In vitro production of transplantable cartilage tissue cohesive cartilage produced thereby, and method for the surgical repair of cartilage damage |
| JP2002537849A (ja) * | 1999-03-10 | 2002-11-12 | ユニヴァーシティ オヴ ピッツバーグ オヴ ザ コモンウェルス システム オヴ ハイアー エデュケーション | 脂肪由来の幹細胞および格子 |
| US20030082152A1 (en) * | 1999-03-10 | 2003-05-01 | Hedrick Marc H. | Adipose-derived stem cells and lattices |
| US6777231B1 (en) | 1999-03-10 | 2004-08-17 | The Regents Of The University Of California | Adipose-derived stem cells and lattices |
| US20050076396A1 (en) * | 1999-03-10 | 2005-04-07 | Katz Adam J. | Adipose-derived stem cells and lattices |
| WO2001011011A2 (en) | 1999-08-05 | 2001-02-15 | Mcl Llc | Multipotent adult stem cells and methods for isolation |
| US6555374B1 (en) | 1999-08-19 | 2003-04-29 | Artecel Sciences, Inc. | Multiple mesodermal lineage differentiation potentials for adipose tissue-derived stromal cells and uses thereof |
| US6429013B1 (en) | 1999-08-19 | 2002-08-06 | Artecel Science, Inc. | Use of adipose tissue-derived stromal cells for chondrocyte differentiation and cartilage repair |
| EP1221956A2 (en) * | 1999-09-30 | 2002-07-17 | McGILL UNIVERSITY | Autologous marrow stem cell (msc) transplantation for myocardial regeneration |
| WO2001034167A1 (en) * | 1999-10-29 | 2001-05-17 | Philadelphia Health & Education Corporation | Isolation and expansion of human marrow stromal cells |
| WO2001048147A1 (en) * | 1999-12-28 | 2001-07-05 | Iso Tis N.V. | Cell culture medium containing growth factors and l-glutamine |
| AU1055201A (en) * | 1999-12-28 | 2001-07-09 | Kyowa Hakko Kogyo Co. Ltd. | Cells capable of differentiating into heart muscle cells |
| US7582292B2 (en) | 2000-02-26 | 2009-09-01 | Artecel, Inc. | Adipose tissue derived stromal cells for the treatment of neurological disorders |
| EP1261694B1 (en) | 2000-02-26 | 2008-01-16 | Artecel, Inc. | Pleuripotent stem cells generated from adipose tissue-derived stromal cells and uses thereof |
| EP1918366A1 (en) | 2000-02-26 | 2008-05-07 | Artecel, Inc. | Pleuripotent stem cells generated from adipose tissue-derived stromal cells and uses thereof |
| US7182781B1 (en) | 2000-03-02 | 2007-02-27 | Regeneration Technologies, Inc. | Cervical tapered dowel |
| PT1276486E (pt) * | 2000-04-25 | 2011-02-07 | Osiris Therapeutics Inc | Reparação de articulação utilizando células estaminais do mesênquima |
| WO2001083709A1 (en) * | 2000-04-28 | 2001-11-08 | Children's Medical Center Corporation | Isolation of mesenchymal stem cells and use thereof |
| US7303769B2 (en) * | 2000-06-05 | 2007-12-04 | University Of South Florida | Method for purifying pluri-differentiated mesenchymal progenitor cells |
| US6936281B2 (en) * | 2001-03-21 | 2005-08-30 | University Of South Florida | Human mesenchymal progenitor cell |
| US7442390B2 (en) * | 2000-06-05 | 2008-10-28 | University Of South Florida | Method for enhancing engraftment of cells using mesenchymal progenitor cells |
| US7049072B2 (en) * | 2000-06-05 | 2006-05-23 | University Of South Florida | Gene expression analysis of pluri-differentiated mesenchymal progenitor cells and methods for diagnosing a leukemic disease state |
| AU2001264763A1 (en) * | 2000-06-05 | 2001-12-17 | University Of South Florida | Human mesenchymal progenitor cell |
| ATE445158T1 (de) * | 2000-06-14 | 2009-10-15 | Vistagen Inc | Toxizitätstypisierung unter verwendung von leberstammzellen |
| WO2002010347A2 (en) * | 2000-08-01 | 2002-02-07 | Yissum Research Development Company | Directed differentiation of embryonic cells |
| US6984522B2 (en) | 2000-08-03 | 2006-01-10 | Regents Of The University Of Michigan | Isolation and use of solid tumor stem cells |
| US8044259B2 (en) | 2000-08-03 | 2011-10-25 | The Regents Of The University Of Michigan | Determining the capability of a test compound to affect solid tumor stem cells |
| US20020045260A1 (en) * | 2000-10-17 | 2002-04-18 | Shih-Chieh Hung | Method of isolating mesenchymal stem cells |
| IL155728A0 (en) * | 2000-11-22 | 2003-11-23 | Geron Corp | Tolerizing allografts of pluripotent stem cells |
| US6921665B2 (en) | 2000-11-27 | 2005-07-26 | Roslin Institute (Edinburgh) | Selective antibody targeting of undifferentiated stem cells |
| US6576464B2 (en) * | 2000-11-27 | 2003-06-10 | Geron Corporation | Methods for providing differentiated stem cells |
| US20080152629A1 (en) * | 2000-12-06 | 2008-06-26 | James Edinger | Placental stem cell populations |
| EP1349918B1 (en) * | 2000-12-06 | 2014-08-06 | Anthrogenesis Corporation | Method of collecting placental stem cells |
| US7311905B2 (en) | 2002-02-13 | 2007-12-25 | Anthrogenesis Corporation | Embryonic-like stem cells derived from post-partum mammalian placenta, and uses and methods of treatment using said cells |
| US20020136709A1 (en) * | 2000-12-12 | 2002-09-26 | Nucleus Remodeling, Inc. | In vitro-derived adult pluripotent stem cells and uses therefor |
| CA2438501C (en) * | 2001-02-14 | 2014-09-16 | Leo T. Furcht | Multipotent adult stem cells, sources thereof, methods of obtaining and maintaining same, methods of differentiation thereof, methods of use thereof and cells derived thereof |
| ES2558626T3 (es) * | 2001-02-14 | 2016-02-05 | Anthrogenesis Corporation | Placenta post-parto de mamíferos, su uso y células madre placentarias de la misma |
| CA2856986C (en) * | 2001-02-14 | 2019-08-13 | Anthrogenesis Corporation | Post-partum mammalian placental stem cells for use in the treatment of neurological or renal diseases and disorders |
| AU2002248484A1 (en) * | 2001-02-21 | 2002-09-12 | Drexel University | Muscle-polymer constructs for bone tissue engineering |
| JP2004532202A (ja) * | 2001-03-15 | 2004-10-21 | シアオ,ヨング−フー | 生存哺乳動物における臨床的に認められた形態の心臓の病状を治療的に処置する方法 |
| WO2002078449A2 (en) * | 2001-04-02 | 2002-10-10 | Advanced Cell Technology, Inc. | Method for facilitating the production of differentiated cell types and tissues from embryonic and adult pluripotent and multipotent cells |
| CN1533431A (zh) * | 2001-04-13 | 2004-09-29 | 细胞移植的方法和试剂 | |
| JP2004533234A (ja) * | 2001-04-13 | 2004-11-04 | アントロジェン カンパニー リミテッド | カプセル化細胞インジケータシステム |
| KR100449141B1 (ko) * | 2001-04-19 | 2004-09-21 | (주)라이프코드 | 간엽 간세포를 신경세포로 분화시키는 방법 |
| ATE433484T1 (de) * | 2001-04-24 | 2009-06-15 | Dolores Baksh | Vorläuferzellpopulationen, deren expansion und die entstehung von nicht-hämatopoetischen zelltypen daraus |
| US20030049236A1 (en) * | 2001-07-27 | 2003-03-13 | Arhus Amt | Immortalized stem cells |
| JP2003052360A (ja) * | 2001-08-20 | 2003-02-25 | Japan Science & Technology Corp | 基底膜細胞外基質を用いた間葉系幹細胞の培養方法 |
| JP2005500847A (ja) * | 2001-08-24 | 2005-01-13 | アドバンスド セル テクノロジー、インコーポレイテッド | 分化誘導薬の同定のためのスクリーニング検定及び細胞治療用の分化細胞の調製 |
| CA2460539C (en) | 2001-09-15 | 2013-10-29 | Rush-Presbyterian-St. Luke's Medical Center | Stratified cartilage tissue and methods to engineer same |
| US7384784B2 (en) * | 2001-09-17 | 2008-06-10 | Ottawa Health Research Institute | Pax-encoding vector and use thereof |
| US20040120933A9 (en) * | 2001-09-17 | 2004-06-24 | Rudnicki Michael A. | Pax-encoding vector and use thereof |
| US9969980B2 (en) * | 2001-09-21 | 2018-05-15 | Garnet Biotherapeutics | Cell populations which co-express CD49c and CD90 |
| US20030165473A1 (en) * | 2001-11-09 | 2003-09-04 | Rush-Presbyterian-St. Luke's Medical Center | Engineered intervertebral disc tissue |
| US7771716B2 (en) * | 2001-12-07 | 2010-08-10 | Cytori Therapeutics, Inc. | Methods of using regenerative cells in the treatment of musculoskeletal disorders |
| US20060204556A1 (en) * | 2001-12-07 | 2006-09-14 | Cytori Therapeutics, Inc. | Cell-loaded prostheses for regenerative intraluminal applications |
| US7585670B2 (en) | 2001-12-07 | 2009-09-08 | Cytori Therapeutics, Inc. | Automated methods for isolating and using clinically safe adipose derived regenerative cells |
| CA2469204A1 (en) * | 2001-12-07 | 2003-06-19 | Regents Of The University Of Michigan | Prospective identification and characterization of breast cancer stem cells |
| US8404229B2 (en) | 2001-12-07 | 2013-03-26 | Cytori Therapeutics, Inc. | Methods of using adipose derived stem cells to treat acute tubular necrosis |
| US20050048035A1 (en) | 2001-12-07 | 2005-03-03 | Fraser John K. | Methods of using regenerative cells in the treatment of stroke and related diseases and disorders |
| US20050008626A1 (en) * | 2001-12-07 | 2005-01-13 | Fraser John K. | Methods of using adipose tissue-derived cells in the treatment of cardiovascular conditions |
| US7595043B2 (en) * | 2001-12-07 | 2009-09-29 | Cytori Therapeutics, Inc. | Method for processing and using adipose-derived stem cells |
| JP4653952B2 (ja) * | 2001-12-07 | 2011-03-16 | サイトリ セラピューティクス インコーポレイテッド | 処理済み脂肪吸引細胞で患者を治療するためのシステムと方法 |
| US9597395B2 (en) | 2001-12-07 | 2017-03-21 | Cytori Therapeutics, Inc. | Methods of using adipose tissue-derived cells in the treatment of cardiovascular conditions |
| US7514075B2 (en) * | 2001-12-07 | 2009-04-07 | Cytori Therapeutics, Inc. | Systems and methods for separating and concentrating adipose derived stem cells from tissue |
| US7651684B2 (en) * | 2001-12-07 | 2010-01-26 | Cytori Therapeutics, Inc. | Methods of using adipose tissue-derived cells in augmenting autologous fat transfer |
| US20050095228A1 (en) * | 2001-12-07 | 2005-05-05 | Fraser John K. | Methods of using regenerative cells in the treatment of peripheral vascular disease and related disorders |
| CA2470031A1 (en) * | 2001-12-20 | 2003-07-03 | Macropore, Inc. | Systems and methods for treating patients with collagen-rich material extracted from adipose tissue |
| IL152904A0 (en) | 2002-01-24 | 2003-06-24 | Gamida Cell Ltd | Utilization of retinoid and vitamin d receptor antagonists for expansion of renewable stem cell populations |
| EP1465982A4 (en) * | 2002-01-25 | 2006-06-07 | Gamida Cell Ltd | PROCESS FOR EXPANSION OF STEM AND PRESERVATIVE CELLS AND EXPANDED CELL POPULATIONS THEREWITH OBTAINED |
| CA2477411A1 (en) * | 2002-03-02 | 2003-09-12 | Board Of Regents, The University Of Texas | Local production and/or delivery of anti-cancer agents by stromal cell precursors |
| US20040091936A1 (en) * | 2002-05-24 | 2004-05-13 | Michael West | Bank of stem cells for producing cells for transplantation having HLA antigens matching those of transplant recipients, and methods for making and using such a stem cell bank |
| US9321992B2 (en) * | 2002-06-14 | 2016-04-26 | Case Western Reserve University | Cell targeting methods and compositions |
| AU2003252559A1 (en) * | 2002-08-17 | 2004-03-03 | Hae-Young Suh | A method for transdifferentiating mesenchymal stem cells into neuronal cells |
| KR100495532B1 (ko) * | 2002-09-18 | 2005-06-14 | 에프씨비파미셀 주식회사 | 간엽 간세포를 신경세포로 분화 및 증식시키는 방법 |
| US9969977B2 (en) * | 2002-09-20 | 2018-05-15 | Garnet Biotherapeutics | Cell populations which co-express CD49c and CD90 |
| EP1556129A4 (en) * | 2002-10-15 | 2011-02-09 | Irm Llc | COMPOSITIONS AND METHODS OF INDUCING OSTEOGENESIS |
| US20050054097A1 (en) * | 2002-11-17 | 2005-03-10 | Tony Peled | EX-VIVO expansion of hematopoietic system cell populations in mononuclear cell cultures |
| US20040101959A1 (en) * | 2002-11-21 | 2004-05-27 | Olga Marko | Treatment of tissue with undifferentiated mesenchymal cells |
| BR0316695A (pt) | 2002-11-26 | 2005-10-18 | Anthrogenesis Corp | Unidade citoterapêutica, kit para tratamento, método de tratamento de uma enfermidade, biblioteca de unidades citoterapêuticas e método de tratamento de um paciente |
| EP1428889A1 (en) * | 2002-12-10 | 2004-06-16 | Epigenomics AG | Method for monitoring the transition of a cell from one state into another |
| KR100484550B1 (ko) * | 2003-01-23 | 2005-04-22 | (주)안트로젠 | 세포 이식을 위한 세포의 생산 방법 |
| JPWO2004076652A1 (ja) * | 2003-02-25 | 2006-06-08 | 学校法人東海大学 | 椎間板再生用の幹細胞用培地及び幹細胞を用いた椎間板の再生 |
| EP1601759A4 (en) * | 2003-03-07 | 2007-02-14 | Gamida Cell Ltd | EXPANSION OF RENEWABLE STEM CELL POPULATIONS USING PI-3 KINASE MODULATORS |
| US8603462B2 (en) * | 2003-04-01 | 2013-12-10 | University Of Utah Research Foundation | Stem-cell, precursor cell, or target cell-based treatment of multi-organ failure and renal dysfunction |
| US7067123B2 (en) | 2003-04-29 | 2006-06-27 | Musculoskeletal Transplant Foundation | Glue for cartilage repair |
| US7901457B2 (en) * | 2003-05-16 | 2011-03-08 | Musculoskeletal Transplant Foundation | Cartilage allograft plug |
| WO2004108908A1 (en) * | 2003-06-06 | 2004-12-16 | The Hospital For Sick Children | Neural crest stem cells and uses thereof |
| EP1639090A4 (en) * | 2003-06-09 | 2008-04-16 | Univ Michigan | COMPOSITIONS AND METHODS OF TREATMENT AND DIAGNOSIS OF CANCER |
| ES2564044T3 (es) | 2003-06-27 | 2016-03-17 | DePuy Synthes Products, Inc. | Células posparto derivadas de tejido del cordón umbilical y métodos de preparación y uso de las mismas |
| US9592258B2 (en) | 2003-06-27 | 2017-03-14 | DePuy Synthes Products, Inc. | Treatment of neurological injury by administration of human umbilical cord tissue-derived cells |
| US9572840B2 (en) | 2003-06-27 | 2017-02-21 | DePuy Synthes Products, Inc. | Regeneration and repair of neural tissue using postpartum-derived cells |
| US8790637B2 (en) | 2003-06-27 | 2014-07-29 | DePuy Synthes Products, LLC | Repair and regeneration of ocular tissue using postpartum-derived cells |
| US7875272B2 (en) | 2003-06-27 | 2011-01-25 | Ethicon, Incorporated | Treatment of stroke and other acute neuraldegenerative disorders using postpartum derived cells |
| US8491883B2 (en) | 2003-06-27 | 2013-07-23 | Advanced Technologies And Regenerative Medicine, Llc | Treatment of amyotrophic lateral sclerosis using umbilical derived cells |
| US8518390B2 (en) | 2003-06-27 | 2013-08-27 | Advanced Technologies And Regenerative Medicine, Llc | Treatment of stroke and other acute neural degenerative disorders via intranasal administration of umbilical cord-derived cells |
| GB0321337D0 (en) * | 2003-09-11 | 2003-10-15 | Massone Mobile Advertising Sys | Method and system for distributing advertisements |
| WO2005032344A2 (en) * | 2003-10-02 | 2005-04-14 | The Regents Of The University Of Michigan | Human prostate cancer cell factor(s) that induce stem cell commitment and osteogenesis |
| EP1687413B8 (en) * | 2003-10-29 | 2008-10-01 | FCB Pharmicell Co., Ltd | Method for differentiating mesenchymal stem cell into neural cell and pharmaceutical composition containing the neural cell for neurodegenerative disease |
| ES2398239T3 (es) * | 2003-11-10 | 2013-03-14 | The Scripps Research Institute | Composiciones y procedimientos para inducir la desdiferenciación celular |
| AU2003286416A1 (en) * | 2003-12-04 | 2005-06-24 | Dr. Ravi Agarwal | A novel process and method for deriving cardiomyocyte precursors from bone-marrow stem cells |
| ES2367694T3 (es) | 2003-12-11 | 2011-11-07 | Isto Technologies Inc. | Sistema de cartílago particulado. |
| EP2319544A1 (en) | 2004-01-16 | 2011-05-11 | Carnegie Mellon University | Cellular labeling for nuclear magnetic resonance techniques |
| AU2005209909B8 (en) * | 2004-02-03 | 2009-01-15 | The Regents Of The University Of Michigan | Compositions and methods for characterizing, regulating, diagnosing, and treating cancer |
| WO2005108559A2 (en) * | 2004-04-23 | 2005-11-17 | Bioe, Inc. | Multi-lineage progenitor cells |
| US7622108B2 (en) * | 2004-04-23 | 2009-11-24 | Bioe, Inc. | Multi-lineage progenitor cells |
| US20050288796A1 (en) * | 2004-06-23 | 2005-12-29 | Hani Awad | Native soft tissue matrix for therapeutic applications |
| US8513011B2 (en) * | 2004-08-26 | 2013-08-20 | Biotech Research Ventures Pte Limited | Methods and compositions for culturing cardiomyocyte-like cells |
| WO2006030442A2 (en) * | 2004-09-16 | 2006-03-23 | Gamida-Cell Ltd. | Methods of ex vivo progenitor and stem cell expansion by co-culture with mesenchymal cells |
| US7837740B2 (en) * | 2007-01-24 | 2010-11-23 | Musculoskeletal Transplant Foundation | Two piece cancellous construct for cartilage repair |
| AU2005304687B2 (en) | 2004-11-11 | 2012-01-19 | The General Hosptial Corporation | Parathyroid hormone receptor activation and stem and progenitor cell expansion |
| US20060165667A1 (en) * | 2004-12-03 | 2006-07-27 | Case Western Reserve University | Novel methods, compositions and devices for inducing neovascularization |
| ES2621847T3 (es) | 2004-12-23 | 2017-07-05 | DePuy Synthes Products, Inc. | Células posparto derivadas de tejido de cordón umbilical, y métodos de elaboración y uso de las mismas |
| WO2006071778A2 (en) | 2004-12-23 | 2006-07-06 | Ethicon Incorporated | Treatment of parkinson's disease and related disorders using postpartum derived cells |
| KR100833612B1 (ko) | 2004-12-29 | 2008-05-30 | 에프씨비파미셀 주식회사 | 간엽 간세포로부터 분화된 신경세포를 유효성분으로함유하는 신경계 질환 치료용 약학 조성물 |
| CA2512667A1 (en) * | 2005-01-07 | 2006-07-07 | Takahiro Ochiya | Human hepatocyte-like cells and uses thereof |
| EP1844434A4 (en) * | 2005-01-10 | 2013-11-13 | Cytori Therapeutics Inc | DEVICES AND METHODS FOR MONITORING, MANAGING AND SERVICING MEDICAL DEVICES |
| JP2006289062A (ja) * | 2005-03-18 | 2006-10-26 | Pentax Corp | 肥大化能を有する軟骨細胞と足場を用いた骨補填材料 |
| EP2399991B1 (en) * | 2005-04-12 | 2017-09-27 | Mesoblast, Inc. | Isolation of adult multipotential cells by tissue non-specific alkaline phosphatase |
| US20060252073A1 (en) * | 2005-04-18 | 2006-11-09 | Regents Of The University Of Michigan | Compositions and methods for the treatment of cancer |
| WO2006121445A2 (en) * | 2005-05-10 | 2006-11-16 | United States Of America Department Of Veteran's Affairs | Therapy of kidney diseases and multiorgan failure with mesenchymal stem cells and mesenchymal stem cell conditioned media |
| WO2006130433A2 (en) | 2005-05-27 | 2006-12-07 | Viacell, Inc. | Treatment of ischemia using stem cells |
| WO2006135886A2 (en) * | 2005-06-13 | 2006-12-21 | The Regents Of The University Of Michigan | Compositions and methods for treating and diagnosing cancer |
| WO2006138275A2 (en) * | 2005-06-13 | 2006-12-28 | The Regents Of The University Of Michigan | Compositions and methods for treating and diagnosing cancer |
| US7815926B2 (en) * | 2005-07-11 | 2010-10-19 | Musculoskeletal Transplant Foundation | Implant for articular cartilage repair |
| US8440460B2 (en) * | 2005-07-27 | 2013-05-14 | The Board Of Regents Of The University Of Texas System | Methods for transdifferentiating cells |
| MX2008001709A (es) * | 2005-08-01 | 2008-11-26 | Nupotential Inc | Produccion de celulas reprogramadas con potencial restablecido. |
| WO2007025290A2 (en) | 2005-08-26 | 2007-03-01 | Isto Technologies, Inc. | Implants and methods for repair, replacement and treatment of joint disease |
| EP1926459B1 (en) | 2005-09-19 | 2015-01-07 | Histogenics Corporation | Cell-support matrix having narrowly defined uniformly vertically and non-randomly organized porosity and pore density and a method for preparation thereof |
| EP1957633B1 (en) | 2005-10-13 | 2013-12-18 | Anthrogenesis Corporation | Immunomodulation using placental stem cells |
| WO2007053648A2 (en) * | 2005-10-31 | 2007-05-10 | The Regents Of The University Of Michigan | Compositions and methods for treating and diagnosing cancer |
| DK1978993T3 (en) | 2005-10-31 | 2017-03-20 | Oncomed Pharm Inc | Compositions and Methods for Treating Cancer Based on Human FZD Receptors |
| US7723477B2 (en) | 2005-10-31 | 2010-05-25 | Oncomed Pharmaceuticals, Inc. | Compositions and methods for inhibiting Wnt-dependent solid tumor cell growth |
| US20070104693A1 (en) * | 2005-11-07 | 2007-05-10 | Quijano Rodolfo C | Breast augmentation system |
| US20070104692A1 (en) * | 2005-11-07 | 2007-05-10 | Quijano Rodolfo C | Breast tissue regeneration |
| US8846393B2 (en) | 2005-11-29 | 2014-09-30 | Gamida-Cell Ltd. | Methods of improving stem cell homing and engraftment |
| US9155762B2 (en) * | 2005-12-08 | 2015-10-13 | University Of Louisville Research Foundation, Inc. | Uses and isolation of stem cells from bone marrow |
| US20090220466A1 (en) * | 2005-12-08 | 2009-09-03 | Mariusz Ratajczak | Very small embryonic-like (vsel) stem cells and methods of isolating and using the same |
| EP1971681B1 (en) | 2005-12-16 | 2017-08-23 | DePuy Synthes Products, Inc. | Compositions and methods for inhibiting adverse immune response in histocompatibility-mismatched transplantation |
| US8741638B2 (en) * | 2005-12-19 | 2014-06-03 | DePuy Synthes Products, LLC | In vitro expansion of postpartum-derived cells in roller bottles |
| US9125906B2 (en) | 2005-12-28 | 2015-09-08 | DePuy Synthes Products, Inc. | Treatment of peripheral vascular disease using umbilical cord tissue-derived cells |
| EP2471907B1 (en) * | 2005-12-29 | 2018-09-26 | Celularity, Inc. | Placental stem cell populations |
| JP2009521930A (ja) | 2005-12-29 | 2009-06-11 | アントフロゲネシス コーポレーション | 胎盤幹細胞及び第2供給源由来幹細胞の共存培養 |
| EP1978977A4 (en) * | 2006-01-24 | 2010-03-17 | Christopher J Centeno | METHOD AND SYSTEM FOR ISOLATION AND TRANSPLANTATION OF MESENCHYMAL STEM CELLS FOR USE IN CLINICAL MEDIA |
| PT1989295T (pt) * | 2006-02-16 | 2020-10-29 | Univ Bruxelles | Processo para diferenciação osteogénica de células estaminais de medula óssea (cemo) e as suas utilizações |
| KR101490449B1 (ko) | 2006-03-23 | 2015-02-05 | 플루리스템 리미티드 | 세포 증식 방법 및 세포의 용도 및 치료를 위해 그 세포에 의해 제조되는 조절된 배지 |
| EP2012832A2 (en) * | 2006-04-14 | 2009-01-14 | Celsense, Inc. | Methods for assessing cell labeling |
| JP2009533684A (ja) * | 2006-04-14 | 2009-09-17 | カーネギー・メロン・ユニバーシティ | 核磁気共鳴技術のための細胞標識及び定量 |
| CA2646491A1 (en) * | 2006-04-17 | 2007-10-25 | Bioe, Inc. | Differentiation of multi-lineage progenitor cells to respiratory epithelial cells |
| US20090304644A1 (en) * | 2006-05-30 | 2009-12-10 | Cytori Therapeutics, Inc. | Systems and methods for manipulation of regenerative cells separated and concentrated from adipose tissue |
| JP2009538615A (ja) * | 2006-05-31 | 2009-11-12 | スティックス エルエルシー | 幹細胞の選別方法およびその使用 |
| KR20090031895A (ko) * | 2006-06-09 | 2009-03-30 | 안트로제네시스 코포레이션 | 태반 니치 및 줄기 세포 배양을 위한 이의 용도 |
| US20080038231A1 (en) | 2006-06-15 | 2008-02-14 | Rodgerson Denis O | Processing procedure for peripheral blood stem cells |
| US20080003681A1 (en) * | 2006-06-28 | 2008-01-03 | Mahalaxmi Gita Bangera | Methods for altering cellular susceptibility to infection |
| WO2008013863A2 (en) * | 2006-07-26 | 2008-01-31 | Cytori Therapeutics, Inc. | Generation of adipose tissue and adipocytes |
| US7993918B2 (en) * | 2006-08-04 | 2011-08-09 | Anthrogenesis Corporation | Tumor suppression using placental stem cells |
| JP2010507392A (ja) | 2006-10-23 | 2010-03-11 | アントフロゲネシス コーポレーション | 胎盤細胞集団で骨欠損を治療するための方法及び組成物 |
| US20090155225A1 (en) * | 2006-11-02 | 2009-06-18 | Mariusz Ratajczak | Uses and isolation of very small of embryonic-like (vsel) stem cells |
| US8163549B2 (en) | 2006-12-20 | 2012-04-24 | Zimmer Orthobiologics, Inc. | Method of obtaining viable small tissue particles and use for tissue repair |
| US20080154233A1 (en) * | 2006-12-20 | 2008-06-26 | Zimmer Orthobiologics, Inc. | Apparatus for delivering a biocompatible material to a surgical site and method of using same |
| EP2106439B1 (en) | 2007-01-24 | 2014-11-12 | The Regents of the University of Michigan | Compositions and methods for treating and diagnosing pancreatic cancer |
| KR20150039214A (ko) | 2007-02-12 | 2015-04-09 | 안트로제네시스 코포레이션 | 태반 줄기세포를 이용한 염증 질환의 치료 |
| US8435551B2 (en) | 2007-03-06 | 2013-05-07 | Musculoskeletal Transplant Foundation | Cancellous construct with support ring for repair of osteochondral defects |
| US7632340B2 (en) * | 2007-03-07 | 2009-12-15 | Hamilton Beach Brands, Inc. | Air purifier for removing particles or contaminants from air |
| EP2134297B1 (en) | 2007-04-12 | 2017-03-08 | Zimmer, Inc. | Apparatus for tissue repair |
| TWM322542U (en) * | 2007-05-23 | 2007-11-21 | Universal Scient Ind Co Ltd | Testing machine |
| US9511076B2 (en) * | 2008-05-30 | 2016-12-06 | Clarion Research Group | Formulations and methods for recovery from dental surgery |
| US20120195938A1 (en) * | 2007-05-30 | 2012-08-02 | James Louis Rutkowski | Formulations and methods for recovery from dental surgery |
| US8124130B1 (en) * | 2007-05-30 | 2012-02-28 | James Louis Rutkowski | Formulations and methods for recovery from dental surgery |
| CA2689484A1 (en) * | 2007-06-06 | 2008-12-11 | The Hospital For Sick Children | Skin-derived precursor cells and uses thereof |
| US8354370B2 (en) * | 2007-06-15 | 2013-01-15 | Garnet Biotherapeutics, Inc. | Administering a biological composition or compositions isolated from self-renewing colony forming somatic cell growth medium to treat diseases and disorders |
| CA2688504A1 (en) | 2007-06-18 | 2008-12-24 | Children's Hospital & Research Center At Oakland | Method of isolating stem and progenitor cells from placenta |
| US9095562B2 (en) | 2007-07-05 | 2015-08-04 | Regenerative Sciences, Inc. | Methods and compositions for optimized expansion and implantation of mesenchymal stem cells |
| WO2009009105A2 (en) * | 2007-07-10 | 2009-01-15 | Carnegie Mellon University | Compositions and methods for producing cellular labels for nuclear magnetic resonance techniques |
| US20090029463A1 (en) * | 2007-07-25 | 2009-01-29 | Bioe, Inc. | Differentiation of Multi-Lineage Progenitor Cells to Chondrocytes |
| US9200253B1 (en) | 2007-08-06 | 2015-12-01 | Anthrogenesis Corporation | Method of producing erythrocytes |
| PT2194121T (pt) * | 2007-09-11 | 2016-12-05 | Univ Sapporo Medical | Método de proliferação celular e agente farmacêutico para reparação e regeneração de tecidos |
| JP2010539228A (ja) | 2007-09-19 | 2010-12-16 | プルリステム リミテッド | 脂肪組織または胎盤組織に由来する接着性細胞および治療におけるその使用 |
| KR20200043517A (ko) * | 2007-09-26 | 2020-04-27 | 안트로제네시스 코포레이션 | 인간 태반 관류액으로부터의 혈관형성 세포 |
| KR101955140B1 (ko) | 2007-09-28 | 2019-03-06 | 안트로제네시스 코포레이션 | 인간 태반 관류액 및 인간 태반-유래 중간체 천연 킬러 세포를 사용한 종양 억제 방법 |
| WO2009046346A2 (en) | 2007-10-04 | 2009-04-09 | Medistem Laboratories, Inc. | Stem cell therapy for weight loss |
| CN102036688B (zh) | 2007-10-05 | 2014-07-02 | 伊西康公司 | 使用人脐带组织来源的细胞进行肾脏组织的修复和再生 |
| WO2009058983A2 (en) * | 2007-10-30 | 2009-05-07 | University Of Louisville Research Foundation, Inc. | Subpopulations of bone marrow-derived adherent stem cells and methods of use therefor |
| EP2210608B1 (en) | 2007-11-02 | 2016-08-31 | JCR Pharmaceuticals CO., LTD. | Pharmaceutical composition containing human mesenchymal stem cell |
| WO2009085969A2 (en) * | 2007-12-19 | 2009-07-09 | Regenerative Sciences, Llc | Compositions and methods to promote implantation and engrafment of stem cells |
| US8236538B2 (en) * | 2007-12-20 | 2012-08-07 | Advanced Technologies And Regenerative Medicine, Llc | Methods for sterilizing materials containing biologically active agents |
| US20100278788A1 (en) * | 2008-01-11 | 2010-11-04 | Bone Therapeutics, S.A. | Osteogenic Differentiation Of Bone Marrow Stem Cells And Mesenchymal Stem Cells Using A Combination Of Growth Factors |
| US8685728B2 (en) * | 2008-01-31 | 2014-04-01 | Rutgers The State University Of New Jersey | Kit containing stem cells and cytokines for use in attenuating immune responses |
| US10046011B2 (en) | 2008-01-31 | 2018-08-14 | Rutgers, The State University Of New Jersey | Compositions for inducing or suppressing an immune response |
| EP2265220A1 (en) | 2008-03-05 | 2010-12-29 | Musculoskeletal Transplant Foundation | Cancellous constructs, cartilage particles and combinations of cancellous constructs and cartilage particles |
| EP2257176B1 (en) | 2008-03-14 | 2013-09-18 | Regenerative Sciences, LLC | Compositions and methods for cartilage repair |
| WO2009154840A2 (en) * | 2008-03-27 | 2009-12-23 | Neostem, Inc. | Compositions and methods using stem cells in cutaneous wound healing |
| WO2009134435A2 (en) * | 2008-05-02 | 2009-11-05 | Celsense Inc. | Compositions and methods for producing emulsions for nuclear magnetic resonance techniques and other applications |
| KR20160065213A (ko) | 2008-05-07 | 2016-06-08 | 본 테라퓨틱스 소시에테아노님 | 간엽 줄기 세포 및 골-형성 세포 |
| US20090291494A1 (en) * | 2008-05-21 | 2009-11-26 | Bioe, Inc. | Differentiation of Multi-Lineage Progenitor Cells to Pancreatic Cells |
| CN102123717A (zh) | 2008-05-27 | 2011-07-13 | 普拉里斯坦有限公司 | 治疗炎性结肠疾病的方法 |
| WO2010021993A1 (en) * | 2008-08-19 | 2010-02-25 | Cytori Therapeutics, Inc. | Methods of using adipose tissue-derived cells in the treatment of the lymphatic system and malignant disease |
| NZ591294A (en) * | 2008-08-20 | 2012-10-26 | Anthrogenesis Corp | Treatment of stroke using isolated placental cells |
| MX339624B (es) | 2008-08-20 | 2016-06-02 | Anthrogenesis Corp | Composiciones mejoradas de celulas y metodos para preparar las mismas. |
| CA2965883C (en) | 2008-08-22 | 2020-05-12 | Anthrogenesis Corporation | Methods and compositions for treatment of bone defects with placental cell populations |
| EP2334783B1 (en) | 2008-09-02 | 2016-06-22 | Pluristem Ltd. | Adherent cells from placenta tissue and use thereof in therapy |
| MX2011003183A (es) | 2008-09-26 | 2011-04-21 | Oncomed Pharm Inc | Agentes que se unen a receptor encrespado y usos de los mismos. |
| US8748177B2 (en) | 2008-09-30 | 2014-06-10 | The Hospital For Sick Children | Compositions for proliferation of cells and related methods |
| EP2182055A1 (en) | 2008-10-14 | 2010-05-05 | Heinrich-Heine-Universität Düsseldorf | Human cord blood derived unrestricted somatic stem cells (USSC) |
| RU2562154C2 (ru) | 2008-11-19 | 2015-09-10 | Антродженезис Корпорейшн | Амниотические адгезивные клетки |
| US9192695B2 (en) | 2008-11-20 | 2015-11-24 | Allosource | Allografts combined with tissue derived stem cells for bone healing |
| WO2010060031A1 (en) * | 2008-11-21 | 2010-05-27 | Anthrogenesis Corporation | Treatment of diseases, disorders or conditions of the lung using placental cells |
| KR20120006481A (ko) | 2008-12-05 | 2012-01-18 | 리제너러티브 사이언시즈, 엘엘씨 | 무혈관 조직의 복구를 촉진하기 위한 방법 및 조성물 |
| US20100168022A1 (en) * | 2008-12-11 | 2010-07-01 | Centeno Christopher J | Use of In-Vitro Culture to Design or Test Personalized Treatment Regimens |
| CN107028983A (zh) | 2008-12-19 | 2017-08-11 | 德普伊新特斯产品有限责任公司 | 肺部疾病和病症的治疗 |
| US10179900B2 (en) * | 2008-12-19 | 2019-01-15 | DePuy Synthes Products, Inc. | Conditioned media and methods of making a conditioned media |
| US8771677B2 (en) * | 2008-12-29 | 2014-07-08 | Vladimir B Serikov | Colony-forming unit cell of human chorion and method to obtain and use thereof |
| EP2411504B1 (en) | 2009-03-26 | 2017-05-10 | DePuy Synthes Products, Inc. | Human umbilical cord tissue cells as therapy for alzheimer's disease |
| ES2405605T3 (es) | 2009-03-27 | 2013-05-31 | Wyeth Llc | Células iniciadoras de tumores y procedimientos de uso de las mismas |
| US9133431B2 (en) * | 2009-05-01 | 2015-09-15 | Bimini Technologies Llc | Systems, methods and compositions for optimizing tissue and cell enriched grafts |
| MX353489B (es) | 2009-07-02 | 2018-01-16 | Anthrogenesis Corp | Metodo para producir eritrocitos sin celulas alimentadoras. |
| SG10201404281YA (en) | 2009-07-21 | 2014-09-26 | Abt Holding Co | Use of stem cells to reduce leukocyte extravasation |
| CN102625829B (zh) | 2009-07-21 | 2015-05-06 | Abt控股公司 | 干细胞用于减少白细胞外渗的用途 |
| US20110054929A1 (en) * | 2009-09-01 | 2011-03-03 | Cell Solutions Colorado Llc | Stem Cell Marketplace |
| US9113950B2 (en) | 2009-11-04 | 2015-08-25 | Regenerative Sciences, Llc | Therapeutic delivery device |
| IN2012DN05181A (ja) | 2009-11-12 | 2015-10-23 | Vbi Technologies Llc | |
| TWI535445B (zh) | 2010-01-12 | 2016-06-01 | 安可美德藥物股份有限公司 | Wnt拮抗劑及治療和篩選方法 |
| US8476227B2 (en) | 2010-01-22 | 2013-07-02 | Ethicon Endo-Surgery, Inc. | Methods of activating a melanocortin-4 receptor pathway in obese subjects |
| US9044606B2 (en) | 2010-01-22 | 2015-06-02 | Ethicon Endo-Surgery, Inc. | Methods and devices for activating brown adipose tissue using electrical energy |
| US9121007B2 (en) * | 2010-01-26 | 2015-09-01 | Anthrogenesis Corporatin | Treatment of bone-related cancers using placental stem cells |
| SG10201914001QA (en) | 2010-02-25 | 2020-03-30 | Abt Holding Co | Modulation of macrophage activation |
| BR112012022946A2 (pt) | 2010-03-12 | 2017-02-07 | Daiichi Sankyo Co Ltd | método para proliferar cardiomiócitos usando micro-rna |
| CA2794674A1 (en) | 2010-04-01 | 2011-10-06 | Oncomed Pharmaceuticals, Inc. | Frizzled-binding agents and uses thereof |
| KR20240096688A (ko) | 2010-04-07 | 2024-06-26 | 셀룰래리티 인코포레이티드 | 태반 줄기 세포를 사용한 혈관신생 |
| US8562973B2 (en) | 2010-04-08 | 2013-10-22 | Anthrogenesis Corporation | Treatment of sarcoidosis using placental stem cells |
| JP5968871B2 (ja) | 2010-04-13 | 2016-08-10 | セルラー ダイナミクス インターナショナル, インコーポレイテッド | フォワードプログラミングによる肝細胞の産生 |
| US8455254B2 (en) * | 2010-04-22 | 2013-06-04 | Taipei Medical University | Method of accelerating osteogenic differentiation and composition thereof |
| WO2011133658A1 (en) | 2010-04-22 | 2011-10-27 | Boston Medical Center Corporation | Compositions and methods for targeting and delivering therapeutics into cells |
| US20110312001A1 (en) | 2010-06-15 | 2011-12-22 | Emile Nuwaysir | Compendium of ready-built stem cell models for interrogation of biological response |
| CA2804595C (en) | 2010-07-07 | 2018-11-13 | Cellular Dynamics International, Inc. | Endothelial cell production by programming |
| EP2590695B1 (en) | 2010-07-09 | 2024-11-20 | GID BIO, Inc. | Apparatus and methods relating to collecting and processing human biological material containing adipose |
| WO2013106655A1 (en) | 2012-01-11 | 2013-07-18 | The Gid Group, Inc. | Method for processing adipose tissue and processing apparatus |
| US9296984B2 (en) | 2010-07-09 | 2016-03-29 | The Gid Group, Inc. | Tissue processing apparatus and method for processing adipose tissue |
| US9206387B2 (en) | 2010-07-09 | 2015-12-08 | The Gid Group, Inc. | Method and apparatus for processing adipose tissue |
| CA2804750C (en) | 2010-07-13 | 2022-05-10 | Anthrogenesis Corporation | Methods of generating natural killer cells |
| EP2625263B1 (en) | 2010-10-08 | 2020-03-11 | Terumo BCT, Inc. | Configurable methods and systems of growing and harvesting cells in a hollow fiber bioreactor system |
| US20120087933A1 (en) | 2010-10-08 | 2012-04-12 | Samson Tom | Enhanced msc preparations |
| WO2012092049A2 (en) | 2010-12-29 | 2012-07-05 | Ethicon Endo-Surgery, Inc. | Brown adipocyte modification |
| US8969315B2 (en) | 2010-12-31 | 2015-03-03 | Anthrogenesis Corporation | Enhancement of placental stem cell potency using modulatory RNA molecules |
| PL2667878T3 (pl) | 2011-01-25 | 2016-10-31 | Kompozycje i sposoby transplantacji komórek | |
| WO2013110354A1 (en) | 2012-01-25 | 2013-08-01 | Université Catholique de Louvain | Compositions and methods for cell transplantation |
| EP2673358B1 (en) | 2011-02-08 | 2019-01-09 | FUJIFILM Cellular Dynamics, Inc. | Hematopoietic precursor cell production by programming |
| KR101903339B1 (ko) | 2011-03-22 | 2018-10-01 | 플루리스템 리미티드 | 방사선 또는 화학적 손상을 치료하는 방법 |
| CA2837871C (en) | 2011-06-01 | 2021-12-07 | Anthrogenesis Corporation | Treatment of pain using placental stem cells |
| BR112013031368B1 (pt) | 2011-06-06 | 2021-12-07 | ReGenesys BVBA | Método de expandir células ex vivo |
| US20130071360A1 (en) | 2011-06-29 | 2013-03-21 | Biorestorative Therapies, Inc. | Brown Fat Cell Compositions and Methods |
| WO2013055476A1 (en) | 2011-09-09 | 2013-04-18 | Anthrogenesis Corporation | Treatment of amyotrophic lateral sclerosis using placental stem cells |
| CA2849380A1 (en) | 2011-10-11 | 2013-04-18 | Bone Therapeutics S.A. | Uses of growth and differentiation factor 8 (gdf-8) |
| CA2869681A1 (en) | 2011-12-23 | 2013-06-27 | Advanced Technologies And Regenerative Medicine, Llc | Detection of human umbilical cord tissue-derived cells |
| US20140377832A1 (en) | 2012-01-15 | 2014-12-25 | Yeda Research And Development Co. Ltd. | Induction of dedifferentiation of mesenchymal stromal cells |
| US10047345B2 (en) | 2012-02-13 | 2018-08-14 | Gamida-Cell Ltd. | Culturing of mesenchymal stem cells with FGF4 and nicotinamide |
| US9434926B1 (en) * | 2012-02-23 | 2016-09-06 | University Of South Florida | Graphene hydrogel and methods of using the same |
| WO2013184966A1 (en) * | 2012-06-06 | 2013-12-12 | University Of Central Florida Research Foundation, Inc. | Compositions, methods and systems for cellular differentiation from stem cells |
| US9175266B2 (en) | 2012-07-23 | 2015-11-03 | Gamida Cell Ltd. | Enhancement of natural killer (NK) cell proliferation and activity |
| US9567569B2 (en) | 2012-07-23 | 2017-02-14 | Gamida Cell Ltd. | Methods of culturing and expanding mesenchymal stem cells |
| BR112015004003B1 (pt) | 2012-09-06 | 2020-05-19 | The Gid Group, Inc. | aparelho para processar material biológico humano contendo tecido fibroso e método para processar tecido adiposo |
| PL2900247T3 (pl) | 2012-09-26 | 2018-05-30 | Bone Therapeutics S.A. | Kompozycje zawierające osocze poddane obróbce rozpuszczalnikiem/detergentem i kwas hialuronowy do zastosowania w leczeniu zaburzeń układu mięśniowo-szkieletowego |
| JP2015536933A (ja) | 2012-10-23 | 2015-12-24 | オンコメッド ファーマシューティカルズ インコーポレイテッド | Wnt経路結合剤を用いて神経内分泌腫瘍を処置する方法 |
| US20140178343A1 (en) | 2012-12-21 | 2014-06-26 | Jian Q. Yao | Supports and methods for promoting integration of cartilage tissue explants |
| JP2016510411A (ja) | 2013-02-04 | 2016-04-07 | オンコメッド ファーマシューティカルズ インコーポレイテッド | Wnt経路インヒビターによる処置の方法およびモニタリング |
| HK1218515A1 (zh) | 2013-02-05 | 2017-02-24 | 人类起源公司 | 来自胎盘的自然杀伤细胞 |
| US10351910B2 (en) | 2013-02-20 | 2019-07-16 | Pluristem Ltd | Gene and protein expression properties of adherent stromal cells cultured in 3D |
| JP2016508726A (ja) | 2013-02-22 | 2016-03-24 | セルラー ダイナミクス インターナショナル, インコーポレイテッド | 組み合わせた遺伝的および化学的操作によるフォワードプログラミングを介した肝細胞の産生 |
| US9168300B2 (en) | 2013-03-14 | 2015-10-27 | Oncomed Pharmaceuticals, Inc. | MET-binding agents and uses thereof |
| CA2899713C (en) | 2013-03-15 | 2022-07-19 | Allosource | Cell repopulated collagen matrix for soft tissue repair and regeneration |
| US10266807B2 (en) | 2013-04-03 | 2019-04-23 | FUJIFILM Cellular Dynamics, Inc. | Methods and compositions for culturing endoderm progenitor cells in suspension |
| ES2827250T3 (es) | 2013-04-12 | 2021-05-20 | Houston Methodist Hospital | Mejora de órganos para trasplante |
| EP3795678B1 (en) | 2013-04-19 | 2023-07-12 | Biorestorative Therapies, Inc. | Human brown adipose derived stem cells and uses |
| ES2753323T3 (es) | 2013-04-30 | 2020-04-08 | Univ Leuven Kath | Terapia celular para síndromes mielodisplásicos |
| WO2015035221A1 (en) | 2013-09-05 | 2015-03-12 | The Gid Group, Inc. | Tissue processing apparatus and method for processing adipose tissue |
| WO2015073918A1 (en) | 2013-11-16 | 2015-05-21 | Terumo Bct, Inc. | Expanding cells in a bioreactor |
| WO2015148704A1 (en) | 2014-03-25 | 2015-10-01 | Terumo Bct, Inc. | Passive replacement of media |
| US20170107486A1 (en) | 2014-04-21 | 2017-04-20 | Cellular Dynamics International, Inc. | Hepatocyte production via forward programming by combined genetic and chemical engineering |
| EP3177709B1 (en) | 2014-08-07 | 2022-05-18 | The J. David Gladstone Institutes, A Testamentary Trust Established under The Will of J. David Gladstone | Reversible stencils for fabricating micro-tissues |
| US20170296589A1 (en) | 2014-09-23 | 2017-10-19 | Case Western Reserve University | Compositions and methods for treating lung remodeling diseases |
| CN106715676A (zh) | 2014-09-26 | 2017-05-24 | 泰尔茂比司特公司 | 按计划供养 |
| US10077420B2 (en) | 2014-12-02 | 2018-09-18 | Histogenics Corporation | Cell and tissue culture container |
| US10092738B2 (en) | 2014-12-29 | 2018-10-09 | Ethicon Llc | Methods and devices for inhibiting nerves when activating brown adipose tissue |
| US10080884B2 (en) | 2014-12-29 | 2018-09-25 | Ethicon Llc | Methods and devices for activating brown adipose tissue using electrical energy |
| WO2016170112A1 (en) | 2015-04-23 | 2016-10-27 | Bone Therapeutics S.A. | In vitro preservation of therapeutic cells |
| WO2017004592A1 (en) | 2015-07-02 | 2017-01-05 | Terumo Bct, Inc. | Cell growth with mechanical stimuli |
| US11312940B2 (en) | 2015-08-31 | 2022-04-26 | University Of Louisville Research Foundation, Inc. | Progenitor cells and methods for preparing and using the same |
| US11578306B2 (en) | 2015-09-24 | 2023-02-14 | Cellect Biotherapeutics Ltd. | Methods for propagating mesenchymal stem cells (MSC) for use in transplantation |
| WO2017143071A1 (en) | 2016-02-18 | 2017-08-24 | The Regents Of The University Of California | Methods and compositions for gene editing in stem cells |
| US9918994B2 (en) | 2016-03-04 | 2018-03-20 | The Board Of Trustees Of The Leland Stanford Junior University | Compositions and methods for muscle regeneration using prostaglandin E2 |
| EP3423568A4 (en) | 2016-03-04 | 2019-11-13 | University Of Louisville Research Foundation, Inc. | METHOD AND COMPOSITIONS FOR EX-VIVO REPRODUCTION OF VERY SMALL EMBRYONAL STEM CELLS (VSELS) |
| JP7002530B2 (ja) | 2016-03-29 | 2022-02-04 | エスエムエスバイオテック インコーポレイテッド | 小型運動性幹細胞を使用した組成物および方法 |
| JP7034949B2 (ja) | 2016-05-25 | 2022-03-14 | テルモ ビーシーティー、インコーポレーテッド | 細胞の増殖 |
| US20200325449A1 (en) | 2016-06-02 | 2020-10-15 | The Cleveland Clinic Foundation | Complement inhibition for improving cell viability |
| US11104874B2 (en) | 2016-06-07 | 2021-08-31 | Terumo Bct, Inc. | Coating a bioreactor |
| US11685883B2 (en) | 2016-06-07 | 2023-06-27 | Terumo Bct, Inc. | Methods and systems for coating a cell growth surface |
| JP6864335B2 (ja) * | 2016-08-24 | 2021-04-28 | 国立大学法人 東京大学 | 軟骨細胞の製造方法 |
| KR20190046844A (ko) | 2016-08-30 | 2019-05-07 | 라이프셀 코포레이션 | 의료 디바이스 제어를 위한 시스템 및 방법 |
| USD851777S1 (en) | 2017-01-30 | 2019-06-18 | Lifecell Corporation | Canister-type device for tissue processing |
| US11624046B2 (en) | 2017-03-31 | 2023-04-11 | Terumo Bct, Inc. | Cell expansion |
| EP3656841A1 (en) | 2017-03-31 | 2020-05-27 | Terumo BCT, Inc. | Cell expansion |
| US12234441B2 (en) | 2017-03-31 | 2025-02-25 | Terumo Bct, Inc. | Cell expansion |
| AU2018280264B2 (en) | 2017-06-09 | 2024-07-11 | Myoforte Therapeutics, Inc. | Compositions and methods for preventing or treating muscle conditions |
| WO2019018002A1 (en) | 2017-07-18 | 2019-01-24 | The Gid Group, Inc. | ADIPOSE TISSUE DIGESTION SYSTEM AND METHOD FOR TREATING TISSUE |
| SG11202003524XA (en) | 2017-10-20 | 2020-05-28 | Bone Therapeutics Sa | Methods for differentiating mesenchymal stem cells |
| SG11202004680UA (en) | 2017-11-22 | 2020-06-29 | Mesoblast Int Sarl | Cellular compositions and methods of treatment i |
| WO2020014528A1 (en) | 2018-07-13 | 2020-01-16 | The Regents Of The University Of California | Retrotransposon-based delivery vehicle and methods of use thereof |
| EP3841205A4 (en) | 2018-08-22 | 2022-08-17 | The Regents of The University of California | Variant type v crispr/cas effector polypeptides and methods of use thereof |
| JP2022501053A (ja) | 2018-09-25 | 2022-01-06 | ボーン、セラピューティクス、エスアーBone Thrapeutics Sa | 間葉系幹細胞を分化させるための方法 |
| SG11202102874UA (en) | 2018-09-25 | 2021-04-29 | Bone Therapeutics Sa | Methods and uses for determining osteogenic potential of in vitro differentiated cells |
| WO2020086687A1 (en) * | 2018-10-23 | 2020-04-30 | The Johns Hopkins University | Partioning of adult mesenchymal stem cells |
| EP3877517A4 (en) | 2018-11-09 | 2022-09-07 | Inari Agriculture, Inc. | RNA-DRIVEN NUCLEASES AND DNA-BINDING PROTEINS |
| AR118008A1 (es) | 2019-02-07 | 2021-09-08 | Vitricell Sa | Composiciones para criopreservación de un material biológico |
| CN116732004B (zh) | 2019-03-07 | 2025-11-28 | 加利福尼亚大学董事会 | CRISPR-Cas效应子多肽和其使用方法 |
| CN113825498A (zh) | 2019-05-13 | 2021-12-21 | 骨治疗公司 | 包括透明质酸和血浆蛋白的改进冻干制剂及其用途 |
| EP3994245A1 (en) | 2019-07-05 | 2022-05-11 | Case Western Reserve University | Priming media and methods for stem cell culture and therapy |
| EP3889255A1 (en) | 2020-03-30 | 2021-10-06 | Rijksuniversiteit Groningen | Small molecule inhibitors of rna guided endonucleases |
| GB2619893A (en) | 2021-03-23 | 2023-12-20 | Terumo Bct Inc | Cell capture and expansion |
| EP4408995A4 (en) | 2021-09-28 | 2025-08-13 | Acrigen Biosciences | COMPOSITIONS AND METHODS FOR NUCLEIC ACID MODIFICATIONS |
| US12209689B2 (en) | 2022-02-28 | 2025-01-28 | Terumo Kabushiki Kaisha | Multiple-tube pinch valve assembly |
| USD1099116S1 (en) | 2022-09-01 | 2025-10-21 | Terumo Bct, Inc. | Display screen or portion thereof with a graphical user interface for displaying cell culture process steps and measurements of an associated bioreactor device |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH07500001A (ja) * | 1991-06-18 | 1995-01-05 | キャプラン,アーノルド,アイ. | 骨髄誘導間葉細胞に特異的なモノクローナル抗体 |
Family Cites Families (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| IL68218A (en) * | 1983-03-23 | 1985-12-31 | Univ Ramot | Compositions for cartilage repair comprising embryonal chondrocytes |
| US4904259A (en) * | 1988-04-29 | 1990-02-27 | Samuel Itay | Compositions and methods for repair of cartilage and bone |
| US5612211A (en) * | 1990-06-08 | 1997-03-18 | New York University | Stimulation, production and culturing of hematopoietic progenitor cells by fibroblast growth factors |
| US5226914A (en) * | 1990-11-16 | 1993-07-13 | Caplan Arnold I | Method for treating connective tissue disorders |
| US5197985A (en) * | 1990-11-16 | 1993-03-30 | Caplan Arnold I | Method for enhancing the implantation and differentiation of marrow-derived mesenchymal cells |
| US5486359A (en) * | 1990-11-16 | 1996-01-23 | Osiris Therapeutics, Inc. | Human mesenchymal stem cells |
| US5733542A (en) * | 1990-11-16 | 1998-03-31 | Haynesworth; Stephen E. | Enhancing bone marrow engraftment using MSCS |
| US5266914A (en) * | 1992-06-15 | 1993-11-30 | The Herman Schmidt Company | Magnetic chuck assembly |
| US5591625A (en) * | 1993-11-24 | 1997-01-07 | Case Western Reserve University | Transduced mesenchymal stem cells |
| US5736396A (en) * | 1995-01-24 | 1998-04-07 | Case Western Reserve University | Lineage-directed induction of human mesenchymal stem cell differentiation |
| EP0852463B1 (en) * | 1995-06-06 | 2008-09-03 | Case Western Reserve University | Myogenic differentiation of human mesenchymal stem cells |
| WO1997018299A1 (en) * | 1995-11-16 | 1997-05-22 | Case Western Reserve University | In vitro chondrogenic induction of human mesenchymal stem cells |
-
1995
- 1995-01-24 US US08/377,461 patent/US5736396A/en not_active Expired - Lifetime
-
1996
- 1996-01-05 WO PCT/US1996/000170 patent/WO1996023059A1/en not_active Ceased
- 1996-01-05 DE DE69636979T patent/DE69636979T2/de not_active Expired - Lifetime
- 1996-01-05 ES ES96903358T patent/ES2285710T3/es not_active Expired - Lifetime
- 1996-01-05 AU AU47469/96A patent/AU719098B2/en not_active Ceased
- 1996-01-05 AT AT96903358T patent/ATE357508T1/de active
- 1996-01-05 JP JP52287196A patent/JP4454697B2/ja not_active Expired - Lifetime
- 1996-01-05 PT PT96903358T patent/PT805853E/pt unknown
- 1996-01-05 EP EP96903358A patent/EP0805853B1/en not_active Expired - Lifetime
- 1996-01-05 EP EP06013290A patent/EP1717310A1/en not_active Withdrawn
- 1996-01-05 DK DK96903358T patent/DK0805853T3/da active
- 1996-01-05 CA CA002211120A patent/CA2211120C/en not_active Expired - Fee Related
-
1997
- 1997-07-23 US US08/899,414 patent/US5942225A/en not_active Expired - Lifetime
-
2009
- 2009-10-21 JP JP2009242480A patent/JP5173982B2/ja not_active Expired - Lifetime
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH07500001A (ja) * | 1991-06-18 | 1995-01-05 | キャプラン,アーノルド,アイ. | 骨髄誘導間葉細胞に特異的なモノクローナル抗体 |
Non-Patent Citations (6)
| Title |
|---|
| JPN6009018863; Journal of Cellular Biochemistry 56, 1994, 283-294 * |
| JPN6009018864; 細胞工学 13, 1994, 803-809 * |
| JPN6009018865; Endocrinology 134, 1994, 277-286 * |
| JPN6009018866; Developmental Biology 161, 1994, 218-228 * |
| JPN6009018867; Journal of Bone and Joint Surgery 76-A, 1994, 579-592 * |
| JPN6009018868; Cell 17, 1979, 771-779 * |
Also Published As
| Publication number | Publication date |
|---|---|
| JP5173982B2 (ja) | 2013-04-03 |
| DE69636979T2 (de) | 2007-12-20 |
| MX9705612A (es) | 1998-10-31 |
| CA2211120C (en) | 2001-04-03 |
| EP0805853A4 (en) | 1999-12-22 |
| US5942225A (en) | 1999-08-24 |
| EP1717310A1 (en) | 2006-11-02 |
| AU719098B2 (en) | 2000-05-04 |
| DK0805853T3 (da) | 2007-07-23 |
| DE69636979D1 (de) | 2007-05-03 |
| JP4454697B2 (ja) | 2010-04-21 |
| CA2211120A1 (en) | 1996-08-01 |
| US5736396A (en) | 1998-04-07 |
| ATE357508T1 (de) | 2007-04-15 |
| AU4746996A (en) | 1996-08-14 |
| ES2285710T3 (es) | 2007-11-16 |
| PT805853E (pt) | 2007-06-27 |
| WO1996023059A1 (en) | 1996-08-01 |
| EP0805853B1 (en) | 2007-03-21 |
| JPH10512756A (ja) | 1998-12-08 |
| EP0805853A1 (en) | 1997-11-12 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5173982B2 (ja) | ヒト間葉幹細胞分化の系列指向誘導 | |
| WO1996023059A9 (en) | Lineage-directed induction of human mesenchymal stem cell differentiation | |
| US5197985A (en) | Method for enhancing the implantation and differentiation of marrow-derived mesenchymal cells | |
| US5972703A (en) | Bone precursor cells: compositions and methods | |
| US9694107B2 (en) | Scaffold-free self-organized 3D synthetic tissue | |
| US5226914A (en) | Method for treating connective tissue disorders | |
| US9370606B2 (en) | Scaffold-free self-organized 3D synthetic tissue | |
| JP6152985B2 (ja) | 骨軟骨再生のためのスキャフォールドフリー自己組織化三次元人工組織と人工骨複合体 | |
| JP2000516802A (ja) | ヒト間葉幹細胞の試験管内軟骨形成誘導 | |
| KR20050032020A (ko) | 지방 조직 유래 줄기 세포 및 격자 | |
| WO2018062269A1 (ja) | 体細胞を製造する方法、体細胞、及び組成物 | |
| KR20200000823A (ko) | 인간 유도 만능 줄기세포로부터 연골세포의 펠렛을 제조하는 방법 및 이의 용도 | |
| Heinemann et al. | Alkaline phosphatase expression during monocyte differentiation overlapping markers as a link between monocytic cells, dendritic cells, osteoclasts and osteoblasts | |
| US20080187518A1 (en) | Production of Osteoclasts from Adipose Tissues | |
| JP2017104091A (ja) | 間葉系細胞の製造方法 | |
| KR20180092523A (ko) | 중간엽 줄기세포의 연골세포로의 분화용 무혈청 배지 첨가제 조성물 및 분화 방법 | |
| JP2001507354A (ja) | 局所的モルフォゲンまたは形態形成処理された筋形成前駆体細胞による哺乳動物心筋層の処置 | |
| MXPA97005612A (en) | Induction directed by lineage of the differentiation of human mesenquimatosas cells of ori | |
| US20070004037A1 (en) | Methods and compositions for culturing keratinocytes | |
| KR102847805B1 (ko) | 전환성장인자 베타1를 유효성분으로 포함하는 줄기세포 오르가노이드의 골분화 촉진용 조성물 | |
| Beaton | The role of the bone marrow niche and G-CSF in osteochondral repair | |
| KR20100108569A (ko) | 염증성 류마티스 질환의 치료에 있어서의 인간 골-형성 세포 | |
| Park et al. | The Effect of Cultured Perichondrial Cell Sheet Covered Highly Active Engineered Cartilage: in vivo Comparative Assessment | |
| MÄNTYMAA | The Effects of hypoxic conditions on the chondrogenic differentiation of | |
| Pacitti | Isolation of Mesenchymal Stem Cells Derived from Adult Bone Marrow and Umbilical Cord Blood and Their Potential to Differentiate into Osteoblasts |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20091021 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20120308 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20120607 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20120612 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20120625 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20121204 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20121227 |
|
| EXPY | Cancellation because of completion of term |