DE69814635T2 - Verfahren zur herstellung von 2-hydroxybenzamidderivaten - Google Patents
Verfahren zur herstellung von 2-hydroxybenzamidderivaten Download PDFInfo
- Publication number
- DE69814635T2 DE69814635T2 DE69814635T DE69814635T DE69814635T2 DE 69814635 T2 DE69814635 T2 DE 69814635T2 DE 69814635 T DE69814635 T DE 69814635T DE 69814635 T DE69814635 T DE 69814635T DE 69814635 T2 DE69814635 T2 DE 69814635T2
- Authority
- DE
- Germany
- Prior art keywords
- group
- branched
- linear
- carbon atoms
- substituted
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Lifetime
Links
- SKZKKFZAGNVIMN-UHFFFAOYSA-N Salicilamide Chemical class NC(=O)C1=CC=CC=C1O SKZKKFZAGNVIMN-UHFFFAOYSA-N 0.000 title claims abstract description 12
- 238000004519 manufacturing process Methods 0.000 title description 4
- 238000000034 method Methods 0.000 claims abstract description 26
- 238000006243 chemical reaction Methods 0.000 claims abstract description 15
- -1 methylenedioxy group Chemical group 0.000 claims description 60
- 125000004432 carbon atom Chemical group C* 0.000 claims description 35
- 125000006165 cyclic alkyl group Chemical group 0.000 claims description 17
- 125000003545 alkoxy group Chemical group 0.000 claims description 16
- 125000003277 amino group Chemical group 0.000 claims description 16
- 125000004122 cyclic group Chemical group 0.000 claims description 15
- 239000000203 mixture Substances 0.000 claims description 13
- 239000002904 solvent Substances 0.000 claims description 12
- 150000001412 amines Chemical class 0.000 claims description 11
- 125000002887 hydroxy group Chemical group [H]O* 0.000 claims description 11
- 125000003903 2-propenyl group Chemical group [H]C([*])([H])C([H])=C([H])[H] 0.000 claims description 9
- KXDAEFPNCMNJSK-UHFFFAOYSA-N benzene carboxamide Natural products NC(=O)C1=CC=CC=C1 KXDAEFPNCMNJSK-UHFFFAOYSA-N 0.000 claims description 9
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 claims description 9
- 239000002798 polar solvent Substances 0.000 claims description 9
- 125000001412 tetrahydropyranyl group Chemical group 0.000 claims description 9
- 125000004390 alkyl sulfonyl group Chemical group 0.000 claims description 8
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims description 8
- 150000003335 secondary amines Chemical class 0.000 claims description 8
- 150000003512 tertiary amines Chemical class 0.000 claims description 8
- 125000004448 alkyl carbonyl group Chemical group 0.000 claims description 7
- 125000005843 halogen group Chemical group 0.000 claims description 7
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 claims description 7
- 125000004093 cyano group Chemical group *C#N 0.000 claims description 6
- 150000003141 primary amines Chemical class 0.000 claims description 4
- 150000001408 amides Chemical class 0.000 claims description 3
- 150000003462 sulfoxides Chemical class 0.000 claims description 3
- 125000000217 alkyl group Chemical group 0.000 description 31
- 150000001875 compounds Chemical class 0.000 description 15
- 239000013078 crystal Substances 0.000 description 13
- 125000001424 substituent group Chemical group 0.000 description 13
- 229910052757 nitrogen Inorganic materials 0.000 description 10
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 9
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 9
- 125000006239 protecting group Chemical group 0.000 description 9
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 9
- 125000004103 aminoalkyl group Chemical group 0.000 description 8
- 238000001914 filtration Methods 0.000 description 8
- 239000000725 suspension Substances 0.000 description 7
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 6
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 6
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 6
- 239000011541 reaction mixture Substances 0.000 description 6
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 5
- 238000002360 preparation method Methods 0.000 description 5
- LODHFNUFVRVKTH-ZHACJKMWSA-N 2-hydroxy-n'-[(e)-3-phenylprop-2-enoyl]benzohydrazide Chemical compound OC1=CC=CC=C1C(=O)NNC(=O)\C=C\C1=CC=CC=C1 LODHFNUFVRVKTH-ZHACJKMWSA-N 0.000 description 4
- WTKFNNVZPKSJBB-UHFFFAOYSA-N 2-hydroxy-n-(1,3-thiazol-2-yl)benzamide Chemical class OC1=CC=CC=C1C(=O)NC1=NC=CS1 WTKFNNVZPKSJBB-UHFFFAOYSA-N 0.000 description 4
- FXHOOIRPVKKKFG-UHFFFAOYSA-N N,N-Dimethylacetamide Chemical compound CN(C)C(C)=O FXHOOIRPVKKKFG-UHFFFAOYSA-N 0.000 description 4
- YGSDEFSMJLZEOE-UHFFFAOYSA-N Salicylic acid Natural products OC(=O)C1=CC=CC=C1O YGSDEFSMJLZEOE-UHFFFAOYSA-N 0.000 description 4
- 239000003153 chemical reaction reagent Substances 0.000 description 4
- 238000006900 dealkylation reaction Methods 0.000 description 4
- 230000002496 gastric effect Effects 0.000 description 4
- 238000010992 reflux Methods 0.000 description 4
- 229960004889 salicylic acid Drugs 0.000 description 4
- 238000007086 side reaction Methods 0.000 description 4
- 239000000243 solution Substances 0.000 description 4
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 3
- LRHPLDYGYMQRHN-UHFFFAOYSA-N N-Butanol Chemical compound CCCCO LRHPLDYGYMQRHN-UHFFFAOYSA-N 0.000 description 3
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 3
- 125000003282 alkyl amino group Chemical group 0.000 description 3
- 230000009435 amidation Effects 0.000 description 3
- 238000007112 amidation reaction Methods 0.000 description 3
- 238000009835 boiling Methods 0.000 description 3
- 239000003814 drug Substances 0.000 description 3
- BWDNVLPYCMAUGL-UHFFFAOYSA-N ethyl 2-[(2,4,5-trimethoxybenzoyl)amino]-1,3-thiazole-4-carboxylate Chemical compound CCOC(=O)C1=CSC(NC(=O)C=2C(=CC(OC)=C(OC)C=2)OC)=N1 BWDNVLPYCMAUGL-UHFFFAOYSA-N 0.000 description 3
- UXEGJHFOZNPWPB-UHFFFAOYSA-N ethyl 2-[(2-hydroxy-4,5-dimethoxybenzoyl)amino]-1,3-thiazole-4-carboxylate Chemical compound CCOC(=O)C1=CSC(NC(=O)C=2C(=CC(OC)=C(OC)C=2)O)=N1 UXEGJHFOZNPWPB-UHFFFAOYSA-N 0.000 description 3
- 238000002844 melting Methods 0.000 description 3
- 230000008018 melting Effects 0.000 description 3
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 3
- WSLDOOZREJYCGB-UHFFFAOYSA-N 1,2-Dichloroethane Chemical compound ClCCCl WSLDOOZREJYCGB-UHFFFAOYSA-N 0.000 description 2
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 2
- KVZUCOGWKYOPID-UHFFFAOYSA-N 2,4,5-Trimethoxybenzoic acid Chemical compound COC1=CC(OC)=C(C(O)=O)C=C1OC KVZUCOGWKYOPID-UHFFFAOYSA-N 0.000 description 2
- HZAXFHJVJLSVMW-UHFFFAOYSA-N 2-Aminoethan-1-ol Chemical compound NCCO HZAXFHJVJLSVMW-UHFFFAOYSA-N 0.000 description 2
- 238000005481 NMR spectroscopy Methods 0.000 description 2
- WQDUMFSSJAZKTM-UHFFFAOYSA-N Sodium methoxide Chemical compound [Na+].[O-]C WQDUMFSSJAZKTM-UHFFFAOYSA-N 0.000 description 2
- DTQVDTLACAAQTR-UHFFFAOYSA-N Trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 2
- 239000002253 acid Substances 0.000 description 2
- 230000002378 acidificating effect Effects 0.000 description 2
- VSCWAEJMTAWNJL-UHFFFAOYSA-K aluminium trichloride Chemical compound Cl[Al](Cl)Cl VSCWAEJMTAWNJL-UHFFFAOYSA-K 0.000 description 2
- ILAHWRKJUDSMFH-UHFFFAOYSA-N boron tribromide Chemical compound BrB(Br)Br ILAHWRKJUDSMFH-UHFFFAOYSA-N 0.000 description 2
- 125000003917 carbamoyl group Chemical group [H]N([H])C(*)=O 0.000 description 2
- 239000003795 chemical substances by application Substances 0.000 description 2
- 238000001816 cooling Methods 0.000 description 2
- 238000002425 crystallisation Methods 0.000 description 2
- 230000008025 crystallization Effects 0.000 description 2
- 230000020335 dealkylation Effects 0.000 description 2
- JQVDAXLFBXTEQA-UHFFFAOYSA-N dibutylamine Chemical compound CCCCNCCCC JQVDAXLFBXTEQA-UHFFFAOYSA-N 0.000 description 2
- UAOMVDZJSHZZME-UHFFFAOYSA-N diisopropylamine Substances CC(C)NC(C)C UAOMVDZJSHZZME-UHFFFAOYSA-N 0.000 description 2
- 229940043279 diisopropylamine Drugs 0.000 description 2
- 230000000694 effects Effects 0.000 description 2
- 150000002148 esters Chemical class 0.000 description 2
- 238000000605 extraction Methods 0.000 description 2
- 238000004992 fast atom bombardment mass spectroscopy Methods 0.000 description 2
- 238000005984 hydrogenation reaction Methods 0.000 description 2
- 239000005457 ice water Substances 0.000 description 2
- KWGKDLIKAYFUFQ-UHFFFAOYSA-M lithium chloride Chemical compound [Li+].[Cl-] KWGKDLIKAYFUFQ-UHFFFAOYSA-M 0.000 description 2
- 150000007522 mineralic acids Chemical class 0.000 description 2
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 2
- 230000003449 preventive effect Effects 0.000 description 2
- AOJFQRQNPXYVLM-UHFFFAOYSA-N pyridin-1-ium;chloride Chemical compound [Cl-].C1=CC=[NH+]C=C1 AOJFQRQNPXYVLM-UHFFFAOYSA-N 0.000 description 2
- 238000001953 recrystallisation Methods 0.000 description 2
- 238000006722 reduction reaction Methods 0.000 description 2
- 239000012453 solvate Substances 0.000 description 2
- 229940124597 therapeutic agent Drugs 0.000 description 2
- FYSNRJHAOHDILO-UHFFFAOYSA-N thionyl chloride Chemical compound ClS(Cl)=O FYSNRJHAOHDILO-UHFFFAOYSA-N 0.000 description 2
- CSRZQMIRAZTJOY-UHFFFAOYSA-N trimethylsilyl iodide Chemical compound C[Si](C)(C)I CSRZQMIRAZTJOY-UHFFFAOYSA-N 0.000 description 2
- 238000005406 washing Methods 0.000 description 2
- 125000005919 1,2,2-trimethylpropyl group Chemical group 0.000 description 1
- 125000005918 1,2-dimethylbutyl group Chemical group 0.000 description 1
- 125000006218 1-ethylbutyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000004912 1-ethylbutylamino group Chemical group C(C)C(CCC)N* 0.000 description 1
- 238000005160 1H NMR spectroscopy Methods 0.000 description 1
- XVXFMSXONCJZEB-UHFFFAOYSA-N 2,4,6-trimethoxybenzoyl chloride Chemical compound COC1=CC(OC)=C(C(Cl)=O)C(OC)=C1 XVXFMSXONCJZEB-UHFFFAOYSA-N 0.000 description 1
- UPUWMQZUXFAUCJ-UHFFFAOYSA-N 2,5-dihydro-1,2-thiazole Chemical compound C1SNC=C1 UPUWMQZUXFAUCJ-UHFFFAOYSA-N 0.000 description 1
- 125000006176 2-ethylbutyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(C([H])([H])*)C([H])([H])C([H])([H])[H] 0.000 description 1
- MNWSGMTUGXNYHJ-UHFFFAOYSA-N 2-methoxybenzamide Chemical class COC1=CC=CC=C1C(N)=O MNWSGMTUGXNYHJ-UHFFFAOYSA-N 0.000 description 1
- 125000004493 2-methylbut-1-yl group Chemical group CC(C*)CC 0.000 description 1
- 125000005916 2-methylpentyl group Chemical group 0.000 description 1
- BMYNFMYTOJXKLE-UHFFFAOYSA-N 3-azaniumyl-2-hydroxypropanoate Chemical compound NCC(O)C(O)=O BMYNFMYTOJXKLE-UHFFFAOYSA-N 0.000 description 1
- 125000003542 3-methylbutan-2-yl group Chemical group [H]C([H])([H])C([H])(*)C([H])(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 125000005917 3-methylpentyl group Chemical group 0.000 description 1
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 1
- TWHZNAUBXFZMCA-UHFFFAOYSA-N Acotiamide Chemical compound C1=C(OC)C(OC)=CC(O)=C1C(=O)NC1=NC(C(=O)NCCN(C(C)C)C(C)C)=CS1 TWHZNAUBXFZMCA-UHFFFAOYSA-N 0.000 description 1
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 1
- 239000007848 Bronsted acid Substances 0.000 description 1
- 0 C*(C)(CCN(*)*)NC(c1c[s]c(NC(c2c(*)c(C)c(*)c(C)c2O)=O)n1)=O Chemical compound C*(C)(CCN(*)*)NC(c1c[s]c(NC(c2c(*)c(C)c(*)c(C)c2O)=O)n1)=O 0.000 description 1
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 1
- ZAFNJMIOTHYJRJ-UHFFFAOYSA-N Diisopropyl ether Chemical compound CC(C)OC(C)C ZAFNJMIOTHYJRJ-UHFFFAOYSA-N 0.000 description 1
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 description 1
- 239000002841 Lewis acid Substances 0.000 description 1
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical compound [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 description 1
- FZWLAAWBMGSTSO-UHFFFAOYSA-N Thiazole Chemical group C1=CSC=N1 FZWLAAWBMGSTSO-UHFFFAOYSA-N 0.000 description 1
- MNZMECMQTYGSOI-UHFFFAOYSA-N acetic acid;hydron;bromide Chemical compound Br.CC(O)=O MNZMECMQTYGSOI-UHFFFAOYSA-N 0.000 description 1
- 238000007605 air drying Methods 0.000 description 1
- 125000004453 alkoxycarbonyl group Chemical group 0.000 description 1
- 125000003806 alkyl carbonyl amino group Chemical group 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 239000012300 argon atmosphere Substances 0.000 description 1
- 239000002585 base Substances 0.000 description 1
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 1
- 229910052794 bromium Inorganic materials 0.000 description 1
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 1
- 239000003054 catalyst Substances 0.000 description 1
- 238000010531 catalytic reduction reaction Methods 0.000 description 1
- KXZJHVJKXJLBKO-UHFFFAOYSA-N chembl1408157 Chemical compound N=1C2=CC=CC=C2C(C(=O)O)=CC=1C1=CC=C(O)C=C1 KXZJHVJKXJLBKO-UHFFFAOYSA-N 0.000 description 1
- 238000001311 chemical methods and process Methods 0.000 description 1
- 229910052801 chlorine Inorganic materials 0.000 description 1
- 239000000460 chlorine Substances 0.000 description 1
- 238000006482 condensation reaction Methods 0.000 description 1
- 125000001995 cyclobutyl group Chemical group [H]C1([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 125000002933 cyclohexyloxy group Chemical group C1(CCCCC1)O* 0.000 description 1
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 1
- 230000017858 demethylation Effects 0.000 description 1
- 238000010520 demethylation reaction Methods 0.000 description 1
- OBTIDFCSHQLONE-UHFFFAOYSA-N diphenylphosphane;lithium Chemical compound [Li].C=1C=CC=CC=1PC1=CC=CC=C1 OBTIDFCSHQLONE-UHFFFAOYSA-N 0.000 description 1
- 238000001035 drying Methods 0.000 description 1
- 125000004185 ester group Chemical group 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 125000006125 ethylsulfonyl group Chemical group 0.000 description 1
- 229910052731 fluorine Inorganic materials 0.000 description 1
- 239000011737 fluorine Substances 0.000 description 1
- 230000002140 halogenating effect Effects 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- 125000004051 hexyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- XMBWDFGMSWQBCA-UHFFFAOYSA-N hydrogen iodide Chemical compound I XMBWDFGMSWQBCA-UHFFFAOYSA-N 0.000 description 1
- 239000000543 intermediate Substances 0.000 description 1
- 239000011630 iodine Substances 0.000 description 1
- 229910052740 iodine Inorganic materials 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- 125000004491 isohexyl group Chemical group C(CCC(C)C)* 0.000 description 1
- 125000001972 isopentyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 150000007517 lewis acids Chemical class 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- JZYQAELZLNBCMH-UHFFFAOYSA-N methyl 2-[(2,4,5-trimethoxybenzoyl)amino]-1,3-thiazole-4-carboxylate Chemical compound COC(=O)C1=CSC(NC(=O)C=2C(=CC(OC)=C(OC)C=2)OC)=N1 JZYQAELZLNBCMH-UHFFFAOYSA-N 0.000 description 1
- WYVZZWKIKAKUKV-UHFFFAOYSA-N methyl 2-amino-1,3-thiazole-4-carboxylate Chemical compound COC(=O)C1=CSC(N)=N1 WYVZZWKIKAKUKV-UHFFFAOYSA-N 0.000 description 1
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 1
- 125000004170 methylsulfonyl group Chemical group [H]C([H])([H])S(*)(=O)=O 0.000 description 1
- 239000012046 mixed solvent Substances 0.000 description 1
- CURJNMSGPBXOGK-UHFFFAOYSA-N n',n'-di(propan-2-yl)ethane-1,2-diamine Chemical compound CC(C)N(C(C)C)CCN CURJNMSGPBXOGK-UHFFFAOYSA-N 0.000 description 1
- POBBCNIVOVKLLB-UHFFFAOYSA-N n-methyl-n',n'-di(propan-2-yl)ethane-1,2-diamine Chemical compound CNCCN(C(C)C)C(C)C POBBCNIVOVKLLB-UHFFFAOYSA-N 0.000 description 1
- XJINZNWPEQMMBV-UHFFFAOYSA-N n-methylhexan-1-amine Chemical compound CCCCCCNC XJINZNWPEQMMBV-UHFFFAOYSA-N 0.000 description 1
- 125000001971 neopentyl group Chemical group [H]C([*])([H])C(C([H])([H])[H])(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 150000007524 organic acids Chemical class 0.000 description 1
- 125000003538 pentan-3-yl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000001147 pentyl group Chemical group C(CCCC)* 0.000 description 1
- 239000002574 poison Substances 0.000 description 1
- 231100000614 poison Toxicity 0.000 description 1
- 238000006116 polymerization reaction Methods 0.000 description 1
- CHKVPAROMQMJNQ-UHFFFAOYSA-M potassium bisulfate Chemical compound [K+].OS([O-])(=O)=O CHKVPAROMQMJNQ-UHFFFAOYSA-M 0.000 description 1
- 229910000343 potassium bisulfate Inorganic materials 0.000 description 1
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 229960000581 salicylamide Drugs 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 125000003548 sec-pentyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 229910052710 silicon Inorganic materials 0.000 description 1
- 239000010703 silicon Substances 0.000 description 1
- 125000003808 silyl group Chemical group [H][Si]([H])([H])[*] 0.000 description 1
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical class O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 1
- 238000003797 solvolysis reaction Methods 0.000 description 1
- 239000007858 starting material Substances 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- 229910052717 sulfur Inorganic materials 0.000 description 1
- 239000011593 sulfur Substances 0.000 description 1
- 125000004434 sulfur atom Chemical group 0.000 description 1
- 125000006318 tert-butyl amino group Chemical group [H]N(*)C(C([H])([H])[H])(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 125000001973 tert-pentyl group Chemical group [H]C([H])([H])C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 238000010792 warming Methods 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D277/00—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings
- C07D277/02—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings
- C07D277/20—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members
- C07D277/32—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D277/56—Carbon atoms having three bonds to hetero atoms with at the most one bond to halogen
Description
- TECHNISCHES GEBIET
- Die vorliegende Endung bezieht sich auf ein Verfahren zum Herstellen von 2-Hydroxybenzamid-Derivaten, die als Pharmazeutika oder Zwischenprodukte brauchbar sind.
- STAND DER TECHNIK
- J. Maillard et al., Bulletin de la Société Chimique de France, Nr. 8, 1966, Seiten 2525-2529, offenbaren die Demethylierung von o-Methoxybenzamid-Derivaten mit Ethanolamin,
- Es ist bekannt, dass 2-Hydroxybenzoylaminothiazol-Derivate mit einer Hydroxylgruppe in der 2-Position am Benzolring Wirkungen hinsichtlich der Verbesserung der gastrointestinalen Dysmotilität zeigen, was sie brauchbar macht als vorbeugende oder therapeutische Mittel für verschiedene Arten der gastrointestinalen Dysmotilität (WO96/36619). Von solchen 2-Hydroxybenzoylaminothiazol-Derivaten hat 2-[N-(4,5-Dimethoxy-2-hydroxybenzoyl)amino]-4-[(2-diisopropylaminoethyl)aminocarbonyl]-1,3-thiazol besonders ausgezeichnete Wirkungen hinsichtlich der Verbesserung der gastrointestinalen Dysmotilität und ist so brauchbar als ein Pharmazeutikum.
- Gemäß der Beschreibung der obigen WO96/36G19 wird das 2-Hydroxybenzoylaminothiazol-Derivat nach dem folgenden Verfahren hergestellt. Als Ausgangsmaterial dienende 2-Hydroxybenzoesäure wird einer Kondensationsreaktion mit 2-Amino-4-alkoxycarbonyl-l,3-thiazol unterworfen (Stufe 1). Dann wird die Alkoxycarbonylgruppe des Thiazolringes amidiert (Stufe 2).
- Ist die Carboxygruppe der 2-Hydroxybenzoesäure jedoch durch den Einsatz eines Kondensationsmittels oder eines Halogenierungsmittels aktiviert, um die oben beschriebene Reaktion der Stufe 1 auszuführen, dann tritt häufig eine Polymerisation auf was die Herstellung des Zielproduktes erschwert. Um dieses Problem zu vermeiden, ist ein vorstellbares Verfahren im Falle der Amidierung der 2-Hydroxybenzoesäure (Stufe 1) folgendes. Die Hydrgxygruppe in der 2-Position des Benzolringes von 2-Hydroxybenzoesäure (im Folgenden als "die 2-Hydroxygruppe" bezeichnet) wird geschützt und dann mit einer Verbindung mit einer Aminogruppe umgesetzt, woraufhin die Entfernung der Schutzgruppe erfolgt. Beispiele der Schutzgruppe für die 2-Hydroxygruppe, die bei dem vorliegenden Verfahren eingesetzt werden, schließen bekannte Schutzgruppen ein, wie eine Alkylgruppe, eine Allylgruppe, eine Benzylgruppe, eine Tetrahydropyranylgruppe und eine Silylgruppe. Von diesen wird eine Alkylgruppe allgemein benutzt. Zur Entfernung der Schutzgruppe kann eine bekannte Desalkylierungsreaktion ausgeführt werden (Umwandlung einer Alkoxygruppe in eine 2-Hydroxygruppe). Beispiele bekannter Desalkylierungsreaktionen schließen solche unter Einsatz sau rer Reagenzien, wie Brönstedsäuren, wie Bromwasserstoffsäure, Iodwasserstoffsäure und Trifluoressigsäure, Lewissäuren, wie Bortribromid und Aluminiumchlorid (häufig einzeln oder in Kombination mit Alkylschwefeln eingesetzt), Pyridinhydrochlorid und Bromwasserstoffsäure-Essigsäure-Lösung; Reaktionen unter Einsatz alkalischer Reagenzien, wie Natriummethoxid, Natriumcyanid, Lithiumdiphenylphosphin und Lithiumchlorid; Reaktionen unter Einsatz von Silicium-Reagenzien, wie Trimethylsilyliodid, und Hydrierungs-Reduktion, wie katalytische Reduktion, ein.
- Mit diesen bekannten Reaktionen zur Entfernung der Schutzgruppe ist eine selektive Desalkylierung in der 2-Position jedoch für eine Verbindung schwierig, die einen Substituenten, wie eine Alkoxygruppe oder eine Estergruppe, in einer anderen Position als der geschützten 2-Hydroxy-Position des Benzolringes, bei der Hydroxy geschützt ist (im Folgenden als "die geschützte 2-Hydroxygruppe" bezeichnet) aufweist. Insbesondere im Falle einer Umsetzung unter Einsatz eines alkalischen Reagenz kann Solvolyse und eine Nebenreaktion durch eine Base auftreten, und wenn eine 2-substituierte N-Thiazolylbenzamid-Verbindung eingesetzt wird, die ein Katalysatorgift, wie Schwefelatome, im Substrat enthält, dann kann eine Hydrierungsreduktion nicht vollständig ausgeführt werden. Es besteht daher noch immer ein Bedarf an einem Verfahren zum wirksamen Herstellen eines 2-Hydroxybenzamid-Derivats, bei dem die geschützte 2-Hydroxygruppe selektiv desalkyliert wird, ohne andere Substituenten am Benzolring zu beeinflussen und ohne eine Nebenreaktion zu verursachen.
- OFFENBARUNG DER ERFINDUNG
- In Anbetracht des Vorstehenden haben die Erfinder ausgedehnte Untersuchungen hinsichtlich eines Verfahrens zum Herstellen eines 2-Hydroxybenzamids-Derivats ausgeführt und festgestellt, dass beim Umsetzen einer 2-substituierten Benzamidverbindung, erhalten aus der Reaktion zwischen einer 2-substituierten Benzoesäure und einer Verbindung mit einer Aminogruppe, mit einem sekundären Amin oder einem tertiären Amin, die geschützte 2-Hydroxygruppe selektiv und ohne Verursachen einer Nebenreaktion von der Schutzgruppe befreit und in eine Hydroxygruppe überführt wird, wobei andere Substituenten am Benzolring nicht beeinflusst werden, und wenn es Substituenten an anderen Stellen als dem Benzolring gibt, dann werden auch solche Substituenten nicht beeinflusst. Sie haben auch festgestellt, dass beim Umsetzen einer 2-substituierten Benzamidverbindung mit einem primären Amin in Anwesenheit eines polaren Lösungsmittels die Entfernung der Schutzgruppe von der geschützten 2-Hydroxygruppe und die Amidierung parallel ablaufen, wodurch industriell und vorteilhaft eine brauchbare Verbindung erhalten wird, die als das oben beschriebene vorbeugende und therapeutische Mittel für gastrointestinale Dysmotilität dient. Die vorliegende Erfindung wurde auf der Grundlage dieser Feststellungen gemacht.
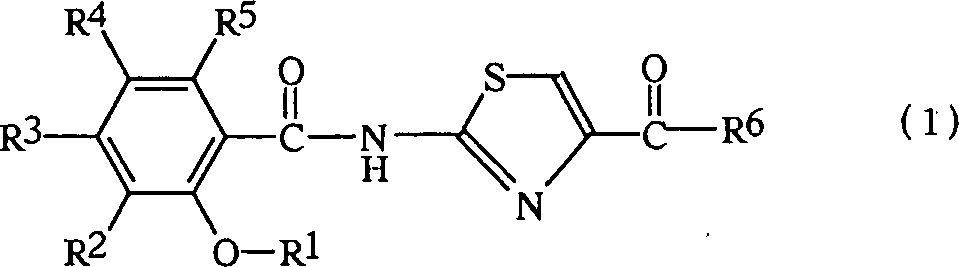
- Die vorliegende Erfindung schafft ein Verfahren zum Herstellen eines 2-Hydroxybenzamid-Derivats der Formel (2): worin R2, R3 und R4 gleich oder verschieden sind und jeweils unabhängig ein Wasserstoffatom, eine Hydroxgruppe, eine niedere Alkylgruppe, eine niedere Alkoxygruppe, eine niedere Alkylsulfonylgruppe, ein Halogenatom, eine Nitrogruppe, eine Cyangruppe, eine mono- oder di-niedere Alkylaminogruppe, oder eine mono- oder di-niedere Alkylcarbonylgruppe repräsentieren oder R2 und R3 können miteinander unter Bildung einer Methylendioxygruppe verbunden sein; R5 ein Wasserstoffatom, eine niedere Alkylgruppe, eine niedere Alkylsulfonylgruppe, ein Halogenatom, eine Nitrogruppe, eine Cyangruppe, eine mono- oder di-niedere Alkylaminogruppe oder eine mono- oder di-niedere Alkylcarbonylgruppe repräsentiert, und R6 eine Hydroxygruppe, eine niedere Alkylgruppe oder eine niedere Alkoxygruppe repräsentiert, wobei das Verfahren gekennzeichnet ist durch Umsetzen einer 2-substituierten Benzamidverbindung der Formel (1): worin R1 eine substituierte oder unsubstituierte niedere Alkylgruppe, eine substituierte oder unsubstituierte Allylgruppe, eine substituierte oder unsubstituierte Benzylgruppe oder eine substituierte oder unsubstituierte Tetrahydropyranylgruppe repräsentiert, und R2, R3, R4, R5 und R6 die oben genannten Bedeutungen haben, mit einem sekundären Amin oder einem tertiären Amin.
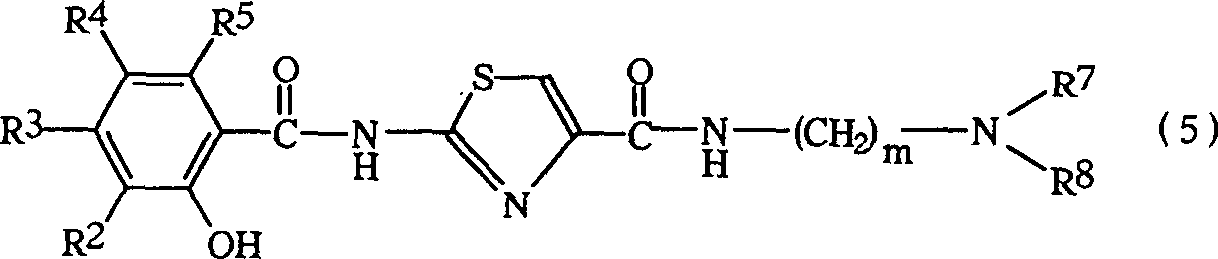
- Die vorliegende Erfindung schafft auch ein Verfahren zum Herstellen eines 2-Hydroxybenzamid-Derivats der Formel (5): worin R2, R3, R4 und R6 die oben genannten Bedeutungen haben, R7 und R8 gleich oder verschieden sind und jeweils unabhängig ein Wasserstoffatom oder eine niedere Alkylgruppe repräsentieren und m eine ganze Zahl von 1 bis einschließlich 4 repräsentiert, wobei das Verfahren gekennzeichnet ist durch Umsetzen einer 2-substituierten Benzamidverbindung der Formel (3): worin A eine Hydroxylgruppe oder eine niedere Alkoxygruppe repräsentiert, und R1, R2, R3, R4 und R5 die oben genannten Bedeutungen haben, mit einem primären Amin der Formel worin m, R7 und R8 die obigen Bedeutungen haben, in Gegenwart eines polaren Lösungsmittels.
- BESTE ART DER AUSFÜHRUNG DER ERFINDUNG
- In der vorliegenden Endung bedeutet der Begriff "niedere" eine lineare, verzeigte oder cyclische Kohlenstoffkette mit 1 bis 6 Kohlenstoffatomen. Demgemäß bezieht sich der Begriff "niedere Alkylgruppe" auf lineare, verzweigte oder cyclische Alkylgruppen mit 1 bis 6 Kohlenstoffatomen. Spezifische Beispiele solcher Alkylgruppen schließen Methyl, Ethyl, Propyl, Isopropyl, Cyclopropyl, Butyl, Isobutyl, sec-Butyl, tert-Butyl, Cyclobutyl, Pentyl, 1-Methylbutyl, 2-Methylbutyl, Isopentyl, tert-Pentyl, 1,2-Dimethylpropyl, Neopentyl, 1-Ethylpropyl, Cyclopentyl, Hexyl, 1-Methylpentyl, 2-Methylpentyl, 3-Methylpentyl, Isohexyl, 1-Ethylbutyl, 2-Ethylbutyl, 1,1-Dimethylbutyl, 1,2-Dimethylbutyl, 1,3-Dimethylbutyl, 2,2-Dimethylbutyl, 2,3-Dimethylbutyl, 3,3-Dimethylbutyl, 1-Methyl-l-ethylpropyl, 1-Ethyl-2-methylpropyl, 1,1,2-Trimethylpropyl, 1,2,2-Trimethylpropyl und Cyclohexyl ein. Von diesen sind lineare oder verzweigte Alkylgruppen mit 1 bis 4 Kohlenstoffatomen bevorzugter.
- Der Begriff "niedere Alkoxygruppe" bezieht sich auf lineare, verzweigte oder cyclische Alkoxygruppen mit 1 bis 6 Kohlenstoffatomen. Spezifische Beispiele solcher Alkoxygruppen schließen Methoxy, Ethoxy, Propoxy, Cyclopropoxy, Isopropoxy, Butoxy, Isobutoxy, sec-Butoxy, tert-Butoxy, Cyclobutoxy, Pentyloxy, 1-Methylbutoxy, 2-Methylbutoxy, Isopentyloxy, tert-Pentyloxy, 1,2-Dimethylpropoxy, Neopentyloxy, 1-Ethylpropoxy, Cyclopentyloxy, Hexyloxy, 1-Methylpentyloxy, 2-Methylpentyloxy, 3-Methylpentyloxy, Isohexyloxy, 1-Ethylbutoxy, 2-Ethylbutoxy, 1,1-Dimethylbutoxy, 1,2-Dimethylbutoxy, 1,3-Dimethylbutoxy, 2,2-Dimethylbutoxy, 2,3-Dimethylbutoxy, 3,3-Dimethylbutoxy, 1-Methyl-1-ethylpropoxy, 1-Ethyl-2-methylpropoxy, 1,1,2-Trimethylpropoxy, 1,2,2-Trimethylpropoxy und Cyclohexyloxy ein. Von diesen sind lineare oder verzweigte Alkoxygruppen mit 1 bis 4 Kohlenstoffatomen bevorzugter.
- In Formel (1) bezieht sich der Begriff "eine substituierte oder unsubstituierte niedere Alkylgruppe, eine substituierte oder unsubstituierte Allylgruppe, eine substituierte oder unsubstituierte Benzylgruppe oder eine substituierte oder unsubstituierte Tetrahydropyranylgruppe" auf die oben beschriebene niedere Alkylgruppe selbst oder eine niedere Alkylgruppe mit ein oder mehreren Substituenten, eine Allylgruppe selbst oder eine Allylgruppe mit ein oder mehreren Substituenten, eine Benzylgruppe selbst oder eine Benzylgruppe mit ein oder mehreren Substituenten oder eine Tetrahydropyranylgruppe selbst oder eine Tetrahydropyranylgruppe mit ein oder mehreren Substituenten. Es kann irgendeine Alkyl, Allyl-, Benzyl- oder Tetrahydropyranylgruppe benutzt werden, solange eine solche Gruppe durch die Reaktion der vorliegenden Erfindung entfernt werden kann, und von diesen wird die oben beschriebene niedere Alkylgruppe selbst vorzugsweise eingesetzt.
- Die Substituentengruppe, auf die in "eine substituierte oder unsubstituierte niedere Alkylgruppe, eine substituierte oder unsubstituierte Allylgruppe, eine substituierte oder unsubstituierte Benzylgruppe oder eine substituierte oder unsubstituierte Tetrahydropyranylgruppe" Bezug genommen ist, kann irgendeine Gruppe sein, solange sie vorteilhaft in der Umsetzung der vorliegenden Erfindung eingesetzt wird. Spezifische Beispiele einer solchen Gruppe schließen die obige niedere Alkylgruppe selbst, die obige niedere Alkoxygruppe, eine Nitrogruppe und eine Hydroxygruppe ein.
- In der vorliegenden Erfindung bezieht sich der Begriff "Halogenatom" auf Fluor, Chlor, Brom und Iod.
- Der Begriff "niedere Alkylsulfonylgruppe" bezieht sich auf lineare, verzweigte oder cyclische Alkylsulfonylgruppen mit 1 bis 6 Kohlenstoffatomen. Spezifische Beispiele solcher Gruppen schließen Methylsulfonyl-, Ethylsulfonyl-, Propylsulfonyl-, Isopropylsulfonyl-, Butylsulfonyl-, Isobutylsulfonyl-, sec-Butylsulfonyl- und tert-Butylsulfonylgruppen ein.
- Der Begriff "mono- oder di-niedere Alkylaminogruppe" bezieht sich auf Aminogruppen, die mit einer oder zwei linearen, verzweigten oder cyclischen Alkylgruppen mit 1 bis 6 Kohlenstoffatomen substituiert sind. Spezifische Beispiele solcher Gruppen schließen ein Methylamino, Ethylamino, Propylamino, Isopropylamino, Cyclopropylamino, Butylamino, Isobutylamino, sec-Butylamino, tert-Butylamino, Cyclobutylamino, Pentylamino, 1-Methylbutylamino, 2-Methylbutylamino, Isopentylamino, tert-Pentylamino, 1,2-Dimethylpropylamino, Neopentylamino, 1-Ethylpropylamino, Cyclopentylamino, Hexylamino, 1-Methylpentylamino, 2-Methylpentylamino, 3-Methylpentylamino, Isohexylamino, 1-Ethylbutylamino; 2-Ethylbutylamino, 1,1-Dimethylbutylamino, 1,2-Dimethylbutylamino, 1,3-Dimethylbutylamino, 2,2-Dimethylbutylamino, 2,3-Dimethylbutylamino, 3,3-Dimethylbutylamino, 1-Methyl-1-ethylpropylamino, 1-Ethyl-2-methylpropylamino, 1,1,2-trimethylpropylamino, 1,2,2-Trimethylpropylamino, Cyclohexylamino, Dimethylamino, Diethylamino, Dipropylamino, Diisopropylamino, Dibutylamino, Diisobutylamino, Methylethylamino, Methylpropylamino, Methylisopropylamino, Methylbutylamino, Methylisobutylamino, Methyl-sec-butylamino, Methyl-tert-butylamino, Methylcyclobutylamino, Methylpentylamino, Methylcyclopentylamino, Methylhexylamino, Ethylpropylamino, 1-Ethylisopropylamino, Ethylbutylamino, Ethylisobutylamino, Ethyl-sec-butylamino, Ethyl-tert-butylamino, Ethylcyclobutylamino, Ethylpentylamino, Ethylneopentylamino, Ethylcyclohexylamino, Propylisopropylamino, Propylbutylamino, Propylisobutylamino, Propyl-sec-butylamino, Propyl-tert-butylamino, Propylcyclobutylamino, Propylpentylamino, Propylisopentylamino, Propyl-tert-pentylamino, Propylcyclohexylamino, Isopropylbutylamino, Isopropylisobutylamino, Isopropyl-secbutylamino, Isopropylpentylamino, Butylisobutylamino, Butyl-sec-butylamino, Butyl-tertbutylamino, Butylcyclobutylamino, Butylpentylamino, Butylisopentylamino, Butyl-tertpentylamino, Butylneopentylamino, Butyl-(1-ethyl)propylamino, Butylcyclopentylamino, Butylhexylamino, Butylisohexylamino, Butylcyclohexylamino, Isobutyl-sec-butylamino, Isobutylpentylamino, Isobutylisopentylamino, Isobutylneopentylamino, Isobutylhexylamino, Isobutylisohexylamino, sec-Butylisopentylamino, sec-Butylneopentylamino, sec-Butylhexylamino, tert-Butylpentylamino, tert-Butylisopentylamino, tert-Butylhexylamino, Cyclobutylpentylamino, Cyclobutylisopentylamino, Cyclobutylhexylamino, Cyclobutylisohexylamino, Pentylneopentylamino, Pentylcyclopentylamino, Pentylhexylamino, Pentylisohexylamino, Pentylcyclohexylamino und Isohexylcyclohexylamino. Von diesen sind Aminogruppen, die mit ein oder zwei linearen oder verzweigten Alkylgruppen mit 1 bis 4 Kohlenstoffatomen substituiert sind, am meisten bevorzugt.
- Der Begriff "mono- oder di-niedere Alkylcarbonylaminogruppe" bezieht sich auf Aminogruppen, die mit ein oder zwei linearen, verzweigten oder cyclischen Alkylcarbonylgruppen mit 2 bis 7 Kohlenstoffatomen substituiert sind. Spezifische Beispiele solcher Gruppen schließen ein Acetylamino, Propionylamino, Butyrylamino, Isobutyrylamino, Cyclopropylcarbonylamino, Valerylamino, Isovalerylamino, sec-Butylcarbonylamino, Pivaloylamino, Cyclobutylcarbonylamino, Pentylcarbonylamino, 1-Methylbutylcarbonylamino, 2-Methylbutylcarbonylamino, Isopentylcarbonylamino, tert-Pentylcarbonylamino, 1,2-Dimethylpropylcarbonylamino, Neopentylcarbonylamino, 1-Ethylpropylcarbonylamina, Cyclopentylcarbonylamino, Hexylcarbonylamino, 1-methylpentylcarbonylamino, 2-Methylpentylcarbonylamino, 3-Methylpentylcarbonylamino, Isohexylcarbonylamino, 1-Ethylbutylcarbonylamino, 2-Ethylbutylcarbonylamino, 1,1-Dimethylbutylcarbonylamino, 1,3-Dimethylbutylcarbonylamino, 2,2-Dimethylbutylcarbonylamino, 2,3-Dimethylbutylcarbonylamino, 3,3-Dimethylbutylcarbonylamino, 1-Methyl-1-ethylpropylcarbonylamino, 1-Ethyl-2-methylpropylcarbonylamino, 1,1,2-Trimethylpropylcarbonylamino, 1,2,2-Trimethylpropylcarbonylamino, Cyclohexylcarbonylamino, Diacetylamino, Dipropionylamino, Dibutyrylamino, Diisobutyrylamino, Divalerylamino, Diisovalerylamino, Acetylpropionylamino, Acetylbutyrylamino, Acetylisobutyrylamino, Acetylvalerylamino, Propionylbutyrylamino, Propionylisobutyrylamino, Propionylvalerylamino, Butyrylisobutyrylamino, Butyrylvalerylamino und Isobutyrylvalerylamino. Von diesen werden Aminogruppen, die mit ein oder zwei linearen oder verzweigten Alkylgruppen mit 2 bis 5 Kohlenstoffatomen substituiert sind, vorzugsweise eingesetzt.
- Es kann irgendein sekundäres Amin oder tertiäres Amin für die Herstellung einer Verbindung der Formel (2) benutzt werden, solange es nicht die anderen Substituenten, die an der 2-substituierten Benzamidverbindung (1) vorhanden sind, beeinflusst, Es kann, z. B. ein sekundäres oder tertiäres Amin mit einer Aminogruppe eingesetzt werden, an die eine lineare, verzweigte oder cyclische Alkylgruppe gebunden ist. Spezifische Beispiele solcher Amine schließen ein N,N-Di(niederalkyl)amin, N,N-Tri(niederalkyl)amin, N,N-(Niederalkyl)- N-[N'-(niederalkyl)aminoalkyl]amin, N-(Niederalkyl)-N-[N',N'-di(niederalkyl)aminoalkyl]amin, N,N-Di[N'-(niederalkyl)aminoalkyl]amin, N,N-Di[N',N'-di(niederalkyl)aminoalkyl]amin, N-[N'-(Niederalkyl)aminoalkyl]-N-[N',N'-di(niederalkyl)aminoalkyl]amin, N,N,N-Tri[N'-(niederalkyl)aminoalkyl]amin und N,N,N-Tri[N',N'-di(niederalkyl)aminoalkyl]amin.
- Die Umsetzung der 2-substituierten Benzamidverbindung (1) mit einem sekundären oder tertiären Amin wird typischerweise in Gegenwart oder Abwesenheit eines Lösungsmittels in einem Temperaturbereich von Raumtemperatur bis Rückflusstemperatur, vorzugsweise 120°C bis Rückflusstemperatur, ausgeführt. Das Lösungsmittel wird geeigneterweise auf bekannten Lösungsmitteln ausgewählt und eine Mischung von zwei oder mehr Arten von Lösungsmitteln kann benutzt werden, wie erforderlich, Bevorzugte Lösungsmittel sind solche mit einem Siedepunkt von 120°C oder mehr. Von diesen sind polare Lösungsmittel besonders bevorzugt und Amid- oder Sulfoxid-Lösungsmittel, wie N,N-Dimethylformamid, N,N-Dimethylacetamid und Dimethylsulfoxid oder deren Mischungen sind am meisten bevorzugt. Nach Abschluss der Umsetzung wird die Zielverbindung isoliert und gereinigt mittels üblicher chemischer Verfahren, wie Filtration, Waschen, Kristallisation, Umkristallisation und Extraktion. Falls erwünscht, können Solvate oder Anlagerungssalze organischer oder anorganischer Säuren hergestellt werden.
- Wie oben beschrieben, reagiert bei der Umsetzung zwischen der 2-substituierten Benzamidverbindung (1) und einem sekundären Amin oder tertiären Amin, selbst wenn die Verbindung (1) eine andere Ester- oder Alkoxygruppe (die die gleiche wie die geschützte 2-Hydroxygruppe sein kann) als die geschützte 2-Hydroxygruppe aufweist, selektiv mit der geschützten 2-Hydroxygruppe zur Entfernung der Schutzgruppe, und sie regiert nicht mit anderen Substituenten. Selbst in Gegenwart eines Substituenten, wie einer Ester- oder Alkoxygruppe – die durch konventionelle Desalkylierung beeinflusst werden – kann das 2-Hydroxybenzamid-Zielderivat (2) selektiv in hoher Ausbeute hergestellt werden.
- Gemäß dem in der obigen WO96/36619 beschriebenen Verfahren kann die Verbindung der Formel (5) aus dem 2-Hydroxybenzamid-Derivat (2) hergestellt werden.
- Ein bei der Umsetzung zwischen der Verbindung der Formel (3) und dem primären Amin der Formel (4) eingesetztes polares Lösungsmittel kann in geeigneter Weise aus bekannten Lösungsmitteln ausgewählt werden. Beispiele polarer Lösungsmittel schließen Lösungsmittel mit einem Siedepunkt von 120°C oder mehr ein und von diesen sind Sulfoxid-Lösungsmittel, wie Dimethylsulfoxid, und Amid-Lösungsmittel, wie N,N-Dimethylformamid und N,N-Dimethylacetamid, bevorzugt. Diese polaren Lösungsmittel können als Mischungen in willkürlichen Verhältnissen benutzt werden. Es gibt keine besondere Beschränkung hinsichtlich der Reaktionstemperatur. Vorzugsweise wird die Umsetzung unter Wärme, insbesondere bei einer Temperatur von 120°C oder mehr, ausgeführt. Nach Abschluss der Umsetzung wird die Reaktionsmischung geeigneterweise üblichen chemischen Verfahren unterworfen, einschließlich Filtration, Waschen, Kristallisation, Umkristallisation und Extraktion, um dadurch die Verbindung zu isolieren und zu reinigen. Falls erwünscht, kann ein Säuread ditionssalz organischer oder anorganischer Säure oder ein Solvat der so erhaltenen Verbindung, der Zielverbindung der Formel (5), hergestellt werden.
- Gemäß dem Verfahren der vorliegenden Endung erfolgen die Entfernung der Schutzgruppe von einer geschützten 2-Hydroxygruppe und die Amidierung gleichzeitig, und die Verfahrensstufen können daher, verglichen mit dem in der vorerwähnten internationalen Patentveröffentlichung beschriebenen Verfahren oder Kombinationen bekannter Reaktionen, vereinfacht werden. Da keine Nebenreaktionen auftreten, ergibt das Verfahren der vorliegenden Erfindung vorteilhafterweise ein hoch reine Zielverbindung in hoher Ausbeute.
- BEISPIELE
- Die vorliegende Erfindung wird nun detaillierter anhand von Beispielen beschrieben, die nicht als die Erfindung einschränkend zu verstehen sind.
- Beispiel 1
- Eine Suspension (30 ml) von 2-[N-(2,4,5-Trimetlioxybenzoyl)amino]-4-(ethoxycarbonyl)-1,3-thiazol (10,0 g) in N,N-Dimethylacetamid ließ man sich unter Erwärmen bei einer Temperatur von mindestens 150°C auflösen und gab dann Di-n-butylamin (8,8 g) tropfenweise zu der Lösung hinzu und erhitzte 5 Stunden lang am Rückfluss. Man ließ sich die Reaktionsmischung abkühlen, goss in eine Mischung von 1 N Chlorwasserstoffsäure (100 ml) und Eiswasser (100 ml) und gab weiter Wasser hinzu. Die so ausgefallenen Kristalle wurden durch Filtration gesammelt, mit Wasser gewaschen und dann einem Lufttrocknen und Trocknen unter verringertem Druck unterworfen, um dadurch Rohkristalle (10,0 g) zu erhalten. Die Kristalle wurden aus 1,4-Dioxan umkristallisiert und ergaben 8,9 g von 2-[N-(4,5-Dimethoxy-2-hydroxybenzoyl)amino]-4-(ethoxycarbonyl)-1,3-thiazol (Ausbeute: 82,3%) Schmelzpunkt: 218–220°C
- 1H-NMR(DMSO-d6)δ: 1,31(3H, t), 3,57(4H, s), 3,78(3H, s), 3,83(3H, s), 4,30(2H, q),
6,61(1H, 5), 7,65(1H, s), 8,12(1H, s), 11,75(1H, s), 12,42(1H, s) - IR(KBr)cm-1 : 3229, 3113,1728, 1643, 1556, 1518,1273, 1232, 1213
- Beispiel 2
- Eine Suspension (6 ml) von 2-[N-(2,4,5-trimethoxybenzoyl)amino]-4-(ethoxycarbonyl)-1,3-thiazol (3,0 g) in Dimethylsulfoxid wurde unter Erwärmen gelöst und N-Methyl-N-hexylamin (2,3 g) wurde tropfenweise zu der Lösung hinzugegeben und für 2 Stunden am Rückfluss erhitzt. Man ließ sich die Reaktionsmischung abkühlen, goss in eine Mischung von 1 N Chlorwasserstoffsäure (30 ml) und Eiswasser (30 ml) und gab weiter Wasser hinzu. So ausgefallene Kristalle wurden durch Filtration gesammelt, mit Wasser gewaschen und luftgetrocknet, um dadurch Rohkristalle zu erhalten. Die Kristalle wurden aus 1,4-Dioxan umkristallisiert und es wurden 2,1 g von 2-[N-(4,5-Dimethoxy-2-hydroxybenzoyl)amino]-4-(ethoxycarbonyl)-1,3-thiazol (Ausbeute: 64,6%) erhalten.
- Beispiel 3
- Eine Suspension (1,5 ml) von 2-[N-(2,4,5-trimethoxybenzoyl)amino]-4-(ethoxycarbonyl)-1,3-thiazol (732 ml) und N,N-Diisopropyl-N'-methylethylendiamin (1,60 g) in Dimethylacetamid wurde 5 Stunden lang bei 140°C gerührt. Zu der Reaktionsmischung wurden eine wässerige Lösung von Kaliumhydrogensulfat, eine geringe Menge Ethylacetat und eine geringe Menge Isopropylether zum Ausfällen von Kristallen hinzugegeben. Die so ausgefallenen Kristalle wurden durch Filtration gesammelt und getrocknet und man erhielt 601 mg von 2-[N-(4,5-Dimethoxy-2-hydroxybenzoyl)amino]-4-(ethoxycarbonyl)-1,3-thiazol (Ausbeute: 86%)
- Beispiel 4
- Herstellung von 2-[N-(4,5-Dimethoxy-2-hydroxybenzoyl)amino]-4-[(2-diisopropylamincethyl)aminocarbonyl]-1,3-thiazol-hydrochlorid
- Stufe 1
- Herstellung von 2-[N-(2,4,5-trimethoxybenzoyl)amino]-4-methoxycarbonyl-l,3-thiazol
- 2,4,5-Trimethoxybenzcesäure (500 g) wurden in getrocknetem Toluol (2 l) suspendiert und zu dieser Suspension wurden Thionylchlorid (206 ml) und N,N-Dimethylformamid (1,0 m l) bei Raumtemperatur hinzugegeben und die Mischung für 1 Stunde bei 80°C gerührt. Die Reaktionsmischung wurde unter verringertem Druck konzentriert. Zu dem resultierenden Rest gab man n-Hexan und durch Sieden der Mischung wurde 2,4,6-Trimethoxybenzoylchlorid erhalten. Zu der resultierenden Verbindung wurden 2-Amino-4-methoxycarbonyl-l,3-thiazol (372,7 g) und 1,2-Dichlorethan (4,5 l) hinzugegeben und die Mischung für 6 Stunden am Rückfluss erhitzt. Nach Abschluss der Umsetzung ließ man sich die Reaktionsmischung abkühlen. Ausgefallene Kristalle wurden durch Filtration gesammelt, mit 1,2-Dichlorethan gewaschen uind luftgetrocknet. Die Kristalle wurden in Wasser (8 l) suspendiert und zu der Suspension Eis (2 kg) hinzugegeben. Unter Kühlen wurden eine Lösung von Natriumhydroxid (94 g) in Wasser (850 ml) hinzugegeben, um den pH der Suspension auf etwa 7,5 einzustellen. Danach rührte man die Mischung für 3 Stunden bei Raumtemperatur. Ausgefallene Kristalle wurden durch Filtration gesammelt, mit Wasser gewaschen und luftgetrocknet, um dadurch die Titelverbindung (702,7 g) zu erhalten.
- Schmelzpunkt: 251–252°C
- 1H-NMR(DMSO-d6)δ : 3,77(3H, s), 3,82(3H, s), 3,91(3H, s), 4,03(3H, s), 6,84(1H, s),
7,44(1H, s), 8,04(1H, s), 11,44(1H, s) - IR(KBr)cm-1 : 3304, 3123, 3019, 1736,1668, 1610
- MS(FAB)m/e : 353(MH+)
- Stufe 2
- Herstellung von 2-[N-(4,5-Dimethoxy-2-hydroxybenzoyl)amino]-4-[(2-diisopropylamincethyl)aminocarbonyl]-1,3-thiazol-hydrochlorid
- Unter Argon-Atmosphäre wurden 2-[N-(2,4,5-trimethoxybenzoyl)amino]-4-methoxycarbonyl-l,3-thiazol (500 g) und N,N-Diisopropylethylendiamin (617 ml) in N,N-Dimethlacetamid (617 ml) suspendiert und die Suspension G Stunden lang bei 135°C gerührt. Man ließ sich die Reaktionsmischung abkühlen und gab 1-Butanol (5 l) hinzu. Die Mischung wurde nacheinander mit 0,5 N wässerigem Natriumhydroxid und gesättigter Salzlauge gewaschen und es wurde 2-Propanol (2 l) zu der Mischung hinzugegeben. Chlorwasserstoffsäuregas wurde unter Eiskühlen in die Mischung geblasen, bis die Flüssigkeit sauer geworden war. Ausgefallene Kristalle wurden durch Filtration gesammelt und luftgetrocknet. Die Kristalle wurden aus einem gemischten Lösungsmittel von 2-Propanol und Wasser (2-Propanol: Wasser = 4 : 1) umkristallisiert und 468,3 g der Titelverbindung erhalten. Schmelzpunkt: 160°C
- 1H-NMR(DMSO-d6)δ : 1,32(6H, d), 1,35(6H, d), 3,17(2H, brs), 3,55–3,70(4H, m), 3,77(3H, s);
3,82(3H, s), 6,87(1H, s), 7,49(1H, s), 7,89(1H, s), 8,23(1H, t), 9,65(1H, brs),
11,79(1H, s), 12,07(1H, brs) - IR(KBr)cm-1 : 3493, 3300, 3096, 1649
- MS(FAB)m/e : 451(MH+)
- INDUSTRIELLE ANWENDBARKEIT
- Das Verfahren der vorliegenden Erfindung ergibt 2-HydroxybenzoylaminothiazolDerivate durch ein einfaches Verfahren in hoher Ausbeute, verglichen mit konventionellen Verfahren, und ist somit industriell vorteilhaft aufgrund seiner ausgezeichneten Arbeitseffizienz und Wirtschaftlichkeit.
Claims (6)
- Verfahren zum Herstellen eines 2-Hydroxybenzamid-Derivats der Formel (2): worin R2, R3 und R4 gleich oder verschieden sind und jeweils unabhängig ein Wasserstoffatom, eine Hydroxylgruppe, eine lineare oder verzweigte oder cyclische Alkylgruppe mit 1 bis 6 Kohlenstoffatomen, eine lineare, verzweigte oder cyclische Alkoxygruppe mit 1 bis 6 Kohlenstoffatomen, eine lineare, verzweigte oder cyclische Alkylsulfonylgruppe mit 1 bis 6 Kohlenstoffatomen, ein Halogenatom, eine Nitrogruppe, eine Cyangruppe, eine Aminogruppe, die mit ein oder zwei linearen verzweigten oder cyclischen Alkylgruppen mit 1 bis 6 Kohlenstoffatomen substituiert ist, oder eine Aminogruppe, die mit ein oder zwei linearen, verzweigten oder cyclischen Alkylcarbonylgruppen mit 2 bis 7 Kohlenstoff atomen substituiert ist, repräsentieren, oder R2 und R3 miteinander unter Bildung einer Methylendioxygruppe verbunden sein können; R5 ein Wasserstoffatom, eine lineare, verzweigte oder cyclische Alkylgruppe mit 1 bis 6 Kohlenstoffatomen, eine lineare, verzweigte oder cyclische Alkylsulfonylgruppe mit 1 bis 6 Kohlenstoffatomen, ein Halogenatom, eine Nitrogruppe, eine Cyangruppe, eine Aminogruppe, die mit ein oder zwei linearen, verzweigten oder cyclischen Alkylgruppen mit 1 bis 6 Kohlenstoffatomen substituiert ist, oder eine Aminogruppe, die mit ein oder zwei linearen, verzweigten oder cyclischen Alkylcarbonylgruppen mit 2 bis 7 Kohlenstoffatomen substituiert ist, repräsentiert, und R6 eine Hydroxygruppe, eine lineare, verzweigte oder cyclische Alkylgruppe mit 1 bis 6 Kohlenstoffatomen oder eine eine lineare, verzweigte oder cyclische Alkoxygruppe mit 1 bis 6 Kohlenstoffatomen repräsentiert, wobei das Verfahren gekennzeichnet ist durch Umsetzen einer 2-substituierten Benzamid-Verbindung der Formel (1): worin R1 eine substituierte oder unsubstituierte lineare, verzweigte oder cyclische Alkylgruppe mit 1 bis 6 Kohlenstoffatomen, eine substituierte oder unsubstituierte Allylgruppe, eine substituierte oder unsubstituierte Benzylgruppe oder eine substituierte oder unsubstituierte Tetrahydropyranylgruppe repräsentiert, und R2, R3, R4, R5 und R6 die obigen Bedeutungen haben, mit einem sekundären Amin oder einem tertiären Amin.
- Verfahren nach Anspruch 1, worin das sekundäre Amin oder das tertiäre Amin ein Amin mit einer Aminogruppe ist, an die eine lineare, verzweigte oder cyclische Alkylgruppe gebunden ist.
- Verfahren nach Anspruch 1 oder 2, worin R1 eine substituierte oder unsubstituierte lineare, verzweigte oder cyclische Alkylgruppe mit 1 bis 6 Kohlenstoffatomen ist.
- Verfahren nach einem der Ansprüche 1 bis 3, worin die Umsetzung in Gegenwart eines polaren Lösungsmittels ausgeführt wird.
- Verfahren zum Herstellen eines 2-Hydroxybenzamid-Derivats der Formel (5): worin R2, R3 und R4 gleich oder verschieden sind und jeweils unabhängig ein Wasserstoffatom, eine Hydroxylgruppe, eine lineare oder verzweigte oder cyclische Alkylgruppe mit 1 bis 6 Kohlenstoffatomen, eine lineare, verzweigte oder cyclische Alkoxygruppe mit 1 bis 6 Kohlenstoffatomen, eine lineare, verzweigte oder cyclische Alkylsulfonylgruppe mit 1 bis 6 Kohlenstoffatomen, ein Halogenatom, eine Nitrogruppe, eine Cyangruppe, eine Aminogruppe, die mit ein oder zwei linearen verzweigten oder cyclischen Alkylgruppen mit 1 bis 6 Kohlenstoffatomen substituiert ist, oder eine Aminogruppe, die mit ein oder zwei linearen, verzweigten oder cyclischen Alkylcarbonylgruppen mit 2 bis 7 Kohlenstoff atomen substituiert ist, repräsentieren, oder R2 und R3 miteinander unter Bildung einer Methylendioxygruppe verbunden sein können; R5 ein Wasserstoffatom, eine lineare, verzweigte oder cyclische Alkylgruppe mit 1 bis 6 Kohlenstoffatomen, eine lineare, ver zweigte oder cyclische Alkylsulfonylgruppe mit 1 bis 6 Kohlenstoffatomen, ein Halogenatom, eine Nitrogruppe, eine Cyangruppe, eine Aminogruppe, die mit ein oder zwei linearen, verzweigten oder cyclischen Alkylgruppen mit 1 bis 6 Kohlenstoffatomen substituiert ist, oder eine Aminogruppe, die mit ein oder zwei linearen, verzweigten oder cyclischen Alkylcarbonylgruppen mit 2 bis 7 Kohlenstoffatomen substituiert ist, repräsentiert, R7 und R8 gleich oder verschieden sind und jeweils unabhängig ein Wasserstoffatom oder eine lineare, verzweigte oder cyclische Alkylgruppe mit 1 bis 6 Kohlenstoffatomen repräsentieren und m eine ganze Zahl von 1 bis einschließlich 4 repräsentiert, wobei das Verfahren gekennzeichnet ist durch Umsetzen einer 2-substituierten Benzamid-Verbindung der Formel (3): worin R1 eine substituierte oder unsubstituierte lineare, verzweigte oder cyclische Alkylgruppe mit 1 bis 6 Kohlenstoffatomen, eine substituierte oder unsubstituierte Allylgruppe, eine substituierte oder unsubstituierte Benzylgruppe oder eine substituierte oder unsubstituierte Tetrahydropyranylgruppe repräsentiert, und R2, R3, R4 und R5 die obigen Bedeutungen haben, und A eine Hydroxygruppe oder eine lineare, verzweigte oder cyclische Alkoxygruppe mit 1 bis 6 Kohlenstoffatomen repräsentiert, mit einem primären Amin der Formel (4): worin m, R7 und R8 die obigen Bedeutungen haben, in Gegenwart eines polaren Lösungsmittels.
- Verfahren nach Anspruch 5, worin das polare Lösungsmittel ein Sulfoxid-Lösungsmittel, ein Amid-Lösungsmittel oder eine Mischung davon ist.
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP18184497A JP4078687B2 (ja) | 1997-06-24 | 1997-06-24 | 2−ヒドロキシ安息香酸アミド誘導体の製造法 |
| JP18184497 | 1997-06-24 | ||
| JP25010697A JP4078690B2 (ja) | 1997-09-01 | 1997-09-01 | アミノチアゾール誘導体の製造法 |
| JP25010697 | 1997-09-01 | ||
| PCT/JP1998/002764 WO1998058918A1 (fr) | 1997-06-24 | 1998-06-22 | Procede de production des derives de 2-hydroxybenzamide |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| DE69814635D1 DE69814635D1 (de) | 2003-06-18 |
| DE69814635T2 true DE69814635T2 (de) | 2004-03-11 |
Family
ID=26500852
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| DE69814635T Expired - Lifetime DE69814635T2 (de) | 1997-06-24 | 1998-06-22 | Verfahren zur herstellung von 2-hydroxybenzamidderivaten |
Country Status (12)
| Country | Link |
|---|---|
| US (1) | US6197970B1 (de) |
| EP (1) | EP0994108B1 (de) |
| KR (1) | KR100528386B1 (de) |
| CN (1) | CN1084739C (de) |
| AT (1) | ATE240305T1 (de) |
| AU (1) | AU725155B2 (de) |
| CA (1) | CA2293361C (de) |
| DE (1) | DE69814635T2 (de) |
| DK (1) | DK0994108T3 (de) |
| ES (1) | ES2198719T3 (de) |
| PT (1) | PT994108E (de) |
| WO (1) | WO1998058918A1 (de) |
Families Citing this family (20)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ATE286036T1 (de) * | 2000-05-03 | 2005-01-15 | Hoffmann La Roche | Heteroaromatische alkynylphenyl-verbindungen als glukokinase-aktivatoren |
| CA2419666C (en) | 2000-09-08 | 2009-10-27 | Zeria Pharmaceutical Co., Ltd. | Colonic motor dysfunction remedies |
| US20050143581A1 (en) * | 2002-03-20 | 2005-06-30 | Mitsui Chemicals, Inc. | Process for preparation of alkoxybenzamides and thiazolyl isocyanates |
| DK1493441T3 (da) * | 2002-04-08 | 2011-10-17 | Zeria Pharm Co Ltd | Terapeutisk middel for næringskompentenceforstyrrelse i maven |
| US7645353B2 (en) * | 2003-12-23 | 2010-01-12 | Kimberly-Clark Worldwide, Inc. | Ultrasonically laminated multi-ply fabrics |
| HUE027855T2 (en) | 2004-08-23 | 2016-11-28 | Zeria Pharm Co Ltd | Process for the preparation of an aminotiazole derivative and an intermediate |
| US8586761B2 (en) | 2004-08-23 | 2013-11-19 | Zeria Pharmaceutical Co., Ltd. | Method for producing aminothiazole derivative and production intermediate |
| NZ553734A (en) * | 2004-09-20 | 2011-01-28 | 4Sc Ag | Novel thiazole derivatives as NF-kappaB inhibitors |
| CN103387552B (zh) * | 2012-05-10 | 2016-06-08 | 常州市第四制药厂有限公司 | 制备盐酸阿考替胺的方法 |
| CN103387494B (zh) * | 2012-05-10 | 2016-08-03 | 上海医药工业研究院 | 制备2-羟基-4,5-二甲氧基苯甲酸的方法 |
| CN103896873B (zh) * | 2013-10-23 | 2015-11-25 | 山东诚创医药技术开发有限公司 | 一种盐酸阿考替胺的精制方法 |
| CN104592147A (zh) * | 2013-10-30 | 2015-05-06 | 江苏豪森药业股份有限公司 | 盐酸阿考替胺中间体的制备方法 |
| CN103665023B (zh) * | 2013-12-23 | 2017-05-24 | 华润赛科药业有限责任公司 | 一种盐酸阿考替胺的合成方法 |
| CN103709120B (zh) * | 2014-01-20 | 2016-01-20 | 华润赛科药业有限责任公司 | 一种盐酸阿考替胺三水合物的制备方法 |
| CN103980226A (zh) * | 2014-05-10 | 2014-08-13 | 杭州新博思生物医药有限公司 | 盐酸阿考替胺水合物晶型及其制备方法 |
| CN104031001B (zh) * | 2014-06-30 | 2015-09-30 | 山东诚创医药技术开发有限公司 | 一锅烩制备2-[n-(2,4,5-三甲氧基苯甲胺基)氨基]-4-乙氧羰基-1,3-噻唑的方法 |
| CN104045606B (zh) * | 2014-07-11 | 2015-09-30 | 杭州新博思生物医药有限公司 | 一锅法制备阿考替胺盐酸盐的方法 |
| CN105924406B (zh) * | 2016-05-04 | 2018-04-10 | 河北国龙制药有限公司 | 一种盐酸阿考替胺三水合物的制备方法 |
| CN106316979B (zh) * | 2016-08-22 | 2018-11-27 | 山东罗欣药业集团股份有限公司 | 一种盐酸阿考替胺的制备方法 |
| CN111518052A (zh) * | 2020-05-27 | 2020-08-11 | 廊坊市泽康医药科技有限公司 | 一种阿考替胺盐酸盐杂质的制备方法 |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5510478A (en) * | 1994-11-30 | 1996-04-23 | American Home Products Corporation | 2-arylamidothiazole derivatives with CNS activity |
| KR100424933B1 (ko) | 1995-05-18 | 2004-07-27 | 제리아 신야쿠 고교 가부시키 가이샤 | 아미노티아졸유도체,이를함유하는의약및이화합물의중간체 |
| JPH0987282A (ja) * | 1995-09-21 | 1997-03-31 | Kyowa Hakko Kogyo Co Ltd | チアゾール誘導体 |
| ATE231137T1 (de) * | 1996-10-24 | 2003-02-15 | Zeria Pharm Co Ltd | Substituierte benzoylthiazolderivate und sie enthaltende medikamente |
-
1998
- 1998-06-22 AT AT98928606T patent/ATE240305T1/de active
- 1998-06-22 AU AU80372/98A patent/AU725155B2/en not_active Ceased
- 1998-06-22 CA CA002293361A patent/CA2293361C/en not_active Expired - Fee Related
- 1998-06-22 PT PT98928606T patent/PT994108E/pt unknown
- 1998-06-22 US US09/446,108 patent/US6197970B1/en not_active Expired - Lifetime
- 1998-06-22 DK DK98928606T patent/DK0994108T3/da active
- 1998-06-22 ES ES98928606T patent/ES2198719T3/es not_active Expired - Lifetime
- 1998-06-22 DE DE69814635T patent/DE69814635T2/de not_active Expired - Lifetime
- 1998-06-22 WO PCT/JP1998/002764 patent/WO1998058918A1/ja active IP Right Grant
- 1998-06-22 EP EP98928606A patent/EP0994108B1/de not_active Expired - Lifetime
- 1998-06-22 CN CN988065797A patent/CN1084739C/zh not_active Expired - Lifetime
-
1999
- 1999-12-13 KR KR10-1999-7011769A patent/KR100528386B1/ko not_active IP Right Cessation
Also Published As
| Publication number | Publication date |
|---|---|
| EP0994108A1 (de) | 2000-04-19 |
| CA2293361C (en) | 2006-06-20 |
| CN1084739C (zh) | 2002-05-15 |
| US6197970B1 (en) | 2001-03-06 |
| KR100528386B1 (ko) | 2005-11-15 |
| KR20010013754A (ko) | 2001-02-26 |
| WO1998058918A1 (fr) | 1998-12-30 |
| DK0994108T3 (da) | 2003-08-18 |
| ES2198719T3 (es) | 2004-02-01 |
| AU725155B2 (en) | 2000-10-05 |
| PT994108E (pt) | 2003-09-30 |
| CN1261357A (zh) | 2000-07-26 |
| CA2293361A1 (en) | 1998-12-30 |
| EP0994108A4 (de) | 2001-07-04 |
| AU8037298A (en) | 1999-01-04 |
| ATE240305T1 (de) | 2003-05-15 |
| DE69814635D1 (de) | 2003-06-18 |
| EP0994108B1 (de) | 2003-05-14 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| DE69814635T2 (de) | Verfahren zur herstellung von 2-hydroxybenzamidderivaten | |
| CH624102A5 (de) | ||
| CH637130A5 (de) | Chinazolin-derivate, verfahren zu ihrer herstellung und verwendung dieser derivate in arzneimitteln. | |
| DE1964712B2 (de) | Basische Aryloxy acetamide und ihre Additionssalze mit pharmazeutisch zulässigen Säuren, sowie Verfahren zur Herstellung dieser Verbindungen und Arzneimittel | |
| DD294023A5 (de) | Therapeutische mittel | |
| DE823595C (de) | Verfahren zur Herstellung von neuen basisch substituierten Tetrahydrochinolinderivaten | |
| AT200578B (de) | Verfahren zur Herstellung von neuen N-Aminoalkylderivaten von Azepinen | |
| DE1543809B2 (de) | Aminophenole und verfahren zu deren herstellung | |
| CH638203A5 (en) | Process for preparing substituted aminoquinazoline derivatives | |
| DE971002C (de) | Verfahren zur Herstellung von Thioxanthonen | |
| JP4078687B2 (ja) | 2−ヒドロキシ安息香酸アミド誘導体の製造法 | |
| DE1470119A1 (de) | Verfahren zur Herstellung substituierter Phenoxyalkylaminoalkyl tertiaeren Aminen und ihrer sauren Additionssalze | |
| DE1620128A1 (de) | Verfahren zur Herstellung von neuen organischen Amiden | |
| DD295158A5 (de) | Verfahren zur herstellung von stereoisomeren der verbindung 4-[3-[ethyl-[3-(propylsulfinyl)-propyl]-amino]-2-hydroxypropoxy]-benzonitril | |
| DE1097995B (de) | Verfahren zur Herstellung von Phenthiazinderivaten | |
| AT214441B (de) | Verfahren zur Herstellung von neuen Benzthiazolen sowie von deren Salzen | |
| AT206890B (de) | Verfahren zur Herstellung von neuen tertiären Aminen | |
| AT211316B (de) | Verfahren zur Herstellung von neuen Phenthiazinverbindungen | |
| DE1543809C3 (de) | Aminophenole und Verfahren zu deren Herstellung | |
| AT361473B (de) | Verfahren zur herstellung von neuen thiazoli- dinderivaten und von deren saeureadditionssalzen | |
| DE2950378C2 (de) | N-eckige Klammer auf 2-(3-Benzoylpheny)-propionyläthylendioxyäthyl eckige Klammer zu -N'-(4-chlorbenzhydril)- piperazin, dessen Salze, Verfahren zu deren Herstellung und pharmazeutische Zubereitung | |
| AT332378B (de) | Verfahren zur herstellung von neuen n-(3,3-diphenylpropyl)-propylendiaminen und deren saureadditionssalzen | |
| DE2429373A1 (de) | Verfahren zur herstellung neuer heterocyclischer verbindungen | |
| DE2521798A1 (de) | Diphenylallylaminoalkanole | |
| DEG0003117MA (de) | Verfahren zur Herstellung von neuen basisch substituierten Tetrahydrochinolinderivaten |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 8364 | No opposition during term of opposition |