WO2012165120A1 - 水添共役ジエン系共重合体の製造方法 - Google Patents
水添共役ジエン系共重合体の製造方法 Download PDFInfo
- Publication number
- WO2012165120A1 WO2012165120A1 PCT/JP2012/062137 JP2012062137W WO2012165120A1 WO 2012165120 A1 WO2012165120 A1 WO 2012165120A1 JP 2012062137 W JP2012062137 W JP 2012062137W WO 2012165120 A1 WO2012165120 A1 WO 2012165120A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- conjugated diene
- diene copolymer
- compound
- hydrogenation
- hydrogenated conjugated
- Prior art date
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08C—TREATMENT OR CHEMICAL MODIFICATION OF RUBBERS
- C08C19/00—Chemical modification of rubber
- C08C19/02—Hydrogenation
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F212/00—Copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and at least one being terminated by an aromatic carbocyclic ring
- C08F212/02—Monomers containing only one unsaturated aliphatic radical
- C08F212/04—Monomers containing only one unsaturated aliphatic radical containing one ring
- C08F212/06—Hydrocarbons
- C08F212/08—Styrene
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F236/00—Copolymers of compounds having one or more unsaturated aliphatic radicals, at least one having two or more carbon-to-carbon double bonds
- C08F236/02—Copolymers of compounds having one or more unsaturated aliphatic radicals, at least one having two or more carbon-to-carbon double bonds the radical having only two carbon-to-carbon double bonds
- C08F236/04—Copolymers of compounds having one or more unsaturated aliphatic radicals, at least one having two or more carbon-to-carbon double bonds the radical having only two carbon-to-carbon double bonds conjugated
- C08F236/10—Copolymers of compounds having one or more unsaturated aliphatic radicals, at least one having two or more carbon-to-carbon double bonds the radical having only two carbon-to-carbon double bonds conjugated with vinyl-aromatic monomers
Definitions
- the present invention relates to a method for producing a hydrogenated conjugated diene copolymer.
- styrene block copolymers consisting of conjugated diene monomers and vinyl aromatic monomers have the same elasticity as vulcanized natural and synthetic rubbers at room temperature without vulcanization.
- it has excellent processability similar to that of thermoplastic resins at high temperatures, so it can be used in fields such as footwear, plastic modifiers, asphalt modifiers, adhesives, household products, home appliances Widely used for packaging materials such as industrial parts and toys.
- the hydrogenated product of the styrene block copolymer is excellent in weather resistance and heat resistance, it is widely used in automobile parts, medical instruments and the like in addition to the above application fields.
- Patent Document 1 discloses a hydrogenated block copolymer obtained by hydrogenating a copolymer having a block made of a vinyl aromatic hydrocarbon and a block having a vinyl bond amount of 62% or more in a diene part, and a polypropylene resin. A composition is disclosed.
- Patent Document 3 a polar modifier, Na alkoxide, and an organolithium compound are used in the polymerization step, and the molar ratio thereof is 0.1 to 10 for Na alkoxide / polar modifier, Na alkoxide / organolithium.
- a method for producing a non-hydrogenated copolymer having a compound in the range of 0.1 to 10 has been proposed.
- Patent Document 4 a polar agent, a metal salt, and an organolithium compound are used in the polymerization step, and the molar ratio thereof is 3 or more for the polar agent / organolithium compound and 0.
- a method for producing a non-hydrogenated copolymer having a range of 01 to 2 and a metal salt / polar agent in the range of 0.001 to 0.5 has been proposed.
- Patent Document 5 proposes a method for producing a hydrogenated copolymer in which a tertiary amine compound and sodium alkoxide are allowed to coexist in the polymerization step and the speed of the subsequent hydrogenation step is improved. ing.
- any of the above-described conventionally proposed manufacturing methods still has room for improvement. Therefore, in the present invention, it is possible to produce a copolymer having a high conjugated diene block portion and a narrow molecular weight distribution in a copolymer obtained by polymerization of a conjugated diene monomer and a vinyl aromatic monomer.
- an object is to provide a method for producing a hydrogenated conjugated diene copolymer having a high hydrogenation rate and excellent productivity.
- the present inventors use a polymerization initiator, a specific ether compound, and an alkali metal alkoxide in the polymerization step, and specify the molar ratio thereof.
- the inventors have found that the above problems can be solved at the same time, and have completed the present invention. That is, the present invention is as follows.
- a method for producing a hydrogenated conjugated diene copolymer is
- a conjugated diene copolymer having a high vinyl bond content in the conjugated diene block portion and a narrow molecular weight distribution is produced.
- a method for producing a hydrogenated conjugated diene copolymer having a high hydrogenation rate and excellent productivity can be provided.
- the present embodiment a mode for carrying out the present invention (hereinafter referred to as “the present embodiment”) will be described in detail.
- this invention is not restrict
- the method for producing the hydrogenated conjugated diene copolymer of the present embodiment is as follows: A polymerization step of copolymerizing a conjugated diene monomer and a vinyl aromatic monomer using an initiator composed of an organolithium compound; A hydrogenation step of hydrogenating the conjugated diene copolymer obtained by the polymerization step; Have In the polymerization step, the organolithium compound, the ether compound (A) having two or more oxygen atoms, and the alkali metal alkoxide (B) are allowed to coexist in the following molar ratio.
- (A) / Organic lithium compound is 0.2 or more and less than 3.0
- B) / Organic lithium compound is 0.01 or more and 0.3 or less.
- a conjugated diene monomer and a vinyl aromatic monomer are copolymerized using a predetermined solvent using an initiator made of an organolithium compound.
- examples of polymerization methods include, for example, Japanese Patent Publication No. 36-19286, Japanese Patent Publication No. 43-171979, Japanese Patent Publication No. 46-32415, Japanese Patent Publication No. 49-36957, Japanese Patent Publication No. 48-2423, and Japanese Patent Publication No. 48. No. -4106, JP-B 56-28925, JP-A 59-166518, JP-A 60-186777, and the like.
- conjugated diene monomer conventionally known materials can be used.
- 1,3-butadiene, isoprene, 2,3-dimethyl-1,3 butadiene, 1,3-pentadiene, 3-methyl-1 , 3-pentadiene, 1,3-heptadiene, 1,3-hexadiene, and the like but are not limited thereto. These may be used alone or in combination of two or more. Of these, 1,3-butadiene and isoprene are preferred.
- vinyl aromatic monomer conventionally known materials can be used, and examples thereof include styrene, ⁇ -methylstyrene, p-methylstyrene, vinylethylbenzene, 2-vinylnaphthalene, divinylbenzene, and diphenylethylene. However, it is not limited to these. These may be used alone or in combination of two or more. Of these, styrene is preferred.
- solvent used for the production of the conjugated diene copolymer conventionally known materials can be used.
- aliphatic hydrocarbons such as butane, pentane, hexane, isopentane, heptane, octane, isooctane; cyclopentane, Alicyclic hydrocarbons such as methylcyclopentane, cyclohexane, methylcyclohexane, and ethylcyclohexane; aromatic hydrocarbons such as benzene, toluene, ethylbenzene, and xylene; and various hydrocarbon solvents, but are not limited to these Absent. These may be used alone or in combination of two or more.
- An initiator composed of an organic lithium compound is a compound in which one or more lithium atoms are bonded in the molecule, such as ethyl lithium, n-propyl.
- examples thereof include, but are not limited to, lithium, isopropyl lithium, n-butyl lithium, sec-butyl lithium, tert-butyl lithium, hexamethylene lithium, butadienyl dilithium, and isoprenyl dilithium. These may be used alone or in combination of two or more. Further, the organolithium compound may be added in two or more portions during the polymerization of the conjugated diene copolymer.
- the polymerization temperature for producing the conjugated diene copolymer is preferably ⁇ 10 to 150 ° C., more preferably 30 to 120 ° C.
- the time required for the polymerization varies depending on the conditions, but is preferably within 48 hours, and more preferably within 10 hours.
- the polymerization atmosphere is preferably an inert gas atmosphere such as nitrogen gas.
- the polymerization pressure is not particularly limited as long as the polymerization pressure is in a range sufficient to maintain the monomer and the solvent in the liquid phase within the above polymerization temperature range. Furthermore, it is preferable that impurities that inactivate the catalyst and the living polymer, for example, water, oxygen, carbon dioxide gas, and the like are not mixed in the polymerization system.
- an ether compound (A) having two or more oxygen atoms (hereinafter sometimes simply referred to as (A)) and described later ( B) Alkali metal alkoxide (hereinafter sometimes simply referred to as (B)) is used.
- the ether compound (A) having two or more oxygen atoms include 2,2-diethoxypropane, 1,2-diethoxypropane, dioxane, ethylene glycol dimethyl ether, ethylene glycol diethyl ether, diethylene glycol dimethyl ether, and diethylene glycol.
- the ether compound (A) having two or more oxygen atoms is preferably an ether compound having two oxygen atoms.
- glycol dialkyl ether or 2,2-bis (2-oxolanyl) propane is more preferable.
- a structure exhibiting symmetry in the molecule is preferable, and in glycol dialkyl ether, two alkyl species in the molecule are preferably the same.
- 2,2-bis (2-oxolanyl) propane and ethylene glycol dialkyl ether are even more preferred.
- the alkali metal alkoxide (B) used in the polymerization step of the conjugated diene copolymer is a compound represented by the general formula MOR (wherein M is an alkali metal and R is an alkyl group).
- the alkali metal of the alkali metal alkoxide (B) is preferably sodium or potassium from the viewpoints of a high vinyl bond content, a narrow molecular weight distribution, and a high polymerization rate.
- the alkali metal alkoxide (B) is not limited to the following, but is preferably sodium alkoxide, lithium alkoxide or potassium alkoxide having an alkyl group having 2 to 12 carbon atoms, more preferably 3 carbon atoms.
- sodium tert-butoxide and sodium tert-pentoxide which are sodium alkoxides, are even more preferable.
- an initiator composed of an organic lithium compound, an ether compound (A) having two or more oxygen atoms
- the alkali metal alkoxide (B) is allowed to coexist in the following molar ratio. That is, the molar ratio of ether compound (A) having 2 or more oxygen atoms / organolithium compound is 0.2 or more and less than 3.0, and the molar ratio of alkali metal alkoxide (B) / organolithium compound is 0.01. More than 0.3.
- the (A) / organolithium compound is 0.2 or more, the molecular weight distribution is narrowed, and from the viewpoint of obtaining high hydrogenation activity, less than 3.0. To do. Further, from the viewpoint of increasing the vinyl bond amount and increasing the polymerization rate, from the viewpoint of setting the (B) / organolithium compound to 0.01 or more, narrowing the molecular weight distribution, and obtaining high hydrogenation activity. The following.
- the polymerization rate is improved, the amount of vinyl bonds in the conjugated diene block portion of the target conjugated diene copolymer can be increased, the molecular weight distribution can be narrowed, and further, the hydrogenation in the hydrogenation step described later. The speed is improved.
- the molar ratio of ether compound (A) / organolithium compound having two or more oxygen atoms in the polymerization step is 1.0 or more, narrow molecular weight distribution and high hydrogenation activity from the viewpoint of high vinyl bond amount and high polymerization rate. In view of the above, 2.5 or less is preferable, and a range of 1.5 or more and 2.0 or less is more preferable. Further, the molar ratio of alkali metal alkoxide (B) / organolithium compound is preferably 0.02 or more from the viewpoint of high vinyl bond amount and high polymerization rate, and 0.2 or less from the viewpoint of narrow molecular weight distribution and high hydrogenation activity.
- the molar ratio of alkali metal alkoxide (B) / ether compound (A) having two or more oxygen atoms is preferably 0.01 or more from the viewpoint of a high vinyl bond amount and a high polymerization rate, and has a narrow molecular weight distribution. Is preferably 0.1 or less, more preferably 0.015 or more and 0.09 or less, still more preferably 0.02 or more and 0.09 or less, and more preferably 0.025 or more and 0.00 or less. Even more preferable is 08 or less.
- the above-described polymerization step is suitable as a method for producing a block copolymer comprising a block mainly composed of a vinyl aromatic monomer and a block mainly composed of a hydrogenated conjugated diene monomer unit.
- the structure of the conjugated diene block copolymer is represented by, for example, the following formulas (1) to (6).
- a represents a block mainly composed of vinyl aromatic monomer units
- b represents a block mainly composed of conjugated diene monomer units.
- the structures such as molecular weight and composition may be the same or different.
- “mainly” means that the monomer unit is contained in an amount of 60% by mass or more, preferably 80% by mass or more, and preferably 90% by mass or more. Is more preferable, and more preferably 95% by mass or more.
- X is, for example, silicon tetrachloride, tin tetrachloride, epoxidized soybean oil, polyhalogenated hydrocarbon compound, carboxylic acid ester compound, polyvinyl compound, bisphenol type epoxy compound, It represents a residue of a coupling agent such as an alkoxysilane compound, a halogenated silane compound or an ester compound, or a residue of an initiator such as a polyfunctional organolithium compound.
- m, n and k each represents an integer of 1 or more, preferably an integer of 1 to 5.
- each block constituting the conjugated diene block copolymer do not necessarily need to be clearly distinguished.
- the distribution of vinyl aromatic monomer units in each polymer block is not limited as long as the content of the vinyl aromatic compound is within the range, and evenly distributed, tapered, stepped, convex Alternatively, it may be distributed in a concave shape.
- a crystal part may be present in the polymer block.
- a plurality of segments having different vinyl aromatic compound contents may coexist.
- Examples of a method of giving variation in the distribution of vinyl units in the conjugated diene moiety constituting the conjugated diene copolymer before hydrogenation described below include, for example, a method of adding a vinylating agent in the polymerization step, polymerization Examples include a method of changing the temperature during the process.
- the hydrogenated conjugated diene copolymer obtained by the production method of the present embodiment is suitable for propylene modification and ensures high compatibility with the polypropylene when polypropylene is used when preparing the composition.
- a hydrogenated conjugated diene copolymer in which the average vinyl bond content in the conjugated diene monomer unit of the conjugated diene copolymer before the hydrogenation step is 62 mol% or more is preferable.
- the average vinyl bond amount is more preferably 69 mol% or more, and further preferably 72 mol% or more.
- 95 mol% or less is preferable from a viewpoint of productivity, 90 mol% or less is more preferable, and 85 mol% or less is more preferable.
- the content of the polymer block mainly composed of vinyl aromatic monomer units in the hydrogenated conjugated diene copolymer after hydrogenation described later is the heat resistance of the target hydrogenated conjugated diene copolymer. Further, from the viewpoint of tensile strength, 5% by mass or more is preferable, and from the viewpoint of flexibility, 40% by mass or less is preferable. The range is more preferably 10 to 30% by mass, and further preferably 13 to 20% by mass.
- the conjugated diene polymer obtained by the polymerization process described above is also characterized by a high block ratio of the vinyl aromatic monomer block. This contributes to the high mechanical strength of the target hydrogenated conjugated diene copolymer and the high mechanical strength and high transparency of the polypropylene composition.
- the conjugated diene copolymer obtained by the polymerization step described above is hydrogenated to obtain the desired hydrogenated conjugated diene copolymer. From the viewpoint of high productivity, a higher hydrogen addition rate is preferable.
- the hydrogenation method include a method in which hydrogen is supplied and an unsaturated group is hydrogenated in the presence of a predetermined hydrogenation catalyst.
- the hydrogenation catalyst is not particularly limited.
- a titanocene catalyst as a hydrogenation catalyst in the hydrogenation step.
- More preferable hydrogenation catalysts include a mixture of a titanocene compound and a reducing organometallic compound.
- the titanocene compound and the hydrogenation method using the same are described in JP-A-8-109219.
- compounds having at least one ligand having a (substituted) cyclopentadienyl skeleton, indenyl skeleton or fluorenyl skeleton such as biscyclopentadienyl titanium dichloride and monopentamethylcyclopentadienyl titanium trichloride.
- the reducing organometallic compound include organoalkali metal compounds such as organolithium, organomagnesium compounds, organoaluminum compounds, organoboron compounds, and organozinc compounds.
- the hydrogenation rate of all unsaturated group units contained in the conjugated diene monomer unit is the viewpoint to obtain high mechanical strength, high aging resistance and high UV resistance in the target hydrogenated conjugated diene copolymer. Therefore, 75 mol% or more is preferable, 85 mol% is more preferable, 90 mol% is further preferable, and 95 mol% or more is even more preferable.
- the hydrogenation rate of all unsaturated group units contained in the conjugated diene monomer unit before hydrogenation can be measured by nuclear magnetic resonance spectrum analysis (NMR).
- the target hydrogenated conjugated diene copolymer is obtained by separating the solvent.
- Solvent separation methods include, for example, a method in which a polar solvent that is a poor solvent for a copolymer such as acetone or alcohol is added to the polymerized solution to precipitate the copolymer, and the copolymer solution is recovered. Putting it in hot water with stirring, removing the solvent by steam stripping, collecting it with a flashing tank, concentrating it in a flushing tank, and then devolatilizing it with a vent extruder, etc., heating the copolymer solution directly and distilling the solvent The method of leaving can be mentioned.
- Stabilizers such as various phenol stabilizers, phosphorus stabilizers, sulfur stabilizers and amine stabilizers can be added to the recovered hydrogenated styrene copolymer.
- a modification step for imparting a functional group to the copolymer may be performed as necessary.
- the modification method include a method in which a modifying agent that generates a functional group-containing atomic group is added to the living terminal of the conjugated diene copolymer or the hydrogenated conjugated diene copolymer.
- functional group-containing atomic groups include, but are not limited to, hydroxyl groups, carbonyl groups, thiocarbonyl groups, acid halide groups, acid anhydride groups, ester groups, carboxyl groups, thiocarboxyl groups, and thiocarboxylic groups.
- Acid ester group, dithiocarboxylic acid ester group, carboxylic acid amide group, thiocarboxylic acid amide group, aldehyde group, thioaldehyde group, carboxylic acid ester group, amide group, sulfonic acid group, sulfonic acid ester group, phosphoric acid group, phosphoric acid Ester group, phosphite group, amino group, imino group, ethyleneimino group, nitrile group, pyridyl group, quinoline group, epoxy group, thioepoxy group, sulfide group, isocyanate group, thioisocyanate group, halogenated silyl group, silanol Group, alkoxysilyl group, tin halide group, alkoxy Tin group, phenyltin group, epithio group, atomic group include that contains at least one functional group selected from a halogen group, preferably, an alkoxysilyl group
- the hydrogenated conjugated diene copolymer obtained by the above-described method for producing a hydrogenated conjugated diene copolymer of the present embodiment preferably has a weight average molecular weight of 40,000 to 500,000, more preferably 50,000. From 400,000 to more preferably 70,000 to 300,000.
- the hydrogenated conjugated diene copolymer obtained by the method for producing a hydrogenated conjugated diene copolymer of the present embodiment has a feature that the molecular weight distribution (ratio of weight average molecular weight to number average molecular weight) is narrow.
- the molecular weight distribution of the hydrogenated conjugated diene copolymer obtained by the present embodiment is preferably 1.5 or less, more preferably 1.3 or less, still more preferably 1.2 or less, and even more preferably 1 0.1 or less, more preferably 1.09 or less, and most preferably 1.07 or less.
- the molecular weight and molecular weight distribution can be determined from measurement by gel permeation chromatography (GPC) shown in the examples described later.
- the hydrogenation catalyst used for the hydrogenation reaction was prepared by the following method. Charge 1 liter of dry and purified cyclohexane to a nitrogen-substituted reaction vessel, add 100 mmol of bis ( ⁇ 5-cyclopentadienyl) titanium dichloride, and add n-hexane solution containing 200 mmol of trimethylaluminum with thorough stirring. The reaction was carried out at room temperature for about 3 days to obtain a hydrogenation catalyst.
- a cyclohexane solution (concentration: 20% by mass) containing 80 parts by mass of butadiene was added over 100 minutes, and then polymerized for another 15 minutes.
- the temperature was controlled at 65 ° C.
- a cyclohexane solution (concentration 20% by mass) containing 10 parts by mass of styrene was added over 10 minutes, and then polymerization was performed for another 10 minutes.
- the temperature was controlled at 65 ° C. Thereafter, methanol was added.
- Measuring equipment JNM-LA400 (manufactured by JEOL)
- Solvent Deuterated chloroform Measurement sample: Sample taken before and after hydrogenation of polymer Sample concentration: 50 mg / mL Observation frequency: 400 MHz
- Chemical shift criteria TMS (tetramethylsilane) Pulse delay: 2.904 seconds
- Number of scans 64 times Pulse width: 45 °
- Measurement temperature 26 ° C (Evaluation methods)
- (1-1) Vinyl Bond Amount The average vinyl bond amount of the conjugated diene before hydrogenation is preferably higher. 70 mol% or more is rated as ⁇ , 65 mol% or more and less than 70 mol% as ⁇ , and less than 65 mol% as ⁇ . .
- Measuring device LC-10 (manufactured by Shimadzu Corporation) Column: TSKgelGMHXL (4.6 mm ID ⁇ 30 cm), 2 solvents: Tetrahydrofuran Calibration curve sample: commercially available standard polystyrene (manufactured by Tosoh Corporation), 10-point measurement (evaluation method) (2-1) Molecular weight distribution From the viewpoint of high tensile strength of the hydrogenated conjugated diene copolymer alone or the composition of the hydrogenated conjugated diene copolymer and polyprene, a smaller molecular weight distribution is preferable. The case where it was less than or equal to 2 was marked with ⁇ , and the case where it exceeded 1.2 was marked with ⁇ .
- the (A) polar compound represents the following compounds (1) to (5).
- B) Alkali metal alkoxide represents the following compounds (I) and (II).
- the symbols in Table 1 indicate the following compounds, respectively.
- Bd Butadiene
- the organolithium compound, the ether compound (A) having two or more oxygen atoms, and the alkali metal alkoxide (B) coexist, and the molar ratio of (A) / organolithium compound is 0.2. More than 3.0, (B) / Organic lithium compound is 0.01 or more and 0.3 or less,
- a hydrogenated conjugated diene copolymer having a high vinyl bond content in the conjugated diene block portion and a narrow molecular weight distribution could be produced while achieving a high productivity and a high hydrogenation rate. .
- the hydrogenated conjugated diene copolymer obtained by the method for producing the hydrogenated conjugated diene copolymer of the present invention is used in the fields of footwear, plastic modifiers, adhesives, etc., household products, home appliances and industrial parts. It has industrial applicability as packaging materials such as medical materials, tube materials, and toy materials.
Abstract
Description
また、前記スチレン系ブロック共重合体の水添物は、耐候性、耐熱性に優れていることから、上記の用途分野以外に、自動車部品や医療器具等にも幅広く実用化されている。
特に共役ジエン部のビニル結合量が高い水添スチレン系共重合体は、ポリプロピレンとの相容性が高いため、ポリプロピレンの改質材として用いられ、それらの組成物が種々の用途に用いられている。
例えば、特許文献1には、ビニル芳香族炭化水素からなるブロックとジエン部のビニル結合量が62%以上であるブロックとを有する共重合体を水素添加した水添ブロック共重合体とポリプロピレン樹脂との組成物が開示されている。
かかる高ビニル結合量を実現するための重合時間の問題を解決するために、特許文献2においては、重合工程で、ジアルキルエーテルとアルカリ有機化合物とを用い、かつこれらのモル比をアルカリ有機化合物/有機リチウム化合物0.5モル以上とする非水添の共重合体の製造方法が提案されている。
また、特許文献3では、重合工程で、極性調整剤とNaアルコキシドと有機リチウム化合物とを用い、かつこれらのモル比を、Naアルコキシド/極性調整剤が0.1~10、Naアルコキシド/有機リチウム化合物が0.1~10の範囲とする非水添の共重合体の製造方法が提案されている。
さらに、特許文献4では、重合工程で、極性剤と金属塩と有機リチウム化合物とを用い、かつこれらのモル比を、極性剤/有機リチウム化合物が3以上、金属塩/有機リチウム化合物が0.01~2の範囲とし、金属塩/極性剤が0.001~0.5の範囲とする非水添の共重合体の製造方法が提案されている。
かかる課題に鑑み、特許文献5には、重合工程で、第3級アミン化合物とナトリウムアルコキシドとを共存させ、その後の水添工程の速度を向上させた水添共重合体の製造方法が提案されている。
そこで本発明においては、共役ジエン系単量体とビニル芳香族系単量体の重合で得られる共重合体の共役ジエンブロック部分のビニル結合量が高く、分子量分布が狭い共重合体を製造可能で、かつ重合工程後の水添工程においては、水添速度が速く、生産性にも優れた水添共役ジエン系共重合体を製造する方法を提供することを目的とする。
すなわち、本発明は以下の通りである。
共役ジエン系単量体とビニル芳香族単量体とを、有機リチウム化合物からなる開始剤を用いて共重合させる重合工程と、
前記重合工程により得られる共役ジエン系共重合体を水添する水添工程と、
を有し、
前記重合工程において、前記有機リチウム化合物と、酸素原子を2個以上有するエーテル系化合物(A)と、アルカリ金属アルコキシド(B)とを下記モル比で共存させる、
水添共役ジエン系共重合体の製造方法。
(A)/有機リチウム化合物が0.2以上3.0未満
(B)/有機リチウム化合物が0.01以上0.3以下
〔2〕
前記重合工程において、アルカリ金属アルコキシド(B)/酸素原子を2個以上有するエーテル化合物(A)のモル比を、0.01以上0.1以下とする、前記〔1〕に記載の水添共役ジエン系共重合体の製造方法。
〔3〕
前記酸素原子を2個以上有するエーテル系化合物(A)が、グリコールジアルキルエーテル又は2,2-ビス(2-オキソラニル)プロパンである、前記〔1〕又は〔2〕に記載の水添共役ジエン系共重合体の製造方法。
〔4〕
前記アルカリ金属アルコキシド(B)のアルカリ金属が、ナトリウム又はカリウムである、前記〔1〕乃至〔3〕のいずれか一に記載の水添共役ジエン系共重合体の製造方法。
〔5〕
前記水添工程において、水添触媒としてチタノセン化合物を用いる、前記〔1〕乃至〔4〕のいずれか一に記載の水添共役ジエン系共重合体の製造方法。
なお、本発明は、以下の実施形態に制限されるものではなく、その要旨の範囲内で種々変形して実施することができる。
本実施形態の水添共役ジエン系共重合体の製造方法は、
共役ジエン系単量体とビニル芳香族単量体とを、有機リチウム化合物からなる開始剤を用いて共重合させる重合工程と、
前記重合工程により得られる共役ジエン系共重合体を水添する水添工程と、
を有し、
前記重合工程において、前記有機リチウム化合物と、酸素原子を2個以上有するエーテル系化合物(A)と、アルカリ金属アルコキシド(B)とを下記モル比で共存させる。
(A)/有機リチウム化合物が0.2以上3.0未満
(B)/有機リチウム化合物が0.01以上0.3以下
重合工程においては、所定の溶媒を用いて共役ジエン系単量体と、ビニル芳香族単量体とを、有機リチウム化合物からなる開始剤を用いて共重合させる。
重合方法としては、例えば、特公昭36-19286号公報、特公昭43-17979号公報、特公昭46-32415号公報、特公昭49-36957号公報、特公昭48-2423号公報、特公昭48-4106号公報、特公昭56-28925号公報、特開昭59-166518号公報、特開昭60-186577号公報等に記載された方法が挙げられる。
共役ジエン単量体としては、従来公知の材料を用いることができ、例えば、1,3-ブタジエン、イソプレン、2,3-ジメチル-1,3ブタジエン、1,3-ペンタジエン、3-メチル-1,3-ペンタジエン、1,3-ヘプタジエン、1,3-ヘキサジエン等が挙げられるが、これらに限定されるものではない。これらは一種のみを単独で用いてもよく、二種以上を併用してもよい。これらの中で、1,3-ブタジエン、イソプレンが好ましい。
ビニル芳香族単量体としては、従来公知の材料を用いることができ、例えば、スチレン、α-メチルスチレン、p-メチルスチレン、ビニルエチルベンゼン、2-ビニルナフタレン、ジビニルベンゼン、ジフェニルエチレン等が挙げられるが、これらに限定されるものではない。これらは一種のみを単独で用いてもよく、二種以上を併用してもよい。これらの中で、スチレンが好ましい。
共役ジエン系共重合体の製造に用いられる溶媒としては、従来公知の材料を用いることができ、例えば、ブタン、ペンタン、ヘキサン、イソペンタン、ヘプタン、オクタン、イソオクタン等の脂肪族炭化水素;シクロペンタン、メチルシクロペンタン、シクロヘキサン、メチルシクロヘキサン、エチルシクロヘキサン等の脂環式炭化水素;ベンゼン、トルエン、エチルベンゼン、キシレン等の芳香族炭化水素等;各種炭化水素溶媒が挙げられるが、これらに限定されるものではない。これらは一種のみを単独で用いてもよく、二種以上を併用してもよい。
有機リチウム化合物からなる開始剤(以下、有機リチウム化合物、有機Li化合物と記載する場合がある。)は、分子中に一個以上のリチウム原子を結合した化合物であり、例えば、エチルリチウム、n-プロピルリチウム、イソプロピルリチウム、n-ブチルリチウム、sec-ブチルリチウム、tert-ブチルリチウム、ヘキサメチレンリチウム、ブタジエニルジリチウム、イソプレニルジリチウム等が挙げられるが、これらに限定されるものではない。これらは一種のみを単独で用いてもよく、二種以上を併用してもよい。
また、有機リチウム化合物は、共役ジエン系共重合体の重合途中で二回以上分割添加してもよい。
共役ジエン系共重合体を製造する際の重合温度は-10~150℃が好ましく、より好ましくは30~120℃である。
重合に要する時間は、条件によって異なるが、48時間以内とすることが好ましく、より好ましくは10時間以内である。
重合系の雰囲気は、窒素ガス等の不活性ガス雰囲気にすることが好ましい。
重合圧力は、上記重合温度範囲でモノマー及び溶媒を液相に維持するために充分な圧力の範囲で行えばよく、特に限定されるものでない。
さらに、重合系内は触媒及びリビングポリマーを不活性化させるような不純物、例えば、水、酸素、炭酸ガス等が混入しないようにすることが好ましい。
本実施形態においては、共役ジエン系共重合体の重合工程で、酸素原子を2個以上有するエーテル系化合物(A)(以下、単に(A)と記載する場合がある。)と、後述する(B)アルカリ金属アルコキシド(以下、単に(B)と記載する場合がある。)とを用いる。
前記酸素原子を2個以上有するエーテル系化合物(A)としては、例えば、2,2-ジエトキシプロパン、1,2-ジエトキシプロパン、ジオキサン、エチレングリコールジメチルエーテル、エチレングリコールジエチルエーテル、ジエチレングリコールジメチルエーテル、ジエチレングリコールジエチルエーテル、エチルエチレングリコール-t-ブチルエーテル、エチルエチレングリコールブチルエーテル、ジメトキシベンゼン、トリエチレングリコールジメチルエーテル、1,2,3-トリアルコキシベンゼン、1,2,4-トリアルコキシベンゼン、ビス(2-オキソラニル)エタン、2,2-ビス(2-オキソラニル)プロパン、1,1-ビス(2-オキソラニル)エタン、2,2-ビス(2-オキソラニル)ブタン、2,2-ビス(5-メチル-2-オキソラニル)プロパン、2,2-ビス(3,4,5-トリメチル-2-オキソラニル)プロパン等のオキソラニルアルカン等が挙げられるが、これらに限定されるものではない。
これらは、単独で用いてもよく、二種以上を併用してもよい。
酸素原子を2個以上有するエーテル系化合物(A)としては、酸素を2個有するエーテル系化合物が好ましい。
特に、グリコールジアルキルエーテル又は2,2-ビス(2-オキソラニル)プロパンがより好ましい。さらに、それらの中でも、分子内で対称性を示す構造が好ましく、グリコールジアルキルエーテルでは、分子内の二つのアルキル種が同じものが好ましい。
2,2-ビス(2-オキソラニル)プロパンやエチレングリコールジアルキルエーテルがさらにより好ましい。
共役ジエン系共重合体の重合工程において使用されるアルカリ金属アルコキシド(B)は、一般式MOR(式中、Mはアルカリ金属、Rはアルキル基である)で表される化合物である。
前記アルカリ金属アルコキシド(B)のアルカリ金属としては、高いビニル結合量、狭い分子量分布、及び高い重合速度の観点から、ナトリウム又はカリウムであることが好ましい。
アルカリ金属アルコキシド(B)としては、以下に限定されるものではないが、好ましくは、炭素数2~12のアルキル基を有するナトリウムアルコキシド、リチウムアルコキシド、カリウムアルコキシドであり、より好ましくは、炭素数3~6のアルキル基を有するナトリウムアルコキシドやカリウムアルコキシドであり、さらに好ましくは、ナトリウム-t-ブトキシド、ナトリウム-t-ペントキシド、カリウム-t-ブトキシド、カリウム-t-ペントキシドである。この中でも、ナトリウムアルコキシドであるナトリウム-t-ブトキシド、ナトリウム-t-ペントキシドがさらにより好ましい。
すなわち、酸素原子を2個以上有するエーテル化合物(A)/有機リチウム化合物のモル比を0.2以上3.0未満とし、アルカリ金属アルコキシド(B)/有機リチウム化合物のモル比が、0.01以上0.3以下とする。
ビニル結合量を高くし、重合速度を高くする観点から、前記(A)/有機リチウム化合物を0.2以上とし、分子量分布を狭くし、かつ高い水添活性を得る観点から3.0未満とする。
また、ビニル結合量を高くし、重合速度を高くする観点から、前記(B)/有機リチウム化合物を0.01以上とし、分子量分布を狭くし、かつ高い水添活性を得る観点から0.3以下とする。
これにより、重合速度の向上が図られ、目的とする共役ジエン系共重合体の共役ジエンブロック部分におけるビニル結合量を高くでき、分子量分布を狭くでき、さらには、後述する水添工程における水添速度の向上が図られる。
また、アルカリ金属アルコキシド(B)/有機リチウム化合物のモル比は、高いビニル結合量及び高い重合速度の観点から0.02以上、狭い分子量分布や高い水添活性の観点から0.2以下が好ましく、0.03以上0.1以下がより好ましく、0.03以上0.08以下がさらに好ましい。
さらに、アルカリ金属アルコキシド(B)/酸素原子を2個以上有するエーテル化合物(A)のモル比は、高いビニル結合量及び高い重合速度の観点から0.01以上であることが好ましく、狭い分子量分布を実現し、かつ高い水添活性を得る観点から0.1以下が好ましく、0.015以上0.09以下がより好ましく、0.02以上0.09以下がさらに好ましく、0.025以上0.08以下がさらにより好ましい。
上述した重合工程は、ビニル芳香族単量体を主体とするブロックと水添共役ジエン単量体単位を主体とするブロックとからなるブロック共重合体の製造方法として好適である。
共役ジエン系ブロック共重合体の構造としては、例えば、下記の式(1)~式(6)で表される。
(a-b)n ・・・(1)
b-(a-b)n ・・・(2)
a-(b-a)n ・・・(3)
a-(b-a)n-X ・・・(4)
[(a-b)k]m-X ・・・(5)
[(a-b)k-a]m-X ・・・(6)
前記式(1)~式(6)中、aはビニル芳香族単量体単位を主体とするブロックを表し、bは共役ジエン単量体単位を主体とするブロックを表す。
共役ジエン系ブロック共重合体中に重合体ブロックa、bが複数存在している場合には、各々の分子量や組成等の構造は同一であってもよいし、異なっていてもよい。
本明細書中、「主体とする」とは、ブロック中、該単量体単位を60質量%以上含有することを意味し、80質量%以上含有することが好ましく、90質量%以上含有することがより好ましく、95質量%以上含有することがさらに好ましい。
m、n及びkは、1以上の整数を表し、1~5の整数であることが好ましい。
また、各重合体ブロック中のビニル芳香族単量体単位の分布は、前記ビニル芳香族化合物含有量の範囲ならば限定されず、均一に分布していても、テーパー状、階段状、凸状、あるいは凹状に分布していてもよい。また、重合体ブロック中に、結晶部が存在していてもよい。各重合体ブロック中には、ビニル芳香族化合物含有量の異なるセグメントが複数個共存していてもよい。
本実施形態の製造方法により得られる水添共役ジエン系共重合体は、プロピレン改質に好適であり、組成物を作製する際、ポリプロピレンを用いる場合に、当該ポリプロピレンとの高い相溶性を確保する観点から、水添工程前における共役ジエン系共重合体の共役ジエン単量体単位中の平均ビニル結合量が62mol%以上である水添共役ジエン系共重合体が好ましい。平均ビニル結合量は、69mol%以上がより好ましく、72mol%以上がさらに好ましい。
また、生産性の観点から95mol%以下が好ましく、90mol%以下がより好ましく、85mol%以下がさらに好ましい。
上述した重合工程により得られた共役ジエン系共重合体を水添し、目的とする水添共役ジエン系共重合体を得る。
高生産性の観点で、水素添加速度は速い方が好ましい。
水素添加の方法としては、所定の水添触媒の存在下で、水素を供給し、不飽和基を水素添加する方法が挙げられる。
前記水添触媒としては、特に限定されないが、例えば、
(1)Ni、Co、Fe、Cr等の有機酸塩又はアセチルアセトン塩等の遷移金属塩と有機アルミニウム等の還元剤とを用いる、いわゆるチーグラー型水添触媒、
(2)Ti、Ru、Rh、Zr等の有機金属化合物等のいわゆる有機金属錯体等の均一系水添触媒、
が挙げられる。
より好ましい水添触媒としては、チタノセン化合物及び還元性有機金属化合物の混合物が挙げられる。
前記チタノセン化合物やそれを用いた水添方法としては、特開平8-109219号公報等に記載されている。例えば、ビスシクロペンタジエニルチタンジクロライド、モノペンタメチルシクロペンタジエニルチタントリクロライド等の(置換)シクロペンタジエニル骨格、インデニル骨格あるいはフルオレニル骨格を有する配位子を少なくとも1つ以上もつ化合物が挙げられる。
また、前記還元性有機金属化合物としては、有機リチウム等の有機アルカリ金属化合物、有機マグネシウム化合物、有機アルミニウム化合物、有機ホウ素化合物あるいは有機亜鉛化合物等が挙げられる。
水素添加前の共役ジエン単量体単位中に含まれる全不飽和基単位の水素添加率は、核磁気共鳴スペクトル解析(NMR)により測定できる。
溶媒の分離の方法としては、例えば、重合後の溶液にアセトン又はアルコール等の共重合体に対する貧溶媒となる極性溶媒を加えて共重合体を沈澱させて回収する方法、共重合体の溶液を撹拌下熱湯中に投入し、スチームストリッピングにより溶媒を除去して回収する方法、フラッシングタンクで濃縮し、さらにベント押出機等で脱揮する方法、直接共重合体溶液を加熱して溶媒を留去する方法等を挙げることができる。
回収された水添スチレン系共重合体には、各種フェノール系安定剤、リン系安定剤、イオウ系安定剤、アミン系安定剤等の安定剤を添加することができる。
本実施形態においては、上述した(重合工程)後、又は(水添工程)後に、必要に応じて、共重合体中に官能基を付与する変性工程を行ってもよい。
変性方法としては、例えば、共役ジエン系共重合体又は水添共役ジエン系共重合体のリビング末端に、官能基含有原子団を生成する変性剤を付加反応させる方法が挙げられる。
官能基含有原子団としては、以下に限定されるものではないが、例えば、水酸基、カルボニル基、チオカルボニル基、酸ハロゲン化物基、酸無水物基、エステル基、カルボキシル基、チオカルボキシル基、チオカルボン酸エステル基、ジチオカルボン酸エステル基、カルボン酸アミド基、チオカルボン酸アミド基、アルデヒド基、チオアルデヒド基、カルボン酸エステル基、アミド基、スルホン酸基、スルホン酸エステル基、リン酸基、リン酸エステル基、亜リン酸エステル基、アミノ基、イミノ基、エチレンイミノ基、ニトリル基、ピリジル基、キノリン基、エポキシ基、チオエポキシ基、スルフィド基、イソシアネート基、チオイソシアネート基、ハロゲン化シリル基、シラノール基、アルコキシシリル基、ハロゲン化スズ基、アルコキシスズ基、フェニルスズ基、エピチオ基、ハロゲン基等から選ばれる官能基を少なくとも一種含有する原子団が挙げられ、好ましくは、アルコキシシリル基、エポキシ基、アミノ基、アミド基、エステル基である。
上述した本実施形態の水添共役ジエン系共重合体の製造方法により得られる水添共役ジエン系共重合体は、重量平均分子量が4万~50万であることが好ましく、より好ましくは5万~40万、さらに好ましくは7万~30万である。
本実施形態の水添共役ジエン系共重合体の製造方法により得られる水添共役ジエン系共重合体は、分子量分布(重量平均分子量と数平均分子量の比)が狭いという特徴を有する。これにより、水添共役ジエン系共重合体や、当該水添共役ジエン系共重合体を用いたポリプロピレン組成物において、高い機械強度が得られる。
本実施形態により得られる水添共役ジエン系共重合体の分子量分布は、1.5以下であることが好ましく、より好ましくは1.3以下、さらに好ましくは1.2以下、さらにより好ましくは1.1以下、よりさらに好ましくは1.09以下、最も好ましくは1.07以下である。
分子量及び分子量分布は、後述する実施例で示すゲルパーミエーションクロマトグラフィー(GPC)による測定から求めることができる。
水添反応に用いた水添触媒は、下記の方法で調製した。
窒素置換した反応容器に乾燥、精製したシクロヘキサン1リットルを仕込み、ビス(η5-シクロペンタジエニル)チタニウムジクロリド100ミリモルを添加し、十分に攪拌しながらトリメチルアルミニウム200ミリモルを含むn-ヘキサン溶液を添加して、室温にて約3日間反応させ、水添触媒を得た。
すべて、市販の試薬を用いた。
(1):2,2-ビス(2-オキソラニル)プロパン
(2):エチレングリコールジブチルエーテル
(3):エチルエチレングリコール-tert-ブチルエーテル
(4):テトラヒドロフラン
(5):テトラメチルエチレンジアミン
なお、前記極性化合物のうち、(1)~(3)は、酸素原子を2個以上有するエーテル系化合物である。
すべて、市販の試薬を用いた。
(I):ナトリウム-t-ペントキシド(シクロヘキサン溶液)
(II):カリウム-t-ペントキシド(シクロヘキサン溶液)
内容積が10Lの攪拌装置及びジャケット付き槽型反応器を使用してバッチ重合を行った。
先ず、1Lのシクロヘキサンを仕込み、その後、n-ブチルリチウムを、全モノマー100質量部に対して0.06質量部添加し、次に下記表1に示したように、エーテル系化合物(A)とアルカリ金属アルコキシド(B)を添加した。
第1ステップとして、スチレン10質量部を含むシクロヘキサン溶液(濃度20質量%)を10分間かけて投入し、その後さらに10分間重合した。重合中、温度は65℃にコントロールした。
次に、第2ステップとして、ブタジエン80質量部を含むシクロヘキサン溶液(濃度20質量%)を100分間かけて投入し、その後さらに15分間重合した。重合中、温度は65℃にコントロールした。
次に第3ステップとして、スチレン10質量部を含むシクロヘキサン溶液(濃度20質量%)を10分間かけて投入し、その後さらに10分間重合した。重合中、温度は65℃にコントロールした。その後、メタノールを添加した。
次に、得られたポリマーに、上記のようにして調製した水添触媒をポリマー100質量部当たりチタンとして150ppm添加し、水素圧0.7MPa、温度70℃で水添反応を行った。
その後、メタノールを添加し、次に安定剤としてオクタデシル-3-(3,5-ジ-t-ブチル-4-ヒドロキシフェニル)プロピオネートを重合体100質量部に対して0.3質量部添加した。
<(1)水添共役ジエン系共重合体におけるスチレン含有量、水素添加前の共役ジエン単量体単位の平均ビニル結合量、共役ジエン単量体単位に基づく二重結合の水素添加率の測定>
水添共役ジエン系共重合体における、スチレン含有量、水素添加前の共役ジエン単量体単位の平均ビニル結合量、共役ジエン単量体単位に基づく二重結合の平均水素添加率は、核磁気共鳴スペクトル解析(NMR)により下記の条件で測定した。
測定機器:JNM-LA400(JEOL製)
溶媒:重水素化クロロホルム
測定サンプル:ポリマーを水素添加する前後の抜き取り品
サンプル濃度:50mg/mL
観測周波数:400MHz
化学シフト基準:TMS(テトラメチルシラン)
パルスディレイ:2.904秒
スキャン回数:64回
パルス幅:45°
測定温度:26℃
(評価方法)
(1-1)ビニル結合量
水素添加前の共役ジエンの平均ビニル結合量は、高い方が好ましく、70mol%以上を○とし、65mol%以上70mol%未満を△とし、65mol%未満を×とした。
(1-2)水素添加率
上記の水添共役ジエン系共重合体の製造方法に記載した条件で、70℃で15分間、水素添加したときの、共役ジエンの二重結合の水素添加率を測定した。
高生産性の観点から、水素添加速度は速い方が良く、98%以上が良く○とし、98%未満は悪く×とした。
水添共役ジエン系共重合体の重量平均分子量、数平均分子量及び分子量分布(Mw/Mn)は、下記の条件のゲルパーミエーションクロマトグラフィー(GPC)により測定した。
分子量分布は、得られた重量平均分子量と数平均分子量の比を取って求めた。
測定装置:LC-10(島津製作所製)
カラム:TSKgelGMHXL(4.6mmID×30cm)、2本
溶媒:テトラヒドロフラン
検量線用サンプル:市販の標準ポリスチレン(東ソー社製)、10点測定
(評価方法)
(2-1)分子量分布
水添共役ジエン系共重合体単体や当該水添共役ジエン系共重合体とポリプレンとの組成物の引張強度が高いという観点から、分子量分布が小さい方が好ましく、1.2以下である場合を○とし、1.2を超えた場合を×とした。
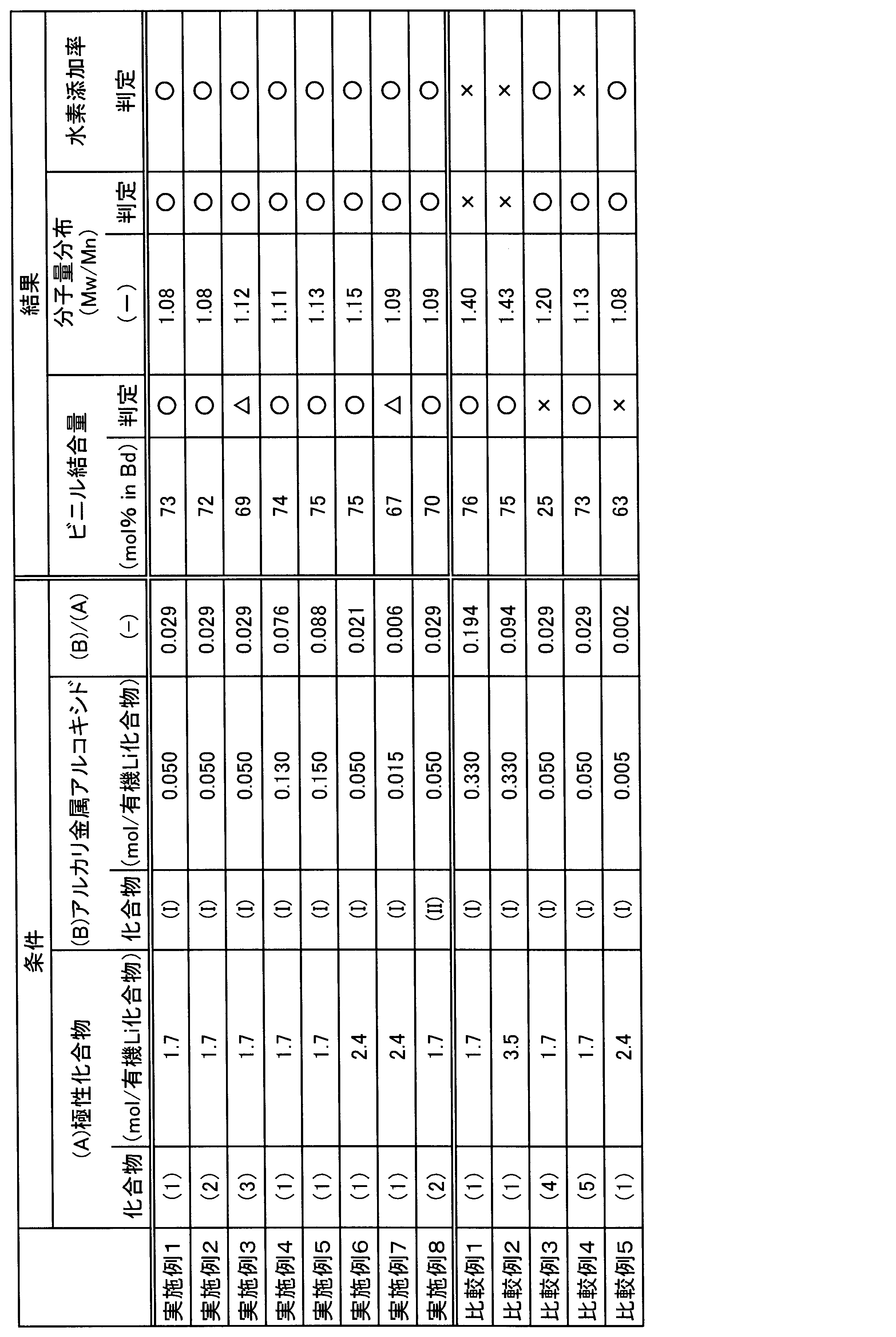
下記表1に示すように(A)極性化合物、(B)アルカリ金属アルコキシドを所定量で用いて、水添共役ジエン系共重合体を作製し、それぞれ評価した。評価結果を下記表1に示す。
(1):2,2-ビス(2-オキソラニル)プロパン
(2):エチレングリコールジブチルエーテル
(3):エチルエチレングリコール-tert-ブチルエーテル
(4):テトラヒドロフラン
(5):テトラメチルエチレンジアミン
前記表1中、(B)アルカリ金属アルコキシドは、下記(I)、(II)の化合物を示す。
(I):ナトリウム-t-ペントキシド(シクロヘキサン溶液)
(II):カリウム-t-ペントキシド(シクロヘキサン溶液)
前記表1中の記号は、それぞれ以下の化合物を示す。
Bd:ブタジエン
(A)/有機リチウム化合物が0.2以上3.0未満、
(B)/有機リチウム化合物が0.01以上0.3以下、
とすることにより、共役ジエンブロック部分のビニル結合量が高く、分子量分布が狭い水添共役ジエン系共重合体を、水添速度が速く、高い生産性を達成しながら、製造することができた。
Claims (5)
- 共役ジエン系単量体とビニル芳香族単量体とを、有機リチウム化合物からなる開始剤を用いて共重合させる重合工程と、
前記重合工程により得られる共役ジエン系共重合体を水添する水添工程と、
を有し、
前記重合工程において、前記有機リチウム化合物と、酸素原子を2個以上有するエーテル系化合物(A)と、アルカリ金属アルコキシド(B)とを下記モル比で共存させる、
水添共役ジエン系共重合体の製造方法。
(A)/有機リチウム化合物が0.2以上3.0未満
(B)/有機リチウム化合物が0.01以上0.3以下 - 前記重合工程において、アルカリ金属アルコキシド(B)/酸素原子を2個以上有するエーテル化合物(A)のモル比を、0.01以上0.1以下とする、請求項1に記載の水添共役ジエン系共重合体の製造方法。
- 前記酸素原子を2個以上有するエーテル系化合物(A)が、グリコールジアルキルエーテル又は2,2-ビス(2-オキソラニル)プロパンである、請求項1又は2に記載の水添共役ジエン系共重合体の製造方法。
- 前記アルカリ金属アルコキシド(B)のアルカリ金属が、ナトリウム又はカリウムである、請求項1乃至3のいずれか一項に記載の水添共役ジエン系共重合体の製造方法。
- 前記水添工程において、水添触媒としてチタノセン化合物を用いる、請求項1乃至4のいずれか一項に記載の水添共役ジエン系共重合体の製造方法。
Priority Applications (6)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN201280016169.5A CN103459431B (zh) | 2011-05-27 | 2012-05-11 | 氢化共轭二烯系共聚物的制造方法 |
| US14/122,144 US9546238B2 (en) | 2011-05-27 | 2012-05-11 | Method for producing hydrogenated conjugated diene copolymer |
| KR1020137024275A KR101575444B1 (ko) | 2011-05-27 | 2012-05-11 | 수소 첨가 공액 디엔계 공중합체의 제조 방법 |
| EP12794087.2A EP2716663B1 (en) | 2011-05-27 | 2012-05-11 | Method for manufacturing hydrogenated conjugated diene copolymer |
| JP2013517944A JP5906238B2 (ja) | 2011-05-27 | 2012-05-11 | 水添共役ジエン系共重合体の製造方法 |
| ES12794087.2T ES2543189T3 (es) | 2011-05-27 | 2012-05-11 | Método para producir un copolímero de dieno conjugado hidrogenado |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2011119647 | 2011-05-27 | ||
| JP2011-119647 | 2011-05-27 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2012165120A1 true WO2012165120A1 (ja) | 2012-12-06 |
Family
ID=47258984
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2012/062137 WO2012165120A1 (ja) | 2011-05-27 | 2012-05-11 | 水添共役ジエン系共重合体の製造方法 |
Country Status (8)
| Country | Link |
|---|---|
| US (1) | US9546238B2 (ja) |
| EP (1) | EP2716663B1 (ja) |
| JP (1) | JP5906238B2 (ja) |
| KR (1) | KR101575444B1 (ja) |
| CN (1) | CN103459431B (ja) |
| ES (1) | ES2543189T3 (ja) |
| TW (1) | TWI506047B (ja) |
| WO (1) | WO2012165120A1 (ja) |
Cited By (26)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20150135482A (ko) * | 2013-04-30 | 2015-12-02 | 아사히 가세이 케미칼즈 가부시키가이샤 | 티타늄 산화물 함유 조성물, 중합체 조성물 및 성형체 |
| CN105944676A (zh) * | 2016-04-26 | 2016-09-21 | 张玲 | 一种呋喃二甲酸庚酯纯化用吸附剂的制备方法 |
| JP2016196583A (ja) * | 2015-04-03 | 2016-11-24 | 旭化成株式会社 | 水素化ブロック共重合体並びにこれを用いたポリプロピレン樹脂組成物及びその成形体 |
| WO2017150048A1 (ja) | 2016-03-03 | 2017-09-08 | 日本ゼオン株式会社 | 非水系二次電池電極用バインダー組成物、非水系二次電池電極用導電材ペースト組成物、非水系二次電池電極用スラリー組成物、非水系二次電池用電極および非水系二次電池 |
| WO2018123624A1 (ja) | 2016-12-28 | 2018-07-05 | 日本ゼオン株式会社 | 非水系二次電池負極用スラリー組成物及びその製造方法、非水系二次電池用負極、並びに非水系二次電池 |
| WO2019021891A1 (ja) | 2017-07-28 | 2019-01-31 | 日本ゼオン株式会社 | 電気化学素子用電極および電気化学素子、並びに電気化学素子用電極の製造方法 |
| WO2019054173A1 (ja) | 2017-09-15 | 2019-03-21 | 日本ゼオン株式会社 | 電気化学素子電極用スラリー組成物、電気化学素子用電極、電気化学素子、および電気化学素子電極用スラリー組成物の製造方法 |
| US10312522B2 (en) | 2015-03-27 | 2019-06-04 | Zeon Corporation | Binder composition for lithium ion secondary battery positive electrode, slurry composition for lithium ion secondary battery positive electrode, positive electrode for lithium ion secondary battery and lithium ion secondary battery |
| WO2019131210A1 (ja) | 2017-12-28 | 2019-07-04 | 日本ゼオン株式会社 | 二次電池正極用バインダー組成物、二次電池正極用スラリー組成物及びその製造方法、二次電池用正極、並びに二次電池 |
| WO2019131211A1 (ja) | 2017-12-28 | 2019-07-04 | 日本ゼオン株式会社 | 二次電池正極用バインダー組成物、二次電池正極用スラリー組成物及びその製造方法、二次電池用正極、並びに二次電池 |
| US10388961B2 (en) | 2015-07-14 | 2019-08-20 | Zeon Corporation | Binder composition for secondary battery electrode, conductive material paste composition for secondary battery electrode, slurry composition for secondary battery electrode, electrode for secondary battery, and secondary battery |
| WO2019159672A1 (ja) * | 2018-02-14 | 2019-08-22 | 日本ゼオン株式会社 | 酸無水物基含有ブロック共重合体、樹脂組成物、樹脂シート、および合わせガラス |
| WO2020021912A1 (ja) * | 2018-07-24 | 2020-01-30 | 日本ゼオン株式会社 | 共重合体の製造方法及び共重合体水素化物の製造方法、共重合体組成物、重合体組成物、並びに成形体 |
| US10566628B2 (en) | 2014-04-02 | 2020-02-18 | Zeon Corporation | Slurry for lithium ion secondary battery positive electrode-use, method for producing slurry for lithium ion secondary battery positive electrode-use, method for producing positive electrode for lithium ion secondary battery-use, and lithium ion secondary battery |
| WO2020241322A1 (ja) | 2019-05-31 | 2020-12-03 | 日本ゼオン株式会社 | 全固体二次電池用スラリー組成物、固体電解質含有層および全固体二次電池、並びに全固体二次電池用スラリー組成物の製造方法 |
| US10964947B2 (en) | 2015-06-29 | 2021-03-30 | Zeon Corporation | Binder composition for secondary battery electrode, slurry composition for secondary battery electrode, electrode for secondary battery, and secondary battery |
| WO2021085344A1 (ja) | 2019-10-31 | 2021-05-06 | 日本ゼオン株式会社 | 二次電池用ペースト、二次電池正極用スラリー、二次電池用正極、二次電池、および二次電池用ペーストの製造方法 |
| WO2021085141A1 (ja) | 2019-10-31 | 2021-05-06 | 日本ゼオン株式会社 | 全固体二次電池用バインダー組成物、全固体二次電池用スラリー組成物、固体電解質含有層および全固体二次電池 |
| WO2021085343A1 (ja) | 2019-10-31 | 2021-05-06 | 日本ゼオン株式会社 | 二次電池用ペースト、二次電池正極用スラリー、二次電池用正極、二次電池、および二次電池用ペーストの製造方法 |
| WO2021085044A1 (ja) | 2019-10-31 | 2021-05-06 | 日本ゼオン株式会社 | 二次電池用バインダー組成物、二次電池用スラリー組成物、二次電池用機能層および二次電池 |
| WO2021131484A1 (ja) | 2019-12-26 | 2021-07-01 | 日本ゼオン株式会社 | 二次電池用バインダー組成物、二次電池用スラリー組成物、および固体電解質含有層、並びに、全固体二次電池および全固体二次電池の製造方法 |
| WO2022044815A1 (ja) | 2020-08-31 | 2022-03-03 | 日本ゼオン株式会社 | 全固体二次電池用バインダー組成物の製造方法、全固体二次電池用スラリー組成物の製造方法、固体電解質含有層の製造方法、および全固体二次電池の製造方法 |
| WO2022113859A1 (ja) | 2020-11-27 | 2022-06-02 | 日本ゼオン株式会社 | 電気化学素子用ペースト、電気化学素子電極用スラリー、電気化学素子用電極及び電気化学素子 |
| WO2022113703A1 (ja) | 2020-11-27 | 2022-06-02 | 日本ゼオン株式会社 | 電気化学素子用電極及び電気化学素子 |
| WO2022249933A1 (ja) | 2021-05-27 | 2022-12-01 | 日本ゼオン株式会社 | 全固体二次電池用バインダー組成物、全固体二次電池用スラリー組成物、全固体二次電池用機能層、および全固体二次電池 |
| US11784313B2 (en) | 2015-09-30 | 2023-10-10 | Zeon Corporation | Conductive material paste composition for secondary battery electrode, slurry composition for secondary battery electrode, undercoating layer-equipped current collector for secondary battery electrode, electrode for secondary battery, and secondary battery |
Families Citing this family (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8790387B2 (en) | 2008-10-10 | 2014-07-29 | Edwards Lifesciences Corporation | Expandable sheath for introducing an endovascular delivery device into a body |
| MY182927A (en) * | 2014-06-02 | 2021-02-05 | Asahi Chemical Ind | Conjugated diene-based polymer, method for producing the same, and composition including the same |
| CN105585809B (zh) * | 2014-10-30 | 2019-04-16 | 旭化成株式会社 | 氢化嵌段共聚物组合物和粘合剂组合物 |
| US10792471B2 (en) | 2015-04-10 | 2020-10-06 | Edwards Lifesciences Corporation | Expandable sheath |
| EP3327041B1 (en) * | 2016-11-29 | 2024-04-10 | TSRC Corporation | Process and catalyst composition for producing selectively hydrogenated conjugated diene polymer |
| CN113845707B (zh) * | 2020-06-26 | 2023-07-07 | 旭化成株式会社 | 橡胶组合物的压块成型体、压块成型体的制造方法、交联用橡胶组合物以及轮胎用胎面 |
Citations (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS3619286B1 (ja) | 1959-05-28 | 1961-10-13 | ||
| JPS4936957B1 (ja) | 1962-08-09 | 1974-10-04 | ||
| JPS5628925A (en) | 1979-08-20 | 1981-03-23 | Sankyo Eng:Kk | Building method for underground continuous wall |
| JPS59166518A (ja) | 1983-03-10 | 1984-09-19 | Japan Synthetic Rubber Co Ltd | 直鎖状ブロック共重合体 |
| JPS60186577A (ja) | 1984-03-06 | 1985-09-24 | Japan Synthetic Rubber Co Ltd | ホツトメルト型粘着剤組成物 |
| JPH0649111A (ja) * | 1992-07-28 | 1994-02-22 | Asahi Chem Ind Co Ltd | 重合体を製造する方法 |
| JPH08109219A (ja) | 1994-10-11 | 1996-04-30 | Asahi Chem Ind Co Ltd | 水添重合体 |
| JPH09132609A (ja) | 1995-09-22 | 1997-05-20 | Goodyear Tire & Rubber Co:The | タイヤトレッド用高性能配合物 |
| JP2000053706A (ja) * | 1998-08-07 | 2000-02-22 | Jsr Corp | 水添共役ジオレフィン系重合体 |
| WO2000015681A1 (en) | 1998-09-14 | 2000-03-23 | Asahi Kasei Kogyo Kabushiki Kaisha | Hydrogenated block copolymer |
| JP2000169521A (ja) * | 1998-12-04 | 2000-06-20 | Nippon Zeon Co Ltd | 水素化重合体、樹脂組成物、及び情報記録媒体基板用成形材料 |
| JP2001240636A (ja) * | 2000-03-01 | 2001-09-04 | Jsr Corp | 共役ジエン系ブロック共重合体およびその水添物の製造法 |
| JP2005513172A (ja) | 2001-07-16 | 2005-05-12 | ソシエテ ド テクノロジー ミシュラン | 環状ビニル単位を持つジエンエラストマー及びその製造方法 |
| JP2006500435A (ja) | 2002-07-30 | 2006-01-05 | サソル ジャーマニー ゲーエムベーハー | 共役ジエン及びビニル芳香族化合物を用いたポリメリセートの生成方法、それによって生成されるポリメリセート、及びその使用 |
| JP2006241289A (ja) * | 2005-03-03 | 2006-09-14 | Asahi Kasei Chemicals Corp | ブロック共重合体の製造方法 |
| WO2008020476A1 (fr) | 2006-08-16 | 2008-02-21 | Asahi Kasei Chemicals Corporation | Procédé servant à produire un copolymère en blocs et copolymère en blocs ou son produit d'hydrogénation |
| JP2010143960A (ja) * | 2008-12-16 | 2010-07-01 | Nippon Zeon Co Ltd | 脂環式炭化水素ランダム共重合体、その製造方法、樹脂組成物、及び成形物 |
Family Cites Families (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3281383A (en) | 1962-08-09 | 1966-10-25 | Phillips Petroleum Co | Branched polymers prepared from monolithium-terminated polymers and compounds having at least three reactive sites |
| JPS5628925B2 (ja) | 1973-01-24 | 1981-07-04 | ||
| US4603155A (en) | 1983-03-10 | 1986-07-29 | Japan Synthetic Rubber Co., Ltd. | Alkenyl aromatic compound-conjugated diene block copolymer and process for the production thereof |
| US5677402A (en) * | 1995-09-22 | 1997-10-14 | The Goodyear Tire & Rubber Company | Process for preparing 3,4-polyisoprene rubber |
| EP1193274B1 (en) | 1998-12-04 | 2006-05-31 | Nippon Zeon Co., Ltd. | Resin composition comprising hydrogenated polymers and process for producing substrate for information-recording medium |
| US20060106150A1 (en) * | 2004-10-29 | 2006-05-18 | Jsr Corporation | Block copolymer, rubber composition containing the same and molded product |
| JP5140918B2 (ja) | 2004-10-29 | 2013-02-13 | Jsr株式会社 | ゴム組成物及び成形品 |
| JP5214236B2 (ja) | 2005-02-21 | 2013-06-19 | 旭化成ケミカルズ株式会社 | 水添ブロック共重合体及びその組成物 |
| CN101384631B (zh) * | 2006-02-13 | 2011-03-09 | 旭化成化学株式会社 | 氢化嵌段共聚物、含有该氢化嵌段共聚物的树脂组合物以及它们的交联体和交联发泡体 |
| DE112009001781B4 (de) | 2008-08-12 | 2014-12-11 | Asahi Kasei Chemicals Corporation | Hydriertes Blockcopolymer enthaltende Zusammensetzung und Formgegenstand unter Verwendung derselben |
-
2012
- 2012-05-11 KR KR1020137024275A patent/KR101575444B1/ko active IP Right Grant
- 2012-05-11 US US14/122,144 patent/US9546238B2/en active Active
- 2012-05-11 EP EP12794087.2A patent/EP2716663B1/en active Active
- 2012-05-11 WO PCT/JP2012/062137 patent/WO2012165120A1/ja active Application Filing
- 2012-05-11 JP JP2013517944A patent/JP5906238B2/ja active Active
- 2012-05-11 ES ES12794087.2T patent/ES2543189T3/es active Active
- 2012-05-11 CN CN201280016169.5A patent/CN103459431B/zh active Active
- 2012-05-24 TW TW101118604A patent/TWI506047B/zh active
Patent Citations (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS3619286B1 (ja) | 1959-05-28 | 1961-10-13 | ||
| JPS4936957B1 (ja) | 1962-08-09 | 1974-10-04 | ||
| JPS5628925A (en) | 1979-08-20 | 1981-03-23 | Sankyo Eng:Kk | Building method for underground continuous wall |
| JPS59166518A (ja) | 1983-03-10 | 1984-09-19 | Japan Synthetic Rubber Co Ltd | 直鎖状ブロック共重合体 |
| JPS60186577A (ja) | 1984-03-06 | 1985-09-24 | Japan Synthetic Rubber Co Ltd | ホツトメルト型粘着剤組成物 |
| JPH0649111A (ja) * | 1992-07-28 | 1994-02-22 | Asahi Chem Ind Co Ltd | 重合体を製造する方法 |
| JPH08109219A (ja) | 1994-10-11 | 1996-04-30 | Asahi Chem Ind Co Ltd | 水添重合体 |
| JPH09132609A (ja) | 1995-09-22 | 1997-05-20 | Goodyear Tire & Rubber Co:The | タイヤトレッド用高性能配合物 |
| JP2000053706A (ja) * | 1998-08-07 | 2000-02-22 | Jsr Corp | 水添共役ジオレフィン系重合体 |
| WO2000015681A1 (en) | 1998-09-14 | 2000-03-23 | Asahi Kasei Kogyo Kabushiki Kaisha | Hydrogenated block copolymer |
| JP2000169521A (ja) * | 1998-12-04 | 2000-06-20 | Nippon Zeon Co Ltd | 水素化重合体、樹脂組成物、及び情報記録媒体基板用成形材料 |
| JP2001240636A (ja) * | 2000-03-01 | 2001-09-04 | Jsr Corp | 共役ジエン系ブロック共重合体およびその水添物の製造法 |
| JP2005513172A (ja) | 2001-07-16 | 2005-05-12 | ソシエテ ド テクノロジー ミシュラン | 環状ビニル単位を持つジエンエラストマー及びその製造方法 |
| JP2006500435A (ja) | 2002-07-30 | 2006-01-05 | サソル ジャーマニー ゲーエムベーハー | 共役ジエン及びビニル芳香族化合物を用いたポリメリセートの生成方法、それによって生成されるポリメリセート、及びその使用 |
| JP2006241289A (ja) * | 2005-03-03 | 2006-09-14 | Asahi Kasei Chemicals Corp | ブロック共重合体の製造方法 |
| WO2008020476A1 (fr) | 2006-08-16 | 2008-02-21 | Asahi Kasei Chemicals Corporation | Procédé servant à produire un copolymère en blocs et copolymère en blocs ou son produit d'hydrogénation |
| JP2010143960A (ja) * | 2008-12-16 | 2010-07-01 | Nippon Zeon Co Ltd | 脂環式炭化水素ランダム共重合体、その製造方法、樹脂組成物、及び成形物 |
Non-Patent Citations (1)
| Title |
|---|
| See also references of EP2716663A4 * |
Cited By (33)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20150135482A (ko) * | 2013-04-30 | 2015-12-02 | 아사히 가세이 케미칼즈 가부시키가이샤 | 티타늄 산화물 함유 조성물, 중합체 조성물 및 성형체 |
| KR101716072B1 (ko) * | 2013-04-30 | 2017-03-13 | 아사히 가세이 케미칼즈 가부시키가이샤 | 티타늄 산화물 함유 조성물, 중합체 조성물 및 성형체 |
| US9745444B2 (en) | 2013-04-30 | 2017-08-29 | Asahi Kasei Chemicals Corporation | Composition containing oxide of titanium, polymer composition, and molded article |
| US10566628B2 (en) | 2014-04-02 | 2020-02-18 | Zeon Corporation | Slurry for lithium ion secondary battery positive electrode-use, method for producing slurry for lithium ion secondary battery positive electrode-use, method for producing positive electrode for lithium ion secondary battery-use, and lithium ion secondary battery |
| US10312522B2 (en) | 2015-03-27 | 2019-06-04 | Zeon Corporation | Binder composition for lithium ion secondary battery positive electrode, slurry composition for lithium ion secondary battery positive electrode, positive electrode for lithium ion secondary battery and lithium ion secondary battery |
| JP2016196583A (ja) * | 2015-04-03 | 2016-11-24 | 旭化成株式会社 | 水素化ブロック共重合体並びにこれを用いたポリプロピレン樹脂組成物及びその成形体 |
| US10964947B2 (en) | 2015-06-29 | 2021-03-30 | Zeon Corporation | Binder composition for secondary battery electrode, slurry composition for secondary battery electrode, electrode for secondary battery, and secondary battery |
| US10388961B2 (en) | 2015-07-14 | 2019-08-20 | Zeon Corporation | Binder composition for secondary battery electrode, conductive material paste composition for secondary battery electrode, slurry composition for secondary battery electrode, electrode for secondary battery, and secondary battery |
| EP3920285A1 (en) | 2015-07-14 | 2021-12-08 | Zeon Corporation | Binder composition for secondary battery electrode, conductive material paste composition for secondary battery electrode, slurry composition for secondary battery electrode, electrode for secondary battery, and secondary battery |
| US11784313B2 (en) | 2015-09-30 | 2023-10-10 | Zeon Corporation | Conductive material paste composition for secondary battery electrode, slurry composition for secondary battery electrode, undercoating layer-equipped current collector for secondary battery electrode, electrode for secondary battery, and secondary battery |
| WO2017150048A1 (ja) | 2016-03-03 | 2017-09-08 | 日本ゼオン株式会社 | 非水系二次電池電極用バインダー組成物、非水系二次電池電極用導電材ペースト組成物、非水系二次電池電極用スラリー組成物、非水系二次電池用電極および非水系二次電池 |
| US11145864B2 (en) | 2016-03-03 | 2021-10-12 | Zeon Corporation | Binder composition for non-aqueous secondary battery electrode, conductive material paste composition for non-aqueous secondary battery electrode, slurry composition for non-aqueous secondary battery electrode, electrode for non-aqueous secondary battery, and non-aqueous secondary battery |
| CN105944676A (zh) * | 2016-04-26 | 2016-09-21 | 张玲 | 一种呋喃二甲酸庚酯纯化用吸附剂的制备方法 |
| US11462738B2 (en) | 2016-12-28 | 2022-10-04 | Zeon Corporation | Slurry composition including lithium titanium oxide and nitrile butadiene rubber and method of producing the same, negative electrode for non-aqueous secondary battery, and non-aqueous secondary battery |
| WO2018123624A1 (ja) | 2016-12-28 | 2018-07-05 | 日本ゼオン株式会社 | 非水系二次電池負極用スラリー組成物及びその製造方法、非水系二次電池用負極、並びに非水系二次電池 |
| WO2019021891A1 (ja) | 2017-07-28 | 2019-01-31 | 日本ゼオン株式会社 | 電気化学素子用電極および電気化学素子、並びに電気化学素子用電極の製造方法 |
| US11387463B2 (en) | 2017-07-28 | 2022-07-12 | Zeon Corporation | Electrode for electrochemical device, electrochemical device, and method of producing electrode for electrochemical device |
| WO2019054173A1 (ja) | 2017-09-15 | 2019-03-21 | 日本ゼオン株式会社 | 電気化学素子電極用スラリー組成物、電気化学素子用電極、電気化学素子、および電気化学素子電極用スラリー組成物の製造方法 |
| WO2019131210A1 (ja) | 2017-12-28 | 2019-07-04 | 日本ゼオン株式会社 | 二次電池正極用バインダー組成物、二次電池正極用スラリー組成物及びその製造方法、二次電池用正極、並びに二次電池 |
| US11742489B2 (en) | 2017-12-28 | 2023-08-29 | Zeon Corporation | Binder composition for secondary battery positive electrode, slurry composition for secondary battery positive electrode and method of producing same, positive electrode for secondary battery, and secondary battery |
| WO2019131211A1 (ja) | 2017-12-28 | 2019-07-04 | 日本ゼオン株式会社 | 二次電池正極用バインダー組成物、二次電池正極用スラリー組成物及びその製造方法、二次電池用正極、並びに二次電池 |
| WO2019159672A1 (ja) * | 2018-02-14 | 2019-08-22 | 日本ゼオン株式会社 | 酸無水物基含有ブロック共重合体、樹脂組成物、樹脂シート、および合わせガラス |
| WO2020021912A1 (ja) * | 2018-07-24 | 2020-01-30 | 日本ゼオン株式会社 | 共重合体の製造方法及び共重合体水素化物の製造方法、共重合体組成物、重合体組成物、並びに成形体 |
| WO2020241322A1 (ja) | 2019-05-31 | 2020-12-03 | 日本ゼオン株式会社 | 全固体二次電池用スラリー組成物、固体電解質含有層および全固体二次電池、並びに全固体二次電池用スラリー組成物の製造方法 |
| WO2021085044A1 (ja) | 2019-10-31 | 2021-05-06 | 日本ゼオン株式会社 | 二次電池用バインダー組成物、二次電池用スラリー組成物、二次電池用機能層および二次電池 |
| WO2021085344A1 (ja) | 2019-10-31 | 2021-05-06 | 日本ゼオン株式会社 | 二次電池用ペースト、二次電池正極用スラリー、二次電池用正極、二次電池、および二次電池用ペーストの製造方法 |
| WO2021085343A1 (ja) | 2019-10-31 | 2021-05-06 | 日本ゼオン株式会社 | 二次電池用ペースト、二次電池正極用スラリー、二次電池用正極、二次電池、および二次電池用ペーストの製造方法 |
| WO2021085141A1 (ja) | 2019-10-31 | 2021-05-06 | 日本ゼオン株式会社 | 全固体二次電池用バインダー組成物、全固体二次電池用スラリー組成物、固体電解質含有層および全固体二次電池 |
| WO2021131484A1 (ja) | 2019-12-26 | 2021-07-01 | 日本ゼオン株式会社 | 二次電池用バインダー組成物、二次電池用スラリー組成物、および固体電解質含有層、並びに、全固体二次電池および全固体二次電池の製造方法 |
| WO2022044815A1 (ja) | 2020-08-31 | 2022-03-03 | 日本ゼオン株式会社 | 全固体二次電池用バインダー組成物の製造方法、全固体二次電池用スラリー組成物の製造方法、固体電解質含有層の製造方法、および全固体二次電池の製造方法 |
| WO2022113859A1 (ja) | 2020-11-27 | 2022-06-02 | 日本ゼオン株式会社 | 電気化学素子用ペースト、電気化学素子電極用スラリー、電気化学素子用電極及び電気化学素子 |
| WO2022113703A1 (ja) | 2020-11-27 | 2022-06-02 | 日本ゼオン株式会社 | 電気化学素子用電極及び電気化学素子 |
| WO2022249933A1 (ja) | 2021-05-27 | 2022-12-01 | 日本ゼオン株式会社 | 全固体二次電池用バインダー組成物、全固体二次電池用スラリー組成物、全固体二次電池用機能層、および全固体二次電池 |
Also Published As
| Publication number | Publication date |
|---|---|
| JPWO2012165120A1 (ja) | 2015-02-23 |
| KR101575444B1 (ko) | 2015-12-07 |
| EP2716663A4 (en) | 2014-06-18 |
| US20140121329A1 (en) | 2014-05-01 |
| TW201302829A (zh) | 2013-01-16 |
| KR20130122976A (ko) | 2013-11-11 |
| US9546238B2 (en) | 2017-01-17 |
| CN103459431B (zh) | 2015-01-21 |
| EP2716663A1 (en) | 2014-04-09 |
| TWI506047B (zh) | 2015-11-01 |
| EP2716663B1 (en) | 2015-06-24 |
| CN103459431A (zh) | 2013-12-18 |
| ES2543189T3 (es) | 2015-08-17 |
| JP5906238B2 (ja) | 2016-04-20 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5906238B2 (ja) | 水添共役ジエン系共重合体の製造方法 | |
| KR101050053B1 (ko) | 블록 공중합체의 제조 방법 및 블록 공중합체 또는 그의 수소 첨가물 | |
| CN109563184B (zh) | 改性共轭二烯系聚合物、橡胶组合物以及轮胎 | |
| JP6435022B2 (ja) | 水添ブロック共重合体およびそれを含む組成物 | |
| US20050107521A1 (en) | Asphalt composition containing hydrogenated conjugated diene copolymer | |
| JP2005509066A (ja) | 線状のブロック共重合体及びその製造方法 | |
| ES2452535T3 (es) | Polímeros acoplados y método de fabricación de los mismos | |
| US9738742B2 (en) | Method for producing polymer | |
| JPWO2005040267A1 (ja) | 履物用ゴム組成物 | |
| JP4651413B2 (ja) | ブロック共重合体の製造方法 | |
| JP5728295B2 (ja) | 変性共役ジエン系共重合体の製造方法、変性共役ジエン系共重合体及び変性共役ジエン系共重合体組成物 | |
| JP4716756B2 (ja) | ランダム共重合体の製造方法 | |
| JP3996790B2 (ja) | アスファルト組成物 | |
| KR102270946B1 (ko) | 공액 다이엔 중합체, 제형 및 이의 제조 방법 | |
| EP2042531B1 (en) | Block copolymer, composition for resin modification, and modified resin composition | |
| JP2008045034A (ja) | 新規なブロック共重合体又はその水素添加物 | |
| WO2014157465A1 (ja) | 放射状共役ジエン系ゴムの製造方法 | |
| JP3580020B2 (ja) | ブロック共重合体及びその水添物の製造方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 12794087 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 20137024275 Country of ref document: KR Kind code of ref document: A |
|
| ENP | Entry into the national phase |
Ref document number: 2013517944 Country of ref document: JP Kind code of ref document: A |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2012794087 Country of ref document: EP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 14122144 Country of ref document: US |