KR20200052384A - 부분입체 이성질성으로 순수한 포스포라미데이트 전구약물의 제조 방법 - Google Patents
부분입체 이성질성으로 순수한 포스포라미데이트 전구약물의 제조 방법 Download PDFInfo
- Publication number
- KR20200052384A KR20200052384A KR1020207012760A KR20207012760A KR20200052384A KR 20200052384 A KR20200052384 A KR 20200052384A KR 1020207012760 A KR1020207012760 A KR 1020207012760A KR 20207012760 A KR20207012760 A KR 20207012760A KR 20200052384 A KR20200052384 A KR 20200052384A
- Authority
- KR
- South Korea
- Prior art keywords
- another aspect
- alkyl
- optionally substituted
- formula
- compound
- Prior art date
Links
- 0 *C(*)(C(O*)=O)N(*)P(*)(O[Al])=O Chemical compound *C(*)(C(O*)=O)N(*)P(*)(O[Al])=O 0.000 description 1
- RBYLMPDQFVJUEN-UHFFFAOYSA-N CC(C(OC1CCCC1)=O)N[O](c(cc1)ccc1[NH+]([O-])OC)[P](Oc1ccccc1)=O Chemical compound CC(C(OC1CCCC1)=O)N[O](c(cc1)ccc1[NH+]([O-])OC)[P](Oc1ccccc1)=O RBYLMPDQFVJUEN-UHFFFAOYSA-N 0.000 description 1
- QDQVXVRZVCTVHE-YFKPBYRVSA-N CC(C)OC([C@H](C)N)=O Chemical compound CC(C)OC([C@H](C)N)=O QDQVXVRZVCTVHE-YFKPBYRVSA-N 0.000 description 1
- KBWYRYDDVDCIDE-GKIKDSKJSA-N CC(C)OC([C@H](C)NP(Oc1ccccc1)(Oc(cc1)ccc1[NH+2]OC)=O)=O Chemical compound CC(C)OC([C@H](C)NP(Oc1ccccc1)(Oc(cc1)ccc1[NH+2]OC)=O)=O KBWYRYDDVDCIDE-GKIKDSKJSA-N 0.000 description 1
- OAXAIMCIYDLXNM-BXSCJQAJSA-N CC(C)OC([C@H](C)N[P@](OC[C@H]([C@H]1O)O[C@@H](C)[C@]1(C)F)(Oc1ccccc1)=[O]C)=O Chemical compound CC(C)OC([C@H](C)N[P@](OC[C@H]([C@H]1O)O[C@@H](C)[C@]1(C)F)(Oc1ccccc1)=[O]C)=O OAXAIMCIYDLXNM-BXSCJQAJSA-N 0.000 description 1
- DPFQJXWZTNUWFB-USXNREEHSA-N CCCCCCCOC([C@H](C)N[P@](Oc(cc1)ccc1[NH+]([O-])OC)(Oc(cc1)ccc1Cl)=O)=O Chemical compound CCCCCCCOC([C@H](C)N[P@](Oc(cc1)ccc1[NH+]([O-])OC)(Oc(cc1)ccc1Cl)=O)=O DPFQJXWZTNUWFB-USXNREEHSA-N 0.000 description 1
- LDYMODJZBIZPGK-RVGOPSQASA-N C[C@@H](C(OC)=O)N[P@@](OC[C@H]([C@H]([C@@]1(C)F)O)O[C@H]1N1C=NC2C(NC3CCCC3)=NC(N)=NC12)(Oc1ccccc1)=O Chemical compound C[C@@H](C(OC)=O)N[P@@](OC[C@H]([C@H]([C@@]1(C)F)O)O[C@H]1N1C=NC2C(NC3CCCC3)=NC(N)=NC12)(Oc1ccccc1)=O LDYMODJZBIZPGK-RVGOPSQASA-N 0.000 description 1
- JLFQIRIZAGIOHM-DFYVNMARSA-N C[C@@H](C(OC1CCCC1)=O)N[P@](Oc1ccccc1)(Oc(cc1)ccc1NOC)=O Chemical compound C[C@@H](C(OC1CCCC1)=O)N[P@](Oc1ccccc1)(Oc(cc1)ccc1NOC)=O JLFQIRIZAGIOHM-DFYVNMARSA-N 0.000 description 1
- ISAKRJDGNUQOIC-UHFFFAOYSA-N O=C(C=CN1)NC1=O Chemical compound O=C(C=CN1)NC1=O ISAKRJDGNUQOIC-UHFFFAOYSA-N 0.000 description 1
- TXFOLHZMICYNRM-UHFFFAOYSA-N O=P(Oc1ccccc1)(Cl)Cl Chemical compound O=P(Oc1ccccc1)(Cl)Cl TXFOLHZMICYNRM-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H1/00—Processes for the preparation of sugar derivatives
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H19/00—Compounds containing a hetero ring sharing one ring hetero atom with a saccharide radical; Nucleosides; Mononucleotides; Anhydro-derivatives thereof
- C07H19/02—Compounds containing a hetero ring sharing one ring hetero atom with a saccharide radical; Nucleosides; Mononucleotides; Anhydro-derivatives thereof sharing nitrogen
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7042—Compounds having saccharide radicals and heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7042—Compounds having saccharide radicals and heterocyclic rings
- A61K31/7052—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D309/00—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only ring hetero atom, not condensed with other rings
- C07D309/02—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only ring hetero atom, not condensed with other rings having no double bonds between ring members or between ring members and non-ring members
- C07D309/08—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only ring hetero atom, not condensed with other rings having no double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D309/10—Oxygen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic System
- C07F9/02—Phosphorus compounds
- C07F9/06—Phosphorus compounds without P—C bonds
- C07F9/22—Amides of acids of phosphorus
- C07F9/24—Esteramides
- C07F9/2454—Esteramides the amide moiety containing a substituent or a structure which is considered as characteristic
- C07F9/2458—Esteramides the amide moiety containing a substituent or a structure which is considered as characteristic of aliphatic amines
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic System
- C07F9/02—Phosphorus compounds
- C07F9/547—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom
- C07F9/6558—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom containing at least two different or differently substituted hetero rings neither condensed among themselves nor condensed with a common carbocyclic ring or ring system
- C07F9/65586—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom containing at least two different or differently substituted hetero rings neither condensed among themselves nor condensed with a common carbocyclic ring or ring system at least one of the hetero rings does not contain nitrogen as ring hetero atom
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic System
- C07F9/02—Phosphorus compounds
- C07F9/547—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom
- C07F9/6561—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom containing systems of two or more relevant hetero rings condensed among themselves or condensed with a common carbocyclic ring or ring system, with or without other non-condensed hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic System
- C07F9/02—Phosphorus compounds
- C07F9/547—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom
- C07F9/6561—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom containing systems of two or more relevant hetero rings condensed among themselves or condensed with a common carbocyclic ring or ring system, with or without other non-condensed hetero rings
- C07F9/65616—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom containing systems of two or more relevant hetero rings condensed among themselves or condensed with a common carbocyclic ring or ring system, with or without other non-condensed hetero rings containing the ring system having three or more than three double bonds between ring members or between ring members and non-ring members, e.g. purine or analogs
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H1/00—Processes for the preparation of sugar derivatives
- C07H1/06—Separation; Purification
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H19/00—Compounds containing a hetero ring sharing one ring hetero atom with a saccharide radical; Nucleosides; Mononucleotides; Anhydro-derivatives thereof
- C07H19/02—Compounds containing a hetero ring sharing one ring hetero atom with a saccharide radical; Nucleosides; Mononucleotides; Anhydro-derivatives thereof sharing nitrogen
- C07H19/04—Heterocyclic radicals containing only nitrogen atoms as ring hetero atom
- C07H19/06—Pyrimidine radicals
- C07H19/10—Pyrimidine radicals with the saccharide radical esterified by phosphoric or polyphosphoric acids
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H19/00—Compounds containing a hetero ring sharing one ring hetero atom with a saccharide radical; Nucleosides; Mononucleotides; Anhydro-derivatives thereof
- C07H19/02—Compounds containing a hetero ring sharing one ring hetero atom with a saccharide radical; Nucleosides; Mononucleotides; Anhydro-derivatives thereof sharing nitrogen
- C07H19/04—Heterocyclic radicals containing only nitrogen atoms as ring hetero atom
- C07H19/16—Purine radicals
- C07H19/20—Purine radicals with the saccharide radical esterified by phosphoric or polyphosphoric acids
Abstract
Description
본 발명은 일반적으로 항바이러스 활성을 가지는 화합물 제조 방법에 관한 것이고,특히 C형 간염 바이러스 RNA-의존성 RNA 폴리머레이즈(polymerase)의 억제제의 전구약물에 관한 것이다.
C 형 간염 바이러스(HCV)는 세계적으로 만성 간 질환의 주요 원인이고 (Boyer, N. et al. J Hepatol. 32:98-112, 2000), 간 섬유증, 경화증 및 간세포 암종을 초래할 수 있다(Cale, P., Gastroenterolgy Clin. Biol. 2009, 33, 958). 현재의 항바이러스 연구의 중요한 주안점은 개선된 인간의 만성 HCV 감염 치료 방법의 개발을 지향한다 (Di Besceglie, A.M. and Bacon, B. R., Scientific American, Oct.: 80-85, (1999); Gordon, C. P., et al., J. Med. Chem. 2005, 48, 1-20; Maradpour, D.; et al., Nat. Rev. Micro. 2007, 5(6), 453-463). 여러 HCV 치료법이 Antiviral Chemistry & Chemotherapy, 11:2; 79-95 (2000)에서 Bymock et a l.에 의하여 리뷰된다.
현재, 주요한 두 가지 항바이러스 화합물로 뉴클레오사이드 유사체인 리바비린(ribavirin) 및 인터페론-알파(α) (IFN)가 존재하며, 이들은 인간의 만성 HCV 감염 치료에 사용된다. 리바비린은 단독으로 바이러스성 RNA 수준 감소에 효과적이지 않고,상당한 독성을 가지며, 빈혈을 유발하는 것으로 알려져 있다. IFN과 리바비린의 병용이 만성 C형 간염의 관리에 효과적인 것으로 보고되었지만(Scott, L. J., et al. Drugs 2002, 62, 507-556), 이 치료를 받은 환자의 절반 미만 만이 지속적인 이점을 나타낸다. C 형 간염 바이러스를 치료하기 위한 뉴클레오사이드 유사체 사용을 개시하는 다른 특허 출원에는 WO 01/32153, WO 01/60315, WO 02/057425, WO 02/057287, WO 02/032920, WO 02/18404, WO 04/046331, WO2008/089105 및 WO2008/141079가 포함되지만 아직 환자가 HCV 감염을 위한 추가적인 치료를 이용할 수 있게 되지는 않았다. 그러므로,HCV 내성의 발현에 대하여 향상된 활성, 개선된 경구 생체이용률, 더 큰 효능, 더 적은 바람직하지 않은 부작용 및 연장된 생체 내 유효 반감기와 함께 개선된 항바이러스 및 약동학 특성을 가지는 약물이 (De Francesco, R. et al. (2003) Antiviral Research 58:1-16) 시급하게 필요하다.
RNA 의존성 RNA 폴리머레이즈 (RdRp)는 신규한 HCV 치료제의 개발을 위하여 가장 많이 연구된 표적 중 하나이다. NS5B 폴리머레이즈는 초기 인간 임상 시험에서 억제제에 대한 표적이다. (Sommadossi, J., WO 01/90121 A2, US 2004/0006002 A1). 이 효소는 선택적 억제제 식별을 위한 선별 검사 (screening assay)로써 생화학적, 구조적 수준에서 광범하게 특징분석되어 있다 (De Clercq, E. (2001) J. Pharmacol. Exp.Ther. 297:1-10; De Clercq, E. (2001) J. Clin. Virol. 22 :73-89). HCV가 실험실에서 복제되지 않고 세포 기반 검사 및 전임상 동물 시스템 개발에 어려움이 있기 때문에,NS5B와 같은 생화학적 표적이 HCV 치료법 개발에서 중요하다.
RdRp를 억제하는 뉴클레오사이드를 포함하여 뉴클레오사이드에 의한 바이러스 복제의 억제가 광범하게 연구되어 왔다 (De Clercq, E. (2001) J. Clin. Virol. 22:73-89). 일반적으로,이러한 뉴클레오사이드의 항바이러스 활성은 뉴클레오사이드에서 뉴클레오사이드 트리포스페이트(NTP)로의 전환에 기인하는데,뉴클레오사이드 트리포스페이트는 DNA 및 RNA 폴리머레이즈의 억제제로서 또는 연장되는 바이러스 DNA 또는 RNA 가닥으로 편입한 후에 사슬 종결제로서 작용한다. 그러나,많은 NTP가 숙주 폴리머레이즈와 비교하여 바이러스 폴리머레이즈에 대한 적절한 특이성이 없고,그 결과,상당한 독성을 초래한다. 이는 더 높은 선택도를 달성하기 위하여 뉴클레오사이드의 중심 구조를 변형시키려는 노력을 유도했지만,구조 변형 중 다수가 동시에 세포 내에서 저하된(compromised) NTP 생산을 일으킨다 (Yamanaka, Antimicrob. Agents Chemother. 1999: 190-193).
뉴클레오사이드에서 NTP로의 불량한 전환은 흔히 뉴클레오사이드를 뉴클레오사이드 5’-모노포스페이트(NMP)로 전환시키는 것에 대한 뉴클레오사이드 카이네이즈의 무능력에 기인할 수 있다. 불량한 뉴클레오사이드 카이네이즈 활성을 우회하기 위하여 NMP 전구약물이 사용되어 왔다(Schultz, Bioorg. Med. Chem. 2003, 11, 885). 이러한 전구약물 중에서, NMP 포스포라미데이트는 뉴클레오사이드 단독에 비하여 NTP의 세포 내 농도를 증가시키는 것으로 보고되었다 (McGuigan, J. Med. Chem. 1993, 36, 1048-1052). 그러나 이러한 NMP 전구약물은,혈액 및 다른 신체 조직에서 전구약물을 각각 하전된 분자 또는 뉴클레오사이드로 분열할 수 있는 에스터레이즈(esterase) 및 포스포디에스터레이즈(phosphodiesterase)에 대한 기질이다. 하전된 분자는 이후 표적 기관 또는 세포에 비투과성이고 뉴클레오사이드는 세포 내에서 불량하게 인산화된다.
고도로 효과적이고 비독성인 NMP 전구약물의 개발은,표적 기관 또는 세포에 도달하고 표적 세포에 의하여 흡수되거나 활발하게 받아들여져 효과적으로 세포 내에서 NMP로 분열되고 추후 바이러스성 폴리머레이즈 억제에 선택적인 NIP로 전환되는 전구약물의 능력과 혈액 중 NMP 전구약물의 안정성의 균형을 필요로 하는 대체로 예측 불가능한 시행착오 활동이다. (Perrone, J. Med. Chem. 2007, 50, 1840-49; Gardelli, J. Med. Chem. 2009, 52, 5394-5407). HCV 감염 치료를 위하여 구강으로 효과적인 RdRp 억제제의 경우에 있어서, NMP 전구약물은 상부위장관의 조건에서 화학적으로 안정하고,장관으로부터 효율적으로 흡수되고,장 세포 및 혈액의 많은 에스터레이즈를 견디고,간세포에 의하여 효율적으로 추출되고,NMP로 분열된 다음 간세포에서 HCV NS5B 폴리머레이즈 억제에 특이적인 NIP로 전환될 필요가 있다. 특히,포스페이트 전구약물의 항-HCV 활성은 전구약물 중 인의 카이랄성 (chirality)에 두드러지게 의존할 수 있다 (Gardelli, J. Med. Chem. 2009, 52, 5394-5407; Meppen, Abstracts of Papers, 236th ACS National Meeting, Philadelphia, PA, United States, August 17-21,2008 (2008), MEDI-404.).
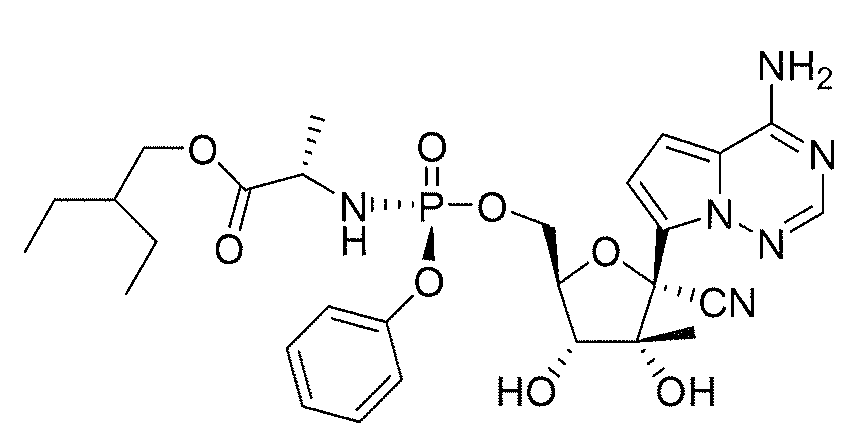
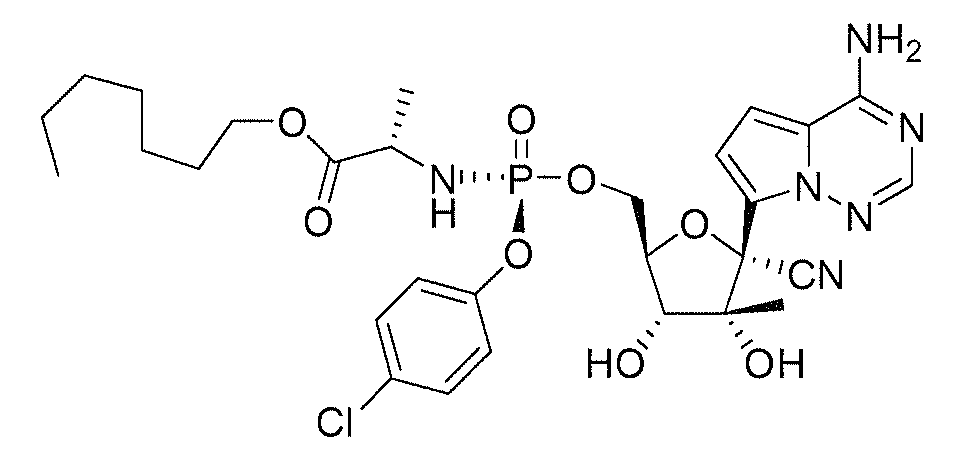
Babu, Y. S., W02008/089105 및 W02008/141079는 항바이러스, 항 HCV, 및 항-RdRp 활성을 가지는 피롤로[1,2-f][1,2,4]트리아진 뉴클레오베이스의 리보사이드를 개시한다.
Butler, et al., W02009132135는 항-HCV 및 항-RdRp 활성을 가지는 피롤로[1,2-f][1,2,4]트리아진 뉴클레오베이스를 포함하는 전구약물 및 1' 치환된 리보사이드를 개시하지만,이러한 리보사이드의 3'-0-아실화 유도체의 화학종 또는 이러한 유도체의 예상된 특성을 개시하지는 않는다. Cho, et al., US 61353351은 항-HCV 활성을 가지고 경구 투여 후 간에 효율적으로 전달되는 피롤로[1,2-f][1,2,4]트리아진 뉴클레오베이스를 포함하는 3'-0-아실화 1' 치환된 리보사이드 포스페이트 전구약물을 개시한다. 간으로의 효율적인 전구약물 전달은 인 전구약물의 카이랄성에 의존한다.
Cho, et al., Gardelli, et al., Perrone et al., 및 Meppen, et al.에 의하여 기재된 것과 같이 카이랄(chiral)인 원자를 가지는 NMP 전구약물인 항-HCV 치료제의 중요성 관점에서, 이러한 전구약물의 카이랄 포스페이트를 생산하는 신규한 효율적 방법이 필요하다.
C형 간염 바이러스를 억제하는 화합물 제조 방법이 제조된다. 상기 화합물은 뉴클레오사이드 모노포스페이트인 전구약물이고, 이는, 동물에 투여 시, 세포 내에서 뉴클레오사이드 트리포스페이트로 전환된다. 인 원자의 카이랄성은 동물에서 뉴클레오사이드 트리포스페이트로의 전환의 효율을 결정한다. 상기 개시된 방법은,종래에 개시된 부분입체 이성질체의 혼합물로부터 단일 부분입체 이성질체를 분리하는 크로마토그래피 방법보다 개선된 상기 단일 부분입체 이성질성 전구약물의 전환적 합성을 제공한다.
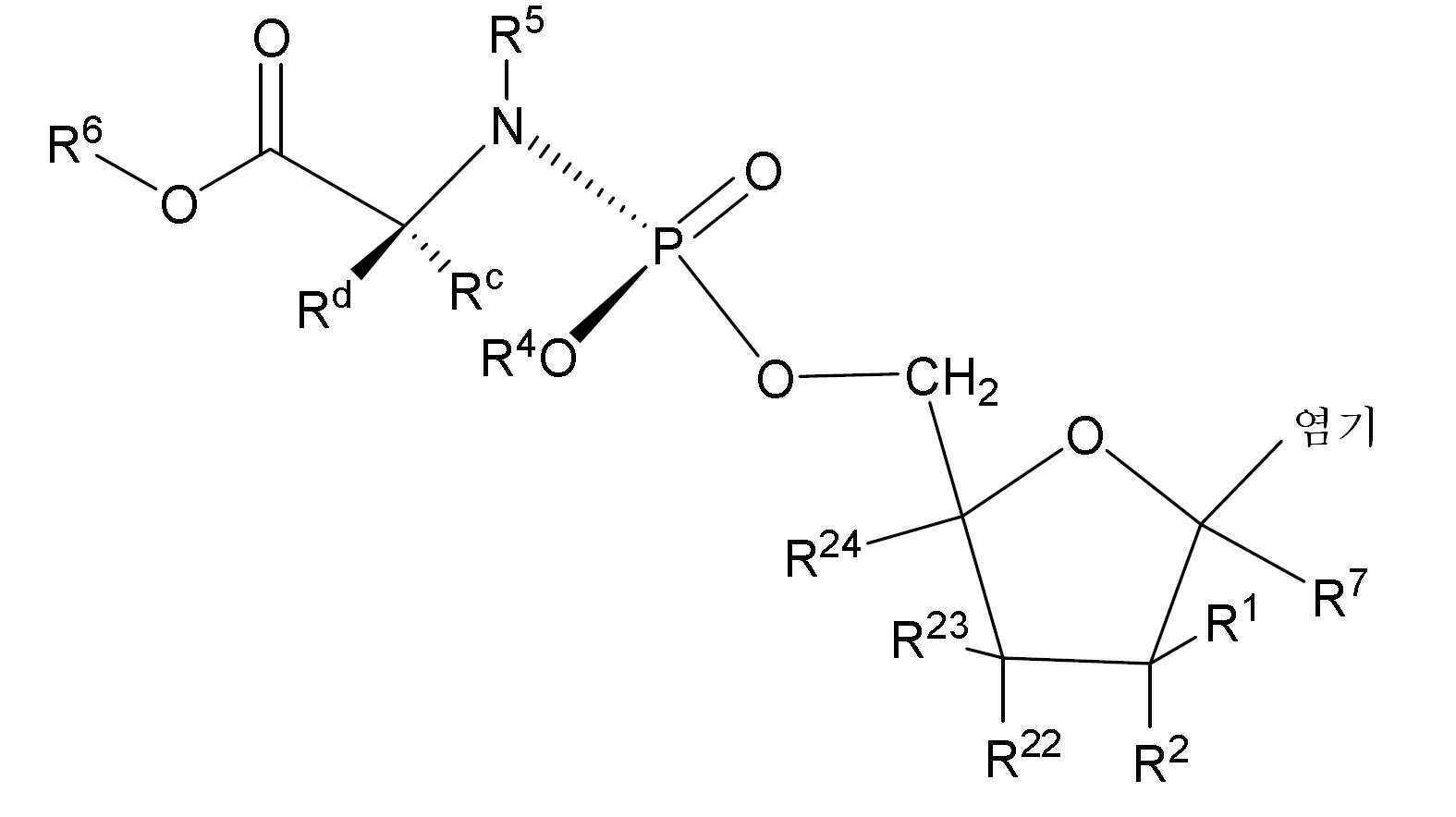
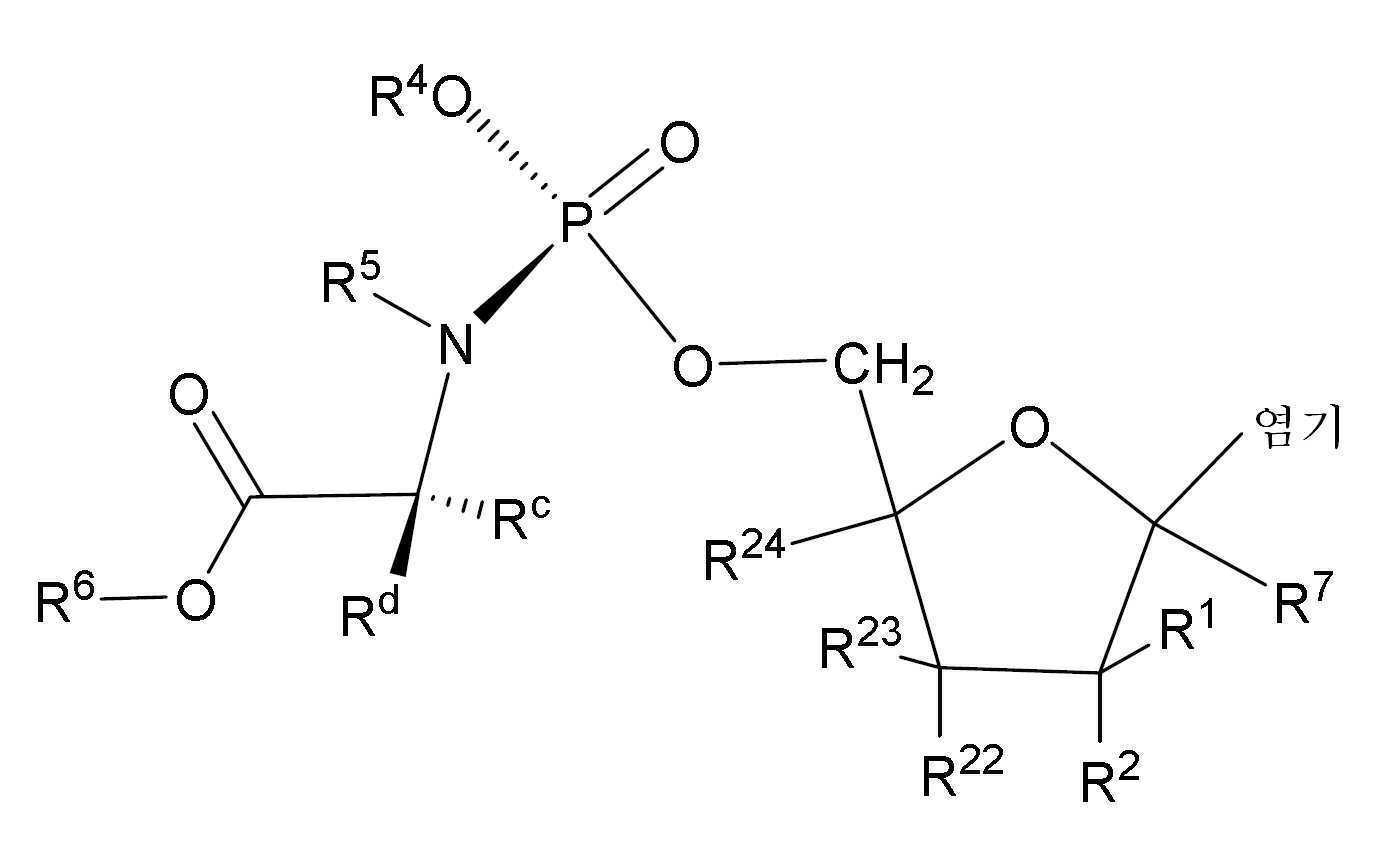
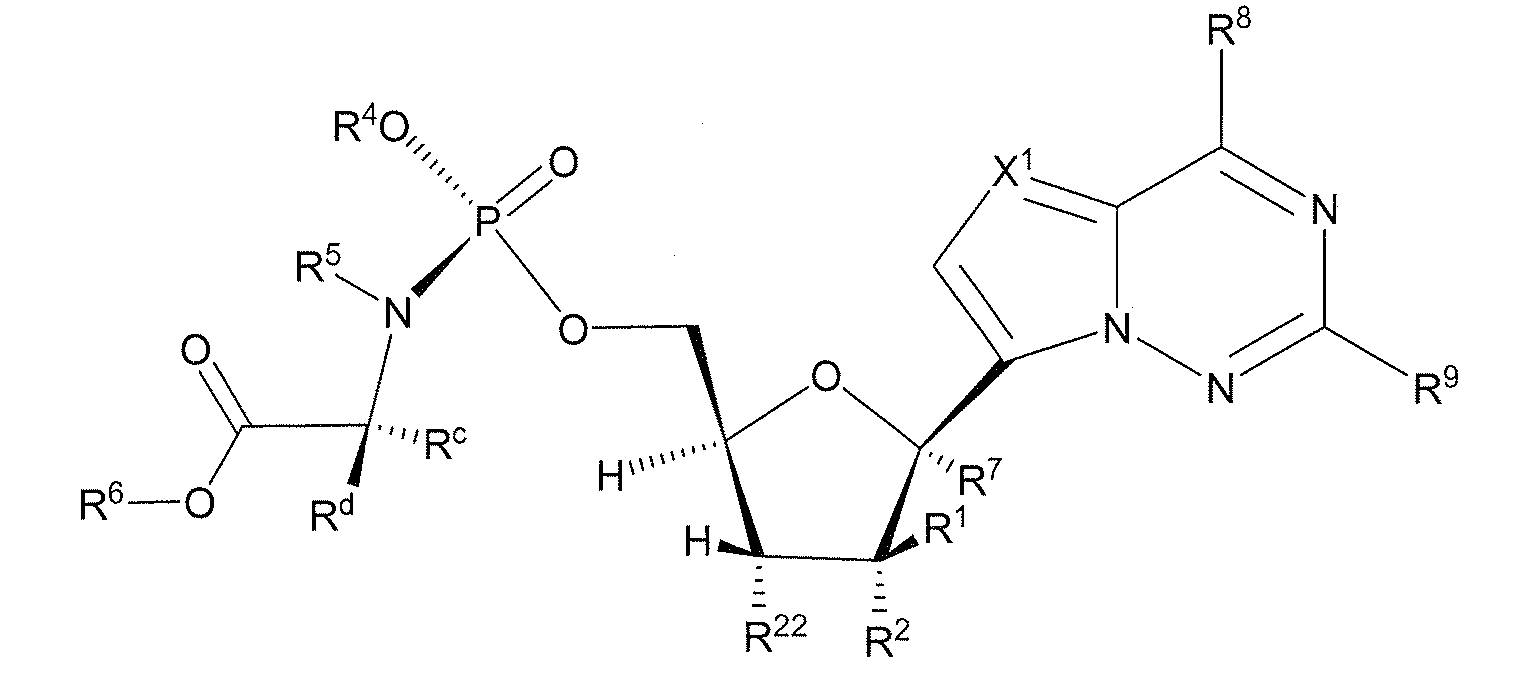
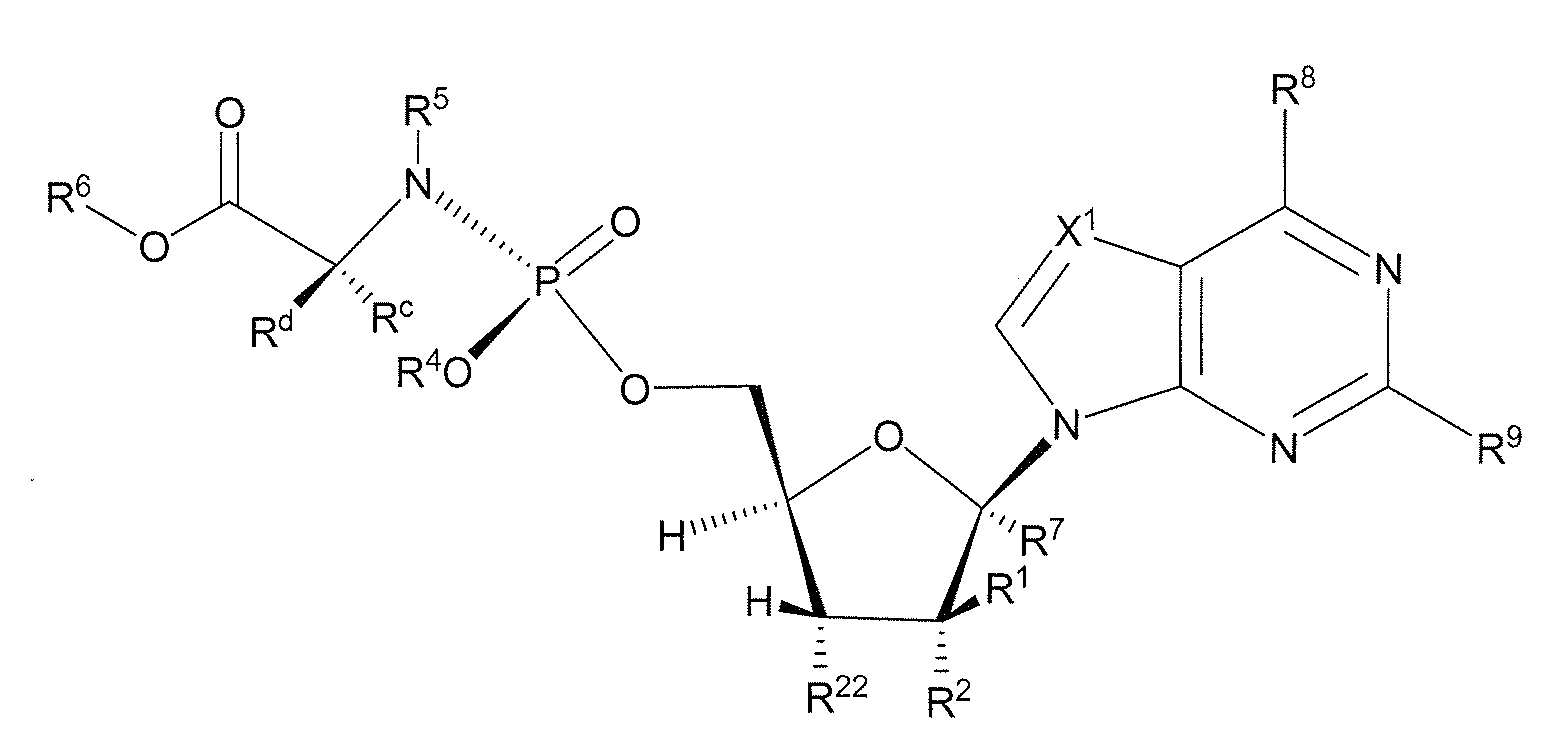
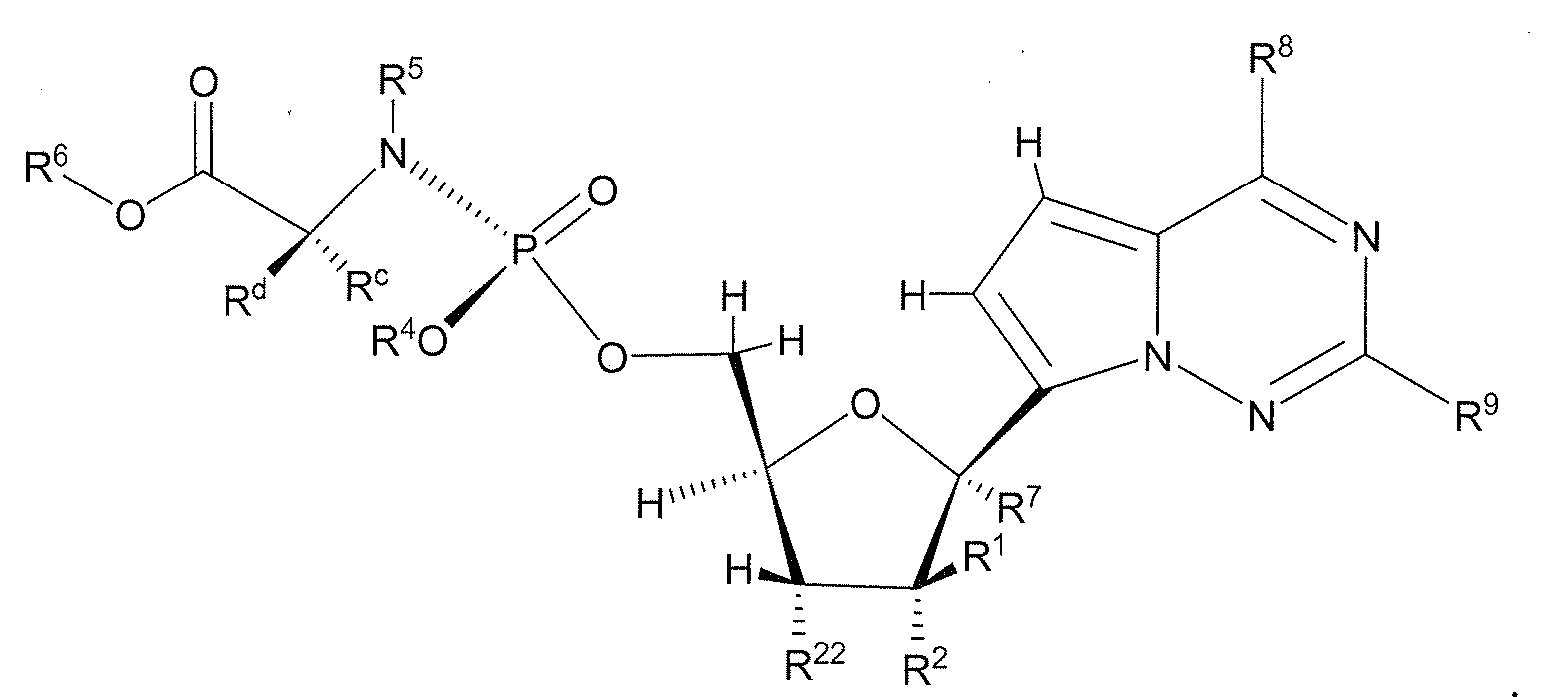
한 구체예에서, 화학식 (Ia) 또는 (Ib)의 화합물:
화학식 (Ia)
화학식 (Ib)
또는 이의 약제학적으로 허용가능한 염 또는 산을 제조하는 방법이 제공되고;
여기서:
각각의 Rl, R2, R7, R22, R23 또는 R24는 독립적으로 H, OR11, NR11R12, C(O)NR11R12, -OC(O)NR11R12, C(O)OR11, OC(O)OR11, S(O)nRa, S(O)2NR11R12, N3, CN, 할로겐, (C1-C8)알킬, (C3-C8)카르보사이클릴, (C4-C8)카르보사이클릴알킬, (C2-C8)알케닐, (C2-C8)알키닐 또는 아릴(C1-C8)알킬이고;
또는 이웃한 탄소 원자 상의 임의의 두 Rl, R2, R7, R22, R23 또는 R24는 합쳐서 -O(CO)O-또는 -O(CR11R12)0-이고,또는 이들이 부착된 고리 탄소 원자와 합쳐서 이중 결합을 형성하고;
각각의 염기는 독립적으로 탄소 또는 질소 원자를 통하여 퓨라노오스 고리에 연결된 천연으로 발생하거나 변형된 퓨린 또는 피리미딘 염기이고;
각각의 n은 독립적으로 0, 1, 또는 2이고;
각각의 Ra, R4 또는 R6는 독립적으로 (C1-C8)알킬,(C2-C8)알케닐,(C2-C8)알키닐, (C3-C8)카르보사이클릴, (C4-C8)카르보사이클릴알킬, 아릴(C1-C8)알킬, 헤테로사이클릴(C1-C8)알킬,(C6-C20)아릴, (C2-C20)헤테로사이클릴 또는 헤테로아릴이고;
각각의 Rc 또는 Rd는 독립적으로 H, (C1-C8)알킬,(C2-C8)알케닐,(C2-C8)알키닐, (C3-C8)카르보사이클릴, (C4-C8)카르보사이클릴알킬, 아릴(C1-C8)알킬, 헤테로사이클릴(C1-C8)알킬, (C6-C20)아릴, (C2-C20)헤테로사이클릴 또는 헤테로아릴이고,단 Rc 및 Rd는 동일하지 않고;
각각의 R5는 독립적으로 H, (C1-C8)알킬, (C2-C8)알케닐, (C2-C8)알키닐, (C3-C8)카르보사이클릴, (C4-C8)카르보사이클릴알킬, 아릴(C1-C8)알킬,헤테로사이클릴(C1-C8)알킬, (C6-C20)아릴, (C2-C20)헤테로사이클릴 또는 헤테로아릴이고;
각각의 R11 또는 R12는 독립적으로 H, (C1-C8)알킬, (C2-C8)알케닐, (C2-C8)알키닐, (C3-C8)카르보사이클릴, (C4-C8)카르보사이클릴알킬, 아릴(C1-C8)알킬, 헤테로사이클릴(C1-C8)알킬, (C6-C20)아릴, (C2-C20)헤테로사이클릴, 헤테로아릴, -C(=O)(C1-C8)알킬, -S(O)n(C1-C8)알킬이고, 또는 R11 및 R12는 이들이 모두 부착된 질소와 합쳐서 3 내지 7원 헤테로사이클릭 고리를 형성하고, 여기서 상기 헤테로사이클릭 고리의 임의의 한 탄소 원자는 -0-, -S(O)n- 또는 -NRa-로 선택적으로 대체될 수 있고; 및
여기서 각각의 Rc, Rd, R1, R2, R22, R23, R24, R4, R5, R6, R7, R11 또는 R12의 각각의 (C1-C8)알킬, (C2-C8)알케닐, (C2-C8)알키닐, (C3-C8)카르보사이클릴, (C4-C8)카르보사이클릴알킬,아릴(C1-C8)알킬,헤테로사이클릴(C1-C8)알킬, (C6-C20)아릴, (C2-C20)헤테로사이클릴 또는 헤테로아릴은,독립적으로,하나 이상의 할로, 하이드록시, CN, N3, N(Ra)2, NH(Ra), NH2, N02, C(O)N(Ra)2, C(O)NH(Ra), C(O)NH2, OC(O)N(Ra)2, OC(O)NH(Ra), OC(O)NH2, C(O)ORa, OC(O)ORa, C(O)Ra, OC(O)Ra, S(O)nRa, S(0)2N(Ra)2, S(O)2NH(Ra), S(O)2NH2, ORa 또는 Ra로 선택적으로 치환되고:
상기 방법은:
(a) 화학식 (II)의 화합물을 제공하는 단계
화학식 (II)
및
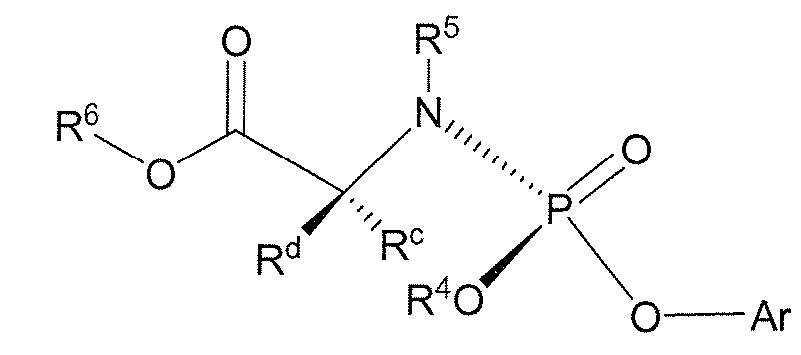
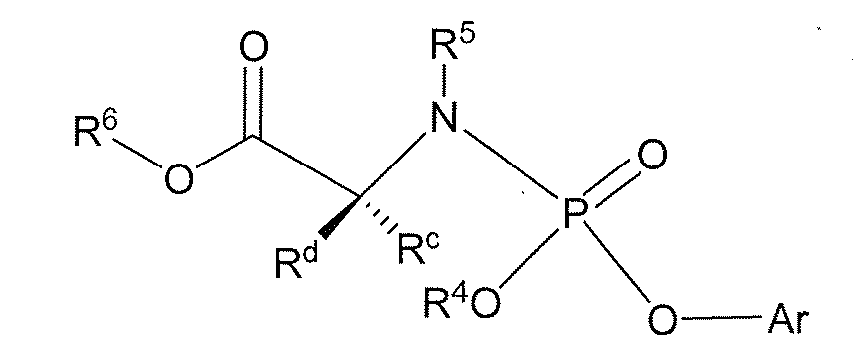
(b) 화학식 (II)의 화합물을 화학식 (IIIa)의 화합물 및 염기로 처리하여
화학식 (IIIa)
화학식 (Ia)의 화합물을 형성하는 단계 또는
(c) 화학식 (II)의 화합물을 화학식 (IIIb)의 화합물 및 염기로 처리하여
화학식 (IIIb)
화학식 (Ib)의 화합물을 형성하는 단계를 포함하고;
여기서:
각각의 Ar은 (C6-C20)아릴 또는 헤테로아릴이고, 여기서 상기 (C6-C20)아릴 또는 헤테로아릴은 하나 이상의 할로겐, NO2, 또는 (C1-C8)할로알킬로 치환되고,하나 이상의 CN, N3, N(Ra)2, C(O)N(Ra)2, OC(O)N(Ra)2, C(O)ORa, OC(O)ORa, C(O)Ra, OC(O)Ra, S(O)nRa, S(O)2N(Ra)2, ORa 또는 Ra로 선택적으로 치환되고,단 Ar은 R4와 상이하다. 또 다른 양태에서,염기는 우라실이 아니다. 또 다른 양태에서,염기는 사이토신이 아니다.
또 다른 양태에서, 본 발명은 화학식 (Ia) 또는 화학식 (Ib) 제조에 유용한 본 명세서에서 개시된 신규한 중간체를 또한 제공한다.
다른 양태에서,본 발명의 신규한 중간체의 합성, 분석, 분리(separation), 단리(isolation),정제,및 특징분석(characterization) 방법이 제공된다.
대표적인 구체예의 상세한 설명
이제 본 발명의 특정 구체예에 대하여 상세히 언급할 것이고,이들의 예가 첨부한 기재,구조식 및 화학식에서 설명된다. 본 발명이 열거된 구체예에 관하여 기재될 것이기는 하지만,본 발명을 이러한 구체예로 제한하려는 의도가 아님이 이해되어야 한다. 반대로,본 발명은 본 발명의 범위에 포함될 수 있는 모든 대안, 변형 및 동등물을 포괄하도록 의도된다.
전형적으로, 화학식 (II) 및 화학식 (IIIa)의 화합물로부터 화학식 (Ia)의 화합물 또는 화학식 (II) 및 화학식 (IIIb)의 화합물로부터 화학식 (Ib)의 화합물을 제조하는 방법은 적절한 용매에서 수행된다. 적절한 용매는 바람직하게는 무수의,비산 (non-acid), 비수산기 용매이다. 적절한 용매의 비제한적 예는 에테르,예를 들어,디에틸 에테르,디이소프로필 에테르,디 t-부틸 에테르,테트라하이드로퓨란,디옥산 및 다양한 글라임(glyme) 용매; 디메틸포름아미드 또는 디메틸아세트아미드이다. 바람직한 용매는 테트라하이드로퓨란이다. 용매 중 화학식 (II)의 농도는 전형적으로 용매 1 리터당 약 0.01 내지 약 l 몰이다. 상기 방법은 약 O℃ 내지 약 80℃, 더욱 바람직하게는 약 20℃ 내지 약 60℃의 온도에서 수행된다.
화학식 (II)의 용액은 전형적으로 가려진(hindered) 염기 또는 비친핵성 염기로 처리된다. 가려진 염기의 전형적이지만 비제한적인 예는 t-부틸리튬, sec- 이소부틸리튬,리튬 또는 소듐 디이소프로필아미드 및 t-부틸마그네슘 할라이드이다. 바람직한 가려진 염기는 t-부틸마그네슘 클로라이드이다. 비친핵성 염기의 전형적이지만 비제한적인 예는 소듐 하이드라이드, 포타슘 하이드라이드, 리튬 하이드라이드 및 칼슘 하이드라이드이다. 가려진 염기 또는 비친핵성 염기는 용액으로서 또는 비희석 염기로서 사용될 수 있다. 바람직하게는,염기는 무수의,비수산기 용매에 녹은 용액으로서 사용되고, 여기서 용매 중 염기의 농도는 1 리터당 약 0.5 내지 약 3 몰이다. 염기 대 화학식 (II)의 화합물의 몰비는 약 1:1 내지 약 3:1, 바람직하게는 약 1.1:1 내지 약 1.5:1이다. 화학식 (II)의 화합물의 용액은 전형적으로 약 5 분 내지 약 두 시간 바람직하게는 30 분 미만 동안 염기로 처리된다.
화학식 (II)의 화합물의 용액과 염기의 혼합물은 화학식 (IIIa) 또는 화학식 (IIIb)의 화합물로 약 30 분 내지 약 24 시간 바람직하게는 약 한 시간 내지 약 네 시간 동안 처리된다. 화학식 (II)의 화합물 대 화학식 (IIIa) 또는 화학식 (IIIb)의 화합물의 몰비는 전형적으로 약 1:1 내지 약 1:4이다. 바람직하게는,몰비는 약 1:1.1 내지 약 1:2이다.
화학식 (Ia) 또는 (Ib)의 화합물 또는 이의 약제학적으로 염 또는 에스테르 제조 방법의 또 다른 구체예에서, 화학식 (Ia)는 화학식 (IVa)이고,화학식 (Ib)는 화학식 (IVb)이고,화학식 (II)는 화학식 (V)이다:
화학식 (IVa)
화학식 (IVb)
화학식 (V)
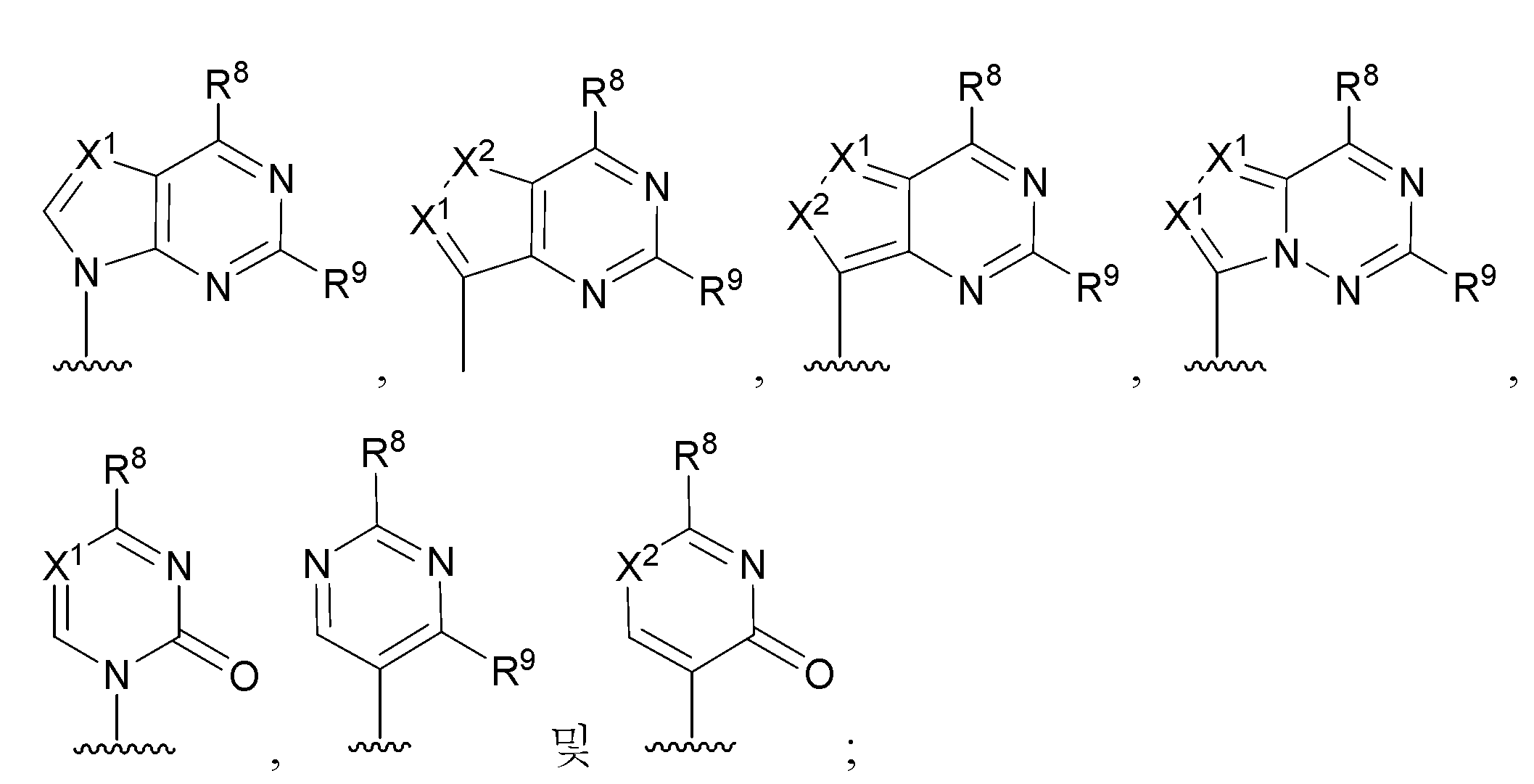
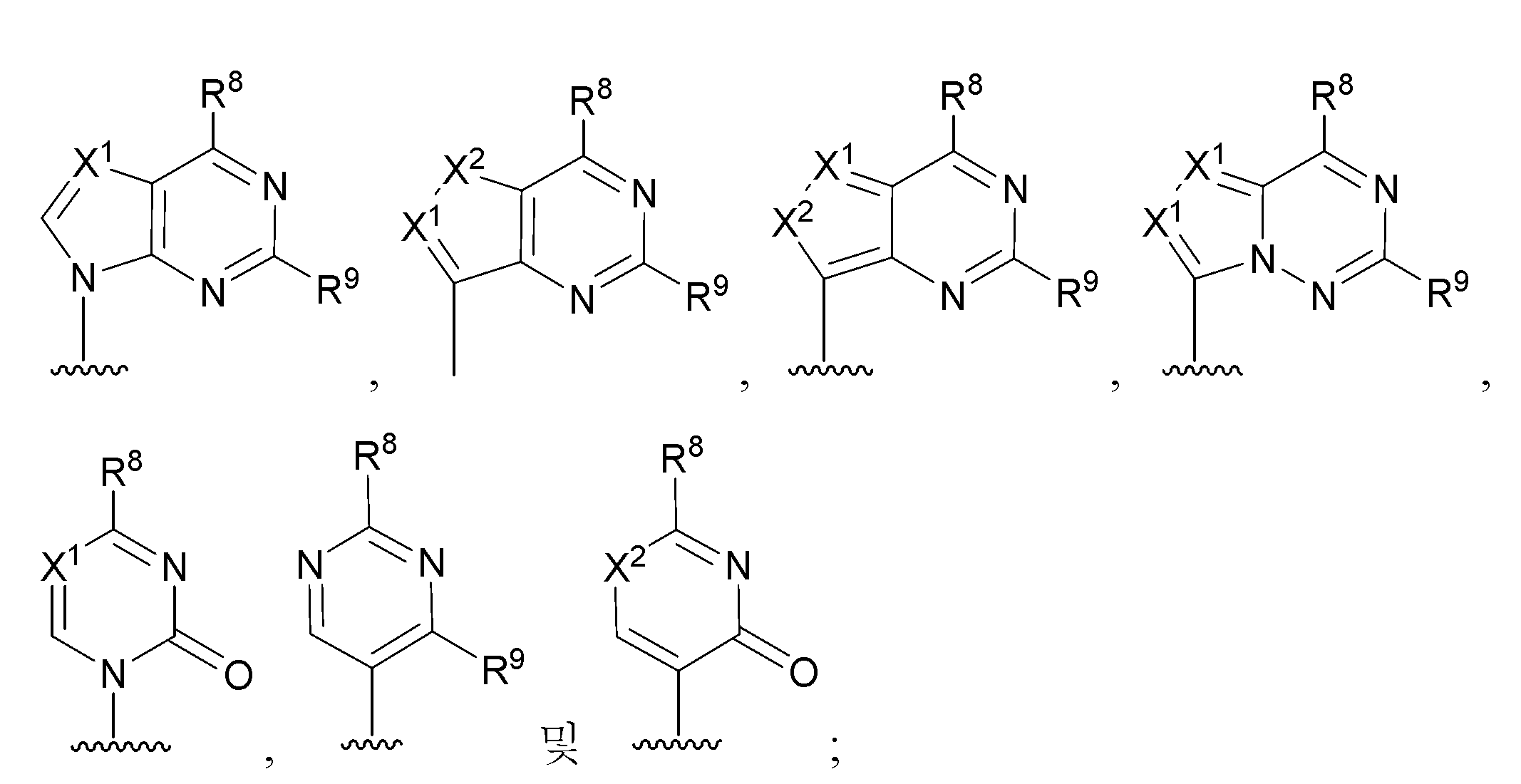
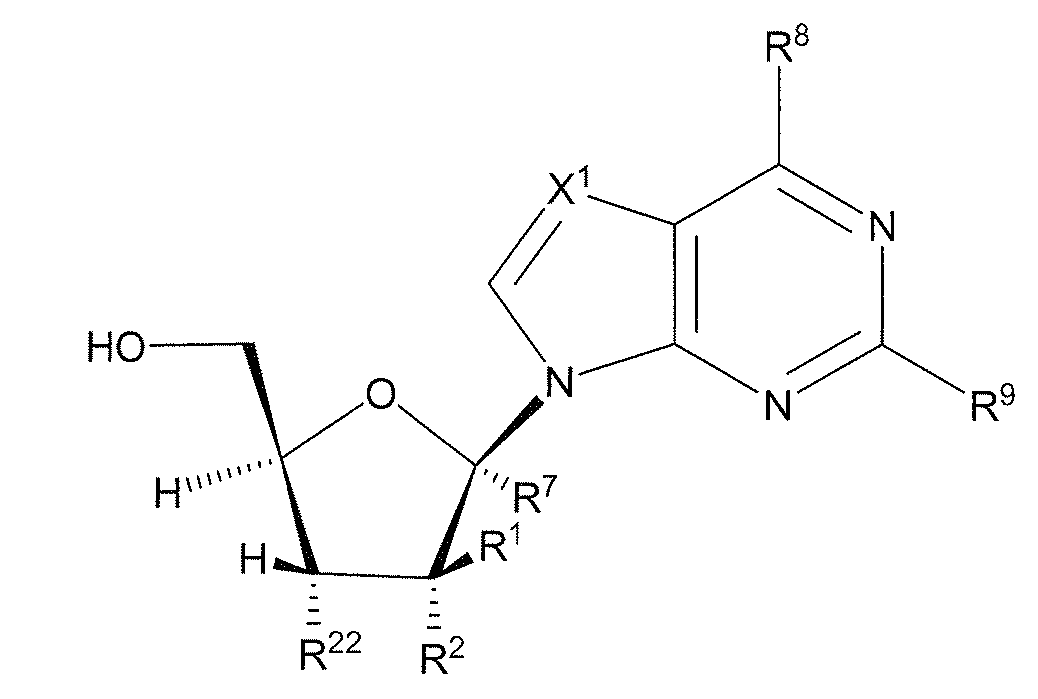
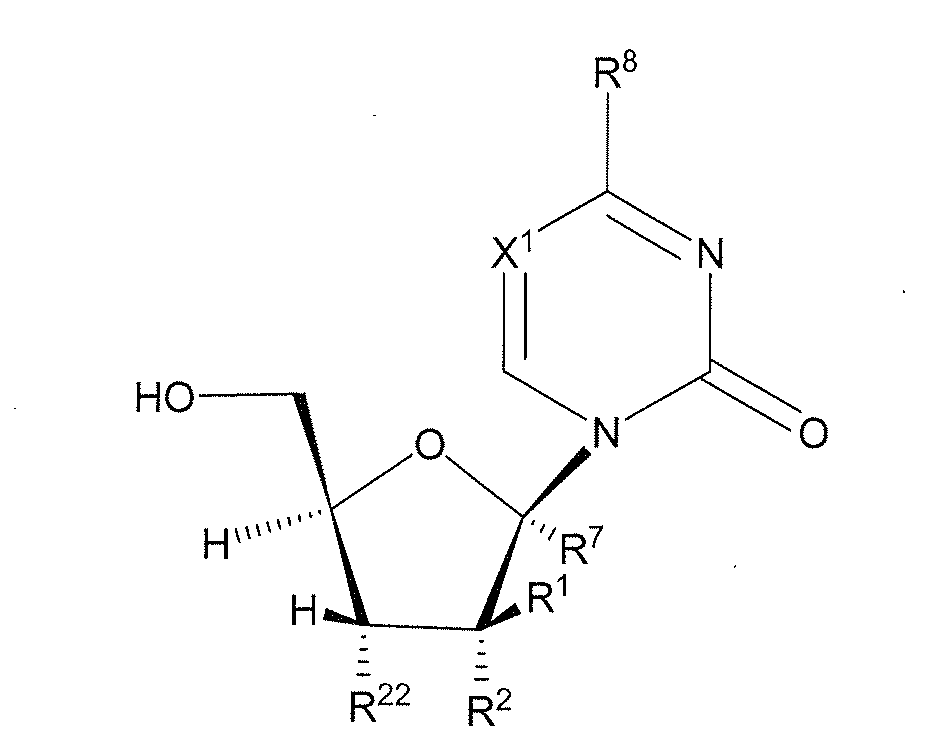
화학식 (V)의 화합물로부터 화학식 (IVa) 또는 화학식 (IVb)의 화합물을 제조하는 방법의 한 구체예에서, R1은 H, 할로겐,선택적으로 치환된 (C1-C8)알킬, 선택적으로 치환된 (C2-C8)알케닐 또는 선택적으로 치환된 (C2-C8)알키닐이다. 이 구체예의 또 다른 양태에서,R1은 H이다. 이 구체예의 또 다른 양태에서,R1은 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서,R1은 메틸이다. 이 구체예의 또 다른 양태에서,R1은 선택적으로 치환된 (C2-C8)알케닐이다. 이 구체예의 또 다른 양태에서,R1은 선택적으로 치환된 (C2-C8)알키닐이다. 이 구체예의 또 다른 양태에서, R1은 F이다. 이 구체예의 또 다른 양태에서, R2는 F이다. 이 구체예의 또 다른 양태에서,R2는 OR11이다. 이 구체예의 또 다른 양태에서,R2는 OH이다. 이 구체예의 또 다른 양태에서,R7은 H이다. 이 구체예의 또 다른 양태에서,R7은 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, R7은 선택적으로 치환된 (C2-C8)알키닐이다. 이 구체예의 또 다른 양태에서,R7은 CN이다. 이 구체예의 또 다른 양태에서,R5는 H이다. 이 구체예의 또 다른 양태에서 RC 또는 Rd 중 하나는 H이다. 이 구체예의 또 다른 양태에서, RC 또는 Rd 중 하나는 H이고 RC 또는 Rd 중 다른 하나는 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서,R6는 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서,R4는 선택적으로 치환된 (C6-C20)아릴이다. 이 구체예의 또 다른 양태에서,Ar은 선택적으로 치환된 니트로페닐이다. 이 구체예의 또 다른 양태에서, R23는 H이다. 이 구체예의 또 다른 양태에서,R22는 OR11이다. 이 구체예의 또 다른 양태에서,R22는 OH이다. 이 구체예의 또 다른 양태에서, R24는 N3이다. 이 구체예의 또 다른 양태에서,R24는 H이다. 이 구체예의 또 다른 양태에서,염기는:
로 이루어진 군에서 선택되고;
여기서:
각각의 X1은 독립적으로 N 또는 CR1O이고;
각각의 x2는 독립적으로 NR11, 0, 또는 S(O)n이고;
각각의 R8는 독립적으로 할로겐, NR11R12, N(R11)OR11, NR11NR11R12, N3, NO, N02, CHO, CN, -CH(=NR11), -CH=NNHR11, -CH=N(OR11), -CH(OR11)2, -C(=0)NR11R12, -C( =S)NR11R12, -C(=O)OR11, (C1-C8)알킬, (C2-C8)알케닐, (C2-C8)알키닐, (C4-C8)카르보사이클릴알킬,(C6-C20)아릴,(C2-C20)헤테로사이클릴,헤테로아릴,-C(=0)(C1-C8)알킬, -S(O)n(C1-C8)알킬, 아릴(C1-C8)알킬, OR11 또는 SRll이고;
각각의 n은 독립적으로 0, 1, 또는 2이고;
각각의 R9 또는 RlO은 독립적으로 H, 할로겐, NR11R12, N(R11)OR11, NR11NR11R12, N3, NO, N02, CHO, CN, -CH(=NR11), -CH=NHNR11,-CH=N(OR11), -CH(OR11)2, -C(=0)NR11R12, -C(=S)NR11R12, C(=O)OR11, R11, OR11 또는 SR11이고;
각각의 R11 또는 R12는 독립적으로 H, (C1-C8)알킬, (C2-C8)알케닐,(C2-C8)알키닐,(C3-C8)카르보사이클릴,(C4-C8)카르보사이클릴알킬,아릴(C1-C8)알킬,헤테로사이클릴(C1-C8)알킬,(C6-C20)아릴,(C2-C20)헤테로사이클릴,헤테로아릴,-C(=0)(C1-C8)알킬,-S(O)n(C1-C8)알킬이고,또는 R11 및 R12는 이들이 모두 부착된 질소와 합쳐서 3 내지 7원 헤테로사이클릭 고리를 형성하고,여기서 상기 헤테로사이클릭 고리의 임의의 한 탄소 원자는 -0-, -S(O)n- 또는 -NRa-로 선택적으로 대체될 수 있고; 및
여기서 각각의 Rc, Rd, R1, R2, R22, R23, R24, R4, R5, R6, R7, R8, R9, R10, R11 또는 R12의 각각의 (C1-C8)알킬, (C2-C8)알케닐, (C2-C8)알키닐, (C3-C8)카르보사이클릴,(C4-C8)카르보사이클릴알킬,아릴(C1-C8)알킬, 헤테로사이클릴(C1-C8)알킬, (C6-C20)아릴, (C2-C20)헤테로사이클릴 또는 헤테로아릴은,독립적으로,하나 이상의 할로,하이드록시, CN, N3, N(Ra)2, NH(Ra), NH2, N02, C(0)N(Ra)2, C(O)NH(Ra), C(0)NH2, OC(O)N(Ra)2, OC(O)NH(Ra), OC(O)NH2, C(O)ORa, OC(O)ORa, C(O)Ra, OC(O)Ra, S(O)nRa, S(O)2N(Ra)2, S(O)2NH(Ra), S(O)2NH2, ORa 또는 Ra로 선택적으로 치환된다. 또 다른 양태에서,염기는 우라실이 아니다. 또 다른 양태에서, 염기는 사이토신이 아니다.
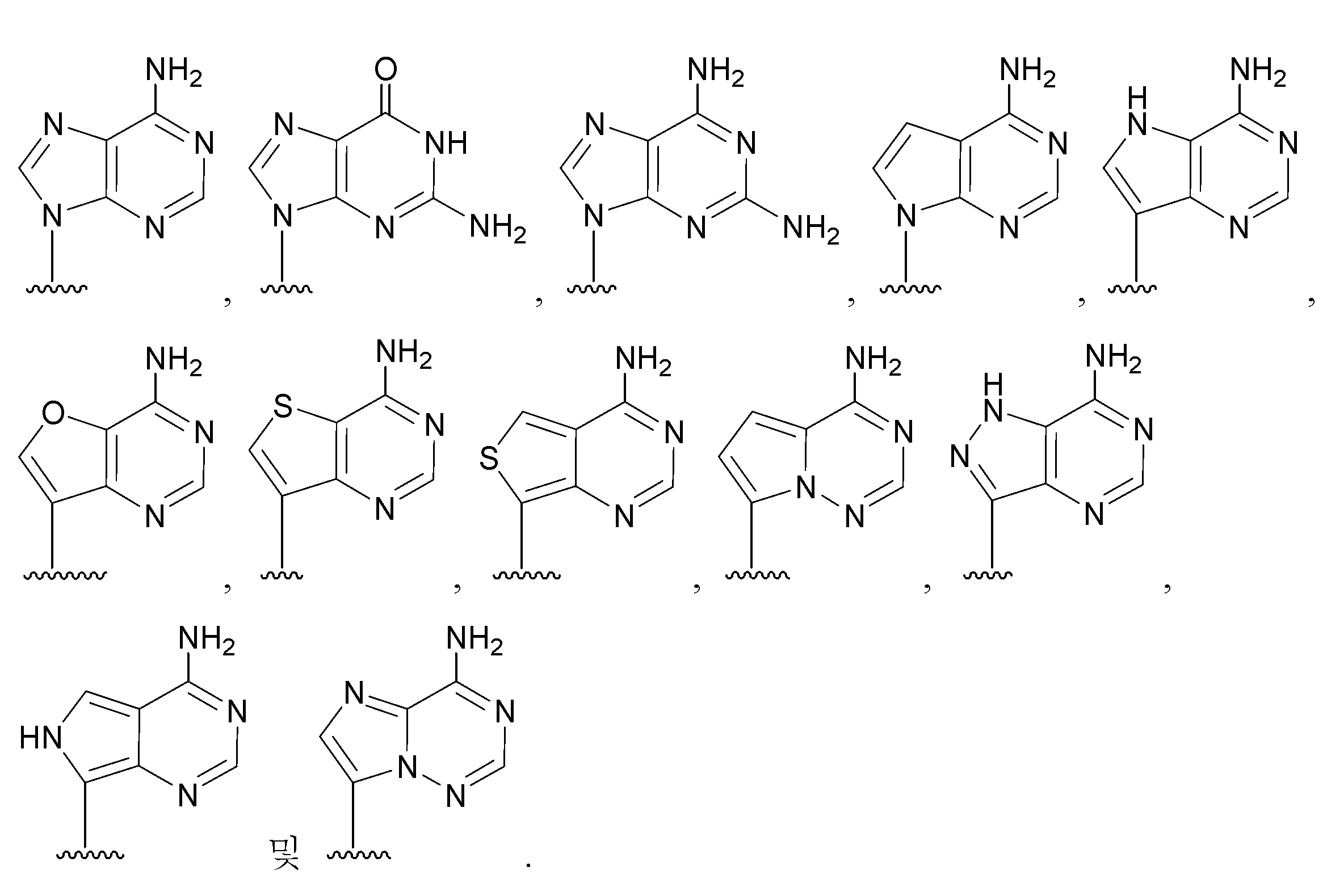
이 구체예의 또 다른 양태에서,염기는:
로 이루어진 군에서 선택된다.
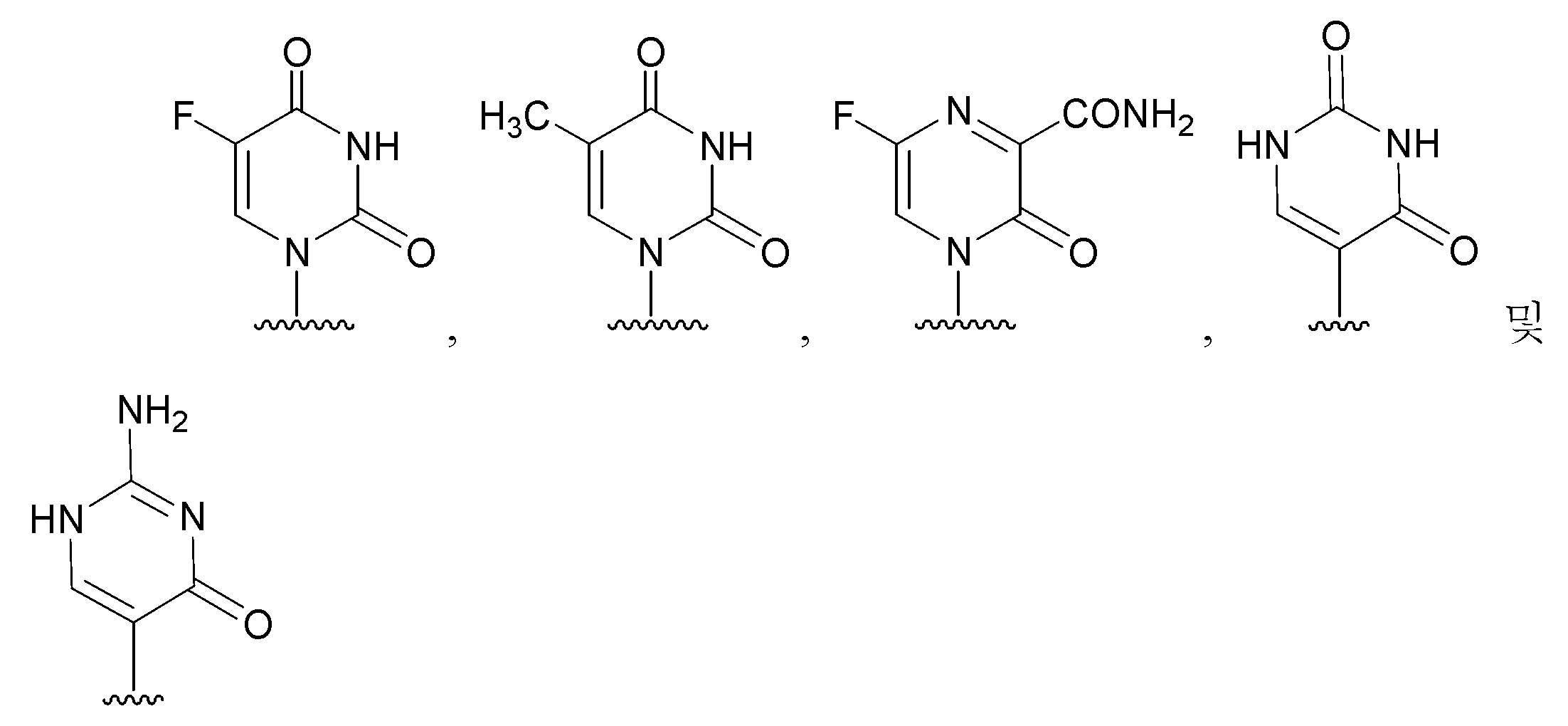
이 구체예의 또 다른 양태에서, 염기는
로 이루어진 군에서 선택된다.
이 구체예의 또 다른 양태에서,염기는
로 이루어진 군에서 선택된다.
화학식 (V)의 화합물로부터 화학식 (IVa) 또는 (IVb)의 화합물을 제조하는 방법의 또 다른 구체예에서, R1은 H, 할로겐,선택적으로 치환된 (C1-C8)알킬, 선택적으로 치환된 (C2-C8)알케닐 또는 선택적으로 치환된 (C2-C8)알키닐이고,R2는 OR11 또는 할로겐이고,R22는 OR11이고 각각의 R5, R23 및 R24는 H이다. 이 구체예의 또 다른 양태에서,R1은 H이다. 이 구체예의 또 다른 양태에서 R1은 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서,R1은 메틸이다. 이 구체예의 또 다른 양태에서,R1은 선택적으로 치환된 (C2-C8)알케닐이다. 이 구체예의 또 다른 양태에서,R1은 선택적으로 치환된 (C2-C8)알키닐이다. 이 구체예의 또 다른 양태에서, R1은 F이다. 이 구체예의 또 다른 양태에서 R2는 F이다. 이 구체예의 또 다른 양태에서,R2는 OH이다. 이 구체예의 또 다른 양태에서,R22는 OH이다. 이 구체예의 또 다른 양태에서, 각각의 R2 및 R22는 OH이다. 이 구체예의 또 다른 양태에서,R7은 H이다. 이 구체예의 또 다른 양태에서,R7은 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, R7은 선택적으로 치환된 (C2-C8)알케닐이다. 이 구체예의 또 다른 양태에서,R7은 CN이다. 이 구체예의 또 다른 양태에서,Rc 또는 Rd 중 하나는 H이다. 이 구체예의 또 다른 양태에서, Rc 또는 Rd 중 하나는 H이고 Rc 또는 Rd 중 다른 하나는 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서,R6는 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서,R4는 선택적으로 치환된 (C6-C20)아릴이다. 이 구체예의 또 다른 양태에서,Ar은 선택적으로 치환된 니트로페닐이다. 이 구체예의 또 다른 양태에서, 염기는:
로 이루어진 군에서 선택되고;
여기서:
각각의 X1은 독립적으로 N 또는 CRlO이고;
각각의 X2는 독립적으로 NR11, 0, 또는 S(O)n이고;
각각의 R8는 독립적으로 할로겐, NRllR12, N(Rll)ORll, NRllNRl1R12, N3, NO, NO2, CHO, CN, -CH(=NRll),-CH=NNHRll, -CH=N(ORll), -CH(ORll)2, -C(=0)NRl1R12, -C(=S)NRllR12, -C(=O)ORll, (C1-C8)알킬, (C2-C8)알케닐, (C2-C8)알키닐, (C4-C8)카르보사이클릴알킬, (C6-C20)아릴, (C2-C20)헤테로사이클릴, 헤테로아릴, -C(=O)(C1-C8)알킬, -S(O)n(C1-C8)알킬, 아릴(C1-C8)알킬, OR11 또는 SR11이고;
각각의 n은 독립적으로 0, 1, 또는 2이고;
각각의 R9 또는 R10은 독립적으로 H, 할로겐, NRllR12, N(Rll)ORll, NRllNRl1R12, N3, NO, NO2, CHO, CN, -CH(=NRll),-CH=NHNRll, -CH=N(ORll), -CH(ORll)2, -C(=0)NRl1R12, -C(=S)NRllR12, -C(=O)ORll, Rll, ORll 또는 SRll이고;
각각의 Rll 또는 R12는 독립적으로 H, (C1-C8)알킬, (C2-C8)알케닐, (C2-C8)알키닐, (C3-C8)카르보사이클릴, (C4-C8)카르보사이클릴알킬,아릴(C1-C8)알킬,헤테로사이클릴(C1-C8)알킬, (C6-C20)아릴,(C2-C20)헤테로사이클릴, 헤테로아릴,-C(=0)(C1-C8)알킬, -S(O)n(C1-C8)알킬이고, 또는 Rll 및 R12는 이들이 모두 부착된 질소와 합쳐서 3 내지 7원 헤테로사이클릭 고리를 형성하고, 여기서 상기 헤테로사이클릭 고리의 임의의 한 탄소 원자는 -O-, -S(O)n- 또는 -NRa-로 선택적으로 대체될 수 있고; 및
여기서 각각의 Rc, Rd, R1, R2, R22, R23, R24, R4, R5, R6, R7, R8, R9, R10, R11 또는 R12의 각각의 (C1-C8)알킬, (C2-C8)알케닐, (C2-C8)알키닐, (C3-C8)카르보사이클릴, (C4-C8)카르보사이클릴알킬,아릴(C1-C8)알킬,헤테로사이클릴(C1-C8)알킬, (C6-C20)아릴,(C2-C20)헤테로사이클릴 또는 헤테로아릴은,독립적으로, 하나 이상의 할로,하이드록시,CN, N3, N(Ra)2, NH(Ra), NH2, N02, C(O)N(Ra)2, C(O)NH(Ra), C(O)NH2, OC(O)N(Ra)2, OC(O)NH(Ra), OC(O)NH2, C(O)ORa, OC(O)ORa, C(O)Ra, OC(O)Ra, S(O)nRa, S(O)2N(Ra)2, S(O)2NH(Ra), S(O)2NH2, ORa 또는 Ra로 선택적으로 치환된다. 또 다른 양태에서,염기는 우라실이 아니다. 또 다른 양태에서,염기는 사이토신이 아니다.
이 구체예의 또 다른 양태에서, 염기는:
로 이루어진 군에서 선택된다.
이 구체예의 또 다른 양태에서, 염기는
로 이루어진 군에서 선택된다.
이 구체예의 또 다른 양태에서,염기는
로 이루어진 군에서 선택된다.
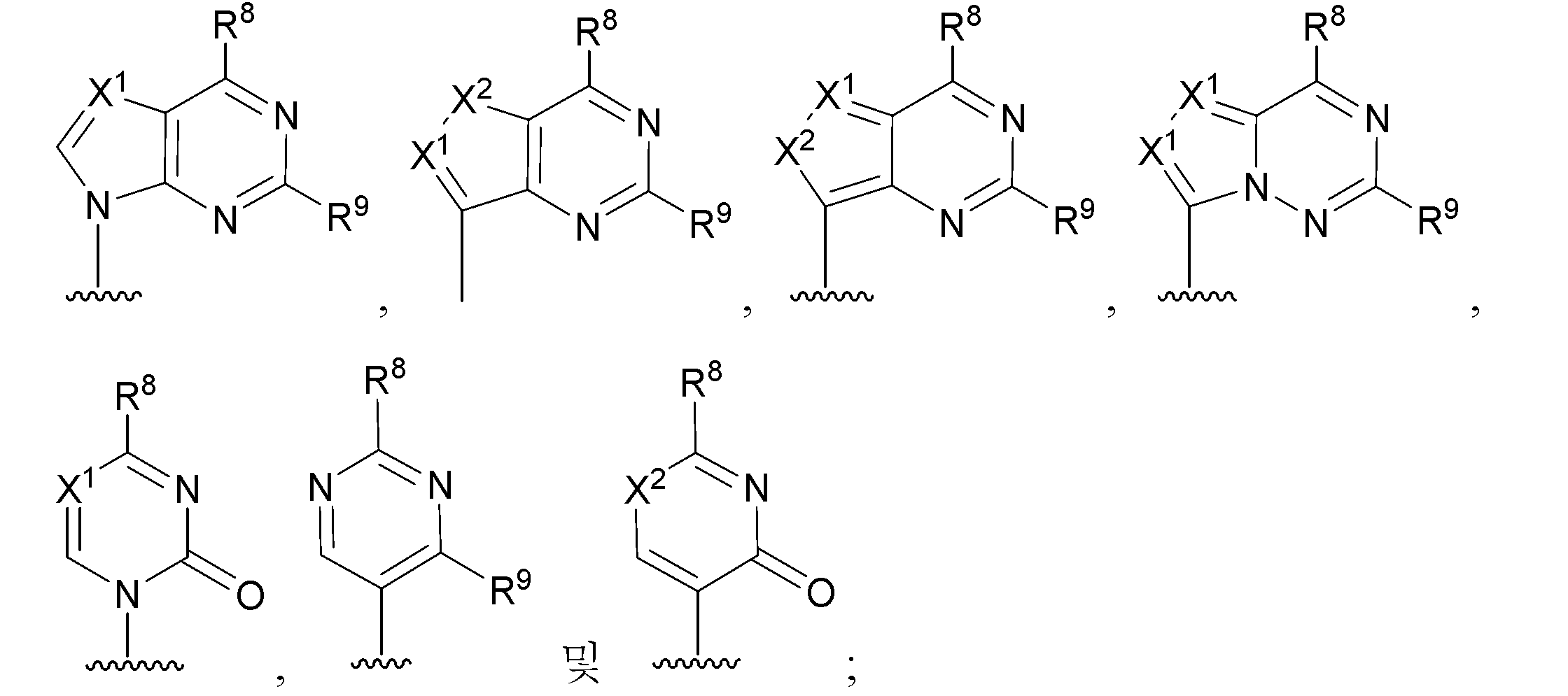
화학식 (V)의 화합물로부터 화학식 (IVa) 또는 (IVb)의 화합물을 제조하는 방법의 또 다른 구체예에서,R1은 H 또는 CH3이고; R2는 OR11 또는 할로겐이고; R6는 선택적으로 치환된 (C1-C8)알킬이고,Rc 또는 Rd 중 하나는 H이고 Rc 또는 Rd 중 다른 하나는 선택적으로 치환된 (C1-C8)알킬이고,R22는 OR11이고,각각의 R5, R23 및 R24는 H이다. 이 구체예의 또 다른 양태에서 R1은 H이다. 이 구체예의 또 다른 양태에서, R1은 CH3이다. 이 구체예의 또 다른 양태에서,R2는 F이다. 이 구체예의 또 다른 양태에서,R2는 OH이다. 이 구체예의 또 다른 양태에서, R22는 OH이다. 이 구체예의 또 다른 양태에서 각각의 R2 및 R22는 OH이다. 이 구체예의 또 다른 양태에서, R7은 H이다. 이 구체예의 또 다른 양태에서,R7은 CH3이다. 이 구체예의 또 다른 양태에서,R7은 에티닐이다. 이 구체예의 또 다른 양태에서,R7은 CN이다. 이 구체예의 또 다른 양태에서,R4는 선택적으로 치환된 (C6-C20)아릴이다. 구체예의 또 다른 양태에서,R4는 선택적으로 치환된 페닐이다. 이 구체예의 또 다른 양태에서, R4는 선택적으로 치환된 나프틸이다. 이 구체예의 또 다른 양태에서, Ar은 선택적으로 치환된 니트로페닐이다. 이 구체예의 또 다른 양태에서, 염기는:
로 이루어진 군에서 선택되고;
여기서:
각각의 X1은 독립적으로 N 또는 CR1O이고;
각각의 x2는 독립적으로 NR11, 0, 또는 S(O)n이고;
각각의 R8는 독립적으로 할로겐, NR11R12, N(R11)OR11, NR11NR11R12, N3, NO, N02, CHO, CN, -CH(=NR11), -CH=NNHR11, -CH=N(OR11), -CH(OR11)2, -C(=0)NR11R12, -C( =S)NR11R12, -C(=O)OR11, (C1-C8)알킬, (C2-C8)알케닐, (C2-C8)알키닐, (C4-C8)카르보사이클릴알킬,(C6-C20)아릴,(C2-C20)헤테로사이클릴,헤테로아릴,-C(=0)(C1-C8)알킬, -S(O)n(C1-C8)알킬, 아릴(C1-C8)알킬, OR11 또는 SRll이고;
각각의 n은 독립적으로 0, 1, 또는 2이고;
각각의 R9 또는 RlO은 독립적으로 H, 할로겐, NR11R12, N(R11)OR11, NR11NR11R12, N3, NO, N02, CHO, CN, -CH(=NR11), -CH=NHNR11,-CH=N(OR11), -CH(OR11)2, -C(=0)NR11R12, -C(=S)NR11R12, C(=O)OR11, R11, OR11 또는 SR11이고;
각각의 R11 또는 R12는 독립적으로 H, (C1-C8)알킬, (C2-C8)알케닐,(C2-C8)알키닐,(C3-C8)카르보사이클릴,(C4-C8)카르보사이클릴알킬,아릴(C1-C8)알킬,헤테로사이클릴(C1-C8)알킬,(C6-C20)아릴,(C2-C20)헤테로사이클릴,헤테로아릴,-C(=0)(C1-C8)알킬,-S(O)n(C1-C8)알킬이고,또는 R11 및 R12는 이들이 모두 부착된 질소와 합쳐서 3 내지 7원 헤테로사이클릭 고리를 형성하고,여기서 상기 헤테로사이클릭 고리의 임의의 한 탄소 원자는 -0-, -S(O)n- 또는 -NRa-로 선택적으로 대체될 수 있고; 및
여기서 각각의 Rc, Rd, R1, R2, R22, R23, R24, R4, R5, R6, R7, R8, R9, R10, R11 또는 R12의 각각의 (C1-C8)알킬, (C2-C8)알케닐, (C2-C8)알키닐, (C3-C8)카르보사이클릴,(C4-C8)카르보사이클릴알킬,아릴(C1-C8)알킬, 헤테로사이클릴(C1-C8)알킬, (C6-C20)아릴, (C2-C20)헤테로사이클릴 또는 헤테로아릴은,독립적으로,하나 이상의 할로,하이드록시, CN, N3, N(Ra)2, NH(Ra), NH2, N02, C(0)N(Ra)2, C(O)NH(Ra), C(0)NH2, OC(O)N(Ra)2, OC(O)NH(Ra), OC(O)NH2, C(O)ORa, OC(O)ORa, C(O)Ra, OC(O)Ra, S(O)nRa, S(O)2N(Ra)2, S(O)2NH(Ra), S(O)2NH2, ORa 또는 Ra로 선택적으로 치환된다. 또 다른 양태에서, 염기는 우라실이 아니다. 또 다른 양태에서 염기는 사이토신이 아니다.
이 구체예의 또 다른 양태에서, 염기는:
로 이루어진 군에서 선택된다.
이 구체예의 또 다른 양태에서, 염기는
로 이루어진 군에서 선택된다.
이 구체예의 또 다른 양태에서,염기는
로 이루어진 군에서 선택된다.
화학식 (V)의 화합물로부터 화학식 (IVa) 또는 (IVb)의 화합물을 제조하는 방법의 또 다른 구체예에서, R1은 H 또는 CH3이고; R2는 OR11 또는 할로겐이고,R6는 선택적으로 치환된 (C1-C8)알킬이고; Rc 또는 Rd 중 하나는 H이고 Rc 또는 Rd 중 다른 하나는 선택적으로 치환된 (C1-C8)알킬이고; R22는 OR11이고,각각의 R5, R23 및 R24는 H이고 염기는:
로 이루어진 군에서 선택되고;
여기서:
각각의 X1은 독립적으로 N 또는 CR1O이고;
각각의 x2는 독립적으로 NR11, 0, 또는 S(O)n이고;
각각의 R8는 독립적으로 할로겐, NR11R12, N(R11)OR11, NR11NR11R12, N3, NO, N02, CHO, CN, -CH(=NR11), -CH=NNHR11, -CH=N(OR11), -CH(OR11)2, -C(=0)NR11R12, -C( =S)NR11R12, -C(=O)OR11, (C1-C8)알킬, (C2-C8)알케닐, (C2-C8)알키닐, (C4-C8)카르보사이클릴알킬,(C6-C20)아릴,(C2-C20)헤테로사이클릴,헤테로아릴,-C(=0)(C1-C8)알킬, -S(O)n(C1-C8)알킬, 아릴(C1-C8)알킬, OR11 또는 SRll이고;
각각의 n은 독립적으로 0, 1, 또는 2이고;
각각의 R9 또는 RlO은 독립적으로 H, 할로겐, NR11R12, N(R11)OR11, NR11NR11R12, N3, NO, N02, CHO, CN, -CH(=NR11), -CH=NHNR11,-CH=N(OR11), -CH(OR11)2, -C(=0)NR11R12, -C(=S)NR11R12, C(=O)OR11, R11, OR11 또는 SR11이고;
각각의 R11 또는 R12는 독립적으로 H, (C1-C8)알킬, (C2-C8)알케닐,(C2-C8)알키닐,(C3-C8)카르보사이클릴,(C4-C8)카르보사이클릴알킬,아릴(C1-C8)알킬,헤테로사이클릴(C1-C8)알킬,(C6-C20)아릴,(C2-C20)헤테로사이클릴,헤테로아릴,-C(=0)(C1-C8)알킬,-S(O)n(C1-C8)알킬이고,또는 R11 및 R12는 이들이 모두 부착된 질소와 합쳐서 3 내지 7원 헤테로사이클릭 고리를 형성하고,여기서 상기 헤테로사이클릭 고리의 임의의 한 탄소 원자는 -0-, -S(O)n- 또는 -NRa-로 선택적으로 대체될 수 있고; 및
여기서 각각의 Rc, Rd, R1, R2, R22, R23, R24, R4, R5, R6, R7, R8, R9, R10, R11 또는 R12의 각각의 (C1-C8)알킬, (C2-C8)알케닐, (C2-C8)알키닐, (C3-C8)카르보사이클릴,(C4-C8)카르보사이클릴알킬,아릴(C1-C8)알킬, 헤테로사이클릴(C1-C8)알킬, (C6-C20)아릴, (C2-C20)헤테로사이클릴 또는 헤테로아릴은,독립적으로,하나 이상의 할로,하이드록시, CN, N3, N(Ra)2, NH(Ra), NH2, N02, C(0)N(Ra)2, C(O)NH(Ra), C(0)NH2, OC(O)N(Ra)2, OC(O)NH(Ra), OC(O)NH2, C(O)ORa, OC(O)ORa, C(O)Ra, OC(O)Ra, S(O)nRa, S(O)2N(Ra)2, S(O)2NH(Ra), S(O)2NH2, ORa 또는 Ra로 선택적으로 치환된다. 또 다른 양태에서,염기는 우라실이 아니다. 또 다른 양태에서, 염기는 사이토신이 아니다.
이 구체예의 또 다른 양태에서 R1은 H이다. 이 구체예의 또 다른 양태에서, R1은 CH3이다. 이 구체예의 또 다른 양태에서,R2는 F이다. 이 구체예의 또 다른 양태에서,R2는 OH이다. 이 구체예의 또 다른 양태에서, R22는 OH이다. 이 구체예의 또 다른 양태에서 각각의 R2 및 R22는 OH이다. 이 구체예의 또 다른 양태에서, R7은 H이다. 이 구체예의 또 다른 양태에서,R7은 CH3이다. 이 구체예의 또 다른 양태에서,R7은 에티닐이다. 이 구체예의 또 다른 양태에서,R7은 CN이다. 이 구체예의 또 다른 양태에서,R4는 선택적으로 치환된 (C6-C20)아릴이다. 구체예의 또 다른 양태에서,R4는 선택적으로 치환된 페닐이다. 이 구체예의 또 다른 양태에서, R4는 선택적으로 치환된 나프틸이다. 이 구체예의 또 다른 양태에서,Rc 또는 Rd 중 하나는 H이고 Rc 또는 Rd 중 다른 하나는 CH3이다. 이 구체예의 또 다른 양태에서,Ar은 선택적으로 치환된 니트로페닐이다. 이 구체예의 또 다른 양태에서, 염기는 이다. 이 구체예의 또 다른 양태에서, 염기는 이다. 이 구체예의 또 다른 양태에서, 염기는 이다. 이 구체예의 또 다른 양태에서, 염기는 이다. 이 구체예의 또 다른 양태에서, 염기는 이다. 이 구체예의 또 다른 양태에서, 염기는 이다. 이 구체예의 또 다른 양태에서, 염기는 이다. 이 구체예의 또 다른 양태에서, 염기는 이다. 이 구체예의 또 다른 양태에서, 염기는 이다. 이 구체예의 또 다른 양태에서, 염기는 이다. 이 구체예의 또 다른 양태에서, 염기는 이다. 이 구체예의 또 다른 양태에서, 염기는 이다. 이 구체예의 또 다른 양태에서, 염기는 이다. 이 구체예의 또 다른 양태에서, 염기는 이다. 이 구체예의 또 다른 양태에서, 염기는 이다. 이 구체예의 또 다른 양태에서, 염기는 이다. 이 구체예의 또 다른 양태에서, 염기는 이다.
화학식 (Ia) 또는 (Ib)의 화합물 또는 이의 약제학적으로 허용가능한 염 또는 에스테르를 제조하는 방법의 또 다른 구체예에서 화학식 (Ia)는 화학식 (VIa) 이고, 화학식 (Ib)는 화학식 (VIb) 이고,화학식 (II)는 화학식 (VII)이고:
화학식 (VIa)
화학식 (VIb)
화학식 (VII)
여기서:
각각의 R1은 독립적으로 H, 할로겐, 선택적으로 치환된 (C1-C8)알킬, 선택적으로 치환된 (C2-C8)알케닐 또는 선택적으로 치환된 (C2-C8)알키닐이고;
각각의 R2는 독립적으로 할로겐 또는 OR11 이고;
각각의 R5는 H이고;
각각의 R22는 OR11 이고
나머지 변수는 화학식 (Ia) 또는 (Ib) 또는 (II) 또는 (IIIa) 또는 (IIIb)에 대하여 정의된 바와 같다.
화학식 (VII)의 화합물로부터 화학식 (VIa) 또는 화학식 (VIb)의 화합물을 제조하는 방법의 한 구체예에서,X1은 CR10이다. 이 구체예의 또 다른 양태에서,R10은 H이다. 이 구체예의 또 다른 양태에서,R1은 H이다. 이 구체예의 또 다른 양태에서,R1은 F이다. 이 구체예의 또 다른 양태에서,R1은 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서,R1은 메틸이다. 이 구체예의 또 다른 양태에서, R1은 선택적으로 치환된 (C2-C8)알케닐이다. 이 구체예의 또 다른 양태에서, R1은 선택적으로 치환된 에테닐이다. 이 구체예의 또 다른 양태에서, R1은 선택적으로 치환된 (C2-C8)알키닐이다. 이 구체예의 또 다른 양태에서, R1은 선택적으로 치환된 에티닐이다. 이 구체예의 또 다른 양태에서, R2는 F이다. 이 구체예의 또 다른 양태에서, R2는 OH이다. 이 구체예의 또 다른 양태에서 R22는 OH이다. 이 구체예의 또 다른 양태에서, 각각의 R2 및 R22는 OH이다. 이 구체예의 또 다른 양태에서, R7은 H이다. 이 구체예의 또 다른 양태에서, R7은 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, R7은 선택적으로 치환된 (C2-C8)알키닐이다. 이 구체예의 또 다른 양태에서, R7은 CN이다. 이 구체예의 또 다른 양태에서, Rc 또는 Rd 중 하나는 H이다. 이 구체예의 또 다른 양태에서, Rc 또는 Rd 중 하나는 H이고 Rc 또는 Rd 중 다른 하나는 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, R6는 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, R4는 선택적으로 치환된 (C6-C20)아릴이다. 이 구체예의 또 다른 양태에서, Ar은 선택적으로 치환된 니트로페닐이다.
화학식 (VII)의 화합물로부터 화학식 (VIa) 또는 화학식 (VIb)의 화합물을 제조하는 방법의 또 다른 구체예에서, X1은 CH이고,R1은 H 또는 CH3이고, Rc 또는 Rd 중 하나는 H이다. 이 구체예의 또 다른 양태에서 R2는 F이다. 이 구체예의 또 다른 양태에서, R2는 OH이다. 이 구체예의 또 다른 양태에서 R22는 OH이다. 이 구체예의 또 다른 양태에서, 각각의 R2 및 R22는 OH이다. 이 구체예의 또 다른 양태에서, R7은 H이다. 이 구체예의 또 다른 양태에서, R7은 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, R7은 CH3이다. 이 구체예의 또 다른 양태에서, R7은 선택적으로 치환된 (C2-C8)알키닐이다. 이 구체예의 또 다른 양태에서, R7은 에티닐이다. 이 구체예의 또 다른 양태에서, R7은 CN이다. 이 구체예의 또 다른 양태에서, Rc 또는 Rd 중 하나는 H이고 Rc 또는 Rd 중 다른 하나는 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, R6는 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, R4는 선택적으로 치환된 (C6-C20)아릴이다. 이 구체예의 또 다른 양태에서, Ar은 선택적으로 치환된 니트로페닐이다. 이 구체예의 또 다른 양태에서, R8는 NR11R12이다. 이 구체예의 또 다른 양태에서 R8는 OR11이다. 이 구체예의 또 다른 양태에서, R8는 NH2이다. 이 구체예의 또 다른 양태에서, R8는 OH이다. 이 구체예의 또 다른 양태에서 R9은 H이다. 이 구체예의 또 다른 양태에서, R9은 NR11R12이다. 이 구체예의 또 다른 양태에서, R9은 OR11이다. 이 구체예의 또 다른 양태에서, R8는 NR11R12이고 R9은 H이다. 이 구체예의 또 다른 양태에서, R8는 NR11R12이고 R9은 NR11R12이다.
화학식 (VII)의 화합물로부터 화학식 (VIa) 또는 화학식 (VIb)의 화합물을 제조하는 방법의 또 다른 구체예에서 X1은 CH이고 R1은 H 또는 CH3이고,Rc 또는 Rd 중 하나는 H이고 R7은 CN이다. 이 구체예의 또 다른 양태에서, R2는 F이다. 이 구체예의 또 다른 양태에서, R2는 OH이다. 이 구체예의 또 다른 양태에서 R22는 OH이다. 이 구체예의 또 다른 양태에서, 각각의 R2 및 R22는 OH이다. 이 구체예의 또 다른 양태에서 Rc 또는 Rd 중 하나는 H이고 Rc 또는 Rd 중 다른 하나는 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, Rc 또는 Rd 중 하나는 H이고 Rc 또는 Rd 중 다른 하나는 CH3이다. 이 구체예의 또 다른 양태에서, R6는 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, R4는 선택적으로 치환된 (C6-C20)아릴이다. 이 구체예의 또 다른 양태에서 R4는 선택적으로 치환된 페닐이다. 이 구체예의 또 다른 양태에서, Ar은 선택적으로 치환된 니트로페닐이다. 이 구체예의 또 다른 양태에서, R8는 NR11R12이다. 이 구체예의 또 다른 양태에서 R8는 OR11이다. 이 구체예의 또 다른 양태에서, R8는 NH2이다. 이 구체예의 또 다른 양태에서, R8는 OH이다. 이 구체예의 또 다른 양태에서, R9은 H이다. 이 구체예의 또 다른 양태에서, R9은 NR11R12이다. 이 구체예의 또 다른 양태에서, R9은 OR11이다. 이 구체예의 또 다른 양태에서, R8는 NR11R12이고 R9은 H이다. 이 구체예의 또 다른 양태에서, R8는 NH2이고 R9은 H이다. 이 구체예의 또 다른 양태에서, R8는 NR11R12이고 R9은 NR11R12이다. 이 구체예의 또 다른 양태에서, R8는 NH2이고 R9은 NH2이다. 이 구체예의 또 다른 양태에서, R8는 OH이고 R9은 NH2이다.
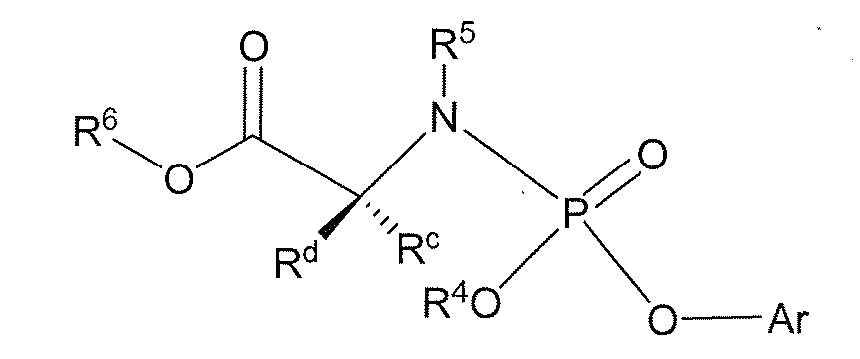
또 다른 구체예에서 화학식 (IIIa) 또는 화학식 (IIIb)의 화합물을 제조하는 방법이 제공되고
화학식 (IIIa)
화학식 (IIIb)
여기서:
각각의 Ra, R4 또는 R6는 독립적으로 (C1-C8)알킬, (C2-C8)알케닐, (C2-C8)알키닐, (C3-C8)카르보사이클릴, (C4-C8)카르보사이클릴알킬, 아릴(C1-C8)알킬,헤테로사이클릴(C1-C8)알킬,(C6-C20)아릴, (C2-C20)헤테로사이클릴 또는 헤테로아릴이고;
각각의 Rc 또는 Rd는 독립적으로 H, (C1-C8)알킬, (C2-C8)알케닐, (C2-C8)알키닐, (C3-C8)카르보사이클릴, (C4-C8)카르보사이클릴알킬, 아릴(C1-C8)알킬,헤테로사이클릴(C1-C8)알킬, (C6-C20)아릴, (C2-C20)헤테로사이클릴 또는 헤테로아릴이고,단 Rc 및 Rd는 동일하지 않고;
각각의 R5는 독립적으로 H, (C1-C8)알킬, (C2-C8)알케닐, (C2-C8)알키닐, (C3-C8)카르보사이클릴, (C4-C8)카르보사이클릴알킬,아릴(C1-C8)알킬,헤테로사이클릴(C1-C8)알킬, (C6-C20)아릴, (C2-C20)헤테로사이클릴 또는 헤테로아릴이고;
여기서 각각의 Rc, Rd, R4, R5 또는 R6의 각각의 (C1-C8)알킬, (C2-C8)알케닐, (C2-C8)알키닐, (C3-C8)카르보사이클릴, (C4-C8)카르보사이클릴알킬,아릴(C1-C8)알킬,헤테로사이클릴(C1-C8)알킬,(C6-C20)아릴, (C2-C20)헤테로사이클릴 또는 헤테로아릴은,독립적으로,하나 이상의 할로,하이드록시, CN, N3, N(Ra)2, NH(Ra), NH2, C(O)N(Ra)2, C(O)NH(Ra), C(O)NH2, OC(O)N(Ra)2, OC(O)NH(Ra), OC(O)NH2, C(O)ORa, OC(O)ORa, S(O)nRa, S(O)2N(Ra)2, S(O)2NH(Ra), S(O)2NH2, ORa 또는 Ra로 선택적으로 치환되고;
각각의 Ar은 (C6-C20)아릴 또는 헤테로아릴이고, 여기서 상기 (C6-C20)아릴 또는 헤테로아릴은 하나 이상의 할로겐, NO2, 또는 (C1-C8)할로알킬로 치환되고,하나 이상의 CN, N3, N(Ra)2, C(O)N(Ra)2, OC(O)N(Ra)2, C(O)ORa, OC(O)ORa, C(O)Ra, OC(O)Ra, S(O)nRa, S(O)2N(Ra)2, ORa 또는 Ra로 선택적으로 치환되고,단 Ar은 R4와 상이하고;
상기 방법은:
(d) 부분입체 이성질성 화학식 (VIII)의 화합물을 제공하는 단계
화학식 (VIII)
및
(e) 적절한 용매로부터 화학식 (VIII)의 화합물을 결정화하여;
순수한 화학식 (IIIa) 또는 화학식 (IIIb)의 부분입체 이성질체를 형성하는 단계를 포함한다.
화학식 (IIIa) 또는 화학식 (IIIb)의 화합물을 제조하는 방법의 한 구체예에서, R5는 H이고 ,Rc 또는 Rd 중 하나는 H이다. 이 구체예의 또 다른 양태에서, Rc 또는 Rd 중 하나는 H이고,Rc 또는 Rd 중 다른 하나는 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, Rc 또는 Rd 중 하나는 H이고,Rc 또는 Rd 중 다른 하나는 CH3이다. 이 구체예의 또 다른 양태에서, R6는 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, R6는 선택적으로 치환된 (C1-C8)이차 또는 삼차알킬이다. 이 구체예의 또다른 양태에서, R4는 선택적으로 치환된 (C6-C20)아릴이다. 이 구체예의 또 다른 양태에서, R4는 선택적으로 치환된 페닐이다. 이 구체예의 또 다른 양태에서 Ar은 선택적으로 치환된 니트로페닐이다. 이 구체예의 또 다른 양태에서 Ar은 선택적으로 치환된 파라-니트로페닐이다. 이 구체예의 또 다른 양태에서, Rc 및 Rd에 직접 부착된 탄소에서 카이랄성은 S이다. 이 구체예의 또 다른 양태에서, Rc 및 Rd에 직접 부착된 탄소에서 카이랄성은 R이다.
화학식 (IIIa) 또는 화학식 (IIIb)의 화합물을 제조하는 방법의 또 다른 구체예에서, R5는 H이고, Rc 또는 Rd 중 하나는 H이고, R6는 선택적으로 치환된 (C1-C8)알킬이고,R4는 선택적으로 치환된 (C6-C20)아릴이다. 이 구체예의 또 다른 양태에서, Rc 또는 Rd 중 하나는 H이고 Rc 또는 Rd 중 다른 하나는 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, Rc 또는 Rd 중 하나는 H이고 Rc 또는 Rd 중 다른 하나는 CH3이다. 이 구체예의 또 다른 양태에서, R6는 선택적으로 치환된 (C1-C8) 이차 또는 삼차알킬이다. 이 구체예의 또 다른 양태에서, R6는 선택적으로 치환된 2-프로필이다. 이 구체예의 또 다른 양태에서, R4는 선택적으로 치환된 페닐이다. 이 구체예의 또 다른 양태에서, Ar은 선택적으로 치환된 니트로페닐이다. 이 구체예의 또 다른 양태에서 Ar은 선택적으로 치환된 파라-니트로페닐이다. 이 구체예의 또 다른 양태에서, Ar은 파라-니트로페닐이다. 이 구체예의 또 다른 양태에서, Rc 및 Rd에 직접 부착된 탄소에서 카이랄성은 S이다. 이 구체예의 또 다른 양태에서, Rc 및 Rd에 직접 부착된 탄소에서 카이랄성은 R이다.
화학식 (IIIa) 또는 화학식 (IIIb)의 화합물을 제조하는 방법의 또 다른 구체예에서, R5는 H이고, Rc 또는 Rd 중 하나는 H이고 Rc 또는 Rd 중 다른 하나는 선택적으로 치환된 (C1-C8)알킬이고,R6는 선택적으로 치환된 (C1-C8)알킬이고, R4는 선택적으로 치환된 페닐이다. 이 구체예의 또 다른 양태에서, Rc 또는 Rd 중 하나는 H이고 Rc 또는 Rd 중 다른 하나는 CH3이다. 이 구체예의 또 다른 양태에서, R6는 선택적으로 치환된 (C1-C8) 이차 또는 삼차알킬이다. 이 구체예의 또 다른 양태에서, R6는 선택적으로 치환된 2-프로필이다. 이 구체예의 또 다른 양태에서, R4는 페닐이다. 이 구체예의 또 다른 양태에서, Ar은 선택적으로 치환된 니트로페닐이다. 이 구체예의 또 다른 양태에서, Ar은 선택적으로 치환된 파라-니트로페닐이다. 이 구체예의 또 다른 양태에서, Ar은 파라-니트로페닐이다. 이 구체예의 또 다른 양태에서, Rc 및 Rd에 직접 부착된 탄소에서 카이랄성은 S이다. 이 구체예의 또 다른 양태에서, Rc 및 Rd에 직접 부착된 탄소에서 카이랄성은 R이다.
화학식 (IIIa) 또는 화학식 (IIIb)의 화합물을 제조하는 방법의 또 다른 구체예에서, R5는 H이고, Rc 또는 Rd 중 하나는 H이고 Rc 또는 Rd 중 다른 하나는 CH3이고, R6는 선택적으로 치환된 (C1-C8)알킬이고,R4는 선택적으로 치환된 페닐이다. 이 구체예의 또 다른 양태에서, R6는 선택적으로 치환된 (C1-C8) 이차 또는 삼차 알킬이다. 이 구체예의 또 다른 양태에서, R6는 선택적으로 치환된 2-프로필이다. 이 구체예의 또 다른 양태에서, R6는 2-프로필이다. 이 구체예의 또 다른 양태에서, R4는 페닐이다. 이 구체예의 또 다른 양태에서 Ar은 선택적으로 치환된 니트로페닐이다. 이 구체예의 또 다른 양태에서 Ar은 선택적으로 치환된 파라-니트로페닐이다. 이 구체예의 또 다른 양태에서, Ar은 파라-니트로페닐이다. 이 구체예의 또 다른 양태에서, Rc 및 Rd에 직접 부착된 탄소에서 카이랄성은 S이다. 이 구체예의 또 다른 양태에서, Rc 및 Rd에 직접 부착된 탄소에서 카이랄성은 R이다.
화학식 (VIII)의 화합물의 부분입체 이성질성 혼합물은 적절한 용매로부터 화학식 (VIII)의 화합물을 결정화하여 분할된다. 적절한 용매의 비제한적 예는 디에틸 에테르, 디프로필 에테르, 디 t-부틸 에테르, 메틸 t-부틸 에테르, C1-C6 할로겐화 알칸, C5-C8 탄화수소, 테트라하이드로퓨란, 톨루엔, 자일렌, 디옥산 등이다. 또 다른 구체예에서, 화학식 (IV)의 화합물은 적절한 용매에 용해되고, C5-C8 탄화수소 또는 C5-C8 사이클릭 탄화수소의 첨가에 의하여 결정화가 유발된다. 바람직한 구체예에서, 화학식 (VIII)의 화합물은 에테르 용매에 용해되고, C5-C8 탄화수소의 첨가에 의하여 결정화가 유발된다. 특히 바람직한 구체예에서, 화학식 (VIII)의 화합물은 디에틸 에테르에 용해되고,헥산의 첨가에 의하여 결정화가 유발된다.
화학식 (VIII)의 화합물의 부분입체 이성질성 혼합물은 약 80 ℃ 내지 약 - 20℃의 온도에서 적절한 용매로부터 화학식 (VIII)의 화합물을 결정화하여 분할된다. 바람직하게는, 온도는 약 30 ℃ 내지 약 -20℃, 더욱 바람직하게는 대략 주위온도 내지 -10℃ 이다.
화학식 (VIII)의 화합물의 부분입체 이성질성 혼합물은 적절한 용매로부터 화학식 (VIII)의 화합물을 결정화하여 분할되고,여기서 용액 중 화학식 (VIII)의 화합물의 농도는 용매 l 리터당 약 25 g 내지 약 1000 g 이다. 더욱 전형적으로, 화학식 (VIII)의 화합물의 농도는 용매 1 리터당 약 50 내지 500 g 이다.
결정화에 의한 화학식 (VIII)의 화합물의 부분입체 이성질성 혼합물의 분할은 순수한 부분입체 이성질체의 종자 결정의 첨가에 의하여 촉진될 수 있다. 순수한 부분입체 이성질체의 종자 결정은 본 명세서에 기재된 비제한적 방법에 의한 것과 같이,액체 크로마토그래피,카이랄 액체 크로마토그래피,고압 액체 크로마토그래피,또는 카이랄 고압 액체 크로마토그래피에 의한 화학식 (VIII)의 화합물의 부분입체 이성질성 혼합물의 정제를 통하여 수득될 수 있다.
전형적으로,화학식 (VIII)의 화합물의 부분입체 이성질성 혼합물의 결정화는 최소 60 %의 단일 부분입체 이성질체를 포함하는 부분입체 이성질체의 혼합물을 생성한다. 더욱 전형적으로,생성된 혼합물은 최소 70 %의 단일 부분입체 이성질체,가장 전형적으로,최소 80 %의 단일 부분입체 이성질체,바람직하게는 최소90 %의 단일 부분입체 이성질체,더욱 바람직하게는 최소 95 %의 단일 부분입체 이성질체를 포함한다. 더 높은 부분입체 이성질체 순도,예를 들어 최소 99 % 부분입체 이성질체 순도가 한 번 이상의 추후의 결정화에 의하여 수득될 수 있다. 단일 결정화로부터의 결정질 물질 수율은 전형적으로 약 10 내지 45 %, 더욱 전형적으로 약 20-35 %이다.
또 다른 구체예에서, 화학식 (IIIa) 또는 화학식 (IIIb)의 화합물
화학식 (IIIa)
화학식 (IIIb)
또는 이의 염 또는 에스테르가 제공되고;
여기서:
각각의 Ra, R4 또는 R6는 독립적으로 (C1-C8)알킬,(C2-C8)알케닐,(C2-C8)알키닐, (C3-C8)카르보사이클릴, (C4-C8)카르보사이클릴알킬, 아릴(C1-C8)알킬, 헤테로사이클릴(C1-C8)알킬,(C6-C20)아릴,(C2-C20)헤테로사이클릴 또는 헤테로아릴이고;
각각의 Rc 또는 Rd는 독립적으로 H, (C1-C8)알킬,(C2-C8)알케닐,(C2-C8)알키닐, (C3-C8)카르보사이클릴, (C4-C8)카르보사이클릴알킬, 아릴(C1-C8)알킬, 헤테로사이클릴(C1-C8)알킬,(C6-C20)아릴,(C2-C20)헤테로사이클릴 또는 헤테로아릴이고,단 Rc 및 Rd는 동일하지 않고;
각각의 R5는 독립적으로 H, (C1-C8)알킬,(C2-C8)알케닐,(C2-C8)알키닐, (C3-C8)카르보사이클릴, (C4-C8)카르보사이클릴알킬, 아릴(C1-C8)알킬, 헤테로사이클릴(C1-C8)알킬,(C6-C20)아릴,(C2-C20)헤테로사이클릴 또는 헤테로아릴이고;
여기서 각각의 Rc, Rd, R4, R5 또는 R6의 각각의 (C1-C8)알킬,(C2-C8)알케닐,(C2-C8)알키닐, (C3-C8)카르보사이클릴, (C4-C8)카르보사이클릴알킬, 아릴(C1-C8)알킬, 헤테로사이클릴(C1-C8)알킬,(C6-C20)아릴,(C2-C20)헤테로사이클릴 또는 헤테로아릴은,독립적으로,하나 이상의 할로,하이드록시, CN, N3, N(Ra)2, NH(Ra), NH2, C(O)N(Ra)2, C(O)NH(Ra), C(O)NH2, OC(O)N(Ra)2, OC(O)NH(Ra), OC(O)NH2, C(O)ORa, OC(O)ORa, S(O)nRa, S(O)2N(Ra)2, S(O)2NH(Ra), S(O)2NH2, ORa 또는 Ra로 선택적으로 치환되고; 및
각각의 Ar은 (C6-C20)아릴 또는 헤테로아릴이고, 여기서 상기 (C6-C20)아릴 또는 헤테로아릴은 하나 이상의 할로겐, NO2, 또는 (C1-C8)할로알킬로 치환되고,하나 이상의 CN, N3, N(Ra)2, C(O)N(Ra)2, OC(O)N(Ra)2, C(O)ORa, OC(O)ORa, C(O)Ra, OC(O)Ra, S(O)nRa, S(O)2N(Ra)2, ORa 또는 Ra로 선택적으로 치환되고,단 Ar은 R4와 상이하다.
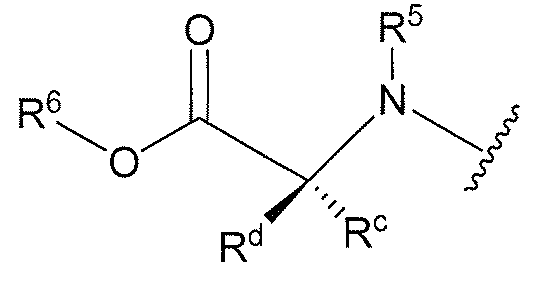
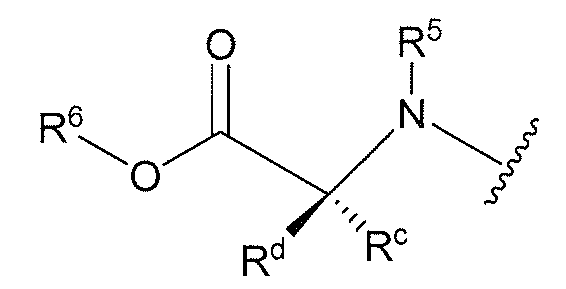
화학식 (IIIa) 또는 화학식 (IIIb)의 화합물의 또 다른 구체예에서, R5는 H이고 Rc 또는 Rd 중 하나는 H이다. 이 구체예의 또 다른 양태에서, Rc 또는 Rd 중 하나는 H이고 Rc 또는 Rd 중 다른 하나는 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, Rc 또는 Rd 중 하나는 H이고 Rc 또는 Rd 중 다른 하나는 CH3이다. 이 구체예의 또 다른 양태에서, R6는 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, R6는 선택적으로 치환된 (C1-C8) 이차 또는 삼차 알킬이다. 이 구체예의 또 다른 양태에서, R4는 선택적으로 치환된 (C6-C20)아릴이다. 이 구체예의 또 다른 양태에서 R4는 선택적으로 치환된 페닐이다. 이 구체예의 또 다른 양태에서, Ar은 선택적으로 치환된 니트로페닐이다. 이 구체예의 또 다른 양태에서, Ar은 선택적으로 치환된 파라니트로페닐이다. 이 구체예의 또 다른 양태에서, Rc 및 Rd에 직접 부착된 탄소에서 카이랄성은 S이다. 이 구체예의 또 다른 양태에서, Rc 및 Rd에 직접 부착된 탄소에서 카이랄성은 R이다. 이 구체예의 또 다른 양태에서, 화학식 (IIIa) 또는 화학식 (IIIb)의 모이어티 (moiety)
는 천연 발생 α-아미노산의 질소-연결 에스테르를 포함한다.
화학식 (IIIa) 또는 화학식 (IIIb)의 화합물의 또 다른 구체예에서, R5는 H이고, Rc 또는 Rd 중 하나는 H이고, R6는 선택적으로 치환된 (C1-C8)알킬이고,R4는 선택적으로 치환된 (C6-C20)아릴이다. 이 구체예의 또 다른 양태에서, Rc 또는 Rd 중 하나는 H이고 Rc 또는 Rd 중 다른 하나는 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, Rc 또는 Rd 중 하나는 H이고 Rc 또는 Rd 중 다른 하나는 CH3이다. 이 구체예의 또 다른 양태에서, R6는 선택적으로 치환된 (C1-C8) 이차 또는 삼차 알킬이다. 이 구체예의 또 다른 양태에서, R6는 선택적으로 치환된 2-프로필이다. 이 구체예의 또 다른 양태에서 R4는 선택적으로 치환된 페닐이다. 이 구체예의 또 다른 양태에서 Ar은 선택적으로 치환된 니트로페닐이다. 이 구체예의 또 다른 양태에서 Ar은 선택적으로 치환된 파라-니트로페닐이다. 이 구체예의 또 다른 양태에서, Ar은 파라-니트로페닐이다. 이 구체예의 또 다른 양태에서, Rc 및 Rd에 직접 부착된 탄소에서 카이랄성은 S이다. 이 구체예의 또 다른 양태에서, Rc 및 Rd에 직접 부착된 탄소에서 카이랄성은 R이다. 이 구체예의 또 다른 양태에서, 화학식 (IIIa) 또는 화학식 (IIIb)의 모이어티
는 천연 발생 α-아미노산의 질소-연결 에스테르를 포함한다.
화학식 (IIIa) 또는 화학식 (IIIb)의 화합물의 또 다른 구체예에서, R5는 H이고, Rc 또는 Rd 중 하나는 H이고 Rc 또는 Rd 중 다른 하나는 선택적으로 치환된 (C1-C8)알킬이고,R6는 선택적으로 치환된 (C1-C8)알킬이고,R4는 선택적으로 치환된 페닐이다. 이 구체예의 또 다른 양태에서, Rc 또는 Rd 중 하나는 H이고 Rc 또는 Rd 중 다른 하나는 CH3이다. 이 구체예의 또 다른 양태에서, R6는 선택적으로 치환된 (C1-C8) 이차 또는 삼차 알킬이다. 이 구체예의 또 다른 양태에서, R6는 선택적으로 치환된 2-프로필이다. 이 구체예의 또 다른 양태에서, R4는 페닐이다. 이 구체예의 또 다른 양태에서, Ar은 선택적으로 치환된 니트로페닐이다. 이 구체예의 또 다른 양태에서, Ar은 선택적으로 치환된 파라-니트로페닐이다. 이 구체예의 또 다른 양태에서, Ar은 파라-니트로페닐이다. 이 구체예의 또 다른 양태에서, Rc 및 Rd에 직접 부착된 탄소에서 카이랄성은 S이다. 이 구체예의 또 다른 양태에서, Rc 및 Rd에 직접 부착된 탄소에서 카이랄성은 R이다. 이 구체예의 또 다른 양태에서, 화학식 (IIIa) 또는 화학식 (IIIb)의 모이어티
는 천연 발생 α-아미노산의 질소-연결 에스테르를 포함한다.
화학식 (IIIa) 또는 화학식 (IIIb)의 화합물의 또 다른 구체예에서, R5는 H이고, Rc 또는 Rd 중 하나는 H이고 Rc 또는 Rd 중 다른 하나는 CH3이고, R6는 선택적으로 치환된 (C1-C8)알킬이고,R4는 선택적으로 치환된 페닐이다. 이 구체예의 또 다른 양태에서, R6는 선택적으로 치환된 (C1-C8) 이차 또는 삼차 알킬이다. 이 구체예의 또 다른 양태에서, R6는 선택적으로 치환된 2-프로필이다. 이 구체예의 또 다른 양태에서, R6는 2-프로필이다. 이 구체예의 또 다른 양태에서, R4는 페닐이다. 이 구체예의 또 다른 양태에서, Ar은 선택적으로 치환된 니트로페닐이다. 이 구체예의 또 다른 양태에서, Ar은 선택적으로 치환된 파라-니트로페닐이다. 이 구체예의 또 다른 양태에서 Ar은 파라-니트로페닐이다. 이 구체예의 또 다른 양태에서, Rc 및 Rd에 직접 부착된 탄소에서 카이랄성은 S이다. 이 구체예의 또 다른 양태에서, Rc 및 Rd에 직접 부착된 탄소에서 카이랄성은 R이다.
이 구체예의 또 다른 양태에서, 화학식 (IIIa) 또는 화학식 (IIIb)의 모이어티
는 천연 발생 α-아미노산의 질소-연결 에스테르를 포함한다.
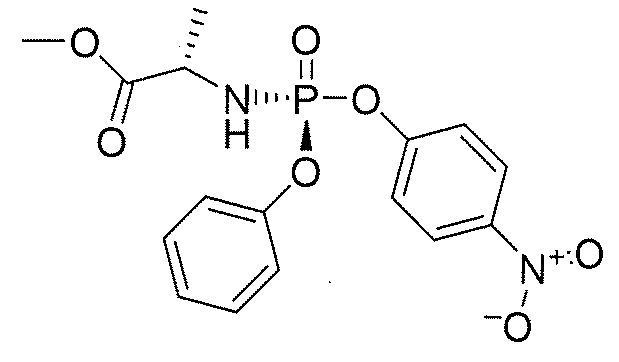
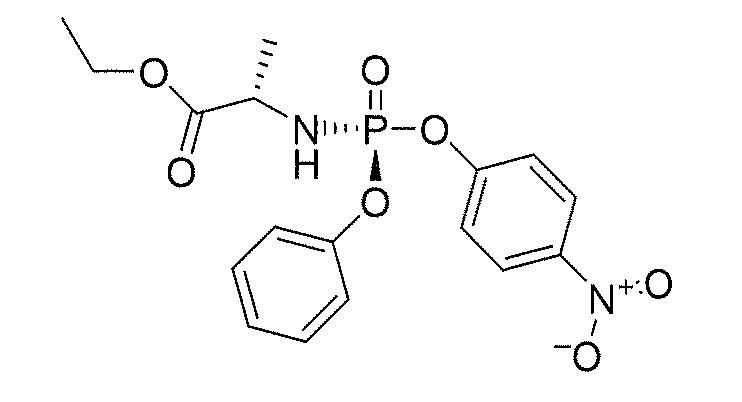
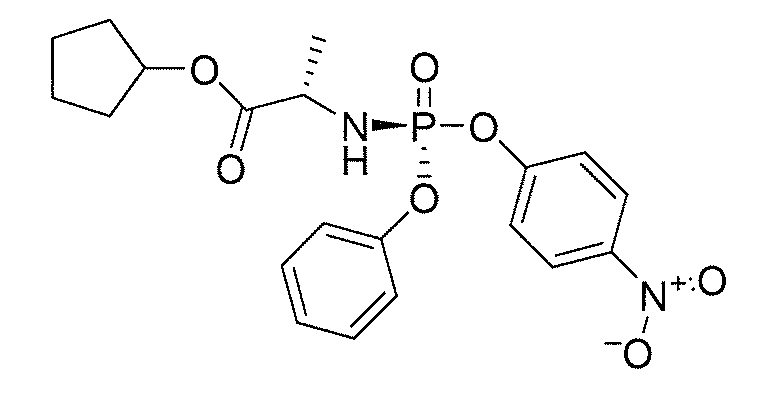
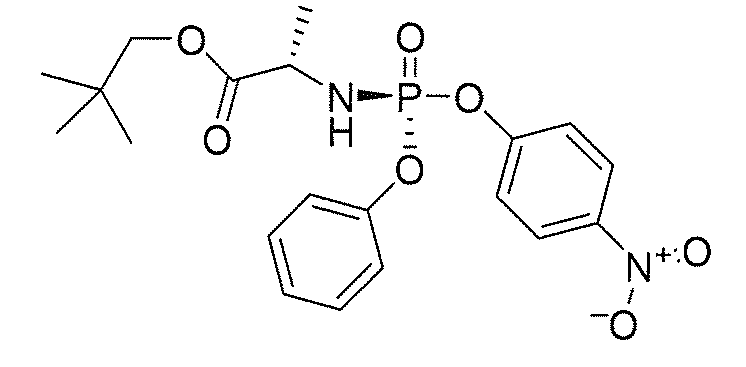
또 다른 구체예에서, 다음으로 이루어진 군에서 선택된 화학식 (IIIa) 또는 화학식 (IIIb)의 화합물:
또 다른 구체예에서, 화학식 (VIII)의 화합물을 제조하는 방법이 제공되고
화학식 (VIII)
여기서
각각의 Ra, R4 또는 R6는 독립적으로 (C1-C8)알킬,(C2-C8)알케닐,(C2-C8)알키닐, (C3-C8)카르보사이클릴, (C4-C8)카르보사이클릴알킬, 아릴(C1-C8)알킬, 헤테로사이클릴(C1-C8)알킬,(C6-C20)아릴,(C2-C20)헤테로사이클릴 또는 헤테로아릴이고;
각각의 Rc 또는 Rd는 독립적으로 H, (C1-C8)알킬,(C2-C8)알케닐,(C2-C8)알키닐, (C3-C8)카르보사이클릴, (C4-C8)카르보사이클릴알킬, 아릴(C1-C8)알킬, 헤테로사이클릴(C1-C8)알킬,(C6-C20)아릴,(C2-C20)헤테로사이클릴 또는 헤테로아릴이고,단 Rc 및 Rd는 동일하지 않고;
각각의 R5는 독립적으로 H, (C1-C8)알킬,(C2-C8)알케닐,(C2-C8)알키닐, (C3-C8)카르보사이클릴, (C4-C8)카르보사이클릴알킬, 아릴(C1-C8)알킬,헤테로사이클릴(C1-C8)알킬,(C6-C20)아릴,(C2-C20)헤테로사이클릴 또는 헤테로아릴이고;
여기서 각각의 Rc, Rd, R4, R5 또는 R6의 각각의 (C1-C8)알킬,(C2-C8)알케닐,(C2-C8)알키닐, (C3-C8)카르보사이클릴, (C4-C8)카르보사이클릴알킬, 아릴(C1-C8)알킬, 헤테로사이클릴(C1-C8)알킬,(C6-C20)아릴,(C2-C20)헤테로사이클릴, 헤테로아릴은,독립적으로,하나 이상의 할로,하이드록시, CN, N3, N(Ra)2, NH(Ra), NH2, C(O)N(Ra)2, C(O)NH(Ra), C(O)NH2, OC(O)N(Ra)2, OC(O)NH(Ra), OC(O)NH2, C(O)ORa, OC(O)ORa, S(O)nRa, S(O)2N(Ra)2, S(O)2NH(Ra), S(O)2NH2, ORa 또는 Ra로 선택적으로 치환되고; 및
각각의 Ar은 (C6-C20)아릴 또는 헤테로아릴이고, 여기서 상기 (C6-C20)아릴 또는 헤테로아릴은 하나 이상의 할로겐, NO2, 또는 (C1-C8)할로알킬로 치환되고,하나 이상의 CN, N3, N(Ra)2, C(O)N(Ra)2, OC(O)N(Ra)2, C(O)ORa, OC(O)ORa, C(O)Ra, OC(O)Ra, S(O)nRa, S(O)2N(Ra)2, ORa 또는 Ra로 선택적으로 치환되고,단 Ar은 R4와 상이하고;
상기 방법은:
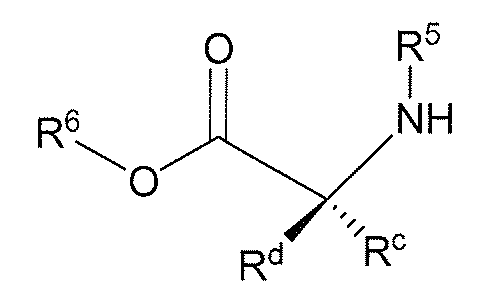
(f) 카이랄성으로 순수한 화학식 (IX)의 아미노산 에스테르 또는 이의 염을 제공하는 단계
화학식 (IX)
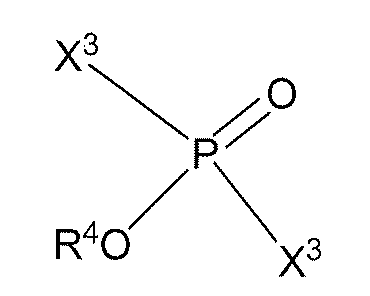
(g) 염기의 존재에서 화학식 (IX)의 화합물을 화학식 (X)의 화합물로 처리하는 단계
화학식 (X)
여기서 각각의 X3는 할로겐임; 및
(h) 생성된 혼합물을 ArOH로 처리하여;
화학식 (VIII)의 화합물을 형성하는 단계를 포함한다.
전형적으로, 카이랄성으로 순수한 화학식 (IX)의 아미노산 또는 이의 염은 적절한 비친핵성 용매에 용해되거나 현탁된다. 비제한적인 비친핵성 용매에는 할로알칸, 예를 들어, 메틸렌 클로라이드, 디클로로에탄 및 에테르, 예를 들어 디옥산, 테트라하이드로퓨란 및 글라임이 포함된다. 전형적으로, 현탁액 또는 용액은 용매 1 리터당 약 0.1 내지 약 5 몰의 화학식 (IX)의 화합물을 포함한다.
카이랄성으로 순수한 화학식 (IX) 의 아미노산의 현탁액 또는 용액은 화학식 (X)의 화합물로 처리된다. 전형적으로, 반응은 약 -20℃ 내지 약 60℃에서 수행된다. 화학식 (IX)의 화합물 대 화학식 (X)의 화합물의 몰비는 약 1:2 내지 약 2:1, 바람직하게는 약 1:1이다. 반응은 비친핵성 염기의 존재에서 수행된다. 비친핵성 염기의 비제한적 예는 삼차 아민, 예를 들어 트리에틸아민, 디이소프로필에틸아민 및 트리에틸아민; 메탈 하이드라이드, 예를 들어 LiH, NaH 및 CaH2; 및 질소 보유 헤테로사이클, 예를 들어 피리딘 및 디메틸아미노피리딘이다. 바람직한 구체예에서, 염기는 트리에틸아민과 같은 삼차 아민이다. 화학식 (IX)의 화합물이 일양성자산의 염일 때, 염기 대 화학식 (IX)의 화합물의 몰비는 전형적으로 약 2:1이다. 만약 화학식 (IX)의 화합물이 유리 염기이면 염기 대 화학식 (IX)의 화합물의 몰비는 약 1:1이다.
화학식 (IX)의 화합물과 화학식 (X)의 화합물의 반응이 당업자에게 공지인 많은 통상적인 수단에 의하여 이어질 수 있다. 이러한 수단에는 박막 크로마토그래피 및 hplc가 포함된다. 화학식 (IX)의 화합물과 화학식 (X)의 화합물 사이의 반응이 완료되면 반응물은 페놀성 화합물 ArOH로 처리되고, 여기서 Ar은 본 명세서에서 정의된 바와 같다. 화학식 (X)의 화합물 대 ArOH의 몰비는 약 1.1: 1 내지 약1: 1.1, 바람직하게는 약 1:1이다. ArOH의 첨가 후, 추가적인 염기, 전형적으로 반응에서 발생한 산을 중화하기에 충분한 염기가 필요하다. 전형적으로, 추가적인 염기는 상기한 바와 같은 비친핵성 염기이다.
화학식 (VIII)의 화합물은 당업자에게 공지인 통상적인 수단에 의하여 단리된다. 예를 들어, 반응에서 형성된 염이 반응 혼합물로부터 침전될 수 있고, 화학식 (VIII)의 화합물이 용매 증발에 이어 결정화 또는 크로마토그래피에 의하여 단리된다.
화학식 (VIII)의 화합물을 제조하는 방법의 한 구체예에서, R5는 H이고 Rc 또는 Rd 중 하나는 H이다. 이 구체예의 또 다른 양태에서, Rc 또는 Rd 중 하나는 H이고 Rc 또는 Rd 중 다른 하나는 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, Rc 또는 Rd 중 하나는 H이고 Rc 또는 Rd 중 다른 하나는 CH3이다. 이 구체예의 또 다른 양태에서, R6는 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, R6는 선택적으로 치환된 (C1-C8) 이차 또는 삼차 알킬이다. 이 구체예의 또 다른 양태에서 R4는 선택적으로 치환된 (C6-C20)아릴이다. 이 구체예의 또 다른 양태에서 R4는 선택적으로 치환된 페닐이다. 이 구체예의 또 다른 양태에서, Ar은 선택적으로 치환된 니트로페닐이다. 이 구체예의 또 다른 양태에서, Ar은 선택적으로 치환된 파라-니트로페닐이다. 이 구체예의 또 다른 양태에서, Rc 및 Rd에 직접 부착된 탄소에서 카이랄성은 S이다. 이 구체예의 또 다른 양태에서, Rc 및 Rd에 직접 부착된 탄소에서 카이랄성은 R이다. 이 구체예의 또 다른 양태에서, 화학식 (IX)의 화합물 또는 이의 염은, 천연 발생 α-아미노산의 에스테르이다.
화학식 (VIII)의 화합물을 제조하는 방법의 또 다른 구체예에서, R5는 H이고, Rc 또는 Rd 중 하나는 H이고, R6는 선택적으로 치환된 (C1-C8)알킬이고, R4는 선택적으로 치환된 (C6-C20)아릴이다. 이 구체예의 또 다른 양태에서, Rc 또는 Rd 중 하나는 H이고 Rc 또는 Rd 중 다른 하나는 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서 Rc 또는 Rd 중 하나는 H이고 Rc 또는 Rd 중 다른 하나는 CH3이다. 이 구체예의 또 다른 양태에서, R6는 선택적으로 치환된 (C1-C8) 이차 또는 삼차 알킬이다. 이 구체예의 또 다른 양태에서, R6는 선택적으로 치환된 2-프로필이다. 이 구체예의 또 다른 양태에서, R4는 선택적으로 치환된 페닐이다. 이 구체예의 또 다른 양태에서, Ar은 선택적으로 치환된 니트로페닐이다. 이 구체예의 또 다른 양태에서, Ar은 선택적으로 치환된 파라-니트로페닐이다. 이 구체예의 또 다른 양태에서, Ar은 파라-니트로페닐이다. 이 구체예의 또 다른 양태에서, Rc 및 Rd에 직접 부착된 탄소에서 카이랄성은 S이다. 이 구체예의 또 다른 양태에서, Rc 및 Rd에 직접 부착된 탄소에서 카이랄성은 R이다. 이 구체예의 또 다른 양태에서, 화학식 (IX)의 화합물 또는 이의 염은, 천연 발생 α-아미노산의 에스테르이다.
화학식 (VIII)의 화합물을 제조하는 방법의 또 다른 구체예에서, R5는 H이고, Rc 또는 Rd 중 하나는 H이고 Rc 또는 Rd 중 다른 하나는 선택적으로 치환된 (C1-C8)알킬이고, R6는 선택적으로 치환된 (C1-C8)알킬이고, R4는 선택적으로 치환된 페닐이다. 이 구체예의 또 다른 양태에서, Rc 또는 Rd 중 하나는 H이고 Rc 또는 Rd 중 다른 하나는 CH3이다. 이 구체예의 또 다른 양태에서, R6는 선택적으로 치환된 (C1-C8) 이차 또는 삼차 알킬이다. 이 구체예의 또 다른 양태에서, R6는 선택적으로 치환된 2-프로필이다. 이 구체예의 또 다른 양태에서, R4는 페닐이다. 이 구체예의 또 다른 양태에서 Ar은 선택적으로 치환된 니트로페닐이다. 이 구체예의 또 다른 양태에서, Ar은 선택적으로 치환된 파라-니트로페닐이다. 이 구체예의 또 다른 양태에서, Ar은 파라-니트로페닐이다. 이 구체예의 또 다른 양태에서, Rc 및 Rd에 직접 부착된 탄소에서 카이랄성은 S이다. 이 구체예의 또 다른 양태에서, Rc 및 Rd에 직접 부착된 탄소에서 카이랄성은 R이다. 이 구체예의 또 다른 양태에서, 화학식 (IX)의 화합물 또는 이의 염은, 천연 발생 α-아미노산의 에스테르이다.
화학식 (VIII)의 화합물을 제조하는 방법의 또 다른 구체예에서, R5는 H이고, Rc 또는 Rd 중 하나는 H이고 Rc 또는 Rd 중 다른 하나는 CH3이고, R6는 선택적으로 치환된 (C1-C8)알킬이고, R4는 선택적으로 치환된 페닐이다. 이 구체예의 또 다른 양태에서, R6는 선택적으로 치환된 (C1-C8) 이차 또는 삼차 알킬이다. 이 구체예의 또 다른 양태에서, R6는 선택적으로 치환된 2-프로필이다. 이 구체예의 또 다른 양태에서, R6는 2-프로필이다. 이 구체예의 또 다른 양태에서, R4는 페닐이다. 이 구체예의 또 다른 양태에서, Ar은 선택적으로 치환된 니트로페닐이다. 이 구체예의 또 다른 양태에서 Ar은 선택적으로 치환된 파라-니트로페닐이다. 이 구체예의 또 다른 양태에서, Ar은 파라-니트로페닐이다. 이 구체예의 또 다른 양태에서, Rc 및 Rd에 직접 부착된 탄소에서 카이랄성은 S이다. 이 구체예의 또 다른 양태에서, Rc 및 Rd에 직접 부착된 탄소에서 카이랄성은 R이다. 이 구체예의 또 다른 양태에서, 화학식 (IX)의 화합물 또는 이의 염은, 천연 발생 α-아미노산의 에스테르이다.
화학식 (Ia) 또는 (Ib)의 화합물 또는 이의 약제학적으로 허용가능한 염 또는 에스테르를 제조하는 방법의 또 다른 구체예에서, 화학식 (Ia)은 화학식 (XIa) 이고, 화학식 (Ib)는 화학식 (XIb)이고, 화학식 (II)는 화학식 (XII)이고:
화학식 (XIa)
화학식 (XIb)
화학식 (XII)
여기서:
각각의 R1은 독립적으로 H, 할로겐,선택적으로 치환된 (C1-C8)알킬, 선택적으로 치환된 (C2-C8)알케닐 또는 선택적으로 치환된 (C2-C8)알키닐이고; 각각의 R2는 독립적으로 할로겐 또는 ORll이고; 각각의 R5는 H이고; 각각의 R22는 ORll이고
나머지 변수는 화학식 (Ia) 또는 (Ib) 또는 (II) 또는 (IIIa) 또는 (IIIb)에 대하여 정의된 바와 같다.
화학식 (XII)의 화합물로부터 화학식 (XIa) 또는 화학식 (XIb)의 화합물을 제조하는 방법의 한 구체예에서, X1은 CR1O이다. 이 구체예의 또 다른 양태에서, RlO은 H이다. 이 구체예의 또 다른 양태에서, R1은 H이다. 이 구체예의 또 다른 양태에서, R1은 F이다. 이 구체예의 또 다른 양태에서, R1은 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, R1은 메틸이다. 이 구체예의 또 다른 양태에서, R1은 선택적으로 치환된 (C2-C8)알케닐이다. 이 구체예의 또 다른 양태에서, R1은 선택적으로 치환된 에테닐이다. 이 구체예의 또 다른 양태에서, R1은 선택적으로 치환된 (C2-C8)알키닐이다. 이 구체예의 또 다른 양태에서, R1은 선택적으로 치환된 에티닐이다. 이 구체예의 또 다른 양태에서, R2는 F이다. 이 구체예의 또 다른 양태에서, R2는 OH이다. 이 구체예의 또 다른 양태에서 R22는 OH이다. 이 구체예의 또 다른 양태에서, 각각의 R2 및 R22는 OH이다. 이 구체예의 또 다른 양태에서, 각각의 R2는 F이고 R22는 OH이다. 이 구체예의 또 다른 양태에서, R7은 H이다. 이 구체예의 또 다른 양태에서, R7은 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, R7은 선택적으로 치환된 (C2-C8)알키닐이다. 이 구체예의 또 다른 양태에서, R7은 CN이다. 이 구체예의 또 다른 양태에서, Rc 또는 Rd 중 하나는 H이다. 이 구체예의 또 다른 양태에서, Rc 또는 Rd 중 하나는 H이고 Rc 또는 Rd 중 다른 하나는 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, R6는 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, R4는 선택적으로 치환된 (C6-C20)아릴이다. 이 구체예의 또 다른 양태에서, Ar은 선택적으로 치환된 니트로페닐이다.
화학식 (XII)의 화합물로부터 화학식 (XIa) 또는 화학식 (XIb)의 화합물을 제조하는 방법의 또 다른 구체예에서, X1은 CH이고, R1은 H 또는 CH3이고, Rc 또는 Rd 중 하나는 H이다. 이 구체예의 또 다른 양태에서, R2는 F이다. 이 구체예의 또 다른 양태에서, R2는 OH이다. 이 구체예의 또 다른 양태에서 R22는 OH이다. 이 구체예의 또 다른 양태에서, 각각의 R2 및 R22는 OH이다. 이 구체예의 또 다른 양태에서, 각각의 R2는 F이고 R22는 OH이다. 이 구체예의 또 다른 양태에서, R7은 H이다. 이 구체예의 또 다른 양태에서, R7은 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, R7은 CH3이다. 이 구체예의 또 다른 양태에서, R7은 선택적으로 치환된 (C2-C8)알키닐이다. 이 구체예의 또 다른 양태에서, R7은 에티닐이다. 이 구체예의 또 다른 양태에서, R7은 CN이다. 이 구체예의 또 다른 양태에서, Rc 또는 Rd 중 하나는 H이고 Rc 또는 Rd 중 다른 하나는 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, R6는 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, R4는 선택적으로 치환된 (C6-C20)아릴이다. 이 구체예의 또 다른 양태에서, Ar은 선택적으로 치환된 니트로페닐이다. 이 구체예의 또 다른 양태에서, R8는 NR11R12이다. 이 구체예의 또 다른 양태에서, R8는 OR11이다. 이 구체예의 또 다른 양태에서, R8는 NH2이다. 이 구체예의 또 다른 양태에서, R8는 OH이다. 이 구체예의 또 다른 양태에서, R9은 H이다. 이 구체예의 또 다른 양태에서, R9은 NR11R12이다. 이 구체예의 또 다른 양태에서, R9은 OR11이다. 이 구체예의 또 다른 양태에서, R8는 NR11R12이고 R9은 H이다. 이 구체예의 또 다른 양태에서 R8는 NR11R12이고 R9은 NR11R12이다.
화학식 (XII)의 화합물로부터 화학식 (XIa) 또는 화학식 (XIb)의 화합물을 제조하는 방법의 또 다른 구체예에서, X1은 CH이고, R1은 H 또는 CH3이고, Rc 또는 Rd 중 하나는 H이고, R7은 H이다. 이 구체예의 또 다른 양태에서, R2는 F이다. 이 구체예의 또 다른 양태에서, R2는 OH이다. 이 구체예의 또 다른 양태에서 R22는 OH이다. 이 구체예의 또 다른 양태에서, 각각의 R2 및 R22는 OH이다. 이 구체예의 또 다른 양태에서, 각각의 R2는 F이고 R22는 OH이다. 이 구체예의 또 다른 양태에서, Rc 또는 Rd 중 하나는 H이고 Rc 또는 Rd 중 다른 하나는 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, Rc 또는 Rd 중 하나는 H이고 Rc 또는 Rd 중 다른 하나는 CH3이다. 이 구체예의 또 다른 양태에서, R6는 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서 R4는 선택적으로 치환된 (C6-C20)아릴이다. 이 구체예의 또 다른 양태에서, R4는 선택적으로 치환된 페닐이다. 이 구체예의 또 다른 양태에서, Ar은 선택적으로 치환된 니트로페닐이다. 이 구체예의 또 다른 양태에서, R8는 NR11R12이다. 이 구체예의 또 다른 양태에서, R8는 OR11이다. 이 구체예의 또 다른 양태에서 R8는 NH2이다. 이 구체예의 또 다른 양태에서, R8는 OH이다. 이 구체예의 또 다른 양태에서, R9은 H이다. 이 구체예의 또 다른 양태에서 R9은 NR11R12이다. 이 구체예의 또 다른 양태에서, R9은 OR11이다. 이 구체예의 또 다른 양태에서 R8는 NR11R12이고 R9은 H이다. 이 구체예의 또 다른 양태에서, R8는 NH2이고 R9은 H이다. 이 구체예의 또 다른 양태에서, R8는 NR11R12이고 R9은 NR11R12이다. 이 구체예의 또 다른 양태에서, R8는 NH2이고 R9은 NH2이다. 이 구체예의 또 다른 양태에서, R8는 OR11이고 R9은 NH2이다. 이 구체예의 또 다른 양태에서, R8는 OH이고 R9은 NH2이다.
화학식 (XII)의 화합물로부터 화학식 (XIa) 또는 화학식 (XIb)의 화합물을 제조하는 방법의 또 다른 구체예에서, X1은 N이다. 이 구체예의 또 다른 양태에서, R1은 H이다. 이 구체예의 또 다른 양태에서 R1은 F이다. 이 구체예의 또 다른 양태에서, R1은 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, R1은 메틸이다. 이 구체예의 또 다른 양태에서, R1은 선택적으로 치환된 (C2-C8)알케닐이다. 이 구체예의 또 다른 양태에서, R1은 선택적으로 치환된 에테닐이다. 이 구체예의 또 다른 양태에서, R1은 선택적으로 치환된 (C2-C8)알키닐이다. 이 구체예의 또 다른 양태에서, R1은 선택적으로 치환된 에티닐이다. 이 구체예의 또 다른 양태에서, R2는 F이다. 이 구체예의 또 다른 양태에서, R2는 OH이다. 이 구체예의 또 다른 양태에서 R22는 OH이다. 이 구체예의 또 다른 양태에서, 각각의 R2 및 R22는 OH이다. 이 구체예의 또 다른 양태에서, 각각의 R2는 F이고 R22는 OH이다. 이 구체예의 또 다른 양태에서 R7은 H이다. 이 구체예의 또 다른 양태에서, R7은 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, R7은 선택적으로 치환된 (C2-C8)알키닐이다. 이 구체예의 또 다른 양태에서, R7은 CN이다. 이 구체예의 또 다른 양태에서, Rc 또는 Rd 중 하나는 H이다. 이 구체예의 또 다른 양태에서, Rc 또는 Rd 중 하나는 H이고 Rc 또는 Rd 중 다른 하나는 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, R6는 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, R4는 선택적으로 치환된 (C6-C20)아릴이다. 이 구체예의 또 다른 양태에서, Ar은 선택적으로 치환된 니트로페닐이다.
화학식 (XII)의 화합물로부터 화학식 (XIa) 또는 화학식 (XIb)의 화합물을 제조하는 방법의 또 다른 구체예에서, X1은 N이고, R1은 H 또는 CH3이고, Rc 또는 Rd 중 하나는 H이다. 이 구체예의 또 다른 양태에서, R2는 F이다. 이 구체예의 또 다른 양태에서, R2는 OH이다. 이 구체예의 또 다른 양태에서 R22는 OH이다. 이 구체예의 또 다른 양태에서, 각각의 R2 및 R22는 OH이다. 이 구체예의 또 다른 양태에서, 각각의 R2는 F이고 R22는 OH이다. 이 구체예의 또 다른 양태에서, R7은 H이다. 이 구체예의 또 다른 양태에서, R7은 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, R7은 CH3이다. 이 구체예의 또 다른 양태에서, R7은 선택적으로 치환된 (C2-C8)알키닐이다. 이 구체예의 또 다른 양태에서 R7은 에티닐이다. 이 구체예의 또 다른 양태에서, R7은 CN이다. 이 구체예의 또 다른 양태에서, Rc 또는 Rd 중 하나는 H이고 Rc 또는 Rd 중 다른 하나는 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, R6는 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, R4는 선택적으로 치환된 (C6-C20)아릴이다. 이 구체예의 또 다른 양태에서, Ar은 선택적으로 치환된 니트로페닐이다. 이 구체예의 또 다른 양태에서, R8는 NR11R12이다. 이 구체예의 또 다른 양태에서, R8는 OR11이다. 이 구체예의 또 다른 양태에서, R8는 NH2이다. 이 구체예의 또 다른 양태에서, R8는 OH이다. 이 구체예의 또 다른 양태에서, R9은 H이다. 이 구체예의 또 다른 양태에서, R9은 NR11R12이다. 이 구체예의 또 다른 양태에서 R9은 OR11이다. 이 구체예의 또 다른 양태에서, R8는 NR11R12이고 R9은 H이다. 이 구체예의 또 다른 양태에서, R8는 NR11R12이고 R9은 NR11R12이다.
화학식 (XII)의 화합물로부터 화학식 (XIa) 또는 화학식 (XIb)의 화합물을 제조하는 방법의 또 다른 구체예에서, X1은 N이고, R1은 H 또는 CH3이고, Rc 또는 Rd 중 하나는 H이고, R7은 H이다. 이 구체예의 또 다른 양태에서, R2는 F이다. 이 구체예의 또 다른 양태에서, R2는 OH이다. 이 구체예의 또 다른 양태에서 R22는 OH이다. 이 구체예의 또 다른 양태에서, 각각의 R2 및 R22는 OH이다. 이 구체예의 또 다른 양태에서, 각각의 R2는 F이고 R22는 OH이다. 이 구체예의 또 다른 양태에서, Rc 또는 Rd 중 하나는 H이고 Rc 또는 Rd 중 다른 하나는 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, Rc 또는 Rd 중 하나는 H이고 Rc 또는 Rd 중 다른 하나는 다른 하나는 CH3이다. 이 구체예의 또 다른 양태에서, R6는 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, R4는 선택적으로 치환된 (C6-C20)아릴이다. 이 구체예의 또 다른 양태에서, R4는 선택적으로 치환된 페닐이다. 이 구체예의 또 다른 양태에서, Ar은 선택적으로 치환된 니트로페닐이다. 이 구체예의 또 다른 양태에서, R8는 NR11R12이다. 이 구체예의 또 다른 양태에서, R8는 OR11이다. 이 구체예의 또 다른 양태에서, R8는 NH2이다. 이 구체예의 또 다른 양태에서, R8는 OH이다. 이 구체예의 또 다른 양태에서, R9은 H이다. 이 구체예의 또 다른 양태에서, R9은 NR11R12이다. 이 구체예의 또 다른 양태에서 R9은 OR11이다. 이 구체예의 또 다른 양태에서, R8는 NR11R12이고 R9은 H이다. 이 구체예의 또 다른 양태에서, R8는 NH2이고 R9은 H이다. 이 구체예의 또 다른 양태에서, R8는 NR11R12이고 R9은 NR11R12이다. 이 구체예의 또 다른 양태에서, R8는 NH2이고 R9은 NH2이다. 이 구체예의 또 다른 양태에서, R8는 OR11이고 R9은 NH2이다. 이 구체예의 또 다른 양태에서, R8는 OH이고 R9은 NH2이다.
화학식 (Ia) 또는 (Ib)의 화합물 또는 이의 약제학적으로 허용가능한 염 또는 에스테르를 제조하는 방법의 또 다른 구체예에서, 화학식 (Ia)는 화학식 (XIIIa) 이고, 화학식 (Ib)는 화학식 (XIIIb)이고, 화학식 (II)는 화학식 (XIV) 이고:
화학식 (XIIIa)
화학식 (XIIIb)
화학식 (XIV)
여기서:
각각의 R1은 독립적으로 H, 할로겐,선택적으로 치환된 (C1-C8)알킬,선택적으로 치환된 (C2-C8)알케닐 또는 선택적으로 치환된 (C2-C8)알키닐이고;
각각의 R2는 독립적으로 할로겐 또는 OR11이고;
각각의 R5는 H이고;
각각의 R22는 OR11이고;
나머지 변수는 화학식 (Ia) 또는 (Ib) 또는 (II) 또는 (IIIa) 또는 (IIIb)에 대하여 정의된 바와 같다.
화학식 (XIV)의 화합물로부터 화학식 (XIIIa) 또는 화학식 (XIIIb)의 화합물을 제조하는 방법의 한 구체예에서, X1은 CR1O이다. 이 구체예의 또 다른 양태에서, R1O은 H이다. 이 구체예의 또 다른 양태에서, R10은 CH3이다. 이 구체예의 또 다른 양태에서, R1은 H이다. 이 구체예의 또 다른 양태에서 R1은 F이다. 이 구체예의 또 다른 양태에서, R1은 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, R1은 메틸이다. 이 구체예의 또 다른 양태에서 R1은 선택적으로 치환된 (C2-C8)알케닐이다. 이 구체예의 또 다른 양태에서 R1은 선택적으로 치환된 에테닐이다. 이 구체예의 또 다른 양태에서 R1은 선택적으로 치환된 (C2-C8)알키닐이다. 이 구체예의 또 다른 양태에서, R1은 선택적으로 치환된 에티닐이다. 이 구체예의 또 다른 양태에서, R2는 F이다. 이 구체예의 또 다른 양태에서, R2는 OH이다. 이 구체예의 또 다른 양태에서 R22는 OH이다. 이 구체예의 또 다른 양태에서, 각각의 R2 및 R22는 OH이다. 이 구체예의 또 다른 양태에서, 각각의 R2는 F이고 R22는 OH이다. 이 구체예의 또 다른 양태에서, R7은 H이다. 이 구체예의 또 다른 양태에서, R7은 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, R7은 (C2-C8)알키닐이다. 이 구체예의 또 다른 양태에서, R7은 CN이다. 이 구체예의 또 다른 양태에서, Rc 또는 Rd 중 하나는 H이다. 이 구체예의 또 다른 양태에서, Rc 또는 Rd 중 하나는 H이고 Rc 또는 Rd 중 다른 하나는 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, R6는 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, R4는 선택적으로 치환된 (C6-C20)아릴이다. 이 구체예의 또 다른 양태에서, Ar은 선택적으로 치환된 니트로페닐이다.
화학식 (XIV)의 화합물로부터 화학식 (XIIIa) 또는 화학식 (XIIIb)의 화합물을 제조하는 방법의 또 다른 구체예에서, X1은 CH이고, R1은 H 또는 CH3이고, Rc 또는 Rd 중 하나는 H이다. 이 구체예의 또 다른 양태에서, R2는 F이다. 이 구체예의 또 다른 양태에서, R2는 OH이다. 이 구체예의 또 다른 양태에서 R22는 OH이다. 이 구체예의 또 다른 양태에서, 각각의 R2 및 R22는 OH이다. 이 구체예의 또 다른 양태에서, 각각의 R2는 F이고 R22는 OH이다. 이 구체예의 또 다른 양태에서, R7은 H이다. 이 구체예의 또 다른 양태에서, R7은 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, R7은 CH3이다. 이 구체예의 또 다른 양태에서, R7은 (C2-C8)알키닐이다. 이 구체예의 또 다른 양태에서, R7은 에티닐이다. 이 구체예의 또 다른 양태에서, R7은 CN이다. 이 구체예의 또 다른 양태에서, Rc 또는 Rd 중 하나는 H이고 Rc 또는 Rd 중 다른 하나는 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, R6는 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, R4는 선택적으로 치환된 (C6-C20)아릴이다. 이 구체예의 또 다른 양태에서, Ar은 선택적으로 치환된 니트로페닐이다. 이 구체예의 또 다른 양태에서 R8는 NR11R12이다. 이 구체예의 또 다른 양태에서, R8는 OR11이다. 이 구체예의 또 다른 양태에서, R8는 NH2이다. 이 구체예의 또 다른 양태에서, R8는 OH이다.
화학식 (XIV)의 화합물로부터 화학식 (XIIIa) 또는 화학식 (XIIIb)의 화합물을 제조하는 방법의 또 다른 구체예에서, X1은 CH이고, R1은 H 또는 CH3이고, Rc 또는 Rd 중 하나는 H이고, R7은 H이다. 이 구체예의 또 다른 양태에서, R2는 F이다. 이 구체예의 또 다른 양태에서, R2는 OH이다. 이 구체예의 또 다른 양태에서 R22는 OH이다. 이 구체예의 또 다른 양태에서, 각각의 R2 및 R22는 OH이다. 이 구체예의 또 다른 양태에서, 각각의 R2는 F이고 R22는 OH이다. 이 구체예의 또 다른 양태에서, Rc 또는 Rd 중 하나는 H이고 Rc 또는 Rd 중 다른 하나는 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, Rc 또는 Rd 중 하나는 H이고 Rc 또는 Rd 중 다른 하나는 CH3이다. 이 구체예의 또 다른 양태에서, R6는 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, R4는 선택적으로 치환된 (C6-C20)아릴이다. 이 구체예의 또 다른 양태에서, R4는 선택적으로 치환된 페닐이다. 이 구체예의 또 다른 양태에서, Ar은 선택적으로 치환된 니트로페닐이다. 이 구체예의 또 다른 양태에서 R8는 NR11R12이다. 이 구체예의 또 다른 양태에서, R8는 OR11이다. 이 구체예의 또 다른 양태에서, R8는 NH2이다. 이 구체예의 또 다른 양태에서, R8는 OH이다.
화학식 (XIV)의 화합물로부터 화학식 (XIIIa) 또는 화학식 (XIIIb)의 화합물을 제조하는 방법의 한 구체예에서, X1은 CF이다. 이 구체예의 또 다른 양태에서, R1은 H이다. 이 구체예의 또 다른 양태에서, R1은 F이다. 이 구체예의 또 다른 양태에서, R1은 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, R1은 메틸이다. 이 구체예의 또 다른 양태에서, R1은 선택적으로 치환된 (C2-C8)알케닐이다. 이 구체예의 또 다른 양태에서, R1은 선택적으로 치환된 에테닐이다. 이 구체예의 또 다른 양태에서, R1은 선택적으로 치환된 (C2-C8)알키닐이다. 이 구체예의 또 다른 양태에서 R1은 선택적으로 치환된 에티닐이다. 이 구체예의 또 다른 양태에서, R2는 F이다. 이 구체예의 또 다른 양태에서, R2는 OH이다. 이 구체예의 또 다른 양태에서 R22는 OH이다. 이 구체예의 또 다른 양태에서, 각각의 R2 및 R22는 OH이다. 이 구체예의 또 다른 양태에서, 각각의 R2는 F이고 R22는 OH이다. 이 구체예의 또 다른 양태에서, R7은 H이다. 이 구체예의 또 다른 양태에서, R7은 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, R7은 선택적으로 치환된 (C2-C8)알키닐이다. 이 구체예의 또 다른 양태에서, R7은 CN이다. 이 구체예의 또 다른 양태에서 Rc 또는 Rd 중 하나는 H이다. 이 구체예의 또 다른 양태에서 Rc 또는 Rd 중 하나는 H이고 Rc 또는 Rd 중 다른 하나는 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, R6는 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, R4는 선택적으로 치환된 (C6-C20)아릴이다. 이 구체예의 또 다른 양태에서, Ar은 선택적으로 치환된 니트로페닐이다.
화학식 (XII)의 화합물로부터 화학식 (XIa) 또는 화학식 (XIb)의 화합물을 제조하는 방법의 또 다른 구체예에서, X1은 CF이고, R1은 H 또는 CH3이고, Rc 또는 Rd 중 하나는 H이다. 이 구체예의 또 다른 양태에서 R2는 F이다. 이 구체예의 또 다른 양태에서, R2는 OH이다. 이 구체예의 또 다른 양태에서 R22는 OH이다. 이 구체예의 또 다른 양태에서, 각각의 R2 및 R22는 OH이다. 이 구체예의 또 다른 양태에서, 각각의 R2는 F이고 R22는 OH이다. 이 구체예의 또 다른 양태에서, R7은 H이다. 이 구체예의 또 다른 양태에서, R7은 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, R7은 CH3이다. 이 구체예의 또 다른 양태에서, R7은 선택적으로 치환된 (C2-C8)알키닐이다. 이 구체예의 또 다른 양태에서, R7은 에티닐이다. 이 구체예의 또 다른 양태에서, R7은 CN이다. 이 구체예의 또 다른 양태에서, Rc 또는 Rd 중 하나는 H이고 Rc 또는 Rd 중 다른 하나는 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서 R6는 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, R4는 선택적으로 치환된 (C6-C20)아릴이다. 이 구체예의 또 다른 양태에서, Ar은 선택적으로 치환된 니트로페닐이다. 이 구체예의 또 다른 양태에서, R8는 NR11Rl2이다. 이 구체예의 또 다른 양태에서, R8는 OR11이다. 이 구체예의 또 다른 양태에서, R8는 NH2이다. 이 구체예의 또 다른 양태에서, R8는 OH이다.
화학식 (XIV)의 화합물로부터 화학식 (XIIIa) 또는 화학식 (XIIIb)의 화합물을 제조하는 방법의 또 다른 구체예에서, X1은 CF이고, R1은 H 또는 CH3이고, Rc 또는 Rd 중 하나는 H이고, R7은 H이다. 이 구체예의 또 다른 양태에서, R2는 F이다. 이 구체예의 또 다른 양태에서, R2는 OH이다. 이 구체예의 또 다른 양태에서 R22는 OH이다. 이 구체예의 또 다른 양태에서, 각각의 R2 및 R22는 OH이다. 이 구체예의 또 다른 양태에서 각각의 R2는 F이고 R22는 OH이다. 이 구체예의 또 다른 양태에서, Rc 또는 Rd 중 하나는 H이고 Rc 또는 Rd 중 다른 하나는 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, Rc 또는 Rd 중 하나는 H이고 Rc 또는 Rd 중 다른 하나는 CH3이다. 이 구체예의 또 다른 양태에서, R6는 선택적으로 치환된 (C1-C8)알킬이다. 이 구체예의 또 다른 양태에서, R4는 선택적으로 치환된 (C6-C20)아릴이다. 이 구체예의 또 다른 양태에서, R4는 선택적으로 치환된 페닐이다. 이 구체예의 또 다른 양태에서 Ar은 선택적으로 치환된 니트로페닐이다. 이 구체예의 또 다른 양태에서, R8는 NR11R12이다. 이 구체예의 또 다른 양태에서, R8는 OR11이다. 이 구체예의 또 다른 양태에서, R8는 NH2이다. 이 구체예의 또 다른 양태에서, R8는 OH이다.
정의
달리 명시되지 않으면, 본 명세서에서 사용된 다음의 용어 및 구절은 다음의 의미를 가지도록 의도된다:
상품명 (trade name)이 본 명세서에서 사용될 경우, 출원인은 독립적으로 상품명 제품 및 상품명 제품의 활성 약제학적 성분(들)을 포함하도록 의도한다. 본 명세서에서 사용된 "본 발명의 화합물" 또는 "화학식 (1)의 화합물"은 화학식 (1)의 화합물 또는 이의 약제학적으로 허용가능한 염을 의미한다. 유사하게, 단리가능한 중간체에 관해서, 구절 "화학식 (숫자)의 화합물"은 그 화학식의 화합물 및 이의 약제학적으로 허용가능한 염을 의미한다.
"알킬"은 노말, 이차, 삼차 또는 사이클릭 탄소 원자를 포함하는 탄화수소이다. 예를 들어, 알킬기는 1 내지 20 개의 탄소 원자(즉, C1-C20 알킬), 1 내지 8 개의 탄소 원자(즉, C1-C8 알킬), 또는 1 내지 6 개의 탄소 원자(즉, C1-C6 알킬)를 가질 수 있다. 적절한 알킬기의 예에는 메틸 (Me, -CH3), 에틸 (Et, -CH2CH3), 1-프로필 (n-Pr, n-프로필, -CH2CH2CH3), 2-프로필 (i-Pr, i-프로필, -CH(CH3)2), 1-부틸(n-Bu, n-부틸, -CH2CH2CH2CH3), 2-메틸-1-프로필 (i-Bu, i-부틸, -CH2CH(CH3)2), 2-부틸 (s-Bu, s-부틸, -CH(CH3)CH2CH3), 2-메틸-2-프로필 (t-Bu, t-부틸, -C(CH3)3), 1-펜틸(n-펜틸, -CH2CH2CH2CH2CH3), 2-펜틸 (-CH(CH3)CH2CH2CH3), 3-펜틸 (-CH(CH2CH3)2), 2-메틸-2-부틸 (-C(CH3)2CH2CH3), 3-메틸-2-부틸 (-CH(CH3)CH(CH3)2), 3-메틸-1-부틸 (-CH2CH2CH(CH3)2), 2-메틸-1-부틸 (-CH2CH(CH3)CH2CH3), 1-헥실 (-CH2CH2CH2CH2CH2CH3), 2-헥실 (-CH(CH3)CH2CH2CH2CH3), 3-헥실 (-CH(CH2CH3)(CH2CH2CH3)), 2-메틸-2-펜틸 (-C(CH3)2CH2CH2CH3), 3-메틸-2-펜틸 (-CH(CH3)CH(CH3)CH2CH3), 4-메틸-2-펜틸 (-CH(CH3)CH2CH(CH3)2), 3-메틸-3-펜틸 (-C(CH3)(CH2CH3)2), 2-메틸-3-펜틸 (-CH(CH2CH3)CH(CH3)2), 2,3-디메틸-2-부틸 (-C(CH3)2CH(CH3)2), 3,3-디메틸-2-부틸 (-CH(CH3)C(CH3)3, 및 옥틸 (-(CH2)7CH3)이 포함되지만 이에 제한되지 않는다.
"알콕시"는 위에서 정의한 알킬기가 산소 원자를 통하여 모 분자 (parent molecule)에 부착되는 화학식 -0-알킬을 가지는 그룹을 의미한다. 알콕시기의 알킬 부분은 1 내지 20 개의 탄소 원자(즉, C1-C20 알콕시), 1 내지 12 개의 탄소 원자(즉, C1-C12 알콕시), 또는 1 내지 6 개의 탄소 원자(즉, C1-C6 알콕시)를 가질 수 있다. 적절한 알콕시기의 예에는 메톡시 (-0-CH3 또는 -OMe), 에톡시 (-OCH2CH3 또는 -OEt), t-부톡시 (-0-C(CH3)3 또는 -OtBu) 등이 포함되지만 이에 제한되지 않는다.
"할로알킬"은 알킬기의 하나 이상의 수소 원자가 할로겐 원자로 대체된 위에서 정의한 알킬기이다. 할로알킬기의 알킬 부분은 1 내지 20 개의 탄소 원자(즉, C1-C20 할로알킬), 1 내지 12 개의 탄소 원자(즉, C1-C12 할로알킬), 또는 1 내지 6 개의 탄소 원자(즉, C1-C6 알킬)를 가질 수 있다. 적절한 할로알킬기의 예에는 -CF3, -CHF2, -CFH2, -CH2CF3 등이 포함되지만 이에 제한되지 않는다.
"알케닐"은 최소 하나의 불포화 부위, 즉 탄소-탄소, sp 2 이중 결합을 가지는 노말, 이차, 삼차 또는 사이클릭 탄소 원자 보유 탄화수소이다. 예를 들어, 알케닐기는 2 내지 20 개의 탄소 원자(즉, C2-C20 알케닐), 2 내지 8 개의 탄소 원자(즉, C2-C8 알케닐), 또는 2 내지 6 개의 탄소 원자(즉, C2-C6 알케닐)를 가질 수 있다. 적절한 알케닐기의 예에는 에틸렌 또는 비닐(-CH=CH2), 알릴(-CH2CH=CH2), 사이클로펜테닐(-C5H7), 및 5 헥세닐(-CH2CH2CH2CH2CH=CH2)이 포함되지만 이에 제한되지 않는다.
"알키닐"은 최소 하나의 불포화 부위, 즉 탄소-탄소, sp 삼중 결합을 가지는 노말, 이차, 삼차 또는 사이클릭 탄소 원자 보유 탄화수소이다. 예를 들어, 알키닐기는 2 내지 20 개의 탄소 원자(즉, C2-C20 알키닐), 2 내지 8 개의 탄소 원자(즉, C2-C8 알킨), 또는 2 내지 6 개의 탄소 원자(즉, C2-C6 알키닐)를 가질 수 있다. 적절한 알키닐기의 예에는 아세틸레닉 (-C≡CH), 프로파길 (-CH2C≡CH) 등이 포함되지만 이에 제한되지 않는다.
"알킬렌"은 모 알칸의 동일하거나 두 개의 상이한 탄소 원자로부터 두 개의 수소 원자를 제거하여 유도된 두 개의 1가(monovalent) 라디칼 중심을 가지는, 포화된 분지 또는 직선의 사슬 또는 사이클릭 탄화수소 라디칼을 지칭한다. 예를 들어, 알킬렌기는 l 내지 20 개의 탄소 원자, 1 내지 10 개의 탄소 원자,또는 1 내지 6 개의 탄소 원자를 가질 수 있다. 전형적인 알킬렌 라디칼에는 메틸렌 (-CH2-), 1,1-에틸 (-CH(CH3)-), 1,2-에틸 (-CH2CH2-), 1,1-프로필 (-CH(CH2CH3)-), 1,2-프로필 (-CH2CH(CH3)-), 1,3-프로필 (-CH2CH2CH2-), 1,4-부틸 (-CH2CH2CH2CH2-) 등이 포함되지만 이에 제한되지 않는다.
"알케닐렌"은 모 알켄의 동일하거나 두 개의 상이한 탄소 원자로부터 두 개의 수소 원자를 제거하여 유도된 두 개의 l가 라디칼 중심을 가지는, 불포화된 분지 또는 직선의, 사슬 또는 사이클릭 탄화수소 라디칼을 지칭한다. 예를 들어, 알케닐렌기는 1 내지 20 개의 탄소 원자, 1 내지 10 개의 탄소 원자,또는 1 내지 6 개의 탄소 원자를 가질 수 있다. 전형적인 알케닐렌 라디칼에는 1,2-에틸렌 (-CH=CH-) 이 포함되지만 이에 제한되지 않는다.
"알카닐렌"은 모 알킨의 동일하거나 두 개의 상이한 탄소 원자로부터 두 개의 수소 원자를 제거하여 유도된 두 개의 1가 라디칼 중심을 가지는, 불포화된 분지 또는 직선의, 사슬 또는 사이클릭 탄화수소 라디칼을 지칭한다. 예를 들어, 알키닐렌기는 1 내지 20 개의 탄소 원자, 1 내지 10 개의 탄소 원자,또는 1 내지 6 개의 탄소 원자를 가질 수 있다. 전형적인 알키닐렌 라디칼에는 아세틸렌 (-C≡C-), 프로파길 (-CH2C≡C-), 및 4-펜티닐 (-CH2CH2CH2C≡C-)이 포함되지만 이에 제한되지 않는다.
"아미노"는 일반적으로, 화학식 -N(X)2를 가지는, 암모니아의 유도체로 간주될 수 있는 질소 라디칼을 지칭하고, 여기서 각각의 "X"는 독립적으로 H, 치환된 또는 치환되지 않은 알킬, 치환되거나 치환되지 않은 알킬, 카르보사이클릴, 치환되거나 치환되지 않은 헤테로사이클릴 등이다. 질소의 혼성화(hybridization)는 대략적으로 sp3이다. 아미노의 비제한적 유형에는 -NH2, -N(알킬)2, -NH(알킬), -N(카르보사이클릴)2, -NH(카르보사이클릴), -N(헤테로사이클릴)2, -NH(헤테로사이클릴), -N(아릴)2, -NH(아릴), -N(알킬)(아릴), -N(알킬)(헤테로사이클릴), -N(카르보사이클릴)(헤테로사이클릴), -N(아릴)(헤테로아릴), -N(알킬)(헤테로아릴) 등이 포함된다. 용어 "알킬아미노"는 최소 하나의 알킬기로 치환된 아미노기를 지칭한다. 아미노기의 비제한적 예에는 -NH2, -NH(CH3), -N(CH3)2, -NH(CH2CH3), - N(CH2CH3)2, -NH(페닐), -N(페닐)2, -NH(벤질), -N(벤질)2 등이 포함된다. 치환된 알킬아미노는 일반적으로, 최소 하나의 본 명세서에서 정의한 치환된 알킬이 아미노 질소 원자에 부착된 위에서 정의한 알킬아미노기를 지칭한다. 치환된 알킬아미노의 비제한적 예에는 -NH(알킬렌-C(O)-OH), -NH(알킬렌-C(O)-O-알킬), -N(알킬렌-C(O)-OH)2, -N(알킬렌-C(O)-O-알킬)2 등이 포함된다.
"아릴"은 모 방향족 고리 시스템의 단일 탄소 원자로부터 하나의 수소 원자를 제거하여 유도된 방향족 탄화수소 라디칼을 의미한다. 예를 들어, 아릴기는 6 내지 20 개의 탄소 원자, 6 내지 14개의 탄소 원자, 또는 6 내지 10개의 탄소 원자를 가질 수 있다. 전형적인 아릴기에는 벤젠으로부터 유도된 라디칼(예를 들어, 페닐), 치환된 벤젠, 나프탈렌, 안트라센, 바이페닐 등이 포함되지만 이에 제한되지 않는다.
"아릴알킬"은 탄소 원자, 전형적으로 말단 또는 sp3 탄소 원자에 결합된 수소 원자 중 하나가 아릴 라디칼로 대체된 사이클릭 알킬 라디칼을 지칭한다. 전형적인 아릴알킬기에는 벤질, 2-페닐에탄-1일, 나프틸메틸, 2-나프틸에탄-1-일, 나프토벤질, 2-나프토페닐에탄-1-일 등이 포함되지만 이에 제한되지 않는다. 아릴알킬기는 7 내지 20개의 탄소 원자를 포함할 수 있고, 예를 들어, 알킬 모이어티는 1 내지 6 개의 탄소 원자이고 아릴 모이어티는 6 내지 14개의 탄소 원자이다.
"아릴알케닐"은 탄소 원자, 전형적으로 말단 또는 sp3 탄소 원자, 그러나 또한 sp2 탄소 원자에 결합된 수소 원자 중 하나가 아릴 라디칼로 대체된 사이클릭 알케닐 라디칼을 지칭한다. 아릴알케닐의 아릴 부분은, 예를 들어, 본 명세서에 개시된 임의의 아릴기를 포함할 수 있고, 아릴알케닐의 알케닐 부분은, 예를 들어, 본 명세서에 개시된 임의의 알케닐기를 포함할 수 있다. 아릴알케닐기는 8 내지 20 개의 탄소 원자를 포함할 수 있고, 예를 들어, 알케닐 모이어티는 2 내지 6 개의 탄소 원자이고 아릴 모이어티는 6 내지 14 개의 탄소 원자이다.
"아릴알키닐"은 탄소 원자, 전형적으로 말단 또는 sp3 탄소 원자, 그러나 또한 sp 탄소 원자에 결합된 수소 원자 중 하나가 아릴 라디칼로 대체된 사이클릭 알키닐 라디칼을 지칭한다. 아릴알키닐의 아릴 부분은, 예를 들어, 본 명세서에 개시된 임의의 아릴기를 포함할 수 있고, 아릴알키닐의 알키닐 부분은, 예를 들어, 본 명세서에 개시된 임의의 알키닐기를 포함할 수 있다. 아릴알키닐기는 8 내지 20 개의 탄소 원자를 포함할 수 있고, 예를 들어, 알키닐 모이어티는 2 내지 6 개의 탄소 원자이고 아릴 모이어티는 6 내지 14 개의 탄소 원자이다.
알킬, 알킬렌, 아릴, 아릴알킬, 알콕시, 헤테로사이클릴, 헤테로아릴, 카르보사이클릴 등과 관련하여, 용어 "치환된", 예를 들어, "치환된 알킬", "치환된 알킬렌", "치환된 아릴", "치환된 아릴알킬", "치환된 헤테로사이클릴", 및 "치환된 카르보사이클릴"은, 달리 언급되지 않으면, 하나 이상의 수소 원자가 각각 독립적으로 비-수소 치환기로 대체된 알킬, 알킬렌, 아릴, 아릴알킬, 헤테로사이클릴, 카르보사이클릴을 각각 의미한다. 전형적인 치환기에는 -X, -Rb, -O, =O, -ORb, -SRb, -S-, -NRb 2, -N+Rb 3, =NRb, -CX3, -CN, -OCN, -SCN, -N=C=O, -NCS, -NO, -NO2, =N2, -N3, -NHC(=O)Rb, -OC(=O)Rb, -NHC(=O)NRb 2, -S(=O)2-, -S(=O)2OH, -S(=O)2Rb, -OS(=O)2ORb, -S(=O)2NRb 2, -S(=O)Rb, -OP(=O)(ORb)2, -P(=O)(ORb)2, -P(=O)(O-)2, -P(=O)(OH)2, -P(O)(ORb)(O-), -C(=O)Rb, -C(=O)X, -C(S)Rb, -C(O)ORb, -C(O)O-, -C(S)ORb, -C(O)SRb, -C(S)SRb, -C(O)NRb 2, -C(S)NRb 2, -C(=NRb)NRb 2가 포함되지만 이에 제한되지 않고, 여기서 각각의 X는 독립적으로 할로겐 : F, Cl, Br, 또는 I이고; 각각의 Rb는 독립적으로 H, 알킬, 아릴, 아릴알킬, 헤테로사이클, 또는 보호기 또는 전구약물 모이어티이다. 알킬렌 알케닐렌 및 알키닐렌기가 또한 유사하게 치환될 수 있다. 달리 명시되지 않으면 용어 "치환된"이 치환 가능한 둘 이상의 모이어티를 가지는 아릴알킬과 같은 그룹과 연계하여 사용될 경우, 치환기는 아릴 모이어티, 알킬 모이어티, 또는 두 가지 모두에 부착될 수 있다.
본 명세서에서 사용된 용어 "전구약물"은 생물학적 시스템에 투여될 때 자발적 화학 반응(들), 효소 촉매화된 화학 반응(들), 광분해, 및/또는 대사적 화학 반응(들)의 결과로서 약물 물질, 즉, 활성 성분을 생성하는 임의의 화합물을 지칭한다. 전구약물은 따라서 치료적으로 활성인 화합물의 잠재적 형태 또는 공유적으로 변형된 유사체이다.
당업자는 화학식 (I-XIV)의 화합물의 치환기 및 다른 모이어티가 만족스럽게 안정한 약제학적 조성물로 제제화될 수 있는 약제학적으로 유용한 화합물을 제공하기에 충분히 안정한 화합물을 제공하기 위하여 선택되어야 함을 인지할 것이다. 이러한 안정성을 가지는 화학식 (I-XIV)의 화합물은 본 발명의 범위 내에 있는 것으로 생각된다.
"헤테로알킬"은 하나 이상의 탄소 원자가 0, N 또는 S와 같은 헤테로 원자로 대체된 알킬기를 지칭한다. 예를 들어 만약 모 분자에 부착된 알킬기의 탄소 원자가 헤테로원자(예를 들어, 0, N, 또는 S)로 대체되면, 결과적인 헤테로알킬기는, 각각, 알콕시기(예를 들어, -OCH3 등), 아민(예를 들어, -NHCH3,-N(CH3)2 등), 또는 티오알킬기(예를 들어, -SCH3)이다. 만약 모 분자에 부착되지 않은 알킬기의 비-말단 탄소 원자가 헤테로원자(예를 들어, 0, N, 또는 S)로 대체되면, 결과적인 헤테로알킬기는, 각각, 알킬 에테르(예를 들어, -CH2CH2-0-CH3 등), 알킬 아민(예를 들어, -CH2NHCH3, -CH2N(CH3)2 등), 또는 티오알킬 에테르(예를 들어, -CH2-S-CH3) 이다. 만약 알킬기의 말단 탄소 원자가 헤테로원자(예를 들어, 0, N, 또는 S)로 대체되면, 결과적인 헤테로알킬기는 각각 하이드록시알킬기(예를 들어, -CH2CH2-OH), 아미노알킬기(예를 들어, -CH2NH2), 알킬 티올기(예를 들어, -CH2-CH2-SH)이다. 헤테로알킬기는, 예를 들어, 1 내지 20 개의 탄소 원자, 1 내지 10 개의 탄소 원자,또는 l 내지 6 개의 탄소 원자를 가질 수 있다. C1-C6 헤테로알킬기는 1 내지 6 개의 탄소 원자를 가지는 헤테로알킬기를 의미한다.
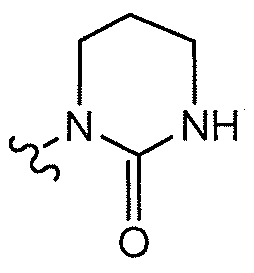
본 명세서에서 사용된 "헤테로사이클" 또는 "헤테로사이클릴"에는 예로서 Paquette, Leo A.; Principles of Modern Heterocyclic Chemistry (W.A. Benjamin, New York, 1968), 특히 챕터 1, 3, 4, 6, 7, 및 9; The Chemistry of Heterocyclic Compounds, A Series of Monographs” (John Wiley & Sons, New York, 1950년부터 현재까지), 특히 13, 14, 16, 19, 및 28권; 및 J. Am. Chem. Soc. (1960) 82:5566에 기재된 헤테로사이클이 포함되지만 이에 제한되지 않는다. 본 발명의 한 특정 구체예에서 "헤테로사이클"은 하나 이상의 (예를 들어 1, 2, 3, 또는 4) 탄소 원자가 헤테로원자(예를 들어 O, N, 또는 S)로 대체된 본 명세서에서 정의한 "카르보사이클"을 포함한다. 용어 "헤테로사이클" 또는 "헤테로사이클릴"은 포화 고리, 부분적 불포화 고리, 및 방향족 고리(즉, 헤테로방향족 고리)를 포함한다. 치환된 헤테로사이클릴에는, 예를 들어, 카르보닐기를 포함하여 본 명세서에 개시된 임의의 치환기로 치환된 헤테로사이클릭 고리가 포함된다. 카르보닐 치환된 헤테로사이클릴의 비제한적 예는:
이다.
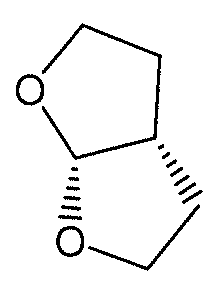
헤테로사이클의 예에는, 제한이 아니고 예로서, 피리딜, 디하이드로이피리딜, 테트라하이드로피리딜(피페리딜), 티아졸릴, 테트라하이드로티오페닐, 황산화(sulfur oxidized) 테트라하이드로티오페닐, 피리미디닐, 퓨라닐, 티에닐, 피롤릴, 피라졸릴, 이미다졸릴, 테트라졸릴, 벤조퓨라닐, 티아나프탈레닐, 인돌릴, 인돌레닐, 퀴놀리닐, 이소퀴놀리닐, 벤즈이미다졸릴, 피페리디닐, 4-피페리도닐, 피롤리디닐, 2-피롤리디닐, 피롤리닐, 테트라하이드로퓨라닐, 테트라하이드로퀴놀리닐, 테트라하이드로이소퀴놀리닐, 데카하이드로퀴놀리닐, 옥타하이드로이소퀴놀리닐, 아조시닐, 트라아지닐, 6H-1,2,5-티아디아지닐, 2H,6H-1,5,2-디티아지닐, 티에닐, 티안트레닐, 피라닐, 이소벤조퓨라닐, 크로메닐, 잔테닐, 페녹사티닐, 2H-피롤릴, 이소티아졸릴, 이속사졸릴, 피라지닐, 피리다지닐, 인돌리지닐, 이소인돌릴, 3H-인돌릴, 1H-인다졸리, 퓨리닐, 4H-퀴놀리지닐, 프탈라지닐, 나프티리디닐, 퀴녹살리닐, 퀴나졸리닐, 신놀리닐, 프테리디닐, 4aH-카르바졸릴, 카르바졸릴, β-카르볼리닐, 페난트리디닐, 아크리디닐, 피리미디닐, 페난트롤리닐, 페나지닐, 페노티아지닐, 퓨라자닐, 페녹사지닐, 이소크로마닐, 크로마닐, 이미다졸리디닐, 이미다졸리닐, 피라졸리디닐, 피라졸리닐, 피페라지닐, 인돌리닐, 이소인돌리닐, 퀴누클리디닐, 모르폴리닐, 옥사졸리디닐, 벤조트리아졸릴, 벤즈이속사졸릴, 옥신돌릴, 벤족사졸리닐, 이사티노일, 및 비스-테트라하이드로퓨라닐:
이 포함된다.
제한이 아니고 예로서, 탄소 결합된 헤테로사이클은 피리딘의 2, 3, 4, 5, 또는 6 위치, 피리다진의 3, 4, 5, 또는 6 위치, 피리미딘의 2, 4, 5, 또는 6 위치, 피라진의 2, 3, 5, 또는 6 위치, 퓨란, 테트라하이드로퓨란, 티오퓨란, 티오펜, 피롤 또는 테트라하이드로피롤의 2, 3, 4, 또는 5 위치, 옥사졸, 이미다졸 또는 티아졸의 2, 4, 또는 5 위치, 이속사졸, 피라졸, 또는 이소티아졸의 3, 4, 또는 5 위치, 아지리딘의 2 또는 3 위치, 아제티딘의 2, 3, 또는 4 위치, 퀴놀린의 2, 3, 4, 5, 6, 7, 또는 8 위치 또는 이소퀴놀린의 1, 3, 4, 5, 6, 7, 또는 8 위치에서 결합된다. 더욱 더 전형적으로, 탄소 결합된 헤테로사이클에는 2-피리딜, 3-피리딜, 4-피리딜, 5-피리딜, 6-피리딜, 3-피리다지닐, 4-피리다지닐, 5-피리다지닐, 6-피리다지닐, 2-피리미디닐, 4-피리미디닐, 5 피리미디닐, 6-피리미디닐, 2-피라지닐, 3-피라지닐, 5-피라지닐, 6-피라지닐, 2-티아졸릴, 4-티아졸릴, 또는 5-티아졸릴이 포함된다.
제한이 아니고 예로서, 질소 결합된 헤테로사이클은 아지리딘, 아제티딘, 피롤, 피롤리딘, 2-피롤린, 3-피롤린, 이미다졸, 이미다졸리딘, 2-이미다졸린, 3-이미다졸린, 피라졸, 피라졸린, 2-피라졸린, 3-피라졸린, 피페리딘, 피페라진, 인돌, 인돌린, 1H-인다졸의 위치 1, 이소인돌, 또는 이소인돌린의 2 위치, 모르폴린의 4 위치, 및 카르바졸, 또는 β-카르볼린의 9 위치에서 결합된다. 더욱 더 전형적으로, 질소 결합된 헤테로사이클에는 1-아지리딜, 1-아제테딜, 1-피롤릴, 1-이미다졸릴, 1-피라졸릴, 및 1-피페리디닐이 포함된다.
"헤테로사이클릴알킬"은 탄소 원자, 전형적으로 말단 또는 sp3 탄소 원자에 결합된 수소 원자 중 하나가 헤테로사이클릴 라디칼(즉, 헤테로사이클릴-알킬렌-모이어티)로 대체된 사이클릭 알킬 라디칼을 지칭한다. 전형적인 헤테로사이클릴 알킬기에는 헤테로사이클릴-CH2-, 2-(헤테로사이클릴)에탄-1-일 등이 포함되지만 이에 제한되지 않고, 여기서 "헤테로사이클릴" 부분은 Principles of Modern Heterocyclic Chemistry에 기재된 것을 포함하여 위에 기재된 임의의 헤테로사이클릴기를 포함한다. 당업자는 또한 생성된 그룹이 화학적으로 안정하다는 조건하에, 헤테로사이클릴기가 탄소-탄소 결합 또는 탄소-헤테로원자 결합에 의하여 헤테로사이클릴 알킬의 알킬 부분에 부착될 수 있음을 이해할 것이다. 헤테로사이클릴 알킬기는 3 내지 20개의 탄소 원자를 포함하고, 예를 들어, 아릴알킬기의 알킬 부분은 1 내지 6개의 탄소 원자이고 헤테로사이클릴 모이어티는 2 내지 14개의 탄소 원자이다. 헤테로사이클릴알킬의 예에는 제한이 아니고 예로서 티아졸릴메틸, 2-티아졸릴에탄-1-일, 이미다졸릴메틸, 옥사졸릴메틸, 티아디아졸릴메틸 등과 같은 5-원 황, 산소, 및/또는 질소 보유 헤테로사이클, 피페리디닐메틸, 피페라지닐메틸, 모르폴리닐메틸, 피리디닐메틸, 피리디질메틸, 피리미딜메틸, 피라지닐메틸 등과 같은 6원 황, 산소, 및/또는 질소 보유 헤테로사이클이 포함된다.
"헤테로사이클릴알케닐"은 탄소 원자, 전형적으로 말단 또는 sp3 탄소 원자, 그러나 또한 sp2 탄소 원자에 결합된 수소 원자 중 하나가 헤테로사이클릴 라디칼로 대체된(즉, 헤테로사이클릴-알케닐렌-모이어티) 사이클릭 알케닐 라디칼을 지칭한다. 헤테로사이클릴 알케닐기의 헤테로사이클릴 부분은 Principles of Modern Heterocyclic Chemistry에 기재된 것을 포함하여 본 명세서에 기재된 임의의 헤테로사이클릴기를 포함하고, 헤테로사이클릴 알케닐기의 알케닐 부분은 본 명세서에 개시된 임의의 알케닐기를 포함한다. 당업자는 또한 생성된 그룹이 화학적으로 안정하다는 조건하에, 헤테로사이클릴기가 탄소-탄소 결합 또는 탄소-헤테로원자 결합에 의하여 헤테로사이클릴 알케닐의 알케닐 부분에 부착될 수 있음을 이해할 것이다. 헤테로사이클릴 알케닐기는 4 내지 20개의 탄소 원자를 포함하고, 예를 들어, 헤테로사이클릴 알케닐기의 알케닐 부분은 2 내지 6개의 탄소 원자이고 헤테로사이클릴 모이어티는 2 내지 14개의 탄소 원자이다.
"헤테로사이클릴알키닐"은 탄소 원자, 전형적으로 말단 또는 sp3 탄소 원자, 그러나 또한 sp 탄소 원자에 결합된 수소 원자 중 하나가 헤테로사이클릴 라디칼로 대체된(즉, 헤테로사이클릴-알키닐렌-모이어티) 사이클릭 알키닐 라디칼을 지칭한다. 헤테로사이클릴 알키닐기의 헤테로사이클릴 부분은 Principles of Modern Heterocyclic Chemistry에 기재된 것을 포함하여 본 명세서에 기재된 임의의 헤테로사이클릴기를 포함하고, 헤테로사이클릴 알키닐기의 알키닐 부분은 본 명세서에 개시된 임의의 알키닐기를 포함한다. 당업자는 또한 생성된 그룹이 화학적으로 안정하다는 조건하에, 헤테로사이클릴기가 탄소-탄소 결합 또는 탄소-헤테로원자 결합에 의하여 헤테로사이클릴 알키닐의 알키닐 부분에 부착될 수 있음을 이해할 것이다. 헤테로사이클릴 알키닐기는 4 내지 20개의 탄소 원자를 포함하고, 예를 들어, 헤테로사이클릴 알키닐기의 알키닐 부분은 2 내지 6개의 탄소 원자이고 헤테로사이클릴 모이어티는 2 내지 14개의 탄소 원자이다.
"헤테로아릴"은 고리에 최소 하나의 헤테로원자를 가지는 방향족 헤테로사이클릴을 지칭한다. 방향족 고리에 포함될 수 있는 적절한 헤테로원자의 비제한적인 예에는 산소, 황 및 질소가 포함된다. 헤테로아릴 고리의 비제한적 예에는 피리디닐, 피롤릴, 옥사졸릴, 인돌릴, 이소인돌릴, 퓨리닐, 퓨라닐, 티에닐, 벤조퓨라닐, 벤조티오페닐, 카르바졸릴, 이미다졸릴, 티아졸릴, 이속사졸릴, 피라졸릴, 이소티아졸릴, 퀴놀릴, 이소퀴놀릴, 피리다질, 피리미딜, 피라질 등을 포함하여 "헤테로사이클릴"의 정의에 나열된 모든 방향족 고리가 포함된다.
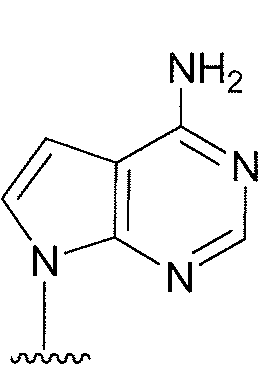
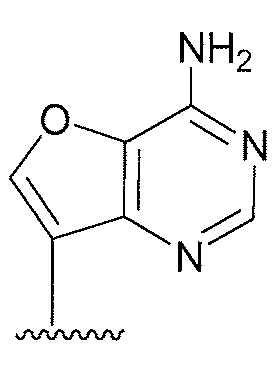
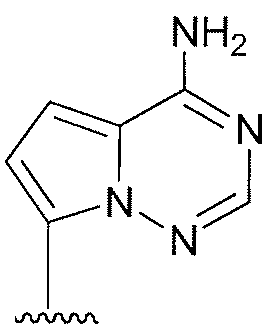
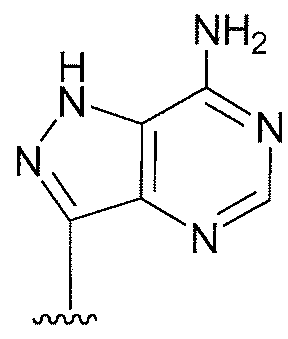
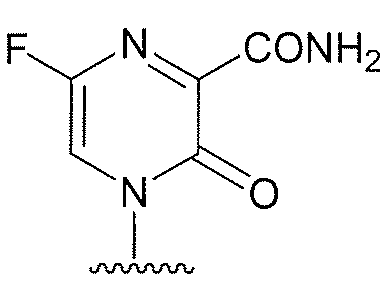
용어 "퓨린" 또는 "피리미딘" 염기에는 아데닌, N6-알킬퓨린, N6-아실퓨린(여기서 아실은 C(O)(알킬, 아릴, 알킬아릴, 또는 아릴알킬), N6-벤질퓨린, N6-할로퓨린, N6-비닐퓨린, N6-아세틸레닉 퓨린, N6-아실 퓨린, N6-히드록시알킬 퓨린, N6-알릴아미노퓨린, N6-티오알릴 퓨린, N2-알킬퓨린, N2-알킬-6-티오퓨린, 타이민, 사이토신, 5-플루오로사이토신, 5-메틸사이토신, 6-아자사이토신을 포함하여 6-아자피리미딘, 2- 및/또는 4-메르캅토피르미딘, 우라실, 5-플루오로우라실을 포함하여 5-할로우라실, C5-알킬피리미딘, C5-벤질피리미딘, C5-할로피리미딘, C5-비닐피리미딘, C5-아세틸레닉 피리미딘, C5-아실 피리미딘, C5-히드록시알킬 퓨린, C5-아미도피리미딘, C5-시아노피리미딘, C5-5-아이오도피리미딘, C6-아이오도-피리미딘, C5-Br-비닐 피리미딘, C6-Br-비닐 피리미딘, C5-니트로피리미딘, C5-아미노-피리미딘, N2-알킬퓨린, N2-알킬-6-티오퓨린, 5-아자시티디닐, 5-아자우라실릴, 트리아졸로피리디닐, 이미다졸로피리디닐, 피롤로피리미디닐, 및 피라졸로피리미디닐이 포함되지만 이에 제한되지 않는다. 퓨린 염기에는 구아닌, 아데닌, 하이포잔틴, 2,6-디아미노퓨린, 및 6-클로로퓨린이 포함되지만, 이에 제한되지 않는다. 추가적인 비전통적 퓨린 염기에는 피롤로[1,2-f][1,2,4]트리아진, 이미다조[1,5-f][1,2,4]트리아진, 이미다조[1,2-f][1,2,4]트리아진, 및 [1,2,4]트리아졸로[4,3-f][1,2,4]트리아진이 포함되고, 이들 모두는 선택적으로 치환된다. 화학식 (II)의 퓨린 및 피리미딘 염기는 염기의 질소 원자 또는 탄소 원자를 통하여 리보오스 당, 또는 이의 유사체에 연결된다. 염기상의 작용성(functional) 산소 및 질소 그룹은 필요하거나 바람직한 대로 보호될 수 있다. 적절한 보호기는 당업자에게 공지이고 트리메틸실릴, 디메틸헥실실릴, t-부틸디메틸실릴, 및 t-부틸디페닐실릴, 트리틸, 알킬기, 및 아세틸 및 프로피오닐과 같은 아실기, 메탄설포닐, 및 p-톨루엔설포닐을 포함하지만 이에 제한되지 않는다.
"카르보사이클" 또는 "카르보사이클릴"은 모노사이클로서 3 내지 7 개의 탄소 원자를 가지고, 바이사이클로서 7 내지 12 개의 탄소 원자를 가지고, 폴리사이클로서 최대 약 20 개의 탄소 원자를 가지는 포화 (즉, 사이클로알킬), 부분적 불포화 (예를 들어, 사이클로아케닐, 사이클로알카디에닐 등) 또는 방향족 고리를 지칭한다. 모노사이클릭 카르보사이클은 3 내지 7 개의 고리 원자,더욱더 전형적으로 5 또는 6 개의 고리 원자를 가진다. 바이사이클릭 카르보사이클은, 예를 들어, 바이사이클로 [4,5], [5,5], [5,6] 또는 [6,6] 시스템으로서 배열된 7 내지 12 개의 고리 원자, 또는 바이사이클로 [5,6] 또는 [6,6] 시스템 또는 스피로-융합된 (Spiro-fused) 고리로서 배열된 9 또는 10 개의 고리 원자를 가진다. 모노사이클릭 카르보사이클의 비제한적 예에는 사이클로프로필, 사이클로부틸, 사이클로펜틸, 1-사이클로펜트-1-에닐, 1-사이클로펜트-2-에닐, 1-사이클로펜트-3-에닐, 사이클로헥실, 1-사이클로헥스-1-에닐, 1-사이클로헥스-2-에닐, 1-사이클로헥스-3-에닐, 및 페닐이 포함된다. 바이사이클로 카르보사이클의 비제한적 예에는 나프틸, 테트라하이드로나프탈렌, 및 데칼린이 포함된다.
"카르보사이클릴알킬"은 탄소 원자에 결합된 수소 원자 중 하나가 본 명세서에 기재된 카르보사이클릴 라디칼로 대체되는 사이클릭 알킬 라디칼을 지칭한다. 전형적이지만 비제한적인 카르보사이클릴알킬기의 예에는 사이클로프로필메틸, 사이클로프로필에틸, 사이클로부틸메틸, 사이클로펜틸메틸 및 사이클로헥실메틸이 포함된다.
"아릴헤테로알킬"은 (탄소 원자 또는 헤테로원자에 부착될 수 있는) 수소 원자가 본 명세서에 정의된 아릴기로 대체된 본 명세서에 정의된 헤테로알킬을 지칭한다. 아릴기는 생성된 아릴헤테로알킬기가 화학적으로 안정한 모이어티를 제공한다는 조건하에, 헤테로알킬기의 탄소 원자, 또는 헤테로알킬기의 헤테로원자에 결합될 수 있다. 예를 들어, 아릴헤테로알킬기는 일반식 -알킬렌-O 아릴-, -알킬렌-O-알킬렌-아릴, -알킬렌-NH-아릴, -알킬렌-NH-알킬렌-아릴, -알킬렌-S-아릴, -알킬렌-S-알킬렌-아릴 등을 가질 수 있다. 더욱이, 상기 일반식에서 임의의 알킬렌 모이어티는 본 명세서에서 정의되거나 예시된 임의의 치환기로 더욱 치환될 수 있다.
"헤테로아릴알킬"은 수소 원자가 본 명세서에 정의된 헤테로아릴기로 대체된 본 명세서에 정의된 알킬기를 지칭한다. 헤테로아릴 알킬의 비제한적인 예에는 -CH2-피리디닐, -CH2-피롤릴, -CH2-옥사졸릴, -CH2-인돌릴, -CH2-이소인돌릴, -CH2-퓨리닐, -CH2-퓨라닐, -CH2-티에닐, -CH2-벤조퓨라닐, -CH2-벤조티오페닐, -CH2-카르바졸릴, -CH2-이미다졸릴, -CH2-티아졸릴, -CH2-이속사졸릴, -CH2-피라졸릴, CH2-이소티아졸릴, -CH2-퀴놀릴, -CH2-이소퀴놀릴, -CH2-피리다질, -CH2-피리미딜, -CH2-피라질, -CH(CH3)-피리디닐, -CH(CH3)-피롤릴, -CH(CH3)-옥사졸릴, -CH(CH3)-인돌릴, -CH(CH3)-이소인돌릴, -CH(CH3)-퓨리닐, -CH(CH3)-퓨라닐, -CH(CH3)-티에닐, -CH(CH3)-벤조퓨라닐, -CH(CH3)-벤조티오페닐, -CH(CH3)-카르바졸릴, -CH(CH3)-이미다졸릴, -CH(CH3)-티아졸릴, -CH(CH3)-이속사졸릴, -CH(CH3)- 피라졸릴, -CH(CH3)-이소티아졸릴, -CH(CH3)-퀴놀릴, -CH(CH3)-이소퀴놀릴, -CH(CH3)-피리다질, -CH(CH3)-피리미딜, -CH(CH3)-피라질 등이 포함된다.
용어 "선택적으로 치환된"은, 화학식 (I-XIV)의 화합물의 특정 모이어티(예를 들어, 선택적으로 치환된 아릴기)에 관하여, 모든 치환기가 수소이거나 모이어티의 하나 이상의 수소가 "치환된"의 정의하에 나열된 것과 같은 치환기에 의하여 대체될 수 있는 모이어티를 지칭한다.
용어 "선택적으로 대체된"은, 화학식 (I-XIV)의 화합물의 특정 모이어티에 관하여 (예를 들어, 상기 (C1-C8)알킬의 하나 이상의 메틸렌기가 0, 1, 2, 또는 그 이상의 명시된 그룹(예를 들어 -O-, -S-, 또는 -NRa-)에 의하여 대체될 수 있음을 의미한다.
용어 "비-말단 탄소 원자(들)"은 알킬, 알케닐, 알키닐, 알킬렌, 알케닐렌, 또는 알키닐렌 모이어티에 관하여, 모이어티의 첫 번째 탄소 원자와 모이어티의 마지막 탄소 원자 사이에 개재된 모이어티의 탄소 원자를 지칭한다. 그러므로, 제한이 아니고 예로서, 알킬 모이어티 -CH2(C*)H2(C*)H2CH3 또는 알킬렌 모이어티 -CH2(C*)H2(C*)H2CH2-에서 C* 원자가 비-말단 탄소 원자로 간주될 것이다.
"링커" 또는 "링크"는 공유 결합 또는 원자의 사슬을 포함하는 화학적 모이어티를 의미한다. 링커에는 알킬옥시(예를 들어 폴리에틸렌옥시, PEG, 폴리메틸렌옥시) 및 알킬아미노 (예를 들어 폴리에틸렌아미노, JeffamineTM); 및 이산(diacid) 에스테르 및 석시네이트, 석신아미드, 디글리콜레이트, 말로네이트, 및 카프로아미드를 포함하는 아미드의 반복 단위가 포함된다.
"산소-연결된", "질소-연결된", "탄소-연결된", "황-연결된", 또는 "인-연결된"과 같은 용어는 만약 두 모이어티 사이의 결합이 모이어티 중의 하나 초과의 유형의 원자를 이용하여 형성될 수 있을 경우, 모이어티 사이에 형성된 결합이 명시된 원자를 통함을 의미한다. 예를 들어, 질소-연결된 아미노산은 아미노산의 산소 또는 탄소 원자를 통하기보다는 아미노산의 질소 원자를 통하여 결합될 것이다.
화학식 (I-XIV)의 화합물의 일부 구체예는 천연 발생 α-아미노산의 질소-연결 에스테르의 라디칼을 포함할 수 있는 모이어티
를 포함한다. 천연 발생 아미노산의 예에는 이소류신, 류신, 리신, 메티오닌, 페닐알라닌, 트레오닌, 트립토판, 발린, 알라닌, 아스파라긴, 아스파르트산, 시스테인, 글루탐산, 글루타민, 글리신, 프롤린, 셀레노시스테인, 세린, 티로신, 아르기닌, 히스티딘, 오르니틴 및 타우린이 포함된다. 이러한 아미노산의 에스테르는 치환기 R6에 대하여 기재된 것, 특히 R6가 선택적으로 치환된 (C1-C8)알킬인 것을 포함한다.
달리 명시되지 않으면, 화학식 (I-XIV)의 화합물의 탄소 원자는 4의 원자가를 가지도록 의도된다. 탄소 원자가 4의 원자가를 생성하기에 충분한 개수의 부착된 변수를 가지지 않는 일부 화학적 구조 표현에서, 4의 원자가를 제공하기 위하여 요구되는 나머지 탄소 치환기는 수소인 것으로 가정되어야 한다. 예를 들어,
는
와 동일한 의미를 가진다.
"보호기"는 작용기의 특성 또는 화합물 전체의 특성을 막거나 변경시키는 화합물의 모이어티를 지칭한다. 보호기의 화학적 하위구조는 광범하다. 보호기의 한 기능은 모 약물 물질의 합성에서 중간체 역할을 하는 것이다. 보호/탈보호를 위한 화학적 보호기 및 계획이 당해 분야에 공지이다. "Protective Groups in Organic Chemistry", Theodora W. Greene (John Wiley &Sons, Inc., New York, 1991을 참조하라. 보호기는 흔히 원하는 화학 반응의 효율을 보조하기 위하여 특정 작용기의 반응성을 차폐하도록 사용되고, 예를 들어 정연하고 계획된 방식으로 화학 결합을 생성하고 파괴한다. 작용기의 보호는 보호된 작용기의 반응성 이외의 다른 물리적 특성, 예컨대 극성 (polarity), 친지성(lipophilicity)(소수성(hydrophobicity)), 및 통상적인 분석 도구로 측정될 수 있는 다른 특성을 변경한다. 화학적으로 보호된 중간체는 그 자체가 생물학적으로 활성 또는 비활성일 수 있다.
보호된 화합물은 또한 생체 외 및 생체 내에서 세포막통과 및 효소적 분해 또는 제거에 대한 저항과 같은, 변경된, 일부 경우에서는, 최적화된 특성을 나타낼 수 있다. 이 역할에서, 의도된 치료 효과를 가지는 보호된 화합물이 전구약물로 지칭될 수 있다. 보호기의 또 다른 기능은 모 약물을 전구약물로 전환하는 것이고, 이에 의하여 생체 내에서 전구약물의 전환시 모 약물이 방출된다. 활성 전구약물이 모 약물보다 더욱 효과적으로 흡수될 수 있기 때문에, 전구약물이 모 약물보다 더 큰 생체 내 효능을 가질 수 있다. 보호기는 화학적 중간체의 사례에서 생체 외에서, 또는 전구약물의 사례에서 생체 내에서 제거된다. 화학적 중간체일 경우, 비록 일반적으로 생성물이 약리학적으로 무해할 경우 더욱 바람직하기는 하지만, 탈보호 후 결과적 생성물, 예를 들어 알코올이, 생리적으로 허용가능함이 특히 중요하지는 않다.
"전구약물 모이어티"는 대사 동안, 전신적으로, 세포 내에서, 가수분해, 효소 분열에 의하여, 또는 다른 과정에 의하여 활성의 억제성 화합물로부터 분리되는 불안정한 작용기를 의미한다 (Blmdgaard, Hans, "Design and Application of Prodrugs" in Textbook of Drug Design and Development (1991), P. Krogsgaard-Larsen and H. Blmdgaard, Eds. Harwood Academic Publishers, pp. 113-191). 본 발명의 포스포네이트 전구약물 화합물로써 효소 활성화 메커니즘이 가능한 효소에는 아미데이즈, 에스터레이즈, 미생물 효소, 포스포리페이즈, 콜린에스터레이즈, 및 포스페이즈가 포함되지만 이에 제한되지 않는다. 전구약물 모이어티는 용해성, 흡수 및 친지성을 향상시켜 약물 전달, 생체이용률 및 효능을 최적화하는 역할을 할 수 있다. 전구약물 모이어티는 활성 대사물질 또는 약물 그 자체를 포함할 수 있다.
포스페이트기는 포스페이트 전구약물 모이어티일 수 있다. 전구약물 모이어티는 가수분해에 민감할 수 있다. 대안으로 전구약물 모이어티는 락테이트 에스테르 또는 포스포나이데이트-에스테르기와 같이 효소 분열에 민감할 수 있다.
화학식 (I-IV)의 범위 내의 화합물 및 이의 약제학적으로 허용가능한 염의 모든 거울상 이성질체(enantiomer), 부분입체 이성질체(diastereomer), 및 라세미 혼합물(racemic mixture), 호변 이성질체(tautomer), 다형체(polymorph), 모조다형체(pseudopolynorph)가 본 발명에 포괄됨에 유의해야 한다. 이러한 거울상 이성질체 및 부분입체 이성질체의 모든 혼합물이 본 발명의 범위 내에 있다
화학식 (I-XIV)의 화합물 및 이의 약제학적으로 허용가능한 염은 상이한 다형체 또는 모조다형체로서 존재할 수 있다. 본 명세서에서 사용된 결정 다형성 (crystalline polymorphism)은 결정 화합물이 상이한 결정 구조로 존재하는 능력을 의미한다. 결정 다형성은 결정 패킹(packing) 차이(패킹 다형성) 또는 동일한 분자의 상이한 형태 이성질체(conformer) 사이의 패킹 차이(형태 다형성)로부터 기인할 수 있다. 본 명세서에서 사용된 결정 모조다형성은 화합물의 수화물 또는 용매화물이 상이한 결정 구조로 존재하는 능력을 의미한다. 본 발명의 모조다형체는 결정 패킹 차이(패킹 모조다형성)로 인하여 또는 동일한 분자의 상이한 형태 이성질체 사이의 패킹 차이(형태 모조다형성)로 인하여 존재할 수 있다. 본 발명은 화학식 (I-IV)의 화합물 및 이의 약제학적으로 허용가능한 염의 모든 다형체 및 모조다형체를 포함한다.
화학식 (I-XIV)의 화합물 및 약제학적으로 허용가능한 염은 또한 비정질 고체로서 존재할 수 있다. 본 명세서에서 사용된 비정질 고체는 고체에서 원자 위치의 원거리 정렬이 없는 고체이다. 이 정의는 결정 크기가 2 나노미터 이하일 때 마찬가지로 적용된다. 용매를 비롯한 첨가제는 본 발명의 비정질 형태를 생성하기 위하여 사용될 수 있다. 본 발명은 화학식 (I-IV)의 화합물 및 이의 약제학적으로 허용가능한 염의 모든 비정질 형태를 포함한다.
화학식 (I-XIV)의 화합물을 포함하는 선택된 치환기는 반복(recursive) 정도까지 존재한다. 이 문맥에서, "반복 치환기"는 치환기가 그 자체의 또 다른 사례를 나열할 수 있음을 의미한다. 이러한 치환기의 반복 특징 때문에, 이론적으로, 임의의 주어진 구체예에 다수의 화합물이 존재할 수 있다. 의약 화학 분야의 당업자는 이러한 치환기의 총 개수가 의도된 화합물의 바람직한 특성에 의하여 타당하게 제한됨을 이해한다. 이러한 특성에는, 제한이 아니고 예로서, 분자량, 용해도 또는 log P와 같은 물리적 특성, 의도한 표적에 대한 활성과 같은 투여 특성, 및 합성의 용이성과 같은 실시 특성이 포함된다. 반복 치환기는 본 발명의 의도된 양태이다. 의약 화학 분야의 당업자는 이러한 치환기의 다재성을 이해한다. 본 발명의 구체예에 반복 치환기가 존재하는 정도까지, 반복 치환기는 그 자신의 또 다른 사례를, 0, 1, 2, 3, 또는 4 회 나열할 수 있다
양과 관련하여 사용된 수식어 "약"은 언급된 값을 포함하고 문맥에 의하여 지시된 의미를 가진다 (예를 들어, 특정 양의 측정에 관한 오차 정도를 포함한다).
본 명세서에 기재된 본 발명의 화합물에 대한 임의의 언급은 또한 이의 생리적으로 허용가능한 염에 대한 언급을 포함한다. 본 발명의 화합물의 생리적으로 허용가능한 염의 예에는 적절한 염기, 예컨대 알칼리 금속 및 알칼리 토금속(예를 들어, Na+, Li+, K+, Ca+2 및 Mg+2), 암모늄 및 NRa 4 +(여기서 Ra는 본 명세서에서 정의됨)로부터 유도된 염이 포함된다. 질소 원자 또는 아미노기의 생리적으로 허용가능한 염에는 (a) 무기산, 예를 들어, 염산, 하이드로브롬산, 황산, 설팜산, 인산, 질산 등을 사용하여 형성된 산 부가염 ; (b) 유기산, 예를 들어, 아세트산,옥살산, 타르타르산,석신산, 말레산, 퓨마르산, 글루콘산, 시트르산, 말산, 아스코르브산, 벤조산, 이세티온산, 락토비온산, 탄닌산, 팔미트산, 알긴산, 폴리글루탐산, 나프탈렌설폰산, 메탄설폰산, p-톨루엔설폰산, 벤젠설폰산, 나프탈렌디설폰산, 폴리갈락투론산, 말론산, 설포살리실산, 글리콜산, 2-하이드록시-3-나프토에이트, 파모에이트, 살리실산, 스테아르산, 프탈산, 만델산, 락트산, 에탄설폰산, 리신, 아르기닌, 글루탐산, 글리신, 세린, 트레오닌, 알라닌, 이소루이신, 루이신 등을 사용하여 형성된 염; 및 (c) 원소 음이온, 예를 들어, 염소, 브로민 및 아이오딘으로부터 형성된 염이 포함된다. 하이드록시기의 화합물의 생리적으로 허용가능한 염에는 Na+ 및 NRa 4 +와 같은 적절한 양이온과 조합으로 상기 화합물의 음이온이 포함된다.
치료적 사용을 위하여, 본 발명의 화합물의 활성 성분의 염은 생리적으로 허용가능할 것이다. 즉 이들은 생리적으로 허용가능한 산 또는 염기로부터 유도된 염일 것이다. 그러나, 생리적으로 허용가능하지 않은 산 또는 염기의 염 또한 용도를 발견할 수 있는데, 예를 들어, 생리적으로 허용가능한 화합물의 제조 또는 정제에서 그러하다. 생리적으로 허용가능한 산 또는 염기로부터 유도되었는지와는 무관하게, 모든 염이 본 발명의 범위 내에 있다.
마지막으로, 본 명세서의 조성물이 비이온화 형태, 또한 양쪽성이온 형태, 및 수화물로서 화학량론적 양의 물과 조합으로 본 발명의 화합물을 포함할 수 있음이 이해되어야 한다.
화학식 (I-XIV)에 의하여 예시된 본 발명의 화합물은 카이랄 중심, 예를 들어 카이랄 탄소 또는 인 원자를 가진다. 예를들어 화학식 (I-XIV)의 인 원자는 네 가지의 상이한 치환기를 가지기 때문에 카이랄일 수 있다. 본 발명의 화합물은 따라서 거울상 이성질체, 부분입체 이성질체, 및 회전장애 이성질체 (atropisomer)를 포함하여 모든 입체 이성질체 (stereoisomer)의 라세미 혼합물을 포함한다. 더욱이, 본 발명의 화합물은 임의의 또는 모든 비대칭, 카이랄 원자에서의, 농후한(enriched) 또는 분할된(resolved) 광학 이성질체(optical isomer)를 포함한다. 달리 말해서, 서술로부터 명백한 카이랄 중심이 가이랄 이성질체 또는 라세미 혼합물로서 제공된다. 라세미 및 부분입체 이성질성 혼합물 모두, 또한 거울상 이성질성 또는 부분입체 이성질성 파트너가 실질적으로 없는 단리되거나 합성된 개별적인 광학 이성질체가 모두 본 발명의 범위 내에 있다. 라세미 혼합물은, 예를 들어, 광학적 활성 부가물, 예를 들어, 산 또는 염기를 사용하여 형성된 부분입체 이성질성 염의 분리에 이어 광학적 활성 물질로의 전환과 같은 공지의 기법을 통하여 개별적인 실질적으로 광학적으로 순수한 이성질체로 분리된다. 대부분의 사례에서, 원하는 광학 이성질체는 원하는 출발 물질의 적절한 입체 이성질체로 시작하여 입체특이성 반응에 의하여 합성된다.
용어 "카이랄"은 거울상 파트너의 비-중첩성의 특성을 가지는 분자를 지칭하는 반면, 용어 "아카이랄(achiral)"은 거울상 파트너에 중첩가능한 분자를 지칭한다.
용어 "입체 이성질체"는 동일한 화학적 구조를 가지지만, 공간에서 원자 또는 그룹의 배열에 대해서는 상이한 화합물을 지칭한다.
"부분입체 이성질체"는 둘 이상의 카이랄성 중심을 가지는 입체 이성질체를 지칭하고, 부분입체 이성질체의 분자는 서로 거울상이 아니다. 부분입체 이성질체는 상이한 물리적 특성, 예를 들어 녹는점, 끓는점, 스펙트럼 특성, 반응성 및 생물학적 특성을 가진다. 예를 들어 화학식 (I-XIV)의 화합물은 인이 네 가지의 상이한 치환기를 가질 때, 예를 들어, 카이랄성이 R 또는 S인 화학식 (XIV), 카이랄 인 원자를 가질 수 있다. 화학식 (IV)의 포스포라미데이트의 아미노산의 Rc와 Rd가 상이할 때, 화합물의 잠재적 부분입체 이성질성 혼합물, 예를 들어 R,S; S,R; S,S 및 R,R 이성질체를 유발하는 분자 내의 둘의 카이랄성 중심이 존재한다. 부분입체 이성질체의 혼합물은 전기영동 결정화 및/또는 크로마토그래피와 같은 고해상 분석 절차하에 분리될 수 있다. 부분입체 이성질체는 용해성 화학적 안정성 및 결정성에 제한되지 않지만 이와 같은 상이한 물리적 속성을 가질 수 있고, 또한 효소 안정성 흡수 및 대사 안정성에 제한되지 않지만 이와 같은 상이한 생물학적 특성을 가질 수 있다.
"거울상 이성질체"은 서로 비중첩성 거울상인 화합물의 두 입체 이성질체를 지칭한다.
본 명세서에서 사용된 입체화학적 정의 및 관습은 일반적으로 S. P. Parker, Ed., McGraw-Hill Dictionary of Chemical Terms(1984) McGraw-Hill Book Company, New York; 및 Eliel, E. and Wilen, S., Stereochemistry of Organic Compounds(1994) John Wiley & Sons, Inc., New York을 따른다. 많은 유기 화합물이 광학적으로 활성인 형태로 존재한다. 즉, 이들은 평면 편광 (plane-polarized 1ight)의 평면을 회전시키는 능력을 가진다. 광학적으로 활성인 화합물 기술에 있어서, 접두사 D 및 L 또는 R 및 S는 분자의 카이랄 중심(들)에 대한 분자의 절대 배향을 표시하도록 사용된다. 접두사 d 및 l, D 및 L, 또는 (+) 및 (-)는 화합물에 의한 평면 편광의 회전 부호를 표시하기 위하여 사용되고, S, (-), 또는 l은 화합물이 좌선성임을 의미하는 한편 R, (+), 또는 d가 접두어인 화합물은 우선성이다. 주어진 화학 구조식에 있어서, 이러한 입체 이성질체는 서로 거울상(mirror image)이라는 것을 제외하고는 동일하다. 특정한 입체 이성질체가 또한 거울상 이성질체(enantiomer)로 지칭될 수 있고 이러한 이성질체의 혼합물은 흔히 거울상 이성질성 혼합물이라고 한다. 거울상 이성질체의 50:50 혼합물은 라세미 혼합물 또는 라세메이트로 지칭되고, 이는 화학 반응 또는 공정에서 입체선택 또는 입체특이성이 없을 경우 발생할 수 있다. 용어 "라세미 혼합물" 및 "라세메이트"는 광학 활성이 없는, 두 거울상 이성질성 화학종의 등몰 혼합물을 지칭한다.
본 명세서에 기재된 화합물이 하나 초과의 동일한 지명 그룹, 예를 들어, "Ra" 또는 "R1"으로 치환되면, 그룹이 동일하거나 상이할 수 있음이 이해되어야 한다. 즉, 각각의 그룹은 독립적으로 선택된다. 물결선, 은 인접한 하위구조, 그룹, 모이어티, 또는 원자로의 공유 결합 부착 부위를 나타낸다.
본 발명의 화합물은 또한 특정 경우에 호변성 이성질체로서 존재할 수 있다. 비록 단지 하나의 비편재화된 공명 구조가 표현될 수 있기는 하지만, 이러한 모든 형태가 본 발명의 범위 내로 생각된다. 예를 들어, 엔-아민 호변 이성질체가 퓨린, 피리미딘, 이미다졸, 구아니딘, 아미딘, 및 테트라졸 시스템에 대하여 존재할 수 있고, 이들의 모든 가능한 호변 이성질성 형태가 본 발명의 범위 내에 있다.
당업자는 피롤로[1,2-f][1,2,4]트리아진 뉴클레오사이드와 같은 뉴클레오사이드 염기가 호변 이성질성 형태로 존재할 수 있음을 인지할 것이다. 예를 들어, 제한이 아니고, 구조 (a) 및 (b)가 아래 나타나는 바와 같이 동등한 호변 이성질성 형태를 가질 수 있다:
본 명세서에 개시된 모든 구체예에서 헤테로사이클 및 뉴클레오베이스의 모든 가능한 호변 이성질성 형태가 본 발명의 범위 내에 있다.
화학식 (I-XIV)의 화합물은 또한 특정 분자에서 명시된 원자의 동위원소를 포함하는 분자를 포함한다. 이러한 동위원소의 비제한적 예에는 D, T, 14C, 13C 및 15N가 포함된다. 상기 분자의 이러한 모든 동위원소성 변형이 본 발명에 의하여 제공된다.
실시예
특정 약어 및 두문자어가 실험 상세사항 기재에 사용된다. 비록 이들 중 대부분을 당업자가 이해할 것이기는 하지만 표 1이 이러한 약어 및 두문자어 중 다수의 목록을 포함한다.
표 1. 약어 및 두문자어의 목록.
화합물의 제조
화합물 Ia-lf
메탄올 (300 mL) 중의 1a(22.0 g, 54.9 mmol, J.O.C., 2004, 6257에 기재된 절차에 따라 제조됨)의 용액에 0℃에서 30 분의 시간에 걸쳐 적하 깔때기를 이용하여 아세틸 클로라이드(22 mL)를 한 방울씩 첨가한 다음 실온에서 16 h 동안 교반했다. 혼합물을 농축하고, 에틸 아세테이트 (400 mL)에 재용해하고, 얼음처럼 차가운(ice-cold) 2N NaOH로 세척하고, 건조로 농축하여, 미정제(crude) 메틸 에테르 1b를 오일로 제공했다. MS = 437.2 (M + Na+).
메탄올 (300 mL) 중의 1b( 이전 단계로부터 수득함)의 용액에 메탄올 중의 0.5 M 소듐 메톡사이드 용액 (20 mL, 10 mmol)에 첨가하고, 16 h 동안 실온에서 교반했다. 반응을 디옥산 중의 4.0 N HCl 용액 (2.5 mL, 10 mmol)으로 권칭 (quenching) 했다. 이후 혼합물을 농축하여, 미정제 1c를 제공했다. MS =201.0 (M + Na+).
톨루엔(500 mL) 중의 1c(이전 단계로부터 수득함), 트리톤 X-405(물에서 70%, 6.0g), 50% KOH(물에서, 85 g) 의 혼합물을 가열하여 부착된 딘-스타크 트랩으로써 환류했다. 1h 후 ~25 mL의 물을 수집하고, 벤질 클로라이드(33 g, 260 mmol)를 첨가하고 16 h 동안 교반하며 환류를 계속했다. 이후 혼합물을 냉각하고 에틸 아세테이트(400 mL)와 물(300mL) 사이에 분배했다. 유기층을 물(300 mL)로 세척하고, 농축했다. 잔류물을 실리카겔 컬럼 크로마토그래피(~20% EtOAc / 헥산)로 정제하여, 메틸 에테르 1d를 오일로 제공했다 (22.0 g, 세 단계에서 89%). 1H NMR (300 MHz, CDCl3): δ 7.3 (m, 15H), 4.5 - 4.9 (m, 7H), 4.37 (m, 1H), 3.87 (d, 1H), 3.56 (m, 2H), 3.52 (s, 3H), 1.40 (s, 3H).
아세트산(110 mL) 중의 1d(22.0 g, 49.0 mmol)의 용액에 ~ 3 M 황산(4.8 g의 진한 황산을 24 mL의 물과 혼합하여 제조됨)을 첨가하고 70℃에서 8 h 동안 교반했다. 혼합물을 -20 mL의 부피까지 농축하고, 에틸 아세테이트와 얼음처럼 차가운 2N NaOH 사이에 분배했다. 에틸 아세테이트 층을 농축하고, 실리카겔 컬럼 크로마토그래피 (~35% EtOAc / 헥산)로 정제하여, 1e를 오일로 제공했다 (17.0 g, 80%). MS = 457.2 (M + Na+).
DMSO(135 mL) 중의 1e(45 g, 104 mmol)의 용액에 아세틱 안하이드라이드 (90 mL, 815 mmol)를 실온에서 아르곤하에 한 방울씩 첨가했다. 혼합물을 16 h 동안 실온에서 교반한 다음, 교반하며 얼음-물(1 L)에 따랐다. 얼음이 완전히 녹은 후 (~30 min), 에틸 아세테이트 (~500 mL)를 첨가했다. 유기층을 분리했다. 이 추출 과정을 세 번 반복했다 (3x500 mL). 유기 추출물을 조합하고 농축했다. 잔류물을 실리카겔 컬럼 크로마토그래피 (~20% EtOAc / 헥산)로 정제하여,1f를 오일로 제공했다 (39 g, 88%). lH NMR (300 MHz, DMSO-d6): δ 7.3 (m, 15H), 4.4 - 4.8 (m, 7H), 4.08 (d, J = 7.5 Hz, 1H), 3.75 (dd, J = 2,4, 11.4 Hz, 1H), 3.64 (dd, J = 5.4, 11.4 Hz, 1H), 1.51 (s, 3H).
화합물 2
건조한 아르곤 퍼지된(purged) 둥근 바닥 플라스크(100 mL)에 7-브로모-피롤로[2,1-f][1,2,4]트리아진-4-일아민(234 mg, 1.10 mmol)(WO2007056170에 따라 제조됨) 및 무수 THF (1.5 mL)를 첨가했다. 이후 TMSCl (276 μL, 2.2 mmol)을 첨가하고 반응 혼합물을 2 h 동안 교반했다. 플라스크를 드라이 아이스/아세톤조(~ -78 ℃)에 두고 BuLi (2.5 mL, 4.0 mmol, 헥산에서 1.6M)를 한 방울씩 첨가했다. 1h 후, THF 중의 1f (432.5 mg, 1.0 mmol)의 용액을 0℃로 냉각한 다음 반응 플라스크에 한 방울씩 첨가했다. -78℃에서 1 h의 교반 후, 플라스크를 0℃로 가온하고 반응을 퀀칭하기 위하여 sat. NH4Cl (5 mL)을 첨가했다. EtOAc (3 x 10 mL)을 이용하여 유기물을 추출하고 조합된 유기층을 MgSO4를 이용하여 건조했다. 용매를 감압하에 제거하고 미정제 물질을 플래쉬 크로마토그래피(헥산 / EtOAc)를 이용하여 정제했다. 560 mg (90 %)의 2a를 두 아노머(anomer)의 혼합물로서 단리했다. LC/MS = 567.2 (M + H+). lH NMR (300 MHz, CDCl3): δ 7.85 (m, 1H), 7.27 (m, 15H), 7.01 (m, 1H), 6.51 (m, 1H), 4.66 (m, 8H), 4.40 (m, 2H), 3.79 (m, 3H), 1.62 (s, 한 아노머로부터의 2'-CH3), 1.18 (s, 다른 아노머로부터의 2'-CH3).
2a를 위한 대안의 절차
건조한 아르곤 퍼지된 둥근 바닥 플라스크에 7-브로모-피롤로[2,1-f][1,2,4]트리아진-4-일아민(9.6g, 45 mmol) 및 무수 THF (60 mL)를 첨가했다. 이후 TMSCl (12.4mL, 99 mmol)을 첨가하고 반응 혼합물을 2 h 동안 교반했다. 플라스크를 드라이 아이스/아세톤조(~ -78 ℃)에 두고 BuLi (98 mL, 158 mmol, 헥산에서 1.6M)를 한 방울씩 첨가했다. 1 h 후, 이 반응 혼합물을 THF 중의 1f (13.0 g, 30 mmol)의 용액에 -78℃에서 캐뉼러를 통하여 첨가했다. -78℃에서 2 h의 교반 후, 플라스크를 0℃로 가온했다. 포화 NH4Cl (150 mL)을 첨가하여 반응을 퀀칭했다. 유기물을 EtOAc (3 x 10 mL)을 이용하여 추출하고 조합된 유기층을 MgSO4를 이용하여 건조했다. 용매를 감압하에 제거하고 미정제 물질을 플래쉬 실리카겔 크로마토그래피(헥산 / EtOAc)를 이용하여 정제했다. 7.5 g (44 %)의 원하는 물질 2a를 단리했다. LC/MS = 567.2 (M + H+).
화합물 5
0℃에서 CH2Cl2 (20 mL) 중의 화합물 2a(1 g, 1.77 mmol)의 용액에 TMSCN (1.4 mL, 10.5 mmol) 및 BF3-Et20(1 mL, 8.1 mmol)를 첨가했다. 반응 혼합물을 0℃에서 0.5 h 동안 교반한 다음, 실온에서 추가로 0.5 h 동안 교반했다. 반응을 0℃에서 NaHC03로 권칭하고, CH3C02Et로 희석했다. 유기상을 분리하고, 브라인 (brine)으로 세척하고, Na2S04로 건조하고, 여과하고 농축했다. 잔류물을 CH3C02 Et-헥산(1:1 내지 2:1)으로 용리하는 실리카겔상의 크로마토그래피로 정제하여, 원하는 화합물 5a(620 mg, 61%)를 이성질성 혼합물로 제공했다. MS = 576.1 (M + H+).
-78℃에서 CH2Cl2 (4 mL) 중의 화합물 5a(150 mg, 0.26 mmo1)의 용액에 BC13(2 mL, CH2Cl2에서 1M)를 첨가했다. 반응 혼합물을 -78℃에서 1 h 동안 교반했다. 반응을 -78℃에서 TEA(2 mL) 및 MeOH(5 mL)를 한 방울씩 첨가하여 권칭했다. 혼합물이 실온까지 가온되도록 하고, 증발시키고, MeOH와 함께 여러 번 공증발시켰다. 잔류물을 NaHC03(10 mL H20 중의 1 g)로 처리하고, 농축하고 HPLC로 정제하여 원하는 생성물 화합물 5(48 mg, 60%) 를 제공했다. lH NMR(300 MHz, D20): δ 7.74 (s 1H), 6.76 (d, J = 5 Hz, 1H), 6.73 (d, J = 5 Hz, 1H), 4.1 (m, 1H), 3.9 (m, 1H), 3.8 (m, 2H), 0.84 (s, 3H). MS = 305.9 (M + H+). 다른 알파-아노머를 또한 수득했다 (9 mg, 11%): lH NMR(300 MHz, D20): δ 7.70 (s 1H), 6.8 (d, J = 5 Hz, 1H), 6.7 (d, J = 5 Hz, 1H), 4.25 (d, J = 9 Hz, 1H), 4.07 (m, 1H), 3.85 (m, 1H), 3.7 (m, 1H), 1.6 (s, 3H). MS = 306.1 (M + H+).
화합물 A( 상용으로 입수 가능함, 4.99 g, 23.8 mmo1)를 디클로로메탄(100 mL)에 용해하고 알라닌 이소프로필 에스테르 하이드로클로라이드 (3.98 g, 23.8 mmol)를 첨가했다. 생성된 투명한 용액을 -78℃에서 30 분 동안 냉각했다. 트리에틸아민(6.63 mL, 47.5 mmo1)을 15 분에 걸쳐 한 방울씩 첨가했다. 이후 혼합물을 실온까지 가온되도록 했다. 16 h 후, 용매를 아르곤 흐름(stream)에 의하여 제거했다. 잔류물을 MTBE(25 mL)에 재용해하고 불용물(insoluble)을 아르곤하에 여과하여 제거했다. 이후 여과액을 아르곤 흐름에 의하여 응축하고 미정제 생성물 B를 추가의 정제 없이 다음 반응을 위하여 사용했다. lH NMR (300 MHz, CDCl3): 7.1-7.4 (m, 5H), 5.1 (m, 1H), 4.35 (m, 1H), 4.15 (m, 1H), 1.5 (d, 3H), 1.2 (m, 6H). 31P NMR (121.4 MHz, CDCl3): δ 7.8 및 8.4 (2s).
알라닌 이소프로필 에스테르 하이드로클로라이드 (7.95 g, 47.4 mmol)를 디클로로메탄(l00 mL)에 현탁시켰다. 화합물 A(lOg, 47 .4 mmol)를 첨가했다. 이후 트리에틸아민(l3.2 mL, 95 mmol)을 15 분의 시간에 걸쳐 한 방울씩 첨가했다 (내부 반응 온도; -10℃ ~ -3℃). 반응이 거의 완료되었을 때 (인 NMR에 의하여), p-니트로페놀(6.29 g, 45.0 mmol)을 고체로서 한 부분에 첨가했다. 생성된 슬러리에 트리에틸아민(6.28 mL, 45 nuno 1)을 15 분의 시간에 걸쳐 첨가했다. 이후 혼합물을 실온까지 가온했다. 반응이 완료되었을 때, MTBE (lOO mL)를 첨가했다. 백색 침전물을 여과로 제거했다. 여과기 케이크를 MTBE(3 x 50 mL)로 세척했다. 여과액 및 세척액을 조합하고 농축했다. 잔류물을 실리카겔 컬럼 크로마토그래피 (0 으로부터 50% 에틸 아세테이트 / 헥산)로 정제하여, 화합물 C를 1:1 비율의 부분입체 이성질성 혼합물로 제공했다 (14.1 g, 77%). 1H NMR (300 MHz, CDCl3): δ 8.22 (2d, 2H), 7.2-7.4 (m, 7H), 5.0 (m, lH), 4.09 (m, lH), 3.96 (m, lH), 1.39 (2d, 3H), 1.22 (m, 6H). MS = 409.0 (M + H+), 407.2 (M -H+).
화합물 C의 두 부분입체 이성질체의 분리
두 부분입체 이성질체는 다음 조건하에 카이랄 컬럼 크로마토그래피로 분리되었다;
컬럼 : Chiralpak IC, 2 x 25 cm
용매 시스템 : 70% 헵탄 및 30% 이소프로판올 (IPA)
유량: 6 mL/분
실행 (run) 당 로딩(loading) 부피 : 1. 0 mL
로딩 샘플의 농도 70% 헵탄 및 30% IPA에서 150 mg/ mL
(S)-화합물 C: 체류시간 43 분 31P NMR (161.9 MHz, CDCl3): δ -2.99 (s).
(R)-화합물 C: 체류시간 62 분 31P NMR (161.9 MHz, CDCl3): δ -3.02 (s).
대안으로, 두 부분입체 이성질체는 다음 절차에 따라 결정화로 분리되었다;
화합물 C를 디에틸 에테르에 용해했다 (-10 mL/그램). 교반하는 동안, 이후 용액이 흐려질 때까지 헥산을 첨가했다. 결정화를 촉진하기 위하여 종자 결정 (~10 mg / 화합물 C 그램)을 첨가했다. 생성된 현탁액을 16 h 동안 부드럽게 교반하고, ~ 0℃로 냉각하고, 추가 2 h 동안 교반하고, 여과하여 결정질 물질을 수집했다(결정질 물질의 회수 수율 35%-35% 결정질 물질은 ~95%의 (S)-화합물 C 및~5%의 (R)-화합물 C를 포함한다. 재결정화가 99% 부분입체 이성질성으로 순수한 (S)-이성질체를 제공했다
화합물 (S)-6
건조한 아르곤 퍼지된 둥근 바닥 플라스크에 화합물 5(1.0 g, 3.28 mmol) 및 무수 THF(15 mL)를 첨가했다. 슬러리를 10 분 동안 교반하고 플라스크를 실온에서 수조에 두었다. THF 중의 t-부틸마그네슘 클로라이드(1.0 M. 4.91 mL)를 한 방울씩 첨가하고, 혼합물을 추가 10 분 동안 교반했다. 이후 THF(10 mL) 중의 (S)-C(2.68 g, 6.55 mmol)의 용액을 첨가했다. 플라스크를 50℃로 미리 설정된 가열 오일조에 두고 화합물 1이 거의 소모될 때까지 혼합물을 교반했다. -2.5 h 후, 반응 혼합물을 실온으로 냉각하고, 메탄올(5 mL)을 첨가했다. 용매를 감압하에 제거하고 잔류물을 실리카겔 컬럼 크로마토그래피(더 적은 극성 불순물을 제거하기 위한 70% 에틸 아세테이트 / 헥산, 생성물을 용리하기 위한 10% 메탄올 / 디클로로메탄)로 정제하여, (S)-6을 회백색 고체로 제공했다(1.45 g, 77%). 1H NMR (400 MHz, DMSO-d6): δ 7.89 (s, 1H), 7.84 (brs, 2H), 7.36 (t, 2H), 7.23 (d, 2H), 7.17 (t, 1H), 6.87 (d, J = 4.4 Hz, 1H), 6.74 (d, J = 4.4 Hz, 1H), 6.02 (dd, 1H), 5.96 (s, 1H), 5.41 (d, 1H), 4.82 (m, 1H), 4.38 (dd, 1H), 4.22 (q, 1H), 4.16 (m, 1H), 3.81 (m, 1H), 3.67 (dd, 1H), 1.22 (d, 3H), 1.11 (dd, 6H), 0.89 (s, 3H). 31P NMR (161.9 MHz, DMSO-d6): δ 3.99 (s). MS = 575.0 (M + H+), 572.7 (M - H+).
화합물 (S)-8
건조한 아르곤 퍼지된 둥근 바닥 플라스크에 화합물 7(J. Med. Chem., 2005, 48, 5504-5508, 100 mg, 0.38 mmol에 따라 제조됨), 무수 THF(3 mL) 및 무수 NMP(1 mL)를 첨가했다. 슬러리를 10 분 동안 교반하고 플라스크를 실온에서 수조에 두었다. THF 중의 t-부틸마그네슘 클로라이드 (1.0 M, 0.76 mL)를 한 방울씩 첨가하고, 혼합물을 추가 10 분 동안 교반했다. 이후 THF(2 mL) 중의 (S)-C(313 mg, 0.76 mmol)의 용액을 첨가했다. 플라스크를 55℃로 미리 설정된 가열 오일조에 두고 화합물 7이 거의 소모될 때까지 혼합물을 교반했다. ~2.5 h 후, 반응 혼합물을 실온으로 냉각하고, 메탄올(1 mL)을 첨가했다. 용매를 감압하에 제거하고 잔류물을 RP-HPLC에 이어 실리카겔 컬럼 크로마토그래피로 정제하여, (S)-8을 제공했다 (130 mg, 65%). 1H NMR (400 MHz, CDCl3): δ 8.51 (brs, 1H), 7.46 (d, 1H), 7.2-7.4 (m, 5H), 6.28 (d, 1H), 5.70 (dd, 1H), 5.01 (m, 1H), 4.49 (m, 2H), 3.8-4.1 (m, 4H), 1.41 (d, 3H), 1.35 (d, 3H), 1.24 (d, 6H). 31P NMR (162.1 MHz, CDCl3): δ 3.70 (s). MS = 530.0 (M + H+), 528.0 (M - H+). 카이랄 HPLC 잔류 시간 (Chiralpak AS-H, 250 x 4.6 mm 5 마이크론, 100% CH3CN, 1 mL/분 유량); 6.5 분 대 R-이성질체에 대한 5.2 분)
화합물 (S)-C 또는 화합물 (R)-c의 제조에 대하여 기재된 일반 절차를 이용하여, 화합물 10-24를 제조할 수 있다.
화합물 10
화합물 11
화합물 12
화합물 13
화합물 14
화합물 15
화합물 16
화합물 17
화합물 18
화합물 19
화합물 20
화합물 21
화합물 22
화합물 23
화합물 24
화합물 (S)-6의 제조에 대하여 기재된 일반 절차를 이용하여, 화합물 25-38을 화합물 ( S )-C 또는 화합물 (R)-C를 이용하여 제조할 수 있다.
화합물 25
화합물 26
화합물 27
화합물 28
화합물 29
화합물 30
화합물 31
화합물 32
화합물 34
화합물 35
화합물 36
화합물 37
화합물 38
Claims (1)
- 본원에 기재된 바와 같은 화합물의 용도.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US36562110P | 2010-07-19 | 2010-07-19 | |
| US61/365,621 | 2010-07-19 | ||
| PCT/US2011/044581 WO2012012465A1 (en) | 2010-07-19 | 2011-07-19 | Methods for the preparation of diasteromerically pure phosphoramidate prodrugs |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020197018279A Division KR102108864B1 (ko) | 2010-07-19 | 2011-07-19 | 부분입체 이성질성으로 순수한 포스포라미데이트 전구약물의 제조 방법 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20200052384A true KR20200052384A (ko) | 2020-05-14 |
Family
ID=44534619
Family Applications (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020137003792A KR101995598B1 (ko) | 2010-07-19 | 2011-07-19 | 부분입체 이성질성으로 순수한 포스포라미데이트 전구약물의 제조 방법 |
| KR1020207012760A KR20200052384A (ko) | 2010-07-19 | 2011-07-19 | 부분입체 이성질성으로 순수한 포스포라미데이트 전구약물의 제조 방법 |
| KR1020197018279A KR102108864B1 (ko) | 2010-07-19 | 2011-07-19 | 부분입체 이성질성으로 순수한 포스포라미데이트 전구약물의 제조 방법 |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020137003792A KR101995598B1 (ko) | 2010-07-19 | 2011-07-19 | 부분입체 이성질성으로 순수한 포스포라미데이트 전구약물의 제조 방법 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020197018279A KR102108864B1 (ko) | 2010-07-19 | 2011-07-19 | 부분입체 이성질성으로 순수한 포스포라미데이트 전구약물의 제조 방법 |
Country Status (24)
| Country | Link |
|---|---|
| US (2) | US9090642B2 (ko) |
| EP (2) | EP2596004B1 (ko) |
| JP (1) | JP5937073B2 (ko) |
| KR (3) | KR101995598B1 (ko) |
| CN (1) | CN103052646A (ko) |
| AP (1) | AP2013006665A0 (ko) |
| AU (1) | AU2011282241B2 (ko) |
| BR (1) | BR112013001267A2 (ko) |
| CA (1) | CA2804375C (ko) |
| CL (1) | CL2013000076A1 (ko) |
| CO (1) | CO6680607A2 (ko) |
| CR (1) | CR20130063A (ko) |
| EA (1) | EA025311B1 (ko) |
| EC (1) | ECSP13012451A (ko) |
| ES (1) | ES2524398T3 (ko) |
| IL (2) | IL224045A (ko) |
| MA (1) | MA34471B1 (ko) |
| MX (1) | MX2013000656A (ko) |
| NZ (1) | NZ606141A (ko) |
| PE (1) | PE20130807A1 (ko) |
| PT (1) | PT2596004E (ko) |
| SG (1) | SG186831A1 (ko) |
| WO (1) | WO2012012465A1 (ko) |
| ZA (1) | ZA201300135B (ko) |
Families Citing this family (106)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| MY164523A (en) | 2000-05-23 | 2017-12-29 | Univ Degli Studi Cagliari | Methods and compositions for treating hepatitis c virus |
| CA2506129C (en) | 2002-11-15 | 2015-02-17 | Idenix (Cayman) Limited | 2'-branched nucleosides and flaviviridae mutation |
| AR071395A1 (es) | 2008-04-23 | 2010-06-16 | Gilead Sciences Inc | Analogos carba-nucleosidos 1'-sustituidos para tratamiento antiviral |
| NZ599404A (en) | 2009-09-21 | 2014-02-28 | Gilead Sciences Inc | Processes and intermediates for the preparation of 1’-substituted carba-nucleoside analogs |
| JP5937073B2 (ja) | 2010-07-19 | 2016-06-22 | ギリード・サイエンシズ・インコーポレーテッド | ジアステレオマーとして純粋なホスホルアミデートプロドラッグの調製方法 |
| PE20171155A1 (es) | 2010-07-22 | 2017-08-16 | Gilead Sciences Inc | Metodos y compuestos para tratar infecciones virales por paramyxoviridae |
| NZ613370A (en) | 2010-12-20 | 2015-05-29 | Gilead Sciences Inc | Combinations for treating hcv |
| HUE060127T2 (hu) | 2011-03-01 | 2023-02-28 | NuCana plc | Az 5-fluor-2'-deoxiuridin foszforamidát-származékot tartalmazó gyógyszerkészítmények a rák kezelésében való felhasználásra |
| EP2691409B1 (en) | 2011-03-31 | 2018-02-21 | Idenix Pharmaceuticals LLC. | Compounds and pharmaceutical compositions for the treatment of viral infections |
| TW201329096A (zh) | 2011-09-12 | 2013-07-16 | Idenix Pharmaceuticals Inc | 經取代羰氧基甲基磷酸醯胺化合物及用於治療病毒感染之藥學組成物 |
| JP6073897B2 (ja) | 2011-09-16 | 2017-02-01 | ギリアド ファーマセット エルエルシー | Hcvを処置するための方法 |
| MX350809B (es) | 2011-12-20 | 2017-09-20 | Riboscience Llc | Derivados nucleósidos con sustitución 2',4'-difluoro-2'-metilo como inhibidores de la replicación del arn del vhc. |
| AU2012357986B2 (en) | 2011-12-20 | 2017-02-02 | Riboscience Llc | 4'-Azido, 3'-fluoro substituted nucleoside derivatives as inhibitors of HCV RNA replication |
| MX356509B (es) | 2011-12-22 | 2018-05-30 | Alios Biopharma Inc | Nucleósidos sustituidos, nucleótidos y análogos de los mismos. |
| USRE48171E1 (en) | 2012-03-21 | 2020-08-25 | Janssen Biopharma, Inc. | Substituted nucleosides, nucleotides and analogs thereof |
| US9441007B2 (en) | 2012-03-21 | 2016-09-13 | Alios Biopharma, Inc. | Substituted nucleosides, nucleotides and analogs thereof |
| WO2013177195A1 (en) | 2012-05-22 | 2013-11-28 | Idenix Pharmaceuticals, Inc. | 3',5'-cyclic phosphate prodrugs for hcv infection |
| WO2013177188A1 (en) | 2012-05-22 | 2013-11-28 | Idenix Pharmaceuticals, Inc. | 3',5'-cyclic phosphoramidate prodrugs for hcv infection |
| CA2873315A1 (en) | 2012-05-22 | 2013-11-28 | Idenix Pharamaceuticals, Inc. | D-amino acid compounds for liver disease |
| HUE029038T2 (en) | 2012-05-25 | 2017-01-30 | Janssen Sciences Ireland Uc | Uracil spirooxetan nucleosides |
| EP2870169A1 (en) * | 2012-07-03 | 2015-05-13 | Bristol-Myers Squibb Company | Process for preparing diastereomerically enriched phosphoramidate derivatives of nucleoside compounds for treatment of viral infections |
| US9556216B2 (en) | 2012-08-31 | 2017-01-31 | Novartis Ag | 2′-Ethynyl nucleoside derivatives for treatment of viral infections |
| WO2014052638A1 (en) | 2012-09-27 | 2014-04-03 | Idenix Pharmaceuticals, Inc. | Esters and malonates of sate prodrugs |
| US10513534B2 (en) * | 2012-10-08 | 2019-12-24 | Idenix Pharmaceuticals Llc | 2′-chloro nucleoside analogs for HCV infection |
| SG11201503750YA (en) * | 2012-11-16 | 2015-06-29 | Univ Cardiff | Process for preparing nucleoside prodrugs |
| RU2015123641A (ru) * | 2012-11-19 | 2017-01-10 | Мерк Шарп И Доум Корп. | 2-алкинилзамещенные производные нуклеозидов, предназначенные для лечения вирусных заболеваний |
| US9211300B2 (en) | 2012-12-19 | 2015-12-15 | Idenix Pharmaceuticals Llc | 4′-fluoro nucleosides for the treatment of HCV |
| GEP201706757B (en) | 2012-12-21 | 2017-10-25 | Alios Biopharma Inc | Substituted nucleosides, nucleotides and analogs thereof |
| BR112014011938B1 (pt) | 2013-01-31 | 2021-03-16 | Gilead Pharmasset Llc | composição farmacêutica na forma de um comprimido com uma combinação de dose fixa de dois compostos antivirais, forma de dosagem farmacêutica compreendendo a referida composição e uso da referida composição |
| US9339541B2 (en) | 2013-03-04 | 2016-05-17 | Merck Sharp & Dohme Corp. | Thiophosphate nucleosides for the treatment of HCV |
| WO2014137926A1 (en) | 2013-03-04 | 2014-09-12 | Idenix Pharmaceuticals, Inc. | 3'-deoxy nucleosides for the treatment of hcv |
| EP2970357A1 (en) | 2013-03-13 | 2016-01-20 | IDENIX Pharmaceuticals, Inc. | Amino acid phosphoramidate pronucleotides of 2'-cyano, azido and amino nucleosides for the treatment of hcv |
| EP2981542B1 (en) | 2013-04-01 | 2021-09-15 | Idenix Pharmaceuticals LLC | 2',4'-fluoro nucleosides for the treatment of hcv |
| JP2016522172A (ja) * | 2013-04-12 | 2016-07-28 | アキリオン ファーマシューティカルズ,インコーポレーテッド | Hcvを治療するのに有用な重水素化されたヌクレオシドプロドラッグ |
| US20180200280A1 (en) | 2013-05-16 | 2018-07-19 | Riboscience Llc | 4'-Fluoro-2'-Methyl Substituted Nucleoside Derivatives as Inhibitors of HCV RNA Replication |
| KR20160039154A (ko) | 2013-05-16 | 2016-04-08 | 리보사이언스 엘엘씨 | 4''-아자이도-3''-데옥시-3''-플루오로 치환된 뉴클레오시드 유도체 |
| WO2014186637A1 (en) | 2013-05-16 | 2014-11-20 | Riboscience Llc | 4'-fluor0-2'-methyl substituted nucleoside derivatives |
| US10005779B2 (en) | 2013-06-05 | 2018-06-26 | Idenix Pharmaceuticals Llc | 1′,4′-thio nucleosides for the treatment of HCV |
| WO2015017713A1 (en) * | 2013-08-01 | 2015-02-05 | Idenix Pharmaceuticals, Inc. | D-amino acid phosphoramidate pronucleotides of halogeno pyrimidine compounds for liver disease |
| EP3055319A4 (en) | 2013-10-11 | 2018-01-10 | Alios Biopharma, Inc. | Substituted nucleosides, nucleotides and analogs thereof |
| UA119050C2 (uk) | 2013-11-11 | 2019-04-25 | Ґілеад Саєнсиз, Інк. | ПІРОЛО[1.2-f][1.2.4]ТРИАЗИНИ, ЯКІ ВИКОРИСТОВУЮТЬСЯ ДЛЯ ЛІКУВАННЯ РЕСПІРАТОРНО-СИНЦИТІАЛЬНИХ ВІРУСНИХ ІНФЕКЦІЙ |
| CN103804446A (zh) * | 2014-02-27 | 2014-05-21 | 苏州东南药业股份有限公司 | 一种3,5-二苯甲酰基-2-去氧-2-氟-2甲基-D-核糖-γ-内酯的制备方法 |
| CZ307789B6 (cs) * | 2014-04-15 | 2019-05-09 | Zentiva, K.S. | Způsob výroby biologicky účinných fosforamidátových léčiv |
| EP3131914B1 (en) | 2014-04-16 | 2023-05-10 | Idenix Pharmaceuticals LLC | 3'-substituted methyl or alkynyl nucleosides for the treatment of hcv |
| EP3137454A1 (en) | 2014-04-28 | 2017-03-08 | Pfizer Inc. | Heteroaromatic compounds and their use as dopamine d1 ligands |
| TWI678369B (zh) | 2014-07-28 | 2019-12-01 | 美商基利科學股份有限公司 | 用於治療呼吸道合胞病毒感染之噻吩並[3,2-d]嘧啶、呋喃並[3,2-d]嘧啶及吡咯並[3,2-d]嘧啶化合物類 |
| CN104130302B (zh) * | 2014-08-08 | 2017-02-15 | 乳源东阳光药业有限公司 | 一种核苷药物的晶型及其制备方法 |
| TWI673283B (zh) | 2014-08-21 | 2019-10-01 | 美商基利科學股份有限公司 | 2’-氯胺基嘧啶酮及嘧啶二酮核苷類 |
| CN104230985B (zh) * | 2014-09-01 | 2017-01-18 | 北京天弘天达医药科技有限公司 | (s)‑2‑[(s)‑(4‑硝基‑苯氧基)‑苯氧基‑磷酰基氨基]丙酸异丙酯的制备方法 |
| CN105461773B (zh) * | 2014-09-30 | 2020-12-01 | 江苏豪森药业集团有限公司 | 索非布韦的制备方法及其中间体 |
| US10251903B2 (en) | 2014-10-20 | 2019-04-09 | Merck Sharp & Dohme Corp. | Process for making nucleoside phosphoramidate compounds |
| TWI740546B (zh) | 2014-10-29 | 2021-09-21 | 美商基利科學股份有限公司 | 製備核糖苷的方法 |
| RS59264B1 (sr) | 2014-11-28 | 2019-10-31 | NuCana plc | Novi 2’ i/ili 5’ derivati 3’-deoksi adenozina supstituisani aminokiselinskim estrom fosforamidata, kao antikancerska jedinjenja |
| CA2969733A1 (en) * | 2014-12-10 | 2016-06-16 | Solstice Biologics, Ltd. | Mononucleotides having a bioreversible disulfide group |
| EP3939985A1 (en) | 2014-12-26 | 2022-01-19 | Emory University | Pharmaceutical compositions comprising n4-hydroxycytidine derivatives for the treatment or prevention of influenza or coronavirus infections |
| SG11201706841PA (en) | 2015-03-06 | 2017-09-28 | Atea Pharmaceuticals Inc | ß-D-2'-DEOXY-2'a-FLUORO-2'-ß-C-SUBSTITUTED-2-MODIFIED-N<sp>6</sp>-SUBSTITUTED PURINE NUCLEOTIDES FOR HCV TREATMENT |
| CN104829673B (zh) * | 2015-03-12 | 2017-10-27 | 南京旗昌医药科技有限公司 | 一种索氟布韦晶型6的制备方法 |
| WO2016160646A1 (en) * | 2015-04-02 | 2016-10-06 | Merck Sharp & Dohme Corp. | Process for making phosphoramidate protected nucleoside compounds |
| CN107646037A (zh) | 2015-05-26 | 2018-01-30 | 桑多斯股份公司 | 选择性合成核苷氨基磷酸酯类化合物的方法 |
| WO2016196735A2 (en) | 2015-06-03 | 2016-12-08 | Teva Pharmaceuticals International Gmbh | Improved processes for the preparation of sofosbuvir and intermediates thereof |
| EP3331895B1 (en) | 2015-08-06 | 2020-07-29 | Chimerix, Inc. | Pyrrolopyrimidine nucleosides and analogs thereof useful as antiviral agents |
| SI3785717T1 (sl) | 2015-09-16 | 2022-04-29 | Gilead Sciences, Inc. | Postopki za zdravljenje okužb s Coronaviridae |
| CN112156102B (zh) | 2015-09-16 | 2023-10-03 | 济南高合医疗科技有限公司 | 一种nuc-1031单一异构体的晶型及其制备方法 |
| CN106543220A (zh) | 2015-09-16 | 2017-03-29 | 博瑞生物医药(苏州)股份有限公司 | 氨基磷酸酯化合物及其制备方法和晶体 |
| WO2017093973A1 (en) * | 2015-12-02 | 2017-06-08 | Sun Pharmaceutical Industries Limited | Process for the preparation of pure sofosbuvir |
| EP3386998B1 (en) | 2015-12-11 | 2021-11-10 | NuCana plc | Diastereoselective synthesis of phosphate derivatives and of the gemcitabine prodrug nuc-1031 |
| CN109311885A (zh) | 2016-03-24 | 2019-02-05 | 诺华股份有限公司 | 炔基核苷类似物作为人类鼻病毒的抑制剂 |
| KR20230111268A (ko) | 2016-03-28 | 2023-07-25 | 인사이트 코포레이션 | Tam 억제제로서 피롤로트리아진 화합물 |
| WO2017197036A1 (en) | 2016-05-10 | 2017-11-16 | C4 Therapeutics, Inc. | Spirocyclic degronimers for target protein degradation |
| CN109562107A (zh) | 2016-05-10 | 2019-04-02 | C4医药公司 | 用于靶蛋白降解的杂环降解决定子体 |
| CN109641874A (zh) | 2016-05-10 | 2019-04-16 | C4医药公司 | 用于靶蛋白降解的c3-碳连接的戊二酰亚胺降解决定子体 |
| US10202412B2 (en) | 2016-07-08 | 2019-02-12 | Atea Pharmaceuticals, Inc. | β-D-2′-deoxy-2′-substituted-4′-substituted-2-substituted-N6-substituted-6-aminopurinenucleotides for the treatment of paramyxovirus and orthomyxovirus infections |
| US10711029B2 (en) | 2016-07-14 | 2020-07-14 | Atea Pharmaceuticals, Inc. | Beta-d-2′-deoxy-2′-alpha-fluoro-2′-beta-c-substituted-4′fluoro-n6-substituted-6-amino-2-substituted purine nucleotides for the treatment of hepatitis c virus infection |
| MY197236A (en) | 2016-09-07 | 2023-06-07 | Atea Pharmaceuticals Inc | 2'-substituted-n6-substituted purine nucleotides for rna virus treatment |
| KR20190085976A (ko) * | 2016-11-18 | 2019-07-19 | 뉴로바이브 파마슈티컬 에이비 | 미토콘드리아 프로톤 이오노포어의 간 프로드러그 |
| CN108276463A (zh) * | 2017-01-06 | 2018-07-13 | 米文君 | 一类新的化合物及其用途 |
| KR102592899B1 (ko) | 2017-02-01 | 2023-10-24 | 아테아 파마슈티컬즈, 인크. | C형 간염 바이러스를 치료하기 위한 뉴클레오티드 헤미-술페이트 염 |
| ES2961460T3 (es) | 2017-03-14 | 2024-03-12 | Gilead Sciences Inc | Métodos para tratar las infecciones por coronavirus felinas |
| EP4219513A1 (en) | 2017-05-01 | 2023-08-02 | Gilead Sciences, Inc. | Crystalline form of (s)-2-ethylbutyl 2-(((s)-(((2r,3s,4r,5r)-5-(4-aminopyrrolo[2,1-f] [1,2,4]triazin-7-yl)-5-cyano-3,4-dihydroxytetrahydrofuran2-yl)methoxy)(phenoxy) phosphoryl)amino)propanoate |
| GB201709471D0 (en) | 2017-06-14 | 2017-07-26 | Nucana Biomed Ltd | Diastereoselective synthesis of hosphate derivatives |
| US10675296B2 (en) | 2017-07-11 | 2020-06-09 | Gilead Sciences, Inc. | Compositions comprising an RNA polymerase inhibitor and cyclodextrin for treating viral infections |
| GB201715011D0 (en) | 2017-09-18 | 2017-11-01 | Nucana Biomed Ltd | Floxuridine synthesis |
| US10682369B2 (en) | 2017-09-21 | 2020-06-16 | Riboscience Llc | 4′-fluoro-2′-methyl substituted nucleoside derivatives as inhibitors of HCV RNA replication |
| WO2019060692A1 (en) | 2017-09-21 | 2019-03-28 | Chimerix, Inc. | MORPHIC FORMS OF 4-AMINO-7- (3,4-DIHYDROXY-5- (HYDROXYMETHYL) -ETRAHYDROFURAN-2-YL) -2-METHYL-7H-PYRROLO [2,3-D] PYRIMIDINE-5-CARBOXAMIDE AND THEIR USES |
| RU2020116571A (ru) | 2017-12-07 | 2021-11-22 | Эмори Юниверсити | N4-гидроксицитидин и производные и связанные с этим противовирусные применения |
| CN112351799A (zh) | 2018-04-10 | 2021-02-09 | 阿堤亚制药公司 | 具有硬化的hcv感染患者的治疗 |
| EP3966222A4 (en) | 2019-05-09 | 2023-10-04 | Aligos Therapeutics, Inc. | MODIFIED CYCLIC DI-NUCLEOSIDE COMPOUNDS AS STING MODULATORS |
| TW202313067A (zh) | 2020-01-27 | 2023-04-01 | 美商基利科學股份有限公司 | 治療sars cov-2感染之方法 |
| CN113214262B (zh) * | 2020-02-05 | 2023-07-07 | 华创合成制药股份有限公司 | 一种含有胍基的化合物及其制备方法和用途 |
| TW202322824A (zh) | 2020-02-18 | 2023-06-16 | 美商基利科學股份有限公司 | 抗病毒化合物 |
| TW202315607A (zh) | 2020-02-18 | 2023-04-16 | 美商基利科學股份有限公司 | 抗病毒化合物 |
| WO2021168004A1 (en) | 2020-02-18 | 2021-08-26 | Gilead Sciences, Inc. | Antiviral compounds |
| US10874687B1 (en) | 2020-02-27 | 2020-12-29 | Atea Pharmaceuticals, Inc. | Highly active compounds against COVID-19 |
| WO2021183750A2 (en) | 2020-03-12 | 2021-09-16 | Gilead Sciences, Inc. | Methods of preparing 1'-cyano nucleosides |
| CN115715190A (zh) * | 2020-04-02 | 2023-02-24 | 密歇根大学董事会 | 用于治疗病毒感染的瑞德西韦和瑞德西韦类似物、溶液剂以及纳米粒子、脂质体和微粒组合物 |
| US11701372B2 (en) | 2020-04-06 | 2023-07-18 | Gilead Sciences, Inc. | Inhalation formulations of 1'-cyano substituted carba-nucleoside analogs |
| CA3179226A1 (en) | 2020-05-29 | 2021-12-02 | Tomas Cihlar | Remdesivir treatment methods |
| CN113754692B (zh) * | 2020-06-03 | 2022-06-10 | 上海交通大学 | 瑞德西韦中间体(s,s)-氨基磷酸酯的不对称催化合成方法 |
| US20230241225A1 (en) | 2020-06-15 | 2023-08-03 | Metro International Biotech, Llc | Anti-viral compounds and methods of use |
| WO2021257569A1 (en) * | 2020-06-15 | 2021-12-23 | Metro International Biotech, Llc | Anti-viral compounds and methods of use |
| IL299202A (en) | 2020-06-24 | 2023-02-01 | Gilead Sciences Inc | 1'-cyano nucleoside analogs and uses thereof |
| TW202233204A (zh) | 2020-08-27 | 2022-09-01 | 美商基利科學股份有限公司 | 用於治療病毒感染之化合物及方法 |
| CN113105504A (zh) * | 2021-03-30 | 2021-07-13 | 澳门科技大学 | Remdesivir衍生物、其类似物及其制备方法与应用 |
| EP4323362A1 (en) | 2021-04-16 | 2024-02-21 | Gilead Sciences, Inc. | Methods of preparing carbanucleosides using amides |
| US20230295172A1 (en) | 2022-03-02 | 2023-09-21 | Gilead Sciences, Inc. | Compounds and methods for treatment of viral infections |
| CN115322237B (zh) * | 2022-10-13 | 2023-03-10 | 广东帕派恩生物科技有限公司 | 一种抑制rna病毒的化合物 |
Family Cites Families (85)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4816570A (en) | 1982-11-30 | 1989-03-28 | The Board Of Regents Of The University Of Texas System | Biologically reversible phosphate and phosphonate protective groups |
| US4968788A (en) | 1986-04-04 | 1990-11-06 | Board Of Regents, The University Of Texas System | Biologically reversible phosphate and phosphonate protective gruops |
| WO1991019721A1 (en) | 1990-06-13 | 1991-12-26 | Arnold Glazier | Phosphorous produgs |
| DE10399025I2 (de) | 1990-09-14 | 2007-11-08 | Acad Of Science Czech Republic | Wirkstoffvorläufer von Phosphonaten |
| JPH07196565A (ja) * | 1993-12-28 | 1995-08-01 | Idemitsu Petrochem Co Ltd | 4−アルキル−2−フルオロシクロヘキサノールとその製造方法及びその光学分割方法 |
| US6887707B2 (en) | 1996-10-28 | 2005-05-03 | University Of Washington | Induction of viral mutation by incorporation of miscoding ribonucleoside analogs into viral RNA |
| AU3247899A (en) | 1998-03-03 | 1999-09-20 | Novo Nordisk A/S | New salt forms of (2e)- 5-amino-5- methylhex-2- enoic acid n-methyl-n-((1r)-1-(n- methyl-n-((1r)-1-(methylcarbamoyl)-2- phenylethyl)carbamoyl)-2- (2-naphtyl)ethyl)amide |
| US6312662B1 (en) | 1998-03-06 | 2001-11-06 | Metabasis Therapeutics, Inc. | Prodrugs phosphorus-containing compounds |
| AU3363499A (en) | 1998-03-27 | 1999-10-18 | George W. Griesgraber | Nucleosides with antiviral and anticancer activity |
| WO2000023449A1 (en) | 1998-10-16 | 2000-04-27 | Merck Sharp & Dohme Limited | Pyrazolo-triazine derivatives as ligands for gaba receptors |
| DE19912636A1 (de) | 1999-03-20 | 2000-09-21 | Aventis Cropscience Gmbh | Bicyclische Heterocyclen, Verfahren zu ihrer Herstellung und ihre Verwendung als Herbizide und pharmazeutische Mittel |
| AU7490600A (en) | 1999-09-15 | 2001-04-17 | Biocryst Pharmaceuticals, Inc. | Inhibiting t-cell proliferation |
| EP1225899A2 (en) | 1999-11-04 | 2002-07-31 | Virochem Pharma Inc. | Method for the treatment or prevention of flaviviridae viral infection using nucleoside analogues |
| EA200200778A1 (ru) | 2000-02-18 | 2003-06-26 | Шайре Байокем Инк. | СПОСОБ ЛЕЧЕНИЯ ИЛИ ПРОФИЛАКТИКИ ИНФЕКЦИИ ГЕПАТИТА С В ОРГАНИЗМЕ ХОЗЯИНА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ПРОТИВ ФЛАВИВИРУСА, СОЕДИНЕНИЕ ФОРМУЛЫ Ib - АКТИВНЫЙ АГЕНТ ДЛЯ ЛЕЧЕНИЯ ИЛИ ПРОФИЛАКТИКИ ИНФЕКЦИИ ГЕПАТИТА С ИЛИ ФЛАВИВИРУСА (ВАРИАНТЫ) |
| MY164523A (en) | 2000-05-23 | 2017-12-29 | Univ Degli Studi Cagliari | Methods and compositions for treating hepatitis c virus |
| CZ301182B6 (cs) | 2000-05-26 | 2009-12-02 | Idenix (Cayman) Limited | Použití nukleosidových derivátu pro výrobu farmaceutických prostredku pro lécení infekcí vyvolaných flaviviry a pestiviry |
| AP1466A (en) | 2000-07-21 | 2005-09-22 | Gilead Sciences Inc | Prodrugs of phosphonate nucleotide analogues and methods for selecting and making same. |
| US20030008841A1 (en) | 2000-08-30 | 2003-01-09 | Rene Devos | Anti-HCV nucleoside derivatives |
| ES2402597T3 (es) | 2000-10-18 | 2013-05-07 | Gilead Pharmasset Llc | Nucleósidos modificados para el tratamiento de infecciones víricas y proliferación celular anormal |
| ATE526339T1 (de) | 2001-01-22 | 2011-10-15 | Merck Sharp & Dohme | Nukleosidderivate als inhibitoren der rna- abhängigen viralen rna-polymerase |
| DE10145223A1 (de) | 2001-09-13 | 2003-04-03 | Basf Ag | Verfahren zur Herstellung von meso-Zeaxanthin |
| JP2003095991A (ja) * | 2001-09-27 | 2003-04-03 | Mitsubishi Rayon Co Ltd | 光学活性3,3,3−トリフルオロ−2−ヒドロキシ−2−メチルプロピオン酸の製造法 |
| EP1438054A4 (en) | 2001-09-28 | 2006-07-26 | Idenix Cayman Ltd | METHODS AND COMPOSITIONS FOR TREATING FLAVIVIRUS AND PESTIVIRUS USING MODIFIED NUCLEOSIDE AT 4 'POSITION |
| AT410792B (de) | 2001-12-28 | 2003-07-25 | Dsm Fine Chem Austria Gmbh | Verfahren zur herstellung von geschützten, enantiomeren-angereicherten cyanhydrinen durch in-situ-derivatisierung |
| US20040023901A1 (en) | 2002-02-28 | 2004-02-05 | Cook Phillip D. | Nucleoside 5'-monophosphate mimics and their prodrugs |
| CA2477741A1 (en) | 2002-02-28 | 2003-09-04 | Biota, Inc. | Nucleotide mimics and their prodrugs |
| US20040138170A1 (en) | 2002-03-06 | 2004-07-15 | Montgomery John A. | Nucleosides, preparation thereof and use as inhibitors of rna viral polymerases |
| GB0210124D0 (en) | 2002-05-02 | 2002-06-12 | Merck Sharp & Dohme | Therapeutic agents |
| GB0210127D0 (en) | 2002-05-02 | 2002-06-12 | Merck Sharp & Dohme | Therapeutic agents |
| US20040063658A1 (en) | 2002-05-06 | 2004-04-01 | Roberts Christopher Don | Nucleoside derivatives for treating hepatitis C virus infection |
| WO2003100009A2 (en) | 2002-05-23 | 2003-12-04 | Biocryst Pharmaceuticals, Inc. | Enhancing the efficacy of reverse transcriptase and dna polymerase inhibitors (nucleoside analogs) using pnp inhibitors and/or 2'-deoxyguanosine and/or prodrug thereof |
| CA2506129C (en) | 2002-11-15 | 2015-02-17 | Idenix (Cayman) Limited | 2'-branched nucleosides and flaviviridae mutation |
| EP1628685B1 (en) | 2003-04-25 | 2010-12-08 | Gilead Sciences, Inc. | Antiviral phosphonate analogs |
| AU2004258750A1 (en) | 2003-07-25 | 2005-02-03 | Centre National De La Recherche Scientifique -Cnrs | Purine nucleoside analogues for treating diseases caused by flaviviridae including hepatitis C |
| RU2006109491A (ru) | 2003-08-27 | 2006-08-10 | Байота, Инк. (Au) | Новые трициклические нуклеозиды или нуклеотиды в качестве терапевтических средств |
| CA2568379A1 (en) | 2004-06-15 | 2005-12-29 | Merck & Co., Inc. | C-purine nucleoside analogs as inhibitors of rna-dependent rna viral polymerase |
| US7560434B2 (en) | 2004-06-22 | 2009-07-14 | Biocryst Pharmaceuticals, Inc. | AZA nucleosides, preparation thereof and use as inhibitors of RNA viral polymerases |
| PL3109244T3 (pl) | 2004-09-14 | 2019-09-30 | Gilead Pharmasset Llc | Wytwarzanie 2'fluoro-2'-alkilo-podstawionych lub innych ewentualnie podstawionych rybofuranozylopirymidyn i puryn oraz ich pochodnych |
| JP2008517912A (ja) | 2004-10-21 | 2008-05-29 | メルク エンド カムパニー インコーポレーテッド | RNA依存性RNAウイルス感染治療用フッ素化ピロロ[2,3−d]ピリミジンヌクレオシド |
| CN101043893A (zh) | 2004-10-21 | 2007-09-26 | 默克公司 | 治疗RNA-依赖性RNA病毒感染的氟化吡咯并[2,3-d]嘧啶核苷 |
| AU2005302448B2 (en) | 2004-10-29 | 2012-07-19 | Biocryst Pharmaceuticals, Inc. | Therapeutic furopyrimidines and thienopyrimidines |
| JP2008532950A (ja) | 2005-03-08 | 2008-08-21 | バイオタ サイエンティフィック マネージメント ピーティーワイ リミテッド | 治療薬としての二環式ヌクレオシドおよび二環式ヌクレオチド |
| EP2537520A1 (en) | 2005-03-29 | 2012-12-26 | Biocryst Pharmaceuticals, Inc. | Hepatics C therapies |
| WO2006116557A1 (en) | 2005-04-25 | 2006-11-02 | Genelabs Technologies, Inc. | Nucleoside compounds for treating viral infections |
| WO2006121820A1 (en) | 2005-05-05 | 2006-11-16 | Valeant Research & Development | Phosphoramidate prodrugs for treatment of viral infection |
| WO2007027248A2 (en) | 2005-05-16 | 2007-03-08 | Valeant Research & Development | 3', 5' - cyclic nucleoside analogues for treatment of hcv |
| CN101321775B (zh) | 2005-10-03 | 2012-05-23 | 大学健康网络 | 用于治疗疟疾的odcase抑制剂 |
| WO2007056170A2 (en) | 2005-11-02 | 2007-05-18 | Bayer Healthcare Ag | Pyrrolo[2,1-f] [1,2,4] triazin-4-ylamines igf-1r kinase inhibitors for the treatment of cancer and other hyperproliferative diseases |
| MX2008007103A (es) | 2005-12-02 | 2008-09-12 | Bayer Healthcare Llc | Derivados 4-amino-pirrolotriazina sustituidos, útiles para tratar trastornos hiperproliferativos y enfermedades asociadas con angiogenesis. |
| PE20070855A1 (es) | 2005-12-02 | 2007-10-14 | Bayer Pharmaceuticals Corp | Derivados de 4-amino-pirrolotriazina sustituida como inhibidores de quinasas |
| WO2007065289A2 (en) | 2005-12-09 | 2007-06-14 | Basilea Pharmaceutica Ag | 4-oxo-(iso)tretinoin for the topical treatment of severe dermatological disorders |
| WO2007097991A2 (en) | 2006-02-16 | 2007-08-30 | Pharmasset, Inc. | Methods and kits for dosing of antiviral agents |
| CL2007001427A1 (es) | 2006-05-22 | 2008-05-16 | Novartis Ag | Sal de maleato de 5-amino-3-(2',3'-di-o-acetil-beta-d-ribofuranosil)-3h-tiazolo[4,5-d]pirimidin-2-ona; procedimiento de preparacion; composicion farmaceutica que comprende a dicho compuesto; y uso del compuesto para el tratamiento de una infeccion po |
| US7842672B2 (en) | 2006-07-07 | 2010-11-30 | Gilead Sciences, Inc. | Phosphonate inhibitors of HCV |
| WO2008033466A2 (en) | 2006-09-14 | 2008-03-20 | Combinatorx (Singapore) Pre. Ltd. | Compositions and methods for treatment of viral diseases |
| CA2672613A1 (en) | 2006-12-20 | 2008-07-03 | Istituto Di Ricerche Di Biologia Molecolare P. Angeletti S.P.A. | Nucleoside cyclic phosphoramidates for the treatment of rna-dependent rna viral infection |
| US20080261913A1 (en) | 2006-12-28 | 2008-10-23 | Idenix Pharmaceuticals, Inc. | Compounds and pharmaceutical compositions for the treatment of liver disorders |
| EP2124555B1 (en) | 2007-01-05 | 2015-07-08 | Merck Sharp & Dohme Corp. | Nucleoside aryl phosphoramidates for the treatment of rna-dependent rna viral infection |
| EP2535345A1 (en) | 2007-01-12 | 2012-12-19 | BioCryst Pharmaceuticals, Inc. | Anticancer nucleoside analogs |
| CN101730699A (zh) | 2007-03-21 | 2010-06-09 | 百时美施贵宝公司 | 可用于治疗增殖性、变应性、自身免疫性和炎症性疾病的稠合杂环化合物 |
| US7964580B2 (en) | 2007-03-30 | 2011-06-21 | Pharmasset, Inc. | Nucleoside phosphoramidate prodrugs |
| PL2155758T3 (pl) | 2007-05-10 | 2013-06-28 | Biocryst Pharm Inc | Pochodne tetrahydrofuro[3,4-d]dioksolanu przeznaczone do stosowania w leczeniu infekcji wirusowych i raka |
| CN100532388C (zh) | 2007-07-16 | 2009-08-26 | 郑州大学 | 2’-氟-4’-取代-核苷类似物、其制备方法及应用 |
| TW200942243A (en) | 2008-03-05 | 2009-10-16 | Biocryst Pharm Inc | Antiviral therapeutic agents |
| US8227431B2 (en) | 2008-03-17 | 2012-07-24 | Hetero Drugs Limited | Nucleoside derivatives |
| US7863291B2 (en) | 2008-04-23 | 2011-01-04 | Bristol-Myers Squibb Company | Quinuclidine compounds as alpha-7 nicotinic acetylcholine receptor ligands |
| AR071395A1 (es) | 2008-04-23 | 2010-06-16 | Gilead Sciences Inc | Analogos carba-nucleosidos 1'-sustituidos para tratamiento antiviral |
| WO2010036407A2 (en) | 2008-05-15 | 2010-04-01 | Biocryst Pharmaceuticals, Inc. | Antiviral nucleoside analogs |
| WO2010002877A2 (en) | 2008-07-03 | 2010-01-07 | Biota Scientific Management | Bycyclic nucleosides and nucleotides as therapeutic agents |
| EP2719701B1 (en) | 2009-02-10 | 2017-04-05 | Gilead Sciences, Inc. | Method for the preparation of thieno[3,4-d]pyrimidin-7-yl ribosides |
| AR075584A1 (es) | 2009-02-27 | 2011-04-20 | Intermune Inc | COMPOSICIONES TERAPEUTICAS QUE COMPRENDEN beta-D-2'-DESOXI-2'-FLUORO-2'-C-METILCITIDINA Y UN DERIVADO DE ACIDO ISOINDOL CARBOXILICO Y SUS USOS. COMPUESTO. |
| MX2011009928A (es) | 2009-03-24 | 2012-03-16 | Biocryst Pharm Inc | Sales farmaceuticas utiles de 7[(3r, 4r)-3-hidroxi-4-hidroximetil- pirrolidin-1-ilmetil]-3,5-dihidro-pirrol[3,2-d]pirimidin-4-ona. |
| TWI576352B (zh) | 2009-05-20 | 2017-04-01 | 基利法瑪席特有限責任公司 | 核苷磷醯胺 |
| NZ599404A (en) | 2009-09-21 | 2014-02-28 | Gilead Sciences Inc | Processes and intermediates for the preparation of 1’-substituted carba-nucleoside analogs |
| US7973013B2 (en) | 2009-09-21 | 2011-07-05 | Gilead Sciences, Inc. | 2'-fluoro substituted carba-nucleoside analogs for antiviral treatment |
| CR20190103A (es) | 2009-09-21 | 2019-09-19 | Gilead Sciences Inc | ANÁLOGOS DE CARBA-NUCLEÓSIDOS SUSTITUIDOS CON 2'-FLUORO PARA TRATAMIENTO ANTIVIRAL (Divisional 2012-0186) |
| US8455451B2 (en) | 2009-09-21 | 2013-06-04 | Gilead Sciences, Inc. | 2'-fluoro substituted carba-nucleoside analogs for antiviral treatment |
| CN102858790A (zh) | 2010-03-31 | 2013-01-02 | 吉利德制药有限责任公司 | 核苷氨基磷酸酯 |
| WO2011123672A1 (en) * | 2010-03-31 | 2011-10-06 | Pharmasset, Inc. | Purine nucleoside phosphoramidate |
| TW201201815A (en) | 2010-05-28 | 2012-01-16 | Gilead Sciences Inc | 1'-substituted-carba-nucleoside prodrugs for antiviral treatment |
| JP5937073B2 (ja) | 2010-07-19 | 2016-06-22 | ギリード・サイエンシズ・インコーポレーテッド | ジアステレオマーとして純粋なホスホルアミデートプロドラッグの調製方法 |
| PE20171155A1 (es) | 2010-07-22 | 2017-08-16 | Gilead Sciences Inc | Metodos y compuestos para tratar infecciones virales por paramyxoviridae |
| TW201305185A (zh) | 2010-09-13 | 2013-02-01 | Gilead Sciences Inc | 用於抗病毒治療之2’-氟取代之碳-核苷類似物 |
| WO2012039791A1 (en) | 2010-09-20 | 2012-03-29 | Gilead Sciences, Inc. | 2' -fluoro substituted carba-nucleoside analogs for antiviral treatment |
| RS54072B1 (en) | 2010-10-15 | 2015-10-30 | Biocryst Pharmaceuticals Inc. | COMPOSITIONS FOR USE IN THE TREATMENT OF Viral INFECTIONS |
-
2011
- 2011-07-19 JP JP2013520821A patent/JP5937073B2/ja active Active
- 2011-07-19 KR KR1020137003792A patent/KR101995598B1/ko active IP Right Grant
- 2011-07-19 KR KR1020207012760A patent/KR20200052384A/ko not_active Application Discontinuation
- 2011-07-19 PT PT117434001T patent/PT2596004E/pt unknown
- 2011-07-19 KR KR1020197018279A patent/KR102108864B1/ko active IP Right Grant
- 2011-07-19 MA MA35666A patent/MA34471B1/fr unknown
- 2011-07-19 PE PE2013000093A patent/PE20130807A1/es not_active Application Discontinuation
- 2011-07-19 EP EP11743400.1A patent/EP2596004B1/en active Active
- 2011-07-19 MX MX2013000656A patent/MX2013000656A/es active IP Right Grant
- 2011-07-19 ES ES11743400.1T patent/ES2524398T3/es active Active
- 2011-07-19 CN CN2011800352819A patent/CN103052646A/zh active Pending
- 2011-07-19 US US13/813,886 patent/US9090642B2/en active Active
- 2011-07-19 NZ NZ606141A patent/NZ606141A/en unknown
- 2011-07-19 EP EP14181224.8A patent/EP2805960A1/en not_active Withdrawn
- 2011-07-19 SG SG2012095691A patent/SG186831A1/en unknown
- 2011-07-19 CA CA2804375A patent/CA2804375C/en active Active
- 2011-07-19 EA EA201390133A patent/EA025311B1/ru unknown
- 2011-07-19 WO PCT/US2011/044581 patent/WO2012012465A1/en active Application Filing
- 2011-07-19 AP AP2013006665A patent/AP2013006665A0/xx unknown
- 2011-07-19 AU AU2011282241A patent/AU2011282241B2/en active Active
- 2011-07-19 BR BR112013001267A patent/BR112013001267A2/pt not_active Application Discontinuation
-
2012
- 2012-12-31 IL IL224045A patent/IL224045A/en active IP Right Grant
-
2013
- 2013-01-07 ZA ZA2013/00135A patent/ZA201300135B/en unknown
- 2013-01-08 CL CL2013000076A patent/CL2013000076A1/es unknown
- 2013-01-10 CO CO13004205A patent/CO6680607A2/es unknown
- 2013-02-14 CR CR20130063A patent/CR20130063A/es unknown
- 2013-02-19 EC ECSP13012451 patent/ECSP13012451A/es unknown
-
2015
- 2015-06-22 US US14/746,430 patent/US9487544B2/en active Active
-
2016
- 2016-07-11 IL IL246704A patent/IL246704A/en active IP Right Grant
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR102108864B1 (ko) | 부분입체 이성질성으로 순수한 포스포라미데이트 전구약물의 제조 방법 | |
| US10118941B2 (en) | Methods for the preparation of diastereomerically pure phosphoramidate prodrugs | |
| EP2719701B1 (en) | Method for the preparation of thieno[3,4-d]pyrimidin-7-yl ribosides | |
| CA2963907C (en) | Methods for the preparation of ribosides | |
| EP2480559B1 (en) | Processes and intermediates for the preparation of 1'-cyano-carbanucleoside analogs | |
| KR20110038683A (ko) | 사이클로프로필 폴리머라제 저해제 | |
| US8119800B2 (en) | Processes for preparing HIV reverse transcriptase inhibitors | |
| OA16292A (en) | Methods for the preparation of diasteromerically pure phosphoramidate prodrugs. | |
| SE1451080A1 (sv) | Medivir AB, Box 1086, 141 22 Huddinge, SE | |
| WO2006122207A1 (en) | 6-hydrazinopurine 2'-methyl ribonucleosides and nucleotides for treatment of hcv | |
| OA20831A (en) | Methods for treating filoviridae virus infections. |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A107 | Divisional application of patent | ||
| A201 | Request for examination | ||
| E902 | Notification of reason for refusal | ||
| E601 | Decision to refuse application |