KR20110122051A - 유기광전소자용 화합물 및 이를 포함하는 유기광전소자 - Google Patents
유기광전소자용 화합물 및 이를 포함하는 유기광전소자 Download PDFInfo
- Publication number
- KR20110122051A KR20110122051A KR1020100106077A KR20100106077A KR20110122051A KR 20110122051 A KR20110122051 A KR 20110122051A KR 1020100106077 A KR1020100106077 A KR 1020100106077A KR 20100106077 A KR20100106077 A KR 20100106077A KR 20110122051 A KR20110122051 A KR 20110122051A
- Authority
- KR
- South Korea
- Prior art keywords
- substituted
- group
- unsubstituted
- formula
- compound
- Prior art date
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/14—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/14—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/14—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D409/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms
- C07D409/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D421/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having selenium, tellurium, or halogen atoms as ring hetero atoms
- C07D421/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having selenium, tellurium, or halogen atoms as ring hetero atoms containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09B—ORGANIC DYES OR CLOSELY-RELATED COMPOUNDS FOR PRODUCING DYES, e.g. PIGMENTS; MORDANTS; LAKES
- C09B57/00—Other synthetic dyes of known constitution
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent, e.g. electroluminescent, chemiluminescent materials
- C09K11/06—Luminescent, e.g. electroluminescent, chemiluminescent materials containing organic luminescent materials
-
- H—ELECTRICITY
- H05—ELECTRIC TECHNIQUES NOT OTHERWISE PROVIDED FOR
- H05B—ELECTRIC HEATING; ELECTRIC LIGHT SOURCES NOT OTHERWISE PROVIDED FOR; CIRCUIT ARRANGEMENTS FOR ELECTRIC LIGHT SOURCES, IN GENERAL
- H05B33/00—Electroluminescent light sources
- H05B33/12—Light sources with substantially two-dimensional radiating surfaces
- H05B33/14—Light sources with substantially two-dimensional radiating surfaces characterised by the chemical or physical composition or the arrangement of the electroluminescent material, or by the simultaneous addition of the electroluminescent material in or onto the light source
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/654—Aromatic compounds comprising a hetero atom comprising only nitrogen as heteroatom
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6572—Polycyclic condensed heteroaromatic hydrocarbons comprising only nitrogen in the heteroaromatic polycondensed ring system, e.g. phenanthroline or carbazole
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1022—Heterocyclic compounds bridged by heteroatoms, e.g. N, P, Si or B
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1029—Heterocyclic compounds characterised by ligands containing one nitrogen atom as the heteroatom
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1044—Heterocyclic compounds characterised by ligands containing two nitrogen atoms as heteroatoms
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1059—Heterocyclic compounds characterised by ligands containing three nitrogen atoms as heteroatoms
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/11—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E10/00—Energy generation through renewable energy sources
- Y02E10/50—Photovoltaic [PV] energy
- Y02E10/549—Organic PV cells
Abstract
Description
수명, 효율, 전기화학적 안정성 및 열적 안정성이 우수한 유기광전소자를 제공할 수 있는 유기광전소자용 화합물 및 이를 포함하는 유기광전소자에 관한 것이다.
유기광전소자(organic photoelectric device)라 함은 정공 또는 전자를 이용한 전극과 유기물 사이에서의 전하 교류를 필요로 하는 소자를 의미한다.
유기광전소자는 동작 원리에 따라 하기와 같이 크게 두 가지로 나눌 수 있다. 첫째는 외부의 광원으로부터 소자로 유입된 광자에 의하여 유기물층에서 엑시톤(exciton)이 형성되고 이 엑시톤이 전자와 정공으로 분리되고, 이 전자와 정공이 각각 다른 전극으로 전달되어 전류원(전압원)으로 사용되는 형태의 전자소자이다.
둘째는 2 개 이상의 전극에 전압 또는 전류를 가하여 전극과 계면을 이루는 유기물 반도체에 정공 또는 전자를 주입하고, 주입된 전자와 정공에 의하여 동작하는 형태의 전자소자이다.
유기광전소자의 예로는 유기발광소자, 유기태양전지, 유기감광체 드럼(organic photo conductor drum), 유기트랜지스터 등이 있으며, 이들은 모두 소자의 구동을 위하여 정공의 주입 또는 수송 물질, 전자의 주입 또는 수송 물질, 또는 발광 물질을 필요로 한다.
특히, 유기발광소자(organic light emitting diodes, OLED)는 최근 평판 디스플레이(flat panel display)의 수요가 증가함에 따라 주목받고 있다. 일반적으로 유기 발광 현상이란 유기 물질을 이용하여 전기에너지를 빛에너지로 전환시켜주는 현상을 말한다.
이러한 유기발광소자는 유기발광재료에 전류를 가하여 전기에너지를 빛으로 전환시키는 소자로서 통상 양극(anode)과 음극(cathode) 사이에 기능성 유기물 층이 삽입된 구조로 이루어져 있다. 여기서 유기물층은 유기광전소자의 효율과 안정성을 높이기 위하여 각기 다른 물질로 구성된 다층의 구조로 이루어진 경우가 많으며, 예컨대 정공주입층, 정공수송층, 발광층, 전자수송층, 전자주입층 등으로 이루어질 수 있다.
이러한 유기발광소자의 구조에서 두 전극 사이에 전압을 걸어주게 되면 양극에서는 정공(hole)이, 음극에서는 전자(electron)가 유기물층에 주입되게 되고, 주입된 정공과 전자가 만나 재결합(recombination)에 의해 에너지가 높은 여기자를 형성하게 된다. 이때 형성된 여기자가 다시 바닥상태(ground state)로 이동하면서 특정한 파장을 갖는 빛이 발생하게 된다.
최근에는, 형광 발광물질뿐 아니라 인광 발광물질도 유기광전소자의 발광물질로 사용될 수 있음이 알려졌으며, 이러한 인광 발광은 바닥상태(ground state)에서 여기상태(excited state)로 전자가 전이한 후, 계간 전이(intersystem crossing)를 통해 단일항 여기자가 삼중항 여기자로 비발광 전이된 다음, 삼중항 여기자가 바닥상태로 전이하면서 발광하는 메카니즘으로 이루어진다.
상기한 바와 같이 유기발광소자에서 유기물층으로 사용되는 재료는 기능에 따라, 발광 재료와 전하 수송 재료, 예컨대 정공주입 재료, 정공수송 재료, 전자수송 재료, 전자주입 재료 등으로 분류될 수 있다.
또한, 발광 재료는 발광색에 따라 청색, 녹색, 적색 발광재료와 보다 나은 천연색을 구현하기 위해 필요한 노란색 및 주황색 발광 재료로 구분될 수 있다.
한편, 발광 재료로서 하나의 물질만 사용하는 경우 분자간 상호 작용에 의하여 최대 발광 파장이 장파장으로 이동하고 색순도가 떨어지거나 발광 감쇄 효과로 소자의 효율이 감소되는 문제가 발생하므로, 색순도의 증가와 에너지 전이를 통한 발광 효율과 안정성을 증가시키기 위하여 발광 재료로서 호스트/도판트 계를 사용할 수 있다.
유기발광소자가 전술한 우수한 특징들을 충분히 발휘하기 위해서는 소자 내 유기물층을 이루는 물질, 예컨대 정공주입 물질, 정공수송 물질, 발광 물질, 전자수송 물질, 전자주입 물질, 발광 재료 중 호스트 및/또는 도판트 등이 안정하고 효율적인 재료에 의하여 뒷받침되는 것이 선행되어야 하며, 아직까지 안정하고 효율적인 유기발광소자용 유기물층 재료의 개발이 충분히 이루어지지 않은 상태이며, 따라서 새로운 재료의 개발이 계속 요구되고 있다. 이와 같은 재료 개발의 필요성은 전술한 다른 유기광전소자에서도 마찬가지이다.
또한, 저분자 유기발광소자는 진공 증착법에 의해 박막의 형태로 소자를 제조하므로 효율 및 수명성능이 좋으며, 고분자 유기 발광 소자는 잉크젯(Inkjet) 또는 스핀코팅(spin coating)법을 사용하여 초기 투자비가 적고 대면적화가 유리한 장점이 있다.
저분자 유기발광소자 및 고분자 유기발광소자는 모두 자체발광, 고속응답, 광시야각, 초박형, 고화질, 내구성, 넓은 구동온도범위 등의 장점을 가지고 있어 차세대 디스플레이로 주목을 받고 있다.특히 기존의 LCD(liquid crystal display)와 비교하여 자체발광형으로서 어두운 곳이나 외부의 빛이 들어와도 시안성이 좋으며, 백라이트가 필요 없어 LCD의 1/3수준으로 두께 및 무게를 줄일 수 있다.
또한, 응답속도가 LCD에 비해 1000배 이상 빠른 마이크로 초 단위여서 잔상이 없는 완벽한 동영상을 구현할 수 있다. 따라서, 최근 본격적인 멀티미디어 시대에 맞춰 최적의 디스플레이로 각광받을 것으로 기대되며, 이러한 장점을 바탕으로 1980년대 후반 최초 개발 이후 효율 80배, 수명 100배 이상에 이르는 급격한 기술발전을 이루어 왔고, 최근에는 40인치 유기발광소자 패널이 발표되는 등 대형화가 급속히 진행되고 있다.
대형화를 위해서는 발광 효율의 증대 및 소자의 수명 향상이 수반되어야 한다. 이때, 소자의 발광 효율은 발광층 내의 정공과 전자의 결합이 원활히 이루어져야 한다. 그러나, 일반적으로 유기물의 전자 이동도는 정공 이동도에 비해 느리므로, 발광층 내의 정공과 전자의 결합이 효율적으로 이루어지기 위해서는, 효율적인 전자 수송층을 사용하여 음극으로부터의 전자 주입 및 이동도를 높이는 동시에, 정공의 이동을 차단할 수 있어야 한다.
또한, 수명 향상을 위해서는 소자의 구동시 발생하는 줄열(Joule heat)로 인해 재료가 결정화되는 것을 방지하여야 한다. 따라서, 전자의 주입 및 이동성이 우수하며, 전기화학적 안정성이 높은 유기 화합물에 대한 개발이 필요하다.
발광, 또는 전자 주입 및 수송역할을 할 수 있고, 적절한 도펀트와 함께 발광 호스트로서의 역할을 할 수 있는 유기광전소자용 화합물을 제공한다.
수명, 효율, 구동전압, 전기화학적 안정성 및 열적 안정성이 우수한 유기광전소자를 제공하고자 한다.
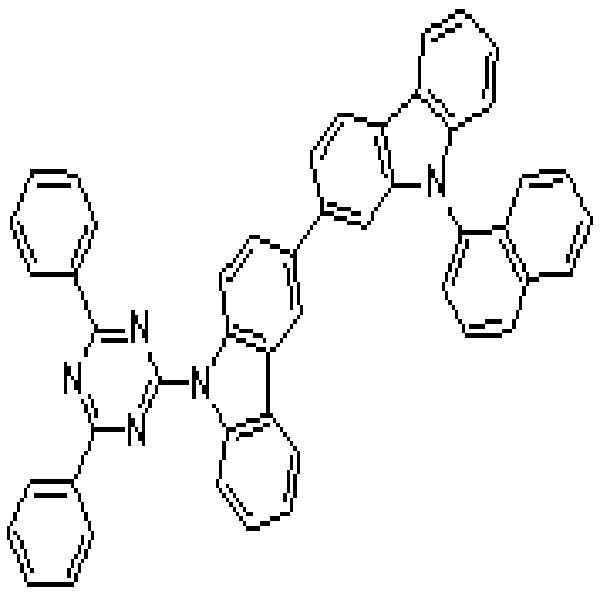
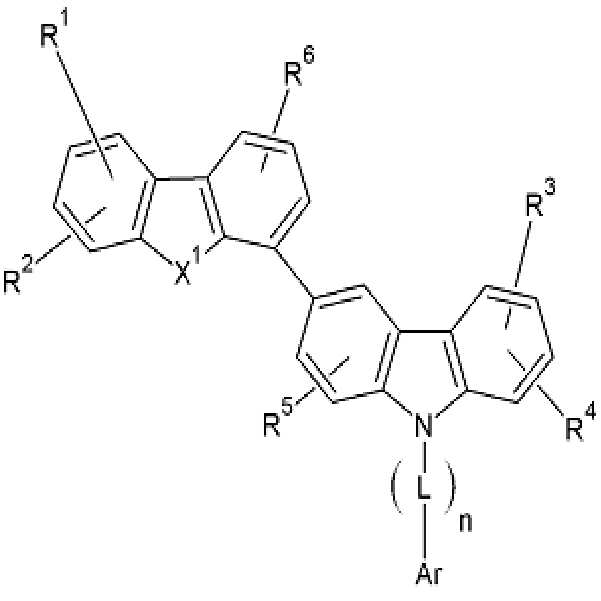
본 발명의 일 측면에서는, 하기 화학식 1로 표시되는 유기광전소자용 화합물을 제공한다.
[화학식 1]
상기 화학식 1에서, X1 및 X2는 서로 동일하거나 상이하며, 독립적으로 NR', O, Se, P 및 S 로 이루어진 군에서 선택되고, 상기 R'는 수소, 중수소, 치환 또는 비치환된 C1 내지 C20 알킬기, 치환 또는 비치환된 C6 내지 C30 아릴기 및 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기로 이루어진 군에서 선택되고, 상기 R1 내지 R6는 서로 동일하거나 상이하며, 독립적으로 수소, 중수소, 치환 또는 비치환된 C1 내지 C20 알킬기, 치환 또는 비치환된 C6 내지 C30 아릴기 및 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기로 이루어진 군에서 선택되고, 상기 R1 내지 R6 또는 R' 중 적어도 어느 하나는 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기다.
상기 유기광전소자용 화합물은 하기 화학식 2로 표시되는 것일 수 있다.
[화학식 2]
상기 화학식 2에서, X1 및 X2는 서로 동일하거나 상이하며, 독립적으로 NR', O, Se, P 및 S 로 이루어진 군에서 선택되고, 상기 R'는 수소, 중수소, 치환 또는 비치환된 C1 내지 C20 알킬기, 치환 또는 비치환된 C6 내지 C30 아릴기 및 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기로 이루어진 군에서 선택되고, 상기 R1 내지 R6는 서로 동일하거나 상이하며, 독립적으로 수소, 중수소, 치환 또는 비치환된 C1 내지 C20 알킬기, 치환 또는 비치환된 C6 내지 C30 아릴기 및 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기로 이루어진 군에서 선택되고, 상기 R1 내지 R6 또는 R' 중 적어도 어느 하나는 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기다.
상기 X1은 NR'일 수 있다.
상기 R'는 수소, 중수소, 치환 또는 비치환된 C1 내지 C20 알킬기, 치환 또는 비치환된 C6 내지 C30 아릴기 및 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기로 이루어진 군에서 선택될 수 있다.
상기 R'는 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기일 수 있다.
X1는 NR'이고, 상기 R'는 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기고, 상기 R1 내지 R6는 서로 동일하거나 상이하며, 독립적으로 수소, 중수소, 치환 또는 비치환된 C1 내지 C20 알킬기 및 치환 또는 비치환된 C6 내지 C30 아릴기로 이루어진 군에서 선택될 수 있다.
상기 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기는 치환 또는 비치환된 이미다졸릴기, 치환 또는 비치환된 트리아졸릴기, 치환 또는 비치환된 테트라졸릴기, 치환 또는 비치환된 옥사다이아졸릴기, 치환 또는 비치환된 옥사트리아졸릴기, 치환 또는 비치환된 싸이아트리아졸릴기, 치환 또는 비치환된 벤즈이미다졸릴기, 치환 또는 비치환된 벤조트리아졸릴기, 치환 또는 비치환된 피리디닐기, 치환 또는 비치환된 피리미디닐기, 치환 또는 비치환된 트리아지닐기, 치환 또는 비치환된 피라지닐기, 치환 또는 비치환된 피리다지닐기, 퀴놀린, 치환 또는 비치환된 이소퀴놀린, 치환 또는 비치환된 프탈라진, 치환 또는 비치환된 나프피리딘, 치환 또는 비치환된 퀴녹살린, 치환 또는 비치환된 퀴나졸린, 치환 또는 비치환된 아크리딘, 치환 또는 비치환된 페난트롤린 및 치환 또는 비치환된 페나진으로 이루어진 군에서 선택될 수 있다.
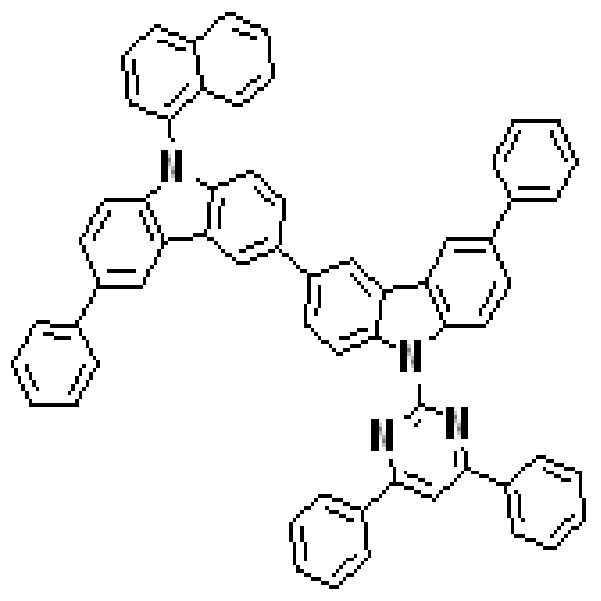
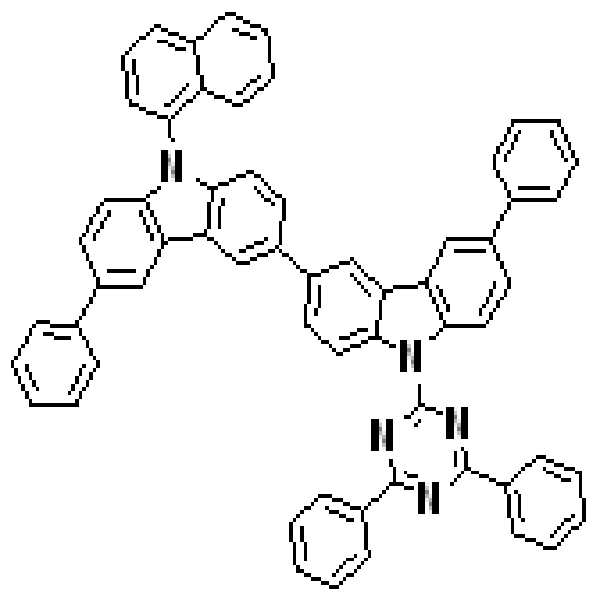
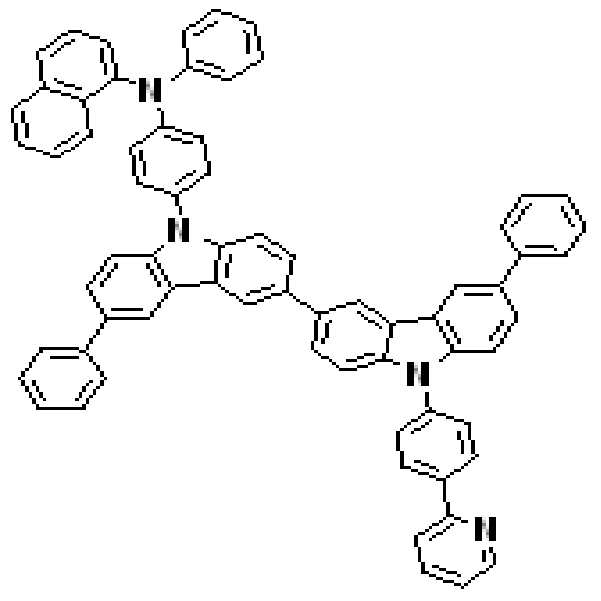
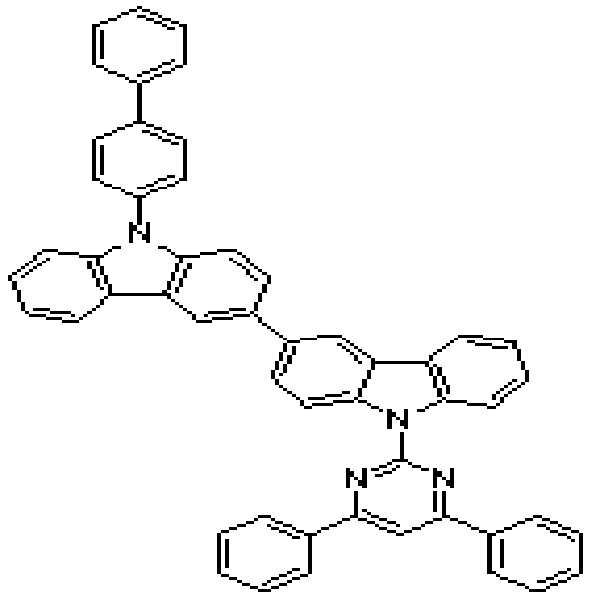
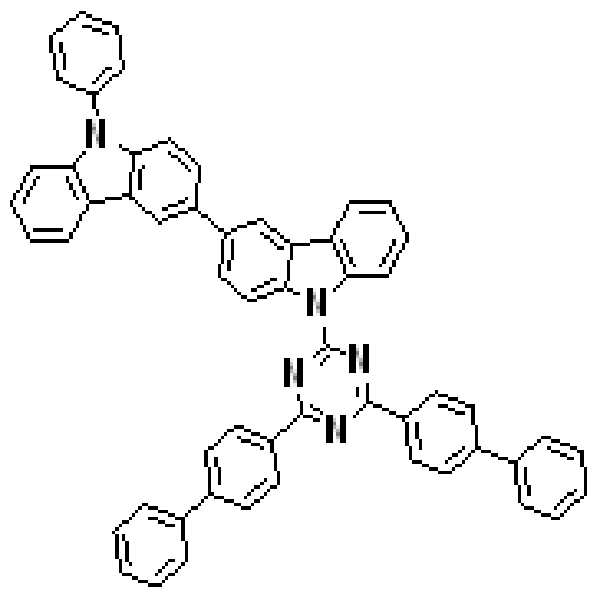
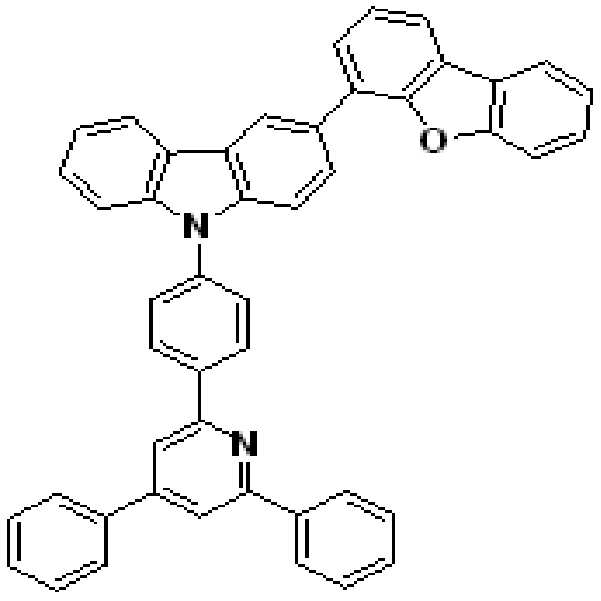
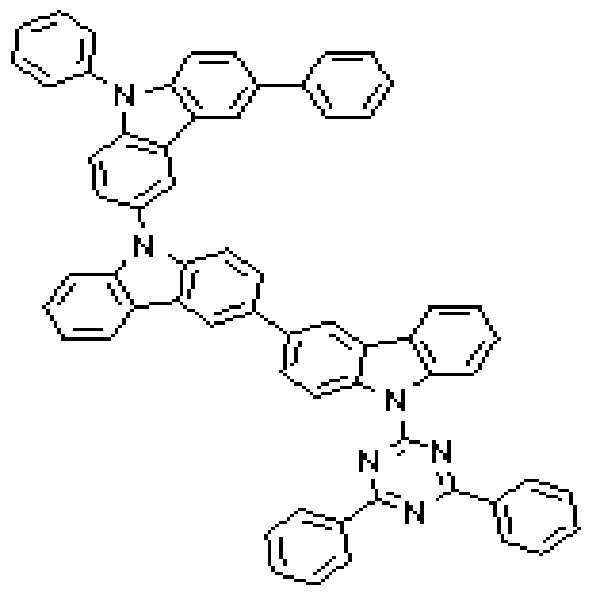
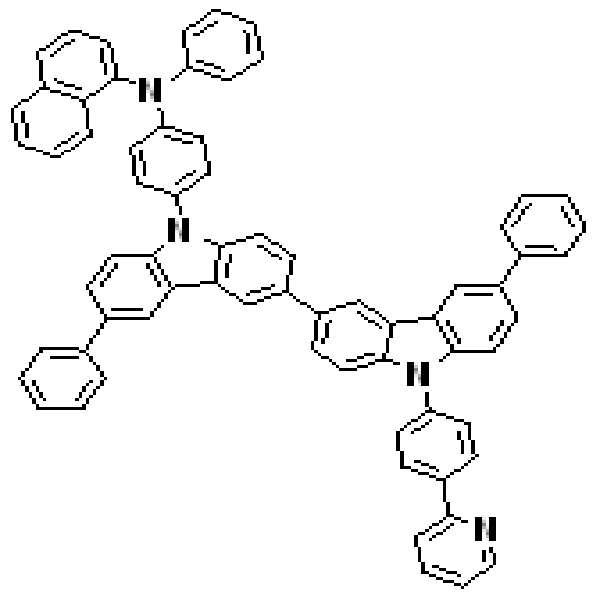
본 발명의 다른 측면에서는, 하기 화학식 3 내지 51 중 어느 하나로 표시되는 유기광전소자용 화합물을 제공한다.
[화학식 3] [화학식 4]
[화학식 5] [화학식 6]
[화학식 7] [화학식 8]
[화학식 9] [화학식 10]
[화학식 11] [화학식 12]
[화학식 13] [화학식 14]
[화학식 15] [화학식 16]
[화학식 17] [화학식 18]
[화학식 19] [화학식 20]
[화학식 21] [화학식 22]
[화학식 23] [화학식 24]
[화학식 25] [화학식 26]
[화학식 27] [화학식 28]
[화학식 29] [화학식 30]
[화학식 31] [화학식 32]
[화학식 33] [화학식 34]
[화학식 35] [화학식 36]
[화학식 37] [화학식 38]
[화학식 39] [화학식 40]
[화학식 41] [화학식 42]
[화학식 43] [화학식 44]
[화학식 45] [화학식 46]
[화학식 47] [화학식 48]
[화학식 49] [화학식 50]
[화학식 51] [화학식 52]
[화학식 53] [화학식 54]
상기 유기광전소자용 화합물은 하기 화학식 A 또는 A1로 표시되는 것일 수 있다.
[화학식 A]
[화학식 A1]
상기 화학식 A 및 A1에서, X1 및 X2는 서로 동일하거나 상이하며, 독립적으로 NR', O, Se, P 및 S 로 이루어진 군에서 선택되고, 상기 R'는 수소, 중수소, 치환 또는 비치환된 C1 내지 C20 알킬기, 치환 또는 비치환된 C6 내지 C30 아릴기 및 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기로 이루어진 군에서 선택되고, 상기 R1 내지 R6는 서로 동일하거나 상이하며, 독립적으로 수소, 중수소, 치환 또는 비치환된 C1 내지 C20 알킬기, 치환 또는 비치환된 C6 내지 C30 아릴기 및 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기로 이루어진 군에서 선택되고, 상기 R1 내지 R6 또는 R' 중 적어도 어느 하나는 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기다.
상기 X1 또는 X2 중 적어도 하나는 NR'이고, 상기 R'는 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기고, 상기 R1 내지 R6는 서로 동일하거나 상이하며, 독립적으로 수소, 중수소, 치환 또는 비치환된 C1 내지 C20 알킬기 및 치환 또는 비치환된 C6 내지 C30 아릴기로 이루어진 군에서 선택되는 것일 수 있다.
상기 X1 또는 X2 중 적어도 하나는 NR'이고, 상기 R'는 치환 또는 비치환된 트리페닐레닐기인 것일 수 있다.
상기 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기는 치환 또는 비치환된 이미다졸릴기, 치환 또는 비치환된 트리아졸릴기, 치환 또는 비치환된 테트라졸릴기, 치환 또는 비치환된 옥사다이아졸릴기, 치환 또는 비치환된 옥사트리아졸릴기, 치환 또는 비치환된 싸이아트리아졸릴기, 치환 또는 비치환된 벤즈이미다졸릴기, 치환 또는 비치환된 벤조트리아졸릴기, 치환 또는 비치환된 피리디닐기, 치환 또는 비치환된 피리미디닐기, 치환 또는 비치환된 트리아지닐기, 치환 또는 비치환된 피라지닐기, 치환 또는 비치환된 피리다지닐기, 치환 또는 비치환된 퓨리닐기, 치환 또는 비치환된 퀴놀리닐기, 치환 또는 비치환된 이소퀴놀리닐기, 치환 또는 비치환된 프탈라지닐기, 치환 또는 비치환된 나프피리디닐기, 치환 또는 비치환된 퀴녹살리닐기, 치환 또는 비치환된 퀴나졸리닐기, 치환 또는 비치환된 아크리디닐기, 치환 또는 비치환된 페난트롤리닐기 및 치환 또는 비치환된 페나지닐기으로 이루어진 군에서 선택되는 것일 수 있다.
상기 유기광전소자용 화합물은 하기 화학식 B로 표시되는 것일 수 있다.
[화학식 B]
상기 화학식 B에서, X1은 O, Se, P 및 S 로 이루어진 군에서 선택되고, R1 내지 R6는 서로 동일하거나 상이하며, 독립적으로 수소, 중수소, 치환 또는 비치환된 C1 내지 C20 알킬기, 치환 또는 비치환된 C6 내지 C30 아릴기 및 치환 또는 비치환된 C2 내지 C30 헤테로아릴기로 이루어진 군에서 선택되고, Ar은 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기이고, L은 단일결합, 치환 또는 비치환된 C2 내지 C10 알케닐렌기, 치환 또는 비치환된 C2 내지 C10 알키닐렌기, 치환 또는 비치환된 C6 내지 C30 아릴렌기 및 치환 또는 비치환된 C2 내지 C30 헤테로아릴렌기로 이루어진 군에서 선택되고, n은 0 내지 2 중 어느 하나의 정수이다.
상기 유기광전소자용 화합물은 하기 화학식 B1 또는 B2로 표시되는 것일 수 있다.
[화학식 B1]
[화학식 B2]
상기 화학식 B1 및 B2에 있어서, X1은 O, Se, P 및 S 로 이루어진 군에서 선택되고, R1 내지 R6는 서로 동일하거나 상이하며, 독립적으로 수소, 중수소, 치환 또는 비치환된 C1 내지 C20 알킬기, 치환 또는 비치환된 C6 내지 C30 아릴기 및 치환 또는 비치환된 C2 내지 C30 헤테로아릴기로 이루어진 군에서 선택되고, Ar은 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기이고, L은 단일결합, 치환 또는 비치환된 C2 내지 C10 알케닐렌기, 치환 또는 비치환된 C2 내지 C10 알키닐렌기, 치환 또는 비치환된 C6 내지 C30 아릴렌기 및 치환 또는 비치환된 C2 내지 C30 헤테로아릴렌기로 이루어진 군에서 선택되고, n은 0 내지 2 중 어느 하나의 정수이다.
상기 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기는 치환 또는 비치환된 이미다졸릴기, 치환 또는 비치환된 트리아졸릴기, 치환 또는 비치환된 테트라졸릴기, 치환 또는 비치환된 옥사다이아졸릴기, 치환 또는 비치환된 옥사트리아졸릴기, 치환 또는 비치환된 싸이아트리아졸릴기, 치환 또는 비치환된 벤즈이미다졸릴기, 치환 또는 비치환된 벤조트리아졸릴기, 치환 또는 비치환된 피리디닐기, 치환 또는 비치환된 피리미디닐기, 치환 또는 비치환된 트리아지닐기, 치환 또는 비치환된 피라지닐기, 치환 또는 비치환된 피리다지닐기, 치환 또는 비치환된 퓨리닐기, 치환 또는 비치환된 퀴놀리닐기, 치환 또는 비치환된 이소퀴놀리닐기, 치환 또는 비치환된 프탈라지닐기, 치환 또는 비치환된 나프피리디닐기, 치환 또는 비치환된 퀴녹살리닐기, 치환 또는 비치환된 퀴나졸리닐기, 치환 또는 비치환된 아크리디닐기, 치환 또는 비치환된 페난트롤리닐기 및 치환 또는 비치환된 페나지닐기으로 이루어진 군에서 선택되는 것일 수 있다.
상기 유기광전소자용 화합물은 하기 화학식 C로 표시되는 것일 수 있다.
[화학식 C]
상기 화학식 C에 있어서, R1 내지 R6 및 Ar2는 서로 동일하거나 상이하며, 독립적으로 수소, 중수소, 치환 또는 비치환된 C1 내지 C20 알킬기, 치환 또는 비치환된 C6 내지 C30 아릴기 및 치환 또는 비치환된 C2 내지 C30 헤테로아릴기로 이루어진 군에서 선택되고, Ar1은 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기이고, L은 단일결합, 치환 또는 비치환된 C2 내지 C10 알케닐렌기, 치환 또는 비치환된 C2 내지 C10 알키닐렌기, 치환 또는 비치환된 C6 내지 C30 아릴렌기 및 치환 또는 비치환된 C2 내지 C30 헤테로아릴렌기로 이루어진 군에서 선택되고, n은 1 또는 2이다.
상기 Ar2는 치환 또는 비치환된 트리페닐레닐기인 것일 수 있다.
상기 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기는 치환 또는 비치환된 이미다졸릴기, 치환 또는 비치환된 트리아졸릴기, 치환 또는 비치환된 테트라졸릴기, 치환 또는 비치환된 옥사다이아졸릴기, 치환 또는 비치환된 옥사트리아졸릴기, 치환 또는 비치환된 싸이아트리아졸릴기, 치환 또는 비치환된 벤즈이미다졸릴기, 치환 또는 비치환된 벤조트리아졸릴기, 치환 또는 비치환된 피리디닐기, 치환 또는 비치환된 피리미디닐기, 치환 또는 비치환된 트리아지닐기, 치환 또는 비치환된 피라지닐기, 치환 또는 비치환된 피리다지닐기, 치환 또는 비치환된 퓨리닐기, 치환 또는 비치환된 퀴놀리닐기, 치환 또는 비치환된 이소퀴놀리닐기, 치환 또는 비치환된 프탈라지닐기, 치환 또는 비치환된 나프피리디닐기, 치환 또는 비치환된 퀴녹살리닐기, 치환 또는 비치환된 퀴나졸리닐기, 치환 또는 비치환된 아크리디닐기, 치환 또는 비치환된 페난트롤리닐기 및 치환 또는 비치환된 페나지닐기으로 이루어진 군에서 선택되는 것일 수 있다.
상기 유기광전소자는 유기발광소자, 유기태양전지, 유기트랜지스터, 유기 감광체 드럼 및 유기메모리소자로 이루어진 군에서 선택되는 것일 수 있다.
본 발명의 또 다른 측면에서는, 양극, 음극 및 상기 양극과 음극 사이에 개재되는 적어도 한 층 이상의 유기박막층을 포함하는 유기발광소자에 있어서, 상기 유기박막층 중 적어도 어느 한 층은 전술한 유기광전소자용 화합물을 포함하는 것인 유기발광소자를 제공한다.
상기 유기박막층은 발광층, 정공수송층, 정공주입층, 전자수송층, 전자주입층, 정공차단층 및 이들의 조합을 이루어진 군에서 선택되는 것일 수 있다.
상기 유기광전소자용 화합물은 전자수송층 또는 전자주입층 내에 포함되는 것일 수 있다.
상기 유기광전소자용 화합물은 발광층 내에 포함되는 것일 수 있다.
상기 유기광전소자용 화합물은 발광층 내에 인광 또는 형광 호스트 재료로서 사용되는 것일 수 있다.
상기 유기광전소자용 화합물은 발광층 내에 형광 청색 도펀트 재료로서 사용되는 것일 수 있다.
본 발명의 다른 측면에서는 전술한 유기발광소자를 포함하는 것인 표시장치를 제공한다.
우수한 전기화학적 및 열적 안정성으로 수명 특성이 우수하고, 낮은 구동전압에서도 높은 발광효율을 가지는 유기광전소자를 제공할 수 있다.
도 1 내지 도 5는 본 발명의 일 구현예에 따른 유기광전소자용 화합물을 이용하여 제조될 수 있는 유기광전소자에 대한 다양한 구현예들을 나타내는 단면도이다.
이하, 본 발명의 구현예를 상세히 설명하기로 한다. 다만, 이는 예시로서 제시되는 것으로, 이에 의해 본 발명이 제한되지는 않으며 본 발명은 후술할 청구범위의 범주에 의해 정의될 뿐이다.
본 명세서에서 "치환"이란 별도의 정의가 없는 한, 치환기 또는 화합물 중의 적어도 하나의 수소가 중수소, 할로겐기, 히드록시기, 아미노기, 치환 또는 비치환된 C1 내지 C20 아민기, 니트로기, 치환 또는 비치환된 C3 내지 C40 실릴기, C1 내지 C30 알킬기, C1 내지 C10 알킬실릴기, C3 내지 C30 시클로알킬기, C6 내지 C30 아릴기, C1 내지 C20 알콕시기, 플루오로기, 트리플루오로메틸기 등의 C1 내지 C10 트리플루오로알킬기, 또는 시아노기로 치환된 것을 의미한다.
본 명세서에서 "헤테로"란 별도의 정의가 없는 한, 하나의 작용기 내에 N, O, S 및 P로 이루어진 군에서 선택되는 헤테로 원자를 1 내지 3개 함유하고, 나머지는 탄소인 것을 의미한다.
본 명세서에서 "이들의 조합"이란 별도의 정의가 없는 한, 둘 이상의 치환기가 연결기로 결합되어 있거나, 둘 이상의 치환기가 축합하여 결합되어 있는 것을 의미한다.
본 명세서에서 "알킬(alkyl)기"이란 별도의 정의가 없는 한, 지방족 탄화수소기를 의미한다. 알킬기는 어떠한 알켄기나 알킨기를 포함하고 있지 않음을 의미하는 "포화 알킬(saturated alkyl)기"일 수 있다. 알킬기는 적어도 하나의 알켄기 또는 알킨기를 포함하고 있음을 의미하는 "불포화 알킬(unsaturated alkyl)기"일 수도 있다. "알켄(alkene)기"는 적어도 두 개의 탄소원자가 적어도 하나의 탄소탄소 이중 결합으로 이루어진 작용기를 의미하며, "알킨(alkyne)기" 는 적어도 두 개의 탄소원자가 적어도 하나의 탄소탄소 삼중 결합으로 이루어진 작용기를 의미한다. 포화이든 불포화이든 간에 알킬기는 분지형, 직쇄형 또는 환형일 수 있다.
알킬기는 C1 내지 C20인 알킬기일 수 있다. 알킬기는 C1 내지 C10인 중간 크기의 알킬기일 수도 있다. 알킬기는 C1 내지 C6인 저급 알킬기일 수도 있다.
예를 들어, C1 내지 C4 알킬기는 알킬쇄에 1 내지 4 개의 탄소원자, 즉, 알킬쇄는 메틸, 에틸, 프로필, 이소프로필, n부틸, 이소부틸, sec부틸 및 t부틸로 이루어진 군에서 선택됨을 나타낸다.
전형적인 알킬기에는 메틸기, 에틸기, 프로필기, 이소프로필기, 부틸기, 이소부틸기, t부틸기, 펜틸기, 헥실기, 에테닐기, 프로페닐기, 부테닐기, 시클로프로필기, 시클로부틸기, 시클로펜틸기, 시클로헥실기 등으로부터 개별적으로 그리고 독립적으로 선택된 하나 또는 그 이상의 그룹들로 치환될 수도 있는 작용기임을 의미한다.
"방향족기"는 고리 형태인 작용기의 모든 원소가 p오비탈을 가지고 있으며, 이들 p오비탈이 공액(conjugation)을 형성하고 있는 작용기를 의미한다. 구체적인 예로 아릴기와 헤테로아릴기가 있다.
"아릴(aryl)기"는 모노시클릭 또는 융합 고리 폴리시클릭(즉, 탄소원자들의 인접한 쌍들을 나눠 가지는 고리) 작용기를 포함한다.
"헤테로아릴(heteroaryl)기"는 아릴기 내에 N, O, S 및 P로 이루어진 군에서 선택되는 헤테로 원자를 1 내지 3개 함유하고, 나머지는 탄소인 것을 의미한다. 상기 헤테로아릴기가 융합고리인 경우, 각각의 고리마다 상기 헤테로 원자를 1 내지 3개 포함할 수 있다.
"스피로(spiro) 구조"는 하나의 탄소를 접점으로 가지고 있는 고리 구조를 의미한다. 또한, 스피로 구조는 스피로 구조를 포함하는 화합물 또는 스피로 구조를 포함하는 치환기로도 쓰일 수 있다.
본 명세서에서 정공 특성이란, HOMO 준위를 따라 전도 특성을 가져 양극에서 형성된 정공의 발광층으로의 주입 및 발광층에서의 이동을 용이하게 하는 특성을 의미한다.
또한 본 명세서에서 전자 특성이란, LUMO 준위를 따라 전도 특성을 가져 음극에서 형성된 전자의 발광층으로의 주입 및 발광층에서의 이동을 용이하게 하는 특성을 의미한다.
본 발명의 일 구현예에 따른 유기광전소자용 화합물은 두 개의 카바졸 또는 카바졸계 유도체가 결합된 코어 부분에 치환기가 선택적으로 결합된 구조를 가진다.
상기 코어에 결합된 치환기 중 적어도 하나는 전자 특성이 우수한 치환기일 수 있다.
따라서, 상기 화합물은 정공 특성이 우수한 카바졸 구조에 전자 특성을 보강하여 발광층에서 요구되는 조건을 만족시킬 수 있다. 보다 구체적으로 발광층의 호스트 재료로 이용이 가능하다.
또한, 상기 유기광전소자용 화합물은 코어 부분과 코어 부분에 치환된 치환기에 다양한 또 다른 치환기를 도입함으로써 다양한 에너지 밴드 갭을 갖는 화합물이 될 수 있다. 이에, 상기 화합물은 전자 주입층 및 전달층 또는 정공 주입층 및 전달층으로서도 이용이 가능하다.
상기 화합물의 치환기에 따라 적절한 에너지 준위를 가지는 화합물을 유기광전소자에 사용함으로써, 전자전달 능력이 강화되어 효율 및 구동전압 면에서 우수한 효과를 가지고, 전기화학적 및 열적 안정성이 뛰어나 유기광전소자 구동시 수명 특성을 향상시킬 수 있다.
이러한 본 발명의 일 구현예에 따르면, 하기 화학식 1로 표시되는 유기광전소자용 화합물을 제공한다.
본 발명의 일 구현예에서는 하기 화학식 1로 표시되는 유기광전소자용 화합물을 제공한다.
[화학식 1]
상기 화학식 1에서, X1 및 X2는 서로 동일하거나 상이하며, 독립적으로 NR', O, Se, P 및 S 로 이루어진 군에서 선택될 수 있다.
또한, 상기 R'는 수소, 중수소, 치환 또는 비치환된 C1 내지 C20 알킬기, 치환 또는 비치환된 C6 내지 C30 아릴기 및 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기로 이루어진 군에서 선택될 수 있다.
즉, 상기 화학식 1로 표시되는 화합물은 바이폴라(bipolar) 특성이 우수한 카바졸 또는 카바졸계 유도체를 코어로 가질 수 있다.
상기 R1 내지 R6는 서로 동일하거나 상이하며, 독립적으로 수소, 중수소, 치환 또는 비치환된 C1 내지 C20 알킬기, 치환 또는 비치환된 C6 내지 C30 아릴기 및 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기로 이루어진 군에서 선택되고, 상기 R1 내지 R6 또는 R' 중 적어도 어느 하나는 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기일 수 있다.
상기 R1 내지 R6 및 R'의 치환기 중 파이 결합이 존재하는 치환기는 화합물 전체의 파이공액길이(πconjugation length)를 조절하여 삼중항 에너지 밴드갭을 크게 함으로서 인광호스트로 유기광전소자의 발광층에 매우 유용하게 적용될 수 있도록 하는 역할을 할 수 있다.
또한, 상기 치환기의 적절한 조합에 의해 열적 안정성 또는 산화에 대한 저항성이 우수한 구조의 화합물을 제조할 수 있게 된다.
의해 비대칭 바이폴라(bipolar)특성의 구조를 제조할 수 있으며, 상기 비대칭 바이폴라특성의 구조는 전공과 전자 전달 능력을 향상시켜 소자의 발광효율과 성능 향상을 기대할 수 있다.
또한, 치환기의 조절로 화합물의 구조를 벌크하게 제조할 수 있으며, 이로 인해 결정화도를 낮출 수 있다. 화합물의 결정화도가 낮아지게 되면 소자의 수명이 길어질 수 있다.
전술한 바와 같이 상기 화합물의 치환기 중 어느 하나는 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기일 수 있다.
상기 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기의 구체적인 예로는 치환 또는 비치환된 이미다졸릴기, 치환 또는 비치환된 트리아졸릴기, 치환 또는 비치환된 테트라졸릴기, 치환 또는 비치환된 옥사다이아졸릴기, 치환 또는 비치환된 옥사트리아졸릴기, 치환 또는 비치환된 싸이아트리아졸릴기, 치환 또는 비치환된 벤즈이미다졸릴기, 치환 또는 비치환된 벤조트리아졸릴기, 치환 또는 비치환된 피리디닐기, 치환 또는 비치환된 피리미디닐기, 치환 또는 비치환된 트리아지닐기, 치환 또는 비치환된 피라지닐기, 치환 또는 비치환된 피리다지닐기, 퀴놀린, 치환 또는 비치환된 이소퀴놀린, 치환 또는 비치환된 프탈라진, 치환 또는 비치환된 나프피리딘, 치환 또는 비치환된 퀴녹살린, 치환 또는 비치환된 퀴나졸린, 치환 또는 비치환된 아크리딘, 치환 또는 비치환된 페난트롤린, 치환 또는 비치환된 페나진 등이 있다.
상기 화학식 1로 표시되는 유기광전소자용 화합물은 하기 화학식 2로 표시되는 것일 수 있다.
[화학식 2]
즉, 코어인 카바졸 또는 카바졸계 유도체의 결합위치가 상기 화학식 2와 같이 결합될 수 있다. 상기 결합위치는 카바졸 또는 카바졸계 유도체의 반응성이 좋은 위치 중 하나로 화합물의 합성 시 이점이 있을 수 있다.
상기 화학식 1 또는 2에서 X1 및 X2는 전술한 헤테로 원자일 수 있으며 서로 동일하거나 상이할 수 있다. 보다 구체적으로는 X1 및 X2 모두 NR' 일 수 있다.
상기 화학식 1 또는 2에서 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기의 결합위치는 X1이 NR'일 때 R'일 수 있다.
상기 위치에 결합하는 경우, 에너지밴드의 변화를 가져올 수 있는 화합물 전체의 공액길이의 변화를 최소화 하면서 전자 전달/수송 특성을 갖는 치환기를 도입할 수 있는 장점이 있다.
상기 유기광전소자용 화합물은 하기 화학식 A 또는 A1로 표시되는 것일 수 있다.
[화학식 A]
[화학식 A1]
상기 화학식 A 및 A1에서, X1 및 X2는 서로 동일하거나 상이하며, 독립적으로 NR', O, Se, P 및 S 로 이루어진 군에서 선택되고, 상기 R'는 수소, 중수소, 치환 또는 비치환된 C1 내지 C20 알킬기, 치환 또는 비치환된 C6 내지 C30 아릴기 및 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기로 이루어진 군에서 선택되고, 상기 R1 내지 R6는 서로 동일하거나 상이하며, 독립적으로 수소, 중수소, 치환 또는 비치환된 C1 내지 C20 알킬기, 치환 또는 비치환된 C6 내지 C30 아릴기 및 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기로 이루어진 군에서 선택되고, 상기 R1 내지 R6 또는 R' 중 적어도 어느 하나는 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기다.
상기 구조는 전술한 화학식 1로 표시되는 유기광전소자용 화합물의 구조에서 양 카바졸릴기의 결합위치가 상이한 구조이다. 이러한 구조의 경우 분자구조를 좀더 비평면화 시켜 공액길이를 한정시키므로 밴드갭 및 삼중항 에너지 밴드갭을 향상시킬 수 있는 장점이 있다.
또한, 상기 X1 또는 X2 중 적어도 하나는 NR'이고, 상기 R'는 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기고, 상기 R1 내지 R6는 서로 동일하거나 상이하며, 독립적으로 수소, 중수소, 치환 또는 비치환된 C1 내지 C20 알킬기 및 치환 또는 비치환된 C6 내지 C30 아릴기로 이루어진 군에서 선택될 수 있다.
또한, 상기 X1 또는 X2 중 적어도 하나는 NR'이고, 상기 R'는 치환 또는 비치환된 트리페닐레닐기일 수 있다.
상기 화합물에서 트리페닐레닐기는 벌크한 구조를 가지고 공명 효과(resonance effect)를 일으키므로 고체 상태에서 발생할 수 있는 부반응을 억제하는 효과를 가져, 유기발광소자의 성능을 증가시킬 수 있다.
또한, 화합물을 벌크하게 만들어 결정화도를 낮추고 수명을 증가시키는 효과를 가질 수 있다.
상기 트리페닐레닐기는 다른 치환체와는 달리 밴드갭이 넓고, 3중항 여기에너지가 크기 때문에 카바졸에 결합하여 화합물의 밴드갭이나 3중항 여기에너지를 줄이지 않아, 더욱 큰 장점을 가진다.
상기 화학식 A 및 A1의 구체적인 치환기와 관련된 내용은 전술한 화학식 1과 유사하기 때문에 생략하도록 한다.
상기 유기광전소자용 화합물은 하기 화학식 B로 표시될 수 있다.
[화학식 B]
상기 화학식 B에서, X1은 O, Se, P 및 S 로 이루어진 군에서 선택되고, R1 내지 R6는 서로 동일하거나 상이하며, 독립적으로 수소, 중수소, 치환 또는 비치환된 C1 내지 C20 알킬기, 치환 또는 비치환된 C6 내지 C30 아릴기 및 치환 또는 비치환된 C2 내지 C30 헤테로아릴기로 이루어진 군에서 선택되고, Ar은 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기이고, L은 단일결합, 치환 또는 비치환된 C2 내지 C10 알케닐렌기, 치환 또는 비치환된 C2 내지 C10 알키닐렌기, 치환 또는 비치환된 C6 내지 C30 아릴렌기 및 치환 또는 비치환된 C2 내지 C30 헤테로아릴렌기로 이루어진 군에서 선택되고, n은 0 내지 2 중 어느 하나의 정수이다.
상기 화학식 B의 구조는 전술한 화학식 1의 구조에서 양 카바졸계 유도체 중 어느 하나가 카바졸이며, 다른 하나는 카바졸을 제외한 카바졸릴계 유도체인 구조이다. 또한, 전자 특성을 가지는 치환기가 카바졸의 N에 결합된 구조이다. 이러한 구조의 경우 물질의 공액길이의 변화에 영향을 주지않고 전자특성을 가지는 치환기를 도입할 수 있는 장점이 있다.
상기 유기광전소자용 화합물은 하기 화학식 B1 또는 B2로 표시될 수 있다.
[화학식 B1]
[화학식 B2]
상기 화학식 B1 및 B2의 구조는 상기 화학식 B의 구조에서 양 카바졸릴계 유도체의 결합위치가 한정된 것이다. 이러한 코어 구조의 경우 적절한 HOMO 에너지를 가질 수 있으며, 합성이 용이한 장점이 있다.
기타 상기 화학식 B, B1 및 B2의 치환기에 대한 설명은 전술한 화학식 1의 설명과 유사하기 때문에 생략하기로 한다.
상기 유기광전소자용 화합물은 하기 화학식 C로 표시될 수 있다.
[화학식 C]
상기 화학식 C에 있어서, R1 내지 R6 및 Ar2는 서로 동일하거나 상이하며, 독립적으로 수소, 중수소, 치환 또는 비치환된 C1 내지 C20 알킬기, 치환 또는 비치환된 C6 내지 C30 아릴기 및 치환 또는 비치환된 C2 내지 C30 헤테로아릴기로 이루어진 군에서 선택되고, Ar1은 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기이고, L은 단일결합, 치환 또는 비치환된 C2 내지 C10 알케닐렌기, 치환 또는 비치환된 C2 내지 C10 알키닐렌기, 치환 또는 비치환된 C6 내지 C30 아릴렌기 및 치환 또는 비치환된 C2 내지 C30 헤테로아릴렌기로 이루어진 군에서 선택되고, n은 1 또는 2이다.
상기 화학식 C의 구조는 상기 화학식 1의 구조에서 양 카바졸계 유도체를 카바졸로 한정하며, 이의 결합위치도 한정한 구조이다. 또한, 카바졸의 질소에 연결기를 두고 전자 특성을 가지는 치환기가 결합된 구조이다. 이러한 구조는 LUMO의 에너지 분포를 좀더 넓게 비편재화시켜 전자 특성을 가지는 치환기의 안정성을 향상시키고 LUMO의 에너지 밴드를 낮게 할 수 있는 장점이 있다.
상기 Ar2는 치환 또는 비치환된 트리페닐레닐기일 수 있다. 트리페닐레닐기에 대한 설명은 전술한 바와 같기 때문에 생략하도록 한다.
또한, 기타 다른 치환기에 대한 설명 역시 전술한 화학식 1의 설명과 유사하기 때문에 생략하도록 한다.
상기 유기광전소자용 화합물은 하기 화학식 3 내지 화학식 54로 표시되는 것을 사용할 수 있다. 그러나 본 발명이 하기 화합물에 한정되는 것은 아니다.
[화학식 3] [화학식 4]
[화학식 5] [화학식 6]
[화학식 7] [화학식 8]
[화학식 9] [화학식 10]
[화학식 11] [화학식 12]
[화학식 13] [화학식 14]
[화학식 15] [화학식 16]
[화학식 17] [화학식 18]
[화학식 19] [화학식 20]
[화학식 21] [화학식 22]
[화학식 23] [화학식 24]
[화학식 25] [화학식 26]
[화학식 27] [화학식 28]
[화학식 29] [화학식 30]
[화학식 31] [화학식 32]
[화학식 33] [화학식 34]
[화학식 35] [화학식 36]
[화학식 37] [화학식 38]
[화학식 39] [화학식 40]
[화학식 41] [화학식 42]
[화학식 43] [화학식 44]
[화학식 45] [화학식 46]
[화학식 47] [화학식 48]
[화학식 49] [화학식 50]
[화학식 51] [화학식 52]
[화학식 53] [화학식 54]
상기 유기광전소자용 화합물은 하기 화학식 A2 내지 A26 중 어느 하나로 표시되될 수 있으나, 이에 한정되는 것은 아니다.
[화학식 A2] [화학식 A3]
[화학식 A4] [화학식 A5]
[화학식 A6] [화학식 A7]
[화학식 A8] [화학식 A9]
[화학식 A10] [화학식 A11]
[화학식 A12] [화학식 A13]
[화학식 A14] [화학식 A15]
[화학식 A16] [화학식 A17]
[화학식 A18] [화학식 A19]
[화학식 A20] [화학식 A21]
[화학식 A22] [화학식 A23]
[화학식 A24] [화학식 A25]
[화학식 A26]
상기 유기광전소자용 화합물은 하기 화학식 B3 내지 B22 중 어느 하나로 표시될 수 있으나, 이에 한정되는 것은 아니다.
[화학식 B3] [화학식 B4] [화학식 B5]
[화학식 B6] [화학식 B7] [화학식 B8]
[화학식 B9] [화학식 B10] [화학식 B11]
[화학식 B12] [화학식 B13] [화학식 B14]
[화학식 B15] [화학식 B16] [화학식 B17]
[화학식 B18] [화학식 B19] [화학식 B20]
[화학식 B21] [화학식 B22]
상기 유기광전소자용 화합물은 하기 화학식 C1 내지 C18 중 어느 하나로 표시될 수 있으나, 이에 한정되는 것은 아니다.
[화학식 C1] [화학식 C2] [화학식 C3]
[화학식 C4] [화학식 C5] [화학식 C6]
[화학식 C7] [화학식 C8] [화학식 C9]
[화학식 C10] [화학식 C11] [화학식 C12]
[화학식 C13] [화학식 C14] [화학식 C15]
[화학식 C16] [화학식 C17] [화학식 C18]
상기와 같은 화합물을 포함하는 유기광전소자용 화합물은 유리전이온도가 110℃ 이상이며, 열분해온도가 400℃이상으로 열적 안정성이 우수하다. 이로 인해 고효율의 유기광전소자의 구현이 가능하다.
상기와 같은 화합물을 포함하는 유기광전소자용 화합물은 발광, 또는 전자 주입 및/또는 수송역할을 할 수 있으며, 적절한 도판트와 함께 발광 호스트로서의 역할도 할 수 있다. 즉, 상기 유기광전소자용 화합물은 인광 또는 형광의 호스트 재료, 청색의 발광도펀트 재료, 또는 전자수송 재료로 사용될 수 있다.
본 발명의 일 구현예에 따른 유기광전소자용 화합물은 유기박막층에 사용되어 유기광전소자의 수명 특성, 효율 특성, 전기화학적 안정성 및 열적 안정성을 향상시키며, 구동전압을 낮출 수 있다.
이에 따라 본 발명의 일 구현예는 상기 유기광전소자용 화합물을 포함하는 유기광전소자를 제공한다. 이 때, 상기 유기광전소자라 함은 유기발광소자, 유기 태양 전지, 유기 트랜지스터, 유기 감광체 드럼, 유기 메모리 소자 등을 의미한다. 특히, 유기 태양 전지의 경우에는 본 발명의 일 구현예에 따른 유기광전소자용 화합물이 전극이나 전극 버퍼층에 포함되어 양자 효율을 증가시키며, 유기 트랜지스터의 경우에는 게이트, 소스드레인 전극 등에서 전극 물질로 사용될 수 있다.
이하에서는 유기광전소자에 대하여 구체적으로 설명한다.
본 발명의 다른 일 구현예는 양극, 음극 및 상기 양극과 음극 사이에 개재되는 적어도 한 층 이상의 유기박막층을 포함하는 유기발광소자에 있어서, 상기 유기박막층 중 적어도 어느 한 층은 본 발명의 일 구현예에 따른 유기광전소자용 화합물을 포함하는 유기발광소자를 제공한다.
상기 유기광전소자용 화합물을 포함할 수 있는 유기박막층으로는 발광층, 정공수송층, 정공주입층, 전자수송층, 전자주입층, 정공차단층 및 이들의 조합으로 이루어진 군에서 선택되는 층을 포함할 수 있는 바, 이 중에서 적어도 어느 하나의 층은 본 발명에 따른 유기광전소자용 화합물을 포함한다. 특히, 전자수송층 또는 전자주입층에 본 발명의 일 구현예에 따른 유기광전소자용 화합물을 포함할 수 있다. 또한, 상기 유기광전소자용 화합물이 발광층 내에 포함되는 경우 상기 유기광전소자용 화합물은 인광 또는 형광호스트로서 포함될 수 있고, 특히, 형광 청색 도펀트 재료로서 포함될 수 있다.
도 1 내지 도 5는 본 발명의 일 구현예에 따른 유기광전소자용 화합물을 포함하는 유기발광소자의 단면도이다.
도 1 내지 도 5를 참조하면, 본 발명의 일 구현예에 따른 유기광전소자(100, 200, 300, 400 및 500)는 양극(120), 음극(110) 및 이 양극과 음극 사이에 개재된 적어도 1층의 유기박막층(105)을 포함하는 구조를 갖는다.
상기 양극(120)은 양극 물질을 포함하며, 이 양극 물질로는 통상 유기박막층으로 정공주입이 원활할 수 있도록 일함수가 큰 물질이 바람직하다. 상기 양극 물질의 구체적인 예로는 니켈, 백금, 바나듐, 크롬, 구리, 아연, 금과 같은 금속 또는 이들의 합금을 들 수 있고, 아연산화물, 인듐산화물, 인듐주석산화물(ITO), 인듐아연산화물(IZO)과 같은 금속 산화물을 들 수 있고, ZnO와 Al 또는 SnO2와 Sb와 같은 금속과 산화물의 조합을 들 수 있고, 폴리(3메틸티오펜), 폴리[3,4(에틸렌1,2디옥시)티오펜](polyehtylenedioxythiophene: PEDT), 폴리피롤 및 폴리아닐린과 같은 전도성 고분자 등을 들 수 있으나, 이에 한정되는 것은 아니다. 바람직하게는 상기 양극으로 ITO(indium tin oxide)를 포함하는 투명전극을 사용할 수 있다.
상기 음극(110)은 음극 물질을 포함하여, 이 음극 물질로는 통상 유기박막층으로 전자주입이 용이하도록 일 함수가 작은 물질인 것이 바람직하다. 음극 물질의 구체적인 예로는 마그네슘, 칼슘, 나트륨, 칼륨, 타이타늄, 인듐, 이트륨, 리튬, 가돌리늄, 알루미늄, 은, 주석, 납, 세슘, 바륨 등과 같은 금속 또는 이들의 합금을 들 수 있고, LiF/Al, LiO2/Al, LiF/Ca, LiF/Al 및 BaF2/Ca과 같은 다층 구조 물질 등을 들 수 있으나, 이에 한정되는 것은 아니다. 바람직하게는 상기 음극으로 알루미늄 등과 같은 금속전극을 사용할 수 있다.
먼저 도 1을 참조하면, 도 1은 유기박막층(105)으로서 발광층(130)만이 존재하는 유기광전소자(100)를 나타낸 것으로, 상기 유기박막층(105)은 발광층(130)만으로 존재할 수 있다.
도 2를 참조하면, 도 2는 유기박막층(105)으로서 전자수송층을 포함하는 발광층(230)과 정공수송층(140)이 존재하는 2층형 유기광전소자(200)를 나타낸 것으로, 도 2에 나타난 바와 같이, 유기박막층(105)은 발광층(230) 및 정공 수송층(140)을 포함하는 2층형일 수 있다. 이 경우 발광층(130)은 전자 수송층의 기능을 하며, 정공 수송층(140)은 ITO와 같은 투명전극과의 접합성 및 정공수송성을 향상시키는 기능을 한다.
도 3을 참조하면, 도 3은 유기박막층(105)으로서 전자수송층(150), 발광층(130) 및 정공수송층(140)이 존재하는 3층형 유기광전소자(300)로서, 상기 유기박막층(105)에서 발광층(130)은 독립된 형태로 되어 있고, 전자수송성이나 정공수송성이 우수한 막(전자수송층(150) 및 정공수송층(140))을 별도의 층으로 쌓은 형태를 나타내고 있다.
도 4를 참조하면, 도 4는 유기박막층(105)으로서 전자주입층(160), 발광층(130), 정공수송층(140) 및 정공주입층(170)이 존재하는 4층형 유기광전소자(400)로서, 상기 정공주입층(170)은 양극으로 사용되는 ITO와의 접합성을 향상시킬 수 있다.
도 5를 참조하면, 도 5는 유기박막층(105)으로서 전자주입층(160), 전자수송층(150), 발광층(130), 정공수송층(140) 및 정공주입층(170)과 같은 각기 다른 기능을 하는 5개의 층이 존재하는 5층형 유기광전소자(500)를 나타내고 있으며, 상기 유기광전소자(500)는 전자주입층(160)을 별도로 형성하여 저전압화에 효과적이다.
상기 도 1 내지 도 5에서 상기 유기박막층(105)을 이루는 전자 수송층(150), 전자 주입층(160), 발광층(130, 230), 정공 수송층(140), 정공 주입층(170) 및 이들의 조합으로 이루어진 군에서 선택되는 어느 하나는 상기 유기광전소자용 화합물을 포함한다. 이 때 상기 유기광전소자용 화합물은 상기 전자 수송층(150) 또는 전자주입층(160)을 포함하는 전자수송층(150)에 사용될 수 있으며, 그중에서도 전자수송층에 포함될 경우 정공 차단층(도시하지 않음)을 별도로 형성할 필요가 없어 보다 단순화된 구조의 유기광전소자를 제공할 수 있어 바람직하다.
또한, 상기 유기 광전 소자용 화합물이 발광층(130, 230) 내에 포함되는 경우 상기 유기 광전 소자용 화합물은 인광 또는 형광호스트로서 포함될 수 있으며, 또는 형광 청색 도펀트로서 포함될 수 있다.
상기에서 설명한 유기발광소자는, 기판에 양극을 형성한 후, 진공증착법(evaporation), 스퍼터링(sputtering), 플라즈마 도금 및 이온도금과 같은 건식성막법; 또는 스핀코팅(spin coating), 침지법(dipping), 유동코팅법(flow coating)과 같은 습식성막법 등으로 유기박막층을 형성한 후, 그 위에 음극을 형성하여 제조할 수 있다.
본 발명의 또 다른 일 구현예에 따르면, 상기 유기광전소자를 포함하는 표시장치를 제공한다.
이하에서는 본 발명의 구체적인 실시예들을 제시한다. 다만, 하기에 기재된 실시예들은 본 발명을 구체적으로 예시하거나 설명하기 위한 것에 불과하며, 이로서 본 발명이 제한되어서는 아니된다.
(
유기광전소자용
화합물의 제조)
실시예
1: 화학식 4로 표시되는 화합물의 합성
본 발명의 유기광전소자용 화합물의 보다 구체적인 예로서 제시된 상기 화학식 4로 표시되는 화합물은 아래의 반응식 1과 같은 방법을 통하여 합성되었다.
[반응식 1]
제 1 단계: 화합물 A의 합성
질소 분위기의 교반기가 부착된 250 mL 둥근바닥 플라스크에서 화합물 3브로모카바졸 5 g(20mmol), N페닐카바졸 보론산 피나콜레이트 9 g(24 mmol) 및 테트라하이드로퓨란 100 mL 와 2M탄산칼륨 수용액을 혼합한 후, 질소기류하에서 12 시간 동안 가열 환류하였다. 반응 종결 후 반응물에 헥산을 부어 생기는 고형물을 필터 한 다음, 고형물을 다시 톨루엔과 테트라하이드로퓨란(50:50 부피비) 혼합용액에 녹여 활성탄 과 무수황산마그네슘을 넣어 교반한다. 용액을 팰터한 다음 디클로로메탄과 헥산을 이용해 재결정 하여 화합물 A 7.8 g(수울 60%)을 얻었다.
제 2 단계 : 화학식 4로 표시되는 화합물의 합성
100 mL의 둥근 플라스크에서 화합물 A로 표시되는 중간체 생성물 3.5 g(8.55 mmol), 2클로로4,6디페닐피리미딘 2.74 g(10.26 mmol), NaH 와 다이메틸포름아마이드를 넣은 다음 질소 기류하에서 실온에서 교반한다. 유기용매를 감압증류하에 제거한 다음 칼럼크로마토그래피를 이용해 분리하여 3.823 g(수율: 70 %)의 화학식 4로 표시되는 화합물을 얻었다.
상기 수득된 화학식 4로 표시되는 화합물을 원소분석으로 분석한 결과는 다음과 같았다.
calcd. C46H30N4: C, 86.49; H, 4.73; N, 8.77; found: C, 86.24; H, 4.89; N, 8.55
실시예
2: 화학식 5로 표시되는 화합물의 합성
본 발명의 유기광전소자용 화합물의 보다 구체적인 예로서 제시된 상기 화학식 5로 표시되는 화합물은 아래의 반응식 2와 같은 방법을 통하여 합성되었다.
[반응식 2]
화학식 5로 표시되는 화합물의 합성
100 mL의 둥근 플라스크에서 화합물 A로 표시되는 중간체 생성물 3.5 g(8.55 mmol), 2클로로4,6디비페닐피리미딘 2.74 g(10.26 mmol), NaH 와 다이메틸포름아마이드를 넣은 다음 질소 기류하에서 실온에서 교반한다. 유기용매를 감압증류하에 제거한 다음 칼럼크로마토그래피를 이용해 분리하여 4.1 g(수율: 75 %)의 화합물 6을 얻었다.
상기 수득된 화학식 5로 표시되는 화합물을 원소분석으로 분석한 결과는 다음과 같았다.
calcd. C45H29N5: C, 84.48; H, 4.57; N, 10.95; found: C, 84.24; H, 4.65; N, 10.55
실시예
3: 화학식 14로 표시되는 화합물의 합성
본 발명의 유기광전소자용 화합물의 보다 구체적인 예로서 제시된 상기 화학식 14로 표시되는 화합물은 아래의 반응식 3과 같은 방법을 통하여 합성되었다.
[반응식 3]
제 1 단계 : 화합물 B의 합성
질소 분위기의 교반기가 부착된 250 mL 둥근바닥 플라스크에서 화합물 3브로모N페닐6페닐카바졸 5 g(12.6mmol), 3페닐카바졸 보론산 피나콜레이트 5.56 g(15 mmol) 및 테트라하이드로퓨란 100 mL 와 2M탄산칼륨 수용액을 혼합한 후, 질소기류하에서 12 시간 동안 가열 환류하였다. 반응 종결 후 반응물에 헥산을 부어 생기는 고형물을 필터 한 다음, 고형물을 다시 톨루엔과 테트라하이드로퓨란(50:50 부피비) 혼합용액에 녹여 활성탄 과 무수황산마그네슘을 넣어 교반한다. 용액을 팰터한 다음 디클로로메탄과 헥산을 이용해 재결정 하여 화합물 B 6.5 g(수울 65%)을 얻었다.
제 2 단계 : 화학식 14로 표시되는 화합물의 합성
250 mL의 둥근 플라스크에서 화합물 B로 표시되는 중간체 생성물 6 g(10.5 mmol), 2클로로4,6디페닐트리아진 3.44 g(12.84 mmol), NaH 와 다이메틸포름아마이드를 넣은 다음 질소 기류하에서 실온에서 교반한다. 유기용매를 감압증류하에 제거한 다음 칼럼크로마토그래피를 이용해 분리하여 3.825 g(수율: 70 %)의 화학식 14로 표시되는 화합물을 얻었다.
상기 수득된 화학식 14로 표시되는 화합물을 원소분석으로 분석한 결과는 다음과 같았다.
calcd. C57H37N5: C, 86.45; H, 4.71; N, 8.84; found: C, 86.15; H, 4.57; N, 8.57
실시예
4: 화학식 A2로 표시되는 화합물의 합성
본 발명의 유기광전소자용 화합물의 보다 구체적인 예로서 제시된 상기 화학식 A2로 표시되는 화합물은 아래의 반응식 4와 같은 방법을 통하여 합성되었다.
[반응식 4]
제 1 단계: 화합물 C의 합성
1000 mL의 둥근 플라스크에서 3브로모카바졸 28.4 g(115.46 mmol), 2클로로4,6디페닐피리미딘 36.95 g(138.55 mmol), NaH 6.93 g 을 다이메틸포름아마이드에 넣은 다음 질소 기류하에서 실온에서 12시간 교반한다. 반응물을 증류수에 넣어 결정화한다. 결정화된 고형분을 필터한 후, 모노클로로벤젠과 헥산으로 재결정하여 53 g(수율: 96 %)의 중간체 C로 표시되는 화합물을 얻었다.
제 2 단계 : 화학식 A2로 표시되는 화합물의 합성
질소 분위기의 교반기가 부착된 1,000 mL 둥근바닥 플라스크에서 화합물 C로 표시되는 화합물 22.26 g(46.7 mmol), N페닐카바졸 보론산 피나콜레이트 20.71 g(56.1 mmol) 및 테트라하이드로퓨란 200 mL 와 톨루엔 200ml 및 2M탄산칼륨 수용액 200ml를 혼합한 후, 질소기류하에서 12 시간 동안 가열 환류하였다. 반응 종결 후 반응물에 헥산을 부어 생기는 고형물을 필터 한 다음, 고형물을 다시 톨루엔과 테트라하이드로퓨란(50:50 부피비) 혼합용액에 녹여 활성탄 과 무수황산마그네슘을 넣어 교반한다. 용액을 필터한 다음 클로로벤젠과 메탄올을 이용해 재결정 하여 화합물 A2, 20 g(수울 70%)을 얻었다.
calcd. C46H30N4: C, 86.49; H, 4.73; N, 8.77; found: C, 86.44; H, 4.74; N, 8.75
실시예
5: 화학식 A10로 표시되는 화합물의 합성
본 발명의 유기광전소자용 화합물의 보다 구체적인 예로서 제시된 상기 화학식 A10으로 표시되는 화합물은 아래의 반응식 5와 같은 방법을 통하여 합성되었다.
[반응식 5]
제 1 단계 : 화학식 D로 표시되는 화합물의 합성
질소 분위기의 교반기가 부착된 500 mL 둥근바닥 플라스크에서 화합물 2브로모카바졸 17.66 g(71.7 mmol), N페닐카바졸 보론산 피나콜레이트 22.08 g(59.8 mmol) 및 테트라하이드로퓨란 100 mL 와 2M탄산칼륨 수용액 100ml를 혼합한 후, 질소기류하에서 12 시간 동안 가열 환류하였다. 반응 종결 후 반응물에 헥산을 부어 생기는 고형물을 필터 한 다음, 고형물을 다시 톨루엔과 테트라하이드로퓨란(50:50 부피비) 혼합용액에 녹여 활성탄 과 무수황산마그네슘을 넣어 교반한다. 용액을 팰터한 다음 디클로로메탄과 헥산을 이용해 재결정 하여 화합물 D 19 g(수울 65%)을 얻었다.
제 2 단계 : 화학식 A10으로 표시되는 화합물의 합성
질소 분위기의 교반기가 부착된 500 mL 둥근바닥 플라스크에서 화합물 D로 표시되는 화합물 8.3 g(20.53 mmol), 2브로모4,6다이페틸피리딘 7.64 g(24.64 mmol) 및 터셔리부톡시나트륨 3.35 g (34.9 mmol)을 톨루엔 200ml 녹인 후, 팔라듐 다이벤질리덴아민 0.47 g (0.51 mmol) 과 터셔리부틸인 0.77ml (1.54 mmol)을 적가한다. 반응용액을 질소기류하에서 12 시간 동안 110도로 가열하여 교반하였다. 반응 종결 후 반응물에 메탄올을 부어 생기는 고형물을 필터 한 다음, 고형물을 다시 클로로벤젠에 녹여 활성탄 과 무수황산마그네슘을 넣어 교반한다. 용액을 필터한 다음 클로로벤젠과 메탄올을 이용해 재결정 하여 화합물 A10 11g(수율 84%)을 얻었다.
calcd. C47H31N3: C, 88.51; H, 4.90; N, 6.59; found: C, 88.49; H, 4.91; N, 6.61
실시예
6: 화학식 A12로 표시되는 화합물의 합성
본 발명의 유기광전소자용 화합물의 보다 구체적인 예로서 제시된 상기 화학식 A12로 표시되는 화합물은 아래의 반응식 3과 같은 방법을 통하여 합성되었다.
[반응식 6]
제 1 단계 : 화합물 E의 합성
질소 분위기의 교반기가 부착된 1,000 mL 둥근바닥 플라스크에서 화합물 2브로모카바졸 22.22 g(90.3 mmol), 4아이요도바이페닐 37.94 g(135.5 mmol) 및 탄산칼륨 18.72 g(135.5 mmol)을 다이메틸설폭사이드 400ml 에 녹인 후, 1,10페난쓰롤린 3.26 g (135.47 mmol) 과 염화구리(I) 1.79 g (18.06 mmol)을 적가한다. 반응용액을 질소기류하에서 12 시간 동안 150도로 가열하여 교반하였다. 반응 종결 후 반응물에 증류수를 부어 생기는 고형물을 필터 한 다음, 고형물을 다시 클로로벤젠에 녹여 활성탄 과 무수황산마그네슘을 넣어 교반한다. 용액을 필터한 다음 클로로벤젠과 메탄올을 이용해 재결정 하여 화합물 E 25 g(수율 70%)을 얻었다.
제 2 단계 : 화학식 F로 표시되는 화합물의 합성
질소 분위기의 교반기가 부착된 1,000 mL 둥근바닥 플라스크에서 화합물 E로 표시되는 화합물 18.2 g(46.7 mmol), 3카바졸 보론산 피나콜레이트 16.4 g(56.1 mmol) 및 테트라하이드로퓨란 200 mL 와 톨루엔 200ml 및 2M탄산칼륨 수용액 200ml를 혼합한 후, 질소기류하에서 12 시간 동안 가열 환류하였다. 반응 종결 후 반응물에 헥산을 부어 생기는 고형물을 필터 한 다음, 고형물을 다시 클로로벤젠에 녹여 활성탄 과 무수황산마그네슘을 넣어 교반한다. 용액을 필터한 다음 클로로벤젠과 메탄올을 이용해 재결정 하여 화합물 F 19.0 g(수율 64%)을 얻었다.
제 3 단계 : 화학식 A12로 표시되는 화합물의 합성
질소 분위기의 교반기가 부착된 500 mL 둥근바닥 플라스크에서 화합물 F로 표시되는 화합물 9.73 g(20.1 mmol), 2브로모4,6다이페틸피리딘 7.47 g(24.10 mmol) 및 터셔리부톡시나트륨 3.28 g (34.1 mmol)을 톨루엔 180ml에 녹인 후, 팔라듐 다이벤질리덴아민 0.46 g (0.5 mmol) 과 터셔리부틸인 0.75ml (1.51 mmol)을 적가한다. 반응용액을 질소기류하에서 12 시간 동안 110도로 가열하여 교반하였다. 반응 종결 후 반응물에 메탄올을 부어 생기는 고형물을 필터 한 다음, 고형물을 다시 클로로벤젠에 녹여 활성탄 과 무수황산마그네슘을 넣어 교반한다. 용액을 필터한 다음 클로로벤젠과 메탄올을 이용해 재결정 하여 화합물 A12 9.9 g(수율 70%)을 얻었다.
calcd. C53H35N3: C, 89.17; H, 4.94; N, 5.89; found: C, 89.29; H, 4.96; N, 5.82.
실시예
7 : 화학식 B5로 표시되는 화합물의 합성
본 발명의 유기광전소자용 화합물의 보다 구체적인 예로서 제시된 상기 화학식 B5로 표시되는 화합물은 아래의 반응식 7과 같은 방법을 통하여 합성되었다.
[반응식 7]
제 1 단계: 화합물 G의 합성
질소 분위기의 교반기가 부착된 500 mL 둥근바닥 플라스크에서 화합물 3브로모카바졸 18.53 g(75.3 mmol), 4디벤조사이오펜 보로닉 엑시드 22.3 g(97.9 mmol) 및 테트라하이드로퓨란 100 mL 와 2M탄산칼륨 수용액 100ml를 혼합한 후, 질소기류하에서 12 시간 동안 가열 환류하였다. 반응 종결 후 반응물에 헥산을 부어 생기는 고형물을 필터 한 다음, 고형물을 다시 톨루엔과 테트라하이드로퓨란(50:50 부피비) 혼합용액에 녹여 활성탄 과 무수황산마그네슘을 넣어 교반한다. 용액을 팰터한 다음 디클로로메탄과 헥산을 이용해 재결정 하여 화합물 D 15 g(수울 60%)을 얻었다.
제 2 단계 : 화학식 B5로 표시되는 화합물의 합성
질소 분위기의 교반기가 부착된 500 mL 둥근바닥 플라스크에서 화합물 G로 표시되는 화합물 10 g(28.80mmol), 2브로모4,6다이페틸피리딘 11.6 g(37.4 mmol) 및 터셔리부톡시나트륨 5.53 g (57.6 mmol)을 톨루엔 160ml 녹인 후, 팔라듐 다이벤질리덴아민 1.32 g (1.44 mmol) 과 터셔리부틸인 0.87ml (4.32 mmol)을 적가한다. 반응용액을 질소기류하에서 12 시간 동안 110도로 가열하여 교반하였다. 반응 종결 후 반응물에 메탄올을 부어 생기는 고형물을 필터 한 다음, 고형물을 다시 클로로벤젠에 녹여 활성탄 과 무수황산마그네슘을 넣어 교반한다. 용액을 필터한 다음 클로로벤젠과 메탄올을 이용해 재결정 하여 화합물 B5 14g(수율 85%)을 얻었다.
calcd. C41H26N2S: C, 85.09; H, 4.53; N, 4.84; S, 5.54; found: C, 85.11; H, 4.50; N, 4.80; S, 5.50
실시예
8: 화학식 B8로 표시되는 화합물의 합성
본 발명의 유기광전소자용 화합물의 보다 구체적인 예로서 제시된 상기 화학식 B8로 표시되는 화합물은 아래의 반응식 8과 같은 방법을 통하여 합성되었다.
[반응식 8]
제 1 단계: 화합물 H의 합성
질소 분위기의 교반기가 부착된 500 mL 둥근바닥 플라스크에서 화합물 3브로모카바졸 9.84g(39.99mmol), 4디벤조퓨란 보로닉 엑시드 10.17g47.99mmol) 및 테트라하이드로퓨란 100 mL 와 2M탄산칼륨 수용액 100ml를 혼합한 후, 질소기류하에서 12 시간 동안 가열 환류하였다. 반응 종결 후 반응물에 헥산을 부어 생기는 고형물을 필터 한 다음, 고형물을 다시 톨루엔과 테트라하이드로퓨란(50:50 부피비) 혼합용액에 녹여 활성탄 과 무수황산마그네슘을 넣어 교반한다. 용액을 팰터한 다음 디클로로메탄과 헥산을 이용해 재결정 하여 화합물 H 11 g(수울 83%)을 얻었다.
제 2 단계 : 화학식 B8로 표시되는 화합물의 합성
질소 분위기의 교반기가 부착된 500 mL 둥근바닥 플라스크에서 화합물 H로 표시되는 화합물 10.8 g(32.58mmol), 2브로모4,6다이페틸피리딘 11.6 g(37.4 mmol) 및 터셔리부톡시나트륨 5.53 g (57.6 mmol)을 톨루엔 160ml 녹인 후, 팔라듐 다이벤질리덴아민 1.32 g (1.44 mmol) 과 터셔리부틸인 0.87ml (4.32 mmol)을 적가한다. 반응용액을 질소기류하에서 12 시간 동안 110도로 가열하여 교반하였다. 반응 종결 후 반응물에 메탄올을 부어 생기는 고형물을 필터 한 다음, 고형물을 다시 클로로벤젠에 녹여 활성탄 과 무수황산마그네슘을 넣어 교반한다. 용액을 필터한 다음 클로로벤젠과 메탄올을 이용해 재결정 하여 화합물 B8 14g(수율 85%)을 얻었다.
calcd. C41H26N2O: C, 87.52; H, 4.66; N, 4.98; O, 2.84; found: C, 87.50; H, 4.68; N, 4.96; O, 2.82
실시예
9: 화학식 B21로 표시되는 화합물의 합성
본 발명의 유기광전소자용 화합물의 보다 구체적인 예로서 제시된 상기 화학식 B21로 표시되는 화합물은 아래의 반응식 9과 같은 방법을 통하여 합성되었다.
[반응식 9]
제 1 단계: 화합물 I의 합성
질소 분위기의 교반기가 부착된 500 mL 둥근바닥 플라스크에서 화합물 3브로모카바졸 18.53 g(75.3 mmol), 4디벤조사이오펜 보로닉 엑시드 22.3 g(97.9 mmol) 및 테트라하이드로퓨란 100 mL 와 2M탄산칼륨 수용액 100ml를 혼합한 후, 질소기류하에서 12 시간 동안 가열 환류하였다. 반응 종결 후 반응물에 헥산을 부어 생기는 고형물을 필터 한 다음, 고형물을 다시 톨루엔과 테트라하이드로퓨란(50:50 부피비) 혼합용액에 녹여 활성탄 과 무수황산마그네슘을 넣어 교반한다. 용액을 필터한 다음 디클로로메탄과 헥산을 이용해 재결정 하여 화합물 I 15 g(수율 60%)을 얻었다.
제 2 단계 : 화학식 B21로 표시되는 화합물의 합성
질소 분위기의 교반기가 부착된 500 mL 둥근바닥 플라스크에서 화합물 G로 표시되는 화합물 10 g(28.80mmol), 2(4브로모페닐)4,6다이페틸피리딘 14.43 g(37.4 mmol) 및 터셔리부톡시나트륨 5.53 g (57.6 mmol)을 톨루엔 160ml 녹인 후, 팔라듐 다이벤질리덴아민 1.32 g (1.44 mmol) 과 터셔리부틸인 0.87ml (4.32 mmol)을 적가한다. 반응용액을 질소기류하에서 12 시간 동안 110도로 가열하여 교반하였다. 반응 종결 후 반응물에 메탄올을 부어 생기는 고형물을 필터 한 다음, 고형물을 다시 클로로벤젠에 녹여 활성탄 과 무수황산마그네슘을 넣어 교반한다. 용액을 필터한 다음 클로로벤젠과 메탄올을 이용해 재결정 하여 화합물 B21 10g(수율 60%)을 얻었다.
calcd. C47H30N2S: C, 86.21; H, 4.62; N, 4.28; S, 4.90; found: C, 86.20; H, 4.60; N, 4.26; S, 4.88
실시예
10: 화학식 3으로 표시되는 화합물의 합성
본 발명의 유기광전소자용 화합물의 보다 구체적인 예로서 제시된 상기 화학식 3으로 표시되는 화합물은 아래의 반응식 10과 같은 방법을 통하여 합성되었다.
[반응식 10]
제 1 단계: 화합물 J의 합성
질소 분위기의 교반기가 부착된 500 mL 둥근바닥 플라스크에서 화합물 N페닐 카바졸3보론산 피나콜레이트 26.96 g(81.4 mmol), 카바졸3보론산 23.96 g(97.36 mmol) 및 테트라하이드로퓨란 230 mL 와 2M탄산칼륨 수용액 100ml를 혼합한 후, 질소기류하에서 12 시간 동안 가열 환류하였다. 반응 종결 후 반응물에 메탄올에 부어 생기는 고형물을 필터 한 다음, 고형물을 다시 클로로벤젠에 녹여 활성탄 과 무수황산마그네슘을 넣어 교반한다. 용액을 필터한 다음 클로로벤젠과 메탄올 이용해 재결정 하여 화합물 J 22.6 g(수율 68%)을 얻었다.
제 2 단계 : 화학식 3으로 표시되는 화합물의 합성
질소 분위기의 교반기가 부착된 500 mL 둥근바닥 플라스크에서 화합물 J로 표시되는 화합물 22.42 g(54.88 mmol), 2브로모4,6다이페틸피리딘 20.43 g(65.85 mmol) 및 터셔리부톡시나트륨 7.92 g (82.32 mmol)을 톨루엔 400ml 녹인 후, 팔라듐 다이벤질리덴아민 1.65 g (1.65 mmol) 과 터셔리부틸인 1.78 g (4.39 mmol)을 적가한다. 반응용액을 질소기류하에서 12 시간 동안 110도로 가열하여 교반하였다. 반응 종결 후 반응물에 메탄올을 부어 생기는 고형물을 필터 한 다음, 고형물을 다시 클로로벤젠에 녹여 활성탄 과 무수황산마그네슘을 넣어 교반한다. 용액을 필터한 다음 클로로벤젠과 메탄올을 이용해 재결정 하여 화합물 3 28.10 g(수율 80%)을 얻었다.
calcd. C47H31N3: C, 88.51; H, 4.90; N, 6.59; found: C, 88.62; H, 4.80; N, 6.47
실시예
11: 화학식 54로 표시되는 화합물의 합성
본 발명의 유기광전소자용 화합물의 보다 구체적인 예로서 제시된 상기 화학식 54로 표시되는 화합물은 아래의 반응식 11과 같은 방법을 통하여 합성되었다.
[반응식 11]
제 1 단계: 화합물 K의 합성
1000 mL의 둥근 플라스크에서 3브로모카바졸 42.97 g(174.57 mmol), 2클로로4,6디페닐트리아진 56.1 g(209.5 mmol), NaH 10.48 g (261.86 mmol) 을 다이메틸포름아마이드에 넣은 다음 질소 기류하에서 실온에서 12시간 교반한다. 반응물을 증류수에 넣어 결정화한다. 결정화된 고형분을 필터한 후, 모노클로로벤젠과 헥산으로 재결정하여 82 g(수율: 98 %)의 중간체 K로 표시되는 화합물을 얻었다.
제 2 단계: 화합물 L의 합성
질소 분위기의 교반기가 부착된 2L 둥근바닥 플라스크에서 화합물 K 70.57 g(147.85 mmol), 카바졸3보론산 피나콜레이트 52.01 g(177.42 mmol) 및 테트라하이드로퓨란:톨루엔 혼합용액 800 mL(부피비=1:1) 와 2M탄산칼륨 수용액 400mL를 혼합한 후, 질소기류하에서 12 시간 동안 가열 환류하였다. 반응 종결 후 반응물에 메탄올에 부어 생기는 고형물을 필터 한 다음, 고형물을 다시 클로로벤젠에 녹여 활성탄 과 무수황산마그네슘을 넣어 교반한다. 용액을 필터한 다음 클로로벤젠과 메탄올 이용해 재결정 하여 화합물 L 66 g(수율 79%)을 얻었다.
제 3 단계 : 화학식 54로 표시되는 화합물의 합성
질소 분위기의 교반기가 부착된 1 L 둥근바닥 플라스크에서 화합물 L로 표시되는 화합물 10.1 g(17.88 mmol), 2브로모바이페닐 5 g(21.46 mmol) 및 터셔리부톡시나트륨 3.44 g (35.76 mmol)을 톨루엔 400ml 녹인 후, 팔라듐 다이벤질리덴아민 1.03 g (1.79 mmol) 과 터셔리부틸인 2.17 g (5.36 mmol)을 적가한다. 반응용액을 질소기류하에서 12 시간 동안 110도로 가열하여 교반하였다. 반응 종결 후 반응물에 메탄올을 부어 생기는 고형물을 필터 한 다음, 고형물을 다시 클로로벤젠에 녹여 활성탄 과 무수황산마그네슘을 넣어 교반한다. 용액을 필터한 다음 클로로벤젠과 메탄올을 이용해 재결정 하여 화합물 54 9.40 g(수율 73%)을 얻었다.
calcd. C52H34N4: C, 87.37; H, 4.79; N, 7.84; found: C, 87.47; H, 4.80; N, 7.78
실시예
12: 화학식
C13
으로 표시되는 화합물의 합성
[반응식 12]
제 1 단계: 화합물 M의 합성
질소 분위기의 교반기가 부착된 500mL 둥근바닥 플라스크에서 화합물 N바이페닐3카바졸 보론산 19.3 g(53.06 mmol), 3브로모 카바졸 10.9 g(44.22 mmol) 및 테트라하이드로퓨란:톨루엔 혼합용액 140 mL(부피비=1:1) 와 2M탄산칼륨 수용액 80 mL를 혼합한 후, 질소기류하에서 12 시간 동안 가열 환류하였다. 반응 종결 후 반응물에 메탄올에 부어 생기는 고형물을 필터 한 다음, 고형물을 다시 클로로벤젠에 녹여 활성탄과 무수황산마그네슘을 넣어 교반한다. 용액을 필터한 다음 클로로벤젠과 메탄올 이용해 재결정 하여 화합물 M 13.7 g(수율 64%)을 얻었다.
제 2 단계 : 화학식
C13
으로 표시되는 화합물의 합성
질소 분위기의 교반기가 부착된 500mL 둥근바닥 플라스크에서 화합물 M으로 표시되는 화합물 9.6 g(19.82 mmol), 2(4브로모페닐)4,6디페닐피리딘 9.2 g(23.8 mmol) 및 터셔리부톡시나트륨 3.2 g (33.7 mmol)을 톨루엔 160mL에 녹인 후, 팔라듐 다이벤질리덴아민 0.454 g (0.5 mmol) 과 터셔리부틸인 0.6 g (1.49 mmol)을 적가한다. 반응용액을 질소기류하에서 12 시간 동안 110도로 가열하여 교반하였다. 반응 종결 후 반응물에 메탄올을 부어 생기는 고형물을 필터 한 다음, 고형물을 다시 클로로벤젠에 녹여 활성탄 과 무수황산마그네슘을 넣어 교반한다. 용액을 필터한 다음 클로로벤젠과 메탄올을 이용해 재결정 하여 화합물 C13 14 g(수율 89%)을 얻었다.
calcd. C59H39N3: C, 89.70; H, 4.98; N, 5.32; found: C, 89.57; H, 4.83; N, 5.65
(유기발광소자의 제조)
실시예
13
상기 실시예 1에서 합성된 화합물을 호스트로 사용하고, Ir(PPy)3를 도펀트로 사용하여 유기발광소자를 제작하였다. 양극으로는 ITO를 1000 Å의 두께로 사용하였고, 음극으로는 알루미늄(Al)을 1000 Å의 두께로 사용하였다.
구체적으로, 유기발광소자의 제조방법을 설명하면, 양극은 15 Ω/cm2의 면저항값을 가진 ITO 유리 기판을 50 mm × 50 mm × 0.7 mm의 크기로 잘라서 아세톤과 이소프로필알코올과 순수물 속에서 각 15 분 동안 초음파 세정한 후, 30 분 동안 UV 오존 세정하여 사용하였다.
상기 기판 상부에 진공도 650×107 Pa, 증착속도 0.1 내지 0.3 nm/s의 조건으로 N,N'디(1나프틸)N,N'디페닐벤지딘 (NPB) (70 nm) 및 4,4',4"트리(N카바졸일)트리페닐아민 (TCTA) (10 nm)를 증착하여 800 Å의 정공수송층을 형성하였다.
이어서, 동일한 진공 증착조건에서 상기 실시예 2에서 합성된 화합물을 이용하여 막 두께 300 Å의 발광층을 형성하였고, 이 때, 인광 도펀트인 Ir(PPy)3을 동시에 증착하였다. 이 때, 인광 도펀트의 증착속도를 조절하여, 발광층의 전체량을 100 중량%로 하였을 때, 인광 도펀트의 배합량이 7 중량%가 되도록 증착하였다.
상기 발광층 상부에 동일한 진공 증착조건을 이용하여 비스(8하이드록시2메틸퀴놀리나토)알루미늄비페녹시드(BAlq)를 증착하여 막 두께 50 Å의 정공저지층을 형성하였다.
이어서, 동일한 진공 증착조건에서 Alq3를 증착하여, 막 두께 200 Å의 전자수송층을 형성하였다.
상기 전자수송층 상부에 음극으로서 LiF와 Al을 순차적으로 증착하여 유기광전소자를 제작하였다.
상기 유기광전소자의 구조는 ITO/ NPB (70 nm)/ TCTA (10 nm)/ EML (실시예 1의 화합물(93 중량%) + Ir(PPy)3(7 중량%), 30 nm)/ Balq (5 nm)/ Alq3 (20 nm)/ LiF (1 nm) / Al (100 nm) 의 구조로 제작하였다.
실시예
14
상기 실시예 1에서 합성된 화합물을 발광층의 호스트로 사용한 것을 대신하여, 실시예 2에서 합성된 화합물을 발광층의 호스트로 사용한 것을 제외하고는 상기 실시예 13과 동일한 방법으로 유기발광소자를 제작하였다.
실시예
15
상기 실시예 1에서 합성된 화합물을 발광층의 호스트로 사용한 것을 대신하여, 실시예 4에서 합성된 화합물을 발광층의 호스트로 사용한 것을 제외하고는 상기 실시예 13과 동일한 방법으로 유기발광소자를 제작하였다.
실시예
16
상기 실시예 1에서 합성된 화합물을 발광층의 호스트로 사용한 것을 대신하여, 실시예 6에서 합성된 화합물을 발광층의 호스트로 사용한 것을 제외하고는 상기 실시예 13과 동일한 방법으로 유기발광소자를 제작하였다.
실시예
17
상기 실시예 1에서 합성된 화합물을 발광층의 호스트로 사용한 것을 대신하여, 실시예 7에서 합성된 화합물을 발광층의 호스트로 사용한 것을 제외하고는 상기 실시예 13과 동일한 방법으로 유기발광소자를 제작하였다.
실시예
18
상기 실시예 1에서 합성된 화합물을 발광층의 호스트로 사용한 것을 대신하여, 실시예 10에서 합성된 화합물을 발광층의 호스트로 사용한 것을 제외하고는 상기 실시예 13과 동일한 방법으로 유기발광소자를 제작하였다.
실시예
19
상기 실시예 1에서 합성된 화합물을 발광층의 호스트로 사용한 것을 대신하여, 실시예 11에서 합성된 화합물을 발광층의 호스트로 사용한 것을 제외하고는 상기 실시예 13과 동일한 방법으로 유기발광소자를 제작하였다.
실시예
20
상기 실시예 1에서 합성된 화합물을 발광층의 호스트로 사용한 것을 대신하여, 실시예 12에서 합성된 화합물을 발광층의 호스트로 사용한 것을 제외하고는 상기 실시예 13과 동일한 방법으로 유기발광소자를 제작하였다.
비교예
1
상기 실시예 2에서 합성된 화합물을 발광층의 호스트로 사용한 것을 대신하여, 4,4N,N다이카바졸바이페닐(CBP)를 발광층의 호스트로 사용한 것을 제외하고는 상기 실시예 13과 동일한 방법으로 유기발광소자를 제작하였다.
비교예
2
한국공개특허 1020050100673의 실시에 6에 제시된 화합물인 비스[9(4메톡시페닐)카바졸3일](Jib79604k)를 사용한 소자의 발광 특성을 본 발명에서 제조된 화합물로 제작된 소자의 특성과 비교하였다.
(유기발광소자의 성능 측정)
실험예
상기 실시예 13 내지 20과 비교예 1 및 2에서 제조된 각각의 유기발광소자에 대하여 전압에 따른 전류밀도 변화, 휘도변화 및 발광효율을 측정하였다. 구체적인 측정방법은 다음과 같고, 그 결과는 하기 표 1에 나타내었다
(1) 전압변화에 따른 전류밀도의 변화 측정
제조된 유기발광소자에 대해, 전압을 0 V 부터 10 V까지 상승시키면서 전류전압계(Keithley 2400)를 이용하여 단위소자에 흐르는 전류값을 측정하고, 측정된 전류값을 면적으로 나누어 결과를 얻었다.
(2) 전압변화에 따른 휘도변화 측정
제조된 유기발광소자에 대해, 전압을 0 V 부터 10 V까지 상승시키면서 휘도계(Minolta Cs1000A)를 이용하여 그 때의 휘도를 측정하여 결과를 얻었다.
(3) 발광효율 측정
상기(1) 및 (2)로부터 측정된 휘도와 전류밀도 및 전압을 이용하여 동일 밝기(9000 cd/m2)의 전류 효율(cd/A)을 계산하였다.
| 발광층의 호스트 재료 | 문턱전압 (V) |
9000 cd/m2 | ||
| 발광효율 (cd/A) |
수명 (h, T97%) |
|||
| 실시예 13 | 실시예 1 | 4.1 | 87.9 | 50 |
| 실시예 14 | 실시예 2 | 4.3 | 88.7 | 50 |
| 실시예 15 | 실시예 4 | 4.1 | 83.8 | 45 |
| 실시예 16 | 실시예 6 | 4.7 | 73.7 | 20 |
| 실시예 17 | 실시예 7 | 5.1 | 73.6 | 10 |
| 실시예 18 | 실시예 10 | 4.8 | 78.7 | 60 |
| 실시예 19 | 실시예 11 | 4.0 | 68.2 | 10 |
| 실시예 20 | 실시예 12 | 5.3 | 69.5 | 5 |
| 비교예 1 | CBP | 4.8 | 31.4 | < 1 |
| 비교예 2 | 비스[9(4메톡시페닐)카바졸3일] | 30 내지 35 | ||
상기 표 1을 참조하면, 본 발명에서 제공된 재료를 사용하여 제작한 소자의 경우 발광효율에서 기준 물질인 CBP 에 비해 구동전압 및 효율에서 훨씬 더 우수하다는 것을 알 수 있다. 또한 수명에 있어서는 3% 발광효율이 감소할 때까지의 시간을 측정한 것으로 CBP의 경우는 1시간 미만으로 급사 수준의 수명을 나타내지만 본 발명에서 제공된 화합물을 사용하여 제작한 소자의 경우 10 시간에서 최고 60 시간 까지의 수명을 나타내었다.
한편 비교예 2에서 제시된 소자의 발광효율은 30 내지 35 cd/A로 제시되어 있으며, 이 역시 상기 실시예 13 내지 20에 비해 현저히 낮은 효율을 보인다. 이와 같은 두 개의 비교예에서 알 수 있듯이 본 발명에서 제조된 화합물이 양호한 유기발광소자용 재료로 사용될 수 있는 가능성을 보여준다.
본 발명은 상기 실시예들에 한정되는 것이 아니라 서로 다른 다양한 형태로 제조될 수 있으며, 본 발명이 속하는 기술분야에서 통상의 지식을 가진 자는 본 발명의 기술적 사상이나 필수적인 특징을 변경하지 않고서 다른 구체적인 형태로 실시될 수 있다는 것을 이해할 수 있을 것이다. 그러므로 이상에서 기술한 실시예들은 모든 면에서 예시적인 것이며 한정적이 아닌 것으로 이해해야만 한다.
100 : 유기광전소자 110 : 음극
120 : 양극 105 : 유기박막층
130 : 발광층 140 : 정공 수송층
150 : 전자수송층 160 : 전자주입층
170 : 정공주입층 230 : 발광층 + 전자수송층
120 : 양극 105 : 유기박막층
130 : 발광층 140 : 정공 수송층
150 : 전자수송층 160 : 전자주입층
170 : 정공주입층 230 : 발광층 + 전자수송층
Claims (28)
- 하기 화학식 1로 표시되는 유기광전소자용 화합물:
[화학식 1]
상기 화학식 1에서,
X1 및 X2는 서로 동일하거나 상이하며, 독립적으로 NR', O, Se, P 및 S 로 이루어진 군에서 선택되고,
상기 R'는 수소, 중수소, 치환 또는 비치환된 C1 내지 C20 알킬기, 치환 또는 비치환된 C6 내지 C30 아릴기 및 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기로 이루어진 군에서 선택되고,
상기 R1 내지 R6는 서로 동일하거나 상이하며, 독립적으로 수소, 중수소, 치환 또는 비치환된 C1 내지 C20 알킬기, 치환 또는 비치환된 C6 내지 C30 아릴기 및 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기로 이루어진 군에서 선택되고,
상기 R1 내지 R6 또는 R' 중 적어도 어느 하나는 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기다.
- 제 1 항에 있어서,
상기 유기광전소자용 화합물은 하기 화학식 2로 표시되는 것인 유기광전소자용 화합물:
[화학식 2]
상기 화학식 2에서,
X1 및 X2는 서로 동일하거나 상이하며, 독립적으로 NR', O, Se, P 및 S 로 이루어진 군에서 선택되고,
상기 R'는 수소, 중수소, 치환 또는 비치환된 C1 내지 C20 알킬기, 치환 또는 비치환된 C6 내지 C30 아릴기 및 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기로 이루어진 군에서 선택되고,
상기 R1 내지 R6는 서로 동일하거나 상이하며, 독립적으로 수소, 중수소, 치환 또는 비치환된 C1 내지 C20 알킬기, 치환 또는 비치환된 C6 내지 C30 아릴기 및 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기로 이루어진 군에서 선택되고,
상기 R1 내지 R6 또는 R' 중 적어도 어느 하나는 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기다.
- 제 1 항에 있어서,
상기 X1은 NR'인 것인 유기광전소자용 화합물:
상기 R'는 수소, 중수소, 치환 또는 비치환된 C1 내지 C20 알킬기, 치환 또는 비치환된 C6 내지 C30 아릴기 및 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기로 이루어진 군에서 선택된다.
- 제 3 항에 있어서,
상기 R'는 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기인 것인 유기광전소자용 화합물.
- 제 1 항에 있어서,
X1는 NR'이고,
상기 R'는 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기고,
상기 R1 내지 R6는 서로 동일하거나 상이하며, 독립적으로 수소, 중수소, 치환 또는 비치환된 C1 내지 C20 알킬기 및 치환 또는 비치환된 C6 내지 C30 아릴기로 이루어진 군에서 선택되는 것인 유기광전소자용 화합물.
- 제 1 항에 있어서,
상기 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기는 치환 또는 비치환된 이미다졸릴기, 치환 또는 비치환된 트리아졸릴기, 치환 또는 비치환된 테트라졸릴기, 치환 또는 비치환된 옥사다이아졸릴기, 치환 또는 비치환된 옥사트리아졸릴기, 치환 또는 비치환된 싸이아트리아졸릴기, 치환 또는 비치환된 벤즈이미다졸릴기, 치환 또는 비치환된 벤조트리아졸릴기, 치환 또는 비치환된 피리디닐기, 치환 또는 비치환된 피리미디닐기, 치환 또는 비치환된 트리아지닐기, 치환 또는 비치환된 피라지닐기, 치환 또는 비치환된 피리다지닐기, 치환 또는 비치환된 퓨리닐기, 치환 또는 비치환된 퀴놀리닐기, 치환 또는 비치환된 이소퀴놀리닐기, 치환 또는 비치환된 프탈라지닐기, 치환 또는 비치환된 나프피리디닐기, 치환 또는 비치환된 퀴녹살리닐기, 치환 또는 비치환된 퀴나졸리닐기, 치환 또는 비치환된 아크리디닐기, 치환 또는 비치환된 페난트롤리닐기 및 치환 또는 비치환된 페나지닐기으로 이루어진 군에서 선택되는 것인 유기광전소자용 화합물.
- 하기 화학식 3 내지 54 중 어느 하나로 표시되는 유기광전소자용 화합물.
[화학식 3] [화학식 4]
[화학식 5] [화학식 6]
[화학식 7] [화학식 8]
[화학식 9] [화학식 10]
[화학식 11] [화학식 12]
[화학식 13] [화학식 14]
[화학식 15] [화학식 16]
[화학식 17] [화학식 18]
[화학식 19] [화학식 20]
[화학식 21] [화학식 22]
[화학식 23] [화학식 24]
[화학식 25] [화학식 26]
[화학식 27] [화학식 28]
[화학식 29] [화학식 30]
[화학식 31] [화학식 32]
[화학식 33] [화학식 34]
[화학식 35] [화학식 36]
[화학식 37] [화학식 38]
[화학식 39] [화학식 40]
[화학식 41] [화학식 42]
[화학식 43] [화학식 44]
[화학식 45] [화학식 46]
[화학식 47] [화학식 48]
[화학식 49] [화학식 50]
[화학식 51] [화학식 52]
[화학식 53] [화학식 54]
- 제 1 항에 있어서,
상기 유기광전소자용 화합물은 하기 화학식 A 또는 A1로 표시되는 것인 유기광전소자용 화합물:
[화학식 A]
[화학식 A1]
상기 화학식 A 및 A1에서,
X1 및 X2는 서로 동일하거나 상이하며, 독립적으로 NR', O, Se, P 및 S 로 이루어진 군에서 선택되고,
상기 R'는 수소, 중수소, 치환 또는 비치환된 C1 내지 C20 알킬기, 치환 또는 비치환된 C6 내지 C30 아릴기 및 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기로 이루어진 군에서 선택되고,
상기 R1 내지 R6는 서로 동일하거나 상이하며, 독립적으로 수소, 중수소, 치환 또는 비치환된 C1 내지 C20 알킬기, 치환 또는 비치환된 C6 내지 C30 아릴기 및 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기로 이루어진 군에서 선택되고,
상기 R1 내지 R6 또는 R' 중 적어도 어느 하나는 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기다.
- 제 8 항에 있어서,
상기 X1 또는 X2 중 적어도 하나는 NR'이고,
상기 R'는 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기고,
상기 R1 내지 R6는 서로 동일하거나 상이하며, 독립적으로 수소, 중수소, 치환 또는 비치환된 C1 내지 C20 알킬기 및 치환 또는 비치환된 C6 내지 C30 아릴기로 이루어진 군에서 선택되는 것인 유기광전소자용 화합물.
- 제 8 항에 있어서,
상기 X1 또는 X2 중 적어도 하나는 NR'이고,
상기 R'는 치환 또는 비치환된 트리페닐레닐기인 것인 유기광전소자용 화합물.
- 제 8 항에 있어서,
상기 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기는 치환 또는 비치환된 이미다졸릴기, 치환 또는 비치환된 트리아졸릴기, 치환 또는 비치환된 테트라졸릴기, 치환 또는 비치환된 옥사다이아졸릴기, 치환 또는 비치환된 옥사트리아졸릴기, 치환 또는 비치환된 싸이아트리아졸릴기, 치환 또는 비치환된 벤즈이미다졸릴기, 치환 또는 비치환된 벤조트리아졸릴기, 치환 또는 비치환된 피리디닐기, 치환 또는 비치환된 피리미디닐기, 치환 또는 비치환된 트리아지닐기, 치환 또는 비치환된 피라지닐기, 치환 또는 비치환된 피리다지닐기, 치환 또는 비치환된 퓨리닐기, 치환 또는 비치환된 퀴놀리닐기, 치환 또는 비치환된 이소퀴놀리닐기, 치환 또는 비치환된 프탈라지닐기, 치환 또는 비치환된 나프피리디닐기, 치환 또는 비치환된 퀴녹살리닐기, 치환 또는 비치환된 퀴나졸리닐기, 치환 또는 비치환된 아크리디닐기, 치환 또는 비치환된 페난트롤리닐기 및 치환 또는 비치환된 페나지닐기으로 이루어진 군에서 선택되는 것인 유기광전소자용 화합물.
- 제 8 항에 있어서,
상기 유기광전소자용 화합물은 하기 화학식 A2 내지 A26 중 어느 하나로 표시되는 것인 유기광전소자용 화합물.
[화학식 A2] [화학식 A3]
[화학식 A4] [화학식 A5]
[화학식 A6] [화학식 A7]
[화학식 A8] [화학식 A9]
[화학식 A10] [화학식 A11]
[화학식 A12] [화학식 A13]
[화학식 A14] [화학식 A15]
[화학식 A16] [화학식 A17]
[화학식 A18] [화학식 A19]
[화학식 A20] [화학식 A21]
[화학식 A22] [화학식 A23]
[화학식 A24] [화학식 A25]
[화학식 A26]
- 제 1 항에 있어서,
상기 유기광전소자용 화합물은 하기 화학식 B로 표시되는 것인 유기광전소자용 화합물:
[화학식 B]
상기 화학식 B에서,
X1은 O, Se, P 및 S 로 이루어진 군에서 선택되고,
R1 내지 R6는 서로 동일하거나 상이하며, 독립적으로 수소, 중수소, 치환 또는 비치환된 C1 내지 C20 알킬기, 치환 또는 비치환된 C6 내지 C30 아릴기 및 치환 또는 비치환된 C2 내지 C30 헤테로아릴기로 이루어진 군에서 선택되고,
Ar은 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기이고,
L은 단일결합, 치환 또는 비치환된 C2 내지 C10 알케닐렌기, 치환 또는 비치환된 C2 내지 C10 알키닐렌기, 치환 또는 비치환된 C6 내지 C30 아릴렌기 및 치환 또는 비치환된 C2 내지 C30 헤테로아릴렌기로 이루어진 군에서 선택되고,
n은 0 내지 2 중 어느 하나의 정수이다.
- 제 13 항에 있어서,
상기 유기광전소자용 화합물은 하기 화학식 B1 또는 B2로 표시되는 것인 유기광전소자용 화합물:
[화학식 B1]
[화학식 B2]
상기 화학식 B1 및 B2에 있어서,
X1은 O, Se, P 및 S 로 이루어진 군에서 선택되고,
R1 내지 R6는 서로 동일하거나 상이하며, 독립적으로 수소, 중수소, 치환 또는 비치환된 C1 내지 C20 알킬기, 치환 또는 비치환된 C6 내지 C30 아릴기 및 치환 또는 비치환된 C2 내지 C30 헤테로아릴기로 이루어진 군에서 선택되고,
Ar은 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기이고,
L은 단일결합, 치환 또는 비치환된 C2 내지 C10 알케닐렌기, 치환 또는 비치환된 C2 내지 C10 알키닐렌기, 치환 또는 비치환된 C6 내지 C30 아릴렌기 및 치환 또는 비치환된 C2 내지 C30 헤테로아릴렌기로 이루어진 군에서 선택되고,
n은 0 내지 2 중 어느 하나의 정수이다.
- 제 13 항에 있어서,
상기 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기는 치환 또는 비치환된 이미다졸릴기, 치환 또는 비치환된 트리아졸릴기, 치환 또는 비치환된 테트라졸릴기, 치환 또는 비치환된 옥사다이아졸릴기, 치환 또는 비치환된 옥사트리아졸릴기, 치환 또는 비치환된 싸이아트리아졸릴기, 치환 또는 비치환된 벤즈이미다졸릴기, 치환 또는 비치환된 벤조트리아졸릴기, 치환 또는 비치환된 피리디닐기, 치환 또는 비치환된 피리미디닐기, 치환 또는 비치환된 트리아지닐기, 치환 또는 비치환된 피라지닐기, 치환 또는 비치환된 피리다지닐기, 치환 또는 비치환된 퓨리닐기, 치환 또는 비치환된 퀴놀리닐기, 치환 또는 비치환된 이소퀴놀리닐기, 치환 또는 비치환된 프탈라지닐기, 치환 또는 비치환된 나프피리디닐기, 치환 또는 비치환된 퀴녹살리닐기, 치환 또는 비치환된 퀴나졸리닐기, 치환 또는 비치환된 아크리디닐기, 치환 또는 비치환된 페난트롤리닐기 및 치환 또는 비치환된 페나지닐기으로 이루어진 군에서 선택되는 것인 유기광전소자용 화합물.
- 제 1 항에 있어서,
상기 유기광전소자용 화합물은 하기 화학식 C로 표시되는 것인 유기광전소자용 화합물:
[화학식 C]
상기 화학식 C에 있어서,
R1 내지 R6 및 Ar2는 서로 동일하거나 상이하며, 독립적으로 수소, 중수소, 치환 또는 비치환된 C1 내지 C20 알킬기, 치환 또는 비치환된 C6 내지 C30 아릴기 및 치환 또는 비치환된 C2 내지 C30 헤테로아릴기로 이루어진 군에서 선택되고,
Ar1은 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기이고,
L은 단일결합, 치환 또는 비치환된 C2 내지 C10 알케닐렌기, 치환 또는 비치환된 C2 내지 C10 알키닐렌기, 치환 또는 비치환된 C6 내지 C30 아릴렌기 및 치환 또는 비치환된 C2 내지 C30 헤테로아릴렌기로 이루어진 군에서 선택되고,
n은 1 또는 2이다.
- 제 17 항에 있어서,
상기 Ar2는 치환 또는 비치환된 트리페닐레닐기인 것인 유기광전소자용 화합물.
- 제 17 항에 있어서,
상기 전자 특성을 가지는, 치환 또는 비치환된 C2 내지 C30 헤테로아릴기는 치환 또는 비치환된 이미다졸릴기, 치환 또는 비치환된 트리아졸릴기, 치환 또는 비치환된 테트라졸릴기, 치환 또는 비치환된 옥사다이아졸릴기, 치환 또는 비치환된 옥사트리아졸릴기, 치환 또는 비치환된 싸이아트리아졸릴기, 치환 또는 비치환된 벤즈이미다졸릴기, 치환 또는 비치환된 벤조트리아졸릴기, 치환 또는 비치환된 피리디닐기, 치환 또는 비치환된 피리미디닐기, 치환 또는 비치환된 트리아지닐기, 치환 또는 비치환된 피라지닐기, 치환 또는 비치환된 피리다지닐기, 치환 또는 비치환된 퓨리닐기, 치환 또는 비치환된 퀴놀리닐기, 치환 또는 비치환된 이소퀴놀리닐기, 치환 또는 비치환된 프탈라지닐기, 치환 또는 비치환된 나프피리디닐기, 치환 또는 비치환된 퀴녹살리닐기, 치환 또는 비치환된 퀴나졸리닐기, 치환 또는 비치환된 아크리디닐기, 치환 또는 비치환된 페난트롤리닐기 및 치환 또는 비치환된 페나지닐기으로 이루어진 군에서 선택되는 것인 유기광전소자용 화합물.
- 제 1 항에 있어서,
상기 유기광전소자는 유기발광소자, 유기태양전지, 유기트랜지스터, 유기 감광체 드럼 및 유기메모리소자로 이루어진 군에서 선택되는 것인 유기광전소자용 화합물.
- 양극, 음극 및 상기 양극과 음극 사이에 개재되는 적어도 한 층 이상의 유기박막층을 포함하는 유기발광소자에 있어서,
상기 유기박막층 중 적어도 어느 한 층은 상기 제 1 항에 따른 유기광전소자용 화합물을 포함하는 것인 유기발광소자.
- 제 22 항에 있어서,
상기 유기박막층은 발광층, 정공수송층, 정공주입층, 전자수송층, 전자주입층, 정공차단층 및 이들의 조합을 이루어진 군에서 선택되는 것인 유기발광소자.
- 제 22 항에 있어서,
상기 유기광전소자용 화합물은 전자수송층 또는 전자주입층 내에 포함되는 것인 유기발광소자.
- 제 22 항에 있어서,
상기 유기광전소자용 화합물은 발광층 내에 포함되는 것인 유기발광소자.
- 제 22 항에 있어서,
상기 유기광전소자용 화합물은 발광층 내에 인광 또는 형광 호스트 재료로서 사용되는 것인 유기발광소자.
- 제 22 항에 있어서,
상기 유기광전소자용 화합물은 발광층 내에 형광 청색 도펀트 재료로서 사용되는 것인 유기발광소자.
- 제 22 항의 유기발광소자를 포함하는 것인 표시장치.
Priority Applications (7)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2013508986A JP5938397B2 (ja) | 2010-05-03 | 2011-04-29 | 有機光電子素子用化合物、これを含む有機発光ダイオードおよび前記有機発光ダイオードを含む表示装置 |
| EP19155679.4A EP3509121B1 (en) | 2010-05-03 | 2011-04-29 | Compound for organic optoelectronic device, organic light emitting diode including same, and display device including the organic light emitting diode |
| PCT/KR2011/003235 WO2011139055A2 (ko) | 2010-05-03 | 2011-04-29 | 유기광전자소자용 화합물, 이를 포함하는 유기발광소자 및 상기 유기발광소자를 포함하는 표시장치 |
| CN201180022469.XA CN102971395B (zh) | 2010-05-03 | 2011-04-29 | 用于有机光电子装置的化合物、包含其的有机发光二极管和包含所述有机发光二极管的显示器 |
| EP11777536.1A EP2568030B1 (en) | 2010-05-03 | 2011-04-29 | Compound for organic optoelectronic device, organic light emitting diode including same, and display device including organic light emitting diode |
| EP19155683.6A EP3514846A1 (en) | 2010-05-03 | 2011-04-29 | Compound for organic optoelectronic device, organic light emitting diode including same, and display device including the organic light emitting diode |
| US13/668,550 US9543530B2 (en) | 2010-05-03 | 2012-11-05 | Compound for organic optoelectronic device, organic light emitting diode including the same and display including the organic light emitting diode |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020100041466 | 2010-05-03 | ||
| KR20100041466 | 2010-05-03 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20110122051A true KR20110122051A (ko) | 2011-11-09 |
Family
ID=45392753
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020100106077A KR20110122051A (ko) | 2010-05-03 | 2010-10-28 | 유기광전소자용 화합물 및 이를 포함하는 유기광전소자 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US9543530B2 (ko) |
| EP (3) | EP3514846A1 (ko) |
| JP (1) | JP5938397B2 (ko) |
| KR (1) | KR20110122051A (ko) |
| CN (1) | CN102971395B (ko) |
| WO (1) | WO2011139055A2 (ko) |
Cited By (28)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2012161382A1 (en) * | 2011-05-26 | 2012-11-29 | Cheil Industries Inc. | Compound for organic optoelectronic device, organic light emitting diode including the same and display including the organic light emitting diode |
| WO2013027906A1 (ko) * | 2011-08-19 | 2013-02-28 | 제일모직 주식회사 | 유기광전자소자용 화합물, 이를 포함하는 유기발광소자 및 상기 유기발광소자를 포함하는 표시장치 |
| KR20130094222A (ko) * | 2010-06-24 | 2013-08-23 | 도레이 카부시키가이샤 | 발광 소자 재료 및 발광 소자 |
| KR20140005804A (ko) * | 2012-07-04 | 2014-01-15 | 제일모직주식회사 | 유기발광소자용 조성물, 이를 포함하는 유기발광층 및 유기발광소자 |
| KR20140018133A (ko) * | 2012-08-03 | 2014-02-12 | 가부시키가이샤 한도오따이 에네루기 켄큐쇼 | 발광 소자 |
| WO2014030872A3 (ko) * | 2012-08-21 | 2014-05-08 | 제일모직 주식회사 | 유기광전자소자 및 이를 포함하는 표시장치 |
| WO2014129764A1 (ko) * | 2013-02-19 | 2014-08-28 | 덕산하이메탈(주) | 유기전기 소자용 화합물, 이를 이용한 유기전기소자 및 그 전자 장치 |
| KR20140108637A (ko) * | 2011-12-05 | 2014-09-12 | 이데미쓰 고산 가부시키가이샤 | 유기 전기발광 소자용 재료 및 유기 전기발광 소자 |
| WO2015053575A1 (ko) * | 2013-10-11 | 2015-04-16 | 에스에프씨 주식회사 | 유기발광 화합물 및 이를 포함하는 유기전계발광소자 |
| WO2015115744A1 (ko) * | 2014-01-29 | 2015-08-06 | 삼성에스디아이 주식회사 | 전자수송보조층용 조성물, 전자수송보조층을 포함하는 유기 광전자 소자 및 표시 장치 |
| WO2015126081A1 (ko) * | 2014-02-21 | 2015-08-27 | 삼성에스디아이 주식회사 | 유기 광전자 소자 및 표시 장치 |
| KR20160003952A (ko) * | 2014-07-01 | 2016-01-12 | 원광대학교산학협력단 | 유기전계발광소자용 정공수송물질 및 이를 이용한 유기전계발광소자 |
| WO2016032066A1 (ko) * | 2014-08-26 | 2016-03-03 | 삼성에스디아이 주식회사 | 유기 광전자 소자 및 표시 장치 |
| WO2016060332A1 (ko) * | 2014-10-15 | 2016-04-21 | 삼성에스디아이 주식회사 | 유기 광전자 소자 및 표시 장치 |
| KR20160076010A (ko) * | 2014-12-19 | 2016-06-30 | 삼성디스플레이 주식회사 | 유기 발광 소자 |
| US9437827B2 (en) | 2013-06-26 | 2016-09-06 | Samsung Display Co., Ltd. | Heterocyclic compound and organic light-emitting device including the same |
| US9472768B2 (en) | 2011-06-20 | 2016-10-18 | Cheil Industries, Inc. | Material for an organic optoelectronic device, organic light emitting diode including the same, and display device including the organic light emitting diode |
| US9537108B2 (en) | 2013-06-07 | 2017-01-03 | Samsung Display Co., Ltd. | Heterocyclic compound and organic light-emitting device including the same |
| US9590184B2 (en) | 2012-12-27 | 2017-03-07 | Samsung Display Co., Ltd. | Organic light-emitting diode |
| WO2017095084A1 (ko) * | 2015-12-03 | 2017-06-08 | 주식회사 두산 | 유기 발광 화합물 및 이를 이용한 유기 전계 발광 소자 |
| KR20170076819A (ko) * | 2010-08-20 | 2017-07-04 | 유니버셜 디스플레이 코포레이션 | Oled를 위한 바이카르바졸 화합물 |
| US9882149B2 (en) | 2012-07-04 | 2018-01-30 | Samsung Sdi Co., Ltd. | Compound for organic optoelectric device, organic optoelectronic device comprsing same, and display apparatus comprising organic optoelectric device |
| US9911924B2 (en) | 2013-01-17 | 2018-03-06 | Samsung Electronics Co., Ltd. | Material for organic optoelectronic device, organic light emitting diode including the same, and display including the organic light emitting diode |
| KR20190039359A (ko) * | 2010-11-24 | 2019-04-10 | 메르크 파텐트 게엠베하 | 유기 전계발광 소자용 재료 |
| US10727417B2 (en) | 2013-08-26 | 2020-07-28 | Samsung Display Co., Ltd. | Organic light-emitting device |
| KR102283849B1 (ko) | 2020-08-21 | 2021-08-02 | 롬엔드하스전자재료코리아유한회사 | 유기 전계 발광 화합물, 복수 종의 호스트 재료 및 이를 포함하는 유기 전계 발광 소자 |
| DE102021121719A1 (de) | 2020-08-21 | 2022-02-24 | Rohm And Haas Electronic Materials Korea Ltd. | Organische elektrolumineszierende verbindung, mehrere wirtsmaterialien und diese umfassende organische elektrolumineszierende vorrichtung |
| KR20230002039A (ko) | 2021-06-29 | 2023-01-05 | 롬엔드하스전자재료코리아유한회사 | 복수 종의 호스트 재료 및 이를 포함하는 유기 전계 발광 소자 |
Families Citing this family (85)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP5712209B2 (ja) * | 2009-06-24 | 2015-05-07 | ジョージア・テック・リサーチ・コーポレーション | リン光ゲストエミッタのための両極性小分子ホスト |
| EP2471771B1 (en) * | 2009-08-28 | 2016-11-16 | Hodogaya Chemical Co., Ltd. | Compound having carbazole ring structure and organic electroluminescent device |
| KR20110122051A (ko) | 2010-05-03 | 2011-11-09 | 제일모직주식회사 | 유기광전소자용 화합물 및 이를 포함하는 유기광전소자 |
| JP5623996B2 (ja) | 2010-09-21 | 2014-11-12 | 株式会社半導体エネルギー研究所 | カルバゾール誘導体 |
| JP5856266B2 (ja) * | 2010-09-21 | 2016-02-09 | 株式会社半導体エネルギー研究所 | 有機半導体素子 |
| US9133173B2 (en) * | 2010-10-15 | 2015-09-15 | Semiconductor Energy Laboratory Co., Ltd. | Carbazole compound, material for light-emitting element, organic semiconductor material, light-emitting element |
| WO2012086170A1 (ja) | 2010-12-20 | 2012-06-28 | 出光興産株式会社 | 芳香族複素環誘導体及びそれを用いた有機エレクトロルミネッセンス素子 |
| KR101478000B1 (ko) * | 2010-12-21 | 2015-01-05 | 롬엔드하스전자재료코리아유한회사 | 신규한 유기 발광 화합물 및 이를 채용하고 있는 유기 전계 발광 소자 |
| US10147888B2 (en) * | 2011-02-07 | 2018-12-04 | Idemitsu Kosan Co., Ltd. | Biscarbazole derivative and organic electroluminescent element using same |
| EP2674429B1 (en) | 2011-02-07 | 2020-12-23 | Idemitsu Kosan Co., Ltd. | Biscarbazole derivative and organic electroluminescent element using same |
| EP2688120B1 (en) | 2011-03-14 | 2017-08-23 | Toray Industries, Inc. | Light-emitting element material and light-emitting element |
| KR20140009393A (ko) * | 2011-03-24 | 2014-01-22 | 이데미쓰 고산 가부시키가이샤 | 비스카바졸 유도체 및 이것을 이용한 유기 전기발광 소자 |
| KR20120109744A (ko) * | 2011-03-25 | 2012-10-09 | 롬엔드하스전자재료코리아유한회사 | 신규한 유기 전자재료용 화합물 및 이를 포함하는 유기 전계 발광 소자 |
| JP6197265B2 (ja) * | 2011-03-28 | 2017-09-20 | 東レ株式会社 | 発光素子材料および発光素子 |
| CN103518271B (zh) | 2011-05-12 | 2016-06-29 | 东丽株式会社 | 发光元件材料和发光元件 |
| JP5946692B2 (ja) * | 2011-05-13 | 2016-07-06 | 株式会社半導体エネルギー研究所 | カルバゾール化合物、有機半導体素子、発光素子、発光装置、照明装置、表示装置、電子機器 |
| KR20130011955A (ko) * | 2011-07-21 | 2013-01-30 | 롬엔드하스전자재료코리아유한회사 | 신규한 유기 발광 화합물 및 이를 채용하고 있는 유기 전계 발광 소자 |
| WO2013012298A1 (en) * | 2011-07-21 | 2013-01-24 | Rohm And Haas Electronic Materials Korea Ltd. | 9h-carbazole compounds and electroluminescent devices involving them |
| JP6034005B2 (ja) * | 2011-08-03 | 2016-11-30 | 出光興産株式会社 | ビスカルバゾール誘導体およびこれを用いた有機エレクトロルミネッセンス素子 |
| WO2013077352A1 (ja) * | 2011-11-22 | 2013-05-30 | 出光興産株式会社 | 芳香族複素環誘導体、有機エレクトロルミネッセンス素子用材料および有機エレクトロルミネッセンス素子 |
| US9153788B2 (en) | 2011-12-02 | 2015-10-06 | Kyushu University National University Corporation | Organic light-emitting device, and delayed fluorescent material and compound used therefor |
| JP2013116975A (ja) * | 2011-12-02 | 2013-06-13 | Kyushu Univ | 遅延蛍光材料、有機発光素子および化合物 |
| KR20130062583A (ko) * | 2011-12-05 | 2013-06-13 | 롬엔드하스전자재료코리아유한회사 | 신규한 유기 발광 화합물 및 이를 채용하고 있는 유기 전계 발광 소자 |
| JPWO2013105206A1 (ja) | 2012-01-10 | 2015-05-11 | 出光興産株式会社 | 有機エレクトロルミネッセンス素子用材料及びそれを用いた素子 |
| EP2816626B1 (en) | 2012-02-15 | 2020-08-26 | Toray Industries, Inc. | Light-emitting element material, and light-emitting element |
| WO2013133223A1 (ja) * | 2012-03-05 | 2013-09-12 | 東レ株式会社 | 発光素子 |
| JP2015155378A (ja) * | 2012-04-18 | 2015-08-27 | 保土谷化学工業株式会社 | トリフェニレン環構造を有する化合物および有機エレクトロルミネッセンス素子 |
| KR20130121479A (ko) * | 2012-04-27 | 2013-11-06 | 롬엔드하스전자재료코리아유한회사 | 신규한 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 |
| TWI564297B (zh) * | 2012-06-18 | 2017-01-01 | Tosoh Corp | ring A compound, a method for producing the same, and an organic electroluminescent device containing the same |
| CN104507927A (zh) * | 2012-06-18 | 2015-04-08 | 东曹株式会社 | 环状吖嗪化合物、其制造方法、及含有其的有机电致发光元件 |
| EP2879196B1 (en) | 2012-07-25 | 2019-06-19 | Toray Industries, Inc. | Light emitting element material and light emitting element |
| JP5966736B2 (ja) * | 2012-07-31 | 2016-08-10 | 東ソー株式会社 | カルバゾール化合物、その製造法、及びその用途 |
| JP2014072417A (ja) * | 2012-09-28 | 2014-04-21 | Idemitsu Kosan Co Ltd | 有機エレクトロルミネッセンス素子用材料及び有機エレクトロルミネッセンス素子 |
| US10297761B2 (en) | 2012-12-10 | 2019-05-21 | Idemitsu Kosan Co., Ltd. | Organic electroluminescent element |
| US10186665B2 (en) * | 2012-12-28 | 2019-01-22 | Idemitsu Kosan Co., Ltd. | Organic electroluminescent element |
| JP2016122672A (ja) * | 2013-03-18 | 2016-07-07 | 出光興産株式会社 | 発光装置 |
| US10043982B2 (en) | 2013-04-26 | 2018-08-07 | Semiconductor Energy Laboratory Co., Ltd. | Light-emitting element, light-emitting device, display device, electronic device, and lighting device |
| WO2014185535A1 (ja) | 2013-05-16 | 2014-11-20 | ダイキン工業株式会社 | フラーレン誘導体、及びn型半導体材料 |
| KR101566434B1 (ko) * | 2013-07-15 | 2015-11-06 | 삼성디스플레이 주식회사 | 유기 발광 장치 |
| KR101547065B1 (ko) | 2013-07-29 | 2015-08-25 | 주식회사 엘지화학 | 헤테로 고리 화합물 및 이를 포함하는 유기 발광 소자 |
| KR20150071624A (ko) * | 2013-12-18 | 2015-06-26 | 롬엔드하스전자재료코리아유한회사 | 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 |
| KR101846436B1 (ko) * | 2014-01-29 | 2018-04-06 | 제일모직 주식회사 | 전자수송보조층용 조성물, 전자수송보조층을 포함하는 유기 광전자 소자 및 표시 장치 |
| KR20150099192A (ko) * | 2014-02-21 | 2015-08-31 | 삼성에스디아이 주식회사 | 유기 광전자 소자 및 표시 장치 |
| KR20150108330A (ko) * | 2014-03-17 | 2015-09-25 | 롬엔드하스전자재료코리아유한회사 | 전자 버퍼 재료 및 이를 포함하는 유기 전계 발광 소자 |
| KR101773363B1 (ko) * | 2014-04-09 | 2017-08-31 | 제일모직 주식회사 | 유기 화합물, 조성물, 유기 광전자 소자 및 표시 장치 |
| KR102255197B1 (ko) | 2014-05-02 | 2021-05-25 | 삼성디스플레이 주식회사 | 유기 발광 소자 |
| US20170301477A1 (en) | 2016-04-04 | 2017-10-19 | Capacitor Sciences Incorporated | Electro-polarizable compound and capacitor |
| US10319523B2 (en) | 2014-05-12 | 2019-06-11 | Capacitor Sciences Incorporated | Yanli dielectric materials and capacitor thereof |
| CA2948008A1 (en) * | 2014-05-12 | 2015-11-19 | Capacitor Sciences Incorporated | Capacitor and method of production thereof |
| US10340082B2 (en) | 2015-05-12 | 2019-07-02 | Capacitor Sciences Incorporated | Capacitor and method of production thereof |
| RU2016143558A (ru) | 2014-05-12 | 2018-06-13 | Кэпэситор Сайенсиз Инкорпорейтед | Устройство для хранения энергии и способ его изготовления |
| US10347423B2 (en) | 2014-05-12 | 2019-07-09 | Capacitor Sciences Incorporated | Solid multilayer structure as semiproduct for meta-capacitor |
| FR3024144B1 (fr) * | 2014-07-28 | 2017-05-19 | Univ De Tours Francois-Rabelais | Nouveaux synthons pour l'elaboration de semi-conducteurs organiques |
| KR102304720B1 (ko) * | 2014-09-19 | 2021-09-27 | 삼성디스플레이 주식회사 | 유기 발광 소자 |
| KR102409803B1 (ko) | 2014-10-10 | 2022-06-17 | 가부시키가이샤 한도오따이 에네루기 켄큐쇼 | 발광 소자, 표시 장치, 전자 기기, 및 조명 장치 |
| KR101818581B1 (ko) * | 2014-10-31 | 2018-01-15 | 삼성에스디아이 주식회사 | 유기 광전자 소자 및 표시 장치 |
| WO2016073522A1 (en) | 2014-11-04 | 2016-05-12 | Capacitor Sciences Incorporated | Energy storage devices and methods of production thereof |
| KR102384649B1 (ko) | 2014-11-10 | 2022-04-11 | 삼성디스플레이 주식회사 | 유기 발광 소자 |
| KR102285388B1 (ko) * | 2014-11-13 | 2021-08-04 | 삼성디스플레이 주식회사 | 유기 발광 소자 |
| KR102385230B1 (ko) | 2014-11-19 | 2022-04-12 | 삼성디스플레이 주식회사 | 유기 발광 소자 |
| KR101706752B1 (ko) * | 2015-02-17 | 2017-02-27 | 서울대학교산학협력단 | 호스트, 인광 도펀트 및 형광 도펀트를 포함하는 유기발광소자 |
| WO2016138310A1 (en) | 2015-02-26 | 2016-09-01 | Capacitor Sciences Incorporated | Self-healing capacitor and methods of production thereof |
| TW202404148A (zh) | 2015-03-09 | 2024-01-16 | 日商半導體能源研究所股份有限公司 | 發光元件、顯示裝置、電子裝置及照明設備 |
| US9932358B2 (en) | 2015-05-21 | 2018-04-03 | Capacitor Science Incorporated | Energy storage molecular material, crystal dielectric layer and capacitor |
| US9941051B2 (en) | 2015-06-26 | 2018-04-10 | Capactor Sciences Incorporated | Coiled capacitor |
| US10651392B2 (en) | 2015-09-30 | 2020-05-12 | Samsung Electronics Co., Ltd. | Organic light-emitting device |
| US10026553B2 (en) | 2015-10-21 | 2018-07-17 | Capacitor Sciences Incorporated | Organic compound, crystal dielectric layer and capacitor |
| JP6788314B2 (ja) | 2016-01-06 | 2020-11-25 | コニカミノルタ株式会社 | 有機エレクトロルミネッセンス素子、有機エレクトロルミネッセンス素子の製造方法、表示装置及び照明装置 |
| US10636575B2 (en) | 2016-02-12 | 2020-04-28 | Capacitor Sciences Incorporated | Furuta and para-Furuta polymer formulations and capacitors |
| US10305295B2 (en) | 2016-02-12 | 2019-05-28 | Capacitor Sciences Incorporated | Energy storage cell, capacitive energy storage module, and capacitive energy storage system |
| US10566138B2 (en) | 2016-04-04 | 2020-02-18 | Capacitor Sciences Incorporated | Hein electro-polarizable compound and capacitor thereof |
| US9978517B2 (en) | 2016-04-04 | 2018-05-22 | Capacitor Sciences Incorporated | Electro-polarizable compound and capacitor |
| US10153087B2 (en) | 2016-04-04 | 2018-12-11 | Capacitor Sciences Incorporated | Electro-polarizable compound and capacitor |
| EP3452471B1 (de) * | 2016-05-04 | 2021-12-08 | Cynora Gmbh | Organische moleküle, insbesondere zur verwendung in optoelektronischen vorrichtungen |
| KR102005867B1 (ko) * | 2016-06-17 | 2019-07-31 | 삼성에스디아이 주식회사 | 유기 광전자 소자용 조성물, 유기 광전자 소자 및 표시 장치 |
| US10137876B2 (en) | 2016-09-30 | 2018-11-27 | Advics Co., Ltd. | Braking control device for vehicle |
| US10395841B2 (en) | 2016-12-02 | 2019-08-27 | Capacitor Sciences Incorporated | Multilayered electrode and film energy storage device |
| KR20200130348A (ko) | 2018-03-07 | 2020-11-18 | 가부시키가이샤 한도오따이 에네루기 켄큐쇼 | 발광 소자, 표시 장치, 전자 기기, 유기 화합물, 및 조명 장치 |
| KR102206482B1 (ko) | 2018-04-24 | 2021-01-22 | 주식회사 엘지화학 | 신규한 헤테로 고리 화합물 및 이를 이용한 유기발광 소자 |
| CN108774239B (zh) * | 2018-06-14 | 2021-04-20 | 宁波卢米蓝新材料有限公司 | 一种稠环化合物及其制备方法和用途 |
| US20200212314A1 (en) * | 2018-12-28 | 2020-07-02 | Samsung Electronics Co., Ltd. | Organic light-emitting device and apparatus including the same |
| JP7341172B2 (ja) | 2019-02-06 | 2023-09-08 | 株式会社半導体エネルギー研究所 | 発光デバイス、電子機器及び照明装置 |
| KR102406563B1 (ko) * | 2020-04-03 | 2022-06-10 | 덕산네오룩스 주식회사 | 유기전기 소자용 화합물, 이를 이용한 유기전기소자 및 그 전자 장치 |
| KR102217079B1 (ko) * | 2020-04-03 | 2021-02-22 | 덕산네오룩스 주식회사 | 유기전기 소자용 화합물, 이를 이용한 유기전기소자 및 그 전자 장치 |
| CN113666918A (zh) * | 2020-05-15 | 2021-11-19 | 南京高光半导体材料有限公司 | 一种高热稳定性的有机电致发光化合物及有机电致发光器件 |
Family Cites Families (61)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS6340160A (ja) | 1986-08-06 | 1988-02-20 | Fuji Xerox Co Ltd | 有機半導体及びその有機半導体を用いた電子写真感光体 |
| JPH03205479A (ja) | 1989-07-21 | 1991-09-06 | Ricoh Co Ltd | 電界発光素子 |
| JP3139321B2 (ja) * | 1994-03-31 | 2001-02-26 | 東レ株式会社 | 発光素子 |
| JPH08143861A (ja) | 1994-11-25 | 1996-06-04 | Toray Ind Inc | 発光素子 |
| JP3050066B2 (ja) | 1994-11-25 | 2000-06-05 | 東レ株式会社 | 発光素子 |
| EP1146034A1 (en) * | 1995-09-25 | 2001-10-17 | Toyo Ink Manufacturing Co., Ltd. | Light-emitting material for organic electroluminescence device, and organic electroluminescence device for which the light-emitting material is adapted |
| JP3674133B2 (ja) | 1996-03-18 | 2005-07-20 | 東レ株式会社 | 発光素子 |
| JP3924868B2 (ja) | 1997-11-05 | 2007-06-06 | 東レ株式会社 | 有機積層薄膜発光素子 |
| JP3924869B2 (ja) | 1997-11-05 | 2007-06-06 | 東レ株式会社 | 有機積層薄膜発光素子 |
| JPH11329737A (ja) | 1998-03-13 | 1999-11-30 | Taiho Ind Co Ltd | 有機多層型エレクトロルミネッセンス素子及び有機多層型エレクトロルミネッセンス素子用構造体の合成方法 |
| JP2000286056A (ja) | 1999-03-30 | 2000-10-13 | Fuji Photo Film Co Ltd | エレクトロルミネッセンス素子材料およびエレクトロルミネッセンス素子 |
| US6458475B1 (en) | 1999-11-24 | 2002-10-01 | The Trustee Of Princeton University | Organic light emitting diode having a blue phosphorescent molecule as an emitter |
| EP3379591A1 (en) | 1999-12-01 | 2018-09-26 | The Trustees of Princeton University | Complexes of form l2mx |
| TW532048B (en) | 2000-03-27 | 2003-05-11 | Idemitsu Kosan Co | Organic electroluminescence element |
| JP2002308837A (ja) | 2001-04-05 | 2002-10-23 | Fuji Photo Film Co Ltd | 新規化合物、およびそれを用いた発光素子 |
| JP2003133075A (ja) | 2001-07-25 | 2003-05-09 | Toray Ind Inc | 発光素子 |
| KR100957288B1 (ko) | 2002-03-15 | 2010-05-12 | 이데미쓰 고산 가부시키가이샤 | 유기 전기발광 소자용 재료 및 이를 이용한 유기 전기발광소자 |
| JP4316387B2 (ja) | 2002-03-22 | 2009-08-19 | 出光興産株式会社 | 有機エレクトロルミネッセンス素子用材料及びそれを用いた有機エレクトロルミネッセンス素子 |
| JP4707082B2 (ja) | 2002-11-26 | 2011-06-22 | コニカミノルタホールディングス株式会社 | 有機エレクトロルミネッセンス素子および表示装置 |
| US20060180806A1 (en) | 2003-01-24 | 2006-08-17 | Takashi Arakane | Organic electroluminescence device |
| CN1748017A (zh) | 2003-02-12 | 2006-03-15 | 皇家飞利浦电子股份有限公司 | 咔唑化合物及其在有机电致发光器件中的应用 |
| US7329722B2 (en) * | 2004-08-30 | 2008-02-12 | Samsung Electronics Co., Ltd | Polymeric charge transport materials having carbazolyl repeating units |
| WO2006025186A1 (ja) | 2004-09-01 | 2006-03-09 | Hirose Engineering Co., Ltd. | ジカルバジル化合物、その製造方法、ジカルバジル系重合体及び発光素子 |
| JP2006131519A (ja) | 2004-11-04 | 2006-05-25 | Idemitsu Kosan Co Ltd | 縮合環含有化合物及びそれを用いた有機エレクトロルミネッセンス素子 |
| EP1719468A1 (de) * | 2004-12-17 | 2006-11-08 | Zimmer GmbH | Intervertebrales Stabilisierungssystem |
| US8007927B2 (en) | 2007-12-28 | 2011-08-30 | Universal Display Corporation | Dibenzothiophene-containing materials in phosphorescent light emitting diodes |
| ATE455162T1 (de) | 2005-05-30 | 2010-01-15 | Basf Se | Elektrolumineszenz-gerät |
| KR20080080306A (ko) | 2005-12-15 | 2008-09-03 | 이데미쓰 고산 가부시키가이샤 | 유기 전기발광 소자용 재료 및 그것을 이용한 유기전기발광 소자 |
| KR20080078072A (ko) | 2005-12-20 | 2008-08-26 | 코닌클리즈케 필립스 일렉트로닉스 엔.브이. | 중합체성 카르바졸 화합물 |
| JP5055818B2 (ja) * | 2006-04-19 | 2012-10-24 | コニカミノルタホールディングス株式会社 | 有機エレクトロルミネッセンス素子材料、有機エレクトロルミネッセンス素子、表示装置及び照明装置 |
| KR100955993B1 (ko) * | 2006-11-09 | 2010-05-04 | 신닛테츠가가쿠 가부시키가이샤 | 유기 전계 발광 소자용 화합물 및 유기 전계 발광 소자 |
| JP2008135498A (ja) | 2006-11-28 | 2008-06-12 | Toray Ind Inc | 発光素子 |
| US7967978B2 (en) | 2006-12-11 | 2011-06-28 | International Business Machines Corporation | Method and apparatus for filter conditioning |
| WO2008090912A1 (ja) * | 2007-01-23 | 2008-07-31 | Konica Minolta Holdings, Inc. | 有機エレクトロルミネッセンス素子の製造方法、該製造方法により得られた有機エレクトロルミネッセンス素子、表示装置及び照明装置 |
| JP5399236B2 (ja) * | 2007-03-26 | 2014-01-29 | 新日鉄住金化学株式会社 | 有機電界発光素子用化合物及び有機電界発光素子 |
| JP5364089B2 (ja) | 2007-04-13 | 2013-12-11 | チェイル インダストリーズ インコーポレイテッド | 正孔輸送ユニットと電子輸送ユニットとを含む有機光電素子用材料及びこれを含む有機光電素子 |
| WO2008156105A1 (ja) * | 2007-06-21 | 2008-12-24 | Konica Minolta Holdings, Inc. | 有機エレクトロルミネッセンス素子材料、有機エレクトロルミネッセンス素子、表示装置及び照明装置 |
| KR20090024998A (ko) | 2007-09-05 | 2009-03-10 | 제일모직주식회사 | 분자 내에 정공수송기와 전자수송기를 동시에 가지는바이폴라 유기화합물을 포함하는 유기광전소자용 재료 및이를 이용한 유기광전소자 |
| US20090153034A1 (en) | 2007-12-13 | 2009-06-18 | Universal Display Corporation | Carbazole-containing materials in phosphorescent light emittinig diodes |
| US8221905B2 (en) | 2007-12-28 | 2012-07-17 | Universal Display Corporation | Carbazole-containing materials in phosphorescent light emitting diodes |
| WO2010044342A1 (ja) * | 2008-10-15 | 2010-04-22 | コニカミノルタホールディングス株式会社 | 有機エレクトロルミネッセンス素子、有機エレクトロルミネッセンス素子の製造方法、白色有機エレクトロルミネッセンス素子、表示装置及び照明装置 |
| JP5493333B2 (ja) * | 2008-11-05 | 2014-05-14 | コニカミノルタ株式会社 | 有機エレクトロルミネッセンス素子、白色有機エレクトロルミネッセンス素子、表示装置及び照明装置 |
| KR101233375B1 (ko) | 2008-12-24 | 2013-02-15 | 제일모직주식회사 | 신규한 유기광전소자용 화합물 및 이를 포함하는 유기광전소자 |
| KR20100079458A (ko) | 2008-12-31 | 2010-07-08 | 덕산하이메탈(주) | 비스-카바졸 화합물 및 이를 이용한 유기전기소자, 그 단말 |
| US9067947B2 (en) * | 2009-01-16 | 2015-06-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| WO2010090077A1 (ja) * | 2009-02-06 | 2010-08-12 | コニカミノルタホールディングス株式会社 | 有機エレクトロルミネッセンス素子、該素子を備えた照明装置及び表示装置 |
| KR20100094415A (ko) * | 2009-02-17 | 2010-08-26 | 에스에프씨 주식회사 | 시클로아르알킬 유도체 및 이를 이용한 유기전계발광소자 |
| KR101170666B1 (ko) | 2009-03-03 | 2012-08-07 | 덕산하이메탈(주) | 비스카바졸 화합물 및 이를 이용한 유기전기소자, 그 단말 |
| JP5509634B2 (ja) * | 2009-03-16 | 2014-06-04 | コニカミノルタ株式会社 | 有機エレクトロルミネッセンス素子、表示装置、照明装置及び有機エレクトロルミネッセンス素子材料 |
| US8247575B2 (en) | 2009-03-20 | 2012-08-21 | Semiconductor Energy Laboratory Co., Ltd. | Carbazole derivative with heteroaromatic ring, and light-emitting element, light-emitting device, and electronic device using carbazole derivative with heteroaromatic ring |
| KR101431644B1 (ko) | 2009-08-10 | 2014-08-21 | 롬엔드하스전자재료코리아유한회사 | 신규한 유기 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 |
| KR101506999B1 (ko) * | 2009-11-03 | 2015-03-31 | 제일모직 주식회사 | 유기광전소자용 화합물 및 이를 포함하는 유기광전소자 |
| KR101212669B1 (ko) | 2009-12-28 | 2012-12-14 | 제일모직주식회사 | 신규한 유기광전소자용 화합물 및 이를 포함하는 유기광전소자 |
| US9461250B2 (en) * | 2009-12-28 | 2016-10-04 | Nippon Steel & Sumikin Chemical Co., Ltd. | Organic electroluminescent device |
| JPWO2011108707A1 (ja) | 2010-03-05 | 2013-06-27 | 出光興産株式会社 | 有機エレクトロルミネッセンス素子用材料及びそれを用いた有機エレクトロルミネッセンス素子 |
| KR101419666B1 (ko) | 2010-03-31 | 2014-07-15 | 이데미쓰 고산 가부시키가이샤 | 유기 전기발광 소자용 재료 및 그것을 이용한 유기 전기발광 소자 |
| JP5562970B2 (ja) * | 2010-04-20 | 2014-07-30 | 出光興産株式会社 | ビスカルバゾール誘導体、有機エレクトロルミネッセンス素子用材料及びそれを用いた有機エレクトロルミネッセンス素子 |
| KR20110122051A (ko) | 2010-05-03 | 2011-11-09 | 제일모직주식회사 | 유기광전소자용 화합물 및 이를 포함하는 유기광전소자 |
| WO2011148909A1 (ja) | 2010-05-24 | 2011-12-01 | 出光興産株式会社 | 有機エレクトロルミネッセンス素子 |
| JP2013200939A (ja) | 2010-06-08 | 2013-10-03 | Idemitsu Kosan Co Ltd | 有機エレクトロルミネッセンス素子 |
| JP2012028634A (ja) | 2010-07-26 | 2012-02-09 | Idemitsu Kosan Co Ltd | 有機エレクトロルミネッセンス素子 |
-
2010
- 2010-10-28 KR KR1020100106077A patent/KR20110122051A/ko not_active Application Discontinuation
-
2011
- 2011-04-29 JP JP2013508986A patent/JP5938397B2/ja active Active
- 2011-04-29 WO PCT/KR2011/003235 patent/WO2011139055A2/ko active Application Filing
- 2011-04-29 EP EP19155683.6A patent/EP3514846A1/en active Pending
- 2011-04-29 CN CN201180022469.XA patent/CN102971395B/zh active Active
- 2011-04-29 EP EP11777536.1A patent/EP2568030B1/en active Active
- 2011-04-29 EP EP19155679.4A patent/EP3509121B1/en active Active
-
2012
- 2012-11-05 US US13/668,550 patent/US9543530B2/en active Active
Cited By (41)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20130094222A (ko) * | 2010-06-24 | 2013-08-23 | 도레이 카부시키가이샤 | 발광 소자 재료 및 발광 소자 |
| KR20180033309A (ko) * | 2010-08-20 | 2018-04-02 | 유니버셜 디스플레이 코포레이션 | Oled를 위한 바이카르바졸 화합물 |
| KR20170076819A (ko) * | 2010-08-20 | 2017-07-04 | 유니버셜 디스플레이 코포레이션 | Oled를 위한 바이카르바졸 화합물 |
| KR20190039359A (ko) * | 2010-11-24 | 2019-04-10 | 메르크 파텐트 게엠베하 | 유기 전계발광 소자용 재료 |
| WO2012161382A1 (en) * | 2011-05-26 | 2012-11-29 | Cheil Industries Inc. | Compound for organic optoelectronic device, organic light emitting diode including the same and display including the organic light emitting diode |
| US9472768B2 (en) | 2011-06-20 | 2016-10-18 | Cheil Industries, Inc. | Material for an organic optoelectronic device, organic light emitting diode including the same, and display device including the organic light emitting diode |
| WO2013027906A1 (ko) * | 2011-08-19 | 2013-02-28 | 제일모직 주식회사 | 유기광전자소자용 화합물, 이를 포함하는 유기발광소자 및 상기 유기발광소자를 포함하는 표시장치 |
| KR20140108637A (ko) * | 2011-12-05 | 2014-09-12 | 이데미쓰 고산 가부시키가이샤 | 유기 전기발광 소자용 재료 및 유기 전기발광 소자 |
| EP2871223A4 (en) * | 2012-07-04 | 2016-02-24 | Samsung Sdi Co Ltd | COMPOSITION FOR ORGANIC LIGHT-EMITTING DIODE, ORGANIC ILLUMINATION WITH IT AND ORGANIC LIGHT-EMITTING DIODE |
| KR20140005804A (ko) * | 2012-07-04 | 2014-01-15 | 제일모직주식회사 | 유기발광소자용 조성물, 이를 포함하는 유기발광층 및 유기발광소자 |
| US9882149B2 (en) | 2012-07-04 | 2018-01-30 | Samsung Sdi Co., Ltd. | Compound for organic optoelectric device, organic optoelectronic device comprsing same, and display apparatus comprising organic optoelectric device |
| KR20210010626A (ko) * | 2012-08-03 | 2021-01-27 | 가부시키가이샤 한도오따이 에네루기 켄큐쇼 | 발광 소자 |
| US10644254B2 (en) | 2012-08-03 | 2020-05-05 | Semiconductor Energy Laboratory Co., Ltd. | Light-emitting element |
| US10734594B2 (en) | 2012-08-03 | 2020-08-04 | Semiconductor Energy Laboratory Co., Ltd. | Light-emitting element |
| US10505132B2 (en) | 2012-08-03 | 2019-12-10 | Semiconductor Energy Laboratory Co., Ltd. | Light-emitting element |
| US11355722B2 (en) | 2012-08-03 | 2022-06-07 | Semiconductor Energy Laboratory Co., Ltd. | Light-emitting element |
| KR20180121852A (ko) * | 2012-08-03 | 2018-11-09 | 가부시키가이샤 한도오따이 에네루기 켄큐쇼 | 발광 소자 |
| US11730007B2 (en) | 2012-08-03 | 2023-08-15 | Semiconductor Energy Laboratory Co., Ltd. | Light-emitting element |
| KR20140018133A (ko) * | 2012-08-03 | 2014-02-12 | 가부시키가이샤 한도오따이 에네루기 켄큐쇼 | 발광 소자 |
| KR101497138B1 (ko) * | 2012-08-21 | 2015-02-27 | 제일모직 주식회사 | 유기광전자소자 및 이를 포함하는 표시장치 |
| WO2014030872A3 (ko) * | 2012-08-21 | 2014-05-08 | 제일모직 주식회사 | 유기광전자소자 및 이를 포함하는 표시장치 |
| US9590184B2 (en) | 2012-12-27 | 2017-03-07 | Samsung Display Co., Ltd. | Organic light-emitting diode |
| US9911924B2 (en) | 2013-01-17 | 2018-03-06 | Samsung Electronics Co., Ltd. | Material for organic optoelectronic device, organic light emitting diode including the same, and display including the organic light emitting diode |
| WO2014129764A1 (ko) * | 2013-02-19 | 2014-08-28 | 덕산하이메탈(주) | 유기전기 소자용 화합물, 이를 이용한 유기전기소자 및 그 전자 장치 |
| US9537108B2 (en) | 2013-06-07 | 2017-01-03 | Samsung Display Co., Ltd. | Heterocyclic compound and organic light-emitting device including the same |
| US9437827B2 (en) | 2013-06-26 | 2016-09-06 | Samsung Display Co., Ltd. | Heterocyclic compound and organic light-emitting device including the same |
| US10727417B2 (en) | 2013-08-26 | 2020-07-28 | Samsung Display Co., Ltd. | Organic light-emitting device |
| WO2015053575A1 (ko) * | 2013-10-11 | 2015-04-16 | 에스에프씨 주식회사 | 유기발광 화합물 및 이를 포함하는 유기전계발광소자 |
| WO2015115744A1 (ko) * | 2014-01-29 | 2015-08-06 | 삼성에스디아이 주식회사 | 전자수송보조층용 조성물, 전자수송보조층을 포함하는 유기 광전자 소자 및 표시 장치 |
| WO2015126081A1 (ko) * | 2014-02-21 | 2015-08-27 | 삼성에스디아이 주식회사 | 유기 광전자 소자 및 표시 장치 |
| KR20160003952A (ko) * | 2014-07-01 | 2016-01-12 | 원광대학교산학협력단 | 유기전계발광소자용 정공수송물질 및 이를 이용한 유기전계발광소자 |
| WO2016032066A1 (ko) * | 2014-08-26 | 2016-03-03 | 삼성에스디아이 주식회사 | 유기 광전자 소자 및 표시 장치 |
| WO2016060332A1 (ko) * | 2014-10-15 | 2016-04-21 | 삼성에스디아이 주식회사 | 유기 광전자 소자 및 표시 장치 |
| KR20160076010A (ko) * | 2014-12-19 | 2016-06-30 | 삼성디스플레이 주식회사 | 유기 발광 소자 |
| KR20170065283A (ko) * | 2015-12-03 | 2017-06-13 | 주식회사 두산 | 유기 발광 화합물 및 이를 이용한 유기 전계 발광 소자 |
| WO2017095084A1 (ko) * | 2015-12-03 | 2017-06-08 | 주식회사 두산 | 유기 발광 화합물 및 이를 이용한 유기 전계 발광 소자 |
| KR102283849B1 (ko) | 2020-08-21 | 2021-08-02 | 롬엔드하스전자재료코리아유한회사 | 유기 전계 발광 화합물, 복수 종의 호스트 재료 및 이를 포함하는 유기 전계 발광 소자 |
| DE102021121719A1 (de) | 2020-08-21 | 2022-02-24 | Rohm And Haas Electronic Materials Korea Ltd. | Organische elektrolumineszierende verbindung, mehrere wirtsmaterialien und diese umfassende organische elektrolumineszierende vorrichtung |
| KR20220023700A (ko) | 2020-08-21 | 2022-03-02 | 롬엔드하스전자재료코리아유한회사 | 유기 전계 발광 화합물, 복수 종의 호스트 재료 및 이를 포함하는 유기 전계 발광 소자 |
| KR20230107488A (ko) | 2020-08-21 | 2023-07-17 | 롬엔드하스전자재료코리아유한회사 | 유기 전계 발광 화합물, 복수 종의 호스트 재료 및이를 포함하는 유기 전계 발광 소자 |
| KR20230002039A (ko) | 2021-06-29 | 2023-01-05 | 롬엔드하스전자재료코리아유한회사 | 복수 종의 호스트 재료 및 이를 포함하는 유기 전계 발광 소자 |
Also Published As
| Publication number | Publication date |
|---|---|
| CN102971395A (zh) | 2013-03-13 |
| EP2568030B1 (en) | 2019-12-25 |
| US9543530B2 (en) | 2017-01-10 |
| WO2011139055A3 (ko) | 2012-04-19 |
| EP2568030A2 (en) | 2013-03-13 |
| EP3514846A1 (en) | 2019-07-24 |
| CN102971395B (zh) | 2016-10-05 |
| EP3509121B1 (en) | 2022-02-23 |
| EP3509121A1 (en) | 2019-07-10 |
| EP2568030A4 (en) | 2014-11-26 |
| US20130056720A1 (en) | 2013-03-07 |
| JP5938397B2 (ja) | 2016-06-22 |
| WO2011139055A2 (ko) | 2011-11-10 |
| JP2013533604A (ja) | 2013-08-22 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR20110122051A (ko) | 유기광전소자용 화합물 및 이를 포함하는 유기광전소자 | |
| KR101432599B1 (ko) | 유기광전소자용 화합물 및 이를 포함하는 유기광전소자 | |
| KR101531612B1 (ko) | 유기광전소자용 화합물 및 이를 포함하는 유기광전소자 | |
| US9601708B2 (en) | Organic light emitting device and materials for use in same | |
| KR101297158B1 (ko) | 유기광전소자용 화합물 및 이를 포함하는 유기광전소자 | |
| KR101763995B1 (ko) | 방향족 아민 유도체, 유기 전기발광 소자 및 전자 기기 | |
| KR101506999B1 (ko) | 유기광전소자용 화합물 및 이를 포함하는 유기광전소자 | |
| TWI405755B (zh) | 用於有機光電裝置之新穎化合物及包括該化合物之有機光電裝置 | |
| KR101247626B1 (ko) | 유기광전소자용 화합물 및 이를 포함하는 유기광전소자 | |
| KR101423174B1 (ko) | 유기광전소자용 화합물 및 이를 포함하는 유기광전소자 | |
| KR101443755B1 (ko) | 유기광전소자용 화합물 및 이를 포함하는 유기광전소자 | |
| TWI447206B (zh) | A compound for an organic electroluminescent device, and an organic electroluminescent device using the same | |
| KR102174066B1 (ko) | 유기 화합물 및 이를 포함하는 유기전계발광소자 | |
| WO2014104535A1 (ko) | 유기광전자소자용 화합물, 이를 포함하는 유기발광소자 및 상기 유기발광소자를 포함하는 표시장치 | |
| KR101474797B1 (ko) | 유기광전자소자용 화합물 및 이를 포함하는 유기발광소자 | |
| TW201245150A (en) | Organic electroluminescent element | |
| KR101474800B1 (ko) | 유기광전자소자용 화합물, 이를 포함하는 유기발광소자 및 상기 유기발광소자를 포함하는 표시장치 | |
| KR101512544B1 (ko) | 신규한 화합물 및 이를 이용한 유기 발광 소자 | |
| KR20130020398A (ko) | 유기광전자소자용 화합물, 이를 포함하는 유기발광소자 및 상기 유기발광소자를 포함하는 표시장치 | |
| KR101233375B1 (ko) | 신규한 유기광전소자용 화합물 및 이를 포함하는 유기광전소자 | |
| WO2014104545A1 (ko) | 유기광전자소자용 화합물, 이를 포함하는 유기발광소자 및 상기 유기발광소자를 포함하는 표시장치 | |
| KR101117621B1 (ko) | 신규 화합물 및 이를 포함하는 유기 광전 소자 | |
| KR101413080B1 (ko) | 유기광전소자용 화합물 및 이를 포함하는 유기광전소자 | |
| KR20230143926A (ko) | 유기 전계 발광 소자 및 표시 장치 | |
| KR20220071769A (ko) | 유기발광 화합물 및 이를 포함하는 유기발광소자 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A201 | Request for examination | ||
| E902 | Notification of reason for refusal | ||
| AMND | Amendment | ||
| E601 | Decision to refuse application | ||
| E902 | Notification of reason for refusal |