JPWO2002024902A1 - ポリヌクレオチドの合成方法 - Google Patents
ポリヌクレオチドの合成方法 Download PDFInfo
- Publication number
- JPWO2002024902A1 JPWO2002024902A1 JP2002529496A JP2002529496A JPWO2002024902A1 JP WO2002024902 A1 JPWO2002024902 A1 JP WO2002024902A1 JP 2002529496 A JP2002529496 A JP 2002529496A JP 2002529496 A JP2002529496 A JP 2002529496A JP WO2002024902 A1 JPWO2002024902 A1 JP WO2002024902A1
- Authority
- JP
- Japan
- Prior art keywords
- primer
- complementary strand
- loop
- base sequence
- strand synthesis
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/10—Processes for the isolation, preparation or purification of DNA or RNA
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6844—Nucleic acid amplification reactions
Landscapes
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Genetics & Genomics (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Biotechnology (AREA)
- General Engineering & Computer Science (AREA)
- General Health & Medical Sciences (AREA)
- Physics & Mathematics (AREA)
- Molecular Biology (AREA)
- Microbiology (AREA)
- Biophysics (AREA)
- Biomedical Technology (AREA)
- Biochemistry (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Crystallography & Structural Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Analytical Chemistry (AREA)
- Plant Pathology (AREA)
- Immunology (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Saccharide Compounds (AREA)
Abstract
Description
本発明は、ポリヌクレオチドの合成方法に関する。
背景技術
PCR(Polymerase Chain Reaction)法による鋳型依存的な核酸の合成方法は、近年の生命科学分野における研究の大きな推進力となった。PCR法は、少量の2本鎖核酸を鋳型として、鋳型に対して相補的な塩基配列で構成される核酸の指数関数的な増幅を可能とした。いまやPCR法は、遺伝子のクローニングや検出のための道具として、広く普及している。PCR法では、目的とする塩基配列の両端に対して相補的な塩基配列からなる1組のプライマーが用いられる。一方のプライマーによってもたらされる伸長生成物には、他方のプライマーがアニールするように設計される。こうして、互いの伸長生成物へのアニールと相補鎖合成が繰り返し行われる合成反応が進み、指数関数的な増幅が達成される。
PCR法においては、複雑な温度制御が不可欠である。複雑な温度制御に対応するには、専用の反応装置を使わなければならない。したがって、ベッドサイドや野外でPCRを実施することは困難である。また、反応特異性の向上も、公知の相補鎖合成反応の重要な課題であった。たとえばPCR法では、相補鎖合成産物が新たな鋳型として用いられるとき、プライマーがアニールする領域は、厳密には試料に由来する塩基配列ではなくプライマーの塩基配列を写し取ったものに過ぎない。したがって、PCR用のプライマーを利用してわずかな塩基配列の相違を認識するのは、一般には困難とされている。
これらの課題を解決するための1つの方法として、本発明者らは、LAMP法(Loop−mediated isothermal amplification)を完成している(Nucleic Acid Res.2000 Vol.28 No.12 e63、WO 00/28082)。LAMP法は、鋳型ポリヌクレオチドに自身の3’末端をアニールさせて相補鎖合成の起点とするとともに、このとき形成されるループにアニールするプライマーを組み合わせることによって等温での相補鎖合成反応を可能とした。またLAMP法では、3’末端が試料に由来する領域に対してアニールするために、塩基配列のチェック機構が繰り返し機能する。その結果、わずかな塩基配列の判別が可能となった。
LAMP法やPCR法のような相補鎖合成反応に基づいて、標的塩基配列の検出を行う場合、その反応に要する時間と、検出感度との間には密接な関係がある。つまり、反応がプラトーに達するまでは、できるだけ長い時間反応させることが、高い検出感度を達成するための条件となる。LAMP法やPCR法のような公知の相補鎖合成反応は、1時間前後で反応がプラトーに達する。つまり、最大の感度を得るためには1時間前後の反応時間を要すると言って良い。1時間は、反応時間としてはそれほど長いものではないが、もしも検出感度や操作性を犠牲にすることなく、より短い反応時間を実現することができれば有用である。
ゲノムドラフトが明らかにされ、時代はポストシーケンスへと移りつつある。SNPsのような遺伝子の機能解析や、その解析結果に基づく遺伝子診断の必要性がますます高まっている。遺伝子の塩基配列をより正確に、より迅速に解析することができる技術の開発は、機能解析を迅速に進めるために、また遺伝子の機能解析の成果を実際の医療の現場で実用化するうえで、重要な課題となっている。
発明の開示
本発明の課題は、ポリヌクレオチドを鋳型として用いる相補鎖合成反応を、より迅速に行うことができる方法の提供である。
本発明者らは、前記課題を解決するために相補鎖合成の条件について研究を重ねた。そして、相補鎖合成に用いるプライマーと、相補鎖合成の起点となる3’末端との組み合わせが、相補鎖合成の反応速度と密接に関連していることを見出した。更に、特定の構造を持った鋳型ポリヌクレオチドと、このポリヌクレオチドの特定の位置で相補鎖合成の起点を与えることができるプライマーを組み合わせることによって、相補鎖合成の反応効率を改善できることを明らかにし、本発明を完成した。すなわち本発明は、以下のポリヌクレオチドの合成方法、ならびにその用途に関する。
〔1〕以下の要素1〜5を混合して下記のDNAポリメラーゼによる鋳型依存性の相補鎖合成が可能な条件下でインキュベートする工程を含むポリヌクレオチドの合成方法。
1:次の条件(a)〜(d)を持つ鋳型ポリヌクレオチド、
(a)少なくとも1組の相補的な塩基配列からなる標的塩基配列を有する、
(b)aの相補的な塩基配列がハイブリダイズしたときに、塩基対結合が可能なループを形成することができる、
(c)3’末端が自身にアニールしてループを形成することができる、
(d)自身にアニールした3’末端は自身を鋳型とする相補鎖合成の起点となることができる
2:鋳型ポリヌクレオチドのループにおいて、異なる位置に相補鎖合成の起点を与えることができる少なくとも2種類のプライマー、
3:鋳型ポリヌクレオチド、および/または鋳型ポリヌクレオチドに2のプライマーがアニールして生成する伸長生成物が形成するループにおいて、2のプライマーとは異なる位置に相補鎖合成の起点を与えることができる少なくとも1種類のプライマー、
4:鎖置換を伴う相補鎖合成を触媒することができるDNAポリメラーゼ、
5:相補鎖合成のための基質、
〔2〕鋳型ポリヌクレオチドが、自身の塩基配列の任意の領域に対して相補的な塩基配列をその5’末端に備えている〔1〕に記載の方法。
〔3〕次の工程によって鋳型ポリヌクレオチドを生成する〔2〕に記載の方法。
a)標的塩基配列に第1のプライマーをアニールさせ、これを起点とする相補鎖合成反応を行う工程;ここで第1のプライマーはその3’末端において標的塩基配列を構成する一方の鎖の3’側を規定する領域に相補鎖合成の起点を与えることができ、かつ第1のプライマーの5’側には、このプライマーを起点とする相補鎖合成反応生成物の任意の領域に対して相補的な塩基配列を備える、
b)工程a)で合成された第1のプライマーの伸長生成物における第2のプライマーがアニールすべき領域を塩基対結合が可能な状態とする工程;ここで第2のプライマーはその3’末端において前記第1のプライマーを起点とする伸長生成物における標的塩基配列の3’側を規定する領域に相補鎖合成の起点を与えることができる塩基配列を備え、かつ第2のプライマーの5’側には、このプライマーを起点とする相補鎖合成反応生成物の任意の領域に対して相補的な塩基配列を備える、
c)工程b)において塩基対結合が可能となった領域に第2のプライマーをアニールさせ、これを起点とする相補鎖合成を行う工程、
d)工程c)によって合成された第2のプライマーの伸長生成物の3’末端を自身にアニールさせて、自身を鋳型とする相補鎖合成を行う工程
〔4〕前記2種類のプライマーが、第1のプライマー、および第2のプライマーであり、前記少なくとも1種類のプライマーが第1のプライマー、または第2のプライマーの伸長生成物における各プライマーに由来する領域と、各プライマーに対する前記任意の領域の間において相補鎖合成の起点を与えることができるループプライマーである〔3〕に記載の方法。
〔5〕前記ループプライマーが、第1のプライマーの伸長生成物における第1のプライマーに由来する領域と、第1のプライマーに対する前記任意の領域の間において相補鎖合成の起点を与えることができる第1のループプライマー;、および第2のプライマーの伸長生成物における第2のプライマーに由来する領域と、第2のプライマーに対する前記任意の領域の間において相補鎖合成の起点を与えることができる第2のループプライマーである〔4〕に記載の方法。
〔6〕ループプライマーが、前記任意の領域に相補的な塩基配列をその5’末端に付加されている〔4〕に記載の方法。
〔7〕工程b)および/または工程c)において、第1のプライマーまたは第2のプライマーに対して鋳型における3’側に相補鎖合成の起点を与えるアウタープライマーからの相補鎖合成によって、第1のプライマーおよび/または第2のプライマーの伸長生成物を置換して第1のプライマーまたは第2のプライマーの各生成物を1本鎖とする〔3〕に記載の方法。
〔8〕工程a)において、標的塩基配列が2本鎖ポリヌクレオチドとして存在しており、第1のプライマーがアニールする領域が、任意のプライマーを起点とする相補鎖合成反応によって塩基対結合が可能な状態とされる〔3〕に記載の方法。
〔9〕工程a)を融解温度調整剤の存在下で行う〔8〕に記載の方法。
〔10〕融解温度調整剤が、ベタイン、プロリン、ジメチルスルホキシド、およびトリメチルアミンN−オキシドで構成される群から選択される少なくとも1つの化合物である〔9〕に記載の方法。
〔11〕〔1〕または〔5〕に記載の方法によって鋳型ポリヌクレオチドを鋳型とする相補鎖合成を繰り返すとともに、この合成反応による伸長生成物を新たな鋳型ポリヌクレオチドとして、〔1〕または〔5〕に記載の方法によって更に別のポリヌクレオチドの合成反応を行う工程を含む鋳型ポリヌクレオチドの増幅方法。
〔12〕〔11〕に記載の増幅方法を行い、増幅反応生成物の生成を標的塩基配列の存在と関連付ける工程を含む、試料中の標的塩基配列を検出する方法。
〔13〕ポリヌクレオチドの検出剤存在下で〔11〕に記載の方法を行い、検出剤のシグナル変化に基づいて増幅反応生成物が生じたかどうかを観察する〔12〕に記載の方法。
〔14〕〔12〕に記載の検出方法によって標的塩基配列における変異を検出する方法であって、標的塩基配列が予測された塩基配列でなかったときに、前記増幅方法を構成する相補鎖合成反応から選択される少なくとも1つの相補鎖合成反応が妨げられるものであり、前記増幅反応の阻害を観察する工程を含む方法。
〔15〕下記第1のプライマーおよび第2のプライマーを用いる〔14〕に記載の方法であって、第1のプライマーおよび第2のプライマーの少なくともいずれかが、その5’側にチェック用配列を有する方法;
ここでチェック用配列とは、前記特定の領域を構成する塩基配列が予測された塩基配列でなかった場合に、チェック用配列を鋳型として合成された相補鎖の3’末端が標的塩基配列、またはその相補鎖にアニールするときにミスマッチを生じ、かつこのミスマッチによって当該3’末端を起点として開始する相補合成反応が阻害される塩基配列を言う、
第1のプライマー:第1のプライマーはその3’末端において標的塩基配列を構成する一方の鎖の3’側を規定する領域に相補鎖合成の起点を与えることができ、かつ第1のプライマーの5’側には、このプライマーを起点とする相補鎖合成反応生成物の任意の領域に対して相補的な塩基配列を備える、
第2のプライマー:第2のプライマーはその3’末端において前記第1のプライマーを起点とする伸長生成物における標的塩基配列の3’側を規定する領域に相補鎖合成の起点を与えることができる塩基配列を備え、かつ第2のプライマーの5’側には、このプライマーを起点とする相補鎖合成反応生成物の任意の領域に対して相補的な塩基配列を備える、
〔16〕前記特定の領域を構成する塩基配列が予測された塩基配列でなかった場合に、チェック用配列を鋳型として合成された相補鎖が、標的塩基配列、またはその相補鎖にアニールするとき、当該相補鎖の3’末端から2〜4番目の塩基においてミスマッチを生じることを特徴とする〔15〕に記載の方法。
〔17〕ループプライマーとして下記第1のループプライマーおよび/または第2のループプライマーを用いる〔15〕に記載の方法;ただしループプライマーはその5’側に前記プライマーの5’側に配置された前記任意の領域に相補的な塩基配列を有するか、またはプライマーの5’側に配置された塩基配列がチェック用配列であるときは、当該チェック用配列における前記ミスマッチを与えるための塩基がチェック用配列と相違する配列をループプライマーの5’側に配置する
第1のループプライマー:第1のプライマーの伸長生成物における第1のプライマーに由来する領域と、第1のプライマーに対する前記任意の領域の間において相補鎖合成の起点を与える;
第2のループプライマー:第2のプライマーの伸長生成物における第2のプライマーに由来する領域と、第2のプライマーに対する前記任意の領域の間において相補鎖合成の起点を与える;
〔18〕前記特定の領域を構成する塩基配列が予測された塩基配列でなかった場合に、チェック用配列を鋳型として合成された相補鎖が、標的塩基配列、またはその相補鎖にアニールするとき、当該相補鎖の3’末端から2〜4番目の塩基においてミスマッチを生じることを特徴とする〔17〕に記載の方法であって、第1のループプライマーおよび/または第2のループプライマーの5’側に配置する塩基配列は、チェック用配列における前記ミスマッチの原因となる塩基において相違する〔17〕に記載の方法。
〔19〕次の要素a)〜f)を含む、標的塩基配列の増幅用キット。
a)第1のプライマー;ここで第1のプライマーはその3’末端において標的塩基配列を構成する一方の鎖の3’側を規定する領域に相補鎖合成の起点を与えることができ、かつ第1のプライマーの5’側には、このプライマーを起点とする相補鎖合成反応生成物の任意の領域に対して相補的な塩基配列を備える、
b)第2のプライマー;ここで第2のプライマーはその3’末端において前記第1のプライマーを起点とする伸長生成物における標的塩基配列の3’側を規定する領域に相補鎖合成の起点を与えることができる塩基配列を備え、かつ第2のプライマーの5’側には、このプライマーを起点とする相補鎖合成反応生成物の任意の領域に対して相補的な塩基配列を備える、
c)第1のループプライマー;ここで第1のループプライマーは、第1のプライマーの伸長生成物における第1のプライマーに由来する領域と、第1のプライマーに対する前記任意の領域の間において相補鎖合成の起点を与える、
d)第2のループプライマー;ここで第2のループプライマーは、第2のプライマーの伸長生成物における第2のプライマーに由来する領域と、第2のプライマーに対する前記任意の領域の間において相補鎖合成の起点を与える、
e)鎖置換を伴う相補鎖合成を触媒することができるDNAポリメラーゼ、
f)相補鎖合成のための基質、
〔20〕更に次の要素g)を含む〔19〕に記載のキット。
g)アウタプライマー;アウタープライマーは、第1のプライマーおよび/または第2のプライマーの鋳型における3’側に相補鎖合成の起点を与えることができる
〔21〕第1のプライマーおよび/または第2のプライマーが、5’側にチェック用配列を有する〔19〕に記載のキット。
〔22〕ループプライマーとして下記第1のループプライマーおよび/または第2のループプライマーを含む〔19〕に記載のキット;ただしループプライマーはその5’側に前記プライマーの5’側に配置された前記任意の領域に相補的な塩基配列を有するか、または前記プライマーの5’側に配置された塩基配列がチェック用配列であるときは、当該チェック用配列における前記ミスマッチを与えるための塩基がチェック用配列と相違する配列をループプライマーの5’側に配置する
第1のループプライマー:第1のプライマーの伸長生成物における第1のプライマーに由来する領域と、第1のプライマーに対する前記任意の領域の間において相補鎖合成の起点を与える、;
第2のループプライマー:第2のプライマーの伸長生成物における第2のプライマーに由来する領域と、第2のプライマーに対する前記任意の領域の間において相補鎖合成の起点を与える、;
〔23〕次の要素a)〜g)を混合し、鎖置換を伴う相補鎖合成反応が可能な条件下でインキュベートする工程を含むポリヌクレオチドの増幅方法。
a)第1のプライマー;ここで第1のプライマーはその3’末端において標的塩基配列を構成する一方の鎖の3’側を規定する領域に相補鎖合成の起点を与えることができ、かつ第1のプライマーの5’側には、このプライマーを起点とする相補鎖合成反応生成物の任意の領域に対して相補的な塩基配列を備える、
b)第2のプライマー;ここで第2のプライマーはその3’末端において前記第1のプライマーを起点とする伸長生成物における標的塩基配列の3’側を規定する領域に相補鎖合成の起点を与えることができる塩基配列を備え、かつ第2のプライマーの5’側には、このプライマーを起点とする相補鎖合成反応生成物の任意の領域に対して相補的な塩基配列を備える、
c)第1のループプライマー;ここで第1のループプライマーは、第1のプライマーの伸長生成物における第1のプライマーに由来する領域と、第1のプライマーに対する前記任意の領域の間において相補鎖合成の起点を与えることができる、
d)第2のループプライマー;ここで第2のループプライマーは、第2のプライマーの伸長生成物における第2のプライマーに由来する領域と、第2のプライマーに対する前記任意の領域の間において相補鎖合成の起点を与えることができる、
e)鎖置換を伴う相補鎖合成を触媒することができるDNAポリメラーゼ、
f)相補鎖合成のための基質、および
g)標的塩基配列を含む被検ポリヌクレオチド
〔24〕更に次の要素h)を加える〔23〕に記載の方法。
h)アウタプライマー;アウタープライマーは、第1のプライマーおよび/または第2のプライマーの3’末端が標的塩基配列にアニールする領域に対して、鋳型における3’側に相補鎖合成の起点を与える
〔25〕次の要素a)〜d)を混合し、鎖置換を伴う相補鎖合成反応が可能な条件下でインキュベートし、a)における(1)〜(4)のプライマーセットによる増幅生成物の生成速度および/または生成量を測定する工程を含む、標的塩基配列における特定の塩基が、第1の塩基であるか第2の塩基であるかを決定するための方法。
a)以下のプライマーセット(1)〜(4)から選択されたいずれかのプライマーセット
(1):第1塩基用インナープライマー対と第1塩基用ループプライマー対
(2):第1塩基用インナープライマー対と第2塩基用ループプライマー対
(3):第2塩基用インナープライマー対と第1塩基用ループプライマー対
(4):第2塩基用インナープライマー対と第2塩基用ループプライマー対
;ここで第1塩基用インナープライマー対および第2塩基用インナープライマー対は、いずれも次の第1のインナープライマーと第2のインナープライマーとからなるプライマー対であり、第1塩基用インナープライマー対においては第1のインナープライマーと第2のインナープライマーの5’側を鋳型として合成された相補鎖の3’末端を起点とする相補鎖合成反応が、前記標的塩基配列における特定の塩基が第1の塩基のときには阻害されず、第2の塩基のときには阻害され;また
第2塩基用インナープライマー対においては、第1のインナープライマーと第2のインナープライマーの5’側を鋳型として合成された相補鎖の3’末端を起点とする相補鎖合成が、前記標的塩基配列における特定の塩基が第2の塩基のときには阻害されず、第1の塩基のときには阻害され;そして
第1のインナープライマーは、3’末端において標的塩基配列を構成する一方の鎖の3’側を規定する領域に相補鎖合成の起点を与える塩基配列を備え、かつ第1のインナープライマーの5’側には、このインナープライマーを起点とする相補鎖合成反応生成物の任意の領域に対して相補的な塩基配列を備える、
第2のインナープライマーはその3’末端において前記第1のインナープライマーを起点とする伸長生成物における標的塩基配列の3’側を規定する領域に相補鎖合成の起点を与える塩基配列を備え、かつ第2のインナープライマーの5’側には、このインナープライマーを起点とする相補鎖合成反応生成物の任意の領域に対して相補的な塩基配列を備える、
次に第1塩基用ループプライマー対および第2塩基用ループプライマー対は、いずれも次の第1のループプライマーと第2のループプライマーとからなる対であり、第1塩基用ループプライマー対においては第1のループプライマーと第2のループプライマーの5’側を鋳型として合成された相補鎖の3’末端を起点とする相補鎖合成反応が、前記標的塩基配列における特定の塩基が第1の塩基のときには阻害されず、第2の塩基のときには阻害され;また
第2塩基用ループプライマー対においては、第1のループプライマーと第2のループプライマーの5’側を鋳型として合成された相補鎖の3’末端を起点とする相補鎖合成が、前記標的塩基配列における特定の塩基が第2の塩基のときには阻害されず、第1の塩基のときには阻害される;
第1のループプライマーは、第1のインナープライマーの伸長生成物における第1のインナープライマーに由来する領域と、第1のインナープライマーに対する前記任意の領域の間において相補鎖合成の起点を与えることができる、
第2のループプライマーは、第2のインナープライマーの伸長生成物における第2のインナープライマーに由来する領域と、第2のインナープライマーに対する前記任意の領域の間において相補鎖合成の起点を与えることができる、
b)鎖置換を伴う相補鎖合成を触媒することができるDNAポリメラーゼ、
c)相補鎖合成のための基質、および
d)標的塩基配列を含む被検ポリヌクレオチド
〔26〕更に次の要素e)を加える〔25〕に記載の方法。
e)アウタプライマー;アウタープライマーは、第1のプライマーおよび/または第2のプライマーの3’末端が標的塩基配列にアニールする領域に対して、鋳型における3’側に相補鎖合成の起点を与える
本発明において、ポリヌクレオチドとは、DNA、またはRNA、あるいはそれらのキメラ分子であることができる。ポリヌクレオチドは、天然のものであることもできるし、人工的に合成されたものであることもできる。また部分的に、あるいは全体が完全に人工的な構造からなるヌクレオチド誘導体であっても、それが塩基対結合を形成しうるものであり、かつ必要に応じて相補鎖合成の鋳型とすることが可能であるかぎり本発明のポリヌクレオチドに含まれる。このような分子としては、たとえばペプチド結合によってバックボーンが形成されているPNAなどを示すことができる。本発明におけるポリヌクレオチドの構成塩基数は、制限されない。ポリヌクレオチドは、用語「核酸」と同義である。一方本発明におけるオリゴヌクレオチドとは、ポリヌクレオチドの中でも特に構成塩基数が少ないものを示す用語として用いる。一般にオリゴヌクレオチドは、2〜100、より一般的には、2〜50程度の塩基数のポリヌクレオチドを指してオリゴヌクレオチドと呼ぶが、これらの数値に限定されるものではない。
本発明において標的塩基配列とは、合成すべきポリヌクレオチドの塩基配列を意味する。一般にポリヌクレオチドの塩基配列は、5’側から3’側に向けてセンス鎖の塩基配列を記載する。本発明における標的塩基配列とは、センス鎖の塩基配列に加えて、その相補鎖、すなわちアンチセンス鎖の塩基配列も含む。すなわち、用語「標的塩基配列」とは、合成すべき塩基配列、およびその相補鎖の少なくともいずれかを意味する用語として用いる。なお本発明はポリヌクレオチドの合成のみならず増幅をも可能とする方法を提供する。本発明に基づいてポリヌクレオチドの増幅を行う場合には、増幅すべき塩基配列を標的塩基配列と呼ぶ。標的塩基配列は、長いポリヌクレオチドの中から選択された任意の連続した塩基配列であることもできるし、あるいは1本鎖や環状のポリヌクレオチドの全長を標的塩基配列とすることもできる。
なお合成(synthesis)とは1つの標的塩基配列を少なくとも2倍以上に増やす行為を意味する。一方、合成された標的塩基配列に基づいて、連続的に新たな標的塩基配列が合成されるとき、特に増幅(amplification)と呼ぶ。増幅とは、合成が連続的に行われること、と言うこともできる。
更に本発明において、相補鎖合成の起点を与えることとは、鋳型となるポリヌクレオチドに対して、相補鎖合成に必要なプライマーとして機能するポリヌクレオチドの3’末端をハイブリダイズさせることを言う。特定の領域において相補鎖合成の起点を与えると言うときは、当該領域の中の任意の位置に相補鎖合成の起点となる3’末端が位置するように、ポリヌクレオチドをハイブリダイズさせることを意味する。このとき、3’末端が目的とする領域に位置する限り、ハイブリダイズに必要な塩基配列の一部をその領域の外に配置することもできる。
一方前記DNAポリメラーゼは、鋳型依存性の相補鎖合成が可能な条件下において、前記鋳型ポリヌクレオチドにアニールした各プライマーや、自身の3’末端を起点とする相補鎖合成反応を触媒する。本発明において、鋳型依存性の相補鎖合成が可能な条件下とは、鋳型にアニールしたポリヌクレオチドの3’末端を起点として、鋳型となるポリヌクレオチドの塩基配列に相補な塩基配列からなる新たなポリヌクレオチド鎖を合成する反応を言う。本発明において、新たなポリヌクレオチド鎖は、鋳型と異なる分子であることもできるし、鋳型と同じ分子であることもできる。たとえば、ポリヌクレオチドの3’末端を自身にアニールさせて進行する相補鎖合成反応によって生成される新たなポリヌクレオチド鎖は、鋳型ポリヌクレオチドと同じ分子となる。本発明において、鋳型依存性の相補鎖合成が可能な条件を、単に相補鎖合成が可能な条件と言う場合がある。
このような反応は、通常、DNAポリメラーゼの至適反応条件を与える緩衝液中で行うことができる。緩衝液には、DNAポリメラーゼの活性を保護する保護剤、活性の維持に必要な無機塩類などを共存させることができる。このような反応条件は、DNAポリメラーゼに応じて当業者が適宜選択することができる。
また本発明において、3’末端、あるいは5’末端とは、単にいずれかの末端の1塩基のみならず、末端の1塩基を含み、かつ末端に位置する領域を意味する。より具体的には、いずれかの末端から500塩基、望ましくは100塩基、あるいは少なくとも20塩基は、3’末端、あるいは5’末端に含まれる。これに対して、末端の1塩基や末端付近に存在する特定の位置の塩基を示すためには、その位置を数値で特定することによって示すものとする。
本発明の標的塩基配列は少なくとも1組の相補的な塩基配列からなっている。本発明において同一、あるいは相補的という用語は、いずれも完全に同一でない場合、あるいは完全に相補的でない場合を含む。すなわち、ある配列と同一とは、ある配列に対してアニールすることができる塩基配列に対して相補的な配列をも含むことができる。他方、相補的とは、ストリンジェントな条件下でアニールすることができ、相補鎖合成の起点となる3’末端を提供することができる配列を意味する。具体的には、ある塩基配列に対して、一般に50−100%、通常は70−100%、好ましくは80−100%の同一性を有する塩基配列は、実質的に同一と言うことができる。同一性はBLASTN等の公知のアルゴリズムに基づいて決定することができる。
本発明の鋳型ポリヌクレオチドは、前記相補的な塩基配列がハイブリダイズしたときに、ループを形成することができる。相補的な塩基配列はハイブリダイズした後には、塩基対結合が安定に維持される条件のもとでは、もはや新たな塩基対結合を生じることは困難である。一方ループは、このループを構成する塩基配列に相補的な塩基配列からなる別のポリヌクレオチドと新たな塩基対結合を形成することができる。ループを構成する塩基配列は任意である。
本発明において用いられるハイブリダイズという用語は、相補的な塩基配列からなるポリヌクレオチドが塩基対結合によって結合することを意味する。塩基対結合するポリヌクレオチドは別の分子であることもできるし、同一の分子であることもできる。異なる分子間で生じたハイブリダイズを解消すれば、複数のポリヌクレオチド分子に解離する。一方、同一の分子上でハイブリダイズしたポリヌクレオチドは、塩基対結合を解消しても1分子のポリヌクレオチドのままである。本発明においては、アニールという用語も用いられる。ポリヌクレオチドが相補的な塩基配列からなるポリヌクレオチドにハイブリダイズして相補鎖合成の起点となる3’末端を与えるとき、特にアニールと表現する場合がある。
本発明の鋳型ポリヌクレオチドは、その3’末端が自身にアニールしてループを形成することができ、更に自身にアニールした3’末端は自身を鋳型とする相補鎖合成の起点となることができる。アニールするための塩基配列は、その3’末端からの相補鎖合成を可能とする限り制限されない。具体的には、たとえばポリヌクレオチドの3’から100−200塩基、通常50−80塩基、望ましくは20−30塩基が前記標的塩基配列中の任意の領域に対して相補的な塩基配列を有する。このとき、アニールした3’末端の塩基は、標的塩基配列に対して完全に相補的であることが望ましい。3’末端の塩基が完全に相補的であることは、必須ではないが、効率的な相補鎖合成の重要な条件である。
本発明の鋳型ポリヌクレオチドは、3’末端の自身へのアニールによって、ループを形成することができる。ループは前記ループと同様に、任意の塩基配列からなり、他のポリヌクレオチドと塩基対結合が可能な状態で存在する。
また本発明の鋳型ポリヌクレオチドは、その5’末端において、自身が有する任意の領域に対して相補的な塩基配列を備えることができる。このような鋳型ポリヌクレオチドの相補鎖が合成されると、合成された新たなポリヌクレオチドの3’末端は、自身の任意の領域に対してアニールして、自身を鋳型とする相補鎖合成反応の起点となることができる。3’末端が自身にアニールすることによって、ループが形成される。こうして形成されるループには、本発明におけるプライマーがアニールすることができる。
このように、鋳型ポリヌクレオチドの5’末端を、自身が有する任意の領域に対して相補的な塩基配列とすることによって、相補鎖合成の生成物を再び鋳型ポリヌクレオチドとして利用することができる。したがって、このような鋳型ポリヌクレオチドは、本発明において、高度に効率的な相補鎖合成反応を達成するための望ましい構造である。
本発明における鋳型ポリヌクレオチドは、酵素的に、あるいは化学的に合成することができる。たとえば、以下の工程a)−d)を経て鋳型ポリヌクレオチドを合成することができる。以下の工程a)−d)は、LAMP法のためのポリヌクレオチドの合成方法と言うことができる。
a)標的塩基配列に第1のプライマーをアニールさせ、これを起点とする相補鎖合成反応を行う工程;ここで第1のプライマーはその3’末端において標的塩基配列を構成する一方の鎖の3’側を規定する領域に相補鎖合成の起点を与えることができ、かつ第1のプライマーの5’側には、このプライマーを起点とする相補鎖合成反応生成物の任意の領域に対して相補的な塩基配列を備える、
b)工程a)で合成された第1のプライマーの伸長生成物における第2のプライマーがアニールすべき領域を塩基対結合が可能な状態とする工程;ここで第2のプライマーはその3’末端において前記第1のプライマーを起点とする伸長生成物における標的塩基配列の3’側を規定する領域に相補鎖合成の起点を与えることができる塩基配列を備え、かつ第2のプライマーの5’側には、このプライマーを起点とする相補鎖合成反応生成物の任意の領域に対して相補的な塩基配列を備える、
c)工程b)において塩基対結合が可能となった領域に第2のプライマーをアニールさせ、これを起点とする相補鎖合成を行う工程、
d)工程c)によって合成された第2のプライマーの伸長生成物の3’末端を自身にアニールさせて、自身を鋳型とする相補鎖合成を行う工程
上記工程を図1に基づいてより具体的に説明する。以下の説明では、仮にR2およびR1cからなる第1のプライマー(RA)、ならびにF2およびF1cからなる第2のプライマー(FA)を用いて、本発明における鋳型ポリヌクレオチドを生成する行程を例示する。以下の説明においては、第1のプライマーおよび第2のプライマーを、それぞれ仮にRAおよびFAと名づける。
第1のプライマーRAは、その3’末端において標的塩基配列を構成する一方の鎖の3’側を規定する領域に相補鎖合成の起点を与えることができ、かつ第1のプライマーRAの5’側には、このプライマーを起点とする相補鎖合成反応生成物の任意の領域に対して相補的な塩基配列を備える。RAの3’側の領域R2、5’側の領域をR1cと称する。一方、第2のプライマーFAは、その3’末端において前記第1のプライマーRAを起点とする伸長生成物における標的塩基配列の3’側を規定する領域に相補鎖合成の起点を与えることができる塩基配列を備え、かつ第2のプライマーFAの5’側には、このプライマーを起点とする相補鎖合成反応生成物の任意の領域に対して相補的な塩基配列を備える。FAの3’側はF2、5’側はF1cと称する。更にRAとFAの3’側と5’側を構成する各領域は、それぞれ次のような領域に対して相補的な塩基配列からなっている。
RAの3’側(R2) :R2c
RAの5’側(R1c):R1
FAの3’側(F2) :F2c
FAの5’側(F1c):F1
結局、RAは標的塩基配列のR2cとR1によって、またFAは標的塩基配列におけるF2cとF1によってその構造が決定されることになる。したがって本発明においては、標的塩基配列は、少なくともその一部の塩基配列が明らかとなっている、あるいは推測が可能な状態にある塩基配列であることが求められる。塩基配列を明らかにすべき部分とは、RAとFAの構造を決定する各領域、あるいはその相補的な塩基配列からなる領域である。R2cとR1c(またはF2cとF1c)は、連続する場合、そして離れて存在する場合とを想定することができる。両者の相対的な位置関係により、生成物であるポリヌクレオチドが自己アニールしたときに形成されるループ部分の状態が決定される。本発明において、自己アニールとは、1本鎖ポリヌクレオチドの3’末端を含む領域が、そのポリヌクレオチド自身の相補的な塩基配列にハイブリダイズして、自身を鋳型とする相補鎖合成の起点となることを意味する。生成物であるポリヌクレオチドが分子間のアニールではなく自己アニールを優先的に行うためには、両者の距離が不必要に離れないほうが望ましい。したがって、両者の位置関係は、通常0−500塩基分の距離を介して連続するようにするのが望ましい。ただし、後に述べる自己アニールによるループの形成において、両者があまりにも接近している場合には望ましい状態のループの形成を行うには不利となるケースも予想される。
ループにおいては、新たなオリゴヌクレオチドのアニールと、それを合成起点とする鎖置換を伴う相補鎖合成反応がスムーズに開始できる構造が求められる。したがってより望ましくは、領域R2cおよびその5’側に位置する領域R1cとの距離が、0〜100塩基、さらに望ましくは10〜70塩基となるように設計する。なおこの数値はR1cとR2cを含まない長さを示している。ループ部分を構成する塩基数は、更にR2に相当する領域を加えた長さとなる。なお同様の条件がFAにおけるF2cとF1cにも適用される。
上記標的塩基配列に対してRAおよびFAを構成する領域R2とR1c(またはF2とF1c)は、通常は重複することなく連続して配置される。あるいはもしも両者の塩基配列に共通の部分があるのであれば、部分的に両者を重ねて配置することもできる。R2(またはF2)はプライマーとして機能する必要があることから、常に3’末端となるようにしなければならない。一方R1c(またはF1c)は、後に述べるように、これを鋳型として合成された相補鎖の3’末端にプライマーとしての機能を与える必要があることから、5’末端に配置する。このオリゴヌクレオチドを合成起点として得られる相補鎖は、次のステップにおいては逆向きからの相補鎖合成の鋳型となり、最終的にはRAとFAも鋳型として相補鎖に写し取られる。写し取られることによって生じる3’末端は塩基配列R1(またはF1)を備えており、同一鎖上のR1c(またはF1c)にアニールするとともに、ループを形成する。
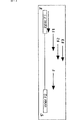
まず標的塩基配列におけるR2cに第1のプライマーのR2がアニールし、相補鎖合成が行われる[図1−(1)]。第1のプライマーの伸長生成物を1本鎖とし、そのF2cに第2のプライマーのF2をアニールさせて相補鎖合成を行うと、相補鎖合成は第1のプライマーの5’末端に達したところで終了する。このとき合成される第2のプライマーの伸長生成物は、その3’末端にR1を備えている。3’末端のR1は、第1のプライマーの5’側R1cを鋳型として合成された領域である。R1は自身のR1cにアニールして相補鎖合成の起点となり、自身を鋳型とする相補鎖合成が行われる[図1−(2)recycling products中]。
以上の反応を経て生成されるポリヌクレオチドは、標的塩基配列とその相補鎖からなる1組の相補的な塩基配列を備え、それがハイブリダイズしたときには塩基対結合が可能なループを形成する。加えて、その3’末端には、自身のF1cに相補的な塩基配列からなるF1を備えている。F1は第2のプライマーのF1cを鋳型として合成された領域である。すなわち、この生成物は本発明における鋳型ポリヌクレオチドに他ならない。
なおポリヌクレオチドの合成反応のための新たな出発材料となることができるポリヌクレオチドを与える構造を、図1にrecycling productsとして示した。これらの構造を鋳型として生成される生成物は、いずれも新たな鋳型ポリヌクレオチドを生成することができる。
なお図1では、いったん生成した鋳型ポリヌクレオチドが、更にその3’末端を自身にアニールさせて相補鎖合成を行う工程を示している。その結果、2組の相補的な標的塩基配列を備えた鋳型ポリヌクレオチドが生成している[図1−(3)]。なお図1−(3)において標的塩基配列を構成しているのは、F2とR2cの間、並びにその相補的な塩基鎖であるR2とF2cの間を構成する塩基配列である。
以上の反応は、実際には標的塩基配列の相補鎖においても並行して進行する。すなわち、第2のプライマーの相補鎖合成から始まって、第1のプライマーの伸長生成物[図1−(2‘)]を経て2組の相補的な標的塩基配列からなる鋳型ポリヌクレオチド[図1−(3’)]を生成する。図1−(3)に示す鋳型ポリヌクレオチドと、図1−(3‘)に示す鋳型ポリヌクレオチドは、相互に相補的な塩基配列からなっている。
次に、LAMP法に基づいて鋳型ポリヌクレオチドを合成するための反応における工程b)、すなわち工程a)で合成された第1のプライマーの伸長生成物における第2のプライマーがアニールすべき領域を塩基対結合が可能な状態とする工程を行うには、アウタープライマーの利用が有利である。本発明において、アウタープライマーとは、標的塩基配列に対してアニールする第1のプライマーおよび第2のプライマーより上流に対して相補的な塩基配列からなるプライマーである。本発明において、上流とは、鋳型における3’側を意味する。したがってアウタープライマーがアニールするのは、第1のプライマーおよび第2のプライマーから見れば5’側の領域となる。
例えば図1−(1)においては、RAがアニールする領域R2cの3’側に位置するR3cにアニールするアウタープライマーR3が記載されている。同様にその相補鎖においては、FAがアニールする領域の3’側に位置するF3cに対してアウタープライマーF3をアニールさせることができる。アウタープライマーは、プライマーとして機能する塩基配列を少なくともその3’側に備えるオリゴヌクレオチドを用いることができる。第1のプライマーおよび第2のプライマー2種は、本発明における3種のプライマーのうちの2種として用いることができる。一方ここで述べたアウタープライマーは、必ずしも本発明の3種のプライマーを構成しなくても良い。アウタープライマーは、鋳型ポリヌクレオチドの合成のために用いられる。
第1のプライマーおよび第2のプライマーが通常2つのプライマーの組み合わせで構成されるのに対して、アウタープライマーは、任意の数であることができる。本発明において、一般的なアウタープライマーは、第1のプライマーおよび第2のプライマーのそれぞれに対して上流に相補鎖合成の起点を与えることができる2つのアウタープライマーからなる。しかし、いずれかの第1のプライマーおよび第2のプライマーに対してのみ、アウタープライマーを配置する場合でも、本発明の方法を実施することができる。あるいは、第1のプライマーおよび第2のプライマーのそれぞれ、あるいは一方に対して、複数のアウタープライマーを組み合わせることもできる。いずれにせよ、より上流からの相補鎖合成を伴う場合に、第1のプライマーおよび第2のプライマーを複製起点とする相補鎖合成反応の生成物を効率良く生じさせることが可能となる。
本発明におけるアウタープライマーからの相補鎖合成は、第1のプライマーおよび第2のプライマーを複製起点とする相補鎖合成よりも後に開始されるように設計する。そのための最も単純な方法は第1のプライマーおよび第2のプライマーの濃度をアウタープライマーの濃度よりも高くすることである。具体的には、通常2〜50倍、望ましくは4〜10倍の濃度差でプライマーを用いることにより、第1のプライマーおよび第2のプライマーからの相補鎖合成を優先的に行わせることができる。またアウタープライマーの融解温度(Tm)を第1のプライマーおよび第2のプライマーのTmより低くなるように設定することによって合成のタイミングをコントロールすることもできる。
すなわち、インナープライマーFAに対して、アウタープライマーのTmを(アウタープライマーF3:F3c)≦(F2c/F2)となるように設計することにより、核酸の増幅を効率的に行うことができる。FAを構成する各領域については、(F1c/F1)間のアニールが(F2c/F2)よりも優先的におきるようにデザインするのが望ましい。デザインに当たっては、Tmや構成塩基等を考慮する。更に、F1c/F1間のアニールが分子内の反応なので優先的に進む可能性が高いことも考慮する。同様の条件は、FAの伸長生成物にアニールするRAの設計においても考慮される。
このような関係とすることにより、確率的に理想的な反応条件を達成することができる。融解温度(Tm)は、他の条件が一定であればアニールする相補鎖の長さと塩基対結合を構成する塩基の組み合わせによって理論的に算出することができる。したがって当業者は、本明細書の開示に基づいて望ましい条件を容易に導くことができる。
更にアウタープライマーのアニールのタイミングを調整するために、コンティギュアス・スタッキング(contiguous stacking)と呼ばれる現象を応用することもできる。コンティギュアス・スタッキングとは、単独ではアニールすることができないオリゴヌクレオチドが2本鎖部分に隣接することによってアニールが可能となる現象である(Chiara Borghesi−Nicoletti et.al.Bio Techniques 12,474−477,1992)。つまり、アウタープライマーを第1のプライマーおよび第2のプライマーに隣接させ、しかもアウタープライマー単独ではインキュベーションの条件下ではアニールできないように設計しておくのである。こうすれば、第1のプライマーおよび第2のプライマーがアニールしたときに初めてアウタープライマーのアニールが可能となるので、必然的に第1のプライマーおよび第2のプライマーのアニールが優先されることになる。この原理に基づいて、一連の反応にプライマーとして必要なオリゴヌクレオチドの塩基配列を設定した例が実施例に記載されている。
上記反応において、標的塩基配列を含むポリヌクレオチド試料は、相補鎖合成の鋳型となりうる任意のポリヌクレオチドを利用することができる。具体的には、DNAやRNA、それらの誘導体、並びにキメラ分子を示すことができる。更にポリヌクレオチド試料には、ゲノムDNAやmRNA等の天然のポリヌクレオチドの他、プラスミドやファージなどに人為的に組みこまれたポリヌクレオチドを用いることもできる。ポリヌクレオチド試料は精製したもののみならず、未精製の状態のまま用いることもできる。細胞中のポリヌクレオチドをin situで合成の対象とすることもできる。
次に本発明においては、ループの異なる領域に相補鎖合成の起点を与えることができる少なくとも3種類のプライマーが用いられる。プライマーが相補鎖合成の起点を与えるループとは、前記鋳型ポリヌクレオチドが備えているループに加え、その3’末端やいずれかのプライマーを起点とする相補鎖合成の結果生成される新たなポリヌクレオチドによって形成されるループが含まれる。
鋳型ポリヌクレオチドは、少なくとも次の2つのループを有する。
1.標的塩基配列がハイブリダイズすることによって形成されるループ
2.鋳型ポリヌクレオチドの3’末端が自身にアニールすることによって形成されるループ
鋳型ポリヌクレオチドが2組以上の相補的な標的塩基配列からなり、かつ相補的な塩基配列が交互に並んでいる場合には、その数に応じたループが鋳型ポリヌクレオチド上に形成される。例えば、ある塩基配列Aと、その相補的な塩基配列aとで構成されるポリヌクレオチドを想定する。複数組の相補的な塩基配列が交互に並んだ状態とは、たとえば次のように表すことができる。
5’−[A]−(L)−[a]−[A]−(L)−[a]−[A]−(L)−[a]−3’
この例では、隣り合う[A]−[a]間でハイブリダイズが起きたときに3つのループを形成することができる。相補的な塩基配列のハイブリダイズによってループが形成される部分を−(L)−で示した。更に3’末端の自身へのアニールによって形成されるループが加わり、この鋳型ポリヌクレオチドは合計4つのループを形成することになる。なお、3’末端が自身へのアニールによってループを形成するときには、[a]の塩基配列の一部がアニールのために利用される。したがって、3’末端の[a]においては、[A]と相補的な塩基配列であると同時に、自身へのアニールに利用される領域を有する。
なお本発明における鋳型ポリヌクレオチドが含むことができる相補的な塩基配列の数は制限されない。したがって、[A]と[a]とで構成される鋳型ポリヌクレオチドを一般式で表すとすれば、次のように表すことができる。式中、nは任意の自然数を意味する。
5’−{[A]−(L)−[a]}n−3’
一方、鋳型ポリヌクレオチドの3’末端、あるいはいずれかのプライマーを起点とする相補鎖合成の結果生成される新たなポリヌクレオチドによって形成されるループは、具体的には次のようにして形成される。まず鋳型ポリヌクレオチドは、その3’末端を自身にアニールさせて自身を鋳型とする相補鎖合成反応を行うことができる。この反応は、3’末端とそれがアニールする領域とを繰り返し塩基対結合が可能な状態にすることができれば、連続的に進行する。その結果、鋳型ポリヌクレオチドに相補的な塩基配列が繰り返し伸長することになる。したがって、鋳型ポリヌクレオチドが1組の相補的な塩基配列からなる場合、相補鎖合成によって得られた新たなポリヌクレオチドには、相補鎖合成反応を繰り返す度に相補的な塩基配列の数は倍になる。ここで新たに生成されたポリヌクレオチドにおける2組の相補的な塩基配列がそれぞれハイブリダイズすると、相補的な塩基配列のセットの数に応じた数のループを生じる[たとえば図1−(4)、あるいは図1−(5)等]。これらのループのうち、あるものは鋳型ポリヌクレオチドがもともと有していたループである。他方のループは、鋳型ポリヌクレオチドのループの相補的な塩基配列からなっている。このようにして生じた新たなループも、本発明におけるプライマーがアニールするループに含まれる。
更に本発明におけるループには、鋳型ポリヌクレオチドが有するループにプライマーがアニールして相補鎖合成の起点となることによって生成した新たなポリヌクレオチドに形成されたループが含まれる。たとえば、鋳型ポリヌクレオチドの3’末端が自身にアニールすることによって形成されるループに相補鎖合成の起点を与えることができるプライマーを起点として相補鎖を合成することができる。その生成物は、鋳型に対して相補的な塩基配列からなるポリヌクレオチドとなる。このポリヌクレオチドは、鋳型ポリヌクレオチドと同様に相補的な塩基配列がハイブリダイズすることによって、ループを形成する。すなわち、鋳型ポリヌクレオチドが有するループに相補的な塩基配列からなるループを備えるポリヌクレオチドが生成する。
本発明におけるプライマーは、このようにして形成される新たなループに相補鎖合成の起点を与えることができるプライマーが含まれる。あるいは、既に述べたように鋳型ポリヌクレオチドが自身の任意の領域に相補的な塩基配列を5’末端に含む場合、これを鋳型として合成されたポリヌクレオチドの3’末端は、自身にアニールしてループを形成することができる。本発明では、このようにして形成されるループに相補鎖合成の起点を与えることができるプライマーを用いることもできる。
なお鋳型ポリヌクレオチドの5’末端が自身の任意の領域に対して相補的な塩基配列を含むとき、5’末端は自身にハイブリダイズしてループが形成することができる。5’末端のループも塩基対結合が可能な状態にはある。しかし、このループに相補鎖合成の起点を与えるプライマーでからは、通常、ループから5’末端までのわずかな領域についてしか相補鎖合成の対象とすることができない。
本発明のプライマーは、前記のような、いくつかの種類のループから選択される少なくとも1種類、好ましくは2種類、あるいは3種類以上のループにおいて相補鎖合成の起点となることができるプライマーを3種以上利用する。3種類以上とは、3つのプライマーが相互に異なる位置において相補鎖合成の起点を与えることを意味する。
本発明におけるプライマーの種類は、少なくとも3種、好ましくは4種、あるいは5種類以上のプライマーを組み合わせることもできる。なお相互に異なる位置とは、プライマーがアニールしたときの各プライマーの3’末端の位置が相互に異なっていることを言う。したがって、アニールに必要な塩基配列を部分的に重複させることもできる。しかしながら、アニールに必要な領域が重複する場合にはプライマーの間で競合を生じるため、できるだけ相互に独立した領域に対してアニールできるようにプライマーの塩基配列を設計することが望ましい。更に、鋳型ポリヌクレオチドにおいてハイブリダイズやアニールの対象となる領域に対しても、できるだけ重複しないようにプライマーの塩基配列を設計することにより、より迅速な相補鎖合成を期待することができる。したがって、たとえば鋳型ポリヌクレオチドと、鋳型ポリヌクレオチドを鋳型として生成する相補鎖合成生成物に形成される、相互に異なるループに対してアニールする3種類以上のプライマーの組み合わせは、本発明に好適なプライマーの組み合わせと言うことができる。
本発明のプライマーを構成する塩基配列は、前述した複数のループの塩基配列に相補的な塩基配列を含む塩基配列とする。その3’側はループに相補鎖合成の起点を与えられることが求められる。したがって、少なくともその3’末端はループ内に位置するべきである。しかしアニールに必要な塩基配列の全てがループ内に配置される必要はない。したがって、プライマーが必要な反応条件の下で相補鎖合成の起点を与えることができる限り、たとえばアニールに必要な塩基配列の一部が、ループに隣接する2本鎖ポリヌクレオチドを構成する塩基配列と重複することが許される。また、プライマーの5’側には任意の塩基配列を付加することもできる。本発明において鋳型ポリヌクレオチドが有するループに相補鎖合成の起点を与えるプライマーとして、前述のLAMP用プライマーを用いることができる。
LAMP法(Nucleic Acid Res.2000 Vol.28 No.12 e63、WO 00/28082)は、鋳型ポリヌクレオチドに自身の3’末端をアニールさせて相補鎖合成の起点とするとともに、このとき形成されるループに相補鎖合成の起点を与えることができるプライマーを組み合わせることによって高度な等温での相補鎖合成反応を可能とする方法である。LAMP法には、少なくとも次の2つのプライマーが用いられる。
[1]第1のプライマー;第1のプライマーはその3’末端において標的塩基配列を構成する一方の鎖の3’側を規定する領域に相補鎖合成の起点を与えることができ、かつ第1のプライマーの5’側には、このプライマーを起点とする相補鎖合成反応生成物の任意の領域に対して相補的な塩基配列を備える、
[2]第2のプライマー;第2のプライマーはその3’末端において前記第1のプライマーを起点とする伸長生成物における標的塩基配列の3’側を規定する領域に相補鎖合成の起点を与えることができる塩基配列を備え、かつ第2のプライマーの5’側には、このプライマーを起点とする相補鎖合成反応生成物の任意の領域に対して相補的な塩基配列を備える、
つまり、上記鋳型ポリヌクレオチドの合成に用いられた第1のプライマー、および第2のプライマーは、本発明に基づくポリヌクレオチドの合成方法における少なくとも3種のプライマーの一部を構成することができる。言い換えれば、鋳型ポリヌクレオチド、あるいは反応生成物に形成されるループ内において、前記第1のプライマーおよび第2のプライマーとは異なる位置で相補鎖合成の起点を与えることができる3つ目のプライマーを組み合わせることにより、本発明を実施することができる。本発明において、標的塩基配列の合成に必要なプライマーに加えて、付加的に組み合わせられるプライマーをループプライマーと呼ぶことがある。
なお鋳型ポリヌクレオチドの合成に用いたプライマーを、標的塩基配列を合成するためのプライマーとしても利用することは、必須の条件ではない。鋳型ポリヌクレオチドを合成するためのプライマーとは別に、更に標的塩基配列の合成用のプライマーを加えることも可能である。しかしながら、通常は、より少ない要素で反応を構成するのが合理的である。
本発明における特に望ましいループプライマーとして、R1−R2間(あるいはF1−F2間)の領域に相補鎖合成の起点を与えることができるプライマーを示すことができる。ループプライマーは、R1−R2間、あるいはF1−F2間にアニールすることができるプライマーのいずれか1つをLAMP用のプライマーに組み合わせるとき、3種のプライマーが用いられることになる。更にR1−R2間、あるいはF1−F2間にアニールすることができるプライマーを両方とも組み合わせれば、LAMP用プライマーに2種類のループプライマーが加わって、合計で4種類のプライマーを用いることになる。本発明におけるループプライマーは、少なくとも1種類、望ましくは2種類、あるいはそれ以上の種類を組み合わせることによって、ポリヌクレオチドの合成反応を促進する作用を期待できる。
このループプライマーは、R2を含むループ[たとえば図1−(4)等]に対してアニールする。このループは、標的塩基配列におけるR1−R2にかけての領域(ただし図1−(4)においてはR2を含み、R1は含まない)で構成されている。このようなループに対して、本発明のループプライマーは、ループを構成する塩基配列に相補的な塩基配列を含む任意の塩基配列からなるヌクレオチドをループプライマーとすることができる。
ただし実施例で明らかにするように、ループ内の領域を選択することによって、より効率的なポリヌクレオチドの合成が可能となる。たとえば、R1cと重ならない領域、すなわちR1cよりも3’側に複製開始点を与えることができるループプライマーは、LAMP法の反応効率を著しく高める。
結局、本発明をLAMP法に適用したときに組み合わせられる望ましいループプライマーとして、次の条件を満たすプライマーを挙げることができる。すなわち、鋳型ポリヌクレオチド、および/または鋳型ポリヌクレオチドと第1のプライマーおよび第2のプライマーとの反応によって生成するポリヌクレオチドに形成されるループのうち、第1のプライマーおよび第2のプライマーがアニールできないループにおいて、相補鎖合成の起点を提供することである。ループプライマーは、ループ内に相補鎖合成の起点となる3’末端を配置する領域にアニールすることができれば良い。したがって、アニールするための塩基配列が完全にループ内に含まれる場合のみならず、その一部がループ以外の領域に重なる場合であっても、3’末端がループ内に位置する場合には、望ましい条件を満たしていると言うことができる。たとえば、ループプライマーがアニールすべき塩基配列の一部が、ループに隣接する2本鎖構造に及んでいる場合であっても、アニールすべき領域を完全にループ内に配置したときと同様の反応促進効果を得られることは、実施例に示すとおりである。
ループプライマーと鋳型ポリヌクレオチドを構成する塩基配列との好ましい位置関係を図3に示した。図3は、自身にアニールするF1の3’末端を起点として相補鎖合成が行われるところを示している。図3は、図1−(2’)と同じ構造を示している。すなわちこの図に示された相補鎖合成が完了すれば、本発明における鋳型ポリヌクレオチドが完成するところである。ループプライマーRは、R2を含むループにアニールするプライマーであることが、図3に示されている。なお図3は、ループプライマーRがアニールする領域を示すために記載したものである。図3の構造に対してアニールしたループプライマーRからの相補鎖合成は、実際にはすぐに5’末端に達してしまう。鋳型ポリヌクレオチドから生成する反応生成物に形成される同様の塩基配列からなるループにアニールして相補鎖合成が行われるとき、ループプライマーRを起点とする相補鎖合成が反応効率の向上に貢献する。
本発明をLAMP法に適用するとき、ループプライマーは、LAMP法の条件と同じ条件下でアニールできることが望ましい。全ての反応を温度変化無しで実施できることは、LAMP法の大きな利点である。この利点を損なわないように、本発明のためのループプライマーを組み合わせるときにも、LAMP法のための反応と同じ温度条件でループプライマーを用いることが理想的である。そのためには、ループプライマーのTmが、LAMP法のためのプライマーと同じレベルとなるように設計する。Tmはプライマーを構成する塩基の種類と数、並びに反応液に含まれる塩類や各種のTmに影響を与える成分によって決定される。したがって、本発明においては、LAMP法のための反応液の条件に合わせて、ループプライマーのTmをその塩基配列によって調整する。当業者は、各種の条件に合わせてプライマーの塩基配列を調整し適切なTmを与えることができる。なお、ループプライマーに関するこれらの条件は、F1c−F2c(あるいはR1c−R2c)によって構成されるループについても適用される。
図1−(4)に示す構造は、鋳型ポリヌクレオチドが自身を鋳型とする相補鎖合成反応を繰り返した結果生成した生成物である。そのループは、鋳型ポリヌクレオチドのループに相補的な塩基配列からなっている。鋳型ポリヌクレオチドに対してアニールするプライマーは、鋳型ポリヌクレオチドの相補的な塩基配列に対してはプライマーとしてアニールすることはできない。つまり、本発明における望ましいループプライマーは、鋳型ポリヌクレオチドを鋳型として合成されることによって生成された新たなポリヌクレオチドに形成されるループに相補鎖合成の起点を与えることができる。このような関係とすることによって、鋳型ポリヌクレオチドを鋳型とする相補鎖合成と、新たに生成されるポリヌクレオチドを鋳型とする相補鎖合成が進行する。その結果、短時間により多くのポリヌクレオチドが迅速に生成される。
本発明におけるループプライマーの3’側が、ループにアニールして相補鎖合成の起点となることは既に述べた。これに対して、ループプライマーの5’側にループプライマーの3’末端を起点として合成される相補鎖の任意の領域を構成する塩基配列に相補的な塩基配列を配置することができる。本発明において、ループプライマーの5’側に配置する塩基配列として望ましい塩基配列としては、前記インナープライマーの5’側に配置された塩基配列(F1cやR1c)と実質的に同一の塩基配列を示すことができる。ここで実質的に同一の配列には、ループプライマーの5’側に配置された塩基配列を鋳型として生成する相補鎖の3’末端が、前記インナープライマーRAあるいはFAの5’側に配置された塩基配列を鋳型として生成する相補鎖の3’末端がアニールする領域において相補鎖合成の起点を与えることができる場合を含む。
すなわち、たとえばプライマーRAの塩基配列を含むループにアニールするループプライマーRには、RAの5’側に配置した塩基配列R1cと実質的に同一の塩基配列を配置することができる。同様にインナープライマーFAの塩基配列を含むループにアニールするループプライマーFにおいては、その5’側にF1cを構成する塩基配列と実質的に同一の塩基配列を配置することができる。
5’側に自身に相補的な塩基配列を有するループプライマーによる伸長生成物は、これを鋳型として生成する相補鎖の3’末端に、自身に相補的な塩基配列を与えることができる。その結果、ループプライマーの生成物もまた、LAMPのrecycling productsとして機能する構造を有する。したがって、ループプライマーによってもLAMPの核酸増幅反応がトリガーされ、高度な増幅効率を期待することができる。
さて、ここまでの説明によって明らかなように、本発明のポリヌクレオチドの合成方法にLAMP法を適用するとき、前記第1のプライマー、第2のプライマー、およびループプライマーを用いれば、標的塩基配列をもとに鋳型ポリヌクレオチドが得られ、更に本発明によるポリヌクレオチドの合成方法を実施できる。つまり、次の成分を標的塩基配列とともにインキュベーションすれば、本発明のポリヌクレオチドの合成方法を行うことができる。これらの反応成分は、任意の順序で混合することができるし、あるいは同時に混合しても差し支えない。またこの反応系に更にアウタープライマー(後述)を加えることによって、2本鎖のポリヌクレオチド試料を対象として、全ての工程を等温で行うこともできる。
・標的塩基配列を含むポリヌクレオチド試料
・第1のプライマー
・第2のプライマー
・ループプライマー(1種、または2種類、あるいはそれ以上)
・鎖置換を伴う相補鎖合成を触媒することができるDNAポリメラーゼ
・相補鎖合成のための基質
更に、これらの成分を相補鎖合成が可能な条件下でインキュベートを続けると、やがて標的塩基配列をもとに合成されたポリヌクレオチドは、新たな鋳型ポリヌクレオチドを連続的に生成する。新たに生成される鋳型ポリヌクレオチドは、全て新たなポリヌクレオチドの合成材料として利用される。すなわちポリヌクレオチドの増幅が起きる。本発明は、このようにして達成されるポリヌクレオチドの増幅方法を含む。本発明のポリヌクレオチドの合成方法に基づいてポリヌクレオチドを増幅することにより、増幅効率は著しく改善される。たとえば、LAMP用のプライマーにループプライマーを組み合わせて本発明に基づく増幅方法を実施することにより、望ましい条件下では、反応時間をループプライマーが無いときに比べて半分以下にまで短縮することができる。
RA(第1のプライマー)、FA(第2のプライマー)、ループプライマーF、およびループプライマーRを利用し、鎖置換型の相補鎖合成反応を触媒するDNAポリメラーゼと組み合わせて2本鎖のポリヌクレオチドを増幅する反応について、基本的な原理を図1−図2を参照しながら以下に説明する。この例においては、RAおよびFAが標的塩基配列の合成のための第1のプライマーおよび第2のプライマーのセットを構成している。ループプライマーFはF2を含むループに相補鎖合成の起点を与えることができ、またループプライマーRはR2を含むループに相補鎖合成の起点を与えることができる。
前記のとおり、図1−(2)、あるいは図1−(2’)に示された、3’末端を自身にアニールさせて相補鎖合成を行う工程が完了すると、本発明における鋳型ポリヌクレオチドが得られる。更にこの鋳型ポリヌクレオチドのループには、それぞれRA[図1−(2)]、あるいはFA[図1−(2’)]がアニールして相補鎖合成が行われ、鋳型ポリヌクレオチドの3’末端は置換によって再び1本鎖となる。1本鎖となった3’末端は、自身にアニールして相補鎖合成が進む結果、図1−(3)、および図1−(3’)が生成する。このように、ループにプライマーRA、あるいはFAのアニール、相補鎖合成、鋳型ポリヌクレオチドの3’末端の置換、自身へのアニールと相補鎖合成というサイクルが繰り返し行われる。
このとき、鋳型ポリヌクレオチドの自身を鋳型とする3’末端の伸長によって、やがてループにアニールしたRAやFAを複製起点とする相補鎖合成の生成物が置換され、新たな1本鎖のポリヌクレオチドが生成する。この1本鎖ポリヌクレオチドは、3’末端と5’末端に自身に相補的な塩基配列を備える。つまり、ちょうど図1−(2)や図1−(2’)と同じ構造の生成物となる。これらは新たな鋳型ポリヌクレオチドとなって、同様の反応が繰り返し進行することとなる。ここまでは、全てLAMP法として明らかにされている反応機序である。
さて、図1−(3)において、ループにアニールしたプライマーFAは、鋳型ポリヌクレオチドの2本鎖構造を置換しながら伸長して、やがてその5’末端に達する。このとき、置換された鋳型ポリヌクレオチドの3’末端側は1本鎖構造となっている。そのため、自身の相補的な塩基配列が相互にハイブリダイズする。こうして形成されるのが図1−(4)に示す構造である。すなわち鋳型ポリヌクレオチドの3’が自身にアニールし、同時に相補的な塩基配列がハイブリダイズしてループを形成している。相補的な塩基配列がハイブリダイズすることによって形成されるループは、もとになった鋳型ポリヌクレオチドのループ部分を写し取った相補鎖となっている。このループは、図からも明らかなようにR2を含むループで、FAやRAはアニールすることができない。しかしループプライマーRは、R2を含むループにアニールすることができる。そこで、R2を含むループにループプライマーRがアニールして相補鎖合成を開始する。
一方で、公知のLAMP法に基づくポリヌクレオチドの増幅反応は継続する。すなわち、鋳型ポリヌクレオチドによる自身を鋳型とする伸長反応と、ループにアニールするプライマーFAとによる増幅反応が継続している。この反応そのものは、新たな鋳型ポリヌクレオチドを連続して生成するポリヌクレオチドの増幅反応に他ならない。なお、既にLAMP法で明らかにされている図1−(4)以降の増幅反応については、ここでは図示しない。
ループプライマーRの伸長に伴って鋳型ポリヌクレオチドや、プライマーFAの伸長生成物はいずれも置換されて塩基対結合が可能な状態となり、再び鋳型ポリヌクレオチドの生成をもたらす。特に図1−(6)として示したループプライマーRの伸長生成物には、ループプライマーF、ループプライマーR,そしてFAという、3種類のプライマーのアニールが可能な構造となっている。このような生成物は、公知のLAMP法では、生成し得ない。本発明の方法は、LAMP法に基づく公知の生成物とは別に図1−(6)に示す鋳型ポリヌクレオチドを生成する。図1−(6)に示す鋳型ポリヌクレオチドは、ループプライマーとともに、更に付加的なポリヌクレオチドの増幅反応を開始する。このようにして、LAMP法で公知となっている相補鎖合成とは別に、更に新たなポリヌクレオチドを生成する反応が進行する。その結果、相補鎖合成の合成効率が著しく改善され、反応時間が大幅に短縮することができるのである。
なお図1−(6)に示す構造において、5’末端付近にあるF2cを含む領域には、プライマーFAがアニールすることができる。しかしこの位置にアニールするプライマーでは、5’末端までのわずかな領域についてしか相補鎖合成の対象とすることができないことから、図1−(6)では図示していない。
以下、本発明の反応を更に継続した場合にどのような生成物が生じるのかについて、続けて説明する。図1−(4)でループプライマーRから生成した伸長生成物は、図1−(6)に示す構造を持つ。図1−(6)においては、図1−(5)と同様に2つのループプライマーと1つのプライマーFAがアニールする構造となっている。うち2つのループプライマーの伸長生成物は、いずれ図1−(6)自身を鋳型とする3’末端からの相補鎖合成反応によって全て置換され、1本鎖ポリヌクレオチドを生じる。
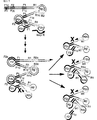
一方、図1−(6)に示すポリヌクレオチドが自身を鋳型として相補鎖合成を完成する。図2−(7)が有するF2cを含むループには、プライマーFAがアニールして相補鎖合成がスタートする。図2−(7)が有するF2cを含むループは、実際には図1−(6)で既に形成されていることから、このループにFAがアニールする反応は、図2−(7)を生成する反応と並行して進行している。いずれにせよ、ループにアニールしたFAの伸長によって、図2−(7)に示したポリヌクレオチドのループから3’末端にかけての領域が置換され1本鎖となる。
1本鎖となった領域に含まれる相補的な塩基配列はそれぞれハイブリダイズし、図2−(8)に示すような構造となる。なおここで1本鎖となったポリヌクレオチドにおいては、物理的に近い領域にある相補的な塩基配列とのハイブリダイズが優先的に起きる可能性が高い。したがって、各種のプライマーのような他の分子や、離れた位置にある相補的な塩基配列とのハイブリダイズよりも、隣接する領域とのハイブリダイズが優先する。図から明らかなように、図2−(8)に示すポリヌクレオチドには、その3’末端にループプライマーRがアニールする。またプライマーFAとRAがアニールすることができる2つのループが形成される。ループにアニールした各プライマーは、それぞれ伸長するとともに、ループプライマーRからの伸長反応によって置換されて1本鎖ポリヌクレオチドとなって図2−(8)のポリヌクレオチドから遊離する。
ループプライマーRの相補鎖合成の結果生じる2本鎖ポリヌクレオチドは、もはや新たなループを生じることは無く、安定な2本鎖ポリヌクレオチド図2−(12)となる。安定とは言いながら、LAMP法の反応条件においては2本鎖のポリヌクレオチドといえども、新たな鋳型として利用することができる。つまり、図2−(12)のようなループを伴わない2本鎖ポリヌクレオチドであっても、FAやRAの鋳型となり、新たな反応を開始することができる。図1−(12)に示す構造は、2本鎖ポリヌクレオチドを鋳型ポリヌクレオチドとするときに使用したアウタープライマーがアニールすべき領域R3やF3[図1−(1)]を持たない。しかし図1−(12)に示す構造においては、プライマーFAやプライマーRAがアニールできる領域が連続して複数配置されていることから、上流のFAが下流のFAに対してアウタープライマーの機能を果たすことが期待できる。なお2本鎖のポリヌクレオチドを鋳型とする反応については後に述べる。
ポリヌクレオチド図2−(8)を鋳型として生成する1本鎖ポリヌクレオチドには、図2−(9)、図2−(10)、そして図2−(11)の3種類の構造がある。それぞれの構造を与える鋳型とプライマーとの関係を以下に示す。なお、各ポリヌクレオチドは図2における(番号)で示す。
鋳型 (7) (8) (8)
プライマー FA RA FA
1本鎖ポリヌクレオチド (9) (10) (11)
これらの1本鎖ポリヌクレオチドは、それぞれが形成するループに対応するプライマーがアニールして次のような反応が進行する。まずポリヌクレオチド図2−(9)は、F2cにアニールするプライマーFA、およびR2cにアニールするRAによる伸長生成物として図2−(14)および図2−(15)に示す生成物を与える。これらの生成物は、いずれもポリヌクレオチド図2−(9)のR2を含むループにアニールしたループプライマーRからの相補鎖合成反応によって置換されて1本鎖ポリヌクレオチドとして遊離する。図2−(14)および図2−(15)に示した2つのポリヌクレオチドは、図1のRecycling productsとして示した一連のポリヌクレオチド図1−(2)、および図1−(3)に相当する構造を有している。厳密に比較すれば、ループが形成されたときにループ内におけるR2やF2(あるいはR2cやF2c)の配置が両者の間では相違する。しかしこれらのポリヌクレオチドは、いずれも更に鋳型ポリヌクレオチドの生成をもたらし、ポリヌクレオチドの増幅反応を構成する。
次に、ポリヌクレオチド図2−(10)に着目する。このポリヌクレオチドからも図2−(9)とほぼ同様に、プライマーFAとプライマーRAの伸長生成物が、図2−(15’)、および図2−(16)の1本鎖ポリヌクレオチドとして生成する。これらのポリヌクレオチドは、ループプライマーRの相補鎖合成に伴って置換され、1本鎖ポリヌクレオチドとして遊離する。図2−(15’)に示すポリヌクレオチドは、図1−(3’)に相当する構造を有している。また、図2−(16)も、図1−(3)と同様に自身にアニールすることができる3’末端を備えた鋳型ポリヌクレオチドである。したがって、いずれも鋳型ポリヌクレオチドとして、あるいは新たな相補鎖合成反応のための鋳型として機能する。
更に、ポリヌクレオチド図2−(11)も、上記ポリヌクレオチドと同様に新たな反応の出発材料を生成する。すなわちループにアニールするプライマーFA、およびRAの伸長生成物として、それぞれ図2−(17)と図2−(18)を生成する。これらの生成物は、ループプライマーRの相補鎖合成に伴って置換され、1本鎖ポリヌクレオチドとして遊離する。生成する図2−(18)は図1−(3)と、そして図2−(17)は図1−(3’)と同様に自身にアニールすることができる3’末端を備えた鋳型ポリヌクレオチドに他ならない。
ループプライマーFAに由来する図2−(13)は、プライマーFAのアニールと相補鎖合成、更にこの相補鎖合成によって置換された領域にアニールするループプライマーRからの相補鎖合成、そして前記FAからの伸長生成物の遊離による1本鎖ポリヌクレオチドの生成といった反応が起きるものと思われる。これらの反応は、新たな鋳型ポリヌクレオチドの生成にはつながらないと考えられるので、図示していない。
結局、図2−(14)〜図2−(18)に示す全ての生成物は、本発明における鋳型ポリヌクレオチドとなって新たな相補鎖合成の出発物質として機能する。すなわち、図1におけるrecycling productとして示した構造の生成につながっている。こうして、本発明に基づくポリヌクレオチドの増幅方法が継続する。
ところで本発明の鋳型ポリヌクレオチドは、2本鎖の状態にあるポリヌクレオチドに含まれる標的塩基配列を出発物質として合成することができる。2本鎖の状態にある標的塩基配列にプライマーをアニールさせ、相補鎖合成を行う方法は、本発明者らによって報告されている(第23回日本分子生物学会年会;2000.12.13−16;神戸、Nagamine,K.,Watanabe,K.,Ohstuka,K.,Hase,T.,and Notomi,T.(2001)Loop−mediated isothermal amplification reaction using a nondenatured template.Clin.Chem.47,1742−1743.)。
図1においては1本鎖の標的塩基配列を出発物質として鋳型ポリヌクレオチドを合成している。しかし2本鎖の状態にあるポリヌクレオチドに含まれる標的塩基配列を出発物質として用いる方法を応用すれば、1本鎖に変性する工程を省略し、2本鎖のポリヌクレオチドをそのまま出発物質として利用することができる。2本鎖ポリヌクレオチドとしては、たとえばcDNAやゲノムDNAを示すことができる。あるいはこれらのDNAを各種のベクターに挿入したものを本発明の2本鎖ポリヌクレオチドとして用いることもできる。一方1本鎖の状態にあるポリヌクレオチドとは、これら2本鎖ポリヌクレオチドを加熱やアルカリ条件等の変性処理によって1本鎖としたものや、あるいはmRNAのようにもともと1本鎖として存在しているポリヌクレオチドを示すことができる。本発明の2本鎖ポリヌクレオチドは、精製されたものであっても良いし、未精製のものであることもできる。また、細胞内に存在する状態(in situ)で、本発明の方法を適用することもできる。細胞内のポリヌクレオチドを鋳型とすることによって、ゲノムのin situ解析が可能となる。
本発明においてcDNAを鋳型として用いる場合、cDNAを合成する工程と、本発明に基づくポリヌクレオチドの合成方法とを、同一の条件下で実施することができる。RNAを鋳型としてcDNAの第1鎖を合成すると、DNA−RNAハイブリッドによる2本鎖ポリヌクレオチドが完成する。この2本鎖ポリヌクレオチドを本発明における鋳型として、ポリヌクレオチドの合成方法を実施することができる。本発明のポリヌクレオチドの合成方法に用いるDNAポリメラーゼが、逆転写酵素活性を備えるものであれば、単一の酵素を用い、同一の条件下でポリヌクレオチドの合成を行うことができる。たとえばBca DNAポリメラーゼは、鎖置換活性を有し、逆転写酵素活性を併せ持つDNAポリメラーゼである。なお、第2鎖を合成したうえで完全な2本鎖cDNAとした後に、本発明によるポリヌクレオチドの合成方法を適用しうる。
2本鎖の状態にあるポリヌクレオチドに含まれる標的塩基配列から鋳型ポリヌクレオチドを合成するときには、まず2本鎖ポリヌクレオチドに任意のプライマーを加え、このプライマーを起点とする相補鎖合成反応が達成できる条件のもとでインキュベートされる。ここで用いられる任意のプライマーとは、第1のプライマーがアニールすべき領域を塩基対結合可能な状態とするために用いられる。したがって、任意のプライマーは、標的塩基配列における、第1のプライマーがアニールすべきポリヌクレオチド鎖に対して、その相補鎖にアニールすることができるものである必要がある。更に、本発明における任意のプライマーを複製起点とする相補鎖合成は、第1のプライマーがアニールすべき領域の方向に向かって進行するような位置関係にあるべきである。言いかえれば、第1のプライマーを起点とする相補鎖合成反応において鋳型として機能する領域の、任意の領域に対してアニールするものであることができる。任意のプライマーは、この条件を満たす限り、任意の領域から選択することができる。たとえば、第2のプライマーを、任意のプライマーとして用いることもできる。このような態様は反応に必要な成分を少なくすることから、本発明における望ましい態様の一つである。
したがってLAMP法に基づいて鋳型ポリヌクレオチドを合成するための反応における工程a)、すなわち標的塩基配列に第1のプライマーをアニールさせ、これを起点とする相補鎖合成反応を行う工程では、任意のプライマーを起点とする相補鎖合成で2本鎖ポリヌクレオチドの一方の鎖を置換し、第1のプライマーによる塩基対結合が可能な状態とすることができる。この条件を採用したことによって、温度変化の不要な合成反応が実現できた。任意のプライマーの2本鎖ポリヌクレオチドに対するアニール、およびこのプライマーを起点とする相補鎖合成反応が達成できる条件とは、実際には次の複数の工程を同じ条件下で進めることができる条件ということができる。
i)2本鎖ポリヌクレオチドの状態にある鋳型に対してプライマーがアニールする
ii)アニールしたプライマーを複製起点とする相補鎖合成が進む
プライマーは、少なくともそれがアニールすべき領域が1本鎖でなければアニールすることはできないと考えられていた。そのため従来は、2本鎖のポリヌクレオチドを鋳型とする場合には、プライマーのアニールに先立って必ず変性によって1本鎖とする工程が実施されてきた。しかし必ずしも完全な1本鎖としなくとも、何らかの手段によって2本鎖が不安定化される条件のもとで、プライマーとインキュベートすることにより、プライマーを起点とする相補鎖合成反応が開始される。2本鎖が不安定化される条件としては、たとえば融解温度(以下、Tmと省略する)近くにまで加温する方法を示すことができる。あるいは、更にTm調整剤を存在させることも有効である。
本発明のポリヌクレオチドの合成方法において、一連の反応は、酵素反応に好適なpHを与える緩衝剤、酵素の触媒活性の維持やアニールのために必要な塩類、酵素の保護剤、更には必要に応じて融解温度(Tm)の調整剤等の共存下で行う。緩衝剤としては、Tris−HCl等の中性から弱アルカリ性に緩衝作用を持つものが用いられる。pHは使用するDNAポリメラーゼに応じて調整する。塩類としてはKCl、NaCl、MgCl2、MgSO4、あるいは(NH4)2SO4等が、酵素の活性維持とポリヌクレオチドの融解温度(Tm)調整のために適宜添加される。酵素の保護剤としては、ウシ血清アルブミンや糖類が利用される。
更に融解温度(Tm)の調整剤には、ベタイン、プロリン、ジメチルスルホキシド(以下、DMSOと省略する)、ホルムアミド、あるいはトリメチルアミンN−オキシド(以下、TMANOと省略する)が一般に利用される。融解温度(Tm)の調整剤を利用することによって、前記オリゴヌクレオチドのアニールを限られた温度条件の下で調整することができる。更にベタイン(N,N,N,−trimethylglycine)やテトラアルキルアンモニウム塩は、そのisostabilize作用によって鎖置換効率の向上にも有効である。ベタインは、反応液中0.2〜3.0M、好ましくは0.5〜1.5M程度の添加により、本発明のポリヌクレオチド増幅反応の促進作用を期待できる。これらの融解温度の調整剤は、融解温度を下げる方向に作用するので、塩濃度や反応温度等のその他の反応条件を考慮して、適切なストリンジェンシーと反応性を与える条件を設定する。
Tm調整剤を利用することにより、酵素反応に好適な温度条件を容易に設定することができる。Tmはプライマーと標的塩基配列の関係によって変動する。したがって、酵素活性を維持できる条件と、本発明の条件を満たすインキュベーションの条件とが一致するように、Tm調整剤の使用量を調整することが望ましい。本発明の開示に基づいて、プライマーの塩基配列に応じて適切なTm調整剤の使用量を設定することは、当業者にとって自明である。たとえば、アニールする塩基配列の長さとそのGC含量、塩濃度、およびTm調整剤の濃度に基づいて、Tmを算出することができる。
このような条件下における2本鎖のポリヌクレオチドに対するプライマーのアニールは、おそらく不安定であると推測される。しかし鎖置換型のポリメラーゼとともにインキュベートすることにより、不安定ながらアニールしたプライマーを複製起点として相補鎖が合成される。相補鎖が合成されれば、プライマーのアニールは次第に安定化されることになる。
本発明に用いるプライマーは、いずれも化学的に合成することができる。DNAの合成方法は公知である。あるいは天然のポリヌクレオチドを制限酵素などによって切断し、必要な塩基配列で構成されるように改変する、あるいは連結することも可能である。また本発明に用いる各種のプライマーは、天然のDNAと同じ構造のもののみならず、人工的な変異体であることもできる。プライマーとは、標的塩基配列と相補的な塩基対結合を形成できること、そしてその3’末端において相補鎖合成の起点となる−OH基を与えること、の2つの条件を満たすものを意味する。更にプライマーは、望ましくは、相補鎖合成の鋳型となることができる。したがって、そのバックボーンは必ずしもホスホジエステル結合によるものに限定されない。たとえばホスホチオエート体やペプチド結合に基づくペプチド核酸からなるものであることもできる。また、塩基は、相補的な塩基対結合を可能とするものであれば良い。天然の状態では、一般にはACTGおよびUの5種類となるが、たとえばブロモデオキシウリジン(bromodeoxyuridine)といった類似体であることもできる。本発明に用いるオリゴヌクレオチドは、合成の起点となるのみならず、相補鎖合成の鋳型としても機能するものであることが望ましい。
本発明に用いるプライマーは、本発明を構成する各種のポリヌクレオチド合成反応において、与えられた環境の下で必要な特異性を維持しながら相補鎖との塩基対結合を行うことができる程度の鎖長を持つ。具体的には、5−200塩基、より望ましくは10−50塩基対とする。配列依存的なポリヌクレオチド合成反応を触媒する公知のポリメラーゼが認識するプライマーの鎖長が、最低5塩基前後であることから、アニールする部分の鎖長はそれ以上である必要がある。加えて、塩基配列としての特異性を期待するためには、確率的に10塩基以上の長さを利用するのが望ましい。一方、あまりにも長い塩基配列は化学合成によって調製することが困難となることから、前記のような鎖長が望ましい範囲として例示される。なお、ここで例示した鎖長はあくまでも相補鎖とアニールする部分の鎖長である。たとえばRAは、少なくとも2つの領域R2およびR1cからなっている。したがって、ここに例示する鎖長は、プライマーを構成する各領域の鎖長と理解するべきである。
本発明において用いられる鋳型という用語は、相補鎖合成の鋳型となる側のポリヌクレオチドを意味する。鋳型に相補的な塩基配列を持つ相補鎖は、鋳型に対応する鎖としての意味を持つが、両者の関係はあくまでも相対的なものに過ぎない。すなわち、相補鎖として合成された鎖は、再び鋳型として機能することができる。つまり、相補鎖は鋳型になることができる。
本発明のポリヌクレオチドの合成方法、あるいは増幅方法には、鎖置換を伴う相補鎖合成反応を触媒することができるDNAポリメラーゼが利用される。この種のポリメラーゼは、SDAなどに用いられたDNAポリメラーゼと同様のものが用いられる。すなわち、ある塩基配列の3’側に相補的なプライマーを合成起点として相補鎖合成を行うときに、5’側に2本鎖の領域が有るとその2本鎖を置換しながら相補鎖の合成を行う特殊なポリメラーゼが公知である。本発明においては、更に相補鎖合成に必要な基質が添加される。
本発明によるポリヌクレオチドの合成方法を支えているのは、鎖置換型の相補鎖合成反応を触媒することができるDNAポリメラーゼである。この種のDNAポリメラーゼには、以下のようなものが知られている。また、これらの酵素の各種変異体についても、それが配列依存型の相補鎖合成活性と鎖置換活性を有する限り、本発明に利用することができる。ここで言う変異体とは、酵素の必要とする触媒活性をもたらす構造のみを取り出したもの、あるいはアミノ酸の変異等によって触媒活性、安定性、あるいは耐熱性を改変したもの等を示すことができる。
Bst DNAポリメラーゼ
Bca(exo−)DNAポリメラーゼ
DNAポリメラーゼIのクレノウ・フラグメント
Vent DNAポリメラーゼ
Vent(Exo−)DNAポリメラーゼ(Vent DNAポリメラー
ゼからエクソヌクレアーゼ活性を除いたもの)
DeepVent DNAポリメラーゼ
DeepVent(Exo−)DNAポリメラーゼ(DeepVent
DNAポリメラーゼからエクソヌクレアーゼ活性を除いたもの)
Φ29ファージDNAポリメラーゼ
MS−2ファージDNAポリメラーゼ
Z−Taq DNAポリメラーゼ(宝酒造)
KOD DNAポリメラーゼ(東洋紡績)
これらの酵素の中でもBst DNAポリメラーゼやBca(exo−)DNAポリメラーゼは、ある程度の耐熱性を持ち、触媒活性も高いことから特に望ましい酵素である。本発明において、特に2本鎖の状態にあるポリヌクレオチドを鋳型として用いる場合には、プライマーのアニールと相補鎖合成反応とを同一条件下で行う。このような反応は、しばしばある程度の加温を必要とすることから、酵素が耐熱性であることは望ましい条件の一つである。耐熱性の酵素を用いることにより、幅広い反応条件に対応することができる。
たとえばVent(Exo−)DNAポリメラーゼは、鎖置換活性と共に高度な耐熱性を備えた酵素である。ところでDNAポリメラーゼによる鎖置換を伴う相補鎖合成反応は、1本鎖結合タンパク質(single strand binding protein)の添加によって促進されることが知られている(Paul M.Lizardi et al,Nature Genetics 19,225−232,July,1998)。この作用を本発明に応用し、1本鎖結合タンパク質を添加することによって相補鎖合成の促進効果を期待することができる。Vent(Exo−)DNAポリメラーゼに対しては、1本鎖結合タンパク質としてT4 gene 32が有効である。
なお3’−5’エクソヌクレアーゼ活性を持たないDNAポリメラーゼには、相補鎖合成が鋳型の5’末端に達した部分で停止せず、1塩基突出させた状態まで合成を進める現象が知られている。本発明では、相補鎖合成が末端に至ったときの3’末端の配列が次の相補鎖合成の開始につながるため、このような現象は望ましくない。しかし、DNAポリメラーゼによる3’末端への塩基の付加は、高い確率でAとなる。したがって、dATPが誤って1塩基付加しても問題とならないように、3’末端からの合成がAで開始するように配列を選択すれば良い。また、相補鎖合成時に3’末端がたとえ突出してしまっても、これを消化してblunt endとする3’→5’エクソヌクレアーゼ活性を利用することもできる。たとえば、天然型のVent DNAポリメラーゼはこの活性を持つことから、Vent(Exo−)DNAポリメラーゼと混合して利用することにより、この問題を回避することができる。
これらのDNAポリメラーゼに対して、PCRなどで一般に用いられているTaqポリメラーゼ等のDNAポリメラーゼは、通常の条件では鎖置換作用は実質的に見られない。しかし、この種のDNAポリメラーゼであっても、鎖置換が可能な条件を与えることができる場合には、本発明に利用することができる。
更に、本発明は、前記ポリヌクレオチドの増幅方法に基づく、ポリヌクレオチドの検出方法に関する。すなわち、前記増幅方法による生成物の量、あるいは有無を指標として、標的塩基配列の量、あるいは有無を知ることができる。ポリヌクレオチドを検出する方法は公知である。たとえば、エチジウムブロマイド(以下、EtBrと省略する)のようなインターカレーターは、2本鎖のDNAと反応して蛍光を発する。本発明に基づく増幅反応の生成物は、この種の指示薬によりその存在、あるいは量を知ることができる。
本発明に基づくポリヌクレオチドの検出方法に基づいて、ポリヌクレオチドの量を求めるには、たとえば次のような方法を利用することができる。まず、一定のシグナルを与えるのに要した時間を測定する方法を利用することができる。本発明の増幅方法は、容量依存的な反応であることから、反応がプラトーに達するまでの時間は、最初に存在する鋳型となるポリヌクレオチドの量に左右される。したがって、他の条件が同一であれば、ポリヌクレオチドの量は、反応がプラトーに達するまでの時間の関数として表すことができる。その他、ポリヌクレオチドの存在量を、一定の反応時間で生成される増幅生成物の量の関数として表すこともできる。
LAMP法は、標的塩基配列のプライマーがアニールすべき領域が適切な位置関係にあり、しかもその塩基配列が設計どおりであった場合に、高度な増幅反応が起きる。言いかえれば、相補鎖合成の起点としなければならない領域において、標的塩基配列が予測された塩基配列と異なっていたときには、LAMP法が著しく阻害される。特に、自身にアニールする3’末端を起点とする相補鎖合成は重要である。LAMP法においては、自身にアニールする3’末端は、プライマーの5’末端に配置された塩基配列を鋳型として合成される相補鎖の3’末端に相当する。したがって、第1のプライマー(RA)および/または第2のプライマー(FA)の5’側に配置された領域(R1あるいはF1)の5’末端、あるいはその近辺に、検出すべき変異部位に相補的な塩基を配置するようにするのが望ましい。そこで、この重要な配列を検出すべき変異に対応するように設計すれば、LAMP法による増幅反応生成物を観察することによって、塩基の欠失や挿入といった変異の有無、あるいはSNPsのような遺伝子多型を分析することができる。
より具体的には、変異や多型が予測される塩基が、相補鎖合成の起点となる3’末端付近(相補鎖が起点となる場合には5’末端付近)に相当するように設計するのである。すなわち、プライマーや、自身に相補的な3’末端がアニールする領域において、いずれかの塩基が予測された塩基とは異なっているときに、そのプライマーを起点とする相補鎖合成が妨げられるように設計するのである。たとえば、相補鎖合成の起点となる3’末端〜10塩基以内、特に望ましくは3’末端からカウントして2〜4番目、より望ましくは2〜3番目の塩基にミスマッチがある場合には、相補鎖合成が著しく阻害される。ここで、予測される塩基配列とは、野生型であっても、変異型であっても良い。変異型を予測した場合には、特定の変異があったときにのみ、相補鎖合成が開始することになる。相補鎖の合成起点となる3’末端や、その付近にミスマッチが存在するとポリヌクレオチドの相補鎖合成反応は著しく阻害される。したがって増幅反応が阻害されていないときには、標的塩基配列は予測された塩基配列からなっていると判定することができる。逆に、もしも増幅反応が阻害されて生成物が対照と同程度に生じないときには、標的塩基配列は予測された塩基配列とは異なっていると判定できる。
LAMP法においては、反応初期の生成物における末端構造が繰り返し反応を行わなければ高度な増幅反応に結びつかない。したがって、たとえ誤った合成が行われたとしても、増幅反応を構成する相補鎖合成がいずれかの段階で常に妨げられるのでミスマッチを含んだままでは高度な増幅は起きない。結果的にミスマッチが増幅反応を効果的に抑制し、最終的には正確な結果をもたらすことになる。つまりLAMP法に基づくポリヌクレオチドの増幅反応は、より完成度の高い塩基配列のチェック機構を備えていると言うことができる。これらの特徴は、たとえば単純に2つの領域で増幅反応を行っているPCR法などでは期待しにくい利点である。LAMP法に基づく多型や変異の検出方法について、本出願人は特許出願している(WO 01/34838)。
本発明は、本発明のループプライマーを応用した標的塩基配列における変異を検出する方法であって、標的塩基配列における特定の塩基が予測された塩基でなかったときに、インナープライマー、ループプライマー、およびこれらプライマーの伸長生成物の3’末端を起点とする相補鎖合成反応から選択される少なくとも1つの相補鎖合成反応が妨げられるものであり、前記増幅反応の生成物を指標として標的塩基配列が予測された塩基配列であるかどうかを検出する方法である。前記相補鎖合成反応に基づく増幅反応生成物の生成を観察し、標的塩基配列が予測された塩基配列である場合に比べてその生成が阻害されている場合には、特定の塩基が予測された塩基でないことを知ることができる。
本発明に基づいてLAMP法を応用して標的塩基における特定の塩基が予測された塩基であるかどうかを検知するためには、たとえばインナープライマーの5’末端を鋳型として合成された相補鎖が自身にアニールして相補鎖合成を開始するときに、前記特定の塩基によって当該相補鎖合成が制御されるようにデザインすればよい。本発明においては、インナープライマーの3’末端から開始される相補鎖合成反応が制御されるようにデザインすることもできる。しかし、鋳型の塩基配列に対するアニールが繰り返し行われるというLAMP法の特徴を生かすには、インナープライマーの5’側にチェック用配列を配置するのが望ましい。本発明においてチェック用配列とは、次の条件(a)、(b)、および(c)を満たす塩基配列を言う。
(a)インナープライマーの5’末端に配置され、その塩基配列を鋳型として合成された相補鎖の3’末端が、標的塩基配列、またはその相補鎖にアニールして相補鎖合成の起点となる、
(b)チェックすべき塩基が予測された塩基でなかった場合に、(a)の3’末端が標的塩基配列、またはその相補鎖にアニールするときにミスマッチを生じる
(c)(b)で生じたミスマッチによって(a)の相補鎖合成が阻害されるすなわち本発明は、インナープライマーとして下記第1のプライマーおよび第2のプライマーを用い、本発明のループプライマーと組み合せて標的塩基配列における特定の塩基が予測された塩基であるかどうかを検知するための方法であって、第1のプライマーおよび第2のプライマーの少なくともいずれかが、その5’側にチェック用配列を有する方法である。
ここでチェック用配列とは、前記特定の領域を構成する塩基配列が予測された塩基配列でなかった場合に、チェック用配列を鋳型として合成された相補鎖の3’末端が標的塩基配列、またはその相補鎖にアニールするときにミスマッチを生じ、かつこのミスマッチによって当該3’末端を起点として開始する相補合成反応が阻害される塩基配列を言う。
第1のプライマー:第1のプライマーはその3’末端において標的塩基配列を構成する一方の鎖の3’側を規定する領域に相補鎖合成の起点を与えることができ、かつ第1のプライマーの5’側には、このプライマーを起点とする相補鎖合成反応生成物の任意の領域に対して相補的な塩基配列を備える、
第2のプライマー:第2のプライマーはその3’末端において前記第1のプライマーを起点とする伸長生成物における標的塩基配列の3’側を規定する領域に相補鎖合成の起点を与えることができる塩基配列を備え、かつ第2のプライマーの5’側には、このプライマーを起点とする相補鎖合成反応生成物の任意の領域に対して相補的な塩基配列を備える、
チェック用配列を利用して、特定の塩基の違いに基づくミスマッチを与える位置は、たとえば相補鎖合成の起点となる3’末端〜10塩基以内、特に望ましくは3’末端からカウントして2〜4番目、より望ましくは2〜3番目の塩基が望ましい。本発明において、この位置におけるミスマッチが、最も効果的に相補鎖合成を阻害する。ここで、予測される塩基配列とは、野生型であっても、変異型であっても良い。相補鎖の合成起点となる3’末端や、その付近にミスマッチが存在するとポリヌクレオチドの相補鎖合成反応は著しく阻害される。
以上の方法は、いずれもインナープライマーの5’側にチェック用配列を配置して、標的塩基配列における特定の塩基をチェックするための方法である。LAMP法において、インナープライマーの5’側に配置された塩基配列を鋳型として合成される相補鎖の3’末端は、相補鎖合成反応の生成物を指標として、標的塩基配列における特定の塩基のチェックに有用である。
更に本発明は、インナープライマーのみならず、ループプライマーの5’側に配置した塩基配列を利用して、標的塩基配列における特定の塩基をチェックするための方法をも提供する。すなわち本発明は、ループプライマーとして下記第1のループプライマーおよび/または第2のループプライマーを、チェック用配列を有する前記インナープライマーとともに用いる標的塩基配列における特定の塩基が予測された塩基であるかどうかを検知するための方法である。ただしこのとき、ループプライマーはその5’側に、インナープライマーの5’に配置された前記任意の領域に相補的な塩基配列を有するか、またはインナープライマーの5’側に配置された塩基配列がチェック用配列であるときは、当該チェック用配列における前記ミスマッチを与えるための塩基がチェック用配列とは相違する配列をループプライマーの5’側に配置する。インナープライマーの5’側に配置された塩基配列がチェック用配列であるときに、ミスマッチを与えるための塩基がチェック用配列とは相違する配列とは、当該塩基のみが相違していても良いし、当該塩基を含む複数の塩基が相違していても良い。
第1のループプライマー:第1のインナープライマーの伸長生成物における第1のインナープライマーに由来する領域と、第1のインナープライマーに対する前記任意の領域の間において相補鎖合成の起点を与える、;
第2のループプライマー:第2のインナープライマーの伸長生成物における第2のインナープライマーに由来する領域と、第2のインナープライマーに対する前記任意の領域の間において相補鎖合成の起点を与える、;
LAMP法に基づく、特定の塩基のチェック機構は、鋳型、あるいはその相補鎖に対してアニールした3’末端を起点とする相補鎖合成反応が繰り返し起きることが大きな特徴である。この特徴によって、鋳型における塩基の違いを相補鎖合成反応を指標として、鋭敏に検知することができる。ところがLAMP法においても、チェック機構を経ない反応は起きる。チェック機構を経ない反応は、鋳型の塩基配列のチェックの結果として生成されたものではないので、この種の反応生成物は結果の判定を妨げる可能性がある。この反応の原因となる生成物は、LAMP法による増幅反応を繰り返す中でしだいに反応系に蓄積される。
増幅反応を指標とする分析方法においては、増幅反応が進行したときと阻害されたときの、増幅反応の生成物の量や生成速度に、できるだけ大きな差を生じることが、より鋭敏な検知のための重要な条件となる。ところが、鋳型の塩基とは無関係に生成する反応生成物が多く存在すると、両者の差を大きくすることが難しくなる。つまり、増幅産物の生成量や生成速度を指標とする分析方法の鋭敏性を損なう恐れがある。
本発明において、ループプライマーの5’側を標的塩基配列における特定の塩基のチェックに利用することは、この種の結果の判定を妨害する可能性のある生成物を抑制する効果を持つ。以下に、本発明においてループプライマーの5’側に配置する塩基配列の機能について説明する。
ループプライマーの5’側に配置した塩基配列は、当該プライマーを鋳型として生成した相補鎖において、自身に対してアニールして相補鎖合成の起点となる3‘末端を与える。このとき、その3’末端を起点とする相補鎖合成は、特定の塩基が予測された塩基である場合に阻害される。以下にその理由を述べる。
既に述べたように本発明の方法においては、インナープライマーの5’側に配置されたチェック用配列は、それを鋳型として生成した相補鎖の3’末端において、特定の塩基が予想された塩基でなかった場合にミスマッチによって相補鎖合成が阻害されるようにデザインされている。言い換えれば、インナープライマーのチェック用配列は、特定の塩基が予想された塩基であった場合に、それを鋳型とする相補鎖の3’末端を起点とする相補鎖合成反応が進行する。さて、この方法において、鋳型の塩基配列における特定の塩基が予測された塩基で無かった場合に起きてしまう、望まれない反応による生成物は、特定の塩基が予測された塩基等の鋳型とは異なる塩基に置き換えられた塩基配列を有している。この生成物は、何らかの理由によって、チェック用配列を鋳型として合成された相補鎖の3’末端によるチェック機構をすり抜けて生成された産物である。以降の説明のために、インナープライマーの5’側を鋳型として生成する相補鎖の3’末端を起点とする相補鎖合成反応において、前記特定の塩基が置換されてしまった生成物を、仮に偽生成物(pseudo products)と呼ぶ。偽生成物(pseudo products)の生成や、生成された偽生成物(pseudo products)を鋳型とする新たな相補鎖合成反応は、特定の塩基の解析する場合には、抑制すべき反応である。
偽生成物(pseudo products)を構成する塩基配列は、特定の塩基が予測された塩基となっていない。ループプライマーは偽生成物を鋳型として反応が進むために、ループプライマーの5’側を鋳型として生成する相補鎖の3’末端を起点とする相補鎖合成反応は、特定の塩基が予測された塩基であった場合に妨げられる。結局、偽生成物(pseudo products)を鋳型とする当該3’末端からの相補鎖合成反応が妨げられることになる。こうして、ループプライマーの5’側に配置した塩基配列を利用して、望まない反応を抑制することができる。
他方、標的塩基配列における特定の塩基が予測された塩基であった時にも、ループプライマーの5’側に配置された塩基配列を鋳型として生成された相補鎖の3’末端を起点とする相補鎖合成反応を阻害することができる。しかし、ループプライマーの3’側を起点とする相補鎖合成反応は、その5’側に配置された塩基配列とは無関係に進行するため、ループプライマーのLAMP反応に対する反応促進作用そのものは阻害されない。更に、特定の塩基が予測された時に生成する生成物の量が多量であるのに対して、前記偽生成物(pseudo products)の生成量はわずかである。その上に、偽生成物(pseudo products)に対しては、先に述べた機構による反応の阻害作用が働く。最終的に、特定の塩基が予測された塩基であるかどうかによって、反応性生物の量や生成速度の差が、より拡大されると考えられる。ループプライマーの5’側に配置した塩基配列が、前記差を拡大する作用を有することは、実施例においても確認されている。
以上に述べたインナープライマーとループプライマーの5’側に配置する塩基配列を利用した特定の塩基のチェック機構を利用して、標的塩基配列における塩基の変異を同定することができる。すなわち本発明は次の要素a)〜d)を混合し、鎖置換を伴う相補鎖合成反応が可能な条件下でインキュベートし、a)における(1)〜(4)のプライマーセットによる増幅生成物の生成速度および/または生成量を測定する工程を含む、標的塩基配列における特定の塩基が、第1の塩基であるか第2の塩基であるかを決定するための方法を提供する。
a)以下のプライマーセット(1)〜(4)から選択されたいずれかのプライマーセット
(1):第1塩基用インナープライマー対と第1塩基用ループプライマー対
(2):第1塩基用インナープライマー対と第2塩基用ループプライマー対
(3):第2塩基用インナープライマー対と第1塩基用ループプライマー対
(4):第2塩基用インナープライマー対と第2塩基用ループプライマー対
;ここで第1塩基用インナープライマー対および第2塩基用インナープライマー対は、いずれも次の第1のインナープライマーと第2のインナープライマーとからなるプライマー対であり、第1塩基用インナープライマー対においては第1のインナープライマーと第2のインナープライマーの5’側を鋳型として合成された相補鎖の3’末端を起点とする相補鎖合成反応が、前記標的塩基配列における特定の塩基が第1の塩基のときには阻害されず、第2の塩基のときには阻害され;また
第2塩基用インナープライマー対においては、第1のインナープライマーと第2のインナープライマーの5’側を鋳型として合成された相補鎖の3’末端を起点とする相補鎖合成が、前記標的塩基配列における特定の塩基が第2の塩基のときには阻害されず、第1の塩基のときには阻害され;そして
第1のインナープライマーは、3’末端において標的塩基配列を構成する一方の鎖の3’を規定する領域に相補鎖合成の起点を与える塩基配列を備え、かつ第1のインナープライマーの5’側には、このインナープライマーを起点とする相補鎖合成反応生成物の任意の領域に対して相補的な塩基配列を備える、
第2のインナープライマーはその3’末端において前記第1のインナープライマーを起点とする伸長生成物における標的塩基配列の3’側を規定する領域に相補鎖合成の起点を与える塩基配列を備え、かつ第2のインナープライマーの5’側には、このインナープライマーを起点とする相補鎖合成反応生成物の任意の領域に対して相補的な塩基配列を備える、
次に第1塩基用ループプライマー対および第2塩基用ループプライマー対は、いずれも次の第1のループプライマーと第2のループプライマーとからなる対であり、第1塩基用ループプライマー対においては第1のループプライマーと第2のループプライマーの5’側を鋳型として合成された相補鎖の3’末端を起点とする相補鎖合成反応が、前記標的塩基配列における特定の塩基が第1の塩基のときには阻害されず、第2の塩基のときには阻害され;また
第2塩基用ループプライマー対においては、第1のループプライマーと第2のループプライマーの5’側を鋳型として合成された相補鎖の3’末端を起点とする相補鎖合成が、前記標的塩基配列における特定の塩基が第2の塩基のときには阻害されず、第1の塩基のときには阻害される;
第1のループプライマーは、第1のインナープライマーの伸長生成物における第1のインナープライマーに由来する領域と、第1のインナープライマーに対する前記任意の領域の間において相補鎖合成の起点を与えることができる、
第2のループプライマーは、第2のインナープライマーの伸長生成物における第2のインナープライマーに由来する領域と、第2のインナープライマーに対する前記任意の領域の間において相補鎖合成の起点を与えることができる、
b)鎖置換を伴う相補鎖合成を触媒することができるDNAポリメラーゼ、
c)相補鎖合成のための基質、および
d)標的塩基配列を含む被検ポリヌクレオチド
前記の各プライマーの塩基配列の説明において、相補鎖合成の阻害とは、先に記載したインナープライマーにおけるチェック用配列と同様に、各プライマーの5’側に配置された塩基配列を鋳型として生成した相補鎖の3’末端が特定の塩基を含む領域にアニールする時に、特定の塩基がある塩基である時にミスマッチを生じ、このミスマッチが原因となって相補鎖合成が妨げられることを言う。本発明の特定の塩基の同定方法は、塩基の変異や多型の同定に有用である。本発明を利用して、たとえば、ある塩基が野生型であるのか変異型であるのかを明らかにすることができる。この場合、たとえば第1の塩基と第2の塩基の、いずれかを野生型とし、他方を変異型として、上記各プライマーをデザインし、本発明の方法を実施する。結果は、相補鎖合成反応生成物の生成速度が最大となる場合と最小となる場合のプライマーセットの組み合わせに基づいて、当該塩基が野生型であるのか変異型であるのかを同定することができる。より具体的には、次の(1)〜(4)の4とおりのプライマーセットに対して、特定の塩基が野生型である場合と変異型である場合の、増幅生成物の生成速度は次の組み合わせとなる。
標的塩基配列が野生型の場合: (1)が最大 (3)が最小
標的塩基配列が変異型の場合: (4)が最大 (2)が最小
(1):野生型用インナープライマー対と野生型用ループプライマー対
(2):野生型用インナープライマー対と変異型基用ループプライマー対
(3):変異型用インナープライマー対と野生型用ループプライマー対
(4):変異型用インナープライマー対と変異型用ループプライマー対
結局この方法は、特定の塩基を2重にチェックしていることに他ならない。このように、複数のプライマーからなるプライマー対を利用することによって、標的塩基配列における特定の塩基の解析結果の信頼性を向上させることができる。PCRのような公知の核酸増幅反応に基づく特定の塩基の同定方法においては、このような解析結果の信頼性を高めるための方法は知られていない。
本発明によるポリヌクレオチドの合成方法、この合成方法を利用した増幅方法、あるいはこの増幅方法を利用する標的塩基配列における変異の検出方法に必要な各種の試薬類は、あらかじめパッケージングしてキットとして供給することができる。具体的には、本発明のために、第1のプライマーおよび第2のプライマー、ループプライマーとして必要な各種のオリゴヌクレオチド、相補鎖合成の基質となるdNTP、鎖置換型の相補鎖合成を行うDNAポリメラーゼ、酵素反応に好適な条件を与える緩衝液といった試薬類で構成されるキットが提供される。本発明のキットには、アウタープライマーを組み合わせることができる。アウタープライマーを組み合わせることにより、等温での反応が可能となる。
本発明のポリヌクレオチドの増幅反応によって、標的塩基配列の検出が可能となることは既に述べたとおりである。したがって、本発明によるポリヌクレオチドの増幅反応用キットは、標的塩基配列の検出用キットや標的塩基配列における変異の検出用キットとして利用することができる。
すなわち本発明は、前記のような構成要素を含む標的塩基配列の検出用キットに関する。更に本発明の標的塩基配列の検出用キットを構成する各プライマーを、変異の検出方法のためのプライマーとすることにより、標的塩基配列における変異の検出用キットとすることができる。本発明によるキットには、アウタープライマーに加えて、更に必要に応じて合成反応生成物の検出のために必要な試薬類を組み合わせることができる。
特に、本発明の望ましい態様においては、反応途中で試薬の添加が不要なことから、1回の反応に必要な試薬を反応容器に分注した状態で供給することにより、サンプルの添加のみで反応を開始できる状態とすることができる。発光シグナルや蛍光シグナルを利用して、反応生成物の検出を反応容器のままで行えるようなシステムとすれば、反応後の容器の開封を全面的に廃止することができる。これは、コンタミネーションの防止上、たいへん望ましいことである。
発明を実施するための最良の形態
以下、実施例に基づいて本発明を更に具体的に説明する。
〔実施例1〕ループプライマーによるポリヌクレオチドの増幅反応の促進作用
1.ループプライマーの設計
LAMP法におけるポリヌクレオチド増幅反応を促進させることを目的として、付加的なプライマーの作用について検討した。プライマーを設計する場所は、LAMP反応中に生成するループ構造のR2あるいはF2領域以外とし、方向はR1あるいはF1と同じ向きとした(以下、ループプライマーと記載する)。なおR1やF1とは、鋳型ポリヌクレオチドが自身にアニールして相補鎖合成を行う方向と同じ方向を意味する。まず公知のLAMP法(WO 00/28082)に基づいて、標的塩基配列(配列番号:1)に対して、以下のプライマーをそれぞれ設計した。鋳型ポリヌクレオチドの塩基配列(配列番号:1)と、各プライマーの塩基配列との位置的な関係を図4に示した。袋文字(アウトライン)で塩基を記載した部分がループプライマーがアニールする部分で、矢印は相補鎖の合成方向を示している。
インナープライマーRA(Inner F、配列番号:2)、
インナープライマーFA(Inner R、配列番号:3)、
アウタープライマーF(Outer F、配列番号:4)、および
アウタープライマーR(Outer R、配列番号:5)
次に、上記プライマーによって規定されるR1とF1に同方向となるように、以下のループプライマーを設計した。
ループプライマーF(Loop F、配列番号:6)、および
ループプライマーR(Loop R、配列番号:8)
全てのプライマーは、公知の方法に基づいて合成した。ループプライマーにより、公知のLAMP法で明らかにされている反応に加えて、更に別の増幅反応が起き、その結果、反応の促進効果が期待できる(図1、および図2)。
2.ループプライマーの効果
λDNA(1x105分子)を鋳型として用い、以下に示す反応条件でLAMP反応を行った。λDNAは熱変性をしないものを用意し、反応液を65℃で反応させABI 7700(パーキンエルマー社)を用いて経時的に反応の推移を観察した。
反応液組成(25μL中)
20mM Tris−HCl pH8.8
10mM KCl
10mM(NH4)2SO4
4mM MgSO4
1M ベタイン(Betaine)
0.1%Triton X−100
0.4mM dNTP
8U Bst DNAポリメラーゼ(NEW ENGLAND BioLabs)
0.25μg/ml EtBr
プライマー:
1600nM Inner F
1600nM Inner R
400nM Outer F
400nM Outer R
λDNAにおける標的塩基配列の塩基配列(λDNA1)を配列番号:1に示す。このとき、ループプライマーを終濃度400nMになるように同時に加えた。この結果、ループプライマーを加えた反応系では反応の促進効果がみられた。一方、ループプライマーの相補鎖からなるプライマー(Loop cF/配列番号:7、およびLoop cR/配列番号:9)は作用しなかった(図5)。
また、λDNA(1x102、1x103、1x105分子)を鋳型として用い、ループプライマーを用いたときの検出限界について検討した結果、1x103分子までは再現性のよい結果が得られた(図6)。ループプライマーを用いなかった場合には、1x105分子でも結果のばらつきがあった(data not shown)。すなわち、ループプライマーを用いることにより少量の鋳型を増幅することが可能となった。
2.ループプライマーの濃度依存性
LAMPの反応系にループプライマーを終濃度が200、400、800、1200、1600、2000nMになるように加え、ループプライマーの濃度変化によるLAMP反応の影響について検討した。この結果、ループプライマーの濃度が増加するに従い、LAMP反応の促進がみられた(図7)。以下の実施例では、800nMのループプライマーを使用することとした。
3.3’末端を修飾したループプライマーのLAMP反応に及ぼす影響
ループプライマーからの伸長反応を阻害するため、ループプライマーの3’末端をアミノ化したプライマーを作成した。LAMPの反応系にアミノ化ループプライマーを終濃度が800nMになるように加え、LAMP反応の反応促進効果について検討した。この結果、アミノ化ループプライマーを加えた場合では反応の促進が起こらなかった。すなわち、ループプライマーからの伸長反応がLAMP反応の反応促進に関与していることが示された(図8)。
4.アウタープライマーの影響
ループプライマー存在下、アウタープライマーの有無によるLAMP反応の影響について検討した。アウタープライマーを加えない場合、反応が10分遅れる結果が得られた(図9)。ループプライマーを用いた場合においても、より速く反応を進めるためにはアウタープライマーを組み合わせることが有利であることが示された。
5.ループプライマーのTmに関する検討
ループプライマー5’末端を短くして、Tmの影響を調べた。実験に用いたループプライマーは次のとおりである。
1塩基短くしたループプライマーF−1(Loop F−1、配列番号:10)、
1塩基短くしたループプライマーR−1(Loop R−1、配列番号:12)、
2塩基短くしたループプライマーF−2(Loop F−2、配列番号:11)、および
2塩基短くしたループプライマーR−2(Loop R−2、配列番号:13)
これらのプライマーを用いて反応を行った結果、1塩基短くしたもの、そして2塩基短くしたものの順に反応が遅くなった(図10)。反応速度の低下は、ループプライマーのTmが低くなったために65℃では作用しにくくなったためと考えられた。
6.ループプライマーの設計部位の検討
ループプライマーの設計部位を検討するために、λDNAの別の領域に新たにプライマーを設計した。標的塩基配列の塩基配列(λDNA2)を配列番号:14に示した。標的塩基配列に対して、次に示すLAMP法用のプライマーを設計した。
インナープライマーRA(Inner F、配列番号:15)、
インナープライマーFA(Inner R、配列番号:16)、
アウタープライマーF(Outer F、配列番号:17)、および
アウタープライマーR(Outer R、配列番号:18)
次に、上記プライマーによって規定されるR1とF1に同方向となるように、以下のループプライマーを設計した。
ループプライマーF3;R2領域と重複が無い(Loop F3、配列番号:19)、
ループプライマーR4;F2領域と重複が無い(Loop R4、配列番号:20)、
ループプライマーF5;R2領域と3塩基重複(Loop F5、配列番号:21)、
ループプライマーR5;F2領域と3塩基重複(Loop R5、配列番号:22)、
ループプライマーF6;R1領域と3塩基重複(Loop F6、配列番号:23)、
ループプライマーR6;F1領域と3塩基重複(Loop R6、配列番号:24)、
ループプライマーF7;R1領域と10塩基重複(Loop F7、配列番号:25)、
ループプライマーR7;F1領域と10塩基重複(Loop R7、配列番号:26)、
ループプライマーF8;R1領域と完全に重複(Loop F8、配列番号:27)、
ループプライマーR8;F1領域と完全に重複(Loop R8、配列番号:28)、
R2およびF2領域との重複の有無は、反応速度に影響を与えず、これらのループプライマーの間で反応速度に差は見られなかった。同様に、R1領域(あるいはF1領域)に関しても3塩基重ねたプライマー(loop F6/loop R6)を用いて反応を行ったが、ほとんど差は無く反応が進んだ(図11)。
さらに、F1領域(あるいはR1領域)に関しては10塩基重ねたプライマー(loop F7/loop R7)を作製した。このループプライマーの設定では、重複が3塩基以下の場合と比べて多少遅くなったものの、なお反応の促進効果が見られた(図11)。R1領域(あるいはF1領域)をすべて重ねたプライマー(loop F8/loop R8)ではループプライマー無しに比べて反応の促進効果が見られた(図11)。これはR1領域(あるいはF1領域)において競合阻害をするためにダンベル構造(図3)が作りにくくなったこと、そして2本鎖となったR1領域にアニールしなければならないことが遅くなった原因であると考えられた。
〔実施例2〕SRY遺伝子の増幅
ヒトゲノムを鋳型として用い、ループプライマーを作用させたときのLAMP反応への影響について検討した。ターゲットとした遺伝子はY染色体上にマップされているSRY遺伝子である。標的塩基配列とした塩基配列を、配列番号:29に示す。この標的塩基配列に対して、次に示すLAMP法用のプライマーを合成した。
インナープライマーRA(Inner F、配列番号:30)、
インナープライマーFA(Inner R、配列番号:31)、
アウタープライマーF(Outer F、配列番号:32)、および
アウタープライマーR(Outer R、配列番号:33)
次に、上記プライマーによって規定されるR1とF1に同方向となるように、以下のループプライマーを設計した。
ループプライマーF(Loop F、配列番号:34)、
ループプライマーR(Loop R、配列番号:35)、
100ngのヒトゲノムを用いてLAMP反応を行った結果、ループプライマーを加えた方が反応が早くなることが確認できた(図12)。すなわち、ヒトゲノムを鋳型として用いたときでもループプライマーによって反応促進効果が得られることがわかった。本発明に基づいて、SNPs検出などのゲノムの解析を迅速に行えることが示された。
〔実施例3〕5’側に塩基配列を付加したループプライマー
ループプライマーの5’側に、ループプライマーの3’から合成される相補鎖の任意の領域に対して相補的な塩基配列を付加することによって、反応速度が向上することを確認した。実験に用いた鋳型は、実施例1と同じλDNA(λDNA2)である。反応条件も、実施例1のとおりである。まず図13に示すようなプライマーF9〜F15を設計した。これらのループプライマーには、その5’側に様々な塩基配列を付加してある。5’側に付加した塩基配列は、以下のとおりである。
上記ループプライマーを構成する各塩基配列は、鋳型となる塩基配列に対して図13に示すような位置関係にある。各塩基配列について、以下に簡単に説明する。また「c」を有する塩基配列は、その相補配列であることを示す。
なお以下の説明は、インナープライマーFAの塩基配列を含むループにおける、各領域の説明となっている。しかし実験には、インナープライマーRAの塩基配列を含むループにおいても、同様のループプライマーをデザインして用いた。実験に用いたプライマーの実際の塩基配列は、最後にまとめて記載した。
inner F1:インナープライマーFAの5’側に配置されたF1cに相補的な塩基配列
F1:ループにおけるinnerF1の5’側に隣接する領域
F2:ループにおけるF1に一部重複し、F1よりもより5’側に3’末端が位置する領域
F3:ループにおけるF1に一部重複し、F2よりもより5’側に3’末端が位置する領域
F:ループにおけるインナープライマーのF2cがアニールする領域に隣接する領域
これらのプライマーを用いてLAMP反応した結果、ループプライマーを用いない場合よりも反応が促進されることが示された。
先の実験でインナープライマーが結合するループにハイブリダイズするループプライマー(loop cF/cR)は作用しないことを示した(図5)。この実験では、図14に示すようにF11/R11の組み合わせにおいて、反応の促進効果が見られた。F11、およびR11は、5’側に、その3’末端から伸長した相補鎖の任意の領域に相補的な塩基配列を配置した構造を有する。この構造は、いわゆるインナープライマーの構造である。そのため、ループプライマーを鋳型として合成された相補鎖は、自身を鋳型とした伸長反応が起こる構造になっていると考えられた。
以下に、実験に用いたプライマーの塩基配列を示す。
〔実施例4〕ループプライマーの5’側に配置した塩基配列による変異の検出
本発明におけるループプライマーの5’側に配置する塩基配列を利用して、標的塩基配列中の特定の塩基が予測された塩基配列でなかった場合に本発明によるポリヌクレオチドの増幅方法が阻害されることを確認した。この阻害の有無に基づいて、特定の塩基の変異を検出することができる。
この実験のために用いたループプライマーの5’側には、インナープライマーの5’側に配置された塩基配列と同じ塩基配列を配置した。すなわち、ループプライマーFの5’側には、インナープライマーFAの5’側の塩基配列を配置した。一方、ループプライマーRの5’側には、インナープライマーRAの5’側の塩基配列を配置した。さらに、各プライマーの5’末端において、変異型に相補的な塩基を有するプライマー(MT)と、野生型の塩基に相補的な塩基を有するプライマー(WT)を用意し、全ての組み合せについて、本発明に基づく増幅反応を行った。これらのプライマーを用いて本発明に基づく増幅反応を行うと、各プライマーを鋳型として合成される相補鎖が自身にアニールして相補鎖合成を開始する段階で、特定の塩基の識別が行われる。すなわち、変異型に相補的な塩基を有するプライマー(MT)を鋳型として合成された相補鎖の3’末端は、特定の塩基が変異型であったときに相補鎖合成の起点となることができる。この実験においては、仮に配列番号:50における82番目の塩基がAではなくTであった場合に、期待された増幅反応を開始できるように、MTのプライマーの塩基配列をデザインした。同様に、野生型の塩基に相補的な塩基を有するプライマー(WT)は、それを鋳型として合成された相補鎖の3’末端が野生型の塩基に対して相補鎖合成の起点となることができる。すなわち、WTは、SNPを認識するプライマーと言える。
鋳型には、配列番号:50に示すλDNA由来の塩基配列からなるポリヌクレオチド(106mer)を用いた。反応条件は次のとおりである。
反応液組成(25μL中)
実験に用いた鋳型、および各プライマーの塩基配列を以下に示す。
鋳型ポリヌクレオチド(ラムダDNA,106分子)は熱変性をしないものを用意し、反応液を66℃で反応させABI 7700(パーキンエルマー社)を用いて経時的に増幅の推移を観察した。
反応の結果を図15、および図16に示した。まずルーフプライマーの5’側にF1(あるいはR1)領域を付加したプライマーの5’末端でSNPを検出できるかを検討した(図15)。このとき、インナープライマーはSNPを認識する配列(WT)を用いた。この結果、5’末端でSNPを認識できないプライマー(MT loop)では認識できるプライマー(WT loop)と比較してシグナルの立ち上がりが遅くなった。すなわち、上記プライマーの5’末端を異なる塩基に変えることによって、反応速度の違いに基づいてSNPを検出できることが示された。
次にSNPを認識するインナープライマーを用いてLAMP反応を行った。すなわち、実施例1と同様に、特に5’側に特定の塩基配列を付加しないループプライマーを用い、インナープライマーの5’側の塩基配列のみを変えて反応させた。その結果、ループプライマーを組み合せた場合であっても、本出願人がWO 01/34838に記載した結果と同様に、インナープライマーの5’側に配置した塩基配列を利用して、1塩基の違いを識別できた(図16の1と2)。
次に、図16の1と2の差を大きくすることを目的として、前述のループプライマー(WTloop)を用いてLAMP反応を行った。この結果、図16の2と比較してシグナルの立ち上がりが遅くなり(図16の4)、差を大きくすることができた。すなわち、インナープライマー単独で見られた野生型と変異型の差は、5’側に塩基配列を付加したループプライマーを使用することによってより明確に区別することができた。
LAMP法に基づく変異の検出方法において、変異型と野生型のシグナルの差が縮まる要因の一つとして、次のような機構が考えられる。まず鋳型が野生型である場合に、誤って変異検出用のインナープライマー(MTinner)で反応が進んでしまったとする。その産物が鋳型として機能するときには、MT innerプライマーがプライマーの塩基配列を鋳型として生成した部分にアニールし相補鎖合成を開始する。その結果、認識すべきSNP部分に塩基置換が起きて変異型となった鋳型が増幅されていく。
本実施例においては、5’側に特定の塩基をチェックすることができるループプライマーを用いたことによって、置換を起こした塩基のチェック機構が実現された。図17にこのチェック機構の原理を示す。その結果、前述のような機構に基づく、望まれない増幅反応が抑制され、図16の4に示すような明らかなシグナルの差を得ることができた。
産業上の利用の可能性
本発明は、迅速なポリヌクレオチドの合成方法を提供する。本発明のポリヌクレオチドの合成方法は、ループを形成することができる鋳型ポリヌクレオチドと、ループに相補鎖合成の起点を与えることができる複数のプライマーによって行うことができる。ループを形成する鋳型ポリヌクレオチドは、LAMP法等の公知の手法によって容易に合成することができる。LAMP法を適用することによって、全ての反応を等温で実施することができる。つまり本発明は、LAMP法の応用によって、全ての反応を等温で実施することができ、しかも高度な特異性を維持しつつ、わずかな時間で多量のポリヌクレオチドを生成する。
LAMP法は、原理的に非特異的な合成生成物を生じにくい方法である。本発明をLAMPに適用するときには、ループプライマーを特定の反応生成物にアニールするように設定することができる。この場合、適切な反応生成物が生じたときにのみ、迅速なポリヌクレオチドの合成が起きることになる。したがって、本発明をLAMP法に応用することにより、非特異的な反応を、より生じにくくすることができる。すなわち本発明は、LAMP法の反応効率のみならず、反応特異性をも改善する。
また、本発明の方法は、LAMP法に必要なプライマーに加えて、少なくとも1種類のループプライマーを組み合わせるだけで本発明を実施することができる。したがって、本発明の方法は、汎用性に優れた方法と言うことができる。また、LAMP用の試薬に加えてループプライマーを追加するだけで、本発明の方法を実施するための試薬を構成することができる。したがって、試薬キットも容易に構成することができる。
LAMP法は、特異性、および操作性に優れたポリヌクレオチドの増幅方法である。本発明は、LAMP法のメリットを全て実現しつつ、その相補鎖合成を大幅に迅速化することを可能とした。
SNPsのような遺伝子の機能解析や、その解析結果に基づく遺伝子診断の必要性がますます高まっている。遺伝子の塩基配列をより正確に、より迅速に解析することができる技術の開発は、機能解析を迅速に進めるために、また遺伝子の機能解析の成果を実際の医療の現場で実用化するうえで、重要な課題である。
実際、SNPsの解析結果に基づく医薬品の臨床試験は既に開始されている。このような臨床試験を経て実用化される医薬品の使用においては、SNPsの解析をベッドサイドで、簡便に、そして迅速に行うことができる遺伝子の解析手法が必須と言って良い。本発明は、このような高度な要求に応えることができる有用な遺伝子解析手法を実現する。
【配列表】
【図面の簡単な説明】
図1は、本発明を利用したポリヌクレオチドの増幅方法の反応原理を示す図。図中、FA:LAMP法用プライマーFA
RA:LAMP法用プライマーRA
loop F:ループプライマーF
loop R:ループプライマーR
図2は、本発明を利用したポリヌクレオチドの増幅方法の反応原理を示す図。図中の略号は図1と同じ意味を表す。
図3は、ループプライマーと鋳型ポリヌクレオチドを構成する塩基配列との好ましい位置関係を示す図。
図4は、実施例で用いた鋳型ポリヌクレオチドの塩基配列(配列番号:1)と、各プライマーの塩基配列との位置的な関係を示す図。袋文字(アウトライン)で塩基を記載した部分がループプライマーがアニールする部分で、矢印は相補鎖の合成方向を示している。
図5は、ループプライマーを用いたときの反応促進効果を示す図。図中、横軸は反応時間、縦軸は蛍光強度の変化(ΔRn)を示す。
loop F/R:ループプライマーRおよびループプライマーFを使用
loop cF/cR:ループプライマーRおよびループプライマーFの相補的な塩基配列からなるループプライマーcFおよびループプライマーcRを使用
−/−:ループプライマーを加えない場合
図6は、鋳型DNA量の検討結果を示す図。図中、横軸は反応時間、縦軸は蛍光強度の変化(ΔRn)を示す。
図7は、ループプライマーの濃度依存性を示す図。図中、横軸は反応時間、縦軸は蛍光強度の変化(ΔRn)を示す。
図8は、3’アミノ化ループプライマーの影響を示す図。図中、横軸は反応時間、縦軸は蛍光強度の変化(ΔRn)を示す。
loop primer:3’末端を修飾していないループプライマーを使用
3’N−loop primer:3’末端をアミノ化したループプライマーを使用
−/−:ループプライマーを加えない場合
図9は、アウタープライマーの有無による影響を示す図。図中、横軸は反応時間、縦軸は蛍光強度の変化(ΔRn)を示す。
Outer primer(+):アウタープライマーを使用
Outer primer(−):アウタープライマーを不使用
Negative Control:鋳型cDNAを加えない場合
図10は、プライマーの長さに関する検討結果を示す図。図中、横軸は反応時間、縦軸は蛍光強度の変化(ΔRn)を示す。
F/R:ループプライマーFおよびループプライマーRを使用
F−1/R−1:5’末端で1塩基短いループプライマーFおよびループプライマーRを使用
F−2/R−2:5’末端で2塩基短いループプライマーFおよびループプライマーRを使用
図11は、ループプライマーの設計部位の検討結果を示す図。図中、横軸は反応時間、縦軸は蛍光強度の変化(ΔRn)を示す。
F3/R4:F2領域と重複が無いループプライマーF3、およびR2領域と重複が無いループプライマーR4を使用
F5/R5:F2領域と3塩基重複させたループプライマーF5、およびR2領域と3塩基重複させたループプライマーR5を使用
F6/R6:F1領域と3塩基重複させたループプライマーF6、およびR1領域と3塩基重複させたループプライマーR6を使用
F7/R7:F1領域と10塩基重複させたループプライマーF7、およびR1領域と10塩基重複させたループプライマーR7を使用
F8/R8:F1領域と完全に重複させたループプライマーF8、およびR1領域と完全に重複させたループプライマーR8を使用
−/−:ループプライマーを加えない場合
図12は、本発明によるSRY遺伝子の増幅結果を示す図。図中、横軸は反応時間、縦軸は蛍光強度の変化(ΔRn)を示す。
loop primer(+):ループプライマーを加えた場合
loop primer(−):ループプライマーを加えない場合
Negative Control:鋳型DNAを加えない場合
図13は、5’に付加したループプライマーの鋳型となる塩基配列に対する位置関係を示す図。「c」は相補配列であることを示す。
図14は、5’に付加したループプライマーを用いたときの反応促進効果を示す図。図中、横軸は反応時間、縦軸は蛍光強度(ΔRn)を示す。
図15は、ループプライマーの5’でのSNP認識の検討結果を示す図。図中、横軸は反応時間、縦軸は蛍光強度(ΔRn)を示す。
図16は、インナープライマーの5’およびループプライマーの5’でのSNP認識の検討結果を示す図。図中、横軸は反応時間、縦軸は蛍光強度(ΔRn)を示す。
図17は、本発明を利用したSNPの検出法の反応原理を示す図。
Claims (26)
- 以下の要素1〜5を混合して下記のDNAポリメラーゼによる鋳型依存性の相補鎖合成が可能な条件下でインキュベートする工程を含むポリヌクレオチドの合成方法。
1:次の条件(a)〜(d)を持つ鋳型ポリヌクレオチド、
(a)少なくとも1組の相補的な塩基配列からなる標的塩基配列を有する、
(b)aの相補的な塩基配列がハイブリダイズしたときに、塩基対結合が可能なループを形成することができる、
(c)3’末端が自身にアニールしてループを形成することができる、
(d)自身にアニールした3’末端は自身を鋳型とする相補鎖合成の起点となることができる
2:鋳型ポリヌクレオチドのループにおいて、異なる位置に相補鎖合成の起点を与えることができる少なくとも2種類のプライマー、
3:鋳型ポリヌクレオチド、および/または鋳型ポリヌクレオチドに2のプライマーがアニールして生成する伸長生成物が形成するループにおいて、2のプライマーとは異なる位置に相補鎖合成の起点を与えることができる少なくとも1種類のプライマー、
4:鎖置換を伴う相補鎖合成を触媒することができるDNAポリメラーゼ、
5:相補鎖合成のための基質 - 鋳型ポリヌクレオチドが、自身の塩基配列の任意の領域に対して相補的な塩基配列をその5’末端に備えている請求項1に記載の方法。
- 次の工程によって鋳型ポリヌクレオチドを生成する請求項2に記載の方法。
a)標的塩基配列に第1のプライマーをアニールさせ、これを起点とする相補鎖合成反応を行う工程;ここで第1のプライマーはその3’末端において標的塩基配列を構成する一方の鎖の3’側を規定する領域に相補鎖合成の起点を与えることができ、かつ第1のプライマーの5’側には、このプライマーを起点とする相補鎖合成反応生成物の任意の領域に対して相補的な塩基配列を備える、
b)工程a)で合成された第1のプライマーの伸長生成物における第2のプライマーがアニールすべき領域を塩基対結合が可能な状態とする工程;ここで第2のプライマーはその3’末端において前記第1のプライマーを起点とする伸長生成物における標的塩基配列の3’側を規定する領域に相補鎖合成の起点を与えることができる塩基配列を備え、かつ第2のプライマーの5’側には、このプライマーを起点とする相補鎖合成反応生成物の任意の領域に対して相補的な塩基配列を備える、
c)工程b)において塩基対結合が可能となった領域に第2のプライマーをアニールさせ、これを起点とする相補鎖合成を行う工程、
d)工程c)によって合成された第2のプライマーの伸長生成物の3’末端を自身にアニールさせて、自身を鋳型とする相補鎖合成を行う工程 - 前記2種類のプライマーが、第1のプライマー、および第2のプライマーであり、前記少なくとも1種類のプライマーが第1のプライマー、または第2のプライマーの伸長生成物における各プライマーに由来する領域と、各プライマーに対する前記任意の領域の間において相補鎖合成の起点を与えることができるループプライマーである請求項3に記載の方法。
- 前記ループプライマーが、第1のプライマーの伸長生成物における第1のプライマーに由来する領域と、第1のプライマーに対する前記任意の領域の間において相補鎖合成の起点を与えることができる第1のループプライマー;、および第2のプライマーの伸長生成物における第2のプライマーに由来する領域と、第2のプライマーに対する前記任意の領域の間において相補鎖合成の起点を与えることができる第2のループプライマーである請求項4に記載の方法。
- ループプライマーが、前記任意の領域に相補的な塩基配列をその5’末端に付加されている請求項4に記載の方法。
- 工程b)および/または工程c)において、第1のプライマーまたは第2のプライマーに対して鋳型における3’側に相補鎖合成の起点を与えるアウタープライマーからの相補鎖合成によって、第1のプライマーおよび/または第2のプライマーの伸長生成物を置換して第1のプライマーまたは第2のプライマーの各生成物を1本鎖とする請求項3に記載の方法。
- 工程a)において、標的塩基配列が2本鎖ポリヌクレオチドとして存在しており、第1のプライマーがアニールする領域が、任意のプライマーを起点とする相補鎖合成反応によって塩基対結合が可能な状態とされる請求項3に記載の方法。
- 工程a)を融解温度調整剤の存在下で行う請求項8に記載の方法。
- 融解温度調整剤が、ベタイン、プロリン、ジメチルスルホキシド、およびトリメチルアミンN−オキシドで構成される群から選択される少なくとも1つの化合物である請求項9に記載の方法。
- 請求項1または請求項5に記載の方法によって鋳型ポリヌクレオチドを鋳型とする相補鎖合成を繰り返すとともに、この合成反応による伸長生成物を新たな鋳型ポリヌクレオチドとして、請求項1または請求項5に記載の方法によって更に別のポリヌクレオチドの合成反応を行う工程を含む鋳型ポリヌクレオチドの増幅方法。
- 請求項11に記載の増幅方法を行い、増幅反応生成物の生成を標的塩基配列の存在と関連付ける工程を含む、試料中の標的塩基配列を検出する方法。
- ポリヌクレオチドの検出剤存在下で請求項11に記載の方法を行い、検出剤のシグナル変化に基づいて増幅反応生成物が生じたかどうかを観察する請求項12に記載の方法。
- 請求項12に記載の検出方法によって標的塩基配列における変異を検出する方法であって、標的塩基配列が予測された塩基配列でなかったときに、前記増幅方法を構成する相補鎖合成反応から選択される少なくとも1つの相補鎖合成反応が妨げられるものであり、前記増幅反応の阻害を観察する工程を含む方法。
- 下記第1のプライマーおよび第2のプライマーを用いる請求項14に記載の方法であって、第1のプライマーおよび第2のプライマーの少なくともいずれかが、その5’側にチェック用配列を有する方法;
ここでチェック用配列とは、前記特定の領域を構成する塩基配列が予測された塩基配列でなかった場合に、チェック用配列を鋳型として合成された相補鎖の3’末端が標的塩基配列、またはその相補鎖にアニールするときにミスマッチを生じ、かつこのミスマッチによって当該3’末端を起点として開始する相補合成反応が阻害される塩基配列を言う、
第1のプライマー:第1のプライマーはその3’末端において標的塩基配列を構成する一方の鎖の3’側を規定する領域に相補鎖合成の起点を与えることができ、かつ第1のプライマーの5’側には、このプライマーを起点とする相補鎖合成反応生成物の任意の領域に対して相補的な塩基配列を備える、
第2のプライマー:第2のプライマーはその3’末端において前記第1のプライマーを起点とする伸長生成物における標的塩基配列の3’側を規定する領域に相補鎖合成の起点を与えることができる塩基配列を備え、かつ第2のプライマーの5’側には、このプライマーを起点とする相補鎖合成反応生成物の任意の領域に対して相補的な塩基配列を備える - 前記特定の領域を構成する塩基配列が予測された塩基配列でなかった場合に、チェック用配列を鋳型として合成された相補鎖が、標的塩基配列、またはその相補鎖にアニールするとき、当該相補鎖の3’末端から2〜4番目の塩基においてミスマッチを生じることを特徴とする請求項15に記載の方法。
- ループプライマーとして下記第1のループプライマーおよび/または第2のループプライマーを用いる請求項15に記載の方法;ただしループプライマーはその5’側に前記プライマーの5’側に配置された前記任意の領域に相補的な塩基配列を有するか、またはプライマーの5’側に配置された塩基配列がチェック用配列であるときは、当該チェック用配列における前記ミスマッチを与えるための塩基がチェック用配列と相違する配列をループプライマーの5’側に配置する
第1のループプライマー:第1のプライマーの伸長生成物における第1のプライマーに由来する領域と、第1のプライマーに対する前記任意の領域の間において相補鎖合成の起点を与える;
第2のループプライマー:第2のプライマーの伸長生成物における第2のプライマーに由来する領域と、第2のプライマーに対する前記任意の領域の間において相補鎖合成の起点を与える - 前記特定の領域を構成する塩基配列が予測された塩基配列でなかった場合に、チェック用配列を鋳型として合成された相補鎖が、標的塩基配列、またはその相補鎖にアニールするとき、当該相補鎖の3’末端から2〜4番目の塩基においてミスマッチを生じることを特徴とする請求項17に記載の方法であって、第1のループプライマーおよび/または第2のループプライマーの5’側に配置する塩基配列は、チェック用配列における前記ミスマッチの原因となる塩基において相違する請求項17に記載の方法。
- 次の要素a)〜f)を含む、標的塩基配列の増幅用キット。
a)第1のプライマー;ここで第1のプライマーはその3’末端において標的塩基配列を構成する一方の鎖の3’側を規定する領域に相補鎖合成の起点を与えることができ、かつ第1のプライマーの5’側には、このプライマーを起点とする相補鎖合成反応生成物の任意の領域に対して相補的な塩基配列を備える、
b)第2のプライマー;ここで第2のプライマーはその3’末端において前記第1のプライマーを起点とする伸長生成物における標的塩基配列の3’側を規定する領域に相補鎖合成の起点を与えることができる塩基配列を備え、かつ第2のプライマーの5’側には、このプライマーを起点とする相補鎖合成反応生成物の任意の領域に対して相補的な塩基配列を備える、
c)第1のループプライマー;ここで第1のループプライマーは、第1のプライマーの伸長生成物における第1のプライマーに由来する領域と、第1のプライマーに対する前記任意の領域の間において相補鎖合成の起点を与える、
d)第2のループプライマー;ここで第2のループプライマーは、第2のプライマーの伸長生成物における第2のプライマーに由来する領域と、第2のプライマーに対する前記任意の領域の間において相補鎖合成の起点を与える、
e)鎖置換を伴う相補鎖合成を触媒することができるDNAポリメラーゼ、
f)相補鎖合成のための基質 - 更に次の要素g)を含む請求項19に記載のキット。
g)アウタプライマー;アウタープライマーは、第1のプライマーおよび/または第2のプライマーの鋳型における3’側に相補鎖合成の起点を与えることができる - 第1のプライマーおよび/または第2のプライマーが、5’側にチェック用配列を有する請求項19に記載のキット。
- ループプライマーとして下記第1のループプライマーおよび/または第2のループプライマーを含む請求項19に記載のキット;ただしループプライマーはその5’側に前記プライマーの5’側に配置された前記任意の領域に相補的な塩基配列を有するか、または前記プライマーの5’側に配置された塩基配列がチェック用配列であるときは、当該チェック用配列における前記ミスマッチを与えるための塩基がチェック用配列と相違する配列をループプライマーの5’側に配置する。
第1のループプライマー:第1のプライマーの伸長生成物における第1のプライマーに由来する領域と、第1のプライマーに対する前記任意の領域の間において相補鎖合成の起点を与える;
第2のループプライマー:第2のプライマーの伸長生成物における第2のプライマーに由来する領域と、第2のプライマーに対する前記任意の領域の間において相補鎖合成の起点を与える - 次の要素a)〜g)を混合し、鎖置換を伴う相補鎖合成反応が可能な条件下でインキュベートする工程を含むポリヌクレオチドの増幅方法。
a)第1のプライマー;ここで第1のプライマーはその3’末端において標的塩基配列を構成する一方の鎖の3’側を規定する領域に相補鎖合成の起点を与えることができ、かつ第1のプライマーの5’側には、このプライマーを起点とする相補鎖合成反応生成物の任意の領域に対して相補的な塩基配列を備える、
b)第2のプライマー;ここで第2のプライマーはその3’末端において前記第1のプライマーを起点とする伸長生成物における標的塩基配列の3’側を規定する領域に相補鎖合成の起点を与えることができる塩基配列を備え、かつ第2のプライマーの5’側には、このプライマーを起点とする相補鎖合成反応生成物の任意の領域に対して相補的な塩基配列を備える、
c)第1のループプライマー;ここで第1のループプライマーは、第1のプライマーの伸長生成物における第1のプライマーに由来する領域と、第1のプライマーに対する前記任意の領域の間において相補鎖合成の起点を与えることができる、
d)第2のループプライマー;ここで第2のループプライマーは、第2のプライマーの伸長生成物における第2のプライマーに由来する領域と、第2のプライマーに対する前記任意の領域の間において相補鎖合成の起点を与えることができる、
e)鎖置換を伴う相補鎖合成を触媒することができるDNAポリメラーゼ、
f)相補鎖合成のための基質、および
g)標的塩基配列を含む被検ポリヌクレオチド - 更に次の要素h)を加える請求項23に記載の方法。
h)アウタプライマー;アウタープライマーは、第1のプライマーおよび/または第2のプライマーの3’末端が標的塩基配列にアニールする領域に対して、鋳型における3’側に相補鎖合成の起点を与える - 次の要素a)〜d)を混合し、鎖置換を伴う相補鎖合成反応が可能な条件下でインキュベートし、a)における(1)〜(4)のプライマーセットによる増幅生成物の生成速度および/または生成量を測定する工程を含む、標的塩基配列における特定の塩基が、第1の塩基であるか第2の塩基であるかを決定するための方法。
a)以下のプライマーセット(1)〜(4)から選択されたいずれかのプライマーセット
(1):第1塩基用インナープライマー対と第1塩基用ループプライマー対
(2):第1塩基用インナープライマー対と第2塩基用ループプライマー対
(3):第2塩基用インナープライマー対と第1塩基用ループプライマー対
(4):第2塩基用インナープライマー対と第2塩基用ループプライマー対
;ここで第1塩基用インナープライマー対および第2塩基用インナープライマー対は、いずれも次の第1のインナープライマーと第2のインナープライマーとからなるプライマー対であり、第1塩基用インナープライマー対においては第1のインナープライマーと第2のインナープライマーの5’側を鋳型として合成された相補鎖の3’末端を起点とする相補鎖合成反応が、前記標的塩基配列における特定の塩基が第1の塩基のときには阻害されず、第2の塩基のときには阻害され;また
第2塩基用インナープライマー対においては、第1のインナープライマーと第2のインナープライマーの5’側を鋳型として合成された相補鎖の3’末端を起点とする相補鎖合成が、前記標的塩基配列における特定の塩基が第2の塩基のときには阻害されず、第1の塩基のときには阻害され;そして
第1のインナープライマーは、3’末端において標的塩基配列を構成する一方の鎖の3’側を規定する領域に相補鎖合成の起点を与える塩基配列を備え、かつ第1のインナープライマーの5’側には、このインナープライマーを起点とする相補鎖合成反応生成物の任意の領域に対して相補的な塩基配列を備える、
第2のインナープライマーはその3’末端において前記第1のインナープライマーを起点とする伸長生成物における標的塩基配列の3’側を規定する領域に相補鎖合成の起点を与える塩基配列を備え、かつ第2のインナープライマーの5’側には、このインナープライマーを起点とする相補鎖合成反応生成物の任意の領域に対して相補的な塩基配列を備える、
次に第1塩基用ループプライマー対および第2塩基用ループプライマー対は、いずれも次の第1のループプライマーと第2のループプライマーとからなる対であり、第1塩基用ループプライマー対においては第1のループプライマーと第2のループプライマーの5’側を鋳型として合成された相補鎖の3’末端を起点とする相補鎖合成反応が、前記標的塩基配列における特定の塩基が第1の塩基のときには阻害されず、第2の塩基のときには阻害され;また
第2塩基用ループプライマー対においては、第1のループプライマーと第2のループプライマーの5’側を鋳型として合成された相補鎖の3’末端を起点とする相補鎖合成が、前記標的塩基配列における特定の塩基が第2の塩基のときには阻害されず、第1の塩基のときには阻害される;
第1のループプライマーは、第1のインナープライマーの伸長生成物における第1のインナープライマーに由来する領域と、第1のインナープライマーに対する前記任意の領域の間において相補鎖合成の起点を与えることができる、
第2のループプライマーは、第2のインナープライマーの伸長生成物における第2のインナープライマーに由来する領域と、第2のインナープライマーに対する前記任意の領域の間において相補鎖合成の起点を与えることができる、
b)鎖置換を伴う相補鎖合成を触媒することができるDNAポリメラーゼ、
c)相補鎖合成のための基質、および
d)標的塩基配列を含む被検ポリヌクレオチド - 更に次の要素e)を加える請求項25に記載の方法。
e)アウタプライマー;アウタープライマーは、第1のプライマーおよび/または第2のプライマーの3’末端が標的塩基配列にアニールする領域に対して、鋳型における3’側に相補鎖合成の起点を与える
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2002529496A JP4918210B2 (ja) | 2000-09-19 | 2001-09-19 | ポリヌクレオチドの合成方法 |
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2000283862 | 2000-09-19 | ||
| JP2000283862 | 2000-09-19 | ||
| JP2002529496A JP4918210B2 (ja) | 2000-09-19 | 2001-09-19 | ポリヌクレオチドの合成方法 |
| PCT/JP2001/008142 WO2002024902A1 (en) | 2000-09-19 | 2001-09-19 | Method of synthesizing polynucleotide |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011289124A Division JP2012085652A (ja) | 2000-09-19 | 2011-12-28 | ポリヌクレオチドの合成方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JPWO2002024902A1 true JPWO2002024902A1 (ja) | 2004-01-29 |
| JP4918210B2 JP4918210B2 (ja) | 2012-04-18 |
Family
ID=18768163
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2002529496A Expired - Lifetime JP4918210B2 (ja) | 2000-09-19 | 2001-09-19 | ポリヌクレオチドの合成方法 |
| JP2011289124A Withdrawn JP2012085652A (ja) | 2000-09-19 | 2011-12-28 | ポリヌクレオチドの合成方法 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011289124A Withdrawn JP2012085652A (ja) | 2000-09-19 | 2011-12-28 | ポリヌクレオチドの合成方法 |
Country Status (9)
| Country | Link |
|---|---|
| US (3) | US7374913B2 (ja) |
| EP (2) | EP2031058B1 (ja) |
| JP (2) | JP4918210B2 (ja) |
| CN (1) | CN1222614C (ja) |
| AT (1) | ATE437225T1 (ja) |
| AU (1) | AU2001288065A1 (ja) |
| DE (1) | DE60139331D1 (ja) |
| ES (2) | ES2390242T3 (ja) |
| WO (1) | WO2002024902A1 (ja) |
Families Citing this family (64)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8445664B2 (en) * | 1998-06-24 | 2013-05-21 | Enzo Diagnostics, Inc. | Kits for amplifying and detecting nucleic acid sequences |
| ATE437225T1 (de) * | 2000-09-19 | 2009-08-15 | Eiken Chemical | Verfahren zur polynukleotidsynthese |
| AU2003211947A1 (en) | 2002-02-20 | 2003-09-09 | Sysmex Corporation | PRIMERS FOR NUCLEIC ACID AMPLIFICATION IN DETECTING HOUSEKEEPING GENE mRNA AND TEST METHOD USING THESE PRIMERS |
| WO2003097878A1 (en) | 2002-05-21 | 2003-11-27 | Sysmex Corporation | Nucleic acid amplification primers for detecting cytokeratins and examination method with the use of the primers |
| WO2004040019A1 (ja) | 2002-10-29 | 2004-05-13 | Riken | 核酸の増幅法 |
| CN1813064B (zh) | 2003-06-27 | 2011-11-02 | 荣研化学株式会社 | 检测sars冠状病毒的方法 |
| JP2005110587A (ja) * | 2003-10-08 | 2005-04-28 | Sapporo Breweries Ltd | アリサイクロバチラス属菌検出用プライマー |
| US8206902B2 (en) | 2003-12-25 | 2012-06-26 | Riken | Method of amplifying nucleic acid and method of detecting mutated nucleic acid using the same |
| JP2008000002A (ja) * | 2004-09-30 | 2008-01-10 | Sysmex Corp | リブロース2リン酸カルボキシラーゼスモールチェーン1A(RBCS−1A)遺伝子及び/又は該遺伝子のmRNAを検出するための核酸増幅用プライマ、及び内部標準として該遺伝子及び/又は該遺伝子のmRNAを用いた検査方法。 |
| ES2382446T3 (es) | 2004-11-01 | 2012-06-08 | Eiken Kagaku Kabushiki Kaisha | Método de detección del virus de la gripe aviar H5 |
| JP2006254784A (ja) * | 2005-03-17 | 2006-09-28 | Institute Of Physical & Chemical Research | プライマーダイマーからの非特異的増幅を減少させる方法 |
| FR2885140B1 (fr) | 2005-04-29 | 2010-12-31 | Millipore Corp | Procede de detection et de caracterisation de microorgarnismes sur une membrane. |
| WO2007069331A1 (ja) * | 2005-12-16 | 2007-06-21 | Eiken Kagaku Kabushiki Kaisha | ヒト免疫不全ウイルス1型の検出方法 |
| JP4580875B2 (ja) * | 2006-01-20 | 2010-11-17 | 株式会社東芝 | 核酸検出法のためのプライマーの設計方法 |
| JP4881623B2 (ja) | 2006-01-27 | 2012-02-22 | シスメックス株式会社 | Cea核酸増幅用プライマー、プライマーセット、及びがんの診断支援方法 |
| EP2108048A1 (en) * | 2007-01-17 | 2009-10-14 | Meridian Bioscience, Inc. | Stable reagents and kits useful in loop-mediated isothermal amplification (lamp) |
| CA2622649C (en) | 2007-03-09 | 2018-04-24 | Riken | Nucleic acid amplification method using primer exhibiting exciton effect |
| JP4410268B2 (ja) | 2007-03-28 | 2010-02-03 | 株式会社東芝 | メチレンテトラヒドロ葉酸還元酵素(mthfr)の遺伝子型を検出するための核酸プライマーセット及び核酸プローブ |
| JP4410269B2 (ja) | 2007-03-28 | 2010-02-03 | 株式会社東芝 | N−アセチルトランスフェラーゼ2(nat2)の遺伝子型を検出するための核酸プライマーセット、キット、及び該プライマーセットを用いた検出方法 |
| JP4490988B2 (ja) | 2007-04-26 | 2010-06-30 | 株式会社東芝 | 血清アミロイドa1(saa1)の遺伝子型を検出するための核酸プライマーセット、キット、及び該プライマーセットを用いた検出方法 |
| US20100221787A1 (en) | 2007-10-25 | 2010-09-02 | Riken | Isothermal amplification method and dna polymerase used in the same |
| WO2009119331A1 (ja) * | 2008-03-28 | 2009-10-01 | シスメックス株式会社 | サイトケラチン7のmRNAの検出用プライマを含む試薬 |
| CN103923991B (zh) | 2008-05-28 | 2016-04-20 | 花王株式会社 | 耐热菌类的检测方法 |
| EP2325309B1 (en) | 2008-05-29 | 2014-10-22 | Kao Corporation | Method for detection of paecilomyces variotii |
| BRPI0909989A2 (pt) * | 2008-06-05 | 2021-06-22 | Butamax Advanced Biofuels Llc | célula de levedura recombinante e método para a produção de um produto |
| JPWO2010061922A1 (ja) | 2008-11-27 | 2012-04-26 | 独立行政法人理化学研究所 | 新規MutSタンパク質およびそれを用いた変異の判定方法 |
| JPWO2010074265A1 (ja) | 2008-12-25 | 2012-06-21 | ユニバーサル・バイオ・リサーチ株式会社 | 検体の前処理方法、および生体関連物質の測定方法 |
| GB0910302D0 (en) * | 2009-06-15 | 2009-07-29 | Lumora Ltd | Nucleic acid amplification |
| EP2746395B1 (en) | 2011-09-08 | 2017-11-29 | Kabushiki Kaisha DNAFORM | Primer set, method for amplifying target nucleic acid sequence using same, and method for detecting mutated nucleic acid using same |
| CN103975061A (zh) | 2011-10-31 | 2014-08-06 | 荣研化学株式会社 | 靶核酸的检测方法 |
| CN105026573A (zh) | 2012-11-28 | 2015-11-04 | 艾布维兹生物公司 | 用于单引物扩增的基因特异模板的制备 |
| US9677981B2 (en) | 2013-03-15 | 2017-06-13 | 3M Innovative Properties Company | Sample concentrator and method of use |
| CN105722977A (zh) | 2013-10-30 | 2016-06-29 | 绿色生活生物技术有限责任公司 | 用于柑橘绿化枯萎病的发病定量系统和治疗方法 |
| CN106661600B (zh) | 2014-07-16 | 2021-04-06 | 唐恩生物科技股份有限公司 | 用于扩增核酸样品的等温方法 |
| US11559801B2 (en) | 2014-11-03 | 2023-01-24 | Tangen Biosciences, Inc. | Apparatus and method for cell, spore, or virus capture and disruption |
| WO2016098892A1 (ja) * | 2014-12-19 | 2016-06-23 | 国立大学法人 長崎大学 | ザイールエボラウイルス検出用プライマーセット、アッセイキットおよび増幅方法 |
| JP6605238B2 (ja) * | 2014-12-19 | 2019-11-13 | 国立大学法人 長崎大学 | ザイールエボラウイルス検出用プライマーセット、アッセイキットおよび増幅方法 |
| KR20180002636A (ko) | 2015-03-30 | 2018-01-08 | 그린라이트 바이오사이언시스, 아이엔씨. | 리보핵산의 무세포 생산 |
| WO2017212904A1 (ja) * | 2016-06-06 | 2017-12-14 | 国立大学法人 宮崎大学 | 複数のプライマーセットを組み合わせたlamp法を用いたアフリカ豚コレラウイルスの迅速検出法 |
| WO2018209092A1 (en) * | 2017-05-10 | 2018-11-15 | Board Of Regents, The University Of Texas System | Methods and devices related to amplifying nucleic acid at a variety of temperatures |
| JP7176682B2 (ja) | 2018-02-22 | 2022-11-22 | 佐藤製薬株式会社 | 白癬菌の遺伝子をlamp法により検出するためのプライマーセット及びそれを含むキット並びにそれらを用いて白癬菌を検出する方法 |
| CN109658982B (zh) * | 2018-12-25 | 2020-06-19 | 人和未来生物科技(长沙)有限公司 | 一种用于基因测序的引物设计方法及系统 |
| WO2020150143A2 (en) * | 2019-01-14 | 2020-07-23 | Camena Bioscience Limited | Compositions and methods for template-free geometric enzymatic nucleic acid synthesis |
| US12325883B2 (en) | 2019-01-15 | 2025-06-10 | Neogen Food Safety Us Holdco Corporation | Loop-mediated isothermal amplification primers for Shiga toxin-producing E. coli (STEC) detection |
| SG10201910254YA (en) | 2019-11-04 | 2021-06-29 | Denka Company Ltd | Nucleic Acid Detection Method Using Lamp And Probe Detection |
| CN110878367A (zh) * | 2019-12-05 | 2020-03-13 | 华南农业大学 | 一种可检测snp的新型cpa方法、引物组和试剂盒 |
| JP7048819B2 (ja) | 2020-02-27 | 2022-04-05 | 栄研化学株式会社 | 一本鎖rnaウイルスを検出する方法 |
| CN115176036A (zh) | 2020-03-05 | 2022-10-11 | 荣研化学株式会社 | 冠状病毒(SARS-CoV-2)的检测方法 |
| EP4118205A4 (en) | 2020-03-13 | 2024-04-17 | UH-OH Labs Inc. | LOOP PRIMER AND LOOP-DELOOP METHODS FOR THE DETECTION OF TARGET NUCLEIC ACIDS |
| WO2021224355A1 (en) | 2020-05-05 | 2021-11-11 | Genomtec Sa | Diagnostic primers, kits and methods for viral detection |
| CA3186580A1 (en) | 2020-06-12 | 2021-12-16 | Sherlock Biosciences, Inc. | Crispr-based sars-cov-2 detection |
| CN116075596A (zh) | 2020-08-07 | 2023-05-05 | 牛津纳米孔科技公开有限公司 | 鉴定核酸条形码的方法 |
| CN112553300A (zh) * | 2020-10-15 | 2021-03-26 | 德歌生物技术(山东)有限公司 | 引物设计方法、引物及等温扩增核酸片段的方法 |
| EP3992300A1 (en) | 2020-10-30 | 2022-05-04 | Nederlandse Organisatie voor toegepast- natuurwetenschappelijk Onderzoek TNO | Sample pre-treatment for isothermal amplification |
| KR20230169935A (ko) | 2021-01-12 | 2023-12-18 | 데피니티브 바이오테크놀로지스 엘엘씨 | 생물학적 시료들에서 핵산을 검출하기 위한 디바이스및 방법 |
| CA3210883A1 (en) | 2021-02-09 | 2022-08-18 | Sherlock Biosciences, Inc. | Nucleic acid amplification using promoter primers |
| US11788129B2 (en) | 2021-02-23 | 2023-10-17 | Industrial Technology Research Institute | Nucleic acid detection kit and nucleic acid detection method |
| PL437280A1 (pl) | 2021-03-12 | 2022-09-19 | Genomtec Spółka Akcyjna | Zestaw starterów do powielania, sposób wykrywania infekcji bakteryjnej przenoszonej drogą płciową oraz zestaw do wykrywania infekcji |
| PL437660A1 (pl) | 2021-04-22 | 2022-10-24 | Genomtec Spółka Akcyjna | Zestaw starterów, skład reagentów oraz metoda wykrywania bakterii Staphylococcus aureus opornej na metycylinę (MRSA) |
| CN113201583B (zh) * | 2021-04-29 | 2022-02-08 | 国科宁波生命与健康产业研究院 | 恒温条件下合成核酸的方法及试剂盒和应用 |
| EP4105327A4 (en) * | 2021-04-29 | 2023-01-18 | Ningbo Institute of Life and Health Industry University of Chinese Academy of Sciences | PROCESS FOR THE PREPARATION OF CONSTANT TEMPERATURE NUCLEIC ACIDS AND KIT AND USE THEREOF |
| JP2025500496A (ja) | 2021-12-24 | 2025-01-09 | エフ. ホフマン-ラ ロシュ アーゲー | Lamp増幅産物の改良された検出 |
| WO2025009968A1 (en) | 2023-07-03 | 2025-01-09 | Erasmus University Medical Center Rotterdam | Methods for specific quantitation of the inducible hiv reservoir |
| EP4488391A1 (en) | 2023-07-04 | 2025-01-08 | Nederlandse Organisatie voor toegepast-natuurwetenschappelijk Onderzoek TNO | Methods and means for detection of legionella |
Family Cites Families (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6743605B1 (en) * | 1998-06-24 | 2004-06-01 | Enzo Life Sciences, Inc. | Linear amplification of specific nucleic acid sequences |
| ATE374833T1 (de) * | 1998-11-09 | 2007-10-15 | Eiken Chemical | Verfahren zur synthese von nukleinsäuren |
| WO2001034790A1 (en) | 1999-11-08 | 2001-05-17 | Eiken Kagaku Kabushiki Kaisha | Method for synthesizing nucleic acid |
| EP1231281B1 (en) * | 1999-11-08 | 2006-02-01 | Eiken Kagaku Kabushiki Kaisha | Method of detecting variation or polymorphism |
| ES2546450T3 (es) * | 2000-04-07 | 2015-09-23 | Eiken Kagaku Kabushiki Kaisha | Método para amplificar y detectar un ácido nucleico usando ácido nucleico bicatenario como molde |
| ATE437225T1 (de) * | 2000-09-19 | 2009-08-15 | Eiken Chemical | Verfahren zur polynukleotidsynthese |
-
2001
- 2001-09-19 AT AT01967728T patent/ATE437225T1/de not_active IP Right Cessation
- 2001-09-19 US US10/380,930 patent/US7374913B2/en not_active Expired - Lifetime
- 2001-09-19 ES ES08019286T patent/ES2390242T3/es not_active Expired - Lifetime
- 2001-09-19 ES ES01967728T patent/ES2327712T3/es not_active Expired - Lifetime
- 2001-09-19 AU AU2001288065A patent/AU2001288065A1/en not_active Abandoned
- 2001-09-19 DE DE60139331T patent/DE60139331D1/de not_active Expired - Lifetime
- 2001-09-19 CN CNB018190839A patent/CN1222614C/zh not_active Expired - Lifetime
- 2001-09-19 JP JP2002529496A patent/JP4918210B2/ja not_active Expired - Lifetime
- 2001-09-19 EP EP08019286A patent/EP2031058B1/en not_active Expired - Lifetime
- 2001-09-19 EP EP01967728A patent/EP1327679B1/en not_active Expired - Lifetime
- 2001-09-19 WO PCT/JP2001/008142 patent/WO2002024902A1/ja not_active Ceased
-
2008
- 2008-04-15 US US12/103,492 patent/US7851186B2/en not_active Expired - Fee Related
- 2008-04-15 US US12/103,506 patent/US7846695B2/en not_active Expired - Fee Related
-
2011
- 2011-12-28 JP JP2011289124A patent/JP2012085652A/ja not_active Withdrawn
Also Published As
| Publication number | Publication date |
|---|---|
| AU2001288065A1 (en) | 2002-04-02 |
| EP2031058A1 (en) | 2009-03-04 |
| JP2012085652A (ja) | 2012-05-10 |
| CN1222614C (zh) | 2005-10-12 |
| CN1474870A (zh) | 2004-02-11 |
| ES2327712T3 (es) | 2009-11-03 |
| US20080213790A1 (en) | 2008-09-04 |
| DE60139331D1 (de) | 2009-09-03 |
| US7374913B2 (en) | 2008-05-20 |
| US20080213842A1 (en) | 2008-09-04 |
| WO2002024902A1 (en) | 2002-03-28 |
| EP1327679A1 (en) | 2003-07-16 |
| ES2390242T3 (es) | 2012-11-07 |
| US20040038253A1 (en) | 2004-02-26 |
| ATE437225T1 (de) | 2009-08-15 |
| EP1327679B1 (en) | 2009-07-22 |
| EP2031058B1 (en) | 2012-07-18 |
| US7851186B2 (en) | 2010-12-14 |
| HK1055445A1 (en) | 2004-01-09 |
| JP4918210B2 (ja) | 2012-04-18 |
| EP1327679A4 (en) | 2005-06-01 |
| US7846695B2 (en) | 2010-12-07 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4918210B2 (ja) | ポリヌクレオチドの合成方法 | |
| JP4726381B2 (ja) | 2本鎖核酸を鋳型とする核酸の増幅方法 | |
| JP5232933B2 (ja) | 変異および/または多型の検出方法 | |
| EP1231281B1 (en) | Method of detecting variation or polymorphism | |
| JP4139424B2 (ja) | 核酸の合成方法 | |
| JPWO2001034838A1 (ja) | 変異および/または多型の検出方法 | |
| JPWO2001077317A1 (ja) | 2本鎖核酸を鋳型とする核酸の増幅方法 | |
| JPWO2000028082A1 (ja) | 核酸の合成方法 | |
| JP2002345499A (ja) | 核酸配列を検出する方法及びその方法に使用するキット | |
| JP3974441B2 (ja) | 核酸の合成方法 | |
| WO2002090538A1 (en) | Method of synthesizing nucleic acid | |
| JP2003159100A (ja) | 改良された遺伝子の変異検出方法 | |
| JP2005318884A (ja) | 核酸の増幅方法 | |
| HK1055445B (en) | Method of synthesizing polynucleotide | |
| HK1097002A1 (zh) | 检测突变和/或多态性的方法 | |
| HK1097002B (en) | Method for detecting mutations and/or polymorphisms | |
| JP2006055081A (ja) | 遺伝子多型のタイピング方法 | |
| HK1054967B (en) | Method of amplifying nucleic acid by using double-stranded nucleic acid as template |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| RD03 | Notification of appointment of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7423 Effective date: 20061107 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20061114 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20061114 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20061107 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20080917 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20081024 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20110517 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20110719 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20110809 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20110823 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20111101 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20111228 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20120124 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20120130 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20150203 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 Ref document number: 4918210 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| EXPY | Cancellation because of completion of term |