JP4209471B2 - プラズモン共鳴粒子、方法、および装置 - Google Patents
プラズモン共鳴粒子、方法、および装置 Download PDFInfo
- Publication number
- JP4209471B2 JP4209471B2 JP53677498A JP53677498A JP4209471B2 JP 4209471 B2 JP4209471 B2 JP 4209471B2 JP 53677498 A JP53677498 A JP 53677498A JP 53677498 A JP53677498 A JP 53677498A JP 4209471 B2 JP4209471 B2 JP 4209471B2
- Authority
- JP
- Japan
- Prior art keywords
- field
- light
- spectral
- prp
- pres
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Lifetime
Links
Images
Classifications
-
- G—PHYSICS
- G06—COMPUTING; CALCULATING OR COUNTING
- G06K—GRAPHICAL DATA READING; PRESENTATION OF DATA; RECORD CARRIERS; HANDLING RECORD CARRIERS
- G06K19/00—Record carriers for use with machines and with at least a part designed to carry digital markings
- G06K19/06—Record carriers for use with machines and with at least a part designed to carry digital markings characterised by the kind of the digital marking, e.g. shape, nature, code
- G06K19/06009—Record carriers for use with machines and with at least a part designed to carry digital markings characterised by the kind of the digital marking, e.g. shape, nature, code with optically detectable marking
- G06K19/06046—Constructional details
- G06K19/06084—Constructional details the marking being based on nanoparticles or microbeads
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B82—NANOTECHNOLOGY
- B82Y—SPECIFIC USES OR APPLICATIONS OF NANOSTRUCTURES; MEASUREMENT OR ANALYSIS OF NANOSTRUCTURES; MANUFACTURE OR TREATMENT OF NANOSTRUCTURES
- B82Y30/00—Nanotechnology for materials or surface science, e.g. nanocomposites
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6813—Hybridisation assays
- C12Q1/6816—Hybridisation assays characterised by the detection means
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6813—Hybridisation assays
- C12Q1/6816—Hybridisation assays characterised by the detection means
- C12Q1/6825—Nucleic acid detection involving sensors
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/17—Systems in which incident light is modified in accordance with the properties of the material investigated
- G01N21/55—Specular reflectivity
- G01N21/552—Attenuated total reflection
- G01N21/553—Attenuated total reflection and using surface plasmons
- G01N21/554—Attenuated total reflection and using surface plasmons detecting the surface plasmon resonance of nanostructured metals, e.g. localised surface plasmon resonance
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/62—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light
- G01N21/63—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light optically excited
- G01N21/64—Fluorescence; Phosphorescence
- G01N21/645—Specially adapted constructive features of fluorimeters
- G01N21/648—Specially adapted constructive features of fluorimeters using evanescent coupling or surface plasmon coupling for the excitation of fluorescence
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/62—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light
- G01N21/63—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light optically excited
- G01N21/65—Raman scattering
- G01N21/658—Raman scattering enhancement Raman, e.g. surface plasmons
-
- G—PHYSICS
- G06—COMPUTING; CALCULATING OR COUNTING
- G06K—GRAPHICAL DATA READING; PRESENTATION OF DATA; RECORD CARRIERS; HANDLING RECORD CARRIERS
- G06K7/00—Methods or arrangements for sensing record carriers, e.g. for reading patterns
- G06K7/10—Methods or arrangements for sensing record carriers, e.g. for reading patterns by electromagnetic radiation, e.g. optical sensing; by corpuscular radiation
- G06K7/14—Methods or arrangements for sensing record carriers, e.g. for reading patterns by electromagnetic radiation, e.g. optical sensing; by corpuscular radiation using light without selection of wavelength, e.g. sensing reflected white light
- G06K7/1404—Methods for optical code recognition
- G06K7/1408—Methods for optical code recognition the method being specifically adapted for the type of code
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2219/00—Chemical, physical or physico-chemical processes in general; Their relevant apparatus
- B01J2219/00274—Sequential or parallel reactions; Apparatus and devices for combinatorial chemistry or for making arrays; Chemical library technology
- B01J2219/00277—Apparatus
- B01J2219/0054—Means for coding or tagging the apparatus or the reagents
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2219/00—Chemical, physical or physico-chemical processes in general; Their relevant apparatus
- B01J2219/00274—Sequential or parallel reactions; Apparatus and devices for combinatorial chemistry or for making arrays; Chemical library technology
- B01J2219/00583—Features relative to the processes being carried out
- B01J2219/00603—Making arrays on substantially continuous surfaces
- B01J2219/00646—Making arrays on substantially continuous surfaces the compounds being bound to beads immobilised on the solid supports
- B01J2219/00648—Making arrays on substantially continuous surfaces the compounds being bound to beads immobilised on the solid supports by the use of solid beads
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2219/00—Chemical, physical or physico-chemical processes in general; Their relevant apparatus
- B01J2219/00274—Sequential or parallel reactions; Apparatus and devices for combinatorial chemistry or for making arrays; Chemical library technology
- B01J2219/00583—Features relative to the processes being carried out
- B01J2219/00603—Making arrays on substantially continuous surfaces
- B01J2219/00659—Two-dimensional arrays
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2219/00—Chemical, physical or physico-chemical processes in general; Their relevant apparatus
- B01J2219/00274—Sequential or parallel reactions; Apparatus and devices for combinatorial chemistry or for making arrays; Chemical library technology
- B01J2219/0068—Means for controlling the apparatus of the process
- B01J2219/00702—Processes involving means for analysing and characterising the products
- B01J2219/00707—Processes involving means for analysing and characterising the products separated from the reactor apparatus
-
- C—CHEMISTRY; METALLURGY
- C40—COMBINATORIAL TECHNOLOGY
- C40B—COMBINATORIAL CHEMISTRY; LIBRARIES, e.g. CHEMICAL LIBRARIES
- C40B70/00—Tags or labels specially adapted for combinatorial chemistry or libraries, e.g. fluorescent tags or bar codes
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10S—TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10S436/00—Chemistry: analytical and immunological testing
- Y10S436/805—Optical property
Landscapes
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Physics & Mathematics (AREA)
- Analytical Chemistry (AREA)
- Organic Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- General Physics & Mathematics (AREA)
- Immunology (AREA)
- Biochemistry (AREA)
- Wood Science & Technology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Zoology (AREA)
- Nanotechnology (AREA)
- Pathology (AREA)
- Molecular Biology (AREA)
- General Engineering & Computer Science (AREA)
- Biotechnology (AREA)
- Microbiology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Biophysics (AREA)
- Genetics & Genomics (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Theoretical Computer Science (AREA)
- Condensed Matter Physics & Semiconductors (AREA)
- Composite Materials (AREA)
- Materials Engineering (AREA)
- Crystallography & Structural Chemistry (AREA)
- Computer Vision & Pattern Recognition (AREA)
- Toxicology (AREA)
- Artificial Intelligence (AREA)
- Electromagnetism (AREA)
- Investigating, Analyzing Materials By Fluorescence Or Luminescence (AREA)
- Investigating Or Analysing Materials By Optical Means (AREA)
- Physical Or Chemical Processes And Apparatus (AREA)
- Crystals, And After-Treatments Of Crystals (AREA)
- Gyroscopes (AREA)
- Adjustment Of Camera Lenses (AREA)
- Electrochromic Elements, Electrophoresis, Or Variable Reflection Or Absorption Elements (AREA)
Description
本発明は、プラズモン共鳴実体(PRE)あるいはプラズモン共鳴粒子、PREを含む場を審問する方法、およびこの方法を行うための装置、ならびにPREの種々の適用に関する。
発明の背景
標的についての情報のために標的を審問する、多くの重要な商業的かつ科学的な適用がある。例えば、分析物診断の試験および方法の目的は、分析物(標的)の存在および/または量を検出することである。標的分析物は、分析物と、(i)分析物に特異的に結合し得るおよび(ii)適切な検出道具を用いて検出可能である検出可能なレポーターとを反応することによって検出され得る。レポーターは、例えば、着色分子もしくは蛍光分子、またはコロイド金属、またはレポーター(例えば、その検出のために特別なフィルムもしくはシンチレーション設備を必要とする放射性標識)であり得る。
いくつかの診断的適用において、標的分析物上の近位に位置される2つのプローブ間の相互作用によって明らかであるように、標的分析物における近接関係を検出することが望ましい。これは、いわゆる同種アッセイの基礎を形成し、ここでは、分析物の存在は、2つの異なるプローブが分析物上の密接して配置された部位において集められる場合に観察される、検出可能なプローブの近位効果によって決定される。例として、2つの蛍光分子は、集められる場合、検出可能な蛍光クエンチングまたは非放射性エネルギー伝導効果を示し得、これは、励起ピークと発光ピークとの間のストークス半径をシフトするために作用する。
化学的、生化学的、または生物学的な標的は、多様な化学的および分光写真的な方法によって、化学構造、特定の化学基の存在、または化学基の環境を決定するために、審問され得る。これらの方法の中で注目すべき物は、化学構造および化学基環境を決定するための磁気共鳴法、特定の化学基を検出するための分光法(例えば、UV、IR、Raman、ORD、およびCD分光法)、ならびにフラグメント分子量分析によって構造を決定するための質量分析法である。
標的サンプルの表面化学分析は、表面を高エネルギー粒子(例えば、電子)で衝撃し、そして表面から放出される原子のエネルギーを検出することによって行われ得る。X線電子分光法(ESCA)は、このようなアプローチの例である。
しばしば、標的における空間的および/または距離的関係を確立することが所望され、一般に、顕微鏡による審問が必要とされる。光学顕微鏡は、単純さという利点、サンプル調製の容易さ、およびサンプルが「湿潤」条件において試験され得るという特性を有する。その不利益は、比較的低い分解能力であり、照射供給源(400〜650nmの範囲)の波長に正比例し、そしてレンズシステムの開口数(良くて、約1.4)に反比例し、数百nmに分解能を制限する。
高エネルギービーム顕微鏡(例えば、透過型電子顕微鏡(TEM)および走査型電子顕微鏡(SEM))は、低いnm範囲に低下した分解能を達成し得るが、標的サンプルの高減圧環境を必要とし、生物学的サンプルを用いる適用を制限する。原子間力顕微鏡(AFM)は、低いnm範囲における分解能をまた伴って、標的サンプルの表面特徴を審問するために有用である。この方法は、表面効果に限られている。
高エネルギー発光の部位を検出および/または局在化するためのX線撮影法およびシンチグラフィー法はまた、広範囲に使用されている。これらの方法は、極めて感度が高い傾向があり、非常に少数の高エネルギー発光事象を検出し得るが、比較的高コスト、および標的の空間情報が所望される場合、乏しい分解能を欠点としてもつ。
現在利用可能な方法の多様性にもかかわらず、現在の方法では困難であるかまたは不可能である商業的および科学的な目的の多くの標的審問課題がある。これらの中には以下がある:
1.単一の(またはわずか数個の)分子事象(例えば、標的における1つもしくは数個の結合部位、または1つもしくは数個の酵素的部位の存在)を検出すること。この能力は、新規な診断的適用(例えば、特異的な細胞内事象の存在または非存在に関する)を開発し、そして信頼できるアッセイのために必要とされるサンプル材料の量を減少させ、そしてアッセイの小型化を許容する。
2.天然の水和化状態において、生物学的標的中の亜波長(sub-wavelength)距離関係を分離すること。上記のように、高エネルギービーム顕微鏡による亜波長分離は、サンプル標的が乾燥された状態にあることを必要とし、天然の細胞プロセスの観察(細胞成分の亜波長移動を含む)を妨げ、そして使用者に、観察の間、サンプルを摂動(perturb)させる。
3.生物学的標的における選択される標的部位の直接的な空間マッピング(例えば、染色体マッピングの目的のための染色体における選択される配列の直接的なマッピング)。現在、このタイプの情報は、実際的でないか、または染色体マッピングの場合において、高分解能および遺伝子配列の正確な位置決めでは可能ではないかのいずれかである。
4.マイクロコード化された情報の光学的読み出し。個々のレポーター基の独特のパターンを検出する能力は、法医学、情報保存、計測学、およびセキュリティー同定マイクロコードにおいて重要な適用を有する。
それゆえ、先行技術の方法によって得ることが非実際的または不可能である上述で概説した情報のタイプについて、場(field)を審問するための方法および装置を提供することが所望される。
本発明の方法を、種々の診断的適用に適用して、改善された感度、空間的および距離的な情報、サンプル調製の容易さ、および審問され得る標的サンプルのタイプにおける柔軟性を達成することがまた、所望される。
発明の要旨
1つの局面において、本発明は、分布された複数のPREを有する場を審問する方法を包含する。この方法は、光学的な光源で場を照射する工程、および場における個々のPREおよび他の光散乱実体についてスペクトル発光特性を検出する工程を包含する。この情報から、場において選択されたスペクトルサインを有するPREを他の光散乱実体から識別するための基準として、場に存在する個々のPREおよび他の光散乱実体の位置および発光スペクトル特性の値のコンピューター画像が構築されて、場についての情報を提供する。
照射する工程は、異なる周波数帯で行われ得、場における個々のPREおよび他の光散乱実体のスペクトル発光特性が、このような各帯で検出される。
あるいは、照射する工程は、持続時間が変化する光の複数の狭帯域パルスに、場を曝露し、持続時間の変化によって生成される発光強度における変化を検出する工程を包含し得る。
別の実施態様において、場は、好ましくは少なくともいくつかの非球状のPREを含む場合、照射する工程は、入射の異なる方向および/または異なる角度で、偏光に場を曝露する工程を包含し得る。検出する工程は、入射光の偏光方向または入射の角度の関数として、スペクトル発光特性の値の変化を検出する工程を包含する。
検出工程は、複数の規定されたスペクトル帯で、場における個々のPREおよび他の光散乱実体のスペクトル発光特性の値を同時に検出する工程を包含し得る。あるいは、場における個々のPREおよび他の光散乱実体のスペクトル発光特性値は、複数の規定されたスペクトルバンドで、連続的に検出され得る。
PREは、場における核形成中心を金属増強することによって、予め形成されたPREを場における標的に添加することによって、または場における標的部位でPREを(例えば、写真平板法によって)作製することによって、場において形成され得るか、または場に添加され得る。
この方法は、場における全ての他の光散乱実体から、選択されるスペクトルサインを有するPREを識別するために実施され得る。識別のための基準として、検出されるスペクトル発光特性は、代表的に、ピーク位置、ピーク強度、またはスペクトル発光曲線の半強度でのピーク幅、画像面におけるピークの半値幅、および/または入射応答の偏光または角度である。他の発光スペクトル特性(例えば、パルスか化光線照射に対する応答)がまた、意図される。
同じスペクトル特性が、単独または組合せてのいずれかで、(i)非PRE光散乱実体からPREを、(ii)他方の選択されるタイプのPREから、一方の選択されるタイプのPREを、および(iii)非相互作用するPRE(代表的に、PRP)から、近位効果を介して、相互作用するPREを識別するために有用である。
別の実施態様において、PREは、表面局在化蛍光分子実体またはRaman活性分子実体(例えば、Raman活性分子)を有し、そして検出する工程は、1つ以上の上記実体から、プラズモン共鳴誘導性の蛍光発光またはRaman分光学発光を検出する工程を包含する。
この方法は、(i)場における選択されるタイプのPREの総数、(ii)場における選択されるスペクトル特性の選択される値の範囲を有するPREの空間的パターン、(iii)2つの近接するPRE、特にRayleigh距離未満の距離によって分離されるPRE間の距離測定、(iv)場の環境の変化(例えば、誘電率、これは、プラズモン共鳴特性の値に影響する)、または(v)場におけるPREの移動についての情報を得るために行われ得る。
別の局面において、本発明は、例えば、場を審問するために上述の方法を実施するにおいて、分散された複数のPREを有する場を審問するための装置を含む。この装置は、場を照射するための光学的な光源、および場が光源によって照射される場合、場における個々のPREおよび他の光散乱実体のスペクトル発光特性の値を検出するための光学検出器を備える。
また、この装置において含まれるものは、検出器から受容されるシグナルから、場に存在する個々のPREおよびこのような他の光散乱実体の位置および発光スペクトル特性の値のコンピューター画像を構築するために、検出器に作動可能に連結される画像処理器、ならびにコンピューター画像において他の光散乱実体から、選択されるスペクトルサイン(すなわち、選択されるスペクトル発光特性の選択される値の範囲)を有するPREを識別するための識別器である。装置は、選択されるPREについての情報に基づいて、場についての情報を提示する(または保存する)ために構築される。
1つの好ましい光源は、場上の光を検出するための明視野/暗視野レンズである。あるいは、照射源は、明視野レンズ、暗視野レンズ、偏光照射源を生成するための偏光子(例えば、平面偏光源)、TIR、パルス化光線、暗視野/明視野レンズを介する半銀鏡(half-silverd mirror)によって光が反射される落射照明システム、および暗視野集光レンズであり得る。光源は、異なる励起波長を有する光で場を分離するための手段を備え得る。
光学検出器は、RPEから発光される光をスペクトル的に分離するための構造を備え得る。この実施態様における検出器は、それぞれの複数の異なる発光波長で、場に存在する個々のPREおよびこのような他の光散乱実体の位置および発光スペクトル特性の値のコンピューター画像を形成するために作動する。
光学検出器は、光ファイバーの二次元配列、配列からの光の線(line)供給源として作用するようにアラインされる場合、光ファイバーの出力に応答するための格子またはプリズム、および光の線供給源における各ファイバーからの広げられたスペクトル光に応答するための二次元検出器配列を備え得る。
画像処理器は、場の位置、ならびにピーク位置、ピーク強度、またはスペクトル発光曲線の半強度でのピーク幅、画像面におけるピークの半値幅、および/または入射応答の偏光もしくは角度の関連する値の画像を構築するために作動する。
別の実施態様において、PREが表面会合された蛍光分子実体またはRaman活性分子実体を有する場合、画像処理器は、プラズモン共鳴誘導性の蛍光、またはプラズモン誘導性のRomanスペクトル発光におけるRamanスペクトル特徴の場の位置おおよび蛍光ピークの画像を構築するために作動する。
識別器は、場における全ての他の光散乱実体から、選択されるタイプのPREを、非PREサブ波長光散乱粒子からのPREと(以下を含む:(i)非PRE光散乱実体からPREを、(ii)他方の選択されるタイプのPREから、一方の選択されるタイプのPREを、そして(iii)非相互作用PRE(代表的に、PRP)から近位効果を介して相互作用するPREを)識別するために作動し得る。
装置によって提示される情報は、(i)場における選択されるタイプのPREの総数、(ii)場における選択されるスペクトル特性を有するPREの空間的パターン、(iii)2つの近接するPRE、特にRayleigh距離未満の距離によって分離されるPRE間の距離測定、(iv)場の環境の変化(例えば、誘電率、これは、プラズモン共鳴特性に影響する)、または(v)場におけるPREの移動についての情報に関連し得る。
別の局面において、本発明は、1つ以上のプラズモン共鳴粒子(PRP)を有するPRPの組成物を含む。組成物は、以下:(a)PRPは、100nm未満の半分の高さ(halfheight)での幅を有する;(b)単一の集団におけるPRPは、全て、40nm以内の規定された波長にある;(c)(a)の規定を満たす組成物中の少なくとも80%のPRPは、1つ以上の集団中にあり、そして>700nm、400〜700nm、<400nmの単一の範囲におけるスペクトル発光波長を有し;および(d)各集団は、組成物中の任意の他の集団と、PRPの数において、多くとも30%の重複を有することによって、特徴付けられる。組成物は、上述の標的審問方法を実施するにおいて、および/または上述の標的審問装置と組合せて、使用され得る。
1つの実施態様において、組成物中の少なくとも80%のPRPが、1つ以上の集団にあり、そして400〜700nmの波長範囲においてスペクトル発光波長を有する。また、この実施態様において、粒子は、固体銀粒子、金コアを有する銀粒子、または誘電性コアおよび少なくとも約5nmの外側の銀シェルを有する粒子から形成される組成を有する。
種々の診断的適用で特に使用するための、1つの一般的な実施態様において、粒子は、それらの表面で、(i)標的上のリガンド結合部位に結合するために適合された表面付着リガンドであって、ここでリガンド/リガンド結合部位は、結合体結合対である、リガンド、(ii)蛍光分子、(iii)Raman-活性分子実体、および(iv)非特異的結合を防止するためのブロッキング試薬、(v)PRPへの共有結合カップリングのための官能基でのコーティング、または(vi)(i)〜(v)の組合せを局在化する。
局在化されたリガンドは、結合対(例えば、抗原/抗体、ホルモン/レセプター、薬物/レセプター、エフェクター/レセプター、酵素/基質、脂質/脂質結合剤、および相補的核酸鎖)のうちの1つであり得る。
組成物はまた、第1および第2の異なる表面局在化分子または実体を有する、第1および第2のPRPの集団を有し得る。第1および第2のリガンド結合部位を有する標的を同定するにおける使用について、第1および第2の表面結合分子は、それぞれ、第1および第2のリガンド結合部位に結合するに効果的である第1および第2のリガンドである。例として、第1および第2の表面局在化分子は、標的ポリヌクレオチドの第1および第2の近位の配列領域に相補的である配列を有するオリゴヌクレオチドである。別の例として、第1および第2の表面局在化実体は、異なるRamanスペクトル特性を有するRaman活性分子実体であり得る。
組成物は、PRPの第1および第2の集団を含み得、それぞれは、異なる形状を有し、そのうちの少なくとも1つは、球状または四面体である。
さらに別の局面において、本発明は、目的の分子特性を有する標的の存在、またはそれについての情報を検出するにおいて使用するための診断方法を包含する。この方法は、表面局在化分子を有する1つ以上のPRE(好ましくは、PRP)と、標的とを接触して、分子の特徴と局在化された分子との間の相互作用を生成する工程、光学的な光源で標的を照射する工程、および標的とのこのような相互作用後の、1つ以上のPRPのプラズモン共鳴スペクトル発光特性を観察することによって、標的の存在またはそれについての情報を決定する工程を包含する。診断方法は、例えば、上述の標的審問法によって、上記の標的審問装置を使用して、行われ得る。
一般的な実施態様において、標的は、リガンド結合部位を含み、そして表面局在化分子は、標的とリガンド/リガンド結合複合体を形成し得るリガンドである。結合相互作用は、複合体のプラズモン共鳴スペクトル発光特性を検出することによって検出される。表面局在化リガンドは、例えば、ポリヌクレオチド、オリゴヌクレオチド、抗原、抗体、レセプター、ホルモン、酵素、または薬物化合物であり得る。
方法の固相形態において、複合体を検出する前に、標的は、洗浄されて、リガンド/リガンド相互作用を介して標的に結合されないPRPを除去する。
方法の同次相において、標的とPREとの相互作用は、非相互作用PREのプラズモン共鳴スペクトル発光特性から区別可能であるプラズモン共鳴スペクトル発光特性を生成するか、または回折中心を分離するかのいずれかに効果的であり、ここでは2つのPREは、異なるピーク波長を有する。これらの特徴のうちの1つを検出することによって、診断的相互作用の存在が決定され得る。
1つの同次相の実施態様において、PREは、表面局在化蛍光レポーター分子を含み、そしてPREと標的との、またはPREと標的での別のPREとの相互作用は、PREにおける蛍光分子のプラズモン共鳴誘導性のスペクトル発光特性を検出可能に変化させるのに効果的である。
別の実施態様において、PREは、表面局在化Raman活性分子実体を含み、そしてPREと標的との、またはPREと標的での別のPREとの相互作用は、PREにおけるRaman活性分子実体のプラズモン共鳴誘導性のスペクトル発光特性を検出可能に変化させるのに効果的である。
さらに別の実施態様において、標的は、2つ以上の近位におかれたリガンド結合部位を有し、そして形成する複合体は、標的に対する結合の非存在下のPREのスペクトル発光サインとは異なるスペクトル発光サイン(例えば、複合体のスペクトル発光曲線における変化)を有する少なくとも2つの近位に置かれたPREを含み、ここで2つのPREは、実質的に同じピーク波長を有する。あるいは、2つのPREが異なるピーク波長を有する場合、個々のPREは、2つの異なる波長で審問され得、そしてPRE間の距離は、画像面における2つの回折パターンの中心間の距離によって決定される。この実施態様は、例えば、第1および第2のリガンド結合部位に結合するために、それぞれ、第1および第2の表面局在化リガンドを有するPREの第1および第2の集団と、標的とを反応することによって実施され得る。
標的の空間画像を形成するにおける使用について、標的は、複数のリガンド結合部位を有する場合、標的とPREとの接触は、複数の部位での結合を生成する。検出する工程は、標的へのPRE付着の部位の空間画像を構築する工程を包含し、これは標的におけるリガンド結合部位の相対的な間隔の指標である。
1つの適用には、ポリヌクレオチドにおける密接におかれた領域のマッピングが挙げられ、ここで検出する工程は、PREの画像面においてPREの回折パターンの中心間の間隔を観察する工程を包含する。
別の適用には、例えば、異なる相補的な表面局在化オリゴヌクレオチドを有するPREを、伸長された条件を伴う、標的ポリヌクレオチドに結合することによる、遺伝子マッピングを包含する。
別の実施態様において、標的配列変異を検出するにおいて使用するために、またはハイブリダイゼーションによって配列決定するために、標的は、異なる配列のオリゴヌクレオチドまたはポリヌクレオチドの配列である。この配列は、PERの表面局在化ポリヌクレオチドが、標的配列オリゴヌクレオチドまたはポリヌクレオチドとハイブリダイズすることを許容する条件下で、1つ以上の表面局在化試験ポリヌクレオチドを有する1つ以上のPREと接触される。標的を洗浄して未結合のPREを除去した後、配列の各領域でPREのスペクトル発光特性が検出され、配列に対するポリヌクレオチド結合のパターンが決定される。
別の実施態様において、標的は、電気泳動ゲルにおいて分離されたバンドとして示されるポリヌクレオチドであり、そして接触する工程は、ハイブリダイゼーション条件下、PREにゲルの表面を曝露することによって行われる。この方法は、DNAバンドのトランスファー工程を排除することによって、サザンハイブリダイゼーション法を単純化する。
この方法の別の一般的な実施態様において、目的の分子特徴は、分子鎖における2つの原子間の結合を破壊するために触媒的に機能する分子である。この方法におけるPRE試薬は、上記鎖によって連結されるPREの対であり、連結されたPREは、個々の(すなわち分離した)PREのスペクトル発光スペクトルとは異なるスペクトル発光スペクトルを有し得る。接触する工程は、分子鎖を切断するに効果的な条件下で行われる。切断剤の存在は、連結されたPREスペクトル発光サインの消失または個々のPREスペクトル発光特性の出現、または2つのPRE間の検出される距離の変化によって検出される。
別の局面において、本発明は、以下、(a)PRPは、100nm未満の半分の高さでの幅を有する;(b)(a)の基準を満たす組成物中の少なくとも80%のPRPが、1つ以上の集団中にあり、そして>700nm、400〜700nm、または<400nmの単一の範囲におけるスペクトル発光波長を有し;および(c)表面局在化リガンドは、標的上のリガンド結合部位に結合するように適合され、ここでリガンド/リガンド結合部位は結合体結合対、(ii)蛍光分子、または(iii)Raman活性分子実体であることによって、特徴付けられるプラズモン共鳴粒子(PRP)の組成物を含む。
本発明はさらに、発明の詳細な説明の第VI節において考察される多様なPRE組成物および方法を含む。
本発明のこれらのおよび他の目的および特徴は、添付の図面と組合せて、以下の詳細な説明が読まれる場合に、より十分に明らかになる。
【図面の簡単な説明】
図1は、異なるピーク散乱波長を有する2つの光学的に観察可能なプラズモン共鳴実体の相対的な散乱強度のグラフである。
図2は、同様なピーク散乱波長を有する4つの光学的に観察可能なプラズモン共鳴実体の相対的な散乱強度のグラフである。
図3は、プラズモン共鳴実体の観察に適切な暗視野顕微鏡検出システムの1つの実施態様の模式的な説明である。
図4は、プラズモン共鳴実体を観察するために使用され得る固形浸漬レンズに対する液体アナログの説明である。
図5は、プラズモン共鳴実体の観察において使用するのに適切な全体の内部反射型サンプル状態の説明である。
図6は、PRE画像化に適切な反射明視野/暗視野レンズの説明である。
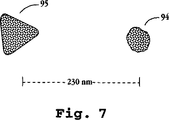
図7は、2つのプラズモン共鳴粒子の透過型電子顕微鏡画像の再現である。
図8は、図7に示されるプラズモン共鳴粒子によって発光される2つの異なる帯域幅での、画像面における位置の関数としての、光強度のグラフである。
図9は、プラズモン共鳴標識を用いて行われたアッセイの結果を示すグラフである。
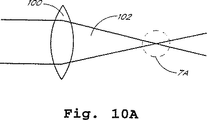
図10Aは、プラズモン共鳴実体で測定可能な強度プロフィール特性を有する、焦点を合わせられた光線を説明する。
図10Bは、図10Aの焦点を合わせられた光線内でのプラズモン共鳴実体の配置を示す。
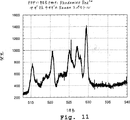
図11は、Raman活性PREからのRamanサインである。
図12は、そのリアノジンレセプターは、抗リアノジンPRPで標識されたニワトリ骨格筋切片である。
図13は、特定の遺伝子が、PRPによって標識されたDrosophila多糸性染色体である。
好ましい実施態様の詳細な説明
定義
以下の用語は、他で示さない限り、以下に与えられる定義を有する:
「プラズモン共鳴粒子」あるいは「PRP」は、物質(例えば、球状粒子)の単一の切片またはフラグメントを意味し、これは電磁エネルギーで励起される場合、プラズモン共鳴を誘発する。プラズモン共鳴粒子は、これが、約180ナノメートル(nm)〜数ミクロンの波長を含む光学的領域において有意な散乱強度を示す場合、「光学的に観察可能」であり得る。プラズモン共鳴粒子は、これが、ヒトの眼によって検出可能である約400〜700nmの波長帯において有意な散乱強度を示す場合、「可視的に観察可能」であり得る。プラズモン共鳴は、基本的に遊離伝導電子と入射光との相互作用を介して作製される。粒子または実体は寸法(dimention)を有し、例えば、直径は、好ましくは約25〜150nm、より好ましくは約40〜100nmである。
用語「プラズモン共鳴実体」または「PRE」は、構造のプラズモン共鳴特性を示す任意の独立した構造をいうために本明細書中で使用され、プラズモン共鳴粒子(PRP)および上述で規定および記載されるようにプラズモン共鳴粒子の組合せまたは会合の両方を含む(が、それらに限定されない)。PREは、単一のPRP、または電磁エネルギーで励起される場合、プラズモン共鳴特性を表す2つ以上のPRPの集合のいずれかを含み得る。
「分布した複数のPREを有する場」は、一次元、二次元、または三次元の領域、例えば、標的または付着されるかもしくはそうでなければそこに分布したPREを有する標的の部分または領域をいい、その結果場におけるPREは、光学的な光源で照射された場合、プラズモン共鳴を示す。
「スペクトル発光特性」は、第III節において記載されるように、PREのプラズモン共鳴に関連するPREのスペクトル散乱特性をいう。本明細書中で使用されるように、「発光」は、PREに対して適用されるように、プラズモン共鳴によって生成または励起される散乱光を意味する。
スペクトル発光特性の「値」は、発光特徴の定性的または定量的値(例えば、検出されるピーク強度、ピーク波長、または最大でのピークの半値幅)である。
「選択されるスペクトルサイン」は、選択されるスペクトル発光特性の値の選択される範囲(例えば、スペクトルピーク強度値の範囲)をいう。
「発光スペクトル特性の位置および値のコンピューター画像」は、審問される場における各領域を、この領域における光散乱実体について測定される1つ以上のスペクトル発光特性値またはサインと結びつけるマトリクスをいう。画像は、保存された値のマトリクスであり得るか、または一方の次元あるいは面(例えばx-y面)における光散乱実体の位置、および別の次元(例えばz軸)における関連されるスペクトル発光値を示す実際の画像であり得る。
「リガンド」は、化学種、代表的に生化学種であり、「リガンド結合」部位または分子と、特異的な、代表的に高親和性の結合を形成し得る。リガンド/坑リガンドは、例えば、抗原/抗体、ホルモン/レセプター、薬物/レセプター、エフェクター/レセプター、酵素/基質、脂質/脂質結合剤、および相補的な核酸鎖を含み得る結合対を形成する。
「Raman活性分子実体」は、分子実体が付着されるプラズモン共鳴粒子の電場によって励起される場合、好ましくは共鳴Raman励起を介してRaman分光学的なサインを提示する分子、分子複合体、または粒子(例えば、ケイ素粒子)である。
「表面局在化」リガンドおよび他の種は、共有結合または他の分子力(例えば、静電力もしくは分散力)によってPREに付着される、またはPRE上のシェルもしくは他の表面コーティング中に包埋される分子種をいう。
II.プラズモン共鳴
本発明は、多様なタイプの情報(以下の第III〜VI節において詳述されるような、標的の存在もしくは非存在、標的の空間特徴、標的の環境、選択されるタイプの標的結合部位の数および/または空間分布、および標的における距離関係を含む)について、場を審問するために、伝導性のプラズモン共鳴粒子(PRPまたはPRE)の1つ以上の多くのスペクトル発光特性を利用する。
プラズモン共鳴実体(PRE)あるいはプラズモン共鳴粒子(PRP)の散乱入射光、および得られる散乱光は、粒子の周波数スペクトル特性を有する。この共鳴性の散乱を首尾良く予測する入射電磁波と球状粒子との相互作用を記載する一般的な理論は、20世紀初期に開発された(H.C.Van Ve Hulst,Light Scattering by Small Particles,Wyley,N.Y.,1957)。金属の範囲において、入射電磁場は、金属のほとんど遊離の伝導電子において、「プラズモン」と呼ばれる振動を含み、そしてこれらのプラズモンは、発光される電磁場を生成する。いくつかの物質について、ならびに粒子サイズ、形状、および形態の至適な選択について、散乱粒子およびその周囲の媒体の波長特性で、最大の散乱効率が存在する。いくつかの物質について、発光される光の強度は、光学顕微鏡下での観察について十分である。銀粒子は、共鳴的に散乱される光の波長が、スペクトルの可視領域内にあり得るので、この効果の最も顕著な表示物(exhibitor)である。
理論的な算定は、球状粒子の共鳴的に散乱される波長が、粒子直径が増加、および周囲の物質の誘電率が増加するにつれ、増加するかまたは「赤色シフト」されることを正確に予測する。球状粒子について、双極子共鳴は、物質に依存する波長で単一のピークを有する散乱される周波数スペクトルを生成し、粒子は、粒子の大きさ、粒子の形状、粒子の形態、および局所環境から作製される。より大きな粒子は、より長い双極子散乱ピーク波長を有し、およびより小さな粒子は、より短い双極子散乱ピーク波長を有する。散乱された光のスペクトルはまた、粒子の四極子共鳴からの寄与を含み得る。所定の形状について、共鳴粒子は、粒子の組成およびサイズに依存する特定の波長帯において優先的に散乱する。
プラズモンを担う伝導性の部位は、固体の幾何的な形状(例えば、球状、三角パラレルピペド(parallelpiped)、楕円、四面体など)を含む多くの異なる形態を取り得るか、または球状、円柱状、または他の形状のシェルを含み得る。表面に銀または金を有する類似の寸法の誘電性の球はまた、プラズモン共鳴を示すこともまた当てはまり、シェルは、少なくとも約3nm、好ましくは5nm以上の厚さを有すると想定される。
さらに、2つのプラズモン共鳴粒子間の接触または至近接触(near contact)は、粒子間の電磁カップリングを生成し、それによって接触する2つの粒子の合計に等しいサイズを有する単一の粒子にいくつかの点で類似する特性を有する実体を生成することが理解される。それゆえ、多くのプラズモン共鳴粒子の集合はまた、集合体の幾何学および性質に依存する特性を有するプラズモン共鳴を示す。
金属性粒子におけるプラズモン作製の別の特徴は、その表面に近い領域における増強された電場の生成である。この電場と隣接の物質との間の相互作用は、共鳴粒子および隣接の物質の散乱特性の両方を有意に変化させ得る。例えば、表面増強Raman分光法(SERS)は、ざらざらのまたは粒子コートされた銀フィルムにおける局在化されたプラズモン共鳴を活用し、6階数の大きさまで種々の物質のRaman散乱を増強する。この技術において、目的の物質からのRaman散乱が観察され、そしてプラズモンによって生成される局所的な場は、その散乱の強度を増強するために使用され得る。
ここで図1に言及すると、2つのPRPの相対的な散乱強度のグラフが説明され、異なるPREが、容易に検出されるスペクトル特性における差異を有し得ることを実証する。図1において示されるスペクトルは、より複雑な構造の個々のPRPまたはPREのいずれかによって生成され得たが、図1に説明される散乱される光スペクトルの供給源は、説明の目的のためにPRPに由来することが想定される。
図1において、任意の単位における散乱された光の相対的な強度が、ナノメートルの波長に対してプロットされる。2つの異なるPRPの個々のスペクトルが示される−1つ目はスペクトル3(約460nmでのピーク発光5を有する)、および2つ目はスペクトル7(約560nmでのピーク発光9を有する)。この図において、それぞれの2つのPREによって発光される光の光強度は、個々に1.0に正規化された。各スペクトルの形状は、ほぼLorentzianであり、470nmピークを有する粒子について約30nmの、および560nmピークを有する粒子について約50nmの半最大での幅を有した。上記のように、個々のPRPによって発光される光は、適切な光学顕微鏡で可視的に観察され得る。図1において説明される発光スペクトルを有する2つのPRPがそのように観察される場合、470nmでピーク5を有するPRPは青色に見え、そして560nmでピーク9を有するPRPは黄色に見える。
図2は、PREの4つの異なる集団の集団についてのスペクトル発光曲線を示し、それぞれほぼ同種の特性を有する。この図において示される4つのPREのスペクトル10、11、12、13は、約460nm〜480nmまで変化するピーク発光波長を有する。可視的に、図2において示されるスペクトルを生成するそれぞれの4つのPREは、青色に見える。しかし、4つの粒子はスペクトルピーク強度(すなわち、ピークの高さ)に基づいて、または異なるスペクトル発光曲線に基づいて、例えば、ピークの高さの半分でのピーク幅に対するピークの高さの比率を比較することによって、識別され得る。他のスペクトル発光特性は、以下に記載される。
III.場を審問するための方法および装置
1つの局面において、本発明は、その中に分散された複数のPREを有する場を審問する方法および装置に関する。本方法は、本質的に、以下:(i)場におけるPREの1つ以上のスペクトル発光特性についてデータを作製する工程、(ii)このデータから、PREの位置(場の領域)のコンピューター画像、ならびに個々のPREおよび場に存在する他の光散乱実体の、スペクトル発光特性の値を作製する工程、ならびに(iii)画像中の選択されたスペクトル特性を用いて、PREと場の中の他の光散乱粒子とを識別することにより、場(例えば、場における標的)についての情報を提供する工程、の3つの部分を有する。
A.スペクトル発光特性
本発明は、場における光散乱粒子の画像を作製するために、1つ以上のいくつかの型のスペクトル発光特性を検出することを意図する。目的のスペクトル発光特性は、単一のPRPのプラズモン共鳴スペクトル特性、非常に近接した2つ以上のPRPの相互作用に起因するスペクトル発光特性における移動、または蛍光、発光、またはPRE上に位置するラマン分子と相互作用する、増強された局部的な電場によって誘導される、蛍光もしくはラマン分光学的特性であり得る。それぞれから入手可能な、情報の特性および型の最重要性を、以下に示す。
ピーク波長は、スペクトル発光曲線のピーク波長(すなわち、最大強度を生じる波長)である。図1に示される2つのスペクトル発光曲線のピーク波長は、5および9で示され、これは上記のように470nmおよび560nmの波長の値に対応する。
ピーク波長の値は、多数の異なる方法の1つで決定され得、そのなかの7つを本明細書中に記載する。これらの方法の個々の実行は、方法のいくつかについて、本発明の装置の光源および検出器の記載において以下に議論されるように、開示された方法から理解される。これらの方法は全て、同時に複数のスペクトル曲線を測定するのに適応可能である。本方法のいくつかはまた、例えば、場の面の上の光検出エレメントをラスタリング(rastering)することによって、場における各光散乱実体のスペクトル曲線の個々の測定に適応可能である。
(i)場は、例えば、一連の狭帯域照射窓の個々で、可視光スペクトルを介して、照射波長の範囲にわたって照射される。代表的には、白色光源と場との間に置かれたフィルター円盤(wheel)は、狭帯域照射周波数を産生するために使用される。
(ii)場から発光する光は、発光された光をいくつかの狭帯域周波数中に散らすために散乱エレメント(例えば、プリズム)を介して方向付けられ、次いで、それぞれ別の検出配列に方向付けられる。例として、プリズムは、発光された光を赤、緑、および青の成分に分けるために使用され、各々は個々のCCD配列に方向付けられる。
(iii)その画像が完全に光ファイバーのコア直径に適合するように、レンズ(例えば、PREに対応する各光散乱スポットを拡大するレンズ)を介して、発光場画像を光ファイバーの密な束に入れる。次いで各ファイバーは、分散エレメントによって異なる周波数に拡がるスペクトル線に散開され、これは次いで2次元配列における検出エレメントの線によって読みとられる。従って、場の各線は2次元配列によって読みとられ、一方の配列の次元は複数の周波数の各々でのスペクトル強度に対応し、他方の次元は場の軸に沿った異なる位置に対応する。このアプローチは複数のスペクトル波長の各々での、複数のPREの同時読み取りを可能にする。
(iv)複数の狭帯光源(例えば、赤、緑、黄、および青の、3または4つの別々のレーザー線)で照射する。各レーザーは、異なる周波数(代表的には全て100Hzより下)で分断される。場から発光された光は、100フレーム/秒で読みとられ得るCCDで検出される。次いで、標準技術を含むコンピューター分析は、CCD配列における各画素に衝突する各色の光量を決定するために使用され、それによってスペクトル発光曲線が構築され得る。
(v)例えば、米国特許第5,539,517号に記載されるように、干渉計を通過した散乱光の経路を決定することにより、同様の情報が得られ得る。
(vi)入射光の波長が共鳴ピークを通過させられる場合の入射光と比較して、散乱光が180度の位相変化を受ける、ということもまたプラズモン共鳴粒子の特性である。ピーク波長において、位相差は90度である。この位相変化は検出され得、そして、90度の位相変化が観察された場合の入射波長として、ピーク散乱波長が決定され得る。
(vii)複数の規定された帯域幅でのPRE発光強度もまた、PREを種々の時間の短いパルスの入射光に曝すことによって、決定され得る。特に、増加または減少するステップ関数に近似するパルスの使用が有効である(すなわち、ほんの1もしくは2フェムト秒の迅速な立ち上がり時間および減衰時間)。PREの散乱応答は、強制振動および減衰振動の散乱応答であり、そして共鳴波長の付近では、狭帯域の励起に対するPREの応答は励起パルス長が増加するのに従って増加する。共鳴波長から離れると、狭帯域の励起に対する応答は小さく、そして比較的励起パルス長に非依存性である。PREを、特定の波長で、種々の時間のパルスに曝すこと(しかし都合の良いことに全て約500フェムト秒未満である)、および発光エネルギーが定常値に達するのにかかった時間を知ることによって、特定の波長がPRE共鳴波長にどのくらい近似しているかについての情報が提供される。いくつかのシリーズの時間変化パルスに対してPREを励起することによって、ここで各シリーズは異なるピーク波長を有し、波長に対する散乱切断面曲線が作製され得る。
銀のPREおよび金のPREのPREのサイズが増加するに従って、一般的に、ピーク波長は赤の方向(より長波長側)に移動する。ピーク波長の値もまた、PREの形状に関する情報を提供し得る。球形から6角形または3角形への形状の変化は、主に赤へのピーク波長の移動を生じる。誘電シェルPRP(すなわち伝導金属中に入れられた内側の誘電性コアからなる粒子)もまた、同じ大きさの固体金属粒子よりも長いピーク波長を有する傾向がある。
ピーク強度はスペクトル発光曲線のピークの強度であり、図2におけるような絶対強度値または相対強度値として示され得、これは3未満から10より大きい範囲の異なる相対ピーク強度を有する4つのPREを示す。ピーク強度値は上のように、ピーク波長で決定されている強度を用いて、PREのスペクトル発光曲線を決定するための種々の方法の内の1つによって、決定され得る。
ピーク強度は材質、形態および形状によって変化する。特定のPREに対して、強度は焦点の枠に対して最大である。
半値幅は、スペクトル発光曲線の、半分のピーク強度での、波長単位における幅である。この値は独立したスペクトル特性として測定され得るか、またはピークスペクトル強度と組み合わせてスペクトル発光曲線を特徴付ける(例えば、ピーク強度/ピーク幅の比)ために測定され得る。
図2に示される4つの曲線は相対的に狭いピーク幅を有する2つのスペクトル(曲線10および11)、および相対的に広いピーク幅を有する2つ(12および13)を図示する。
一般的にピーク幅はPREの大きさの増加と共に増加し、そして模倣され得る様式において、PREの形状が球形形状から非球形形状へと変化するに従って変化する。
画像面における幅は画像面におけるAiryパターンにおける中央回折領域の半分の幅である。全てのPRPはサブ波長光源であり、従ってその空間画像は使用される光学システムによって規定される特性を有する近似点拡大関数である。CCDを含む光学システムを仮定して、光検出エレメントの画素配列を用いて、いくつかの画素に及び得る中央回折領域の幅は、回析画像の中心のピークから、強度がそのピーク値の半分になる画像中心位置までを(円形画像と仮定して)、放射状に測定される。
PRPはサブ波長散乱体であるので、画像面において記録されるような強度パターンの半分の幅が、散乱される光の波長に比例する。それゆえ、供給源(例えば、キセノンアーク)からの光の強度における妥当に円滑な変化について、光はピーク強度において最も強く散乱され、そして各PRPについての画像における中央回折領域の半分の強度の幅を測定することによって、ピーク波長の良好な評価が作製され得る。
以下に示されるように、このスペクトル特性は、場におけるPREの位置の正確な決定、および特に、レイリー分解距離よりも近い間隔の、異なるピーク波長の2つのPREの間の距離を決定するために有用である。画像面における回折パターンのピークの強度は、最もよい焦点を与える最大値を用いて、場に対して検出器レンズの焦点を合わせるために使用され得る。
偏光は、PREの場を照射する光の偏光の方向の関数、または偏光された光の入射角として、スペクトル特性(例えば、画像面におけるピーク波長、ピーク高、波長の半値幅、またはピーク強度の半値幅)を測定する。偏光の特性はPREの大きさよりもPREの形状に依存し、そして非球形PREは、例えば、楕円形のPREの長軸および短軸方向に1つ以上の共鳴を有し得る。後者の場合、長軸方向の照射光は赤の方に移動し、一方短軸方向の照射光は青の方に移動する。
パルスまたは時間応答は十分な強度の散乱を「汲み上げる(pump up)」ことを必要とされる照射光の光サイクルの数の測定を提供する。PREは非常に速い時間応答(ピコ秒以下)を有し、散乱光子の非常に大きなパルスが発生され得、吸収された平均の入力した力であることを制限するのみである。これらは、2つの光子プロセスまたは第2の調和振動の発生および他のより高度な命令プロセスを行うために、5と500との間のフェムト秒でパルスを受容し得る。
上記のように、パルス型または時間型照射測定は、一般に場のPREを種々の時間の入射光の短パルスに曝すことによって行われ、ピーク波長が検出される。強度対パルス時間によって測定された場合、完全な共鳴に対する時間はまた、プラズモン共鳴器として物質の純度の測定を提供する。より高い純度の物質は、ピーク波長の光のパルスにより照射された場合、より狭い幅の共鳴サイン、より高いピーク強度、および散乱の最大強度に到達までのより長い時間によって特徴付けられる。
移相は、上記の、90度の移相でのスペクトルピークを決定する章において、議論される。移相もまた、共鳴ピーク波長から離れた励起波長に対する応答についての情報を与え得る。
蛍光発光寿命は、表面局在化蛍光分子を有するPRE粒子中で観察され得る。蛍光励起は、プラズモン共鳴ピーク内の光によってPREの表面付近で発生された局所電場により、増強され得る。また、蛍光発光の光の波長がプラズモン共鳴ピーク内にある場合、蛍光発光は増強され得る。適切な条件下において、蛍光寿命はこのプロセスで測定できるまで短縮され得る。
本方法を使用して、蛍光分子の励起環境における変化(例えば、他の分子または実体との近接相互作用)を検出し得る。
表面増強化ラマン散乱(SERS)は、PREの表面付近の領域での増強された電場の発生に依存する。この電場とすぐ近傍の物質との間の相互作用は、共鳴粒子の散乱特性およびすぐ近傍の物質の散乱特性の両方を有意に変化させ得る。表面増強化ラマン散乱分光法(SERS)は、伝統的に粗面または粒子乾燥化銀フィルムに局在化したプラズモン共鳴を利用して、種々の物質のラマン散乱を6桁の大きさまで増強する。本発明に従って行われるSERSは、PRE単独で確認される。本技術において、目的の物質からのラマン散乱が観察され、そしてプラズモンによって発生される局部的な場を用いて、伝統的なSERSより数桁まで散乱の強度が増強される。ラマン活性分子がPREのスペクトル発光曲線のピーク近傍で共鳴吸収を有する場合、さらなるSERS増強は第III章において開示される本発明の方法に従って、PRE分子の混成検出可能物のラマンシグナルを作製するのに十分である。PRE共鳴ラマンスペクトルにおける変化を測定することは、ラマン分子の局部的環境において、変化(例えば、結合)を検出するのに使用され得る。
B.審問される場
本発明の方法および装置による、審問される場は、複数、すなわち、2つ以上の、標的中に分散するPREを有する標的および標的領域を含む。
標的は、光学顕微鏡によって見るのに適したいずれの標的でもあり得、生体の細胞または組織;植物または動物の部分もしくは細胞凝集体;表面局在化リガンド結合分子を有する固体表面;標的分析物の分子、粒子または細胞を含む体液サンプル;伸長した条件に配置された染色体物質のような生物学的サンプル物質;人工の単分子または2分子膜基質;コンピューターマイクロチップのような微小作製デバイス;およびチップ上のオリゴヌクレオチドまたはオリゴペプチドのマイクロアレイのような、マイクロアレイ、を含む。
PREの形成およびそこに分散されたPREを有する標的を調製するための方法は、以下に詳細に議論される。この点において、3つの一般的な場合が簡単に考察される。第1に、前もって形成されたPREが、特異的標的部位への接着のために、標的に添加される。非結合型PREまたは非特異的結合型PREを除去するために、標的は洗浄され得る。標的は、PRE結合の前または後に、所望の配置(例えば、伸長型染色体)を達成するように操作され得る。第2に、核形成部位が標的に添加され得る。標的上の選択された位置への結合後、金属エンハンサー溶液、例えば、銀溶液が、適切な大きさのPREが形成されるまで添加される。第3の場合として、写真平板法、例えば、フォトマスキングおよびフォトエッチングによって、PREが金属基板、例えば、銀基板上に形成される。
本発明に従って、標的およびPREを含む場を審問することによって、決定されることが望まれる情報の型は、以下を含む:(i)場における選択された型のPERの総数、(ii)場における選択されたスペクトル特性を有するPREの空間的パターン、(iii)2つの隣接したPRE(特にレイリー分解距離より短い距離で分離したPRE)の間の距離の測定値、(iv)プラズモン共鳴特性に影響を与える、場における環境中の変化(例えば、誘電率)、(v)場におけるPREの運動、(vi)2つのPREが連結されているかどうか、または(vii)PREに局在して付着した分子または物質の蛍光もしくはラマン発光。他の型の情報もまた意図され、そして以下の第IV章〜第VI章において考察される。
C.本発明の装置
図3は、本発明に従って構築された装置20の、簡略化した概略図である。ここでは22に示される、審問される標的は、以下に記載される装置の他のコンピューターの構成要素を含む、コンピューター28の制御下の台ステップモーター(stepper motor)装置(一般的に、26に示される)の制御下にある、x-y平面に選択的に可動性である、顕微鏡台24上に保持された基板23上に支持されている。
以下に詳述される様式において、標的は光学光光源30によって照射され、この光源は照射光、代表的に、可視範囲かつ1つ以上の選択された波長範囲での光を、標的表面に向ける。以下に詳述するように、代表的に光源は、所定の波長またはスペクトル振動数の光を生成する手段32、照射光の所望の周波数帯域を生成するためのフィルター34のような1つ以上のフィルター、および光を標的に合わせるレンズシステム36を備える。
標的からのスペクトル発光、この場合、標的から散乱された光は、レンズ56を通して光学検出器58に向けられる。光学検出器は、以下に詳述される様式で、場の照射部分における個々のPREの1つ以上のスペクトル発光特性を検出するように機能する。代表的に、検出器はCCD(電荷結合素子)配列であり、これは以下に詳述するように、配列画素に対応する光学強度の値の配列を生成し、そして記録するように作動する。
コンピューター28に含まれる画像処理装置は検出器に作動可能に連結され、各々選択された照射条件(例えば、異なる波長または偏光状態)下での、検出配列の位置の各々での光強度の値を受け取る。画像処理装置は、検出器によって測定される1つ以上のスペクトル発光特性の位置および値のコンピューター画像を構築するために機能する。代表的に、このことは、照射された場におけるポジション位置としての検出配列における各画素を処理する工程、および各画素「ポジション」に、画素によって記録された光強度の値を割り当てる工程によって行われる。画像処理装置によって生成された画像は、各画素位置について、記録された数(例えば、位置座標および関連スペクトル発光特性値、または、位置が示される(例えば、x-y平面において)実際の地図、ならびにz軸に沿う量として示される各測定スペクトル発光値)の行列であり得る。
装置の選別器42(これはまた、コンピューター28の一部を形成する)は、コンピューター画像において、選択されたスペクトルサイン(すなわち、選択された範囲の値の1つ以上の選択されたスペクトル発光特性)を有するPREを、他の光散乱実体から選別するように機能する。選別器の操作例は以下に示される。
C1.基板
上述のように、標的は顕微鏡台上に載置された基板上に支持される。適切な基板には、標準ガラススライド、カバースリップ、透明なスチレン、および透明なマイカが例として挙げられる。他の適切な透明な基板は、TEMグリッドに関連する基板(例えば、ホルムバール、炭素、および窒化ケイ素)である。これらのTEM関連基板はすべて、使用する厚さでは光学的に透明である。伝導性基板、半導体基板、および反射性基板もまた、PREの適応に適している。
本発明での使用に適切な別の基板は、PREの観察に関して目的のスペクトル波長に対して最初は不透明である可能性があり得るが、適切な流体または蒸気の適用によって、適切になり得るものである。例には、「サザン」、「ノザン」、「ウエスタン」および他のブロッティング、スポッティング、または「ディップスティック(dip stick)」試験のような診断技術での、目的の生物学的サンプルの転移に使用される場合、白色ニトロセルロース「紙」がある。一旦、目的の物質が移され、そして所望のように固定されると、PREは、予め形成された実体として適応され得るか、または以下のようにPRE核形成実体に適応されそして増強され得る。この段階での白色ニトロセルロースは、代表的にPREを視覚化し難くする有意な非反射型光散乱を示し得る。しかし、非反射型散乱の有意な減少を生じ得る適切な処理が使用される場合(例えば、アセトン蒸気でニトロセルロース基板を囲ませ、一方でPREをモニターする)基板はましてや不透明になり得、そしてPREの有効な観察が可能になる。
シリコンは多くのPRE検出適応物に対して好ましい基板である。なぜならば、非常に滑らかでかつ欠損物がないようにすることが可能であり、その結果として暗場照射下で、非反射型散乱をほとんど生じないからである。特に好ましいシリコン基板の1つの例は、非常に光沢があり、エッチングされ、および欠損のないシリコンウェハの表面であり、通常半導体の製造に使用されている。このような基板は汚染物質および表面の不完全さがほとんど全く存在せず、暗場の照射条件下でPRE散乱とすばらしいコントロールを生成する。しかし、代表的に、このようなシリコンウェハは種々のプロセシング工程の結果としてその表面上に存在するSiO2の薄い層を有することが理解される。その表面にほぼ100nm以上のSiO2を有するシリコン基板は、これまでに固形基板から観察された、最も強烈な、高度なコントラストPREスペクトルのいくつかを生成するということができる。そしてこのことは、シリコンウェハ表面上にSiO2のサブミクロン層を故意に形成させるのに有利であり得る。
迅速な酸化層の再形成を阻害する様式(例えば、HF酸中でのエッチングおよび水素での表面保護によって)で酸化層がシリコン表面から除去される場合、「点供給源」であるPREの光学画像は、明るい中心領域を有する通常のAiry環パターンではなく、円環形態で観察される。この「ドーナツ」現象は(シリコン表面と平行な)横方向の駆動電界の減衰の結果として生じている可能性が高く、これによって、良好に放射されるが、直接垂直に沿っては全く放射されないプラズモンモードを励起し得る、垂直な駆動場のみが残される。裸のシリコン基板のこの性質は、特定のPREがシリコン基板の表面に近接して結合されているかどうか、または限界分子、もしくはそれを表面から離れて配置するシステムを介して束縛されているかどうかを決定し、それによって双極子成分散乱比を変化させるのに有用であり得る。
C2.光源および検出器
続けて図3を参照すると、光源中の光発生手段32は、適切に水銀、キセノンもしくは等価なアーク;または、約20〜250ワットのクオーツ−タングステンハロゲン電球であり得、これは可視光PRE散乱については約350nm〜800nmの波長に対応する周波数帯での入射光、または低波長PRE散乱については従来のUV源、を提供する。
代表的にフィルター34は、前もって選択された狭帯域幅のフィルター一式を備え、それぞれのフィルターの手動式挿入またはコンピューターで制御された挿入を可能にする。このようなフィルターの帯域幅は、代表的には5〜10nmである。
一連の選択された帯域幅で標的を照射する他の方法には、非常に狭い帯域幅を使用し得る、全ての型のレーザーのような光源の使用が含まれる。複数の周波数源、例えば、規定された強力な「線」源のいずれかの特徴を選択するための調整(tuned)レーザー(すなわち、Arイオン)のような、周波数源もまた、意図される。あるいは、回折格子またはプリズムモノクロメーターが使用され得る。全ての光源は連続またはパルス様式のいずれかであり得るか、あるいは適切な光振幅変調装置(示さず)を入射経路に挿入して、所定の暫定様式で強度レベルを変化させ得る。サンプルに入射される光の偏光は、適切なフィルターまたは当該分野で周知の他の装置の挿入によって変更され得る。
図3の顕微鏡は上面照射(epi-illumination)システムと一致するように図示され、それによって、所望のようにフィルターされた光源由来の平行光は、半銀鏡38に衝突し、そして暗場/明場(DF/BF)レンズ40にむかって下方に反射される。この特定の型のDF/BF適用において、対物レンズを通過したであろう光線を有している入射光は、不透明サークル42によって物理的にブロックされる。これは、放射状(radially)に結合されたようなそして光線46によって示される、同心帯の光のみが通過し得るように、非常に微細なウエブ44によって妨害される。鏡38および不透明サークル42を備えるユニットは、調節可能ブロック48中に組み込まれ得、これは手動で(またはロボット的に)移動可能であり、それによって、顕微鏡をDF/BFから別の操作形態に変換させ得る。
鏡からの反射光は、次いで、屈折または反射されて(適切な円レンズエレメント50、これは入射光52の中空円錐に取付られた対物レンズに固定されている)、標的のサンプル平面の焦点へ変換させる。上記のように、このような光線の鏡反射は、入射円錐軌跡の線に沿って戻らせる。ここで、これらは最終的に吸収され、さもなければ、光学システムから除去される。
図3に図示されるこの暗場システムにおいて、光学軸とサンプルを照射する入射光線との間の角度は、光学軸と対物レンズエレメント45に受け入れられるPREによって散乱される光線(これは屈折形態のものとして図示される)との間の最大角度よりも大きい。また、示さないが、光学顕微鏡の全てに組み込まれたものは、検出器38から光線を他の部分(それによって標準両眼接眼レンズを介して可視的に画像が観察され得る)にそらし、または例えば、照射された場を撮影するために、さらに別の部分にそらす能力である。
レンズシステム54として100×の倍率および開口数(N.A.)0.8を有するNikon DF/BFレンズモデルCF Plan BD ELWDを用いることが適切であることが見出され、そして20×の倍率およびN.A.0.4を有するモデルCF Plan BD ELWDもまた、適切であることが見出された。この場合に、レンズの対物エレメントに入る光線は50%の鏡38において平行および入射とされ得、そして検出器(画像キャプチャー装置)58上の画像面に対する光線に焦点を合わせる、中継レンズ56中に入り得る(代表的に2×または5×の倍率である)。ここで検出は適切なCCDカメラシステムによって行われる。
レンズ56を備える光学システムは、好ましくは、検出器の配列に対応する領域内に視覚化される場を投影し、その結果として配列中の各画素が場の規定領域からの光を読みとるように構築される。
当該分野で公知の種々の画像キャプチャー装置が使用され得、これにはファイバー結合されたフォトダイオードアレイ、写真フィルムなどが含まれる。1つの例示的な装置は、熱電冷却型CCD配列カメラシステム、モデルCH250(これはTucson AZのPhotometricsによって製造される)である。この装置はCCDチップモデルKAF1400を利用し、1032×1037画素配列を有する。
検出装置が、場における個々のPREおよび他の光散乱実体のスペクトル発光の特徴を検出するように作用することが理解されており、場が光源により照射される場合、場におけるそれぞれの領域で、同時に配列画素を対応させる。
C3.画像処理、識別および出力
例えば、検出器がスペクトルピーク波長、ピーク強度および/またはスペクトルピークの半値幅を検出するために使用される場合、検出器は、複数の異なる照射光周波数の多くの各々で光の強度を計測し、それぞれの場の領域(regions)について同時に検出器の配列画素に対応させる。
各周波数で計測された発光(散乱)値は保存され、全スペクトルの照明の後に構築される、それぞれの領域についてのスペクトルの発光曲線を与える。これらの曲線から、ピーク波長、ピーク強度、および強度での半値幅を、それぞれの領域について計算する。同様に、画像面でのピークの半値幅を上記に記載のCCDアレイを使用して計測し得る。
検出器は、時限曝露、データ保存のための適切なファイルへの画素の読み出し、統計学的分析、および画像処理(コンピューター28の機能の1つとして)を可能にする包括的なソフトウェアおよびハードウェアとともに供給され得る。この能力は、検出器から受信されたシグナルから構築するための画像処理装置として作用し、最初にスペクトルの発光特性の値を検出し、次いでこれらの値のコンピューター画像および対応する関連する場の位置を検出する。
画像処理装置により構築された画像は、保存された点の行列(例えば、それぞれの場の位置(場における領域)に関連する値の行列および1つ以上の計測されたスペクトル特性についての値)であり得るか、または場の実際の位置のマップ(例えば、x-y平面、およびz平面での関連するスペクトル発光値)であり得る。
装置内のコンピューターはまた、コンピューター画像における他の光散乱実体由来の選択されたスペクトルのサインでPREを識別するための識別手段を提供する。この識別についての基礎は、種々のスペクトル発光特性および光散乱実体の物理的特性とのこれらの相関性の議論において上記で述べている。
従って、例えば、選択されたスペクトルのピーク波長および強度でのピークの半値幅を有するPREを識別するために、生成されたコンピューター画像は、全ての場の領域の行列ならびに関連するスペクトルピークの波長および幅の値を提供し得る。次いで識別器は、PREを含むこれらの領域を選択し、このスペクトルサインは、これら2つのスペクトルの発光値の特定の範囲を満たす。選択された特定の値に応じて、識別器は、以下を識別する多くの方法で場での光散乱実体を分類し得る:
1.場における他の全ての光散乱実体から選択されたスペクトルサインを有するPRE;
2.場での非PRE光散乱実体由来のPRE;
3.選択された型のPREについて、お互いに相互作用するもの、および相互作用しないそれらの選択されたPRE;ならびに
4.場において別の選択されたPREの型に由来するPREの1つの選択された型。
それぞれの場合では、識別の基礎は、場におけるそれぞれの光散乱実体について、ピーク位置、ピーク強度、またはスペクトル発光曲線の強度でのピークの半値幅、画像面のピークの半値幅、および入射角応答または入射偏光応答の検出された値に基づき得る。他の上記で言及されるスペクトルの特性もまた意図される。特に、PREが表面局在性の蛍光分子またはラマン活性分子実体を有する場合、検出は、それぞれ1つ以上の上記の分子または実体に由来するプラズモン共鳴誘導性蛍光発光、またはラマン分光発光を検出することであり得、そしてこれらの値は、他の光散乱実体から、このようなPREを識別する基礎として使用される。図11は、PREの表面上に有されるラマン活性分子の代表的なラマンスペクトラルを示す。
次いで、識別工程から入手される情報は、場についての情報を提供するために使用される。利用可能な様々の型の情報は以下のIV〜VI節で議論される。これらには、以下のものがある。
1.場で選択された型のPREの全数。ここで、識別工程は構築されたコンピューター画像において選択されたスペクトル発光特性の選択された範囲の値を有するPREの数を計数することを含む;
2.場での選択されたスペクトル特性の選択された範囲の値を有するPREの空間パターンの検出。ここで識別工程は、これらのスペクトル特性値を有するPREの相対位置の画像を構築することを含む;
3.2つの隣接するPREの間の距離、特に、この距離がレイリー解像距離よりも小さい距離。ここで検出工程は、1つの波長の光に場を曝露して場でのPREの回折像を入手すること、第2の波長の光に場を曝露し、場における第2のPREの回折像を入手すること、および2つの回折パターンのピーク間の距離を比較することを含む;
4.場の環境における変化の審問。ここで、識別工程は、変化(例えば、場の誘導体の変化)の前後で、場でのPREの検出されたスペクトル特性の値の比較を含む;
5.場でのPREの運動の検出。ここで検出工程は、時間の関数として、画像面でのPREの回折パターンの中心の検出を含む。
C4.他の実施態様
照射された場において100以上ものPRPの同時画像化は、先程記載されるような装置を使用して容易および効率的に達成され得る。あるいは、この装置は、上記に記載の方法に従って集束光線光源で場の各領域を連続的にスキャンすることおよび/または場での各領域からの光散乱を連続的に検出すること、固定光学により定義される小審問領域を通して顕微鏡のステージを移動させ、各領域を連続的に審問して選択されたスペクトル特性の値を検出することによって場におけるそれぞれのPREのスペクトル特性を「読みとる」ように設計され得る。
蛍光画像を検出するために、光源は所望の発蛍光団の励起スペクトルについて適切にフィルターされ、そして適切なフィルター(示さず)は、鏡38とリレーレンズ56の間の領域に配置される。このフィルターは、励起光を実質的にブロックするために選択され、そして目的の発蛍光団の発光スペクトルのバンドマッチでの光の通過を可能にする。
暗視野PRP処理、明視野染色および/または蛍光染色した試料(例えば、生物学および医学研究者ならびに臨床適用の対象である細胞および他の実体物)の多重画像を比較する能力の価値は、容易に認識され得る。
PREによって散乱した光を優先的かつ効率的に観察するための適切な手段に関連しての有効な暗視野条件を確立するように入射光を導入するための幾つかの適切な手段がある。透明な基板については、入射光は、図3で示されそして以下でより詳細に記載されるように、PREが位置する近傍の境界で、基板を通じての透過率、「対物側方表面」からの反射率、またはTIR(内部全反射)のいずれかで導入され得る。後者の場合では、TIR光の消失尾部はまた、それらが反射境界の外側に直接ある場合、このような光の場の分布が対物レンズに直接照射しない場合でさえPREを励起するために使用され得る。
非透明基板については、光は、対物に到達するような最小限の光を有し、可能な限り近い正反射をもたらすような様式で入射されなければならない。この条件を達成するためのいくつかの手段がある。1例として、入射光が1つ以上の光ファイバーを介して視野に導かれ得る。このファイバーは、光が入射角で基板に反射しないように配向され得、そしてPREを画像化するために使用される顕微鏡システムの対物レンズには入らない。市販されているDF/BF対物レンズを使用することもまた利点である。実施例はNikon Company、Long Island N.Y.により販売されているものである。このようなDF/BFレンズが使用され得る方法の例は、図3に示される。
装置でのシステムの対物レンズは、反射レンズまたは屈折レンズのいずれかとして作られ得る。特定のPRE適用、特に、光波長の関数としての対物レンズの最も正確および迅速な集束を要求する適用について、反射レンズは色収差がかなり減少され得ることから好ましくあり得る。屈折レンズは、PREにより放射される光を観察する場合、色収差を慎重に補正しても、焦点距離のそれらの周波数に依存して有意な偏差をなおも示し得る。これらのプラズモン共鳴のピーク近傍のPREが、準波長(sub-wavelength)にサイズ化された供給源についてこのように異常な明るさのものであり得るという事実は、光学成分の評価について利用されることを可能にし、それによって成分の理想的な「点源」応答からの種々の偏差を観察し得る。
対物レンズの開口数を増加させる特定のレンズ型の使用もまた意図される。PREは、球状の頂部および平坦な低い表面を有する標準的な「固体液浸」レンズを用いて画像化され得る。このような別に意図されるレンズは、切断された固体液浸レンズ下部表面とレンズ材料としてのほぼ等しい屈折率を有する基板との間に液体を有する固体液浸レンズ(SIL)の液体アナログである。
このようなレンズは、図4で図示される。レンズの底部平坦表面80は、標準的な固体液浸レンズよりも短く切断される。底部表面80と基板84との間の液体82に一致する率については、レンズの焦点面は、通常のr/n(ここで、nはレンズ材料の屈折率である)の位置にあり、これはここで、(屈折)率が一致した液体の内部にある。従って、この焦点面での液体中のPRPは、このシステムを用いて画像化され、溶液中の基板に結合していないPREにおける集束を可能にする。このようなレンズは、当業者によって市販のDF/BF顕微鏡レンズに容易に追加され得、従って、液体マトリックス中の試料表示のための改良された開口数および倍率の増加をもたらす。詳細には、この改造はPREの可視化における輝度および明度の増加をもたらす。この構成は、ユーザーが大きな開口数を維持しながら液体試料中の焦点位置を変化することを可能にし、そしてSILについて使用される場合の内部全反射に基づく照射の通常の必要性を除去する。それゆえこのシステムは、溶液中の特定のPREの挙動のモニタリングを可能にする。
他の好ましい実施態様では、暗視野の光学は、PREシグナルのシグナル/ノイズ比を最適化するために選択される。これはしばしば、最小量へ、または観察されるPRE散乱光の量に対して最小量へとバックグラウンド(非PRE)散乱光を減少させることによってコントラストを改良することを含む。例えば、通常の1”×3”のガラス製顕微鏡スライドを使用して、動作距離が長いクラスのNikon DF/BFレンズが、同じ倍率レベル(100×)において、レンズのNAが高くなるほどPREから集められる光がより散乱するという事実にも拘わらず、0.9NAレンズと比較して、0.8NAレンズを使用する観察について良好なコントラストを有することが決定された。これは、暗視野照度光の入射角が対物のNAが変化する場合変化することから、むき出しのガラス製基板の特性を反映する変化に帰させ得る。
偏光入射光もまた、基板表面からの反射光の量を減少させるために特定角度(例えば、ブルースターの角度)で使用され得る。これは対物レンズに入る非PRE散乱光の量を減少させることによりコントラストを改良する。上記に記載される楕円体PREのような非球状PREを画像化する場合、平面偏光入射光への反応もまた、異なるPREの集団を識別するために使用され得る。
別の実施態様では、検出器に到達する底部表面から散乱する光量を減少させるために十分に厚い透明基板を使用する。粒子が薄いガラス基板の底部表面に存在する場合、いくらかの散乱入射光が検出システムに再び入りそしてバックグラウンドを増加させる。基板の厚さを増加させることによって、光軸からさらなるスプリアス散乱の領域を置換し、それによって検出器に入る非PRE散乱光の量を減少させる。
内部全反射(TIR)はまた、下部からの透明基板におけるPREを照射するために使用され得る。このような光の消失尾部は、その境界の近傍に位置するPREを励起するために有効に使用され得る。内部に全反射する光を用いてPREを励起するための幾つかの方法(例えば、その寸法および内部コアおよび外部層の屈折率がそれに配置されたPREを励起させるためにファイバーの外側表面で充分にする場が不在するように選択される光ファイバーを用いる)がある。PREから放射された光は、ファイバーに戻され得、標準的方法により観察され得る反射光源を形成する。
図5で図示される別の実施態様では、Doveプリズム70は側面から照射される。標準ガラススライド72は、適切な(屈折)率に一致する油74をその間に有して、Doveプリズム70の頂部表面上の間に置かれる。入射光76はプリズム70の主表面に対して並行に導入され、そしてスライド72に向かって反射される。スライドでの入射角はより臨界角を超えるように選択され、そしてスライド72の上部表面での内部全反射をもたらす。次いで、光はDoveプリズムの反対側から出、再びプリズム70の主面に対し並行になる。消失電磁場は、スライドの上部表面に結合するPREを励起し、そして通常のプラズモン共鳴散在光を、スライドの上に配置された対物レンズに放射する。
このDoveプリズムの相対位置(geometry)は、多様な供給源(例えば、レーザー、水晶ハロゲン、アークランプなど)から光を光ファイバーまたはレンズを介してもたらして、Doveプリズムの側面に衝突するのに都合が良く、そしてフィルターは、入射光の性質をさらに制御するためにその間に都合が良いように挿入され得る。
Micro-Video of Avon、MAのDARKLIGHT(TM)光源もまた、内部全反射照明システムで使用され得るが、図5を参照して記載されるDoveプリズムの実施態様よりは一般に劣ることが見出されている。この内部全反射するスライド照射器は、ハロゲン供給源から光ファイバーへ光を運び、次いでガラススライドの端へと運ぶ。光は、スライドに拡散しながらかなりの回数の内部全反射を受け、図5の実施態様のように消失場を有するPREを励起させる。このシステムは、米国特許第5,249,077号で詳細に記載されている。さらに、PREは米国特許第3,856,398号に記載される照明を介して観察され得る。
油浸レンズシステムもまた、TIR照明と共に利用され得る。もっとも、これらのシステムにおいて内部反射による媒体の屈折率は、使用される油の屈折率より大きくなくてはならない。従って、1.7の屈折率を有するフリントガラスは、1つの好ましいプリズム物質である。
図6は、別な照明スキームとして、適切に取り囲む暗視野照明リングエレメント92を組み合わせた反射対物レンズ90を備えたDF/BF対物レンズシステムの横断面を示す。このような2つの構成要素の反射レンズの使用は、回折パターンの中央部における強度を減少させる。しかし、この使用が先行技術に記述される屈折レンズに比べ実質的に色収差もまた減少させるという事実は、多くのPREおよび観察領域中の他の非PRE散乱実体について(これらは、画像化され得、そして多くの適用において識別され、そして退けられる必要のある)、同時周波数依存性散乱データを得るための手段との組み合わせで、この2つの構成要素の反射レンズ使用を好ましい実施態様とする。
いくつかの適用において、光学顕微鏡観察の方法は、光学的にPREを画像化しそして分析する両方のこと、ならびにさらなる機器を用いて同じPREおよび関連するサンプル物質を観察すること(例えば、1つ以上の形態の電子顕微鏡観察)に適合されなけらばならない。これらの場合、暗視野光学顕微鏡観察は、電子顕微鏡観察にもまた適切な基材を用い実施されなければならない。電子は、サンプルおよび基材を通過するので、基材は非常に薄くなければならない(代表的には1μmを十分に下回る)。一般的な基材は、支持グリッド上に沈着したホルムバールおよび/または炭素を含む。バックグラウンドの散乱は、入射暗視野照明の適用領域が、グリッド「バー」の間隔内にあるように、そして/または観察下のサンプルの一部について収集(collecting)対物光の視野を制限するようアレンジすることにより、グリッド境界または「バー」より減少される。BF/DF対物および顕微鏡システムについて、1インチにつき400バーまでの間隔のグリッドおよび窒化珪素膜がとくに適切である。別の暗視野照明の形態として、グリッド基板より下部からの暗視野照明を用いた別々の光ファイバーまたはレンズ、ならびにBF対物レンズを用い上部からの散乱PRE光の観察を包含する。
IV.PRP組成物
本発明は、さらに、プラズモン共鳴粒子(PRP)の1つ以上の集団を有するPRPの懸濁物を含む。組成物は、4つの顕著な特徴を有する:(i)各集団のPRPが100nm未満のスペクトル半値幅を有する;(ii)単一の集団のPRPがすべて規定されたスペクトル発光ピーク波長の40nm以内、好ましくは20nm以内である;(iii)組成物中の少なくとも80%のPRPは1つ以上の集団にあり、>700nm、400〜700nm;および<400nmの3つ範囲のうちの1つにスペクトル発光波長を有する;および(iv)各集団は組成物中の任意の他の集団とPRPの数において、多くとも30%の重複を有する。
第1の特徴は、PRPの質を述べる(高品質発光は、散乱光の比較的狭い周波数範囲により特徴づけられる)。第2の特徴は、所定の集団内の全PRPのスペクトル発光特性の均質性を提供する。特に、所定の集団内のPRPは全て、規定された波長の40nm以内のピーク波長を有する。第3の要件は、PRPの大多数(少なくとも数量で80%)は、3つの異なる波長範囲のうちの1つにあることを提供する。第4の要件は、各集団が所定のピーク波長の40nm以内のスペクトルピーク波長の分布を有すると仮定して、集団の独自性を規定する。2つの分布曲線は、1つの集団の粒子の30%(数量)が、隣接する集団により規定される分布曲線中に属する距離より近くにあり得ない。
代表的には、組成物中のPRPは、1つ以上の集団に存在し、全て400〜700nmの波長の範囲に存在する。PRPは均質であり得(例えば、全て青粒子)、あるいは集合的に組成物中のPRPの80%を構成する1以上の集団に存在し得る(例えば、赤粒子、緑粒子および青粒子の個別の集団)。
このスペクトル範囲の粒子は、下記のとおり、固形銀粒子、金核を有する銀粒子、または誘電性の核および少なくとも5nmの外側の銀殻を有する粒子として形成され得る。
1つの一般的な実施態様において、特に種々の診断への適用での使用のために、粒子は、その表面に、(i)標的のリガンド結合部位に結合するよう適応された表面付着リガンド、(ii)蛍光分子、および(iii)ラマン活性分子実体を配置する。リガンドは結合対のメンバーの1つである。結合対としては、抗原/抗体、ホルモン/レセプター、薬物/レセプター、エフェクター/レセプター、酵素/基質、脂質/脂質結合因子、および相補核酸鎖が例として挙げられ得る。
組成物中のPRPは、異なるグループのPRPに異なる表面局在化分子を有し得る。これらの異なるグループは、異なるPRPの集団(すなわち異なるスペクトルピーク波長を有するPRP)であり得るか、あるいは均質なPRP集団においてPRPに局在し得る。
第1のおよび第2のリガンド結合部位を有する標的の同定に使用するために、異なる表面局在化分子は、異なるリガンド結合部位(例えば、共通の標的ポリヌクレオチドの異なる配列領域に結合する2つの異なる配列のオリゴヌクレオチド、または高分子標的上の異なるリガンド結合部位に結合する2つの異なるリガンド)への結合に効果的な異なるリガンドであり得る。
PRPは種々の公知の方法により形成され得る。公知の方法としては、コロイド化学、水溶性ゲル、エバポレーション/アニーリング、エンハンサーを介する核形成/成長、オートラジオグラフィー、ならびに銀ハロゲン化物および光、X線または他の入射波長の様式での電磁エネルギーを介する他の物質における光反応が挙げられる。加えて、リソグラフィー、電着、電気メッキおよび走査型トンネル顕微鏡(STM)先端によるスパッタリングが使用され得る。
PRPが、例えば、付着リガンドを表面に配置している場合、PRPは、リガンド/リガンド結合性結合対の他の半分を有する目的の標的と選択的に結合し得る。
上記のとおり、異なる規定されたピーク波長値を有するPRPの集団を産生することにはまた、利点がある。規定されたPRPの集団が、特定の結合特性と組み合わせられた場合、現在使用されている全ての標識技術より有意な利点を有する、準微視的プローブの新しいクラスが作成される。以下に記載されるPRP形成技術は、このようなプローブを作成するために使用され得る。
A.金属増強メントによるPRPの形成
PRP形成のこの方法において、核形成中心(代表的には1〜20nmのサイズ範囲の金属核形成中心)は標的位置に配置される。その後、インサイチュでのPRPの完全に伝導性の本体の発達(増強(enhancing))を行う。いくつかの適用において、空間的にあらかじめ特定した位置は、核形成中心の配置のために指定される。このことは、位置が未知である特定の物質または特徴についてマトリックスを探索するために核形成中心が用いられる他の適用と、対照的である。予め特定した配置は、下記にさらに記述するような計測学および/または器械類への適用において有利であり得る。例えば、単一のPRPを、光ファイバーの末端または走査型顕微鏡先端に配置することが望まれ得る。特定の幾何学的配置において、PRPの所定のパターンを作成することもまた、望まれ得る。
制御されたスペクトル特性を伴うPRPの作成が頻繁に望まれるので、モニターしながら増強は有利に行われ得、いくらかのあらかじめ規定したスペクトル特性を有するPRPが形成される場合にプロセスを止める。これは、光の影響を受けない増強化学が用いられる場合、特に便利である。定期的に増強プロセスを終結し、形成された実体の特性を観察し、そして1つ以上のスペクトル特性(例えば、色)が、例えば所望の範囲内にない場合、増強プロセスを再度開始することによりPR形成をモニターすることもまた、可能である。
核形成中心は、代表的に、直径1〜10nmの金粒子であり、この核形成部位をPRPサイズにまで増強するのに用いられる金属は銀である。しかし、例えば、プラチナ、ニッケル、およびパラジウム、ならびにポリヌクレオチド分子のような高分子を含む他のエレメントもまた、続いての増強プロセスのための核形成中心として意図される。非金属物質もまた、核形成中心として用いられ得る(例えば、タンパク質および核酸)。
所望の形および特性を有するPRPを産生するために、核形成中心の配置は制御され得る。例えば、核形成物質の三角形または楕円形の領域が形成され得る。析出プロセスは、多くの当該分野で公知の金属析出技術(例えば、蒸着、スパッタリング、所望の物質より調製した薄膜のGa-焦点イオン光線(FIB)ミル、およびナノポア(nanopore)への電気メッキ)を包含し得る。特に、十分に制御された核形成物質の配置は、走査型トンネル顕微鏡の金属先端から核形成物質を放出することにより可能である。個々の金属原子を走査型トンネル顕微鏡の先端で拾い上げ、移動し、所望の位置へ降ろす技術が開発されてきた。個々の原子はまた、走査型トンネル顕微鏡の先端で所望の位置へ「押し込まれ」得る。本技術は、核形成中心として使用するために、例えば、10の金原子を空間的にあらかじめ特定した位置へ配置するのに使用され得る。
1つの実施態様において、標準的な微小操作技術を用い、延伸(drawn)マイクロピペットの先端へのPRPまたはPRP核形成中心の導入、PRPまたはPRP核形成中心の所望の位置への移動、およびPRPの所望の位置への沈着により、PRPまたはPRP核形成中心は所望の位置へ配置される。ピペット先端は、種々の粘度を有する溶液中(すなわち、ゼラチンまたは他のマトリックスを用いて)の所望の物質で満たされ、次に先端は、顕微鏡下で観察しながら、選択された位置へ、操作される。ピペット中の溶液に圧力を加えることにより、非常に少量が所望の基板上に沈着され得る。他の微小操作技術もまた、可能である。
PRP物質は、共鳴周波数以上の周波数で正の誘電率を有するので、現在行われているプラスチック粒子の光学的トラップと同様な原理を用い、適切な波長の焦点光線中で金属粒子を光学的にトラップし得る。従って、PRPがトラップされた光線の操作により、PRPは、空間的にあらかじめ特定された位置へ配置され得る。PRPを空間的にあらかじめ特定された位置へ電気泳動的に送るために、ゲルの導管もまた作成され得る。導管が、指定した位置の近位を通過するように配置される場合、導管内のPRPは、電場の影響下で移動し、指定した位置へ導かれる。静電的結合技術はまた、PRPを空間的にあらかじめ特定された位置へ除去可能に付着するために用いられ得る。
1つの実施態様において、直径約10〜100ミクロンの1つ以上の伝導性パッドの配列は、標準的な集積回路リングラフ技術を用い作成され得る。各パッドは、さらに電圧源と選択的に接続され得る。溶液中のPRPは負に荷電しているので、適切な電位をパッドに加えると、溶液中から伝導性パッドへ、PRPが引きつけられる。PRPとパッドとの間の表面結合力が弱い場合(すなわち、およそ1ピコニュートン)、電圧を除去し、そして加えた電位の符号を逆にすると、PRPが遊離し得る。
結合体化核形成中心および/または結合体化PRPはまた、結合体対の他の半分を空間的にあらかじめ特定された位置へ固定化し、そして核形成中心上の結合体またはPRPを結合体対の他の半分と結合させることにより、空間的にあらかじめ特定された位置へ配置され得る。
個々の核形成中心(または完全に形成されたPRP)はまた、基板への金属粒子含有液の小滴を噴出し、そしてインク−ジェット印刷で用いられるのと類似の技術によりその液体をエバポレートさせること、沈着され得る。この技術において、1つ以上の金属粒子が、滴下位置により規定される特異的な位置へ、送達され得る。いくつかの実施態様において、液体中のPRPまたは核形成中心の濃度は、統計学的に、PRPまたは核形成中心が各1滴に1つ含まれるかまたは含まれない可能性が高いように選択される。核形成中心が沈着する場合、核形成中心は引き続きPRPを形成するように銀増強され得る。さらに、これらの技術は、PRPの所望の幾何学的パターンを作成するために使用され得ることは、注目される。このようなパターンを作成する場合、滴下は、最初の通過の間にPRPが噴出されなかった位置に、再沈着され得る。このようなPRPパターンを有するものは、目的物の同定、半導体マスクの整合(registration)、および下記により詳細に記述する用法にとって有用であり得る。
本明細書中に定義するように、「インサイチュ」という用語は、PRPが基板に結合しているか、溶液中に浸漬されているか、またはマトリックス中に懸濁されていることを示す。「基板」という定義は、下記に論じた。「基板」としては、例えば、組織切片、細胞、TEMグリッド(例えば、ホルムバール、シリコン(窒化珪素および二酸化珪素を含む)、雲母、ポリスチレン等より作成される)などのPRPが会合しうる任意の実体が挙げられる。これら核形成中心は、代表的には、金コロイド調製物であり、そして核形成中心の適切な集団は、遊離型あるいは種々の生物学的分子に付着した形態のいずれかで市販されている。
電子顕微鏡および/または光学顕微鏡下で可視であり得るより大きな銀塊を産生するために、金核形成中心の銀増強は現在実施されている。そして、銀増強した金粒子を用いて生物学的システムを画像化するためのいくつかの手順が広範囲に開発されてきた。従って、増強を行う試薬および核形成中心自体は市販されている。抗原に結合した金核形成中心は、いくつかの供給源より入手可能である。供給源としては、E-Y Laboratories(San Mateo,CA)およびAmersham(Arlington Heights,IL)が挙げられる。さらに、大量の文献が、このような増強を行う種々の適切な方法を記述している(例えば、M.A.Hayat編、Immunogold-Silver Staining-Principles,Methods,and Applications,CRC Press,1995を参照、この開示は本明細書中でその全体が参考として援用される。最も特に、銀増強金核形成中心についてのいくつかの実験技術を記述し、そしてそれにより形成される銀塊について考察する第2章および第7章)。
増強プロセスは、好ましくは、金核形成中心を、銀塩(例えば、酢酸銀、乳酸銀または硝酸銀)の溶液および還元剤(例えば、pHが約3.5〜3.8のクエン酸緩衝液中のヒドロキノン)と混合することにより実施される。約6mMの濃度の銀塩および約33mMの濃度のヒドロキノンを提供するのが適切であった。適切な量の銀および還元剤を含有する市販の銀増強溶液は、例えば、BBI(英国)より市販されている。当業者は、緩衝システム、銀塩、還元剤および他の増強パラメータの選択が、局所環境、標的位置等について好ましく最適化され、そしてそのような最適化は過度の実験を要することなく行われ得ると理解する。
本発明の1つの局面に従い、本発明における有用なPRPは、粒子がプラズモン共鳴粒子の性質を有するまで、銀増強核形成中心により調製される。最も好ましくは、銀増強パラメーターは、作成されたPRPが、暗視野顕微鏡観察で観察する場合、特定の所望の色を表すというような、あらかじめ規定されたスペクトル特性を有するように制御される。増強の間、個々の進化中のPRPを1つずつまたは個々のPRPを複数同時に、スペクトル特性が観察され得る。従って、特定の物理的性質を有するPRPが作成され、そして、所望の位置へ配置され得る。加えて、PRP核形成中心は、インサイチュ、インビトロまたはインビボのいずれかにおいて、所望の位置に配置され得る。その後、その特定位置において銀増強によりPRPを産生する。
B.金属増強によるPRP(またはPRE)形成の具体例
PRPを、以下の実施例に記載する金核形成中心の銀増強により調製した。
実施例1
基板への金コロイドの配置
アルシアンブルー法は、基板の空間的にあらかじめ特定された1以上の部位を化学的に処理することにより、金コロイド核形成中心を基板に付着させるための一方法である。アルシアンブルーは、電荷相互作用により負に荷電した金コロイドの付着を促進する正荷電色素である。PRPが望まれていない基板部分を、BSAのようなブロッキング剤でコートし得る。5%酢酸および2%アルシアンブルーの100:1希釈の100マイクロリットルの液滴を、注意深く清浄にしたスライドガラス上に10分間置いた。次いで、基板の活性部位を、二回蒸留水に浸漬し、リンスし、次いで乾燥させた。
金コロイドを、所望の濃度に希釈した。溶液を、基板のアルシアンブルー処理領域に置き、そして10分間インキュベートした。次いで、基板を蒸留水でリンスした。
基板に付着した金コロイドを、実施例2に記載される方法により増強した。
実施例2
個々の金核形成中心の銀増強
ゼラチンの0.1mg/ml溶液1mlを、エッペンドルフチューブ内で50μlイニシエーターおよび50μlエンハンサーと混合した。イニシエーターおよびエンハンサーは、BBI International(英国)銀増強キット、光学顕微鏡(LM)バージョン、カタログ番号SEKL15から入手した。基板を直ちにエンハンサー溶液でカバーして、時間測定を開始した。次いで、PRが存在するか否かを決定するために、基板を暗視野照明下で観察した。ガラス、シリコン、またはTEM基板上におけるコロイドのおよその増強時間は約1分であったが、生物学的基板上に付着した結合体コロイドのおよその増強時間は約7分であった。これらの時間を、増強が起こっている間に、暗視野顕微鏡下で個々の伸展PRPからの散乱光を連続的に観察することにより決定した。正確な増強持続期間は、散乱反応、従って生成するPRPの色を制御するために利用され得ることが理解され得る。蒸留水で徹底的にリンスすることにより、増強を停止させた。
実施例3
溶液中でのPRPの生成
コートされないコロイドについては、100μlのストック金コロイド(BBI International、英国)を、20mlゼラチン溶液(0.1mg/ml)に添加した。タンパク質結合体化コロイドについては、100μlのストック結合体化金コロイドを、表面をブロックするために、1%ウシ血清アルブミン(BSA)を有する20mlの二回蒸留水に添加した。使用した結合体化コロイドは、ウシ血清アルブミン、ヤギ抗ビオチンおよびウサギ抗ヤギIgGであった。代表的な金コロイド濃度は、以下の通りである:
コートされないコロイドについて:
3nmストック−約3×1013粒子/ml
10nmストック−約5.7×1012粒子/ml
20nmストック−約7×1011粒子/ml
タンパク質結合体化コロイドについて:
1nmストック−約2×1015粒子/ml
5nmストック−約1.7×1014粒子/ml
10nmストック−約1.7×1013粒子/ml
20nmストック−約2×1012粒子/ml
次いで、3滴(150μl)のイニシエーターを添加した。次いで、エンハンサーの10μlの増分を、所望のPRP散乱ピーク波長に相当する量を添加するまで、撹拌しながら添加した。PRP共鳴を、先に記載したように、暗視野測定または吸収分光法によりチェックした。
C.リソグラフィーおよび照射によるPRPおよびPRE形成
リソグラフィー技術を、PRP(またはPRE)の形成部位を特定し、その形状、形態、および組成を制御するために使用し得る。ポジティブレジスト法およびネガティブレジスト法の両方を、核形成中心または完全に形成したPRPのいずれかを下に配置するために利用し得る。ポジティブレジスト法においては、レジスト層の部分を、モールドを形成するために除去し、このモールドの中に金属を沈着させる。このような沈着後、レジストおよび過剰の金属を離昇し、核形成中心または完全に形成されたPRPを後に残す。ネガティブレジスト法においては、銀またはその他の適切な金属の選択される層をレジストの層により被覆する。次いで、このレジスト層の部分を重合する。本技術を用いて核形成中心を形成する場合は、本重合領域の固有サイズは好都合には約5〜20nmであり得る。ピーク波長が光学スペクトル内であるPRPを下に配置するためには、重合領域の固有サイズは、好都合には、4〜125nmである。次いで、銀および非重合レジストは、エッチングにより除去されて、レジストの重合領域の下に金属核形成中心または完全に形成したPRPを残す。別の代替法としては、所望されるよりも大きな金属型を作製し、そして所望の特性のPRPが形成されるまでイオンミリングにより材料をエッチングにより除去し得る。これらの技術の全ては、電子工学およびその他の産業において使用されており、当業者には周知である。
さらに、金属塩およびハロゲン化物(すなわち、フィルム内)を核形成中心または粒子全体を得るために照射し得る。増強を、上記の技術により実施し得るか、または金属粒子を熱アニーリングすることにより実施し得るか、またはPRPを生成するまで光化学金属塩または金属ハロゲン化物のフィルムを光で局部的に照射し、次いでフィルムを固定、および現像する、写真現像工程で行われるように実施し得る。核形成中心またはPRPを所望の位置に形成するために、局所化された光のスポットを作製し得る、いくつかの方法がある。一つの実施様態においては、核形成を適切な小さなサイズに制限するのを助けるため、または銀粒子を直接成長させるために、金属側をコートしたテーパーファイバー「近距離場」スキャンチップを使用して、極めて局所化された光のスポットを生成し得る。あるいは、末端にPRPを有する、好ましくは直径約150nmの、あらかじめ作製された特製光ファイバーチップは、感光性表面物質上にこれらの核形成中心を「描く」ために所望の位置に光を集中させる。別の実施様態においては、固体-液浸レンズを、金属塩またはハロゲン化物上に光線を収束するために利用し得る。基板の局所照射をさらに増強するために、固体-液浸レンズは、PRPをその焦点に含み得る。
光化学銀塩またはハロゲン化物はまた、電子およびイオンビーム照射、ならびに放射線元素からの照射に感受性である。これらの写真法はまた、所望の配置のPRPの配列またはパターンを生成するために使用され得ることが理解される。
現像中のPRPが溶液内にあっても、または基板と結合していても、増強工程は、暗視野顕微鏡でインサイチュで観察され得、そしてPRPが、特定の色に対応する所望のサイズに一旦達すると、プロセスは停止し得る。光感受性増強手順の間、エンハンサーを洗浄により除去し、生成された粒子の光散乱特性を観察することにより増強プロセスの進行を測定し得、そして所望のスペクトル特性を有するPRPが得られるまで、増強を再開し得る。代替的な実施様態においては、比較的光非感受性のエンハンサーを使用し得、そして増強プロセスを、連続的な暗視野照射および散乱データ収集により観察し得る。勿論、所定の特性を有するPRPを生成するための、エンハンサー量、インキュベーション時間などを示す特定のプロトコルが一旦開発されれば、増強プロセスの観察は不必要となる。
D.結合体化PRPの形成
上記の実施例3に示したように、抗体のような生物学的高分子に結合される核形成中心を増強することが可能である。結合体化金抗体のこの増強は、結合体化金/抗体が水性溶液中に存在するか、または細胞内もしくは細胞オルガネラ内で抗体とあらかじめ結合されていない場合においてさえ、好結果で実施され得る。驚くべきことには、PRPを生成するための遊離の結合体化金核形成中心の銀増強後、金コロイド中にもともと存在している結合体分子のかなりの部分は、生じるPRPに表面で結合することが見出されている。さらに、生物学的分子は、増強プロセス後も生物学的活性を保持し得る。
本方法に関して、所定のPRP上に結合する結合体の量を、結合体に結合させる核形成中心のサイズを制御することにより制御し得る。例えば、市販の直径1nmの核形成中心は、結合体化分子を一つだけ有し得、そしてその最外部表面に付着されるその結合体分子を有するPRPを形成するために銀増強され得る。20nmの核形成中心は、相応じて多数の付着結合体を有し、そのうちのいくつかは、銀増強にされたPRPの表面に結合することになる。銀増強の間、結合体に結合されるPRPを、PRPの表面上の非特異的結合部位の存在を減少させるために、ウシ血清アルブミン(BSA)のようなブロッキング剤とともにインキュベートし得る。
別の実施様態においては、PRPの作製後に、結合体をPRPに添加する。結合体は、PRPと共有結合または非共有結合のいずれかにより結合する。例えば、完全に形成されたPRPを、非特異的電荷相互作用を防止するために、ゼラチン、寒天、ポリテトラフルオロエチレン(TeflonTM)、PVP、またはラテックスでコーティングし、次いで周知の方法により1以上の官能基を共有結合によりそこに付着させ、従って特定の結合体対の最初の半分に付着されたPRPを生成する。結合体を免疫金核形成中心または形成されるPRPに結合するために必要とされる試薬は、全て市販である。
結合体に結合されるPRPを形成する本方法はまた、PRE表面に結合される結合体分子(すなわち、「最初の半分」の結合体対)の数の制御を可能とする。この場合、結合体およびBSAのようなブロッキング剤溶液中で、裸のPRPをインキュベートし得る。結合体およびBSAの相対濃度は、平均して、各PRP上の結合体の所望の量を生成するために調整され得る。普通でない形状のPRP、または異なる物質の同心円状のシェルを含むPRPについては、形成後に結合体でコーティングすることが、代表的にはより便利である。しかし、ほぼ球形である、結合体に結合されたPRPは、上記の通りに市販の結合体に結合された金コロイド核形成中心および銀エンハンサーから好都合に生成され得る。
結合体または他の分子は、PRPの金属表面に直接結合され得る。そのような結合に関わる表面化学は複雑であるが、多くの非PRP免疫金銀染色技術において、現在広範囲に開発されている。あるいは、PRPを、結合体のようなさらなる分子の結合に先だってラテックスのようなプラスチック材料のシェルによりコートし得る。ラテックスに分子を結合するための技術もまた既知である。金属に直接結合する分子またはプラスチックシェルに結合する分子は、結合体自体であり得るか、またはスルフィド、アミド、ホスフェート、アルデヒド、カルボキシル、アルコールのような他の中間反応基、または結合体もしくは他の目的の分子が結合し得る他の物質であり得る。結合体または他の目的の分子は、組み合わせ化学の公知の方法を用いて、そのような反応性基礎の上に合成され得る。
E.所望の特徴を有するPRP集団の形成
図1に示すような、2つの別々のPRPについての発光スペクトルにおける相違は、多数の因子から生じ得る。一つの重大な因子は、サイズであり、粒子のサイズが大きいほど、より長い波長において共鳴ピークを有し、そしてまた増加した半波高幅値を伴うスペクトル形を有する。従って、生成されるPRPのサイズの制御は、いくつかのスペクトル特性にわたる制御となる。
従って、制御された量のエンハンサー添加により、4つの型のPRPについて図2に図示したような、狭い直径範囲を有する、従って相対して狭い共鳴ピーク周波数範囲を有するPRPの集団を生成し得る。いくつかの有利なPRP生成方法においては、粒子は、増強プロセスの間に適切な顕微鏡を使用して観察され得ることが理解され得る。これらの方法は、増強プロセスの間のPRPの伸展を観察するために必要とされる入射光により比較的影響されない、本明細書中において説明するような増強化学物質を使用する。従って、PRPの伸展は観察され得、そして所望の終点に達した時点で停止され得る。光感受性増強プロセスを使用することが所望され得る適用については、または顕微鏡外における伸展が所望される場合、時間計測による連続増強を行う。各適用後に試料をリンスし、そしてPRP光散乱の状態を決定する。所望な数の連続増強プロセスを継続し得る。
上記で示したように、本発明によるPRP組成物は、規定された波長のピーク波長40nmを有する、1以上のPRP集団を含む。PRP集団におけるそのような均質性は上記のようなPRP生成の暗視野観察と対にした、エンハンサーの段階的添加によって可能である。プラズモン共鳴ピークの幅は代表的には20〜40nmであるので、一般的にはPRP集団の共鳴ピークにおける分散をさらに減少させる必要はない。
あるいは、均一なスペクトル特性を有するPRPの集団はまた、非均質性集団を精製することにより調製され得る。PRP結合体および遊離PRPは、カラムクロマトグラフィー、遠心分離、電気泳動、および濾過を含む従来の生化学的方法により分離され得る。表面局在分子または実体を有するPRPは、同じサイズの遊離PRPの移動度と有意に異なる易動度を有し得るので、これらは、遊離のPRPが溶出するのと異なる速度でゲル濾過カラムから溶出する。PRPは荷電粒子であるので、これらは、電界内を移動する。従って、PRPは、電気泳動中に操作され得、そしてさらに観察され得る。
特定の所望の特性を有するPRPはまた、ゼータ電位に基づいて分離され得る。本使用に適切であるゼータ電位分離装置は市販である(Coulter Corp.、Florida)。PRPをその構造的特性に基づいて異なる速度でマトリックスを通過させるために、放射圧もまた適用され得る。結合PRPおよび遊離PRPを、例えば、アガロースまたはアクリルアミドゲルでの電気泳動に供する場合は、遊離PRPは結合PRPが移動するよりも迅速に移動する。同様に、PRP結合体は、フィルターにより優先的に保持され得る。あるいは、精製は、遠心分離によって実施され得る。従って、これらの方法を使用して、広い範囲のスペクトル特性を有するもともとのPRPの集団を、より狭い範囲のスペクトル特性を有するサブ集団に分離し得る。
PRPの個々の集団は、別々に調製し、そして所望の量におけるPRP特性(例えば色)の所望の組み合わせに従って後に混合され得、各々は、適用に応じて同一もしくは異なる生物学的高分子を用いて標識されるか、または標識されない。そのような組成物においては、PRPの異なる集団の共鳴ピークが、上記で規定したように、実質的にオーバーラップしないことが好ましい。いくつかの好ましい実施様態においては、PRPの1集団のピーク位置における分散は、ある規定された波長の約20nm以内であるように制御され、そして混合物内のPRPの別の集団のピーク位置の分散は第二の規定される波長の約20nm以内に制御される。かなりのオーバーラップを回避するために、2つのピーク波長が少なくとも30〜40nmは離れていること、およひ最も好ましくは50以上のナノメーター離れていることを確実にすることが好ましい。
上記の方法を適用することにより、新しいタイプの分子プローブを、選択されたPRPに選択された結合体を結合することにより生成し得る。前述のように、異なる選択的結合特性を有する2種の区別可能なPRP集団を生成するために、第一のスペクトル特性を有するPRP集団を第一の結合体に結合させ、そして第二のスペクトル特性を有するPRP集団を第二の異なる結合体と結合させ得る。このようなあらかじめ規定したPRPの混合物は、以下でさらに説明するような、量の少ない分子の検出精度の改善に特に有用である。
F.単離された非球形および複合PRP
PRPの発光スペクトルは、さらにその構造の細部により影響を受ける。楕円形PRPは、同定および弁別のためのさらなるパラメーターを与える。各楕円形PRPは、それぞれ、1本の等方軸が存在するかまたは3つの異なる主軸次元が存在するかに依存して、2または3のプラズモン共鳴ピークを有し得る。1本の等方性軸を有する楕円形PRPは、2つの直交偏光発光に対応するピークを示し、一方は楕円の主軸にそったプラズモン励起に付随し、他方は短軸にそったプラズモン励起に付随する。入射光の偏りが対応する主軸にそっている場合、別個のプラズモン共鳴ピークは最大強度で出現する。従って、固定楕円形PRPの偏光に対する反応は入射方向によって変化し得る。
楕円形銀粒子を作製するプロセスは、粘度により所望の扁平率を有する長楕円形粒子へのPRPの伸長がもたらされるような温度にて、球形PRPを含むガラスマトリックス上で引っ張ることから成る。そのような粒子を「押しつぶし」、その結果、扁平楕円粒子を形成する条件についてもまた説明されている。PolarcorTM(Corning Company、Corning、NY)というマトリックスを含む1つの楕円形PRPは、ガラスマトリックス中に整列された楕円形PRPから成る。この複合材料は、主として赤色以上の、特定の光学的周波数に対して効果的な偏光子である。そのようなガラスマトリックス内に含まれる個々の楕円形PRPは、PRPを妨害しないような様式でマトリックスを溶解することにより単離され得る。適切なマトリックス中で適切な扁平率およびサイズの楕円形金粒子を調製し、次いで粒子を妨害しない様式でマトリックスを溶解することにより、ほぼ等価であるプラズモン共鳴散乱特性を有する大量の楕円形PRPを、例えば、以下で詳細に記載する生化学的アッセイのための液体試薬調製での使用のために調製し得る。
他の方法は、楕円形PRPを調製するために使用され得る。楕円形PRPは、銀ハロゲン化物の光反応を介して、または適切なリソグラフ用モールドを用いて生成され得る。あるいは、最初は実質的に球形に形成されたPRPを、2つの表面の間で所望の扁平楕円外形または長楕円外形につぶすために、プレスまたはロールし得る。
非球形および非楕円形のPRPは、球形または楕円形粒子と異なる特徴的なスペクトルサインを有し、有利なサイズおよび散乱特性を有するプラズモン共鳴プローブの作製に有用であることが観察される。青色領域に強度に散乱するPRPは、球形銀粒子を生成することにより簡便に生成され得ることが見いだされている。上記で考察したように、粒子直径の増加により、共鳴ピークは赤色シフトする。しかし、球形粒子については、ピークが赤色にシフトするにつれ、散乱光のピーク強度が低下し始め、従って、強青色散乱体と比較して、強赤色散乱体の球状粒子による生成はずっと困難である。しかし、他の幾何学的形状の粒子は、より長波長において強い散乱を生じ得る。そのような3種類の粒子は、断面が三角形、四角形、およびほぼ六角形である。三角形、四角形、および六角形の銀粒子は、例えば、銀ハロゲン化物の光反応を介して、または適当なリソグラフモールドを用いて生成され得る。青色球状粒子と類似のサイズである、単離された六角形粒子は、代表的には緑色のプラズモン共鳴ピークを有する。50〜150nmの特徴的寸法を有し得る、単離された三角形粒子は、特に興味深い。なぜなら、これらは、しばしば、可視スペクトルの赤色部において共鳴ピークを示すからである。三角形PRPの生成は、赤色に現れるPRPを得る適切な方法の1つであることが見いだされている。赤色三角形粒子および青色球状粒子の具体的な例は、図7および8を参照して以下で考察する。小さな球形の金属粒子を、対または他の集合体に結合させることにより、様々のプラズモン共鳴粒子形状を形成することもまた可能である。
さらに、誘電性および導電性物質から成る同心円状シェルを有するPRPを調製し得る。PRPのこれらの実施様態においては、プラズモン共鳴のピークを所望の周波数に変換し得る。特に、コアまたは外部シェルは共鳴ピークを赤色シフトさせる傾向があり、そして比較的強い散乱体を生成するので、誘電性物質を添加にすることにより、PRPを作製し得る。この理由によって、赤色PRPはそのような誘電性シェルまたは核の封入を伴って、有利に生成し得る。誘電性コアおよびアルミニウムのシェルを有する粒子は、紫外線域の約240〜280nmにおいてプラズモン共鳴ピークを有することが見いだされている。
誘電性コア/金属シェル/外部誘電性シェルを含む3層から成る粒子は、ピーク共鳴および散乱強度の変化におけるさらなる柔軟性のために有用であり得る。さらに、複数の同心円状導電性シェルを有するPRPを作製し得る。各シェルは異なる直径を有するので、しばしばいくつかの別々のピークを含む複雑な散乱スペクトルが生成され得る。これらのピークは、導電性シェルを隔てる誘電性物質内で変動を伴ってシフトし得る。以下にさらに詳細に説明するように、ラテックス、テフロン、または他のポリマーコーティングを含む誘電性外部シェルはまた、PRPの外部への目的の高分子の結合に適切な基板として有用である。
導電性物質および誘電性物質の複数のシェルを有するPRPの生成はより複雑であり得るが、これらは、化学蒸着法またはスパッタリングを含む様々なフィルム沈着技術を使用して製造され得る。複数シェルPRPの実施様態を作製するための他の方法は、上記のBirnboimらによる米国特許第5,023,139号において記載される。
誘電性コアおよび外部金属シェルを有するPRPはまた、非電着性メッキ技術を用いて生成され得る。このプロセスにおいては、例えば、ラテックスから構成されるコア粒子は、その表面が、白金原子であり得る金属原子により活性化される。上記のような増強手順を使用することにより、これらの白金原子は、銀増強およびラテックスコア周囲のシェル形成のための核形成中心を含む。
ちょうど記載したPRP組成物における(i)〜(iv)の全ての限定を含み得るが、その必要はない、PRP組成物もまた、第III節に開示する一般的方法を含む、本明細書中で考察する様々な適用における使用のための新規なPRP組成物として、本明細書中で意図される。
2リガンド組成物。組成物は、PRPの2つの集団を含み、その各々は、PRP表面上に担持される異なるリガンド種を有する。2つのリガンドは、標的上の異なるリガンド結合部位と結合するように設計される。2つのPRP集団は、異なるスペクトル特性を有し得る。
蛍光レポーター組成物。組成物は、標的のリガンド結合部位に結合するための、表面付着リガンドを有するPRPを含む。組成物は、結合粒子のプラズモン共鳴スペクトル発光により励起される蛍光発光が、励起光を蛍光分子の部位に収束させるように作用するという点で、極めて高感度な「一部位」レポーターである。組成物はまた、これらがもし蛍光クエンチング分子または蛍光エネルギー転移分子を含むように設計されるならば、標的環境に対して高感度であり得る。
蛍光クエンチングまたはエネルギー転移。本組成物は、PRPの2集団を含み、各々は、標的の近傍の2つの部位に結合するための表面付着リガンド(同一であってもよく、または異なってもよい)を有する。各々の集団は、近傍に配置された場合に蛍光クエンチングを生じる表面局在化蛍光分子、または近傍に配置された場合の非照射エネルギー転移のためのドナーおよびアクセプターの蛍光分子を含む表面局在化蛍光分子を含む。組成物は、例えば、第一および第二の近傍リガンド結合部位を有する標的を検出するための均質アッセイにおいて有用である。
ラマン活性実体を有するPRP。組成物は、複数のPRP集団を含み、各々はPRP表面上に局在化された異なるラマン活性実体を有する。各々の集団は、さらなる表面局在化分子(例えば、異なる塩基配列を有するオリゴヌクレオチドまたは組み合わせライブラリー分子)を含み得、ここで、各表面局在化分子の正体は、公知の独特のラマンスペクトルサインを有するラマン活性実体(例えば、分子)に結びついている。組成物は、例えば、(i)標準的なビーズ合成法に従ってPRP上に形成される、および(ii)所望の化合物活性を有すると同定される、組み合わせライブラリーの化合物を同定するために使用される。
別の例として、組成物は、染色体地図作成のために使用され、ここで、既知の配列領域(例えば、ESTまたはSST)の相対的な空間的位置は、(i)独特なラマンスペクトルサインを有する各PRPに、染色体配列の1つと相補的なオリゴ配列フラグメントを付着させること、(ii)プローブを染色体DNAとハイブリダイズさせること、および(iii)各PRPの独特のスペクトルサインから、DNAに結合するPRPの相対的位置を同定することにより決定される。DNAを上記のように伸長条件に置くことにより、配列を隔てる地図作成距離もまた決定され得る。
図13は、Drosophila多糸染色体に対するDNA配列標識PREの結合を示し、染色体領域にPREを局在させる能力を例示する。
V.診断方法および組成物
本発明の診断方法は、目的の分子特徴を有する標的の存在またはその情報の決定における使用が意図される。本方法は、好ましくは、第III節に記載される方法および装置に従って、そして好ましくは、第IV節に記載されるPRP(ここで、PRPは、表面局在化リガンドを有する)を使用して、実施される。
本方法の実施において、表面局在化分子を有する1以上のPREと標的を接触させて、分子特徴と局在化分子との間の相互作用を生じさせる。この相互作用は、(A)PRE/標的複合体を生成するための、例えば、リガンド/リガンド結合相互作用を介する標的結合部位へのPREの結合、(B)PRE/PRE相互作用を実証するスペクトル特徴を生じるための、近接して間隔をあけられた標的部位への2つのPRPの結合、(C)連結されていないPREを生じるための、2つのPRE間の連結の切断、(D)検出可能な様式でPRE上のラマン活性分子のラマンスペクトルを変更するための、例えば、リガンド/リガンド結合相互作用を介する、標的へのPREの結合、(E)検出可能な様式でPRE上の蛍光分子の蛍光発光の強度を変更(例えば、クエンチングまたは増強)するための、例えば、リガンド/リガンド結合相互作用を介する、標的へのPREの結合、および(F)結合されたPREを生成するためのPRE間の連結の形成、を含み得る。
標的は、第III節に詳説されるように、1以上の選択されたプラズモン共鳴スペクトル発光特性の測定を可能にする様式で、光学的光源を使用して照射される。次いで、標的の存在または標的についての情報は、標的とのそのような相互作用の後に、1以上のPREのプラズモン共鳴スペクトル発光特性を検出することにより決定される。
本方法に使用されるPREは、好ましくは、抗原/抗体、ホルモン/レセプター、薬物/レセプター、エフェクター/レセプター、酵素/基質、脂質/脂質結合因子、および相補的な核酸鎖のような、リガンド/リガンド結合部位結合体対の1つである表面局在化分子を含むように、上記の通りに構築されたPRPである。検知されるスペクトル発光特性がラマンスペクトル特性または蛍光スペクトル特性のシフトまたは変化に関連する場合、PRPはまたそれぞれ、表面局在化蛍光活性分子または表面局在化ラマン活性分子の実体を含む。使用されるPRPは、第IV節に開示されるPRP組成物の品質および均質性の属性を有し得るか、またはさほど厳密ではない均質性の属性を有し得る。
PREプローブは極めて高感度である(上記のように、単一PREを観察およびスペクトル分析し得る)ので、本方法は、標的分析物の量に対して(最低1事象まで)極めて高感度になされ得る。これにより、HIV、腫瘍マーカーおよび細菌性病原体のより早期の検出を含む、体液中の病原体のより早期の検出、より少ない液体容量からの検出、ならびに多数の現行の診断テストを小規模化することが可能である。
A.標的結合部位へのPREの結合
この一般的実施様態においては、標的上のリガンド結合部位へのPRP結合リガンド結合を導く条件下で、表面リガンド分子を有するPREを、標的と接触させて、標的との1以上のPRE/標的複合体を形成させる。代表的には、測定されるスペクトル発光特性は、複合体の形成によっては不変である。すなわち、PRP/PRP近傍のスペクトル発光効果も、標的とのPRPの相互作用により引き起こされるスペクトル発光特性における変化も、いずれも観察されなかった。
代表的には、本実施様態においては、分析される標的は、固定化されるか、または固定化結合部位について競合する。固相へのPRP結合の後、標的を照射し、そして標的複合体のプラズモン共鳴スペクトル特性を検出する前に、固定化表面、固相を、結合していないPRPを除去するために洗浄する。標的と接触したPREは、2以上の集団を含み得、各々は異なるリガンドを有し、そして好ましくは、各々は、異なるリガンド(例えば、一方のリガンドについては青色粒子、そして他方については赤色粒子)に結びついた異なるスペクトルサインを有する。下記で詳述するように、本実施様態は以下の適用を有する:
(i)標的分析物の存在の検出、ここで、分析物は、固定化されているか、固定化された結合因子と競合するか、または接触混合物中の結合していないPRPから分離され得るかのいずれかである;
(ii)配列ハイブリダイゼーション部位においてPRPを単離するための、DNA標的とのPRP-オリゴヌクレオチド結合体のインサイチュハイブリダイゼーション;
(iii)標的の空間的特徴(例えば、染色体地図作成のための標的細胞もしくは組織上での、またはDNA標的内での特異的結合部位の配置)の地図作成;および
(iv)隔てられたDNAバンドの同定のための、DNA分画ゲルへプローブ標識PRPを直接結合する、例えば、サザンブロット法における、標的のインサイチュ標識。
以下の実施例は、結合部位の空間的特徴、および/または結合部位の密度の検出の目的のために、表面付着リガンド分子を有するPRPを固定化標的組織に結合させる様々なアッセイを例示する。
実施例4
ニワトリ筋肉内のリアノジンレセプターのPREによる標識
パラホルムアルデヒド内で固定した凍結ニワトリ肋間筋を2〜3μm切片に切断し、調製済みのカバーガラス(Pap penウエル内のCell Takコーティングスポット)に移した。組織切片を3回、各回5〜10分間、PBSで洗浄した。非特異的結合部位を、PBS中の3%正常ヤギ血清、1%ゼラチン、0.01% Triton X-100で20分間インキュベートすることによりブロックした。カバーガラスをブロッキング緩衝液(作業緩衝液)の1:3希釈液で5分間洗浄して、次いで作業緩衝液中のマウス抗リアノジンモノクローナル抗体(34C)の1:5希釈液中で1時間インキュベートした。次いで、カバーグラスを6回、各回3〜5分間、作業緩衝液で洗浄して、次いで、ヤギ抗マウスIgG(AuroProbe EM、Amersham)に結合体化させた5nmまたは10nmの金粒子の1:40希釈液と30分間インキュベートした。カバーガラスを各々3〜5分間、作業緩衝液で3回洗浄して、次いで3〜5分間、PBSで3回洗浄した。試料を2分間、二重蒸留水中で3回洗浄して、次いで50μlイニシエーター、50μlエンハンサー(IntenSE M Silver Enhancementキット、Amersham)および1mlの0.1mg/mlゼラチンを使用して、8分間銀増強した。試料を3〜5分間、二重蒸留水で3回洗浄して、ゲルバトール(Gelvatol)抗退色培地で被覆して、暗視野顕微鏡下で可視観測した。リアノジンレセプターを含む個々のPREは、筋肉のZ線に沿って規則的間隔で観測された。結果を図12に表示する。
実施例5
ニトロセルロース上のDNAへのPREの結合
ニトロセルロース膜の1cm×3cm片を切断し、DNA表面を同定するために、一端で頂部表面を鉛筆でマークした。ビオチン標識化DNA(100ng)を、マークしたニトロセルロース表面の一端にピペットで滴下した。非ビオチン標識化DNA(100ng)をコントロールとして他端に付与した。ニトロセルロースをDNAスポットを乾燥させるためにデシケーターに入れて、次いで紫外線で架橋結合させた。DNA表面を上にした、ニトロセルロースを小パラフイルム皿に入れて、少なくとも4時間、ブロッキング溶液(50mM リン酸ナトリウム、150mM NaCl、2%BSA、1% Tween-20)中、室温で、蒸発防止のために100%湿度チャンバー内でインキュベートした。ヤギ抗ビオチン免疫金結合体(Nanoprobes,Inc.、Stony Brook、NY;約1×108コロイド)を添加して、室温で2時間インキュベーションを継続した。免疫金結合体を除去して、ブロッキング溶液(500μl)を添加し、ニトロセルロースを室温で1時間洗浄した。ブロッキング溶液を除去して、二重蒸留水でフィルターを十分にリンスした。二重蒸留水(2ml)を30分間洗浄したフィルターに添加した。水の除去後、1mlエンハンサー溶液(1ml 0.1mg/mlゼラチン、50μlイニシエーター、50μlエンハンサー;エンハンサーおよびイニシエーターはBBI International、英国、Ted Pella カタログ番号SEKL15により入手した)をニトロセルロース上に8分間置いた。次いで、エンハンサー溶液を蒸留水で十分に洗い流した。ニトロセルロースを、デシケーター中で、DNA側面を上にして濾紙上に置いて1時間乾燥させ、次いでスライドガラス上にDNA側面を上にして置いて、カバーガラスで被覆した。スライドをアセトン蒸気チャンバー内に20分間、またはニトロセルロースが透明になるまで置いた。PREを暗視野顕微鏡を使用して観察した。非ビオチン標識化DNAをスポットした位置を含む、ニトロセルロース上の他の箇所でのPREの低密度と比較して、PREの高密度が、ビオチン標識DNAをスポットした位置に観察された。同じ実験が又、ヤギ抗ビオチンに結合体化する完全形成PREを使用した時、ビオチン標識化DNAを首尾良く検出した。
実施例6
ポリスチレン細胞培養皿内におけるDNAへのPREの結合
48ウエル培養皿内の1列のウエルに二重蒸留水(150μl)および1M NaHCO3(17μl)を添加した。各皿にニュートラビジン(10μg)を添加して、その後一晩インキュベートした。全てのインキュベートは、4℃、100%相対湿度において実施した。ニュートラビジン(Neutravidin)を除去して、ウエルを二重蒸留水で十分にリンスした。150μlのブロッキング緩衝液(50mM リン酸ナトリウム、150mM NaCl、2%BSA、1% Tween−20)を各ウエルに添加して次いで4時間インキュベートした。第二ウエルから開始して、1μgのビオチン標識化DNAをブロッキング緩衝液に添加した。引き続くウエルには、ビオチン標識化DNAの10倍希釈を順次添加して(0.1μg、0.01μg、…)プレートを4時間インキュベートした。ビオチン標識化DNAを除去して、ウエルを二重蒸留水で十分にリンスした。ブロッキング緩衝液(上記の緩衝液、150μl)および約108ヤギ抗ビオチン結合体化免疫金コロイドを各ウエルに添加して4時間インキュベートした。次いで、免疫金コロイドを除去して、ウエルを二重蒸留水で十分にリンスし、7分間各ウエルに100μlエンハンサー溶液を加えてコロイドを増強した。エンハンサー溶液を除去して、ウエルを二重蒸留水で十分にリンスして、ウエルを塵を含まない圧縮空気で乾燥させた。暗視野顕微鏡を使用して、各ウエル内のPRE濃度を決定した。PRE濃度は、各ウエル中のDNA濃度と相関した。同じ実験がまた、ヤギ抗ビオチンに結合体化された完全形成PREを使用したとき、ビオチン標識化DNAを首尾良く検出した。
蛍光インサイチュハイブリダイゼーション(FISH)は、蛍光標識の代わりにPREを使用して実施され得る(PRISH)。本方法においては、PRE標識オリゴヌクレオチドを目的のDNA分子と共にインキュベートする。PRE結合オリゴヌクレオチド上に相補配列が存在するならば、結合PREが観察され得る。あるいは、各々が異なるオリゴヌクレオチドに付着された2つのPREを目的のDNA分子と共にインキュベートする。ある特定の障害と関連する遺伝子欠失が存在し、そしてPREが欠失領域のどちらかの側で結合すると、それらは、欠失対野生型においてよりずっと密接であり得る。本方法において、PREの結合対は、散乱パラメータの改変、または同一または異なるかのいずれかのスペクトル特性のPREの相関対の観察により検出され得る。PRISHは、より小さな欠損、または局在化の増加に起因する選択ゲノム領域の検出を可能とする。適切に結合体化されたPREを使用して、結合PREは、核酸鎖に沿っていくつかの位置において観察され得、これは、一度にいくつかの部位に関する情報を提供する。上記に詳説するように、距離測定もまたなされ得る。図7および8に図示するように、約640塩基対に相当するPRE間の230nmの距離は、光学顕微鏡を使用してほんの10ナノメーター以下の精度まで容易に分析し得る。さらに、PCR増強もまたPREハイブリダイゼーション試験と共に使用し得るが、通常増強を必要とするFISHとは対照的に、PCRまたはその他の増強工程の使用は不必要である。遺伝的欠失および変異はまた、PREカップリング核酸の2つの近接する鎖を接合させるリガーゼを使用して、検出され得る。もしPREカップリング鎖が、正確に近接してハイブリダイズすると、変性によって、1対のPREにカップリングされた核酸の遊離鎖が生じる。次いで、これらの結合対を上述のように観察し得る。もし鎖がより近接すぎたりまたはより離れすぎる部位においてハイブリダイズすると、リガーゼ反応は生じず、結合対は形成しない。PREが核酸のハイブリダイズ鎖にカップリングされる場合、PREの結合対はまた、PCR法により生成され得、そして標準PCR法を用いて、存在する標的核酸量を増幅する。
これらの手順の全てにおいて、PREは、オリゴヌクレオチドが標的核酸に結合する前後いずれかにオリゴヌクレオチドに結合体化され得る。さらには、このような試験はインビトロ、または細胞内において実施され得る。選択的PREハイブリダイゼーションはまた、異なった核酸配列のライブラリーを含む多重核酸含有試料ウエルをスクリーニングするために有利に適用される。そのような試料ウエルは、ライブラリーチップアレイまたは標準マルチウェル皿において提供され得る。
PREはまた、様々な高分子の酵素結合免疫吸着アッセイ(ELISA)検出に類似のアッセイにおける用途のために抗体でコートし得る。1つの有利な実施態様においては、マルチウェル皿(すなわち、96ウェルマイクロタイタープレート)を目的の分子に特異的な抗体でコートする。次いで、試験する生物学的液体を、固定化抗体を含むウエルに入れる。固定化抗体と異なる分子の領域を結合する、PRE標識二次抗体をウエルに添加する。次いで、プレートを暗視野光学的検出と互換性のプレートリーダーを使用して読みとる。PRE結合の存在およびレベルは、生物学的液体中の分子の存在および量を示す。
その他の実施態様において、特定の試料はまた、PREの多重集団(各々が異なったスペクトルサインを有する)を使用して可視化され得、標的分子上の異なった結合部位を識別するか、または異なる標的分子を認識する別々の抗体に結合体化され得る。あるいは、PREを、同一標的タンパク質上の複数のエピトープを認識するポリクローナル抗体とカップリングさせる。同一位置における2つのスペクトル的に異なるPREの存在はポジティブシグナルを示し、どちらかの粒子の別々な存在は、不完全な同定となり、拒否される。本アプローチは、臨床診断アッセイにおける誤まったポジティブシグナルを有意に減少させる。
PRE免疫アッセイのさらなる利点は、良好なシグナル対ノイズ比を有する1つのPREを検出する能力は、二次抗体または酵素およびその基質の使用によるシグナル増幅の必要性を排除するという事実を含む。これはさらに、非特異的バックグラウンドを排除する。さらには、光学顕微鏡による処理中に試料を分析する能力は、シグナル対ノイズをさらに至適化するように、インキュベーションおよび洗浄条件のリアルタイム修正を可能とする。PREアッセイは、直接法、サンドイッチ法、およびその他の広範囲に使用されている試験フォーマットにおいて、本質的にはどんな標的物質および様々な結合パートナーとも便利に使用され得、それらのいくつかを以下により詳細に説明する。PREと試験され、これに結合体化される物質は、タンパク質、核酸、リガンド、レセプター、抗原、糖類、レクチン、酵素などを含む。
実施例7
ヤギ抗ビオチンのPRPアッセイ
ポリスチレンマルチウエル皿のウエルをビオチン標識化BSAでコートした。通常BSAをウエル内の残存非特異的結合部位をブロックするために添加した。濃度0.06から600ピコグラム(pg)の範囲のヤギ抗ビオチン抗体の試料を個々のウエルに添加した。ヤギ抗ビオチン抗体を含まないコントロール試料もまたアッセイした。次いで、ウサギ抗ヤギ抗体に結合されたPRPを、各々のウエルに添加してインキュベートした。非結合PRPsをウエルから洗浄して、各ウエル内の結合PRPsを暗視野光学顕微鏡で観測した。視野の光源を上述の識別法に従って分析し、残りの散乱部位を各ウエル内で個別に計数した。本試験の結果を図9に示す。コントロール試料では、画像処理後1計数を残存しており、図9に黒帯(dark bar)として図示する。試験濃度範囲にわたる計数されたPRE数は、0.06pg分析物における4から600pg分析物における1000以上と変化した。
ほぼ均一なスペクトル特性を有するPREの1以上の集団を使用してこれらのアッセイを実施することが好都合であるために、そのようなほぼ均一集団の形成につながる条件下でまずPRE標識を形成することが好都合である。上述のように、結合部位への核形成中心の結合と、それに続く金属増強および光学的観測を説明したが、本技術は、このように作出された粒子のスペクトル特性よりも極めて小さな制御を提供する。しかもこれらの技術が実施されるにしても、バックグラウンドを識別したりまた高感度アッセイを作製するためにPRE散乱特性を使用する努力は未だなされておらず、提案すらされていない。従って、(結合前にPREを形成するより)第一に核形成中心で標的種を標識化して、次いでPRE形成のために金属増強することにより実施するPREアッセイは、PRE散乱体およびバックグラウンド間の光識別が実施される場合なお改善される。さらに、いかなる種類ものあらかじめ形成された光学的観測可能であるサブ波長光エミッタを使用するアッセイは、感度の高いアッセイを作出するために個別に粒子を計数する技術を利用していない。バックグラウンドのスペクトルおよび空間識別を実施する場合は、そのようなカウンティングはPRE標識に加えて、蛍光または発光ビーズ標識のために有用であり得る。以下に説明するように、蛍光は局所的プラズモン共鳴により増強され得、従ってPRE増強蛍光ビーズはそのようなアッセイに有用である付加的サブ波長光発光標識を提供する。
これらのアッセイのタイプの多数の変型がPRE標識を使用して実施し得ることもまた理解される。現在は蛍光分子標識を使用して実施する免疫吸着アッセイの様々な型の全てが、PREを使用して実施され得る。例えば、サンドイッチアッセイおよび競合アッセイが、PREを使用して実施され得る。第一の場合は、検出する標的物質に親和性を有する抗体のような実体をアッセイウエル底に固定化し得る。標的物質を含む試験試料をウエルに添加すると、標的物質は第一実体に結合する。次いで、標的物質の異なった部分に対する親和性を有する第二実体を、ウエルに添加し得る。ここで、それが標的種に結合する。最後に、第二実体に対する親和性を有する第三実体に結合されたPREをウエルに添加し、これは順に第二実体に結合する。リンス後、PREは、標的物質が先に結合した部位にのみ結合することが理解される。本試験は、上述の第一および第二実体が、アッセイする抗原上の異なったエピトープに対する親和性を有する抗体である場合、極めて有用である。PREと結合された第三実体は、標的物質の特異的結合パートナーというよりは、むしろ抗種抗体であり得る。
競合アッセイにおいては、第一実体をアッセイウエル内に固定化し得、PREカップリング第二実体および標的物質の両方をウエルに添加する。ここで、第二実体および標的物質は第一実体への結合について競合する。非結合PREを分離する時、ウエル内に残存するPRE数は、標的物質が結合部位を占有し得た度合いを示す。この型のアッセイにおいては、PRE結合第二実体は標的物質と同一であり得るか、または第一実体に対する親和性もまた有する異なった物質であり得る。
当業者は、感度の高いアッセイを生成するために、広範な種々の方法で広範な種々の分子複合体に結合するために、PRE標識が使用され得ることを認識している。さらなる例として、PRE標識上の結合体は、試験される分析物の特異的結合パートナーであり得る。それは固定化分析物/抗体複合体の特異的結合パートナーであり得る。その他では、PREが固定化抗体と結合し得るが、その固定化抗体が分析物分子とあらかじめ結合する時のみである。これらの様々な技術の各々は、試験される分析物の化学的性質に基づいて、所定のアッセイに本質的に適応し得る。
さらには、異なったスペクトルサインを有するPRE集団を使用して、複数分析物のためのアッセイを同時に実施し得ることが理解される。異なった色または異なった偏極反応を有するPRE集団を、異なった標的物質を認識するために結合体化され得る。いくつかの異なった分析物の未知濃度を含むマトリックス中に導入する時に、各々の異なったスペクトル特性と関連するPREを別々にカウンティングすることにより、本明細書中に発表する全てのアッセイを一度にいくつかの標的物質において実施し得た。
PREプローブはまた、インビトロにおけるコンビナトリアルライブラリーのスクリーニングに使用され得る。本技術のある従来の方法においては、薬物レセプターを発蛍光団で標識して、ビーズ、コンビナトリアルライブラリーを構成する収集物と混合して、スライドの上に塗布する。蛍光ビーズの存在は、レセプター結合およびビーズと結合された潜在薬物の存在を指摘する。本発明の1つの実施態様においては、蛍光レセプターを、アッセイの感度および光安定性を増加するPRE標識化レセプターと置換して、それにより、より小さなビーズ上における元来のコンビナトリアルライブラリーの生成を可能とし、またより大きな化学ライブラリーの合成およびスクリーン能力を可能とする。
ライブラリーは、マイクロチップ上においても合成され得、PREプローブの存在はレセプター結合を示す。最近における、薬物発見を改善するためのコンビナトリアルライブラリーの適用は、従って有力候補物質検出のための方法としてのPREプローブを使用することにより増強され得る。選択的に付着されたPREは、バイオ−チップ検出スキームの分解能および感度を増加する。
これらのアッセイの全てにおいて、PRE較正を、標的実体の検出のために使用されるのとは異なったスペクトル特性のPREを用いて、好都合に実施する。本質において、アッセイは、アッセイ機能のために使用するPREと共に検出および測定され得るPREのコントロール集団を生成するための選択スペクトル特性を有するPREをあらかじめ決定した量導入することにより較正される。ある特異的サンドイッチアッセイ較正例として、赤色PREを、試験する標的実体と結合体化され得、本PRE結合体化標的実体の既知量(勿論、飽和量よりはかなり低量であるが)を試料と共に、連続的または同時に、ウエルに添加する。非結合結合体化赤色PREをリンスして流した後、標的実体に対する抗体を添加する。非結合標的実体抗体をリンスした後、抗種抗体に結合体化する青色PRE(例えば)を添加すると、これは抗体を標的実体に結合する。リンス後、赤色および青色PRE両方を計数する。ここで赤色PRE計数は較正計数を提供する。このサンドイッチフォーマットに替わる方法においては、直接結合アッセイ較正もまた利用され得、ここで異なった固定化抗体を試料ウエルの底に用意し、較正PREを固定化抗体の一つに対する特異的結合パートナーに結合体化させる。
PREを使用するアッセイは、細胞においても実施され得る。結合体化PREは、細胞内の固定または遊離部位に結合され得、その位置は個々に観察され得る。細胞内への粒子の配置の周知技術があり、粒子に細胞膜を穿孔させる高圧バースト法、および加速過程のために高電圧放電を使用する電気穿孔法を含む(PREは代表的には電気穿孔技術に先だって荷電される)。これらの技術を実施する装置は、BioRad Laboratories of Hercules、CAにより市販されている。PREおよびPRE結合体はまた、エレクトポレーションを含む従来のトランスフェクション技術により細胞内に導入され得る。PREはまた、マイクロピペットで細胞膜を刺し通し、細胞内に1以上のPREを直接的に注入することにより直接的に細胞内に配置され得る。好ましい実施態様においては、生化学的損傷から保護するために周知の方法によって、PREをコート(すなわち、ラテックス)する。
生細胞内におけるPREアッセイのある有利な実施態様においては、別に結合体化されたPREの2つの集団を1以上の細胞内に挿入する。各別々の集団と会合した別々の結合体は、細胞内で製造される標的物質上の異なったエピトープと結合するように選択され得る。細胞内への注入後、標的物質の存在はPRE対合により指示され、これは上述の技術を使用して検出される。標的物質の性質により、各結合体と会合される同様な、または異なるスペクトル特性を有するPREを有することが望ましい。
暗視野顕微鏡による観測に適切である、PREアッセイとの使用のためのウエルを調製すると好都合である。暗視野顕微鏡に適切である基板を含むためのマルチウエルプレートのためには、ウエル底を、光散乱不完全の形成を防ぐために、均一、平滑、および清潔を特に強調して好都合に製造する。現在では標準96ウエル皿の生産において、このような注意は払われていない。さらに、ウエル下の外部表面もまた望ましくないバックグラウンドシグナルを導入し得る光散乱表面を提供するので、この外部表面もまた比較的清潔で平滑であるべきである。ある有利な実施態様においては、ウエル表面は、その光散乱不完全が約100未満であり、また約10未満ですらある。これらのアッセイにおいてシグナル対ノイズ比を増加するためのさらなる方法として、ウエル内の不完全位置が記録され得、その特定ウエルでアッセイを実施する時に、これらの位置からの散乱シグナルを無視し得る。
代表的には、これらのアッセイに使用する光学顕微鏡の視野は、ウエル底の全てまたは一部分を含む。従って、低レベルの分析物を検出する場合は、ウエル底よりはむしろウエル壁に付着する分析物が最小量であることを確保することが重要である。従って、生産中にウエル壁上にブロッキング剤を含むと好都合である。そのようなウエルを作製するためには、皿を倒置してBSAのようなブロッキング剤を含む溶液上に配置し得る。皿を溶液中に押し沈めるか、またはウエル内に捕捉された空気をピペットまたはキャピラリによる吸い出しによって除去すると、BSA溶液は、ウエル底に接触することなしにウエル壁に接触し得る。本工程後、所望の抗体または他の結合剤をウエル底に固定化し、次いでウエル底において残存する非特異的結合部位をブロックするためにさらなるブロッキング剤を添加し得る。
本発明に従うアッセイ方法はまた、例えば第III章に説明する本発明の方法および装置を使用することにより自動化され得る。自動化プレートリーダーは、現在、従来のアッセイ技術に使用されており、ロボットPREプレートリーダーの原理は、ある意味では同様である。現在市販のプレートリーダーと同様に、ロボット試料装填器具が付属していても、いなくてもよい。ロボットPREアッセイプレートリーダーは、好都合には、試料ウエルとウエル底の全てまたはその一部の観測のための顕微鏡を備える。ある実施態様においては、極めて小型の対物レンズ(その直径が約2mmであり得る)を、ウエル底部分を画像化している間に高開口度を獲得するために、ウエル内におよびウエル底の近くに低下させる。これらの実施態様においては、PREは、透明ウエル底の底部をはずして総内部反射を有する底部から照射され得る。対物レンズにより光線が集められると、上述の自動画像分析技術を使用して、光発光実体を検出し、そしてバックグラウンドから識別し得る。残存する識別粒子源の計数もまた、自動的に実施され得る。ある実施態様においては、顕微鏡の視野がアッセイウエル底の一部であり得、特定の先決計数が読みとられるまで、同一アッセイウエルのいくつかの領域における粒子を識別および計数するように、リーダーが設定され得る。この計数を達成した後のみ、リーダーは異なったアッセイウエルへと移動する。本技術は、大量シグナルが存在する時にウエルからウエルへと迅速に移動することにより時間を節約し、またウエル内に少数の結合PREが存在する時には適切な計数統計を獲得するために必要とする時間をかける。リーダーはまた、受容計数に依存して識別の付加レベルを実施するように設定され得る。例えば、予測される点拡散機能からの空間的偏差に基づく第一識別は、全視野において実施され得るが、低計数値が得られる場合には付加スペクトル偏差測定法を行い得る。識別の様々なレベルを実施するための全ての閾値がリーダーにプレプログラムされ得、低PRE計数を有するウエルを分析してシグナル対ノイズ比を最大化し、一方、シグナルレベルが既に高い多数計数を有するウエルにおいては時間を節約することを再度保証する。
本明細書中に説明するアッセイの実施のための成分を含む市販のキットが、成分の新規な組み合わせを有するように作出され得ることもまた理解される。好都合には、そのようなキットは、ほぼ等価であるスペクトル特性を有するPREの容器を含み得る。PREは、抗体または選択物質の特異的結合パートナーのその他のタイプのような選択生物分子と結合体化され得る。PREは、のちには結合体のカスタム形成のために反応基にカップリングされ得る。洗浄およびブロッキング溶液もまた提供され得る。PREの第二容器もまた、上述の較正または多重アッセイのために提供され得る。
B. 近接する標的部位への2つのPRPの結合
上述のように、PREにより発光された光のスペクトル特性は他のPREの隣接に依存する。発光周波数における観測ピークの変化、例えばピーク波長、スペクトルの半値幅、1ピークより多くの出現、および偏光に応じた変化などは全て、PREが互いに接近したり、遠ざかると観察され得る。これらの特徴は、その相互反応の度合いを測定することにより、PRE間の概算距離を決定するためにさえ使用され得る。
凝集反応および集塊依存性免疫アッセイは、従ってPREプローブを使用して実施され、また単一分子検出能力を有する。一つの実施態様においては、同一または異なるのいずれかのスペクトルサインを有するPREプローブに2つの抗体をそれぞれ付着させる。これらの抗体は、目的の同一生物分子と、しかし非競合部位において結合する。2結合部位間の距離は、その相互作用の結果による独特なスペクトルサインにより、2つのPREが別々のプラズモン共鳴周波数を有するか、または同一プラズモン共鳴周波数を有する場合、狭帯域照射を介して直接的に検出される近接位に、PREプローブを配置する。例えば、特定の血清成分に特異的である抗体でコートしたPREプローブを含む試験管に、血清を添加する。インキュベート後、試料をスライドガラス上に塗布して集塊(すなわち近接する)PREプローブの周波数を測定する。これを、目的の分子を血清が含む又は含まないコントロールスライドと比較する。本技術は、複数PRE標識への適用、および全細胞またはウイルスまたはその部分と同様に、ペプチド、核酸オリゴマーまたは遺伝子の結果としての検出を有する。
二実体間の結合定数の測定は、現在ではいくつかの手順を用いて実施される。肉眼的結合は、例えば、等温滴定熱量測定法で直接的に測定され得る。間接法は、吸収、蛍光、複合体形成と関連する円二色性における変化を含む。これらの方法に関連する一つの問題は、シグナルの検知可能な変化を観測するためには物質の高濃度を必要とし、この高濃度において試料は本質的に100%複合体化され得、従って、これらの条件下においては結合定数の測定を妨害する。好ましい実施態様においては、2つの実体をPREプローブで標識して、平衡を達成させ、遊離対結合比により結合定数の計算を行う。
2つのPREが隣接するときを検出する能力はまた、分子会合また解離のアッセイとして重要である。2つのPREが適切な結合体対と会合して一緒に混合されると、対、または限られるわけではないが、より高度な複合体を形成するように結合する。一つの例として、オリゴヌクレオチドに結合体化されたPREは、PREの異なった集団上のオリゴヌクレオチド配列が相補配列を含む場合、またはPRE結合体化オリゴヌクレオチド配列が、マトリックス内にまた存在する標的オリゴヌクレオチドの異なった領域と相補的である場合に、そのような対または複合体を形成する。
C. 2つのPRE間の連結の切断
この実施態様においては、1つのPREが、切断可能であるリンカー(例えば、ペプチド、オリゴヌクレオチド、オリゴサッカライド、または他の化学的または酵素的に切断可能なリンカー)を介して別のPREと連結する。連結組成物の目的は、単一の化学物質または酵素切断事象を、連結PREが個別の非連結PREとなることから生じる観察可能なスペクトル変化に基づいて、パートB実施態様に従って、検出することである。
より一般的には、PRPの連結対を区別して、例えばPRE間のペプチドリンカーの酵素による分解または変性により、結合が破壊される場合、これは対形成したまたは複合体PREのスペクトルにおける変化に反映される。酵素の操作は、この技術により、酵素の存在下での複合体形成または解離の比率の増加を観察することによりモニターし得る。これらの方法の一つの有利な適用は、細胞内におけるシグナル伝達カスケードの操作のモニタリングを含む。シグナル伝達カスケードの産物の存在が、あらかじめ結合したPREを解離するか、または解離PREを結合させるように、結合PREを選択する。従って、カスケードの開始は細胞内のPREの会合または解離を観察することにより生細胞内において光学顕微鏡により観察し得る。
各PREを、ペプチドまたはDNA分子のようなリンカーとの結合により結合対を高確率で生起する様式でコートし得る。本明細書中に論説するように、同一PRピーク周波数を有する2つのPREが互いに極めて近接した場合、周波数シフト、さらなる共鳴、および偏光効果が生ずる。溶液中に特定の酵素が存在するか否かを測定することを望む場合、その酵素による分解に対して感受性であるリンカーを使用する。例えば、セリンプロテアーゼは、その中にプロテアーゼ認識部位を含むペプチドリンカーを使用してアッセイし得る。タンパク質分解後、結合PREのスペクトルは、PREが分離するにつれて劇的に変化する。いくつかの場合には、PREは、それらが認識可能なほど相互作用せず、そして連結した場合および連結していない場合の両方で、本質的に独立した散乱スペクトルを保持するように、連結した場合十分な距離をとって空間的に分離され得る。この場合、対形成および解離はなお、PRE位置をCCD検知器で評価することにより観察および測定し得、そして連結されていることを示す相対的運動を有するPRE対を観察する。
VI.PREのさらなる組成物および適用
A.局部誘電環境のモニタリング
空気中におけるPREが空気の誘電率と異なる誘電率を有する媒体で包囲されている場合、散乱パラメーターは、空気中にある粒子の散乱パラメーター特性に比例して変化し得る。この効果は、誘電性媒体が除去される場合可逆的である。そのようなパラメーターは、例えば、共鳴ピークの波長の強度またはシフトの変化、偏光に対するPRE応答の変化、および共鳴ピーク数の変化を含む。共鳴ピークおよび強度のシフトは、PREを包囲する異なる屈折指数を有する液体の添加後に観察され、そして適切な洗浄工程による除去後、PREはその以前の特性を示す。プラズモン共鳴を示す多くの物質については、周囲の媒体の屈折指数が増加すると共鳴ピークが長波長側に赤色シフトする。
目的の特定の物質または試験される試料中のその他の摂動の存在は、従って、PREと相互作用する基板に対するPREのスペクトル応答を記録することにより検出し得る。例えば、PREが基板と結合した適切な試料を調製し得る。選択分子をPRE表面に結合し得る。各々のそのようなPREの光学散乱パラメーター(強度、偏光依存性、角度依存性、波長依存性、等)を記録する。次いで、試料を、初回処理および/またはそれに引き続くさらなる処理後にPRE散乱パラメーターが変化して、このことがさらなる物質の局所吸収または、さらなる物質もしくは開始物質の脱離、または局所誘電性環境におけるその他の変化を確認することによるような様式で、選択的にPRE表面に結合する目的の分子を含む物質で処理する。開始PRE試料を試験「ライブラリー」として調製し得るか、またはタンパク質、抗体等の「適用」ライブラリーをスクリーニングするために使用し得ることが理解され得る。
(D) 蛍光スペクトルのシフト
これらのピークシフトおよび強度の変化もまた、PRE局所誘電性環境における変化に起因する会合および解離のような分子摂動の検出のために使用し得る。
被験体マトリックス特性に関する情報をまた、PREの相対的位置におけるスペクトル依存性および平滑Si表面のような近接基板を観察することにより獲得し得る。例えば、所定の試料内のPRE局在およびスペクトルサインの記録を作成したら、酵素を添加するかまたは結合を光分解するし、基板からのPREの運動を生起して、それによりPREの空間的および/またはスペクトルサインを変化し得る。実際、そのようなPRE対が互いに結合し、そして他方が表面に結合している間に一方が移動した場合には、得られるスペクトルサインはこの事象を明確に示す。基板上のコーティングもまた、PREを使用する検出および分析システムの作成におけるさらなる柔軟性を提供するために使用し得る。例えば、コーティングは、望ましいポリペプチドまたはポリヌクレオチドを結合する基板に対して適用し得るか、または遮断コーティングを適用して、PRE結合体の非特異性結合をブロックし得る。1つの適切なコーティングは、例えば、抗反射特性を生成する誘電性物質の1つ以上の層を含む。コーティングはまた、観察光学システムに入射する光のPREによる増強される放射を生成する誘電性物質の1つ以上の層を含み得る。コーティングはまた、PREを塩基性基板表面から離れた距離に変位するために選択し得る。PREにより散乱される光の所定の偏光は、反射表面からの距離に応じて阻害または増強される。例えば、シリコン上にSiO2から成る適切なスペーサー層を配置すると、予測通りに中心にピークを有する良好な点源イメージが観察される。SiO2層を調整するかまたは別の誘電性物質を使用すると、条件が基板(界面)および誘電性層の上面からの反射光の重畳に起因するPREの破壊的および構築的干渉が存在するPRE共鳴波長、ならびに誘電的厚さ(thickness)、および物質に関して見出され得る。シリコンまたは導電性表面を使用することにより、PREが表面との接触から離れたりまたは誘電性層が介在する場合とは顕著に異なるスペクトルサインが得られる。
B.運動のモニタリング
三次元PRE運動は、2つの観察レンズを互いに直角になるように使用して、各々がそれぞれの光軸に対して垂直な平面において2軸運動(two axis motion)を起こすことによりに、直接的に可視化し得る。これは、特に、対物レンズ視野の深度よりも小さな運動に適している。観察する運動が対物レンズの焦点深度よりも大きな成分を有する場合は、三次元運動のためには1つのレンズのみを使用して、それにより影像面上にPRE強度の焦点を合わせるフィードバックシグナルを介して「深度」方向を測定する。他の二次元は通常方法により測定される。基板表面からのPRE距離はまた、位置の変化に伴うPREによる散乱光の強度を測定することにより、TIRイルミネーションシステムにおいてモニターし得る。励起電場が反射界面からの距離と指数関数的に降下するために、PRE強度は、基板表面から離れて移動すると減少する。
PREプローブは極めて明るくそして非常に小さいので、速度および相対的運動のリアルタイム測定に使用し得る。例えば、PREは、モータータンパク質(すなわち、キネシン)、細胞分裂、小細胞輸送等を含む動的細胞プロセスのモニタリングに使用し得る。PREプローブは光退色しないので、特に広範囲の時間スケールにわたるインビボでの時間的な実験のために有用である。PREまたは前駆体金核形成中心は、細胞膜に取り込まれる脂質に付着する。特異的PRE結合体を、細胞膜と結合する細胞表面レセプター上のその対に結合するように設計する。この方法は、例えば、イオンチャンネル開口のモニタリングを可能にする。PREはまた、筋肉細胞内のアクチンおよびミオシンの運動をモニターするために使用し得る。結合体に結合する、または結合体でコートされるPREは細胞内に導入され得る。次いで、結合体は、サイトゾル、核または様々なオルガネラ膜内のその結合パートナーを結合する。例えば、特定の薬物による、細胞レセプターの活性化は、細胞構造内の形態学的変化を導き得る。従って、細胞内または細胞上にあるPREは、薬物発見またはレセプター活性化のための光学アッセイシステムとして使用し得る。一旦結合すると、PREは局在してその運動を観察し得る。PREはまた、巨視的運動のアッセイにも使用し得る。例えば、血液細胞を標識して、循環において観察し得る。あるいは、血液またはその他の液体の流れは、PREの対応する運動を誘導し得る。PREはまた、Biolistic装置(BioRad Inc.、Richmond、CA)または電気穿孔法により細胞内に導入し得る。
PREで目的の実体を標識することにより、適切なリアルタイムデータの取得および分析システムを統合することにより、本明細書中に記載される検出プロセスを使用して、この実体の運動をモニターし得る。そのようなシステムは運動を三次元的に測定することが可能であり、運動が平面に限定される場合は、二次元的に測定し得る。目的の特異的システムにおける運動についての正確な情報入手が可能なだけでなく、薬物処理、あるいは温度、pH、照射、電場もしくは磁場の強度、または目的の任意の化合物の濃度における変化のような物理的および化学的環境におけるその他の変化の後の分子運動における変化もまた観察可能である。
PREはまた、より巨視的な対象物の物理的運動のモニターするためにも使用し得る。例えば、昆虫の触角上に配置した単一PREはその正常な運動または外的分子に対する反応における運動を感知するために使用し得る。これは特に、嗅いおよびフェロモンに対する分子応答の検出に有用である。PREはまた、顕微鏡的または顕微鏡下限的スケールの機械的運動の分析を可能とするための理想的ツールである。PREをいわゆる「ナノベアリングス」の成分またはその他のミクロンサイズの機械部品と結合させることにより、三次元的運動を可視化し、そしてナノメータースケールで分析し得る。電子顕微鏡のためのさらなる出費に加えて、電子顕微鏡は走査装置であるために、電子顕微鏡を介して運動をとらえることは困難であり、そして視野は、従って、光学顕微鏡で可能であるようにリアルタイムで観察するよりはむしろ連続的スキャンにより生起される。さらには、電子顕微鏡では、真空化した測定領域に加えて、大規模な試料調製を必要とする。これらの要素はリアルタイム運動分析に対して、電子顕微鏡の適用の可能性を大幅に制限する。
C. 近距離場(near-field)効果
前記に論説されるPREの適用は、PREによって散乱された光の遠距離場(far-field)観察に焦点を合わせていた。しかし、PREはまた、強力な、非照射性短域電場を生成するので、近接分子の物理的、化学的および分光特性を有用な方法で影響を及ぼすために使用し得る。表面増強ラマン散乱(Surface Enhanced Raman Scattering)の分光技術は、増強PREの中間近傍におけるその物質のみの特異的増強を含むように拡張し得る。例えば、PREを既知ラマンサインを有する標的に結合するために結合し得る。首尾よい結合は、標的の表面増強ラマンスペクトルを観察することにより検出し得る。また局部的に増強された励起および近接蛍光団の改変された発光のために有用であり得る。驚くべきことには、PREの表面が蛍光団から約1〜5nmの距離に配置されると、PREは、高量子効率蛍光団からさえも増強された発光を生成し得る。対照的に、金属の存在が高量子効率蛍光団の蛍光発光を消光すると一般的に考えられている。この事実は、結合しない場合と比較して、より高度の輝度または変化した寿命を有する蛍光標識を作製するために使用し得る。プラズモン共鳴導電性核(例えば、40〜100nm直径を有する銀粒子)および、例えば、ラテックスから作製される、非導電性シェルを含む標識を作製し得、ここで、このシェル上またはその内部に蛍光またはラマン活性分子を埋蔵する。おそらく、プラズモン共鳴のピークは、蛍光団またはラマン活性分子の効率励起帯と顕著なオーバーラップを有する。その標識が照射を受けると、核のプラズモン共鳴励起が、観察される蛍光を大きく増強する。上記の議論によれば、蛍光増強を生起するためには、非導電性シェルの厚さは好ましくは約5nmに等しいかまたはそれ以下である。従って、選択された波長で共鳴するために選択された、プラズモン共鳴核は、現在市販蛍光ラテックス粒子に対して標識性能を劇的に改善する。
楕円形PRE応答はまた、蛍光分光法と共用して好都合に使用し得る。楕円形粒子は、2または3の異なった周波数において共鳴励起を同時に起こすので、1つのそのようなプラズモン共鳴による選択された蛍光団の局在的励起に特に効果的であり、そして他のプラズモン共鳴に対応する波長での励起蛍光団の放射(すなわち、発光)に影響するために同時に効果的である。
従って標的化PREは、極めて局在化した分光効果を誘導し得、再び顕微鏡下限システムについての情報収集を改善する。蛍光共鳴エネルギー移動(FRET)の場合と同様に、PREのクラスターは、局在化したおよび光子バンド空隙(Photonic Band Gap)モードを含む新たな光学的特性を生じ、これは分子結合事象の高度に反応性のPREに基づく検出器の作製を便宜にするために使用し得る。
D. 計測学および計器化
励起PREは局在熱を発生し、そして個々のPREはポリカーボネート基板への書き込みのために使用し得る。個々の高度に局在化した光源である、PREは、精密リトグラフィ、光化学、または光活性化化学反応の誘起のために有用であり得る。
PREはまた、電子、原子力、および走査型トンネル顕微鏡を含む、極めて高解像度顕微鏡の全てのその他の非光学型と共にマーカーとして使用し得る。これらの適用においては、DNAのセグメントのような、目的の高分子を1つ以上の光学的観察可能なPREで標識する。好ましくは、高解像度顕微鏡がまた、非光学顕微鏡により影像される表面の部分を光学的に観察するための暗視野光学顕微鏡装置を備える。分子に結合したPREは、光学的に観察可能であり、そして原子力または走査型トンネルプローブチップのような高解像度度顕微鏡の関連部分を、観察される分子上の目的の部位に直ちに配置し得る。これは、影像される対象物を局在化させるために通常使用される余計な走査時間を節約して高解像度顕微鏡の使用の効率を増加し得る。原子力、走査型トンネル、または他の任意の型の走査型高解像度顕微鏡は、PREの本特徴を利用するために暗視野顕微鏡システムを組み込むために有利に構築され得る。
高精度アライメントまたはレジストレーションを必要とする産業的適用はまた、PREの使用の恩恵を受け得る。1つのそのような適用は、半導体製造工程であり、リトグラフマスクが処理されるセミコンダクターウエハと正確に整列されなければならない。PREを数ナノメーターまたはそれ以下の精度でさえ局在され得るので、セミコンダクターウェーハ上の1つ以上のPREの位置の、リトグラフマスク上の1つ以上のPREとの位置の比較は、ナノメーターレベルにおいてウエハに対するマスクの局在を決定し得る。相対的配置のみが重要であるので、マスクおよびウエハ上のランダムまたは制御されたPREパターンのいずれかを使用し得る。
本発明の他の適用は、PREが、本質的には、発光波長よりも大幅に小さい直径を有する光学的周波数光の点源であるという事実を利用する。従って、その構造の画像ではなく観察される計器の点散布機能パターン特性のみを生成する。この点拡散機能を、それを作成するために使用される光学システムにおける不完全を検出するために分析し得る。1つの例として、円形干渉縞強度における角度変化は、視野システムにおける円周非対称を有するレンズを示す。2つ以上の発光波長におけるエアリーパターンの中心の局在はまた、色収差のためのレンズシステムを評価する。
PREの点源性質はまた、光学システムのその解像度を試験するために使用され得る。個々のPREの特定位置での配置について上記に説明する技術を使用して、PRE対のセットの較正を、PRE間の距離を変化させることにより作製し得る。次いで、それぞれの点拡散機能の中心ピークが重複して、単一の非識別ピークを生成する前に、2つのPREがどのように接近されるべきかを決定し得る。ある程度は、対象のレンズシステムを有する焦点面における単一PREのピークの幅を測定することにより実施し得る。
PREをまた、集束光光線の強度分布をプロフィールするために使用し得、それによりそのような光線を生成するために使用するレンズおよび他の光学システムの特性に関与する情報を収集し得る。図10AおよびBに図示されるように、集束レンズ100は、レンズの焦点面に狭光線を集中させる光線102を発生する。当該分野に既知であるように、光線は焦点面において点に集中されないが、その強度は、集束光線の中心からの距離の関数としてはぼガウス強度を有する。焦点面における位置の関数としての強度の詳細は、集束光線を生成する光学システムの特性に依存する。
図10Aを参照して、薄い透明プレート104を焦点面における光線102に配置し得る。この透明プレート104は、その上にマウントされるPREを含む。好ましくは、勿論、PREのプラズモン共鳴反応のピークを、入射光光線102の優勢周波数帯にほぼ一致するように選択する。PREによる散乱光強度が照射強度に依存することが認識される。従って、プレート104または光線102が、焦点面内の異なった位置にPREを移動させるように移動する場合、位置の関数としての強度は、観測顕微鏡の適切に配置した対物レンズで散乱光を収集することにより決定し得る。上記の他の暗視野技術を使用して、PREによる発光を収集するが、プレート104を通過して伝達されるまたはプレート104によってスペクトル反射される光は収集しないように、観測顕微鏡の対物レンズを配置し得る。本システムは固体液浸レンズ、レーザー、および他の光学システムの特性を試験するために使用し得る。
E. 対象同定法
本発明のさらに他の適用は、紙幣もしくはクレジットカード、または身分証明バッジのような偽造の対象となる紙またはプラスチック項目の標識および同定である。PREのランダムまたは予め定義されたパターンのいずれかを項目の表面に結合し得る。有利な実施様態においては、PREを保護層またはフィルムでコートする。上記のように顕微鏡技術を用いて項目上の適切なPREパターンの後の観察は、鑑定目的に使用し得る。そのような認証を、店頭末端、施設入り口位置などにおいて、リアルタイム鑑定を可能にするコンピューターによるパターン認識システムを介してし得る。あるいは、PRE配列に加えて、磁気性ストリップ、バーコード、または他のデータ保存媒体を、項目上に(例えばクレジットカード)配置し得る。PRE配列のコードバージョンはまたこの媒体に保存されて、一致は項目が正当に作製されたことを示す。勿論、配列自身から容易に推測し得ないPRE配列に基づく一致磁性コードを生成する暗号アルゴリズムが使用されるべきであり、そしてそのようなアルゴリズムは暗号分野においては周知である。
G. 法医学
PREの強靭性および容易な可視性はまた、ある種の法医学的適用にとって理想的にする。指紋に存在する、身体油、体液、DNAなどはPREと結合し得、適切な照明下で指紋を容易に可視化する。多数の異なった物もまた、痕跡追跡可能性(traceability)を提供するためにPREで標識し得る。異なった散乱特性を有するPREを、爆発物、食物、薬物、毒物またはその他の毒素等と混合し得る。特定のPREは供給源同定を提供し得た。PREはその分解に対する抵抗性および試料中の単一の個々のPREでさえ検出する能力のために本適用に理想的である。
H. ラマンスペクトルPREによる組み合わせライブラリー内の小分子の同定法
PREはまた、1つ以上の結合体分子に加えて提供され得る表面に付着する分子の特性により識別し得る。個々のPREに隣接するラマン活性分子からのラマン散乱により増強された表面が報告されている。(NieおよびEmory、Science第275巻、1102ー1106、1997)。異なるラマンスペクトルを有する分子がPREの異なる集団に付着すると、異なる集団からのPREを、その異なるラマン散乱サインにより同定し得る。広範な種々の入手可能であるラマン分子があり、組み合わせライブラリー技術と組み合わせて特に有用であり得る多数の識別プローブが可能である。ラマンマーカーはまた、各々の塩基に1つずつ、4個の識別可能マーカーを使用するDNA配列決定技術において有用である、4個の識別可能PRE集団を生成するための別の方法(4個の異なるプラズモン共鳴波長に加えて)としして使用され得る。蛍光分子もまた、PREに結合して、そのスペクトル特性よりはむしろ優先的ハイブリダイゼーション特性によって区別される、オリゴヌクレオチドであり得るような付加マーカーを提供する。所望であれば、導電性共鳴核およびラテックスのような非導電性誘電性シェルを有するPREは、その誘電性シェル内に埋蔵される蛍光分子を含み得る。この標識実施様態を以下に詳細に説明する。異なる共鳴散乱特性、異なる蛍光マーカー、および異なるラマンマーカーの組み合わせを、数百または数千のスペクトル識別可能プローブさえ調製するために使用し得ることもまた認識される。例えば、ライブラリーは4個の異なるプラズモン共鳴サイン、4個の異なる蛍光サイン、および10個の異なるラマンサインを含み得、それにより、入手可能なスペクトルサインの異なる組合わせにより160個の異なる区別可能なプローブを作製し得る。従って、PRE集団は、サイズまたは形状の差異に基づいて、またはそれに結合する物質の差異により区別し得る。
さらには、組み合わせ化学の公知技術を、同時の一連の分子組立て工程のにおいて、PRE上にマーカー分子と抱合体分子を同時に合成するために使用し得る。ある実施様態においては、本プロセスは、結合する1つ以上の反応基を有するPREを含み、組み合わせ化学合成を開始する塩基を形成し得る、標識前駆実体により開始する。反応基は、例えば、リン酸塩、アルデヒド、カルボキシル、アルコール、アミド、硫化物、アミノ酸、または核酸塩基を含み得る。例えば、選択されたラマン活性分子を、オリゴヌクレオチド抱合体と同時に合成し得た。あるいは、薬物候補化合物のライブラリーをオリゴヌクレオチドマーカーの同定と同時に合成し得る。
I. 細胞分類
PREプローブはまた、細胞分類法に適切であり、蛍光活性化細胞分類(FACS)に類似である。混合細胞集団を特定のPREプローブを使用することにより、特定の表面抗原を発現する1つの細胞型について分析する。さらに、作製可能な個別のスペクトルサインを有する独特に同定可能であるPREプローブの数のために、複数のPREプローブを同時に使用していくつかの細胞型が単離される。本明細書中に記載のPRE検出法および局在法の全てが、他の項目の中でも、細胞ソーターを生成するのために完全に自動化され得ることを意図する。PRE細胞ソーターを使用して、目的の細胞集団を実質的には1つずつ暗視野顕微鏡の場内に通過させることは利点である。上記に詳説する検出、識別、分析技術は、PRE標識化細胞の同定のために細胞分類状況において使用し得る。
多数の異なる細胞経路指定スキームをそのような装置において使用し得る。1つの有利な実施様態においては、細胞を水のような液体の流れの中に沈着させて、第1液体中で実質的に混合しない、油のような第2液体の包囲シェルの制限内で強制的に動かす。この力は、顕微鏡の視野の場を通過するので、暗視野のための小領域に細胞を閉じこめたままにする。2つの液体の屈折指数は、それらの間の界面における入射光の反射を最小化するために、ほぼ等価であることが好ましい。
さらに、PRE標識を、細胞分類技術においては蛍光標識の代りではなく、むしろ蛍当標識に加えて使用し得る。この場合、蛍光標識およびPRE標識を、同一標的細胞に結合するために作製する。細胞分類を、蛍光マーカーの観察に基づいて実施し得る。分類された細胞の一部分が分類プロセスの結果の記録として保存される場合は、将来において首尾よい分類結果を証明するためにPREを使用し得る。このことは、保存試料の蛍光を観測するよりも、PREの安定性および非光退色特性のためにより効果的である。
同技術のさらなる適用は、インビボまたはエクスビボにおいて実施される。本技術においては、細胞を透過化して、そして目的の細胞内生物分子に対する抗体に付着するPREプローブを透過化細胞内に導入する。次いで、細胞を、組合わせ化学ライブラリーとともにインキュベートする。生存細胞をスライド上に塗布して、そして化学ライブラリーにより”影響された”細胞を選択する。”影響された”とは、付着した生物分子の局在の変化に起因するPREプローブの局在または分布における変化を示し得るか、または、新スペクトルサインを導くPREプローブのクラスターを示し得る。目的の任意の実体(すなわち、細胞、DNA、オルガネラ)は、PREで標識可能であるので、次いで、PREの収集物がユニットとして動くことが観測され得るために、光学的に検出し得る。
J. PREの臨床適用
PREはまた、広範囲の臨床適用において使用し得る。1つの重要な分野は、動物(ヒトを含む)における異なる条件の診断であり、これは動物内の特定器官に対する抱合体の選択的結合により同定し得る。本技術において、選択散乱特性を有するPREを動物によって血流内に注射するかまたは摂取させ得る。これらのPREをさらに、動物内にある特定物質の存在を標的または同定するために抗体または他の抱合体と結合し得る。次いで、組織を、動物から剥離して顕微鏡下でPREの存在について試験し得る。所望であれば、特異的結合抱合体に結合しないコントロールPREもまた、非特異的結合バックグラウンドを測定するために注射または摂取させ得る。これらの技術は、着色ラテックス粒子をプローブとして開発され、そしてラテックス粒子でこれらの試験を実施するための試薬は、例えば、Triton Technologies of San Diego、CAおよびMolecular Probes of Eugene、ORから市販されている。PREの使用は、その明るさ、生体適合性、および分解に対する抵抗性に起因して、そのような試験の感受性を改善する。
細胞改変および遺伝子治療のような治療技術もまたPREにより増強し得る。この場合は、望ましい遺伝的特性を有する細胞をPREで標識して、上記の技術を使用して細胞ソーターで選択する。次いで、選択された細胞を患者におく。所望であれば、PREを患者に配置する前に解離させて除去し得る。
選択的加熱および薬物送達もまたPREにより可能である。PREを患者の選択された組織または領域に局在させると、身体の隣接領域を有意に影響することなく、その組織または領域を局部的に加熱するために照射し得る。光活性化薬物の投与および活性化はまたPREにより増強される。光活性化薬物は、電場が増強されているPREに結合することにより極めて少量の総光エネエルギーにより活性化され得る。乳ガンを処置するための光活性化薬物の使用は、近来注目を集めており、そして組織内のより深い位置におけるその活性化を増強するためにPREに薬物を結合させることにより改善され得る。
生化学システムに対する光学的PRE検出および分析の適用は、現在の標識技術を越える多大の恩恵を提供すると考えられ、そしてPRE分析法が大きなインパクトを有し得る領域を含むようである。しかし、その他の領域もまた、本発明によるPRE検出およびスペクトル分析の恩恵を受け得る。
前述から、本発明の種々の対象物および特徴がいかに見合っているかを評価する。本発明の方法および装置は、これまで困難または不可能であった様々な標的を審問する課題に理想的に適合しており、その代表的実例として以下を含む:
1. 単一分子事象の検出;
2. 天然水和状態における生物標的内の準波長距離関係の解明;
3. 染色体マッピング目的のための染色体内の選択された配列の直接マッピングのような、生物学的標的における選択された標的部位の直接空間的マッピング;および
4. マイクロコードされた情報の光学的読みとり;
本方法および装置はさらに、改善された感受性、空間および距離情報、試料調製の簡易さ、および審問され得る標的試料のタイプにおける柔軟性を達成するために、広範囲の診断的適用に適用し得る。
本発明は、特定の方法、組成物、およびデバイスに関して記載されているが、本発明から逸脱することなく種々の変更または修正を加え得ることが認識される。
Claims (28)
- 分配された複数のPREを有する場を審問する方法であって、
光学的な光源で該場を照射する工程、
該場における個々のPREおよび他の光散乱実体のスペクトル発光特性を、検出する工程、
該場に存在する個々のPREおよび他の光散乱実体について測定された1つ以上の発光スペクトル特性値と該場の中の各領域を結びつける画像であるマトリクスを構築する工程、ならびに
選択されたサインPREに独特の検出されたスペクトル特性の値に基づいて、他の光散乱実体から、選択されたスペクトルサインを有するPREを識別し、該場についての情報を提供する工程であって、該場における各光散乱実体についての、スペクトル発光曲線の半強度でのピーク位置、ピーク強度、またはピーク幅、画像面におけるピーク半幅、および入射応答の偏光または角度の、検出された値に基づいて、該場における全ての他の光散乱実体から、選択されたタイプのPREを識別する工程を包含する、該場における他の光散乱実体から、選択されたスペクトルサインを有するPREを識別することを包含する工程、を包含する、方法。 - 請求項1に記載の方法であって、前記検出する工程が、前記場における光散乱実体のスペクトル発光特性を同時に検出する工程を包含する、方法。
- 請求項2に記載の方法であって、前記検出する工程がさらに、複数の規定されたスペクトル周波数で、同時に、前記場における光散乱実体のスペクトル発光特性を検出する工程を包含する、方法。
- 請求項1に記載の方法であって、前記照射する工程および検出する工程が、第1の周波数帯において、主に、入射光で前記PREを照射する工程;
該第1の周波数帯での照射下で、前記場における個々のPREおよび他の光散乱実体のスペクトル発光特性を検出する工程;
第2の周波数帯において、主に、入射光で該PREを照射する工程;ならびに
該第2の周波数帯での照射下で、該場における個々のPREおよび他の光散乱実体のスペクトル発光特性を検出する工程、
を包含する、方法。 - 請求項1に記載の方法であって、前記検出する工程が、複数の規定されたスペクトル帯で、前記場における個々のPREおよび他の光散乱実体のスペクトル発光特性を逐次的に検出する工程を包含する、方法。
- 請求項1に記載の方法であって、前記照射する工程が、継続時間において変化する光の複数の狭帯域パルスに、前記場を曝露する工程を包含し、および前記検出する工程が、継続時間における変化によって生成される発光の強度における変化を検出する工程を包含する、方法。
- 請求項1に記載の方法であって、少なくともいくつかのPREが非球状であり、前記照射する工程が、入射の異なる方向および/または異なる角度で、偏光に前記場を曝露する工程を包含し、そして前記識別する工程が、入射光の偏光方向または入射の角度の関数として、スペクトル発光特性における変化を検出する工程を包含する、方法。
- 請求項1に記載の方法であって、前記PREが、以下
(i)核形成中心を場に結合し、該核中心を金属増強し、該金属増強プロセスの間、該核形成中心の増強を観察し、そして所望のスペクトル特性のPREが形成されている場合、増強を終結する工程;
(ii)該場において、予め形成されたPREを標的に添加する工程、
(iii)該場において、標的部位でPREを作製する工程、
からなる群より選択される工程によって、該場において形成される、方法。 - 請求項1に記載の方法であって、前記識別する工程が、選択されたタイプのPREについて、互いに相互作用する選択されたPREおよび互いに相互作用しない選択されたPREを識別する、方法。
- 請求項1に記載の方法であって、前記識別する工程が、前記場において別の選択されたタイプのPREから、選択されたタイプのPREを識別する、方法。
- 請求項1に記載の方法であって、前記PREが、表面局在化蛍光分子またはRaman活性分子実体を有し、そして前記検出する工程が、1つ以上の該分子または実体から、それぞれ、プラズモン共鳴誘導性の蛍光発光またはRaman分光法発光を検出する工程を包含する、方法。
- 場において選択されたタイプのPREの総数を決定することにおいて使用するための請求項1に記載の方法であって、前記識別する工程が、構築されたマトリクスにおける選択されたスペクトル発光特性の選択された範囲の値を有するPREの数を計数する工程を包含する、方法。
- 前記場において選択されたスペクトル特性の選択された範囲の値を有するPREの空間的パターンを決定することにおいて使用するための請求項1に記載の方法であって、識別する工程が、PREの相対的な位置の画像を、それらのスペクトル特性値を用いて構築する工程を包含する、方法。
- 請求項13に記載の方法であって、2つの隣接するPRE間の位置が、Rayleigh分解距離未満であり、そして前記検出する工程が、第1の波長の光で前記場を曝露して、該場におけるPREの回折画像を得る工程、第2の波長の光で該場を曝露して、該場におけるPREの第2の回折画像を得る工程、および2つの回折パターンにおけるピーク間の距離を比較する工程を包含する、方法。
- 前記場の環境の変化を審問することにおいて使用するための請求項1に記載の方法であって、前記識別する工程が、該変化の前および後の該場におけるPREの検出されるスペクトル特性の値を比較する工程を包含する、方法。
- 請求項15に記載の方法であって、前記場が、環境の誘電率における変化について審問される、方法。
- 前記場におけるPREの動きを検出することにおいて使用するための請求項1に記載の方法であって、前記検出する工程が、時間の関数として、画像面におけるPREの回折パターンの中心を検出する工程を包含する、方法。
- 分配された複数のPREを有する場を審問するための、請求項1に記載の方法における使用のための装置であって、
該場を照射するための光学的な光源、
該場が該光源によって照射される場合、該場における個々のPREおよび他の光散乱実体のスペクトル発光特性を検出するための光学検出器、
該検出器から受容されるシグナルから、該場に存在する個々のPREおよびこのような他の光散乱実体について測定された1つ以上のスペクトル発光特性値と該場中の各領域を結びつける画像であるマトリクスを構築するための、検出器に作動可能に連結される画像処理器、
該マトリクスにおいて他の光散乱実体から、選択されたスペクトルサインを有するPREを識別するための識別器手段、ならびに
選択されたPREについての情報に基づいて、該場についての情報を表示するための出力手段、
を備える、装置。 - 請求項18に記載の装置であって、前記光源が、前記場上に光を指向するための明視野/暗視野レンズを備える、装置。
- 請求項18に記載の装置であって、前記光源が、それぞれの複数の異なる波長で前記場を照射するための手段を備える、装置。
- 請求項18に記載の装置であって、前記検出器が、照射された場における複数の照射されたPREから同時にスペクトル発光特性を検出し得る、二次元光検出器配列である、装置。
- 請求項18に記載の装置であって、前記検出器が、PREから発光される光をスペクトル的に分離するための手段を備え、そして前記画像処理器が、それぞれの複数の異なる発光波長で、前記場に存在する個々のPREおよびこのような他の光散乱実体について測定された1つ以上の発光スペクトル特性値をもつ該場中の各領域を結びつけるマトックスを形成するために作動する、装置。
- 請求項22に記載の装置であって、前記光学検出器が、その出力が線源に応答するための格子またはプリズム内に送られる線源を構成するように整列される光ファイバーの二次元配列、および検出された光の該線源における各ファイバーのスペクトル光の広がりに応答するための二次元検出器配列を備える、装置。
- 請求項18または22に記載の装置であって、x-y平面において前記光源に対して標的を移動して、前記場における個々の光散乱実体を連続的に照射するための手段をさらに備える、装置。
- 請求項18に記載の装置であって、前記画像処理器が、PREの位置、ならびに、前記場における各光散乱実体について、スペクトル発光曲線の半強度でのピーク位置、ピーク強度、またはピーク幅、画像面におけるピーク半幅、および入射応答の偏光もしくは角度からなる群より選択されるスペクトル特性の値の画像を構築するために作動する、装置。
- 請求項18に記載の装置であって、前記画像処理器が、PREの位置、ならびに、前記場における各光散乱実体について、蛍光発光スペクトルおよびRamanスペクトルからなる群より選択されるスペクトル特性の値の画像を構築するために作動する、装置。
- 請求項18に記載の装置であって、前記識別器手段が、前記場における各光散乱実体についての、ピーク位置、ピーク強度、またはスペクトル発光曲線の半強度でのピーク幅、画像面におけるピーク半幅、および入射応答の偏光または角度の、検出された値に基づいて、該場における全ての他の光散乱実体から、選択されたスペクトルのサインを有するPREを識別するための手段を備える、装置。
- 請求項18に記載の装置であって、前記識別する工程が、選択されたタイプのPREについて、互いに相互作用する選択されたPREおよび互いに相互作用しない選択されたPREを識別するのに、または前記場における他方の選択されたタイプのPREから、一方の選択されたタイプのPREを識別する、装置。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US3867797P | 1997-02-20 | 1997-02-20 | |
| US60/038,677 | 1997-02-20 | ||
| PCT/US1998/002995 WO1998037417A1 (en) | 1997-02-20 | 1998-02-20 | Plasmon resonant particles, methods and apparatus |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2001513198A JP2001513198A (ja) | 2001-08-28 |
| JP2001513198A5 JP2001513198A5 (ja) | 2005-10-06 |
| JP4209471B2 true JP4209471B2 (ja) | 2009-01-14 |
Family
ID=21901272
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP53677498A Expired - Lifetime JP4209471B2 (ja) | 1997-02-20 | 1998-02-20 | プラズモン共鳴粒子、方法、および装置 |
Country Status (8)
| Country | Link |
|---|---|
| US (6) | US6180415B1 (ja) |
| EP (1) | EP0979409B1 (ja) |
| JP (1) | JP4209471B2 (ja) |
| AT (1) | ATE349697T1 (ja) |
| AU (1) | AU748939B2 (ja) |
| CA (1) | CA2280794A1 (ja) |
| DE (1) | DE69836734D1 (ja) |
| WO (1) | WO1998037417A1 (ja) |
Families Citing this family (333)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6490913B1 (en) * | 1995-05-19 | 2002-12-10 | The United States Of America As Represented By The Secretary Of Commerce | Humidity chamber for scanning stylus atomic force microscope with cantilever tracking |
| US6586193B2 (en) * | 1996-04-25 | 2003-07-01 | Genicon Sciences Corporation | Analyte assay using particulate labels |
| ATE357663T1 (de) * | 1996-04-25 | 2007-04-15 | Genicon Sciences Corp | Teilchenförmiges markierungsmittel verwendendes analytassay |
| US6582921B2 (en) | 1996-07-29 | 2003-06-24 | Nanosphere, Inc. | Nanoparticles having oligonucleotides attached thereto and uses thereof |
| US6413786B1 (en) | 1997-01-23 | 2002-07-02 | Union Biometrica Technology Holdings, Inc. | Binding assays using optical resonance of colloidal particles |
| CA2280794A1 (en) * | 1997-02-20 | 1998-08-27 | The Regents Of The University Of California | Plasmon resonant particles, methods and apparatus |
| US6852252B2 (en) | 1997-03-12 | 2005-02-08 | William Marsh Rice University | Use of metalnanoshells to impede the photo-oxidation of conjugated polymer |
| US6344272B1 (en) * | 1997-03-12 | 2002-02-05 | Wm. Marsh Rice University | Metal nanoshells |
| US7144627B2 (en) * | 1997-03-12 | 2006-12-05 | William Marsh Rice University | Multi-layer nanoshells comprising a metallic or conducting shell |
| US6428811B1 (en) | 1998-03-11 | 2002-08-06 | Wm. Marsh Rice University | Temperature-sensitive polymer/nanoshell composites for photothermally modulated drug delivery |
| US6699724B1 (en) | 1998-03-11 | 2004-03-02 | Wm. Marsh Rice University | Metal nanoshells for biosensing applications |
| JP3380744B2 (ja) * | 1998-05-19 | 2003-02-24 | 株式会社日立製作所 | センサおよびこれを利用した測定装置 |
| US6723517B1 (en) * | 1998-06-02 | 2004-04-20 | Minerva Biotechnologies Corporation | Use of self-assembled monolayers to probe the structure of a target molecule |
| JP2002522789A (ja) * | 1998-08-11 | 2002-07-23 | ユニオン バイオメトリカ テクノロジー ホールディングス インコーポレイテッド | コロイド粒子の光学的共鳴を用いた結合分析 |
| US7079241B2 (en) | 2000-04-06 | 2006-07-18 | Invitrogen Corp. | Spatial positioning of spectrally labeled beads |
| IL126776A (en) | 1998-10-27 | 2001-04-30 | Technion Res & Dev Foundation | A method of investing gold |
| JP2002532728A (ja) * | 1998-12-17 | 2002-10-02 | ライカ ミクロジュステムス ハイデルベルク ゲーエムベーハー | 有利には生体試料における種々の構造体を識別検査するための方法 |
| US6633660B1 (en) * | 1999-02-05 | 2003-10-14 | John Carl Schotland | Near-field tomography |
| JP3468149B2 (ja) * | 1999-02-19 | 2003-11-17 | 松下電器産業株式会社 | 微細物体の操作装置および操作方法 |
| US6136541A (en) * | 1999-02-22 | 2000-10-24 | Vialogy Corporation | Method and apparatus for analyzing hybridized biochip patterns using resonance interactions employing quantum expressor functions |
| US6142681A (en) * | 1999-02-22 | 2000-11-07 | Vialogy Corporation | Method and apparatus for interpreting hybridized bioelectronic DNA microarray patterns using self-scaling convergent reverberant dynamics |
| EP1175505A4 (en) * | 1999-04-15 | 2005-04-20 | Vitra Bioscience Inc | COMBINATORY CHEMICAL BANK HOLDERS HAVING BRANDS AT CODING POSITIONS, AND METHODS OF USE |
| US20030096321A1 (en) * | 1999-05-19 | 2003-05-22 | Jose Remacle | Method for the identification and/or the quantification of a target compound obtained from a biological sample upon chips |
| US7074586B1 (en) * | 1999-06-17 | 2006-07-11 | Source Precision Medicine, Inc. | Quantitative assay for low abundance molecules |
| AU6505700A (en) | 1999-08-13 | 2001-03-13 | California Institute Of Technology | Optoelectronic device and method utilizing nanometer-scale particles |
| DE19943704C1 (de) * | 1999-09-08 | 2001-05-10 | Inst Physikalische Hochtech Ev | Affinitätssensor zum Nachweis biologischer und/oder chemischer Spezies und dessen Verwendung |
| US8497131B2 (en) * | 1999-10-06 | 2013-07-30 | Becton, Dickinson And Company | Surface enhanced spectroscopy-active composite nanoparticles comprising Raman-active reporter molecules |
| US20020154803A1 (en) * | 1999-11-01 | 2002-10-24 | Inflamet Ltd. | Biological sample carrier |
| IL132687A0 (en) * | 1999-11-01 | 2001-03-19 | Keren Mechkarim Ichilov Pnimit | System and method for evaluating body fluid samples |
| US6528993B1 (en) * | 1999-11-29 | 2003-03-04 | Korea Advanced Institute Of Science & Technology | Magneto-optical microscope magnetometer |
| US7198939B2 (en) * | 2000-01-28 | 2007-04-03 | Agilent Technologies, Inc. | Apparatus for interrogating an addressable array |
| FR2804784B1 (fr) * | 2000-02-04 | 2003-04-11 | Novatec | Procede universel d'identification et d'authentification d'objets, de vegetaux ou d'etres vivants |
| US6530944B2 (en) | 2000-02-08 | 2003-03-11 | Rice University | Optically-active nanoparticles for use in therapeutic and diagnostic methods |
| US6970811B1 (en) * | 2000-03-22 | 2005-11-29 | Hewlett-Packard Development Company, L.P. | Hardware modeling of LED relative brightness |
| US6760124B1 (en) | 2000-03-22 | 2004-07-06 | Hewlett-Packard Development Company, L.P. | Software determination of led brightness and exposure |
| WO2001096604A2 (en) * | 2000-06-12 | 2001-12-20 | Genicon Sciences Corporation | Assay for genetic polymorphisms using scattered light detectable labels |
| US20020102617A1 (en) * | 2000-08-03 | 2002-08-01 | Macbeath Gavin | Protein microarrays |
| WO2002029076A1 (en) * | 2000-10-03 | 2002-04-11 | Mirari Biosciences, Inc. | Methods and compositions for directed microwave chemistry |
| US20040209303A1 (en) | 2000-10-03 | 2004-10-21 | Martin Mark T. | Methods and compositions for directed microwave chemistry |
| US7348182B2 (en) * | 2000-10-03 | 2008-03-25 | Mirari Biosciences, Inc. | Directed microwave chemistry |
| US6818907B2 (en) * | 2000-10-17 | 2004-11-16 | The President And Fellows Of Harvard College | Surface plasmon enhanced illumination system |
| US7118710B2 (en) * | 2000-10-30 | 2006-10-10 | Sru Biosystems, Inc. | Label-free high-throughput optical technique for detecting biomolecular interactions |
| US6953694B2 (en) * | 2000-12-06 | 2005-10-11 | The Trustees Of Columbia University In The City Of New York | Attachment of second harmonic-active moiety to molecules for detection of molecules at interfaces |
| WO2002054071A1 (en) * | 2001-01-08 | 2002-07-11 | Salafsky Joshua S | Method and apparatus using a surface-selective nonlinear optical technique |
| US6515749B2 (en) * | 2001-01-10 | 2003-02-04 | The United States Of America As Represented By The Secretary Of Commerce | Sensitive and selective chemical sensor with nanostructured surfaces |
| US6861263B2 (en) * | 2001-01-26 | 2005-03-01 | Surromed, Inc. | Surface-enhanced spectroscopy-active sandwich nanoparticles |
| US6696362B2 (en) * | 2001-02-08 | 2004-02-24 | Applied Materials Inc. | Method for using an in situ particle sensor for monitoring particle performance in plasma deposition processes |
| US7361472B2 (en) | 2001-02-23 | 2008-04-22 | Invitrogen Corporation | Methods for providing extended dynamic range in analyte assays |
| US7203342B2 (en) * | 2001-03-07 | 2007-04-10 | Schlumberger Technology Corporation | Image feature extraction |
| US7354733B2 (en) * | 2001-03-29 | 2008-04-08 | Cellect Technologies Corp. | Method for sorting and separating living cells |
| US6838121B2 (en) * | 2001-05-10 | 2005-01-04 | Zyvex Corporation | System and method for controlling deposition parameters in producing a surface to tune the surface's plasmon resonance wavelength |
| US7238472B2 (en) | 2001-05-25 | 2007-07-03 | Nanosphere, Inc. | Non-alloying core shell nanoparticles |
| US7147687B2 (en) * | 2001-05-25 | 2006-12-12 | Nanosphere, Inc. | Non-alloying core shell nanoparticles |
| WO2003001869A2 (en) * | 2001-06-29 | 2003-01-09 | California Institute Of Technology | Method and apparatus for use of plasmon printing in near-field lithography |
| US7473767B2 (en) | 2001-07-03 | 2009-01-06 | The Institute For Systems Biology | Methods for detection and quantification of analytes in complex mixtures |
| US6714299B2 (en) * | 2001-07-13 | 2004-03-30 | Genicon Sciences Corporation | Use of light scattering particles in design, manufacture, and quality control of small volume instruments, devices, and processes |
| WO2003064991A2 (en) * | 2001-07-17 | 2003-08-07 | Salafsky Joshua S | Method and apparatus using a nonlinear optical technique for detection of probe-target interactions in a field |
| EP1421365A1 (en) * | 2001-07-19 | 2004-05-26 | Tufts University | Optical array device and methods of use thereof for screening, analysis and manipulation of particles |
| JP4347053B2 (ja) * | 2001-08-03 | 2009-10-21 | ナノスフェアー インコーポレイテッド | ナノ粒子撮像システムおよび方法 |
| EP1286152B1 (en) * | 2001-08-07 | 2005-10-26 | Sysmex Corporation | Apparatus and method for measuring particle size |
| US20030139886A1 (en) * | 2001-09-05 | 2003-07-24 | Bodzin Leon J. | Method and apparatus for normalization and deconvolution of assay data |
| US20030049866A1 (en) * | 2001-09-05 | 2003-03-13 | Genicon Sciences Corporation | Sample device preservation |
| WO2003025635A1 (en) * | 2001-09-19 | 2003-03-27 | Technion Research & Development Foundation Ltd. | Space-variant subwavelength dielectric grating and applications thereof |
| US6972173B2 (en) * | 2002-03-14 | 2005-12-06 | Intel Corporation | Methods to increase nucleotide signals by raman scattering |
| US7238477B2 (en) * | 2001-09-24 | 2007-07-03 | Intel Corporation | Methods to increase nucleotide signals by Raman scattering |
| US7135054B2 (en) * | 2001-09-26 | 2006-11-14 | Northwestern University | Nanoprisms and method of making them |
| US20030148391A1 (en) * | 2002-01-24 | 2003-08-07 | Salafsky Joshua S. | Method using a nonlinear optical technique for detection of interactions involving a conformational change |
| US20070059760A1 (en) * | 2002-02-21 | 2007-03-15 | Dorsel Andreas N | Multi-featured arrays with reflective coating |
| US6795777B1 (en) * | 2002-03-04 | 2004-09-21 | The Texas A&M University System | Identifying molecules of a sample |
| US7476501B2 (en) * | 2002-03-26 | 2009-01-13 | Intel Corporation | Methods and device for DNA sequencing using surface enhanced raman scattering (SERS) |
| US20040110208A1 (en) * | 2002-03-26 | 2004-06-10 | Selena Chan | Methods and device for DNA sequencing using surface enhanced Raman scattering (SERS) |
| EP1594607A1 (de) * | 2002-05-06 | 2005-11-16 | Universität Tübingen | Verfahren zur erzeugung von mustern von physikalischen, chemischen oder biochemischen strukturen auf trägern |
| EP1508027A4 (en) * | 2002-05-28 | 2009-04-22 | Autogenomics Inc | MICROARRAY DETECTOR AND ASSOCIATED METHODS |
| US20050170356A1 (en) * | 2002-05-28 | 2005-08-04 | Fareed Kureshy | Multi-reagent pack |
| AU2002337504A1 (en) * | 2002-06-08 | 2003-12-22 | Kwon Soo Ha | Method for protein chip analysis by using surface plasmon resonance spectroscopic imaging technology |
| US7361313B2 (en) | 2003-02-18 | 2008-04-22 | Intel Corporation | Methods for uniform metal impregnation into a nanoporous material |
| US6970239B2 (en) * | 2002-06-12 | 2005-11-29 | Intel Corporation | Metal coated nanocrystalline silicon as an active surface enhanced Raman spectroscopy (SERS) substrate |
| US6989897B2 (en) * | 2002-06-12 | 2006-01-24 | Intel Corporation | Metal coated nanocrystalline silicon as an active surface enhanced Raman spectroscopy (SERS) substrate |
| US6788477B2 (en) | 2002-10-22 | 2004-09-07 | Taiwan Semiconductor Manufacturing Co., Ltd. | Apparatus for method for immersion lithography |
| WO2004042403A2 (en) * | 2002-11-04 | 2004-05-21 | Ludwig-Maximilian-Uni Versität München | Methods, device and instrument for detection of analytes |
| US7122384B2 (en) * | 2002-11-06 | 2006-10-17 | E. I. Du Pont De Nemours And Company | Resonant light scattering microparticle methods |
| US20040101822A1 (en) * | 2002-11-26 | 2004-05-27 | Ulrich Wiesner | Fluorescent silica-based nanoparticles |
| EP1445601A3 (en) | 2003-01-30 | 2004-09-22 | Fuji Photo Film Co., Ltd. | Localized surface plasmon sensor chips, processes for producing the same, and sensors using the same |
| US7192703B2 (en) * | 2003-02-14 | 2007-03-20 | Intel Corporation, Inc. | Biomolecule analysis by rolling circle amplification and SERS detection |
| WO2004074508A2 (en) * | 2003-02-15 | 2004-09-02 | Golovlev Valeri V | Method of visualization and quantification of biopolymer molecules immobilized on solid support |
| US20080050842A1 (en) * | 2003-02-15 | 2008-02-28 | Golovlev Valeri V | Method of visualization and quanitification of biopolymer molecules immobilized on solid support |
| AU2003900924A0 (en) * | 2003-02-28 | 2003-03-13 | Medsaic Pty Ltd | Imaging device |
| CN1798858B (zh) * | 2003-04-02 | 2010-06-16 | 西北大学 | 控制纳米颗粒生长的方法 |
| US20040197841A1 (en) * | 2003-04-02 | 2004-10-07 | Apffel James Alexander | Methods and reagents for multiplexed analyses |
| US7976169B2 (en) * | 2003-05-14 | 2011-07-12 | Sun Innovations, Inc. | Waveguide display |
| US20040227694A1 (en) * | 2003-05-14 | 2004-11-18 | Xiao-Dong Sun | System and method for a three-dimensional color image display utilizing laser induced fluorescence of nanopartcles and organometallic molecules in a transparent medium |
| US7002681B1 (en) * | 2003-06-25 | 2006-02-21 | The United States Of America As Represented By The Secretary Of The Navy | Spectroscopy system for the detection of chemicals |
| WO2005029031A2 (en) * | 2003-08-01 | 2005-03-31 | Biacore Ab | Method and apparatus for quantitating surface-binding optical resonance profiles |
| IL157206A0 (en) * | 2003-08-03 | 2004-02-19 | Correlating spatial position of chemical species on a substrate with molecular weight, structure and chemical reactivity | |
| US20050191665A1 (en) * | 2003-12-29 | 2005-09-01 | Xing Su | Composite organic-inorganic nanoclusters |
| US20050147963A1 (en) * | 2003-12-29 | 2005-07-07 | Intel Corporation | Composite organic-inorganic nanoparticles and methods for use thereof |
| US20080076119A9 (en) * | 2003-12-29 | 2008-03-27 | Lei Sun | Composite organic inorganic nanoclusters |
| US7361410B2 (en) * | 2003-12-29 | 2008-04-22 | Intel Corporation | External modification of composite organic inorganic nanoclusters comprising raman active organic compound |
| US20050148100A1 (en) * | 2003-12-30 | 2005-07-07 | Intel Corporation | Methods and devices for using Raman-active probe constructs to assay biological samples |
| WO2005066613A1 (en) * | 2003-12-31 | 2005-07-21 | President And Fellows Of Harvard College | Assay device and method |
| US20050141843A1 (en) * | 2003-12-31 | 2005-06-30 | Invitrogen Corporation | Waveguide comprising scattered light detectable particles |
| JP4261375B2 (ja) * | 2004-01-15 | 2009-04-30 | 富士フイルム株式会社 | 押し形の採取方法 |
| US7243548B2 (en) * | 2004-04-07 | 2007-07-17 | Ut-Battelle, Llc | Surface wave chemical detector using optical radiation |
| SG185329A1 (en) * | 2004-04-23 | 2012-11-29 | Becton Dickinson Co | Surface enhanced spectroscopy-active composite nanoparticles |
| JP2005309295A (ja) * | 2004-04-26 | 2005-11-04 | Nec Corp | 光増幅素子、光増幅装置および光増幅システム |
| US7351588B2 (en) * | 2004-05-19 | 2008-04-01 | Vladimir Poponin | Optical sensor with layered plasmon structure for enhanced detection of chemical groups by SERS |
| EP1766449A4 (en) * | 2004-06-18 | 2009-05-13 | Univ Pennsylvania | OPTICAL CIRCUITS AND SWITCHING ELEMENTS AND METHOD FOR THE PRODUCTION THEREOF |
| US7511285B2 (en) * | 2004-07-16 | 2009-03-31 | The Charles Stark Draper Laboratory, Inc. | Methods and apparatus for biomolecule identification |
| US20070048797A1 (en) * | 2004-08-11 | 2007-03-01 | Xing Su | Composite organic inorganic nanoclusters as carriers and identifiers of tester molecules |
| US7626179B2 (en) * | 2005-09-30 | 2009-12-01 | Virgin Island Microsystems, Inc. | Electron beam induced resonance |
| US20070034518A1 (en) * | 2005-08-15 | 2007-02-15 | Virgin Islands Microsystems, Inc. | Method of patterning ultra-small structures |
| US7791290B2 (en) * | 2005-09-30 | 2010-09-07 | Virgin Islands Microsystems, Inc. | Ultra-small resonating charged particle beam modulator |
| US7586097B2 (en) * | 2006-01-05 | 2009-09-08 | Virgin Islands Microsystems, Inc. | Switching micro-resonant structures using at least one director |
| US8057655B1 (en) * | 2004-08-20 | 2011-11-15 | The Board Of Trustees Of The Leland Stanford Junior University | Sub-micron object control arrangement and approach therefor |
| US9494581B2 (en) | 2004-08-24 | 2016-11-15 | University Of Wyoming | System and method for Raman spectroscopy assay using paramagnetic particles |
| US7776547B2 (en) * | 2004-08-26 | 2010-08-17 | Intel Corporation | Cellular analysis using Raman surface scanning |
| WO2006130165A2 (en) | 2004-09-02 | 2006-12-07 | Vialogy Corp. | Detecting events of interest using quantum resonance interferometry |
| US7612769B2 (en) * | 2004-09-14 | 2009-11-03 | E.I. Du Pont De Nemours And Company | Computer-implemented methods for organizing image data produced by resonant Mie scattering of light from microparticles and resulting data structures |
| US7321422B2 (en) * | 2004-09-16 | 2008-01-22 | Hewlett-Packard Development Company, L.P. | SERS-active structures having nanoscale dimensions |
| ITMI20041801A1 (it) * | 2004-09-21 | 2004-12-21 | Solvay Solexis Spa | Uso di lattici submicrometrici di perfluoropolimeri nella determinazione di interazione molecolari mediante laser light scattering (lls) |
| US7285427B2 (en) * | 2004-10-06 | 2007-10-23 | General Electric Company | Raman-active particles and methods of making and using them |
| JP2006118920A (ja) * | 2004-10-20 | 2006-05-11 | Institute Of Physical & Chemical Research | 相互作用観察方法 |
| US7583379B2 (en) | 2005-07-28 | 2009-09-01 | University Of Georgia Research Foundation | Surface enhanced raman spectroscopy (SERS) systems and methods of use thereof |
| US7880876B2 (en) * | 2004-10-21 | 2011-02-01 | University Of Georgia Research Foundation, Inc. | Methods of use for surface enhanced raman spectroscopy (SERS) systems for the detection of bacteria |
| US7656525B2 (en) * | 2004-10-21 | 2010-02-02 | University Of Georgia Research Foundation, Inc. | Fiber optic SERS sensor systems and SERS probes |
| US7658991B2 (en) * | 2004-10-21 | 2010-02-09 | University Of Georgia Research Foundation, Inc. | Structures having aligned nanorods and methods of making |
| US7738096B2 (en) * | 2004-10-21 | 2010-06-15 | University Of Georgia Research Foundation, Inc. | Surface enhanced Raman spectroscopy (SERS) systems, substrates, fabrication thereof, and methods of use thereof |
| WO2006060734A2 (en) * | 2004-12-03 | 2006-06-08 | Trustees Of Boston University | Nanostructured substrate for for surface enhanced raman scattering |
| US20060147941A1 (en) * | 2004-12-30 | 2006-07-06 | Intel Corporation | Methods and apparatus for SERS assay of biological analytes |
| US20060170444A1 (en) * | 2005-02-02 | 2006-08-03 | Wu Zong M | Novel fluorescent and photoemission apparatus and method for submicron IC failure analysis |
| US7889334B2 (en) * | 2005-03-15 | 2011-02-15 | University Of Georgia Research Foundation, Inc. | Surface enhanced Raman spectroscopy (SERS) systems for the detection of bacteria and methods of use thereof |
| US7940387B2 (en) * | 2005-03-15 | 2011-05-10 | Univeristy Of Georgia Research Foundation, Inc. | Surface enhanced Raman spectroscopy (SERS) systems for the detection of viruses and methods of use thereof |
| JP2006279228A (ja) * | 2005-03-28 | 2006-10-12 | Fuji Xerox Co Ltd | 撮像装置 |
| US20060221335A1 (en) * | 2005-04-04 | 2006-10-05 | Bangalore Arjun S | Method and apparatus for interactive hyperspectral image subtraction |
| US7956991B2 (en) | 2005-04-04 | 2011-06-07 | Chemimage Corporation | Method and apparatus for interactive hyperspectral image subtraction |
| US20060222869A1 (en) * | 2005-04-04 | 2006-10-05 | Yuguang Cai | Electropen lithography |
| US20060250613A1 (en) * | 2005-04-14 | 2006-11-09 | Chem Image Corporation | Method and applications to enhance and image optical signals from biological objects |
| EP1715326A1 (en) * | 2005-04-22 | 2006-10-25 | Universität Heidelberg | Sensor chip with connected non-metallic particles comprising a metallic coating |
| US8084001B2 (en) * | 2005-05-02 | 2011-12-27 | Cornell Research Foundation, Inc. | Photoluminescent silica-based sensors and methods of use |
| US20070111327A1 (en) * | 2005-05-05 | 2007-05-17 | Jay Gregory D | Methods of detecting lubricin |
| US8254227B2 (en) * | 2005-05-10 | 2012-08-28 | The Trustees Of The University Of Pennsylvania | Frequency-modulated coding and data recording and storage using plasmonic nanostructures |
| WO2007053201A2 (en) * | 2005-06-15 | 2007-05-10 | University Of Maryland Biotechnology Institute | Bioassays using plasmonic scattering from noble metal nanostructures |
| US7471388B1 (en) * | 2005-06-22 | 2008-12-30 | University Of Central Florida Research Foundation, Inc. | Frequency tunable resonant apparatus |
| EP1957987B1 (en) * | 2005-08-02 | 2011-09-21 | University of Maryland, Baltimore County | Nanostructures for polarized imaging and receptor/ligand quantization: breaking the diffraction limit for imaging |
| DE102005037531A1 (de) * | 2005-08-09 | 2007-02-15 | Leica Microsystems Cms Gmbh | Verfahren und Vorrichtung zur Reduzierung systematischer Messfehler bei der mikroskopischen Untersuchung von Objekten |
| US20070042510A1 (en) * | 2005-08-19 | 2007-02-22 | Wafermasters, Incorporated | In situ process monitoring and control |
| US20070092870A1 (en) * | 2005-10-20 | 2007-04-26 | Yiping Zhao | Detection of biomolecules |
| FR2893131A1 (fr) * | 2005-11-09 | 2007-05-11 | Centre Nat Rech Scient | Procede de detection de nanoparticules et ses applications |
| US7579609B2 (en) * | 2005-12-14 | 2009-08-25 | Virgin Islands Microsystems, Inc. | Coupling light of light emitting resonator to waveguide |
| US7391032B1 (en) * | 2005-12-21 | 2008-06-24 | Searete Llc | Multi-stage waveform detector |
| US8207907B2 (en) * | 2006-02-16 | 2012-06-26 | The Invention Science Fund I Llc | Variable metamaterial apparatus |
| US7601967B2 (en) * | 2005-12-21 | 2009-10-13 | Searete Llc | Multi-stage waveform detector |
| US7649182B2 (en) * | 2006-10-26 | 2010-01-19 | Searete Llc | Variable multi-stage waveform detector |
| US7649180B2 (en) * | 2005-12-21 | 2010-01-19 | Searete Llc | Multi-stage waveform detector |
| US7427762B2 (en) | 2005-12-21 | 2008-09-23 | Searete Llc | Variable multi-stage waveform detector |
| CA2640385C (en) | 2005-12-23 | 2014-07-15 | Nanostring Technologies, Inc. | Nanoreporters and methods of manufacturing and use thereof |
| US20070155022A1 (en) * | 2005-12-30 | 2007-07-05 | Mineo Yamakawa | Degenerate binding detection and protein identification using Raman spectroscopy nanoparticle labels |
| US20070152781A1 (en) * | 2006-01-05 | 2007-07-05 | Virgin Islands Microsystems, Inc. | Switching micro-resonant structures by modulating a beam of charged particles |
| US7619373B2 (en) * | 2006-01-05 | 2009-11-17 | Virgin Islands Microsystems, Inc. | Selectable frequency light emitter |
| US7470920B2 (en) * | 2006-01-05 | 2008-12-30 | Virgin Islands Microsystems, Inc. | Resonant structure-based display |
| US20070190794A1 (en) * | 2006-02-10 | 2007-08-16 | Virgin Islands Microsystems, Inc. | Conductive polymers for the electroplating |
| US7443358B2 (en) * | 2006-02-28 | 2008-10-28 | Virgin Island Microsystems, Inc. | Integrated filter in antenna-based detector |
| US20070200063A1 (en) * | 2006-02-28 | 2007-08-30 | Virgin Islands Microsystems, Inc. | Wafer-level testing of light-emitting resonant structures |
| US20070200646A1 (en) * | 2006-02-28 | 2007-08-30 | Virgin Island Microsystems, Inc. | Method for coupling out of a magnetic device |
| US7605835B2 (en) * | 2006-02-28 | 2009-10-20 | Virgin Islands Microsystems, Inc. | Electro-photographic devices incorporating ultra-small resonant structures |
| US8259297B1 (en) * | 2006-03-03 | 2012-09-04 | Nanometrics Incorporated | Scanning focal length metrology |
| US7697135B1 (en) * | 2006-03-03 | 2010-04-13 | Nanometrics Incorporated | Scanning focal length metrology |
| JP2009533545A (ja) * | 2006-03-08 | 2009-09-17 | ノースウエスタン ユニバーシティ | ナノプリズムを形成するための2種類の成分からなるナノ粒子中における金の光誘起相分離 |
| US9068917B1 (en) * | 2006-03-14 | 2015-06-30 | Kla-Tencor Technologies Corp. | Systems and methods for inspection of a specimen |
| ITMI20060480A1 (it) * | 2006-03-16 | 2007-09-17 | Solvay Solexis Spa | Usom di perfluoropolimeri nella dtermibnazione della costante di legame recettore-ligando |
| US7923240B2 (en) * | 2006-03-31 | 2011-04-12 | Intel Corporation | Photo-activated field effect transistor for bioanalyte detection |
| US7558490B2 (en) * | 2006-04-10 | 2009-07-07 | Virgin Islands Microsystems, Inc. | Resonant detector for optical signals |
| US20070247729A1 (en) * | 2006-04-25 | 2007-10-25 | Rudolph Technologies, Inc. | Reflective objective |
| US7646991B2 (en) * | 2006-04-26 | 2010-01-12 | Virgin Island Microsystems, Inc. | Selectable frequency EMR emitter |
| US7492868B2 (en) * | 2006-04-26 | 2009-02-17 | Virgin Islands Microsystems, Inc. | Source of x-rays |
| US20070252089A1 (en) * | 2006-04-26 | 2007-11-01 | Virgin Islands Microsystems, Inc. | Charged particle acceleration apparatus and method |
| US7876793B2 (en) | 2006-04-26 | 2011-01-25 | Virgin Islands Microsystems, Inc. | Micro free electron laser (FEL) |
| US20070264023A1 (en) * | 2006-04-26 | 2007-11-15 | Virgin Islands Microsystems, Inc. | Free space interchip communications |
| JP4890926B2 (ja) * | 2006-04-28 | 2012-03-07 | キヤノン株式会社 | 検出方法、およびキット |
| US7986113B2 (en) * | 2006-05-05 | 2011-07-26 | Virgin Islands Microsystems, Inc. | Selectable frequency light emitter |
| US7710040B2 (en) * | 2006-05-05 | 2010-05-04 | Virgin Islands Microsystems, Inc. | Single layer construction for ultra small devices |
| US20070272931A1 (en) * | 2006-05-05 | 2007-11-29 | Virgin Islands Microsystems, Inc. | Methods, devices and systems producing illumination and effects |
| US20070258675A1 (en) * | 2006-05-05 | 2007-11-08 | Virgin Islands Microsystems, Inc. | Multiplexed optical communication between chips on a multi-chip module |
| US7732786B2 (en) * | 2006-05-05 | 2010-06-08 | Virgin Islands Microsystems, Inc. | Coupling energy in a plasmon wave to an electron beam |
| US7728702B2 (en) * | 2006-05-05 | 2010-06-01 | Virgin Islands Microsystems, Inc. | Shielding of integrated circuit package with high-permeability magnetic material |
| US7557647B2 (en) * | 2006-05-05 | 2009-07-07 | Virgin Islands Microsystems, Inc. | Heterodyne receiver using resonant structures |
| US7586167B2 (en) * | 2006-05-05 | 2009-09-08 | Virgin Islands Microsystems, Inc. | Detecting plasmons using a metallurgical junction |
| US7656094B2 (en) | 2006-05-05 | 2010-02-02 | Virgin Islands Microsystems, Inc. | Electron accelerator for ultra-small resonant structures |
| US7728397B2 (en) * | 2006-05-05 | 2010-06-01 | Virgin Islands Microsystems, Inc. | Coupled nano-resonating energy emitting structures |
| US8188431B2 (en) * | 2006-05-05 | 2012-05-29 | Jonathan Gorrell | Integration of vacuum microelectronic device with integrated circuit |
| US7723698B2 (en) * | 2006-05-05 | 2010-05-25 | Virgin Islands Microsystems, Inc. | Top metal layer shield for ultra-small resonant structures |
| US7569836B2 (en) * | 2006-05-05 | 2009-08-04 | Virgin Islands Microsystems, Inc. | Transmission of data between microchips using a particle beam |
| US7718977B2 (en) | 2006-05-05 | 2010-05-18 | Virgin Island Microsystems, Inc. | Stray charged particle removal device |
| US7554083B2 (en) * | 2006-05-05 | 2009-06-30 | Virgin Islands Microsystems, Inc. | Integration of electromagnetic detector on integrated chip |
| US7741934B2 (en) * | 2006-05-05 | 2010-06-22 | Virgin Islands Microsystems, Inc. | Coupling a signal through a window |
| US7583370B2 (en) * | 2006-05-05 | 2009-09-01 | Virgin Islands Microsystems, Inc. | Resonant structures and methods for encoding signals into surface plasmons |
| US7746532B2 (en) * | 2006-05-05 | 2010-06-29 | Virgin Island Microsystems, Inc. | Electro-optical switching system and method |
| US20070257273A1 (en) * | 2006-05-05 | 2007-11-08 | Virgin Island Microsystems, Inc. | Novel optical cover for optical chip |
| US20070258720A1 (en) * | 2006-05-05 | 2007-11-08 | Virgin Islands Microsystems, Inc. | Inter-chip optical communication |
| WO2007129325A2 (en) * | 2006-05-09 | 2007-11-15 | Xceed Imaging Ltd. | Optical sub wavelength super resolution imaging system and method |
| US7573045B2 (en) * | 2006-05-15 | 2009-08-11 | Virgin Islands Microsystems, Inc. | Plasmon wave propagation devices and methods |
| US8980179B2 (en) * | 2006-05-17 | 2015-03-17 | University Of Maryland, Baltimore County | Angular-dependent metal-enhanced fluorescence |
| US20070274365A1 (en) * | 2006-05-26 | 2007-11-29 | Virgin Islands Microsystems, Inc. | Periodically complex resonant structures |
| US7679067B2 (en) * | 2006-05-26 | 2010-03-16 | Virgin Island Microsystems, Inc. | Receiver array using shared electron beam |
| JP4923763B2 (ja) * | 2006-06-09 | 2012-04-25 | 富士ゼロックス株式会社 | 銀三角錐粒子の製造方法、及び銀三角錐粒子 |
| US7655934B2 (en) | 2006-06-28 | 2010-02-02 | Virgin Island Microsystems, Inc. | Data on light bulb |
| JP5151097B2 (ja) * | 2006-09-01 | 2013-02-27 | 株式会社リコー | 複合金属ナノ粒子、複合金属ナノ粒子を含む多光子吸収反応材料と反応生成物、複合金属ナノ粒子を含む多光子吸収反応助剤 |
| JP2008058209A (ja) * | 2006-09-01 | 2008-03-13 | Ricoh Co Ltd | 複合金属ナノ粒子、複合金属ナノ粒子を含む多光子吸収反応材料と反応生成物、複合金属ナノ粒子を含む多光子吸収反応助剤 |
| US8124598B2 (en) * | 2006-09-14 | 2012-02-28 | Sharon Sageman | 7-keto DHEA for psychiatric use |
| US7560716B2 (en) * | 2006-09-22 | 2009-07-14 | Virgin Islands Microsystems, Inc. | Free electron oscillator |
| WO2008108824A2 (en) * | 2006-10-10 | 2008-09-12 | The Trustees Of The University Of Pennsylvania | Lumped plasmonic diode and lumped plasmonic rectifier |
| JP2010508404A (ja) * | 2006-10-30 | 2010-03-18 | エスティーシー. ユーエヌエム | 磁気感受性粒子およびその混合装置 |
| US7714997B2 (en) | 2006-11-07 | 2010-05-11 | Hitachi High-Technologies Corporation | Apparatus for inspecting defects |
| US8078420B2 (en) * | 2006-11-15 | 2011-12-13 | Miller Gary L | Raman spectrometry authentication |
| US7659513B2 (en) * | 2006-12-20 | 2010-02-09 | Virgin Islands Microsystems, Inc. | Low terahertz source and detector |
| FR2910632B1 (fr) * | 2006-12-22 | 2010-08-27 | Commissariat Energie Atomique | Dispositif de codage optique par effet plasmon et methode d'authentification le mettant en oeuvre |
| US7738094B2 (en) | 2007-01-26 | 2010-06-15 | Becton, Dickinson And Company | Method, system, and compositions for cell counting and analysis |
| US20080199880A1 (en) * | 2007-02-21 | 2008-08-21 | Porter Marc D | Spin array method |
| ES2500219T3 (es) | 2007-03-20 | 2014-09-30 | Becton Dickinson And Company | Ensayos que utilizan partículas activas en espectroscopia Raman potenciada en superficie (SERS) |
| GB2447698A (en) * | 2007-03-23 | 2008-09-24 | Univ Exeter | Fabrication of photonic biosensor arrays |
| GB2447696A (en) * | 2007-03-23 | 2008-09-24 | Univ Exeter | Photonic biosensor arrays |
| US20080241853A1 (en) * | 2007-03-29 | 2008-10-02 | Concurrent Analytical, Inc. | Microtiter spin array |
| US8376013B2 (en) | 2008-03-11 | 2013-02-19 | Duke University | Plasmonic assisted systems and methods for interior energy-activation from an exterior source |
| ES2754814T3 (es) * | 2007-04-18 | 2020-04-20 | Sicpa Holding Sa | Ensayos de nanomarcadores de DRPS |
| US7460238B2 (en) * | 2007-04-24 | 2008-12-02 | Corporation De L'ecole Polytechnique De Montreal | Plasmon excitation by the gaussian-like core mode of a photonic crystal waveguide |
| JP5116362B2 (ja) * | 2007-05-28 | 2013-01-09 | 株式会社リコー | バイオセンサ |
| US7990336B2 (en) * | 2007-06-19 | 2011-08-02 | Virgin Islands Microsystems, Inc. | Microwave coupled excitation of solid state resonant arrays |
| JP2009025295A (ja) | 2007-06-21 | 2009-02-05 | Canon Inc | 標的物質検出装置、および標的物質検出方法 |
| JP5157284B2 (ja) | 2007-06-28 | 2013-03-06 | 株式会社リコー | 光増感型複合材料及び三次元メモリ材料と記録媒体、光制限材料と素子、光硬化材料と光造形システム、多光子蛍光顕微鏡用蛍光材料と装置 |
| US8611619B2 (en) * | 2007-08-22 | 2013-12-17 | Phadia Ab | Read-out method and apparatus |
| WO2009029262A1 (en) * | 2007-08-27 | 2009-03-05 | The Regents Of The University Of California | Systems and methods for producing multi-component colloidal structures |
| US20100160274A1 (en) * | 2007-09-07 | 2010-06-24 | Sharon Sageman | 7-KETO DHEA for Psychiatric Use |
| US7791053B2 (en) | 2007-10-10 | 2010-09-07 | Virgin Islands Microsystems, Inc. | Depressed anode with plasmon-enabled devices such as ultra-small resonant structures |
| JP2009098010A (ja) * | 2007-10-17 | 2009-05-07 | Fujifilm Corp | 近接場光学顕微鏡用カンチレバー、それを用いたプラズモン増強蛍光顕微鏡及び蛍光検出方法 |
| WO2009055702A1 (en) * | 2007-10-24 | 2009-04-30 | Purdue Research Foundation | Time of death biosensor |
| US8507785B2 (en) | 2007-11-06 | 2013-08-13 | Pacific Integrated Energy, Inc. | Photo induced enhanced field electron emission collector |
| US8004673B2 (en) * | 2007-11-21 | 2011-08-23 | Hitachi High-Technologies Corporation | Photometric instrument |
| WO2009073121A1 (en) * | 2007-11-29 | 2009-06-11 | Cornell Research Foundation, Inc. | Amplifier and array for measuring small current |
| KR20090070886A (ko) * | 2007-12-27 | 2009-07-01 | 삼성전자주식회사 | 압전 센서를 이용한 바이오 센서에서 신호의 주파수변화량을 증폭하는 방법 |
| JP5094484B2 (ja) * | 2008-03-11 | 2012-12-12 | 富士フイルム株式会社 | 蛍光検出方法および蛍光検出装置 |
| JP2009229103A (ja) * | 2008-03-19 | 2009-10-08 | Toshiba Corp | 金属コロイドの定量方法 |
| JP5097590B2 (ja) * | 2008-03-26 | 2012-12-12 | 富士フイルム株式会社 | ラマン信号測定方法およびラマン信号測定装置 |
| JP5450993B2 (ja) * | 2008-07-14 | 2014-03-26 | 富士フイルム株式会社 | 検出方法、検出用試料セルおよび検出用キット |
| US9182406B2 (en) * | 2008-08-04 | 2015-11-10 | Biodesy, Inc. | Nonlinear optical detection of molecules comprising an unnatural amino acid possessing a hyperpolarizability |
| EP2331704B1 (en) | 2008-08-14 | 2016-11-30 | Nanostring Technologies, Inc | Stable nanoreporters |
| WO2010029471A1 (en) * | 2008-09-09 | 2010-03-18 | Koninklijke Philips Electronics N.V. | Method for determining the presence of a sample on a sample receiving surface |
| JP5707021B2 (ja) * | 2008-09-30 | 2015-04-22 | 株式会社日立ハイテクノロジーズ | 磁場計測装置 |
| US8982353B2 (en) * | 2008-09-30 | 2015-03-17 | Valorisation-Recherche, Limited Partnership | High resolution surface plasmon resonance instrument using a dove prism |
| GB2464747B (en) * | 2008-10-10 | 2013-05-15 | Hai Kang Life Corp Ltd | Method for detection of analyte in microarray of samples and apparatus for performing such method |
| GB2464300A (en) | 2008-10-10 | 2010-04-14 | Univ Dublin City | Microfluidic multiplexed cellular and molecular analysis device and method |
| DK200801722A (en) * | 2008-12-05 | 2010-06-06 | Unisensor As | Optical sectioning of a sample and detection of particles in a sample |
| US20100163759A1 (en) * | 2008-12-31 | 2010-07-01 | Stmicroelectronics S.R.L. | Radiation sensor with photodiodes being integrated on a semiconductor substrate and corresponding integration process |
| US20100197508A1 (en) * | 2009-02-03 | 2010-08-05 | The Administrator of the National Aeronautics and Space Administration, United States of America | Integrated Universal Chemical Detector with Selective Diffraction Array |
| NZ595456A (en) | 2009-03-02 | 2012-12-21 | Genia Photonics Inc | Assessing interactions of a sample with light beams having different wavelengths with the use of an intensity modulation function |
| US8039272B2 (en) | 2009-04-01 | 2011-10-18 | Nova Biomedical | Rapid quantification assay involving concentrated and ligand-coated gold colloid |
| US20100252514A1 (en) * | 2009-04-03 | 2010-10-07 | Min-Ju Chung | Foldable baseball equipment rack |
| JP5908396B2 (ja) | 2009-04-21 | 2016-04-26 | イミュノライト・エルエルシー | insituフォトバイオモジュレーションのための、非侵襲的エネルギーアップコンバージョン方法およびシステム |
| US8697435B2 (en) * | 2009-08-31 | 2014-04-15 | Mbio Diagnostics, Inc. | Integrated sample preparation and analyte detection |
| ES2627063T3 (es) | 2009-10-13 | 2017-07-26 | Nanostring Technologies, Inc | Detección de proteína a través de nanoinformadores |
| US9339813B2 (en) * | 2009-12-18 | 2016-05-17 | Koninklijke Philips N.V. | Substance determining apparatus |
| EP2516681B1 (en) | 2010-02-11 | 2017-10-18 | Nanostring Technologies, Inc | Compositions and methods for the detection of preferably small rnas by bridge hybridisation and ligation |
| EP2372348A1 (en) * | 2010-03-22 | 2011-10-05 | Imec | Methods and systems for surface enhanced optical detection |
| JP5609241B2 (ja) * | 2010-04-28 | 2014-10-22 | セイコーエプソン株式会社 | 分光方法及び分析装置 |
| CN103081126A (zh) | 2010-06-08 | 2013-05-01 | 太平洋银泰格拉泰德能源公司 | 具有增强场和电子发射的光学天线 |
| US8950684B1 (en) * | 2010-10-25 | 2015-02-10 | The Boeing Company | Fluorescent barcode for identification |
| US9036144B2 (en) * | 2010-11-05 | 2015-05-19 | Ondavia, Inc. | Nano-/micro-droplets for the detection of analytes |
| AU2011336707A1 (en) * | 2010-11-29 | 2013-07-04 | Dako Denmark A/S | Methods and systems for analyzing images of specimens processed by a programmable quantitative assay |
| CN102162792B (zh) * | 2011-01-10 | 2012-10-24 | 南京航空航天大学 | 基于表面等离激元共振的hprt体基因突变检测方法 |
| JP5984852B2 (ja) * | 2011-02-28 | 2016-09-06 | コーニンクレッカ フィリップス エヌ ヴェKoninklijke Philips N.V. | 物質決定装置 |
| WO2012129347A1 (en) | 2011-03-21 | 2012-09-27 | Biodesy, Llc | Classification of kinase inhibitors using nonlinear optical techniques |
| US9072473B2 (en) | 2011-03-24 | 2015-07-07 | The Arizona Board Of Regents On Behalf Of The University Of Arizona | In-vivo optical sensor |
| WO2012135340A2 (en) | 2011-03-28 | 2012-10-04 | Nanostring Technologies, Inc. | Compositions and methods for diagnosing cancer |
| US8810789B2 (en) | 2011-11-07 | 2014-08-19 | University Of Georgia Research Foundation, Inc. | Thin layer chromatography-surfaced enhanced Raman spectroscopy chips and methods of use |
| PL2783216T3 (pl) | 2011-11-21 | 2019-03-29 | Abay Sa | Testy immunologiczne ze wzmocnionym sygnałem |
| US20130135617A1 (en) * | 2011-11-30 | 2013-05-30 | General Electric Company | Plasmonic optical transducer |
| US20130196449A1 (en) * | 2012-01-17 | 2013-08-01 | Hewlett-Packard Development Company, L.P. | Electrically driven devices for surface enhanced raman spectroscopy |
| US9395358B2 (en) | 2012-02-05 | 2016-07-19 | Biodesy, Inc. | Methods for detecting allosteric modulators of protein |
| US9938560B2 (en) | 2012-02-05 | 2018-04-10 | Biodesy, Inc. | Methods for identifying modulators of Ras using nonlinear techniques |
| US20130288271A1 (en) | 2012-04-25 | 2013-10-31 | Biodesy, Llc | Methods for detecting allosteric modulators of protein |
| CN107815713B (zh) | 2012-06-22 | 2020-11-17 | 苹果公司 | 白色外观阳极化膜及其形成方法 |
| JP6351180B2 (ja) * | 2012-07-09 | 2018-07-04 | サーモ エレクトロン サイエンティフィック インストルメンツ リミテッド ライアビリティ カンパニー | 分光測定用電動光路長可変セル |
| US9493876B2 (en) * | 2012-09-14 | 2016-11-15 | Apple Inc. | Changing colors of materials |
| TWI688760B (zh) * | 2013-03-11 | 2020-03-21 | 美商克萊譚克公司 | 使用表面增強電場之缺陷偵測 |
| EP3764083A1 (en) | 2013-03-12 | 2021-01-13 | Ventana Medical Systems, Inc. | Digitally enhanced microscopy for multiplexed histology |
| WO2014191003A1 (en) * | 2013-05-28 | 2014-12-04 | Chemometec A/S | Image forming cytometer |
| US20150049332A1 (en) * | 2013-07-30 | 2015-02-19 | The Curators Of The University Of Missouri | Gold nanoisland arrays |
| CN105723195B (zh) * | 2013-08-07 | 2019-09-03 | 撒拉弗生物科学有限责任公司 | 基于显微拉曼的手持式检测仪器及检测方法 |
| CN105764526B (zh) | 2013-08-26 | 2020-12-15 | 生物技术研发公司 | 编码抗唾液酸化路易斯a抗原的人抗体的核酸 |
| US9181629B2 (en) | 2013-10-30 | 2015-11-10 | Apple Inc. | Methods for producing white appearing metal oxide films by positioning reflective particles prior to or during anodizing processes |
| US9839974B2 (en) | 2013-11-13 | 2017-12-12 | Apple Inc. | Forming white metal oxide films by oxide structure modification or subsurface cracking |
| US9097737B2 (en) | 2013-11-25 | 2015-08-04 | Oxford Instruments Asylum Research, Inc. | Modular atomic force microscope with environmental controls |
| US9492840B2 (en) * | 2013-12-02 | 2016-11-15 | Samsung Electronics Co., Ltd. | Methods of removing surface ligand compounds |
| CN104808329B (zh) * | 2014-01-25 | 2017-08-08 | 清华大学 | 一种光学显微镜系统 |
| CA2939975C (en) * | 2014-02-17 | 2022-05-10 | Eaton Limited | Oxygen sensor comprising a tip coated optical fibre with a large diameter |
| US9659360B2 (en) | 2014-02-26 | 2017-05-23 | Georg-August-Universitaet Goettingen Stiftung Oeffentlichen Rechts | Identifying an original object in a forgery-proof way |
| EP3111214B1 (en) * | 2014-02-26 | 2020-09-30 | Lamdagen Corporation | Digital lspr for enhanced assay sensitivity |
| AU2015271685B2 (en) | 2014-06-04 | 2021-02-18 | Biontech Research And Development, Inc. | Human monoclonal antibodies to ganglioside GD2 |
| EP3936622A1 (en) | 2014-06-30 | 2022-01-12 | Bluelight Therapeutics, Inc. | Methods for high throughput analysis of conformation in biological entities |
| TWI691716B (zh) | 2014-08-13 | 2020-04-21 | 美商艾巴希斯公司 | 電漿特異性結合搭配物檢定中之信號放大 |
| WO2016088024A1 (en) | 2014-12-03 | 2016-06-09 | Bombardier Inc. | Online inspection for composite structures |
| EP3037861A1 (en) * | 2014-12-23 | 2016-06-29 | Commissariat à l'Énergie Atomique et aux Énergies Alternatives | Imaging method, and system, for obtaining an super-resolution image of an object |
| EP3237906B8 (en) | 2014-12-23 | 2020-10-28 | Bluelight Therapeutics, Inc. | Attachment of proteins to interfaces for use in nonlinear optical detection |
| CN107430352B (zh) * | 2015-03-25 | 2020-01-21 | Asml荷兰有限公司 | 量测方法、量测设备和器件制造方法 |
| JP2018516358A (ja) | 2015-04-02 | 2018-06-21 | バイオデシー, インコーポレイテッド | 表面選択的非線形光学技法を使用してタンパク質構造を決定するための方法 |
| CN107924477A (zh) | 2015-04-14 | 2018-04-17 | 第资本服务公司 | 用于动态交易卡的系统、方法和设备 |
| EP3317624B1 (en) * | 2015-07-05 | 2019-08-07 | The Whollysee Ltd. | Optical identification and characterization system and tags |
| EP4368992A3 (en) | 2015-07-17 | 2024-08-07 | Bruker Spatial Biology, Inc. | Simultaneous quantification of a plurality of proteins in a user-defined region of a cross-sectioned tissue |
| EP3325650B1 (en) | 2015-07-17 | 2024-01-03 | Nanostring Technologies, Inc. | Simultaneous quantification of gene expression in a user-defined region of a cross-sectioned tissue |
| US9835622B2 (en) * | 2015-08-04 | 2017-12-05 | Abaxis, Inc. | Signal amplification in solution-based plasmonic specific-binding partner assays |
| US10395895B2 (en) * | 2015-08-27 | 2019-08-27 | Mks Instruments, Inc. | Feedback control by RF waveform tailoring for ion energy distribution |
| US11531024B2 (en) | 2015-09-24 | 2022-12-20 | Purdue Research Foundation | Mass tag analysis for rare cells and cell free molecules |
| WO2017087823A1 (en) | 2015-11-18 | 2017-05-26 | Mir Kalim U | Super-resolution sequencing |
| US10809195B2 (en) | 2015-12-23 | 2020-10-20 | Koninklijke Philips N.V. | Optical detection of particles in a fluid |
| EP3397942B1 (en) | 2015-12-30 | 2024-05-08 | Bio-Rad Laboratories, Inc. | Detection and signal processing system for particle assays |
| US9846111B2 (en) * | 2015-12-30 | 2017-12-19 | Bio-Rad Laboratories, Inc. | Optical detection system for particles |
| TW201725385A (zh) * | 2016-01-05 | 2017-07-16 | 財團法人工業技術研究院 | 具有薄層層析之拉曼檢測晶片及分離檢測分析物之方法 |
| US11232940B2 (en) * | 2016-08-02 | 2022-01-25 | Virgin Instruments Corporation | Method and apparatus for surgical monitoring using MALDI-TOF mass spectrometry |
| EP3494382A4 (en) * | 2016-08-22 | 2020-07-15 | Highland Innovations Inc. | DATABASE MANAGEMENT BY SPECTROMETER WITH FLIGHT-TIME ANALYSIS BY MATRIX-SUPPORTED LASER DESORPTION / -IONISATION |
| KR101810846B1 (ko) | 2016-08-23 | 2017-12-20 | 한국기초과학지원연구원 | 원거리장 플라즈모닉 렌즈 및 원거리장 플라즈모닉 렌즈 조립체 |
| US10409052B2 (en) * | 2016-09-28 | 2019-09-10 | University Of Washington | Inverted light-sheet microscope |
| JP6747939B2 (ja) * | 2016-10-28 | 2020-08-26 | 日本電信電話株式会社 | 検出方法及びデバイス |
| KR102476709B1 (ko) | 2016-11-21 | 2022-12-09 | 나노스트링 테크놀로지스, 인크. | 화학적 조성물 및 이것을 사용하는 방법 |
| IL268238B (en) | 2017-01-30 | 2022-09-01 | Abaxis Llc | Tests for a specific plasmon-based solution for co-linking and metallic nanostructures |
| WO2019073069A1 (en) | 2017-10-13 | 2019-04-18 | Boehringer Ingelheim International Gmbh | HUMAN ANTIBODIES AGAINST THOMSEN-NEW ANTIGEN (TN) |
| KR20200121329A (ko) | 2018-02-12 | 2020-10-23 | 나노스트링 테크놀로지스, 인크. | 유전자 및 단백질 발현을 검출하는 생체 분자 프로브 및 방법 |
| AU2019271028A1 (en) | 2018-05-14 | 2020-12-03 | Bruker Spatial Biology, Inc. | Chemical compositions and methods of using same |
| US11698304B2 (en) | 2019-02-15 | 2023-07-11 | Wayne State University | Apparatuses, systems, and methods for detecting materials based on Raman spectroscopy |
| KR102191673B1 (ko) * | 2019-03-04 | 2020-12-17 | 한국과학기술원 | 초소형 렌즈형 광섬유 프로브를 갖는 내시현미경 |
| US20220258232A1 (en) * | 2019-07-31 | 2022-08-18 | Nanyang Technological University | Platform for stand-off and real-time sers sensing of airborne analytes |
| US10613012B1 (en) * | 2019-10-17 | 2020-04-07 | Horiba Instruments Incorporated | Apparatus and method for observation of microscopic movements and counting of particles in colloids |
| EP4067102A1 (en) | 2021-04-02 | 2022-10-05 | Kaunas University of Technology | An optical device with ordered scatterer arrays for secure identity and a method of producing the same |
| CN113281323B (zh) * | 2021-06-29 | 2024-01-26 | 集美大学 | 一种复杂体系中有机污染物特征信息提取方法及其快速检测方法、系统 |
| WO2023243490A1 (ja) * | 2022-06-14 | 2023-12-21 | 国立大学法人徳島大学 | ナノ粒子体、ナノ粒子体を含む複合体、ならびにナノ粒子体に含まれる高分子膜の形成方法 |
Family Cites Families (56)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3856398A (en) | 1972-11-13 | 1974-12-24 | D Taylor | Apparatus and method for wide area, dark field, high resolution autoradiography |
| US3801183A (en) * | 1973-06-01 | 1974-04-02 | Minnesota Mining & Mfg | Retro-reflective film |
| US4099854A (en) | 1976-10-12 | 1978-07-11 | The Unites States Of America As Represented By The Secretary Of The Navy | Optical notch filter utilizing electric dipole resonance absorption |
| US4202626A (en) * | 1978-02-24 | 1980-05-13 | A Patent Partnership | Signature verification and authentication systems |
| NL7807532A (nl) | 1978-07-13 | 1980-01-15 | Akzo Nv | Metaal-immunotest. |
| US4481091A (en) | 1981-02-17 | 1984-11-06 | At&T Bell Laboratories | Chemical processing using electromagnetic field enhancement |
| US4416998A (en) | 1981-04-02 | 1983-11-22 | The Upjohn Company | Silver stain procedure and kit for same |
| US4514085A (en) * | 1982-06-28 | 1985-04-30 | Beckman Instruments, Inc. | Marking and authenticating documents with liquid crystal materials |
| US4645301A (en) * | 1983-02-07 | 1987-02-24 | Minnesota Mining And Manufacturing Company | Transparent sheet containing authenticating image and method of making same |
| US5501949A (en) | 1985-12-10 | 1996-03-26 | Murex Diagnostics Corporation | Particle bound binding component immunoassay |
| US5236826A (en) * | 1985-12-10 | 1993-08-17 | Murex Corporation | Immunoassay for the detection or quantitation of an analyte |
| US4877647A (en) | 1986-04-17 | 1989-10-31 | Kansas State University Research Foundation | Method of coating substrates with solvated clusters of metal particles |
| EP0308537B1 (en) | 1987-09-25 | 1991-08-28 | International Business Machines Corporation | Sensor for converting a distance to optical and further to electrical energy, and surface scanning apparatus using same |
| US4979821A (en) | 1988-01-27 | 1990-12-25 | Ortho Diagnostic Systems Inc. | Cuvette for receiving liquid sample |
| GB8830039D0 (en) * | 1988-12-22 | 1989-02-15 | Renishaw Plc | Raman microscope |
| US5023139A (en) | 1989-04-04 | 1991-06-11 | Research Corporation Technologies, Inc. | Nonlinear optical materials |
| US5338353A (en) | 1989-04-07 | 1994-08-16 | Nippon Shokubai Kagaku Kogyo | Method for production of powder of fine inorganic particles |
| US5376556A (en) | 1989-10-27 | 1994-12-27 | Abbott Laboratories | Surface-enhanced Raman spectroscopy immunoassay |
| US5790693A (en) * | 1990-02-05 | 1998-08-04 | Cummins-Allison Corp. | Currency discriminator and authenticator |
| GB9012099D0 (en) * | 1990-05-31 | 1990-07-18 | Kodak Ltd | Optical article for multicolour imaging |
| FI85768C (fi) | 1990-07-04 | 1992-05-25 | Valtion Teknillinen | Foerfarande foer utfoerning av ytplasmonresonansmaetning samt i foerfarandet anvaendbar givare. |
| US5225900A (en) * | 1990-12-31 | 1993-07-06 | Xerox Corporation | Method of storing information within a reproduction system |
| US5817462A (en) * | 1995-02-21 | 1998-10-06 | Applied Spectral Imaging | Method for simultaneous detection of multiple fluorophores for in situ hybridization and multicolor chromosome painting and banding |
| EP0517930B1 (en) * | 1991-06-08 | 1995-05-24 | Hewlett-Packard GmbH | Method and apparatus for detecting the presence and/or concentration of biomolecules |
| US5249077A (en) | 1991-12-12 | 1993-09-28 | Microvideo Instruments, Inc. | Darkfield illuminator for a microscope slide |
| US5248772A (en) | 1992-01-29 | 1993-09-28 | Coulter Corporation | Formation of colloidal metal dispersions using aminodextrans as reductants and protective agents |
| US5451525A (en) | 1992-02-14 | 1995-09-19 | Coulter Corporation | Method and materials for determining particle count in a flow cytometer |
| CA2076709A1 (en) * | 1992-08-24 | 1994-02-25 | Ulrich J. Krull | Amplified fluorescence emission for chemical transduction |
| US5618063A (en) * | 1992-12-09 | 1997-04-08 | Wallace Computer Services, Inc. | Multicolor heat-sensitive verification and highlighting system |
| DE4244086C2 (de) * | 1992-12-24 | 1994-10-27 | Florin Ernst Ludwig | Verfahren und Vorrichtung zum Nachweis von Oberflächenplasmonen |
| US5485277A (en) * | 1994-07-26 | 1996-01-16 | Physical Optics Corporation | Surface plasmon resonance sensor and methods for the utilization thereof |
| US5479024A (en) | 1994-08-11 | 1995-12-26 | The Regents Of The University Of California | Method and apparatus for performing near-field optical microscopy |
| US5599668A (en) | 1994-09-22 | 1997-02-04 | Abbott Laboratories | Light scattering optical waveguide method for detecting specific binding events |
| US6025202A (en) * | 1995-02-09 | 2000-02-15 | The Penn State Research Foundation | Self-assembled metal colloid monolayers and detection methods therewith |
| US6363164B1 (en) * | 1996-05-13 | 2002-03-26 | Cummins-Allison Corp. | Automated document processing system using full image scanning |
| CA2220551A1 (en) * | 1995-05-12 | 1996-11-14 | Schering Corporation | Surface plasmon resonance based enzymatic assay |
| US5935755A (en) * | 1995-08-21 | 1999-08-10 | Xerox Corporation | Method for document marking and recognition |
| US5633724A (en) * | 1995-08-29 | 1997-05-27 | Hewlett-Packard Company | Evanescent scanning of biochemical array |
| US6174677B1 (en) * | 1995-10-13 | 2001-01-16 | Ut-Battelle, Llc | Advanced surface-enhanced Raman gene probe systems and methods thereof |
| WO1997015821A1 (en) * | 1995-10-25 | 1997-05-01 | University Of Washington | Surface plasmon resonance probe systems based on a folded planar lightpipe |
| ATE357663T1 (de) | 1996-04-25 | 2007-04-15 | Genicon Sciences Corp | Teilchenförmiges markierungsmittel verwendendes analytassay |
| US5717518A (en) * | 1996-07-22 | 1998-02-10 | Kla Instruments Corporation | Broad spectrum ultraviolet catadioptric imaging system |
| CA2280794A1 (en) * | 1997-02-20 | 1998-08-27 | The Regents Of The University Of California | Plasmon resonant particles, methods and apparatus |
| US6344272B1 (en) * | 1997-03-12 | 2002-02-05 | Wm. Marsh Rice University | Metal nanoshells |
| US6002476A (en) * | 1998-04-22 | 1999-12-14 | Chemicon Inc. | Chemical imaging system |
| US6992770B2 (en) * | 2001-01-25 | 2006-01-31 | Fuji Photo Film Co., Ltd. | Sensor utilizing attenuated total reflection |
| US6914668B2 (en) * | 2003-05-14 | 2005-07-05 | International Technologies (Laser) Ltd. | Personal identification verification and controlled substance detection and identification system |
| US7956997B2 (en) * | 2003-05-27 | 2011-06-07 | Optotrace Technologies, Inc. | Systems and methods for food safety detection |
| WO2007081381A2 (en) * | 2005-05-10 | 2007-07-19 | The Regents Of The University Of California | Spinodally patterned nanostructures |
| WO2008048970A2 (en) * | 2006-10-16 | 2008-04-24 | The Arizona Board Of Regents, A Body Corporate Of The State Of Arizona Acting For And On Behalf Of Arizona State University | Synthetic antibodies |
| US7869030B2 (en) * | 2007-01-03 | 2011-01-11 | Research Foundation Of State University Of New York | Aggregates of plural transition metal nanoparticles and plural cyanine dye molecules |
| EP2260108B1 (en) * | 2008-03-03 | 2014-09-17 | Kansas State University Research Foundation | Protease assay |
| WO2009140039A2 (en) * | 2008-04-23 | 2009-11-19 | The Arizona Board Of Regents Acting For And On Behalf Of Arizona State University | Synthetic antibodies |
| US20120065123A1 (en) * | 2009-03-24 | 2012-03-15 | Johnston Stephen A | Synthetic Antibodies |
| WO2010123941A2 (en) * | 2009-04-20 | 2010-10-28 | Enhanced Spectrometry, Inc. | Method for storing and coding information with raman-active substances |
| CA2731892A1 (fr) * | 2011-02-18 | 2012-08-18 | Universite De Montreal | Sondes a diffusion raman a capsule nanometrique, methode de fabrication et utilisation |
-
1998
- 1998-02-20 CA CA002280794A patent/CA2280794A1/en not_active Abandoned
- 1998-02-20 JP JP53677498A patent/JP4209471B2/ja not_active Expired - Lifetime
- 1998-02-20 DE DE69836734T patent/DE69836734D1/de not_active Expired - Lifetime
- 1998-02-20 US US09/027,048 patent/US6180415B1/en not_active Expired - Lifetime
- 1998-02-20 AT AT98906473T patent/ATE349697T1/de not_active IP Right Cessation
- 1998-02-20 AU AU61690/98A patent/AU748939B2/en not_active Expired
- 1998-02-20 EP EP98906473A patent/EP0979409B1/en not_active Expired - Lifetime
- 1998-02-20 WO PCT/US1998/002995 patent/WO1998037417A1/en active IP Right Grant
-
2000
- 2000-12-18 US US09/740,615 patent/US7501288B2/en not_active Expired - Fee Related
-
2009
- 2009-03-05 US US12/398,180 patent/US7981695B2/en not_active Expired - Fee Related
-
2011
- 2011-06-09 US US13/157,151 patent/US8309370B2/en not_active Expired - Fee Related
-
2012
- 2012-10-17 US US13/654,005 patent/US8759116B2/en not_active Expired - Fee Related
-
2014
- 2014-03-26 US US14/226,173 patent/US20140209683A1/en not_active Abandoned
Also Published As
| Publication number | Publication date |
|---|---|
| ATE349697T1 (de) | 2007-01-15 |
| WO1998037417A1 (en) | 1998-08-27 |
| US20090161104A1 (en) | 2009-06-25 |
| US6180415B1 (en) | 2001-01-30 |
| US8309370B2 (en) | 2012-11-13 |
| US20010002315A1 (en) | 2001-05-31 |
| AU748939B2 (en) | 2002-06-13 |
| US7501288B2 (en) | 2009-03-10 |
| US20110244479A1 (en) | 2011-10-06 |
| US7981695B2 (en) | 2011-07-19 |
| JP2001513198A (ja) | 2001-08-28 |
| US20130038868A1 (en) | 2013-02-14 |
| CA2280794A1 (en) | 1998-08-27 |
| US8759116B2 (en) | 2014-06-24 |
| EP0979409B1 (en) | 2006-12-27 |
| EP0979409A1 (en) | 2000-02-16 |
| AU6169098A (en) | 1998-09-09 |
| EP0979409A4 (en) | 2005-08-03 |
| DE69836734D1 (de) | 2007-02-08 |
| US20140209683A1 (en) | 2014-07-31 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4209471B2 (ja) | プラズモン共鳴粒子、方法、および装置 | |
| WO1998037417A9 (en) | Plasmon resonant particles, methods and apparatus | |
| RU2251572C2 (ru) | Анализ аналитов с использованием частиц в качестве метки | |
| JP4247770B2 (ja) | 微粒子標識を使用した分析物アッセイ | |
| US7076092B2 (en) | High-throughput, dual probe biological assays based on single molecule detection | |
| US20090015831A1 (en) | Methods for providing extended dynamic range in analyte assays | |
| AU2002245537A1 (en) | Methods for providing extended dynamic range in analyte assays | |
| Docherty et al. | Multiple labelled nanoparticles for bio detection | |
| US6756014B2 (en) | Biochemical sensor and biochemical testing system using the same | |
| DE4301005A1 (de) | Verfahren und Vorrichtung zur Bewertung der Fitness von Biopolymeren | |
| KR100808762B1 (ko) | 나노 바이오칩 검사 방법 | |
| JP2002253233A (ja) | 生化学センサ及びこれを用いた生化学検査装置 | |
| KR20060066053A (ko) | 분자 화합물을 인식하는 방법 및 장치 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20050214 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20050214 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20070828 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20071106 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20071217 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20071211 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20080128 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20080124 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20080303 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20080219 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20080507 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20080804 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20080930 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20081023 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20111031 Year of fee payment: 3 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20121031 Year of fee payment: 4 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20121031 Year of fee payment: 4 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20131031 Year of fee payment: 5 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| EXPY | Cancellation because of completion of term |