JP4025035B2 - 組織因子抑制因子に対する抗体 - Google Patents
組織因子抑制因子に対する抗体 Download PDFInfo
- Publication number
- JP4025035B2 JP4025035B2 JP2001226122A JP2001226122A JP4025035B2 JP 4025035 B2 JP4025035 B2 JP 4025035B2 JP 2001226122 A JP2001226122 A JP 2001226122A JP 2001226122 A JP2001226122 A JP 2001226122A JP 4025035 B2 JP4025035 B2 JP 4025035B2
- Authority
- JP
- Japan
- Prior art keywords
- tfi
- protease inhibitor
- basic protease
- antibody
- amino acids
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Lifetime
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/81—Protease inhibitors
- C07K14/8107—Endopeptidase (E.C. 3.4.21-99) inhibitors
- C07K14/811—Serine protease (E.C. 3.4.21) inhibitors
- C07K14/8114—Kunitz type inhibitors
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
- A61P7/02—Antithrombotic agents; Anticoagulants; Platelet aggregation inhibitors
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N1/00—Microorganisms; Compositions thereof; Processes of propagating, maintaining or preserving microorganisms or compositions thereof; Processes of preparing or isolating a composition containing a microorganism; Culture media therefor
- C12N1/20—Bacteria; Culture media therefor
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Organic Chemistry (AREA)
- Genetics & Genomics (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Health & Medical Sciences (AREA)
- Wood Science & Technology (AREA)
- Zoology (AREA)
- Biotechnology (AREA)
- Medicinal Chemistry (AREA)
- Biochemistry (AREA)
- General Engineering & Computer Science (AREA)
- Biomedical Technology (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Microbiology (AREA)
- Biophysics (AREA)
- Molecular Biology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Gastroenterology & Hepatology (AREA)
- Hematology (AREA)
- Immunology (AREA)
- Epidemiology (AREA)
- Virology (AREA)
- General Chemical & Material Sciences (AREA)
- Tropical Medicine & Parasitology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Diabetes (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Physics & Mathematics (AREA)
- Plant Pathology (AREA)
- Peptides Or Proteins (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
- Compounds Of Unknown Constitution (AREA)
Description
(発明の背景)
本発明は、組織因子抑制因子(TFI)あるいはリポタンパク質関連凝固抑制因子(LACI)として知られる凝固抑制因子に関する。更に詳細には、本発明は全長TFIを本質的に表現しているcDNAクローンに関する。
【0002】
哺乳動物の血液での凝固カスケードには、2つの異なるシステム、即ち内因性システムと外因性システムとがある。後者の外因性システムは、血液が組織スロンボプラステイン(第III 因子)(以後、組織因子(TF)と言う)にさらされることによって活性化される。この組織因子は、各種の細胞のプラズマメンブレン中で生じるリポタンパク質であり、特に脳及び肺において多く存在する。プラズマ第VII因子あるいはその活性体である第VIIa因子がTFと接触すると、TFとともにカルシウム依存性複合体を形成し、これがタンパク加水分解作用を発揮して第X因子を第Xa因子にまた第IX因子を第IXa因子に活性化する。
【0003】
TFによりイニシエイトされる凝固系の制御に関するこれまでの研究により、TFを血清とともにインキュベーション(粗組織スロンボプラステイン調製物中で)すると、その活性がin vitroで抑制されまたTFをマウスに注入した時の致死効果が阻止されることが明らかにされている。Hjortの精力的な研究によって、この分野におけるそれまでの研究成果が確認され更に研究が進められて、血清中の抑制成分が第VII−TF複合因子を認識することが結論として示された〔Scand.J.Clin.Lab.Invest.9,suppl.27,76〜97(1957)〕。この結論は、プラズマ中で生じるTFの抑制にはCa2+の存在が必要であり(第VII/VIIa因子がTFに結合する際にもCa2+の存在が必要)TFの抑制はEDTAによる2価のカチオンのキレート化によって阻止され及び/又は逆転されるという事実と符合している。
【0004】
最近の研究によって、プラズマあるいは血清中でTFを抑制するには第VIIa因子だけではなく触媒的に活性な第Xa因子と更に他の因子が必要であることが明らかにされている〔BrozeとMiletich、Blood69,150〜155(1987);Sandersら、Ibid.,66,204〜212(1985)〕。この他の因子は組織因子抑制因子(TFI)あるいはリポタンパク質関連凝固抑制因子(LACI)と定義されるものであり、バリウム吸着プラズマ中に存在している。また血清を遠心して密度1.21g/cm3とした時の浮遊液中のリポタンパク質フラクションとともにTFI活性が分離されることから、この因子はリポタンパク質と関連しているものと考えられる。
【0005】
BrozeとMiletich、Blood69,150〜155(1987)及びProc.Natl.Acad.Sci.USA84、1886〜1890(1987)によればHepG2細胞(ヒトヘパトーマセルライン)が、プラズマ中に存在するTFIと同様の特性を有する抑制成分を分泌することが示されている。
【0006】
米国同時係属出顧Ser.No.77,366号明細書(出願日:1987年7月23日)には、HepG2細胞から分泌された精製組織因子抑制因子が記戴されている。この組織因子抑制因子には2つの形態、即ちナトリウムドデシルスルフェートポリアクリルアミドゲル電気泳動(SDS−PAGE)で測定した時に約37,000〜40,000ダルトンの位置に現われるTFI1と約25,000〜26,000ダルトンの位置に現われるTFI2との2つの形態が存在することが見出されている。TFIのアミノ酸配列のN−末端部分が以下のように決定されている。
【化1】
(X−Xは未決定である)
上記米国出願明細書の記載は本明細書に引用する。
【0007】
発明の要旨
本発明によれば、本質的に組織因子抑制因子の全長を表現するcDNAクローンの完全コード配列が見出された。
最初に、ヒト胎盤及び胎児肝λgt11 cDNAライブラリーを、精製TFIに対するラビットポリクローナル血清でスクリーニングした。免疫学的にポジティブなクローンについて、更に125I−第Xa因子結合活性をスクリーニングした。免疫学的にかつ機能的に活性な7個のクローンが得られた。最も長いクローンは胎盤由来λP9であって1.4キロベース(kb)であり、他の6個のクローンは1.0kbであった。部分的DNA配列決定により、1.0kbクローンは1.4kbクローンの1部分と同じ配列を有することが明らかになった。ヌクレオチド配列分析により、λP9は、133bpの5′非コード領域、912bpのオープン・リーディング・フレーム、ストップコドン及び384bpの3′非コード領域を含む1432塩基対(bp)のcDNAインサート配列からなることが明らかにされた。
【0008】
このcDNA配列は、18個のシステイン及び7個のメチオニンを含む276個のアミノ酸からなる31,950ダルトンの蛋白質をコードしている。翻訳されたアミノ配列により、成熟TFI蛋白の先には約28個のアミノ酸からなるシグナルペプチドが存在することが明らかにされた。ここで言う“成熟”TFIとは、本明細書において記載するλP9クローンのATG翻訳コドンによってTFIとメチオニルTFIとの両者を含むように定義されるものであり、このことは以下の記載から理解することができよう。
TFI蛋白には、Asn−X−Ser/Thr(Xは普通の20個のアミノ酸のうちのいずれでもよい)の配列を有する3個のN−結合グリコシル化部位が存在する。これらの部位は、5′非コード領域の後の最初のメチオニンの位置をアミノ酸の位置+1とした時、Asn145,Asn195及びAsn256の位置にある。
【0009】
TFIの翻訳されたアミノ酸配列により、該アミノ酸配列は、高度にマイナスに荷電したN末端部分、高度にプラスに荷電したカルボキシ末端部分、及びKunitz型酵素抑制因子の典型的配列を有する3個の相同ドメインからなる介在配列部分などのいくつかの識別可能な領域を有していることが明らかにされた。相同性についての研究から、TFIは塩基性プロテアーゼ抑制因子遺伝子スーパーファミリーに属するものと考えられる。
【0010】
cDNAクローンλP9を開発するために用いた蛋白材料はヒト胎盤組織であり、この組織は通常の外科的手法による分娩後に広く入手することができる。本発明において用いられているλgt11(lac5 nin5 c1857 s100)はよく知られたものであって、普通に入手することのできるラムダファージ発現ベクターである。その構成及び制限酵素地図は、YoungとDavis,Proc.Natl.Acad.Sci.USA80,1194〜1198(1983)に記載されている。
ノーザン・ブロット分析により、肝由来セルライン、即ちChangリバー、HepG2ヘパトーマ及びSK−HEP−1ヘパトーマは、TFI cDNAとハイブリダイズする2つの主要なmRNA(1.4kbと4.4kb)を有していることが明らかにされた。
【0011】
本明細書に記載した如き、TFIのためのcDNAのクローニング及びその全蛋白配列及び構造の解明により、詳細な構造−機能分析が可能となり、またその生合成的レギュレーションの研究のための基本的知識が得られる。
しかして本発明は、第Xa因子及び第VIIa/TF酵素複合因子を抑制することのできる試薬についての血液凝固カスケード研究にとって重要なものである。
【0012】
図面の詳細な記述
本明細書においては、特許請求の範囲の記載によって本発明を形成すると考えられる対象が特に指摘され明白にクレームされているが、以下に記述する図面についての説明とともに本発明の好ましい態様についての記載により本発明がよりよく理解されるものと考える。
【0013】
図1は、125I−第Xa因子を用いたλgt11クローンのスクリーニングを示したものである。
クローン化ファージの溶解物(0.1ml)を、ドット・プロット装置を用いたサクションによりニトロセルロースペーパー上にスポットし、次いでニトロセルロースペーパーを125I−第Xa因子でプローブし、以後に記述するようにしてオートラジオグラフィーに付した。黒いスポットとして現われているクローンが125I−第Xa因子と結合したポジティブ・クローンである。コントロールλgt11(下の右側のコーナー)及び他のクローンは125I−第Xa因子と結合しなかった。
【0014】
図2は、部分的制限酵素地図及びλP9のインサート配列の配列決定に用いた技法を示している。下に示したスケールはヌクレオチドの位置を示している。太い棒線はコード領域を示しており、細い棒線は5′及び3′非コード領域を示している。制限酵素部位は消化により確認した。矢印はcDNAの配列決走に用いたオーバーラッピングM13クローンを示している。
【0015】
図3および4はヒトTFI cDNAのヌクレオチド配列及び翻訳されたアミノ酸配列を示している。ヌクレオチドの番号は左側に示されており、アミノ酸の番号は右側に示されている。下線を引いた配列は、精製したTFI蛋白と、V8プロテアーゼとトリプシンで消化したペプチドとを用いたアミノ酸配列分析によって独立に確認された配列である。+1のアミノ酸は、5′非コード領域のストップコドンの後にある最初のメチオニンである。N−結合グリコシル化部位は星印で示されている。
【0016】
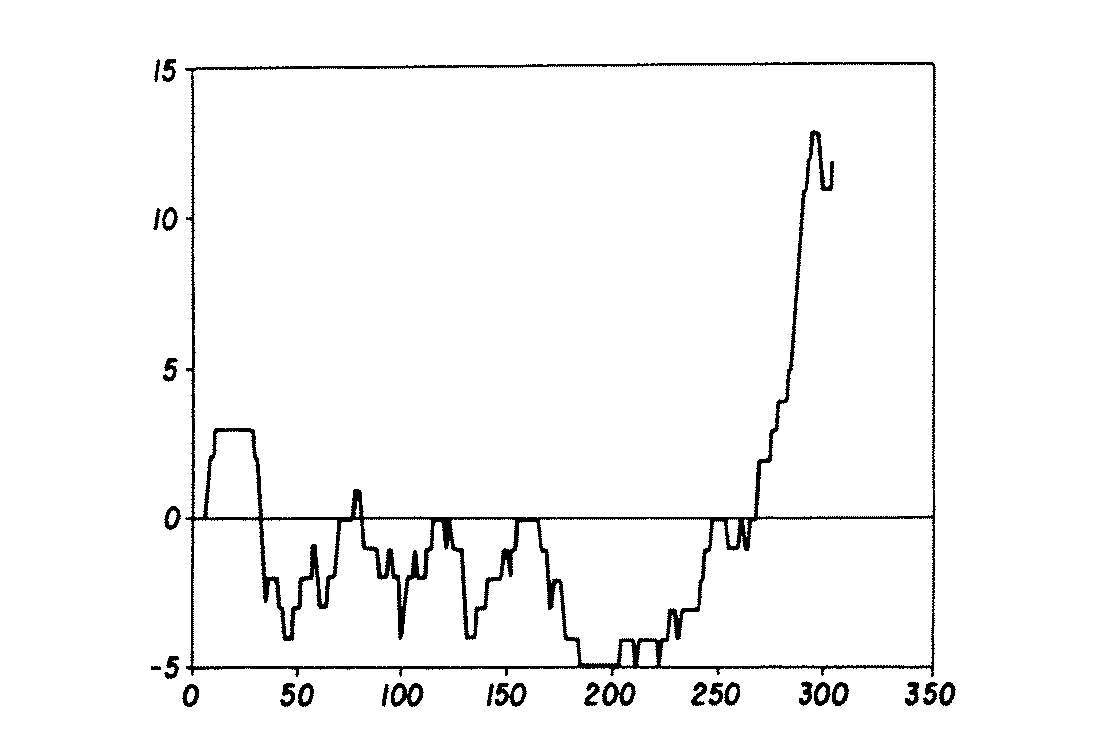
図5は、TFIのアミノ酸配列における電荷分布を示すグラフである。電荷は最初のアミノ酸残基からi番目のアミノ酸残基までを計算したものであり、その電荷の値がi番目の残基に示されている。従って、i番目の位置の値は、最初のアミノ酸残基からi番目のアミノ酸残基までの全ての電荷を合計したものであり、i番目とj番目(j>i)のアミノ酸残基における値の差は、i番目からj番目までのアミノ酸残基の合計電荷を示すものである。
【0017】
図6は、TFIの疎水性プロファイルを示すグラフである。アミノ酸残基の疎水性の指数をアミノ酸残基が蛋白内に埋没された深さ(X線による結晶学的データから得られる)として定義するコンピュータープログラムによって、疎水性プロファイルを分析した〔Kinderaら、J.Protein Chem.4,23〜55(1985)〕。アミノ酸配列に沿った疎水性プロファイルは、IMSL LIbraryのプログラムICSSCUを用いることによって、滑らかになった〔IMSL Library Reference Manual,9th ed.,Institute for Mathematical and Statistical Subroutine Library,Houston,Texas(1982)〕。
【0018】
図7は、TFIの塩基性プロテアーゼ抑制因子ドメインと他の塩基性プロテアーゼ抑制因子とのアラインメントを示す。TFI以外の他の全ての配列は、National Biomedical Research Foundationの蛋白配列データベース(Geogetown University,Washington,D.C.,レリース13,June1987)から得たものである。
1:牛塩基性プロテアーゼ抑制因子前駆体;
2:牛初乳トリプシン抑制因子;
3:牛血清塩基性プロテアーゼ抑制因子;
4:食用カタツムリ・イソ抑制因子K;
5:紅海ウミガメ塩基性プロテアーゼ抑制因子
(1〜79のアミノ酸のみ);
6:ウエスタン・サンド毒ヘビ毒の塩基性プロテアーゼ抑制因子I;
7:リンガルス毒の塩基性プロテアーゼ抑制因子II;
8:ケープ・コブラ毒の塩基性プロテアーゼ抑制因子II;
9:ルッセル毒ヘビ毒の塩基性プロテアーゼ抑制因子II;
10:サンド毒ヘビ毒の塩基性プロテアーゼ抑制因子III ;
11:イースタン・グリーン・マーンバ毒の塩基性プロテアーゼ抑制因子Iホモローグ;
12:ブラック・マーンバ毒の塩基性プロテアーゼ抑制因子B;
13:ブラック・マーンバ毒の塩基性プロテアーゼ抑制因子E;
14:ブラック・マーンバ毒の塩基性プロテアーゼ抑制因子I;
15:ブラック・マーンバ毒の塩基性プロテアーゼ抑制因子K;
16:β−1−ブンガロトキシンB鎖(マイナー);
17:β−1−ブンガロトキシンB鎖(メジャー);
18:β−2−ブンガロトキシンB鎖;
19:ウマ・インターα−トリプシン抑制因子〔アミノ酸1〜57(1);58〜123(2)〕;
20:ブタ・インター−α−トリプシン抑制因子〔アミノ酸1〜57(1);58〜123(2)〕;
21:ウシ・インター−α−トリプシン抑制因子〔アミノ酸1〜57(1);58〜123(2)〕;
22:ヒト・α−1−マイクログロブリン/インター−α−トリプシン抑制因子前駆体〔アミノ酸227〜283(1);284〜352(2)〕;
23:TFI〔アミノ酸47〜117(1);118〜188(2);210〜280(3)〕。
最良のアラインメントを達成するためには16,17,18にギャップが含まれていた。
アミノ酸を示す標準的1文字コードを用いた。
【0019】
図8は、3個の肝由来セルラインから得たRNAのノーザン・ブロット分析を示す。1レーン当り10μgのポリ(A)+RNAを用いた。
レーン1:changリバー細胞、
レーン2:SK−HEP−1ヘパトーマ細胞、
レーン3:HepG2ヘパトーマ細胞.
本明細書においては、標準的生化学命名法を用いており、ヌクレオチド塩基は、アデニン(A);チミン(T);グアニン(G);シトシン(C)として表わされている。対応するヌクレオチドは、例えばデオキシグアノシン−5′−トリホスフェート(dGTP)である。DNAヌクレオチド配列は、便宜上慣用的に1本鎖のみで示されており、1本鎖におけるAはその相補性塩基としてTを内包しており、GはCを内包している。アミノ酸は、以下の表に示すように1文字あるいは3文字で示されている。
【0020】
【表1】
【0021】
本明細書において記載される普通に入手し得る制限酵素は、以下に示す制限配列及び開裂パターン(矢印で示した)を有している。
【化2】
【0022】
本発明の好ましい態様を更に詳細に説明するために、以下に記述する実験を実施した。
【0023】
例1
材料
ヒト胎盤及び胎児肝cDNAライブラリーをClonetechから得た。プロトブロット(Protoblot)・イムノスクリーニング・キットはPromega Biotechから講入した。制限酵素はNew EnglandBiolabsから講入した。牛腸アルカリ・ホスファターゼ、T4DNAリガーゼ、DNAポリメラーゼI(クレノー)、エキソヌクレアーゼIII 及びS1ヌクレアーゼは、Boehringer Mannheimから購入した。dNTPはP.L.Biochemicalsから購入した。5′−〔α−35S〕−チオ−dATP(600Ci/m mol)はAmershamから購入した。配列決定用キット(Sequenase)はUnited States Biochemicalsから購入した。Changリバー細胞(ATCC CCL13)及びHepG2ヘパトーマ細胞(ATCC HB8065)は、アメリカン・タイプ・カルチャー・コレクションから得た。SK−HEP−1ヘパトーマ細胞は、Sloan−Kettering Institute for Cancer ResearchのG.Trempeによって1971年に肝アデノカルシノーマから誘導されたものであり、現在で広く容易に入手可能である。
【0024】
125I−第Xa因子は、ヨード源を用いて放射標識することにより調製した。この比活性は2000dpm/ngであった。放射活性の97%以上は10%トリクロロ酢酸(TCA)により沈澱可能であった。ヨード化蛋白は、SepectrozymeXa(American Diagnostica製)に対してその触媒活性を80%以上保持していた。
【0025】
抗−TFI−IgセファロースTM4Bカラムは以下のようにして調製した。即ち、成熟TFIのアミノ酸3−25の配列に相当する配列を含むペプチド(TFI−ペプチド)を、Biosystemの固相ペプチド合成システムを用いて合成した。TFI−ペプチド(5mg)を、グルタルアルデヒドによりキーホール(Keyhole)・リンペット(lympet)・ヘモシアニン10mgに結合させてコンジュゲートを調製した。2匹のNew Zealandホワイト・ラビットに、フロイント・完全・アジュバンド1mlと、上記コンジュゲート1ml(TFI−ペプチド200μg)を含むホモジェネートを皮内注射して、それぞれ免疫化した。1ケ月後に、フロイント・不完全・アジュバント1mlとコンジュゲート1ml(TFI−ペプチド100μg)を含むホモジェネートで、2匹のラビットをそれぞれブースターした。3ケ月の間、1週間毎に抗血清を採取し、1ケ月毎にブースター注射を行なった。TFI−ペプチドに対する特異的抗体を単離するために、抗血清をTFI−ペプチドセファロース4Bカラムを用いたクロマトグラフィーに付した。カラムを、10倍量のPBS(0.4M Nacl−0.1Mベンズアミジン−1%トリトンTMX−100)及びトリトンX−100を含まない同様の溶液で洗った。0.1Mグリシン/HCl、pH2.2で抗体を溶出させ、直ちに1/10倍量の1Mトリス−OHを加えて中和し、次いで食塩水に対して透析した。単離された抗体を、シアノゲン・ブロマイドで活性化させたセファロース4Bに製造業者(Pharmacia)の指針に従って結合させ、これを細胞培養培地からのTFIの単離に用いた。
【0026】
Changリバー細胞を、BrozeとMiletich,Proc.Nat1.Acad.Sci.USA84,1886〜1890(1987)に記載された方法に従って培養した。ならし培地を、抗−TFI−Igセファロース4Bカラムを用いたクロマトグラフィーに付した。次いでカラムを、10倍量のPBS−1%トリトンX−100とPBSで洗った。結合したTFIを0.1Mグリシン/HCl、pH2.2で溶出した。イムノ・アフィニティーにより単離したTFIを更に分離用ナトリウム・ドデシルスルフェート・ポリアクリルアミドゲル電気泳動(Savant apparatus)により精製した。最終取得物のアミノ酸を分析した所、米国同時係属出願Ser.No.77,366号明細書(出願日:1987年7月23日)に記載されたHePG2細胞から単離したTFIと同様のN末端アミノ酸配列を有していた。単離したChangリバーTFIを用いて、上記したと同じ免疫化プロトコールによりラビットを免疫化した。得られた抗血清は、2重免疫拡散法テストで約100μg/mlの力価を示した。この抗血清を用いてλgt11cDNAライブラリーのイムノ・スクリーニングを行なった。
【0027】
方法
cDNAクローンの単離
抗体を用いた胎盤及び胎児肝cDNAのスクリーニング法、プラーク精製法及びλ−ファージ溶解物とDNAの調製法はWunとKretzmer,FEBSLETT.1,11〜16(1987)に記載されている。抗血清にあらかじめBNN97λgt11溶解物を吸着させ、ライブラリーのスクリーニング用に1/500に希釈した。
【0028】
第Xa因子結合活性のスクリーニング
イソプロピル−β−チオガラクトシドによってイムノ・ポジティブλ−ファージ溶解物あるいはコントロールλgt11から誘導される組換え蛋白について、その第Xa因子結合活性をスクリーニングした。λ−ファージ溶解物(0.1ml)は、ドット−ブロット装置(Bio Rad)を用いてニトロセルロースペーパーで濾過した。次いでニトロセルロースペーパーを、5mg/ml牛血清アルブミン及び2.5mg/ml牛ガンマグロブリンを含むリン酸緩衝化食塩水に浸し、室温で1時間激しく撹拌した。次いで、0.1mg/mlヘパリンを添加した同様の溶液に更に125I−第Xa因子(1.0×106cmp/ml)を溶解した溶液で置換し、更に1時間激しく撹拌した。次いでニトロセルロースペーパーを、0.05%TweenTM20を含むリン酸緩衝化食塩水で洗った。洗浄緩衝液を5分毎に4回交換した。次いでニトロセルロースペーパーを空気中で乾燥し、Kodak XR5nフィルムを用いてオートラジオグラフィー用に調製した。フィルムを1週間さらした後に現像した。
【0029】
ポリ(A) + RNAの調製及びノーザン・ブロッティング
LizardiとEngelbergのナトリウム・パークロレート抽出法〔Anal.Biochem.98,116〜122,(1979)〕により、培養したchangリバー細胞、HepG2ヘパトーマ細胞及びSK−HEP−1ヘパトーマ細胞から全RNAを調製した。製造業者の指針に従い、オリゴ(dT)−セルロース(P−L Biochemica1,タイプ77F)ヘのバッチ吸着によりポリ(A)+RNAを単離した。ノーザン・ブロット分析用に、それぞれのポリ(A)+RNA10μgをグリオキサールで処理し〔Thomas,Methods Enzymol.100,255〜266(1983)〕、10mMリン酸ナトリウム、pH7.0を含む緩衝液でアガロースゲル電気泳動に付した。Bethesda Research LaboratoryのRNAラダー(1adder)を分子量マーカーとして用いた。RNAをニトロセルロースペーパー上にブロットし、次いで80℃で2時間焼いた。λP9クローンのインサートDNAを、ニックトランスレーションにより32Pで放射標識化し、プローブとして用いた〔Maniatisら、Molecular Cloning:A Laboratory Model,Cold Spring Laboratory Harbor,N.Y.,(1982)〕。50%ホルムアミド、5X SSC,50mMリン酸ナトリウム、pH7.0、250μg/ml変性サケスペルマDNA及び1X Denhard溶液を含む溶液5ml中のプローブ(5×106cpm)で42℃で16時間ハイブリダイズさせた。フィルターを、0.1%ナトリウムドデシルスルフェート(SDS)、2X SSSで室温で3回、それぞれ5分間洗った。次いでニトロセルロースペーパーを空気中で乾燥し、Kodak XAR−5フィルム及び増感板を用いて−70℃で3日間オートラジオグラフィーに付した。
【0030】
他の組操えDNA法
クローン化λgt1lDNAの調製、pUC19プラスミド及びM13mp18ベクターでのサブクローニング、エキソヌクレアーゼIII を用いた消化による欠失、及びジデオキ法によるDNA配列決定〔Sangerら、Proc.Natl.Acad.Sci.USA83,6776〜6780(1977)〕は、WunとKretzmer,FEBS Lett.1,11−16(1987)に記載された方法に従って実施した。
LipmamとPearsonによって書かれたプログラムFASTP〔science,227,1435〜1441(1985)〕を用いて、National Biochemical Research Foundationの配列データバンク(レリース13,1987年6月)から相同性を示す蛋白のファミリーを同定し、該ファミリー内で配列のアラインメントを行なった。
【0031】
結果 cDNAライブラリーのスクリーニング
多数のセルラインについて、そのならし培地中にTFIが存在するか否かをスクリーニングした。いくつかの肝由来セルライン、即ちChangリバー、HepG2ヘパトーマ及びSK−HEP−1ヘパトーマが培地中にTFIを分泌することが見出された。初めに、TFIに対する抗血清を用いてヒト胎児肝λgt11cDNAライブラリー(106プラーク・フォーミング・ユニット)をスクリーニングし、15個の免疫学的にポジティブなクローンが得られた。次いで同様の方法により胎盤λgtllcDNAライブラリーをスクリーニングした。106プラーク・フォーミング・ユニットのうち10個の免疫学的にポジティブなクローンが得られた。これらのクローンをプラーク精製し、精製クローンの溶解物についてTFIの機能活性をテストした。イソプロピルチオガラクトシドで誘導したファージの溶解物をニトロセルロースペーパーに吸着せしめ、125I−第Xa因子結合活性をスクリーニングした。上記の免疫学的にポジティブなクローンのいくつかは、ニトロセルロースペーパー上の125I−第Xa因子と結合する能力を示したことが、図1により証明されている。免疫学的にポジティブな胎児肝クローン15個のうち3個、及び免疫学的にポジティブな胎盤クローン10個のうち4個のクローンが125I−第Xa因子結合活性を示した。これらの免疫学的に且つ機能的にポジティブなクローンをEcoRIで消化し、インサート配列のサイズをゲル電気泳動により調べた。胎盤ライブラリー(λP9)から得た1つのクローンは約1.4kbのインサート配列を有しており、他のすべてのクローンは約1.0kbのインサート配列を有していた。部分的DNA配列決定により、1.0kbクローンはより長い1.4kb胎盤クローンの1部分の配列と同じ配列を有していることが判った。従って、完全なDNA配列決定を行なうためにλP9を選択した。
【0032】
TFI cDNA単離物のヌクレオチド配列及びその予想蛋白配列
λP9クローンについて、制限酵素地図の作成、M13サブクローニング及び図2に示した技法を用いた配列決定を実施した。エキソヌクレアーゼIII 欠失法〔Henikoff,Gene28,351〜359(1984)〕により、2本のストランドの両者について全配列を決定し、1432個の塩基からなることが見出された。その配列は図3および4に示した通りである。該配列には、133塩基の5′非コード領域、912ヌクレオチドのオープン・リーディング・フレーム及び387ヌクレオチドの3′非コード領域が含まれている。最初のATGはTAGATGA配列中のヌクレオチド134にあり、その直ぐ後のACAATGA配列中のヌクレオチド146に第2のATGがある。真核細胞のリボゾームによってイニシエートされるためのコンセンサス配列として提案された配列、ACCATGG〔Kozak,Cell,44,283〜292(1982)〕とは、上記の配列は異なるが、これらはイニシエーション配列と考えられる。成熟蛋白のN末端に相当する配列の前に28個のアミノ酸配列がある。これら28個のアミノ酸からなる疎水性セグメントの組成及び長さは、シグナルペプチドに典型的なものである〔Von Heijne,Eur.J.Biochem.133,17〜21(1983);J.Mol.Biol,184,99〜105(1985)〕。シグナルペプチドはAla28−Asp29で開裂し、成熟蛋白を与えると考えられる。成熟TFIとして予想されるアミノ酸配列は、18個のシスティン残基及び7個のメチオニンを含む276個のアミノ酸からなる。成熟TFIの推定蛋白配列に基いて計算される分子量31,950ダルトンは、単離して得た蛋白についてナトリウムドデシルスルフェートポリアクリルアミドゲル電気泳動で調べた分子量37−40kDaよりもいく分小さい。この分子量の相違は、天然蛋白でのグリコシル化の移動性を反映したものと考えられる。成熟蛋白に相当する推定蛋白配列は、Asn−X−Thr/Serの構成を有する3ケのN−結合グリコシル化部位(アミノ酸の位置145,195及び256)を有している。精製した全長TFI及び加水分解された2つの単離体のアミノ酸分析の結果は、cDNA配列から推定される蛋白配列(図3および4の下線を引いた部分)と正確にマッチする。このことは、単離したcDNAクローンはTFIをコードしていることを示している。3′非コード領域はA+Tを豊富に含んでいる(70%A+T)。このクローンには、コンセンサス・ポリアデニル化シグナル、AATAAA〔ProudfootとBrownlee,Nature,252,359〜362(1981)〕も、ポリAテイルも見出されなかった。これは、ライブラリー構築の間に3′末端部分の1部分が失なわれたためと考えられる。
【0033】
電荷分布、疎水性/親水性及び内部相同性
TFIの翻訳されたアミノ酸配列には、27リシン、17アルギニン、11アスパラギン酸及び25グルタミン酸が含まれている。蛋白にそった電荷分布は図5に示したようにかなり高低のあるものである。シグナルペプチド領域には、26個の中性残基とともに2個のプラスに荷電したリシンが含まれていた。成熟蛋白のアミノ末端領域には、高度にマイナスに荷電した配列が含まれていた。最初の7個の残基のうち6個はアスパラギン酸あるいはグルタミン酸であり、この後に更に高度にマイナスに荷電した2個のアミノ酸のダウンストリームがあり、その後にプラスに荷電したリシン残基がある。中心部分は一般的にマイナスに荷電している。カルボキシ末端には高度にプラスに荷電したセグメントがある。TFIのアミノ酸265〜293には、6−共役アルギニン+リシン残基を含むプラスに荷電した14個のアミノ酸がある。
【0034】
TFI蛋白の予想疎水性/親水性プロファイルは図6に示した通りである。シグナルペプチドには、予想されたように高度に疎水性の領域が含まれている。残りの部分はむしろ親水性である。
TFIの翻訳されたアミノ酸配列には、いくつかの区別し得るドメインが含まれている。高度にマイナスに荷電したN末端ドメイン及び高度にプラスに荷電したC末端ドメインに加えて、Kunitz型抑制因子の典型的配列(下記参照)を有する3個の相同ドメインからなる中心部分がある。
【0035】
他の蛋白との相同性
National Biochemical Research Foundationの配列データベースを調べた所、TFIのN末端ドメインとC末端ドメインとは、他の公知蛋白と有意な相同性を有していないことが見出された。しかしながら、3個の内部相同ドメインは、牛膵臓塩基性プロテアーゼ抑制因子(アプロチニン)、毒塩基性プロテアーゼ抑制因子、インター−α−トリプシン抑制因子(図7)などの他の塩基性プロテアーゼ抑制因子の配列とそれぞれ相同性を示した。これらすべての抑制因子にはジスルフィド結合溝造が高度に保持されており、これは注目すべき事実である。これらの相同性から明らかなように、TFIは塩基性プロテアーゼ抑制因子遺伝子スーパーファミリーに属する。
【0036】
ノーザン・ブロッテング
TFI産生肝由来セルライン、即ちChangリバー、HepG2ヘパトーマ及びSK−HEP−1ヘパトーマ細胞からポリ(A)+RNAを精製した。変性アガロースゲル電気泳動によりポリ(A)+RNAを溶解し、ニトロセルロースペーパー上にブロットし、32P−標識化TFI cDNA(λP9)をプローブとして用いて調べた。図8に示したように、2つの主要なハイブリダイゼーションバンドが観察された。これらはテストした3つの全てのセルラインに見られる1.4kb mRNA及び4.4kb mRNAに対応するものである。検出し得る量のTFIを産生しない他のセルラインについてテストしたが、プローブとのハイブリダイゼーションは観察されなかった(データを示していない)。
本明細書の記載から、当業者にとっては本発明の思想及び範囲内にある他の各種の例が自明であろう。これらの例の全ては本明細書のクレームの範囲内のものである。
【図面の簡単な説明】
【図1】125I−第Xa因子を用いたλgt1lクローンのスクリーニングを示した写真である。
【図2】部分的制限酵素地図及びλP9のインサート配列の配列決定に用いた技法を示している。
【図3】ヒトTFI cDNAのヌクレオチド配列及び翻訳されたアミノ酸配列を示している。
【図4】ヒトTFI cDNAのヌクレオチド配列および翻訳されたアミノ酸配列。
【図5】TFIのアミノ酸配列における電荷分布を示すグラフである。
【図6】TFIの疎水性プロファイルを示すグラフである。
【図7】TFIの塩基性プロテアーゼ抑制因子ドメインと他の塩基性プロテアーゼ抑制因子とのアラインメントを示す。
【図8】3個の肝由来セルラインから得たRNAのノーザン・ブロット分析を示す写真である。
Claims (7)
- 組織因子抑制因子(TFI)の、図3および図4に示されるアミノ酸31−53の配列からなる領域に結合する、組織因子抑制因子(TFI)に対する結合特異性を有する単離精製された抗体。
- 以下からなる群から選択されるポリペプチドに結合しない請求項1の抗体:
牛塩基性プロテアーゼ抑制因子前駆体、
牛初乳トリプシン抑制因子、
牛血清塩基性プロテアーゼ抑制因子、
食用カタツムリ・イソ抑制因子K、
紅海ウミガメ塩基性プロテアーゼ抑制因子、
ウエスタン・サンド毒ヘビ毒の塩基性プロテアーゼ抑制因子I、
リンガルス毒の塩基性プロテアーゼ抑制因子II、
ケープ・コブラ毒の塩基性プロテアーゼ抑制因子II、
ルッセル毒ヘビ毒の塩基性プロテアーゼ抑制因子II、
サンド毒ヘビ毒の塩基性プロテアーゼ抑制因子III 、
イースタン・グリーン・マーンバ毒の塩基性プロテアーゼ抑制因子Iホモローグ、
ブラック・マーンバ毒の塩基性プロテアーゼ抑制因子B、E、IおよびK、
β−1−ブンガロトキシンB鎖(マイナー)、
β−1−ブンガロトキシンB鎖(メジャー)、
β−2−ブンガロトキシンB鎖、
ウマ・インター−α−トリプシン抑制因子(アミノ酸1〜57;58〜123)、
ブタ・インター−α−トリプシン抑制因子(アミノ酸1〜57;58〜123)、
ウシ・インター−α−トリプシン抑制因子(アミノ酸1〜57;58〜123)、
ヒト・α−1−マイクログロブリン/インター−α−トリプシン抑制因子前駆体(アミノ酸227〜283;284〜352)。 - ポリクロナル抗体である請求項1または2の抗体。
- 図3および図4に示されるアミノ酸31−53からなるTFIペプチドで精製される請求項1または2の抗体。
- イムノアフィニティーマトリックスに結合した請求項1または2の抗体。
- 前記イムノアフィニティーマトリックスが「セファロースTM4B」である請求項5の抗体。
- 生物学的液体を、TFIに対して結合特異性を有する抗体を結合したイムノアフィニティーマトリックスと接触させ、それにより、該生物学的液体中のTFI及び/又はその断片を、該抗体と結合させる工程を含む、生物学的液体からTFI及び/又はその断片を精製する方法であって、
請求項5または6のイムノアフィニティーマトリックスを使用して、生物学的液体からTFI及び/又はその断片を精製する方法。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US07/123,753 US4966852A (en) | 1987-07-23 | 1987-11-23 | DNA clone of human tissue factor inhibitor |
| US123753 | 1987-11-23 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP18131998A Division JP3565714B2 (ja) | 1987-11-23 | 1998-05-25 | ヒト組織因子抑制因子 |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2005124415A Division JP2005306875A (ja) | 1987-11-23 | 2005-04-22 | 組織因子抑制因子に対する抗体 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2002097200A JP2002097200A (ja) | 2002-04-02 |
| JP4025035B2 true JP4025035B2 (ja) | 2007-12-19 |
Family
ID=22410671
Family Applications (5)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP63183423A Expired - Lifetime JP2836823B2 (ja) | 1987-11-23 | 1988-07-22 | ヒト組織因子抑制因子のdnaクローン |
| JP18131998A Expired - Lifetime JP3565714B2 (ja) | 1987-11-23 | 1998-05-25 | ヒト組織因子抑制因子 |
| JP2001226122A Expired - Lifetime JP4025035B2 (ja) | 1987-11-23 | 2001-07-26 | 組織因子抑制因子に対する抗体 |
| JP2004120081A Pending JP2004201696A (ja) | 1987-11-23 | 2004-04-15 | ヒト組織因子抑制因子 |
| JP2005124415A Withdrawn JP2005306875A (ja) | 1987-11-23 | 2005-04-22 | 組織因子抑制因子に対する抗体 |
Family Applications Before (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP63183423A Expired - Lifetime JP2836823B2 (ja) | 1987-11-23 | 1988-07-22 | ヒト組織因子抑制因子のdnaクローン |
| JP18131998A Expired - Lifetime JP3565714B2 (ja) | 1987-11-23 | 1998-05-25 | ヒト組織因子抑制因子 |
Family Applications After (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2004120081A Pending JP2004201696A (ja) | 1987-11-23 | 2004-04-15 | ヒト組織因子抑制因子 |
| JP2005124415A Withdrawn JP2005306875A (ja) | 1987-11-23 | 2005-04-22 | 組織因子抑制因子に対する抗体 |
Country Status (15)
| Country | Link |
|---|---|
| EP (1) | EP0318451B1 (ja) |
| JP (5) | JP2836823B2 (ja) |
| KR (1) | KR930000274B1 (ja) |
| AT (1) | ATE111518T1 (ja) |
| AU (1) | AU604139B2 (ja) |
| CA (1) | CA1341223C (ja) |
| DE (1) | DE3851511T2 (ja) |
| DK (1) | DK173536B1 (ja) |
| ES (1) | ES2063769T3 (ja) |
| FI (1) | FI93365C (ja) |
| IE (1) | IE65393B1 (ja) |
| IL (1) | IL87171A (ja) |
| NO (2) | NO310466B1 (ja) |
| NZ (1) | NZ225535A (ja) |
| PT (1) | PT88076B (ja) |
Families Citing this family (25)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5378614A (en) * | 1989-08-18 | 1995-01-03 | Novo Nordisk A/S | Vector and method for making tissue factor pathway inhibitor (TFPI) analogues in yeast |
| DK408089D0 (da) * | 1989-08-18 | 1989-08-18 | Novo Nordisk As | Proteiner |
| DE69117545T2 (de) * | 1990-01-25 | 1996-10-31 | Univ Washington | Faktor X-LACI-Hybridprotein |
| DE69118056T2 (de) * | 1990-08-27 | 1996-10-24 | Monsanto Co | Anticoagulatorische Zusammensetzung aus LACI und sulfatierten Polysacchariden |
| DK261490D0 (da) * | 1990-10-31 | 1990-10-31 | Novo Nordisk As | New pharmaceutical compound |
| US5346991A (en) * | 1991-06-13 | 1994-09-13 | Genentech, Inc. | Tissue factor mutants useful for the treatment of myocardial infarction and coagulopathic disorders |
| US5276015A (en) * | 1992-03-18 | 1994-01-04 | Washington University | Method of inhibiting microvascular thrombosis |
| US20030171292A1 (en) | 1992-06-01 | 2003-09-11 | Creasey Abla A. | Method for using lipoprotein associated coagulation inhibitor to treat sepsis |
| US6063764A (en) * | 1992-06-01 | 2000-05-16 | Washington University & Chiron Corp. | Method for using lipoprotein associated coagulation inhibitor to treat sepsis |
| US5455338A (en) * | 1993-11-05 | 1995-10-03 | Zymogenetics, Inc. | DNA encoding novel human kunitz-type inhibitors and methods relating thereto |
| US6057287A (en) | 1994-01-11 | 2000-05-02 | Dyax Corp. | Kallikrein-binding "Kunitz domain" proteins and analogues thereof |
| EP1446140A4 (en) | 2001-10-15 | 2007-03-07 | Novartis Vaccines & Diagnostic | TREATMENT OF HEAVY PNEUMONIA BY ADMINISTRATION OF TFPI (TISSUE FACTOR PATHWAY INHIBITOR) |
| US7153829B2 (en) | 2002-06-07 | 2006-12-26 | Dyax Corp. | Kallikrein-inhibitor therapies |
| WO2003103475A2 (en) | 2002-06-07 | 2003-12-18 | Dyax Corp. | Prevention and reduction of blood loss |
| US7235530B2 (en) | 2004-09-27 | 2007-06-26 | Dyax Corporation | Kallikrein inhibitors and anti-thrombolytic agents and uses thereof |
| SI1981519T1 (en) | 2005-12-29 | 2018-05-31 | Dyax Corp. | INHIBITION PROTEAZE |
| WO2010071894A2 (en) | 2008-12-19 | 2010-06-24 | Baxter International Inc. | Tfpi inhibitors and methods of use |
| CA2744235A1 (en) | 2009-01-06 | 2010-07-15 | Dyax Corp. | Treatment of mucositis with kallikrein inhibitors |
| EP3459564B1 (en) | 2010-01-06 | 2021-10-27 | Takeda Pharmaceutical Company Limited | Plasma kallikrein binding proteins |
| AU2011227714B2 (en) | 2010-03-19 | 2014-09-04 | Takeda Pharmaceutical Company Limited | TFPI inhibitors and methods of use |
| CA2823776A1 (en) | 2011-01-06 | 2012-07-12 | Dyax Corp. | Plasma kallikrein binding proteins |
| CA2837914A1 (en) * | 2011-06-15 | 2012-12-20 | F. Hoffmann-La Roche Ag | Anti-human epo receptor antibodies and methods of use |
| WO2013141965A1 (en) | 2012-03-21 | 2013-09-26 | Baxter International Inc. | Tfpi inhibitors and methods of use |
| AU2016366557B2 (en) | 2015-12-11 | 2024-01-25 | Takeda Pharmaceutical Company Limited | Plasma kallikrein inhibitors and uses thereof for treating hereditary angioedema attack |
| US12528880B2 (en) | 2020-01-13 | 2026-01-20 | Takeda Pharmaceutical Company Limited | Plasma kallikrein inhibitors and uses thereof for treating pediatric hereditary angioedema attack |
Family Cites Families (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4775624A (en) * | 1985-02-08 | 1988-10-04 | Eli Lilly And Company | Vectors and compounds for expression of human protein C |
| IL87172A (en) * | 1987-07-23 | 1994-12-29 | Univ Washington | Method of isolating highly purified tissue factor inhibitor |
-
1988
- 1988-07-21 IL IL8717188A patent/IL87171A/en not_active IP Right Cessation
- 1988-07-22 NZ NZ225535A patent/NZ225535A/en unknown
- 1988-07-22 PT PT88076A patent/PT88076B/pt not_active IP Right Cessation
- 1988-07-22 DK DK198804134A patent/DK173536B1/da not_active IP Right Cessation
- 1988-07-22 AU AU19287/88A patent/AU604139B2/en not_active Expired
- 1988-07-22 NO NO19883270A patent/NO310466B1/no not_active IP Right Cessation
- 1988-07-22 FI FI883487A patent/FI93365C/fi active IP Right Grant
- 1988-07-22 AT AT88870127T patent/ATE111518T1/de not_active IP Right Cessation
- 1988-07-22 EP EP88870127A patent/EP0318451B1/en not_active Expired - Lifetime
- 1988-07-22 DE DE3851511T patent/DE3851511T2/de not_active Expired - Lifetime
- 1988-07-22 CA CA000572753A patent/CA1341223C/en not_active Expired - Fee Related
- 1988-07-22 KR KR1019880009237A patent/KR930000274B1/ko not_active Expired - Lifetime
- 1988-07-22 JP JP63183423A patent/JP2836823B2/ja not_active Expired - Lifetime
- 1988-07-22 IE IE224388A patent/IE65393B1/en not_active IP Right Cessation
- 1988-07-22 ES ES88870127T patent/ES2063769T3/es not_active Expired - Lifetime
-
1998
- 1998-05-25 JP JP18131998A patent/JP3565714B2/ja not_active Expired - Lifetime
-
2001
- 2001-07-20 NO NO20013608A patent/NO20013608D0/no not_active Application Discontinuation
- 2001-07-26 JP JP2001226122A patent/JP4025035B2/ja not_active Expired - Lifetime
-
2004
- 2004-04-15 JP JP2004120081A patent/JP2004201696A/ja active Pending
-
2005
- 2005-04-22 JP JP2005124415A patent/JP2005306875A/ja not_active Withdrawn
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4025035B2 (ja) | 組織因子抑制因子に対する抗体 | |
| US5849875A (en) | Human tissue factor inhibitor | |
| Wun et al. | Cloning and characterization of a cDNA coding for the lipoprotein-associated coagulation inhibitor shows that it consists of three tandem Kunitz-type inhibitory domains. | |
| US7060805B2 (en) | Methods for isolating tissue factor inhibitor | |
| Deutsch et al. | Sequencing of bovine enamelin (“tuftelin”) a novel acidic enamel protein | |
| Sallenave et al. | Characterization and gene sequence of the precursor of elafin, an elastase-specific inhibitor in bronchial secretions | |
| US6197519B1 (en) | Pancreas-derived serpin | |
| MXPA97008427A (en) | Serpina derived from pancr | |
| AU711113B2 (en) | Novel serpin derived from human hypothalamus | |
| US6025143A (en) | Antibodies directed against peptides derived from the SMR1 polypeptide | |
| JP2533869B2 (ja) | Husi―i型インヒビタ―の生物学的活性を有するタンパク質をコ―ドするdna配列、前記dna配列を含む組換え体クロ―ニングベクタ―及び前記ベクタ―により形質転換された細菌 | |
| US20030190637A1 (en) | Mutations in spink5 responsible for netherton's syndrome and atopic diseases | |
| DK175431B1 (da) | Antistoffer som binder fragmenter af vævsfaktorinhibitor (TFI), sammensætninger omfattende disse antistoffer, og fremgangsmåde til anvendelse af en immunoaffinitetsmatrix omfattende et sådant antistof til at oprense et polypeptid fra et biologisk fluidum | |
| DK174754B1 (da) | Humane vævsfaktorinhibitor (TFI), antistof med bindingsspecificitet herfor, fremgangsmåde til anvendelse af en TFI-peptid-kolonne til at oprense et antistof og fremgangsmåder til detektion af TFI eller et polypeptid omfattende.... | |
| CARMICHAEL et al. | Chemistry and biology of secretory leukoprotease inhibitor | |
| JP3558364B2 (ja) | 新規ポリペプチド |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20040330 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20040630 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20040705 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20041004 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20050104 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20050404 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20050502 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20050512 |
|
| A912 | Re-examination (zenchi) completed and case transferred to appeal board |
Free format text: JAPANESE INTERMEDIATE CODE: A912 Effective date: 20050826 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20060707 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20060712 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20070604 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20070803 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20071004 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20081012 Year of fee payment: 1 |
|
| EXPY | Cancellation because of completion of term |