JP4007828B2 - 低分子量ポリフェニレンエーテルの製造方法 - Google Patents
低分子量ポリフェニレンエーテルの製造方法 Download PDFInfo
- Publication number
- JP4007828B2 JP4007828B2 JP2002063626A JP2002063626A JP4007828B2 JP 4007828 B2 JP4007828 B2 JP 4007828B2 JP 2002063626 A JP2002063626 A JP 2002063626A JP 2002063626 A JP2002063626 A JP 2002063626A JP 4007828 B2 JP4007828 B2 JP 4007828B2
- Authority
- JP
- Japan
- Prior art keywords
- polyphenylene ether
- group
- substituted
- compound
- molecular weight
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 0 Cc1ccc(*)c(*)c1O Chemical compound Cc1ccc(*)c(*)c1O 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G65/00—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule
- C08G65/34—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule from hydroxy compounds or their metallic derivatives
- C08G65/38—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule from hydroxy compounds or their metallic derivatives derived from phenols
- C08G65/44—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule from hydroxy compounds or their metallic derivatives derived from phenols by oxidation of phenols
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08L—COMPOSITIONS OF MACROMOLECULAR COMPOUNDS
- C08L71/00—Compositions of polyethers obtained by reactions forming an ether link in the main chain; Compositions of derivatives of such polymers
- C08L71/08—Polyethers derived from hydroxy compounds or from their metallic derivatives
- C08L71/10—Polyethers derived from hydroxy compounds or from their metallic derivatives from phenols
- C08L71/12—Polyphenylene oxides
- C08L71/123—Polyphenylene oxides not modified by chemical after-treatment
-
- H—ELECTRICITY
- H05—ELECTRIC TECHNIQUES NOT OTHERWISE PROVIDED FOR
- H05K—PRINTED CIRCUITS; CASINGS OR CONSTRUCTIONAL DETAILS OF ELECTRIC APPARATUS; MANUFACTURE OF ASSEMBLAGES OF ELECTRICAL COMPONENTS
- H05K1/00—Printed circuits
- H05K1/02—Details
- H05K1/03—Use of materials for the substrate
- H05K1/0313—Organic insulating material
- H05K1/032—Organic insulating material consisting of one material
- H05K1/0326—Organic insulating material consisting of one material containing O
Landscapes
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Organic Chemistry (AREA)
- Polyethers (AREA)
Description
【発明の属する技術分野】
本発明は効率的な低分子量ポリフェニレンエーテルの製造方法、およびこの方法で得られた低分子量のポリフェニレンエーテルに関するものである。
【0002】
【従来の技術】
ポリフェニレンエーテルは加工性・生産性に優れ、溶融射出成形法や溶融押出成形法などの成形方法により所望の形状の製品・部品を効率よく生産できるため、電気・電子分野、自動車分野、その他の各種工業材料分野、食品・包装分野の製品・部品用の材料として幅広く用いられている。
ポリフェニレンエーテルを製造する方法としては、特公昭36−18692号公報、米国特許第3306875号明細書、同3344116号、同3432466号をはじめ多くの製法が提案されている。これらの公知の公報において、工業的に最も重要なモノマーは2,6−ジメチルフェノールであり、このモノマーを使用することにより工業上きわめて重要なポリフェニレンエーテルが得られている。
【0003】
一般にポリフェニレンエーテルを製造するに関して低分子量体が生成する状況の場合には、副生成物が多くなったり、収率が低下することが知られている。
しかし低分子量のオリゴマー領域のポリフェニレンエーテルは用途が殆どなかったため意図的に作られることはなく、通常は分子量を大きくして利用価値のある高分子量のポリフェニレンエーテルを得るために低分子量のものができないように改良が加えられてきた。米国特許3432469号明細書において、不純物を除く中間段階として低分子量体を経由しているが、これが目的でないことは第二段の重合により高分子量体としていることからも明らかである。
【0004】
しかしながら最近、通常の高分子量ポリフェニレンエーテルよりも、きわめて低分子量のポリフェニレンエーテルが他の樹脂の改質や、電子材料用途に対して有効であることが期待されてきており、極低分子量のポリフェニレンエーテルの効率的な製造方法が望まれている。
【0005】
比較的低分子量のポリフェニレンエーテルの製造方法として米国特許3440217号には、2,4,6−トリメチルフェノールを加えることでその添加量に応じ得られるポリフェニレンエーテルの分子量が変化すること、また同明細書中には、溶媒としてポリフェニレンエーテルの良溶媒(例えばベンゼン、トルエン、キシレン)とポリフェニレンエーテルの非溶媒(例えばケトン、エーテル、アルコール)の混合溶媒を用い、良溶媒/非溶媒の比を変えることにより種々の分子量のポリマーが得られるがこの方法は不正確で要求する分子量のポリマーを得る方法としては適当なものではないと述べられている。
【0006】
また特公昭36−18692号公報明細書中には、アルコール類としてn−プロパノールを用い、良溶媒に対してその量の増大に伴い分子量が減少することが示されている。
更に特公昭50−6520号公報にはポリフェニレンエーテルの良溶媒として芳香族炭化水素(例えばベンゼン、トルエン、キシレン等)、ポリフェニレンエーテルの貧溶媒として脂肪族炭化水素(例えばn−ヘキサン、イソヘキサン、n−ヘプタン等)の混合溶媒中で実施された改良方法が開示されているが、実施例中でも明白なようにηsp/cが0.1dl/g以下となるような領域の極低分子量域に至っては収率が低下するという問題が発生している。また同公報明細書中並びに比較例中には生成水やアミン類が反応系内に均一に存在した状態で反応を進めると、オリゴポリフェニレンエーテルが粒子を不均一状態に生じた場合に反応容器などに付着しやすくなる欠点があると記載されている。
【0007】
上記の様な低分子量ポリフェニレンエーテルの製造方法では、いずれもポリフェニレンエーテルの良溶媒(例えばベンゼン、トルエン、キシレン等)を使用しており、該良溶媒は得られたポリフェニレンエーテルに対して親和性が良いため良溶媒を含む溶媒を用いる場合、ηsp/cが0.1dl/g以下となるような領域の極低分子量では反応器へのスケールの発生や収率が低下する問題、ポリフェニレンエーテルの良溶媒をポリフェニレンエーテル中から洗浄、乾燥により除去させる設備が過大となったり、その設備の温度コントロールに関してきわめて神経質にならざるを得ないという問題点があった。
【0008】
特に最近の状況においてはηsp/cが0.1dl/g前後あるいはそれ以下の極めて低分子量のポリフェニレンエーテルが希求されている状態であるが、上記方法で効率よく得られる低分子量ポリフェニレンエーテルのηsp/cは低くても0.2dl/g付近に留まっているのが現状である。
特開昭62−39628号公報では数平均分子量が2800未満の低分子量ポリフェニレンエーテルを製造するに関し、水を含有する炭素数1から5の単官能性アルコールを用いて行う改良方法が示されている。しかし該明細書中に記載されているように収率が95%までしか得られない(実際に実施例では90%未満である)こと、また実施例中に記載されているように極めて重合に時間がかかるという問題を有し、工業的には効率的な方法ではない。
【0009】
最近、極限粘度で0.08から0.16dl/gの低分子量ポリフェニレンエーテルの製造方法として、米国特許6211327号並びにWO00/46273号では低分子量ポリフェニレンエーテルの重合溶液から水性相に触媒成分を除去し、次いでポリフェニレンエーテル溶液からポリフェニレンエーテルの良溶媒を直接脱気(例えば脱気押出機などを用いて)する事により、低分子量ポリフェニレンエーテルを製造する方法が記載されている。
【0010】
この方法はηsp/cが0.1dl/g前後あるいはそれ以下の極めて低分子量のポリフェニレンエーテルの製造に関して、収率問題が殆どない改良された方法ではあるものの、製品中に好ましくない酸化体が残存し、ポリフェニレンエーテルの色調が悪くなったり、製品の性能に好ましくない影響を与えるなど問題点が多い方法である。
【0011】
【発明が解決しようとする課題】
上記従来技術において明らかなように、必要とされている極めて低分子量のポリフェニレンエーテルを意図的に製造しようとするときの解決し得ない問題点は、極低分子量では反応器へのスケールの発生や収率が低下する問題、良溶媒を使用するに当たっては、洗浄や乾燥により除去させる設備が過大となったり、その設備の温度コントロールに関してきわめて神経質にならざるを得ないという問題、製品中に好ましくない酸化体が残存し、ポリフェニレンエーテルの色調が悪くなったり、製品の性能に好ましくない影響を与えるという問題などである。
よって上記問題点を有しない低分子量ポリフェニレンエーテルの製造方法に関して、根本的な解決方法が望まれていた。
【0012】
【課題を解決するための手段】
本発明者らは上記問題点を有しない低分子量ポリフェニレンエーテルの製造方法に関して、鋭意努力を重ねた結果、本発明に至った。即ち、本発明は、
1.触媒と酸素含有ガスを用いてフェノール性化合物を酸化重合させるポリフェニレンエーテルの製造方法において、2種以上のアルコールからなり、キシレンの含有量が0〜5重量%である混合溶媒を重合溶媒とし、かつ、触媒の構成成分が銅化合物、ハロゲン化合物および一般式(1)で表されるジアミン化合物からなる触媒を用いることを特徴とする、30℃において0.5g/dlの濃度のクロロホルム溶液で測定された還元粘度(ηsp/c)が0.04〜0.20dl/gの低分子量ポリフェニレンエーテルの製造方法、
【0013】
【化4】
【0014】
(式中、R1,R2,R3,R4はそれぞれ独立に水素、炭素数1から6の直鎖状または分岐状アルキル基で、全てが同時に水素ではない。R5は炭素数2から5の直鎖状またはメチル分岐を持つアルキレン基である)
2.該フェノール性化合物が、一般式(2)で表される一価フェノール化合物である1記載の方法、
【0015】
【化5】
【0016】
(式中、R6,R7,R8は各々独立の置換基を表し、R6はアルキル基,置換アルキル基,アラルキル基,置換アラルキル基,アリール基,置換アリール基,アルコキシ基,置換アルコキシ基であり、R7,R8はR6について定義されたものと同一の基に加え更に水素,ハロゲンであっても良い)
3.該フェノール性化合物が、一般式(3)で表される二価フェノール化合物を含有する1または2記載の方法、
【0017】
【化6】
【0018】
(式中、R9、R10は各々同一または異なる置換基を表し、水素、アルキル基,置換アルキル基,アラルキル基,置換アラルキル基,アリール基,置換アリール基,アルコキシ基,置換アルコキシ基,ハロゲンを表し、Xは脂肪族炭化水素残基及びそれらの置換誘導体、酸素、イオウ、スルホニル基を表し、R10,Xの結合位置はフェノール水酸基に対してオルソ位またはパラ位を表す)
【0019】
4.触媒の構成成分として、更に3級モノアミン化合物または2級モノアミン化合物をそれぞれ単独で、またはこれらを組み合わせて含む1〜3のいずれかに記載の方法、
5.重合溶媒が、メタノールと炭素数が2個以上のアルコールの混合溶媒からなる1〜4のいずれかに記載の方法、
6.重合溶媒が、メタノールと炭素数が6個以上のアルコールの混合溶媒からなる1〜4のいずれかに記載の方法に関する。
【0020】
以下本発明を詳細に説明する。
本発明における重合溶媒は以下のような条件が必要である。即ち、該重合溶媒が2種以上のアルコールからなりポリフェニレンエーテルの良溶媒を実質的に含まない混合溶媒を重合溶媒として用いる必要がある。
ポリフェニレンエーテルの良溶媒とは、ベンゼン、トルエン、キシレン(o−、m−、p−の各異性体を含む)、エチルベンゼン、スチレン等の芳香族炭化水素、クロロホルム、塩化メチレン、1,2−ジクロロエタン、クロロベンゼン、ジクロロベンゼン等のハロゲン化炭化水素、ニトロベンゼンのようなニトロ化合物が挙げられる。
また若干の貧溶媒性を持ってはいるものの良溶媒に分類されるものとしては、ペンタン、ヘキサン、ヘプタン、シクロヘキサン、シクロヘプタン等の脂肪族炭化水素類、酢酸エチル、ギ酸エチル等のエステル類、テトラヒドロフラン、ジエチルエーテル等のエーテル類、ジメチルスルホキシド等が例示される。
【0021】
本発明においてはこのような低分子量ポリフェニレンエーテルの良溶媒を実質的に含まないことが必要である。実質的に含まないとは、30℃において0.5g/dlの濃度のクロロホルム溶液で測定された還元粘度(ηsp/c)が0.04〜0.20dl/gのポリフェニレンエーテルを殆ど溶解しない重合溶媒であればよいということ、並びに本発明の効果(即ち、極低分子量のポリフェニレンエーテルの収率の驚くべき改善効果、スケール等のトラブルの改善、品質の良い低分子量ポリフェニレンエーテルの製造)を妨げない程度であれば含まれても良いということも意味している。従って全く含まれないという意味ではないことに注意すべきである。例えば、多量のメタノールとエタノールのアルコール混合溶媒中に少量(例えば5%程度)のキシレンを含む溶媒は、30℃において0.5g/dlの濃度のクロロホルム溶液で測定された還元粘度(ηsp/c)が0.04〜0.20dl/gのポリフェニレンエーテルを殆ど溶解しない重合溶媒であって、この場合には収率も良いし、このように調整された混合溶媒の場合には反応器へのスケール発生は極めて抑制されうる。
【0022】
実質的に良溶媒がどこまで含まれても良いかについては、良溶媒のポリフェニレンエーテルに対する親和性の程度によって異なるため一概にはいえず、それぞれの溶媒種によって異なることは当然である。しかしながら本発明においてはポリフェニレンエーテルの良溶媒を全く含んでいない方が好ましい。
本発明においてはアルコールの混合溶媒が使用できる。これらの溶媒を例示すると、メタノール、エタノール、n−プロパノール、iso−プロパノール、n−ブタノール、iso−ブタノール、sec−ブタノール、tert−ブタノール、n−ペンタノール、n−ヘキサノール、シクロヘキサノール、n−ヘプタノール、n−オクタノール、アリルアルコール等の一価アルコール類、エチレングリコール、プロピレングリコールなどの多価アルコール類が挙げられるがこれらの例には限定されない。これらのアルコールから選ばれた混合溶媒が本発明に使用できる。混合溶媒中にアルコールを何種類選ぶかについては特に制限されない。混合溶媒中の各種アルコールの比率は特に限定されないし、本発明の方法を達成するのに必要な重合溶媒の組み合わせと比率はこれらのアルコールの中から選ばれ得るので非常に広範囲に選択可能であるが、工業的見地からは、価格、回収方法の難易などを考慮して、ある程度の制限が加えられることは当然である。
【0023】
驚くべきことに本発明の方法を用いるとそれぞれが低分子量ポリフェニレンエーテルに対して貧溶媒であるにもかかわらず、これらの比率を変えることにより得られる低分子量ポリフェニレンエーテルの分子量を制御することが可能であること、本発明の触媒を用いる場合にはアルコール1種のみの単独溶媒で用いた場合よりも活性や収率が向上するという極めて特異的な挙動を示すことが判った。好ましい重合溶媒はメタノールと炭素数が2個以上のアルコールからなる混合溶媒である方法である。より好ましい重合溶媒はメタノールと炭素数が6個以上のアルコールからなる混合溶媒である方法である。なお、ポリフェニレンエーテルの良溶媒を全く含んでいない方が更に好ましいことは前述の通りである。メタノールと炭素数が2個以上の比率については特に制限されないし、更に好ましくはメタノールと炭素数が6個以上のアルコールの比率についても特に制限されない。
【0024】
本発明に用いられる重合触媒の構成は次のようなものである。
(a)銅化合物、ハロゲン化合物
(b)下記一般式(1)の構造を持つジアミン化合物
【0025】
【化7】
【0026】
(式中、R1,R2,R3,R4はそれぞれ独立に水素、炭素数1から6の直鎖状または分岐状アルキル基で、全てが同時に水素ではない。R5は炭素数2から5の直鎖状またはメチル分岐を持つアルキレン基である)
【0027】
ここで述べられた触媒成分(a)の銅化合物の例を列挙する。好適な銅化合物としては第一銅化合物、第二銅化合物またはそれらの混合物を使用することができる。
第二銅化合物としては、例えば塩化第二銅、臭化第二銅、硫酸第二銅、硝酸第二銅等を例示することができる。また第一銅化合物としては、例えば塩化第一銅、臭化第一銅、硫酸第一銅、硝酸第一銅等を例示することができる。これらの中で特に好ましい金属化合物は第一銅,第二銅化合物については塩化第一銅、塩化第二銅、臭化第一銅、臭化第二銅である。またこれらの銅塩は酸化物(例えば酸化第一銅)、炭酸塩、水酸化物等と対応するハロゲンまたは酸から使用時に合成しても良い。しばしば用いられる方法は先に例示の酸化第一銅とハロゲン化水素(またはハロゲン化水素の溶液)を混合して作成する方法である。
【0028】
ハロゲン化合物としては例えば塩化水素、臭化水素、ヨウ化水素、塩化ナトリウム、臭化ナトリウム、ヨウ化ナトリウム、塩化カリウム、臭化カリウム、ヨウ化カリウム、塩化テトラメチルアンモニウム、臭化テトラメチルアンモニウム、ヨウ化テトラメチルアンモニウム、塩化テトラエチルアンモニウム、臭化テトラエチルアンモニウム、ヨウ化テトラエチルアンモニウム等である。またこれらは水溶液や適当な溶媒を用いた溶液として使用できる。これらのハロゲン化合物は、成分として単独でも用いられるし、2種類以上組み合わせて用いても良い。好ましいハロゲン化合物は、塩化水素の水溶液、臭化水素の水溶液である。
【0029】
これらの化合物の使用量は特に限定されないが、銅原子のモル量に対してハロゲン原子として2倍以上20倍以下が好ましく、フェノール性化合物の100モルに対して好ましい銅原子の使用量としては0.02モルから0.6モルの範囲である。
【0030】
次に触媒成分(b)のジアミン化合物の例を列挙する。例えばN,N,N’,N’−テトラメチルエチレンジアミン、N,N,N’−トリメチルエチレンジアミン、N,N’−ジメチルエチレンジアミン、N,N−ジメチルエチレンジアミン、N−メチルエチレンジアミン、N,N,N’,N’−テトラエチルエチレンジアミン、N,N,N’−トリエチルエチレンジアミン、N,N’−ジエチルエチレンジアミン、N,N−ジエチルエチレンジアミン、N−エチルエチレンジアミン、N,N−ジメチル−N’−エチルエチレンジアミン、N,N’−ジメチル−N−エチルエチレンジアミン、N−n−プロピルエチレンジアミン、N,N’−n−プロピルエチレンジアミン、N−i−プロピルエチレンジアミン、N,N’−i−プロピルエチレンジアミン、N−n−ブチルエチレンジアミン、N,N’−n−ブチルエチレンジアミン、N−i−ブチルエチレンジアミン、N,N’−i−ブチルエチレンジアミン、N−t−ブチルエチレンジアミン、N,N’−t−ブチルエチレンジアミン、N,N,N’,N’−テトラメチル−1,3−ジアミノプロパン、N,N,N’−トリメチル−1,3−ジアミノプロパン、N,N’−ジメチル−1,3−ジアミノプロパン、N−メチル−1,3−ジアミノプロパン、N,N,N’,N’−テトラメチル−1,3−ジアミノ−1−メチルプロパン、N,N,N’,N’−テトラメチル−1,3−ジアミノ−2−メチルプロパン、N,N,N’,N’−テトラメチル−1,4−ジアミノブタン、N,N,N’,N’−テトラメチル−1,5−ジアミノペンタン等が挙げられる。本発明にとって好ましいジアミン化合物は2つの窒素原子をつなぐアルキレン基の炭素数が2または3のものである。これらのジアミン化合物の使用量は特に限定されないが、通常フェノール性化合物100モルに対して0.01モルから10モルの範囲で用いられる。
【0031】
本発明の溶媒を用いるときに上記の様な触媒を用いると、他の触媒からは到底想定できない程収率の向上効果は顕著であることが判った。
この触媒成分には本発明にとって好ましい構成成分として次の成分を加えることができる。即ち、前記銅化合物、ハロゲン化合物、ジアミン化合物からなる触媒構成成分に、更に3級モノアミン化合物並びに2級モノアミン化合物をそれぞれ単独で、またはこれらを組み合わせて使用することである。
【0032】
3級モノアミン化合物とは、脂環式3級アミンを含めた脂肪族3級アミンである。例えばトリメチルアミン、トリエチルアミン、トリプロピルアミン、トリブチルアミン、トリイソブチルアミン、ジメチルエチルアミン、ジメチルプロピルアミン、アリルジエチルアミン、ジメチル−n−ブチルアミン、ジエチルイソプロピルアミン、N−メチルシクロヘキシルアミン等が挙げられる。これらの第3級モノアミンは単独でも用いられるし、2種類以上組み合わせて用いても良い。これらの使用量は特に限定されないが、通常フェノール性化合物100モルに対して0.1モルから10モルの範囲で用いられる。
【0033】
2級モノアミン化合物の例として、第2級脂肪族アミンとしては例えば、ジメチルアミン、ジエチルアミン、ジ−n−プロピルアミン、ジ−iso−プロピルアミン、ジ−n−ブチルアミン、ジ−iso−ブチルアミン、ジ−tert−ブチルアミン、ジペンチルアミン類、ジヘキシルアミン類、ジオクチルアミン類、ジデシルアミン類、ジベンジルアミン類、メチルエチルアミン、メチルプロピルアミン、メチルブチルアミン、シクロヘキシルアミンが挙げられる。芳香族を含む2級モノアミン化合物の例としては、N−フェニルメタノールアミン、N−フェニルエタノールアミン、N−フェニルプロパノールアミン、N−(m−メチルフェニル)エタノールアミン、N−(p−メチルフェニル)エタノールアミン、N−(2’,6’−ジメチルフェニル)エタノールアミン、N−(p−クロロフェニル)エタノールアミン、N−エチルアニリン、N−ブチルアニリン、N−メチル−2−メチルアニリン、N−メチル−2,6−ジメチルアニリン、ジフェニルアミン等が挙げられるがこれらの例には限定されない。これらの2級モノアミン化合物は単独でも用いられるし、2種類以上組み合わせて用いても良い。使用量は特に限定されないが通常フェノール性化合物100モルに対し0.05モルから15モルの範囲であり、好ましくは0.1から10モルの範囲である。
【0034】
2級モノアミン化合物と3級モノアミン化合物はそれぞれ触媒の構成成分としてそれぞれ単独で用いても良いし、これらを組み合わせて用いても良い。
本発明には従来より活性に向上効果を有することが知られている界面活性剤を添加することについて何ら制限されない。例えば、Aliquat336やCapriquatの商品名で知られるトリオクチルメチルアンモニウムクロライドである。使用量はフェノール性化合物を添加し終わった後の全反応混合物の全量に対して0.1wt%を超えない範囲が好ましい。
【0035】
本発明で用いられる好ましいフェノール性化合物は次のような一般式(2)の構造を持つ化合物である。
【0036】
【化8】
【0037】
(式中、R6,R7,R8は各々独立の置換基を表し、R6はアルキル基,置換アルキル基,アラルキル基,置換アラルキル基,アリール基,置換アリール基,アルコキシ基,置換アルコキシ基であり、R7,R8はR6について定義されたものと同一の基に加え更に水素,ハロゲンであっても良い)
【0038】
またフェノール性化合物として下記一般式(3)で表される二価フェノール化合物を含有させることは好ましい。
【0039】
【化9】
【0040】
(式中、R9、R10は各々同一または異なる置換基を表し、水素、アルキル基,置換アルキル基,アラルキル基,置換アラルキル基,アリール基,置換アリール基,アルコキシ基,置換アルコキシ基,ハロゲンを表し、Xは脂肪族炭化水素残基及びそれらの置換誘導体、酸素、イオウ、スルホニル基を表し、R10,Xの結合位置はフェノール水酸基に対してオルソ位またはパラ位を表す)
【0041】
以下これらの例を例示する。
一般式(2)で表されるような一価フェノール性化合物としては、例えば、o−クレゾール、2,6−ジメチルフェノール、2,3,6−トリメチルフェノール、2−エチルフェノール、2−メチル−6−エチルフェノール、2,6−ジエチルフェノール、2−n−プロピルフェノール、2−エチル−6−n−プロピルフェノール、2−メチル−6−クロルフェノール、2−メチル−6−ブロモフェノール、2−メチル−6−イソプロピルフェノール、2−メチル−6−n−プロピルフェノール、2−エチル−6−ブロモフェノール、2−メチル−6−n−ブチルフェノール、2,6−ジ−n−プロピルフェノール、2−エチル−6−クロルフェノール、2−メチル−6−フェニルフェノール、2−フェニルフェノール、2,6−ジフェニルフェノール、2,6−ビス−(4−フルオロフェニル)フェノール、2−メチル−6−トリルフェノール、2,6−ジトリルフェノール等が挙げられる。これらの一価フェノール性化合物の中でも2,6−ジメチルフェノールは工業上非常に重要である。これらの一価フェノール性化合物は一種類でも用いられるし、いくつか組み合わせて用いても良い。例えば、2,6−ジメチルフェノールと2,3,6−トリメチルフェノールを組み合わせて使用する方法、2,6−ジメチルフェノールとo−クレゾールを組み合わせて用いる方法などである。
【0042】
また使用する化合物の中に、少量のm−クレゾール、p−クレゾール、2,4−ジメチルフェノール、2,4,6−トリメチルフェノール等が含まれていても全くかまわない。
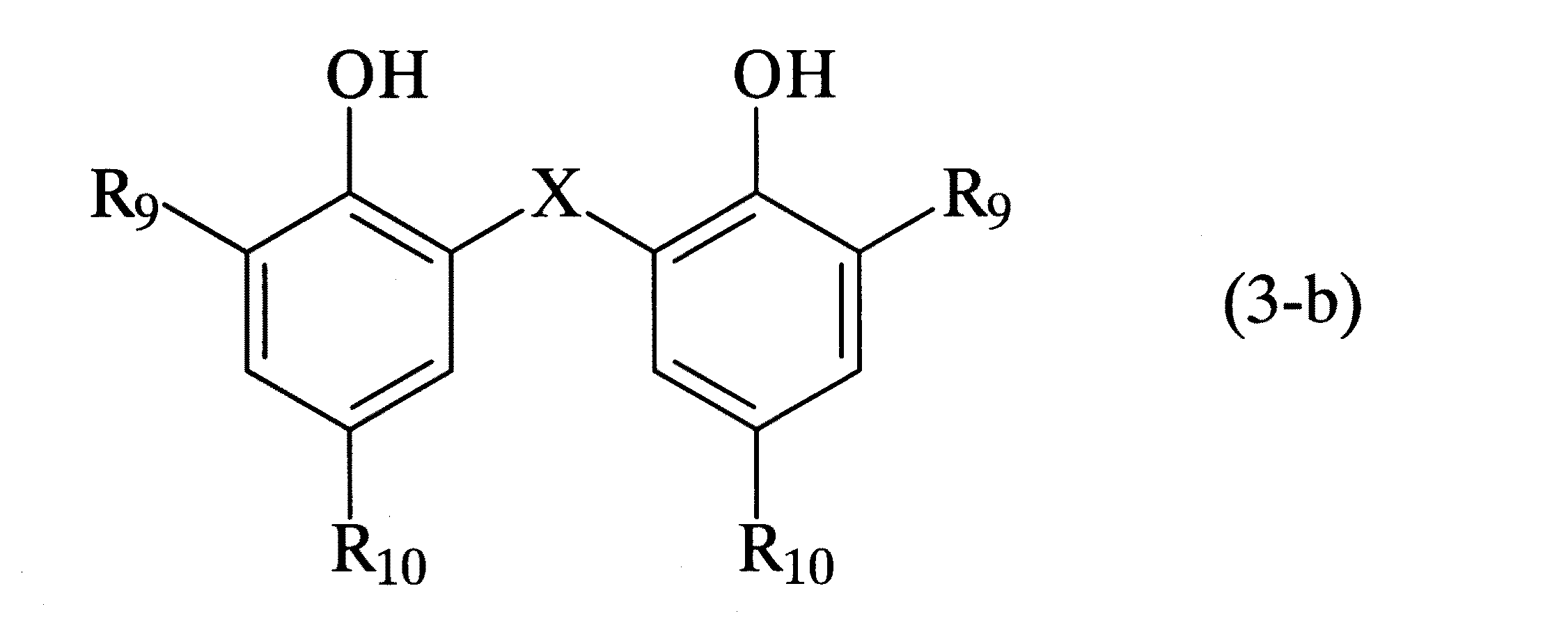
一般式(3)で表されるような二価フェノール性化合物は該当する一価フェノール性化合物とケトン類またはジハロゲン化脂肪族炭化水素との反応等により工業的に有利に製造できる。例えばホルムアルデヒド、アセトン、メチルエチルケトン、メチルイソブチルケトン、アセトフェノン、シクロヘキサノン等の汎用のケトン化合物と、一価フェノール性化合物の反応により得られる化合物群がある。例えば、下記一般式(3−a)、(3−b)、(3−c)の各々の構造に挙げる化合物群がある。
【0043】
【化10】
【0044】
【化11】
【0045】
【化12】
【0046】
(一般式(3−a)、(3−b)、(3−c)の式中、R9、R10は各々同一または異なる置換基を表し、水素、アルキル基,置換アルキル基,アラルキル基,置換アラルキル基,アリール基,置換アリール基,アルコキシ基,置換アルコキシ基,ハロゲンを表し、Xは脂肪族炭化水素残基及びそれらの置換誘導体、酸素、イオウ、スルホニル基を表す)
【0047】
上記一般式の構造を持つもので代表的なものは、R9とR10がメチル基でXがイソプロピリデンである化合物、R9とR10がメチル基でXがメチレンである化合物、R9とR10がメチル基でXがチオである化合物、R9とR10がメチル基でXがシクロヘキシリデンである化合物等であるがこれらの例に限定されないことはいうまでもない。
【0048】
これらの二価フェノール性化合物は一種類でも用いられるし、いくつか組み合わせて用いても良い。
一般式(3)で表される二価フェノール性化合物を含有させる場合には、一般式(2)記載の一価フェノール性化合物に対する一般式(3)の二価フェノール性化合物の量は特に制限されないけれども、一価フェノール性化合物に対して、0.1から25モル%とするのが好ましい。
【0049】
本発明で使用できる溶媒と上記フェノール性化合物との比は好ましくは重量比で1:1から10:1の範囲である。
重合形式については特に制限はない。本発明はバッチ重合法、連続重合法いずれの方法にも適用できる。
重合反応系にアルカリ金属の水酸化物、アルカリ土類金属の水酸化物、アルカリ金属のアルコキサイド、硫酸マグネシウム等の中性塩、ゼオライト等も添加することができる。
重合反応温度については、低すぎると反応が進行しにくく、また高すぎると反応の選択性が低下することがあるので、0〜80℃、好ましくは10〜70℃の範囲である。
【0050】
本発明の酸化重合における酸素含有ガスは純酸素の他、酸素と窒素等の不活性ガスとを任意の割合で混合したもの、空気、更には空気と窒素等の不活性ガスとを任意の割合で混合したもの等が使用できる。重合反応中の系内圧力は常圧で充分であるが必要に応じて減圧でも加圧でも使用できる。
【0051】
本発明では、重合の進行に伴い、低分子量ポリフェニレンエーテルが粒子として析出してくる沈殿重合の様態を呈することが観測される。また生成水や触媒成分のアミン類の分離は見られず、反応系内に均一な状態でいることが判る。ところが驚異的なことに、本発明においては、特公昭50−6520号公報で記載されているような「生成水やアミン類が反応系内に均一に存在した状態で反応を進めると、オリゴポリフェニレンエーテルが粒子を不均一状態に生じた場合に反応容器などに付着しやすくなる欠点がある」というスケール付着現象は観測されないことが判った。またηsp/cが0.1dl/g以下となるような領域の極低分子量域に至っても収率は全く低下せず、驚くべき高収率で低分子量ポリフェニレンエーテルが得られることが判明した。
【0052】
重合反応終了後の後処理方法については、特に制限はなく、既知のいかなる処理方法を用いても処理することができる。例えば、塩酸や酢酸等の酸、またはエチレンジアミン4酢酸(EDTA)及びその塩、ニトリロトリ酢酸及びその塩等を反応液に加えて触媒を失活させた後、粒子として生成している重合体を分離してメタノール等で洗浄後、乾燥するという簡単な操作でポリフェニレンエーテルが回収できる。重合中に副生成物として発生することが知られているジフェノキノンは重合後、溶剤洗浄や公知の還元剤などで処理するか、または特公昭61−20576号公報記載の方法や特開平7−278293号公報記載の方法に従って処理できる。
【0053】
得られた低分子量ポリフェニレンエーテルは30℃において0.5g/dlの濃度のクロロホルム溶液で測定された還元粘度(ηsp/c)が0.04〜0.20dl/gのものである。好ましい還元粘度(ηsp/c)は0.06〜0.16dl/gのものである。本発明の方法で得られた低分子量ポリフェニレンエーテルも本発明範囲に含まれる。この低分子量ポリフェニレンエーテルは色調に優れ、好ましくない酸化体を殆ど含まないために様々な用途に対して提供することができる。
【0054】
一般にポリフェニレンエーテルは難燃性、電気特性に優れるが、本発明によるポリフェニレンエーテルは色調に優れるために他の物質に難燃性を付与するための難燃助剤的な添加剤としても有用であるし、低誘電率や低誘電損失等を要求される電子材料用途として極めて有用である。また、本発明によるポリフェニレンエーテルは色調に優れることにより、種々の熱可塑性樹脂組成物や熱硬化性樹脂等に適用することも有用である。当然のことながら通常の高分子量のポリフェニレンエーテルを用いた変性ポリフェニレンエーテル樹脂に本発明の低分子量ポリフェニレンエーテルを適用し、その流動特性の改善にも寄与することができる。
【0055】
熱可塑性樹脂としては例えば、ポリスチレン系樹脂(ゴム補強ポリスチレンやAS,ABS樹脂等も含む)、ポリアミド樹脂、ポリオレフィン系樹脂、ポリエステル樹脂、液晶樹脂等との組成物であり、熱硬化性樹脂としては例えば、エポキシ系、不飽和ポリエステル系、ポリウレタン、架橋アリール、ビスマレイミド、フェノール性樹脂等との組成物が挙げられるがこの例に限定されない。
また本発明によって得られたポリフェニレンエーテルを用いた組成物を製造させる際に他の添加剤、例えば可塑剤、安定剤、変性剤、紫外線吸収剤、難燃剤、着色剤、離型剤及びガラス繊維、炭素繊維等の繊維状補強剤、更にはガラスビーズ、炭酸カルシウム、タルク等の充填剤を添加することができる。安定剤や変性剤としては、亜リン酸エステル類、ヒンダードフェノール類、含イオウ酸化防止剤、アルカノールアミン類、酸アミド類、ジチオカルバミン酸金属塩類、無機硫化物、金属酸化物類、無水カルボン酸類、スチレンやステアリルアクリレート等のジエノフィル化合物類、エポキシ基含有化合物などが挙げられるがこれらの例には限定されない。これらの添加剤は単独でまたは組み合わせて使用することができる。
【0056】
本発明のポリフェニレンエーテルを含有する組成物を構成する各成分を混合する方法はいかなる方法でも良いが、例えば、溶液ブレンドと脱気方法、押出機、加熱ロール、バンバリーミキサー、ニーダー、ヘンシェルミキサー等使用することができる。
【0057】
【発明の実施の形態】
次に実施例により本発明を更に詳細に説明するが、本発明はこれらの例によってなんら限定されるべきではない。
なお、測定は以下の方法に従って行った。
(1)ηsp/cの測定方法
各々の例で得られたポリフェニレンエーテルを0.5g/dlのクロロホルム溶液として、ウベローデ粘度管を用いて30℃における還元粘度(ηsp/c)を求めた。単位はdl/gである。
(2)ポリフェニレンエーテル収率の測定方法
仕込みのフェノール性化合物重量に対して、得られた乾燥ポリフェニレンエーテルの重量の割合を100分率で表した。
【0058】
(3)ポリフェニレンエーテルの色調(カラーインデックス)の測定方法
重合によって得られたポリフェニレンエーテルの混合物を、下記3−1及び3−2項記載の2通りの方法で処理して製品としてのポリフェニレンエーテルを得た。その各方法で得られたポリフェニレンエーテル0.5gの10mlクロロホルム溶液を作成し、紫外可視吸光光度計(日立製作所:U−3210型)を用いて、その溶液の480nmでの吸光度(セル長1cmの吸光度測定用セルを使用)を測定し、その測光値を濃度(0.05g/ml)で割ってカラーインデックスと定義した。よってカラーインデックス値が小さい方がポリフェニレンエーテルの色調に優れることを意味している。
【0059】
3−1.還元剤による処理
得られた重合混合物にエチレンジアミン四酢酸3カリウム塩(同仁化学研究所製試薬)の10%水溶液を添加し、50℃に温めた。次いでハイドロキノン(和光純薬社製試薬)を少量ずつ添加し、スラリー状のポリフェニレンエーテルが白色となるまで、50℃での保温を続けた。終了後、濾過してメタノールで繰り返し洗浄し、湿潤ポリフェニレンエーテルを得た。次いで100℃で真空乾燥し乾燥ポリフェニレンエーテルを得た。
【0060】
3−2.特開平7−278293号公報記載の方法に準拠した処理
得られた重合混合物にエチレンジアミン四酢酸3カリウム塩(同仁化学研究所製試薬)の10%水溶液を添加し、80℃に温めた。スラリー状のポリフェニレンエーテルが白色となるまで、80℃での保温を続けた。終了後冷却し、濾過してメタノールで繰り返し洗浄し、湿潤ポリフェニレンエーテルを得た。次いで100℃で真空乾燥し乾燥ポリフェニレンエーテルを得た。
【0061】
【実施例1】
反応器底部に酸素含有ガス導入の為のスパージャー、攪拌タービン翼及びバッフル、反応器上部のベントガスラインに還流冷却器を備えた1.5リットルのジャケット付き反応器に、0.2512gの塩化第二銅2水和物、1.1062gの35%塩酸、3.6179gのジ−n−ブチルアミン、9.5937gのN,N,N‘,N’−テトラメチルプロパンジアミン、211.63gのメタノール及び493.80gのn−ブタノール、180.0gの2,6−ジメチルフェノールを入れた。使用した溶媒の組成重量比はn−ブタノール:メタノール=70:30である。次いで激しく攪拌しながら反応器へ180ml/minの速度で酸素をスパージャーより導入を始めると同時に、重合温度は40℃を保つようにジャケットに熱媒を通して調節した。重合液は次第にスラリーの様態を呈した。重合中、反応器に付着は観測されなかった。酸素を導入し始めてから120分後、酸素含有ガスの通気をやめ、ポリフェニレンエーテルの色調(カラーインデックス)の測定方法の項の中に述べられた3−1.記載の方法に従って処理を行った。ηsp/cは0.103dl/g、収率は97%、カラーインデックスは0.35であった。
【0062】
【実施例2】
使用した溶媒の全量は変えずに組成重量比をn−ブタノール:メタノール=50:50とした以外は実施例1の方法で行った。重合中、反応器に付着は観測されなかった。ηsp/cは0.101dl/g、収率は97%、カラーインデックスは0.32であった。
【0063】
【実施例3】
使用した溶媒の全量は変えずに組成重量比をn−ブタノール:メタノール=30:70とした以外は実施例1の方法で行った。重合中、反応器に付着は観測されなかった。ηsp/cは0.082dl/g、収率は98%、カラーインデックスは0.33であった。
【0064】
【実施例4】
使用した溶媒の全量は変えずに組成重量比をn−ブタノール:メタノール=10:90とした以外は実施例1の方法で行った。重合中、反応器に付着は観測されなかった。ηsp/cは0.075dl/g、収率は98%、カラーインデックスは0.36であった。
【0065】
【比較例1】
使用した溶媒の全量は変えずに組成重量比をn−ブタノール:メタノール=0:100即ち、メタノール単独溶媒とし、重合時間を240分とした以外は実施例1の方法で行った。重合中、反応器に付着は観測されなかった。ηsp/cは0.073dl/g、収率は88%、カラーインデックスは0.35であった。
【0066】
【比較例2】
使用した溶媒の全量は変えずに組成重量比をn−ブタノール:メタノール=100:0即ち、n−ブタノール単独溶媒とし、重合時間を240分とした以外は実施例1の方法で行った。重合中、反応器に付着は観測されなかった。ηsp/cは0.072dl/g、収率は76%、カラーインデックスは0.39であった。
【0067】
【実施例5】
重合終了後の処理をポリフェニレンエーテルの色調(カラーインデックス)の測定方法の項の中に述べられた3−2.記載の方法に従って処理を行った以外は実施例4の方法で行った。ηsp/cは0.083dl/g、収率は97%、カラーインデックスは0.34であった。
【0068】
【比較例3】
使用した溶媒の全量は変えずに組成重量比をキシレン:n−ブタノール:メタノール=60:20:20とした以外は実施例1の方法で行った。重合中に反応器に多量の付着が観測された。ηsp/cは0.476dl/g、収率は97%、カラーインデックスは0.39であった。
【0069】
【比較例4】
重合時間を65分とした以外は比較例3の方法で行った。重合中に反応器に多量の付着が観測された。ηsp/cは0.211dl/g、収率は83%、カラーインデックスは0.39であった。
【0070】
【比較例5】
重合時間を55分とした以外は比較例3の方法で行った。重合中に反応器に多量の付着が観測された。ηsp/cは0.176dl/g、収率は64%、カラーインデックスは0.52であった。
【0071】
【比較例6】
使用した溶媒の全量は変えずに組成重量比をキシレン:メタノール=20:80とした以外は実施例1の方法で行った。重合中に反応器に多量の付着が観測された。ηsp/cは0.223dl/g、収率は77%、カラーインデックスは0.62であった。
【0072】
【実施例6】
使用した溶媒の全量は変えずに組成重量比をキシレン:n−ブタノール:メタノール=5:15:80とした以外は実施例1の方法で行った。重合中に反応器に付着は観測されなかった。ηsp/cは0.079dl/g、収率は98%、カラーインデックスは0.34であった。
【0073】
【実施例7】
使用した溶媒の全量は変えずに組成重量比をn−ヘキサノール:メタノール=10:90とした以外は実施例1の方法で行った。重合中、反応器に付着は観測されなかった。ηsp/cは0.085dl/g、収率は98%、カラーインデックスは0.33であった。
【0074】
【実施例8】
使用したフェノール性化合物を2.5モル%の2,2−ビス(3,5−ジメチル−4−ヒドロキシフェニル)プロパンを含む2,6−ジメチルフェノールを用いた以外は実施例3の方法で行った。重合中、反応器に付着は観測されなかった。ηsp/cは0.085dl/g、収率は98%、カラーインデックスは0.36であった。
【0075】
【実施例9】
使用したフェノール性化合物を2.5モル%の2,2−ビス(3,5−ジメチル−4−ヒドロキシフェニル)プロパンを含む2,6−ジメチルフェノールを用いた以外は実施例7の方法で行った。重合中、反応器に付着は観測されなかった。ηsp/cは0.091dl/g、収率は98%、カラーインデックスは0.34であった。
【0076】
【実施例10】
使用したフェノール性化合物を20重量%のo−クレゾールを含む2,6−ジメチルフェノールを用いた以外は実施例6の方法で行った。重合中、反応器に付着は観測されなかった。ηsp/cは0.089dl/g、収率は97%、カラーインデックスは0.39であった。
【0077】
【比較例7】
米国特許6211327号明細書実施例記載の方法に従って行った。即ち、臭化銅とジ−n−ブチルアミンを触媒とし、トルエン溶媒中、40℃から45℃の温度範囲で、酸素供給下攪拌しながら2,6−ジメチルフェノールを重合し、次いで酸素の供給を止め、窒素シール下ニトリロトリ酢酸の水溶液を攪拌しながら加えて水相に銅触媒を抽出しつつ温度を55℃にしこの状態で70分保った。次いで得られた混合物をシャープレス型の液液遠心分離器でポリフェニレンエーテルが溶解したトルエン溶液相と銅が溶解した水相に分けた。得られたポリフェニレンエーテルの溶液を固形分が65%になるまでトルエンを留去させて濃縮し、更に脱気押出機を用いて脱気押出を行い、ペレット状の低分子量ポリフェニレンエーテルを得た。ηsp/cは0.120dl/g、カラーインデックスは1.51であった。
【0078】
【発明の効果】
本発明によれば、低分子量ポリフェニレンエーテルを効率的に製造するに際し、特定のアルコール混合溶媒と特定の触媒を用いることにより、特にηsp/cが約0.1dl/gよりも低いような極低分子量のポリフェニレンエーテルの収率に顕著な改善効果を有し、生産性が向上する製造方法を提供するとともに品質の良い低分子量ポリフェニレンエーテルを提供することができる。
Claims (6)
- 触媒と酸素含有ガスを用いてフェノール性化合物を酸化重合させるポリフェニレンエーテルの製造方法において、2種以上のアルコールからなり、キシレンの含有量が0〜5重量%である混合溶媒を重合溶媒とし、かつ、触媒の構成成分が銅化合物、ハロゲン化合物および一般式(1)で表されるジアミン化合物からなる触媒を用いることを特徴とする、30℃において0.5g/dlの濃度のクロロホルム溶液で測定された還元粘度(ηsp/c)が0.04〜0.20dl/gの低分子量ポリフェニレンエーテルの製造方法。
- 触媒の構成成分として、更に3級モノアミン化合物または2級モノアミン化合物をそれぞれ単独で、またはこれらを組み合わせて含む請求項1〜3のいずれかに記載の方法。
- 重合溶媒が、メタノールと炭素数が2個以上のアルコールの混合溶媒からなる請求項1〜4のいずれかに記載の方法。
- 重合溶媒が、メタノールと炭素数が6個以上のアルコールの混合溶媒からなる請求項1〜4のいずれかに記載の方法。
Priority Applications (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2002063626A JP4007828B2 (ja) | 2002-03-08 | 2002-03-08 | 低分子量ポリフェニレンエーテルの製造方法 |
| KR1020047013995A KR100619641B1 (ko) | 2002-03-08 | 2003-02-28 | 저분자량 폴리페닐렌에테르 |
| PCT/JP2003/002302 WO2003076495A1 (fr) | 2002-03-08 | 2003-02-28 | Polyphenylene ether de faible poids moleculaire |
| US10/500,701 US7282554B2 (en) | 2002-03-08 | 2003-02-28 | Low molecular weight polyphenylene ether |
| TW092104827A TW583221B (en) | 2002-03-08 | 2003-03-06 | Low molecular weight polyphenylene ether |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2002063626A JP4007828B2 (ja) | 2002-03-08 | 2002-03-08 | 低分子量ポリフェニレンエーテルの製造方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2003261674A JP2003261674A (ja) | 2003-09-19 |
| JP4007828B2 true JP4007828B2 (ja) | 2007-11-14 |
Family
ID=27800197
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2002063626A Expired - Fee Related JP4007828B2 (ja) | 2002-03-08 | 2002-03-08 | 低分子量ポリフェニレンエーテルの製造方法 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US7282554B2 (ja) |
| JP (1) | JP4007828B2 (ja) |
| KR (1) | KR100619641B1 (ja) |
| TW (1) | TW583221B (ja) |
| WO (1) | WO2003076495A1 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2016516871A (ja) * | 2013-04-29 | 2016-06-09 | エボニック デグサ ゲーエムベーハーEvonik Degussa GmbH | ポリ(アリーレンエーテル)の精製方法 |
Families Citing this family (40)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7235192B2 (en) | 1999-12-01 | 2007-06-26 | General Electric Company | Capped poly(arylene ether) composition and method |
| US6384176B1 (en) | 2000-07-10 | 2002-05-07 | General Electric Co. | Composition and process for the manufacture of functionalized polyphenylene ether resins |
| US6878781B2 (en) | 2001-03-27 | 2005-04-12 | General Electric | Poly(arylene ether)-containing thermoset composition in powder form, method for the preparation thereof, and articles derived therefrom |
| JP4471073B2 (ja) * | 2003-07-02 | 2010-06-02 | 三菱瓦斯化学株式会社 | 2官能性フェニレンエーテルオリゴマー体の製造法 |
| US7148296B2 (en) * | 2003-10-03 | 2006-12-12 | General Electric Company | Capped poly(arylene ether) composition and process |
| US7151158B2 (en) | 2004-01-30 | 2006-12-19 | General Electric Company | Method of preparing a poly(arylene ether), apparatus therefor, and poly(arylene ether) prepared thereby |
| US20080070096A1 (en) * | 2004-08-09 | 2008-03-20 | Ionescu Lucia D | Proton Conducting Copolymers |
| US7429800B2 (en) * | 2005-06-30 | 2008-09-30 | Sabic Innovative Plastics Ip B.V. | Molding composition and method, and molded article |
| US20070004871A1 (en) * | 2005-06-30 | 2007-01-04 | Qiwei Lu | Curable composition and method |
| US7378455B2 (en) * | 2005-06-30 | 2008-05-27 | General Electric Company | Molding composition and method, and molded article |
| US20070106051A1 (en) * | 2005-11-10 | 2007-05-10 | Alvaro Carrillo | Polyfunctional poly(arylene ether) method |
| US7541421B2 (en) | 2005-12-08 | 2009-06-02 | Sabic Innovative Plastics Ip B.V. | Poly(arylene ether) copolymer |
| JP4988218B2 (ja) * | 2006-02-13 | 2012-08-01 | 株式会社日立製作所 | 低誘電損失樹脂の製造方法 |
| JP5099805B2 (ja) * | 2006-03-10 | 2012-12-19 | 旭化成ケミカルズ株式会社 | 分子量分布のピークを2個有するポリフェニレンエーテルの製造方法 |
| US7439310B2 (en) | 2006-07-06 | 2008-10-21 | Asahi Kasei Chemicals Corporation | Polyphenylene ether modified by reaction with cresol novolac epoxy resin |
| US7638566B2 (en) * | 2006-10-30 | 2009-12-29 | Sabic Innovative Plastics Ip B.V. | Poly(arylene ether) compositions |
| US7655278B2 (en) * | 2007-01-30 | 2010-02-02 | Sabic Innovative Plastics Ip B.V. | Composite-forming method, composites formed thereby, and printed circuit boards incorporating them |
| US8075812B2 (en) | 2007-04-04 | 2011-12-13 | Sabic Innovative Plastics Ip B.V. | Method of separating a poly(arylene ether) composition from a solvent, and poly(arylene ether) composition prepared thereby |
| JP5390128B2 (ja) * | 2008-06-20 | 2014-01-15 | 株式会社カネカ | 低分子量ポリ(2,6−ジアリールフェニレンエーテル)の製造方法 |
| US8642719B2 (en) * | 2011-02-28 | 2014-02-04 | Corning Incorporated | Solvent mixture for molecular weight control |
| US8901544B2 (en) | 2011-12-06 | 2014-12-02 | Corning Incorporated | Organic thin film transistor with ion exchanged glass substrate |
| JP5759087B2 (ja) * | 2012-04-25 | 2015-08-05 | サビック グローバル テクノロジーズ ベスローテン フェンノートシャップ | ポリ(フェニレンエーテル)コポリマーと製造方法 |
| US8703848B1 (en) * | 2012-10-09 | 2014-04-22 | Sabic Innovative Plastics | Blends of micronized polyphenylene ether and thermoplastic polyurethanes blend |
| US9455067B2 (en) | 2013-03-18 | 2016-09-27 | Iteq Corporation | Low dielectric materials |
| US9245667B2 (en) * | 2013-03-18 | 2016-01-26 | Iteq Corporation | Circuit board |
| US20150028247A1 (en) | 2013-07-23 | 2015-01-29 | Sabic Innovative Plastics Ip B.V. | Rigid foam and associated article and method |
| US9175160B2 (en) | 2013-08-28 | 2015-11-03 | Sabic Global Technologies B.V. | Blend of poly(phenylene ether) particles and polyoxymethylene, article thereof, and method of preparation |
| US9447227B2 (en) | 2013-10-03 | 2016-09-20 | Sabic Global Technologies B.V. | Flexible polyurethane foam and associated method and article |
| US9074086B1 (en) * | 2013-12-18 | 2015-07-07 | Sabic Global Technologies B.V. | Polyolefin composition with poly(phenylene ether) filler and article thereof |
| TWI548453B (zh) | 2014-12-05 | 2016-09-11 | 財團法人工業技術研究院 | 水相催化劑組成物及聚酚醚之製備方法 |
| CN107849239B (zh) * | 2015-06-09 | 2019-03-08 | 沙特基础工业全球技术有限公司 | 用于聚(苯醚)制造的方法和相关聚(苯醚) |
| CN107227015B (zh) * | 2016-03-23 | 2020-04-24 | 联茂电子股份有限公司 | 低介电材料 |
| EP3612583B1 (en) | 2017-04-21 | 2023-01-18 | SHPP Global Technologies B.V. | Poly(phenylene ether) copolymer process and compositions |
| KR102559877B1 (ko) | 2017-04-21 | 2023-08-03 | 에스에이치피피 글로벌 테크놀러지스 비.브이. | 폴리(페닐렌 에테르) 공중합체 조성물 및 관련 방법 및 물품 |
| JP2021014556A (ja) * | 2019-07-16 | 2021-02-12 | 旭化成株式会社 | ポリフェニレンエーテル樹脂の製造方法 |
| CN110804174B (zh) * | 2019-12-06 | 2022-07-08 | 中国科学院大连化学物理研究所 | 一种负载型催化剂及其在制备低分子量双端羟基聚苯醚中的应用 |
| WO2022158180A1 (ja) * | 2021-01-25 | 2022-07-28 | 旭化成株式会社 | ポリフェニレンエーテル、その製造方法、熱硬化組成物、プリプレグ、及び積層体 |
| CN121495109A (zh) * | 2021-03-10 | 2026-02-10 | 旭化成株式会社 | 聚苯醚、其制造方法、热固化组合物、预浸料和层积体 |
| WO2023277624A1 (ko) * | 2021-07-02 | 2023-01-05 | 주식회사 엘지화학 | 폴리페닐렌 옥사이드의 제조방법 |
| TWI870858B (zh) * | 2022-05-23 | 2025-01-21 | 日商旭化成股份有限公司 | 聚苯醚、樹脂組合物、樹脂膜、預浸體、及金屬貼合積層板 |
Family Cites Families (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS506520B2 (ja) * | 1972-05-29 | 1975-03-14 | ||
| JPS5312932B2 (ja) | 1972-07-06 | 1978-05-06 | ||
| JPS4926919A (ja) | 1972-07-08 | 1974-03-09 | ||
| US4463164A (en) * | 1983-02-15 | 1984-07-31 | Borg-Warner Chemicals, Inc. | Process for preparing polyphenylene ethers |
| DE3529093A1 (de) * | 1985-08-14 | 1987-02-19 | Bayer Ag | Verfahren zur herstellung von mono- und bifunktionellen oligophenylenoxiden |
| EP1152948A4 (en) * | 1999-01-19 | 2003-02-12 | Volusia Holding Corp | MARKER FOR PIPES, CONDUITS, TUBES AND RODS |
| US6211327B1 (en) | 1999-02-05 | 2001-04-03 | General Electric Company | Process for the manufacture of low molecular weight polyphenylene ether resins |
| JP4314666B2 (ja) * | 1999-03-29 | 2009-08-19 | 三菱瓦斯化学株式会社 | 低粘度ポリフェニレンエーテルの製造方法 |
| JP4736254B2 (ja) | 2001-06-28 | 2011-07-27 | 三菱瓦斯化学株式会社 | 2官能性フェニレンエーテルのオリゴマー体とその製造法 |
-
2002
- 2002-03-08 JP JP2002063626A patent/JP4007828B2/ja not_active Expired - Fee Related
-
2003
- 2003-02-28 US US10/500,701 patent/US7282554B2/en not_active Expired - Fee Related
- 2003-02-28 KR KR1020047013995A patent/KR100619641B1/ko not_active Expired - Fee Related
- 2003-02-28 WO PCT/JP2003/002302 patent/WO2003076495A1/ja not_active Ceased
- 2003-03-06 TW TW092104827A patent/TW583221B/zh not_active IP Right Cessation
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2016516871A (ja) * | 2013-04-29 | 2016-06-09 | エボニック デグサ ゲーエムベーハーEvonik Degussa GmbH | ポリ(アリーレンエーテル)の精製方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| KR100619641B1 (ko) | 2006-09-08 |
| WO2003076495A1 (fr) | 2003-09-18 |
| US20050070685A1 (en) | 2005-03-31 |
| US7282554B2 (en) | 2007-10-16 |
| JP2003261674A (ja) | 2003-09-19 |
| TW200304456A (en) | 2003-10-01 |
| TW583221B (en) | 2004-04-11 |
| KR20040107475A (ko) | 2004-12-20 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4007828B2 (ja) | 低分子量ポリフェニレンエーテルの製造方法 | |
| JP4108395B2 (ja) | ポリフェニレンエーテル | |
| JP2004099824A (ja) | 低分子量ポリフェニレンエーテルパウダー | |
| US7060781B2 (en) | 2,6-dimethyphenol composition | |
| JP5046351B2 (ja) | ポリフェニレンエーテルの製造方法 | |
| JP4176536B2 (ja) | 低分子量ポリフェニレンエーテルの製造方法 | |
| JP5588297B2 (ja) | ポリフェニレンエーテル | |
| JP2004339343A (ja) | ポリフェニレンエーテル | |
| JP6914109B2 (ja) | ポリフェニレンエーテル粉体の製造方法 | |
| JP2005272631A (ja) | 低分子量ポリフェニレンエーテル樹脂 | |
| JP5626877B2 (ja) | ポリフェニレンエーテル | |
| JP2010189548A (ja) | ポリフェニレンエーテルの製造方法 | |
| JP5311717B2 (ja) | 多官能性ポリフェニレンエーテルの製造方法 | |
| JP2009275208A (ja) | ポリフェニレンエーテルの製造方法 | |
| JPH1112354A (ja) | ポリフェニレンエーテルの製造方法及びその組成物 | |
| JP5635862B2 (ja) | ポリフェニレンエーテル | |
| JP5099805B2 (ja) | 分子量分布のピークを2個有するポリフェニレンエーテルの製造方法 | |
| CN112239536B (zh) | 聚苯醚树脂的制造方法 | |
| JPH0670131B2 (ja) | ポリフェニレンエ−テルの製造法 | |
| JP2006257227A (ja) | ポリフェニレンエーテルを製造する方法 | |
| JP2000281778A (ja) | ポリフェニレンエーテルの製造方法 | |
| JP2006265298A (ja) | ポリフェニレンエーテルの重合方法 | |
| JP2005281615A (ja) | 熱硬化性樹脂組成物前駆体の製造方法 | |
| JP2010260978A (ja) | ポリフェニレンエーテルの製造方法 | |
| JP2011099052A (ja) | ポリフェニレンエーテルの製造方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20040401 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20061219 |
|
| RD03 | Notification of appointment of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7423 Effective date: 20070213 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20070216 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20070828 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20070828 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20100907 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20100907 Year of fee payment: 3 |
|
| S531 | Written request for registration of change of domicile |
Free format text: JAPANESE INTERMEDIATE CODE: R313531 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20100907 Year of fee payment: 3 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20110907 Year of fee payment: 4 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20110907 Year of fee payment: 4 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20120907 Year of fee payment: 5 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20130907 Year of fee payment: 6 |
|
| LAPS | Cancellation because of no payment of annual fees |