JP2009542649A - スルホアルキルエーテルシクロデキストリンおよびコルチコステロイドを含む吸入製剤 - Google Patents
スルホアルキルエーテルシクロデキストリンおよびコルチコステロイドを含む吸入製剤 Download PDFInfo
- Publication number
- JP2009542649A JP2009542649A JP2009518094A JP2009518094A JP2009542649A JP 2009542649 A JP2009542649 A JP 2009542649A JP 2009518094 A JP2009518094 A JP 2009518094A JP 2009518094 A JP2009518094 A JP 2009518094A JP 2009542649 A JP2009542649 A JP 2009542649A
- Authority
- JP
- Japan
- Prior art keywords
- corticosteroid
- formulation
- dose
- sae
- nebulizer
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/08—Solutions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6835—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site
- A61K47/6851—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site the antibody targeting a determinant of a tumour cell
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/56—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids
- A61K31/57—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids substituted in position 17 beta by a chain of two carbon atoms, e.g. pregnane or progesterone
- A61K31/573—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids substituted in position 17 beta by a chain of two carbon atoms, e.g. pregnane or progesterone substituted in position 21, e.g. cortisone, dexamethasone, prednisone or aldosterone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/56—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids
- A61K31/58—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids containing heterocyclic rings, e.g. danazol, stanozolol, pancuronium or digitogenin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/715—Polysaccharides, i.e. having more than five saccharide radicals attached to each other by glycosidic linkages; Derivatives thereof, e.g. ethers, esters
- A61K31/716—Glucans
- A61K31/724—Cyclodextrins
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/30—Macromolecular organic or inorganic compounds, e.g. inorganic polyphosphates
- A61K47/36—Polysaccharides; Derivatives thereof, e.g. gums, starch, alginate, dextrin, hyaluronic acid, chitosan, inulin, agar or pectin
- A61K47/40—Cyclodextrins; Derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/56—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule
- A61K47/61—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule the organic macromolecular compound being a polysaccharide or a derivative thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/69—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit
- A61K47/6949—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit inclusion complexes, e.g. clathrates, cavitates or fullerenes
- A61K47/6951—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit inclusion complexes, e.g. clathrates, cavitates or fullerenes using cyclodextrin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/007—Pulmonary tract; Aromatherapy
- A61K9/0073—Sprays or powders for inhalation; Aerolised or nebulised preparations generated by other means than thermal energy
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/007—Pulmonary tract; Aromatherapy
- A61K9/0073—Sprays or powders for inhalation; Aerolised or nebulised preparations generated by other means than thermal energy
- A61K9/0078—Sprays or powders for inhalation; Aerolised or nebulised preparations generated by other means than thermal energy for inhalation via a nebulizer such as a jet nebulizer, ultrasonic nebulizer, e.g. in the form of aqueous drug solutions or dispersions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/02—Nasal agents, e.g. decongestants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/06—Antiasthmatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
- A61P27/14—Decongestants or antiallergics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/16—Otologicals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/08—Antiallergic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B82—NANOTECHNOLOGY
- B82Y—SPECIFIC USES OR APPLICATIONS OF NANOSTRUCTURES; MEASUREMENT OR ANALYSIS OF NANOSTRUCTURES; MANUFACTURE OR TREATMENT OF NANOSTRUCTURES
- B82Y5/00—Nanobiotechnology or nanomedicine, e.g. protein engineering or drug delivery
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08B—POLYSACCHARIDES; DERIVATIVES THEREOF
- C08B37/00—Preparation of polysaccharides not provided for in groups C08B1/00 - C08B35/00; Derivatives thereof
- C08B37/0006—Homoglycans, i.e. polysaccharides having a main chain consisting of one single sugar, e.g. colominic acid
- C08B37/0009—Homoglycans, i.e. polysaccharides having a main chain consisting of one single sugar, e.g. colominic acid alpha-D-Glucans, e.g. polydextrose, alternan, glycogen; (alpha-1,4)(alpha-1,6)-D-Glucans; (alpha-1,3)(alpha-1,4)-D-Glucans, e.g. isolichenan or nigeran; (alpha-1,4)-D-Glucans; (alpha-1,3)-D-Glucans, e.g. pseudonigeran; Derivatives thereof
- C08B37/0012—Cyclodextrin [CD], e.g. cycle with 6 units (alpha), with 7 units (beta) and with 8 units (gamma), large-ring cyclodextrin or cycloamylose with 9 units or more; Derivatives thereof
- C08B37/0015—Inclusion compounds, i.e. host-guest compounds, e.g. polyrotaxanes
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08L—COMPOSITIONS OF MACROMOLECULAR COMPOUNDS
- C08L5/00—Compositions of polysaccharides or of their derivatives not provided for in groups C08L1/00 or C08L3/00
- C08L5/16—Cyclodextrin; Derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2300/00—Mixtures or combinations of active ingredients, wherein at least one active ingredient is fully defined in groups A61K31/00 - A61K41/00
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Animal Behavior & Ethology (AREA)
- Engineering & Computer Science (AREA)
- Epidemiology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Organic Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Molecular Biology (AREA)
- Pulmonology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Polymers & Plastics (AREA)
- Nanotechnology (AREA)
- Otolaryngology (AREA)
- Inorganic Chemistry (AREA)
- Biochemistry (AREA)
- Biophysics (AREA)
- Biotechnology (AREA)
- General Engineering & Computer Science (AREA)
- Medical Informatics (AREA)
- Crystallography & Structural Chemistry (AREA)
- Dispersion Chemistry (AREA)
- Materials Engineering (AREA)
- Immunology (AREA)
- Cell Biology (AREA)
- Ophthalmology & Optometry (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicinal Preparation (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
Abstract
SAE−CDおよびコルチコステロイドを含む吸入可能な製剤が提供される。製剤は、あらゆる公知のネブライザーにより被験者に噴霧投与するように適合される。製剤は、キットに含めることができる。製剤は、水溶液として投与される。しかしながら、ドライパウダー、即使可能溶液、または濃縮組成物として貯蔵することができる。製剤は、コルチコステロイドの吸入投与を行う改善された噴霧システムで使用される。製剤内に存在するSAE−CDは、ブデソニドの化学的安定性を著しく高める。製剤を吸入投与する方法が提供される。製剤は、従来の経鼻送達装置により投与することもできる。
Description
先の出願との相互参照
本願は、2006年6月30日に出願された米国特許出願第11/479,979号の一部継続出願であり、その優先権を主張するものである。
本願は、2006年6月30日に出願された米国特許出願第11/479,979号の一部継続出願であり、その優先権を主張するものである。
本発明は、スルホアルキルエーテルシクロデキストリンおよびブデソニドなどのコルチコステロイドの製剤を、噴霧および吸入によって投与する方法およびシステムに関する。本発明は、さらに、呼吸器疾患又は気道の疾患を治療する方法にも関する。
吸入による薬剤の送達により、呼吸管のさまざまな部位、例えば、咽喉、気管、気管支、および肺胞への薬剤の沈着が可能になる。一般に、粒径が小さいほど、粒子は空中に浮遊している時間が長くなり、薬剤は呼吸管の奥深くまで到達できる。コルチコステロイドは、ネブライザー、定量式吸入器、または乾燥粉末式吸入器を使用して、吸入により送達される。肺への導入の他の方法に比べて勝るネブライザーの主な利点は、患者の協力を必要とせず、高用量の薬物を容易に送達できる点である。しかし、ネブライザーに関する主な問題点は、コストが高いこと、携帯性に劣ること、予め薬物を調製する必要があり不便であること、治療を行うのに長い時間を要することである。コルチコステロイドなどの薬剤の噴霧投与を改善する方法が望まれる。
ブデソニド(ブチルアルデヒドとの(R,S)−11β,16α,17,21−テトラヒドロキシプレグナ−1,4−ジエン−3,20−ジオン環状16,17−アセタール、C25H34O6、Mw:430.5)はよく知られている。これは、2つの異性体(22Rおよび22S)の混合物として市販されている。ブデソニドは、強力な糖質コルチコイド作用を示す抗炎症性コルチコステロイドである。ブデソニドの投与は、小児の喘息の維持治療のため、また予防治療として適応される。
ブデソニドの市販製剤は、AstraZeneca LP(デラウェア州ウィルミントン)により、ENTOCORT(商標) EC、PULMICORT RESPULES(登録商標)、Rhinocort Aqua(登録商標)、Rhinocort(登録商標)Nasal Inhaler、およびPulmicort Turbuhaler(登録商標)という商標で、またそのジェネリック名で販売されている。微粉末化ブデソニドの滅菌水性懸濁液である、PULMICORT RESPULES(登録商標)suspensionは、ネブライザー、特に公称投入量に含まれる薬剤質量2から18%を送達する圧縮空気駆動ジェット式ネブライザーで吸入投与される。PULMICORT RESPULESの単位投与用の一般的製剤は、米国特許第6,598,603号に記載されており、そしてこれはブデソニドが、水1ml当たり約0.05〜1.0mgのブデソニド、0.05〜0.15mgのNaEDTA、8.0〜9.0mgのNaCl、0.15〜0.25mgのポリソルベート、0.25〜0.30mgの無水クエン酸、および0.45〜0.55mgのクエン酸ナトリウムを含む水性媒体中に懸濁されている水性懸濁液である。RHINOCORT(登録商標)NASAL INHALER(商標)は、推進剤の混合物中に微粉末化ブデソニドの懸濁液を含む加圧式定量噴霧式エアロゾルユニットである。RHINOCORT(登録商標)AQUA(商標)は、水性媒体に微粉末化ブデソニドを混ぜた懸濁液を含む無香定量手動ポンプ式噴霧製剤である。この懸濁液は、超音波ネブライザーで投与すべきではない。
作動様式の異なる多種多様なネブライザー、例えば、ジェットネブライザー(場合により圧縮機付きで売られている)、超音波ネブライザー、振動膜ネブライザー、振動メッシュネブライザー、振動板(plate)ネブライザー、振動円錐ネブライザーなどが利用可能である。振動メッシュ、振動円錐又は振動板ネブライザーは、送達に空気圧縮機の使用が不要であり、単位用量の送達後リザーバ中の残留量が最小であり、また低容量の吸入可能溶液を送達するために使用できることから、特に興味深い。典型的な振動膜、振動メッシュ又は振動板ネブライザーは、R. Dhand (Respiratory Care、(2002年12月)、47(12)、1406〜1418頁)によって記載されている。Kellerら(ATS 99th International Conference、シアトル、2003年5月16〜21日;ポスター2727)は、PARI eFlowネブライザーによるAZTREONAMの投与に関する研究の結果を開示し、また低い口腔咽頭の沈着、充填体積によって影響されない噴霧効率、82±1.7%の呼吸可能画分、吸入サイクル時間当たりの一定した用量投与、及び送達用量、充填用量及び噴霧時間の間の優れた相関、及び予測される高い肺沈着について報告している。
噴霧用薬液の所望の特性は、一般に、1)低粘度、2)無菌媒体、3)低表面張力、4)ネブライザーのメカニズムに対する安定性、5)約4〜10の中程度のpH、6)MMADが5μm未満、または好ましくは3μm未満である液滴を形成する能力、7)刺激性の保存剤および安定剤を含まないこと、8)好適な張度を含む。一方で、懸濁液は、いくつかの利点を有するが、他方で、溶液は、他のいくつかの利点を有する。
Smaldoneら(J.Aerosol Med.(1998年)、11、113〜125頁)は、ブデソニド懸濁液の吸入質量および粒子分布のインビトロ測定に関する研究結果を開示している。Smaldoneらは、ブデソニドのネブライザー投入量の2%〜18%が、懸濁液から送達された、すなわち、ブデソニド送達は不完全であり、その結果、薬剤の著しい無駄が生じたと結論付けている。13の最も効率的なシステムでは、懸濁液は、下気道送達に対し十分うまく噴霧できる。
他の研究では、さらに、ネブライザー毎に噴霧効率がかなりばらつくことが実証されている。Barryら(J.Allergy Clin.Immunol.(1998年)、320〜321頁)は、霧状ブデソニドで患者を治療する際に、このようなばらつきを考慮しなければならないと主張している。Bergら(J.Aerosol Sci.(1998年)、19(7)、1101〜1104頁)は、さらに、ネブライザー毎にPULMICORT(商標) 懸濁液の噴霧効率が非常にばらつくことを報告している。さらに、噴霧される液滴の質量平均空気動力学的直径(MMAD)は、ネブライザー毎に非常にばらつく。一般に、懸濁液は、溶液に比べて噴霧効率があまりよくない(O’Riordan(Respiratory Care、(2002)、1305〜1313頁)。吸入コルチコステロイドは、喘息の治療で使用され、作用部位、すなわち肺に直接送達されるため著しく有益である。吸入コルチコステロイドの目標は、肺の局部療法で即効性薬剤作用を利用できるようにすることである。吸入コルチコステロイドは、肺からよく吸収される。実際、肺の受容体部位で使用できる薬剤はすべて、全身的に吸収されると仮定できる。しかし、現行の方法および製剤を使用するのでは、吸入コルチコステロイド投薬量の大部分が嚥下され、経口吸収に利用されることになり、望ましくない全身的影響が生じることがよく知られている。吸入コルチコステロイドでは、肺は標的器官であるため、高い肺利用率(high pulmonary availability)は、高い経口生物学的利用率(high oral bioavailability)よりも重要である。肺利用率の高い製品は、肺に陽性効果をもたらす可能性が高い。理想的な吸入コルチコステロイド製剤であれば、経口送達を最小限に抑え、それにより全身への悪影響が生じる可能性を低減する。
肺に送達されるコルチコステロイド投薬量の大半は、全身的に吸収され、利用可能である。経口送達される吸入コルチコステロイド投薬量の部分について、利用率は、胃腸管からの吸収および肝臓における初回通過代謝の程度に左右される。コルチコステロイド薬剤送達投薬量のこの経口成分は薬効をもたらさないが、全身的副作用を高める可能性があるため、吸入コルチコステロイドの経口利用率を比較的低く抑えることが望ましい。
粒径と処方は両方とも、吸入コルチコステロイドの効能に影響を及ぼす。薬剤の処方は、その薬剤を肺に送達することに対して、したがってその効能に対して重大な影響を及ぼす。肺に薬剤を送達する上で最も重要なのは、エアロゾルビヒクルと送達される粒子のサイズである。さらに、肺への沈着度が低いことから、口腔咽頭への沈着度が高いことが示唆される。採用される特定の処方により、いくつかのコルチコステロイドは、口および喉に沈着する可能性が比較的高く、局所的悪影響を引き起こす可能性がある。
受容体分布が、気管支拡張薬の効能の主要な決定因子であるが、粒径は、吸入コルチコステロイド(corticodsteroid)の効能を決定する際により重要であるように見える。最小気道の内径は、2ミクロン(mcm)以下である。そのため、平均空気動力学的直径が1mcmである粒子を使用する吸入器は、平均直径が3.5から4mcmである粒子を使用する吸入器よりも大きな呼吸可能画分を持つべきである。閉塞性肺疾患の患者の場合、すべての粒子は、2から3mcm以下であるのが理想的である。小さな(5mcm未満の)粒子は、肺のより小さな気道内に吸入される可能性が高く、そのため、効能が改善される。対照的に、5mcmよりも大きな粒子は、口および喉に沈着する可能性があり、両方とも、肺に到達する粒子の割合を減らし、口腔カンジダ症および嗄声(発声困難)などの局所的悪影響を引き起こす可能性がある。質量平均空気動力学的直径(MMAD)が1mcmに近い粒子は、3.5mcm以上の直径を有する粒子よりも用量当たりの呼吸可能画分が大きいと考えられる。
ブデソニド懸濁液の噴霧の他の欠点は、MMADが約3μm未満と非常に小さな液滴を発生させる必要がある点である。噴霧される液滴は非常に小さいため、微粉末化されたブデソニドは、なおいっそう小さくなければならないか、または0.5〜2.0μmの範囲内になければならず、粒子は、狭い粒径分布を持つべきである。このような粒子の生成は、困難である。
そうであっても、1ミクロン未満の粒子を使用することにより超音波ネブライザーによるブデソニド懸濁液の噴霧を改善する努力が行われている(Kellerら、Respiratory Drug Delivery VIII(2002年)、197〜206頁)。コルチコステロイドのナノ粒子(0.1〜1.0μm)の懸濁液を使用して、PULMICORT(商標)懸濁液の場合のようなより粗い懸濁液と比較して呼吸性粒子の割合を増やすことが可能である。PULMICORT(商標)懸濁液(懸濁液中約4.4μmのブデソニド粒径)に対する改善は観察されなかった。さらに、ナノ粒子懸濁液の使用に関して、小さな粒子(0.05μm未満)は被験者にアレルギー性反応を誘発する可能性があるという点で問題が存在する。Sheffield Pharmaceuticals,Inc.(ミズーリ州セントルイス、Kraftら「The Pharmacoki
netics of Nebulized Nanocrystal Budesonide Suspension in Healthy Volunteers」J.Clin.Pharmacol.、(2004年)、44:67〜72頁)は、液体媒体中に分散されたブデソニドのナノ粒子を含む懸濁液ベースの製剤である、UDB(単位用量ブデソニド)の調製および評価を開示している。この製品は、MAP Pharmaceuticals,Inc.(カリフォルニア州マウンテンビュー)により開発されている。Seemanら(ATS 99th International Conference、Seattle、5月16〜21日、2003年;ポスター2727)は、ブデソニド懸濁液を用いるARI eFlowネブライザー(PULMICORT RESPULES、2mlアンプル中500mg/ml)の性能を評価する研究の結果を開示し、そして3.6〜4.2μmのMMAD及び67%以上の呼吸可能画分を達成したことを報告している。
netics of Nebulized Nanocrystal Budesonide Suspension in Healthy Volunteers」J.Clin.Pharmacol.、(2004年)、44:67〜72頁)は、液体媒体中に分散されたブデソニドのナノ粒子を含む懸濁液ベースの製剤である、UDB(単位用量ブデソニド)の調製および評価を開示している。この製品は、MAP Pharmaceuticals,Inc.(カリフォルニア州マウンテンビュー)により開発されている。Seemanら(ATS 99th International Conference、Seattle、5月16〜21日、2003年;ポスター2727)は、ブデソニド懸濁液を用いるARI eFlowネブライザー(PULMICORT RESPULES、2mlアンプル中500mg/ml)の性能を評価する研究の結果を開示し、そして3.6〜4.2μmのMMAD及び67%以上の呼吸可能画分を達成したことを報告している。
溶解薬剤とは反対に薬剤粒子の吸入は、不利であることが知られている。Brainら(Bronchial Asthma、2nd Ed.)(Ed.E.B.Weisら、Little Brown & Co.(1985年)、594〜603頁)は、肺気道および鼻腔を覆う粘液の層に沈着する低溶解性粒子は、線毛により咽頭の方へ送られることを報告している。このような粒子は、上気道内に沈着したより大きな薬剤粒子を含む。鼻腔および肺に由来する粘液、細胞、および残屑は、咽頭に集まり、唾液と混ざり、嚥下された後、胃腸管に入る。このメカニズムにより、粒子は、数分から数時間のハーフタイムで肺から取り出されることが報告されている。したがって、ブデソニドなどのゆっくり溶解する薬剤を可溶化するにはほとんど時間がない。対照的に、肺胞などの非線毛性区画内に沈着した粒子は、滞留時間がかなり長い。深い肺沈着のためのブデソニドの非常に小さな粒子を生成することは困難であるため、吸入懸濁液の大半は、上から中までの気道に見られる可能性が高い。しかし、溶液から小さな液滴を生成するのは、固形物の懸濁液から小さな液滴を生成するよりもかなり簡単である。これらの理由から、ブデソニド含有溶液の噴霧は、懸濁液の噴霧よりも好ましい。
O’Riordan(Respiratory Care(2002年11月)、47(11)、1305〜1313頁)では、溶液または懸濁液のいずれかの噴霧により薬剤を送達できるが、一般に、溶液の噴霧は、懸濁液の噴霧よりも好ましいと主張している。O’Riordanは、超音波ネブライザーは、懸濁液では使用すべきではなく、溶液でのみ使用すべきであると主張している。
O’Callaghan(Thorax、(1990年)、45、109〜111頁)、Storrら(Arch.Dis.Child(1986年)、61、270〜273頁)、およびWebbら(Arch.Dis.Child(1986年)、61、1108〜1110頁)は、コルチコステロイド(特に、ベクロメタゾン)溶液の噴霧は、懸濁液の噴霧よりも好ましい場合があるが、それは、後者が、噴霧粒子が大きすぎて治療有効量が肺に入りきらない場合に不効率であるためであることを示唆している。しかし、フルニソリド溶液対懸濁液の噴霧に関してO’Callaghan(J.Pharm.Pharmacol.(2002年)、54、565〜569頁)によって提示されているデータは、両者とも同様の効能を示していた。したがって、溶液の噴霧は、懸濁液の噴霧よりも好ましいということは一般化できない。
したがって、噴霧による投与用のコルチコステロイドを含む非懸濁液製剤が必要であることは広く認識されている。しかし、PULMICORT(登録商標)懸濁液単位用量製剤は、吸入療法の分野では広く利用されて、そして受け入れられている。PULMICORT(登録商標)懸濁液単位用量製剤、またはより一般的には、コルチコステロイドを含む懸濁液単位用量製剤の投与を改善する方法を提供することは、この治療分野には非常に有益であろう。
しかし、ネブライザー療法で現在重視しているのは、より高い濃度の薬剤を投与し、溶液、可能ならば好ましくは非水性もしくはアルコール性もしくは非水性アルコール性の溶液または懸濁液よりもむしろ主に水溶液を使用し、治療時間を最短にし、噴霧と吸入との同期をとり、薬剤のより深い肺沈着のため、より小さな液滴を投与することである。
噴霧用のコルチコステロイド含有溶液は公知である。噴霧用の溶液を調製する方法は多数あり、さまざまである。これらは、一般に、共溶媒、界面活性剤、または緩衝液を添加することにより製造されている。しかし、エタノール、ポリエチレングリコール、およびプロピレングリコールなどの共溶媒は、気道の炎症のため吸入投与される場合に低量でしか許容されない。吸入製品におけるこれらの共溶媒の許容レベルには限界がある。典型的には、共溶媒は、噴霧組成物の約35質量%未満を占めるが、これは共溶媒の全用量であると共に、これらの限界を決定する濃度でもある。これらの限界は、これらの溶媒の肺組織の局部炎症を引き起こす、流体を肺に導き入れる高浸透圧溶液を形成する、および/または患者を酩酊させる傾向により定められる。さらに、最も有望な疎水性治療薬は、これらの共溶媒混合液に必ずしも十分に溶解するわけではない。
Saidiら(米国特許第6,241,969号)は、経鼻および経肺送達用のコルチコステロイド含有溶液の調製を開示している。溶解されたコルチコステロイドは、貯蔵用として濃縮された本質的に非水性の形態で、または投与用として希釈された水性ベース形態で提供される。
Kellerら(in Respiratory Drug Delivery IX、(2004年)、221〜231頁)は、小児に対してブデソニド及び界面活性剤を含有する溶液製剤の沈着を開示している。
Lintzら(AAPS Annual Meeting and Exposition、ボルティモア、11月8日、2004年、ポスターM1128)は、ブデソニド、水、クエン酸塩、塩化ナトリウム、およびアルコール、プロピレングリコール、ならびに/またはTween、Pluronic、もしくはHLB値が10から20までのリン脂質などの界面活性剤を含む液体製剤の調製及びエアロゾル特性を開示している。振動膜/メッシュネブライザー(Pari eFlow)におけるこのような組み合わせ界面活性剤溶液の懸濁液と比較したエアロゾル特性が、成人及び小児の呼吸シミュレーションを用いて検討された。かれらは、その溶液でPari eFlowに関し83.3%、及びPARILC+でPULMICORT RESPULESに関し61%の呼吸可能画分を報告した。かれらはまた、呼吸性ドラッグデリバリー率(薬剤%<5μm/分)、送達用量(装置に充填された薬剤の%)、ドラッグデリバリー率(薬剤%/分)、及び呼吸可能用量(5μm未満%)についての結果を報告した。
Schueeppら(ATS 99th International Conference、シアトル、5月16〜21日、2003年;ポスター1607)は、ベビーキャストモデルを利用し、また種々の呼吸パターンを適用して実験的ブデソニド溶液(0.5ml中100μg)による特注eFLow Baby Functional Modelの性能評価を開示している。
PULMICORT(商標)懸濁液を投与するための代替アプローチは、リポソーム製剤の投与である。Waldrepら(J.Aerosol Med.(1994年)、7(2)、135〜145頁)は、ブデソニドおよびホスファチジルコリン誘導体のリポソーム製剤を調製することに成功したことを報告した。
上記のいずれの製剤も、コルチコステロイドを含む懸濁液ベースの単位用量製剤の投与を改善する方法を提供してはいない。むしろ、当該技術分野の一般的な焦点は、液体製剤を最初に調製することによって懸濁液の製剤化を完全に回避することにあり、この液体製剤は次に複数の単位用量に分割され、この単位用量は販売用にパッケージングされ、使用のために販売される。
シクロデキストリンおよびその誘導体による薬剤の可溶化はよく知られている。シクロデキストリンは、デンプンから誘導される環状糖質である。未修飾のシクロデキストリンは、円柱構造に結合しているグルコピラノース単位の数の点で異なる。親シクロデキストリンは、6、7、または8個のグルコピラノース単位を含み、これらは、それぞれα−、β−、およびγ−シクロデキストリンと呼ばれる。それぞれのシクロデキストリンサブユニットは、2−位および3−位に第二ヒドロキシル基を、6−位に第一ヒドロキシル基を持つ。シクロデキストリンは、親水性の外面と疎水性の内部空洞を持つ中空の円錐台として描くことができる。水溶液では、これらの疎水性空洞は、疎水性有機化合物の構造の全部または一部をそれらの空洞に納めることができるその疎水性有機化合物のおさまり場所となる。この方法は、包接錯体化として知られ、錯体化された薬剤に対する見かけの水溶解度および安定度を高めることができる。錯体は、疎水性相互作用により安定化され、共有結合の形成を伴わない。
この動的で可逆的な平衡過程は、式1および2により記述することができ、錯体化された形態の量は、薬剤およびシクロデキストリンの濃度、ならびに平衡または結合定数Kbの関数である。シクロデキストリン製剤が、血流への注入により投与されると、錯体は、希釈の効果、および血液および組織成分への薬剤の非特異的結合により急速に解離する。
シクロデキストリンおよび活性物質の結合定数は、平衡溶解度法により決定することができる(T.Higuchiら「Advances in Analytical Chemistry and Instrumentation Vol.4」、C.N.Reilly ed.、John Wiley & Sons,Inc、1965年、117〜212頁)。一般に、シクロデキストリンの濃度が高いほど、式1および2の平衡過程はより錯体の形成に移行する、すなわち、遊離薬剤濃度は、一般に、溶液中のシクロデキストリンの濃度を高めることにより減少する。
未誘導体化親シクロデキストリンは、ヒトの組織と相互作用し、コレステロールやその他の膜成分を、特に腎臓尿細管細胞において蓄積する際に、抽出することが知られており、そのことが有毒で、ときに致死的な腎臓への影響をもたらすことが知られている。
親シクロデキストリンは、与えられた基質に対する異なる親和性を示すことが多い。例えば、γ−シクロデキストリンは、限定された溶解度の錯体を形成することが多く、得られる溶解度曲線はBs型である。この挙動は、液体調製物においてγ−CDの使用に対し重大な制限を課す多数のステロイドについて知られている。一方、β−CDは、多数の異なるクラスのホスト化合物とうまく錯体を形成しない。β−CDおよびγ−CDについては、誘導体化、例えば、アルキル化を行うと、親CDに比べて誘導体の水溶解度がよくなるだけでなく、溶解度曲線の型も制限のあるBs型からより直線性の高いA型曲線に変化することが示されている(Bernd W.MullerおよびUlrich Brauns「Change of Phase−Solubility Behavior by Gamma−Cyclodextrin Derivatization」Pharmaceutical Research(1985年)、309〜310頁)。
親シクロデキストリンの化学修飾(通常は、ヒドロキシル基において)の結果、錯化能力を保持または改善しつつ安全性を向上させた誘導体が得られている。今日まで製造された多数の誘導体化シクロデキストリンのうち2つ、すなわち、2−ヒドロキシプロピル誘導体(HP−CD、中性シクロデキストリンはJanssenおよび他により商業的に開発中である)、およびスルホブチルエーテルなどのスルホアルキルエーテル誘導体(SBE−CD、アニオン性シクロデキストリンはCyDex Inc.により開発中である)のみが商業的に実現可能であるように思われる。しかし、HP−β−CDは、それでも、SBE−CDが有しない毒性を有する。
Stellaらの米国特許第5,376,645号および第5,134,127号Parmerterらの米国特許第3,426,011号、Lammersら(Recl.Trav.Chim.Pays−Bas(1972年)、91(6)、733〜742頁)、Staerke(1971年)、23(5)、167〜171頁)、およびQuら(J.Inclusion Phenom.Macro.Chem.、(2002年)、43、213〜221頁)は、スルホアルキルエーテル誘導体化シクロデキストリンを開示している。これらの参考文献は、SAE−CDが、一連のさまざまな化合物を可溶化するのに適していることを示唆している。しかしながら、Stellaは、有効成分、コルチコステロイドでさえ、水中への可溶化に好適な活性成分に対するスルホアルキルエーテル誘導体化シクロデキストリンのモル比が、10:1から1:10まで変動することを開示している。
ベータシクロデキストリンのスルホブチルエーテル誘導体(SBE−β−CD)、特にシクロデキストリン分子1個当たり平均約7個の置換基を含む誘導体(SBE7−β−CD)は、CAPTISOL(登録商標)としてCyDex,Inc.により商品化されている。アニオン性スルホブチルエーテル置換基は、親シクロデキストリンの水溶解度を劇的に改善する。さらに、電荷の存在は、ヒドロキシプロピル誘導体と比較して分子がコレステロールと錯体を形成する能力を低下させる。薬剤とCAPTISOL(登録商標)シクロデキストリンとの可逆非共有錯体により、水溶液中の薬剤の溶解性および安定性を増大させることができる。CAPTISOL(登録商標)は、比較的新しく知られているシクロデキストリンであるが、噴霧用のコルチコステロイド含有溶液の調製での使用は、まだ評価されていない。
溶血アッセイは、一般に、非経口製剤の分野で、特定の製剤が被験者の血流に注入するのに不適当である可能性があるかどうかを予測するために使用される。検査される製剤が著しい量の溶血を誘発する場合、その製剤は、一般に、被験者への投与に適しないものと考えられる。一般に、より高いオスモル濃度は、より高い溶血潜在性(hemolytic potential)に関連することが予想される。図1に示されているように(Thompson、D.O.、Critical Reviews in Therapeutic Drug Carrier Systems、(1997年)、14(1)、1〜104頁)、CAPTISOL(登録商標)の溶血挙動は、親β−シクロデキストリン、市販のヒドロキシプロピル誘導体、ENCAPSIN(商標)シクロデキストリン(置換度約3−4)、およびMOLECUSOL(登録商標)シクロデキストリン(置換度約7−8)、および他の2つのスルホブチルエーテル誘導体であるSBE1−β−CDおよびSBE4−β−CDに対する溶血挙動と比較される。他のシクロデキストリン誘導体とは異なり、スルホアルキルエーテル(SAE−CD)誘導体、特に、CAPTISOL(登録商標)(置換度約7)およびSBE4−β−CD(置換度約4)などの誘導体は、本質的に、溶血挙動をまったく示さず、医薬品製剤を可溶化するために典型的に使用される濃度の市販のヒドロキシプロピル誘導体よりも実質的に低い膜障害潜在性しか示さない。図に示されている濃度の範囲は、注入後血流内で最初に希釈されたときに医薬品製剤を可溶化するために典型的に使用される濃度を含む。経口投与後、SAE−CDは、著しい全身的吸収を受けない。
製剤のオスモル濃度は、一般に、溶血潜在性に関連し、オスモル濃度が高いほど(または高張度であるほど)、溶血潜在性は高まる。Zannouら(「Osmotic properties of sulfobutyl ether and hydroxypropyl cyclodextrins」、Pharma.Res.(2001年)、18(8)、1226〜1231頁)は、SBE−CDおよびHP−CDを含む溶液のオスモル濃度を比較した。図2に示されているように、SBE−CD含有溶液のオスモル濃度は、類似の濃度のシクロデキストリン誘導体を含むHP−CD含有溶液よりも高い。そのため、SAE−CDは、HP−CDが低いオスモル濃度を有するとしても、同等の濃度でHP−CDが示す場合よりも低い溶血しか示さなかったことは驚くべきことである。
メチル化シクロデキストリンが調製されており、ヒト赤血球に対する溶血効果が評価されている。これらのシクロデキストリンは、中等度から重度の溶血を引き起こすことが判明した(Jodalら、Proc.4th Int.Symp.Cyclodextrins、(1988年)、421〜425頁、Yoshidaら、Int.J.Pharm.、(1988年)、46(3)、217〜222頁)。
哺乳類の肺の中へのシクロデキストリンの投与は、許容されない場合がある。実際、天然のシクロデキストリンおよびシクロデキストリン誘導体の潜在的な、または観察された毒性に関する文献が存在する。NTP Chemical Repositoryは、α−シクロデキストリンは吸入により害を及ぼす可能性のあることを示している。Nimbalkarら(Biotechnol.Appl.Biochem.(2001年)、33、123〜125頁)は、肺細胞の細胞増殖を遅らせる初期効果のためHP−β−CD/ジアセチルダプソン錯体(diacetyldapsone complex)の肺における利用について警告している。
それでも、吸入に対するシクロデキストリンの利用に関する多数の研究が、何も商業化されていないが、報告されている。これらの研究は、特定の最適な、またはさらには有用な吸入または経鼻投与製剤には異なる薬剤−シクロデキストリンの組み合わせが必要であることを示唆している。これまで、経口腔、経肺、および/または経鼻送達用のシクロデキストリン含有粉末および溶液の開発が試みられてきた。
Otterbeckらの米国特許第5,914,122号では、発泡体として直腸投与用の安定したブデソニド含有溶液の調製を開示している。Otterbeckらは、安定剤としてのβ−CD、γ−CDもしくはHP−β−CD、および/またはEDTAなどの、シクロデキストリンの好ましい利用を実証した。シクロデキストリンは、さらに、溶液中のブデソニドの濃度を高めるための可溶化剤としても示唆されている。それぞれの場合に、活性物質の受け入れ可能な保持に関して、その製剤のいくつかについてOtterbeckらが報告している最大の貯蔵寿命は、わずか、3ヶ月から6ヶ月である。
McCoyらの米国特許付与前特許公開第20020055496号は、HP−β−CDを含む本質的に非水性の口腔内製剤を開示している。これらの製剤は、エアロゾル、噴霧器、または噴霧剤を使用して投与することができる。
Chuchalinのロシア特許第2180217号では、吸入用の安定したブデソニド含有溶液を開示している。溶液は、ブデソニド、プロピレングリコール、ポリ(エチレンオキシド)、コハク酸、トリロンB、ニパゾール、チオ尿素、水、および場合によってはHP−β−CDを含む。
Mullerら(Proceed.Int’l.Symp.Control.Rel.Bioact.Mater.(1997年)、24、69〜70頁)は、乾燥粉末式吸入器で使用するASES(エアロゾル溶媒抽出システム(Aerosol Solvent Extraction System))超臨界二酸化炭素プロセスによるブデソニド微粒子の調製に関する研究結果を開示している。HP−β−CDは、粉末の担体として提案されている。
Muellerら(米国特許第6,407,079号)は、HP−β−CDを含む薬剤組成物を開示している。Mullerらは、シクロデキストリンを含む溶液の経鼻投与が可能であることを示唆している。
当技術分野では、特定の種類のシクロデキストリン誘導体の構造上関係するバラツキの評価を、特定の化合物とその種類のシクロデキストリン誘導体との結合を最適化するために行う必要がある場合があることを認識している。しかし、特定の化合物と特定のシクロデキストリン誘導体の第1の実施態様との結合と、第2の実施態様との結合との間には極端な違いがない場合が多い。例えば、第1のシクロデキストリン誘導体に対する特定の治療薬の結合と、構造上関係のある第2のシクロデキストリン誘導体に対する特定の治療薬の結合との間に極端な違いがある場合は稀である。このような状況がまさに存在する場合、そのような違いは予期できない。Worthら(24th International Symposium on Controlled Release of Bioactive Materials(1997年))は、経肺送達用のステロイド/シクロデキストリン錯体の効用を評価する研究の結果を開示している。並べた比較において、β−CD、SBE7−β−CD、およびHP−β−CDは、ジプロピオン酸ベクロメタゾン(BDP)およびその活性代謝産物モノプロピオン酸ベクロメタゾン(BMP)との包接錯体を形成する能力に従って評価された。BMPは、シクロデキストリンでより容易に可溶化され、可溶化力(solubilizing power)の観察された順序は、HP−β−CD(最高)>β−CD>SBE7−β−CDであった。そのため、当業者であれば、SAE−CD誘導体は、BMPまたはBDPなどのコルチコステロイドの可溶化での使用に適しないと予想するであろう。吸入製剤における実際の効用に関する結果はいっさい開示されていないが、BDPよりはむしろBMPのほうが、ネブライザー溶液の開発の代替手段として優れていることを示唆している。
Kinnarinenら(11th International Cyclodextrin Symposium CD(2002年))は、乾燥粉末式吸入用のブデソニド/γ−CD包接錯体のインビトロの肺への沈着の研究結果を開示している。γ−CDとの錯化に利点は観察されなかった。Vozoneら(11th International Cyclodextrin Symposium CD(2002年))は、乾燥粉末式吸入で使用するブデソニドとγ−シクロデキストリンとの錯化に関する研究結果を開示している。シクロデキストリン錯体、またはブデソニドとCDの物理的混合物の放出用量に、違いは観察されなかった。しかし、両方の製剤の微粒子画分で観察される違いから、経肺薬剤送達にシクロデキストリン錯体を使用すると、乾燥粉末の呼吸可能画分が増大しうることが示唆された。
Pintoら(S.T.P.Pharma.Sciences(1999年)、9(3)、253〜256頁)は、ベクロメタゾンの吸入可能乾燥粉末製剤でHP−β−CDを使用することに関する研究結果を開示している。HP−β−CDは、MICRO−HALER(商標)吸入装置から放出用量のインビトロ沈着の研究において、薬剤との錯体または物理的混合物として評価された。呼吸性薬剤画分の量は、錯体併用では最高であり、微粉末化薬剤単独では、最低であると報告された。
Rajewskiら(J.Pharm.Sci.(1996年)、85(11)、1142〜1169年)は、シクロデキストリンの薬剤としての適用についてレビューしている。そのレビューでは、乾燥粉末吸入システムにおけるシクロデキストリン錯体の使用を評価する研究を引用している。
Shaoら(Eur.J.Pharm.Biopharm.(1994年)、40、283〜288頁)は、肺吸収促進剤としてシクロデキストリンの有効性に関して報告した。肺インスリン吸収を増強するシクロデキストリンの相対的有効性は、薬力学により測定されたとおりであり、相対的薬効は、ジメチル−β−シクロデキストリン>α−シクロデキストリン>β−シクロデキストリン>γ−シクロデキストリン>ヒドロキシプロピル−β−シクロデキストリンのようにランク付けされた。この報告に鑑みて、当業者であれば、未誘導体化β−CDは未誘導体化γ−CDよりも適しているため、γ−CDの水溶性誘導体は、β−CDのそれぞれの誘導体に比べて吸入を介した化合物送達にはあまり適しないと予想するであろう。
Williamsら(Eur.J.Pharm.Biopharm.(1999年3月)、47(2)、145〜52頁)は、2−ヒドロキシプロピル−β−シクロデキストリン(HP−β−CD)の製剤手法がヒドロフルオロアルカン(HFA)噴霧剤を含む懸濁液ベースの加圧式定量噴霧式吸入器(pMDI)製剤中のアスピリンの安定性に及ぼす影響を調べた研究結果を報告した。HP−β−CDは、アスピリンとの凍結乾燥包接錯体または物理的混合物としてpMDI内に処方された。凍結乾燥包接錯体中のアスピリンは、6ヶ月間貯蔵したときに最も著しい分解度を示したが、pMDIの単独のアスピリンで示した分解度は中程度であった。物理的混合物中に処方されたアスピリンが示す分解度は最小であった。HP−β−CDを使用して、化学的に不安定な薬剤の安定性を高めることができるが、薬剤安定性は、製剤の調製方法の影響を受ける可能性があると報告されている。
Gudmundsdottirら(Pharmazie(2001年12月)、56(12)、963−6)は、ミダゾラムが水性スルホブチルエーテル−β−シクロデキストリン緩衝液で処方された研究結果を開示している。経鼻スプレーは、健常人ボランティアで試験し、オープンクロスオーバー臨床試験(open crossover trial)で静脈内注射ミダゾラムと比較した。経鼻製剤は、吸収、血清濃度、および臨床鎮静効果の速度の点で静脈内注射形態に近づいていると報告されている。重篤な副作用は観察されなかった。
Srichanaら(Respir.Med.(2001年6月)、95(6)、513−9)は、乾燥粉末エアロゾルの新しい担体を開発する研究結果を報告している。2種類のシクロデキストリン;ガンマシクロデキストリン(γ−CD)とジメチル−ベータ−シクロデキストリン(DMCD)が、乾燥粉末製剤の担体として選択された。サルブタモールを、モデル薬剤として使用し、また乳糖を含む対照製剤を使用し、その薬剤を含有させた。ツインステージインピンジャー(twin−stage impinger)(TSI)を使用して、それらの乾燥粉末製剤の送達効率を評価した。得られた結果から、γ−CD−増強薬剤を含む製剤は、DMCDを含む製剤(沈着=50%)および対照(沈着=40%)の両方よりもかなり大きくTSIの下側ステージに送達すること(沈着=65%)が判明した(P<0.05)。DMCD錯体でインキュベートされた赤血球の溶血は、γ−CD錯体で得られる溶血よりも高かった。γ−CDおよびDMCDを含む両方の製剤の薬剤放出は、高速であり(70%超が5分以内に放出された)、ほぼすべての薬剤が30分以内に放出された。
van der Kuyら(Eur.J.Clin.Pharmacol.(1999年11月)、55(9)、677−80)は、市販の経鼻調製物を使用し、メシル酸ジヒドロエルゴタミン(DHEM)含有製剤の2つの経鼻調製物の薬物動態学的特性の結果を報告している。これらの製剤は、さらに、無作為メチル化β−シクロデキストリン(RAMEB)を含んでいた。3つの経鼻調製物について最大血漿濃度(Cmax)、Cmax到達時間(tmax)、血漿濃度−時間曲線下面積(AUC0−8h)、Frel(t=8h)、およびCmax/AUC(t=8h)に統計的に有意な違いは見られなかった。これらの結果から、経鼻調製物の薬物動態学的特性は、市販の経鼻スプレーと著しく異なることはないことがわかる。
Merkusの米国特許第5,942,251号および第5,756,483号は、シクロデキストリンおよび/または二糖類および/または多糖類および/または糖アルコールと組み合わせたこれら薬理活性物質のうちの1つを含むジヒドロエルゴタミン、アポモルヒネ、およびモルヒネの経鼻投与用の医薬組成物を対象としている。
米国特許第5,955,454号では、プロゲストゲンおよび置換度が0.5〜3.0のメチル化β−シクロデキストリンを含む経鼻投与に適した医薬調製物を開示している。
Piazzaらの米国特許第5,977,070号では、有効量のPTHまたはPTHrpの生理的活性のある短縮類似体(trancated analog)、またはそれらの塩、およびジメチル−β−シクロデキストリンからなる群から選択される吸収促進剤を含む、骨粗鬆症の治療に役立つ化合物の経鼻送達用の医薬組成物を開示している。
Backstromらの米国特許第6,436,902号では、乾燥粉末の少なくとも50%が(a)直径最大10ミクロンまでの粒子、または(b)そのような粒子の凝集体からなる吸入に適している乾燥粉末の形態の副甲状腺ホルモンの経肺投与の組成物および方法を開示している。乾燥粉末式吸入装置は、(i)副甲状腺ホルモン(PTH)、および(ii)下気道内でのPTHの吸収を増強する物質を含む乾燥粉末からなる調製物を含み、(i)および(ii)の少なくとも50%は、直径最大10ミクロンまでの一次粒子からなり、物質は、脂肪酸の塩、胆汁塩またはそれらの誘導体、リン脂質、およびシクロデキストリンまたはそれらの誘導体からなる群から選択される。
Kuoらの米国特許第6,518,239号は、肺へのエアロゾル投与用の活性物質およびジペプチドまたはトリペプチドを含む分散性エアロゾル製剤を開示している。組成物は、さらに、ポリマー賦形剤/添加剤、例えば、ポリビニルピロリドン、ヒドロキシメチルセルロース、ヒドロキシエチルセルロース、およびヒドロキシプロピルメチルセルロースなどの誘導体化セルロース、フィコール(ポリマー糖)、ヒドロキシエチルでんぷん、デキストレート(例えば、2−ヒドロキシプロピル−β−シクロデキストリンおよびスルホブチルエーテル−β−シクロデキストリンなどのシクロデキストリン)、ポリエチレングリコール、およびペクチンも含むことができることが報告されている。
Nakateら(Eur.J.Pharm.Biopharm.(2003年3月)、55(2)、147−54)は、β−シクロデキストリンと共に処方することによりラットにおける環状ペプチドFK224(低水溶解度)の肺吸収の改善を調べる研究結果を開示している。この研究の目的は、他の投与経路と比較してFK224の全身的吸収に対する経肺送達の効果を調べ、さまざまな投薬形態を使用してラットにおける経肺投与の後のFK224の生体利用率(BA)を決定することであった。水性懸濁液の投与後、生体利用率は、溶液の16.8%と比べて、2.7%に下がった。しかし、β−シクロデキストリン(β−CD)は、FK224の溶解度を改善することに関する限り有効な添加剤であることがわかった。β−CDを含む水性懸濁液の生体利用効率は、19.2%に高められた。FK224のC(max)とAUCは両方とも、β−CDの量が増えるにつれて増大することが観察された。血漿プロファイルは、持続性吸収を示した。これらは、β−CDが、FK224の肺吸収を改善することに関する限りきわめて有効な添加剤であることを示唆している。また、さまざまな水溶解度を有するβ−CDまたは誘導体は、経肺吸収を制御する有望な薬剤担体であることも示唆している。
Kobayashiら(Pharm.Res.(1996年1月)、13(1)、80−3)は、ラットにおいて吸収促進剤を含むサケカルシトニン(sCT)乾燥粉末を経肺送達することに関する研究結果を開示している。ラットにsCT乾燥粉末および液体(溶液)調製物を気管内投与した後、血漿sCTレベルおよびカルシウムレベルを測定した。乾燥粉末および液体中のsCTは、ほぼ同じ程度に吸収されたと報告されている。吸収促進剤(オレイン酸、レシチン、クエン酸、タウロコール酸、ジメチル−β−シクロデキストリン、オクチル−β−D−グルコシド)は、溶液よりも、乾燥粉末のほうがかなり効果的であった。
Adjeiら(Pharm.Res.(1992年2月)、9(2)、244−9)は、ラットおよび健常人への経鼻および吸入送達の後、酢酸ロイプロリドの生物学的利用率に関する研究結果を開示している。酢酸ロイプロリド、黄体形成ホルモン放出ホルモン(LHRH)アゴニストの全身的送達は、吸入(i.h.)および経鼻(i.n.)投与後に比較された。ラットのi.n.生物学的利用率は、α−シクロデキストリン(CD)、EDTA、および溶液体積により著しく増大した。吸収の範囲は、i.v.対照と比較して8〜46%であった。健常人男子について、噴霧による酢酸ロイプロリドi.n.、吸入エアロゾル(i.h.)、ならびに皮下(s.c.)および静脈内(i.v.)注入で研究が実施された。s.c.注入は、i.v.と比較して94%の生物学的利用率であった。i.n.生物学的利用率は平均2.4%であり、被験者間のバラツキが著しかった。吸入送達により、被験者間バラツキは少し低かった。溶液エアロゾル1mg投薬での平均Cmaxは0.97ng/mlであり、それに対してそれぞれ1および2mgのボーラス投与で与えられる懸濁液エアロゾルについては4.4および11.4ng/mlであった。懸濁液エアロゾルの平均生物学的利用率(s.c.投与に関して28%)は、溶液エアロゾル(6.6%)と比べて4倍大きかった。
CyDex(Cyclopedia(2002年)、5(1)、3)では、SBE−CDは、単独で存在する場合の吸入エアロゾル組成物においてラットに対し非毒性であることを開示している。これは、薬剤、特にコルチコステロイド、およびSBE−CDを含む噴霧可能な組成物を開示していない。種々のネブライザーでのPULMICORT RESPULES、ならびにブデソニドおよびSAE−CDの吸入可能水溶液の噴霧を比較する研究が開示されている(Zimmererら、Respiratory Drug Delivery IX、(2004年)、461〜464頁)。
また懸濁液を投与するのか、溶液を投与するのかを決定する際に、使用するネブライザーの種類も考慮しなければならない。2つの最も一般的な種類のネブライザーは、超音波ネブライザーおよび空気駆動ジェット式ネブライザーである。この2つの型間には著しい違いがある。例えば、ジェット式ネブライザーは、リザーバ内の液体を加熱するのではなく冷却するが、超音波ネブライザーは、液体を加熱する。リザーバ内の溶液の加熱は溶液の粘度を下げ、液滴の形成を高めるが、過剰な加熱は、薬剤分解をもたらしかねない。超音波ネブライザーは、ジェット式ネブライザーに比べて、静かであり、送達も高速であるが、超音波ネブライザーは、高価であり、噴霧療法に現在利用可能なステロイドの投与には勧められない。しかし、最も重要なことは、超音波ネブライザーは、一般に、ジェット式ネブライザーよりも投与速度が著しく高速であることである。
喘息の患者は、吸入される短時間作用型または長時間作用型のβ2−アゴニスト、吸入抗コリン剤、および単独の吸入コルチコステロイドを使用して、順に、または組み合わせて、治療されることが多い。吸入コルチコステロイドおよび長時間作用型β2−アゴニストの組み合わせが知られており、例えば、ブデソニドにホルモテロールを加えたものまたはフルチカゾンにサルメテロールを加えたものが、乾燥粉末式吸入器で利用可能である。しかし、噴霧用の溶液として利用可能なそのような組み合わせの実例はない。複数の薬物を組み合わせて1つの溶液にまとめると、薬物を別々に投与するのに要する時間が短縮される。
吸入コルチコステロイドにとって、肺が標的臓器であることから、高い肺アベイラビリティは高い経口バイオアベイラビリティよりも重要である。高い肺アベイラビリティを有する製品は、肺で陽性効果を発揮するより高い能力を有する。理想的なICSは、最小の経口バイオアベイラビリティを有し、全身性副作用の可能性を低減するものといえる。
喘息の治療には非常に有効であるが、吸入コルチコステロイドは、口腔カンジダ症、嗄声(発声困難)、及び咽頭炎などの多くの副作用を有する可能性がある。したがって、吸入コルチコステロイドは、コルチコステロイドの経口および/または咽頭沈着を最小にし、代わりに肺送達を最大にする方法により、最もよく送達される。
いくつかのコルチコステロイドは、コルチコステロイドの21位に水酸基を有する。それらの化合物としては、ブデソニド、フルニソリド、トリアムシノロンアセトニド、モノプロピオン酸ベクロメタゾン、およびシクレソニド(デスイソブチリルシクレソニド)の活性型が含まれる。シクレソニドが不活性化合物として吸入され、肺のエステラーゼによってその活性型のデスイソブチリルシクレソニド(des−CIC)に変換されることは公知である。ブデソニドは接合して高親油性の細胞内脂肪酸エステルを形成する。ブデソニドは5つの脂肪酸:オレイン酸、パルミチン酸、リノール酸、パルミトオレイン酸、及びアラキドン酸と接合体を形成する。
すなわち、当技術分野では、場合によっては、溶液の噴霧は、懸濁液の噴霧よりも好ましい場合があり、また場合によっては、超音波ネブライザー、振動メッシュ、エアロゾル化の電子または他のメカニズムによるエアロゾルは、比較対象の噴霧液体製剤に応じて空気駆動ジェット式ネブライザーよりも好ましい場合があることが示唆される。当技術分野では、コルチコステロイドおよびシクロデキストリンを含む吸入可能溶液製剤を開示しているとしても、当技術分野の結果は、予測不可能である。すなわち、1つのシクロデキストリンと1つの薬剤との組み合わせは、他のシクロデキストリンが適している可能性のあることを示唆しないということである。当技術分野は、1つのシクロデキストリン−コルチコステロイド吸入可能製剤が、他のシクロデキストリン−コルチコステロイド吸入可能製剤に勝る利点を有することも示唆しない。
当技術分野では、保存剤の添加を要しない、また他の安定化された水溶液ブデソニド含有吸入可能製剤よりも著しい利点をもたらす安定化された水溶液ブデソニド含有吸入可能製剤も依然として必要である。また、懸濁液を溶液に転換することによりブデソニド含有懸濁液製剤の噴霧投与を改善する方法も依然として必要である。
また、噴霧用の不水溶性薬剤を可溶化することができる改善されたシステムを開発し、これを実現するために必要な共溶媒のレベルを最小にする必要もある。理想的なシステムであれば、無毒の成分からなり、室温で長期間貯蔵しても安定であろう。噴霧化された場合、それは10ミクロン未満または5ミクロン未満または3ミクロン未満の吸入可能な液滴、および約1ミクロン未満のサイズ範囲の極微細エアロゾルの相当部分を生成するであろう。
懸濁液ベースの単位用量製剤の噴霧投与を改善する方法も引き続き必要である。このような方法であれば、投与時間全体が短縮され、投与される薬剤の総量が増加させ、ネブライザーのリザーバ内に残る薬剤の量が減らされ、コルチコステロイドの口腔咽頭沈着と比較して肺沈着の部分が増え、および/または懸濁液ベースの単位用量製剤の、改善がない場合の投与と比べて、コルチコステロイドの肺への深い浸透が増強されるであろう。
本発明は、公知の製剤に存在する不利を克服しようとするものである。そのようなものとして、誘導体化シクロデキストリンベースの、例えば、スルホアルキルエーテルシクロデキストリン(SAE−CD)ベースの、吸入可能製剤が提供される。本発明の製剤は、コルチコステロイドを主要な活性物質として含む。本発明の製剤は、製剤中の活性物質または他の成分の高められた溶解性ならびに/または高められた化学的、熱化学的、加水分解的および/もしくは光化学的安定性をもたらすことができる。さらに、本発明の製剤は、ブデゾニドなどのコルチコステロイドを含む他の吸入可能溶液または懸濁液製剤にまさる、例えば、薬剤送達が増強されること、薬剤投与が高速化されること、治療時間が短縮されること、毒性が低減されること、製造が容易になること、無菌性が保証されること、安定性が改善されること、生体吸収性が強化されること、粒径の制御が不要であること、アウトプット率が高められること、全アウトプット量が増えること、固形粒子成長の懸念がないこと、薬物動態学的プロファイルが強化されること、コルチコステロイド関連副作用が低減されること、肺沈着が増強されること、口腔咽頭沈着が減少されること、噴霧性能が改善されること、および/または懸濁液形成の確認が不要であること、といった他の利点を有することができる。
本発明は、コルチコステロイド療法に対して治療反応性の呼吸器疾患または障害を治療する製剤、システム及び方法を提供する。本発明のシステムは、ネブライザー、及び本発明の液体製剤を含む。本発明の液体製剤は、コルチコステロイドの1回用量、水性液体担体および溶解促進剤を含む。
本発明は、被験者に臨床的または治療的利点を与えることができるコルチコステロイドの治療的有効量を用いて治療することができる被験者の疾患又は障害を意味する、コルチコステロイド反応性疾患または障害の被験者において治療、予防および改善する方法を提供する。本方法は以下を含む:すなわち、コルチコステロイド、水性液体担体、及び溶解促進剤を含む水性吸入製剤を提供すること;約少なくとも25μg、40μg、少なくとも45μg、少なくとも48μg、45〜1000μg、約1μg〜20mg、もしくは1μg〜10mg、0.01mg〜10mg、0.025mg〜10mg、0.05mg〜5mg、0.1mg〜5mg、0.125mg〜5mg、0.25mg〜5mg、0.5mg〜5mg、0.05mg〜2mg、0.1mg〜2mg、0.125mg〜2mg、0.25mg〜2mg、0.5mg〜2mg、1μg、10μg、25μg、50μg、100μg、125μg、200μg、250μg、25〜66μg、48〜81μg、73〜125μg、40μg、64μg、95μg、35〜95μg、25〜125μg、60〜170μg、110μg、170μg、45〜220μg、45〜85μg、48〜82μg、85〜160μg、140〜220μg、120〜325μg、205μg、320μg、325μg、90〜400μg、95〜170μg、165〜275μg、又は275〜400μgのコルチコステロイドの1回用量をそれを必要とする被験者に噴霧を介して送達または投与することを含む。幾つかの実施態様では、コルチコステロイドはブデソニドである。
幾つかの実施態様において:1)吸入製剤は、約10μl〜100ml、50μl〜50ml、50μl〜10ml、0.1〜10ml、0.1ml〜10ml未満、0.1ml〜7.5ml、0.1ml〜5ml、0.1ml〜3ml、0.1ml〜2ml、0.1ml〜1ml、0.05ml〜7.5ml、0.05ml〜5ml、0.05ml〜3ml、0.05ml〜2ml、または0.05ml〜1mlの体積を有し;2)送達または投与の工程は、30分未満、20分未満、10分未満、7分未満、5分未満、3分未満、もしくは2分未満の期間にわたって行われ、またはその時間が約0.05〜10分、約0.1〜5分、約0.1〜3分、約0.1〜2分、約0.1〜1.5分、約0.5分〜約1.5分、もしくは約1分であり、またはその時間は被験者が1回の呼吸に要するほどの時間(約1〜3または1〜5秒)であり;3)コルチコステロイドの用量の20%〜85%、または30%〜80%、または少なくとも30%、少なくとも40%、少なくとも56%、少なくとも59%、少なくとも62%が被験者の肺に送達され;4)製剤、システムまたは方法は、コルチコステロイドのほぼ同量を含み、そして実質的に同じ条件下に送達される懸濁液製剤の投与に比べて、正規化用量に対してCmaxで1.5〜8倍の、1.5〜6倍の、1.5〜4倍の、1.5〜2倍の、1.64〜3.55倍の、Cmaxで1.48〜6.25倍の、AUCinfで1.59〜3.55または1.19〜6.11倍の、AUClastで1.69〜3.67又は1.21〜7.66倍の、薬物動態学的プロファイルの強化を提供し;5)コルチコステロイドの用量の15%〜85%以下、15%〜70%、20%〜70%以下、50%以下、40%以下、または60%以下が患者の肺の外に送達されるだけである。
本発明者は、思いがけなく、SAE−CDが吸入投与後全身に吸収されることを発見した。それはまた肺からも排泄される。SAE−CDは、また吸入可能水性液体製剤中のコルチコステロイドと錯体を形成する。コルチコステロイドとSAE−CDとの共投与(coadministration)は、SAE−CDを除いた対照に比べてアウトプット率及び全薬物送達の増加をもたらす可能性がある。更に、噴霧により投与される本発明の吸入可能溶液は、実質的に同じ条件下に投与された場合、実質的に同じ容積の液体中実質的に同じ量のコルチコステロイドを含む懸濁液の対照/参照試料と比べて、本明細書に示される他の利点をもたらす。
懸濁液は振動メッシュネブライザーを詰まらせ、また超音波ネブライザーではよく機能しない可能性があるため、吸入可能溶液は多くのタイプのネブライザーで使用できる。ネブライザーは残存コルチコステロイドをより容易にクリーニングでき、汚染が少ないと考えられる。溶液中の薬剤はネブライザーを離れて大小の液滴となって等しく分布すると考えられることから、微粒子画分はより多くのコルチコステロイドを含み、肺末梢部およびより小さい気道に到達させ得るより大きな吸入可能用量をもたらすことになる。これは、口腔咽頭腔に沈着するまた嚥下される全薬剤を少なくでき、その結果好ましくない副作用の可能性を減少させる一方で、バイオアベイラビリティを増加させ、所望の効果を最大にし得る。吸入可能溶液はまた、単位量の薬剤量を減少させ、及び/又は肺における所望の薬剤量を達成する噴霧時間を減少させることが可能である。吸入溶液はより容易に製造され単位投与剤に充填され、そして製品性能は中にあるコルチコステロイドの粒径の非常に厳格な制御及び充填時の均一懸濁液の維持に左右されない。とはいえ、小粒径は、一般的に製造の際、より速い溶解を促進する。上記のように厳格な制御を維持する必要はない。懸濁コルチコステロイド中のコルチコステロイド粒径を変化させるリスクなしに、最終的に滅菌することができる。吸入溶液はオストワルドの熟成または凝集を介する粒子成長に因る変化にさらされることはなく、それゆえ呼吸可能画分の薬剤の量は経時的に変化することはない。大きな投与量変動を生じないように、発泡を減少させる注意深い下準備の手順により、投与に先立って再懸濁する必要はない。ネブライザー内に収容される体積中の所望の薬剤量を達成するのにより正確に希釈することができる。あるいは、吸入溶液の濃度は、特に空気ジェットネブライザー中のように懸濁液の濃度ほどにネブライザー中で急速に変化しないことから、投与量調整は噴霧時間を調整することでより容易にコントロールできる。
SAE−CD含有製剤は、市販製品としての活性物質の十分な溶解度および安定性をもって調製することができる。必要ならば、SAE−CD含有製剤は、孔径が0.45μm以下のフィルターを通して細菌濾過でき、またさまざまな貯蔵条件下に安定で保存可能な澄明水溶液として製造することができる。本発明は、このように、本発明の溶液を含む濾過滅菌液体製剤およびフィルターを通した滅菌濾過により本発明の溶液を滅菌する方法を提供する。滅菌濾過は、可溶化コルチコステロイドの実質的質量損失なしに、つまり質量損失5%未満で行うことができる。
吸入投与に好適ないずれのコルチコステロイドも、本発明により使用することができる。典型的な好適コルチコステロイドが本明細書中に例示されている。本発明の幾つかの実施態様は、ブデソニドに近いかまたはそれを超える親油性を有するコルチコステロイドを含む。本発明の幾つかの実施態様は、フルニソリド以下の親油性を有するコルチコステロイドを除外する、すなわち、これらの実施態様はヒドロコルチゾン、プレドニゾロン、プレドニゾン、デキサメタゾン、ベタメタゾン、メチルプレドニゾロン、トリアムシノロン、フルオコルトロンを除外する。
本発明の一側面では、ブデソニドなどの有効量のコルチコステロイドおよびSAE−CDを含み、SAE−CDは貯蔵時にコルチコステロイドを溶解し安定化するのに十分な量で存在する、液体製剤を提供する。
本発明の他の側面では、被験者へのコルチコステロイドの噴霧投与を改善する方法を提供し、この方法は、
水および水の中に懸濁されたコルチコステロイドを含む水性懸濁液製剤を単位用量で提供する工程と、
懸濁液と、コルチコステロイドを可溶化し溶液を形成するのに十分な量のSAE−CDを、そうするのに十分な時間、組み合わせる工程と、
その溶液を被験者に投与する工程とを含み、ここで治療用量のコルチコステロイドを溶液で投与するのに要する時間は、類似の、さもなければ匹敵する、噴霧条件の下で、懸濁液で同じ治療用量のコルチコステロイドを投与するのに要する時間よりも短い。
水および水の中に懸濁されたコルチコステロイドを含む水性懸濁液製剤を単位用量で提供する工程と、
懸濁液と、コルチコステロイドを可溶化し溶液を形成するのに十分な量のSAE−CDを、そうするのに十分な時間、組み合わせる工程と、
その溶液を被験者に投与する工程とを含み、ここで治療用量のコルチコステロイドを溶液で投与するのに要する時間は、類似の、さもなければ匹敵する、噴霧条件の下で、懸濁液で同じ治療用量のコルチコステロイドを投与するのに要する時間よりも短い。
ネブライザーで投与する場合、噴霧用の懸濁液は、噴霧条件の第1のセットの下では、第1のコルチコステロイドアウトプット率をもたらす。しかし、SAE−CDを懸濁液に添加し、そこで混合した場合、十分な量のコルチコステロイドが溶解され、実質的に同じ条件の下で投与された場合にSAE−CDを除外した製剤に比べてコルチコステロイドのアウトプット率が大きい噴霧用の液体製剤が形成される。一実施形態では、製剤の薬剤アウトプット率は、噴霧化組成物の全体積、すなわちネブライザーにより放出される溶液の全体積が増えなかったとしても、懸濁液の場合よりも増大する。別の実施形態では、SAE−CDは、コルチコステロイドの少なくとも50%、少なくとも75%、少なくとも90%、少なくとも95%、または実質的にすべてを可溶化するのに十分な量で存在する。本発明の幾つかの実施態様は、少なくとも50質量%、少なくとも75質量%、少なくとも90質量%、少なくとも95質量%、少なくとも98質量%、またはすべてのコルチコステロイドが吸入可能液体製剤に溶解しているものを含む。
幾つかの実施態様では、SAE−CDは、懸濁液製剤中の未可溶化コルチコステロイドの量を減らし、懸濁液製剤の噴霧投与を改善するのに十分な量で存在する。幾つかの実施態様では、SAE−CDは、SAE−CDが添加された懸濁液製剤が溶液、実質的に澄明溶液(5%未満の沈殿物または固体を含む)、または澄明溶液に転換されるように十分なコルチコステロイドを可溶化するのに十分な量で存在する。懸濁液製剤の他の成分は、SAE−CDを含む溶液製剤中に完全には溶解しないか、またはそこから分離する場合があるということが可能である。
幾つかの実施態様によれば、コルチコステロイド/SAE−CD含有溶液を充填されたネブライザーは、他の類似の条件の下で操作されるコルチコステロイド/HP−β−CD−含有溶液を充填された同じネブライザーの場合よりも小さな液滴を生成する。より小さな液滴を生成する結果、SAE−CDを含むシステムは、HP−β−CDを含む他の類似のシステムよりも改善されるが、それは、SAE−CDベースのシステムが、より大きな割合の吸入可能な液滴を生成し、より深い肺浸透を可能にするからである。
本発明の幾つかの側面は、噴霧可能単位用量液体製剤におけるSAE−CD
の使用を提供する。一実施態様では、本発明は、噴霧可能なコルチコステロイド含有懸濁液ベースの単位用量製剤を、噴霧可能コルチコステロイド含有液体単位用量製剤に転換するための、SAE−CDの使用を提供する。
の使用を提供する。一実施態様では、本発明は、噴霧可能なコルチコステロイド含有懸濁液ベースの単位用量製剤を、噴霧可能コルチコステロイド含有液体単位用量製剤に転換するための、SAE−CDの使用を提供する。
本発明の幾つかの実施態様は、1)コルチコステロイド対SAE−CDのモル比が、0.5〜0.0001(1:2〜1:10,000)、1:1〜1:100、1:1〜1:10,000、または0.1(1:10)〜0.03(1:33.33)であるものを含む。製剤又はシステム中のSAE−CD対コルチコステロイドのモル比は、一般的に10:1より大きく、約11:1より大きく、13:1より大きく、または14:1より大きい。製剤中に使用されるコルチコステロイドに応じて、コルチコステロイド対SAE−CDのモル比は、呼吸器疾患または障害の治療のための吸入を介する投与に好適な溶液を得るために変動し得る。幾つかの実施態様では、噴霧組成物は、SAE−CDを少なくとも4.8±0.5%(質量/体積)含み、所定期間用の自己保存製剤を提供する。幾つかの実施態様では、噴霧組成物は、約21.5±2%(質量/質量)以下のSAE−CDを含む。幾つかの実施態様では、SAE−CDは、澄明溶液を与えるのに十分な量で存在する。例えば、噴霧組成物は、肉眼で見て澄明に見ている。
幾つかの好適なSAE−CDは、例えば、スルホブチルエーテル4−β−CDもしくはスルホブチルエーテル7−β−CD、スルホブチルエーテル6−γ−CD、スルホブチルエーテル4−γ−CD、スルホブチルエーテル3から8−γ−CD、もしくはスルホブチルエーテル5−γ−CD、もしくは式1の化合物、またはそれらの混合物を含む。
本発明の組成物は、さらに、従来の保存剤、酸化防止剤、緩衝剤、酸性化剤、可溶化剤、錯化促進剤、食塩水、電解質、他の治療薬、アルカリ性化剤、張度調整剤、表面張力調整剤、粘度調整剤、界面活性剤、密度調整剤、揮発度調整剤、またはそれらの組み合わせを含むことができる。所望ならば、組成物は、更に水以外の液体担体を含む。従来の保存剤が組成物に含まれる場合には、ブデソニドなどのコルチコステロイドは、従来の保存剤の場合よりもSAE−CDと大きい結合性を有する可能性がある。組成物は、製剤中に含まれる酸素の実質的にすべてを除去するために貯蔵前に不活性ガスでパージし得る。一般的に、本発明の製剤または組成物は、使用目的によるが少なくとも6か月の貯蔵寿命を有する。
製剤は、5℃以上、25℃以上、35℃以上、45℃以上、または50℃以上の温度で調製し得る。液体製剤を製造する方法の特定の実施態様は、1)この方法が、さらに、細孔の大きさが0.1ミクロン以上である濾過媒体を通じて製剤を滅菌濾過する工程を含む、2)液体製剤が、放射線滅菌または高圧蒸気滅菌される、3)噴霧溶液が、その溶液に溶解している、及び/又はその溶液と接触している表面の酸素の実質的な部分が除去されるように、貯蔵前に窒素またはアルゴンまたは他の薬剤として許容される不活性ガスでパージされる、実施態様を含む。
本発明は、SAE−CDを、SAE−CDを除外した対照試料と比べてコルチコステロイドの分解率を低減するのに十分な量で水性コルチコステロイド含有懸濁液または溶液製剤に加える工程を含む、水性コルチコステロイド含有製剤中のコルチコステロイドを安定化する方法を提供する。
本発明は、さらに、吸入可能水性コルチコステロイド含有懸濁液単位用量製剤の噴霧投与を改善する方法も提供し、この方法は、SAE−CDを、コルチコステロイドを可溶化し吸入可能な水性コルチコステロイド含有溶液単位用量製剤を形成するのに十分な量で水性コルチコステロイド懸濁液単位用量製剤に加える工程を含み、この改善は、アウトプット率及び/又は噴霧化コルチコステロイドの程度を高めることを含む。
本発明は、ネブライザーを使用するコルチコステロイド含有組成物の吸入により治療有効量のコルチコステロイドを被験者に供給するのに要する時間を短縮する方法を提供し、この方法は、SAE−CDを、コルチコステロイドを可溶化し、吸入可能な水性コルチコステロイド含有水溶液を形成するのに十分な量で組成物内に含める工程と、ネブライザーを使った吸入により溶液を被験者に投与する工程とを含み、溶液と共に治療有効量のコルチコステロイドを被験者に供給するのに要する時間は、懸濁液および溶液がその他の点では類似の噴霧条件の下で投与される場合に、同じ量、または濃度のコルチコステロイドを含むコルチコステロイド含有懸濁液と共に治療有効量のコルチコステロイドを被験者に供給するのに要する時間に比べて短縮される。幾つかの実施態様において、コルチコステロイドの1回用量を投与または送達するのに必要な時間は、30分未満、20分未満、10分未満、7分未満、5分未満、3分未満、もしくは2分未満であり、またはその時間が約0.05〜10分、約0.1〜5分、約0.1〜3分、約0.1〜2分、約0.1〜1.5分、約0.5分〜約1.5分、もしくは約1分であり、又はその時間は患者が1回の呼吸に要するほどの時間(約1〜3、または1〜5秒)である。その時間は、ネブライザーのリザーバ中のコルチコステロイド量、コルチコステロイド濃度、及び吸入可能組成物の体積によって変動することになり、またネブライザーの形式、噴霧効率、およびリザーバの容積にも依存することになる。所定のネブライザーにおいて、吸入可能組成物の体積が小さいほど、対応する用量のコルチコステロイドはより速く噴霧される。吸入可能組成物中のコルチコステロイドの濃度が高いほど、1回用量のコルチコステロイドが速やかに投与または送達され得る。
アウトプット率(用量のコルチコステロイドがこの比率で投与または送達される)は、それを投与するために使用されるネブライザーの性能パラメータによって変動することになる。所定のネブライザーのアウトプット率が高いほど、本明細書に定義される吸入可能組成物、またはコルチコステロイドの用量を送達又は投与するのに必要な時間はより短くなる。
本発明は、さらに、水溶性γ−CD誘導体、コルチコステロイド(エステル化または未エステル化)、および水性液体媒体を含む吸入可能組成物をも提供する。本発明の他の実施態様は、さらに、水溶性β−CD誘導体、コルチコステロイド(未エステル化)、および水性液体媒体を含む吸入可能組成物をも提供する。
さらに、本発明は、コルチコステロイド含有吸入可能製剤の吸入投与を行うための改善されたシステムを実現し、この改善は、SAE−CDがSAE−CDを除外した、ただしその他の点ではほぼ同じ条件の下で投与される、対照吸入可能製剤の投与と比較してコルチコステロイド吸入速度を高めるのに十分な量で存在するように吸入可能製剤中にSAE−CDを入れることを含む。
本発明は、コルチコステロイドの吸入投与を行うシステムを提供するために使用することができ、このシステムは、ネブライザーなどの吸入装置を含み、医薬組成物は、治療有効量のコルチコステロイド、液体担体、および水性環境に与えられたときにコルチコステロイドを可溶化できる十分な量で存在するSAE−CDを含み、ここでコルチコステロイド対SAE−CDのモル比は約0.072(1:13.89または約1:14)から0.0001(1:10,000)または0.063(1:15.873又は約1:16)から0.003(1:333.33または約1:333)の範囲内である。SAE−CD対コルチコステロイドのモル比は、>10:1から約1000:1まで、>10:1から約100:1まで、>10:1から約50:1まで、>10:1から約30:1まで、>10:1から約500:1に及ぶ。操作中、システムは、MMADが約1〜8μまたは3〜8μの範囲内にある液滴を形成する。コルチコステロイドは、少なくとも約20〜50μg/minの比率で送達され、この範囲は、ネブライザーのリザーバ内の噴霧溶液中のコルチコステロイド濃度に応じて増減できる。
SAE−CDコルチコステロイド療法を吸入可能噴霧溶液と共に使用した結果として、吸入可能噴霧懸濁液クロロフルオロカーボン(CFC)、またはヒドロフルオロアルカン(HFA)加圧式定量吸入器(pMDI)に匹敵するコルチコステロイド療法と比較して、薬剤送達の増強、特に、細かなエアロゾル発生により容易になる周囲または小さな気道への送達の増強、夜間無症候喘息の治療および急性喘息発作からの回復の潜在的改善、薬剤投与速度の増大、薬物動態学的プロファイルの強化、治療時間の短縮、製剤安定性の改善および/または患者の服薬遵守の改善などの利点が期待できる。
本発明は、SAE−CD、水性担体、およびコルチコステロイドを含むキットで使用することができ、このキットは、噴霧溶液の調製に適合されている。キットの実施態様について以下で詳述する。本発明は、他の溶液投薬形態による懸濁液との不適合性を克服するために組み合わせ製品を提供する潜在性を有する。
本発明の液体製剤及び組成物は、ほぼ同量のコルチコステロイドを含み、そしてSAE−CDを除外した懸濁液ベースの水性製剤に比べて、コルチコステロイドのバイオアベイラビリティ/生体吸収性の増強をもたらす。液体製剤または組成物は、被験者に送達されるブデソニド量に対して、懸濁液ベース製剤よりも高率のAUCi(またはAUCt)をもたらす。このように、液体製剤および/または組成物は、懸濁液ベース製剤に勝る臨床的有益性または治療的有益性の向上をもたらす。
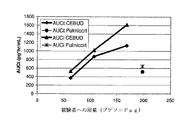
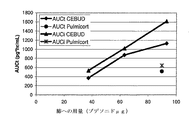
本発明は、さらに、それに溶解した単位用量のコルチコステロイドを含む水性液体製剤を被験者に吸入により投与する工程を含む、被験者にコルチコステロイドを投与する方法をも提供し、ここで、組成物は、投与したコルチコステロイドμg当り少なくとも6(pg*h/ml)の、コルチコステロイドの用量で正規化した平均AUCtを与える。幾つかの実施態様では、単位用量は、コルチコステロイドの少なくとも45μg、少なくとも48μg、45〜1000μg、約1μg〜20mg、約1μg〜10mg、0.01mg〜10mg、0.025mg〜10mg、0.05mg〜5mg、0.1mg〜5mg、0.125mg〜5mg、0.25mg〜5mg、0.5mg〜5mg、0.05mg〜2mg、0.1mg〜2mg、0.125mg〜2mg、0.25mg〜2mg、0.5mg〜2mg、1μg、10μg、25μg、50μg、100μg、125μg、200μg、250μg、25〜66μg、48〜81μg、73〜125μg、40μg、64μg、95μg、35〜95μg、25〜125μg、60〜170μg、110μg、170μg、45〜220μg、45〜85μg、48〜82μg、85〜160μg、140〜220μg、120〜325μg、205μg、320μg、325μg、90〜400μg、95〜170μg、165〜275μg、または275〜400μgを含む。幾つかの実施態様では、正規化AUCtは被験者への用量に基づき、正規化AUCtは被験者の肺への用量に基づき、または正規化AUCtは放出用量若しくは名目用量に基づく。本明細書で用いるAUCt(またはAUClast、AUC0−t)は、定量可能値がある最後の時点tまでの血漿レベル対時間曲線下の面積である。
本発明は、さらに、それに溶解したコルチコステロイドの単位用量を含む水性液体製剤を被験者に吸入を介して投与する工程を含み、被験者にコルチコステロイドを投与する方法も提供し、ここで組成物は、投与したコルチコステロイドμg当り少なくとも8(pg*h/ml)のコルチコステロイドの用量で正規化した平均AUCiを与える。幾つかの実施態様では、単位用量は、コルチコステロイドの少なくとも45μg、少なくとも48μg、45〜1000μg、約1μg〜20mg、約1μg〜10mg、0.01mg〜10mg、0.025mg〜10mg、0.05mg〜5mg、0.1mg〜5mg、0.125mg〜5mg、0.25mg〜5mg、0.5mg〜5mg、0.05mg〜2mg、0.1mg〜2mg、0.125mg〜2mg、0.25mg〜2mg、又は0.5mg〜2mgを含む。幾つかの実施態様では、正規化したAUCiは被験者への用量に基づき、正規化したAUCiは被験者の肺への用量に基づき、又は正規化したAUCiは放出用量若しくは名目用量に基づく。本明細書で用いるAUCi(AUCinf、AUC0−∞)は、無限大まで外挿したAUCである。
本発明の水溶液製剤を吸入投与する場合、この製剤は、それに懸濁した実質的に同量のコルチコステロイドを含む水性液体懸濁製剤の吸入投与に比べて、投与したコルチコステロイドの1μg当たりのコルチコステロイドの用量で正規化して、少なくとも2倍のAUCtまたはAUCiの増加をもたらすことができる。幾つかの実施態様では、製剤は、投与したコルチコステロイドのμg当たりのコルチコステロイドの用量で正規化して、少なくとも1.6〜5倍(個々の被験者に基づいて測定した範囲、または個々の被験者データから測定して±1の標準偏差を有する3の平均)または2〜4倍(患者集団を横断した幾何平均を使用して測定して)のAUCtまたはAUCiの増加をもたらす。「投与したコルチコステロイド」の量の基準は、「被験者への用量」」または「肺への用量」または「放出用量」または「名目用量」または「名目利用用量」または「充填用量」であってよい。
水性液体製剤は、液体製剤の肺への投与に適したいずれのタイプの装置によって投与することができる。例えば、製剤は、空気駆動ジェット式、超音波、毛細管、電磁、脈動膜、脈動板(ディスク)、拍動メッシュネブライザー、振動発生器および水チャンバーを含むネブライザー、ならびにノズルアレイを含むネブライザーで投与することができる。
幾つかの実施態様において、本発明は、本明細書に開示のネブライザーおよび水性液体製剤/組成物を含むシステムを提供する。コルチコステロイドの1回用量を含む本発明の液体製剤を装填する場合、ネブライザーは、特にネブライザーにおいて液体製剤の性能を懸濁液ベースの製剤、例えばPULMICORT RESPULESの性能と比較すると、ネブライザーのリザーバ内の製剤中のコルチコステロイドの濃度増加率(RIC)の低下を可能にする。幾つかの実施態様では、RICの減少パーセントは、10%〜60%、15%〜60%、20%〜60%、30%〜60%、または40%〜60%の範囲である。幾つかの実施態様で、本システムは、操作/噴霧の分当たり、0〜40、1〜40、5〜30、または10〜30mcgコルチコステロイド/溶液体積のmLのRICを与えることができる。
本発明のシステムおよび製剤/組成によってもたらされる薬物動態学的の向上は、Cmax、AUC及びTmaxパラメータの比較によって測定し得る。幾つかの実施態様では、本発明の製剤及びシステムは、用量非正規化基準で90〜900、200〜600、200〜550、200〜250、400〜450、500〜600、225、437、または545のCmax(コルチコステロイドのpg/ml)を与えることができる。本発明の製剤及びシステムは、以下の用量正規化Cmax(pg/ml/μg):1)名目利用用量正規化基準で0.3〜2、0.35〜2、0.6〜1.5、0.5〜1.2、0.8〜1、0.8〜0.9、0.7〜0.8、0.4、1.9、0.6、1.5、0.5、1.2、0.35、2、0.7、0.8、または0.9;2)肺への用量正規化基準で3.4〜9.2、3.5〜8.5、5.5〜9.2、4.5〜7.5、5.8〜7、3.4、3.5、4.5、5.5、9.2、8.5、7.5、5.8、5.9、6、または7;3)被験者への用量正規化基準で1.7〜7.5、3.2〜4.1、1.9〜6、3.2〜7.5、1.7〜5.2、3.6、4.1、3.2、1.9、6、3.2、7.4、7.5、1.7、5.2または5.3;4)放出用量正規化基準で0.9〜3.3、1.7〜2.2、0.9〜3、1〜3、1.7〜3.3、1〜2.7、1.9、2.1、2.2、1.7、0.9、1、2、3、2.9、3.2、3.3、または2.7、を与えることができる。
幾つかの実施態様では、溶液及び懸濁液中のコルチコステロイドの充填された用量がほぼ同量の場合、コルチコステロイドの非正規化用量基準で、コルチコステロイド溶液によって与えられたCmaxは、懸濁液ベースの製剤によって与えられたCmaxよりも1.6〜2、1.5〜3、1.5〜2.5、1.5〜2、1.5、1.6、2、2.5、または3倍高い。コルチコステロイドの名目利用用量正規化基準で、コルチコステロイド溶液によって与えられたCmaxは、懸濁液ベースの製剤によって与えられたCmaxよりも、1.8〜6.2、1.5〜6.5、2〜6.5、1.5〜5.5、2〜4、1.5〜4、1.5〜3、2.7、3.3、3.4、1.5、6.5、2、5.5、4、又は3倍高い。コルチコステロイドの肺への用量正規化基準で、コルチコステロイド製剤によって与えられたCmaxは、懸濁液ベースの製剤によって与えられたCmaxよりも、1.4〜4.3、1.4〜4.5、1.5〜4.5、1.5〜3.5、1.5〜3、1.4〜3、1.5〜2.5、1.5〜2、2、2.3、1.4、4.5、3.5、3、1.5または2.5倍高い。コルチコステロイドの被験者への用量正規化基準で、コルチコステロイド溶液によって与えられたCmaxは、懸濁液ベースの製剤によって与えられたCmaxよりも、2〜3.5、2〜5、1.7〜3.8、1.7〜5、2.7、3、2.4、2、3.5、5、1.7、または3.8倍高い。コルチコステロイドの放出用量正規化基準で、コルチコステロイド製剤によって与えられたCmaxは、懸濁液ベースの製剤によって与えられたCmaxよりも、1.9〜6.3、1.75〜6.5、2.2〜4.2、2.2〜6.3、1.9〜4.2、3.2、3.5、3.6、2.8、1.75、6.5、2.2、4.2、または6.3倍高い。
幾つかの実施態様において、コルチコステロイド溶液によって与えられたCmaxは、溶液中のコルチコステロイドの用量が懸濁液中の用量より約2倍低い場合、懸濁液ベースの製剤によって与えられたCmaxよりも少なくとも1.5、1.6、2、2.6、および3倍高い。
幾つかの実施態様において、本発明の製剤及びシステムは、用量非正規化基準で、500〜1700、530〜1650、250〜2500、280〜1300、780〜1300、980〜2450、275、775、980、2400、2500、1300、1290、530、1650、250、280または780のAUCinf(pg*h/ml)を与えることができる。本発明の製剤及びシステムは、1)名目利用用量正規化基準で、1〜5.5、2〜2.2、1〜5.3、1.1〜5.2、1.5〜2.6、1.3〜3.3、2、2.1、2.2、1、5.5、5.3、5.2、1.5、2.6、1.3、または3.3の;2)肺への用量正規化基準で、10〜25、14〜18、10.2〜20、13.6〜18.8、11.2〜24.7、10.2、20、13.6、14、19、18.8、11、11.2、25、24.7、14.2、16.2、17.3の;3)被験者への用量正規化基準で、4〜16、4.2〜16.1、8〜12.2、5.4〜16、5.4〜17、8.5〜9.6、8.5、9.5,9.6、4.2、16.1、8、12.2、12、5.4、16、17、又は16.5の;4)放出用量正規化基準で、2.5〜9、2.6〜8.5、4.5〜5.1、2.5〜8、2.6〜7.9、4.2〜6.7、3.1〜8.5、3.2〜8.5、4.5、4.6、5、5.1、2.5、2.6、4.2、3.1、9、8.5、5.1、8、7.9、または6.7の用量正規化AUCinf(pg/ml/μg)を与えることができる。
幾つかの実施態様において、溶液及び懸濁液中のコルチコステロイドの用量がほぼ同量の場合、コルチコステロイドの非正規化用量基準で、コルチコステロイド溶液によって与えられたAUCinfは、懸濁液ベースの製剤によって与えられたAUCinfよりも1.6〜2.5、1.6〜3.1、1.5〜3.5、1.5〜3.3、2.5〜3.3、3.1、1.5、3.3、1.6、または2.5倍高い。コルチコステロイドの名目利用用量正規化基準で、コルチコステロイド溶液によって与えられたAUCinfは、懸濁液ベースの製剤によって与えられたAUCinfよりも、1.75〜6.5、1.75〜6.1、2〜6.5、2〜6.1、2〜4.5、2〜4.4、3.3、3.2、3.5、3.4、1.75、6.5、6.1、2、4.5、または4.4倍高い。コルチコステロイドの肺への用量正規化基準で、コルチコステロイド溶液によって与えられたAUCinfは、懸濁液ベースの製剤によって与えられたAUCinfよりも、1.2〜3.5、1.2〜4、1.2〜3、1.2〜2.85、1.5〜3.5、1.4〜3.5、2、2.2、2.3、2.4、1.2、3、4、2.85、1.5、3.5、または1.4倍高い。コルチコステロイドの被験者への用量正規化基準で、コルチコステロイド溶液によって与えられたAUCinfは、懸濁液ベースの製剤によって与えられたAUCinfよりも、1.6〜4.9、1.5〜5、1.6〜5、1.6〜3.7、1.6〜3.6、2〜4.9、1.9〜4、2.6、1.5、5、1.6、3.7、3.6、2、4.9、1.9、または4倍高い。コルチコステロイドの放出用量正規化基準で、コルチコステロイド溶液によって与えられたAUCinfは、懸濁液ベースの製剤によって与えられたAUCinfよりも、1.5〜6、1.7〜6、1.9〜6、1.9〜5.4、2.3〜5.8、1.9〜5.5、1.9〜5.8、1.5、6、1.7、1.9、5.4、2.3、5.8、5.8、3.2、3.5、または3.6倍高い。
幾つかの実施態様において、溶液中のコルチコステロイドの用量が懸濁液中の用量よりも約2倍低い場合、コルチコステロイド溶液によって与えられたAUCinfは、懸濁液ベースの製剤によって与えられたAUCinfよりも少なくとも1.5、1.6、2、2.5、3、または3.1倍高い。
本発明の製剤及びシステムは、コルチコステロイドの用量非正規化基準で、2000〜3000、2500〜2700、2000、3000、または2600のAUC0−8hr(pg*h/ml)を与えることができる。本発明の製剤及びシステムは、1)コルチコステロイドの充填用量公称正規化基準で、2〜3、2.5〜2.7、又は2.6;2)コルチコステロイドの放出用量正規化基準で、3〜4、3.4〜3.5、または3.4の用量正規化AUCinf(pg/ml/μg)を与えることができる。
幾つかの実施態様において、溶液及び懸濁液中のコルチコステロイドの用量がほぼ同一の場合、コルチコステロイドの正規化名目(充填)用量基準で、コルチコステロイド溶液によって与えられたAUC0−8hrは、懸濁液ベースの製剤によって与えられたAUC0−8hrより少なくとも1.7、1.8、1.9、または2倍高い。コルチコステロイドの放出用量の正規化基準で、コルチコステロイド溶液によって与えられたAUC0−8hrは、懸濁液ベースの製剤によって与えられたAUC0−8hrより少なくとも1.5、1.6、または2倍高い。
本発明の製剤及びシステムは、用量非正規化基準で、1600〜1800、1650〜1750、または1700のCmax(pg/ml)を与えることができる。本発明の製剤及びシステムは、1)充填用量名目正規化基準で、1〜2、1.6〜1.8、または1.7;2)放出用量正規化基準で、2〜2.5、または2.2の用量正規化Cmax(pg/ml/μg)を与えることができる。
幾つかの実施態様では、溶液及び懸濁液中のコルチコステロイドの用量がほぼ同じ場合、コルチコステロイドの正規化名目(充填)用量基準で、コルチコステロイド溶液によって与えられたCmaxは、懸濁液ベースの製剤によって与えられたCmaxより少なくとも1.7、1.8、1.9、又は2倍高い。コルチコステロイドの放出用量正規化基準で、コルチコステロイド溶液によって与えられたCmaxは、懸濁液ベースの製剤によって与えられたCmaxよりも、1.5、1.6、2倍まで高い。
幾つかの実施態様では、放出用量の20%以上、25%以上、29%以上、35%以上が、患者の血流内に吸収され得る。幾つかの実施態様では、被験者への用量の40%以上、50%以上、55%以上が、患者の血流内に吸収され得る。幾つかの実施態様では、名目利用用量の10%以上、12%以上、15%以上が、患者の血流内に吸収され得る。
本発明の幾つかの側面は、それを必要とする患者の気道に1回用量のコルチコステロイドを投与または送達する方法を提供し、この方法は、水性液体製剤、すなわち水性液体担体、スルホアルキルエーテルシクロデキストリン、及びそれに溶解したコルチコステロイドを含む製剤の1装填を含むネブライザーによりコルチコステロイドを投与または送達する方法であって、操作の際にこのシステムは、ネブライザーおよびコルチコステロイドの懸濁液ベースの製剤からなる別のシステムに勝る、強化されたドラッグデリバリー、増大した薬物投与速度、短縮された処置時間、低減した毒性、改善された安定性、強化された生体吸収、増加したアウトプット率、増加した全アウトプット、強化された薬物動態学的プロファイル、低減したコルチコステロイド関連副作用、増加した肺沈着、低減した口腔咽頭沈着、および/または向上した噴霧性能をもたらす。このシステムは、類似した条件下または異なる条件下で操作し得る。
本発明は、本明細書に開示された実施態様及び側面のすべての組合せを含む。したがって、本発明は、本明細書において特に開示され、広範囲に開示され、または狭義に開示された実施態様及び側面、ならびにその組合せおよび上記実施態様および側面の個々の要素のサブコンビネーションを含む。
本発明のこれらの態様及び他の態様は、以下の詳細な説明、実施例、特許請求の範囲及び添付の図面を参照することにより明らかになるであろう。
添付の図面は、単に例示する目的で示されているのであり、そのため、本発明の範囲を限定することを意図していない。
本願で特許請求される製剤は、他の公知の吸入可能水溶液または懸濁液コルチコステロイド含有製剤の多くの望ましくない特性を克服する。SAE−CDをコルチコステロイド含有吸入可能液体製剤に入れることにより、コルチコステロイドは溶解される。意外にも、コルチコステロイドの噴霧は、空気駆動ジェット式ネブライザーと超音波ネブライザーの両方において改善される。さらに、コルチコステロイドは、SAE−CDが存在する場合のほうが存在しない場合よりも大きな安定性を示す。
本発明の吸入可能製剤およびシステムは、ほぼ同量のコルチコステロイドを含み、かつ実質的に同条件下で送達される懸濁液製剤に勝る改善された薬物動態学的プロファイルを与える。「増強した薬物動態学的プロファイル」なる用語は、送達または投与したコルチコステロイドのより高いAUC(例えば、AUClastまたはAUC(0→∞))/μg、送達または投与したコルチコステロイドのより高いCmax/μg、送達部位でのコルチコステロイドのバイオアベイラビリティ、吸収または分布の増加、より短いTmaxまたはより長いTmaxを意味する。
あるいは、本発明の吸入可能製剤及びシステムは、おおよそより多量のコルチコステロイドを含み、かつ実質的に同条件下で送達される懸濁液製剤と、同じ薬物動態学的プロファイル、またはそれに勝る増強した薬物動態学的プロファイルをもたらす。製剤中のコルチコステロイドは、懸濁液中のそれの80%未満、70%未満、60%未満、50%未満、40%未満、20%未満、または10%未満である1回用量で存在し得る。
コルチコステロイドは、単回投与または反復投与に十分な量で存在し得る。SAE−CDは、コルチコステロイドと共に水性担体中に置かれたときにコルチコステロイドを可溶化するのに十分な量で存在し得る。水性担体は、コルチコステロイドの溶解を助ける十分な量で存在し、ネブライザーで単回投与または反復投与を可能にする十分な体積と十分に低い粘度の噴霧溶液を形成し得る。SAE−CDは、水性担体中に固形で、または溶液で存在し得る。コルチコステロイドは、ドライパウダー/粒子形態で、または水性担体中に懸濁液で存在し得る。
市販の空気駆動ジェット式、超音波、または脈動膜型ネブライザーは、AERONEB(商標)(Aerogen、カリフォルニア州サンフランシスコ)、AERONEB(GO)(Aerogen);、PARI LC PLUS(商標)、PARI BOY(商標)N、PARI eflow、PARI LC SINUS、PARI SINUSTAR(商標)、PARI、SINUNEB、およびPARI DURANEB(商標)(PARI Respiratory Equipment,Inc.、カリフォルニア州モンテレー);MICROAIR(商標)(Omron Healthcare,Inc、イリノイ州ヴァーノンヒルズ)、HALOLITE(商標)(Profile Therapeutics Inc、マサチューセッツ州ボストン)、RESPIMAT(商標)(Boehringer Ingelheim Ingelheim、ドイツ)、AERODOSE(商標)(Aerogen,Inc、カリフォルニア州マウンテンビュー)、OMRON ELITE(商標)(Omron Healthcare,Inc、イリノイ州ヴァーノンヒルズ)、OMRON MICROAIR(商標)(Omron Healthcare,Inc、イリノイ州ヴァーノンヒルズ)、MABISMIST(商標)II(Mabis Healthcare,Inc.、イリノイ州レークフォレスト)、LUMISCOPE(商標)6610(The Lumiscope Company,Inc、ニュージャージー州イーストブランズウィック)、AIRSEP MYSTIQUE(商標)(AirSep Corporation、ニューヨーク州バッファロー)、ACORN−1およびACORN−II(Vital Signs,Inc、ニュージャージー州トトワ)、AQUATOWER(商標)(Medical Industries America、アイオワ州アデル)、AVA−NEB(Hudson Respiratory Care Incorporated、カリフォルニア州テメキュラ)、AEROCELL(商標)ディスポーザブルカートリッジを利用するAEROCURRENT(商標)(AerovectRx、Corporation、Atlanta、Georgia)、CIRRUS(Intersurgical Incorporated、ニューヨーク州リバプール)、DART(Professional Medical Products、サウスカロライナ州グリーンウッド)、DEVILBISS(商標)PULMO AIDE(DeVilbiss Corp、ペンシルバニア州サマセット)、DOWNDRAFT(商標)(Marquest、コロラド州エングルウッド)、FAN JET(Marquest、コロラド州エングルウッド)、MB−5(Mefar、イタリア、ボベッツオ)、MISTY NEB(商標)(Baxter、カリフォルニア州バレンシア)、SALTER 8900(Salter Labs、カリフォルニア州アービン)、SIDESTREAM(商標)(Medic−Aid、英国サセックス)、UPDRAFT−II(商標)(Hudson Respiratory Care、カリフォルニア州テメキュラ)、WHISPER JET(商標)(Marquest Medical Products、コロラド州エングルウッド)、AIOLOS(商標)(Aiolos Medicnnsk Teknik、スウェーデン、カルルスタード)、INSPIRON(商標)(Intertech Resources,Inc.、イリノイ州バノックバーン)、OPTIMIST(商標)(Unomedical Inc.、テキサス州マッカレン)、PRODOMO(商標)、SPIRA(商標)(Respiratory Care Center、フィンランド、ヘメーンリンナ)、AERx(商標)Essence(商標)およびUltra(商標)(Aradigm Corporation、カリフォルニア州ヘーワード)、SONIK(商標)LDI Nebulizer(Evit Labs、カリフォルニア州サクラメント)、およびSWIRLER(登録商標)Radioaerosol System(AMICI,Inc.、ペンシルバニア州スプリングシティー)を含む。噴射剤を含まない液体製剤を噴霧するネブライザーは、本発明で提供される組成物での使用に適している。これらおよび他の公知のネブライザーはどれも、本発明の製剤を送達するために使用することができ、これらは、限定はされないが以下を含む:Pari GmbH(ドイツ、シュタルンベルク)、DeVilbiss Healthcare(英国ミドルセックス州ヘストン)、Healthdyne、Vital Signs、Baxter、Allied Health Care、Invacare、Hudson、Omron、Bremed、AirSep、Luminscope、Medisana、Siemens、Aerogen、Mountain Medical、Aerosol Medical Ltd.(英国エセックス州コルチェスター)、AFP Medical(英国ウォリックシャー州ラグビー)、Bard Ltd.(英国サンダーランド)、Carri−Med Ltd.(英国ドーキング)、Plaem Nuiva(イタリア、ブレシア)、Henleys Medical Supplies(英国ロンドン)、Intersurgical(英国バークシャー州)、Lifecare Hospital Supplies(英国リース)、Medic−Aid Ltd.(英国ウェストサセックス州)、Medix Ltd.(英国エセックス州)、Sinclair Medical Ltd.(英国サリー州)、およびその他の多くの会社から入手可能なネブライザーである。AERxおよびRESPIMATネブライザーは、D.E.Geller(Respir.Care(2002年)、47(12)、1392〜1404頁)によって記述され、その開示全体は、参照により本明細書に組み入れられている。
本発明において使用のためのネブライザーは、限定はされないが、ジェット式ネブライザー(場合によってはコンプレッサ付きで売られている)、超音波式ネブライザー、振動膜、振動メッシュネブライザー、振動板ネブライザー、振動円錐ネブライザー、などを含む。本発明において使用のための例示的なジェット式ネブライザーは、Pari LC plus/ProNeb、Pari LC plus/ProNeb Turbo、Pari LC Plus/Dura Neb 1000 & 2000 Pari LC plus/Walkhaler、Pari LC plus/Pari Master、Pari LC star、Omron CompAir XL Portable Nebulizer System(NE−C18およびJetAir Disposable Nebulizer)、Omron compare Elite Compressor Nebulizer System(NE−C21およびElite Air Reusable Nebulizer)、Proneb Ultraコンプレッサ付きPari LC PlusまたはPari LC Starネブライザー、Pulomo−aide、Pulmo−aide LT、Pulmo−aide traveler、Invacare Passport、Inspiration Healthdyne 626、Pulmo−Neb Traverler、DeVilbiss 646、Whisper Jet、Acorn II、Misty−Neb、Allied aerosol、Schuco Home Care、Lexan Plasic Pocet Neb、SideStream Hand Held Neb、Mobil Mist、Up−Draft、Up−Draft II、T Up−Draft、ISO−NEB、Ava−Neb、Micro Mist、およびPulmoMateを含む。本発明において使用のための例示的な超音波ネブライザーは、MicroAir、UltraAir、Siemens Ultra Nebulizer 145、CompAir、Pulmosonic、Scout、5003 Ultrasonic Neb、5110 Ultrasonic Neb、5004 Desk Ultrasonic Nebulizer、Mystique Ultrasonic、LumiscopeのUltrasonic Nebulizer、Medisana Ultrasonic Nebulizer、Microstat Ultrasonic Nebulizer、およびMabismist Hand Held Ultrasonic Nebulizerを含む。本発明において使用のための他のネブライザーは、5000 Electromagnetic Neb、5001 Electromagnetic Neb 5002 Rotary Piston Neb、Lumineb I Piston Nebulizer 5500、Aeroneb Portable Nebulizer System、Aerodose(商標)Inhaler、およびAeroEclipse Breath Actuated Nebulizerを含む。典型的な振動膜、メッシュ又はプレートネブライザーは、R.Dhand(Respir.Care(Dec.2002)、47(12)、1406−1418)によって記述され、その開示全体は、参照により本明細書に組み入れられている。
その他の好適なネブライザーは、米国特許第5,954、047、第6、026、808、第6、095、141、および第6、527、151に記載され、その開示全体は、参照により本明細書に組み入れられている。
本発明は、SAE−CDベースの製剤を提供し、ここでSAE−CDは、式1:
の化合物である。
[式中、
nは、4、5、または6であり、
R1、R2、R3、R4、R5、R6、R7、R8、およびR9は、それぞれ独立に−O−または−O−(C2−C6アルキレン)−SO3 -基であり、R1からR9の少なくとも1つは独立に−O−(C2−C6アルキレン)−SO3 -基、好ましくは−O−(CH2)mSO3 -基であり、mは2から6、好ましくは2から4であり(例えば、−OCH2CH2CH2SO3 -ま
たは−OCH2CH2CH2CH2SO3 -)であり、
S1、S2、S3、S4、S5、S6、S7、S8、およびS9はそれぞれ独立に例えば、H+、アルカリ金属(例えば、Li+、Na+、K+)、アルカリ土類金属(例えば、Ca+2、Mg+2)、アンモニウムイオン、および(C1−C6)−アルキルアミン、ピペリジン、ピラジン、(C1−C6)−アルカノールアミンおよび(C4−C8)−シクロアルカノールアミンのカチオンなどのアミンカチオンを含む、医薬として許容されるカチオンである]。
[式中、
nは、4、5、または6であり、
R1、R2、R3、R4、R5、R6、R7、R8、およびR9は、それぞれ独立に−O−または−O−(C2−C6アルキレン)−SO3 -基であり、R1からR9の少なくとも1つは独立に−O−(C2−C6アルキレン)−SO3 -基、好ましくは−O−(CH2)mSO3 -基であり、mは2から6、好ましくは2から4であり(例えば、−OCH2CH2CH2SO3 -ま
たは−OCH2CH2CH2CH2SO3 -)であり、
S1、S2、S3、S4、S5、S6、S7、S8、およびS9はそれぞれ独立に例えば、H+、アルカリ金属(例えば、Li+、Na+、K+)、アルカリ土類金属(例えば、Ca+2、Mg+2)、アンモニウムイオン、および(C1−C6)−アルキルアミン、ピペリジン、ピラジン、(C1−C6)−アルカノールアミンおよび(C4−C8)−シクロアルカノールアミンのカチオンなどのアミンカチオンを含む、医薬として許容されるカチオンである]。
本発明のSAE−CD誘導体の例示的な実施態様は、以下のような、「x」を1から18までの範囲とする式II(SAEx−α−CD)の誘導体、「y」を1から21までの範囲とする式III(SAEy−β−CD)の誘導体、および「z」を1から24までの範囲とする式IV(SAEz−γ−CD)の誘導体を含む。
「SAE」は、シクロデキストリンに結合されたスルホアルキルエーテル置換基を表す。値「x」、「y」、および「z」は、CD1分子当たりのスルホアルキルエーテル基の個数に関して本明細書で定義されているような平均置換度を表す。
使用されるSAE−CDは、Stellaらの米国特許第5,376,645号および第5,134,127号で説明されており、その開示全体は、参照により本明細書に組み込まれる。Parmerterらの米国特許第3,426,011号では、スルホアルキルエーテル置換基を有するアニオン性シクロデキストリン誘導体を開示している。Lammersら(Recl.Trav.Chim.Pays−Bas(1972年)、91(6)、733〜742頁、Staerke(1971年)、23(5)、167〜171頁)、およびQuら(J.Inclusion Phenom.Macro.Chem.、(2002年)、43、213〜221頁)は、スルホアルキルエーテル誘導体化シクロデキストリンを開示している。Shahらの米国特許第6,153,746号では、スルホアルキルエーテルシクロデキストリン誘導体の調製方法を開示している。SAE−CDは、Stellaら、Parmerterら、Lammersら、またはQuらの開示に従って作ることができ、未誘導体化親シクロデキストリンの大部分(>50%)を取り除くように処理すれば、本発明により使用することができる。SAE−CDは、未誘導体化親シクロデキストリンの0%から50重量%未満までを含んでいてもよい。
「アルキレン」および「アルキル」という用語は、本明細書で使用されているように(例えば、−0−(C2−C6−アルキレン)SO3 -基またはアルキルアミン)、直鎖、環状、および分枝の飽和および不飽和(すなわち、1個の二重結合を含む)二価アルキレン基および一価アルキル基をそれぞれ含む。本明細書の「アルカノール」という用語は、同様に、直鎖、環状、および分枝の飽和および不飽和双方のアルキル成分のアルカノール基を含み、ここで水酸基はアルキル部分上の任意の位置にあっていよい。「シクロアルカノール」という用語は、非置換または置換(例えば、メチルまたはエチルによる)環式アルコールを含む。
本発明の一実施態様は、構造が式(I)で提示されている、シクロデキストリン誘導体の混合物を含む組成物を提供し、ここで組成物全体は、平均して、シクロデキストリン1分子当たり少なくとも1つおよび最大3n+6個までのアルキルスルホン酸部分を含む。本発明は、さらに、単一種類のシクロデキストリン誘導体を含む、または単一種類のシクロデキストリン誘導体の少なくとも50%を含む組成物を提供する。本発明は、さらに、狭いまたは広い、および高いまたは低い置換度を有するシクロデキストリン誘導体を含む製剤も含む。これらの組み合わせは、必要に応じて、特定の特性を有するシクロデキストリンが得られるように最適化できる。
本発明は、さらに、2つまたはそれ以上の異なる種類のシクロデキストリン誘導体が組成物内に含まれるシクロデキストリン誘導体の混合物を含む組成物を提供する。異なる種類とは、異なる種類の官能基、例えば、ヒドロキシアルキルおよびスルホアルキルで誘導体化されたシクロデキストリンを意味する。それぞれの独立の異なる種類は、1つまたはそれ以上の官能基、例えば、シクロデキストリン環がスルホブチル官能基のみを有するSBE−CD、およびシクロデキストリン環がヒドロキシプロピル官能基とエチル官能基の両方を有するヒドロキシプロピル−エチル−β−CDを含むことができる。存在するそれぞれの種類のシクロデキストリン誘導体の量は、好きなように変えて、所望の特性を持つ混合物を作ることができる。
例示的なSAE−CD誘導体は、SBE4−β−CD、SBE7−β−CD、SBE11−β−CD、SBE3.4−γ−CD、SBE4.2−γ−CD、SBE4.9−γ−CD、SBE5.2−γ−CD、SBE6.1−γ−CD、SBE7.5−γ−CD、SBE7.8−γ−CD、およびSBE5−γ−CDを含み、これらは式IのSAE−CD誘導体に対応し、ただし、n=5、5、5、および6であり、mは、4であり、それぞれ、平均して、4、7、11、および5個のスルホアルキルエーテル置換基が存在する。これらのSAE−CD誘導体は、水に溶けにくい活性物質の溶解度をさまざまな程度まで高める。
SAE−CDは、多価アニオンシクロデキストリンであるため、異なる塩形態で提供することができる。好適な対イオンは、カチオン有機原子または分子およびカチオン無機原子または分子を含む。SAE−CDは、単一種類の対イオンまたは異なる対イオンの混合物を含むことができる。SAE−CDの特性は、存在する対イオンのアイデンティティを変えることにより改変することができる。例えば、SAE−CDの第1の塩形態は、SAE−CDの異なる第2の塩形態よりも大きなコルチコステロイド安定化および/または可溶化力を有することができる。同様に、第1の置換度を有するSAE−CDは、異なる置換度を有する第2のSAE−CDよりも大きなコルチコステロイド安定化および/または可溶化力を持つことができる。あるSAE−CDによる、他のそれとの対比におけるコルチコステロイドの可溶化の増強は、以下の表のデータにより示されており、これは、約0.03から0.12Mの濃度の異なるSAE−CDとのプロピオン酸フルチカゾンのモル溶解度を表しており、それによれば可溶化力がSAE−CDのこの濃度範囲で大体以下のランク順序:SBE5.2−γ−CD>SPE5.4−γ−CD>SBE6.1−γ−CD>SBE9.7−γ−CD>>SBE7−α−CD>SBE6.7−β−CD>SPE7−β−CDとなった。フランカルボン酸モメタゾンでは、可溶化力はSAE−CDのこの濃度範囲で、大体以下のランク順序:SBE9.7−γ−CD>SBE6.1−γ−CD>SBE5.2−γ−CD>>SPE5.4−γ−CD>SBE7−α−CD>SBE6.7−β−CD>SPE7−β−CDとなった。ブデソニドおよびトリアムシノロンとSAE−CDの特定の実施態様との結合について違いが観察された。本発明によれば、SAE−γ−CDは、SAE−β−CDに比べてコルチコステロイドとよく結合する。また、SAE−β−CDは、SAE−α−CDよりもよくブデソニドと結合する。データは、図13〜14にまとめられている。
本発明者は、さらに、SAE−γ−CDは、同じコルチコステロイドとSAE−β−CDまたはSAE−α−CDとの錯体を形成することと比較して、特にエステル化および非エステル化コルチコステロイドの錯化に使用するのに適していることも発見した。上の表は、さらに、置換度が5から10の範囲内のさまざまな異なるSAE−γ−CD化学種とのフルチカゾンおよびプロピオン酸フルチカゾンについて図15に示されている相溶解度データをまとめたものである。
本発明者は、SAE−γ−CDは、さらに、SAE−β−CDまたはSAE−α−CDよりも、エステル化コルチコステロイドの特定の位置異性体との結合においてかなり有効であることも発見した。実施例18で説明されている手順では、SAE−γ−CDおよびSAE−β−CDと一連の構造的に関係のあるコルチコステロイド誘導体との結合の比較評価を詳しく述べている。以下の表は、SBEx−γ−CD(xは平均置換度を表す)、誘導体、およびSBE−β−CD誘導体と異なる形態のベクロメタゾンとの結合を比較する研究結果をまとめたものである。
調査研究から、SBE(3.4)γ−CD(0.04M)が存在している場合、すべての形態のベクロメタゾンはその最高溶解度であるか、またはその近くにあったことがわかる。B17P、すなわちBDPの活性代謝産物が、全ての誘導体化されたCDにおいて、エステル化されたベクロメタゾン形態の最高溶解度となっている。これらの結果から、SBE−γ−CDは、Captisolまたはγ−CD単独の場合よりも、ジプロピオン酸ベクロメタゾンとよく錯体を形成することがわかる。評価されたSAE−CD誘導体のうち、BDPの溶解度の最高の増強を与えるSBEγ−CDの最適な置換度は、DS=3.4であり、溶解度は、置換度が上昇すると共にほぼ直線的に低下する。これは、24時間および5日の両方の平衡時間についてあてはまる。したがって、SAE−CDによるBDP可溶化に関して、SBE(3.4)γ−CD>SBE(5.2)γ−CD>SBE(6.1)γ−CD>SBE(7.5)γ−CD>γ−CD>Captisol(SBE7−β−CD)となる。データは、図16にまとめられている。したがって、本発明者らは、SAE−γ−CDシクロデキストリン誘導体が思いがけなくSAE−β−CD誘導体よりもコルチコステロイドの可溶化に優れることを発見した。さらに、SAE−γ−CDベースの製剤は、SAE−CD誘導体がそうでないことを示唆する、Worthら(上記)の開示とは反対に、吸入可能製剤での使用に適している。
「錯化された」とは、「〜とのクラスレート化合物または包接錯体の一部である」、すなわち、錯化された治療剤は、シクロデキストリン誘導体とのクラスレート化合物または包接錯体の一部であるということである。「大部分」とは、少なくとも約50質量%を意味する。そのため、本発明による製剤は、約50質量%を超える量がシクロデキストリンと錯体を形成する活性物質を含むことができる。錯化された活性物質の実際の割合は、特定のシクロデキストリンと特定の活性物質との錯体形成を特徴付ける錯体生成平衡定数により異なる。本発明は、さらに、活性物質がシクロデキストリンと錯体を形成していない、または活性物質の小部分が誘導体化されたシクロデキストリンと錯体を形成する実施態様も含む。SAE−CD、または他の何らかのアニオン性誘導体化シクロデキストリンは、プラスに帯電した化合物と1つまたはそれ以上のイオン結合を形成できることに留意されたい。イオン会合は、プラスに帯電した化合物が空洞への包摂、または塩橋の形成のいずれかにより、シクロデキストリンと錯体を形成するかどうかに関係なく発生しうる。
薬剤の誘導体化シクロデキストリンへの結合は、酸または塩基を薬剤およびシクロデキストリンと共に含めることにより改善することができる。例えば、塩基性薬剤のシクロデキストリンへの結合は、酸をその塩基性薬剤およびシクロデキストリンと共に含めることにより改善することができる。同様に、酸性薬剤のシクロデキストリンへの結合は、塩基(アルカリ物質)を酸性薬剤およびシクロデキストリンと共に含めることにより改善することも可能である。中性薬剤の結合は、塩基性、酸性、または他の中性化合物を中性薬剤およびシクロデキストリンと共に含めることにより改善することができる。好適な酸化合物は、無機酸および有機酸を含む。無機酸の実例としては、塩化水素酸および臭化水素酸などの鉱酸がある。他の好適な酸は、硫酸、スルホン酸、スルフェン酸、およびリン酸を含む。有機酸の実例は、酢酸、アスコルビン酸、炭酸、クエン酸、酪酸、フマル酸、グルタル酸、グリコール酸、α−ケトグルタル酸、乳酸、リンゴ酸、メバロン酸、マレイン酸、マロン酸、シュウ酸、ピメリン酸、プロピオン酸、コハク酸、酒石酸、またはタルトロン酸などの脂肪族カルボン酸である。脂肪族鎖内に1つ以上の含酸素置換基を持つ脂肪族カルボン酸も有用である。複数の酸の組み合わせを使用することもできる。
好適な塩基化合物は、無機塩基および有機塩基を含む。好適な無機塩基は、アンモニア、金属酸化物、および金属水酸化物を含む。好適な有機塩基は、第一級アミン、第二級アミン、第三級アミン、イミダゾール、トリアゾール、テトラゾール、ピラゾール、インドール、ジエタノールアミン、トリエタノールアミン、ジエチルアミン、メチルアミン、トロメタミン(TRIS)、芳香族アミン、不飽和アミン、第一級チオール、および第二級チオールを含む。複数の塩基の組み合わせを使用することもできる。
アニオン性誘導体化シクロデキストリンは、酸イオン化剤と錯体を形成するか、または他の何らかの形で結合することができる。本明細書で使用されているように、酸イオン化剤という用語は、酸の存在下でイオン化状態になるか、またはイオン化される化合物を意味するものと解釈する。酸イオン化剤は、酸に曝されたとき、または酸性媒体中に置かれたときにイオン化状態になる少なくとも1つの酸イオン化官能基を含む。例示的な酸イオン化官能基は、第一級アミン、第二級アミン、第三級アミン、第四級アミン、芳香族アミン、不飽和アミン、第一級チオール、第二級チオール、スルホニウム、水酸基、エノール、および化学分野の当業者に公知の他の基を含む。
酸イオン化剤が、包摂錯体形成に対する非共有イオン結合により結合される程度を、例えば1HNMR、13CNMR、または円偏光二色性などの方法を使用する分光光度法により、また酸イオン化剤およびアニオン性誘導体化シクロデキストリンの相溶解度データの分析により、決定することができる。当業者であれば、これらの従来の方法を使用して、化学種間の結合が、主に、非共有イオン結合または包接錯体形成により発生しているかどうかを判別するために溶液中に生じているそれぞれの種類の結合の量を近似することができる。両方の手段により誘導体化シクロデキストリンに結合する酸イオン化剤は、一般に、二相性相溶解度曲線を示す。非共有イオン結合が包接錯体形成よりも優位である条件の下では、包接錯体形成の量(NMRまたは円偏光二色性により測定される)は、これらの条件の下で相溶解度データが化学種間の有意な結合を示すとしても、低下し、さらに、酸イオン化剤の固有溶解度(相溶解度データから決定されるものとして)は、一般に、これらの条件の下で予想される以上に高くなる。
本明細書で使用されているように、非共有イオン結合という用語は、アニオン種とカチオン種との間に形成される結合を指す。この結合は、2つの化学種が一緒になって塩またはイオン対を形成するような非共有である。アニオン性誘導体化シクロデキストリンは、イオン対のアニオン種を与え、酸イオン化剤は、イオン対のカチオン種を与える。アニオン性誘導体化シクロデキストリンは多価であるため、SAE−CDは、1つ以上の酸イオン化剤とイオン対を形成することができる。
親シクロデキストリンは、SAE−CDおよびHPCDと比べて、限られた水溶解度を有する。未誘導体化α−CDの水溶解度は、飽和時に約14.5%w/vである。未誘導体化β−CDの水溶解度は、飽和時に約1.85%w/vである。未誘導体化γ−CDの水溶解度は、飽和時に約23.2%w/vである。ジメチル−β−シクロデキストリン(DMCD)は、飽和時に43%w/wの水溶液を形成する。SAE−CDを吸入可能溶液中で1つまたはそれ以上の他のシクロデキストリンまたはシクロデキストリン誘導体と組み合わせて、コルチコステロイドを可溶化することができる。
本発明に従って使用することができる他の水溶性シクロデキストリン誘導体は、ヒドロキシエチル、ヒドロキシプロピル(2−および3−ヒドロキシプロピルを含む)、およびジヒドロキシプロピルエーテル、その対応する混合エーテルおよびα−、β−、およびγ−シクロデキストリンのメチルヒドロキシエチル、エチル−ヒドロキシエチル、およびエチルヒドロキシプロピルエーテルなどのメチルまたはエチル基との他の混合エーテル;ならびに1つ以上の糖残基、例えば、グルコシルまたはジグルコシル、マルトシルまたはジマルトシル、さらにはそれらのさまざまな混合物、例えば、マルトシルおよびジマルトシル誘導体の混合物を含むことができる、α−、β−、およびγ−シクロデキストリンのマルトシル、グルコシル、およびマルトトリオシル誘導体を含む。本発明で使用する特定のシクロデキストリン誘導体は、ヒドロキシプロピル−β−シクロデキストリン、ヒドロキシエチル−β−シクロデキストリン、ヒドロキシプロピル−γ−シクロデキストリン、ヒドロキシエチル−γ−シクロデキストリン、ジヒドロキシプロピル−β−シクロデキストリン、グルコシル−α−シクロデキストリン、グルコシル−β−シクロデキストリン、ジグルコシル−β−シクロデキストリン、マルトシル−α−シクロデキストリン、マルトシル−β−シクロデキストリン、マルトシル−γ−シクロデキストリン、マルトトリオシル−β−シクロデキストリン、マルトトリオシル−γ−シクロデキストリンおよびジマルトシル−β−シクロデキストリン、ならびにマルトシル−β−シクロデキストリン/ジマルトシル−β−シクロデキストリン、さらにはメチル−β−シクロデキストリンなどのそれらの混合物を含む。そのようなシクロデキストリン誘導体を製造する手順は、よく知られており、例えば、1991年6月18日に発行されたBodorの米国特許第5,024,998号およびそこに引用されている文献に記載されている。本発明で使用するのに適している他のシクロデキストリンは、ORGANON(AKZO−NOBEL)により製造されているORG 26054およびORG 25969などのカルボキシアルキルチオエーテル誘導体、EASTMANにより製造されているヒドロキシブテニルエーテル誘導体、スルホアルキル−ヒドロキシアルキルエーテル誘導体、スルホアルキル−アルキルエーテル誘導体、ならびに米国特許付与前特許出願公開第2002/0128468号、第2004/0106575号、第2004/0109888号、および第2004/0063663号、または米国特許第6,610,671号、第6,479,467号、第6,660,804号、または第6,509,323号で説明されているような他の誘導体を含む。
HP−β−CDは、Research Diagnostics Inc.(ニュージャージー州フランダーズ)から入手できる。HP−β−CDは、異なる置換度のものを利用できる。例示的な製品は、ENCAPSIN(商標)(置換度約4、HP4−β−CD)およびMOLECUSOL(商標)(置換度約8、HP8−β−CD)を含むが、他の置換度を含む実施態様も利用可能である。HPCDは、非イオン性なので、塩形態のものは入手できない。
ジメチルシクロデキストリンは、FLUKA Chemie(Buchs,CH)またはWacker(アイオワ州)から入手できる。本発明に適している他の誘導体化シクロデキストリンは、水溶性誘導体化シクロデキストリンを含む。例示的な水溶性誘導体化シクロデキストリンは、カルボキシル化誘導体、硫酸化誘導体、アルキル化誘導体、ヒドロキシアルキル化誘導体、メチル化誘導体、およびカルボキシ−β−シクロデキストリン、例えば、スクシニル−β−シクロデキストリン(SCD)、および6A−アミノ−6A−デオキシ−N−(3−カルボキシプロピル)−β−シクロデキストリンを含む。これらの物質はすべて、従来技術で公知の方法に従って製造できる。好適な誘導体化シクロデキストリンは、「Modified Cyclodextrins:Scaffolds and Templates for Supramolecular Chemistry」(Eds.Christopher J.Easton、Stephen F.Lincoln、Imperial College Press、London、UK、1999年)および「New Trends in Cyclodextrins and Derivatives」(Ed.Dominique Duchene、Editions de Sante、Paris、France、1991年)で開示されている。
スルホブチルエーテルβ−シクロデキストリン(CAPTISOL、CyDex Inc.、置換度=6.6)、2−ヒドロキシプロピルβ−シクロデキストリン(HP−β−CD、CERESTAR、置換度=5.5)、コハク酸化−β−シクロデキストリン(S−CD、Cyclolab)、および2,6,ジ−o−メチル−β−シクロデキストリン(DM−CD、Fluka)%w/w溶液は、その固有pHで調製されるか、または必要に応じて緩衝化される。スルホアルキルエーテルγ−CDおよびスルホアルキルエーテルα−CD誘導体は、CyDex,Inc.(カンザス州レネクサ)およびカンザス大学(カンザス州ロレンス)から入手した。
所望の効果を得るために必要な誘導体化シクロデキストリンの量は、製剤を含む物質に応じて異なる。
異なるシクロデキストリンは、異なる程度でコルチコステロイドを可溶化することができる。図3は、水と比較してHP−β−CD、SBE7−β−CD、およびγ−CDを含むブデソニドのモル相溶解度曲線を示している。本発明者らは、SAE−CDがブデソニドを可溶化することに対し、他のシクロデキストリンおよびシクロデキストリン誘導体よりも優れていることを発見した。モルに基づくと、SBE−β−CDは、HP−β−CDよりも優れた、ブデソニドの可溶化剤である。さらに、SAE−CD誘導体の間の可溶力は、0.04から0.1MのSAE−CD濃度範囲でブデソニドに対し大体以下のランク順序:SBE5.2−γ−CD〜SPE5.4−γ−CD>SBE6.1−γ−CD>SBE7−α−CD>SBE9.7−γ−CD〜SBE6.7−β−CD>SPE7−β−CDとなった。例えば、0.1Mの濃度のSBE7−β−CDは、γ−CDまたはHP−β−CDよりも多くの量のブデソニドを可溶化することができた。さらに、SAE−CD含有噴霧可能製剤では、他の類似条件の下で投与されたγ−CDまたはHP−β−CDと比べて噴霧によるコルチコステロイドのアウトプット率が高い。
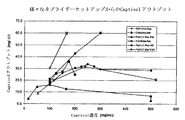
Captisol溶液の噴霧には、他のシクロデキストリンに関していくつかの利点があることが思いがけなく発見された。ネブライザーから出た液滴は、より有利なサイズであり、Captisol溶液は、他のシクロデキストリンの類似の溶液よりも高速に噴霧化される。以下の表は、Captisol溶液の平均粒径(Dv50)は、HP−β−CDまたはγ−CDのと比べて小さいことを示している。より重要なのは、以下の表からわかるように、Dv90は、他のシクロデキストリンが著しい数の非常に大きな液滴を有していたことを示していることである。データ(Malvern粒径)は、それぞれの製剤がPARI PRONEB ULTRAエアコンプレッサを備えたPARI LC PLUSネブライザーから放出されるそれぞれの製剤について得られた。小さな液滴サイズならばコルチコステロイドなどの活性物質が肺の奥深く送達することができるのに、吸入可能組成物より小さな液滴サイズが好ましい。
この利点は、さらに、これらの溶液のアウトプット率に示されている。以下の表は、Captisolがネブライザーからより高速に、また他のシクロデキストリンよりも大きな度合いで放出され、Captisolが噴霧されるときにネブライザーのアウトプット率がより大きいことを示している。
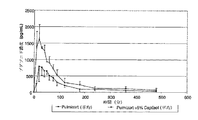
Captisolの利点は、さらに、さまざまなシクロデキストリンに溶解されているブデソニドを含む溶液を調製し、噴霧の性能と市販の懸濁液ベースの単位用量製剤である市販のPULMICORT(登録商標)、RESPULES(登録商標)の性能とを比較することにより実証された。PULMICORT(商標)の複数の単位投与アンプルから得られる懸濁液をプールして、複数回使用する懸濁液ベースの単位投与製剤を形成し、SAE−CD(特に、CAPTISOL)、HP−β−またはγ−シクロデキストリン粉末を加えて、0.25mg/mlのブデソニド溶液濃度とした。これらのブデソニド含有溶液は、Captisol(P5C)5%w/v、γ−CD(P1γCD)1%w/v、およびヒドロキシプロピル−β−シクロデキストリン(P5HPβCD)5%w/vを含んでいた。それぞれ、すべての試験の少なくとも30分前に調製された。3つの製剤はすべて、無色澄明な溶液であった。(注意:ブデソニドの250mg/mL溶液は、「B」型溶解性挙動を示すのでγ−シクロデキストリンの5%w/v溶液中に作ることはできない)。懸濁液または溶液2mlアリコートを同じPari LC Plusネブライザーセットアップに入れ、放出液滴内のブデソニドの量を決定するためにフィルター上に集め、HPLCを使用してブデソニドを測定した。以下の表に示されているように、全アウトプット率(μg回収ブデソニド/スパッター時間)は、それぞれの懸濁液または溶液に対するものである。
アウトプット率は、Captisol溶液で最も高く、等しい量の薬剤をより短時間のうちに送達することができることを示している。使用された条件の下では、β−CDは、水に対するβ−CDの限られた溶解性のせいで等しい量のコルチコステロイドを可溶化することはできない。
本発明は、他の懸濁液ベースの水性製剤と併用することができ、その製剤は、経鼻送達または経肺送達に適合させることができる。例示的な懸濁液ベースの水性製剤は、UDB製剤(Sheffield Pharmaceuticals,Inc.)、VANCENASE(商標)AQ(ジプロピオン酸ベクロメタゾン水性懸濁液、Schering Corporation、ニュージャージー州ケニルワース)、ATOMASE(商標)(ジプロピオン酸ベクロメタゾン水性懸濁液、Douglas Pharmaceuticals Ltd.、オーストラリア、オークランド)、BECONASE(商標)(プロピオン酸ベクロメタゾン水性懸濁液、Glaxo Wellcome)、NASACORT AQ(商標)(トリアムシノロンアセトニド経鼻スプレー、Aventis Pharmaceuticals)、TRI−NASAL(商標)(トリアムシノロンアセトニド水性懸濁液、Muro Pharmacaceuticals Inc.)、およ
びAEROBID−M(商標)(フルニソリド吸入エアロゾル、Forest Pharmaceuticals)、NASALIDE(商標)およびNASAREL(商標)(フルニソリド経鼻スプレー、Ivax Corporation)、FLONASE(商標)(プロピオン酸フルチカゾン、GlaxoSmithKline)、およびNASONEX(商標)(フランカルボン酸モメタゾン、Schering−Plough Corporation)を含む。
びAEROBID−M(商標)(フルニソリド吸入エアロゾル、Forest Pharmaceuticals)、NASALIDE(商標)およびNASAREL(商標)(フルニソリド経鼻スプレー、Ivax Corporation)、FLONASE(商標)(プロピオン酸フルチカゾン、GlaxoSmithKline)、およびNASONEX(商標)(フランカルボン酸モメタゾン、Schering−Plough Corporation)を含む。
懸濁液製剤は、粒子、微粒子、ナノ微粒子、またはナノ結晶形態で存在するコルチコステロイドを含むことができる。したがって、SAE−CDは、コルチコステロイド懸濁液ベースの単位用量製剤の投与を改善するために使用することができる。さらに、SAE−CDは、他のシクロデキストリン誘導体よりも性態が優れている。
一実施態様によれば、SAE−CD(固体または液体)およびコルチコステロイドを含む懸濁液ベースの単位用量製剤を混合する。SAE−CDは、可溶化されたコルチコステロイドの量を増やす、すなわち、その中の未可溶化コルチコステロイドの量を減らすのに十分な量で存在する。投与前に、液体を、場合により滅菌濾過または最終滅菌することができる。その後、ネブライザーを使用してこの液体を被験者に吸入投与する。その結果、被験者が服用する薬剤の量は、改変していない懸濁液製剤が投与された場合に被験者が服用していたはずの量よりも多い。
他の実施態様により、SAE−CD(液体形態で、すぐに使用できる液体として、または濃縮物として)およびコルチコステロイドを含む固体単位用量製剤を混合して、液体製剤を形成する。SAE−CDは、コルチコステロイドの相当部分を可溶化するのに十分な量で存在する。その後、ネブライザーを使用してこの液体を吸入投与する。
他の実施態様により、SAE−CD(固体)および、コルチコステロイドを含む固体単位用量製剤を混合し、固体混合物を形成し、これに、噴霧可能製剤を形成するのに十分な量で水性液体担体を加える。場合によっては、液体担体を加えた後、混合および/または加熱を使用して、製剤を形成する。SAE−CDは、コルチコステロイドの相当部分を可溶化するのに十分な量で存在する。その後、ネブライザーを使用してこの製剤を吸入投与する。
リザーバのサイズは、ネブライザーの種類毎に異なる。特定の種類またはブランドのネブライザーのリザーバ内に装填するのに必要な容積になるように、液体製剤の容積を必要に応じて調整することができる。追加液体担体またはSAE−CDを含む追加溶液を加えることにより、容積を調整することができる。一般的に、ネブライザーのリザーバ容積は約10μl〜100mlである。超音波及び振動メッシュ/振動板/振動円錐/振動膜ネブライザーなどの低容積ネブライザー、送達ノズルを含めてプレ充填リザーバストリップは、一般には10μl〜6mlまたは10μl〜5mlのリザーバ容積を有する。低容積ネブライザーは、大容積ネブライザーに比べて投与時間が短いという利点がある。
実施例28は、AERxネブライザーなどの低容積(低リザーバ容積および/またはリザーバ残留量)ネブライザーで使用される本発明の溶液の調製造手順について詳述している。本発明の溶液は、いずれのネブライザーでも噴霧可能である;しかしながら、深部肺浸透を最適化する吸入および送達方法の両方を調和させたAERxシステムでは、約10〜100、または50μlの初期試料量が、AERx Strip単位投与容器を充填するために使用し得る。本システムによるこの溶液の投与は、噴霧を介して単回パフ(被験者による単回完全吸入、すなわち3〜5秒)で被験者に投与しようとする治療用量の投与を実行可能にする。放出用量が60〜65%で、またその結果肺用量が65〜85%である、このような装置の一般的な性能予想に基づいて、約10μg〜60μgまたは10μg〜110μgのブデソニドが、SAE−CDで調製したブデソニド溶液を用いる単回の投与イベントで肺への送達が期待できる。
実施例32は、本発明の製剤およびPULMICORT RESPULES(懸濁液ベースの製剤)を用いた、4つの異なるネブライザーにおける噴霧パラメータの比較手順を詳述している。各例において、本発明の製剤は、懸濁液ベースの製剤より性能が優れる。本発明の製剤は、送達したブデソニドの量の1.25,1.4、2.1、3.3、3.67、1.25〜3.7、または1.25〜4倍の増加を示す。試験条件下で、AIRSEP MYSTIQUEはSAE−CD/ブデソニド製剤を放出/噴霧するのに最も効率的であった。
特に明記しない限り、有効用量を含むと当然理解される「用量」なる用語は、名目用量、放出用量、名目利用用量、被験者への用量、肺への用量または他の当該技術のこのような用語を意味するものとする。「名目用量」なる用語は、ネブライザーのリザーバに入れられるコルチコステロイド量をいい、ここでリザーバ中の液体の容量はリザーバのサイズによって決定される。「名目利用用量」なる用語は、噴霧により本発明の製剤が投与されたが、しかし製剤が全部投与されない/されなかった場合、被験者に利用されることになるかまたは利用された筈のコルチコステロイド量を指す。「放出用量」なる用語は、ネブライザーから放出されたコルチコステロイド量を指す。「被験者への用量」なる用語は、本発明の製剤を噴霧により投与後、被験者に送達され保持されたコルチコステロイド量を指す。「肺への用量」なる用語は、本発明の製剤を噴霧により投与後、被験者の肺に送達されそして保持されたコルチコステロイド量を指す。
一般に、コルチコステロイドの単回使用の懸濁液ベースの単位投与製剤は、液体担体約50μl〜10ml中に懸濁されたコルチコステロイド約0.125、0.25、0.5、1、2、または約0.125〜約2mgを含む。それとは別に、コルチコステロイドは、懸濁液1ml当たりコルチコステロイドの約20mcg〜約30mgの濃度で存在する。その結果、SAE−CDの約10〜500mg、またはSAE−CDの10〜250mg、またはSAE−CDの10〜300mgを、固体形態であるにせよ、液体担体に溶解されているにせよ、各懸濁液1mL当りで加え、それによってコルチコステロイドの相当部分を溶解し、噴霧可能単位投与液体製剤を形成し、その後これを被験者に投与する。
本製剤、方法またはシステムでは、コルチコステロイドの約1μg〜20mg、または1μg〜10mg、0.01mg〜10mg、0.025mg〜10mg、0.05mg〜5mg、0.1mg〜5mg、0.125mg〜5mg、0.25mg〜5mg、0.5mg〜5mg、0.05mg〜2mg、0.1mg〜2mg、0.125mg〜2mg、0.25mg〜2mg、0.5mg〜2mgの用量を使用することができる。これらの用量は本発明のコルチコステロイド、特にフルニソリドと同等の親油性かまたはそれよりも高い親油性のコルチコステロイドに適しており、そのコルチコステロイドとしては、ベクロメタゾン、ジプロピオン酸ベクロメタゾン、モノプロピオン酸ベクロメタゾン、ブデソニド、シクレソニド、デスイソブチリル−シクレソニド、フルニソリド、フルチカゾン、プロピオン酸フルチカゾン、モメタゾン、フランカルボン酸モメタゾン、トリアムシノロンアセトニドが含まれる。
本発明の製剤は、10μl〜100ml、50μl〜50ml、50μl〜10ml、0.1〜10ml、0.1ml〜10ml未満、0.1ml〜7.5ml、0.1ml〜5ml、0.1ml〜3ml、0.1ml〜2ml、0.1ml〜1ml、0.05ml〜7.5ml、0.05ml〜5ml、0.05ml〜3ml、0.05ml〜2ml、又は0.05ml〜1mlの近似溶液体積のコルチコステロイドの1回用量を含む。
コルチコステロイド間で利用可能な広範囲のネブライザーリザーバ体積及び広範囲に変化する所要用量に因り、本発明の製剤は、0.01ml〜100mlの溶液体積中に1μg〜20mgのコルチコステロイドを含むことができる。
一般に、コルチコステロイドの複数回使用する懸濁液ベースの単位投与製剤は、液体担体1から100ml中に懸濁されたコルチコステロイド約0.125から約2mgを含む。複数回使用する製剤は、実際には、コルチコステロイドの2つ以上の単位投与剤を含む。単回の単位投与アリコートを複数回使用する単位投与製剤から取り出し、その単回の単位投与剤を典型的には1つずつ被験者に投与する。その結果、SAE−CD約10から500mgを、固体形態であるにせよ、液体担体に溶解されているにせよ、各懸濁液1ml当りで、それによってコルチコステロイドの相当部分を溶解し、複数回使用する単位投与液体製剤を形成し、その後これを単回の単位用量アリコートで被験者に投与する。
本発明の1つの側面は、懸濁液ベースの単位投与製剤が、被験者に(噴霧化されたミストで)経肺吸入投与する前に液体単位投与製剤に転換されることである。この転換は、懸濁液が用意される同じ容器内で、または異なる容器内で、またはネブライザーのリザーバ内で行うことができる。液体製剤を形成するために、コルチコステロイドの相当部分を溶解しなければならない。溶解されたコルチコステロイドの量に関連して使用されるように、「相当部分」は、コルチコステロイドの少なくとも20質量%、少なくとも30質量%、少なくとも40質量%、または少なくとも20質量%、および50質量%未満である。溶解されたコルチコステロイドの量に関連して使用されるように、「大部分」は、コルチコステロイドの少なくとも50質量%である。
調剤薬局に勤めている薬剤師は、コルチコステロイドを含む懸濁液ベースの単位投与製剤を調製することができ、また調製することはよく知られている。このような薬剤師は、本明細書で説明されている方法を採用することにより単回使用の、または複数回使用の液体単位投与製剤を調製することができる。それとは別に、コルチコステロイド治療を受ける被験者(患者)は、本明細書で説明されている方法を採用することにより懸濁液ベースの製剤を本発明の液体製剤に転換することができる。薬局で懸濁液から液体製剤を調製する代わりに、懸濁液製剤およびSAE−CDを含むキットを用意することができる。
溶液中のSAE−CDの濃度は、質量対質量または質量対体積に基づいて表すことができるが、これら2つの単位は、相互交換できる。公知の質量のシクロデキストリンが公知の質量の水の中に溶解された場合、%w/wシクロデキストリン濃度は、グラム単位のシクロデキストリンの質量を同様の単位の総質量(シクロデキストリン+水の質量)で除算し、100を掛けることにより決定される。公知の質量のシクロデキストリンが公知の全体積に溶解された場合、%w/vシクロデキストリン濃度は、グラム単位のシクロデキストリンの質量をミリリットル単位の全体積で除算し、100を掛けることにより決定される。2つのシクロデキストリン濃度百分率の間の相関関係は、さまざまな%w/wシクロデキストリン溶液を調製し、25℃で比重瓶を使ってそれぞれの密度を測定することにより実験的に決定された。それぞれの%w/w CAPTISOL溶液の密度(g/mL)は以下の表に示されている。
その結果の直線的関係から、%w/wで表されているCAPTISOL濃度を、式:
%w/v=((%w/w×勾配)+y−切片)* %w/w
により%w/vで表された濃度に容易に変換することができるが、ただし、勾配および切片の値は、表の中の密度データの直線回帰から決定される。例えば、上記の式を使用することにより、40%w/wのCAPTISOL溶液は、約48.3%w/vのCAPTISOL溶液に相当する。
%w/v=((%w/w×勾配)+y−切片)* %w/w
により%w/vで表された濃度に容易に変換することができるが、ただし、勾配および切片の値は、表の中の密度データの直線回帰から決定される。例えば、上記の式を使用することにより、40%w/wのCAPTISOL溶液は、約48.3%w/vのCAPTISOL溶液に相当する。
ネブライザーにおける本発明の吸入可能溶液の性能は、リザーバ内の溶液、噴霧溶液の粘度に左右される場合がある。SBE7−β−CDの水溶液の粘度は、上の表に近似的に示されているように濃度に関して変化する。吸入可能組成物の粘度は、ネブライザーから放出される噴霧組成物の割合、噴霧化コルチコステロイドのアウトプット率、および液滴サイズ分布に影響を及ぼす可能性がある。
ネブライザーのリザーバ内に残されている残留噴霧吸入可能組成物の量は、ブデソニド含有懸濁液の場合よりもSAE−CDを含む溶液の場合のほうが大きい場合がある。例えば、図4は、4つの異なる噴霧組成物(PULMICORT RESPULES懸濁液、5%w/w SBE7−β−CD溶液、10%w/w SBE7−β−CD溶液、および20%w/w SBE7−β−CD溶液)のそれぞれに対し3つの異なるネブライザー(PARI LC PLUS、HUDSON UPDRAFT II NEB−U−MIST、およびMYSTIQUE)から放出される噴霧組成物の推定パーセンテージのグラフである。PULMICORT RESPULES懸濁液は、対照として使用された。PARI LC PLUS、MYSTIQUE、およびHUDSONネブライザーは、この比較のために使用された。MYSTIQUEネブライザーは、懸濁液および濃縮SAE−CD溶液(20%w/w)を効率よく噴霧化することができず、そのネブライザーでは評価されなかった。これらの結果から、試験された条件の下で、PULMICORT RESPULES懸濁液を噴霧すると、噴霧化される組成物の割合が多くなる、すなわち懸濁液の場合、溶液の場合と比べて噴霧の完了後にネブライザーのリザーバに噴霧組成物はあまり残っていないことが示唆される。場合によっては、懸濁液を噴霧することで、ネブライザーにより放出される全組成物は最大質量%になった。すなわち、類似の噴霧条件の下で、PARI LC PLUSおよびHUDSONネブライザーは、噴霧溶液よりも効率的に噴霧懸濁液の体積を減らしているが、これは、ネブライザーにより放出される薬剤の総量に対応しなかったということである。
それぞれブデソニドを含む、SAE−CD噴霧溶液のアウトプット率と懸濁液のアウトプット率を比較した。実施例10の方法の修正バージョンに従って、アウトプット率を決定した。以下の表は、観察されたデータをまとめたものである。
上記の製剤はすべて、ブデソニド約250μg/mLを含む。「P5C」と示されている試料は、SBE7−β−CD 50mg/mL(または約5%)を含んでいる。
以下の表は、SAE−CDのさまざまなレベルを含む溶液に対するネブライザーアウトプット率を示している。
驚いたことに、SAE−CD含有溶液の噴霧化により、ネブライザーが放出する懸濁液の総量が多かったとしてもブデソニドのアウトプット率は、PULMICORT RESPULES懸濁液の噴霧化よりも高かった。特定のメカニズムへの束縛を受けるものではないが、ネブライザーは懸濁液の粒子よりもむしろ懸濁液の水を噴霧化し、それにより、リザーバ内の懸濁液中のブデソニドのモル濃度が高まるものと考えられる。SAE−CD濃度が25%w/vを超えて高いほど、いったん粘度がほぼ上限を超えると、噴霧時間はわずかに長くなり、アウトプット率は低下した。
特定のメカニズムに束縛を受けることなしに、ネブライザーは、懸濁液の粒子よりむしろ懸濁液の水(上清)を優先的に噴霧し、その結果リザーバの懸濁液中のブデソニドのモル濃度の増加を引き起こすと考えられる。コルチコステロイドは本発明の溶液に溶解するので、このタイプの分離は有意な度合いで起こることはない。結果として、リザーバ内のコルチコステロイドの濃度の増加率は、溶液では懸濁液中よりも低い。この現象の更なる裏づけは、以下の表で詳述される。
上記データは、PARI PROBEB ULTRA空気圧縮機を装備したPARI LCを用いて、本発明の溶液(CEB、SAE−CD、5%wt./v、2ml;ブデソニド、250μg/ml)およびPULMICORT RESPULES懸濁液2ml;ブデソニド、250μg/ml)の溶液の噴霧を比較することによって得られた。リザーバ内のブデソニドの濃度は2分でおよびスパッターの時間で測定した(TTS)。次いで、リザーバ内の溶液のコルチコステロイド濃度の増加率(RIC)を、各時間間隔にわたって各製剤で算出した。本発明の溶液のRICは2分にわたって約48%のRICの減少を、そしてTTSにわたって約42%のRICの減少を示した。幾つかの実施態様では、RICの減少パーセントは、10%〜60%、15%〜60%、20%〜60%、30%〜60%、または40%〜60%まで及ぶ。幾つかの実施態様では、システムは、操作/噴霧の分当たり溶液体積のコルチコステロイド/mLの0〜40、1〜40、5〜30、または10〜30mcgのRICをもたらすことが可能である。
したがって、本発明は、リザーバを含むネブライザー、ならびにSAE−CDを含む吸入可能な水性組成物およびコルチコステロイドの1回投与量:を含む噴霧によるコルチコステロイドの投与のシステムを提供し、ここで、システムは、ほぼ同量のコルチコステロイドおよびほぼ同条件下に操作された水性組成物の体積を含む懸濁液によって与えられたRICに比べて、リザーバ内のコルチコステロイドのRICの低下を与える。
上のデータに基づき、21.5±5%w/wのSBE7−β−CD濃度は、試験されたネブライザーの近似的な高い方の許容レベルであると同定されたが、ただし「許容」は、噴霧時間およびアウトプット率に悪影響を及ぼす可能性のある、過剰な粘度を発生することなく使用できるSBE7−β−CDの高い方の濃度と定義される。SAE−CDの濃度に対する実用上の上限は、ネブライザーの形式により変動する。ネブライザーで使用する液体製剤中のSAE−CDの許容上限濃度は、誘導体のDS、スルホアルキル官能基のアルキル鎖の長さ、および/またはSAE−CDのCD環の大きさによって変動する場合がある。
気道への投与、特に肺への投与では、ネブライザーを使用して、適切なサイズの液滴を生成させる。典型的には、ネブライザーにより吸入用に生成される液滴の粒径は、約0.5から約5ミクロンまでの範囲である。液滴が気道の下側領域、すなわち肺胞および終末細気管支に到達するのが望まれる場合、粒径範囲は、約0.5から約2.5ミクロンであってよい。液滴が上気道に到達するのが望まれる場合、粒径範囲は、2.5ミクロンから5ミクロンであってよい。
上述のように、噴霧組成物の粘度は、液滴サイズおよび液滴サイズ分布に影響を及ぼす可能性がある。例えば、本発明の製剤は、ブデソニドが存在しない場合にSAE−CDのより低い濃度で、したがって、より低い粘度で、Dv50に関してより大きな液滴を形成する傾向がある。図5a〜5bは、PARI LC PLUSネブライザーでの吸入可能組成物の噴霧に対する液滴サイズデータを示している。図のそれぞれについて、MALVERNレーザー光散乱装置(Mastersizer S、Malvern Instruments Ltd.Malvern、英国ウスターシャー州)を使用して、MMADを測定した。図5aは、ブデソニドが存在しない場合のさまざまな濃度(5%w/v、10%w/v、および20%w/v)のγ−CD溶液を使用して得られた結果を示している。これらの結果から、γ−CDはそのままでは、ネブライザー内で許容できる挙動を示さないことがわかるが、それは、溶液の集まり(mass)のほとんどすべてが、許容できない液滴サイズ範囲にあるからである。ネブライザーにより大幅なリサイクルおよび液滴サイズ選択を行ったとしても、コルチコステロイドを含むγ−CDベースの噴霧溶液は、適切な液滴サイズ範囲にある集まりの割合が低いため、特に、γ−CDが試験される濃度でブデソニドの有効な可溶化剤でないので、きわめて長い投薬期間を要することになる。
対照的に、図5bは、PULMICORT RESPULES懸濁液または異なる濃度(5%w/v、10%w/v、および20%w/v)のSAE−CDを含む改変されたPULMICORT RESPULES溶液と共に同じネブライザーを使用して得られた結果を示している。これらの試料のそれぞれで、噴霧化された集まりの大半は、呼吸可能なサイズ範囲にある。さらに、SAE−CDを含む溶液は、明らかに、サイズの面で噴霧懸濁液に匹敵する液滴を形成する。
図6は、PULMICORT RESPULES懸濁液または異なる濃度(5%w/v、10%w/v、および20% w/v)のSAE−CDを含む溶液を充填したHUDSON UPDRAFT II NEBUMISTネブライザーを使った吸入可能組成物の噴霧に関する液滴サイズデータを示している。PARI LC PLUSネブライザーと比較して、NEB−U−MISTは、少し大きな粒径分布を形成し、噴霧集まりのかなりの部分がまだ適切なサイズ範囲にある。したがって、懸濁液から作られ、SAE−CDを含む噴霧溶液は、さまざまな異なる空気駆動ジェット式ネブライザーで使用するのに適している。
PULMICORT RESPULES懸濁液の説明書には、この懸濁液は超音波ネブライザーで噴霧してはならないと記載されている。図7は、MYSTIQUE超音波ネブライザーでの吸入可能組成物の噴霧についての液滴サイズデータを示している。これらの組成物は、3つの異なるSAE−CD含有溶液を含む。懸濁液とは異なり、SAE−CD含有溶液は、超音波ネブライザーで噴霧できる。そこで、本発明は、超音波ネブライザーから懸濁液ベースの単位投与製剤中のコルチコステロイドの経肺投与を改善する方法を提供し、この方法は、懸濁液ベースの単位投与製剤中の未溶解コルチコステロイドの量を減らすのに十分な量でSAE−CDを製剤に含める工程を含む。
ネブライザー全般に亘る噴霧組成物の性能は、典型的には、それぞれの組成物についての液滴サイズ分布のDv50を比較することにより比較される。図8は、上述の3つのネブライザーでの吸入可能組成物の噴霧についての比較Dv50液滴サイズデータを示している。それぞれの場合において、SAE−CD含有溶液は、濃度範囲に亘って噴霧投与に適している。さらに、液滴サイズ分布は、SAE−CDの濃度を調整することにより部分的に制御することができる。
図9は、特定のセットアップに異なる圧縮空気源を必要とするさまざまな異なるネブライザー、RAINDROP−Rat、RAINDROP−Dog、PARI LC STAR−UNC、PARI LC STAR−Rat PARI LC PLUS、およびDEVILBISS PULMO AIDE空気駆動ジェット式ネブライザーにおけるSAE−CDの濃度とSAE−CDのアウトプット率との関係を示すグラフである。これらのネブライザーは、独立式だけでなく動物曝露室(animal exposure chambers)および/または個人曝露マスク(individual exposure masks)を含むさまざまなセットアップで使用された。一般に、これらのデータから、SAE−CDのアウトプットは、SAE−CD濃度の増大と共に増大することがわかっている。使用されるネブライザー、ネブライザーの操作条件、および溶液中のSAE−CDの濃度に応じて、異なる最高アウトプット率が得られる。例えば、Raindrop−Dogセットアップの最大アウトプット率は、250mg/mL以上のCAPTISOL濃度である。
PULMICORT RESPULES懸濁液の超音波ネブライザー噴霧化が推奨されないとしても、行うことはできる。図10a〜10bは、PULMICORT RESPULES懸濁液および改変したPULMICORT RESPULESベースのSAE−CD溶液のPARI LC PLUSおよびMYSTIQUEネブライザーを使用する噴霧溶液に関する比較液滴サイズデータを示す図である。5%w/v SBE7−β−CDを含む場合と含まない場合のPULMICORT RESPULES懸濁液を試験試料として使用した。実施例12の手順に従った。図10aは、PARI LC PLUS空気駆動ジェット式ネブライザーで放出される溶液のDv10およびDv50データを示しており、図10bは、MYSTIQUE超音波ネブライザーで放出される溶液のDv10およびDv50データを示している。それぞれの場合において、2つの異なる溶液についての液滴サイズデータは比較可能である。しかし、2つの溶液についてのブデソニドアウトプット率は、著しく異なっていた。しかし、噴霧組成物にSAE−CDを使用すると、ネブライザーの形式に関係なくブデソニドのアウトプット率が増大する。そこで、本発明は、ネブライザーにより送達されるコルチコステロイド含有懸濁液ベースの単位用量製剤のアウトプット率を高める方法を提供し、この方法は、改変した製剤を形成するために製剤中に溶解されているコルチコステロイドの量を高めるのに十分な量でSAE−CDを製剤中に含める工程を含み、これにより、改変した製剤に対するコルチコステロイドのアウトプット率は、懸濁液製剤に対するコルチコステロイドのアウトプット率よりも高くなる。
2つの脈動膜ネブライザー(AERONEB GOおよび米国特許第6,962,151号)を、それぞれ実施例21及び22に従って評価し、本発明の溶液で装置の性能を明らかにし、効率的電子ネブライザーにおいてコルチコステロイドの濃縮溶液を用いる有用性を明らかにした。コルチコステロイドの臨床使用に重要な幾つかのインビトロのパラメータを測定し、実施例6に記載の溶液製剤および2mLの市販の参照懸濁液の両方を空気ジェット式ネブライザーにおいてこれらパラメータと比較した。全送達/噴霧時間(エアロゾルの生成がもはや見えなくなるスパッターまでの時間)、MMAD液滴サイズおよび微粒子画分パラメータが、各装置で得られた。カスケードインパクタを各装置のアウトプットに使用して噴霧時の性能を測定し、またインビトロ・エアロゾル・ドラッグ・アウトプットを特性化した。
ブデソニド(500μg/0.5ml)を含む溶液(0.5ml)、CAPTISOL(10%w/v)、水、及びTween80(任意)を用いて、AERONEB GO装置で使用される溶液を、RAINDROP空気ジェットネブライザーと並行比較し、ここで、溶液は以下で詳述するようにブデソニド粒子(RESPULES)の懸濁液にCAPTISOLを添加することによって作製された。各装置において、対照懸濁液ベースの試料はRESPULES懸濁液とした(500μgのブデソニドを含む2ml)。RAINDROPネブライザーには、PARI PRONEB ULTRA圧縮機が装備された。AERONEB GOマイクロポンプネブライザーには、OnQ Aerosol Generatorが装備された。噴霧の停止時(スパッター)でのブデソニドの全アウトプットを定量した。放出用量及び微粒子用量をカスケードインパクタで測定した。‘151特許のネブライザー中の溶液は、ブデソニド、CAPTISOL、水、およびブデソニドの代用マーカーとしてのジエチレントリアミンペンタ酢酸の形態でのテクネチウム99放射標識で構成された。2つの研究のデータは以下の表にまとめられる。
電子脈動膜ネブライザー(AERONEB GOネブライザーおよび‘151特許のネブライザー)を用いることによって、1単位用量のコルチコステロイドの送達は1分以内に完了した。RAINDROPネブライザーは、RESPULESでは丁度5.5分で、また本発明の溶液では丁度5分で1単位用量の送達を完了させた。加えて、脈動膜ネブライザーは、5μ未満の粒子の画分または6μ未満のカットオフ値をもつカスケードインパクタステージの粒子の画分と一般的に定義される、FPFにおいて実質的に大きな割合のコルチコステロイドを送達した。したがって、AERONEB GOの全噴霧時間は、Pari LC+空気ジェット式ネブライザーでスパッターするまでの時間の1/4であった。結果として、処置時間は脈動膜ネブライザーでは、空気ジェット式ネブライザーに比べて短縮し、また脈動膜ネブライザーから放出されたブデソニドの量は空気ジェット式ネブライザーより2から3倍多かった。ネブライザーから排出する薬剤の%(放出用量)は、リザーバ内に初期充填された量の81%であった(名目用量)。それ故に、空気ジェット式ネブライザーによる同じ「被験者への用量」を与えるために、それを必要とする患者を治療するためには脈動膜ネブライザーにはより少量の薬剤を充填すればよい。
エアロゾル液滴サイズは、Malvern Spraytec機器を用いて測定された。脈動膜ネブライザーからのDv10、Dv50、及びDv90は、参照製品(PULMICORT RESPULES)および空気ジェット式ネブライザー中の同じ濃度のCAPTISOL溶液に非常に類似している。これは、製剤が吸入後患者内に類似の分布をする可能性を示唆する。
実施例17による臨床研究が、血漿中のブデソニドの出現によって測定して放射標識液体製剤からブデソニドの肺沈着、及び肺からのブデソニドのクリアランスを比較するために行われた。本発明の溶液製剤は、ブデソニドの懸濁液ベースの製剤と比較された。24時間までの種々の時間に、血漿試料を採取しブデソニドを検定し、種々の薬物動態学的パラメータを測定した。コルチコステロイドの経口吸収は活性炭の投与によってブロックされたことから、血漿中濃度−時間曲線下面積(AUC)は肺へのブデソニドの送達の尺度となる。AUCデータの比較は、各被験者に送達された用量(「被験者への用量」)または各被験者の肺への用量(「肺への用量」)またはネブライザーもしくは装置によって放出された用量(「放出用量」)または噴霧もしくは送達によって得られる用量(「名目用量」または「名目利用用量」または「充填用量」)を検討することによって行われた。AUCデータ(0−t、および0−∞)は、被験者への対応用量によりAUCデータを割ることによって各被験者に送達されたブデソニド(μg)に関して正規化した。本明細書で使用される「被験者への用量」なる用語は、ネブライザーによる投薬サイクルの完了後被験者に送達されるコルチコステロイドの量を意味するものであり、ネブライザーのリザーバ内に初期に存在する薬剤量から、ネブライザーに残留する薬剤、被験者の口から除去された薬剤、および呼気フィルターから収集される量の合計を差し引くことによって算出される。以下の式を、被験者への用量(Ds)の算出に使用することができる:Ds=Drinit−(Dmw+Ddev)、ここで、Drinitはネブライザーのリザーバ内に初期に存在する薬剤量を意味し、Dmwは洗口剤を用いることによって被験者の口から除去される薬剤量を意味し、Ddevは投薬サイクルの完了後装置内に残留する薬剤量を意味する。Ddevなる用語は、投薬の完了後リザーバ内に残留している薬剤、及び投薬の完了後装置の残余に残留している薬剤を意味する。本明細書で使用される「肺への用量」なる用語は、被験者の肺へ送達される薬剤量を意味するものであり、その量は「被験者への用量」の一部である。本実施例で使用される投与パラメータは下記に詳述され、また算術平均に基づいて与えられる。
実施例17の検討から得られた薬物動態学的データは下記にまとめられている。データは、幾何平均または個々の被験者ベースで表される。下表のデータは「被験者への用量」に基づいている。
上記データに基づいて、本発明の製剤は「被験者への用量」に基づき、約60〜65μgのブデソニドを送達する場合ブデソニドの3〜15(または約少なくとも6)(pg*h/ml)/μgの正規化AUCt、約105〜110μgのブデソニドを送達する場合ブデソニドの7〜11(または約少なくとも8)(pg*h/ml)/μgの正規化AUCt、及び約165〜170μgのブデソニドを送達する場合ブデソニドの4〜11(または約少なくとも7)(pg*h/ml)/μgの正規化AUCt、を与える。その上、本発明の製剤は「被験者への用量」に基づいて、約60〜65μgのブデソニドを送達する場合ブデソニドの4〜16(または約少なくとも8)(pg*h/ml)/μgの正規化AUCi、約105〜110μgのブデソニドを送達する場合ブデソニドの8〜12(または約少なくとも10)(pg*h/ml)/μgの正規化AUCi、および約165〜170μgのブデソニドを送達する場合ブデソニドの5〜16(又は約少なくとも10)(pg*h/ml)/μgの正規化AUCi、を与えた。またデータは、「被験者への用量」の幾何平均(μgブデソニド)対AUC(pg*h/ml)の幾何平均のグラフである、図17、および「肺への用量」の幾何平均(μgブデソニド)対AUC(pg*h/ml)の幾何平均のプロットである、図18にまとめられている。
幾つかの実施態様において、本発明は、スルホアルキルエーテルシクロデキストリンを含む水性液体担体に溶解したコルチコステロイドの少なくとも45μg、少なくとも48μg、45〜1000μg、約1μg〜20mg、約1μg〜10mg、0.01mg〜10mg、0.025mg〜10mg、0.05mg〜5mg、0.1mg〜5mg、0.125mg〜5mg、0.25mg〜5mg、0.5mg〜5mg、0.05mg〜2mg、0.1mg〜2mg、0.125mg〜2mg、0.25mg〜2mg、または0.5mg〜2mgを含む単位用量を噴霧によって被験者に投与することを含み、被験者への用量として送達されたコルチコステロイドの少なくとも6(pg*h/ml)/μgの、被験者へコルチコステロイドの用量で正規化した平均血漿AUCtを被験者に与える方法を含む。
図19は検討の各個別の被験者に対して「被験者への用量」(μgブデソニド)対対応AUC(pg*h/ml)のプロットである。送達した3つの異なる用量を横断するデータから得られた実質的に線形の実線の傾きは、コルチコステロイドを服用する患者に対する用量反応曲線を規定する。結果として、患者が最初の投与量を服用し、またコルチコステロイドのμg当たりの患者のAUCが決定されれば、この傾きは、患者が次の投与量で標的血漿レベルを与える必要がある用量を予測するために使用可能である。この傾きは、データを個々の被験者ベースでみる場合、5.7から16に、さらに具体的には、9から10に及ぶ。
臨床研究の被験者に対するブデソニドの血漿中濃度プロファイルを図20に示す。
この正規化AUCデータ及び関連放射標識分布データは、ブデソニドを懸濁液として投与した場合よりブデソニドを溶液として投与した場合に、被験者に送達された用量の多くはそれを肺へ、そしてそこから全身循環に進ませたことを示す。肺に沈着した等価用量が類似の効能および全身吸収をもたらすと仮定して、これらの結果は、参照懸濁液製品と同じように有効な溶液で投与した場合に、被験者に対して1.6〜5倍または2〜4倍必要とする用量が少ないことを示唆する。それが個体ベースまたは幾何平均ベースのいずれかに関して決定されるかによって、本発明の溶液の投与は、PULMICORT RESPULES懸濁液ベースの水性製剤の投与に比べて、送達されたブデソニドのμg当たりAUCt又はAUCiにおいて1.6倍増加、2.2倍増加、2.5倍増加、5倍増加、1.6〜5倍増加、2〜4倍増加、2〜3.5倍増加、2〜3.3倍増加または少なくとも2倍増加をもたらす。送達されたブデソニドの1μg当たりのAUCtまたはAUCiは、個体毎に変動することが認められ、その値は幾人かの個体では上記の値よりも高く、またその他の個体では上記の値よりも低かった。
下に挙げた表中のデータは、検討中に測定または決定された種々の異なる用量に基づくものであり、そして名目上有効用量、肺への用量、被験者への用量、又は放出用量に基づいて非正規化又は正規化されたCmax薬物動態学的プロファイルパラメータの強化のレベル(要素)をまとめている。
上記の表により、本発明の製剤及びシステムは、用量非正規化に基づいて90〜900、200〜600、200〜550、200〜250、400〜450、500〜600、225、437、または545のCmax(pg/ml)を与えることができる。本発明の製剤及びシステムは、以下の用量正規化Cmax(pg/ml/μg):1)0.3〜2、0.35〜2、0.6〜1.5、0.5〜1.2、0.8〜1、0.8〜0.9、0.7〜0.8、0.4、1.9、0.6、1.5、0.5、1.2、0.35、2、0.7、0.8、または0.9を名目利用用量正規化ベースに関して;2)3.4〜9.2、3.5〜8.5、5.5〜9.2、4.5〜7.5、5.8〜7、3.4、3.5、4.5、5.5、9.2、8.5、7.5、5.8、5.9、6、または7を肺への用量正規化ベースに関して;3)1.7〜7.5、3.2〜4.1、1.9〜6、3.2〜7.5、1.7〜5.2、3.6、4.1、3.2、1.9、6、3.2、7.4、7.5、1.7、5.2または5.3を被験者への用量正規化ベースに関して;4)0.9〜3.3、1.7〜2.2、0.9〜3、1〜3、1.7〜3.3、1〜2.7、1.9、2.1、2.2、1.7、0.9、1、2、3、2.9、3.2、3.3、または2.7を放出用量正規化ベースに関して、与えることができる。
本発明の溶液は、懸濁液ベースの製剤に勝る薬物動態学的プロファイルの強化をもたらす。コルチコステロイドの非正規化用量に基づいて、コルチコステロイド溶液によって与えられたCmaxは、溶液及び懸濁液中のコルチコステロイドの用量が充填されたのとほぼ同量の場合、懸濁液ベースの製剤によって与えられたCmaxよりも1.6〜2、1.5〜3、1.5〜2.5、1.5〜2、1.5、1.6、2、2.5、または3倍高い。コルチコステロイドの名目利用用量正規化に基づいて、コルチコステロイド製剤によって与えられたCmaxは、懸濁液ベースの製剤によって与えられたCmaxよりも、1.8〜6.2、1.5〜6.5、2〜6.5、1.5〜5.5、2〜4、1.5〜4、1.5〜3、2.7、3.3、3.4、1.5、6.5、2、5.5、4、または3倍高い。コルチコステロイドの肺への用量正規化に基づいて、コルチコステロイド溶液によって与えられたCmaxは、懸濁液ベースの製剤によって与えられたCmaxよりも、1.4〜4.3、1.4〜4.5、1.5〜4.5、1.5〜3.5、1.5〜3、1.4〜3、1.5〜2.5、1.5〜2、2、2.3、1.4、4.5、3.5、3、1.5または2.5倍高い。コルチコステロイドの被験者への用量正規化に基づいて、コルチコステロイド溶液によって与えられたCmaxは、懸濁液ベースの製剤によって与えられたCmaxよりも、2〜3.5、2〜5、1.7〜3.8、1.7〜5、2.7、3、2.4、2、3.5、5、1.7、または3.8倍高い。コルチコステロイドの放出用量正規化に基づいて、コルチコステロイド製剤によって与えられたCmaxが、懸濁液ベースの製剤によって与えられたCmaxよりも、1.9〜6.3、1.75〜6.5、2.2〜4.2、2.2〜6.3、1.9〜4.2、3.2、3.5、3.6、2.8、1.75、6.5、2.2、4.2、または6.3倍高い。
あるいは、コルチコステロイド溶液によって与えられたCmaxが、溶液のコルチコステロイドの用量が懸濁液の用量より約2倍低い場合、懸濁液ベースの製剤によって与えられたCmaxよりも少なくとも1.5、1.6、2、2.6、および3倍高い。
下に掲げた表中のデータは、検討中に測定または決定された種々の異なる用量に基づくものであり、そして非正規化または名目利用用量、肺への用量、被験者への用量、または放出用量に基づいて正規化された薬物動態学的プロファイルパラメータAUCinfの強化のレベル(要素)をまとめている。
上記の表によれば、本発明の製剤およびシステムは、用量非正規化ベースに関し500〜1700、530〜1650、250〜2500、280〜1300、780〜1300、980〜2450、275、775、980、2400、2500、1300、1290、530,1650、250、280または780のAUCinf(pg*h/ml)を与えることができる。本発明の製剤及びシステムは、以下の用量正規化AUCinf(pg/ml/μg):1)1〜5.5、2〜2.2、1〜5.3、1.1〜5.2、1.5〜2.6、1.3〜3.3、2、2.1、2.2、1、5.5、5.3、5.2、1.5、2.6、1.3、または3.3を名目利用用量正規化ベースに関し;2)10〜25、14〜18、10.2〜20、13.6〜18.8、11.2〜24.7、10.2、20、13.6、14、19、18.8、11、11.2、25、24.7、14.2、16.2、17.3を肺への用量正規化ベースに関し;3)4〜16、4.2〜16.1、8〜12.2、5.4〜16.5、5.4〜17、8.5〜9.6、8.5、9.5、9.6、4.2、16.1、8、12.2、12、5.4、16、17、または16.5を被験者への用量正規化ベースに関し;4)2.5〜9、2.6〜8.5、4.5〜5.1、2.5〜8、2.6〜7.9、4.2〜6.7、3.1〜8.5、3.2〜8.5、4.5、4.6、5、5.1、2.5、2.6、4.2、3.1、9、8.5、5.1、8、7.9、または6.7を放出用量正規化ベースに関し、与えることができる。
したがって、本発明の溶液は、懸濁液ベースの製剤にまさる薬物動態学的プロファイルの強化をもたらす。コルチコステロイドの非正規化用量に基づいて、コルチコステロイド溶液によって与えられたAUCinfは、溶液及び懸濁液中のコルチコステロイドの用量がほぼ同量の場合、懸濁液ベースの製剤によって与えられたAUCinfよりも1.6〜2.5、1.6〜3、1.5〜3.5、1.5〜3.3、2.5〜3.3、3.1、1.5、3.3、1.6、または2.5倍高い。コルチコステロイドの名目利用用量に対する正規化に基づいて、コルチコステロイド溶液によって与えられたAUCinfは、懸濁液ベースの製剤によって与えられたAUCinfよりも、1.75〜6.5、1.75〜6.1、2〜6.5、2〜6.1、2〜4.5、2〜4.4、3.3、3.2、3.5、3.4、1.75、6.5、6.1、2、4.5、または4.4倍高い。肺へのコルチコステロイドの用量に対する正規化に基づいて、コルチコステロイド溶液によって与えられたAUCinfは、懸濁液ベースの製剤によって与えられたAUCinfよりも、1.2〜3.5、1.2〜4、1.2〜3、1.2〜2.85、1.5〜3.5、1.4〜3.5、2、2.2、2.3、2.4、1.2、3、4、2.85、1.5、3.5、または1.4倍高い。被験者に対するコルチコステロイドの用量に対する正規化に基づいて、コルチコステロイド溶液によって与えられたAUCinfは、懸濁液ベースの製剤によって与えられたAUCinfよりも、1.6〜4.9、1.5〜5、1.6〜5、1.6〜3.7、1.6〜3.6、2〜4.9、1.9〜4、2、2.6、1.5、5、1.6、3.7、3.6、2、4.9、1.9、または4倍高い。コルチコステロイドの放出用量に対する正規化に基づいて、コルチコステロイド溶液によって与えられたAUCinfは、懸濁液ベースの製剤によって与えられたAUCinfよりも、1.5〜6、1.7〜6、1.9〜6、1.9〜5.4、2.3〜5.8、1.9〜5.5、1.9〜5.8、1.5、6、1.7、1.9、5.4、2.3、5.8、5.8、3.2、3.5、または3.6倍高い。
あるいは、コルチコステロイド溶液によって与えられたAUCinfは、溶液中のコルチコステロイドの用量が懸濁液の用量よりも約2倍低い場合、懸濁液ベースの製剤によって与えられたAUCinfよりも少なくとも1.5、1.6、2、2.5、3、または3.1倍高い。
下に掲げた表中のデータは、検討中に測定または決定された種々の異なる用量に基づくものであり、そして非正規化、または名目利用用量、肺への用量、被験者への用量、または放出用量に基づいて正規化された薬物動態学的プロファイルパラメータAUClastの強化のレベル(要素)をまとめている。
被験者の用量分布の測定(実施例17)が、肺への用量沈着の効率を測定するために行われた。結果は、下表及び図22に詳述されている。
これらのデータは、本発明の溶液の投与が、対照の懸濁液製剤の投与に比べてコルチコステロイドの低い口腔咽頭沈着をもたらしたことを示す。さらに、本製剤は、放出用量に基づきコルチコステロイドの少なくとも20%〜85%、もしくは30%〜80%、または少なくとも30%、少なくとも40%、少なくとも56%、少なくとも59%、少なくとも62質量%の肺沈着をもたらした。肺沈着の割合は、高い吸入性画分および噴霧化ミストの低いMMADを与えることが可能なネブライザーを用いることによってさらに増加し得る。好適なネブライザーとは、超音波式、振動メッシュ、振動円錐、振動板ネブライザーまたは内蔵型ノズルアレイを通して液体製剤を排出するネブライザーである。例えば、Aradigm AERx肺送達システム、AERx EssenceおよびAERx Ultraは特に本発明での使用に好適であり、これは制御用量発現、発生エアロゾル粒子サイズの制御、吸入エアロゾル粒子サイズの制御、及び吸入及び送達方法の管理 (Farr et al.、Drug Delivery Technology、2002年5月、 Vol.2、 No.3、42〜44頁)をもたらすものとして当技術で認識されていると同様である。例えば、PARI eFLOW振動板ネブライザーは、本発明での使用に特に好適であり、これは上記の所望の性能パラメータを与えるものとして当技術で認識されていると同様である(Keller et al.、ATS 99th International Conference、Seattle、2003年5月16〜21日; poster、2727頁)。
本発明の肺投与によって肺へ送達されたコルチコステロイドの全身バイオアベイラビリティの改善に基づいて、本発明の組成物または製剤は、水性懸濁液として投与されたコルチコステロイド等価用量より優れた治療有益性の改善または臨床有益性の改善をもたらすことになる。
実施例30は、本発明のブデソニド溶液及び参照製剤(PULMICORT RESPULES懸濁液)をPari LC空気ジェット式ネブライザーにより噴霧投与した、イヌで行った研究について詳述する。図21に示した結果は、時間の関数としてのブデソニドの平均血漿レベルを表す。溶液製剤のAUC0→8hrは、参照懸濁液製剤よりも1.9倍大きかった。溶液製剤は、また同じ長さの時間で参照製剤よりも1.23倍多いブデソニドを放出した。詳細な結果は、下表にも示される。
上記の表によれば、本発明の製剤及びシステムは、コルチコステロイドの用量非正規化に基づき2000〜3000、2500〜2700、2000、3000、または2600のAUC0−8hr(pg*h/ml)を与えることができる。本発明の製剤およびシステムは、1)充填用量名目正規化計算で2〜3、2.5〜2.7、または2.6;2)放出用量正規化計算で3〜4、3.4〜3.5、または3.4の用量正規化AUCinf(pg/ml/μg)を与えることができる。
本発明の製剤、システム及び方法は、懸濁液ベースのPULMICORT RESPULES製剤よりも高いAUC0−8hrを与えた。コルチコステロイドの正規化名目(充填)用量に基づき、コルチコステロイド溶液によって与えられたAUC0−8hrは、溶液及び懸濁液中のコルチコステロイドの用量がほぼ同一の場合に、懸濁液ベースの製剤によって与えられたAUC0−8hrより少なくとも1.7、1.8、1.9、または2倍高い。コルチコステロイドの放出用量の正規化に基づき、コルチコステロイド溶液によって与えられたAUC0−8hrは、懸濁液ベースの製剤によって与えられたAUC0−8hrより少なくとも1.5、1.6、2倍高い。
上記の表によれば、本発明の製剤及びシステムは、用量非正規化計算で1600〜1800、1650〜1750、または1700のCmax(pg/ml)を与えることができる。本発明の製剤及びシステムは、1)充填用量名目正規化計算で1〜2、1.6〜1.8、または1.7;2)放出用量正規化計算で2〜2.5、または2.2の用量正規化Cmax(pg/ml/μg)を与えることができる。
本発明の製剤、システムおよび方法は、懸濁液ベースのPULMICORT RESPULES製剤で与えたよりも高いCmaxを与えた。コルチコステロイドの正規化名目用量に基づき、コルチコステロイド溶液によって与えられたCmaxは、溶液および懸濁液のコルチコステロイドの用量がほぼ同じ場合、懸濁液ベースの製剤によって与えられたCmaxより少なくとも1.7、1.8、1.9、または2倍高い。コルチコステロイドの
放出用量に対する正規化に基づいて、コルチコステロイド溶液によって与えられたCmaxは、懸濁液ベースの製剤によって与えられたCmaxよりも、1.5、1.6、2倍高い。
放出用量に対する正規化に基づいて、コルチコステロイド溶液によって与えられたCmaxは、懸濁液ベースの製剤によって与えられたCmaxよりも、1.5、1.6、2倍高い。
幾つかの側面において、本発明の方法及び剤形は、従ってコルチコステロイド懸濁液ベースの単位用量を投与する改善法、懸濁液を透明溶液に変換するために十分量のSAE−CDを添加すること、次いで被験者に透明溶液を投与することの工程を含む方法を提供する。その結果、本発明の方法は、初期単位用量の懸濁液製剤に比べて、コルチコステロイドの全送達量の増加ならびに投与速度の増大をもたらす。
本明細書のデータは、また患者の血流に吸収される放出したまたは送達されたコルチコステロイド用量の割合を算出するためにも使用することができる。幾つかの実施態様では、放出用量の20%以上、25%以上、29%以上、35%以上が、患者の血流に吸収され得る。幾つかの実施態様では、被験者への用量の40%以上、50%以上、55%以上が、患者の血流に吸収され得る。幾つかの実施態様では、名目利用用量の10%以上、12%以上、15%以上が、患者の血流に吸収され得る。
本発明で有用なコルチコステロイドは、一般に、糖質コルチコイドおよび鉱質コルチコイドを含む副腎皮質により製造されるステロイド、および抗炎症性を有する天然に生ずるコルチコステロイドの合成類似化合物および誘導体を含む。好適な合成類似化合物は、プロドラッグ、エステル誘導体を含む。本発明の組成物中で使用できるコルチコステロイドの実例は、アルドステロン、ベクロメタゾン、ベタメタゾン、ブデソニド、シクレソニド(Altana Pharma AG)、クロプレドノール、コルチゾン、コルチバゾール、デオキシコルトン(deoxycortone)、デソニド、デスオキシメタゾン、デキサメタゾン、ジフルオロコルトロン、フルクロロロン(fluclorolone)、フルメタゾン、フルニソリド、フルオシノロン、フルオシノニド、フルオコルチンブチル、フルオロコルチゾン、フルオロコルトロン、フルオロメトロン、フルランドレノロン(flurandrenolone)、フルチカゾン、ハルシノニド、ヒドロコルチゾン、イコメタゾン(icomethasone)、メプレドニゾン、メチルプレドニゾロン、モメタゾン、パラメタゾン、プレドニゾロン、プレドニゾン、ロフレポニド、RPR 106541、チクソコルトール(tixocortol)、トリアムシノロン、およびジプロピオン酸ベクロメタゾン(無水物または一水和物)、モノプロピオン酸ベクロメタゾン、デキサメタゾン21−イソニコチネート、プロピオン酸フルチカゾン、イコメタゾンエンブテート(icomethasone enbutate)、チクソコルトール21−ピバレート、およびトリアムシノロンアセトニドなどのそれらのそれぞれの薬剤として許容される誘導体を含む。特に好ましいのは、ジプロピオン酸ベクロメタゾン、ブデソニド、フルニソリド、プロピオン酸フルチカゾン、フランカルボン酸モメタゾン、およびトリアムシノロンアセトニドなどの化合物である。まだ商品化されていないが、本出願の出願以降に商品化される他のコルチコステロイドは、他の形で適当でないと実験により確立されない限り本発明において有用であるとされる。
コルチコステロイドは、Barnesら(Am.J.Respir.Care Med.(1998年)、157、S1〜S53頁)、Miller−Larssonら(Am J.Respir.Crit.Care Med.(2003年)、167、A773頁)、D.E.Magerら(J.Pharm.Sci.(2002年11月)、91(11)、2441〜2451頁)または Schleimer RP、O’Byrne PMO、Szefler SJ、Brattsand R編集、「喘息での吸入ステロイド:気道での最適化効果」、ニューヨーク、Marcel Dekker、2002年、213〜246頁の中の、S.Edsbacker(肺及び気道のコルチコステロイドの取り込み、保持、および生体内変換)によって記載されたそれらの相対的親油性に基づいてグループ分けできる。一般的に、コルチコステロイドの親油性が小さいほど、水性媒体中にそれを溶解するのに要するSAE−CDの量は低下し、そして逆もまた真である。フルニソリドよりも低親油性のコルチコステロイドは、一般的に水性媒体中にコルチコステロイドを溶解するために、10:1より小さいSAE−CD対コルチコステロイドのモル比を必要とする。この群の典型的コルチコステロイドとしては、ヒドロコルチゾン、プレドニゾロン、プレドニゾン、デキサメタゾン、ベタメタゾン、メチルプレドニゾロン、トリアムシノロン、およびフルオコルトロンが含まれる。本発明の幾つかの実施態様は、フルニソリドより小さい親油性のコルチコステロイドを除外する。
フルニソリドと少なくとも同じ親油性かまたはより大きい親油性のコルチコステロイドは、一般的に水性媒体中にコルチコステロイドを溶解するために、10:1より大きいSAE−CD対コルチコステロイドのモル比を必要とする。幾つかの実施態様では、本発明で使用されるコルチコステロイドは、フルニソリドより少なくとも同じ親油性かまたはより大きい親油性を有する。この群の典型的コルチコステロイドとしては、ベクロメタゾン、ジプロピオン酸ベクロメタゾン、モノプロピオン酸ベクロメタゾン、ブデソニド、シクレソニド、デスイソブチリル−シクレソニド、フルニソリド、フルチカゾン、プロピオン酸フルチカゾン、モメタゾン、フランカルボン酸モメタゾン、およびトリアムシノロンアセトニドが含まれる。
吸入可能液体組成物/製剤に使用ためのコルチコステロイドの適合性は、実施例23に詳述する相溶解度結合研究を行うことによって決定できる。相溶解度結合データを用いて、水性液体担体中の種々の量のSAE−CDの存在下にコルチコステロイドの飽和溶解度が測定される。図3に示される相溶解度結合曲線は、γ−CD、HP−β−CDまたはSBE7−β−CDを含む水性液体担体中でのブデソニドの飽和溶解度を示す。グラフ中の相溶解度曲線は、種々の異なる濃度のシクロデキストリンを含有する溶液のコルチコステロイドの飽和溶解度に対する境界を定める。モル相溶解度曲線を使用して、SAE−CD対コルチコステロイドまたはコルチコステロイド対SAE−CDのモル比を種々のコルチコステロイド濃度で測定することができる。例えば、図3の相溶解度曲線下の面積は、コルチコステロイドが水性液体媒体に溶解して実質的に透明な水溶液を与える領域を示す。この領域では、SAE−CDは、コルチコステロイドより過剰モルで、液体担体に存在するコルチコステロイドを可溶化するのに十分な量で存在する。相溶解度曲線で規定される境界は、本発明の組成物または製剤内のコルチコステロイドおよびSAE−CDによって変動する。下表は、試験した条件下で本発明の組成物または製剤中のコルチコステロイドの飽和溶解度を達成するために必要なSAE−CD対コルチコステロイドの最小モル比の要約を示す。
一定量のSAE−CDの存在下におけるコルチコステロイドの飽和溶解度は、コルチコステロイドおよびSAE−CDの同一性によって変動する。下表は、本発明で測定して2つの異なるSAE−CDの不存在下(水性試験媒体中のコルチコステロイドの真の溶解度)、および存在下にリストしたコルチコステロイドの幾つかの溶解度データをまとめている。
上記データは、コルチコステロイドおよびSAE−CDの標的濃度を有する本発明による製剤を調製するために、相溶解度データと組み合わせて使用することができる。したがって、本発明の幾つかの実施態様は、本発明で測定された水でのフルニソリドの固有溶解度(約11×10−5M未満又は約11.3×10−5M未満)に近似の、またはより小さい水での固有溶解度を有するコルチコステロイドを含む。
本発明の組成物または製剤が、特定濃度のSAE−CDの存在下その飽和溶解度までの濃度で水性媒体中に存在するコルチコステロイドで構成され得るものであるとしても、本発明の幾つかの実施態様には、コルチコステロイドがその濃度のSAE−CDの存在下その飽和溶解度より小さい濃度で存在するものが含まれる。コルチコステロイドは、SAE−CDの存在下で測定してその飽和溶解度の95%以下、90%以下、85%以下、80%以下、または50%以下の濃度で存在し得る。一般に、SAE−CDの存在下にその飽和溶解度より小さい濃度でコルチコステロイドを含む溶液を調製することは容易である。
したがって、本発明の製剤または組成物中のSAE−CD対コルチコステロイドのモル比は、コルチコステロイドについての相溶解度結合曲線によって規定されるような、SAE−CDの存在下のコルチコステロイドの飽和溶解度で得られるモル比を超え得る。このような場合、製剤または組成物中のSAE−CD対コルチコステロイドのモル比は、SAE−CDの存在下コルチコステロイドの飽和溶解度でのモル比よりも、少なくとも1%、少なくとも2%、少なくとも5%、少なくとも7.5%、少なくとも10%、少なくとも15%、少なくとも20%、少なくとも25%、少なくとも50%、少なくとも75%、少なくとも100%、又は少なくとも200%大きい。例えば、飽和溶解度でのモル比が約14:1の場合には、組成物又は製剤中のモル比は、少なくとも14.1:1(少なくとも1%より高い)、少なくとも14.3:1(少なくとも2%より高い)、少なくとも14.7:1(少なくとも5%より高い)、少なくとも15.4:1(少なくとも10%より高い)、少なくとも16.1:1(少なくとも15%より高い)、少なくとも16.8:1(少なくとも20%より高い)、少なくとも17.5:1(少なくとも25%より高い)、少なくとも21:1(少なくとも50%より高い)、少なくとも24.5:1(少なくとも75%より高い)、少なくとも28:1(少なくとも100%より高い)、または少なくとも42:1(少なくとも100%より高い)、であり得る。
SAE−CD対コルチコステロイドのモル比の変化は、ネブライザーの全アウトプットに影響を及ぼし得る。PARI LC PLUS空気ジェット式ネブライザーおよび250μg/mlのPULMICORT RESPULESの2ml中に異なる量のSAE−CDを含有する溶液を用いて検討を行なった。各製剤を、これ以上持続気体が肉眼的に見て放出されなくなるまでの間噴霧した。各実験の終わりに、ネブライザーのリザーバに残留したブデソニドの量を測定した。SAE−CD対コルチコステロイドのモル比は、10:1、14:1、及び20:1であった。データは、モル比の増加が、送達されたブデソニドの量の増加およびリザーバに残存するブデソニドの量の減少をもたらしたことを示す。
SAE−CD対コルチコステロイドのモル比の変化は、また、水性媒体中のコルチコステロイドの溶解速度に影響を及ぼし得る。異なる量のSAE−CD、例えば、CAPTISOL、および一定量のプロピオン酸フルチカゾンまたはフランカルボン酸モメタゾンを含有する溶液を入れた容器を有するローラーミキサーで試験を行った。試料は、約30秒間ボルテックサー中SAE−CDを含有する溶液とコルチコステロイドを混合して調製し、次いでローラーミキサーに容器を入れた。アリコートを各容器から経時的に採取し、溶解したコルチコステロイドの量を定量した。用いたSAE−CD対コルチコステロイドのモル比は、10:1、14:1、および20:1であった。データは、モル比の増加がコルチコステロイドの溶解速度の増加をもたらしたことを示す。
コルチコステロイド化合物は、約1μg/mlから約10mg/ml、約10μg/mlから約1mg/ml、または約20μg/mlから約500μg/mlの量で吸入用に設計された最終的な希釈コルチコステロイド組成物中に存在している。例えば、薬剤濃度は、投与される体積に応じて、トリアムシノロンアセトニドについては約30から1000μg/mlの間、ブデソニドについては約50から2000μg/mlの間であってよい。本発明の好ましい方法に従うことによって、比較的高濃度のコルチコステロイドが水溶液ベースの組成物で達成することができる。
同様に、コルチコステロイド化合物は、約10μg/mlから6mg/ml、50μg/mlから約10mg/ml、約100μg/mlから約2mg/ml、または約300μg/mlから約1mg/mlの量で経鼻投与用に設計された最終的な希釈コルチコステロイド組成物中に存在している。例えば、薬剤濃度は、投与される体積に応じて、トリアムシノロンアセトニドでは約250μg/mlから1mg/mlの間または約250μg/mlから6mg/mlの間、そしてブデソニドでは約400μg/mlから1.6mg/mlの間または約250μg/mlから6mg/mlの間であってよい。
肺障害及び洞関連障害の治療用には、希釈コルチコステロイド組成物が本明細書で説明されているように調製される。当該治療用のコルチコステロイドは、好ましくはジプロピオン酸ベクロメタゾン、モノプロピオン酸ベクロメタゾン、ベタメゾン、ブデソニド、シクレソニド、デスイソブチリルシクレソニド、フルニソリド、フルチカゾン、プロピオン酸フルチカゾン、フランカルボン酸フルチカゾン、モメタゾン、フランカルボン酸モメタゾン、またはトリアムシノロンアセトニドであり、本明細書に記載の濃度で製剤化される。コルチコステロイドの1日用量は、薬剤と疾患に依存するが「Physician’s Desk Reference」(PDR)に従い、一般に約0.05から10mgである。しかしながら、本発明の溶液として投与する場合のコルチコステロイドのバイオアベイラビリティの改善の観点から、所望の臨床エンドポイント、臨床的有益性または治療的有益性を達成するために必要な用量は、PDRに示される対応用量よりも低くてよい。
また、ブデソニドの1単位用量は、米国特許第6,598,603号および第6,899,099号に提示のように、1日1回、隔日に1回、週1回、毎月1回、またはそれ以下の頻度で投与することができ、ここで1用量が0.05〜2.0mgまたは0.25〜1.0mgのブデソニドを含む。投与は昼間および/または夜間であってよい。ブデソニド、又はコルチコステロイドの1用量は、1日当たり2回、3回もしくは多数回、または必要に応じて投与してもよい。
幾つかの実施態様では、1用量は、ブデソニドの1μg〜20mg、0.01mg〜10mg、0.025mg〜10mg、0.05mg〜5mg、0.1mg〜5mg、0.125mg〜5mg、0.25mg〜5mg、0.5mg〜5mg、0.05mg〜2mg、0.1mg〜2mg、0.125mg〜2mg、0.25mg〜2mg、0.5mg〜2mg、1μg、10μg、25μg、50μg、100μg、125μg、200μg、250μg、25〜66μg、48〜81μg、73〜125μg、40μg、64μg、95μg、35〜95μg、25〜125μg、60〜170μg、110μg、170μg、45〜220μg、45〜85μg、48〜82μg、85〜160μg、140〜220μg、120〜325μg、205μg、320μg、325μg、90〜400μg、95〜170μg、165〜275μg、または275〜400μgを含み、上記用量は名目用量、名目利用用量、放出用量、送達用量、被験者への用量、または肺への用量であり得る。
コルチコステロイドは、中性、イオン、塩、塩基性、酸性、天然、合成、ジアステレオマー、異性体、鏡像体純度、ラセミ化合物、溶媒和物、無水物、水和物、キレート、誘導体、類似物、エステル化、非エステル化、または他の一般的な形態で存在しうる。活性物質が本明細書で指定されている場合はいつでも、そのような利用可能なすべての形態が含まれる。例えば、ブデソニドの公知のすべての形態は、本発明の範囲内にあると考えられる。
本発明の製剤は、2つまたはそれ以上の異なる活性物質(有効成分、治療薬など)を送達するために使用することができる。活性物質の特定の組み合わせを、本発明の製剤により提供できる。活性物質のいくつかの組み合わせとしては、1)第1の治療クラスからの第1の薬剤、および同じ治療クラスからの異なる第2の薬剤、2)第1の治療クラスからの第1の薬剤、および異なる治療クラスからの異なる第2の薬剤、3)第1の種類の生物活性を有する第1の薬剤、およびほぼ同じ生物活性を有する異なる第2の薬剤、4)第1の種類の生物活性を有する第1の薬剤、および異なる第2の種類の生物活性を有する異なる第2の薬剤を含む。活性物質の例示的な組み合わせは、本明細書で説明されている。
ブデソニドなどのコルチコステロイドは、1つまたはそれ以上の他の薬剤(有効成分、治療薬、活性物質など、これらの用語は特に明記しない限り本明細書中において交換可能に使用される)と組み合わせて投与することができる。このような他の薬剤は、β2アドレナリン受容体アゴニスト、局所麻酔剤、D2受容体アゴニスト、抗コリン剤を含む。
本発明で提供される組成物と組み合わせて使用するβ2−アドレナリン受容体アゴニストは、限定はされないが、アルブテロール(α1−(((1,1−ジメチルエチル)アミノ)メチル)−4−ヒドロキシ−1,3−ベンゼンジメタノール);バンブテロール(ジメチルカルバミン酸5−(2−((1,1−ジメチルエチル)アミノ)−1−ヒドロキシエチル)−1,3−フェニレンエステル);ビトルテロール(4−メチル安息香酸4−(2−((1,1−ジメチルエチル)アミノ)−1−ヒドロキシエチル)−1,2−フェニレンエステル);ブロキサテロール(3−ブロモ−α−(((1,1−ジメチルエチル)アミノ)メチル)−5−イソオキサゾールメタノール);イソプロテレノール(4−(1−ヒドロキシ−2−((1−メチルエチル−)アミノ)エチル)−1,2−ベンゼン−ジオール);トリメトキノール(1,2,3,4−テトラヒドロ−1−((3,4,5−トリメトキシフェニル)−メチル)−6,7−イソキノリンジオール);クレンブテロール(4−アミノ−3,5−ジクロロ−α−(((1,1−ジメチルエチル)アミノ)メチル)ベンゼンメタノール);フェノテロール(5−(1−ヒドロキシ−2−((2−(4−ヒドロキシフェニル)−1−メチルエチル)アミノ)エチル)−1,3−ベンゼンジオール);ホルモテロール(2−ヒドロキシ−5−((1RS)−1−ヒドロキシ−2−(((1RS)−2−(p−メトキシフェニル)−1−メチルエチル)アミノ)エチル)ホルムアニリド);(R,R)−ホルモテロール;デスホルモテロール((R,R)または(S,S)−3−アミノ−4−ヒドロキシ−α−(((2−(4−メトキシフェニル)−1−メチル−エチル)アミノ)メチル)ベンゼンメタノール);ヘキソプレナリン(4,4’−(1,6−ヘキサン−ジイル)−ビス(イミノ(1−ヒドロキシ−2,1−エタンジイル)))ビス−1,2−ベンゼンジオール);イソエタリン(4−(1−ヒドロキシ−2−((1−メチルエチル)アミノ)ブチル)−1,2−ベンゼンジオール);イソプレナリン(4−(1−ヒドロキシ−2−((1−メチルエチル)アミノ)エチル)−1,2−ベンゼンジオール);メタ−プロテレノール(5−(1−ヒドロキシ−2−((1−メチルエチル)アミノ)エチル)−1,3−ベンゼンジオール);ピクメテロール(4−アミノ−3,5−ジクロロ−α−(((6−(2−(2−ピリジニル)エトキシ)ヘキシル)−アミノ)メチル)ベンゼンメタノール);ピルブテロール(α6−(((1,1−ジメチルエチル)−アミノ)メチル)−3−ヒドロキシ−2,6−ピリジンメタノール);プロカテロール(((R*,S*)−(±)−8−ヒドロキシ−5−(1−ヒドロキシ−2−((1−メチルエチル)アミノ)ブチル)−2(1H)−キノリン−オン);レプロテロール((7−(3−((2−(3,5−ジヒドロキシフェニル)−2−ヒドロキシエチル)アミノ)−プロピル)−3,7−ジヒドロ−1,3−ジメチル−1H−プリン−2,6−ジオン);リミテロール(4−(ヒドロキシ−2−ピペリジニルメチル)−1,2−ベンゼンジオール);サルブタモール((±)−α1−(((1,1−ジメチルエチル)アミノ)メチル)−4−ヒドロキシ−1,3−ベンゼンジメタノール);(R)−サルブタモール;サルメテロール((±)−4−ヒドロキシ−α1−(((6−(4−フェニルブトキシ)ヘキシル)−アミノ)メチル)−1,3−ベンゼンジメタノール);(R)−サルメテロール;テルブタリン(5−(2−((1,1−ジメチルエチル)アミノ)−1−ヒドロキシエチル)−1,3−ベンゼンジオール);ツロブテロール(2−クロロ−α−(((1,1−ジメチルエチル)アミノ)メチル)ベンゼンメタノール);およびTA−2005(8−ヒドロキシ−5−((1R)−1−ヒドロキシ−2−(N−((1R)−2−(4−メトキシフェニル)−1−メチルエチル)アミノ)エチル)カルボスチリル塩酸塩)を含む。
ドーパミンD2受容体アゴニストは、限定はされないが、アポモルヒネ((r)−5,6,6a,7−テトラヒドロ−6−メチル−4H−ジベンゾ[de,glキノリン−10,11−ジオール];ブロモクリプチン((5’α)−2−ブロモ−12’−ヒドロキシ−2’−(1−メチルエチル)−5’−(2−メチルプロピル)エルゴタマン−3’,6’,18−トリオン);カベルゴリン((8β)−N−(3−(ジメチルアミノ)プロピル)−N−((エチルアミノ)カルボニル)−6−(2−プロペニル)エルゴリン−8−カルボキサミド);リスリド(N’−((8−α−)−9,10−ジデヒドロ−6−メチルエルゴリン−8−イル)−N,N−ジエチル尿素);ペルゴリド((8−β−)−8−((メチルチオ)メチル)−6−プロピルエルゴリン);レボドーパ(3−ヒドロキシ−L−チロシン);プラミペキソール((s)−4,5,6,7−テトラヒドロ−N6−プロピル−2,6−ベンゾチアゾールジアミン);塩酸キンピロール(trans−(−)−4aR−4,4a,5,6,7,8,8a,9−オクタヒドロ−5−プロピル−1H−ピラゾロ[3,4−g]キノリン塩酸塩);ロピニロール(4−(2−(ジプロピルアミノ)エチル)−1,3−ジヒドロ−2H−インドール−2−オン);およびタリペキソール(5,6,7,8−テトラヒドロ−6−(2−プロペニル)−4H−チアゾロ[4,5−d]アゼピン−2−アミン)を含む。本発明で使用する他のドーパミンD2受容体アゴニストは、国際特許出願公開WO99/36095で開示されており、その関連する開示は、参照により本明細書に組み込まれる。
本発明で使用する抗コリン剤は、限定はされないが、臭化イプラトロピウム、臭化オキシトロピウム、硝酸メチルアトロピン、硫酸アトロピン、イプラトロピウム、ベラドンナエキス、スコポラミン、臭化メチルスコポラミン、臭化メチルホマトロピン、ヒヨスチアミン、イソプリオプラミド(isopriopramide)、オルフェナドリン、塩化ベンザルコニウム、臭化チオトロピウム、および臭化グリコピロニウムを含む。いくつかの実施態様では、組成物は、約5μg/mLから約5mg/mL、または約50μg/mLから約200μg/mLの濃度の臭化イプラトロピウムまたは臭化チオトロピウムなどの抗コリン剤を含む。他の実施態様では、本発明の方法で使用する組成物は、約83μg/mLまたは約167μg/mLの濃度の臭化イプラトロピウムおよび臭化チオトロピウムを含む、抗コリン剤を含む。
本発明において併用療法で使用する他の有効成分は、限定はされないが、米国特許第5,668,110号、第5,683,983号、第5,677,280号、第6,071,910号、第5,654,276号(関連する開示は参照により本明細書に組み込まれる)で開示されたものなどのIL−5阻害剤、米国特許第6,136,603号(関連する開示は参照により本明細書に組み込まれる)で開示されたものなどのIL−5のアンチセンス調節剤(antisense modulators)、ミルリノン(1,6−ジヒドロ−2−メチル−6−オキソ−[3,4’−ビピリジン]−5−カルボニトリル)、乳酸ミルリノン、米国特許第5,525,623号(関連する開示は参照により本明細書に組み込まれる)で開示されたものなどのトリプターゼ阻害剤、米国特許第5,691,336号、第5,877,191号、第5,929,094号、第5,750,549号、および第5,780,467号(関連する開示は参照により本明細書に組み込まれる)で開示されたものなどのタキキニン受容体アンタゴニスト、モンテルカストナトリウム(Singular(商標)、R−(E))−1−[[[1−[3−[2−(7−クロロ−2−キノリニル)エテニル]フェニル]−3−[2−(1−ヒドロキシ−1−メチルエチル)フェニル]−プロピル]チオ]メチル]シクロプロパン酢酸、モノナトリウム塩)などのロイコトリエン受容体アンタゴニスト、ジレウトン(Zyflo(商標)、Abbott Laboratories、Abbott Park、Ill)などの5−リポキシゲナーゼ阻害剤、Xolair(商標)(組み換え型ヒト化抗−IgEモノクローナル抗体(CGP 51901、IGE 025A、rhuMAb−E25)、Genentech,Inc.、カリフォルニア州サウスサンフランシスコ)などの抗−IgE抗体、およびリドカイン、N−アリールアミド、アミノアルキルベンゾエート、プリロカイン、エチドカイン(米国特許第5,510,339号、第5,631,267号、および第5,837,713号(関連する開示は参照により本明細書に組み込まれる))などの局所麻酔剤を含む。
コルチコステロイドおよび別の有効成分を含む製剤は、下記の実施例に従って調製することができる。1つの実施態様では、SAE−CDはコルチコステロイドおよび他の有効成分を可溶化するのに十分な量で存在する。別の実施態様では、SAE−CDは、コルチコステロイドまたは他の有効成分を可溶化するのに十分な量で存在する。
使用する他の有効成分に応じて、それはSAE−CDとコルチコステロイドに対して競合的に結合してもよく又は競合的に結合しなくともよい。幾つかの実施態様では、SAE−CDは、それがコルチコステロイドに対して有するよりも他の活性成分に対して高い平衡結合定数を有する。幾つかの実施態様では、SAE−CDは、それが他の活性成分に対して有するよりもコルチコステロイドに対して高い平衡結合定数を有する。幾つかの実施態様では、SAE−CDは、それがコルチコステロイドに対して有するのと、他の活性成分に対してと、ほぼ同じ平衡結合定数を有する。あるいは、他の有効成分は、コルチコステロイドがSAE−CDと結合するにもかかわらず、SAE−CDと結合しない。したがって、本発明は、SAE−CDが、コルチコステロイド、他の有効成分、またはその組み合わせを可溶化する実施態様を提供する。本発明は、また、SAE−CDがコルチコステロイド、他の有効成分、又はそれぞれの、少なくとも主要部を可溶化する実施態様を提供する。本発明は、また、SAE−CDが、他の有効成分を可溶化しない実施態様をも提供する。
SAE−CD対コルチコステロイドおよびSAE−CD対他の有効成分のモル比は、本明細書に記載の組合せ製剤を提供するために必要に応じて変動し得る。SAE−CDは、一般的には、コルチコステロイド、他の有効成分、または両方に対してモル過剰で存在する。
キシナホ酸サルメテロールおよびブデソニドについての相溶解度結合曲線は、本明細書に記載のように測定され、各々CAPTISOLとの概算の平衡結合定数(Ki)が測定された。キシナホ酸サルメテロールの概算Kiはおおよそ3,500であり、ブデソニドの概算Kiは、用いた試験条件下では600であった。飽和溶解度でCAPTISOL:キシナホ酸サルメテロールのモル比は、試験条件下で約3.2であった。それらはキシナホ酸サルメテロールの存在下CAPTISOLで溶解されるブデソニドの量において、減少する可能性がある;しかしながら、ブデソニドおよびキシナホ酸サルメテロールの治療的有効量を含む透明水性溶液製剤が調製された。
ブデソニド、アルブテロールおよびSAE−CDを含む製剤は実施例25により調製された。本製剤は調製後透明であった。ブデソニドおよびアルブテロールの組み合わせは物理的及び化学的に安定なことが示されており、そしてブデソニド単独の溶液と比べて同じエアロゾル性能及び投与ブデソニドμg当たりのAUCの改善もたらすことが期待される。更に、患者は2つの薬剤の同時投与の恩恵を受けることができる。
本発明は、コルチコステロイド反応性障害、気道の疾患または障害、例えば、気管支収縮疾患などの呼吸器または肺障害;副鼻洞炎などの洞障害の、1つまたはそれ以上の症状の治療、予防、または改善のための方法を含む。この方法は、さらに、(a)β2−アドレナリン受容体アゴニスト;(b)ドーパミン(D2)受容体アゴニスト;(c)ステロイドなどの、予防的治療薬;または(d)抗コリン剤;のような(a)、(b)、(c)または(d)のうちの1つまたはそれ以上を、本明細書で提示されている組成物と同時に、または前に、または後に、投与することを含む。
本発明の実施態様は、組み合わせを以下のさまざまな方法で調製することを可能にする。
1)レバルブテロールなどのβ2−アゴニストまたは臭化イパトロピウム(ipatropium)などの抗コリン剤の即使用可能(ready−to−use)溶液を、SAE−CD中のコルチコステロイドの即使用可能溶液と混合する。
2)β2−アゴニストまたは抗コリン剤の即使用可能溶液を、SAE−CDを使用して溶解したコルチコステロイドの濃縮溶液と混合する。
3)β2−アゴニストまたは抗コリン剤の即使用可能溶液を、実質的に乾燥しているSAE−CDおよび実質的に乾燥しているコルチコステロイドと混合する。
4)β2−アゴニストまたは抗コリン剤の即使用可能溶液を、SAE−CDおよびコルチコステロイドの実質的に乾燥している混合物と、またはより便利に、カプセルなどのユニット容器内の予め測定された量の混合物と混合する(カプセルを即使用可能溶液内に空ける)。
5)ブデソニドなどのコルチコステロイドの即使用可能溶液を、実質的に乾燥している長時間作用型もしくは短時間作用型β2−アゴニストと、および/または臭化イパトロピウムもしくは臭化チオトロピウムなどの実質的に乾燥している抗コリン剤と混合する。または
6)実質的に乾燥しているβ2−アゴニスト、ならびに/または実質的に乾燥している抗コリン剤および実質的に乾燥しているSAE−CD、それに加えて、実質的に乾燥しているコルチコステロイドを溶解する。
1)レバルブテロールなどのβ2−アゴニストまたは臭化イパトロピウム(ipatropium)などの抗コリン剤の即使用可能(ready−to−use)溶液を、SAE−CD中のコルチコステロイドの即使用可能溶液と混合する。
2)β2−アゴニストまたは抗コリン剤の即使用可能溶液を、SAE−CDを使用して溶解したコルチコステロイドの濃縮溶液と混合する。
3)β2−アゴニストまたは抗コリン剤の即使用可能溶液を、実質的に乾燥しているSAE−CDおよび実質的に乾燥しているコルチコステロイドと混合する。
4)β2−アゴニストまたは抗コリン剤の即使用可能溶液を、SAE−CDおよびコルチコステロイドの実質的に乾燥している混合物と、またはより便利に、カプセルなどのユニット容器内の予め測定された量の混合物と混合する(カプセルを即使用可能溶液内に空ける)。
5)ブデソニドなどのコルチコステロイドの即使用可能溶液を、実質的に乾燥している長時間作用型もしくは短時間作用型β2−アゴニストと、および/または臭化イパトロピウムもしくは臭化チオトロピウムなどの実質的に乾燥している抗コリン剤と混合する。または
6)実質的に乾燥しているβ2−アゴニスト、ならびに/または実質的に乾燥している抗コリン剤および実質的に乾燥しているSAE−CD、それに加えて、実質的に乾燥しているコルチコステロイドを溶解する。
本明細書で使用される物質は、微粉化又は非微粉化形態及び結晶、多形又は非晶質の形態で使用できる。これは特にコルチコステロイド及び他の有効成分に当てはまる。
当業者であれば、上記の溶液または粉末は、場合によっては、緩衝液および/もしくは等張化剤および/もしくは抗菌剤および/もしくは添加剤、または本明細書で述べているような、もしくはネブライザーのアウトプットを改善するために吸入可能液体製剤で現在使用されているような、他の賦形剤などの他の成分を含むことができることを当然のこととよく理解する。
本明細書で開示されている治療剤の投薬、使用、および投与は、一般にPhysician’s Desk Reference,55th Edition(Thompson Healthcare,Montvale,NJ,2005)(関連する開示が参照により本明細書に組み込まれる)に記載されているガイドラインに従うことが意図されている。
治療される、予防される、または1つまたはそれ以上の症状が改善しようとする気管支収縮疾患は、喘息(気管支喘息、アレルギー喘息および内因性喘息、例えば、遅発型喘息および気道過敏症を含むがこれに限定されない)ならびに、特に、抗コリン剤が使用される実施態様にあっては、他の慢性閉塞性肺疾患(COPD)[慢性気管支炎、肺気腫、および肺高血圧症、右心室肥大、および右心不全を伴う、関連する肺性心(肺および呼吸器系の疾病の二次性心疾患)を含むがこれに限定されない]と関連する。COPDは、喫煙、感染、環境汚染、および職業性粉塵曝露に関連することが多い。
本発明による製剤の貯蔵寿命は、一般的に6ヶ月以上である。この場合、貯蔵寿命は、コルチコステロイド分解副生成物の量の増大または製剤中に残っているコルチコステロイドの量の減少に関してのみ決定される。例えば、貯蔵寿命が少なくとも6ヶ月ある製剤の場合、この製剤は、少なくとも6ヶ月間の貯蔵期間中に分解生成物の量の許容できない、実質的増加を示さないことになる。許容可能な貯蔵寿命に対する基準は、与えられた製品およびその貯蔵安定性要件により必要に応じて設定される。すなわち、許容可能な貯蔵寿命を持つ製剤中の分解物の量は、意図された貯蔵期間中に所定の値を超えて増大することはないことになる。他方、許容されない貯蔵寿命を持つ製剤の分解物の量は、意図された貯蔵期間中に所定の値を超えて増大すると予想される。
実施例3の方法に従って、溶液中のブデソニドの安定性を調べた。貯蔵寿命は、有効性が10%失われるまでの時間と定義された。試験された条件の下で、有効性の喪失は一次のオーダーであった。Captisol−Enabled(登録商標)Budesonide Inhalation Solution(ブデソニドおよびSBE7−β−CDを含む溶液)の貯蔵寿命は、4から5までのpHにおいて約3年を超える、すなわち、EDTAなどの他の安定剤を約5質量%/vol.のSAE−CDの存在下で水の中に加えなくても、pH 4.0では約90ヶ月、pH 5.0では約108ヶ月である。この貯蔵寿命は、Otterbeckにより報告されている寿命よりも長い(米国特許第5,914,122号、EDTA、HP−β−CD、および他の添加剤の存在下で水の中でpH4.0〜6.0により最大6週間)。
発明者は、さらに、SAE−CDがブデソニドの異性体をさまざまな程度に安定化することができることも発見した。SBE7−β−CDがブデソニド溶液を安定化したかどうか、優先的に一方の異性体を安定化したかどうかを調べる研究が実施例13に従って行われた。図11は、60℃で貯蔵されている試料に対するそれぞれの時点における初期濃度の%の半対数のグラフである。ブデソニドの損失は、それぞれの温度で一次のオーダーであった。以下の表は、60℃および80℃における、それぞれの異性体について計算された擬似一次速度定数を示している。
SBE7−β−CDは、pH4とpH6の両方の溶液中のブデソニドのR−およびS−異性体を両方とも安定化した。CAPTISOLがある場合とない場合の速度定数比は、すべての温度において1よりもかなり小さかった。SBE7−β−CDは、R−およびS−の両方の異性体の安定性に対し、pH4よりもpH6で大きな影響を及ぼした。所与の温度において、SBE7−β−CDがある場合とない場合の速度定数の比は、pH4よりもpH6で、小さかった。SBE7−β−CDは、両方の異性体を安定化したが、S−異性体は、R−異性体よりも、なおいっそう大きく安定化したように見える。テストされたすべての温度およびpHにおいて、SBE7−β−CDがある場合とない場合の速度定数の比は、S−異性体の場合に低かった。60℃のときにSBE7−β−CDの影響を受ける安定化の程度は、80℃のときよりも大きい。40℃および/または室温(20〜30℃)では、安定化の程度はさらに大きくなることが予想される。
上の溶液の試料は、さらに、蛍光灯列の下のチャンバ内に置かれた。バイアルびんを定期的に取り出して、ブデソニドについてアッセイ分析を行った。図12は、残っている初期値の%を露光量の関数として表した半対数グラフである(光度×時間)。以下の表に示されているように、SBE7−β−CDは、ブデソニドの光分解を著しく低減した。ブデソニドの損失は、一次のオーダーであり、pHとは無関係であった。
本発明の製剤は、噴霧用の吸入可能溶液を形成するように適合されたキットとして提供することができる。このキットは、コルチコステロイド、SAE−CD、水性担体、および場合によっては、1つ以上の他の成分を含むことができる。コルチコステロイドおよびSAE−CDは、一緒に、または別々に、固体形態、懸濁液形態、または溶液形態で提供することができる。水性担体の存在下で、SAE−CDをコルチコステロイドと混合した後、固形物は溶解し、噴霧用の懸濁液というよりはむしろ吸入可能溶液を形成する。それぞれの成分は、個々の容器に入れるか、または他の成分と合わせて提供することができる。例えば、SAE−CDは、水溶液で提供できるが、ブデソニドは、乾燥した固形または湿った懸濁形態で提供される。それとは別に、SAE−CDは、乾燥形態で提供され、またブデソニドは、水性懸濁液、例えば、PULMICORT RESPULES(商標)として提供される。このキットは、その代わりに、固体誘導体化シクロデキストリンと固体コルチコステロイドの混合物を含み、場合によっては、少なくとも1つの固体医薬賦形剤を含み、それにより、活性物質の大部分は、水性担体との固体混合物の再構成の前に誘導体化シクロデキストリンと錯体を形成する。キットの貯蔵温度に応じて、水性担体は、液体または凍結固体とすることができる。一実施態様では、キットは、貯蔵時に水性担体を除外するが、水性担体は、噴霧溶液を形成するために使用する前にSAE−CDおよびコルチコステロイドに加えられる。コルチコステロイドおよびSAE−CDは、水性担体を加える前に、錯化され、水性濃縮形態で存在することができ、水性担体は、溶液を噴霧用の体積ならびに適切な粘度および濃度にするために後から加えられる。再構成可能な製剤は、以下の方法のどれかに従って調製できる。本発明の液体製剤が、まず最初に調製され、次いで、凍結乾燥(フリーズドライ)、噴霧乾燥、噴霧フリーズドライ、アンチソルベント沈殿(antisolvent precipitation)、超臨界または近超臨界流体を利用するさまざまな方法、または再構成のため固体を形成する当業者に公知の他の方法により固体が形成される。実施例29は、本発明の液体組成物または製剤の凍結乾燥によるコルチコステロイドおよびSAE−CDを含む凍結乾燥固体組成物の調製方法を詳述している。凍結乾燥固体は、噴霧投与前に水性液体担体に溶解することができる。乾燥粉末は長期保存の安定形態を与え、そしてまた大規模に吸入組成物を迅速調製するのに、または組み合わせ製品を調製するための別の吸入溶液投薬の添加物として有用となる。
本発明の液体組成物または製剤は、肺に投与できるが、また経鼻、経口、経眼、経耳または局所投与にも適するものとなる。液体組成物または製剤は、また、ポンプスプレー、定量吸入器、または加圧定量吸入器などの装置を用いて吸入投与することができる。したがって、本発明は、治療を必要とする対象に本液体を投与することによる、コルチコステロイド反応性疾患又は障害の治療方法を提供する。
本発明の製剤に含まれる液体ビヒクル(担体)は、水、水性アルコール、プロピレングリコール、または水性有機溶媒などの水性液体担体を含む。実施例30は、20%w/vのSAE−CD、コルチコステロイド、水およびエタノール(0〜5%)を含む液体製剤の調製を詳述している。液体中のエタノール濃度の増加は、コルチコステロイドの最大飽和溶解度の減少をもたらした。
必須というわけではないが、本発明の製剤は、従来の保存剤、酸化防止剤、緩衝剤、酸性化剤、アルカリ性化剤、着色剤、溶解度促進剤、錯化促進剤、電解質、ブドウ糖、安定剤、等張化剤、増量剤、消泡剤、油、乳化剤、抗凍結剤、可塑剤、着香料、甘味料、等張化剤、表面張力調整剤、粘度調整剤、密度調整剤、揮発性調整剤、保存される製剤で使用するための当業者に公知の他の添加剤、またはこれらの組み合わせを含むことができる。
本明細書で使用されているように、「アルカリ性化剤」という用語は、製品安定性のためなどに、アルカリ媒体を供給するために使用される化合物を意味することが意図されている。このような化合物は、例えば、限定はされないが、アンモニア溶液、炭酸アンモニウム、ジエタノールアミン、モノエタノールアミン、水酸化カリウム、ホウ酸ナトリウム、炭酸ナトリウム、重炭酸ナトリウム、水酸化ナトリウム、トリエタノールアミン、ジエタノールアミン、有機アミン塩基、アルカリ性アミノ酸およびトロラミン、ならびに当業者に公知の他の物質を含む。
本明細書で使用されているように、「酸性化剤」という用語は、製品安定性のために、酸性媒体を供給するために使用される化合物を意味することが意図されている。このような化合物は、例えば、限定はされないが、酢酸、酸性アミノ酸、クエン酸、フマル酸および他のαヒドロキシ酸、塩酸、アスコルビン酸、リン酸、硫酸、酒石酸、および硝酸、ならびに当業者に公知の他の物質を含む。
吸入可能溶液製剤に従来の保存剤を入れることは、任意であるが、その製剤は溶液中の濃度に応じてSAE−CDにより自己保存されるからである。しかしながら、従来の保存剤は、さらに、必要に応じて、製剤の中に含めることができる。保存剤は、組成物内の微生物増殖を阻害するために使用することができる。保存剤の量は、一般に、少なくとも6ヶ月の貯蔵期間に組成物内に微生物が増殖するのを防ぐために必要な量である。本明細書で使用されているように、従来の保存剤は、生物負荷(bioburden)が増加する速度を少なくとも低減するために使用される化合物であるが、好ましくは、汚染が発生した後、バイオバーデンを定常状態に維持するか、またはバイオバーデンを低減する。このような化合物は、例えば、限定はされないが、塩化ベンザルコニウム、塩化ベンゼトニウム、安息香酸、ベンジルアルコール、塩化セチルピリジニウム、クロロブタノール、フェノール、フェニルエチルアルコール、硝酸フェニル水銀、酢酸フェニル水銀、チメロサール、メタクレゾール、ミリスチルγ塩化ピコリニウム、安息香酸カリウム、ソルビン酸カリウム、安息香酸ナトリウム、プロピオン酸ナトリウム、ソルビン酸、チモール、およびメチル、エチル、プロピル、またはブチルパラベン、ならびに当業者に公知の他の物質を含む。
本明細書で使用されているように、「酸化防止剤」という用語は、酸化を阻害し、そのため、酸化過程による調製品の分解を防止するために使用される薬剤を意味することが意図されている。このような化合物は、例えば、限定はされないが、アセトン、メタ重亜硫酸カリウム、亜硫酸カリウム、アスコルビン酸、パルミチン酸アスコルビル、クエン酸、ブチル化ヒドロキシアニソール、ブチル化ヒドロキシトルエン、次亜リン酸、モノチオグリセロール、没食子酸プロピル、アスコルビン酸ナトリウム、クエン酸ナトリウム、硫化ナトリウム、亜硫酸ナトリウム、重亜硫酸ナトリウム、ホルムアルデヒドスルホキシル酸ナトリウム、チオグリコール酸、EDTA、ペンテト酸塩、およびメタ重亜硫酸ナトリウムならびに当業者に公知の他の物質を含む。
本明細書で使用されているように、「緩衝剤」という用語は、酸またはアルカリの希釈または添加による、pHの変化に抵抗するために使用される化合物を意味することが意図されている。緩衝剤は、本発明の組成物において、pHを約2から約8、約3から約7、または約4から約5までの範囲に調整するために使用される。このような化合物は、例えば、限定はされないが、酢酸、酢酸ナトリウム、アジピン酸、安息香酸、安息香酸ナトリウム、ホウ酸、ホウ酸ナトリウム、クエン酸、グリシン、マレイン酸、第一リン酸ナトリウム、第二リン酸ナトリウム、HEPES、乳酸、酒石酸、メタリン酸カリウム、リン酸カリウム、一塩基性の酢酸ナトリウム、重炭酸ナトリウム、トリス、酒石酸ナトリウム、および無水クエン酸ナトリウムおよび二水和物ならびに当業者に公知の他の物質を含む。他の緩衝剤は、クエン酸/リン酸塩混合液、酢酸塩、バルビタール、ホウ酸塩、Britton−Robinson、カコジル酸塩、クエン酸塩、コリジン、ギ酸塩、マレイン酸塩、Mcllvaine、リン酸塩、Prideaux−Ward、コハク酸塩、クエン酸塩−リン酸塩−ホウ酸塩(Teorell−Stanhagen)、酢酸ベロナール、MES(2−(N−モルホリノ)エタンスルホン酸)、BIS−TRIS(ビス(2−ヒドロキシエチル)イミノ−トリス(ヒドロキシメチル)メタン)、ADA(N−(2−アセトアミド)−2−イミノ二酢酸)、ACES(N−(カルバモイルメチル)−2−アミノエタンスルホン酸)、PIPES(ピペラジン−N,N’−ビス(2−エタンスルホン酸))、MOPSO(3−(N−モルホリノ)−2−ヒドロキシプロパンスルホン酸)、BISTRIS PROPANE(1,3−ビス(トリス(ヒドロキシメチル)メチルアミノ)プロパン)、BES(N,N−ビス(2−ヒドロキシエチル)−2−アミノエタンスルホン酸)、MOPS(3−(N−モルホリノ)プロパンスルホン酸)、TES(N−トリス(ヒドロキシメチル)メチル−2−アミノエタンスルホン酸)、HEPES(N−(2−ヒドロキシエチル)ピペラジン−N’−(2−エタンスルホン酸)、DIPSO(3−(N,N−ビス(2−ヒドロキシエチル)アミノ)−2−ヒドロキシプロパンスルホン酸)、MOBS(4−(N−モルホリノ)−ブタンスルホン酸)、TAPSO(3−(N−トリス(ヒドロキシメチル)メチルアミノ)−2−ヒドロキシプロパンスルホン酸)、TRIZMA(商標)(トリス(ヒドロキシメチルアミノメタン)、HEPPSO(N−(2−ヒドロキシエチル)ピペラジン−N’−(2−ヒドロキシプロパンスルホン酸)、POPSO(ピペラジン−N,N’−ビス(2−ヒドロキシプロパンスルホン酸))、TEA(トリエタノールアミン)、EPPS(N−(2−ヒドロキシエチル)ピペラジン−N’−(3−プロパンスルホン酸)、TRICINE(N−トリス(ヒドロキシメチル)メチルグリシン)、GLY−GLY(グリシルグリシン)、BICINE(N,N−ビス(2−ヒドロキシエチル)グリシン)、HEPBS(N−(2−ヒドロキシエチル)ピペラジン−N’−(4−ブタンスルホン酸))、TAPS(N−トリス(ヒドロキシメチル)メチル−3−アミノプロパンスルホン酸)、AMPD(2−アミノ−2−メチル−1,3−プロパンジオール)、および/または当業者に公知の他の緩衝剤を含む。
錯化促進剤を本発明の製剤に加えることができる。このような薬剤が存在する場合、シクロデキストリン/活性物質の比は、変更可能である。錯化促進剤は、活性物質とシクロデキストリンとの錯体形成を増強する1つの化合物、または複数の化合物である。好適な錯化促進剤は、1つまたはそれ以上の薬理学的に不活性な水溶性ポリマー、ヒドロキシ酸、および特定の薬剤とシクロデキストリンとの錯体形成を増強するために液体製剤で典型的に使用される他の有機化合物を含む。
親水性ポリマーを錯化増強、溶解促進、および/または水分活性低下剤として使用し、シクロデキストリンを含む製剤の性能を改善することができる。Loftssonは、シクロデキストリンの性能および/または特性を増強するためにシクロデキストリン(未誘導体化または誘導体化)との併用に適した多数のポリマーを開示している。好適なポリマーが開示されているのは、Pharmazie(2001年)、56(9)、746−747頁、International Journal of Pharmaceutics(2001年)、212(1)、29〜40頁、Cyclodextrin:From Basic Research to Market,International Cyclodextrin Symposium,10th,Ann Arbor,MI,United States、5月21日〜24日、2000年、10−15(Wacker Biochem Corp.:Adrian,Mich.)、PCT国際公開WO9942111号、Pharmazie、53(11)、733〜740(1998年)、Pharm.Technol.Eur.、9(5)、26〜34頁(1997年)、J.Pharm.Sci.85(10)、1017〜1025頁(1996年)、欧州特許出願EP0579435、Proceedings of the International Symposium on Cyclodextrins,9th,Santiago de Comostela,Spain、5月31日〜6月3日、1998年(1999年)、261〜264頁(Editor(s):Labandeira,J.J.Torres;Vila−Jato,J.L.Kluwer Academic Publishers,Dordrecht,Neth)、S.T.P.Pharma Sciences(1999年)、9(3)、237〜242頁、ACS Symposium Series(1999年)、737(Polysaccharide Applications)、24〜45頁、Pharmaceutical Research(1998年)、15(11)、1696〜1701頁、Drug Development and Industrial Pharmacy(1998年)、24(4)、365〜370頁、International Journal of Pharmaceutics(1998年)、163(1−2)、115〜121頁、Book of Abstracts,216th ACS National Meeting,Boston、8月23日〜27日(1998年)、CELL−016、American Chemical Society、Journal of Controlled Release(1997年)、44/1(95−99)、Pharm.Res.(1997年)14(11)、S203、Investigative Ophthalmology & Visual Science(1996年)、37(6)、1199〜1203頁、Proceedings of the International Symposium on Controlled Release of Bioactive Materials(1996年)、23rd、453〜454頁、Drug Development and Industrial Pharmacy(1996年)、22(5)、401〜405頁、Proceedings of the International Symposium on Cyclodextrins,8th,Budapest、3月31日〜4月2日(1996年)、373〜376頁(Editor(s):Szejtli,J.;Szente,L.Kluwer:Dordrecht,Neth.)、Pharmaceutical Sciences(1996年)、2(6)、277〜279頁、European Journal of Pharmaceutical Sciences(1996年)4(SUPPL.)、S144、Third European Congress of Pharmaceutical Sciences、Edinburgh、Scotland、UK、1996年9月15〜17日、Pharmazie(1996年)、51(1)、39〜42頁、Eur.J.Pharm.Sci.(1996年)、4(Suppl.)、S143、米国特許第5,472,954および第5,324,718号、International Journal of Pharmaceutics(Netherlands)、(1995年12月29日)126、73〜78頁、Abstracts of Papers of the American Chemical Society(1995年4月2日)209(1)、33−CELL、European Journal of Pharmaceutical Sciences(1994年)2、297〜301頁、Pharmaceutical Research(New York)、(1994年)11(10)、S225、International Journal of Pharmaceutics(Netherlands)、(1994年4月11日)104、181〜184頁、およびInternational Journal of Pharmaceutics(1994年)、110(2)、169−77であり、これらの開示全体は、参照により本明細書に組み込まれる。
他の好適なポリマーは、医薬製剤の分野で一般に使用されるよく公知の賦形剤であり、例えば、Remington’s Pharmaceutical Sciences,18th Edition,Alfonso R.Gennaro(editor),Mack Publishing Company,Easton,PA,1990年、291〜294頁、Alfred Martin、James Swarbrick、およびArthur Commarata、Physical Pharmacy.Physical Chemical Principles in Pharmaceutical Sciences,3rd edition(Lea & Febinger,Philadelphia,PA,1983年、592〜638頁)、A.T.FlorenceおよびD.Altwood(Physicochemical Principles of Pharmacy,2nd Edition,MacMillan Press,London,1988年、281〜334頁に記載されている。本明細書で引用されている文献の開示全体は、参照により本明細書に組み込まれる。さらに他の好適なポリマーは、水溶性天然ポリマー、水溶性半合成ポリマー(セルロースの水溶性誘導体など)および水溶性合成ポリマーを含む。天然ポリマーは、イヌリン、ペクチン、アルギン誘導体(例えば、アルギン酸ナトリウム)、および寒天などの多糖類、ならびにカゼインおよびゼラチンなどのポリペプチドを含む。半合成ポリマーは、メチルセルロース、ヒドロキシエチルセルロース、ヒドロキシプロピルセルロースなどのセルロース誘導体、ヒドロキシプロピルメチルセルロースなどのそれらの混合エーテルおよびヒドロキシエチルエチルセルロースおよびヒドロキシプロピルエチルセルロースなどの他の混合エーテル、ヒドロキシプロピルメチルセルロースフタレート、ならびにカルボキシメチルセルロースおよびその塩、特にカルボキシメチルセルロースナトリウムを含む。合成ポリマーは、ポリオキシエチレン誘導体(ポリエチレングリコール)およびポリビニル誘導体(ポリビニルアルコール、ポリビニルピロリドンおよびポリスチレンスルホネート)ならびにアクリル酸のさまざまなコポリマー(例えば、カルボマー)を含む。水溶解度、医薬としての許容性、および薬理学的不活性の基準を満たしているここで取りあげていない他の天然、半合成、および合成ポリマーも、同様に、本発明の範囲内にあるものと考えられる。
乳化剤は、エマルジョンの形成を補助する化合物を意味することが意図されている。乳化剤を使用することで、コルチコステロイドを濡らし、溶解しやすくすることができる。本明細書で使用する乳化剤は、限定はされないが、ポリエチレンソルビタンモノオレエート(ポリソルベート80)、ポリソルベート20(ポリオキシエチレン(20)ソルビタンモノラウレート)、ポリソルベート65(ポリオキシエチレン(20)ソルビタントリステアレート)、ポリオキシエチレン(20)ソルビタンモノオレエート、ポリオキシエチレン(20)ソルビタンモノパルミテート、ポリオキシエチレン(20)ソルビタンモノステアレートなどのポリオキシエチレンソルビタン脂肪酸エステルまたはポリソルベート、レシチン、アルギン酸、アルギン酸ナトリウム、アルギン酸カリウム、アルギン酸アンモニウム、アルギン酸カルシウム、プロパン−1,2−ジオールアルギネート、寒天、
カラギナン、ローカストビーンガム、グァーガム、トラガカント、アラビアゴム、キサンタンガム、カラヤゴム、ペクチン、アミド化ペクチン、アンモニウムホスファチド、微結晶セルロース、メチルセルロース、ヒドロキシプロピルセルロース、ヒドロキシプロピルメチルセルロース、エチルメチルセルロース、カルボキシメチルセルロース、脂肪酸のナトリウム塩、カリウム塩、およびカルシウム塩、脂肪酸のモノグリセリドおよびジグリセリド、脂肪酸のモノグリセリドおよびジグリセリドの酢酸エステル、脂肪酸のモノグリセリドおよびジグリセリドの乳酸エステル、脂肪酸のモノグリセリドおよびジグリセリドのクエン酸エステル、脂肪酸のモノグリセリドおよびジグリセリドの酒石酸エステル、脂肪酸のモノグリセリドおよびジグリセリドのモノアセチル酒石酸エステルおよびジアセチル酒石酸エステル、脂肪酸のモノグリセリドおよびジグリセリドの酢酸および酒石酸の混合エステル、脂肪酸のショ糖エステル、スクログリセリド、脂肪酸のポリグリセロールエステル、ヒマシ油の重縮合脂肪酸のポリグリセロールエステル、脂肪酸のプロパン−1,2−ジオールエステル、ステアロイル−2−乳酸ナトリウム、ステアロイル−2−乳酸カルシウム、ステアロイルタルトレート、モノステアリン酸ソルビタン、トリステアリン酸ソルビタン、モノラウリン酸ソルビタン、モノオレイン酸ソルビタン、モノパルミチン酸ソルビタン、キラヤ抽出物、大豆油の二量化脂肪酸のポリグリセロールエステル、酸化的に重合された大豆油、およびペクチン抽出物を含む。
カラギナン、ローカストビーンガム、グァーガム、トラガカント、アラビアゴム、キサンタンガム、カラヤゴム、ペクチン、アミド化ペクチン、アンモニウムホスファチド、微結晶セルロース、メチルセルロース、ヒドロキシプロピルセルロース、ヒドロキシプロピルメチルセルロース、エチルメチルセルロース、カルボキシメチルセルロース、脂肪酸のナトリウム塩、カリウム塩、およびカルシウム塩、脂肪酸のモノグリセリドおよびジグリセリド、脂肪酸のモノグリセリドおよびジグリセリドの酢酸エステル、脂肪酸のモノグリセリドおよびジグリセリドの乳酸エステル、脂肪酸のモノグリセリドおよびジグリセリドのクエン酸エステル、脂肪酸のモノグリセリドおよびジグリセリドの酒石酸エステル、脂肪酸のモノグリセリドおよびジグリセリドのモノアセチル酒石酸エステルおよびジアセチル酒石酸エステル、脂肪酸のモノグリセリドおよびジグリセリドの酢酸および酒石酸の混合エステル、脂肪酸のショ糖エステル、スクログリセリド、脂肪酸のポリグリセロールエステル、ヒマシ油の重縮合脂肪酸のポリグリセロールエステル、脂肪酸のプロパン−1,2−ジオールエステル、ステアロイル−2−乳酸ナトリウム、ステアロイル−2−乳酸カルシウム、ステアロイルタルトレート、モノステアリン酸ソルビタン、トリステアリン酸ソルビタン、モノラウリン酸ソルビタン、モノオレイン酸ソルビタン、モノパルミチン酸ソルビタン、キラヤ抽出物、大豆油の二量化脂肪酸のポリグリセロールエステル、酸化的に重合された大豆油、およびペクチン抽出物を含む。
本明細書で使用されているように、「安定剤」という用語は、治療薬の治療活性を下げる物理的、化学的、または生化学的過程に対してその治療薬を安定化させるために使用される化合物を意味することが意図されている。好適な安定剤は、例えば、限定はされないが、アルブミン、シアル酸、クレアチニン、グリシンおよび他のアミノ酸、ナイアシンアミド、ナトリウムアセチルトリプトフォネート(sodium acetyltryptophonate)、酸化亜鉛、ショ糖、ブドウ糖、乳糖、ソルビトール、マンニトール、グリセロール、ポリエチレングリコール、カプリル酸ナトリウムおよびサッカリンナトリウムならびに当業者に公知の他の物質を含む。
本明細書で使用されているように、「等張化剤」という用語は、液体製剤の張度を調整するために使用できる1つの化合物または複数の化合物を意味することが意図されている。好適な等張化剤は、グリセリン、乳糖、マンニトール、デキストロース、塩化ナトリウム、硫酸ナトリウム、ソルビトール、トレハロース、および当業者に公知の他の物質を含む。他の等張化剤は、無機と有機の両方の等張化剤(tonicity adjusting agents)を含む。等張化剤は、限定はされないが、炭酸アンモニウム、塩化アンモニウム、乳酸アンモニウム、硝酸アンモニウム、リン酸アンモニウム、硫酸アンモニウム、アスコルビン酸、酒石酸ビスマスナトリウム、ホウ酸、塩化カルシウム、エデト酸二ナトリウムカルシウム、グルコン酸カルシウム、乳酸カルシウム、クエン酸、デキストロ−ス、ジエタノールアミン、ジメチルスルホキシド、エデト酸二ナトリウム、エデト酸三ナトリウム一水和物、フルオレセインナトリウム、果糖、ガラクトース、グリセリン、乳酸、乳糖、塩化マグネシウム、硫酸マグネシウム、マンニトール、ポリエチレングリコール、酢酸カリウム、塩素酸カリウム、塩化カリウム、ヨウ化カリウム、硝酸カリウム、リン酸カリウム、硫酸カリウム、プロピレングリコール、硝酸銀、酢酸ナトリウム、重炭酸ナトリウム、重リン酸ナトリウム、重亜硫酸ナトリウム、ホウ酸ナトリウム、臭化ナトリウム、カコジル酸ナトリウム、炭酸ナトリウム、塩化ナトリウム、クエン酸ナトリウム、ヨウ化ナトリウム、乳酸ナトリウム、メタ重亜硫酸ナトリウム、硝酸ナトリウム、亜硝酸ナトリウム、リン酸ナトリウム、プロピオン酸ナトリウム、コハク酸ナトリウム、硫酸ナトリウム、亜硫酸ナトリウム、酒石酸ナトリウム、チオ硫酸ナトリウム、ソルビトール、ショ糖、酒石酸、トリエタノールアミン、尿素、ウレタン、ウリジン、および硫酸亜鉛を含む。一実施態様では、液体製剤の張度は、呼吸管内の組織の張度に近似する。
浸透圧性薬剤を組成物に使用し、コルチコステロイド組成物の送達により患者に対する全体的な快適さを高めることができる。浸透圧性薬剤は、SAE−CD含有溶液の張度を調整するために加えることができる。オスモル濃度は、水中のSAE−CDの濃度に関係する。約11〜13%w/vよりも低いSBE7−β−CD濃度では、溶液は、血液に関して低張または低浸透圧であり、約11〜13%w/vよりも高いSBE7−β−CD濃度では、SBE7−β−CD含有溶液は、血液に関して高張または高浸透圧である。赤血球が低または高張である溶液に曝された場合、サイズが縮小または膨張し、溶血に至る可能性がある。上で述べたように、また図1に示されているように、SBE−CDは、他の誘導体化シクロデキストリンよりも、溶血を誘発する傾向が小さい。好適な浸透圧性薬剤は、塩化ナトリウム、乳糖、およびブドウ糖などの経肺および経鼻送達用に医薬品として認可されている低分子量水溶性化学種を含む。本発明の製剤は、さらに、生物学的塩、塩化カリウム、または他の電解質を含むこともできる。
本明細書で使用されているように、「消泡剤」という用語は、液体製剤の表面上に形成される泡を防ぐか、または量を減らす1つの化合物または複数の化合物を意味することが意図されている。好適な消泡剤は、ジメチコーン、シメチコーン、オクトキシノール、エタノール、および当業者に知られている他の物質を含む。
本明細書で使用されているように、「増量剤」という用語は、凍結乾燥製品にかさ高さを加え、および/または凍結乾燥時に製剤の特性の制御を助けるために使用される化合物を意味することが意図されている。このような化合物は、例えば、限定はされないが、デキストラン、トレハロース、ショ糖、ポリビニルピロリドン、乳糖、イノシトール、ソルビトール、ジメチルスルホキシド、グリセロール、アルブミン、ラクトビオン酸カルシウム、および当業者に公知の他の物質を含む。
本明細書で使用されているように、「抗凍結剤」という用語は、凍結乾燥時に活性治療薬の物理的または化学的分解を防ぐために使用される化合物を意味することが意図されている。このような化合物は、例えば、限定はされないが、ジメチルスルホキシド、グリセロール、トレハロース、プロピレングリコール、ポリエチレングリコール、および当業者に公知の他の物質を含む。
溶解促進剤を本発明の製剤に加えることができる。溶解促進剤は、液体製剤の場合にコルチコステロイドの溶解度を増強する、1つの化合物、または複数の化合物である。別の溶解促進剤が存在する場合、SAE−CD対コルチコステロイドの比を変えることができ、それによりコルチコステロイドを溶解するのに要するSAE−CDの量を低減させることができる。好適な溶解促進剤としては、1つまたはそれ以上のシクロデキストリン、シクロデキストリン誘導体、SAE−CD、有機溶媒、洗浄剤、石鹸、界面活性剤、および特定の薬剤の溶解度を増強するため非経口製剤において通常使用される他の有機化合物を含む。典型的な溶解促進剤は米国特許第6,451,339号に開示されている;しかし、製薬産業で使用される他の界面活性剤は、本発明の製剤において使用可能である。幾つかの好適なシクロデキストリンとしては、SAE−CD、SAE−CD誘導体、ヒドロキシアルキルエーテルおよび誘導体、アルキルエーテルシクロデキストリンおよび誘導体、硫酸化シクロデキストリンおよび誘導体、ヒドロキシプロピル−β−シクロデキストリン、2−HP−β−CD、メチル−β−シクロデキストリン、カルボキシアルキルチオエーテル誘導体、スクシニルシクロデキストリンおよび誘導体、および製薬学的用途に好適な他のシクロデキストリン、などの非誘導体化シクロデキストリンおよびシクロデキストリン誘導体が含まれる。SAE−CDシクロデキストリン類は特に有利である。
製剤で使用できる好適な有機溶媒は、例えば、エタノール、グリセリン、ポリ(エチレングリコール)、プロピレングリコール、ポロキサマー、その水性形態および当業者に公知の他の物質を含む。
医薬製剤の分野で使用される化合物は、一般に、さまざまな機能または目的のために使用されることは当然理解されるであろう。そのため、ここに挙げられている化合物が1回しか言及されていないか、またここで複数の用語を定義するために使用されている場合、その目的または機能は、指定された目的または機能にのみ限られると解釈すべきではない。
本発明の製剤に含まれる活性物質は、その薬剤として許容される塩として存在しうる。本明細書で使用されているように、「医薬として許容される塩」は、開示されている化合物の誘導体を指し、活性物質は、必要に応じて酸または塩基と反応させることにより修飾され、イオン結合対を形成する。薬剤として許容される塩の実例は、従来の非毒性の塩または例えば、非毒性の無機または有機酸から形成された親化合物の第四アンモニウム塩を含む。好適な非毒性の塩は、塩化水素酸、臭化水素酸、硫酸、スルホン酸、スルファミン酸、リン酸、硝酸、および当業者に公知の他の物質などの無機酸から誘導される塩を含む。塩は、アミノ酸、酢酸、プロピオン酸、コハク酸、グリコール酸、ステアリン酸、乳酸、リンゴ酸、酒石酸、クエン酸、アスコルビン酸、パモ酸、マレイン酸、ヒドロキシマレイン酸、フェニル酢酸、グルタミン酸、安息香酸、サリチル酸、スルファニル酸、2−アセトキシ安息香酸、フマル酸、トルエンスルホン酸、メタンスルホン酸、エタンジスルホン酸、シュウ酸、イセチオン酸、および当業者に公知の他の物質などの有機酸から製造される。本発明の薬剤として許容される塩は、従来の化学的方法により塩基または酸性部分構造を含む親活性物質から合成することができる。他の好適な塩の一覧は、Remington’s Pharmaceutical Sciences,17th.ed.,Mack Publishing Company,Easton、PA、195年に記載されており、関連する開示は、参照により本明細書に組み込まれる。
「医薬として許容される」という用語は、本明細書では、正しい医薬的判断の範囲内で、妥当なメリット/リスクの比と釣り合う形で、過剰な毒性、刺激、アレルギー反応、または他の問題または面倒な事態を引き起こすことなくヒトおよび動物の組織に接触させて使用するのに適している化合物、材料、組成物、および/または投薬形態を指すために使用されている。
本明細書で使用されているように、「患者」または「被験者」は、哺乳類、例えば、ネコ、イヌ、マウス、モルモット、ウマ、ウシ、ヒツジ、およびヒトなどの温血動物を意味するものとする。
本発明の製剤は、有効量、有効用量又は治療的有効用量で存在する活性物質、を含む。「有効量」又は「有効用量」又は「治療的有効用量」という用語は、必要な、もしくは所望の応答を引き出すのに十分な活性物質の量もしくは数量、または言い換えると、被験者に投与する場合に適切な生物学的反応を引き出すのに十分な量を意味する。
上の説明および以下の実施例を鑑みて、当業者であれば、過度の実験を行わずに、特許請求されているような本発明を実施することができる。前記は、本発明により製剤の調製のいくつかの手順を詳述している以下の実施例を参照するとさらによく理解できる。これらの実施例に対する参照はすべて、例示目的である。以下の実施例は、網羅されていると考えるべきではなく、本発明により考察された多数の実施態様のうちのごくわずかを例示するだけであると考えるべきである。
〔実施例1〕
本発明による例示的な製剤は、以下の一般的手順に従って作られた。
本発明による例示的な製剤は、以下の一般的手順に従って作られた。
方法A
シクロデキストリンを水(または緩衝液)に溶解して、既知の濃度のシクロデキストリンを含む溶液を形成した。この溶液を、混合しながら、場合によっては加熱しながら、固体、懸濁液、ゲル、液体、ペースト、粉末、または他の形態の活性物質と混合し、吸入可能溶液を形成した。
シクロデキストリンを水(または緩衝液)に溶解して、既知の濃度のシクロデキストリンを含む溶液を形成した。この溶液を、混合しながら、場合によっては加熱しながら、固体、懸濁液、ゲル、液体、ペースト、粉末、または他の形態の活性物質と混合し、吸入可能溶液を形成した。
方法B
既知の量の実質的に乾燥しているシクロデキストリンを、既知の量の実質的に乾燥している活性物質と混合した。液体をこの混合物に加えて、懸濁液、ゲル、溶液、シロップまたはペーストを形成し、場合によっては加熱しながら、場合によっては1つまたはそれ以上の他の添加剤の存在下、さらに混合して、吸入可能溶液を形成した。
既知の量の実質的に乾燥しているシクロデキストリンを、既知の量の実質的に乾燥している活性物質と混合した。液体をこの混合物に加えて、懸濁液、ゲル、溶液、シロップまたはペーストを形成し、場合によっては加熱しながら、場合によっては1つまたはそれ以上の他の添加剤の存在下、さらに混合して、吸入可能溶液を形成した。
方法C
既知の量の実質的に乾燥しているシクロデキストリンを、既知の量の活性物質を含む懸濁液、ゲル、溶液、シロップまたはペーストに加え、場合によっては加熱しながら、場合によっては1つまたはそれ以上の他の添加剤の存在下、さらに混合して吸入可能溶液を形成した。
既知の量の実質的に乾燥しているシクロデキストリンを、既知の量の活性物質を含む懸濁液、ゲル、溶液、シロップまたはペーストに加え、場合によっては加熱しながら、場合によっては1つまたはそれ以上の他の添加剤の存在下、さらに混合して吸入可能溶液を形成した。
この実施例の方法を、湿潤剤を組成物内に含めることにより改変し、コルチコステロイドの溶解およびその後の包接錯体を形成しやすくできる。界面活性剤、石鹸、洗浄剤、または乳化剤を湿潤剤として使用できる。
方法D
既知の濃度または量のSAE−CD、水性液体担体、および場合により1つまたはそれ以上の添加剤を含む溶液に、本発明で測定してSAE−CDの存在下、コルチコステロイドの飽和溶解度のポイントでのSAE−CD対コルチコステロイドのモル比に基づき、モル過剰のコルチコステロイドを加える。例えば、コルチコステロイドは、5%、10%、15%、20%、25%、30%またはそれ以上のモル過剰で加えることになる。その成分を平衡になるまでに混合し、そのポイントでは1時間経過する間ブデソニドの濃度にわずかな変化しか存在しない。次いで、過剰コルチコステロイドは、本発明の標的の溶液を残して除去される。
既知の濃度または量のSAE−CD、水性液体担体、および場合により1つまたはそれ以上の添加剤を含む溶液に、本発明で測定してSAE−CDの存在下、コルチコステロイドの飽和溶解度のポイントでのSAE−CD対コルチコステロイドのモル比に基づき、モル過剰のコルチコステロイドを加える。例えば、コルチコステロイドは、5%、10%、15%、20%、25%、30%またはそれ以上のモル過剰で加えることになる。その成分を平衡になるまでに混合し、そのポイントでは1時間経過する間ブデソニドの濃度にわずかな変化しか存在しない。次いで、過剰コルチコステロイドは、本発明の標的の溶液を残して除去される。
ブデソニドを、水、緩衝液、水性アルコール、水性有機溶媒またはその組み合わせであってよい、水性液体担体中の固体かまたは懸濁液としてSAE−CD含有溶液に加える。アルコールおよび有機溶媒は、薬学的に許容されるグレードのもの、例えば、エタノール、プロピレングリコール、およびその他の明細書に記載のものである。
方法E
SAE−CDおよびコルチコステロイドは摩砕して混合物を形成させる。次いで水性液体担体を混合物に加えて、本発明の標的溶液を形成させる。
摩砕は、乾式又は湿気、水、緩衝液、アルコール、界面活性剤、有機溶媒、グリセリン、ポリ(エチレングリコール)、ポロキサマーもしくはその組み合わせの存在下で行うことができる。
SAE−CDおよびコルチコステロイドは摩砕して混合物を形成させる。次いで水性液体担体を混合物に加えて、本発明の標的溶液を形成させる。
摩砕は、乾式又は湿気、水、緩衝液、アルコール、界面活性剤、有機溶媒、グリセリン、ポリ(エチレングリコール)、ポロキサマーもしくはその組み合わせの存在下で行うことができる。
方法F
ここでのいずれかの方法を、熱の存在下、例えば、最小40℃の温度で行う。
ここでのいずれかの方法を、熱の存在下、例えば、最小40℃の温度で行う。
方法G
ここでのいずれかの方法を、冷却して、例えば、20℃未満または10℃未満または5℃未満の温度で行う。
ここでのいずれかの方法を、冷却して、例えば、20℃未満または10℃未満または5℃未満の温度で行う。
方法H
ここでのいずれかの方法を、超音波発生装置、ナローゲージシリンジ、ミキサー/ホモジナイザー(KINEMATICA(ヨーロッパ)製POLYTRON; FLUKO(上海、中国);GEA Niro, Inc.(メリーランド州コロンビア)製ULTIMAGRAL、回転子/固定子ミキサー、又は鋸歯ミキサーなどによる、高せん断混合の存在下行う。
ここでのいずれかの方法を、超音波発生装置、ナローゲージシリンジ、ミキサー/ホモジナイザー(KINEMATICA(ヨーロッパ)製POLYTRON; FLUKO(上海、中国);GEA Niro, Inc.(メリーランド州コロンビア)製ULTIMAGRAL、回転子/固定子ミキサー、又は鋸歯ミキサーなどによる、高せん断混合の存在下行う。
方法I
ここでのいずれかの方法を減圧下に行う。
ここでのいずれかの方法を減圧下に行う。
〔実施例2〕
SBE7−β−CDおよびブデソニドを含む噴霧溶液のMMDは、以下のように決定した。
3つの異なるシクロデキストリンのプラセボ溶液を異なる濃度で調製した。溶液2mlを、Pari Proneb Ultraコンプレッサから給気されるPari LC Plusネブライザーのカップに加えた。Malvern Mastersizer Sレーザー光散乱測定装置を使用して、放出液滴の粒径を決定した。
SBE7−β−CDおよびブデソニドを含む噴霧溶液のMMDは、以下のように決定した。
3つの異なるシクロデキストリンのプラセボ溶液を異なる濃度で調製した。溶液2mlを、Pari Proneb Ultraコンプレッサから給気されるPari LC Plusネブライザーのカップに加えた。Malvern Mastersizer Sレーザー光散乱測定装置を使用して、放出液滴の粒径を決定した。
〔実施例3〕
貯蔵されている液体から定期的に引き出されるアリコートのHPLCクロマトグラフィによりSAE−CDを含む液体製剤の安定性を決定した。
種々の量の0.01Mのクエン酸を0.02MのNa2HPO4に混合して、pH4、5、6、7または8のクエン酸リン酸塩(McIlvaines)緩衝液を調製した。これらの原液は、5%w/w Captisolを含んでいた。約250μg/mLのブデソニドをそれぞれの緩衝液中に溶解した。溶液のアリコートを40℃、50℃、および60℃で保管した。対照試料を5℃で保管したが、ここでは報告していない。試料のHPLC分析を最初と、1、2、および3ヶ月間貯蔵後に、実行した。
貯蔵されている液体から定期的に引き出されるアリコートのHPLCクロマトグラフィによりSAE−CDを含む液体製剤の安定性を決定した。
種々の量の0.01Mのクエン酸を0.02MのNa2HPO4に混合して、pH4、5、6、7または8のクエン酸リン酸塩(McIlvaines)緩衝液を調製した。これらの原液は、5%w/w Captisolを含んでいた。約250μg/mLのブデソニドをそれぞれの緩衝液中に溶解した。溶液のアリコートを40℃、50℃、および60℃で保管した。対照試料を5℃で保管したが、ここでは報告していない。試料のHPLC分析を最初と、1、2、および3ヶ月間貯蔵後に、実行した。
〔実施例4〕
コーンプレート粘度計を使用して、SAE−CDを含む水溶液の粘度を測定した。
Brookfield Programmable DV−III+Rheometer、CPE−40コーンおよびCPE 40Yプレート(Brookfield Engineering Laboratories、マサチューセッツ州ミドルボロ)を使用し、1、2、3、5、および10rpmで試料0.5mlについて測定を行った。それぞれの測定の前に約5回転している間に試料を剪断した。これにより、試料の正確なレオロジー特性が得られた。電子制御恒温循環水槽(Model、8001、Fisher Scientific、ペンシルバニア州ピッツバーグ)から水が供給される二重壁粘度計コーンを使用してすべての試料の温度を25±1℃に合わせた。シリコーンオイル較正基準を使用し、5および50センチポアズを使って粘度計を較正した。5以上の回転速度で粘度測定を行い、ずり流動化挙動(ずり速度が増加すると減少する粘度)を調べた。高回転になる程、ずり速度が増した。
コーンプレート粘度計を使用して、SAE−CDを含む水溶液の粘度を測定した。
Brookfield Programmable DV−III+Rheometer、CPE−40コーンおよびCPE 40Yプレート(Brookfield Engineering Laboratories、マサチューセッツ州ミドルボロ)を使用し、1、2、3、5、および10rpmで試料0.5mlについて測定を行った。それぞれの測定の前に約5回転している間に試料を剪断した。これにより、試料の正確なレオロジー特性が得られた。電子制御恒温循環水槽(Model、8001、Fisher Scientific、ペンシルバニア州ピッツバーグ)から水が供給される二重壁粘度計コーンを使用してすべての試料の温度を25±1℃に合わせた。シリコーンオイル較正基準を使用し、5および50センチポアズを使って粘度計を較正した。5以上の回転速度で粘度測定を行い、ずり流動化挙動(ずり速度が増加すると減少する粘度)を調べた。高回転になる程、ずり速度が増した。
〔実施例5〕
以下の一般的手順に従って、SAE−CD濃度の関数としてのネブライザーアウトプット率を測定した。
43%、21.5%、10.75%、および5.15%w/wのSBE7−β−CDを含む溶液について、Pari LC Plus NebulizerをPari ProNeb Ultra Air Compressorと共に使用し(最小ネブライザー体積=2ml、最大ネブライザー体積=8ml)、ネブライザーアウトプットを試験した。放出された試料のパーセンテージを質量測定法で推定した。噴霧が完了する前後にネブライザーカップを計量した。噴霧時間は、ネブライザー作動が開始してから最初のスパッター時間までの持続時間と定義した。ネブライザーアウトプット率は、放出%を噴霧時間で割って計算した。
以下の一般的手順に従って、SAE−CD濃度の関数としてのネブライザーアウトプット率を測定した。
43%、21.5%、10.75%、および5.15%w/wのSBE7−β−CDを含む溶液について、Pari LC Plus NebulizerをPari ProNeb Ultra Air Compressorと共に使用し(最小ネブライザー体積=2ml、最大ネブライザー体積=8ml)、ネブライザーアウトプットを試験した。放出された試料のパーセンテージを質量測定法で推定した。噴霧が完了する前後にネブライザーカップを計量した。噴霧時間は、ネブライザー作動が開始してから最初のスパッター時間までの持続時間と定義した。ネブライザーアウトプット率は、放出%を噴霧時間で割って計算した。
〔実施例6〕
ブデソニドを含む吸入可能溶液の調製。
クエン酸緩衝液3mMおよびNaCl 82mMを含むpH4.45の緩衝液を調製した。CAPTISOL約12.5グラムを250ml容量フラスコ内に入れた。ブデソニド約62.5mgを同じフラスコに入れた。フラスコをクエン酸緩衝液3mM/NaCl溶液82mMの体積にした。フラスコをボルテクサーで10分間よく混ぜ、10分間超音波処理した。磁気攪拌機でフラスコを週末に攪拌した。約62時間後に攪拌を止め、再びそれぞれ10分間フラスコを激しく攪拌し、超音波処理した。0.22μm Durapore Millex−GV Milliporeシリンジフィルターユニットを通して溶液を濾過した。最初の数滴を捨ててから、溶液の濾過の残り部分を、テフロン(登録商標)でライニングされたネジ蓋付きのアンバーグラスジャーに入れた。試料濃度は、約237μg/mlであった。
ブデソニドを含む吸入可能溶液の調製。
クエン酸緩衝液3mMおよびNaCl 82mMを含むpH4.45の緩衝液を調製した。CAPTISOL約12.5グラムを250ml容量フラスコ内に入れた。ブデソニド約62.5mgを同じフラスコに入れた。フラスコをクエン酸緩衝液3mM/NaCl溶液82mMの体積にした。フラスコをボルテクサーで10分間よく混ぜ、10分間超音波処理した。磁気攪拌機でフラスコを週末に攪拌した。約62時間後に攪拌を止め、再びそれぞれ10分間フラスコを激しく攪拌し、超音波処理した。0.22μm Durapore Millex−GV Milliporeシリンジフィルターユニットを通して溶液を濾過した。最初の数滴を捨ててから、溶液の濾過の残り部分を、テフロン(登録商標)でライニングされたネジ蓋付きのアンバーグラスジャーに入れた。試料濃度は、約237μg/mlであった。
〔実施例7〕
ブデソニドを含む吸入可能溶液の調製。
CAPTISOL約5グラムを100ml容量フラスコ内に入れた。ブデソニド約26.3mgを同じフラスコに入れた。フラスコをクエン酸緩衝液3mM/NaCl溶液82mMの体積にした。混合液をボルテクサーで10分間よく混ぜ、10分間超音波処理した。磁気攪拌機で混合液を一晩攪拌した。約16時間後に攪拌を止め、再びそれぞれ10分間フラスコを激しく攪拌し、超音波処理した。0.22μm Durapore Millex−GV Milliporeシリンジフィルターユニットを通して溶液を濾過した。最初の5滴を捨ててから、溶液の濾過の残り部分を、テフロンでライニングされたネジ蓋付きのアンバーグラスジャーに入れた。試料は、233μg/mlのブデソニドであると分析された。
ブデソニドを含む吸入可能溶液の調製。
CAPTISOL約5グラムを100ml容量フラスコ内に入れた。ブデソニド約26.3mgを同じフラスコに入れた。フラスコをクエン酸緩衝液3mM/NaCl溶液82mMの体積にした。混合液をボルテクサーで10分間よく混ぜ、10分間超音波処理した。磁気攪拌機で混合液を一晩攪拌した。約16時間後に攪拌を止め、再びそれぞれ10分間フラスコを激しく攪拌し、超音波処理した。0.22μm Durapore Millex−GV Milliporeシリンジフィルターユニットを通して溶液を濾過した。最初の5滴を捨ててから、溶液の濾過の残り部分を、テフロンでライニングされたネジ蓋付きのアンバーグラスジャーに入れた。試料は、233μg/mlのブデソニドであると分析された。
〔実施例8〕
ブデソニドを含む吸入可能溶液の調製。
12.5gのCAPTISOL、62.5mgのブデソニド、および約250mlの緩衝液を用いた以外は、実施例7の手順に従った。十分なEDTA二ナトリウムを加えて、EDTA濃度約0.01または0.05%wt/vEDTAを有する溶液を調製した。
ブデソニドを含む吸入可能溶液の調製。
12.5gのCAPTISOL、62.5mgのブデソニド、および約250mlの緩衝液を用いた以外は、実施例7の手順に従った。十分なEDTA二ナトリウムを加えて、EDTA濃度約0.01または0.05%wt/vEDTAを有する溶液を調製した。
〔実施例9〕
PULMICORT RESPULES懸濁液から調製されるようなSAE−CDおよびブデソニドを含む溶液の調製。
方法A
Pulmicort Respulesの1つまたはそれ以上の容器の内容物に対し(懸濁液公称2mL)、CAPTISOL約50mg(水分について補正)をRespuleの1mL毎に加え、数分間よく混ぜるか、振った。約30分間から数時間の間放置後、インビトロ特徴付けの場合のように溶液を使用した。ブデソニドおよび水に加えて、PULMICORT RESPULE(懸濁液)は、さらに、ラベルごとに、不活性成分として以下のもの:クエン酸、クエン酸ナトリウム、塩化ナトリウム、EDTA二ナトリウム、およびポリソルベート80も含む。
方法B
CAPTISOL(水分について補正)約200mgの量を計って2−ドラムアンバーバイアルに入れた。CAPTISOLの計量した量を含むそれぞれのバイアル内に、変形可能プラスチック容器を軽く押しつぶして最後の1滴まで絞り出すことにより2つのPulmicort Respules容器の中身(0.5mg/2mL、Lot#308016Feb05)を空けた。Respulesはすでに回転させ、ブデソニド粒子を再懸濁させてあった。バイアルはネジ蓋付きであり、ボルテックスで激しく混合し、次いでホイルで包んだ。この材料は、使用するまで冷蔵庫に保管しておくことができる。
これらの方法で調製された吸入可能液体組成物は、公知のどのネブライザーでも使用できる。懸濁液を液体に転換することにより、ブデソニド(コルチコステロイド)の送達の改善が観察される。
PULMICORT RESPULES懸濁液から調製されるようなSAE−CDおよびブデソニドを含む溶液の調製。
方法A
Pulmicort Respulesの1つまたはそれ以上の容器の内容物に対し(懸濁液公称2mL)、CAPTISOL約50mg(水分について補正)をRespuleの1mL毎に加え、数分間よく混ぜるか、振った。約30分間から数時間の間放置後、インビトロ特徴付けの場合のように溶液を使用した。ブデソニドおよび水に加えて、PULMICORT RESPULE(懸濁液)は、さらに、ラベルごとに、不活性成分として以下のもの:クエン酸、クエン酸ナトリウム、塩化ナトリウム、EDTA二ナトリウム、およびポリソルベート80も含む。
方法B
CAPTISOL(水分について補正)約200mgの量を計って2−ドラムアンバーバイアルに入れた。CAPTISOLの計量した量を含むそれぞれのバイアル内に、変形可能プラスチック容器を軽く押しつぶして最後の1滴まで絞り出すことにより2つのPulmicort Respules容器の中身(0.5mg/2mL、Lot#308016Feb05)を空けた。Respulesはすでに回転させ、ブデソニド粒子を再懸濁させてあった。バイアルはネジ蓋付きであり、ボルテックスで激しく混合し、次いでホイルで包んだ。この材料は、使用するまで冷蔵庫に保管しておくことができる。
これらの方法で調製された吸入可能液体組成物は、公知のどのネブライザーでも使用できる。懸濁液を液体に転換することにより、ブデソニド(コルチコステロイド)の送達の改善が観察される。
・濃縮物Aを無水ベースで5%w/vのCAPTISOLを含むようにpH4.5の食塩クエン酸緩衝液(salinated citrate buffer)(塩化ナトリウム109mMを含む4mM)で1対4に希釈した。0.22μm Millipore Durapore Millex−GVシリンジフィルターユニットを通して希釈濃縮物を濾過した。濾過された溶液をHPLCでアッセイし、次いで補助ブデソニドを必要に応じて加えて、溶液の最終濃度を約250μg/mL(±<5%)にした。
・濃縮物Bを無水ベースで5%w/vのCAPTISOLを含むようにpH4.5の食塩クエン酸緩衝液(塩化ナトリウム109mMを含む4mM)で1対4に希釈した。0.22μmのMillipore Durapore Millex−GVシリンジフィルターユニットを通して希釈濃縮物を濾過した。濾過された溶液をHPLCでアッセイし、次いでpH4.5の食塩クエン酸緩衝液(5%w/vのCAPTISOLを含む塩化ナトリウム82mMを含む3mM)で必要に応じてさらに希釈し、最終溶液濃度を約250μg/mL(±<5%)にした。この手法は、溶液を飽和させるために使用される過剰固体ブデソニドを利用した。
・濃縮物Bを無水ベースで5%w/vのCAPTISOLを含むようにpH4.5の食塩クエン酸緩衝液(塩化ナトリウム109mMを含む4mM)で1対4に希釈した。0.22μmのMillipore Durapore Millex−GVシリンジフィルターユニットを通して希釈濃縮物を濾過した。濾過された溶液をHPLCでアッセイし、次いでpH4.5の食塩クエン酸緩衝液(5%w/vのCAPTISOLを含む塩化ナトリウム82mMを含む3mM)で必要に応じてさらに希釈し、最終溶液濃度を約250μg/mL(±<5%)にした。この手法は、溶液を飽和させるために使用される過剰固体ブデソニドを利用した。
〔実施例11〕
目視検査または計測器で溶液の澄明度を測定した。肉眼による目視検査では、澄明溶液は少なくとも澄明であった。
目視検査または計測器で溶液の澄明度を測定した。肉眼による目視検査では、澄明溶液は少なくとも澄明であった。
〔実施例12〕
以下の方法を使用して、図10a〜10bに従い、ネブライザーから放出された噴霧組成物の性能を決定した。
2mlの試験CD溶液またはPulmicort懸濁液を容積ピペットで、清浄ネブライザーカップ内に正確に取り、その後、それぞれの実験を開始した。製造業者の取扱説明書に従って、試験ネブライザーを組み立てて、試験吸入溶液または懸濁液を充填した。マウスピースの末端をMALVERN MASTERSIZERの台からネブライザーマウスピースの先端の中点まで約18cmの高さに置いた。真空源を、マウスピースの反対側に約6cm離して配置し、サイジングの後にエアロゾルをスカベンジした。マウスピースと検出器との間の距離は約8cmであった。マウスピースの中心を、レーザービームと同じ高さにした(または、それぞれのネブライザーの個々の設計に応じて、適宜調節した)。レーザーは、ネブライザーが稼働したときに放出雲の中心を通過した。測定は、噴霧してから15秒後に手動で開始した。データ収集は、ビームの暗さが10%に到達したときに開始し、15,000回のスイープ(30秒)にわたって平均をとった。「Standard−Wet」モデルを使用して、検出器リング上の散乱光強度データをモデル化した。測定時に低い相対湿度のためチャネル1および2を殺し、ビームステアリングを防いだ。累積体積アンダーサイズの10、50(体積中央値)、および90%を定義する液滴の体積直径を決定した。(Dv10は、物質の体積の10%が存在する最大のサイズであり、Dv50は、物質の体積の50%が存在する最大のサイズであり、Dv90は、物質の体積の90%が存在する最大のサイズである。)
ネブライザーによって放出した液滴の粒径を測定するために、MALVERNSPRAYTECをわずかに改変して上記手順で実行することができる。
以下の方法を使用して、図10a〜10bに従い、ネブライザーから放出された噴霧組成物の性能を決定した。
2mlの試験CD溶液またはPulmicort懸濁液を容積ピペットで、清浄ネブライザーカップ内に正確に取り、その後、それぞれの実験を開始した。製造業者の取扱説明書に従って、試験ネブライザーを組み立てて、試験吸入溶液または懸濁液を充填した。マウスピースの末端をMALVERN MASTERSIZERの台からネブライザーマウスピースの先端の中点まで約18cmの高さに置いた。真空源を、マウスピースの反対側に約6cm離して配置し、サイジングの後にエアロゾルをスカベンジした。マウスピースと検出器との間の距離は約8cmであった。マウスピースの中心を、レーザービームと同じ高さにした(または、それぞれのネブライザーの個々の設計に応じて、適宜調節した)。レーザーは、ネブライザーが稼働したときに放出雲の中心を通過した。測定は、噴霧してから15秒後に手動で開始した。データ収集は、ビームの暗さが10%に到達したときに開始し、15,000回のスイープ(30秒)にわたって平均をとった。「Standard−Wet」モデルを使用して、検出器リング上の散乱光強度データをモデル化した。測定時に低い相対湿度のためチャネル1および2を殺し、ビームステアリングを防いだ。累積体積アンダーサイズの10、50(体積中央値)、および90%を定義する液滴の体積直径を決定した。(Dv10は、物質の体積の10%が存在する最大のサイズであり、Dv50は、物質の体積の50%が存在する最大のサイズであり、Dv90は、物質の体積の90%が存在する最大のサイズである。)
ネブライザーによって放出した液滴の粒径を測定するために、MALVERNSPRAYTECをわずかに改変して上記手順で実行することができる。
〔実施例13〕
SBE7−β−CDがある場合とない場合のブデソニドの溶液を2つの異なるpH(4および6)で調製し、2つの異なる温度(60℃および80℃)で保管した。クエン酸50mMおよびクエン酸ナトリウム溶液(三塩基性、二水和物)50mMの異なる部分を混合することによりそれぞれのpH値のクエン酸塩緩衝剤(50mM)を調製した。正確な測定を行うのに十分なSBE7−β−CDなしで緩衝液中のブデソニドの濃度を得るために、まず、ブデソニドを100%エチルアルコールに溶解した。次いでエタノール/ブデソニドのアリコートを攪拌しつつ1滴ずつそれぞれの緩衝液に加えた。理論的ブデソニド濃度は、100μg/mlであり、最終エタノール含有量はそれぞれの緩衝液中で5%であった。ブデソニドを伴うすべての溶液の調製および手順は、赤色光で照らした暗室内で行った。溶液を24時間振った後、両方の緩衝液をMillipore Millex−GV 0.22μmシリンジフィルターに通して濾過し、溶液から沈殿した固体(有意な量は観察されなかった)を取り除いた。最終的なブデソニド濃度は約50μg/mLであった。pH4および6の溶液の両方を2つに分けて、固体SBE7−β−CDを一方の部分に加え、それぞれのpHで1%w/vのSBE7−β−CDがある場合とない場合の溶液を作成した。それぞれの溶液を等分して個々のアンバーバイアルに入れた。次いで、60℃および80℃のオーブンに入れた。試料バイアルをオーブンから取り出して、0、96、164、および288時間でHPLCにより分析した。HPLCアッセイ条件を以下にまとめた。
SBE7−β−CDがある場合とない場合のブデソニドの溶液を2つの異なるpH(4および6)で調製し、2つの異なる温度(60℃および80℃)で保管した。クエン酸50mMおよびクエン酸ナトリウム溶液(三塩基性、二水和物)50mMの異なる部分を混合することによりそれぞれのpH値のクエン酸塩緩衝剤(50mM)を調製した。正確な測定を行うのに十分なSBE7−β−CDなしで緩衝液中のブデソニドの濃度を得るために、まず、ブデソニドを100%エチルアルコールに溶解した。次いでエタノール/ブデソニドのアリコートを攪拌しつつ1滴ずつそれぞれの緩衝液に加えた。理論的ブデソニド濃度は、100μg/mlであり、最終エタノール含有量はそれぞれの緩衝液中で5%であった。ブデソニドを伴うすべての溶液の調製および手順は、赤色光で照らした暗室内で行った。溶液を24時間振った後、両方の緩衝液をMillipore Millex−GV 0.22μmシリンジフィルターに通して濾過し、溶液から沈殿した固体(有意な量は観察されなかった)を取り除いた。最終的なブデソニド濃度は約50μg/mLであった。pH4および6の溶液の両方を2つに分けて、固体SBE7−β−CDを一方の部分に加え、それぞれのpHで1%w/vのSBE7−β−CDがある場合とない場合の溶液を作成した。それぞれの溶液を等分して個々のアンバーバイアルに入れた。次いで、60℃および80℃のオーブンに入れた。試料バイアルをオーブンから取り出して、0、96、164、および288時間でHPLCにより分析した。HPLCアッセイ条件を以下にまとめた。
クロマトグラフィー条件
(Hou、S.、Hindle、M.、およびByron、P.R.A.、Stability−Indicating HPLC Assay Method for Budesonide、Journal of Pharmaceutical and Biomedical Analysis、2001年、24:371〜380頁から適合させた)
(Hou、S.、Hindle、M.、およびByron、P.R.A.、Stability−Indicating HPLC Assay Method for Budesonide、Journal of Pharmaceutical and Biomedical Analysis、2001年、24:371〜380頁から適合させた)
〔実施例14〕
SAE−CD、ブデソニド、および硫酸アルブテロールを含む併用溶液の調製および使用。
実施例9(SAE−CDをPULMICORT RESPULES懸濁液と混合する)に従ってブデソニド溶液を調製し、硫酸アルブテロールとして提供される2.5mgのアルブテロール(アルブテロール塩基の世界保健機関推奨名は、サルブタモールである)を含む溶液3mlに加えた。アルブテロール溶液は、事前希釈で市販されており、PROVENTIL(登録商標)Inhalation Solution(0.083%)という名前で販売されているか、または市販の濃縮物0.5%(吸入用にPROVENTIL(登録商標)Solutionという名前で、またVENTOLIN(登録商標)Inhalation Solutionという名前で販売されている)から調製した。
2歳から12歳の小児に必要用量を与えるために、初期投薬は体重(1用量当たり0.1から0.15mg/kg)に基づき、その後、用量を漸増して、所望の臨床反応を得るようにした。投薬は、1日3から4回噴霧で、2.5mgを超えてはならない。0.5%吸入溶液の適切な体積は、噴霧投与前に、無菌生理食塩水で希釈し全体積を3mLにしなければならない。2.5mgを与えるために、濃縮物0.5mLを無菌生理食塩水で3mLに希釈した。アルブテロール水溶液は、さらに、塩化ベンザルコニウムも含み、硫酸を使用して、pHを3から5の範囲に調整した。それとは別に、保存剤塩化ベンザルコニウムを添加した場合またはしない場合に適切な強度のアルブテロールの水溶液を硫酸アルブテロールから調製することができ、硫酸を使用するpH調整は、コルチコステロイド溶液と組み合わせる場合には不要な場合もある。さらに、適切な用量のコルチコステロイドを含む体積を、以下の実施例で説明されているように4倍減らして、全体積を小さくし、投与時間をそれに応じて短縮することができる。
SAE−CD、ブデソニド、および硫酸アルブテロールを含む併用溶液の調製および使用。
実施例9(SAE−CDをPULMICORT RESPULES懸濁液と混合する)に従ってブデソニド溶液を調製し、硫酸アルブテロールとして提供される2.5mgのアルブテロール(アルブテロール塩基の世界保健機関推奨名は、サルブタモールである)を含む溶液3mlに加えた。アルブテロール溶液は、事前希釈で市販されており、PROVENTIL(登録商標)Inhalation Solution(0.083%)という名前で販売されているか、または市販の濃縮物0.5%(吸入用にPROVENTIL(登録商標)Solutionという名前で、またVENTOLIN(登録商標)Inhalation Solutionという名前で販売されている)から調製した。
2歳から12歳の小児に必要用量を与えるために、初期投薬は体重(1用量当たり0.1から0.15mg/kg)に基づき、その後、用量を漸増して、所望の臨床反応を得るようにした。投薬は、1日3から4回噴霧で、2.5mgを超えてはならない。0.5%吸入溶液の適切な体積は、噴霧投与前に、無菌生理食塩水で希釈し全体積を3mLにしなければならない。2.5mgを与えるために、濃縮物0.5mLを無菌生理食塩水で3mLに希釈した。アルブテロール水溶液は、さらに、塩化ベンザルコニウムも含み、硫酸を使用して、pHを3から5の範囲に調整した。それとは別に、保存剤塩化ベンザルコニウムを添加した場合またはしない場合に適切な強度のアルブテロールの水溶液を硫酸アルブテロールから調製することができ、硫酸を使用するpH調整は、コルチコステロイド溶液と組み合わせる場合には不要な場合もある。さらに、適切な用量のコルチコステロイドを含む体積を、以下の実施例で説明されているように4倍減らして、全体積を小さくし、投与時間をそれに応じて短縮することができる。
〔実施例15〕
SAE−CD、ブデソニド、および硫酸アルブテロール、またはレバルブテロールHCL(XOPENEX)を含む併用溶液の調製および使用。
以下のようにクエン酸緩衝剤(3mM pH4.5)を調製した。1つの100ml容量フラスコでクエン酸約62.5mgを水に溶解し、水を入れてその体積にした。もう1つの100ml容量フラスコでクエン酸ナトリウム約87.7mgを水に溶解し、水を入れてその体積にした。ビーカー内で、クエン酸ナトリウム溶液をクエン酸溶液に加え、pHを約4.5にした。
約10.4mgのブデソニドおよび1247.4mgのCaptisolをすり鉢とすりこぎで一緒にすり、10mLフラスコに移した。緩衝液を加えて、混合物を激しく攪拌し、超音波処理し、さらに1.4mgのブデソニドを加えた。一晩振って、0.22μm Durapore Millex−GV Milliporeシリンジフィルターユニットを通して溶液を濾過した。その結果得られるブデソニド濃度は約1mg/mlであった。ほぼ0.5mlのブデソニド溶液を単位用量のProventil(2.5mg/3mL)またはXopenex(1.25mg/3mL)のいずれかに加えて、本発明の組み合わせ澄明液体投薬形態を形成した。その結果得られる混合物は、光を遮った室温条件で少なくとも17日間本質的に澄明のままであった。
SAE−CD、ブデソニド、および硫酸アルブテロール、またはレバルブテロールHCL(XOPENEX)を含む併用溶液の調製および使用。
以下のようにクエン酸緩衝剤(3mM pH4.5)を調製した。1つの100ml容量フラスコでクエン酸約62.5mgを水に溶解し、水を入れてその体積にした。もう1つの100ml容量フラスコでクエン酸ナトリウム約87.7mgを水に溶解し、水を入れてその体積にした。ビーカー内で、クエン酸ナトリウム溶液をクエン酸溶液に加え、pHを約4.5にした。
約10.4mgのブデソニドおよび1247.4mgのCaptisolをすり鉢とすりこぎで一緒にすり、10mLフラスコに移した。緩衝液を加えて、混合物を激しく攪拌し、超音波処理し、さらに1.4mgのブデソニドを加えた。一晩振って、0.22μm Durapore Millex−GV Milliporeシリンジフィルターユニットを通して溶液を濾過した。その結果得られるブデソニド濃度は約1mg/mlであった。ほぼ0.5mlのブデソニド溶液を単位用量のProventil(2.5mg/3mL)またはXopenex(1.25mg/3mL)のいずれかに加えて、本発明の組み合わせ澄明液体投薬形態を形成した。その結果得られる混合物は、光を遮った室温条件で少なくとも17日間本質的に澄明のままであった。
〔実施例16〕
SAE−CD、ブデソニド、およびホルモテロール(FORADIL(登録商標)(フマル酸ホルモテロール吸入粉末)を含む併用溶液の調製および使用。
乳糖25mgとブレンドされた12mcgのフマル酸ホルモテロールを含む1カプセルの内容物をバイアルに空けて、そこに、前の実施例で説明されているように調製された3mMのクエン酸緩衝液(pH4.5)3mLを加えた。バイアルの内容物を激しく攪拌して、存在する固形物を溶解した。前の実施例で説明されているようにブデソニド濃縮物を調製し、濃度を約1mg/mLとした。約1mlのブデソニド溶液をフマル酸ホルモテロール緩衝化溶液に加えた。その結果得られる溶液は、光を遮った室温条件で少なくとも1ヶ月間本質的に澄明のままであった。
SAE−CD、ブデソニド、およびホルモテロール(FORADIL(登録商標)(フマル酸ホルモテロール吸入粉末)を含む併用溶液の調製および使用。
乳糖25mgとブレンドされた12mcgのフマル酸ホルモテロールを含む1カプセルの内容物をバイアルに空けて、そこに、前の実施例で説明されているように調製された3mMのクエン酸緩衝液(pH4.5)3mLを加えた。バイアルの内容物を激しく攪拌して、存在する固形物を溶解した。前の実施例で説明されているようにブデソニド濃縮物を調製し、濃度を約1mg/mLとした。約1mlのブデソニド溶液をフマル酸ホルモテロール緩衝化溶液に加えた。その結果得られる溶液は、光を遮った室温条件で少なくとも1ヶ月間本質的に澄明のままであった。
〔実施例17〕
投薬形態の噴霧投与の前後に、被験者に対しガンマシンチグラフィー分析を実施することにより本発明による投薬形態の臨床評価を行った。
Pari LC空気ジェット式ネブライザーを使用したPulmicort Respules(登録商標)、およびCaptisol−Enabled(登録商標)ブデソニド製剤を介したブデソニドの経肺送達を比較するシングルセンター・フォーウェイクロスオーバーガンマシンチグラフィー研究を実施した。この研究の目的は、健常男性ボランティアにブデソニド懸濁液(Pulmicort Respules(登録商標)、Astra Zeneca、基準製剤)およびCaptisol(登録商標)−Enabledブデソニド溶液(試験製剤)を噴霧した後の放射性標識ブデソニドの肺内沈着をガンマシンチグラフィーにより調べることであった。検討の過程において、24時間まで経時的に採血し、血漿を分離した。薬物動態学的パラメータを決定するために、血漿中のブデソニドの濃度を妥当性が確認されたHPLC MS−MS法を用いて測定した。投薬は、Pari LC Plus空気ジェット式ネブライザーを使用して行った。ガンマシンチグラフィーを放射性標識研究薬剤および/またはビヒクルと共に使用することは、吸入薬剤および/またはビヒクルの肺沈着および除去の定量的評価を行うための標準的手法である。
投薬形態の噴霧投与の前後に、被験者に対しガンマシンチグラフィー分析を実施することにより本発明による投薬形態の臨床評価を行った。
Pari LC空気ジェット式ネブライザーを使用したPulmicort Respules(登録商標)、およびCaptisol−Enabled(登録商標)ブデソニド製剤を介したブデソニドの経肺送達を比較するシングルセンター・フォーウェイクロスオーバーガンマシンチグラフィー研究を実施した。この研究の目的は、健常男性ボランティアにブデソニド懸濁液(Pulmicort Respules(登録商標)、Astra Zeneca、基準製剤)およびCaptisol(登録商標)−Enabledブデソニド溶液(試験製剤)を噴霧した後の放射性標識ブデソニドの肺内沈着をガンマシンチグラフィーにより調べることであった。検討の過程において、24時間まで経時的に採血し、血漿を分離した。薬物動態学的パラメータを決定するために、血漿中のブデソニドの濃度を妥当性が確認されたHPLC MS−MS法を用いて測定した。投薬は、Pari LC Plus空気ジェット式ネブライザーを使用して行った。ガンマシンチグラフィーを放射性標識研究薬剤および/またはビヒクルと共に使用することは、吸入薬剤および/またはビヒクルの肺沈着および除去の定量的評価を行うための標準的手法である。
研究投薬形態は、1)2mL×0.5mg/mL Pulmicort Respules(登録商標)として1mgブデソニド、または2)7.5% w/v Captisol(登録商標)が加えられた2mL×0.5mg/mL Pulmicort Respulesとして1mgブデソニドで構成された。
それぞれの被験者は、無作為でない形で、放射性標識ブデソニドの4回の研究投与のそれぞれを受けた。この研究に、非無作為実験計画を使用したが、それは、スパッター時間(TTS)を決定するために、基準製剤(Pulmicort Respule(登録商標))は、最初に、すべての被験者に投与されなければならないからである。TTSは、被験者間で異なっていた。その後の投与では、投与される用量は、基準製剤の投与の後に決定されたスパッター時間の分数(すなわち、25% TTS、50% TTS、および75% TTS)として表される投与の長さにより制御された。同じ濃度のブデソニドが短時間の間に噴霧されるとしても、ボランティアの肺に到達する薬剤の量は、研究の複数の区間の1つに対する基準懸濁液と本質的に同じであると予想された。ボランティアへの投薬の完了直後に、ガンマカメラを使用してシンチグラフィー像を得た。
基準製品からの像と25%TTS区間を比較すると、投与直後、Respuleからのより大きな割合のブデソニドが胃および喉に入っていた。そのため、Captisolを使用してブデソニドを溶解した場合、より大きな割合のブデソニドが標的肺組織に到達した。これにより、薬剤により引き起こされる望ましくない副作用を軽減することができた。そこで、本発明の方法および投薬形態の一態様では、コルチコステロイド懸濁液ベースの単位用量を投与する改善された方法を提供し、この方法は、懸濁液を澄明溶液に転換する十分な量のSAE−CDを加え、次いで、澄明溶液を被験者に投与する工程を含む。その結果、本発明の方法は、初期単位用量懸濁液製剤に比較して、投与速度を高めるだけでなく、コルチコステロイドの全経肺送達を高速化した。
〔実施例18〕
コルチコステロイド誘導体の可溶化におけるさまざまな形態のSAE−CDの比較評価。
CAPTISOLおよびさまざまなSBEnγ−CDを含む溶液中のジプロピオン酸ベクロメタゾン(BDP)、17−モノプロピオン酸ベクロメタゾン(B17P)、21−モノプロピオン酸ベクロメタゾン(B21P)、およびベクロメタゾン(非エステル化)の溶解度を評価した。BDP、B17P、およびB21Pは、Hovioneから入手した。ベクロメタゾンは、Spectrum Chemicalsから入手した。CAPTISOL、SBE(3.4)γ−CD、SBE(5.23)γ−CD、およびSBE(6.1)γ−CDは、CyDex,Inc.(カンザス州レネクサ)が提供した。γ−CDは、Wacker Chemical Co.から入手した。SBE(5.24)γ−CDおよびSBE(7.5)γ−CDは、カンザス大学から提供された。
それぞれの選択されるCDの0.04M溶液を調製した。それぞれの形態のベクロメタゾンは、2mlのCD溶液を必要とした。したがって0.04M溶液を20または25mL容量フラスコ内で二重(N=2)に調製した。以下の表は、それぞれのCD内の水の含有量を計算した後に使用されたそれぞれのCDの量を示している。
コルチコステロイド誘導体の可溶化におけるさまざまな形態のSAE−CDの比較評価。
CAPTISOLおよびさまざまなSBEnγ−CDを含む溶液中のジプロピオン酸ベクロメタゾン(BDP)、17−モノプロピオン酸ベクロメタゾン(B17P)、21−モノプロピオン酸ベクロメタゾン(B21P)、およびベクロメタゾン(非エステル化)の溶解度を評価した。BDP、B17P、およびB21Pは、Hovioneから入手した。ベクロメタゾンは、Spectrum Chemicalsから入手した。CAPTISOL、SBE(3.4)γ−CD、SBE(5.23)γ−CD、およびSBE(6.1)γ−CDは、CyDex,Inc.(カンザス州レネクサ)が提供した。γ−CDは、Wacker Chemical Co.から入手した。SBE(5.24)γ−CDおよびSBE(7.5)γ−CDは、カンザス大学から提供された。
それぞれの選択されるCDの0.04M溶液を調製した。それぞれの形態のベクロメタゾンは、2mlのCD溶液を必要とした。したがって0.04M溶液を20または25mL容量フラスコ内で二重(N=2)に調製した。以下の表は、それぞれのCD内の水の含有量を計算した後に使用されたそれぞれのCDの量を示している。
ベクロメタゾン形態は、予想溶解度を超える量だけ計量して2−ドラムのテフロンでライニングされたネジ蓋付きバイアル内に直接入れた。これらの量では、典型的に、約6mg/mLの固体が得られた。次いで、それぞれのバイアルは、適切なCD溶液2mLを受け入れた。バイアルを激しく攪拌し、約10分間超音波処理し、固形物を流体で濡らすのを助けた。次いで、バイアルをアルミホイルで包んで光から保護し、ラブクエーク(lab quake)上に置いて平衡させた。バイアルを定期的に目視検査し、固体が適切に濡れ、流体に接触していることを確認した。サンプリングの時間点は、すべての試料について24時間、BDPのみについては72時間であった。
SBE(6.1)γ−CDの溶液を0.04、0.08、および0.1Mで、SBE(5.23)γ−CDの溶液を0.04および0.08Mでのみ調製した。ジプロピオン酸ベクロメタゾンは、予想溶解度を超える量だけ計量して2−ドラムのテフロンでライニングされたネジ蓋付きバイアル内に直接入れた。これらの量では、典型的に、約2mg/mLの固体が得られた。次いで、それぞれのバイアルは、適切なCD溶液2mLを受け入れた(N=1)。バイアルを激しく攪拌し、約10分間超音波処理し、固形物を流体で濡らすのを助けた。次いで、バイアルをアルミホイルで包んで光から保護し、ラブクエーク上に置いて5日間で平衡させた。
γ−CDの溶液を0.01および0.02Mで調製した。ジプロピオン酸ベクロメタゾンは、予想溶解度を超える量だけ計量して2−ドラムのテフロンでライニングされたネジ蓋付きバイアル内に直接入れた。これらの量では、典型的に、約2mg/mLの固体が得られた。次いで、それぞれのバイアルは、γ−CD溶液2mLを受け入れた(N=2)。さらに、BDPの固有溶解度を測定するために、CDの代わりにHPLCグレード水を使用して溶液を調製した。試料をホイルにくるみ、5日間ラブクエーク上に置いた。
各段階で平衡時間が終わると、バイアルを遠心分離器にかけ、上清1mlを取り除いた。次いで、Durapore PVDF 0.22μmシリンジフィルターを使用して(最初の数滴を捨てる)、取り除いた浮遊物を濾過し、移動相で希釈して標準曲線内の適切な濃度にした。次いで、HPLCにより試料を分析し、可溶化されたコルチコステロイドの濃度を決定した。
〔実施例19〕
SAE−CD、ブデソニド、およびフマル酸ホルモテロールを含む併用溶液の調製および使用。
フマル酸ホルモテロール乾燥粉末をCaptisol乾燥粉末と混合したが、両方とも、質量比12mcgフマル酸ホルモテロール/100mg Captisolで含有量一様になるように適切なサイズにした。単位用量のフマル酸ホルモテロールに対応する粉末ブレンドの量を後で使用するためのHPMCカプセルなどの適当な単位用量容器に入れるか、または直接、単位用量のPulmicort Respulesブデソニド吸入用懸濁液(500mcg/2mL)に加え、次いで、混合して、すべての固体の溶解を行い(澄明溶液)、投与用のネブライザーリザーバ内に入れた。
SAE−CD、ブデソニド、およびフマル酸ホルモテロールを含む併用溶液の調製および使用。
フマル酸ホルモテロール乾燥粉末をCaptisol乾燥粉末と混合したが、両方とも、質量比12mcgフマル酸ホルモテロール/100mg Captisolで含有量一様になるように適切なサイズにした。単位用量のフマル酸ホルモテロールに対応する粉末ブレンドの量を後で使用するためのHPMCカプセルなどの適当な単位用量容器に入れるか、または直接、単位用量のPulmicort Respulesブデソニド吸入用懸濁液(500mcg/2mL)に加え、次いで、混合して、すべての固体の溶解を行い(澄明溶液)、投与用のネブライザーリザーバ内に入れた。
〔実施例20〕
SAE−CD、ブデソニド、および臭化イプラトロピウムを含む併用溶液の調製および使用。
ブデソニド溶液を実施例9に従って調製し、市販されており、ATROVENT(登録商標)Inhalation Solution Unit Doseという名称で販売されている臭化イプラトロピウム溶液に加えた。ATROVENT(登録商標)(臭化イプラトロピウム)吸入用溶液は、1日3回から4回に分けて、6時間から8時間間隔の投薬で経口噴霧投与される500mcg(1単位用量バイアル)である。ATROVENT(登録商標)吸入用溶液単位用量バイアルは、塩酸で3.4(3から4)にpH調整された2.5mlの無菌保存剤不使用等張食塩水中に500mcgの無水臭化イプラトロピウムを含んでいる。さらに、適切な用量のコルチコステロイドを含む体積を、上記の実施例(ブデソニド濃縮物約1mg/mL)で説明されているように4倍減らして、全体積を小さくし、投与時間をそれに応じて短縮することができる。
SAE−CD、ブデソニド、および臭化イプラトロピウムを含む併用溶液の調製および使用。
ブデソニド溶液を実施例9に従って調製し、市販されており、ATROVENT(登録商標)Inhalation Solution Unit Doseという名称で販売されている臭化イプラトロピウム溶液に加えた。ATROVENT(登録商標)(臭化イプラトロピウム)吸入用溶液は、1日3回から4回に分けて、6時間から8時間間隔の投薬で経口噴霧投与される500mcg(1単位用量バイアル)である。ATROVENT(登録商標)吸入用溶液単位用量バイアルは、塩酸で3.4(3から4)にpH調整された2.5mlの無菌保存剤不使用等張食塩水中に500mcgの無水臭化イプラトロピウムを含んでいる。さらに、適切な用量のコルチコステロイドを含む体積を、上記の実施例(ブデソニド濃縮物約1mg/mL)で説明されているように4倍減らして、全体積を小さくし、投与時間をそれに応じて短縮することができる。
〔実施例21〕
ブデソニド、水性液体担体及びSAE−CDを含む溶液を用いた、AERONEB GOネブライザー対RAINDROPネブライザーの評価。
AERONEB GOネブライザー(AEROGEN Inc.、マウンテンビュー、カリフォルニア)は、Powerらの米国特許付与前特許公開第2005−011514
号(2004年4月27日に出願された特願USSN10/833,932)、Aerogen, Inc.らのPCT国際特許公開公報WO第2005/009323号(2004年7月6日に出願されたPCT出願PCT/US第2004/021268号)、及び欧州出願EP第16426276号中に詳述され、その開示全体は参照により本明細書に組み入れられている。
RAINDROPネブライザーはNellcor(Tyco Healthcare)から入手することができる。
本検討に用いる本発明の溶液は、実施例28に従って調製された。
カスケードインパクタを用いるエアロゾル化溶液の液滴粒度分布の特性評価は、実施例26に従って測定された。
本発明の液体を含むネブライザーからの全薬剤アウトプット及び薬剤アウトプット率の測定は、実施例27に従って行われた。
ブデソニド、水性液体担体及びSAE−CDを含む溶液を用いた、AERONEB GOネブライザー対RAINDROPネブライザーの評価。
AERONEB GOネブライザー(AEROGEN Inc.、マウンテンビュー、カリフォルニア)は、Powerらの米国特許付与前特許公開第2005−011514
号(2004年4月27日に出願された特願USSN10/833,932)、Aerogen, Inc.らのPCT国際特許公開公報WO第2005/009323号(2004年7月6日に出願されたPCT出願PCT/US第2004/021268号)、及び欧州出願EP第16426276号中に詳述され、その開示全体は参照により本明細書に組み入れられている。
RAINDROPネブライザーはNellcor(Tyco Healthcare)から入手することができる。
本検討に用いる本発明の溶液は、実施例28に従って調製された。
カスケードインパクタを用いるエアロゾル化溶液の液滴粒度分布の特性評価は、実施例26に従って測定された。
本発明の液体を含むネブライザーからの全薬剤アウトプット及び薬剤アウトプット率の測定は、実施例27に従って行われた。
〔実施例22〕
ブデソニド、水性液体担体及びSAE−CDを含む溶液による米国特許第6,962,151号の脈動膜ネブライザーの評価。Pari電子ネブライザー発生Tc99m−DTPA標識Captisol−Enabled(登録商標)ブデソニドエアロゾルの慣性衝突特性化。
米国特許第6,962,151号に詳述されるネブライザーも、2000年10月27日に出願されたPCT国際出願PCT/US00/29541号、および2005年11月7日に出願された米国特許出願第11/269,783号に記載されている。
ブデソニド、水性液体担体及びSAE−CDを含む溶液による米国特許第6,962,151号の脈動膜ネブライザーの評価。Pari電子ネブライザー発生Tc99m−DTPA標識Captisol−Enabled(登録商標)ブデソニドエアロゾルの慣性衝突特性化。
米国特許第6,962,151号に詳述されるネブライザーも、2000年10月27日に出願されたPCT国際出願PCT/US00/29541号、および2005年11月7日に出願された米国特許出願第11/269,783号に記載されている。
エアロゾルの特性評価は、Anderson Cascade Impactor(ACI)を用いる標準インビトロ慣性衝突検査によって行われた。ジエチレントリアミンペンタ酢酸(DTPA GE Healthcare)の形態でのテクネチウム−99m(99mTc)を、Captisol−Enabled(登録商標)ブデソニド吸入溶液(CEBUD)に加えた。CEBUD製剤中のブデソニドの代替として機能する99mTc−DTPA標識の適切性を、早期臨床治験の過程で検証した(実施例17参照)。試験用のブデソニド溶液製剤の調製を、下記に記述のように行った。インビトロ・イメージングに十分な活性を与えるために、検査日にほぼ10MBqの99mTcをブデソニド製剤(11.05g)に加えるべきであることが算出された。
2種のPari電子振動膜ネブライザーを使用した。この電子ネブライザーのコアは数千のレーザードリル穴を有するステンレススチール膜である。レーザードリルでは、粒径をカスタマイズし、再現性を保証し、更に小粒子の高アウトプット率を維持するフレキシビリティを可能にする。有孔膜は、高い粒子アウトプット率をもたらす共振「曲げ」様式にて高周波で振動する。ネブライザーは、迅速薬剤送達、効率性、理想的粒度測定、低い残留量、および吸入製剤にマッチした最適性能をもたらす(Rajiv Dhand、 Respiratory Care 2002年;(12):1406〜1416頁を参照)。ほぼ0.5mLの薬剤溶液を充填し、その後3回の別々の機会に各ネブライザーから送達した。試行1、3及び5は装置1で実施し、そして試行2、4及び6は装置2で実施した。
投与前(pre−dose)
投与量送達に先立ち、その度毎に、充填ネブライザーを二重頭部ガンマカメラ(Axis、 Philips Medical Systems)の頭部Iで60秒間撮像した。また、ネブライザーをブデソニド製剤の添加前後に計量した。
投与量送達に先立ち、その度毎に、充填ネブライザーを二重頭部ガンマカメラ(Axis、 Philips Medical Systems)の頭部Iで60秒間撮像した。また、ネブライザーをブデソニド製剤の添加前後に計量した。
慣性衝突試験
ネブライザーを、ACIのUSP(アメリカ薬局方)インレットに配置し、そして28.3L/分の流量で真空ポンプを用いてインパクターを介して引いた。インパクター通過の流れを、電子ネブライザーを起動する前に開始した。用量送達の時間を測定するために、ストップウォッチを使用した。
ACI試験条件は、初期臨床試験の過程でPari LC Plus空気ジェット式ネブライザー評価に使用したものと同じであった。
沈着後にUSPスロウトをACIから取り出し、120秒間撮像した。回収プレートをインパクターから取り外し、次いでガンマカメラの頭部Iに置いて120秒間撮像した。その後プレートを洗浄し、更なるインパクション試験の実行前に乾燥した。
ネブライザーを、ACIのUSP(アメリカ薬局方)インレットに配置し、そして28.3L/分の流量で真空ポンプを用いてインパクターを介して引いた。インパクター通過の流れを、電子ネブライザーを起動する前に開始した。用量送達の時間を測定するために、ストップウォッチを使用した。
ACI試験条件は、初期臨床試験の過程でPari LC Plus空気ジェット式ネブライザー評価に使用したものと同じであった。
沈着後にUSPスロウトをACIから取り出し、120秒間撮像した。回収プレートをインパクターから取り外し、次いでガンマカメラの頭部Iに置いて120秒間撮像した。その後プレートを洗浄し、更なるインパクション試験の実行前に乾燥した。
投与後(post−dose)
その度毎に、用量の送達後ネブライザー重量を記録した。ネブライザーを下記のように撮像した。
その度毎に、用量の送達後ネブライザー重量を記録した。ネブライザーを下記のように撮像した。
画像処理
投与前ネブライザーを撮像するために矩形ROIを使用した。このROIは投与量送達後にネブライザーを撮像するために再使用した。
矩形ROIはUSPインレット画像にも適用した。
円形ROIは、収集プレート0の周りに集められ、写されそしてプレート1の周りに置かれた。これをプレート2〜7およびフィルターで繰り返した。矩形ROIはバックグラウンドカウントを評価するためにも行なわれた。概数カウントはバックグラウンドアクティビティで補正され、1分当りのカウント(cpm)に調整された。
エアロゾル性能は、微粒子画分(PFP)の項目、すなわち5.8μmより小さい粒径を有する放出用量%、空気動力学的中央粒子径(MMAD)、幾何標準偏差(GSD)および噴霧送達時間で、表中で特徴付けられている。
投与前ネブライザーを撮像するために矩形ROIを使用した。このROIは投与量送達後にネブライザーを撮像するために再使用した。
矩形ROIはUSPインレット画像にも適用した。
円形ROIは、収集プレート0の周りに集められ、写されそしてプレート1の周りに置かれた。これをプレート2〜7およびフィルターで繰り返した。矩形ROIはバックグラウンドカウントを評価するためにも行なわれた。概数カウントはバックグラウンドアクティビティで補正され、1分当りのカウント(cpm)に調整された。
エアロゾル性能は、微粒子画分(PFP)の項目、すなわち5.8μmより小さい粒径を有する放出用量%、空気動力学的中央粒子径(MMAD)、幾何標準偏差(GSD)および噴霧送達時間で、表中で特徴付けられている。
CEBUDの調製
5つのPulmicort Respules(1mg/mL)の放出量を一緒に合わせた。乾燥ベースのCaptisol(登録商標)(165mg)を、約7.5%w/vのCaptisol濃度を与えるように市販懸濁液の合計含量に使用されたRespule当りで加えた。
混合物をCaptisol(登録商標)を手短に分散し溶解するためにボルテックスした。次いで、ローラー−ベッドミキサーに入れて、2〜4又は数時間混合させた。平衡混合物のアリコートを使用し、元のRespule容器に残存したすべてのブデソニドを回収して一緒に再度合わせた。混合物は、更にローラー−ベッドミキサーで一夜(約20時間)平衡化させた。すべての懸濁固体が溶解したことを目視確認後、99m Tc−D5PA/生理食塩水(Medical Physical Department、UHW提供)の必要量を加えた。そして、約180μlの放射標識溶液をCaptisol−Enabled(登録商標)ブデソニド吸入溶液に加えて、少しの間ボルテックスした。
5つのPulmicort Respules(1mg/mL)の放出量を一緒に合わせた。乾燥ベースのCaptisol(登録商標)(165mg)を、約7.5%w/vのCaptisol濃度を与えるように市販懸濁液の合計含量に使用されたRespule当りで加えた。
混合物をCaptisol(登録商標)を手短に分散し溶解するためにボルテックスした。次いで、ローラー−ベッドミキサーに入れて、2〜4又は数時間混合させた。平衡混合物のアリコートを使用し、元のRespule容器に残存したすべてのブデソニドを回収して一緒に再度合わせた。混合物は、更にローラー−ベッドミキサーで一夜(約20時間)平衡化させた。すべての懸濁固体が溶解したことを目視確認後、99m Tc−D5PA/生理食塩水(Medical Physical Department、UHW提供)の必要量を加えた。そして、約180μlの放射標識溶液をCaptisol−Enabled(登録商標)ブデソニド吸入溶液に加えて、少しの間ボルテックスした。
〔実施例23〕
SAE−CDでのコルチコステロイド溶解の相溶解度曲線の決定。
SAE−CDを含むコルチコステロイド溶液の溶解度を、以下のように平衡濾過又は遠心分離したコルチコステロイド溶液からのアリコートのHPLCクロマトグラフィーで測定した。
SAE−CD/ステロイド溶液を、SAE−CDの固体(0.04モルにする)および過剰のステロイド薬(6mg/mL)を秤量し、スクリューキャップバイアルに一緒にすることによって調製した。一定量の水を各バイアルに等分した(各ステロイドを別々のバイアルに)。固有溶解度を、過剰のステロイド(6mg/mL)を秤量して、そしてCDの不存在下に一定量の水を加えることによって測定した。バイアルの栓をして、最初にボルテックスしてから超音波処理した。次いでバイアルを、ローラーミキサー(モデル:SRT2;メーカー:Stuart Scientific;製造番号:R000100052)またはロッカー/ミキサー(モデル:LabQuake;メーカー:Barnstcad/Thermolyne;製造番号:110410438202)にセットした。次いで大過剰の固体ステロイド(10mg/mLまで)をいずれのバイアルにも加えて、一夜で液体内容物を透明にした(例えば、プレドニゾロン、ヒドロコルチゾン、およびプレドニゾン)。試料を、ローラー又はロッカーで72時間ロールし、混合した。平衡時の種々の時点で、試料をさらに少しの間ボルテックスまたは超音波処理した(30分まで)。所定の平衡時間の後に、遠心分離してその上清を透明バイアルに移したジプロピオン酸ベクロメタゾンの固有溶解度試料を除いて、試料を透明バイアル中に濾過した(0.22μm、25mm、Duropore−PVDF、メーカー:Millipore)。試料を通常のHPLC法で分析した。
SAE−CDでのコルチコステロイド溶解の相溶解度曲線の決定。
SAE−CDを含むコルチコステロイド溶液の溶解度を、以下のように平衡濾過又は遠心分離したコルチコステロイド溶液からのアリコートのHPLCクロマトグラフィーで測定した。
SAE−CD/ステロイド溶液を、SAE−CDの固体(0.04モルにする)および過剰のステロイド薬(6mg/mL)を秤量し、スクリューキャップバイアルに一緒にすることによって調製した。一定量の水を各バイアルに等分した(各ステロイドを別々のバイアルに)。固有溶解度を、過剰のステロイド(6mg/mL)を秤量して、そしてCDの不存在下に一定量の水を加えることによって測定した。バイアルの栓をして、最初にボルテックスしてから超音波処理した。次いでバイアルを、ローラーミキサー(モデル:SRT2;メーカー:Stuart Scientific;製造番号:R000100052)またはロッカー/ミキサー(モデル:LabQuake;メーカー:Barnstcad/Thermolyne;製造番号:110410438202)にセットした。次いで大過剰の固体ステロイド(10mg/mLまで)をいずれのバイアルにも加えて、一夜で液体内容物を透明にした(例えば、プレドニゾロン、ヒドロコルチゾン、およびプレドニゾン)。試料を、ローラー又はロッカーで72時間ロールし、混合した。平衡時の種々の時点で、試料をさらに少しの間ボルテックスまたは超音波処理した(30分まで)。所定の平衡時間の後に、遠心分離してその上清を透明バイアルに移したジプロピオン酸ベクロメタゾンの固有溶解度試料を除いて、試料を透明バイアル中に濾過した(0.22μm、25mm、Duropore−PVDF、メーカー:Millipore)。試料を通常のHPLC法で分析した。
〔実施例24〕
SAE−CD、ブデソニドおよびキシナホ酸サルメテロールを含有する透明液体製剤の調製。この種の製剤は、コルチコステロイド、SAE−CDおよび第二の治療薬の組み合せを含む本明細書の他の実施例に従って調製することができる。
SAE−CD、ブデソニドおよびキシナホ酸サルメテロールを含有する透明液体製剤の調製。この種の製剤は、コルチコステロイド、SAE−CDおよび第二の治療薬の組み合せを含む本明細書の他の実施例に従って調製することができる。
〔実施例25〕
SAE−CD、ブデソニドおよび硫酸アルブテロールを含有する透明液体製剤の製造。
SAE−CD、ブデソニドおよび硫酸アルブテロールを含有する透明液体製剤の製造。
CAPTISOL(40.0g)、水(1L)、クエン酸(387.6mg)、クエン酸ナトリウム(519.6mg)、EDTA(120mg)、およびNaCl(6.36mg)を含有するストック溶液を、これらの成分を一緒に混ぜ合わせることによって調製した。
ブデソニド(37.5mg)および硫酸アルブテロール(150mg)をストック溶液のアリコート(150ml)に加えて、全成分が溶解するまで周囲温度でローラーミキサーにより混合した。最終溶液は透明であったが、しかし必要に応じて濾過することが可能である。製剤中の成分の最終濃度は次のとおりであった:CAPTISOL(0.018M);ブデソニド(5.9mMまたは254μg/ml);および硫酸アルブテロール(1mg/ml)。
ブデソニド(37.5mg)および硫酸アルブテロール(150mg)をストック溶液のアリコート(150ml)に加えて、全成分が溶解するまで周囲温度でローラーミキサーにより混合した。最終溶液は透明であったが、しかし必要に応じて濾過することが可能である。製剤中の成分の最終濃度は次のとおりであった:CAPTISOL(0.018M);ブデソニド(5.9mMまたは254μg/ml);および硫酸アルブテロール(1mg/ml)。
〔実施例26〕
カスケードインパクターを用いるエアロゾル化溶液の液滴粒度分布の特徴付け。
本発明のエアロゾル化溶液の液滴粒度分布を、NGIカスケードインパクターを用いて特徴付けした。1000μg/mLの約0.5mLを、AERONEB GOなどのネブライザーに入れた。インパクターと連動した真空ポンプを作動させた。ネブライザーマウスピースをUSPのインダクションポートの中心に位置するようにし、パラフィンでそれを密封した。ネブライザーをもはや蒸気が見えなくなるまで作動させた。試料の完全な収集を確実するために更に45秒間収集を継続した。真空を解除し、インパクターを取り外した。各ステージにおいて収集カップを既知量のHPLC移動相で抽出して、ブデソニドを分析した。各ステージのブデソニドの累積量を定量した。ネブライザーから排出する薬剤の割合は81%であり、また微粒子画分(<5μm)の薬剤の割合は66%であった。
カスケードインパクターを用いるエアロゾル化溶液の液滴粒度分布の特徴付け。
本発明のエアロゾル化溶液の液滴粒度分布を、NGIカスケードインパクターを用いて特徴付けした。1000μg/mLの約0.5mLを、AERONEB GOなどのネブライザーに入れた。インパクターと連動した真空ポンプを作動させた。ネブライザーマウスピースをUSPのインダクションポートの中心に位置するようにし、パラフィンでそれを密封した。ネブライザーをもはや蒸気が見えなくなるまで作動させた。試料の完全な収集を確実するために更に45秒間収集を継続した。真空を解除し、インパクターを取り外した。各ステージにおいて収集カップを既知量のHPLC移動相で抽出して、ブデソニドを分析した。各ステージのブデソニドの累積量を定量した。ネブライザーから排出する薬剤の割合は81%であり、また微粒子画分(<5μm)の薬剤の割合は66%であった。
〔実施例27〕
本発明の液体を含むネブライザーからの全薬剤アウトプットおよび薬剤アウトプット率の決定。
投薬収集装置を、HPLC移動相を濾過するために使用したタイプの300mlガラスフィルターユニットにより構築した。特製のPlexiglasのふたにはリザーバを覆い、そしてエアロゾルをリザーバに受け入れる開口部があった。このリザーバは、金網に支えられたガラス繊維フィルターに向かって先細りになっていた。網はガラス管で終端となる円錐ガラス容器に入っており、流量調節器及び真空ポンプに接続していた。リザーバおよびフィルター支持ハウジングは互いに固定された。2つのフィルターは、放出エアロゾルを収集する装置に互いに挟まれた。このことは、その後の真空内への薬剤損失でフィルターを引き裂き、そしてエアロゾル収集の経過中気流速度の変化をもたらし得る、フィルターの飽和を避けるために必要であった。噴霧の終了は、間欠的なエアロゾルアウトプットおよび/またはネブライザー音のピッチの変化で判定された。噴霧ブデソニドの大気へのロスを防止するために、それがネブライザーから追い出されるより速く空気をフィルター内に引き込むようにした。エアロゾルがあらゆるネブライザーの背部から逃げないことを視認することにより、15±5%l/分の流量は十分と考えられた。これは、TPK流量調節器(Copley Instruments、4312)および真空ポンプによって制御し、また較正流量計を用いて各実験前に確認した。
本発明の液体を含むネブライザーからの全薬剤アウトプットおよび薬剤アウトプット率の決定。
投薬収集装置を、HPLC移動相を濾過するために使用したタイプの300mlガラスフィルターユニットにより構築した。特製のPlexiglasのふたにはリザーバを覆い、そしてエアロゾルをリザーバに受け入れる開口部があった。このリザーバは、金網に支えられたガラス繊維フィルターに向かって先細りになっていた。網はガラス管で終端となる円錐ガラス容器に入っており、流量調節器及び真空ポンプに接続していた。リザーバおよびフィルター支持ハウジングは互いに固定された。2つのフィルターは、放出エアロゾルを収集する装置に互いに挟まれた。このことは、その後の真空内への薬剤損失でフィルターを引き裂き、そしてエアロゾル収集の経過中気流速度の変化をもたらし得る、フィルターの飽和を避けるために必要であった。噴霧の終了は、間欠的なエアロゾルアウトプットおよび/またはネブライザー音のピッチの変化で判定された。噴霧ブデソニドの大気へのロスを防止するために、それがネブライザーから追い出されるより速く空気をフィルター内に引き込むようにした。エアロゾルがあらゆるネブライザーの背部から逃げないことを視認することにより、15±5%l/分の流量は十分と考えられた。これは、TPK流量調節器(Copley Instruments、4312)および真空ポンプによって制御し、また較正流量計を用いて各実験前に確認した。
〔実施例28〕
SAE−CDおよびブデソニドを含み、場合によりTweenを含有する液体製剤の調製。
pH4.5で3mMのクエン酸緩衝液を、血清バイアル中に2グラムのCAPTISOLおよび25mgのブデソニドに加えて、最終体積を10mLにした。この懸濁液をボルテックス及び超音波処理によって良く混合した。ブデソニドなしのCAPTISOLの20%のストック溶液も、また3mMのクエン酸緩衝液で調製した。これらの混合物を緩衝液と合わせて別々のバイアルに封入し、121℃サイクルで20分保持を使ってオートクレーブ処理した。透明なブデソニド溶液のHPLC分析の結果、その濃度は2100μg/mLであることを示した。20%のCAPTISOLストック溶液を使用して、試料を2000μg/mLに希釈した。得られた上記溶液の一部を、場合により等量の3mMのクエン酸緩衝液で希釈した。HPLC分析は、最終濃度が990μgブデソニド/mLであることを示した。
Tweenは以下のように上記溶液に加えることができた。0.02%Tweenの溶液を、上記溶液用の希釈剤として用いるためのTweenストック溶液を作るために、オートクレーブした緩衝液のみの溶液を用いて調製した。10%captisol/1mg/mLブデソニドの希釈は重量によって行なわれた。ほぼ9グラムの10%captisol/2000μg/mLを、約9グラムのオートクレーブした緩衝液のみの溶液かまたはオートクレーブした緩衝液/0.02%Tween溶液と混合した。これらの溶液をよく混合し、濾過してさらにHPLCにより再分析した。
上記製剤のブデソニド濃度は、Tweenなし溶液では986μg/mLで、Tweenありの溶液では962μg/mLであることが分かった。
溶液はいずれのネブライザーでも噴霧できる;しかし、AERxネブライザーでは50μlの始めの試料量で使用できる。ネブライザーによる本溶液の投与は、治療用量が噴霧による単回パフ(被検者による単回フル吸入)で被検者に投与できることを可能にする。
SAE−CDおよびブデソニドを含み、場合によりTweenを含有する液体製剤の調製。
pH4.5で3mMのクエン酸緩衝液を、血清バイアル中に2グラムのCAPTISOLおよび25mgのブデソニドに加えて、最終体積を10mLにした。この懸濁液をボルテックス及び超音波処理によって良く混合した。ブデソニドなしのCAPTISOLの20%のストック溶液も、また3mMのクエン酸緩衝液で調製した。これらの混合物を緩衝液と合わせて別々のバイアルに封入し、121℃サイクルで20分保持を使ってオートクレーブ処理した。透明なブデソニド溶液のHPLC分析の結果、その濃度は2100μg/mLであることを示した。20%のCAPTISOLストック溶液を使用して、試料を2000μg/mLに希釈した。得られた上記溶液の一部を、場合により等量の3mMのクエン酸緩衝液で希釈した。HPLC分析は、最終濃度が990μgブデソニド/mLであることを示した。
Tweenは以下のように上記溶液に加えることができた。0.02%Tweenの溶液を、上記溶液用の希釈剤として用いるためのTweenストック溶液を作るために、オートクレーブした緩衝液のみの溶液を用いて調製した。10%captisol/1mg/mLブデソニドの希釈は重量によって行なわれた。ほぼ9グラムの10%captisol/2000μg/mLを、約9グラムのオートクレーブした緩衝液のみの溶液かまたはオートクレーブした緩衝液/0.02%Tween溶液と混合した。これらの溶液をよく混合し、濾過してさらにHPLCにより再分析した。
上記製剤のブデソニド濃度は、Tweenなし溶液では986μg/mLで、Tweenありの溶液では962μg/mLであることが分かった。
溶液はいずれのネブライザーでも噴霧できる;しかし、AERxネブライザーでは50μlの始めの試料量で使用できる。ネブライザーによる本溶液の投与は、治療用量が噴霧による単回パフ(被検者による単回フル吸入)で被検者に投与できることを可能にする。
〔実施例29〕
SAE−CDおよびブデソニドを含む凍結乾燥製剤の調製および溶解。
過剰のブデソニド、3.5mg/mLを、3Lの0.1mg/mLのEDTAを含む3mMのクエン酸緩衝液中の30%Captisolに加えた。2日間混合後、さらに1mg/mLのブデソニドを加えて、さらに4日間平衡化した。調合液を0.22μのDuraporeフィルターを通して濾過し、そして凍結乾燥機内の3つのステンレススチールトレイに入れた。溶液を−30℃で1時間凍結し、30時間にわたって凍結乾燥して本質的に全水分を除去した。凍結乾燥物を粉末化して篩にかけ、その粉末をプラスチックビンに移した。最終組成物は粉末1グラム当り8.2mgのブデソニドを含有した。
ほぼ65mgの粉末を2mLの水に加えた場合、参照懸濁液製品と同じ量のブデソニドを含む本質的に透明な溶液が迅速に得られた。
SAE−CDおよびブデソニドを含む凍結乾燥製剤の調製および溶解。
過剰のブデソニド、3.5mg/mLを、3Lの0.1mg/mLのEDTAを含む3mMのクエン酸緩衝液中の30%Captisolに加えた。2日間混合後、さらに1mg/mLのブデソニドを加えて、さらに4日間平衡化した。調合液を0.22μのDuraporeフィルターを通して濾過し、そして凍結乾燥機内の3つのステンレススチールトレイに入れた。溶液を−30℃で1時間凍結し、30時間にわたって凍結乾燥して本質的に全水分を除去した。凍結乾燥物を粉末化して篩にかけ、その粉末をプラスチックビンに移した。最終組成物は粉末1グラム当り8.2mgのブデソニドを含有した。
ほぼ65mgの粉末を2mLの水に加えた場合、参照懸濁液製品と同じ量のブデソニドを含む本質的に透明な溶液が迅速に得られた。
〔実施例30〕
SAE−CD、エタノールおよびブデソニドを含む水性液体製剤の調製。
Captisol/エタノール溶液を、0、1、2、5%エタノールの4溶液及び約20%w/vのCaptisolを作製するために、種々の量のエタノールかまたは水で希釈した22.2%(〜0.1M)w/vの原液を作ることによって製造された。Captisol/エタノール/ブデソニド溶液は、乾燥ブデソニド(2.5mg/mL)を一定量の調製Captisol/エタノール溶液に加え、次にこれらをLabquakeで72時間平衡化した。これらの溶液を濾過し(Duroporeシリンジフィルター)、そしてHPLCで分析して製剤に溶解したブデソニドの濃度(μg/ml)を測定した。
SAE−CD、エタノールおよびブデソニドを含む水性液体製剤の調製。
Captisol/エタノール溶液を、0、1、2、5%エタノールの4溶液及び約20%w/vのCaptisolを作製するために、種々の量のエタノールかまたは水で希釈した22.2%(〜0.1M)w/vの原液を作ることによって製造された。Captisol/エタノール/ブデソニド溶液は、乾燥ブデソニド(2.5mg/mL)を一定量の調製Captisol/エタノール溶液に加え、次にこれらをLabquakeで72時間平衡化した。これらの溶液を濾過し(Duroporeシリンジフィルター)、そしてHPLCで分析して製剤に溶解したブデソニドの濃度(μg/ml)を測定した。
〔実施例31〕
本発明による剤形のインビボ評価を、噴霧による剤形の投与後にブデソニドの薬物動態学的分析を行なうことによって実施した。
Pari LC空気ジェットネブライザーを用いて、Pulmicort Respules(登録商標)、およびCaptisol−Enabled(登録商標)のブデソニド製剤によりブデソニドの肺送達を比較するため4頭のイヌのクロスオーバーを研究した。この研究の目的は、健常イヌにおけるブデソニド懸濁液(Pulmicort Respules(登録商標)、AstraZeneca、参照製剤)およびCaptisol−Enabled(登録商標)ブデソニド吸入溶液(試験製剤)の噴霧後に、血漿のブデソニドの薬物動態学を、HPLC−MS/MS分析によって測定することであった。投薬は、Pari LC Star空気ジェット式ネブライザー及び麻酔マスクを用いて行なった。
試験する剤形は:1)2つの2mL×0.25mg/mLのPulmicort Respules(登録商標)として1mgのブデソニド;または2)5%w/vのCaptisol(登録商標)が添加された、2つの2mL×0.25mg/mLのPulmicort Respulesとして1mgのブデソニドから構成された。
投薬に先立ち、チャコールを含む2つのカプセルに続いて約30mLの水を、ブデソニドの経口吸収をブロックするために各イヌに投与した。各イヌには、一週離して無作為化した様式で各々試験投与した。投与時間は、各製剤で同じにした(試験製剤では23.9分及び参照では23.4分)。血液を8時間まで経時的に採取し、血漿を分離して、そして分析するまで−70℃で保存した。各投与後に、ネブライザーおよび試験溶液の容器について、送達した薬剤量を決めるために残存ブデソニド量を分析した。
本発明による剤形のインビボ評価を、噴霧による剤形の投与後にブデソニドの薬物動態学的分析を行なうことによって実施した。
Pari LC空気ジェットネブライザーを用いて、Pulmicort Respules(登録商標)、およびCaptisol−Enabled(登録商標)のブデソニド製剤によりブデソニドの肺送達を比較するため4頭のイヌのクロスオーバーを研究した。この研究の目的は、健常イヌにおけるブデソニド懸濁液(Pulmicort Respules(登録商標)、AstraZeneca、参照製剤)およびCaptisol−Enabled(登録商標)ブデソニド吸入溶液(試験製剤)の噴霧後に、血漿のブデソニドの薬物動態学を、HPLC−MS/MS分析によって測定することであった。投薬は、Pari LC Star空気ジェット式ネブライザー及び麻酔マスクを用いて行なった。
試験する剤形は:1)2つの2mL×0.25mg/mLのPulmicort Respules(登録商標)として1mgのブデソニド;または2)5%w/vのCaptisol(登録商標)が添加された、2つの2mL×0.25mg/mLのPulmicort Respulesとして1mgのブデソニドから構成された。
投薬に先立ち、チャコールを含む2つのカプセルに続いて約30mLの水を、ブデソニドの経口吸収をブロックするために各イヌに投与した。各イヌには、一週離して無作為化した様式で各々試験投与した。投与時間は、各製剤で同じにした(試験製剤では23.9分及び参照では23.4分)。血液を8時間まで経時的に採取し、血漿を分離して、そして分析するまで−70℃で保存した。各投与後に、ネブライザーおよび試験溶液の容器について、送達した薬剤量を決めるために残存ブデソニド量を分析した。
〔実施例32〕
5%w/vのCaptisolのPulmicort Respulesへの組み込みが、異なるタイプのネブライザーの性能にどのように影響するかを調べる。
4種の異なるネブライザー(PARI LC PLUS(空気ジェット式)、OMRON MICROAIR NE−U22、AIRSEP MYSTIQUE(超音波)、AEROGEN AERONEB)からのブデソニドの放出用量を測定した。添付文書−承認Pari空気ジェットシステムを、他のネブライザーの性能を判定する基準として使用した。放出用量は、Captisolをブデソニド懸濁液に加えた場合、1.25から3.7倍高かった。放出用量(ED)は:
1) 噴霧した製剤を15l/分で300mLのガラスフィルター装置を通過させて吸引し、そしてガラス繊維深部フィルターの二重または三重層および内壁の薬剤を収集すること。収集を2分毎に停止し、ブデソニドを定量的に回収し、そしてフィルターを濾過フィルター飽和または気流変動を防止するために取り替えた。ブデソニドの回収をHPLCによって定量した;および/または
2) 噴霧後カスケードインパクター段階のブデソニドの量を合計することによって測定した。
5%w/vのCaptisolのPulmicort Respulesへの組み込みが、異なるタイプのネブライザーの性能にどのように影響するかを調べる。
4種の異なるネブライザー(PARI LC PLUS(空気ジェット式)、OMRON MICROAIR NE−U22、AIRSEP MYSTIQUE(超音波)、AEROGEN AERONEB)からのブデソニドの放出用量を測定した。添付文書−承認Pari空気ジェットシステムを、他のネブライザーの性能を判定する基準として使用した。放出用量は、Captisolをブデソニド懸濁液に加えた場合、1.25から3.7倍高かった。放出用量(ED)は:
1) 噴霧した製剤を15l/分で300mLのガラスフィルター装置を通過させて吸引し、そしてガラス繊維深部フィルターの二重または三重層および内壁の薬剤を収集すること。収集を2分毎に停止し、ブデソニドを定量的に回収し、そしてフィルターを濾過フィルター飽和または気流変動を防止するために取り替えた。ブデソニドの回収をHPLCによって定量した;および/または
2) 噴霧後カスケードインパクター段階のブデソニドの量を合計することによって測定した。
本明細書に引用された書類は、それぞれ参照によりその全体が本明細書に組み入れられている。上記の説明は、本発明の特定の実施態様の詳細な説明である。本明細書では例示を目的として本発明の特定の実施態様が説明されているが、本発明の趣旨および範囲を逸脱することなくさまざまな修正を加えられることは理解されるであろう。したがって、本発明は、添付の特許請求の範囲以外では限定されない。本明細書で開示され、特許請求されている実施態様は、すべて本発明の開示に照らして過度の実験を行うことなく、実施することができる。
Claims (111)
- 製剤中に溶解した治療的有効量のコルチコステロイド、SAE−CD、および水性液体担体を含み、SAE−CD対コルチコステロイドのモル比が10:1より大きい水性液体製剤。
- SAE−CDの存在下のコルチコステロイドの飽和溶解度でコルチコステロイドに必要なSAE−CD対コルチコステロイドのモル比が10:1より大きい、請求項1に記載の製剤。
- コルチコステロイドが、フルニソリドと少なくとも同等の親油性、またはより大きい親油性である、請求項2に記載の製剤。
- コルチコステロイドが、ベクロメタゾン、ジプロピオン酸ベクロメタゾン、モノプロピオン酸ベクロメタゾン、ブデソニド、シクレソニド、デスイソブチリル−シクレソニド、フルニソリド、フルチカゾン、プロピオン酸フルチカゾン、フランカルボン酸フルチカゾン、モメタゾン、フランカルボン酸モメタゾン、イコメタゾンエンブテート、チキソコルトール21−ピバレート、およびトリアムシノロンアセトニドからなる群から選択される、請求項3に記載の製剤。
- コルチコステロイドが、ジプロピオン酸ベクロメタゾン、モノプロピオン酸ベクロメタゾン、ブデソニド、シクレソニド、デスイソブチリル−シクレソニド、フルニソリド、プロピオン酸フルチカゾン、フランカルボン酸フルチカゾン、フランカルボン酸モメタゾン、イコメタゾンエンブテート、チキソコルトール21−ピバレート、およびトリアムシノロンアセトニドからなる群から選択される、請求項3に記載の製剤。
- コルチコステロイドがSAE−CDの存在下で測定してその飽和溶解度より低い濃度で存在する、請求項3に記載の製剤。
- 組成物または製剤中のSAE−CD対コルチコステロイドのモル比が、SAE−CDの存在下で測定してコルチコステロイドの飽和溶解度でのモル比より少なくとも1%大きい、請求項6に記載の製剤。
- SAE−CD対コルチコステロイドのモル比が、10:1より大きく約10,000:1までの範囲にあるか、または10:1より大きく約1000:1までの範囲にある、請求項7に記載の製剤。
- SAE−CDの存在下のコルチコステロイドの飽和溶解度で、SAE−CD対コルチコステロイドのモル比が少なくとも14:1である、請求項7に記載の製剤。
- 製剤が5質量%より少ない非溶解コルチコステロイドしか含まない実質的に透明な溶液である、請求項9に記載の製剤。
- 21.5±2質量/質量%以下のSAE−CDを含む、請求項10に記載の製剤。
- コルチコステロイドがSAE−CDの存在下で測定してその飽和溶解度より低い濃度で存在する、請求項2に記載の製剤。
- コルチコステロイドがSAE−CDの存在下で測定してその飽和溶解度の95%以下の濃度で存在する、請求項12に記載の製剤。
- 組成物または製剤中のSAE−CD対コルチコステロイドのモル比が、SAE−CDの存在下で測定してコルチコステロイドの飽和溶解度でのモル比より少なくとも1%大きい、請求項2に記載の製剤。
- 組成物または製剤中のSAE−CD対コルチコステロイドのモル比が、SAE−CDの存在下で測定してコルチコステロイドの飽和溶解度でのモル比より少なくとも5%大きい、請求項14に記載の製剤。
- 製剤が5質量%より少ない非溶解コルチコステロイドしか含まない実質的に透明な溶液である、請求項1に記載の製剤。
- SAE−CDの存在下のコルチコステロイドの飽和溶解度で、SAE−CD対コルチコステロイドのモル比が少なくとも14:1である、請求項1に記載の製剤。
- 水性液体担体が水、緩衝剤、アルコール、有機溶媒、グリセリン、ポリ(エチレングリコール)、ポロキサマー、界面活性剤またはその組み合わせを含む、請求項1に記載の製剤。
- 21.5±2質量/質量%以下のSAE−CDを含む、請求項1に記載の製剤。
- SAE−CD対コルチコステロイドのモル比が、10:1より大きく約10,000:1までの範囲にあるか、または10:1より大きく約1,000:1までの範囲にある、請求項1に記載の製剤。
- SAE−CD対コルチコステロイドのモル比が、10:1より大きく約333:1、>10:1から約1000:1まで、約>10:1から約100:1まで、>10:1から約50:1まで、>10:1から約30:1まで、または>10:1から約500:1までの範囲にある、請求項20に記載の製剤。
- コルチコステロイドが、フルニソリドより小さい親油性を有するいずれのコルチコステロイドをも除く、請求項1に記載の製剤。
- ヒドロコルチゾン、プレドニゾロン、プレドニゾン、デキサメタゾン、ベタメタゾン、メチルプレドニゾロン、トリアムシノロン、およびフルオコルトロンを除く、請求項22に記載の製剤。
- コルチコステロイドが、アルドステロン、ベクロメタゾン、ベタメタゾン、ブデソニド、シクレソニド、クロプレドノール、コルチバゾール、デオキシコルトン、デソニド、デスオキシメタゾン、デキサメタゾン、ジフルオロコルトロン、フルクロロロン、フルメタゾン、フルニソリド、フルオシノロン、フルオシノニド、フルオコルチンブチル、フルオロコルチゾン、フルオロコルトロン、フルオロメトロン、フルランドレノロン、フルチカゾン、ハルシノニド、イコメタゾン、モメタゾン、パラモメタゾン、ロフレポニド、RPR 106541、チキソコルトール、トリアムシノロン、およびそれらの各薬学的に許容される誘導体からなる群から選択される、請求項1に記載の製剤。
- コルチコステロイドが、水におけるフルニソリドの固有溶解度に近似するかまたはそれより小さい水における固有溶解度を有する、請求項1に記載の製剤。
- SAE−CDがコルチコステロイドの少なくとも90%を可溶化するのに十分な量で存在する、請求項1に記載の製剤。
- SAE−CDがコルチコステロイドの少なくとも95%を可溶化するのに十分な量で存在する、請求項1に記載の製剤。
- SAE−CDが1mlの製剤当りSAE−CD約10mgから約500mgの濃度で存在する、請求項1に記載の製剤。
- 製剤が少なくとも6か月の貯蔵寿命を有する、請求項1に記載の製剤。
- 従来の保存剤、酸化防止剤、緩衝剤、酸性化剤、可溶化剤、着色剤、錯化促進剤、食塩水、電解質、他の治療薬、アルカリ性化剤、張度調整剤、表面張力調整剤、粘度調整剤、密度調整剤、揮発性調整剤、消泡剤、着香料、甘味料、親水性ポリマー、界面活性剤またはその組み合わせをさらに含む、請求項1に記載の製剤。
- β2−アドレナリン受容体アゴニスト、ドーパミン(D2)受容体アゴニスト、局所麻酔剤、抗コリン剤、IL−5阻害剤、IL−5のアンチセンス調節剤、ミルリノン(1,6−ジヒドロ−2−メチル−6−オキソ−[3,4’−ビピリジン]−5−カルボニトリル)、乳酸ミルリノン、トリプターゼ阻害剤、タキキニン受容体アンタゴニスト、ロイコトリエン受容体アンタゴニスト、5−リポキシゲナーゼ阻害剤、および抗−IgE抗体からなる群から各場合において独立に選択される1種またはそれ以上の治療薬をさらに含む、請求項1に記載の製剤。
- β2−アドレナリン受容体アゴニストが、アルブテロール(α1−(((1,1−ジメチルエチル)アミノ)メチル)−4−ヒドロキシ−1,3−ベンゼンジメタノール);バンブテロール(ジメチルカルバミン酸5−(2−((1,1−ジメチルエチル)アミノ)−1−ヒドロキシエチル)−1,3−フェニレンエステル);ビトルテロール(4−メチル安息香酸4−(2−((1,1−ジメチルエチル)アミノ)−1−ヒドロキシエチル)−1,2−フェニレンエステル);ブロキサテロール(3−ブロモ−α−(((1,1−ジメチルエチル)アミノ)メチル)−5−イソオキサゾールメタノール);イソプロテレノール(4−(1−ヒドロキシ−2−((1−メチルエチル−)アミノ)エチル)−1,2−ベンゼン−ジオール);トリメトキノール(1,2,3,4−テトラヒドロ−1−((3,4,5−トリメトキシフェニル)−メチル)−6,7−イソキノリンジオール);クレンブテロール(4−アミノ−3,5−ジクロロ−α−(((1,1−ジメチルエチル)アミノ)メチル)ベンゼンメタノール);フェノテロール(5−(1−ヒドロキシ−2−((2−(4−ヒドロキシフェニル)−1−メチルエチル)アミノ)エチル)−1,3−ベンゼンジオール);ホルモテロール(2−ヒドロキシ−5−((1RS)−1−ヒドロキシ−2−(((1RS)−2−(p−メトキシフェニル)−1−メチルエチル)アミノ)エチル)ホルムアニリド);(R,R)−ホルモテロール;デスホルモテロール((R,R)または(S,S)−3−アミノ−4−ヒドロキシ−α−(((2−(4−メトキシフェニル)−1−メチル−エチル)アミノ)メチル)ベンゼンメタノール);ヘキソプレナリン(4,4’−(1,6−ヘキサン−ジイル)−ビス(イミノ(1−ヒドロキシ−2,1−エタンジイル)))ビス−1,2−ベンゼンジオール);イソエタリン(4−(1−ヒドロキシ−2−((1−メチルエチル)アミノ)ブチル)−1,2−ベンゼンジオール);イソプレナリン(4−(1−ヒドロキシ−2−((1−メチルエチル)アミノ)エチル)−1,2−ベンゼンジオール);メタ−プロテレノール(5−(1−ヒドロキシ−2−((1−メチルエチル)アミノ)エチル)−1,3−ベンゼンジオール);ピクメテロール(4−アミノ−3,5−ジクロロ−α−(((6−(2−(2−ピリジニル)エトキシ)ヘキシル)−アミノ)メチル)ベンゼンメタノール);ピルブテロール(α6−(((1,1−ジメチルエチル)−アミノ)メチル)−3−ヒドロキシ−2,6−ピリジンメタノール);プロカテロール(((R*,S*)−(±)−8−ヒドロキシ−5−(1−ヒドロキシ−2−((1−メチルエチル)アミノ)ブチル)−2(1H)−キノリン−オン);レプロテロール((7−(3−((2−(3,5−ジヒドロキシフェニル)−2−ヒドロキシエチル)アミノ)−プロピル)−3,7−ジヒドロ−1,3−ジメチル−1H−プリン−2,6−ジオン);リミテロール(4−(ヒドロキシ−2−ピペリジニルメチル)−1,2−ベンゼンジオール);サルブタモール((±)−α1−(((1,1−ジメチルエチル)アミノ)メチル)−4−ヒドロキシ−1,3−ベンゼンジメタノール);(R)−サルブタモール;サルメテロール((±)−4−ヒドロキシ−α1−(((6−(4−フェニルブトキシ)ヘキシル)−アミノ)メチル)−1,3−ベンゼンジメタノール);(R)−サルメテロール;テルブタリン(5−(2−((1,1−ジメチルエチル)アミノ)−1−ヒドロキシエチル)−1,3−ベンゼンジオール);ツロブテロール(2−クロロ−α−(((1,1−ジメチルエチル)アミノ)メチル)ベンゼンメタノール);およびTA−2005(8−ヒドロキシ−5−((1R)−1−ヒドロキシ−2−(N−((1R)−2−(4−メトキシフェニル)−1−メチルエチル)アミノ)エチル)カルボスチリル塩酸塩)からなる群から選択される、請求項31に記載の製剤。
- ドーパミン(D2)受容体アゴニストが、アポモルヒネ((r)−5,6,6a,7−テトラヒドロ−6−メチル−4H−ジベンゾ[de,glキノリン−10,11−ジオール];ブロモクリプチン((5’α)−2−ブロモ−12’−ヒドロキシ−2’−(1−メチルエチル)−5’−(2−メチルプロピル)エルゴタマン−3’,6’,18−トリオン);カベルゴリン((8β)−N−(3−(ジメチルアミノ)プロピル)−N−((エチルアミノ)カルボニル)−6−(2−プロペニル)エルゴリン−8−カルボキサミド);リスリド(N’−((8α−)−9,10−ジデヒドロ−6−メチルエルゴリン−8−イル)−N,N−ジエチル尿素);ペルゴリド((8β−)−8−((メチルチオ)メチル)−6−プロピルエルゴリン);レボドーパ(3−ヒドロキシ−L−チロシン);プラミペキソール((s)−4,5,6,7−テトラヒドロ−N6−プロピル−2,6−ベンゾチアゾールジアミン);塩酸キンピロール(trans−(−)−4aR−4,4a,5,6,7,8,8a,9−オクタヒドロ−5−プロピル−1H−ピラゾロ[3,4−g]キノリン塩酸塩);ロピニロール(4−(2−(ジプロピルアミノ)エチル)−1,3−ジヒドロ−2H−インドール−2−オン);およびタリペキソール(5,6,7,8−テトラヒドロ−6−(2−プロペニル)−4H−チアゾロ[4,5−d]アゼピン−2−アミン)からなる群から選択される、請求項31に記載の製剤。
- 抗コリン剤が、臭化イプラトロピウム、臭化オキシトロピウム、硝酸メチルアトロピン、硫酸アトロピン、イプラトロピウム、ベラドンナエキス、スコポラミン、スコポラミンメトブロミド、ホマトロピンメトブロミド、ヒヨスチアミン、イソプリオプラミド、オルフェナドリン、塩化ベンザルコニウム、臭化チオトロピウム、および臭化グリコピロニウムからなる群から選択される、請求項31に記載の製剤。
- 局所麻酔剤が、リドカイン、N−アリールアミド、アミノアルキルベンゾエート、プリロカイン、およびエチドカインからなる群から選択される、請求項31に記載の製剤。
- ジプロピオン酸ベクロメタゾン、モノプロピオン酸ベクロメタゾン、ブデソニド、シクレソニド、デスイソブチリル−シクレソニド、フルニソリド、プロピオン酸フルチカゾン、フランカルボン酸フルチカゾン、フランカルボン酸モメタゾン、イコメタゾンエンブテート、チキソコルトール21−ピバレート、およびトリアムシノロンアセトニドからなる群から選択されるコルチコステロイド;およびサルメテロール、ホルモテロール、アルブテロール、イパトロピウム、それらの薬学的に許容される塩、およびそれらの異性体からなる群から選択される治療薬を含む、請求項31に記載の製剤。
- コルチコステロイドが他の治療薬に対してモル過剰で存在する、請求項31に記載の製剤。
- 他の治療薬がコルチコステロイドに対してモル過剰で存在する、請求項31に記載の製剤。
- SAE−CDが他の治療薬に対してモル過剰で存在する、請求項31に記載の製剤。
- SAE−CDが他の治療薬に対するよりもコルチコステロイドに対し高い平衡結合定数を有する、請求項31に記載の製剤。
- SAE−CDがコルチコステロイドに対するよりも他の治療薬に対し高い平衡結合定数を有する、請求項31に記載の製剤。
- SAE−CDが他の治療薬に対する平衡結合定数に近似する平衡結合定数を有する、請求項31に記載の製剤。
- シクロデキストリンが、式1:
nは、4、5、または6であり、
R1、R2、R3、R4、R5、R6、R7、R8、およびR9は、それぞれ独立に−O−または−O−(C2−C6アルキレン)−SO3 -基であり、ここでR1〜R9の少なくとも1つは独立に−O−(C2−C6アルキレン)−SO3 -基、−O−(CH2)mSO3 -基であり、ここでmは2〜6、−OCH2CH2CH2SO3 -または−OCH2CH2CH2CH2SO3 -であり、そして
S1、S2、S3、S4、S5、S6、S7、S8、およびS9は、それぞれ独立に薬剤として許容されるカチオンである]の化合物である、請求項1〜42、46〜110または111のいずれか1項に記載の発明。 - シクロデキストリンが、「x」が1〜18の範囲である式IIの化合物(SAEx−α−CD)、「y」が1〜21の範囲である式IIIの化合物(SAEy−β−CD)、または「z」が1〜24の範囲である式IVの化合物(SAEz−γ−CD)であり、「SAE」がスルホアルキルエーテル置換基を表し、値「x」、「y」、および「z」がCD1分子当たりのスルホアルキルエーテル基の個数に関する平均置換度を表す、請求項1〜42、46〜110または111のいずれか1項に記載の発明。
- 請求項1に記載の製剤を乾燥することによって調製される固形組成物。
- 製剤が、経鼻、経口、点眼、耳内または局所投与に適合する、請求項1に記載の液体製剤。
- 水性液体担体、スルホアルキルエーテルシクロデキストリン、および製剤中に溶解したコルチコステロイドの治療的有効量を含む液体製剤の吸入を介して投与することを含む、それを必要とする被験者における、気道の疾患または障害を治療する方法であって、コルチコステロイドが160〜1600pg*h/mlの平均血漿中AUCtを与えるのに十分な量で存在し、ここでSAE−CD対コルチコステロイドのモル比が10:1より大きい治療方法。
- 治療的有効量が45〜1000μgのコルチコステロイドを含む、請求項48に記載の方法。
- SAE−CDの存在下のコルチコステロイドの飽和溶解度でコルチコステロイドに必要なSAE−CD対コルチコステロイドのモル比が10:1より大きい、請求項49に記載の方法。
- 液体製剤が噴霧投与される、請求項50に記載の方法。
- 製剤が約5ml未満の水性液体担体を含む、請求項51に記載の方法。
- 製剤が0.05〜2mlの水性液体担体を含む、請求項52に記載の方法。
- 液体製剤が、超音波ネブライザー、空気ジェット式ネブライザー、電子ネブライザー、振動膜ネブライザー、振動メッシュネブライザー、強制キャリア/有孔ディスク併用ネブライザー、振動板ネブライザー、振動発生器と水性チャンバーを含むネブライザー、およびノズルアレイを含むネブライザーで投与される、請求項51に記載の方法。
- コルチコステロイドが、ジプロピオン酸ベクロメタゾン、モノプロピオン酸ベクロメタゾン、ブデソニド、シクレソニド、デスイソブチリル−シクレソニド、フルニソリド、プロピオン酸フルチカゾン、フランカルボン酸フルチカゾン、フランカルボン酸モメタゾン、イコメタゾンエンブテート、チキソコルトール21−ピバレート、およびトリアムシノロンアセトニドからなる群から選択される、請求項50に記載の方法。
- 被験者への用量として、スルホアルキルエーテルシクロデキストリンを含む水性液体担体に溶解したコルチコステロイドの48〜220μgを被験者へ噴霧投与することを含む、個々の被験者のコルチコステロイドについて150〜1600pg*h/mlの平均血漿中AUCtを与える方法。
- 噴霧が、空気ジェット式ネブライザー、超音波ネブライザー、電子ネブライザー、振動膜ネブライザー、振動メッシュネブライザー、振動板ネブライザー、振動発生器および水性チャンバーを含むネブライザー、およびノズルアレイを含むネブライザーからなる群から選択されるネブライザーを用いて行われる、請求項56に記載の方法。
- コルチコステロイドがブデソニドである、請求項57に記載の方法。
- スルホアルキルエーテルシクロデキストリンを含む水性液体担体に溶解した少なくとも45μgのコルチコステロイドを被験者に噴霧投与することを含む、被験者への用量として送達された少なくとも6(pg*h/ml)/μgのコルチコステロイドの、被験者へのコルチコステロイドの用量で正規化した平均血漿中AUCtを被験者に与える方法。
- 噴霧が、空気ジェット式ネブライザー、超音波ネブライザー、電子ネブライザー、振動膜ネブライザー、振動メッシュネブライザーおよび振動板ネブライザーからなる群から選択されるネブライザーを用いて行われる、請求項59に記載の方法。
- 単位用量が45から1000μgである、請求項60に記載の方法。
- コルチコステロイドがブデソニドである、請求項60に記載の方法。
- スルホアルキルエーテルシクロデキストリンを含む水性液体担体に溶解した少なくとも45μgのコルチコステロイドを被験者に噴霧投与することを含む、被験者への用量として送達された少なくとも8(pg*h/ml)/μgのコルチコステロイドの、被験者へのコルチコステロイドの用量で正規化した平均血漿中AUCiを被験者に与える方法。
- 噴霧が、空気ジェット式ネブライザー、超音波ネブライザー、電子ネブライザー、振動膜ネブライザー、振動メッシュネブライザーおよび振動板ネブライザーからなる群から選択されるネブライザーを用いて行われる、請求項63に記載の方法。
- コルチコステロイドがブデソニドである、請求項64に記載の方法。
- 単位用量が45から1000μgである、請求項64に記載の方法。
- 参照単位用量の水性懸濁液ベースの液体製剤の噴霧投与に比べて、被験者に送達されるコルチコステロイドの2倍〜4倍未満増加分の平均血漿中AUCt/μgを与える、請求項59に記載の方法。
- 参照単位用量の水性懸濁液ベースの液体製剤の噴霧投与に比べて、被験者に送達されるコルチコステロイドの1.5〜5倍増加分の個体の血漿中AUCt/μgを与える、請求項59に記載の方法。
- 参照単位用量の水性懸濁液ベースの液体製剤の噴霧投与に比べて、被験者に送達されるコルチコステロイドの2〜4倍未満増加分の平均血漿中AUCi/μgを与える、請求項63に記載の方法。
- 参照単位用量の水性懸濁液ベースの液体製剤の噴霧投与に比べて、被験者に送達されるコルチコステロイドの1.5倍〜5倍増加分の個体の血漿中AUCi/μgを与える、請求項63に記載の方法。
- 水性液体担体、スルホアルキルエーテルシクロデキストリン、及び製剤中に溶解したコルチコステロイドの1回用量を含む水性液体製剤を、被験者に対して吸入によって投与または送達することを含む、それを必要とする被験者における、気道の疾患または障害を治療する方法であって、ここで製剤が同様の条件下に投与された懸濁液ベースの製剤にまさる薬物動態学的プロファイルの強化をもたらす、方法。
- それを必要とする被験者の気道に1回用量のコルチコステロイドを投与または送達する方法であって、水性液体担体、スルホアルキルエーテルシクロデキストリン、および製剤中に溶解したコルチコステロイドを含む水性液体製剤の1回量を含むネブライザーで、コルチコステロイドを投与または送達することを含み、ここで操作中、このシステムが、ネブライザーとコルチコステロイドの懸濁液ベースの製剤を含む別のシステムにまさって、強化された薬物送達、増大した薬物投与率、短縮された処置時間、低減した毒性、改善した安定性、強化された生体吸収、増加したアウトプット率、増加した全アウトプット、強化された薬物動態学的プロファイル、低減したコルチコステロイド関連副作用、増加した肺沈着、低減した口腔咽頭沈着、および/または改善した噴霧性能をもたらす、上記方法。
- 製剤が、同様の条件下において投与された懸濁液ベースの製剤にまさって、強化された薬物送達、増大した薬物投与率、短縮された処置時間、低減した毒性、改善した安定性、強化された生体吸収、増加したアウトプット率、増加した全アウトプット、強化された薬物動態学的プロファイル、低減したコルチコステロイド関連副作用、増加した肺沈着、低減した口腔咽頭沈着、および/または向上した噴霧性能をもたらす、請求項71に記載の方法。
- コルチコステロイドの用量が、少なくとも25μg、40μg、少なくとも45μg、少なくとも48μg、45〜1000μg、約1μg〜20mg、または1μg〜10mg、0.01mg〜10mg、0.025mg〜10mg、0.05mg〜5mg、0.1mg〜5mg、0.125mg〜5mg、0.25mg〜5mg、0.5mg〜5mg、0.05mg〜2mg、0.1mg〜2mg、0.125mg〜2mg、0.25mg〜2mg、0.5mg〜2mg、1μg、10μg、25μg、50μg、100μg、125μg、200μg、250μg、25〜66μg、48〜81μg、73〜125μg、40μg、64μg、95μg、35〜95μg、25〜125μg、60〜170μg、110μg、170μg、45〜220μg、45〜85μg、48〜82μg、85〜160μg、140〜220μg、120〜325μg、205μg、320μg、325μg、90〜400μg、95〜170μg、165〜275μg、または275〜400μgである、請求項71または72に記載の方法。
- 液体が、10μl〜100ml、50μl〜50ml、50μl〜10ml、0.1〜10ml、0.1ml〜10ml未満、0.1ml〜7.5ml、0.1ml〜5ml、0.1ml〜3ml、0.1ml〜2ml、0.1ml〜1ml、0.05ml〜7.5ml、0.05ml〜5ml、0.05ml〜3ml、0.05ml〜2ml、または0.05ml〜1mlの体積を有する、請求項71または72に記載の方法。
- 送達または投与の工程が、30分未満、20分未満、10分未満、7分未満、5分未満、3分未満、もしくは2分未満の時間にわたって行われ、またはその時間が約0.05〜10分、約0.1〜5分、約0.1〜3分、約0.1〜2分、約0.1〜1.5分、約0.5分 約1.5分、もしくは約1分であり、またはその時間が被験者が1回の呼吸に要するほどの時間(約1〜3または1〜5秒)である、請求項71又は72に記載の方法。
- 強化された薬物動態学的プロファイルが、懸濁液製剤の投与に比べて、Cmaxで1.5〜8倍高い、1.5〜6倍高い、1.5〜4倍高い、1.5〜2倍高い、1.64〜3.55倍高い、Cmaxで1.48〜6.25倍高い、AUCinfで1.59〜3.55または1.19〜6.11倍高い、AUClastで1.69〜3.67または1.21〜7.66倍高い強化である、請求項71または72に記載の方法。
- コルチコステロイドの用量の20%〜85%、または30%〜80%、または少なくとも30%、少なくとも40%、少なくとも56%、少なくとも59%、少なくとも62%が被験者の肺に送達される、請求項71または72に記載の方法。
- 用量非正規化ベースで、90〜900、200〜600、200〜550、200〜250、400〜450、500〜600、225、437、又は545のCmax(コルチコステロイドのpg/ml)を被験者に与える、請求項71または72に記載の方法。
- 以下の用量正規化Cmax(pg/ml/μg):1)名目利用用量正規化ベースで0.3〜2、0.35〜2、0.6〜1.5、0.5〜1.2、0.8〜1、0.8〜0.9、0.7〜0.8、0.4、1.9、0.6、1.5、0.5、1.2、0.35、2、0.7、0.8、または0.9;2)肺への用量正規化ベースで3.4〜9.2、3.5〜8.5、5.5〜9.2、4.5〜7.5、5.8〜7、3.4、3.5、4.5、5.5、9.2、8.5、7.5、5.8、5.9、6、または7;3)被験者への用量正規化ベースで1.7〜7.5、3.2〜4.1、1.9〜6、3.2〜7.5、1.7〜5.2、3.6、4.1、3.2、1.9、6、3.2、7.4、7.5、1.7、5.2または5.3;4)放出用量正規化べースで0.9〜3.3、1.7〜2.2、0.9〜3、1〜3、1.7〜3.3、1〜2.7、1.9、2.1、2.2、1.7、0.9、1、2、3、2.9、3.2、3.3、または2.7を被験者に与える、請求項71または72に記載の方法。
- 製剤および懸濁液剤中のコルチコステロイドの用量がほぼ同量充填された場合、コルチコステロイドの非正規化用量に基づいて、製剤によって与えられたCmaxが、懸濁液ベースの製剤によって与えられたCmaxよりも1.6〜2、1.5〜3、1.5〜2.5、1.5〜2、1.5、1.6、2、2.5、または3倍高い、請求項71または72に記載の方法。
- コルチコステロイドの名目利用用量正規化に基づいて、コルチコステロイド製剤によって与えられたCmaxが、懸濁液ベースの製剤によって与えられたCmaxよりも、1.8〜6.2、1.5〜6.5、2〜6.5、1.5〜5.5、2〜4、1.5〜4、1.5〜3、2.7、3.3、3.4、1.5、6.5、2、5.5、4、または3倍高い、請求項71または72に記載の方法。
- コルチコステロイドの肺への用量正規化に基づいて、コルチコステロイド製剤によって与えられたCmaxが、懸濁液ベースの製剤によって与えられたCmaxよりも、1.4〜4.3、1.4〜4.5、1.5〜4.5、1.5〜3.5、1.5〜3、1.4〜3、1.5〜2.5、1.5〜2、2、2.3、1.4、4.5、3.5、3、1.5または2.5倍高い、請求項71または72に記載の方法。
- コルチコステロイドの被験者への用量正規化に基づいて、コルチコステロイド製剤によって与えられたCmaxが、懸濁液ベースの製剤によって与えられたCmaxよりも、2〜3.5、2〜5、1.7〜3.8、1.7〜5、2.7、3、2.4、2、3.5、5、1.7、または3.8倍高い、請求項71または72に記載の方法。
- コルチコステロイドの放出用量正規化に基づいて、コルチコステロイド製剤によって与えられたCmaxが、懸濁液ベースの製剤によって与えられたCmaxよりも、1.9〜6.3、1.75〜6.5、2.2〜4.2、2.2〜6.3、1.9〜4.2、3.2、3.5、3.6、2.8、1.75、6.5、2.2、4.2、または6.3倍高い、請求項71または72に記載の方法。
- 製剤中のコルチコステロイドの用量が懸濁液剤中の用量より約2倍低い場合、コルチコステロイド製剤によって与えられたCmaxが、懸濁液ベースの製剤によって与えられたCmaxよりも、少なくとも1.5、1.6、2、2.6、および3倍高い、請求項71または72に記載の方法。
- 用量非正規化に基づいて1600〜1800、1650〜1750、または1700のCmax(pg/ml)を与える、請求項71または72に記載の方法。
- 1)充填用量名目正規化ベースで、1)1〜2、1.6〜1.8、又は1.7;2)放出用量正規化ベースで、2〜2.5、または2.2の用量正規化Cmax(pg/ml/μg)を与える、請求項71または72に記載の方法。
- 製剤及び懸濁液剤中のコルチコステロイドの用量がほぼ同じ場合、コルチコステロイドの正規化名目用量に基づき、コルチコステロイド製剤によって与えられたCmaxが、懸濁液ベースの製剤によって与えられたCmaxより少なくとも1.7、1.8、1.9、または2倍高い、請求項71または72に記載の方法。
- コルチコステロイドの放出用量正規化に基づき、コルチコステロイド製剤によって与えられたCmaxが、懸濁液ベースの製剤によって与えられたCmaxよりも、1.5、1.6、2倍まで高い、請求項71または72に記載の方法。
- 用量非正規化ベースで、500〜1700、530〜1650、250〜2500、280〜1300、780〜1300、980〜2450、275、775、980、2400、2500、1300、1290、530,1650、250、280または780のAUCinf(pg*h/ml)を被験者に与える、請求項71または72に記載の方法。
- 以下の用量正規化AUCinf(pg/ml/μg):1)名目利用用量正規化ベースで1〜5.5、2〜2.2、1〜5.3、1.1〜5.2、1.5〜2.6、1.3〜3.3、2,2.1、2.2、1、5.5、5.3、5.2、1.5、2.6、1.3、または3.3;2)肺への用量正規化ベースで10〜25、14〜18、10.2〜20、13.6〜18.8、11.2〜24.7、10.2、20、13.6、14、19、18.8、11、11.2、25、24.7、14.2、16.2、17.3;3)被験者への用量正規化ベースで4〜16、4.2〜16.1、8〜12.2、5.4〜16、5.4〜17、8.5〜9.6、8.5、9.5,9.6、4.2、16.1、8、12.2、12、5.4、16、17、または16.5;4)放出用量正規化ベースで2.5〜9、2.6〜8.5、4.5〜5.1、2.5〜8、2.6〜7.9、4.2〜6.7、3.1〜8.5、3.2〜8.5、4.5、4.6、5、5.1、2.5、2.6、4.2、3.1、9、8.5、5.1、8、7.9、または6.7を、被験者に与える、請求項71または72に記載の方法。
- 製剤および懸濁液剤中のコルチコステロイドの用量がほぼ同量の場合、コルチコステロイドの非正規化用量に基づいて、コルチコステロイド製剤によって与えられたAUCinfが、懸濁液ベースの製剤によって与えられたAUCinfよりも1.6〜2.5、1.6〜3.1、1.5〜3.5、1.5〜3.3、2.5〜3.3、3.1、1.5、3.3、1.6、または2.5倍高い、請求項71または72に記載の方法。
- コルチコステロイドの名目利用用量正規化に基づいて、コルチコステロイド製剤によって与えられたAUCinfが、懸濁液ベースの製剤によって与えられたAUCinfよりも、1.75〜6.5、1.75〜6.1、2〜6.5、2〜6.1、2〜4.5、2〜4.4、3.3、3.2、3.5、3.4、1.75、6.5、6.1、2、4.5、または4.4倍高い、請求項71または72に記載の方法。
- コルチコステロイドの肺への用量正規化に基づいて、コルチコステロイド製剤によって与えられたAUCinfが、懸濁液ベースの製剤によって与えられたAUCinfよりも、1.2〜3.5、1.2〜4、1.2〜3、1.2〜2.85、1.5〜3.5、1.4〜3.5、2、2.2、2.3、2.4、1.2、3、4、2.85、1.5、3.5、または1.4倍高い、請求項71または72に記載の方法。
- コルチコステロイドの被験者への用量正規化に基づいて、コルチコステロイド製剤によって与えられたAUCinfが、懸濁液ベースの製剤によって与えられたAUCinfよりも、1.6〜4.9、1.5〜5、1.6〜5、1.6〜3.7、1.6〜3.6、2〜4.9、1.9〜4、2、2.6、1.5、5、1.6、3.7、3.6、2、4.9、1.9、または4倍高い、請求項71または72に記載の方法。
- コルチコステロイドの放出用量正規化に基づいて、コルチコステロイド製剤によって与えられたAUCinfが、懸濁液ベースの製剤によって与えられたAUCinfよりも、1.5〜6、1.7〜6、1.9〜6、1.9〜5.4、2.3〜5.8、1.9〜5.5、1.9〜5.8、1.5、6、1.7、1.9、5.4、2.3、5.8、5.8、3.2、3.5、または3.6倍高い、請求項71または72に記載の方法。
- 製剤中のコルチコステロイドの用量が懸濁液剤中の用量よりも約2倍低い場合、コルチコステロイド製剤によって与えられたAUCinfが、懸濁液ベースの製剤によって与えられたAUCinfよりも、少なくとも1.5、1.6、2、2.5、3、または3.1倍高い、請求項71または72に記載の方法。
- コルチコステロイドの用量非正規化に基づき、2000〜3000、2500〜2700、2000、3000、または2600のAUC0−8hr(pg*h/ml)を被験者に与える、請求項71または72に記載の方法。
- 被験者において、1)充填用量名目正規化ベースで、2〜3、2.5〜2.7、または2.6;および/または2)放出用量正規化ベースで、3〜4、3.4〜3.5、または3.4の1回用量正規化AUCinf(pg/ml/μg)を与える、請求項71または72に記載の方法。
- リザーバを装備したネブライザー;ならびに水性液体担体、溶解促進剤、および1回用量のコルチコステロイドを含む水性液体製剤を含むシステムであって、ここで製剤の噴霧中、ネブライザーが、同様の条件下にネブライザーで噴霧する懸濁液ベースの製剤の濃度増加率に比べて、リザーバの製剤中のコルチコステロイドの濃度増加率の減少パーセントをもたらすシステム。
- 濃度増加率の減少パーセントが10%〜60%、15%〜60%、20%〜60%、30%〜60%、または40%〜60%である、請求項101に記載のシステム。
- システムが、噴霧1分当たり0〜40、1〜40、5〜30、または10〜30mcgコルチコステロイド/mL製剤体積の濃度増加率を与える、請求項101に記載のシステム。
- 水性液体担体、スルホアルキルエーテルシクロデキストリン、および製剤に溶解した1回用量のコルチコステロイドを含む液体製剤を被験者に吸入投与することを含む、それを必要とする被験者における気道の疾患または障害を治療する方法であって、ここでコルチコステロイドの用量が160〜1600pg*h/mlの平均血漿中AUCtを与えるのに十分な量で存在し、そしてSAE−CD対コルチコステロイドのモル比が10:1より大きい、方法。
- コルチコステロイドについて150〜1600pg*h/mlの血漿中AUCtを与えるために、スルホアルキルエーテルシクロデキストリンを含む水性液体担体に溶解した25〜400μgのコルチコステロイドを被験者に噴霧投与することを含む、被験者へコルチコステロイドを与える方法。
- スルホアルキルエーテルシクロデキストリンを含む水性液体担体に溶解した少なくとも25μgの1回用量のコルチコステロイドを、被験者に噴霧投与することを含む、被験者に、少なくとも6(pg*h/ml)/μgのコルチコステロイドの、コルチコステロイドの用量で正規化した、血漿中AUCtを与える方法。
- 被験者に、少なくとも8(pg*h/ml)/μgのコルチコステロイドの、コルチコステロイドの用量で正規化した、AUCiを与える方法であって、スルホアルキルエーテルシクロデキストリンを含む水性液体担体に溶解した少なくとも25μgの1回用量のコルチコステロイドを、被験者に噴霧投与することを含む、方法。
- コルチコステロイドがブデソニドである、請求項71〜107のいずれか1項に記載の発明。
- コルチコステロイドがフルニソリドの親油性に近似するか又はそれを超える親油性を有する、請求項71〜107のいずれか1項に記載の発明。
- コルチコステロイドが、ジプロピオン酸ベクロメタゾン、モノプロピオン酸ベクロメタゾン、ブデソニド、シクレソニド、デスイソブチリル−シクレソニド、フルニソリド、プロピオン酸フルチカゾン、フランカルボン酸フルチカゾン、フランカルボン酸モメタゾン、イコメタゾンエンブテート、チキソコルトール21−ピバレート、およびトリアムシノロンアセトニドからなる群から選択される、請求項109に記載の発明。
- 投与または送達の工程が、空気ジェット式ネブライザー、超音波ネブライザー、電子ネブライザー、振動膜ネブライザー、振動メッシュネブライザー、振動板ネブライザー、振動発生器および水性チャンバーを含むネブライザー、およびノズルアレイを含むネブライザーからなる群から選択されるネブライザーを用いて行われる、請求項71〜107のいずれか1項に記載の発明。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US11/479,979 US20070020299A1 (en) | 2003-12-31 | 2006-06-30 | Inhalant formulation containing sulfoalkyl ether cyclodextrin and corticosteroid |
| PCT/US2006/062346 WO2008005053A1 (en) | 2006-06-30 | 2006-12-19 | Inhalant formulation containing sulfoalkyl ether cyclodextrin and corticosteroid |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2009542649A true JP2009542649A (ja) | 2009-12-03 |
| JP2009542649A5 JP2009542649A5 (ja) | 2010-01-28 |
Family
ID=38894876
Family Applications (4)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2009518094A Withdrawn JP2009542649A (ja) | 2006-06-30 | 2006-12-20 | スルホアルキルエーテルシクロデキストリンおよびコルチコステロイドを含む吸入製剤 |
| JP2014096717A Pending JP2014159467A (ja) | 2006-06-30 | 2014-05-08 | 鼻および眼へのコルチコステロイド水溶液送達 |
| JP2017088045A Active JP6409090B2 (ja) | 2006-06-30 | 2017-04-27 | 鼻および眼へのコルチコステロイド水溶液送達 |
| JP2018175728A Pending JP2019006818A (ja) | 2006-06-30 | 2018-09-20 | 鼻および眼へのコルチコステロイド水溶液送達 |
Family Applications After (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2014096717A Pending JP2014159467A (ja) | 2006-06-30 | 2014-05-08 | 鼻および眼へのコルチコステロイド水溶液送達 |
| JP2017088045A Active JP6409090B2 (ja) | 2006-06-30 | 2017-04-27 | 鼻および眼へのコルチコステロイド水溶液送達 |
| JP2018175728A Pending JP2019006818A (ja) | 2006-06-30 | 2018-09-20 | 鼻および眼へのコルチコステロイド水溶液送達 |
Country Status (13)
| Country | Link |
|---|---|
| US (9) | US20070020299A1 (ja) |
| EP (1) | EP2043599A4 (ja) |
| JP (4) | JP2009542649A (ja) |
| KR (3) | KR101691222B1 (ja) |
| CN (2) | CN102319231A (ja) |
| AU (1) | AU2006345712A1 (ja) |
| BR (1) | BRPI0621773A2 (ja) |
| CA (2) | CA2656318A1 (ja) |
| IL (1) | IL196185A0 (ja) |
| MX (1) | MX2009000065A (ja) |
| NZ (1) | NZ597354A (ja) |
| RU (2) | RU2009102994A (ja) |
| WO (3) | WO2008005053A1 (ja) |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2014505717A (ja) * | 2011-02-17 | 2014-03-06 | シプラ・リミテッド | 医薬組成物 |
| JP2018521987A (ja) * | 2015-06-18 | 2018-08-09 | セージ セラピューティクス, インコーポレイテッド | 神経活性ステロイド溶液およびその使用方法 |
| JP2020100658A (ja) * | 2014-03-28 | 2020-07-02 | ユニベルシテ・ド・リエージュUniversite De Liege | シクロデキストリン及びブデソニド誘導体組成物ならびに方法 |
Families Citing this family (92)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7650004B2 (en) * | 2001-11-15 | 2010-01-19 | Starkey Laboratories, Inc. | Hearing aids and methods and apparatus for audio fitting thereof |
| US20090215735A1 (en) * | 2002-02-25 | 2009-08-27 | Alcon, Inc. | Topical solution formulations containing a corticosteroid and a cyclodextrin |
| US20070020299A1 (en) | 2003-12-31 | 2007-01-25 | Pipkin James D | Inhalant formulation containing sulfoalkyl ether cyclodextrin and corticosteroid |
| US20070020298A1 (en) * | 2003-12-31 | 2007-01-25 | Pipkin James D | Inhalant formulation containing sulfoalkyl ether gamma-cyclodextrin and corticosteroid |
| US8497258B2 (en) | 2005-11-12 | 2013-07-30 | The Regents Of The University Of California | Viscous budesonide for the treatment of inflammatory diseases of the gastrointestinal tract |
| GB0604141D0 (en) * | 2006-03-01 | 2006-04-12 | Arrow Int Ltd | Nebulizer formulation |
| US7986790B2 (en) * | 2006-03-14 | 2011-07-26 | Starkey Laboratories, Inc. | System for evaluating hearing assistance device settings using detected sound environment |
| US8681999B2 (en) * | 2006-10-23 | 2014-03-25 | Starkey Laboratories, Inc. | Entrainment avoidance with an auto regressive filter |
| EP2120875B1 (en) | 2007-02-11 | 2018-07-11 | Map Pharmaceuticals Inc. | Method of therapeutic administration of dhe to enable rapid relief of migraine while minimizing side effect profile |
| ES2493641T3 (es) * | 2007-06-28 | 2014-09-12 | Cydex Pharmaceuticals, Inc. | Administración nasal de soluciones acuosas de corticosteroides |
| CN106038481A (zh) * | 2007-06-28 | 2016-10-26 | 锡德克斯药物公司 | 皮质类固醇水溶液的鼻部和眼部给药 |
| ES2781949T3 (es) | 2007-11-13 | 2020-09-09 | Meritage Pharma Inc | Composiciones para el tratamiento de la inflamación gastrointestinal |
| US20090123390A1 (en) * | 2007-11-13 | 2009-05-14 | Meritage Pharma, Inc. | Compositions for the treatment of gastrointestinal inflammation |
| US8718288B2 (en) * | 2007-12-14 | 2014-05-06 | Starkey Laboratories, Inc. | System for customizing hearing assistance devices |
| US20110082150A1 (en) * | 2008-02-11 | 2011-04-07 | Robert Owen Cook | Headache pre-emption by dihydroergotamine treatment during headache Precursor events |
| US8571244B2 (en) * | 2008-03-25 | 2013-10-29 | Starkey Laboratories, Inc. | Apparatus and method for dynamic detection and attenuation of periodic acoustic feedback |
| US7635773B2 (en) | 2008-04-28 | 2009-12-22 | Cydex Pharmaceuticals, Inc. | Sulfoalkyl ether cyclodextrin compositions |
| US20110224232A1 (en) * | 2008-05-06 | 2011-09-15 | Board Of Regents, The University Of Texas System | Treatment of Pulmonary Fungal Infection With Voriconazole via Inhalation |
| EP2282725A4 (en) * | 2008-06-05 | 2012-07-04 | Cpex Pharmaceuticals Inc | NASAL FORMULATIONS OF INSULIN |
| US20100196483A1 (en) * | 2009-02-04 | 2010-08-05 | Activaero Gmbh Research & Development | Method for treatmentof severe and uncontrollable asthma |
| US8668901B2 (en) * | 2009-02-04 | 2014-03-11 | Activaero Gmbh Research & Development | Use of a glucocorticoid composition for the treatment of severe and uncontrolled asthma |
| US8834848B2 (en) * | 2009-02-04 | 2014-09-16 | Activaero Gmbh Research & Development | Flow and volume regulated inhalation for treatment of severe oral corticosteroid-dependent asthma |
| WO2010151804A1 (en) * | 2009-06-26 | 2010-12-29 | Map Pharmaceuticals, Inc. | Administration of dihydroergotamine mesylate particles using a metered dose inhaler |
| US8359283B2 (en) * | 2009-08-31 | 2013-01-22 | Starkey Laboratories, Inc. | Genetic algorithms with robust rank estimation for hearing assistance devices |
| EP2473161B1 (en) | 2009-08-31 | 2017-05-17 | Dr. Reddy's Laboratories Ltd. | Topical formulations comprising a steroid |
| US20120208857A1 (en) * | 2009-10-13 | 2012-08-16 | Burak Eric S | Pharmaceutical Compositions |
| US9729976B2 (en) * | 2009-12-22 | 2017-08-08 | Starkey Laboratories, Inc. | Acoustic feedback event monitoring system for hearing assistance devices |
| IN2012DN04858A (ja) * | 2009-12-23 | 2015-09-25 | Map Pharmaceuticals Inc | |
| WO2011135585A2 (en) | 2010-04-28 | 2011-11-03 | Cadila Healthcare Limited | Aqueous pharmaceutical solution of ciclesonide |
| AU2011305567A1 (en) * | 2010-09-22 | 2013-05-02 | Map Pharmaceuticals, Inc. | Corticosteroid particles and method of production |
| CN102416179B (zh) * | 2010-09-28 | 2014-05-07 | 益得生物科技股份有限公司 | 用于哮喘的吸入性复方组合物 |
| WO2012066086A1 (en) * | 2010-11-17 | 2012-05-24 | Sanofi-Aventis Deutschland Gmbh | PHARMACEUTICAL FORMULATION COMPRISING INSULIN GLARGINE AND SULFOBUTYL ETHER 7-ß-CYCLODEXTRIN |
| EP2723735A4 (en) | 2011-06-23 | 2015-02-18 | Map Pharmaceuticals Inc | NOVEL ANALOGUES OF FLUORO-ERGOLINE |
| CA2859173A1 (en) | 2011-12-19 | 2013-06-27 | Map Pharmaceuticals, Inc. | Novel iso-ergoline derivatives |
| SG11201403433PA (en) * | 2011-12-21 | 2014-07-30 | Map Pharmaceuticals Inc | Novel neuromodulatory compounds |
| WO2013112605A2 (en) | 2012-01-23 | 2013-08-01 | Sage Therapeutics, Inc. | Neuroactive steroid formulations and methods of treating cns disorders |
| DK2814849T3 (da) | 2012-02-15 | 2020-03-09 | Cydex Pharmaceuticals Inc | Fremgangsmåde til fremstilling af cyclodextrin-derivater |
| JP2015508846A (ja) | 2012-02-28 | 2015-03-23 | サイデックス・ファーマシューティカルズ・インコーポレイテッド | アルキル化シクロデキストリン組成物ならびにその調製方法および使用方法 |
| US9012640B2 (en) | 2012-06-22 | 2015-04-21 | Map Pharmaceuticals, Inc. | Cabergoline derivatives |
| HUE056838T2 (hu) | 2012-08-21 | 2022-04-28 | Sage Therapeutics Inc | Allopregnanolon makacs epileptikus állapot kezelésére |
| SG11201503089WA (en) | 2012-10-22 | 2015-05-28 | Cydex Pharmaceuticals Inc | Alkylated cyclodextrin compositions and processes for preparing and using the same |
| WO2014100351A2 (en) | 2012-12-21 | 2014-06-26 | Map Pharmaceuticals, Inc. | 8'-hydroxy-dihydroergotamine compounds and compositions |
| EP2938339B1 (en) * | 2012-12-27 | 2020-08-19 | Massachusetts Eye & Ear Infirmary | Treatment of rhinosinusitis with p-glycoprotein inhibitors |
| CN105188758A (zh) * | 2013-03-15 | 2015-12-23 | 梅迪奇斯医药公司 | 氟尼缩松的局部组合物及治疗方法 |
| ES2746951T3 (es) * | 2013-03-29 | 2020-03-09 | Ocean Farma S R L | Suspensión oral para tratar esofagitis eosinofílica |
| US9393177B2 (en) | 2013-08-20 | 2016-07-19 | Anutra Medical, Inc. | Cassette assembly for syringe fill system |
| US20160184431A1 (en) | 2014-03-11 | 2016-06-30 | Promius Pharma Llc | Topical compositions comprising a corticosteroid |
| WO2015150968A2 (en) * | 2014-03-29 | 2015-10-08 | Intas Pharmaceuticals Ltd. | Lyophilized pharmaceutical composition of fc-peptide fusion protein |
| AU2015252908B2 (en) * | 2014-05-01 | 2017-12-07 | Integral Biosystems Llc | Membrane-adherent self-assembled systems for treatment of ocular disorders |
| USD774182S1 (en) | 2014-06-06 | 2016-12-13 | Anutra Medical, Inc. | Anesthetic delivery device |
| USD750768S1 (en) | 2014-06-06 | 2016-03-01 | Anutra Medical, Inc. | Fluid administration syringe |
| USD763433S1 (en) | 2014-06-06 | 2016-08-09 | Anutra Medical, Inc. | Delivery system cassette |
| US9421199B2 (en) | 2014-06-24 | 2016-08-23 | Sydnexis, Inc. | Ophthalmic composition |
| WO2016172712A2 (en) | 2015-04-23 | 2016-10-27 | Sydnexis, Inc. | Ophthalmic composition |
| HUE063851T2 (hu) | 2014-08-22 | 2024-02-28 | Cydex Pharmaceuticals Inc | Frakcionált alkilezett ciklodextrin készítmények és eljárás ezek elõállítására és alkalmazására |
| US11382909B2 (en) | 2014-09-05 | 2022-07-12 | Sydnexis, Inc. | Ophthalmic composition |
| JOP20200195A1 (ar) | 2014-09-08 | 2017-06-16 | Sage Therapeutics Inc | سترويدات وتركيبات نشطة عصبياً، واستخداماتها |
| GB201500447D0 (en) * | 2015-01-12 | 2015-02-25 | Glaxosmithkline Ip Dev Ltd | Novel Combination Product |
| KR20170129126A (ko) * | 2015-02-13 | 2017-11-24 | 벤더르빌트 유니버시티 | 밀리논 조성물 및 이를 투여하기 위한 방법 |
| US11091543B2 (en) | 2015-05-07 | 2021-08-17 | Swedish Orphan Biovitrum Ag | Methods, compositions and dosing regimens for treating or preventing interferon-gamma related indications |
| IL302519A (en) | 2015-05-07 | 2023-07-01 | Novimmune Sa | Methods and preparations for diagnosis and treatment of disorders in patients with high levels of chemokine C.-X.-C. Ligand 9 and other biomarkers |
| JP2018521000A (ja) | 2015-05-29 | 2018-08-02 | シドネキシス,インク. | D2oで安定化された医薬製剤 |
| CN104971039B (zh) * | 2015-07-07 | 2018-04-17 | 上海通用药业股份有限公司 | 一种含溶液型醋酸曲安奈德的医用产品 |
| KR20180101438A (ko) | 2016-01-08 | 2018-09-12 | 테론 파마슈티칼즈, 인크. | 7-아조니아바이사이클로[2.2.1]헵탄 유도체의 건조 분말 흡입기 조성물 |
| US11291672B2 (en) | 2016-01-12 | 2022-04-05 | Grace Therapeutics Inc. | Betamethasone oral spray formulation and method of use to treat ataxia |
| WO2017123933A1 (en) | 2016-01-15 | 2017-07-20 | Massachusetts Eye And Ear Infirmary | Secreted p-glycoprotein is a non-invasive biomarker of chronic rhinosinusitis |
| IL300422A (en) | 2016-03-08 | 2023-04-01 | Sage Therapeutics Inc | Neuroactive steroids, preparations and their uses |
| CN106070189A (zh) * | 2016-06-17 | 2016-11-09 | 京博农化科技股份有限公司 | 一种展膜油剂成膜助剂 |
| IT201600075246A1 (it) * | 2016-07-19 | 2018-01-19 | Jointherapeutics S R L | Composizioni comprendenti una matrice polisaccaridica per il rilascio controllato di principi attivi. |
| US11000490B2 (en) | 2016-11-02 | 2021-05-11 | Centrexion Therapeutics Corporation | Stable aqueous capsaicin injectable formulations and medical uses thereof |
| EA201990606A1 (ru) * | 2016-11-16 | 2019-10-31 | Распыляемый тиотропий | |
| US20200206166A1 (en) | 2017-07-20 | 2020-07-02 | Centrexion Therapeutics Corporation | Methods and compositions for treatment of pain using capsaicin |
| US11119094B2 (en) * | 2017-09-27 | 2021-09-14 | Cd Diagnostics, Inc. | Aqueous citrate-buffered metal solutions |
| WO2019100362A1 (en) * | 2017-11-27 | 2019-05-31 | Wise Ally Holdings Ltd | Vaporizer system |
| US10583081B1 (en) * | 2017-11-27 | 2020-03-10 | Richard A. Myers | Apparatus and formulation for treating mouth ulcers |
| WO2020247376A1 (en) * | 2019-06-03 | 2020-12-10 | Cai Gu Huang | Inhalable formulation of a solution containing indacaterol maleate and glycopyrronium bromide |
| US11572295B1 (en) * | 2019-06-11 | 2023-02-07 | Swamp Fox Innovations, LLC | Compositions and methods for reduction of free chlorine and related odor |
| CN110551226B (zh) * | 2019-07-30 | 2021-06-08 | 大连理工大学 | 一种亲/疏水性可控转换的叔胺型含氮聚糖衍生物及其制备方法和应用 |
| CN110559675A (zh) * | 2019-09-20 | 2019-12-13 | 新疆天业(集团)有限公司 | 糊树脂干燥生产控制方法 |
| IT201900022881A1 (it) * | 2019-12-03 | 2021-06-03 | Ntc Srl | Budesonide per uso oftalmico in un metodo di trattamento dell’occhio |
| CN114746098A (zh) * | 2019-12-03 | 2022-07-12 | Ntc有限公司 | 用于眼科的包含布地奈德的组合物 |
| US20210205223A1 (en) * | 2020-01-04 | 2021-07-08 | Cai Gu Huang | Propellant-free formulation for inhalation |
| US20210275449A1 (en) * | 2020-03-01 | 2021-09-09 | Cai Gu Huang | Inhalable Formulation of a Solution Containing Glycopyrronium Bromide |
| WO2021252577A1 (en) * | 2020-06-09 | 2021-12-16 | Anovent Pharmaceutical (U.S.), Llc | Pharmaceutical formulation containing umeclidinium bromide and vilanterol trifenatate |
| CN115884756A (zh) * | 2020-06-09 | 2023-03-31 | 广州谷森制药有限公司 | 含有格隆溴铵和马来酸茚达特罗的药物制剂 |
| CN115835885A (zh) * | 2020-06-23 | 2023-03-21 | 广州谷森制药有限公司 | 包含奥达特罗和布地奈德的药物组合物的制备 |
| US20230263725A1 (en) * | 2020-07-09 | 2023-08-24 | Beyond Barriers Therapeutics, Inc. | Intranasal administration of an antioxidant compound for treating coronavirus infection |
| US20230285350A1 (en) * | 2020-07-15 | 2023-09-14 | Lyotip, Inc. | Formulations for tetracaine and lidocaine |
| WO2022073009A1 (en) | 2020-09-29 | 2022-04-07 | iPharma Labs, Inc. | Liquid formulations of indacaterol |
| GB202107153D0 (en) * | 2021-05-19 | 2021-06-30 | UCB Biopharma SRL | Method for filling vials containing liquid drug products |
| US11904046B1 (en) * | 2022-11-14 | 2024-02-20 | Eton Pharmaceuticals, Inc. | Hydrocortisone oral liquid formulations |
| CN116693704B (zh) * | 2023-06-26 | 2024-08-23 | 郑州轻工业大学 | 一种基于烟草废弃物的纤维素纳米晶的制备方法 |
Family Cites Families (163)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3008875A (en) * | 1960-01-08 | 1961-11-14 | Upjohn Co | Neomycin and mirystyl-gamma-picolinium halide compositions |
| NL289785A (ja) * | 1962-11-29 | |||
| US3426011A (en) * | 1967-02-13 | 1969-02-04 | Corn Products Co | Cyclodextrins with anionic properties |
| HU190356B (en) * | 1981-10-27 | 1986-08-28 | Richter Gedeon Vegyeszeti Termekek Gyara Rt,Hu | Process for preparing steroid-gamma-cyclodextrin inclusion complexes with high water-solubility |
| US4383992A (en) | 1982-02-08 | 1983-05-17 | Lipari John M | Water-soluble steroid compounds |
| JPS58225010A (ja) | 1982-06-25 | 1983-12-27 | Dai Ichi Seiyaku Co Ltd | コルチコステロイド類外用製剤 |
| SE8305864D0 (sv) | 1983-10-25 | 1983-10-25 | L E Medical | Ogondroppar |
| JPS61221120A (ja) | 1985-03-28 | 1986-10-01 | Nitto Electric Ind Co Ltd | 外用医薬部材 |
| US5192528A (en) * | 1985-05-22 | 1993-03-09 | Liposome Technology, Inc. | Corticosteroid inhalation treatment method |
| US6407079B1 (en) * | 1985-07-03 | 2002-06-18 | Janssen Pharmaceutica N.V. | Pharmaceutical compositions containing drugs which are instable or sparingly soluble in water and methods for their preparation |
| DE3877904D1 (de) | 1987-11-13 | 1993-03-11 | Asta Pharma Ag | Azelastin enthaltende arzneimittel zur anwendung in der nase und/oder am auge. |
| US5002935A (en) * | 1987-12-30 | 1991-03-26 | University Of Florida | Improvements in redox systems for brain-targeted drug delivery |
| EP0381747A4 (en) | 1988-08-15 | 1991-09-11 | American Maize-Products Company | Water soluble branched beta cyclodextrin steroid complex |
| EP0491812A4 (en) | 1989-09-14 | 1992-11-04 | Australian Commercial Research & Development Limited | Drug delivery compositions |
| SE8903219D0 (sv) | 1989-10-02 | 1989-10-02 | Astra Ab | Process for the manufacture of budesonide |
| KR0166088B1 (ko) | 1990-01-23 | 1999-01-15 | . | 수용해도가 증가된 시클로덱스트린 유도체 및 이의 용도 |
| US5376645A (en) * | 1990-01-23 | 1994-12-27 | University Of Kansas | Derivatives of cyclodextrins exhibiting enhanced aqueous solubility and the use thereof |
| WO1991013100A1 (en) | 1990-03-02 | 1991-09-05 | Australian Commercial Research & Development Limited | Cyclodextrin compositions and methods for pharmaceutical and industrial applications |
| JPH04198180A (ja) | 1990-11-28 | 1992-07-17 | Eezai Kagaku Kk | ベンジルフタラゾン誘導体の製造方法 |
| US5318780A (en) * | 1991-10-30 | 1994-06-07 | Mediventures Inc. | Medical uses of in situ formed gels |
| DE4207922A1 (de) | 1992-03-13 | 1993-09-23 | Pharmatech Gmbh | Wasserloesliche einschlussverbindungen und verfahren zu deren herstellung |
| US5324718A (en) | 1992-07-14 | 1994-06-28 | Thorsteinn Loftsson | Cyclodextrin/drug complexation |
| US5472954A (en) | 1992-07-14 | 1995-12-05 | Cyclops H.F. | Cyclodextrin complexation |
| US5977070A (en) | 1992-07-14 | 1999-11-02 | Piazza; Christin Teresa | Pharmaceutical compositions for the nasal delivery of compounds useful for the treatment of osteoporosis |
| US5840881A (en) | 1992-11-27 | 1998-11-24 | Takeda Chemical Industries, Ltd. | Composition containing a water-insoluble or slightly water-soluble compound with enhanced water-solubility |
| TW401300B (en) * | 1992-12-25 | 2000-08-11 | Senju Pharma Co | Antiallergic composition for ophthalmic or nasal use |
| IT1263831B (it) | 1993-01-29 | 1996-09-04 | Paolo Chiesi | Complessi di inclusione multicomponente ad elevata solubilita' costituiti da un farmaco di tipo basico, un acido ed una ciclodestrina |
| US5510339A (en) | 1993-02-02 | 1996-04-23 | Mayo Foundation For Medical Education And Research | Method for the treatment of bronchial asthma by administration of topical anesthetics |
| US5525623A (en) | 1993-03-12 | 1996-06-11 | Arris Pharmaceutical Corporation | Compositions and methods for the treatment of immunomediated inflammatory disorders |
| AU6428894A (en) * | 1993-03-26 | 1994-10-24 | Franciscus W.H.M. Merkus | Pharmaceutical compositions for intranasal administration of dihydroergotamine, apomorphine and morphine |
| BE1007402A5 (nl) * | 1993-03-26 | 1995-06-06 | Adir | Nasale farmaceutische preparaten met progestagene stof. |
| TW385308B (en) | 1994-03-04 | 2000-03-21 | Merck & Co Inc | Prodrugs of morpholine tachykinin receptor antagonists |
| DE4425255A1 (de) * | 1994-07-16 | 1996-01-18 | Asta Medica Ag | Formulierung zur inhalativen Applikation |
| EP0709099A3 (en) | 1994-09-28 | 1996-07-24 | Senju Pharma Co | Aqueous suspension for nasal administration containing cyclodextrin |
| US5576311A (en) | 1994-11-30 | 1996-11-19 | Pharmos Corporation | Cyclodextrins as suspending agents for pharmaceutical suspensions |
| EE9700136A (et) | 1994-12-22 | 1997-12-15 | Astra Aktiebolag | Paratüroidhormooni PTH sisaldav ravimpreparaat inhaleerimiseks |
| DE4446891A1 (de) * | 1994-12-27 | 1996-07-04 | Falk Pharma Gmbh | Stabile wäßrige Budesonid-Lösung |
| US5840713A (en) | 1995-04-03 | 1998-11-24 | Weisz; Paul B. | Therapy for tissue membrane insufficiency |
| US5576645A (en) | 1995-06-05 | 1996-11-19 | Hughes Aircraft Company | Sample and hold flip-flop for CMOS logic |
| US5654276A (en) | 1995-06-07 | 1997-08-05 | Affymax Technologies N.V. | Peptides and compounds that bind to the IL-5 receptor |
| US5668110A (en) | 1995-06-07 | 1997-09-16 | Affymax Technologies N.V. | Peptides and compounds that bind to the IL-5 receptor |
| US5683983A (en) | 1995-06-07 | 1997-11-04 | Glaxo Group Limited | Peptides and compounds that bind to the IL-5 receptor |
| US5677280A (en) | 1995-06-07 | 1997-10-14 | Glaxo Group Limited | Peptides and compounds that bind to the IL-5 receptor |
| US5824668A (en) * | 1996-11-07 | 1998-10-20 | Supergen, Inc. | Formulation for administration of steroid compounds |
| US5935941A (en) * | 1997-10-24 | 1999-08-10 | Pitha; Josef | Alkylations of cyclodextrins leading to derivatives which have a ridgidly extended cavity |
| WO1997046243A1 (en) | 1996-06-04 | 1997-12-11 | The Procter & Gamble Company | A nasal spray containing an intranasal steroid and an antihistamine |
| US5750549A (en) | 1996-10-15 | 1998-05-12 | Merck & Co., Inc. | Cycloalkyl tachykinin receptor antagonists |
| US5929094A (en) | 1996-10-25 | 1999-07-27 | Merck & Co., Inc. | Heteroaryl spiroethercycloalkyl tachykinin receptor antagonists |
| GB9625843D0 (en) | 1996-12-12 | 1997-01-29 | Merck & Co Inc | Phenyl spiroethercycloalkyl tachykinn receptor antagonists |
| AU4717997A (en) | 1996-10-28 | 1998-05-22 | Farmarc Nederland Bv | Inclusion complexes of beta-2-andrenergics for oral mucosal delivery |
| SE9604486D0 (sv) * | 1996-12-05 | 1996-12-05 | Astra Ab | Novel formulation |
| US6071910A (en) | 1996-12-05 | 2000-06-06 | Mayo Foundation For Medical Education And Research | Use of agents to treat eosinophil-associated pathologies |
| FR2756739B1 (fr) * | 1996-12-05 | 2000-04-28 | Astra Ab | Nouvelle formulation de budesonide |
| SE9700133D0 (sv) * | 1997-01-20 | 1997-01-20 | Astra Ab | New formulation |
| SE9700135D0 (sv) * | 1997-01-20 | 1997-01-20 | Astra Ab | New formulation |
| US5837713A (en) | 1997-02-26 | 1998-11-17 | Mayo Foundation For Medical Education And Research | Treatment of eosinophil-associated pathologies by administration of topical anesthetics and glucocorticoids |
| US5874418A (en) | 1997-05-05 | 1999-02-23 | Cydex, Inc. | Sulfoalkyl ether cyclodextrin based solid pharmaceutical formulations and their use |
| US6046177A (en) * | 1997-05-05 | 2000-04-04 | Cydex, Inc. | Sulfoalkyl ether cyclodextrin based controlled release solid pharmaceutical formulations |
| SE9701956D0 (sv) * | 1997-05-23 | 1997-05-23 | Astra Ab | New composition of matter |
| GB9711643D0 (en) * | 1997-06-05 | 1997-07-30 | Janssen Pharmaceutica Nv | Glass thermoplastic systems |
| DE69834154T2 (de) * | 1997-07-01 | 2007-01-25 | Pfizer Products Inc., Groton | Verfahren zur Herstellung von einem Cyclodextrin |
| AU2006200277B2 (en) | 1997-09-29 | 2008-04-10 | Novartis Ag | Perforated microparticles and methods of use |
| US6598603B1 (en) * | 1997-12-31 | 2003-07-29 | Astra Aktiebolag | Method for treating respiratory diseases |
| JP2003522207A (ja) | 1998-02-23 | 2003-07-22 | サイクロプス・イーエイチエフ | 高エネルギーシクロデキストリン複合体 |
| RU2157214C2 (ru) | 1998-04-16 | 2000-10-10 | Государственный научный центр лекарственных средств | Противовоспалительное и антимикробное лекарственное средство для местного применения |
| US6241969B1 (en) * | 1998-06-26 | 2001-06-05 | Elan Corporation Plc | Aqueous compositions containing corticosteroids for nasal and pulmonary delivery |
| US6509323B1 (en) * | 1998-07-01 | 2003-01-21 | California Institute Of Technology | Linear cyclodextrin copolymers |
| AU757896B2 (en) * | 1998-09-02 | 2003-03-13 | Allergan, Inc. | Preserved cyclodextrin-containing compositions |
| US20020198174A1 (en) | 2001-05-07 | 2002-12-26 | Allergan Sales, Inc. | Disinfecting and solubilizing steroid compositions |
| US6297227B1 (en) * | 1998-09-10 | 2001-10-02 | Schering Corporation | Methods and compositions for treating sinusitis, otitis media and other related disorders using antihistamines |
| MA25590A1 (fr) | 1998-09-14 | 2002-12-31 | Inhale Therapeutic Syst | Agent actif de delivraison de poudre seche |
| US6509327B1 (en) | 1998-09-30 | 2003-01-21 | Alcon Manufacturing, Ltd. | Compositions and methods for treating otic, ophthalmic and nasal infections |
| US6740664B2 (en) | 1998-09-30 | 2004-05-25 | Alcon, Inc. | Methods for treating otic and ophthalmic infections |
| AU772204B2 (en) | 1999-01-21 | 2004-04-22 | Bristol-Myers Squibb Company | Complex of ras-farnesyltransferase inhibitor and sulfobutylether-7-beta-cyclodextrin or 2-hydroxypropyl-beta-cyclodextrin and method |
| AU2879100A (en) | 1999-02-12 | 2000-08-29 | Miles A. Libbey Iii | Formulation and system for intra-oral delivery of pharmaceutical agents |
| FR2789685B1 (fr) * | 1999-02-15 | 2001-05-04 | Univ Lille Sciences Tech | Procede de fabrication de polymeres solubles et insolubles a base de cyclodextrine(s) et/ou de derives de cyclodextrine(s) et polymeres solubles a base de cyclodextrine(s) et/ou de derives de cyclodextrine(s) |
| US6267985B1 (en) * | 1999-06-30 | 2001-07-31 | Lipocine Inc. | Clear oil-containing pharmaceutical compositions |
| US6761903B2 (en) * | 1999-06-30 | 2004-07-13 | Lipocine, Inc. | Clear oil-containing pharmaceutical compositions containing a therapeutic agent |
| US6136603A (en) | 1999-03-26 | 2000-10-24 | Isis Pharmaceuticals Inc. | Antisense modulation of interleukin-5 signal transduction |
| DE60025019T2 (de) | 1999-10-29 | 2006-08-24 | Nektar Therapeutics, San Carlos | Trockenpulverzusammensetzungen mit verbesserter dispersivität |
| US6962151B1 (en) * | 1999-11-05 | 2005-11-08 | Pari GmbH Spezialisten für effektive Inhalation | Inhalation nebulizer |
| US6479467B1 (en) * | 1999-12-16 | 2002-11-12 | Eastman Chemical Company | Cyclodextrin ethers |
| RU2180217C2 (ru) | 2000-03-21 | 2002-03-10 | Закрытое акционерное общество "Пульмомед" | Стабильный водный раствор противовоспалительного действия, содержащий будесонид |
| WO2001072338A1 (en) | 2000-03-28 | 2001-10-04 | Farmarc Nederland Bv | Alprazolam inclusion complexes and pharmaceutical compositions thereof |
| US7871598B1 (en) | 2000-05-10 | 2011-01-18 | Novartis Ag | Stable metal ion-lipid powdered pharmaceutical compositions for drug delivery and methods of use |
| US20020025946A1 (en) * | 2000-05-11 | 2002-02-28 | Buchanan Charles M. | Acylated cyclodextrin: guest molecule inclusion complexes |
| GB0016876D0 (en) | 2000-07-11 | 2000-08-30 | Astrazeneca Ab | Novel formulation |
| PE20020146A1 (es) | 2000-07-13 | 2002-03-31 | Upjohn Co | Formulacion oftalmica que comprende un inhibidor de ciclooxigenasa-2 (cox-2) |
| MXPA03004241A (es) | 2000-11-15 | 2004-12-03 | Chandavarkar Mohan A | Preparaciones farmaceuticas que comprenden corticosteroides y agentes antiinfecciosos. |
| ES2266310T3 (es) * | 2000-11-24 | 2007-03-01 | Breath Limited | Esterizacion de suspensiones de glucocorticosteriodes. |
| WO2002055562A2 (en) * | 2001-01-11 | 2002-07-18 | Eastman Chem Co | Cyclodextrin sulfonates, guest inclusion complexes, methods of making the same and related materials |
| ATE325135T1 (de) * | 2001-02-14 | 2006-06-15 | Akzo Nobel Nv | 2-alkylierte cyclodextrinderivate : umkehrungsmittel von medikament-induzierter neuromuskulärer blockierung |
| US7034013B2 (en) | 2001-03-20 | 2006-04-25 | Cydex, Inc. | Formulations containing propofol and a sulfoalkyl ether cyclodextrin |
| EP1383445A4 (en) | 2001-03-20 | 2005-04-13 | Cydex Inc | PREPARATION CONTAINING PROPOFOL AND SULFOALKYL ETHER CYCLODEXTRIN |
| US8137699B2 (en) * | 2002-03-29 | 2012-03-20 | Trustees Of Princeton University | Process and apparatuses for preparing nanoparticle compositions with amphiphilic copolymers and their use |
| US6667344B2 (en) | 2001-04-17 | 2003-12-23 | Dey, L.P. | Bronchodilating compositions and methods |
| US20030055026A1 (en) * | 2001-04-17 | 2003-03-20 | Dey L.P. | Formoterol/steroid bronchodilating compositions and methods of use thereof |
| US20030118512A1 (en) | 2001-10-30 | 2003-06-26 | Shen William W. | Volatilization of a drug from an inclusion complex |
| US20030091513A1 (en) * | 2001-10-03 | 2003-05-15 | Mohsen Nahed M. | Method to generate water soluble or nonwater soluble in nanoparticulates directly in suspension or dispersion media |
| CA2463687A1 (en) | 2001-10-18 | 2003-04-24 | Decode Genetics Ehf | Cyclodextrin complexes |
| CA2464250C (en) | 2001-10-24 | 2008-08-05 | Frank-Christophe Lintz | Kit for the preparation of a pharmaceutical composition |
| KR20030041577A (ko) | 2001-11-20 | 2003-05-27 | 디디에스텍주식회사 | 난용성 약물과 치환된 시클로덱스트린을 함유하는고체분산체 및 이를 함유하는 약제학적 조성물 |
| US20030129242A1 (en) * | 2002-01-04 | 2003-07-10 | Bosch H. William | Sterile filtered nanoparticulate formulations of budesonide and beclomethasone having tyloxapol as a surface stabilizer |
| AU2003217623A1 (en) | 2002-02-20 | 2003-09-09 | Sepracor Inc. | Amino acid and peptide-modified forms of glucocorticoids |
| US7128928B2 (en) | 2002-02-22 | 2006-10-31 | Pharmacia Corporation | Ophthalmic formulation with novel gum composition |
| US6780324B2 (en) * | 2002-03-18 | 2004-08-24 | Labopharm, Inc. | Preparation of sterile stabilized nanodispersions |
| ITMI20020808A1 (it) * | 2002-04-17 | 2003-10-17 | Chiesi Farma Spa | Procedimento per la preparazione di una sospensione sterile di particelle di beclometasone dipropionato da somministrare per inalazione |
| CN1232539C (zh) | 2002-05-10 | 2005-12-21 | 刘云清 | 有机药物与倍他环糊精衍生物的配合物及其制备方法 |
| GB2389530B (en) | 2002-06-14 | 2007-01-10 | Cipla Ltd | Pharmaceutical compositions |
| US7029657B2 (en) | 2002-08-02 | 2006-04-18 | Balance Pharmaceuticals, Inc. | Nasal spray steroid formulation and method |
| EP2319584A1 (en) * | 2002-08-29 | 2011-05-11 | Cipla Ltd. | Pharmaceutical products and compositions comprising salmeterol, ciclesonide and tiotropium |
| US20040045546A1 (en) * | 2002-09-05 | 2004-03-11 | Peirce Management, Llc | Pharmaceutical delivery system for oral inhalation through nebulization consisting of inert substrate impregnated with substance (S) to be solubilized or suspended prior to use |
| AU2003275329B2 (en) * | 2002-09-13 | 2008-04-03 | Cydex Pharmaceuticals, Inc. | Capsules containing aqueous fill compositions stabilized with derivatized cyclodextrin |
| US20040220153A1 (en) * | 2002-09-24 | 2004-11-04 | Jost-Price Edward Roydon | Methods and reagents for the treatment of diseases and disorders associated with increased levels of proinflammatory cytokines |
| AU2003295344B2 (en) * | 2002-10-09 | 2008-01-31 | Insert Therapeutics, Inc. | Cyclodextrin-based materials, compositions and uses related thereto |
| WO2004069280A1 (en) * | 2003-02-06 | 2004-08-19 | Cipla Ltd | Pharmaceutical inclusion complexes containing a steroid and optionally an antibacterial agent |
| MXPA05008649A (es) | 2003-02-14 | 2005-11-23 | Combinatorx Inc | Terapia de combinacion para el tratamiento de desordenes inmunoinflamatorios. |
| EP1596822A2 (en) | 2003-02-17 | 2005-11-23 | Sun Pharmaceuticals Industries Ltd. | A low dose corticosteroid composition |
| BRPI0407583A (pt) | 2003-02-21 | 2006-02-14 | Sun Pharmaceutical Ind Ltd | solução oftálmica lìmpida e estável |
| US20040204394A1 (en) * | 2003-04-11 | 2004-10-14 | Aderis Pharmaceuticals, Inc. | Triptolide analogues |
| CA2532874A1 (en) * | 2003-07-22 | 2005-02-03 | Baxter International Inc. | Small spherical particles of low molecular weight organic molecules and methods of preparation and use thereof |
| WO2005027853A2 (en) | 2003-09-19 | 2005-03-31 | University Of Louisville Research Foundation Inc | Method for treating snoring and sleep apnea with leukotriene antagonists |
| US20050112199A1 (en) | 2003-09-24 | 2005-05-26 | Mahesh Padval | Therapeutic regimens for administering drug combinations |
| US20060263350A1 (en) | 2003-09-26 | 2006-11-23 | Fairfield Clinical Trials Llc | Combination antihistamine medication |
| TW200517114A (en) | 2003-10-15 | 2005-06-01 | Combinatorx Inc | Methods and reagents for the treatment of immunoinflammatory disorders |
| DE10347994A1 (de) * | 2003-10-15 | 2005-06-16 | Pari GmbH Spezialisten für effektive Inhalation | Wässrige Aerosol-Zubereitung |
| EP1678211A4 (en) * | 2003-10-31 | 2008-04-02 | Univ Kansas | SULFOALKYL ETHER-ALKYL ETHER CYCLODEXTRINS DERIVATIVES |
| GB0329918D0 (en) | 2003-12-24 | 2004-01-28 | West Pharm Serv Drug Res Ltd | Intranasal compositions |
| US20070020299A1 (en) | 2003-12-31 | 2007-01-25 | Pipkin James D | Inhalant formulation containing sulfoalkyl ether cyclodextrin and corticosteroid |
| US20070020298A1 (en) | 2003-12-31 | 2007-01-25 | Pipkin James D | Inhalant formulation containing sulfoalkyl ether gamma-cyclodextrin and corticosteroid |
| US20070020196A1 (en) | 2003-12-31 | 2007-01-25 | Pipkin James D | Inhalant formulation containing sulfoalkyl ether cyclodextrin and corticosteroid prepared from a unit dose suspension |
| WO2005065435A2 (en) * | 2003-12-31 | 2005-07-21 | Cydex, Inc. Et Al. | Inhalant formulation containing sulfoalkyl ether cyclodextrin and corticosteroid |
| US20050234018A1 (en) | 2004-04-15 | 2005-10-20 | Allergan, Inc. | Drug delivery to the back of the eye |
| EP2708225B1 (en) * | 2004-04-23 | 2018-12-26 | CyDex Pharmaceuticals, Inc. | DPI Formulation Containing Sulfoalkyl Ether Cyclodextrin |
| US20050244472A1 (en) | 2004-04-30 | 2005-11-03 | Allergan, Inc. | Intraocular drug delivery systems containing excipients with reduced toxicity and related methods |
| US6969706B1 (en) | 2004-05-12 | 2005-11-29 | Allergan, Inc. | Preserved pharmaceutical compositions comprising cyclodextrins |
| US20060045850A1 (en) | 2004-08-30 | 2006-03-02 | Qpharma, Llc | Nasal delivery of cyclodextrin complexes of anti-inflammatory steroids |
| GB0422413D0 (en) * | 2004-10-08 | 2004-11-10 | Breath Ltd | High efficiency nebulisation |
| WO2006043965A1 (en) * | 2004-10-14 | 2006-04-27 | Allergan, Inc. | Therapeutic ophthalmic compositions containing retinal friendly excipients and related methods |
| US20060105045A1 (en) | 2004-11-08 | 2006-05-18 | Buchanan Charles M | Cyclodextrin solubilizers for liquid and semi-solid formulations |
| US20070020330A1 (en) | 2004-11-24 | 2007-01-25 | Medpointe Healthcare Inc. | Compositions comprising azelastine and methods of use thereof |
| SI2522365T1 (sl) * | 2004-11-24 | 2017-02-28 | Meda Pharmaceuticals Inc. | Sestavki, ki obsegajo azelastin, in postopki njihove uporabe |
| US20060120967A1 (en) | 2004-12-07 | 2006-06-08 | Qpharma, Llc | Solution forms of cyclodextrins for nasal or throat delivery of essential oils |
| CN101180038A (zh) | 2005-03-23 | 2008-05-14 | 伊兰制药国际有限公司 | 纳米颗粒皮质类固醇和抗组胺药制剂 |
| US7893040B2 (en) | 2005-07-22 | 2011-02-22 | Oculis Ehf | Cyclodextrin nanotechnology for ophthalmic drug delivery |
| WO2007054974A2 (en) | 2005-09-28 | 2007-05-18 | Arch Pharmalab Limited | A green chemistry process for the preparation of pregnadiene esters |
| EP1971346A2 (en) | 2005-12-20 | 2008-09-24 | Tika Läkemedel AB | Systems and methods for the delivery of corticosteroids |
| US20070178049A1 (en) | 2005-12-20 | 2007-08-02 | Verus Pharmaceuticals, Inc. | Systems and methods for the delivery of corticosteroids having an enhanced pharmacokinetic profile |
| US20070160542A1 (en) | 2005-12-20 | 2007-07-12 | Verus Pharmaceuticals, Inc. | Methods and systems for the delivery of corticosteroids having an enhanced pharmacokinetic profile |
| US20070197487A1 (en) | 2005-12-20 | 2007-08-23 | Verus Pharmaceuticals, Inc. | Systems and methods for the delivery of corticosteroids having an increased lung deposition |
| US20070185066A1 (en) | 2005-12-20 | 2007-08-09 | Verus Pharmaceuticals, Inc. | Systems and methods for the delivery of corticosteroids |
| US20070197486A1 (en) | 2005-12-20 | 2007-08-23 | Verus Pharmaceuticals, Inc. | Methods and systems for the delivery of corticosteroids |
| US20070178050A1 (en) | 2005-12-20 | 2007-08-02 | Verus Pharmaceuticals, Inc. | Methods and systems for the delivery of corticosteroids having an increased lung depositon |
| US20070249572A1 (en) | 2005-12-20 | 2007-10-25 | Verus Pharmaceuticals, Inc. | Systems and methods for the delivery of corticosteroids |
| US20070202051A1 (en) | 2006-02-10 | 2007-08-30 | Pari Gmbh | Aerosols for sinunasal drug delivery |
| EP1988878A2 (en) | 2006-02-15 | 2008-11-12 | Tika Läkemedel AB | Sterilization of corticosteroids with reduced mass loss |
| EP1894559A1 (en) | 2006-09-01 | 2008-03-05 | PARI Pharma GmbH | Means to solubilise steroids for inhalation |
| CN101199855A (zh) | 2006-12-13 | 2008-06-18 | 天津药业研究院有限公司 | 皮质激素包合物水溶液及其应用 |
| CN101273993A (zh) | 2007-03-27 | 2008-10-01 | 北京亚欣保诚医药科技有限公司 | 糠酸莫米松溶液型液体制剂 |
| CN106038481A (zh) * | 2007-06-28 | 2016-10-26 | 锡德克斯药物公司 | 皮质类固醇水溶液的鼻部和眼部给药 |
| CA2707158A1 (en) | 2007-11-28 | 2009-06-04 | Revision Therapeutics, Inc. | Modulators of ocular oxidative stress |
| UY33367A (es) | 2010-05-05 | 2011-10-31 | Glaxo Wellcome Mfg Pte Ltd | Composiciones farmacéuticas y métodos para su elaboración |
| WO2015109201A1 (en) | 2014-01-17 | 2015-07-23 | Nephron Pharmaceuticals Corporation | Budesonide cyclodextrin formulation |
-
2006
- 2006-06-30 US US11/479,979 patent/US20070020299A1/en not_active Abandoned
- 2006-12-19 EP EP06850326A patent/EP2043599A4/en not_active Withdrawn
- 2006-12-19 KR KR1020087031723A patent/KR101691222B1/ko active IP Right Grant
- 2006-12-19 US US11/613,187 patent/US20070202054A1/en not_active Abandoned
- 2006-12-19 WO PCT/US2006/062346 patent/WO2008005053A1/en active Application Filing
- 2006-12-19 KR KR1020167016536A patent/KR101807726B1/ko active IP Right Grant
- 2006-12-19 CN CN2011102267579A patent/CN102319231A/zh active Pending
- 2006-12-19 CN CN200680055726A patent/CN101636144A/zh active Pending
- 2006-12-19 AU AU2006345712A patent/AU2006345712A1/en not_active Abandoned
- 2006-12-19 RU RU2009102994/15A patent/RU2009102994A/ru not_active Application Discontinuation
- 2006-12-19 KR KR20157009220A patent/KR20150043563A/ko active Application Filing
- 2006-12-19 NZ NZ597354A patent/NZ597354A/xx not_active IP Right Cessation
- 2006-12-19 CA CA002656318A patent/CA2656318A1/en not_active Abandoned
- 2006-12-20 BR BRPI0621773-7A patent/BRPI0621773A2/pt not_active IP Right Cessation
- 2006-12-20 JP JP2009518094A patent/JP2009542649A/ja not_active Withdrawn
- 2006-12-20 MX MX2009000065A patent/MX2009000065A/es not_active Application Discontinuation
-
2007
- 2007-06-28 WO PCT/US2007/072387 patent/WO2008005802A2/en active Application Filing
- 2007-06-29 WO PCT/US2007/072442 patent/WO2008005819A2/en active Application Filing
-
2008
- 2008-06-30 CA CA2728386A patent/CA2728386C/en active Active
- 2008-12-25 IL IL196185A patent/IL196185A0/en unknown
-
2010
- 2010-10-14 US US12/904,897 patent/US20110123518A1/en not_active Abandoned
-
2011
- 2011-01-28 US US13/015,959 patent/US20110251157A1/en not_active Abandoned
- 2011-02-04 RU RU2011104059/15A patent/RU2011104059A/ru unknown
-
2012
- 2012-08-15 US US13/586,380 patent/US9827324B2/en active Active
- 2012-11-14 US US13/676,744 patent/US10159752B2/en active Active
-
2014
- 2014-05-08 JP JP2014096717A patent/JP2014159467A/ja active Pending
-
2017
- 2017-04-27 JP JP2017088045A patent/JP6409090B2/ja active Active
- 2017-11-17 US US15/817,056 patent/US10207008B2/en active Active
-
2018
- 2018-09-20 JP JP2018175728A patent/JP2019006818A/ja active Pending
- 2018-12-05 US US16/210,561 patent/US10799599B2/en active Active
- 2018-12-18 US US16/224,189 patent/US20190192684A1/en not_active Abandoned
Cited By (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2014505717A (ja) * | 2011-02-17 | 2014-03-06 | シプラ・リミテッド | 医薬組成物 |
| JP2017061456A (ja) * | 2011-02-17 | 2017-03-30 | シプラ・リミテッド | 医薬組成物 |
| JP2020100658A (ja) * | 2014-03-28 | 2020-07-02 | ユニベルシテ・ド・リエージュUniversite De Liege | シクロデキストリン及びブデソニド誘導体組成物ならびに方法 |
| JP7008097B2 (ja) | 2014-03-28 | 2022-02-10 | ユニベルシテ・ド・リエージュ | シクロデキストリン及びブデソニド誘導体組成物ならびに方法 |
| JP2018521987A (ja) * | 2015-06-18 | 2018-08-09 | セージ セラピューティクス, インコーポレイテッド | 神経活性ステロイド溶液およびその使用方法 |
| JP2021127350A (ja) * | 2015-06-18 | 2021-09-02 | セージ セラピューティクス, インコーポレイテッド | 神経活性ステロイド溶液およびその使用方法 |
| JP7374954B2 (ja) | 2015-06-18 | 2023-11-07 | セージ セラピューティクス, インコーポレイテッド | 神経活性ステロイド溶液およびその使用方法 |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US10799599B2 (en) | Inhalant formulation containing sulfoalkyl ether cyclodextrin and corticosteroid | |
| JP6186478B2 (ja) | スルホアルキルエーテルシクロデキストリンおよびコルチコステロイドを含む吸入製剤 | |
| US20110008325A1 (en) | Inhalant Formulation Containing Sulfoalkyl Ether Cyclodextrin and Corticosteroid Prepared from a Unit Dose Suspension | |
| US20070020298A1 (en) | Inhalant formulation containing sulfoalkyl ether gamma-cyclodextrin and corticosteroid | |
| MXPA06007583A (en) | Inhalant formulation containing sulfoalkyl ether cyclodextrin and corticosteroid prepared from a unit dose suspension |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20091204 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20091204 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20120626 |
|
| A761 | Written withdrawal of application |
Free format text: JAPANESE INTERMEDIATE CODE: A761 Effective date: 20120904 |